Применение наночастиц бората свинца, нацеленных на мутантный ген 53, в лечении и способ получения данных наночастиц - RU2781098C1
Код документа: RU2781098C1
Чертежи


Описание
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ НАСТОЯЩЕЕ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к применению наноразмерных соединений бората свинца в лечебных целях в связи с избирательной противораковой активностью данных соединений в отношении линии p53-мутантных клеток рака молочной железы T47D.
УРОВЕНЬ ТЕХНИКИ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Бораты свинца (PbxByOzHt-PbxByOz) в последнее время привлекли большой интерес исследователей благодаря их превосходным оптическим и фотоэлектрическим свойствам, а также возможности их использования как в качестве катализатора, так и материала для захвата нейтрон-гамма-лучей, и данные бораты пытались синтезировать с использованием различных способов синтеза. Однако следует заметить, что влияние данных соединений на здоровье и биологические применение данной группы соединений до сих пор не изучены. Некоторые из соединений группы бората свинца, синтезированные, согласно литературным данным, с использованием традиционных способов синтеза, таких как твердофазный, золь-гель и сольвотермический синтез, следующие: PbB4O7, Pb(BO2)2H2O, Pb6B10O21, Pb3B10O18.2H2O, Pb2[B5O9]OH.H2O, Pb5B3O8(OH)3.H2O, Pb6B12O24.H2O, Pb2B3O5,5(OH)2, [Pb3(B3O7)]. NO3, Pb6B11O18(OH)9 и Pb6B6O15.
Как известно, многие физические свойства материалов изменяются и приобретают более высокое качество при переходе от микроскопических размеров к наноразмерным. Поэтому является важным наноразмерный синтез соединений бората свинца , но количество литературных данных по исследованию синтеза данных соединений остается ограниченным. Одним из таких исследований является получение бората свинца способом соосаждения в микроволновой печи, который описан в заявке на китайский патент № CN1562840. В этом синтезе растворы бората натрия и нитрата свинца смешивали в соответствующих стехиометрических пропорциях в присутствии 2-этилгексилсульфосукцината и полученную смесь подвергали воздействию микроволновых лучей в микроволновой печи лабораторного типа при температуре 35-45°C в течение 1,5 минут -2 часа при мощности 500 Вт. Полученные продукты промывали дистиллированной водой и этанолом, а затем сушили в сушильном шкафу при 60°C в течение 10 часов для удаления примесей. Второе исследование посвящено синтезу наноразмерного соединения Pb3B10O16(OH)4 с помощью сольвотермического способа, который описан в заявке на китайский патент № CN105568378. В указанном синтезе растворы ацетата свинца и борной кислоты смешивали в соответствующих стехиометрических соотношениях в присутствии пиридина, а pH среды регулировали с помощью раствора аммиака. Полученную смесь переносили в автоклав и нагревали при 230 градусах в течение 12 часов. Полученные продукты промывали дистиллированной водой и этанолом и нагревали при 60 градусах в течение 12 часов.
Рак - общее название болезней, возникающих в результате неконтролируемого роста и деления клеток. В то время как раковые клетки могут образовываться в большинстве тканей тела, образующиеся раковые клетки могут метастазировать в различные части тела посредством крови. Рак имеет шесть основных отличительных черт. Данные черты включают в себя:
1.Самостоятельный синтез факторов роста,
2.Уклонение от сигналов, подавляющих рост,
3.Поиск других способов выживания, чтобы противостоять запрограммированной гибели клеток, апоптозу,
4.Возможность неограниченной пролиферации,
5.Способность производить новые кровеносные сосуды (ангиогенез) для поддержания жизнедеятельности и
6.Инвазия и метастазирование в другие ткани через кровеносные сосуды [1].
Спустя одиннадцать лет после идентификации этих шести признаков, Ханахан и Вайнберг опубликовали обновленную статью, в которой они увеличили количество признаков рака опухоли до десяти. Дополнительные четыре отличительных признака:
7. Нерегулярные метаболические пути,
8. Нестабильный геном, открытый для мутаций,
9. Умение избегать иммунного ответа и
10. Опухоль, стимулирующая воспаление [2].
Эти десять признаков являются основной причиной смертей, связанных с раком, а раковые заболевания статистически являются второй по частоте причиной смерти после сердечно-сосудистых заболеваний. Ежегодно миллиарды долларов тратятся на то, чтобы найти лекарство для лечения рака, что является одной из проблем, привлекающих наибольшее внимание ученых всего мира, и на лечение пациентов. Хотя NCI (Национальный институт рака) поддерживает только 250 противораковых препаратов, все они имеют 23 известных побочных эффекта.
В исследовании, проведенном под руководством Паулы Гарсия Калавиа в 2018 году, было изучено фотодинамическое действие наночастиц золота, функционализированных лактозофталоцианином, на клетки рака молочной железы. Лактоза, в качестве углевода в указанном исследовании использовалась как для стабилизации наночастиц золота, так и для нацеливания на клетки рака молочной железы через рецептор галектина-1. Было проведено сравнение клеточной линии аденокарциномы молочной железы MDA-MB-231 и здорового эпителия молочной железы MCF-10A, и в результате было обнаружено, что наночастицы золота избирательно убивали клеточную линию аденокарциномы со сверхэкспрессией рецептора галектина-1, но не влияли на клеточную линию MCF-10A [3].
В статье, опубликованной Hekmat A. и др. в 2012 году, влияние комбинаций наночастиц серебра и доксорубицина на линии клеток рака молочной железы T47D и MCF-7 было показано путем сравнения со стволовыми эндометриальными клетками человека. Было замечено, что использование комбинации 0,3 мкМ доксорубицина и 10 мкМ наночастиц серебра на линии клеток T47D привело к уровню смертности в 60%. В линии клеток MCF-7 уровень смертности от идентичной комбинации составил 49% [4].
Нанотехнологические продукты имеют размер примерно от одной тысячи до десяти тысяч раз меньше, чем размер клетки, и этим свойством они схожи с биологическими молекулами, такими как рецепторы или некоторые ферменты. Благодаря своему небольшому размеру наночастицы могут легко взаимодействовать со многими молекулами внутри и/или вне клетки. Наночастицы размером менее двадцати нанометров могут легко выходить из кровеносных сосудов и легко перемещаться в любую часть тела (эффект ЭПР - улучшенные проницаемость и удерживание), и эта простота доступа к любой и каждой части тела имеет большое значение, поскольку дает возможность идентифицировать раковые клетки и полностью предоставить их лечение наночастицам. Однако, процент эффективности эффекта ЭПР может уменьшаться при некоторых типах рака из-за изменения проницаемости кровеносных сосудов [5]. Более того, идентификация раковой клетки имеет важное значение в результате такой легкости доступа. В противном случае наночастицы убьют и здоровые клетки вместе с раковыми клетками. В этом отношении важно разработать подходящие для пациента наночастицы.
Исследования составов наночастиц привлекают внимание и интерес исследователей, поскольку они позволяют улучшить существующие способы лечения рака.
Хирургическая операция и/или химиотерапия часто используются для лечения рака. В то время как хирургическая операция в некоторых случаях дает полный и эффективный результат; обычно после операции вводят химиотерапевтический препарат, чтобы избежать возможности присутствия раковых клеток, которые выживут и спровоцируют образование раковой опухоли в долгосрочной перспективе. В основном химиотерапия вызывает ряд побочных эффектов, повреждая как здоровые, так и раковые клетки. Химиотерапия оказывает наибольшее влияние на клетки с высокой скоростью пролиферации в организме: волосковые клетки, клетки крови, продуцируемые в костном мозге, и клетки пищеварительной системы. Побочные эффекты, часто наблюдаемые после химиотерапии, следующие:
• Усталость: хотя это в основном вызвано анемией, вызванной поражением клеток крови, причина также может быть психологической.
• Тошнота и рвота: данный эффект может быть связан с чувствительностью к лекарствам, но может иметь психологические причины.
• Выпадение волос: выпадение волос, на которое негативно влияет химиотерапия из-за их быстро растущих клеток, является одной из наиболее серьезных причин депрессии у пациентов.
• Снижение показателей крови: костный мозг, пораженный химиотерапией, приводит к значительному уменьшению количества клеток крови. Поскольку в результате этого снижения к тканям не может быть доставлено достаточное количество кислорода, могут наблюдаться многие побочные эффекты, такие как ослабление иммунной системы и затруднение свертывания крови.
• Язвы в ротовой полости: химиотерапевтические препараты могут иногда вызывать воспалительные язвы в ротовой полости. Во время лечения пациенты должны избегать чрезмерно горячих или холодных напитков и уделять особое внимание гигиене полости рта.
• Диарея и запор: Диарея или запор могут наблюдаться в результате реакции клеток пищеварительной системы на различные химиотерапевтические агенты. Данная ситуация, последствия которой в основном можно уменьшить с помощью диеты, в некоторых случаях может привести к тяжелой диарее, требующей внутривенного приема жидкости.
• Изменения кожи и ногтей: химиотерапевтические препараты имеют побочные эффекты, такие как потемнение цвета кожи, шелушение кожи, покраснение или сухость кожи. Также может наблюдаться легкая ломка ногтей или потемнение их цвета. Особое внимание следует уделять шелушению кожи, так как это приведет к появлению открытых ран у пациентов с ослабленным иммунитетом.
• Проблемы со сном: хотя это обычно происходит по психологическим причинам, неспособность организма отдыхать, особенно во время процесса химиотерапии, снижает эффект химиотерапии и еще больше подрывает психическое здоровье пациента.
Чтобы повысить эффективность лечения, требуется использовать химиотерапию в сочетании с хирургическими и другими способами, а также обилие и непредсказуемость ее побочных эффектов, варьирующихся от пациента к пациенту, побудили ученых искать новые способы лечения. Наночастицы стали популярными в исследованиях, начатых с целью улучшения существующих методов лечения и уменьшения побочных эффектов.
В дополнение ко всему вышеуказанному, в современном уровне техники наночастицы используются либо в сочетании с известным химическим веществом - где при этом указанные химические вещества могут избирательно убивать раковые опухоли, даже если наночастица не используется, так что здесь воздействие нацелено на усиление дейсвтия - или выполняется нацеливание, осуществляемое добавкой глюкозы, чтобы клетки могли распознавать наночастицы. Поскольку потребность в глюкозе является общей для всех клеток, способность убивать пропорционально больше раковых клеток не причинит вреда здоровым клеткам. Кроме того, как упоминалось выше, из-за эффекта ЭПР многие наночастицы, которые могут неконтролируемым образом проникать в незлокачественные клетки, могут быть опасными для здоровья этих клеток.
Заявка на японский патент № JP2005300232 в данной области техники относится к применению позитронно-эмиссионной томографии с использованием аэрогеля и способу получения указанного аэрогеля. Целью настоящего изобретения является создание позитронно-эмиссионной томографии, которая позволяет с высокой точностью определять положение аномальных тканей, таких как раковые клетки. Одним из сырьевых материалов, используемых в производстве аэрогелей, являются оксиды свинца, и для этой цели используется соль свинца, относящаяся к группе, в которую также входит борат свинца.
Международная заявка на патент № WO2011022350 в данной области техники относится к фармацевтически приемлемым наночастицам цинка для лечения инфекций и рака. Наночастицы цинка имеют ядра, содержащие элементарный цинк без значительных количеств других металлов или оксидов металлов. Другое применение наночастиц цинка по настоящему изобретению - диагностика и визуализация. Наночастицы цинка обладают врожденной автофлуоресцентной способностью и, таким образом, могут использоваться для визуализации таких участков, как инфекции и опухоли. Поскольку это полезно в таких ситуациях, как рентгеновское изображение, можно использовать ион, выбранный из группы, в которую также входит свинец (II).
Заявка на китайский патент № CN103046113 в данной области техники относится к составному борату свинца и нелинейно-оптическому кристаллу бората свинца, а также способу их получения. Соединение бората свинца имеет химическую формулу Pb4O(BO3)2 и молекулярную массу 962,38 и синтезируется с использованием твердофазной реакции. Молярное соотношение свинца и бора в соединении составляет 2 : 1, и соединение, содержащее свинец, представляет собой карбонат свинца, нитрат свинца, оксид свинца, ацетат свинца или оксалат свинца; и борсодержащее соединение представляет собой борную кислоту или оксид бора.
Очевидно, что в литературе отсутствуют публикации или патенты, касающиеся действия наноразмерных соединений бората свинца по настоящему изобретению на раковые опухоли и связанные с ними физиологические нарушения.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Целью настоящего изобретения является применение наноразмерного соединения бората свинца в процессе лечения из-за его избирательного токсического действия на раковые клетки.
Другой целью изобретения является синтез наноразмерного соединения бората свинца с использованием нового способа синтеза с буферным осаждением.
Еще одна цель изобретения состоит в том, чтобы эти соединения имели размер менее 100 нм, чтобы использовать их в биологических применениях in vivo.
Другой целью изобретения является использование способа синтеза, который является намного более простым, экономичным и подходящим для изготовления по сравнению с методами синтеза гидротермальным/сольвотермическим и микроволновым осаждением благодаря тому факту, что его можно проводить без какой-либо необходимости в высокой температуре, длительном времени реакции, высоком давлении и любого вида облучения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
«ПРИМЕНЕНИЕ НАНОЧАСТИЦ БОРАТА СВИНЦА, НАЦЕЛЕННЫХ НА МУТАНТНЫЙ ГЕН 53, В ЛЕЧЕНИИ и СПОСОБ ПОЛУЧЕНИЯ ДАННЫХ НАНОЧАСТИЦ» разработано для достижения цели настоящего изобретения, изображенного на прилагаемом рисунке, на котором;
Фигура 1. представляет собой графическое представление влияния переменных концентраций наноразмерного бората свинца на жизнеспособность (A) Hacat (здоровый контрольный кератиноцит), (B) T47D (рак молочной железы), (C) MCF7 (рак молочной железы) и (D) Клетки A549 (рак легкого).
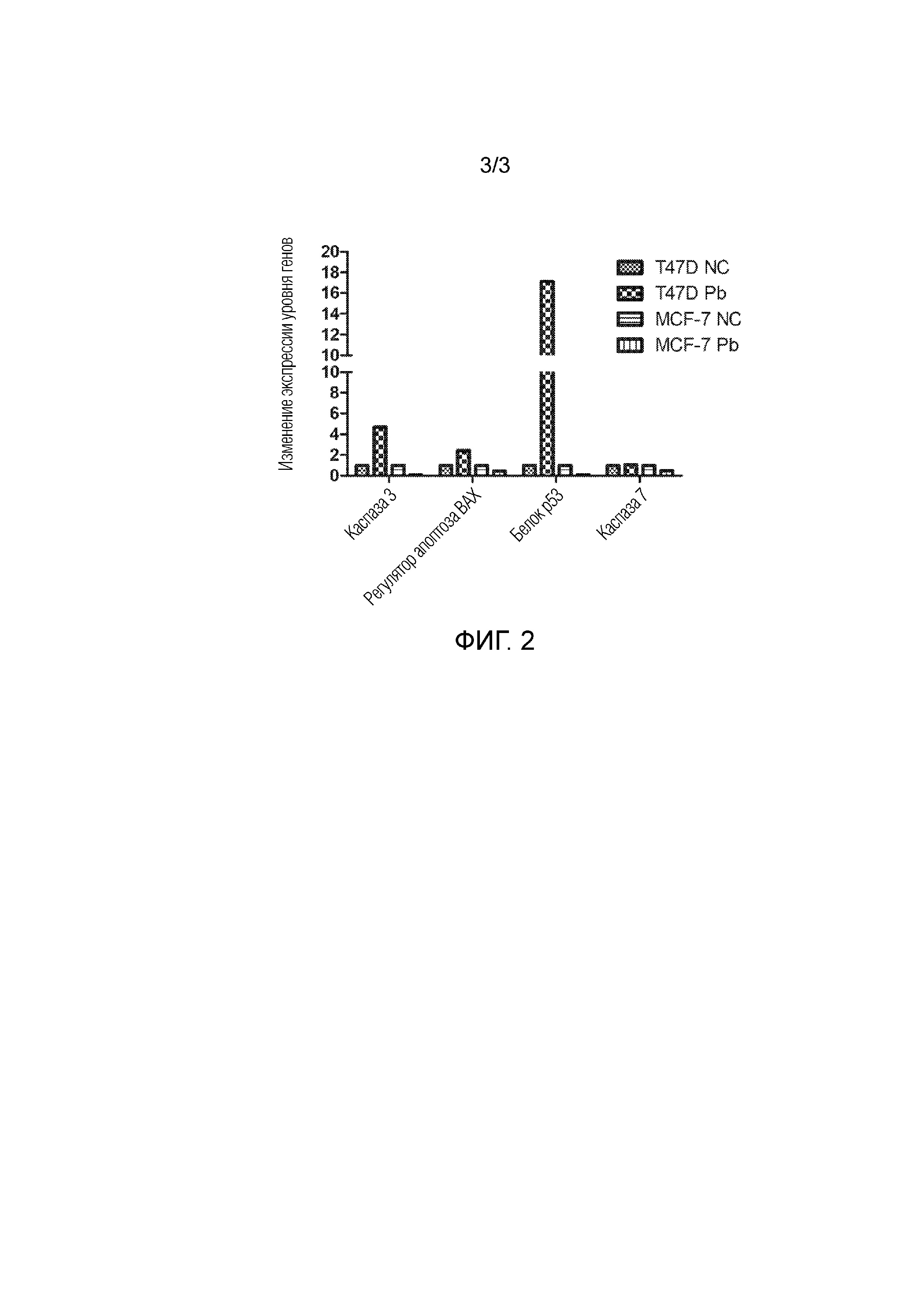
Фигура 2. представляет собой графическое представление изменения экспрессии гена в клеточной линии T47D, имеющей мутацию р53, и в клеточной линии MCF7, не имеющей мутации р53, после обработки свинцовой наночастицей посредством полимеразной цепной реакции в реальном времени. (Результаты были определены после нормализации, где в качестве контроля использовались клетки, несвязанные с нанесением наночастиц, и уровень экспрессии гена GAPDH, который также может называться охранным геном.)
Настоящее изобретение относится к наноразмерным соединениям метабората свинца, используемым для лечения раковых опухолей из-за их селективного токсического действия на раковые клетки. В рамках настоящего изобретения из-за их селективного противоракового действия (токсического действия) на линию p53-мутантных клеток рака молочной железы, T47D, наноразмерные соединения бората свинца используются с целью лечения данных раковых клеток.
Синтез наноразмерных (менее 100 нм) соединений бората свинца, разработанных для использования в процессе лечения раковых опухолей в рамках данного изобретения, проводят в комнатных условиях с помощью метода буферного осаждения. Этапы данного синтеза представляют собой:
1- Гидроксид натрия и борная кислота растворяются и смешиваются друг с другом в стехиометрическом соотношении 1: 2 в дистиллированной воде и боратном буфере (буферный раствор NaOH/H3BO3), имеющем значение pH от 9 до 9,5 и способном к поддерживать значение pH реакционной среды в этом диапазоне.
2- Нитрат свинца (и предпочтительно ПЭГ (от 400 до 20000 Да)) снова растворяют в 200 мл дистиллированной воды в отдельном стакане в стехиометрическом соотношении 1: 1,5. Раствор нитрата свинца (и предпочтительно ПЭГ) и раствор боратного буфера перемешивают в течение 30 минут при 2000 об/мин при механическом перемешивании.
3- Полученный продукт промывают 4 раза дистиллированной водой и затем сушат при 60°C в течение 24 часов для удаления примесей.
ПЭГ (полиэтиленгликоль) - биосовместимое поверхностно-активное вещество. В способе, описанном выше, также можно проводить реакцию без использования поверхностно-активных веществ, таких как ПЭГ. В этом случае всего 10 ммоль нитрата свинца растворяется в 20 мл воды в химическом стакане. Целью использования ПЭГ в реакции является получение наночастиц бората свинца, имеющих меньший размер частиц.
Размер частиц наноразмерных соединений бората свинца, синтезированных согласно данному изобретению, составляет менее 100 нм. Размер частиц менее 100 нм позволяет использовать эти соединения в биологических приложениях in vivo.
Используемый способ синтеза является намного более простым, экономичным и подходящим для изготовления по сравнению со способами синтеза гидротермальным/сольвотермическим и микроволновым осаждением, поскольку его можно проводить без необходимости использования высоких температур и длительного времени реакции, высоких значений давления и любых видов облучения.
Добавленный в среду ПЭГ (полиэтиленгликоль) является биосовместимым поверхностно-активным веществом. Данный фактор позволяет получать частицы меньшего размера (50 нм и ниже) и дает возможность легко диспергироваться данным частицам в воде. Также чтобы иметь возможность использовать соединения бората свинца в биологических назначениях и получать более мелкие наночастицы, во время или после реакции можно использовать ПЭГ и другие биосовместимые поверхностно-активные вещества с различными молекулярными массами.
Указанный способ буферного осаждения для формирования наночастиц, согласно настоящему изобретению, представляет собой новый способ осаждения для синтеза только боратов металлов, полученных путем усовершенствования некоторых частей обычного способа осаждения, ранее известного в литературе. Наиболее важной особенностью данного способа является способность буфера гидроксид натрия/борная кислота, используемого в качестве источника бората, поддерживать значение pH среды в диапазоне от 9 до 9,5 на протяжении всей реакции. Данный способ синтеза может быть использован не только для получения бората свинца, но и для получения всех других (+2) и (+3) заряженных боратов металлов. Металлы других боратных соединений металлов, которые могут быть синтезированы с использованием данного способа синтеза, следующие: Ca+2, Mn+2, Ni+2, Co+2, Cu+2, Zn+2, Sr+2, Ba+2, Sc+3, Fe+3, Cr+3, Al+3, Y+3, La+3, Ce+3, Pr+3, Nd+3, Sm+3, Eu+3, Gd+3, Tb+3, Dy+3, Ho+3, Er+3, Tm+3, Yb+3, Lu+3, Bi+3, Tl+3. Приведенные здесь примеры являются примерами других примеров боратов металлов, которые могут быть получены данным способом синтеза.
ЭКСПЕРИМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ
Эксперимент для определения цитотоксичности
Влияние полученных наночастиц на жизнеспособность клеток определяли с использованием способа MTS (системы тестирования материалов), приведенного в литературе. Молекулы, использованные в продукте, получали по отдельности или в комбинации в среде и наносили на клетки T47D (рак молочной железы), MCF7 (рак груди), A549 (рак легких) и Hacat (здоровый контрольный кератиноцит), которые высевали на клеточные планшеты для культивирования с 96 лунками путем подсчета при концентрации 4000 клеток на каждую лунку. Ответ клеток на токсичность молекул определяли путем измерения жизнеспособности клеток в течение 3 дней. Жизнеспособность клеток определялась с помощью способа под названием MTS, который измеряет активность фермента митохондриальной дегидрогеназы в клетке. Вещество MTS, добавленное к клеткам вместе со средой, приводит к образованию окрашенных кристаллов формазана как индикатора жизнеспособности клеток. Конечное изменение цвета оценивали на основании измерения оптической плотности с использованием планшет-ридера для ELISA. Полученные результаты проанализированы.
Полимеразная цепная реакция в реальном масштабе времени
Анализ полимеразной цепной реакции в масштабе реального времени проводится для наблюдения за изменениями уровней генов в клетках, обработанных наночастицами. Эти изменения происходят как на морфологическом уровне, так и на уровне экспрессии генов. Использованные праймеры были разработаны с использованием программного обеспечения Primer BLAST (Национальный центр биотехнологии=NCBI). Совокупный объем РНК выделяли из клеток, на которые наносили комбинацию гелей, и синтезировали кДНК. Синтезированные кДНК смешивали с праймерами в продукте смеси Fermentas Maxima SYBR Green так, чтобы конечный объем составлял 20 мкл, а уровни экспрессии генов анализировали с использованием устройства BIO-RAD.
ЦИТИРУЕМАЯ ЛИТЕРАТУРА
[1]. Hanahan, D. and R. A. Weinberg (2000). "The hallmarks of cancer." Cell100(1): 57-70.
[2]. Hanahan, D. and R. A. Weinberg (2011). "Hallmarks of cancer: the next generation." Cell144(5): 646-674.
[3]. Garcia Calavia, P., I. Chambrier, M. J. Cook, A. H. Haines, R. A. Field and D. A. Russell (2018). "Targeted photodynamic therapy of breast cancer cells using lactose-phthalocyanine functionalized gold nanoparticles." J Colloid Interface Sci512: 249-259.
[4]. Hekmat, A., A. A. Saboury and A. Divsalar (2012). "The effects of silver nanoparticles and doxorubicin combination on DNA structure and its antiproliferative effect against T47D and MCF7 cell lines." J Biomed Nanotechnol8(6): 968-982.
[5]. Fang, J., H. Nakamura and H. Maeda (2011). "The EPR effect: Unique features of tumor blood vessels for drug delivery, factors involved, and limitations and augmentation of the effect." Adv Drug Deliv Rev63(3): 136-151.
Реферат
Настоящее изобретение относится к способу синтеза наноразмерных соединений бората свинца. Способ включает стадии: растворения и смешивания гидроксида натрия и борной кислоты друг с другом в дистиллированной воде с получением боратного буферного раствора NaOH/H3BO3, растворения нитрата свинца в дистиллированной воде в отдельном стакане при перемешивании, смешивания раствора нитрата свинца с боратным буферным раствором, промывания полученного продукта дистиллированной водой с последующей сушкой для удаления примесей. Предложенный способ является более простым, экономичным и подходящим для изготовления по сравнению с методами синтеза гидротермальным/сольвотермическим и микроволновым осаждением благодаря тому, что его можно проводить без какой-либо необходимости в высокой температуре, длительном времени реакции, высоком давлении и любого вида облучения. 8 з.п. ф-лы, 5 ил.
Формула
Документы, цитированные в отчёте о поиске
Наночастицы гетерокристаллического минерала для применения в качестве лекарственного средства

Комментарии