Содержащий кремний, биологически разлагаемый материал для противовоспалительной терапии - RU2571504C2
Код документа: RU2571504C2
Чертежи










Описание
Настоящее изобретение касается содержащего кремний, биологически разлагаемого материала для профилактики и/или лечения заболеваний, которые сопровождаются повышенной активностью интерлейкина-1β, и/или интерлейкина-6, и/или интерлейкина-8, или которые можно лечить понижением таких или такой активности цитокинов.
Кремний является микроэлементом, который в связанной силикатной форме необходим для людей. Кремний является компонентом тех белков, которые отвечают за прочность и эластичность ткани. К тому же, он также присутствует в соединительной ткани, костях, коже, волосах, ногтях и кровеносных сосудах. Кроме того, кремний укрепляет защитную систему организма, так называемую иммунную систему, и способствует заживлению ран. Недостаток кремния влечет за собой нарушение роста, ломкость костей с повышенным риском образования остеопороза, а также преждевременное выпадение волос, ломкие ногти и изменения кожи. Возможными изменениями кожи являются повышенное образование морщин, сухость, шелушение, повышенное ороговение, зуд, уплотнения и растущие болезненные трещины на коже из-за пониженной эластичности. Кроме того, защитная система организма, так называемая иммунная система, ослабевает из-за недостатка кремния, и возникает повышенная восприимчивость к инфекциям.
US 2006/0178268 A1 описывает водный раствор, состоящий из неколлоидной кремниевой и борной кислоты, для лечения заболеваний костей, хрящей, кожи, артерий, соединительных тканей, суставов, волос, ногтей, кожи, а также остеопороза, ревматических заболеваний, артериосклероза, артрита, сердечно-сосудистых, аллергических и дегенеративных заболеваний.
US 2006/0099276 A1 раскрывает способ получения производного кремниевой кислоты при помощи гидролиза кремнийорганического соединения до олигомеров при одновременном присутствии четвертичного аммониевого соединения, аминокислоты или источника аминокислоты или их комбинаций. Содержащий кремниевую кислоту экструдат можно применять в качестве лекарства для лечения инфекций, заболеваний ногтей, волос, кожи, зубов, коллагеновых заболеваний, диффузных болезней соединительной ткани, для лечения остеопатии, остеопении, для образования клеток при дегенеративных процессах (старения).
US 6,335,457 B1 раскрывает твердое вещество, в котором кремниевая кислота образует комплекс с полипептидом. Также этот патент раскрывает применяемые при лечении смеси, содержащие указанное твердое вещество.
WO 2009/018356 A1 касается смеси, содержащей соединение фосфата натрия, аммониевое соединение и соль кремниевой кислоты для профилактики или лечения заболеваний, таких как рак предстательной железы, колоректальный рак, рак легких, рак молочной железы, рак печени, нейрональные опухоли, рак костей, ВИЧ, ревматический артрит, рассеянный склероз, вирус Эпштейна-Барр, фибромиалгия, синдром хронической усталости, диабет, синдром Бехчета, синдром раздраженного кишечника, болезнь Крона, пролежни, трофические язвы, ослабленная лучевой или химиотерапией иммунная система, гематомы или их комбинации.
WO 2009/052090 A2 описывает способ лечения воспалительных, аутоиммунных заболеваний, бактериальных или вирусных инфекций и рака путем применения композиции, содержащей соли кремниевой кислоты.
US 2003/0018011 A1 касается фармацевтической композиции с жирной кислотой и водорастворимым силикат-полимером в качестве противоаллергического или противовоспалительного вещества.
US 5,534,509 касается фармацевтической композиции, содержащей водорастворимый силикат-полимер в качестве активного вещества с сахаридом или сахарным спиртом в качестве инертного наполнителя для лечения аллергии, воспалений, боли, или для улучшения периферической циркуляции крови или парестезии.
DE 19609551 C1 описывает получение биологически рассасывающихся филаментных волокон на основе сложного этилового эфира полигидрокси-кремниевой кислоты. Волокна используют в качестве армирующих волокон для биологически разлагающихся и/или биологически рассасывающихся (имплантатов) материалов. Также волокна можно применять для изготовления биологически разлагающихся нетканых материалов.
WO 01/42428 A1 описывает способ изготовления кожного имплантата, причем клетки кожи наносят на поверхность питательного раствора и наращивают с помощью элементов поверхности, состоящих из волокон, описанных в DE 19609551 C1.
ЕР 1262542 A2 касается способа получения клеток, тканей и органов in-vitro, причем в качестве опорного клеточного вещества и/или проводящей структуры согласно DE 19609551 C1 применяют волокнистую матрицу.
WO 2006/069567 A2 касается многослойного соединения, в котором в слое также используют волокнистую матрицу согласно DE 19609551 C1. Многослойное соединение можно использовать для лечения таких ран, как хронические диабетические нейропатические язвы, язвы голени, пролежни, вторично инфицированные раны, первично инфицированные раны, как, в частности, рваные раны или ссадины после абляции.
Кроме этого WO 2008/086970 A1, WO 2008148384 A1, РСТ/ЕР 2008/010412 и РСТ/ЕР 2009/004806 описывают получение другого применяемого согласно изобретению соединения сложного этилового эфира полигидрокси-кремниевой кислоты. В общем, соединения описывают для применения в качестве биологически рассасывающихся материалов в медицине, медицинской промышленности, технологии фильтрования, биотехнологии или производстве изоляционных материалов. Также упомянуто, что материалы можно предпочтительно использовать при лечении и заживлении ран. Волокна, например, можно использовать в качестве хирургического материала для наложения швов или армирующих волокон. Нетканый материал можно использовать на поверхностных ранах, при фильтрации биологической жидкости (например, крови) или в области биореакторов в качестве веществ, способствующих выращиванию.
В уровне техники не указано, что можно использовать вышеназванные биологически разлагаемые соединения сложного этилового эфира полигидрокси-кремниевой кислоты (например, в форме волокна или нетканого материала) для профилактики и/или лечения заболеваний, которые сопровождаются повышенной активностью интерлейкина-1β, и/или интерлейкина-6, и/или интерлейкина-8, или которые можно лечить понижением такой или таких активностей цитокина. Хотя в вышеуказанных документах описано использование соединений сложного этилового эфира полигидрокси-кремниевой кислоты для лечения и заживления ран, и известно, что заживление ран связано с противовоспалительными процессами, однако уровень техники не указывает, что можно использовать вышеназванные биологически разлагаемые соединения сложного этилового эфира полигидрокси-кремниевой кислоты, главным образом, в профилактических и/или терапевтических целях, в частности, для воспалительных и/или аутоиммунологических заболеваний.
Поэтому предметом настоящего изобретения является содержащий кремний, биологически разлагаемый материал для профилактики и/или лечения заболеваний, которые сопровождаются повышенной активностью интерлейкина-1β, и/или интерлейкина-6, и/или интерлейкина-8, или заболеваний, в которых снижение активности интерлейкина-1β, и/или интерлейкина-6, и/или интерлейкина-8 является необходимым для процесса заживления, причем содержащий кремний, биологически разлагаемый материал является соединением сложного этилового эфира полигидрокси-кремниевой кислоты, при условии, что исключают такие раны, как хронические диабетические нейропатические язвы, язвы голени, пролежни, инфицированные раны, заживающие вторичным натяжением, чистые раны, заживающие первичным натяжением, как, в частности, рваные раны или ссадины после абляции. Изобретение также охватывает применение содержащего кремний, биологически разлагаемого соединения сложного этилового эфира полигидрокси-кремниевой кислоты для получения лекарств для профилактики и/или лечения заболеваний, которые сопровождаются повышенной активностью интерлейкина-1β, и/или интерлейкина-6, и/или интерлейкина 8, и/или заболеваний в которых снижение активности интерлейкина-1β, и/или интерлейкина-6, и/или интерлейкина-8 является необходимым для процесса заживления, при условии, что исключают такие раны, как хронические диабетические нейропатические язвы, язвы голени, пролежни, вторично инфицированные раны, первично инфицированные раны, как в частности, рваные раны или ссадины после абляции.
В изобретение не включены те способы применения материала согласно изобретению, которые описаны в следующих патентных описаниях DE 19609551 C1, WO 01/42428 A1, ЕР 1262542 A2, WO 2006/069567 A2, WO 2008/086970 A1, WO 2008148384 A1, РСТ/ЕР 2008/010412 и РСТ/ЕР 2009/004806, и которые связаны с настоящим изобретением. Применение нетканого волокна из сложного этилового эфира полигидрокси-кремниевой кислоты в качестве составной части многослойного соединения для лечения таких ран, как хронические диабетические нейропатические язвы, язвы голени, пролежни, вторично инфицированные раны, первично инфицированные раны, как в частности, рваные раны или ссадины после абляции, описано в WO 2006/069567 A2. ЕР 1262542A2 описывает самые различные применения технологии культивирования тканей соединения сложного этилового эфира полигидрокси-кремниевой кислоты согласно изобретению. Понятие "применения технологии культивирования тканей" согласно настоящему изобретению ориентируется на продукты, способы и применение, описанные в ЕР 1262542 A2. Поэтому из изобретения исключены применения технологии культивирования тканей из содержащего кремний, биологически разлагаемого материала, обсуждаемые в ЕР 1262542 A2, при условии, что они должны быть связаны с предметом настоящего изобретения.
Понятие "соединение сложного этилового эфира полигидрокси-кремниевой кислоты" описывает все соединения общей формулы H[OSi8O12(OH)x(OC2H5)6-x]nOH согласно изобретению, где x означает 2-5 и n>1 (полимер).
Содержащий кремний, биологически разлагаемый материал, являющийся предметом изобретения, существует предпочтительно как материал в виде волокна, волокнистой матрицы, порошка, монолита и/или покрытия. Такой содержащий кремний, биологически разлагаемый материал может быть получен согласно изобретению нижеописанными способами:
a) по меньшей мере, одной реакции гидролиз-конденсации тетраэтоксисилана,
b) выпаривания для получения однофазного раствора предпочтительно при одновременном бережном перемешивании реакционной системы,
c) охлаждения однофазного раствора и
d) созревания для получения материала на основе кремниевого золя,
e) вытягивания волокон материала на основе кремниевого золя для образования волокна или волокнистой матрицы и/или высушивания, в частности, распылительной сушки или лиофилизирования материала на основе кремниевого золя для образования порошка и при необходимости растворения порошка в растворителе для образования жидкой препаративной формы и/или нанесения слоя из материала на основе кремниевого золя на предмет, подлежащий нанесению на него содержащего кремний биологически разлагаемого вещества, и/или литья материала на основе кремниевого золя в форму для образования монолита.
Согласно изобретению содержащий кремний, биологически разлагаемый материал предпочтительно находится в виде волокна, волокнистой матрицы (нетканого материала), порошка, жидкой препаративной формы и/или наносимого слоя.
В другом предпочтительном варианте осуществления изобретения содержащий кремний, биологически разлагаемый материал получают описанным выше способом, причем тетраэтоксисилан на этапе a) при первоначальном значении pH 0-≤7, при необходимости в присутствии водорастворимого растворителя, предпочтительно этанола, при температуре 0-80°C подвергают кислотному катализу, и на этапе b) проводят выпаривание до получения однородного раствора с вязкостью в диапазоне 0,5-2 Па·с при скорости сдвига 10 с-1 при 4°C.
В другом варианте осуществления изобретения содержащий кремний, биологически разлагаемый материал получают описанным выше способом, причем кислотный катализ на этапе а) проводят с азотнокислой H2O в молярном соотношении к кремниевому соединению в диапазоне 1:1,7-1:1,9, предпочтительно в диапазоне 1:1,7-1:1,8. Реакцию гидролиз-конденсации на этапе а) осуществляют преимущественно при температурах 20-60°С, предпочтительно 20-50°С в течение, по меньшей мере, 1 часа. Предпочтительно реакция гидролиз-конденсации на этапе а) происходит в течение нескольких часов, как, например, 8 или 16 часов. Эту реакцию также можно проводить в течение 4 недель. Этап (b) в предпочтительном варианте осуществления изобретения проводят в закрытом оборудовании, в котором может происходить перемешивание (предпочтительно в ротационном выпарном аппарате или емкости с мешалкой) при одновременном удалении растворителя (вода, этанол) с помощью выпаривания при давлении 1-1013 мбар, предпочтительно при давлении <600 мбар, выборочно при непрерывной подаче химически инертного газа-носителя для снижения парциального давления выпариваемых компонентов до 1-8 м3/ч (предпочтительно при 2,5-4,5 м3/ч), температуре реакции 30°C-90°C, предпочтительно 60-75°C, в частности, предпочтительно 60-70°C и преимущественно при бережном перемешивании реакционной системы при 80 об/мин (предпочтительно при 20-80 об/мин) до вязкости смеси 0,5-30 Па·с при скорости сдвига 10 с-1 при 4°С, предпочтительно 0,5-2 Па·с при скорости сдвига 10 с-1 при 4°С, в частности, предпочтительно около 1 Па·с (измерение при 4°С, скорости сдвига 10 с-1). В другом варианте осуществления изобретения содержащий кремний, биологически разлагаемый материал на этапе с) охлаждают предпочтительно до 2-4°С. При этих низких температурах также предпочтительно проводят созревание (этап d). Для созревания может потребоваться несколько часов или дней, до 3-4 недель. Процесс созревания на этапе d) проводят предпочтительно до вязкости золя 30-100 Па·с при скорости сдвига 10 с-1 при 4°C и коэффициенте потерь 2-5 (при 4°С, 10 л/с, 1% деформации).
Вытягивание волокон материала на основе кремниевого золя на этапе е) предпочтительно проводят в процессе формования. Такой этап процесса формования может происходить в обычных условиях, как, например, описано в DE 19609551 C1 и DE 102004063599 A1.
Высушивание материала на основе кремниевого золя для образования порошка предпочтительно проводят при распылительной сушке или лиофизировании. Порошок также может быть получен при измельчении монолита или также волокон согласно изобретению и перемалывании. Для образования жидкой препаративной формы порошок растворяют в растворителе. Подходящие растворители в зависимости от применения (например, раствор для инъекций или суспензии) могут быть жидкими или маслянистыми.
Нанесение покрытия из содержащего кремний, биологически разлагаемого материала на предмет, покрываемый материалом на основе кремниевого золя, предпочтительно осуществляют при погружении покрываемого предмета в кремниевый золь, при обливании или нанесении покрытия центробежным методом или распылении кремниевого золя.
Материал на основе кремниевого золя можно также согласно этапу d) - для образования монолита - наливать в форму и затем высушивать.
Другие конкретизирующие данные относительно получения содержащего кремний, биологически разлагаемого материала, являющегося предметом изобретения, заимствованы из DE 19609551 C1, WO 01/42428 A1, ЕР 1262542 A2, WO 2006/069567 A2, WO 2008/086970 A1, WO 2008148384 A1, РСТ/ЕР 2008/010412 и РСТ/ЕР 2009/004806.
В смысле настоящего изобретения выражение "биологически разлагаемый" означает, что свойство согласно изобретению соединения сложного этилового эфира полигидрокси-кремниевой кислоты должно снижаться, если материал подвергают условиям, которые существуют, например, при регенерации ткани (например, раны). "Биологически разлагаемым" или "биоразлагаемым" в смысле изобретения соединение сложного этилового эфира полигидрокси-кремниевой кислоты является особенно в том случае, если оно полностью растворяется через 48 часов, предпочтительно 36 часов и, в частности, предпочтительно через 24 часа в 0,05 М трис pH 7,4 буферного раствора (Fluka 93371), подвергаясь термостатированию при 37°C.
Цитокины и хемокины регулируют воспаление и реакции на инфекции, ранения и рак. В то время как некоторые цитокины усиливают реакции на чужеродный, как, например, гомологичный материал, другие цитокины снижают воспаления и таким образом способствуют выздоровлению. Экспрессию и получение почти всех провоспалительных цитокинов контролируют в рамках воспалительных реакций с помощью сигнальных путей, которые регулируются транскрипционным фактором NFκB. Таким образом, NFκB является центральной регулирующей молекулой также в индукции интерлейкина-1β, интерлейкина-6 и интерлейкина-8. Интерлейкин-1β, интерлейкин-6 и интерлейкин-8 являются усиливающими или инициирующими воспалительные процессы цитокинами, которые сопровождаются лихорадкой, воспалениями, разрушением ткани и в некоторых случаях шок и смерть. Поэтому снижение биологической активности IL-1β, и/или IL-6, и/или IL-8 является целью различных терапевтических мероприятий и успешно используется для множества воспалительных заболеваниях.
Понятие "заболевания, которые сопровождаются повышенной активностью интерлейкина-1β, и/или интерлейкина-6, и/или интерлейкина-8 и/или заболевания, в которых снижение активности интерлейкина-1β, и/или интерлейкина-6, и/или интерлейкина-8 способствует процессу заживления" предпочтительно описывает заболевания, включающие:
аутоимунные заболевания, аллергии, энтерит, колит, гастрит, артрит, миокардит, дерматит, отит, пневмонит, шоковое легкое, нарушения свертывания крови, воспалительные заболевания костей и суставов, ревматоидный артрит, сепсис, септический шок, последствия трансплантации, острые и хронические воспалительные процессы, воспалительные кишечные заболевания (Bowel disease), реакция "трансплантат против хозяина", шок, апоплексический удар, острый респираторный дистресс-синдром (ОРДС), псориаз, рестеноз, СПИД, кахексия, черепно-мозговая травма, аллергия, паразитарная инфекция, аллергический ринит, аллергическая астма, рассеянный склероз, системная красная волчанка, отторжение трансплантата, астма и хроническое абструктивное заболевание легких, хронический гастрит, острые и хронические воспаления кожи, псориаз, аллергия кожи, паразитарная инфекция кожи, атопический дерматит, в частности, нейродермит, дерматомиозит, обыкновенная пузырчатка и/или другие локальные и системные инфекции и/или острые и хронические воспалительные процессы.
К аутоиммунным заболеваниям в частности, относят следующие: Круговидное облысение, антифосфолипидный синдром, боковой амиотрофический склероз, синдром MEDAC (аутоиммунный полиэндокринный синдром), болезнь Хортона, атеросклероз, аутоиммунная энтеропатия, CREST-синдром, болезнь Крона, дерматомиозит, герпетиформный дерматит Дюринга, сахарный диабет 1 типа, приобретенный буллезный эпидермолиз, фибромиалгия, хронический аутоиммунный гастрит, синдром Гудпасчера, синдром Гийена-Барре, тиреоидит Хасимото, PANDAS, гипертиреоз, идиопатическая тромбопеническая пурпура, заболевание соединительной ткани, хронический ревматоидный артрит, коронарные сердечные заболевания, краниомандибулярная дисфункция, криоглобулинемия, криоагглютининовая болезнь, лишай склеротический, линеарный IgA дерматоз, лаймский артрит, системная красная волчанка, синдром Шарпа, болезнь Аддисона, Базедова болезнь, миастения, нарколепсия, обыкновенная пузырчатка, злокачественная анемия (болезнь Аддисона-Бирмера), болезнь Верльгофа, миастения, полимиозит, первичный билиарный цирроз печени, ревматическая полимиалгия, ревматоидный артрит, синдром Шегрена, склеродермия, синдром мышечной скованности, симпатическая офтальмия, гигантоклеточный артрит, язвенный колит, васкулит, гранулематоз Вегенера, болезнь Бехтерева, аутоиммунный гепатит, буллезный пемфигоид, себорейная пузырчатка, полиангиит, полиневропатия, синдром Рейтера, ревматическая лихорадка, синдром Чарг-Страуса, синусит, саркоидоз, синдром Такаясу, токсоплазмоз, гломерулонефрит, зоб Хасимото, болезнь Бехчета, рецидивирующий полихондрит, полихондрит, системная хондромаляция, аутоиммунный полиэндокринный синдром, геморрагический васкулит (Purpura anaphylactoides, Vasculitis allergica), витилиго, целиакия, аутоиммунные нефриты и васкулиты и/или аутоиммунные анемии.
Заболеваниями, которые можно предпочтительно лечить с помощью соединения согласно изобретению, являются острые и хронические воспаления кожи, псориаз, аллергии кожи, паразитарные инфекции кожи, атопический дерматит, в частности, нейродермит, дерматомиозит и/или обыкновенная пузырчатка.
Подходящая дозировка применяемого согласно изобретению соединения сложного этилового эфира полигидрокси-кремниевой кислоты составляет, в общем, 0,001-100 мг/кг массы тела в день и отпускается в одно- или многократной дозировке. Предпочтительно дозировка составляет 0,01-25 мг/кг, более предпочтительно 0,1-5 мг/кг в день. Способность к биологическому расщеплению соединений сложного этилового эфира полигидрокси-кремниевой кислоты также способствует тому, что соединения можно применять в более высокой дозировке и, например, они могут разлагаться в организме, например, храниться подкожно в течение длительного времени.
Материал согласно изобретению или его предшественник (как, например, вышеописанный на этапе d) содержащий кремниевый золь материал) можно обрабатывать используемыми в галеновых средствах носителями, наполнителями, веществами, влияющими на распад, связующими веществами, веществами, придающими скользкость, абсорбентами, разбавляющими средствами, веществами, улучшающими вкус, красителями и т.д., и преобразовывать в желаемую форму применения. При этом ссылаются на Remington's Pharmaceutical Science, 15-oe изд. Mack Publishing Company, East Pennsylvania (1980).
Материал согласно изобретению можно выпускать в подходящей форме для орального, мукозального (как, например, сублингвального, буккального, ректального, назального или вагинального), парентерального (как, например, подкожного, внутримышечного применения, с помощью болюсных инъекций, внутриартериального, внутривенного), трансдермального или локального применения (как, например, прямое нанесение на кожу или в виде местных аппликаций на незащищенный орган или рану).
Для орального применения, в частности, принимают во внимание таблетки, драже, таблетки в целлофановой упаковке, капсулы, пилюли, порошки, гранулят, пастилки, суспензии, эмульсии или растворы.
Таблетки, драже, капсулы и т.д. можно получить, например, как описано выше, при литье полученного на этапе d) содержащего кремниевый золь материала в таблетированной или капсульной форме для образования монолита. Таблетки и капсулы также могут быть получены согласно изобретению из вышеописанного материала в виде порошка обычными способами. Материал согласно изобретению или его предшественник можно смешивать с известными вспомогательными веществами, например, инертными разбавителями, как декстроза, сахар, сорбит, маннит, поливинилпирролидон, взрывчатое вещество, как кукурузный крахмал или альгиновые кислоты, связующие вещества, как крахмал или желатин, связывающие вещества, как стеарат магния или тальк и/или средствами, улучшающими хранение, как, например, карбоксилполиметилен, карбоксиметилцеллюлоза, ацетатфталат целлюлозы или поливинилацетат. Таблетки также могут состоять из нескольких слоев. Материалы, содержащиеся в капсулах согласно изобретению, могут, например, быть получены при смешивании материалов согласно изобретению или их предшественника с инертным носителем, как молочный сахар или сорбит, полученное вещество помещают в желатиновые капсулы. Соответственно драже можно изготовить при нанесении на ядро, аналогично таблеткам, используемые материалы, например, поливинилпирролидон или шеллак, гуммиарабик, тальк, окись титана или сахар. При этом оболочка драже также может состоять из нескольких слоев, причем можно использовать вышеназванные в таблетках вспомогательные вещества.
Для парентерального применения возможно применение растворов для вливания и инъекций. Для внутрисуставных инъекций соответственно можно применять приготовленные суспензии кристаллов. Для внутримышечных инъекций можно применять жидкие препаративные формы, как водные и маслянистые растворы для инъекций или суспензии и соответственные дюрантные препараты. Для ректального применения можно использовать вещество согласно изобретению, находящееся в суппозиториях, капсулах, растворах (например, клизмы) и мази, а также для системной, а также для локальной терапии. Далее в качестве препарата также должны быть названы средства для вагинального применения. Жидкие препаративные формы, как растворы для инъекций или суспензии, например, могут быть получены при смешивании вышеописанного вещества в виде порошка с подходящим водным или масляным растворителем. Другие способы получения известны специалисту. Растворы или суспензии, содержащие вещество согласно изобретению, могут дополнительно содержать средства для улучшения вкуса, как сахарин, цикламат или сахар, а также, например, ароматизаторы, как ванилин или экстракт апельсина. Кроме того они могут содержать суспендирующие вспомогательные вещества, как натрий-карбоксиметилцеллюлоза или консерванты, как p-гидроксибензоат. Подходящие суппозитории могут быть получены, например, при смешивании с предусмотренными для этого носителями, как нейтральные жиры или полиэтиленгликоль или их производные.
Для трансдермального применения существуют пластыри или смеси для местного нанесения в виде гелей, мазей, жирных мазей, крема, паст, пудры, молочка и настойки. Пластыри для раны предпочтительно состоят из волокон или волокнистой матрицы (нетканый материал) из веществ согласно изобретению, как описано в уровне техники.
В другом варианте осуществления изобретения на вещества согласно изобретению или на их предшественники можно наносить покрытие, например, при погружении предмета, на который необходимо нанести покрытие, или корпуса, в вещество, содержащее кремниевый золь, описанное на этапе d), при обливании или нанесении покрытий центробежным методом или опрыскиванием таким веществом, содержащим кремниевый золь. Например, можно наносить покрытие из вещества, содержащего кремниевый золь, на пластырь или бинты.
Вышеназванные наносимые формы могут также содержать другие фармацевтические биологически активные вещества, которые можно дополнительно добавлять во время процесса изготовления.
Примеры
1. Получение согласно изобретению матричного волокна из сложного этилового эфира полигидрокси-кремниевой кислоты
В качестве эдукта для реакции гидролизной конденсации помещают 1124,98 г ТЭОС (тетраэтоксисилана) в емкость с мешалкой. Добавляют 313,60 г EtOH в качестве растворителя. Смесь перемешивают. Отделенную смесь разбавляют 1 н HNO3 (55,62 г) с H2O (120,76 г) и добавляют смесь ТЭОС-этанола. Смесь перемешивают в течение 18 часов.
Затем смесь, полученную на этом этапе, выпаривали при температурах от 62°С под воздействием вынужденного потока и перемешивании (60 об/мин) до динамической вязкости (скорость сдвига 10 с-1 при 4°С) от 1 Па·с.
Затем раствор созревал в закрытом пропиленовом сосуде для созревания в неподвижном состоянии и вертикальном положении при температуре 4°С до динамической вязкости примерно 55 Па·с (скорость сдвига 10 с-1 при 4°С) и коэффициенте потерь 3,0.
Изготовление волокон осуществляли на обычном прядильном устройстве. С этой целью прядильную массу загружали в охлажденный до -15°С напорный цилиндр, в который нагнетали воздух под давлением 20 бар. Под действием давления происходило выдавливание золя через фильеры и формирование нитей. В зависимости от диаметра фильер нити обладали диаметром от 5 до 100 мкм.
Затем золь, полученный при созревании, подвергают прядению. Изготовление волокон осуществляли на обычном прядильном устройстве. С этой целью прядильную массу загружали в охлажденный до -15°С напорный цилиндр. Прядильный раствор выдавливали под давлением через насадку. Выходящие формуемые нити в зависимости от локальной температуры и вязкости прядильного раствора обнаруживают диаметр примерно 50 мкм. Текучий, похожий на мед материал под воздействием собственного веса падает в прядильную шахту, находящуюся ниже напорного цилиндра длиной 2 м. В прядильной шахте установлена контролируемая температура и влажность. Температура составила 25°С, влажность воздуха 19%. При попадании волокон на специальный стол они почти сохранили цилиндрическую форму, однако были настолько текучими, что прилипли друг другу при соприкосновении в месте расположения волокон (нетканое полотно).
2. Основной и индуцированный синтез интерлейкина-1β кератиноцитов
Для определения полученного в примере 1 матричного волокна из сложного этилового эфира полигидрокси-кремниевой кислоты (на рисунках показаны с сокращ. PKSEE) основного синтеза интерлейкина-1β кератиноцитов применяли 6-валовые пластинки с культурой с 200.000 кератиноцитов и 3 мл среды роста в каждом вале. Пластинки с культурой были снабжены подходящим устройством для синтетического материала. Во время испытания соединения сложного этилового эфира полигидрокси-кремниевой кислоты соответственно 1 см2 матричного волокна сложного этилового эфира полигидрокси-кремниевой кислоты поместили в вертикальное положение и покрыли слоем из 1 мл среды. Во время проверки в устройство для вертикального хранения добавили 1 мл среды. Содержимое устройства для вертикального хранения синтетического материала отделяли с помощью мембраны среды культуры клеток. Однако, по причине проницаемости мембраны, возможен массообмен растворимыми веществами между содержимым устройства для вертикального хранения и питательной клеточной средой. Пластинки с культурой культивировали 2-4 дня. Затем определили абсолютное и относительное количество интерлейкина-1β в жидкой фракции культуры клеток с помощью теста ELISA [человеческий ИЛ-1 бета ELISA комплект системы R&D]. Фигура 1a показывает характерное сильное сокращение основного синтеза интерлейкина-1β после 72 часов культивации [t-критерий Стьюдента].
Следующий опыт проводили аналогичным образом с единственным отличием: кератиноциты были активированы за 24 часа до начала с помощью добавления ИЛ-β [500 ед./мл]. Затем в культурах с помощью многократного промывания удалили внешне добавленный ИЛ-1β и культуры культивировали следующие 24 часов в нормальной среде роста. Фигура 1b в сравнении с необработанными культурами показывает характерное сильное сокращение [t-критерий Стьюдента] индуцированного синтеза интерлейкина 1β культуры кератиноцитов, обрабатываемой веществом согласно изобретению.
3. Основной и индуцированный синтез интерлейкина-6 кератиноцитов. эндотелиальных клеток и фибробластов
Такие опыты, как описанные в примере 2, проводили с тем отличием, что вместо интерлейкина-1β определяли абсолютное и относительное количество интерлейкина-6 в жидкой фракции культуры клеток с помощью теста ELISA [человеческий ИЛ-6 ELISA комплект системы R&D]. Фигура 2a показывает характерное сильное сокращение [t-критерий Стьюдента] основного синтеза интерлейкина-6 кератиноцитов после 72 часов культивации.
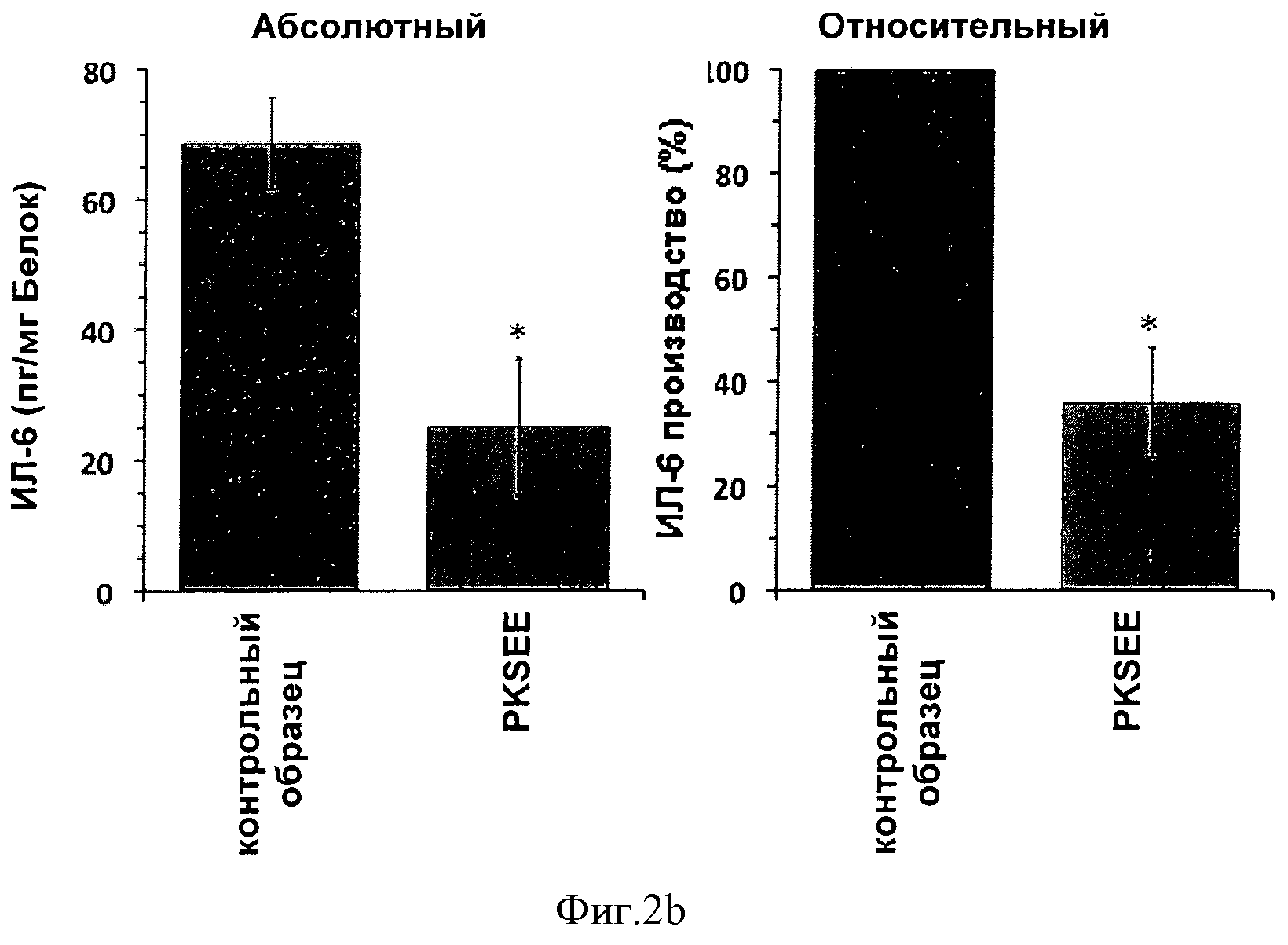
Следующий опыт проводили аналогичным образом с единственным отличием, что кератиноциты были активированы за 24 часа до начала с помощью добавления ИЛ-1β [500 ед./мл]. Затем в культурах с помощью многократного промывания удалили внешне добавленный ИЛ-1β и культуры культивировали следующие 24 часов в нормальной среде роста. Фигура 2b в сравнении с необработанными культурами показывает характерное сильное сокращение [t-критерий Стьюдента] индуцированного с помощью ИЛ-1β синтеза интерлейкина-6 культурой кератиноцитов, обрабатываемой веществом согласно изобретению.
Такие опыты проводили для эндотелиальных клеток и фибробластов вместо кератиноцитов. Фигура 3a показывает характерное сильное сокращение [t-критерий Стьюдента] основного синтеза интерлейкина-6 эндотелиальных клеток после 72 часов. Фигура 3b показывает характерное сильное сокращение [t-критерий Стьюдента] индуцированного ИЛ-1β синтеза интерлейкина-6 эндотелиальных клеток после 72 часов. Фигура 4a показывает характерное сильное сокращение [t-критерий Стьюдента] основного синтеза интерлейкина-6 фибробластов после 72 часов. Фигура 4b не показывает характерного сокращения IL-1β [t-критерий Стьюдента] синтеза интерлейкина-6 фибробластов.
4. Основной и индуцированный синтез интерлейкина-8 кератиноцитов, эндотелиальных клеток и фибробластов
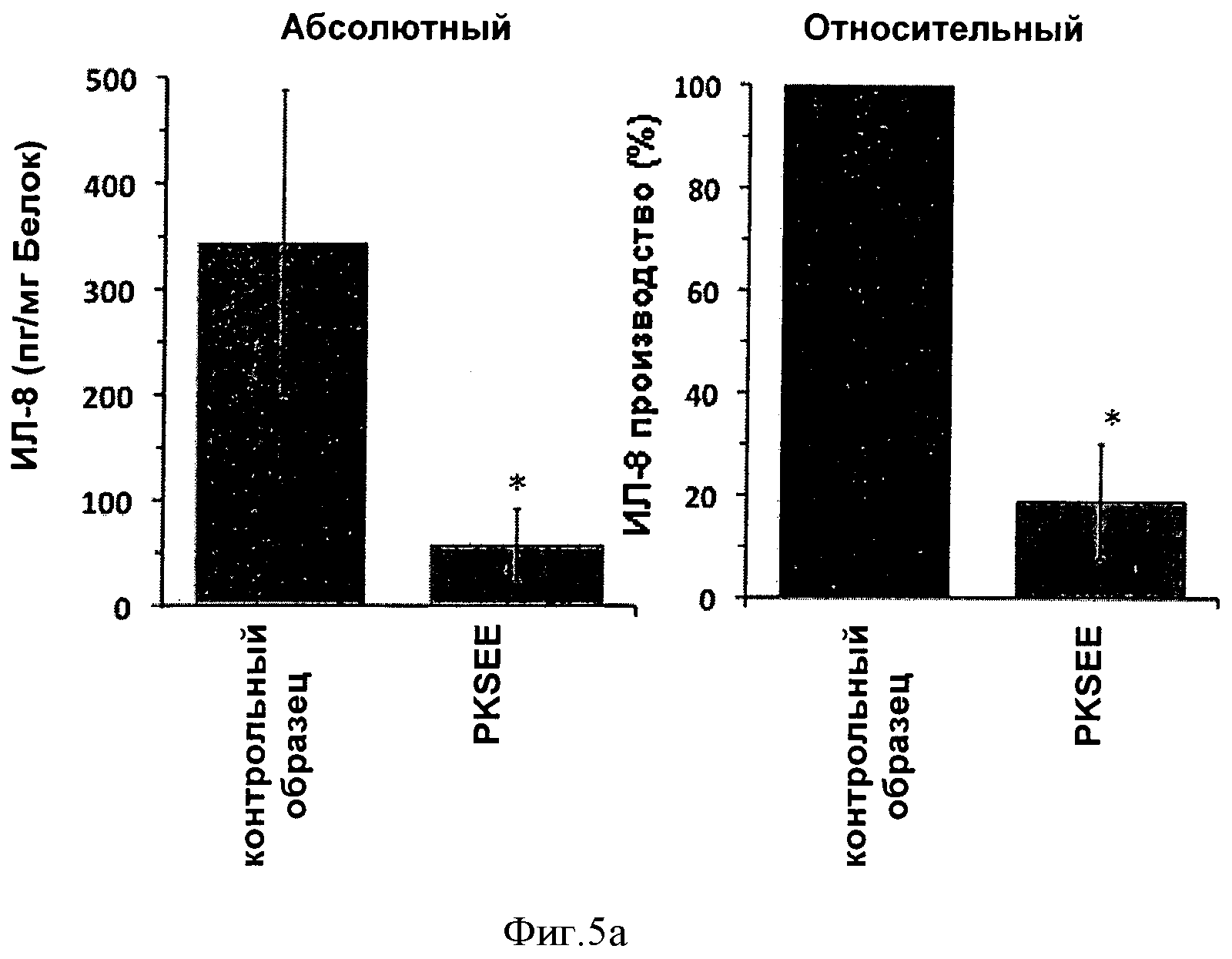
Такие опыты, как описанные в примере 2, проводили с тем отличием, что вместо интерлейкина-1β определяли абсолютное и относительное количество интерлейкина-8 в жидкой фракции культур клеток с помощью теста ELISA [человеческий ИЛ-8 ELISA комплект системы R&D]. Фигура 5α показывает характерное сильное сокращение [t-критерий Стьюдента] основного синтеза интерлейкина-8 кератиноцитов после 72 часов.
Следующий опыт проводили аналогичным образом с единственным отличием, что кератиноциты были активированы за 24 часа до начала с помощью добавления ИЛ-β [500 ед./мл]. Затем в культурах с помощью многократного промывания удалили внешне добавленный ИЛ-1β и культуры культивировали следующие 24 часов в нормальной среде роста. Фигура 5b в сравнении с необработанными культурами показывает характерное сильное сокращение [t-критерий Стьюдента] индуцированного с помощью ИЛ-1β синтеза интерлейкина-8 культурой кератиноцитов, обрабатываемой веществом согласно изобретению.
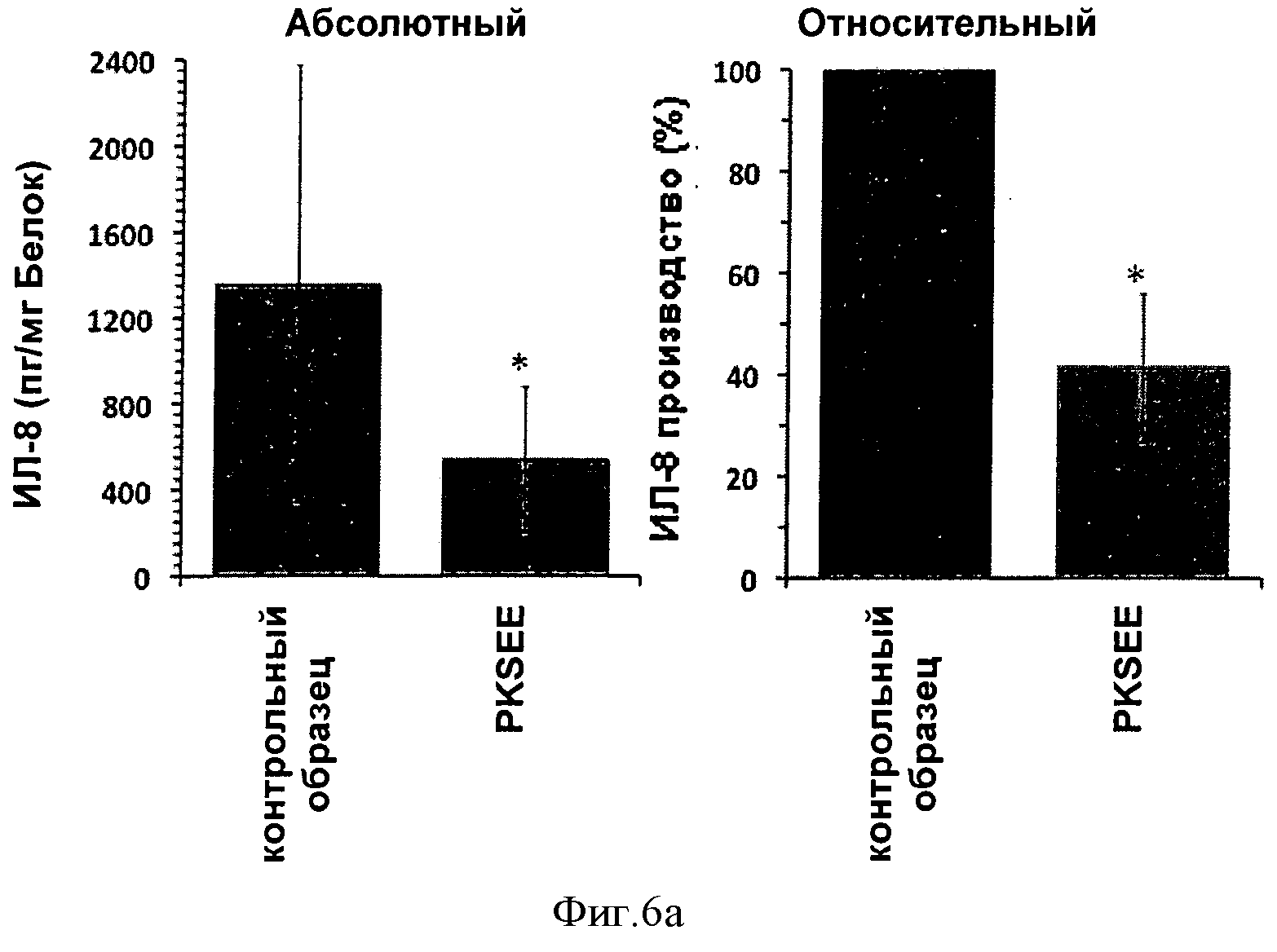
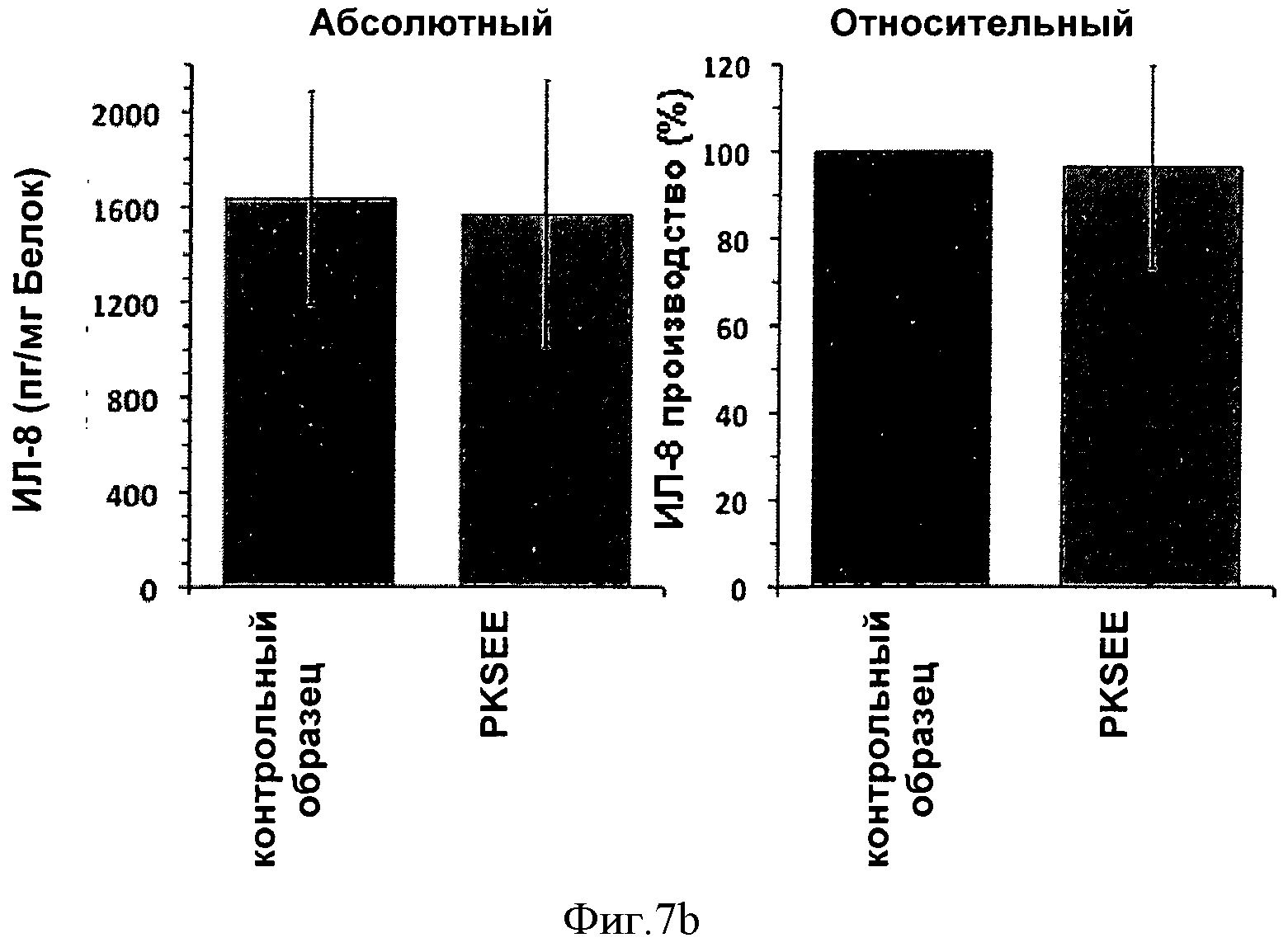
Такие опыты проводили с эндотелиальными клетками и фибробластами вместо кератиноцитов. Фигура 6a показывает характерное сильное сокращение основного синтеза интерлейкина-8 эндотелиальных клеток после 72 часов культивирования. Фигура 6b показывает характерное сокращение [t-критерий Стьюдента] индуцированного синтеза интерлейкина-8 эндотелиальных клеток после 72 часов. Фигура 7a показывает характерное сильное сокращение [t-критерий Стьюдента] основного синтеза интерлейкина-8 фибробластов после 72 часов. Фигура 7b не показывает характерного сокращения индуцированного синтеза интерлейкина-8 фибробластов.
Фигуры 1a, 2a, 3a, 4a, 5a, 6a и 7a: *; p<0.05 по сравнению с контрольным образцом; n=9; фигуры 1b, 2b, 3b, 4b, 5b, 6b и 7b: *; p<0.05 по сравнению с контрольным образцом; n=12; анализ статистических данных осуществляют с помощью t-критерия Стьюдента.
Реферат
Изобретение относится к медицине. Описан содержащий кремний, биологически разлагаемый материал для профилактики и/или лечения заболеваний, которые сопровождаются повышенной активностью интерлейкина-1β, и/или интерлейкина-6, и/или интерлейкина-8, или которые можно лечить понижением таких или такой активности цитокинов. Содержащий кремний, биологически разлагаемый материал применяют в более высокой дозировке, и он может разлагаться в организме, например, храниться подкожно в течение длительного времени. 5 з.п. ф-лы, 7 ил., 4 пр.
Формула
причем содержащий кремний, биологически разлагаемый материал является соединением сложного этилового эфира полигидрокси-кремниевой кислоты общей формулы H[OSi8O12(OH)x(OC2H5)6-x]nOH, где х означает 2-5 и n>1,
причем материал находится в виде волокна, волокнистой матрицы, порошка, жидкой препаративной формы, монолита и/или наносимого слоя, и является полученным посредством:
a) по меньшей мере, одной реакции гидролиз-конденсации тетраэтоксисилана,
b) выпаривания для получения однофазного раствора,
c) охлаждения однофазного раствора,
d) созревания, которое проводят до образования материала на основе кремниевого золя, и
e) получения материала на основе кремниевого золя, путем вытягивания волокон для образования материала в виде волокна или волокнистой матрицы,
или
высушивания материала на основе кремниевого золя для образования порошка,
или
высушивания материала на основе кремниевого золя для образования порошка и растворения порошка в растворителе для образования жидкой препаративной формы,
или
нанесения слоя из материала на основе кремниевого золя на предмет, подлежащий нанесению на него содержащего кремний биологически разлагаемого материала
или
литья материала на основе кремниевого золя в форму для образования монолита,
причем тетраэтоксисилан подвергают кислотному катализу на этапе а) при первоначальном значении pH от 0-≤7 при температуре 0-80°C, и на этапе b) выпаривание проводят до получения однофазного раствора с вязкостью в диапазоне 0,5-2 Па·с при скорости сдвига 10 с-1 при 4°C,
причем кислотный катализ на этапе а) проводят с водным раствором азотной кислоты в молярном соотношении к кремниевому соединению в диапазоне 1:1,7-1:1,9,
а заболевания выбраны из группы:
аутоиммунных заболеваний, аллергий, энтерита, колита, гастрита, артрита, миокардита, дерматита, отита, пневмонита, шокового легкого, нарушений свертывания крови, воспалительных заболеваний костей и суставов, ревматоидного артрита, сепсиса, септического шока, последствий трансплантации, острых и хронических воспалительных процессов, воспалительных кишечных заболеваний (Bowel disease), реакции "трансплантат против хозяина", шока, апоплексического удара, острого респираторного дистресс-синдрома (ОРДС), псориаза, рестеноза, СПИД, кахексии, черепно-мозговой травмы, аллергии, паразитарной инфекции, аллергического ринита, аллергической астмы, атопического дерматита, рассеянного склероза, системной красной волчанки, отторжения трансплантата, астмы и хронического абструктивного заболевания легких, хронического гастрита, острых и хронических воспалений кожи, аллергии кожи, паразитарной инфекции кожи и/или других локальных и системных инфекции и/или острых и хронических воспалительных процессов.
выпаривание для получения однофазного раствора на этапе b) осуществляют при одновременном бережном перемешивании реакционной системы, и/или
на этапе е) осуществляют высушивание путем распылительной сушки или лиофилизирования материала на основе кремниевого золя для образования порошка.
острых и хронических воспалений кожи, псориаза, аллергии кожи, паразитарных инфекций кожи, атопического дерматита, в частности нейродермита, дерматомиозита и/или обыкновенной пузырчатки.

Комментарии