Самоподдерживающая биоразлагаемая пленка на основе гидрофобизованной гиалуроновой кислоты, способ ее получения и применение - RU2712174C2
Код документа: RU2712174C2
Чертежи



Описание
Область техники, к которой относится настоящее изобретение
Настоящее изобретение относится к самоподдерживающейся биоразлагаемой пленке на основе гидрофобизованной гиалуроновой кислоты, к способу ее получения и к ее применению, особенно в медицинских целях, благодаря ее контролированным растворимости, биоразлагаемости, морфологии поверхности, механическим и другим свойствам.
Предшествующий уровень техники настоящего изобретения
Гиалуроновая кислота или ее соль (НА) представляет собой линейный полисахарид, который состоит из повторяющихся дисахаридных звеньев, образованных из глюкуроновой кислоты, которая связана β-1,3-гликозидной связью с N-ацетил-глюкозамином.
Она представляет собой вещество, которое встречается в организме, где является частью внеклеточного матрикса, действует в качестве смазки в суставах, глазах и т.п. Она также взаимодействует с клеточными рецепторами, благодаря чему способна регулировать клетки. Свойства НА предопределяют ее применение в различных медицинских целях (Necas, Bartosikova et al. 2008). Поскольку НА очень быстро растворяется в водной среде или в жидкостях организма, ее необходимо модифицировать для ряда применений. Существуют многочисленные типы модификаций, например, получение растворимой формы НА, дериватизированной тирамином, которая при добавлении сшивающих средств образует нерастворимую гидрогелевую сеть (Calabro, Darr et al. 2004, Wolfova, Pravda et al. 2013). Растворимость цепи НА также может быть снижена путем связывания ее гидрофобных групп (Valle and Romeo 1987, Smejkalova, Huerta-Angeles et al. 2014,


Такое производное затем становится нерастворимым в водных средах и растворяется в основном в смеси воды и органического растворителя (в зависимости от степени замещения гидрофобной цепью в сочетании с молекулярной массой).
Международная заявка на выдачу патента № WO 2014082609 (Smejkalova, Huerta-Angeles et al. 2014) относится к получению гидрофобизованной гиалуроновой кислоты в качестве носителя биологически активных гидрофобных веществ. Гидрофобизацию гиалуронана выполняют с помощью реакции эстерификации гиалуронана с длинноцепочечной карбоновой кислотой, при этом активацию выполняют посредством 2,4,6-трихлорбензойной кислоты (ТСВА) или другого органического хлорида.
Одной из представляющих интерес форм применения гидрофобизованного гиалуронана является получение тонких пленок для наружного или внутреннего применения. Известны пленки, которые применимы в медицинских целях, например, Seprafilm использовали для предупреждения спаек при повторной лапаротомии. Seprafilm представляет собой прозрачный противоспаечный барьер, состоящий из двух анионных полисахаридов, НА и карбоксиметилцеллюлозы, которые сшиваются вместе 1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлоридом (EDC) (Altuntas, Kement et al. 2008, Beck 2008).
На экспериментальной основе были получены несколько пленок, содержащих НА, см., например, Luo, Kirker et al. (2000). Также в некоторых патентных документах раскрывается получение пленки, сделанной из нерастворимого или сшитого гиалуронана, необязательно гиалуронана в смеси с другим полимером (Becker, Dayton et al. 1996, Beck 2008). Слой гиалуронана также использовали в патентном документе № CN 202822230, в котором, однако, он не представлял собой самоподдерживающуюся пленку, и, кроме того, упоминался только нативный гиалуронан. В статье был описан нативный гиалуронан вместе с лецитином, который добавляли для усиления гидрофобности (Bialopiotrowicz,

Пленки в соответствии с заявкой на выдачу патента № US 20100092545 получают из растворимых или нерастворимых в воде полимеров, предпочтительно из полиэтиленоксида, его предполагаемое применение является альтернативой пероральных лекарственных форм. По этой причине очень важным является однородное распределение лекарственного средства (вариация между образцами до 10%) и то, что при получении не происходит агрегация и перераспределение лекарственного средства. Это достигается, прежде всего, тем, что добавляется полимер с высокой вязкостью (которая может быть дополнительно повышена путем добавления других веществ, таких как альгинат, каррагенан, гуаровая камедь и другие), а также могут быть добавлены стабилизаторы, которые предотвращают агрегацию и перемещение лекарственного средства. Более того, часть растворителя должна быть удалена в течение первых 10 минут, так что из полимерного раствора образуется вязкоупругая пленка, в которой, по мнению авторов, не могут происходить перемещение или агрегация. Это достигается применением высокой температуры, которая, однако, в случае гиалуронана и его производных не может быть использована, поскольку это приведет к разложению пленки. В патентном документе № US 20100092545 авторы не обсуждают полученный в результате внешний вид пленки, на который влияет прилипание пленки к подложке во время сушки и после сушки. Шероховатость поверхности пленки не определяется и не подвергается влиянию. Свойства пленки, которые могут быть модулированы таким образом, такие как набухающая способность и скорость разложения, не раскрываются в документе. Что касается предполагаемого применения, авторы предпочитают, чтобы пленки растворялись в водной среде.
В патентном документе № JP 06025306 раскрывается синтез высокозамещенных ацилированных гиалуронановых производных и их применение для получения волокон и пленок. Синтез предусматривает получение суспензии полисахарида в органической кислоте. Поскольку это суспензия, полисахарид полностью не растворяется в системе, что тем самым вызывает неоднородные реакции и потерю совместимости полисахарида в системе. Авторы утверждают, что реакция катализируется суперкислотой, в данном случае суперэлектрофильным ангидридом трифторуксусной кислоты, что активно реагирует с водой. Поэтому, существует высокий риск в случае промышленных процессов. Остатки трифторуксусной кислоты, которая образуется при гидролизе ангидрида при контакте с влагой воздуха, могут присутствовать в продуктах и представлять серьезную опасность при использовании производных в биомедицинских целях (Maeda N. et al., 2014). Более того, используют хлорированные растворители в синтезе производных, но FDA не рекомендует их применение в медицинских устройствах из-за высокого риска переноса их остатков в волокна и пленки. В патентном документе упоминается получение волокон и пленок только в общих чертах, и не приводится определение их свойств.
Согласно другой заявке на выдачу патента США № US 20120088832 раскрывается получение пористой пленки на основе гиалуронана и альгината, при этом пленка подлежит применению в медицине, особенно в качестве противоспаечного препарата. Пленка представляет собой сшитую взаимопроникающую сеть пористого характера. В примерах указанного документа не упоминается набухание, биоразложение, растворимость пленки, и не предусматривается определение остаточных растворителей.
Для получения пленок в патентном документе № ЕР 0216453 используют гидрофобизованный гиалуронан с эстерифицированными карбоксильными группами глюкуроновой кислоты, которые, таким образом, были блокированы и стали недоступными для связывания на рецепторе CD44. Для эстерификации использовали низкомолекулярные или ароматические спирты. Способ получения самоподдерживающейся пленки предусматривает растворение сложного эфира НА в диметилсульфоксиде (DMSO), нанесение его на стекло после растворения, погружение стекла в этанол, который экстрагирует DMSO (пленка не растворяется в этаноле) и последующее отделение пленки от стеклянной подложки, промывание этанолом, водой и снова этанолом. Полученную в результате пленку сушат в течение 48 часов при 30°С в компрессионном устройстве.
В патентном документе № US 20040192643 также упоминаются пленки, сделанные из гидрофобизованного гиалуронана, предпочтительно бензоильного производного НА. Как и в предыдущем случае, выполняют замещение по карбоксилу, при этом с целью достижения нерастворимости гиалуронана блокируют от 80 до 100% всех карбоксильных групп в НА. Способ получения пленки соответствует уже упомянутому способу, раскрытому в вышеупомянутом патентном документе № ЕР 216453. Однако сушка осуществляется при 63°С в течение 30 минут в вакууме.
При экстракции DMSO в другом растворителе могут образовываться неконтролируемые дефекты поверхности, что может быть неприемлемо при некоторых применениях. Более того, в случае необходимости применения экстракционного растворителя низкая концентрация остаточных растворителей в конечном продукте не может быть гарантирована. Кроме того, нет упоминаний о механических, физических или биологических свойствах пленок в вышеупомянутых документах №№ ЕР 0216453 и US 20040192643.
В патентном документе № WO 2010137374 раскрывается самоподдерживающаяся полимерная проницаемая мембрана, содержащая блок-сополимер, в котором компоненты гидрофильного полимера и гидрофобного полимера ковалентно связаны, при этом компонент гидрофильного полимера образует перпендикулярно ориентированные цилиндрические структуры, а компонент гидрофобного полимера является сшиваемым. Поэтому, мембрана состоит из ковалентно сшитого блок-сополимера. Гиалуроновая кислота не упоминается. Что касается способа получения указанной мембраны, необходимо наличие так называемого «жертвенного слоя», который присутствует на подложке. Раствор блок-полимера наносят на «жертвенный слой», на котором после испарения растворителя компонент гидрофобного полимера в блок-сополимере фотосшивается, а затем «жертвенный слой» должен быть удален из полученной в результате мембраны посредством растворения, предпочтительно в растворителе, в котором сама мембрана является нерастворимой.
Как упоминалось выше, недостатки известных в настоящее время пленок на основе гиалуроновой кислоты включают в себя, в частности, их сложное многостадийное получение. Другие известные способы получения пленки не могут быть использованы для гиалуронана и его производных. Авторы некоторых патентов или заявок на выдачу патентов не упоминают никакой возможности влияния на растворимость, набухание и биоразлагаемость пленки, что желательно при применении в медицинских устройствах. Внешний вид пленки и ее механические свойства могут зависеть от повторяющегося контакта с растворителем в случае способа в соответствии с патентным документом № ЕР 0216453 или US 20040192643 (этанол, с помощью которого экстрагируется DMSO, является осаждающим средством для гиалуронана). Кроме того, используют, например, DMSO, который не может быть удален в пределах приемлемого срока посредством сушки. Другим недостатком является применение большого количества растворителей, что приводит к большей вероятности наличия остаточных растворителей в продукте. В некоторых способах помимо гиалуронана также используют другие полимеры для усиления нерастворимости конечного материала или для влияния на свойства исходного полимерного раствора.
Краткое раскрытие настоящего изобретения
Вышеупомянутые недостатки уровня техники преодолеваются самоподдерживающейся пленкой на основе сложного эфира гиалуроновой кислоты в соответствии с настоящим изобретением, объектом которого является то, что она содержит С10-С22-ацилированное производное гиалуроновой кислоты в соответствии с общей формулой (I)

в которой R представляет собой Н+ или Na+, и в которой R1 представляет собой Н или -С(=O)СхНу, при этом х представляет собой целое число в диапазоне от 9 до 21, а у представляет собой целое число в диапазоне от 11 до 43, предпочтительно от 19 до 43, и CxHy представляет собой линейную или разветвленную, насыщенную или ненасыщенную цепь С9-С21, в которой по меньшей мере в одном повторяющемся звене один или несколько R1представляют собой -С(=O)СхНу, и в которой п находится в диапазоне от 12 до 4000, предпочтительно от 250 до 4000, более предпочтительно от 250 до 2500, наиболее предпочтительно от 250 до 1000. Предпочтительно пленка в соответствии с настоящим изобретением содержит пальмитоилгиалуронан, поскольку пальмитиновая кислота разлагается в организме посредством β-окисления жирных кислот. Более того, пленка в соответствии с настоящим изобретением предпочтительно содержит лауроилгиалуронан. Пленка в соответствии с настоящим изобретением содержит С10-С22-ацилированное производное гиалуронана (т.е. гидрофобизованный гиалуронан), в котором одна или несколько связей в С10-С22-ацилах могут быть ненасыщенными, и в котором С10-С22-ацил предпочтительно связан только по первичному спирту в положении 6 N-ацетилглюкозамина. Поэтому, карбоксильные группы не являются модифицированными, их удерживание является необходимым для взаимодействий гиалуронана с рецептором CD44, который участвует во взаимодействии, прилипании и миграции клеток и который также участвует во взаимодействии клетки с гиалуронаном. Было доказано, что чем выше степень замещения гиалуронанового карбоксила, тем хуже процесс взаимодействия клеток с гиалуронаном (Qiu, Li et al. 2014). С этой точки зрения целесообразно не проводить модификацию карбоксила и фокусироваться на других реакционных участках, которые являются группами
первичных и/или вторичных спиртов, особенно там, где требуется более высокие степени замещения, что необходимо при большинстве применений.
Пленка в соответствии с настоящим изобретением, полученная из С10-С22-ацилированного производного гиалуроновой кислоты в соответствии с вышеупомянутой формулой I, не является цитотоксической в отношении клеток, является биосовместимой и биоразлагаемой, даже в случае применения высокозамещенного производного (включая 100% степень замещения ацилом). Для применений в медицине, при которых имеются предпосылки воздействия на пленку механического напряжения (противоспаечные барьеры, тканевая инженерия и т.д.), более предпочтительно использовать форму, которая нерастворима в водных средах, т.е. пленку в соответствии с настоящим изобретением, вместо ковалентно сшитой формы, которая зачастую становится хрупкой при набухании. Пленка в соответствии с настоящим изобретением при гидратации образует устойчивую эластичную мембрану, которая может быть подвергнута механическому напряжению определенной степени (посредством удлинения, изгиба, сжатия).
Пленки не являются цитотоксическими в отношении клеток (in vitro тестирование).
Согласно предпочтительному варианту осуществления настоящего изобретения пленка содержит ацилированные производные гиалуроновой кислоты с молекулярной массой от 1×105 до 1×106 г/моль, предпочтительно от 1×105 до 5×105 г/моль, более предпочтительно от 2×105 до 3×105 г/моль.
Согласно другому предпочтительному варианту осуществления настоящего изобретения пленка содержит ацилированные производные гиалуроновой кислоты со степенью замещения в диапазоне от 15 до 160%, предпочтительно от 50 до 100%, более предпочтительно от 80 до 100%.
Степень замещения 100% означает, что каждая группа первичного спирта (-С6) гиалуронанового димера замещается одной алифатической цепью. Степень замещения выше 100% означает, что помимо каждой группы первичного спирта (-С6) в димере также произвольно замещены некоторые группы вторичного спирта (-С4 в N-ацетилглюкозамине или -С2 или -С3 в глюкуроновой кислоте).
Неожиданно обнаружили, что пленка в соответствии с настоящим изобретением является биоразлагаемой даже в случае применения производного с высокой степенью замещения, которая составляет от 80 до 100% и доходит даже до 160%.
Согласно другому предпочтительному варианту осуществления настоящего изобретения пленка имеет толщину в диапазоне от 2 до 100 мкм, предпочтительно в диапазоне от 5 до 25 мкм, и модуль Юнга в диапазоне от 1 до 5000 МПа в сухом состоянии, предпочтительно в диапазоне от 500 до 5000 МПа, более предпочтительно от 1000 до 3000 МПа.
В случае сухих негидратированных пленок в соответствии с настоящим изобретением модуль Юнга не зависит от степени замещения, заместителя и молекулярной массы НА. В гидратированном состоянии очень сложно количественно определить модуль Юнга по техническим причинам, однако, с помощью визуальных тестов можно оценить, что при уменьшении молекулярной массы прочность пленки уменьшается, пленка становится более хрупкой. Кроме того, с увеличением степени замещения модуль Юнга в гидратированном состоянии повышается.
Согласно другому предпочтительному варианту осуществления настоящего изобретения RMS (среднеквадратическое значение) шероховатости поверхности по меньшей мере одной из поверхностей пленки находится в диапазоне от 0,5 до 100 нм, предпочтительно в диапазоне от 0,5 до 2 нм.
Согласно другому предпочтительному варианту осуществления настоящего изобретения пленка может содержать биологически активные вещества, которые выбраны из группы, содержащей фармацевтически и косметически активные вещества, предпочтительно витамины, лекарственные средства, предпочтительно цитостатики, стероиды, дополнительные фитоэкстракты, фитокомплексы или фитоактивные вещества и т.п.
Уникальные свойства пленки в соответствии с настоящим изобретением заключаются в том, что 1) пленка состоит только из гидрофобизованного гиалуронана, 2) не используются синтетические полимеры, 3) пленка не содержит какие-либо токсические растворители, 4) возможные остаточные растворители не являются токсическими и ниже пределов для медицинского применения, 5) способность набухания и растворимость пленки может быть контролирована путем модификации степени замещения гиалуронана, 6) скорость разложения пленки может быть контролирована путем модификации степени замещения гиалуронана, 7) пленка не деформируется на поверхности, и ее толщина является однородной, 8) внешний вид поверхности пленки может быть контролирован, 9) механические свойства пленки могут быть контролированы, особенно в ее гидратированной форме, 10) RMS шероховатости по меньшей мере одной из поверхностей пленки может быть ниже 2 нм, 11) толщина пленки может быть контролирована, 12) пленка не прилипает к клеткам, 13) пленка не coдержит так называемую «кожеподобную поверхность». «Кожеподобная поверхность» представляет собой поверхностную корку, из-за которой пленка будет деформироваться, скручиваться, и под которой могут образовываться пузырьки. Она образуется во время сушки полимерного раствора на воздухе, когда часто близко к поверхности появляется слой высококонцентрированного полимера. Этот слой характеризуется существенно отличающимися реологическими свойствами по сравнению к остальной частью пленки. Сушка пленки в соответствии с настоящим изобретением протекает таким образом, что пленка не подвергается окружающим ее воздействиям (ее сушат в замкнутом пространстве), и, следовательно, ее сушат медленнее, и над раствором наблюдается более высокое давление паров растворителя. Такое расположение помогает предотвратить образование поверхностной корки. Неожиданно выяснили, что даже в том случае, если влажность в замкнутом пространстве во время сушки пленки была низкой, поверхностная корка не образуется.
В пленках в соответствии с настоящим изобретением не обнаружили остатков средств гидрофобизации, которые могут образовываться в подложке, на которой получают пленку.
По сравнению с известными из уровня техники процессами способ получения пленки в соответствии с настоящим изобретением является очень простым и заключается в растворении гидрофобизованного гиалуронана (с любой раскрываемой молекулярной массой и с любой раскрываемой степенью замещения) в соответствующем растворителе, нанесении соответствующего количества его на определенную подложку и выпаривании растворителя в устройстве, при этом наблюдается более высокое давление пара растворителя над раствором, подлежащим сушке в замкнутом пространстве. Выпаривание растворителя выполняют либо посредством выпаривания свободного растворителя, либо посредством нагревания нижней поверхности пленки, лежащей на подложке, при нагревании или охлаждении верхней поверхности пленки (сушка в градиенте температуры и в замкнутом пространстве). Следовательно, способ получения пленки в соответствии с настоящим изобретением является очень дешевым и простым. Также важно, что поверхность пленки в соответствии с настоящим изобретением является очень гладкой (RMS до 2 нм) на стороне, соприкасающейся с подложкой (т.е. нижней поверхности пленки). Противоположная сторона пленки (т.е. верхняя поверхность пленки) является более шероховатой в зависимости от условий сушки и от типа производного.
В соответствии с другим аспектом настоящее изобретение, кроме того, относится к способу получения пленки в соответствии с настоящим изобретением, который заключается в том, что получают раствор, содержащий С10-С22-ацилированное производное гиалуроновой кислоты в соответствии с вышеупомянутой общей формулой (I) в смеси воды и C1-С6-спирта, предпочтительно этанола или пропан-2-ола, который перемешивают, затем его наносят на подложку и сушат в замкнутом пространстве, после чего его удаляют с подложки.
Согласно другому предпочтительному варианту осуществления способа в соответствии с настоящим изобретением количество С10-С22-ацилированного производного гиалуроновой кислоты в растворе находится в диапазоне от 0,5 до 3 мас. %, содержание C1-С6-спирта, предпочтительно этанола или пропан-2-ола, находится в диапазоне от 25 до 55 об. %, а содержание воды в растворе находится в диапазоне от 45 до 75 об. %. Полученный раствор имеет относительно низкую вязкость, в результате чего предотвращается образование пузырьков при перемешивании и дозировании раствора.
Согласно другому предпочтительному варианту осуществления способа в соответствии с настоящим изобретением раствор перемешивают в течение 20-72 часов, предпочтительно от 20 до 48 часов.
Согласно другому предпочтительному варианту осуществления способа в соответствии с настоящим изобретением сушку пленки выполняют в замкнутом пространстве при температуре от 20°С до 50°С, предпочтительно от 30°С до 40°С; в течение 3-6 часов, предпочтительно от 4 до 5 часов.
Согласно другому предпочтительному варианту осуществления способа в соответствии с настоящим изобретением сушку пленки выполняют в градиенте температуры, что осуществляют путем нагревания нижней поверхности пленки, лежащей на подложке, до температуры, которая по меньшей мере на 1°С выше температуры, до которой нагревают или охлаждают верхнюю поверхность пленки. Предпочтительно нижнюю поверхность пленки, лежащую на подложке, нагревают до температуры в диапазоне от 20°С до 60°С, а противоположную верхнюю поверхность пленки нагревают или охлаждают до температуры в диапазоне от 10°С до 59°С. Более предпочтительно, нижнюю поверхность пленки, лежащую на подложке, нагревают до температуры 50°С, а противоположную верхнюю поверхность пленки охлаждают до температуры 20°С. При применении градиента температуры пленку сушат в замкнутом пространстве.
Согласно другому предпочтительному варианту осуществления способа в соответствии с настоящим изобретением раствор сушат в градиенте температуры в течение 6-12 часов, предпочтительно 6 часов.
Преимущество получения пленки в соответствии с настоящим изобретением заключается в том, что пленка является нерастворимой в водных средах, и что она образуется только из ацилированного гиалуронана в соответствии с общей формулой I, определенной выше, без необходимости добавления сшивающих средств и без дополнительной обработки. Пленка в соответствии с настоящим изобретением также содержит большое количество сухого вещества, предпочтительно более 85%.
Раствор ацилированного производного гиалуронана, используемый для получения пленок в соответствии с настоящим изобретением, может быть предпочтительно модифицирован различными путями, в растворе могут быть смешаны биологически активные вещества, при этом биологически активные вещества выбирают из группы, содержащей фармацевтически и косметически активные вещества, предпочтительно витамины, лекарственные средства, предпочтительно цитостатики, стероиды, дополнительные фитоэкстракты, фитокомплексы или фитоактивные вещества и т.п.
Согласно другому предпочтительному варианту осуществления способа в соответствии с настоящим изобретением подложка представляет собой полимер, выбранный из группы, содержащей поливиниловый спирт, полипропилен, полиэтилен, полиоксиметилен или полистирол. Более того, подложкой может быть гидрофобизованное стекло. Согласно предпочтительному варианту осуществления используют гидрофобизованное стекло. Контактный угол смачивания поверхности подложки деминерализованной водой находится в диапазоне от 30° до 120°, предпочтительно от 50° до 70°.
Преимущество раскрываемого выше способа в соответствии с настоящим изобретением заключается, помимо его простоты, также в возможности получения пленки с очень гладкой поверхностью со стороны подложки (т.е. с очень гладкой нижней поверхностью пленки) посредством выбора подходящей подложки, которая сама является очень гладкой.
Возможность воздействия на деформацию и общий внешний вид пленки представляется очень полезной, при этом воздействие осуществляют путем влияния на прилипание (взаимодействие) полимерного раствора, сушку и высушенную пленку на подложке, на которую наносят раствор и на которой осуществляется сушка. Предпочтительно, чтобы полимерная пленка полностью прилипала к подложке, не отслаивалась спонтанно, и, в то же время, чтобы пленка могла быть удалена с подложки просто путем приложения минимального усилия.
Хорошее смачивание поверхности подложки полимерным раствором представляет собой первую стадию прилипания. На прилипание при сушке и высушенную пленку в соответствии с настоящим изобретением на подложке и, таким образом, на внешний вид пленки может влиять выбор подложки, характеризующейся различной смачиваемостью поверхности, выраженной посредством угла контакта. Для каждого типа производного (разной модификации, разной молекулярной массы и разной степени замещения) предпочтительно использовать подложку, характеризующуюся совершенно специфическим значением смачиваемости. В случае хорошо прилипших пленок их поверхность является плоской после их отслаивания, в случае менее хорошо прилипших пленок или не прилипших пленок их поверхность является более или менее деформированной или сморщенной. В качестве подложки предпочтительно использовать гидрофобизованное стекло.
Пленку получают путем выпаривания смеси органического растворителя (как правило, C1-С6-спирта) с водой. Поверхность полученной таким образом пленки характеризуется внешним видом и RMS шероховатости, контролируемыми выбором оптимальных растворителей, производного, условий сушки и подложки, и может быть выполнена прозрачной. Толщина пленки составляет от 2 до 100 мкм, предпочтительно от 5 до 25 мкм. Поскольку пленку получают на подложке, смачиваемость которой может быть модулирована, можно влиять на прилипание пленки к подложке и, таким образом, также на морфологию поверхности пленки.
Получение пленки происходит следующим образом: раствор ацилированного производного гиалуронана с относительно низкой вязкостью после достаточного перемешивания наносят на подходящую подложку и сушат. Низкая вязкость раствора, который наносят на подложку, предотвращает образование пузырьков при перемешивании и дозировании раствора. Затем пленку удаляют с подложки. Время сушки варьируется от 5 до 12 часов в зависимости от объема и концентрации раствора, а также от заданных температур и от используемого растворителя. Пленка содержит менее 0,02% растворителя, например, этанола или пропан-2-ола, что обеспечивает безопасное выполнение требований по количеству остаточных растворителей для медицинского применения. Такой материал может быть использован для изготовления медицинского устройства. Преимуществом способа получения такой пленки в соответствии с настоящим изобретением является то, что пленка нерастворима в водных средах и состоит только из модифицированного гиалуронана без необходимости добавления сшивающих средств и дальнейшей обработки.
Пленка в соответствии с настоящим изобретением может быть использована в соответствии с настоящим изобретением, например, для получения противоспаечных барьеров и для других применений медицине человека и ветеринарной медицине. Разложение пленки в организме человека может быть модулировано с помощью молекулярной массы используемого производного и с помощью степени замещения гиалуронана алкилом, и варьирует от нескольких часов до нескольких месяцев. Ацилированные производные гиалуронана, а также получаемые из них пленки являются разлагаемыми in vitro.
Способность набухания пленки или ее растворимость также контролируется с помощью молекулярной массы используемого производного и с помощью степени замещения гиалуронановой цепи С10-С22-алкилом.
Важно, что в отличие от производных, раскрытых в известных из уровня техники патентных документах, пленка в соответствии с настоящим изобретением содержит только С10-С22-ацилированное производное гиалуроновой кислоты, в котором сохраняются все карбоксильные группы глюкуроновой кислоты, которые являются группами, отвечающими за биологические свойства гиалуронана.
Другой аспект настоящего изобретения относится к воздействию на внешний вид поверхности пленки посредством воздействия на прилипание высушенного полимера к подложке, на которой получают пленку. Результатом этого может быть очень плоская пленка без изгибов или складок.
Согласно следующему варианту осуществления пленку в соответствии с настоящим изобретением, определяемую выше, используют в медицинских целях, биотехнологических целях или в качестве носителя для отложения активных компонентов. Предпочтительно, ее используют для создания медицинского устройства, такого как противоспаечные барьеры, поскольку клетки не прилипают к ней. Кроме того, предпочтительные медицинские применения, при которых может быть использована пленка в соответствии с настоящим изобретением, предусматривают, например, медицинские фармацевтические применения, такие как лечение хронических и острых ран, или, например, стоматологические применения.
Определения терминов
Термин «степень замещения» означает число С10-С22-ацилов, связанных со 100 гиалуронановыми димерами. Например, степень замещения 20% означает, что 20 из каждых 100 гиалуронановых димеров замещены С10-С22-ацилами. При замещении атом водорода в первичной гидроксильной группе N-ацетил-глюкозамина или во вторичных ОН-группах глюкуроновой кислоты замещается С10-С22-ацилом.
Термин «пленка» означает самоподдерживающийся тонкий полимерный лист, плоскую структуру.
Термин «площадь пленки» означает площадь пленки, вычисленную по ее размерам (в м2).
Термин «медицинское устройство» означает средство, которое можно использовать самостоятельно или в сочетании с какими-либо аксессуарами для конкретного применения в диагностических или медицинских целях, такое как противоспаечный барьер.
Термин «замкнутое пространство» означает пространство, в котором выполняют сушку пленки при определенной температуре или в градиенте температуры, и которое является закрытым без свободного доступа окружающего воздуха.
Термин «кондиционированная среда» означает кондиционированную среду для ТНР-1 (линии клеток моноцитарной злокачественной опухоли человека), которая является стандартной средой RPMI (средой Roswell Per Memorial Institute), обогащенной 10% фетальной бычьей сыворотки, в которой человеческие клетки линии ТНР-1 культивировали непрерывно в течение 7 суток. Клетки ТНР-1 используют в качестве модели моноцитов человека, и они продуцируют помимо ряда факторов роста и цитокинов также ферменты, вызывающие разложение компонентов внеклеточного матрикса, особенно матричные металлопротеиназы, гиалуронидазы или эстеразы. Перед применением или замораживанием среду центрифугируют и фильтруют через 0,22-мкм фильтр для обеспечения чистоты и стерильности.
Краткое описание графических материалов
На фиг. 1 показан эффект прилипания пленки (а, b) на основе олеильного производного натрия гиалуроната на внешний вид ее поверхности (с).
На фиг. 2 показан эффект прилипания пленки на основе пальмитоильного производного натрия гиалуроната на внешний вид ее поверхности.
На фиг. 3 показано сравнение пленок, полученных согласно примерам 2 (b) и 18 (а), после 3 недель разложения в кондиционированной среде.
На фиг. 4 показано испытание присутствия основанных на НА олигосахаридов в растворе пленки согласно примеру 5 (DS=20%) после инкубации в DMEM (модифицированной по способу Дульбекко среде Игла) с добавлением фермента, с помощью HPLC. На фиг. показаны 3 хроматограммы, соответствующие (i) разделению стандартов олигосахарида НА (стандарта НА2 (tR = 4,1 минуты), НА4 (tR = 12 минут), НА6 (tR = 18,1 минуты), НА8 (tR = 22,9 минуты)), (ii) пустому образцу - DMEM с добавлением фермента, и (iii) раствору, в котором выполняли инкубацию пленки.
На фиг. 5 показана морфология пленки, полученной согласно примеру 16, со стороны подложки.
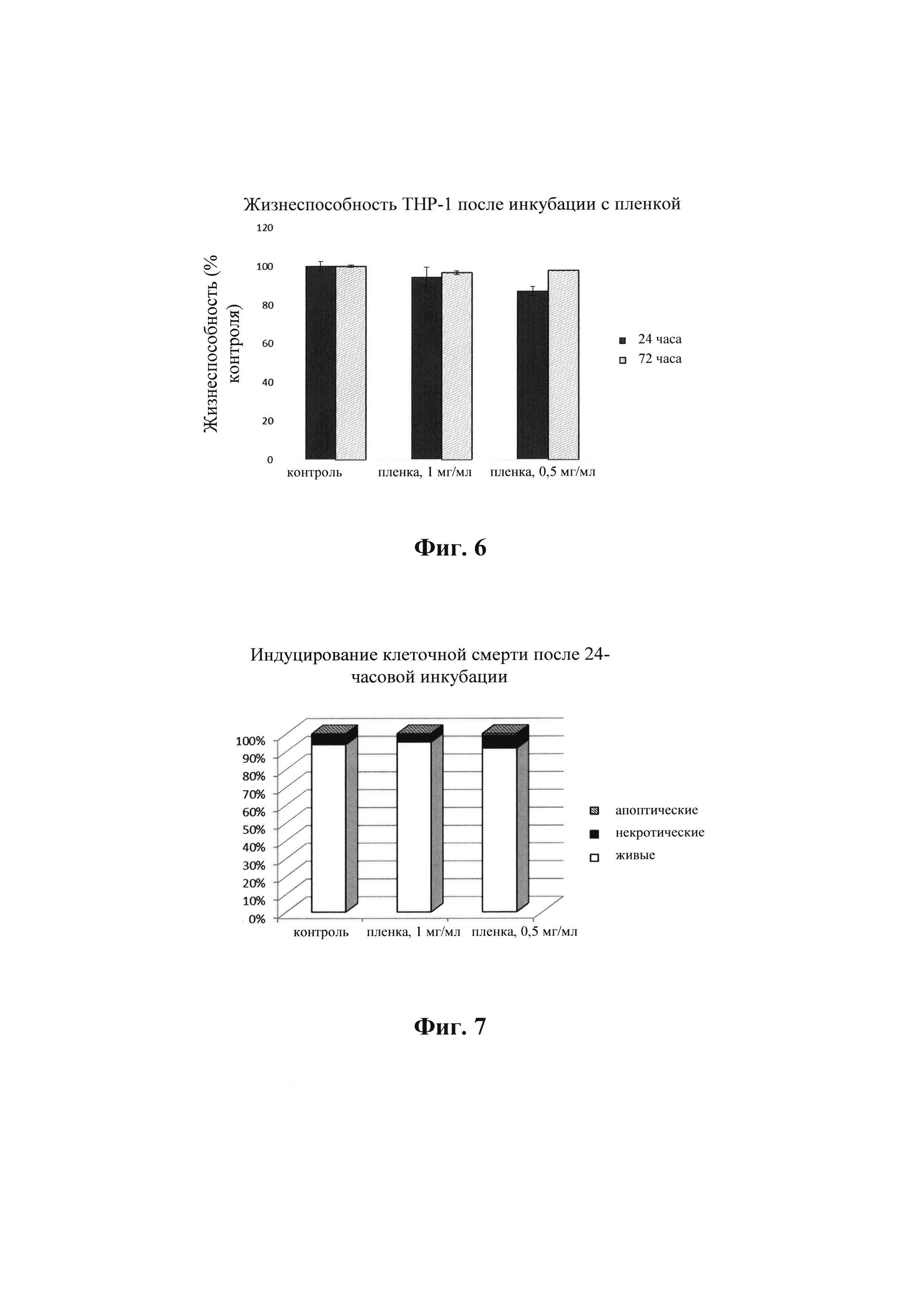
На фиг. 6 показана жизнеспособность суспензии клеток ТНР-1 после 24 и 72 часов инкубации с пленкой полученной согласно примеру 1, на основе пальмитоильного производного натрия гиалуроната.
На фиг. 7 показано индуцирование клеточной смерти после 24 часов инкубации с пленкой, полученной согласно примеру 1, на основе пальмитоильного производного натрия гиалуроната.
На фиг. 8 показано индуцирование клеточной смерти после 72 часов инкубации с пленкой, полученной согласно примеру 1, на основе пальмитоильного производного натрия гиалуроната.
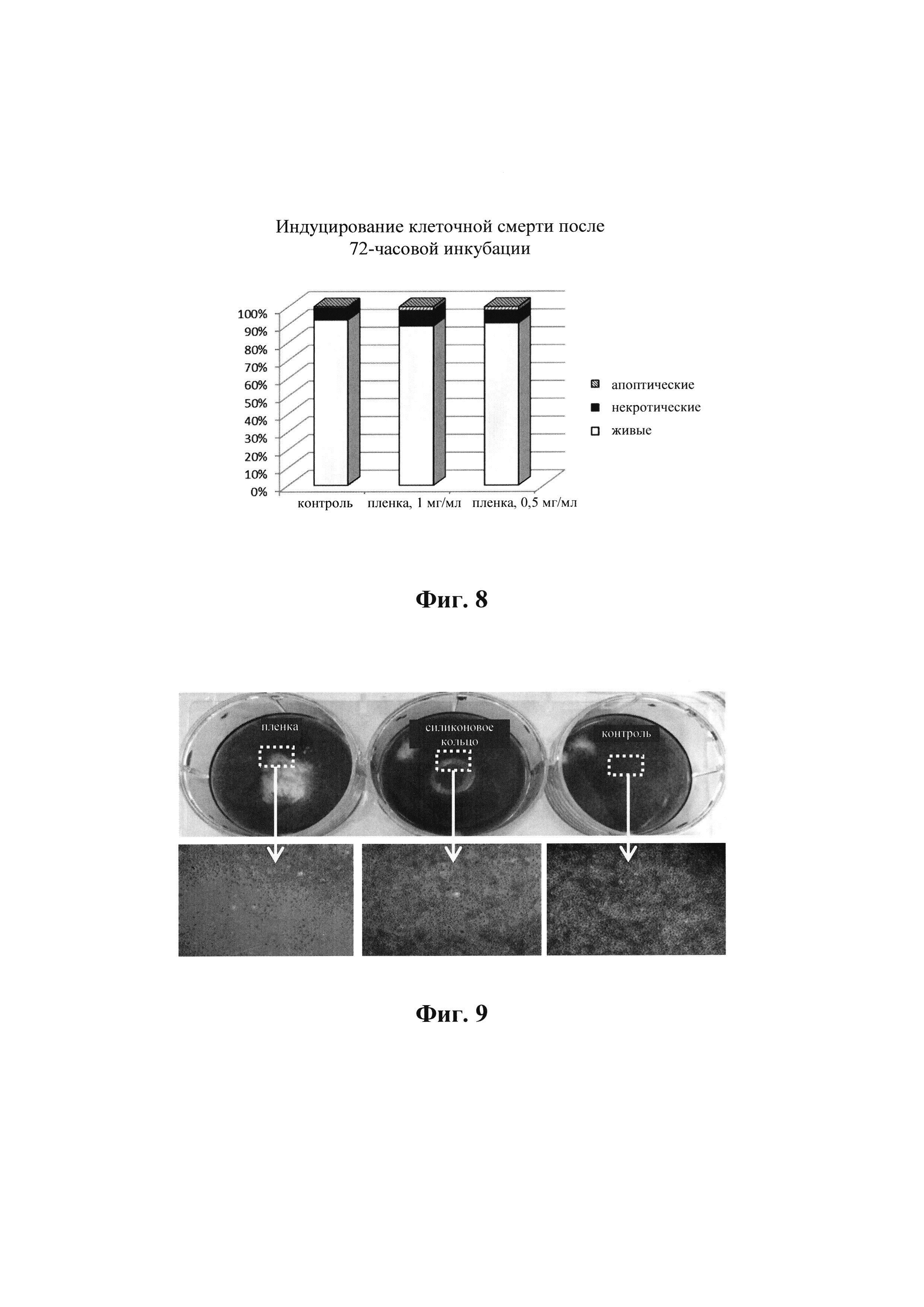
На фиг. 9 показано контактное ингибирование роста фибробластов мыши 3Т3 Swiss, вызываемое пленкой, полученной согласно примеру 1.
На фиг. 10 показаны антиадгезионные свойства пленки в отношении клеток, А - пленка, полученная согласно примеру 17, верхняя поверхность пленки, В - пленка, полученная согласно примеру 17, нижняя поверхность пленки, С - пленка, полученная согласно примеру 2, верхняя поверхность пленки, D - пленка, полученная согласно примеру 2, нижняя поверхность пленки, CTRL - контроль.
Подробное раскрытие настоящего изобретения
Примеры
Пример 1. Получение пленки на основе пальмитоильного производного натрия гиалуроната
100 мг пальмитоильного производного натрия гиалуроната со степенью замещения 100% и молекулярной массой 2,8×105 г/моль растворяли в 20 мл 55% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 72 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 61° (+/- 2° и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 40°С в течение 12 часов. После сушки пленку оценивали, удаляли с гидрофобизованного стекла и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм. Сухое вещество определяли равным приблизительно 92%.
Пример 2. Получение пленки на основе пальмитоильного производного натрия гиалуроната
100 мг пальмитоильного производного натрия гиалуроната со степенью замещения 100% и молекулярной массой 2,12×105 г/моль растворяли в 20 мл 55% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 48 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 61° (+/- 2° и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 6 часов. После сушки пленку оценивали, удаляли с гидрофобизованного стекла и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 3. Получение пленки на основе пальмитоильного производного натрия гиалуроната
100 мг пальмитоильного производного натрия гиалуроната со степенью замещения 55% и молекулярной массой 6,0×105 г/моль растворяли в 20 мл 50% раствора этанола и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на полиэтиленовую подложку со смачиваемостью деминерализованной водой 79° (+/- 4°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 30°С и температуре верхней пластины 29°С в течение 12 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 4. Получение пленки на основе пальмитоильного производного натрия гиалуроната
50 мг пальмитоильного производного натрия гиалуроната со степенью замещения 31% и молекулярной массой 9,9×105 г/моль растворяли в 20 мл 45% раствора этанола и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 61° (+/- 2°) и сушили в замкнутом пространстве путем выпаривания растворителя при температуре 30°С в течение 4 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 8 мкм.
Пример 5. Получение пленки на основе пальмитоильного производного натрия гиалуроната
100 мг пальмитоильного производного натрия гиалуроната со степенью замещения 20% и молекулярной массой 2,4×105 г/моль растворяли в 20 мл 25% раствора этанола и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на полистирольную подложку со смачиваемостью деминерализованной водой 102° (+/- 4°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 12 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 6. Получение пленки на основе эрукоильного производного натрия гиалуроната
100 мг эрукоильного производного натрия гиалуроната со степенью замещения 160% и молекулярной массой 2,04×105 г/моль растворяли в 20 мл 60% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на полипропиленовую подложку со смачиваемостью деминерализованной водой 105° (+/- 2°) и сушили в замкнутом пространстве путем выпаривания растворителя при температуре 50°С в течение 3 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 7. Получение пленки на основе лауроильного производного натрия гиалуроната
100 мг лауроильного производного натрия гиалуроната со степенью замещения 64% и молекулярной массой 3,2×105 г/моль растворяли в 20 мл 50% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 50° (+/- 3°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 6 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 8. Получение пленки на основе лауроильного производного натрия гиалуроната
100 мг лауроильного производного натрия гиалуроната со степенью замещения 90% и молекулярной массой 1,88×105 г/моль растворяли в 20 мл 50% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 61° (+/- 2°) и сушили в замкнутом пространстве путем выпаривания растворителя при температуре 20°С в течение 6 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 9. Получение пленки на основе олеильного производного натрия гиалуроната
100 мг олеильного производного натрия гиалуроната со степенью замещения 20% и молекулярной массой 2,8×105 г/моль растворяли в 20 мл 50% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на поливинилхлоридную подложку со смачиваемостью деминерализованной водой 95° (+/- 5°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 6 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 10. Получение пленки на основе олеильного производного натрия гиалуроната
300 мг олеильного производного натрия гиалуроната со степенью замещения 20% и молекулярной массой 2,8×105 г/моль растворяли в 20 мл 30% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 57° (+/- 3°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 12 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 40 мкм.
Пример 11. Получение пленки на основе олеильного производного натрия гиалуроната
300 мг олеильного производного натрия гиалуроната со степенью замещения 20% и молекулярной массой 2,8×105 г/моль растворяли в 20 мл 30% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 107° (+/- 1°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 12 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 40 мкм.
Пример 12. Получение пленки на основе капринильного (С10) производного натрия гиалуроната
100 мг капринильного (С10) производного натрия гиалуроната со степенью замещения 87% и молекулярной массой 2,50×105 г/моль растворяли в 20 мл 50% этаноле и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 61° (+/- 2° и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 60°С и температуре верхней пластины 40°С в течение 10 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм, сухое вещество определяли составляющим приблизительно 92%. Способность набухания пленки определяли превышающей 100% (измеряли вариацию площади пленки) в состоянии равновесия.
Пример 13. Получение пленки на основе бехеноильного производного натрия гиалуроната
100 мг бехеноильного производного натрия гиалуроната со степенью замещения 16% и молекулярной массой 3,3×105 г/моль растворяли в 20 мл 50% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на полипропиленовую подложку со смачиваемостью деминерализованной водой 105° (+/- 2°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 6 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 14. Получение пленки на основе лауроильного производного натрия гиалуроната
100 мг лауроильного производного натрия гиалуроната со степенью замещения 29% и молекулярной массой 1,88×105 г/моль растворяли в 20 мл 50% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 61° (+/- 2°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 7 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 15. Получение пленки на основе олеильного производного натрия гиалуроната
100 мг олеильного производного натрия гиалуроната со степенью замещения 15% и молекулярной массой 2,8×105 г/моль растворяли в 20 мл 50% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 48 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 61° (+/- 2°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 12 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 16. Получение пленки на основе пальмитоильного производного натрия гиалуроната
100 мг пальмитоильного производного натрия гиалуроната со степенью замещения 34% и молекулярной массой 2,67×105 г/моль растворяли в 20 мл 50% раствора этанола и взбалтывали по меньшей мере в течение 48 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 61° (+/- 2°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 12 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 17. Получение пленки на основе пальмитоильного производного натрия гиалуроната
100 мг пальмитоильного производного натрия гиалуроната со степенью замещения 60% и молекулярной массой 2,8×105 г/моль растворяли в 20 мл 50% раствора этанола и взбалтывали по меньшей мере в течение 48 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 61° (+/- 2°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 12 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 18. Получение пленки на основе пальмитоильного производного натрия гиалуроната
100 мг пальмитоильного производного натрия гиалуроната со степенью замещения 31% и молекулярной массой 2,7×105 г/моль растворяли в 20 мл 50% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 20 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 61° (+/- 2°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 12 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 19. Получение пленки на основе лауроильного производного натрия гиалуроната
100 мг лауроильного производного натрия гиалуроната со степенью замещения 58% и молекулярной массой 1,88×105 г/моль растворяли в 20 мл 50% раствора пропан-2-ола и взбалтывали по меньшей мере в течение 48 часов. После взбалтывания раствор дозировали на гидрофобизованное стекло со смачиваемостью деминерализованной водой 61° (+/- 2°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 20°С и температуре верхней пластины 10°С в течение 12 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину полученной таким образом пленки определяли равной приблизительно 15 мкм.
Пример 20. Сравнение смачиваемости подложек, полученных с использованием различных средств гидрофобизации
Стекло, предназначенное для гидрофобизации, сначала тщательно очищали, так что получаемая в результате смачиваемость деминерализованной водой не превышала 10°. Затем проводили гидрофобизацию стекла. Для гидрофобизации стекла использовали следующие средства гидрофобизации: хлортриметилсилан (CTMS), (3-аминопропил)триметоксисилан (APTMS) и октадецилтрихлорсилан (OTS). Полученные в результате значения смачиваемости стекла (с концентрацией средства, составляющей 1%) приведены в таблице 1. Более того, для CTMS тестировали различные концентрации средства в гексане. Полученные значения измеренной смачиваемости стекла приведены в таблице 2.

СА означает контактный угол.

СА означает контактный угол.
Пример 21. Определение остатков средства гидрофобизации в пленке, полученной согласно примеру 1
Триметилсиланол анализировали как остаток триметилсилилхлорида после его реакции с -ОН-группами производного гиалуронана. Анализ выполняли на газовом хроматографе, оснащенном парофазным пробоотборником и масс-спектрометрическим датчиком в форме простого квадруполя. Образец пленки, полученной согласно примеру 1, растворяли до концентрации 6 мг/мл в 50% (объем/объем) пропан-2-оле и после растворения 4,75 мл образца и 0,25 мл н-бутанола (1 мг/мл), который действовал как внутренний стандарт, пипетировали во флакон. Также готовили стоковый раствор триметилсилилхлорида (1 мг/мл) в 50% пропан-2-оле, который реагировал непосредственно с триметилсиланолом. Из этого раствора получали калибровочные серии, варьирующие от 0,5 до 15,0 мкг/мл, с добавлением н-бутанола в качестве внутреннего стандарта. Ни один анализируемый образец пленки не демонстрировал присутствие триметилсиланола в концентрации, превышающей первую калибровочную точку, т.е. содержание триметилсиланола в образцах пленки было ниже 0,008 мас. %.
Пример 22. Эффект прилипания пленки на основе олеильного производного натрия гиалуроната на внешний вид ее поверхности
Пленки, полученные согласно примерам 10 и 11, получали на двух стеклах с различной смачиваемостью, а именно 57° (+/- 3°) и 107° (+/- 1°). После сушки оценивали внешний вид поверхности пленки и сопоставляли с прилипанием. В случае хорошего прилипания пленки к подложке поверхность пленки является плоской, без каких-либо поверхностных деформаций. Пленка полностью прилипала к подложке, имеющей меньший контактный угол, на подложке, имеющей больший контактный угол, она частично отслаивалась и деформировалась. Результаты приведены на фиг. 1а, 1b, 1с. Из фиг. следует, что, если пленка полностью прилипает к поверхности, она становится ровной и не имеет деформаций поверхности после отслаивания (фиг. 1с справа). Напротив, в случае неполного прилипания пленка более или менее деформируется (фиг. 1с слева).
Пример 23. Эффект прилипания пленки на основе пальмитоильного производного натрия гиалуроната на внешний вид ее поверхности
Оценивали пленку на основе пальмитоильного производного натрия гиалуроната, полученную согласно примеру 2 на стекле со смачиваемостью 61° (+/- 2°) После сушки оценивали прилипание и внешний вид пленки. Пленка хорошо прилипала, и ее поверхность была абсолютно плоской, без каких-либо деформаций. Результаты прилипания приведены на фиг. 2.
Пример 24. Определение остаточного пропан-2-ола в пленках
Остаточную концентрацию органического растворителя пропан-2-ола определяли посредством газовой хроматографии в пленках, полученных согласно примерам 1, 8 и 12. Принцип определения растворителя заключается в превращении его в газообразную фазу при повышенной температуре, отделении его на газовом хроматографе и в последующем выявлении с помощью пламенно-ионизационного детектора. Концентрацию пропан-2-ола в пленке всегда определяли дважды (т.е. для двух образцов) путем считывания с калибровочной кривой. Масса образца всегда составляла 50 мг. После завершения анализа во всех пленках определяли концентрацию остаточного пропан-2-ола, которая была ниже самой нижней точки калибровочной кривой и была выражена как < 0,02 мас. %. Это значение отвечает требованиям безопасности в отношении количеств остаточных растворителей класса 3 в соответствии с фармакопеей ЕС.
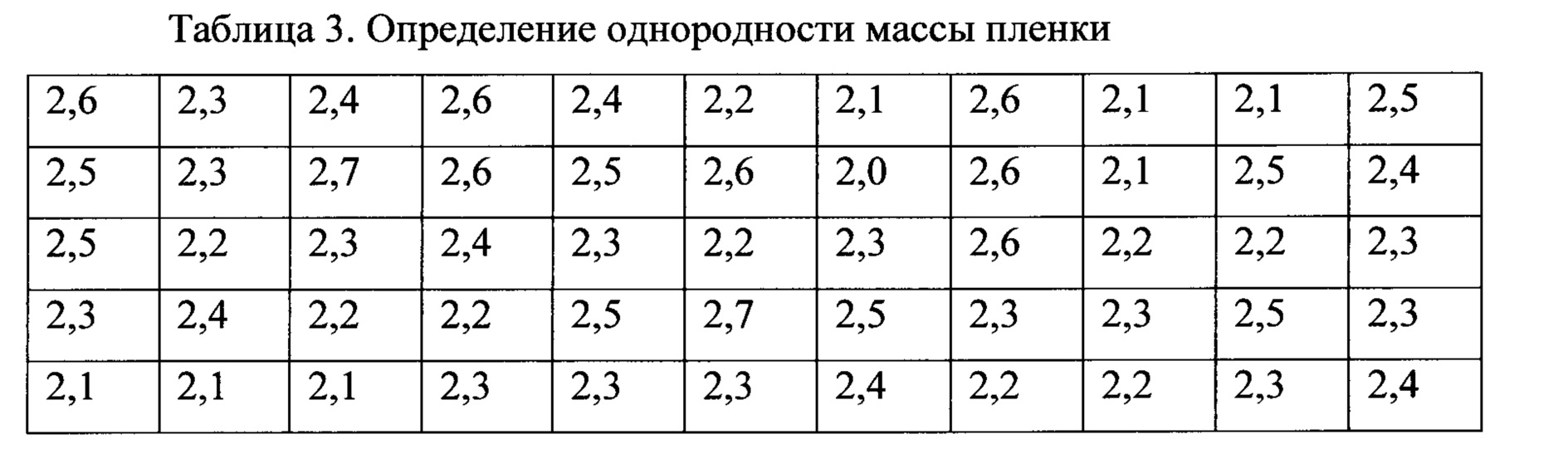
Пример 25. Определение однородности распределения массы по площади
Пленку, полученную согласно примеру 1, разрезали на 55 квадратов площадью 1 см2. Перед измерением отдельные образцы оставляли при комнатной влажности и температуре на 5 часов. Затем отдельные квадраты взвешивали на аналитических весах. Полученные массы отдельных квадратов приведены в таблице 3. Среднее, стандартное отклонение и вариационный коэффициент вычисляли на основе всех значений, приведенных в таблице. Вычисленные значения: среднее 2,35 мг, стандартное отклонение 0,18 мг, вариационный коэффициент 7,51%.
Пример 26. Определение однородности распределения толщины по площади
Квадратную сетку с площадью одного квадрата 1 см2 и с общим числом квадратов 35 рисовали на пленке, полученной согласно примеру 15. На каждом квадрате измеряли толщину пленки с помощью механического прибора для измерения толщины Mytutoyo VL-50. Измерение проводили в соответствующей окружающей среде с влажностью 50% и температурой 25°С. Значения измерения приведены в таблице 4. Среднее, стандартное отклонение и вариационный коэффициент вычисляли на основе всех значений, приведенных в таблице. Вычисленные значения: среднее 14,6 мкм, стандартное отклонение 1,17 мкм, вариационный коэффициент 8,02%.

Пример 27. Сравнение способности набухания пленок, полученных из пальмитоильных производных натрия гиалуроната с различными степенями замещения, в 0,1 М фосфатном буфере, pH 7,4
Пленки, полученные согласно примерам 2, 16 и 17, разрезали на точно определенные квадраты, взвешивали, измеряли и помещали в 0,1 М фосфатный буфер (PBS), pH 7,4. Способность набухания пленок контролировали при 37°С; каждый эксперимент выполняли в трех повторностях. Оценивали изменения массы и размеров пленок, результаты приведены в таблице 5. Из данной таблицы видно, что чем ниже степень замещения, тем выше способность набухания пленки. В случае использования высоких степеней замещения может быть достигнуто лишь небольшое изменение площади пленки, что может быть очень важным в ряде применений.

Пример 28. Разложение полученных из пальмитоильного производного натрия гиалуроната пленок в кондиционированной среде, сравнение двух степеней замещения
Пленки, полученные согласно примерам 2 и 18, разрезали на точно определенные квадраты, взвешивали, измеряли и помещали в кондиционированную среду. Всю подготовку осуществляли в ламинарном боксе, во избежание загрязнения и нежелательных реакций в среде. С заданными интервалами при 37°С проверяли изменение площади пленки и визуально определяемый ее внешний вид - свойства, которые могут быть ассоциированы с разложением. Кондиционированную среду меняли с регулярными интервалами; эксперимент выполняли в трех повторностях. Пленка, полученная согласно примеру 2, начинала разлагаться значительно позже, чем пленка, полученная согласно примеру 18. Результаты показаны на фиг. 3а и 3b, при этом показан внешний вид пленки после 3 недель разложения в кондиционированной среде. В таблице 6 представлено изменение площади пленки после 1 недели разложения для пленки согласно примеру 2, а также согласно примеру 18, и после трех недель для пленки согласно примеру 2 (пленка согласно примеру 18 разлагалась до кусочков или даже растворялась после трех недель разложения). Из результатов видно, что скорость разложения существенно зависит от степени замещения натрия гиалуроната ацильной цепью. В случае высокозамещенной пленки, полученной согласно примеру 2, разложение протекало в течение нескольких месяцев.

Пример 29. Разложение пленки на основе пальмитоильного производного натрия гиалуроната
Образцы пленки, полученной согласно примеру 5, инкубировали в стандартной среде для клеточных культур (модифицированной по способу Дульбекко среде Игла) с добавлением 300 ME фермента на 1 мг пленки. Инкубацию проводили при 37°С и образцы анализировали через 24 часа. Анализ образцов осуществляли на системе HPLC Alliance (Waters) в соответствии с внутренней стандартной операционной процедурой. Через 24 часа все еще можно было видеть неразложенные кусочки пленки. Несмотря на это, в растворе выявляли олигосахариды на основе гиалуронана, как показано на фиг. 4.
Пример 30. Разложение пленки на основе пальмитоильного производного натрия гиалуроната
Образцы пленки, полученной согласно примеру 2, инкубировали в стандартной среде для клеточных культур (модифицированной по способу Дульбекко среде Игла) с добавлением 300 ME фермента на 1 мг пленки. Инкубацию проводили при 37°С и образцы анализировали через 24 часа. Анализ образцов осуществляли на системе HPLC Alliance (Waters) в соответствии с внутренней стандартной операционной процедурой. Через 24 часа не выявляли олигосахариды на основе гиалуронана в растворе, соответствующем примеру 28, при этом довольно длительное время разложения наблюдали для пленки согласно примеру 2, и это демонстрирует возможность модуляции разложения посредством степени замещения.
Пример 31. Определение характеристик пленок посредством модуля Юнга
Модуль Юнга определяли для пленок, полученных согласно примерам 10, 15, 16 и 19, в сухом состоянии. Пленки тестировали на предмет механических свойств с помощью машины для одностадийного испытания на растяжение INSTRON3343 с головкой 100N. Модуль Юнга вычисляли на основании среднего значения по меньшей мере 9 корректных измерений. В таблице 7 показано, что модуль Юнга сухих негидратированных пленок не зависит от молекулярной массы, заместителя или степени замещения.

Пример 32. Определение характеристик морфологии поверхности пленки и определение RMS посредством AFM
Определяли характеристики пленок, полученных согласно примерам 8 и 16, с помощью способа атомно-силовой микроскопии (AFM), при котором контролировали, в частности, внешний вид и характер поверхности. В частности, определяли RMS шероховатости (среднеквадратическое значение шероховатости). Выявили, что очень гладкая поверхность, характеризующаяся значением RMS до 2 нм, может быть получена со стороны подложки (см. фиг. 5 для пленки согласно примеру 16). Сторона пленки, которая подвергается воздействию воздуха при сушке, всегда более шероховатая, при этом RMS составляет около 50 нм или больше.
Пример 33. Сравнение пленок, высушенных в градиенте температуры и в замкнутом пространстве
Пленки, полученные согласно примерам 8 и 19, после сушки визуально сравнивали. Поверхность обеих пленок не была деформированной, поверхностная корка не образовывалась ни на одной из пленок. Обе пленки были одинаковы по качеству (визуальное сравнение).
Пример 34. Жизнеспособность клеток ТНР-1 в суспензии после 24- и 72-часовой инкубации с пленкой, полученной согласно примеру 1 на основе пальмитоильного производного натрия гиалуроната
Линию клеток ТНР-1 культивировали в среде с добавлением 10% фетальной бычьей сыворотки. После достижения достаточной плотности и жизнеспособности (измеренных с помощью автоматического устройства для подсчета клеток CASY ТТ, Roche) клетки высевали в 6-луночный планшет в 2 мл 10% среды. Тестируемую пленку добавляли к клеткам в количестве 1 и 0,5 мг/мл. Через 24 и 72 часа инкубации клетки промывали и выявляли их жизнеспособность и случаи клеточной смерти с помощью набора для выявления ApoFlowEx® FITC Kit (Exbio) на проточном цитометре MACSQuant® (Miltenyi Biotec). Клетки оценивали как жизнеспособные, если не выявляли флуоресценции йодида пропидия. На фиг. 6 показано незначительное снижение жизнеспособности после 24 часов инкубации, которое больше не выявляли через 72 часа. Следовательно, тестируемую пленку оценивали как нецитотоксическую при указанных концентрациях.
Пример 35. Анализ клеточной смерти клеток ТНР-1 в суспензии после 24 и 72 часов инкубации с пленкой, полученной согласно примеру 1 на основе пальмитоильного производного натрия гиалуроната
Линию клеток ТНР-1 культивировали в среде с добавлением 10% фетальной бычьей сыворотки. После достижения достаточной плотности и жизнеспособности (измеренных с помощью автоматического устройства для подсчета клеток CASY ТТ, Roche) клетки высевали в шести-луночный планшет в 2 мл 10% среды. Тестируемую пленку добавляли к клеткам в количестве 1 и 0,5 мг/мл. Через 24 и 72 часа инкубации клетки промывали и выявляли их жизнеспособность и случаи клеточной смерти с помощью набора для выявления ApoFlowEx® FITC Kit (Exbio) на проточном цитометре MACSQuant® (Miltenyi Biotec). Оценивание наличия клеточной смерти (апоптоза и некроза) осуществляли в соответствии с рекомендацией изготовителя набора. Вкратце: популяцию отдельных клеток разделяли на основании интенсивности флуоресценции йодида пропидия и Annexin V-FITC на 3 группы: отрицательные в обоих каналах (живые клетки), положительные только в канале для Annexin V-FITC (апоптические клетки) и положительные клетки для канала йодид пропидия +/- Annexin V-FITC (некротические клетки).
Фиг. 7 и 8 указывают на то, что через 24, а также через 72 часа не происходит дальнейшее увеличение числа апоптических или некротических клеток в культуре, и, поэтому, тестируемый материал может быть оценен как не вызывающий смерть клеток.
Пример 36. Контактное ингибирование роста фибробластов мыши 3Т3 Swiss
Линию фибробластов мыши 3Т3 Swiss культивировали в среде с добавлением 10% фетальной бычьей сыворотки. В экспоненциальной фазе роста клетки высевали в шести-луночный планшет в 2 мл 10% среды. После достижения конфлюэнтности добавляли тестируемую пленку, полученную согласно примеру 1, с площадью 1 см2, которую загружали с помощью силиконового стерильного кольца, чтобы не происходило сильное движение пленки в монокультуре. В то же время инкубировали контрольные клетки без какой-либо обработки и только с силиконовым кольцом. После 72 часов инкубации образцы пленки и силиконовые кольца извлекали, клетки промывали с помощью PBS и фиксировали 4% формальдегидом (10 минут/комнатная температура). После промывания деионизированной водой клетки окрашивали кристаллическим фиолетовым (0,1% в воде, 30 минут/комнатная температура) и после вымывания красителя площадь клеток фотографировали и рассматривали под световым микроскопом. Оценивали площадь клеток под тестируемым материалом, степень повреждения клеток и размер поврежденной зоны.
На макрофотографиях (фиг. 9) четко видно, что поврежденная зона монослоя ограничена, и что повреждены только клетки, находившиеся непосредственно под пленкой, наиболее вероятно, из-за легкого трения; подробности под световым микроскопом показывают, что клетки демонстрируют тенденцию к повторному нарастанию под пленкой. Не наблюдали какое-либо повреждение или изменение морфологии клеток на границах тестируемой пленки. Следовательно, можно предположить, что материал не проявляет контактное ингибирование роста клеток.
Пример 37. Антиадгезионные свойства пленки в отношении клеток
Пленки, полученные согласно примерам 2 и 17 (производные с двумя разными степенями замещения), разрезали в условиях стерильности на части с размерами 1 см2. Эти части помещали в шести-луночные планшеты для культивирования лицевой стороной вверх или лицевой стороной вниз. Затем их погружали с помощью стерильных силиконовых колец и культуральную среду (2 мл) для первичных человеческих фибробластов (NHDF), содержащую 10% фетальной бычей сыворотки, пипетировали в полученные таким образом образцы. При этом готовили суспензию NHDF и пипетировали в середину силиконового кольца на поверхность пленки в количестве 100000 клеток/образец. Образцы с клетками инкубировали в течение 72 часов и осматривали с 24-часовыми интервалами под световым микроскопом. Использовали приспособленный для клеточных культур полистирол с хорошими адгезионными свойствами в качестве положительного контроля (CTRL). После завершения инкубации силиконовые кольца извлекали и пленки вместе с клетками фиксировали 4% формальдегидом в течение 10 минут, а затем окрашивали 1% кристаллическим фиолетовым в воде (10 минут). После тщательного вымывания несвязанного кристаллического фиолетового (2-кратное 5-минутное ополаскивание дистиллированной водой) образцы фотографировали с использованием инвертированного микроскопа Nikon со 100-кратным увеличением. Результаты показаны на фиг. 10. На фотографии CTRL можно видеть почти конфлюэнтный клеточный слой. На фотографиях пленок (A-D) наблюдается некоторая структура, вероятно, сформированная из-за длительной инкубации в среде и ставшая видимой благодаря кристаллическому фиолетовому. Однако на пленках нет клеток. Следовательно, можно констатировать тот факт, что пленки совершенно не прилипают в этой системе, и даже присутствие белков в культуральной среде не способствует прилипанию.
Пример 38. Получение пленки с октенидина дигидрохлоридом
Смешивали 20 мкл стокового раствора октенидина дигидрохлорида в этаноле с массовой концентрацией 10 мг/мл с 20 мл 50% пропан-2-олом. После тщательного взбалтывания в раствор добавляли 100 мг пальмитоильного производного натрия гиалуроната со степенью замещения 57% и молекулярной массой 2,67×105 г/моль. Раствор взбалтывали в течение 72 часов, после взбалтывания его дозировали на гидрофобизованное стекло со значением смачиваемости 65 (+/- 3°) и сушили в замкнутом пространстве, в градиенте температуры при температуре нижней пластины 50°С и температуре верхней пластины 20°С в течение 6 часов. После сушки пленку оценивали, удаляли с подложки и определяли характеристики. Толщину пленки определяли равной 15 мкм.
Реферат
Настоящее изобретение относится к самоподдерживающейся пленке на основе сложного эфира гиалуроновой кислоты и к способу ее получения. Указанная пленка содержит C-С-ацилированное производное гиалуроновой кислоты в соответствии с общей формулой (I),, в которой R представляет собой Нили Naи в которой Rпредставляет собой Н или -С(=O)CH, при этом x представляет собой целое число в диапазоне от 9 до 21, а у представляет собой целое число в диапазоне от 11 до 43, и CHпредставляет собой линейную или разветвленную, насыщенную или ненасыщенную цепь С-С, в которой по меньшей мере в одном повторяющемся звене один или несколько Rпредставляют собой -С(=O)СНи в которой n находится в диапазоне от 12 до 4000. Толщина пленки составляет 2-100 мкм. Способ получения пленки включает получение раствора, содержащего С-С-ацилированное производное гиалуроновой кислоты в соответствии с формулой (I) в смеси воды и С-С-спирта, перемешивание раствора и нанесение его на подложку, сушка в замкнутом пространстве и удаление с подложки. Полученная пленка нерастворима в водных средах, образуется только из ацилированного гиалуронана общей формулы (I) без необходимости добавления сшивающих веществ и без дополнительной обработки, содержит большое количество сухого вещества и может быть использована в медицине и ветеринарии, в частности для получения противоспаечных барьеров. 2 н. и 16 з.п. ф-лы, 10 ил., 7 табл., 37 пр.
Формула


Комментарии