Средства для рнки, композиции и способы их применения для лечения заболеваний, ассоциированных с транстиретином (ttr) - RU2678807C2
Код документа: RU2678807C2
Чертежи


























































































































































































































































































































































































































































































Описание
Родственные заявки
По настоящей заявке испрашивается приоритет временной заявки на патент США №61/561710, поданной 18 ноября 2011 года, временной заявки на патент США №61/615618, поданной 26 марта 2012 года, и временной заявки на патент США №61/680098, поданной 6 августа 2012 года, полное содержание каждой из которых включено в настоящее описание посредством ссылки.
Список последовательностей
Настоящая заявка содержит список последовательностей, который был подан в формате ASCII через EFS-Web и включен, таким образом, полностью посредством ссылки. Указанная копия ASCII, созданная 13 ноября 2012 года, названа 121301WO.txt, и ее размер составляет 541508 бит.
Уровень техники, предшествующий изобретению
Транстиретин (TTR) (также известный как преальбумин) обнаруживают в сыворотке и цереброспинальной жидкости (CSF). TTR транспортирует ретинолсвязывающий белок (RBP) и тироксин (T4), а также действует как носитель ретинола (витамина A) вследствие своей ассоциации с RBP в крови и CSF. Транстиретин назван так из-за того, что он транспортирует тироксин и ретинол. TTR также функционирует как протеаза и может расщеплять белки, содержащие apoA-I (основной HDL аполипопротеин), пептид амилоид-β и нейропептид Y. См. Liz, M.A. et al., (2010) IUBMB Life, 62 (6):429-435.
TTR представляет собой тетрамер из четырех идентичных субъединиц длиной 127 аминокислот (мономеров), в которых наблюдают преобладание структуры бета-листа. Каждый мономер содержит два 4-цепочечных бета-листа и имеет форму сплющенного эллипсоида. Взаимодействия антипараллельного бета-листа связывают мономеры в димеры. Короткая петля каждого мономера образует основное взаимодействие димер-димер. Эти две пары петель разделяют противоположные выпуклые бета-листы димеров с образованием внутреннего канала.
Печень представляет собой основной участок, экспрессирующий TTR. Другие значительные участки экспрессии включают хориоидное сплетение, сетчатку (в частности пигментный эпителий сетчатки) и поджелудочную железу.
Транстиретин представляет собой один по меньшей мере из 27 отдельных типов белков, который представляет собой белок-предшественник при образовании амилоидных фибрилл. См. Guan J. et al., (Nov. 4, 2011) Current perspectives on cardiac amyloidosis. Am. J. Physiol. Heart Circ. Physiol., doi:10.1152/ajpheart.00815.2011. Внеклеточное отложение амилоидных фибрилл в органах и тканях является признаком амилоидоза. Амилоидные фибриллы состоят из неправильно свернутых белковых агрегатов, которые могут возникать в результате избыточной продукции или конкретных мутаций в белках-предшественниках. Амилоидогенный потенциал TTR может быть связан с его преобладающей структурой бета-листа, рентгено-кристаллографические исследования свидетельствуют о том что, определенные амилоидогенные мутации снижают устойчивость тетрамерной структуры белка. См., например, Saraiva M.J.M., (2002) Expert Reviews in Molecular Medicine, 4(12):1-11.
Амилоидоз представляет собой общий термин для группы заболеваний, связанных с амилоидом, которые характеризуются отложением амилоида. Связанные с амилоидом заболевания классифицируют на основе их белка-предшественника, например, названия, начинающиеся "A" для амилоида и с последующим сокращенным обозначением белка-предшественника, например, ATTR для амилоидного транстиретина, там же.
Существует целый ряд ассоциированных с TTR заболеваний, большая часть из которых представляет собой связанные с амилоидом заболевания. TTR с нормальной последовательностью ассоциирован с амилоидозом сердца у людей пожилого возраста и называется старческим системным амилоидозом (SSA) (также называемый старческим амилоидозом сердца (SCA) или амилоидозом сердца). SSA, как правило, сопровождается микроскопическими отложениями во многих других органах. TTR амилоидоз проявляется в различных формах. Когда в большей степени поражается периферическая нервная система, заболевание называется семейной амилоидотической полинейропатией (FAP). Когда поражается сердце, а нервная система не поражена, заболевание называют семейной амилоидотической кардиомиопатией (FAC). Третий основной тип TTR амилоидоза представляет собой лептоменингеальный амилоидоз, также известный как лептоменингеальный или менингоцереброваскулярный амилоидоз, амилоидоз центральной нервной системы (ЦНС) или амилоидоз VII формы. Мутации в TTR также могут вызывать амилоидотические помутнения стекловидного тела, синдром запястного канала и эутиреоидную гипертироксинемию, которая представляют собой неамилоидотическое заболевание, для которого предполагают, что оно является вторичным по отношению к повышенной ассоциации тироксина с TTR вследствие мутантной молекулы TTR с увеличенной аффинностью к тироксину. См., например, Moses et al., (1982) J. Clin. Invest., 86, 2025-2033.
Аномальные амилоидогенные белки могут быть наследственными или приобретенными в результате соматических мутаций. Guan J. et al., (Nov. 4, 2011) Current perspectives on cardiac amyloidosis, Am. J. Physiol. Heart Circ. Physiol., doi:10.1152/ajpheart.00815.2011. Ассоциированный с транстиретином ATTR является наиболее распространенной формой наследственного системного амилоидоза. Lobato L. (2003) J. Nephrol., 16:438-442. Мутации TTR ускоряют процесс образования TTR амилоида и представляют собой наиболее важный фактор риска развития ATTR. Известно, что более 85 амилоидогенных вариантов TTR вызывают системный семейный амилоидоз. Мутации TTR, как правило, ведут к образованию системных отложений амилоида, в частности с поражением периферической нервной системы, хотя некоторые мутации ассоциированы с кардиомиопатией или помутнениями стекловидного тела, там же.
Мутация V30M представляет собой наиболее распространенную мутацию TTR. См., например, Lobato L., (2003) J. Nephrol., 16:438-442. Мутацию V122I несут 3,9% афро-американской популяции, и она является наиболее общей причиной FAC. Jacobson D.R. et al., (1997) N. Engl. J. Med., 336(7):466-73. Оценивают, что SSA поражает более 25% популяции в возрасте более 80 лет. Westermark P. et al., (1990) Proc. Natl. Acad. Sci. USA, 87(7):2843-5.
Таким образом, в данной области существует необходимость эффективных видов лечения ассоциированных с TTR заболеваний.
Сущность изобретения
Настоящее изобретение относится к средствам для РНКи, например, двухцепочечные средства для РНКи, направленной на ген транстиретина (TTR). Настоящее изобретение также относится к способам ингибирования экспрессии TTR и к способам лечения или профилактики ассоциированного с TTR заболевания у индивидуума с использованием средств для РНКи, например, двухцепочечных средств для РНКи по изобретению. Настоящее изобретение по меньшей мере частично основано на открытии, что средства для РНКи, которые содержат конкретные химические модификации, обладают прекрасной способностью ингибировать экспрессию TTR. В настоящем описании продемонстрировано, что средства, содержащие определенный паттерн химических модификаций (например, чередующийся паттерн), и лиганд являются эффективными для подавления активности гена TTR. Кроме того, средства, содержащие один или более мотивов трех идентичных модификаций в трех последовательных нуклеотидах, содержащих один такой мотив на участке расщепления средств или около него, обладают неожиданно повышенной активностью подавления гена TTR. Когда один такой химический мотив содержится в средстве, предпочтительно он располагается в области расщепления или около нее для усиления активности подавления экспрессии гена. Область расщепления представляет собой область, окружающую участок расщепления, т.е. участок на мРНК-мишени, на котором происходит расщепление.
Таким образом, в одном из аспектов настоящее изобретение относится к средствам для РНКи, например, двухцепочечными средствам для РНКи, для ингибирования экспрессии транстиретина (TTR). Двухцепочечное средство для РНКи содержит смысловую цепь, комплементарную антисмысловой цепи. Антисмысловая цепь содержит область, комплементарную участку мРНК, кодирующей транстиретин. Каждая цепь содержит от 14 до 30 нуклеотидов, и двухцепочечное средство для РНКи представлено формулой (III):

В формуле III i, j, k и l каждый независимо представляет собой 0 или 1; p, p', q и q' каждый независимо представляет собой 0-6; каждый Na и



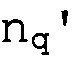

В некоторых вариантах осуществления i равно 1; j равно 1; или i и j равны 1.
В некоторых вариантах осуществления k равно 1; l равно 1; или k и l равны 1.
В некоторых вариантах осуществления i равно 0; j равно 1.
В некоторых вариантах осуществления i равно 1; j равно 0.
В некоторых вариантах осуществления k равно 0; l равно 1.
В некоторых вариантах осуществления k равно 1; l равно 0.
В некоторых вариантах осуществления XXX является комплементарным X'X'X', YYY является комплементарным Y'Y'Y', и ZZZ является комплементарным Z'Z'Z'.
В некоторых вариантах осуществления мотив YYY находится на участке расщепления смысловой цепи или около него.
В некоторых вариантах осуществления мотив Y'Y'Y' находится в положениях 11, 12 и 13 антисмысловой цепи от 5'-конца.
В некоторых вариантах осуществления Y' представляет собой 2'-O-метил.
В некоторых вариантах осуществления Y' представляет собой 2'-фтор.
В некоторых вариантах осуществления формула (III) представлена в виде формулы (IIIa):

В формуле IIIa каждый Nb и

В некоторых вариантах осуществления формула (III) представлена в виде формулы (IIIb):

В формуле IIIb каждый Nb и

В некоторых вариантах осуществления формула (III) представлена в виде формулы (IIIc):

В формуле IIIc каждый Nb и


Во многих вариантах осуществления длина дуплексной области составляет 15-30 пар нуклеотидов. В некоторых вариантах осуществления длина дуплексной области составляет 17-23 пары нуклеотидов, 17-25 пар нуклеотидов, 23-27 пар нуклеотидов, 19-21 пару нуклеотидов или 21-23 пары нуклеотидов.
В определенных вариантах осуществления каждая цепь содержит 15-30 нуклеотидов.
В некоторых вариантах осуществления модификации в нуклеотидах выбраны из группы, состоящей из LNK, HNA, CeNA, 2'-метоксиэтила, 2'-O-алкила, 2'-O-аллила, 2'-C-аллила, 2'-фтора, 2'-дезокси, 2'-гидроксила и их комбинаций. В некоторых предпочтительных вариантах осуществления модификации в нуклеотидах представляют собой 2'-O-метил или 2'-фтор.
В некоторых вариантах осуществления лиганд представляет собой одно или более производных N-ацетилгалактозамина (GalNAc), присоединенных посредством двухвалентного или трехвалентного разветвленного линкера. В конкретных вариантах осуществления лиганд представляет собой

В некоторых вариантах осуществления лиганд присоединен к 3-концу смысловой цепи.
В некоторых вариантах осуществления средство для РНКи конъюгировано с лигандом, как продемонстрировано на следующем ниже схематическом чертеже

где X представляет собой O или S.
В некоторых вариантах осуществления средство для РНКи конъюгировано с лигандом, как продемонстрировано на следующем ниже схематическом чертеже

В некоторых вариантах осуществления средство для РНКи дополнительно содержит по меньшей мере одну тиофосфатную или метилфосфонатную межнуклеотидная связь. В некоторых вариантах осуществления тиофосфатная или метилфосфонатная межнуклеотидная связь находится на 3'-конце одной цепи. В некоторых вариантах осуществления цепь представляет собой антисмысловую цепь. В других вариантах осуществления цепь представляет собой смысловую цепь.
В определенных вариантах осуществления пара оснований в положении 1 5'-конца дуплекса представляет собой пару оснований AU.
В некоторых вариантах осуществления нуклеотиды Y содержат 2'-фтор-модификацию.
В некоторых вариантах осуществления нуклеотиды Y' содержат 2'-O-метил-модификацию.
В некоторых вариантах осуществления p'>0. В некоторых таких вариантах осуществления, каждый n является комплементарным мРНК-мишени. В других таких вариантах осуществления каждый n не является комплементарным мРНК-мишени. В некоторых вариантах осуществления p, p', q и q' равны 1-6. В некоторых предпочтительных вариантах осуществления p'=1 или 2. В некоторых предпочтительных вариантах осуществления p'=2. В некоторых таких вариантах осуществления q'=0, p=0, q=0, и выступающие нуклеотиды p' являются комплементарными мРНК-мишени. В других таких вариантах осуществления q'=0, p=0, q=0, и выступающие нуклеотиды p' не являются комплементарными мРНК-мишени.
В некоторых вариантах осуществления смысловая цепь содержит всего 21 нуклеотид, и антисмысловая цепь содержит всего 23 нуклеотида.
В определенных вариантах осуществления связи между


В некоторых вариантах осуществления средство для РНКи выбрано из группы средств, перечисленных в таблице 1.
В предпочтительных вариантах осуществления средство для РНКи выбрано из группы, состоящей из AD-51544, AD-51545, AD-51546 и AD-51547.
Даже в более предпочтительном варианте осуществления средство для РНКи представляет собой AD-51547 со следующей ниже структурой:
смысловая цепь: 5'-UfgGfgAfuUfuCfAfUfgUfaacCfaAfgAfL96-3' (SEQ 10 NO: 2)
антисмысловая цепь: 5'-uCfuUfgGfUfUfaCfaugAfaAfuCfcCfasUfsc-3' (SEQ 10 NO: 3),
где обозначаемые строчными буквами нуклеотиды (a, u, g, c) означают 2'-O-метил-нуклеотиды; Nf (например, Af) означает 2'-фтор-нуклеотид; s означает фосфотиоратную связь; L96 означает лиганд GalNAc3.
В другом аспекте настоящее изобретение относится к клетке, содержащей средство для РНКи для ингибирования экспрессии TTR.
В дополнительном аспекте настоящее изобретение относится к фармацевтической композиции, содержащей средство для РНКи для ингибирования экспрессии TTR. В некоторых вариантах осуществления фармацевтическая композиция представляет собой раствор, содержащий средство для РНКи. В некоторых вариантах осуществления раствор, содержащий средство для РНКи представляет собой незабуференный раствор, например, физиологический раствор или воду. В других вариантах осуществления раствор представляет собой забуференный раствор, например, раствор фосфатно-солевого буфера (PBS). В других вариантах осуществления фармацевтическая композиция представляет собой липосому или липидный состав. В некоторых вариантах осуществления липидный состав содержит XTC или MC3.
В еще одном аспекте настоящее изобретение относится к способам ингибирования экспрессии транстиретина (TTR) в клетке. Способы включают приведение клетки в контакт со средством для РНКи, например, двухцепочечным средством для РНКи, в количестве, эффективном для ингибирования экспрессии TTR в клетке, таким образом, ингибируя экспрессию TTR в клетке.
В некоторых вариантах осуществления экспрессию TTR ингибируют по меньшей мере приблизительно на 10%, по меньшей мере приблизительно на 20%, по меньшей мере приблизительно на 30%, по меньшей мере приблизительно на 40%, по меньшей мере приблизительно на 50%, по меньшей мере приблизительно на 60%, по меньшей мере приблизительно на 70%, по меньшей мере приблизительно на 80% или по меньшей мере приблизительно на 90%.
В других вариантах осуществления клетку приводят в контакт in vitro со средством для РНКи. В других вариантах осуществления клетка содержится у индивидуума. В предпочтительных вариантах осуществления индивидуум представляет собой человека.
В дополнительных вариантах осуществления индивидуум представляет собой индивидуума, страдающего ассоциированным с TTR заболеванием, и эффективное количество представляет собой терапевтически эффективное количество. В других вариантах осуществления индивидуум представляет собой индивидуума, подвергающегося риску развития ассоциированного с TTR заболевания, и эффективное количество представляет собой профилактически эффективное количество. В некоторых вариантах осуществления индивидуум, подвергающийся риску развития ассоциированного с TTR заболевания, представляет собой индивидуума, который несет мутацию гена TTR, которая ассоциирована с развитием ассоциированного с TTR заболевания.
В некоторых вариантах осуществления ассоциированное с TTR заболевание выбрано из группы, состоящей из старческого системного амилоидоза (SSA), системного семейного амилоидоза, семейной амилоидотической полинейропатии (FAP), семейной амилоидотической кардиомиопатии (FAC), лептоменингеального/амилоидоза центральной нервной системы (ЦНС) и гипертироксинемии.
В некоторых вариантах осуществления индивидуум страдает ассоциированным с TTR амилоидозом, и способ уменьшает отложение амилоидного TTR у индивидуума.
В других вариантах осуществления средство для РНКи вводят индивидууму способами введения, выбранными из группы, состоящей из подкожного, внутривенного, внутримышечного, внутрибронхиального, интраплеврального, интраперитонеального, внутриартериального, лимфатического, цереброспинального и любых их комбинаций. В определенных вариантах осуществления средство для РНКи вводят индивидууму путем подкожного или внутривенного введения. В предпочтительных вариантах осуществления средство для РНКи вводят индивидууму путем подкожного введения. В некоторых таких вариантах осуществления подкожное введение включает введение посредством подкожного насоса или подкожного депо.
В некоторых вариантах осуществления средство для РНКи вводят индивидууму таким образом, что средство для РНКи поставляют в конкретный участок у индивидуума. В некоторых вариантах осуществления участок выбран из группы, состоящей из печени, хориоидного сплетения, сетчатки и поджелудочной железы. В предпочтительных вариантах осуществления участок представляет собой печень. В некоторых вариантах осуществления доставка средства для РНКи опосредована асиалогликопротеиновым рецептором (ASGP-R), содержащимся в гепатоцитах.
В некоторых вариантах осуществления средство для РНКи вводят в дозе приблизительно от 0,25 мг/кг приблизительно до 50 мг/кг, например, приблизительно от 0,25 мг/кг приблизительно до 0,5 мг/кг, приблизительно от 0,25 мг/кг приблизительно до 1 мг/кг, приблизительно от 0,25 мг/кг приблизительно до 5 мг/кг, приблизительно от 0,25 мг/кг приблизительно до 10 мг/кг, приблизительно от 1 мг/кг приблизительно до 10 мг/кг, приблизительно от 5 мг/кг приблизительно до 15 мг/кг, приблизительно от 10 мг/кг приблизительно до 20 мг/кг, приблизительно от 15 мг/кг приблизительно до 25 мг/кг, приблизительно от 20 мг/кг приблизительно до 30 мг/кг, приблизительно от 25 мг/кг приблизительно до 35 мг/кг или приблизительно от 40 мг/кг приблизительно до 50 мг/кг.
В некоторых вариантах осуществления средство для РНКи вводят в дозе приблизительно 0,25 мг/кг, приблизительно 0,5 мг/кг, приблизительно 1 мг/кг, приблизительно 2 мг/кг, приблизительно 3 мг/кг, приблизительно 4 мг/кг, приблизительно 5 мг/кг, приблизительно 6 мг/кг, приблизительно 7 мг/кг, приблизительно 8 мг/кг, приблизительно 9 мг/кг, приблизительно 10 мг/кг, приблизительно 11 мг/кг, приблизительно 12 мг/кг, приблизительно 13 мг/кг, приблизительно 14 мг/кг, приблизительно 15 мг/кг, приблизительно 16 мг/кг, приблизительно 17 мг/кг, приблизительно 18 мг/кг, приблизительно 19 мг/кг, приблизительно 20 мг/кг, приблизительно 21 мг/кг, приблизительно 22 мг/кг, приблизительно 23 мг/кг, приблизительно 24 мг/кг, приблизительно 25 мг/кг, приблизительно 26 мг/кг, приблизительно 27 мг/кг, приблизительно 28 мг/кг, приблизительно 29 мг/кг, 30 мг/кг, приблизительно 31 мг/кг, приблизительно 32 мг/кг, приблизительно 33 мг/кг, приблизительно 34 мг/кг, приблизительно 35 мг/кг, приблизительно 36 мг/кг, приблизительно 37 мг/кг, приблизительно 38 мг/кг, приблизительно 39 мг/кг, приблизительно 40 мг/кг, приблизительно 41 мг/кг, приблизительно 42 мг/кг, приблизительно 43 мг/кг, приблизительно 44 мг/кг, приблизительно 45 мг/кг, приблизительно 46 мг/кг, приблизительно 47 мг/кг, приблизительно 48 мг/кг, приблизительно 49 мг/кг или приблизительно 50 мг/кг.
В некоторых вариантах осуществления средство для РНКи вводят в двух или более дозах. В конкретных вариантах осуществления средство для РНКи вводят в интервалах, выбранных из группы, состоящей из один раз каждые приблизительно 2 часа, один раз каждые приблизительно 3 часа, один раз каждые приблизительно 4 часа, один раз каждые приблизительно 6 часов, один раз каждые приблизительно 8 часов, один раз каждые приблизительно 12 часов, один раз каждые приблизительно 24 часа, один раз каждые приблизительно 48 часов, один раз каждые приблизительно 72 часа, один раз каждые приблизительно 96 часов, один раз каждые приблизительно 120 часов, один раз каждые приблизительно 144 часа, один раз каждые приблизительно 168 часов, один раз каждые приблизительно 240 часов, один раз каждые приблизительно 336 часов, один раз каждые приблизительно 504 часа, один раз каждые приблизительно 672 часа и один раз каждые приблизительно 720 часов.
В других вариантах осуществления способ дополнительно включает оценку уровня экспрессии мРНК TTR или экспрессии белка TTR в образце, получаемом у индивидуума.
В предпочтительных вариантах осуществления введение средства для РНКи не приводит к воспалительному ответу у индивидуума, как оценивают на основании уровня цитокина или хемокина, выбранного из группы, состоящей из G-CSF, IFN-γ, IL-10, IL-12 (p70), IL1β, IL-1ra, IL-6, IL-8, IP-10, MCP-1, MIP-1α, MIP-1β, TNFα и любых их комбинаций, в образце у индивидуума.
В некоторых вариантах осуществления средство для РНКи вводят с использованием фармацевтической композиции.
В предпочтительных вариантах осуществления средство для РНКи вводят в растворе. В некоторых таких вариантах осуществления миРНК вводят в незабуференном растворе. В одном из вариантов осуществления миРНК вводят в воде. В других вариантах осуществления миРНК вводят с буферным раствором, таким как ацетатный буфер, цитратный буфер, буфер на основе проламина, карбонатный буфер или фосфатный буфер или любую их комбинацию. В некоторых вариантах осуществления буферный раствор представляет собой фосфатно-солевой буфер (PBS).
В другом варианте осуществления фармацевтическая композиция представляет собой липосому или липидный состав, содержащий SNALP или XTC. В одном из вариантов осуществления липидный состав содержит MC3.
В другом аспекте изобретение относится к способам лечения или профилактики ассоциированного с TTR заболевания у индивидуума. Способы включают введение индивидууму терапевтически эффективного количества или профилактически эффективного количества средства для РНКи, например, двухцепочечного средства для РНКи, таким образом, обеспечивая лечение или профилактику ассоциированного с TTR заболевания у индивидуума.
В некоторых вариантах осуществления экспрессию TTR в образце, получаемом у индивидуума, ингибируют по меньшей мере приблизительно на 10%, по меньшей мере приблизительно на 20%, по меньшей мере приблизительно на 30%, по меньшей мере приблизительно на 40%, по меньшей мере приблизительно на 50%, по меньшей мере приблизительно на 60% или по меньшей мере приблизительно на 70%, по меньшей мере приблизительно на 80% или по меньшей мере приблизительно на 90%.
В некоторых вариантах осуществления индивидуум представляет собой человека.
В некоторых вариантах осуществления индивидуум представляет собой индивидуума, страдающего ассоциированным с TTR заболеванием. В других вариантах осуществления индивидуум представляет собой индивидуума, подвергающегося риску развития ассоциированного с TTR заболевания.
В некоторых вариантах осуществления индивидуум представляет собой индивидуума, который несет мутацию гена TTR, которая ассоциирована с развитием ассоциированного с TTR заболевания.
В некоторых вариантах осуществления ассоциированное с TTR заболевание выбрано из группы, состоящей из старческого системного амилоидоза (SSA), системного семейного амилоидоза, семейной амилоидотической полинейропатии (FAP), семейной амилоидотической кардиомиопатии (FAC), лептоменингеального/амилоидоза центральной нервной системы (ЦНС) и гипертироксинемии.
В некоторых вариантах осуществления индивидуум страдает ассоциированным с TTR амилоидозом, и способ уменьшает отложение амилоидного TTR у индивидуума.
В некоторых вариантах осуществления средство для РНКи вводят индивидууму способом введения, выбранным из группы, состоящей из подкожного, внутривенного, внутримышечного, внутрибронхиального, интраплеврального, интраперитонеального, внутриартериального, лимфатического, цереброспинального и любых их комбинаций. В некоторых вариантах осуществления средство для РНКи вводят индивидууму путем подкожного или внутривенного введения. В предпочтительных вариантах осуществления средство для РНКи вводят индивидууму путем подкожного введения. В некоторых таких вариантах осуществления, подкожное введение включает введение посредством подкожного насоса или подкожного депо.
В некоторых вариантах осуществления средство для РНКи вводят индивидууму, таким образом, что средство для РНКи доставляют в конкретный участок у индивидуума. В некоторых таких вариантах осуществления участок выбран из группы, состоящей из печени, хориоидного сплетения, сетчатки и поджелудочной железы. В предпочтительных вариантах осуществления участок представляет собой печень. В некоторых вариантах осуществления доставка средства для РНКи опосредована асиалогликопротеиновым рецептором (ASGP-R), содержащимся в гепатоцитах.
В некоторых вариантах осуществления средство для РНКи вводят в дозе приблизительно от 0,25 мг/кг приблизительно до 50 мг/кг, например, приблизительно от 0,25 мг/кг приблизительно до 0,5 мг/кг, приблизительно от 0,25 мг/кг приблизительно до 1 мг/кг, приблизительно от 0,25 мг/кг приблизительно до 5 мг/кг, приблизительно от 0,25 мг/кг приблизительно до 10 мг/кг, приблизительно от 1 мг/кг приблизительно до 10 мг/кг, приблизительно от 5 мг/кг приблизительно до 15 мг/кг, приблизительно от 10 мг/кг приблизительно до 20 мг/кг, приблизительно от 15 мг/кг приблизительно до 25 мг/кг, приблизительно от 20 мг/кг приблизительно до 30 мг/кг, приблизительно от 25 мг/кг приблизительно до 35 мг/кг или приблизительно от 40 мг/кг приблизительно до 50 мг/кг.
В некоторых вариантах осуществления средство для РНКи вводят в дозе приблизительно 0,25 мг/кг, приблизительно 0,5 мг/кг, приблизительно 1 мг/кг, приблизительно 2 мг/кг, приблизительно 3 мг/кг, приблизительно 4 мг/кг, приблизительно 5 мг/кг, приблизительно 6 мг/кг, приблизительно 7 мг/кг, приблизительно 8 мг/кг, приблизительно 9 мг/кг, приблизительно 10 мг/кг, приблизительно 11 мг/кг, приблизительно 12 мг/кг, приблизительно 13 мг/кг, приблизительно 14 мг/кг, приблизительно 15 мг/кг, приблизительно 16 мг/кг, приблизительно 17 мг/кг, приблизительно 18 мг/кг, приблизительно 19 мг/кг, приблизительно 20 мг/кг, приблизительно 21 мг/кг, приблизительно 22 мг/кг, приблизительно 23 мг/кг, приблизительно 24 мг/кг, приблизительно 25 мг/кг, приблизительно 26 мг/кг, приблизительно 27 мг/кг, приблизительно 28 мг/кг, приблизительно 29 мг/кг, 30 мг/кг, приблизительно 31 мг/кг, приблизительно 32 мг/кг, приблизительно 33 мг/кг, приблизительно 34 мг/кг, приблизительно 35 мг/кг, приблизительно 36 мг/кг, приблизительно 37 мг/кг, приблизительно 38 мг/кг, приблизительно 39 мг/кг, приблизительно 40 мг/кг, приблизительно 41 мг/кг, приблизительно 42 мг/кг, приблизительно 43 мг/кг, приблизительно 44 мг/кг, приблизительно 45 мг/кг, приблизительно 46 мг/кг, приблизительно 47 мг/кг, приблизительно 48 мг/кг, приблизительно 49 мг/кг или приблизительно 50 мг/кг.
В некоторых вариантах осуществления средство для РНКи вводят в двух или более дозах. В конкретных вариантах осуществления средство для РНКи вводят в интервалах, выбранных из группы, состоящей из один раз каждые приблизительно 2 часа, один раз каждые приблизительно 3 часа, один раз каждые приблизительно 4 часа, один раз каждые приблизительно 6 часов, один раз каждые приблизительно 8 часов, один раз каждые приблизительно 12 часов, один раз каждые приблизительно 24 часа, один раз каждые приблизительно 48 часов, один раз каждые приблизительно 72 часа, один раз каждые приблизительно 96 часов, один раз каждые приблизительно 120 часов, один раз каждые приблизительно 144 часа, один раз каждые приблизительно 168 часов, один раз каждые приблизительно 240 часов, один раз каждые приблизительно 336 часов, один раз каждые приблизительно 504 часа, один раз каждые приблизительно 672 часа и один раз каждые приблизительно 720 часов.
В других вариантах осуществления способ дополнительно включает оценку уровня экспрессии мРНК TTR или экспрессии белка TTR в образце, получаемом у индивидуума.
В предпочтительных вариантах осуществления введение средства для РНКи не приводит к воспалительному ответу у индивидуума, как оценивают на основании уровня цитокина или хемокина, выбранного из группы, состоящей из G-CSF, IFN-γ IL-10, IL-12 (p70), IL1β, IL-1ra, IL-6, IL-8, IP-10, MCP-1, MIP-1α, MIP-1β, TNFα и любых их комбинаций, в образце у индивидуума.
В некоторых вариантах осуществления средство для РНКи вводят с использованием фармацевтической композиции, например, липосомы.
В некоторых вариантах осуществления средство для РНКи вводят в растворе. В некоторых таких вариантах осуществления миРНК вводят в незабуференном растворе. В одном из вариантов осуществления миРНК вводят в физиологическом растворе или воде. В других вариантах осуществления миРНК вводят в буферном растворе, таком как ацетатный буфер, цитратный буфер, буфер на основе проламинов, карбонатный буфер или фосфатный буфер, или любой их комбинации. В некоторых вариантах осуществления буферный раствор представляет собой фосфатно-солевой буфер (PBS).
В другом аспекте настоящее изобретение относится к способу ингибирования экспрессии транстиретина (TTR) в клетке, включающему приведение клетки в контакт со средством для РНКи, например, двухцепочечным средством для РНКи, в количестве, эффективном для ингибирования экспрессии TTR в клетке. В одном из аспектов двухцепочечное средство для РНКи выбирают из группы средств, перечисленных в таблице 1, таким образом, ингибируя экспрессию транстиретина (TTR) в клетке.
В другом аспекте настоящее изобретение относится к способу ингибирования экспрессии транстиретина (TTR) в клетке, включающему приведение клетки в контакт со средством для РНКи, например, двухцепочечным средством для РНКи, в количестве, эффективном для ингибирования экспрессии TTR в клетке. В одном из аспектов двухцепочечное средство для РНКи выбирают из группы, состоящей из AD-51544, AD-51545, AD-51546 и AD-51547, таким образом, ингибируя транстиретин (TTR) в клетке.
В дополнительном аспекте настоящее изобретение относится к способу лечения или профилактики ассоциированного с TTR заболевания у индивидуума, включающему введение индивидууму терапевтически эффективного количество или профилактически эффективного количества средства для РНКи, например, двухцепочечного средства для РНКи. В одном из аспектов двухцепочечное средство для РНКи выбирают из группы средств, перечисленных в таблице 1, таким образом, обеспечивая лечение или профилактику ассоциированного с TTR заболевания у индивидуума.
В еще одном аспекте настоящее изобретение относится к способу лечения или профилактики ассоциированного с TTR заболевания у индивидуума, включающему введение индивидууму терапевтически эффективного количества или профилактически эффективного количества средства для РНКи, например, двухцепочечного средства для РНКи. В одном из аспектов двухцепочечное средство для РНКи выбирают из группы, состоящей из AD-51544, AD-51545, AD-51546 и AD-51547, таким образом, обеспечения лечение или профилактику ассоциированного с TTR заболевания у индивидуума.
В дополнительных аспектах изобретение относится к наборам для проведения способов по изобретению. В одном из аспектов изобретение относится к набору для проведения способа ингибирования экспрессии транстиретина (TTR) в клетке, включающему приведение клетки в контакт со средством для РНКи, например, двухцепочечным средством для РНКи, в количестве, эффективном для ингибирования экспрессии указанного TTR в указанной клетке, таким образом, ингибируя экспрессию TTR в клетке. Набор содержит средство для РНКи и инструкции по применению и необязательно средство для введения средства для РНКи индивидууму.
Настоящее изобретение дополнительно проиллюстрировано следующим ниже подробным описанием и чертежами.
Краткое описание чертежей
Фигура 1 представляет собой график, отображающий введение мышам однократной подкожной дозы конъюгированного с GalNAc средства для РНКи, направленного на TTR, приводящее к дозозависимому подавлению мРНК TTR.
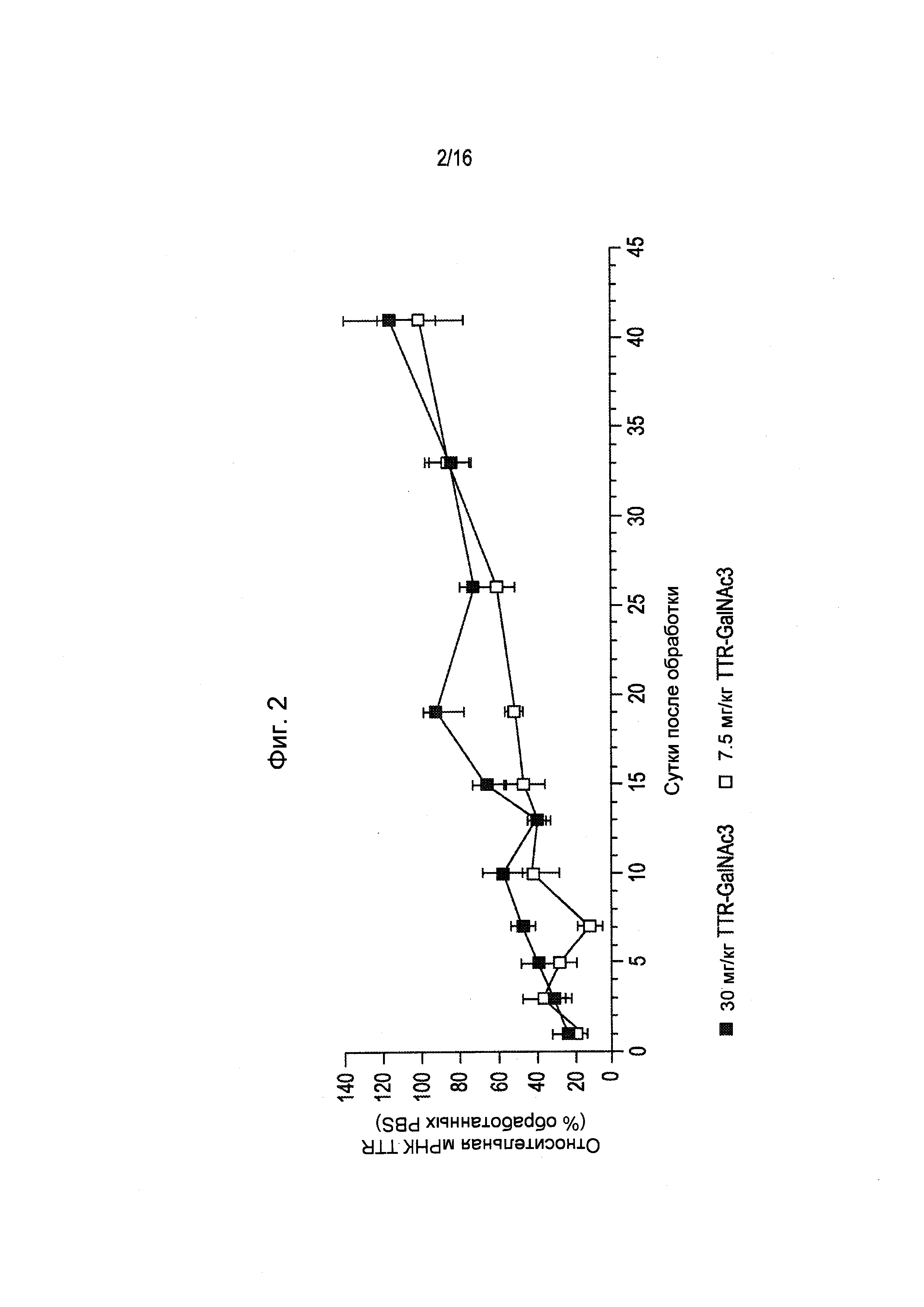
Фигура 2 представляет собой график, отображающий введение мышам однократной подкожной дозы 7,5 мг/кг или 30 мг/кг конъюгированного с GalNAc средства для РНКи, направленного на TTR, приводящее к длительному подавлению мРНК TTR.
На фигуре 3 представлена последовательность мРНК TTR человека.
Фигура 4 представляет собой график, отображающий улучшенную подавляющую активность средств для РНКи, модифицированных относительно исходного AD-45163.
Фигура 5 представляет собой график, отображающий улучшенную подавляющую активность средств для РНКи, модифицированных относительно исходного AD-45165.
Фигура 6 представляет собой график, отображающий улучшенное подавление в результате свободного поглощения после 4 часов инкубации со средствами для РНКи, модифицированными относительно исходного AD-45163.
Фигура 7 представляет собой график, отображающий улучшенное подавление в результате свободного поглощения после 24 часов инкубации со средствами для РНКи, модифицированными относительно исходного AD-45163.
Фигура 8 представляет собой график, отображающий улучшенное подавление в результате свободного поглощения после 4 часов инкубации со средствами для РНКи, модифицированными относительно исходного AD-45165.
Фигура 9 представляет собой график, отображающий улучшенное подавление в результате свободного поглощения после 24 часов инкубации со средствами для РНКи, модифицированными относительно исходного AD-45165.
Фигура 10 представляет собой график, отображающий подавление экспрессии мРНК TTR у трансгенных мышей, которые экспрессируют V30M hTTR после введения однократной подкожной дозы средств для РНКи AD-51544, AD-51545, AD-45163, AD-51546, AD-51547 или AD-45165.
Фигура 11 представляет собой график, отображающий подавление экспрессии белка TTR у трансгенных мышей, которые экспрессируют V30M hTTR после введения однократной подкожной дозы 5 мг/кг или 1 мг/кг средств для РНКи AD-51544, AD-51545 или AD-45163.
Фигура 12 представляет собой график, отображающий подавление экспрессии белка TTR у трансгенных мышей, которые экспрессируют V30M hTTR после введения однократной подкожной дозы 5 мг/кг или 1 мг/кг средств для РНКи AD-51546, AD-51547 или AD-45165.
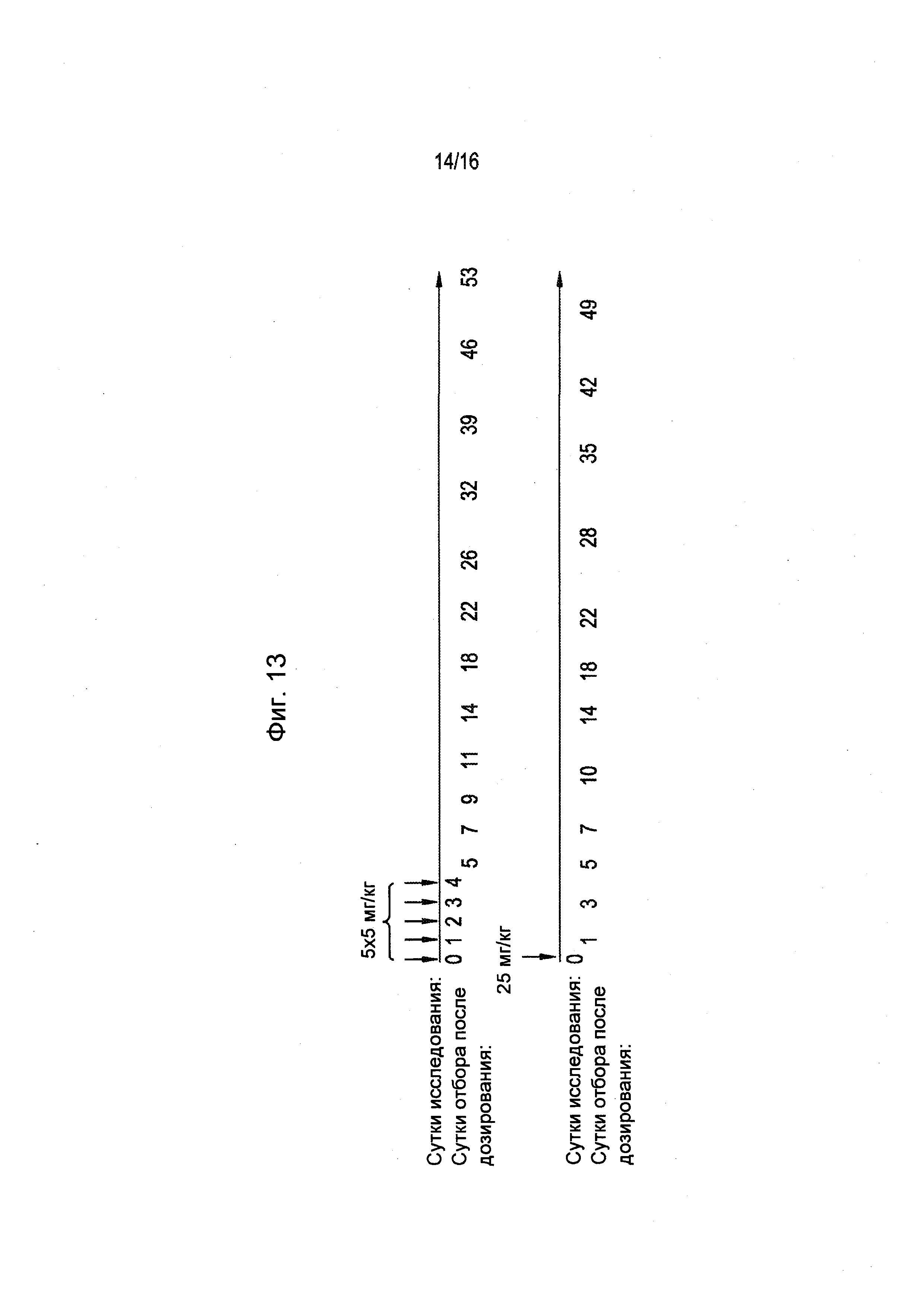
На фигуре 13 продемонстрирован протокол взятия крови после дозирования у обезьян, которые получали 5×5 мг/кг средства для РНКи (верхняя линия) или 1×25 мг/кг средства для РНКи (нижняя линия).
Фигура 14 представляет собой график, отображающий подавление экспрессии белка TTR у не являющихся человеком приматов после подкожного введения пяти доз 5 мг/кг (верхняя панель) или однократной дозы 25 мг/кг (нижняя панель) AD-45163, AD-51544, AD-51545, AD-51546 или AD-51547.
Фигура 15 представляет собой график, отображающий подавление экспрессии белка TTR у не являющихся человеком приматов после подкожного введения AD-51547 в дозе 2,5 мг/кг (белые квадраты), 5 мг/кг (черные квадраты) или 10 мг/кг (заштрихованные квадраты) или введения PBS в качестве отрицательного контроля (серые квадраты).
Подробное описание изобретения
Настоящее изобретение относится к средствам для РНКи, например, двухцепочечным средствам для РНКи, и композициям, направленным на ген транстиретина (TTR). Настоящее изобретение также относится к способам ингибирования экспрессии TTR и способам лечения или профилактики ассоциированного с TTR заболевания у индивидуума с использованием средств для РНКи по изобретению, например, двухцепочечных средств для РНКи. Настоящее изобретение по меньшей мере частично основано на открытии, что средства для РНКи, которые содержат конкретные химические модификации, обладают превосходной способностью ингибировать экспрессию TTR. В настоящем описании продемонстрировано, что средства, содержащие определенный паттерн химических модификаций (например, чередующийся паттерн) и лиганд, являются эффективными для подавления активности гена TTR. Кроме того, средства, содержащие один или более мотивов трех идентичных модификаций в трех последовательных нуклеотидах, содержащих один такой мотив на участке расщепления средств или около него, проявляют неожиданно повышенную активность подавления гена TTR. Когда в средстве содержится один такой химический мотив, предпочтительно он находится в области расщепления или около нее для повышения активности подавления гена. Область расщепления представляет собой область, окружающую участок расщепления, т.е. участок на мРНК-мишени, в котором происходит расщепление.
I. Определения
Как используют в настоящем описании, каждый из следующих ниже терминов имеет значение, ассоциированное со значением в этом разделе.
Термин "включая" используют в настоящем описании для обозначения и используют взаимозаменяемо с фразой "включая, но, не ограничиваясь ими".
Термин "или" используют в настоящем описании для обозначения и используют взаимозаменяемо с термином "и/или", если из контекста явное не следует иное.
Как используют в настоящем описании, "транстиретин" ("TTR") относится к хорошо известному гену и белку. TTR также известен как преальбумин, HsT2651, PALB и TBPA. TTR функционирует как транспортер ретинолсвязывающего белка (RBP), тироксина (T4) и ретинола, а также способен действовать как протеаза. Печень секретирует TTR в кровь, и хориоидное сплетение секретирует TTR в цереброспинальную жидкость. TTR также экспрессируется в поджелудочной железе и пигментном эпителии сетчатки. Наибольшее клиническое значение TTR заключается в том, что нормальный и мутантный белок TTR могут образовывать амилоидные фибриллы, которые агрегируют во внеклеточные отложения, вызывающие амилоидоз. Для обзора см., например, Saraiva M.J.M., (2002) Expert Reviews in Molecular Medicine, 4(12):1-11. Молекулярное клонирование и нуклеотидная последовательность транстиретина крысы, а также распределение экспрессии мРНК описаны Dickson P.W. et al., (1985) J. Biol. Chem., 260(13) 8214-8219. Рентгеновская кристаллическая структура TTR человека описана у Blake C.C. et al., (1974) J. Mol. Biol., 88, 1-12. Последовательность транскрипта мРНК TTR человека можно найти в National Center for Biotechnology Information (NCBI) номер доступа RefSeq NM_000371. Последовательность мРНК TTR мыши можно найти по номеру доступа RefSeq NM_013697.2, и последовательность мРНК TTR крысы можно найти по номеру доступа RefSeq NM_012681.1.
Как используют в настоящем описании, "последовательность-мишень" относится к смежному участку нуклеотидной последовательности молекулы мРНК, образуемой во время транскрипции гена TTR, включая мРНК, которая представляет собой продукт процессинга РНК продукта первичной транскрипции.
Как используют в настоящем описании, термин "цепь, содержащая последовательность" относится к олигонуклеотиду, содержащему цепь нуклеотидов, которая описана последовательностью, обозначаемой с использованием стандартной номенклатуры нуклеотидов.
"G", "C", "A" и "U", как правило, каждый обозначает нуклеотид, который содержит гуанин, цитозин, аденин и урацил в качестве основания соответственно. "T" и "dT" в настоящем описании используют взаимозаменяемо, и он означает дезоксирибонуклеотид, где нуклеиновое основание представляет собой тимин, например, дезоксириботимин, 2'-дезокситимидин или тимидин. Однако следует понимать, что термин "рибонуклеотид" или "нуклеотид", или "дезоксирибонуклеотид" также может обозначать модифицированный нуклеотид, как более подробно описано ниже, или группу заместителя-имитатора. Специалисту хорошо понятно, что гуанин, цитозин, аденин и урацил могут быть замещены другими группами по существу без изменения свойств спаривания оснований олигонуклеотида, содержащего нуклеотид, несущий такую группу заместителя. Например, без ограничения нуклеотид, содержащий инозин в качестве своего основания, может образовывать пару с нуклеотидами, содержащими аденин, цитозин или урацил. Таким образом, нуклеотиды, содержащие урацил, гуанин или аденин, могут быть заменены в нуклеотидных последовательностях по изобретению нуклеотидом, содержащим, например, инозин. Последовательности, содержащие такие группы заместителей, представляют собой варианты осуществления изобретения.
"Двухцепочечное средство для РНКи", двухцепочечная молекула РНК (дцРНК), также обозначаемая как "средство на основе дцРНК", "дцРНК", "миРНК", "средство на основе иРНК", как взаимозаменяемо используют в настоящем описании, относится к комплексу молекул рибонуклеиновой кислоты, обладающему дуплексной структурой, содержащей две антипараллельные и по существу комплементарные, как определено ниже, цепи нуклеиновой кислоты. Как правило, большая часть нуклеотидов, каждой цепи представляет собой рибонуклеотиды, но, как подробно описано в настоящем описании, каждая цепь или обе цепи также могут содержать один или более нерибонуклеотидов, например, дезоксирибонуклеотид и/или модифицированный нуклеотид. Кроме того, как используют в этом описании, "средство для РНКи" может содержать рибонуклеотиды с химическими модификациями; средство для РНКи может содержать существенные модификации во многих нуклеотидах. Такие модификации могут включать все типы модификаций, описываемых в настоящем описании или известные в данной области. Любые такие модификации, как используют в молекуле типа миРНК, входят в термин "средство для РНКи" для целей настоящего описания и формулы изобретения.
В другом варианте осуществления средство для РНКи может представлять собой одноцепочечную миРНК, которую вводят в клетку или организм для ингибирования мРНК-мишени. Одноцепочечные средства для РНКи связываются с Argonaute 2 RISC, обладающим эндонуклеазной активностью, который затем расщепляет мРНК-мишень. Одноцепочечная миРНК, как правило, содержит 15-30 нуклеотидов и является химически модифицированной. Конструирование и тестирование одноцепочечной миРНК описаны в патенте США №8101348 и у Lima et al., (2012) Cell, 150:883-894, таким образом, полное содержание каждого из которых включено в настоящее описание посредством ссылки. Любую из антисмысловых нуклеотидных последовательностей, описываемых в настоящем описании, можно использовать в качестве одноцепочечной миРНК, как описано в настоящем описании, или в качестве химически модифицированной способами, описанными у Lima et al., (2012) Cell, 150:883-894.
Два цепи, образующие дуплексную структуру, могут представлять собой различные участки одной более крупной молекулы РНК, или они могут представлять собой отдельные молекулы РНК. Когда две цепи представляют собой часть одной более крупной молекулы, и, таким образом, являются соединенными непрерывной цепью нуклеотидов между 3'-концом одной цепи и 5'-концом соответствующей другой цепи, образуя дуплексную структуру, соединяющую цепь РНК обозначают как "петля шпилька". Когда две структуры ковалентно связаны средством, отличным от непрерывной цепи нуклеотидов, между 3'-концом одной цепи и 5'-концом соответствующей другой цепи, образуя дуплексную структуру, соединительную структуру обозначают как "линкер". Цепи РНК могут содержать одинаковое или различное число нуклеотидов. Максимальное число пар оснований представляет собой число нуклеотидов в наиболее короткой цепи дцРНК минус любые выступающие нуклеотиды, которые содержатся в дуплексе. В дополнение к дуплексной структуре средство для РНКи может содержать один или более выступающих нуклеотидов. Термин "миРНК" в настоящем описании также используют для обозначения средства для РНКи, как описано выше.
В другом аспекте средство представляет собой одноцепочечную антисмысловую молекулу РНК. Антисмысловая молекула РНК является комплементарной последовательности в мРНК-мишени. Антисмысловая РНК может ингибировать трансляцию стехиометрическим образом путем спаривания оснований с мРНК и физического препятствия механизму трансляции, см. Dias N. et al., (2002) Mol. Cancer Ther., 1:347-355. Антисмысловая молекула РНК может содержать приблизительно 15-30 нуклеотидов, которые являются комплементарными мРНК-мишени. Например, антисмысловая молекула РНК может содержать последовательность из по меньшей мере 15, 16, 17, 18, 19, 20 или более смежных нуклеотидов из одной из антисмысловых последовательностей из таблицы 1.
Как используют в настоящем описании, "выступающий нуклеотид" относится к неспаренному нуклеотиду или нуклеотидам, которые выступают из дуплексной структуры средства для РНКи, когда 3'-конец одной цепи средства для РНКи выступают за 5'-конец другой цепи или наоборот. "Тупой" или "тупой конец" означает, что не содержится неспаренных нуклеотидов на конце двухцепочечного средства для РНКи, т.е. не содержится выступающих нуклеотидов. Средство для РНКи с "тупыми концами" представляет собой дцРНК, которая является двухцепочечной на всем протяжении длины, т.е. не содержит нуклеотидов, выступающих на любом конце молекулы. Средства для РНКи по изобретению включают средства для РНКи, где нуклеотид выступает на одном конце (т.е. средства с одним липким и одним тупым концом), или нуклеотидом выступает на обоих концах.
Термин "антисмысловая цепь" относится к цепи двухцепочечного средства для РНКи, которая содержит область, которая по существу является комплементарной последовательности-мишени (например, мРНК TTR человека). Как используют в настоящем описании, термин "область, комплементарная участку мРНК, кодирующей транстиретин" относится к области в антисмысловой цепи, которая по существу является комплементарной участку последовательности мРНК TTR. Когда область комплементарности не является полностью комплементарной последовательности-мишени, несоответствия являются наиболее допустимыми в концевых областях и при наличии, как правило, находятся в концевой области или областях, например, в 6, 5, 4, 3 или 2 нуклеотидах 5'- и/или 3'-конца.
Термин "смысловая цепь", как используют в настоящем описании, относится к стандартной дцРНК, которая содержит область, которая является по существу комплементарной области антисмысловой цепи.
Как используют в настоящем описании, термин "область расщепления" относится к области, которая располагается непосредственно вблизи участка расщепления. Участок расщепления представляет собой участок в мишени, в котором происходит расщепление. В некоторых вариантах осуществления область расщепления содержит три основания на конце и непосредственно вблизи участка расщепления. В некоторых вариантах осуществления область расщепления содержит два основания на конце и непосредственно вблизи участка расщепления. В некоторых вариантах осуществления участок расщепления конкретно располагается на участке, связанном нуклеотидами 10 и 11 антисмысловой цепи, и область расщепления содержит нуклеотиды 11, 12 и 13.
Как используют в настоящем описании, и если не указано иное, термин "комплементарный", когда используют для описания первой нуклеотидной последовательности относительно второй нуклеотидной последовательности, относится к способности олигонуклеотида или полинуклеотида, содержащего первую нуклеотидную последовательность, гибридизоваться и образовывать дуплексную структуру в определенных условиях с олигонуклеотидом или полинуклеотидом, содержащим вторую нуклеотидную последовательность, как будет понятно специалисту. Такие условия могут, например, представлять собой жесткие условия, где жесткие условия могут включать: 400 мМ NaCl, 40 мМ PIPES pH 6,4, 1 мМ EDTA, 50°C или 70°C в течение 12-16 часов с последующим промыванием. Можно применять другие условия, такие как соответствующие физиологическим условия, как могут встречаться внутри организма. Специалист может определять набор условий, наиболее подходящих для тестирования комплементарности двух последовательностей в соответствии с конечным применением гибридизуемых нуклеотидов.
Последовательности могут являться "полностью комплементарными" по отношению друг к другу, когда происходит спаривание оснований нуклеотидов первой нуклеотидной последовательности с нуклеотидами второй нуклеотидной последовательности на всем протяжении длины первой и второй нуклеотидных последовательностях. Однако в случае, когда первую последовательность обозначают как "по существу комплементарная" по отношению ко второй последовательности в настоящем описании, две последовательности могут являться полностью комплементарными, или они могут образовывать одну или более, но, как правило, не более 4, 3 или 2 несовпадающих пар оснований при гибридизации, при этом сохраняя способность гибридизоваться в условиях, наиболее соответствующих их конечному применению. Однако когда два олигонуклеотида конструируют с возможностью образовывать при гибридизации один или более одноцепочечных липких концов, такие липкие концы не следует рассматривать как несоответствия в отношении определения комплементарности. Например, дцРНК, содержащая один олигонуклеотид длиной 21 нуклеотид и другой олигонуклеотид длиной 23 нуклеотида, где наиболее длинный олигонуклеотид содержит последовательность из 21 нуклеотида, которая является полностью комплементарной более короткому олигонуклеотиду, также можно обозначать как обозначаемый как "полностью комплементарная" для целей, описываемых в настоящем описании.
"Комплементарные" последовательности, как используют в настоящем описании, также могут содержать или являться полностью образованными парами оснований, не относящихся к типу Уотсона-Крика, и/или парами оснований, образованными из неприродных и модифицированных нуклеотидов, при условии, что выполняются указанные выше требования в отношении их способности гибридизоваться. Такие пары оснований, не относящиеся к типу Уотсона-Крика, включают, но не ограничиваются ими, неоднозначное G:U или Хугстиновское спаривание оснований.
Термины "комплементарная", "полностью комплементарная" и "по существу комплементарная" в настоящем описании можно использовать в отношении совпадения пар оснований смысловой цепи и антисмысловой цепи дцРНК или антисмысловой цепи дцРНК и последовательности-мишени, как будет понятно из контекста, в котором их используют.
Как используют в настоящем описании, полинуклеотид, который является "по существу комплементарный по меньшей мере части" матричной РНК (мРНК) относится к полинуклеотиду, который является по существу комплементарным смежному участку представляющей интерес мРНК (например, мРНК, кодирующей TTR), включая 5'-UTR, открытую рамку считывания (ORF) или 3'-UTR. Например, полинуклеотид является комплементарным по меньшей мере части TTR мРНК, если последовательность является по существу комплементарный непрерывному участку мРНК, кодирующей TTR.
Термин "ингибирование", как используют в настоящем описании, используют взаимозаменяемо с "уменьшением", "подавлением", "снижением", "ослаблением" и другими аналогичными терминами, и он включает любой уровень ингибирования.
Фраза "ингибирование экспрессии TTR", как используют в настоящем описании, включает ингибирование экспрессии любого гена TTR (такого как, например, гена TTR мыши, гена TTR крысы, гена TTR обезьяны или гена TTR человека), а также вариантов или мутантов гена TTR. Таким образом, ген TTR может представлять собой ген TTR дикого типа, мутантный ген TTR (такой как, мутантный ген TTR, приводящий к образованию системного отложения амилоида) или трансгенный ген TTR по отношению к клеткам, группе клеток или организму, которых подвергали генетической манипуляции.
"Ингибирование экспрессии гена TTR" включает любой уровень ингибирования гена TTR, например, по меньшей мере частичное подавление экспрессии гена TTR, такое как ингибирование по меньшей мере приблизительно на 5%, по меньшей мере приблизительно на 10%, по меньшей мере приблизительно на 15%, по меньшей мере приблизительно на 20%, по меньшей мере приблизительно на 25%, по меньшей мере приблизительно на 30%, по меньшей мере приблизительно на 35%, по меньшей мере приблизительно на 40%, по меньшей мере приблизительно на 45%, по меньшей мере приблизительно на 50%, по меньшей мере приблизительно на 55%, по меньшей мере приблизительно на 60%, по меньшей мере приблизительно на 65%, по меньшей мере приблизительно на 70%, по меньшей мере приблизительно на 75%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 91%, по меньшей мере приблизительно на 92%, по меньшей мере приблизительно на 93%, по меньшей мере приблизительно на 94%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98% или по меньшей мере приблизительно на 99%.
Экспрессию гена TTR можно оценивать на основании уровня любой переменной, ассоциированной с экспрессией гена TTR, например, уровнем мРНК TTR, уровнем белка TTR, уровнем ретинолсвязывающего белка, уровнем витамина A или числом или степенью отложений амилоида. Ингибирование можно оценивать по снижению абсолютного или относительного уровня одной или более таких переменных по сравнению с контрольным уровнем. Контрольный уровень может представлять собой любой тип контрольного уровня, который используют в данной области, например, исходный уровень до дозирования или уровень, определяемый у такого же индивидуума, в клетке или в образце, которые не подвергали обработке или обрабатывали контролем (таким как, например, только контроль буфером или контроль неактивным средством).
Фраза "приведение клетки в контакт со средством для РНКи", как используют в настоящем описании, включает приведение клетки в контакт любым возможным способом. Приведение клетки в контакт со средством для РНКи, например, двухцепочечным средством для РНКи, включает приведение клетки в контакт in vitro со средством для РНКи или приведение клетки в контакт in vivo со средством для РНКи. Приведение в контакт можно проводить прямо или опосредованно. Таким образом, например, средство для РНКи можно приводить в физический контакт с клеткой отдельно проводимым способом или, альтернативно, для средства для РНКи можно создавать ситуацию, которая обеспечивает или вызывает в дальнейшем его контактирование с клеткой.
Приведение клетки в контакт in vitro можно проводить, например, путем инкубации клеток со средством для РНКи. Приведение клетки в контакт in vivo можно проводить, например, путем инъекционного введения средства для РНКи в ткань или около нее, где локализована клетка, или путем инъекционного введения средства для РНКи в другую область, например, кровоток или подкожное пространство, таким образом, что средство затем попадает в ткань, где локализована клетка, которую необходимо подвергать контактированию. Например, средство для РНКи может содержать и/или являться сопряженным с лигандом, например, лигандом GalNAc3, который направляет средство для РНКи в представляющий интерес участок, например, печень. Также возможными являются комбинации способов in vitro и in vivo. В отношении способов по изобретению клетку также можно приводить в контакт in vitro со средством для РНКи, а затем трансплантировать индивидууму.
"Пациент" или "индивидуум", как используют в настоящем описании, предназначен включать человека или не являющееся человеком животное, предпочтительно млекопитающее, например, обезьяну. Наиболее предпочтительно индивидуум или пациент представляет собой человека.
"Ассоциированное с TTR заболевание", как используют в настоящем описании, предназначено включать любое заболевание, ассоциированное с геном TTR или белком. Такое заболевание может быть вызвано, например, избытком продукции белка TTR, мутацией гена TTR, аномальным расщеплением белка TTR, аномальным взаимодействием между TTR и другими белками или другими эндогенными или экзогенными веществами. "Ассоциированное с TTR заболевание" включает любой тип TTR амилоидоза (ATTR), где TTR играет основою роль в образовании аномальных внеклеточных агрегатов или отложений амилоида. Ассоциированные с TTR заболевания включают старческий системный амилоидоз (SSA), системный семейный амилоидоз, семейную амилоидотическую полинейропатию (FAP), семейную амилоидотическую кардиомиопатию (FAC), лептоменингеальный/амилоидоз центральной нервной системы (ЦНС), амилоидотическое помутнения стекловидного тела, синдром запястного канала и гипертироксинемию. Симптомы TTR амилоидоза включают сенсорную нейропатия (например, парестезию, гипестезию в дистальных конечностях), вегетативную нейропатию (например, нарушение желудочно-кишечной функции, такое как язва желудка, или ортостатическую гипотензию), моторную нейропатию, судороги, деменцию, миелопатию, полинейропатию, синдром запястного канала, вегетативную недостаточность, кардиомиопатию, помутнения стекловидного тела, почечную недостаточность, нефропатию, значительно сниженный mBMI (модифицированный индекс массы тела), нарушение функции черепно-мозгового нерва и решетчатую дегенерацию роговицы.
"Терапевтически эффективное количество", как используют в настоящем описании, предназначено включать количество средства для РНКи, которое при введении пациенту для лечения ассоциированного с TTR заболевания, является достаточным для обеспечения лечения заболевания (например, путем ослабления, улучшения состояния или поддержания существующего заболевание или одного или более симптомов заболевания). "Терапевтически эффективное количество" может изменяться в зависимости от средства для РНКи, того как вводят средство, заболевания и его тяжести и истории, возраста, массы, семейного анамнеза, набора генов, стадии патологического процесса, опосредованного экспрессией TTR, типов предшествовавших или сопутствующих видов лечения при наличии и других индивидуальных характеристик подлежащего лечению пациента.
"Профилактически эффективное количество", как используют в настоящем описании, предназначено включать количество средства для РНКи, которое при введении индивидууму, который еще не испытывает, или у которого не выявляют симптомы ассоциированное с TTR заболевания, но который может быть предрасположен к заболеванию, является достаточным для профилактики или улучшения состояния заболевание или одного или более симптомов заболевания. Симптомы, которые можно улучшать, включают сенсорную нейропатию (например, парестезию, гипестезию в дистальных конечностях), вегетативную нейропатию (например, нарушение желудочно-кишечной функции, такое как язва желудка, или ортостатическую гипотензию), моторную нейропатию, судороги, деменцию, миелопатию, полинейропатию, синдром запястного канала, вегетативную недостаточность, кардиомиопатию, помутнения стекловидного тела, почечную недостаточность, нефропатию, значительное снижение mBMI (модифицированного индекса массы тела), нарушение функции черепно-мозгового нерва и решетчатую дегенерацию роговицы. Улучшение состояния заболевание включает замедление течения заболевания или снижение тяжести развивающегося позднее заболевания. "Профилактически эффективное количество" может изменяться в зависимости от средства для РНКи, того как вводят средство, степени риска заболевания и истории, возраста, массы, семейного анамнеза, набора генов, типов предшествовавших или сопутствующих видов лечения при наличии и других индивидуальных характеристик подлежащего лечению пациента.
"Терапевтически-эффективное количество" или "профилактически эффективное количество" также включает количество средства для РНКи, которое оказывает некоторое желаемое местное или системное действие при обоснованном отношении риск/польза, применимом для любого лечения. Средства для РНКи, применяемые в способах по настоящему изобретению, можно вводить в достаточном количестве для обеспечения обоснованного отношения риск/польза, применимого для такого лечения.
Термин "образец", как используют в настоящем описании, включает набор аналогичных жидкостей, клеток или тканей, получаемых у индивидуума, а также жидкости, клетки или ткани, содержащиеся у индивидуума. Примеры биологических жидкостей включают кровь, сыворотку и серозные жидкости, плазму, цереброспинальную жидкость, внутриглазные жидкости, лимфу, мочу, слюну и т.п. Ткань образцов может включать образцы из тканей, органов или локализованных областей. Например, образцы можно получать из конкретных органов, частей органов или жидкостей, или клеток в таких органах. В определенных вариантах осуществления образцы можно получать из печени (например, целой печени или определенных сегментов печени, или определенных типов клеток в печени, таких как, например, гепатоциты), сетчатки или частей сетчатки (например, пигментного эпителия сетчатки), центральной нервной системы или отделов центральной нервной системы (например, желудочков или хориоидного сплетения) или поджелудочной железы или определенных типов клеток или частей поджелудочной железы. В некоторых вариантах осуществления "образец, получаемый у индивидуума" относится к цереброспинальной жидкости, получаемой у индивидуума. В предпочтительных вариантах осуществления "образец, получаемый у индивидуума" относится к крови или плазме, получаемой у индивидуума. В дополнительных вариантах осуществления "образец, получаемый у индивидуума" относится к ткани печени (или ее подкомпонентам) или ткани сетчатки (или ее подкомпонентам), получаемым у индивидуума.
II. Средства для РНКи
Настоящее изобретение относится к средствам для РНКи с превосходной активность подавления экспрессии гена. В настоящем описании и во временной заявке на патент №61/561710 (на основании которой по настоящей заявке испрашивается приоритет) продемонстрировано, что превосходный результат можно получать посредством введения одного или более мотивов трех идентичных модификаций в три последовательных нуклеотида в смысловой цепи и/или антисмысловой цепи средства для РНКи, в частности в участок расщепления или около него. Смысловую цепь и антисмысловую цепь средства для РНКи можно иным образом полностью модифицировать. Введение таких мотивов нарушает паттерны модификации, при их наличии, смысловой и/или антисмысловой цепи. Средство для РНКи также необязательно конъюгировано с лигандом производного GalNAc, например, в смысловой цепи. Получаемые средства для РНКи обладают превосходной подавляющей экспрессию гена активностью.
Авторы изобретения неожиданно обнаружили, что когда смысловую цепь и антисмысловую цепь средства для РНКи полностью модифицируют, так чтобы она содержала один или более мотивов трех идентичных модификаций в трех последовательных нуклеотидах в участке расщепления или около него по меньшей мере одной цепи средства для РНКи, значительно повышается активность подавления экспрессии гена средства для РНКи.
Таким образом, изобретение относится к средствам для РНКи, например, двухцепочечным средствам для РНКи, способным ингибировать экспрессию гена-мишени (т.е. гена TTR) in vivo. Средство для РНКи содержит смысловую цепь и антисмысловую цепь. Длина каждой цепи средства для РНКи может находиться в диапазоне 12-30 нуклеотидов. Например, длина каждой цепи может составлять 14-30 нуклеотидов, 17-30 нуклеотидов, 25-30 нуклеотидов, 27-30 нуклеотидов, 17-23 нуклеотида, 17-21 нуклеотид, 17-19 нуклеотидов, 19-25 нуклеотидов, 19-23 нуклеотида, 19-21 нуклеотид, 21-25 нуклеотидов или 21-23 нуклеотида.
Смысловая цепь и антисмысловая цепь, как правило, образуют дуплексную двухцепочечную РНК ("дцРНК"), также обозначаемую в настоящем описании как "средство для РНКи". Длина дуплексной области средства для РНКи может составлять 12-30 пар нуклеотидов. Например, длина дуплексной области может составлять 14-30 пар нуклеотидов, 17-30 пар нуклеотидов, 27-30 пар нуклеотидов, 17-23 пары нуклеотидов, 17-21 пару нуклеотидов, 17-19 пар нуклеотидов, 19-25 пар нуклеотидов, 19-23 пары нуклеотидов, 19-21 пару нуклеотидов, 21-25 пар нуклеотидов или 21-23 пары нуклеотидов. В другом примере дуплексная область выбрана из 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26 и 27.
В одном из вариантов осуществления средство для РНКи может содержать одну или более областей липких концов и/или копирующих групп средства для РНКи на 3'-конце или 5'-конце, или на обоих концах цепи. Липкий конец может составлять 1-6 нуклеотидов, например, 2-6 нуклеотидов, 1-5 нуклеотидов, 2-5 нуклеотидов, 1-4 нуклеотида, 2-4 нуклеотида, 1-3 нуклеотида, 2-3 нуклеотида или 1-2 нуклеотида. Липкие концы могут являться результатом того, что одна цепь является длиннее другой, или результатом того, что две цепи одинаковой длины подвергают ступенчатому разрыву. Липкий конец может образовывать несоответствие с мРНК-мишенью, или он может являться комплементарным последовательностям гена для направленного воздействия или может представлять собой другую последовательность. Первую и вторую цепи также можно соединять, например, посредством дополнительных оснований с образованием шпильки, или посредством других не являющихся основанием линкеров.
Средства для РНКи, предоставленные настоящим изобретением, включают средства с химическими модификациями, как описано, например, во временной заявке США №61/561710, поданной 18 ноября 2011 года, международной заявке № PCT/US 2011/051597, поданной 15 сентября 2010 года, и публикации PCT WO 2009/073809, полное содержание каждой из которых включено в настоящее описание посредством ссылки.
В одном из вариантов осуществления каждый нуклеотид в выступающей области средства для РНКи может независимо представлять собой модифицированный или немодифицированный нуклеотид, включая, но, не ограничиваясь ими, модифицированный 2'-сахар, такой как, 2-F, 2'-O-метил, тимидин (T), 2'-O-метоксиэтил-5-метилуридин (Teo), 2'-O-метоксиэтиладенозин (Aeo), 2'-O-метоксиэтил-5-метилцитидин (m5Ceo) или любые их комбинации. Например, TT может представлять собой последовательность липкого конца для любого конца любой цепи. Липкий конец может образовывать несоответствие мРНК-мишени, или он может являться комплементарным последовательностям гена для направленного воздействия или может представлять собой другую последовательность.
5'- или 3'-липкие концы в смысловой цепи, антисмысловой цепи или обеих цепях средства для РНКи могут быть фосфорилированными. В некоторых вариантах осуществления область липких концов содержит два нуклеотида, содержащих тиофосфат между двумя нуклеотидами, где два нуклеотиды могут являться одинаковыми или различными. В одном из вариантов осуществления липкий конец находится на 3'-конце смысловой цепи, антисмысловой цепи или обеих цепях. В одном из вариантов осуществления такой 3'-липкий конец содержится в антисмысловой цепи. В одном из вариантов осуществления такой 3'-липкий конец содержится в смысловой цепи.
Средство для РНКи может содержать только один липкий конец, который может повышать активность интерференции РНКи, не влияя на ее общую стабильность. Например, одноцепочечный липкий конец располагается на 3'-конце смысловой цепи или, альтернативно, на 3'-конце антисмысловой цепи. РНКи может также содержать тупой конец, расположенный на 5'-конце антисмысловой цепи (или 3'-конце смысловой цепи) или наоборот. Как правило, антисмысловая цепь РНКи содержит выступающий нуклеотид на 3'-конце, и 5'-конец является тупым. Несмотря на то, что заявители не связаны теорией, теоретический механизм заключается в том, что асимметричный тупой конец на 5'-конце антисмысловой цепи и 3'-липкий конец антисмысловой цепи способствуют тому, что направляющая цепь подвергается процессу RISC.
В одном из вариантов осуществления средство для РНКи представляет собой олигонуклеотид с двумя тупыми концами длиной 19 нуклеотидов, где смысловая цепь содержит по меньшей мере один мотив из трех 2'-F-модификаций в трех последовательных нуклеотидах в положениях 7, 8, 9 от 5'-конца. Антисмысловая цепь содержит по меньшей мере один мотив из трех 2'-O-метил-модификаций в трех последовательных нуклеотидах в положениях 11, 12, 13 от 5'-конца.
В одном из вариантов осуществления средство для РНКи представляет собой олигонуклеотид с двумя тупыми концами длиной 20 нуклеотидов, где смысловая цепь содержит по меньшей мере один мотив их трех 2'-F-модификаций в трех последовательных нуклеотидах в положениях 8, 9, 10 от 5'-конца. Антисмысловая цепь содержит по меньшей мере один мотив из трех 2'-O-метил-модификаций в трех последовательных нуклеотидах в положениях 11, 12, 13 от 5'-конца.
В одном из вариантов осуществления средство для РНКи представляет собой олигонуклеотид с двумя тупыми концами длиной 21 нуклеотид, где смысловая цепь содержит по меньшей мере один мотив из трех 2'-F-модификаций в трех последовательных нуклеотидах в положениях 9, 10, 11 от 5'-конца. Антисмысловая цепь содержит по меньшей мере один мотив из три 2'-O-метил-модификаций в трех последовательных нуклеотидах в положениях 11, 12, 13 от 5'-конца.
В одном из вариантов осуществления средство для РНКи содержит смысловую цепь длиной 21 нуклеотид (nt) и антисмысловую цепь длиной 23 нуклеотида (nt), где смысловая цепь содержит по меньшей мере один мотив из трех 2'-F модификаций в трех последовательных нуклеотидах в положениях 9, 10, 11 от 5'-конца; антисмысловая цепь содержит по меньшей мере один мотив из трех 2'-O-метил-модификаций в трех последовательных нуклеотидах в положениях 11, 12, 13 от 5'-конца, где один конец средства для РНКи является тупым, в то время как другой конец содержит липкий конец с 2 нуклеотидами. Предпочтительно липкий конец с 2 нуклеотидами находится на 3'-конце антисмысловой цепи. Необязательно средство для РНКи дополнительно содержит лиганд (предпочтительно GalNAC3).
В одном из вариантов осуществления средство для РНКи содержит смысловую и антисмысловую цепь, где длина смысловой цепе составляет 25-30 нуклеотидных остатков, где начиная от положений от 1 до 23 5'-концевого нуклеотида (положение 1) первой цепи, содержится по меньшей мере 8 рибонуклеотидов; длина антисмысловой цепи составляет 36-66 нуклеотидных остатка и, начиная от 3'-концевого нуклеотида, содержит по меньшей мере 8 рибонуклеотидов в положениях, спаренных с положениями 1-23 смысловой цепи с образованием дуплекса; где по меньшей мере 3'-концевой нуклеотид антисмысловой цепи является неспаренным с со смысловой цепью, и до 6 последовательных 3'-концевых нуклеотида являются неспаренными со смысловой цепью, таким образом, образуя одноцепочечный 3'-липкий конец из 1-6 нуклеотидов; где 5'-конец антисмысловой цепи содержит 10-30 последовательных нуклеотидов, которые являются неспаренными со смысловой цепью, таким образом, образуя одноцепочечный 5'-липкий конец длиной 10-30 нуклеотидов; где по меньшей мере 5'-концевые и 3'-концевые нуклеотиды смысловой цепи являются спаренными с нуклеотидами антисмысловой цепи, где смысловая и антисмысловая цепи являются выровненными для максимальной комплементарности, таким образом, образуя по существу дуплексную область между смысловой и антисмысловой цепями; и антисмысловая цепь является достаточно комплементарной РНК-мишени на протяжении по меньшей мере 19 рибонуклеотидов антисмысловой цепи для снижения экспрессии гена-мишени, когда двухцепочечную нуклеиновую кислоту вводят в клетку млекопитающего; и где смысловая цепь содержит по меньшей мере один мотив из трех 2'-F-модификаций в трех последовательных нуклеотидах, где по меньшей мере один из мотивов располагается в участке расщепления или около него. Антисмысловая цепь содержит по меньшей мере один мотив из трех 2'-O-метил-модификаций в трех последовательных нуклеотидах в участке расщепления или около него.
В одном из вариантов осуществления средство для РНКи содержит смысловую и антисмысловую цепи, где средство для РНКи содержит первую цепь, длина которой составляет по меньшей мере 25 и не более 29 нуклеотидов, и вторую цепь, длина, которой составляет не более 30 нуклеотидов, с по меньшей мере одним мотивов из трех 2'-O-метил-модификаций в трех последовательных нуклеотидах в положении 11, 12, 13 от 5'-конца; где 3'-конец первой цепи и 5'-конец второй цепи образуют тупой конец, и вторая цепь является на 1-4 нуклеотида длиннее на своем 3'-конце чем первая цепь, где дуплексная область, длина которой составляет по меньшей мере 25 нуклеотидов, и вторая цепь являются достаточно комплементарными мРНК-мишени на протяжении по меньшей мере 19 нуклеотидов второй цепи для снижения экспрессии гена-мишени, когда средство для РНКи вводят в клетку млекопитающего, и где расщепление ферментом Dicer средства для РНКи предпочтительно приводит к миРНК, содержащей 3'-конец второй цепи, таким образом, снижая экспрессию гена-мишени у млекопитающего. Необязательно средство для РНКи дополнительно содержит лиганд.
В одном из вариантов осуществления смысловая цепь средства для РНКи содержит по меньшей мере один мотив из трех идентичных модификаций в трех последовательных нуклеотидах, где один из мотивов располагается в участке расщепления в смысловой цепи.
В одном из вариантов осуществления антисмысловая цепь средства для РНКи также может содержать по меньшей мере один из мотив их трех идентичных модификаций в трех последовательных нуклеотидах, где один из мотивов располагается в участке расщепления или около него в антисмысловой цепи.
Для средства для РНКи, содержащего дуплексную область длиной 17-23 нуклеотидов, участок расщепления антисмысловой цепи, как правило, располагается вокруг положений 10, 11 и 12 от 5'-конца. Таким образом, мотивы из трех идентичных модификаций могут располагаться в положениях 9, 10, 11; положениях 10, 11, 12; положениях 11, 12, 13; положениях 12, 13, 14 или положениях 13, 14, 15 антисмысловой цепи, где нумерация начинается от 1-го нуклеотида 5'-конца антисмысловой цепи, или нумерация начинается от 1-го спаренного нуклеотида в дуплексной области от 5'-конца антисмысловой цепи. Участок расщепления в антисмысловой цепи также может изменяться в зависимости от длины дуплексной области РНКи от 5'-конца.
Смысловая цепь средства для РНКи может содержать по меньшей мере один мотив из трех идентичных модификаций в трех последовательных нуклеотидах в участке расщепления цепи, и антисмысловая цепь может содержать по меньшей мере один мотив из трех идентичных модификаций в трех последовательных нуклеотидах в участке расщепления цепи или около него. Когда смысловая цепь и антисмысловая цепь образуют дуплекс дцРНК, смысловая цепь и антисмысловая цепь могут быть выровнены таким образом, что один мотив из трех нуклеотидов в смысловой цепи и один мотив из трех нуклеотидов в антисмысловой цепи содержат по меньшей мере одно перекрытие нуклеотидов, т.е. по меньшей мере один из трех нуклеотидов мотива в смысловой цепи образует комплементарную пару оснований по меньшей мере с одним из трех нуклеотидов мотива в антисмысловой цепи. Альтернативно, могут перекрываться по меньшей мере два нуклеотиды, или все три нуклеотида могут перекрываться.
В одном из вариантов осуществления смысловая цепь средства для РНКи может содержать более одного мотива из трех идентичных модификаций в трех последовательных нуклеотидах. Первый мотив должен располагаться в участке расщепления или около него цепи, и другие мотивы могут представлять собой крыльевые модификации. Термин "крыльевая модификация" в настоящем описании относится к мотиву, располагающемуся на другом участке цепи, который является отделенным от мотива в участке расщепления или около него той же самой цепи. Крыльевая модификация примыкает к первому мотиву или отделена от него по меньшей мере одним или более нуклеотидами. Когда мотивы являются непосредственно примыкающими друг к другу, то химическая структура мотивов отличается друг от друга, и когда мотивы разделены одним или более нуклеотидами, то химические структуры могут быть одинаковыми или различными. Могут присутствовать две или более крыльевых модификаций. Например, когда содержатся две крыльевые модификации, каждая крыльевая модификация может располагаться на одном конце относительно первого мотива, который располагается в участке расщепления или около него, или на любой стороне лидерного мотива.
Аналогично смысловой цепи антисмысловая цепь средства для РНКи может содержать по меньшей мере два мотива из трех идентичных модификаций в трех последовательных нуклеотидах, где по меньшей мере один из мотивов располагается в участке расщепления или около него цепи. Такая антисмысловая цепь также может содержать одну или более крыльевых модификаций в выравнивании, аналогичном крыльевым модификациям, которые содержатся в смысловой цепи.
В одном из вариантов осуществления крыльевая модификация в смысловой цепи или антисмысловой цепи средства для РНКи, как правило, не включает первый один или два концевых нуклеотида на 3'-конце, 5'-конце или обоих концах цепи.
В другом варианте осуществления крыльевая модификация в смысловой цепи или антисмысловой цепи средства для РНКи, как правило, не включает первый один или два спаренных нуклеотида в дуплексной области на 3'-конце, 5'-конце или обоих концах цепи.
Когда смысловая цепь и антисмысловая цепь средства для РНКи содержат по меньшей мере одну крыльевую модификацию, крыльевые модификации могут находиться на одном и том же конце дуплексной области и содержать перекрывание одного, двух или трех нуклеотидов.
Когда смысловая цепь и антисмысловая цепь средства для РНКи содержат по меньшей мере две крыльевые модификации, смысловая цепь и антисмысловая цепь могут являться выровненными таким образом, что две модификации, каждая из одной цепи, находятся на одном конце дуплексной области с перекрыванием одного, двух или трех нуклеотидов; две модификации, каждая из одной цепи, находятся на другом конце дуплексной области с перекрыванием одного, двух или трех нуклеотидов; две модификации одной цепи находятся на каждой стороне лидерного мотива с перекрыванием одного, двух или трех нуклеотидов в дуплексной области.
В одном из вариантов осуществления можно модифицировать каждый нуклеотид в смысловой цепи и антисмысловой цепи средства для РНКи, включая нуклеотиды, которые являются частью мотивов. Каждый нуклеотид можно модифицировать одинаковыми или различными модификациями, которые могут включать одно или более изменений одного или обоих не образующих связей кислородов фосфатов и/или одного или более образующих связи кислородов фосфатов; изменение компонента сахара рибозы, например, 2'-гидроксила в сахаре рибозы; полную замену фосфатной группы "дефосфо"-линкерами; модификацию или замену природного основания и замену или модификацию рибоза-фосфатного остова.
Вследствие того, что нуклеиновые кислоты представляют собой полимеры из субъединиц, многие модификации находятся в положении, которое повторяется в нуклеиновой кислоте, например, модификация основания или фосфатной группы, или не образующего связей O фосфатной группы. В некоторых случаях модификация находится во всех отдельных положениях в нуклеиновой кислоте, но во многих случаях этого не происходит. В качестве примера, модификация может находиться только в 3'- или 5'-концевом положении, может находиться только в концевой области, например, в положении в концевом нуклеотиде или в последних 2, 3, 4, 5 или 10 нуклеотидах цепи. Модификация может располагаться в области двойной цепи, области одной цепи или в обеих. Модификация может находиться только в области двойной цепи РНК или может находиться только в области одной цепи РНК. Например, модификация тиофосфата в положении не образующего связей O может находиться только на одном или обоих концах, может находиться только в концевой области, например, в положении в концевом нуклеотиде или в последних 2, 3, 4, 5 или 10 нуклеотидах цепи, или может находиться в областях двойной цепи и одной цепи, в частности на концах. 5'-конец или концы могут являться фосфорилированными.
Возможно, например, для повышения стабильности, вводить конкретные основания в липкие концы или вводить модифицированные нуклеотиды или имитаторы нуклеотидов в липкие концы одной цепи, например, в 5'- или 3'-липкие концы, или в обеих цепях. Например, желательным может являться введение в липкие концы пуриновых нуклеотидов. В некоторых вариантах осуществления можно модифицировать все или некоторые основания в 3'- или 5'-липком конце, например, модификацией, описываемой в настоящем описании. Модификации могут включать, например, использование модификаций в 2'-положении сахара рибозы с модификациями, которые известны в данной области, например, использование дезоксирибонуклеотидов, 2'-дезокси-2'-фтор- (2'-F) или 2'-O-метил-модифицированных вместо сахара рибозы нуклеинового основания, и модификации в фосфатной группе, например, модификации тиофосфатов. Липкие концы должны быть гомологичными последовательностям-мишеням.
В одном из вариантов осуществления каждый остаток смысловой цепи и антисмысловой цепи независимо модифицируют LNA, HNA, CeNA, 2'-метоксиэтилом, 2'-O-метилом, 2'-O-аллилом, 2'-C-аллилом, 2'-дезокси, 2'-гидроксилом или 2'-фтором. Цепи могут содержать более одной модификации. В одном из вариантов осуществления каждый остаток смысловой цепи и антисмысловой цепи независимо модифицируют 2'-O-метилом или 2'-фтором.
По меньшей мере две различные модификации, как правило, содержатся в смысловой цепи и антисмысловой цепи. Такие две модификации могут представлять собой 2'-O-метил- или 2'-фтор-модификации, или другие.
В одном из вариантов осуществления Na и/или Nb содержат модификации чередующегося паттерна. Термин "чередующийся мотив", как используют в настоящем описании, относится к мотиву, содержащему одну или более модификаций, где каждая модификация находится в чередующихся нуклеотидах одной цепи. Чередующийся нуклеотид может относиться к одному на каждый второй нуклеотид или одному на каждые три нуклеотида или аналогичный паттерн. Например, если A, B и C каждые представляют собой один тип модификации нуклеотида, чередующийся мотив может представлять собой "АВАВАВАВАВАВ…", "ААВВААВВААВВ…", "ААВААВААВААВ…", "АААВАААВАААВ…", "АААВВВАААВВВ…" или "АВСАВСАВСАВС…" и т.д.
Тип модификаций, содержащихся в чередующемся мотиве, может являться одинаковым или различным. Например, если каждый A, B, C, D представляет собой один тип модификации в нуклеотиде, чередующийся паттерн, т.е. модификации в каждом последующем нуклеотиде могут являться одинаковыми, но каждый для смысловой цепи или антисмысловой цепь можно выбирать из нескольких возможностей модификаций в чередующемся мотиве, таком как "АВАВАВ…", "АСАСАС…", "BDBDBD…" или "CDCDCD…" и т.д.
В одном из вариантов осуществления средство для РНКи по изобретению содержит паттерн модификации для чередующегося мотива в смысловой цепи, который сдвинут относительно паттерна модификации чередующегося мотива в антисмысловой цепи. Сдвиг может представлять собой такой, что модифицированная группа нуклеотидов смысловой цепи соответствует различным образом модифицированной группе нуклеотидов антисмысловой цепи и наоборот. Например, смысловая цепь, когда является спаренной с антисмысловой цепью в дуплекс дцРНК, чередующийся мотив в смысловой цепи может начинаться с "АВАВАВ" от 5'-3' цепи, и чередующийся мотив в антисмысловой цепь может начинаться с "ВАВАВА" от 5'-3' цепи в дуплексной области. В качестве другого примера, чередующийся мотив в смысловой цепи может начинаться с "ААВВААВВ" от 5'-3' цепи, и чередующийся мотив в антисмысловой цепи может начинаться с "ВВААВВАА" от 5'-3' цепи в дуплексной области, таким образом, что существует полный или частичный сдвиг паттерном модификации между смысловой цепью и антисмысловой цепью.
В одном из вариантов осуществления средство для РНКи содержит паттерн чередующегося мотива 2'-O-метил-модификации и 2'-F-модификации в смысловой цепи, который исходно имеет сдвиг относительно паттерна чередующегося мотива 2'-O-метил-модификации и 2'-F-модификации в антисмысловой цепи, т.е. 2'-O-метил-модифицированный нуклеотид в парах оснований смысловой цепи с 2'-F-модифицированным нуклеотидом в антисмысловой цепи и наоборот. 1 положение смысловой цепи может начинаться с 2'-F-модификации, и 1 положение антисмысловой цепи может начинаться с 2'-O-метил-модификации.
Введение одного или более мотивов из трех идентичных модификаций в трех последовательных нуклеотидах в смысловую цепь и/или антисмысловую цепь нарушает исходный паттерн модификации, содержащийся в смысловой цепи и/или антисмысловой цепи. Такое нарушение паттерна модификации смысловой и/или антисмысловой цепи посредством введения одного или более мотивы из трех идентичных модификаций в трех последовательных нуклеотидах в смысловую и/или антисмысловую цепь неожиданно повышает активность подавления экспрессии гена-мишени.
В одном из вариантов осуществления, когда мотив из трех идентичных модификаций в трех последовательных нуклеотидах вводят в любую из цепей, модификация нуклеотида следующего после мотива представляет собой отличную модификацию по сравнению с модификацией мотива. Например, участок последовательности, содержащий мотив, представляет собой "…NaYYYNb…", где "Y" представляет собой модификацию мотива из трех идентичных модификаций в трех последовательных нуклеотидах, и "Na" и "Nb" представляют собой модификацию в нуклеотиде, следующем после мотива "YYY", которая отличается от модификации Y, и где Na и Nb могут представлять собой одинаковые или различные модификации. Альтернативно, Na и/или Nb могут присутствовать или отсутствовать, когда содержится крыльевая модификация.
Средство для РНКи может дополнительно содержать по меньшей мере одну тиофосфатную или метилфосфонатную межнуклеотидную связь. Модификация тиофосфатной или метилфосфонатной межнуклеотидной связи может находиться в любом нуклеотиде смысловой цепи или антисмысловой цепи или в обеих в любом положении цепи. Например, модификация межнуклеотидной связи может находиться в любом нуклеотиде в смысловой цепи или антисмысловой цепи; каждая модификация межнуклеотидной связи может находиться в чередующемся паттерне в смысловой цепи или антисмысловой цепи, или смысловая цепь или антисмысловая цепь могут содержать модификации межнуклеотидной связи в чередующемся паттерне. Чередующийся паттерн модификации межнуклеотидной связи в смысловой цепи может быть одинаковым или отличным от антисмысловой цепи, и чередующийся паттерн модификации межнуклеотидной связи в смысловой цепи может содержать сдвиг относительно чередующегося паттерна модификации межнуклеотидной связи, в антисмысловой цепи.
В одном из вариантов осуществления средство для РНКи содержит тиофосфатную или метилфосфонатную модификацию межнуклеотидной связи в области липких концов. Например, область липких концов может содержать два нуклеотида, содержащих тиофосфатную или метилфосфонатную межнуклеотидную связь между двумя нуклеотидами. Модификации межнуклеотидной связи также можно проводить для связывания выступающих нуклеотидов с концевыми спаренными нуклеотидами в дуплексной области. Например, по меньшей мере 2, 3, 4 или все выступающие нуклеотиды могут являться связанными тиофосфатной или метилфосфонатной межнуклеотидной связью, и необязательно могут присутствовать дополнительные тиофосфатные или метилфосфонатные межнуклеотидные связи, связывающие выступающий нуклеотид со спаренным нуклеотидом, который является следующим после выступающего нуклеотида. Например, может существовать по меньшей мере две тиофосфатные межнуклеотидные связи между концевыми тремя нуклеотидами, в которых два из трех нуклеотидов представляют собой выступающие нуклеотиды, и третий представляет собой спаренный нуклеотид, следующий после выступающего нуклеотида. Предпочтительно эти концевые три нуклеотида могут находиться на 3'-конце антисмысловой цепи.
В одном из вариантов осуществления средство для РНКи содержит несоответствие(я) с мишенью в дуплексе или их комбинации. Несоответствие может находиться в области липких концов или дуплексной области. Пару оснований можно классифицировать на основании ее способности способствовать диссоциации или плавлению (например, в отношении свободной энергии ассоциации или диссоциации конкретного спаривания, наиболее простой подход представляет собой такой, как на основании индивидуальных пар независимо от соседа, или также можно использовать аналогичный анализ). В отношении возможности способствовать диссоциации: A:U является предпочтительным чем G:C; G:U является предпочтительным чем G:C; и I:C является предпочтительным чем G:C (I=инозин). Несоответствия, например, неканонические или отличные от канонического спаривания (как описано где-либо в настоящем описании) являются предпочтительными по сравнению с каноническими (A:T, A:U, G:C) спариваниями; и спаривания, которые содержат универсальное основание, являются предпочтительными по сравнению с каноническим спариванием.
В одном из вариантов осуществления средство для РНКи содержит по меньшей мере одну из первых 1, 2, 3, 4 или 5 пар оснований в дуплексных областях от 5'-конца антисмысловой цепи, которые можно независимо выбирать из группы: A:U, G:U, I:C и несовпадающих пар, например, неканонических или отличных от канонических спариваний или спариваний, которые содержат универсальное основание, для обеспечения диссоциации антисмысловой цепи в 5'-конце дуплекса.
В одном из вариантов осуществления нуклеотид в положении 1 в дуплексной области от 5'-конца в антисмысловой цепи выбран из группы, состоящей из A, dA, dU, U и dT. Альтернативно, по меньшей мере одна из первых 1, 2 или 3 пар оснований в дуплексной области от 5'-конца антисмысловой цепи представляет собой пару оснований AU. Например, первая пара оснований в дуплексной области от 5'-конца антисмысловой цепи представляет собой пару оснований AU.
В одном из вариантов осуществления последовательность смысловой цепи можно представить формулой (I):

где:
i и j каждый независимо представляет собой 0 или 1;
p и q каждый независимо представляет 0-6;
каждый Na независимо представляет собой олигонуклеотидную последовательность, содержащую 0-25 модифицированных нуклеотидов, где каждая последовательность содержит по меньшей мере два различно модифицированных нуклеотида;
каждый Nb независимо представляет собой олигонуклеотидную последовательность, содержащую 0-10 модифицированных нуклеотидов;
каждый np и nq независимо представляет собой выступающий нуклеотид;
XXX, YYY и ZZZ каждый независимо представляет собой один мотив из трех идентичных модификаций в трех последовательных нуклеотидах. Предпочтительно YYY представляет собой все 2'-F-модифицированные нуклеотиды.
В одном из вариантов осуществления Na и/или Nb содержит модификации чередующегося паттерна.
В одном из вариантов осуществления мотив YYY располагается в участке расщепления смысловой цепи или около него. Например, когда средство для РНКи содержит дуплексную область из 17-23 нуклеотидов, мотив YYY может располагаться в участок расщепления или вблизи него (например, может располагаться в положениях 6, 7, 8, 7, 8, 9, 8, 9, 10, 9, 10, 11, 10, 11, 12 или 11, 12, 13) смысловой цепи, где нумерация начинается от 1-го нуклеотида от 5'-конца, или необязательно нумерация начинается с 1-го спаренного нуклеотида в дуплексной области от 5'-конца.
В одном из вариантов осуществления i равно 1 и j равно 0, или i равно 0 и j равно 1, или i и j равны 1. Таким образом, смысловую цепь можно представить следующими ниже формулами:



Когда смысловая цепь представлена формулой (Ia), Nb представляет собой олигонуклеотидную последовательность, содержащую 0-10, 0-7, 0-5, 0-4, 0-2 или 0 модифицированных нуклеотидов. Каждый Na независимо может представлять собой олигонуклеотидную последовательность, содержащую 2-20, 2-15 или 2-10 модифицированных нуклеотида.
Когда смысловая цепь представлена в виде формулы (Ib), Nb представляет собой олигонуклеотидную последовательность, содержащую 0-10, 0-7, 0-10, 0-7, 0-5, 0-4, 0-2 или 0 модифицированных нуклеотидов. Каждый Na может независимо представлять собой олигонуклеотидную последовательность, содержащую 2-20, 2-15 или 2-10 модифицированных нуклеотида.
Когда смысловая цепь представлена в виде формулы (Ic), каждый Nb независимо представляет собой олигонуклеотидную последовательность, содержащую 0-10, 0-7, 0-5, 0-4, 0-2 или 0 модифицированных нуклеотидов. Предпочтительно Nb равно 0, 1, 2, 3, 4, 5 или 6. Каждый Na может независимо представлять собой олигонуклеотидную последовательность, содержащую 2-20, 2-15 или 2-10 модифицированных нуклеотида.
Каждый из X, Y и Z может быть одинаковым или отличным друг от друга.
В одном из вариантов осуществления последовательность антисмысловой цепи РНКи можно представить формулой (II):

где:
k и l каждый независимо представляет собой 0 или 1;
p' и q' каждый независимо представляет собой 0-6;
каждый

каждый
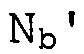
каждый
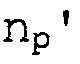
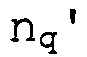
где
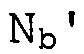
и
X'X'X', Y'Y'Y' и Z'Z'Z' каждый независимо представляет собой один мотив из трех идентичных модификаций в трех последовательных нуклеотидах.
В одном из вариантов осуществления

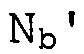
Мотив Y'Y'Y' располагается в участке расщепления антисмысловой цепи или около него. Например, когда средство для РНКи содержит дуплексную область длиной 17-23 нуклеотидов, мотив Y'Y'Y' может находиться в положениях 9, 10, 11; 10, 11, 12; 11, 12, 13; 12, 13, 14; или 13, 14, 15 антисмысловой цепи, где нумерация начинается от 1-го нуклеотида от 5'-конца; или необязательно нумерация начинается от 1-го спаренного нуклеотида в дуплексной области от 5'-конца. Предпочтительно мотив Y'Y'Y' находится в положениях 11, 12, 13.
В одном из вариантов осуществления мотив Y'Y'Y' представляет собой все 2'-OMe-модифицированные нуклеотиды.
В одном из вариантов осуществления k равно 1 и l равно 0, или k равно 0 и l равно 1, или k и l равны 1.
Таким образом, антисмысловую цепь можно представить следующими ниже формулами:



Когда антисмысловая цепь представлена формулой (IIa), Nb представляет собой олигонуклеотидную последовательность, содержащую 0-10, 0-7, 0-10, 0-7, 0-5, 0-4, 0-2 или 0 модифицированных нуклеотидов. Каждый

Когда антисмысловая цепь представлена в виде формулы (IIb),
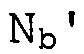

Когда антисмысловая цепь представлена в виде формулы (IIc), каждый
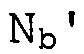

Каждый из X', Y' и Z' может являться одинаковым или отличным друг от друга.
Каждый нуклеотид смысловой цепи и антисмысловой цепи можно независимо модифицировать LNA, HNA, CeNA, 2'-метоксиэтилом, 2'-O-метилом, 2'-O-аллилом, 2'-C-аллилом, 2'-гидроксилом, 2'-дезокси или 2'-фтором. Например, каждый нуклеотид смысловой цепи и антисмысловой цепи независимо модифицируют 2'-O-метилом или 2'-фтором. В частности, каждый X, Y, Z, X', Y' и Z' может представлять собой 2'-O-метил-модификацию или 2'-фтор-модификацию.
В одном из вариантов осуществления смысловая цепь средства для РНКи может содержать мотив YYY, находящийся в положениях 9, 10 и 11 цепи, когда длина дуплексной области составляет 21 нуклеотид, где нумерация начинается с 1-го нуклеотида от 5'-конца, или необязательно нумерация начинается с 1-го спаренного нуклеотида в дуплексной области от 5'-конца, и Y представляет собой 2'-F-модификацию. Смысловая цепь может дополнительно содержать мотив XXX или мотивы ZZZ в качестве крыльевых модификаций с противоположного конца дуплексной области, и XXX и ZZZ каждый независимо представляет собой 2'-OMe-модификацию или 2'-F модификацию.
В одном из вариантов осуществления антисмысловая цепь может содержать мотив Y'Y'Y', находящийся в положениях 11, 12, 13 цепи, где нумерация начинается с 1-го нуклеотида от 5'-конца, или необязательно нумерация начинается с 1-го спаренного нуклеотида в дуплексной области от 5'-конца, и Y' представляет собой 2'-O-метил-модификацию. Антисмысловая цепь может дополнительно содержать мотив X'X'X' или мотивы Z'Z'Z' в качестве крыльевых модификаций с противоположного конца дуплексной области, и X'X'X' и Z'Z'Z' каждый независимо представляет собой 2'-OMe-модификацию или 2'-F-модификацию.
Смысловая цепь, представленная любой из указанных выше формул (Ia), (Ib) и (Ic), образует дуплекс, где антисмысловая цепь представлена любой из указанных выше формул (IIa), (IIb) и (IIc) соответственно.
Таким образом, средства для РНКи по изобретению могут содержать смысловую цепь и антисмысловую цепь, где каждая цепь содержит от 14 до 30 нуклеотидов, дуплекс РНКи, представленный формулой (III):

где:
i, j, k и l каждый независимо представляет собой 0 или 1;
p, p' q и q' каждый независимо представляет собой 0-6;
каждый Na и Na независимо представляет собой олигонуклеотидную последовательность, содержащую 0-25 модифицированных нуклеотидов, где каждая последовательность содержит по меньшей мере два различным образом модифицированных нуклеотида;
каждый Nb и
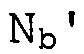
где
каждый


XXX, YYY, ZZZ, X'X'X', Y'Y'Y' и Z'Z'Z' каждый независимо представляет собой один мотив из трех идентичных модификаций в трех последовательных нуклеотидах.
В одном из вариантов осуществления i равно 1 и j равно 0, или i равно 0 и j равно 1, или i и j равны 1. В другом варианте осуществления k равно 1 и l равно 0, k равно 0 и l равно 1, или k и l равны 1.
Иллюстративные комбинации смысловой цепи и антисмысловой цепи, образующих дуплекс РНКи, включают указанные ниже формулы:



Где средство для РНКи представлено формулой (IIIa), каждый Nb независимо представляет собой олигонуклеотидную последовательность, содержащую 1-10, 1-7, 1-5 или 1-4 модифицированных нуклеотидов. Каждый Na независимо представляет собой олигонуклеотидную последовательность, содержащую 2-20, 2-15 или 2-10 модифицированных нуклеотидов.
Где средство для РНКи представлено в виде формулы (IIIb), каждый Nb,

Где средство для РНКи представлено в виде формулы (IIIc), каждый Nb,


Каждый из X, Y и Z в формулах (III), (IIIa), (IIIb) и (IIIc) может являться одинаковым или отличным друг от друга.
Когда средство для РНКи представлено формулой (III), (IIIa), (IIIb) или (IIIc), по меньшей мере один из нуклеотидов Y может образовывать пару оснований с одним из нуклеотидов Y'. Альтернативно, по меньшей мере два из нуклеотидов Y образуют пару оснований с соответствующими нуклеотидами Y', или все три нуклеотида Y все образуют пару оснований с соответствующими нуклеотидами Y'.
Когда средство для РНКи представлено формулой (IIIa) или (IIIc), по меньшей мере один из нуклеотидов Z может образовывать пару оснований с одним из нуклеотидов Z'. Альтернативно, по меньшей мере два из нуклеотидов Z образуют пару оснований с соответствующими нуклеотидами Z', или все три нуклеотида Z все образуют пару оснований с соответствующими нуклеотидами Z'.
Когда средство для РНКи представлено в виде формулы (IIIb) или (IIIc), по меньшей мере один из нуклеотидов X может образовывать пару оснований с одним из нуклеотидов X'. Альтернативно, по меньшей мере два из нуклеотидов X образуют пару оснований с соответствующими нуклеотидами X', или все три нуклеотида X все образуют пару оснований с соответствующими нуклеотидами X'.
В одном из вариантов осуществления модификация в нуклеотиде Y отличается от модификации в нуклеотиде Y', модификация в нуклеотиде Z отличается от модификации в нуклеотиде Z', и/или модификация в нуклеотиде X отличается от модификации в нуклеотиде X'.
В одном из вариантов осуществления средство для РНКи представляет собой мультимер, содержащий по меньшей мере два дуплекса, представленных формулой (III), (IIIa), (IIIb) или (IIIc), где дуплексы соединены линкером. Линкер может являться расщепляемым или нерасщепляемым. Необязательно мультимер дополнительно содержит лиганд. Каждый из дуплексов может воздействовать на один и тот же ген или два различных гена, или каждый из дуплексов может воздействовать на один и тот же ген в двух различных участках-мишенях.
В одном из вариантов осуществления средство для РНКи представляет собой мультимер, содержащий три, четыре, пять, шесть или более дуплексов, представленных формулой (III), (IIIa), (IIIb) или (IIIc), где дуплексы соединены линкером. Линкер может являться расщепляемым или нерасщепляемым. Необязательно мультимер дополнительно содержит лиганд. Каждый из дуплексов может воздействовать на один и тот же ген или два различных гена, или каждый из дуплексов может воздействовать на один и тот же ген в двух различных участках-мишенях.
В одном из вариантов осуществления два средства для РНКи, представленные формулой (III), (IIIa), (IIIb) или (IIIc), связаны друг с другом 5'-конецом, и один или оба 3'-конца необязательно являются конъюгированными с лигандом. Каждое из средств может воздействовать на один и тот же ген или на два различных гена, или каждое из средств может воздействовать на один и тот же ген в двух различных участках-мишенях.
В различных публикациях описаны мультимерные средства для РНКи. Такие публикации включают WO 2007/091269, патент США №7858769, WO 2010/141511, WO 2007/117686, WO 2009/014887 и WO 2011/031520, полное содержание которых, таким образом, включено в настоящее описание посредством ссылки.
Средство для РНКи содержит конъюгации одной или более углеводных групп со средством для РНКи, которые могут оптимизировать одно или более свойств средства для РНКи. Во многих случаях углеводная группа является связанной с модифицированной субъединицей средства для РНКи. Например, сахар рибозы одной или более рибонуклеотидных субъединиц средства дцРНК можно замещать другими группами, например, неуглеводным (предпочтительно циклическим) носителем, к которому прикреплен углеводный лиганд. Рибонуклеотидная субъединица, в которой сахар рибозы субъединицы замещен таким образом, обозначают в настоящем описании как субъединицу модификации замены рибозы (RRMS). Циклический носитель может представлять собой карбоциклическую систему, т.е. все атомы кольца представляют собой атомы углерода, или гетероциклическую система, т.е. один или более атомов кольца могут представлять собой гетероатом, например, азот, кислород, серу. Циклический носитель может представлять собой моноциклическую систему или может содержать два или более колец, например, конденсированных колец. Циклический носитель может представлять собой полностью насыщенную циклическую систему, или он может содержать одну или более двойных связей.
Лиганд может быть связан с полинуклеотидом через носитель. Носители содержат (i) по меньшей мере одну "точку присоединения в остове", предпочтительно две "точки присоединения в остове" и (ii) по меньшей мере одну "связывающую точку присоединения". "Точка присоединения в остове", как используют в настоящем описании, относится к функциональной группе, например, гидроксильной группе, или, как правило, доступной связи, и которая является подходящей для введения носителя в остов, например, фосфат или модифицированный фосфат, например, содержащий серу остов рибонуклеиновой кислоты. "Связывающая точка присоединения" (TAP) в некоторых вариантах осуществления относится к входящему в состав кольца атому циклического носителя, например, атому углерода или гетероатому (отличному от атома, который представляет собой точку присоединения в остове), которая соединяет выбранную группу. Группа может представлять собой, например, углевод, например, моносахарид, дисахарид, трисахарид, тетрасахарид, олигосахарид и полисахарид. Необязательно выбранная группа соединена посредством промежуточной связи с циклическим носителем. Таким образом, циклический носитель часто содержит функциональную группу, например, аминогруппу или, как правило, обеспечивает связь, которая является подходящей для введения или связывания другой химической структуры, например, лиганда с компонентом кольца.
Средства для РНКи можно быть конъюгированы с лигандрм посредством носителя, где носитель может представлять собой циклическую группу или ациклическую группу; предпочтительно циклическая группа выбрана из пирролидинила, пиразолинила, пиразолидинила, имидазолинила, имидазолидинила, пиперидинила, пиперазинила, [1,3]диоксолана, оксазолидинила, изоксазолидинила, морфолинил, тиазолидинила, изотиазолидинила, хиноксалинила, пиридазинонила, тетрагидрофурила и декалина; предпочтительно, ациклическая группа выбрана из остова серинола или остова диэтаноламина.
В определенных конкретных вариантах осуществления средство для РНКи по изобретению представляет собой средство, выбранное из группы средств, перечисленных в таблице 1, и состоящей из




Эти средства могут дополнительно содержать лиганд, такой как лиганд GalNAc.
Лиганды
Средства для РНКи по изобретению, например, двухцепочечные средства для РНКи, можно необязательно конъюгировать с одним или более лигандов. Лиганд можно присоединять к смысловой цепи, антисмысловой цепи или обеим цепям на 3'-конце, 5'-конце или обоих концах. Например, лиганд может быть конъюгирован со смысловой цепью. В предпочтительных вариантах осуществления лиганд конъюгирован с 3'-концом смысловой, цепи. В одном из предпочтительных вариантов осуществления лиганд представляет собой лиганд GalNAc. В особенно предпочтительных вариантах осуществления лиганд представляет собой GalNAc3:

Широкий спектр соединений можно связывать со средствами для РНКи по настоящему изобретению. Предпочтительные молекулы представляют собой лиганды, которые являются предпочтительно ковалентно связанными непосредственно или опосредованно через промежуточную связь.
В предпочтительных вариантах осуществления лиганд изменяет распределение, направленное воздействие или время жизни молекулы, в которую его вводят. В предпочтительных вариантах осуществления лиганд обеспечивает повышенную аффинность к выбранной мишени, например, молекулам, клеткам или типу клеток, компартменту, рецептору, например, компартменту клетки или органа, ткани, органу или отделу организма, например, по сравнению с отсутствием молекул, таких как лиганд. Лиганды, обеспечивающие повышенную аффинность к выбранной мишени, также называются направленными лигандами.
Некоторые лиганды могут обладать эндосомолитическими свойствами. Эндосомолитические лиганды способствуют лизису эндосом и/или транспорту композиции по изобретению или ее компонентам из эндосом в цитоплазму клетки. Эндосомолитический лиганд может представлять собой полианионный пептид или пептидомиметик, который проявляет зависимую от pH мембранную активность и способность к слиянию. В одном из вариантов осуществления эндосомолитический лиганд приобретает свою активную конформацию при эндосомальном pH. "Активная" конформация представляет собой конформацию, в которой эндосомолитический лиганд способствует лизису эндосомы и/или транспорту композиции по изобретению или ее компонентам из эндосомы в цитоплазму клетки. Иллюстративные Эндосомолитические лиганды включают пептид GALA (Subbarao et al., Biochemistry, 1987, 26:2964-2972), пептид EALA (Vogel et al., J. Am. Chem. Soc., 1996, 118:1581-1586) и их производные (Turk et al., Biochem. Biophys. Acta, 2002, 1559:56-68). В одном из вариантов осуществления эндосомолитический компонент может содержать химическую группу (например, аминокислоту), которая также претерпевает изменение заряда или протонирование в ответ на изменение pH. Эндосомолитический компонент может быть линейным или разветвленным.
Лиганды могут улучшать транспорт, гибридизацию и конкретные свойства, а также могут улучшать устойчивость к нуклеазе получаемого природного или модифицированного олигорибонуклеотида или полимерной молекулы, содержащей любую комбинацию мономеров, описываемых в настоящем описании, и/или природные или модифицированные рибонуклеотиды.
Лиганды в основном могут включать терапевтические модификаторы, например, для повышения поглощения, диагностические соединения или репортерные группы, например, для наблюдения распределения, сшивающие средства и группы, придающие устойчивость к нуклеазе. Общие примеры включают липиды, стероиды, витамины, сахара, белки, пептиды, полиамины и миметики пептидов.
Лиганды могут включать природное вещество, такое как белок (например, сывороточный альбумин человека (HSA), липопротеин низкой плотности (LDL), липопротеин высокой плотности (HDL) или глобулин), углевод (например, декстран, пуллулан, хитин, хитозан, инулин, циклодекстрин или гиалуроновую кислоту) или липид. Лиганд также может представлять собой рекомбинантную или синтетическую молекулу, такую как синтетический полимер, например, синтетическую полиаминокислоту, олигонуклеотид (например, аптамер). Примеры полиаминокислот включают полиаминокислоту, которая представляет собой полилизин (PLL), поли-L-аспарагиновую кислоту, поли-L-глутаминовую кислоту, сополимер стирол-ангидрид малеиновой кислоты, сополимер поли(L-лактид-со-гликолида), сополимер дивиниловый эфир-малеиновый ангидрид, сополимер N-(2-гидроксипропил)метакриламида (HMPA), полиэтиленгликоль (PEG), поливиниловый спирт (PVA), полиутеран, поли(2-этилакриловую кислоту), полимеры N-изопропилакриламида, или полифосфазин. Примеры полиаминов включают полиэтиленимин, полилизин (PLL), спермин, спермидин, полиамин, псевдопептид-полиамин, пептидомиметический полиамина, дендримерный полиамин, аргинин, амидин, протамин, катионный липид, катионный форфирин, четвертичную соль полиамина или альфа-спиральный пептид.
Лиганды также могут содержать группы для направленного воздействия, например, средства направленного воздействия на клетку или ткань, например, лектин, гликопротеин, липид или белок, например, антитело, которое связывается с конкретным типом клеток, таких как клетки почка. Группа для направленного воздействия может представлять собой тиреотропин, меланотропин, лектин, гликопротеин, поверхностно-активный белок A, углевод муцина, поливалентную лактозу, поливалентную галактозу, N-ацетилгалактозамин, N-ацетилглюкозамин, поливалентную маннозу, поливалентную фукозу, гликозилированные полиаминокислоты, поливалентную галактозу, трансферрин, бисфосфонат, полиглутаминат, полиаспартат, липид, холестерин, стероид, желчную кислоту, фолат, витамин B12, биотин, пептид RGD, миметик пептида RGD или аптамер.
Другие примеры лигандов включают красители, интеркаляторы (например, акридины), перекрестносшивающие средства (например, псорален, митомицин C), порфирины (TPPC4, тексапирин, сапфирин), полициклические ароматические углеводороды (например, феназин, дигидрофеназин), искусственные эндонуклеазы или хелатор.
(например, EDTA), липофильные молекулы, например, холестерин, холевую кислоту, адамантануксусную кислоту, 1-пиренмасляную кислоту, дигидротестостерон, 1,3-бис-O(гексадецил)глицерин, геранилоксигексильную группу, гексадецилглицерин, борнеол, ментол, 1,3-пропандиол, гептадецильную группу, пальмитиновую кислоту, миристиновую кислоту, O3-(олеоил)литохолевую кислоту, O3-(олеоил)холеновую кислоту, диметокситритил или феноксазин) и конъюгаты пептидов (например, пептид antennapedia, пептид Tat), алкилирующие средства, фосфат, амино, меркапто, PEG (например, PEG-40K), MPEG, [MPEG]2, полиамино, алкил, замещенный алкил, радиоактивно меченые маркеры, ферменты, гаптены (например, биотин), способствующие транспорту/всасыванию вещества (например, аспирин, витамин E, фолиевую кислоту), синтетические рибонуклеазы (например, имидазол, бисимидазол, гистамин, кластеры имидазола, конъюгаты акридин-имидазол, Eu3+ комплексы тетраазамакроциклов), динитрофенил, HRP или AP.
Лиганды могут представлять собой белки, например, гликопротеины или пептиды, например, молекулы с конкретной аффинностью к со-лиганду, или антитела например, антитело, которое связывается с конкретным типом клеток, таким как злокачественная клетка, эндотелиальная клетка или костная клетка. Лиганды также могут содержать гормоны и рецепторы гормонов. Они также могут содержать не являющиеся пептидами молекулы, такие как липиды, пектины, углеводы, витамины, кофакторы, поливалентная лактоза, поливалентная галактоза, N-ацетилгалактозамин, N-ацетилглюкозамин, поливалентная манноза, поливалентная фукоза или аптамеры. Лиганд может представлять собой, например, липополисахарид, активатор p38 MAP киназы или активатор NF-kB.
Лиганд может представлять собой вещество, например, лекарственное средство, которое может повышать поступление средства на основе иРНК в клетку, например, посредством разрушения цитоскелета клетки, например, посредством разрушения микротрубочек клетки, микрофиламентов и/или промежуточных микрофиламентов. Лекарственное средство может представлять собой, например, таксой, винкристин, винбластин, цитохалазин, нокодазол, джасплакинолид, латрункулин A, фаллоидин, свинхолид A, инданоцин или миосервин.
Лиганд может повышать поступление олигонуклеотида в клетку, например, путем активации воспалительного ответа. Иллюстративные лиганды, которые обладают таким эффектом, включают фактор некроза опухоли альфа (TNF-альфа), интерлейкин-1 бета или интерферон гамма.
В одном из аспектов лиганд представляет собой липид или молекулу на основе липида. Такой липид или молекула на основе липида предпочтительно связывается с сывороточным белком, например, сывороточным альбумином человека (HSA).
Связывание лиганда. с HSA обеспечивает распределение конъюгата в ткани-мишени, например, непочечной ткани-мишени организма. Например, ткань-мишень может представлять собой печень, включая паренхиматозные клетки печени. В качестве лигандов также можно использовать другие молекулы, которые могут связываться с HSA. Например, можно использовать напроксен или аспирин. Липид или лиганд на основе липида может (a) повышать устойчивость к деградации конъюгата, (b) повышать направленную доставку или транспорт в клетку-мишень или клеточную мембрану, и/или (c) его можно использовать для регуляции связывания с сывороточным белком, например, HSA.
Лиганд на основе липида можно использовать для модулирования, например, контроля связывания конъюгата с тканью-мишенью. Например, менее вероятно, что липид или лиганд на основе липида, который сильнее связывается с HSA, является направленным на почку, и, таким образом, менее вероятно, что он будет выводиться из организма. Липид или лиганд на основе липида, который слабее связывается с HSA, можно использовать для направленной доставки конъюгата в почку.
В предпочтительном варианте осуществления лиганд на основе липида связывается с HSA. Предпочтительно он связывается с HSA с достаточной аффинностью, таким образом, что такой конъюгат предпочтительно распределяется в непочечной ткани. Однако предпочтительно, чтобы аффинность не являлась настолько сильной, чтобы связывание HSA-лиганд было необратимым.
В другом предпочтительном варианте осуществления лиганд на основе липида слабо связывается с HSA или не связывается совсем, таким образом, что конъюгат предпочтительно распределится в почке. Также можно использовать другие группы, которые обеспечивают направленную доставку в клетки почки, вместо лиганда на основе липида или в дополнение к нему.
В другом аспекте лиганд представляет собой молекулу, например, витамин, который поглощается клеткой-мишенью, например, пролиферирующей клеткой. Такие молекулы являются особенно пригодными для лечения нарушений, характеризующихся нежелательной клеточной пролиферацией, например, злокачественного или незлокачественного типа, например, злокачественных клеток. Иллюстративные витамины включают витамин A, E и K. Другие иллюстративные витамины включают витамины B, например, фолиевую кислоту, B12, рибофлавин, биотин, пиридоксаль, или другие витамины или питательные вещества, поглощаемые злокачественными клетками. Также включают HAS, липопротеин низкой плотности (LDL) и липопротеин высокой плотности (HDL).
В другом аспекте лиганд представляет собой средство, проникающее в клетку, предпочтительно спиральное средство, проникающее в "клетку. Предпочтительно средство является амфалипатическим. Иллюстративное средство представляет собой пептид, такой как tat или antennopedia. Если средство представляет собой пептид, его можно модифицировать, включая пептидилмиметик, инвертромеры, непептидные или псевдопептидные связи и использование D-аминокислот. Спиральное средство предпочтительно представляют собой альфа-спиральное средство, которое предпочтительно содержит липофильную и липофобную фазу.
Лиганд может представлять собой пептид или пептидомиметик. Пептидомиметик (также обозначаемый в настоящем описании как олигопептидомиметик) представляет собой молекулу, способную сворачиваться в определенную трехмерную структуру, аналогичную природному пептиду. Длина молекулы пептида или пептидомиметика может составлять приблизительно 5-50 аминокислот, например, приблизительно 5, 10, 15, 20, 25, 30, 35, 40, 45 или 50 аминокислот. Пептид или пептидомиметик может представлять собой, например, проникающий в клетку пептид, катионный пептид, амфипатический пептид или гидрофобный пептид (например, состоящий преимущественно из Tyr, Trp или Phe). Молекула пептида может представлять собой дендримерный пептид, пептид с ограниченной конформационной свободой или сшитый пептид. В другом альтернативном варианте осуществления молекула пептида может содержать гидрофобную последовательность мембранной транслокации (MTS). Иллюстративный пептид, содержащий гидрофобную MTS, представляет собой RFGF, содержащий аминокислотную последовательность AAVALLPAVLLALLAP (SEQ ID NO: 4). Аналог RFGF (например, аминокислотная последовательность AALLPVLLAAP) (SEQ ID NO: 5), содержащий гидрофобную MTS, также может представлять собой направленную молекулу. Молекула пептида может представлять собой "транспортный" пептид, который может переносить большие полярные молекулы, включая пептиды, олигонуклеотиды, и белок через клеточные мембраны. Например, было выявлено, что последовательности из белка Tat ВИЧ (GRKKRRQRRRPPQ) (SEQ ID NO: 6) и белка Drosophila Antennapedia (RQIKIWFQNRRMKWKK) (SEQ ID NO: 7) могут функционировать как транспортные пептиды. Пептид или пептидомиметик может кодироваться случайной последовательностью ДНК, такой как пептид, идентифицируемый в библиотеке фагового дисплея или комбинаторной библиотеке одна гранула-одно соединение (OBOC) (Lam et al., Nature, 354:82-84, 1991). Предпочтительно пептид или пептидомиметик, связанный со средством на основе иРНК через встроенную мономерную единицу, представляет собой направленный на клетку пептид, такой как аргининглицинаспарагиновая кислота (RGD)-пептид или имитатор RGD. Длина молекулы пептида может находиться в диапазоне приблизительно от 5 аминокислот приблизительно до 40 аминокислот. Молекулы пептида могут содержать такую структурную модификацию, чтобы повышать стабильность или непосредственно конформационные свойства. Можно использовать любую из описанных ниже структурных модификаций. Молекулу RGD-пептида можно использовать для направленной доставки в опухолевую клетку, такую как эндотелиальная опухолевая клетка или опухолевая клетка рака молочной железы (Zitzmann et al., Cancer Res., 62:5139-43, 2002). RGD-пептид может облегчать направленную доставку средства на основе иРНК в опухоли различных других тканей, включая легкое, почку, селезенку или печень (Aoki et al., Cancer Gene Therapy, 8:783-787, 2001). Предпочтительно RGD-пептид облегчает направленную доставку средства на основе иРНК в почку. RGD-пептид может быть линейным или циклическим и может быть модифицированным, например, гликозилированным или метилированным, для облегчения направленной доставки в конкретные ткани. Например, гликозилированный RGD-пептид может доставлять средство на основе иРНК в опухолевую клетку, экспрессирующую αvβ3 (Haubner et al., Jour. Nucl. Med., 42:326-336, 2001). Можно использовать пептиды, которые направлены на маркеры, содержащиеся в большом количестве в пролиферирующих клетках. Например, содержащие RGD пептиды и пептидомиметики могут быть направленными на злокачественные клетки, в частности клетки, которые содержат интегрин. Таким образом, можно использовать RGD-пептиды, циклические пептиды, содержащие RGD, RGD-пептиды, которые содержат D-аминокислоты, а также синтетические имитаторы RGD. В дополнение к RGD можно использовать другие молекулы, которые направлены на лиганд интегрина. Как правило, такие лиганды можно использовать для регуляции пролиферирующих клеток и ангиогенеза. Предпочтительные конъюгаты такого типа лиганда направлены на РЕСАМ-1, VEGF или другой ген злокачественной опухоли, например, ген злокачественной опухоли, описываемый в настоящем описании.
"Проникающий в клетку пептид" способен проникать в клетку, например, микробную клетку, такую как бактериальная или грибная клетка, или клетку млекопитающего, такую как клетка человека. Проникающий в микробную клетку пептид может представлять собой, например, α-спиральный линейный пептид (например, LL-37 или церопин P1), содержащий дисульфидную связь пептид (например, α-дефензин, β-дефензин или бактенецин) или пептид, содержащий только одну или две преобладающих аминокислоты (например, PR-39 или индолицидин). Проникающий в клетку пептид также содержит сигнал внутриядерной локализации (NLS). Например, проникающий в клетку пептид может представлять собой двухсоставной амфипатический пептид, такой как MPG, который получают из домена слитого пептида gp41 ВИЧ-1 и NLS большого T-антигена SV40 (Simeoni et al., Nucl. Acids Res., 31:2717-2724, 2003).
В одном из вариантов осуществления направленный пептид может представлять собой амфипатический α-спиральный пептид. Иллюстративные амфипатические α-спиральные пептиды включают, но не ограничиваются ими, цекропины, ликотоксины, парадаксины, буфорин, CPF, бомбинин-подобный пептид (BLP), кателицидины, цератотоксины, пептиды S. clava, противомикробные пептиды из кишечника миксины (HFIAP), магаинины, бревинины-2, дермасептины, мелиттины, плеуроцидин, пептиды H2A, пептиды Xenopus, эскулентины-1 и каерины. Предполагают, что ряд факторов предпочтительно поддерживает сохранение стабильности спирали. Например, используют максимальное число остатков, стабилизирующих спираль (например, leu, ala или lys), и минимальное число дестабилизирующих остатков (например, пролин или циклические мономерные единицы). Предполагают, что можно использовать кэпирующий остаток (например, Gly представляет собой иллюстративный N-кэпирующий остаток) и/или амидирование C-конца для обеспечения дополнительной H-связи для стабилизации спирали. Стабильность может обеспечивать образование солевых мостиков между остатками с противоположными зарядами, разделенными положениями i±3 или i±4. Например, катионные остатки, такие как лизин, аргинин, гомоаргинин, орнитин или гистидин, могут образовывать солевые мостики с анионными остатками глутамината или аспартата.
Лиганды на основе пептидов и пептидомиметиков включают лиганды, содержащие природные или модифицированные пептиды, например, D- или L-пептиды, α-, β- или γ-пептиды, N-метилпептиды, азапептиды, пептиды, содержащие один или более амидом, т.е. пептид со связями, замененными одном или более связями мочевины, тиомочевины, карбамата или сульфонилмочевины, или циклические пептиды.
Направленный лиганд может представлять собой любой лиганд, который способен обеспечивать направленное воздействие на конкретный рецептор. Примеры представляют собой фолат, GalNAc, галактозу, маннозу, маннозу-6P, кластеры сахаров, такие как кластер GalNAc, кластер маннозы, кластер галактозы или аптамер. Кластер представляет собой комбинацию двух или более звеньев сахара. Направленные лиганды также включают лиганды рецептора интегрина, лиганды рецептора хемокина, лиганды рецептора трансферрина, биотина, серотонина, лиганды PSMA, эндотелина, GCPII, соматостатина, LDL и HDL. Лиганды также могут быть основаны на нуклеиновой кислоте, например, аптамер. Аптамер может являться немодифицированным или содержать любую комбинацию модификаций, описываемых в настоящем описании.
Средства контроля эндосомального высвобождения включают имидазолы, поли- или олигоимидазолы, PEI, пептиды, способствующие слиянию пептиды, поликарбоксилаты, поликатионы, маскированные олиго или поликатионы или полианионы, ацетали, полиацетали, кетали/поликетали, ортоэфиры, полимеры с экранированными или неэкранированными катионными или анионными зарядами, дендримеры с экранированными или неэкранированными катионными или анионными зарядами.
Модулятор PK означает фармакокинетический модулятор. Модуляторы PK включают липофильные вещества, желчные кислоты, стероиды, аналоги фосфолипидов, пептиды, связывающие белок средства, PEG, витамины и т.д. Иллюстративные модуляторы PK включают, но не ограничиваются ими, холестерин, жирные кислоты, холевую кислоту, литохолевую кислоту, диалкилглицериды, диацилглицериды, фосфолипиды, сфинголипиды, напроксен, ибупрофен, витамин E, биотин и т.д. Известно, что олигонуклеотиды, которые содержат ряд тиофосфатных связей, связываются с сывороточным белком, таким образом, короткие олигонуклеотиды, например, олигонуклеотиды приблизительно из 5 оснований, 10 оснований, 15 оснований или 20 оснований, содержащие много тиофосфатных связей в остове, также являются пригодными по настоящему изобретению в качестве лигандов (например, в качестве модулирующих PK лигандов).
Кроме того, также пригодными по настоящему изобретению в качестве модулирующих PK лигандов являются аптамеры, которые связываются с компонентами сыворотки (например, сывороточными белками).
Другие конъюгаты лигандов, пригодные по изобретению, описаны в патентных заявках США USSN: 10/916185, зарегистрированной 10 августа 2004 года, USSN: 10/946873, зарегистрированной 21 сентября 2004 года, USSN: 10/833934, зарегистрированной 3 августа 2007 года, USSN: 11/115989, зарегистрированной 27 апреля 2005 года, и USSN: 11/944227, зарегистрированной 21 ноября 2007 года, полностью включенных посредством ссылки для всех целей.
Когда содержится два или более лигандов, все лиганды могут обладать одинаковыми свойствами, все могут обладать различными свойствами, или некоторые лиганды обладают одинаковыми свойствами, тогда как другие обладают различными свойствами. Например, лиганд может обладать свойствами направленной доставки, обладать эндосомолитической активностью или обладать модулирующими PK свойствами. В предпочтительном варианте осуществления все лиганды обладают различными свойствами.
Лиганды можно присоединять к олигонуклеотидам в различных местах, например, на 3'-конце, 5'-конце и/или во внутреннем участке. В предпочтительных вариантах осуществления лиганд присоединен к олигонуклеотидам через промежуточную связь, например, носитель, описываемый в настоящем описании. Лиганд или связанный лиганд может содержаться в мономере, когда мономер встраивается в растущую цепь. В некоторых вариантах осуществления лиганд можно вводить путем связывания с мономером-"предшественником", после того как мономер-"предшественник" был встроен в растущую цепь. Например, мономер, содержащий, к примеру, аминоконцевую связь (т.е. содержащий не связанный лиганд), например, TAP-(CH2)nNH2, может встраиваться в растущую олигонуклеотидную цепь. На последующей стадии, т.е. после встраивания мономера-предшественника в цепь, затем можно присоединять лиганд, содержащий электрофильную группу, например, группу сложного пентафторфенильного эфира или альдегидную группу, к мономеру-предшественнику путем присоединения электрофильной группы лиганда с концевой нуклеофильной группой связи мономера-предшественника.
В другом примере можно вводить мономер, содержащий химическую группу, подходящую для участия в реакции "клик-химии", например, заканчивающуюся азидом или алкином связь/линкер. На последующей стадии, т.е. после введения мономер-предшественника в цепь, к мономеру-предшественнику можно присоединять лиганд, содержащий комплементарную химическую группу, например, алкин или азид, путем связывания алкина и азида друг с другом.
Для двухцепочечных олигонуклеотидов лиганды можно присоединять к одной или обеим цепям. В некоторых вариантах осуществления двухцепочечное средство на основе иРНК содержит лиганд, конъюгированный со смысловой цепью. В других вариантах осуществления двухцепочечное средство на основе иРНК содержит лиганд, конъюгированный с антисмысловой цепью.
В некоторых вариантах осуществления лиганд может быть конъюгирован с нуклеиновыми основаниями, группами сахаров, или межнуклеотидными связями молекул нуклеиновой кислоты. Конъюгация с пуриновыми нуклеиновыми основаниями или их производными может происходить в любом положении, включая эндоциклические и экзоциклические атомы. В некоторых вариантах осуществления 2-, 6-, 7- или 8-положений пуринового нуклеинового основания являются связанными с группой конъюгата. Конъюгация с пиримидиновыми нуклеиновыми основаниями или их производными также может находиться в любом положении. В некоторых вариантах осуществления 2-, 5- и 6-положения пиримидинового нуклеинового основания можно заменять группой конъюгата. Конъюгация с группами сахаров нуклеозидов может находиться при любом атоме углерода. Пример атомов углерода групп сахаров, которые могут быть связаны с группой конъюгата, включают 2'-, 3'- и 5'-атомы углерода. Положение 1' также можно присоединять к группе конъюгата, такой как в остатке с удаленными азотистыми основаниями. Межнуклеозидные связи также могут нести группы конъюгата. Для содержащих фосфор связей (например, фосфодиэфиров, тиофосфата, фосфородитиоата, фосфороамидата и т.п.) группу конъюгата можно присоединять непосредственно к атому фосфора или к атому O, N или S, связанному с атомом фосфора. Для содержащих амины или амиды межнуклеозидных связей (например, PNA) группу конъюгата можно присоединять к атому азота амина или амида или к прилежащему атому углерода.
Можно использовать любой подходящий лиганд в области РНК-интерференции, хотя лиганд, как правило, представляет собой углевод, например, моносахарид (такой как GalNAc), дисахарид, трисахарид, тетрасахарид, полисахарид.
Линкеры, которые конъюгируют лиганд с нуклеиновой кислотой, включают описанные выше линкеры. Например, лиганд может представлять собой одно или более производных GalNAc (N-ацетилглюкозамина), присоединенных посредством двухвалентного или трехвалентного разветвленного линкера.
В одном из вариантов осуществления дцРНК по изобретению конъюгирована с двухвалентными и трехвалентными разветвленными линкерами, содержащими структуры, представленные в любой из формул (IV)-(VII):



где:
q2A, q2B, q3A, q3B, q4A, q4B, q5A, q5B и q5C представляют собой независимо в каждом случае 0-20, и где повторяющиеся единицы могут быть одинаковыми или различными;
p2A, p2B, p3A, p3B, p4A, p4B, p5A, p5B, p5C, T2A, T2B, T3A, T3B, T4A, T4B, T5A, T5B, T5C каждый независимо в каждом случае отсутствует, представляют собой CO, NH, O, S, OC(O), NHC(O), CH2, CH2NH или CH2O;
Q2A, Q2B, Q3A, Q3B, Q4A, Q4B, Q5A, Q5B, Q5C независимо в каждом случае отсутствуют, представляют собой алкилен, замещенный алкилен, где один или более метиленов могут прерываться или оканчиваться одним или более из O, S, S(O), SO2, N(RN), C(R')=C(Rʺ), C≡C или C(O);
R2A, R2B, R3A, R3B, R4A, R4B, R5A, R5B, R5C каждый независимо для каждого случая отсутствует, представляет собой NH, O, S, CH2, C(O)O, C(O)NH, NHCH(Ra)C(O), -C(O)-CH(Ra) -, NH-, CO, CH=N-O,

L2A, L2B, L3A, L3B, L4A, L4B, L5A, L5B и L5C представляют собой лиганд, т.е. каждый независимо в каждом случае представляет собой моносахарид (такой как GalNAc), дисахарид, трисахарид, тетрасахарид, олигосахарид или полисахарид, и Ra представляет собой H или боковую цепь аминокислоты.
Трехвалентные производные конъюгации GalNAc являются особенно пригодными для использования со средствами для РНКи для ингибирования экспрессии гена-мишени, такие как производные формулы (VII):

где L5A, L5B и L5C представляют собой моносахарид, такой как производное GalNAc.
Примеры подходящих двухвалентных и трехвалентных разветвленных линкерных групп, конъюгирующих с производными GalNAc, включают, но не ограничиваются ими, следующие соединения:



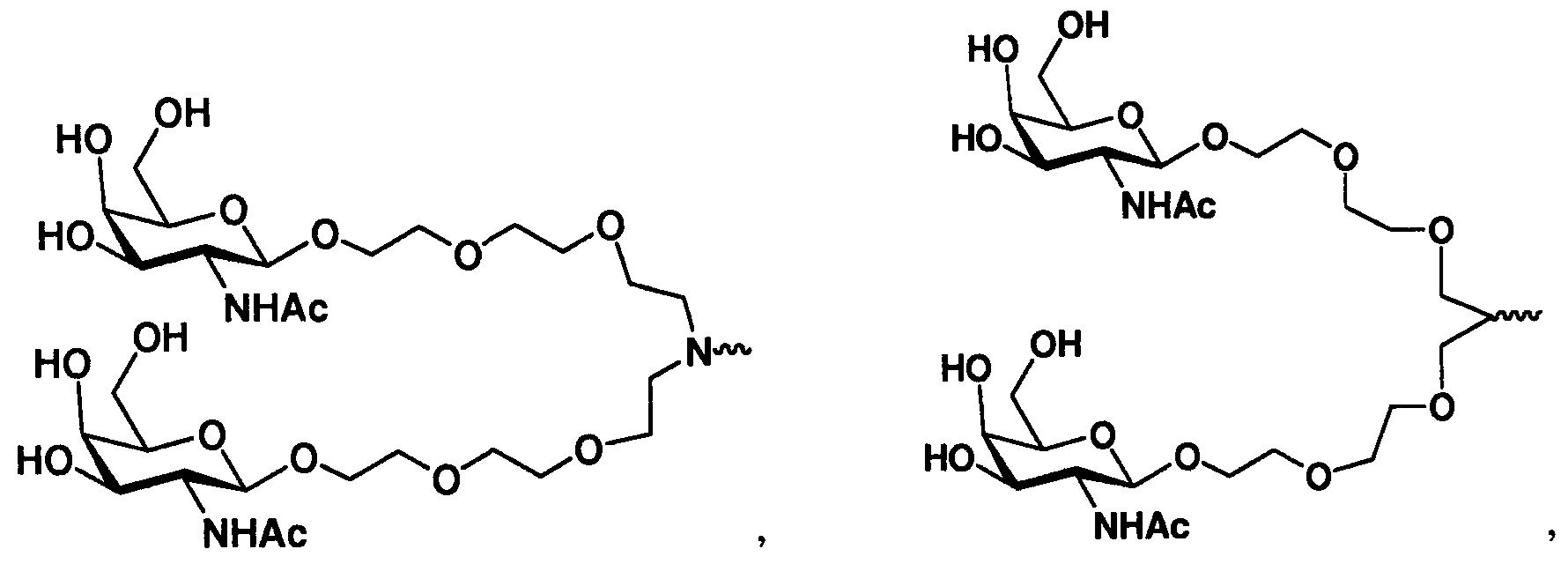




В других вариантах осуществления средство для РНКи по изобретению представляет собой средство, выбранное из группы, состоящей из AD-45163, AD-45165, AD-51544, AD-51545, AD-51546 и AD-51547.
III. Фармацевтические композиции
Средства для РНКи по изобретению можно формулировать для введения любым подходящим путем для применения для человека или в ветеринарной медицине, по аналогии с другими фармацевтическими средствами. Фармацевтические композиции, содержащие средства для РНКи по изобретению могут представлять собой, например, растворы с буфером или без него, или композиции, содержащие фармацевтически приемлемые носители. Такие композиции включают, например, водные или кристаллические композиции, липосомальные составы, мицеллярные составы, эмульсии и генотерапевтические векторы.
В способах по изобретению, средство для РНКи можно вводить в растворе. Свободное средство для РНКи можно вводить в незабуференном растворе, например, в физиологическом раствор или в воде. Альтернативно, свободные миРНК также можно вводить в подходящем буферном растворе. Буферный раствор может содержать ацетат, цитрат, проламин, карбонат или фосфат, или любую их комбинацию. В предпочтительном варианте осуществления буферный раствор представляет собой фосфатно-солевой буфер (PBS). pH и осмолярность буферного раствора, содержащего средство для РНКи, можно регулировать таким образом, чтобы он являлся подходящим для введения индивидууму.
В некоторых вариантах осуществления буферный раствор дополнительно содержит средство для регуляции осмолярности раствора, таким образом, чтобы поддерживать осмолярность при желаемом значении, например, при физиологических значениях плазмы человека. Растворенные вещества, которые можно добавлять в буферный раствор для регуляции осмолярности включают, но не ограничиваются ими, белки, пептиды, аминокислоты, неметаболизируемые полимеры, витамины, ионы, сахара, метаболиты, органические кислоты, липиды или соли. В некоторых вариантах осуществления средство для регуляции осмолярности раствора представляет собой соль. В определенных вариантах осуществления средство для регуляции осмолярности раствора представляет собой хлорид натрия или хлорид калия.
В других вариантах осуществления средство для РНКи формулируют в виде композиции, которая содержит одно или более средств для РНКи и фармацевтически приемлемый носитель. Как используют в настоящем описании, формулировка "фармацевтически приемлемый носитель" предназначена включать любой и все растворители, диспергирующие среды, покрытия, антибактериальные и противогрибковые средства, изотонические и замедляющие всасывание средства и т.п., совместимые с фармацевтическим введением. Использование таких сред и средств для фармацевтически активных веществ хорошо известно в данной области. За исключением случаев, когда любая общепринятая среда или средство является несовместимым с активным соединением, предусматривают его использование в композициях. В композиции также можно вводить дополнительные активные соединения.
В одном из вариантов осуществления препарат средства для РНКи содержит по меньшей мере второе терапевтическое средство (например, средство, отличное от РНК или ДНК). Например, композиция средства для РНКи для лечения ассоциированного с TTR заболевания, например, связанного с транстиретином наследственного амилоидоза (семейной амилоидной полинейропатии, FAP), может содержать известное лекарственное средство для улучшения состояния FAP, например, тафамидис (INN или Fx-1006A, или Vyndaqel).
Формулируемая композиция средства для РНКи может находиться в различных состояниях. В некоторых примерах композиция является по меньшей мере частично кристаллической, однородно кристаллической и/или безводной (например, она содержит менее 80, 50, 30, 20 или 10% воды). В другом примере средство для РНКи находится в водной фазе, например, в растворе, который содержит воду.
Композиции с водной фазой или кристаллические композиции можно вводить в носитель, например, липосому (в частности для водной фазы) или частицу (например, микрочастицу, как может являться подходящим для кристаллической композиции). Как правило, композицию средства для РНКи формулируют таким способом, что она является совместимой с предполагаемым способом введения, как описано в настоящем описании. Например, в конкретных вариантах осуществления композицию получают по меньшей мере одним из следующих ниже способов: сушкой распылением, лиофилизацией, вакуумной сушкой, выпариванием, сушкой в псевдоожиженном слое, или комбинацией этих техник, или обработкой ультразвуком с липидом, сушкой вымораживанием, конденсацией и другими способами самосборки.
Препарат средства для РНКи можно формулировать в комбинации с другим средством, например, другим терапевтическим средством или средством, которое стабилизирует средство для РНКи, например, белком, который образует комплекс со средством для РНКи с образованием иРНК. Еще другие средства включают хелаторы, например, EDTA (например, для удаления двухвалентных катионов, таких как Mg2+, соли, ингибиторы РНКазы (например, ингибитор РНКазы с широкой специфичностью, такой как RNAsin) и т.д.
В одном из вариантов осуществления препарат средства для РНКи содержит другое соединение миРНК, например, второе средство для РНКи, которое может опосредовать РНКи в отношении второго гена или в отношении того же самого гена. Еще один другой препарат может содержать по меньшей мере 3, 5, десять, двадцать, пятьдесят или сто или более различных видов средств для РНКи. Такие средства для РНКи могут опосредовать РНКи в отношении аналогичного числа различных генов.
Средства на основе иРНК по изобретению можно формулировать для фармацевтического применения. Фармацевтически приемлемые композиции содержат терапевтически или профилактически эффективное количество одного или более средств на основе дцРНК в любом из предшествовавших вариантов осуществления, взятых отдельно или формулируемых совместно с одним или более фармацевтически приемлемых носителей (добавок), эксципиентом и/или разбавителей.
Способы получения фармацевтических композиции по изобретению включают этап приведения средства для РНКи по настоящему изобретению в контакт с носителем и необязательно с один или более вспомогательных ингредиентов. Как правило, композиции получают путем равномерного и однородного приведения средства для РНКи по настоящему изобретению в контакт с жидкими носителями или тонкоизмельченными твердыми носителями, или обоими, а затем при необходимости придавая форму продукту.
Фармацевтические композиции можно конкретно формулировать для введения в твердой или жидкой форме, включая формы, адаптированные для следующего: (1) перорального введения, например, пропитки (водные или неводные растворы или суспензии), таблетки, например, таблетки, предназначенные для буккального, сублингвального и системного всасывания, болюсы, порошки, гранулы, пасты для нанесения на язык; (2) парентерального введения, например, посредством подкожной, внутримышечной, внутривенной или эпидуральной инъекции, например, в виде стерильного раствор или суспензии или состава с длительным высвобождением; (3) местного применения, например, в виде крема, мази или пластыря с контролируемым высвобождением или спрея, наносимого на кожу; (4) внутривлагалищно или интраректально, например, в виде пессарий, крема или пены; (5) сублингвально; (6) окулярно; (7) трансдермально или (8) назально. Доставка с использованием подкожных или внутривенных способов может являться особенно эффективной.
Фразу "фармацевтически приемлемый" применяют в настоящем описании для обозначения таких соединений, веществ, композиций и/или лекарственных форм, которые с медицинской точки зрения являются пригодными для использования при контактирование с тканями человека и животных, не вызывая повышенную токсичность, раздражение, аллергический ответ или другую проблему или осложнение, в соответствии с обоснованным отношением польза/риск.
Фраза "фармацевтически приемлемый носитель", как используют в настоящем описании, означает фармацевтически приемлемое вещество, композицию или носитель, такой как жидкий или твердый наполнитель, разбавитель, эксципиент, вспомогательное для производства средство (например, смазочное средство, тальк, стеарат магния, кальция или цинка или стеариновую кислоту) или инкапсулирующее растворитель вещество, участвующее в переносе или транспорте рассматриваемого соединения из одного органа или отдела организма в другой орган или отдел организма. Каждый носитель должен являться "приемлемым" в том смысле, что является совместимым с другими ингредиентами композиции и не вредный для пациента. Некоторые примеры веществ, которые могут служить в качестве фармацевтически приемлемых носителей, включают: (1) сахара, такие как лактоза, глюкоза и сахароза; (2) крахмалы, такие как кукурузный крахмал и картофельный крахмал; (3) целлюлозу и ее производные, такие как карбоксиметилцеллюлоза натрия, этилцеллюлоза и ацетатцеллюлозы; (4) порошкообразный трагакант; (5) солод; (6) желатин; (7) смазки, такие как стеарат магния, лаурилсульфат натрия и тальк; (8) эксципиенты, такие как масло какао и воски для суппозиториев; (9) масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; (10) гликоли, такие как пропиленгликоль; (11) полиолы, такие как глицерин, сорбит, маннит и полиэтиленгликоль; (12) сложные эфиры, такие как этилолеат и этиллаурат; (13) агар; (14) буферные средства, такие как гидроксид магния и гидроксид алюминия; (15) альгиновую кислоту; (16) апирогенную воду; (17) изотонический физиологический раствор; (18) раствор Рингера; (19) этиловый спирт; (20) pH забуференные растворы; (21) сложные полиэфиры, поликарбонаты и/или полиангидриды; (22) наполнители, такие как полипептиды и аминокислоты; (23) компонент сыворотки, такой как сывороточный альбумин, HDL и LDL, и (22) другие нетоксические совместимые вещества, применяемые в фармацевтических композициях.
Композиции можно подходящим способом предоставлять в стандартной лекарственной форме и можно получать любыми способами, хорошо известными в данной области фармацевтики. Количество средства для РНКи, которое можно комбинировать с веществом носителя для получения однократной лекарственной формы изменяется в зависимости от подлежащего лечению хозяина и конкретного способа введения. Средство для РНКи, которое можно комбинировать с веществом носителя для получения однократной лекарственной формы, как правило, представляет собой такое количество средства для РНКи, которое оказывает желаемое действие, например, терапевтическое или профилактическое действие. Как правило, из ста процентов такое количество находится в диапазоне приблизительно от 0,1 процентов приблизительно до девяноста девяти процентов средства для РНКи, предпочтительно приблизительно от 5 процентов приблизительно до 70 процентов, наиболее предпочтительно приблизительно от 10 процентов приблизительно до 30 процентов.
В определенных вариантах осуществления композиция по настоящему изобретению содержит эксципиент, выбранный из группы, состоящей из циклодекстринов, целлюлоз, липосом, образующих мицеллу средств, например, желчных кислот, и полимерных носителей, например, сложных полиэфиров и полиангидридов, и средство для РНКи по настоящему изобретению. В определенных вариантах осуществления указанная выше композиция обеспечивает перорально биодоступное средство для РНКи по настоящему изобретению.
В некоторых случаях с целью продления эффекта средства для РНКи желательным является замедление всасывания средства от подкожной или внутримышечной инъекции. Это можно получать с использованием жидкой суспензии кристаллического или аморфного вещества со слабой растворимостью в воде. Скорость всасывания средства для РНКи в дальнейшем зависит от его скорости растворения, которая в свою очередь может завесить от размера кристалла и кристаллической формы. Альтернативно, замедленное всасывание парентерально вводимого средства для РНКи можно получать посредством растворения или суспендирования средства в масляном носителе.
Липосомы
Средство для РНКи по изобретению можно формулировать для доставки в мембранном молекулярном агрегате, например, липосоме или мицелле. Как используют в настоящем описании, термин "липосома" относится к везикуле, состоящей из амфифильных липидов, располагаемых по меньшей мере в один бислой, например, один бислой или ряд бислоев. Липосомы включают однослойные и многослойные везикулы, которые содержат мембрану, образованную из липофильного вещества и водного внутреннего содержимого. Водная часть содержит композицию средства для РНКи. Липофильное вещество изолирует водное внутреннее содержимое от водного внешнего содержимого, которое, как правило, не содержит композицию средства для РНКи, хотя в некоторых примерах может содержать. Липосомы пригодны для переноса и доставки активных ингредиентов в участок приложения действия. Вследствие того, что липосомальная мембрана является структурно сходной с биологической мембраной, когда липосомы наносят на ткань, липосомальный бислой сливается с бислоем клеточных мембран. По мере прогрессирования слияния липосомы и клетки происходит доставка внутреннего водного содержимого, которое содержит средство для РНКи, в клетку, где средство для РНКи может специфически связываться с РНК-мишенью и может опосредовать РНКи. В некоторых случаях липосомы также являются конкретно направленными, например, для направленной доставки средства для РНКи в конкретные типы клеток.
Липосому, содержащую средство для РНКи, можно получать различными способами. В одном из примеров липидный компонент липосомы растворяют в детергенте, таким образом, чтобы образовывались мицеллы с липидным компонентом. Например, липидный компонент может представлять собой амфипатический катионный липид или липидный конъюгат. Детергент может иметь высокую критическую концентрацию мицелл и может быть неионным. Иллюстративные детергенты включают холаты, CHAPS, октилглюкозид, дезоксихолат и лауроилсаркозин. Препарат средства для РНКи затем добавляют к мицеллам, которые содержат липидный компонент. Катионные группы в липиде взаимодействуют со средством для РНКи и конденсируются вокруг средства для РНКи с образованием липосомы. После конденсации детергент удаляют, например, посредством диализа, с получением липосомального препарата средства для РНКи.
При необходимости можно добавлять соединение носителя, которое способствует конденсации, в ходе реакции конденсации, например, путем контролируемого добавления. Например, соединение носителя может представлять собой полимер, отличный от нуклеиновой кислоты (например, спермин или спермидин). Также можно регулировать pH, чтобы способствовать конденсации.
Способы получения стабильных носителей для доставки полинуклеотида, которые содержат комплекс полинуклеотид/катионный липид в виде структурного компонента носителя для доставки, дополнительно описаны, например, в WO 96/37194, полное содержание которой включено в настоящее описание посредством ссылки. Получение липосом также моет включать один или более аспектов иллюстративных способов, описанных у Feigner P.L. et al., Proc. Natl. Acad. Sci., USA 8:7413-7417, 1987; в патенте США №4897355; патенте США №5171678; у Bangham et al., M. Mol. Biol., 23:238, 1965; Olson et al., Biochim. Biophys. Acta, 557:9, 1979; Szok, et al., Proc. Natl. Acad. Sci., 75:4194, 1978; Mayhew et al., Biochim. Biophys. Acta, 775:169, 1984. Kim et al., Biochim. Biophys. Acta, 728:339, 1983, и Fukunaga et al., Endocrinol., 115:757, 1984. Широко используемые способы получения липидных агрегатов подходящего размера для применения в качестве носителей для доставки включают обработку ультразвуком и сушку вымораживанием плюс экструзия (см., например, Mayer et al., Biochim. Biophys. Acta, 858:161, 1986). Можно использовать микрофлюидизацию, когда желательны сопоставимые небольшие (от 50 до 200 нм) и относительно однородные агрегаты (Mayhew et al., Biochim. Biophys. Acta, 775:169, 1984). Эти способы можно легко адаптировать для упаковки препаратов средства для РНКи в липосомы.
Липосомы, которые являются чувствительными к pH или отрицательно заряженными, улавливают молекулы нуклеиновой кислоты, а не комплекс с ними. Вследствие того, что молекулы нуклеиновой кислоты и липида являются одинаково заряженными, происходит отталкивание, а не образование комплекса. Однако некоторые молекулы нуклеиновой кислоты удерживаются в водном внутреннем содержимом таких липосом. Использовали чувствительные к pH липосомы для доставки ДНК, кодирующей ген тимидинкиназы, в монослои клеток в культуре. Экспрессию экзогенного гена детектировали в клетках-мишенях (Zhou et al., Journal of Controlled Release, 19, (1992) 269-274).
Один основной тип липосомальной композиции включает фосфолипиды, отличные от природного фосфатидилхолина. Композиции нейтральных липосом, например, можно получать из димиристоилфосфатидилхолина (DMPC) или дипальмитоилфосфатидилхолина (DPPC). Композиции анионных липосом, как правило, получают из димиристоилфосфатидилглицерина, тогда как способствующие слиянию анионные липосомы получают преимущественно из диолеоилфосфатидилэтаноламина (DOPE). Другой тип липосомальной композиции получают из фосфатидилхолина (PC), такого как, например, соевый PC и яичный PC. Другой тип получают из смеси фосфолипида и/или фосфатидилхолина, и/или холестерина.
Примеры других способов введения липосом в клетки in vitro и in vivo включают патент США №5283185, патент США №5171678, WO 94/00569, WO 93/24640, WO 91/16024, Feigner J., Biol. Chem., 269:2550, 1994, Nabel, Proc. Natl. Acad. Sci., 90:11307, 1993, Nabel, Human Gene Ther., 3:649, 1992, Gershon, Biochem., 32:7143, 1993, и Strauss, EMBO J., 11:417, 1992.
В одном из вариантов осуществления используют катионные липосомы. Катионные липосомы обладают преимуществом, заключающемся в том, что они способны сливаться с клеточной мембраной. Некатионные липосомы, хотя не способны так эффективно сливаться с плазматической мембраной, поглощаются макрофагами in vivo, и их можно использовать для доставки средства для РНКи в макрофаги.
Дополнительные преимущества липосом включают: липосомы, получаемые из природных фосфолипидов, являются биосовместимыми и биоразлагаемыми; липосомы могут содержать широкий спектр растворимых в воде и липидах лекарственных средств; липосомы могут защищать инкапсулированные средства для РНКи в своих внутренних компартментах от метаболизма и деградации (Rosoff в "Pharmaceutical Dosage Forms", Lieberman, Rieger and Banker (Eds.), 1988, volume 1, p. 245). Важными рассматриваемыми факторами при получении липосомных составов является поверхностный заряд липидов, размер везикул и водный объем липосомы.
Можно использовать положительно заряженный синтетический катионный липид N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламонийхлорид (DOTMA) для получения небольших липосом, которые спонтанно взаимодействуют с нуклеиновой кислотой с образованием комплексов липид-нуклеиновая кислота, которые способны сливаться с отрицательно заряженными липидами клеточных мембран клеток тканых культур, приводя к доставке средства для РНКи (для описания DOTMA и его применения с ДНК см., например, Feigner, P.L. et al., Proc. Natl. Acad. Sci., USA 8:7413-7417, 1987, и патент США №4897355).
Аналог DOTMA 1,2-бис(олеоилокси)-3-(триметиламмоний)пропан (DOTAP) можно использовать в комбинации с фосфолипидом для получения везикул, образующих комплекс с ДНК. Lipofectin™ (Bethesda Research Laboratories, Gaithersburg, Md.) представляет собой эффективное средство для доставки высоко анионных нуклеиновых кислот в живые клетки тканевых культур, которые содержат положительно заряженные липосомы DOTMA, которые спонтанно взаимодействуют с отрицательно заряженными полинуклеотидами с образованием комплексов. Когда используют достаточно положительно заряженные липосомы, суммарный заряд на получаемых комплексах также является положительным. Положительно заряженные комплексы, получаемые таким образом, спонтанно присоединяются к отрицательно заряженным клеточным поверхностям, сливаются с плазматической мембраной и эффективно доставляют функциональные нуклеиновые кислоты, например, в клетки тканевой культуры. Другой коммерчески доступный катионный липид 1,2-бис(олеоилокси)-3,3-(триметиламмоний)пропан ("DOTAP") (Boehringer Mannheim, Indianapolis, Indiana) отличается от DOTMA тем, что группы олеоила связаны сложноэфирными, а не простыми эфирными связями.
Другие репортерные соединения катионных липидов включают такие, которые конъюгированы с рядом молекул, включая, например, карбоксиспермин, который конъюгирован с одним из двух типов липидов и включает соединения, такие как 5-карбоксиспермилглициндиоктаолеоиламид ("DOGS") (Transfectam™, Promega, Madison, Wisconsin) и дипальмитоилфосфатидилэтаноламин-5-карбоксиспермиламид ("DPPES") (см., например, патент США №5171678).
Другой конъюгат катионного липида включает производное липида и холестерина ("DC-Chol"), которое формулируют в липосомы в комбинации с DOPE (см., Gao X. and Huang L., Biochim. Biophys. Res. Commun., 179:280, 1991). Опубликовано, что липополилизин, получаемый конъюгацией полилизина с DOPE, является эффективным для трансфекции в присутствии сыворотки (Zhou X. et al., Biochim. Biophys. Acta, 1065:8, 1991). Указано, что для определенных линий клеток такие липосомы, содержащие конъюгированные катионные липиды, проявляют более низкую токсичность и обеспечивают более эффективную трансфекцию по сравнению с содержащими DOTMA композициями. Другие коммерчески доступные продукты катионных липидов включают DMRIE и DMRIE-HP (Vical, La Jolla, California) и липофектамин (DOSPA) (Life Technology, Inc., Gaithersburg, Maryland). Другие катионные липиды, подходящие для доставки олигонуклеотидов, описаны в WO 98/39359 и WO 96/37194.
В частности, липосомальные составы исследуют с целью местного введения, липосомы предоставляют несколько преимуществ перед другими составами. Такие преимущества включают сниженные побочные эффекты, связанные с высоким системным всасыванием вводимого лекарственного средства, повышенным накоплением вводимого лекарственного средства в желаемой мишени и возможность введения средства для РНКи в кожу. В некоторых реализациях липосомы используют для доставки средства для РНКи в эпидермальные клетки, а также для повышения проникновения средства для РНКи в дермальные ткани, например, в кожу. Например, липосомы можно применять местно. Документально описана местная доставка лекарственных средств, формулируемых в виде липосом, в кожу (см., например, Weiner et al., Journal of Drug Targeting, 1992, vol. 2, 405-410 и du Plessis et al., Antiviral Research, 18, 1992, 259-265, Mannino R.J. and Fould-Fogerite S., Biotechniques 6:682-690, 1988, Itani T. et al., Gene, 56:267-276, 1987, Nicolau C. et al., Meth. Enz., 149:157-176, 1987, Straubinger R.M. and Papahadjopoulos D., Meth. Enz., 101:512-527, 1983, Wang C.Y. and Huang L., Proc. Natl. Acad. Sci. USA, 84:7851-7855, 1987).
Также исследовали неионные липосомальные системы для определения их пригодности для доставки лекарственных средств в кожу, в частности системы, содержащие неионное поверхностно-активное вещество и холестерин. Использовали неионные липосомальные составы, содержащие новасом I (глицерилдилаурат/холестерин/полиоксиэтилен-10-стеариловый эфир) и новасом II (глицерилдистеарат/холестерин/полиоксиэтилен-10-стеариловый эфир), в отношении доставки лекарственного средства в дерму кожи мыши. Такие составы со средством для РНКи являются пригодными для лечения дерматологического нарушения.
Липосомы, которые содержат средство для РНКи, можно получать как высоко деформируемые. Такая деформируемость может способствовать тому, что липосомы проникают через пору, которая является меньше, чем средний радиус липосомы. Например, трансферсомы представляют собой тип деформируемых липосом. Трансферсомы можно получать путем добавления активаторов поверхности раздела фаз, как правило, поверхностно-активных веществ, в стандартную липосомальную композицию. Трансферсомы, которые содержат средство для РНКи, можно доставлять, например, подкожно посредством инфекции с целью доставки средства для РНКи в кератиноциты в коже. Для прохождения через интактную млекопитающих кожу липидные везикулы должны пройти через ряд мелких пор, где диаметром каждой составляет менее 50 нм, под действием подходящего трансдермального градиента. Кроме того, благодаря свойствам липидов такие трансферсомы могут самоорганизовываться (адаптируются к форме пор, например, в коже), саморепарации и могут часто достигать свои мишени без фрагментации и часто являются самонагружающимися.
Другие составы, пригодные по настоящему изобретению, описаны во временной заявки на патент США с серийным №61/018616, поданной 2 января 2008 года, 61/018611, поданной 2 января 2008 года, 61/039748, поданной 26 марта 2008 года, 61/047087, поданной 22 апреля 2008 года, и 61/051528, поданной 8 мая 2008 года. В заявке PCT № PCT/US 2007/080331, поданной 3 октября 2007 года, также описаны составы, которые являются пригодными для настоящего изобретения.
Поверхностно-активные вещества
Поверхностно-активные вещества находят широкое применение в составах, таких как эмульсии (включая микроэмульсии) и липосомы (см. выше). Композиции средства для РНКи (или предшественник, например, более крупная дц-иРНК, которая может подвергаться процессингу до миРНК, или ДНК, которая кодирует миРНК или предшественник) могут содержать поверхностно-активное вещество. В одном из вариантов осуществления миРНК формулируют в виде эмульсии, которая содержит поверхностно-активное вещество. Наиболее распространенный путь классификации и ранжирования свойств многих различных типов поверхностно-активных веществ, как природных, так и синтетических, сводится к использованию гидрофильного/липофильного баланса (HLB). Для определения категории различных поверхностно-активных веществ, используемых в составах, наиболее часто применяемым критерием является природа гидрофильной группы (Rieger, in "Pharmaceutical Dosage Forms", Marcel Dekker, Inc., New York, NY, 1988, p. 285).
Если молекула поверхностно-активного вещества не является ионизированной, его классифицируют как неионное поверхностно-активное вещество. Неионные поверхностно-активные вещества находят широкое применение в фармацевтических препаратах и являются пригодными в широком диапазоне значений pH. В основном их значения HLB находятся в диапазоне от 2 приблизительно до 18 в зависимости от их структуры. Неионные поверхностно-активные вещества включают неионные сложные эфиры, такие как сложные эфиры этиленгликоля, сложные эфиры пропиленгликоля, сложные эфиры глицерина, сложные эфиры полиглицерина, сложные эфиры сорбитана, сложные эфиры сахарозы и этоксилированные сложные эфиры. В этот класс также входят неионные алканоламиды и простые эфиры, такие как этоксилаты жирных спиртов, пропоксилированные спирты и этоксилированные/пропоксилированные блокполимеры. Поверхностно-активные вещества на основе полиоксиэтилена являются наиболее популярными представителями класса неионных поверхностно-активных веществ.
Если молекула поверхностно-активного вещества несет отрицательный заряд, когда ее растворяют или диспергируют в воде, поверхностно-активное вещество классифицируют как анионное. Анионные поверхностно-активные вещества включают карбоксилаты, такие как мыла, ациллактилаты, ациламиды аминокислот, сложные эфиры серной кислоты, такие как алкилсульфаты и этоксилированные алкилсульфаты, сульфонаты, такие как алкилбензолсульфонаты, ацилизетионаты, ацилтаураты и сульфосукцинаты и фосфаты. Наиболее важные представители класса анионных поверхностно-активных веществ представляют собой алкилсульфаты и мыла.
Если молекула поверхностно-активного вещества несет положительный заряд, когда ее растворяют или диспергируют в воде, поверхностно-активное вещество классифицируют как катионное. Катионные поверхностно-активные вещества включают четвертичные аммонийные соли и этоксилированные амины. Четвертичные аммонийные соли являются наиболее используемыми представителями этого класса.
Если молекула поверхностно-активного вещества обладает способностью нести положительный или отрицательный заряд, поверхностно-активное вещество классифицируют как амфотерное. Амфотерные поверхностно-активные вещества включают производные акриловой кислоты, замещенные алкиламиды, N-алкилбетаины и фосфолипиды.
Использование поверхностно-активных веществ в лекарственных продуктах, составах и в эмульсиях описано в литературе (Rieger, in "Pharmaceutical Dosage Forms", Marcel Dekker, Inc., New York, NY, 1988, p. 285).
Мицеллы и другие мембранные составы
Средства для РНКи по изобретению также можно предоставлять в виде мицеллярных составов. "Мицеллы" определяют в настоящем описании как конкретный тип молекулярного агрегата, в котором амфипатические молекулы располагаются в сферическую структуру, таким образом, что все гидрофобные участки молекулы являются направленными внутрь, оставляя гидрофильные участки в контакте с окружающей водной фазой. Существует обратное расположение, если окружающая среда является гидрофобной.
Смешанный мицеллярный состав, подходящий для доставки через трансдермальные мембраны можно получать смешиванием водного раствора композиции миРНК, C8-C22алкилсульфата щелочного металла и образующего мицеллы соединения. Иллюстративные образующие мицеллы соединения включают лецитин, гиалуроновую кислоту, фармацевтически приемлемые соли гиалуроновой кислоты, гликолевую кислоту, молочную кислоту, экстракт ромашки, экстракт огурца, олеиновую кислоту, линолевую кислоту, линоленовую кислоту, моноолеин, моноолеаты, монолаураты, масло бурачника, масло энотеры, ментол, тригидроксиоксохоланилглицин и его фармацевтически приемлемые соли, глицерин, полиглицерин, лизин, полилизин, триолеин, простые эфиры полиоксиэтилена и их аналоги, простые полидоканолалкиловые эфиры и их аналоги, хенодезоксихолат, дезоксихолат и их смеси. Образующие мицеллы соединения можно добавлять одновременно или после добавления алкилсульфата щелочного металла. Смешанные мицеллы образуются по существу при любом типе перешивания ингредиентов, но при интенсивном перемешивании для обеспечения мицелл с меньшим размером.
В одном из способом получают первую мицеллярную композицию, которая содержит композицию миРНК и по меньшей мере алкилсульфат щелочного металла. Затем первую мицеллярную композицию смешивают по меньшей мере с тремя образующими мицеллы соединениями для получения смешанной мицеллярной композиции. В другом способе мицеллярную композицию получают смешиванием композиции миРНК, алкилсульфата щелочного металла и по меньшей мере одного из образующих мицеллы соединений с последующим добавлением оставшихся образующих мицеллы соединений при интенсивном перемешивании.
К смешанной мицеллярной композиции можно добавлять фенол и/или мега-крезол для стабилизации состава и защиты от бактериального роста. Альтернативно, фенол и/или мега-крезол можно добавлять с образующими мицеллы ингредиентами. После получения смешанной мицеллярной композиции также можно добавлять средство придания изотоничности.
Для доставки мицеллярного состава в виде спрея состав можно помещать в аэрозольный распылитель и наполнять распылитель пропеллентом. Пропеллент, который находится под давлением, в распылителе находится в жидкой форме. Отношения ингредиентов регулируют таким образом, чтобы водная фаза и фаза пропеллента становились одной, т.е. присутствовала одна фаза. Если существует две фазы, необходимо встряхивать распылитель перед распылением части содержимого, например, через дозирующий клапан. Распыляемая доза фармацевтического средства дозируется из дозирующего клапана в виде тонкодисперсного спрея.
Пропелленты могут включать содержащие водород хлорфторуглероды, содержащие водород фторуглероды, простой диметиловый эфир и простой диэтиловый эфир. В определенных вариантах осуществления можно использовать HFA 134a (1,1,1,2-тетрафторэтан).
Конкретные концентрации основных ингредиентов можно определять относительно простым экспериментированием. Для всасывания через ротовую полость, как правило, желательным является повышение, например, по меньшей мере вдвое или втрое дозы посредством инъекции или введения через желудочно-кишечный тракт.
Частицы
В другом варианте осуществления средство для РНКи по изобретению можно вводить в частицу, например, микрочастицу. Микрочастицы можно получать сушкой распылением, а также можно получать другими способами, включая лиофилизацию, выпаривание, сушку в псевдоожиженном слое, вакуумную сушку или комбинацию этих техник.
IV. Способы ингибирования экспрессии TTR
Настоящее изобретение также относится к способам ингибирования экспрессии транстиретина (TTR) в клетке. Способы включают приведение клетки в контакт со средством для РНКи, например, двухцепочечным средством для РНКи, в количестве эффективном для ингибирования экспрессии TTR в клетке, таким образом, ингибируя экспрессию TTR в клетке.
Приведение клетки в контакт со средством для РНКи, например, двухцепочечным средством для РНКи, можно проводить in vitro или in vivo. Приведение клетки в контакт in vivo со средством для РНКи включает приведение клетки или группы клеток у индивидуума, например, являющегося человек индивидуума, в контакт со средством для РНКи. Также возможной является комбинация способов in vitro и in vivo приведения клетки в контакт. Приведение клетки в контакт может являться прямым или опосредованным, как указано выше. Кроме того, приведение клетки в контакт можно проводить путем направления лиганда, включая любой лиганд, описываемый в настоящем описании или известный в данной области. В предпочтительных вариантах осуществления направленный лиганд представляет собой углеводную группу, например, лиганд GalNAc3 или любой другой лиганд, который направляет средство для РНКи в представляющий интерес участок, например, печень индивидуума.
Термин "ингибирование", как используют в настоящем описании, используют взаимозаменяемо с "уменьшением", "подавлением", "снижением", "ослаблением" и другими аналогичными терминами, и он включает любой уровень ингибирования.
Фраза "ингибирование экспрессии TTR" предназначено обозначать ингибирование экспрессии любого гена TTR (такого как, например, гена TTR мыши, гена TTR крысы, гена TTR обезьяны или гена TTR человека), а также вариантов или мутантов гена TTR. Таким образом, ген TTR может представлять собой ген TTR дикого типа, мутантный ген TTR (такой как мутантный ген TTR, взывающий отложение амилоида) или трансгенный ген TTR в отношении клетки, группы клеток или организма, подвергнутых генетической манипуляции.
"Ингибирование экспрессии гена TTR" включает любой уровень ингибирования гена TTR, например, по меньшей мере частичное подавление экспрессии гена TTR. Экспрессию гена TTR можно оценивать на основании уровня или изменения уровня любой переменной, ассоциированной с экспрессией гена TTR, например, уровнем мРНК TTR, уровнем белка TTR или числом или степенью отложений амилоида. Такой уровень можно оценивать в индивидуальной клетке или в группе клеток, включая, например, образец, получаемый у индивидуума.
Ингибирование можно оценивать по снижению абсолютного или относительного уровня одной или более переменных, которые ассоциированы с экспрессией TTR, по сравнению с контрольным уровнем. Контрольный уровень может представлять собой любой тип контрольного уровня, который используют в данной области, например, исходный уровень до дозирования, или уровень, определяемый у аналогичного индивидуума, в клетке или в образце, который не обрабатывали или обрабатывали контролем (таким как, например, контроль только буфером или контроль только неактивным средством).
В некоторых вариантах осуществления способов по изобретению экспрессию гена TTR ингибируют по меньшей мере приблизительно на 5%, по меньшей мере приблизительно на 10%, по меньшей мере приблизительно на 15%, по меньшей мере приблизительно на 20%, по меньшей мере приблизительно на 25%, по меньшей мере приблизительно на 30%, по меньшей мере приблизительно на 35%, по меньшей мере приблизительно на 40%, по меньшей мере приблизительно на 45%, по меньшей мере приблизительно на 50%, по меньшей мере приблизительно на 55%, по меньшей мере приблизительно на 60%, по меньшей мере приблизительно на 65%, по меньшей мере приблизительно на 70%, по меньшей мере приблизительно на 75%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 91%, по меньшей мере приблизительно на 92%, по меньшей мере приблизительно на 93%, по меньшей мере приблизительно на 94%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98% или по меньшей мере приблизительно на 99%.
Ингибирование экспрессии гена TTR может проявляться в уменьшении количества мРНК, экспрессируемой первой клеткой или группой клеток (такие клетки могут содержаться, например, в образце, получаемом у индивидуума), в которых транскрибируется ген TTR, и которые обрабатывали (например, посредством приведения клетки или клеток в контакт со средством для РНКи по изобретению, или посредством введения средства для РНКи по изобретению индивидууму, у которого присутствуют или присутствовали клетки), таким образом, что ингибируют экспрессию гена TTR по сравнению со второй клеткой или группой клеток по существу идентичных первой клетке или группе клеток, но которые так не обрабатывали (как контрольную клетку(и)). В предпочтительных вариантах осуществления ингибирование оценивают по уровню экспрессии мРНК в обрабатываемых клетках в виде процентного содержания уровня мРНК в контрольных клетках с использованием следующей ниже формулы:

Альтернативно, ингибирование экспрессии гена TTR можно оценивать в отношении уменьшения параметра, который является функционально связанным с экспрессией гена TTR, например, экспрессия белка TTR, уровень ретинолсвязывающего белка, уровень витамина A или наличие отложений амилоида, содержащих TTR. Подавление экспрессии гена TTR можно определять в любой клетке, экспрессирующей TTR, конститутивно или в результате геномной инженерии, и любым известным в данной области анализом. Печень является основным участком экспрессии TTR. Другие значительные участки экспрессии включают хориоидное сплетение, сетчатку и поджелудочную железу.
Ингибирование экспрессии белка TTR может проявляться в снижении уровня белка TTR, который экспрессируется клеткой или группой клеток (например, уровня белка, экспрессируемого в образце, получаемом у индивидуума). Как объясняется выше, для оценки подавления мРНК ингибирование уровней экспрессии белка в обрабатываемых клетках или группе клеток можно аналогичным образом выражать в виде процента от уровня белка в контрольной клетке или группе клеток. Контрольная клетка или группа клеток, которые можно использовать для оценки ингибирования экспрессии гена TTR, включают клетку или группу клеток, которые еще не контактировали со средством для РНКи по изобретению. Например, контрольную клетку или группу клеток можно получать у отдельного индивидуума (например, являющегося человеком или животным индивидуума) для лечения индивидуума средством для РНКи.
Уровень мРНК TTR, который экспрессируется клеткой или группой клеток, или уровень циркулирующей мРНК TTR можно определять любым известным в данной области способом для оценки экспрессии мРНК. В одном из вариантов осуществления уровень экспрессии TTR в образце определяют путем детекции транскрибируемого полинуклеотида или его участка, например, мРНК гена TTR. РНК можно выделять из клетки способами выделения РНК, включая, например, выделение с использованием кислого фенола/гуанидинизотиоцианата (RNAzol B, Biogenesis), наборов RNeasy RNA preparation (Qiagen) или PAXgene (PreAnalytix, Switzerland). Характерные форматы анализа, в которых используют гибридизацию рибонуклеиновой кислоты, включают анализы транскрипции на изолированных ядрах, ПЦР с обратной транскрипцией, анализ с использованием защиты от РНКазы (Melton et al., Nuc. Acids Res., 12:7035), нозерн-блоттинг, гибридизацию in situ и анализ на микропанелях. Циркулирующую мРНК TTR можно детектировать способами, описанными в PCT/US 2012/043584, полное содержание которой, таким образом, включено в настоящее описание посредством ссылки.
В одном из вариантов осуществления уровень экспрессии TTR определяют с использованием зонда нуклеиновой кислоты. Термин "зонд", как используют в настоящем описании, относится к любой молекуле, которая способна селективно связываться с конкретным TTR. Специалист в данной области может синтезировать зонды, или их получают из соответствующих биологических препаратов. Зонды можно специально конструировать, чтобы они являлись мечеными. Примеры молекул, которые можно использовать в качестве зондов включают, но не ограничиваются ими, РНК, ДНК, белки, антитела и органические молекулы.
Выделяемую мРНК можно использовать в анализах гибридизации или амплификации, которые включают, но не ограничиваются ими, саузерн- или нозерн-анализы, анализы на основе полимеразной цепной реакции (ПЦР) и анализы с использованием зондов. Один из способов для определения уровней мРНК включает приведение выделенной мРНК в контакт с молекулой нуклеиновой кислоты (зондом), которая может гибридизоваться с мРНК TTR. В одном из вариантов осуществления мРНК иммобилизуют на твердой поверхности и приводят в контакт с зондом, например, посредством электрофореза выделенной мРНК в агарозном геле и переноса мРНК из геля на мембрану, такую как нитроцеллюлоза. В альтернативном варианте осуществления зонд(ы) иммобилизуют на твердой поверхности и приводят мРНК в контакт с зондом(ами), например, в анализе с использованием генного чипа Affymetrix. Специалист в данной области может легко адаптировать известные способы детекции мРНК для применения для определения уровня мРНК TTR.
Альтернативный способ определения уровня экспрессии TTR в образце включает процесс амплификации и/или обратной транскрипции нуклеиновой кислоты (с получением кДНК), например, мРНК в образце, например, ПЦР в реальном времени (экспериментальный вариант осуществления, указанный у Mullis, 1987, в патенте США №4683202), лигазной цепной реакцией (Barany, (1991) Proc. Natl. Acad. Sci. USA, 88:189-193), самоподдерживающуюся репликацию последовательностей (Guatelli et al., (1990) Proc. Natl. Acad. Sci. USA, 87:1874-1878), транскрипционно-опосредованную амплификационную систему (Kwoh et al., (1989) Proc. Natl. Acad. Sci. USA, 86:1173-1177), использование Q-бета репликазы (Lizardi et al., (1988) Bio/Technology, 6:1197), репликацию по типу "катящегося кольца" (Lizardi et al., патент США №5854033) или любой способ амплификации нуклеиновой кислоты с последующей детекцией амплифицируемых молекул с использованием хорошо известных специалистам в данной области техник. Такие схемы детекции являются особенно пригодными для детекции молекул нуклеиновой кислоты, в случае если такие молекулы содержатся в очень маленьких количествах. В конкретных аспектах изобретения уровень экспрессии TTR определяют количественной ПЦР в реальном времени с использованием флуорогенных зондов (т.е. системой TaqMan™).
Уровни экспрессии мРНК TTR можно наблюдать с использованием мембранного блота (такого как используют в анализе гибридизации, таком как нозерн-анализ, саузерн-анализ, дог-анализ и т.п.) или микролунок, пробирок, гелей, гранул или волокон (или любой твердой подложки, содержащей связанные нуклеиновые кислоты). См. патенты США №№5770722, 5874219, 5744305, 5677195 и 5445934, которые включены в настоящее описание посредством ссылки. Определение уровня экспрессии TTR также может включать использование зондов нуклеиновой кислоты в растворе.
В предпочтительных вариантах осуществления уровень экспрессии мРНК оценивают анализами разветвленной ДНК (pДНК) или с использованием ПЦР в реальном времени (qПЦР). Применение этих способов описано и проиллюстрировано в примерах, предоставленных в настоящем описании.
Уровень экспрессии белка TTR можно определять любым известным в данной области способом измерения уровней белка. Такие способы включают, например, электрофорез, капиллярный электрофорез, высокоэффективную жидкостную хроматографию (ВЭЖХ), тонкослойную хроматографию (TLC), гипердиффузную хроматографию, реакции преципитации в жидкости или геле, абсорбционную спектроскопию, колориметрические анализы, спектрометрические анализы, проточную цитометрию, иммунодиффузию (одиночную или двойную), иммуноэлектрофорез, вестерн-блоттинг, радиоиммунологический анализ (RIA), твердофазные иммуноферментные анализы (ELISA), иммунофлуоресцентные анализы, электрохемолюминесцентные анализы и т.п.
В некоторых вариантах осуществления мониторинг эффективности способов по изобретению можно проводить посредством детекции или мониторинга снижения отложения амилоидного TTR. Снижение отложения амилоидного TTR, как используют в настоящем описании, включает любое уменьшение размера, числа или степени выраженности отложений TTR, или относится к предотвращению или снижению образования отложений TTR в органе или отделе у индивидуума, как можно оценивать in vitro или in vivo любым известным в данной области способом. Например, некоторые способы оценки отложений амилоида описаны у Gertz M.A. & Rajukumar S.V., (Editors) (2010), Amyloidosis: Diagnosis and Treatment, New York: Humana Press. Способы оценки отложений амилоида могут включать биохимические анализы, а также визуальную или компьютеризированную оценку отложений амилоида, как можно визуализировать, например, с использованием иммуногистохимического окрашивания, флуоресцентного мечения, световой микроскопии, электронной микроскопии, флуоресцентной микроскопии или других типов микроскопии. Для оценки отложений амилоида можно применять инвазивные или неинвазивные способы получения изображения, включая, например, CT, PET или NMR/MRI визуализацию.
Способы по изобретению могут снижать отложения TTR во многих тканях или отделах организма, включая, но, не ограничиваясь ими, сердце, печень, селезенку, пищевод, желудок, кишечник (подвздошную кишку, двенадцатиперстную кишку и толстую кишку), головной мозг, седалищный нерв, ганглий заднего корешка, почку и сетчатку.
Термин "образец", как используют в настоящем описании, относится к набору аналогичных жидкостей, клеток или тканей, получаемых у индивидуума, а также жидкостям, клеткам или тканям, содержащимся у индивидуума. Примеры биологических жидкостей включают кровь, сыворотку и серозные жидкости, плазму, цереброспинальную жидкость, слюну, внутриглазные жидкости и т.п. Образцы ткани могут включать образцы из тканей, органов или локализованных участков. Например, образцы можно получать из конкретных органов, частей органов или жидкостей, или клеток в этих органах. В определенных вариантах осуществления образцы можно получать из печени (например, целой печени или определенных сегментов печени или определенных типов клеток в печени, таких как, например, гепатоциты), сетчатки или частей сетчатки (например, пигментного эпителия сетчатки), центральной нервной системы или отделов центральной нервной системы (например, желудочков или хориоидного сплетения), или поджелудочной железы или определенных клеток или частей поджелудочной железы. В предпочтительных вариантах осуществления "получаемый у индивидуума образец" относится к крови или плазме, получаемой у индивидуума. В дополнительных вариантах осуществления "получаемый у индивидуума образец" относится к ткани печени или ткани сетчатки, получаемой у индивидуума.
В некоторых вариантах осуществления способов по изобретению средство для РНКи вводят индивидууму таким образом, что средство для РНКи доставляют в конкретный участок у индивидуума. Ингибирование экспрессии TTR можно оценивать с использованием измерений уровня или изменения уровня мРНК TTR или белка TTR в образце, получаемом из жидкости или ткани из конкретного участка у индивидуума. В предпочтительных вариантах осуществления участок выбран из группы, состоящей из печени, хориоидного сплетения, сетчатки и поджелудочной железы. Участок также может представлять собой подотдел или подгруппу клеток из любого из указанных выше участков (например, гепатоцитов или пигментного эпителия сетчатки). Участок также может включать клетки, которые экспрессируют конкретный тип рецептора (например, гепатоциты, которые экспрессируют асиалогликопротеиновый рецептор).
V. Способы лечения или профилактики ассоциированного с TTR заболевания
Настоящее изобретение также относится к способам лечения или профилактики ассоциированного с TTR заболевания у индивидуума. Способы включают введение индивидууму терапевтически эффективного количества или профилактически эффективного количества средства для РНКи по изобретению.
Как используют в настоящем описании, "индивидуум" включает человека или не являющееся человеком животное предпочтительно позвоночное и более предпочтительно млекопитающее. Индивидуум может включать трансгенный организм. Наиболее предпочтительно индивидуум представляет собой человека, такого как человек, страдающий или предрасположенный к развитию ассоциированного с TTR заболевания.
В некоторых вариантах осуществления индивидуум страдает от ассоциированного с TTR заболевания. В других вариантах осуществления индивидуум представляет собой индивидуума, подвергающегося риску развития ассоциированного с TTR заболевания, например, индивидуума с мутацией гена TTR, которая ассоциирована с развитием ассоциированного с TTR заболевания, индивидуума с семейным анамнезом ассоциированного с TTR заболевания или индивидуума, который проявляет признаки или симптомы, подтверждающие развитие TTR амилоидоза.
"Ассоциированное с TTR заболевание", как используют в настоящем описании, включает любое заболевание, вызываемое или ассоциированное с образованием отложений амилоида, в которых предшественники фибрилл состоят из варианта или белка TTR дикого типа. Мутантный и TTR дикого типа обуславливает различные формы отложения амилоида (амилоидоза). Амилоидоз включает образование и агрегацию неправильно свернутых белков, приводящих к внеклеточным отложениям, которые нарушают функцию органа. Клинические синдромы, ассоциированные с агрегацией TTR, включают, например, старческий системный амилоидоз (SSA), системный семейный амилоидоз, семейную амилоидотическую полинейропатию (FAP), семейную амилоидотическую кардиомиопатию (FAC) и лептоменингеальный амилоидоз, также известный как лептоменингеальный или менингоцереброваскулярный амилоидоз, амилоидоз центральной нервной системы (ЦНС) или амилоидоз VII формы.
В некоторых вариантах осуществления способов по изобретению средства для РНКи по изобретению вводят индивидуумам, страдающим семейной амилоидотической кардиомиопатией (FAC) и старческим системным амилоидозом (SSA). TTR с нормальной последовательностью вызывает амилоидоз сердца у людей пожилого возраста, и который называют старческим системным амилоидозом (SSA) (также называемый сенильным амилоидозом сердца (SCA) или амилоидозом сердца). SSA часто сопровождается микроскопическими отложениями во многих других органах. Мутации TTR ускоряют процесс образования амилоида TTR и являются наиболее важным фактором риска развития клинически значимого амилоидоза TTR (также называемого ATTR (типа амилоидоз-транстиретин)). Известно, что более 85 амилоидогенных вариантов TTR вызывают системный семейный амилоидоз.
В некоторых вариантах осуществления способов по изобретению средства для РНКи по изобретению вводят индивидуумам, страдающим связанной с транстиретином (TTR) семейной амилоидотической полинейропатией (FAP). Такие индивидуумы могут страдать офтальмологическими проявлениями, такими как помутнение стекловидного тела и глаукома. Специалисту в данной области известно, что амилоидогенный транстиретин (ATTR), синтезируемый пигментным эпителием сетчатки (RPE), играет важную роль в прогрессировании амилоидоза глаза. Проведенные ранее исследования показали, что панретинальная лазерная фотокоагуляция, которая уменьшает количество клеток RPE, предотвращает прогрессирование отложения амилоида в стекловидном теле, свидетельствуя о том, что эффективное подавление экспрессии ATTR в RPE может стать новой терапией амилоидоза глаза (см., например, Kawaji T. et al., Ophthalmology, (2010) 117:552-555). Способы по изобретению являются пригодными для лечения офтальмологических проявлений связанной с TTR FAP, например, амилоидоза глаза. Средство для РНКи можно доставлять подходящим способом для направленной доставки в конкретную ткань, такую как глаз. Модели доставки в глаз включают ретробульбарную, подкожную в веко, субконъюнктивальную, субтеноновую, в переднюю камеру или интравитреальную инъекцию (или внутреннюю инъекцию или вливание). Конкретные составы для доставки в глаз включают глазные капли или мази.
Другое ассоциированное с TTR заболевание представляет собой гипертироксинемию, также известную как "дистранстиретиновая гипертироксинемия" или "диспреальбуминовая гипертироксинемия". Этот тип гипертироксинемии может являться вторичным по отношению к повышенной ассоциации тироксина с TTR в результате мутантной молекулы TTR с повышенной аффинностью к тироксину. См., например, Moses et al., (1982) J. Clin. Invest., 86, 2025-2033.
Средства для РНКи по изобретению можно вводить индивидууму любым способом введения, известным в данной области, включая, но, не ограничиваясь ими, подкожный, внутривенный, внутримышечный, внутриглазной, внутрибронхиальный, интраплевральный, интраперитонеальный, внутриартериальный, лимфатический, цереброспинальный и любыми их комбинациями. В предпочтительных вариантах осуществления средства вводят подкожно.
В некоторых вариантах осуществления введение проводят посредством депо-инъекции. Депо-инъекция может постоянно высвобождать средство для РНКи в течение длительного периода времени. Таким образом, депо-инъекция может снижать частоту дозирования, необходимую для получения желаемого действия, например, желаемого ингибирования TTR, или терапевтического или профилактического эффекта. Депо-инъекция также может обеспечивать более постоянные концентрации в сыворотке. Депо-инъекции могут включать подкожные инъекции или внутримышечные инъекции. В предпочтительных вариантах осуществления депо-инъекция представляет собой подкожную инъекцию.
В некоторых вариантах осуществления введение проводят через насос. Насос может представлять собой внешний насос или хирургически имплантированный насос. В определенных вариантах осуществления насос представляет собой подкожно имплантированный осмотический насос. В других вариантах осуществления насос представляет собой инфузионный насос. Инфузионный насос можно использовать для внутривенных, подкожных, артериальных или эпидуральных инфузий. В предпочтительных вариантах осуществления инфузионный насос представляет собой подкожный инфузионный насос. В других вариантах осуществления насос представляет собой хирургически имплантированный насос, который доставляет средство для РНКи в печень.
Другие способы введения включают эпидуральное, интарцеребральное, интрацеребровентрикулярное, назальное введение, внутриартериальную, внутрисердечную, внутрикостную инфузию, интратекальное и интравитреальное, и легочное. Способ введения можно выбирать в зависимости от того, является ли желательным местное или системное лечение, и в зависимости от подлежащей лечению области. Путь и участок введения можно выбирать, чтобы усиливать направленное воздействие.
В некоторых вариантах осуществления средство для РНКи вводят индивидууму в количестве, эффективном для ингибирования экспрессии TTR в клетку индивидуума. Количество, эффективное для ингибирования экспрессии TTR в клетке у индивидуума, можно оценивать описанными выше способами, включая способы, которые включают оценку ингибирования мРНК TTR, белка TTR или связанных переменных, таких как отложения амилоида.
В некоторых вариантах осуществления средство для РНКи вводят индивидууму в терапевтически или профилактически эффективном количестве.
"Терапевтически эффективное количество", как используют в настоящем описании, предназначено включать количество средства для РНКи, которое при введении пациенту для лечения ассоциированного с TTR заболевания, является достаточным для эффективного лечения заболевания (например, путем ослабления, улучшения состояния или поддержания существующего заболевания или одного или более симптомов заболевания). "Терапевтически эффективное количество" может изменяться в зависимости от средства для РНКи, того каким образом вводят средства, заболевания и его тяжести и истории, возраста, массы, семейного анамнеза, набора генов, стадии патологических процессов, опосредованных экспрессией TTR, типов предшествовавшей или сопутствующей терапии при наличии и других индивидуальных характеристик пациента, подлежащего лечению.
"Профилактически эффективное количество", как используют в настоящем описании, предназначено включать количество средства для РНКи, которое при введении индивидууму, который еще не испытывает или не проявляет симптомов ассоциированного с TTR заболевания, но который может быть предрасположен к заболеванию, является достаточным для профилактики или улучшения состояния заболевание или одного или более симптомов заболевания. Симптомы, которые можно улучшать, включают сенсорную нейропатию (например, парестезию, гипестезию в дистальных конечностях), вегетативную нейропатию (например, нарушение желудочно-кишечной функции, такое как язва желудка, или ортостатическую гипотензию), моторную нейропатию, судороги, деменцию, миелопатию, полинейропатию, синдром запястного канала, вегетативную недостаточность, кардиомиопатию, помутнения стекловидного тела, почечную недостаточность, нефропатию, значительное снижение mBMI (модифицированного индекса массы тела), нарушение функции черепно-мозгового нерва и решетчатую дегенерацию роговицы. Улучшение состояния заболевание включает замедление течения заболевания или снижение тяжести развивающегося позднее заболевания. "Профилактически эффективное количество" может изменяться в зависимости от средства для РНКи, того как вводят средство, степени риска заболевания и истории, возраста, массы, семейного анамнеза, набора генов, типов предшествовавшего или сопутствующего лечения при наличии и других индивидуальных характеристик пациента, подлежащего лечению.
"Терапевтически-эффективное количество" или "профилактически эффективное количество" также включает количество средства для РНКи, которое обеспечивает желаемое местное или системное действие при обоснованном отношении польза/риск, применимом для любого лечения. Средства для РНКи, применяемые в способах по настоящему изобретению, можно вводить в достаточном количестве для обеспечения обоснованного отношения польза/риск, применимом для такого лечения.
Как используют в настоящем описании, фраза "терапевтически эффективное количество" и "профилактически эффективное количество" также включает количество, которое оказывает благоприятное действие на лечение, профилактику или ведение патологических процессов или симптома(ов) патологических процессов, опосредованных экспрессией TTR. Симптомы TTR амилоидоза включают сенсорную нейропатию (например, парестезию, гипестезию в дистальных конечностях), вегетативную нейропатию (например, нарушение желудочно-кишечной функции, такое как язва желудка, или ортостатическую гипотензию), моторную нейропатию, судороги, деменцию, миелопатию, полинейропатию, синдром запястного канала, вегетативную недостаточность, кардиомиопатию, помутнения стекловидного тела, почечную недостаточность, нефропатию, значительное снижение mBMI (модифицированного индекса массы тела), нарушение функции черепно-мозгового нерва и решетчатую дегенерацию роговицы.
Доза средства для РНКи, которую вводят индивидууму, можно подбирать для уравновешивания рисков и пользы от конкретной дозы, например, для получения желаемого уровня подавления гена TTR (как оценивают, например, на основании подавления мРНК TTR, экспрессии белка TTR или снижения отложения амилоида, как определено выше) или желаемого терапевтического или профилактического действия, при одновременном устранении нежелательных побочных эффектов.
В одном из вариантов осуществления средство для РНКи вводят в дозе приблизительно от 0,25 мг/кг приблизительно до 50 мг/кг, например, приблизительно от 0,25 мг/кг приблизительно до 0,5 мг/кг, приблизительно от 0,25 мг/кг приблизительно до 1 мг/кг, приблизительно от 0,25 мг/кг приблизительно до 5 мг/кг, приблизительно от 0,25 мг/кг приблизительно до 10 мг/кг, приблизительно от 1 мг/кг приблизительно до 10 мг/кг, приблизительно от 5 мг/кг приблизительно до 15 мг/кг, приблизительно от 10 мг/кг приблизительно до 20 мг/кг, приблизительно от 15 мг/кг приблизительно до 25 мг/кг, приблизительно от 20 мг/кг приблизительно до 30 мг/кг, приблизительно от 25 мг/кг приблизительно до 35 мг/кг или приблизительно от 40 мг/кг приблизительно до 50 мг/кг.
В некоторых вариантах осуществления средство для РНКи вводят в дозе приблизительно 0,25 мг/кг, приблизительно 0,5 мг/кг, приблизительно 1 мг/кг, приблизительно 2 мг/кг, приблизительно 3 мг/кг, приблизительно 4 мг/кг, приблизительно 5 мг/кг, приблизительно 6 мг/кг, приблизительно 7 мг/кг, приблизительно 8 мг/кг, приблизительно 9 мг/кг, приблизительно 10 мг/кг, приблизительно 11 мг/кг, приблизительно 12 мг/кг, приблизительно 13 мг/кг, приблизительно 14 мг/кг, приблизительно 15 мг/кг, приблизительно 16 мг/кг, приблизительно 17 мг/кг, приблизительно 18 мг/кг, приблизительно 19 мг/кг, приблизительно 20 мг/кг, приблизительно 21 мг/кг, приблизительно 22 мг/кг, приблизительно 23 мг/кг, приблизительно 24 мг/кг, приблизительно 25 мг/кг, приблизительно 26 мг/кг, приблизительно 27 мг/кг, приблизительно 28 мг/кг, приблизительно 29 мг/кг, 30 мг/кг, приблизительно 31 мг/кг, приблизительно 32 мг/кг, приблизительно 33 мг/кг, приблизительно 34 мг/кг, приблизительно 35 мг/кг, приблизительно 36 мг/кг, приблизительно 37 мг/кг, приблизительно 38 мг/кг, приблизительно 39 мг/кг, приблизительно 40 мг/кг, приблизительно 41 мг/кг, приблизительно 42 мг/кг, приблизительно 43 мг/кг, приблизительно 44 мг/кг, приблизительно 45 мг/кг, приблизительно 46 мг/кг, приблизительно 47 мг/кг, приблизительно 48 мг/кг, приблизительно 49 мг/кг или приблизительно 50 мг/кг.
В некоторых вариантах осуществления средство для РНКи вводят в двух или более дозах. При желании для облегчения повторных или частых инфузий можно порекомендовать имплантацию средства доставки, например, насоса, полупостоянного стента (например, внутривенного, интраперитонеального, интрацистернального или внутрикапсулярного) или резервуара. В некоторых вариантах осуществления число или количество последующих доз зависит от получения желаемого действия, например, подавления гена TTR, или получения терапевтического или профилактического действия, например, уменьшения отложения амилоида или уменьшения симптома ассоциированного с TTR заболевания. В некоторых вариантах осуществления средство для РНКи вводят в соответствии со схемой введения. Например, средство для РНКи можно вводить дважды в неделю, три раза в неделю, четыре раза в неделю или пять раза в неделю. В некоторых вариантах осуществления схема введения включает введение через равные интервалы времени, например, каждый час, каждые четыре часа, каждые шесть часов, каждые восемь часов, каждые двенадцать часов, ежесуточно, каждые 2 суток, каждые 3 суток, каждые 4 суток, каждые 5 суток, еженедельно, раз в две недели или ежемесячно. В других вариантах осуществления схема введения включает введения с небольшими интервалами времени с последующим более длительным периодом, во время которого средство не вводят. Например, схема введения может включать начальную совокупность доз, которые вводят в относительно короткий период времени (например, приблизительно каждые 6 часов, приблизительно каждые 12 часов, приблизительно каждые 24 часа, приблизительно каждые 48 часов, или приблизительно каждые 72 часа), с последующим более длительным периодом времени (например, приблизительно 1 неделя, приблизительно 2 недели, приблизительно 3 недели, приблизительно 4 недели, приблизительно 5 недель, приблизительно 6 недель, приблизительно 7 недель или приблизительно 8 недель), во время которого не вводят средство для РНКи. В одном из вариантов осуществления средство для РНКи сначала вводят каждый час, а затем вводят в более длительном интервале времени (например, ежесуточно, еженедельно, раз в две недели или ежемесячно). В другом варианте осуществления средство для РНКи сначала вводят ежесуточно, а затем вводят в более длительном интервале времени (например, еженедельно, раз в две недели или ежемесячно). В определенных вариантах осуществления более длительный интервал увеличивается со временем, или его определяют на основании получения желаемого действия. В конкретном варианте осуществления средство для РНКи вводят один раз в сутки в течение первой недели с последующим еженедельным дозированием, начиная на восьмые сутки введения. В другом конкретном варианте осуществления средство для РНКи вводят через сутки во время первой недели с последующим еженедельным дозированием, начиная на восьмые сутки введения.
Любую из этих схем можно необязательно повторять в течение одного или более циклов. Число циклов может зависеть от получения желаемого действия, например, подавления гена TTR, уровня ретинолсвязывающего белка, уровня витамина A и/или получения терапевтического или профилактического действия, например, снижения отложения амилоида или уменьшения симптома ассоциированного с TTR заболевания.
В некоторых вариантах осуществления средство для РНКи вводят совместно с другими терапевтическими средства или в соответствии с другими схемами лечения. Например, другие средства или другие схемы лечения, подходящие для лечения ассоциированного с TTR заболевания, могут включать трансплантацию печени, которая может снижать уровни мутантного TTR в организме, тафамидис (Vyndaqel), который кинетически стабилизирует тетрамер TTR, предотвращая диссоциацию, необходимую для амилоидогенеза TTR, и диуретики, которые можно применять, например, для снижения отека при TTR амилоидозе с поражением сердца.
В одном из вариантов осуществления индивидууму вводят начальную дозу и одну или более поддерживающих доз средства для РНКи. Поддерживающая доза или дозы могут являться такими же или ниже, чем начальная доза, например, половина начальной дозы. Поддерживающая схема лечения может включать лечение индивидуума дозой или дозами в диапазоне от 0,01 мкг до 15 мг/кг массы тела в сутки, например, 10 мг/кг, 1 мг/кг, 0,1 мг/кг, 0,01 мг/кг, 0,001 мг/кг или 0,00001 мг/кг массы тела в сутки. Поддерживающие дозы вводят, например, не более чем один раз в 2 суток, один раз в 5 суток, один раз в 7 суток, одни раз в 10 суток, один раз в 14 суток, один раз в 21 сутки или один раз в 30 суток. Кроме того, схема лечения может длиться в течение периода времени, который изменяется в зависимости от природы конкретного заболевания, его тяжести и общего состояния пациента. В определенных вариантах осуществления дозирование можно проводить не более одного раз в сутки, например, не более одного раз в 24, 36, 48 или более часов, например, не более одного раза в 5 или 8 суток. После лечения можно проводить наблюдение у пациента за изменением его/ее состояния. Дозу средства для РНКи можно повышать в случае, если пациент не отвечает в значительно степени на текущие уровни дозирования, или дозу можно снижать, если наблюдают ослабление симптомов состояния болезни, если устраняют состояние болезни, или если наблюдают нежелательные побочные эффекты.
VI. Наборы
Настоящее изобретение также относится к наборам для проведения любых способов по изобретению. Такие наборы включают одно или более средств для РНКи и инструкции по применению, например, инструкции для ингибирования экспрессии TTR в клетке посредством приведения в контакт клетки со средством(ами) для РНКи в количестве, эффективном для ингибирования экспрессии TTR. Наборы могут необязательно дополнительно содержать средства для приведения клетки в контакт со средством для РНКи (например, устройство для инъекции) или средства для измерения ингибирования TTR (например, средства для измерения ингибирования мРНК TTR или белка TTR). Такие средства для измерения ингибирования TTR могут содержать средство для получения образца у индивидуума, такого как, например, образец плазмы. Наборы по изобретению могут необязательно дополнительно содержать средство для введения средства(в) для РНКи индивидууму или средство для определения терапевтически эффективного или профилактически эффективного количества.
Настоящее изобретение дополнительно проиллюстрировано следующими ниже примерами, которые не следует интерпретировать как ограничивающие. Содержание всех ссылок и опубликованных патентов и патентных заявок, цитируемых на всем протяжении заявки, таким образом, включены в настоящее описание посредством ссылки.
ПРИМЕРЫ
Пример 1: Ингибирование TTR конгьюгатами TTR-GalNAc
Однократную дозу средства для РНКи AD-43527 TTR вводили подкожно мышам и определяли уровень мРНК TTR через 72 часа после введения.
Выбирали перекрестнореагирующий у мыши/крысы GalNAc-конъюгат AD-43527 для оценки in vivo подавления экспрессии мРНК TTR в печени у мышей WT C57BL/6. Последовательность каждой цепи AD-43527 представлена ниже.
Цепь: s=смысловая; as=антисмысловая

Используемый лиганд представлял собой GalNAc3:
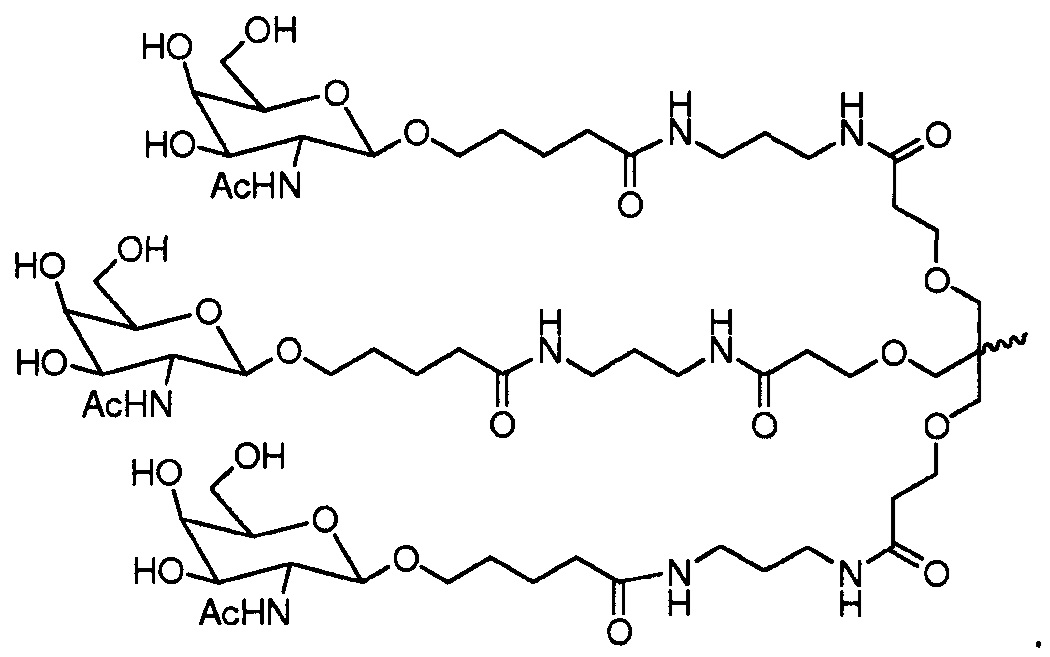
Этот лиганд GalNAc3 конъюгировали с 3'-концом смысловой цепи с использованием линкера и связи, как показано ниже:

Структура получаемого GalNAc3, конъюгированного со смысловой цепью, показана в на следующей ниже схеме:

Синтезировали и оценивали дополнительные средства для РНКи, которые направлены на TTR и содержат следующие последовательности и модификации.
Средства для РНКи TTR, перекрестнореагирующие у мыши/крысы

Средства для РНКи TTR перекрестнореагирующие у человека/яванского макака; исходный дуплекс представляет собой AD-18328 [содержащий последовательность смысловой цепи 5'-3' GuAAccAAGAGuAuuccAudTdT (SEQ ID NO: 12) и последовательность антисмысловой цепи 5'-3' AUGGAAuACUCUUGGUuACdTdT (SEQ ID NO: 13) со следующими ниже модификациями: чередование 2'F/2'OMe w/2 PS на AS.

L96=GalNAc3; нуклеотиды строчными буквами (a, u, g, c) представляют собой 2'-O-метилнуклеотиды, Nf (т.е. Af) представляет собой 2'-фто нуклеотид; Q11 представляет собой холестерин; s представляет собой тиофосфат.
AD-43527 вводили самкам мышей C57BL/6 (6-10 недель, 5 в группе) посредством подкожной инъекции в объеме дозы 10 мкл/г в дозе 30, 15, 7,5, 3,5, 1,75 или 0,5 мг/кг AD-43527. Контрольные животные получали PBS посредством подкожной инъекции в том же объеме дозы.
Приблизительно через семьдесят два часа мышей анестезировали 200 мкл кетамина, а затем выпускали кровь посредством разреза правой хвостовой артерии. Собирали ткань печени, быстро замораживали и хранили при -80°C до обработки.
Эффективность лечения оценивали путем измерения мРНК TTR в печени через 72 часа после дозирования. Уровни мРНК TTR в печени оценивали с использованием анализов с разветвленной ДНК - QuantiGene 1.0 (Panomics). В кратком изложении, образцы печени мыши измельчали и получали лизаты ткани. Лизирующую смесь с печенью (смесь 1 объема лизирующей смеси, 2 объемов не содержащей нуклеазы воды и 10 мкл протеиназы-K/мл в конечной концентрации 20 мг/мл) инкубировали при 65°C в течение 35 минут. В планшет для захвата добавляли 5 мкл лизата печени и 95 мкл панель рабочих зондов (зонд TTR для гена-мишени и GAPDH для эндогенного контроля). Планшет для захвата инкубировали при 53°C ± 1°C (приблизительно 16-20 часов). На следующие сутки планшет для захвата промывали 3 раза 1X промывочным буфером (не содержащая нуклеаз вода, компонент 1 буфера и компонент 2 промывочного буфера), затем сушили центрифугированием в течение 1 минуты при 240 g. В планшет для захвата добавляли 100 мкл на лунку амплификационной смеси зонда, который герметично закрывали алюминиевой фольгой, и инкубировали в течение 1 часа при 46°C ± 1°C. После инкубации в течение 1 часа повторяли этап промывания, затем добавляли 100 мкл на лунку смеси меченого зонда. Планшеты для захвата инкубировали при 46°C ± 1°C в течение 1 часа. Затем планшеты промывали 1X промывочным буфером, сушили и добавляли в планшеты для захвата 100 мкл субстрата на лунку. Планшеты для захвата инкубировали в течение 30 минут при 46°C с последующей инкубацией в течение 30 минут при комнатной температуре. После инкубации планшеты считывали с использованием люминометра SpectraMax. Данные b-ДНК анализировали путем вычитания среднего фонового значения из каждого повторного образца, усредняя повторные значения GAPDH (контрольного зонда) и TTR (экспериментального зонда), а затем вычисляя отношение: (экспериментальный зонд - фоновое значение) / (контрольный зонд - фоновое значение). Для каждой группы рассчитывали средний уровень мРНК TTR и нормализовали на среднее значение группы PBS с получением относительной мРНК TTR в виде % от группы контроля PBS.
Результаты представлены на фигуре 1. Конъюгированное с GalNAc средство для РНКи, направленное на TTR, имело ED50 приблизительно 5 мг/кг для нокдауна мРНК TTR. Эти результаты демонстрируют, что конъюгированные с GalNAc средства для РНКи, направленные на TTR, являются эффективными для ингибирования экспрессии мРНК TTR.
Пример 2: Ингибирование TTR конгьюгатами TTR-GalNAc является стойким
Мышам вводили подкожную дозу (7,5 или 30,0 мг/кг) AD-43527 конъюгированного с GalNAc средства для РНКи, направленного на TTR. Способом, описанным в примере 1, оценивали уровень мРНК TTR в печени на 1, 3, 5, 7, 10, 13, 15, 19, 26, 33 и 41 сутки после дозирования.
Результаты представлены на фигуре 2. На 19 сутки введение 30,0 мг/кг конъюгированных с GalNAc средств для РНКи все еще проявляло приблизительно 50% подавление. Полное восстановление экспрессии наступало на 41 сутки.
Эти результаты демонстрировали, что ингибирование, обеспечиваемое конъюгированной с GalNAc миРНК, направленной на TTR, является стойким, длящимся до 3, 5, 7, 10, 13, 15, 19, 26 или 33 суток после обработки.
Пример 3. Синтез РНК и отжиг дуплекса
1. Синтез олигонуклеотида
Олигонуклеотиды синтезировали на синтезаторе AKTA Oligopilot или синтезаторе ABI 394. Если не указано иное для синтеза олигонуклеотидов использовали коммерчески доступную твердую подложку из стекла с контролируемым размером пор (dT-CPG, 500Å, Prime Synthesis) и фосфорамидиты РНК со стандартными защитными группами 5'-O-диметокситритил-N6-бензоил-2'-трет-бутилдиметилсилиладенозин-3'-O-N,N'-диизопропил-2-цианоэтилфосфорамидит, 5'-O-диметокситритил-N4-ацетил-2'-трет-бутилдиметилсилилцитидин-3'-O-N,N'-диизопропил-2-цианоэтилфосфорамидит, 5'-O-диметокситритил-N2-изобутрил-2'-трет-бутилдиметилсилилгуанозин-3'-O-N,N'-диизопропил-2-цианоэтилфосфорамидит и 5'-O-диметокситритил-2'-трет-бутилдиметилсилилуридин-3'-O-N,N'-диизопропил-2-цианоэтилфосфорамидит (Pierce Nucleic Acids Technologies). 2'-F-фосфорамидиты, 5'-O-диметокситритил-N4-ацетил-2'-фторцитидин-3'-O-N,N'-диизопропил-2-цианоэтилфосфорамидит и 5'-O-диметокситритил-2'-фторуридин-3'-O-N,N'-диизопропил-2-цианоэтилфосфорамидит приобретали от Promega. Все фосфорамидиты использовали в концентрации 0,2 М в ацетонитриле (CH3CN) за исключением гуанозина, который использовали в концентрации 0,2 М в 10% THF/ANC (об./об.). Использовали время связывания/рециклинга 16 минут. Активатор представлял собой 5-этилтиотетразол (0,75 М, American International Chemicals), для PO-окисления использовали йод/вода/пиридин и для PS-окисления использовали PADS (2%) в 2,б-лутидине/ACN (1:1 об./об.).
Конъюгированные с лигандом цепи синтезировали с использованием твердой подложки, содержащей соответствующий лиганд. Например, введение углеводной группы/лиганда (например, GalNAc) в 3'-конец последовательности получали посредством начала синтеза с соответствующей углеводной твердой подложкой. Аналогично молекулу холестерина в 3'-конец вводили посредством начала синтеза на подложке на основе холестерина. Как правило, молекула лиганда связывали с транс-4-гидроксипролинолом посредством связи, выбираемой, как описано в предыдущих примерах, с получением молекулы гидроксипролинол-лиганд. Затем молекулу гидроксипролинол-лиганд связывали с твердой подложкой через сукцинатный линкер или преобразовывали в фосфорамидит посредством стандартных условий фосфорилирования с получением желаемых строительных блоков углеводного конъюгата. Синтезировали меченную флуорофором миРНК из соответствующего фосфорамидита или с использованием твердой подложки, приобретаемой от Biosearch Technologies. Полимерную подложку на основе олеила и литохолиевой кислоты (GalNAc)3 изготавливали в лаборатории, в которой проводили испытание, при нагрузке 38,6 мкмоль/грамм. Полимерную подложку на основе маннозы (Man)3 также изготавливали в лаборатории, в которой проводили испытание, при нагрузке 42,0 мкмоль/грамм.
Конъюгацию лиганда выбираемого в желаемом положении, например, в 5'-конце последовательности, получали связыванием соответствующего фосфорамидита с растущей цепью в стандартных условиях связывания фосфорамидитов, если не указано иное. Длительное связывание в течение 15 минут 0,1 М раствора фосфорамидита в безводном CH3CN в присутствии активатора 5-(этилтио)-1H-тетразол со связанным с твердой подложкой олигонуклеотидом. Окисление межнуклеотидого фосфита до фосфата проводили с использованием стандарта йод-вода, как опубликовано у Beaucage S.L., (2008) Solid-phase synthesis of siRNA oligonucleotides, Curr. Opin. Drug Discov. Devel., 11, 203-216; Mueller S., Wolf J. and Ivanov S.A., (2004) Current Strategies for the Synthesis of RNA, Curr. Org. Synth., 1, 293-307; Xia J., Noronha A., Toudjarska I., Li F., Akinc A., Braich R., Frank-Kamenetsky M., Rajeev K.G., Egli M. and Manoharan M., (2006) Gene Silencing Activity of siRNAs with a Ribo-difluorotoluyl Nucleotide, ACS Chem. Biol., 1, 176-183, или обработкой трет-бутилгидропероксид/ацетонитрил/водой (10:87:3) с временем выдержки окисления конъюгируемого олигонуклеотида 10 минут. Тиофосфат вводили путем окисления фосфита до тиофосфата с использованием переносящего серу реагента, такого как DDTT (приобретаемого от AM Chemicals), PADS и/или реагента Бокажа. Амидофосфит холестерина синтезировали в лаборатории, в которой проводили испытание, и использовали в концентрации 0,1 М в дихлорметане. Время связывания для фосфорамидита холестерина составляло 16 минут.
2. Снятие защиты I (снятие защиты нуклеинового основания)
После завершения синтеза подложку переносили в 100 мл стеклянный флакон (VWR). Олигонуклеотид отщепляли от подложки с одновременным снятием защиты основания и фосфатных групп с использованием 80 мл смеси этанольного раствора аммиака [аммиак : этанол (3:1)] в течение 6,5 часов при 55°C. Флаконы быстро охлаждали на льду, а затем смесь этанольного раствора аммиака фильтровали в новый 250 мл флакон. CPG промывали частями 2×40 мл этанола/воды (1:1 об./об.). Затем уменьшали объем смеси до ~30 мл роторным вакуумным испарителем. Затем смесь замораживали на сухом льду и сушили в вакууме на концентраторе SpeedVac.
3. Снятие защиты II (удаление группы 2'-TBDMS)
Сухой остаток ресуспендировали в 26 мл триэтиламина, триэтиламинтригидрофторида (TEA.3HF) или пиридина-HF и DMSO (3:4:6) и нагревали при 60°C в течение 90 минут для удаления групп трет-бутилдиметилсилила (TBDMS) в 2'-положении. Реакцию затем гасили 50 мл 20 мМ ацетата натрия и подводили pH до 6,5, и хранили в морозильной камере до очистки.
4. Анализ
Олигонуклеотиды анализировали высокоэффективной жидкостной хроматографией (ВЭЖХ) до очистки, и выбор буфера и колонки зависит от природы последовательности и/или конъюгированного лиганда.
5. Очистка ВЭЖХ
Конъюгированные с лигандом олигонуклеотиды очищали обращено-фазовой препаративной ВЭЖХ. Неконъюгированные олигонуклеотиды очищали анионообменной ВЭЖХ на колонке с гелем TSK, наполняемой в лаборатории, в которой проводили испытание. Буферы представляли собой 20 мМ фосфат натрия (pH 8,5) в 10% CH3CN (буфер A) и 20 мМ фосфат натрия (pH 8,5) в 10% CH3CN, 1M NaBr (буфер B). Фракции, содержащие полноразмерные олигонуклеотиды, объединяли, обессоливали и лиофилизировали. Приблизительно 0,15 OD обессоленные олигонуклеотиды разбавляли в воде до 150 мкл, а затем пипетировали в специальные флаконы для анализа CGE и LC/MS. Соединения в конечном итоге анализировали LC-ESMS и CGE.
6. Получение средства для РНКи
Для получения средства для РНКи эквимолярные количества смысловой и антисмысловой цепи нагревали в 1×PBS при 95°C в течение 5 минут и медленно охлаждали до комнатной температуры. Целостность дуплекса подтверждали анализом ВЭЖХ. В таблице 1 ниже представлены средства для РНКи, которые направлены на мРНК TTR человека или грызуна.
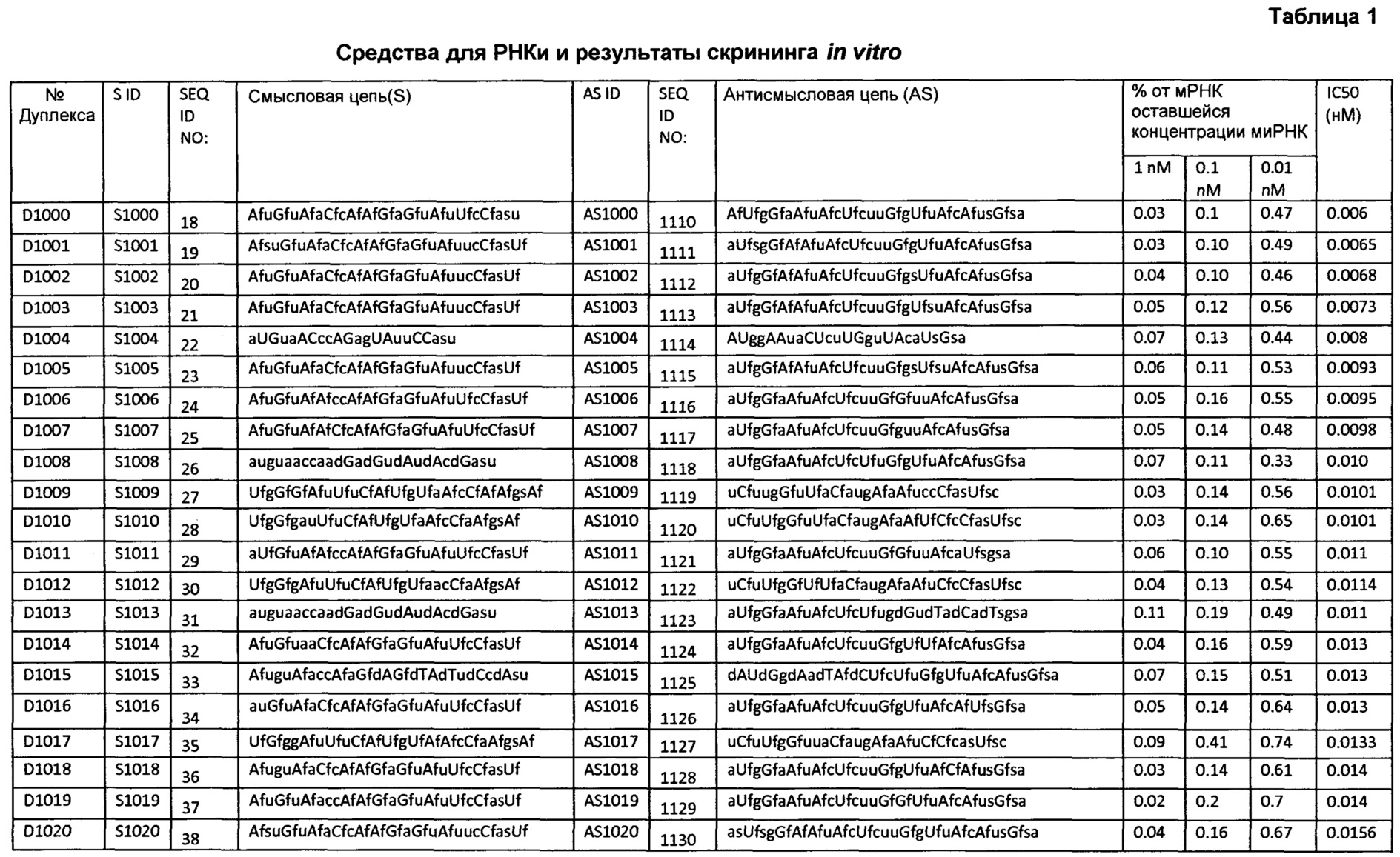
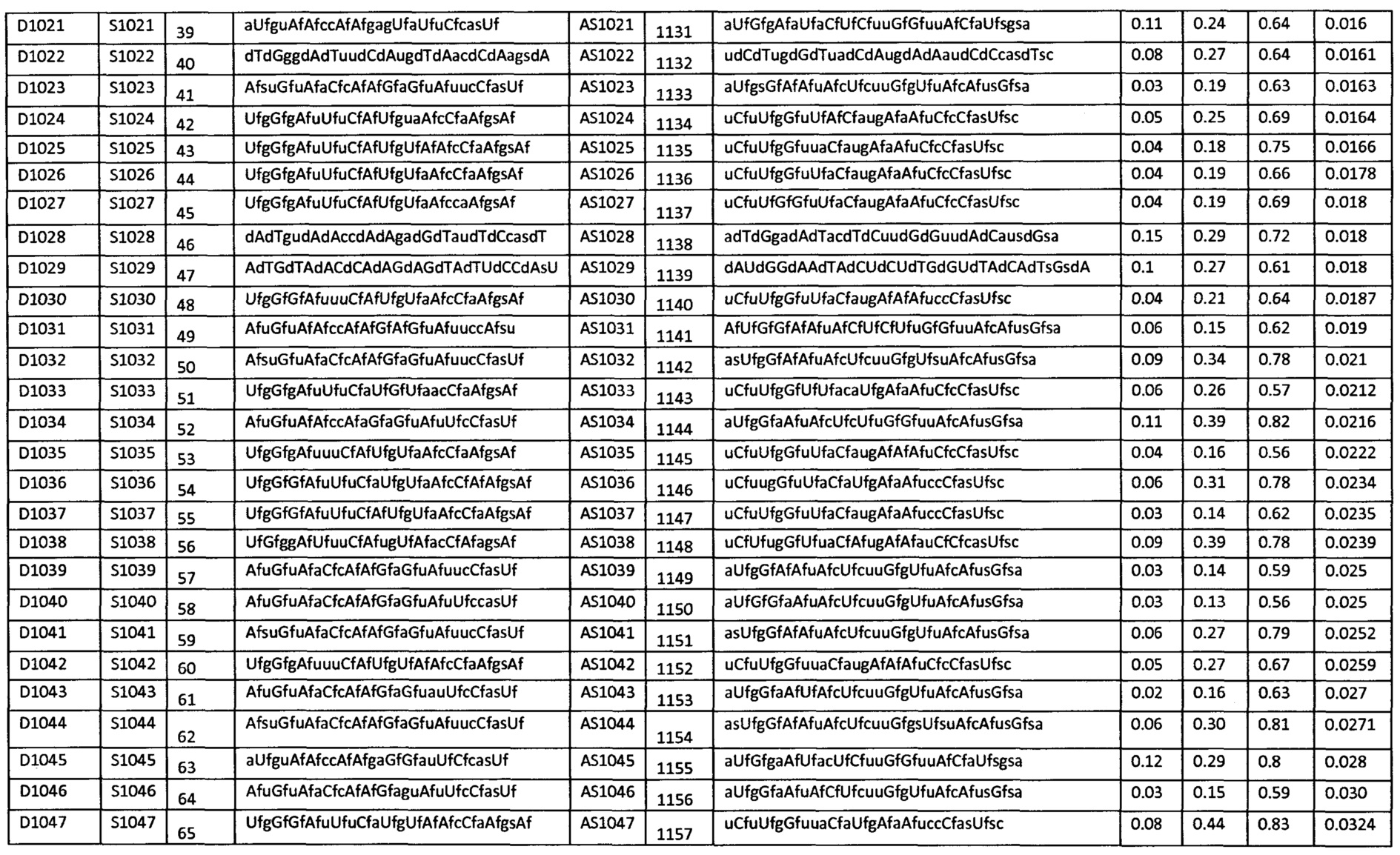






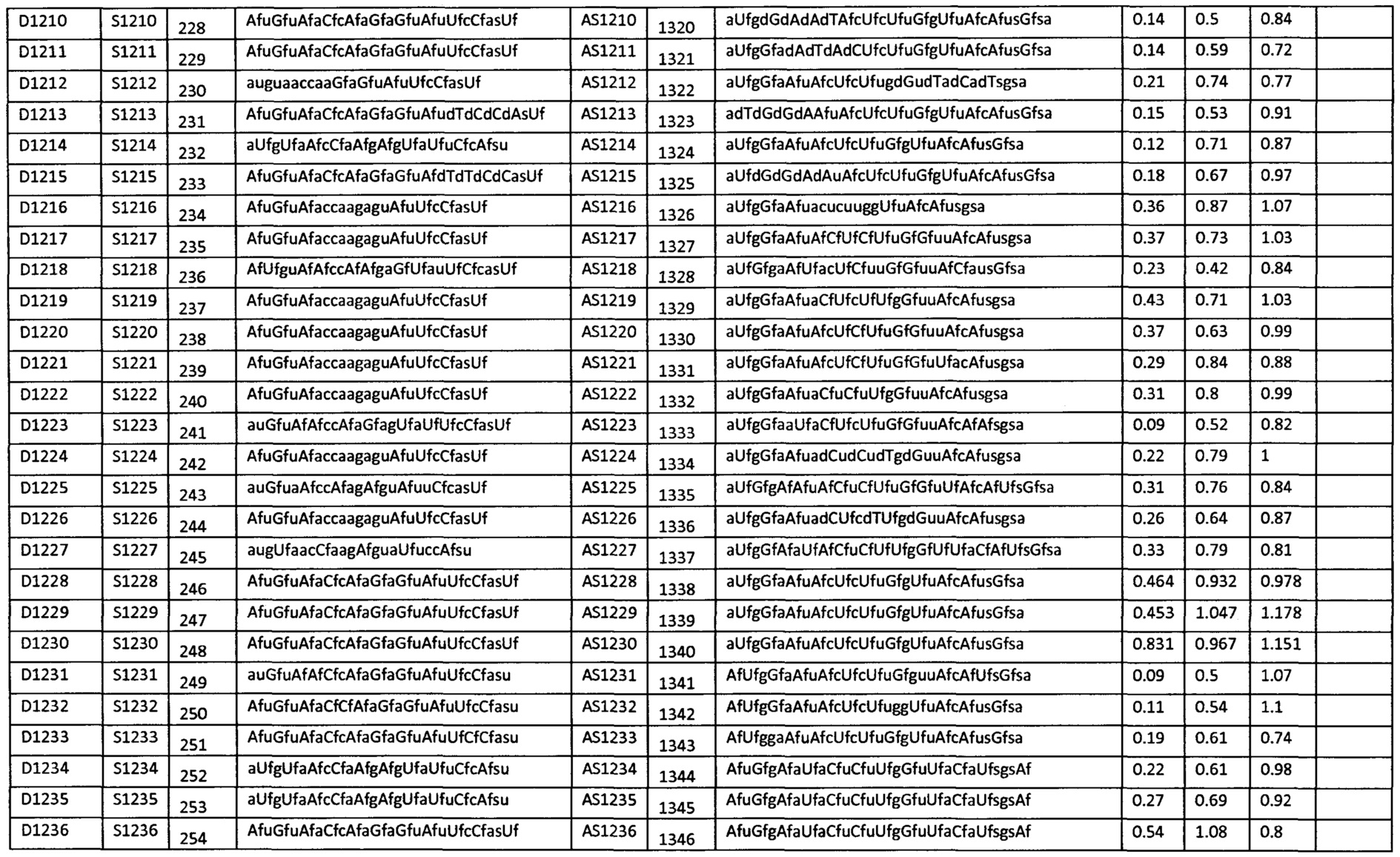
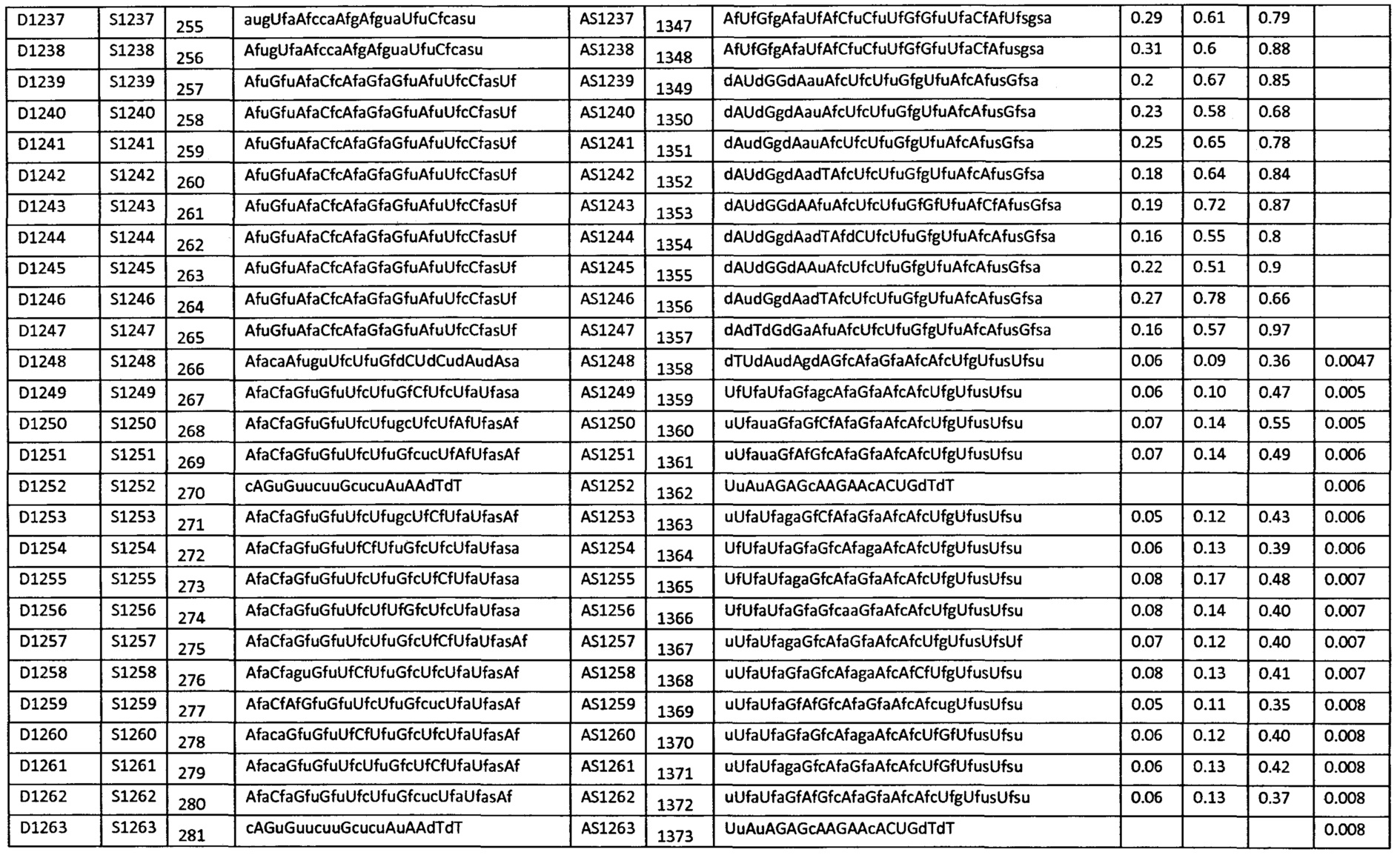























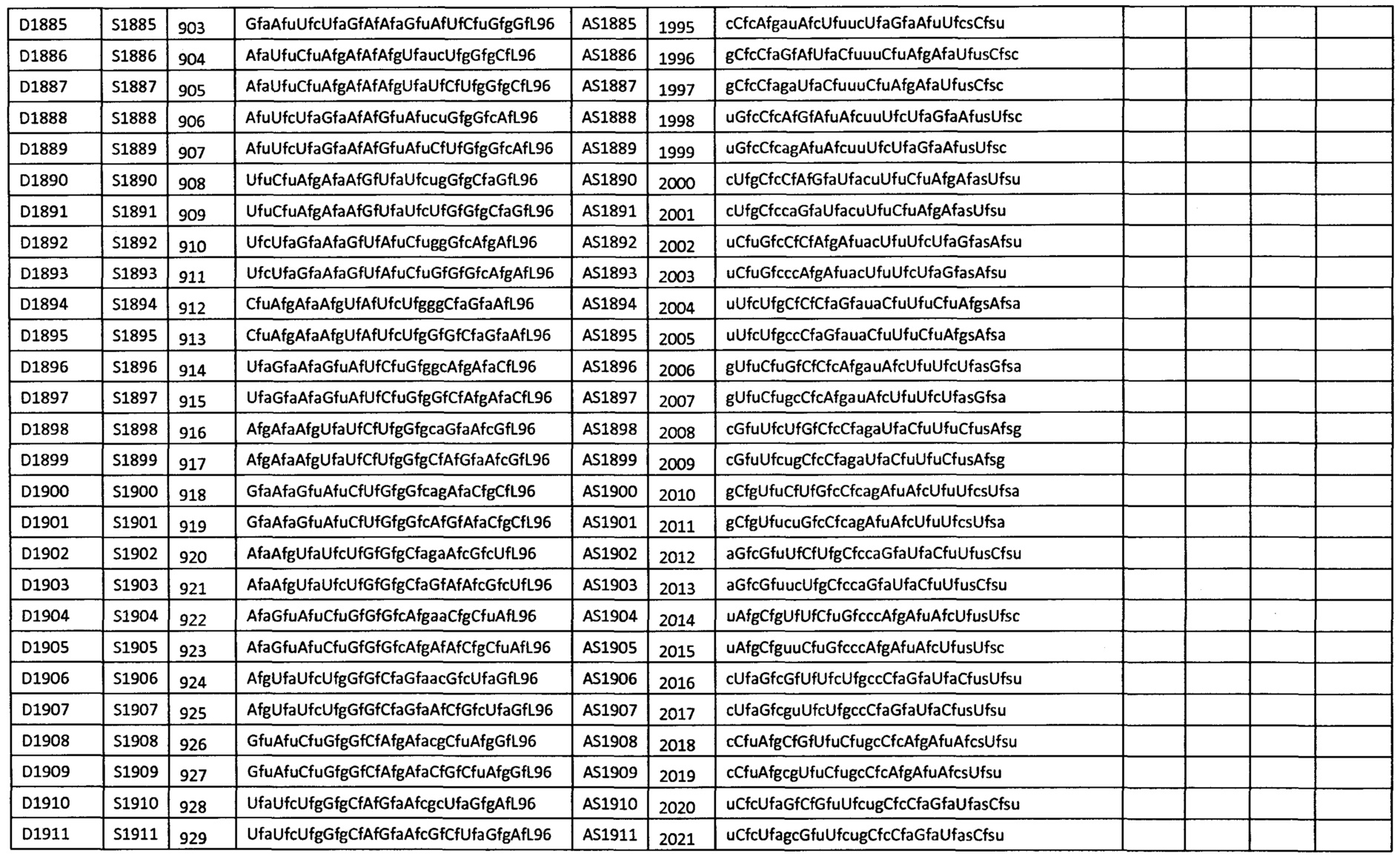


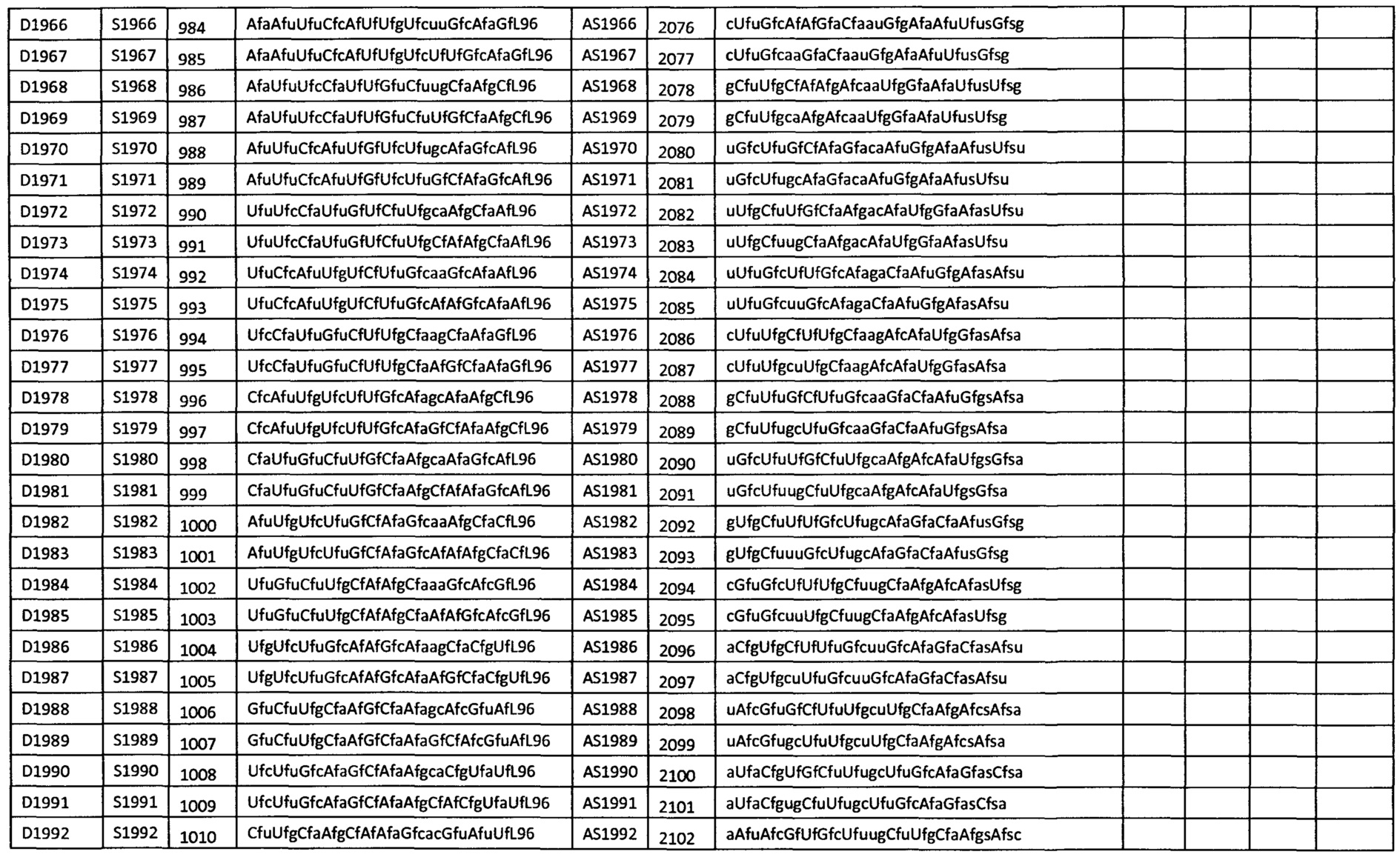




Пример 4: Скрининг in vitro средств для РНКи
Культура клеток и трансфекции
Клетки Hep3B человека или клетки H.II.4.E крысы (ATCC, Manassas, VA) выращивали почти до конфлюэнтного состояния при 37°C в атмосфере 5% CO2 в RPMI (ATCC) с добавлением 10% FBS, стрептомицина и глутамина (ATCC) перед отделением от планшета трипсинизацией. Трансфекцию проводили посредством добавления 14,8 мкл Opti-MEM плюс 0,2 мкл липофектамина RNAiMax на лунку (Invitrogen, Carlsbad CA. каталожный №13778-150) к 5 мкл дуплексов миРНК на лунку в 96-луночнойм планшете и инкубировали при комнатной температуре в течение 15 минут. Затем к смеси миРНК добавляли 80 мкл полной среды для выращивания без антибиотика, содержащей ~2×104 клеток Hep3B. Перед очисткой РНК клетки инкубировали в течение 24 или 120 часов. Эксперименты с однократной дозой проводили при конечной концентрации дуплекса 10 нМ и 0,1 нМ и эксперименты эффекта дозы проводили с использованием 8, 4 кратных серийных разведении с максимальной дозой конечной концентрации дуплекса 10 нМ.
Выделение тотальной РНК с использованием набора для выделения мРНК DYNABEADS (Invitrogen, № партии: 610-12)
Клетки собирали и лизировали в 150 мкл лизирующего/связывающего буфера, затем перемешивали в течение 5 минут при 850 об/мин с использованием термомиксера Eppendorf (скорость смешивания являлась одинаковой в течение всего процесса). В круглодонный планшет добавляли десять микролитров магнитных гранул и 80 мкл смеси лизирующего/связывающего буфера и перемешивали в течение 1 минуты. Магнитные гранулы улавливали с использованием магнитного держателя и удаляли супернатант, не затрагивая гранулы. После удаления супернатанта лизированные клетки добавляли к оставшимся гранулам и перемешивали в течение 5 минут. После удаления супернатанта магнитные гранулы промывали 2 раза 150 мкл промывочного буфера A и перемешивали в течение 1 минуты. Снова улавливали гранулы и удаляли супернатант. Затем промывали гранулы 150 мкл промывочного буфера B, улавливали и удаляли супернатант. Затем промывали гранулы 150 мкл элюирующего буфера, улавливали и удаляли супернатант. Гранулы оставляли высыхать в течение 2 минут. После сушки добавляли 50 мкл элюирующего буфера и перемешивали в течение 5 минут при 70°C. Гранулы улавливали магнитом в течение 5 минут. Удаляли 40 мкл супернатанта и добавляли в другой 96-луночный планшет.
Синтез кДНК с использованием набора ABI High capacity cDNA reverse transcription (Applied Biosystems, Foster City, CA, каталожный №4368813)
К 5 мкл тотальной РНК добавляли основную смесь из 1 мкл 10X буфера, 0,4 мкл 25X dNTP, 1 мкл случайных праймеров, 0,5 мкл обратной транскриптазы, 0,5 мкл ингибитора РНКазы и 1,6 мкл H2O на реакцию. кДНК получали с использованием термального циклера Bio-Rad C-1000 или S-1000 (Hercules, CA) с использованием следующих этапов: 25°C 10 минут, 37°C 120 минут, 85°C 5 секунд, хранение при 4°C.
ПЦР в реальном времени
2 мкл кДНК добавляли к основной смеси, содержащей 0,5 мкл GAPDH TaqMan Probe (Applied Biosystems каталожный №4326317E (человека), каталожный №4308313 (грызуна)), 0,5 мкл TTR TaqMan probe (Applied Biosystems каталожный № HS00174914_m1 (человека), каталожный № Rn00562124_m1 (крысы)) и 5 мкл основной смеси Lightcycler 480 probe (Roche, каталожный №04887301001) на лунку в 384-луночный планшет (Roche, каталожный №04887301001). ПЦР в реальном времени проводили в устройстве для ПЦР в реальном времени Roche LC 480 (Roche). Каждый дуплекс тестировали по меньшей мере в двух независимых трансфекциях и оценивали каждую трансфекцию в двух повторениях, если не указано иное.
Для расчета относительной кратности изменения данные в реальном времени анализировали способом ΔΔCt и нормализовали на анализы, проводимые с клетками, трансфицированными 10 нМ AD-1955, или имитационно трансфицированными клетками. IC50 рассчитывали с использованием подобранной модели с 4 параметрами с использованием XLFit и нормализовали на клетки, трансфицированные AD-1955 (смысловая последовательность: cuuAcGcuGAGuAcuucGAdTsdT (SEQ ID NO: 2202), антисмысловая последовательность: UCGAAGuCUcAGCGuAAGdTsdT (SEQ ID NO: 2203)), или нативные клетки в аналогичном диапазоне доз, или на их наименьшую дозу. IC50 рассчитывали для каждой индивидуальной трансфекции, а также в комбинации, где отдельная IC50 совпадала с данным обеих трансфекции.
Результаты подавления гена иллюстративного дуплекса миРНК с различными модификациями мотива по изобретению представлены в таблице 1 выше.
Пример 5: Активность подавления in vitro химически модифицированных средств для РНКи, направленных на TTR
Следующие ниже эксперименты демонстрировали положительное действие химических модификаций, включая введение мотивов триплетных повторов совместно с лигандом GalNAc3, на подавление активности средств для РНКи, направленных на TTR. Последовательности исследуемых средств предоставлены в таблице 2 ниже. Области комплементарности к мРНК TTR представляют собой такие, как указано ниже: область комплементарности средств для РНКи AD-45165, AD-51546 и AD-51547 представляет собой GGATGGGATTTCATGTAACCAAGA (SEQ ID NO: 2204) и область комплементарности средств для РНКи AD-45163, AD-51544 и АО-51545 представляет собой TTCATGTAACCAAGAGTATTCCAT (SEQ ID NO: 2205).
Протокол оценки IC50 в клетках Hep3B
В клетках Hep3B (линия клеток гепатомы человека) определяли IC50 для каждой модифицированной миРНК посредством стандартной временной трансфекцией с использованием Lipofectamine RNAiMax. В кратком описании, временную трансфекцию проводили посредством добавления 5 мкл Opti-MEM к 5 мкл дуплекса миРНК на лунку в 96-луночный планшет наряду с 10 мкл Opti-MEM плюс 0,5 мкл Lipofectamine RNAiMax на лунку (Invitrogen, Carlsbad CA., каталожный №13778-150) и инкубации при комнатной температуре в течение 15-20 минут. Затем после инкубации в каждую лунку добавляли 100 мкл полной среды для выращивания без антибиотика, содержащей 12000-15000 клеток Hep3B. Перед лизисом и анализом мРНК TTR и GAPDH посредством анализа с рДНК (Quantigene) клетки инкубировали в течение 24 часов при 37°C в атмосфере 5% CO2. Для определения IC50 оценивали семь различных концентраций миРНК в диапазоне от 10 нМ до 0,6 пМ и TTR/GAPDH для трансфицированных миРНК клеток нормализовали на клетки, трансфицированные 10 нМ миРНК Luc. Результаты представлены в таблице 2.
Протокол оценки IC50 свободного поглощения
После инкубации с миРНК, направленными на TTR, в течение 4 часов или 24 часов оценивали подавление при свободном поглощении в первичных гепатоцитах яванского макака. Подавление измеряли на 24 час от начальной экспозиции. В кратком изложении, за 24 часа до начала эксперимента 96-луночные культуральный планшеты покрывали 0,05%-0,1% коллагеном (Sigma C3867-1VL) при комнатной температуре. На сутки анализа миРНК разбавляли в предварительно подогретой среде для высевания, состоящей из DMEM с добавлением набора поддерживающей среды GIBCO (не содержащего сыворотки, Life Technologies CM4000), и добавляли в 96-луночные культуральные планшеты покрытые коллагеном. Криоконсервированные первичные гепатоциты яванского макака быстро размораживали на водяной бане 37°C и сразу же разбавляли в среде для посева в концентрации 360000 клеток/мл. Объем клеточной суспензии аккуратно пипетировали на верхнюю часть предварительно нанесенной миРНК, таким образом, что конечное число клеток на лунку составляло 18000 клеток/лунку. Планшет слегка вращали для перемешивания и распространения клеток даже через лунки и помещали в инкубатор при 37°C, 5% CO2 в течение 24 часов до лизиса и анализа мРНК TTR и GAPDH посредством рДНК (Quantigene, Affymetrix). В случае инкубации в течение 4 часов с миРНК среду сливали через 4 часа экспонирования клеток и заменяли свежей средой для посева в течение оставшихся 20 часов инкубации. Анализ последующих процессов мРНК TTR и GAPDH являлся таким, как описано выше. Для характерной кривой доза-ответ миРНК титровали
от 1 мкМ до 0,24 нМ посредством 4 кратного серийного разведения.

Нуклеотиды строчными буквами (a, u, g, c) означают 2'-O-метилнуклеотиды; Nf (например, Af) означают 2'-фторнуклеотид; s означает фосфотиоратную связь; L96 означает лиганд GalNAc3; нуклеотиды жирным шрифтом означают изменения относительно соответствующего исходного средства. Каждый нуклеотид жирным шрифтом располагается в центре триплетного мотива.
Результаты представлены в таблице 2 и демонстрируют, что модифицированные средства для РНКи, направленные на TTR, обеспечивают повышенную активность подавления.
Результаты: Улучшенная активность модифицированных средств для РНКи
Исходные средства для РНКи с чередующимися химическими модификациями и лигандом GalNAc3 обеспечивали IC50 в клетках Hep3B приблизительно 0,01 нМ. Как показано на фигурах 4-5 и в таблице 2 средства, модифицированные относительно исходных средств, например, путем добавления одного или более повторяющихся триплетов 2'-фтор- и 2'-O-метилмодификаций, проявляли неожиданно повышенную активность подавления, достигая значений IC50 в клетках Hep3B, которые являлись в 5-8 раз лучше, чем соответствующее исходное средство.
Результаты: IC50 при свободном поглощении в клетках Hep3B
Как показано в таблице 2 и на фигурах 6-7, средства для РНКи, модифицированные относительно исходного AD-45163, также проявляли повышенное подавление при свободном поглощении. Модифицированные средства проявляли более чем вдвое большую активность подавления исходного соединения после периода инкубации 24 часа и приблизительно в 10 раз большую активность подавления исходного соединения после периода инкубации 4 часа.
Как показано в таблице 2 и на фигурах 8-9, средства для РНКи, модифицированные относительно исходного AD-45165, также проявляли повышенное подавление при свободном поглощении. Модифицированные средства проявляли в 2-3 раза большую активность подавления исходного средства после периода инкубации 24 часа и в 5-8 раз большую активность подавления исходного соединения после периода инкубации 4 часа.
В совокупности эти результаты демонстрируют, что модифицированные средства для РНКи, предоставленные в настоящем описании, например, AD-51544, AD-51545, АО-51546 и AD-51547, все проявляют неожиданно хорошее ингибирование мРНК TTR в экспериментах подавления in vitro.
Пример 6: Подавление РНК TTR и ингибирование белка TTR у трансгенных мышей
Для оценки эффективности средств для РНКи AD-45163, AD-51544, AD-51545, AD-45165, AD-51546 и AD-51547 эти средства вводили трансгенным мышам, которые экспрессировали транстиретин человека с мутацией V30M (см. Santos SD., Fernaande, R. and Saraiva M.J., (2010) Neurobiology of Aging, 31, 280-289). Известно, что мутация V30M вызывает семейную амилоидную полинейропатию I типа у людей. См., например, Lobato L., (2003) J. Nephrol., 16(3):438-42.
Средства для РНКи (в буфере PBS) или контроль PBS вводили мышам (2 самцам и 2 самкам) в возрасте 18-24 месяцев в однократной подкожной дозе 5 мг/кг или 1 мг/кг. Приблизительно через 48 часов мышей анестезировали 200 мкл кетамина, а затем выпускали кровь путем разреза правой хвостовой артерии. Выделяли цельную кровь и выделяли плазму и хранили при -80°C до анализа. Собирали ткань печени, быстро замораживали и хранили при -80°C до обработки.
Эффективность лечения оценивали (i) измерением мРНК TTR в печени через 48 часов после дозирования и (ii) измерением белка TTR в плазме до введения средства и через 48 часов после дозирования. Анализировали уровни мРНК TTR в печени с использованием анализов разветвленной ДНК - QuantiGene 2.0 (Panomics, каталожный №: QS0011). В кратком изложении, образцы печени мышей измельчали и получали лизаты ткани. Лизирующую смесь для печени (смесь из 1 объема лизирующей смеси, 2 объемов не содержащей нуклеазы воды и 10 мкл протеиназы-K/мл до конечной концентрации 20 мг/мл) инкубировали при 65°C в течение 35 минут. Затем в планшет для захвата добавляли 20 мкл набора рабочих зондов (зонд TTR для гена-мишени и GAPDH для эндогенного контроля) и 80 мкл лизата ткани. Планшеты для захвата инкубировали при 55°C ± 1°C (приблизительно 16-20 часов). На следующие сутки планшеты для захвата промывали 3 раза 1X промывочным буфером (не содержащая нуклеаз вода, компонент 1 буфера и компонент промывочного буфера 2), затем сушили центрифугированием в течение 1 минуты при 240 g. В планшет для захвата добавляли 100 мкл предварительно амплифицированных рабочих реагентов, который герметично закрывали алюминиевой фольгой и инкубировали в течение 1 часа при 55°C ± 1°C. После инкубации в течение 1 часа повторяли этап промывания, затем добавляли 100 мкл амплифицирующего рабочего реагента. Через 1 час повторяли этапы промывания и сушки и добавляли 100 мкл меченого зонда. Планшеты для захвата инкубировали при 50° ± 1°C в течение 1 часа. Затем планшет промывали 1X промывочным буфером, сушили и добавляли 100 мкл субстрата. Планшеты для захвата считывали с использованием люминометра SpectraMax после инкубации от 5 до 15 минут. Данные рДНК анализировали путем вычитания среднего фонового значения из каждого образца в трех повторениях, усредняя получаемые значения трех повторений GAPDH (контрольного зонда) и TTR (экспериментального зонда), а затем вычисляя отношение: (экспериментальный зонд - фоновое значение) / (контрольный зонд - фоновое значение).
Уровни TTR в плазме анализировали с использованием коммерчески доступного набора "AssayMax Human Prealbumin ELISA Kit" (AssayPro, St. Charles, MO, каталожный № EP3010-1) в соответствии с инструкциями производителя. В кратком изложении, плазму мышей разбавляли 1:10000 в 1X смеси разбавителей и добавляли к предварительно покрытым планшетам наряду с набором стандартов и инкубировали в течение 2 часов при комнатной температуре с последующим 5X промываниями промывающим буфером из набора. В каждую лунку добавляли пятьдесят микролитров биотинилированного антитела против преальбумина и инкубировали в течение 1 часа при комнатной температуре с последующими 5X промываниями промывающим буфером. К каждой лунке добавляли пятьдесят микролитров конъюгата стрептавидин-пероксидаза и инкубировали планшеты в течение 30 минут при комнатной температуре с последующим промыванием, как описано ранее. Реакцию начинали добавлением 50 мкл/лунку субстрата хромогена и инкубацию в течение 10 минут при комнатной температуре, где реакцию останавливают добавлением 50 мкл/лунку останавливающего раствора. Оптическую плотность при 450 нм регистрировали на микропланшетном спектрофотометре Versamax (Molecular Devices, Sunnyvale, CA) и анализировали данные с использованием пакета программного обеспечения Softmax 4.6 (Molecular Devices).
Результаты представлены на фигурах 10-12. На фигуре 10 продемонстрировано, что средства для РНКи, модифицированные относительно исходного средства AD-45163 и AD-45165, проявляли активность подавления РНК, которая являлась аналогичной или более сильной по сравнению с активностью исходных соединений. На фигуре 11 продемонстрировано, что средства AD-51544 и AD-51545 проявляли дозозависимую активность подавления, и что активность подавления этих средств в дозе 5 мг/кг являлась сходной с активностью подавления соответствующего исходного AD-45163. На фигуре 12 продемонстрировано, что средства AD-51546 и AD-51547 также проявляли дозозависимую активность подавления. Кроме того, активность подавления AD-51546 и AD-51547 в дозе 5 мг/кг являлась сходной с активностью подавления соответствующего исходного AD-45165.
Пример 7: Фармакокинетические профили средств для РНКи, направленных на TTR, в сыворотке и печени у мыши
Для оценки фармакокинетических профилей средств для РНКи AD-45163, AD-51544, AD-51545, AD-51546 и AD-51547 эти средства в буфере PBS вводили мышам C57BL/6 с использованием однократного болюсного в/в или подкожного (п/к) введения. Концентрации средств в плазме и концентрации в печени оценивали в различные временные точки после введения.
Фармакокинетические параметры в плазме представлены в таблицах 3 и 4 ниже. Среднее время удержания препарата (MRT) в плазме составляло приблизительно 0,2 часа после дозирования в/в и приблизительно 1 час после дозирования п/к. В дозе 25 мг/кг средства AD-51544, AD-51545, AD-51546 и AD-51547 обладали сходными фармакокинетическими свойствами в плазме. Каждое из этих средств обладало более 75% биодоступностью из подкожного пространства. Их биодоступность превосходила биодоступность исходного средства АО-45163, которое вводили в более высокой дозе 30 мг/кг. Биодоступность при подкожном введении AD-51544 и AD-51547 составляла приблизительно 100%, тогда как AD-51545 составляла 90%, и биодоступность AD-51546 составляла 76%.


Результаты также свидетельствовали, что средства для РНКи AD-45163, AD-51544, AD-51545, АО-51546 и AD-51547 обеспечивали аналогичные или более высокие концентрации в печени при подкожном введении по сравнению с введением посредством в/в болюса. Фармакокинетические параметры для печени представлены в таблицах 5 и 6 ниже. Пиковая концентрация (Cmax) и площадь под кривой (AUC0-последний) в печени являлись в два-три раза выше после подкожного введения по сравнению с в/в введением аналогичного средства в аналогичной дозе. Концентрации в печени являлись наиболее высокими для AD-51547 и самыми низкими для AD-51545. Среднее время удержания (MRT) и период полувыведения являлось больше для AD-51546 и AD-51547 по сравнению с АО-51544 и AD-51545. После подкожного введения приблизительные величины MRT составляли 40 часов для AD-51546 и 25 часов для AD-51547, тогда как MRT для AD-51544 и AD-51545 являлись меньше (приблизительно 6-9 часов). Период полувыведения AD-51546 и AD-51547 также являлся более высоким (41-53 часов), чем являлся период полувыведения AD-51544 и AD-51545 (6-10 часов).


Пример 8: Стабильность in vitro средств для РНКи в сыворотке обезьяны
Также оценивали стабильность средств для РНКи AD-51544, AD-51545, AD-51546 и AD-51547 в сыворотке у обезьян. Результаты демонстрировали, что антисмысловые и смысловые цепи AD-51544, AD-51545 и AD-51547 обладают стабильностью в сыворотке в течение периода времени приблизительно 24 часа (данные не показаны).
Пример 9: Средства для РНКи обеспечивают длительное подавление белка TTR у не являющихся человеком приматов
Активность подавления РНК средствами для РНКи AD-45163, AD-51544, AD-51545, AD-51546 и AD-51547 оценивали измерением подавления белка TTR в сыворотке яванских макак после подкожного введения пяти доз 5 мг/кг (одну дозу каждые сутки в течение 5 суток) или однократную дозу 25 мг/кг. Pre-dose Уровни белка TTR перед дозированием в сыворотке оценивали путем усреднения уровней за 11 суток перед первой дозой, за 7 суток перед первой дозой и 1 сутки перед первой дозой. Уровни белка TTR в сыворотке после дозирования оценивали путем определения уровня в сыворотке, начиная на 1 сутки после последней дозы (т.е. на 5 сутки исследования в группе 5×5 мг/кг и 1 сутки исследования в группе 1×25 мг/кг) до 49 суток после последней дозы (т.е. на 53 сутки исследования в группе 5×5 мг/кг и на 49 сутки в группе 1×25 мг/кг). См. фигуру 13.
Уровни белка TTR оценивали, как описано в пример 6. Результаты представлены на фигуре 14 и в таблицах 7 и 8.
Максимальное подавление белка TTR приблизительно до 50% получали в группе, которые получали 25 мг/кг AD-45163, AD-51544, AD-51546 и AD-51547 (см. таблицу 8). Наивысшее подавление белка TTR приблизительно 70% получали в группах, которые получали 5×5 мг/кг AD-45163, AD-51544, AD-51546 и AD-51547 (см. таблицу 7). Средство AD-51545 обеспечивало меньшую степень подавления в обоих протоколах введения. Значительное подавление приблизительно 20% или более сохранялось до 49 суток после последней дозы AD-51546 и AD-51547 в обоих протоколах 1×25 мг/кг и 5×5 мг/кг. Как правило, лучшее подавление получали в протоколе 5×5 мг/кг по сравнению с протоколом 1×25 мг/кг.


Пример 10: Переносимость средств РНКи, направленных на TTR
Оценка цитокинов в анализе цельной крови
Для оценки переносимости средств для РНКи, направленных на TTR, (включая AD-45163, AD-51544, AD-51545, AD-51546 и AD-51547) каждое средство тестировали в анализе цельной крови с использованием крови от трех доноров, являющихся человеком. Средства представляли собой 300 нМ трансфицируемый DOTAP или 1 мкМ реагент без трансфекции (свободная миРНК). Наблюдали менее чем двукратное изменение для следующих ниже цитокинов/хемокинов: G-CSF, IFN-γ, IL-10, IL-12 (p70), IL1β, IL-1ra, IL-6, IL-8, IP-10, MCP-1, MIP-1α, MIP-1β, TNFα. (Результаты не показаны).
Оценка in vivo
Для оценки переносимости in vivo средства для РНКи инъецировали подкожно мышам CD1 в дозе 125 мг/кг. Не наблюдали индукции цитокинов через 2, 4, 6, 24 или 48 часов после подкожной инъекции AD-45163. Не наблюдали значительной индукции цитокинов через 6 или 24 часа после подкожной инъекции AD-51544, AD-51545, AD-51546 или AD-51547.
Для полной оценки переносимости in vivo тестировали ряд средств для РНКи (включая AD-45163, AD-51544, AD-51545, AD-51546 и AD-51547) посредством подкожной инъекции 5 и 25 мг не являющимся человеком приматам (яванским макакам) с объемами дозы 1-2 мл на участок. Не наблюдали эритему или отек на участках инъекции.
Исследование переносимости однократной п/к дозы у крыс
Для оценки токсичности крыс инъецировали однократной подкожной дозой 100, 250, 500 или 750 мг/кг AD-45163 (см. таблицу 9). Проводили следующие ниже оценки: клинические признаки токсичности, массы тела, общий анализ крови, клинической биохимии и свертывания, массы органов (печени и селезенки), макроскопическую и микроскопическую оценку (почки, печени, легкого, лимфоузла, селезенки, семенников, тимуса, аорты, сердца, кишечника (тонкого и толстого).

Результаты демонстрируют отсутствие связанных с тестируемым препаратом клинических признаков токсичности, эффектов на массу тела, массу органов или клиническую биохимию. Не наблюдали гистопатологию сердца, почек, семенников, селезенки, печени, и тимуса. Наблюдали не являющееся неблагоприятным незначительное связанное с тестируемым препаратом повышение WBC (↑ 68%, преимущественно относящееся к повышению NEUT и MONO) при 750 мг/кг. Эти результаты свидетельствуют о том, что однократная доза до 750 мг/кг является хорошо переносимой крысами.
Переносимость повторных подкожных введений у крыс
Для оценки переносимости повторных подкожных введений AD-45163 проводили ежесуточные подкожные инъекции 300 мг/кг в течение 5 суток и на 6 сутки проводили вскрытие. План исследования представлен в таблице 10.

Оценивали следующие ниже выходные параметры: клинические признаки, массы тела, гематологию, клиническую биохимию и свертывание, массы органа, макроскопическую и микроскопическую оценку (печени, селезенки, почки, сердца, желудочно-кишечного тракта и первого и последнего участка инъекции). Результаты демонстрировали отсутствие связанных с тестируемым препаратом клинических признаков, эффектов на массу тела или массу органов, а также отсутствие связанных с тестируемым препаратом данных клинической гематологии или биохимии. Существовало возможное незначительное увеличение активированного частичного тромбопластинового времени (APTT) на сутки 6 (20,4 в сравнении с 17,4 секундами). Гистопатология не выявляла связанных с тестируемым препаратом данных в печени, селезенке, сердце и желудочно-кишечном тракте. В почке наблюдали от минимальной до незначительной гипертрофию канальцевого эпителия (не относящуюся к неблагоприятной). На последнем участке наблюдали минимальный многоочаговый мононуклеарный инфильтрат, не относящийся к неблагоприятным. Эти результаты свидетельствуют о том, что пять ежесуточных доз 300 мг/кг исходного средства для РНКи AD-45163 являются хорошо переносимыми у крыс.
Пример 11: Средства РНКи обеспечивают длительное подавление белка TTR у не являющихся человеком приматов
Активность подавления РНК средства для РНКи AD-51547 оценивали посредством измерения подавления белка TTR в сыворотке яванских макак после подкожного введения "интенсивной фазы" средства для РНКи: пять суточных доз 2,5 мг/кг, 5 мг/кг или 10 мг/кг (одна доза каждые сутки в течение 5 суток) с последующей "поддерживающей фазой" средства для РНКи: еженедельное дозирование 2,5 мг/кг, 5 мг/кг или 10 мг/кг в течение 4 недель. Уровни белка TTR перед дозированием в сыворотке оценивали путем усреднения уровней за 11 суток до первой дозы, 7 суток до первой дозы и 1 сутки до первой дозы. Уровни белка TTR в сыворотке после дозирования оценивали посредством определения уровня в сыворотке относительно периода пред дозированием, начиная на 1 сутки после интенсивной фазы, завершали на 40 суток после последней дозы поддерживающей фазы (т.е. 70 сутки исследования).
Уровни белка TTR оценивали, как описано в пример 6. Результаты приведены на фигуре 15.
Максимальное подавление белка TTR приблизительно до 80% получали во всех группах, которые получали 2,5 мг/кг, 5 мг/кг или 10 мг/кг AD-51547. Самый низкий уровень нокдауна получали во всех группах приблизительно на сутки 14, подавление сохранялось на уровнях самого низкого нокдауна при еженедельной поддерживающей дозе 2,5 мг/кг, 5 мг/кг или 10 мг/кг AD-51547. Уровни TTR не возвращались к исходному уровню более 40 суток после суток введения последней поддерживающей дозы при уровнях дозирования 5 и 2,5 мг/кг.
Эквиваленты
Специалистам в данной области будет понятно, или они могут устанавливать использованием только общепринятого экспериментирования многие эквиваленты конкретных вариантов осуществления и способов, описываемых в настоящем описании. Предполагают, что такие эквиваленты входят в объем следующей ниже формулы изобретения.
Реферат
Изобретение относится к биохимии. Описано двухцепочечное средство для РНКи для ингибирования экспрессии транстиретина (TTR), содержащее смысловую цепь, комплементарную антисмысловой цепи, где указанная антисмысловая цепь содержит последовательность, комплементарный нуклеотидам 504-526 гена транстиретина (TTR) (SEQ ID NO:1), где смысловая цепь имеет длину 21 нуклеотид, а антисмысловая цепь имеет длину 23 нуклеотида. Так описано средство для РНКи для ингибирования экспрессии транстиретина (TTR), включающее смысловую цепь и антисмысловую цепь, в котором смысловая цепь содержит нуклеотидную последовательность 5’-UfgGfgAfuUfuCfAfUfgUfaacCfaAfgAfL96-3’ (SEQ ID NO:2), и антисмысловая цепь содержит нуклеотидную последовательность 5’-uCfuUfgGfUfUfaCfaugAfaAfuCfcCfasUfsc-3’ (SEQ ID NO:3),где a, g, c и u обозначают 2’—О-метил (2’-OMe) A, G, C и U; Af, Gf, Cf и Uf обозначают 2’-фтор A, G, C и U; s обозначает фосфоротиоатную связь; и L96 обозначает лиганд GalNAc. Описана фармацевтическая композиция, содержащая любое из указанных средств. Представлен способ ингибирования экспрессии транстиретина (TTR) в клетке, включающий приведение указанной клетки в контакт с указанным средством для РНКи. Представлен способ лечения ассоциированного с TTR заболевания у индивидуума, включающий введение указанному индивидууму терапевтически эффективного количества указанного средства для РНКи. 6 н. и 29 з.п. ф-лы, 10 табл., 11 пр.
Формула



Документы, цитированные в отчёте о поиске
Стабилизация транстиретина

Комментарии