Композиции и способы модулирования экспрессии аполипопротеина c-iii - RU2650510C2
Код документа: RU2650510C2
Чертежи



















































Описание
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящее изобретение зарегистрировано вместе с перечнем последовательностей в электронном формате. Перечень последовательностей приведен в виде файла под названием BIOL0249WOSEQ_ST25.txt, созданного 1 мая 2014 года, размером 68 Кб. Информация о перечне последовательностей в электронном формате в полном объеме включена в настоящий документ посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
Принцип, лежащий в основе антисмысловой технологии, заключается в том, что антисмысловое соединение гибридизуется с целевой нуклеиновой кислотой и модулирует количество, активность и/или функцию целевой нуклеиновой кислоты. Например, в некоторых случаях антисмысловые соединения приводят к изменению транскрипции или трансляции мишени. Такое модулирование экспрессии может быть достигнуто, например, разрушением целевой мРНК или замещающим ингибированием. Пример модулирования целевой функции РНК за счет разрушения представляет собой разрушение за счет РНКазы Н целевой РНК при гибридизации с ДНК-подобным антисмысловым соединением. Другой пример модулирования генной экспрессии за счет нацеленного разрушения представляет собой РНК-интерференция (РНКи). РНКи относится к антисмысл-опосредованному сайленсингу гена по механизму, в котором применяется РНК-индуцируемый комплекс сайленсинга (RISC). Дополнительный пример модулирования целевой функции РНК представляет собой механизм замещения, такой как использует в естественных условиях микроРНК. МикроРНК представляют собой небольшие некодирующие РНК, которые регулируют экспрессию РНК, кодирующих белки. Связывание антисмыслового соединения с микроРНК препятствует связыванию микроРНК с ее матричными РНК мишенями, и, следовательно, затрудняет функцию микроРНК. МикроРНК-миметики могут усиливать естественную функцию микроРНК. Некоторые антисмысловые соединения изменяют сплайсинг пре-мРНК. Независимо от конкретного механизма, специфичность в отношении последовательностей делает антисмысловые соединения перспективными в качестве средств для подтверждения нацеленности и функционализации генов, а также в качестве терапевтических средств для селективного модулирования экспрессии генов, участвующих в патогенезе заболеваний.
Антисмысловая технология представляет собой эффективный способ модулирования экспрессии одного или более специфических генных продуктов и, следовательно, может быть признана исключительно подходящей в ряде терапевтических, диагностических и исследовательских применений. Химически модифицированные нуклеозиды могут быть внедрены в антисмысловые соединения для усиления одного или более свойств, таких как устойчивость к нуклеазе, фармакокинетика или аффинность к целевой нуклеиновой кислоте. В 1998 году антисмысловое соединение Vitravene® (фомивирсен; разработанный компанией Isis Pharmaceuticals Inc., Карлсбад, штат Калифорния) стал первым антисмысловым лекарством, получившим разрешение на продажу от Администрации США по пищевым продуктам и лекарственным веществам (FDA), и в настоящее время представляет собой средство для лечения вызванного цитомегаловирусом (CMV) ретинита у пациентов со СПИДом.
Новые химические модификации обладают улучшенной активностью и эффективностью антисмысловых соединений, раскрывая потенциал для пероральной доставки, а также для усовершенствования подкожного введения, снижения возможных побочных эффектов, и приводят к улучшению удобства для пациента. Химические модификации, усиливающие активность антисмысловых соединений, позволяют осуществлять введение более низких доз, что снижает возможность токсичности, а также уменьшает общую стоимость лечения. Модификации, увеличивающие устойчивости к разрушению, приводят к более медленному выведению из организма, обеспечивая возможность менее частого введения доз. Различные типы химических модификаций могут быть комбинированы в одном соединении для дальнейшей оптимизации эффективности соединения.
Аполипопротеин C-III (называемый также АРОС3, APOC-III, АроCIII и APOC-III) входит в состав липопротеинов высокой плотности (HDL) и богатых на триглицериды (TG) липопротеинов. Повышенные уровни АроCIII связаны с повышенными уровнями TG и такими заболеваниями, как сердечно-сосудистые заболевания, метаболический синдром, ожирение и диабет (Chan et al., Int J Clin Pract, 2008, 62: 799-809; Onat et at., Atherosclerosis, 2003, 168: 81-89; Mendivil et al., Circulation, 2011, 124: 2065-2072; Mauger et al., J. Lipid Res, 2006. 47: 1212-1218; Chan et al., Clin. Chem, 2002. 278-283; Ooi et al., Clin. Sci, 2008. 114: 611-624; Davidsson et al., J. Lipid Res. 2005. 46: 1999-2006; Sacks et al., Circulation, 2000. 102: 1886-1892; Lee et al., Arterioscler Thromb Vasc Biol, 2003. 23: 853-858). АроCIII замедляет клиренс богатых на TG липопротеинов путем ингибирования липолиза из-за подавления липопротеин-липазы (LPL) и за счет взаимодействия с липопротеином, связанным с гликозаминогликановой матрицей клеточной поверхности (Shachter, Curr. Opin. Lipidol, 2001, 12, 297-304).
Антисмысловая технология развивается как эффективное средство снижения экспрессии определенных генных продуктов, и может быть подтверждена ее уникальная полезность в ряде терапевтических, диагностических и исследовательских применений для модулирования АроCIII. Ранее были описаны антисмысловые соединения, нацеленные на АроCIII, и родственные способы ингибирования АроCIII (см., например, патент США 7598227, патент США 7750141, публикацию РСТ WO 2004/093783, публикацию РСТ WO 2012/149495 и PCT/US 14/016546, которые включены в настоящий документ посредством ссылки). Антисмысловое соединение, нацеленное на АроCIII, ISIS-APOCIIIRx, было испытано в клинических испытаниях I и II фазы. Однако ни одно антисмысловое соединение, нацеленное на АроCIII, не было одобрено для промышленного применения, соответственно, все еще существует необходимость в обеспечении пациентов дополнительными и более эффективными возможностями лечения.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В некоторых вариантах реализации настоящего описания приведены конъюгированные антисмысловые соединения. В некоторых вариантах реализации настоящего описания приведены конъюгированные антисмысловые соединения, содержащие антисмысловый олигонуклеотид, комплементарный транскрипту нуклеиновой кислоты. В некоторых вариантах реализации настоящего описания приведены способы, включающие контакт клетки с конъюгированным антисмысловым соединением, содержащим антисмысловый олигонуклеотид, комплементарный транскрипту нуклеиновой кислоты. В некоторых вариантах реализации настоящего описания приведены способы, включающее контакт клетки с конъюгированным антисмысловым соединением, содержащим антисмысловый олигонуклеотид, и уменьшение количества или активности транскрипта нуклеиновой кислоты в клетке.
Ранее был описан асиалогликопротеиновый рецептор (ASGP-R). См., например, Paik et al., PNAS, том 102, №47, cc. 17125-17129 (2005). Такие рецепторы экспрессируются на клетках печени, в частности, гепатоцитах. Кроме того, было показано, что соединения, содержащие кластеры трех N-ацетилгалактозаминовых (GalNAc) лигандов, способны связываться с ASGP-R, приводя к захвату указанного соединения в клетку. См., например, Khorev et al., Bioorganic and Medicinal Chemistry, 16, 9, cc. 5216-5231 (май, 2008). Соответственно, конъюгаты, содержащие такие кластеры GalNAc, применяли для облегчения захвата некоторых соединений в клетки печени, в частности, гепатоциты. Например, было показано, что некоторые GalNAc-содержащие конъюгаты увеличивают активности дуплексных миРНК соединений в клетках печени in vivo. В таких случаях GalNAc-содержащий конъюгат, как правило, прикрепляется к смысловой спирали дуплекса миРНК. Поскольку смысловая спираль отбрасывается перед окончательной гибридизацией антисмысловой спирали с целевой нуклеиновой кислотой, то маловероятно, что такой конъюгат будет влиять на активность. Как правило, конъюгат присоединяется к 3'-концу смысловой спирали миРНК. См., например, патент США 8106022. Некоторые конъюгирующие группы, описанные в настоящем документе, более активны и/или синтезируются легче, чем конъюгирующие группы, описанные ранее.
В некоторых вариантах реализации настоящего изобретения конъюгаты присоединяются к односпиральным антисмысловым соединениям, включая, но не ограничиваясь ими, антисмысловые соединения на основе РНКазы Н и антисмысловые соединения, которые изменяют сплайсинг целевой нуклеиновой кислоты пре-мРНК. В таких вариантах реализации конъюгат должен оставаться присоединенным к антисмысловому соединению достаточно долго для обеспечения преимущества (улучшенного захвата в клетки), но затем он должен либо расщепляться, либо иным образом не препятствовать последующим стадиям, необходимым для активности, таким как гибридизация с целевой нуклеиновой кислотой и взаимодействие с РНКазой Н или ферментами, связанными со сплайсингом или модулированием сплайсинга. Такой баланс свойств более важен при осаждении односпиральных антисмысловых соединений, чем соединений миРНК, где конъюгат может быть просто присоединен к смысловой спирали. В настоящем документе описаны односпиральные антисмысловые соединения, обладающие улучшенной активностью в клетках печени in vivo, по сравнению с таким же антисмысловым соединением, не имеющим конъюгата. Учитывая необходимый баланс свойств для этих соединений, такая улучшенная активность является неожиданной.
В некоторых вариантах реализации конъюгирующие группы по настоящему документу содержат расщепляемый фрагмент. Как было отмечено, не ограничиваясь каким-либо механизмом, логично, что конъюгат должен сохраняться у соединения достаточно долго для обеспечения усиления захвата, но после этого желательно, чтобы некоторая его часть или, в идеале, весь конъюгат расщеплялся, выделяя исходное соединение (например, антисмысловое соединение) в его наиболее активной форме. В некоторых вариантах реализации расщепляемый фрагмент представляет собой расщепляемый нуклеозид. Такие варианты реализации обладают преимуществом эндогенных нуклеаз в клетке за счет присоединения остальной части конъюгата (кластера) к антисмысловому олигонуклеотиду через нуклеозид при помощи одной или более расщепляемых связей, таких как фосфодиэфирные связи. В некоторых вариантах реализации кластер связан с расщепляемым нуклеозидом через фосфодиэфирную связь. В некоторых вариантах реализации расщепляемый нуклеозид присоединен к антисмысловому олигонуклеотиду (антисмысловому соединению) фосфодиэфирной связью. В некоторых вариантах реализации конъюгирующая группа может содержать два или три расщепляемых нуклеозида. В таких вариантах реализации указанные расщепляемые нуклеозиды связаны друг с другом, с антисмысловым соединением и/или с кластером посредством расщепляемых связей (таких как фосфодиэфирная связь). Некоторые конъюгаты по настоящему документу не содержат расщепляемый нуклеозид, а вместо этого содержат расщепляемую связь. Показано, что достаточное расщепление конъюгата из олигонуклеотида обеспечивается по меньшей мере за счет одной связи, которая легко поддается расщеплению в клетке (расщепляемая связь).
В некоторых вариантах реализации конъюгированные антисмысловые соединения представляют собой пролекарства. Такие пролекарства вводят животному, и они в конечном итоге метаболизируются до более активной формы. Например, конъюгированные антисмысловые соединения расщепляются с удалением всего или части конъюгата, приводя к активной (или более активной) форме антисмыслового соединения, не содержащего всего или части конъюгата.
В некоторых вариантах реализации конъюгаты присоединены на 5'-конце олигонуклеотида. Некоторые такие 5'-конъюгаты расщепляются более эффективно, чем аналоги, имеющие такую же конъюгирующую группу, присоединенную на 3'-конце. В некоторых вариантах реализации улучшенная активность может коррелировать с улучшенным расщеплением. В некоторых вариантах реализации олигонуклеотиды, содержащие конъюгат на 5'-конце, обладают более высокой эффективностью, чем олигонуклеотиды, содержащие конъюгат на 3'-конце (см., например, Примеры 56, 81, 83 и 84). Кроме того, 5'-присоединение обеспечивает более простой синтез олигонуклеотида. Как правило, олигонуклеотиды синтезируют на твердой подложке в направлении от 3' к 5'. Для получения 3'-конъюгированного олигонуклеотида, как правило присоединяют предварительно конъюгированный 3'-нуклеозид к твердой подложке, а затем обычным путем создают олигонуклеотид. Однако присоединение такого конъюгированного нуклеозида к твердой подложке усложняет синтез. Кроме того, применяя такой подход, конъюгат затем присутствует в ходе всего синтеза олигонуклеотида и может разрушаться во время последующих стадий или может ограничивать типы реакций и реагентов, которые можно применять. Применяя структуры и методики, описанные в настоящем документе для 5'-конъюгированных олигонуклеотидов, можно синтезировать олигонуклеотид при помощи стандартных автоматизированных методик и внедрять в конъюгат окончательный (5'-ближайший) нуклеозид или после отделения олигонуклеотида от твердой подложки.
С учетом известного уровня техники и настоящего описания, специалисты в данной области техники могут легко получить любые из конъюгатов и конъюгированных олигонуклеотидов, описанных в настоящем документе. Кроме того, синтез некоторых таких конъюгатов и конъюгированных олигонуклеотидов, описанных в настоящем документе, проще и/или требует меньше стадий и, следовательно, менее дорогой, чем синтез ранее описанных конъюгатов, что дает преимущество при производстве. Например, синтез некоторых конъюгирующих групп состоит из меньшего количество синтетических стадий, что приводит к увеличению выхода, по сравнению с ранее описанными конъюгирующими группами. Конъюгирующие группы, такие как GalNAc3-10 в Примере 46 и GalNAc3-7 в Примере 48, гораздо проще, чем ранее описанные конъюгаты, такие как описаны а публикациях U.S. 8106022 или U.S. 7262177, для которых необходима сборка большего количества химических промежуточных соединений. Соответственно, эти и другие конъюгаты, описанные в настоящем документе, обладают преимуществом по сравнению с ранее описанными соединениями для применения с любым олигонуклеотидом. включая односпиральные олигонуклеотиды и любую спираль двухспиральных олигонуклеотидов (например, миРНК).
Точно так же в настоящем документе описаны конъюгирующие группы, имеющие только один или два лиганда GalNAc. Как показано, такие конъюгированные группы усиливают активность антисмысловых соединений. Такие соединения гораздо проще получить, чем конъюгаты, содержащие три лиганда GalNAc. Конъюгирующие группы, содержащие один или два лиганда GalNAc, могут быть присоединены к любым антисмысловым соединениям, включая односпиральные олигонуклеотиды и любую спираль двухспиральных олигонуклеотидов (например, миРНК).
В некоторых вариантах реализации конъюгаты, описанные в настоящем документе, существенно не изменяют некоторые показатели переносимости. Например, в настоящем документе показано, что конъюгированные антисмысловые соединения являются не более иммуногенными, чем неконъюгированные исходные соединения. Поскольку активность улучшается, то варианты реализации, в которых переносимость остается такой же (или, в действительности, если даже переносимость ухудшается лишь незначительно, по сравнению с приростом активности), обладают улучшенными характеристиками для терапии.
В некоторых вариантах реализации конъюгация позволяет изменять антисмысловые соединения так, чтобы они обладали менее выраженными последствиями в отсутствие конъюгации. Например, в некоторых вариантах реализации замена одной или более тиофосфатных связей полностью тиофосфатного антисмыслового соединения w фосфодиэфирные связи приводит к улучшению некоторых показателей переносимости. Например, в некоторых случаях такие антисмысловые соединения, имеющие один или более фосфодиэфиров, являются менее иммуногенными, чем такие же соединения, в которых каждая связь представляет собой тиофосфат. Однако в некоторых случаях, как показано в Примере 26, такое же замещение одной или более тиофосфатных связей на фосфодиэфирные связи приводит также к снижению клеточного захвата и/или к снижению активности. В некоторых вариантах реализации конъюгированные антисмысловые соединения, описанные в настоящем документе, допускают такое изменение связей с небольшим снижением или без снижения захвата и активности, по сравнению с конъюгированным полностью тиофосфатным аналогом. В действительности, в некоторых вариантах реализации, например в Примерах 44, 57, 59 и 86, олигонуклеотиды, содержащие конъюгат и по меньшей мере одну фосфодиэфирную межнуклеозидную связь, фактически демонстрируют повышенную активность in vivo даже по сравнению с полностью тиофосфатным аналогом, также содержащим такой же конъюгат. Более того, поскольку конъюгация приводит к значительному увеличению захвата/активности, то небольшое снижение такого существенного прироста может быть приемлемым для достижения улучшенной переносимости. Соответственно, в некоторых вариантах реализации конъюгированные антисмысловые соединения содержат по меньшей мере одну фосфодиэфирную связь.
В некоторых вариантах реализации конъюгация антисмысловых соединений по настоящему документу приводит к улучшенной доставке, захвату и активности в гепатоцитах. Следовательно, в ткань печени доставляется большее количество соединения. Однако в некоторых вариантах реализации изобретения такая улучшенная доставка сама по себе не объясняет общего увеличения активности. В некоторых таких вариантах реализации изобретения большее количество соединения поступает в гепатоциты. В некоторых вариантах реализации изобретения даже такой улучшенный захват гепатоцитов сам по себе не объясняет общего увеличения активности. В таких вариантах реализации изобретения увеличивается продуктивный захват конъюгированного соединения. Например, как показано в Примере 102, некоторые варианты реализации GalNAc-содержащих конъюгатов увеличивают обогащение антисмысловых олигонуклеотидов в гепатоцитах, по сравнению с не паренхимальными клетками. Такое обогащение преимущественно для олигонуклеотидов, которые нацелены на гены, экспрессируемые в гепатоцитах.
В некоторых вариантах реализации конъюгированные антисмысловые соединения ненастоящему документу приводят к уменьшению воздействия на почки. Например, как показано в Примере 20, концентрации антисмысловых олигонуклеотидов, содержащих некоторые варианты реализации GalNAc-содержащих конъюгатов, в почках ниже, чем концентрации антисмысловых олигонуклеотидов, не имеющих GalNAc-содержащего конъюгата. Это имеет несколько преимущественных терапевтических применений. Для терапевтических показаний, в которых не требуется проявление активности в почках, воздействие на почки подвергает их риску токсичности без соответствующей пользы. Более того, высокая концентрация в почках обычно приводит к выводу соединения с мочой, обеспечивая более быстрое выведение. Соответственно, для внепочечных мишеней накопление в почках является нежелательным.
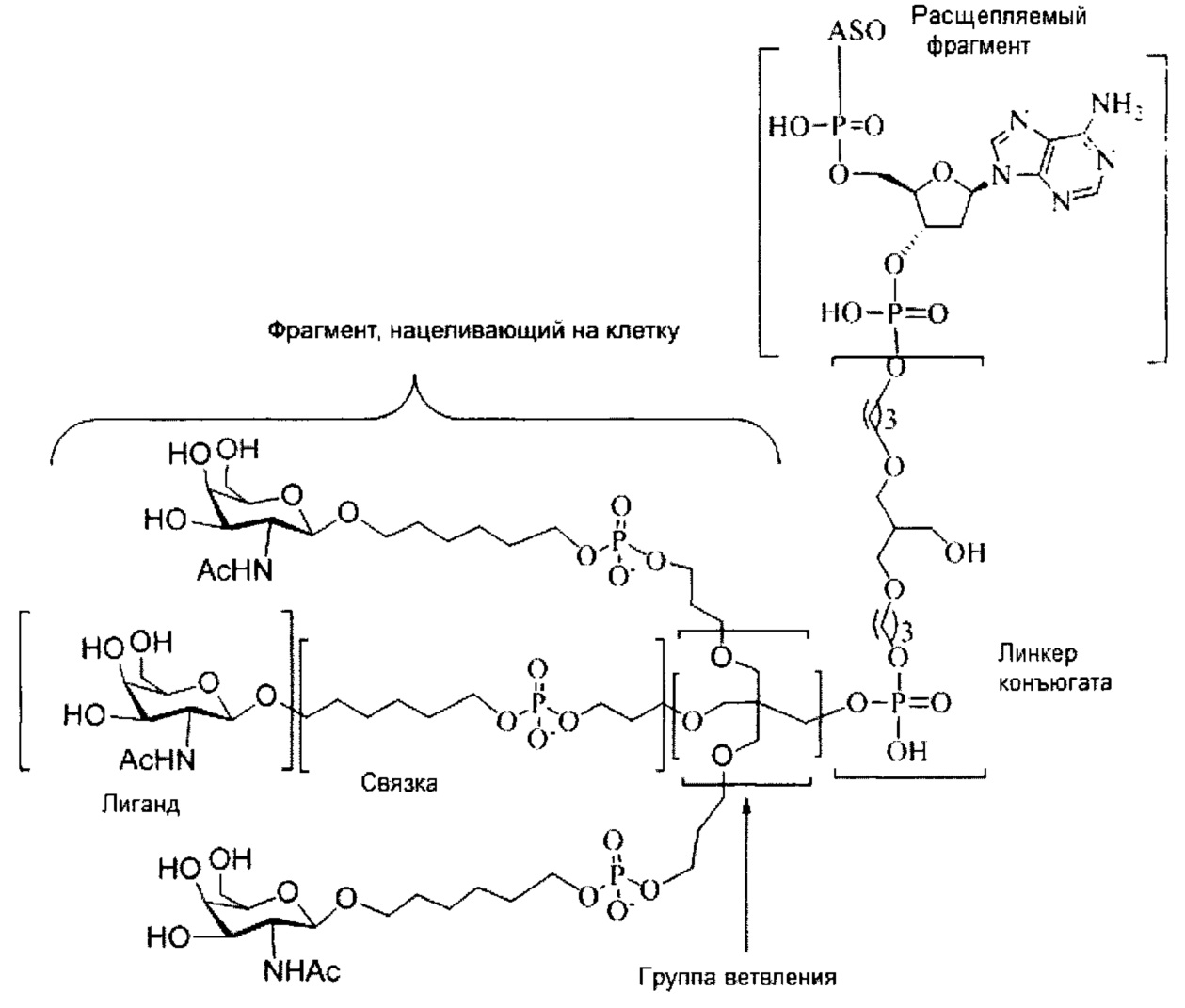
В некоторых вариантах реализации настоящего описания приведены конъюгированные антисмысловые соединения, приведенные формулой:
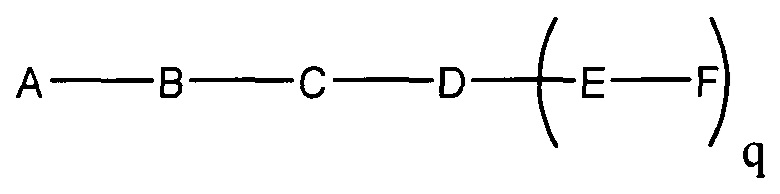
где
А представляет собой антисмысловый олигонуклеотид;
В представляет собой расщепляемый фрагмент;
С представляет собой линкер конъюгата;
D представляет собой группу ветвления;
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
На приведенной выше схеме и в аналогичных схемах в настоящем документе группа ветвления «D» разветвляется такое количество раз, которое необходимо для соответствия количеству групп (E-F), указанному количеством «q». Так, если q=1, то формула представляет собой:
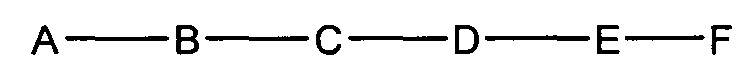
если q=2, то формула представляет собой:
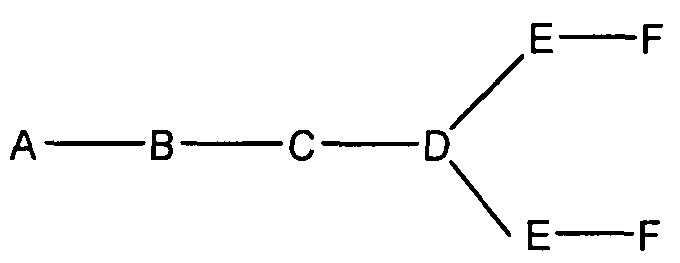
если q=3, то формула представляет собой:
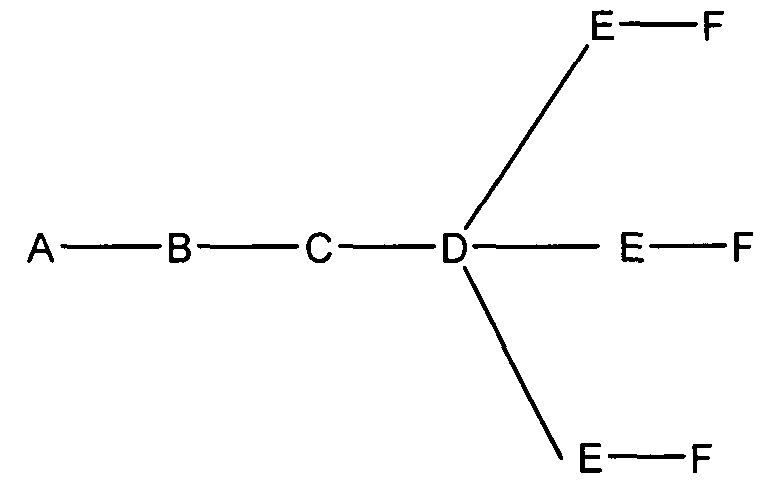
если q=4, то формула представляет собой:
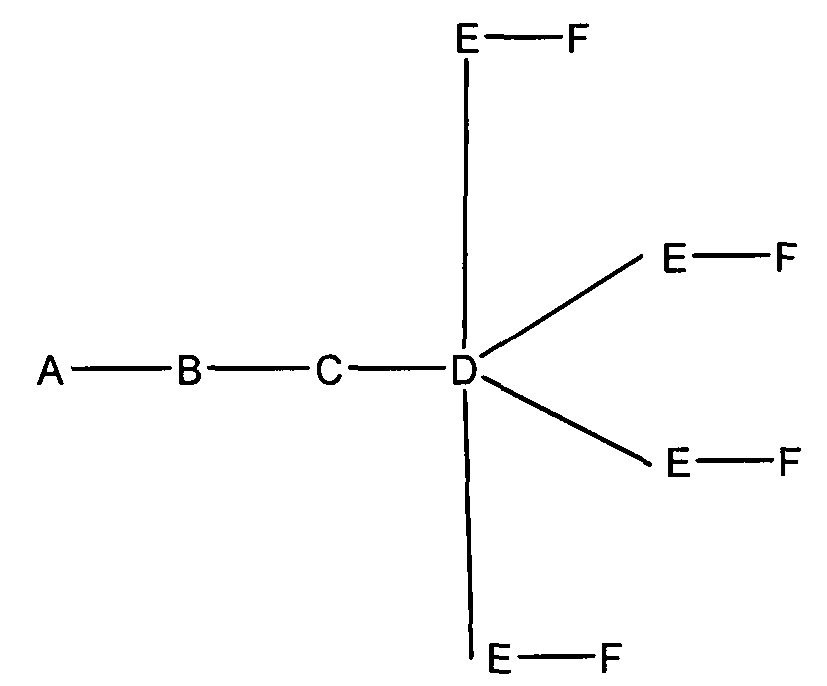
если q=5, то формула представляет собой:
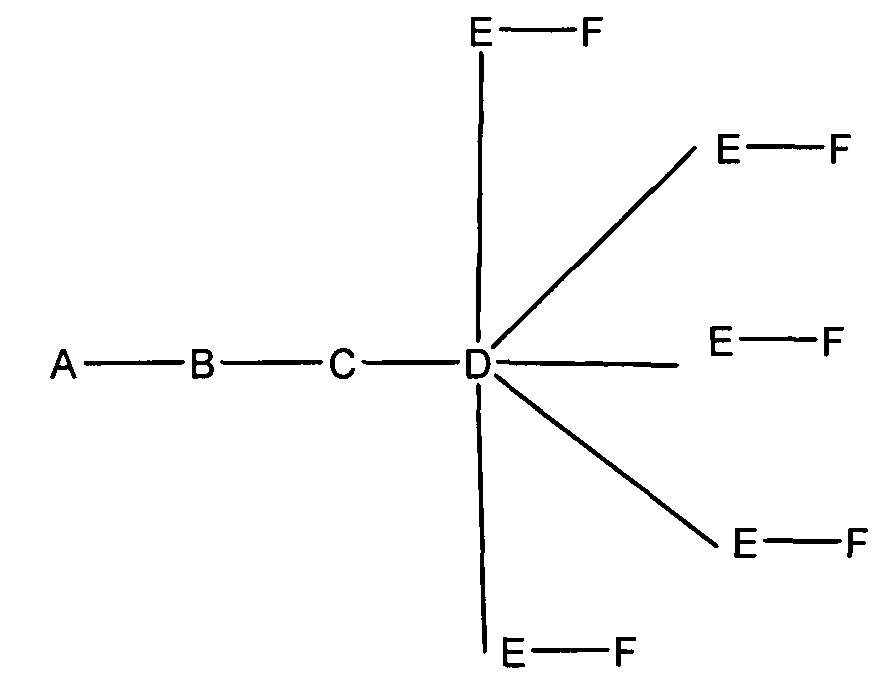
В некоторых вариантах реализации изобретения приведены конъюгированные антисмысловые соединения, имеющие структуру:
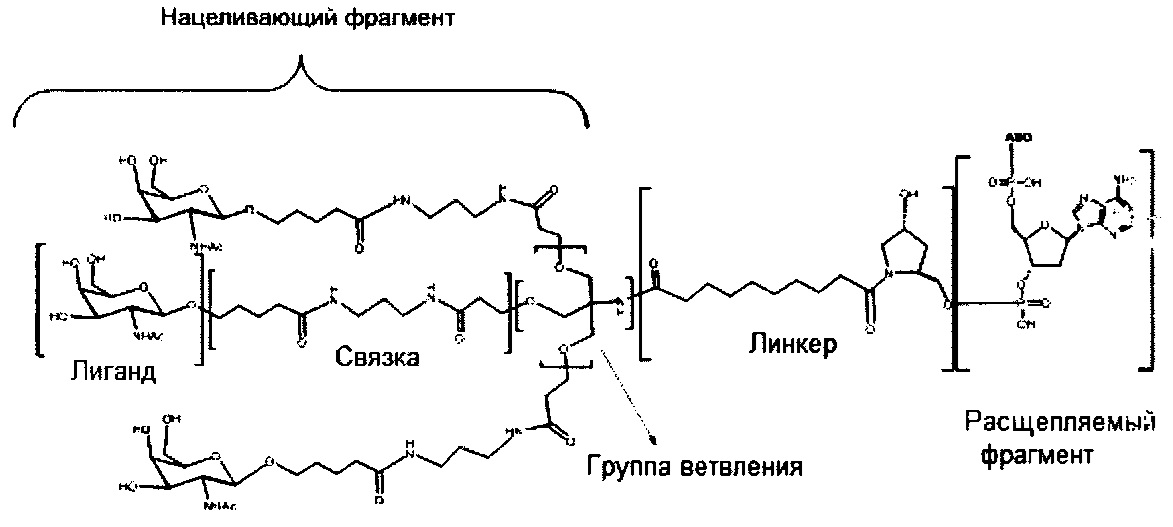
В некоторых вариантах реализации изобретения приведены конъюгированные антисмысловые соединения, имеющие структуру:
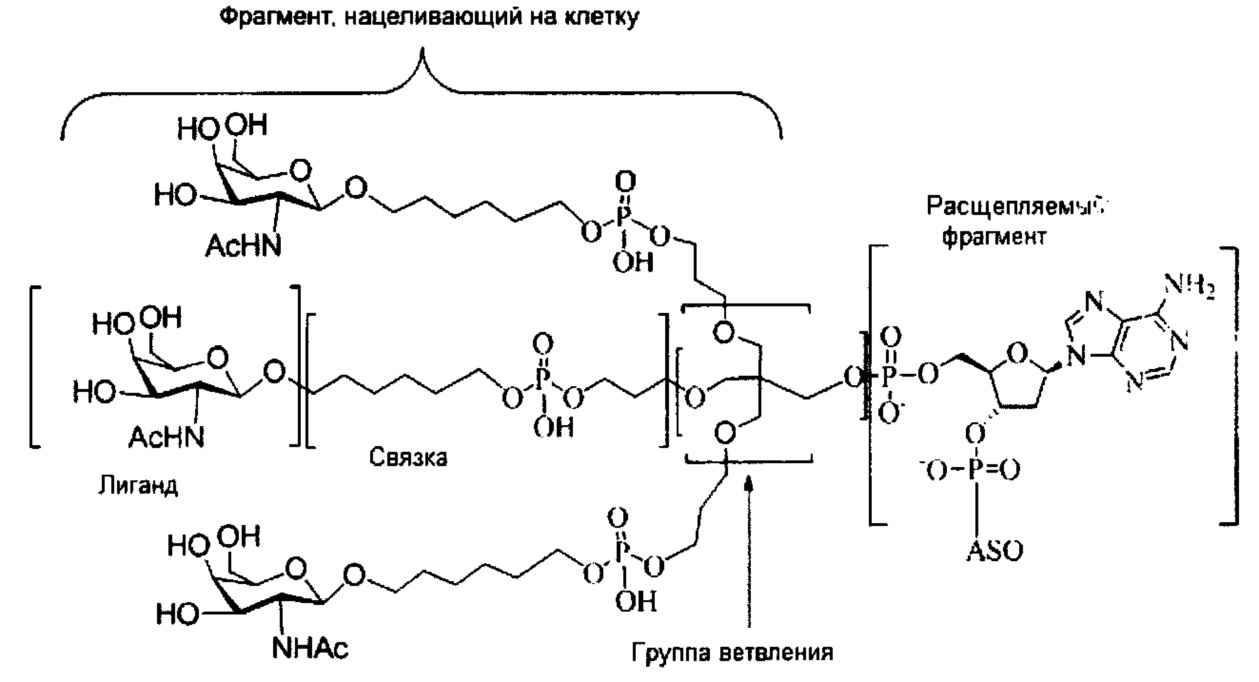
В некоторых вариантах реализации изобретения приведены конъюгированные антисмысловые соединения, имеющие структуру:
В некоторых вариантах реализации изобретения приведены конъюгированные антисмысловые соединения, имеющие структуру:

В настоящем описании приведены следующие неограничивающие варианты реализации изобретения:
В вариантах реализации изобретения, имеющих более одной конкретной переменную (например, более одного «m» или «n»), если не указано иное, каждая такая конкретная переменная выбрана независимо. Следовательно, для структуры, имеющей более одного n, каждый n выбран независимо, так что они могут быть или не быть одинаковыми между собой.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроCIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 12-30 связанных нуклеозидов. В некоторых вариантах реализации изобретения модифицированный олигонуклеотид с конъюгирующей группой состоит из 20 связанных нуклеозидов.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроCIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 12-30 связанных нуклеозидов и содержит последовательность азотистых оснований, комплементарную равной по длине части азотистых оснований 3533-3552 в SEQ ID NO: 3, причем указанная последовательность азотистых оснований модифицированного олигонуклеотида по меньшей мере на 80% комплементарна к SEQ ID NO: 3.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроCIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 12-30 связанных нуклеозидов и содержит последовательность азотистых оснований, комплементарную равной по длине части азотистых оснований 3514-3558 в SEQ ID NO: 3, причем указанная последовательность азотистых оснований модифицированного олигонуклеотида по меньшей мере на 80% комплементарна к SEQ ID NO: 3,
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроCIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 12-30 связанных нуклеозидов и имеет последовательность азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 19-96, 209-221. В некоторых вариантах реализации изобретения конъюгированный модифицированный олигонуклеотид имеет последовательность азотистых оснований, содержащую по меньшей мере 8 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 19-96, 209-221. В некоторых вариантах реализации изобретения соединение состоит из любой из SEQ ID NO: 19-96, 209-221 и конъюгирующие группы.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроCIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 12-30 связанных нуклеозидов и имеет последовательность азотистых оснований SEQ ID NO: 87. В некоторых вариантах реализации изобретения модифицированный олигонуклеотид с конъюгирующей группой имеет последовательность азотистых оснований, содержащую по меньшей мере 8 смежных азотистых оснований последовательности азотистых оснований SEQ ID NO: 87. В некоторых вариантах реализации соединение состоит из SEQ ID NO: 87 и конъюгирующие группы.
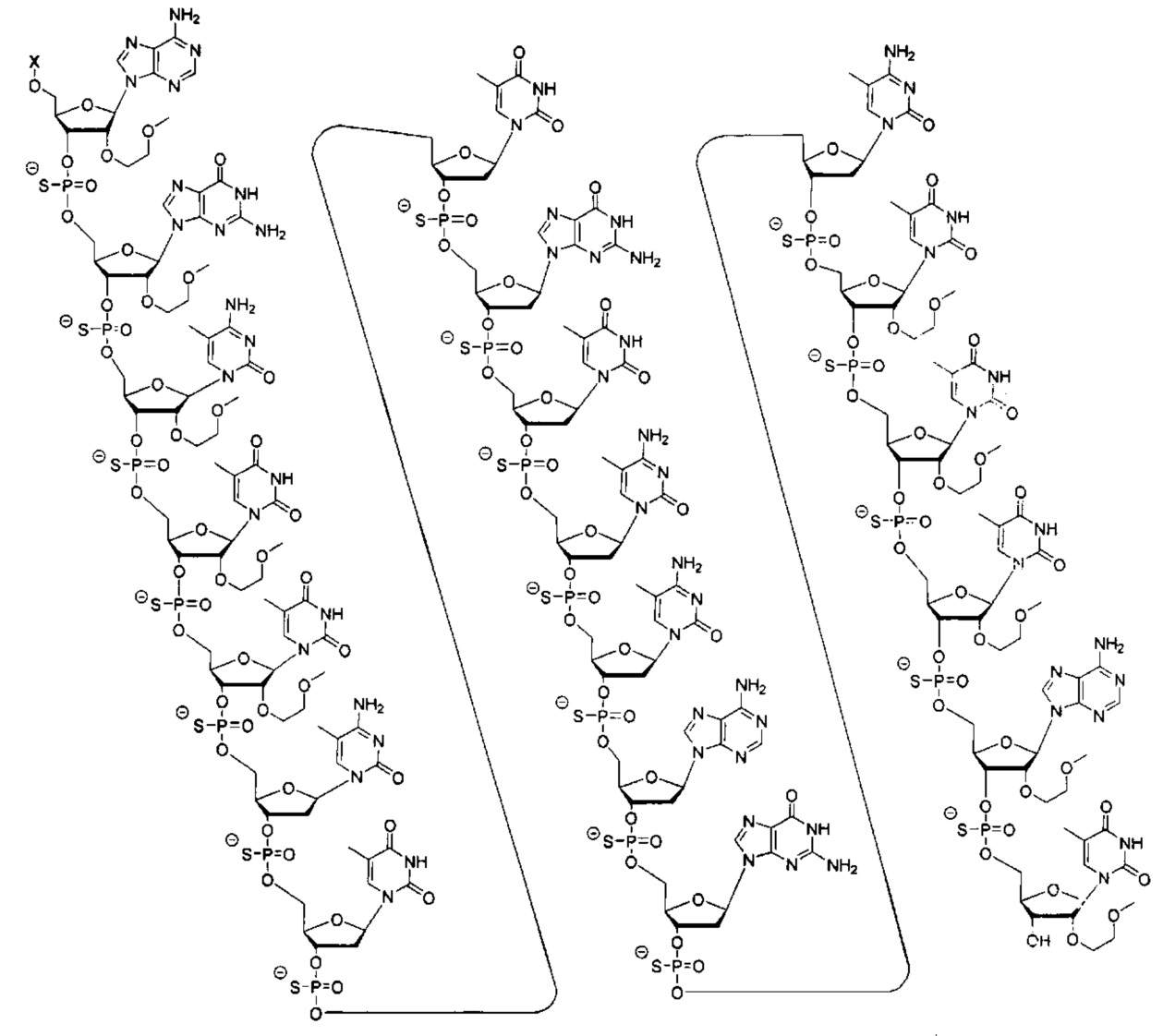
В некоторых вариантах реализации настоящего описания предложены конъюгированные антисмысловые соединения, приведенные следующей структурой. В некоторых вариантах реализации изобретения антисмысловое соединение содержит модифицированный олигонуклеотид ISIS 304801 с 5'-Х, где Х представляет собой конъюгирующую группу, содержащую GalNAc. В некоторых вариантах реализации изобретения антисмысловое соединение состоит из модифицированного олигонуклеотида ISIS 304801 с 5'-Х, где Х представляет собой конъюгирующую группу, содержащую GalNAc.
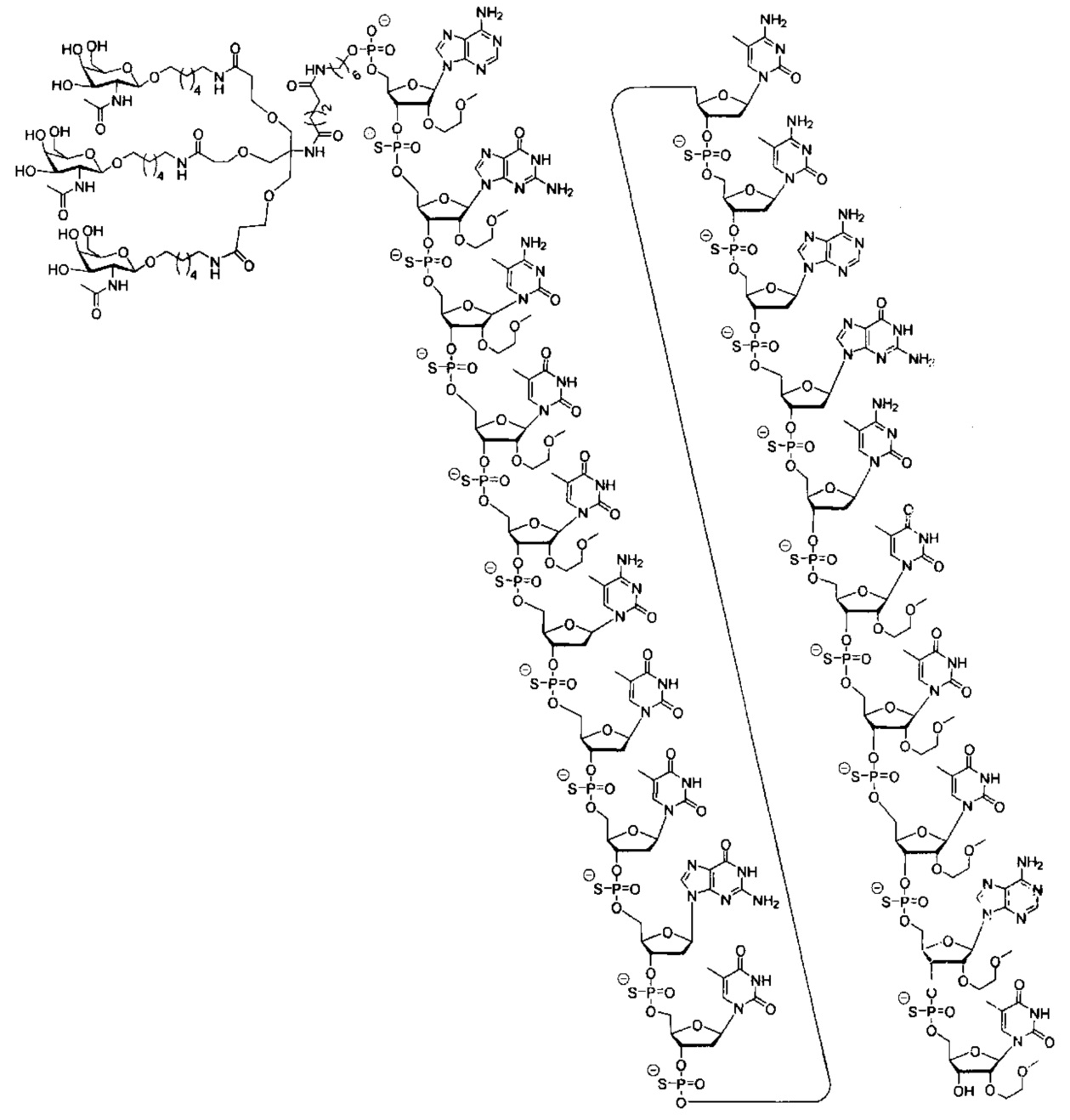
В некоторых вариантах реализации настоящего описания предложены конъюгированные антисмысловые соединения, приведенные следующей структурой. В некоторых вариантах реализации изобретения антисмысловое соединение содержит конъюгированный модифицированный олигонуклеотид ISIS 678354. В некоторых вариантах реализации изобретения антисмысловое соединение состоит из конъюгированного модифицированного олигонуклеотида ISIS 678354.
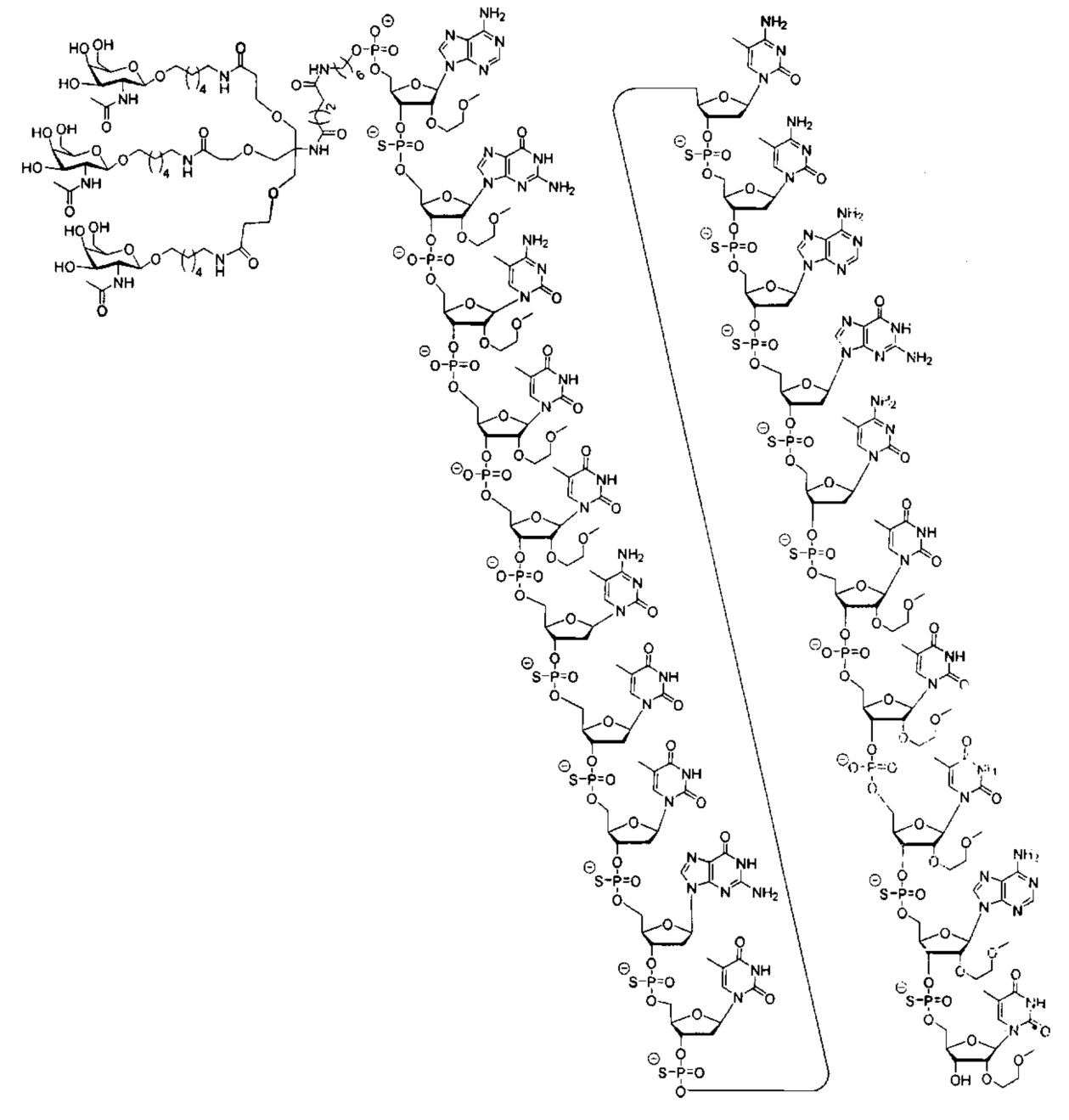
В некоторых вариантах реализации настоящего описания предложены конъюгированные антисмысловые соединения, приведенные следующей структурой. В некоторых вариантах реализации изобретения антисмысловое соединение содержит конъюгированный модифицированный олигонуклеотид ISIS 678357. В некоторых вариантах реализации изобретения антисмысловое соединение состоит из конъюгированного модифицированного олигонуклеотида ISIS 678357.
В некоторых вариантах реализации настоящего описания предложены конъюгированные антисмысловые соединения, приведенные следующей структурой. В некоторых вариантах реализации изобретения антисмысловое соединение содержит модифицированный олигонуклеотид с последовательностью азотистых оснований SEQ ID-NO: 87 с 5'-GalNAc с вариабельностью в сахарных структурах крыльев. В некоторых вариантах реализации изобретения антисмысловое соединение состоит из модифицированного олигонуклеотида с последовательностью азотистых оснований SEQ ID NO: 87 с 5'-GalNAc с вариабельностью в сахарных структурах крыльев.
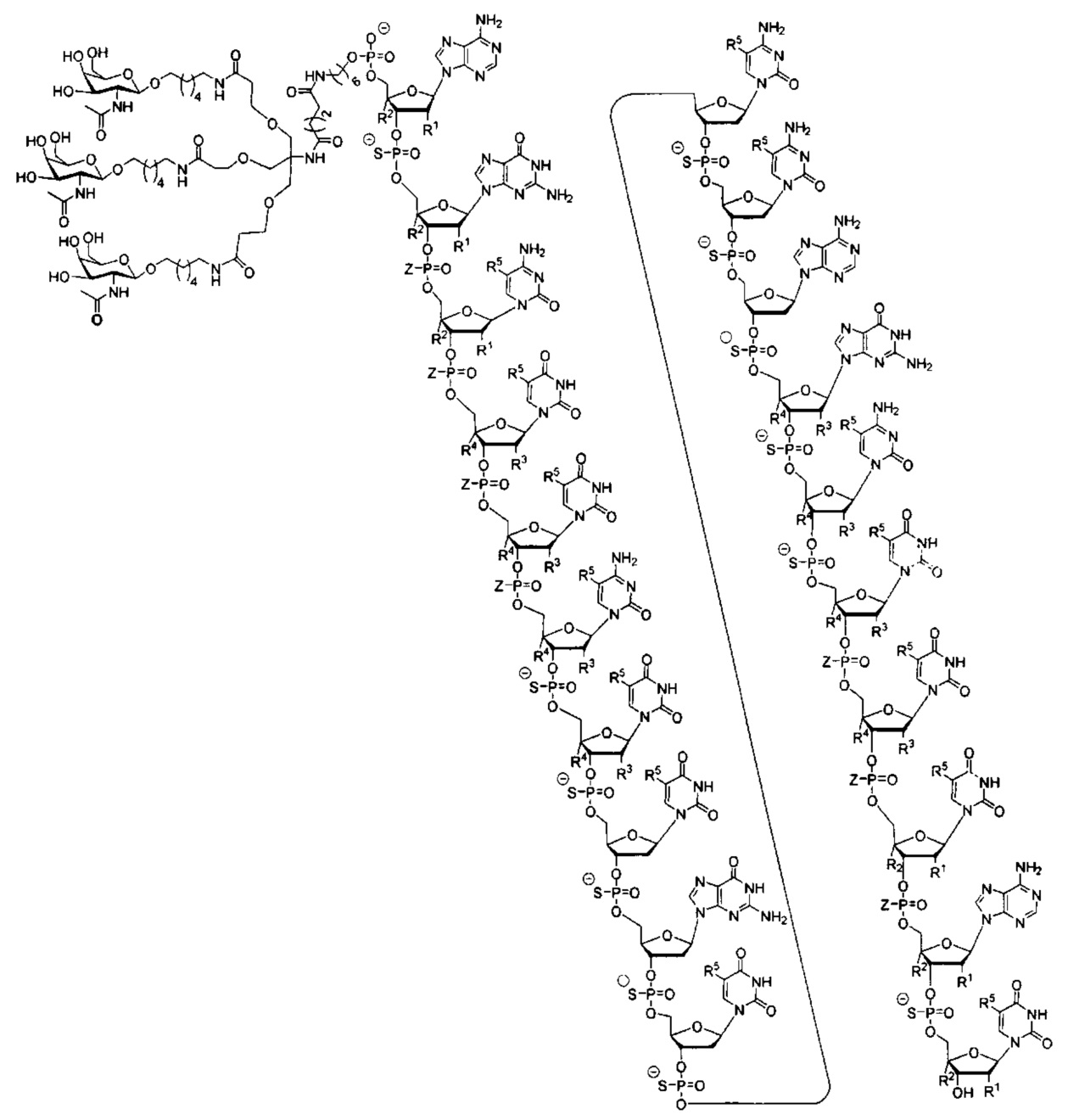
Где либо R1 представляет собой -OCH2CH2OCH3 (МОЕ), и R2 представляет собой Н; либо R1 и R2 вместе образуют мостик, где R1 представляет собой -O-, и R2 представляет собой -CH2-, -СН(СН3)- или -CH2CH2-, и R1 и R2 связаны напрямую, так что образующийся мостик выбран из: -O-CH2-, -О-СН(СН3)- и -O-CH2CH2-;
и для каждой пары R3 и R4 у одного кольца, независимо для каждого кольца: либо R3 выбран из Н и -OCH2CH2OCH3, и R4 представляет собой Н; либо R3 и R4 вместе образуют мостик, где R3 представляет собой -O-, и R4 представляет собой -CH2-, -СН(СН3)- или -CH2CH2-, и R3 и R4 связаны напрямую, так что образующийся мостик выбран из: -O-CH2-, -О-СН(СН3)- и -O-CH2CH2-;
и R5 выбран из Н и -СН3;
и Z выбран из S- и О-.
В настоящем описании приведены следующие неограничивающие нумерованные варианты реализации изобретения:
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Следует понимать, что и приведенное выше общее описание, и следующее подробное описание являются лишь типичными и пояснительными, и они не ограничивают настоящее-описание. В настоящем документе использование единственного числа включает множественное число, если специально не указано иное. При использовании в настоящем документе, термин «или» означает «и/или», если не указано иное. Кроме того, использовании термина «включая», а также других форм, таких как «включает» и «включенный», не является ограничивающим. Также, такие термины как «элемент» или «компонент» охватывают как элементы и компоненты, содержащие одну единицу, так и элементы и компоненты, которые содержат более одной субъединицы, если специально не указано иное.
Названия разделов, используемые в настоящем документе, предназначены лишь для организационных целей, и их не следует толковать как ограничение описанного объекта изобретения. Все документы или части документов, цитируемые в настоящей заявке, включая, но не ограничиваясь ими, патенты, патентные заявки, статьи, книги и монографии, в явной форме включены в настоящий документ посредством ссылки в полном объеме для всех целей.
А. Определения
При отсутствии конкретных определений, номенклатура, используемая в связи с ними, а также в связи с приемами и методиками аналитической химии, синтетической органической химии, а также медицинской и фармацевтической химии, описанная в настоящем документе, является общеизвестной и общепринятой в данной области техники. Для химического синтеза и химического анализа могут быть использованы стандартные методики. Некоторые такие методики и приемы приведены, например, в публикациях "Carbohydrate Modifications in Antisense Research" под редакцией Sangvi и Cook, American Chemical Society, федеральный округ Вашингтон, 1994; "Remington's Pharmaceutical Sciences," Mack Publishing Co., Истон, штат Пенсильвания, 21е издание, 2005; и "Antisense Drug Technology, Principles, Strategies, and Applications" под редакцией Stanley Т. Crooke, CRC Press, Бока-Ратон, штат Флорида; а также в книге Sambrook et al., "Molecular Cloning, A laboratory Manual," 2е издание, Cold Spring Harbor Laboratory Press, 1989, которые включены в настоящий документ посредством ссылки для всех целей. Если это допустимо, все патенты, заявки, опубликованные заявки и другие публикации, а также другие данные, упоминаемые в тексте настоящего описания, включаны в настоящий документ посредством ссылки в полном объеме.
Если не указано иное, следующие термины имеют следующие значения:
При использовании в настоящем документе, «нуклеозид» означает соединение, содержащее фрагмент азотистого основания и сахарный фрагмент. Нуклеозиды включают, но не ограничиваются ими, природные нуклеозиды (которые находятся в ДНК и РНК) и модифицированные нуклеозиды. Нуклеозиды могут быть связаны с фосфатным фрагментом.
При использовании в настоящем документе, «химическая модификация» означает химическое отличие в соединении, по сравнению с природным аналогом. Химические модификации олигонуклеотидов включают нуклеозидные модификации (включая модификации сахарного фрагмента и модификации азотистых оснований) и модификации межнуклеозидных связей. В отношении олигонуклеотида химическая модификация включает не только отличия в последовательности азотистых оснований.
При использовании в настоящем документе, «фуранозил» означает структуру, содержащую 5-членное кольцо, содержащее четыре атома углерода и один атом кислорода.
При использовании в настоящем документе, «природный сахарный фрагмент» означает рибофуранозил, встречающийся в природной РНК, или дезоксирибофуранозил, встречающийся в природной ДНК.
При использовании в настоящем документе, «сахарный фрагмент» означает природный сахарный фрагмент или модифицированный сахарный фрагмент нуклеозида.
При использовании в настоящем документе, «модифицированный сахарный фрагмент» означает замещенный сахарный фрагмент или заменитель сахара.
При использовании в настоящем документе, «замещенный сахарный фрагмент» означает фуранозил, который не является природным сахарным фрагментом. Замещенные сахарные фрагменты включают, но не ограничиваются ими, фуранозилы, содержащие заместители в 2'-положении, 3'-положении, 5'-положении и/или 4'-положении. Некоторые замещенные сахарные фрагменты представляют собой бициклические сахарные фрагменты.
При использовании в настоящем документе, «2'-замещенный сахарный фрагмент» означает фуранозил, содержащий заместитель в 2'-положении, отличный от Н или ОН. Если не указано иное, то 2'-замещенный сахарный фрагмент не является бициклическим сахарным фрагментом (т.е. 2'-заместитель 2'-замещенного сахарного фрагмента не образует мостик с другим атомом радикала фуранозного кольца).
При использовании в настоящем документе, «МОЕ» означает -OCH2CH2OCH3.
При использовании в настоящем документе, «2'-F нуклеозид» относится к нуклеозиду, содержащему сахар, который содержит фтор в 2'-положении. Если не указано иное, то фтор в 2'-F нуклеозиде находится в рибо-положении (заменяя ОН природной рибозы).
При использовании в настоящем документе, термин «заменитель сахара» означает структуру, которая не содержит фуранозила и способна заменять природный сахарный фрагмент нуклеозида, так что образующиеся нуклеозидные субъединицы могут связываться вместе и/или связываться с другими нуклеозидами с образованием олигомерного соединения, которое может гибридизоваться с комплементарным олигомерным соединением. Такие струтуры включают кольца, содержащие другое количество атомов, чем фуранозил (например, 4, 6 или 7-членные кольца); замену кислорода фуранозила некислородным атомом (например, углеродом, серой или азотом); или одновременное изменение количество атомов и замену кислорода. Такие структуры также могут содержать замещения, соответствующие замещениям, описанным для замещенных сахарных фрагментов (например, 6-членные карбоциклические бициклические заменители сахара, необязательно содержащие дополнительные заместители). Заменители сахара включают также более сложные сахарные заместители (например, некольцевые системы пептидной нуклеиновой кислоты). Заменители сахара включают, без ограничения, морфолино, циклогексенилы и циклогекситолы.
При использовании в настоящем документе, «бициклический сахарный фрагмент» означает модифицированный сахарный фрагмент, содержащий 4-7-членное кольцо (включая, но не ограничиваясь фуранозилом), содержащее мостик, связывающий два атома 4-7-членного кольца с образованием второго кольца, что приводит к получению бициклическом структуры. В некоторых вариантах реализации 4-7-членное кольцо представляет собой сахарное кольцо. В некоторых вариантах реализации 4-7-членное кольцо представляет собой фуранозил. В некоторых таких вариантах реализации мостик соединяет 2'-углерод и 4'-углерод фуранозила.
При использовании в настоящем документе, «нуклеотид» означает нуклеозид, дополнительно содержащий фосфатную связывающую группу. При использовании в настоящем документе, «связанные нуклеозиды» могут быть или не быть связаны фосфатными связями и, следовательно, включают, но не ограничиваются ими, «связанные нуклеотиды». При использовании в настоящем документе, «связанные нуклеозиды» представляют собой нуклеозиды, которые связаны в непрерывную последовательность (т.е. между связанными нуклеозидами нет дополнительных нуклеозидов).
Используемый в настоящем документе термин «нуклеиновая кислота» относится к молекулам, состоящим из мономерных нуклеотидов. Нуклеиновая кислота включает рибонуклеиновые кислоты (РНК), дезоксирибонуклеиновые кислоты (ДНК), одноцепочечные нуклеиновые кислоты (оцДНК), двухцепочечные нуклеиновые кислоты (дцДНК), малые интерферирующие рибонуклеиновые кислоты (миРНК) и микроРНХ (микроРНК). Нуклеиновая кислота может также содержать любую комбинацию этих элементов в одной молекуле.
Используемый в настоящем документе термин «нуклеотид» означает нуклеотид, дополнительно содержащий фосфатную линкерную группу. При использовании в настоящем документе, «связанные нуклеозиды» могут быть или не быть связанными фосфатными линкерами, и, следовательно, этот термин включает, но не ограничивается этим, «связанные нуклеотиды». При использовании в настоящем документе, «связанные нуклеозиды» представляют собой нуклеозиды, которые связаны в непрерывную последовательность (т.е. между связанными нуклеозидами нет дополнительных нуклеозидов).
При использовании в настоящем документе, «азотистое основание» означает группу атомов, которая может быть связана с сахарным фрагментом с образованием нуклеозида, который может быть внедрен в олигонуклеотид, и при этом указанная группа атомов может связываться с комплементарным природным с азотистым основанием другого олигонуклеотида или нуклеиновой кислоты. Азотистые основания могут быть природными или могут быть модифицированными. При использовании в настоящем документе «последовательность азотистых оснований» обозначает порядок смежных азотистых оснований, независимый от какого-либо сахара, связи или модификации азотистых оснований.
При использовании в настоящем документе, термины «немодифицированное азотистое основание» или «природное азотистое основание» означают природные гетероциклические азотистые основания РНК или ДНК: пуриновые основания адении (А) и гуанин (G) и пиримидиновые основания тимин (Т), цитозин (С) (включая 5-метил С) и урацил (U).
При использовании в настоящем документе, «модифицированное азотистое основание» означает любое азотистое основание, которое не является природным азотистым основанием.
При использовании в настоящем документе, «модифицированный нуклеозид» означает нуклеозид, содержащий по меньшей мере одну химическую модификацию, по сравнению с природными нуклеозидами РНК или ДНК. Модифицированные нуклеозиды содержат модифицированный сахарный фрагмент и/или модифицированное азотистое основание.
При использовании в настоящем документе, «бициклический нуклеозид» или «BNA» означает нуклеозид, содержащий бициклический сахарный фрагмент.
При использовании в настоящем документе, «стерически затрудненный этил-нуклеозид» или «cEt» означает нуклеозид, содержащий бициклический сахарный фрагмент, который содержит мостик 4'-СН(СН3)-O-2'.
При использовании в настоящем документе, «нуклеозид закрытой нуклеиновой кислоты» или «LNA» означает нуклеозид, содержащий бициклический сахарный фрагмент, который содержит мостик 4'-CH2-O-2'.
При использовании в настоящем документе, «2'-замещенный нуклеозид» означает нуклеозид, содержащий заместитель в 2'-положении, отличный от И или ОН. Если не указано иное, то 2'-замещенный нуклеозид не является бициклическим нуклеозидом.
При использовании в настоящем документе, «дезоксинуклеозид» означает нуклеозид, содержащий 2'-Н фуранозильный сахарный фрагмент, находящийся в природных дезоксирибонуклеозидах (ДНК). В некоторых вариантах реализации 2'-дезоксинуклеозид может содержать модифицированное азотистое основание или может содержать азотистое основание РНК (например, урацил).
При использовании в настоящем документе, «олигонуклеотид» означает соединение, содержащее множество связанных нуклеозидов. В некоторых вариантах реализации олигонуклеотид содержит один или более немодифицированных рибонуклеозидов (РНК) и/или немодифицированных дезоксирибонуклеозидов (ДНК), и/или один или более модифицированных нуклеозидов.
При использовании в настоящем документе, «олигонуклеозид» означает олигонуклеотид, в котором ни один из межнуклеозидных связей не содержит атом фосфора. При использовании в настоящем документе, олигонуклеотиды включают олигонуклеозиды.
При использовании в настоящем документе, «модифицированный олигонуклготид» означает олигонуклеотид, содержащий по меньшей мере один модифицированный нуклеозид и/или по меньшей мере одну модифицированную межнуклеозидную связь.
При использовании в настоящем документе, «связь» или «связывающая группа» означает группу атомов, которая связывает вместе две или более других групп атомов.
При использовании в настоящем документе, «межнуклеозидцая связь» означает ковалентную связь между соседними нуклеозидами в олигонуклеотиде.
При использовании в настоящем документе, «природная межнуклеозидная связь» означает фосфодиэфирную связь 3' с 5'.
При использовании в настоящем документе, «модифицированная межнуклеозидная связь» означает любую межнуклеозидную связь, отличную от природной межнуклеозидной связи.
При использовании в настоящем документе, «концевая межнуклеозидная связь", означает связь между последними двумя нуклеозидами олигонуклеотида или его определенной области.
При использовании в настоящем документе, «фосфорная связывающая группа» означает связывающую группу, содержащую атом фосфора. Фосфорные связывающие группы включают, без ограничения, группы, имеющие формулу:
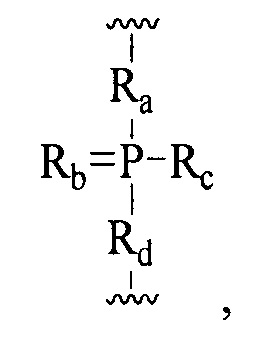
где:
Ra и Rd, каждый независимо, представляют собой О, S, СН2, NH или NJ1, где J1 представляет собой C1-C6 алкил или замещенный C1-C6 алкил;
Rb представляет собой О или S;
Rc представляет собой ОН, SH, C1-C6 алкил, замещенный C1-C6 алкил, C1-C6 алкокси, замещенный C1-C6 алкокси, амино или замещенный амино; и
J1 представляет собой Rb представляет собой О или S.
Фосфорные связывающие группы включают, без ограничения, фосфодиэфир, тиофосфат, дитиофосфат, фосфонат, фосфорамидат, фосфортиоамидат, тионоалкил-фосфонат, фосфотриэфиры, тионоалкил-фосфотриэфиры и боранофосфат.
При использовании в настоящем документе, «межнуклеозидная фосфорная связывающая группа» означает фосфорную связывающую группу, которая напрямую связывает два нуклеозида.
При использовании в настоящем документе, «не межнуклеозидная фосфорная связывающая группа» означает фосфорную связывающую группу, которая не связывает напрямую два нуклеозида. В некоторых вариантах реализации не межнуклеозидная фосфорная связывающая группа связывает нуклеозид с группой, отличной от нуклеозида. В некоторых вариантах реализации не межнуклеозидная фосфорная связывающая группа связывает две группы, ни одна из которых не является нуклеозидом.
При использовании в настоящем документе, «нейтральная связывающая группа» означает связывающую группу, которая не имеет заряда. Нейтральные связывающие группы включают, без ограничения, фосфотриэфиры, метилфосфонаты, MMI (-CH2-N(CH3)-O-), амид-3 (-CH2-C(=O)-N(H)-), амид-4 (-CH2-N(H)-C(=O)-), формацеталь (-O-CH2-O-) тиоформацеталь (-S-CH2-O-). Дополнительные нейтральные связывающие группы включают неионные связи, содержащие силоксан (диалкилсилоксан), карбоксильный эфир, карбоксамид, сульфид, сульфоновый эфир и амиды (см., например: Carbohydrate Modifications in Antisense Research; под ред. Y.S. Sanghvi и P.D. Cook, ACS Symposium, серия 580; главы 3 и 4, (с. 40-65)). Дополнительные нейтральные связывающие группы включают неионные связи, содержащие смешанные составные части N, О, S и CH2.
При использовании в настоящем документе, «межнуклеозидная нейтральная связывающая группа» означает нейтральную связывающую группу, которая напрямую связывает два нуклеозида.
При использовании в настоящем документе, «не межнуклеозидная нейтральная связывающая группа» означает нейтральную связывающую группу, которая не связывает напрямую два нуклеозида. В некоторых вариантах реализации не межнуклеозидная нейтральная связывающая группа связывает нуклеозид с группой, отличной от нуклеозида. В некоторых вариантах реализации не межнуклеозидная нейтральная связывающая группа связывает две группы, ни одна из которых не является нуклеозидом.
При использовании в настоящем документе, «олигомерное соединение» означает полимерную структуру, содержащую две или более субструктур. В некоторых вариантах реализации олигомерное соединение содержит олигонуклеотид. В некоторых вариантах реализации олигомерное соединение содержит одну или более конъюгирующих групп и/или концевых групп. В некоторых вариантах реализации олигомерное соединение состоит из олигонуклеотида. Олигомерные соединения включают также природные нуклеиновые кислоты. В некоторых вариантах реализации олигомерное соединение содержит скелет одной или более связанных мономерных субъединиц, при этом каждая связанная мономерная субъединица прямо или косвенно присоединена к гетероциклическому основному фрагменту. В некоторых вариантах реализации олигомерные соединения могут содержать также мономерные субъединицы, которые не связаны с гетероциклическим основным фрагментом, обеспечивая таким образом сайты с удаленными основаниями. В некоторых вариантах реализации связи, соединяющие мономерные субъединицы, сахарные фрагменты или заменители и гетероциклические основные фрагменты, могут быть независимо модифицированы. В некоторых вариантах реализации единица связь-сахар, которая может содержать или не содержать гетероциклическое основание, может быть замещена миметиком, таким как мономеры в пептидных нуклеиновых кислотах.
При использовании в настоящем документе, «концевая группа» означает один или более атомов, присоединенных к любому или к обоим 3'- или 5'-концам олигонуклеотида. В некоторых вариантах реализации концевая группа представляет собой конъюгирующую группу. В некоторых вариантах реализации концевая группа содержит один или более нуклеозидов концевой группы.
При использовании в настоящем документе, «конъюгат» или «конъюгирующая группа» означает атом или группу атомов, связанную с олигонуклеотидом или олигомерным соединением. Как правило, конъюгирующие группы модифицируют одно или белее свойств соединения, к которому они присоединены, включая, но не ограничиваясь ими, свойства фармакодинамики, фармакокинетики, связывания, поглощения, клеточного распределения, клеточного захвата, заряда и/или выведения.
При использовании в настоящем документе, «линкер конъюгата» или «линкер» к контексту конъюгирующие группы означает часть конъюгирующие группы, содержащую любой атом или группу атомов и ковалентно связывающую (1) олигонуклеотид с другой частью конъюгирующие группы или (2) две или более частей конъюгирующие группы.
Конъюгирующие группы показаны в настоящем документе как радикалы, обеспечивающие связь для образования ковалентного присоединения к олигомерному соединению, такому как антисмысловый олигонуклеотид. В некоторых вариантах реализации точка присоединения у олигомерного соединения представляет собой 3'-атом кислорода 3'-гидроксильной группы 3'-концевого нуклеозида олигомерного соединения. В некоторых вариантах реализации точка присоединения у олигомерного соединения представляет собой 5'-атом кислорода 5'-гидроксильной группы 5'-концевого нуклеозида олигомерного соединения. В некоторых вариантах реализации связь для образования присоединения к олигомерному соединению представляет собой расщепляемую связь. В некоторых таких вариантах реализации такая расщепляемая связь составляет весь или часть расщепляемого фрагмента.
В некоторых вариантах реализации конъюгирующие группы содержат расщепляемый фрагмент (например, расщепляемую связь или расщепляемый нуклеозид) и часть углеводного кластера, такую как часть кластера GalNAc. Такая часть углеводного кластера содержит: нацеливающий фрагмент и, необязательно, линкер конъюгата. В некоторых вариантах реализации часть углеводного кластера определяют по количеству и сущности лиганда. Например, в некоторых вариантах реализации часть углеводного кластера содержит три группы GalNAc и обозначена «GalNAc3». В некоторых вариантах реализации часть углеводного кластера содержит 4 группы GalNAc и обозначена «GalNAc4». Конкретные части углеводных кластеров (имеющие конкретную связку, группы ветвления и линкера конъюгата) описаны в настоящем документе и обозначены римской цифрой с последующим нижним индексом «а». Соответственно, «GalNac3-1a» относится к конкретной части углеводного кластера конъюгирующие группы, имеющей 3 группы GalNac и конкретно определенную связку, группы ветвления и линкера. Такой фрагмент углеводного кластера присоединен к олигомерному соединению через расщепляемый фрагмент, такой как расщепляемая связь или расщепляемый нуклеозид.
При использовании в настоящем документе, «расщепляемый фрагмент» означает связь или группу, которая может быть расщеплена при физиологических условиях. В некоторых вариантах реализации расщепляемый фрагмент расщепляется внутри клетки или во внутриклеточных отделах, таких как лизосома. В некоторых вариантах реализации расщепляемый фрагмент расщепляется эндогенными ферментами, такими как нуклеазы. В некоторых вариантах реализации расщепляемый фрагмент содержит группу атомов, имеющую один, два, три, четыре или более четырех расщепляемых связей.
При использовании в настоящем документе, «расщепляемая связь» означает любую химическую связь, которая может быть расщеплена. В некоторых вариантах реализации расщепляемая связь выбрана из: амида, полиамида, сложного эфира, эфира, одного или обоих сложных эфиров фосфодиэфира, фосфатного сложного эфира, карбамата, дисульфида или пептида.
При использовании в настоящем документе, «углеводный кластер» означает соединение, имеющее один или более углеводных остатков, присоединенных скелету или связывающей группе, (см., например, публикацию Maier et al., "Synthesis of Antisense Oligonucleotides Conjugated to a Multivalent Carbohydrate Cluster for Cellular Targeting," Bioconjugate Chemistry, 2003, (14): 18-29, которая в полном объеме включена в настоящий документ посредством ссылки, или Rensen et al., "Design and Synthesis of Novel N-Acetylgalactosamine-Terminated Glycolipids for Targeting of Lipoproteins to the Hepatic Asiaglycoprotein Receptor," J. Med. Chem. 2004, (47): 5798-5808, где приведены примеры углеводных конъюгированных кластеров).
При использовании в настоящем документе, «модифицированный углевод» означает любой углевод, имеющий одну или более модификаций, по сравнению с природными углеводами.
При использовании в настоящем документе, «производное углевода» означает любое соединение, которое может быть синтезировано с использованием углевода в качестве исходного материала или промежуточного соединения.
При использовании в настоящем документе, «углевод» означает природный углевод, модифицированный углевод или производное углевода.
При использовании в настоящем документе, «защитная группа» означает любое соединение или защитную группу, известную специалистам в данной области техники. Не ограничивающие примеры защитных групп приведены в публикации "Protective Groups in Organic Chemistry", Т.W. Greene, P.G.M. Wuts, ISBN 0-471-62301-6, John Wiley & Sons, Inc, Нью-Йорк, полное содержание которой включено в настоящий документ посредством ссылки.
При использовании в настоящем документе, «односпиральное» означает олигомерное соединение, которое не гибридизовано с его комплементом и которое не имеет достаточной самокомплементарностью для образования устойчивого собственного дуплекса.
При использовании в настоящем документе, «двухспиральное» означает пару олигомерных соединений, которые гибридизованы друг с другом, или одно самокомплементарное олигомерное соединение, которое образует шпилечную структуру. В некоторых вариантах реализации двухспиральное олигомерное соединение содержит первое и второе олигомерное соединение.
При использовании в настоящем документе, «антисмысловое соединение» означает соединение, содержащее или состоящее из олигонуклеотида, по меньшей мере часть которого комплементарна целевой нуклеиновой кислоте, с которой возможна его гибридизация, что приводит к получению по меньшей мере одной антисмысловой активности.
При использовании в настоящем документе, «антисмысловая активность» означает любое обнаруживаемое и/или измеримое изменение, обусловленное гибридизацией антисмыслового соединения с его целевой нуклеиновой кислотой. В некоторых вариантах реализации антисмысловая активность включает модулирование количества или активности транскрипта целевой нуклеиновой кислоты (например, мРНК). В некоторых вариантах реализации антисмысловая активность включает модулирование сплайсинга пре-мРНК.
При использовании в настоящем документе, «антисмысловое соединение на основе РНКазы Н» означает антисмысловое соединение, в котором по меньшей мере части антисмысловой активности антисмыслового соединения обусловлена гибридизацией антисмыслового соединения с целевой нуклеиновой кислотой и последующим расщеплением целевой нуклеиновой кислоты под действием РНКазы Н.
При использовании в настоящем документе, «антисмысловое соединение на основе RISC» означает антисмысловое соединение, в котором по меньшей мере часть антисмысловой активности антисмыслового соединения обусловлена РНК-индуцируемым комплексом сайленсинга (RISC).
При использовании в настоящем документе, «обнаружение» или «измерение» означает, что выполнено испытание или анализ для обнаружения или измерения. Такое обнаружение и/или измерение может приводить к результату с нулевым значением. Следовательно, даже если испытание для обнаружения или измерения приводит к обнаружению отсутствия активности (нулевой активности), то стадия обнаружения или измерения активности была выполнена.
При использовании в настоящем документе, «обнаруживаемая и/или измеримая активность» означает статистически значимую активность, которая не является нулевой.
При использовании в настоящем документе, «по существу не измененный» означает небольшое или отсутствие изменения конкретного параметра, в частности, по сравнению с другим параметром, который изменился гораздо больше. В некоторых вариантах реализации параметр является по существу не измененным, если его изменение составило менее 5%. В некоторых вариантах реализации параметр является по существу не измененным, если его изменение составило менее двух раз, тогда как изменение другого параметра составило по меньшей мере десять раз. Например, в некоторых вариантах реализации антисмысловая активность представляет собой изменение количества целевой нуклеиновой кислоты. В некоторых таких вариантах реализации количество нецелевой нуклеиновой кислоты является по существу не измененным, если оно изменяется гораздо меньше, чем изменяется количество целевой нуклеиновой кислоты, но это изменение не обязательно должно быть нулевым.
При использовании в настоящем документе, «экспрессия» означает процесс, посредством которого ген в конечном итоге преобразуется в белок. Экспрессия включает, но не ограничивается этим, транскрипцию, посттранскрипционную модификацию (например, сплайсинг, полиаденилирование, добавление 5'-кэпа) и трансляцию.
При использовании в настоящем документе, «целевая нуклеиновая кислота», означает молекулу нуклеиновой кислоты, с которой предполагается гибридизация антисмыслового соединения с получением заданной антисмысловой активности. Антисмысловые олигонуклеотиды обладают достаточной комплементарностью с их целевыми нуклеиновыми кислотами для обеспечения гибридизации при физиологических условиях.
При использовании в настоящем документе, «комплементарность азотистых оснований» или «комплементарность» в отношении азотистых оснований означает азотистое основание, которое способно к спариванию оснований с другим с азотистым основанием. Например, в ДНК аденин (А) комплементарен тимину (Т). Например, в РНК аденин (А) комплементарен урацилу (U). В некоторых вариантах реализации комплементарное азотистое основание означает азотистое основание антисмыслового соединения, которое способно к спариванию оснований с азотистым основанием его целевой нуклеиновой кислоты. Например, если азотистое основание в определенном положении антисмыслового соединения способно к водородному связыванию с азотистым основанием в определенном'положение целевой нуклеиновой кислоты, то это положение водородного связывания между олигонуклеотидом и целевой нуклеиновой кислотой считается комплементарным по этой паре азотистых оснований. Азотистые основания, содержащие определенные модификации, могут сохранять способность к спариванию с противоположным с азотистым основанием и, следовательно, все еще могут обладать комплементарностью азотистых оснований.
При использовании в настоящем документе, «не комплементарные» в отношении азотистых оснований означает пару азотистых оснований, которые не образуют водородные связи друг с другом.
При использовании в настоящем документе, «комплементарные» в отношении олигомерных соединений (например, связанных нуклеозидов, олигонуклеотидов или нуклеиновых кислот) означает способность таких олигомерных соединений или их областей к гибридизации с другим олигомерным соединением или его областью за счет комплементарности азотистых оснований. Комплементарные олигомерные соединения не обязательно должны обладать комплементарностью азотистых основании в каждом нуклеозиде. До не которой степени допустимы некоторые несоответствия. В некоторых вариантах реализации комплементарные олигомерные соединения или области комплементарны по 70% азотистых оснований (комплементарность 70%). В некоторых вариантах реализации комплементарные олигомерные соединения, или области комплементарны на 80%. В некоторых вариантах реализации комплементарные олигомерные соединения или области комплементарны на 90%. В некоторых вариантах реализации комплементарные олигомерные соединения или области комплементарны на 95%. В некоторых вариантах реализации комплементарные олигомерные соединения или области комплементарны на 100%.
При использовании в настоящем документе, «несоответствие» означает азотистое основание первого олигомерного соединения, которое не способно спариваться с азотистым основанием в соответствующем положении второго олигомерного соединения при выравнивании первого и второго олигомерного соединения. Любое или оба первое и второе олигомерные соединения могут быть олигонуклеотидами.
При использовании в настоящем документе, «гибридизация» означает спаривание комплементарных олигомерных соединений (например, антисмыслового соединения и его целевой нуклеиновой кислоты). Не ограничиваясь конкретным механизмом, наиболее распространенный механизм спаривания включает водородное связывание, которое может представлять собой уотсон-криковское, хугстиновское или обратное хугстиновское водородное связывание между комплементарными азотистыми основаниями.
При использовании в настоящем документе, «специфически гибридизуется» означает способность олигомерного соединения гибридизоваться с одним сайтом нуклеиновой кислоты с большей аффинностью, чем оно гибридизуется с другим сайтом нуклеиновой кислоты.
При использовании в настоящем документе, «полностью комплементарный» в отношении олигонуклеотида или его части означает, что каждое азотистое основание олигонуклеотида или его части способно к спариванию с азотистым основанием комплементарной нуклеиновой кислоты или ее непрерывной частью. Следовательно, полностью комплементарная область не содержит несоответствий или не гибридиованных азотистых оснований в обеих спиралях.
При использовании в настоящем документе, «процент комплементарности» означает процент азотистых оснований олигомерного соединения, которые комплементарны равной по длине части целевой нуклеиновой кислоты. Процент комплементарности рассчитвают делением количества азотистых оснований олигомерного соединения, которые комплементарны азотистым основаниям в соответствующих положениях целевой нуклеиновой кислоты, на общую длину олигомерного соединения.
При использовании в настоящем документе, «процент идентичности» означает количество азотистых оснований в первой нуклеиновой кислоте, которые относятся к тому же типу (независимо от химической модификации), что и азотистые основания в соответствующих положениях второй нуклеиновой кислоты, деленное на общее количество азотистых оснований в первой нуклеиновой кислоте.
При использовании в настоящем документе, «модулирование» означает изменение количества или качества молекулы, функции или активности, по сравнению с количеством или качеством молекулы, функции или активности до модулирования. Например, модулирование включает изменение, как увеличение (стимуляцию или индукцию), так и снижение (ингибирование или уменьшение) генной экспрессии. В качестве дополнительного примера, модулирование экспрессии может включать изменение выбора сайта сплайсинга при процессинге пре-мРНК, что приводит к изменению абсолютного или относительного количества определенного сплайс-варианта, по сравнению с его количеством в отсутствие модулирования.
При использовании в настоящем документе, «химический мотив» означает характерный участок химических модификаций в олигонуклеотиде или его области. Мотивы могут быть определены по модификациям в определенных нуклеозидах и/или в определенных связывающих группах олигонуклеотида.
При использовании в настоящем документе, «нуклеозидный мотив» означает характерный участок нуклеозидных модификаций в олигонуклеотиде или его области. Связи такого олигонуклеотида могут быть модифицированными или немодифицированными. Если не указано иное, мотивы, описывающие в настоящем документе только нуклеозиды, представляют собой нуклеозидные мотивы. Следовательно, в таких случаях связи не ограничены.
При использовании в настоящем документе, «сахарный мотив» означает характерный участок сахарных модификаций в олигонуклеотиде или его области.
При использовании в настоящем документе, «связывающий мотив» означает характерный участок связывающих модификаций в олигонуклеотиде или его области. Нуклеозиды такого олигонуклеотида могут быть модифицированными или немодифицированными. Если не указано иное, мотивы, описывающие в настоящем документе только связи, представляют собой связывающие мотивы. Следовательно, в таких случаях нуклеозиды не ограничены.
При использовании в настоящем документе, «мотив модификации азотистых оснований» означает характерный участок модификаций азотистых оснований вдоль олигонуклеотида. Если не указано иное, то мотив модификации азотистых оснований не зависит от последовательности азотистых оснований.
При использовании в настоящем документе, «мотив последовательности» означает характерный участок азотистых оснований, расположенных вдоль олигонуклеотида или его части. Если не указано иное, то мотив последовательности не зависит от химических модификаций и, следовательно, может иметь любую комбинацию химических модификация, включая отсутствие химических модификаций.
При использовании в настоящем документе, «тип модификации» ^ отношения нуклеозида или нуклеозида определенного «типа» означает химическую модификацию нуклеозида и включает модифицированные и немодифицированные нуклеозиды. Соответственно, если не указано иное, «нуклеозид, имеющий модификацию первого типа,) может быть немодифицированным нуклеозидом.
При использовании в настоящем документе, «по-разному модифицированные» означает химические модификации или химические заместители, которые отличны друг от друга, включая их отсутствие или модификации. Так, например, МОЕ нуклеозид и немодифицированный нуклеозид ДНК являются «по-разному модифицированными», даже несмотря на то, что нуклеозид ДНК является немодифицированным. Точно так же, ДНК и РНК являются «по-разному модифицированными», даже несмотря на то, что оба представляют собой природные немодифицированные нуклеозиды. Нуклеозиды. которые являются одинаковыми, но содержат различные азотистые основания, не являются си-разному модифицированными. Например, нуклеозид, содержащий 2'-ОМе модифицированный сахар и немодифицированное адениновое азотистое основание, и нуклеозид, содержащий 2'-ОМе модифицированный сахар и немодифицированное тиминовое азотистое основание, не являются по-разному модифицированными.
При использовании в настоящем документе, «модификации одного типа» относится к модификациям, которые являются одинаковыми друг относительно друга, включая отсутствие модификаций. Так, например, два немодифицированных нуклеозида ДНК имеют «модификацию одного типа», даже несмотря на то, что нуклеозид ДНК является немодифицированным. Такие нуклеозиды, имеющие модификацию одного типа, могут содержать различные азотистые основания.
При использовании в настоящем документе, «отдельные области» означает части олигонуклеотида, в которых химические модификации или мотив химических модификаций любой из соседних частей содержит по меньшей мере одно отличие для обеспечения возможности различать области друг от друга.
При использовании в настоящем документе, «фармацевтически приемлемей носитель или разбавитель» означает любое вещество, подходящее для использования при введении животному. В некоторых вариантах реализации фармацевтически приемлемый носитель или разбавитель представляет собой стерильный солевой раствор. В некоторых вариантах реализации такой стерильный солевой раствор представляет собой солевой раствор фармацевтической марки.
При использовании в настоящем документе, термин «метаболическое расстройство» означает заболевание или патологическое состояние, которое характеризуется, прежде всего, дисрегуляцией метаболизма - сложного набора химических реакций, связанных с расщеплением пищи с выработкой энергии.
При использовании в настоящем документе, термин «сердечно-сосудистое расстройство» означает заболевание или патологическое состояние, которое характеризуется, прежде всего, ухудшенной функцией сердца или кровеносных сосудов.
При использовании в настоящем документе, термин «моно- или полициклическая кольцевая система» включает все кольцевые системы, выбранные из одиночных или полициклических радикальных кольцевых систем, в которых указанные кольца конденсированы или связаны, и включает одиночные или смешанные кольцевые системы, индивидуально выбранные из алифатических, алициклических, арильных, гетероарильных, аралкильных, арилалкильных, гетероциклических, гетероарильных, гетероароматических и гетероарилалкильных. Такие моно- и полициклические структуры могут содержать кольца, каждое из которых имеет одинаковую степень насыщенности, или каждое независимо имеет переменные степени насыщенности, включая полностью насыщенные, частично насыщенные или полностью ненасыщенные. Каждое кольцо может содержать кольцевые атомы, выбранные из С, N, О и S с образованием гетероциклических колец, а также колец, содержащих только кольцевые атомы С, которые могут быть приведены в смешанном мотиве, как, например, в бензимидазоле, в котором одно кольцо имеет только кольцевые атомы углерода, а конденсированное кольцо имеет два атома азота. Моно- или полициклическая кольцевая система может быть дополнительно замещена группами заместителей, как, например, фталимид, который имеет две группы =O, присоединенные к одному из колец. Моно- или полициклические кольцевые системы могут быть присоединены к исходным молекулам при помощи различных способов, таких как непосредственно через кольцевой атом, путем конденсации через несколько кольцевых атомов, через группу заместителя или через бифункциональный связывающий фрагмент.
При использовании в настоящем документе, «пролекарство» означает неактивную или менее активную форму соединения, которая при введении субъекту метаболизируется с образованием активного или более активного соединения (например, лекарства).
При использовании в настоящем документе, «заместитель» и «группа заместителям означает атом или группу, которая вытесняет атом или группу указанного исходного соединения. Например, заместитель модифицированного нуклеозида представляет собой любой атом или группу, которая отлична от атома или группы, находящейся в природном нуклеозиде (например, модифицированный 2'-заместитель представляет собой любой атом или группу в 2'-положении нуклеозида, отличную от Н или ОН). Группы заместителей могут быть защищенными или не защищенными. В некоторых вариантах реализации соединения настоящего описания имеют заместители в одном или более чем в одном положении исходного соединения. Заместители также могут быть дополнительно замещены другими группами заместителей и могут быть присоединены напрямую или через связывающую группу, такую как алкильная или углеводородная группа, к исходному соединению.
Точно так же, при использовании в настоящем документе, «заместитель» в отношении химической функциональной группы означает атом или группу атомов, которая отлична от атома или группы атомов, обычно содержащихся в указанной функциональной группе. В некоторых вариантах реализации заместитель вытесняет атом водорода функциональной группы (например, в некоторых вариантах реализации заместитель замещенной метильной группы представляет собой атом или группу, отличную от водорода, которая вытесняет один или более атомов водорода незамещенной метильной группы). Если не указано иное, группы. которые могут быть использованы в качестве заместителей, включают, без ограничения, галоген, гидроксил, алкил, алкенил, алкинил, ацил (-C(O)Raa), карбоксил (-C(O)O-Raa), алифатические группы, алициклические группы, алкокси, замещенный окси (-O-Raa), арил, аралкил, гетероциклический радикал, гетероарил, гетероарилалкил, амино (-N(Rbb)(Rcc)), имино (=NRbb), амидо (-C(O)N(Rbb)(Rcc) или -N(Rbb)C(O)Raa), азидо (-N3), нитро (-NO2), циано (-CN), карбамидо (-OC(O)N(Rbb)(Rcc) или -N(Rbb)C(O)ORaa), уреидо (-N(Rbb)C(O)N(Rbb)(Rcc)), тиоуреидо (-N(Rbb)C(S)N(Rbb)(Rcc)), гуанидинил (-N(Rbb)C(=NRbb)N(Rbb)(Rcc)), амидинил (-C(=NRbb)N(Rbb)(Rcc) или -N(Rbb)C(=NRbb)(Raa)), тиол (-SRbb), сульфинил (-S(O)Rbb), сульфонил (-S(O)2Rbb) и сульфонамидил (-S(O)2N(Rbb)(Rcc) или -N(Rbb)S(O)2Rbb). Где каждый Raa, Rbb и Rcc независимо представляет собой Н, необязательно связанную химическую функциональную группу или дополнительную группу заместителя, при этом предпочтительный перечень включает, без ограничения, алкил, алкенил, алкинил, алифатические, алококси, ацил, арил, аралкил, гетероарил, алициклические, гетероциклические и гетероарилалкил. Выбранные заместители с соединениями, описанными в настоящем документе, находятся в рекурсивной степени.
При использовании в настоящем документе, «алкил», используемый в настоящем документе, означает насыщенный прямой или разветвленный углеводородный радикал. содержащий до двадцати четырех атомов углерода. Примеры алкильных групп включают, без ограничения, метил, этил, пропил, бутил, изопропил, н-гексил, октил, децил, додецил и т.п. Алкильные группы обычно содержат от 1 до около 24 атомов углерода, более часто от 1 до около 12 атомов углерода (C1-C12 алкил), при этом более предпочтительно от 1 до около 6 атомов углерода.
При использовании в настоящем документе, «алкенил» означает прямой или разветвленный углеводородный радикал, содержащий до двадцати четырех атомов углерода и имеющий по меньшей мере одну двойную углерод-углеродную связь. Примеры алкенильных групп включают, без ограничения, этенил, пропенил, бутенил, 1-метил-2-бутен-1-ил, диены, такие как 1,3-бутадиен и т.п. Алкенильные группы обычно содержат от 2 до около 24 атомов углерода, более часто от 2 до около 12 атомов углерода, при этом более предпочтительно от 2 до около 6 атомов углерода. Алкенильные группы, используемые в настоящем документе, могут необязательно содержать одну или более дополнительных групп заместителей.
При использовании в настоящем документе, «алкинил» означает прямой или разветвленный углеводородный радикал, содержащий до двадцати четырех атомов углерода и имеющий по меньшей мере одну тройную углерод-углеродную связь. Примеры алкинильных групп включают, без ограничения, этинил, 1-пропинил, 1-бутинил и т.п. Алкинильные группы обычно содержат от 2 до около 24 атомов углерода, более часто от 2 до около 12 атомов углерода, при этом более предпочтительно от 2 до около 6 атомов углерода. Алкинильные группы, используемые в настоящем документе, могут необязательно содержать одну или более дополнительных групп заместителей.
При использовании в настоящем документе, «ацил» означает радикал, образованный за счет удаления гидроксильной группы от органической кислоты, и имеет общую формулу -С(O)-Х, где Х обычно является алифатическим, алициклическим или ароматическим. Примеры включают алифатические карбонилы, ароматические карбонилы, алифатические сульфонилы, ароматические сульфинилы, алифатические сульфинилы, ароматические фосфаты, алифатические фосфаты и т.п. Ацильные группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей.
При использовании в настоящем документе, «алициклическая» означает циклическую кольцевую систему, в которой кольцо является алифатическим. Кольцевая система может содержать одно или более колец, при этом по меньшей мере одно кольцо является алифатическим. Предпочтительные алициклические системы включают кольца, имеющие от около 5 до около 9 атомов углерода в кольце. Алициклические группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей.
При использовании в настоящем документе, «алифатический» означает прямой или разветвленный углеводородный радикал, содержащий до двадцати четырех атомов углерода, в котором насыщенность между любыми двумя атомами углерода представляет собой одинарную, двойную или тройную связь. Алифатическая группа предпочтительно содержит от 1 до около 24 атомов углерода, более часто от 1 до около 12 атомов углерода, при этом более предпочтительно от 1 до около 6 атомов углерода. Прямая или разветвленная цепь алифатической группы может быть прервана одним или более гетероатомами, которые включают азот, кислород, серу и фосфор. Такие алифатические группы, прерванные гетероатомами, включают, без ограничения, полиалкокси, такие как полиалкиленгликоли, полиамины и полиимины. Алифатические группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей.
При использовании в настоящем документе, «алкокси» означает радикал, образованный между алкильной группой и атомом кислорода, при этом атом кислорода используется для присоединения алкокси-группы к исходной молекуле. Примеры алкокси-групп включают, без ограничения, метокси, этокси, пропокси, изопропокси, н-бутокси, втор-бутокси, трет-бутокси, н-пентокси, неопентокси, н-гексокси и т.п. Алкокси-группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей.
При использовании в настоящем документе, «аминоалкил» означает аминозамещенный С1-С12 алкильный радикал. Алкильная часть указанного радикала образует ковалентную связь с исходной молекулой. Аминогруппа может быть расположена в любом положении, и аминоалкильная группа может быть замещена дополнительной группой заместителя в алкильной и/или амино-части.
При использовании в настоящем документе, «аралкил» и «арилалкил» означает ароматическую группу, которая ковалентно связана с С1-С12 алкильным радикалом. Часть алкильного радикала образовавшейся аралкильной (или арилалкильной) группы образует ковалентную связь с исходной молекулой. Примеры включают, без ограничения, бекзил, фенетил и т.п. Аралкильные группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей, присоединенные к алкильной, арильной или к обеим группам, которые образуют указанную радикальную группу.
При использовании в настоящем документе, «арил» и «ароматический» означает радикалы моно- или полициклической карбоциклической кольцевой системы, имеющие одно или более ароматических колец. Примеры арильных групп включают, без ограничения, фенил, нафтил, тетрагидронафтил, инданил, инденил и т.п. Предпочтительные арильные кольцевые системы имеют от около 5 до около 20 атомов углерода в одном или более кольцах. Арильные группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей.
При использовании в настоящем документе, «галогено» и «галоген» означает атом, выбранный из фтора, хлора, брома и йода.
При использовании в настоящем документе, «гетероарил» и «гетероароматический» означает радикал, содержащий моно- или полициклическое ароматическое кольцо, кольцевую систему или конденсированную кольцевую систему, в котором по меньшей мере одно из колец является ароматическим и содержит один или более гетероатомов. Гетероарил включает также конденсированные кольцевые системы, включая системы, в которых одно или более из конденсированных колец не содержат гетероатомов. Гетероарильные группы, как правило, содержат один кольцевой атом, выбранный из серы, азота или кислорода. Примеры гетероарильных групп включают, без ограничения, пиридинил, пиразинил, пиримидинил, пирролил, пиразолил, имидазолил, тиазолил, оксазолил, изооксазолил, тиадиазолил, оксадиазолил, тиофенил, фуранил, хинолинил, изохинолинил, бензимидазолит, бензоксазолил, хиноксалинил и т.п. Гетероарильные радикалы могут быть присоединены к исходной молекуле напрямую или через связывающий фрагмент, такой как анифатическая группа или гетероатом. Гетероарильные группы, используемые в настоящем документе, могут необязательно содержать дополнительные группы заместителей.
При использовзании в настоящем документе, «конъюгированное соединение» означает любые атомы, группы атомов или группу связанных атомов, подходящую для применения в качестве конъюгирующие группы. В некоторых вариантах реализации конъюгированные соединения могут обладать или влиять на одно или более свойств, включая, но не ограничиваясь этим, свойства фармакодинамики, фармакокинетики, связывания, адсорбции, клеточного распределения, клеточного захвата, заряда и/или выведения.
При использовании в настоящем документе, если не указано или немодифицировано иным образом, «двухспиральные» относится к двум отдельным олигомерным соецинениям, которые гибридизованы друг с другом. Такие двухспиральные соединения могут иметь один или более не гибридизованных нуклеозидов у одного или обоих концов одной или обеих спиралей (выступы) и/или один или более внутренних не гибридизованных нуклеозидов (несоответствий), при условии, что существует достаточная комплементарность для сохранения гибридизации при физиологически релевантных условиях.
При использовании в настоящем документе «5'-сайт-мишень» относится к нуклеотиду целевой нуклеиновой кислоты, который комплементарен к 5'-основному нуклеотиду конкретного антисмыслового соединения.
При использовании в настоящем документе термин «около» обозначает в пределах ±10% от значения. Например, если указано, что «маркер может быть увеличен на около 50%», то подразумевается, что маркер может быть увеличен на значение в диапазоне 45%-55%.
При использовании в настоящем документе выражение «введенные параллельно» относится к совместному введению двух средств любым способом, при котором фармакологическое действие обоих средств проявляется у пациента одновременно. При параллельном введении не требуется, чтобы оба агенты были введены в одной фармацевтической композиции, в одной лекарственной форме или одним способом введения. Действие обоих средств не обязательно должно проявляться одновременно. Их действие должно лишь перекрываться в течение определенного периода времени, и оно не обязательно должно иметь одинаковую протяженность по времени.
При использовании в настоящем документе термин «введение» обозначает предоставление фармацевтического агента индивидууму и включает, но не ограничивается этим, введение медицинским специалистом или самостоятельное введение. Введение фармацевтического агента индивидууму может быть непрерывным, хроническим, кратковременным или периодическим. Введение может быть парентеральным или не парентеральным.
При использовании в настоящем документе «агент» обозначает активное вещество, которое может обеспечивать благоприятный терапевтический эффект при введении животному. «Первый агент» обозначает терапевтическое соединение согласно настоящему изобретению. Например, первый агент может быть антисмысловым олигонуклеотидом, нацеленным на apoCIII. «Второй агент» обозначает второе терапевтическое соединение согласно настоящему изобретению (например, второй антисмысловый олигонуклеотид, нацеленный на apoCIII) и/или не-apoCIII терапевтическое соединение.
При использовании в настоящем документе «облегчение» или «облегчать», или «облегчающий» относится к снижению по меньшей мере одного показателя, признака или симптома ассоциированного заболевания, расстройства или состояния. Тяжесть показателей может быть определена субъективными или объективными оценками, известными специалистам в данной области техники.
Используемый в настоящем документе термин «животное» относится к человеку или животному, не являющемуся человеком, включая, но не ограничиваясь этим, мышей, крыс, кроликов, собак, котов, свиней и приматов, не являющихся человеком, включая, но не ограничиваясь этим, обезьян и шимпанзе.
При использовании в настоящем документе «АроCIII», «аполипопротеин C-III» или «АроС3» означает любую последовательность нуклеиновых кислот или белка, кодирующую АроCIII. Например, в некоторых вариантах реализации изобретения АроCIII включает последовательность ДНК, кодирующую АроCIII, последовательность РНК, транскрибированную из ДНК, кодирующей АроCIII (включая геномную ДНК, содержащую интроны и экзоны), последовательность мРНК, кодирующую АроCIII, или пептидную последовательность, кодирующую АроCIII.
При использовании в настоящем документе «нуклеиновая кислота АроCIII» означает любую нуклеиновую кислоту, кодирующую АроCIII. Например, в некоторых вариантах реализации нуклеиновая кислота АроCIII включает последовательность ДНК, кодирующую АроCIII, последовательность РНК, транскрибированную из ДНК, кодирующей АроCIII (включая геномную ДНК, содержащую интроны и экзоны), и последовательность мРНК, кодирующую АроCIII.
При использовании в настоящем документе «специфический ингибитор АроCIII» относится к любому агенту, способному специфически ингибировать экспрессию мРНК АроCIII и/или экспрессию или активность белка АроCIII на молекулярном уровне Например. специфические ингибиторы АроCIII включают нуклеиновые кислоты (в том числе антисмысловые соединения), пептиды, антитела, небольшие молекулы и другие агенты, способные ингибировать экспрессию мРНК АроCIII и/или белка АроCIII. В некоторых вариантах реализации изобретения нуклеиновая кислота представляет собой антисмысловое соединение. В некоторых вариантах реализации изобретения антисмысловое соединение представляет собой олигонуклеотид, нацеленный на АроCIII. В некоторых вариантах реализации изобретения олигонуклеотид, нацеленный на АроCIII, представляет собой модифицированный олигонуклеотид, нацеленный на АроCIII. В некоторых вариантах реализации изобретения олигонуклеотид, нацеленный на АроCIII, представляет собой модифицированный олигонуклеотид, нацеленный на АроCIII, с конъюгирующей группой. В некоторых вариантах реализации изобретения олигонуклеотид, нацеленный на АроCIII, имеет последовательность, приведенную в SEQ ID NO: 19-96, 209-221 пли в другой последовательности (например, в последовательности, описанной в публикации РСТ WO 2004/093783 или в публикации РСТ WO 2012/149495, которые включены в настоящий документ посредством ссылки). В некоторых вариантах реализации изобретения за счет специфического модулирования уровня мРНК АроCIII и/или экспрессии белка АроCIII специфические ингибиторы АроCIII могут влиять на компоненты липогенного или глюкогенного пути. Точно так же в некоторых вариантах реализации изобретения специфические ингибиторы АроCIII могут влиять на другие молекулярные процессы у животного.
При использовании в настоящем документе «мРНК АроCIII» означает мРНК, кодирующую белок АроCIII.
При использовании в настоящем документе «белок АроCIII» означает любую белковую последовательность, кодирующую АроCIII.
При использовании в настоящем документе «атеросклероз» означает затвердевание артерий, поражающее крупные и средние артерии, и характеризуется наличием жировых отложений. Жировые отложения называют «атеромами» или «бляшками», которые состоят, в основном, из холестерина и других жиров, кальция и рубцовой ткани, и они повреждают выстилку артерий.
При использовании в настоящем документе «коронарная болезнь сердца (КБС)» означает сужение мелких кровяных сосудов, которые поставляют кровь и кислород в сердце, что зачастую приводит к атеросклерозу.
При использовании в настоящем документе «сахарный диабет» или «диабет» представляет собой синдром, характеризующийся нарушенным метаболизмом и патологически высоким содержанием сахара в крови (гипергликемией) из-за недостаточного содержания инсулина или сниженной чувствительности к инсулину. Характерные симптомы представляют собой избыточное выделение мочи (полиурия) из-за высокого содержания глюкозы в крови, избыточную жажду и повышенное потребление жидкости (полидипсия) в попытке компенсировать усиленное мочевыделение, расплывчатое зрение из-за того, что высокое содержание глюкозы в крови влияет на оптические свойства глаз, необъяснимую потерю веса и летаргию.
При использовании в настоящем документе «диабетическая дислипидемия» или «диабет 2-го типа с дислипидемией» означает патологическое состояние, характеризующееся диабетом 2-го типа, сниженным содержанием холестерина липопротеинов высокой плотности (HDL-C), повышенным уровнем триглицеридов (TG) и повышенным уровнем мелких, плотных частиц липопротеинов низкой плотности (LDL).
При использовании в настоящем документе «разбавитель» обозначает ингредиент в композиции, который не обладает фармакологической активностью, но является фармацевтически необходимым или желательным. Например, разбавитель в композиции для инъекций может быть жидкостью, например, солевым раствором.
При использовании в настоящем документе «дислипидемия» относится к нарушению метаболизма липидов и/или липопротеинов, включая избыточную выработку или дефицит липидов и/или липопротеинов. Дислипидемия может проявляться в повышении содержания липидов, таких как хиломикрон, холестерин и триглицериды, а также липопротеинов, таких как холестерин липопротеинов низкой плотности (LDL).
При использовании в настоящем документе «лекарственная форма» означает форму, в которой приведен фармацевтический агент, например, пилюлю, таблетку или другую лекарственную форму, известную в данной области техники. В некоторых вариантах реализации изобретения лекарственная форма представляет собой пробирку, содержащую лиофилизированный антисмысловый олигонуклеотид. В некоторых вариантах реализации изобретения лекарственная форма представляет собой пробирку, содержащую восстановленный антисмысловый олигонуклеотид.
При использовании в настоящем документе «доза» обозначает определенное количество фармацевтического агента, которое обеспечивается при разовом введении или в течение определенного периода времени. В некоторых вариантах реализации изобретения доза может быть введена одним, двумя или более болюсами, таблетками или инъекциями. Например, в некоторых вариантах реализации изобретения, в которых желательно подкожное введение, для требуемой дозы необходим объем, который трудно ввести за одну инъекцию, поэтому можно использовать две или более инъекций для достижения требуемой дозы. В некоторых вариантах реализации изобретения фармацевтический агент вводят инфузией в течение продолжительного периода времени или непрерывно. Дозы могут быть определены как количество фармацевтического средства в час, день, неделю или месяц. Дозы также могут быть указаны в мг/кг или г/кг.
При использовании в настоящем документе «эффективное количество» или терапевтически эффективное количество» означает количество активного фармацевтического агента, достаточное для достижения заданного физиологического результата у индивидуума, нуждающегося в таком агенте. Эффективное количество может варьироваться у различных индивидуумов в зависимости от состояния здоровья и физического состояния индивидуума, подлежащего лечению, таксономической группы индивидуумов, подлежащих лечению, состава композиции, оценки медико-санитарной обстановки и других релевантных факторов.
При использовании в настоящем документе «болезнь Фредриксона типа I» известна также как «дефицит липопротеин-липазы», «недостаточность ЛПЛ (LPLD)» «синдром наследственной хиломикронемии» или «FCS» и существует в нескольких формах: тип 1а (известный также как синдром Бюргера-Грютца) представляет собой дефицит липопротеин-липазы, обычно из-за недостатка LPL или измененного АроС-II; тип Ib (известный также как семейный дефицит апопротеина CII) представляет собой патологическое состояние, обусловленное недостатком активатора липопротеин-липазы, апопротеина C-II; и тип Ic представляет собой хиломикронемию в результате циркулирующего ингибитора липопротеин-липазы. Тип I представляет собой редкое расстройство, которое обычно встречается в детстве. Оно характеризуется сильным увеличением хиломикронов и чрезвычайно повышенными уровнями TG (которые всегда достигают значений гораздо выше 1000 мг/дл и нередко поднимаются до 10000 мг/дл или более) с эпизодами боли в животе, рецидивирующим острым панкреатитом, сыпной кожной ксантомой и гепатоспленомегалией. У пациентов редко развивается атеросклероз, возможно, из-за того, что частицы липопротеина в их плазме слишком крупные для вхождения в артериальную интиму (Nordestgaard et al., J Lipid Res, 1988, 29: 1491-1500; Nordestgaard et al., Arteriosclerosis, 1988, 8: 421-428). Тип I обычно обусловлен мутациями либо гена LPL, либо кофактора этого гена АроС-II, что приводит к неспособности пораженных болезнью индивидуумов вырабатывать достаточно функциональноактивный LPL. Пациенты являются либо гомозиготными для таких мутаций, либо компаунд-гетерозиготными. Болезнь Фредриксона типа I также может быть обусловлена мутациями в GPIHBP1, АРОА5, LMF1 или других генах, что приводит к дисфункциональности LPL. Brunzell, в публикации: Pagon RA, Adam MP, Bird TD, Dolan CR, Fong CT, Stephens K, editors. GeneReviews™ [Интернет]. Сиэтл (штат Вашингтон): Университет Вашингтона, Сиэтл; 1993-2013. 1999 12 окт. [обновлено 15 дек. 2011]. Кроме того, в некоторых случаях болезнь Фредриксона типа I может быть вызвана наличием ингибитора LPL (например, анти-LPL антител) у индивидуума, что приводит к дисфункциональности LPL. Распространенность болезни Фредриксона типа I составляет около 1 на 1000000 человек общего населения и гораздо больше в Южной Африке и Восточном Квебеке из-за эффекта основателя. Пациенты минимально или совсем не реагируют на TG-понижающие лекарства (Tremblay et al., J Clin Lipidol, 2011, 5: 37-44; Brisson et al., Pharmacogenet Genom, 2010, 20:742-747) и поэтому применяют ограничение потребления жиров до 20 грамм/сутки или менее для контролирования симптомов этого редкого расстройства.
При использовании в настоящем документе «полная комплементарность» или «100% комплементарность» означает, что каждое азотистое основание последовательности азотистых оснований первой нуклеиновой кислоты имеет комплементарное азотистое основание во второй последовательности азотистых оснований второй нуклеиновой кислоты. В некоторых вариантах реализации изобретения первая нуклеиновая кислота представляет собой антисмысловое соединение, а вторая нуклеиновая кислота представляет собой целевую нуклеиновую кислоту.
При использовании в настоящем документе «глюкоза» представляет собой моносахарид, используемый клетками в качестве источника энергии и воспалительного посредника. «Глюкоза в плазме» относится к содержанию глюкозы в плазме.
При использовании в настоящем документе «холестерин липопротеина высокой плотности» или «HDL-C» означает холестерин, связанный с частицами липопротеина высокой плотности. Концентрацию HDL-C в сыворотке (или в плазме) обычно определяют в мг/дл или в нмоль/л. «HDL-C в сыворотке» и «HDL-C в плазме» означает содержание HDL-C в сыворотке и плазме, соответственно.
При использовании в настоящем документе «ингибитор редуктазы HMG-CoA» означает агент, который действует за счет ингибирования фермента редуктазы HMG-CoA, такой как аторвастатин, розувастатин, флувастатин, ловастатин, правастатин и симвастатин.
При использовании в настоящем документе «гиперхолестеринемия» означает патологическое состояние, характеризующееся повышенным холестерином или циркулирующим холестерином (в плазме), LDL-холестерином и VLDL-холестерином, согласно указаниям Заключения экспертной группы Национальной холестериновой образовательной программы (NCEP) по определению, оценке и лечению высокого уровня холестерина у взрослых людей (см. Arch. Int. Med. (1988) 148, 36-39).
При использовании в настоящем документе «гиперлипидемия» или «гиперлипемия» представляет собой патологическое состояние, характеризующееся повышенным содержанием липидов в сыворотке или циркулирующих липидов (в плазме). Это патологическое состояние проявляется в патологически высоких концентрациях жиров. Липидная фракция в циркулирующей крови представляет собой холестерин, липопротеины низкой плотности, липопротеины очень низкой плотности, хиломикроны и триглицериды. Классификации гиперлипидемий по Фредриксону основана на каскаде TG и содержании богатых на холестерин липопротеиновых частиц, измеренном электрофорезом или ультрацентрифугированием и обычно используемом для характеристики основных причин гиперлипидемий, таких как гипертриглицеридемия (Fredrickson and Lee, Circulation, 1965, 31: 321-327; Fredrickson et al., New Eng J Med, 1967, 276 (1): 34-42).
При использовании в настоящем документе «гипертриглицеридемия» означает патологическое состояние, характеризующееся повышенными уровнями триглицеридов. Гипертриглицеридемия представляет собой следствие повышенной выработки и/или сниженного или отсроченного катаболизма богатых на триглицерид (TG) липопротеинов: VLDL и, в меньшей степени, хиломикронов (СМ). Ее этиология включает первичные (т.е. генетические причины) и вторичные (другие первопричины, такие как диабет, метаболический синдром/инсулинорезистентность, ожирение, физическая инертность, табакокурение, избыточное употребление алкоголя и пищи с очень высоким содержанием углеводородов) факторы или, более часто, комбинацию обоих факторов (Yuan et al. CMAJ, 2007, 176: 1113-1120). Гипертриглицеридемия представляет собой общий клинический признак, связанный с повышенным риском кардиометаболических заболеваний (Hegele et al. 2009, Hum Mol Genet, 18: 4189-4194; Hegele and Pollex 2009, Mol Cell Biochem, 326: 35-43), a также возникновения острого панкреатита в самых тяжелых формах (Toskes 1990, Gastroenterol Clin North Am, 19: 783-791; Gaudetet al. 2010, Atherosclerosis Supplements, 11: 55-60; Catapano et al. 2011, Atherosclerosis, 217S: S1-S44; Tremblay et al. 2011, J Clin Lipidol, 5: 37-44). Примеры кардиометаболических заболеваний включают, но не ограничиваются ими, диабет, метаболический синдром/инсулинорезистентность и генетические расстройства, такие как синдром наследственной хиломикронемии (FCS), семейная комбинированная гиперлипидемия и семейная гипертриглицеридемия. Содержание TG выше предельного значения (150-199 мг/дл) обычно встречается у всего населения, и оно является распространенным компонентом состояний метаболического синдрома/инсулинорезистентности. Это же относится к высоким уровням TG (200-499 мг/дл), за исключением того, что при увеличении содержания TG в плазме возрастает этиологическое значение первопричинных генетических факторов. Очень высокие уровни TG (≥500 мг/дл) наиболее часто связаны также с повышенным содержанием СМ, и они сопровождаются повышенным риском острого панкреатита. Риск панкреатита считается клинически значимым, если уровни TG превышают 880 мг/дл (>10 ммоль), а в руководстве Европейского общества по изучению атеросклероза/Европейского общества кардиологии (EAS/ESC) от 2011 года указано, что обязательными являются действия по предотвращению острого панкреатита (Catapano et al. 2011, Atherosclerosis, 217S: S1-S44). В соответствии с руководством EAS/ESC от 2011 года, гипертриглицеридемия является причиной приблизительно 10% случаев панкреатита, а развитие панкреатита может происходи при уровнях TG 440-880 мг/дл. На основании данных, полученных в клинических испытаниях, демонстрирующих, что повышенные уровни TG представляют собой независимый фактор риска для атеросклеротических CVD, в руководствах экспертной группы III Национальной холестериновой образовательной программы по лечению взрослых людей (NCEP 2002, Circulation, 106: 3143-421) и Американской ассоциации по диабету (ADA 2008, Diabetes Care, 31: S12-S54.) рекомендовано, чтобы целевой уровень TG составлял менее 150 мг/дл для снижения сердечно-сосудистого риска.
При использовании в настоящем документе «идентификация» или «выбор животного с метаболическим или сердечно-сосудистым заболеванием» означает определение или выбор субъекта, предрасположенного к или диагностированного с метаболическим заболеванием, сердечно-сосудистым заболеванием или метаболическим синдромом; или определение или выбор субъекта, имеющего любой симптом метаболического заболевания, сердечнососудистого заболевания или метаболического синдрома, включая, но не ограничиваясь этим, гиперхолестеринемию, гипергликемию, гиперлипидемию, гипертриглицеридемию, гипертонию, повышенную инсулинорезистентность, пониженную чувствительность к инсулину, увеличенную массу тела и/или увеличенное содержание жира в организме, или любую их комбинацию. Такая идентификация может быть выполнена любым способом, включая, но не ограничивась ими, стандартные клинические испытания или оценки, такие как измерение холестерина в сыворотке или циркулирующего холестерина (в плазме), измерение глюкозы в сыворотке или циркулирующей глюкозы (в плазме), измерение триглицеридов в сыворотке или циркулирующих триглицеридов (в плазме), измерение кровяного давления, измерение содержания жира в организме, измерение массы тела и т.п.
При использовании в настоящем документе, «улучшенный сердечно-сосудистый результат» означает снижение возникновения неблагоприятных сердечно-сосудистых явлений или их риска. Примеры неблагоприятных сердечно-сосудистых явлений включают, без ограничения, смерть, повторный инфаркт, инсульт, кардиогенный шок, отек легких, остановку сердца и атриальную аритмию.
При использовании в настоящем документе «непосредственно рядом» означает, что между элементами, расположенными непосредственно рядом, не существует промежуточных элементов, например, между областями, сегментами, нуклеотидами и/или нуклеозидами.
При использовании в настоящем документе «увеличение HDL» или «повышение HDL» означает повышение уровня HDL у животного после введения по меньшей мере одного соединения согласно настоящему изобретению, по сравнению с уровнем HDL у животного, которому не вводили ни одного соединения.
При использовании в настоящем документе «индивидуум» или «субъект» или «животное» означает человека или животное, не являющееся человеком, выбранное для лечения или терапии.
При использовании в настоящем документе «индивидуум, нуждающийся в этом» относится к человеку или животному, не являющемуся человеком, выбранному для лечения или терапии, которое нуждается в таком лечении или терапии.
При использовании в настоящем документе «вызывает», «ингибирует», «потенцирует», «повышает», «увеличивает», «снижает», «уменьшает» или подобные термины означают количественное различие между двумя состояниями. Например, «количество, эффективное для ингибирования активности или экспрессия apoCIII», обозначает, что уровень активности или экспрессии apoCIII в обработанном образце отличается от уровня активности или экспрессии apoCIII в необработанном образце. Такие термины применяют, например, к уровням экспрессии и уровням активности.
При использовании в настоящем документе «воспалительное патологическое состояние» относится к заболеванию, болезненному состоянию, синдрому или другому состоянию, приводящему к воспалению. Например, ревматоидный артрит и фиброз печени представляют собой воспалительные состояния. Другие примеры воспалительных состояний включают сепсис, ишемию миокарда/реперфузионное повреждение, респираторный дистресс-синдром взрослых, нефрит, отторжение трансплантата, воспалительную болезнь кишечника, рассеянный склероза, артериосклероз, атеросклероз и васкулит.
При использовании в настоящем документе «ингибирование экспрессии или активности» относится к снижению или блокированию экспрессии или активности РНК или белка и не обязательно обозначает полное исключение экспрессии или активности.
При использовании в настоящем документе «инсулинорезистентность» определяется как патологическое состояние, при котором нормальные количества инсулина недостаточны для получения нормального ответа на инсулин от жировых, мышечных и печеночных клеток. Инсулинорезистентность в жировых клетках приводит к гидролизу запасенных триглицеридов, что повышает содержание свободных жирных кислот в плазме крови. Инсулинорезистентность в мышцах снижает поглощение глюкозы, а инсулинорезистентность в печени снижает запас глюкозы, и оба эффекта приводят к повышению глюкозы в крови. Высокие уровни инсулина и глюкозы в плазме из-за инсулинорезистентности зачастую приводят к метаболическому синдрому и диабету 2-го типа.
При использовании в настоящем документе «чувствительность к инсулину» представляет собой меру эффективности переработки глюкозы у индивидуума. Индивидуум с высокой чувствительностью к инсулину эффективно перерабатывает глюкозу, тогда как индивидуум с низкой чувствительностью к инсулину перерабатывает глюкозу неэффективно.
При использовании в настоящем документе «понижение содержания липидов» означает уменьшение содержания одного или более липидов (например, LDL, VLDL) у субъекта. «Повышение содержания липидов» означает увеличение содержания липидов (например, HDL) у субъекта. Понижение или повышение уровня липидов может возникать при введении одной или более доз с течением времени.
При использовании в настоящем документе «терапия для понижения содержания липидов» или «агент для понижения содержания липидов» означает терапевтический режим, предоставленный субъекту для снижения содержания одного или более липидов у субъекта. В некоторых вариантах реализации изобретения терапия для понижения содержания липидов предоставлена для снижения одного или более из аро(а), apoCIII, СЕТР, ароВ. общего холестерина, LDL-C, VLDL-C, IDL-C, не-HDL-C, триглицеридов, частиц LDL низкой плотности и Lp(a) у субъекта. Примеры терапии для понижения содержания липидов включают, но не ограничиваются ими, ингибиторы ароВ, статины, фибраты и ингибиторы МТР.
При использовании в настоящем документе «липопротеин», такой как VLDL, LDL и HDL, относится к группе белков, находящихся в сыворотке, плазме и лимфе, которые важны для транспорта липидов. Химический состав каждого липопротеина различен, например, HDL имеет более высокое содержание белка по сравнению с липидом, a VLDL имеет более низкое содержание белка по сравнению с липидом.
При использовании в настоящем документе «липопротеин-липаза» или «LPL» относится к ферменту, который гидролизует TG, находящиеся в липопротеинах, такие как СМ или VLDL, в свободные жирные кислоты и моноацилглицерины. Для LPL в качестве кофактора необходим ароC-II для выполнения функции гидролиза TG. LPL вырабатывается, в основном, в скелетных мышцах, жировой ткани и сердечной мышце. Гидролиз и удаление TG из СМ и VLDL обычно защищает от избыточного повышения массы СМ и TG после приема пищи.
При использовании в настоящем документе «дефицит липопротеин-липазм», «недостаток липопротеин-липазы», «дефицит LPL» или «недостаточность ЛПЛ (LPLD)» известны также как «дислипидемия Фредриксона типа I», «хиломикронемия», «синдром наследственной хиломикронемии» или «FCS». Хотя субъекты с недостаточностью ЛПЛ (LPLD) обычно страдают от недостатка LPL или активности LPL, необходимой для эффективного разложения жирных кислот, таких как TG, эти субъекты все же могут иметь минимальную активность LPL или экспрессировать минимальный уровень LPL. В некоторых случаях субъект с недостаточностью ЛПЛ (LPLD) может экспрессировать LPL или иметь активность LPL, составляющую около или не более чем 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% активности. В других случаях субъект с недостаточностью ЛПЛ (LPLD) не имеет измеримой LPL или активности LPL. В одном из вариантов реализации изобретения недостаточностью ЛПЛ (LPLD) включает субъектов с «гиперлипопротеинемией типа Ia» (известной также как «болезнь Фредрикгона типа Ia») и относится к неспособности субъектов вырабатывать достаточное количество функциональных ферментов липопротеин-липазы, необходимое для эффективною разложения жирных кислот, таких как TG. Неспособность к разложению TG приводит к гипертриглицеридемии у субъекта и зачастую к тому, что в течение более 12 часов после приема пищи в качестве липемии все еще наблюдаются избыточные уровни триглицеридов и хиломикронемия. Тип Ia зачастую обусловлен одной или более мутаций в гене LPL. Как описано в настоящем документе, недостаточность ЛПЛ (LPLD) включает также субъектов, которые имеют дисфункциональную липопротеин-липазу, такую как у субъектов с «гиперлипопротеинемией типа Ib» (также известной как «болезнь Фредриксона типа Ib») и с «гиперлипопротеинемией типа Ic» (изветной также как «болезно Фредриксона типа Ic»). Тип Ib обусловлен недостатком активатора липопротеин-липазы апопротеина C-II. Тип Ic обусловлен циркулирующим ингибитором липопротеин-липазы. Как и в случае типа 1а, субъекты типа 1b/1с страдают от неспособности разлагать TG, что приводит к гипертриглицеридемии, а избыточные уровни триглицеридов и хиломикронемия сохраняются и наблюдаются как липемия, которая зачастую длится более 12 часов после приема пищи. В некоторых вариантах реализации изобретения недостаточность ЛПЛ (LPLD) связана по меньшей мере с одной мутацией в гене LPL, такой как P207L, G188L или D9N, или другие мутации, которые поражают LPL (Brunzell, In: Pagon RA, Adam MP, Bird TO, Dolan CR, Fong CT, Stephens K, ред. GeneReviews™ [Интернет]. Сиэтл (штат Вашингтон): Университет Вашингтона, Сиэтл; 1993-2013. 1999 12 окт.[обновлено 15 дек. 2011]).
При использовании в настоящем документе «холестерин липопротеина низкой плотности (LDL-C)» означает холестерин, который содержится в частицах липопротеина низкой плотности. Концентрацию LDL-C в сыворотке (или в плазме) обычно определяют в мг/дл или в нмоль/л. «LDL-C в сыворотке» и «LDL-C в плазме» означает содержание LDL-C в сыворотке и плазме, соответственно.
При использовании в настоящем документе «основные факторы риска» относится к факторам, которые способствуют высокому риску конкретного заболевания или состояния. В некоторых вариантах реализации изобретения основные факторы риска для коронарной болезни сердца включают, без ограничения, табакокурение, гипертонию, высокое содержание LDL, низкое содержание HDL-C, семейный анамнез коронарной болезни сердца, возраст и другие факторы, описанные в настоящем документе.
При использовании в настоящем документе «метаболическое расстройство» или «метаболическое заболевание» относится к состоянию, характеризующемуся изменением или нарушением метаболической функции. «Метаболический» и «метаболизм» представляют собой термины, общеизвестные в данной области техники, и обычно включают весь диапазон биохимических процессов, происходящих в живом организме. Метаболические расстройства включают, но не ограничиваются ими, гипергликемию, преддиабет, диабет (типа 1 и типа 2). ожирение, инсулинорезистентность, метаболический синдром и дислипидемию на фоне диабета 2-го типа.
При использовании в настоящем документе «метаболический синдром» означает патологическое состояние, характеризующееся группировкой липидных и нелипидных сердечно-сосудистых факторов риска метаболического происхождения. В некоторых вариантах реализации изобретения метаболический синдром определяют по наличию любых 3 из следующих факторов: окружность талии более 102 см у мужчин или более 88 см у женщин; содержание триглицеридов в сыворотке по меньшей мере 150 мг/дл; содержание HDL-C менее 40 мг/дл у мужчин или менее 50 мг/дл у женщин; кровяное давление по меньшей мере 130/85 мм рт.ст.; и содержание глюкозы натощак по меньшей мере 110 мг/дл. Эти детерминанты могут быть легко измерены в клинической практике (JAMA, 2001, 285: 2486-2497).
«Парентеральное введение» обозначает введение инъекцией или инфузией. Парентеральное введение включает подкожное введение, внутривенное введение, внутримышечное введение, внутриартериальное введение, внутрибрюшинное введение или внутричерепное введение, например, интратекальное или интрацеребровентрикулярное введение. Введение может быть непрерывным, хроническим, кратковременным или периодическим.
При использовании в настоящем документе «пептид» обозначает молекулу, образованную связыванием по меньшей мере двух аминокислот амидными связями. Пептид относится к полипептидам и белкам.
При использовании в настоящем документе «фармацевтический агент» обозначает вещество, которое обеспечивает благоприятный терапевтический эффект при введении индивидууму. Например, в некоторых вариантах реализации изобретения антисмысловый олигонуклеотид, нацеленный на apoCIII, представляет собой фармацевтический агент.
При использовании в настоящем документе «фармацевтическая композиция» или «композиция» означает смесь веществ, подходящая для введения индивидууму. Например, фармацевтическая композиция может содержать один или более активных агентов и фармацевтический носитель, например, стерильный водный раствор.
При использовании в настоящем документе «фармацевтически приемлемое производное» включает производные соединений, описанных в настоящем документе, такие как сольваты, гидраты, сложные эфиры, пролекарства, полиморфы, изомеры, меченные изотопами разновидности, фармацевтически приемлемые соли и другие производные, известные в данной области техники.
При использовании в настоящем документе «фармацевтически приемлемые соли» обозначает физиологически и фармацевтически приемлемые соли антисмысловых соединений, то есть соли, которые сохраняют желаемую биологическую активность исходного соединения и не наделяют его нежелательным токсикологическим действием. Термин «фармацевтически приемлемая соль» или «соль» включает соль, полученную из фармацевтически приемлемых нетоксичных кислот или оснований, включая неорганические или органические кислоты и основания. «Фармацевтически приемлемые соли» соединений, описанных в настоящем документе, могут быть получены по общеизвестным в данной области техники способам. Обзор фармацевтически приемлемых солей приведен в публикации Stahl and Wermuth, Handbook of Pharmaceutical Salts: Properties, Selection and Use (Wiley-VCH, Вайнхайм, Германия, 2002). Натриевые соли антисмысловых олигонуклеотидов являются пригодными и приемлемыми для терапевтического введения людям. Соответственно, в одном из вариантов реализации изобретения соединения, описанные в настоящем документе, приведены в форме натриевой соли.
При использовании в настоящем документе «часть» обозначает определенное количество смежных (то есть связанных) азотистых оснований нуклеиновой кислоты. В некоторых вариантах реализации изобретения часть является определенным количеством смежных азотистых оснований целевой нуклеиновой кислоты. В некоторых вариантах реализации изобретения часть является определенным количеством смежных азотистых оснований антисмыслового соединения.
При использовании в настоящем документе «предупреждать» или «предупреждение» относится к отсрочке или предотвращению возникновения или развития заболевания, расстройства или состояния в течение периода времени от нескольких минут до бесконечности. Предупреждение означает также снижение риска развития заболевания, расстройства или состояния.
При использовании в настоящем документе «повышение» означает увеличение количества. Например, повышение уровня HDL в плазме означает увеличение количества HDL в плазме.
При использовании в настоящем документе «снижение» означает уменьшение до меньшей степени, размера, количества или числа. Например, снижение уровня триглицеридов в плазме означает уменьшение количества триглицеридов в плазме.
При использовании в настоящем документе «область» или «целевая область» определяют как часть целевой нуклеиновой кислоты, имеющую по меньшей мере одну идентифицируемую структуру, функцию или характеристику. Например, целевая область может охватывать 3' нетранслируемую область (UTR), 5' нетранслируемую область, экзон, интрон, экзон-интронное сочленение, кодирующую область, область инициации трансляции, область обрыва трансляции или другую определенную область нуклеиновой кислоты. Структурно определенные области для ароСIII могут быть получены по номеру доступа из базы данных последовательностей, такой как NCBI, и такая информация включена в настоящий документ путем ссылки. В некоторых вариантах реализации изобретения целевая область может охватывать последовательность от 5' целевого сайта любого целевого сегмента в пределах целевой области от 3' целевого сайта другого целевого сегмента в пределах целевой области.
При использовании в настоящем документе «второй агент» или «второй терапевтический агент» означает агент, который может быть использован в комбинации с «первым агентом». Второй терапевтический агент может включать, но не ограничивается ими, антисмысловые олигонуклеотиды, нацеленные на ароСIII. Второй агент также может включать анти-ароСIII антитела, ингибиторы пептида ароСIII, агенты для понижения холестерина, агенты для понижения липидов, агенты для понижения глюкозы с; противовоспалительные агенты.
При использовании в настоящем документе «сегменты» определяют как более мелкие или субфрагменты областей нуклеиновой кислоты. Например, «целевой сегмент» обозначает последовательность нуклеотидов целевой нуклеиновой кислоты, на которую нацелено одно или несколько антисмысловых соединений. «Сайт-мишень 5'» относится к 5'-основному нуклеотиду целевого сегмента. «Сайт-мишень 3'» относится к 3'-основному нуклеотиду целевого сегмента. Альтернативно, «сайт инициации» может относиться к 5'-основному нуклеотиду целевого сегмента, а «терминирующий сайт» относится к 3'-основному нуклеотиду целевого сегмента. Целевой сегмент также может начинаться с «сайта инициации» одной последовательности и заканчиваться у «терминирующего сайта» другой последовательности.
При использовании в настоящем документе «статин» означает агент, который подавляет активность редуктазы HMG-CoA.
При использовании в настоящем документе «подкожное введение» обозначает введение непосредственно под кожу.
При использовании в настоящем документе «субъект» обозначает человека или животное, не являющееся человеком, выбранное для лечения или терапии.
При использовании в настоящем документе «симптом сердечно-сосудистого заболевания или расстройства» означает явление, которое возникает в результате и сопутствует сердечно-сосудистому заболеванию или расстройству и служит его признаком. Например, стенокардия; боль в груди, одышка, учащенное сердцебиение; слабость; головокружение; тошнота; потоотделение; тахикардия; брадикардия; аритмия; мерцательная аритмия; опухание нижних конечностей; цианоз; усталость; обморок; онемение лица; онемение конечностей; хромота или судороги мышц; вздутие живота; или лихорадка - представляют собой симптомы сердечно-сосудистого заболевания или расстройства.
При использовании в настоящем документе «нацеливание» или «нацеленный» обозначает процесс разработки и выбора антисмыслового соединения, которое будет специфически гибридизоваться с целевой нуклеиновой кислотой и вызывать требуемый эффект.
При использовании в настоящем документе «терапевтически эффективное количество» обозначает количество фармацевтического агента, которое обеспечивает индивидууму терапевтическое преимущество.
При использовании в настоящем документе «терапевтическое изменение образа жизни» означает изменение питания и образа жизни, направленное на снижение массы жировой/адипозной ткани и/или холестерина. Такое изменение может снижать риск развития сердечного заболевания и может включать рекомендации по диетическому употреблению общих суточных калорий, общих жиров, насыщенных жиров, полиненасыщенных жиров, мононенасыщенных жиров, углеводов, белков, холестерина, нерастворимых волокон, а также рекомендации по физической активности.
При использовании в настоящем документе «лечить» или «лечение» относится к введению соединения, описанного в настоящем документе, для обеспечения изменения или улучшения заболевания, расстройства или состояния.
При использовании в настоящем документе «триглицерид» или «TG» обозначает липид или нейтральный жир, состоящий из глицерина, связанного с тремя молекулами жирной кислоты.
При использовании в настоящем документе «диабет 2-го типа» (известный также как «сахарный диабет 2-го типа», «сахарный диабет, 2-й тип», «инсулинонезависимый диабет», «NIDDM», «диабет на фоне ожирения» или «диабет взрослого возраста») представляет собой метаболическое расстройство, которое характеризуется, главным образом, инсулинорезистентностью, относительным дефицитом инсулина и гипергликемией.
Некоторые варианты реализации изобретения
В некоторых вариантах реализации изобретения приведены соединения и способы снижения экспрессии мРНК и белка АроСIII. В некоторых вариантах реализации изобретения соединение представляет собой специфический ингибитор АроСIII для лечении, предупреждения или улучшения заболевания, связанного с АроСIII. В некоторых вариантах реализации изобретения соединение представляет собой антисмысловый олигонуклеотид, нацеленный на АроСIII. В некоторых вариантах реализации изобретения соединение представляет собой модифицированный олигонуклеотид, нацеленный на АроСIII, с конъюгирующей группой.
В некоторых вариантах реализации изобретения соединение содержит миРНК или антисмысловый олигонуклеотид, нацеленный на аполипопротеин С-III (АроС-III), известный в данной области техники, и конъюгирующую группу, описанную в настоящем документе. Примеры антисмысловых олигонуклеотидов, нацеленных на АроС-III, подходящих для конъюгации, включают, но не ограничиваются ими, те, которые описаны в публикации заявки на патент США №2013/0317085, которая включена в настоящий документ посредством ссылки в полном объеме. В некоторых вариантах реализации: изобретения соединение содержит антисмысловый олигонуклеотид, имеющий последовательность азотистых оснований любой из SEQ ID NO 19-96 и 209-221, описанных в заявке на патент США №2013/0317085, и конъюгирующую группу, описанную в настоящем документе. Последовательности азотистых оснований всех вышеупомянутных ссылочных SEQ ID NO включены в настоящий документ посредством ссылки.
В некоторых вариантах реализации изобретения модифицированный олигонуклеотид с конъюгирующей группой имеет последовательность азотистых оснований, содержащую по меньшей мере 8 смежных азотистых оснований последовательности, выбранной из любой последовательности, описанной в патенте США 7598227, патенте США 7750141, публикации РСТ WO 2004/093783 или публикации РСТ WO 2012/149495, которые включены в настоящий документ посредством ссылки. В некоторых вариантах реализации изобретения модифицированный олигонуклеотид имеет последовательность, выбранную из любой последовательности, описанной в патенте США 7598227, патенте США 7750141, публикации РСТ WO 2004/093783 или публикации РСТ WO 2012/149495, которые включены в настоящий документ посредством ссылки.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 12-30 связанных нуклеозидов. В некоторых вариантах реализации изобретения модифицированный олигонуклеотид а конъюгирующей группой состоит из 15-30, 18-24, 19-22, 13-25, 14-25, 15-25 связанных нуклеозидов. В некоторых вариантах реализации изобретения модифицированный олигонуклеотид с группой конъюгат содержит по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19, по меньшей мере 20, по меньшей мере 21, по меньшей мере 22, по меньшей мере 23, по меньшей мере 24, по меньшей мере 25, по меньшей мере 26, по меньшей мере 27, по меньшей мере 28, по меньшей мере 29 или 30 связанных нуклеозидов. В некоторых вариантах реализации изобретения модифицированный олигонуклеотид с конъюгирующей группой состоит из 20 связанных нуклеозидов.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид с конъюгирующей группой, нацеленный на АроСIII, и имеет последовательность, комплементарную любой из последовательностей, приведенных в GENBANK с номером доступа NM_000040.1 (включена в настоящий документ как SEQ ID NO: 1), с номером доступа GENBANK NT_033899.8, усеченная по нуклеотидам с 20262640 по 20266603 (включена в настоящий документ как SEQ ID NO: 2) и/или с номером доступа GENBANK NT_035088.1, усеченная по нуклеотидам с 6238608 по 6242565 (включена в настоящий документ как SEQ ID NO: 3). В некоторых вариантах реализации изобретения модифицированный олигонуклеотид по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98% или по меньшей мере на 100% комплементарен любой из SEQ ID NO: 1-3. В некоторых вариантах реализации изобретения соединение содержит модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид содержит по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19 или 20 смежных азотистых оснований, комплементарных равной по длине части любой из SEQ ID NO: 1-3. В некоторых вариантах реализации соединение содержит модифицированный олигонуклеотид, нацеленный на сегмент АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид содержит по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19 или 20 смежных азотистых оснований, комплементарных равной по длине части любого из целевых сегментов, приведенных в Таблицах 121 и 124. В этих таблицах «сайт инициации» относится к 5'-основному нуклеотиду целевого сегмента, а «терминирующий сайт» относится к 3'-основному нуклеотиду целевого сегмента. Целевой сегмент может иметь длину от сайта инициации до терминирующего сайта каждой последовательности, перечисленной в таблицах. Альтернативно, целевой сегмент может иметь длину от сайта инициации одной последовательности до конца терминирующего сайта другой последовательности. Например, как показано в таблицах, целевой сегмент может иметь длину от 3533 до 3552, от сайта инициации до терминирующего сайта SEQ ID NO: 87. В другом примере, как показано, в таблицах, целевой сегмент может иметь длину от 3514 до 3558, от сайта инициации SEQ ID NO: 83 до терминирующего сайта SEQ ID NO: 88. В некоторых вариантах реализации изобретения антисмысловое соединение содержит по меньшей мере 8 азотистых оснований последовательности SEQ ID NO: 87. В некоторых вариантах реализации антисмысловое соединение содержит последовательность SEQ ID NO: 87. В некоторых вариантах реализации изобретения антисмысловое соединение состоит из последовательности SEQ ID NO: 87. В некоторых вариантах реализации изобретения антисмысловое соединение представляет собой ISIS 304801.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом последовательность азотистых оснований модифицированного олигонуклеотида по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или на 100% комплементарна любой из SEQ ID NO: 1-3. В некоторых вариантах реализации приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом последовательность азотистых оснований модифицированного олигонуклеотида по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или на 100% комплементарна любому из целевых сегментов, описанных в настоящем документе.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 12-30 связанных нуклеозидов т: содержит последовательность азотистых оснований, содержащую часть из по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19 или 20 смежных азотистых оснований, комплементарных равной по длине части азотистых оснований 3533-3552 SEQ ID, NO: 3, причем указанная последовательность азотистых оснований модифицированного олигонуклеотида по меньшей мере на 80% комплементарна к SEQ ID NO: 3.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 12-30 связанных нуклеозидов и содержит последовательность азотистых оснований, содержащую по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19, по меньшей мере 20, по меньшей мере 21, по меньшей мере 22, по меньшей мере 23, по меньшей мере 24, по меньшей мере 25, по меньшей мере 26, по меньшей мере 27, по меньшей мере 28, по меньшей мере 29 или 30 смежных азотистых оснований, комплементарных равной по длине части азотистых оснований 3514-3558 SEQ ID NO: 3, причем указанная последовательность азотистых оснований модифицированного олигонуклеотида по меньшей мере на 80% комплементарна к SEQ ID NO: 3.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 12-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19 или 20 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 19-96, 209-221. В некоторых вариантах реализации изобретения конъюгированный модифицированный олигонуклеотид имеет последовательность азотистых оснований, содержащую по меньшей мере 8 смежных азотистых оснований любой из последовательностей азотистых оснований SEQ ID NO: 19-96, 209-221. В некоторых вариантах реализации изобретения соединение состоит из любой из SEQ ID NO: 19-96, 209-221 и конъюгирующие группы.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 12-30 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19 или 20 смежных азотистых оснований последовательности азотистых оснований SEQ ID NO: 87. В некоторых вариантах реализации модифицированный олигонуклеотид с конъюгирующей группой имеет последовательность азотистых оснований, содержащую по меньшей мере 8 смежных азотистых оснований последовательности азотистых оснований SEQ ID NO: 87. В некоторых вариантах реализации соединение состоит из SEQ ID NO: 87 и конъюгирующие группы.
В некоторых вариантах реализации настоящего описания приведены конъюгированные антисмысловые соединения, приведенные следующей структурой. В некоторых вариантах реализации изобретения антисмысловое соединение содержит модифицированный олигонуклеотид ISIS 304801 с 5'-Х, где X представляет собой конъюгирующую группу, содержащую GalNAc. В некоторых вариантах реализации изобретения антисмысловое соединение состоит из модифицированного олигонуклеотида ISIS 304801 с 5'-Х, где X представляет собой конъюгирующую группу, содержащую GalNAc.

В некоторых вариантах реализации настоящего описания приведены конъюгированные антисмысловые соединения, приведенные следующей структурой. В некоторых вариантах реализации изобретения антисмысловое соединение содержит конъюгированный модифицированный олигонуклеотид ISIS 678354. В некоторых вариантах реализации изобретения антисмысловое соединение состоит из конъюгированного модифицированного олигонуклеотида ISIS 678354.

В некоторых вариантах реализации настоящего описания приведены конъюгированные антисмысловые соединения, приведенные следующей структурой. В некоторых вариантах реализации изобретения антисмысловое соединение содержит конъюгированный модифицированный олигонуклеотид ISIS 678357. В некоторых вариантах реализации изобретения антисмысловое соединение состоит из конъюгированного модифицированного олигонуклеотида ISIS 678357.

В некоторых вариантах реализации настоящего описания приведены конъюгированные антисмысловые соединения, приведенные следующей структурой. В некоторых вариантах реализации изобретения антисмысловое соединение содержит модифицированный олигонуклеотид с последовательностью азотистых оснований SEQ ID NO: 87 с 5'-GalNAc с вариабельностью в сахарных структурах крыльев. В некоторых вариантах реализации изобретения антисмысловое соединение состоит из модифицированного олигонуклеотида с последовательностью азотистых оснований SEQ ID NO: 87 с 5'-GalNAc с вариабельностью в сахарных структурах крыльев.

Где либо R1 представляет собой -OCH2CH2OCH3 (МОЕ), и R2 представляет собой Н; либо R1 и R2 вместе образуют мостик, где R1 представляет собой -O-, и R2 представляет собой -CH2-, -СН(CH3)- или -CH2CH2-, и R1 и R2 связаны напрямую, так что образующийся мостик выбран из: -O-CH2-, -О-СН(CH3)- и -O-CH2CH2-;
и для каждой пары R3 и R4 у одного кольца, независимо для каждого кольца: либо R3 выбран из Н и -OCH2CH2OCH3, и R4 представляет собой Н; либо R3 и R4 вместе образуют мостик, где R3 представляет собой -O-, и R4 представляет собой -CH2-, -СН(CH3)- или -CH2CH2-, и R3 и R4 связаны напрямую, так что образующийся мостик выбран из: -O-CH2-, -О-СН(CH3)- и -O-CH2CH2-;
и R5 выбран из Н и -CH3;
и Z выбран из S- и О-.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид является одноцепочечным.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом по меньшей мере одна межнуклеозидная связь представляет собой модифицированную межнуклеозидную связь. В некоторых вариантах реализации изобретения модифицированная межнуклеозидная связь представляет собой тиофосфатную межнуклеозидную связь. В некоторых вариантах реализации изобретения по меньшей мере 1, по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8, по меньшей мере 9 или по меньшей мере 10 межнуклеозидных связей указанного модифицированного олигонуклеотида представляют собой тиофосфатные межнуклеозидные связи. В некоторых вариантах реализации изобретения каждая межнуклеозидная связь представляет собой тиофосфатную межнуклеозидную связь. В некоторых вариантах реализации изобретения модифицированный олигонуклеотид содержит по меньшей мере 1, по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8, по меньшей мере 9 или по меньшей мере 10 фосфодиэфирных межнуклеозидных связей. В некоторых вариантах реализации изобретения каждая межнуклеозидная связь модифицированного олигонуклеотида выбрана из фосфодиэфирной межнуклеозидной связи и тиофосфатной межнуклеозидной связи.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом по меньшей мере один нуклеозид содержит модифицированное азотистое основание. В некоторых вариантах реализации изобретения модифицированное азотистое основание представляет собой 5-метилцитозин.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид содержит по меньшей мере один модифицированный сахар. В некоторых вариантах реализации изобретения модифицированный сахар представляет собой бициклический сахар. В некоторых вариантах реализации изобретения модифицированный сахар содержит 2'-O-метоксиэтиловый, стерически затрудненный этиловый, 3'-фтор-ГНК (hexitol nucleic acid (HNA)) или 4'-(CH2)n-O-2' мостик, где n равен 1 или 2.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 12-30 связанных нуклеозидов и содержит: (а) сегмент гэп, состоящий из связанных дезоксинуклеозидов; (b) сегмент 5'-крыла, состоящий из связанных нуклеозидов; (с) сегмент 3'-крыла, состоящий, из связанных нуклеозидов; и при этом сегмент гэп находится между сегментом 5'-крыла и сегментом 3'-крыла, и каждый нуклеозид каждого сегмента крыла содержит модифицированный сахар.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 20 связанных нуклеозидов и содержит: (а) сегмент гэп, состоящий из десяти связанных дезоксинуклеозидов; (b) сегмент 5'-крыла, состоящий из пяти связанных нуклеозидов; (с) сегмент 3'-крыла, состоящий из пяти связанных нуклеозидов; и при этом сегмент гэп находится между сегментом 5'-крыла и сегментом 3'-крыла, и каждый нуклеозид каждого сегмента крыла содержит 2'-O-метоксиэтиловый сахар, и по меньшей мере одна межнуклеозидных связей представляет собой тиофосфатную связь, а каждый цитозиновый остаток представляет собой 5-метилцитозин.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 20 связанных нуклеозидов, и имеет последовательность азотистых оснований, содержащую по меньшей мере 8 смежных азотистых оснований любой из SEQ ID NO: 19-96, 209-221, при этом модифицированный олигонуклеотид содержит: (а) сегмент гэп, состоящий из десяти связанных дезоксинуклеозидов; (b) сегмент 5'-крыла, состоящий из пяти связанных нуклеозидов; (с) сегмент 3'-крыла, состоящий из пяти связанных нуклеозидов; и при этом сегмент гэп находится между сегментом 5'-крыла и сегментом 3'-крыла, и каждый нуклеозид каждого сегмента крыла содержит 2'-O-метоксиэтиловый сахар, и по меньшей мере одна межнуклеозидных связей представляет собой тиофосфатную связь, а каждый цитозиновый остаток представляет собой 5-метилцитозин.
В некоторых вариантах реализации изобретения приведено соединение, содержащее модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, при этом модифицированный олигонуклеотид состоит из 20 связанных нуклеозидов и имеет последовательность азотистых оснований, содержащую по меньшей мере 8 смежных азотистых оснований SEQ ID NO: 87, при этом модифицированный олигонуклеотид содержит: (а) сегмент гэп, состоящий из десяти связанных дезоксинуклеозидов; (b) сегмент 5'-крыла, состоящий из пяти связанных нуклеозидов; (с) сегмент 3'-крыла, состоящий из пяти связанных нуклеозидов; и при этом сегмент гэп находится между сегментом 5'-крыла и сегментом 3'-крыла, и каждый нуклеозид каждого сегмента крыла содержит 2'-O-метоксиэтиловый сахар, и по меньшей мере одна межнуклеозидных связей представляет собой тиофосфатную связь, а каждый цитозиновый остаток представляет собой 5-метилцитозин.
В некоторых вариантах реализации изобретения приведен модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующая группа, при этом модифицированный олигонуклеотид состоит из 20 связанных нуклеозидов с последовательностью азотистых оснований SEQ ID NO: 87, при этом модифицированный олигонуклеотид содержит: (а) сегмент гэп, состоящий из десяти связанных дезоксинуклеозидов; (b) сегмент 5'-крыла, состоящий из пяти связанных нуклеозидов; (с) сегмент 3'-крыла, состоящий из пяти связанных нуклеозидов; и при этом сегмент гэп находится между сегментом 5'-крыла и сегментом 3'-крыла, и каждый нуклеозид каждого сегмента крыла содержит 2'-O-метоксиэтиловый сахар, и по меньшей мере одна межнуклеозидных связей представляет собой тиофосфатную связь, а каждый цитозиновый остаток представляет собой 5-метилцитозин.
В некоторых вариантах реализации изобретения конъюгирующая группа связана с модифицированным олигонуклеотидом на 5'-конце модифицированного олигонуклеотида. В некоторых вариантах реализации изобретения конъюгирующая группа связана с модифицированным олигонуклеотидом на 3'-конце модифицированного олигонуклеотида.
В некоторых вариантах реализации изобретения конъюгирующая группа содержит только один лиганд. В некоторых вариантах реализации изобретения конъюгирующая группа содержит один или более лигандов. В некоторых вариантах реализации изобретения конъюгирующая группа содержит только два лиганда. В некоторых вариантах реализации изобретения конъюгирующая группа содержит два или более лигандов. В некоторых вариантах реализации изобретения конъюгирующая группа содержит три или более лигандов. В некоторых вариантах реализации изобретения конъюгирующая группа содержит только три лиганда. В некоторых вариантах реализации изобретения каждый лиганд выбран из: полисахарида, модифицированного полисахарида, маннозы, галактозы, производного маннозы, производного галактозы, D-маннопиранозы, L-маннопиранозы, D-арабинозы, L-галактозы, D-ксилофуранозы, L-ксилофуранозы, D-глюкозы, L-глюкозы, D-галактозы, L-галактозы, α-D-маннофуранозы, β-D-маннофуранозы, α-D-маннопирапозы, β-D-маннопиранозы, α-D-глюкопиранозы, β-D-глюкопиранозы, α-D-глюкофуранозы, β-D-глюкофуранозы, α-D-фруктофуранозы, α-D-фруктопиранозы, α-D-галактопиранозы, β-D-галактопиранозы, α-D-галактофуранозы, β-D-галактофуранозы, глюкозамина, сиаловой кислоты, α-D-галактозамина, N-ацетилгалактозамина, 2-амино-3-O-[(R)-1-карбоксиэтил]-2-дезокси-β-D-глюкопиранозы, 2-дезокси-2-метиламино-L-глюкопиранозы, 4,6-дидезокси-4-формамидо-2,3-ди-O-метил-D-маннопиранозы, 2-дезокси-2-сульфоамино-D-глюкопиранозы, N-гликолоил-α-нейраминовой кислоты, 5-тио-β-D-глюкопиранозы, метил 2,3,4-три-О-ацетил-1-тио-6-O-тритил-α-D-глюкопиранозида, 4-тио-β-D-галактопиранозы, этил 3,4,6,7-тетра-O-ацетил-2-дезокси-1,5-дитио-α-D-глюкогептопиранозида, 2,5-ангидро-D-аллононитрила, рибозы, D-рибозы, D-4-тиорибозы, L-рибозы, L-4-тиорибозы. В некоторых вариантах реализации изобретения каждый лиганд представляет собой N-ацетилгалактозамин.
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
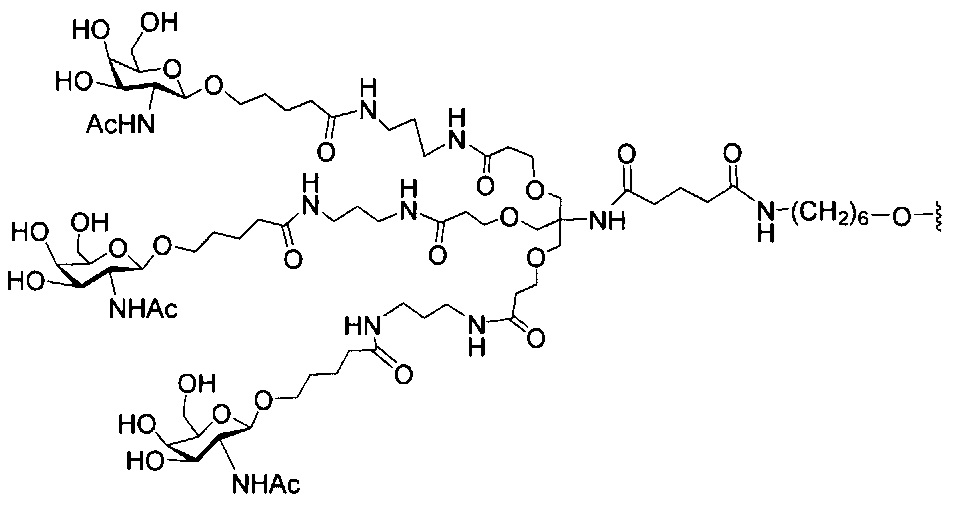
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
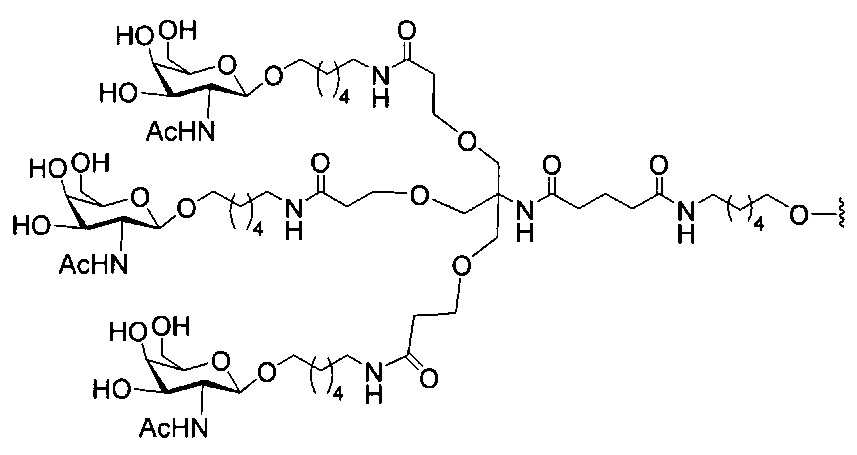
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
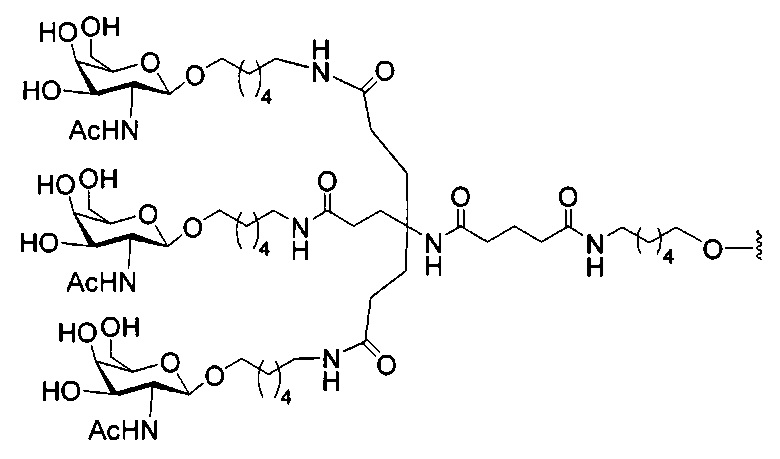
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
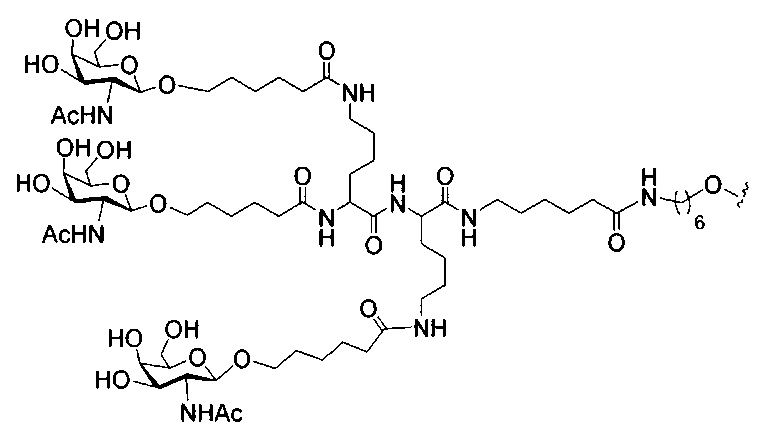
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
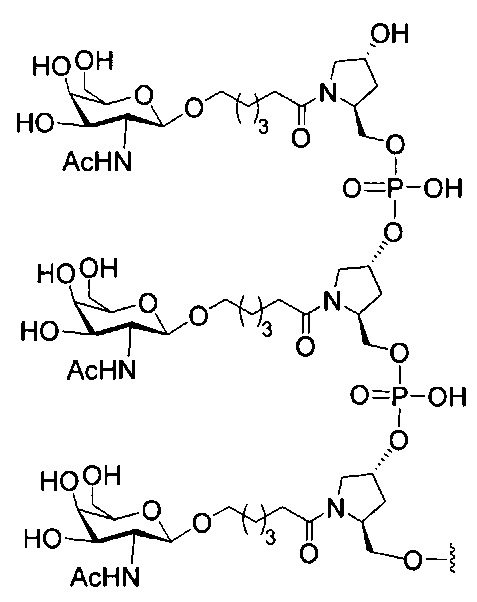
В некоторых вариантах реализации изобретения конъюгирующая группа содержит по меньшей мере одну фосфорную связывающую группу или нейтральную связывающую группу.
В некоторых вариантах реализации изобретения конъюгирующая группа содержит структуру, выбранную из:
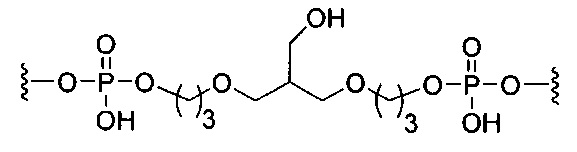
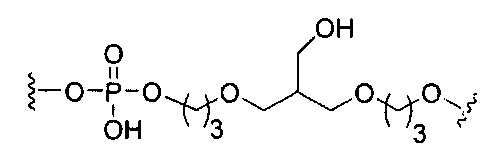
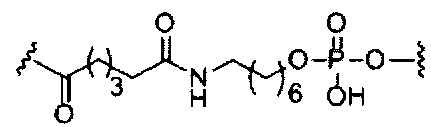
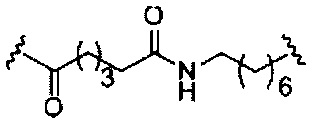
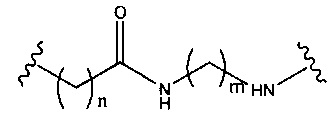
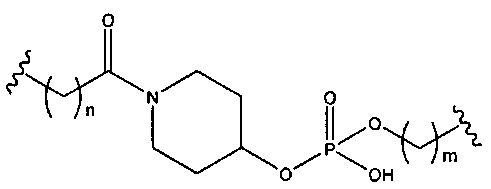
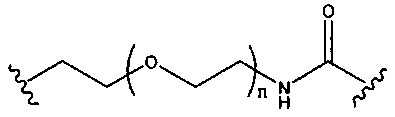
где n равен от 1 до 12; и
где m равен от 1 до 12.
В некоторых вариантах реализации изобретения конъюгирующая группа имеет связку имеющую структуру, выбранную из:

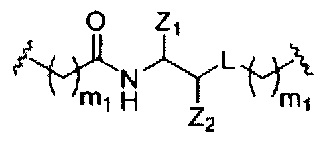
где L представляет собой либо фосфорную связывающую группу, либо нейтральную связывающую группу;
Z1 представляет собой C(=O)O-R2;
Z2 представляет собой Н, C1-C6 алкил или замещенный C1-С6 алкил;
R2 представляет собой Н, C1-С6 алкил или замещенный C1-C6 алкил; и
каждый m1 независимо равен от 0 до 20, при этом по меньшей мере один m1 больше 0 для каждой связки.
В некоторых вариантах реализации изобретения конъюгирующая группа имеет связку, имеющую структуру, выбранную из:
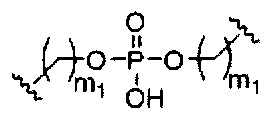
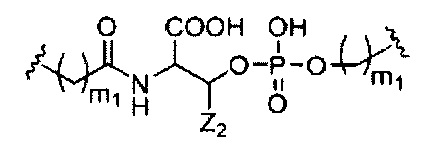
где Z2 представляет собой Н или CH3; и
каждый m1 независимо равен от 0 до 20, при этом по меньшей мере один m1 больше 0 для каждой связки.
В некоторых вариантах реализации изобретения конъюгирующая группа имеет связку, имеющую структуру, выбранную из:
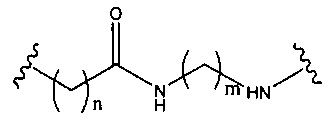
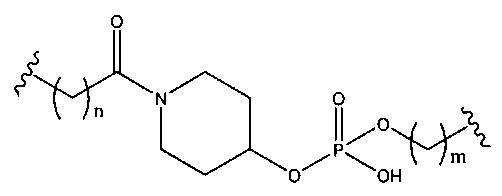
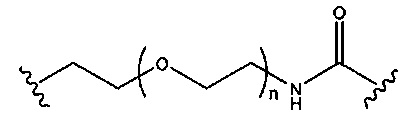
где n равен от 1 до 12; и
где m равен от 1 до 12.
В некоторых вариантах реализации изобретения конъюгирующая группа ковалентно связана с модифицированным олигонуклеотидом.
В некоторых вариантах реализации изобретения соединение имеет структуру, приведенную формулой:
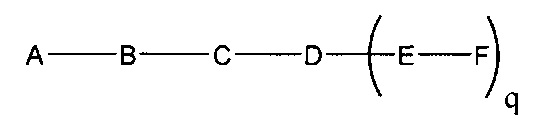
где
А представляет собой модифицированный олигонуклеотид;
В представляет собой расщепляемый фрагмент
С представляет собой линкер конъюгата
D представляет собой группу ветвления
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации изобретения соединение имеет структуру, приведенную формулой:
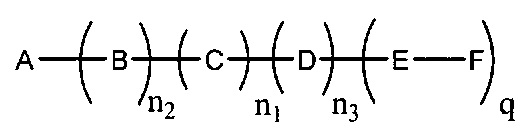
где:
А представляет собой модифицированный олигонуклеотид;
В представляет собой расщепляемый фрагмент
С представляет собой линкер конъюгата
D представляет собой группу ветвления
каждый Е представляет собой связку;
каждый F представляет собой лиганд;
каждый n независимо равен 0 или 1; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации изобретения соединение имеет структуру, приведенную формулой:
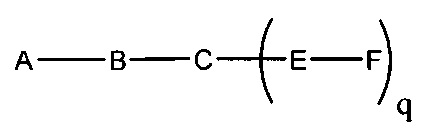
где
А представляет собой модифицированный олигонуклеотид;
В представляет собой расщепляемый фрагмент;
С представляет собой линкер конъюгата;
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации изобретения соединение имеет структуру, приведенную формулой:
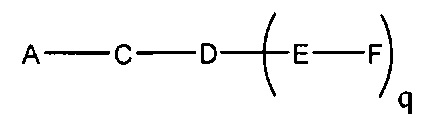
где
А представляет собой модифицированный олигонуклеотид;
С представляет собой линкер конъюгата;
D представляет собой группу ветвления;
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации изобретения соединение имеет структуру, приведенную формулой:
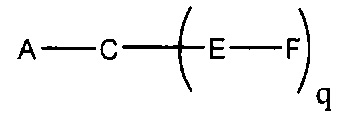
где
А представляет собой модифицированный олигонуклеотид;
С представляет собой линкер конъюгата;
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации изобретения соединение имеет структуру, приведенную формулой:
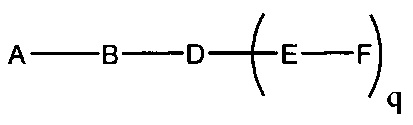
где
А представляет собой модифицированный олигонуклеотид;
В представляет собой расщепляемый фрагмент;
D представляет собой группу ветвления;
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации изобретения соединение имеет структуру, приведенную формулой:
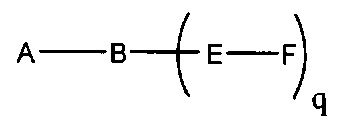
где
А представляет собой модифицированный олигонуклеотид;
В представляет собой расщепляемый фрагмент;
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации изобретения соединение имеет структуру, приведенную формулой:
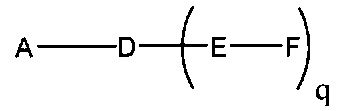
где
А представляет собой модифицированный олигонуклеотид;
D представляет собой группу ветвления;
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации изобретения линкер конъюгата имеет структуру, выбранную из:
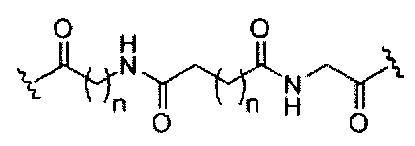
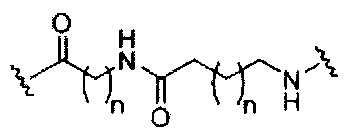
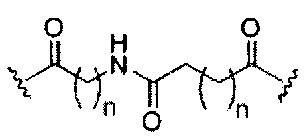
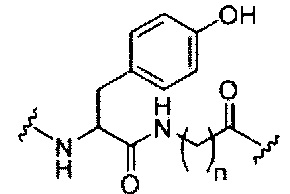
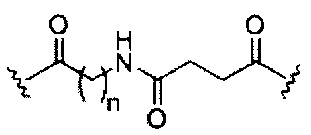
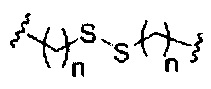
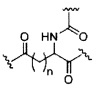
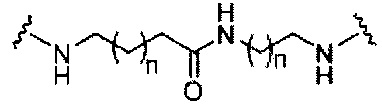
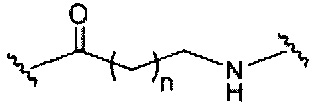

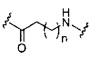
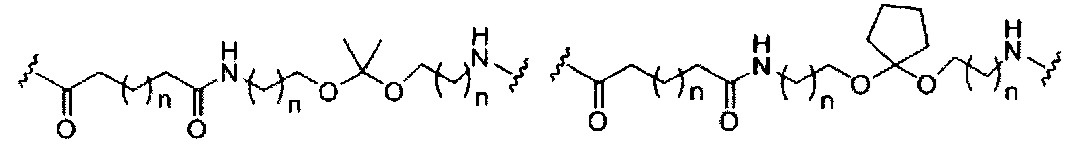

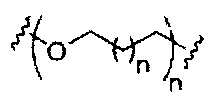
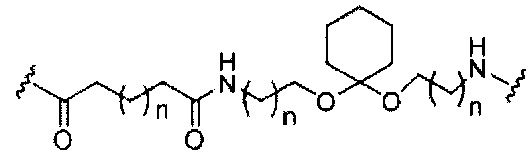
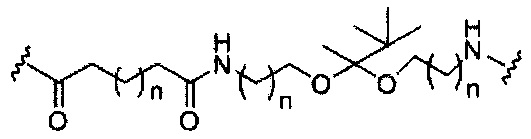
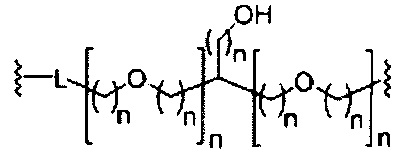
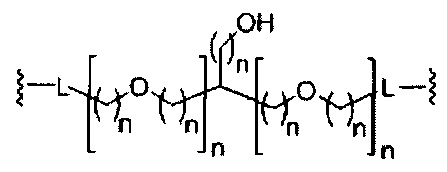
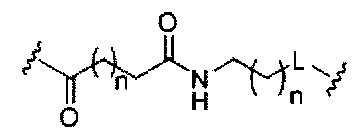
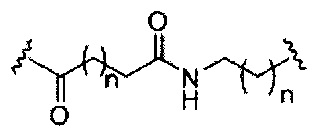
где каждый L независимо представляет собой либо фосфорную связывающую группу, либо нейтральную связывающую группу; и
каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации изобретения линкер конъюгата имеет структуру, выбранную из:
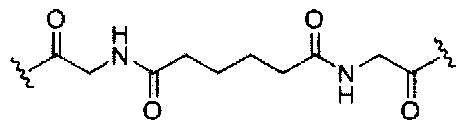
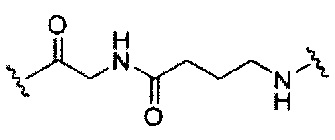
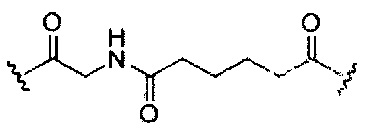
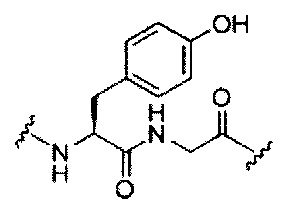
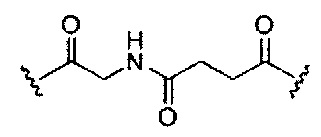
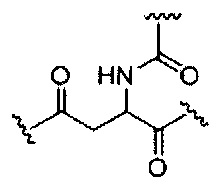
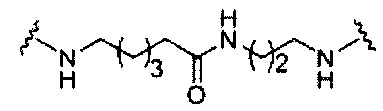

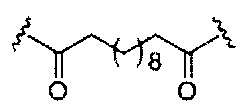
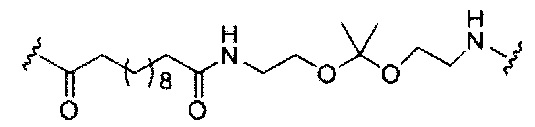
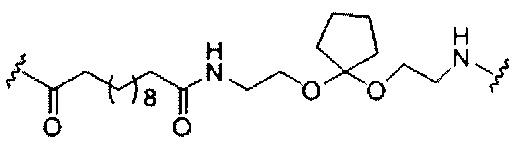
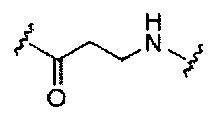
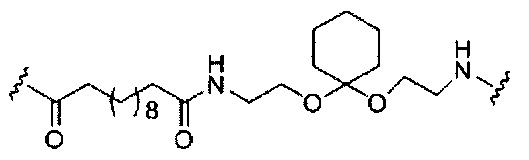
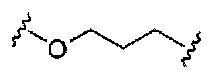
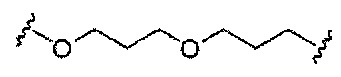
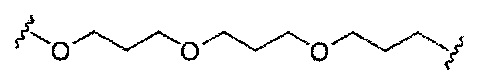
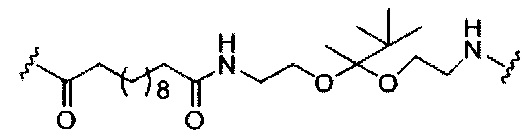
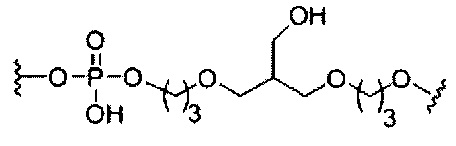
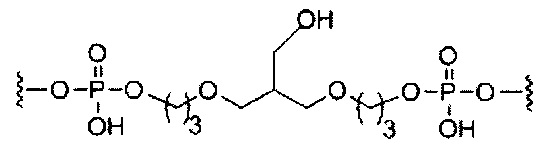
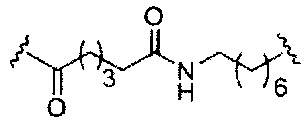
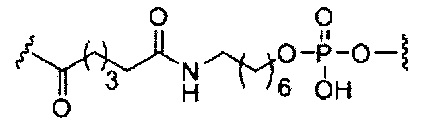
В некоторых вариантах реализации изобретения линкер конъюгата имеет следующую структуру:
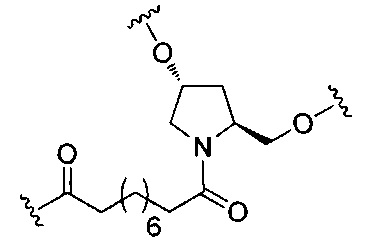
В некоторых вариантах реализации изобретения линкер конъюгата имеет структуру, выбранную из:
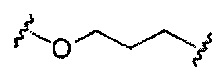
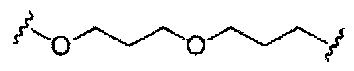
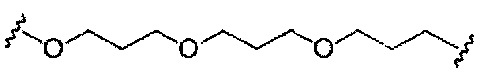
В некоторых вариантах реализации изобретения линкер конъюгата имеет структуру, выбранную из:
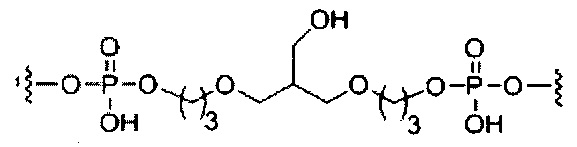
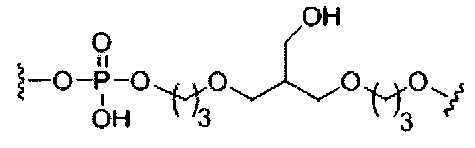
В некоторых вариантах реализации изобретения линкер конъюгата имеет структуру, выбранную из:
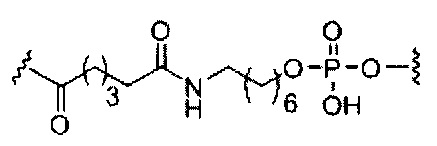
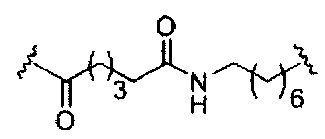
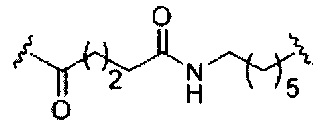
В некоторых вариантах реализации изобретения линкер конъюгата содержит пирролидин. В некоторых вариантах реализации изобретения линкер конъюгата не содержит пирролидин.
В некоторых вариантах реализации изобретения линкер конъюгата содержит ПЭГ.
В некоторых вариантах реализации изобретения линкер конъюгата содержит амид. В некоторых вариантах реализации изобретения линкер конъюгата содержит по меньшей мере два амида. В некоторых вариантах реализации изобретения линкер конъюгата не содержит амид. В некоторых вариантах реализации линкер конъюгата содержит полиамид.
В некоторых вариантах реализации изобретения линкер конъюгата содержит амин.
В некоторых вариантах реализации изобретения линкер конъюгата содержит одну или более дисульфидных связей.
В некоторых вариантах реализации изобретения линкер конъюгата содержит белок-связывающий фрагмент. В некоторых вариантах реализации изобретения белок-связывающий фрагмент содержит липид. В некоторых вариантах реализации изобретения белок-связывающий фрагмент выбран из: холестерина, холевой кислоты, адамантан-уксусной кислоты, 1-пиренмасляной кислоты, дигидротестостерона, 1,3-бис-O-(гексадецил)глицерина, геранилоксигексиловой группы, гексадецилглицерина, борнеола, ментола, 1,3-пропандиола, гептадециловой группы, пальмитиновой кислоты, миристиновой кислоты, O3-(олеоил)литохолевой кислоты, O3-(олеоил)холеновой кислоты, диметокситритила или феноксазина, витамина (например, фолата, витамина А, витамина Е, биотина, пиридоксаля), пептида, углевода (например, моносахарида, дисахарида, трисахарида, тетрасахарида, олигосахарида, полисахарида), эндосомолитического компонента, стероида (например, уваола, гецигенина, диосгенина), терпена (например, тритерпена, например, сарсасапогепина, фриделина, эпифриделанол-дериватизованной литохолевой кислоты) или катионного липида. В некоторых вариантах реализации изобретения каждый белок-связывающий фрагмент выбран из: насыщенной или ненасыщенной жирной кислоты с длиной цепи С16-С22, холестерина, холевой кислоты, витамина Е, адамантана или 1-пентафторпропила.
В некоторых вариантах реализации изобретения линкер конъюгата имеет структуру, выбранную из:
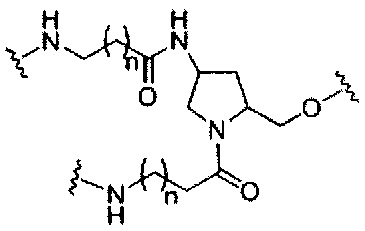
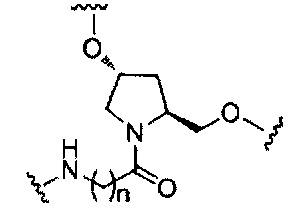
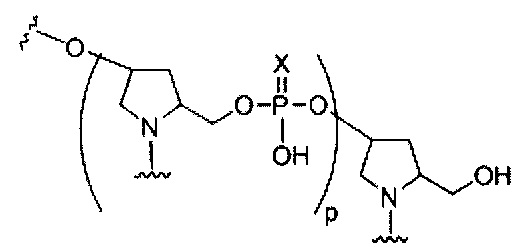
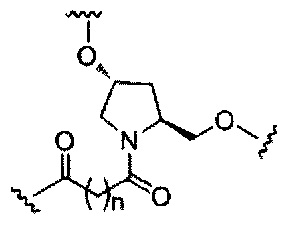
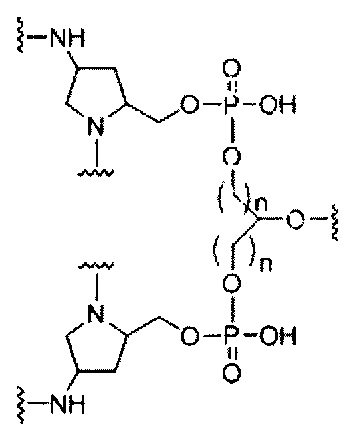
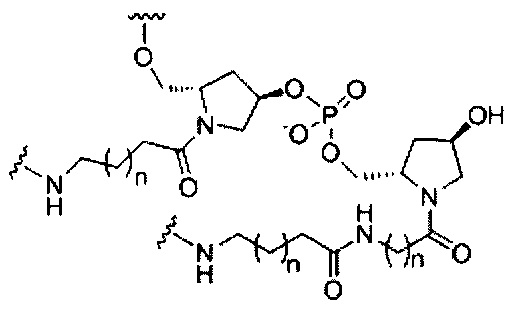
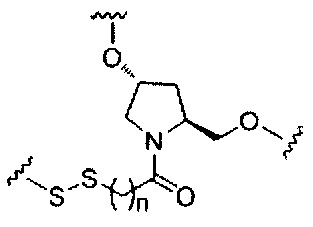
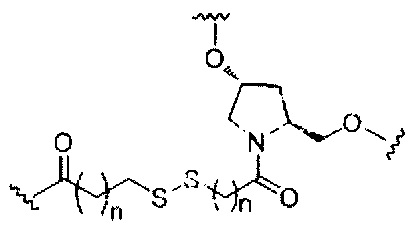
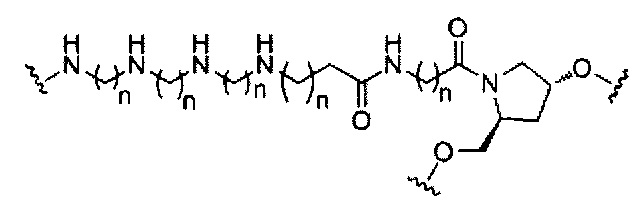
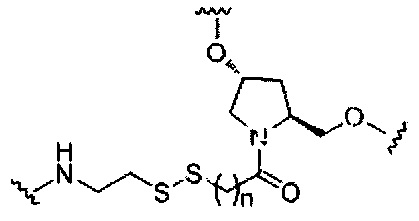
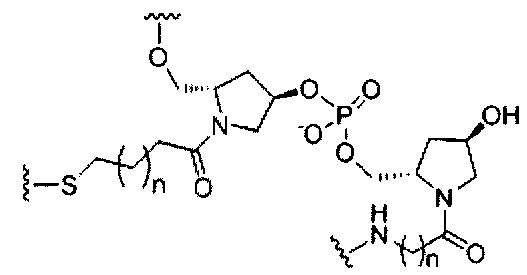
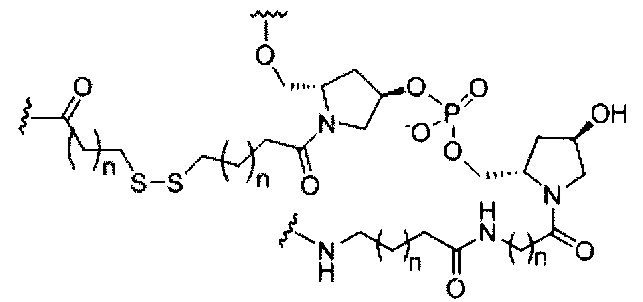
где каждый n независимо равен от 1 до 20; и р равен от 1 до 6.
В некоторых вариантах реализации изобретения линкер конъюгата имеет структуру, выбранную из:
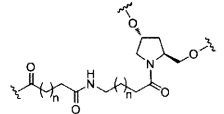
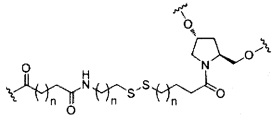
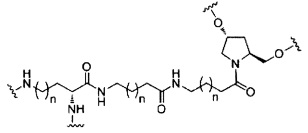
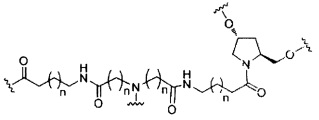
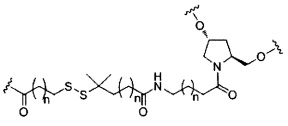
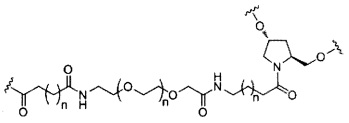
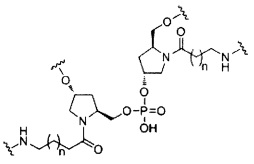
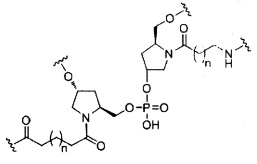
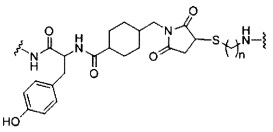
где каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации изобретения линкер конъюгата имеет структуру, выбранную из:
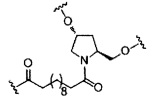
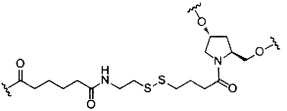
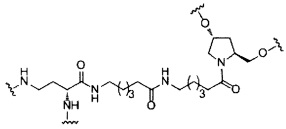
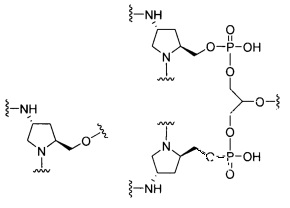
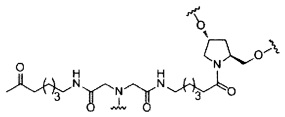
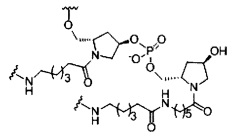
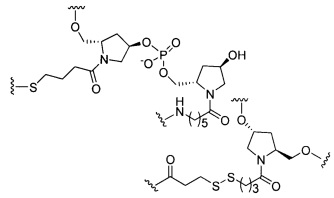
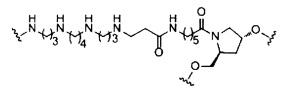
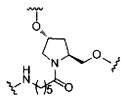
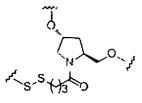
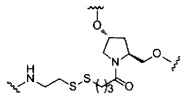
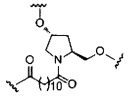
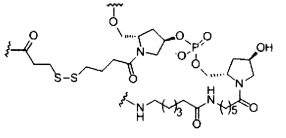
В некоторых вариантах реализации изобретения линкер конъюгата имеет структуру, выбранную из:
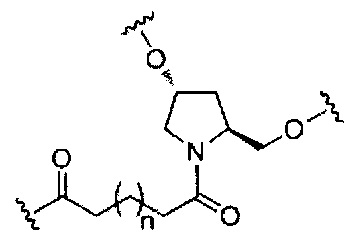
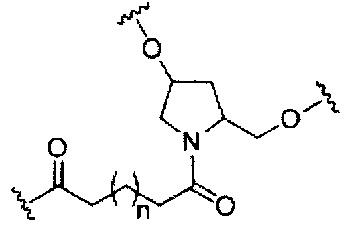
где n равен от 1 до 20.
В некоторых вариантах реализации изобретения линкер конъюгата имеет структуру, выбранную из:
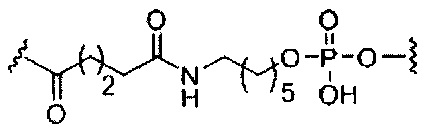
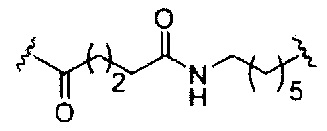
В некоторых вариантах реализации изобретения линкер конъюгата имеет структуру, выбранную из:
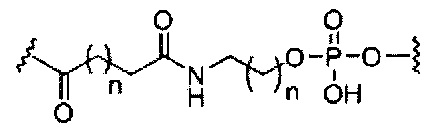
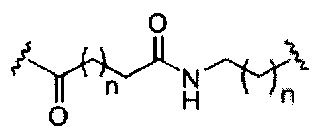
где каждый n независимо равен 0, 1, 2, 3, 4, 5, 6 или 7.
В некоторых вариантах реализации изобретения линкер конъюгата имеет следующую структуру:
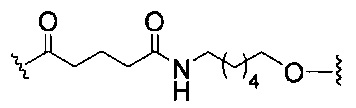
В некоторых вариантах реализации изобретения группа ветвления имеет одну из следующих структур:
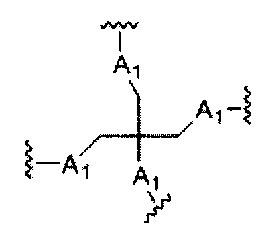
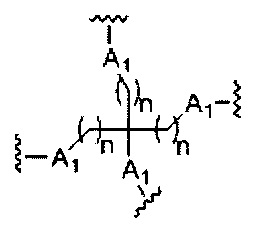
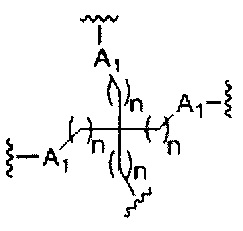
где каждый A1 независимо представляет собой О, S, С=O или NH; и
каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации изобретения группа ветвления имеет одну из следующих структур:
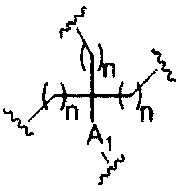
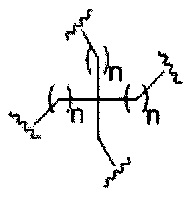
где каждый А1 независимо представляет собой О, S, С=O или NH; и
каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации изобретения группа ветвления имеет следующую структуру:
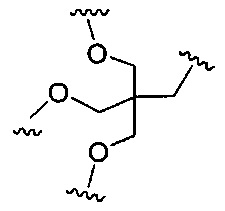
В некоторых вариантах реализации изобретения группа ветвления имеет следующую структуру:
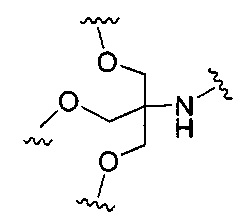
В некоторых вариантах реализации изобретения группа ветвления имеет следующую структуру:
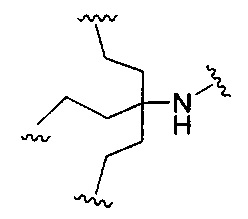
В некоторых вариантах реализации изобретения группа ветвления имеет следующую структуру:
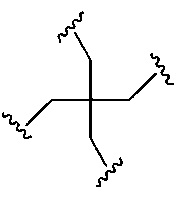
В некоторых вариантах реализации изобретения группа ветвления содержит простой эфир.
В некоторых вариантах реализации изобретения группа ветвления имеет следующую структуру:
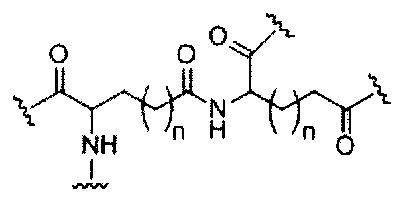
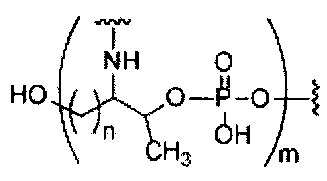
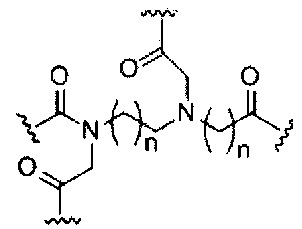
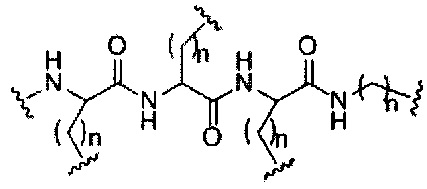
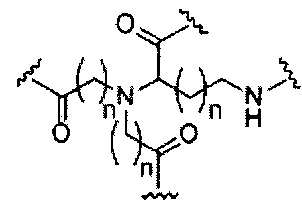
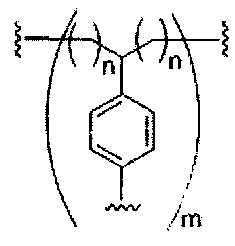
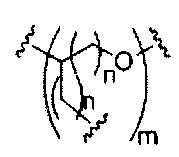
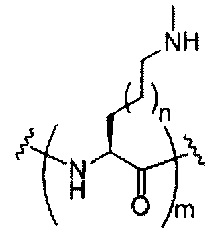
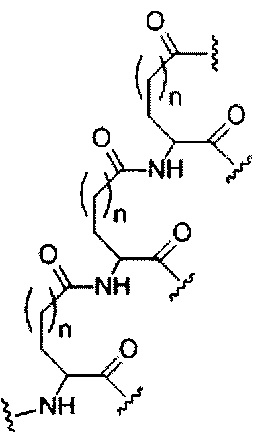
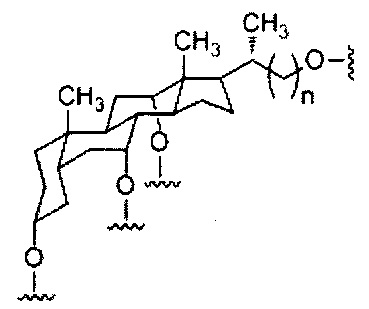
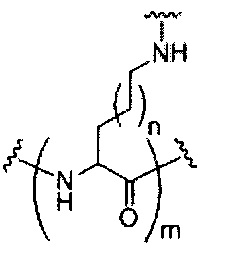
каждый n независимо равен от 1 до 20; и
m равен от 2 до 6.
В некоторых вариантах реализации изобретения группа ветвления имеет следующую структуру:
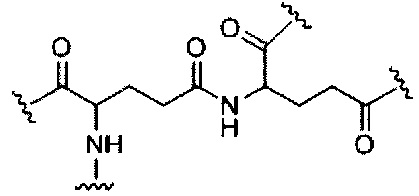
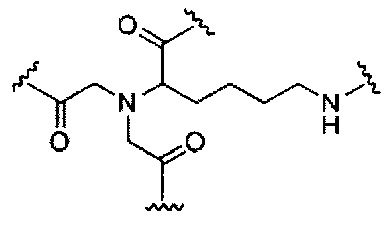
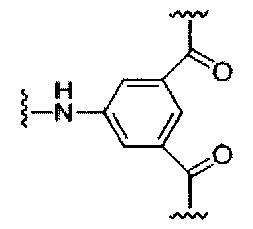
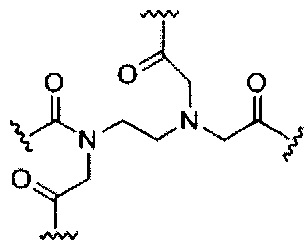
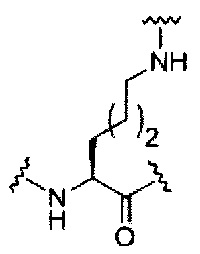
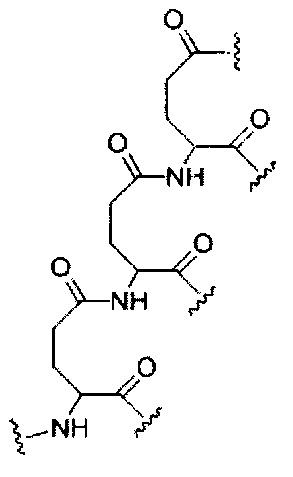
В некоторых вариантах реализации изобретения группа ветвления имеет следующую структуру:
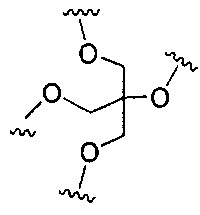
В некоторых вариантах реализации изобретения группа ветвления содержит:
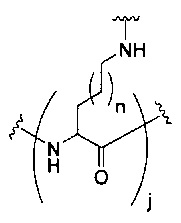
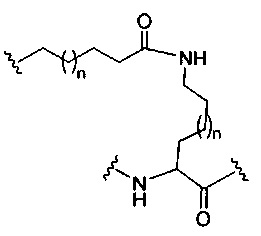
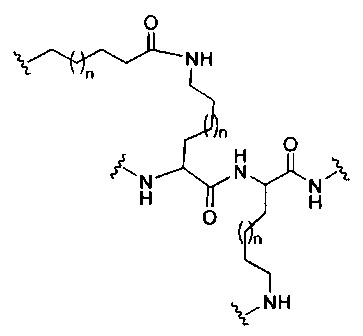
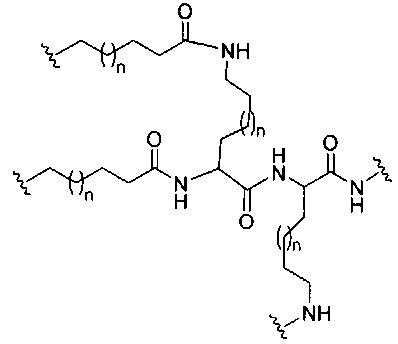
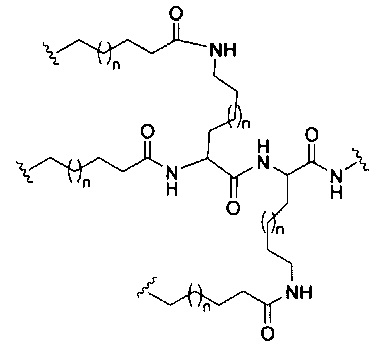
где каждый j представляет собой целое число от 1 до 3; и
где каждый n представляет собой целое число от 1 до 20.
В некоторых вариантах реализации изобретения группа ветвления содержит:
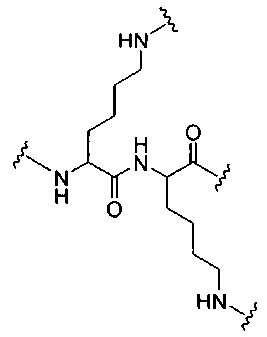
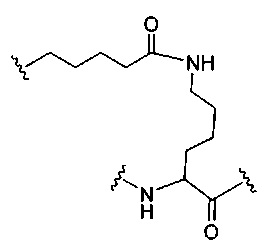
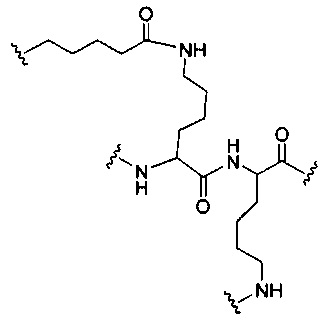
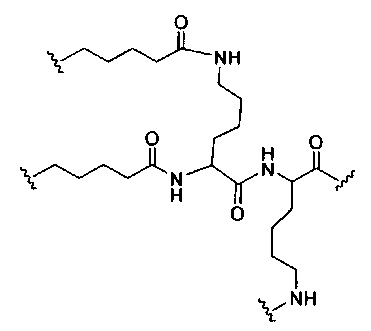
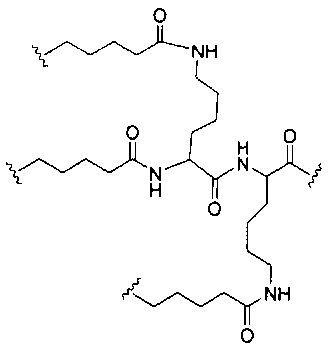
В некоторых вариантах реализации изобретения каждая связка выбрана из:

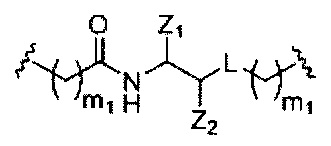
где L выбран из фосфорной связывающей группы и нейтральной связывающей группы;
Z1 представляет собой C(=O)O-R2;
Z2 представляет собой Н, С1-С6 алкил или замещенный С1-С6 алкил;
R2 представляет собой Н, C1-С6 алкил или замещенный С1-С6 алкил;
и каждый m1 независимо равен от 0 до 20, при этом по меньшей мере один m1 больше 0 для каждой связки.
В некоторых вариантах реализации изобретения каждая связка выбрана из:
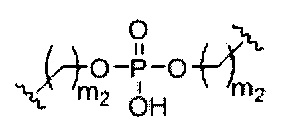
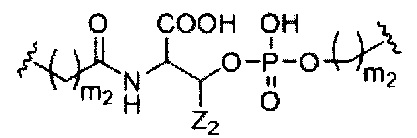
где Z2 представляет собой Н или CH3; и
каждый m2 независимо равен от 0 до 20, при этом по меньшей мере один m2 больше 0 для каждой связки.
В некоторых вариантах реализации изобретения каждая связка выбрана из:
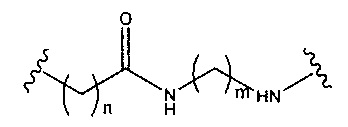
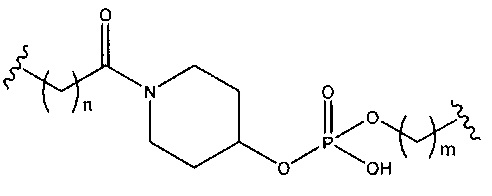
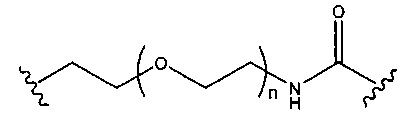
где n равен от 1 до 12; и
где m равен от 1 до 12.
В некоторых вариантах реализации изобретения по меньшей мере одна связка содержит этиленгликоль.
В некоторых вариантах реализации изобретения по меньшей мере одна связка содержит амид. В некоторых вариантах реализации изобретения по меньшей мере одна связка содержит полиамид.
В некоторых вариантах реализации изобретения по меньшей мере одна связка содержит амин.
В некоторых вариантах реализации изобретения по меньшей мере две связки отличны друг от друга. В некоторых вариантах реализации изобретения все связки являются одинаковыми.
В некоторых вариантах реализации изобретения каждая связка выбрана из:
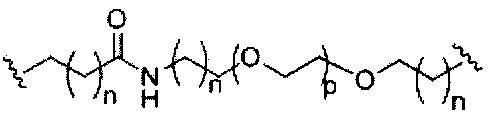
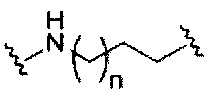
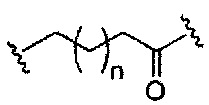
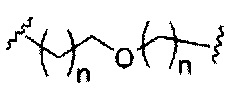
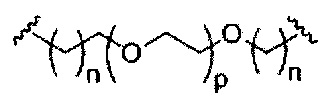
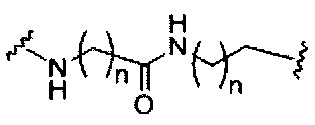
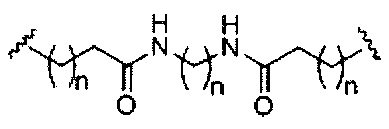
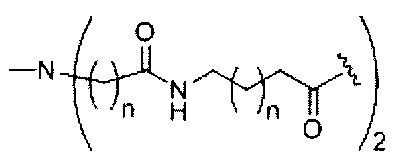
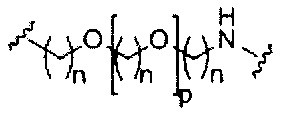
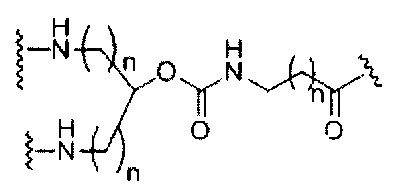
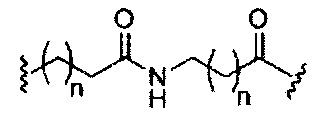

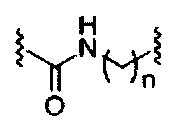
где каждый n независимо равен от 1 до 20; и
каждый р равен от 1 до около 6.
В некоторых вариантах реализации изобретения каждая связка выбрана из:
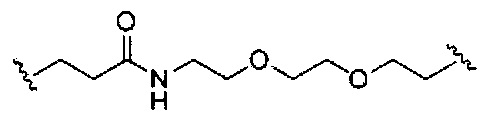
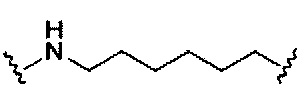
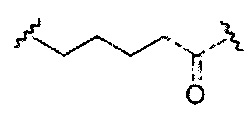
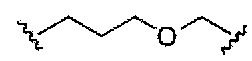
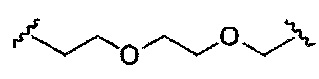
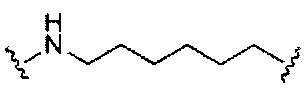
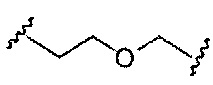
В некоторых вариантах реализации изобретения каждая связка имеет следующую структуру:
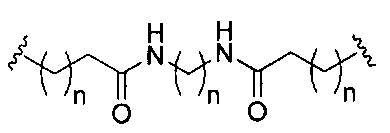
где каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации изобретения каждая связка имеет следующую структуру:
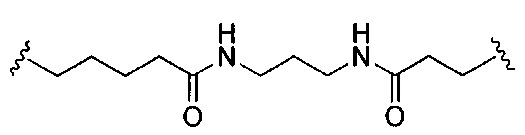
В некоторых вариантах реализации изобретения связка имеет структуру, выбранную из:
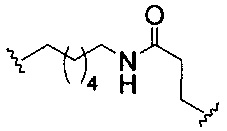
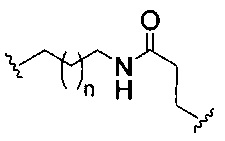
В некоторых вариантах реализации изобретения связка имеет структуру, выбранную из:
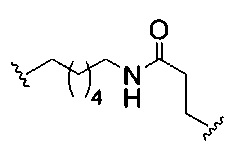
В некоторых вариантах реализации изобретения лиганд представляет собой галактозу.
В некоторых вариантах реализации изобретения лиганд представляет собой манноза-6-фосфат.
В некоторых вариантах реализации изобретения каждый лиганд выбран из:
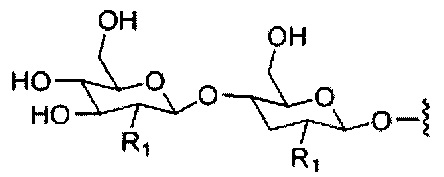
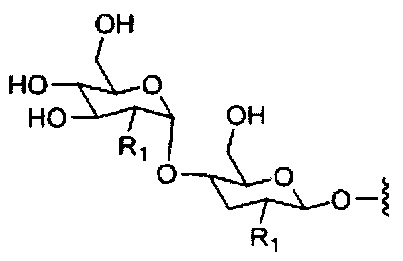
где каждый R1 выбран из ОН и NHCOOH.
В некоторых вариантах реализации изобретения каждый лиганд выбран из:
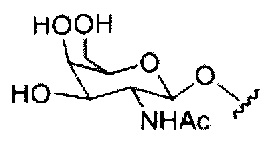
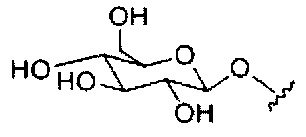
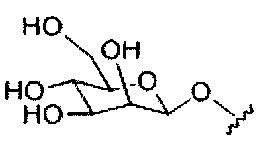
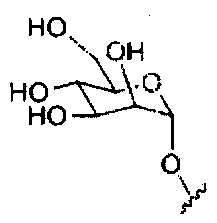
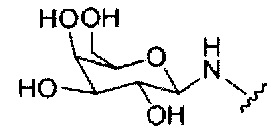
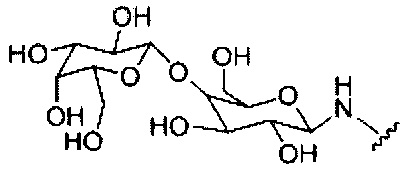
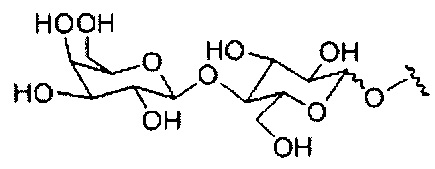
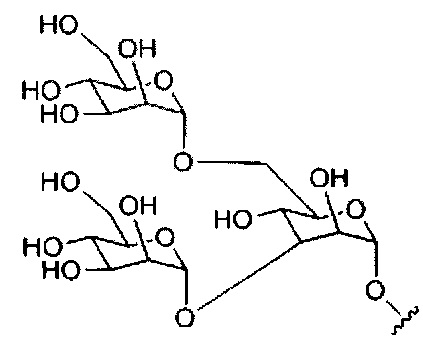
В некоторых вариантах реализации изобретения каждый лиганд имеет следующую структуру:
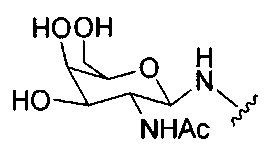
В некоторых вариантах реализации изобретения каждый лиганд имеет следующую структуру:
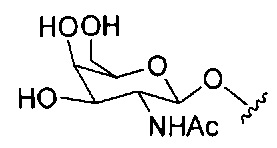
В некоторых вариантах реализации изобретения конъюгирующая группа содержит фрагмент, нацеливающий на клетку.
В некоторых вариантах реализации изобретения конъюгирующая группа содержит фрагмент, нацеливающий на клетку, имеющий следующую структуру:
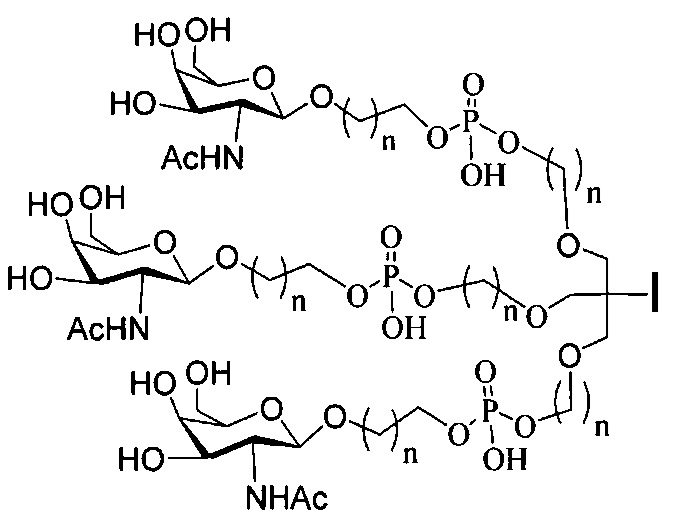
где каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
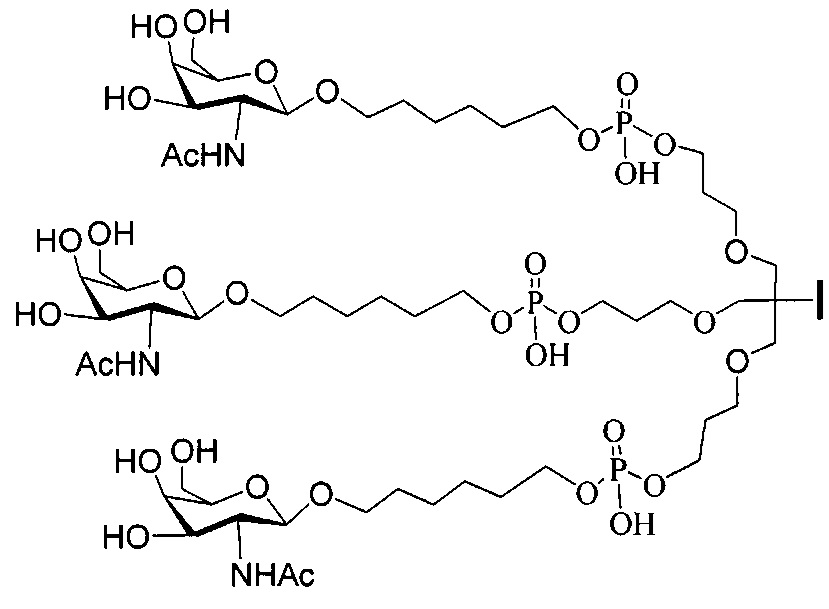
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
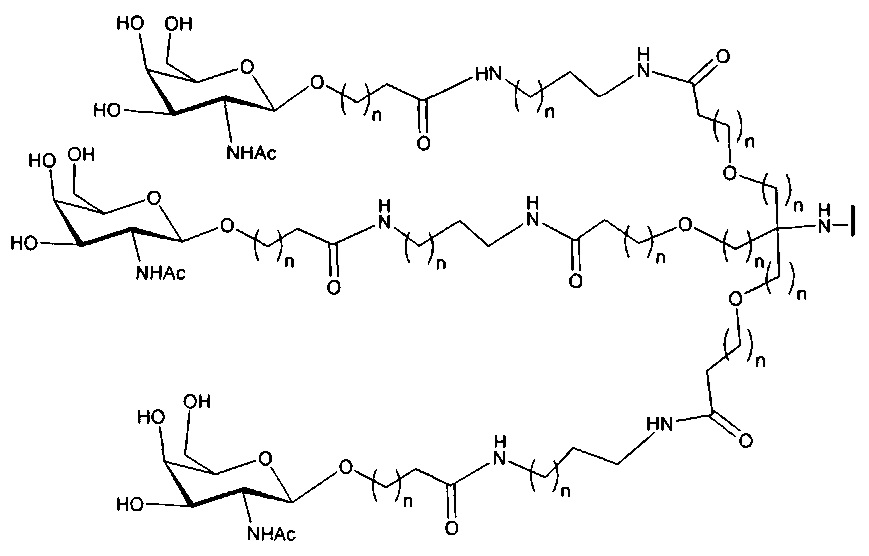
где каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
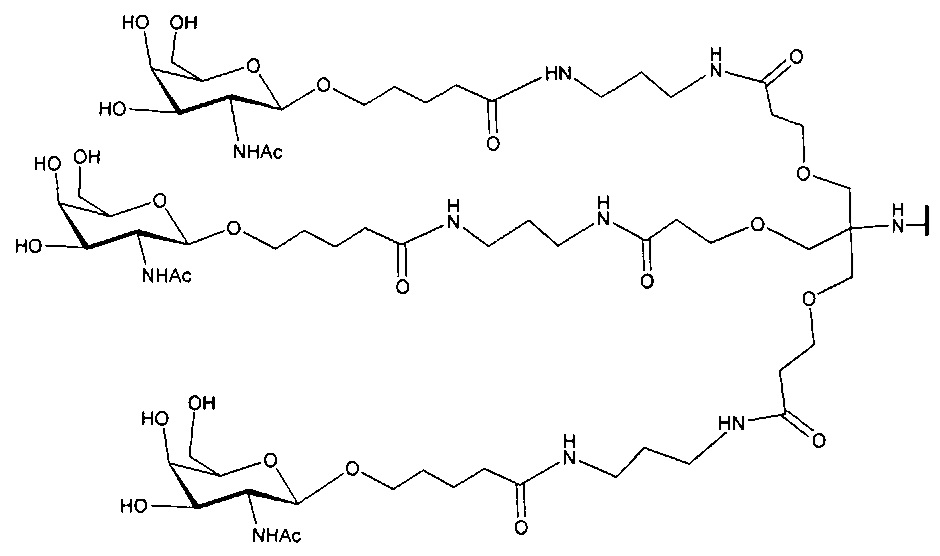
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, содержит:
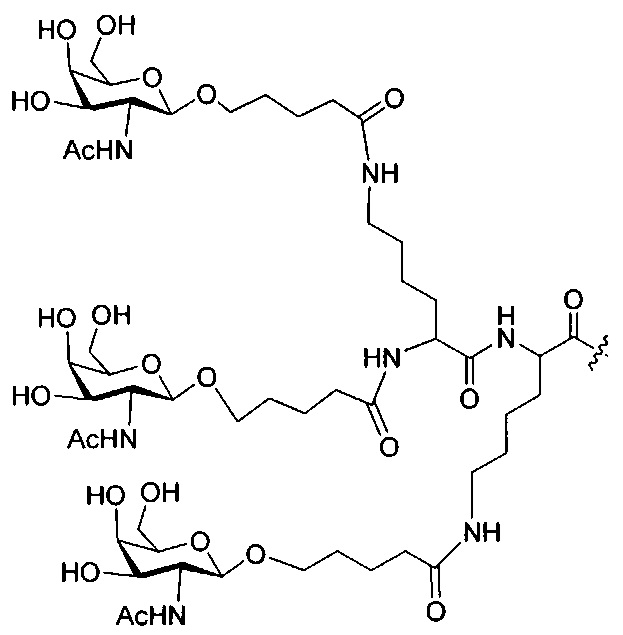
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, содержит:
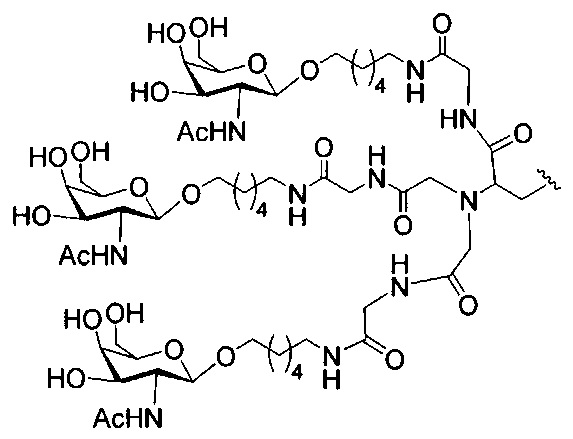
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
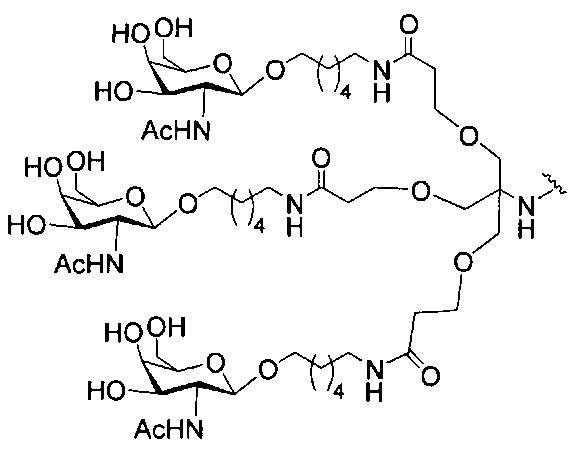
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:

В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, содержит:
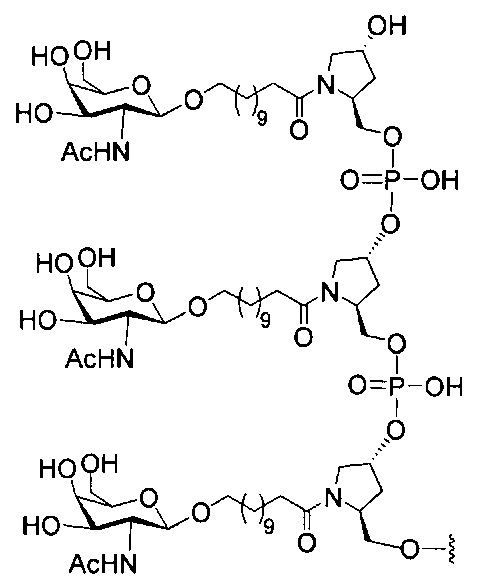
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
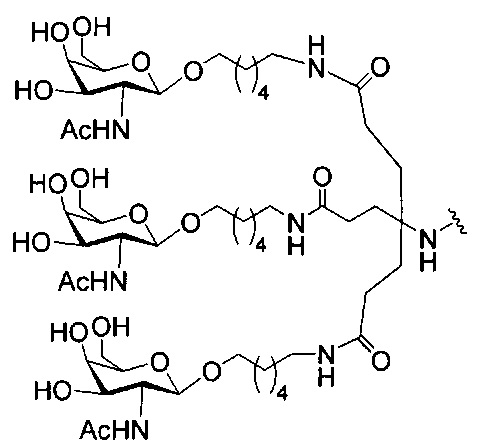
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, содержит:
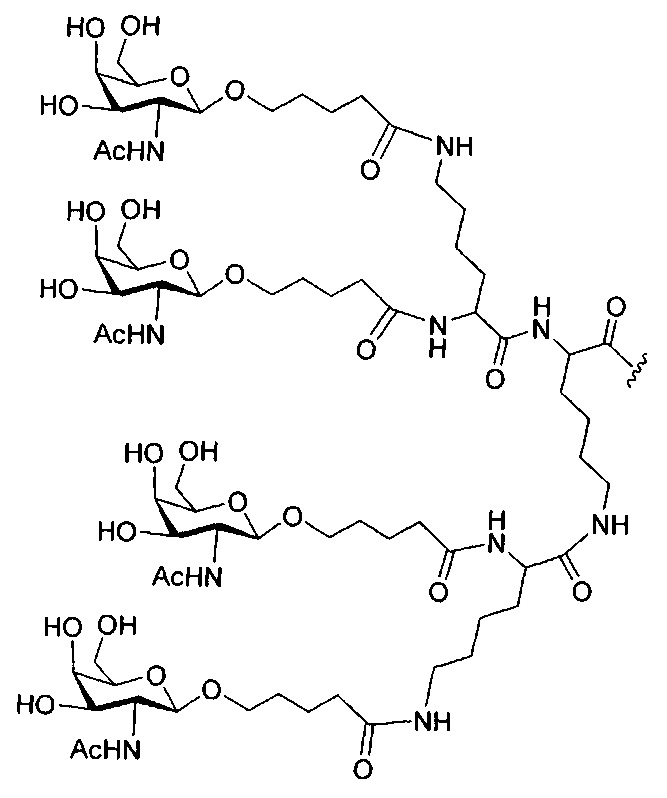
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, содержит:
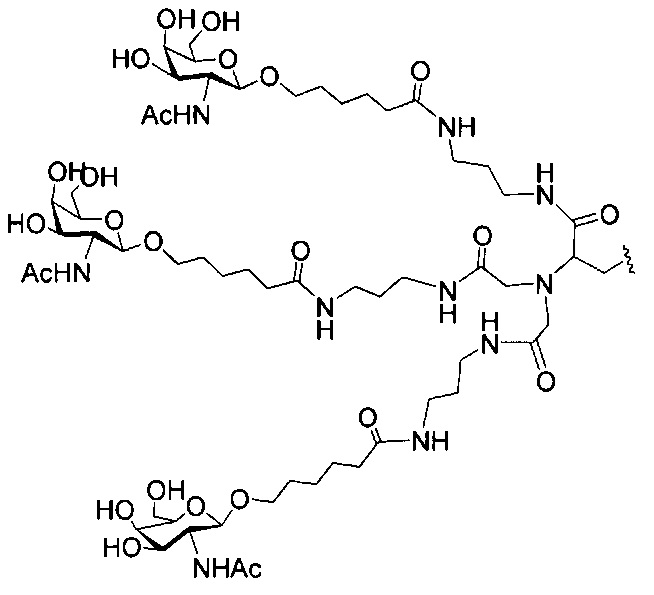
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, содержит:
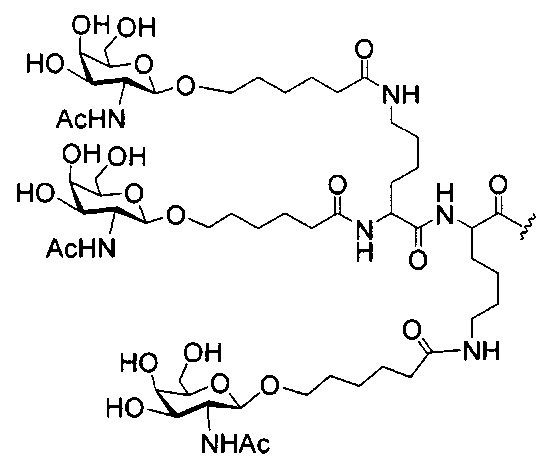
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
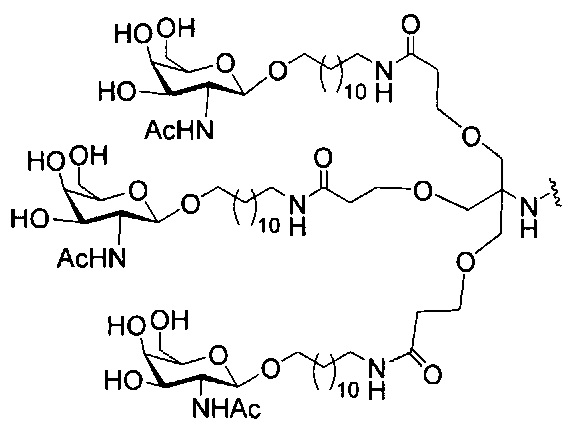
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
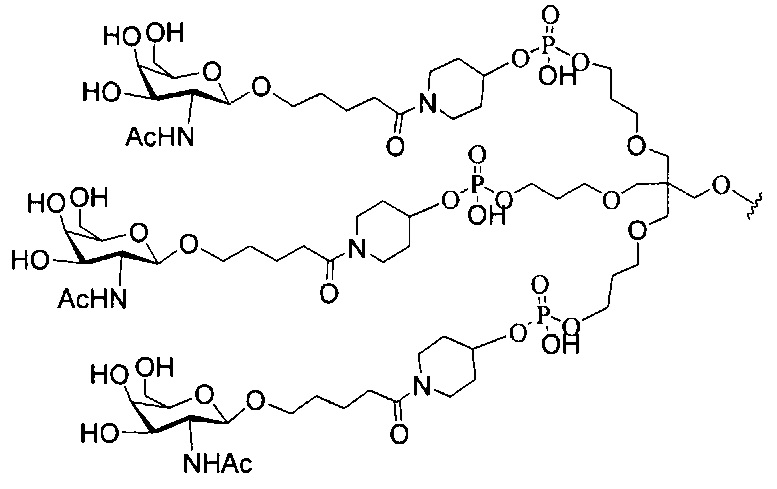
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
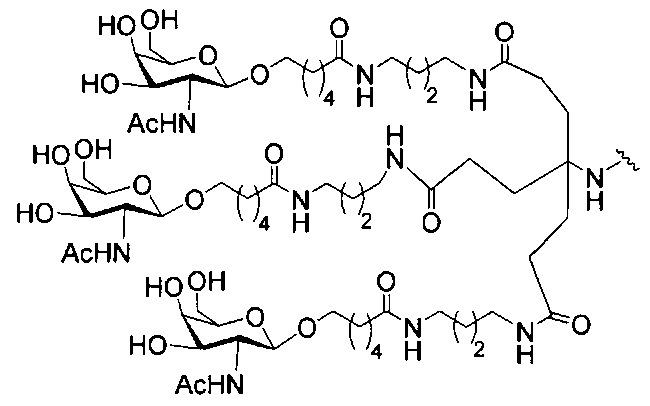
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
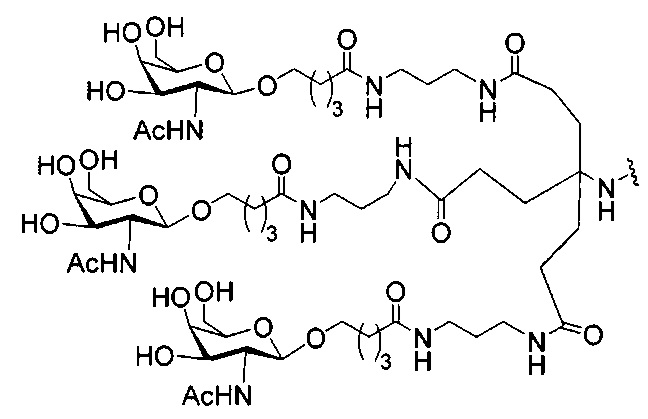
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
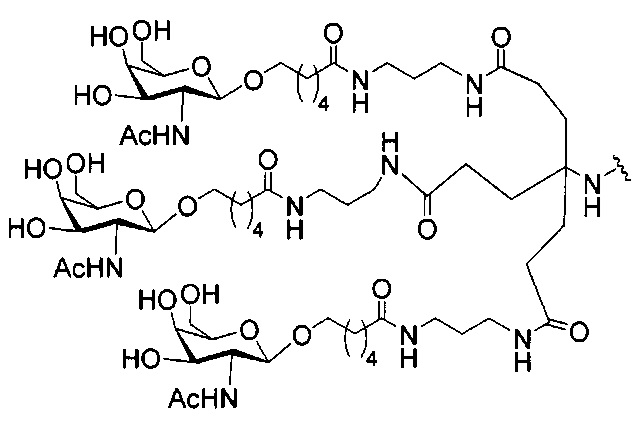
В некоторых вариантах реализации изобретения фрагмент, нацеливающий ли клетку, содержит:
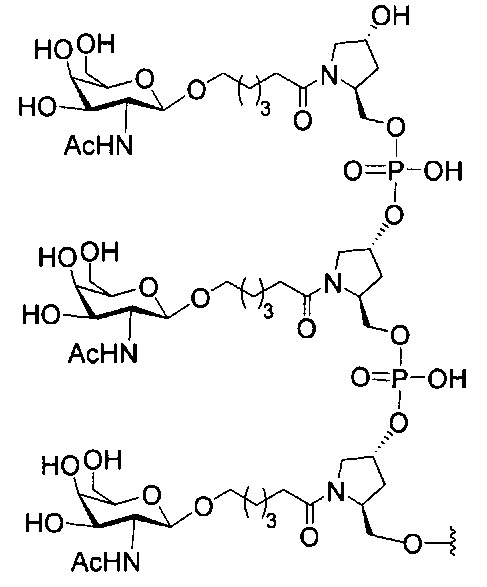
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, содержит:
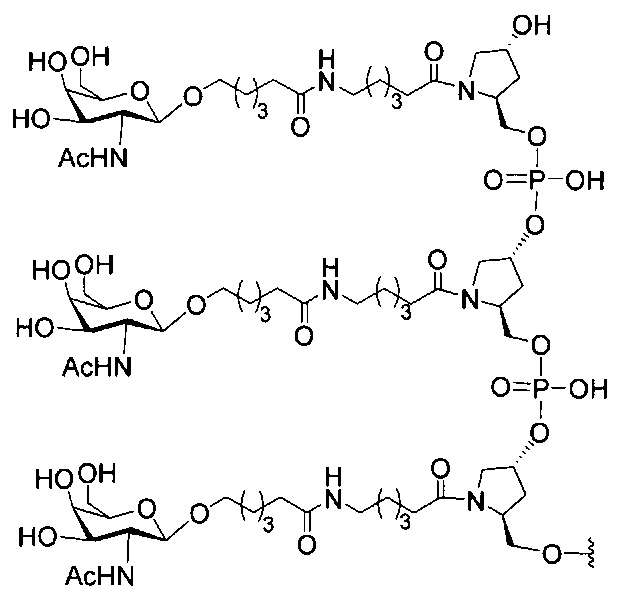
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, содержит:
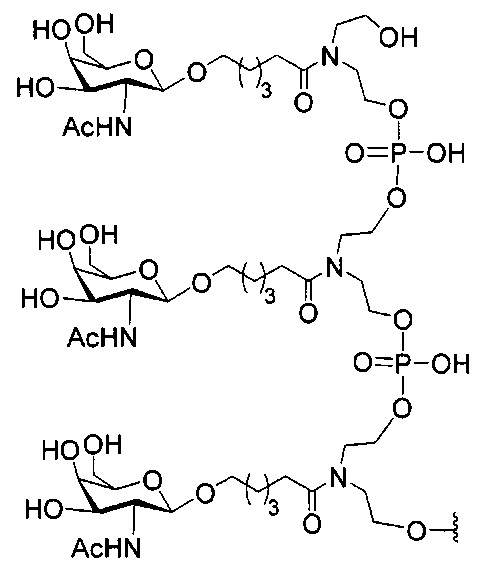
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, содержит:
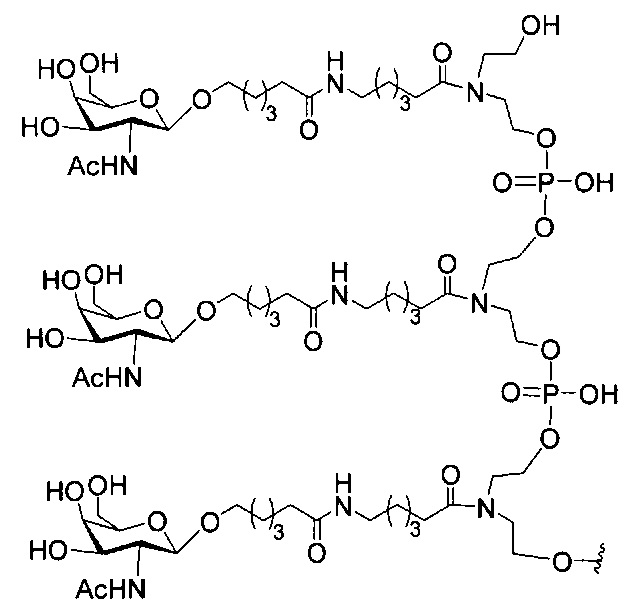
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
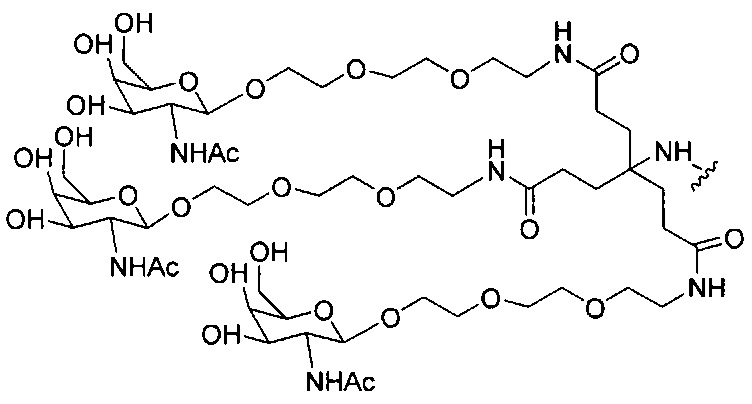
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, содержит:
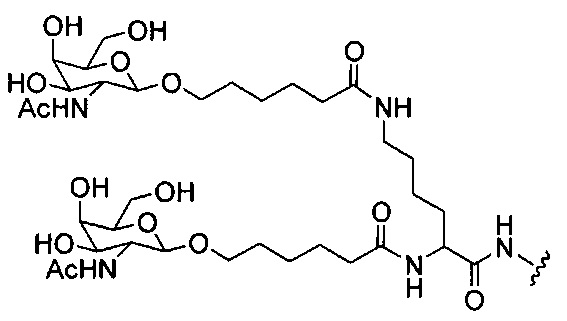
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
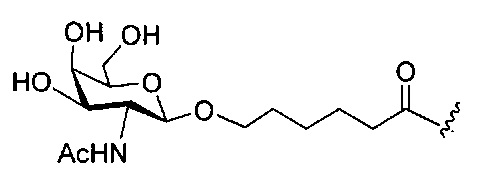
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, содержит:
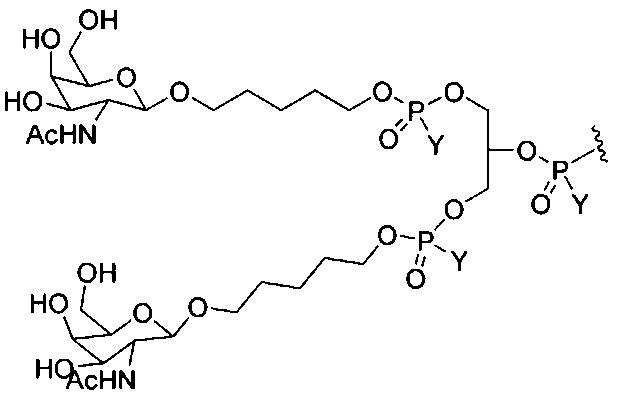
где каждый Y выбран из О, S, замещенного или незамещенного C1-С10 алкила, амино, замещенного амино, азидо, алкенила или алкинила.
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
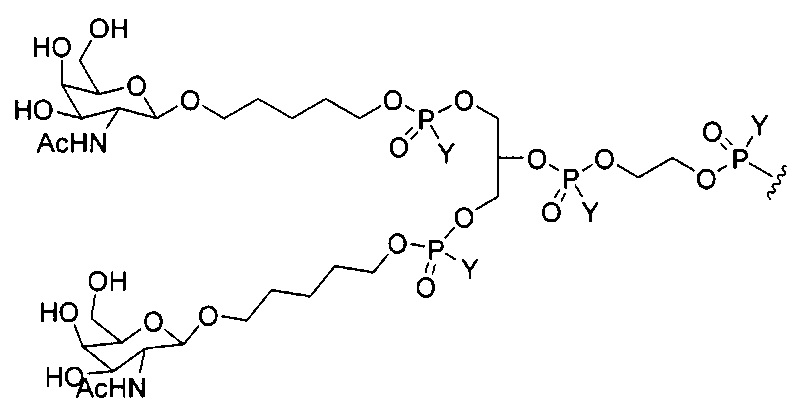
где каждый Y выбран из О, S, замещенного или незамещенного C1-С10 алкила, амино, замещенного амино, азидо, алкенила или алкинила.
В некоторых вариантах реализации изобретения фрагмент, нацеливающий на клетку, имеет следующую структуру:
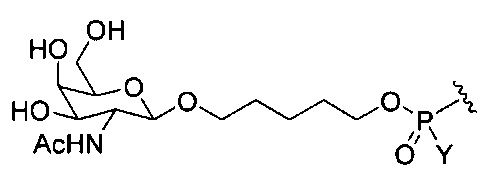
где каждый Y выбран из О, S, замещенного или незамещенного C1-С10 алкила, амино, замещенного амино, азидо, алкенила или алкинила.
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
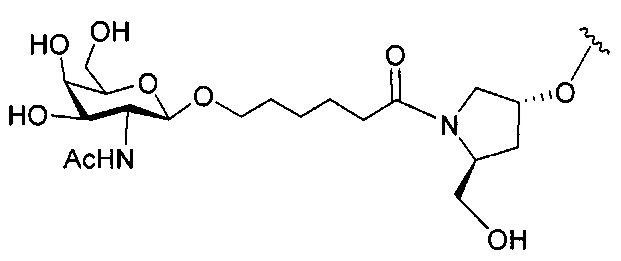
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
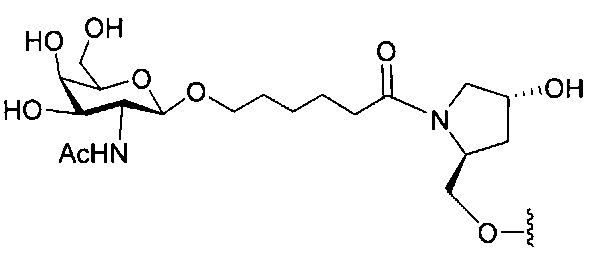
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
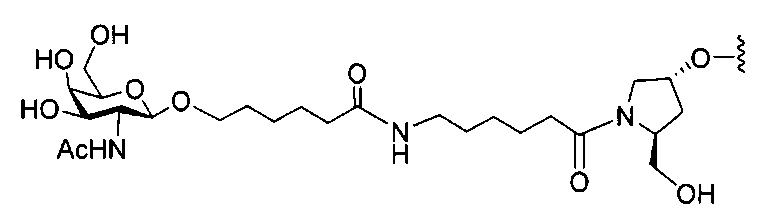
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
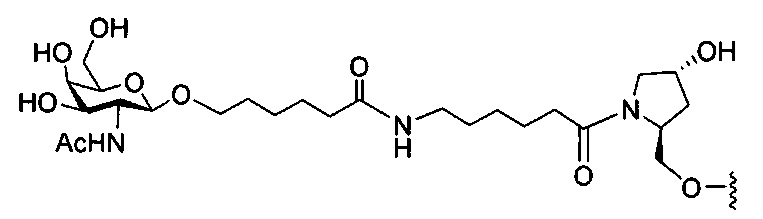
В некоторых вариантах реализации изобретения конъюгирующая группа содержит фрагмент, выбранный из: фосфодиэфира, амида или сложного эфира.
В некоторых вариантах реализации изобретения конъюгирующая группа содержит фосфодиэфирный расщепляемый фрагмент.
В некоторых вариантах реализации изобретения конъюгирующая группа не содержит расщепляемый фрагмент, и при этом конъюгирующая группа содержит тиофосфатную связь между конъюгирующей группой и олигонуклеотидом.
В некоторых вариантах реализации изобретения конъюгирующая группа содержит амидный расщепляемый фрагмент.
В некоторых вариантах реализации изобретения конъюгирующая группа содержит сложноэфирный расщепляемый фрагмент.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
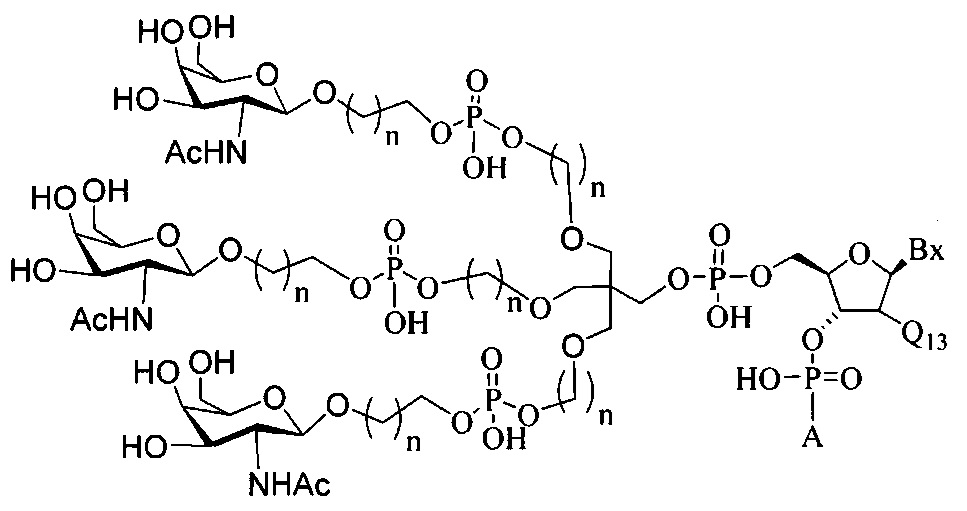
где каждый n независимо равен от 1 до 20;
Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:

где каждый n независимо равен от 1 до 20;
Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
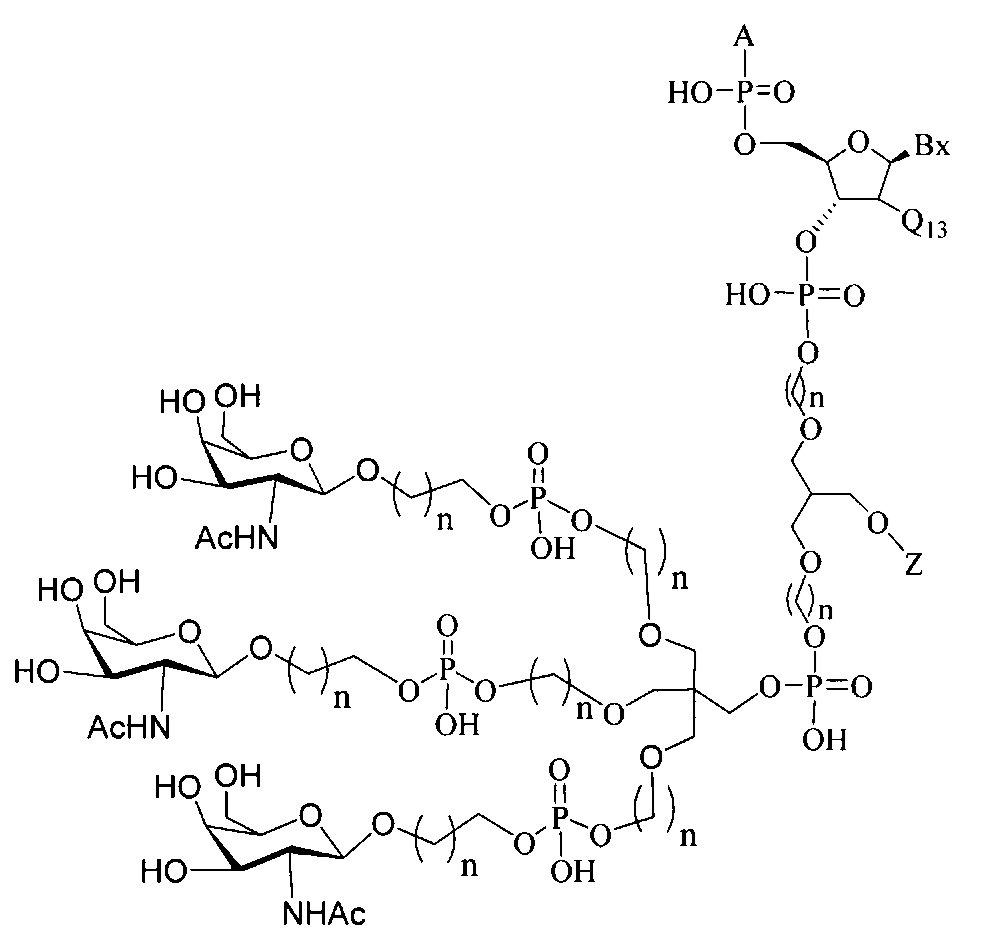
где каждый n независимо равен от 1 до 20;
Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид;
Z представляет собой Н или связанную твердую подложку; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
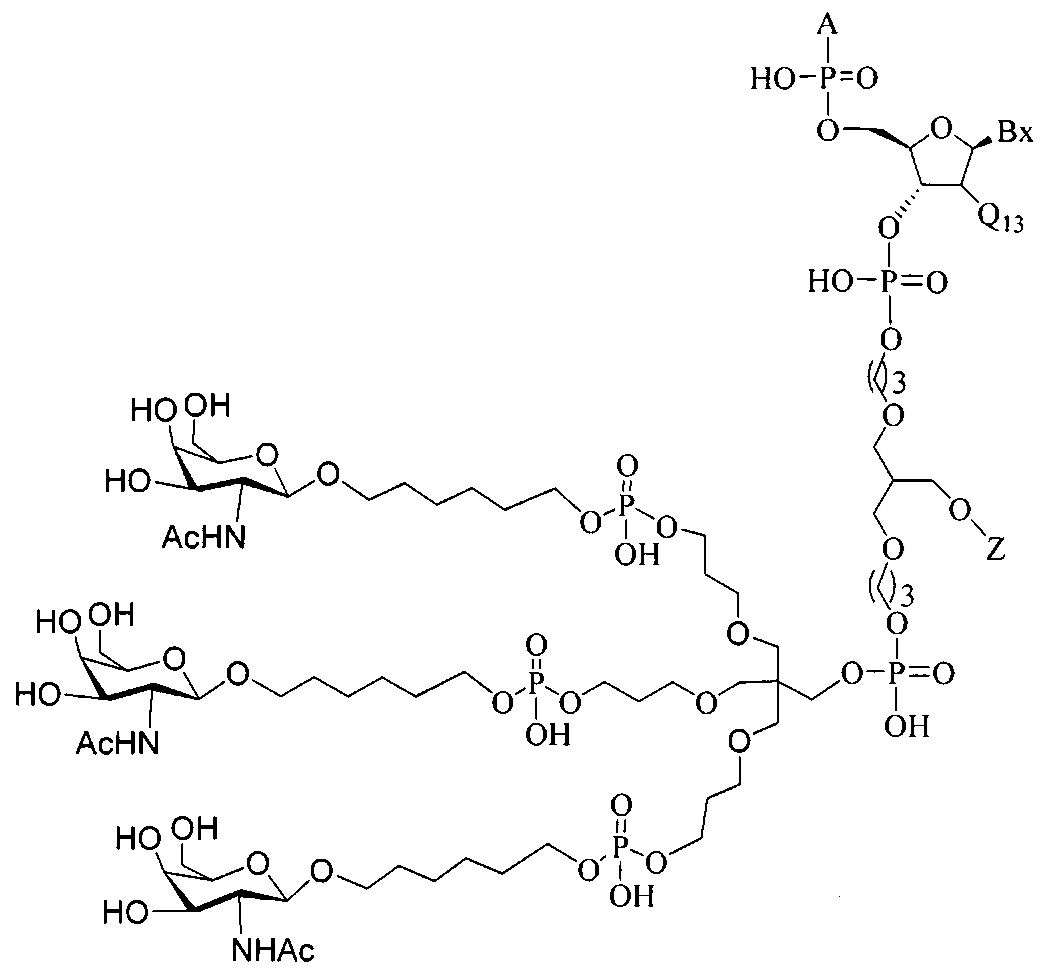
где каждый n независимо равен от 1 до 20;
Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид;
Z представляет собой Н или связанную твердую подложку; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
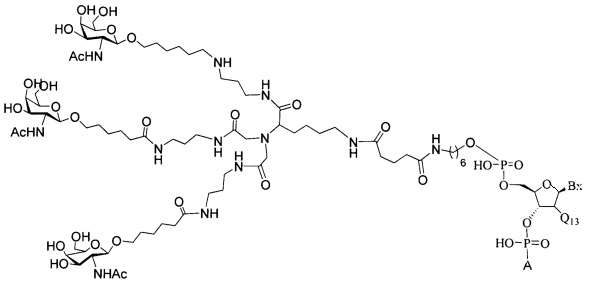
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
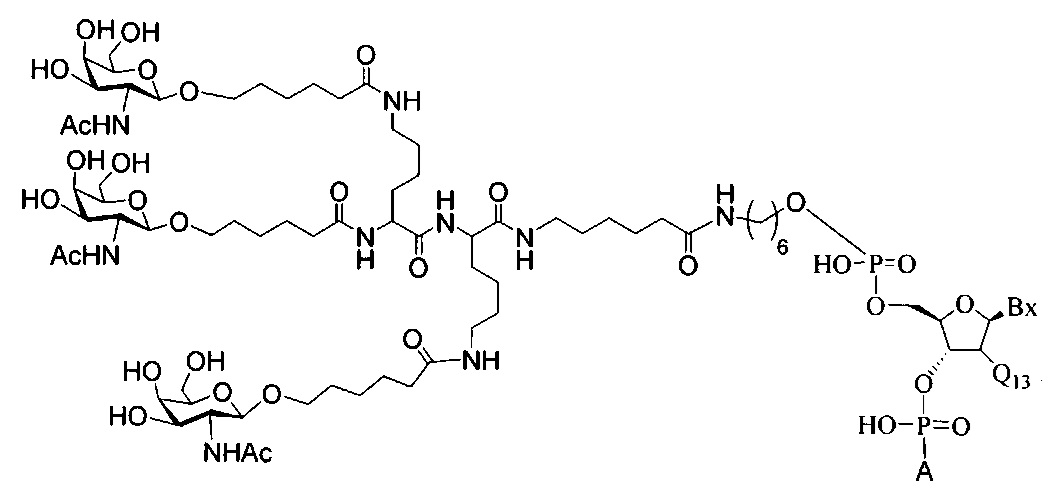
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
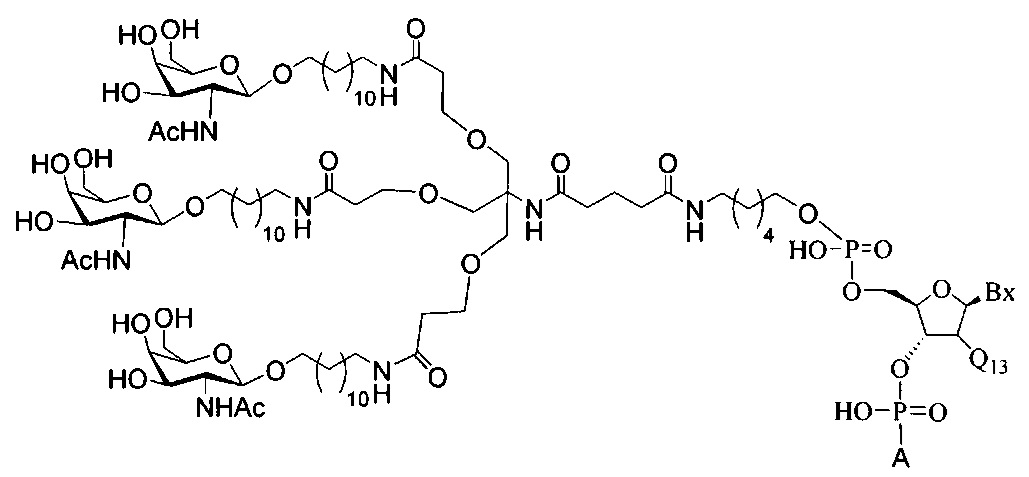
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
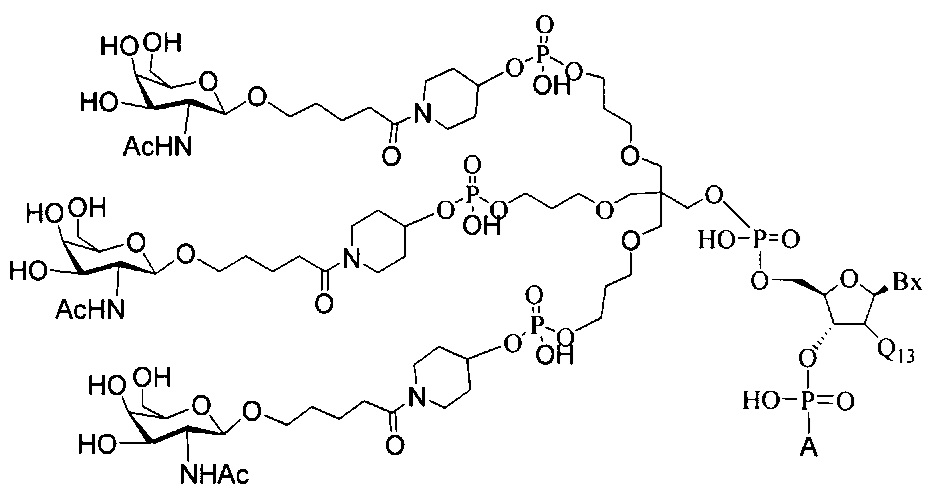
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
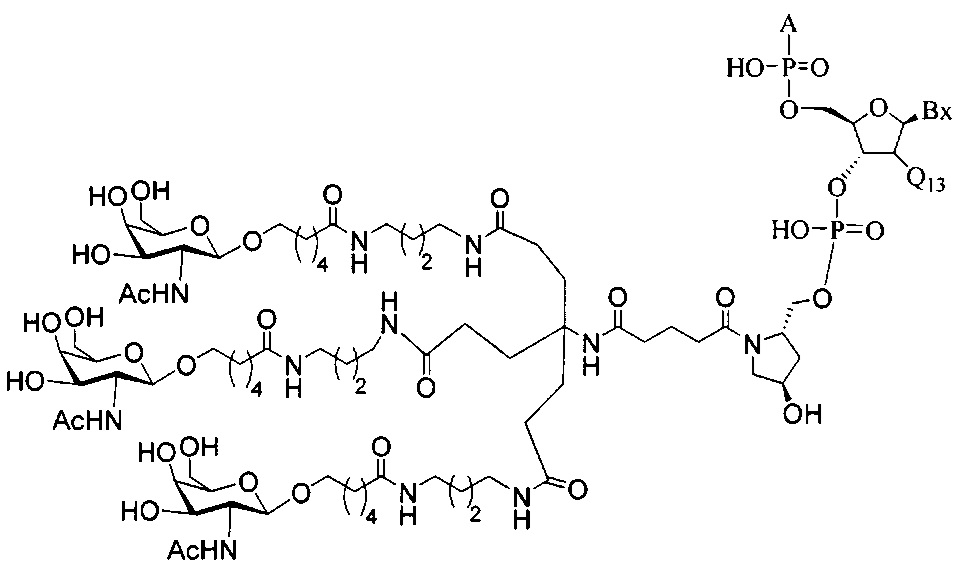
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
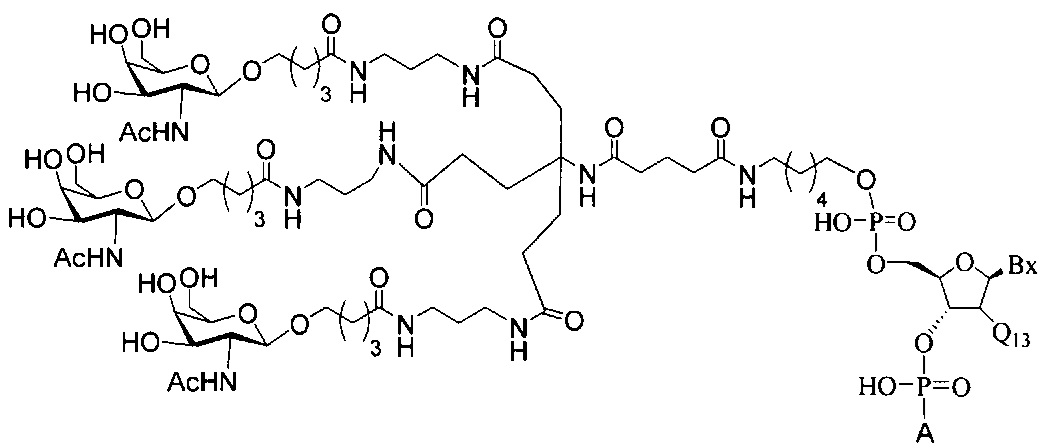
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
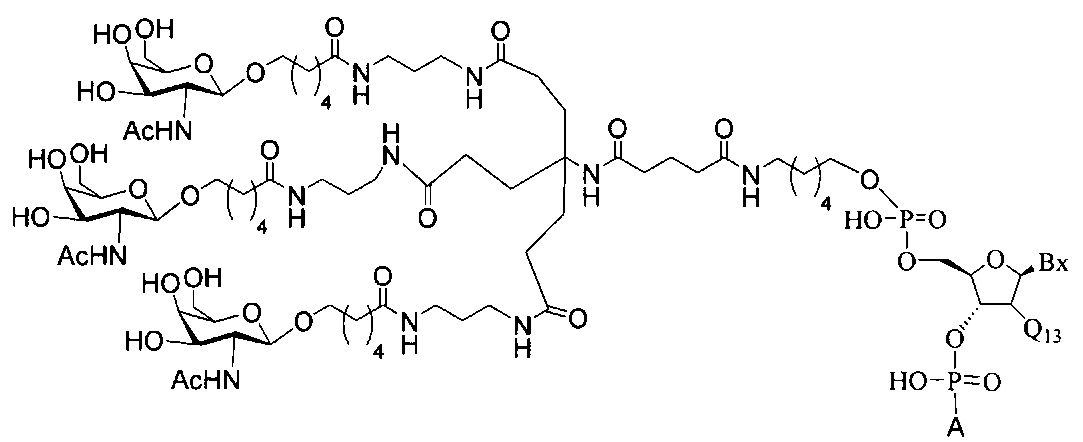
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
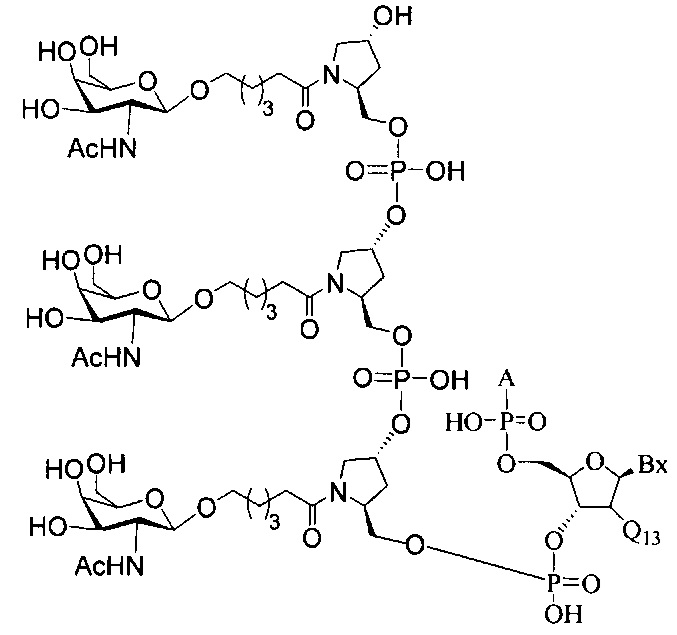
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
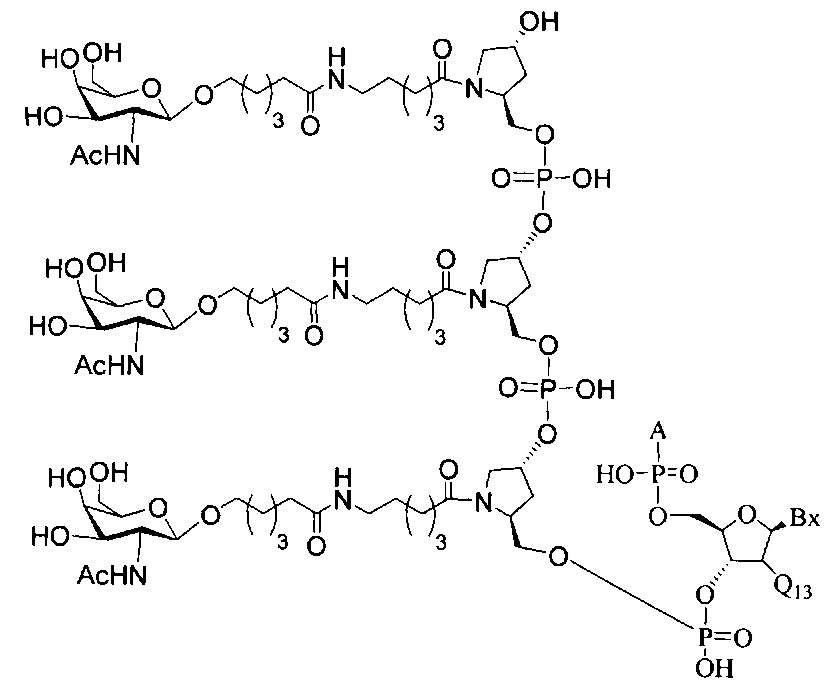
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
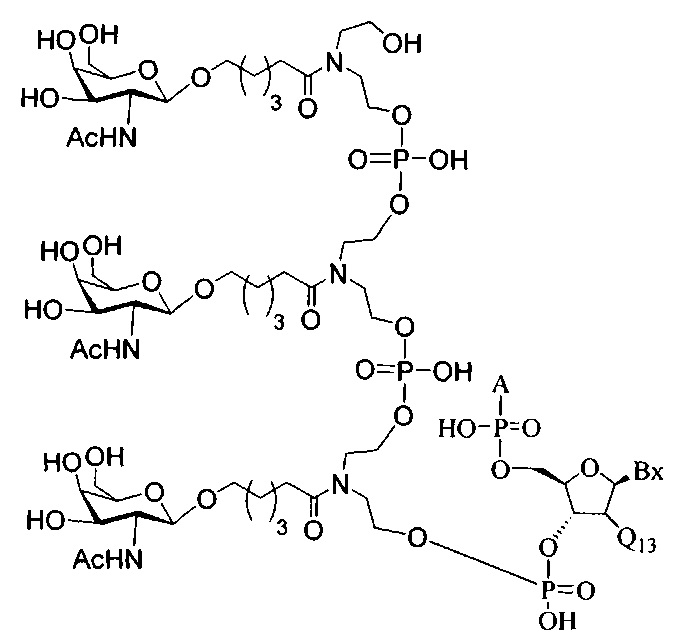
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения соединение имеет следующую структуру:
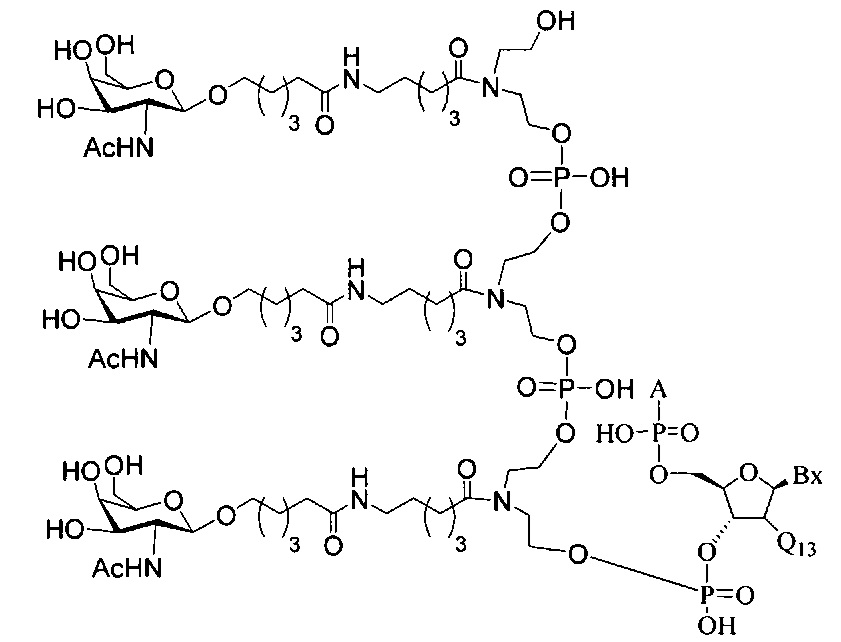
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
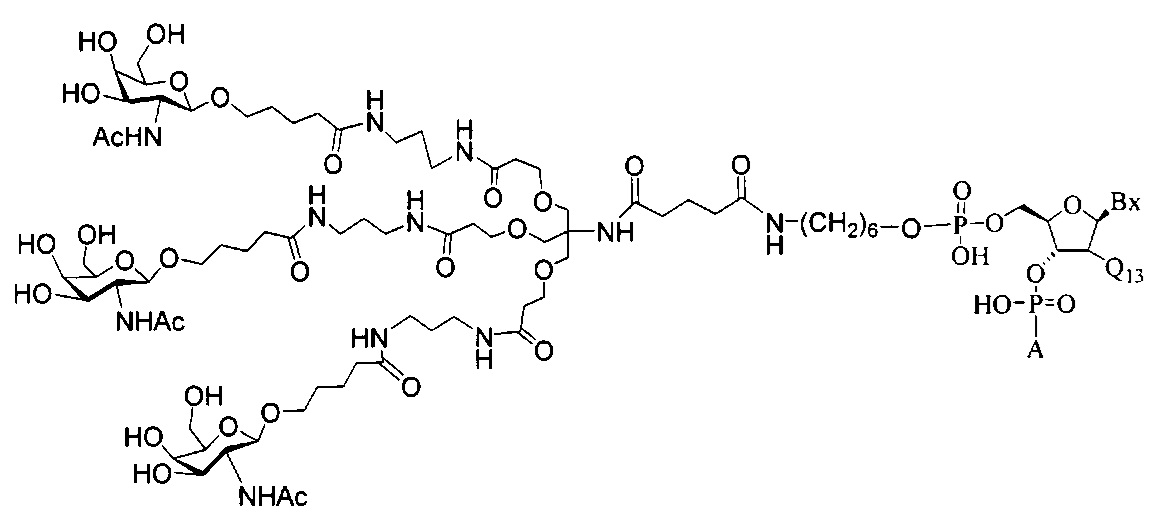
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
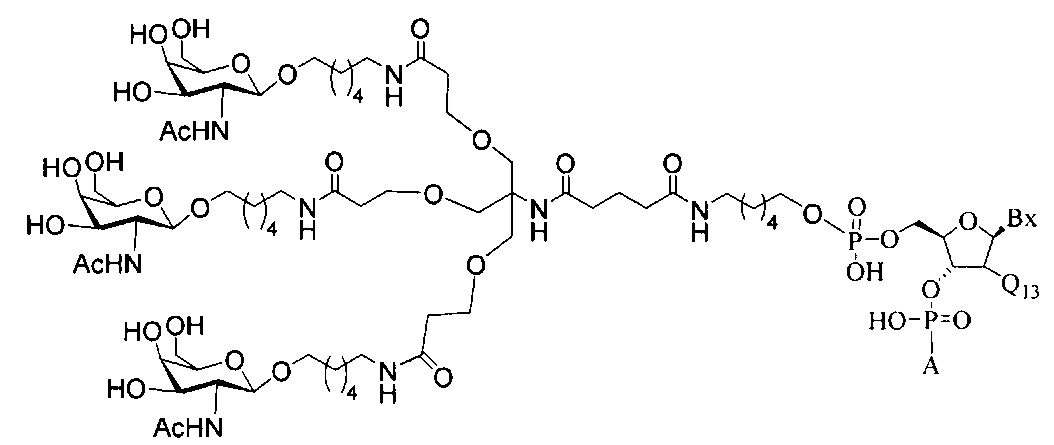
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения конъюгирующая группа содержит:
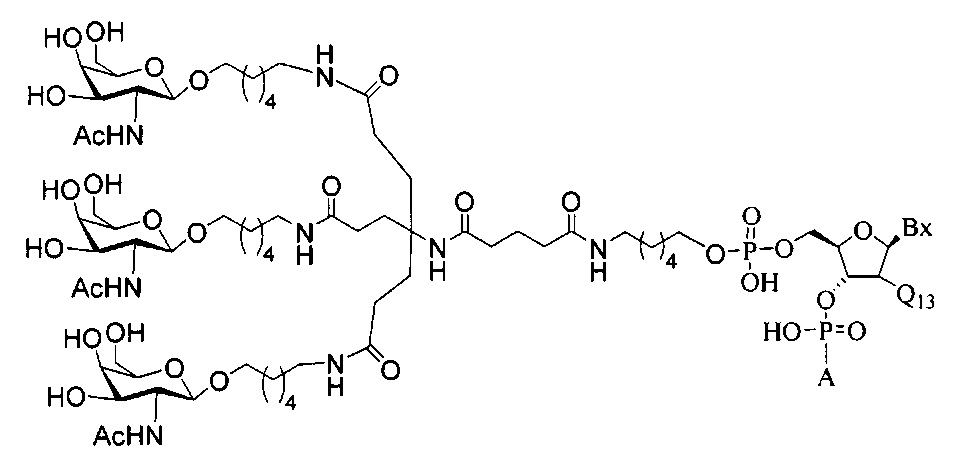
где Q13 представляет собой Н или O(CH2)2-OCH3;
А представляет собой модифицированный олигонуклеотид; и
Вх представляет собой фрагмент гетероциклического основания.
В некоторых вариантах реализации изобретения Вх выбран из аденина, гуанина, тимина, урацила или цитозина, или 5-метилцитозина. В некоторых вариантах реализации изобретения Вх представляет собой аденин. В некоторых вариантах реализации изобретения Вх представляет собой тимин. В некоторых вариантах реализации изобретения Q13 представляет собой O(CH2)2-OCH3. В некоторых вариантах реализации изобретения Q13 представляет собой Н.
В некоторых вариантах реализации настоящего изобретения приведено пролекарство, содержащее композиции или соединения, описанные в настоящем документе.
В некоторых вариантах реализации изобретения соединение приведено в форме соли. В дополнительных вариантах реализации соединение дополнительно содержит фармацевтически приемлемый носитель или разбавитель. В некоторых вариантах реализации изобретения соединение содержит модифицированный олигонуклеотид, нацеленный на АроСIII, и конъюгирующую группу, или его соль, и фармацевтически приемлемый носитель или разбавитель.
В некоторых вариантах реализации изобретения приведены композиции и способы, включающие введение животному конъюгированного антисмыслового соединения или композиции, описанной в настоящем документе. В некоторых вариантах реализации изобретения введение конъюгированного антисмыслового соединения предупреждает, лечит, облегчает или замедляет прогрессирование сердечно-сосудистого, метаболического и/или воспалительного заболевания.
В некоторых вариантах реализации изобретения приведены композиции и способы применил в терапии для лечения заболевания, расстройства или состояния, связанного с АроСIII. В некоторых вариантах реализации изобретения у животного повышены уровни АроСIII. В некоторых вариантах реализации изобретения композиция представляет собой соединение, содержащее АроСIII-специфический ингибитор. В некоторых вариантах реализации АроСIII-специфический ингибитор представляет собой нуклеиновую кислоту. В некоторых вариантах реализации изобретения нуклеиновая кислота представляет собой антисмысловое соединение. В некоторых вариантах реализации изобретения антисмысловое соединение представляет собой модифицированный олигонуклеотид, нацеленный на АроСIII. В некоторых вариантах реализации изобретения антисмысловое соединение представляет собой модифицированный олигонуклеотид, нацеленный на АроСIII, с конъюгирующей группой. В некоторых вариантах реализации изобретения модифицированный олигонуклеотид, нацеленный на АроСIII, с конъюгирующей группой используют при лечении, предупреждении, замедлении прогрессирования, облегчении воспалительного, сердечно-сосудистого и/или метаболического заболевания, расстройства или состояния. В некоторых вариантах реализации изобретения композиции и способы терапии включают введение АроСIII-специфического ингибитора индивидууму, нуждающемуся в этом.
В некоторых вариантах реализации изобретения приведены конъюгированные антисмысловые соединения и композиции, а также способы снижения уровней АроСIII. В некоторых вариантах реализации уровни АроСIII снижают в печени, адипозной ткани, сердце, скелетных мышцах или тонком кишечнике.
В некоторых вариантах реализации изобретения снижение уровней АроСIII в ткани, органе или организме субъекта приводит к повышению уровней HDL. В некоторых вариантах реализации изобретения уровни HDL повышаются по меньшей мере на 90%, по меньшей мере на 80%, по меньшей мере на 70%, по меньшей мере на 60%, по меньшей мере на 50%, по меньшей мере на 45%, по меньшей мере на 40%, по меньшей мере на 35%, по меньшей мере на 30%, по меньшей мере на 25%, по меньшей мере на 20%, по меньшей мере на 15%, по меньшей мере на 10% или по меньшей мере на 5% от исходного уровня HDL.
В некоторых вариантах реализации изобретения снижение уровней АроСIII в ткани, органе или организме субъекта приводит к снижению уровней TG. В некоторых вариантах реализации изобретения уровень триглицеридов у субъекта составляет ≤100 мг/дл, ≥200 мг/дл, ≥300 мг/дл, ≥400 мг/дл, ≥440 мг/дл, ≥500 мг/дл, ≥600 мг/дл, ≥700 мг/дл, ≥800 мг/дл, ≥880 мг/дл, ≥900 мг/дл, ≥1000 мг/дл, ≥1100 мг/дл, ≥1200 мг/дл, ≥1300 мг/дл, ≥1400 мг/дл, ≥1500 мг/дл, ≥1600 мг/дл, ≥1700 мг/дл, ≥1800 мг/дл, ≥1900 мг/дл, ≥2000 мг/дл.
В некоторых вариантах реализации изобретения уровни TG (после приема пищи или натощак) снижаются по меньшей мере на 90%, по меньшей мере на 80%, по меньшей мере на 70%, по меньшей мере на 60%, по меньшей мере на 50%, по меньшей мере на 45%, по меньшей мере на 40%, по меньшей мере на 35%, по меньшей мере на 30%, по меньшей мере на 25%, по меньшей мере на 20%, по меньшей мере на 15%, по меньшей мере на 10%, по меньшей мере на 5% или по меньшей мере на 1% от исходного уровня TG. В некоторых вариантах реализации изобретения уровень TG (после приема пищи или натощак) у субъекта снижается до ≤1900 мг/дл, ≤1800 мг/дл, ≤1700 мг/дл, ≤1600 мг/дл, ≤1500 мг/дл, ≤1400 мг/дл, ≤1300 мг/дл, ≤1200 мг/дл, ≤1100 мг/дл, ≤1000 мг/дл, ≤900 мг/дл, ≤800 мг/дл, ≤750 мг/дл, ≤700 мг/дл, ≤650 мг/дл, ≤600 мг/дл, ≤550 мг/дл, ≤500 мг/дл, ≤450 мг/дл, ≤400 мг/дл, ≤350 мг/дл, ≤300 мг/дл, ≤250 мг/дл, ≤200 мг/дл, ≤150 или ≤100 мг/дл.
В некоторых вариантах реализации изобретения снижение уровней АроСIII в ткани, органе или организме субъекта улучшает соотношение LDL к HDL или соотношение TG к HDL.
В некоторых вариантах реализации снижение уровней АроСIII в ткани, органе или организме субъекта приводит к улучшению восприимчивости инсулина.
В некоторых вариантах реализации снижение уровней АроСIII в ткани, органе или организме субъекта приводит к повышению клиренса хиломикрона.
В некоторых вариантах реализации изобретения предложены композиции и способы снижения экспрессии мРНК или белка АроСIII у животного, включающие введение указанному животному конъюгированного антисмыслового соединения или композиции, описанной в настоящем документе, для снижения экспрессии мРНК или белка АроСIII у животного.
В некоторых вариантах реализации изобретения приведены конъюгированные антисмысловые соединения и композиции, а также способы предупреждения, лечение, отсрочки, замедления прогрессирования и/или улучшения заболеваний, расстройств и состояний, связанных с АроСIII, у субъекта, нуждающегося в этом. В некоторых вариантах реализации такие заболевания, расстройства и состояния включают воспалительные, сердечно-сосудистые и/или метаболические заболевания, расстройства и состояния. Некоторые такие сердечно-сосудистые заболевания, расстройства или состояния включают, но не ограничиваются ими, хиломикронемию, гипертриглицеридемию, стеноз аортального отверстия, аневризму (например, аневризма брюшной аорты), стенокардию, аритмию, атеросклероз, церебро-сосудистое заболевание, коронарно-артериальное заболевание, коронарную болезнь сердца, дислипидемию, гиперхолестеринемию, гиперлипидемию, гипертонию, инфаркт миокарда, болезнь периферических сосудов (например, болезнь периферической артерии, окклюзионная болезнь периферической артерии), дислипидемию Фредриксона типа I, синдром наследственной хиломикронемии (FCS), дефицит LPL, окклюзию сосудов сетчатки или инсульт. Некоторые такие метаболические заболевания, расстройства или состояния включают, но не ограничиваются ими, гипергликемию, преддиабет, диабет (типа I и типа II), ожирение, инсулинорезистентность, метаболический синдром и диабетическую дислипидемию. Некоторые такие воспалительные заболевания, расстройства или состояния включают, но не ограничиваются ими, панкреатит, стеноз аортального отверстия, коронарно-артериальную болезнь (CAD), болезнь Альцгеймера и тромбоэмболические заболевания, расстройства или состояния. Некоторые тромбоэмболические заболевания, расстройства или состояния включают, но не ограничиваются ими, инсульт, тромбоз (например, венозный тромбоэмболизм), инфаркт миокарда и болезнь периферических сосудов. В некоторых вариантах реализации изобретения приведены конъюгированные антисмысловые соединения и композиции, а также способы предупреждения, лечения, отсрочки, замедления прогрессирования и/или улучшения гипертриглицеридемии. В некоторых вариантах реализации изобретения приведены конъюгированные антисмысловые соединения и композиции, а также способы предупреждения, лечения, отсрочки, замедления прогрессирования и/или улучшения хиломикронемии. В некоторых вариантах реализации изобретения приведены конъюгированные антисмысловые соединения и композиции, а также способы предупреждения, лечения, отсрочки, замедления прогрессирования и/или улучшения панкреатита.
В некоторых вариантах реализации изобретения приведен способ уменьшения по меньшей мере одного симптома сердечно-сосудистого заболевания, расстройства или состояния. В некоторых вариантах реализации изобретения симптомы включают, но не ограничиваются ими, стенокардии, боль в груди, одышку, учащенное сердцебиение, слабость, головокружение, тошноту, потоотделение, тахикардию, брадикардию, аритмию, мерцательную аритмию, опухание нижних конечностей, цианоз, усталость, обморок, онемение лица, онемение конечностей, хромоту или судороги мышц, вздутие живота и лихорадку. В некоторых вариантах реализации изобретения симптомы метаболического заболевания, расстройства или состояния включают, но не ограничиваются ими, частое мочеиспускание, необычную жажду, сильный голод, необычную потерю веса, сильную усталость, раздражительность, частые инфекции, расплывчатое зрение, порезы/ушибы, которые долго не заживают, покалывание/онемение рук/ног и рецидив кожных, слизистых или мочеполовых инфекций. В некоторых вариантах реализации изобретения приведен способ ослабления по меньшей мере одного симптома гипертриглицеридемии. В некоторых вариантах реализации изобретения приведен способ ослабления по меньшей мере одного симптома хиломикронемии. В некоторых вариантах реализации изобретения приведен способ ослабления по меньшей мере одного симптома панкреатита.
В некоторых вариантах реализации изобретения модулирование экспрессии АроСIII происходит в клетке, ткани или органе. В некоторых вариантах реализации модулирование происходит в клетке, ткани или органе животного. В некоторых вариантах реализации модулирование представляет собой снижение уровня мРНК АроСIII. В некоторых вариантах реализации изобретения модулирование представляет собой снижение уровня белка АроСIII. В некоторых вариантах реализации изобретения снижаются и уровни мРНК, и уровни белка АроСIII. Такое снижение может происходить в зависимости от времени или в зависимости от дозы.
В некоторых вариантах реализации изобретения субъект или животное представляет собой человека.
В некоторых вариантах реализации изобретения соединение вводят парентерально. В дополнительных вариантах реализации изобретения парентеральное введение является подкожным.
В некоторых вариантах реализации изобретения конъюгированное антисмысловое соединение или композицию вводят вместе со вторым агентом или терапией. В некоторых вариантах реализации изобретения конъюгированное антисмысловое соединение или композицию и второй агент вводят параллельно.
В некоторых вариантах реализации изобретения второй агент представляет собой агент, понижающий уровень глюкозы. В некоторых вариантах реализации изобретения второй агент представляет собой агент, понижающий уровень LDL, TG или холестерина. В некоторых вариантах реализации изобретения второй агент представляет собой противовоспалительный агент. В некоторых вариантах реализации изобретения второй агент представляет собой противовоспалительный агент. В некоторых вариантах реализации изобретения второй агент может быть, но не ограничиваясь этим, нестероидным противовоспалительным лекарством (NSAID, например, аспирин), ниацином (например, ниаспан), никотиновой кислотой, ингибитором ароВ (например, мипомерсен), ингибитором СЕТР (например, анасетрапиб), ингибитором аро(а), аналогом гормона щитовиной железы (например, эпротиром), ингибитором редуктазы HMG-CoA (например, статин), фибратом (например, гемфиброзил) и ингибитором микросомального белка-переносчика триглицеридов (например, ломитапид). Агенты или терапии могут быть введены совместно или параллельно. Агенты или терапии могут быть введены последовательно или позже.
В некоторых вариантах реализации изобретения приведено применение композиций и конъюгированных антисмысловых соединений, описанных в настоящем документе, нацеленных на АроСIII для снижения уровней АроСIII у животного. В некоторых вариантах реализации приведено применение соединения, нацеленного на АроСIII, для снижения уровней АроСIII у животного. В некоторых вариантах реализации изобретения приведено применение соединения, нацеленного на АроСIII, для повышения уровней HDL у животного. В некоторых вариантах реализации изобретения приведено применение соединения, нацеленного на АроСIII, для повышения клиренса хиломикрона у животного. В некоторых вариантах реализации изобретения приведено применение соединений, нацеленных на АроСIII, для лечения, предупреждения или улучшения заболевания, расстройства или состояния, связанного с АроСIII. В некоторых вариантах реализации изобретения приведено применение соединения, нацеленного на АроСIII, для лечения, предупреждения, улучшения гипертриглицеридемии. В некоторых вариантах реализации изобретения приведено применение соединения, нацеленного на АроСIII, для лечения, предупреждения или улучшения хиломикронемии (например, синдром наследственной хиломикронемии (FCS) и/или недостаточность ЛПЛ (LPLD)). В некоторых вариантах реализации изобретения приведено применение соединения, нацеленного на АроСIII, для лечения, предупреждения или улучшения панкреатита.
В некоторых вариантах реализации изобретения приведено применение композиций и конъюгированных антисмысловых соединений, описанных в настоящем документе, нацеленных на АроСIII, для получения лекарственного средства для снижения уровней АроСIII у животного. В некоторых вариантах реализации изобретения приведено применение соединений для получения лекарственного средства для лечения, предупреждения или улучшения заболевания, расстройства или состояния, связанного с АроСIII.
В некоторых вариантах реализации изобретения приведено применение композиций и конъюгированных антисмысловых соединений, описанных в настоящем документе, в производстве лекарственного средства для лечения, улучшения, отсрочки пли предупреждения одного или более заболеваний, связанных с АроСIII.
В некоторых вариантах реализации приведен набор для лечения, предупреждения или улучшения заболевания, расстройства или состояния, описанного в настоящем документе, который содержит: (i) АроСIII-специфический ингибитор, описанный в настоящем документе; и необязательно (ii) второй агент или терапию, описанную в настоящем документе.
Набор согласно настоящему изобретению может дополнительно содержать инструкции по применению набора для лечения, предупреждения, улучшения заболевания, расстройства или состояния, описанного в настоящем документе, при помощи комплексной терапии, описанной в настоящем документе.
В. Некоторые соединения
В некоторых вариантах реализации настоящего изобретения приведены конъюгированные антисмысловые соединения, содержащие антисмысловые олигонуклеотиды и конъюгат.
а. Некоторые антисмысловые олигонуклеотиды
В некоторых вариантах реализации настоящего изобретения приведены антисмысловые олигонуклеотиды. Такие антисмысловые олигонуклеотиды содержат связанные нуклеозиды, и каждый нуклеозид содержит сахарный фрагмент к азотистое основание. Структура таких антисмысловых олигонуклеотидов может быть рассмотрена с точки зрения химических особенностей (например, модификаций и характерных участков модификаций) и последовательности азотистых оснований (например, последовательность антисмыслового олигонуклеотида, сущность и последовательность целевой нуклеиновой кислоты).
i. Некоторые химические особенности
В некоторых вариантах реализации антисмысловый олигонуклеотид содержит одну или более модификаций. В некоторых таких вариантах реализации антисмысловые олигонуклеотиды содержат один или более модифицированных нуклеозидов и/или модифицированных межнуклеозидных связей. В некоторых вариантах реализации модифицированные нуклеозиды содержат модифицированный сахарный фрагмент и/или модифицированное азотистое основание.
1. Некоторые сахарные фрагменты
В некоторых вариантах реализации соединения настоящего описания содержат один или более модифицированных нуклеозидов, содержащих модифицированный сахарный фрагмент. Такие соединения, содержащие один или более модифицированных по сахару нуклеозидов, могут обладать заданными свойствами, такими как улучшенная стабильность к нуклеазе или увеличенная связывающая аффинность к целевой нуклеиновой кислоте, па сравнению с олигонуклеотидом, содержащим только нуклеозиды, которые содержат природные сахарные фрагменты. В некоторых вариантах реализации модифицированные сахарные фрагменты представляют собой замещенные сахарные фрагменты. В некоторых вариантах реализации модифицированные сахарные фрагменты представляют собой заменители сахара. Такие заменители сахара могут содержать одно или более замещений, соответствующих замещениям замещенных сахарных фрагментов.
В некоторых вариантах реализации модифицированные сахарные фрагменты представляют собой замещенные сахарные фрагменты, содержащие один или более немостиковых сахарных заместителей, включая, но не ограничиваясь этим, заместители в 2' и/или 5'-положениях. Примеры заместителей сахара, подходящих для 2'-положения, включают, но не ограничиваются ими: 2'-F, 2'-OCH3 («ОМе» или «О-метил») и 2'-O(CH2)2OCH3 («МОЕ»). В некоторых вариантах реализации заместитель сахара в 2'-положении выбран из аллила, амино, азидо, тио, О-аллила, O-C1-С10 алкила, O-C1-C10 замещенного алкила; OCF3, O(CH2)2SCH3, O(CH2)2-O-N(Rm)(Rn) и O-CH2-C(=O)-N(Rm)(Rn), где каждый Rm и Rn независимо представляет собой Н или замещенный или незамещенный C1-С10 алкил. Примеры заместителей сахара в 5'-положении включают, но не ограничиваются ими: 5'-метил (R или S), 5'-винил и 5'-метокси. В некоторых вариантах реализации замещенные сахара содержат более одного немостикового сахарного заместителя, например, 2'-F-5'-метил-сахарные фрагменты (см., например, Международную заявку РСТ WO 2008/101157, где приведены дополнительные 5', 2'-бис-замещенные сахарные фрагменты и нуклеозиды).
Нуклеозиды, содержащие 2'-замещенные сахарные фрагменты, упоминаются как 2'-замещенные нуклеозиды. В некоторых вариантах реализации 2'-замещенный нуклеозид содержит 2'-группу заместителя, выбранную из галогена, аллила, амино, азидо, SH, CN, OCN, CF3, OCF3, О, S или N(Rm)-алкила; О, S или N(Rm)-алкенила; О, S или N(Rm)-алкинила; О-алкиленил-О-алкила, алкинила, алкарила, аралкила, О-алкарила, О-аралкила; O(CH2)2SCH3, O-(CH2)2-O-N(Rm)(Rn) или O-CH2-C(=O)-N(Rm)(Rn), где каждый Rm и Rn независимо представляет собой Н, аминозащитную группу или замещенный или незамещенный C1-С10 алкил. Эти 2'-группы заместителей могут быть дополнительно замещены одной или более группами заместителей, независимо выбранными Из гидроксила, амино, алкокси, карбокси, бензила, фенила, нитро (NO2), тиола, тиоалкокси (S-алкила), галогена, алкила, арила, алкенила и алкинила.
В некоторых вариантах реализации 2'-замещенный нуклеозид содержит 2'-группу заместителя, выбранную из F, NH2, N3, OCF3, О-CH3, O(CH2)3NH2, CH2-СН=CH2, O-CH2-СН=CH2, OCH2CH2OCH3, O(CH2)2SCH3, O-(CH2)2-O-N(Rm)(Rn), O(CH2)2O(CH2)2N(CH3)2 и N-замещенного ацетамида (O-CH2-C(=O)-N(Rm)(Rn), где каждый Rm и Rn независимо представляет собой Н, аминозащитную группу или замещенный или незамещенный C1-С10 алкил.
В некоторых вариантах реализации 2'-замещенный нуклеозид содержит сахарный фрагмент, содержащий 2'-группу заместителя, выбранную из F, OCF3, O-CH3, OCH2CH2OCH3, O(CH2)2SCH3, O-(CH2)2-O-N(CH3)2, -O(CH2)2O(CH2)2N(CH3)2 и O-CH2-C(=O)-N(H)CH3.
В некоторых вариантах реализации 2'-замещенный нуклеозид содержит сахарный фрагмент, содержащий 2'-группу заместителя, выбранную из F, О-CH3 и OCH2CH2OCH3.
Некоторые модифицированные сахарные фрагменты содержат мостиковый сахарный заместитель, который образует второе кольцо, что приводит к получению бициклического сахарного фрагмента. В некоторых таких вариантах реализации бициклический сахарный фрагмент содержит мостик между 4' и 2' атомами фуранозного кольца. Примеры таких 4'-2' сахарных заместителей включают, но не ограничиваются ими: -[C(Ra)(Rb)]n-, -[C(Ra)(Rb)]n-O-, -C(RaRb)-N(R)-O- или -C(RaRb)-O-N(R)-; 4'-CH2-2', 4'-(CH2)2-2', 4'-(CH2)3-2', 4'-(CH2)-O-2' (LNA); 4'-(CH2)-S-2'; 4'-(CH2)2-O-2' (ENA); 4'-СН(CH3)-O-2' (cEt) и 4'-СН(CH2OCH3)-O-2', и его аналоги (см., например, патент США 7399845, выданный 15 июля 2008 года); 4'-С(СН3)(СН3)-O-2' и его аналоги (см., например, WO 2009/006478, опубликованный 8 января 2009 года); 4'-CH2-N(OCH3)-2' и его аналоги (см., например, WO 2008/150729, опубликованный 11 декабря 2008 года); 4'-CH2-O-N(CH3)-2' (см., например, US 2004/0171570, опубликованный 2 сентября 2004 года); 4'-CH2-O-N(R)-2' и 4'-CH2-N(R)-O-2'-, где каждый R независимо представляет собой Н, защитную группу или С1-С12 алкил; 4'-CH2-N(R)-O-2', где R представляет собой Н, С1-С12 алкил или защитную группу (см., например, патент США 7427672, выданный 23 сентября 2008 года); 4'-CH2-С(Н)(СН3)-2' (см., например, Chattopadhyaya, et al, J. Org. Chem., 2009, 74, 118-134); и 4'-CH2-C(=CH2)-2' и его аналоги (сл. опубликованную Международную заявку РСТ WO 2008/154401, опубликованную 8 декабря 2008 года).
В некоторых вариантах реализации такие мостики 4'-2' независимо содержат от 1 до 4 связанных групп, независимо выбранных из -[C(Ra)(Rb)]n-, -C(Ra)=C(Rb)-, -C(Ra)=N-, -C(=NRa)-, -C(=O)-, -C(=S)-, -O-, -Si(Ra)2-, -S(=O)x- и -N(Ra)-;
где:
x равен 0, 1 или 2;
n равен 1, 2, 3 или 4;
каждый Ra и Rb независимо представляет собой Н, защитную группу, гидроксил, С1-С12 алкил, замещенный С1-С12 алкил, C2-C12 алкенил, замещенный C2-C12 алкенил. С7-С12 алкинил, замещенный C2-C12 алкинил, С5-С20 арил, замещенный C5-C20 арил, гетероциклический радикал, замещенный гетероциклический радикал, гетероарил, замещенный гетероарил, С5-С7 алициклический радикал, замещенный С5-С7 алициклический радикал, галоген, OJ1, NJ1J2, SJ1, N3, COOJ1, ацил (C(=O)-H), замещенный ацил, CN, сульфонил (S(=O)2-J1) или сульфоксил (S(=O)-J1); и
каждый J1 и J2 независимо представляет собой Н, С1-С12 алкил, замещенный С1-С12 алкил, C2-C12 алкенил, замещенный C2-C12 алкенил, C2-C12 алкинил, замещенный C2-C12 алкинил, С5-С20 арил, замещенный С5-С20 арил, ацил (С(=O)-Н), замещенный ацил, гетероциклический радикал, замещенный гетероциклический радикал, С1-С12 аминоалкил, замещенный С1-С12 аминоалкил или защитную группу.
Нуклеозиды, содержащие бициклические сахарные фрагменты, упоминаются как бициклические нуклеозиды или BNA. Бициклические нуклеозиды включают, но не ограничиваются ими, (А) α-L-метиленокси (4'-CH2-O-2') BNA, (В) β-D-метиленокси (4'-CH2-O-2') BNA (также упоминаемый как закрытая нуклеиновая кислота или LNA), (С) этиленокси (4'-(CH2)2-O-2') BNA, (D) аминоокси (4'-CH2-O-N(R)-2') BNA, (Е) оксиамино (4'-CH2-N(R)-O-2') BNA, (F) метил(метиленокси) (4'-СН(CH3)-O-2') BNA (также упоминаемый как стерически затрудненный этил или cEt), (G) метилен-тио (4'-CH2-S-2') BNA, (Н) метилен-амино (4'-CH2-N(R)-2') BNA, (I) метил-карбоциклический (4'-CH2-СН(СН3)-2') BNA и (J) пропилен-карбоциклический (4'-(CH2)3-2') BNA, как показано ниже.
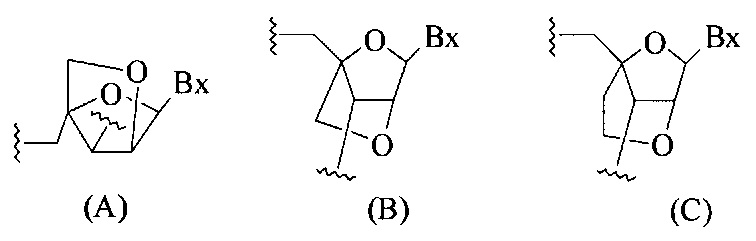
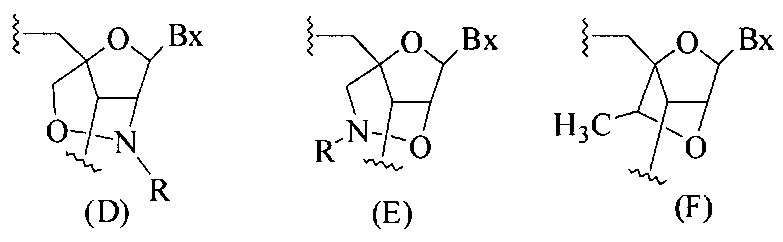
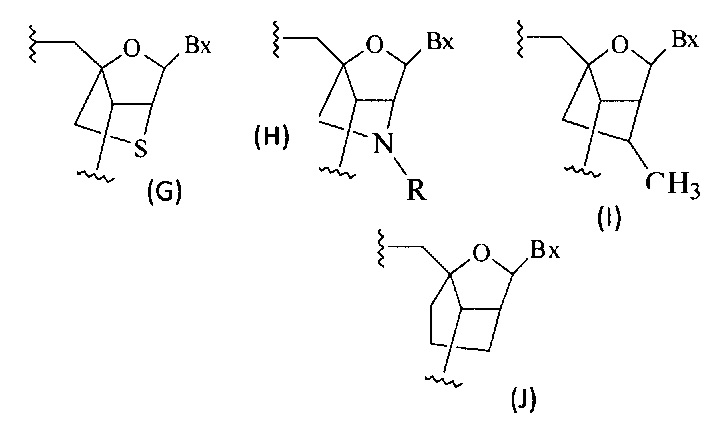
где Вх представляет собой фрагмент азотистые основания, a R независимо представляет собой Н, защитную группу или C1-C12 алкил.
В данной области техники известны дополнительные бициклические сахарные фрагменты, например: Singh et al., Chem. Commun., 1998, 4, 455-456; Koshkin et al., Tetrahedron, 1998, 54, 3607-3630; Wahlestedt et al., Proc. Natl. Acad. Sci. U.S.A., 2000, 97, 5633-5638; Kumar et al., Bioorg. Med. Chem. Lett., 1998, 8, 2219-2222; Singh et al., J. Org. Chem., 1998, 63, 10035-10039; Srivastava et al., J. Am. Chem. Soc., 129(26) 8362-8379 (4 июля 2007 года); Elayadi et al., Curr. Opinion Invens. Drugs, 2001, 2, 558-561; Braasch et al., Chem. Biol., 2001, 8, 1-7; Oram et al., Curr. Opinion Mol. Ther., 2001, 3, 239-243; патенты США №7053207 6268490 6770748 6794499 7034133 6525191 6670461 и 7399845; WO 2004/106356, WO 1994/14226, WO 2005/021570 и WO 2007/134181; публикации патентов США № US 2004/0171570, US 2007/0287831 и US 2008/0039618; патенты США с серийными номерами 12/129154 60/989574 61/026995 61/026998 61/056564 61/086231 61/097787 и 61/099844; и Международные заявки РСТ № PCT/US 2008/064591, PCT/US 2008/066154 и PCT/US 2008/068922.
В некоторых вариантах реализации бициклические сахарные фрагменты и нуклеозиды, содержащие такие бициклические сахарные фрагменты, дополнительно определяют по изомерной конфигурации. Например, нуклеозид, содержащий мостик 4'-2'-метилен-окси, может быть в α-L конфигурации или в β-D конфигурации. Ранее α-L-метиленокси (4'-CH2-O-2') бициклические нуклеозиды были внедрены в антисмысловые олигонуклеотиды, которые обладают антисмысловой активностью (Frieden et al., Nucleic Acids Research, 2003, 21, 6365-6372).
В некоторых вариантах реализации замещенные сахарные фрагменты содержат один или более немостиковых сахарных заместителей и один или более мостиковых сахарных заместителей (например, 5'-замещенные и 4'-2'-мостиковые сахара), (см., например, Международную заявку РСТ WO 2007/134181, опубликованную 11/22/07, в которой LNA замещена, например, 5'-метальной или 5'-виниловой группой).
В некоторых вариантах реализации модифицированные сахарные фрагменты представляют собой заменители сахара. В некоторых таких вариантах реализации атом кислорода природного сахара является замещенным, например, атомом серы, углерода или азота. В некоторых таких вариантах реализации такой модифицированный сахарный фрагмент содержит также мостиковые и/или немостиковые заместители, как описано выше. Например, некоторые заменители сахара содержат 4'-атом серы и замещение в 2'-положении (см., например, опубликованную патентную заявку США US 2005/0130923, опубликованную 16 июня 2005 года) и/или 5'-положении. В качестве дополнительного примера, были описаны карбоциклические бициклические нуклеозиды, имеющие мостик 4'-2' (см., например, Freier et al., Nucleic Acids Research, 1997, 25(22), 4429-4443 и Albaek et al., J. Org. Chem., 2006, 71, 7731-7740).
В некоторых вариантах реализации заменители сахара содержат кольца, имеющие не 5 атомов. Например, в некоторых вариантах реализации заменитель сахара содержит морфолино. Морфолино-соединения и их применение в олигомерных соединениях было описано в многочисленных патентах и опубликованных статьях (см., например: Braasch et al., Biochemistry, 2002, 41, 4503-4510; и патенты США 5698685; 5166315; 5185444; и 5034506). При использовании в настоящем документе, термин «морфолино» означает заменитель сахара, имеющий следующую структуру:
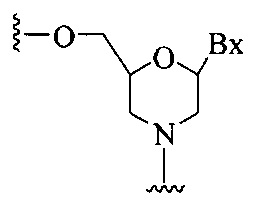
В некоторых вариантах реализации морфолино могут быть модифицированными, например, добавлением или изменением различных групп заместителей в приведенной выше структуре морфолино. Такие заменители сахара упомянуты в настоящем документе как «модифицированные морфолино».
В качестве другого примера, в некоторых вариантах реализации заменитель сахара содержит шестичленный тетрагидропиран. Такие тетрагидропираны могут быть дополнительно модифицированы или замещены. Нуклеозиды, содержащие такие модифицированные тетрагидропираны, включают, но не ограничиваются ими, гекситоловую нуклеиновую кислоту (HNA), анитоловую нуклеиновую кислоту (ANA), манитоловую нуклеиновую кислоту (MNA) (см. Leumann, CJ. Bioorg. & Med. Chem. (2002) 10: 841-854), фтор-HNA (F-HNA) и соединения, имеющие Формулу VI:
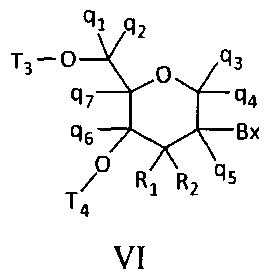
где независимо для каждого из указанного по меньшей мере одного тетрагидропиранового нуклеозидного аналога Формулы VI:
Вх представляет собой фрагмент азотистого основания;
Т3 и Т4, каждый независимо, представляют собой межнуклеозидную связывающую группу, связывающую тетрагидропирановый нуклеозидный аналог с антисмысловым соединением, или один из Т3 и Т4 представляет собой межнуклеозидную связывающую группу, связывающую тетрагидропирановый нуклеозидный аналог с антисмысловым соединением, а другой из Т3 и Т4 представляет собой Н, гидроксил-защитную группу, связанную конъюгирующую группу или 5' или 3'-концевую группу;
q1, q2, q3, q4, q5, q6 и q7, каждый независимо, представляют собой Н, С1-С6 алкил, замещенный C1-С6 алкил, C2-C6 алкенил, замещенный C2-C6 алкенил, C2-C6 алкинил или замещенный C2-C6 алкинил; и
каждый из R1 и R2 независимо выбран из: водорода, галогена, замещенного или незамещенного алкокси, NJ1J2, SJ1, N3, OC(=X)J1, OC(=X)NJ1J2, NJ3C(=X)NJ1J2 и CN, где X представляет собой О, S или NJ1, и каждый J1, J2 и J3 независимо представляет собой Н или C1-С6 алкил.
В некоторых вариантах реализации приведены модифицированные ТНР нуклеозиды Формулы VI, в которых каждый q1, q2, q3, q4, q5, q6 и q7 представляет собой Н. В некоторых вариантах реализации по меньшей мере один из q1, q2, q3, q4, q5, q6 и q7 отличен от Н. В некоторых вариантах реализации по меньшей мере один из q1, q2, q3, q4, q5, q6 и q7 представляет собой метил. В некоторых вариантах реализации приведены ТНР нуклеозиды Формулы VI, в которых один из R1 и R2 представляет собой F. В некоторых вариантах реализации R1 представляет собой фтор, a R2 представляет собой Н, R1 представляет собой метокси, a R2 представляет собой Н, и R1 представляет собой метоксиэтокси, a R2 представляет собой Н.
В данной области техники известны также многие другие бициклические и трициклические кольцевые системы заменителей сахара, которые могут быть использованы для модификации нуклеозидов для внедрения в антисмысловые соединения (см., например, обзорную статью: Leumann, J.С, Bioorganic & Medicinal Chemistry, 2002, 10, 841-854).
Без ограничения, приведены также комбинации модификаций, такие как 2'-F-5'-метил-замещенные нуклеозиды (см. Международную заявку РСТ WO 2008/101157, опубликованную 8/21/08, где описаны другие 5', 2'-бис-замещенные нуклеозиды) и замена атома кислорода рибозильного кольца на S и дополнительное замещение в 2'-положении (см. опубликованную заявку на патент США US 2005-0130923, опубликованную 16 июня 2005 года) или, альтернативно, 5'-замещение бициклической нуклеиновой кислоты (см. Международную заявку РСТ WO 2007/134181, опубликованную 11/22/07, в которой 4'-CH2-O-2' бициклический нуклеозид дополнительно замещен в 5'-положении 5'-метильной или 5'-виниловой группой). Был описан также синтез и получение карбоциклических бициклических нуклеозидов вместе с их олигомеризацией и биохимическими исследованиями (см., например, Srivastava et al., J. Am. Chem. Soc. 2007, 129(26), 8362-8379).
В некоторых вариантах реализации настоящего описания приведены олигонуклеотиды, содержащие модифицированные нуклеозиды. Такие модифицированные нуклеотиды могут содержать модифицированные сахара, модифицированные азотистые основания и/или модифицированные связи. Конкретные модификации выбирают так, чтобы полученные олигонуклеотиды обладали желаемыми характеристиками. В некоторых вариантах реализации олигонуклеотиды содержат один или более РНК-подобных нуклеозидов. В некоторых вариантах реализации олигонуклеотиды содержат один или более ДНК-подобных нуклеотидов.
2. Некоторые модификации азотистых оснований
В некоторых вариантах реализации нуклеозиды настоящего описания содержат одно или более немодифицированных азотистых оснований. В некоторых вариантах реализации нуклеозиды настоящего описания содержат одно или более модифицированных азотистых оснований.
В некоторых вариантах реализации модифицированные азотистые основания выбраны из: универсальных оснований, гидрофобных оснований, смешанных оснований, увеличенных в размере оснований и фторированных оснований, описанных в настоящем документе. 5-замещенные пиримидины, 6-азапиримидины и N-2, N-6 и О-6-замещенные пурины, включая 2-аминопропиладенин, 5-пропинилурацил; 5-пропинилцитозин; 5-гидроксиметил-цитозин, ксантин, гипоксантин, 2-аминоаденин, 6-метил и другие алкильные производные аденина и гуанина, 2-пропил и другие алкильные производные аденина и гуанина, 2-тиоурацил, 2-тиотимин и 2-тиоцитозин, 5-галогенурацил и цитозин, 5-пропинил (-С≡С-СН3) урацил и цитозин и другие алкинильные производные пиримидиновых оснований, 6 азоурацил, цитозин и тимин, 5-урацил (псевдоурацил), 4-тиоурацил, 8-галоген, 8-амино, 8-тиол, 8-тиоалкил, 8-гидроксил и другие 8-замещенные аденины и гуанины, 5-галоген, в частности, 5-бром, 5-трифторметил и другие 5-замещенные урацилы и цитозины, 7-метилгуанин и 7-метиладенин, 2-F-аденин, 2-аминоаденин, 8-азагуанин и 8-азааденин, 7-деазагуанин и 7-деазааденин, 2-деазагуанин и 3-деазааденин, универсальные основания, гидрофобные основания, смешанные основания, увеличенные в размере основания и фторированные основания, описанные в настоящем документе. Дополнительные модифицированные азотистые основания включают трициклические пиримидины, такие как феноксазина цитидин ([5,4-b][1,4]бензоксазин-2(3Н)-он), фенотиазина цитидин (1Н-пиримидо[5,4-b][1,4]бензотиазин-2(3Н)-он), так называемые G-clamp, такие как замещенный феноксазина цитидин (например, 9-(2-аминоэтокси)-Н-пиримидо[5,4-b][1,4]бензоксазин-2(3Н)-он), карбазола цитидин (2Н-пиримидо[4,5-b]индол-2-он), пиридоиндола цитидин (Н-пиридо[3',2':4,5]пирроло[2,3-d]пиримидин-2-он). Модифицированные азотистые основания также могут включать азотистые основания, в которых пуриновое или пиримидиновое основание заменено другими гетероциклами, например, 7-деаза-аденин, 7-деазагуанозин, 2-аминопиридин и 2-пиридон. Дополнительные азотистые основания включают азотистые основания, описанные в патенте США №3687808, описанные в публикации The Concise Encyclopedia Of Polymer Science And Engineering, Kroschwitz, J.I., ред., John Wiley & Sons, 1990, 858-859; описанные авторами Englisch et al., Angewandte Chemie, Международное издание, 1991, 30, 613; и описанные в публикации Sanghvi, Y.S., глава 15, Antisense Research and Applications, Crooke, S.T. и Lebleu, В., ред., CRC Press, 1993, 273-288.
Типичные патенты США, в которых описано получение некоторых из вышеупомянутых модифицированных азотистых оснований, а также других модифицированных азотистых оснований, включают, без ограничения, U.S. 3687808; 4845205; 5130302; 5134066; 5175273; 5367066; 5432272; 5457187; 5459255; 5484908; 5502177; 5525711; 5552540; 5587469; 5594121; 5596091; 5614617; 5645985; 5681941; 5750692; 5763588; 5830653 и 6005096, некоторые из которых находятся на рассмотрении одновременно с настоящей заявкой, и каждый из которых включен в настоящий документ посредством ссылки в полном объеме.
3. Некоторые межнуклеозидные связи
В некоторых вариантах реализации настоящего описания приведены олигонуклеотиды, содержащие связанные нуклеозиды. В таких вариантах реализации нуклеозиды могут быть связаны вместе при помощи любой межнуклеозидной связи. Два основных класса межнуклеозидных связывающих групп определяются по наличию или отсутствию атома фосфора. Типичные фосфорсодержащие межнуклеозидные связи включают, но не ограничиваются мим и, фосфодиэфиры (РО), фосфотриэфиры, метилфосфонаты, фосфорамидаты и тиофосфаты (PS). Типичные не содержащие фосфора межнуклеозидные связывающие группы включают, но не ограничиваются ими, метиленметилимино (-CH2-N(СН3)-O-CH2-), тиодиэфир (-O-C(O)-S-), тионокарбамат (-O-C(O)(NH)-S-); силоксан (-O-Si(H)2-O-); и N,N'-диметилгидразин (-CH2-N(СН3)-N(СН3)-). Модифицированные связи, в сравнении с природными фосфодиэфирными связями, могут быть использованы для изменения, обычно увеличения устойчивости олигонуклеотида к нуклеазе. В некоторых вариантах реализации межнуклеозидные связи, имеющие хиральный атом, могут быть получены в виде рацемической смеси или в виде отдельных энантиомеров. Типичные хиральные связи включают, но не ограничиваются ими, алкилфосфонаты и тиофосфаты. Способы получения фосфорсодержащих и не содержащих фосфора межнуклеозидных связей хорошо известны специалистам в данной области техники.
Олигонуклеотиды, описанные в настоящем документе, содержат один или более асимметричных центров и, следовательно, могут образовывать энантиомеры, диастереомеры и другие стереоизомерные конфигурации, которые в соответствии с абсолютной стереохимией могут быть определены как (R) или (S), или, как для аномеров сахара или как (D) или (L), как для аминокислот и т.д. В антисмысловые соединения, приведенные в настоящем документе, включены все такие возможные изомеры, а также их рацемические и оптически чистые формы.
Нейтральные связывающие линкеры включают, без ограничения, фосфотриэфиры, метилфосфонаты, MMI (3'-CH2-N(СН3)-O-5'), амид-3 (3'-CH2-C(=O)-N(H)-5'), амид-4 (3'-CH2-N(H)-C(=O)-5'), формацеталь (3'-O-CH2-O-5') и тиоформацеталь (3'-S-CH2-O-5'). Дополнительные нейтральные межнуклеозидные связи включают неионные связи, содержащие силоксан (диалкилсилоксан), карбоксильный эфир, карбоксамид, сульфид, сульфоновый эфир и амиды (см., например: Carbohydrate Modifications in Antisense Research; Y.S. Sanghvi и P.D. Cook, ред., ACS Symposium Series 580; главы 3 и 4, 40-65). Дополнительные нейтральные межнуклеозидные связи включают неионные связи, содержащие смешанные составные части N, О, S и CH2.
4. Некоторые мотивы
В некоторых вариантах реализации антисмысловые олигонуклеотиды содержат один или более модифицированных нуклеозидов (например, нуклеозид, содержащий модифицированный сахар и/или модифицированное азотистое основание) и/или один или более модифицированных межнуклеозидных связей. Характерный участок таких модификаций в олигонуклеотиде упоминается в настоящем документе как мотив. В некоторых вариантах реализации мотивы сахара, азотистые основания и линкера не зависят друг от друга.
а. Некоторые сахарные мотивы
В некоторых вариантах реализации олигонуклеотиды содержат один или более типов модифицированных сахарных фрагментов и/или природных сахарных фрагментов, расположенных вдоль олигонуклеотида или его области определенным образом или в виде мотива сахарной модификации. Такие мотивы могут содержать любые сахарные модификации, рассмотренные в настоящем документе и/или другие известные модификации сахара.
В некоторых вариантах реализации олигонуклеотиды содержат или состоят из области, имеющей сахарный мотив гэпмера, который содержит две внешних области или «крыла» и центральную или внутреннюю область, или «гэп». Эти три области сахарного мотива гэпмера (5'-крыло, гэп и 3'-крыло) образуют непрерывную последовательность азотистых оснований, в которой по меньшей мере некоторые из сахарных фрагментов нуклеозидов в каждом крыле отличаются по меньшей мере от некоторых сахарных фрагментов нуклеозидов в гэпе. В частности, по меньшей мере те сахарные фрагменты нуклеозидов каждого крыла, которые расположены ближе всего к гэпу (3'-ближайший нуклеозид 5'-крыла и 5'-ближайший нуклеозид 3'-крыла), отличаются от сахарного фрагмента соседних нуклеозидов в гэпе, определяя таким образом границу между крыльями и гэпом. В некоторых вариантах реализации сахарные фрагменты в гэпе являются одинаковыми между собой. В некоторых вариантах реализации гэп содержит один или более нуклеозидов, имеющих сахарный фрагмент, который отличается от сахарного фрагмента одного или более других нуклеозидов в гэпе. В некоторых вариантах реализации сахарные мотивы двух крыльев являются одинаковыми между собой (симметричный сахарный гэпмер). В некоторых вариантах реализации сахарные мотивы 5'-крыла отличаются от сахарного мотива 3'-крыла (асимметричный сахарный гэпмер).
i. Некоторые 5'-крылья
В некоторых вариантах реализации 5'-крыло гэпмера состоит из 1-8 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 1-7 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 1-6 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 1-5 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 2-5 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 3-5 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 4 или 5 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 1-4 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 1-3 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 1 или 2 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 2-4 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 2 или 3 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 3 или 4 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 1 нуклеозида. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 2 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 3 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 4 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 5 связанных нуклеозидов. В некоторых вариантах реализации 5'-крыло гэпмера состоит из 6 связанных нуклеозидов.
В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере два бициклических нуклеозида. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере три бициклических нуклеозида. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере четыре бициклических нуклеозида. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один LNA нуклеозид. В некоторых вариантах реализации каждый нуклеозид 5'-крыла гэпмера представляет собой бициклический нуклеозид. В некоторых вариантах реализации каждый нуклеозид 5'-крыла гэпмера представляет собой стерически затрудненный этил-нуклеозид. В некоторых вариантах реализации каждый нуклеозид 5'-крыла гэпмера представляет собой LNA нуклеозид.
В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один не бициклический модифицированный нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один 2'-замещенный нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один 2'-МОЕ нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один 2'-ОМе нуклеозид. В некоторых вариантах реализации каждый нуклеозид 5'-крыла гэпмера представляет собой не бициклический модифицированный нуклеозид. В некоторых вариантах реализации каждый нуклеозид 5'-крыла гэпмера представляет собой 2'-замещенный нуклеозид. В некоторых вариантах реализации каждый нуклеозид 5'-крыла гэпмера представляет собой 2'-МОЕ нуклеозид. В некоторых вариантах реализации каждый нуклеозид 5'-крыла гэпмера представляет собой 2'-ОМе нуклеозид.
В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один 2'-дезоксинуклеозид. В некоторых вариантах реализации каждый нуклеозид 5'-крыла гэпмера представляет собой 2'-дезоксинуклеозид. В некоторых вариантах реализаций 5'-крыло гэпмера содержит по меньшей мере один рибонуклеозид. В некоторых вариантах реализации каждый нуклеозид 5'-крыла гэпмера представляет собой рибонуклеозид. В некоторых вариантах реализации один, более одного или каждый из нуклеозидов Закрыла представляет собой РНК-подобный нуклеозид.
В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид и по меньшей мере один не бициклический модифицированный нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид и по меньшей мере один 2'-замещенный нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид и по меньшей мере один 2'-МОЕ нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один бициклический; нуклеозид и по меньшей мере один 2'-ОМе нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид и по меньшей мере один 2'-дезоксинуклеозид.
В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид и по меньшей мере один не бициклический модифицированный нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид и по меньшей мере один 2'-замещенный нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид и по меньшей мере один 2'-МОЕ нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид и по меньшей мере один 2'-ОМе нуклеозид. В некоторых вариантах реализации 5'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид и по меньшей мере один 2'-дезоксинуклеозид.
ii. Некоторые 3'-крылья
В некоторых вариантах реализации 3'-крыло гэпмера состоит из 1-8 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 1-7 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 1-6 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 1-5 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 2-5 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 3-5 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 4 или 5 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 1-4 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 1-3 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 1 или 2 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 2-4 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 2 или 3 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 3 или 4 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 1 нуклеозида. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 2 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 3 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 4 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 5 связанных нуклеозидов. В некоторых вариантах реализации 3'-крыло гэпмера состоит из 6 связанных нуклеозидов.
В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один LNA нуклеозид. В некоторых вариантах реализации каждый нуклеозид 3'-крыла гэпмера представляет собой бициклический нуклеозид. В некоторых вариантах реализации каждый нуклеозид 3'-крыла гэпмера представляет собой стерически затрудненный этил-нуклеозид. В некоторых вариантах реализации каждый нуклеозид 3'-крыла гэпмера представляет собой LNA нуклеозид.
В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере един не бициклический модифицированный нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере два не бициклических модифицированных нуклеозида. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере три не бициклических модифицированных нуклеозида. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере четыре не бициклических модифицированных нуклеозида. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один 2'-замещенный нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один 2'-МОЕ нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один 2'-ОМе нуклеозид. В некоторых вариантах реализации каждый нуклеозид 3'-крыла гэпмера представляет собой не бициклический модифицированный нуклеозид. В некоторых вариантах реализации каждый нуклеозид 3'-крыла гэпмера представляет собой 2'-замещенный нуклеозид. В некоторых вариантах реализации каждый нуклеозид 3'-крыла гэпмера представляет собой 2'-МОЕ нуклеозид. В некоторых вариантах реализации каждый нуклеозид 3'-крыла гэпмера представляет собой 2'-ОМе нуклеозид.
В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один 2'-дезоксинуклеозид. В некоторых вариантах реализации каждый нуклеозид 3'-крыла гэпмера представляет собой 2'-дезоксинуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один рибонуклеозид. В некоторых вариантах реализации каждый нуклеозид 3'-крыла гэпмера представляет собой рибонуклеозид. В некоторых вариантах реализации один, более одного или каждый из нуклеозидов 5'-крыла представляет собой РНК-подобный нуклеозид.
В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид и по меньшей мере один не бициклический модифицированный нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид и по меньшей мере один 2'-замещенный нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид и по меньшей мере один 2'-МОЕ нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид и по меньшей мере один 2'-ОМе нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид и по меньшей мере один 2'-дезоксинуклеозид.
В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид и по меньшей мере один не бициклический модифицированный нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид и по меньшей мере один 2'-замещенный нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид и по меньшей мере один 2'-МОЕ нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид и по меньшей мере один 2'-ОМе нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит не меньшей мере один стерически затрудненный этил-нуклеозид и по меньшей мере один 2'-дезоксинуклеозид.
В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один LNA нуклеозид и по меньшей мере один не бициклический модифицированный нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один LNA нуклеозид и по меньшей мере один 2'-замещенный нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один LNA нуклеозид и по меньшей мере один 2'-МОЕ нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один LNA нуклеозид и по меньшей мере один 2'-ОМе нуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один LNA нуклеозид и по меньшей мере один 2'-дезоксинуклеозид.
В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид, по меньшей мере один не бициклический модифицированный нуклеозид и по меньшей мере один 2'-дезоксинуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид, по меньшей мере один не бициклический модифицированный нуклеозид и по меньшей мере один 2'-дезоксинуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один LNA нуклеозид, по меньшей мере один не бициклический модифицированный нуклеозид и по меньшей мере один 2'-дезоксинуклеозид.
В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид, по меньшей мере один 2'-замещенный нуклеозид и по меньшей мере один 2'-дезоксинуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид, по меньшей мере один 2'-замещенный нуклеозид и по меньшей мере один 2'-дезоксинуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один LNA нуклеозид, по меньшей мере один 2'-замещенный нуклеозид и по меньшей мере один 2'-дезоксинуклеозид.
В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид, по меньшей мере один 2'-МОЕ нуклеозид и по меньшей мере один 2'-дезоксинуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид, по меньшей мере один 2'-МОЕ нуклеозид и по меньшей мере один 2'-дезоксинуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один LNA нуклеозид, по меньшей мере один 2'-МОЕ нуклеозид и по меньшей мере один 2'-дезоксинуклеозид.
В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один бициклический нуклеозид, по меньшей мере один 2'-ОМе нуклеозид и по меньшей мере один 2'-дезоксинуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один стерически затрудненный этил-нуклеозид, по меньшей мере один 2'-ОМе нуклеозид и по меньшей мере один 2'-дезоксинуклеозид. В некоторых вариантах реализации 3'-крыло гэпмера содержит по меньшей мере один LNA нуклеозид, по меньшей мере один 2'-ОМе нуклеозид и по меньшей мере один 2'-дезоксинуклеозид.
iii. Некоторые центральные области (гэпы)
В некоторых вариантах реализации гэп гэпмера состоит из 6-20 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 6-15 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 6-12 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 6-10 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 6-9 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 6-8 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 6 или 7 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 7-10 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 7-9 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 7 или 8 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 8-10 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 8 или 9 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 6 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 7 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 8 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 9 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 10 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 11 связанных нуклеозидов. В некоторых вариантах реализации гэп гэпмера состоит из 12 связанных, нуклеозидов.
В некоторых вариантах реализации каждый нуклеозид гэпа гэпмера представляет собой 2'-дезоксинуклеозид. В некоторых вариантах реализации гэп содержит один или более модифицированных нуклеозидов. В некоторых вариантах реализации каждый нуклеозид гэпа гэпмера представляет собой 2'-дезоксинуклеозид или представляет собой модифицированный «ДНК-подобный» нуклеозид. В таких вариантах реализации «ДНК подобный» означает, что нуклеозид имеет такие же характеристики, что и ДНК, то есть что дуплекс, содержащий гэпмер и молекулу РНК может активировать РНКазу Н. Например, было показано, что при некоторых условиях 2'-(ara)-F поддерживает активацию РНКазы Н и, следовательно, является ДНК-подобным. В некоторых вариантах реализации один или более нуклеозидов гэпа гэпмера не представляет собой 2'-дезоксинуклеозид и не является ДНК-подобным. В некоторых таких вариантах реализации гэпмер тем не менее поддерживает активацию РНКазы Н (например, за счет количества или положения не-ДНК нуклеозидов).
В некоторых вариантах реализации гэпы содержат участок немодифицированного 2'-дезоксинуклеозида, прерванный одним или более модифицированными нуклеозидами, что приводит к образованию трех субрайонов (двух участков одного или более 2'-дезоксинуклеозидов и участка одного или более прерывающих модифицированных нуклеозидов). В некоторых вариантах реализации ни один участок немодифицированных 2'-дезоксинуклеозидов не длиннее 5, 6 или 7 нуклеозидов. В некоторых вариантах реализации такие короткие участки образуются за счет использования коротких гэп-областей. В некоторых вариантах реализации короткие участки образуются за счет прерывания более длинной области гэп.
В некоторых вариантах реализации гэп содержит один или более модифицированных нуклеозидов. В некоторых вариантах реализации гэп содержит один или более модифицированных нуклеозидов, выбранных из cEt, FHNA, LNA и 2-тиотимидина. В некоторых вариантах реализации гэп содержит один модифицированный нуклеозид. В некоторых вариантах реализации гэп содержит 5'-замещенный сахарный фрагмент, выбранный из 5'-Ме и 5'-(R)-Me. В некоторых вариантах реализации гэп содержит два модифицированных нуклеозида. В некоторых вариантах реализации гэп содержит три модифицированных нуклеозида. В некоторых вариантах реализации гэп содержит четыре модифицированных нуклеозида. В некоторых вариантах реализации гэп содержит два или более модифицированных нуклеозидов, и каждый модифицированный нуклеозид является таким же. В некоторых вариантах реализации гэп содержит два или более модифицированных нуклеозидов, и каждый модифицированный нуклеозид является другим.
В некоторых вариантах реализации гэп содержит одну или более модифицированных связей. В некоторых вариантах реализации гэп содержит одну или более метилфосфонатных связей. В некоторых вариантах реализации гэп содержит две или более модифицированных связей. В некоторых вариантах реализации гэп содержит одну или более модифицированных связей и один или более модифицированных нуклеозидов. В некоторых вариантах реализации гэп содержит одну модифицированную связь и один модифицированный нуклеозид. В некоторых вариантах реализации гэп содержит две модифицированных связи и два или более модифицированных нуклеозидов.
b. Некоторые мотивы межнуклеозидных связей
В некоторых вариантах реализации олигонуклеотиды содержат модифицированные межнуклеозидные связи, расположенные вдоль олигонуклеотида или его области определенным образом или в виде мотива модифицированной межнуклеозидной связи. В некоторых вариантах реализации олигонуклеотиды содержат область, имеющую мотив чередующихся межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотиды по настоящему описанию содержат область одинаково модифицированных межнуклеозидных связей. В некоторых таких вариантах реализации олигонуклеотид содержит область, которая равномерно связана тиофосфатными межнуклеозидными Связями. В некоторых вариантах реализации олигонуклеотид равномерно связан тиофосфатными межнулеозидными связями. В некоторых вариантах реализации каждая межнуклеозидная связь олигонуклеотида выбран из фосфодиэфира и тиофосфата. В некоторых вариантах реализации каждая межнуклеозидная связь олигонуклеотида выбран из фосфодиэфира и тиофосфата, и по меньшей мере одна межнуклеозидная связь представляет собой тиофосфат.
В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 6 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 7 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 8 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 9 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 10 тиофосфатных межнуклеозидных связей. 3 некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 11 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 12 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 13 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере 14 тиофосфатных межнуклеозидных связей.
В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок по меньшей мере из 6 последовательных тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок по меньшей мере из 7 последовательных тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок по меньшей мере из 8 последовательных тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок по меньшей мере из 9 последовательных тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок по меньшей мере из 10 последовательных тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит по меньшей мере один блок по меньшей мере из 12 последовательных тиофосфатных межнуклеозидных связей. В некоторых таких вариантах реализации по меньшей мере один такой блок расположен на 3'-конце олигонуклеотида. В некоторых таких вариантах реализации по меньшей мере один такой блок расположен в пределах 3 нуклеозидов 3'-конца олигонуклеотида. В некоторых вариантах реализации олигонуклеотид содержит менее 15 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит менее 14 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит менее 13 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит менее 12 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит менее 11 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит менее 10 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит менее 9 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит менее 8 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит менее 7 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит менее 6 тиофосфатных межнуклеозидных связей. В некоторых вариантах реализации олигонуклеотид содержит менее 5 тиофосфатных межнуклеозидных связей.
с. Некоторые мотивы модификаций азотистых оснований
В некоторых вариантах реализации олигонуклеотиды содержат химические модификации азотистых оснований, расположенные вдоль олигонуклеотида или его области определенным образом или в виде мотива модификации азотистых оснований. В некоторых таких вариантах реализации модификации азотистых оснований расположены в разорванном мотиве. В некоторых вариантах реализации модификации азотистых оснований расположены в чередующемся мотиве. В некоторых вариантах реализации каждое азотистое основание является модифицированным. В некоторых вариантах реализации ни одно из азотистых оснований не является химически модифицированным.
В некоторых вариантах реализации олигонуклеотиды содержат блок модифицированных азотистых оснований. В некоторых таких вариантах реализации блок находится на 3'-конце олигонуклеотида. В некоторых вариантах реализации блок находится в пределах 3 нуклеотидов 3'-конца олигонуклеотида. В некоторых таких вариантах реализации блок находится на 5'-конце олигонуклеотида. В некоторых вариантах реализации блок находится в пределах 3 нуклеотидов 5'-конца олигонуклеотида.
В некоторых вариантах реализации модификации азотистых оснований зависят от природного основания в конкретном положении олигонуклеотида. Например, в некоторых вариантах реализации каждый пурин или каждый пиримидин в олигонуклеотиде являемся модифицированным. В некоторых вариантах реализации модифицированным является каждый аденин. В некоторых вариантах реализации модифицированным является каждый гуанин. В некоторых вариантах реализации модифицированным является каждый тимин. В некоторых вариантах реализации модифицированным является каждый цитозин. В некоторых вариантах реализации модифицированным является каждый урацил.
В некоторых вариантах реализации некоторые, все или никакие из цитозиновых фрагментов в олигонуклеотиде не представляют собой 5-метилцитозиновые фрагменты. В настоящем документе 5-метилцитозин не является «модифицированным с азотистым основанием». Соответственно, если не указано иное, то немодифицированные азотистые основания включают как цитозиновые остатки, содержащие 5-метил, так и те, которые не содержат 5-метил. В некоторых вариантах реализации оговорено патологическое состояние метилирования всех или некоторых цитозиновых азотистых оснований.
В некоторых вариантах реализации химические модификации азотистых оснований включают присоединение некоторых конъюгирующих групп к азотистым основаниям. В некоторых вариантах реализации каждый пурин или каждый пиримидин в олигонуклеотиде может быть необязательно модифицирован так, чтобы он содержал конъюгирующую группу.
d. Некоторые общие длины
В некоторых вариантах реализации настоящего описания приведены олигонуклеотиды любого из различных диапазонов длин. В некоторых вариантах реализации олигонуклеотиды содержат от X до Y связанных нуклеозидов, где X представляет собой наименьшее количество нуклеозидов в диапазоне, a Y представляет собой наибольшее количество нуклеозидов в диапазоне. В некоторых таких вариантах реализации каждый X и Y независимо выбран из 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49 и 50; при условии, что X≤Y. Например, в некоторых вариантах реализации олигонуклеотид может состоять из 8-9, 8-10, 8-11, 8-12, 8-13, 8-14, 8-15, 8-16, 8-17, 8-18, 8-19, 8-20, 8-21, 8-22, 8-23, 8-24, 8-25, 8-26, 8-27, 8-28, 8-29, 8-30, 9-10, 9-11, 9-12, 9-13, 9-14, 9-15, 9-16, 9-17, 9-18, 9-19, 9-20, 9-21, 9-22, 9-23, 9-24, 9-25, 9-26, 9-27, 9-28, 9-29, 9-30, 10-11, 10-12, 10-13, 10-14, 10-15, 10-16, 10-17, 10-18, 10-19, 10-20, 10-21, 10-22, 10-23, 10-24, 10-25, 10-26, 10-27, 10-28, 10-29, 10-30, 11-12, 11-13, 11-14, 11-15, 11-16, 11-17, 11-18, 11-19, 11-20, 11-21, 11-22, 11-23, 11-24, 11-25, 11-26, 11-27, 11-28, 11-29, 11-30, 12-13, 12-14, 12-15, 12-16, 12-17, 12-18, 12-19, 12-20, 12-21, 12-22, 12-23, 12-24, 12-25, 12-26, 12-27, 12-28, 12-29, 12-30, 13-14, 13-15, 13-16, 13-17, 13-18, 13-19, 13-20, 13-21, 13-22, 13-23, 13-24, 13-25, 13-26, 13-27, 13-28, 13-29, 13-30, 14-15,14-16, 14-17. 14-18, 14-19, 14-20, 14-21, 14-22, 14-23, 14-24, 14-25, 14-26, 14-27, 14-28, 14-29, 14-30, 15-16, 15-17, 15-18, 15-19, 15-20, 15-21, 15-22, 15-23, 15-24, 15-25, 15-26, 15-27, 15-28, 15-29, 15-30, 16-17, 16-18, 16-19, 16-20, 16-21, 16-22, 16-23, 16-24, 16-25, 16-26, 16-27, 16-28, 16-29, 16-30, 17-18, 17-19, 17-20, 17-21, 17-22, 17-23, 17-24, 17-25, 17-26, 17-27, 17-28, 17-29, 17-30, 18-19, 18-20, 18-21, 18-22, 18-23, 18-24, 18-25, 18-26, 18-27, 18-28, 18-29, 18-30, 19-20, 19-21, 19-22, 19-23, 19-24, 19-25, 19-26, 19-29, 19-28, 19-29, 19-30, 20-21, 20-22, 20-23, 20-24, 20-25, 20-26, 20-27, 20-28, 20-29, 20-30, 21-22, 21-23, 21-24, 21-25, 21-26, 21-27, 21-28, 21-29, 21-30, 22-23, 22-24, 22-25, 22-26, 22-27, 22-28, 22-29, 22-30, 23-24, 23-25, 23-26, 23-27, 23-28, 23-29, 23-30, 24-25, 24-26, 24-27, 24-28, 24-29, 24-30, 25-26, 25-27, 25-28, 25-29, 25-30, 26-27, 26-28, 26-29, 26-30, 27-28, 27-29, 27-30, 28-29, 28-30 или 29-30 связанных нуклеозидов. В тех вариантах реализации, в которых количество нуклеозидов в олигонуклеотиде соединения является ограниченным, либо до диапазона, либо до определенного числа, то соединение может, тем не менее, дополнительно содержать другие дополнительные заместители. Например, олигонуклеотид, содержащий 8-30 нуклеозидов, исключает олигонуклеотиды, имеющие 31 нуклеозид, но, если не указано иное, такой олигонуклеотид может дополнительно содержать, например, одну или более конъюгирующих групп, концевых групп или других заместителей.
Более того, если олигонуклеотид описан общим диапазоном длины и областями, имеющими определенную длину, и если сумма указанных длин областей меньше, чем верхняя граница диапазона общей длины, то олигонуклеотид может иметь дополнительные нуклеозиды, помимо тех, которые находятся в указанных областях, при условии, что общее количество нуклеозидов не превышает верхнюю границу диапазона общей длины.
5. Некторые химические мотивы антисмысловых олигонуклеотидов
В некоторых вариантах реализации химические структурные особенности антисмысловых олигонуклеотидов описываются их сахарным мотивом, мотивом межнуклеозидной связи, мотивом модификации азотистых оснований и общей длиной. В некоторых вариантах реализации такие параметры не зависят друг от друга. Так, каждая межнуклеозидная связь олигонуклеотида, имеющий сахарный мотив гэпмера, может быть модифицированным или немодифицированным и может повторять или не повторять характер модификации сахарных модификаций гэпмера. Следовательно, межнуклеозидные связи в областях крыльев сахара-гэпмера могут быть одинаковыми или отличными друг от друга и могут быть одинаковыми или отличными от межнуклеозидных связей области гэп. Точно так же, такие сахар-гэпмерные олигонуклеотиды могут содержать одно или более модифицированных азотистых оснований, независимо от характера сахарных модификаций гэпмера. Специалистам в данной области техники понятно, что такие мотивы могут быть комбинированы с получением множества олигонуклеотидов.
В некоторых вариантах реализации выбор межнуклеозидной связи и модификации нуклеозида не зависят друг от друга.
i. Некоторые последовательности и мишени
В некоторых вариантах реализации настоящего изобретения приведены антисмысловые олигонуклеотиды, имеющие последовательность, комплементарную целевой нуклеиновой кислоте. Такие антисмысловые соединения могут гибридизоваться с целевой нуклеиновой кислотой с получением по меньшей мере одной антисмысловой активности. В некоторых вариантах реализации антисмысловые соединения специфически гибридизуются с одной или более целевыми нуклеиновыми кислотами. В некоторых вариантах реализации специфически гибридизующееся антисмысловое соединение имеет последовательность азотистых оснований, содержащую область с достаточной комплементарностью с целевой нуклеиновой кислотой для обеспечения возможности гибридизации и получению антисмысловой активности, и недостаточной комплементарностью к любой нецелевой нуклеиновой кислоте для предотвращения или снижения неспецифической гибридизации с последовательностями нецелевых нуклеиновых кислот в условиях, в которых необходима специфическая гибридизация (например, в физиологических условиях для in vivo или терапевтических применений и в условиях выполнения анализов - в случае in vitro анализов). В некоторых вариантах реализации олигонуклеотиды являются селективными между мишенью и не мишенью, даже если мишень и не мишень содержат целевую последовательность. В таких вариантах реализации селективность может быть результатом относительной доступности целевой области одной молекулы нуклеиновой кислоты, по сравнению с другой.
В некоторых вариантах реализации настоящего описания приведены антисмысловые соединения, содержащие олигонуклеотиды, которые полностью комплементарны целевой нуклеиновой кислоте по всей длине олигонуклеотида. В некоторых вариантах реализации олигонуклеотиды на 99% комплементарны целевой нуклеиновой кислоте. В некоторых вариантах реализации олигонуклеотиды на 95% комплементарны целевой нуклеиновой кислоте. В некоторых вариантах реализации такие олигонуклеотиды на 90% комплементарны целевой нуклеиновой кислоте.
В некоторых вариантах реализации такие олигонуклеотиды на 85% комплементарны целевой нуклеиновой кислоте. В некоторых вариантах реализации такие олигонуклеотиды на 80% комплементарны целевой нуклеиновой кислоте. В некоторых вариантах реализации антисмысловое соединение содержит область, которая полностью комплементарна целевой нуклеиновой кислоте, и по меньшей мере на 80% комплементарно целевой нуклеиновой кислоте по всей длине олигонуклеотида. В некоторых таких вариантах реализации область полной комплементарности имеет от 6 до 14 нуклеозидов в длину.
В некоторых вариантах реализации олигонуклеотиды содержат область гибридизации и концевую область. В некоторых таких вариантах реализации область гибридизации состоит из 12-30 связанных нуклеозидов и полностью комплементарна целевой нуклеиновой кислоте. В некоторых вариантах реализации область гибридизации содержит одно несоответствие в сравнении с целевой нуклеиновой кислотой. В некоторых вариантах реализации область гибридизации содержит два несоответствия в сравнении с целевой нуклеиновой кислотой. В некоторых вариантах реализации область гибридизации содержит три несоответствия в сравнении с целевой нуклеиновой кислотой. В некоторых вариантах реализации концевая область состоит из 1-4 концевых нуклеозидов. В некоторых вариантах реализации концевые нуклеозиды находятся на 3'-конце. В некоторых вариантах реализации один или более концевых нуклеозидов не комплементарны целевой нуклеиновой кислоте.
Антисмысловые механизмы включают любой механизм, затрагивающий гибридизацию олигонуклеотида с целевой нуклеиновой кислотой, при этом гибридизации приводит к биологическому эффекту. В некоторых вариантах реализации такая гибридизация приводит либо к разрушению, либо к применению целевой нуклеиновой кислоты с сопутствующим подавлением или стимулированием клеточного механизма, затрагивающего, например, трансляцию, транскрипцию или сплайсинг целевой нуклеиновой кислоты.
Один из типов антисмыслового механизма, затрагивающий разрушение целевой РНК представляет собой антисмысл, опосредованный РНКазой Н. РНКаза Н представляет собой клеточную эндонуклеазу, которая расщепляет спираль РНК дуплекса РНК : ДНК. В данной области техники известно, что односпиральные антисмысловые соединения, которые являются «ДНК-подобными», вызывают активность РНКазы Н в клетках млекопитающих. Следовательно, активация РНКазы Н приводит к расщеплению РНК-мишени, посредством этого в значительной степени усиливая эффективность подавления генной экспрессии, опосредованного ДНК-подобным олигонуклеотидом.
В некоторых вариантах реализации конъюгирующая группа содержит расщепляемый фрагмент. В некоторых вариантах реализации конъюгирующая группа содержит одну или более расщепляемых связей. В некоторых вариантах реализации конъюгирующая группа содержит линкер. В некоторых вариантах реализации линкер содержит белковый связывающий фрагмент. В некоторых вариантах реализации конъюгирующая группа содержит фрагмент, нацеливающий на клетку (упоминаемый также как группа, нацеливающая на клетку). В некоторых вариантах реализации фрагмент, нацеливающий на клетку, содержит группу ветвления. В некоторых вариантах реализации фрагмент, нацеливающий на клетку, содержит одну или более связок. В некоторых вариантах реализации фрагмент, нацеливающий на клетку, содержит углевод или углеводный кластер.
ii. Некоторые расщепляемые фрагменты
В некоторых вариантах реализации расщепляемый фрагмент представляет собой расщепляемую связь. В некоторых вариантах реализации расщепляемый фрагмент содержит расщепляемую связь. В некоторых вариантах реализации конъюгирующая группа содержит расщепляемый фрагмент. В некоторых таких вариантах реализации расщепляемый фрагмент присоединяется к антисмысловому олигонуклеотиду. В некоторых таких вариантах реализации расщепляемый фрагмент присоединяется непосредственно к фрагменту, нацеливающему на клетку. В некоторых таких вариантах реализации расщепляемый фрагмент присоединяется к линкеру конъюгата. В некоторых вариантах реализации расщепляемый фрагмент содержит фосфат или фосфодиэфир. В некоторых вариантах реализации расщепляемый фрагмент представляет собой расщепляемый нуклеозид или нуклеозидный аналог. В некоторых вариантах реализации нуклеозид или нуклеозидный аналог содержит необязательно защищенное гетероциклическое основание, выбранное из пурина, замещенного пурина, пиримидина или замещенного пиримидина. В некоторых вариантах реализации расщепляемый фрагмент представляет собой нуклеозид, содержащий необязательно защищенное гетероциклическое основание, выбранное из урацила, тимина, цитозина, 4-N-бензоилцитозина, 5-метилцитозина, 4-N-бензоил-5-метилцитозина, аденина, 6-N-бензоиладенина, гуанина и 2-N-изобутирилгуанина. В некоторых вариантах реализации расщепляемый фрагмент представляет собой 2'-дезоксинуклеозид, который присоединен к 3'-положению антисмыслового олигонуклеотида фосфодиэфирной связью и присоединен к линкеру фосфодиэфирной или тиофосфатной связью. В некоторых вариантах реализации расщепляемый фрагмент представляет собой 2'-дезоксиаденозин, который присоединен к 3'-положению антисмыслового олигонуклеотида фосфодиэфирной связью и присоединен к линкеру фосфодиэфирной или тиофосфатной связью. В некоторых вариантах реализации расщепляемый фрагмент представляет собой 2'-дезоксиаденозин, который присоединен к 3'-положению антисмыслового олигонуклеотида фосфодиэфирной связью и присоединен к линкеру фосфодиэфирной связью.
В некоторых вариантах реализации расщепляемый фрагмент присоединен к 3'-положению антисмыслового олигонуклеотида. В некоторых вариантах реализации расщепляемый фрагмент присоединен к 5'-положению антисмыслового олигонуклеотида. В некоторых вариантах реализации расщепляемый фрагмент присоединен к 2'-положению антисмыслового олигонуклеотида. В некоторых вариантах реализации расщепляемый фрагмент присоединен к антисмысловому олигонуклеотиду фосфодиэфирной связью. В некоторых вариантах реализации расщепляемый фрагмент присоединен к указанному линкеру либо фосфодиэфирной, либо тиофосфатной связью. В некоторых вариантах реализации расщепляемый фрагмент присоединен к указанному линкеру фосфодиэфирной связью. В некоторых вариантах реализации конъюгирующая группа не содержит расщепляемый фрагмент.
В некоторых вариантах реализации расщепляемый фрагмент расщепляется после введения указанного комплекса в организм животного только после его поглощение целевой клеткой. Внутри клетки расщепляемый фрагмент расщепляется, высвобождая таким образом активный антисмысловый олигонуклеотид. Не ограничиваясь теорией, предполагается, что расщепляемый фрагмент расщепляется под действием одной или более нуклеаз внутри клетки. В некоторых вариантах реализации одна или более нуклеаз расщепляют фосфодиэфирную связь между расщепляемым фрагментом и линкером. В некоторых вариантах реализации расщепляемый фрагмент имеет структуру, выбранную из следующих:
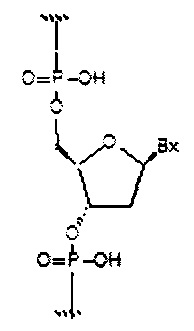
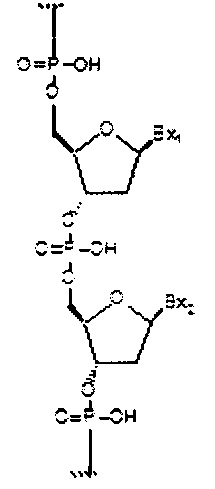
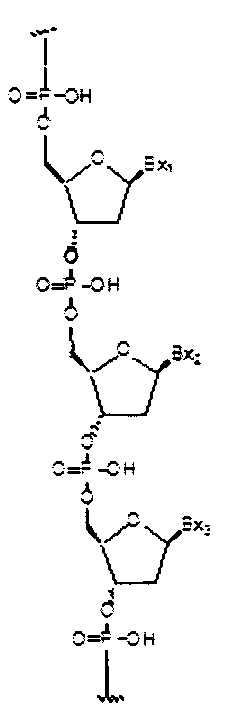
где каждый из Вх, Bx1, Вх2 и Вх3 независимо представляет собой гетероциклический основной фрагмент. В некоторых вариантах реализации расщепляемый фрагмент имеет структуру, выбранную из следующих:
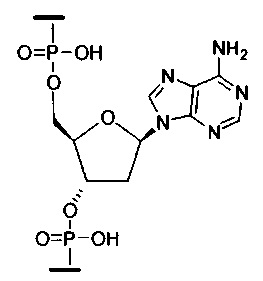
iii. Некоторые линкеры
В некоторых вариантах реализации конъюгирующие группы содержат линкер. В некоторых таких вариантах реализации линкер ковалентно связан с расщепляемым фрагментом. В некоторых таких вариантах реализации линкер ковалентно связан с антисмысловым олигонуклеотидом. В некоторых вариантах реализации линкер ковалентно связан с фрагментом, нацеливающим на клетку. В некоторых вариантах реализации линкер дополнительно содержит ковалентное присоединение к твердой подложке. В некоторых вариантах реализации линкер дополнительно содержит ковалентное присоединение к белковому связывающему фрагменту. В некоторых вариантах реализации линкер дополнительно содержит ковалентное присоединение к твердой подложке и дополнительно содержит ковалентное присоединение к белковому связывающему фрагменту. В некоторых вариантах реализации линкер содержит несколько положений для присоединения связанных лигандов. В некоторых вариантах реализации линкер содержит несколько положений для присоединения связанных лигандов и не присоединен к группе ветвления. В некоторых вариантах реализации линкер дополнительно содержит одну или более расщепляемых связей. В некоторых вариантах реализации конъюгирующая группа не содержит линкер.
В некоторых вариантах реализации линкер содержит по меньшей мере одну линейную группу, содержащую группы, выбранные из алкильных, амидных, дисульфидных, полиэтиленгликолевых, тиоэфирных (-S-) и гидроксиламино (-O-N(H)-) групп. В некоторых вариантах реализации линейная группа содержит группы, выбранные из алкильных, амидных и простых эфирных групп. В некоторых вариантах реализации линейная группа содержит группы, выбранные из алкильных и простых эфирных групп. В некоторых вариантах реализации линейная группа содержит по меньшей мере одну фосфорную связывающую группу. В некоторых вариантах реализации линейная группа содержит по меньшей мере одну фосфодиэфирную группу. В некоторых вариантах реализации линейная группа содержит по меньшей мере одну нейтральную связывающую группу. В некоторых вариантах реализации линейная группа ковалентно присоединена к фрагменту, нацеливающему на клетку, и к расщепляемому фрагменту. В некоторых вариантах реализации линейная группа ковалентно присоединена к фрагменту, нацеливающему на клетку, и к антисмысловому олигонуклеотиду. В некоторых вариантах реализации линейная группа ковалентно присоединена к фрагменту, нацеливающему на клетку, к расщепляемому фрагменту и к твердой подложке. В некоторых вариантах реализации линейная группа ковалентно присоединена к фрагменту, нацеливающему на клетку, к расщепляемому фрагменту, к твердой подложке и к белковому связывающему фрагменту. В некоторых вариантах реализации линейная группа содержит одну или более расщепляемых связей.
В некоторых вариантах реализации линкер содержит линейную группу, ковалентно присоединенную к группе скелета. В некоторых вариантах реализации скелет содержит разветвленную алифатическую группу, которая содержит группы, выбранные из алкильных, амидных, дисульфидных, полиэтиленгликолевых, простых эфирных, тиоэфирных и гидроксиламино-групп. В некоторых вариантах реализации скелет содержит разветвленную алифатическую группу, которая содержит группы, выбранные из алкильных, амидных и простых эфирных групп. В некоторых вариантах реализации скелет содержит по меньшей мере одну моно- или полициклическую кольцевую систему. В некоторых вариантах реализации скелет содержит по меньшей мере две моно- или полициклические кольцевые системы. В некоторых вариантах реализации линейная группа ковалентно присоединена к группе скелета, а группа скелета ковалентно присоединена к расщепляемому фрагменту и линкеру. В некоторых вариантах реализации линейная группа ковалентно присоединена к группе скелета, а группа скелета ковалентно присоединена к расщепляемому фрагменту, линкеру и твердой подложке. В некоторых вариантах реализации линейная группа ковалентно присоединена к группе скелета, а группа скелета ковалентно присоединена к расщепляемому фрагменту, линкеру и белковому связывающему фрагменту. В некоторых вариантах реализации линейная группа ковалентно присоединена к группе скелета, а группа скелета ковалентно присоединена к расщепляемому фрагменту, линкеру, белковому связывающему фрагменту и твердой подложке. В некоторых вариантах реализации группа скелета содержит одну или более расщепляемых связей.
В некоторых вариантах реализации линкер содержит белковый связывающий фрагмент. В некоторых вариантах реализации белковый связывающий фрагмент представляет собой липид, такой как, например, включая, но не ограничиваясь ими, холестерин, холевая кислота, адамантан-уксусная кислота, 1-пирен-масляная кислота, дигидротестостерон, 1,3-бис-O(гексадецил)глицерин, геранилоксигексиловая группа, гексадецилглицерин, борнеол, ментол, 1,3-пропандиол, гептадециловая группа, пальмитиновая кислота, миристиновая кислота, O3-(олеоил)литохолевая кислота, O3-(олеоил)холеновая кислота, диметокситритил или феноксазин, витамин (например, фолат, витамин А, витамин Е, биотин, пиридоксаль), пептид, углевод (например, моносахарид, дисахарид, трисахарид, тетрасахарид, олигосахарид, полисахарид), эндосомолитичсский компонент, стероид (например, уваол, гецигенин, диосгенин), терпен (например, тритерпеи. например, сарсасапогенин, фриделин, литохолевая кислота, дериватизованная эпифриделанолом) или катионный липид. В некоторых вариантах реализации белковый связывающий фрагмент представляет собой насыщенную или ненасыщенную жирную кислоту с длиной цепи от С16 до С22, холестерин, холевую кислоту, витамин Е, адамантан или 1-пентафторпропил.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
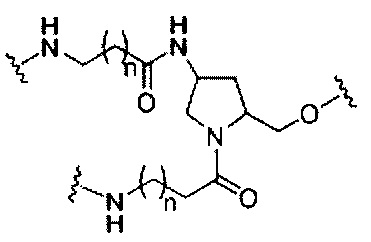
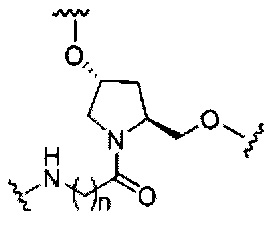
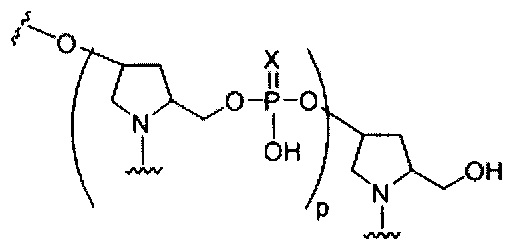
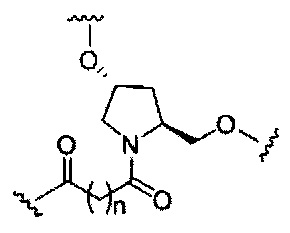
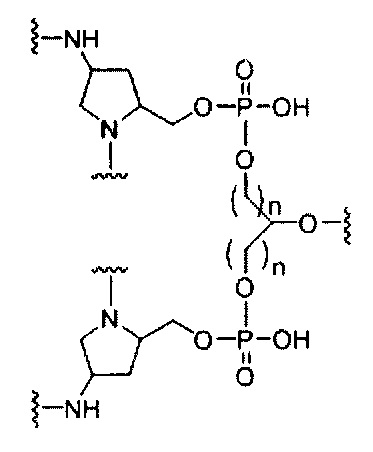
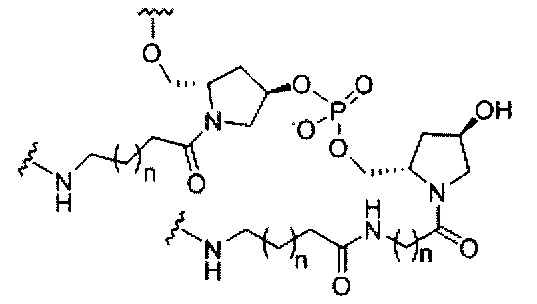
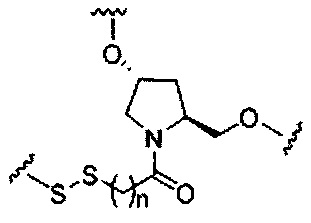
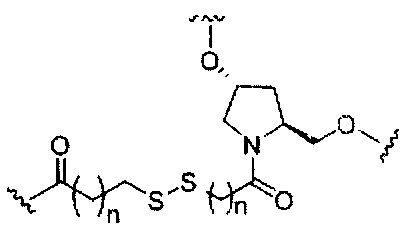
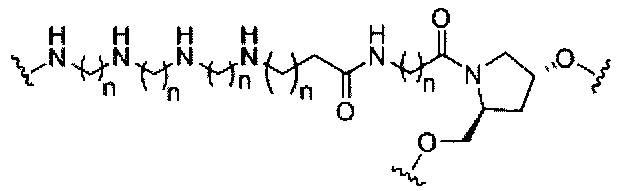
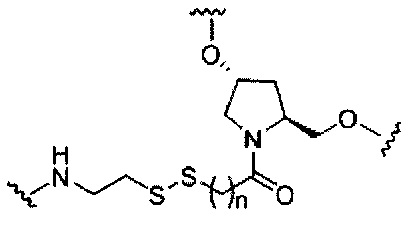
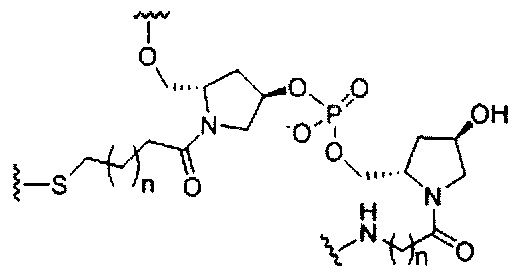
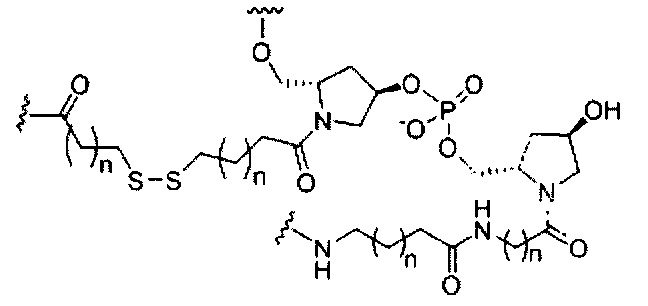
где каждый n независимо равен от 1 до 20; и р равен от 1 до 6.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
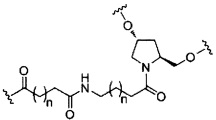
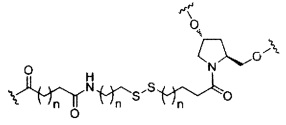
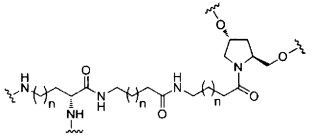

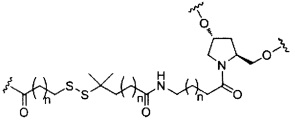
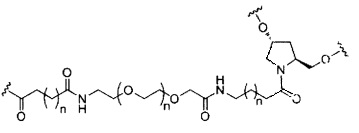
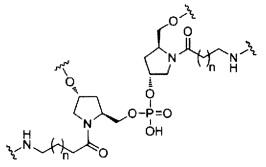
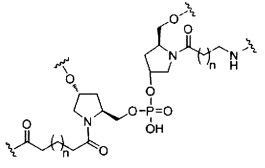
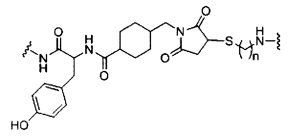
где каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
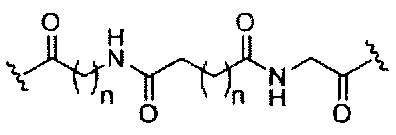
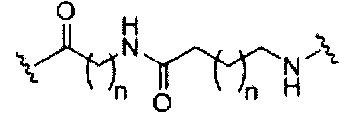
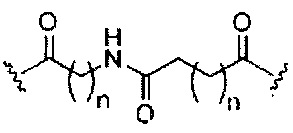
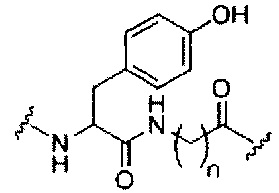
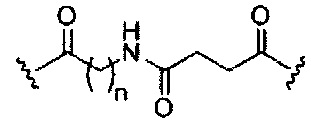
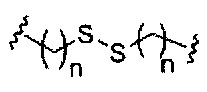
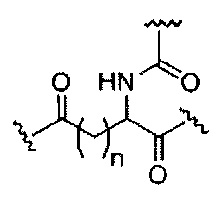
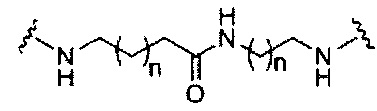

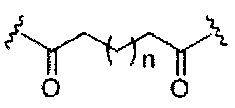
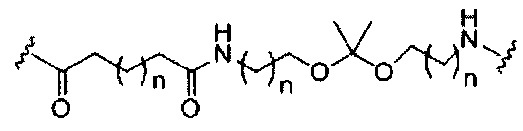
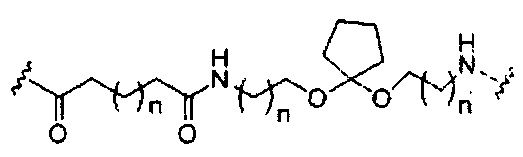
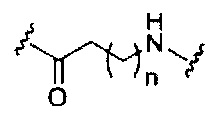
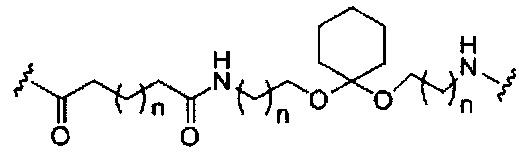
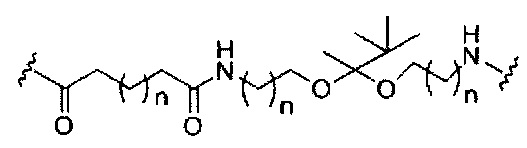
где n равен от 1 до 20.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
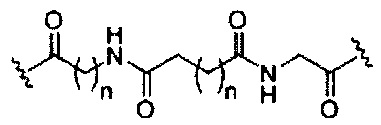
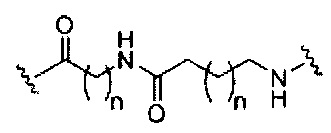
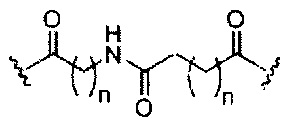
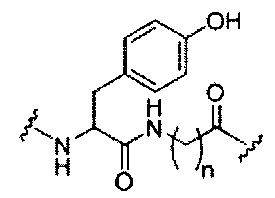
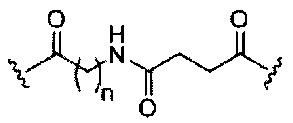
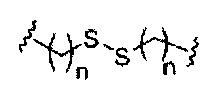
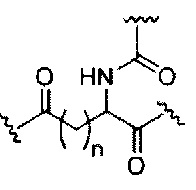
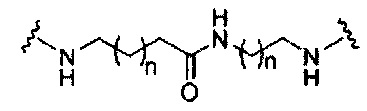

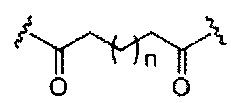
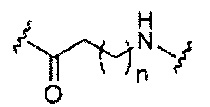
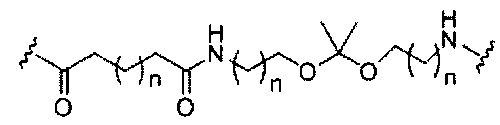

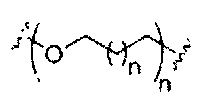
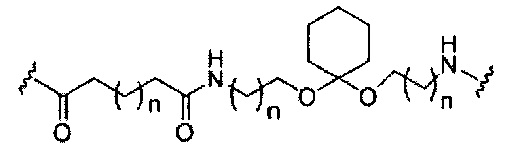
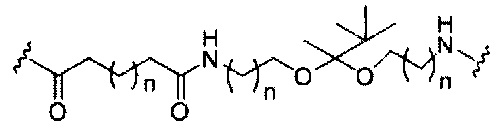
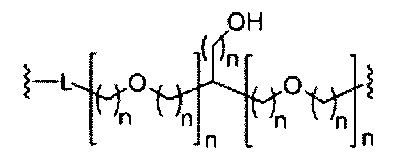
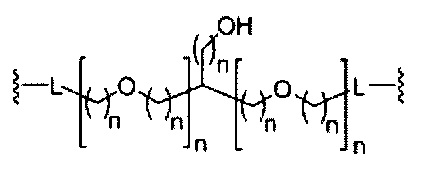
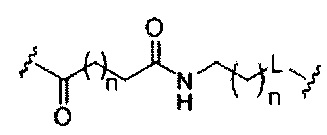
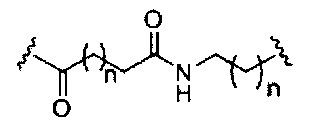
где каждый L независимо представляет собой фосфорную связывающую группу или нейтральную связывающую группу; и
каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
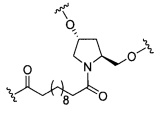
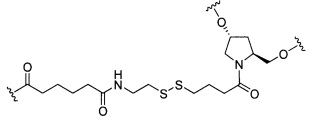
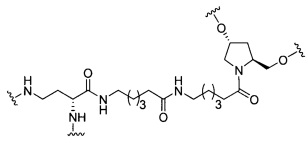

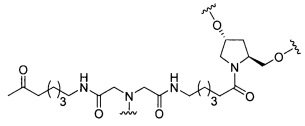
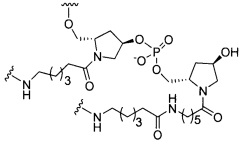

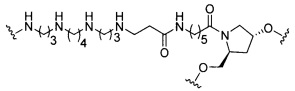
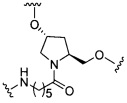
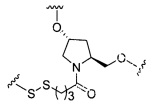
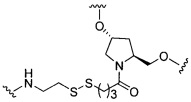
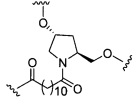
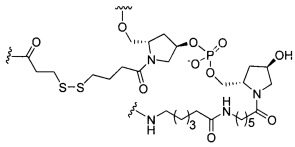
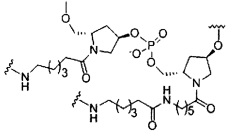
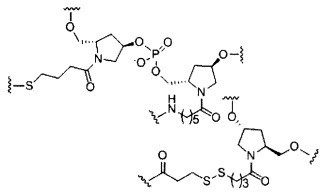
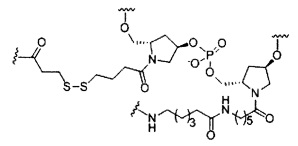
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
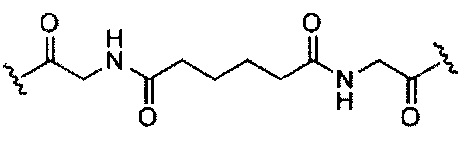
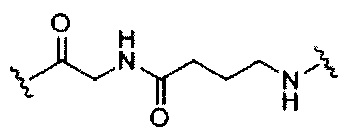
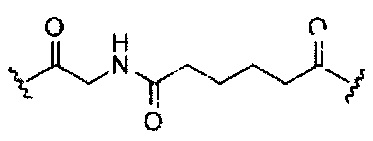
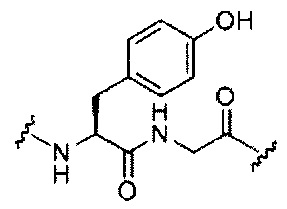
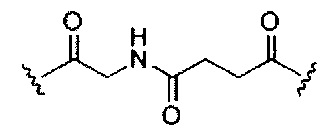
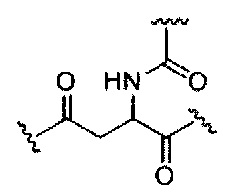
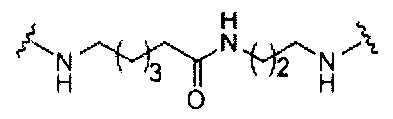

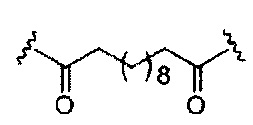
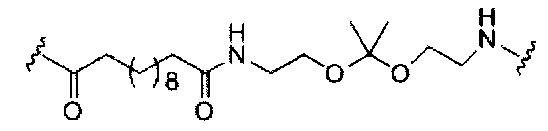
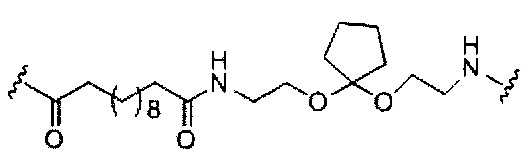
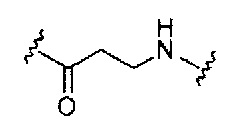
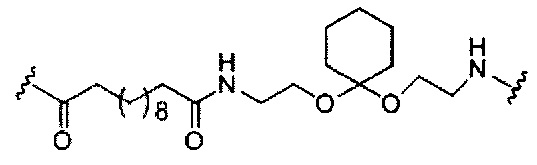
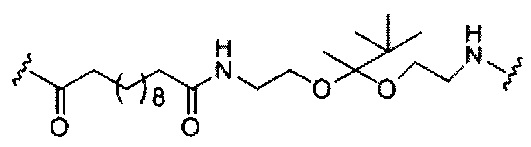
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
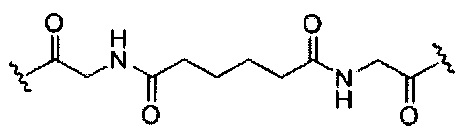
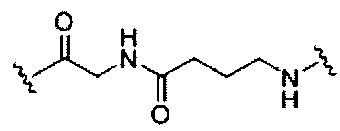
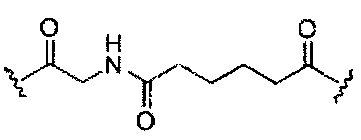
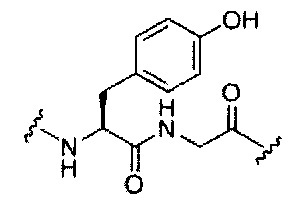
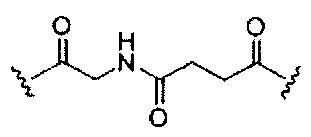
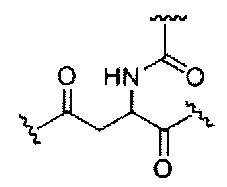
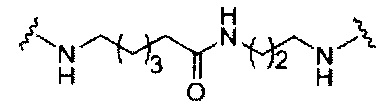

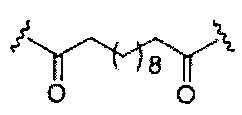
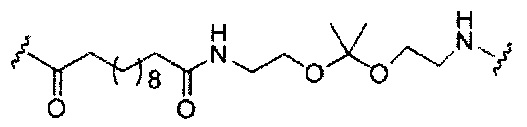
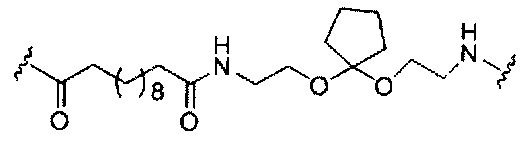
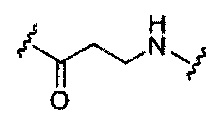
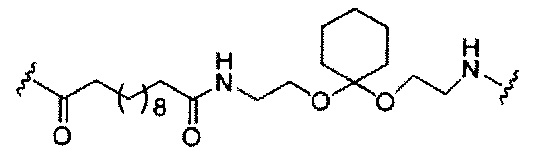
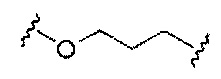
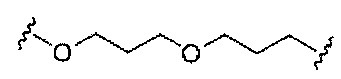
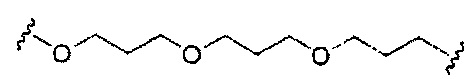
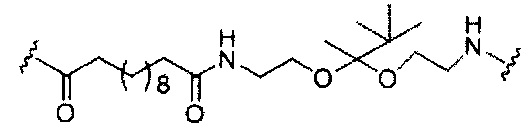
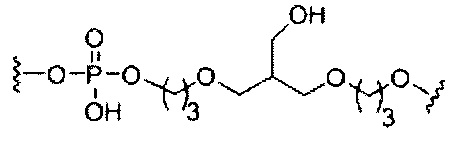
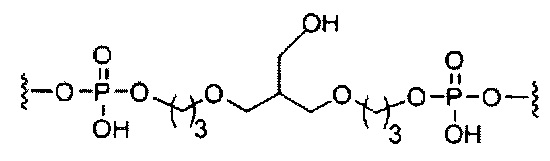
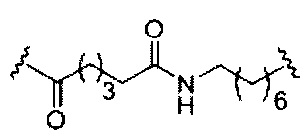
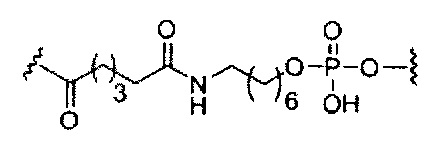
В некоторых вариантах реализации линкер имеет структуру, выбранную из:

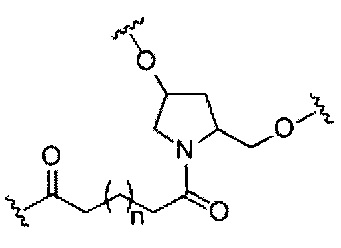
где n равен от 1 до 20.
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
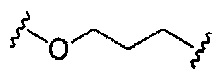
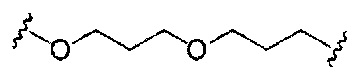
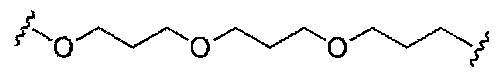
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
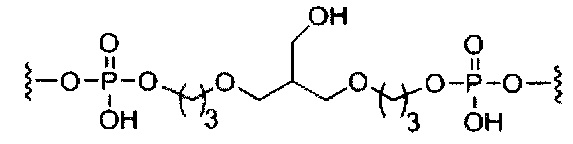
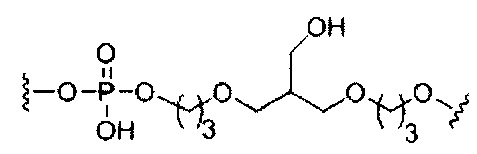
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
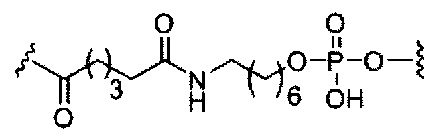
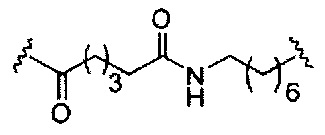
В некоторых вариантах реализации линкер конъюгата имеет структуру:
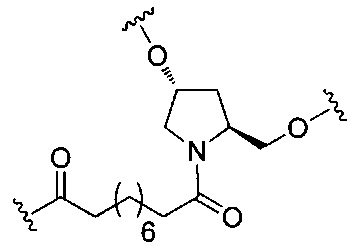
В некоторых вариантах реализации линкер конъюгата имеет структуру:
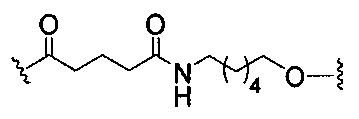
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
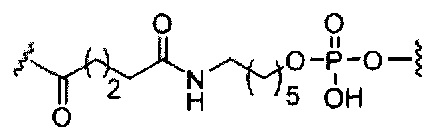
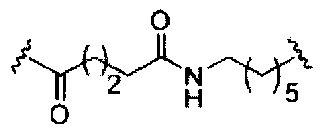
В некоторых вариантах реализации линкер имеет структуру, выбранную из:
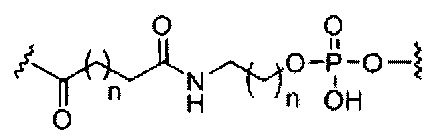
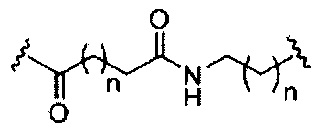
где каждый n независимо равен 0, 1, 2, 3, 4, 5, 6 или 7.
iv. Некоторые фрагменты, нацеливающие на клетку
В некоторых вариантах реализации конъюгирующие группы содержат фрагменты, нацеливающие на клетку. Некоторые такие фрагменты, нацеливающие на клетку, увеличивают клеточный захват антисмысловых соединений. В некоторых вариантах реализации фрагменты, нацеливающие на клетку, содержат группу ветвления, одну или более связок и один или более лигандов. В некоторых вариантах реализации фрагменты, нацеливающие на клетку, содержат группу ветвления, одну или более связок, один или более лигандов и одну или более расщепляемых связей.
1. Некоторые группы ветвления
В некоторых вариантах реализации конъюгирующие группы содержат нацеливающий фрагмент, содержащий группу ветвления и по меньшей мере два связанных лиганда. В некоторых вариантах реализации группа ветвления присоединяет линкер конъюгата. В некоторых вариантах реализации группа ветвления присоединяет расщепляемый фрагмент. В некоторых вариантах реализации группа ветвления присоединяет антисмысловый олигонуклеотид. В некоторых вариантах реализации группа ветвления ковалентно присоединена к линкеру и каждому из связанных лигандов. В некоторых вариантах реализации группа ветвления содержит разветвленную алифатическую группу, которая содержит группы, выбранные из алкильных, амидных, дисульфидных, полиэтиленгликолевых, простых эфирных, тиоэфирных и гидроксиламино-групп. В некоторых вариантах реализации группа ветвления содержит группы, выбранные из алкильных, амидных и простых эфирных групп. В некоторых вариантах реализации группа ветвления содержит группы, выбранные из алкильных и простых эфирных групп. В некоторых вариантах реализации группа ветвления содержит моно- или полициклическую кольцевую систему. В некоторых вариантах реализации группа ветвления содержит одну или более расщепляемых связей. В некоторых вариантах реализации конъюгирующая группа не содержит группу ветвления.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
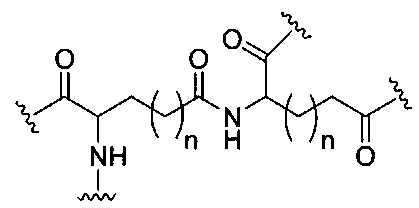
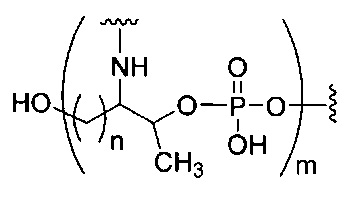
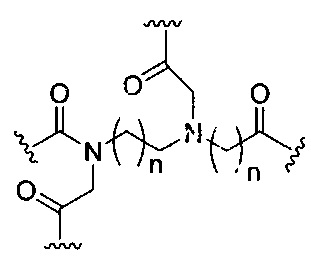
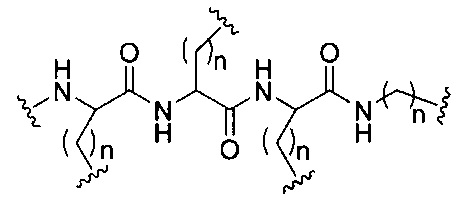
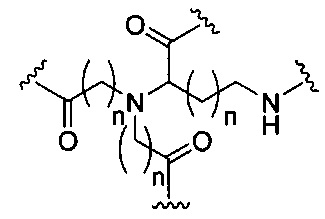
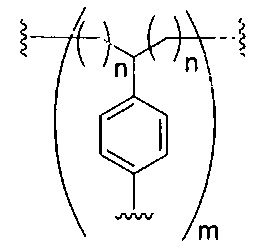
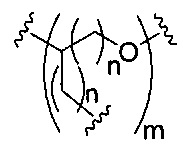
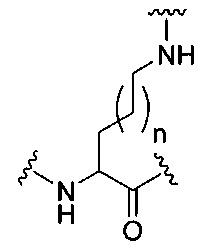
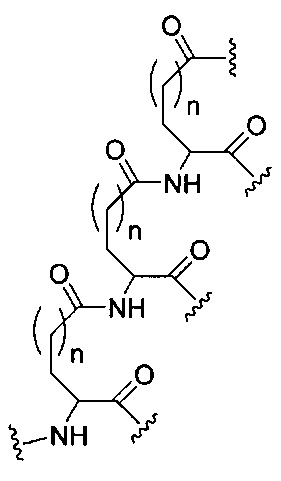
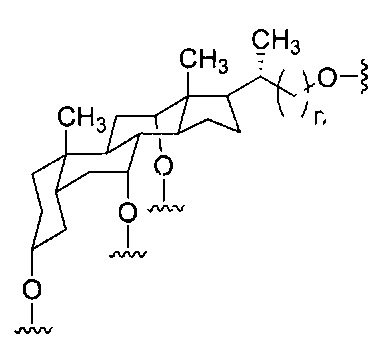
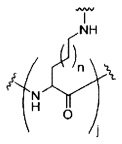
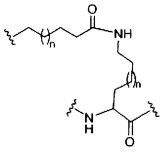
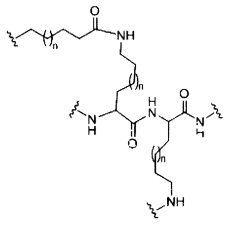
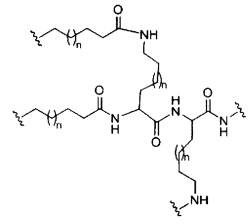
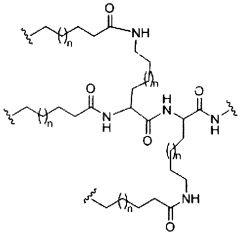
где каждый n независимо равен от 1 до 20;
j равен от 1 до 3; и
m равен от 2 до 6.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
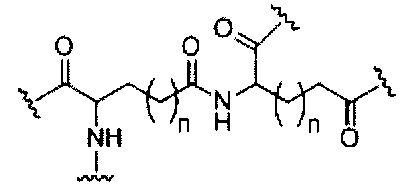
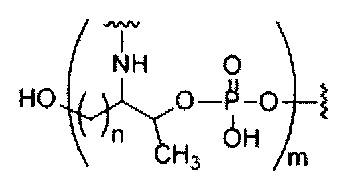
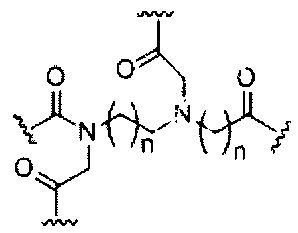
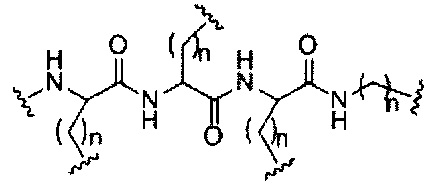
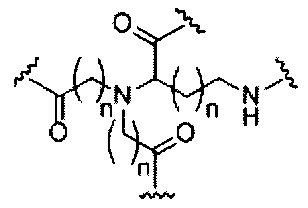
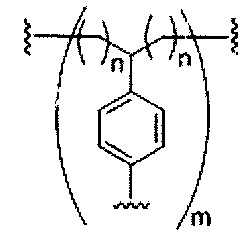
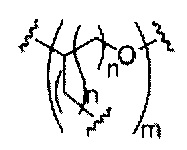
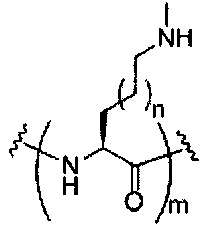
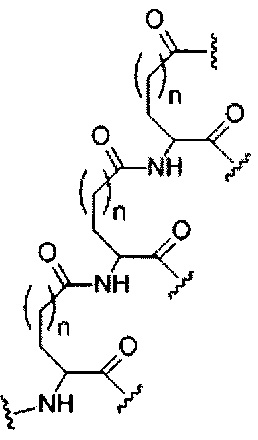
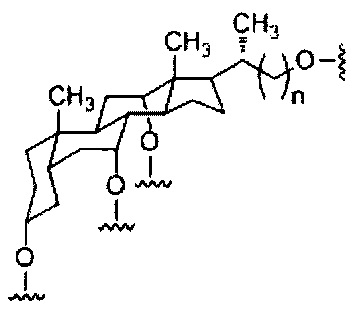
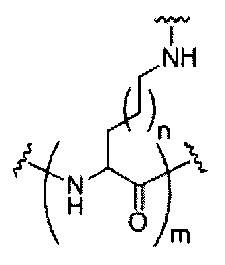
где каждый n независимо равен от 1 до 20; и
m равен от 2 до 6.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
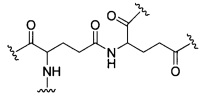
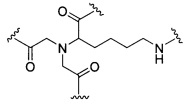
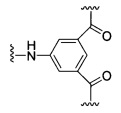
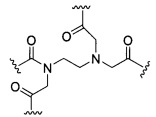
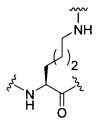
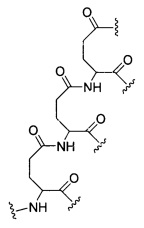
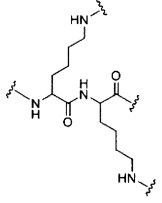
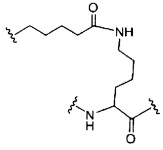
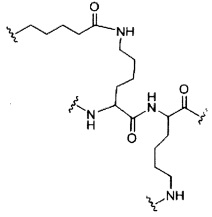
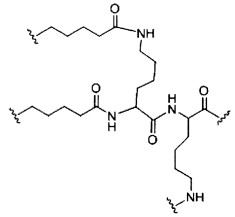
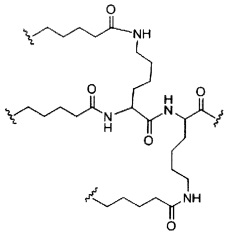
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
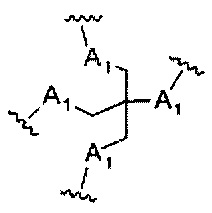
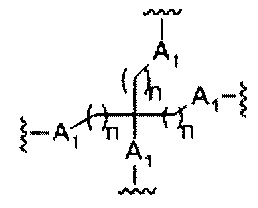
где каждый A1 независимо представляет собой О, S, С=O или NH; и
каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
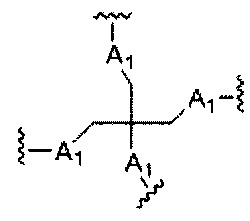
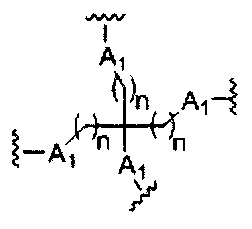
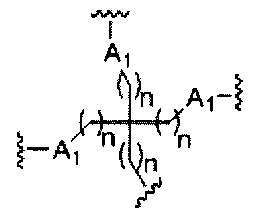
где каждый A1 независимо представляет собой О, S, С=O или NH; и
каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
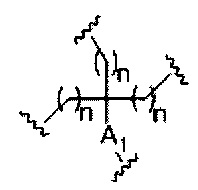
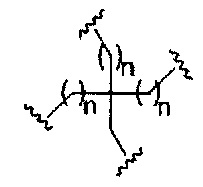
где А1 представляет собой О, S, С=O или NH; и
каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
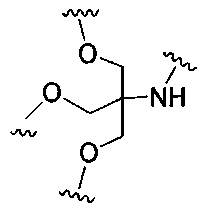
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
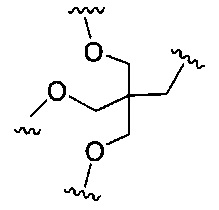
В некоторых вариантах реализации группа ветвления имеет структуру, выбранную из:
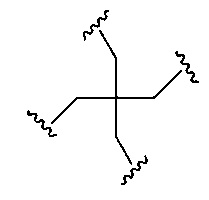
2. Некоторые связки
В некоторых вариантах реализации конъюгирующие группы содержат одну или более связок, ковалентно присоединенных к группе ветвления. В некоторых вариантах реализации конъюгирующие группы содержат одну или более связок, ковалентно присоединенных к связывающей группе. В некоторых вариантах реализации каждая связка представляет собой линейную алифатическую группу, содержащую одну или более групп, выбранных из алкильных, простых эфирных, тиоэфирных, дисульфидных, амидных и полиэтиленгликолевых групп в любой комбинации. В некоторых вариантах реализации каждая связка представляет собой линейную алифатическую группу, содержащую одну или более групп, выбранных из алкильных, замещенных алкильных, простых эфирных, тиоэфирных, дисульфидных, амидных, фосфодиэфирных и полиэтиленгликолевых групп в любой комбинации. В некоторых вариантах реализации каждая связка представляет собой линейную алифатическую группу, содержащую одну или более групп, выбранных из алкильных, простых эфирных и амидных групп в любой комбинации. В некоторых вариантах реализации каждая связка представляет собой линейную алифатическую группу, содержащую одну или более групп, выбранных из алкильных, замещенных алкильных, фосфодиэфирных, простых эфирных и амидных групп в любой комбинации. В некоторых вариантах реализации каждая связка представляет собой линейную алифатическую группу, содержащую одну или более групп, выбранных из алкила и фосфодиэфира в любой комбинации. В некоторых вариантах реализации каждая связка содержит по меньшей мере одну фосфорную связывающую группу или нейтральную связывающую группу.
В некоторых вариантах реализации связка содержит одну или более расщепляемых связей. В некоторых вариантах реализации связка присоединена к группе ветвления через амидную или простую эфирную группу. В некоторых вариантах реализации связка присоединена к группе ветвления через фосфордиэфирную группу. В некоторых вариантах реализации связка присоединена к группе ветвления через фосфорную связывающую группу или через нейтральную связывающую группу. В некоторых вариантах реализации связка присоединена к группе ветвления через простую эфирную группу. В некоторых вариантах реализации связка присоединена к лиганду либо через амидную, либо через простую эфирную группу. В некоторых вариантах реализации связка присоединена к лиганду через простую эфирную группу. В некоторых вариантах реализации связка присоединена к лиганду либо через амидную, либо через простую эфирную группу. В некоторых вариантах реализации связка присоединена к лиганду через простую эфирную группу.
В некоторых вариантах реализации каждая связка имеет длину от около 8 до около 20 атомов в цепи между лигандом и группой ветвления. В некоторых вариантах реализации каждая связка имеет длину от около 10 до около 18 атомов в цепи между лигандом и группой ветвления. В некоторых вариантах реализации каждая связка имеет длину около 13 атомов в цепи.
В некоторых вариантах реализации связка имеет структуру, выбранную из:
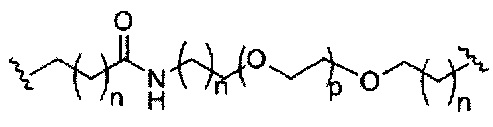
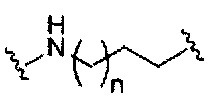
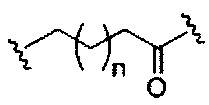
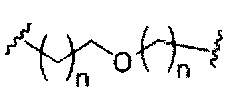
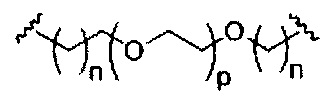
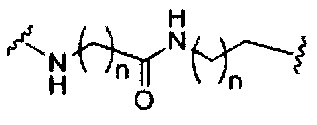
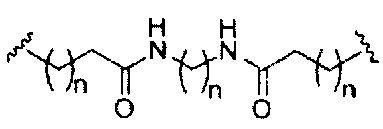
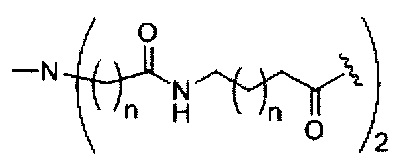
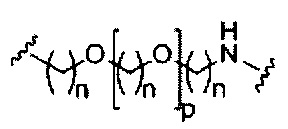
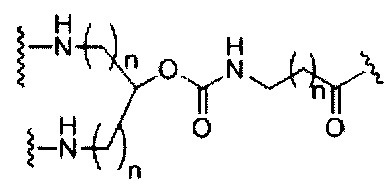
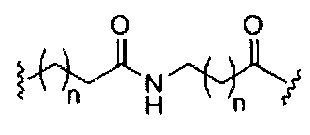

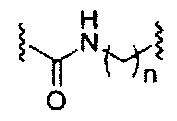
где каждый n независимо равен от 1 до 20; и
каждый р равен от 1 до около 6.
В некоторых вариантах реализации связка имеет структуру, выбранную из:
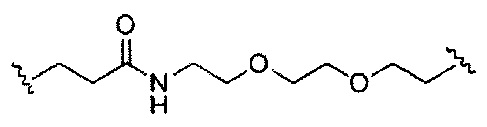
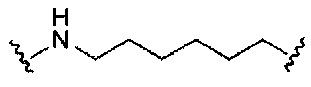
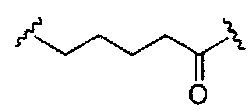
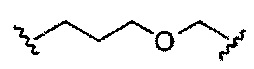
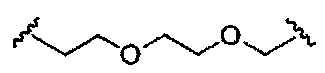
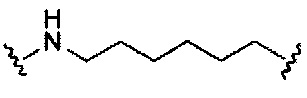
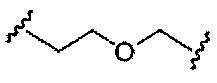
В некоторых вариантах реализации связка имеет структуру, выбранную из:
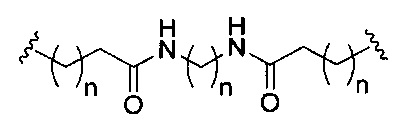
где каждый n независимо равен от 1 до 20.
В некоторых вариантах реализации связка имеет структуру, выбранную из:
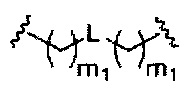
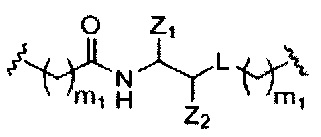
где L представляет собой либо фосфорную связывающую группу, либо нейтральную связывающую группу;
Z1 представляет собой C(=O)O-R2;
Z2 представляет собой Н, C1-С6 алкил или замещенный C1-С6 алкил;
R2 представляет собой Н, С1-С6 алкил или замещенный C1-С6 алкил;
и каждый m1 независимо равен от 0 до 20, при этом по меньшей мере один m1 больше 0 для каждой связки.
В некоторых вариантах реализации связка имеет структуру, выбранную из:
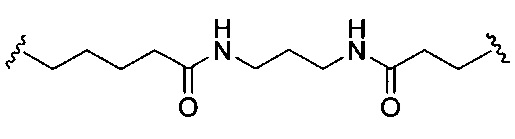
В некоторых вариантах реализации связка имеет структуру, выбранную из:
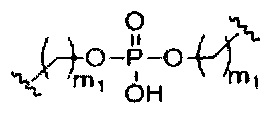
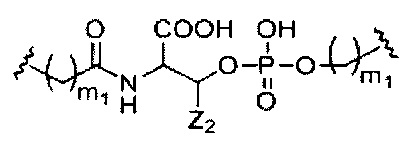
где Z2 представляет собой Н или СН3; и
каждый m1 независимо равен от 0 до 20, при этом по меньшей мере один m1 больше 0 для каждой связки.
В некоторых вариантах реализации связка имеет структуру, выбранную из:
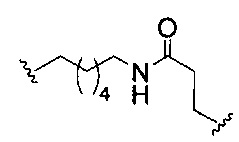
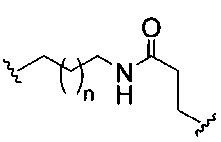
В некоторых вариантах реализации связка содержит фосфорную связывающую группу. В некоторых вариантах реализации связка не содержит ни одной амидной связи. В некоторых вариантах реализации связка содержит фосфорную связывающую группу и не содержит ни одной амидной связи.
3. Некоторые лиганды
В некоторых вариантах реализации настоящего описания приведены лиганды, при этом каждый лиганд ковалентно присоединен к связке. В некоторых вариантах реализации каждый лиганд выбран так, чтобы он обладал аффинностью по меньшей мере к одному типу рецептора на клетке-мишени. В некоторых вариантах реализации лиганды выбраны гак, чтобы они обладали аффинностью по меньшей мере к одному типу рецептора на поверхности клетки печени млекопитающего. В некоторых вариантах реализации лиганды выбраны так, чтобы они обладали аффинностью к печеночному асиалогликопротеиновому рецептору (ASGP-R). В некоторых вариантах реализации каждый лиганд представляет собой углевод. В некоторых вариантах реализации каждый лиганд независимо выбран из галактозы, N-ацетилгалактозамина, маннозы, глюкозы, глюкозамина и фукозы. В некоторых вариантах реализации каждый лиганд представляет собой N-ацетилгалактозамин (GalNAc). В некоторых вариантах реализации нацеливающий фрагмент содержит 2-6 лигандов. В некоторых вариантах реализации нацеливающий фрагмент содержит 3 лиганда. В некоторых вариантах реализации нацеливающий фрагмент содержит 3 N-ацетилгалактозаминовых лиганда.
В некоторых вариантах реализации лиганд представляет собой углевод, углеводное производное, модифицированный углевод, поливалентный углеводный кластер, полисахарид, модифицированный полисахарид или полисахаридное производное. В некоторых вариантах реализации лиганд представляет собой аминосахар или тиосахар. Например, аминосахара могут быть выбраны из любого количества соединений, известных в данной области техники, например, глюкозамина, сиаловой кислоты, α-D-галактозамина, N-ацетилгалактозамина, 2-ацетамидо-2-дезокси-D-галактопиранозы (GalNAc), 2-амино-3-O-[(R)-1-карбоксиэтил]-2-дезокси-β-D-глюкопиранозы (β-мурамовой кислоты), 2-дезокси-2-метиламино-L-глюкопиранозы, 4,6-дидезокси-4-формамидо-2,3-ди-O-метил-D-маннопиранозы, 2-дезокси-2-сульфоамино-D-глюкопиранозы и N-сульфо-D-глюкозамина, и N-гликолоил-α-нейраминовой кислоты. Например, тиосахара могут быть выбраны из группы, состоящей из 5-тио-β-D-глюкопиранозы, метил 2,3,4-три-O-ацетил-1-тио-6-O-тритил-α-D-глюкопиранозида, 4-тио-β-D-галактопиранозы и этил 3,4,6,7-тетра-O-ацетил-2-дезокси-1,5-дитио-α-О-глюко-гептопиранозида.
В некоторых вариантах реализации «GalNac» или «Gal-NAc» относится к 2-(ацетиламино)-2-дезокси-D-галактопиранозе, обычно упоминаемой в литературе как N-ацетилгалактозамин. В некоторых вариантах реализации «N-ацетилгалактозамин» относится к 2-(ацетиламино)-2-дезокси-D-галактопиранозе. В некоторых вариантах реализации «GalNac» или «Gal-NAc» относится к 2-(ацетиламино)-2-дезокси-D-галактопиранозе. В некоторых вариантах реализации «GalNac» или «Gal-NAc» относится к 2-(ацетиламино)-2-дезокси-О-галактопиранозе, которая включает и β-форму: 2-(ацетиламино)-2-дезокси-β-D-галактопиранозу, и α-форму: 2-(ацетиламино)-2-дезокси-D-галактопиранозу. В некоторых вариантах реализации обе формы, β-форма: 2-(ацетиламино)-2-дезокси-β-D-галактопираноза, и α-форма: 2-(ацетиламино)-2-дезокси-D-галактопираноза, могут быть использованы взаимозаменяемо. Соответственно, в структурах, в которых изображена одна форма, подразумевается, что эти структуры включают также и другую форму. Например, если показана структура для α-формы: 2-(ацетиламино)-2-дезокси-D-галактопиранозы, то подразумевается, что эта структура включает также и другую форму. В некоторых, предпочтительных вариантах реализации β-форма 2-(ацетиламино)-2-дезокси-D-галактопиранозы является предпочтительным вариантом реализации.
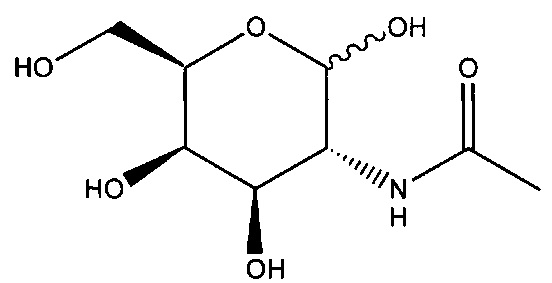
2-(Ацетиламино)-2-дезокси-D-галактопираноза
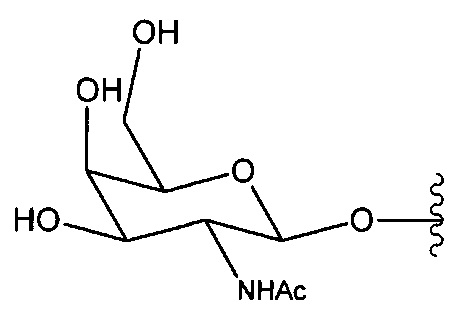
2-(Ацетиламино)-2-дезокси-β-D-галактопираноза
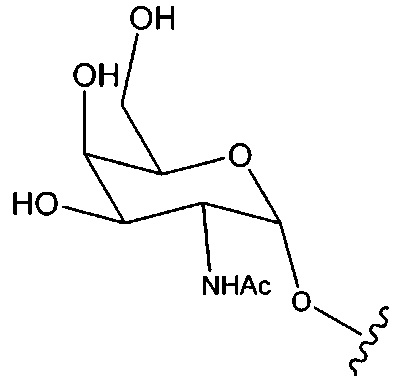
2-(Ацетиламино)-2-дезокси-α-D-галактопираноза
В некоторых вариантах один или более лигандов имеют структуру, выбранную из:
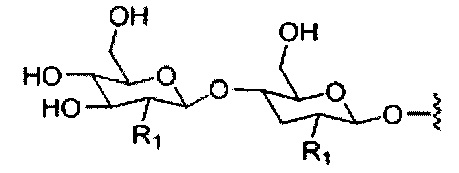
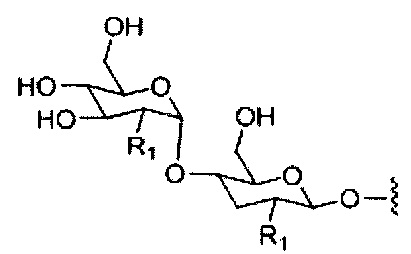
где каждый R1 выбран из ОН и NHCOOH.
В некоторых вариантах один или более лигандов имеют структуру, выбранную из:
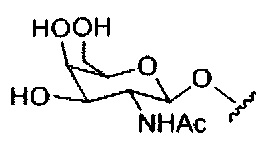
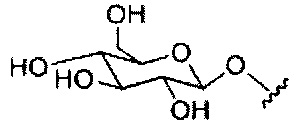
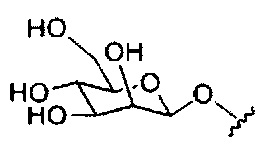
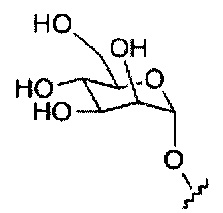
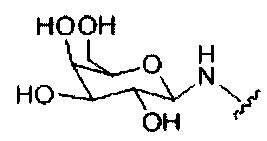
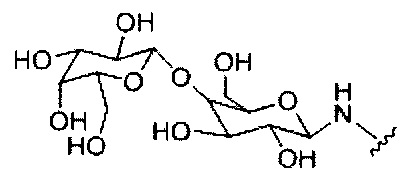
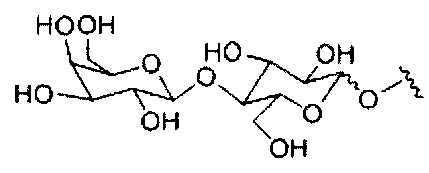
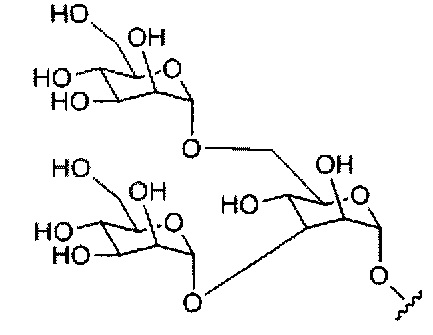
В некоторых вариантах один или более лигандов имеют структуру, выбранную из:
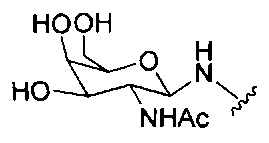
В некоторых вариантах один или более лигандов имеют структуру, выбранную из:
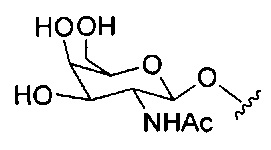
i. Некоторые конъюгаты
В некоторых вариантах реализации конъюгирующие группы содержат структурные особенности, приведенные выше. В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
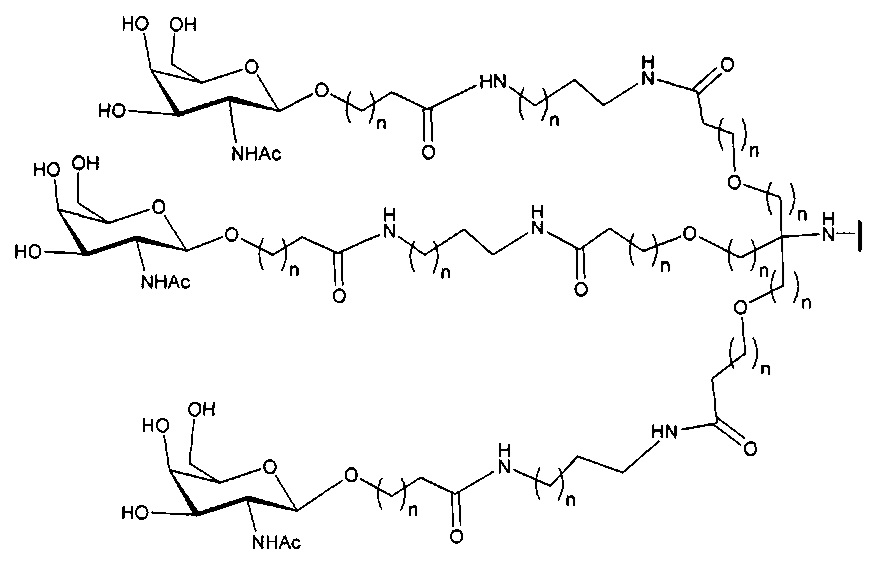
где каждый n независимо равен от 1 до 20.
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
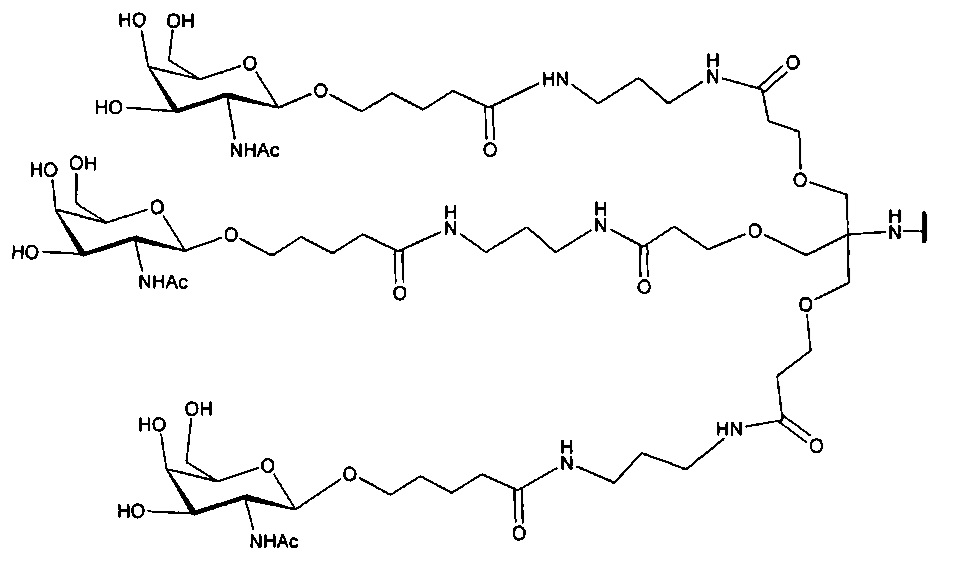
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
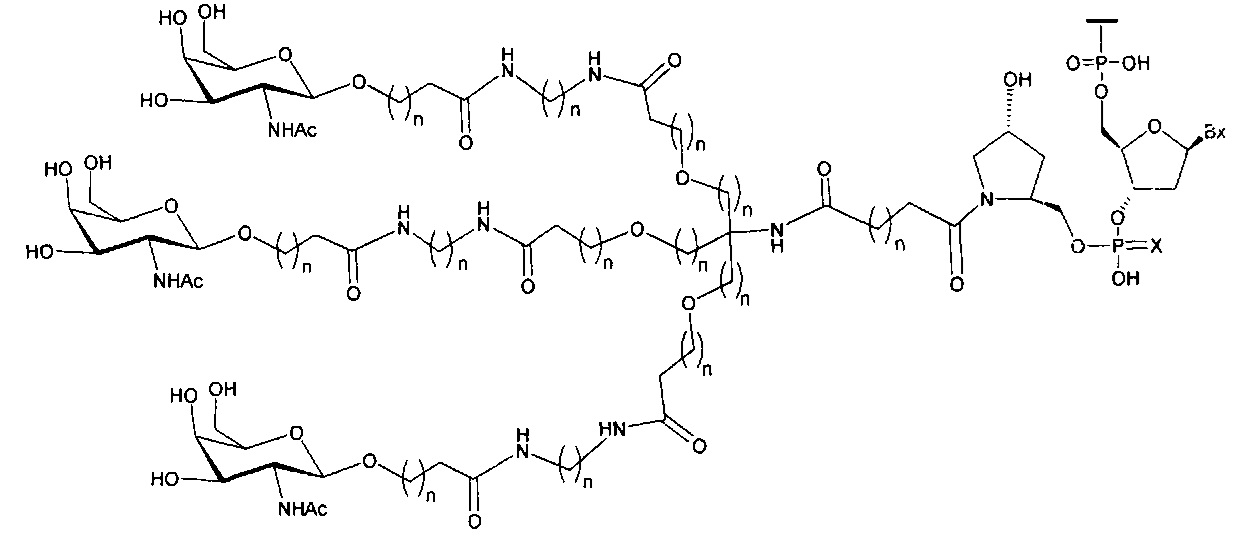
где каждый n независимо равен от 1 до 20;
Z представляет собой Н или связанную твердую подложку;
Q представляет собой антисмысловое соединение;
X представляет собой О или S; и
Вх представляет собой гетероциклический основной фрагмент.
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
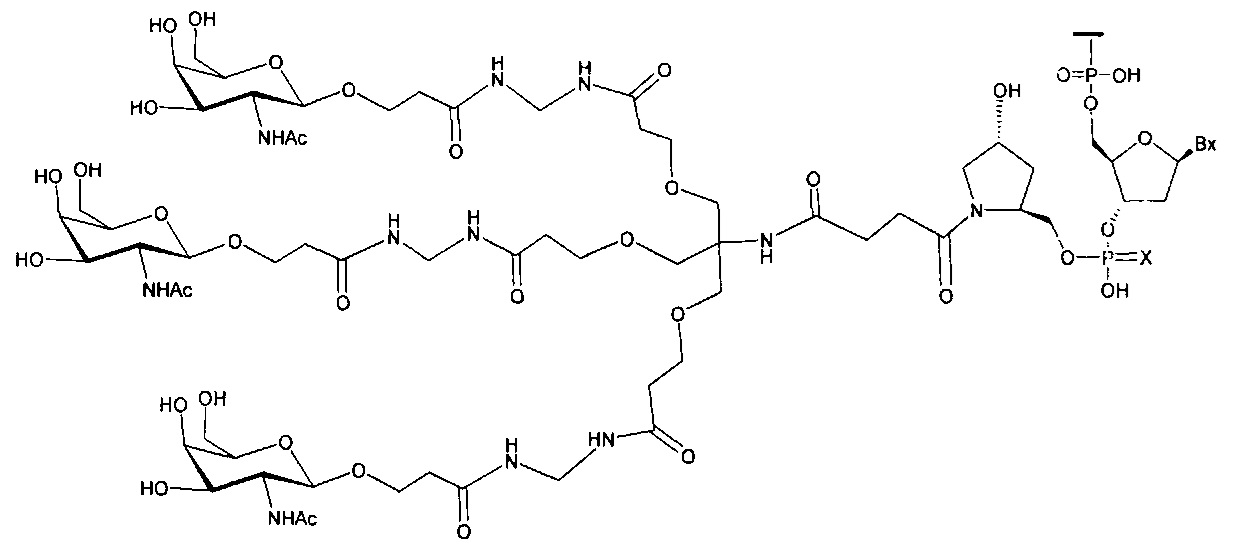
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
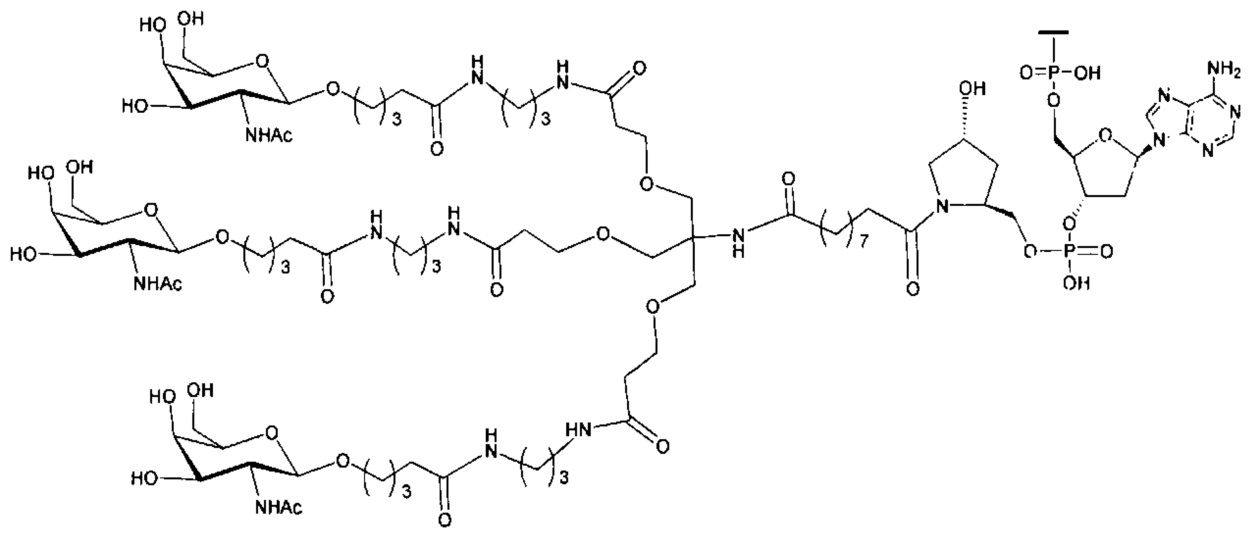
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
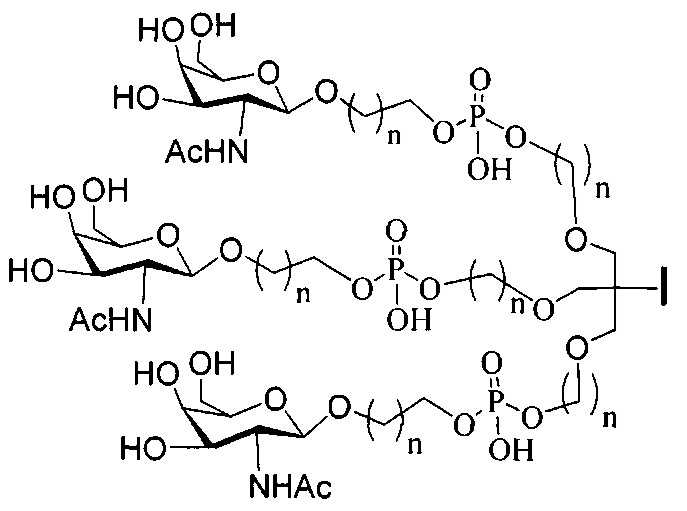
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
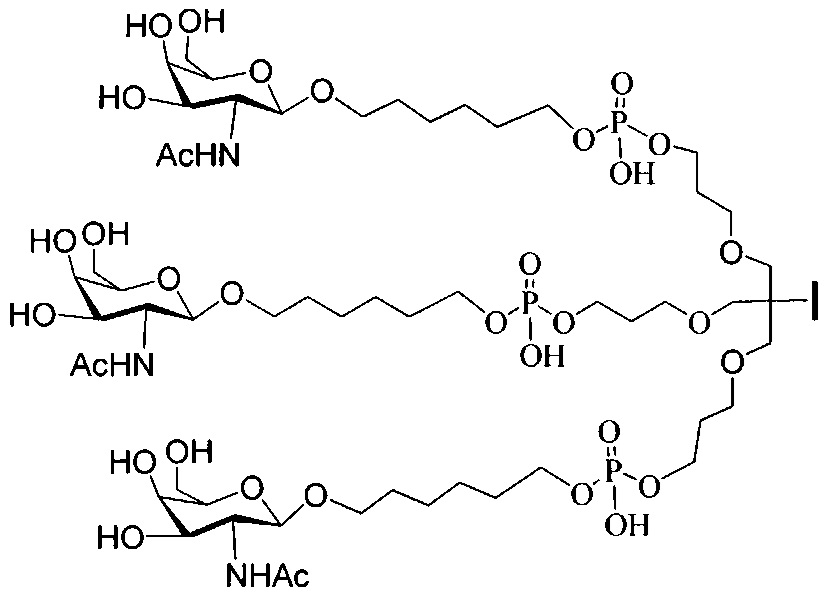
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
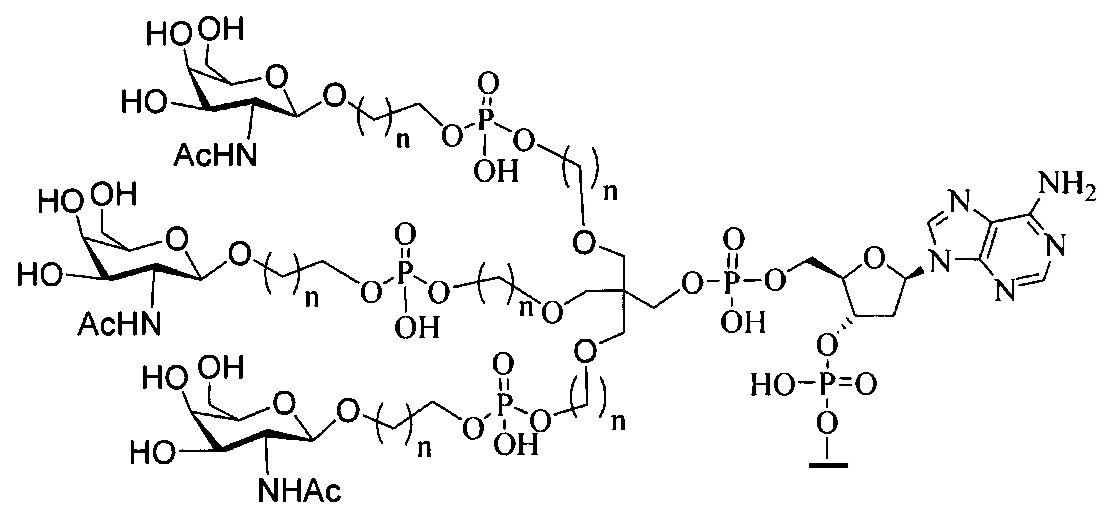
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
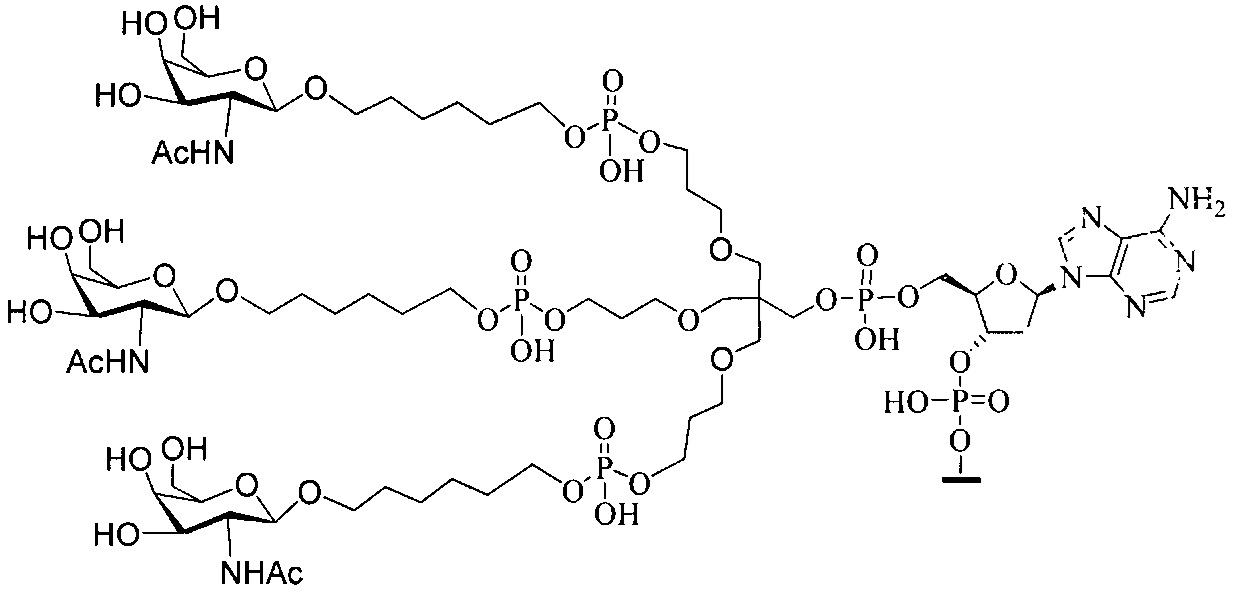
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
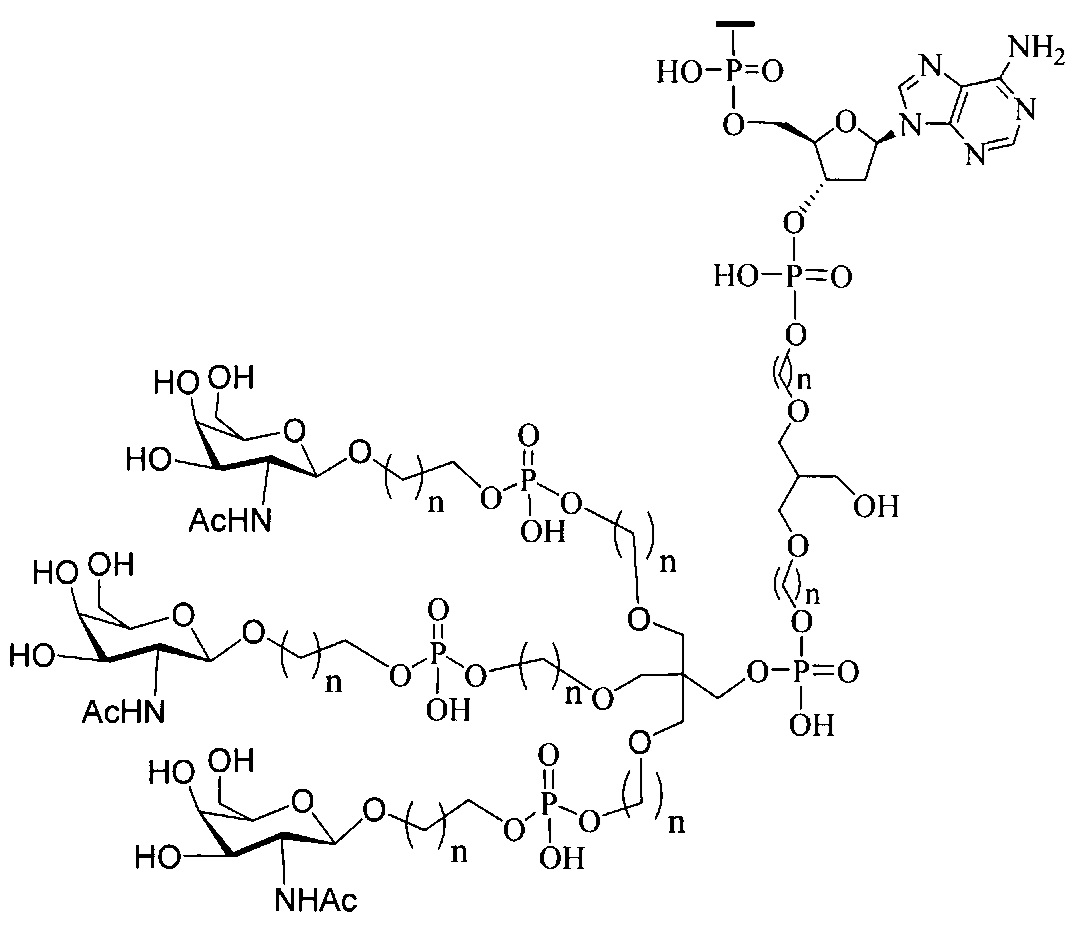
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
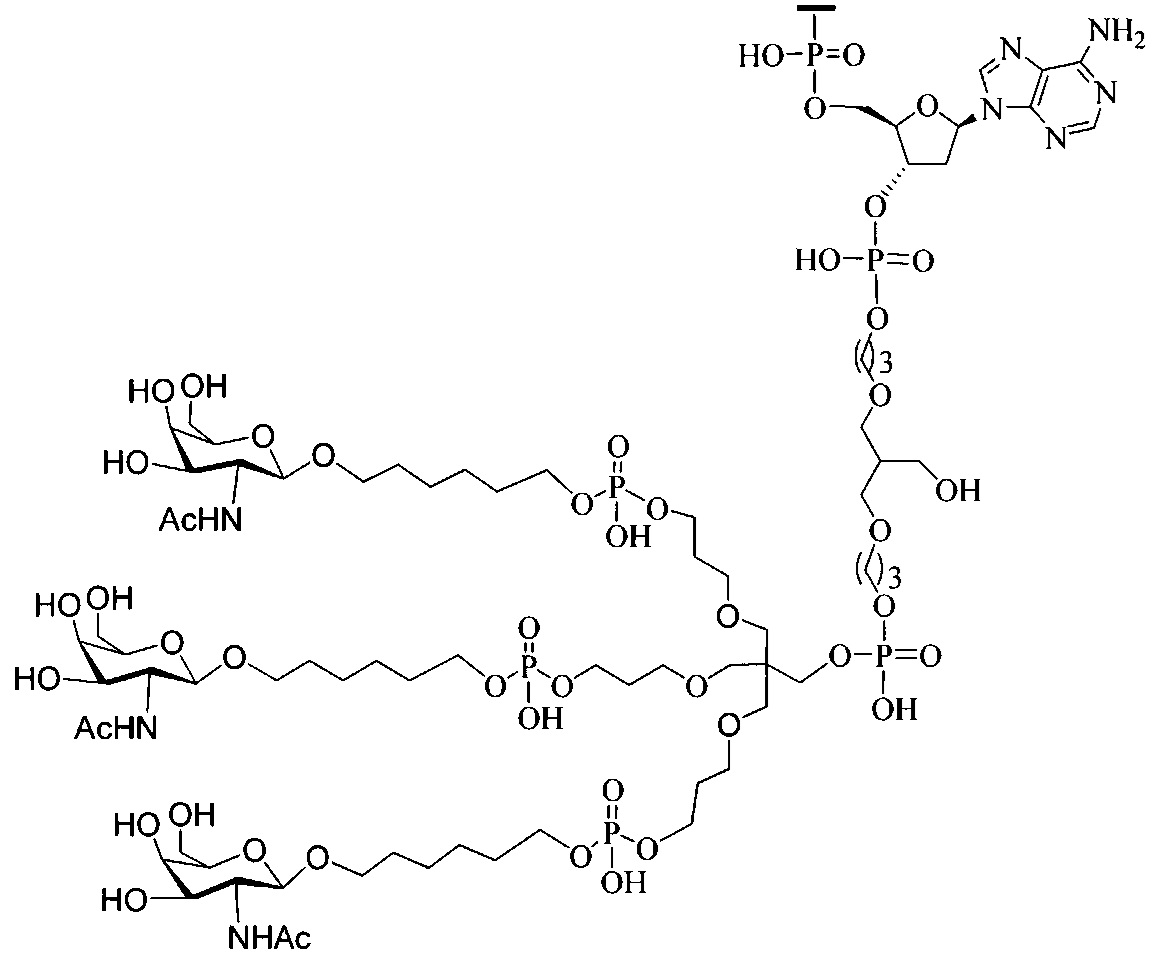
В некоторых вариантах реализации конъюгаты не содержат пирролидин.
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
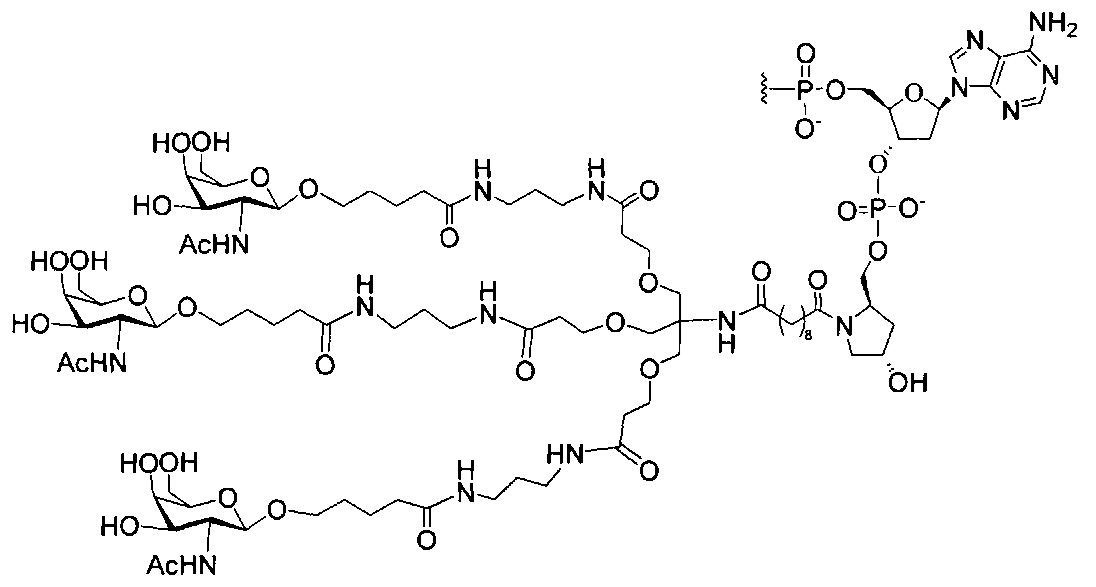
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
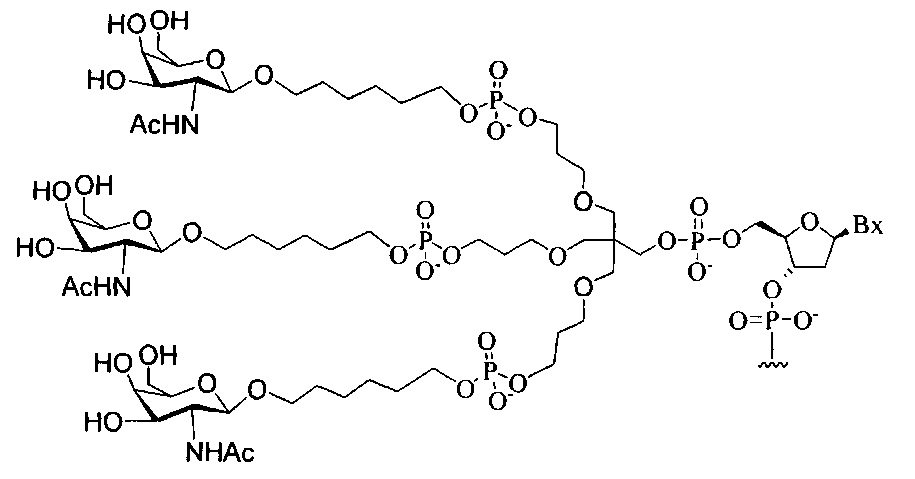
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
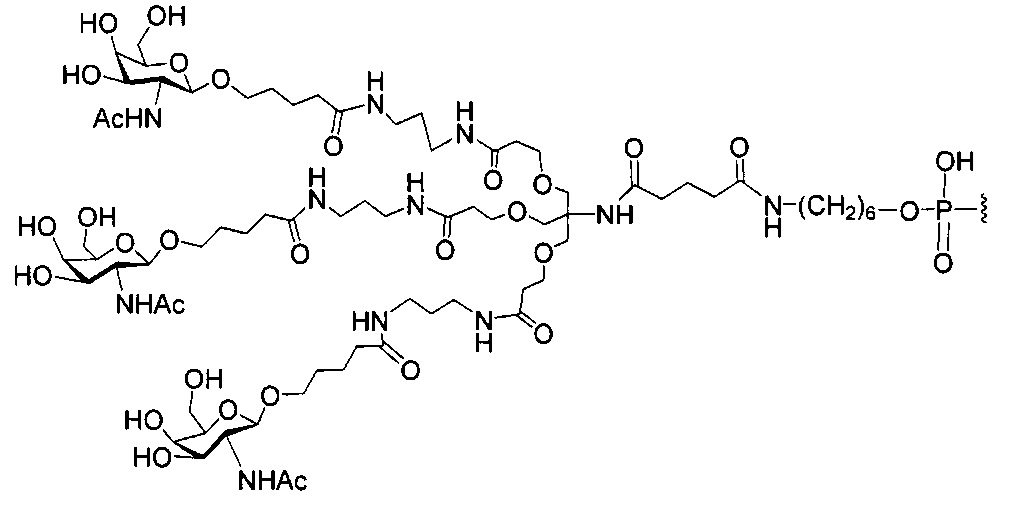
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
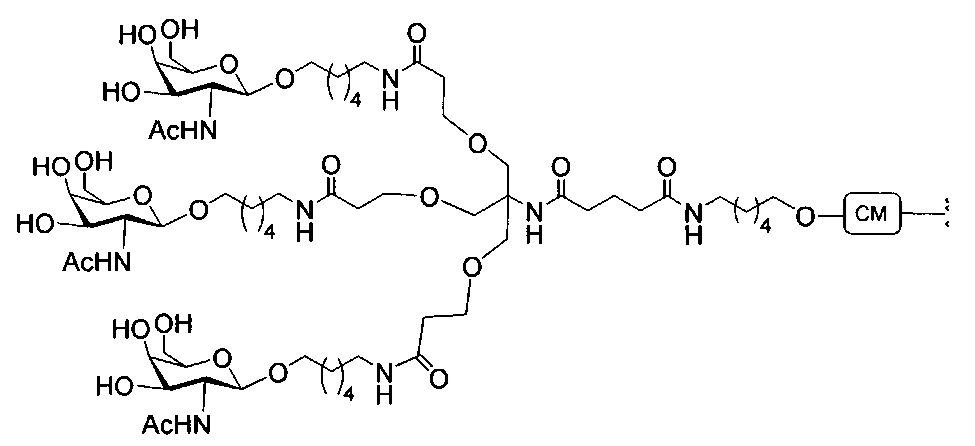
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
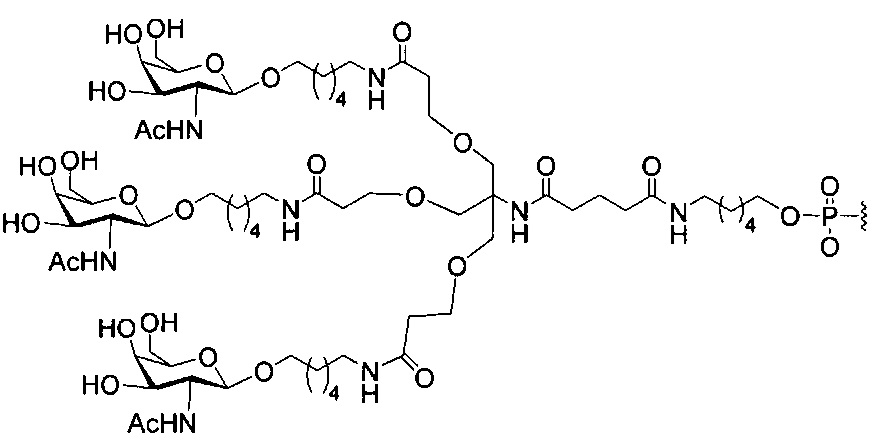
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
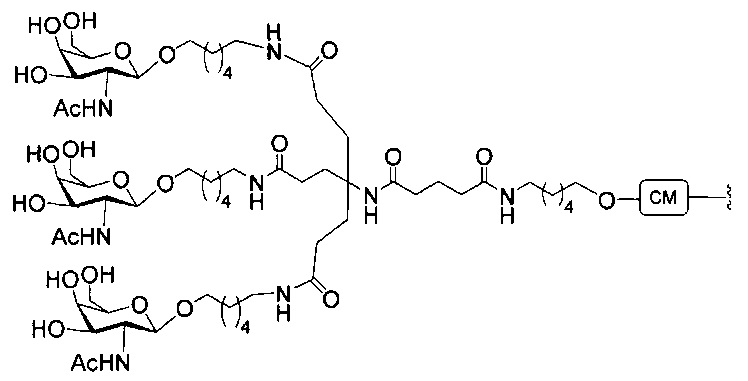
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
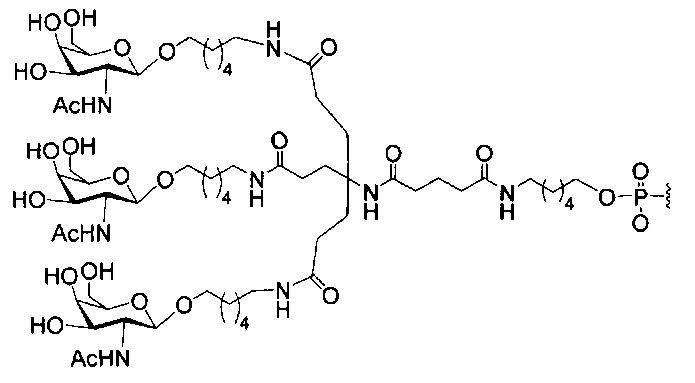
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
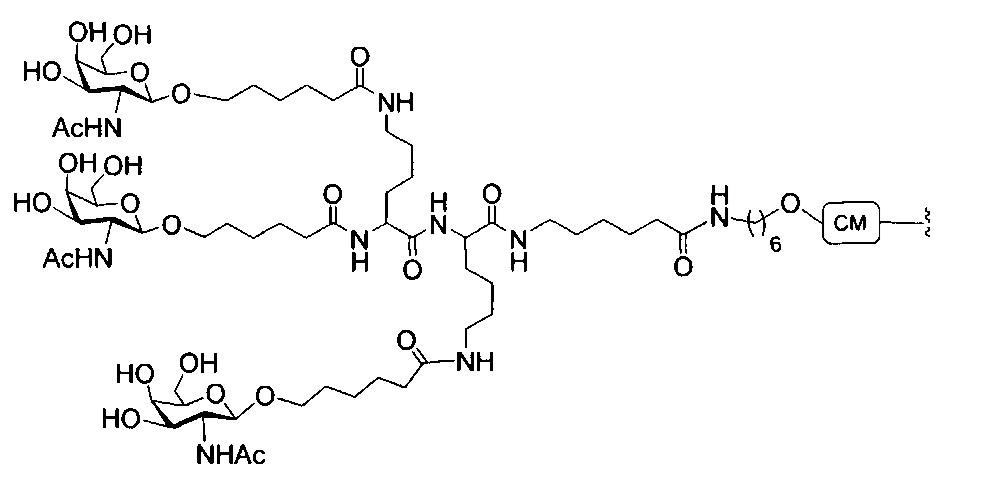
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
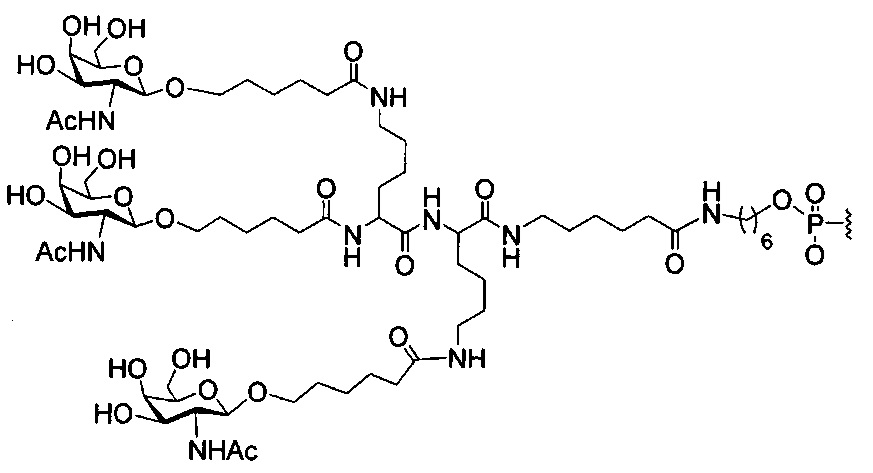
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
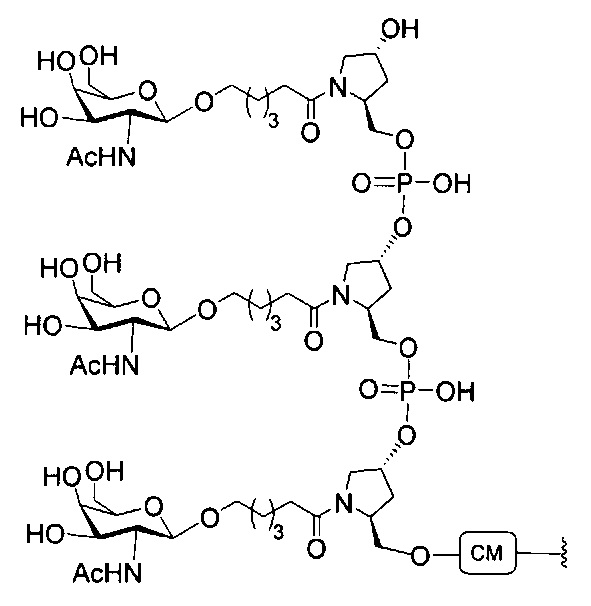
В некоторых таких вариантах реализации конъюгирующие группы имеют следующую структуру:
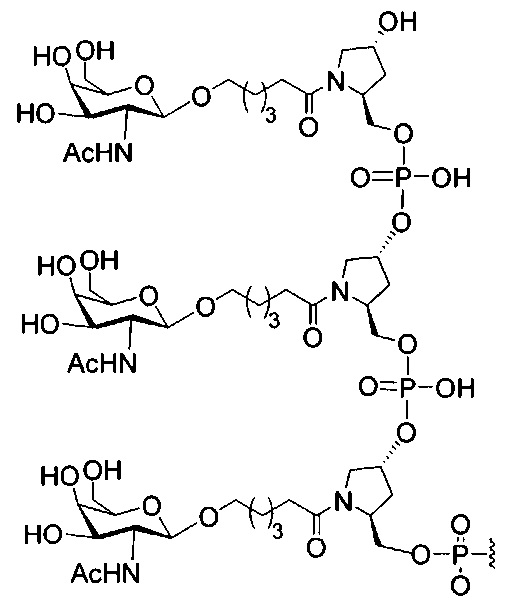
В некоторых вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
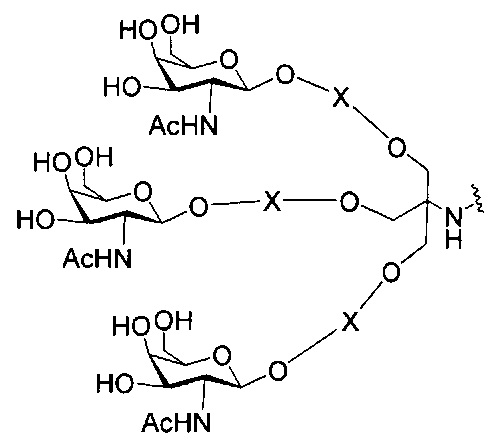
где X представляет собой замещенную или незамещенную связку из шести-одиннадцати последовательно связанных атомов.
В некоторых вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
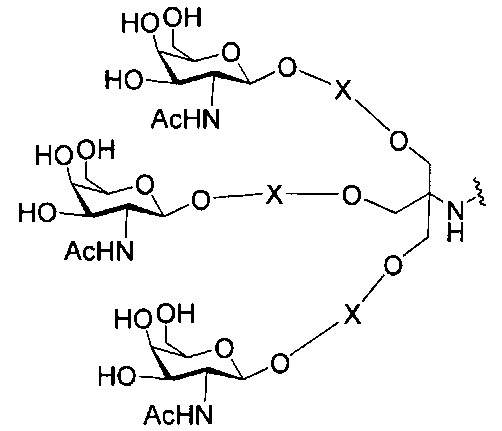
где X представляет собой замещенную или незамещенную связку из десяти последовательно связанных атомов.
В некоторых вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
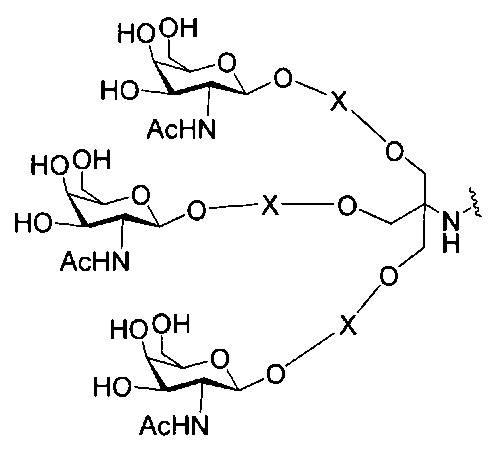
где X представляет собой замещенную или незамещенную связку из четырех-одиннадцати последовательно связанных атомов, и при этом указанная связка содержит только одну амидную связь.
В некоторых вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
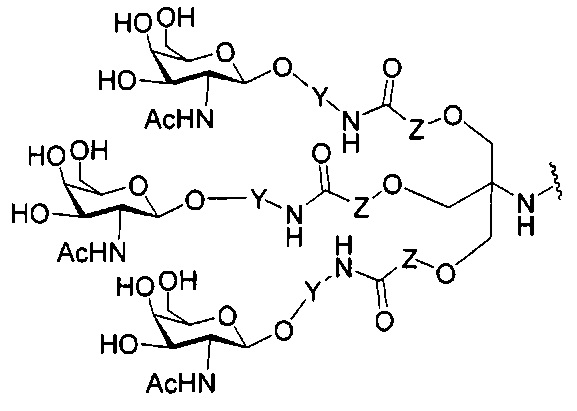
где Y и Z независимо выбраны из C1-C12 замещенной или незамещенной алкильной, алкенильной или алкинильной группы или группы, содержащей эфир, кетон, амид, сложный эфир, карбамат, амин, пиперидин, фосфат, фосфодиэфир, тиофосфат, триазол, пирролидин, дисульфид или тиоэфир.
В некоторых таких вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
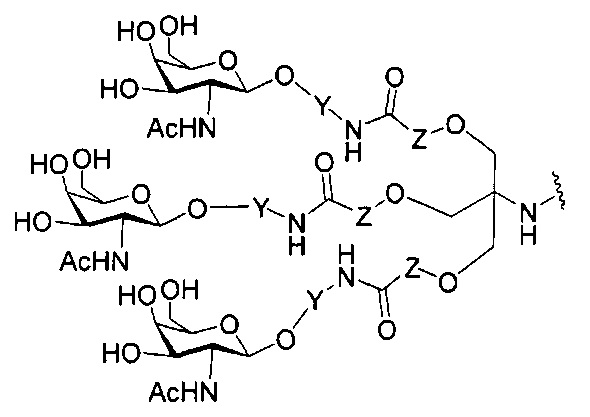
где Y и Z независимо выбраны из C1-C12 замещенной или незамещенной алкильной группы или группы, содержащей только один эфир или только два эфира, амид, амин, пиперидин, фосфат, фосфодиэфир или тиофосфат.
В некоторых таких вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
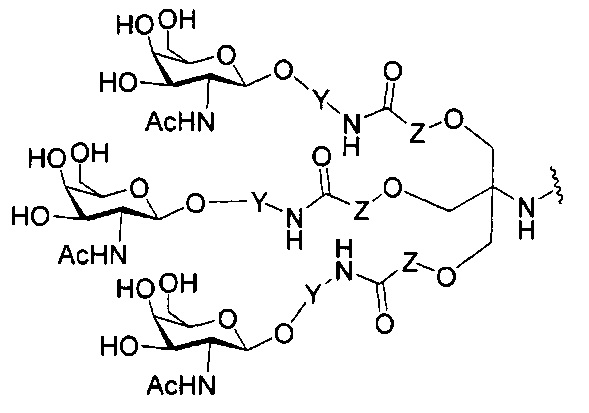
где Y и Z независимо выбраны из C1-C12 замещенной или незамещенной алкильной группы.
В некоторых таких вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
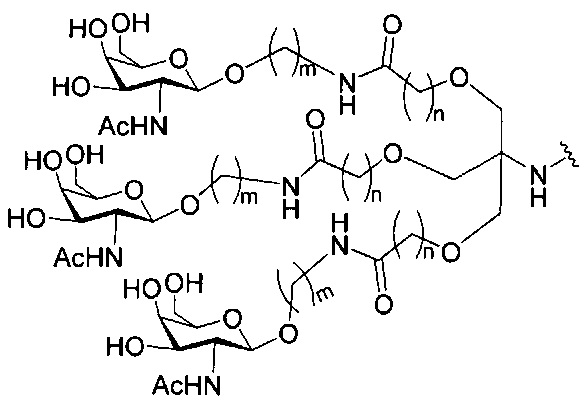
где m и n независимо выбраны из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 и 12.
В некоторых таких вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
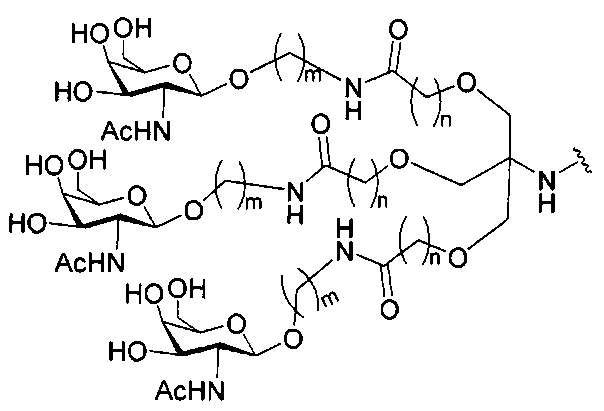
где m равен 4, 5, 6, 7 или 8, и n равен 1, 2, 3 или 4.
В некоторых вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
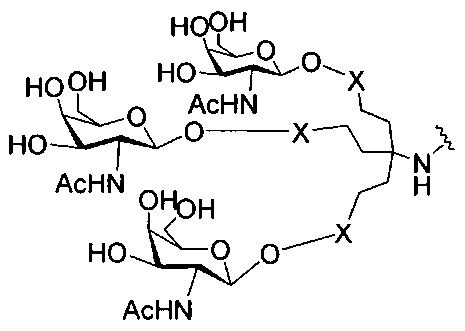
где X представляет собой замещенную или незамещенную связку из четырех-тринадцати последовательно связанных атомов, и при этом X не содержит эфирную группу.
В некоторых вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
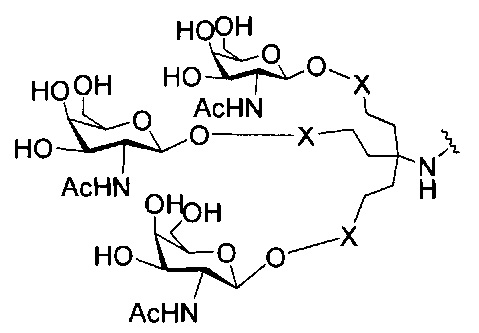
где X представляет собой замещенную или незамещенную связку из восьми последовательно связанных атомов, и при этом X не содержит эфирную группу.
В некоторых вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
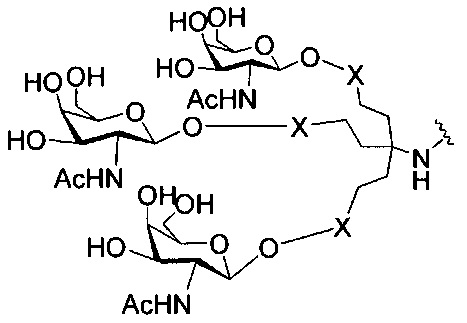
где X представляет собой замещенную или незамещенную связку из четырех-тринадцати последовательно связанных атомов, и при этом указанная связка содержит только одну амидную связь, а X не содержит эфирную группу.
В некоторых вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
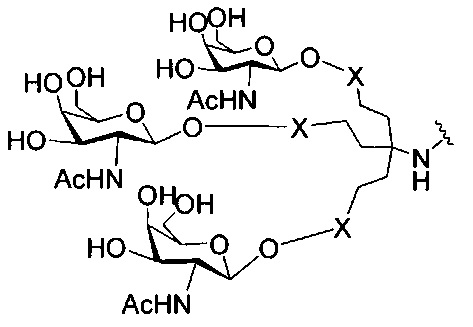
где X представляет собой замещенную или незамещенную связку из четырех-тринадцати последовательно связанных атомов, и при этом указанная связка состоит из амидной связи и замещенной или незамещенной С2-С11 алкильной группы.
В некоторых вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
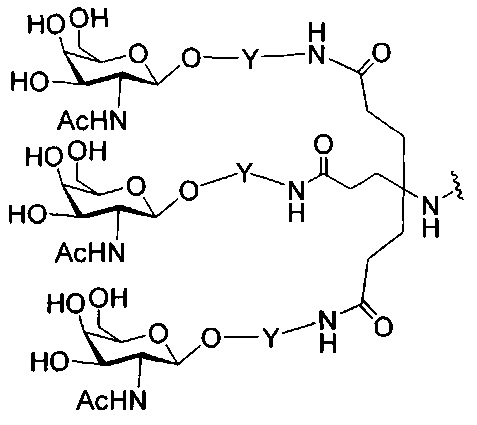
где Y выбран из C1-C12 замещенной или незамещенной алкильной, алкенильной или алкинильной группы или группы, содержащей эфир, кетон, амид, сложный эфир, карбамат, амин, пиперидин, фосфат, фосфодиэфир, тиофосфат, триазол, пирролидин, дисульфид или тиоэфир.
В некоторых таких вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
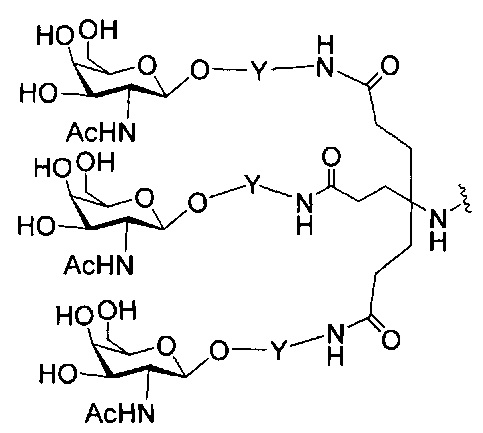
где Y выбран из C1-C12 замещенной или незамещенной алкильной группы или группы, содержащей эфир, амин, пиперидин, фосфат, фосфодиэфир или тиофосфат.
В некоторых таких вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
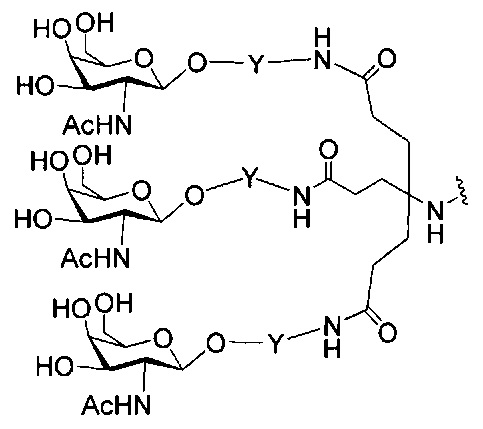
где Y выбран из С1-С12 замещенной или незамещенной алкильной группы.
В некоторых таких вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
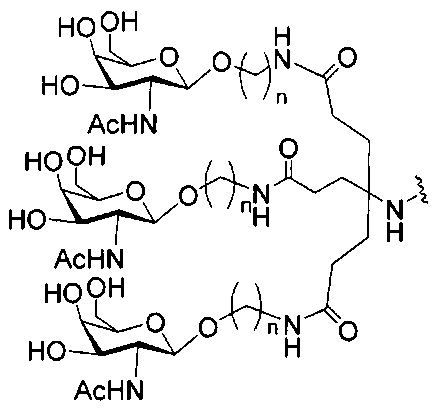
где n равен 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12.
В некоторых таких вариантах реализации фрагмент конъюгирующие группы, нацеливающий на клетку, имеет следующую структуру:
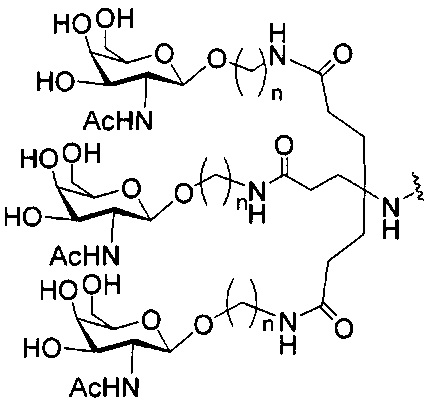
где n равен 4, 5, 6, 7 или 8.
b. Некоторые конъюгированные антисмысловые соединения
В некоторых вариантах реализации конъюгаты связаны с нуклеозидом антисмыслового олигонуклеотида в 2', 3' или 5' положении нуклеозида. В некоторых вариантах реализации конъюгированное антисмысловое соединение имеет следующую структуру:
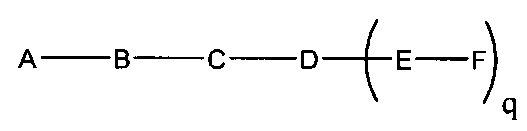
где
А представляет собой антисмысловый олигонуклеотид;
В представляет собой расщепляемый фрагмент
С представляет собой линкер конъюгата
D представляет собой группу ветвления
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации конъюгированное антисмысловое соединение имеет следующую структуру:
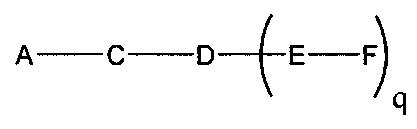
где
А представляет собой антисмысловый олигонуклеотид;
С представляет собой линкер конъюгата
D представляет собой группу ветвления
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых таких вариантах реализации линкер конъюгата содержит по меньшей мере одну расщепляемую связь.
В некоторых таких вариантах реализации группа ветвления содержит по меньшей мере одну расщепляемую связь.
В некоторых вариантах реализации каждая связка содержит по меньшей мере одну расщепляемую связь.
В некоторых вариантах реализации конъюгаты связаны с нуклеозидом антисмыслового олигонуклеотида в 2', 3' или 5' положении нуклеозида.
В некоторых вариантах реализации конъюгированное антисмысловое соединение имеет следующую структуру:
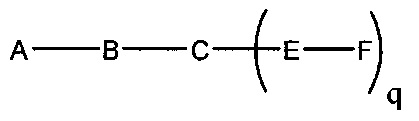
где
А представляет собой антисмысловый олигонуклеотид;
В представляет собой расщепляемый фрагмент
С представляет собой линкер конъюгата
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации конъюгаты связаны с нуклеозидом антисмыслового олигонуклеотида в 2', 3' или 5' положении нуклеозида. В некоторых вариантах реализации конъюгированное антисмысловое соединение имеет следующую структуру:
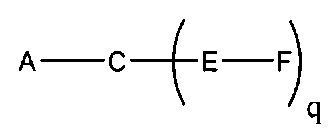
где
А представляет собой антисмысловый олигонуклеотид;
С представляет собой линкер конъюгата
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации конъюгированное антисмысловое соединение имеет следующую структуру:
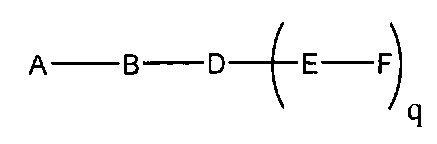
где
А представляет собой антисмысловый олигонуклеотид;
В представляет собой расщепляемый фрагмент
D представляет собой группу ветвления
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых вариантах реализации конъюгированное антисмысловое соединение имеет следующую структуру:
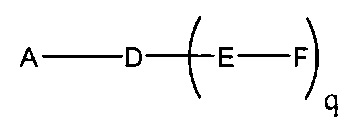
где
А представляет собой антисмысловый олигонуклеотид;
D представляет собой группу ветвления
каждый Е представляет собой связку;
каждый F представляет собой лиганд; и
q представляет собой целое число от 1 до 5.
В некоторых таких вариантах реализации линкер конъюгата содержит по меньшей мере одну расщепляемую связь.
В некоторых вариантах реализации каждая связка содержит по меньшей мере одну расщепляемую связь.
В некоторых вариантах реализации конъюгированное антисмысловое соединение имеет структуру, выбранную из следующих:

В некоторых вариантах реализации конъюгированное антисмысловое соединение имеет структуру, выбранную из следующих:
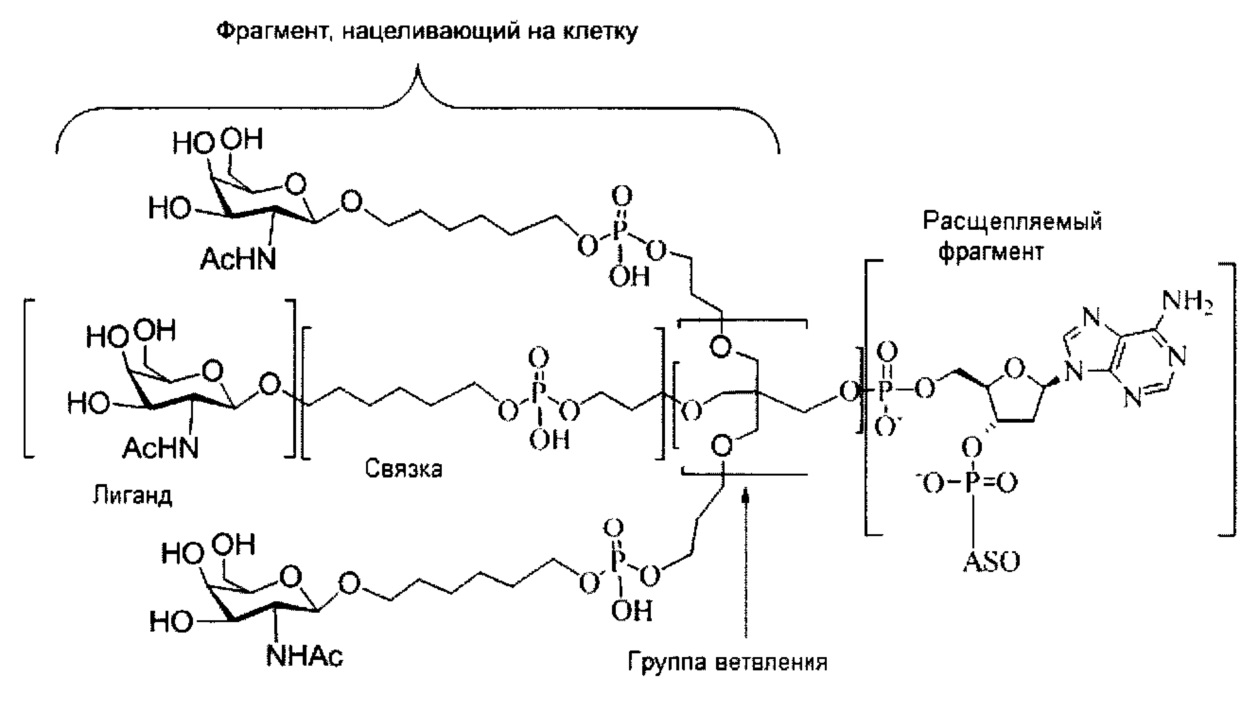
В некоторых вариантах реализации конъюгированное антисмысловое соединение имеет структуру, выбранную из следующих:
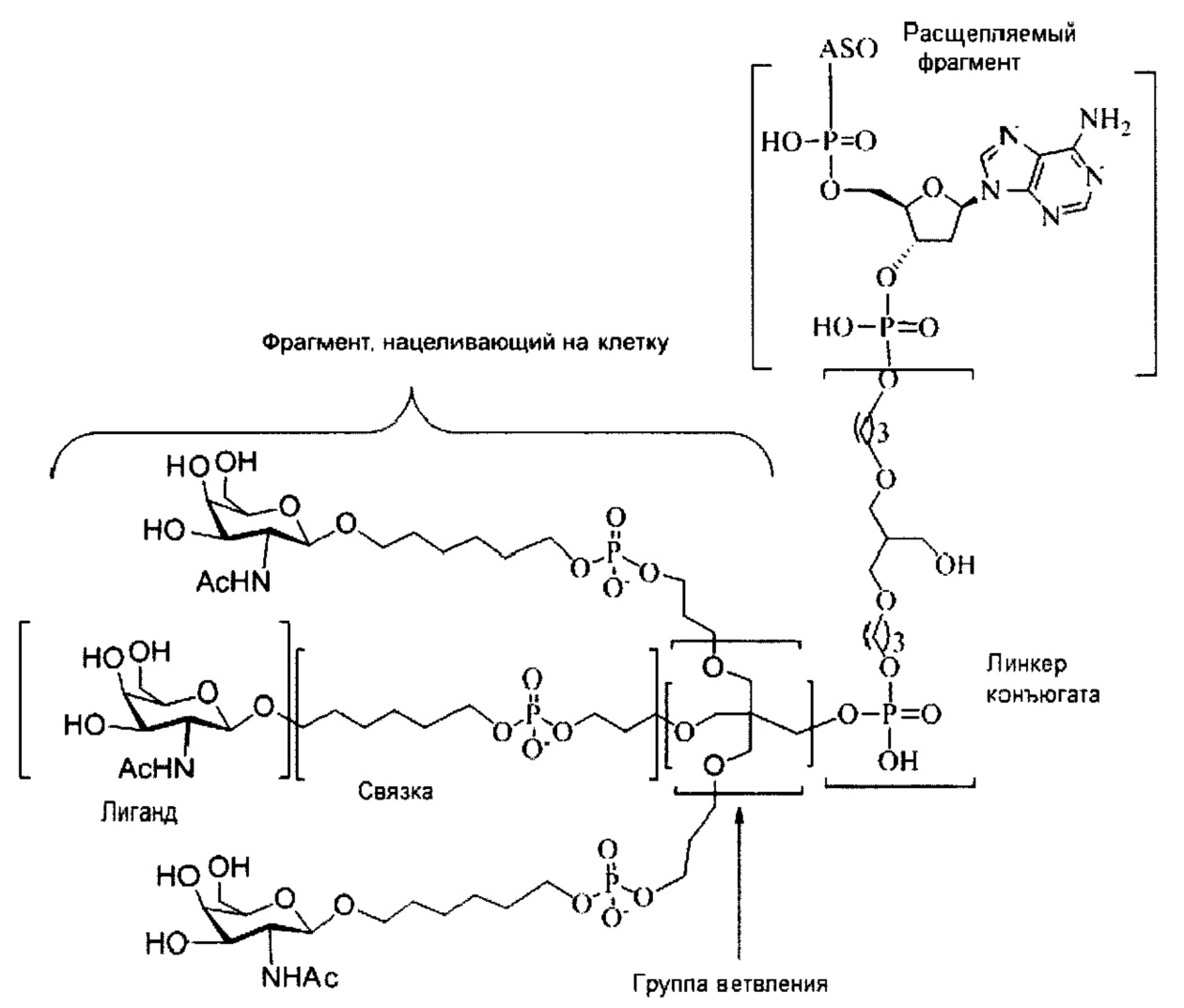
В некоторых вариантах реализации конъюгированное антисмысловое соединение имеет следующую структуру:

Типичные патенты Соединенных штатов Америки, публикации патентных заявок Соединенных штатов Америки и публикации международных патентных заявок, в которых описано получение некоторых из указанных выше конъюгатов, конъюгированных антисмысловых соединений, связок, линкеров, групп ветвления, лигандов, расщепляемых фрагментов, а также других модификаций, включают, без ограничения, US 5994517, US 6300319, US 6660720, US 6906182, US 7262177, US 7491805, US 8106022, US 7723509, US 2006/0148740, US 2011/0123520, WO 2013/033230 и WO 2012/037254, каждая из которых включена в настоящий документ посредством ссылки в полном объеме.
Типичные публикации, в которых описано получение некоторых из указанных выше конъюгатов, конъюгированных антисмысловых соединений, связок, линкеров, групп ветвления, лигандов, расщепляемых фрагментов, а также других модификаций, включают, без ограничения, BIESSEN et al., "The Cholesterol Derivative of a Triantennary Galactoside with High Affinity for the Hepatic Asialoglycoprotein Receptor: a Potent Cholesterol Lowering Agent" J. Med. Chem. (1995) 38: 1846-1852, BIESSEN et al., "Synthesis of Cluster Galactosides with High Affinity for the Hepatic Asialoglycoprotein Receptor" J. Med. Chem. (1995) 38: 1538-1546, LEE et al., "New and more efficient multivalent glyco-ligands for asialoglycoprotein receptor of mammalian hepatocytes" Bioorganic & Medicinal Chemistry (2011) 19: 2494-2500, RENSEN et al., "Determination of the Upper Size Limit for Uptake and Processing of Ligands by the Asialoglycoprotein Receptor on Hepatocytes in Vitro and in Vivo" J. Biol. Chem. (2001) 276(40): 37577-37584, RENSEN et al., "Design and Synthesis of Novel N-Acetylgalactosamine-Terminated Glycolipids for Targeting of Lipoproteins to the Hepatic Asialoglycoprotein Receptor" J. Med. Chem. (2004) 47: 5798-5808, SLIEDREGT et al., "Design and Synthesis of Novel Amphiphilic Dendritic Galactosides for Selective Targeting of Liposomes to the Hepatic Asialoglycoprotein Receptor" J. Med. Chem. (1999) 42: 609-618 и Valentijn et al., "Solid-phase synthesis of lysine-based cluster galactosides with high affinity for the Asialoglycoprotein Receptor" Tetrahedron, 1997, 53(2), 759-770, каждая из которых включена в настоящий документ посредством ссылки в полном объеме.
В некоторых вариантах реализации конъюгированные антисмысловые соединения содержат олигонуклеотид на основе РНКазы Н (такой как гэпмер) или сплайс-модулирующий олигонуклеотид (такой как полностью модифицированный олигонуклеотид) и любую конъюгирующую группу, содержащую по меньшей мере одну, две или три группы GalNAc. В некоторых вариантах реализации конъюгированное антисмысловое соединение содержит любую конъюгирующую группу, приведенную в следующих ссылках: Lee, Carbohydr Res, 1978, 67, 509-514; Connolly et al., J Biol Chem, 1982, 257, 939-945; Pavia et al., Int J Pep Protein Res, 1983, 22, 539-548; Lee et al., Biochem, 1984, 23, 4255-4261; Lee et al., Glycoconjugate J, 1987, 4, 317-328; Toyokuni et al., Tetrahedron Lett, 1990, 31, 2673-2676; Biessen et al., J Med Chem, 1995, 38, 1538-1546; Valentijn et al., Tetrahedron, 1997, 53, 759-770; Kim et al., Tetrahedron Lett, 1997, 38, 3487-3490; Lee et al., Bioconjug Chem, 1997, 8, 762-765; Kato et al., Glycobiol, 2001, 11, 821-829; Rensen et al., J Biol Chem, 2001, 276, 37577-37584; Lee et al., Methods Enzymol, 2003, 362, 38-43; Westerlind et al., Glycoconj J, 2004, 21, 227-241; Lee et al., Bioorg Med Chem Lett, 2006, 16(19), 5132-5135; Maierhofer et al., Bioorg Med Chem, 2007, 15, 7661-7676; Khorev et al., Bioorg Med Chem, 2008, 16, 5216-5231; Lee et al., Bioorg Med Chem, 2011, 19, 2494-2500; Kornilova et al., Analyt Biochem, 2012, 425, 43-46; Pujol et al., Angew Chemie Int Ed Engl, 2012, 51, 7445-7448; Biessen et al., J Med Chem, 1995, 38, 1846-1852; Sliedregt et al., J Med Chem, 1999, 42, 609-618; Rensen et al., J Med Chem, 2004, 47, 5798-5808; Rensen et al., Arterioscler Thromb Vase Biol, 2006, 26, 169-175; van Rossenberg et al., Gene Ther, 2004, 11, 457-464; Sato et al., J Am Chem Soc, 2004, 126, 14013-14022; Lee et al., J Org Chem, 2012, 77, 7564-7571; Biessen et al., FASEB J, 2000, 14, 1784-1792; Rajur et al., Bioconjug Chem, 1997, 8, 935-940; Duff et al., Methods Enzymol, 2000, 313, 297-321; Maier et al., Bioconjug Chem, 2003, 14, 18-29; Jayaprakash et al., Org Lett, 2010, 12, 5410-5413; Manoharan, Antisense Nucleic Acid Drug Dev, 2002, 12, 103-128; Merwin et al., Bioconjug Chem, 1994, 5, 612-620; Tormya et al., Bioorg Med Chem, 2013, 21, 5275-5281; Международные заявки WO 1998/013381; WO 2011/038356; WO 1997/046098; WO 2008/098788; WO 2004/101619; WO 2012/037254; WO 2011/120053; WO 2011/100131; WO 2011/163121; WO 2012/177947; WO 2013/033230; WO 2013/075035; WO 2012/083185; WO 2012/083046; WO 2009/082607; WO 2009/134487; WO 2010/144740; WO 2010/148013; WO 1997/020563; WO 2010/088537; WO 2002/043771; WO 2010/129709; WO 2012/068187; WO 2009/126933; WO 2004/024757; WO 2010/054406; WO 2012/089352; WO 2012/089602; WO 2013/166121; WO 2013/165816; патенты США 4751219; 8552163; 6908903; 7262177; 5994517; 6300319; 8106022; 7491805; 7491805; 7582744; 8137695; 6383812; 6525031; 6660720; 7723509; 8541548; 8344125; 8313772; 8349308; 8450467; 8501930; 8158601; 7262177; 6906182; 6620916; 8435491; 8404862; 7851615; опубликованные заявки на патент США US 2011/0097264; US 2011/0097265; US 2013/0004427; US 2005/0164235: US 2006/0148740; US 2008/0281044; US 2010/0240730; US 2003/0119724; US 2006/0183886; US 2008/0206869; US 2011/0269814; US 2009/0286973; US 2011/0207799; US 2012/0136042; US 2012/0165393; US 2008/0281041; US 2009/0203135; US 2012/0035115; US 2012/0095075; US 2012/0101148; US 2012/0128760; US 2012/0157509; US 2012/0230938; US 20I3/0109817; US 2013/0121954; US 2013/0178512; US 2013/0236968; US 2011/0123520; US 2003/0077829; US 2008/0108801; и US 2009/0203132; каждая из которых включена посредством ссылки в полном объеме.
С. Некоторые применения и особенности
В некоторых вариантах реализации конъюгированные антисмысловые соединения демонстрируют эффективное снижение целевой РНК in vivo. В некоторых вариантах реализации неконъюгированные антисмысловые соединения накапливаются в почках. В некоторых вариантах реализации конъюгированные антисмысловые соединения накапливаются в печени. В некоторых вариантах реализации конъюгированные антисмысловые соединения являются хорошо переносимыми. Такие свойства делают конъюгированные антисмысловые соединения особенно пригодными для ингибирования многих целевых РНК, включая, но не ограничиваясь ими, те, которые участвуют в метаболических, сердечно-сосудистых и других заболеваниях, расстройства или состояниях. Таким образом, в настоящем документе приведены способы лечения таких заболеваний, расстройств или состояний приведением тканей печени в контакт с конъюгированными антисмысловыми соединениями, нацеленными на РНК, связанные с такими заболеваниями, расстройствами или состояниями. Следовательно, приведены также способы улучшения любых из множества метаболических, сердечно-сосудистых и других заболеваний, расстройств или состояний при помощи конъюгированных антисмысловых соединений настоящего изобретения.
В некоторых вариантах реализации конъюгированные антисмысловые соединения являются более эффективными, чем неконъюгированные аналоги при определенной концентрации в ткани. Не ограничиваясь какой-либо теорией или механизмом, в некоторых вариантах реализации конъюгат может обеспечивать возможность более эффективного вхождения конъюгированного антисмыслового соединения в клетку или возможность более продуктивного вхождения в клетку. Например, в некоторых вариантах реализации конъюгированные антисмысловые соединения могут демонстрировать более значительное снижение мишени, по сравнению с неконъюгированным аналогом, при этом и конъюгированное антисмысловое соединение, и его неконъюгированный аналог находятся в ткани в одинаковых концентрациях. Например, в некоторых вариантах реализации конъюгированные антисмысловые соединения могут демонстрировать более значительное снижение мишени, по сравнению с их неконъюгированными аналогами, при этом и конъюгированное антисмысловое соединение, и его неконъюгированный аналог находятся в печени в одинаковых концентрациях.
Ранее был рассмотрен продуктивный и непродуктивный захват олигонуклеотидов (см., например, Geary, R.S., Е. Wancewicz, et al. (2009). "Effect of Dose and Plasma Concentration on Liver Uptake and Pharmacologic Activity of a 2'-Methoxyethyl Modified Chimeric Antisense Oligonucleotide Targeting PTEN." Biochem. Pharmacol. 78(3): 284-91; и Koller, E., Т.M. Vincent, et al. (2011). "Mechanisms of single-stranded phosphorothioate modified antisense oligonucleotide accumulation in hepatocytes." Nucleic Acids Res. 39(11): 4795-807). Конъюгирующие группы, описанные в настоящем документе, могут улучшать продуктивный захват.
В некоторых вариантах реализации конъюгирующие группы, описанные настоящем документе, могут дополнительно усиливать эффективность за счет увеличения аффинности конъюгированного антисмыслового соединения к конкретному типу клетки или ткани. В некоторых вариантах реализации конъюгирующие группы, описанные в настоящем документе, могут дополнительно усиливать эффективность за счет увеличения распознавания конъюгированного антисмыслового соединения одним или более рецепторами клеточной поверхности. В некоторых вариантах реализации конъюгирующие группы, описанные в настоящем документе, могут дополнительно усиливать эффективность за счет облегчения эндоцитоза конъюгированного антисмыслового соединения.
В некоторых вариантах реализации расщепляемый фрагмент может дополнительно усиливать эффективность за счет обеспечения возможности расщепления конъюгата из антисмыслового олигонуклеотида после попадания конъюгированного антисмыслоого соединения в клетку. Соответственно, в некоторых вариантах реализации конъюгированные антисмысловые соединения могут быть введены в более низких дозах, чем необходимы для неконъюгированных антисмысловых олигонуклеотидов.
Ранее в антисмысловые олигонуклеотиды уже были внедрены тиофосфатные связи. Такие тиофосфатные связи являются устойчивыми к нуклеазам и за счет этого улучшают стабильность олигонуклеотида. Кроме того, тиофосфатные связи связывают также некоторые белки, что приводит к накоплению антисмыслового олигонуклеотида в печени. Олигонуклеотиды с меньшим количеством тиофосфатных связей меньше накапливаются в печени и больше - в почках (см., например, Geary, R., "Pharmacokinetic Properties of 2'-O-(2-Methoxyethyl)-Modified Oligonucleotide Analogs in Rats," Journal of Pharmacology and Experimental Therapeutics, том 296, №3, 890-897; и Pharmacological Properties of 2'-O-Methoxyethyl Modified Oligonucleotides in Antisense a Drug Technology, глава 10, Crooke, S.T., ред., 2008). В некоторых вариантах реализации олигонуклеотиды с меньшим количеством тиофосфатных межнуклеозидных связей и с большим количеством фосфодиэфирных межнуклеозидных связей меньше накапливаются в печени и больше - в почках. При лечении заболеваний печени это нежелательно по нескольким причинам: (1) меньше лекарства попадает в центр заданного действия (печень); (2) лекарство выводится с мочой; (3) почки подвергаются воздействию относительно высокой концентрации лекарства, что может приводить к токсичности в почках. Следовательно, для заболеваний печени тиофосфатные связи обеспечивают важное преимущество.
Однако в некоторых вариантах реализации введение олигонуклеотидор, равномерно связанных тиофосфатными межнуклеозидными связями, вызывает одну или более провоспалительных реакций. (См., например: J Lab Clin Med. 1996 Sep; 128(3): 329-38. "Amplification of antibody production by phosphorothioate oligodeoxynucleotides". Branda et al.; и см. также, например: Toxicologic Properties in Antisense a Drug Technology, глава 12, страницы 342-351, Crooke, S.T., ред., 2008). В некоторых вариантах реализации введение олигонуклеотидов, в которых большая часть межнуклеозидных связей содержит тиофосфатные межнуклеозидные связи, вызывает одну или более провоспалительных реакций.
В некоторых вариантах реализации степень провоспалительного эффекта может зависеть от нескольких переменных (например, модификация скелета, нецелевое действие, модификации азотистых оснований и/или модификации нуклеозида), см., например: Toxicologic Properties in Antisense a Drug Technology, глава 12, страницы 342-351, Crooke, S.T., ред., 2008). В некоторых вариантах реализации степень провоспалительного эффекта может быть ослаблена за счет подбора одной или более переменных. Например, степень провоспалительного эффекта данного олигонуклеотида может быть ослаблена за счет замены любого количества тиофосфатных межнуклеозидных связей на фосфодиэфирные межнуклеозидные связи с уменьшением посредством этого общего количества тиофосфатных межнуклеозидных связей.
В некоторых вариантах реализации может быть желательно снизить количество тиофосфатных связей, если это может быть выполнено без потери стабильности и без сдвига распределения из печени в почки. Например, в некоторых вариантах реализации количество тиофосфатных связей может быть уменьшено за счет замены тиофосфатных связей на фосфодиэфирные связи. В таком варианте реализации антисмысловое соединение, имеющее меньшее количество тиофосфатных связей и большее количество фосфодиэфирных связей, может вызывать меньшее количество провоспалительных реакций или не вызывать провоспалительных реакций. Хотя антисмысловое соединение, имеющее меньшее количество тиофосфатных связей и большее количество фосфодиэфирных связей, может вызывать меньшее количество провоспалительных реакций, антисмысловое соединение, имеющее меньшее количество тиофосфатных связей и большее количество фосфодиэфирных связей, может не накапливаться в печени и может быть менее эффективным в такой же или аналогичной дозе, по сравнению с антисмысловым соединением, имеющим большее количество тиофосфатных связей. Поэтому в некоторых вариантах реализации желательно разработать антисмысловое соединение, которое имеет множество фосфодиэфирных связей и множество тиофосфатных связей, но которое при этом обладает также стабильностью и хорошим распределением в печени.
В некоторых вариантах реализации конъюгированные антисмысловые соединения больше накапливаются в печени и меньше - в почках, чем неконъюгированные аналоги, даже если некоторые тиофосфатные связи заменены менее провоспалительными фосфодиэфирными межнуклеозидными связями. В некоторых вариантах реализации конъюгированные антисмысловые соединения больше накапливаются в печени и не так сильно выводятся с мочой, как их неконъюгированные аналоги, даже если некоторые тиофосфатные связи заменены менее провоспалительными фосфодиэфирными межнуклеозидными связями. В некоторых вариантах реализации применение конъюгата обеспечивает возможность разрабатывать более эффективные и лучше переносимые антисмысловые лекарства. Действительно, в некоторых вариантах реализации конъюгированные антисмысловые соединения имеют более широкий терапевтический индекс, чем неконъюгированные аналоги. Это позволяет вводить конъюгированное антисмысловое соединение в более высокой абсолютной дозе благодаря меньшему риску провоспалительной реакции и меньшему риску токсичности для почек. Такая более высокая доза дает возможность вводить дозу реже, поскольку ожидается такой же коэффициент очищения (метаболизм). Кроме того, поскольку соединение является более эффективным, как описано выше, то можно допускать снижение концентрации перед введением следующей дозы, без потери терапевтической активности, что обеспечивает еще более продолжительные периоды между введениями доз.
В некоторых вариантах реализации сохраняется необходимость во внедрении некоторого количества тиофосфатных связей. Например, концевые связи легко подвергаются действию экзонуклеаз, и поэтому в некоторых вариантах реализации эти связи представляют собой тиофосфатные или другие модифицированные связи. Межнуклеозидные связи, соединяющие два дезоксинуклеозида, легко подвергаются действию эндонуклеаз, и поэтому в некоторых вариантах реализации эти связи представляют собой тиофосфатные или другие модифицированные связи. Межнуклеозидные связи между модифицированным нуклеозидом и дезоксинуклеозидом, где дезоксинуклеозид расположен на 5'-стороне связывающего дезоксинуклеозида, легко подвергаются действию эндонуклеаз, и поэтому в некоторых вариантах реализации эти связи представляют собой тиофосфатные или другие модифицированные связи. Межнуклеозидные связи между двумя модифицированными нуклеозидами определенных типов и между дезоксинуклеозидом и модифицированным нуклеозидом определенного типа, где модифицированный нуклеозид расположен на 5'-стороне линкера, являются достаточно устойчивыми к нуклеазному расщеплению, поэтому связь может быть фосфодиэфиром.
В некоторых вариантах реализации антисмысловый олигонуклеотид конъюгированного антисмыслового соединения содержит менее 16 тиофосфатных связей. В некоторых вариантах реализации антисмысловый олигонуклеотид конъюгированного антисмыслового соединения содержит менее 15 тиофосфатных связей. В некоторых вариантах реализации антисмысловый олигонуклеотид конъюгированного антисмыслового соединения содержит менее 14 тиофосфатных связей. В некоторых вариантах реализации антисмысловый олигонуклеотид конъюгированного антисмыслового соединения содержит менее 13 тиофосфатных связей. В некоторых вариантах реализации антисмысловый олигонуклеотид конъюгированного антисмыслового соединения содержит менее 12 тиофосфатных связей. В некоторых вариантах реализации антисмысловый олигонуклеотид конъюгированного антисмыслового соединения содержит менее 11 тиофосфатных связей. В некоторых вариантах реализации антисмысловый олигонуклеотид конъюгированного антисмыслового соединения содержит менее 10 тиофосфатных связей. В некоторых вариантах реализации антисмысловый олигонуклеотид конъюгированного антисмыслового соединения содержит менее 9 тиофосфатных связей. В некоторых вариантах реализации антисмысловый олигонуклеотид конъюгированного антисмыслового соединения содержит менее 8 тиофосфатных связей.
В некоторых вариантах реализации антисмысловые соединения, содержащие одну или более конъюгирующих групп, описанных в настоящем документе, обладают повышенной активностью и/или эффективностью, и/или переносимостью, по сравнению с исходным антисмысловым соединением, не имеющим такой одной или нескольких конъюгирующих групп. Соответственно, в некоторых вариантах реализации присоединение таких конъюгирующих групп к олигонуклеотиду является желательным. Такие конъюгирующие группы могут быть присоединены у 5'- и/или 3'-конца олигонуклеотида. В некоторых случаях синтетически желательно присоединение на 5'-конце. Как правило, олигонуклеотиды синтезируют присоединением 3'-концевого нуклеозида к твердой подложке с последующим связыванием нуклеозидов от 3' к 5' при помощи методик, общеизвестных в данной области техники. Соответственно, если конъюгирующая группа необходима на 3'-конце, то можно (1) присоединить конъюгирующую группу к 3'-концевому нуклеозиду и присоединить этот конъюгированный нуклеозид к твердой подложке для последующего получения олигонуклеотида или (2) присоединить конъюгирующую группу к 3'-концевому нуклеозиду готового олигонуклеотида после синтеза. Ни один из этих подходов не является особенно эффективным, и поэтому оба они затратны. В частности, присоединение конъюгированного нуклеозида к твердой подложке, хотя и приведено в настоящем документе в разделе «Примеры», не является эффективным способом. В некоторых вариантах реализации присоединение конъюгирующие группы к 5'-концевому нуклеозиду синтетически проще, чем присоединение к 3'-концу. Можно присоединить неконъюгированный 3'-концевой нуклеозид к твердой подложке и получить олигонуклеотид по стандартным и хорошо описанным реакциям. Затем нужно лишь присоединить 5'-нуклеозид, имеющий конъюгирующую группу, на последней стадии связывания. В некоторых вариантах реализации это более эффективно, чем присоединение конъюгированного нуклеозида непосредственно к твердой подложке, как это обычно делают для получения 3'-конъюгированного олигонуклеотида. В приведенных в настоящем документе Примерах показано присоединение к 5'-концу. Кроме того, некоторые конъюгирующие группы имеют синтетические преимущества. Например, некоторые конъюгирующие группы, содержащие фосфорные связывающие группы, получают синтетически проще и более эффективно, чем другие конъюгирующие группы, включая конъюгирующие группы, описанные ранее (например, WO/2012/037254).
В некоторых вариантах реализации конъюгированные антисмысловые соединения вводят субъекту. В таких вариантах реализации антисмысловые соединения, содержащие одну или более конъюгирующих групп, описанных в настоящем документе, обладают повышенной активностью и/или эффективностью, и/или переносимостью, по сравнению с исходным антисмысловым соединением, не имеющим такой одной или нескольких конъюгирующих групп. Не ограничиваясь механизмом, предполагается, что конъюгирующая группа способствует распределению, доставке и/или поглощению в целевой клетке или ткани. В некоторых вариантах реализации, после попадания в целевую клетку или ткань желательно, чтобы вся или часть конъюгирующие группы расщеплялась с высвобождением активного олигонуклеотида. В некоторых вариантах реализации не обязательно, чтобы из олигонуклеотида расщеплялась вся конъюгирующая группа. Например, в Примере 20а конъюгированный олигонуклеотид вводили мышам и обнаруживали множество различных химических частиц, каждая из которых содержала различные части конъюгирующие группы, оставшиеся на олигонуклеотиде (Таблица 23а). Это конъюгированное антисмысловое соединение показало хорошую эффективность (Таблица 23). Так, в некоторых вариантах реализации такой метаболитный профиль многократного частичного расщепления конъюгирующие группы не влияет на активность/эффективность. Тем не менее, в некоторых вариантах реализации желательно, чтобы пролекарство (конъюгированный олигонуклеотид) давало одно активное соединение. В некоторых случаях, при обнаружении многочисленных форм активного соединения, может быть необходимо определить относительные количества и действие для каждой из них. В некоторых вариантах реализации, при необходимости регуляционного тестирования (например, FDA США или другого органа), желательно иметь одну (или преимущественно одну) активную частицу. В некоторых таких вариантах реализации желательно, чтобы такая одна активная частица представляла собой антисмысловый олигонуклеотид, не содержащий никаких частей конъюгирующие группы. В некоторых вариантах реализации конъюгирующие группы на 5'-конце более вероятно приводят к полному метаболизму конъюгирующие группы. Не ограничиваясь механизмом, может быть, что эндогенные ферменты, отвечающие за метаболизм на 5'-конце (например, 5'-нуклеазы), более активны/эффективны, чем 3'-аналоги. В некоторых вариантах реализации определенные конъюгирующие группы более подвержены метаболизму до одной активной частицы. В некоторых вариантах реализации некоторые конъюгирующие группы более подвержены метаболизму до олигонуклеотида.
D. Антисенс
В некоторых вариантах реализации олигомерные соединения настоящего изобретения представляют собой антисмысловые соединения. В таких вариантах реализации олигомерное соединение комплементарно целевой нуклеиновой кислоте. В некоторых вариантах реализации целевая нуклеиновая кислота представляет собой РНК. В некоторых вариантах реализации целевая нуклеиновая кислота представляет собой некодирующую РНК. В некоторых вариантах реализации целевая нуклеиновая кислота кодирует белок. В некоторых вариантах реализации целевая нуклеиновая кислота выбрана из мРНК, пре-мРНК, микроРНК, некодирующей РНК, включая малую некодирующую РНК, и промотор-нацеливающей РНК. В некоторых вариантах реализации олигомерные соединения по меньшей мере частично комплементарны более чем одной целевой нуклеиновой кислоте. Например, олигомерные соединения настоящего изобретения могут представлять собой миметики микроРНК, которые обычно связываются с несколькими мишенями.
В некоторых вариантах реализации антисмысловые соединения содержат часть, имеющую последовательность азотистых оснований, которая по меньшей мере на 70% комплементарна последовательности азотистых оснований целевой нуклеиновой кислоты. В некоторых вариантах реализации антисмысловые соединения содержат часть, имеющую последовательность азотистых оснований, которая по меньшей мере на 80% комплементарна последовательности азотистых оснований целевой нуклеиновой кислоты. В некоторых вариантах реализации антисмысловые соединения содержат часть, имеющую последовательность азотистых оснований, которая по меньшей мере на 90% комплементарна последовательности азотистых оснований целевой нуклеиновой кислоты. В некоторых вариантах реализации антисмысловые соединения содержат часть, имеющую последовательность азотистых оснований, которая по меньшей мере на 95% комплементарна последовательности азотистых оснований целевой нуклеиновой кислоты. В некоторых вариантах реализации антисмысловые соединения содержат часть, имеющую последовательность азотистых оснований, которая по меньшей мере на 98% комплементарна последовательности азотистых оснований целевой нуклеиновой кислоты. В некоторых вариантах реализации антисмысловые соединения содержат часть, имеющую последовательность азотистых оснований, которая на 100% комплементарна последовательности азотистых оснований целевой нуклеиновой кислоты. В некоторых вариантах реализации антисмысловые соединения по меньшей мере на 70%, 80%, 90%, 95%, 98% или 100% комплементарны последовательности азотистых оснований целевой нуклеиновой кислоты по всей длине антисмыслового соединения.
Антисмысловые механизмы включают любой механизм, затрагивающий гибридизацию олигомерного соединения с целевой нуклеиновой кислотой, при этом гибридизация приводит к биологическому эффекту. В некоторых вариантах реализации такая гибридизация приводит либо к разрушению, либо к применению целевой нуклеиновой кислоты с сопутствующим подавлением или стимулированием клеточного механизма, затрагивающего, например, трансляцию, транскрипцию или полиаденилирование целевой нуклеиновой кислоты или нуклеиновой кислоты, с которой целевая кислота может взаимодействовать иным образом.
Один из типов антисмыслового механизма, затрагивающий разрушение целевой РНК представляет собой антисмысл, опосредованный РНКазой Н. РНКаза Н представляет собой клеточную эндонуклеазу, которая расщепляет спираль РНК дуплекса РНК : ДНК. В данной области техники известно, что односпиральные антисмысловые соединения, которые являются «ДНК-подобными», вызывают активность РНКазы Н в клетках млекопитающих. Следовательно, активация РНКазы Н приводит к расщеплению РНК-мишени, посредством этого в значительной степени усиливая эффективность подавления генной экспрессии, опосредованного ДНК-подобным олигонуклеотидом.
Антисмысловые механизмы включают также, без ограничения, РНКи механизмы, в которых используется путь RISC. Такие РНКи механизмы включают, без ограничения, миРНК, оцРНК и микроРНК механизмы. Такие механизмы включают создание миметика микроРНК и/или анти-микро РНК.
Антисмысловые механизмы включают также, без ограничения, механизмы, которые гибридизуют или имитируют некодирующую РНК, отличную от микроРНК или мРНК. Такие некодирующие РНК включают, но не ограничиваются ими, промотор-нацеленную РНК и малую и длинную РНК, которая влияет на транскрипцию или трансляцию одной или более нуклеиновых кислот.
В некоторых вариантах реализации олигонуклеотиды, содержащие описанные в настоящем документе конъюгаты, представляют собой РНКи соединения. В некоторых вариантах реализации олигомерные олигонуклеотиды, содержащие описанные в настоящем документе конъюгаты, представляют собой оцРНК соединения. В некоторых вариантах реализации олигонуклеотиды, содержащие описанные в настоящем документе конъюгаты, спарены со вторым олигомерным соединением с образованием миРНК. В некоторых таких вариантах реализации второе олигомерное соединение также содержит конъюгат. В некоторых вариантах реализации второе олигомерное соединение представляет собой любую модифицированную или немодифицированную нуклеиновую кислоту. В некоторых вариантах реализации олигонуклеотиды, содержащие описанные в настоящем документе конъюгаты, представляют собой антисмысловую цепь в миРНК соединении. В некоторых вариантах реализации олигонуклеотиды, содержащие описанные в настоящем документе конъюгаты, представляют собой смысловую цепь в миРНК соединении. В тех вариантах реализации, в которых конъюгированное олигомерное соединение представляет собой двухцепочечную миРНК, конъюгат может находиться на смысловой цепи, антисмысловой цепи или и на смысловой цепи, и на антисмысловой цепи.
D. Аполипопротеин C-III (apoCIII)
В некоторых вариантах реализации конъюгированные антисмысловые соединения нацелены на любую нуклеиновую кислоту АроСIII. В некоторых вариантах реализации целевая нуклеиновая кислота кодирует белок-мишень АроСIII, который является клинически значимым. В таких вариантах реализации модулирование целевой нуклеиновой кислоты приводит к клиническому преимуществу.
Процесс таргетинга обычно включает определение по меньшей мере одной целевой области, сегмента или сайта в целевой нуклеиновой кислоте для антисмыслового взаимодействия с возникновением в результате такого заданного эффекта.
В некоторых вариантах реализации целевая область представляет собой структурно определенную область нуклеиновой кислоты. Например, в некоторых таких вариантах реализации целевая область может охватывать 3' UTR, 5' UTR, экзон, интрон, кодирующую область, область инициации трансляции, область терминации трансляции или другую определенную область или целевой сегмент нуклеиновой кислоты.
В некоторых вариантах реализации целевой сегмент представляет собой часть целевой области по меньшей мере примерно из 8 азотистых оснований, на которую нацелено конъюгированное антисмысловое соединение. Целевые сегменты могут содержать последовательности ДНК или РНК, которые содержат по меньшей мере 8 смежных азотистых оснований от 5'-конца одного из целевых сегментов (остальные азотистые основания тянутся друг за другом из той же ДНК или РНК, начинаясь сразу перед 5'-концом целевого сегмента и продолжаясь до момента, когда ДНК или РНК будет содержать от около 8 до около 30 азотистых оснований). Целевые сегменты приведены также последовательностями ДНК или РНК, которые содержат по меньшей мере 8 смежных азотистых оснований от 3'-конца одного из целевых сегментов (остальные азотистые основания тянутся друг за другом из той же ДНК или РНК, начинаясь сразу после 3'-конца целевого сегмента и продолжаясь до момента, когда ДНК или РНК будет содержать от около 8 до около 30 азотистых оснований). Целевые сегменты также могут быть приведены последовательностями ДНК или РНК, которые содержат по меньшей мере 8 смежных азотистых оснований из внутренней части последовательности целевого сегмента, и могут тянуться в любом или в обоих направлениях до момента, когда конъюгированное антисмысловое соединение будет содержать от около 8 до около 30 азотистых оснований.
В некоторых вариантах реализации антисмысловые соединения, нацеленные на нуклеиновую кислоту АроСIII, могут быть модифицированы так, как описано в настоящем документе. В некоторых вариантах реализации антисмысловые соединения могут иметь модифицированный сахарный фрагмент, немодифицированный сахарный фрагмент или смесь модифицированных и немодифицированных сахарных фрагментов, как описано в настоящем документе. В некоторых вариантах реализации антисмысловые соединения могут иметь модифицированная межнуклеозидная связь, немодифицированная межнуклеозидная связь или смесь модифицированных и немодифицированных межнуклеозидных связей, как описано в настоящем документе. В некоторых вариантах реализации антисмысловые соединения могут иметь модифицированное азотистое основание, немодифицированное азотистое основание или смесь модифицированных и немодифицированных азотистых оснований, как описано в настоящем документе. В некоторых вариантах реализации антисмысловые соединения могут иметь мотив, описанный в настоящем документе.
В некоторых вариантах реализации антисмысловые соединения, нацеленные на нуклеиновые кислоты АроСIII, могут быть конъюгированы так, как описано в настоящем документе.
АроСIII представляет собой составную часть HDL и богатых триглицеридами (TG) липопротеинов. Повышенные уровни АроСIII связаны с повышенными уровнями TG и такими заболеваниями как сердечно-сосудистое заболевание, метаболический синдром, ожирение и диабет. Повышенные уровни TG связаны с панкреатитом. АроСIII замедляет выведение богатых триглицеридами липопротеинов за счет ингибирования липолиза посредством подавления липопротеин-липазы (LPL) и препятствия связыванию липопротеина с гликозаминогликановой матрицей клеточной поверхности. Антисмысловые соединения, нацеленные на АроСIII, были описаны ранее в WO 2004/093783 и WO 2012/149495, полное содержание каждого из которых включено в настоящий документ посредством ссылки.
Некоторые конъюгированные антисмысловые соединения, нацеленные на нуклеиновую кислоту АроСIII
В некоторых вариантах реализации конъюгированные антисмысловые соединения нацелены на нуклеиновую кислоту АроСIII, имеющую любую последовательность с номером доступа GENBANK® NM_000040.1 (включенную в настоящий документ как SEQ ID NO: 1); с номером доступа GENBANK NT_033899.8, усеченную по нуклеотидам с 20262640 по 20266603 (включенную в настоящий документ как SEQ ID NO: 2); и с номером доступа GenBank NT_035088.1, усеченную по нуклеотидам с 6238608 по 6242565 (включенную в настоящий документ как SEQ ID NO: 3). В некоторых таких вариантах реализации конъюгированное антисмысловое соединение по меньшей мере на 90%, по меньшей мере на 95% или на 100% комплементарно любой из SEQ ID NO: 1-3.
В некоторых вариантах реализации конъюгированное антисмысловое соединение, нацеленное на SEQ ID NO: 1, содержит по меньшей мере 8 смежных азотистых оснований последовательности SEQ ID NO: 87. В некоторых вариантах реализации конъюгированное антисмысловое соединение, нацеленное на SEQ ID NO: 1, содержит последовательность азотистых оснований SEQ ID NO: 87.
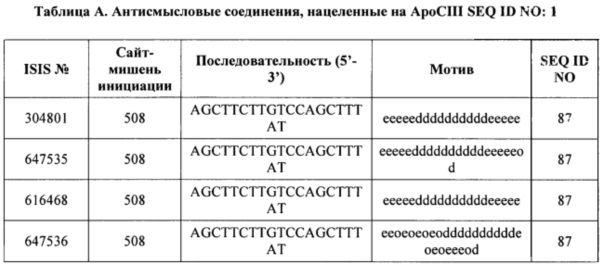
Терапевтические показания для АроСIII
В некоторых вариантах реализации настоящего изобретения приведены способы применения конъюгированного антисмыслового соединения, нацеленного на нуклеиновую кислоту АроСIII, для модулирования экспрессии АроСIII у субъекта. В некоторых вариантах реализации экспрессия АроСIII снижена.
В некоторых вариантах реализации настоящего изобретения приведены способы применения конъюгированного антисмыслового соединения, нацеленного на нуклеиновую кислоту АроСIII, в фармацевтической композиции для лечения субъекта. В некоторых вариантах реализации субъект страдает сердечно-сосудистым и/или метаболическим заболеванием, расстройством или патологическим состоянием. В некоторых вариантах реализации субъект страдает гипертриглицеридемией, несемейной гипертриглицеридемией, семейной гипертриглицеридемией, гетерозиготной семейной гипертриглицеридемией, гомозиготной семейной гипертриглицеридемией, смешанной дислипидемией, атеросклерозом, риском развития атеросклероза, ишемической болезнью сердца, анамнезом ишемической болезни сердца, ишемической болезнью сердца с ранним началом, одним или более факторами риска ишемической болезни сердца, диабетом II типа, диабетом II типа с дислипидемией, дислипидемией, гиперлипидемией, гиперхолестеринемией, повышенной концентрацией жирных кислот, стеатозом печени, неалкогольным стеатогепатитом, панкреатитом и/или неалкогольной жировой инфильтрацией печени.
В некоторых вариантах реализации настоящего изобретения приведены способы применения конъюгированного антисмыслового соединения, нацеленного на нуклеиновую кислоту АроСIII, для производства лекарственного средства.
Е. Некоторые конъюгаты GalNAc с нуклеиновыми кислотами
В некоторых вариантах реализации конъюгированные антисмысловые соединения содержат антисмысловые соединения, имеющие последовательности азотистых оснований и модификации антисмысловых соединений, приведенные ниже в таблице, присоединенные к конъюгату GalNAc. Все межнуклеозидные связи представляют собой тиофосфатные межнуклеозидные связи, если не указано иное. Нижний индекс «1» означает LNA-бициклический нуклеозид. Нижний индекс «d» означает 2'-дезоксинуклеозид. Нижний индекс «е» означает 2'-МОЕ модифицированный нуклеозид. Нижний индекс «V» означает 2 амино-2' -дезоксиаденозин.
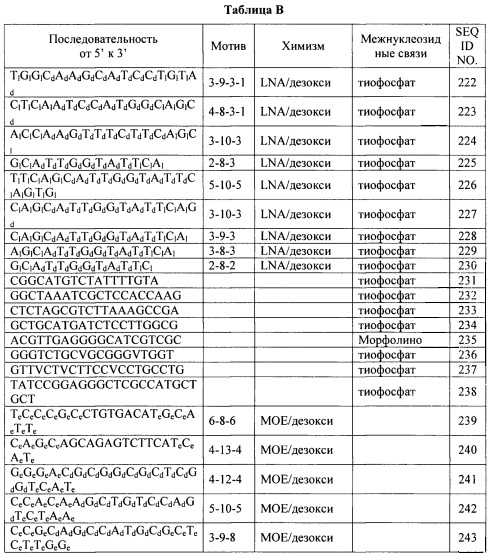
F. Некоторые фармацевтические композиции
В некоторых вариантах реализации настоящего описания приведены фармацевтические композиции, содержащие одно или более антисмысловых соединений. В некоторых вариантах реализации такая фармацевтическая композиция содержит подходящий фармацевтически приемлемый разбавитель или носитель. В некоторых вариантах реализации фармацевтическая композиция содержит стерильный солевой раствор и одно или. более антисмысловых соединений. В некоторых вариантах реализации такая фармацевтическая композиция состоит из стерильного солевого раствора и одного или более антисмысловых соединений. В некоторых вариантах реализации стерильный солевой раствор представляет собой солевой раствор фармацевтической марки. В некоторых вариантах реализации фармацевтическая композиция содержит одно или более антисмысловых соединений и стерильную воду. В некоторых вариантах реализации фармацевтическая композиция состоит из одного или более антисмысловых соединений и стерильной воды. В некоторых вариантах реализации стерильный солевой раствор представляет собой воду фармацевтической марки. В некоторых вариантах реализации фармацевтическая композиция содержит одно или более антисмысловых соединений и фосфатно-солевой буферный раствор (PBS). В некоторых вариантах реализации фармацевтическая композиция состоит из одного и ни более антисмысловых соединений и фосфатно-солевого буферного раствора (PBS). В некоторых вариантах реализации стерильный солевой раствор представляет собой PBS фармацевтической марки.
В некоторых вариантах реализации антисмысловые соединения могут быть смешаны с фармацевтически приемлемыми активными и/или инертными веществами для получения фармацевтических композиций или составов. Композиции и способы составления фармацевтических композиций зависят от множества критериев, включая, но не ограничиваясь этим, способ введения, тяжесть заболевания или дозу, подлежащую введению.
Фармацевтические композиции, содержащие антисмысловые соединения, охватывают любые фармацевтически приемлемые соли, сложные эфиры или соли таких сложных эфиров. В некоторых вариантах реализации фармацевтические композиции, содержащие антисмысловые соединения, содержат один или более олигонуклеотидов, которые при введении млекопитающему, включая человека, могут обеспечивать (прямо или косвенно) его биологически активный метаболит или остаток. Соответственно, например, настоящее описание относится также к фармацевтически приемлемым солям антисмысловых соединений, пролекарствам, фармацевтически приемлемым солям таких пролекарств и к другим биоэквивалентам. Подходящие фармацевтически приемлемые соли включают, но не ограничиваются ими, соли натрия и калия.
Пролекарство может включать внедрение дополнительных нуклеозидов у одного или обоих концов олигонуклеотида, которые расщепляются в организме под действием эндогенных нуклеаз с образованием активного антисмыслового олигонуклеотида.
В многочисленных способах в терапиях с нуклеиновыми кислотами были применены липидные фрагменты. В некоторых таких способах нуклеиновую кислоту вводят в предварительно сформированные липосомы или липоплексы, полученные из смесей катионных липидов и нейтральных липидов. В некоторых способах получают ДНК комплексы с моно- или поликатионными липидами без участия нейтрального липида. В некоторых вариантах реализации липидный фрагмент выбран для улучшения распределения фармацевтического агента в определенной клетке или ткани. В некоторых вариантах реализации липидный фрагмент выбран для улучшения распределения фармацевтического агента в жировой ткани. В некоторых вариантах реализации липидный фрагмент выбран для улучшения распределения фармацевтического агента в мышечной ткани.
В некоторых вариантах реализации фармацевтические композиции, приведенные в настоящем документе, содержат один или более модифицированных олигонуклеотидов и одно или более вспомогательных веществ. В некоторых таких вариантах реализации вспомогательные вещества выбраны из воды, солевых растворов, спирта, полиэтиленгликолей, желатина, лактозы, амилазы, стеарата магния, талька, кремниевой кислоты, вязкого парафина, гидроксиметилцеллюлозы и поливинилпирролидона.
В некоторых вариантах реализации фармацевтическая композиция, приведенная в настоящем документе, содержит систему доставки. Примеры систем доставки включают, но не ограничиваются ими, липосомы и эмульсии. Некоторые системы доставки подходят для получения некоторых фармацевтических композиций, включая композиции, содержащие гидрофобные соединения. В некоторых вариантах реализации применяют некоторые органические растворители, такие как диметилсульфоксид.
В некоторых вариантах реализации фармацевтическая композиция, приведенная в настоящем документе, содержит одну или более тканеспецифичных молекул доставки, предназначенных для доставки одного или более фармацевтических агентов настоящего описания в определенную ткань или типы клеток. Например, в некоторых вариантах реализации фармацевтические композиции включают липосомы, покрытые тканеспецифичным антителом.
В некоторых вариантах реализации фармацевтическая композиция, приведенная в настоящем документе, содержит систему совместного растворителя. Некоторые такие системы совместных растворителей содержат, например, бензиловый спирт, неполярное поверхностно-активное вещество, смешиваемый с водой органический полимер и водную фазу. В некоторых вариантах реализации такие системы совместных растворителей применяют для гидрофобных соединений. Не ограничивающий пример такой системы совместных растворителей представляет собой система совместных растворителей VPD, которая представляет собой раствор абсолютного этанола, содержащего 3% масс./об. бензилового спирта, 8% масс./об. неполярного поверхностно-активного вещества Polysorbate 80™ и 65% масс./об. полиэтиленгликоля 300. Пропорции таких систем совместных растворителей могут существенно варьироваться без значительного изменения их характеристик растворимости и токсичности. Кроме того, может варьироваться сущность компонентов совместных растворителей: например, вместо Polysorbate 80™ могут быть применены другие поверхностно-активные вещества; может варьироваться размер фракции полиэтиленгликоля; вместо полиэтиленгликоля могут быть применены другие биосовместимые полимеры, например, поливинилпирролидон; и вместо декстрозы могут быть применены другие сахара или полисахариды.
В некоторых вариантах реализации фармацевтическую композицию, приведенную в настоящем документе, получают для перорального введения. В некоторых вариантах реализации фармацевтические композиции получают для буккального введения.
В некоторых вариантах реализации фармацевтическую композицию получают для введения инъекцией (например, внутривенной, подкожной, внутримышечной и т.д.). В некоторых таких вариантах реализации фармацевтическая композиция содержит носитель и составлена в водном растворе, таком как вода или физиологически совместимые буферы, такие как раствор Хэнкса, раствор Рингера или физиологический солевой буфер. В некоторых вариантах реализации включены другие ингредиенты (например, ингредиенты, улучшающие растворимость или служащие консервантами). В некоторых вариантах реализации суспензии для инъекций получают при помощи подходящих жидких носителей, суспендирующих агентов и т.п.Некоторые фармацевтические композиции для инъекций приведены в форме разовой дозы, например, в ампулах, или в многодозовых контейнерах. Некоторые фармацевтические композиции для инъекций представляют собой суспензии, растворы или эмульсии в масляных или водных жидких носителях, и они могут содержать вспомогательные агенты, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. Некоторые растворители, подходящие для применения в фармацевтических композициях для инъекций, включают, но не ограничиваются ими, липофильные растворители и жирные масла, такие как кунжутное масло, синтетические сложные эфиры жирных кислот, такие как этилолеат или триглицериды, и липосомы. Водные суспензии для инъекций могут содержать вещества, которые увеличивают вязкость суспензии, такие как карбоксиметилцеллюлоза натрия, сорбит или декстран. Такие суспензия могут также необязательно содержать подходящие стабилизаторы или агенты, которые увеличивают растворимость фармацевтических агентов с обеспечением возможности получения высококонцентрированных растворов.
В некоторых вариантах реализации фармацевтическую композицию получают для трансмукозального введения. В некоторых таких вариантах реализации в составе применяют пенетранты, соответствующие барьеру, через который необходимо проникнуть. Такие пенетранты общеизвестны в данной области техники.
В некоторых вариантах реализации фармацевтическая композиция, приведенная в настоящем документе, содержит олигонуклеотид в терапевтически эффективном количестве. В некоторых вариантах реализации терапевтически эффективное количество является достаточным для предотвращения, облегчения или улучшения симптомов заболевания или для увеличения продолжительности жизни субъекта, подлежащего лечению. Определение терапевтически эффективного количества находится в пределах возможностей специалистов в данной области техники.
В некоторых вариантах реализации один или более модифицированных олигонуклеотидов, приведенных в настоящем документе, составляют в виде пролекарства. В некоторых вариантах реализации при введении in vivo пролекарство химически превращается в биологически, фармацевтически или терапевтически более активную форму олигонуклеотида. В некоторых вариантах реализации пролекарства пригодны благодаря тому, что их проще вводить, чем соответствующую активную форму. Например, в некоторых случаях пролекарство может быть более биодоступным (например, при пероральном введении), чем соответствующая активная форма. В некоторых случаях пролекарство может обладать улучшенной растворимостью, по сравнению с соответствующей активной формой. В некоторых вариантах реализации пролекарства менее растворимы в воде, чем соответствующая активная форма. В некоторых случаях такие пролекарства обладают превосходной передачей через клеточные мембраны, при этом растворимость в воде ухудшает их подвижность. В некоторых вариантах реализации пролекарство представляет собой сложный эфир. В некоторых таких вариантах реализации сложный эфир при введении метаболически гидролизуется до карбоновой кислоты. В некоторых случаях соединение, содержащее карбоновую кислоту, представляет собой соответствующую активную форму. В некоторых вариантах реализации пролекарство содержит короткий пептид (полиаминокислоту), связанный с кислотной группой. В некоторых таких вариантах реализации пептид расщепляется при введении с образованием соответствующей активной формы.
В некоторых вариантах реализации настоящего описания приведены композиции и способы снижения количества или активности целевой нуклеиновой кислоты в клетке. В некоторых вариантах реализации клетка находится у животного. В некоторых вариантах реализации животное представляет собой млекопитающее. В некоторых вариантах реализации животное представляет собой грызуна. В некоторых вариантах реализации животное представляет собой примата. В некоторых вариантах реализации животное представляет собой примата, не являющегося человеком. В некоторых вариантах реализации животное представляет собой человека.
В некоторых вариантах реализации настоящего описания приведены способы введения животному фармацевтической композиции, содержащей олигонуклеотид настоящего описания. Подходящие способы введения включают, но не ограничиваются ими, пероральный, ректальный, трансмукозальный, интестинальный, энтеральный, местный, суппозитории, через ингаляции, интратекальный, интрацеребровентрикулярный, внутрибрюшинный, интраназальный, интраокулярный, внутриопухолевый и парентеральный (например, внутривенный, внутримышечный, интрамедуллярный и подкожный). В некоторых вариантах реализации вводят фармацевтические интратекальные средства для достижения местного, а не системного воздействия. Например, фармацевтические композиции могут быть введены инъекцией непосредственно в область заданного эффекта (например, в печень).
Неограничивающее описание и включение посредством ссылки
Несмотря на то, что некоторые соединения, композиции и способы, описанные в настоящем документе, были подробно описаны в соответствии с некоторыми вариантами реализации изобретения, следующие примеры служат лишь для иллюстрации соединений, описанных в настоящем документе, и их не следует считать их ограничением. Каждая из ссылок, номера доступа GenBank и подобные ссылки, упоминаемые в настоящей заявке, включены в настоящий документ посредством ссылки в полном объеме.
Несмотря на то, что перечень последовательностей, сопровождающий этот файл, указывает каждую последовательность либо как «РНК», либо как «ДНА», по необходимости в действительности эти последовательности могут быть модифицированы любой комбинацией химических модификаций. Специалистам в данной области техники понятно, что такое обозначение как «РНК» или «ДНК» для описания модифицированных олигонуклеотидов, является в некоторых случаях произвольным. Например, олигонуклеотид, содержащий нуклеозид, содержащий 2'-ОН сахарный фрагмент и тиминовое основание, может быть описан как ДНК, имеющая модифицированный сахар (2'-ОН вместо природного 2'-Н в ДНК) или как РНК, имеющая модифицированное основание (тимин (метилированный урацил) вместо природного урацила в РНК).
Соответственно, последовательности нуклеиновых кислот, приведенные в настоящем документе, включая, но не ограничиваясь ими, последовательности в перечне последовательностей, предназначены для охвата нуклеиновых кислот, содержащих любую комбинацию природных или модифицированных РНК и/или ДНК, включая, но не ограничиваясь ими, такие нуклеиновые кислоты, которые содержат модифицированные азотистые основания. В качестве дополнительного примера и без ограничения, олигонуклеотид, содержащий последовательность азотистых оснований «ATCGATCG», охватывает любые олигонуклеотиды, имеющие такую последовательность азотистых оснований, модифицированных или немодифицированных, включая, но не ограничиваясь ими, такие соединения, которые содержат РНК основания, такие как те, которые имеют последовательность «AUCGAUCG», и те, которые имеют некоторые ДНК основания и некоторые РНК основания, такие как «AUCGATCG», а также олигонуклеотиды, имеющие другие модифицированные основания, такие как «ATmeCGAUCG», гдеmeС означает цитозиновое основание, содержащее метиловую группу в 5-положении.
Примеры
Следующие примеры иллюстрируют некоторые варианты реализации настоящего описания и не являются ограничивающими. Более того, если приведены конкретные варианты реализации, авторы изобретения подразумевают общее применение указанных конкретных вариантов реализации. Например, описание олигонуклеотида, содержащего конкретный мотив, дает обоснованное основание для дополнительных олигонуклеотидов содержащих такой же или похожий мотив. И, например, если конкретная высокооффинная модификация возникает в определенном положении, то в этом же положении считаются подходящими другие высокоаффинные модификации, если не указано иное.
Пример 1. Общий способ получения фосфорамидитов, Соединений 1,1а и 2
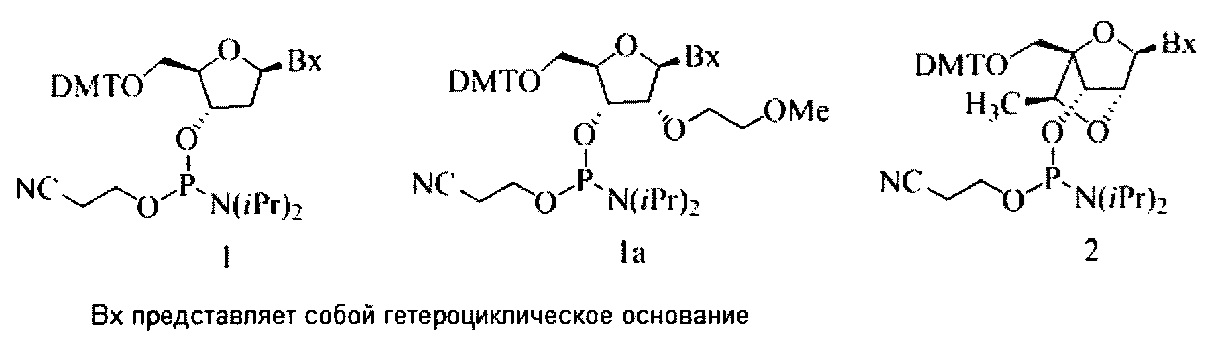


Bx представляет собой гетероциклическое основание
Соединения 1, 1а и 2 получили по методикам, общеизвестным в данной области техники, описанным в данном описании (см. Seth et al., Bioorg. Med. Chem., 2011, 21(4), 1122-1125, J. Org. Chem., 2010, 75(5), 1569-1581, Nucleic Acids Symposium Series, 2008, 52(1), 553-554); и см. также опубликованные Международные заявки РСТ (WO 2011/15818, WO 2010/077578, WO 2010/036698, WO 2009/143369, WO 2009/006478 и WO 2007/090071) и патент США 7569686).
Пример 2. Получение Соединения 7
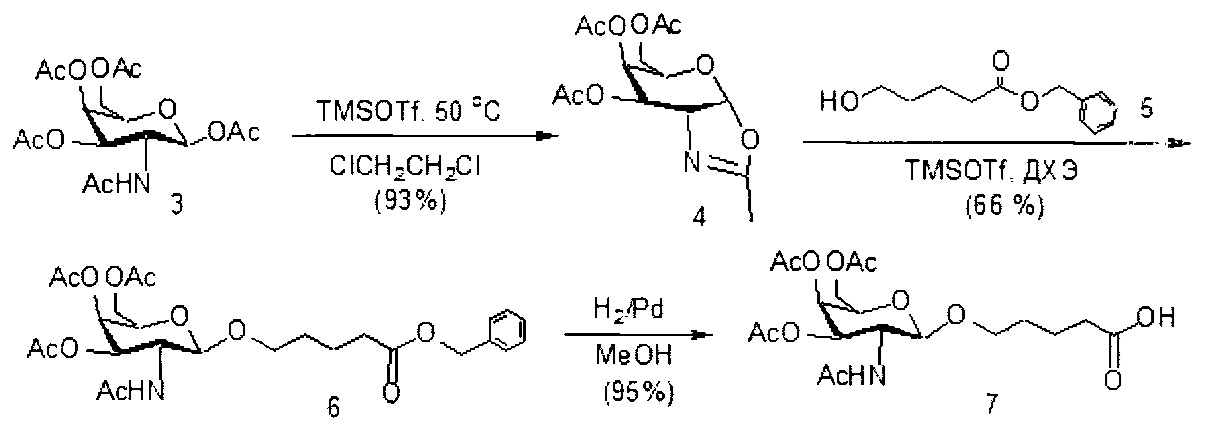
Соединение 3 (2-ацетамидо-1,3,4,6-тетра-O-ацетил-2-дезокси-β-D-галактопираноза или галактозамина пентаацетат) имеется в продаже. Соединение 5 получили по опубликованным методикам (Weber et al., J. Med. Chem., 1991, 34, 2692).
Пример 3. Получение Соединения 11
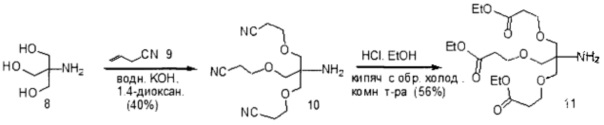
Соединения 8 и 9 имеются в продаже.
Пример 4. Получение Соединения 18
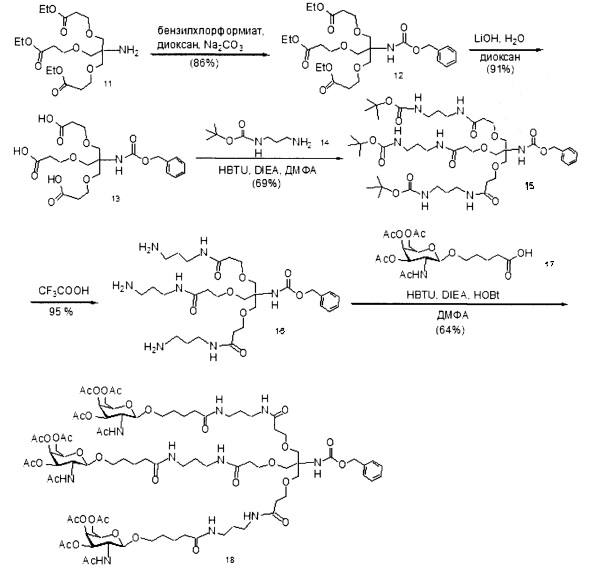
Соединение 11 получили по способам, описанным в Примере 3. Соединение 14 имеется в продаже. Соединение 17 получили по такому же способу, как описан в публикации Rensen et al., J. Med. Chem., 2004, 47, 5798-5808.
Пример 5. Получение Соединения 23
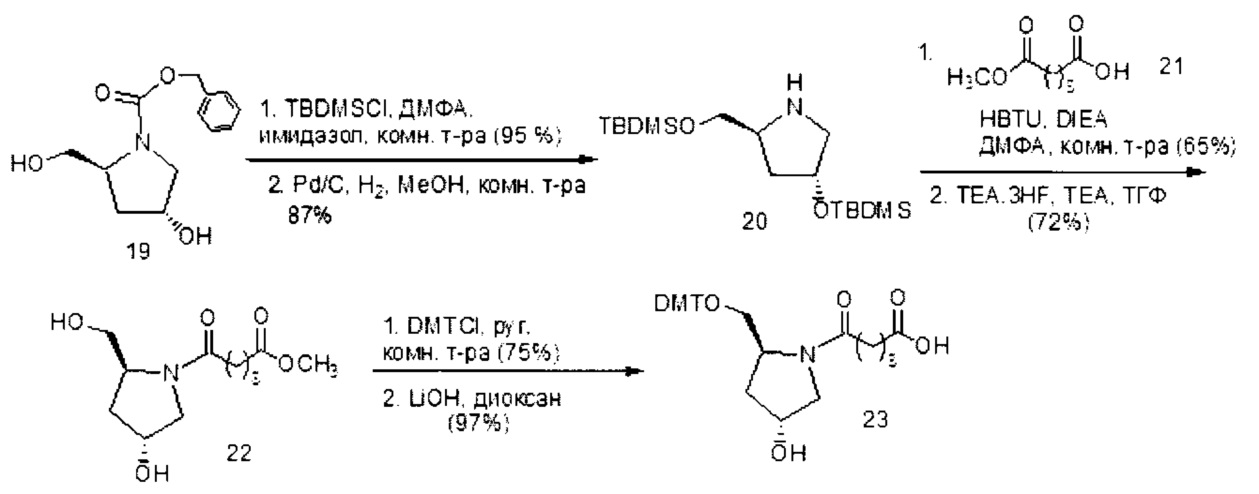
Соединения 19 и 21 имеются в продаже.
Пример 6. Получение Соединения 24

Соединения 18 и 23 получили так, как описано в способах в Примерах 4 и 5.
Пример 7. Получение Соединения 25

Соединение 24 получили по способам, приведенным в Примере 6.
Пример 8. Получение Соединения 26
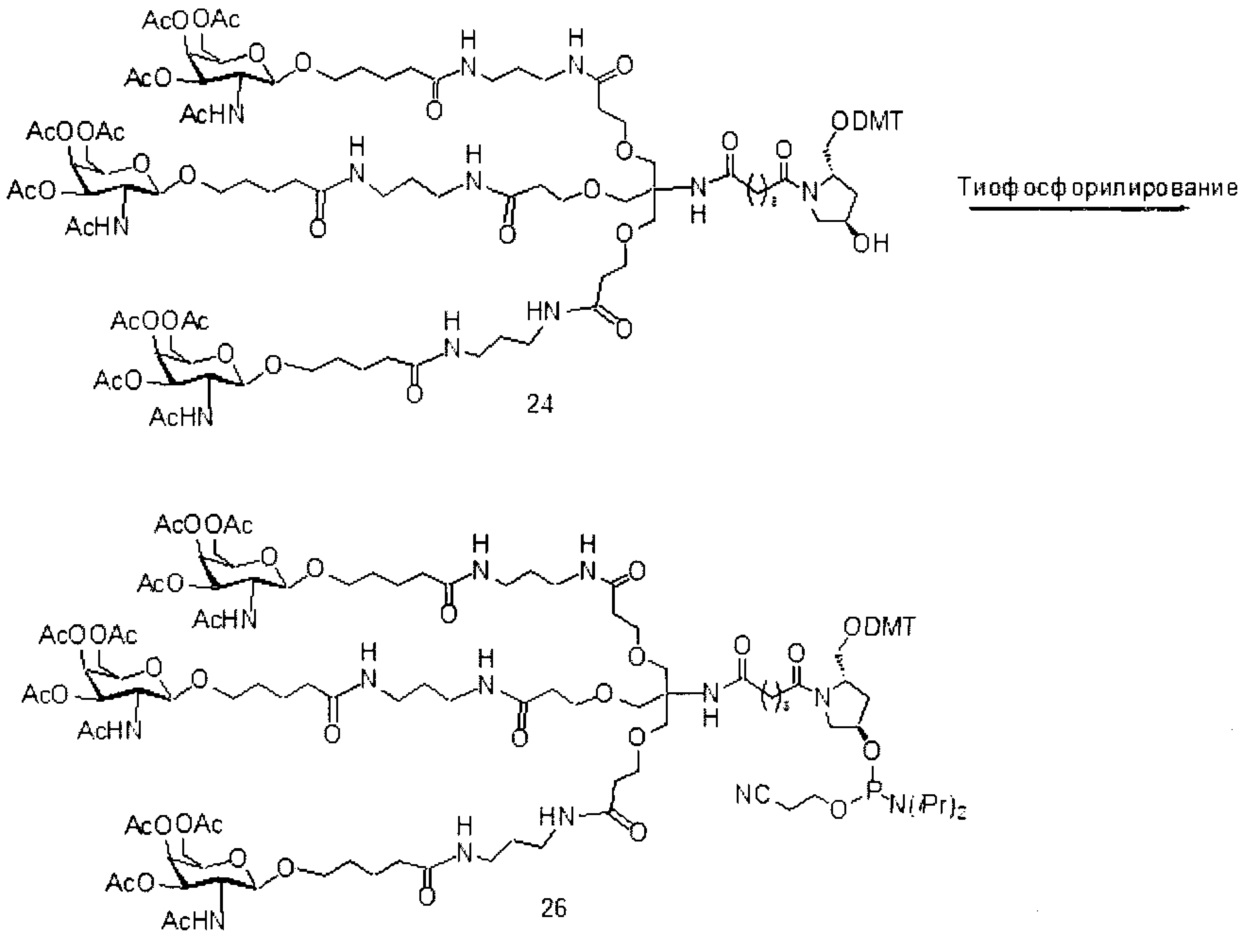
Соединение 24 получили по способам, приведенным в Примере 6.
Пример 9. Общее получение конъюгированных ASO, содержащих GalNAc3-1 на 3'-конце, Соединения 29
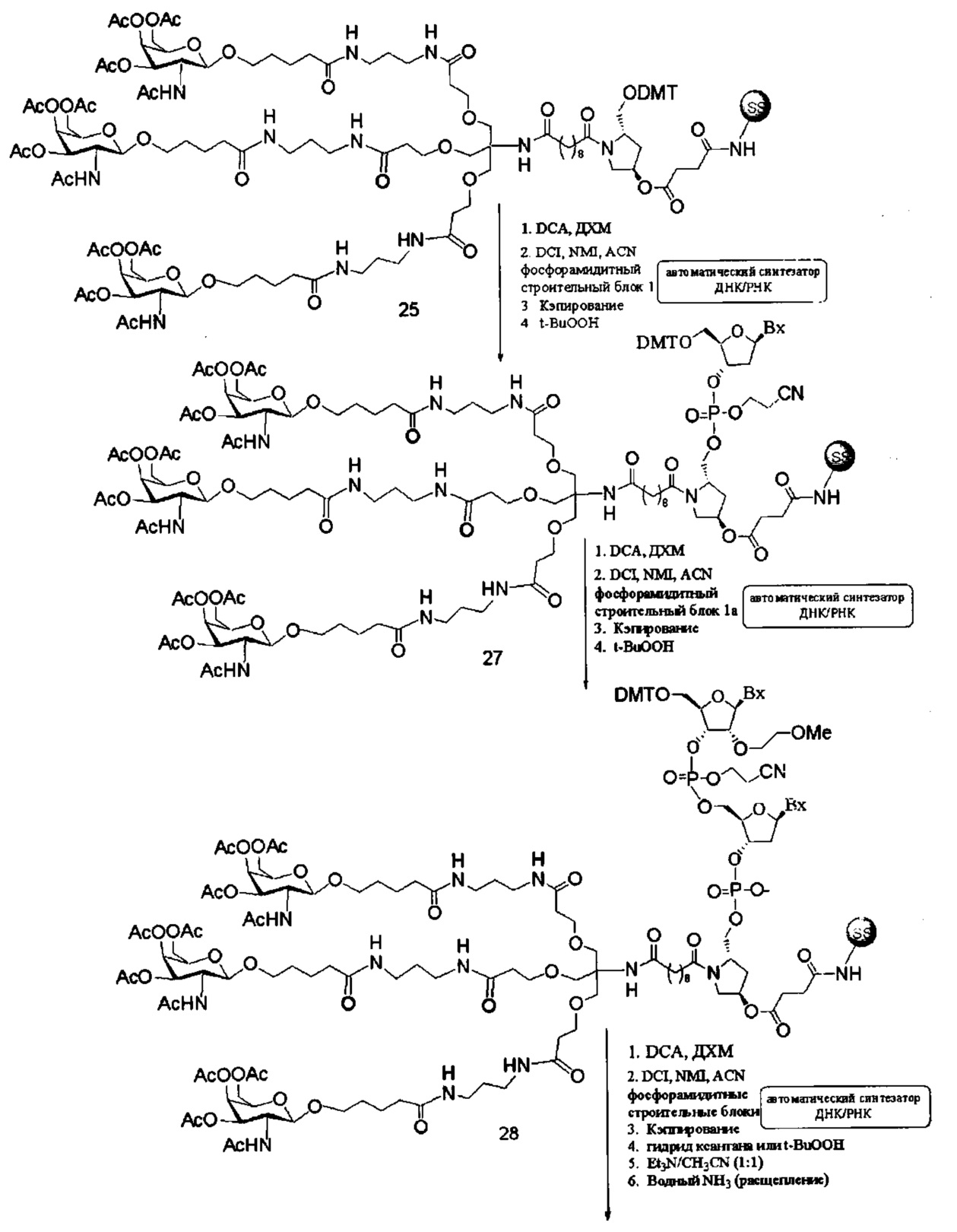
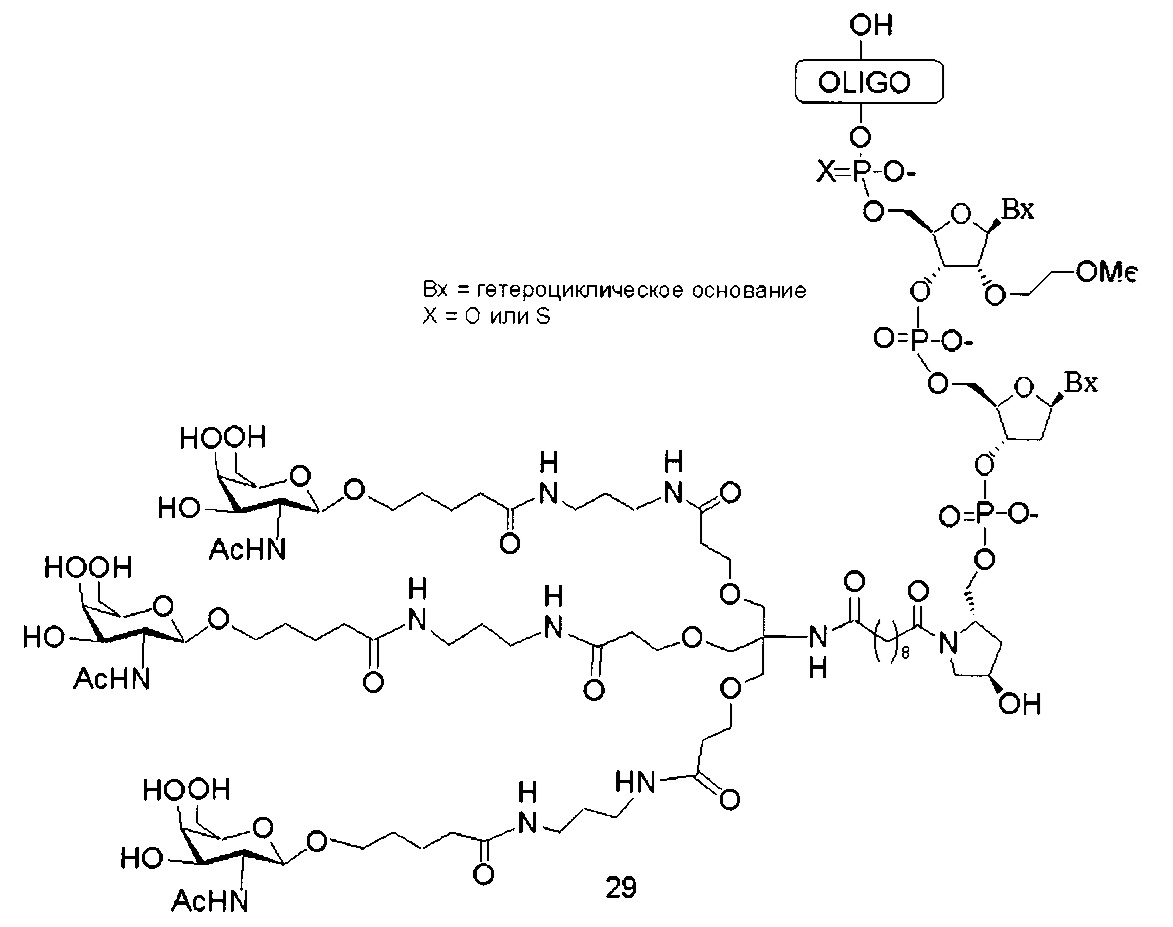
Где защищенный GalNAc3-1 имеет структуру:
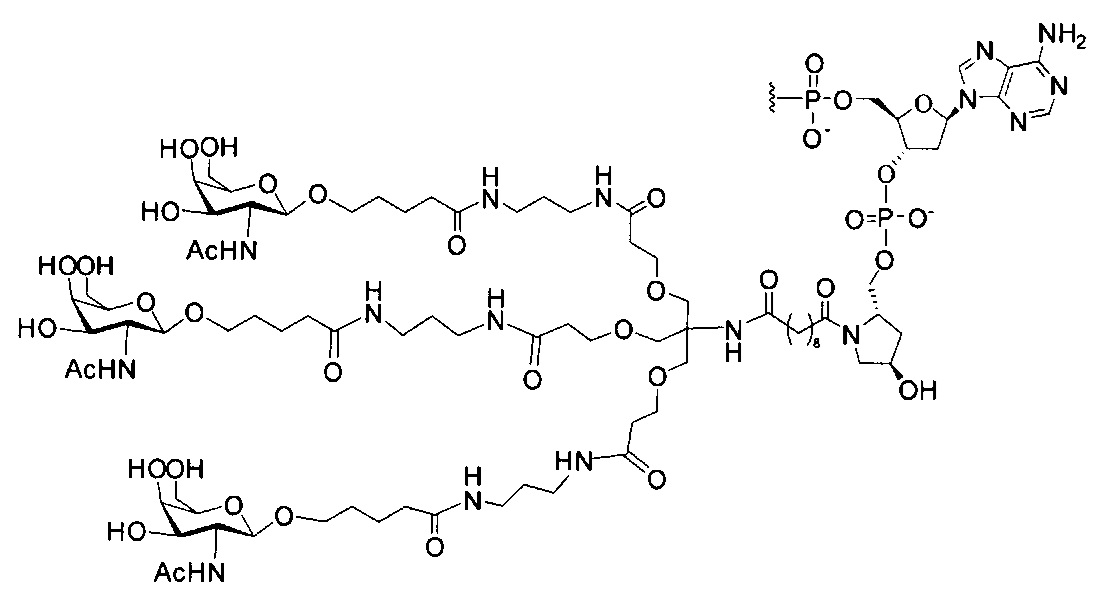
Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-1 (GalNAc3-1a) может быть комбинирована с любым расщепляемым фрагментом с получением различных конъюгирующих групп. При этом GalNAc3-1a имеет формулу:
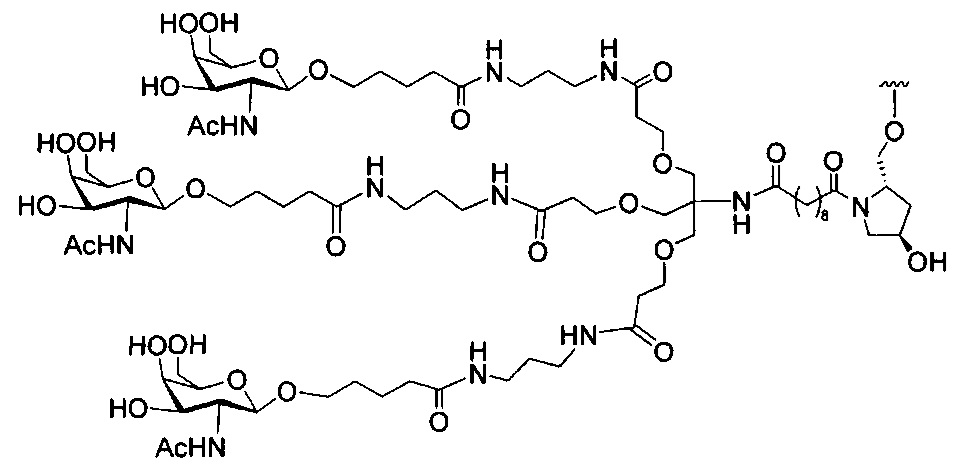
Твердую подложку, связывающую защищенный GalNAc3-1, Соединение 25, получили по способам, приведенным в Примере 7. Олигомерное Соединение 29, содержащее GalNAc3-1 на 3'-конце, получили по стандартным методика в автоматическом синтезаторе ДНК/РНК (см. Dupouy et al., Angew. Chem. Int. ред., 2006, 45, 3623-3627). Фосфорамидитные строительные блоки, Соединения 1 и 1а, получили по способам, приведенным в Примере 1. Изображенные фосфорамидиты являются типичными и не предназначены для ограничения, поскольку могут быть применены другие фосфорамидитные строительные блоки для получения олигомерных соединений, имеющих заданную последовательность и состав. Порядок и количество фосфорамидитов, добавляемых к твердой подложке, может быть подобрано для получения разорванных олигомерных соединений, описанных в настоящем документе. Такие разорванные олигомерные соединения могут иметь заданный состав и последовательность оснований, продиктованную любой данной мишенью.
Пример 10. Общее получение конъюгированных ASO, содержащих GalNAc3-1 на 5'-конце, Соединения 34
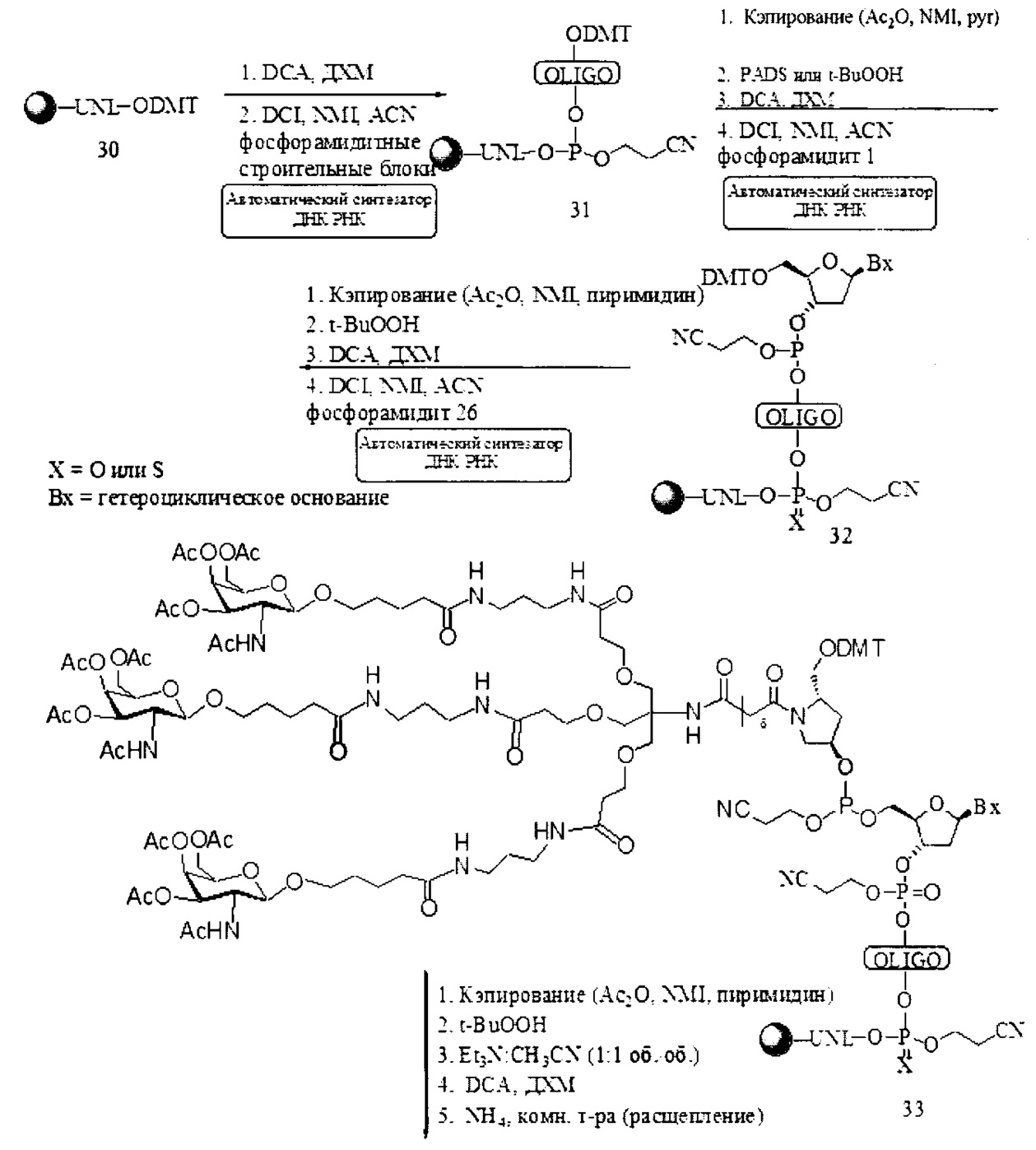
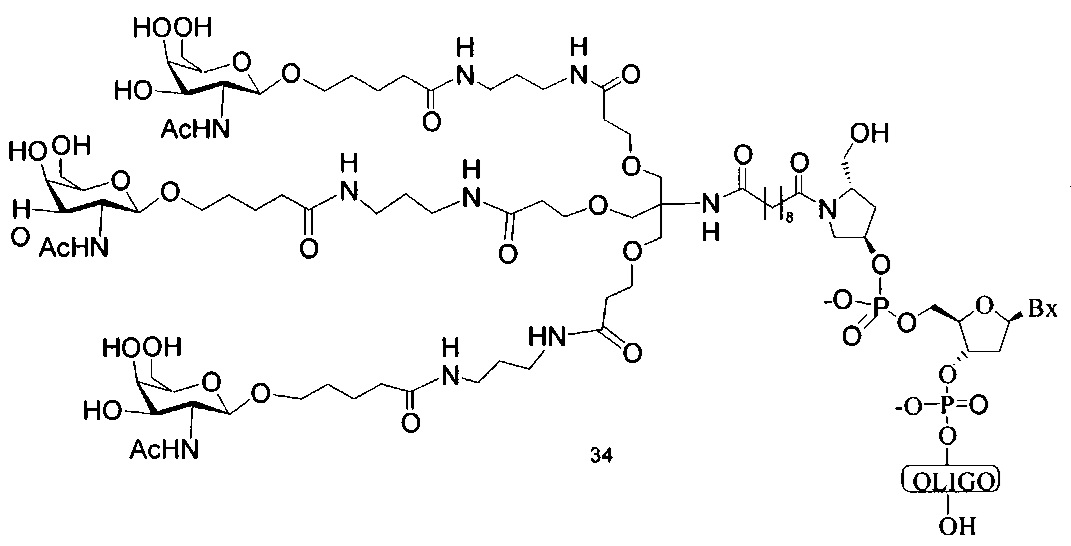
Unylinker™ 30 имеется в продаже. Олигомерное соединение 34, содержащее кластер GalNAc3-1 на 5'-конце, получили по стандартным способам в автоматическом синтезаторе ДНК/РНК (см. Dupouy et al., Angew. Chem. Int. Ed., 2006, 45, 3623-3627). Фосфорамидитные строительные блоки, Соединения 1 и 1a, получили по способам, приведенным в Примере 1. Изображенные фосфорамидиты являются типичными и не предназначены для ограничения, поскольку могут быть применены другие фосфорамидитные строительные блоки для получения олигомерного соединения, имеющего заданную последовательность и состав. Порядок и количество фосфорамидитов, добавляемых к твердой подложке, может быть подобрано для получения разорванных олигомерных соединений, описанных в настоящем документе. Такие разорванные олигомерные соединения могут иметь заданный состав и последовательность оснований, продиктованную любой данной мишенью.
Пример 11. Получение Соединения 39
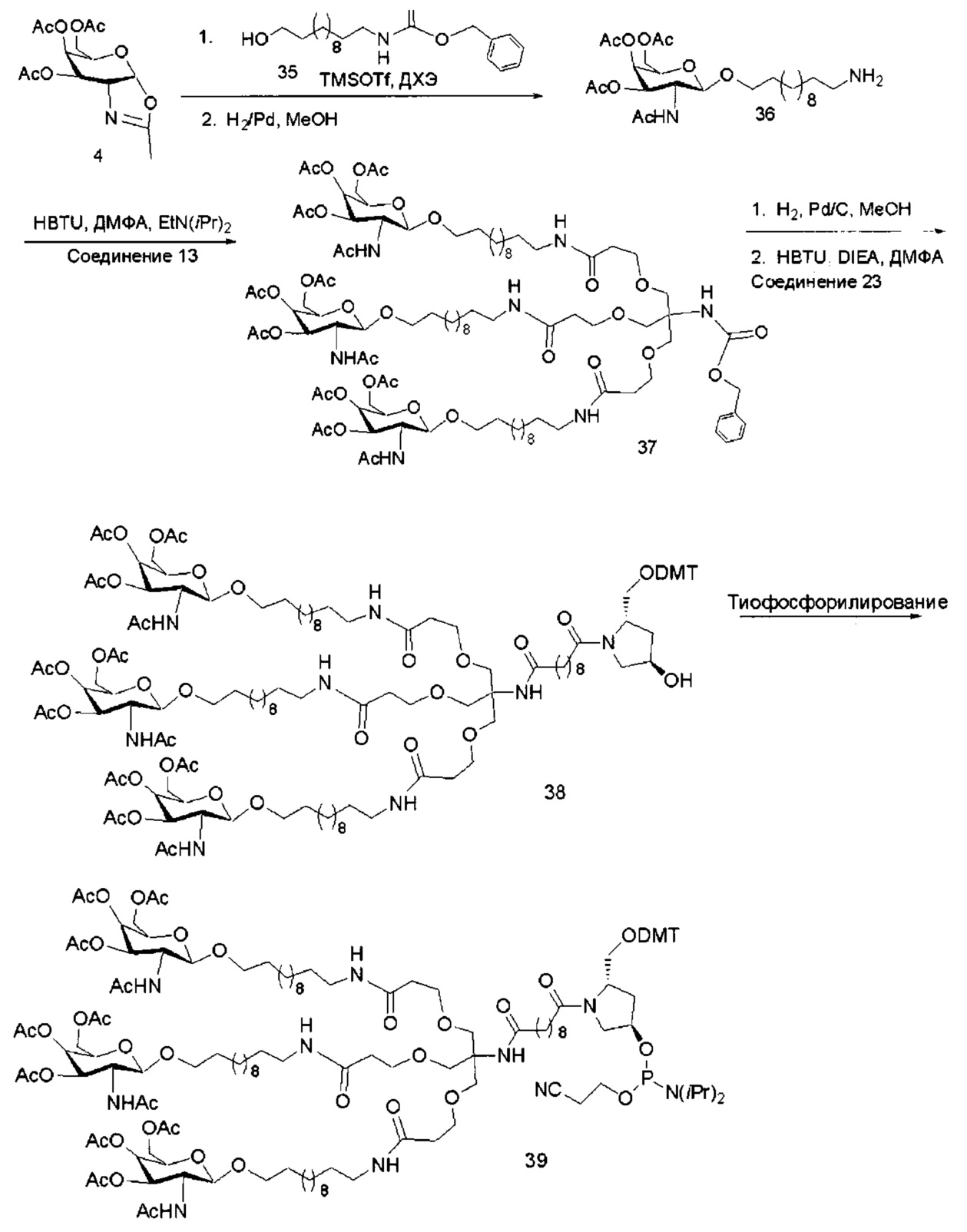
Соединения 4, 13 и 23 получили по способам, описанным в Примерах 2, 4 и 5. Соединение 35 получили по таким же способам, как описаны в публикации Rouchaud el al., Eur. J. Org. Chem., 2011, 12, 2346-2353.
Пример 12. Получение Соединения 40
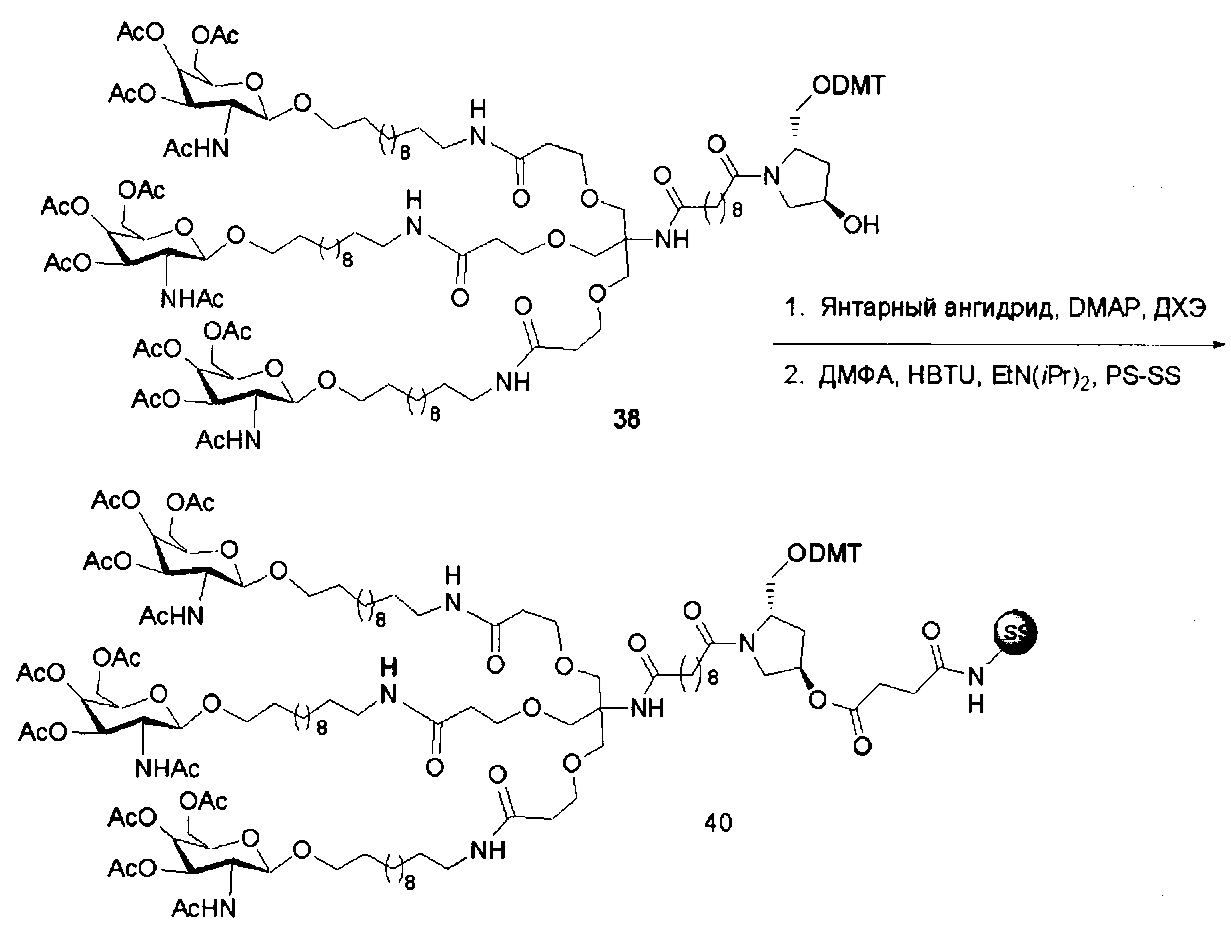
Соединение 38 получили по способам, приведенным в Примере 11.
Пример 13. Получение Соединения 44
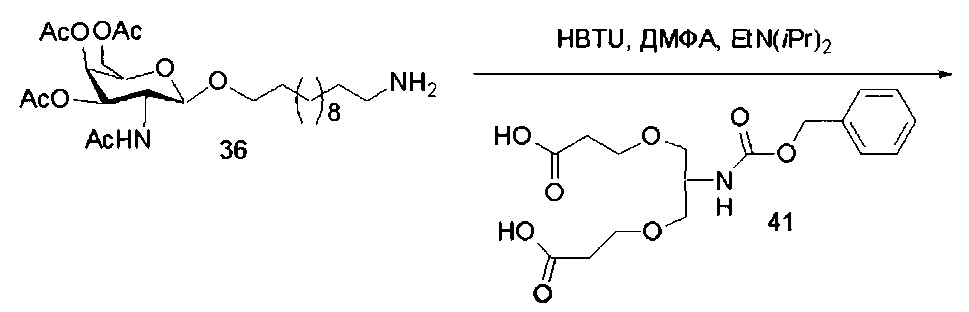
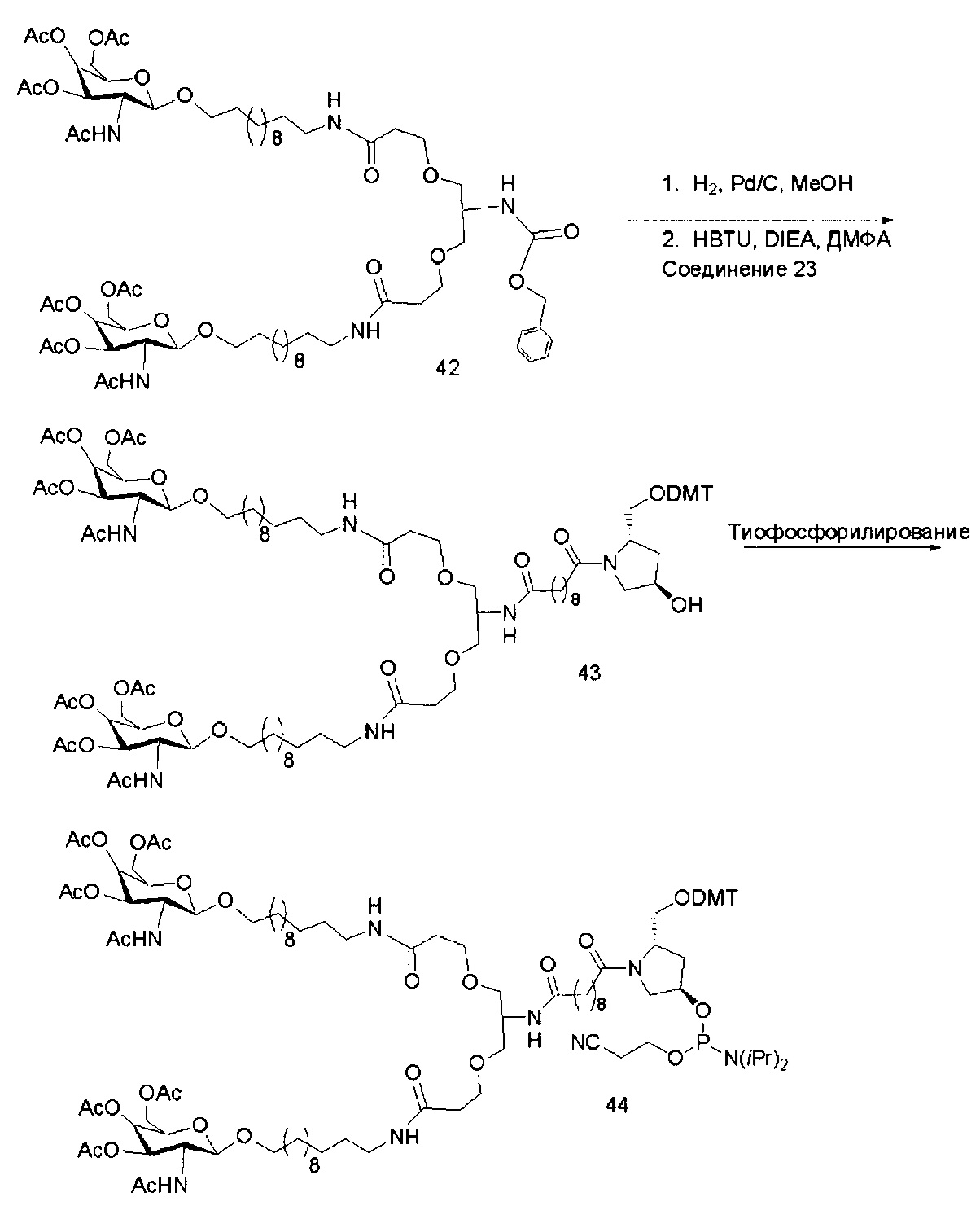
Соединения 23 и 36 получили по способам, приведенным в Примерах 5 и 11. Соединение 41 получили по таким же способам, как описаны в публикации WO 2009082607.
Пример 14. Получение Соединения 45
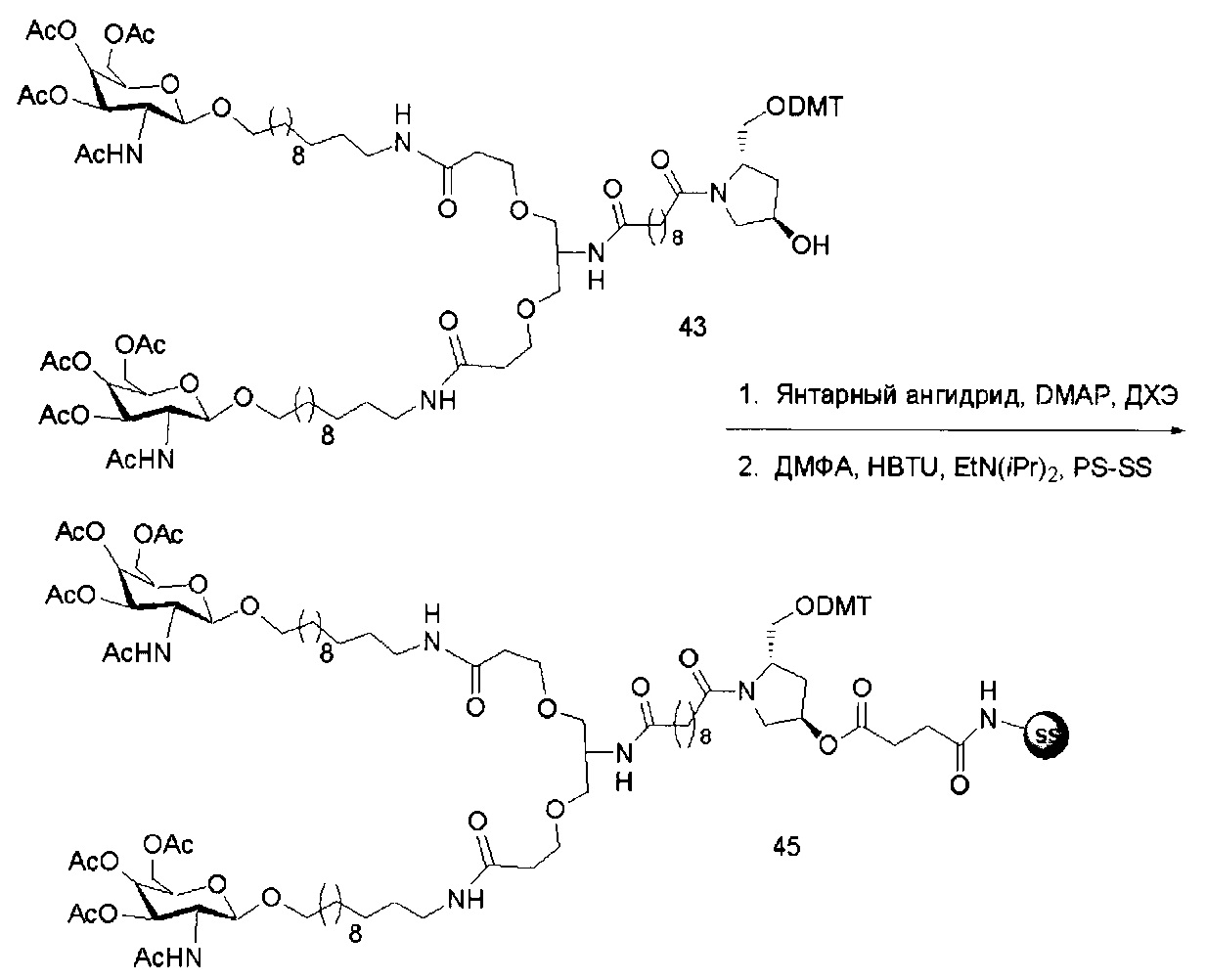
Соединение 43 получили по способам, приведенным в Примере 13.
Пример 15. Получение Соединения 47

Соединение 46 имеется в продаже.
Пример 16. Получение Соединения 53
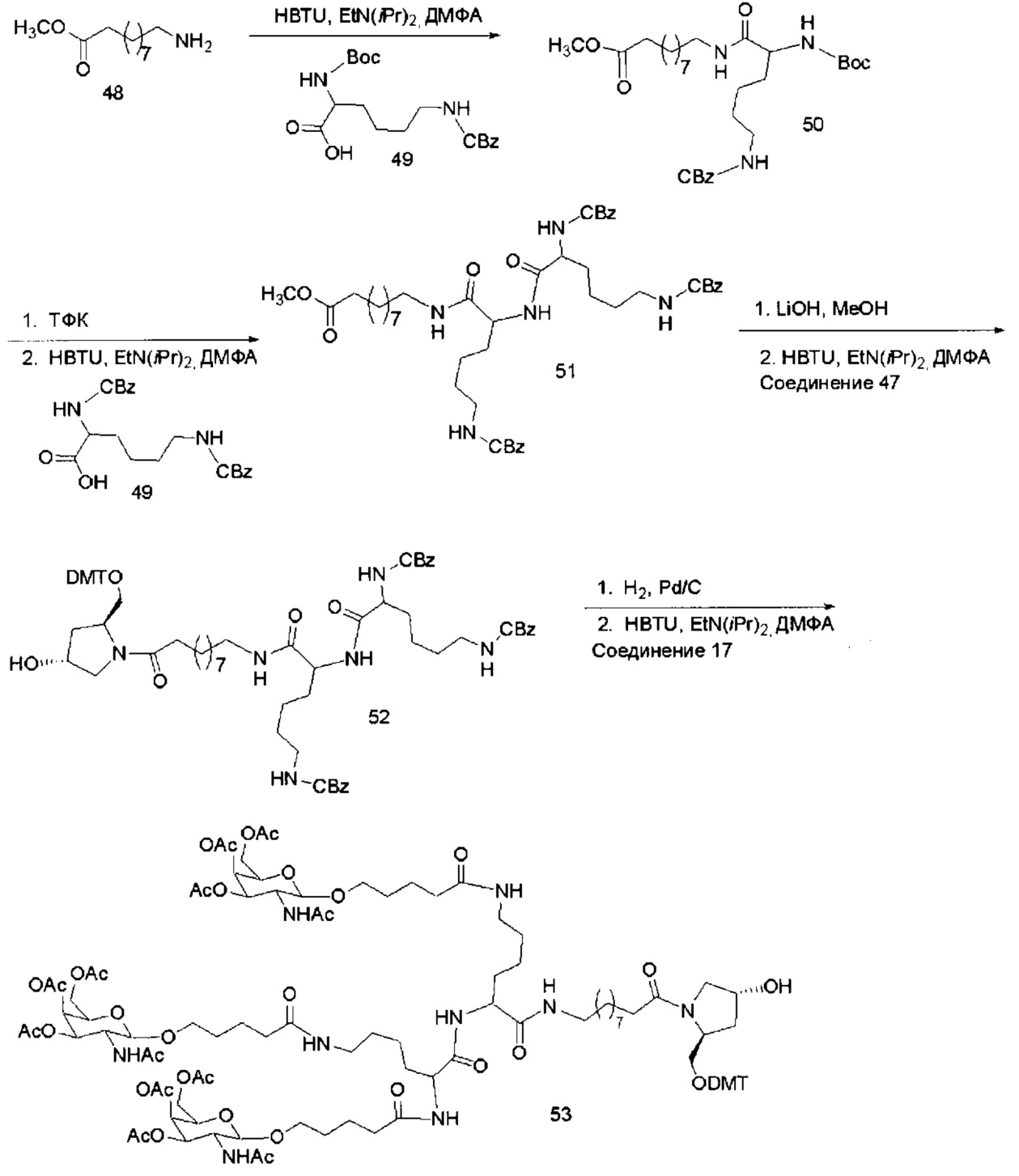
Соединения 48 и 49 имеются в продаже. Соединения 17 и 47 получили так, как описано в способах в Примерах 4 и 15.
Пример 17. Получение Соединения 54
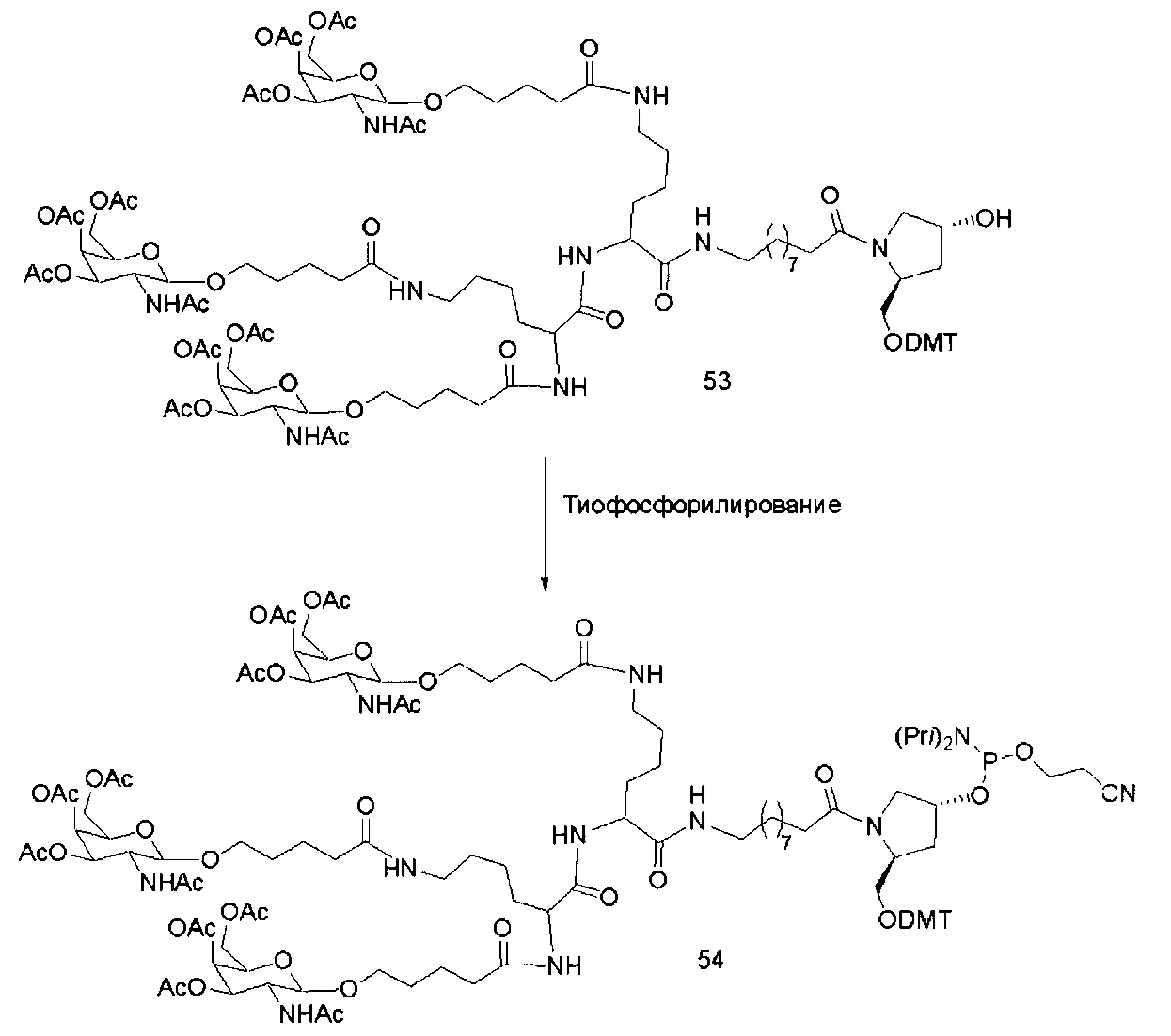
Соединение 53 получили по способам, приведенным в Примере 16.
Пример 18. Получение Соединения 55
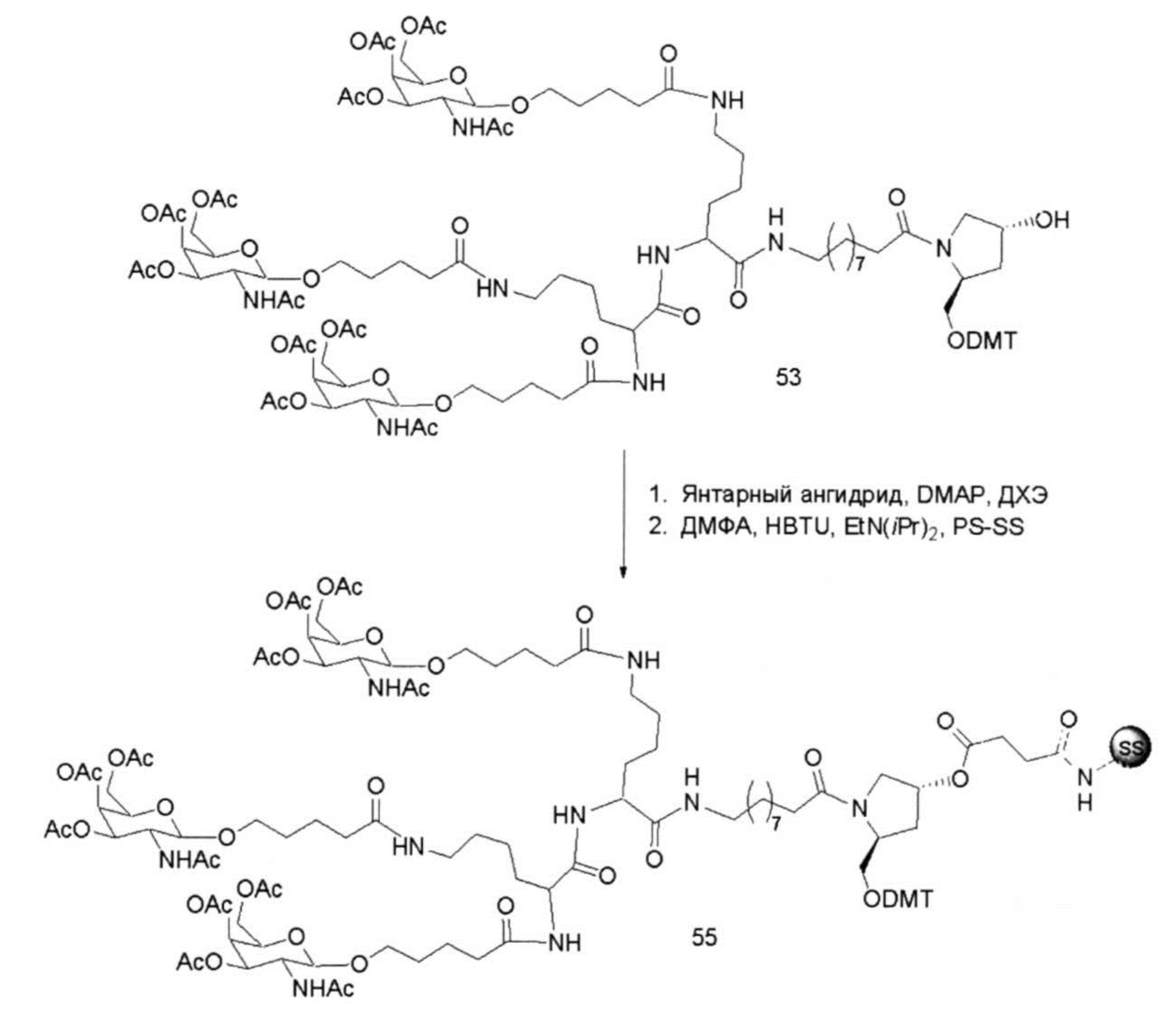
Соединение 53 получили по способам, приведенным в Примере 16.
Пример 19. Общий способ получения конъюгированных ASO, содержащих GalNAc3-1 в 3'-положении, при помощи твердофазных методик (получение ISIS 647535, 647536 и 651900)
Если не указано иное, все реагенты и растворы, применяемые для синтеза олигомерных соединений, приобретены у коммерческих поставщиков. Стандартные фосфорамидитные строительные блоки и твердую подложку применили для внедрения нуклеозидных остатков, которые включают, например, остатки Т, A, G иmC. 0,1 М раствор фосфорамидита в безводном ацетонитриле применили для β-D-2'-дезоксирибонуклеозида и 2'-МОЕ.
Синтез антисмысловых олигонуклеотидов (ASO) выполнили на синтезаторе ABI 394 (в масштабе 1-2 мкмоль) или на синтезаторе
После сборки требуемой последовательности цианоэтил-фосфатные защитные группы снимали при помощи 1:1 (об./об.) смеси триэтиламина и ацетонитрила в течение 45 минут времени контакта. Связанные с твердой подложкой ASO суспендировали в водном растворе аммиака (28-30 масс. %) и нагревали при 55°С в течение 6 часов.
Затем отфильтровывали не связанные ASO и выпаривали аммиак кипячением. Остаток очищали жидкостной хроматографией высокого давления на сильной анионообменной колонке (GE Healthcare Bioscience, Source 30Q, 30 мкм, 2,54×8 см, А=100 мМ ацетата аммония в 30% водном CH3CN, В=1,5 М NaBr в А, 0-40% В за 60 мин., скорость потока 14 мл⋅мин-1, λ=260 нм). Остаток обессоливали при помощи ВЭЖХ на обращенно-фазовой колонке с получением заданных ASO с выделенным выходом 15-30% относительно первоначальной загрузки на твердую подложку. ASO характеризовали при помощи ион-парной ВЭЖХ, совмещенной с МС-анализом на системе Agilent 1100 MSD.
Антисмысловые олигонуклеотиды, не содержащие конъюгат, синтезировали по стандартным способам синтеза олигонуклеотидов, общеизвестным в данной области техники.
Применяя эти способы, получили три отдельных антисмысловых соединения, нацеленных на ApoCIII. Как показано ниже в Таблице 17, каждое из трех антисмысловых соединений, нацеленных на АроСIII, имеет одну и ту же последовательность азотистых оснований. ISIS 304801 представляет собой 5-10-5 МОЕ гэпмер, содержащий только тиофосфатные связи; ISIS 647535 является таким же, как ISIS 304801, за исключением того, что он содержит GalNAc3-1, конъюгированный у его 3'-конца; и ISIS 647536 является таким же, как ISIS 647535, за исключением того, что некоторые межнуклеозидные связи этого соединения представляют собой фосфодиэфирные связи. Как дополнительно показано в Таблице 17, были синтезированы два отдельных антисмысловых соединения, нацеленных на SRB-1. ISIS 440762 представляет собой 2-10-2 cEt гэпмер, содержащий только тиофосфатные межнуклеозидные связи; ISIS 651900 является таким же, как ISIS 440762, за исключением того, что он содержит GalNAc3-1 у его 3'-конца.

Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «к» означает 6'-(S)-СНз бициклический нуклеозид (например, cEt); «s» означает тиофосфатные межнуклеозидные связи (PS); «о» означает фосфодиэфирные межнуклеозидные связи (РО); и «o'» означает -O-Р(=O)(ОН)-. Верхний индекс «т» означает 5-метилцитозины. «GalNAc3-1» означает конъюгирующую группу, имеющую структуру, изображенную ранее в Примере 9. Следует отметить, что GalNAc3-1 содержит расщепляемый аденозин, который связывает ASO с остальной частью конъюгата, который обозначен как «GalNAc3-1a». Номенклатура, используемая в приведенной выше таблице, показывает полную последовательность азотистых оснований, включая аденозин, который является частью конъюгата. Следовательно, в приведенной выше таблице последовательности также могут быть перечислены с окончанием «GalNAc3-1», без «Ado». Такое условное применение нижнего индекса «а» для обозначения части конъюгирующие группы, не содержащей расщепляемого нуклеозида или расщепляемого фрагмента, используется во всех приведенных Примерах. Эта часть конъюгирующие группы, не содержащая расщепляемого фрагмента, упоминается в настоящем документе как «кластер» или «кластер конъюгата» или «кластер GalNAc3». В некоторых случаях конъюгирующая группа для удобства описана путем отдельного приведения ее кластера и ее расщепляемого фрагмента.
Пример 20. Дозозависимое антисмысловое ингибирование человеческого АроСIII у huApoCIII трансгенных мышей
ISIS 304801 и ISIS 647535, каждый из которых нацелен на человеческий АроСIII и описан выше, отдельно испытывали и оценивали в дозозависимом исследовании на их способность ингибировать человеческий АроСIII у трансгенных мышей с человеческим АроСIII.
Лечение
Трансгенных мышей с человеческим ApoCIII выдерживали при 12-часовом цикле освещения/темноты и обеспечивали свободный доступ к пище Teklad lab. До начала эксперимента животных акклиматизировали по меньшей мере в течение 7 дней в исследовательской лаборатории. Приготовили ASO в PBS и стерилизовали фильтрованием через фильтр 0,2 микрона. ASO растворили в 0,9% PBS для инъекций.
Трансгенным мышам с человеческим АроСIII один раз в неделю в течение двух неделю внутрибрюшинно вводили инъекции ISIS 304801 или 647535 при 0,08, 0,25, 0,75, 2,25 или 6,75 мкмоль/кг или PBS в качестве контрольного образца. Каждая экспериментальная группа состояла из 4 животных. Через сорок восемь часов после введения последней дозы каждую мышь обескровили и умертвили, и собрали ткани.
Анализ мРНКАроСIII
Уровни мРНК АроСIII в печени мышей определили при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc. Юджин, штат Орегон) по стандартным протоколам. Уровни мРНК АроСIII определяли относительно общей РНК (при помощи Ribogreen), затем нормализовали к контрольному образцу, обработанному PBS. Результаты, показанные ниже, приведены как средний процент уровней мРНК АроСIII для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному PBS, и обозначены как «% PBS». Ниже в Таблице 18 приведена также полумаксимальная эффективная доза (ED50) для каждого ASO.
Показано, что оба антисмысловых соединения снижают РНК АроСIII, по сравнению с контрольным образцом, обработанным PBS. Кроме того, антисмысловое соединение, конъюгированное с GalNAc3-1 (ISIS 647535), было значительно более эффективным, чем антисмысловое соединение, не содержащее конъюгат GalNAc3-1 (ISIS 304801).
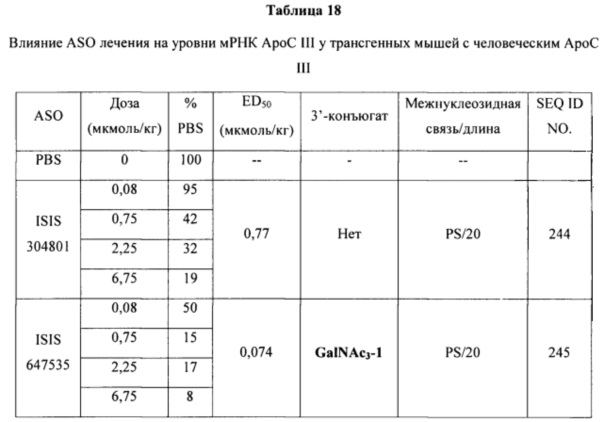
Анализ белка АроСIII (турбидиметрический анализ)
Анализ белка АроСIII в плазме выполнили по способам, описанным в работе Graham et al., Circulation Research, до печати опубликованной онлайн 29 марта 2013 года.
Приблизительно 100 мкл плазмы, выделенной из мышей, анализировали без разбавления, применяя клинический анализатор Olympus и имеющийся в продаже турбидиметрический аналитический набор АроСIII (Kamiya, кат. № KAI-006, Kamiya Biomedical, Сиэтл, штат Вашингтон). Протокол анализа выполняли по описанию поставщика.
Как показано ниже в Таблице 19, оба антисмысловых соединения снижают белок АроСIII, по сравнению с PBS контрольным образцом. Кроме того, антисмысловое соединение, конъюгированное с GalNAc3-1 (ISIS 647535), было значительно более эффективным, чем антисмысловое соединение, не содержащее конъюгат GalNAc3-1 (ISIS 304801).
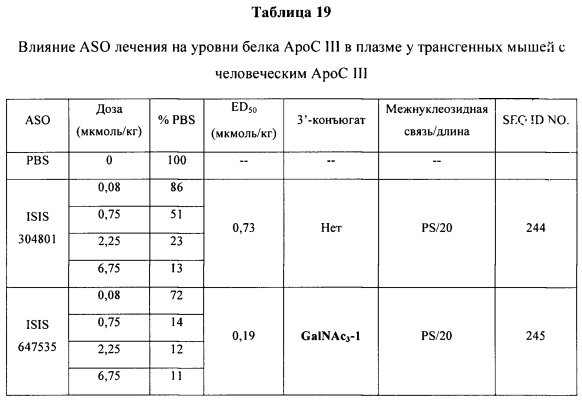
Триглицериды и холестерин плазмы выделили по способу Bligh и Dyer (Bligh, E.G. and Dyer, W.J. Can. J. Biochem. Physiol. 37: 911-917, 1959) (Bligh, E and Dyer, W, Can J Biochem Physiol, 37, 911-917, 1959) (Bligh, E and Dyer, W, Can J Biochem Physiol, 37, 911-917, 1959) и измерили при помощи клинического анализатора Beckmann Coulter и имеющихся в продаже реагентов.
Уровни триглицеридов измерили относительно мышей, инъецированных PBS, и выразили как «% PBS». Результаты приведены в Таблице 20. Показано, что оба антисмысловых соединения снижают уровни триглицеридов. Кроме того, антисмысловое соединение, конъюгированное с GalNAc3-1 (ISIS 647535), было значительно более эффективным, чем антисмысловое соединение, не содержащее конъюгат GalNAc3-1 (ISIS 304801).
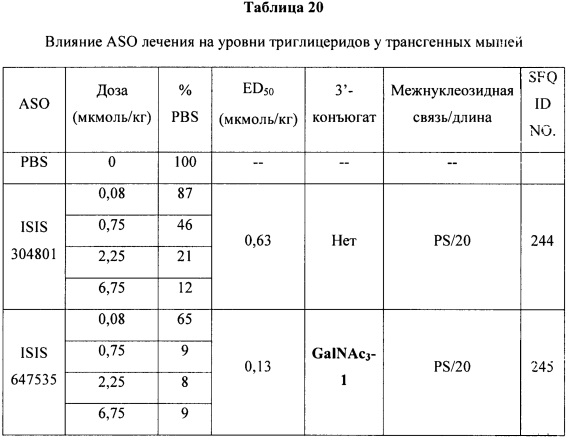
Образцы плазмы анализировали при помощи ВЭЖХ для определения количества общего холестерина и различных фракций холестерина (HDL и LDL). Результаты приведены в Таблицах 21 и 22. Показано, что оба антисмысловых соединения снижают общие уровне холестерина; оба снижают LDL; и оба повышают HDL. Кроме того, антисмысловое соединение, конъюгированное с GalNAc3-1 (ISIS 647535), было значительно более эффективным, чем антисмысловое соединение, не содержащее конъюгат GalNAc3-1 (ISIS 304801). Увеличение уровней HDL и снижение уровней LDL представляет собой преимущественный сердечно-сосудистый эффект антисмыслового ингибирования АроСIII.
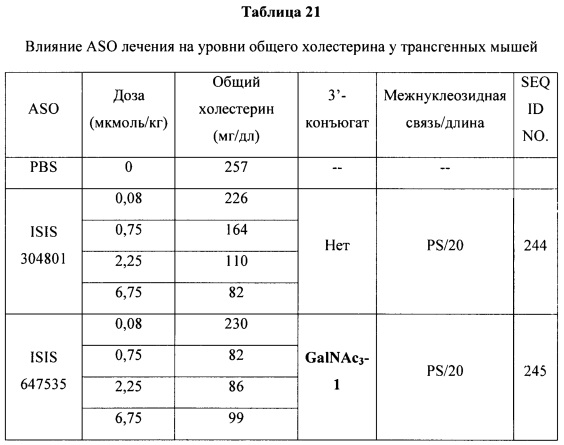

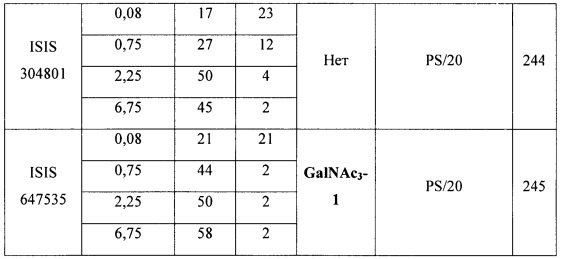
Фармакокинетический анализ (ФК)
Оценили также ФК ASO. Образцы печени и почек измельчили и экстрагировали по стандартным протоколам. Образцы анализировали на MSD1 при помощи ИП-ВЭЖХ-МС. Определили содержание (мкг/г) в ткани ISIS 304801 и 647535 полной длины, и результаты приведены в Таблице 23. Показано, что концентрации в печени антисмысловых соединений полной длины были схожими для двух антисмысловых соединений. Следовательно, даже несмотря на то, что GalAc3-1-конъюгированное антисмысловое соединение является более активным в печени (как показано по данным РНК и белка, приведенным выше), его содержание в печени не намного выше. Действительно, рассчитанное значение ЕС50 (приведенное в Таблице 23) подтверждает, что наблюдаемое увеличение эффективности конъюгированного соединения не может быть приписано исключительно повышенному накоплению. Такой результат позволяет предположить, что конъюгат улучшает эффективность по другому механизму, чем простое накопление в печени, возможно за счет увеличения продуктивного захвата антисмыслового соединения в клетки.
Эти результаты показывают также, что концентрация GalNAc3-1-конъюгированного антисмыслового соединения почках ниже, чем концентрация антисмыслового соединения, не содержащего конъюгата GalNAc. Это имеет несколько преимущественных терапевтических применений. Для терапевтических показаний, в которых не требуется проявление активности в почках, воздействие на почки подвергает их риску токсичности без соответствующей пользы. Более того, высокая концентрация в почках обычно приводит к выводу соединения с мочой, обеспечивая более быстрое выведение. Соответственно, для внепочечных мишеней накопление в почках является нежелательным. Эти данные позволяют предположить, что конъюгация с GalNAc3-1 снижает накопление в почках.
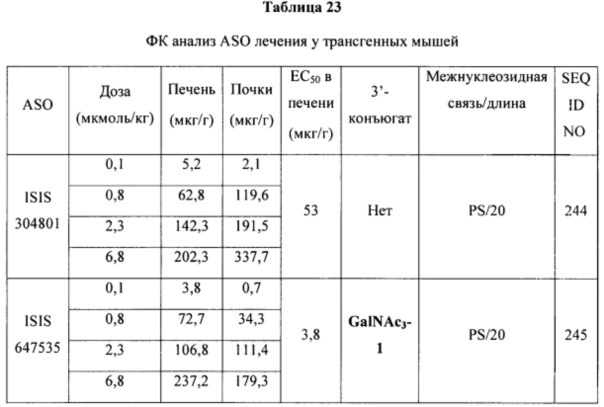
Идентифицировали также метаболиты ISIS 647535 и подтвердили их массы при помощи масс-спектрометрического анализа высокого разрешения. Сайты расщепления и структуры наблюдаемых метаболитов приведены ниже. Относительный % от общей длины ASO рассчитали по стандартным приемам, а результаты приведены в Таблице 23a. Основной метаболит ISIS 647535 представляет собой ASO полной длины без всего конъюгата (то есть ISIS 304801), который образуется в результате расщепления по сайту расщепления А, приведенному ниже. Кроме того, наблюдали также дополнительные метаболиты, образующиеся из других сайтов расщепления. Эти результаты позволяют предположить, что может быть пригодным также внедрение других расщепляемых связей, таких как сложные эфиры, пептиды, дисульфиды, фосфорамидаты или ацил-гидразоны, между сахаром GalNAc3-1 и ASO, которые могут расщепляться под действием ферментов внутри клетки или которые могут расщепляться в восстановительной среде цитозоля, или которые лабильны в кислотном рН внутри эндосом и лизосом.
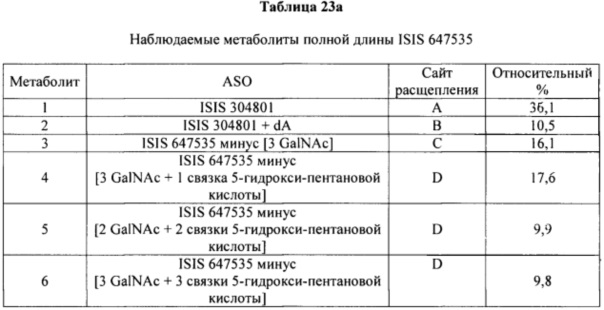
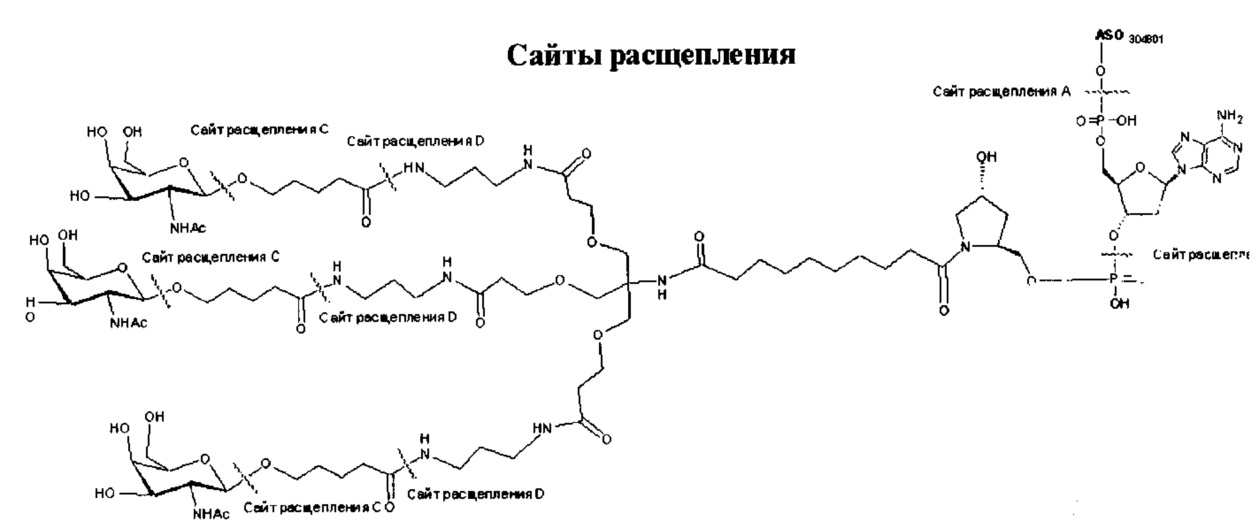

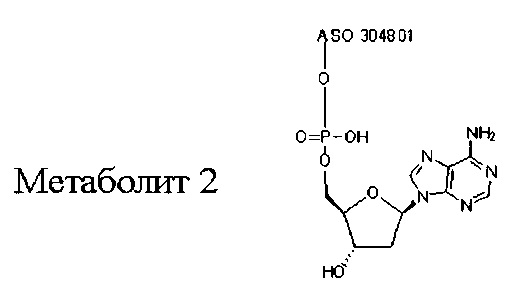
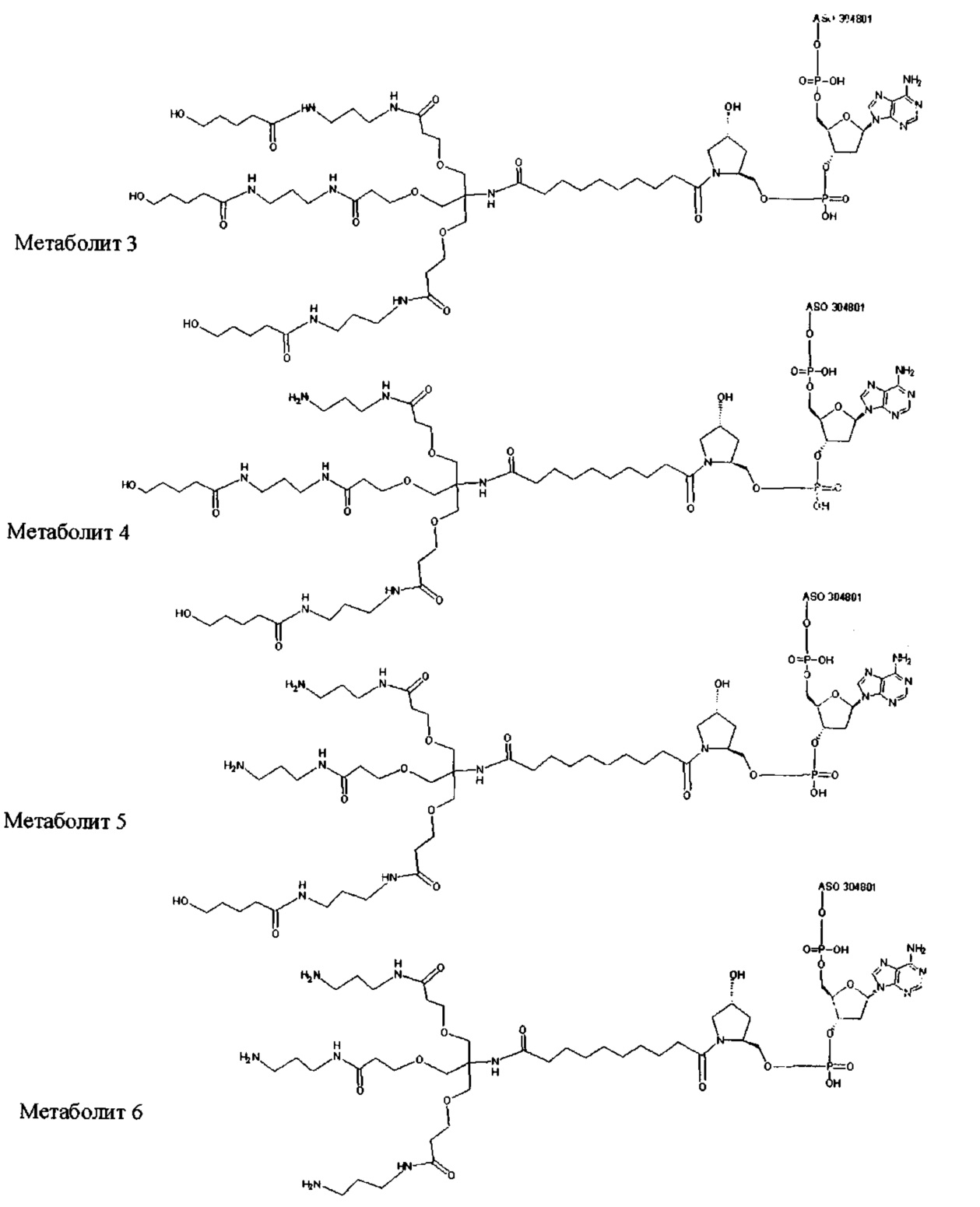
Пример 21. Антисмысловое ингибирование человеческого АроСIII у трансгенных мышей с АроСIII в исследовании одного введения
ISIS 304801, 647535 и 647536, каждый из которых нацелен на человеческий АроСIII и описан в Таблице 17, дополнительно оценивали в исследовании однократного введения на их способность ингибировать человеческий АроСIII у трансгенных мышей с человеческим АроСIII.
Лечение
Трансгенных мышей с человеческим ApoCIII выдерживали при 12-часовом цикле освещения/темноты и обеспечивали свободный доступ к пище Teklad lab. До начала эксперимента животных акклиматизировали по меньшей мере в течение 7 дней в исследовательской лаборатории. Приготовили ASO в PBS и стерилизовали фильтрованием через фильтр 0,2 микрона. ASO растворили в 0,9% PBS для инъекций.
Трансгенным мышам с человеческим АроСIII внутрибрюшинно ввели однократную инъекцию дозы, приведенной ниже, соединения ISIS 304801, 647535 или 647536 (описанных выше), или PBS в качестве контрольного образца. Экспериментальная группа состояла из 3 животных, а контрольная группа состояла из 4 животных. Перед лечением, а также после последней дозы у каждой мыши брали кровь и анализировали образцы плазмы. Мышей умертвили через 72 часа после последнего введения.
Образцы собрали и анализировали для определения уровней мРНК АроСIII и белка в печени; триглицеридов в плазме; и холестерина, включая фракции HDL и LDL, которые анализировали так, как описано выше (Пример 20). Данные этих анализов приведены ниже в Таблицах 24-28. Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT; и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, применяя стандартные протоколы. Уровни ALT и AST показали, что антисмысловые соединения хорошо переносятся при всех введенных дозах.
Эти результаты демонстрируют усиление эффективности антисмысловых соединений, содержащих конъюгат GalNAc3-1 на 3'-конце (ISIS 647535 и 647536), по сравнению с антисмысловым соединением, не содержащим конъюгат GalNAc3-1 (ISIS 304801). Кроме того, ISIS 647536, который содержит конъюгат GalNAc3-1 и несколько фосфодиэфирных связей, был таким же эффективным, как ISIS 647535, который содержит тот же конъюгат, и все межнуклеозидные связи в этом ASO являются тиофосфатными.
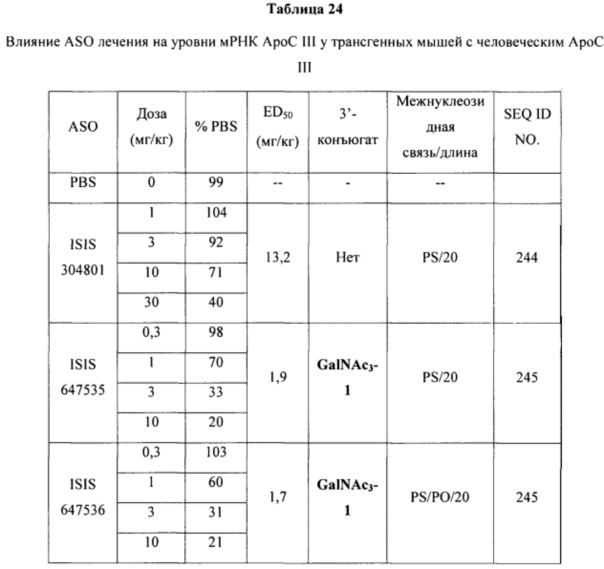
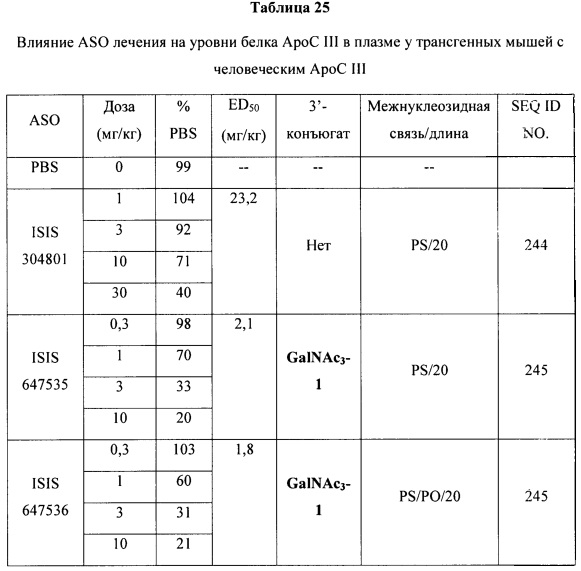
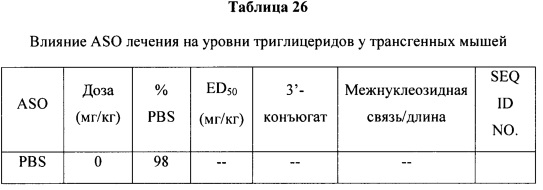
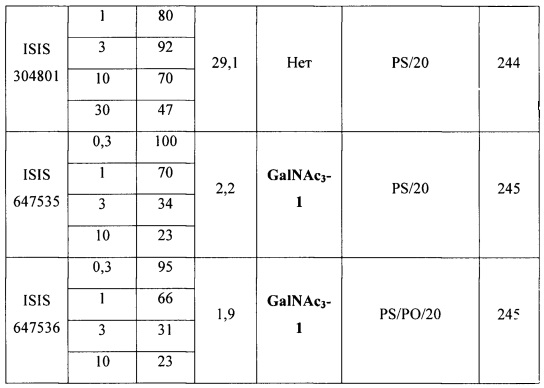
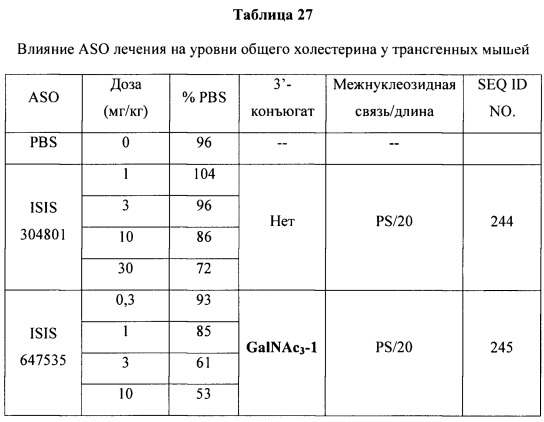
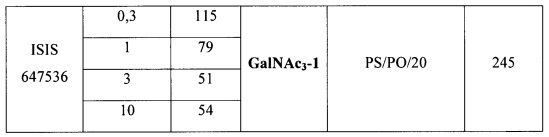
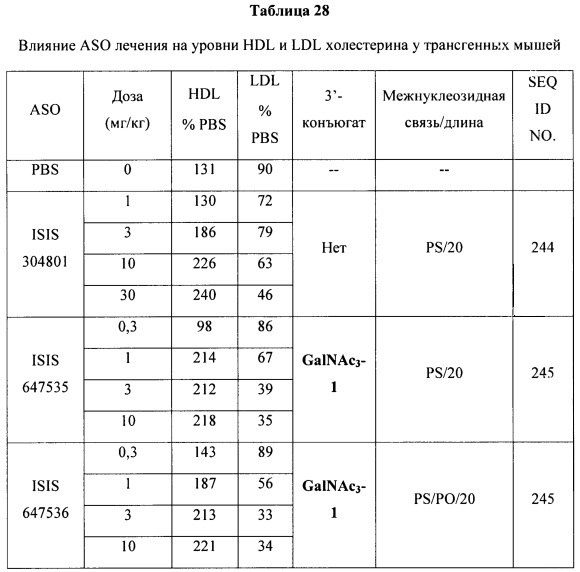
Эти результаты подтверждают, что конъюгат GalNAc3-1 улучшает эффективность антисмыслового соединения. Эти результаты показывают также равную эффективность GalNAc3-1-конъюгированных антисмысловых соединений, в которых антисмысловые олигонуклеотиды имеют смешанные связи (ISIS 647536, который имеет шесть фосфодиэфирных связей), и полностью тиофосфатной версии того же антисмыслового соединения (ISIS 647535).
Тиофосфатные связи обеспечивают несколько свойств антисмысловых соединений. Например, они устойчивы к нуклеазному расщеплению и связываются с белками, что приводит к накоплению соединения в печени, а не в почках/моче. Эти свойства являются желательными, особенно при лечении показаний в печени. Однако тиофосфатные связи связаны также с воспалительной реакцией. Соответственно, уменьшение количества тиофосфатных связей в соединении предположительно снижает риск воспаления, но снижает также концентрацию соединения в печени, повышает концентрацию в почках и моче, снижает стабильность в присутствии нуклеаз и уменьшает общую эффективность. Приведенные результаты демонстрируют, что GalNAc3-1-конъюгированное антисмысловое соединение, в котором некоторые тиофосфатные связи заменены фосфодиэфирными связями, настолько же эффективно против мишени в печени, как и аналог, содержащий только тиофосфатные связи. Такие соединения предположительно являются менее провоспалительными (см. Пример 24, в котором описан эксперимент, демонстрирующий, что уменьшение тиофосфатов (PS) приводит к снижению воспалительного действия).
Пример 22. Влияние модифицированного GalNAc3-1-конъюгированного ASO, нацеленного на SRB-1, in vivo
ISIS 440762 и 651900, каждый из которых нацелен на SRB-1 и описан в Таблице 17, оценили в дозозависимом исследовании на их способность ингибировать SRB-1 у Balb/c мышей.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэк) ввели однократную подкожную инъекцию дозы, приведенной ниже, соединения ISIS 440762, 651900 или PBS в качестве контрольного образца. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 48 часов после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Уровни мРНК SRB-1 определяли относительно общей РНК (при помощи Ribogreen), затем нормализовали к контрольному образцу, обработанному PBS. Результаты, показанные ниже, приведены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному PBS, и обозначены как «% PBS».
Как показано в Таблице 29, оба антисмысловых соединения снижают уровни мРНК SRB-1. Кроме того, антисмысловое соединение, содержащее конъюгат GalNAc3-1 (ISIS 651900), было значительно более эффективным, чем антисмысловое соединение, не содержащее конъюгат GalNAc3-1 (ISIS 440762). Эти результаты демонстрируют, что преимущество эффективности конъюгатов GalNAc3-1 наблюдается при применении антисмысловых олигонуклеотидов, комплементарных различным мишеням и имеющих различные химически модифицированные нуклеозиды, в этом случае модифицированные нуклеозиды содержат затрудненные этил-сахарные фрагменты (бициклический сахарный фрагмент).
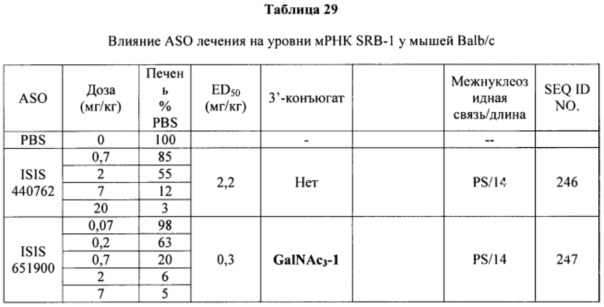
Пример 23. Протокол анализа человеческих мононуклеарных клеток периферической крови (hPBMC)
Анализ hPBMC выполнили при помощи пробирочного способа BD Vautainer CPT. Получили образец цельной крови, полученной от доноров-добровольцев, давших информированное согласие в Медицинской клинике США (Faraday & El Camino Real, Карлсбад), и собрали его в 4-15 пробирки BD Vacutainer CPT по 8 мл (VWR, кат. № BD362753). Приблизительный исходный общий объем цельной крови в пробирка CPT для каждого донора записали в формуляре анализа РВМС.
Перед центрифугированием образец крови незамедлительно повторно перемешали, осторожно переворачивая пробирки 8-10 раз. Пробирки CPT центрифугировали при комнатной температуре (18-25°С) в горизонтальном (с избыточной поворачиваемостью) роторе в течение 30 минут с фактором разделения (RCF) 1500-1800 с затормаживанием (2700 об./мин. Beckman Allegra 6R). Клетки сняли с лейкоцитарной поверхности раздела (между слоями фиколла и полимерного геля); перенесли в стерильную 50 мл коническую пробирку и сгруппировали по 5 CPT пробирок/50 мл коническая пробирка/донор. Затем клетки дважды промыли PBS (без Са++, Mg++; GIBCO). Пробирки пополнили до 50 мл и перемешали, переворачивая несколько раз. Затем образец центрифугировали при 330×g в течение 15 при комнатной температуре (1215 об./мин в Beckman Allegra 6R) и аспирировали максимальное количество надосадочной жидкости, не нарушая осадок. Клеточный осадок сняли, осторожно поворачивая пробирку, и повторно суспендировали клетки в RPMI+10% FBS+пенициллин/стрептомицин (~1 мл / 10 мл исходного объема цельной крови). Пипеткой взяли 600 мкл образца и поместили во флакон с пробой (Beckman Coulter), содержащий 600 мкл реагента VersaLyse (Beckman Coulter, кат. № А09777), и осторожно перемешивали на вортексе в течение 10-15 секунд. Образец оставили инкубироваться в течение 10 минут при комнатной температуре, и снова перемешали перед подсчетом. Суспензию клеток считывали на анализаторе жизнеспособности клеток Vicell XR (Beckman Coulter), используя клетки типа РВМС (сохранили фактор разбавления 1:11 с другими параметрами). Записали количество живых клеток/мл и жизнеспособность. Клеточную суспензию разбавили до 1×107 живых РВМС/мл в RPMI+10% FBS+пенициллин/стрептомицин.
Клетки поместили на планшет при 5×105 в 50 мкл/лунку 96-луночноого тканевого культурального планшета (Falcon Microtest). 50 мкл/лунку 2х концентрации олигомеров/контроля, разбавленных в RPMI+10% FBS+пенициллин/стрептомицин, добавили в соответствии с экспериментальной матрицей (в целом 100 мкл/лунку). Планшеты поместили на шейкер и оставили перемешиваться приблизительно на 1 минуту. После инкубации в течение 24 часов при 37°С; 5% СО2, планшеты центрифугировали при 400×g в течение 10 минут, затем удалили надосадочную жидкость для анализа цитокинов MSD (то есть человеческих IL-6, IL-10, IL-8 и МСР-1).
Пример 24. Оценка провоспалительных эффектов в анализе hPBMC для GalNAc3-1-конъюгированных ASO
Антисмысловые олигонуклеотиды (ASO), перечисленные в Таблице 30, оценили на провоспалительное действие в анализе hPBMC, используя протокол, описанный в Примере 23. ISIS 353512 представляет собой внутренний стандарт, который, как известно, обладает высоким ответом на высвобождение IL-6 в этом анализе. hPBMC выделили из свежих образцов, полученных от доноров-добровольцев, и обработали ASO в концентрациях 0, 0,0128, 0,064, 0,32, 1,6, 8, 40 и 200 мкМ. Через 24 часа обработки измерили уровни цитокинов.
Уровни IL-6 применили в качестве первичного показания. ЕС50 и Emax рассчитали по стандартным способам. Результаты выразили как среднее отношение Emax/ЕС50 для двух доноров и обозначили как «Emax/ЕС50». Более низкое соотношение означает относительное снижение провоспалительного ответа, а более высокое соотношение означает относительное увеличение провоспалительного ответа.
В отношении исследуемых соединений, наименее провоспалительным соединением было ASO, соединенное при помощи PS/PO (ISIS 616468). GalNAc3-1-конъюгированное ASO, ISIS 647535, было немного менее провоспалительным, чем его неконъюгированный аналог, ISIS 304801. Эти результаты показывают, что внедрение нескольких РО связей снижает провоспалительную реакцию, а добавление конъюгата GalNAc3-1 не делает соединение более провоспалительным, и может снижать провоспалительную реакцию. Соответственно, можно ожидать, что антисмысловое соединение, содержащее смешанные PS/PO связи и конъюгат GalNAc3-1, может вызывать более слабые провоспалительные реакции, по сравнению с антисмысловым соединением, связанным только посредством PS, с конъюгатом GalNAc3-1 или без него. Эти результаты показывают, что GalNAc3-1-конъюгированные антисмысловые соединения, в частности, соединения, имеющие меньшее содержание PS, являются менее провоспалительными.
В целом, эти результаты позволяют предположить, что GalNAc3-1-конъюгированное соединение, в частности, соединение со сниженным содержанием PS, может быть введено в более высокой дозе, чем аналогичное полностью PS антисмысловое соединение без конъюгата GalNAc3-1. Поскольку не ожидается, что период полувыведения для этих соединений будет существенно различаться, то такое введение в более высокой дозе обусловит менее частое введение доз. В действительности, такое введение может быть еще более редким, поскольку GalNAc3-1конъюгированные соединения являются более эффективными (см. Примеры 20-22), а повторное введение дозы необходимо только при снижении концентрации соединения ниже заданного уровня, при этом такси заданный уровень обусловлен эффективностью.

Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «k» означает 6'-(S)-СН3 бициклический нуклеозид (например, cEt); «s» означает тиофосфатные межнуклеозидные связи (PS); «о» означает фосфодиэфирные межнуклеозидные связи (РО); и «o'» означает -O-Р(=O)(ОН)-. Верхний индекс «m» означает 5-метилцитозины. «Ado'-GalNAc3-1a» означает конъюгат, имеющий структуру GalNAc3-1, приведенную в Примере 9, присоединенный к 3'-концу указанного антисмыслового олигонуклеотида.
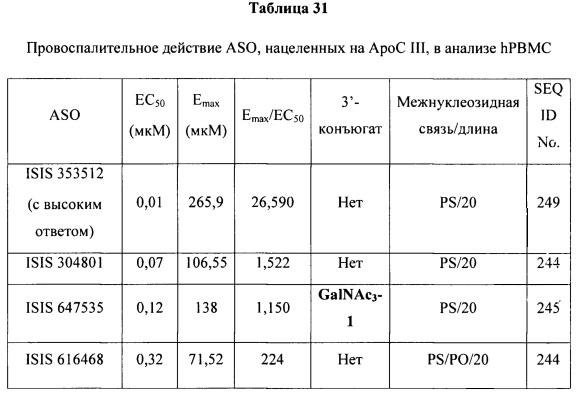
Пример 25. Влияние модифицированного GalNAc3-1-конъюгированного ASO, нацеленного на человеческий АроСIII, in vitro
ISIS 304801 и 647535, описанные выше, испытали in vitro. Первичные гепатоцитарные клетки трансгенных мышей при плотности 25000 клеток на лунку обработали концентрациями 0,03, 0,08, 0,24, 0,74, 2,22, 6,67 и 20 мкМ модифицированных олигонуклеотидов. После обработки в течение приблизительно 16 часов, из клеток выделили РНК и измерили уровни мРНК при помощи количественной ПЦР в реальном времени, а уровни мРНК hApoCIII скорректировали в соответствии с общим содержанием РНК, измеренным при помощи RIBOGREEN.
IC50 рассчитали по стандартным способам, а результаты приведены в Таблице 32. Показано, что наблюдали сравнимую эффективность в клетках, обработанных ISIS 647535, по сравнению с контрольным образцом, ISIS 304801.
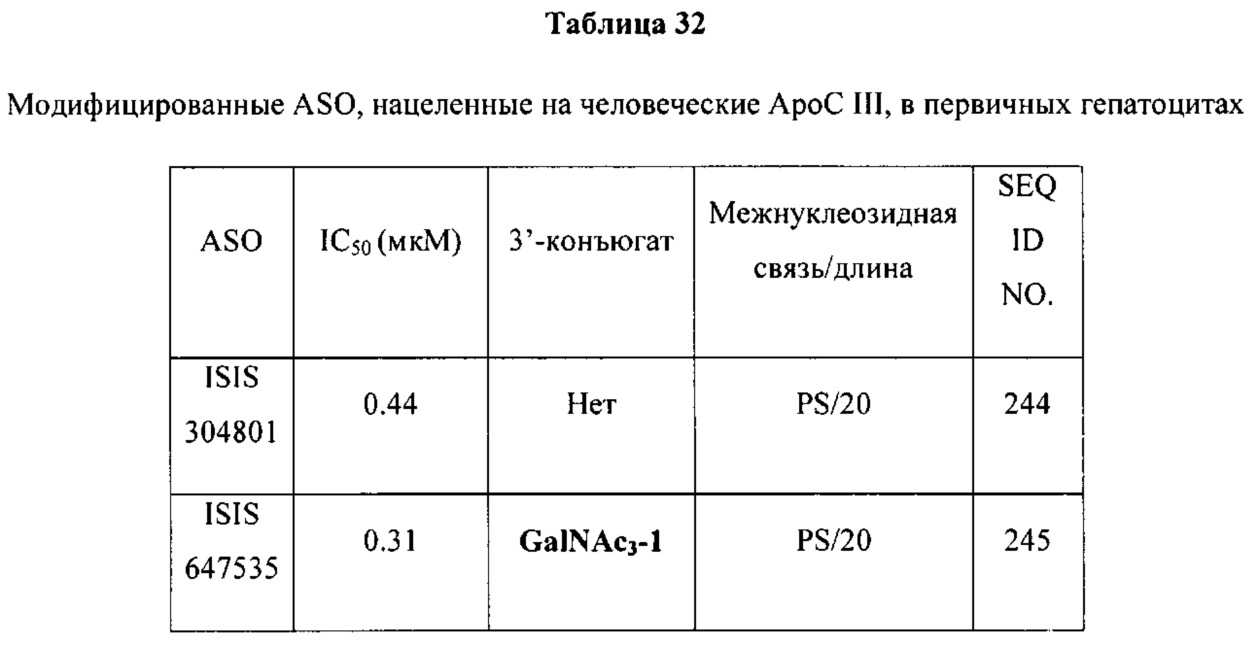
В этом эксперименте in vitro не наблюдали такого большого преимущества эффективности конъюгации с GalNAc3-1, как наблюдали in vivo. Последующие эксперименты свободного захвата в первичных гепатоцитах in vitro не показали повышенной эффективности олигонуклеотидов, содержащих различные конъюгаты GalNAc, по сравнению с олигонуклеотидами, не содержащими конъюгаты GalNAc (см. Примеры 60, 82 и 92).
Пример 26. Влияние связей PO/PS на ативность ASO в отношении АроСIII
Трансгенным мышам с человеческим АроСIII внутрибрюшинной инъекцией вводили 25 мг/кг ISIS 304801 или ISIS 616468 (оба описаны выше) или PBS в качестве контрольного образца, один раз в неделю в течение двух недель. Экспериментальная группа состояла из 3 животных, а контрольная группа состояла из 4 животных. Перед лечением, а также после последней дозы у каждой мыши брали кровь и анализировали образцы плазмы. Мышей умертвили через 72 часа после последнего введения.
Образцы собрали и анализировали для определения уровней белка АроСIII в печени, как описано выше (Пример 20). Данные этих анализов приведены ниже в Таблице 33.
Эти результаты демонстрируют снижение эффективности антисмысловых соединений с PO/PS (ISIS 616468) в крыльях, по сравнению с соединениями, содержащими только PS (ISIS 304801).
Пример 27. Соединение 56
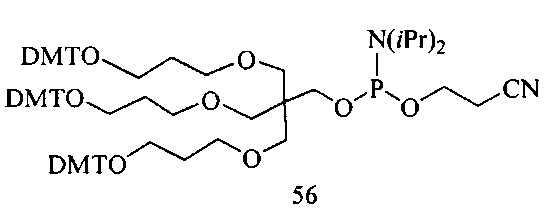
Соединение 56 имеется в продаже у компании Glen Research или может быть получено по опубликованным методикам, описанным авторами Shchepinov et al., Nucleic Acids Research, 1997, 25(22), 4447-4454.
Пример 28. Получение Соединения 60
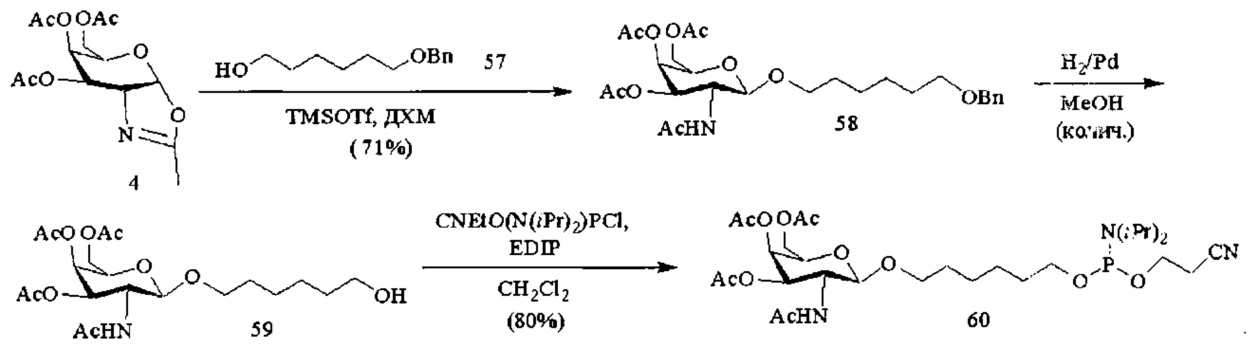
Соединение 4 получили по способам, описанным в Примере 2. Соединение 57 имеется в продаже. Соединение 60 подтвердили структурным анализом.
Соединение 57 является типичным, и его не следует считать ограничивающим, поскольку могут быть применены другие монозащищенные замещенные или незамещенные алкилдиолы, включая, но не ограничиваясь ими, те, которые приведены в данном описании, для получения фосфорамидитов, имеющих заданный состав.
Пример 29. Получение Соединения 63
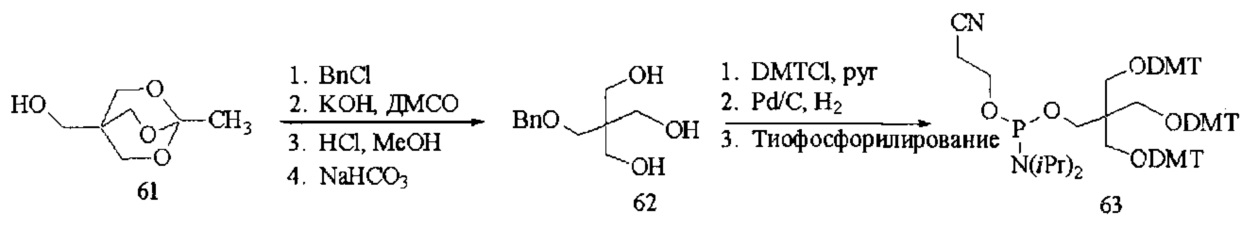
Соединения 61 и 62 получили по таким же способам, как описаны авторами Tober et al., Eur. J. Org. Chem., 2013, 3, 566-577; и Jiang et al., Tetrahedron, 2007, 63(19), 3982-3988.
Альтернативно, Соединение 63 получили по таким же способам, как описаны в научной и патентной литературе авторами Kim et al., Synlett, 2003, 12, 1838-1840; и Kim et al., в опубликованной Международной заявке РСТ WO 2004063208.
Пример 30. Получение Соединения 63b
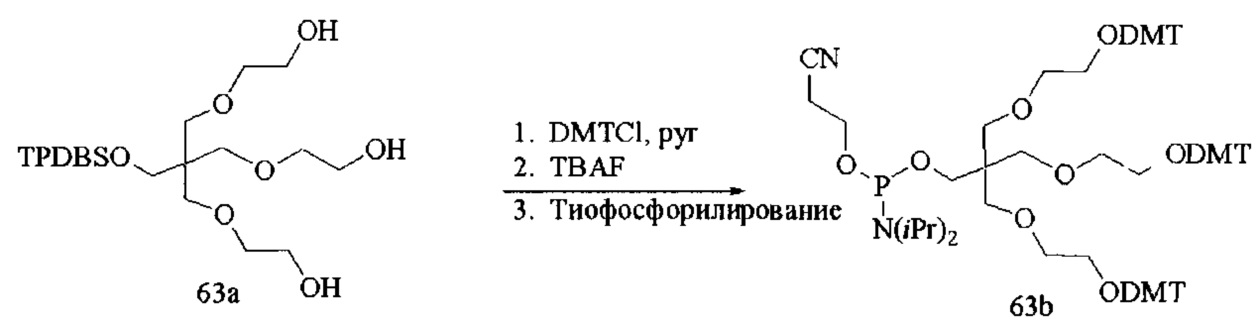
Соединение 63а получили по таким же способам, как описаны авторами Hanessian et al., Canadian Journal of Chemistry, 1996, 74(9), 1731-1737.
Пример 31. Получение Соединения 63d
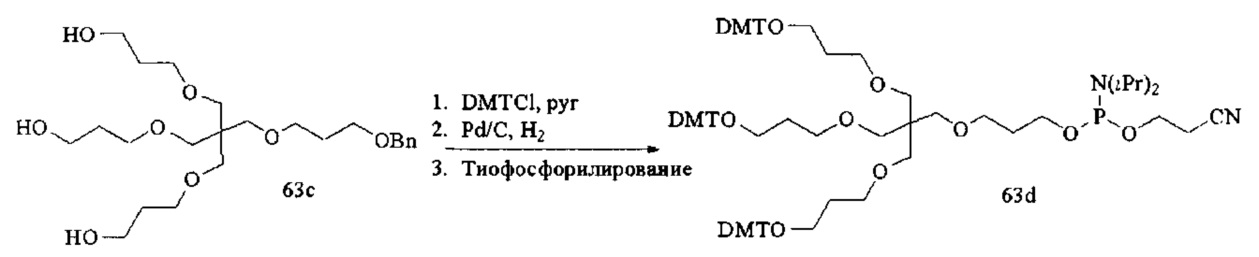
Соединение 63c получили по таким же способам, как описаны авторами Chen et al., Chinese Chemical Letters, 1998, 9(5), 451-453.
Пример 32. Получение Соединения 67
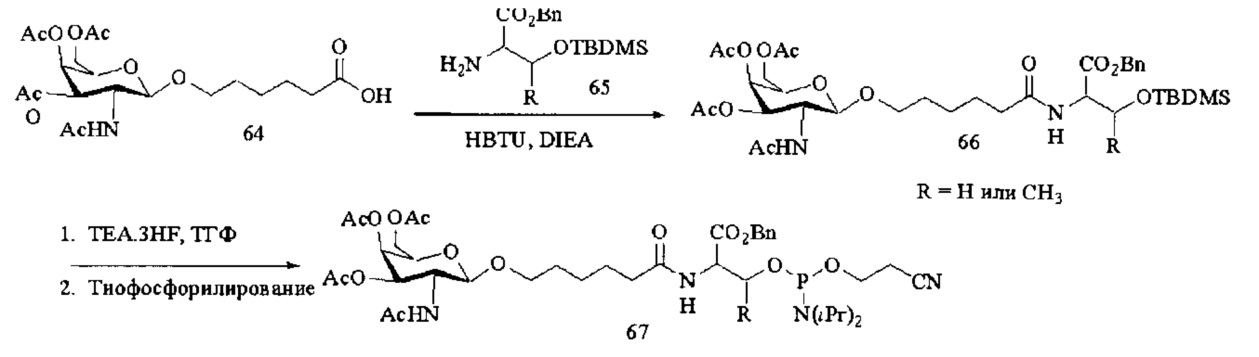
Соединение 64 получили по способам, приведенным в Примере 2. Соединение 65 получили по таким же способам, как описаны авторами Or et al., в опубликованной Международной заявке РСТ WO 2009003009. Защитные группы, применяемые для Соединения 65, являются типичными, и их не следует считать ограничением, поскольку могут быть применены другие защитные группы, включая, но не ограничиваясь ими, те, которые приведены в данном описании.
Пример 33. Получение Соединения 70
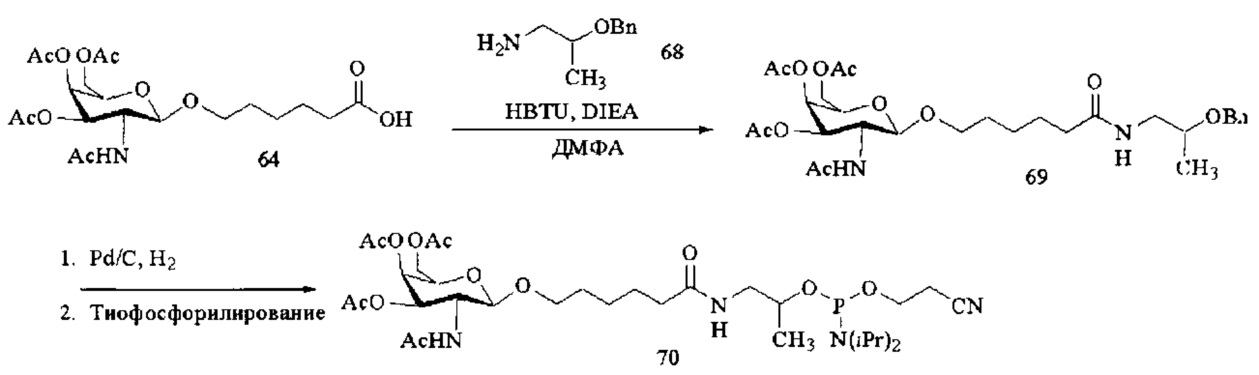
Соединение 64 получили по способам, описанным в Примере 2. Соединение 68 имеется в продаже. Защитная группа, примененная для Соединения 68, является типичной, и ее не следует считать ограничением, поскольку могут быть применены другие защитные группы, включая, но не ограничиваясь ими, те, которые приведены в данном описании.
Пример 34. Получение Соединения 75а
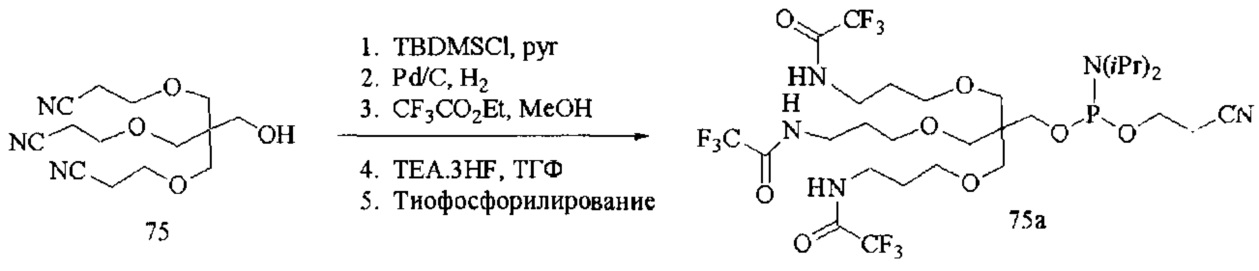
Соединение 75 получили по опубликованным методикам, описанным авторами Shchepinov et al., Nucleic Acids Research, 1997, 25(22), 4447-4454.
Пример 35. Получение Соединения 79
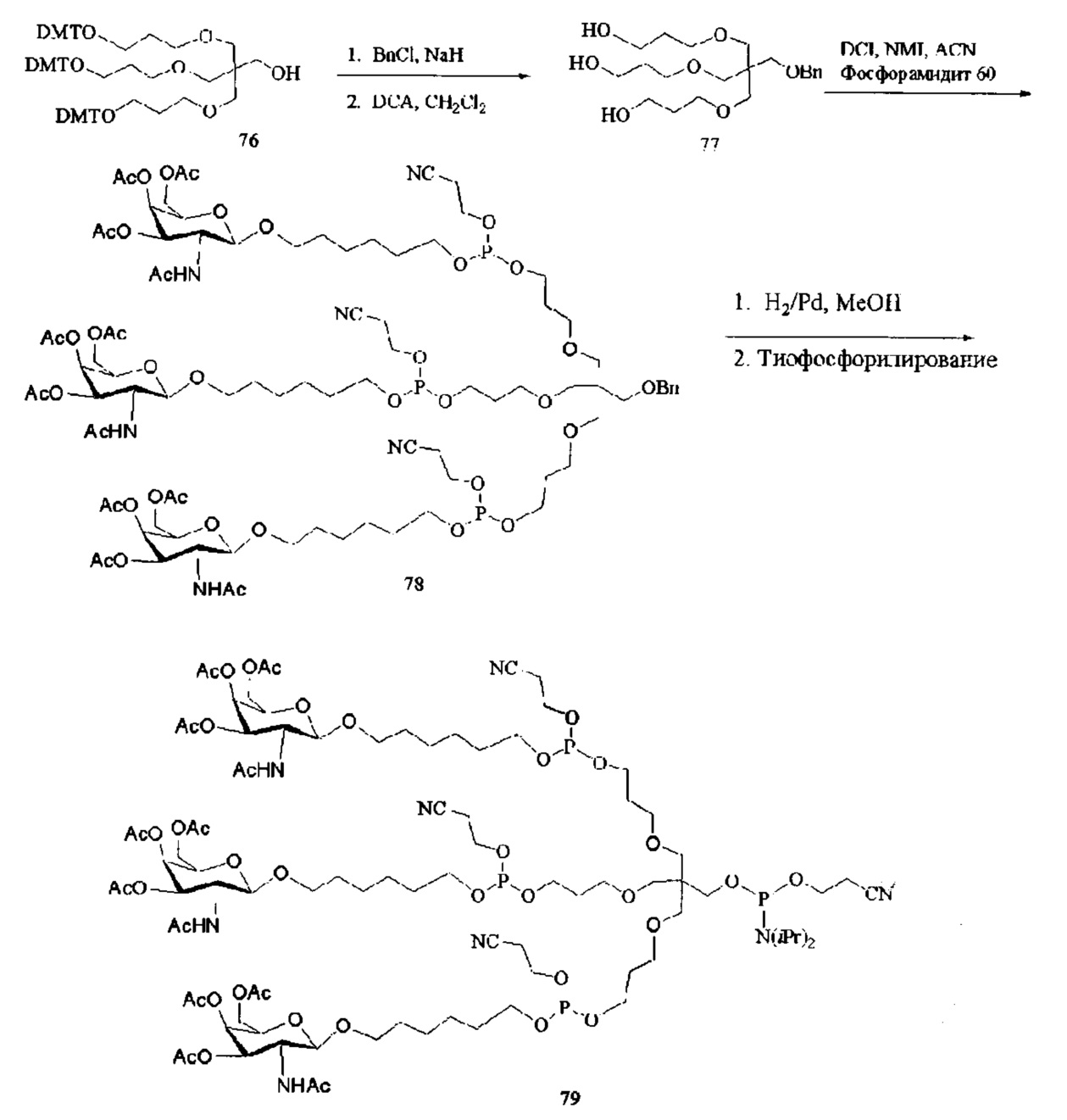
Соединение 76 получили по опубликованным методикам, описанным авторами Shchepinov et al., Nucleic Acids Research, 1997, 25(22), 4447-4454.
Пример 36. Получение Соединения 79а
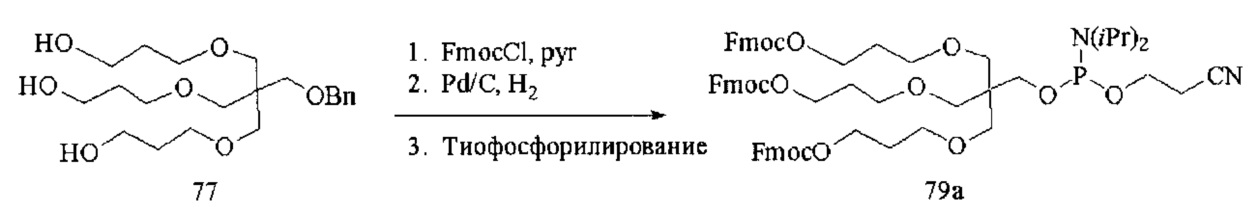
Соединение 77 получили по способам, приведенным в Примере 35.
Пример 37. Общий способ получения конъюгированного олигомерного соединения 82, содержащего фосфодиэфир-связанный конъюгат GalNAc3-2 на 5'-конце, на твердой подложке (Способ I)
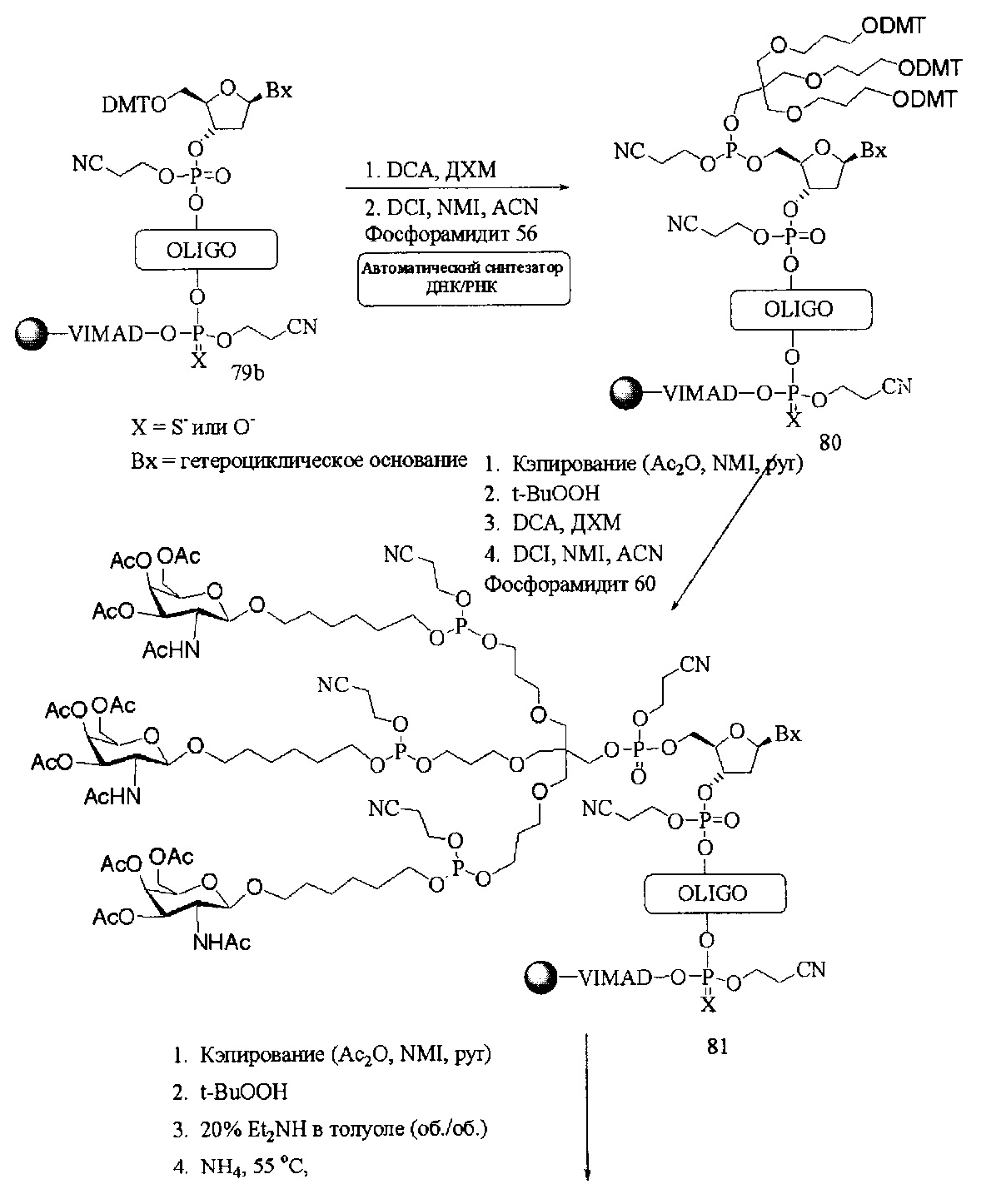

где GalNAc3-2 имеет структуру:
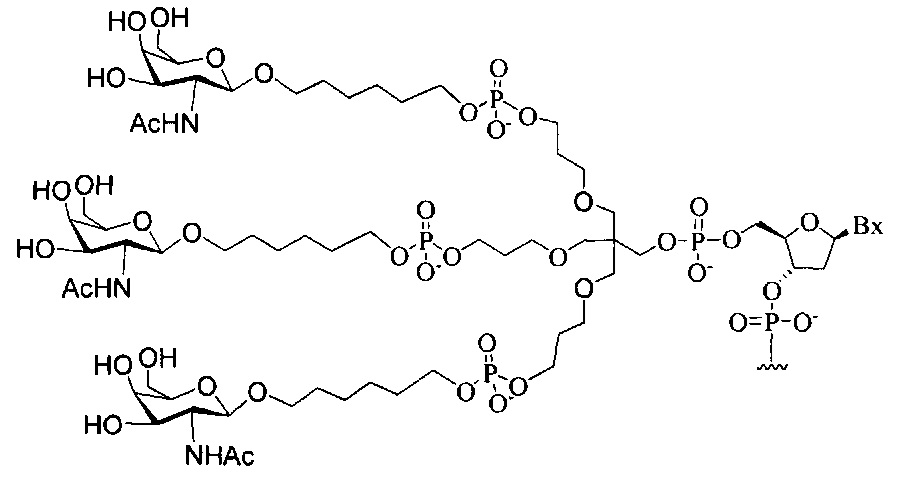
Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-2 (GalNAc3-2a) может быть комбинирована с любым расщепляемым фрагментом с получением различных конъюгирующих групп. При этом GalNAc3-2a имеет формулу:
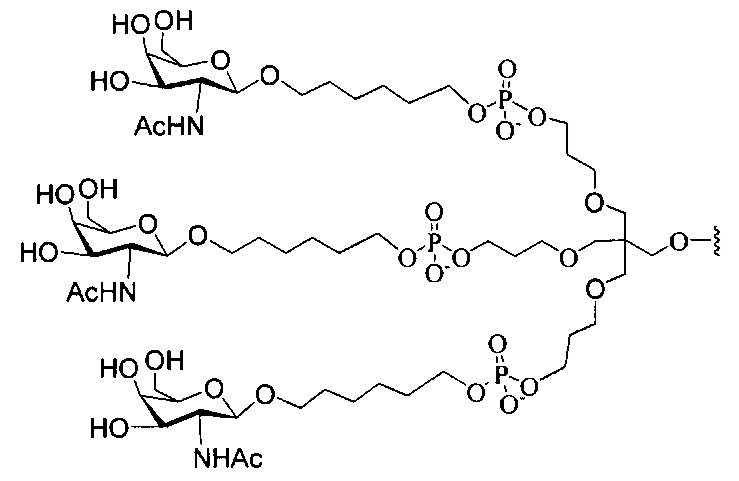
VIMAD-связанное олигомерное соединение 79b получили по стандартным способам в автоматическом синтезаторе ДНК/РНК (см. Dupouy et al., Angew. Chem. Int. Ed., 2006, 45, 3623-3627). Фосфорамидитные Соединения 56 и 60 получили так, как описано в способах в Примерах 27 и 28, соответственно. Изображенные фософорамидиты являются типичными, и их не следует считать ограничением, поскольку могут быть применены другие фосфорамидитные строительные блоки, включая, но не ограничиваясь ими, те, которые приведены в данном описании, для получения олигомерного соединения, содержащего фосфодиэфир-связанную конъюгирующую группу на 5'-конце. Порядок и количество фосфорамидитов, добавляемых к твердой подложке, может быть подобрано для получения олигомерных соединений, описанных в настоящем документе, которые имеют любую заданную последовательность и состав.
Пример 38. Альтернативный способ получения олигомерного соединения 82, содержащего фосфодиэфир-связанный конъюгат GalNAc3-2 на 5'-конце (Способ II)
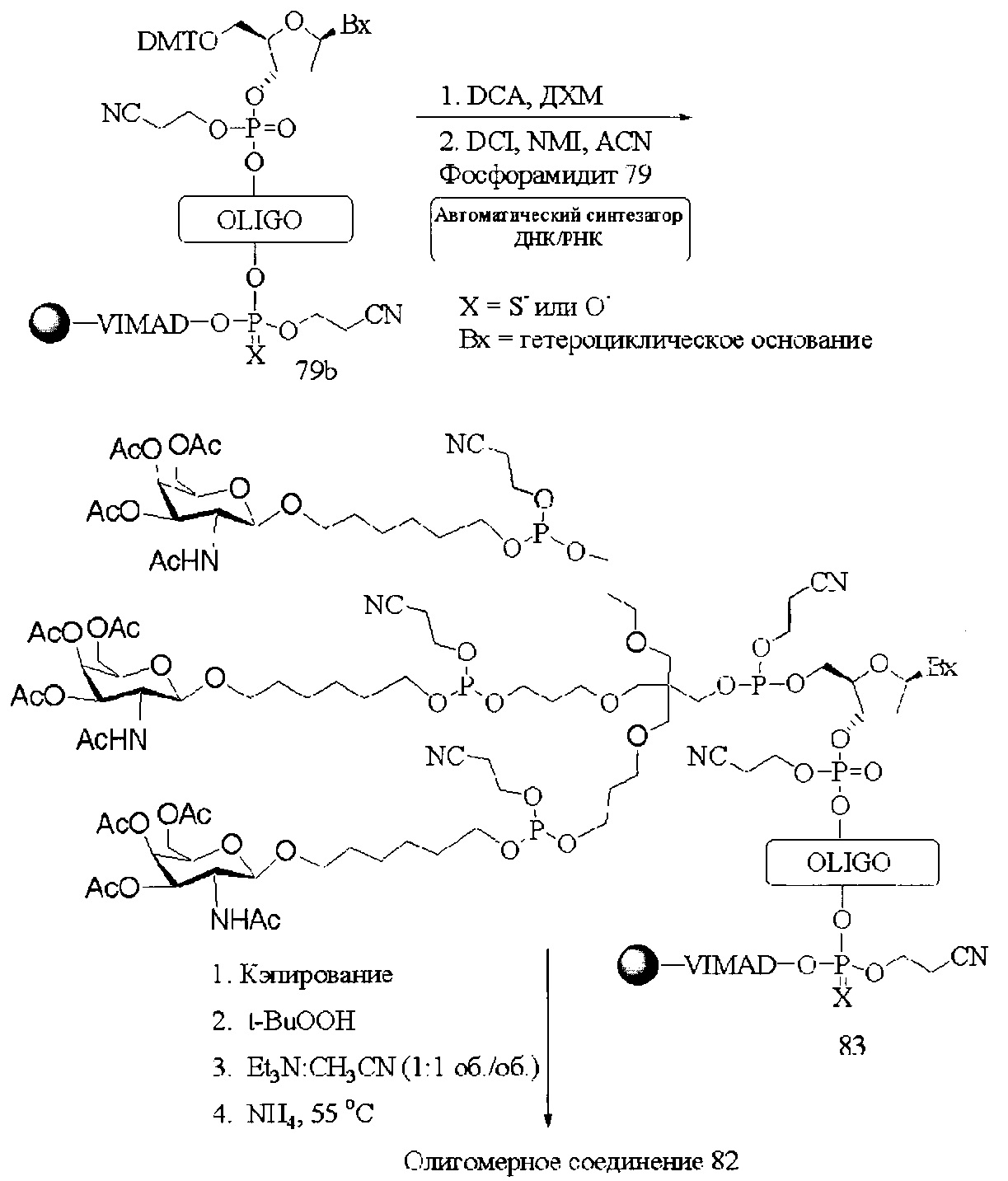
VIMAD-связанное олигомерное соединение 79b получили по стандартным способам в автоматическом синтезаторе ДНК/РНК (см. Dupouy et al., Angew. Chem. Int., Ed., 2006, 45, 3623-3627). GalNAc3-2-кластерный фосфорамидит, Соединение 79, получили по способам, приведенным в Примере 35. Альтернативный способ обеспечивает возможность одностадийной установки фосфодиэфир-связанного GalNAc3-2 конъюгата на олигомерное соединение на последней стадии синтеза. Изображенные фософорамидиты являются типичными, и их не следует считать ограничением, поскольку могут быть применены другие фосфорамидитные строительные блоки, включая, но не ограничиваясь ими, те, которые приведены в данном описании, для получения олигомерных соединений, содержащих фосфодиэфирный конъюгат на 5'-конце. Порядок и количество фосфорамидитов, добавляемых к твердой подложке, может быть подобрано для получения олигомерных соединений, описанных в настоящем документе, которые имеют любую заданную последовательность и состав.
Пример 39. Общий способ получения олигомерного соединения 83h, содержащего конъюгат GalNAc3-3 на 5'-конце (GalNAc3-1, модифицированный для 5'-концевого присоединения), на твердой подложке
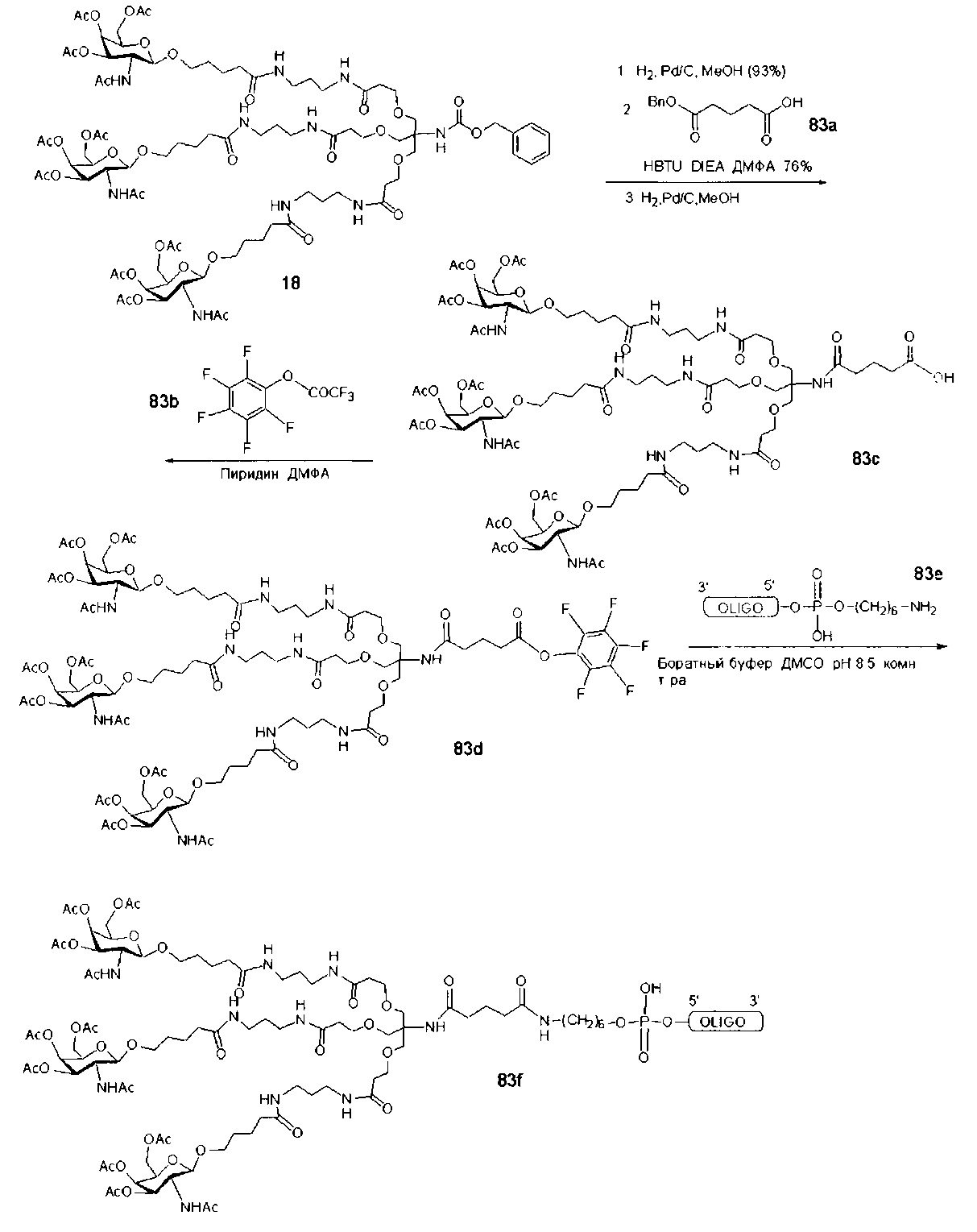
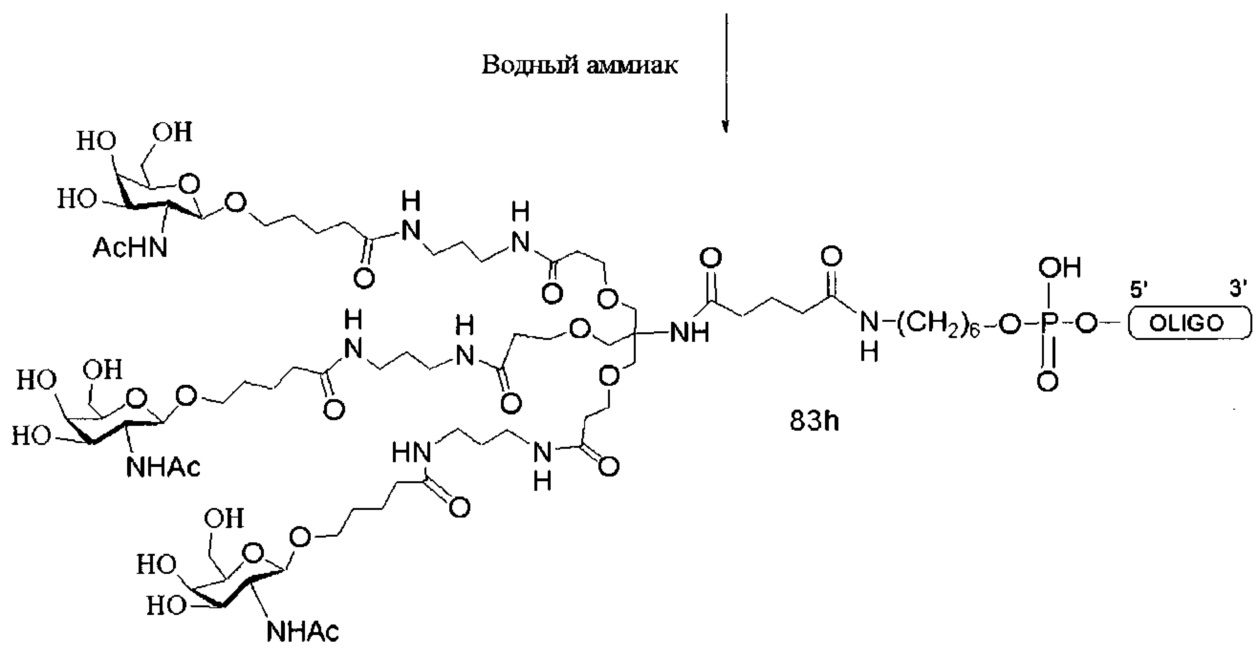
Соединение 18 получили по способам, описанным в Примере 4. Соединения 83а и 83b имеются в продаже. Олигомерное Соединение 83е, содержащее связанный через фосфодиэфир гексиламин, получили по стандартным способам синтеза олигонуклеотидов. В результате обработки защищенного олигомерного соединения водным раствором аммиака получили 5'-GalNAc3-3 конъюгированное олигомерное соединение (83h).
где GalNAc3-3 имеет структуру:
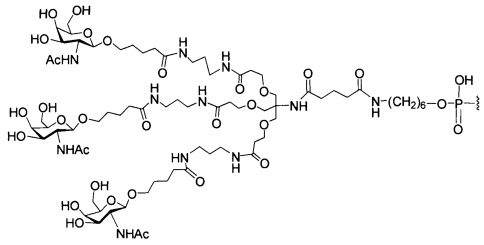
Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-3 (GalNAc3-3a) может быть комбинирована с любым расщепляемым фрагментом с получением различных конъюгирующих групп. При этом GalNAc3-3a имеет формулу:
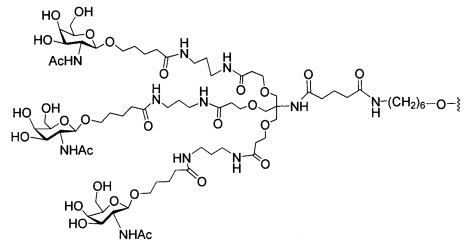
Пример 40. Общий способ получения олигомерного соединения 89, содержащего фосфодиэфир-связанный конъюгат GalNAc3-4 на 3'-конце, на твердой подложке
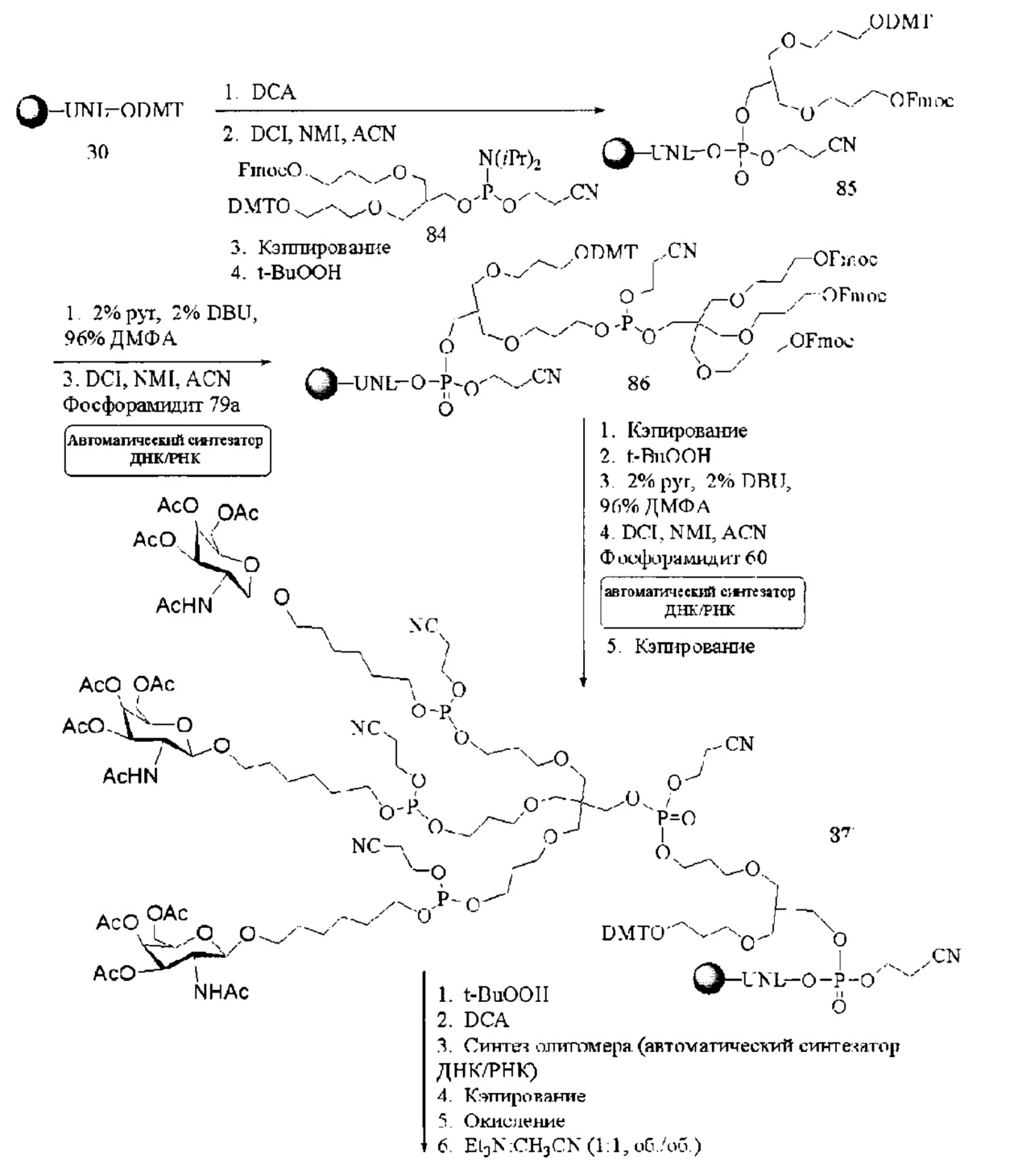
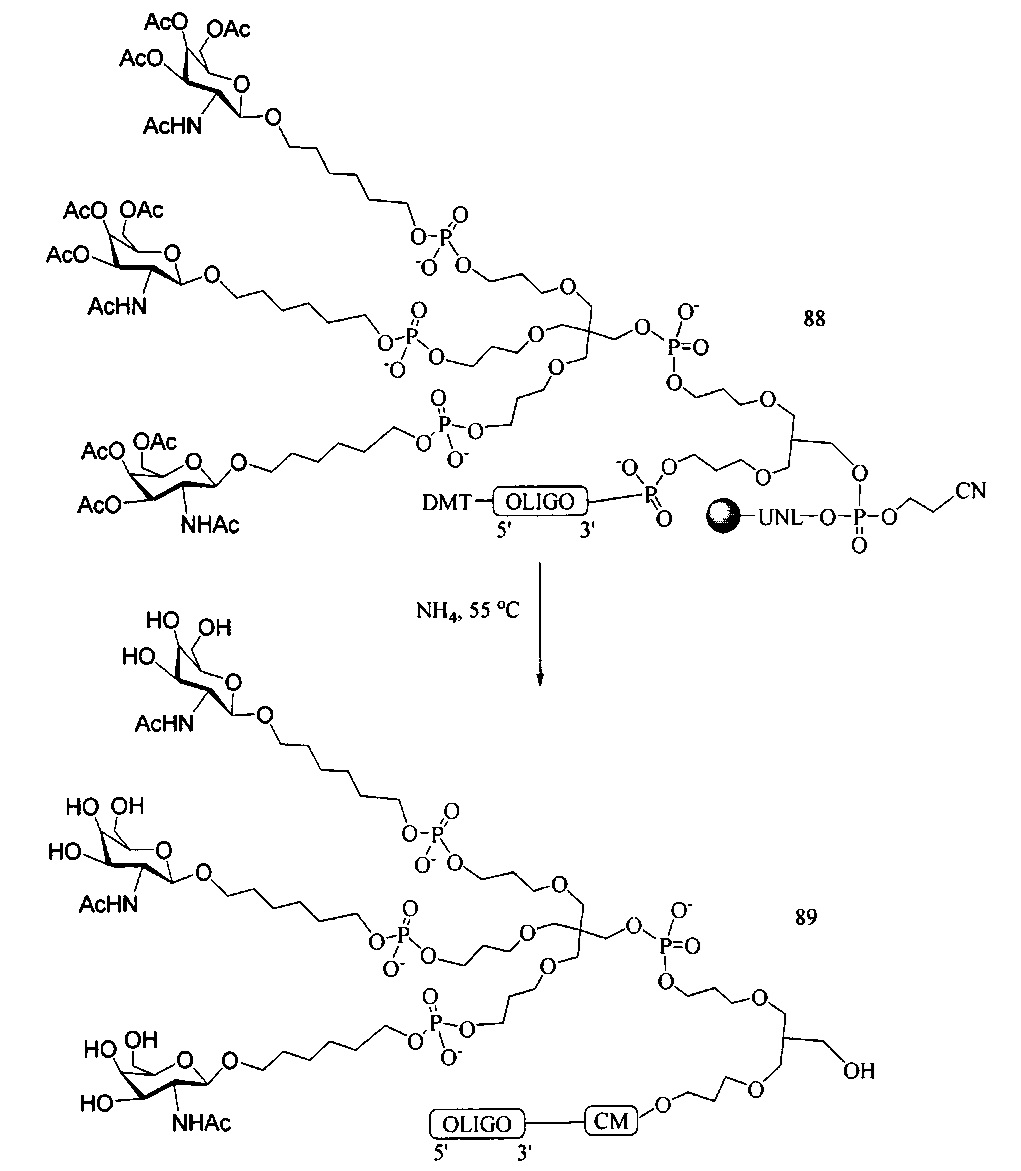
где GalNAc3-4 имеет структуру:
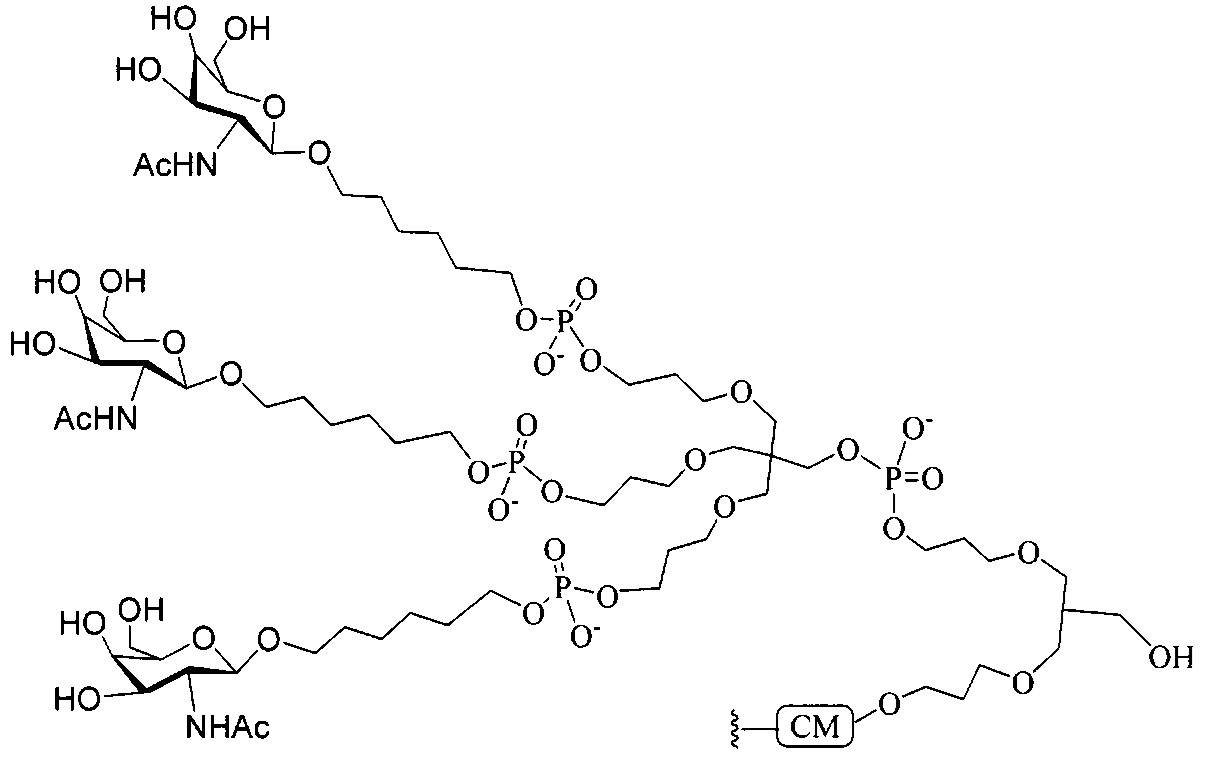
Где СМ представляет собой расщепляемый фрагмент. В некоторых вариантах реализации расщепляемый фрагмент представляет собой:
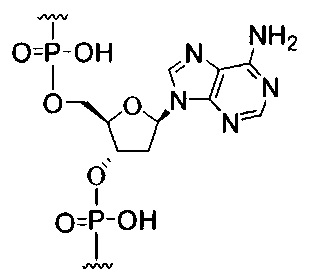
Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-4 (GalNAc3-4a) может быть комбинирована с любым расщепляемым фрагментом с получением различных конъюгирующих групп. При этом GalNAc3-4a имеет формулу:
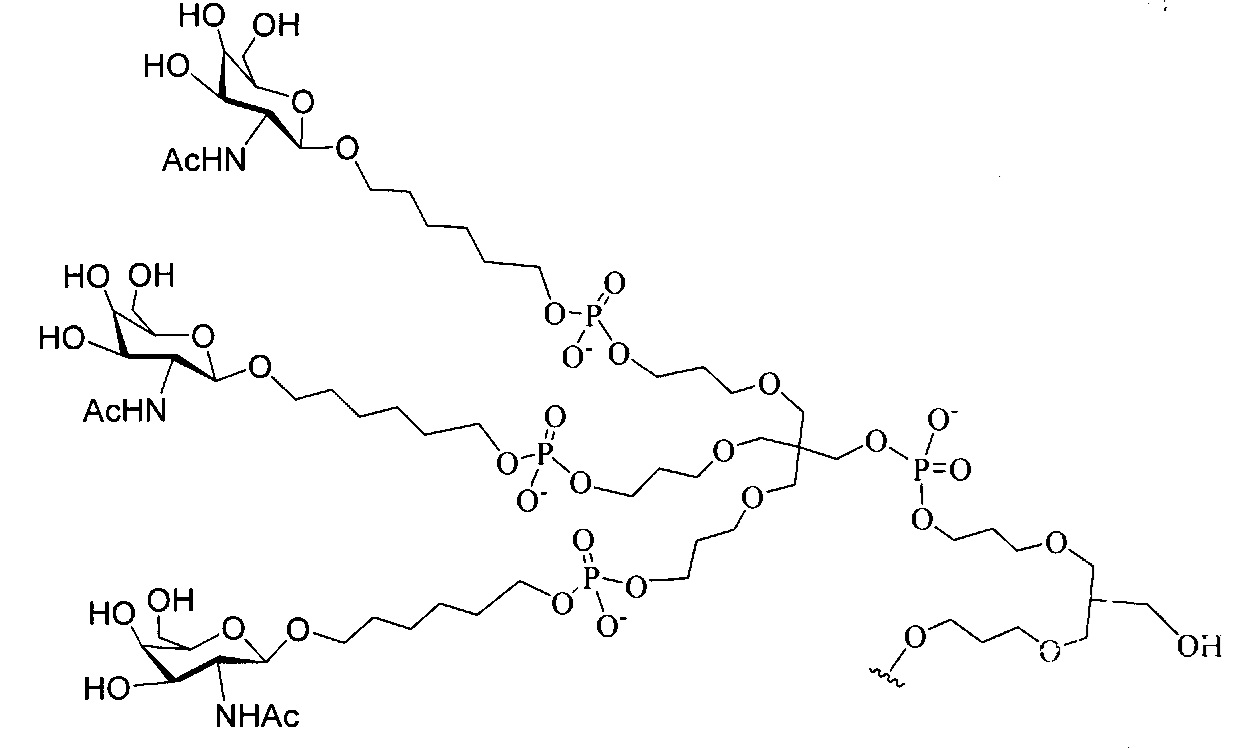
Защищенное Соединение 30 на функционализированной твердой подложке Unylinker имеется в продаже. Соединение 84 получили по таким же способам, как описаны в литературе (см. Shchepinov et al., Nucleic Acids Research, 1997, 25(22), 4447-4454; Shchepinov et al., Nucleic Acids Research, 1999, 27, 3035-3041; и Hornet et al., Nucleic Acids Research, 1997, 25, 4842-4849).
Фосфорамидитные строительные блоки, Соединения 60 и 79а, получили по способам, приведенным в Примерах 28 и 36. Изображенные фосфорамидиты являются типичными и не предназначены для ограничения, поскольку могут быть применены другие фосфорамидитные строительные блоки для получения олигомерного соединения, имеющего фосфодиэфир-связанный конъюгат на 3'-конце, которое имеет заданную последовательность и состав. Порядок и количество фосфорамидитов, добавляемых к твердой подложке, может быть подобрано для получения олигомерных соединений, описанных в настоящем документе, которые имеют любую заданную последовательность и состав.
Пример 41. Общий способ получения ASO, содержащих фосфодиэфир-связанный конъюгат GalNAc3-2 (см. Пример 37, Вх представляет собой аденин) в 5'-положении, по твердофазному способу (получение ISIS 661134)
Если не указано иное, все реагенты и растворы, примененные для синтеза олигомерных соединений, приобретены у коммерческих поставщиков. Стандартные фосфорамидитные строительные блоки и твердую подложку применили для внедрения нуклеозидных остатков, которые включают, например, остатки Т, A, G иmC. Фосфорамидитные соединения 56 и 60 применили для синтеза фосфодиэфир-связанного конъюгата GalNAc3-2 на 5'-конце. 0,1 М раствор фосфорамидита в безводном ацетонитриле применили для β-D-2'-дезоксирибонуклеозида и 2'-МОЕ.
Синтез антисмысловых олигонуклеотидов (ASO) выполнили на синтезаторе ABI 394 (в масштабе 1-2 мкмоль) или на синтезаторе
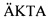
После сборки требуемой последовательности цианоэтил-фосфатные защитные группы снимали при помощи 20% диэтиламина в толуоле (об./об.) в течение 45 минут времени контакта. Связанные с твердой подложкой ASO суспендировали в водном растворе аммиака (28-30 масс. %) и нагревали при 55°С в течение 6 часов.
Затем отфильтровывали не связанные ASO и выпаривали аммиак кипячением. Остаток очищали жидкостной хроматографией высокого давления на сильной анионообменной колонке (GE Healthcare Bioscience, Source 30Q, 30 мкм, 2,54×8 см, А=100 мМ ацетата аммония в 30% водном CH3CN, В=1,5 М NaBr в А, 0-40% В за 60 мин., скорость потока 14 мл.мин-1, λ=260 нм). Остаток обессоливали при помощи ВЭЖХ на обращенно-фазовой колонке с получением заданных ASO с выделенным выходом 15-30% относительно первоначальной загрузки на твердую подложку. ASO характеризовали при помощи ион-парной ВЭЖХ, совмещенной с МС-анализом на системе Agilent 1100 MSD.


Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «k» означает 6'-(S)-СН3 бициклический нуклеозид (например, cEt); «s» означает тиофосфатные межнуклеозидные связи (PS); «о» означает фосфодиэфирные межнуклеозидные связи (РО); и «o'» означает -O-Р(=O)(ОН)-. Верхний индекс «m» означает 5-метилцитозины. Структура GalNAc3-2a приведена в Примере 37.
Пример 42. Общий способ получения ASO, содержащих конъюгат GalNAc3-3 в 5'-положении, по твердофазным методикам (получение ISIS 661166)
Синтез ISIS 661166 выполнили по таким же способам, как приведены в Примерах 39 и 41.
ISIS 661166 представляет собой 5-10-5 МОЕ гэпмер, в котором 5'-положение содержит конъюгат GalNAc3-3. Это ASO характеризовали при помощи ион-гарной ВЭЖХ, совмещенной с МС-анализом на системе Agilent 1100 MSD.

Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид, «d» означает β-D-2'-дезоксирибонацеленный нуклеозид; «s» означает тиофосфатные межнуклеозидные связи (PS); «о» означает фосфодиэфирные межнуклеозидные связи (РО); и «o'» означает -O-Р(=O)(ОН)-. Верхний индекс «m» означает 5-метилцитозины. Структура «5'-GalNAc3-3a» приведена в Примере 39.
Пример 43. Дозозависимое исследование фосфодиэфир-связанного GalNAc3-2 (см. Примеры 37 и 41, Вх представляет собой аденин) на 5'-конце, нацеленного на SRB-1, in vivo
ISIS 661134 (см. Пример 41), содержащий фосфодиэфир-связанный конъюгат GalNAc3-2 на 5'-конце, испытывали в дозозависимом исследовании на антисмысловое ингибирование SRB-1 у мышей. Неконъюгированные ISIS 440762 и 651900 (конъюгат GalNAc3-1 у 3'-конца, см. Пример 9) включены в исследование для сравнения и описаны ранее в Таблице 17.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, приведенной ниже, соединения ISIS 440762, 651900, 661134 или PBS в качестве контрольного образца. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часов после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Уровни мРНК SRB-1 определяли относительно общей РНК (при помощи Ribogreen), затем нормализовали к контрольному образцу, обработанному PBS. Результаты, показанные ниже, приведены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному PBS, и обозначены как «% PBS». ED50 измеряли по таким же способам, как описаны ранее, и они приведены ниже.
Как показано в Таблице 35, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Действительно, антисмысловые олигонуклеотиды, содержащие фосфодиэфир-связанный конъюгат GalNAc3-2 на 5'-конце (ISIS 661134) или конъюгат GalNAc3-1, связанный на 3'-конце (ISIS 651900), демонстрируют значительное улучшение эффективности, по сравнению с неконъюгированным антисмысловым олигонуклеотидом (ISIS 440762). Кроме того, ISIS 661134, который содержит фосфодиэфир-связанный конъюгат GalNAc3-2 на 5'-конце, был настолько же эффективным, как ISIS 651900, который содержит конъюгат GalNAc3-1 на 3'-конце.
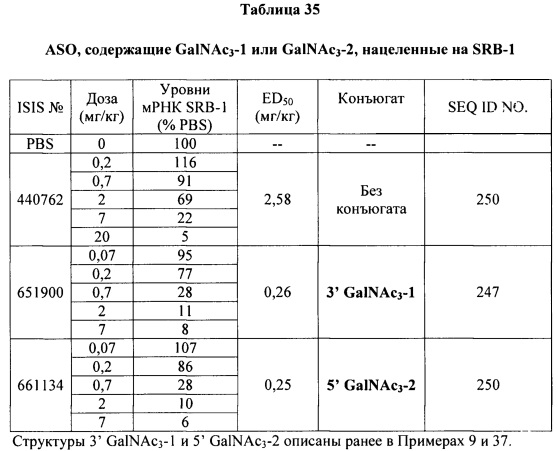
Фармакокинетический анализ (ФК)
ФК для ASO из группы высокой дозы (7 мг/кг) исследовали и оценили таким же образом, как описано в Примере 20. Образцы печени измельчили и экстрагировали по стандартным протоколам. Идентифицировали метаболиты полной длины 661134 (5' GalNAc3-2) и ISIS 651900 (3' GalNAc3-1) и подтвердили их массы при помощи масс-спектрометрического анализа высокого разрешения. Результаты показали, что основной метаболит, обнаруженный для ASO, содержащего фосфодиэфир-связанный конъюгат GalNAc3-2 на 5'-конце (ISIS 661134), представлял собой ISIS 440762 (данные не показаны). Не наблюдали никаких дополнительных метаболитов в обнаруживаемом количестве. В отличие от него, для ASO, содержащего конъюгат GalNAc3-1 на 3'-конце (ISIS 651900), наблюдали дополнительные метаболиты, аналогичные тем, которые описаны ранее в Таблице 23а. Эти результаты позволяют предположить, что наличие фосфодизфир-связанного конъюгата GalNAc3-1 или GalNAc3-2 может улучшать ФК профиль ASO без ухудшения их эффективности.
Пример 44. Влияние PO/PS связей на антисмысловое ингибирование ASO, содержащих конъюгат GalNAc3-1 (см. Пример 9) на 3'-конце, нацеленных на SRB-1
ISIS 655861 и 655862, содержащие конъюгат GalNAc3-1 на 3'-конце, каждый из которых нацелен на SRB-1, испытали в исследовании однократного введения на их способность ингибировать SRB-1 у мышей. Исходное неконъюгированное соединение, ISIS 353382, включили в исследование для сравнения.
Эти ASO представляют собой 5-10-5 МОЕ гэпмеры, в которых гэп-область содержит десять 2'-дезоксирибонуклеозидов, и каждая область крыльев содержит пять 2'-МОЕ модифицированных нуклеозидов. Эти ASO получили по таким же способам, как показаны ранее в Примере 19, и они описаны ниже в Таблице 36.

Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатные межнуклеозидные связи (PS); «о» означает фосфодиэфирные межнуклеозидные связи (РО); и «o'» означает -O-Р(=O)(ОН)-. Верхний индекс «m» означает 5-метилцитозины. Структура «GalNAc3-1» приведена в Примере 9.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, приведенной ниже, соединения ISIS 353382, 655861, 655862 или PBS в качестве контрольного образца. Каждая экспериментальная группа состояла из 4 животных. Перед лечением, а также после последней дозы у каждой мыши брали кровь и анализировали образцы плазмы. Мышей умертвили через 72 часов после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Уровни мРНК SRB-1 определяли относительно общей РНК (при помощи Ribogreen), затем нормализовали к контрольному образцу, обработанному PBS. Результаты, показанные ниже, приведены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному PBS, и обозначены как «% PBS». ED50 измеряли по таким же способам, как описаны ранее, и они приведены ниже.
Как показано в Таблице 37, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом, по сравнению с контрольным образцом, обработанным PBS. Действительно, антисмысловые олигонуклеотиды, содержащие конъюгат GalNAc3-1 на 3'-конце (ISIS 655861 и 655862), демонстрируют значительное усиление эффективности, по сравнению с неконъюгированным антисмысловым олигонуклеотидом (ISIS 353382). Кроме того, ISIS 655862 со смешанными PS/PO связями демонстрирует усиление эффективности, по сравнению с соединением, содержащим только PS (ISIS 655861).
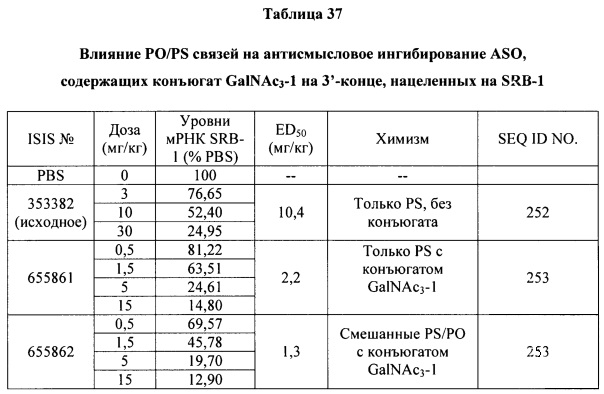
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, применяя стандартные протоколы. Оценили также массу органов. Результаты показывают, что не наблюдали какого-либо увеличения уровней трансаминазы (Таблица 38) или массы органов (данные не показаны) у мышей, обработанных ASO, по сравнению с PBS контролем. Кроме того, ASO со смешанными PS/PO связями (ISIS 655862) демонстрирует схожие уровни трансаминазы, по сравнению с соединением, содержащим только PS (ISIS 655861).
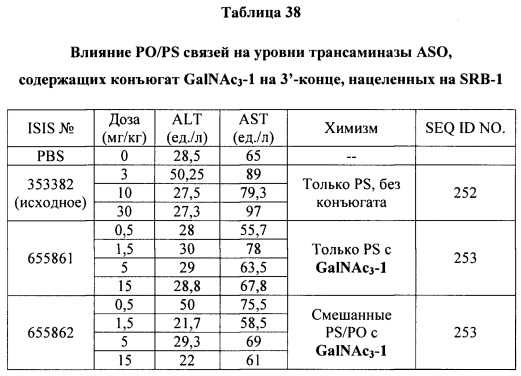
Пример 45. Получение PFP эфира, Соединения 110а
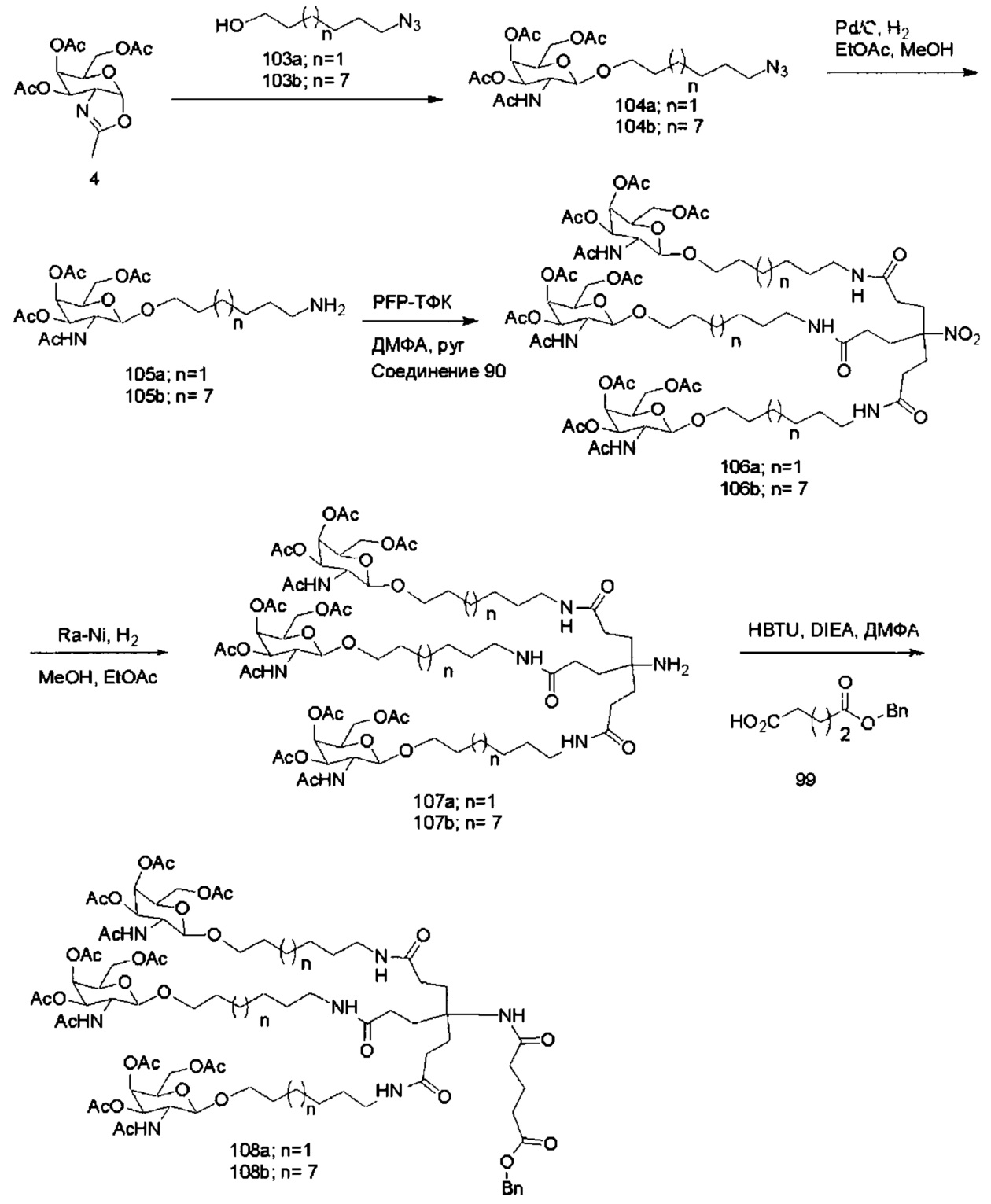
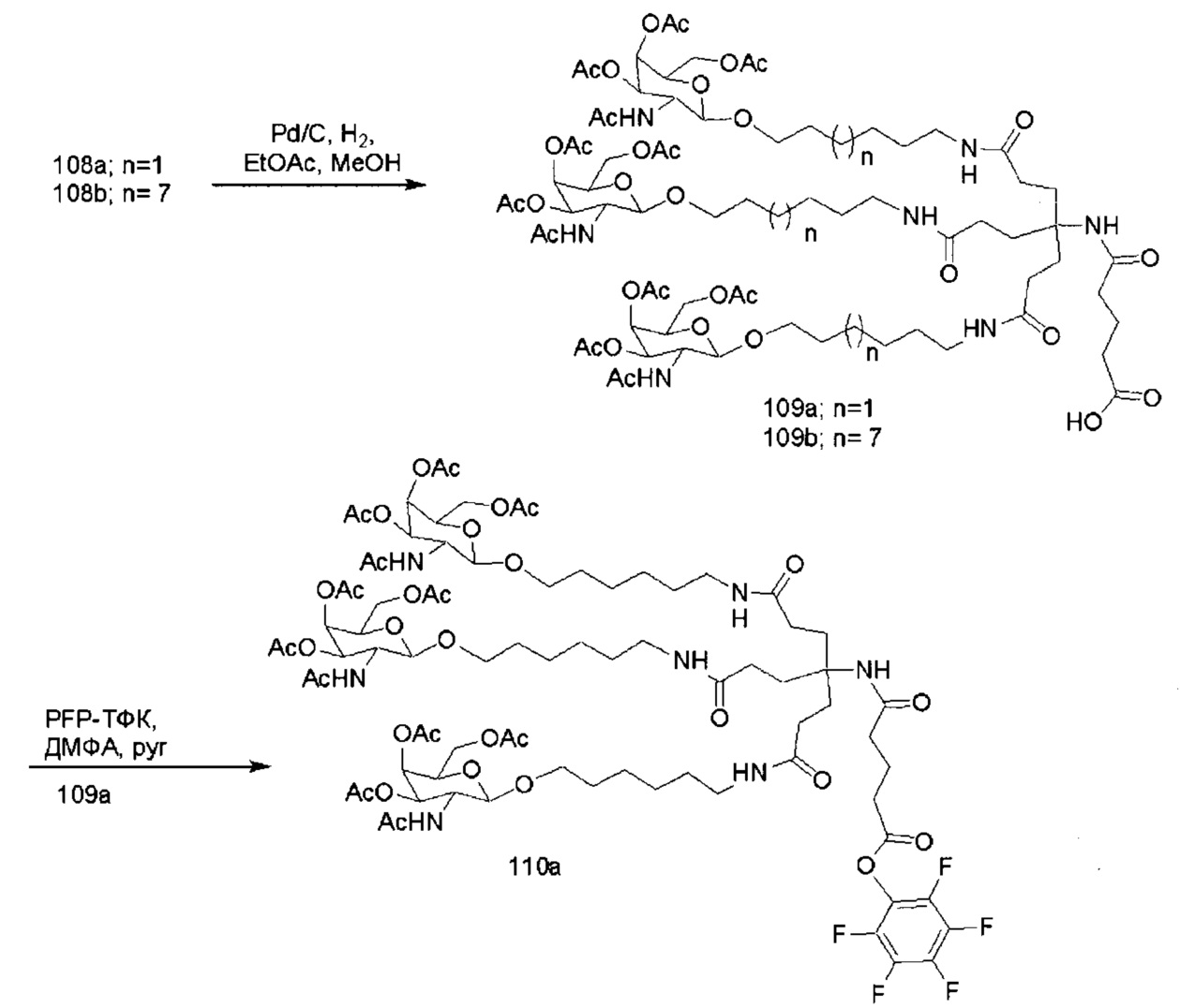
Соединение 4 (9,5 г, 28,8 ммоль) обработали по отдельности соединением 103а или 103b (38 ммоль) и TMSOTf (0,5 экв.), и молекулярными ситами в дихлорметане (200 мл), и перемешивали в течение 16 часов при комнатной температуре. Затем органический слой отфильтровали через целит, затем промыли бикарбонатом натрия, водой и насыщенным солевым раствором. Затем отделили органический слой и высушили над сульфатом натрия, отфильтровали и упарили при пониженном давлении. Полученное маслянистее вещество очистили хроматографией на силикагеле (2%-->10% метанол/дихлорметан) с получением соединений 104а и 104b с выходом >80%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 104а и 104b обработали в тех же условиях, что и соединения 100a-d (Пример 47), с получением соединений 105а и 105b с выходом >90%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 105а и 105b по отдельности обработали соединением 90 при тех же условиях, что и соединения 901a-d, с получением соединений 106а (80%) и 106b (20%). Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 106а и 106b обработали в тех же условиях, что и соединения 96a-d (Пример 47), с получением соединения 107а (60%) и 107b (20%). Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 107а и 107b обработали в тех же условиях, что и соединения 97a-d (Пример 47), с получением соединений 108а и 108b с выходом 40-60%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 108а (60%) и 108b (40%) обработали в тех же условиях, что и соединения 100а-d (Пример 47), с получением соединений 109а и 109b с выходом >80%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединение 109а обработали в тех же условиях, что и соединения 101a-d (Пример 47), с получением соединения 110а с выходом 30-60%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой. Альтернативно, Соединение 110b может быть получено таким же образом, исходя из Соединения 109b.
Пример 46. Общий способ конъюгации с PFP эфирами (олигонуклеотид 111); получение ISIS 666881 (GalNAc3-10)
Синтезировали и очистили 5'-гексиламино-модифицированный олигонуклеотид по стандартным способам твердофазного получения олигонуклеотидов. 5'-Гексиламино-модифицированный олигонуклеотид растворили в 0,1 М растворе тетрабората натрия, рН 8,5 (200 мкл) и добавили 3 эквивалента выбранного PFP-эстерифицированного кластера GalNAc3, растворенного в ДМСО (50 мкл). Если при добавлении раствора ASO эфир PFP выпадал в осадок, то добавляли ДМСО до перехода всего эфира PFP в раствор. Реакция была завершена примерно через 16 часов перемешивания при комнатной температуре. Полученный раствор разбавили водой до 12 мл, а затем центрифугировали при 3000 об./мин. в центробежном фильтре с отсечением по массе 3000 Да. Этот прием повторили два раза для удаления низкомолекулярных примесей. Затем раствор лиофилизировали досуха и повторно растворили в концентрированном водном растворе аммиака, и перемешивали при комнатной температуре в течение 2,5 часов, затем концентрировали in vacuo для удаления большей части аммиака. Конъюгированный олигонуклеотид очистили и обессолили при помощи ОФ-ВЭЖХ, и лиофилизировали с получением GalNAc3 конъюгированного олигонуклеотида.
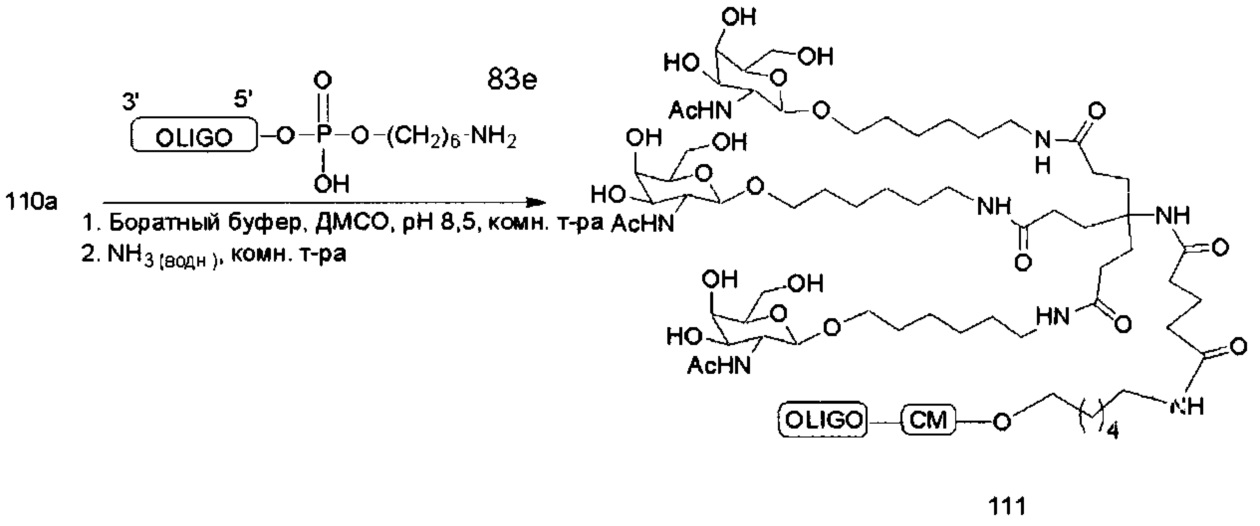
Олигонуклеотид 111 конъюгирован с GalNAc3-10. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-10 (GalNAc3-10a) может быть комбинирована с любым расщепляемым фрагментом с получением различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -Р(=O)(ОН)-Аа-Р(=O)(ОН)-, как показано ниже в олигонуклеотиде (ISIS 666881), синтезированном с GalNAc3-10. Структура GalNAc3-10 (GalNAc3-10a-CM-) приведена ниже:
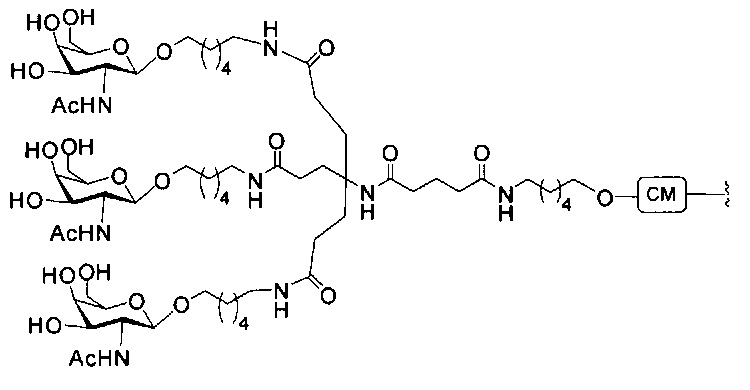
По указанному общему способу получили ISIS 666881. Синтезировали и очистили 5'-гексиламино-модифицированный олигонуклеотид, ISIS 660254, по стандартным способам твердофазного получения олигонуклеотидов. ISIS 660254 (40 мг, 5,2 мкмоль) растворили в 0,1 М растворе тетрабората натрия, рН 8,5 (200 мкл) и добавили 3 эквивалента PFP эфира (Соединения 110а), растворенного в ДМСО (50 мкл). Эфир PFP выпал в осадок при добавлении раствора ASO, поэтому потребовалось добавление дополнительного количества ДМСО (600 мкл) для полного растворения PFP эфира. Реакция была завершена через 16 часов перемешивания при комнатной температуре. Раствор разбавили водой до общего объема 12 мл, а затем центрифугировали при 3000 об./мин. в центробежном фильтре с отсечением по массе 3000 Да. Этот прием повторили два раза для удаления низкомолекулярных примесей. Раствор лиофилизировали досуха и повторно растворили в концентрированном водном растворе аммиака, перемешивая при комнатной температуре в течение 2,5 часов, затем концентрировали in vacuo для удаления большей части аммиака. Конъюгированный олигонуклеотид очистили и обессолили при помощи ОФ-ВЭЖХ, и лиофилизировали с получением ISIS 666881 с выходом 90% по массе (42 мг, 4,7 мкмоль).
GalNAc3-10-конъюгированный олигонуклеотид

Заглавные буквы указывают азотистое основание для каждого нуклеозида, аmC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатную межнуклеозидную связь(PS); «о» означает фосфодиэфирную межнуклеозидную связь (РО); и «o'» означает -O-Р(=O)(ОН)-. Конъюгирующие группы выделены жирным шрифтом.
Пример 47. Получение олигонуклеотида 102, содержащего GalNAc3-8
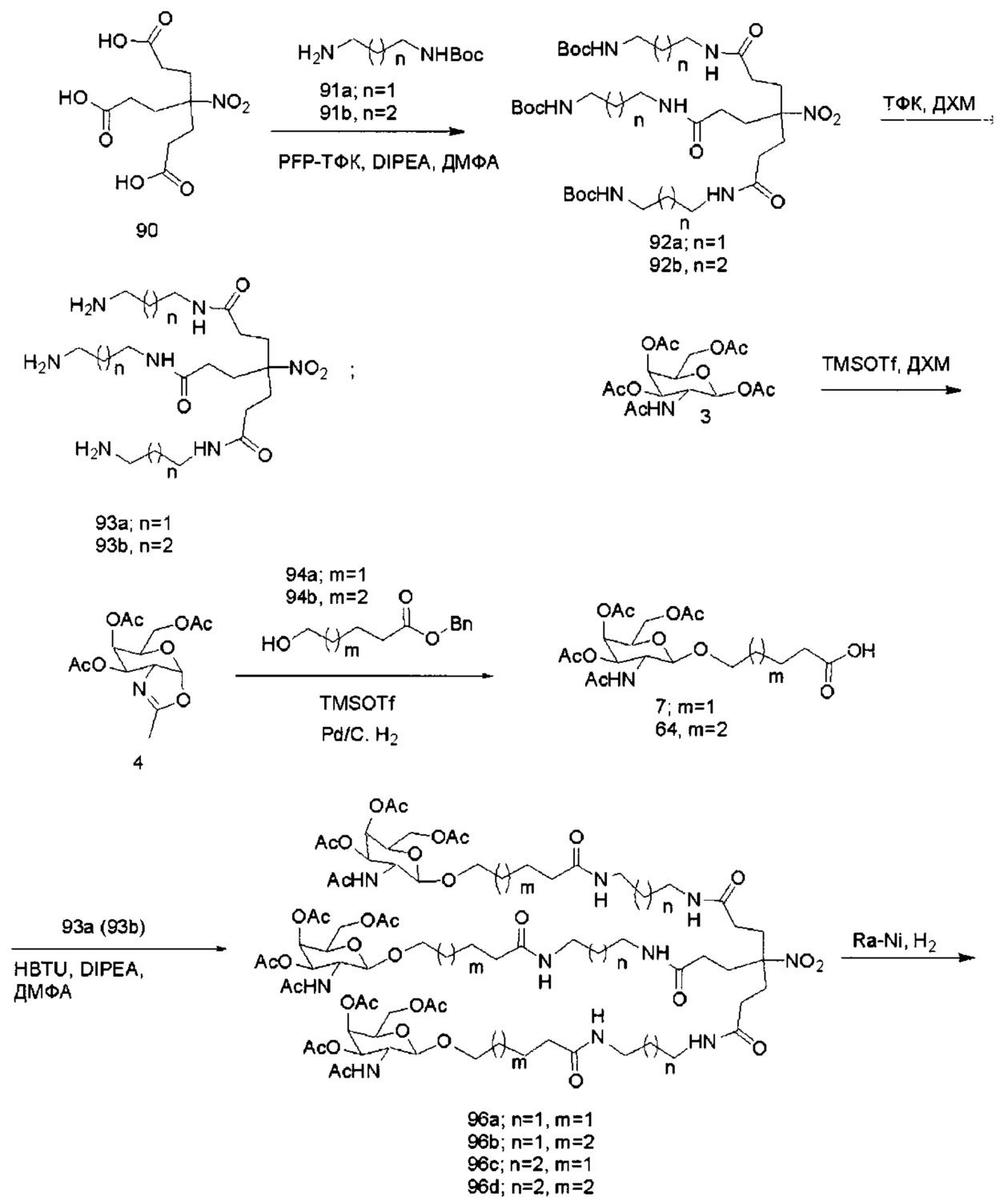
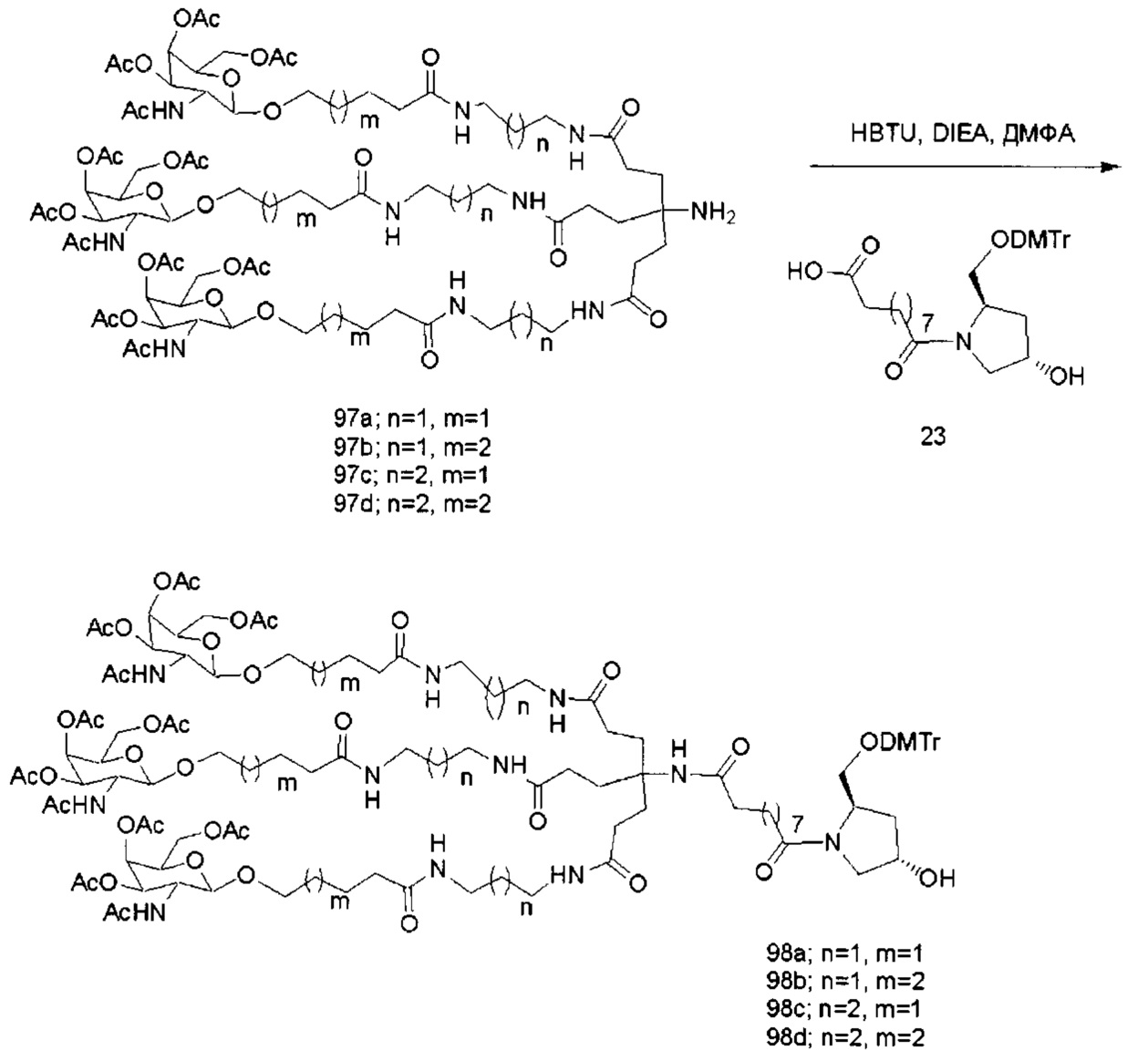
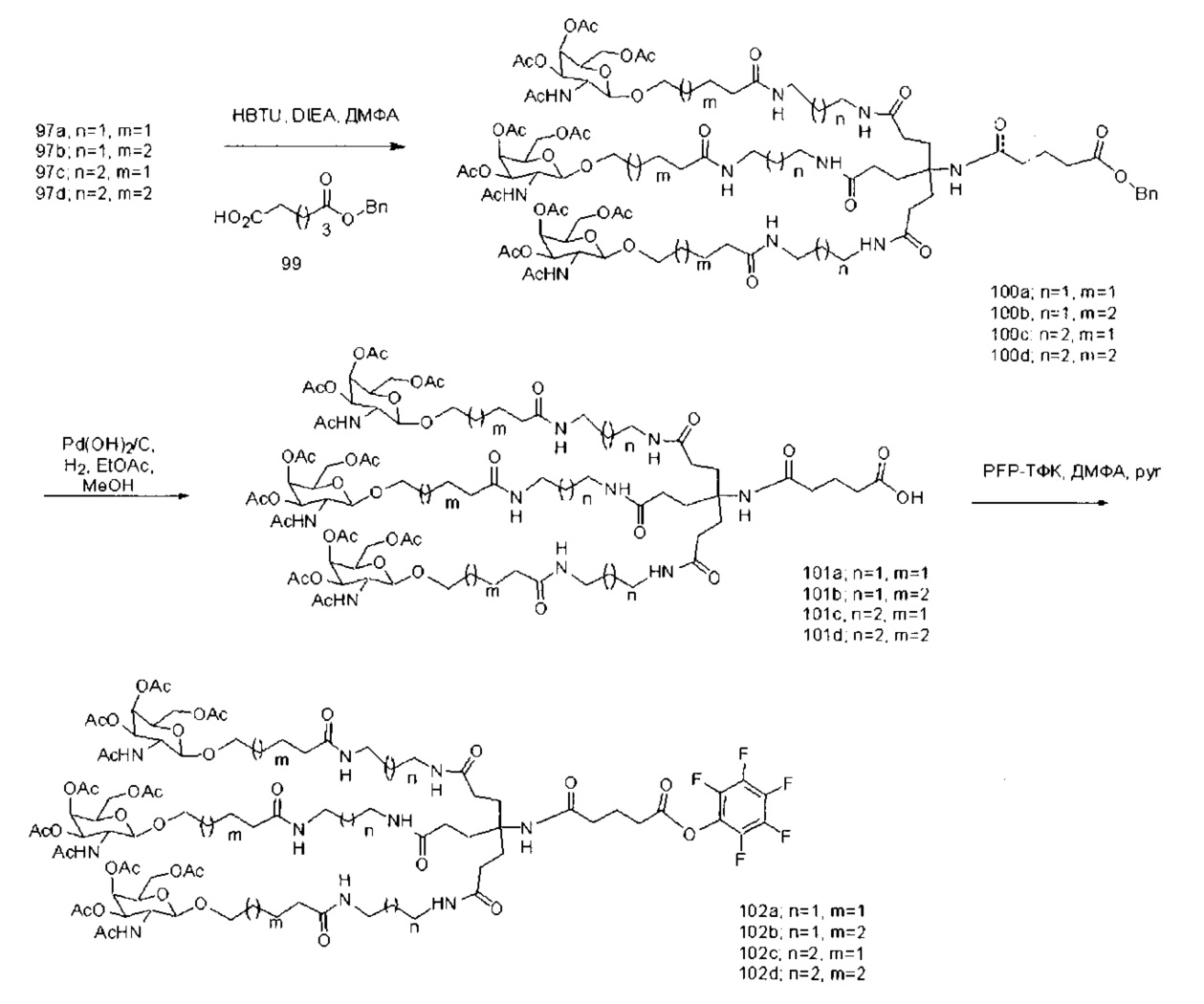
Трехкислотное соединение 90 (4 г, 14,43 ммоль) растворили в ДМФА (120 мл) и N,N-диизопропилэтиламине (12,35 мл, 72 ммоль). По каплям добавили пентафторфенила трифторацетат (8,9 мл, 52 ммоль) под аргоном и оставили реакционную смесь перемешиваться при комнатной температуре в течение 30 минут. Добавили Вос-диамин 91а или 91b (68,87 ммоль) вместе с N,N-диизопропилэтиламином (12,35 мл, 72 ммоль) и оставили реакционную смесь перемешиваться при комнатной температуре в течение 16 часов. Затем упарили ДМФА на >75% при пониженном давлении, а затем растворили смесь в дихлорметане. Органический слой промыли бикарбонатом натрия, водой и насыщенным солевым раствором. Затем отделили органический слой и высушили над сульфатом натрия, отфильтровали и упарили при пониженном давлении до маслянистого остатка. Полученное маслянистое вещество очистили хроматографией на силикагеле (2%-->10% метанол/дихлорметан) с получением соединений 92а и 92b с приблизительным выходом 80%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединение 92а или 92b (6,7 ммоль) обрабатывали 20 мл дихлорметана и 20 мл трифторуксусной кислоты при комнатной температуре в течение 16 часов. Полученный раствор выпарили, а затем растворили в метаноле и обрабатывали смолой DOWEX-OH в течение 30 минут. Полученный раствор отфильтровали и упарили до маслянистого вещества при пониженном давлении с получением 85-90% выхода соединений 93а и 93b.
Соединения 7 или 64 (9,6 ммоль) обрабатывали HBTU (3,7 г, 9,6 ммоль) и диизопропилэтиламином (5 мл) в ДМФА (20 мл) в течение 15 минут. К смеси добавили либо соединение 93а, либо 93b (3 ммоль) и оставили перемешиваться при комнатной температуре на 16 часов. Затем упарили ДМФА на >75% при пониженном давлении, а затем растворили смесь в дихлорметане. Органический слой промыли бикарбонатом натрия, водой и насыщенным солевым раствором. Затем отделили органический слой и высушили над сульфатом натрия, отфильтровали и упарили при пониженном давлении до маслянистого остатка. Полученное маслянистое вещество очистили хроматографией на силикагеле (5%-->20% метанол/дихлорметан) с получением соединений 96a-d с выходом 20-40%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 96a-d (0,75 ммоль) по отдельности гидрировали на никеле Ренея в течение 3 часов в этаноле (75 мл). Затем катализатор удалили фильтрованием через целит, а этанол удалили при пониженном давлении с получением соединений 97a-d с выходом 80-90%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединение 23 (0,32 г, 0,53 ммоль) обрабатывали HBTU (0,2 г, 0,53 ммоль) и N,N-диизопропилэтиламином (0,19 мл, 1,14 ммоль) в ДМФА (30 мл) в течение 15 минут. К смеси по отдельности добавили соединения 97a-d (0,38 ммоль) и оставили перемешиваться при комнатной температуре на 16 часов. Затем упарили ДМФА на >75% при пониженном давлении, а затем растворили смесь в дихлорметане. Органический слой промыли бикарбонатом натрия, водой и насыщенным солевым раствором. Затем отделили органический слой и высушили над сульфатом натрия, отфильтровали и упарили при пониженном давлении до маслянистого остатка. Полученное маслянистое вещество очистили хроматографией на силикагеле (2%-->20% метанол/дихлорметан) с получением соединений 98a-d с выходом 30-40%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединение 99 (0,17 г, 0,76 ммоль) обрабатывали HBTU (0,29 г, 0,76 ммоль) и диизопропилэтиламином (0,35 мл, 2,0 ммоль) в ДМФА (50 мл) в течение 15 минут. К смеси по отдельности добавили соединения 97a-d (0,51 ммоль) и оставили перемешиваться при комнатной температуре на 16 часов. Затем упарили ДМФА на >75% при пониженном давлении, а затем растворили смесь в дихлорметане. Органический слой промыли бикарбонатом натрия, водой и насыщенным солевым раствором. Затем отделили органический слой и высушили над сульфатом натрия, отфильтровали и упарили при пониженном давлении до маслянистого остатка. Полученное маслянистое вещество очистили хроматографией на силикагеле (5%-->20% метанол/дихлорметан) с получением соединимой 100а-d с выходом 40-60%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 100a-d (0,16 ммоль) по отдельности гидрировали на 10% Pd(OH)2/C в течение 3 часов в метаноле/этилацетате (1:1, 50 мл). Затем катализатор удалили фильтрованием через целит, а органические растворители удалили при пониженном давлении с получением соединений 101a-d с выходом 80-90%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
Соединения 101a-d (0,15 ммоль) по отдельности растворили в ДМФА (15 мл) и пиридине (0,016 мл, 0,2 ммоль). По каплям добавили пентафторфенила трифторацетат (0,034 мл, 0,2 ммоль) под аргоном и оставили реакционную смесь перемешиваться при комнатной температуре в течение 30 минут. Затем упарили ДМФА на >75% при пониженном давлении, а затем растворили смесь в дихлорметане. Органический слой промыли бикарбонатом натрия, водой и насыщенным солевым раствором. Затем отделили органический слой и высушили над сульфатом натрия, отфильтровали и упарили при пониженном давлении до маслянистого остатка. Полученное маслянистое вещество очистили хроматографией на силикагеле (2%-->5% метанол/дихлорметан) с получением соединений 102a-d с приблизительным выходом 80%. Данные ЖХМС и протонного ЯМР согласовались с указанной структурой.
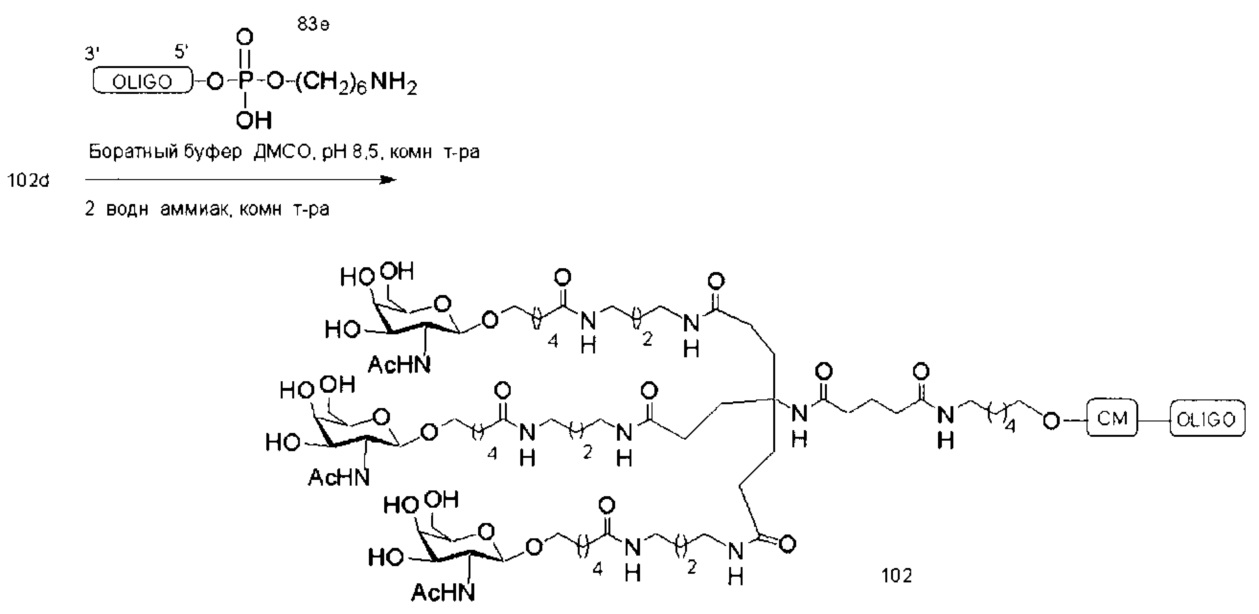
Олигомерное Соединение 102, содержащее конъюгирующую группу GalNAc3-8, получили по общим способам, приведенным в Примере 46. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-8 (GalNAc3-8a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В предпочтительном варианте реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-.
Структура GalNAc3-8 (GalNAc3-8a-CM-) приведена ниже:
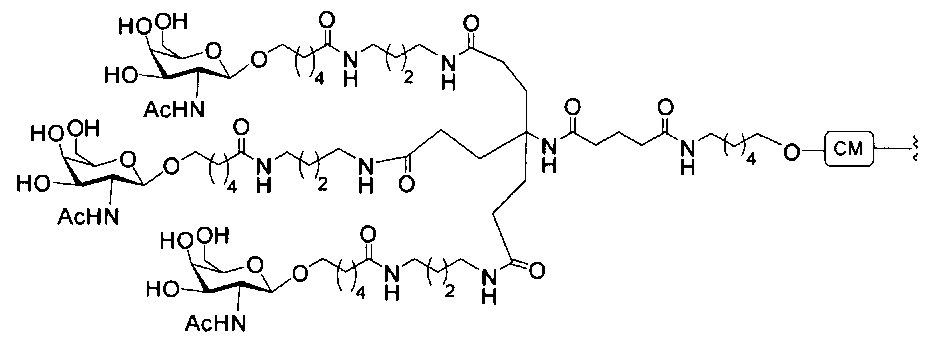
Пример 48. Получение олигонуклеотида 119, содержащего GalNAc3-7
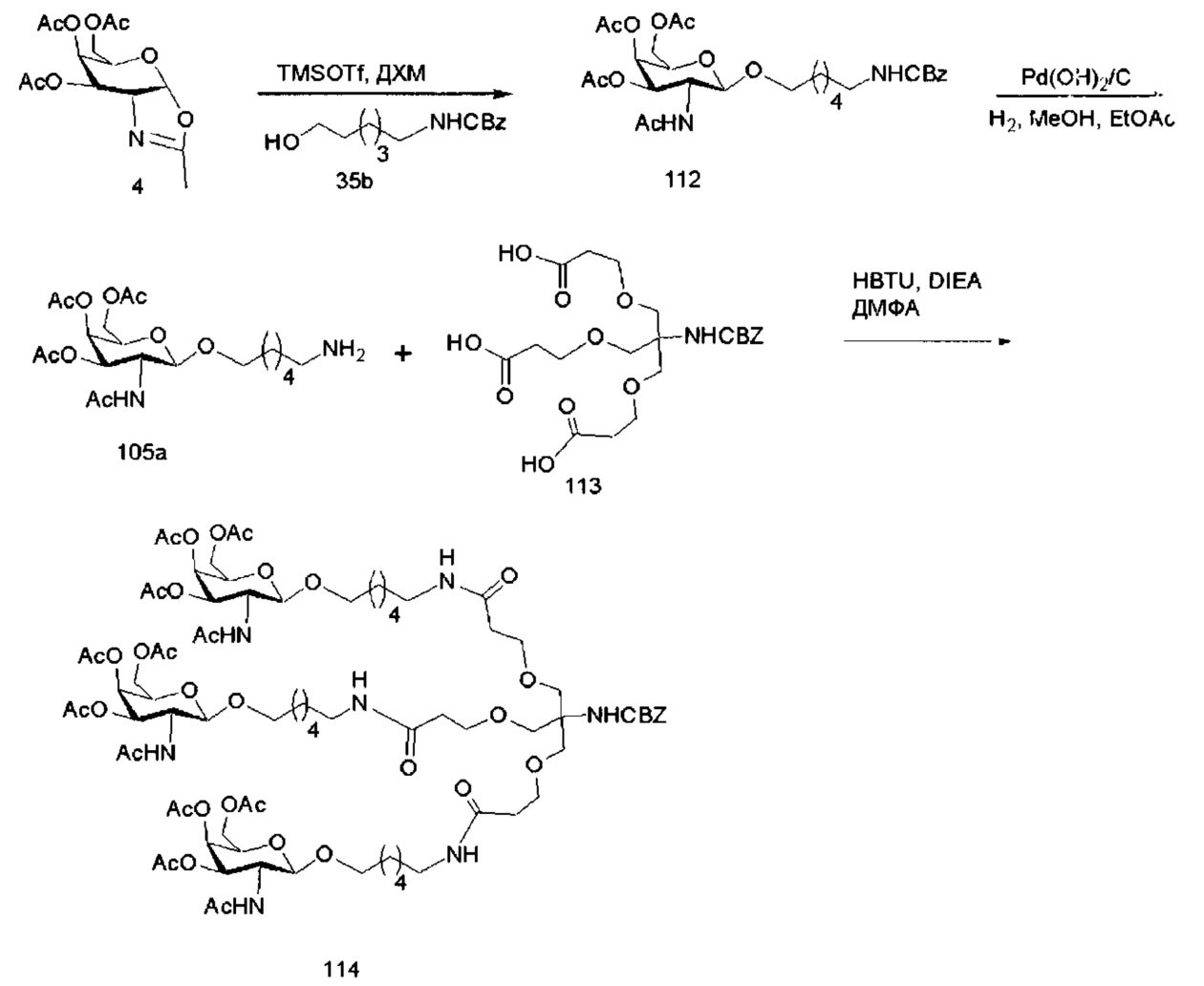
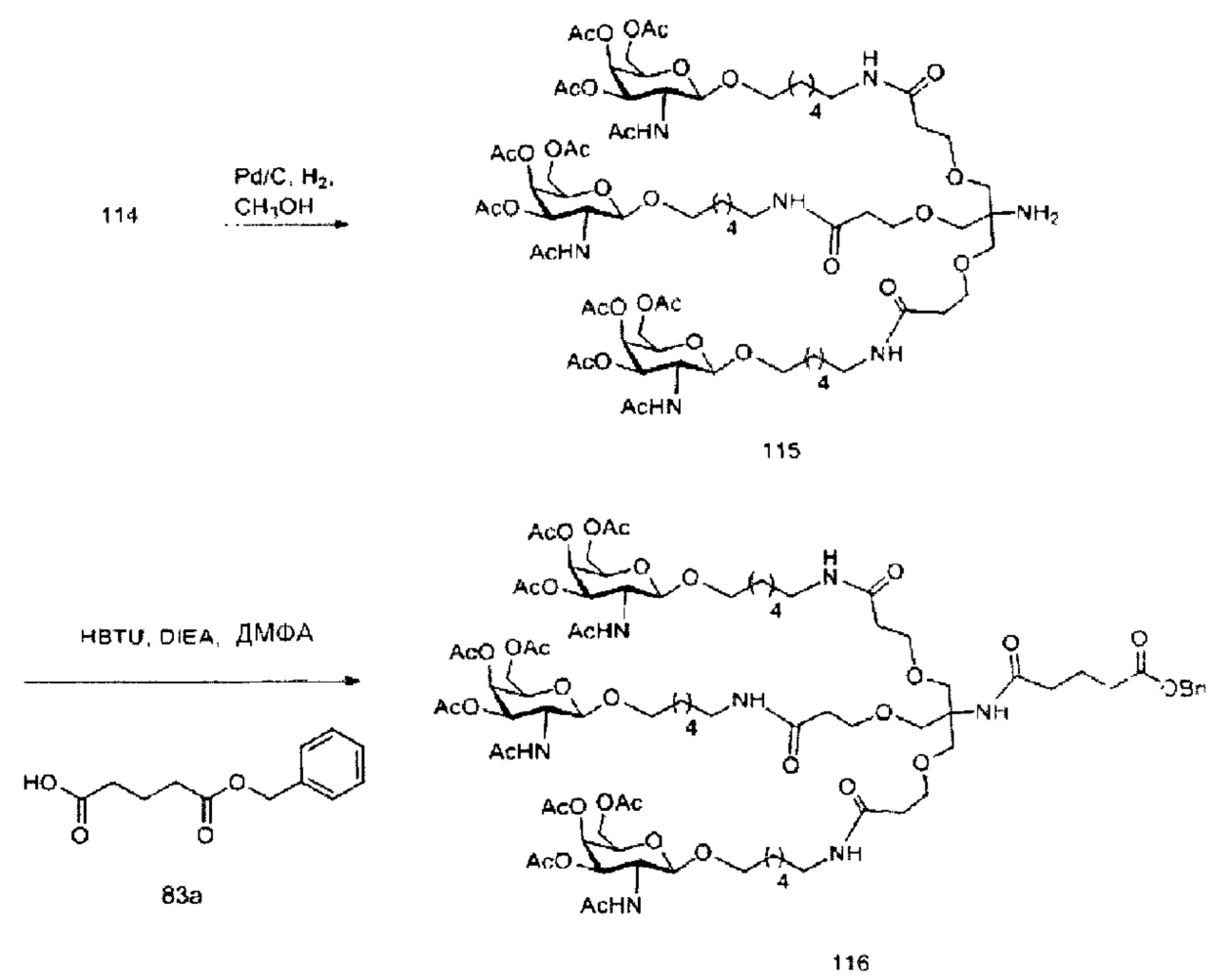
Соединение 112 синтезировали по способу, описанному в литературе (J. Med. Chem. 2004, 47, 5798-5808).
Соединение 112 (5 г, 8,6 ммоль) растворили в 1:1 смеси метанола/этилацетата (22 мл/22 мл). Добавили гидроксид палладия на углероде (0,5 г). Реакционную смесь перемешивали при комнатной температуре в атмосфере водорода в течение 12 часов. Реакционную смесь отфильтровали через слой целита и промыли этот слой 1:1 смесью метанола/этилацетата. Фильтрат и промывочные растворы объединили и концентрировали досуха с получением Соединения 105а (количественно). Структуру подтвердили по ЖХМС.
Соединение 113 (1,25 г, 2,7 ммоль), HBTU (3,2 г, 8,4 ммоль) и DIEA (2,8 мл, 16,2 ммоль) растворили в безводном ДМФА (17 мл) и перемешивали реакционную смесь при комнатной температуре в течение 5 минут. К этой смеси добавили раствор Соединения 105а (3,77 г, 8,4 ммоль) в безводном ДМФА (20 мл). Реакционную смесь перемешивали при комнатной температуре в течение 6 часов. Растворитель удалили при пониженном, давлении с получением маслянистого вещества. Остаток растворили в CH2Cl2 (100 мл) и промыли насыщенным водным раствором NaHCO3 (100 мл) и насыщенным солевым раствором (100 мл). Органическую фазу отделили, высушили (Na2SO4), отфильтровали и выпарили. Остаток очистили колоночной хроматографией на силикагеле и элюировали от 10 до 20% МеОН в дихлорметане с получением Соединения 114 (1,45 г, 30%). Структуру подтвердили анализом ЖХМС и1Н ЯМР.
Соединение 114 (1,43 г, 0,8 ммоль) растворили в 1:1 смеси метанола/этилацетата (4 мл/4 мл). Добавили палладий на углероде (влажный, 0,14 г). Реакционную смесь продували водородом и перемешивали при комнатной температуре в атмосфере водорода в течение 12 часов. Реакционную смесь отфильтровали через слой целита. Слой целита промыли метанолом/этилацетатом (1:1). Фильтрат и промывочные растворы объединили и выпарили при пониженном давлении с получением Соединения 115 (количественно). Структуру подтвердили анализом ЖХМС и1Н ЯМР.
Соединение 83а (0,17 г, 0,75 ммоль), HBTU (0,31 г, 0,83 ммоль) и DIEA (0,26 мл, 1,5 ммоль) растворили в безводном ДМФА (5 мл) и перемешивали реакционную смесь при комнатной температуре в течение 5 минут. К этой смеси добавили раствор Соединения 115 (1,22 г, 0,75 ммоль) в безводном ДМФА и перемешивали реакционную смесь при комнатной температуре в течение 6 часов. Растворитель удалили при пониженном давлении, а остаток растворили в CH2Cl2. Органический слой промыли насыщенным водным раствором NaHCO3 и насыщенным солевым раствором, и высушили над безводным Na2SO4, и отфильтровали. Органический слой концентрировали досуха, а полученный остаток очистили колоночной хроматографией на силикагеле и элюировали от 3 до 15% МеОН в дихлорметане с получением Соединения 116 (0,84 г, 61%). Структуру подтвердили анализом ЖХМС и1Н ЯМР.
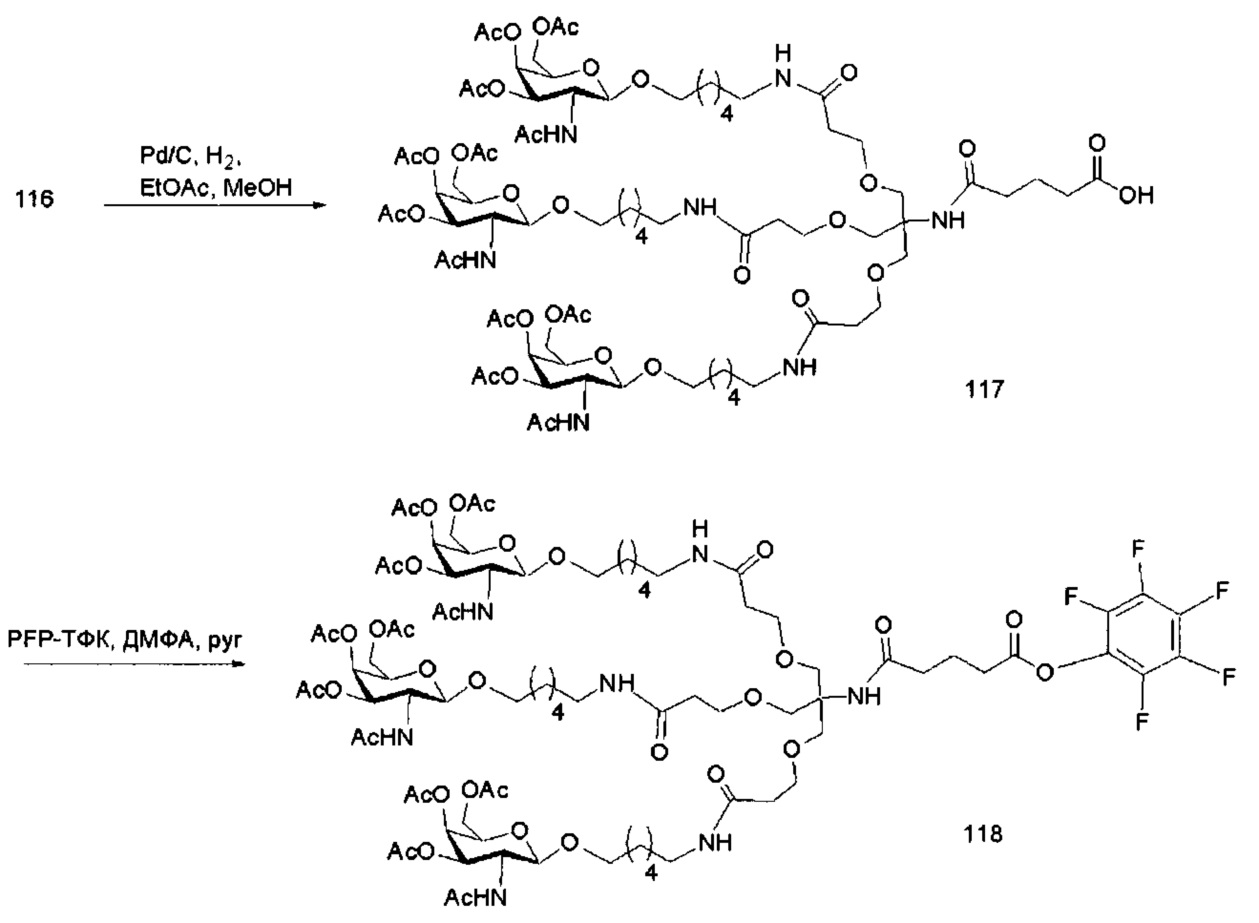
Соединение 116 (0,74 г, 0,4 ммоль) растворили в 1:1 смеси метанола/этилацетата (5 мл/5 мл). Добавили палладий на углероде (влажный, 0,074 г). Реакционную смесь продували водородом и перемешивали при комнатной температуре в атмосфере водорода в течение 12 часов. Реакционную смесь отфильтровали через слой целита. Слой целита промыли метанолом/этилацетатом (1:1). Фильтрат и промывочные растворы объединили и выпарили при пониженном давлении с получением соединения 117 (0,73 г, 98%). Структуру подтвердили анализом ЖХМС и1Н ЯМР.
Соединение 117 (0,63 г, 0,36 ммоль) растворили в безводном ДМФА (3 мл). К этому раствору добавили N,N-диизопропилэтиламин (70 мкл, 0,4 ммоль) и пентафторфенила трифторацетат (72 мкл, 0,42 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 12 часов и вылили в насыщенный водный раствор NaHCO3. Смесь экстрагировали дихлорметаном, промыли насыщенным солевым раствором и высушили та безводным Na2SO4. Дихлорметановый раствор концентрировали досуха и очистили колоночной хроматографией на силикагеле, и элюировали от 5 до 10% МеОН в дихлорметане с получением соединения 118 (0,51 г, 79%). Структуру подтвердили по ЖХМС и1Н, а также1Н и19F ЯМР.
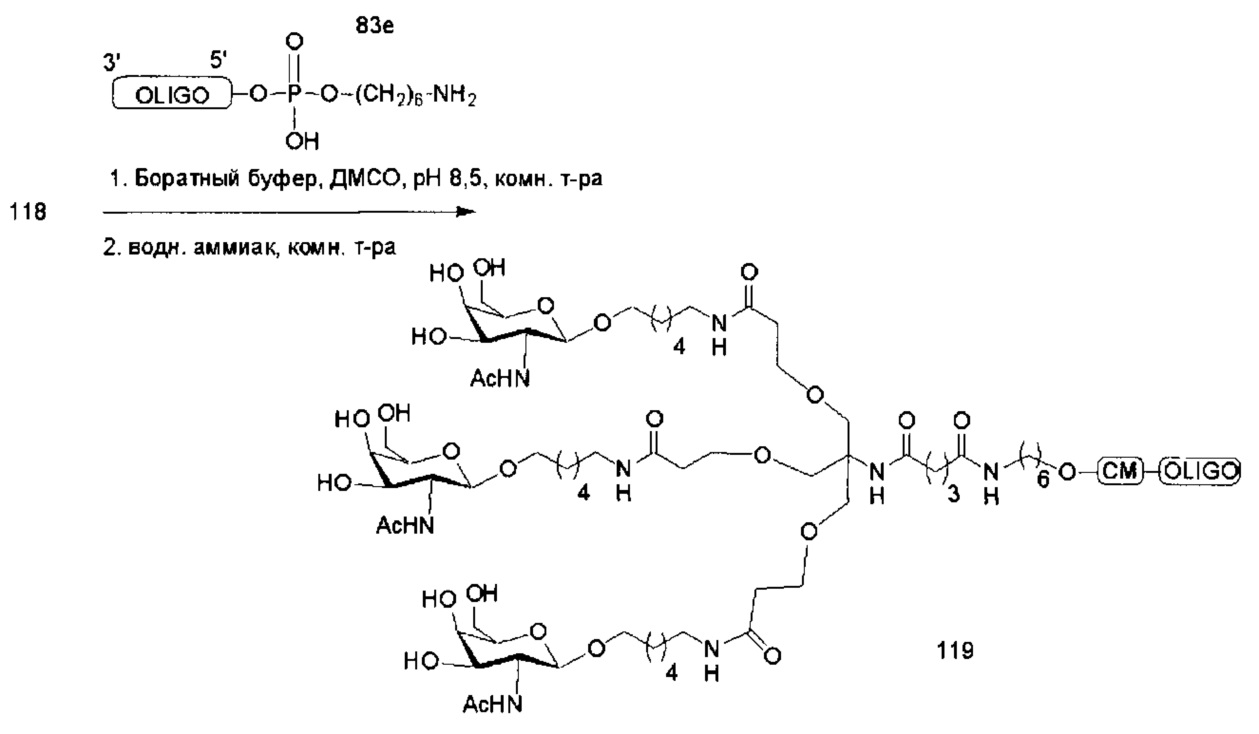
Олигомерное Соединение 119, содержащее конъюгирующую группу GalNAc3-7, получили по общим способам, приведенным в Примере 46. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-7 (GalNAc3-7a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-Р(=O)(ОН)-.
Структура GalNAc3-7 (GalNAc3-7a-CM-) приведена ниже:
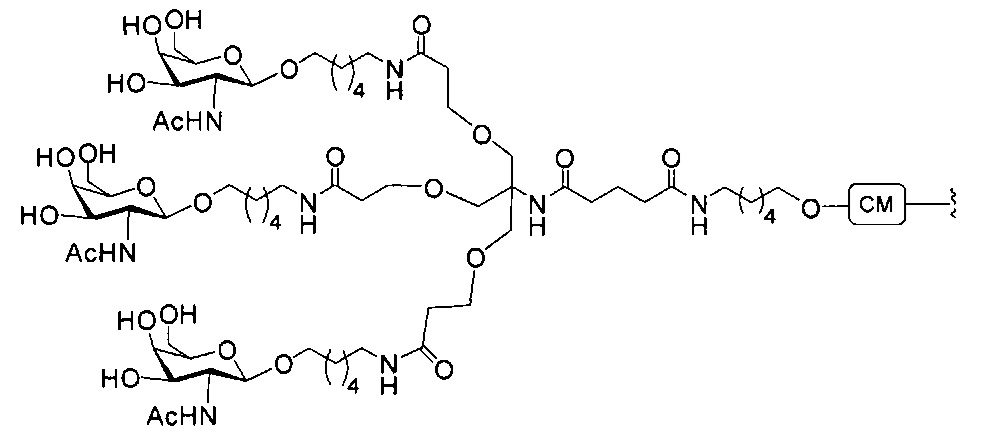
Пример 49. Получение олигонуклеотида 132, содержащего GalNAc3-5
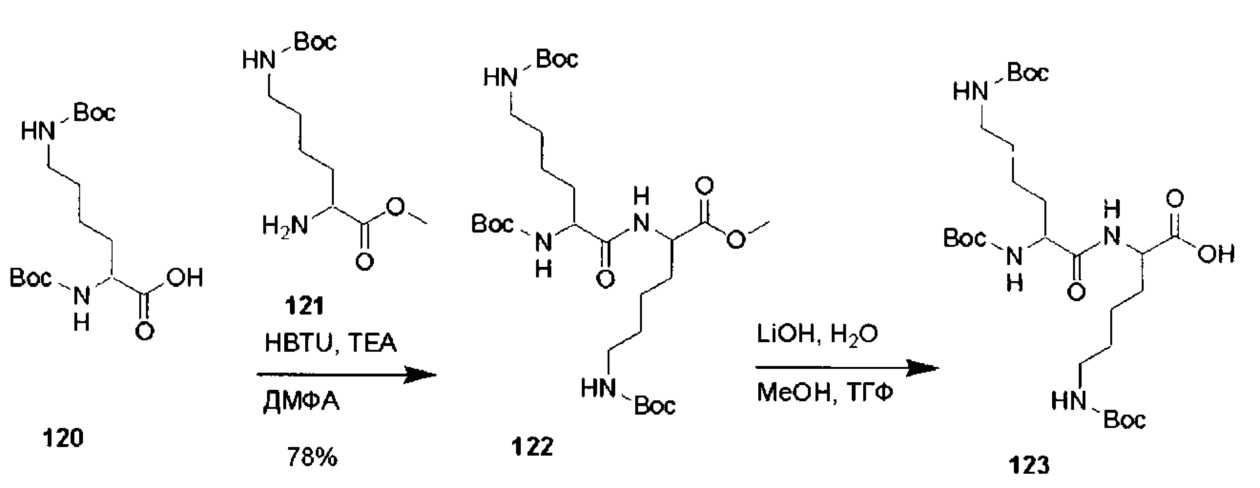
Соединение 120 (14,01 г, 40 ммоль) и HBTU (14,06 г, 37 ммоль) растворили [; безводном ДМФА (80 мл). Добавили триэтиламин (11,2 мл, 80,35 ммоль) и перемешивали в течение 5 минут. Реакционную смесь охладили на ледяной бане и добавили раствор соединения 121 (10 г, ммоль) в безводном ДМФА (20 мл). Добавили дополнительное количество триэтиламина (4,5 мл, 32,28 ммоль) и перемешивали реакционную смесь в течение 18 часов в атмосфере аргона. Реакцию контролировали по ТСХ (этилацетат:гексан; 1:1; Rf=0,47). Растворитель удалили при пониженном давлении. Остаток растворили в EtOAc (300 мл) и промыли 1 М раствором NaHSO4 (3×150 мл), насыщенным водным раствором NaHCO3 (3×150 мл) и насыщенным солевым раствором (2×100 мл). Органический слой высушили при помощи Na2SO4. Высушивающий агент удалили фильтрованием, а органический слой концентрировали на ротационном испарителе. Неочищенную смесь очистили колоночной хроматографией на силикагеле и элюировали при помощи 35-50% EtOAc в гексане с получением соединения 122 (15,50 г, 78,13%). Структуру подтвердили анализом ЖХМС и1Н ЯМР. Масса m/z 589,3 [М+Н]+.
К охлажденному раствору соединения 122 (7,75 г, 13,16 ммоль), растворенного в метаноле (15 мл) добавили раствор LiOH (92,15 ммоль) в воде (20 мл) и ТГФ (10 мл). Реакционную смесь перемешивали при комнатной температуре в течение 45 минут и контролировали по ТСХ (EtOAc : гексан; 1:1). Реакционную смесь концентрирован до половины объема при пониженном давлении. Оставшийся раствор охладили на ледяной бане и нейтрализовали добавлением концентрированной HCl. Реакционную смесь разбавили, экстрагировали EtOAc (120 мл) и промыли насыщенным солевым раствором (100 мл). При стоянии в течение ночи образовалась и осветлилась эмульсия. Органический слой отделили, высушили (Na2SO4), отфильтровали и выпарили с получением Соединения 123 (8,42 г). Избыточную массу вероятно обусловливает остаточная соль. ЖХМС согласовался со структурой. Продукт применили без какой-либо дополнительной очистки. Мол. масса, расчетная: 574,36% мол. масса, найденная: 575,3 [М+Н]+.
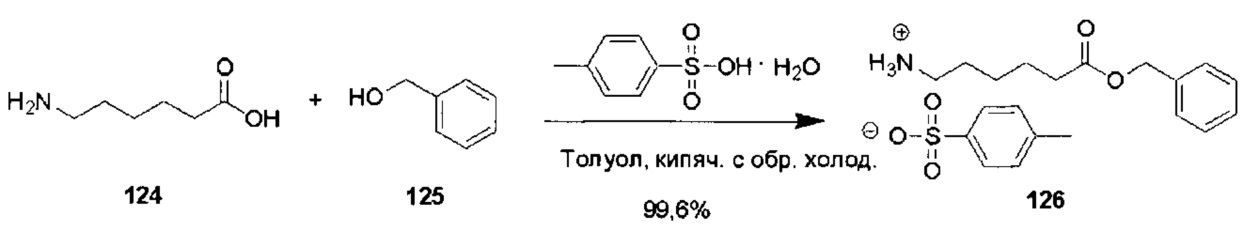
Соединение 126 синтезировали по способу, описанному в литературе (J Am. Chem. Soc. 2011, 133, 958-963).
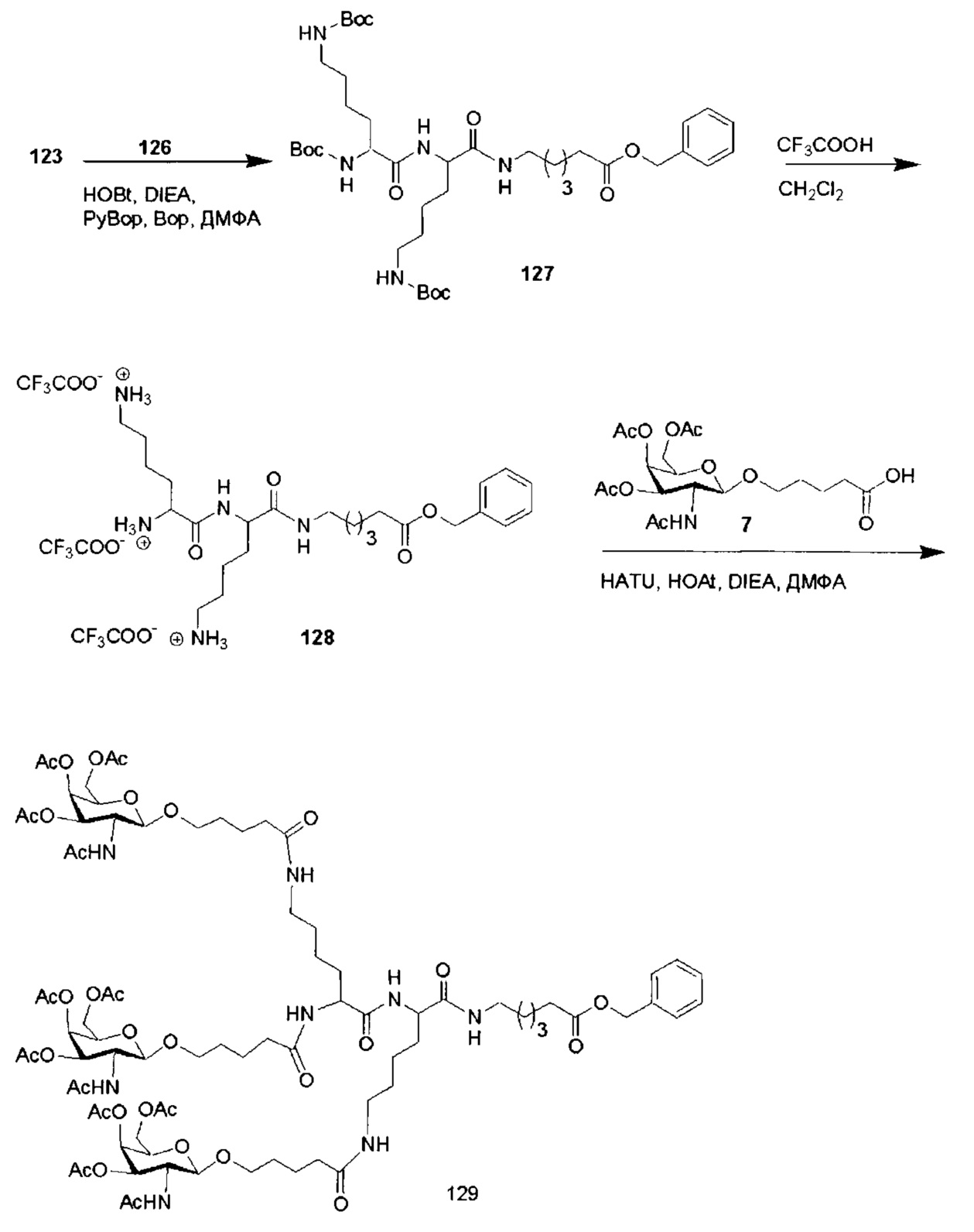
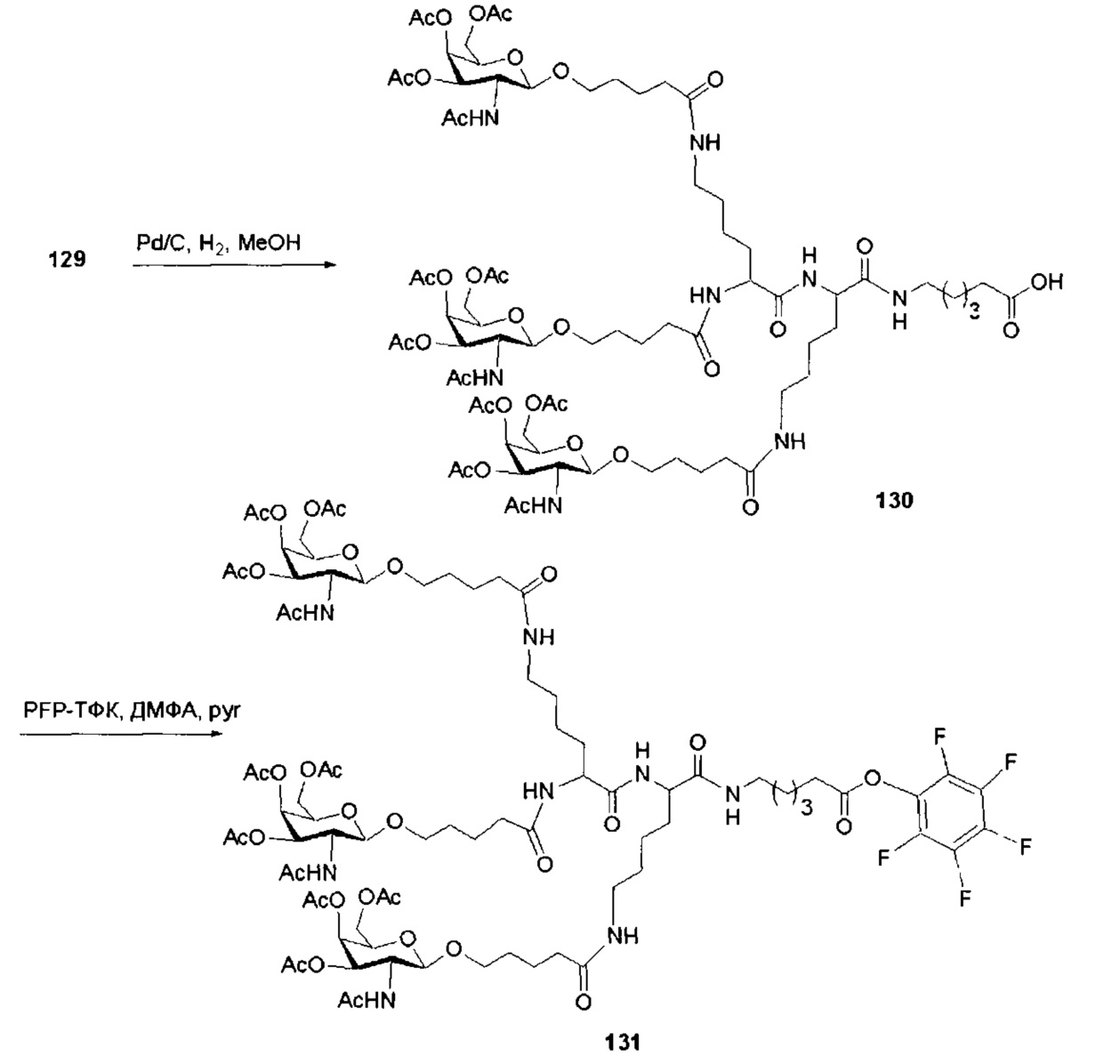
Соединение 123 (7,419 г, 12,91 ммоль), HOBt (3,49 г, 25,82 ммоль) и соединение 126 (6,33 г, 16,14 ммоль) растворили в ДМФА (40 мл), а полученную реакционную смесь охладили на ледяной бане. К этой смеси добавили N,N-диизопропилэтиламин (4,42 мл, 25,82 ммоль), PyBop (8,7 г, 16,7 ммоль), затем связывающий агент Вор (1,17 г, 2,66 ммоль) в атмосфере аргона. Ледяную баню убрали, а раствор оставили нагреваться до комнатной температуры. Реакция завершилась через 1 час, что определили по ТСХ (ДХМ : МеОН : АА; 89:10:1). Реакционную смесь концентрировали при пониженном давлении. Остаток растворили в EtOAc (200 мл) и промыли 1 М раствором NaHSO4 (3×100 mмл), насыщенным водным раствором NaHCO3 (3×100 мл) и насыщенным солевым раствором (2×100 мл). Органическую фазу отделили, высушили (Na2SO4), отфильтровали и концентрировали. Остаток очистили колоночной хроматографией на силикагеле с градиентом от 50% гексанов в EtOAc до 100% EtOAc с получением Соединения 127 (9,4 г) в виде белого пенистого вещества. ЖХМС и1Н ЯМР согласовались со структурой. Масса m/z 778,4 [М+H]+.
Трифторуксусную кислоту (12 мл) добавили к раствору соединения 127 (1,57 г, 2,02 ммоль) в дихлорметане (12 мл) и перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь выпарили совместно с толуолом (30 мл) при пониженном давлении досуха. Полученный остаток два раза совместно выпарили с ацетонитрилом (30 мл) и толуолом (40 мл) с получением Соединения 128 (1,67 г) в виде трифторацетатной соли, и применили его на следующей стадии без дополнительной очистки. ЖХМС и1Н ЯМР согласовались со структурой. Масса m/z 478,2 [М+Н]+.
Соединение 7 (0,43 г, 0,963 ммоль), HATU (0,35 г, 0,91 ммоль) и HOAt (0,035 г, 0,26 ммоль) смешали вместе и высушивали в течение 4 часов над Р2О5 при пониженном давлении в круглодонной колбе, а затем растворили в безводном ДМФА (1 мл) и перемешивали в течение 5 минут. К этой смеси добавили раствор соединения 128 (0,20 г, 0,26 ммоль) в безводном ДМФА (0,2 мл) и добавили N,N-диизопропилэтиламин (0,2 мл). Реакционную смесь перемешивали при комнатной температуре в атмосфере аргона. Реакция завершилась через 30 минут, что определили по ЖХМС и ТСХ (7% МеОН/ДХМ). Реакционную смесь концентрировали при пониженном давлении. Остаток растворили в ДХМ (30 мл) и промыли 1 М раствором NaHSO4 (3×20 мл), насыщенным водным раствором NaHCO3 (3×20 мл) и насыщенным солевым раствором (3×20 мл). Органическую фазу отделили, высушили над Na2SO4, отфильтровали и концентрировали. Остаток очистили колоночной хроматографией на силикагеле, применив 5-15% МеОН в дихлорметане, с получением Соединения 129 (96,6 мг). ЖХМС и1Н ЯМР согласовались со структурой. Масса m/z 883,4 [М+2Н]+.
Соединение 129 (0,09 г, 0,051 ммоль) растворили в метаноле (5 мл) в 20 мл сцинтилляционной пробирке. К нему добавили небольшое количество 10% Pd/C (0,015 мг) и продували реакционный сосуд газообразным Н2. Реакционную смесь перемеривали при комнатной температуре в атмосфере Н2 в течение 18 часов. Реакционную смесь отфильтровали через слой Целита, а слой Целита промыли метанолом. Фильтрат и промывочные растворы слили вместе и концентрировали при пониженном давлении с получением Соединения 130 (0,08 г). ЖХМС и1Н ЯМР согласовались со структурой. Продукт применили без дополнительной очистки. Масса m/z 838,3 [М+2Н]+.
В 10 мл мерную круглодонную колбу добавили соединение 130 (75,8 мг, 0,046 ммоль), 0,37 М раствор пиридина в ДМФА (200 мкл) и установили мешалку. К этому раствору по каплям добавили 0,7 М раствор пентафторфенила трифторацетата в ДМФА (100 мкл) при перемешивании. Реакция завершилась через 1 час, что определили по ЖХМС. Растворитель удалили при пониженном давлении, а остаток растворили в CHCl3 (~ 10 мл). Органический слой обработали NaHSO4 (1 М, 10 мл), насыщенным водным раствором NaHCO3 (10 мл) и насыщенным солевым раствором (10 мл), каждый по три раза. Органическую фазу отделили и высушили над Na2SO4, отфильтровали и концентрировали с получением Соединения 131 (77,7 мг). ЖХМС согласовался со структурой. Применили без дополнительной очистки. Масса m/z 921,3 [М+2Н]+.
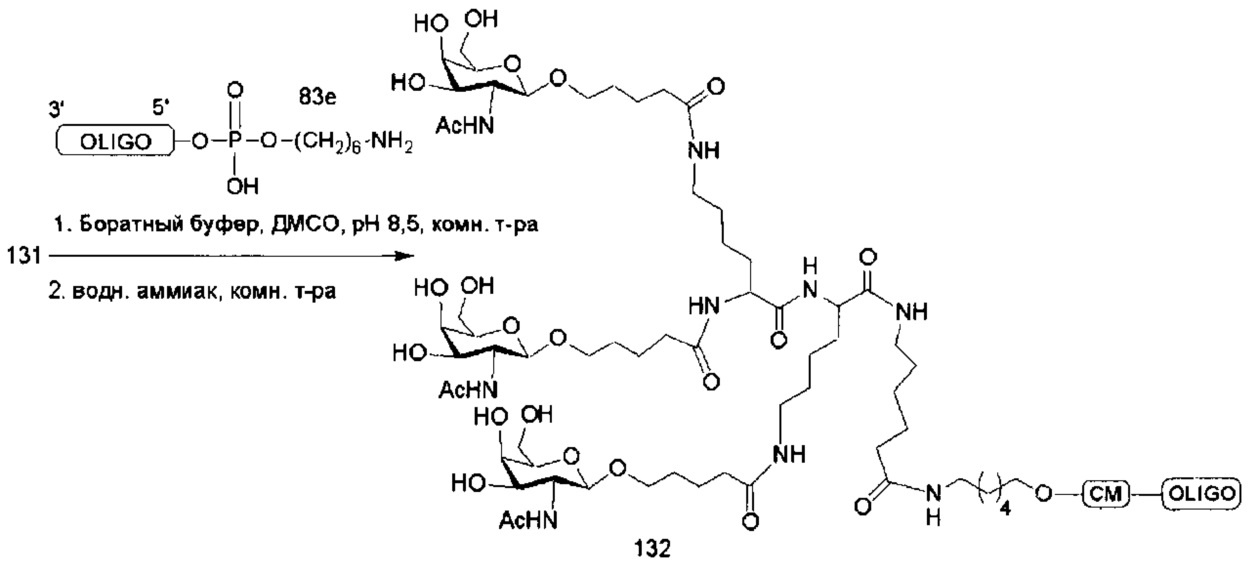
Олигомерное Соединение 132, содержащее конъюгирующую группу GalNAc3-5, получили по общим способам, приведенным в Примере 46. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-5 (GalNAc3-5a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -Р(=O)(ОН)-Ad-Р(=O)(ОН)-.
Структура GalNAc3-5 (GalNAc3-5a-CM-) приведена ниже:
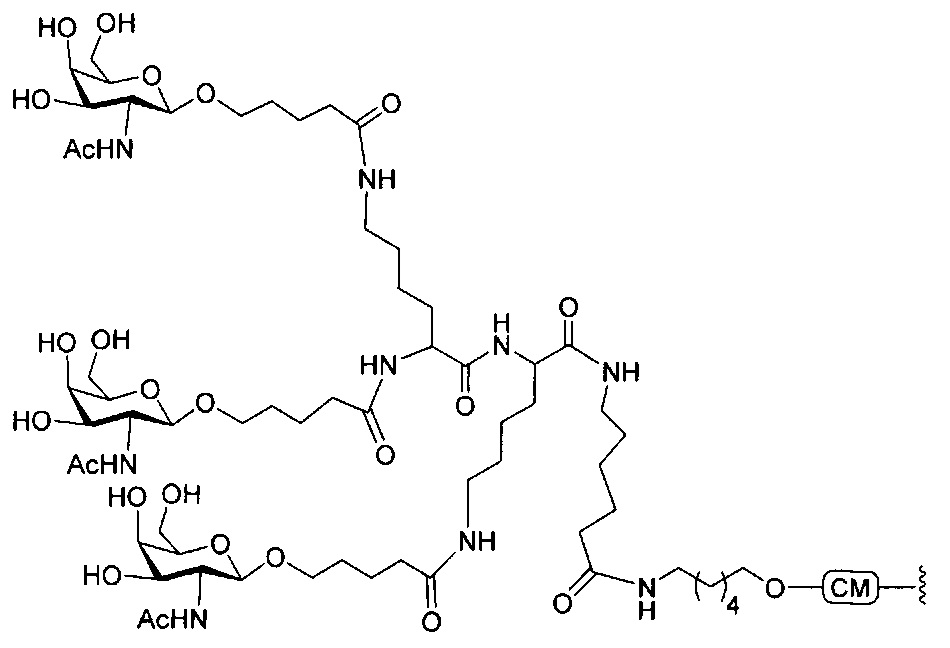
Пример 50. Получение олигонуклеотида 144, содержащего GalNAc4-11
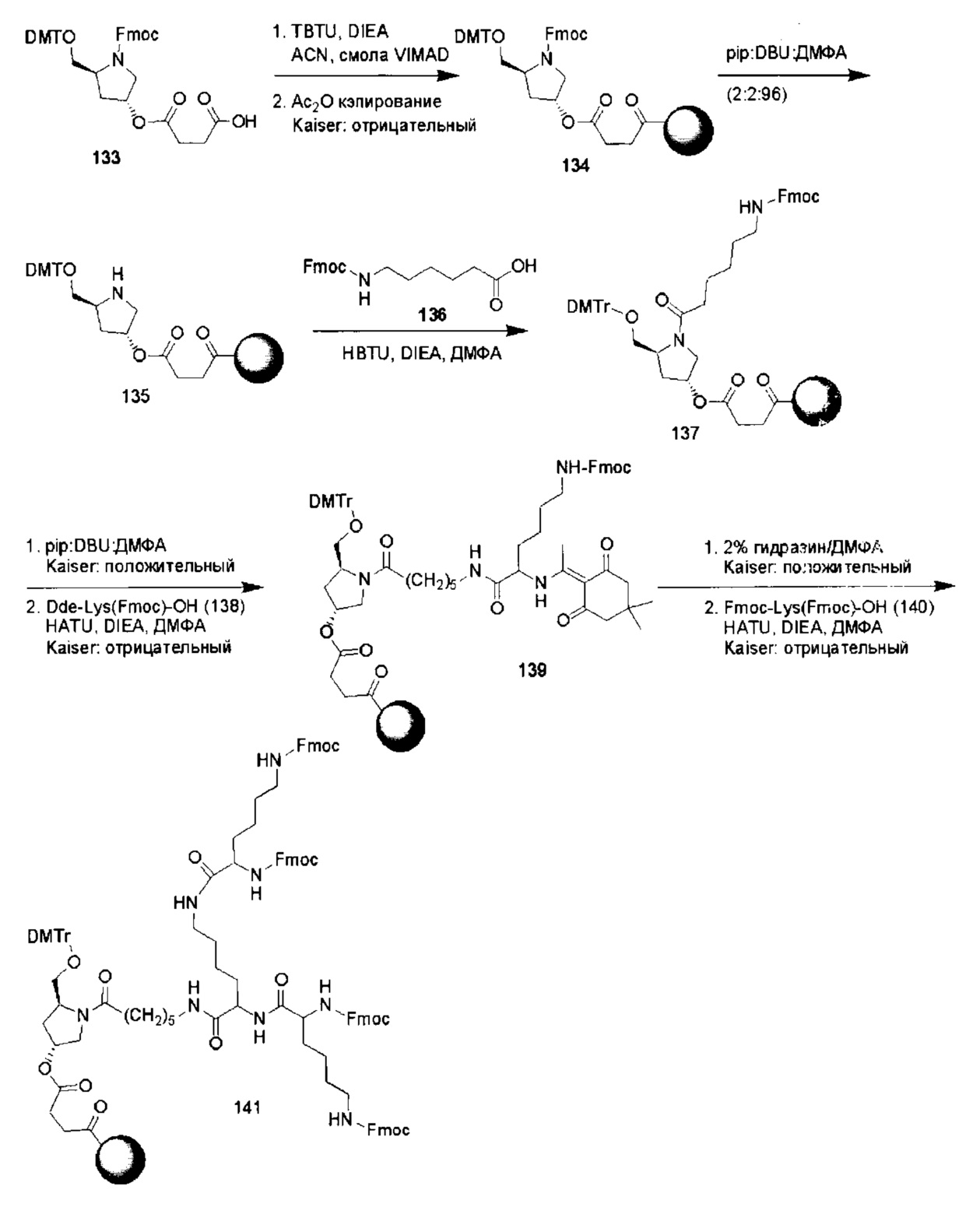
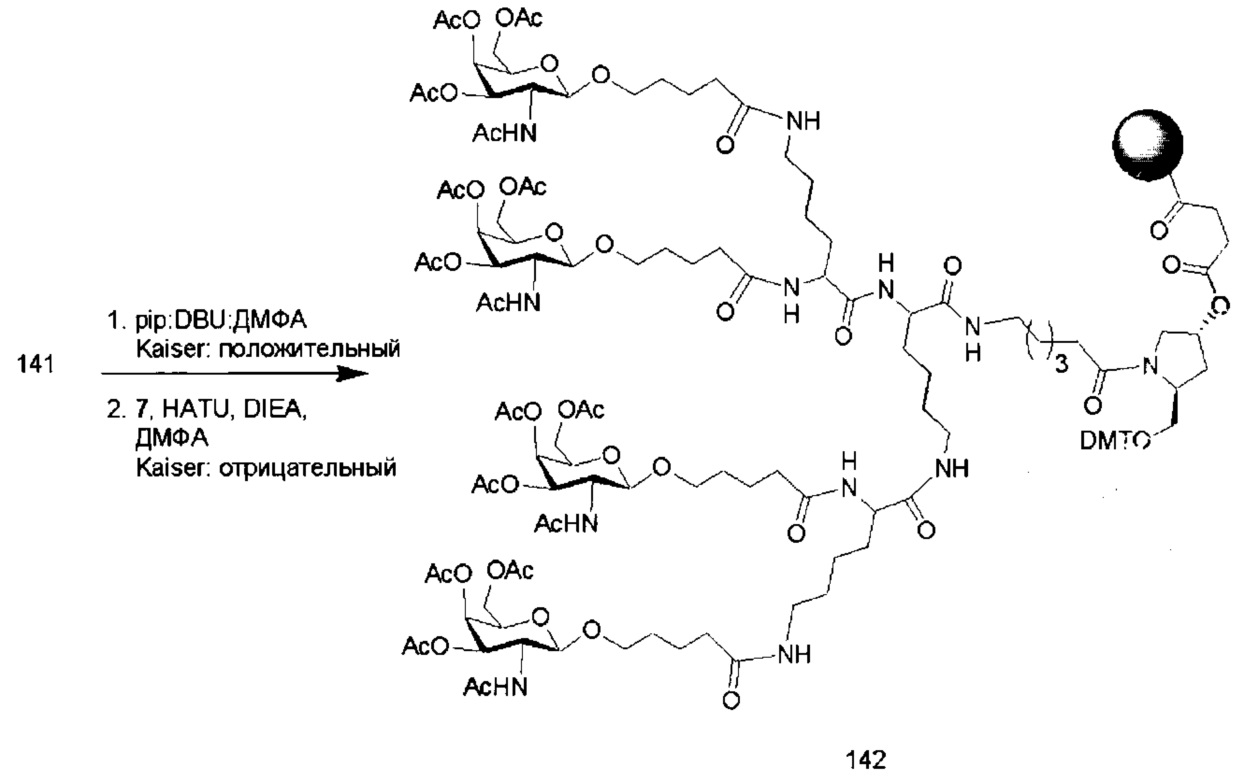
Синтез Соединения 134. В колбу Меррифилда добавили аминометиловую смолу VIMAD (2,5 г, 450 мкмоль/г), которую промыли ацетонитрилом, диметилформамидом, дихлорметаном и ацетонитрилом. Смолу оставили набухать в ацетонитриле (4 мл). Соединение 133 предварительно активировали в 100 мл круглодонной колбе путем добавления 20 (1,0 ммоль, 0,747 г), TBTU (1,0 ммоль, 0,321 г), ацетонитрила (5 мл) и DIEA (3,0 ммоль, 0,5 мл). Этот раствор оставили перемешиваться на 5 минут, а затем добавили в колбу Меррифилда при встряхивании. Суспензию оставили встряхиваться на 3 часа. Реакционную смесь слили, а смолу промыли ацетонитрилом, ДМФА и ДХМ. Заполнение новой смолы количественно определили по измерению абсорбции DMT катиона при 500 нм (коэффициент экстинкции = 76000) в ДХМ, которое составило 238 мкмоль/г. Смолу кэппировали трехкратным суспендированием в растворе уксусного ангидрида в течение десяти минут.
Соединение 141, связанное с твердой подложкой, синтезировали многократным повторением способов твердофазного синтеза пептидов при помощи Fmoc. Взяли небольшое количество твердой подложки и суспендировали в водном растворе аммиака (28-30 масс. %) в течение 6 часов. Расщепленное соединение анализировали по ЖХ-МС и наблюдали, что масса согласуется со структурой. Масса m/z 1063,8 [М+2Н]+.
Соединение 142, связанное с твердой подложкой, синтезировали по способам твердофазного синтеза пептидов.
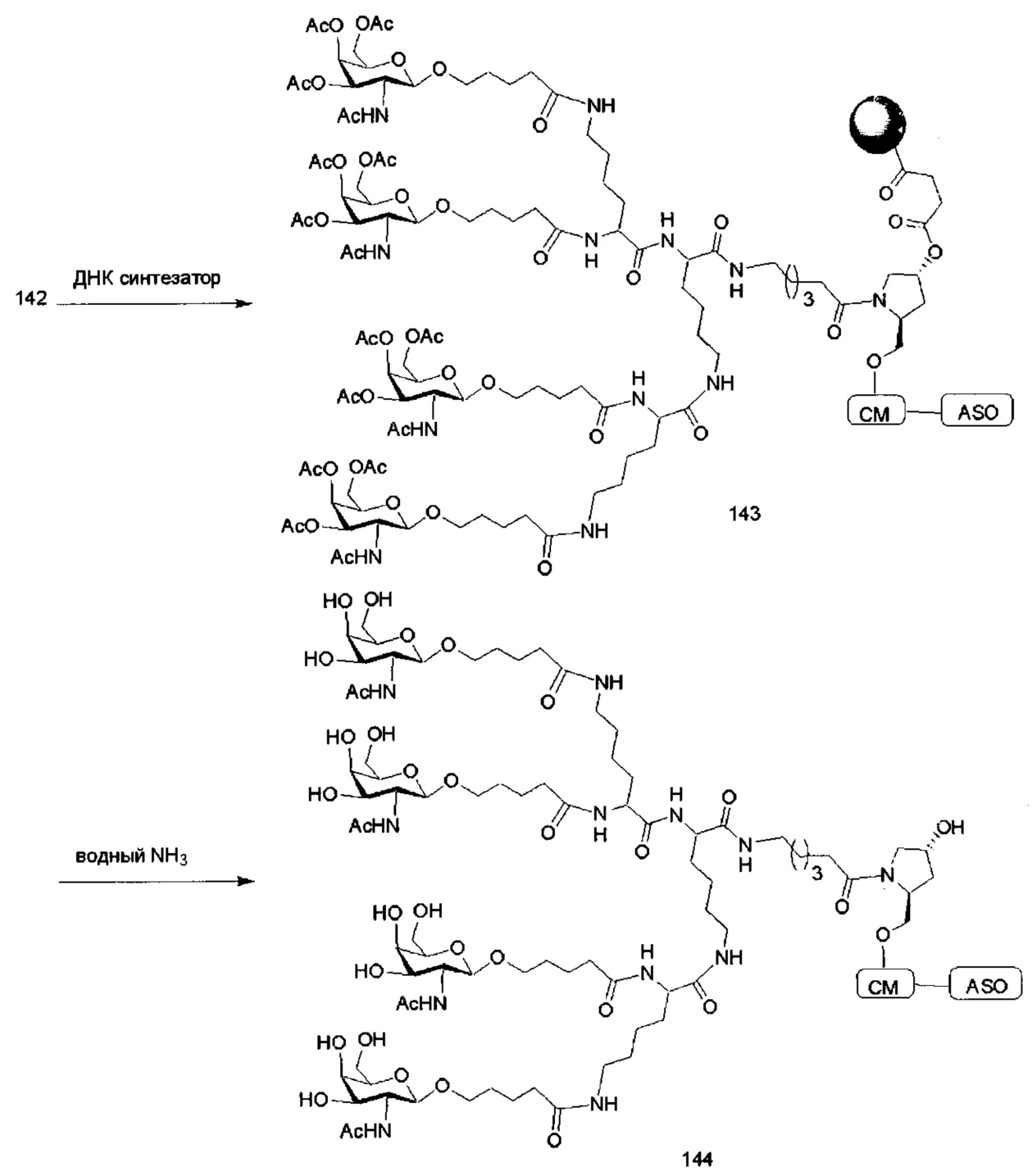
Соединение 143, связанное с твердой подложкой, синтезировали при помощи стандартного твердофазного синтеза на ДНК синтезаторе.
Соединение 143, связанное с твердой подложкой, суспендировали в водном аммиаке (28-30 масс. %) и нагревали при 55°С в течение 16 часов. Раствор охладили, а твердую подложку отфильтровали. Фильтрат концентрировали, а остаток растворили в воде и очистили при помощи ВЭЖХ на сильной анионообменной колонке. Фракции, содержащие соединение 144 полной длины, слили вместе и обессолили. Полученное GalNAc4-11-конъюгированное олигомерное соединение анализировали при помощи ЖХ-МС и наблюдали, что масса согласуется со структурой.
Кластерная часть GalNAc4 конъюгирующие группы GalNAc4-11 (GalNAc4-11а) может быть комбинирована с любым расщепляемым фрагментом с получением различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-.
Структура GalNAc4-11 (GalNAc4-11а-СМ) приведена ниже:
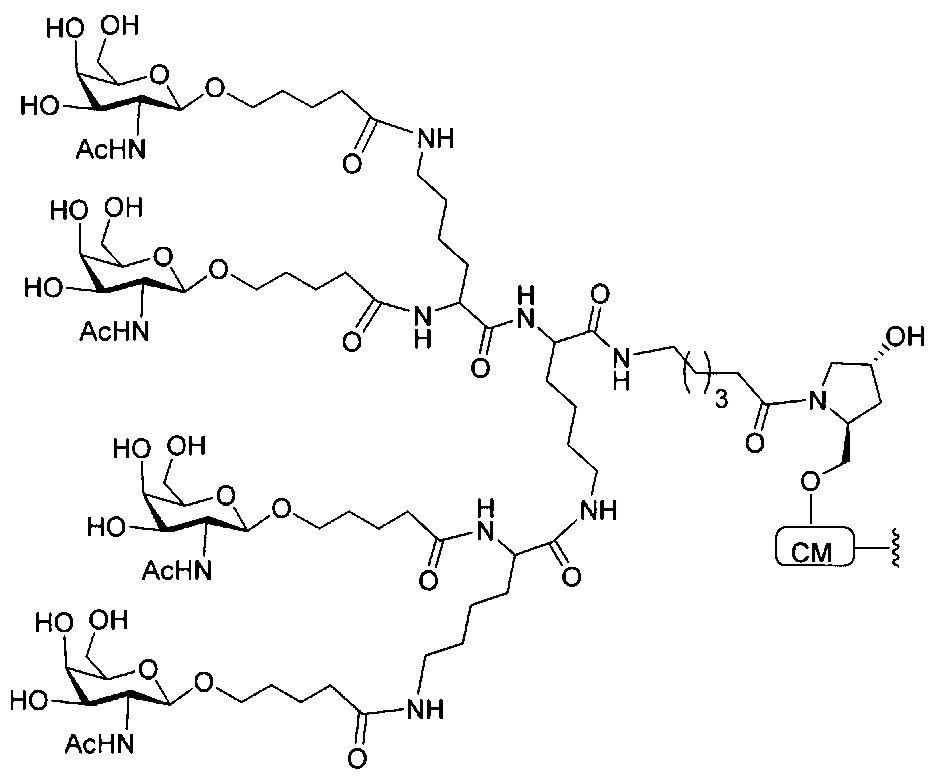
Пример 51. Получение олигонуклеотида 155, содержащего GalNAc3-6
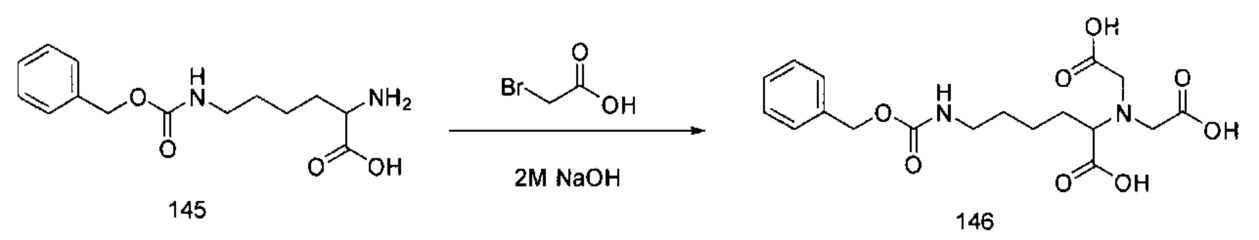
Соединение 146 синтезировали так, как описано в литературе (Analytical Biochemistry 1995, 229, 54-60).
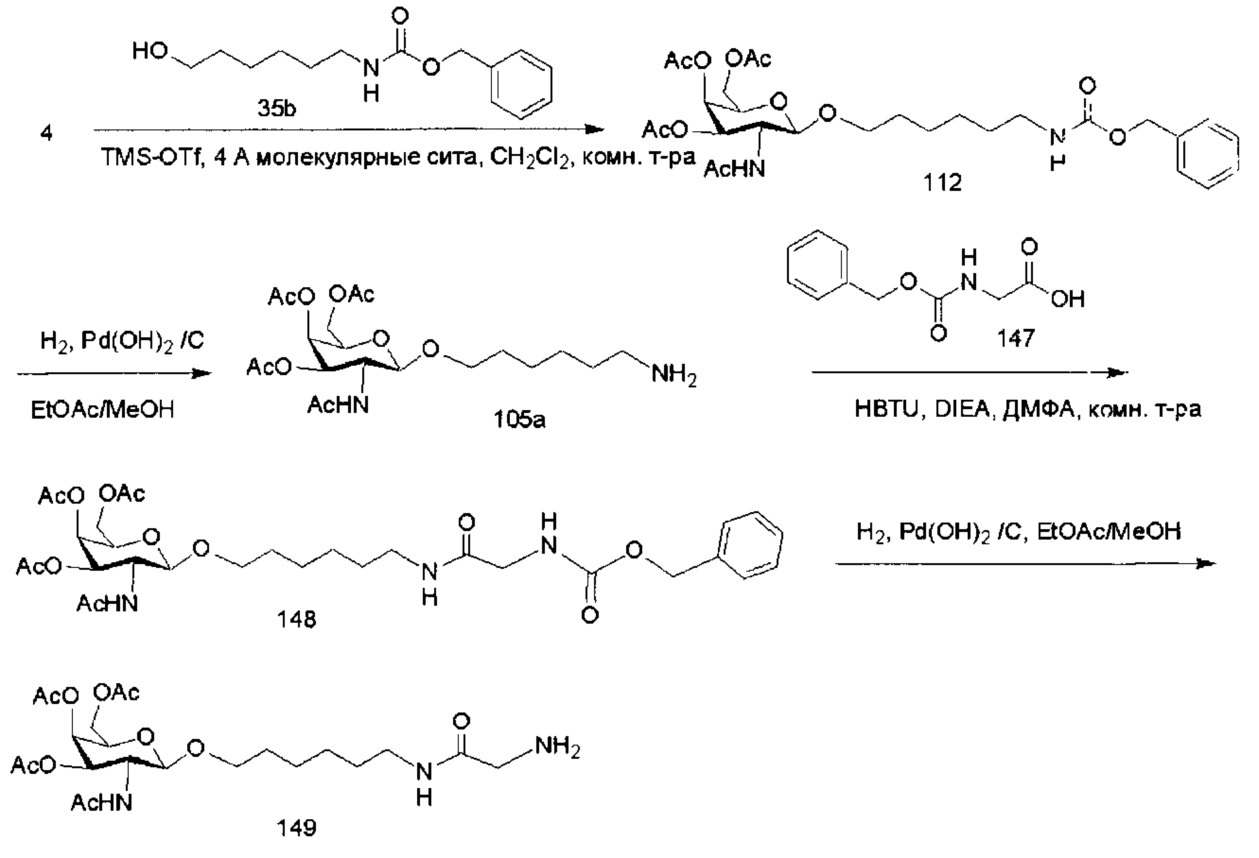
Соединение 4 (15 г, 45,55 ммоль) и соединение 35b (14,3 грамм, 57 ммоль) растворили в CH2Cl2 (200 мл). Добавили активированные молекулярные сита (4 Å, 2 г, порошкообразные) и оставили реакционную смесь перемешиваться в течение 30 минут в атмосфере азота. Добавили TMS-OTf (4,1 мл, 22,77 ммоль) и оставили реакционную смесь перемешиваться при комнатной температуре в течение ночи. После завершения реакции смесь погасили, вылив в насыщенный водный раствор NaHCO3 (500 мл) с дробленым льдом (~ 150 г). Органический слой отделили, промыли насыщенным солевым раствором, высушили над MgSO4, отфильтровали и концентрировали до оранжевого маслянистого вещества при пониженном давлении. Неочищенный материал очистили колоночной хроматографией на силикагеле и элюировали 2-10% МеОН в CH2Cl2 с получением Соединения 112 (16,53 г, 63%). Данные ЖХМС и1Н ЯМР согласовались с предполагаемым соединением.
Соединение 112 (4,27 г, 7,35 ммоль) растворили в 1:1 МеОН/EtOAc (40 мл). Реакционную смесь очистили пропусканием потока аргона через раствор в течение 15 минут. Добавили катализатор Перлмана (гидроксид палладия на углероде, 400 мг) и пропускали через раствор газообразный водород в течение 30 минут. После завершения (ТСХ, 10% МеОН в CH2Cl2, и ЖХМС), катализатор удалили фильтрованием через слой целита. Фильтрат концентрировали на ротационном испарителе и быстро высушили под высоким вакуумом с получением Соединения 105а (3,28 г). Данные ЖХМС и 1Н ЯМР согласовались с желаемым продуктом.
Соединение 147 (2,31 г, 11 ммоль) растворили в безводном ДМФА (100 мл). Добавили N,N-диизопропилэтиламин (DIEA, 3,9 мл, 22 ммоль), затем HBTU (4 г, 10,5 ммоль). Реакционную смесь оставили перемешиваться в течение ~15 минут под азотом. К этой смеси добавили раствор соединения 105а (3,3 г, 7,4 ммоль) в сухом ДМФА и перемешивали в течение 2 часов в атмосфере азота. Реакционную смесь разбавили EtOAc и промыли насыщенным водным раствором NaHCO3 и насыщенным солевым раствором. Органическою фазу отделили, высушили (MgSO4), отфильтровали и концентрировали до оранжевого сиропообразного вещества. Неочищенный материал очистили колоночной хроматографией с 2-5% МеОН в CH2Cl2 с получением Соединения 148 (3,44 г, 73%). Данные ЖХМС и1Н ЯМР согласовались с предполагаемым продуктом.
Соединение 148 (3,3 г, 5,2 ммоль) растворили в 1:1 МеОН/EtOAc (75 мл). Реакционную смесь очистили пропусканием потока аргона через раствор в течение 15 минут. Добавили катализатор Перлмана (гидроксид палладия на углероде (350 мг). Через раствор продували газообразный водород в течение 30 минут. После завершения (ТСХ, 10% МеОН в ДХМ, и ЖХМС), катализатор удалили фильтрованием через слой целита. Фильтрат концентрировали на ротационном испарителе и быстро высушили под высоким вакуумом с получением Соединения 149 (2,6 г). Данные ЖХМС согласовались с желаемым продуктом. Остаток растворили в сухом ДМФА (10 мл) и сразу применили на следующей стадии.
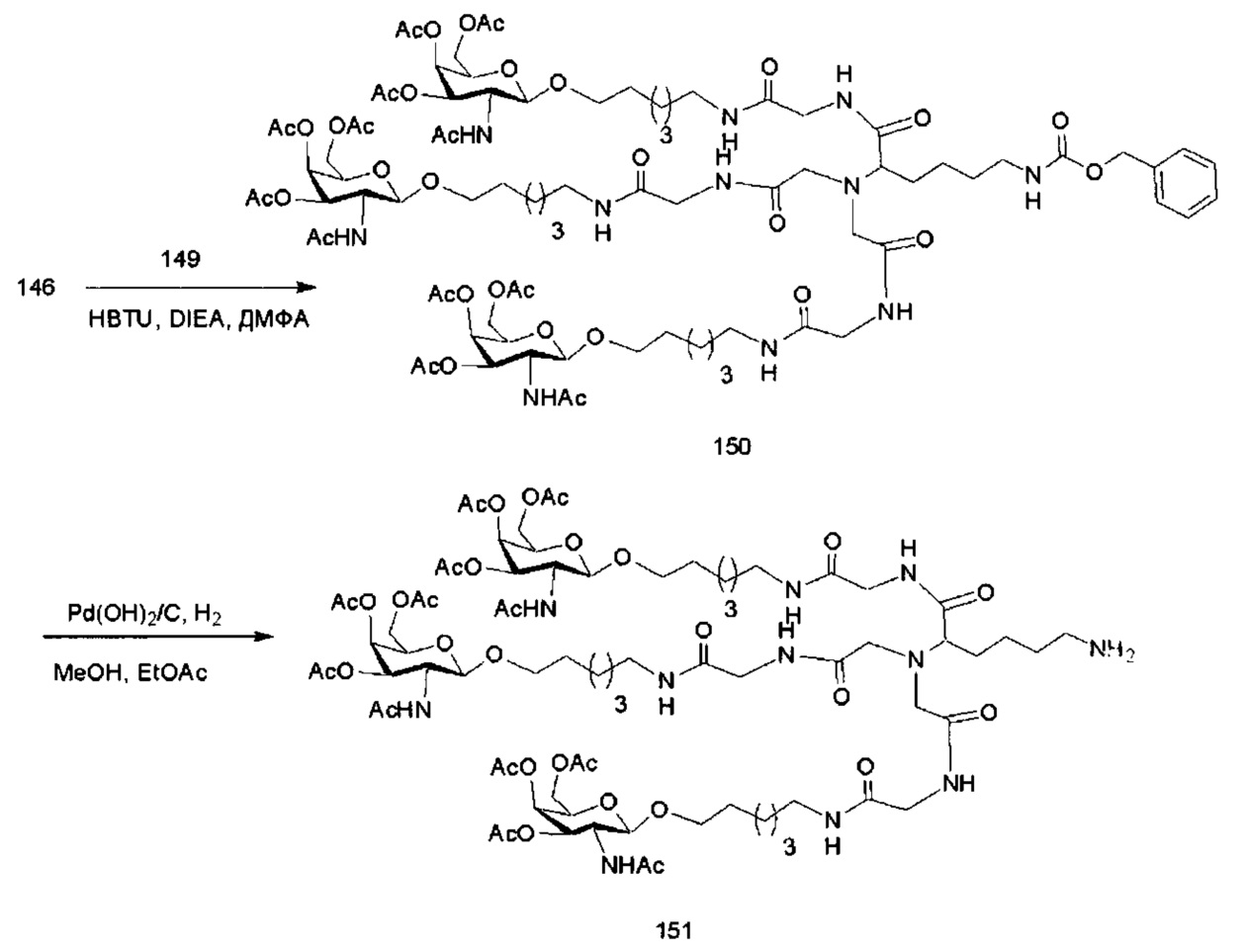
Соединение 146 (0,68 г, 1,73 ммоль) растворили в сухом ДМФА (20 мл). К нему добавили DIEA (450 мкл, 2,6 ммоль, 1,5 экв.) и HBTU (1,96 г, 0,52 ммоль). Реакционную смесь оставили перемешиваться в течение 15 минут при комнатной температуре под азотом. Добавили раствор соединения 149 (2,6 г) в безводном ДМФА (10 мл). рН реакционной смеси довели до рН=9-10 добавлением DIEA (при необходимости). Реакционную смесь оставили перемешиваться при комнатной температуре под азотом в течение 2 часов. После завершения реакции смесь разбавили EtOAc (100 мл) и промыли насыщенным водным раствором NaHCO3, затем насыщенным солевым раствором. Органическую фазу отделили, высушили над MgSO4, отфильтровали и концентрировали. Остаток очистили колоночной хроматографией на силикагеле и элюировали 2-10% МеОН в CH2Cl2 с получением Соединения 150 (0,62 г, 20%). Данные ЖХМС и1Н ЯМР согласовались с желаемым продуктом.
Соединение 150 (0,62 г) растворили в 1:1 МеОН/EtOAc (5 л). Реакционную смесь очистили пропусканием потока аргона через раствор в течение 15 минут. Добавили катализатор Перлмана (гидроксид палладия на углероде (60 мг). Через раствор продували газообразный водород в течение 30 минут. После завершения (ТСХ, 10% МеОН в ДХМ, и ЖХМС), катализатор удалили фильтрованием (тефлоновый фильтр с переходной канюлей шприца, 0,45 мкм). Фильтрат концентрировали на ротационном испарителе и быстро высушили под высоким вакуумом с получением Соединения 151 (0,57 г). Данные ЖХМС согласовались с желаемым продуктом. Продукт растворили в 4 мл сухого ДМФА и сразу применили на следующей стадии.
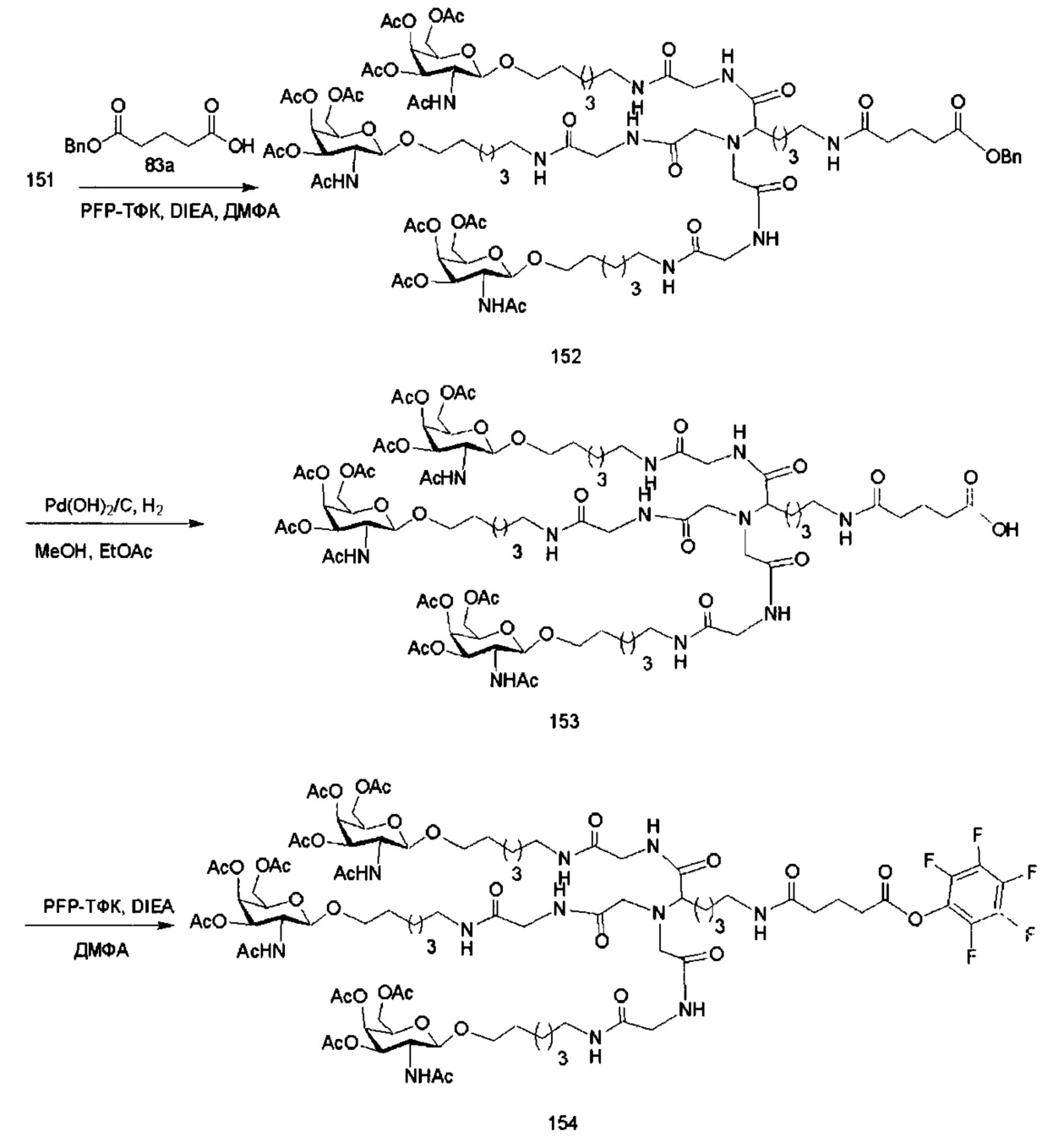
Соединение 83а (0,11 г, 0,33 ммоль) растворили в безводном ДМФА (5 мл) и добавили N,N-диизопропилэтиламин (75 мкл, 1 ммоль) и PFP-ТФК (90 мкл, 0,76 ммоль). При соприкосновении реакционная смесь стала пурпурной и постепенно изменила цвет на оранжевый в течение следующих 30 минут. Ход реакции контролировали по ТСХ и ЖХМС. После завершения (образования эфира PFP) добавили раствор соединения 151 (0,57 г, 0,33 ммоль) в ДМФА. рН реакционной смеси довели до рН=9-10 добавлением N,N-диизопропилэтиламина (при необходимости). Реакционную смесь перемешивали под азотом в течение ~30 минут. После завершения реакции большую часть растворителя удалили при пониженном давлении. Остаток разбавили CH2Cl2 и промыли насыщенным водным раствором NaHCO3, затем насыщенным солевым раствором. Органическую фазу отделили, высушили над MgSO4, отфильтровали и концентрировали до оранжевого сиропообразного вещества. Остаток очистили колоночной хроматографией на силикагеле (2-10% МеОН в CH2Cl2) с получением Соединения 152 (0,35 г, 55%). Данные ЖХМС и1Н ЯМР согласовались с желаемым продуктом.
Соединение 152 (0,35 г, 0,182 ммоль) растворили в 1:1 МеОН/EtOAc (10 мл). Реакционную смесь очистили пропусканием потока аргона через раствор в течение 15 мину г.Добавили катализатор Перлмана (гидроксид палладия на углероде (35 мг). Через раствор продували газообразный водород в течение 30 минут. После завершения (ТСХ, 10% МеОН в ДХМ, и ЖХМС), катализатор удалили фильтрованием (тефлоновый фильтр с переходной канюлей шприца, 0,45 мкм). Фильтрат концентрировали на ротационном испарителе и быстро высушили под высоким вакуумом с получением Соединения 153 (0,33 г, количественно). Данные ЖХМС согласовались с желаемым продуктом.
Соединение 153 (0,33 г, 0,18 ммоль) растворили в безводном ДМФА (5 мл) при перемешивании под азотом. К нему добавили N,N-диизопропилэтиламин (65 мкл, 0,37 ммоль) и PFP-ТФК (35 мкл, 0,28 ммоль). Реакционную смесь перемешивали под азотом в течение -30 минут. При соприкосновении реакционная смесь стала пурпурной и постепенно изменила цвет на оранжевый. рН реакционной смеси поддерживали при рН=9-10 добавлением дополнительного количества N,N-диизопропилэтиламина. Ход реакции контролировали по ТСХ и ЖХМС. После завершения реакции большую часть растворителя удалили при пониженном давлении. Остаток разбавили CH2Cl2 (50 мл) и промыли насыщенным водным раствором NaHCO3, затем насыщенным солевым раствором. Органический слой отделили, высушили над MgSO4, отфильтровали и концентрировали до оранжевого сиропообразного вещества. Остаток очистили колоночной хроматографией и элюировали 2-10% МеОН в CH2Cl2 с получением Соединения 154 (0,29 г, 79%). Данные ЖХМС и1Н ЯМР согласовались с желаемым продуктом.
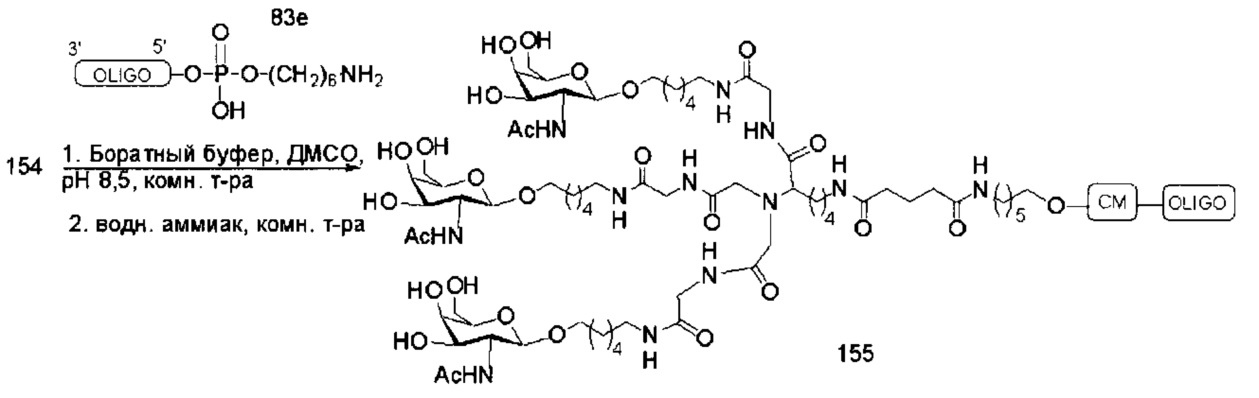
Олигомерное Соединение 155, содержащее конъюгирующую группу GalNAc3-6, получили по общим способам, приведенным в Примере 46. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-6 (GalNAc3-6a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-Р(=O)(ОН)-.
Структура GalNAc3-6 (GalNAc3-6a-CM-) приведена ниже:
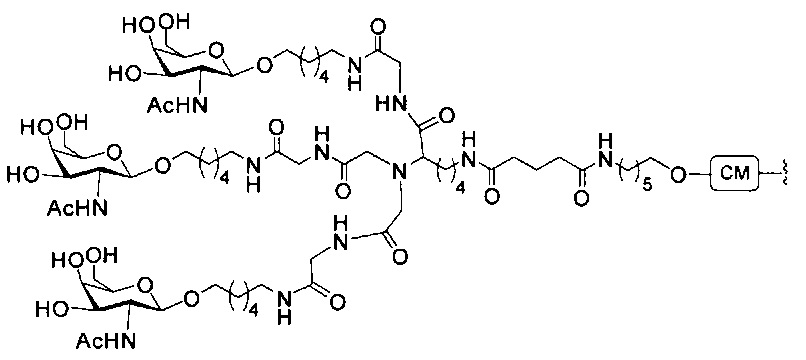
Пример 52. Получение олигонуклеотида 160, содержащего GalNAc3-9
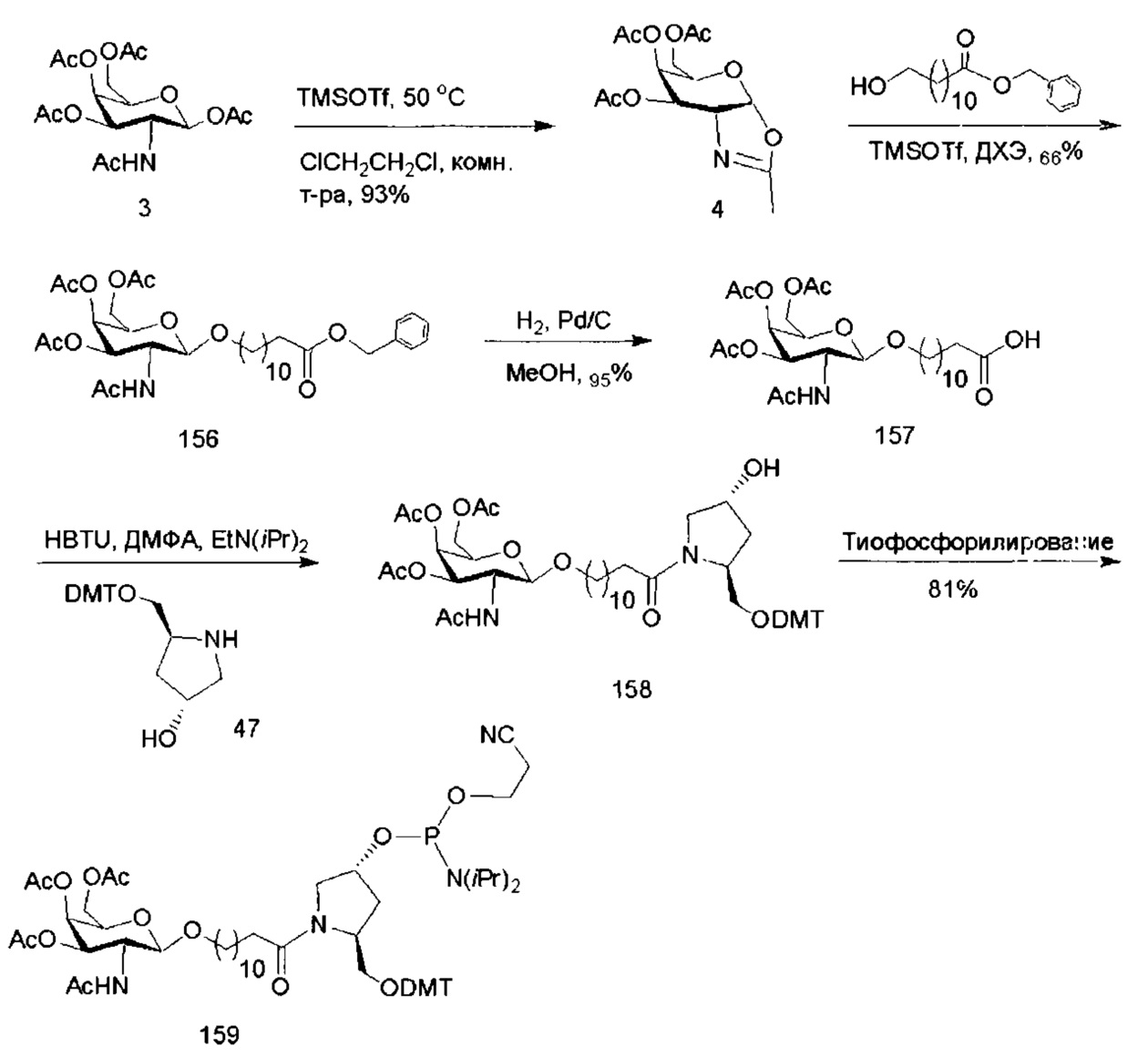
Соединение 156 синтезировали по способу, описанному в литературе (J. Med. Chem. 2004, 47, 5798-5808).
Соединение 156 (18,60 г, 29,28 ммоль) растворили в метаноле (200 мл). Добавили палладий на углероде (6,15 г, загрузка 10 масс. % (в пересчете на сухое вещество), матрица из порошкообразного углерода, влажный). Реакционную смесь перемешивали при комнатной температуре в атмосфере водорода в течение 18 часов. Реакционную смесь отфильтровали через слой целита и тщательно промыли слой целита метанолом. Объединенный фильтрат промыли и концентрировали досуха. Остаток очистили колоночной хроматографией на силикагеле и элюировали 5-10% метанола в дихлорметане с получением Соединения 157 (14,26 г, 89%). Масса m/z 544,1 [М-Н]-.
Соединение 157 (5 г, 9,17 ммоль) растворили в безводном ДМФА (30 мл). Добавили HBTU (3,65 г, 9,61 ммоль) и N,N-диизопропилэтиламин (13,73 мл, 78,81 ммоль) и перемешивали реакционную смесь при комнатной температуре в течение 5 минут. К нему добавили раствор соединения 47 (2,96 г, 7,04 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 8 часов. Реакционную смесь вылили в насыщенный водный раствор NaHCO3. Смесь экстрагировали этилацетатом, а органический слой промыли насыщенным солевым раствором и высушили (Na2SO4), отфильтровали и выпарили. Полученный остаток очистили колоночной хроматографией на силикагеле и элюировали 50% этилацетатом в гексане с получением Соединения 158 (8,25 г, 73,3%). Структуру подтвердили анализом МС и1Н ЯМР.
Соединение 158 (7,2 г, 7,61 ммоль) высушили над Р2О5 при пониженном давлении. Высушенное соединение растворили в безводном ДМФА (50 мл). К нему добавили 1Н-тетразол (0,43 г, 6,09 ммоль) и N-метилимидазол (0,3 мл, 3,81 ммоль), и цианоэтил-N,N,N',N'-тетраизопропил-фосфородиамидит (3,65 мл, 11,50 ммоль). Реакционную смесь перемешивали в атмосфере аргона в течение 4 часов. Реакционную смесь разбавили этилацетатом (200 мл). Реакционную смесь промыли насыщенным раствором NaHCO3 и насыщенным солевым раствором. Органическую фазу отделили, высушили (Na2SO4), отфильтровали и выпарили. Остаток очистили колоночной хроматографией на силикагеле и элюировали 50-90% этилацетатом в гексане с получением Соединения 159 (7,82 г, 80,5%). Структуру подтвердили анализом ЖХМС и31Р ЯМР.
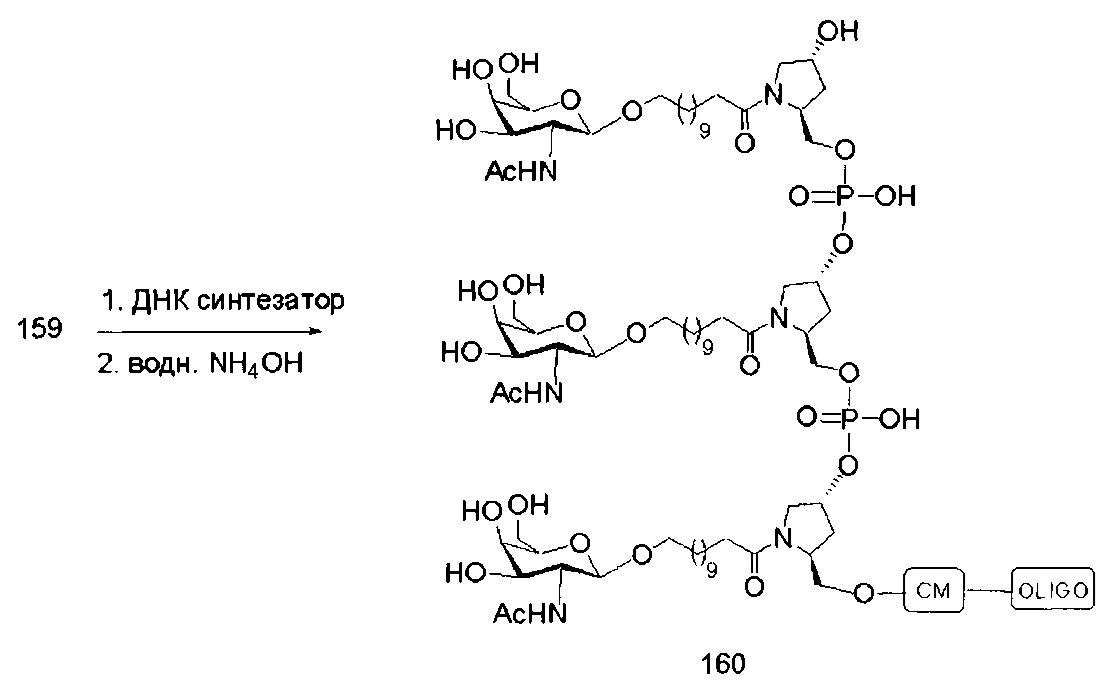
Олигомерное соединение 160, содержащее конъюгирующую группу GalNAc3-9, получили по стандартным способам синтеза олигонуклеотидов. Три единицы соединения 159 связали с твердой подложкой, затем с фосфорамидитами нуклеотидов. В результате обработки защищенного олигомерного соединения водным аммиаком получили соединение 160. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-9 (GalNAc3-9a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-. Структура GalNAc3-9 (GalNAc3-9a-CM) приведена ниже:
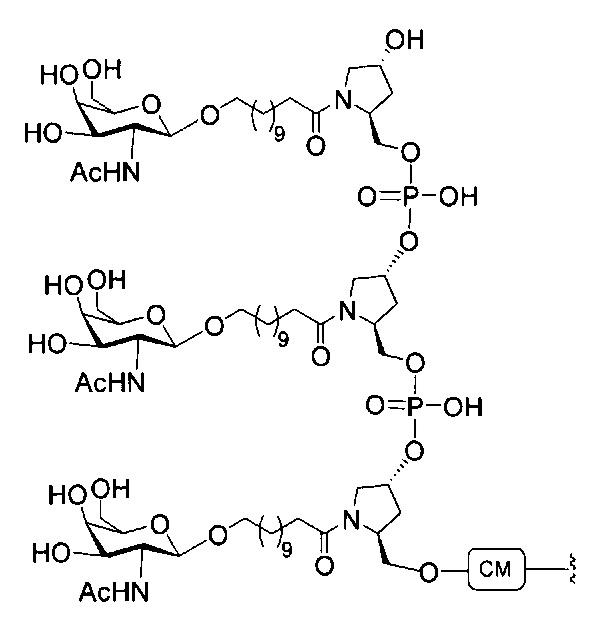
Пример 53. Альтернативный способ получения Соединения 18 (GalNAc3-1a и GalNAc3-3а)
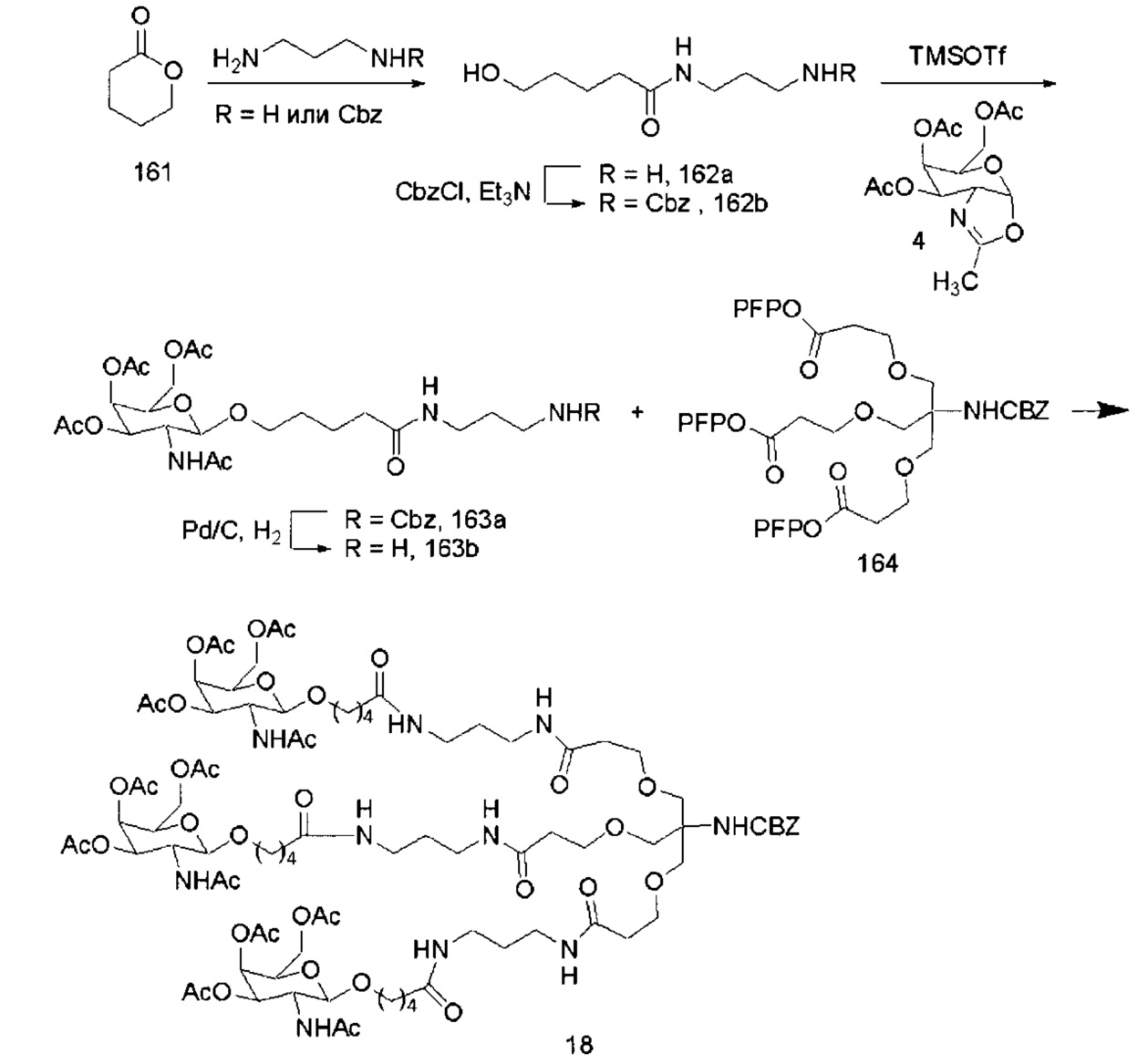
Выполнили реакцию лактона 161 с диаминопропаном (3-5 экв.) или моно-Вос-защищенным диаминопропаном (1 экв.) с получением спирта 162а или 162b. При применении для описанной выше реакции незащищенного пропандиамина, избыток диамина удалили выпариванием под высоким вакуумом, а свободную аминогруппу в 162а защитили при помощи CbzCl с получением 162b в виде белого твердого вещества после очистки колоночной хроматографией. Спирт 162b затем взаимодействовал с соединением 4 в присутствии TMSOTf с получением 163а, которое преобразовали в 163b путем снятия Cbz группы при помощи каталитического гидрирования. Пентафторфениловый (PFP) эфир 164 получили взаимодействием трехкислотного соединения 113 (см. Пример 48) с PFP-ТФК (3,5 экв.) и пиридином (3,5 экв.) в ДМФА (от 0,1 до 0,5 М). Триэфир 164 непосредственно взаимодействовал с амином 163b (3-4 экв.) и DIPEA (3-4 экв.) с получением Соединения 18. Приведенный выше способ значительно облегчает очистку промежуточных соединений и минимизирует образование побочных продуктов, которые образуются при применении способа, описанного в Примере 4.
Пример 54. Альтернативный способ получения Соединения 18 (GalNAc3-1a и GalNAc3-3а)
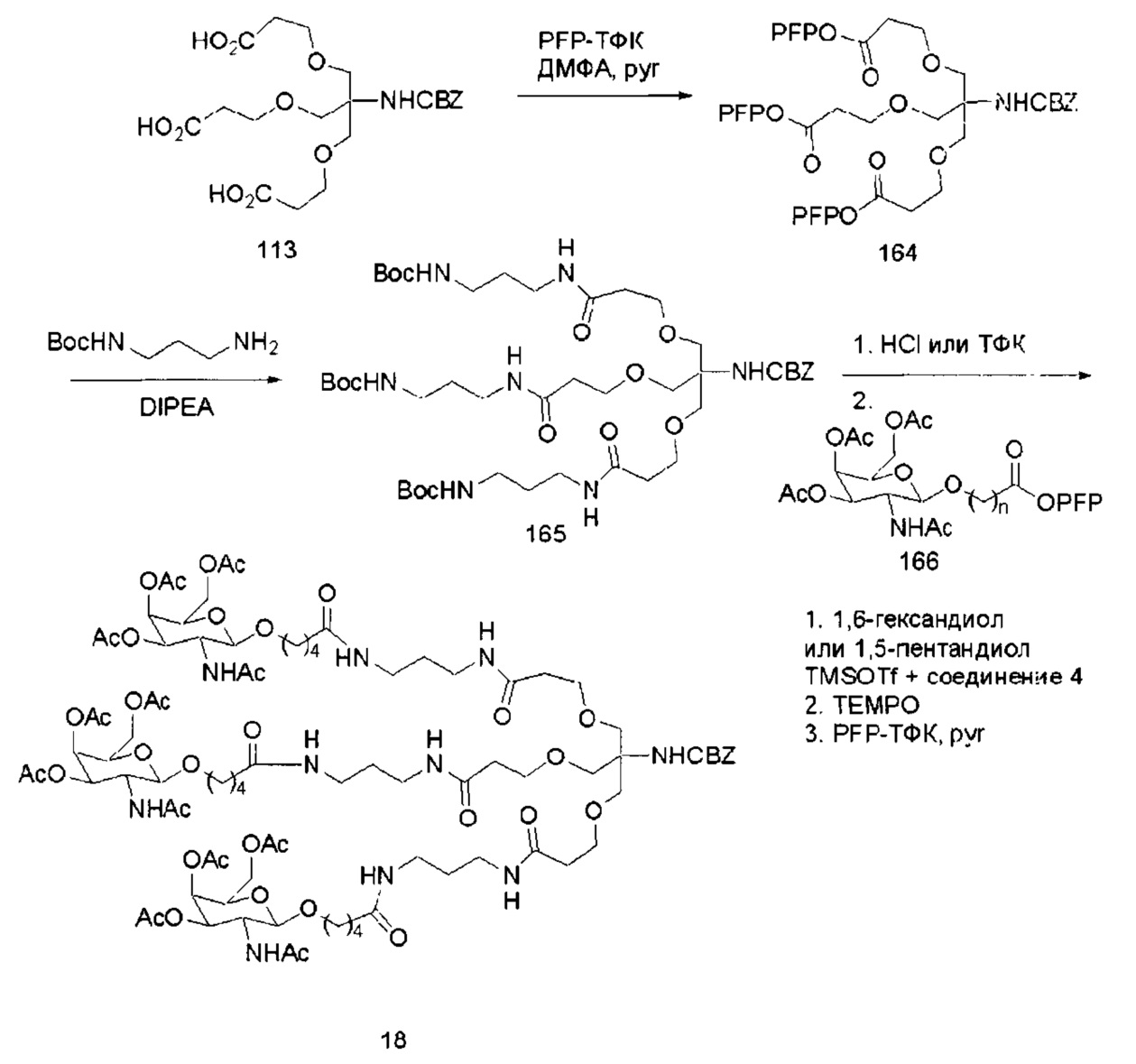
Три-PFP эфир 164 получили из кислоты 113 по способу, приведенному выше в Примере 53, выполнили реакцию этого эфира с моно-Вос-защищенным диамином с получением 165 практически с количественным выходом. Вое группы сняли хлористоводородной кислотой или трифторуксусной кислотой с получением триамина, который взаимодействовал с активированной кислотой PFP 166 в присутствии подходящего основания, такого как DIPEA, с получением Соединения 18.
PFP-защищенную кислоту Gal-NAc 166 получили из соответствующей кислоты обработкой PFP-ТФК (1-1,2 экв.) и пиридином (1-1,2 экв.) в ДМФА. Кислоту-предшественник, в свою очередь, получили из соответствующего спирта окислением с применением TEMPO (0,2 экв.) и BAIB в ацетонитриле и воде. Спирт-предшественник получили из сахарного промежуточного соединения 4 взаимодействием с 1,6-гександиолом (или 1,5-гександиолом или другим диолом для других значений n) (2-4 экв.) и TMSOTf, применив условия, описанные ранее в Примере 47.
Пример 55. Дозозависимое исследование олигонуклеотидов, содержащих либо 3', либо 5'-конъюгирующую группу (сравнение GalNAc3-1, 3, 8 и 9), нацеленных на SRB-1, in vivo
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей. Неконъюгированный ISIS 353382 включили в качестве стандарта. Каждая из различных конъюгирующих групп GalNAc3 быта присоединена либо к 3', либо к 5'-концу соответствующего олигонуклеотида при помощи фосфодиэфир-связанного 2'-дезоксиаденозинового нуклеозида (расщепляемый фрагмент).


Заглавные буквы указывают азотистое основание для каждого нуклеозида, аmC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатную межнуклеозидную связь(PS); «о» означает фосфодиэфирную межнуклеозидную связь(РО); и «o'» означает -O-Р(=O)(ОН)-. Конъюгирующие группы выделены жирным шрифтом.
Структура GalNAc3-1a показана ранее в Примере 9. Структура GalNAc3-9 показана ранее в Примере 52. Структура GalNAc3-3 показана ранее в Примере 39. Структура GalNAc3-8 показана ранее в Примере 47.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, приведенной ниже, соединения ISIS 353382, 655861, 664078, 661161, 665001 или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часов после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, приведены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 40, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Действительно, антисмысловые олигонуклеотиды, содержащие фосфодиэфир-связанные конъюгаты GalNAc3-1 и GalNAc3-9 на 3'-конце (ISIS 655861 и ISIS 664078), а также конъюгаты GalNAc3-3 и GalNAc3-8, связанные на 5'-конце (ISIS 661161 и ISIS 665001) демонстрируют существенное улучшение эффективности, по сравнению с неконъюгированным антисмысловым олигонуклеотидом (ISIS 353382). Кроме того, ISIS 664078, содержащий конъюгат GalNAc3-9 на 3'-конце, был по существу настолько же эффективным, как ISIS 655861, который содержит конъюгат GalNAc3-1 на 3'-конце. 5'-конъюгированные антисмысловые олигонуклеотиды, ISIS 661161 и ISIS 665001, содержащие GalNAc3-3 или GalNAc3-9, соответственно, обладают повышенной эффективностью, по сравнению с 3'-конъюгированными антисмысловыми соединениями (ISIS 655861 и ISIS 664078).
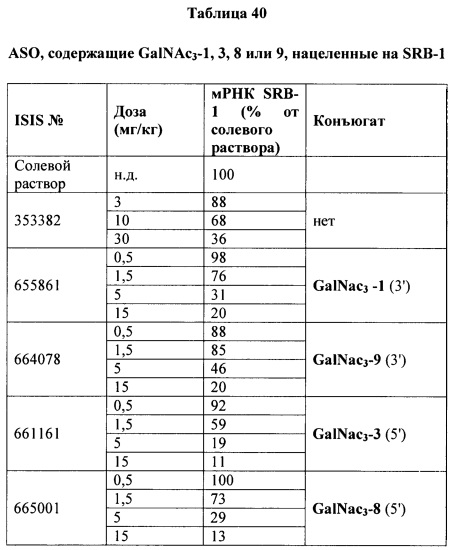
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, применяя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором. Значения ALT, AST, общего билирубина и АМК приведены ниже в таблице.
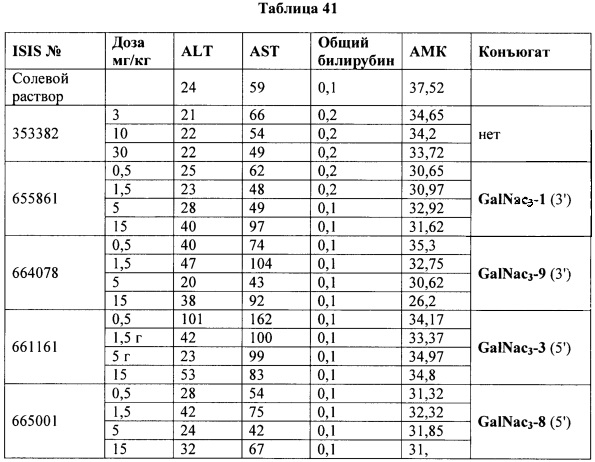
Пример 56. Дозозависимое исследование олигонуклеотидов, содержащих либо 3', либо 5'-конъюгирующую группу (сравнение GalNAc3-1, 2, 3, 5, 6, 7 и 10), нацеленных на SRB 1, in vivo
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей. Неконъюгированный ISIS 353382 включили в качестве стандарта. Каждая из различных конъюгирующих групп GalNAc3 была присоединена к 5'-концу соответствующего олигонуклеотида фосфодиэфир-связанным 2'-дезоксиаденозиновым нуклеозидом (расщепляемый фрагмент), за исключением ISIS 655861, в котором конъюгирующая группа GalNAc3 присоединена к 3'-концу.
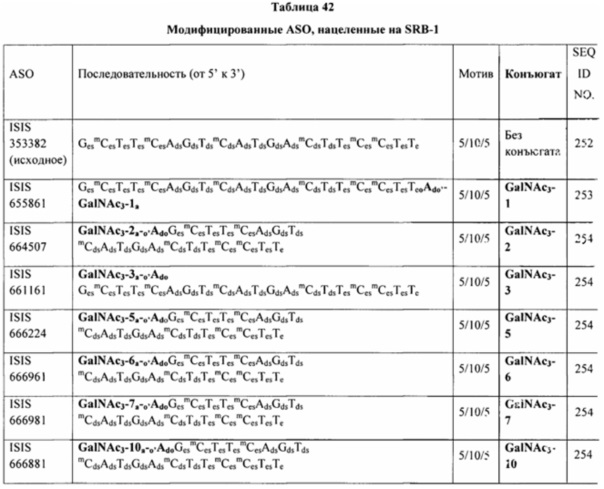
Заглавные буквы указывают азотистое основание для каждого нуклеозида, аmC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатную межнуклеозидную связь(PS); «о» означает фосфодиэфирную межнуклеозидную связь(РО); и «o'» означает -O-Р(=O)(ОН)-. Конъюгирующие группы выделены жирным шрифтом.
Структура GalNAc3-1a показана ранее в Примере 9. Структура GalNAc3-2a показана ранее в Примере 37. Структура GalNAc3-3a показана ранее в Примере 39. Структура GalNAc3-5а показана ранее в Примере 49. Структура GalNAc3-6a показана ранее в Примере 51. Структура GalNAc3-7a показана ранее в Примере 48. Структура GalNAc3-10a показана ранее в Примере 46.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, приведенной ниже, соединения ISIS 353382, 655861, 664507, 661161, 666224, 666961, 666981, 666881 или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часов после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР 6 реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, приведены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 43, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Действительно, конъюгированные антисмысловые олигонуклеотиды демонстрируют значительное усиление эффективности, по сравнению с неконъюгированным антисмысловым олигонуклеотидом (ISIS 353382). 5'-конъюгированные антисмысловые олигонуклеотиды демонстрируют небольшое усиление эффективности, по сравнению с 3'-конъюгированным антисмысловым олигонуклеотидом.
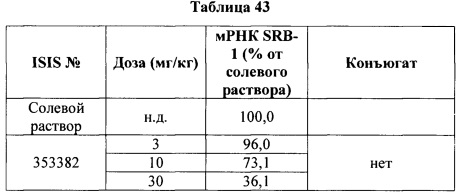
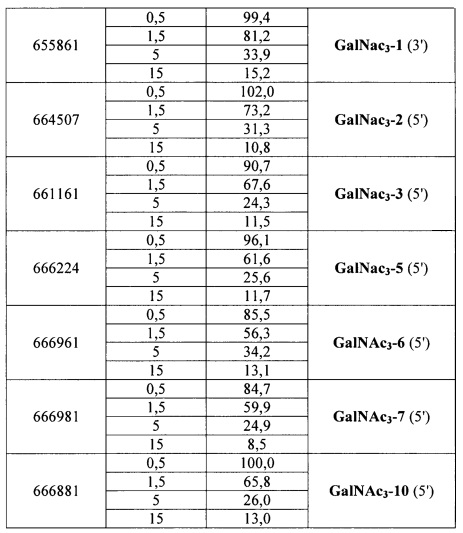
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, применяя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором. Значения ALT, AST, общего билирубина и АМК приведены ниже в Таблице 44.
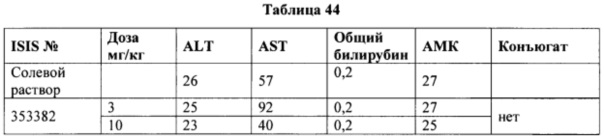
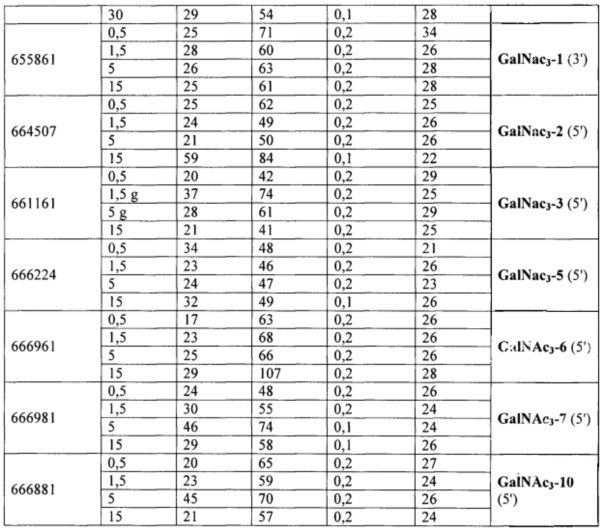
Пример 57. Исследование продолжительности действия олигонуклеотидов, содержащих 3'-конъюгирующую группу, нацеленных на АроСIII, in vivo
Мышам однократно ввели инъекцию дозы, указанной ниже, и в течение 42 дней наблюдали уровни АроС-III и триглицеридов в плазме (TG в плазме). Исследование выполнили, используя в каждой группе 3 трансгенных мышей, которые экспрессируют человеческий АРОС-III.

Заглавные буквы указывают азотистое основание для каждого нуклеозида. аmC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатную межнуклеозидную связь(PS); «о» означает фосфодиэфирную межнуклеозидную связь(РО); и «o'» означает -O-Р(=O)(ОН)-. Конъюгирующие группы выделены жирным шрифтом.
Структура GalNAc3-1a показана ранее в Примере 9.
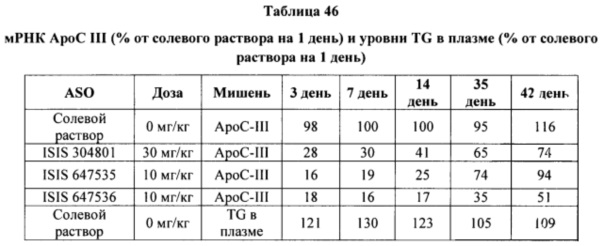
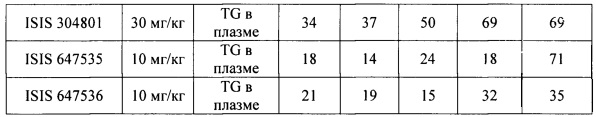
Как можно видеть в приведенной выше таблице, продолжительность действия увеличивается при добавлении 3'-конъюгирующие группы, по сравнению с неконъюгированным олигонуклеотидом. Дополнительное увеличение продолжительности действия наблюдали для смешанного конъюгированного PO/PS олигонуклеотида 647536, по сравнению с конъюгированным олигонуклеотидом 647535, содержащим только PS.
Пример 58. Дозозависимое исследование олигонуклеотидов, содержащих 31 конъюгирующую группу (сравнение GalNAc3-1 и GalNAc4-11), нацеленных на SRB-1, in vivo
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей. Неконъюгированный ISIS 440762 включили в качестве неконъюгированного стандарта. Каждая из конъюгирующих групп была присоединена к 3'-концу соответствующего олигонуклеотида при помощи расщепляемого фрагмента фосфодиэфир-связанного 2'-дезоксиаденозинового нуклеозида.
Структура GalNAc3-1a показана ранее в Примере 9. Структура GalNAc3-11a показана ранее в Примере 50.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, приведенной ниже, соединения ISIS 440762, 651900, 663748 или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часов после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, приведены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 47, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Антисмысловые олигонуклеотиды, содержащие фосфодиэфир-связанные конъюгаты GalNAc3-1 и GalNAc4-11 на 3'-конце (ISIS 651900 и ISIS 663748), демонстрируют значительное усиление эффективности, по сравнению с неконъюгированным антисмысловым олигонуклеотидом (ISIS 440762). Эти два конъюгированных олигонуклеотида, GalNAc3-1 и GalNAc4-11, были одинаково эффективными.
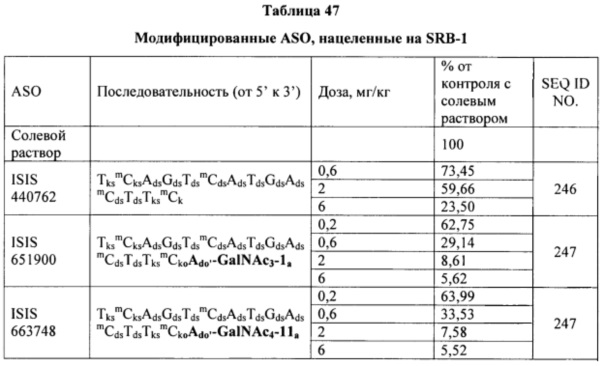
Заглавные буквы указывают азотистое основание для каждого нуклеозида, аmC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «k» означает 6'-(S)-СН3 бициклический нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатные межнуклеозидные связи (PS); «о» означает фосфодиэфирные межнуклеозидные связи (РО); и «o'» означает -O-Р(=O)(ОН)-. Конъюгирующие группы выделены жирным шрифтом.
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, применяя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором. Значения ALT, AST, общего билирубина и АМК приведены ниже в Таблице 48.
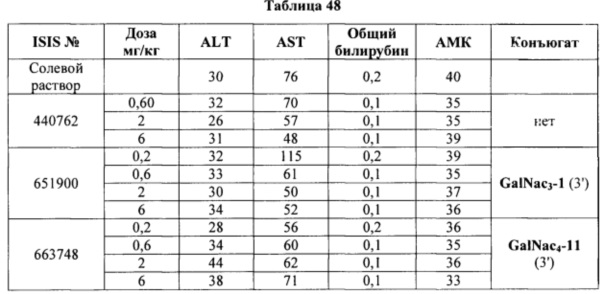
Пример 59. Действие GalNAc3-1-конъюгированных ASO, нацеленных на FXI, in vivo
Олигонуклеотиды, перечисленные ниже, испытали в исследовании действия многократных нарастающих доз на антисмысловое ингибирование FXI у мышей. ISIS 404071 включили в качестве неконъюгированного стандарта. Каждая из конъюгирующих групп была присоединена к 3'-концу соответствующего олигонуклеотида при помощи расщепляемого фрагмента фосфодиэфир-связанного 2'-дезоксиаденозинового нуклеозида.


Заглавные буквы указывают азотистое основание для каждого нуклеозида, аmC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатную межнуклеозидную связь(PS); «о» означает фосфодиэфирную межнуклеозидную связь(РО); и «o'» означает -O-Р(=O)(ОН)-. Конъюгирующие группы выделены жирным шрифтом.
Структура GalNAc3-1a показана ранее в Примере 9.
Лечение
Шестинедельным самцам мышей Balb/c (Jackson Laboratory, Бар-Харбор, штат Мэн) дважды в неделю в течение 3 недель вводили подкожную инъекцию дозы, приведенной ниже, соединения ISIS 404071, 656172, 656173 или PBS в качестве контрольного образца. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часов после последнего введения для определения уровней мРНК FXI в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Измерили также уровни белка FXI в плазме при помощи твердофазного иммуноферментного анализа. Уровни мРНК FXI определяли относительно общей РНК (при помощи RIBOGREEN®), затем нормализовали к контрольному образцу, обработанному PBS. Результаты, показанные ниже, приведены как средний процент уровней мРНК FXI для каждой экспериментальной группы. Данные нормализовали к контрольному образцу, обработанному PBS, и обозначили как «% PBS». ED50s измеряли по таким же способам, как описаны ранее, и они приведены ниже.
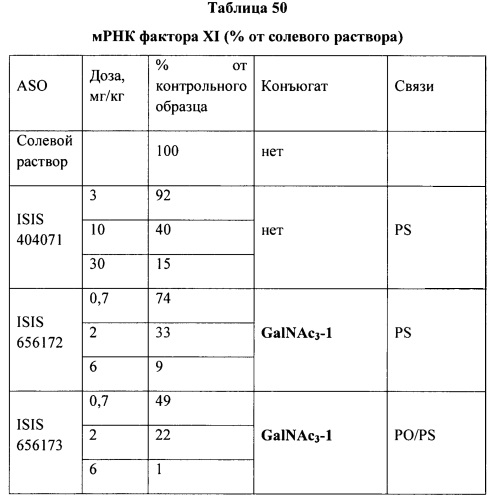
Как показано в Таблице 50, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК FXI дозозависимым образом. Олигонуклеотиды, содержащие конъюгирующую группу 3'-GalNAc3-1, демонстрируют значительное усиление эффективности, по сравнению с неконъюгированным антисмысловым олигонуклеотидом (ISIS 404071). Между эти двумя конъюгированными олигонуклеотидами дополнительное усиление эффективности было обеспечено за счет замены некоторых PS связей на РО (ISIS 656173).
Как показано в Таблице 50а, лечение антисмысловыми олигонуклеотидами снижает уровни белка FXI дозозависимым образом. Олигонуклеотиды, содержащие конъюгирующую группу 3'-GalNAc3-1, демонстрируют значительное усиление эффективности, по сравнению с неконъюгированным антисмысловым олигонуклеотидом (ISIS 404071). Между эти двумя конъюгированными олигонуклеотидами дополнительное усиление эффективности было обеспечено за счет замены некоторых PS связей на РО (ISIS 656173).
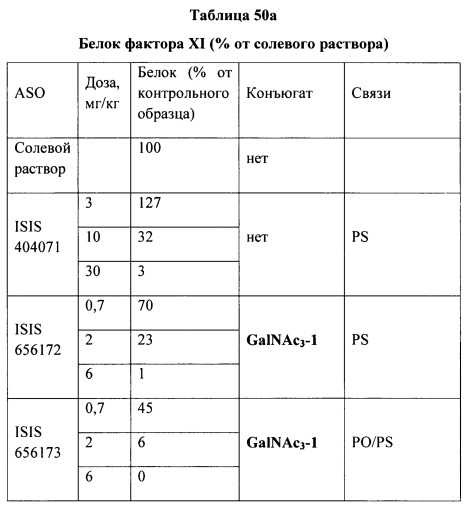
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, применяя стандартные протоколы. Оценили также общий билирубин, общий альбумин, CRE и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором. Значения ALT, AST, общего билирубина и АМК приведены ниже в таблице.
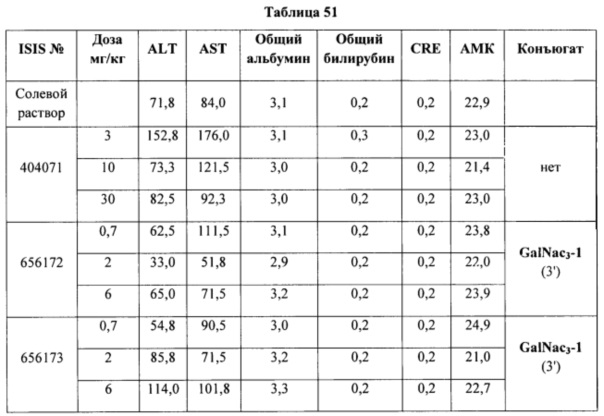
Пример 60. Действие конъюгированных ASO, нацеленных на SRB-1, in vitro
Олигонуклеотиды, перечисленные ниже, испытали в исследование действия многократных нарастающих доз на антисмысловое ингибирование SRB-1 в первичных гепатоцитах мышей. ISIS 353382 включили в качестве неконъюгированного стандарта. Каждая из конъюгирующих групп была присоединена к 3' или 5'-концу соответствующего олигонуклеотида при помощи расщепляемого фрагмента фосфодиэфир-связанного 2'-дезоксиаденозинового нуклеозида.
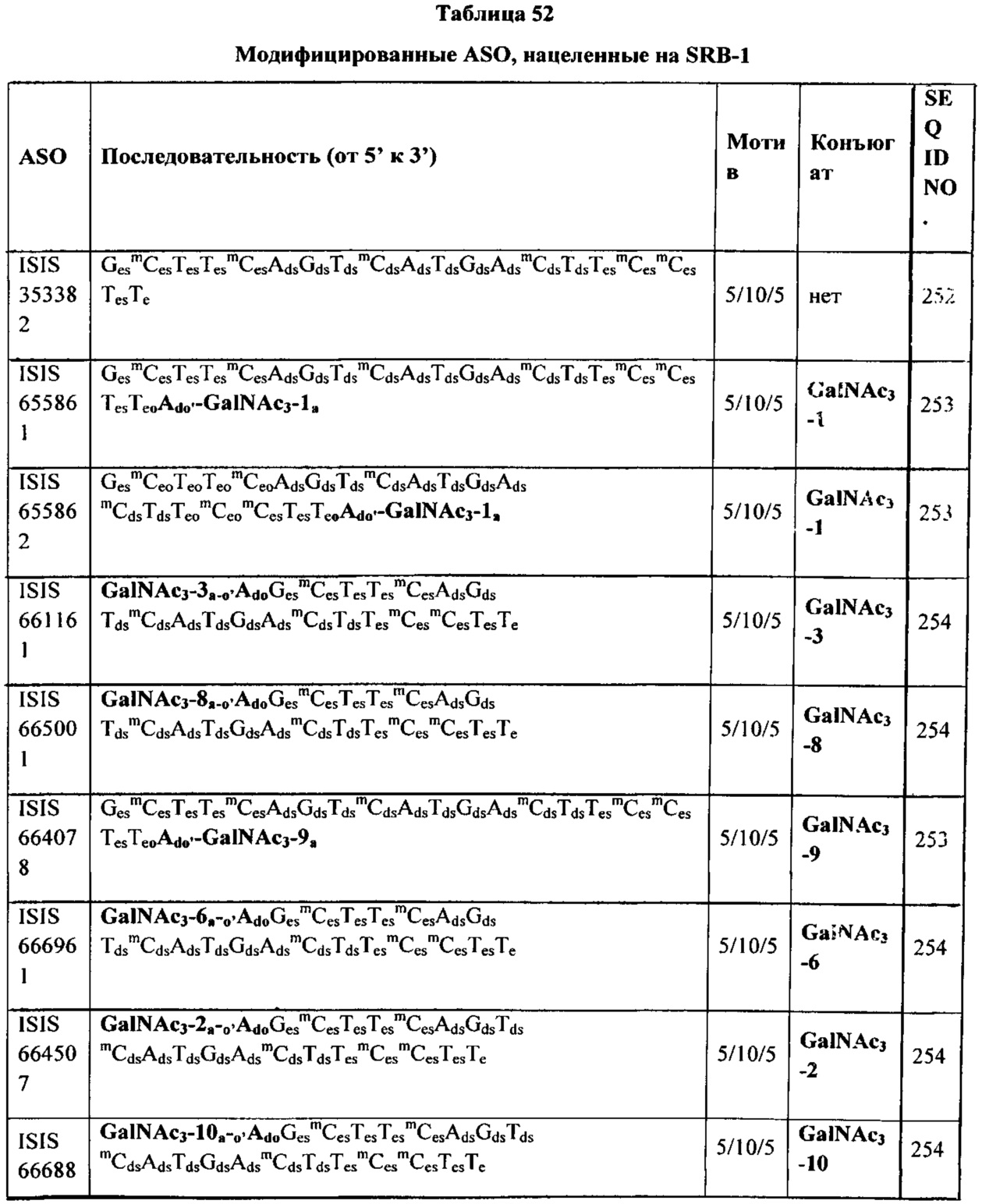
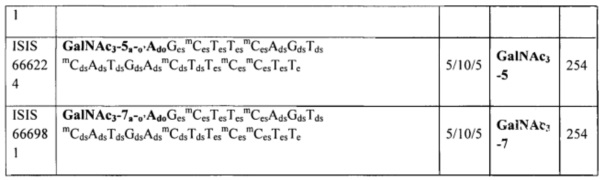
Заглавные буквы указывают азотистое основание для каждого нуклеозида, аmC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатную межнуклеозидную связь(PS); «о» означает фосфодиэфирную межнуклеозидную связь(РО), и «o'» означает -O-Р(=O)(ОН)-. Конъюгирующие группы выделены жирным шрифтом.
Структура GalNAc3-1a показана ранее в Примере 9. Структура GalNAc3-3a показана ранее в Примере 39. Структура GalNAc3-8a показана ранее в Примере 47. Структура GalNAc3-9a показана ранее в Примере 52. Структура GalNAc3-6a показана ранее в Примере 51. Структура GalNAc3-2a показана ранее в Примере 37. Структура GalNAc3-10a показана ранее в Примере 46. Структура GalNAc3-5a показана ранее в Примере 49. Структура GalNAc3-7a показана ранее в Примере 48.
Лечение
Олигонуклеотиды, перечисленные выше, испытывали in vitro в первичных гепатоцитарных клетках мышей, помещенных на планшеты при плотности 25000 клеток на лунку и обработанных 0,03, 0,08, 0,24, 0,74, 2,22, 6,67 или 20 нМ модифицированного олигонуклеотида. После обработки в течение приблизительно 16 часов, из клеток выделил» РНК и измерили уровни мРНК при помощи количественной ПЦР в реальном времени, а уровни мРНК SRB-1 III скорректировали в соответствии с общим содержанием РНК, измеренным при помощи RIBOGREEN®.
IC50 рассчитали по стандартным способам, а результаты приведены в Таблице 53. Результаты показывают, что при условиях свободного поглощения, в которых не применяли никакие реагенты или электроимпульсные приемы для искусственного ускорения входа олигонуклеотидов в клетки, олигонуклеотиды, содержащие конъюгат GalNAc, были существенно более эффективными в гепатоцитах, чем исходный олигонуклеотид (ISIS 353382), который не содержит конъюгат GalNAc.
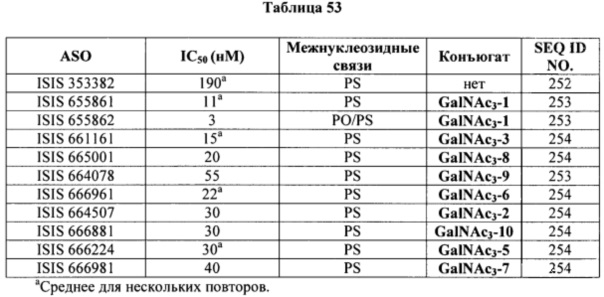
Пример 61. Получение олигомерного соединения 175, содержащего GalNAc3-12
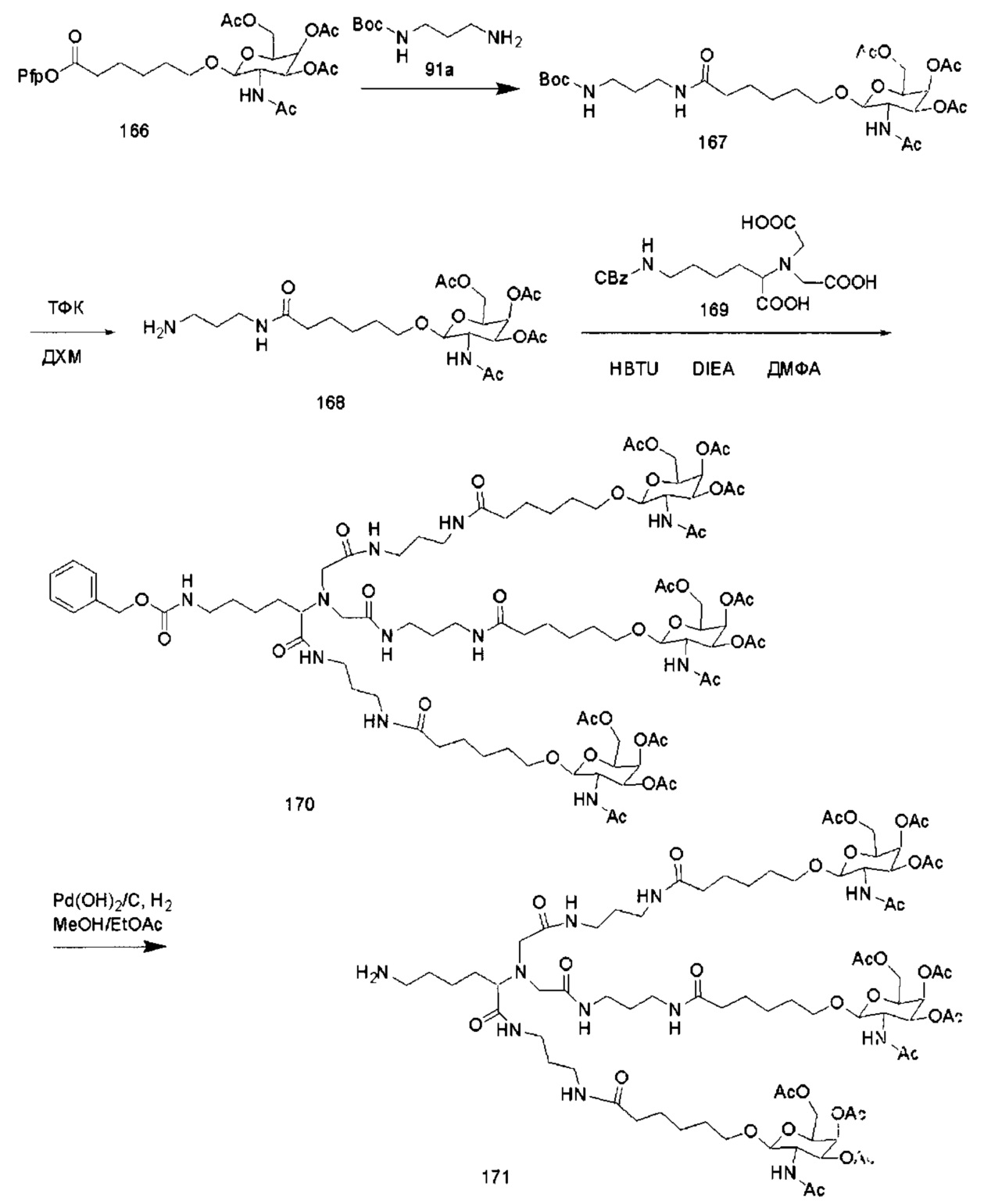
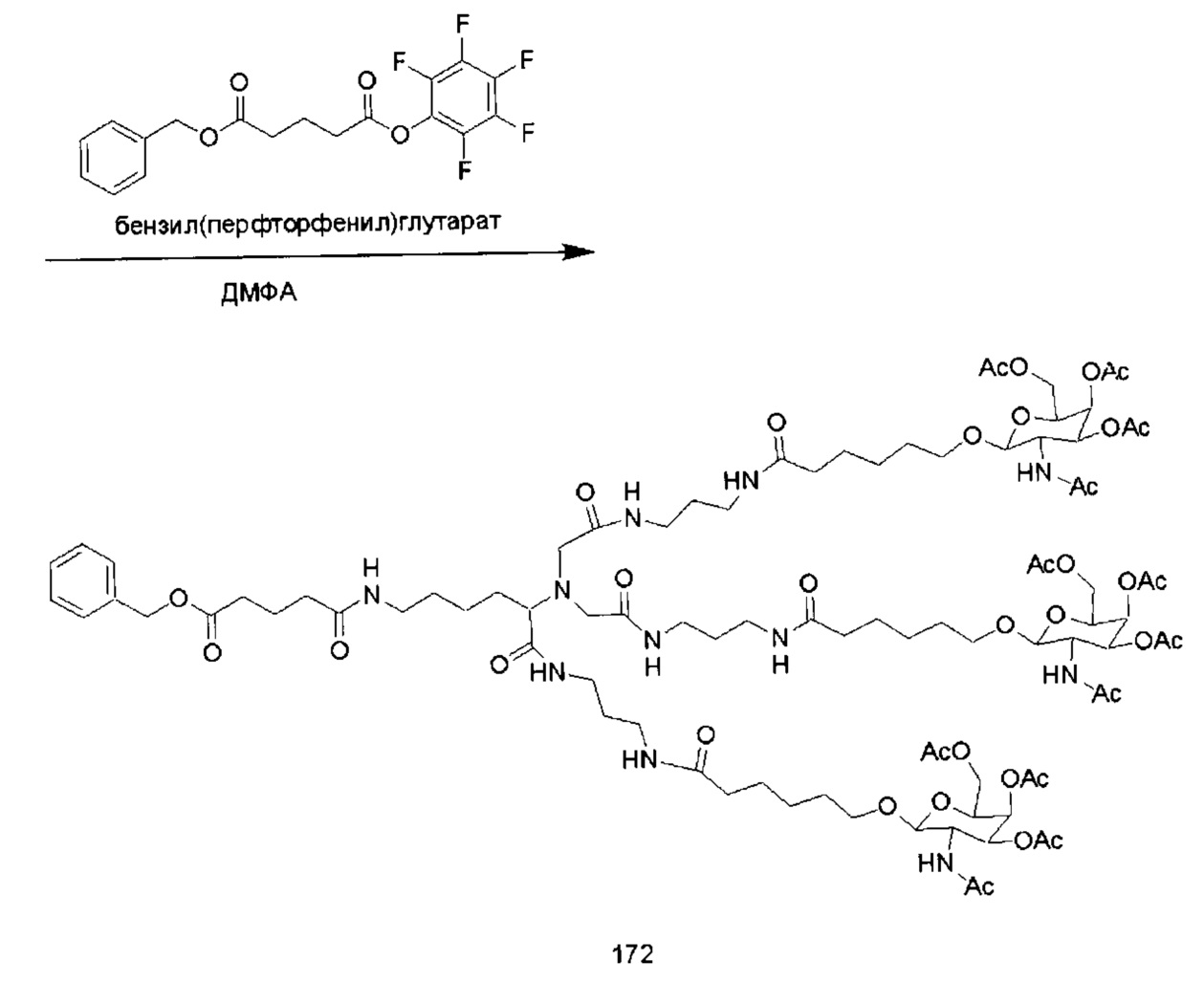
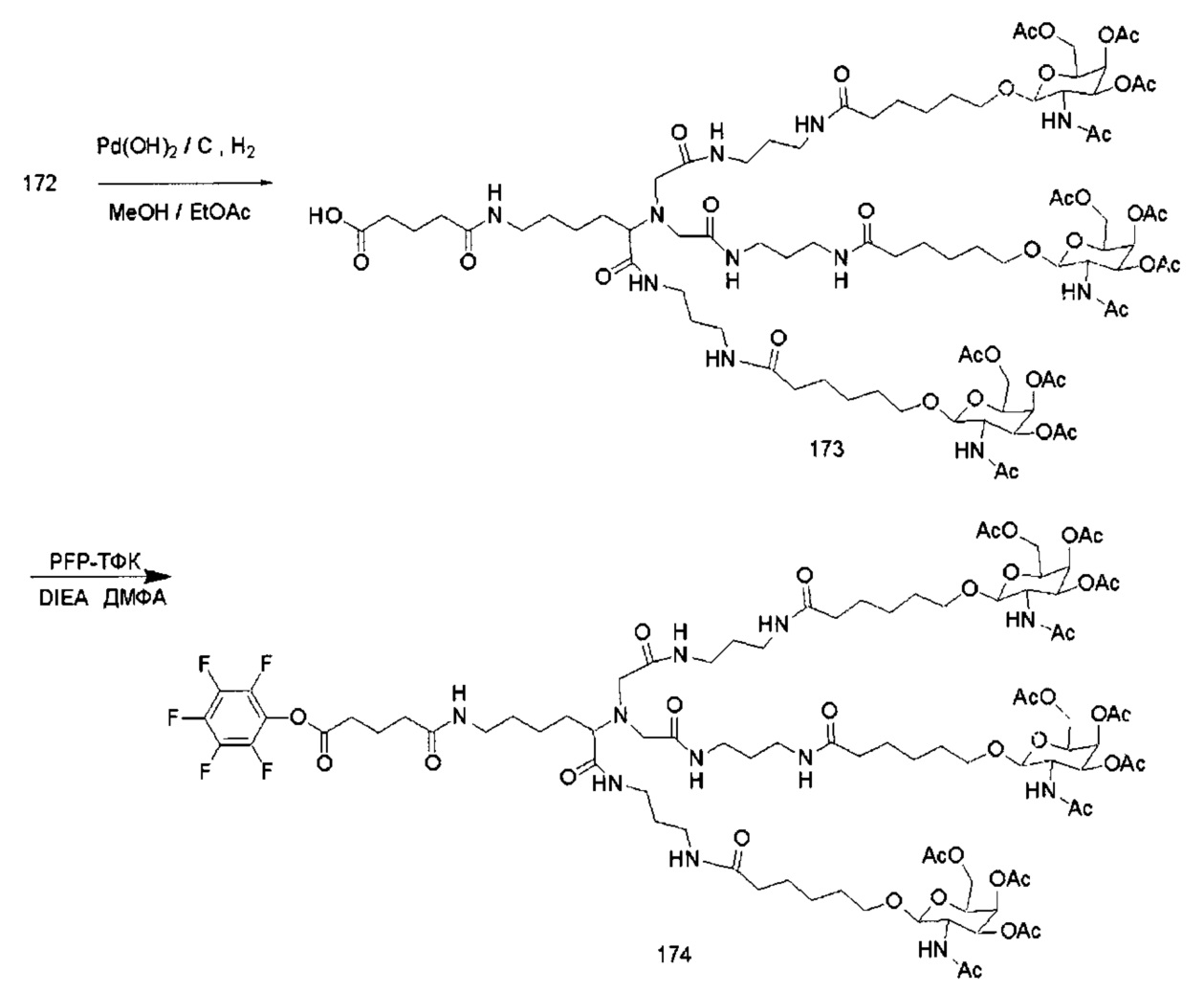
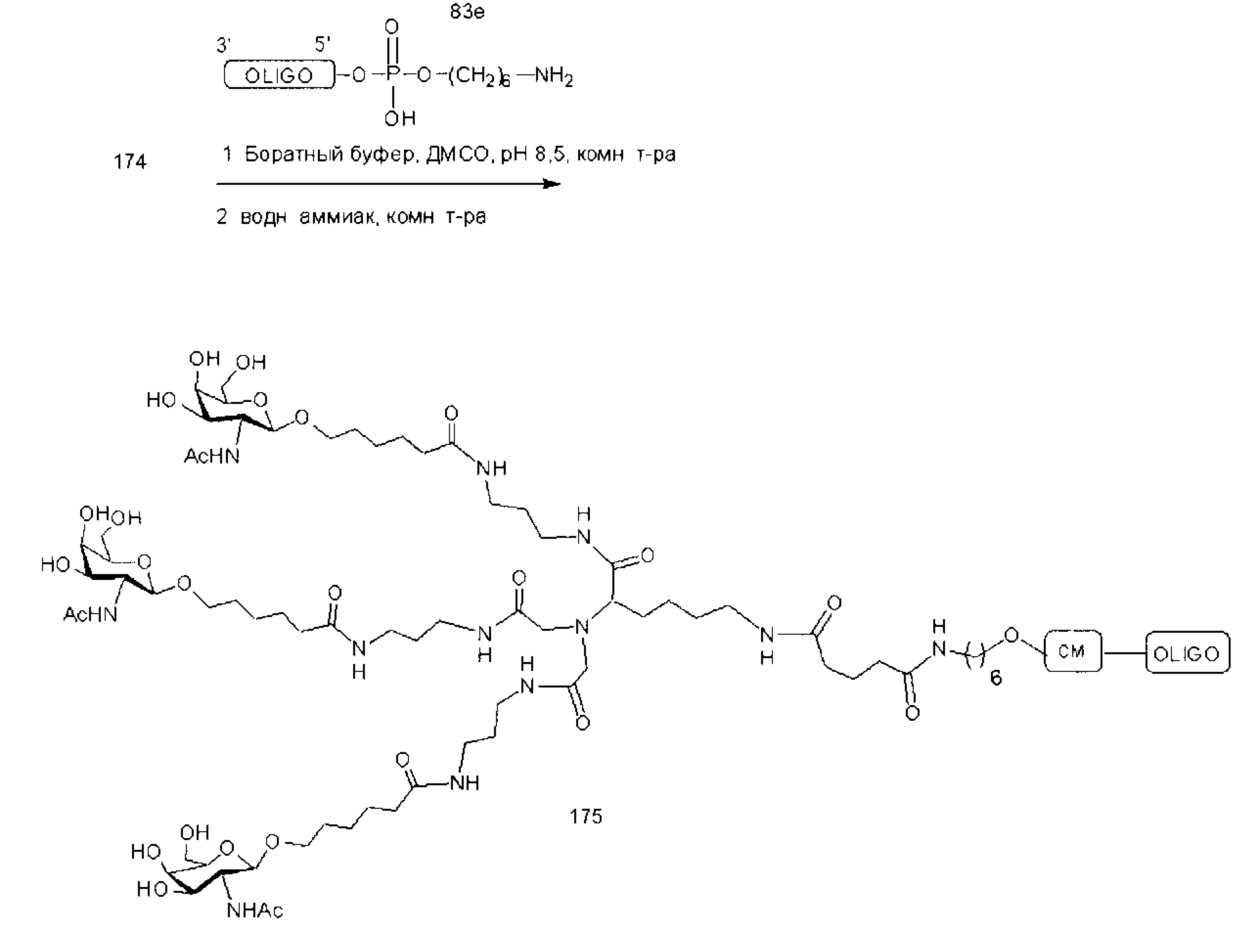
Соединение 169 имеется в продаже. Соединение 172 получили добавлением бензил(перфторфенил)глутарата к соединению 171. Бензил(перфторфенил)глутарат получили добавлением PFP-ТФК и DIEA к 5-(бензилокси)-5-оксопентановой кислоте в ДМФА. Олигомерное Соединение 175, содержащее конъюгирующую группу GalNAc3-12, получили из соединения 174 по общим способам, приведенным в Примере 46. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-12 (GalNAc3-12a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -Р(=O)(ОН)-Ad-P(=O)(OH)-. Структура GalNAc3-12 (GalNAc3-12a-CM-) приведена ниже:
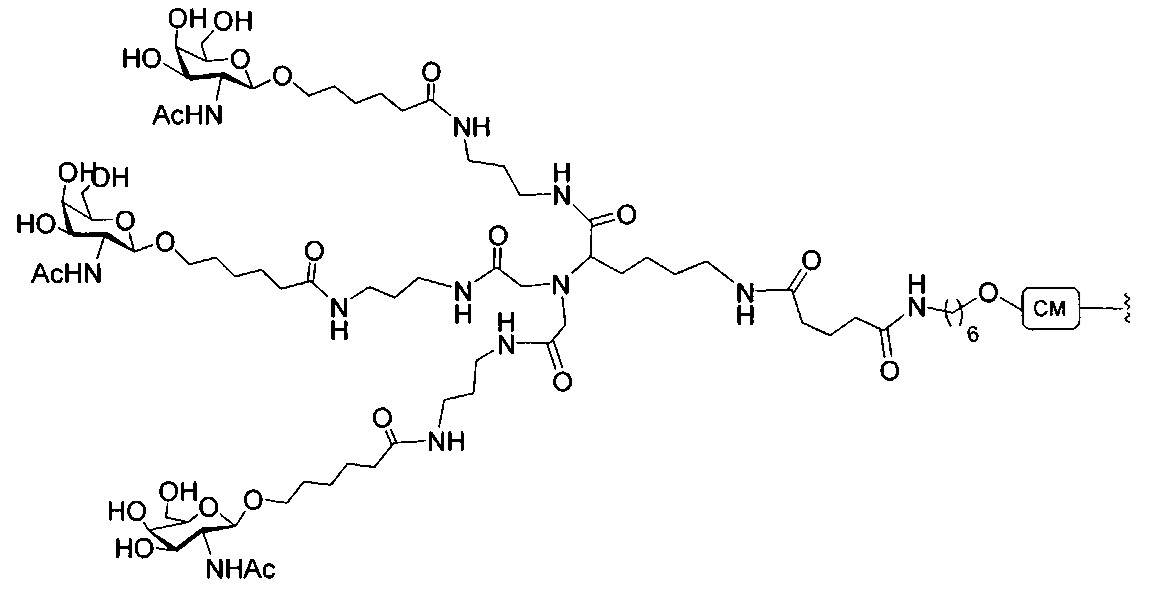
Пример 62. Получение олигомерного соединения 180, содержащего GalNAc3-13
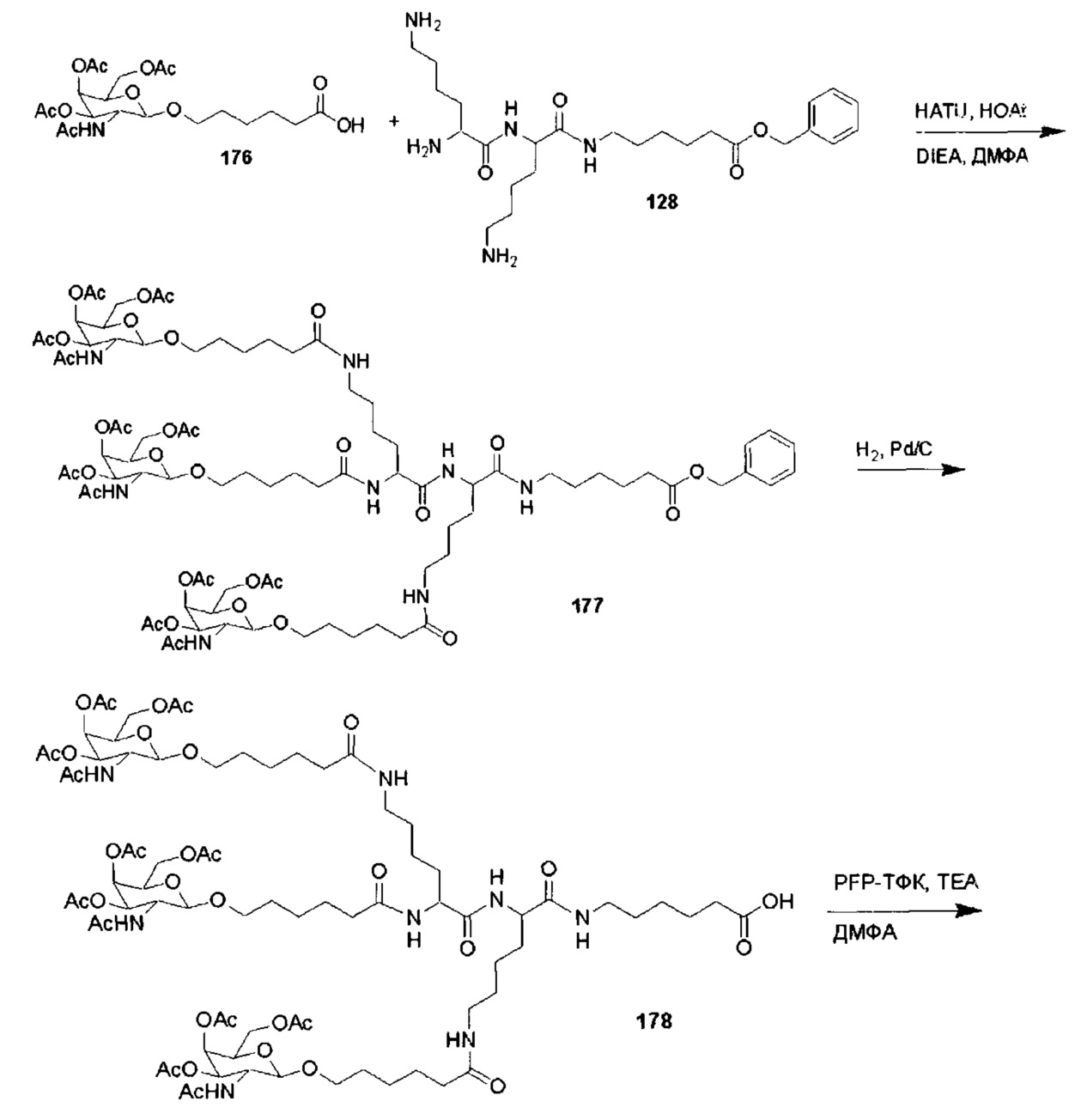
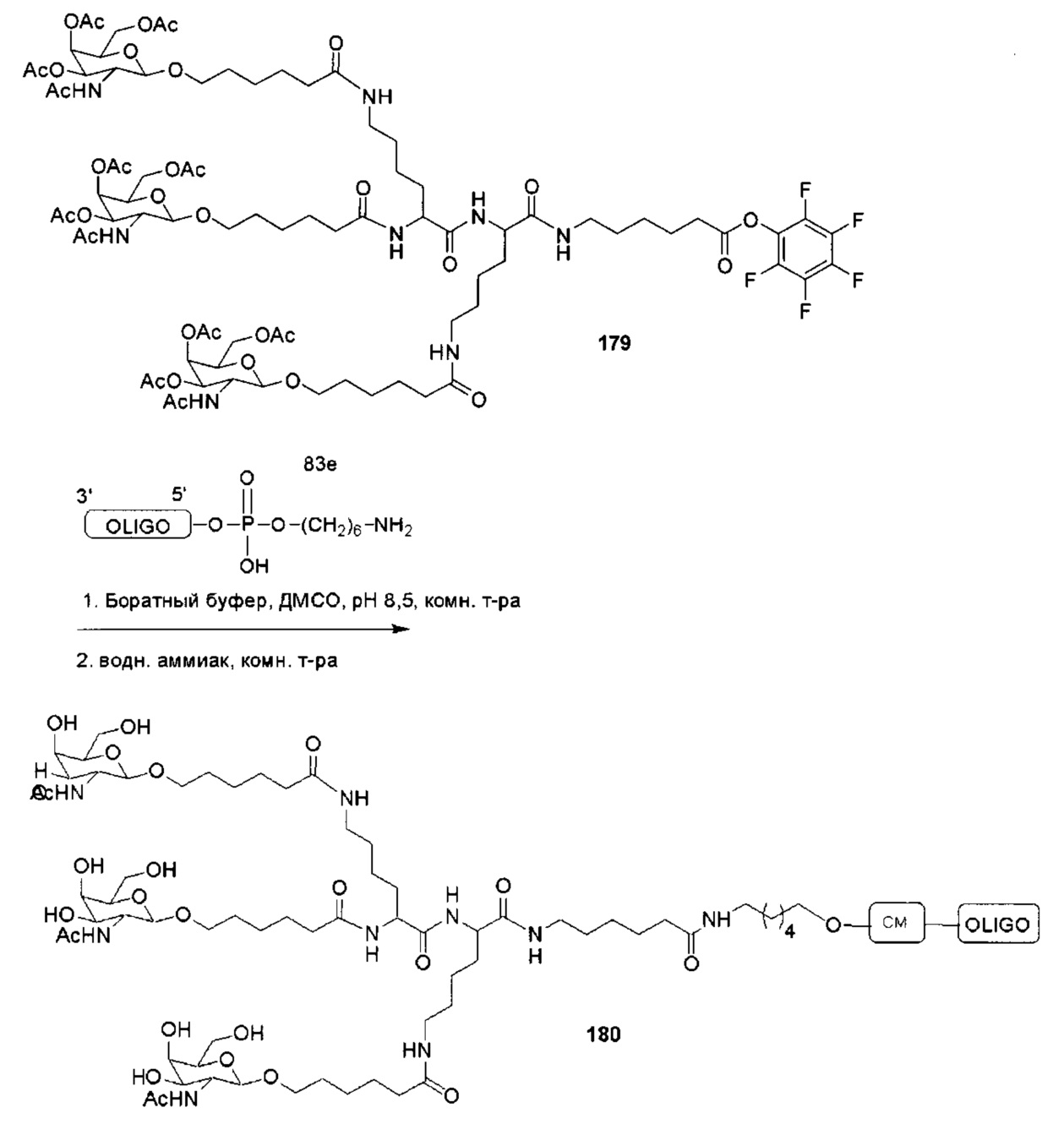
Соединение 176 получили по общему способу, приведенному в Примере 2. Олигомерное соединение 180, содержащее конъюгирующую группу GalNAc3-13, получили из соединения 177 по общим способам, приведенным в Примере 49. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-13 (GalNAc3-13a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -Р(=O)(ОН)-Ав-Р(=O)(ОН)-. Структура GalNAc3-13 (GalNAc3-13a-CM-) приведена ниже:
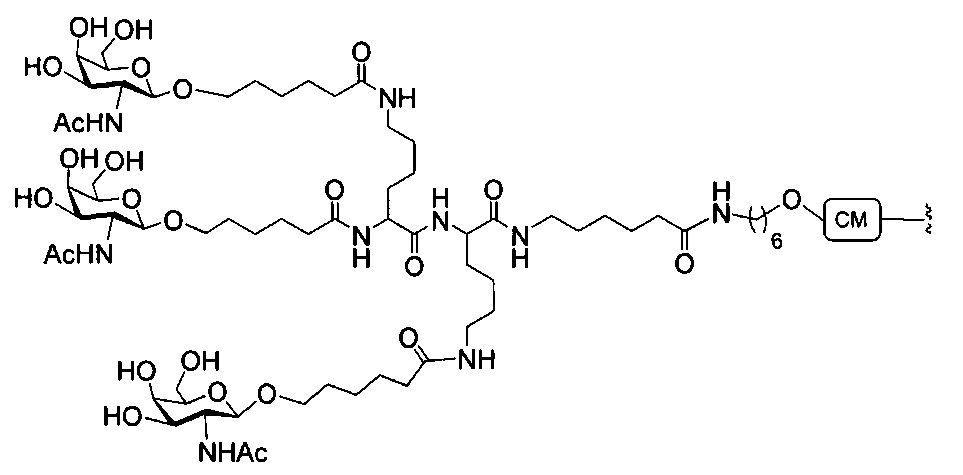
Пример 63. Получение олигомерного соединения 188, содержащего GalNAc3-14
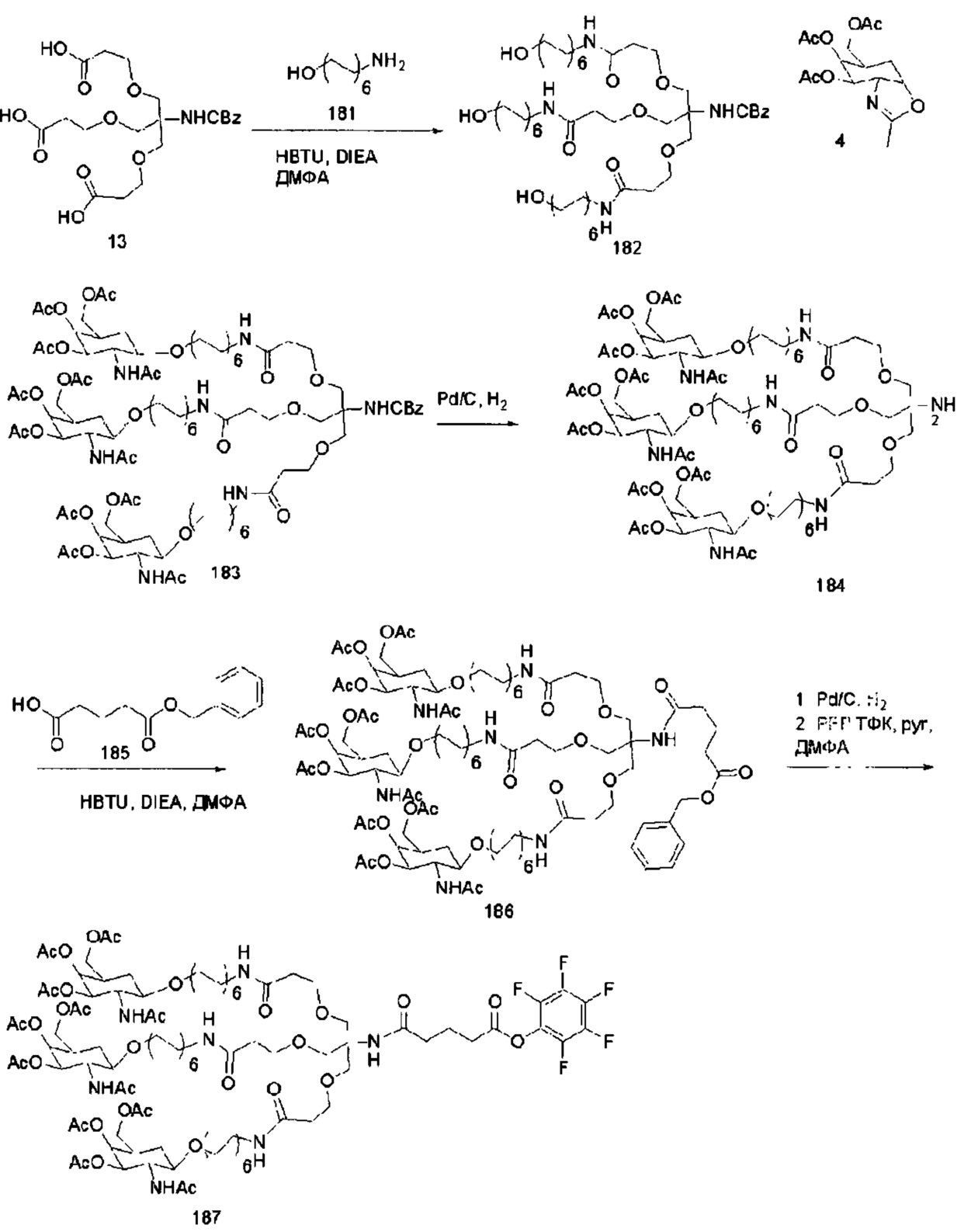
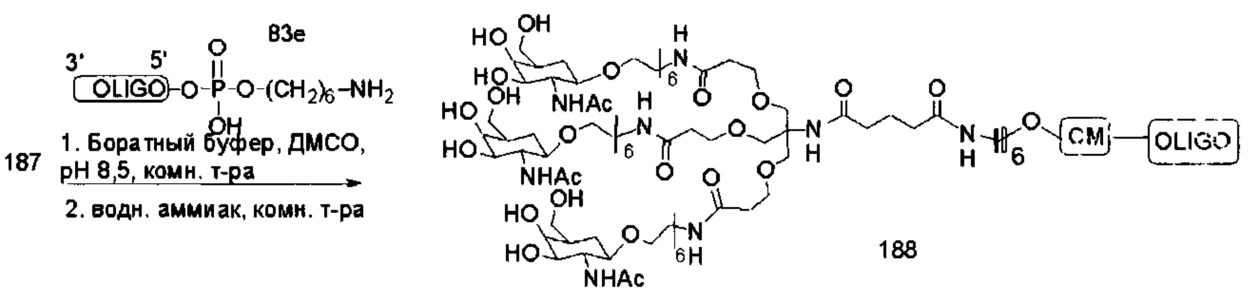
Соединения 181 и 185 имеются в продаже. Олигомерное Соединение 188, содержащее конъюгирующую группу GalNAc3-14, получили из соединения 187 по общим способам, приведенным в Примере 46. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-14 (GalNAc3-14a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -Р(=O)(ОН)-Ad-Р(=O)(ОН)-. Структура GalNAc3-14 (GalNAc3-14a-CM-) приведена ниже:
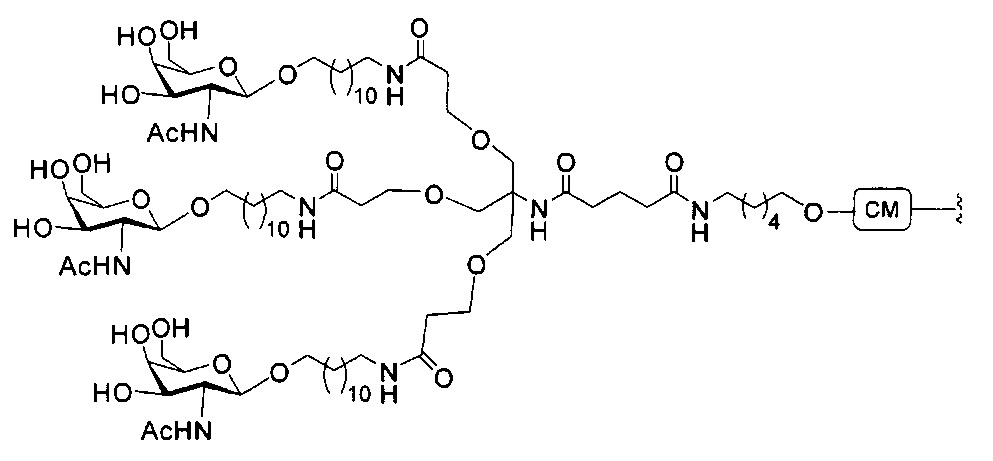
Пример 64. Получение олигомерного соединения 197, содержащего GalNAc3-15
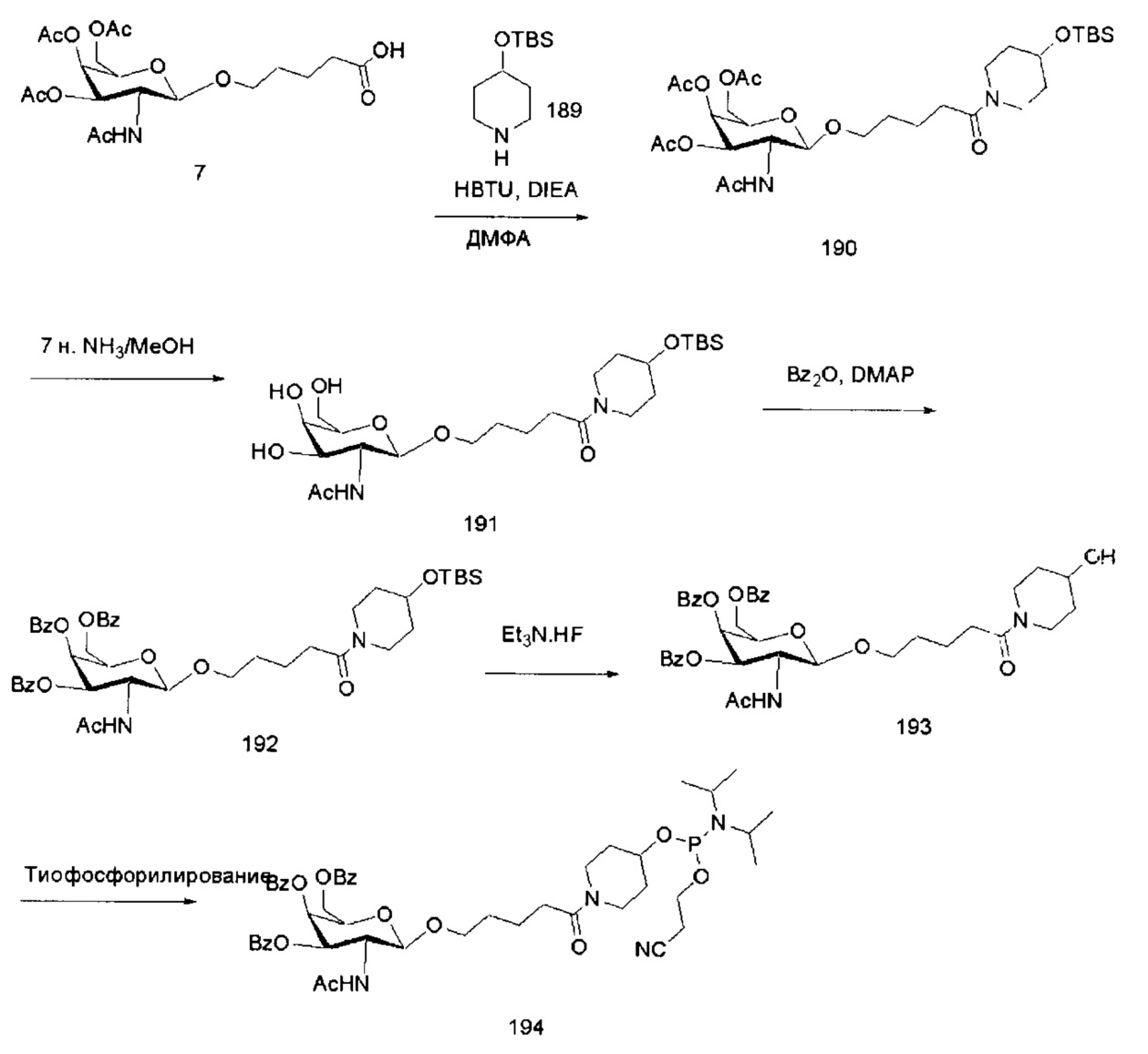
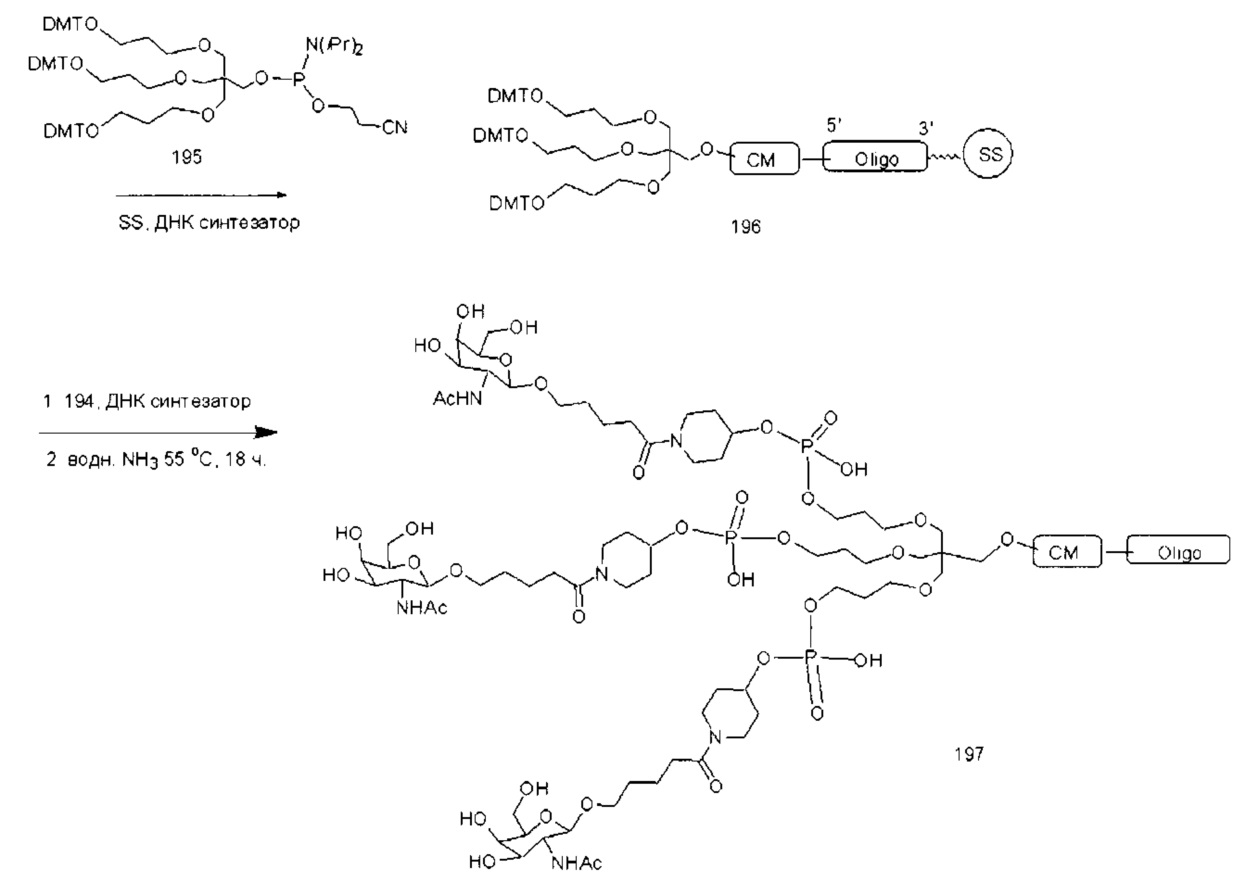
Соединение 189 имеется в продаже. Соединение 195 получили по общему способу, приведенному в Примере 31. Олигомерное соединение 197, содержащее конъюгирующую группу GalNAc3-15, получили из соединений 194 и 195, применив стандартные способы синтеза олигонуклеотидов. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-15 (GalNAc3-15a) может быть комбинирована с любым расщепляемым фрагментом с получением различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-. Структура GalNAc3-15 (GalNAc3-15а-СМ-) приведена ниже:
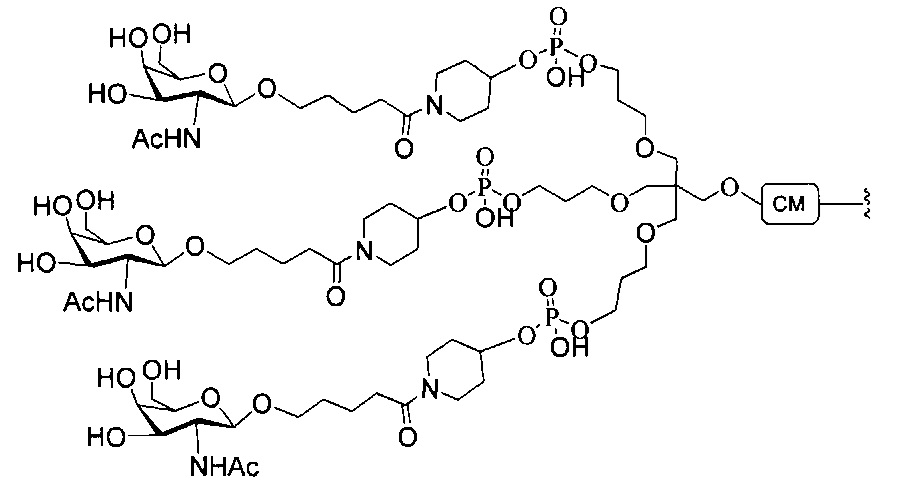
Пример 65. Дозозависимое исследование олигонуклеотидов, содержащих 5'-конъюгирующую группу (сравнение GalNAc3-3, 12, 13, 14 и 15), нацеленных на SRB-1, in vivo
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей. Неконъюгированный ISIS 353382 включили в качестве стандарта. Каждая из конъюгирующих групп GalNAc3 была присоединена к 5'-концу соответствующего олигонуклеотида при помощи расщепляемого фрагмента фосфодиэфир-связанного 2'-дезоксиаденозинового нуклеозида.


Заглавные буквы указывают азотистое основание для каждого нуклеозида, аmC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатную межнуклеозидную связь(PS); «о» означает фосфодиэфирную межнуклеозидную связь(РО); и «o'» означает -O-Р(=O)(ОН)-. Конъюгирующие группы выделены жирным шрифтом.
Структура GalNAc3-3a показана ранее в Примере 39. Структура GalNAc3-12a показана ранее в Примере 61. Структура GalNAc3-13a показана ранее в Примере 62. Структура GalNAc3-14a показана ранее в Примере 63. Структура GalNAc3-15a показана ранее в Примере 64.
Лечение
Шести-восьминедельным мышам C57bl6 (Jackson Laboratory, Бар-Харбор, штат Мэн) один или два раза ввели подкожную инъекцию дозы, приведенной ниже, соединения ISIS 353382, 661161, 671144, 670061, 671261, 671262 или солевого раствора. Мыши, которые вводили дозу два раза, вторую дозу вводили через три дня после первой дозы. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часов после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, приведены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 55, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Не наблюдали значительной разницы нокдауна мишени между животными, получавшими одну дозу, и животными, получавшими две дозы (см. ISIS 353382 в дозах 30 и 2×15 мг/кг; и ISIS 661161 в дозах 5 и 2×2,5 мг/кг). Антисмысловые олигонуклеотиды, содержащие фосфодиэфир-связанные конъюгаты GalNAc3-3, 12, 13, 14 и 15, демонстрируют существенное усиление эффективности, по сравнению с неконъюгированным антисмысловым олигонуклеотидом (ISIS 335382).
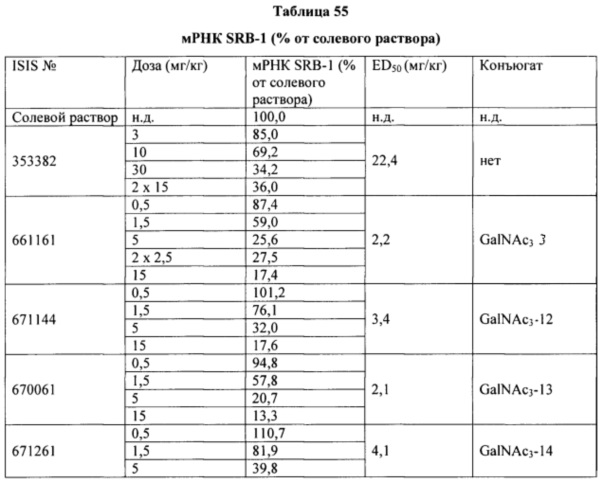
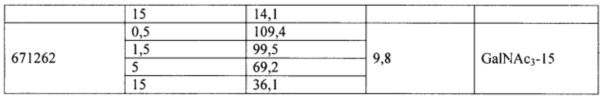
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, применяя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором (данные не показаны). Значения ALT, AST, общего билирубина и АМК приведены ниже в Таблице 56.
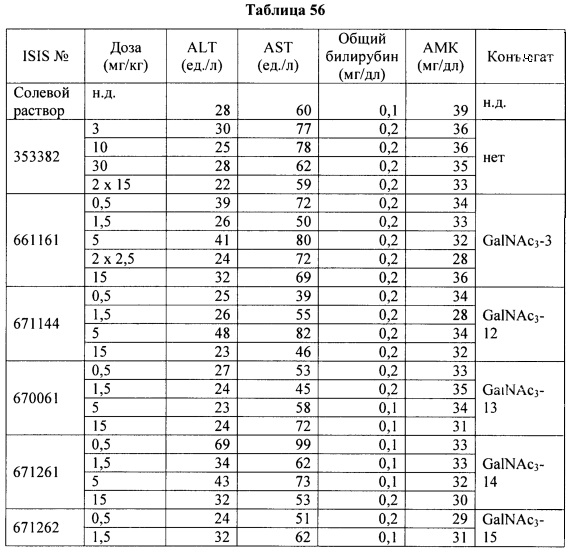

Пример 66. Влияние различных расщепляемых фрагментов на антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на SRB-1, содержащих кластер 5'-GalNAc3
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей. Каждая из конъюгирующих групп GalNAc3 была присоединена к 5'-концу соответствующего олигонуклеотида при помощи фосфодиэфир-связанного нуклеозида (расщепляемый фрагмент (СМ)).
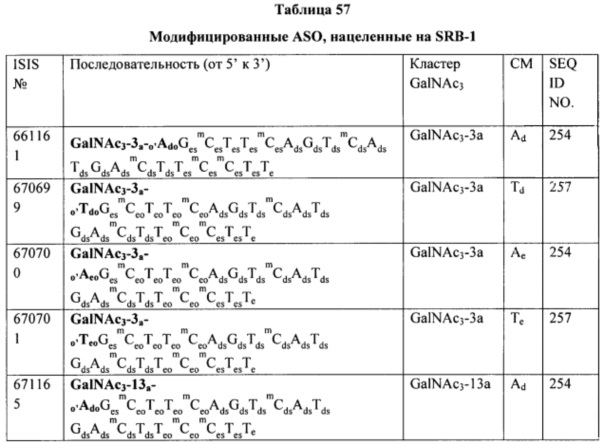
Заглавные буквы указывают азотистое основание для каждого нуклеозида, аmC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатную межнуклеозидную связь(PS); «о» означает фосфодиэфирную межнуклеозидную связь(РО); и «o'» означает -O-Р(=O)(ОН)-. Конъюгирующие группы выделены жирным шрифтом.
Структура GalNAc3-3a показана ранее в Примере 39. Структура GalNAc3-13a показана ранее в Примере 62.
Лечение
Шести-восьминедельным мышам C57bl6 (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, приведенной ниже, соединения ISIS 661161, 670699, 670700, 670701, 671165 или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часов после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, приведены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 58, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом. Все антисмысловые олигонуклеотиды, содержащие различные расщепляемые фрагменты, демонстрируют одинаковую эффективность.
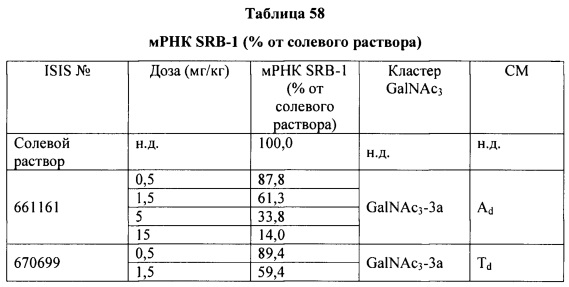
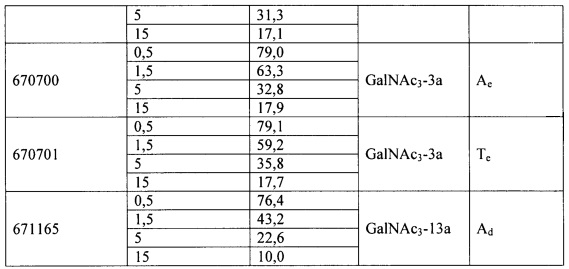
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, применяя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором (данные не показаны). Значения ALT, AST, общего билирубина и АМК приведены ниже в Таблице 56.
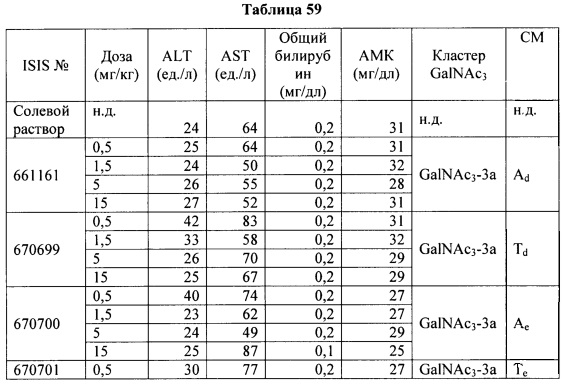
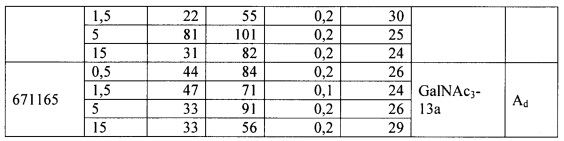
Пример 67. Получение олигомерного соединения 199, содержащего GalNAc3-16
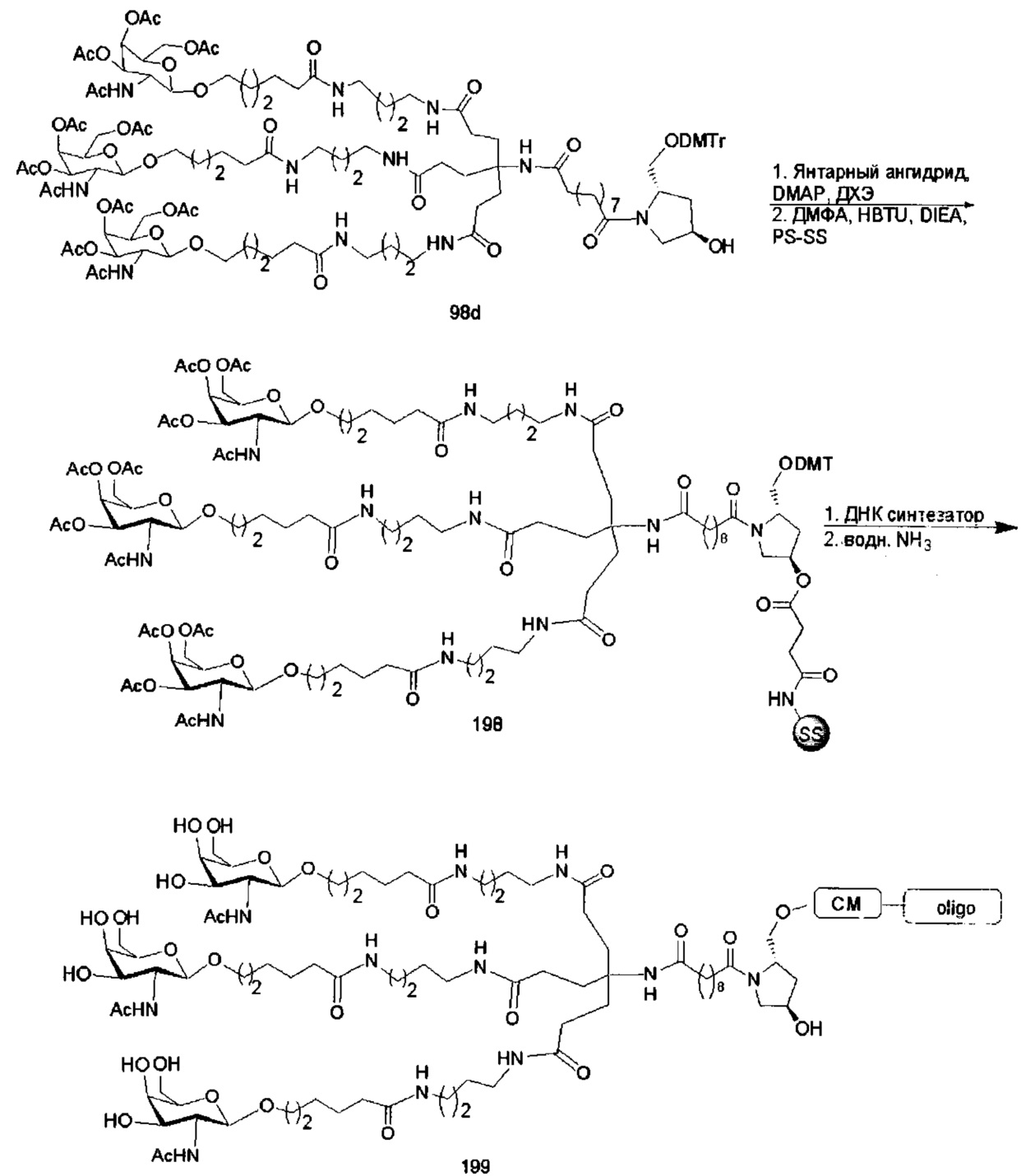
Олигомерное соединение 199, содержащее конъюгирующую группу GalNAc3-16, получили по общим способам, приведенным в Примерах 7 и 9. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-16 (GalNAc3-16a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-Р(=O)(ОН)-. Структура GalNAc3-16 (GalNAc3-16a-CM-) приведена ниже:
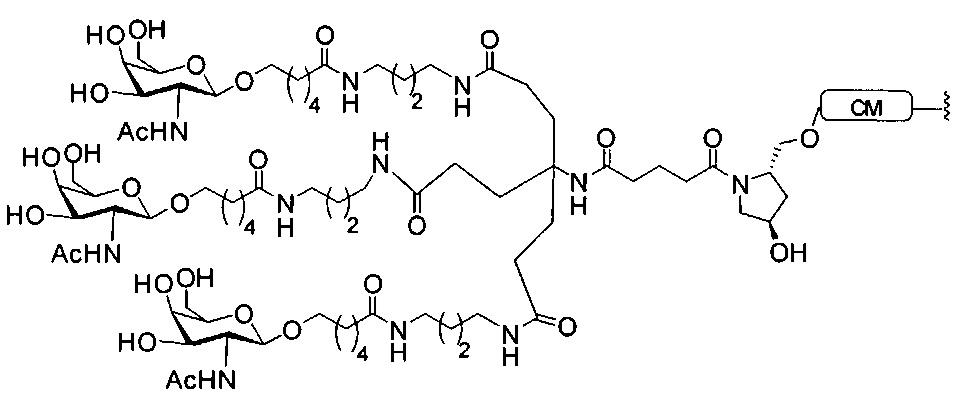
Пример 68. Получение олигомерного соединения 200, содержащего GalNAc3-17
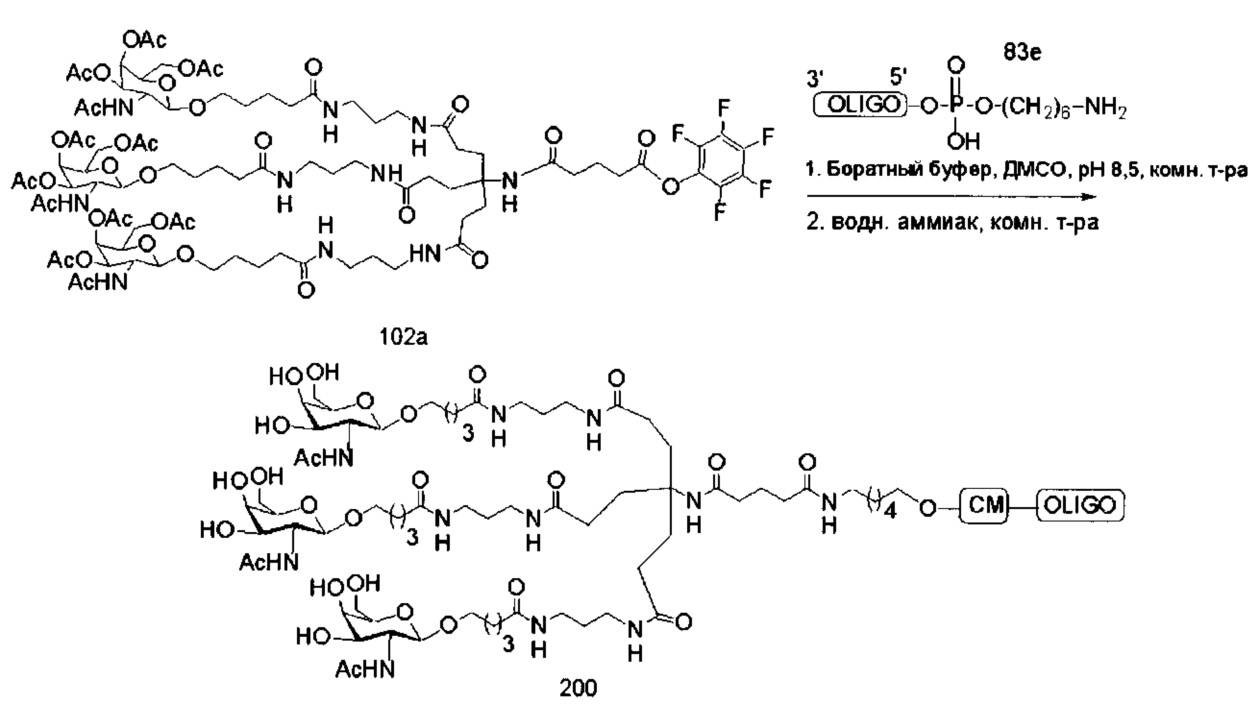
Олигомерное соединение 200, содержащее конъюгирующую группу GalNAc3-17, получили по общим способам, приведенным в Примере 46. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-17 (GalNAc3-17a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(-O)(OH)-. Структура GalNAc3-17 (GalNAc3-17а-СМ-) приведена ниже:
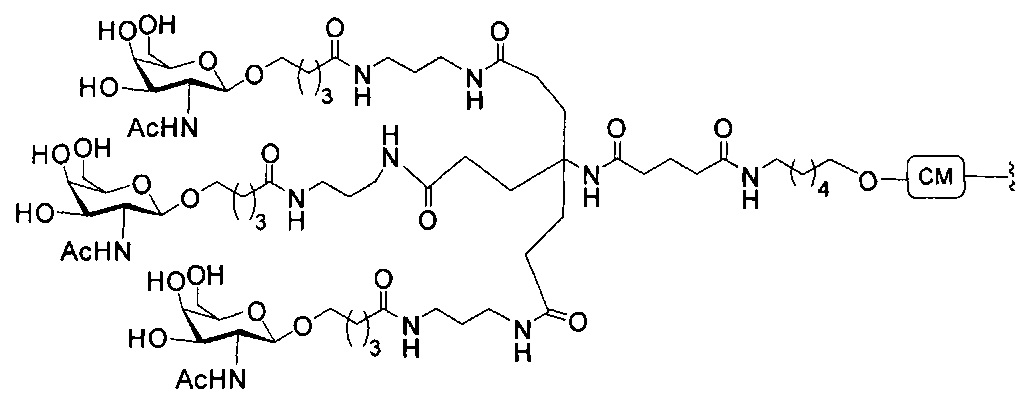
Пример 69. Получение олигомерного соединения 201, содержащего GalNAc3-18
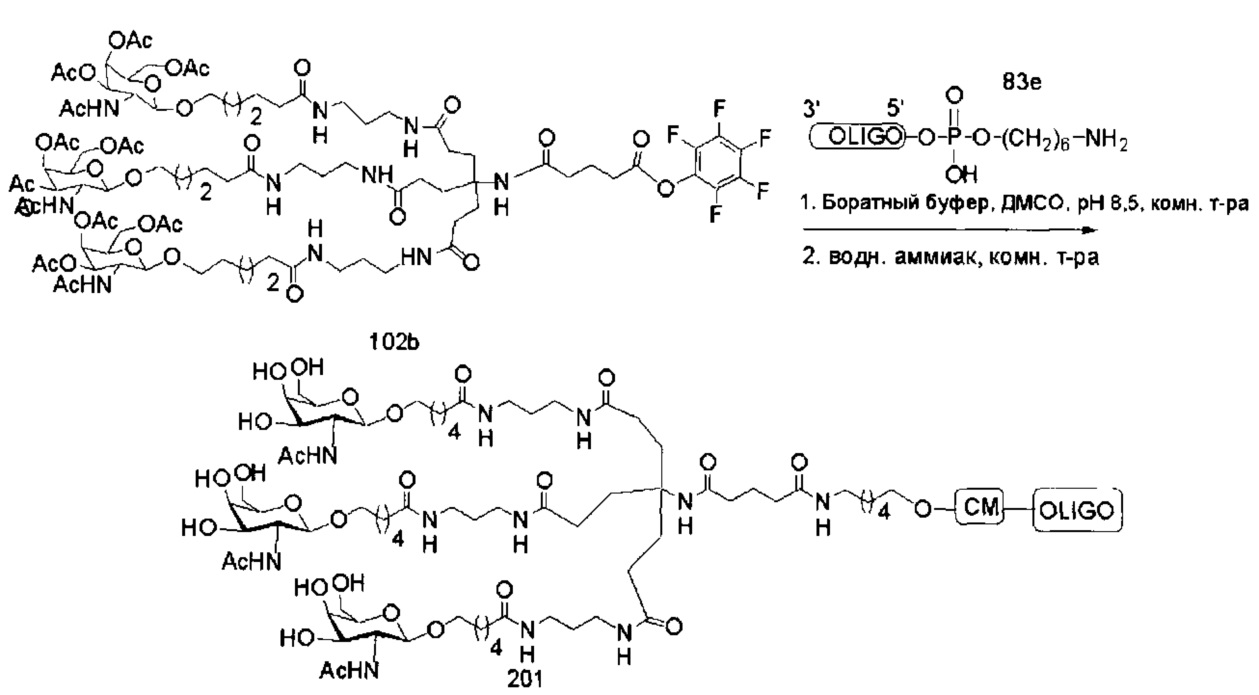
Олигомерное соединение 201, содержащее конъюгирующую группу GalNAc3-18, получили по общим способам, приведенным в Примере 46. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-18 (GalNAc3-18a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-. Структура GalNAc3-18 (GalNAc3-18a-CM-) приведена ниже:
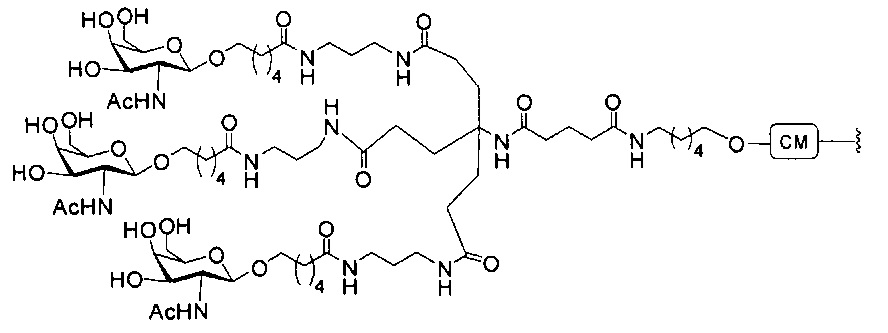
Пример 70. Получение олигомерного соединения 204, содержащего GalNAc3-19
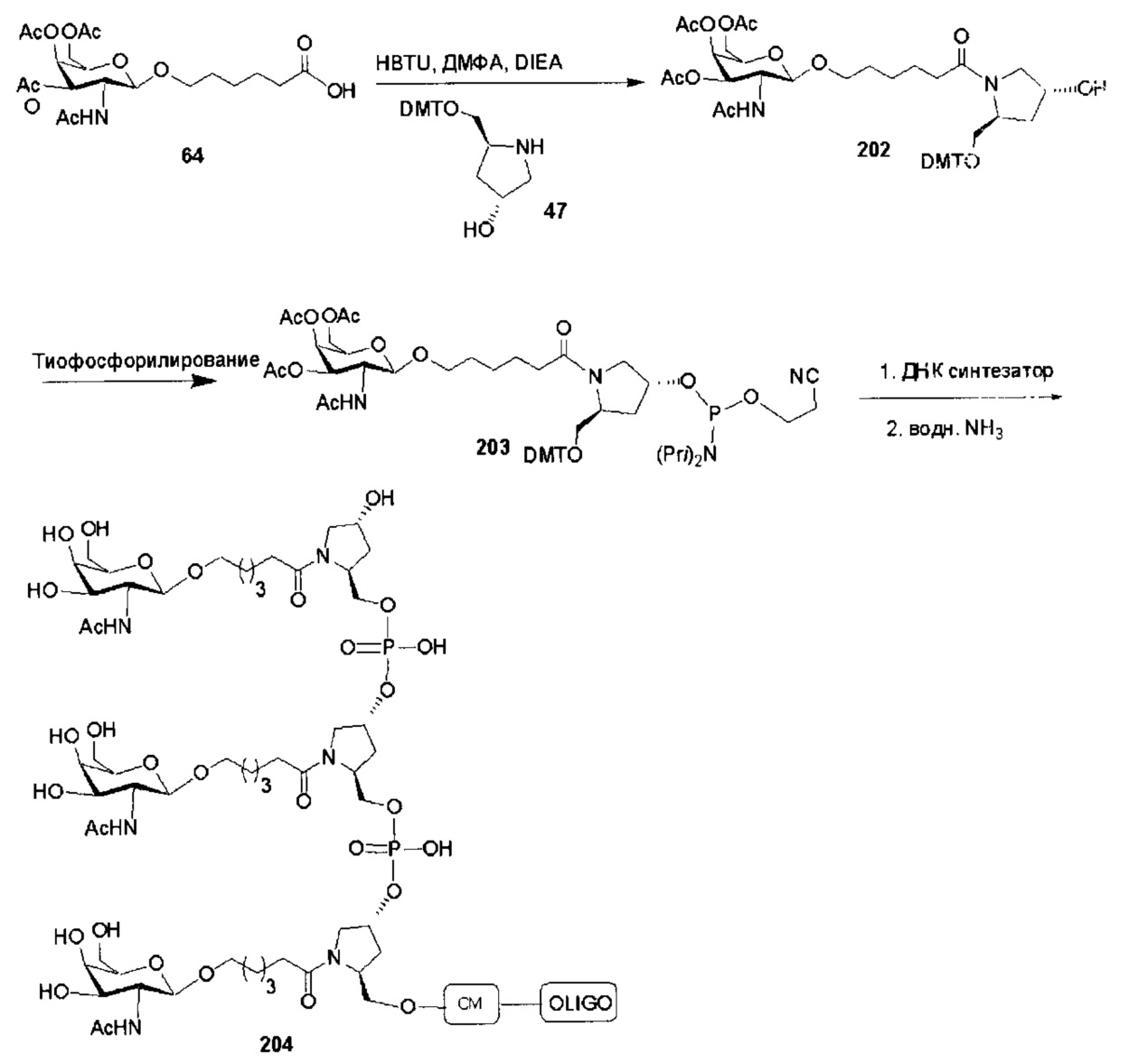
Олигомерное Соединение 204, содержащее конъюгирующую группу GalNAc3-19, получили из соединения 64 по общим способам, приведенным в Примере 52. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-19 (GalNAc3-19a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-Р(=O)(ОН)-. Структура GalNAc3-19 (GalNAc3-19a-CM-) приведена ниже:
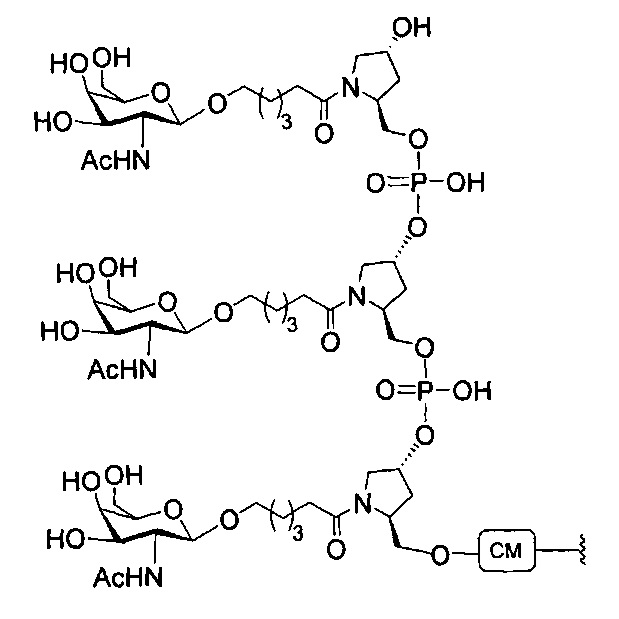
Пример 71. Получение олигомерного соединения 210, содержащего GalNAc3-20
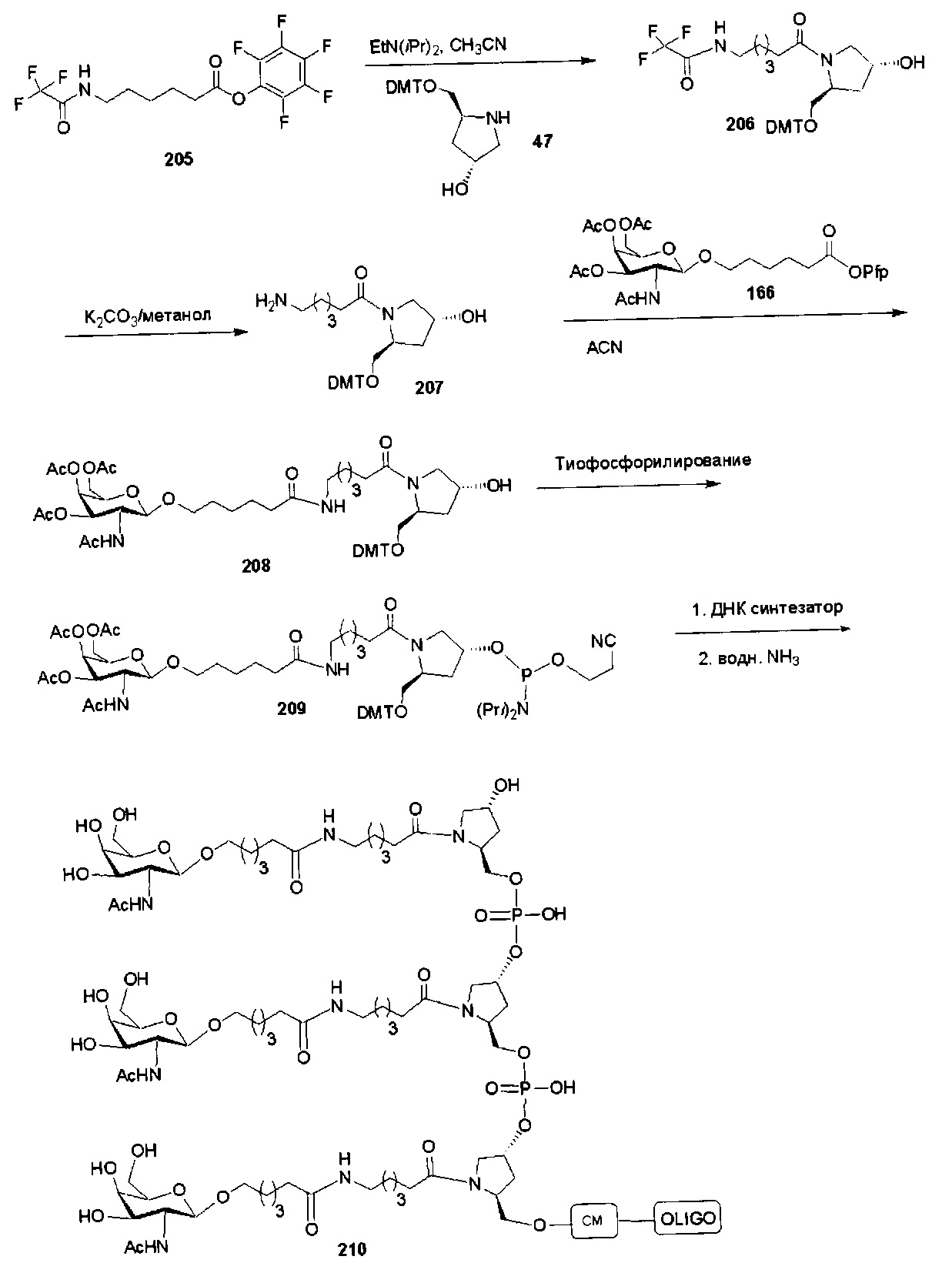
Соединение 205 получили добавлением PFP-ТФК и DIEA к 6-(2,2,2-трифторацетамидо)гексановой кислоте в ацетонитриле, которую получили добавлением трифторуксусного ангидрида к 6-аминогексановой кислоте. Реакционную смесь нагрели до 80°С, затем охладили до комнатной температуры. Олигомерное Соединение 210, содержащее конъюгирующую группу GalNAc3-20, получили из соединения 208 по общим способам, приведенным в Примере 52. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-20 (GalNAc3-20a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-. Структура GalNAc3-20 (GalNAc3-20a-CM-) приведена ниже:
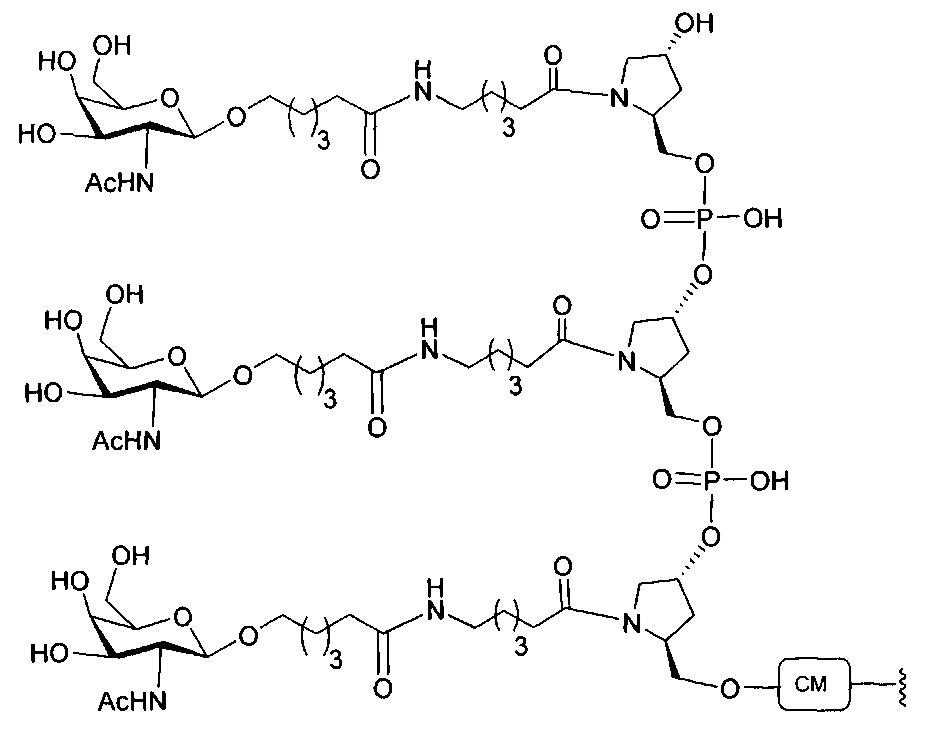
Пример 72. Получение олигомерного соединения 215, содержащего GalNAc3-21
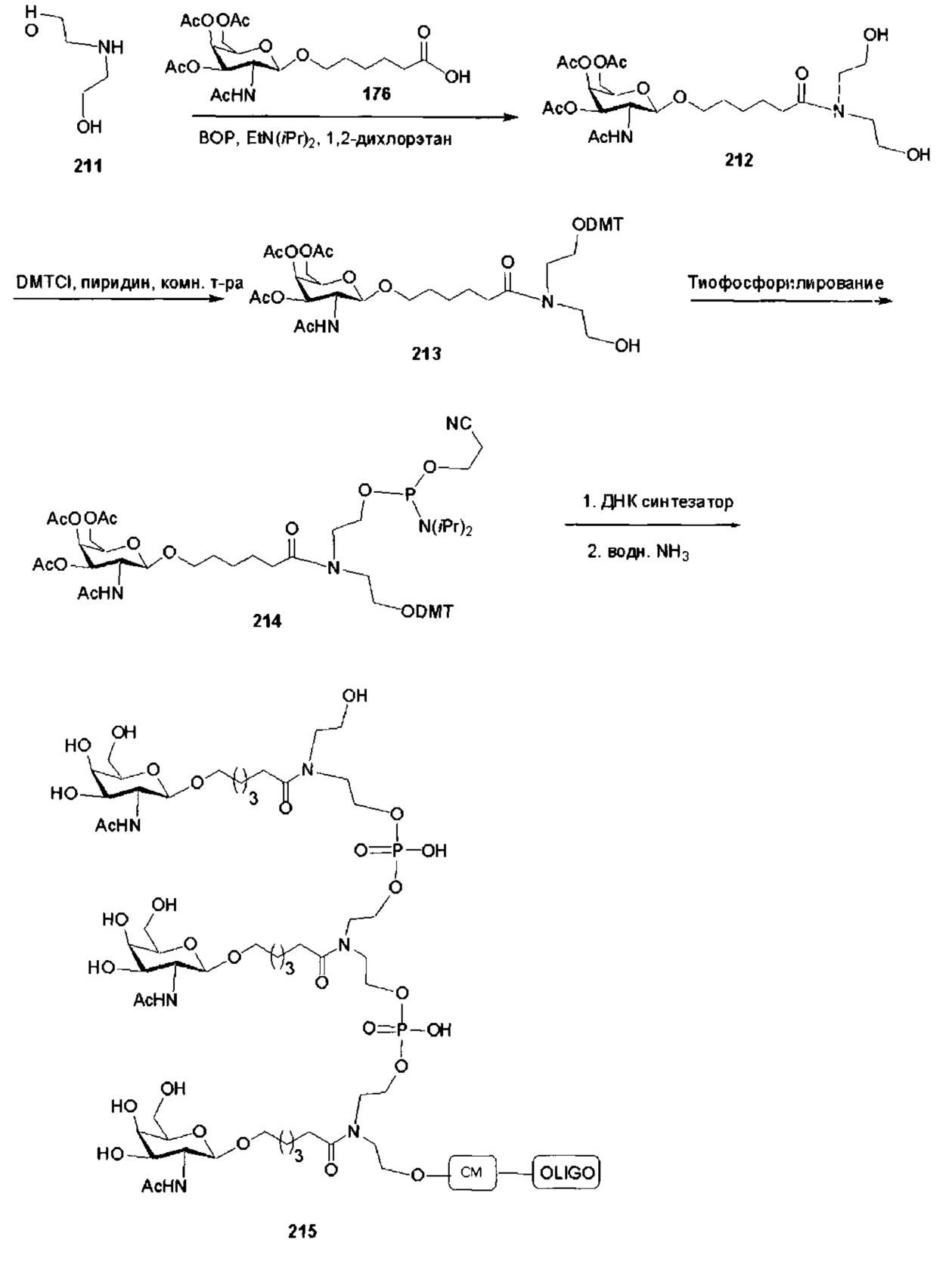
Соединение 211 имеется в продаже. Олигомерное Соединение 215, содержащее конъюгирующую группу GalNAc3-21, получили из соединения 213 по общим способам, приведенным в Примере 52. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-21 (GalNAc3-21a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-P(=O)(OH)-. Структура GalNAc3-21 (GalNAc3-21a-CM-) приведена ниже:
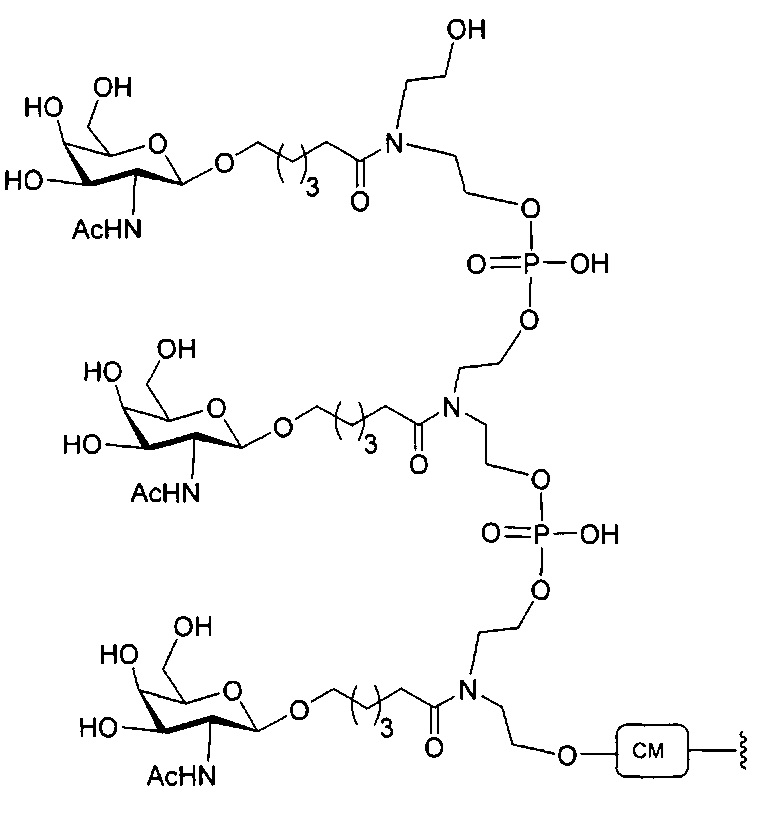
Пример 73. Получение олигомерного соединения 221, содержащего GalNAc3-22
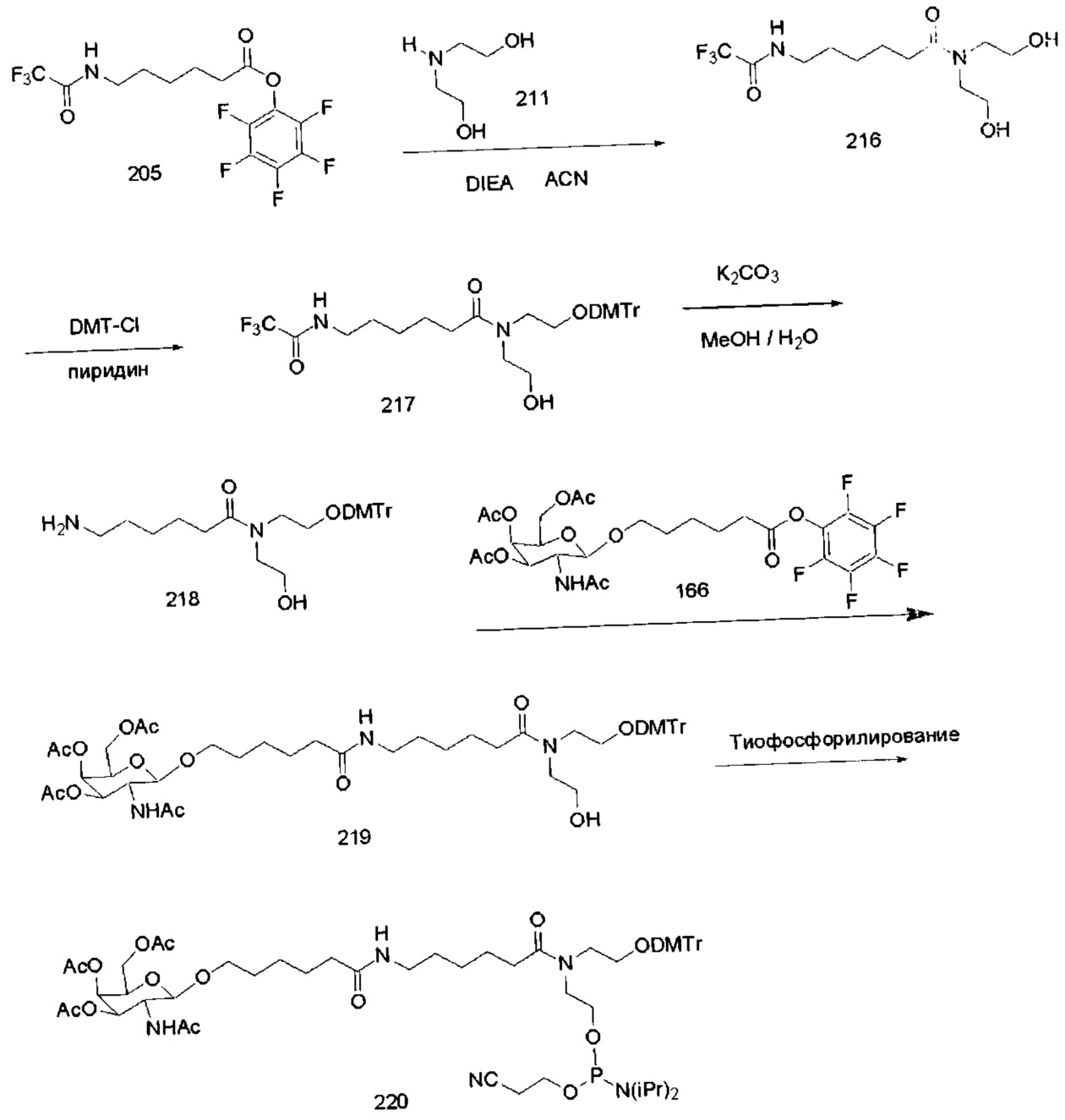
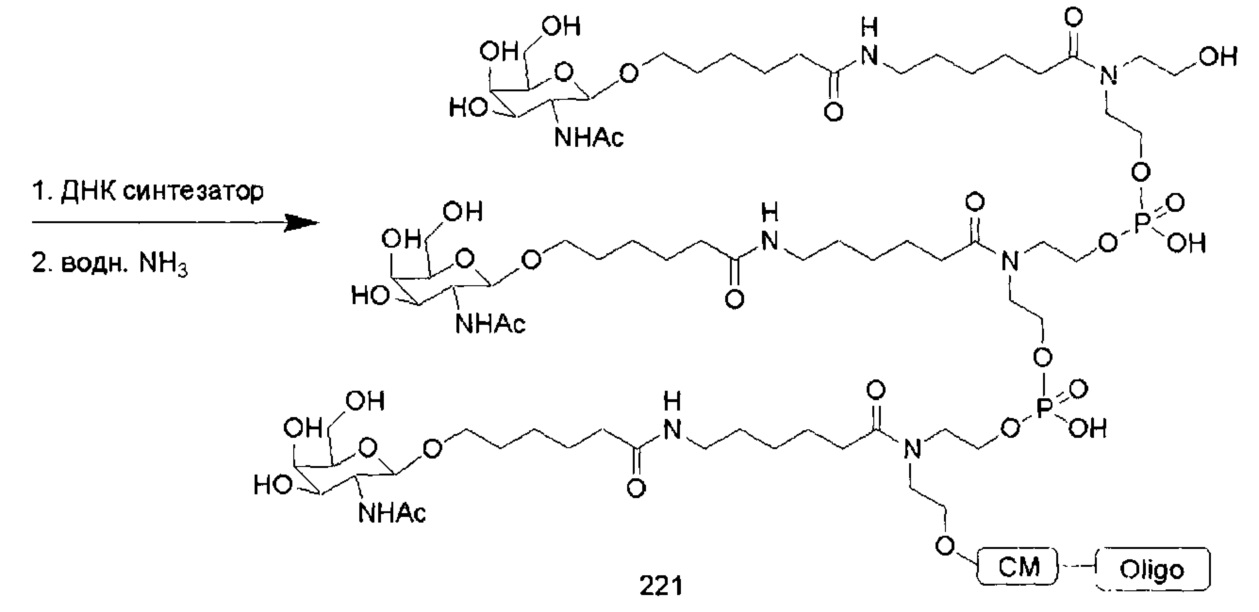
Соединение 220 получили из соединения 219, применив тетразолид диизопропиламмония. Олигомерное соединение 221, содержащее конъюгирующую группу GalNAc3-21, получили из соединения 220 по общему способу, приведенному в Примере 52. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-22 (GalNAc3-22a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. В некоторых вариантах реализации расщепляемый фрагмент представляет собой -P(=O)(OH)-Ad-Р(=O)(ОН)-. Структура GalNAc3-22 (GalNAc3-22a-CM-) приведена ниже:
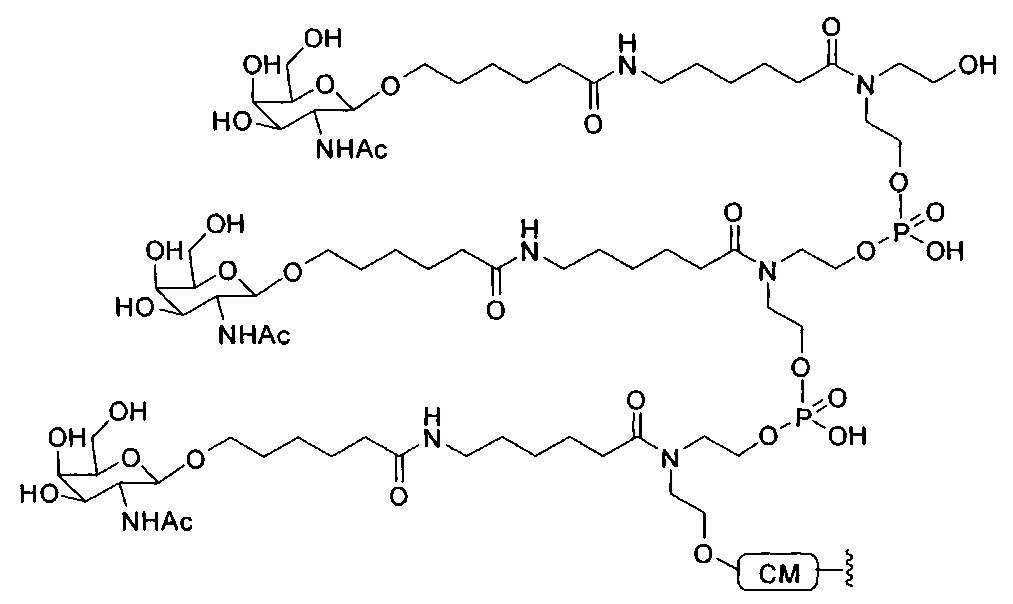
Пример 74. Влияние различных расщепляемых фрагментов на антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на SRB-1, содержащих конъюгат 5'-GalNAc3
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей. Каждая из конъюгирующих групп GalNAc3 была присоединена к 5'-концу соответствующего олигонуклеотида.

Во всех таблицах заглавные буквы указывают азотистое основание для каждого нуклеозида, аmC означает 5-метилцитозин. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «d» означает β-D-2'-дезоксирибонуклеозид; «s» означает тиофосфатную межнуклеозидную связь(PS); «о» означает фосфодиэфирную межнуклеозидную связь(РО); и «o'» означает -O-Р(=O)(ОН)-. Конъюгирующие группы выделены жирным шрифтом.
Структура GalNAc3-3a показана ранее в Примере 39. Структура GalNAc3-17а показана ранее в Примере 68, а структура GalNAc3-18a показана в Примере 69.
Лечение
Шести-восьминедельным мышам C57bl6 (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, приведенной ниже, олигонуклеотида, перечисленного в Таблице 60, или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часов после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, приведены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 61, лечение антисмысловыми олигонуклеотидами снимет уровни мРНК SRB-1 дозозависимым образом. Антисмысловые олигонуклеотиды. содержащие конъюгат GalNAc, демонстрируют равные эффективности и являются значительно более эффективными, чем исходный олигонуклеотид, не имеющий коньюгата GalNAc.
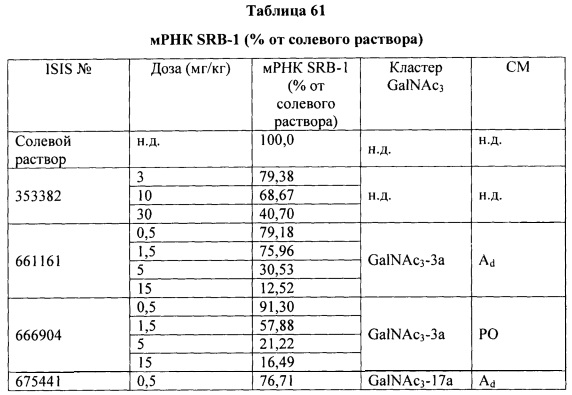
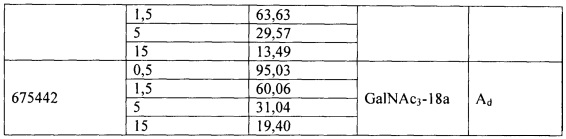
Уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке измеряли относительно мышей, инъецированных солевым раствором, применяя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором (данные не показаны). Значения ALT, AST, общего билирубина и АМК приведены ниже в Таблице 62.
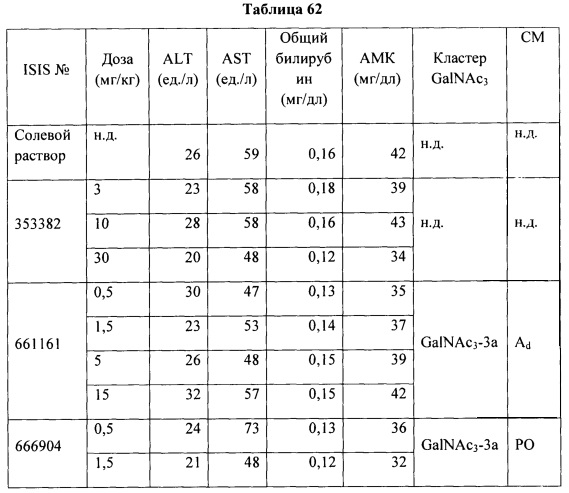
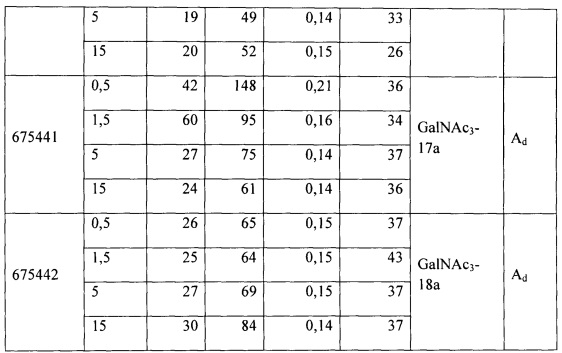
Пример 75. Фармакокинетический анализ олигонуклеотидов, содержащих 5'-конъюгирующую группу
ФК ASO, приведенных выше в Таблицах 54, 57 и 60, оценили с применением образцов печени, которые получили после выполнения способов лечения, описанных в Примерах 65, 66 и 74. Образцы печени измельчили и экстрагировали по стандартным протоколам, и анализировали при помощи ИП-ВЭЖХ-МС вместе с внутренним стандартом. Суммарный уровень (мкг/г) всех метаболитов в ткани измерили интегрированием соответствующих УФ пиков, а уровни в ткани ASO полной длины, не содержащих конъюгата («исходное», в данном случае Isis №353382), измерили с применением подходящих ион-экстракционных хроматограмм (EIC).

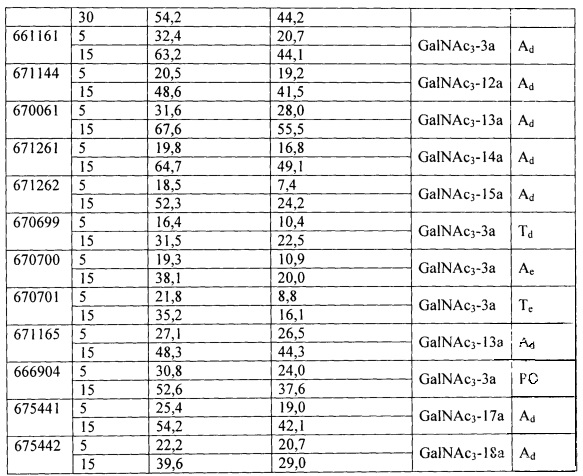
Результаты, приведенные выше в Таблице 63, демонстрируют, что наблюдали более высокие уровни в печени олигонуклеотидов, содержащих конъюгирующую группу GalNAc3, чем исходного олигонуклеотида, не содержащего конъюгирующую группу GalNAc3 (ISIS 353382) через 72 часа после введения олигонуклеотида, особенно с учетом введения различных доз для олигонуклеотидов с конъюгирующей группой GalNAc3 и без нее. Кроме того, через 72 часа 40-98% каждого олигонуклеотида, содержащего конъюгирующую группу GalNAc3, было метаболизировано до исходного соединения, что указывает кг то, что конъюгирующие группы GalNAc3 расщепляются в указанных олигонуклеотидах.
Пример 76. Получение олигомерного соединения 230, содержащего GalNAc3-23
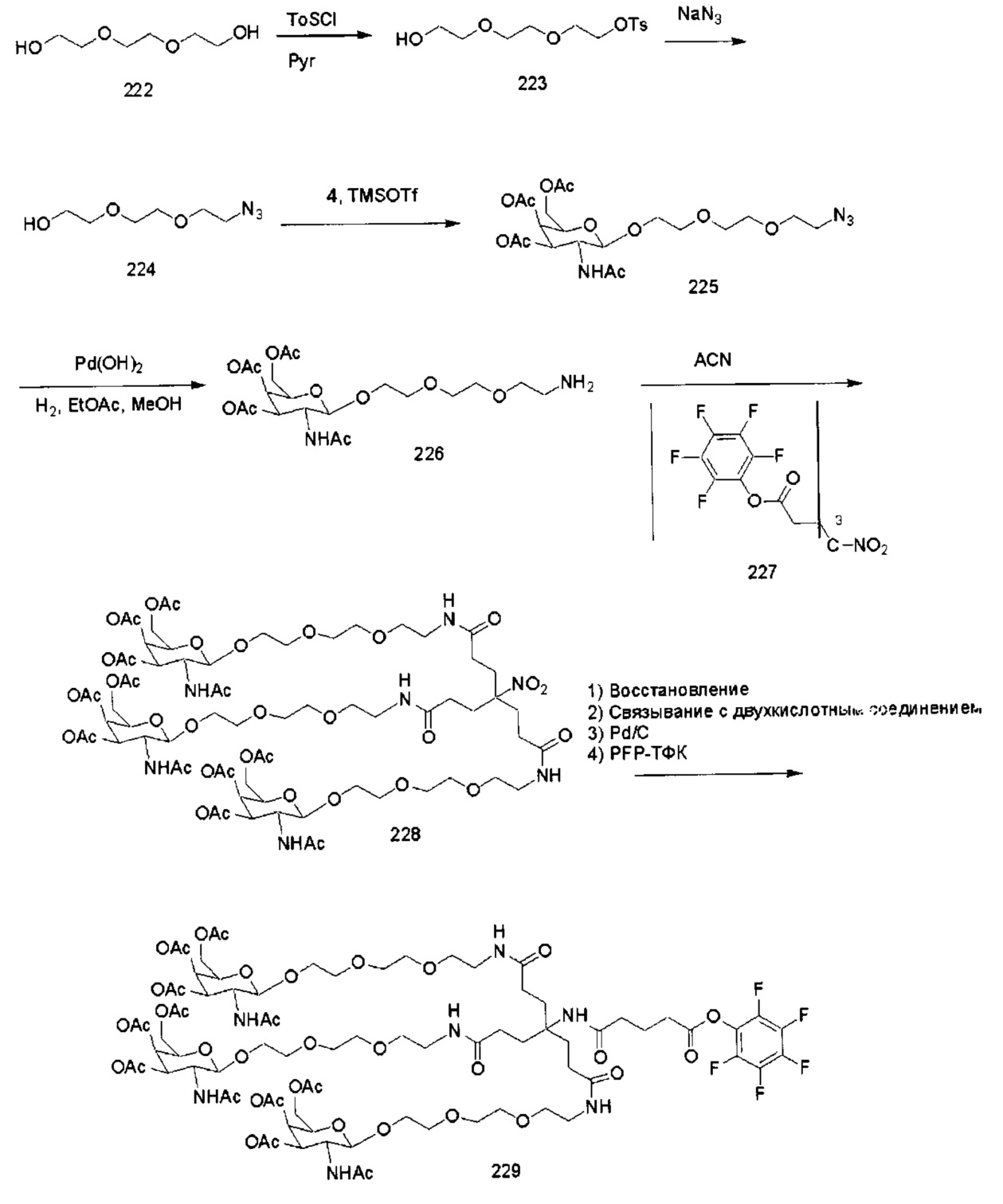
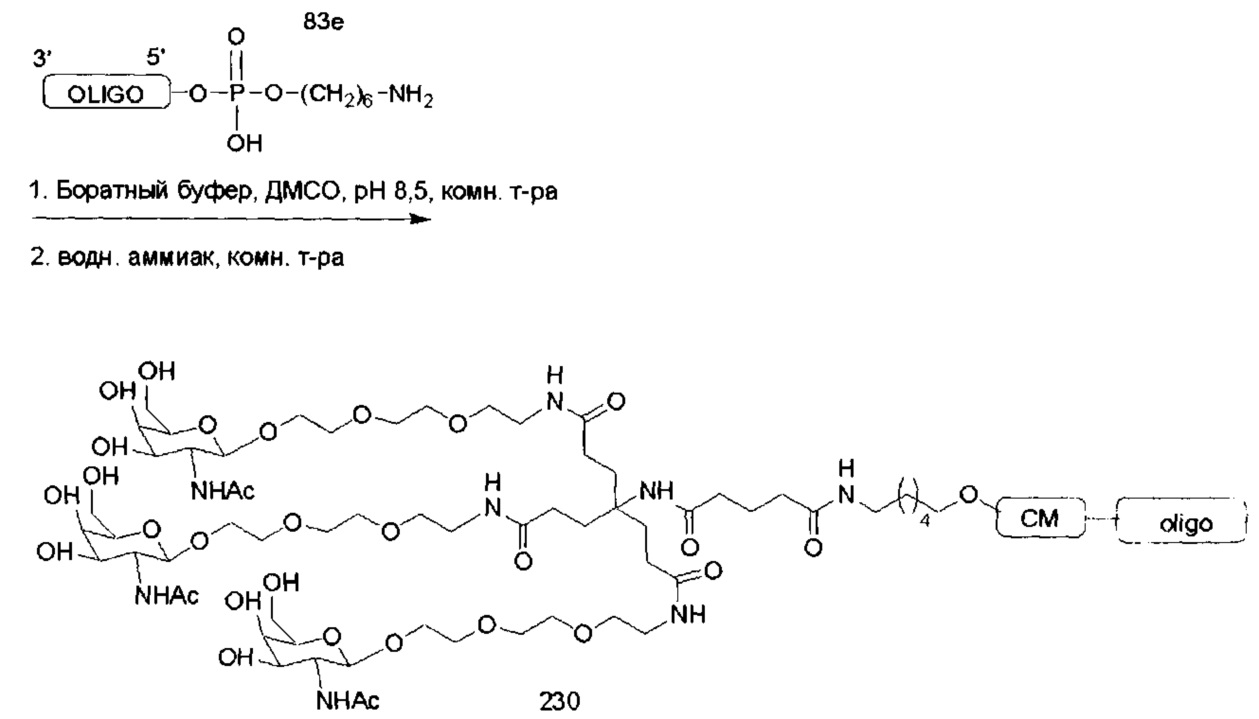
Соединение 222 имеется в продаже. 44,48 мл (0,33 моль) соединения 222 обрабатывали тозилхлоридом (25,39 г, 0,13 моль) в пиридине (500 мл) в течение 16 часов. Затем реакционную смесь выпарили до маслянистого вещества, растворили в EtOAc и промыли водой, насыщенным раствором NaHCO3, насыщенным солевым раствором и высушили над Na2SO4. Этилацетат концентрировали досуха и очистили колоночной хроматографией, элюировали EtOAc в гексанах (1:1), затем 10% метанола в CH2Cl2 получением соединения 223 в виде бесцветного маслянистого вещества. Данные ЖХМС и ЯМР согласовались с указанной структурой. 10 г (32,86 ммоль) 1-тозилтриэтиленгликоля (соединение 223) обрабатывали азидом натрия (10,68 г, 164,28 ммоль) в ДМСО (100 мл) при комнатной температуре в течение 17 часов. Затем реакционную смесь вылили в воду и экстрагировали EtOAc. Органический слой три раза промыли водой и высушили над Na2SO4. Органический слой концентрировали досуха с получением 5,3 г соединения 224 (92%). Данные ЖХМС и ЯМР согласовались с указанной структурой. 1-Азидотриэтиленгликоль (соединение 224, 5,53 г, 23,69 ммоль) и соединение 4 (6 г, 18,22 ммоль) обработали 4А молекулярными ситами (5 г) и TMSOTf (1,65 мл, 9,11 ммоль) в дихлорметане (100 мл) под инертной атмосферой. Через 14 часов реакционную смесь отфильтровали для удаления сит, а органический слой промыли насыщенным раствором NaHCO3, водой, насыщенным солевым раствором и высушили над Na2SO4. Органический слой концентрировали досуха и очистили колоночной хроматографией, элюировали градиентом от 2 до 4% метанола в дихлорметане с получением соединения 225. Данные ЖХМС и ЯМР согласовались со структурой. Соединение 225 (11,9 г, 23,59 ммоль) гидрировали в EtOAc/метаноле (4:1, 250 мл) на катализаторе Перлмана. Через 8 часов катализатор удалили фильтрованием, а растворители удалили до сухого остатка с получением соединения 226. Данные ЖХМС и ЯМР согласовались со структурой.
Для получения соединения 227 раствор нитрометантриспропионовой кислоты (4,17 г, 15,04 ммоль) и основание Хюнига (10,3 мл, 60,17 ммоль) в ДМФА (100 мл) по каплям обработали пентафтортрифторацетатом (9,05 мл, 52,65 ммоль). Через 30 минут реакционную смесь вылили в ледяную воду и экстрагировали EtOAc. Органический слой промыли водой, насыщенным солевым раствором и высушили над Na2SO4. Органический слой концентрировали досуха, а затем перекристаллизовали из гептана с получением соединен л 227 в виде белого твердого вещества. Данные ЖХМС и ЯМР согласовались с указанной структурой. Соединение 227 (1,5 г, 1,93 ммоль) и соединение 226 (3,7 г, 7,74 ммоль) перемешивали при комнатной температуре в ацетонитриле (15 мл) в течение 2 часов. Затем реакционную смесь выпарили досуха и очистили колоночной хроматографией, элюируя градиентом от 2 до 10% метанола в дихлорметане, с получением соединения 228. Данные ЖХМС и ЯМР согласовались со структурой. Соединение 228 (1,7 г, 1,02 ммоль) обработали никелем Ренея (около 2 г, влажный) в этаноле (100 мл) в атмосфере водорода. Через 12 часов катализатор удалили фильтрованием, а органический слой выпарили до твердого вещества, которое применили непосредственно на следующей стадии. Данные ЖХМС и ЯМР согласовались с указанной структурой. Это твердое вещество (0,87 г, 0,53 ммоль) обработали бензилглутаровой кислотой (0,18 г, 0,8 ммоль), HBTU (0,3 г, 0,8 ммоль) и DIEA (273,7 мкл, 1,6 ммоль) в ДМФА (5 мл). Через 16 часов ДМФА удалили при пониженном давлении при 65°С до маслянистого вещества, и это маслянистое вещество растворили в дихлорметане. Органический слой промыли насыщенным раствором NaHCO3, насыщенным солевым раствором и высушили над Na2SO4. После выпаривания органического слоя соединение очистили колоночной хроматографией и элюировали градиентом от 2 до 20% метанола в дихлорметане с получением связанного продукта. Данные ЖХМС и ЯМР согласовались с указанной структурой. С бензилового эфира сняли защиту на катализаторе Перлмана в атмосфере водорода в течение 1 часа. Затем катализатор удалили фильтрованием, а растворители удалили до сухого остатка с получением кислоты. Данные ЖХМС и ЯМР согласовались с указанной структурой. Эту кислоту (486 мг, 0,27 ммоль) растворили в сухом ДМФА (3 мл). Добавили пиридин (53,61 мкл, 0,66 ммоль) и продули реакционную смесь аргоном. К реакционной смеси медленно добавили пентафтортрифторацетат (46,39 мкл, 0,4 ммоль). Цвет реакционной смеси изменился с бледно-желтого на винный, и появился легкий дымок, который улетучился с потоком аргона. Реакционную смесь оставили перемешиваться при комнатной температуре на один час (завершение реакции подтвердили по ЖХМС). Растворитель удалили при пониженном давлении (ротационный испаритель) при 70°С. Остаток разбавили ДХМ и промыли 1 н. NaHSO4, насыщенным солевым раствором, насыщенным раствором бикарбоната натрия и снова насыщенным солевым раствором. Органический слой высушили над Na2SO4, отфильтровали и концентрировали досуха с получением 225 мг соединения 229 в виде хрупкой желтой пены. Данные ЖХМС и ЯМР согласовались с указанной структурой.
Олигомерное Соединение 230, содержащее конъюгирующую группу GalNAc3-23, получили из соединения 229 по общим способам, приведенным в Примере 46. Кластерная часть GalNAc3 конъюгирующие группы GalNAc3-23 (GalNAc3-23a) может быть комбинирована с любым расщепляемым фрагментом для получения различных конъюгирующих групп. Структура GalNAc3-23 (GalNAc3-23a-CM) приведена ниже:
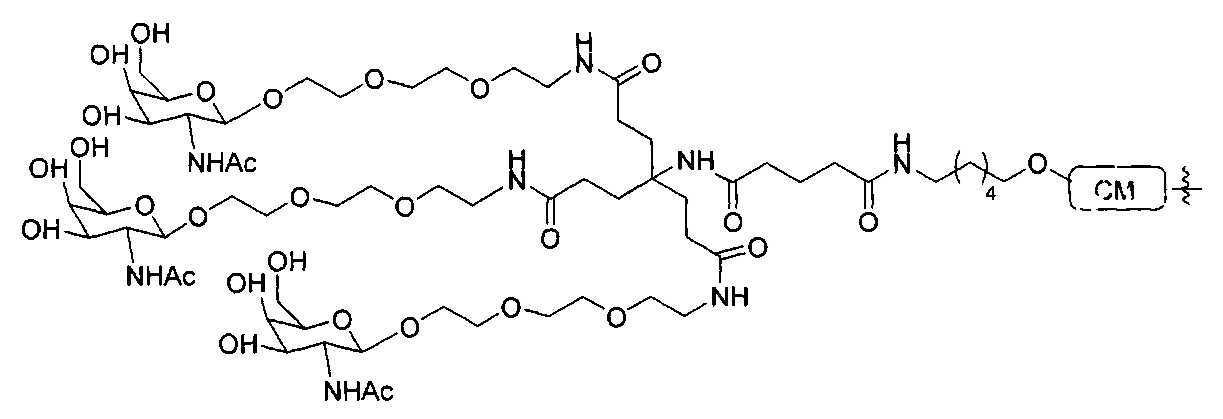
Пример 77. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на SRB-1, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей.
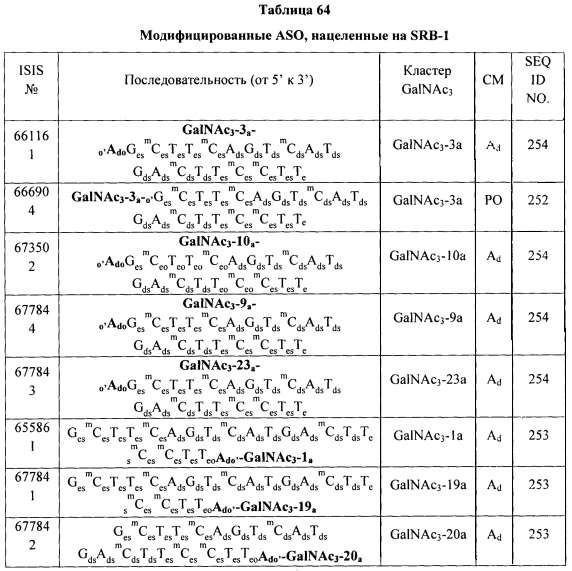
Структура GalNAc3-1a показана ранее в Примере 9, GalNAc3-3a показана в Примере 39, GalNAc3-9a показана в Примере 52, GalNAc3-10a показана в Примере 46, GalNAc3-19a показана в Примере 70, GalNAc3-20a показана в Примере 71, и GalNAc3-23a показана в Примере 76.
Лечение
Шести-восьминедельным мышам C57bl6 (Jackson Laboratory, Бар-Харбор,штат Мэн) ввели однократную подкожную инъекцию дозы, приведенной ниже, олигонуклеотида, перечисленного в Таблице 64, или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часов после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, приведены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблице 65, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом.
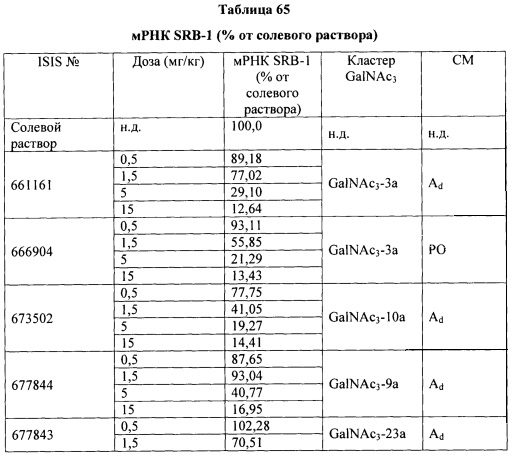
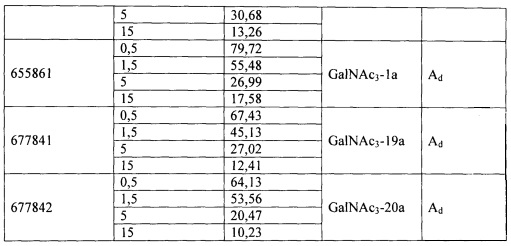
Измерили также уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в сыворотке, применяя стандартные протоколы. Оценили также общий билирубин и азот мочевины крови (АМК). Проверили изменение массы тела, которое существенно не отличалось от группы с солевым раствором (данные не показаны). Значения ALT, AST, общего билирубина и АМК приведены ниже в Таблице 66.
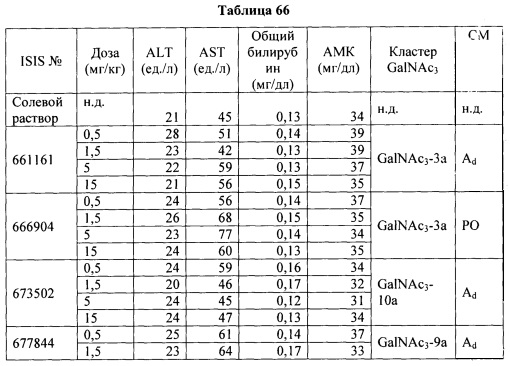
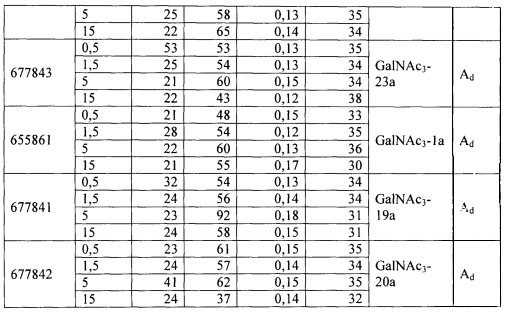
Пример 78. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на ангиотензиноген, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные ниже, испытали в дозозависимом исследовании антисмыслового ингибирования ангиотензиногена (AGT) у нормотензивных мышей Спрага-Доули.

Структура GalNAc3-1a показана ранее в Примере 9.
Лечение
Шестинедельным самцам крыс Спрага-Доули один раз в неделю вводили подкожную инъекцию дозы, приведенной ниже, в целом три дозы олигонуклеотида, перечисленного в Таблице 67, или PBS. Каждая экспериментальная группа состояла из 4 животных. Крыс умертвили через 72 часа после последней дозы. Уровни мРНК AGT в печени измерили при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Уровни белка AGT в плазме измерили при помощи твердофазного иммуноферментного анализа для определения общего ангиотензиногена (кат. № JP27412, IBL International, Торонто, штат Онтарио) с разбавлением плазмы 1:20000. Результаты, показанные ниже, приведены как средний процент от уровней мРНК AGT в печени или от уровней белка AGT в плазме для каждой экспериментальной группы, нормализованных к контрольному образцу с PBS.
Как показано в Таблице 68, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК AGT в печени и уровни белка в плазме дозозависимым образом, и олигонуклеотид, содержащий конъюгат GalNAc, был значительно более эффективным, чем исходный олигонуклеотид, не содержащий конъюгата GalNAc.
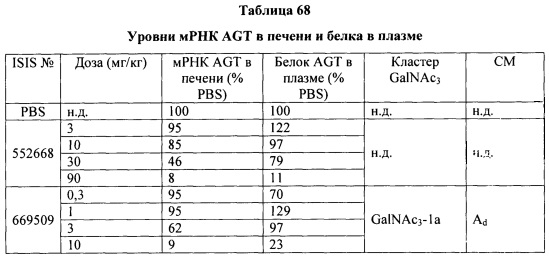
Измерили также уровни трансаминазы в печени, аланин-аминотрансферазы (ALT) и аспартат-аминотрансферазы (AST) в плазме, а также массу тела в момент умерщвления, применяя стандартные протоколы. Результаты приведены ниже в Таблице 69.
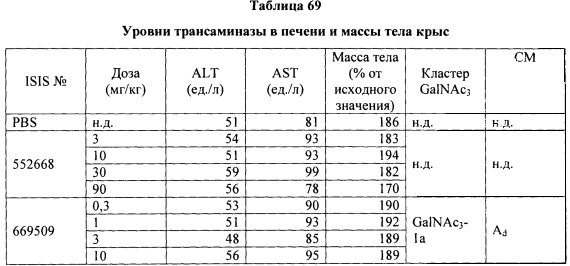
Пример 79. Продолжительность действия in vivo олигонуклеотидов, нацеленных на АРОС-III, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 70, испытали в исследовании однократной дозы на продолжительность действия у мышей.

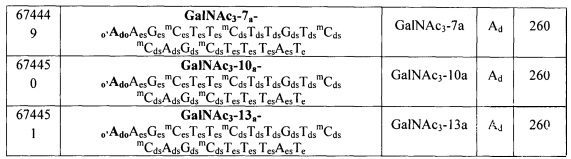
Структура GalNAc3-1a показана ранее в Примере 9, GalNAc3-3a показана в Примере 39, GalNAc3-7a показана в Примере 48, GalNAc3-10a показана в Примере 46, и GalNAc3-13a показана в Примере 62.
Лечение
Шести-восьминедельным трансгенным мышам, экспрессирующим человеческий АРОС-III, ввели однократную подкожную инъекцию олигонуклеотида, перечисленного в Таблице 70, или PBS. Каждая экспериментальная группа состояла из 3 животных. Образцы крови брали до введения дозы для определения исходного значения, а также через 72 часа. 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель и 6 недель после введения дозы. Уровни триглицеридов и белка АРОС-III в плазме измерили так, как описано е Примере 20. Результаты, показанные ниже, приведены как средний процент от уровней триглицеридов и АРОС-III в плазме для каждой экспериментальной группы, нормализованных и исходным значениям, и они демонстрируют, что олигонуклеотиды, содержащие конъюгирующую группу GalNAc, обладают более продолжительным действием, чем исходный олигонуклеотид, не содержащий конъюгирующую группу (ISIS 304801) даже несмотря на то, что доза исходного соединения была в три раза выше, чем доза олигонуклеотидов, содержащих конъюгирующую группу GalNAc.
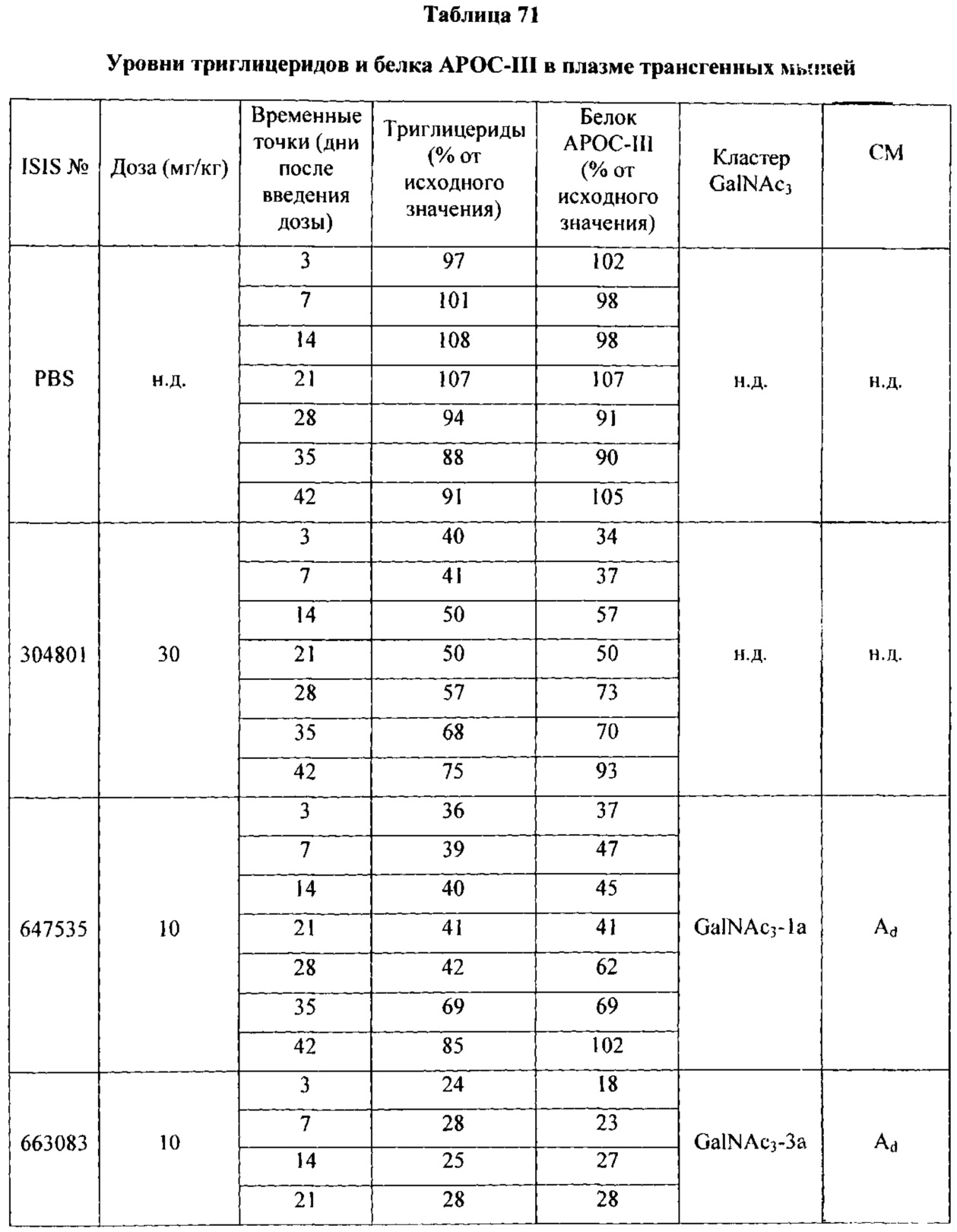
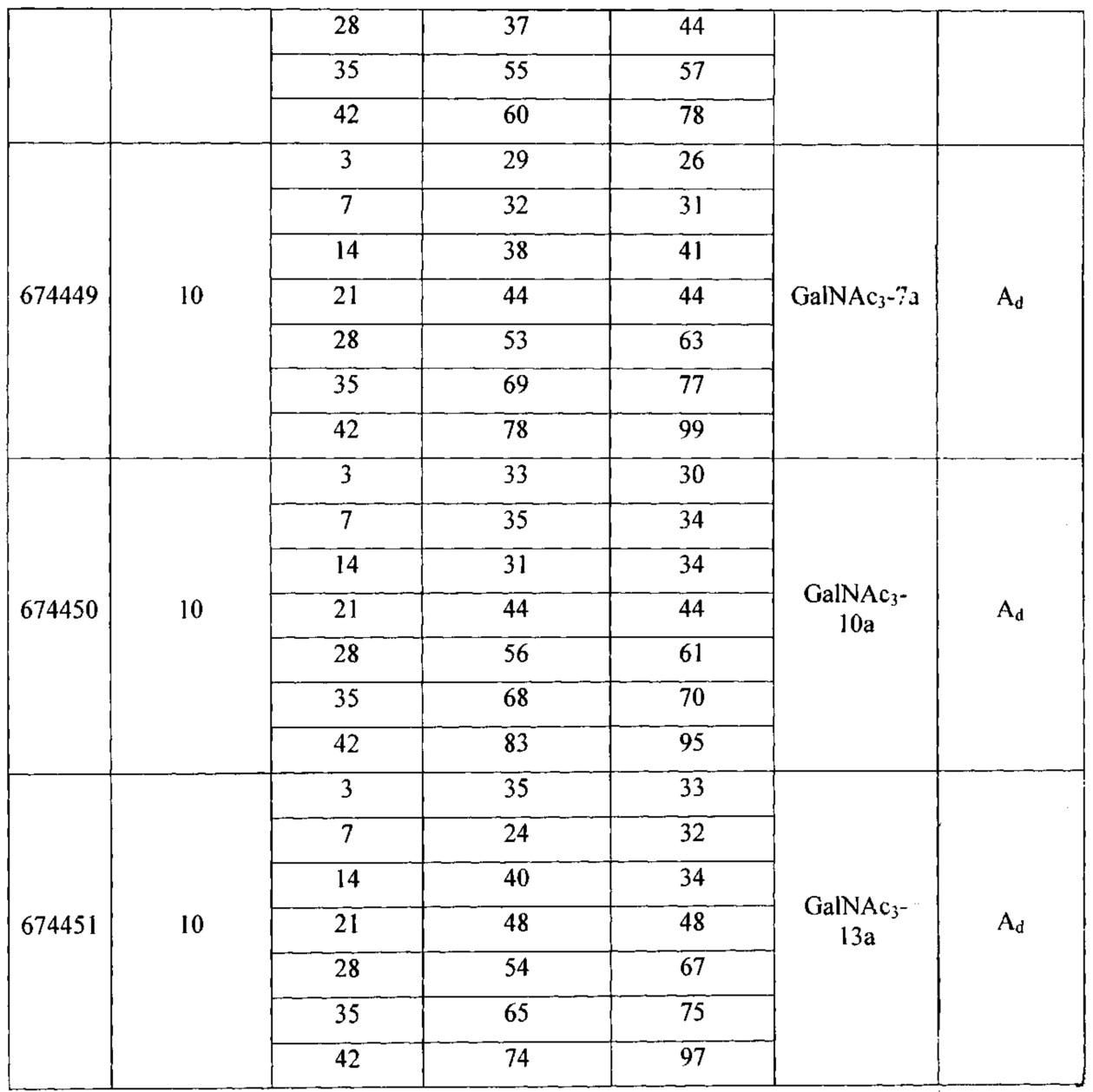
Пример 80. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на альфа-1 антитрипсин (А1АТ), содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 72, испытали в исследовании дозозависимого ингибирования А1АТ у мышей.
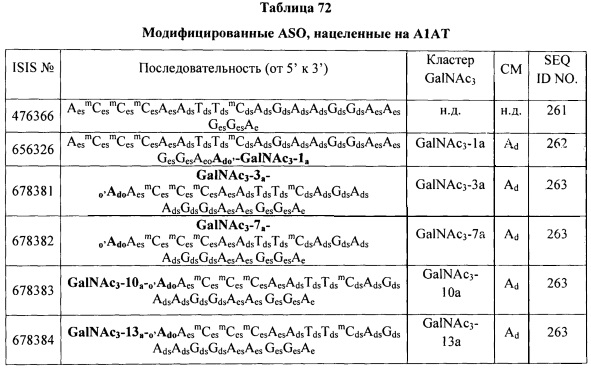
Структура GalNAc3-1a показана ранее в Примере 9, GalNAc3-3a показана в Примере 39, GalNAc3-7a показана в Примере 48, GalNAc3-10a показана в Примере 46, и GalNAc3-13a показана в Примере 62.
Лечение
Шестинедельным самцам мышей C57BL/6 (Jackson Laboratory, Бар-Харбор, штат Мэн) один раз в неделю вводили подкожную инъекцию дозы, приведенной ниже, в целом три дозы олигонуклеотида, перечисленного в Таблице 72, или PBS. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часа после последнего введения. Уровни мРНК А1АТ в печени определили при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Уровни белка А1АТ в плазме определили при помощи твердофазного иммуноферментного анализа для определения мышиного альфа 1-антитрипсина (кат. №41-A1AMS-E01, Alpco, Салем, штат Нью-Гэмпшир). Результаты, показанные ниже, приведены как средний процент уровней мРНК А1АТ в печени и белка в плазме для каждой экспериментальной группы, нормализованных к контрольному образцу с PBS.
Как показано в Таблице 73, лечение антисмысловыми олигонуклеотидамн снижает уровни мРНК А1АТ в печени и уровни белка А1АТ в плазме дозозависимым образом. Олигонуклеотиды, содержащие конъюгат GalNAc, были значительно более эффективными, чем исходное соединение (ISIS 476366).
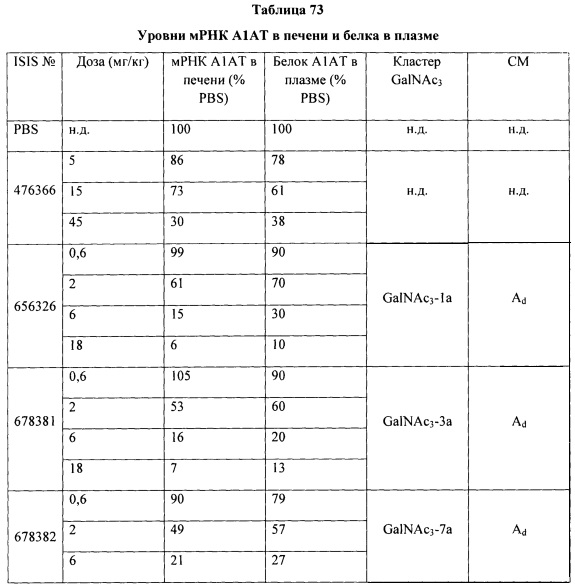
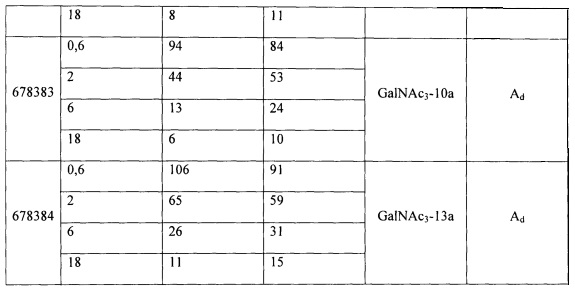
Во время умерщвления измерили уровни трансаминазы в печени и АМК в плазме по стандартным протоколам. Измерили также массы тела и массы органов. Результаты приведены ниже в Таблице 74. Масса тела приведена как % относительно исходного значения. Массы органов приведены как % от массы тела относительно контрольной группы с PBS.
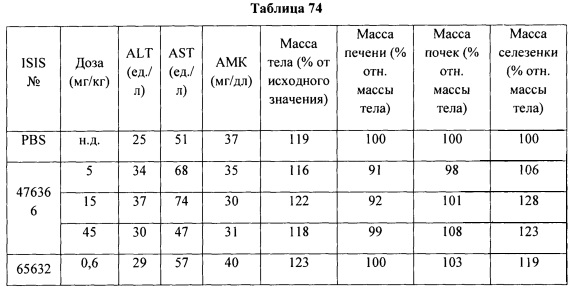
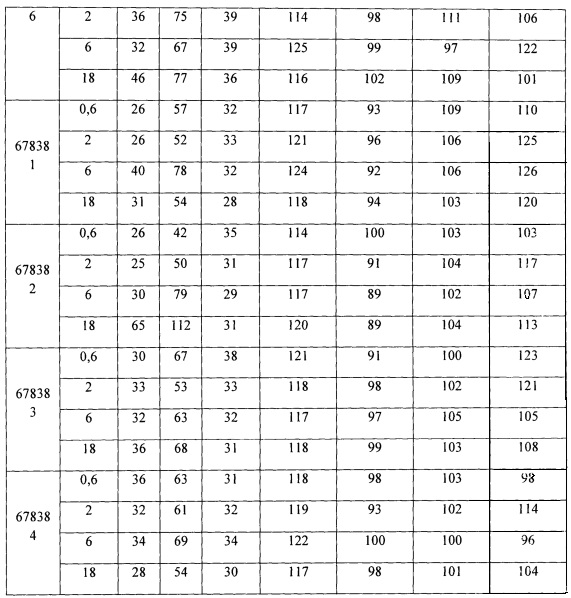
Пример 81. Продолжительность действия in vivo олигонуклеотидов, нацеленных на А1АТ, содержащих кластер GalNAc3
Олигонуклеотиды, перечисленные в Таблице 72, испытали в исследовании однократной дозы на продолжительность действия у мышей.
Лечение
Шестинедельным самцам мышей C57BL/6 ввели однократную подкожную инъекцию олигонуклеотида, перечисленного в Таблице 72, или PBS. Каждая экспериментальная группа состояла из 4 животных. Образцы крови брали за день до введения дозы для определения исходного значения, а также на 5, 12, 19 и 25 день после введения дозы. Уровни белка A1AT в плазме измерили при помощи твердофазного иммуноферментного анализа (см. Пример 80). Результаты, показанные ниже, приведены как средний процент уровней белка A1AT в плазме для каждой экспериментальной группы, нормализованных к исходным уровням. Результаты демонстрируют, что олигонуклеотиды, содержащие конъюгат GalNAc, были более эффективными и имели более продолжительное действие, чем исходное соединение без конъюгата GalNAc (ISIS 476366). Кроме того, олигонуклеотиды, содержащие 5'-GalNAc конъюгат (ISIS 678381, 678382, 678383 и 678384), были, в целом, еще более эффективными с еще более продолжительным действием, чем олигонуклеотид, содержащий 3'-GalNAc конъюгат (ISIS 656326).
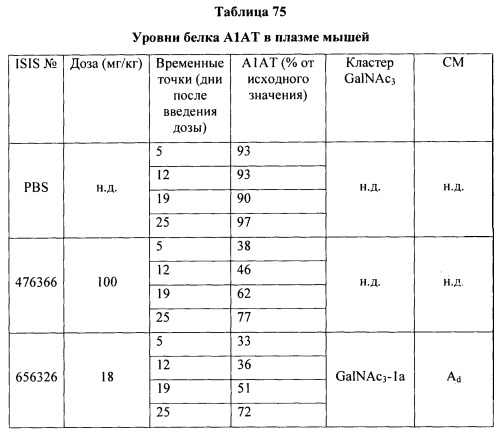
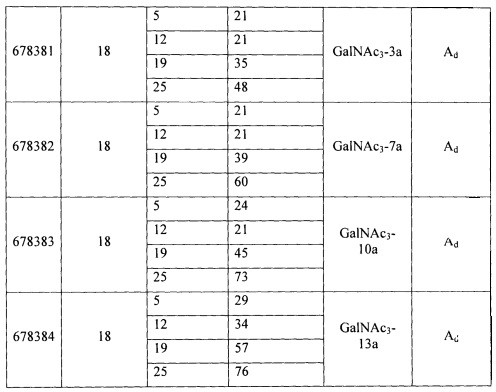
Пример 82. Антисмысловое ингибирование in vitro под действием олигонуклеотидов, нацеленных на SRB-1, содержащих конъюгат GalNAc3
Первичные гепатоциты печени мышей высеивали в 96-луночные планшеты при 15000 клеток на лунку за 2 часа до обработки. Олигонуклеотиды, перечисленные в Таблице 76, добавили в концентрации 2, 10, 50 или 250 нМ в среде Уильяма Е, и инкубировали клетка в течение ночи при 37°С в 5% СО2. Клетки лизировали через 16 часов после добавления олигонуклеотида, а общую РНК очистили при помощи RNease 3000 BioRobot (Qiagen). Уровни мРНК SRB-1 определили при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Значения IC50 определили при помощи программы Prism 4 (GraphPad). Результаты демонстрируют, что олигонуклеотиды, содержащие множество различных конъюгирующих групп GalNAc и множество различных расщепляемых фрагментов, являются значительно более эффективными в in vitro эксперименте свободного поглощения, чем исходные олигонуклеотиды, не содержащие конъюгирующую группу GalNAc (ISIS 353382 и 666841).
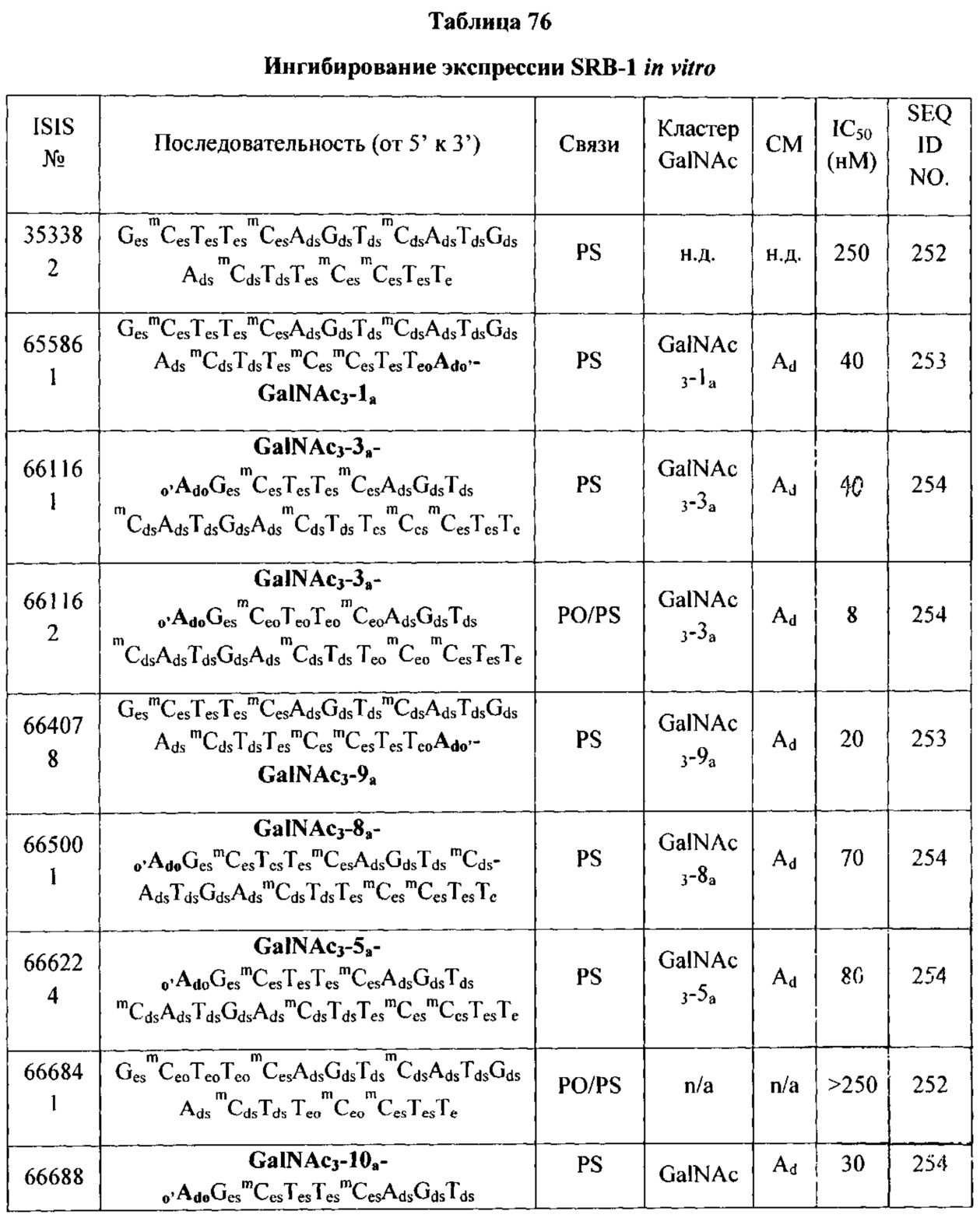
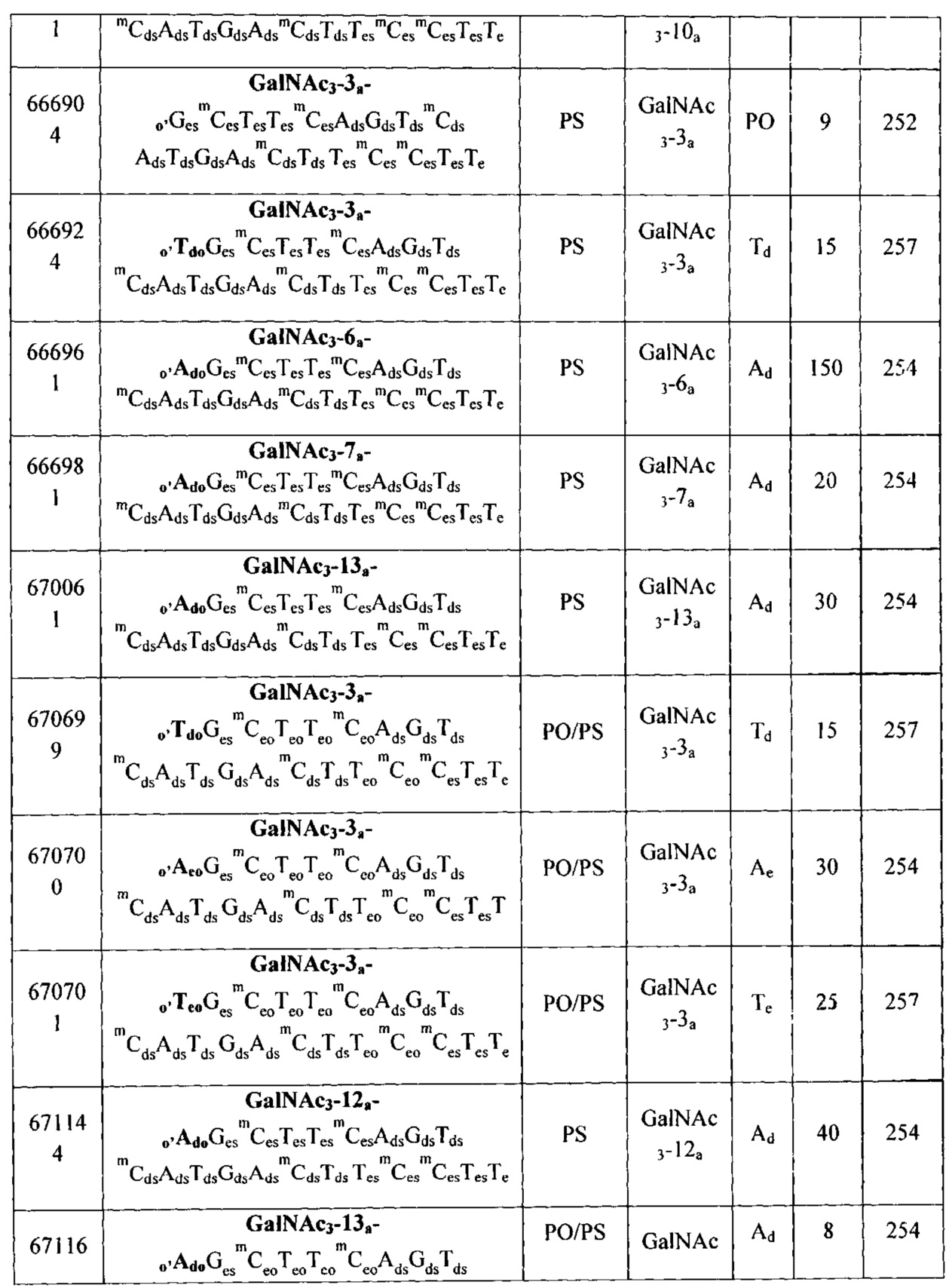
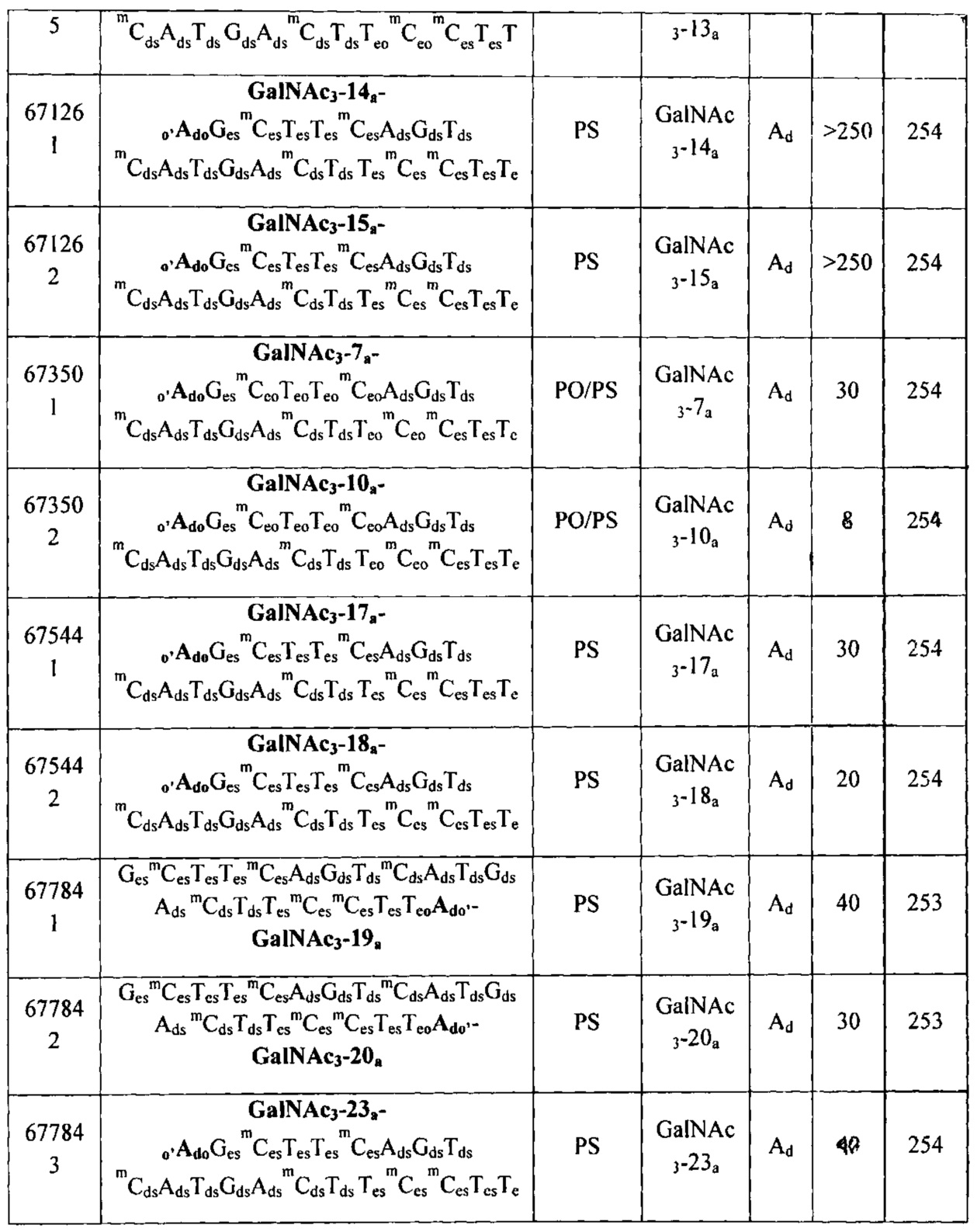
Структура GalNAc3-1a показана ранее в Примере 9, GalNAc3-3a показана в Примере 39, GalNAc3-5a показана в Примере 49, GalNAc3-6a показана в Примере 51, GalNAc3-7a показана в Примере 48, GalNAc3-8a показана в Примере 47, GalNAc3-9a показана в Примере 52, GalNAc3-10а показана в Примере 46, GalNAc3-12a показана в Примере 61, GalNAc3-13a показана в Примере 62, GalNAc3-14a показана в Примере 63, GalNAc3-15a показана в Примере 64, GalNAc3-17а показана в Примере 68, GalNAc3-18a показана в Примере 69, GalNAc3-19a показана в Примере 70, GalNAc3-20a показана в Примере 71, и GalNAc3-23a показана в Примере 76.
Пример 83. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на фактор XI, содержащих кластер GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 77, испытали в исследовании дозозависимого ингибирования фактора XI у мышей.


Структура GalNAc3-1a показана ранее в Примере 9, GalNAc3-3a показана в Примере 39, GalNAc3-7a показана в Примере 48, GalNAc3-10a показана в Примере 46, и GalNAc3-13a показана в Примере 62.
Лечение
Шести-восьминедельным мышам один раз в неделю вводили подкожную инъекцию дозы, приведенной ниже, в целом три дозы олигонуклеотида, перечисленного ниже, или PBS. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часа после последней дозы. Уровни мРНК фактора XI в печени измерили при помощи ПЦР в реальном времени и нормализовали к циклофилину по стандартным протоколам. Измерили также трансаминазы в печени, АМК и билирубин. Результаты, показанные ниже, приведены как средний процент для каждой экспериментальной группы, нормализованный к контролю с PBS.
Как показано в Таблице 78, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК фактора XI в печени дозозависимым образом. Результаты демонстрируют, что олигонуклеотиды, содержащие конъюгат GalNAc, были более эффективными, чем исходное соединение без конъюгата GalNAc (ISIS 404071). Кроме того, олигонуклеотиды, содержащие 5'-GalNAc конъюгат (ISIS 663086, 678347, 678348 и 678349), были еще более эффективными, чем олигонуклеотид, содержащий 3'-GalNAc конъюгат (ISIS 656173).
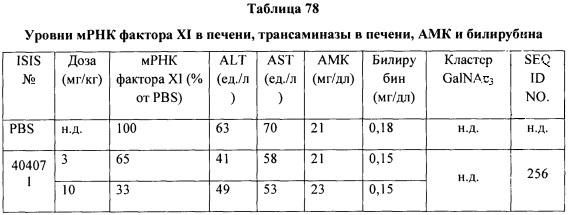
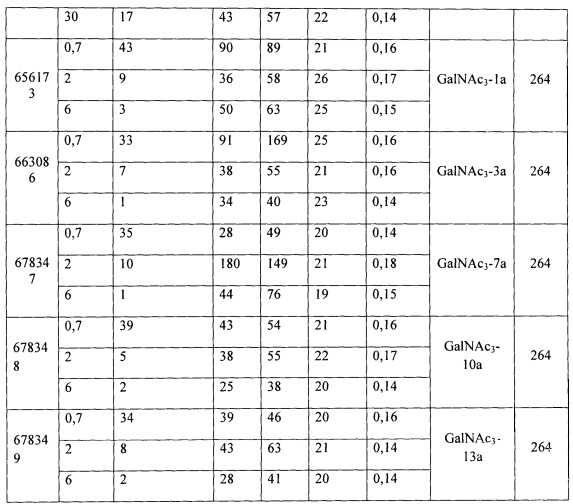
Пример 84. Продолжительность действия in vivo олигонуклеотидов, нацеленных на фактор XI, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные в Таблице 77, испытали в исследовании однократной дозы на продолжительность действия у мышей.
Лечение
Шести-восьминедельным мышам ввели однократную подкожную инъекцию олигонуклеотида, перечисленного в Таблице 77, или PBS. Каждая экспериментальная группа состояла из 4 животных. Образцы крови брали из хвостовой вены за день до введения дозы для определения исходного значения, а также на 3, 10 и 17 день после введения дозы. Уровни белка фактора XI в плазме определяли твердофазным иммуноферментным анализом, применяя иммобилизованные и биотинилированные детекторные антитела для фактора XI производства R&D Systems, Миннеаполис, штат Миннесота (кат. № AF2460 и № BAF2460, соответственно), а также реагент OptEIA, набор В (кат. №550534, BD Biosciences, Сан-Хосе, штат Калифорния). Результаты, показанные ниже, приведены как средний процент уровней белка фактора XI в плазме для каждой экспериментальной группы, нормализованных к исходным уровням. Результаты демонстрируют, что олигонуклеотиды, содержащие конъюгат GalNAc, были более эффективными и имели более продолжительное действие, чем исходное соединение без конъюгата GalNAc (ISIS 404071). Кроме того, олигонуклеотиды, содержащие 5'-GalNAc конъюгат (ISIS 663086, 678347, 678348 и 678349), были еще более эффективными с еще более продолжительным действием, чем олигонуклеотид, содержащий 3'-GalNAc конъюгат (ISIS 656173).
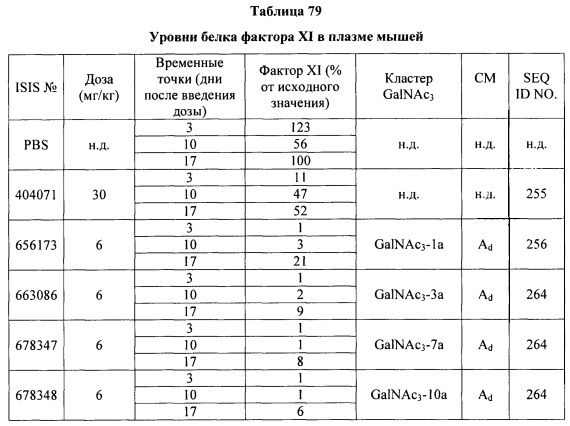
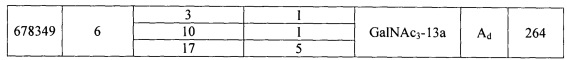
Пример 85. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на SRB-1, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные в Таблице 76, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей.
Лечение
Шести-восьминедельным мышам C57BL/6 один раз в неделю вводили подкожную инъекцию дозы, приведенной ниже, в целом три дозы олигонуклеотида, перечисленного в Таблице 76, или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 48 часов после последнего введения для определения уровней мРНК SRB-1 в печени при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Результаты, показанные ниже, приведены как средний процент уровней мРНК SRB-1 в печени для каждой экспериментальной группы, нормализованных к контрольному образцу, обработанному солевым раствором.
Как показано в Таблицах 80 и 81, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом.
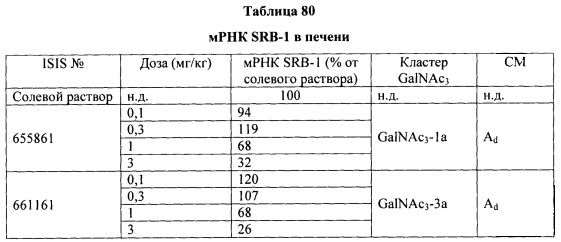
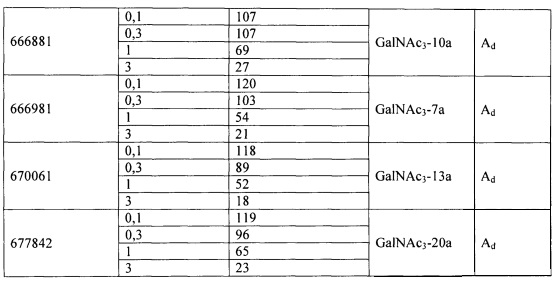

Измерили также уровни трансаминазы в печени, общего билирубина, АМК и массы тела по стандартным протоколам. Средние значения для каждой экспериментальной группы приведены ниже в Таблице 82.
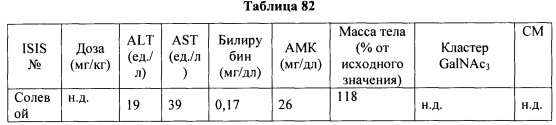
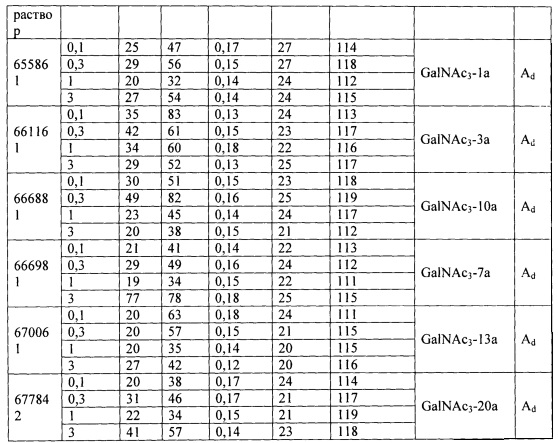
Пример 86. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на TTR, содержащих кластер GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 83, испытали в дозозависимом исследовании антисмыслового ингибирования человеческого транстиретина (TTR) у трансгенных мышей, экспрессирующих человеческий TTR ген.
Лечение
Восьминедельным TTR трансгенным мышам один раз в неделю в течение трех недель, в целом три дозы, вводили подкожную инъекцию олигонуклеотида и дозы, перечисленных в приведенных ниже таблицах, или PBS. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часа после последнего введения. В течение эксперимента в различных временных точках брали образцы крови из хвостовой вены и измеряли уровни белка TTR в плазме, ALT и AST, которые приведены в Таблицах 85-87. После умерщвления животных измерили уровни ALT, AST и человеческого TTR в плазме, а также массы тела, массы органов и уровни мРНК человеческого TTR в печени. Уровни белка TTR измерили при помощи клинического анализатора (AU480, Beckman Coulter, штат Калифорния). ПЦР в реальном времени и реагент для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) применяли по стандартным протоколам для определения уровней мРНК человеческого TTR в печени. Результаты, показанные в Таблицах 84-87, представляют собой средние значения для каждой экспериментальной группы. Уровни мРНК представляют собой средние значения относительно среднего значения для PBS группы. Уровни белка в плазме представляют собой средние значения относительно среднего значения для PBS группы в исходном состоянии. Массы тела представляют собой среднее процентное изменение массы от исходного значения до умерщвления для каждой отдельной экспериментальной группы. Приведенные массы органов нормализованы к массе тела животного, а затем приведена средняя нормализованная масса органов для каждой экспериментальной группы относительно средней нормализованной массы органов для PBS группы.
В Таблицах 84-87 «BL» означает исходное значения измерений, выполненных непосредственно перед введением первой дозы. Как показано в Таблицах 84 и 85, лечение антисмысловыми олигонуклеотидами снижает уровни экспрессии TTR дозозависимым образом. Олигонуклеотиды, содержащие конъюгат GalNAc, были более эффективными, чем исходное соединение без конъюгата GalNAc (ISIS 420915). Кроме того, олигонуклеотиды, содержащие конъюгат GalNAc и смешанные PS/PO межнуклеозидные связи, были еще более эффективными, чем олигонуклеотид, содержащий конъюгат GalNAc и только PS связи.


Легенда для Таблицы 85 приведена в Примере 74. Структура GalNAc3-1 показана в Примере 9. Структура GalNAc3-3a показана в Примере 39. Структура GalNAc3-7a показана в Примере 48. Структура GalNAc3-10a показана в Примере 46. Структура GalNAc3-13a показана в Примере 62. Структура GalNAc3-19a показана в Примере 70.
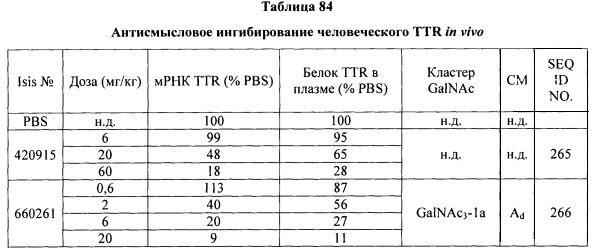
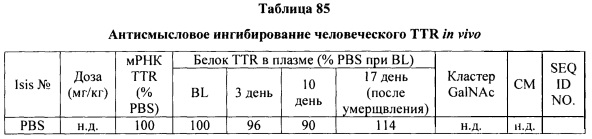
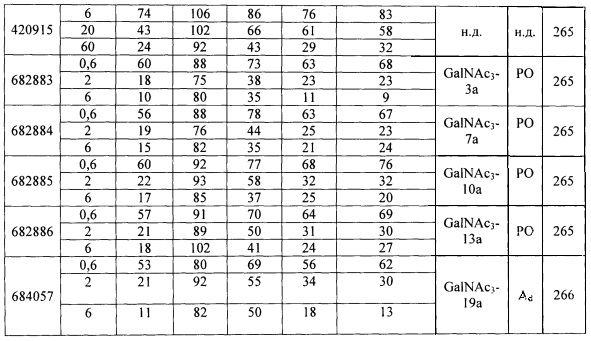
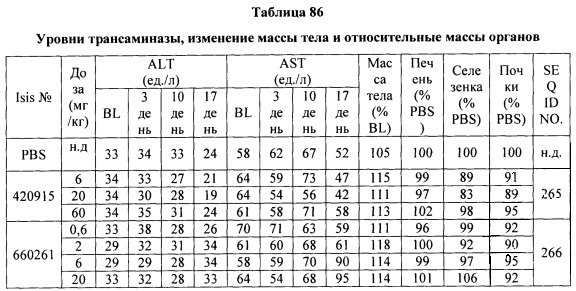
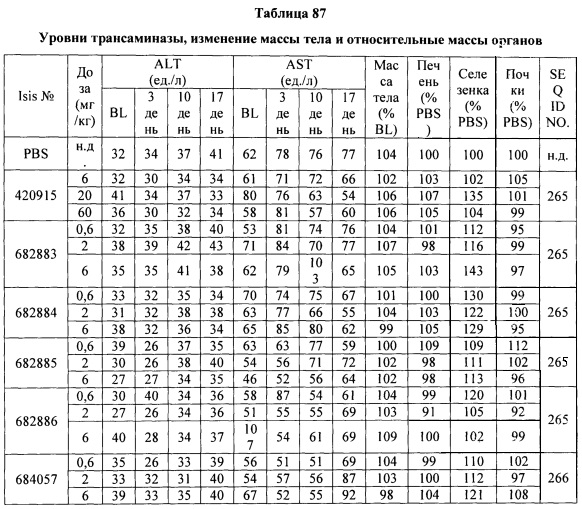
Пример 87. Продолжительность действия in vivo однократных доз олигонуклеотидов, нацеленных на TTR, содержащих кластер GalNAc3
ISIS №420915 и 660261 (см. Таблицу 83) испытали в исследовании однократной дозы на продолжительность действия у мышей. ISIS №420915, 682883 и 682885 (см. Таблицу 83) также испытали в исследовании однократной дозы на продолжительность действия у мышей.
Лечение
Восьминедельным самцам трансгенных мышей, которые экспрессируют человеческий TTR, ввели однократную подкожную инъекцию 100 мг/кг ISIS №420915 или 13,5 мг/кг ISIS №660261. Каждая экспериментальная группа состояла из 4 животных. Образцы крови из хвостовой вены брали до введения дозы для определения исходных показателей и на 3-й, 7-й, 10-й, 17-й, 24-й и 39-й день после введения дозы. Уровни белка TTR в плазме измеряли так, как описано в Примере 86. Результаты, показанные ниже, приведены как средний процент уровней TTR в плазме для каждой экспериментальной группы, нормализованных к исходным уровням.
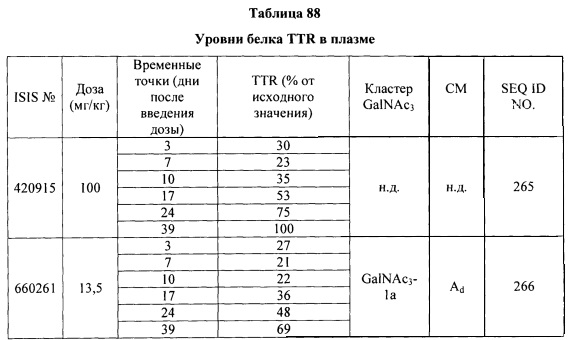
Лечение
Восьминедельным самкам трансгенных мышей, которые экспрессируют человеческий TTR, ввели однократную подкожную инъекцию 100 мг/кг ISIS №420915, 10,0 мг/кг ISIS №682883 или 10,0 мг/кг ISIS №682885. Каждая экспериментальная группа состояла из 4 животных. Образцы крови из хвостовой вены брали до введения дозы для определения исходных показателей и на 3-й, 7-й, 10-й, 17-й, 24-й и 39-й день после введения дозы. Уровни белка TTR в плазме измеряли так, как описано в Примере 86. Результаты, показанные ниже, приведены как средний процент уровней TTR в плазме для каждой экспериментальной группы, нормализованных к исходным уровням.
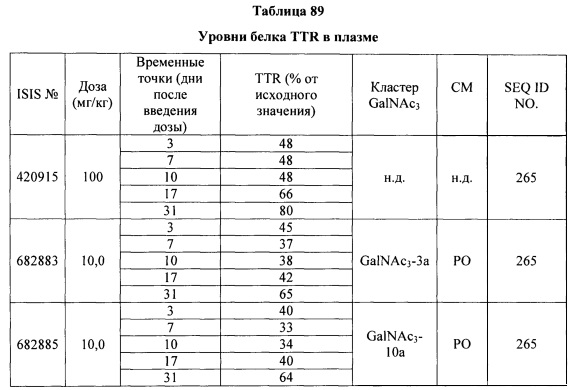
Результаты в Таблицах 88 и 89 демонстрируют, что олигонуклеотиды, содержащие конъюгат GalNAc, являются более эффективными и имеют более продолжительное действие, чем исходный олигонуклеотид без конъюгата (ISIS 420915).
Пример 88. Сплайсинг-модулирование in vivo под действием олигонуклеотидов, нацеленных на SMN, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные в Таблице 90, испытали на сплайсинг-модулирование человеческих генов выживаемости мотонейтронов (SMN) у мышей.

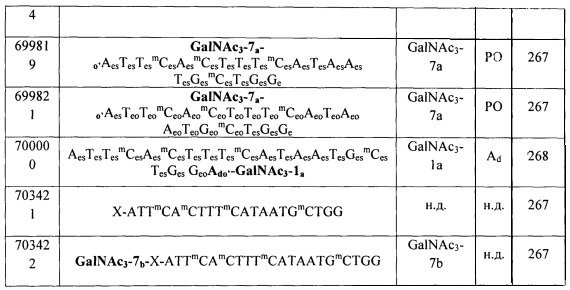
Структура GalNAc3-7a показана ранее в Примере 48. «X» означает 5'-первичный амин, полученный компанией Gene Tools (Филомат, штат Орегон), а GalNAc3-7b означает структуру GalNAc3-7a, не содержащую часть -NH-С6-О связи, как показано ниже:
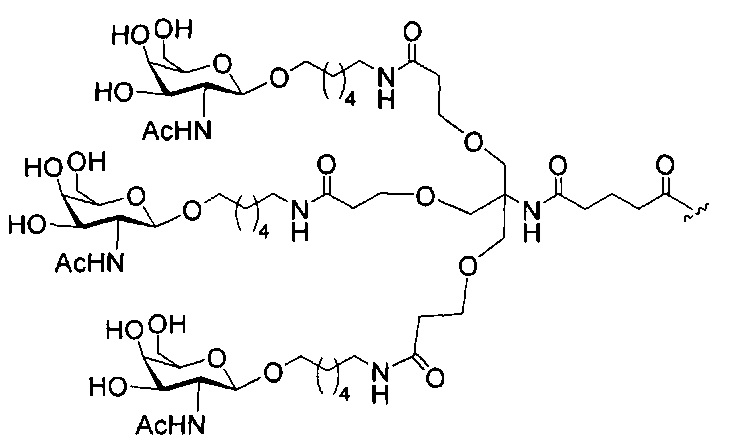
ISIS №703421 и 703422 представляют собой морфолино-олигонуклеотиды, при этом каждый нуклеотид из двух олигонуклеотидов представляет собой морфолино-нуклеотид.
Лечение
Шестинедельным трансгенным мышам, экспрессирующим человеческий SMN, ввели однократную подкожную инъекцию олигонуклеотида, перечисленного в Таблице 91, или солевого раствора. Каждая экспериментальная группа состояла из 2 самцов и 2 самок. Мышей умертвили через 3 дня после введения дозы для определения уровней мРНК человеческого SMN в печени с экзоном 7 и без него, применив ПЦР в реальном времени по стандартным протоколам. Общую РНК измерили при помощи реагента Ribogreen. Уровни мРНК SMN нормализовали к общей мРНК, а затем нормализовали к средним значениям и группе, обработанной солевым раствором. Полученные средние отношения мРНК SMN, содержащей экзон 7, к мРНК SMN, не содержащей экзон 7, приведены в Таблице 91 Результаты демонстрируют, что полностью модифицированные олигонуклеотиды, которые модулируют сплайсинг и содержат конъюгат GalNAc, являются значительно более эффективными для изменения сплайсинга в печени, чем исходные олигонуклеотиды, не содержащие конъюгат GalNAc. Кроме того, эта тенденция сохраняется для химизма многократных модификаций, включая 2'-МОЕ и морфолино-модифицированные олигонуклеотиды.
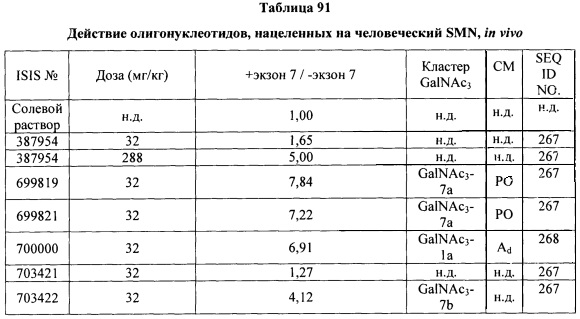
Пример 89. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на аполипопротеин А (Аро(а)), содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 92, испытали в исследовании дозозависимого ингибирования Аро(а) у трансгенных мышей.

Структура GalNAc3-7a показана в Примере 48.
Лечение
Восьминедельным самкам мышей C57BL/6 (Jackson Laboratory, Бар-Харбор, штат Мэн) один раз в неделю вводили подкожную инъекцию дозы, приведенной ниже, в целом шесть доз олигонуклеотида, перечисленного в Таблице 92, или PBS. Каждая экспериментальная группа состояла из 3-4 животных. Образцы крови из хвостовой вены брали за день до введения первой дозы и еженедельно после введения каждой дозы для определения уровней белка Аро(а) в плазме. Мышей умертвили через два дня после последнего введения. Уровни мРНК Аро(а) в печени определили при помощи ПЦР у реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) по стандартным протоколам. Уровни белка Аро(а) в плазме определили при помощи твердофазного иммуноферментного анализа, и определили уровни трансаминазы в печени. Результаты анализа мРНК и белка в плазме в Таблице 93 приведены как среднее процентное значение для экспериментальной группы относительно группы, обработанной PBS. Уровни белка в плазме дополнительно нормализовали к исходному значению (BL) для группы с PBS. Средние абсолютные уровни трансаминазы и массы тела (% относительно среднего исходного значения) приведены в Таблице 94.
Как показано в Таблице 93, лечение олигонуклеотидами снижает уровни мРНК Аро(а) в печени и уровни белка в плазме дозозависимым образом. Кроме того, олигонуклеотид, содержащий конъюгат GalNAc, был значительно более эффективным с более продолжительным действием, чем исходный олигонуклеотид, не содержащий конъюгат GalNAc. Как показано в Таблице 94, приведенные олигонуклеотиды не влияют на уровни трансаминазы и массы тела, что указывает на хорошую переносимость олигонуклеотидов.
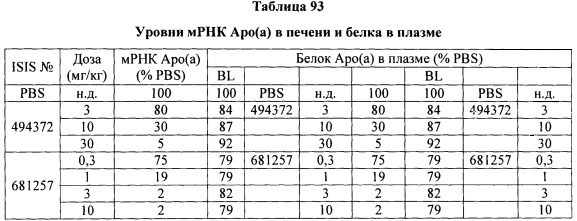
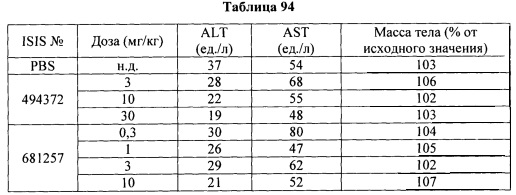
Пример 90. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на TTR, содержащих кластер GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 95, испытали в дозозависимом исследовании антисмыслового ингибирования человеческого транстиретина (TTR) у трансгенных мышей, экспрессирующих человеческий TTR ген.
Лечение
TTR трансгенным мышам один раз в неделю в течение трех недель, в целом три дозы, вводили подкожную инъекцию олигонуклеотида и дозы, перечисленных в Таблице 96, или PBS. Каждая экспериментальная группа состояла из 4 животных. Перед введением первой дозы взяли образец крови из хвостовой вены для определения уровней белка TTR в плазме в исходном состоянии (BL). Мышей умертвили через 72 часа после последнего введения. Уровни белка TTR измерили при помощи клинического анализатора (AU480, Beckman Coulter, штат Калифорния). ПЦР в реальном времени и реагент для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc., Юджин, штат Орегон) применяли по стандартным протоколам для определения уровней мРНК человеческого TTR в печени. Результаты, показанные в Таблице 96, представляют собой средние значения для каждой экспериментальной группы. Уровни мРНК представляют собой средние значения относительно среднего значения для PBS группы. Уровни белка в плазме представляют собой средние значения относительно среднего значения для PBS группы в исходном состоянии. «BL» означает исходное значения измерений, выполненных непосредственно перед введением первой дозы. Как показано в Таблице 96, лечение антисмысловыми олигонуклеотидами снижает уровни экспрессии TTR дозозависимым образом. Олигонуклеотид, содержащий конъюгат GalNAc, был более эффективным, чем исходное соединение без конъюгата GalNAc (ISIS 420915), а олигонуклеотиды, содержащие фосфодиэфирный или дезоксиаденозиновый расщепляемый фрагмент, демонстрировали значительное усиление эффективности, по сравнению с исходным соединением, не содержащим конъюгат (см. ISIS №682883 и 666943 по сравнению с 420915, а также см. Примеры 86 и 87).
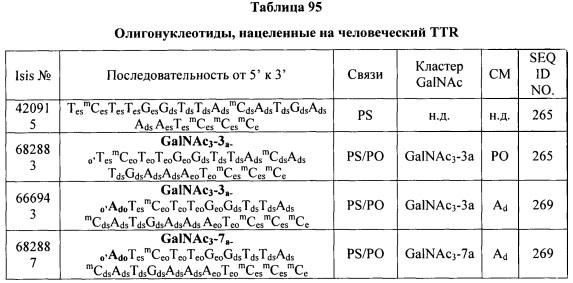

Легенда для Таблицы 95 приведена в Примере 74. Структура GalNAc3-3a показана в Примере 39. Структура GalNAc3-7a показана в Примере 48. Структура GalNAc3-10a показана в Примере 46. Структура GalNAc3-13a показана в Примере 62.
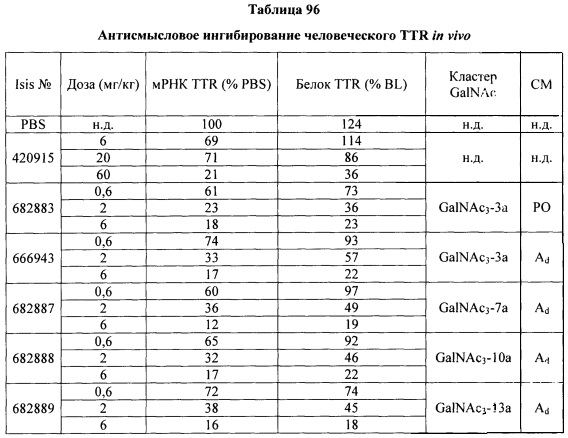
Пример 91. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на фактор VII, содержащих конъюгат GalNAc3, у приматов, не являющихся человеком
Олигонуклеотиды, перечисленные ниже в Таблице 97, испытали в нетерминальном исследовании повышения дозы на антисмысловое ингибирование фактора VII у обезьян.
Лечение
Обезьянам, ранее не подверженным экспериментам, на 0-й, 15-й и 29-й день вводили подкожные инъекции повышающихся доз олигонуклеотидов, перечисленных в таблице 97. или PBS. Каждая экспериментальная группа состояла из 4 самцов и 1 самки. Перед введением первой дозы и в различные временные точки после нее брали образцы крови для определения уровней белка фактора VII в плазме. Уровни белка фактора VII определяли с помощью твердофазного иммуноферментного анализа. Результаты, показанные в Таблице 98, представляют собой средние значения для каждой экспериментальной группы относительно среднего значения для группы PBS в исходном состоянии (BL), измерения выполнены непосредственно перед введением первой дозы. Как показано в Таблице 98, лечение антисмысловыми олигонуклеотидами снижает уровни экспрессии фактора VII дозозависимым образом, и олигонуклеотид, содержащий конъюгат GalNAc, был значительно более эффективным у обезьян, чем олигонуклеотид, не содержащий конъюгата GalNAc.

Легенда для Таблицы 97 приведена в Примере 74. Структура GalNAc3-10a показана в Примере 46.
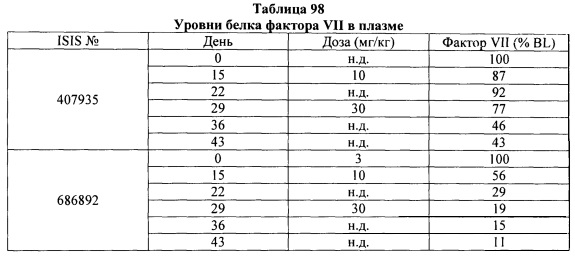
Пример 92. Антисмысловое ингибирование в первичных гепатоцитах под действием олигонуклеотидов, нацеленных на АроC-III, содержащих конъюгат GalNAc3
Первичные мышиные гепатоциты высеивали в 96-луночные планшеты при 15000 клеток на лунку и добавляли олигонуклеотиды, перечисленные в Таблице 99, нацеленные на мышиный АроС-III в концентрации 0,46, 1,37, 4,12 или 12,35, 37,04, 111,11 или 333,33 нМ, или 1,00 мкМ. После инкубации с олигонуклеотидами в течение 24 часов клетки лизировали и очистили общую РНК при помощи RNeasy (Qiagen). Уровни мРНК АроС-III определили при помощи ПЦР в реальном времени и реагента для количественного определения РНК RIBOGREEN® (Molecular Probes, Inc.) по стандартным протоколам. Значения IC50 определили при помощи программы Prism 4 (GraphPad). Результаты демонстрируют, что независимо от того, является ли расщепляемый фрагмент фосфодиэфиром или фосфодиэфир-связанным дезоксиаденозином, олигонуклеотиды, содержащие конъюгат GalNAc, были значительно более эффективными, чем исходный олигонуклеотид, не содержащий конъюгата.
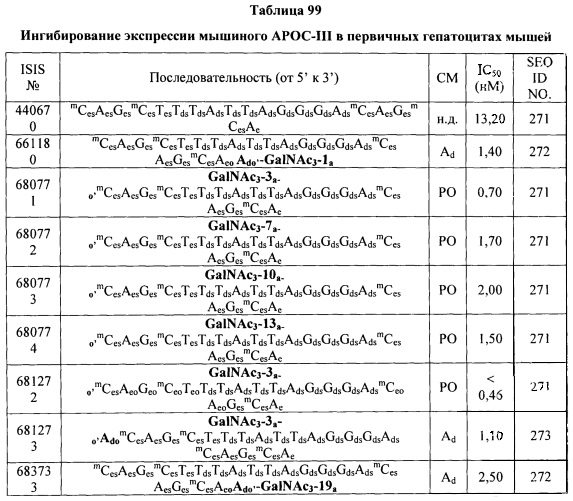
Структура GalNAc3-1a показана ранее в Примере 9, GalNAc3-3a показана в Примере 39, GalNAc3-7a показана в Примере 48, GalNAc3-10a показана в Примере 46, и GalNAc3-13a показана в Примере 62, и GalNAc3-19a показана в Примере 70.
Пример 93. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на SRB-1, содержащих смешанные крылья и 5'-GalNAc3 конъюгат
Олигонуклеотиды, перечисленные в Таблице 100, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей.
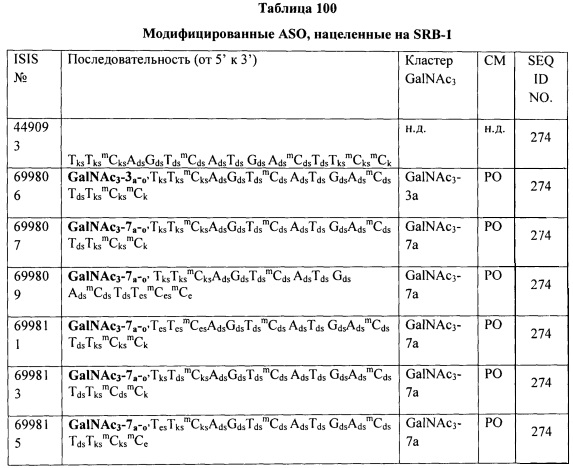
Структура GalNAc3-3a показана ранее в Примере 39, а структура GalNAc3-7a показана ранее в Примере 48. Нижние индексы: «е» означает 2'-МОЕ модифицированный нуклеозид; «ó» означает β-D-2'-дезоксирибонуклеозид; «k» означает 6'-(S)-СН3 бициклический нуклеозид (cEt); «s» означает тиофосфатные межнуклеозидные связи (PS); «о» означает фосфодиэфирные межнуклеозидные связи (РО). Верхний индекс «m» означает 5-метилцитозины.
Лечение
Шести-восьминедельным мышам C57bl6 (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию дозы, приведенной ниже, олигонуклеотида, перечисленного в Таблице 100, или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часа после последнего введения. Уровни мРНК SRB-1 в печени измерили при помощи ПЦР в реальном времени. Уровни мРНК SRB-1 нормализовали к уровням мРНК циклофилина по стандартным протоколам. Результаты, показанные ниже, приведены как средний процент уровней мРНК SRB-1 для каждой экспериментальной группы, по сравнению с контрольной группой, обработанной солевым раствором. Как показано в Таблице 101, лечение антисмысловыми олигонуклеотидами снижает уровни мРНК SRB-1 дозозависимым образом, а гэпмерные олигонуклеотиды, содержащие конъюгат GalNAc и имеющие крылья, которые представляют собой либо полностью cEt, либо смешанные сахарные модификации, были существенно более эффективными, чем исходный олигонуклеотид, не содержащий конъюгата и содержащий полностью cEt модифицированные крылья.
Измерили также массы тела, уровни трансаминазы в печени, общий билирубин и АМК, а средние значения для каждой экспериментальной группы приведены в Таблице 101. Масса тела показана как средний процент массы тела относительно исходной массы тела (% BL), измеренный непосредственно перед введением дозы олигонуклеотида.
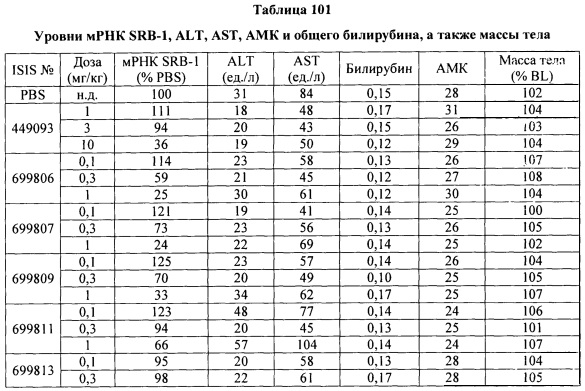

Пример 94. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на SRB-1, содержащих 2'-сахарные модификации и 5'-GalNAc3 конъюгат
Олигонуклеотиды, перечисленные в Таблице 102, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей.

Нижний индекс «m» означает 2'-O-метил-модифицированный нуклеозид. Полная легенда к таблице приведена в Примере 74. Структура GalNAc3-3a показана ранее в Примере 39, а структура GalNAc3-7a показана ранее в Примере 48.
Лечение
Исследование выполнили по протоколу, описанному в Примере 93. Результаты приведены ниже в Таблице 103 и демонстрируют, что и 2'-МОЕ, и 2'-ОМе-модифицированные олигонуклеотиды, содержащие конъюгат GalNAc, были значительно более эффективными, чем соответствующие исходные олигонуклеотиды, не содержащие конъюгата. Результаты измерений массы тела, трансаминазы в печени, общего билирубина и АМК демонстрируют, что эти соединения хорошо переносятся.
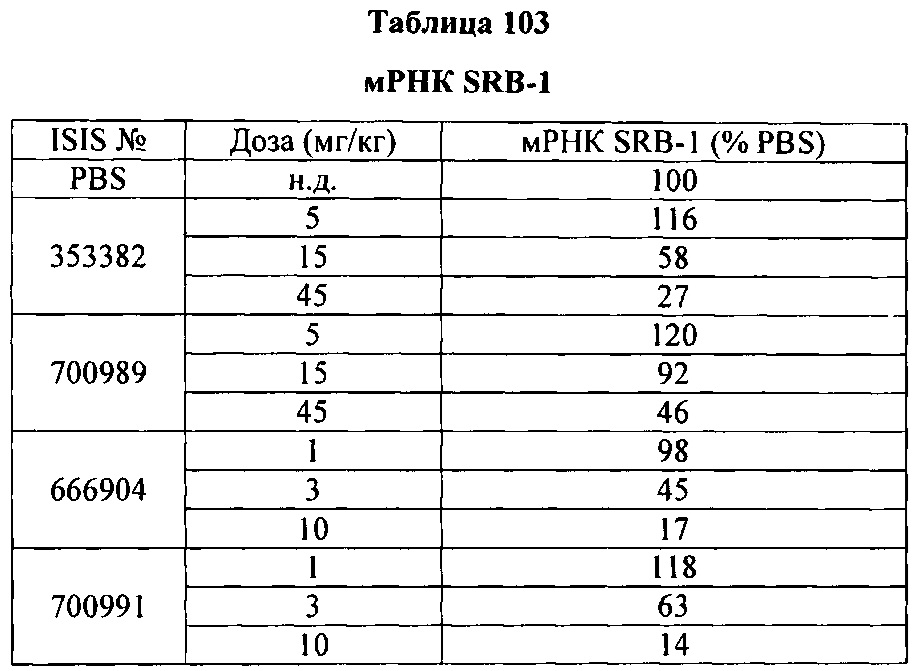
Пример 95. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на SRB-1, содержащих бициклические нуклеозиды и 5'-GalNAc3 конъюгат
Олигонуклеотиды, перечисленные в Таблице 104, испытали в дозозависимом исследовании антисмыслового ингибирования SRB-1 у мышей.

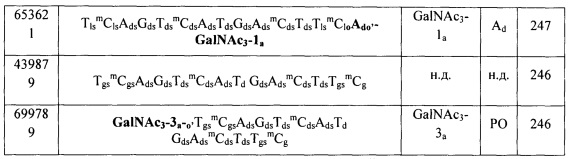
Нижний индекс «g» означает фтор-HNA нуклеозид, нижний индекс «1» означает закрытый нуклеозид, содержащий мостик 2'-O-СН2-4'. Другие сокращения приведены в легенде таблицы Примера 74. Структура GalNAc3-1a показана ранее в Примере 9, структура GalNAc3-3а показана ранее в Примере 39, а структура GalNAc3-7a показана ранее в Примере 48.
Лечение
Исследование выполнили по протоколу, описанному в Примере 93. Результаты приведены ниже в Таблице 105 и демонстрируют, что олигонуклеотиды, содержащие конъюгат GalNAc и различные бициклические нуклеозидные модификации, были значительно более эффективными, чем исходный олигонуклеотид, не содержащий конъюгата и содержащий бициклические нуклеозидные модификации. Кроме того, олигонуклеотид, содержащий конъюгат GalNAc и фтор-HNA модификации, был существенно более эффективным, чем исходное соединение, не содержащее конъюгата и содержащее фтор-HNA модификации. Результаты измерений массы тела, трансаминазы в печени, общего билирубина и АМК демонстрируют, что эти соединения хорошо переносятся.
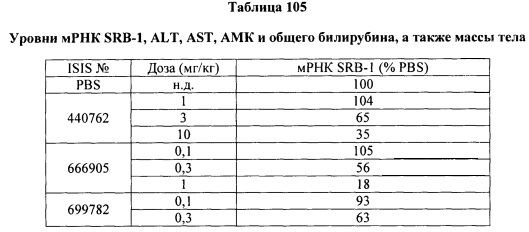
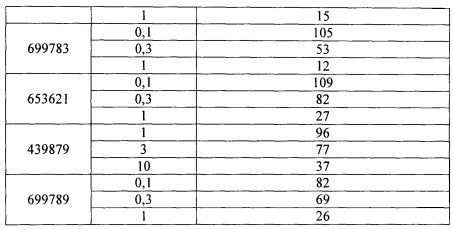
Пример 96. Связывание белка плазмы антисмысловыми олигонуклеотидами, содержащими конъюгирующую группу GalNAc3
Олигонуклеотиды, перечисленные в Таблице 70, нацеленные на АроС-III, и олигонуклеотиды в Таблице 106, нацеленные на Аро(а), испытали в анализе ультрафильтрации для оценки связывания белка в плазме.

Легенда таблицы приведена в Примере 74. Структура GalNAc3-7a показана ранее в Примере 48.
Элементы для ультрафильтрации Ultrafree-MC (номинальное ограничение молекулярной массы 30000, слабосвязывающая регенерированная целлюлозная мембрана, Millipore, Бедфорд, штат Массачусетс) предварительно кондиционировали с 300 мкл 0,5% Tween 80 и центрифугировали при 2000 g в течение 10 минут, затем с 300 мкл 300 мкг/мл раствора контрольного олигонуклеотида в Н2О и центрифугировали при 2000 g в течение 16 минут. Для оценки неспецифического связывания с фильтрами каждого исследуемого олигонуклеотида из Таблиц 70 и 106, применяемых в испытаниях, 300 мкл 250 нг/мл раствора олигонуклеотида в in при рН 7,4 поместили в предварительно кондиционированные фильтры и центрифугировали при 2000 г в течение 16 минут. Нефильтрованные и фильтрованные образцы анализировали твердофазным иммуноферментным анализом для определения концентраций олигонуклеотидов. Для получения средней концентрации для каждого образца применяли три экземпляра. Среднюю концентрацию фильтрованного образца относительно нефильтрованного образца применяли для определения процента олигонуклеотида, прошедшего через фильтр без плазмы (% выделения).
Замороженные образцы цельной плазмы, собранные в K3-ЭДТК и полученные от здоровых, не принимающих лекарства людей-добровольцев, яванских макак и мышей CD-1, приобрели у компании Bioreclamation LLC (Вестбери, штат Нью-Йорк). Исследуемые олигонуклеотиды добавляли к 1,2 мл аликвотам плазмы в двух концентрациях (5 и 150 мкг/мл). Аликвоту (300 мкл) каждого маркированного образца плазмы поместили на предварительно кондиционированный фильтровальный элемент и инкубировали при 37°С в течение 30 минут, затем сразу выполнили центрифугирование при 2000 g в течение 16 минут. Аликвоты фильтрованных и нефильтрованных маркированных образцов плазмы анализировали твердофазным иммуноферментным анализом для определения концентрации олигонуклеотида в каждом образце. Применили три экземпляра каждой концентрации для определения среднего процента связанного и несвязанного олигонуклеотида в каждом образце. Среднюю концентрацию фильтрованного образца относительно концентрации нефильтрованного образца применили для определения процента олигонуклеотида в плазме, не связанного с белками плазмы (% несвязанного). Окончательные значения несвязанного олигонуклеотида корректировали на неспецифическое связывание путем деления % несвязанного на % выделения для каждого олигонуклеотида. Окончательные значения % связанного олигонуклеотида определили вычитанием окончательных значений % несвязанного из 100. Результаты показаны в Таблице 107 для двух концентраций испытанного олигонуклеотида (5 и 150 мкг/мл) в плазме каждого вида. Результаты демонстрируют, что конъюгирующие группы GalNAc не оказывают существенного влияния на связывание белка плазмы. Кроме того, олигонуклеотиды, содержащие только PS межнуклеозидные связи и смешанные PO/PS связи, - оба варианта связывают белки плазмы, при этом олигонуклеотиды, содержащие только PS связи, связывают белки плазмы в несколько большей степени, чем олигонуклеотиды, содержащие смешанные PO/PS связи.
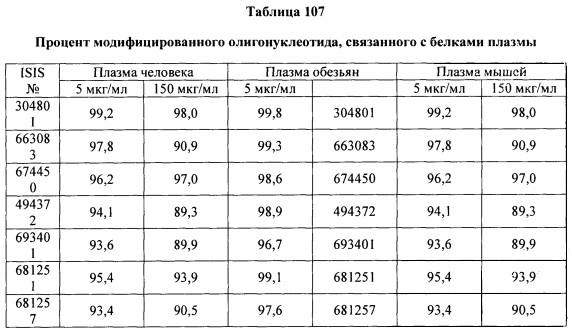
Пример 97. Модифицированные олигонуклеотиды, нацеленные на TTR, содержащие конъюгирующую группу GalNAc3
Олигонуклеотиды, приведенные в Таблице 108, содержащие конъюгат GalNAc, предназначены для воздействия на TTR.

Легенда для Таблицы 108 приведена в Примере 74. Структура GalNAc3-1 показана в Примере 9. Структура GalNAc3-3a показана в Примере 39. Структура GalNAc3-7a показана в Примере 48. Структура GalNAc3-10a показана в Примере 46. Структура GalNAc3-13a показана в Примере 62. Структура GalNAc3-19а показана в Примере 70.
Пример 98. Оценка провоспалительного действия олигонуклеотидов, содержащих конъюгат GalNAc, в анализе hPMBC
Олигонуклеотиды, перечисленные в Таблице 109, исследовали на провоспалительное действие в анализе hPMBC, описанном в Примерах 23 и 24 (см. Таблицы 30, 83, 95 и 108, где приведено описание олигонуклеотидов). ISIS 353512 обладает высоким ответом, и его применяли в качестве положительного контроля, а другие олигонуклеотиды описаны в Таблицах 83, 95 и 108. Результаты, приведенные в Таблице 109, получены с применением крови, полученной от одного донора-добровольца. Результаты демонстрируют, что олигонуклеотиды, содержащие смешанные PO/PS межнуклеозидные связи, вызывают значительно более слабые провоспалительные реакции, по сравнению с теми же олигонуклеотидами, содержащими только PS связи. Кроме того, в этом анализе конъюгирующая группа GalNAc не оказывает существенного влияния.

Пример 99. Связывающие аффинности олигонуклеотидов, содержащих конъюгат GalNAc, в отношении асиалогликопротеинового рецептора
Связывающие аффинности олигонуклеотидов, перечисленных в Таблице 110 (см. Таблицу 76, в которой приведено описание олигонуклеотидов), в отношении асиалогликопротеинового рецептора испытали в анализе конкурентного связывания рецепторов. Конкурирующий лиганд, α1-кислый гликопротеин (AGP), инкубировали в 50 мМ ацетатно-натриевом буфере (рН 5) с 1 ед. нейраминидазы-агарозы в течение 16 часов при 37°С, а >90% дезалилирование подтвердили анализом с сиаловой кислотой или эксклюзионной хроматографией (SEC). Для йодирования АГФ применили монохлорид йода по способу, описанному авторами Atsma et al. (см. J Lipid Res. январь 1991 г.; 32(1): 173-81.) В этом способе дезалилированный α1-кислый гликопротеин (de-AGP) добавляли к 10 мМ хлориду йода, Na125I и 1 М глицина в 0,25 М NaOH. После инкубации в течение 10 минут при комнатной температуре,125I-меченный de-AGP отделили от свободного125I двукратным концентрированием смеси с применением спин-колонки с номинальным отсечением по молекулярной массе 3 кД. Белок испытали на эффективность мечения и чистоту на системе ВЭЖХ, оснащенной колонкой Agilent SEC-3 (7,8×300 мм) и счетчиком β-RAM. Конкуретные исследования с применением1251-меченного de-AGP и ASO, содержащих различные GalNAc-кластеры, выполнили следующим образом. Человеческие клетки HepG2 (106 клеток/мл) поместили на 6-луночные планшеты в 2 мл соответствующей питательной среды. Использовали среду MEM с добавлением 10% фетальной бычьей сыворотки (FBS), 2 мМ L-глутамина и 10 мМ HEPES. Клетки выращивали в течение 16-20 часов при 37°C с 5% и 10% CO2, соответственно. Перед экспериментом клетки промыли средой без FBS. Клетки выращивали в течение 30 минут при 37°C с 1 мл конкурентной смеси, содержащей соответствующую питательную среду с 2% FBS, 10-8 М125I-меченным de-AGP и ASO, содержащим GalNAc-кластер в концентрациях в диапазоне от 10-11 до 10-5 М. Неспецифическое связывание определили в присутствии 10-2 М GalNAc сахара. Клетки дважды промыли средой без FBS для удаления несвязанного125I-меченного de-AGP и конкурирующего GalNAc ASO. Клетки лизировали с использованием буфера RLT производства компании Qiagen, содержащего 1% β-меркаптоэтанола. Лизаты перенесли в круглодонные аналитические пробирки после быстрого 10-минутного цикла замораживания/оттаивания, и анализировали на γ-счетчике. Неспецифическое связывание вычли, а затем разделили импульсы белка125I на значение импульсов при самой низкой концентрации GalNAc-ASO. Кривые ингибирования построили по уравнению моносайтового конкурентного связывания, применив алгоритм нелинейной регрессии для расчета связывающей аффинности (KD).
Результаты в Таблице 110 были получены в экспериментах, выполненных в пять разных дней. Результаты для олигонуклеотидов, отмеченных верхним индексом «а», представляют собой средние значения экспериментов, выполненных в два разных дня. Результаты демонстрируют, что олигонуклеотиды, содержащие конъюгирующую группу GalNAc на 5'-конце, связывают асиалогликопротеиновый рецептор человеческих клеток HepG2 с аффинностью, которая в 1,5-16 раз больше, чем для олигонуклеотидов, содержащих конъюгирующую группу GalNAc на 3'-конце.
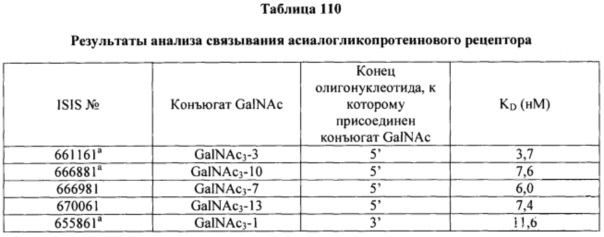

Пример 100. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, содержащих конъюгирующую группу GalNAc, нацеленных на Аро(а), in vivo
Олигонуклеотиды, перечисленные ниже в Таблице 111а, испытали в исследовании однократной дозы на продолжительность действия у мышей.

Структура GalNAc3-7a показана в Примере 48.
Лечение
Каждой самке трансгенных мышей, экспрессирующих человеческий Аро(а), один раз в неделю, в целом 6 доз, вводили подкожную инъекцию олигонуклеотида и дозы, перечисленной в Таблице 111b, или PBS. Каждая экспериментальная группа состояла из животных. Образцы крови брали за день до введения дозы для определения исходных уровней белка Аро(а) в плазме, а также через 72 часа, 1 неделю и 2 недели после введения первой дозы. Дополнительные пробы крови брали через 3 недели, 4 недели, 5 недель и 6 недель после введения первой дозы. Уровни белка Аро(а) в плазме измеряли при помощи твердофазного иммуноферментного анализа. Результаты в Таблице 111b приведены как средний процент от уровней белка Аро(а) в плазме для каждой экспериментальной группы, нормализованных к исходным уровням (% BL). Результаты показывают, что олигонуклеотиды, содержащие конъюгирующую группу GalNAc, демонстрируют эффективное снижение экспрессии Аро(а). Этот мощный эффект наблюдали для олигонуклеотида, содержащего только PS межнуклеозидные связи, и для олигонуклеотида, содержащего смешанные РО и PS связи.
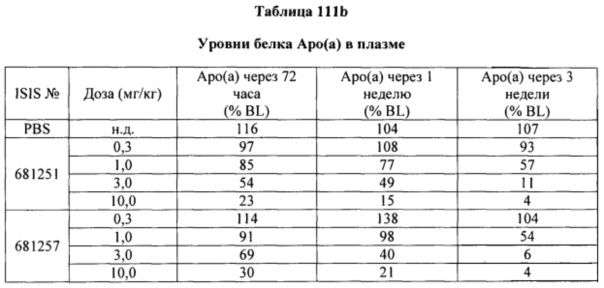
Пример 101. Антисмысловое ингибирование олигонуклеотидами, содержащими кластер GalNAc, связанный через стабильный фрагмент
Олигонуклеотиды, перечисленные в Таблице 112, испытали на ингибирование экспрессии мышиного АРОС-III in vivo. Мышам С57В1/6 ввели однократную подкожную инъекцию олигонуклеотида, перечисленного в Таблице 112, или PBS. Каждая экспериментальная группа состояла из 4 животных. Каждой мыши, обработанной соединением ISIS 440670, вели дозу 2, 6, 20 или 60 мг/кг. Каждой мыши, обработанной соединением ISIS 680772 или 696847, ввели 0,6, 2, 6 или 20 мг/кг. Конъюгирующая группа GalNAc в ISIS 696847 связана через стабильный фрагмент, тиофосфатную связь, вместо легко расщепляемого фосфодиэфир-содержащей связи. Животных умертвили через 72 часа после введения дозы. Уровни мРНК АРОС-III в печени измерили при помощи ПЦР в реальном времени. Уровни мРНК АРОС-III нормализовали к уровням мРНК циклофилина по стандартным протоколам. Результаты приведены в Таблице 112 как средний процент уровней мРНК АРОС-III для каждой экспериментальной группы, по сравнению с контрольной группой, обработанной солевым раствором. Результаты демонстрируют, что олигонуклеотиды, содержащие конъюгирующую группу GalNAc, были существенно более эффективными, чем олигонуклеотид, не содержащий конъюгирующую группу. Кроме того, олигонуклеотид, содержащий конъюгирующую группу GalNAc, связанную с олигонуклеотидом через расщепляемый фрагмент (ISIS 680772), был еще более эффективным, чем олигонуклеотид, содержащий конъюгирующую группу GalNAc, связанную с олигонуклеотидом через стабильный фрагмент (ISIS 696847).
Структура GalNAc3-7a показана в Примере 48.
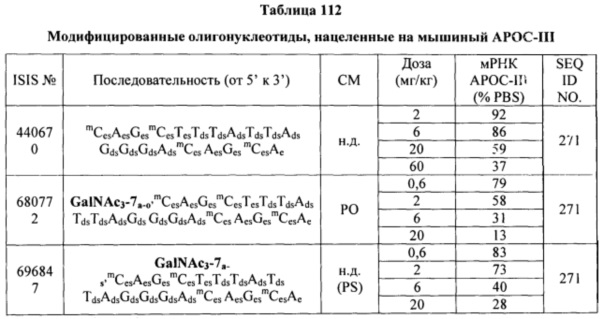
Пример 102. Распределение в печени антисмысловых олигонуклеотидов, содержащих конъюгат GalNAc
Оценили распределение в печени ISIS 353382 (см. Таблицу 36), который не содержит конъюгата GalNAc, и ISIS 655861 (см. Таблицу 36), который содержит конъюгат GalNAc. Самцам мышей balb/c ввели однократную подкожную инъекцию ISIS 353382 или 655861 в дозе, перечисленной в Таблице 113. Каждая экспериментальная группа состояла из 3 животных, за исключением группы с дозой 18 мг/кг для ISIS 655861, которая состояла из 2 животных. Животных умертвили через 48 часов после введения дозы для определения распределения олигонуклеотидов в печени. Для измерения количества молекул антисмыслового олигонуклеотида на клетку, метку трис-бипиридина рутения (II) (MSD TAG, Meso Scale Discovery) конъюгировали с олигонуклеотидным образцом, применяемым для обнаружения антисмысловых олигонуклеотидов. Результаты, приведенные в Таблице 113, представляют собой средние концентрации олигонуклеотида для каждой экспериментальной группы в единицах измерения миллионов молекул олигонуклеотида на клетку. Результаты демонстрируют, что при равных дозах олигонуклеотид, содержащий конъюгат GalNAc, содержался в более высоких концентрациях в целом в печени и в гепатоцитах, чем олигонуклеотид, не содержащий конъюгата GalNAc. Кроме того, олигонуклеотид, содержащий конъюгат GalNAc, содержался в более низких концентрациях в непаренхиматозных клетках печени, чем олигонуклеотид, не содержащий конъюгата GalNAc. И тогда как концентрации ISIS 655861 в гепатоцитах и непаренхиматозных клетках печени были одинаковыми в расчете на одну клетку, содержание гепатоцитов в печени составляет приблизительно 80% по объему. Следовательно, основная часть олигонуклеотида ISIS 655861, содержащегося в печени, находилась в гепатоцитах, тогда как основная часть олигонуклеотида ISIS 353382, содержащегося в печени, находилась в непаренхиматозных клетках печени.
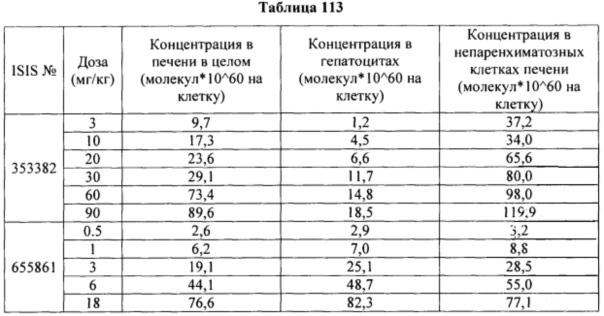
Пример 103. Продолжительность действия in vivo олигонуклеотидов, нацеленных на АРОС-III, содержащих конъюгат GalNAc3
Олигонуклеотиды, перечисленные ниже в Таблице 114, испытали в исследовании однократной дозы на продолжительность действия у мышей.

Структура GalNAc3-3a показана в примере 39, а GalNAc3-19a показана в Примере 70. Лечение
Самкам трансгенных мышей, экспрессирующим человеческий АРОС-III, ввели однократную подкожную инъекцию олигонуклеотида, перечисленного в Таблице 114, или PBS. Каждая экспериментальная группа состояла из 3 животных. Образцы крови из брали до введения дозы для определения исходных показателей и на 3-й, 7-й, 14-й, 21-й, 28-й, 35-й и 42-й день после введения дозы. Уровни триглицеридов и белка АРОС-III в плазме измеряли так, как описано в Примере 20. Результаты в Таблице 115 приведены как средний процент уровней триглицеридов и АРОС-III в плазме для каждой экспериментальной группы, нормализованных к исходным уровням. Сравнение результатов в Таблице 71 примера 79 с результатами, приведенными ниже в Таблице 115, демонстрирует, что олигонуклеотиды, содержащие смесь фосфодиэфирных и тиофосфатных межнуклеозидных связей, обладают увеличенной продолжительностью действия, чем эквивалентные олигонуклеотиды, содержащие только тиофосфатные межнуклеозидные связи.
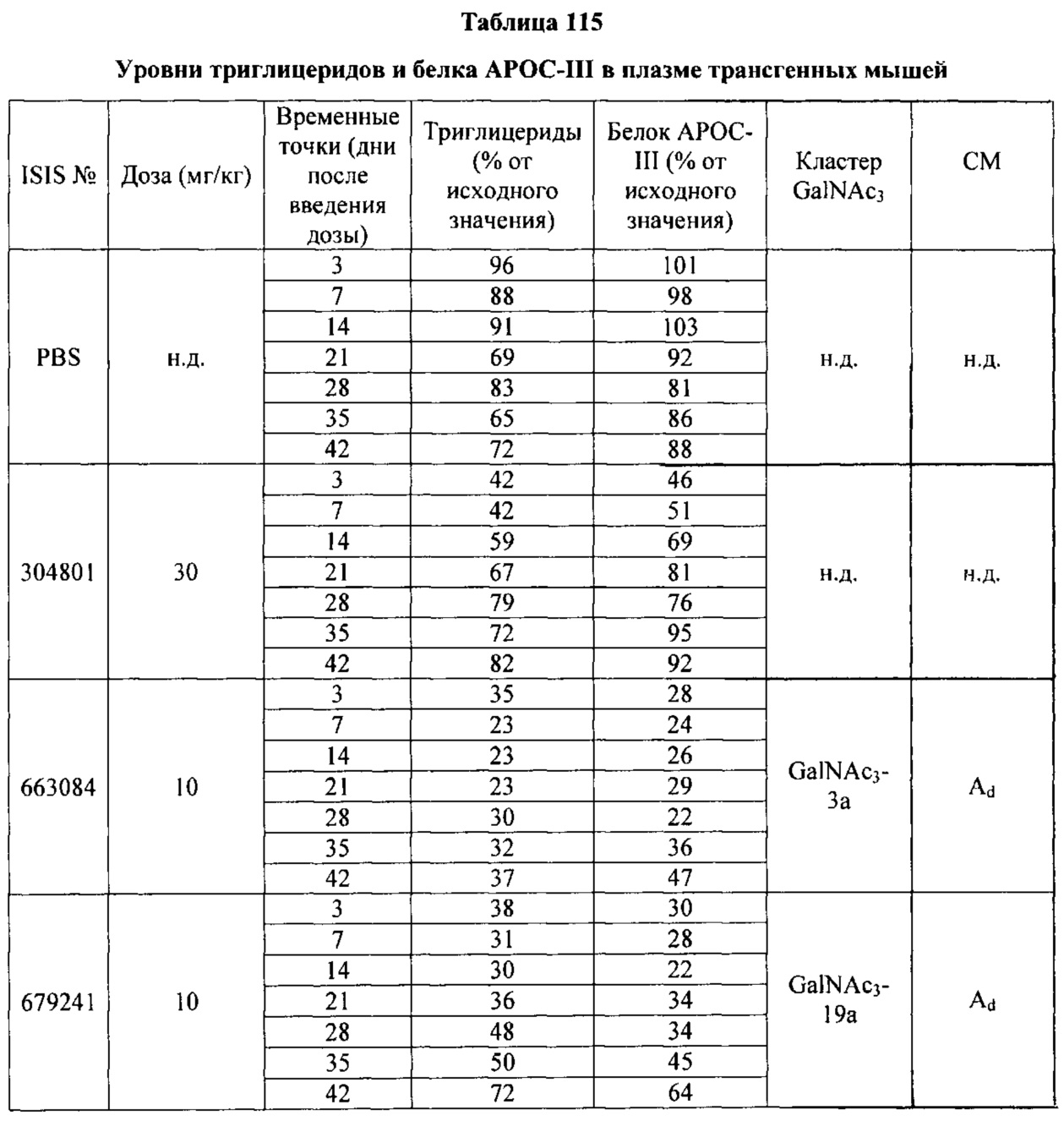
Пример 104. Синтез олигонуклеотидов, содержащих конъюгат 5'-GalNAc2
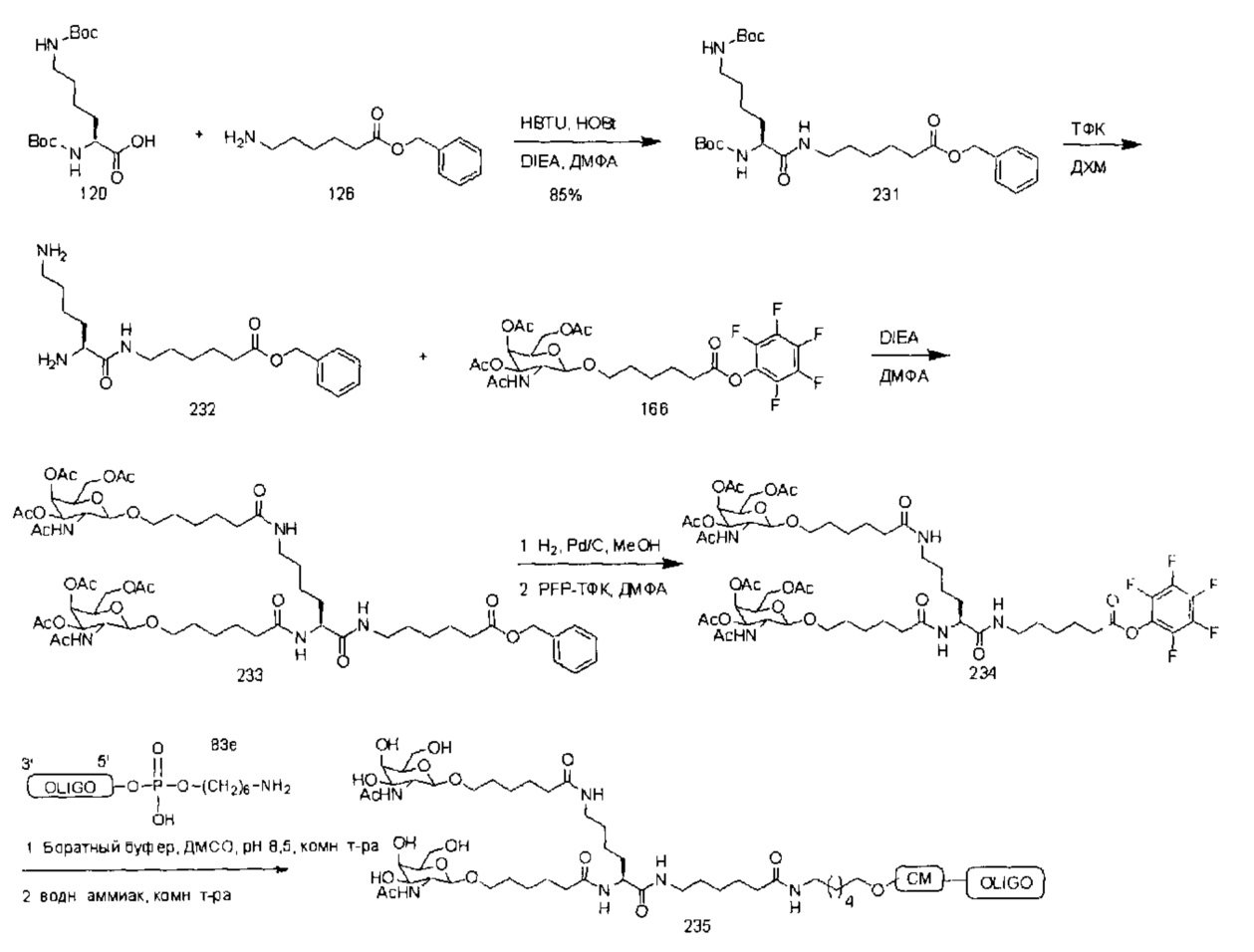
Соединение 120 имеется в продаже, а синтез соединения 126 описан в Примере 49. Соединение 120 (1 г, 2,89 ммоль), HBTU (0,39 г, 2,89 ммоль) и HOBt (1,64 г, 4,33 ммоль) растворили в ДМФА (10 мл) и добавили N,N-диизопропилэтиламин (1,75 мл, 10,1 ммоль). Примерно через 5 минут в реакционную смесь добавили бензиловый эфир аминогексановой кислоты (1,36 г, 3,46 ммоль). Через 3 часа реакционную смесь вылили в 100 мл 1 М раствора NaHSO4 и экстрагировали 2×50 мл этилацетата. Органические слои объединили и промыли 3×40 мл насыщенного раствора NaHCO3 и 2х насыщенным солевым раствором, высушили при помощи Na2SO4, отфильтровали и концентрировали. Продукт очистили колоночной хроматографией на силикагеле (ДХМ : ЕА : гексаны, 1:1:1) с получением соединения 231. Данные ЖХМС и ЯМР согласовались со структурой. Соединение 231 (1,34 г, 2,438 ммоль) растворили в дихлорметане (10 мл) и добавили трифторуксусную кислоту (10 мл). После перемешивания при комнатной температуре в течение 2 часов, реакционную смесь концентрировали при пониженном давлении и выпарили вместе с толуолом (3×10 мл). Остаток высушили при пониженном давлении с получением соединения 232 в виде трифторацетатной соли. Синтез соединения 166 описан в Примере 54. Соединение 166 (3,39 г, 5,40 ммоль) растворили в ДМФА (3 мл). Раствор соединения 232 (1,3 г, 2,25 ммоль) растворили в ДМФА (3 мл) и добавили N,N-диизопропилэтиламин (1,55 мл). Реакционную смесь перемешивали при комнатной температуре в течение 30 минут, затем вылили в воду (80 мл), а водный слой экстрагировали EtOAc (2×100 мл). Органическую фазу отделили и промыли насыщенным водным раствором NaHCO3 (3×80 ил), 1 М NaHSO4 (3×80 мл) и насыщенным солевым раствором (2×80 мл), затем высушили (Na2SO4), отфильтровали и концентрировали. Остаток очистили колоночной хроматографией на силикагеле с получением соединения 233. Данные ЖХМС и ЯМР согласовались со структурой. Соединение 233 (0,59 г, 0,48 ммоль) растворили в метаноле (2,2 мл) и этилацетате (2,2 мл;. Добавили палладий на углероде (10 масс. % Pd/C, влажный, 0,07 г) и перемешивали реакционную смесь в атмосфере водорода в течение 3 часов. Реакционную смесь отфильтровали через слой целита и концентрировали с получением карбоновой кислоты. Карбоновую кислоту (1,32 г, 1,15 ммоль, не содержащая кластера кислота) растворили в ДМФА (3,2 мл). К ней добавили добавили N,N-диизопропилэтиламин (0,3 мл, 1,73 ммоль) и PFP-ТФК (0,30 мл, 1,73 ммоль). Через 30 минут перемешивания при комнатной температуре реакционную смесь вылили в воду (40 мл) и экстрагировали EtOAc (2×50 мл). Выполнили стандартную процедуру выделения продукта, как описано выше, с получением соединения 234. Данные ЖХМС и ЯМР согласовались со структурой. Олигонуклеотид 235 получили по общему способу, описанному в Примере 46. Кластерная часть GalNAc2 (GalNAc2-24a) конъюгирующие группы GalNAc2-24 может быть комбинирована с любым расщепляемым фрагментом, содержащимся в олигонуклеотиде, с получением различных конъюгирующих групп. Структура GalNAc2-24 (GalNAc2-24a-CM) приведена ниже:
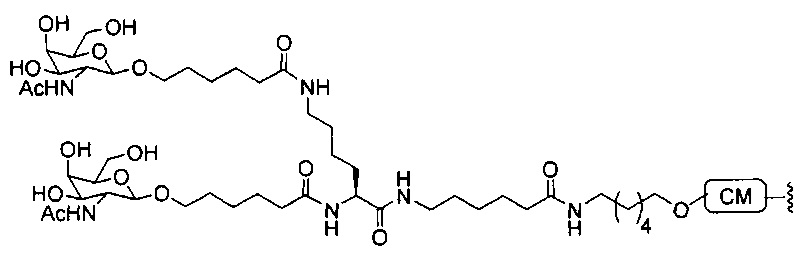
Пример 105. Синтез олигонуклеотидов, содержащих конъюгат GalNAc1-25
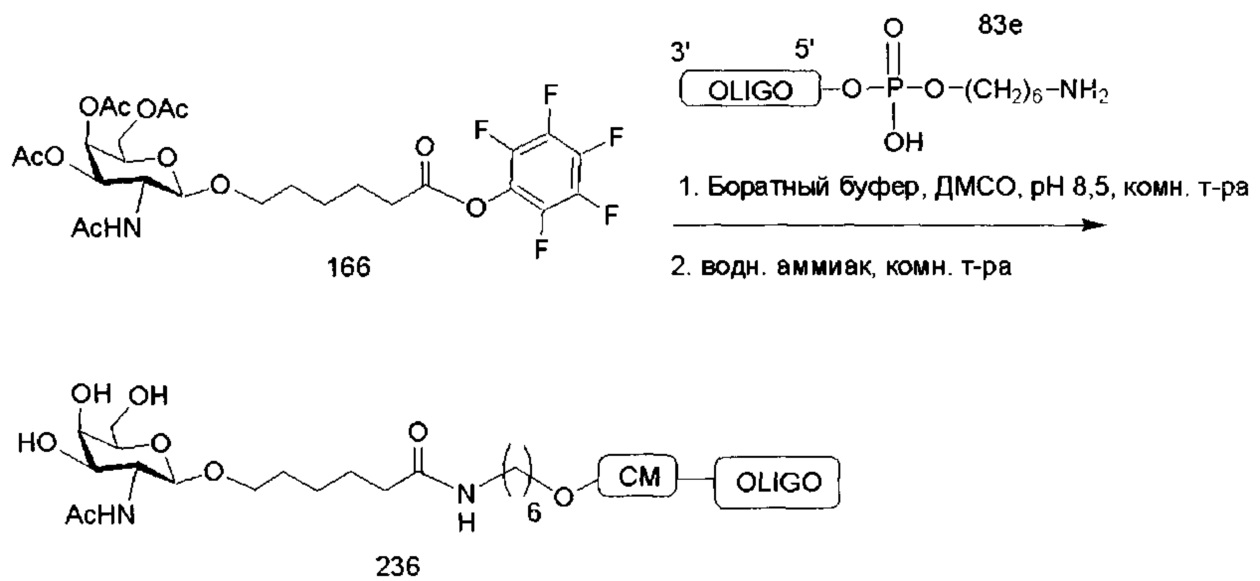
Синтез соединения 166 описан в Примере 54. Олигонуклеотид 236 получили по общему способу, описанному в Примере 46.
Альтернативно, олигонуклеотид 236 синтезировали по схеме, изображенной ниже, а соединение 238 применяли для получения олигонуклеотида 236 по способам, описанным в Примере 10.
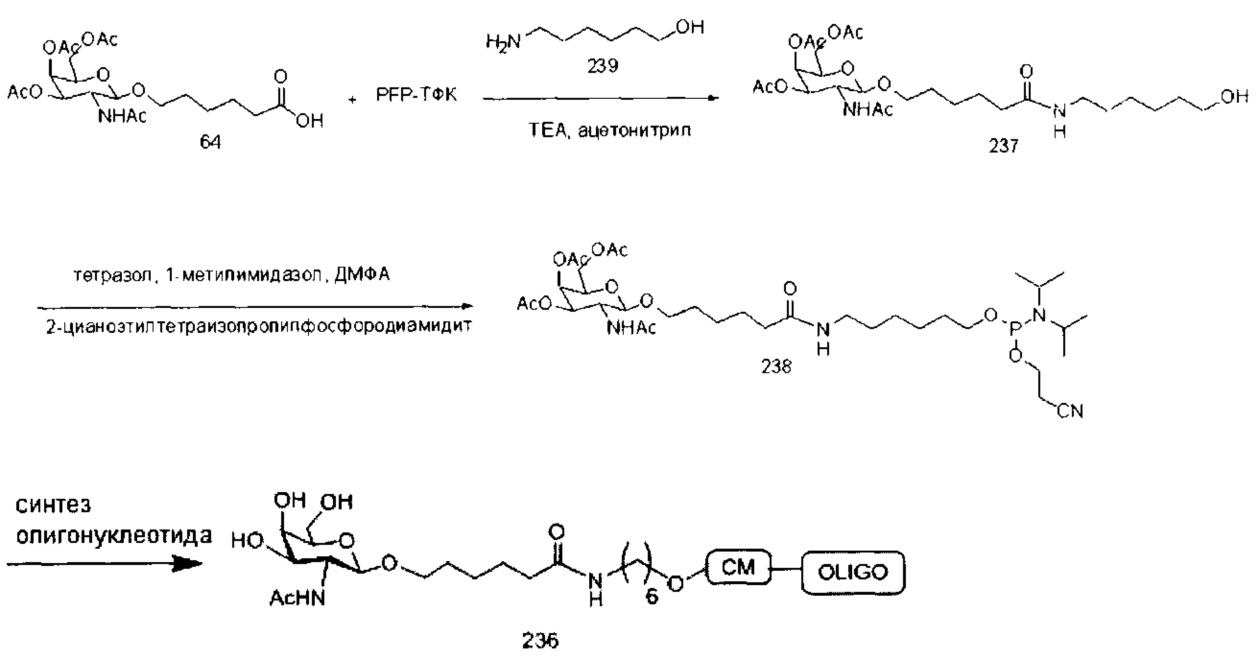
Кластерная часть GalNAc1 (GalNAc1-25a) конъюгирующие группы GalNAc1-25 может быть комбинирована с любым расщепляемым фрагментом, содержащемся в олигонуклеотиде с получением различных конъюгирующих групп. Структура GalNAc1-25 (GalNAc1-25a-CM) приведена ниже:
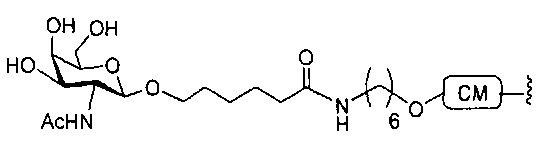
Пример 106. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, нацеленных на SRB-1, содержащих конъюгат 5'-GalNAc2 или 5'-GalNAc3
Олигонуклеотиды, перечисленные в Таблицах 116 и 117, испытали в дозозависимых исследованиях антисмыслового ингибирования SRB-1 у мышей.
Лечение
Шестинедельным самцам мышей C57BL/6 (Jackson Laboratory, Бар-Харбор, штат Мэн) ввели однократную подкожную инъекцию 2, 7 или 20 мг/кг ISIS №440762; или 0,2, 0,6, 2, 6 или 20 мг/кг ISIS №686221, 686222 или 708561; или солевого раствора. Каждая экспериментальная группа состояла из 4 животных. Мышей умертвили через 72 часа после последнего введения. Уровни мРНК SRB-1 в печени измерили при помощи ПЦР в реальном времени. Уровни мРНК SRB-1 нормализовали к уровням мРНК циклофилина по стандартным протоколам. Антисмысловые олигонуклеотиды снижают уровни мРНК SRB-1 дозозависимым образом, а результаты ED50 приведены в Таблицах 116 и 117. Хотя в предыдущих исследованиях показано, что тривалентные GalNAc-конъюгированные олигонуклеотиды существенно более эффективны, чем двухвалентные GalNAc-конъюгированные олигонуклеотиды, которые, в свою очередь, существенно более эффективны, чем одновалентные GalNAc-конъюгированные олигонуклеотиды (см., например, Khorev et al., Bioorg. & Med. Chem., том 16, 5216-5231 (2008)), обработка антисмысловыми олигонуклеотидами, содержащими одновалентные, двухвалентные и тривалентные кластеры GalNAc, приводит к снижению уровней мРНК SRB-1 с одинаковой эффективностью, как показано в Таблицах 116 и 117.

Легенда к таблице приведена в Примере 93. Структура GalNAc3-13a показана в Примере 62, а структура GalNAc2-24a показана в Примере 104.

Легенда к таблице приведена в Примере 93. Структура GalNAc1-25a показана в Примере 105.
Оценили также концентрации олигонуклеотидов, приведенных в Таблицах 116 и 117, в печени, применив способы, описанные в Примере 75. Результаты, показанные ниже в Таблицах 117а и 117b, представляют собой средние значения общего содержания антисмысловых олигонуклеотидов в тканях для каждой экспериментальной группы, измеренные по УФ, в единицах измерения мкг олигонуклеотида на грамм ткани печени. Результаты демонстрируют, что олигонуклеотиды, содержащие группу конъюагата GalNAc, накапливаются в печени в существенно более высоких количествах, чем при той же дозе олигонуклеотида, не содержащего конъюгирующую группу GalNAc. Кроме того, антисмысловые олигонуклеотиды, содержащие один, два или три лиганда GalNAc в своих соответствующих группах конъюгата, накапливаются в печени в равных количествах. Этот результат является неожиданным с учетом данных, приведенных выше в литературном источнике Khorev et al., и он согласуется с данными активности, приведенными выше в Таблицах 116 и 117.
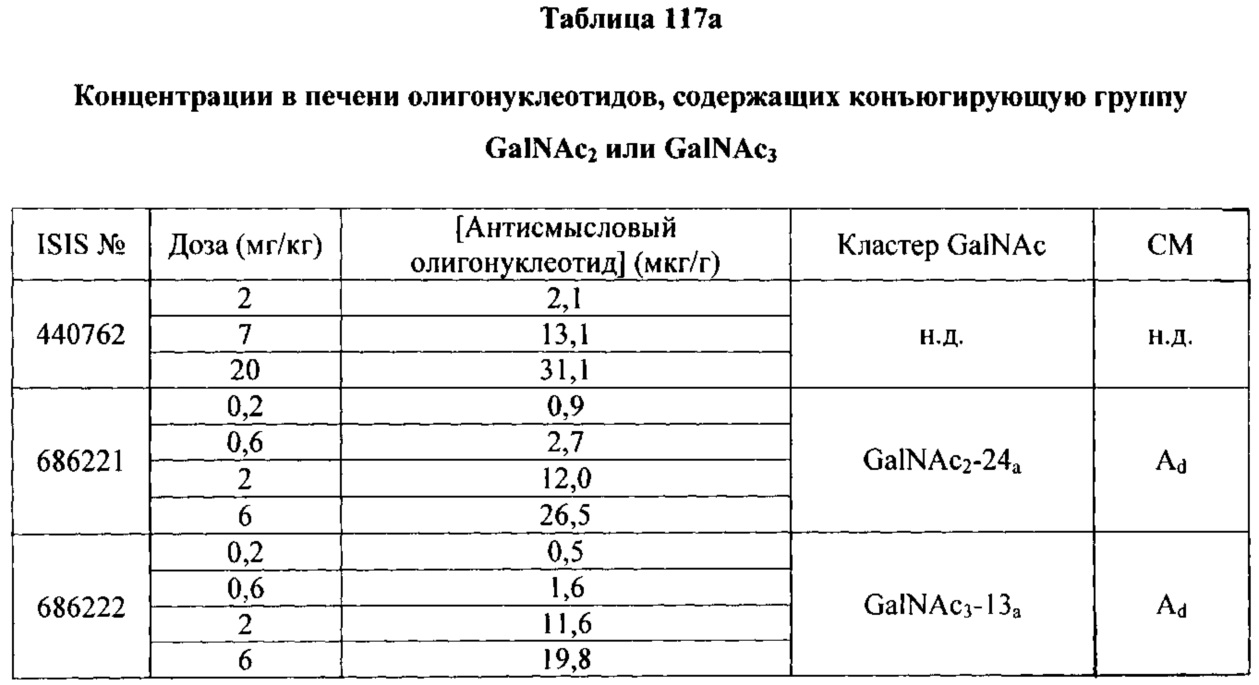
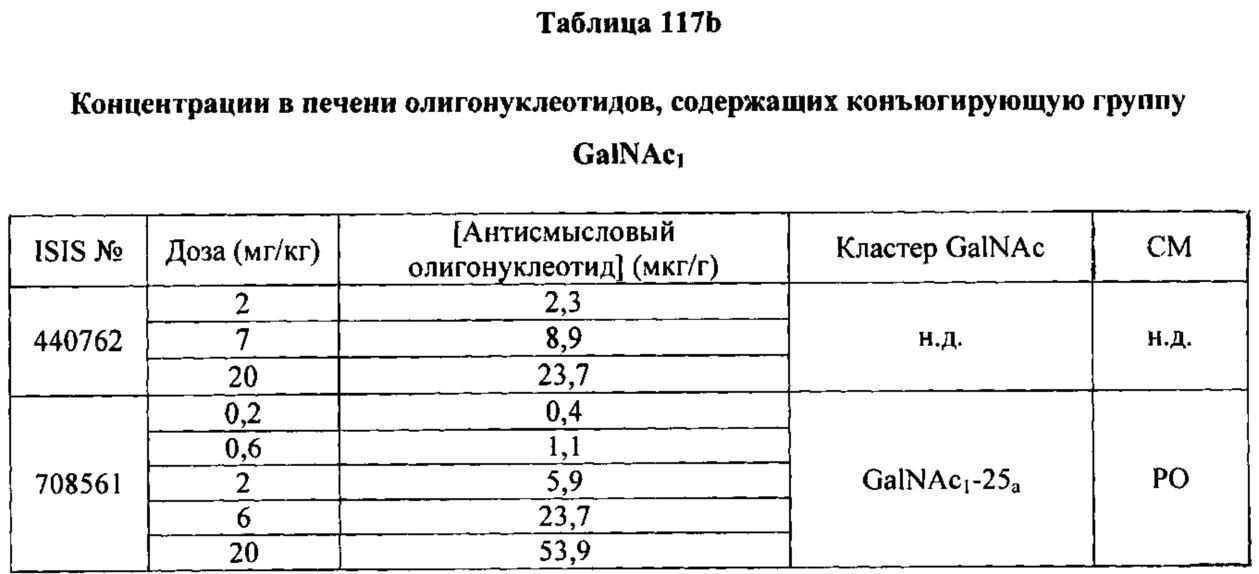
Пример 107. Синтез олигонуклеотидов, содержащих конъюгат GalNAc1-26 или GalNAc1-27
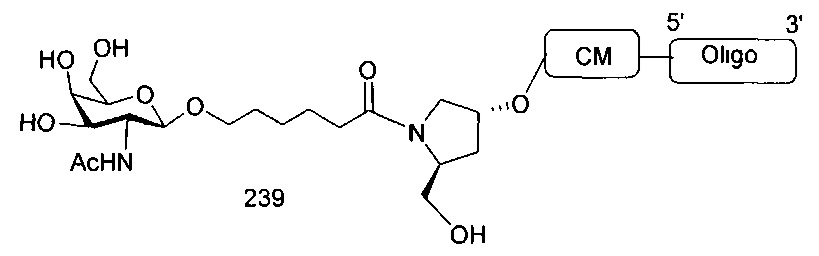
Олигонуклеотид 239 синтезировали связыванием соединения 47 (см. Пример 15) с кислотой 64 (см. Пример 32), применяя HBTU и DIEA в ДМФА. Полученное амид-содержащее соединение фосфитилировали, затем присоединили к 5'-концу олигонуклеотида по способам, описанным в Примере 10. Кластерная часть GalNAc1 (GalNAc1-26a) конъюгирующие группы GalNAc1-26 может быть комбинирована с любым расщепляемым фрагментом, содержащимся в олигонуклеотиде, с получением различных конъюгирующих групп. Структура GalNAc1-26 (GalNAc1-26a-CM) приведена ниже:
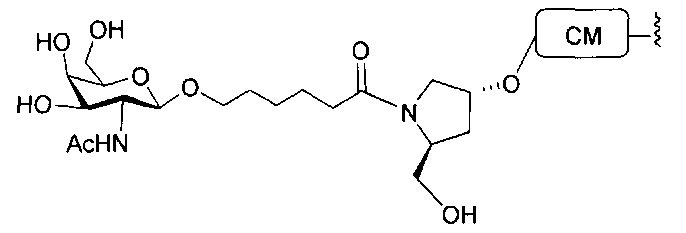
Для присоединения конъюгирующие группы GalNAc1 к 3'-концу олигонуклеотида амид, образованный по реакции соединений 47 и 64, присоединили к твердой подложке по способам, описанным в Примере 7. Затем выполнили синтез олигонуклеотида по способам, описанным в Примере 9, с получением олигонуклеотида 240.

Кластерная часть GalNAc1 (GalNAc1-27a) конъюгирующие группы GalNAc1-27 может быть комбинирована с любым расщепляемым фрагментом, содержащемся в олигонуклеотиде, с получением различных конъюгирующих групп. Структура GalNAc1-27 (GalNAc1-27a-CM) приведена ниже:
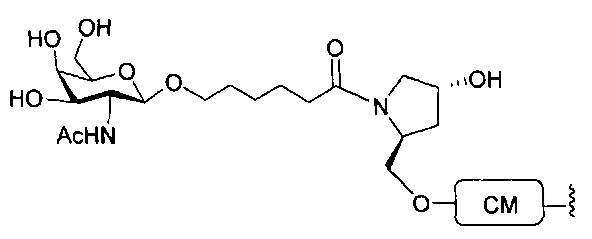
Пример 108. Антисмысловое ингибирование in vivo под действием олигонуклеотидов, содержащих конъюгирующую группу GalNAc, нацеленных на Аро(а), in vivo
Олигонуклеотиды, перечисленные ниже в Таблице 118, испытали в исследовании однократной дозы на мышах.

Структура GalNAc3-7a показана в Примере 48.
Лечение
Самцам трансгенных мышей, экспрессирующим человеческий Аро(а), ввели однократную подкожную инъекцию олигонуклеотида и дозы, перечисленных в Таблице 119, или PBS. Каждая экспериментальная группа состояла из 4 животных. Образцы крови брали за день до введения дозы для определения исходных уровней белка Аро(а) в плазме, а также через 1 неделю после введения первой дозы. Образцы крови брали дополнительно еженедельно в течение около 8 недель. Уровни белка Аро(а) в плазме измеряли при помощи твердофазного иммуноферментного анализа. Результаты в Таблице 119 приведены как средний процент от уровней белка Аро(а) в плазме для каждой экспериментальной группы, нормализованных к исходным уровням (% BL). Результаты показывают, что антисмысловые олигонуклеотиды снижают экспрессию белка Аро(а). Кроме того, олигонуклеотиды, содержащие конъюгирующую группу GalNAc, демонстрируют еще более эффективное снижение экспрессии Аро(а), чем олигонуклеотид, не содержащий конъюгирующую группу.
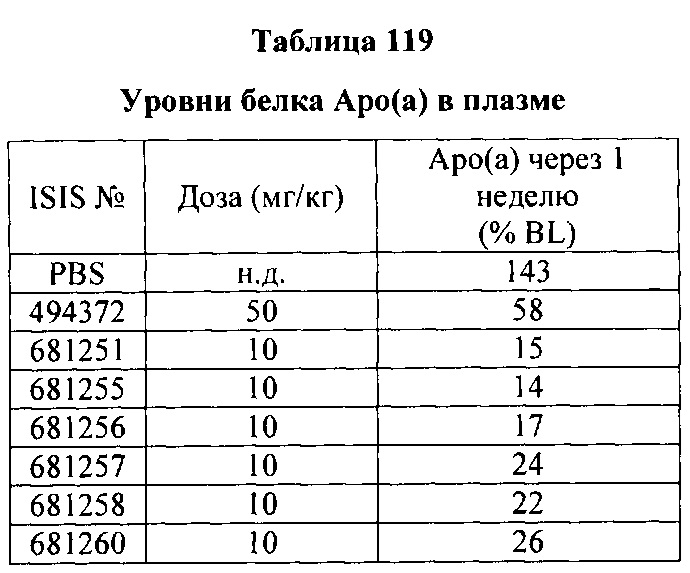
Пример 109. Синтез олигонуклеотидов, содержащих конъюгат GalNAc1-28 или GalNAc1-29
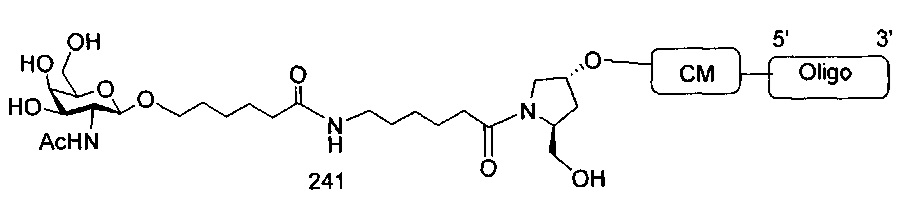
Олигонуклеотид 241 синтезировали по таким же способам, как описаны в Примере 71, с получением фосфорамидитного промежуточного соединения, после чего выполнили приемы, описанные в Примере 10, для синтеза олигонуклеотида. Кластерная часть GalNAc1 (GalNAc1-28a) конъюгирующие группы GalNAc1-28 может быть комбинирована с любым расщепляемым фрагментом, содержащемся в олигонуклеотиде, с получением различных конъюгирующих групп. Структура GalNAc1-28 (GalNAc1-28a-CM) приведена ниже:
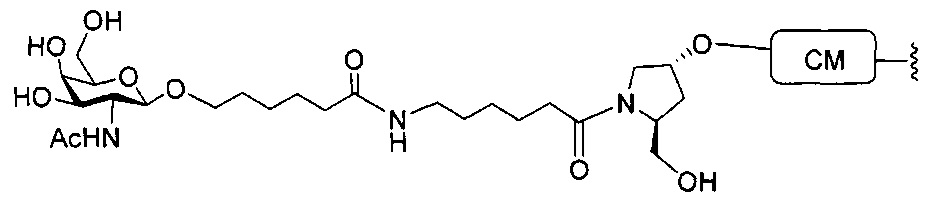
Для присоединения конъюгирующие группы GalNAc1 к 3'-концу олигонуклеотида применяли такие же способы, как описаны в Примере 71, с получение гидроксильного промежуточного соединения, которое затем присоединили к твердой подложке по способам, описанным в Примере 7. Затем выполнили синтез олигонуклеотида по способам, описанным в Примере 9, с получением олигонуклеотида 242.
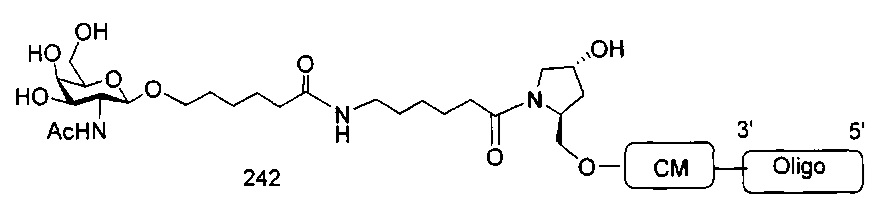
Кластерная часть GalNAc1 (GalNAc1-29a) конъюгирующие группы GalNAc1-29 может быть комбинирована с любым расщепляемым фрагментом, содержащемся в олигонуклеотиде, с получением различных конъюгирующих групп. Структура GalNAc1-29 (GalNAc1-29a-CM) приведена ниже:
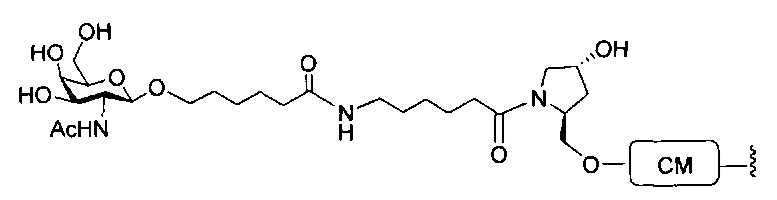
Пример 110. Синтез олигонуклеотидов, содержащих конъюгат GalNAc1-30
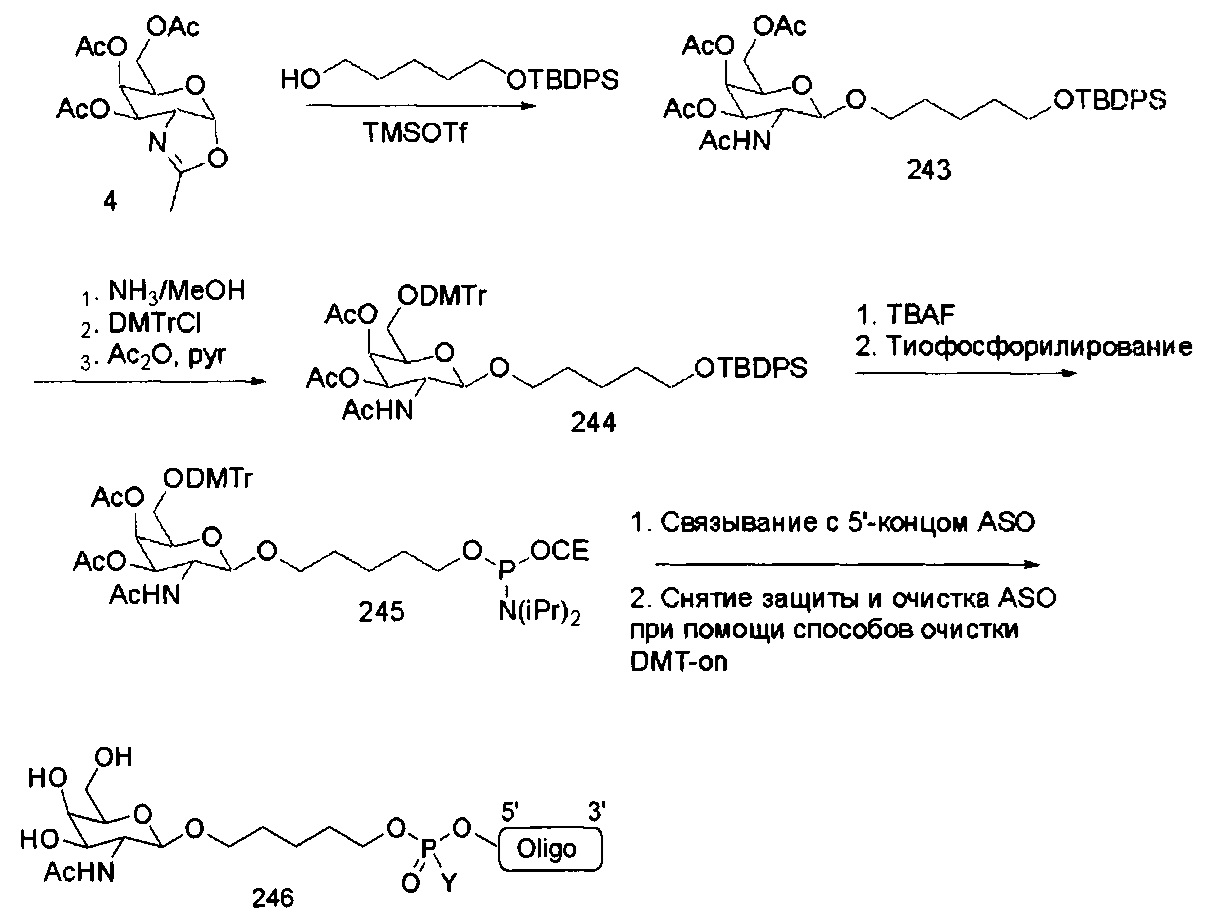
Олигонуклеотид 246, содержащий конъюгирующую группу GalNAc1-30, где Y выбран из О, S, замещенного или незамещенного C1-С10 алкила, амино, замещенного амино, азидо, алкенила или алкинила, синтезировали так, как показано выше. Кластерная часть GalNAc1 (GalNAc1-30a) конъюгирующие группы GalNAc1-30 может быть комбинирована с любым расщепляемым фрагментом с получением различных конъюгирующих групп. В некоторых вариантах реализации Y представляет собой часть расщепляемого фрагмента. В некоторых вариантах реализации Y представляет собой часть стабильного фрагмента, а расщепляемый фрагмент находится в олигонуклеотиде. Структура GalNAc1-30a приведена ниже:
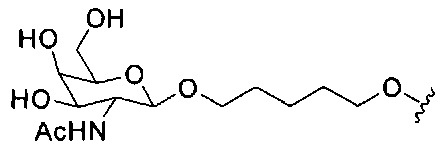
Пример 111. Синтез олигонуклеотидов, содержащих конъюгат GalNAc2-31 или GalNAc2-32
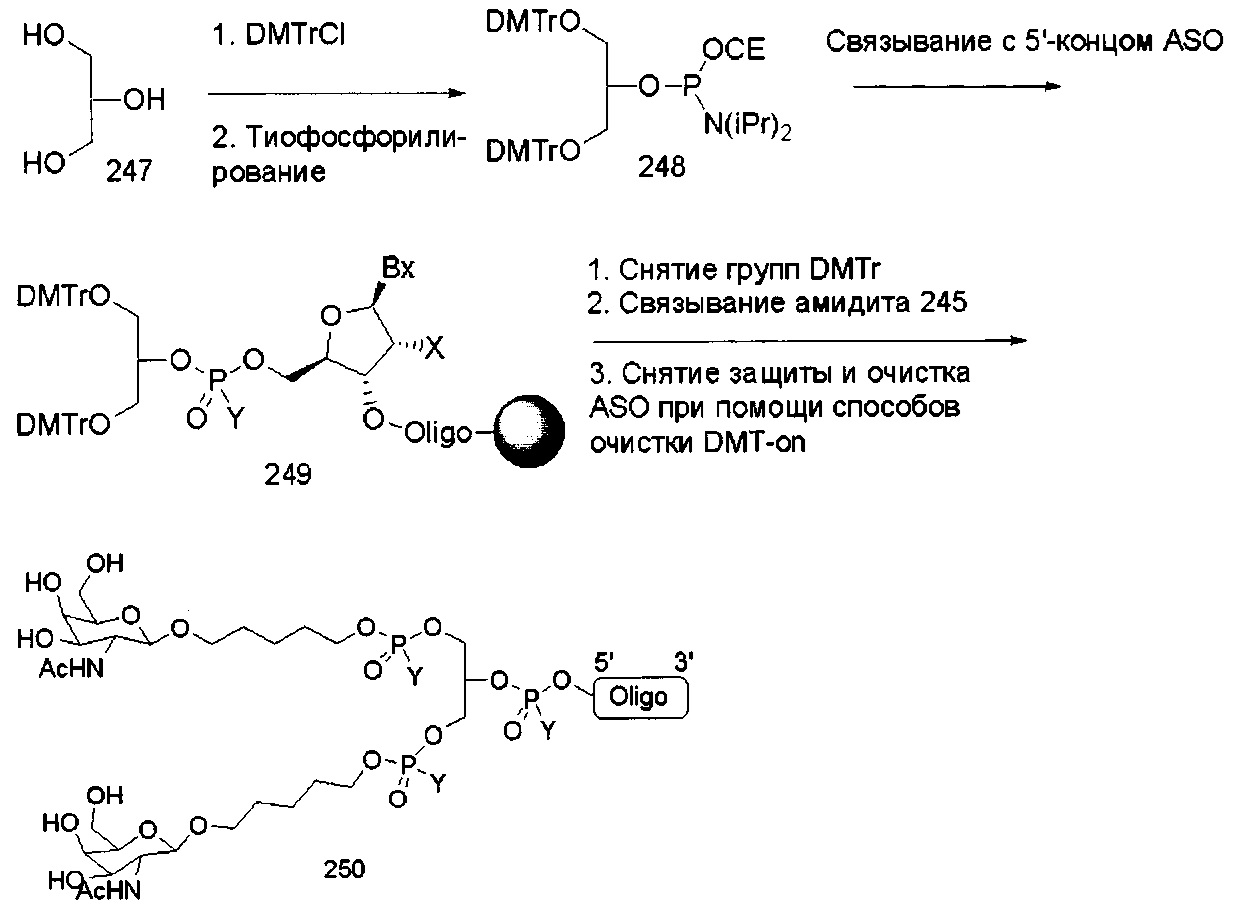
Олигонуклеотид 250, содержащий конъюгирующую группу GalNAc2-31, где Y выбран из О, S, замещенного или незамещенного C1-С10 алкила, амино, замещенного амино, азидо, алкенила или алкинила, синтезировали так, как показано выше. Кластерная часть GalNAc2 (GalNAc2-31a) конъюгирующие группы GalNAc2-31 может быть комбинирована с любым расщепляемым фрагментом с получением различных конъюгирующих групп. В некоторых вариантах реализации Y-содержащая группа, которая находится непосредственно возле 5'-конца олигонуклеотида, представляет собой часть расщепляемого фрагмента. В некоторых вариантах реализации Y-содержащая группа, которая находится непосредственно возле 5'-конца олигонуклеотида, представляет собой часть стабильного фрагмента, а расщепляемый фрагмент находится в олигонуклеотиде. Структура GalNAc2-31a приведена ниже:
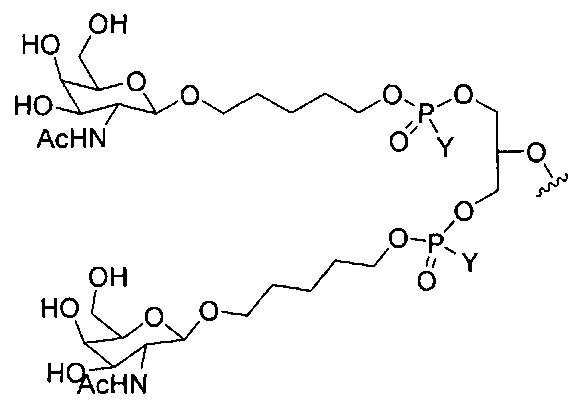
Синтез олигонуклеотида, содержащего конъюгат GalNAc2-32, приведен ниже.
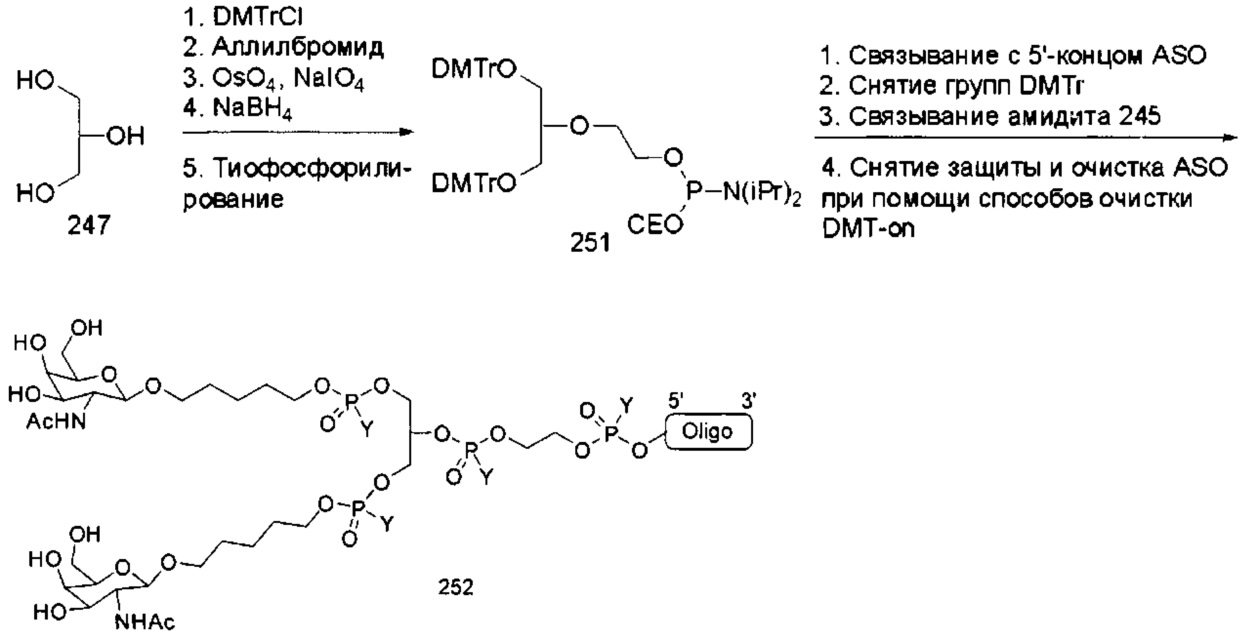
Олигонуклеотид 252, содержащий конъюгирующую группу GalNAc2-32, где Y выбран из О, S, замещенного или незамещенного С1-С10 алкила, амино, замещенного амино, азидо, алкенила или алкинила, синтезировали так, как показано выше. Кластерная часть GaiNAc2 (GalNAc2-32a) конъюгирующие группы GalNAc2-32 может быть комбинирована с любым расщепляемым фрагментом с получением различных конъюгирующих групп. В некоторых вариантах реализации Y-содержащая группа, которая находится непосредственно возле 5'-конца олигонуклеотида, представляет собой часть расщепляемого фрагмента. В некоторых вариантах реализации Y-содержащая группа, которая находится непосредственно возле 5'-конца олигонуклеотида, представляет собой часть стабильного фрагмента, а расщепляемый фрагмент находится в олигонуклеотиде. Структура GalNAc2-32a приведена ниже:
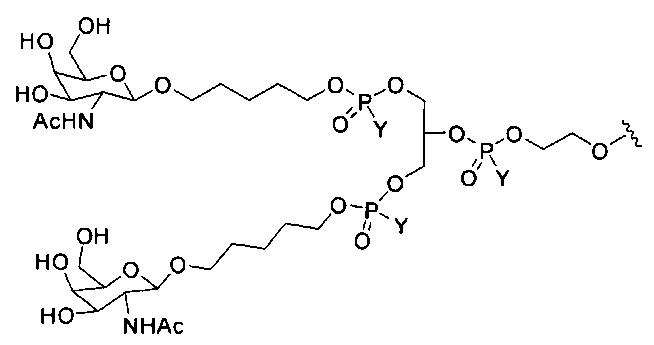
Пример 112. Модифицированные олигонуклеотиды, содержащие конъюгат GalNAc1
Олигонуклеотиды в Таблице 120, нацеленные на SRB-1, были синтезированы с конъюгирующей группой GalNAc1 для дополнительной проверки эффективности олигонуклеотидов, содержащих конъюгирующие группы, которые содержат лиганд GalNAc.
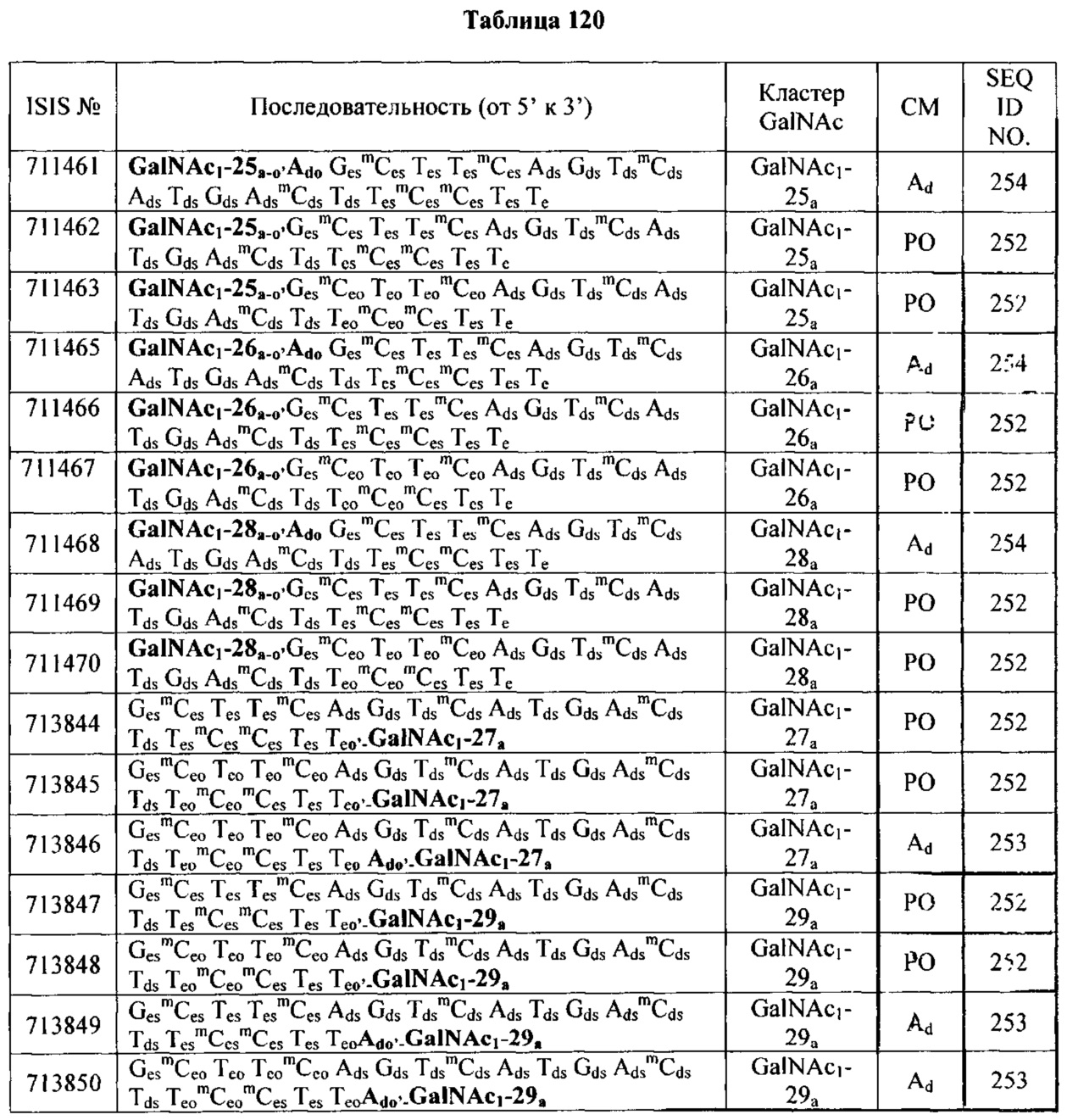
Пример 113. Разработка и скрининг дуплексных антисмысловых соединений, нацеленных на аполипопротеин С-III
В соответствии с настоящим изобретением, для нацеливания на аполипопротеин С-III разрабатывают серию дуплексов нуклеиновых кислот, содержащих антисмысловые соединения согласно настоящему изобретению и их комплементы. Последовательность азотистых оснований антисмысловой цепи дуплекса содержит по меньшей мере часть олигонуклеотида, приведенного в Таблице 121. Концы цепи могут быть модифицированы путем добавления одного или более природных или модифицированных азотистых оснований с образованием выступающего конца. Затем разрабатывают смысловую цепь дцРНК и синтезируют ее в качестве комплемента антисмысловой цепи, и она также может содержать модификации или добавления на концах. Например, в одном из вариантов реализации изобретения обе цепи дуплекса дцРНК комплементарны по центральным азотистым основаниям, и каждая из них имеет выступающие концы с одной или с обеих сторон.
Например, дуплекс, содержащий антисмысловую цепь, имеющую последовательность CGAGAGGCGGACGGGACCG (SEQ ID NO: 12) и содержащую выступающий конец из двух нуклеозидов дезокситимидина (dT), имеет следующую структуру (антисмысловая SEQ ID NO: 13, комплемент SEQ ID NO: 14):
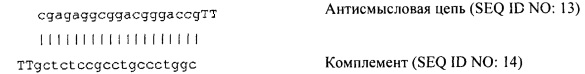
В другом варианте реализации изобретения дуплекс, содержащий антисмысловую цепь, имеющую ту же последовательность CGAGAGGCGGACGGGACCG (SEQ ID NO: 12), может быть получен с тупыми концами (ни у одной цепи нет выступающих концов), как показано ниже (антисмысловая SEQ ID NO: 15, комплемент SEQ ID NO: 16):
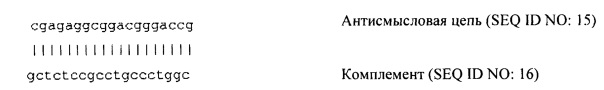
Цепи РНК дуплекса могут быть синтезированы по способам, описанным в настоящем документе, или могут быть приобретены у компании Dharmacon Research Inc., (Лафайет, штат Колорадо). После синтеза комплементарные цепи соединяют. Берут аликвоты одиночных цепей и разбавляют до концентрации 50 мкМ. После разбавления 30 мкл каждой цепи смешивают с 15 мкл 5Х раствора ренатурирующего буфера. Конечная концентрация указанного буфера составляет 100 мМ ацетата калия, 30 мМ HEPES-KOH, рН 7,4 и 2 мМ ацетата магния. Конечный объем составляет 75 мкл. Этот раствор инкубируют в течение 1 минуты при 90°С, а затем центрифугируют в течение 15 секунд. Пробирку оставляют осаждаться в течение 1 часа при 37°С, а затем используют дуплексы дцРНК для экспериментов. Конечная концентрация дуплекса дцРНК равна 20 мкМ. Этот раствор можно хранить в замороженном состоянии (-20°С) и замораживать-оттаивать до 5 раз.
После получения дуплексные антисмысловые соединения оценивают на их способность модулировать экспрессию аполипопротеина C-III.
Когда клетки достигают 80% конфлюентности, их обрабатывают дуплексными антисмысловыми соединениями согласно настоящему изобретению. Для роста клеток в 96-луночных планшетах лунки один раз промывают 200 мкл среды со сниженным содержанием сыворотки OPTI-MEM-1™ (Gibco BRL), а затем обрабатывают 130 мкл среды OPTI-MEM-1™, содержащей 12 мкг/мл реагента LIPOFECTIN™ (Gibco BRL) и заданное дуплексное антисмысловое соединение в конечной концентрации 200 нМ. Через 5 часов обработки среду заменяют свежей средой. Через 16 часов обработки клетки собирают, и в это время выделяют РНК и измеряют заданное снижение при помощи ПЦР в реальном времени.
Пример 114. Антисмысловое ингибирование экспрессии человеческого аполипопротеина С-III при помощи химерных тиофосфатных олигонуклеотидов, имеющих крылья 2'-МОЕ и дезокси-гэп.
В соответствии с настоящим изобретением, разработали серию антисмысловых соединений для нацеливания на различные области РНК человеческого аполипопротеина С-III, используя опубликованные последовательности (нуклеотиды 6238608 - 6242565 из последовательности GenBank с номером доступа NT_035088.1, которая представляет собой геномную последовательность, включенную в настоящий документ как SEQ ID NO: 3, и GenBank с номером доступа NM_000040.1, включенную в настоящий документ как SEQ ID NO: 1). Соединения приведены в Таблице 121. «Сайт-мишень» указывает номер первого (5'-основной) нуклеотида в конкретной целевой последовательности, с которым связывается соединение. Все соединения в Таблице 121 представляют собой химерные олигонуклеотиды («гэпмеры») длиной 20 нуклеотидов, состоящие из центральной области «гэп», состоящей из десяти 2'-дезоксинуклеотидов, к которой с обеих сторон (направления 5' и 3') присоединены пятинуклеотидные «крылья». Эти крылья состоят из 2'-O-(2-метоксиэтил)-нуклеотидов, известных также как (2'-МОЕ)-нуклеотиды. Межнуклеозидные (скелетные) связи являются тиофосфатными (P=S) по всему олигонуклеотиду. Все цитидиновые остатки представляют собой 5-метилцитидин. Соединения анализировали на их влияние на уровни мРНК человеческого аполипопротеина С-III при помощи количественной ПЦР в реальном времени, как описано в других примерах настоящего документа. Данные являются средними значениями для трех экспериментов, в которых клетки HepG2 обрабатывали антисмысловыми олигонуклеотидами согласно настоящему изобретению. Положительный контроль для каждой точки данных указан в таблице в столбце ID номер последовательности. «Н.д.», при наличии, означает «нет данных».
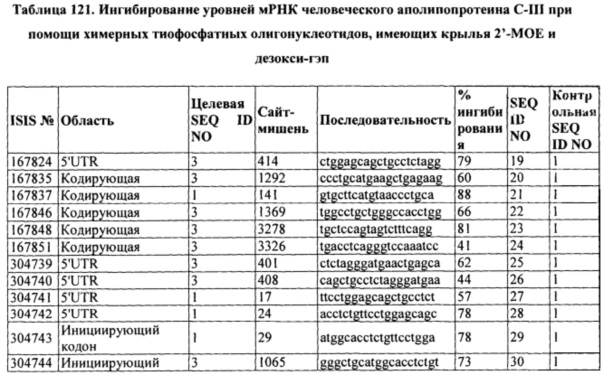
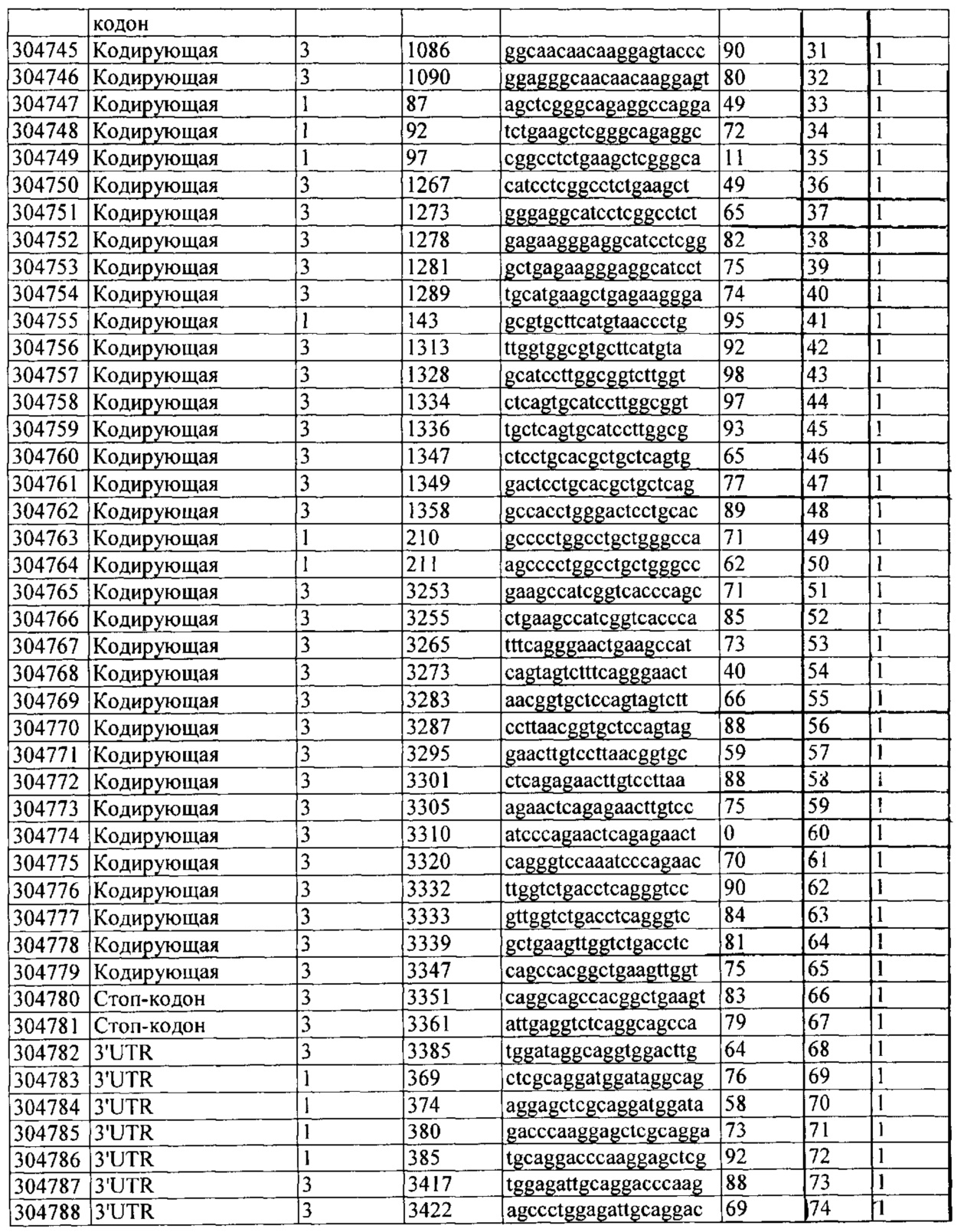
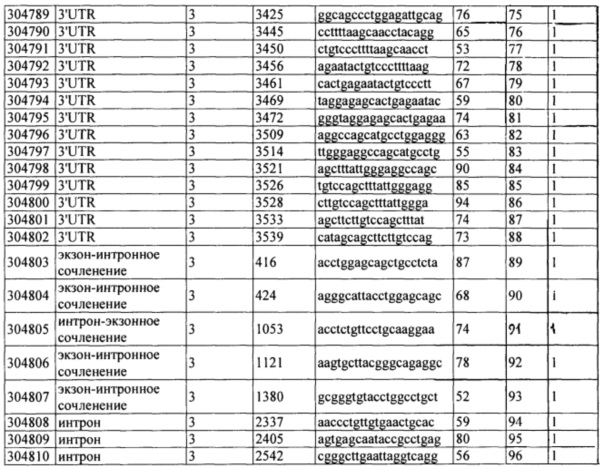
Как показано в таблице выше, SEQ ID NO 19, 20, 21, 22, 23, 25, 27, 28, 29, 30, 31, 32, 33, 34, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 55, 56, 57, 58, 59, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95 и 96 в этом анализе демонстрируют по меньшей мере 45% ингибирование экспрессии человеческого аполипопротеина С-III и, следовательно, являются предпочтительными. Более предпочтительны SEQ ID NO 75, 86 и 85. Целевые области, к которым комплементарны эти предпочтительные последовательности, упомянуты в настоящем документе как «предпочтительные целевые сегменты» и, следовательно, они являются предпочтительными для нацеленных на них соединений согласно настоящему изобретению. Эти предпочтительные целевые сегменты приведены ниже в Таблице 123. Эти последовательности представляют собой обратный комплемент предпочтительных антисмысловых соединений, приведенных в таблице выше. «Сайт-мишень» означает номер первого (5'-основного) нуклеотида в конкретной целевой нуклеиновой кислоте, с которым связывается олигонуклеотид. В Таблице 123 показаны также виды, в которых встречаются каждый из предпочтительных целевых сегментов.
Пример 115. Антисмысловое ингибирование экспрессии мышиного аполипопротеина С-III при помощи химерных тиофосфатных олигонуклеотидов, имеющих крылья 2'-МОЕ и дезокси-гэп
В соответствии с настоящим изобретением, разработали вторую серию антисмысловых соединений для нацеливания на различные области РНК мышиного аполипопротеина С-III, используя опубликованные последовательности (GenBank с номером доступа L04150.1, включенную в настоящий документ как SEQ ID NO: 11). Соединения приведены в Таблице 2. «Сайт-мишень» указывает номер первого (5'-основной) нуклеотида в конкретной целевой нуклеиновой кислоте, с которым связывается соединение. Все соединения в Таблице 2 представляют собой химерные олигонуклеотиды («гэпмеры») длиной 20 нуклеотидов, состоящие из центральной области «гэп», состоящей из десяти 2'-дезоксинуклеотидов, к которой с обеих сторон (направления 5' и 3') присоединены пятинуклеотидные «крылья». Эти крылья состоят из 2'-O-(2-метоксиэтил)-нуклеотидов, известных также как (2'-МОЕ)-нуклеотиды. Межнуклеозидные (скелетные) связи являются тиофосфатными (P=S) по всему олигонуклеотиду. Все цитидиновые остатки представляют собой 5-метилцитидин. Соединения анализировали на их влияние на уровни мРНК мышиного аполипопротеина С-III при помощи количественной ПЦР в реальном времени, как описано в других примерах настоящего документа. Данные являются средними значениями для трех экспериментов, в которых первичные гепатоциты обрабатывали антисмысловыми олигонуклеотидами согласно настоящему изобретению. «Н.д.», при наличии, означает «нет данных».
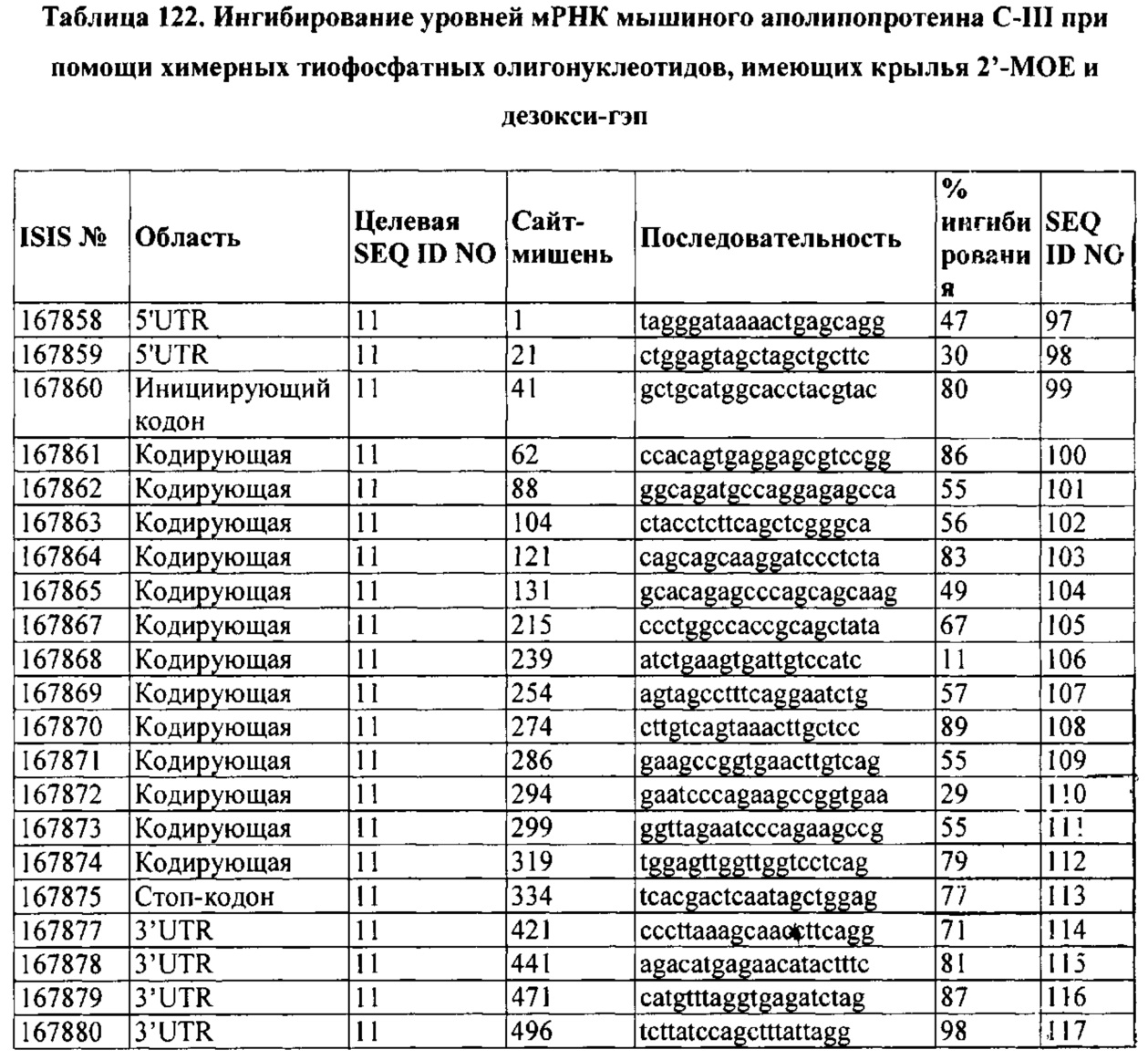
Как показано в таблице выше, в этом эксперименте SEQ ID NO 97, 99, 100, 101, 102, 103, 104, 105, 107, 108, 109, 111, 112, 113, 114, 115, 116 и 117 демонстрируют по меньшей мере 45% ингибирование экспрессии мышиного аполипопротеина С-III и, следовательно, являются предпочтительными. Более предпочтительны SEQ ID NO 117, 116 и 100. Целевые области, к которым комплементарны эти предпочтительные последовательности, упомянуты в настоящем документе как «предпочтительные целевые сегменты» и, следовательно, они являются предпочтительными для нацеленных на них соединений согласно настоящему изобретению. Эти предпочтительные целевые сегменты приведены в таблице ниже. Эти последовательности представляют собой обратный комплемент предпочтительных антисмысловых соединений, приведенных в таблице выше. Эти последовательности показаны как содержащие тимин (Т), но специалистам в данной области техники понятно, что тимин (Т) обычно заменен урацилом (U) в последовательностях РНК. «Сайт-мишень» означает номер первого (5'-основного) нуклеотида в конкретной целевой нуклеиновой кислоте, с которым связывается олигонуклеотид. В Таблице 3 показаны также виды, в которых встречается каждый из предпочтительных целевых сегментов.
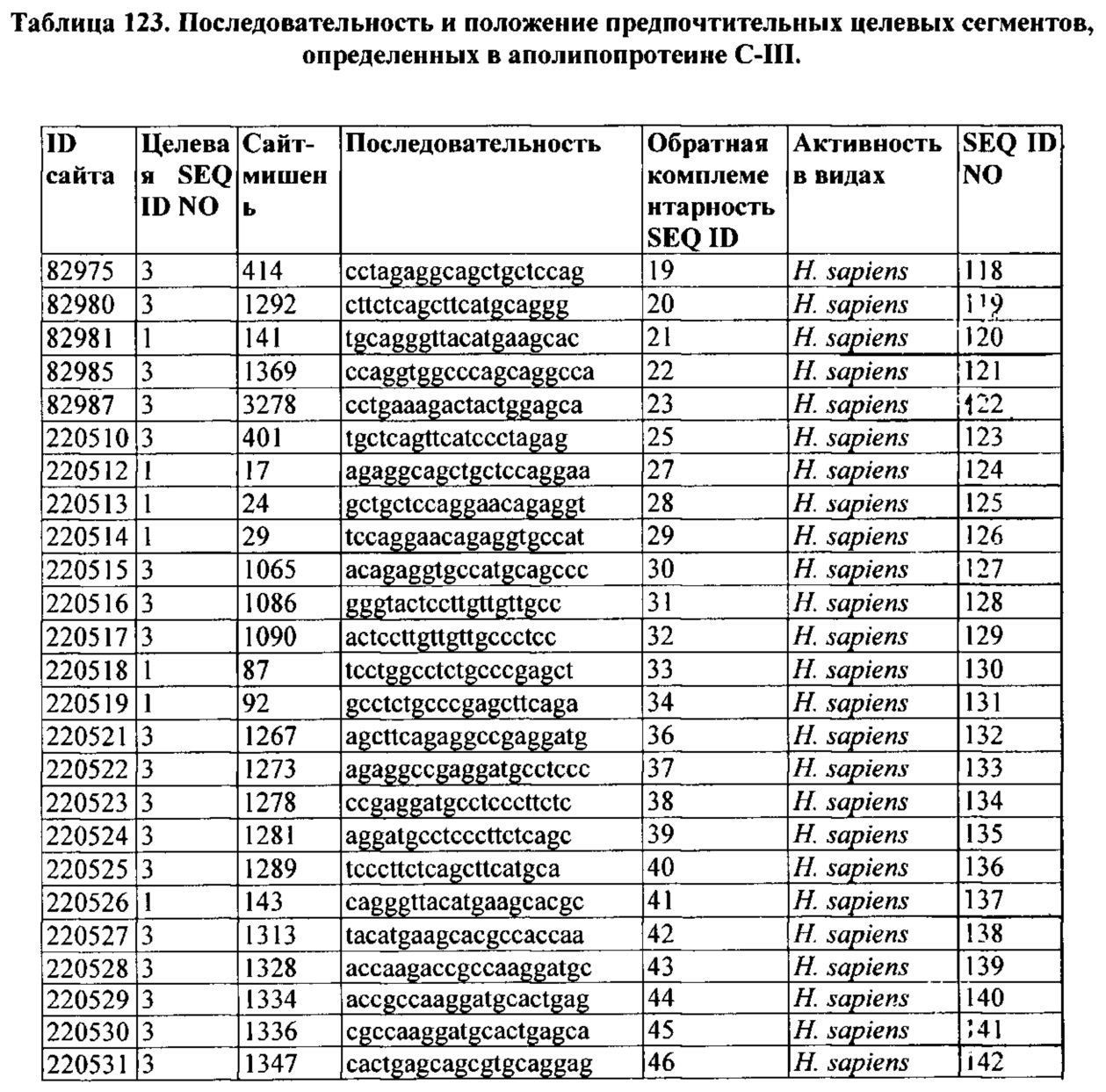
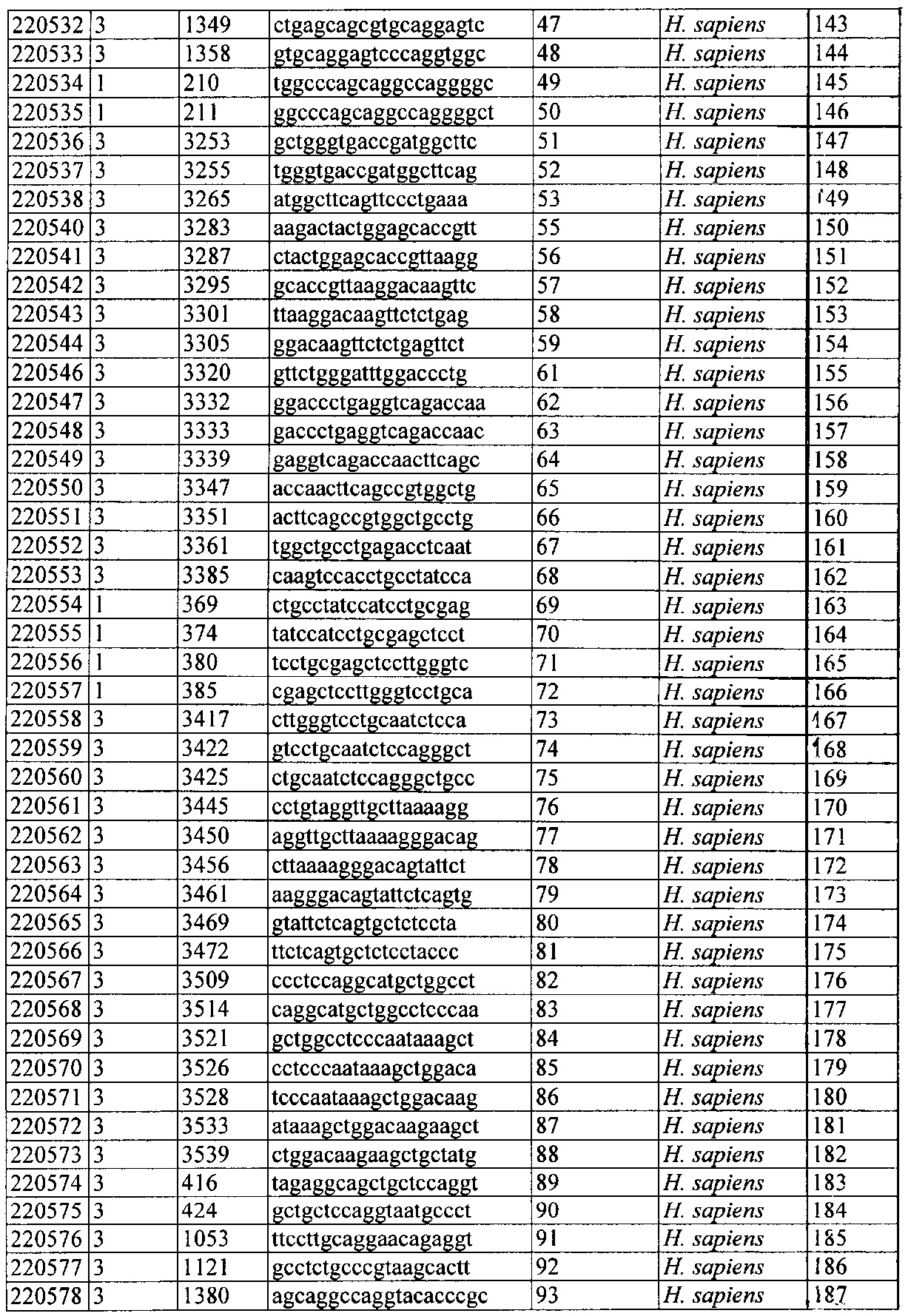
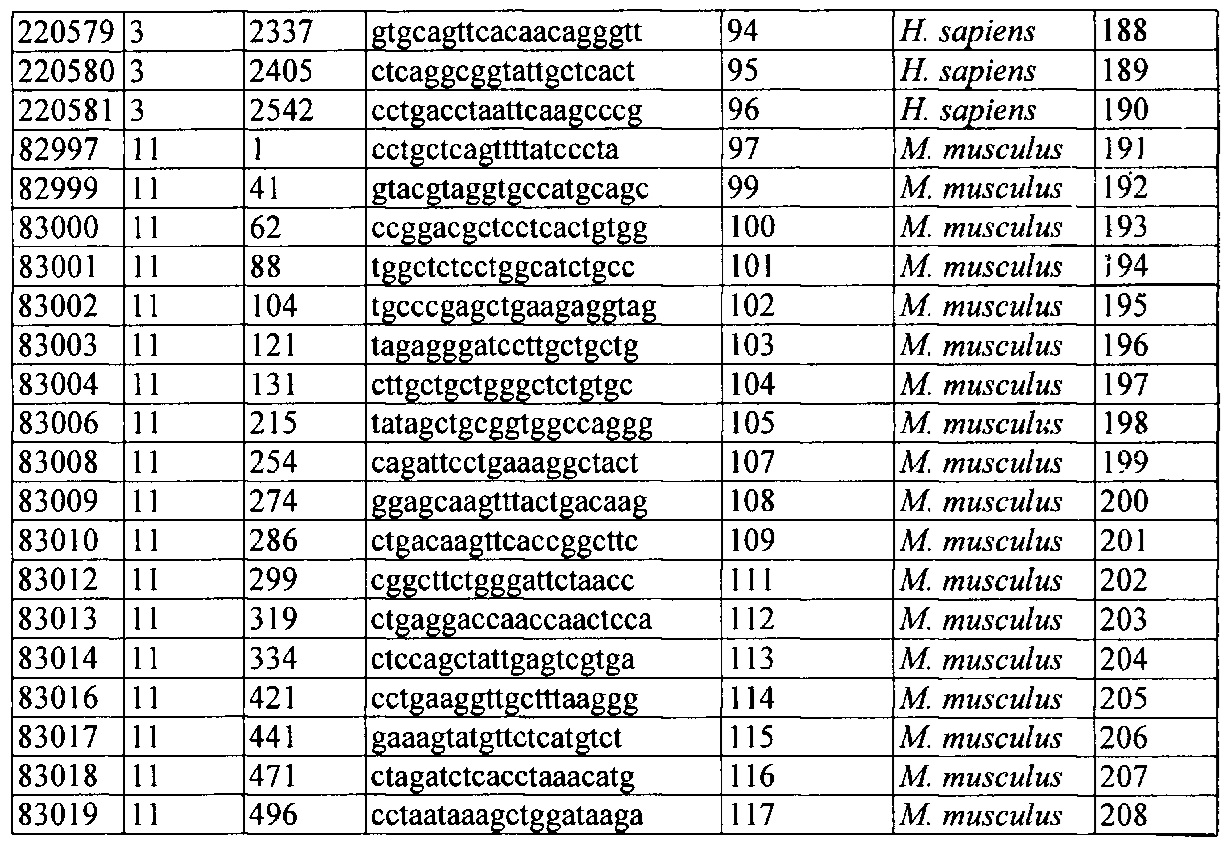
Поскольку в экспериментах было обнаружено, что эти «предпочтительные целевые сегменты» открыты и доступны для гибридизации с антисмысловыми соединениями согласно настоящему изобретению, то специалисты в данной области техники могут понять или предположить, используя не более чем стандартные эксперименты, дополнительные варианты реализации настоящего изобретения, которые охватывают другие соединения, который специфически гибридизуются с указанными предпочтительными целевыми сегментами и, следовательно, ингибируют экспрессию аполипопротеина С-III.
В соответствии с настоящим изобретением, антисмысловые соединения включают антисмысловые олигомерные соединения, антисмысловые олигонуклеотиды, рибозимы, олигонуклеотиды с внешней нацеливающей последовательностью (EGS), альтернативные сплайсеры, праймеры, зонды и другие короткие олигомерные соединения, которые гибридизуются по меньшей мере с частью целевой нуклеиновой кислоты.
Пример 116. Антисмысловое ингибирование экспрессии человеческого аполипопротеина С-III при помощи химерных тиофосфатных олигонуклеотидов, имеющих крылья 2'-МОЕ и дезокси-гэп - дополнительные антисмысловые соединения
В соответствии с настоящим изобретением, разработали дополнительную серию антисмысловых соединений для нацеливания на различные области РНК человеческого аполипопротеина С-III, используя опубликованные последовательности (нуклеотиды 6238608 - 6242565 из последовательности с номером доступа GenBank NT_035088.1, которая представляет собой геномную последовательность, включенную в настоящий документ как SEQ ID NO: 3, и с номером доступа GenBank NM_000040.1, включенную в настоящий документ как SEQ ID NO: 1). Соединения приведены в Таблице 124. «Сайт-мишень» указывает номер первого (5'-основной) нуклеотида в конкретной целевой последовательности, с которой связывается соединение. Все соединения в Таблице 124 представляют собой химерные олигонуклеотиды («гэпмеры») длиной 20 нуклеотидов, состоящие из центральной области «гэп», состоящей из десяти 2'-дезоксинуклеогидов, к которой с обеих сторон (направления 5' и 3') присоединены пятинуклеотидиые «крылья». Эти крылья состоят из 2'-0-(2-метоксиэтил)-нуклеотидов, известных также как (2'-МОЕ)-нуклеотиды. Межнуклеозидные (скелетные) связи являются тиофосфатными (Р=S) по всему олигонуклеотиду. Все цитидиновые остатки представляют собой 5-метилцитидин. Соединения анализировали на их влияние на уровни мРНК человеческого аполипопротеина С-III при помощи количественной ПЦР в реальном времени, как описано в других примерах настоящего документа. Данные являются средними значениями для трех экспериментов, в которых клетки HepG2 обрабатывали антисмысловыми олигонуклеотидами согласно настоящему изобретению. «Н.д.», при наличии, означает «нет данных».


Пример 117. Антисмысловое ингибирование экспрессии человеческого аполипопротеина С-III при помощи химерных тиофосфатных олигонуклеотидов, имеющих крылья 2'-МОЕ и дезокси-гэп: исследование зависимости эффективности от дозы в клетках HepG2
В соответствии с настоящим изобретением дополнительно исследовали подгруппу антисмысловых олигонуклеотидов из Примеров 15 и 17 в исследовании зависимости эффективности от дозы. Экспериментальные дозы ISIS 167842 (SEQ ID NO: 214), ISIS 167844 (SEQ ID NO: 215), ISIS 167846 (SEQ ID NO: 22), ISIS 167837 (SEQ ID NO: 21), ISIS 304789 (SEQ ID NO: 75), ISIS 304799 (SEQ ID NO: 85) и ISIS 304800 (SEQ ID: 86) составили 50, 150 и 300 нМ. Соединения анализировали на их влияние на уровни мРНК человеческого аполипопротеина С-III в клетках HepG2 при помощи количественной ПЦР в реальном времени, как описано в других примерах настоящего документа. Данные представляют собой средние значения для двух экспериментов и приведены в таблице ниже.
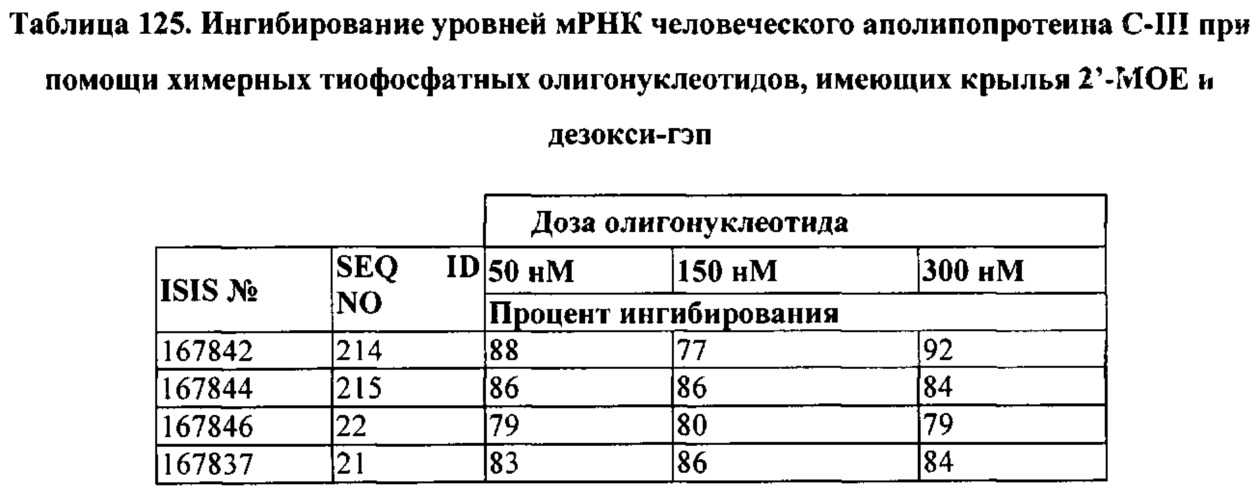
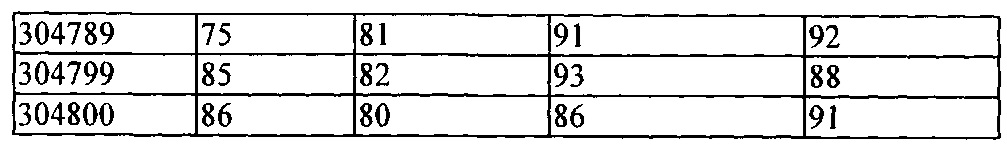
Эти данные демонстрируют, что экспрессия аполипопротеина С-III ингибируется дозозависимым образом при обработке клеток антисмысловыми соединениями, нацеленными на аполипопротеин С-III. Эти соединения дополнительно анализировали в клетках Нер3В на их способность снижать уровни мРНК в клетках Нер3В, и установили, что в этой клеточной линии ISIS 167842 и 167837 также ингибируют экспрессию аполипопротеина С-III дозозависимым образом.
Пример 118. Антисмысловое ингибирование аполипопротеина С-III в первичных гепатоцитах яванских макак
В дополнительном варианте реализации изобретения испытали влияние антисмысловых соединений, нацеленных на человеческий аполипопротеин С-III, на экспрессию аполипопротеина С-III в первичных гепатоцитах яванских макак. Заранее размещенные на планшете первичные гепатоциты яванских макак приобрели у компании InVitro Technologies (Балтимор, штат Мэриленд). Клетки выращивали в среде DMEM с высоким содержанием глюкозы (Invitrogen Life Technologies, Карлсбад, штат Калифорния) с добавлением 10% эмбриональной бычьей сыворотки (Invitrogen Life Technologies, Карлсбад, штат Калифорния), 100 ед./мл и 100 мкг/мл стрептомицина (Invitrogen Life Technologies, Карлсбад, штат Калифорния).
При плотности 80000 клеток на лунку в 24-луночном планшете клетки обработали 10, 50, 150 и 300 нМ ISIS 304789 (SEQ ID NO: 75), ISIS 304799 (SEQ ID NO: 85) или ISIS 304800 (SEQ ID NO: 86). ISIS 113529 (CTCTTACTGTGCTGTGGACA, SEQ ID NO: 17) использовали в качестве контрольного олигонуклеотида. ISIS 113529 представляет собой химерный олигонуклеотид («гэпмер») длиной 20 нуклеотидов, состоящий из центральной области «гэп», состоящей из десяти 2'-дезоксинуклеотидов, к которой с обеих сторон (направления 5' и 3') присоединены пятинуклеотидные «крылья». Эти крылья состоят из 2'-O-(2-метоксиэтил)-нуклеотидов, известных также как (2'-МОЕ)-нуклеотиды. Межнуклеозидные (скелетные) связи являются тиофосфатными (P=S) по всему олигонуклеотиду. Все цитидиновые остатки представляют собой 5-метилцитидин.
Через 24 часа обработки антисмысловыми олигонуклеотидами выполнили измерение мРНК аполипопротеина С-III при помощи ПЦР в реальном времени, как описано у других примерах настоящего документа, используя праймеры и зонд, разработанные для последовательности человеческого аполипопротеина С-III (прямой праймер: TCAGCTTCATGCAGGGTTACAT (SEQ ID NO: 5), обратный праймер: ACGCTGCTCAGTGCATCCT (SEQ ID NO: 6) и зонд ПЦР: FAM-AAGCACGCCACCAAGACCGCC-TAMRA (SEQ ID NO: 7)) для измерения мРНК аполипопротеина С-III яванских макак. Праймеры и зонд, разработанные для человеческой (прямой праймер: GAAGGTGAAGGTCGGAGTC (SEQ ID NO: 8), обратный праймер: GAAGATGGTGATGGGATTTC (SEQ ID NO: 9) и зонд ПЦР: 5' JOE-CAAGCTTCCCGTTCTCAGCC-TAMRA 3' (SEQ ID NO: 10)) использовали для измерения экспрессии мРНК GAPDH яванских макак, чтобы нормализовать количества заданных генов. полученные в ПЦР в реальном времени. Необработанные клетки использовали в качестве контроля, к которому нормализовали полученные данные. Данные представляют собой среднее значение для трех испытаний и приведены в таблице ниже.

Пример 119. Последовательность аполипопротеина С-III яванских макак
В дополнительном варианте реализации изобретения секвенировали часть гена аполипопротеина С-III яванских макак. Положения 8-476 последовательности мРНК человеческого аполипопротеина С-III (включенные в настоящий документ в полном объеме как SEQ ID NO: 1) содержат целевой сегмент, с которым гибридизуется ISIS 304789. Секвенировали соответствующую область мРНК аполипопротеина С-III яванских макак. РНК выделили и очистили из первичных гепатоцитов яванских макак (InVitro Technologies, Гейтерсберг, штат Мэриленд) и подвергли реакции с обратной транскриптазой (набор от Invitrogen Life Technologies, Карлсбад, штат Калифорния). Полученная кДНК служила субстратом для 40 циклов ПЦР амплификации с использованием 5' и 3' праймеров, разработанных для положений 8 и 476, соответственно, мРНК человеческого аполипопротеина С-III (набор Amplitaq PCR, Invitrogen Life Technologies, Карлсбад, штат Калифорния). После гелевой очистки полученного фрагмента размером 468 п.о. в компании Retrogen (Санд-Диего, штат Калифорния) выполнили прямую и обратную реакцию секвенирования каждого продукта. Эта последовательность яванских макак включена в настоящий документ как SEQ ID NO: 223 и она на 92% идентична положениям 8-476 мРНК человеческого аполипопротеина С-III.
Пример 120. Химерный тиофосфатный олигонуклеотид, имеющий 2'-МОЕ крылья и дезокси-гэп, нацеленный на аполипопротеин С-III яванских макак.
В дополнительном варианте реализации использовали последовательность аполипопротеина С-III яванских макак, включенную в настоящий документ как SEQ ID NO: 223, для разработки антисмыслового олигонуклеотида, имеющего 100% комплементарность с мРНК аполипопротеина С-III яванских макак. ISIS 340340 (GGCAGCCCTGGAGGCTGCAG; включенный в настоящий документ как SEQ ID NO: 18) нацелен на нуклеотид 397 в SEQ ID NO: 223 в области, соответствующей 3' UTR человеческого аполипопротеина С-III, с которой гибридизуется ISIS 304789. ISIS 340340 представляет собой химерный олигонуклеотид («гэпмер») длиной 20 нуклеотидов, состоящий из центральной области «гэп», состоящей из 2'-дезоксинуклеотидов, к которой с обеих сторон (направления 5' и 3') присоединены 5-нуклеотидные «крылья». Эти крылья состоят из 2'-метоксиэтиловых (2'-МОЕ) нуклеотидов. Межнуклеозидные (скелетные) связи являются тиофосфатными (P=S) по всему нуклеотиду. Все цитидиновые остатки представляют собой 5-метилцитидин.
Реферат
Изобретение относится к пригодному для применения в медицине соединению, содержащему модифицированный олигонуклеотид и конъюгирующую группупри этом модифицированный олигонуклеотид состоит из 20 связанных азотистых оснований, комплементарных равной по длине части азотистых оснований 3533-3552 в SEQ ID NO: 3, при этом модифицированный олигонуклеотид содержит сегмент гэп, состоящий из связанных дезоксинуклеозидов; сегмент крыла 5', состоящий из связанных нуклеозидов; сегмент крыла 3', состоящий из связанных нуклеозидов; при этом сегмент гэп расположен между сегментом крыла 5' и сегментом крыла 3', и при этом каждый нуклеозид каждого сегмента крыла содержит модифицированный сахар, и где по меньшей мере один нуклеозид содержит модифицированное азотистое основание; и модифицированный олигонуклеотид содержит по меньшей мере одну модифицированную межнуклеозидную связь. Предложены новые конъюгаты модифицированных олигонуклеотидов и композиции на их основе для лечения, предупреждения или замедления прогрессирования заболевания, связанного с повышенным уровнем аполипопротеина C-III (ApoCIII). 5 н. и 16 з.п. ф-лы, 120 пр., 119 табл.
Формула
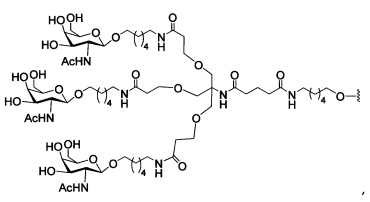
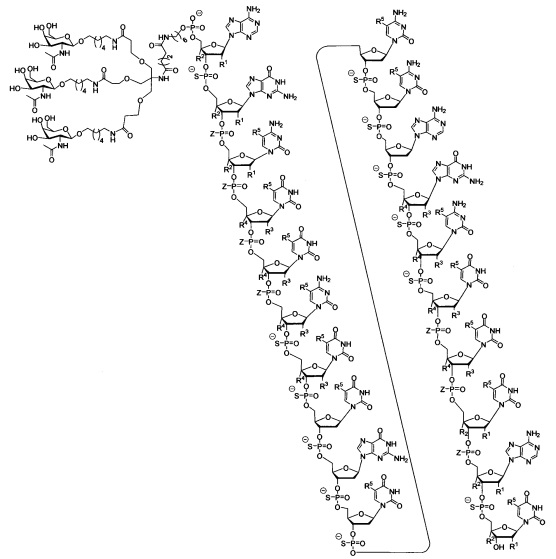

Комментарии