Применение золедроновой кислоты, ее солей, гидратов и способ антиноцицептивного или антиаллодинического лечения боли, способ лечения невропатической боли - RU2325913C2
Код документа: RU2325913C2
Описание
Настоящее изобретение относится к фармацевтическим композициям и их применению, в частности, к содержащим бисфосфонаты фармацевтическим композициям и новым терапевтическим применениям бисфосфонатов.
Бисфосфонаты широко используются для ингибирования активности остеокластов при различных как доброкачественных, так и злокачественных заболеваниях, связанных с избыточной или нарушенной резорбцией костной ткани. Эти пирофосфатные аналоги позволяют не только уменьшать количество случаев нарушения скелета, но также улучшают клиническое состояние пациентов и повышают их выживаемость. Бисфосфонаты обладают способностью предупреждать резорбцию костной ткани in vivo; доказана терапевтическая эффективность бисфосфонатов при лечении остеопороза, нарушения остеогенеза, болезни Педжета, индуцированной опухолью гиперкальциемии (ОИГ), а в последние годы также метастазов в костную ткань (КМ) и множественной миеломы (ММ) (см. обзор Fleisch H. Bisphosphonates clinical (1997) в: Bisphosphonates in Bone Disease. From the Laboratory to the Patient, изд-во The Parthenon Publishing Group, New York/London cc. 68-163). Механизмы, посредством которых бисфосфонаты ингибируют резорбцию костной ткани, пока не полностью выяснены, и они, вероятно, варьируются в зависимости от конкретных бисфосфонатов. Установлено, что бисфосфонаты обладают высоким сродством к связыванию с гидроксиапатитными кристаллами костной ткани, способностью снижать обновление и резорбцию костной ткани, снижать уровни гидроксипролина или щелочных фосфатаз в крови и, кроме того, ингибировать образование, рекруитмент, активацию и активность остеокластов. В настоящее время установлено, что фарнесилдифосфатсинтаза, фермент мевалонатного пути биосинтеза холестерина, является молекулярной мишенью азотсодерджащихбисфосфонатов (см. обзор Rogers MJ, Gordon S, Benford HL, Coxon FP, Luckman SP, Monkkonen J, Frith JC. Cellular and molecular mechanisms of action ofbisphosphonates Cancer 88 (прилож.):2961-2978 (2000)).
Костная боль, являющаяся результатом структурного повреждения, периостеального раздражения и ущемления нерва, представляет собой наиболее часто встречающееся осложнение как доброкачественного, так и метастатического заболевания костной ткани и является серьезной проблемой как в клинической практике, так и в целом для населения. (Coleman, 1997, Cancer 80; 1588-1594).
MM представляет собой злокачественное плазмоцитарное заболевание, отличающееся пролиферацией и накоплением злокачественных плазматических клеток в костном мозге. Ее основными клиническими следствиями являются литические поражения кости, связанные с патологическими переломами, и боль костной ткани. Эти поражения являются результатом избыточной резорбции костной ткани, часто приводящей к гиперкальциемии. Бисфосфонаты были включены в систему продолжительного лечения ММ в сочетании с общепринятой химиотерапией. В настоящее время установлено, что применение бисфосфонатов, таких как клодронат и памидронат, может снижать количество случаев нарушения скелета, таких как литические поражения костной ткани и патологические переломы, и может облегчать связанную с этими состояниями костную боль и улучшать качество жизни пациентов (Laktinen и др., Lancet 1992, 340, 1049-1052; McCloskey и др., B.J.Haematol., 1998, 100, 317-325; и Berenson и др. N. Eng. J. Med. 1996, т.334, No.8, 488-493). Аналогичные действия выявлены при лечении бисфосфонатами пациентов, страдающих раком молочной железы. При создании настоящего изобретения в опытах in vivo на моделях с использованием животных неожиданно было установлено, что определенные бисфосфонаты обладают выраженными и четко направленными ослабляющими боль (паллиативными) действиями. Например, было установлено, что золендроновая кислота приводит к реверсии вызванной механическим стимулом гипералгезии и невропатической боли на моделях хронического воспаления у крыс, проявляя быстрое действие с эффективностью, близкой к 100%. Кроме того, при исследовании на моделях связанной с раком боли костной ткани у крыс установлено, что золедроновая кислота снижает вызванную механическим стимулом аллодинию и снижает отдергивание (защитная реакция) задних конечностей. Эти результаты свидетельствуют о том, что золедроновая кислота и родственные бисфосфонаты могут оказывать непосредственное быстрое действие, обладают антиноцицептивным и антиаллодиническим воздействием на боль.
В настоящем изобретении предложен способ лечения боли у пациента, который нуждается в таком лечении, заключающийся во введении пациенту эффективного количества бисфосфоната.
Изобретение относится также к применению бисфосфоната для приготовления лекарственного средства, предназначенного для лечения боли.
Изобретение относится также к применению бисфосфоната для лечения у млекопитающих боли, связанной с заболеваниями или патологическими состояниями.
Настоящее изобретение, в частности, можно применять для паллиативного лечения боли, т.е. непосредственного ослабления боли в сочетании с ослаблением боли в результате облегчения обусловливающего ее заболевания или медицинского состояния. Таким образом, объектами изобретения являются способы и их применение для непосредственного аналгезирующего или экстренного лечения боли.
Предпочтительно изобретение применяют для непосредственного лечения боли при заболеваниях и медицинских состояниях, при которых показано применение бисфосфонатов для ингибирования активности остеокластов. Например, изобретение можно применять для непосредственного лечения боли при заболеваниях и состояниях, включающих избыточную или неадекватную потерю костной ткани, например, в результате нарушенной активности остеокластов. Примеры таких заболеваний и состояний включают доброкачественные заболевания и состояния, такие как остеопороз различного происхождения, болезнь Педжета, остеоартрит, ревматоидный артрит (РА), болезнь периодонта; и прежде всего злокачественные заболевания, такие как ММ, ОИГ и КМ, связанные с различными типами рака, например раком молочной железы, предстательной железы, легкого, почки, яичника или остеосаркомой. В целом изобретение можно применять для лечения боли в других ситуациях, когда показано применение бисфосфонатов, и которые сопровождаются болью, например, когда бисфосфонаты применяют для заживления переломов кости, остеонекрозе или для лечения боли, связанной с неплотным прилеганием протезов.
Пути применения и способы по настоящему изобретению улучшают существующие методы лечения злокачественных заболеваний, при которых бисфосфонаты используют для предупреждения или ингибирования развития метастазов в костную ткань или избыточной резорбции костной ткани, а также методы лечения воспалительных заболеваний, таких как ревматоидный артрит и остеоартрит, а также всех форм остеопороза и нарушения остеогенеза.
Таким образом, в контексте настоящего описания понятия «лечение» или «лечить» относится как к профилактическому или превентивному лечению, так и к исцеляющему или паллиативному лечению боли, в частности к антиноцицептивному и антиаллодиническому лечению боли, прежде всего лечению костной боли.
Таким образом, конкретными вариантами осуществления изобретения являются:
- способ лечения костной боли у пациента, нуждающегося в таком лечении, заключающийся в том, что пациенту вводят эффективное количество бисфосфоната;
- применение бисфосфоната для приготовления лекарственного средства, предназначенного для лечения боли; или
- применение бисфосфоната в качестве агента для лечения костной боли.
Применяемые согласно настоящему изобретению бисфосфонаты, как правило, представляют собой бисфосфонаты, которые облегчают боль, в частности, обладающие антиноцицептивным или антиаллодиническим действием, и предпочтительно быстро проявляют начальную активность в отношении боли.
Так, например, приемлемые бисфосфонаты, которые можно применять согласно изобретению, включают следующие соединения или их фармацевтически приемлемые соли или любые гидраты: 3-амино-1-гидроксипропан-1,1-дифосфоновая кислота (памидроновая кислота), например памидронат (APD); 3-(N,N-димеламино)-1-гидроксипропан-1,1-дифосфоновая кислота, например диметил-APD; 4-амино-1-гидроксибутан-1,1-дифосфоновая кислота (алендроновая кислота), например алендронат; 1-гидроксиэтиденбисфосфоновая кислота, например этидронат; 1-гидрокси-3-(метилпентиламино)пропилиденбисфосфоновая кислота, ибандроновая кислота, например ибандронат; 6-амино-1-гидроксигексан-1,1-дифосфоновая кислота, например аминогексил-ВР; 3-(N-метил-N-н-пентиламино)-1 -гидроксипропан-1,1-дифосфоновая кислота, например метилпентил-APD (= ВМ 21.0955); 1-гидрокси-2-(имидазол-1-ил)этан-1,1-дифосфоновая кислота, например золедроновая кислота; 1-гидрокси-2-(3-пиридил)этан-1,1-дифосфоновая кислота (ризедроновая кислота), например ризедронат, включая ее N-метилпиридиниевые соли, например йодиды N-метилпиридиния, такие как NE-10244 или NE-10446; 1-(4-хлорфенилтио)метан-1,1-дифосфоновая кислота (тилудроновая кислота), например тилудронат; 3-[N-(2-фенилтиоэтил)-N-метиламино]-1-гидроксипропан-1,1-дифосфоновая кислота; 1-гидрокси-3-(пирролидин-1-ил)пропан-1,1-дифосфоновая кислота, например ЕВ 1053 (фирма Leo); 1-(N-фениламинотиокарбонил)метан-1,1-дифосфоновая кислота, например FR 78844 (фирма Fujisawa); тетраэтиловый эфир 5-бензоил-3,4-дигидро-2Н-пиразол-3,3-дифосфоновой кислоты, например U-81581 (фирма Upjohn); 1-гидрокси-2-(имидазо[1,2-а]пиридин-3-ил)этан-1,1-дифосфоновая кислота, например YM 529; и 1,1-дихлорметан-1,1-дифосфоновая кислота (клодроновая кислота), например клодронат.
Предпочтительно применяемые согласно изобретению бисфосфонаты представляют собой азотсодержащие бисфосфонаты. В контексте настоящего описания азотсодержащий бисфосфонат представляет собой соединение, которое помимо характерного сдвоенного бисфосфататного (Р-С-Р) фрагмента несет содержащую азот боковую цепь, например соединение формулы I
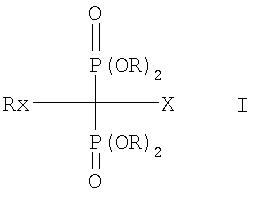
где
Х обозначает водород, гидроксил, амино, алканоил или аминогруппу, замещенную С1-С4алкилом или алканоилом;
R обозначает водород или С1-С4алкил и
Rx обозначает боковую цепь, которая содержит необязательно замещенную аминогруппу или азотсодержащий гетероцикл (включая ароматические азотсодержащие гетероциклы), и его фармацевтически приемлемые соли или любые гидраты.
Особенно предпочтительными азотсодержащими бисфосфонатами являются бисфосфонаты, которые имеют боковые цепи, несущие азотсодержащие гетероциклы, наиболее предочтительно несущие ароматические азотсодержащие гетероциклы.
Так, согласно одному из вариантов осуществления изобретения особенно предпочтительный для применения согласно изобретению бисфосфонат представляет собой соединение формулы I'

где
Het обозначает имидазол, оксазол, изоксазол, оксадиазол, тиазол, тиадиазол, пиридин, 1,2,3-триазол, 1,2,4-триазол или бензимидазол, необязательно замещенные алкилом, алкоксигруппой, галогеном, гидроксилом, карбоксилом, аминогруппой, необязательно замещенной алкильными или алканоильными радикалами, или бензил, необязательно замещенный алкилом, нитро-, аминогруппой или аминоалкилом;
А обозначает насыщенный или ненасыщенный углеводородный фрагмент с прямой или разветвленной цепью, содержащий от 1 до 8 атомов углерода;
Х обозначает атом водорода, необязательно замещенный алканоилом, или аминогруппу, необязательно замещенную алкильными или алканоильными радикалами, и
R обозначает атом водорода или C1-C4 алкил,
и его фармакологически приемлемые соли.
Согласно следующему варианту осуществления изобретения особенно предпочтительный для применения согласно изобретению бисфосфонат представляет собой соединение формулы II

где
Het' обозначает замещенное или незамещенное гетероароматическое 5-членное кольцо, выбранное из ряда, включающего имидазолил, имидазолинил, изоксазолил, оксазолил, оксазолинил, тиазолил, тиазолинил, триазолил, оксадиазолил и тиадиазолил, причем кольцо может быть частично гидрировано, и где заместители выбирают по меньшей мере из одного представителя ряда, включающего С1-С4алкил, С1-С4алкокси, фенил, циклогексил, циклогексилметил, галоген и амино, и где два соседних алкильных заместителя Het могут вместе образовывать второе кольцо;
Y обозначает водород или С1-С4алкил;
X" обозначает водород, гидроксил, амино- или аминогруппу, замещенную C1-С4алкилом, и
R обозначает водород или С1-С4алкил;
а также его фармакологически приемлемые соли и изомеры.
И согласно еще одному из вариантов осуществления изобретения особенно предпочтительный для применения согласно изобретению бисфосфонат представляет собой соединение формулы III
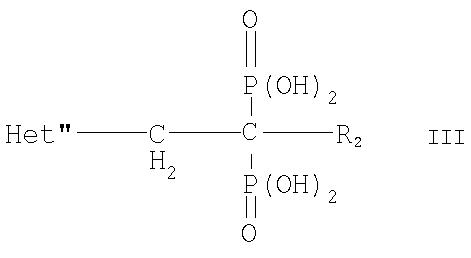
где
Het" обозначает имидазолил, 2Н-1,2,3-, 1H-1,2,4- или 4Н-1,2,4-триазолил, тетразолил, оксазолил, изоксазолил, оксадиазолил, тиазолил или тиадиазолил, незамещенные или С-моно- или дизамещенные (низш.)алкилом, (низш.)алкоксигруппой, фенилом, который в свою очередь может быть моно- или дизамещен (низш.)алкилом, (низш.)алкоксигруппой и/или галогеном, гидроксигруппой, ди(низш.)алкиламиногруппой, (низш.)алкилтиогруппой и/или галогеном, и N-замещенные на замещаемом атоме N (низш.)алкилом или фенил(низш.)алкилом, который в свою очередь может быть моно- или дизамещен в фенильном фрагменте (низш.)алкилом, (низш.)алкоксигруппой и/или галогеном, и
R2 обозначает водород, гидрокси, амино, (низш.)алкилтио или галоген, где (низш.)радикалы имеют до 7 включительно атомов углерода,
или его фармакологически приемлемые соли.
Примерами особенно предпочтительных для применения согласно изобретению бисфосфонатов являются:
2-(1-метилимидазол-2-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота,
2-(1-бензилимидазол-2-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота,
2-(1-метилимидазол-4-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота,
1-амино-2-(1-метилимидазол-4-ил)этан-1,1-дифосфоновая кислота,
1-амино-2-(1-бензилимидазол-4-ил)этан-1, 1-дифосфоновая кислота,
2-(1-метилимидазол-2-ил)этан-1,1-дифосфоновая кислота,
2-(1-бензилимидазол-2-ил)этан-1,1-дифосфоновая кислота;
2-(имидазол-1-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота;
2-(имидазол-1-ил)этан-1,1-дифосфоновая кислота;
2-(4Н-1,2,4-триазол-4-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота;
2-(тиазол-2-ил)этан-1,1-дифосфоновая кислота;
2-(имидазол-2-ил)этан-1,1-дифосфоновая кислота;
2-(2-метилимидазол-4(5)-ил)этан-1,1-дифосфоновая кислота;
2-(2-фенилимидазол-4(5)-ил)этан-1,1-дифосфоновая кислота;
2-(4,5-диметилимидазол-1-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота, и
2-(2-метилимидазол-4(5)-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота, и их фармакологически приемлемые соли.
Наиболее предпочтительным для применения согласно изобретению бисфосфонатом является 2-(имидазол-1-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота (золедроновая кислота) или ее фармакологически приемлемая соль или любой гидрат.
Фармакологически приемлемые соли предпочтительно представляют собой соли присоединения оснований, как правило, соли металлов из групп Ia, Ib, IIa и IIb Периодической таблицы элементов, включая соли щелочных металлов, например калийные и предпочтительно натриевые соли, или соли щелочноземельных металлов, предпочтительно кальциевые или магниевые соли, а также аммонийные соли, полученные с помощью аммиака или органических аминов.
Особенно предпочтительными фармацевтически приемлемыми солями являются соли, в которых 1, 2, 3 или 4, в частности, 1 или 2 кислотных атома водорода бисфосфоновой кислоты заменены фармацевтически приемлемым катионом, в частности, натрием, калием или аммонием, прежде всего натрием. Наиболее предпочтительная группа фармацевтически приемлемых солей отличается наличием одного кислотного атома водорода и одного фармацевтически приемлемого катиона, прежде всего натрия, в каждом фрагменте фосфоновой кислоты.
Все указанные выше производные бисфосфоновой кислоты хорошо известны из литературы. В том числе известно их получение (см., например, ЕР-А-513760, с.13-48). Например, 3-амино-1-гидроксипропан-1,1-дифосфоновую кислоту получают согласно методу, описанному, например, в патенте US 3962432, ее динатриевую соль получают согласно методу, описанному в патентах US 4639338 и 4711880, а 1-гидрокси-2-(имидазол-1-ил)этан-1,1-дифосфоновую кислоту получают согласно методу, описанному, например, в патенте US 4939130 (см. также патенты US 4777163 и 4687767).
Бисфосфонаты (обозначенные далее как агенты по изобретению) можно применять в форме изомера или при необходимости в форме смеси изомеров, как правило, оптических изомеров, таких как энантиомеры или диастереоизомеры, или геометрических изомеров, как правило, цис-транс-изомеров. Оптические изомеры получают в форме чистых антиподов и/или рацематов.
Агенты по изобретению можно также применять в форме их гидратов или других сольватов, содержащих растворители, которые применяют для их кристаллизации.
Агенты по изобретению (бисфосфонаты) предпочтительно применяют в форме фармацевтических композиций, которые содержат терапевтически эффективное количество действующего вещества, необязательно в сочетании или в смеси в неорганическими или органическими, твердыми или жидкими фармацевтически приемлемыми носителями, которые можно применять для введения.
Фармацевтические композиции могут представлять собой, например, композиции для энтерального, например перорального, ректального введения, введения путем распыления аэрозоля или назального введения, композиции для парентерального, например внутривенного или подкожного введения, или композиции для трансдермального введения (например, пассивного или ионофоретического введения).
Предпочтительно фармацевтические композиции адаптируют для перорального или парентерального введения (прежде всего внутривенного, внутриартериального или трансдермального). Наиболее важным является внутривенное и пероральное, но прежде всего и наиболее предпочтительно внутривенное введение. Предпочтительно действующее вещество в виде бисфосфоната находится в форме для парентерального, наиболее предпочтительно в форме для внутривенного введения.
Конкретный путь введения и дозу может выбирать лечащий врач с учетом особенностей пациента, прежде всего возраста, веса, стиля жизни, уровня активности, гормонального статуса (например, постменопаузальный) и при необходимости плотности минерального вещества костной ткани. Однако наиболее предпочтительно бисфосфонат вводят внутривенно.
Доза агента по изобретению может зависеть от различных факторов, таких как эффективность и продолжительность действия действующего вещества, путь введения, виды теплокровных животных и/или пол, возраст, вес и индивидуальное состояние теплокровного животного.
Как правило, представляющее собой действующее вещество бисфосфонат водят теплокровному животному весом примерно 75 кг в виде однократной дозы, составляющей 0,002-20,0 мг/кг, предпочтительно 0,01-10,0 мг/кг. При необходимости эту дозу можно также вводить в виде нескольких, необязательно одинаковых разделенных доз.
Понятие «мг/кг» обозначает количество мг лекарственного средства на кг веса тела млекопитающего, включая человека, которое нуждается в лечении.
Ведение указанной выше дозы либо в виде однократной дозы (что предпочтительно), либо в виде нескольких разделенных доз, можно повторять, например, один раз в день, один раз в неделю, один раз в месяц или каждые три месяца, каждые шесть месяцев или один раз в год. Другими словами, фармацевтические композиции можно использовать в режимах от продолжительной ежесуточной терапии до прерывистой циклической терапии.
Предпочтительно бисфосфонаты вводят в дозах, которые имеют такой же уровень, что и дозы, применяемые для лечения заболеваний, классическими средствами лечения которых являются производные бисфосфоновой кислоты, такие как болезнь Педжета, индуцируемая опухолью гиперкальциемия или остеопороз. Другими словами, предпочтительно производные бисфосфоновой кислоты вводят в дозах, которые являются также терапевтически эффективными дозами для лечения болезни Педжета, индуцируемой опухолью гиперкальциемии или остеопороза, т е. их предпочтительно вводят в дозах, которые должны эффективно ингибировать резорбцию костной ткани. Например, предпочтительные азотсодержащие бисфосфонаты, например золедроновую кислоту и ее соли, используя дозы бисфосфоната от примерно 0,5 до примерно 20 мг, предпочтительно от примерно 1 до примерно 10 мг, можно применять для лечения человека.
Композиции в виде однократных стандартных доз предпочтительно содержат от примерно 1 до примерно 90%, а композиции в формах, отличных от однократных стандартных доз, содержат предпочтительно от примерно 0,1 до примерно 20% действующего вещества. Однократные стандартные дозируемые формы, такие как капсулы, таблетки или драже, содержат, например, от примерно 1 до примерно 500 мг действующего вещества.
Фармацевтические композиции для энтерального и парентерального введения представляют собой, например, стандартные дозы, например, в форме драже, таблеток или капсул, а также ампул. Их получают хорошо известным методом, например с помощью общепринятых методов смешении, грануляции, конфекции, растворения или лиофилизации.
Например, фармацевтические композиции для перорального введения можно получать объединением действующего вещества с твердыми носителями, при необходимости грануляцией полученной смеси и обработки смеси или гранул, если это желательно или необходимо, после добавления приемлемых вспомогательных веществ с получением таблеток или ядер драже.
Приемлемыми носителями являются, прежде всего, носители, такие как сахара, например лактоза, сахароза, маннит или сорбит, препараты целлюлоза и/или фосфатов кальция, например трикальций фосфат или вторичный кислый фосфат кальция, а также связующие вещества, такие как крахмальные пасты, например, на основе кукурузного, пшеничного, рисового или картофельного крахмала, желатин, трагакант, метилцеллюлоза и/или поливинилпирролидон, и при необходимости разрыхлители, такие как вышеуказанные крахмалы, а также карбоксиметилкрахмал, сшитый поливинилпирролидон, агар, альгиновая кислота или ее соль, например альгинат натрия. Вспомогательные вещества, прежде всего, представляют собой регулирующие текучесть агенты и замасливатели, такие как кремнеевая кислота, тальк, стеариновая кислота или ее соли, например стеарат магния или кальция, и/или полиэтиленгликоль. На ядра драже можно наносить приемлемые покрытия, которые могут обладать устойчивостью к желудочным сокам, для этого среди прочего можно использовать концентрированные сахарные растворы, которые необязательно содержат гуммиарабик, тальк, поливинилпирролидон, полиэтиленгликоль и/или диоксид титана, или растворы лака в пригодных органических растворителях или смесях растворителей, или для получения покрытия, устойчивого к желудочным сокам, растворы приемлемых препаратов целлюлозы, таких как фталат ацетилцеллюлозы или фталат гидроксипропилметилцеллюлозы. В таблетки или покрытие драже можно добавлять красители или пигменты, например, с целью идентификации или для обозначения различных доз действующего вещества.
Другие применяемые для перорального введения фармацевтические композиции представляют собой заполненные сухим веществом капсулы из желатина, а также мягкие запечатываемые капсулы из желатина и пластификатора, такого как глицерин или сорбит. Заполненные сухим веществом капсулы могут содержать действующее вещество в форме гранул, например, в смеси с наполнителями, такими как лактоза, связующими веществами, такими как крахмалы, и/или способствующими скольжению веществами, такими как стеарат магния, и при необходимости со стабилизаторами. В мягких капсулах действующее вещество предпочтительно растворяют или суспендируют в приемлемых жидкостях, таких как жирные масла, вазелиновое масло или жидкие полиэтиленгликоли, также можно добавлять стабилизаторы.
Композиции для парентерального введения представляют собой, прежде всего, инъецируемые жидкости, которые являются эффективными при различных путях введения, например внутриартериально, внутримышечно, внутрибрюшинно, интраназально, внутрикожно, подкожно или предпочтительно внутривенно. Такие жидкости предпочтительно представляют собой изотонические водные растворы или суспензии, которые можно готовить перед применением, например, из лиофилизированных препаратов, которые содержат действующее вещество индивидуально или в сочетании с фармацевтически приемлемым носителем. Фармацевтические композиции могут быть стерильными и/или могут содержать вспомогательные вещества, например консерванты, стабилизаторы, смачивающие вещества и/или эмульгаторы, солюбилизаторы, соли для регулирования осмотического давления и/или буферы.
Приемлемые композиции для трансдермального нанесения включают эффективное количество действующего вещества в сочетании с носителем. Предпочтительными носителями являются абсорбируемые фармакологически приемлемые растворители, способствующие проникновению через кожу хозяина.
Как правило, трансдермальные устройства имеют форму повязки, содержащей мембранную подложку, резервуар, содержащий соединение необязательно в сочетании с носителями, необязательно контролирующий скорость барьер для поступления действующего вещества на кожу хозяина с контролируемой и предварительно установленной скоростью в течение длительного периода времени, и приспособления для прикрепления устройства к коже.
Ниже изобретение проиллюстрировано на примерах. В приведенных ниже примерах под понятием «действующее вещество» следует понимать любое указанное выше производное бисфосфоновой кислоты, которое можно применять согласно настоящему изобретению.
Примеры
Пример 1: Капсулы, содержащие действующее вещество, например пентагидрат динатрийпамидроната, в виде пилюль с покрытием:
Смесь, содержащую динатрийпамидронат и Avicel® PH 105, увлажняют водой и разминают, экструдируют и формуют с получением сфер. Затем на высушенные пилюли в псевдоожиженном слое последовательно наносят сначала внутренне покрытие, состоящее из целлюлозы НР-М 603, полиэтиленгликоля (ПЭГ) 8000 и талька, а затем водное устойчивое к желудочным сокам покрытие, содержащее Eudragit L 30 D, триэтилцитрат и Antifbam® AF. Пилюли с покрытием опудривают тальком и заполняют ими капсулы (размер капсулы 0) с помощью поступающей в продажу машины для заполнения капсул, например, фирмы Hofliger и Karg.
Пример 2: Монолитная адгезивная трансдермальная система, содержащая в качестве действующего вещества, например, 1-гидрокси-2-(имидазол-1-ил)этан-1,1-дифосфорную кислоту:
Приготовление:
Вышеперечисленные компоненты растворяют вместе в 150 г петролейной фракции 100-125 с определенной температурой кипения на роликовом настиле. Раствор наносят на полиэфирную пленку (тип Hostaphan, фирма Kalle) с помощью распределительного устройства с использованием ракеля размером 300 мм, получая покрытие с плотностью приблизительно 75 г/м2. После сушки (15 мин при 60°С), накладывают обработанную силиконом пленку (толщиной 75 мм, фирма Laufenberg) в качестве отделяемой пленки. Конечные системы штампуют с использованием пуансона требуемой формы размером от 5 до 30 см2. Конечные системы запечатывают по отдельности в саше из фольгированной бумаги.
Пример 3: Пузырек, содержащий 1,0 мг сухого лиофилизированного 1-гидрокси-2-(имидазол-1-ил)этан-1,1-дифосфоновой кислоты (ее смешанные натриевые соли). После разбавления 1 мл воды получают раствор (концентрация 1 мг/мл) для внутривенной (i.v.) инфузии.
Состав:
В 1 мл воды действующее вещество титруют с тринатрийцитратом × 2 Н2О до получения значения рН 6,0. Затем добавляют маннит и раствор лиофилизуют и лиофилизатом заполняют пузырек.
Пример 4: Ампула, содержащая растворенное в воде действующее вещество, например пентагидрат динатрийпамидроната. После разбавления получают раствор (концентрация 3 мг/мл) для i.v. инфузии.
Состав:
Пример 5: Эффективность бисфосфонатов при использовании моделей воспаления и невропатической боли у крыс
Методы
Воспалительная гипералгезия
Вызываемую механическим стимулом гипералгезию оценивают с помощью модели связанной с воспалением боли у крыс. Пороговые уровни отдергивания лапы при повышающемся давлении стимула оценивают с помощью методики Рандала-Селлито (Randal-Sellito) с использованием анальгезиметра (фирма Ugo Basile, Милан) у необработанных животных (до опыта) перед инъекцией в подошву левой задней лапы полного адъюванта Фрейнда (FCA). Через 24 ч вновь оценивают пороговые уровни отдергивания лапы (до обработки), а затем через промежуток времени от 10 мин до 6 ч после введения лекарственного средства или носителя. Реверсию гипералгезии в ипсилатеральной лапе рассчитывают с помощью следующего уравнения:
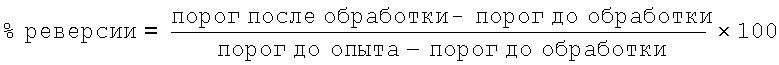
Невропатическая боль
Вызываемую механическим стимулом гипералгезию оценивают с помощью модели невропатической боли у крыс, индуцированной частичной лигатурой левого седалищного нерва. Примерно через 14 дней после хирургического вмешательства пороговые уровни отдергивания как лапы с наложенной лигатурой (ипсилатеральная), так и без лигатуры (контралетаральная) оценивают перед обработкой (до обработки), а затем через промежуток времени от 10 мин до 6 ч после обработки лекарственным средством или носителем. Снижение гипералгезии в каждый момент времени рассчитывают с помощью следующего уравнения:

Все эксперименты осуществляют на группах, состоящих из 6 животных. Маточные растворы лекарственных средств растворяют в дистиллированной воде и для последующих разбавлений используют 0,9%-ный физиологический раствор, осуществляя подкожное введение из расчета 4 мл/кг. Все растворы лекарственных средств приготавливают в пластиковых флаконах и хранят в темноте.
Осуществляют статистический анализ данных о пороговых уровнях отдергивания лап (g), взятых с дублированием, на основе дисперсионного анализа с последующей оценкой с помощью HSD-критерия Тукея (Tukey). Критерием эффективности служит максимальная реверсия гипералгезии при применяемых дозах лекарственного средства.
Результаты
1. На модели воспалительной гипералгезии, индуцированной односторонней инъекции в заднюю лапу полного адъюванта Фрейнда, золедронат (0,003-0,1 мгкг-1 s.c.) вызывал зависящее от дозы снижение вызванной механическим стимулом гипералгезии. Это действие быстро начиналось, максимальный уровень снижения, составляющий 100%, происходил через 30 мин, и было непродолжительным, никакой заметной активности не обнаружено через 3 ч после введения. При использовании наиболее высокой из изученных доз обнаружено некоторое контралатеральное действие.
2. Памидронат (0,03-1 мгкг-1 s.c.) и клодронат (0,3-10 мгкг-1 s.c.) оба оказались неэффективными в отношении снижения вызванной механическим стимулом гипералгезии, однако в наиболее высокой из изученных доз вызывали небольшое снижение пороговых уровней отдергивания лап.
3. На модели хронической невропатической боли, индуцированной односторонней частичной лигатурой седалищного нерва, золедронат (0,003-0,1 мгкг-1 s.c.) вызывал умеренное 40%-ное снижение вызванной механическим стимулом гипералгезии, максимум которого достигался через 30 мин после введения лекарственного средства. Однако при этом при использовании самой высокой из изученных доз также обнаружено существенное снижение пороговых уровней отдергивания контралатеральной лапы.
4. Памидронат (0,03-1 мгкг-1 s.c.) обладал лишь незначительной активностью в опытах на модели невропатической боли, вызывая максимум 20%-ное снижение гипералгезии, а клодронат (0, 3-10 мгкг-1 s.c.) не обладал активностью. И в этом случае оба лекарственных средства вызывали некоторое снижение пороговых уровней отдергивания контралатеральной лапы.
5. Эти данные свидетельствуют о том, что золедронат снижает вызванную механическим стимулом гипералгезию на моделях хронического воспаления и невропатической боли у крыс.
Пример 6: Воздействие бисфосфонатов на связанную с раком костной ткани боль у крыс
Взрослым самкам крыс индуцируют с помощью интратибиальных инъекций клетки карциномы молочной железы линии MRMZ-1 (3 мкл, 107 клеток/мл). У этих животных постепенно развивается вызываемая механическим стимулом гипералгезия, механическая аллодиния (кожная чувствительность к неболезненным стимулам) и отдергивание задней лапы, проявление которых начинается через 12-14 дней после инъекции. Золедроновую кислоту (ZOL) (10 и 30 мкг/кг s.c.) вводят трижды в неделю, начиная с дня инъекции клеток, что приводит к выраженному ингибированию отдергивания задних конечностей и механической аллодинии. По сравнению с контрольными обработанными носителями животными, у которых максимальный уровень отдергивания задних лап происходит через 19 дней, у крыс, обработанных более высокой дозой ZOL, в течение 19 дней после интратибиальной инъекции клеток не развиваются никакие признаки отдергивания задних лап. Однако при использовании однократной инъекции (100 мкг/кг, s.c.) в 19 день не обнаружено острого действия ZOL. В противоположность этому введение морфина (1-10 мг/кг, s.c.) обладает острым зависящем от дозы действием, обусловливающем снижение механической аллодинии, только в наиболее высокой дозе, что также приводит к заметному снижению отдергивания задних лап.
Реферат
Предложенная группа изобретений относится к медицине, к лечению невропатической боли, к антиноцицептивному или антиаллодиническому лечению боли, например, у пациента, страдающего остеопорозом или нарушением остеогенеза, опухолью, воспалительным заболеванием. Группа изобретений касается способов и применения золедроновой кислоты либо ее фармацевтически приемлемых солей или гидратов при приготовлении лекарственного средства для указанного лечения. Изобретение обеспечивает анальгетический эффект при указанных заболеваниях за счет ранее неизвестных антиноцицептивных, антиаллодинических свойств золедроновой кислоты. 3 н. и 14 з.п. ф-лы.

Комментарии