Кристаллические формы тайгециклина и способы их получения - RU2478612C2
Код документа: RU2478612C2
Чертежи





Описание
Настоящая заявка испрашивает приоритет предварительной заявки на патент US 60/684955 от 27 мая 2005 года, содержание которой включено в данное описание посредством ссылки.
[001] Данное изобретение относится к твердой кристаллической форме тайгециклина, составам, его содержащим, и способам его получения.
[002] Тайгециклин является антибиотиком ряда тетрациклинов и химическим аналогом миноциклина. Его можно использовать в качестве лечебного препарата против лекарственно-устойчивых бактерий; показано, что он проявляет эффективность там, где другие антибиотики не оказывают действия. Например, он эффективен против метициллин-устойчивого Staphylococcus aureus, пенициллинорезистентных штаммов пневмококка (Streptococcus pneumonia), ванкомицинрезистентных энтерококков (Enterococci) (DJ. Beidenbach et al., Diagnostic Microbiology and Infectious Disease 40:173-177 (2001); H.W. Boucher et al., Antimicrobial Agents & Chemotherapy 44:2225-2229 (2000); P.A. Bradford Clin. Microbiol. Newslett. 26:163-168 (2004); D. Milatovic et al., Antimicrob. Agents Chemother. 47:400-404 (2003); R. Patel et al., Diagnostic Microbiology and Infectious Disease 38:177-179 (2000); PJ. Petersen et al., Antimicrob. Agents Chemother. 46:2595-2601 (2002); and PJ. Petersen et al., Antimicrob. Agents Chemother. 43:738-744(1999)), а также против организмов, которые являются носителями одной из двух основных форм резистентности к тетрациклинам: эффлюкса и рибосомной защиты (С.Betriu et al., Antimicrob. Agents Chemother. 48:323-325 (2004); Т. Hirata et al. Antimicrob. Agents Chemother. 48:2179-2184 (2004); and PJ. Petersen et al., Antimicrob. Agents Chemother. 43:738-744(1999)).
[003] Исторически тайгециклин применяли внутривенно вследствие его низкой биодоступности при пероральном применении. Раствор для внутривенных инъекций может быть получен при растворении аморфной формы препарата в стерильной воде, в 0.9% растворе хлорида натрия для инъекций, USP, или в 5% растворе декстрозы, USP. Тайгециклин переходит в аморфное состояние при лиофилизации в отсутствие стерилизующих наполнителей. Однако из-за склонности тайгециклина к разложению, порошок препарата получают и используют в условиях низких температур и в атмосфере инертного газа. Такая обработка весьма дорогостоящая, так как требует специального оборудования и особых методов работы. Аморфное состояние, также обычно менее стабильно по сравнению с кристаллической формой того же вещества (Polymorphism in Pharmaceutical Solids, H.G.Brittain (ed.), 1999, p.208). Исходя из этого, было бы желательно найти способ получения и использования твердой кристаллической формы тайгециклина без необходимости применения специальных аппаратов.
[004] Кристаллические соединения представляют собой твердые вещества с упорядоченным расположением молекул, в отличие от аморфных соединений, в которых молекулы расположены хаотично. Эти упорядоченные структуры также называются кристаллическими решетками и в свою очередь состоят из повторяющихся структурных фрагментов, которые называются элементарными ячейками. Явление, при котором одинаковые молекулы, например органические молекулы, могут образовывать вещества, одинаковые по составу, но отличающиеся по структуре, называется полиморфизм. В качестве примера полиморфизма можно привести углерод (для простых элементов это явление называется аллотропизм). Углерод существует в трех твердых кристаллических модификациях: графит, алмаз и фуллерены. Несмотря на то что все эти модификации состоят из углерода, из-за различий в кристаллической решетке они проявляют различные свойства. Например, в то время как алмаз представляет собой одно из самых твердых известных веществ, графит является очень мягким веществом. Многие из органических соединений также проявляют полиморфизм, и их кристаллическая структура зависит от упаковки молекул в кристалле. (См., например, Stephenson, G.A; Stowell, J.G; Toma, P.H; Dorman, D.E.; Greene, J.R.; Byrne, S.R.; "Solid state analysis of polymorphic, isomorphic and solvated forms of Dirithromycin", J.Am.Chem. Soc, 1994, 116, 5766.)
[005] На основе химической структуры, которая показывает взаимосвязь между атомами и строением молекулы, невозможно предсказать, будет ли это вещество кристаллическим, в каких условиях оно будет кристаллизоваться, как много кристаллических форм оно может образовывать и будет ли какая-либо из этих форм относится к твердотельной структуре. Использованный здесь термин «твердотельная структура» означает структуру, полученную в результате совместной упаковки молекул с образованием твердого вещества.
[006] В ряде случаев молекулы растворителей или воды оказываются включенными в кристаллическую решетку твердого кристаллического вещества. Такие твердые кристаллические формы могут рассматриваться как сольваты или гидраты соответственно. Сольваты, гидраты и полиморфные формы часто называются твердыми кристаллическими формами вещества. Сюда, как обычно принято в химии твердого тела, также могут быть включены такие слабосвязанные твердые сольватные и гидратные кристаллические формы, где растворитель или молекулы воды находятся в каналах или не включены в кристаллическую решетку. Аморфную форму также часто относят к твердым формам вещества, но она не является твердой кристаллической формой.
[007] Различные твердые кристаллические формы одного соединения часто обладают различными свойствами, такими как температура плавления, растворимость, стабильность и технологические свойства. Таким образом, различные твердые кристаллические формы одного и того же соединения могут быть идентифицированы, и может быть найден оптимальный набор условий и способов получения одной твердой кристаллической формы также, как и могут быть определены различные свойства каждой из этих твердых кристаллических форм.
[008] В химии твердого тела существует ряд типовых аналитических методов, используемых для анализа твердых форм. Термин "анализ", используемый в настоящем описании, в данном случае означает получение информации о твердотельной структуре твердых форм. Например, порошковая рентгеновская дифрактометрия является хорошим методом для определения, в какой твердой форме, аморфной или кристаллической, находится вещество, а также для определения параметров и идентификации твердой кристаллической формы соединения. Порошковая дифрактометрия также может быть использована для определения содержания твердой кристаллической формы (или форм) в смесях. В порошковой дифрактометрии рентгеновские лучи направляют на кристаллы, а измеряют интенсивность отраженного рентгеновского излучения как функцию двойного угла между источником рентгеновского излучения и пучком рентгеновских лучей, отраженных образцом. Интенсивность отраженного рентгеновского излучения может быть выражена на графике в виде пиков, где координата Х представляет собой двойной угол (известный как угол "2θ") между источником рентгеновского излучения и отраженным рентгеновским излучением, а координата Y представляет собой максимум интенсивности отраженного рентгеновского излучения. Этот график называется моделью рентгеновской дифракции или порошковой дифрактограммой. Различные твердые кристаллические формы дают различные порошковые дифрактограммы, так как положение дифракционных пиков на оси Х определяется твердотельной структурой кристаллов.
[009] Такие порошковые дифрактограммы или их фрагменты могут быть использованы как «отпечатки пальцев» для идентификации твердой кристаллической формы. Так, можно получить порошковую дифрактограмму неизвестного образца и можно сравнить с дифрактограммой известного образца. При их совпадении можно будет с уверенностью утверждать, что первый образец имеет ту же твердую кристаллическую форму, как и образец с известной структурой. Этим методом также можно анализировать образцы, содержащие смеси различных кристаллических форм путем добавления или вычитания порошковых дифрактограмм известных соединений.
[010] Порошковые дифрактограммы могут быть использованы для описания твердой кристаллической формы или при сравнении с известными образцами дифрактограмм для идентификации, так как дифракционные пики одной формы никогда не совпадают с дифракционными пиками других твердых форм.
[011] Термин «описать» или «охарактеризовать», используемый в настоящем описании, в данном случае означает выделение набора данных, позволяющих однозначно отличить одну кристаллическую форму от другой. Таким набором данных в случае порошковой рентгеновской дифрактометрии является положение одного или нескольких пиков. Определение пиков методом порошковой дифрактометрии, характерных для конкретной формы тайгециклина, означает охарактеризовать или описать эту форму.
[012] Использованный здесь термин «идентифицировать» означает определение набора данных, характерных для данной твердой формы, и использование этих данных для определения наличия этой твердой формы в образце. В порошковой рентгеновской дифрактометрии, как уже было сказано выше, этими данными являются положения на оси Х одного или нескольких дифракционных пиков, характеризующих данную форму. Например, определив ряд пиков, характерных для определенной кристаллической формы тайгециклина, их можно использовать для нахождения данной формы в образце, содержащем тайгециклин.
[013] При описании и/или идентификации твердой кристаллической формы одного химического соединения при помощи порошковой дифрактометрии часто нет необходимости использовать порошковую дифрактограмму целиком. Для описания и идентификации часто достаточно небольшой части дифрактограммы. Выделив набор пиков, отличающих одну твердую кристаллическую форму от другой, можно достаточно точно охарактеризовать эту форму и идентифицировать, например, в смеси неизвестного состава. Дополнительно могут быть добавлены данные других аналитических методов или дополнительные пики порошковой дифрактограммы при описании и/или идентификации формы, например, для отождествления полиморфных образцов.
[014] Из-за различий оборудования, образцов и методов значения пиков обычно приводятся с приставкой «примерно». Это обычная практика в химии твердого тела, так как значения пиков могут меняться. Типовая погрешность для значения 2θ единиц на оси Х рентгеновской дифрактограммы составляет порядка плюс-минус 0.2° 2θ. Таким образом, значение пика рентгеновской дифрактограммы при значении угла 2θ «примерно 9.2°» означает, что этот пик находится при значениях угла 2θ в диапазоне 9.0° и 9.4° при измерении на большинстве рентгеновских дифрактометров в большинстве используемых условий измерения. Изменение в положении максимумов интенсивности пиков - результат разной ориентации отдельных кристаллов в держателе образцов по отношению к источнику рентгеновского излучения (явление известное как «преимущественная ориентация»). Эти эффекты не дают информации о структуре кристаллов.
[015] Рентгеновская порошковая дифрактометрия является лишь одним из нескольких аналитических методов, которые могут быть использованы для описания и/или идентификации твердых кристаллических форм. Такие спектроскопические методы как Раман (включая Раман-микроскопию), ИК и твердофазная ЯМР спектроскопии могут быть использованы для количественного определения одного или нескольких видов твердых кристаллических форм в смесях.
[016] Такого физического параметра как температура плавления самого по себе недостаточно для описания и/или идентификации различных твердых кристаллических форм, так как различные формы могут иметь близкие температуры плавления. Однако даже в этом случае температура плавления может использоваться совместно с другими аналитическими методами, такими как рентгеновская порошковая дифракция, для описания и/или идентификации твердой кристаллической формы.
[017] Данное изобретение относится к твердым кристаллическим формам тайгециклина, называемым как Форма I, Форма II, Форма III, Форма IV и Форма V. Изобретение также относится к составам, в том числе фармацевтическим, содержащим одну или несколько твердых кристаллических форм тайгециклина. Кроме того, изобретение относится к способам получения твердых кристаллических форм тайгециклина.
КРАТКОЕ ОПИСАНИЕ ФИГУР
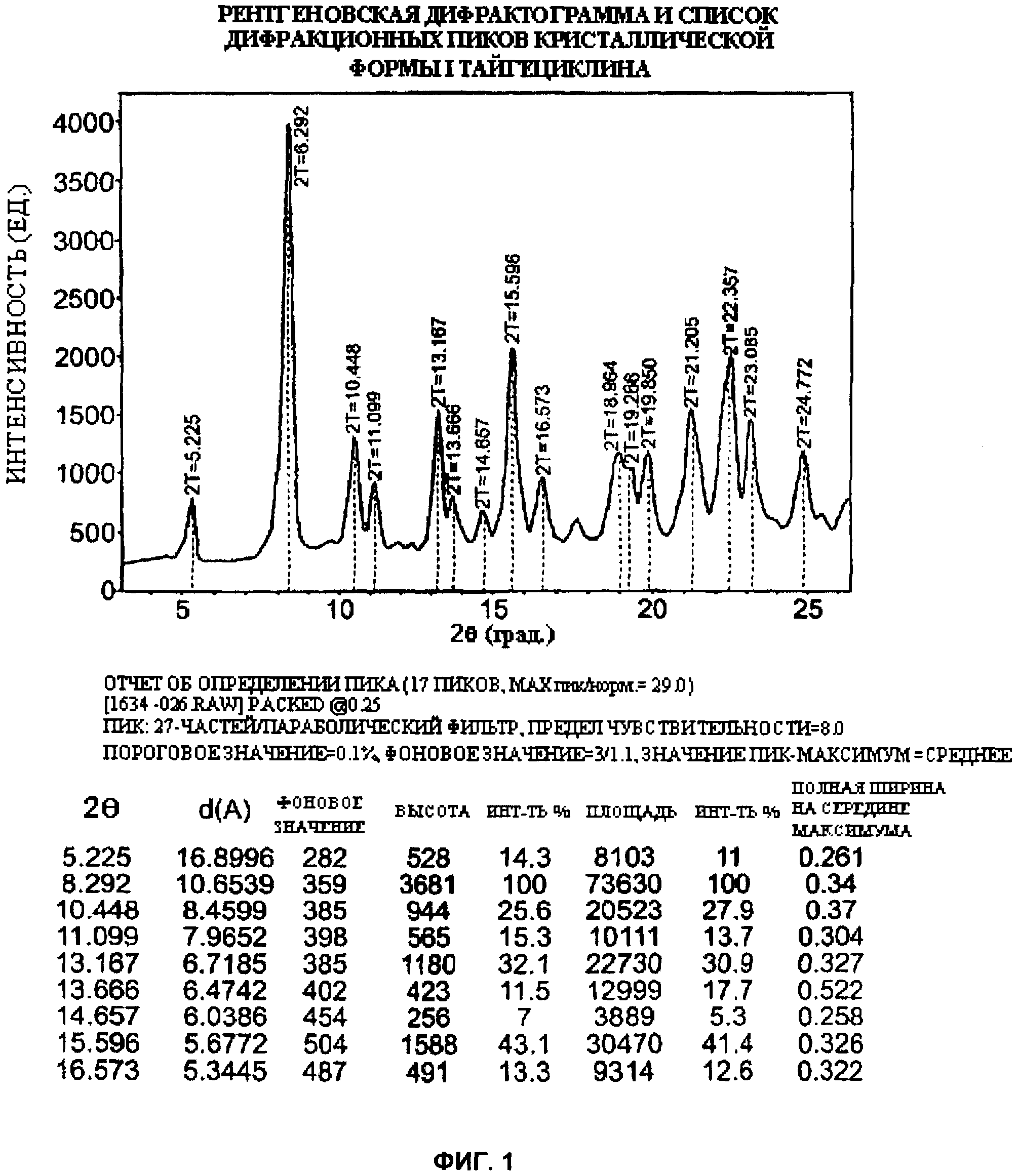
[018] Фиг.1 - рентгеновская дифрактограмма и список дифракционных пиков кристаллической формы I тайгециклина.
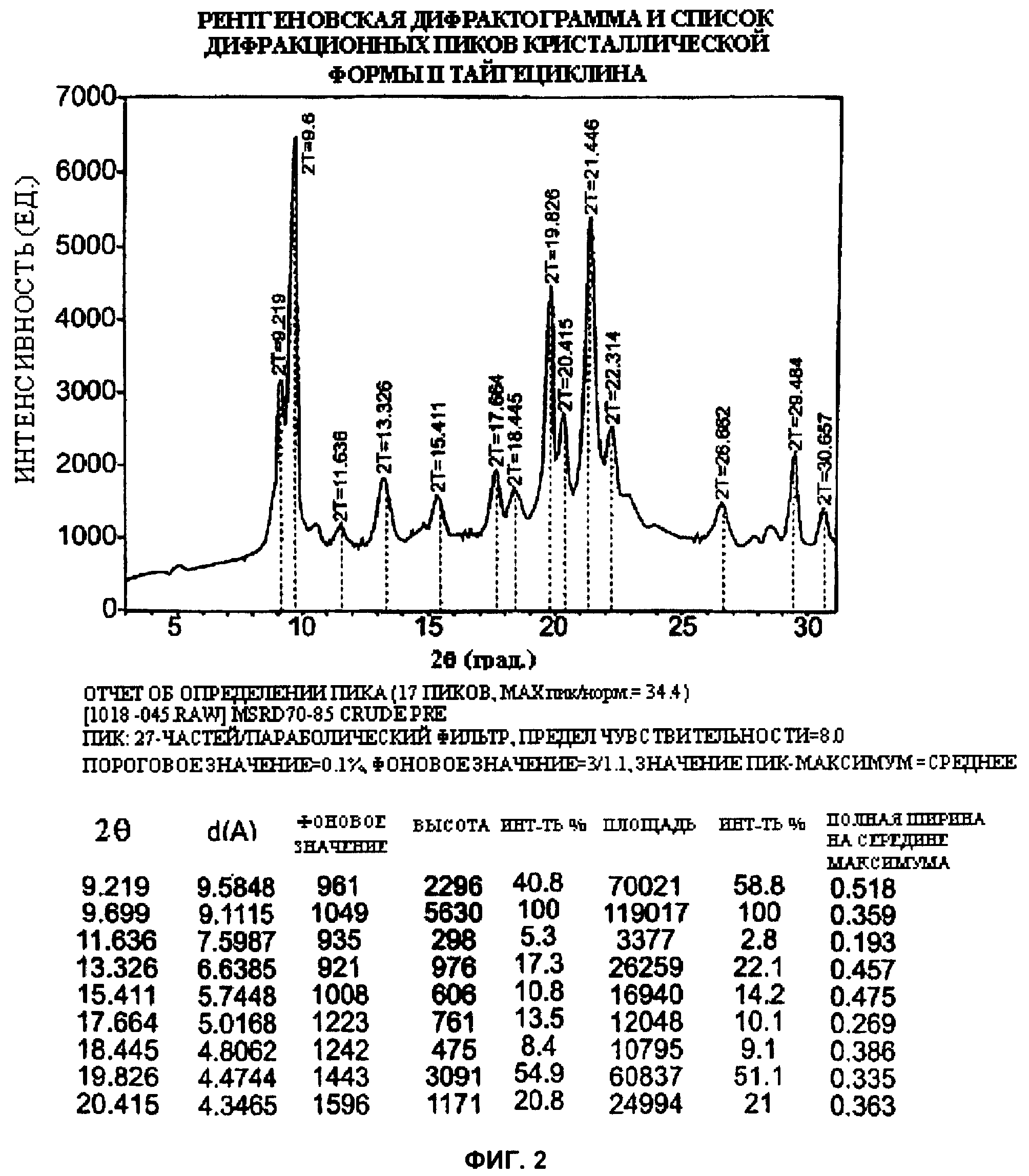
[019] Фиг.2 - рентгеновская дифрактограмма и список дифракционных пиков кристаллической формы II тайгециклина.
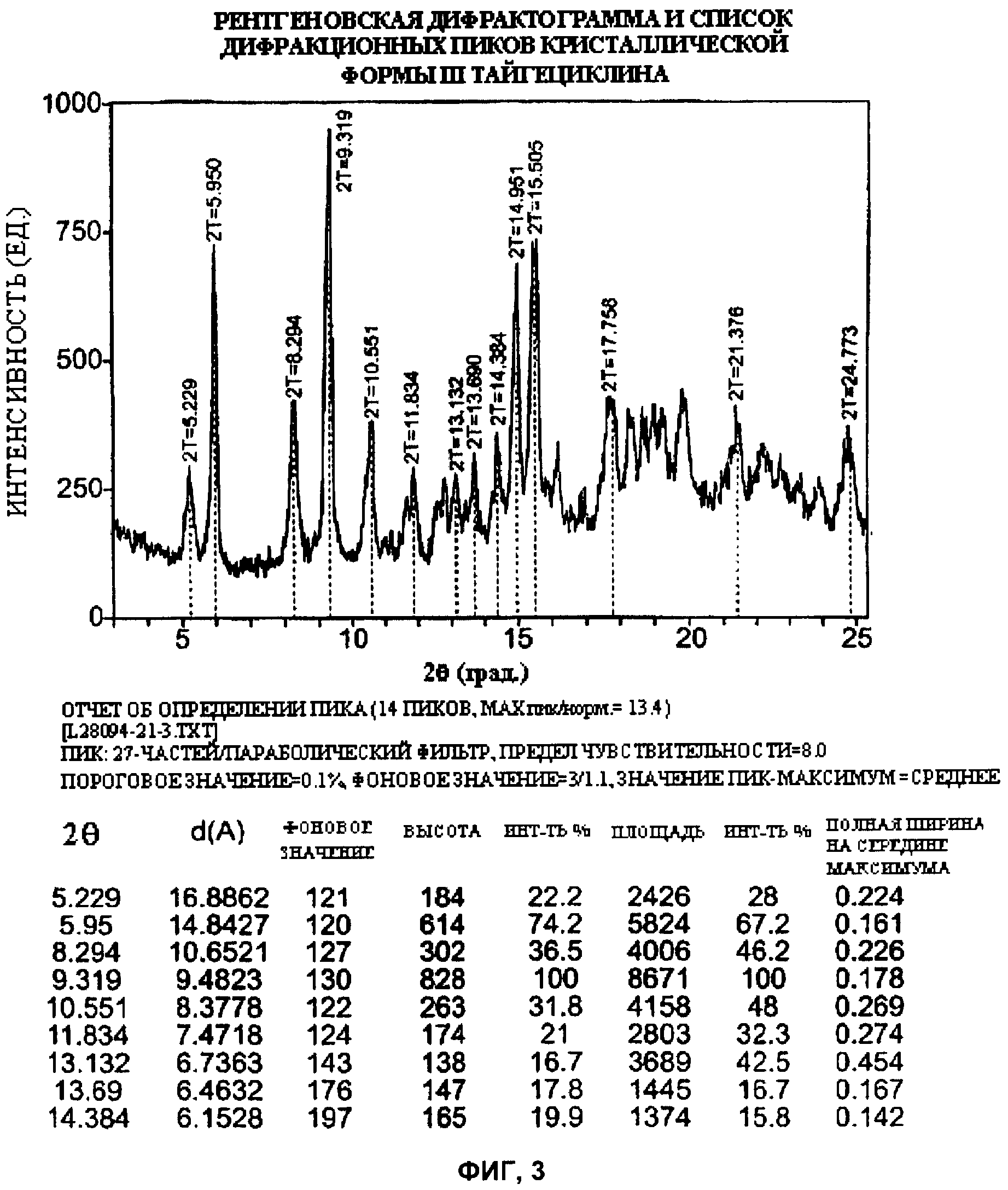
[020] Фиг.3 - рентгеновская дифрактограмма и список дифракционных пиков кристаллической формы III тайгециклина.
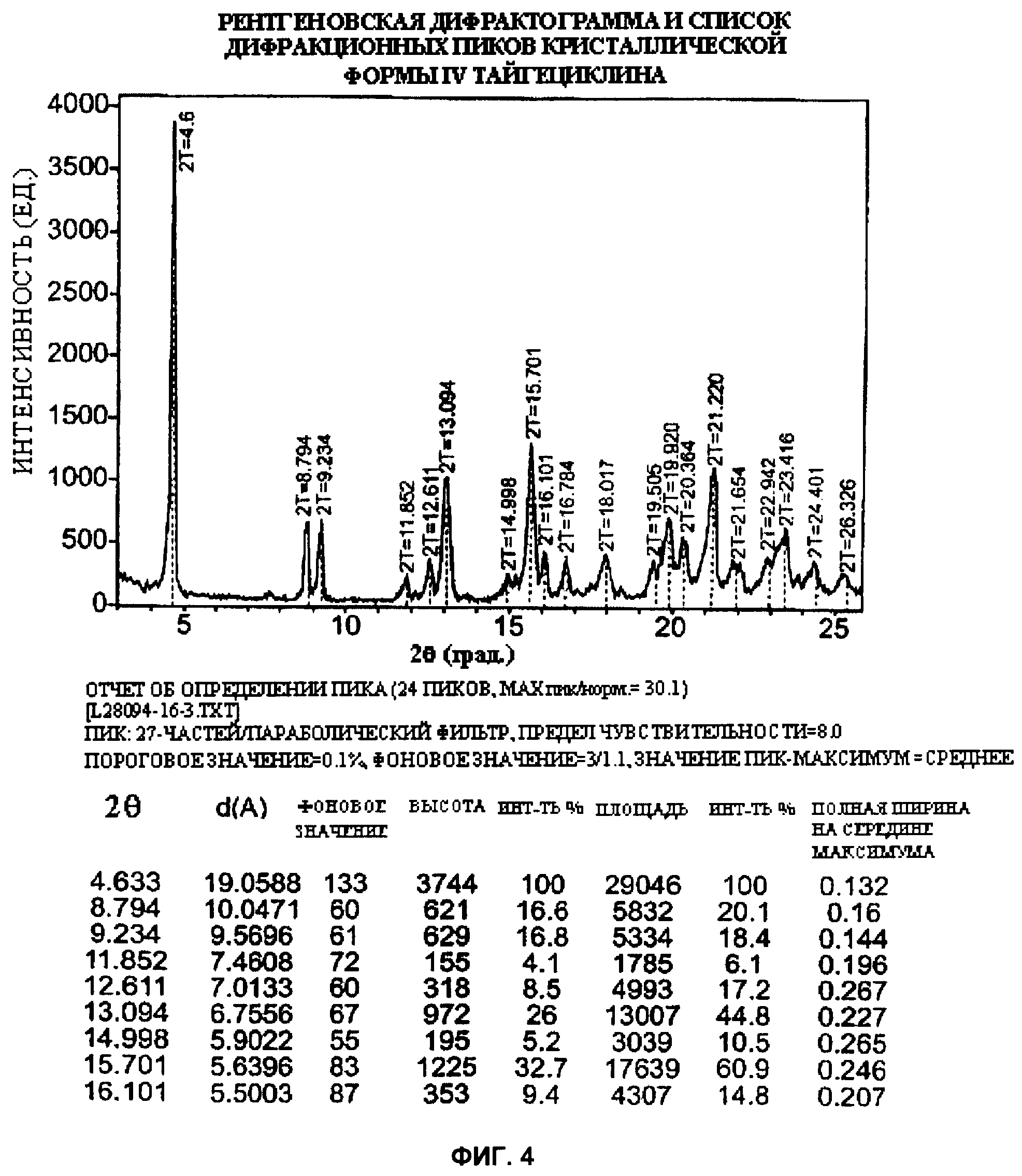
[021] Фиг.4 - рентгеновская дифрактограмма и список дифракционных пиков кристаллической формы IV тайгециклина.
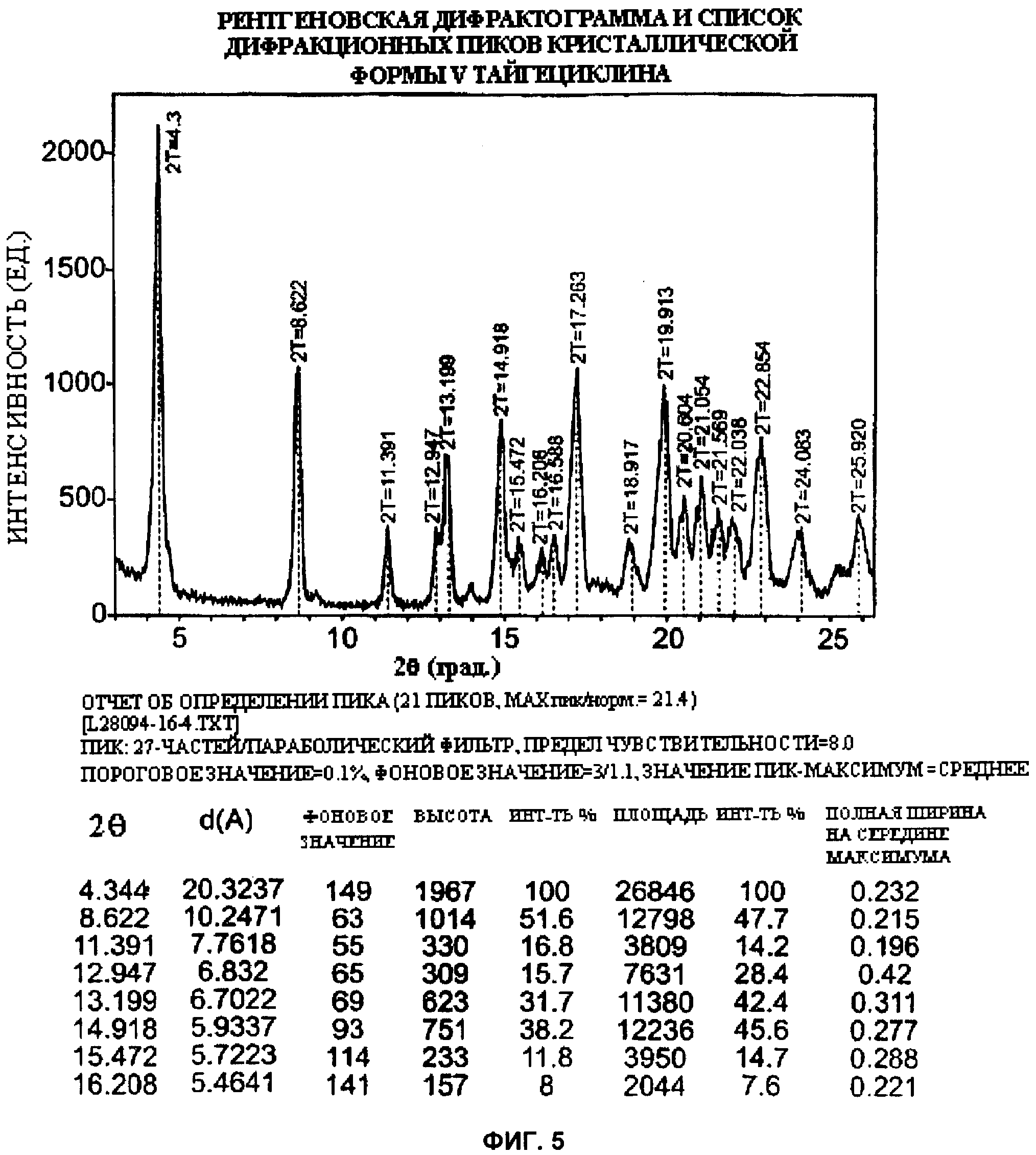
[022] Фиг.5 - рентгеновская дифрактограмма и список дифракционных пиков кристаллической формы V тайгециклина.
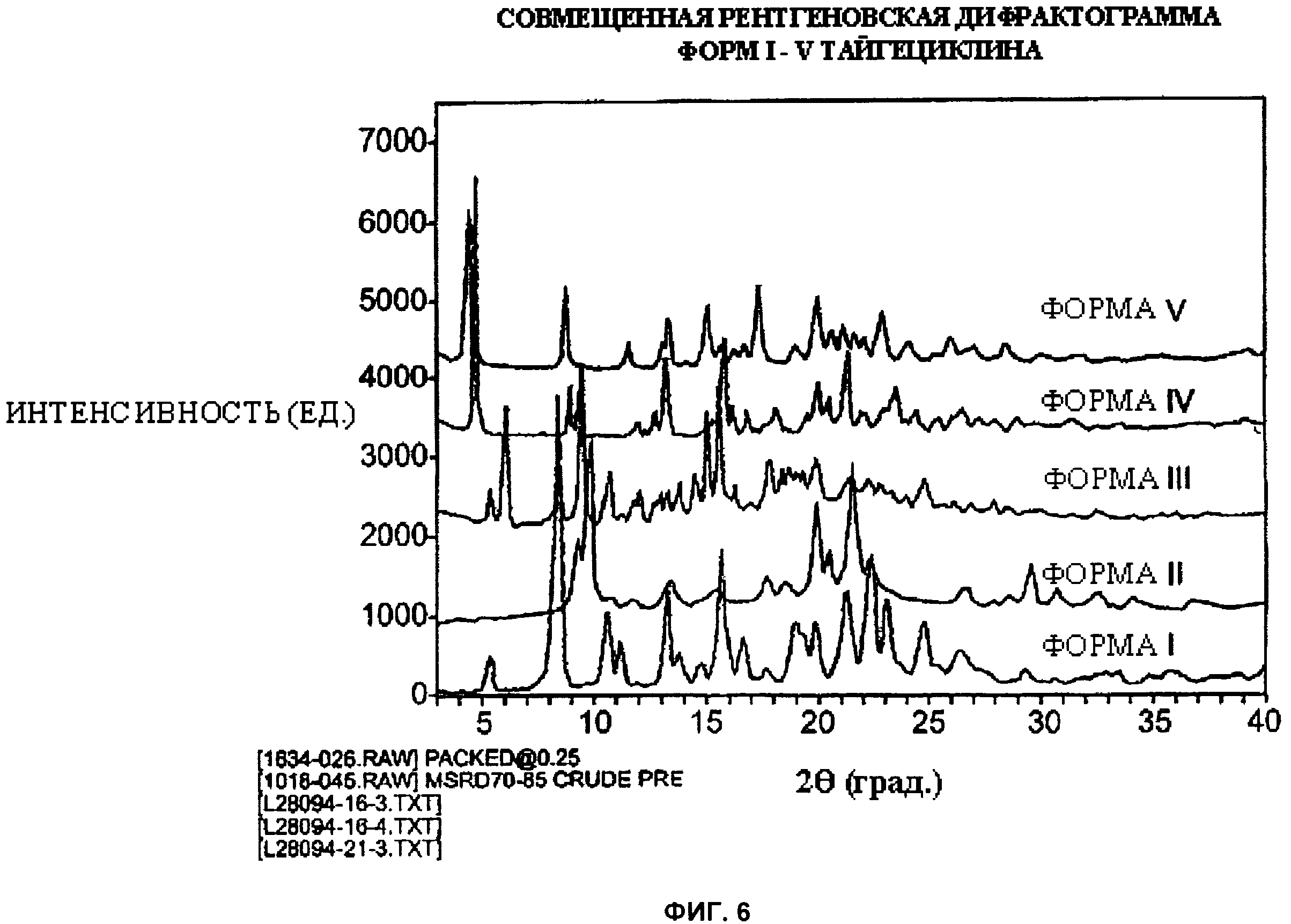
[023] Фиг.6 - совмещенная рентгеновская дифрактограмма кристаллических форм I-V тайгециклина.
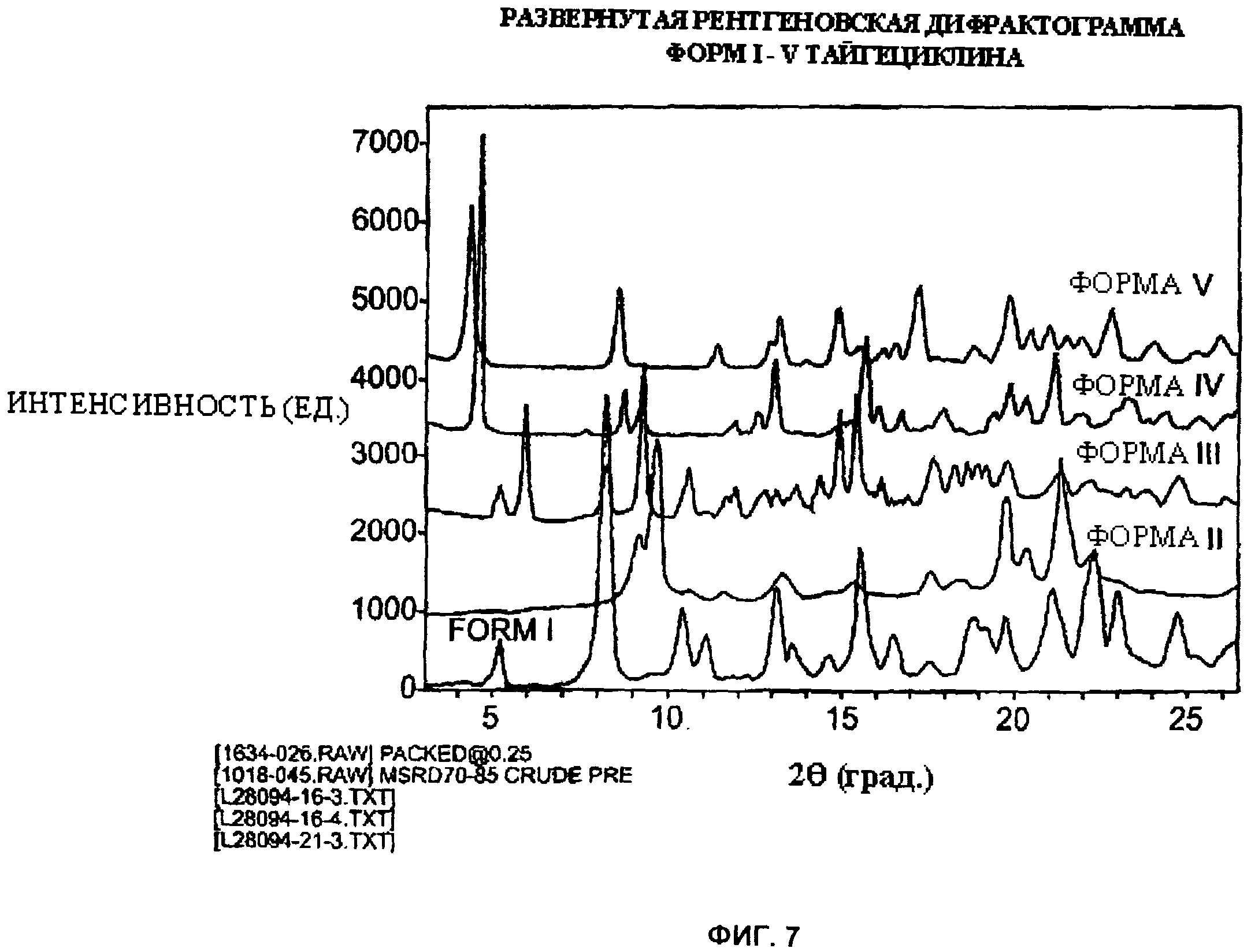
[024] Фиг.7 - развернутая рентгеновская дифрактограмма кристаллических форм I-V тайгециклина.
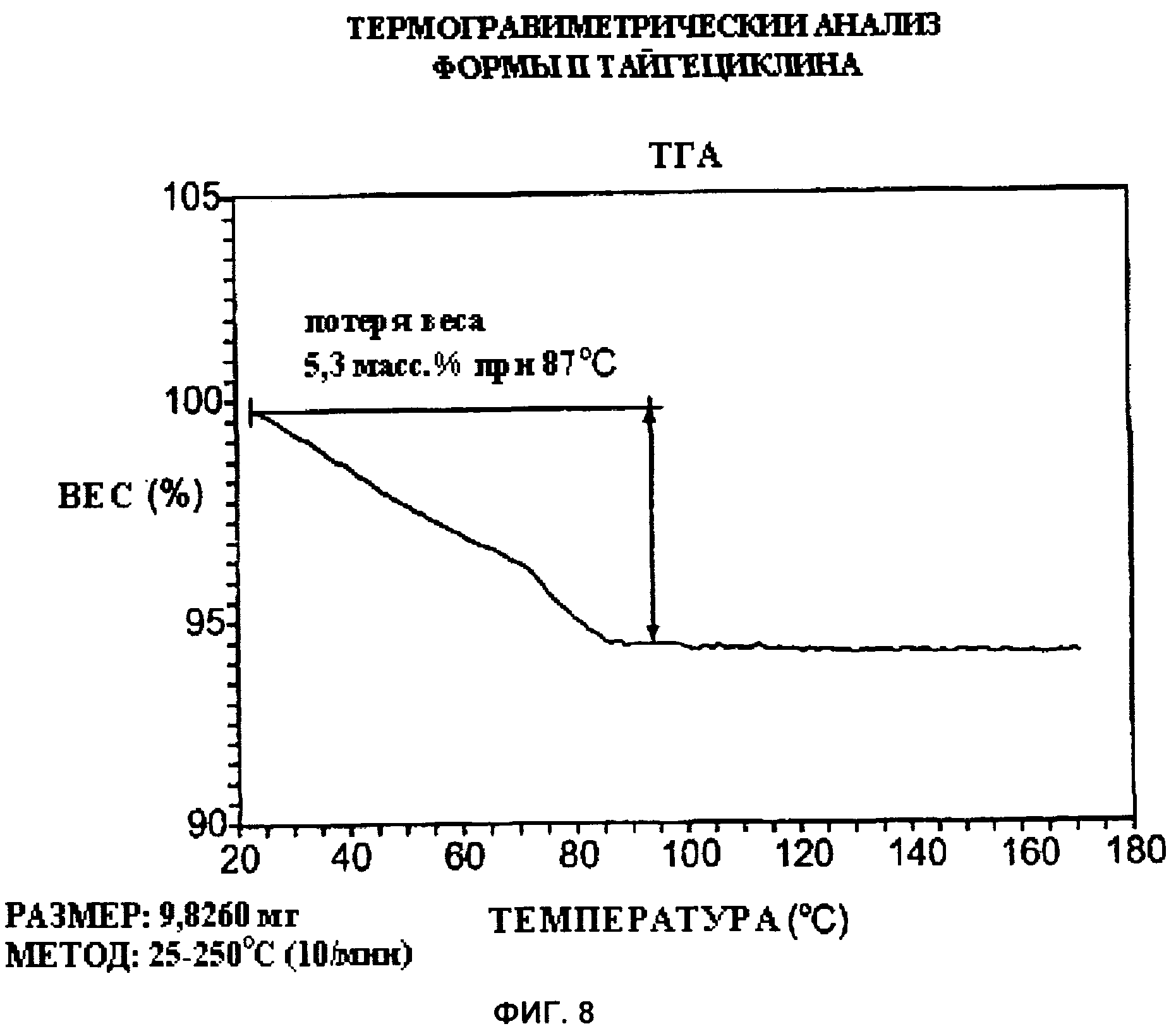
[025] Фиг.8 - термогравиметрический анализ («ТГА») формы II тайгециклина.
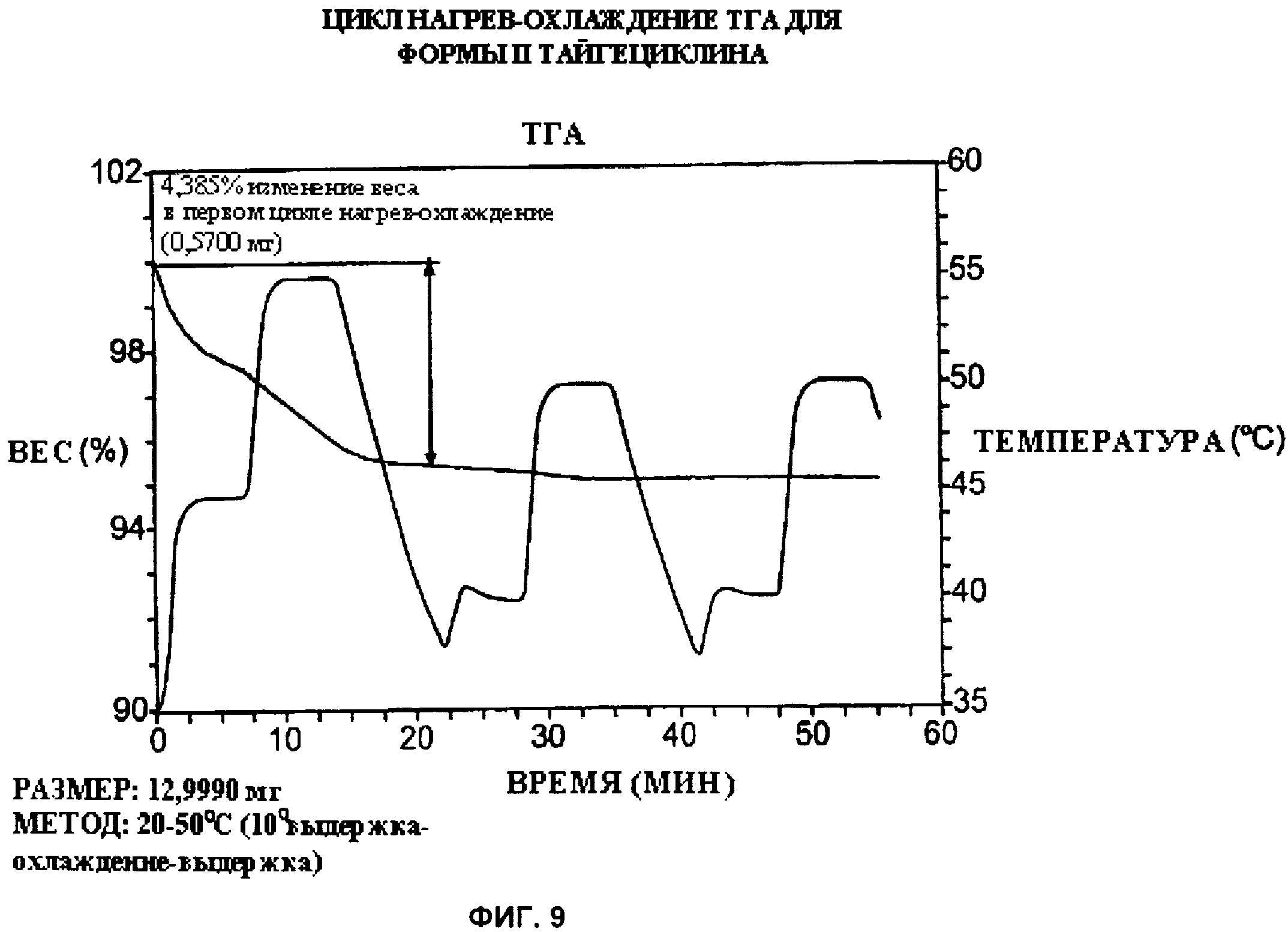
[026] Фиг.9 - цикл нагрев-охлаждение ТГА для формы II тайгециклина.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[027] В работе, которая стала основой данного изобретения, были использованы два рентгеновских дифрактометра. Данные на фиг.1 и 2 были получены с использованием дифрактометра Rigaku Miniflex Diffraction System (Rigaku MSC Inc., Tokyo, Japan). Порошки для анализа были размещены на нулевом фоновом полированном кремниевом держателе образцов. В качестве источника ренгеновского излучения использовалась нормально сфокусированная медная трубка при напряжении 30 кВ и током 15 мА, установка также была снабжена Ni-Kd фильтром. Образцы сканировались с шагом 0.027 при значениях угла 2θ в диапазоне от 3.00 до 40.00°. Полученные данные обрабатывались с использованием Jade 6.0 software (Molecular Data Systems Inc., Livermore, CA). Данные на фиг.3, 4 и 5 были получены на рентгеновском дифрактометре Scintag Advanced Diffraction System Model X2 (Scintag, Inc. Cupertino, CA) с кварцевым держателем образцов. В качестве источника ренгеновского излучения использовалась нормально сфокусированная медная трубка при напряжении 45 кВ и силой тока 49 мА, сканирование производилось при значениях угла 2θ от 3.00 до 40.00° с шагом 0.02°. Полученные данные также обрабатывались с использованием Jade 6.0 software (Molecular Data Systems Inc., Livermore, CA). Фиг.1-5 состоят из двух частей: рентгеновской порошковой дифрактограммы с выделением пиков и таблицы пиков. Таблицы пиков были созданы с применением стандартных параметров и коммерчески доступного программного обеспечения.
[028] В химии твердого тела при анализе двух разных дифрактограмм с целью определения, действительно ли по-видимому различные дифрактограммы фактически соответствуют различным твердым кристаллическим формам, обычной практикой является их совмещение на проекторе или экране компьютера. Например, только в результате такого совмещения может быть получена фиг.6, которая представляет собой совмещение всех пяти форм тайгециклина, которые были описаны и идентифицированы. Расширенная версия совмещенной дифрактораммы приведена на фиг 7.
[029] Полная рентгеновская дифрактограмма может быть использована для описания каждой из твердых кристаллических форм тайгециклина, однако для описания достаточно выделить небольшое подмножество пиков для каждой из этих форм. Эти выбранные пики затем могут быть использованы для идентификации каждой конкретной твердой кристаллической формы тайгециклина в неизвестных образцах, содержащих тайгециклин.
[030] Для иллюстрации в таблице 1 приведены первые 6 пиков из дифрактограмм формы I и формы II тайгециклина.
[031] Основываясь на сравнении этих данных и принимая во внимание только эти две формы тайгециклина, очевидно, что можно уверенно охарактеризовать форму I по первым 6 пикам, так как в случае формы II при значениях угла 2θ примерно +0.2° аналогичного набора из первых шести пиков нет. Однако нет необходимости использовать все 6 пиков, чтобы сделать вывод о том, что форма I отличается от формы II. Например, один из одиночных пиков формы I при значении угла 2θ примерно 5.2° однозначно характеризует форму I, так как ближайший пик формы II находится при значениях угла 2θ примерно 9.2°, т.е. разность составляет 4 градуса. Отличие в 4° намного больше, чем разница в 0.4°, которая получается в результате сложения погрешностей измерения (0.2°) для двух пиков. Другими словами, в случае если пик одного образца отличается от пика другого образца больше, чем на 0.4°, то эти пики соответствуют разным твердым кристаллическим формам, так как вероятность того, что данный пик твердой кристаллической формы изменялся бы больше, чем на 0.4° от образца к образцу или от дифрактометра к дифрактометру, чрезвычайно мал. Следовательно, в смеси, содержащей только формы I и II тайгециклина, порошковая дифрактограмма, имеющая пик при значении угла 2θ примерно 5.2°, однозначно характеризует форму I тайгециклина, и наличие этого пика может быть использовано для идентификации формы I. Аналогично при идентификации формы II, достаточно использовать пик при значении угла 2θ 9.2°, так как в пределах 0.4° отсутствуют пики формы I.
[032] Не все пики, указанные в таблице 1, могут быть использованы для идентификации формы I. Например, пик при значении угла 2θ примерно 13.2° формы I ни отдельно, ни вместе с другими пиками не может быть использован для описания формы I, так как пик формы II расположен при значениях угла 2θ примерно 13,3°, т.е. разница составляет всего 0.1°.
[033] В соответствии с данным изобретением, данные порошкового дифракционного анализа были получены для пяти кристаллических форм тайгециклина. Ниже, в таблице 2, приведены пики форм I, II, III, IV и V при значениях угла 2θ примерно 26°. Было определено, что пики высокой интенсивности более восприимчивы к эффектам ориентации. Пики, приведенные в таблице 2, были выбраны при рассмотрении списка пиков на фиг.1-5. Таким образом, данные в таблице 2 могут быть использованы для нахождения групп пиков, пригодных для описания и/или идентификации твердых кристаллических форм тайгециклина, что и является объектом данного изобретения.
[034] Согласно данному изобретению, так как ни один из пиков, приведенных для формы I, отличается не более чем на 0.4° от одного из пиков форм II, III, IV и V, т.е. нет ни одного отдельного пика, по которому можно было бы отличить форму I от каждой из форм II, III, IV и V. Например, если пик при значении угла 2θ примерно 5.2° формы I может быть использован, чтобы отличить форму I от формы II, то этот пик не может быть использован для сравнения формы I и формы III, так как форма III также дает пик примерно при 5.2°. Однако набор из двух пиков при значениях угла 2θ примерно 5.2° и 11.1° может быть использован для того, чтобы отличить форму I от форм II и III, так как пик при примерно 11.1° находится более чем в 0.4° от любого пика формы III. По этим же причинам пик примерно при 5.2° может быть использован, чтобы отличить форму I от форм IV и V. Таким образом, дифракционные пики при значениях угла 2θ примерно 5.2° и примерно 11.1° характерны для формы I и могут быть использованы для идентификации указанной формы I в образцах. Для описания и идентификации формы I также могут быть использованы несколько или все другие пики рентгеновской дифрактограммы формы I из списка пиков фиг.1.
[035] Аналогичным образом после анализа рентгеновских дифрактограмм форм II, III, IV и V были получены наборы пиков, которые могут быть использованы для описания и идентификации различных твердых кристаллических форм тайгециклина.
[036] В соответствии с изобретением пик формы II при значении угла 2θ примерно 9.2° является характерной особенностью, позволяющей отличить форму II от форм I и V. Однако само по себе это не дает возможности отличить форму II от форм III и IV. Пик в районе 9.7° может служить отличительным признаком при сравнении с формой IV, но он находится на расстоянии в 0.4° от пика формы III. Пик примерно 20.4° формы II отличает ее от формы III. Поэтому пики формы II при значениях угла 2θ примерно 9.2°, 9.7° и 20.4° служат отличительным признаком формы II по отношению к формам I, III, IV и V и, таким образом, описывают форму II в образце. Более того, эти пики могут служить для идентификации формы II. При описании и идентификации формы II можно также опираться на некоторые или все остальные пики формы II из таблицы на фиг.2.
[037] Согласно настоящему изобретению, пик формы III при значении угла 2θ примерно 6.0° служит отличительным признаком формы III от форм I, II, IV и V и, таким образом, описывает указанную форму III. Кроме того, этот пик может использоваться для идентификации формы III в образце. При описании и идентификации формы III можно также опираться на несколько или все остальные пики формы III из таблицы на фиг.3.
[038] Согласно настоящему изобретению, пик формы IV при значении угла 2θ примерно 4.6° служит отличительным признаком формы IV от форм I, II и III, a пик при примерно 9.2° отличается более чем на 0.4° от пика формы V. Таким образом, пики при примерно 4.6° и 9.2° служат отличительными признаками формы IV по отношению к формам I, II, III и V и являются характеризующими форму IV. Кроме того, эти пики могут использоваться для идентификации формы IV в образце. При описании и идентификации формы IV можно также опираться на несколько или все остальные пики формы IV из таблицы на фиг.4.
[039] Согласно настоящему изобретению, пик формы V при значении угла 2θ примерно 4.3° служит отличительным признаком формы V от форм I, II и III. Пик при примерно 11.4° формы V отличает ее от формы IV. Таким образом, пики при значениях угла 2θ примерно 4.3° и 11.4° служат отличительными признаками формы V по отношению к формам I, II, III и IV и поэтому являются характеристикой формы V. Кроме того, эти пики могут использоваться для идентификации формы V в образце. При описании и идентификации формы V можно также опираться на несколько или все остальные пики формы V из таблицы на фиг.5.
[040] Другие аналитические методы также могут быть использованы для анализа твердых кристаллических форм тайгециклина. Такие спектроскопические методы, как Раман (включая Раман-микроскопию), ИК и твердофазная ЯМР спектроскопии, могут быть использованы для описания и идентификации твердых кристаллических форм. Эти методы также можно использовать для количественного определения твердых кристаллических форм в смесях.
[041] В таблице 3 приведены температуры начала плавления нескольких образцов каждой из форм I, II, III, IV и V, полученных методом высокотемпературной микроскопии. Данные термических методов анализа, такие как температура начала плавления методом высокотемпературной микроскопии, в совокупности с другими данными или в целом сами по себе, не могут быть использованы для описания и/или идентификации различных твердых кристаллических состояний тайгециклина на основании данных, приведенных в таблице 3. Например, измеренные при помощи метода высокотемпературной микроскопии температуры начала плавления форм I и IV составляют примерно 170°С и по этому параметру указанные кристаллические формы отличить невозможно. В то же время, температуры начала плавления форм III и V отличаются весьма значительно: форма V плавится примерно 174°С, форма III - примерно 167°С. Температуры начала плавления, полученные с применением метода высокотемпературной микроскопии, могут быть использованы вместе с другими аналитическими методами, например, вместе с методом порошковой дифрактометрии, для описания и/или идентификации твердых кристаллических форм тайгециклина.
[042] При использовании метода высокотемпературной микроскопии температура держателя измерялась при помощи Creative Devices, Inc (Neshanic Station, NJ), Model 50-600 Controller. Скорость нагрева образцов составляла 10°С в минуту. При проведении анализов использовался микроскоп Nikon (Tokyo, Japan) DIAPHOT 300 system. Изображения были обработаны при помощи Image-Pro Plus software. Значения температур начала плавления приведены в соответствии с терминологией, принятой в химии твердых тел, с приставкой «примерно», что означает учет различных факторов, влияющих на температуру плавления: присутствие в образцах воды, растворителей или примесей, изменения, связанные с различием используемого оборудования и методологии эксперимента.
[043] Термогравиметрический анализ, выполненный с применением оборудования ТА Instruments (New Castle, DE), показал, что форма II представляет собой гидрат молекулы тайгециклина. На фиг.7 показана потеря веса образца формы II при нагревании от ~25°С до ~100°С со скоростью 10°С в минуту. Основная потеря веса, предположительно из-за потери молекулы воды, показана при помощи цикла нагрев-охлаждение ТГА (Фиг.8). При использовании циклов нагрев-охлаждение образец сначала нагревается до примерно 55°С, а затем охлаждается до ~37°С, снова нагревается и затем охлаждается и т.д. Потеря веса на первом цикле составила 4.4%, на втором и последующих циклах потеря веса была незначительна. Отсутствие значительной потери веса на втором и дальнейших циклах нагрев-охлаждение говорит о том, что образец находится в форме гидрата. Таким образом, можно с уверенностью утверждать, что форма II находится в форме гидрата со степенью гидратации примерно 4.4%.
[044] Кристаллизацию тайгециклина в пять различных твердых кристаллических форм невозможно предсказать исходя из его структурной формулы. Невозможно также заранее предсказать структуру и физические свойства любой из этих форм. Пять кристаллических форм тайгециклина, составляющих основу данного изобретения, были получены в ходе работы по определению набора условий для их кристаллизации.
[045] В данном изобретении приведены способы приготовления твердых кристаллических форм тайгециклина. Кристаллические формы II-V тайгециклина могут быть получены суспендированием формы I в органических растворителях в разных условиях. Форма I обрабатывалась одним или несколькими органическими растворителями в таком количестве, чтобы не допустить полного растворения и перемешивалась в виде суспензии в течение некоторого времени. В некоторых случаях суспензии нагревались или обрабатывались другими растворителями. Перед анализом вещества выделялись фильтрованием с последующей сушкой под вакуумом.
[046] В случае, если было показано, что определенный растворитель способствует превращению одной формы в другую, этот растворитель далее назывался «подходящим растворителем» для подобного превращения. Например, было обнаружено, что при суспендировании формы I в дихлорметане форма I переходит в форму III. Соответственно, дихлорметан представляет собой подходящий растворитель для такого превращения. Форма I также может быть переведена в форму III при кристаллизации из тетрагидрофурана (ТГФ) и суспендировании в дихлорметане. Форма II может быть получена при суспендировании формы I в метаноле. Таким образом, метанол представляет собой подходящий растворитель для такого превращения. Форма II также может быть получена при суспендировании формы I в смеси метанол/дихлорметан при содержании метанола свыше 10%. Аналогично, форма VI образуется из формы I при суспендировании последней в ацетонитриле. Ацетонитрил является подходящим растворителем для этого превращения. Форма IV также может быть получена при суспендировании формы I в смеси ацетонитрил/n-гептан. Наконец, при суспендировании формы I в тетрагидрофуране может быть получена форма V. Таким образом, тетрагидрофуран представляет собой подходящий растворитель для такого превращения. Суспендирование или перекристаллизация формы I из смеси ацетон/метанол (1:1) дает форму I.
[047] Кроме суспендирования, для превращения кристаллических форм могут использоваться и другие виды обработки в подходящих растворителях. Например, форма II тайгециклина может быть получена при кристаллизации из метанола. Форма II тайгециклина в виде частиц размером >20 мкм также может быть получена при медленном добавлении метанола в раствор тайгециклина в воде. При добавлении водного раствора тайгециклина в метанол образуется форма II тайгециклина с размером частиц <20 мкм. Таким образом, метанол, метанол/вода или вода/метанол представляют собой подходящие растворители для кристаллизации формы II тайгециклина.
[048] Данные о размере частиц тайгециклина были получены при помощи оптической техники. При выполнении оптической микроскопии использовался микроскоп Nikon Eclipse Е600 с увеличением от 5Х до 100Х, совмещенный с цифровой камерой (Nikon DXM 1200) и градуированной системой вывода изображения (Nikon ACT-1 v 2.12). Полученные фотографии были обработаны при помощи программного обеспечения ImagePro plus (Media Cybernetics, Silver Spring, MD). Данное программное обеспечение использует алгоритм контрастного разделения для определения частиц тайгециклина в однородном фоне. Результаты анализа приведены в таблице 4.
[049] Форма III может быть получена при кристаллизации тайгециклина из дихлорметана. Форма IV может быть получена кристаллизацией тайгециклина из ацетонитрила, и, наконец, форма V образуется при кристаллизации из тетрагидрофурана.
[050] В соответствии с настоящим изобретением, составы тайгециклина для применения животным или людям могут содержать формы I-V согласно настоящему изобретению. Растворимость всех пяти твердых кристаллических форм тайгециклина в воде превышает 25 мг/мл, т.е. все они биоэквивалентны друг другу.
[051] Фармацевтические составы для парентерального введения могут быть получены с использованием любой из форм I-V, с использованием или без использования лиофилизации. Фармацевтические составы на основе кристаллического тайгециклина могут быть получены с использованием одной или нескольких форм I-V согласно настоящему изобретению. Такие составы могут быть использованы для доставки фармацевтически эффективных количеств одной или нескольких форм I-V тайгециклина. Состав может содержать кристаллическую форму тайгециклина в сочетании или ассоциации с фармацевтически пригодным носителем.
[52] Следующие неограничительные примеры иллюстрируют несколько способов получения кристаллических форм I-V тайгециклина.
Пример 1 - Получение формы I
[053] В 5-литровую круглодонную трехгорлую колбу с термометром и мешалкой, содержащую 2000 мл t-бутиламина, медленно при интенсивном перемешивании добавили при комнатной температуре (25-28°С) 300 г неочищенного 9-хлорацетамидоминоциклина. В реакционную массу добавили сорок восемь граммов йодида натрия и перемешивали в течение 6 часов при температуре 35-40°С. Реакцию контролировали анализом ВЭЖХ, при содержании исходного вещества менее 2% реакционную массу обработали 500 мл метанола, и растворитель выпарили в роторном испарителе при 40°С. В остаток после упаривания добавили 1100 мл метанола и 1700 мл воды. Раствор охладили до 0-2°С и подкислили концентрированной соляной кислотой (~250 мл) до рН 7.2. На этой стадии общий объем реакционной массы составил 3500 мл. Реакционную массу разбавили до 8.5 л водой и подкислили концентрированной соляной кислотой до рН 4.0-4.2. К смеси прибавили 1.6 кг промытой модифицированной смолы для твердофазной экстракции Amberchrom® (CG 161 cd) (NVM 27%) и перемешивали 30 минут, поддерживая рН 4.0-4.2. Смолу отфильтровали, и полученный водный раствор проанализировали на содержание продукта и оставили на хранение при температуре 4-8°С. Смолу суспендировали в 2 л смеси 20 об.%. метанола в воде. Суспензию перемешивали в течение 15 минут, поддерживая рН 4.0-4.2. Смолу опять профильтровали, а фильтрат проанализировали на наличие продукта. Экстракцию повторили еще два раза с 2.0 л 20% метанола в воде. Все экстракты и водный раствор объединили и подщелачили до рН 7-7.2 30%-ным водным раствором аммиака. Водный раствор экстрагировали 6×3.0 л метиленхлоридом, после каждой экстракции рН доводили до 7-7.2. Объединенные экстракты метиленхлорида отфильтровали через 250 г безводного сульфата натрия, упарили до 500 мл и охладили до 0-3°С. При этом наблюдали кристаллизацию продукта реакции. Суспензию перемешивали 1 час при 0-3°С, отфильтровали, промыли 2×50 мл холодного метиленхлорида и высушили под вакуумом (74 мм рт.ст.) при 40°С. Вес полученного твердого вещества составил 110 г. Полученное вещество идентифицировали при помощи порошковой дифрактометрии как форму I тайгециклина. (Площадь пика ВЭЖХ% 97.9, содержание эпимера % 0.3.)
Пример 1А - Получение смолы для твердофазной экстракции
[054] Смолу, использованную в примере 1, получали из смолы Amberchrom® (CG 161 CD Toso Haas), 1 кг которой суспендировали в 6-7 л раствора 12 об.% 2-пропанола в воде и перемешивали в течение 12-16 часов. Суспензию отфильтровали, осадок перемешивали 30 минут в 6-7 л смеси ацетонитрил-вода 50:50. Суспензию снова отфильтровали и осадок суспендировали в 7 л ацетонитрила, перемешивали еще 30 минут и отфильтровали. Промывку в ацетонитриле с последующим фильтрованием повторили еще два раза. Далее смолу обработали 6 л метанола, смесь перемешивали в течение 1 часа и отфильтровали. Полученный осадок суспендировали в 7 л деионизированной воды, перемешивали 16 часов, отфильтровали. Смолу снова суспендировали в 7 л воды, перемешивали 1 час, отфильтровали. Промывку в воде с последующим фильтрованием повторили еще три раза. Смолу отфильтровали и на фильтре удалили воду, насколько это возможно, в течение 10-12 часов. Полученную смолу упаковали во флаконы и хранили при температуре 5-8°С.
Пример 2 - Получение формы I
[055] 10.00 г 9-аминоминоциклина порциями добавили в 60 мл воды при 0-5°С. Порциями добавили 10.98 г солянокислого 2-(трет-бутиламино)ацетилхлорида при температуре 0-5°С. Смесь перемешивали в течение 40-60 минут и при температуре 0-5°С добавили по каплям 30% раствор аммиака до рН 7.2. В раствор добавили 83 мл метанола и 60 мл метиленхлорида. Смесь перемешивали 15 минут, затем разделили слои. Водный слой экстрагировали 4×40 мл метиленхлоридом, перед каждой экстракцией рН доводили до 7.2. Экстракты метиленхлорида объединили, добавили 10 мл метанола, высушили над сульфатом натрия, отфильтровали. Раствор упарили. Полученную суспензию перемешивали при 5-10°С 1 час и отфильтровали. Осадок промыли холодным метиленхлоридом 2×10 мл и высушили. Получили 8.8 г продукта (выход 76.8%). Содержание основного вещества (площадь пика ВЭЖХ) % 98.4, С-4 эпимер 0.1%; MS(FAB): m/z 586 (M+H); 585 (М+).
Пример 3 - Получение формы II
[056] 0.5 г формы I суспендировали в 8 мл метанола при 22°С. Смесь нагрели до 35°С, перемешивали до растворения, и охладили до 22°С, и оставили до образования густой красной суспензии. Суспензию отфильтровали, осадок оставили сушиться под вакуумом в течение ночи при 25°С. Полученное вещество проанализировали термогравиметрическим методом («ТГА») и методом рентгеновской порошковой дифрактометрии. График ТГА (Фиг.8) показал потерю веса 5.3% при температуре до 87°С и скорости нагрева 10°С в минуту.
[057] Для цикла нагрев-охлаждение взяли свежеприготовленный образец, эксперимент проводили в камере прибора в атмосфере азота (Фиг.9). После первого цикла нагрев-охлаждение наблюдали потерю веса 4.4%, потеря веса при втором и третьем цикле была незначительной и, вероятно, была связана с потерей воды. После третьего цикла полученный порошок по внешнему виду имел красный цвет.
Пример 4 - Получение формы II
[058] 30 мг неочищенного тайгециклина растворили в 500 мкл деионизированной воды при 40°С и перемешивали раствор при 23°С. В раствор сначала добавили 500 мкл метанола, порциями по 100 мкл через каждые 15 минут. После того как весь метанол был добавлен, мутный раствор перемешивали примерно 10 минут до образования красного кристаллического осадка. После фильтрования на воздухе и сушки под вакуумом при 40°С в течение 8 часов получили 21,4 мг формы II (по данным порошковой дифрактометрии).
Пример 5 - получение формы II
[059] 30 мг неочищенного тайгециклина растворили в 500 мкл деионизированной воды при 40°С и перемешивали раствор при 23°С. В раствор добавили 800 мкл метанола и перемешивали примерно 15 минут при 10°С. В ходе добавления образовался кристаллический осадок. После фильтрования на воздухе и сушки под вакуумом при 40°С в течение 8 часов получили 20,2 мг формы II (по данным порошковой дифрактометрии).
Пример 6 - Получение формы III
[060] 0.25 г формы I суспендировали в 2 мл метиленхлорида при 22°С. В качестве затравки добавили 0.01 г формы V. Суспензию перемешивали 96 часов при 22°С. Далее суспензию отфильтровали и высушили под вакуумом при 22°С. По результатам высокотемпературной микроскопии и порошковой рентгеновской дифрактометрии, ВЭЖХ и оптической микроскопии получили форму III с содержанием основного вещества 99.98%.
Пример 7 - получение формы IV
[061] 0.15 г формы I добавили в 2 мл ацетонитрила при 22°С. Образовавшийся прозрачный раствор перемешивали 30 минут до образования осадка. Осадок отфильтровали и сушили под вакуумом при 22°С. Полученный бесцветный осадок формы IV анализировали методами высокотемпературной микроскопии, полученное твердое вещество промыли 5 мл н-гептана и высушили под вакуумом при 22°С. Полученную таким образом форму IV анализировали методами высокотемпературной микроскопии, порошковой рентгеновской дифрактометрии, ВЭЖХ (содержание основного вещества 96.39%) и оптической микроскопии.
Пример 9 - получение формы V
[063] 0.22 г формы I добавили в 2 мл тетрагидрофурана при 22°С и перемешивали 5 минут. В полученный прозрачный раствор добавили 2 мл н-гептана. Образовавшуюся суспензию перемешивали 30 минут при 22°С. Полученную таким образом форму V анализировали методами высокотемпературной микроскопии, порошковой рентгеновской дифрактометрии, ВЭЖХ (содержание основного вещества 93.57%) и оптической микроскопии.
Пример 10 - Сравнение стабильности Формы I со стабильностью аморфного тайгециклина
Стабильность разных форм тайгециклина изменяли как степень эпимеризации в зависимости от времени. Полученные данные представлены в таблице 5.
Таким образом, стабильность кристаллической формы тайгециклина согласно настоящему изобретению существенно выше, чем у аморфного тайгециклина.
Реферат
Изобретение относится к кристаллической форме тайгециклина I, характеризующейся тем, что на рентгенограмме, полученной методом порошковой рентгеновской дифракции, присутствуют дифракционные пики при значениях угла 2θ 5.2° и 11.1°, а также дифракционный пик при значении угла 2θ 8.3° и дифракционный пик при значении угла 2θ 24.8°. Кристаллическую форму тайгециклина I применяют для изготовления фармацевтических составов, для лечения бактериальных заболеваний. Технический результат - твердая кристаллическая форма тайгециклина, обладающая улучшенными показателями стабильности. 3 н. и 5 з.п. ф-лы, 9 ил., 5 табл., 10 пр.

Комментарии