Аналоги витамина d, композиции, содержащие указанные аналоги, и их применение - RU2320644C2
Код документа: RU2320644C2
Описание
Область изобретения
Данное изобретение относится к новым аналогам витамина D, к их использованию в терапии, к фармацевтическим композициям, содержащим указанные аналоги, к способам лечения, включающим в себя введение указанных аналогов нуждающимся в этом пациентам, и к использованию указанных аналогов при производстве лекарственных препаратов.
Уровень техники данного изобретения
В течение последних десятилетий понимание биологического действия витамина D все более возрастало. Классические эффекты витамина D включают в себя кальциевую и фосфатную абсорбцию из кишечника, которая жизненно необходима для минерального баланса и для роста и сохранения костей. Другим основополагающим действием витамина D является регулирование выделения паратиреоидного гормона (РТН) паращитовидными железами. Витамин D ингибирует выработку паратиреоидного гормона таким образом, чтобы низкий уровень витамина D в крови приводил к высокому уровню паратиреоидного гормона, и наоборот. Витамин D оказывает свое действие за счет интересного механизма, посредством которого ингибируется выработка мРНК, транслируемой в паратиреоидный гормон или его проформу. Однако влияние витамина D в биологических системах выходит за пределы данных эффектов. По-видимому, витамин D оказывает сильное воздействие на мышцы, иммунную систему, репродуктивную систему и пролиферацию и дифференцировку клеток. Фактически, клетки, содержащие рецептор витамина D (VDR), были найдены во многих частях тела, включая кишечник, почки, предстательную железу, кости, костный мозг, паращитовидные железы, кожу, печень, мышцы и лимфатическую ткань. Широкое распространение VDR сделало витамин D и его аналоги привлекательными соединениями для лечения различных заболеваний, включая рак, заболевания кожи и костей и аутоиммунные заболевания.
Данное изобретение относится к новому классу аналогов витамина D, оказывающих сильный супрессивный эффект на секрецию паратиреоидного гормона, которые, таким образом, можно использовать для лечения вторичного гиперпаратиреоидизма (s-HPT). Ключевым структурным элементом в активном витамине D являются две гидроксильные группы в положениях 1 и 25. В отличие от этого соединения по настоящему изобретению характеризуются блокированием 25-положения с тем, чтобы у них не было гидроксильных групп в данном положении; их также нельзя гидроксилировать в данное положение in vivo Р450-подобным ферментом.
Ранее были описаны аналоги витамина D, обладающие некоторым структурным сходством с соединениями по настоящему изобретению. В качестве примера в WO95/02577 исследованы соединения формулы

В WO91/00855 описаны соединения формулы

и Onisko, Tetrahedron Lett., 1107-1108, 13, 1977 описывает соединение формулы

которое может быть использовано для ингибирования ферментов печени, ответственных за гидроксилирование витамина D3 в 25-ОН витамин D3.
Наконец, Bogoslovsky et al., Vitamin D - Basic Research and its Clinical Application, proceedings of the Fourth Workshop on Vitamin D, Berlin West Germany 1979, A. W. Norman et al. (Eds.), p.1257-1259, Walter de Gruyter, Berlin 1979, представляли синтетическое исследование, включающее в себя получение 3(S)-гидрокси-9,10-секохолеста-5(Z),7(Е),10(19),22(Е),24-пентаена. Однако в данной ссылке не раскрыто никаких биологических данных относительно этого конкретного соединения.
Витамин D и его аналоги уже применяют при лечении s-HTP. Парикальцитол (19-нор-1,25-дигидроксивитамин D2) и доксеркальциферол (1α-гидроксивитамин D2) одобрены в США для лечения s-HTP, а 22-оксакальцитриол (максакальцитол) и гексафторкальцитриол (фалекальцитриол) одобрены в Японии [Malluche, Kidney Int., 367-374, 62, 2002]. Кроме того, кальцитриол как таковой и его пролекарство 1α(ОН)D3 также применяют при лечении и профилактики s-HTP [Brandi, Nephrol Dial Transplant, 829-842, 17, 2002].
При всех терапевтических вмешательствах, которые включают в себя введение витамина D и его аналогов, необходимо обращать внимание на неблагоприятные побочные эффекты, часто связанные с данным видом терапии, в частности с кальцемическими эффектами соединений витамина D. Эти побочные эффекты могут жестко ограничить, или даже воспрепятствовать использованию подобных соединений, несмотря на остальные клинически положительные эффекты. Поэтому в настоящем изобретении стремятся предоставить аналоги витамина D, которые обладают сниженным кальцемическим эффектом, сохраняя, в то же время, супрессивный эффект на секрецию паратиреоидного гормона.
Сущность изобретения
Соответственно, в настоящем изобретении предоставлены соединения, представленные формулой I

в которой
R1 и R2, которые могут быть одинаковыми или различными, представляют собой галоген, (С1-С6)углеводородный радикал, необязательно замещенный одной или двумя гидроксильными группами, или одним или более атомами фтора,
или вместе с атомом углерода, с которым они оба связаны, R1 и R2 образуют (С3-С6)карбоцикл,
или один из R1 и R2 вместе с R3 образует прямую связь, так что возникает тройная связь,
или оба R1 и R2 представляют собой водород;
R3, в том случае, когда он не образует прямой связи с одним из R1 и R2, представляет собой водород или (С1-С3)углеводородный радикал;
Х представляет собой (Е)-этилен, (Z)-этилен, этинилен или связь;
Y и Z независимо представляют собой водород или метил;
связь между С#16 и С#17 изображена пунктиром для иллюстрации того, что указанная связь может быть либо одинарной связью, в этом случае положением заместителя цикла является бета, или двойной связью;
А представляет собой гидроксил, фтор или водород;
В представляет собой СН2 или Н2;
конфигурация в 3-положении соответствует той же конфигурации, что и в природном витамине D3 (нормальная), или конфигурация в 3-положении противоположна природному витамину D3 (эпи);
при условии, что, если Х представляет собой (Е)-этилен или (Z)-этилен, один из R1 и R2 вместе с R3 не может образовывать прямой связи так, чтобы возникала тройная связь;
и при следующем условии, что, если Х представляет собой связь, R1 и R2 не являются водородом;
и при следующем условии, что соединение формулы I не является 3(S)-гидрокси-9,10-секохолеста-5(Z),7(Е), 10(19),22(Е),24-пентаеном;
и его пролекарства и стереоизомерные формы.
В соединениях формулы I блокировка 25-положения достигается за счет присутствия углерод-углеродной двойной или тройной связи между углеродом #24 и #25. Таким образом, 25-положение не может быть гидроксилировано. Как более подробно обсуждается далее, на основании недавних данных предполагают, что гидроксилирование 25-положения имеет ограниченные последствия на супрессивный эффект по отношению к паратиреоидному гормону. Поэтому аналоги витамина D, которые блокированы для гидроксилирования в 25-положение, сохраняют свой супрессивный эффект по отношению к паратиреоидному гормону, лишаясь в то же время других видов активности витамина D, например кальцемического эффекта, связанного с ненарушенной структурой витамина D.
В следующем аспекте изобретение относится к применению соединения формулы I в терапии.
В следующем аспекте изобретение относится к фармацевтической композиции, содержащей соединение формулы I.
В еще одном аспекте изобретение относится к способам лечения, включающим в себя стадию введения соединения формулы I нуждающемуся в этом пациенту.
В еще одном аспекте изобретение относится к применению соединения формулы I при получении лекарственного средства.
Подробное описание изобретения
В предпочтительном варианте осуществления данного изобретения R1 и R2, рассматриваемые по отдельности, независимо представляют собой бром, хлор, метил, этил, трифторметил, гидроксиметил, (1- или 2-)гидроксиэтил, нормальный, изо- или циклопропил, 2-гидрокси-2-пропил, 2-метил-2-пропил, 3-пентил или 3-гидрокси-3-пентил.
В другом предпочтительном варианте осуществления R1 и R2 являются одинаковыми и оба представляют собой водород, метил, этил, бром, хлор или трифторметил.
В другом варианте осуществления R1 и R2, взятые вместе с атомом углерода, с которым они оба связаны, образуют С3 карбоцикл, С4 карбоцикл или С5 карбоцикл.
В другом предпочтительном варианте осуществления R1 и R2, взятые вместе, включают в себя этилен, триметилен, тетраметилен или пентаметилен, например, R1 и R2, взятые вместе с атомом углерода, с которым они оба связаны, образуют С3 карбоцикл, С4 карбоцикл, С5 карбоцикл или С6 карбоцикл.
В другом предпочтительном варианте осуществления, если R2 составляет часть тройной связи, то R1 представляет собой разветвленный С1-6 углеводородный радикал, необязательно замещенный одной или двумя гидроксильными группами. В частности, R1 представляет собой разветвленный С1-6 углеводородный радикал, необязательно замещенный одной гидроксильной группой, такой как -СМе3, -С(ОН)Ме2 или -С(ОН)Et2.
В другом предпочтительном варианте осуществления R3 в случае, когда он не является частью тройной связи, представляет собой водород, метил или циклопропил.
В следующем предпочтительном варианте осуществления А является гидроксилом или фтором.
В следующем предпочтительном варианте осуществления R1 и R2 представляют собой радикал, полученный при удалении одного атома водорода из линейного, разветвленного или циклического насыщенного С1-6 углеводорода.
В частности, соединения формулы I можно выбрать из перечня, включающего в себя
1(S), 3(R)-дигидрокси-9,10-секохолеста-5(Z),7(E),10(19),22(E),24-пентаен (соединение 1),
1(S),3(R)-дигидрокси-9,10-секохолеста-5(Z),7(E),10(19),22(Z),24-пентаен (соединение 2),
20(S),1(S),3(R)-дигидрокси-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 3),
1(S),3(R)-дигидрокси-9,10-секо-26,27-циклохолеста- 5(Z),7(E),10(19),22(Е),24-пентаен (соединение 4),
20(S),1(S),3(R)-дигидрокси-9,10-секо-26,27-циклохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 5),
1(S),3(R)-дигидрокси-9,10-секо-26, 27-метанохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 6),
20(S),1(S),3(R)-дигидрокси-9,10-секо-26,27-метанохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 7),
1(S),3(R)-дигидрокси-20(S)-(4,4-дибром-1,3-бутадиен-1-ил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 8),
1(S),3(R),26-тригидрокси-9,10-секохолеста-5(Z),7(E),10(19), 22(Е),24(Е)-пентаен (соединение 9),
20(S),1(S),3(R),26-тригидрокси-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24(Е)-пентаен (соединение 10),
1(S),3(R),26-тригидрокси-9, 10-секохолеста-5(Z),7(E),10(19),22(Е),24(Z)-пентаен (соединение 11),
20(S),1(S),3(R),26-тригидрокси-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24(Z)-пентаен (соединение 12),
1(S),3(R)-дигидрокси-20(R)-(4-метил-5-этил-5-гидрокси-1(Е),3(Е)-гептадиенил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 13),
1(S),3(R)-дигидрокси-20(R)-(3-циклопропил-1(Е), 3-бутадиенил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 14),
1(S),3(R)-дигидрокси-9,10-секохолеста-5(Z),7(E),10(19),24-тетраен-22-ин (соединение 15),
1(S), 3(R)-дигидрокси-20(R)-(5-метил-5-гидрокси-1,3-гексадиинил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 16),
1(S),3(R)-дигидрокси-20(S)-(5-этил-5-гидрокси-1,3-гептадиинил)-9, 10-секопрегна-5(Z),7(E),10(19)-триен (соединение 17),
1(S),3(R)-дигидрокси-20(R)-(5-этил-5-гидрокси-1,3-гептадиинил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 18),
1(S),3(R)-дигидрокси-20(R)-(5,5-диметил-1,3-гексадиинил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 19),
1(S),3(R)-дигидрокси-20(S)-(5,5-диметил-1,3-гексадиинил)-9, 10-секопрегна-5(Z),7(E),10(19)-триен (соединение 20),
1(S)-фтор-3(R)-гидрокси-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 21),
1(S), 3(R)-дигидрокси-19-нор-9,10-секохолеста-5,7(E),22(Е),24-тетраен (соединение 22),
1(S),3(S)-дигидрокси-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 23),
1(S),3(R)-дигидрокси-9,10-секохолеста-5(Z),7(E),10(19),16,22(Е),24-гексаен (соединение 24),
1(S),3(R)-дигидрокси-26,26,26,27,27,27-гексафтор-9,10-секохолеста-5(Z),7(E),10(19),22(Е), 24-пентаен (соединение 25),
3(S),26-дигидрокси-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24(Е)-пентаен (соединение 26),
1(S),3(R)-дигидрокси-20(R)-(4,4-дибром-1, 3-бутадиен-1-ил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 27),
1(S),3(R)-дигидрокси-26,27-диметил-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 28),
1(S),3(S)-дигидрокси-26,27-диметил-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 29),
1(S),3(R)-дигидрокси-24-метил-26,27-метано-9,10-секохолеста-5(Z),7(E), 10(19),22(Е),24-пентаен (соединение 30),
1(S),3(R)-дигидрокси-20(R)-(4,4-дихлор-1,3-бутадиен-1-ил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 31),
1(S), 3(R)-дигидрокси-26,27-этано-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 32),
1(S),3(R)-дигидрокси-26,27-пропано-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 33),
1(S),3(R)-дигидрокси-20(S)-циклопропилиденметил-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 34),
1(S),3(R)-дигидрокси-20(R)-циклопропилиденметил-9, 10-секопрегна-5(Z),7(E),10(19)-триен (соединение 35),
20(S),1(S),3(R)-дигидрокси-26,26,26,27,27,27-гексафтор-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 36).
Соединения формулы I могут содержать хиральные центры, такие как асимметрично замещенные атомы углерода, и углерод-углеродные двойные связи, которые приводят к появлению стереоизомерных форм, таких как энантиомеры, диастереомеры и геометрические изомеры (цис/транс). Настоящее изобретение относится ко всем таким формам, либо в чистом виде либо в виде их смесей.
Например, конфигурация при С-3, или при С-20 (когда Y отличается от Z) в формуле I может быть R или S, или, если Х представляет собой этилен, конфигурация может быть Е или Z.
Соединения формулы I можно получить в кристаллическом виде, либо непосредственно концентрированием из органического растворителя, либо кристаллизацией или перекристаллизацией из органического растворителя или смеси указанного растворителя и сорастворителя, который может быть органическим или неорганическим, например водой. Кристаллы можно выделить в форме, в существенной степени не содержащей растворителя, или в виде сольвата, такого как гидрат. Данное изобретение включает в себя все кристаллические модификации и формы, а также их смеси.
В настоящем контексте, если не заявлено иначе, под термином «пролекарство» имеют в виду соединения, в которых одна или несколько гидроксильных групп замаскированы в виде групп, которые могут быть повторно преобразованы в гидроксильные группы in vivo с тем, чтобы получить соединения формулы I при введении пациенту. Примерами подобных групп являются сложные эфиры, например эфиры карбоновых кислот и эфиры фосфорной кислоты. Хорошо известно, что проформы витамина D гидроксилируются в печени и почках для достижения биологически активного состояния. В соответствии с этим соединения формулы I, в которых А представляет собой гидроксил, являются предпочтительными соединениями, но соединения, в которых А является водородом, фактически представляют собой пролекарства другого типа, которые могут быть гидроксилированы до активного состояния при введении пациенту.
В настоящем контексте под термином «углеводородный радикал» имеют в виду радикал, полученный при удалении одного атома водорода из линейного, разветвленного и/или циклического, насыщенного или ненасыщенного углеводорода. Указанный линейный, разветвленный и/или циклический, насыщенный или ненасыщенный углеводород включает в себя, но не ограничивается этим, метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-бутил, 1-пентил, 2-пентил, 3-пентил, 1-гексил, 2-гексил, 3-гексил, циклопропил, циклобутил, циклопентил, циклогексил, 2-метил-2-пропил, 2-метилциклопропил, 2-метилаллил, 1-проп-2-инил, 1-бут-2-инил, 3-метил-1-пентил, 1-гекс-1-ен-3-инил.
В настоящем контексте под термином «галоген» имеют в виду соединения седьмой основной группы Периодической системы, то есть фтор, хлор, бром и йод, и, в особенности, хлор и бром.
Термины «нормальный» и «эпи», используемые для описания абсолютной конфигурации соединения по настоящему изобретению, относятся к абсолютной конфигурации самого природного витамина D3. Следовательно, если конфигурацию данного углерода называют «нормальной», она соответствует конфигурации витамина D3 для данного конкретного атома углерода. Аналогичным образом, если конфигурацию данного углерода называют «эпи», это конфигурация, противоположная конфигурации витамина D3 для данного конкретного атома углерода.
Особенное значение для настоящего изобретения имеет лечение вторичного гиперпаратиреоидизма (s-HPT), например, в связи с почечной недостаточностью, с использованием витамина D и его аналогов. Гиперпаратиреоидизм является заболеванием, которое характеризуется повышенной секрецией паратиреоидного гормона из паращитовидных желез. При s-HPT причиной увеличенной секреции является не дисфункция данных желез, а скорее факторы вне желез, например почечная недостаточность. Витамин D абсорбируется из пищи или вырабатывается в коже в проформе, которую нужно активировать, чтобы достигнуть биологически активного состояния. Часть этой активации происходит в почках как гидроксилирование данной проформы. У пациентов с почечной недостаточностью, например у пациентов, подвергаемых диализу, данное гидроксилирование снижено, что приводит к более низкому уровню активного витамина D в крови. Как указывалось выше, низкий уровень витамина D приводит к большой выработке паратиреоидного гормона, и это патологическое состояние называется вторичным паратиреоидизмом.
Паратиреоидный гормон оказывает значительное влияние на клетки в костях, приводя к выделению ими кальция в кровоток. При непатологических условиях данный процесс является хорошо сбалансированным для обеспечения соответствующего уровня кальция в костях. Однако при повышенных уровнях паратиреоидного гормона в течение продолжительных периодов времени кости будут терять слишком много кальция и станут хрупкими и, таким образом, более склонными к переломам. Данное состояние называется остеодистрофией и остемаляцией, от которых часто страдают почечные пациенты. Кроме того, найдено, что продолжительное воздействие паратиреоидных гормонов оказывает токсическое действие на многие жизненно важные органы, например мышцы скелета, нервы и репродуктивную систему [Malluche, Kidney Int., 367-374, 62, 2002].
Один из способов регулирования уровня паратиреоидного гормона состоит во введении витамина D или его аналогов, которые будут ингибировать секрецию указанного гормона. Однако подобное терапевтическое вмешательство может быть затруднено серьезными неблагоприятными побочными эффектами, часто сопровождающими терапию витамином D. Как указывалось ранее, эффект витамина D и многих его аналогов заключается в повышенном поглощении кальция из кишечника, что может привести к гиперкальцемии. Данный эффект может ограничить полезность аналогов, которые выгодны в других отношениях. Таким образом, цель многих проводимых исследований витамина D заключается в сведении к минимуму кальцемического эффекта, при максимизации, в то же время, клинического эффекта. В идеале, если были идентифицированы структурные звенья в молекуле витамина D, ответственные за различные активности, можно было бы манипулировать этими структурами для получения селективности, например никакой кальцемической активности, но высокий супрессивный эффект по отношению к секреции паратиреоидного гормона. К сожалению, до сих пор не установлено подобной ясной зависимости структура-активность. Однако в этом отношении может помочь недавнее наблюдение Brandi в Nephrol Dial Transplant, 829-842, 17, 2002. Brandi сравнивает РТН супрессивный эффект кальцитриола, то есть 1,25(ОН)2D3 и его проформы, 1α(ОН)D3. 1α(ОН)D3 гидроксилируется в печени до 1,25(ОН)2D3, и вследствие различной фармакокинетики этих двух соединений биодоступность 1,25(ОН)2D3 была значительно ниже, когда пациенту вводили 1α(ОН)D3, чем когда пациенту вводили 1,25(ОН)2D3. Несмотря на разницу в биодоступности 1,25(ОН)2D3 при двух режимах дозировок, в подавлении секреции РТН не было существенного различия. Это приводит к предположению о том, что 25-гидроксильная группа не является обязательной для РТН супрессивного эффекта. Таким образом, одним из способов достижения желательной селективности могло бы стать блокирование 25-положения в структуре витамина D так, чтобы его нельзя было гидроксилировать, и таким образом сохраняя или даже повышая РТН супрессивный эффект, лишая, в то же время, молекулу другого витамина D родственных активностей и, в частности, ее кальцемического эффекта.
Кальцемические активности соединений по настоящему изобретению определяли на крысах in vivo, как описано ранее (Binderup, L., Bramm, E., Biochem. Pharmacol. 37, 889-895 (1988)). РТН супрессивный эффект соединений по настоящему изобретению определяли in vitro на бычьих паратиреоидных клетках: у взрослого крупного рогатого скота отбирали свежие бычьи паращитовидные железы через 20 минут после забоя. Из рубленой паратиреоидной ткани диспергированные паратиреоидные клетки получали, как описано ранее (E.M. Brown, S. Hurwitz and G.D. Aurbach; Preparation of viable bovine parathyroid cells; Endocrinology, 1976, vol. 99, no 6, 1582-1588). Затем клетки обрабатывали аналогами витамина D в течение 60 часов при 37°С и определяли РТН секрецию витамина D.
В таблице А перечислены супрессивные эффекты РТН и кальцемические активности соединений по настоящему изобретению. В качестве соединения сравнения использовали кальцитриол (1,25(ОН)2D3).
Данные, приведенные в таблице А, показывают, что соединения по настоящему изобретению обладают сопоставимым РТН супрессивным эффектом по сравнению с соединением сравнения кальцитриолом (1,25(ОН)2D3) наряду с неожиданно более низким кальцемическим эффектом, чем соединение сравнения.
Таким образом, соединения по настоящему изобретению неожиданно проявляют высокую селективность, например ингибирование выработки паратиреоидного гормона, без нежелательного влияния аналогов витамина D, таких как 1,25(ОН)2D3, на баланс кальция в организме, включая кальцемическую и кальциурическую активности.
Таким образом, в конкретном варианте осуществления изобретение предоставляет способ лечения, предупреждения или улучшения состояния при s-НРТ, а в частности, s-НРТ, связанного с почечной недостаточностью, при этом данный способ включает в себя введение нуждающемуся в этом пациенту эффективного количества соединения формулы I. Необязательно указанный способ может включать в себя лечение другими терапевтически активными соединениями, обычно применяемыми при лечении указанного выше заболевания. Указанные соединения можно вводить сопутствующим образом или последовательно с соединениями по настоящему изобретению, и, в частности, они включают в себя фосфатные связывающие вещества.
Применение соединений по настоящему изобретению не может быть ограничено лечением s-PTH. Хорошо известно, что витамин D и его аналоги могут оказаться полезными при лечении множества заболеваний благодаря их высокой активности при вызывании дифференцировки и ингибировании нежелательной пролиферации некоторых клеток, включая клетки кожи и раковые клетки, а также иммуномодулирующему эффекту и эффекту роста и сохранения костей (Brown AJ: Vitamin D analogues. Am J Kidney Dis 32 (Suppl): S25-S39, 1988; Brown AJ et al.: Vitamin D. Am Physiol 277:F157-F175, 1999). Соответственно, в изобретении также предложен способ лечения, предупреждения или улучшения состояния при заболеваниях, характеризуемых аномальной дифференцировкой клеток и/или пролиферацией клеток, рака, лейкемии, рака груди, глиального рака мозга, остеосаркомы, меланомы, миелосклероза, псориаза, первичного гиперпаратиреоидизма, сахарного диабета, дискоидальной и системной красной волчанки, хронических кожных болезней аутоиммунного типа, гипертензии, угрей, алопеции, старения кожи, СПИДа, нейродегенеративных нарушений, болезни Альцгеймера, реакций хозяина против трансплантата и трансплантата против хозяина, отторжений трансплантатов, вызванной стероидами атрофии кожи и остеопороза, и для вызывания остеогенеза, при этом данный способ включает в себя введение нуждающемуся в этом пациенту эффективного количества соединения формулы I. Необязательно, указанный способ может включать в себя лечение другими терапевтически активными соединениями, обычно используемыми при лечении указанных выше заболеваний. Указанные соединения можно вводить сопутствующим образом, или последовательно с соединениями по настоящему изобретению, и они включают в себя фосфатные связывающие вещества, стероиды и анти-пролиферативные агенты.
При системном лечении с использованием настоящего изобретения вводят дневные дозы 0,001-2 мкг на килограмм массы тела, предпочтительно 0,002-0,3 мкг/кг массы тела млекопитающего, например 0,003-0,3 мкг/кг соединения формулы I, обычно соответствующие дневной дозе для взрослого человека от 0,1 до 200 мкг. Однако подходящий режим дозировки может включать в себя дозировку с более длительными интервалами, например каждый следующий день, каждую неделю, или даже с более продолжительными интервалами. При местном лечении дерматологических нарушений вводят мази, кремы или лосьоны, содержащие 0,1-1000 мкг/г и предпочтительно 0,1-500 мкг/г, например, 0,1-200 мкг/г соединения формулы I. Для местного применения в офтальмологии вводят мази, капли или гели, содержащие 0,1-1000 мкг/г и предпочтительно 0,1-500 мкг/г, например, 0,1-100 мкг/г соединения формулы I. Пероральные композиции составляют предпочтительно в виде таблеток, капсул или капель, содержащих от 0,07-100 мкг, предпочтительно 0,1-50 мкг соединения формулы I на разовую дозу.
В следующем предпочтительно аспекте изобретение относится к фармацевтической композиции, содержащей соединение формулы I. Препараты по настоящему изобретению как для ветеринарного медицинского применения, так и для использования для человека содержат активные ингредиенты в сочетании с фармацевтически приемлемыми носителем(лями) и, необязательно, другой терапевтический ингредиент(ы). Носитель(ли) должны быть «приемлемыми» в смысле совместимости с прочими ингредиентами данных препаратов и невредными по отношению к их реципиенту.
Обычно единичная доза состава содержит от 0,05 мкг до 100 мкг, предпочтительно от 0,1 мкг до 50 мкг соединения формулы I.
Под термином «единичная доза» имеют в виду единичную, то есть разовую дозу, которую можно ввести пациенту и с которой легко обращаться и упаковывать, которая остается в виде физически и химически стабильной разовой дозы, содержащей либо активное вещество как таковое, либо его смесь с твердыми или жидкими фармацевтическими разбавителями или носителями.
Препараты включают в себя, например, препараты в форме, пригодной для перорального (включая продолжительное или рассчитанное по времени высвобождение), ректального, парентерального (включая подкожное, внутрибрюшинное, внутримышечное, внутрисуставное и внутривенное), чрескожного, офтальмологического, местного, назального или буккального ведения.
Препараты можно удобно представить в виде стандартной лекарственной формы и их можно изготовить любым из способов, известным в области фармации, например, как описано Remington, The Science and Practice of Pharmacy, 20th ed., 2000. Все способы включают в себя стадию объединения активного ингредиента с носителем, который представляет собой один или несколько дополнительных ингредиентов. Как правило, составы изготавливают равномерно и тонко смешивая активный ингредиент с жидким носителем или тонкоизмельченным твердым носителем, или ими обоими, а затем, в случае необходимости, формуя продукт в желательный препарат.
Препараты по настоящему изобретению, подходящие для перорального введения, могут иметь форму отдельных единиц, таких как капсулы, саше, таблетки или пастилки, каждая из которых содержит заранее определенное количество активного ингредиента; форму порошка или гранул; форму раствора или суспензии в водной жидкости или неводной жидкости, такой как этанол или глицерин; или форму эмульсии масло-в-воде или вода-в-масле. Подобные масла могут быть пищевыми маслами, например хлопковым маслом, кунжутным маслом, кокосовым маслом или арахисовым маслом. Подходящие диспергирующие или суспендирующие агенты для водных суспензий включают в себя синтетические или природные смолы, такие как трагакантовая камедь, альгинат, аравийская камедь, декстран, карбоксиметилцеллюлоза натрия, желатин, метилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксипропилцеллюлоза, карбомеры и поливинилпирролидон. Кроме того, активные ингредиенты можно вводить в виде болюса, электуария или пасты.
Таблетку можно изготовить, прессуя или формуя активный ингредиент необязательно с одним или более дополнительными ингредиентами. Прессованные таблетки можно изготовить прессованием в подходящем аппарате активного ингредиента(ов) в сыпучей форме, такой как порошок или гранулы, необязательно, смешанного со связывающим веществом, например, таким как лактоза, глюкоза, крахмал, желатин, аравийская камедь, трагакантовая камедь, альгинат натрия, карбоксиметилцеллюлоза, метилцеллюлоза, гидроксипропилметилцеллюлоза, полиэтиленгликоль, воски или тому подобное; смазывающим веществом, например, таким как олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия или тому подобное; разрыхляющим агентом, например, таким как крахмал, метилцеллюлоза, агар-агар, бентонит, кроскармеллоза натрия, гликолят натриевого крахмала, кросповидон или тому подобное, или диспергирующим агентом, таким как полисорбат 80. Формованные таблетки можно изготовить формованием, в подходящем аппарате, смеси порошкообразного активного ингредиента и подходящего носителя, увлажненного инертным жидким разбавителем.
Препараты для ректального введения могут иметь вид суппозиториев, в которых соединение по настоящему изобретению смешано с низкоплавкими растворимыми в воде или нерастворимыми в воде твердыми веществами, такими как масло какао, гидрогенизированные растительные масла, полиэтиленгликоль или сложные эфиры жирных кислот полиэтиленгликолей, хотя можно изготовить эликсиры с использованием миристилпальмитата.
Удобно, чтобы препараты, подходящие для парентерального введения, содержали стерильный масляный или водный препарат активных ингредиентов, предпочтительно изотоничный крови реципиента, например изотонический раствор соли, изотонический раствор глюкозы или буферный раствор. Препарат удобно стерилизовать, например, фильтрованием через удерживающий бактерии фильтр, добавлением стерилизующего агента к препарату, облучением препарата или нагреванием препарата. Также для парентерального введения подходят липосомные препараты, описанные, например, в Encyclopedia of Pharmaceutical Technology, vol.9, 1994.
Альтернативно, соединение формулы I можно представить в виде стерильного твердого препарата, например высушенного вымораживанием порошка, который легко растворяется в стерильном растворителе перед использованием.
Чрескожные препараты могут иметь вид пластыря или повязки.
Препараты, подходящие для офтальмологического введения, могут иметь вид стерильного водного препарата активных ингредиентов, которые могут быть в микрокристаллической форме, например в виде водной микрокристаллической суспензии. Для представления активного ингредиента для офтальмологического введения можно также использовать липосомные препараты или системы биоразлагаемых полимеров, например, описанные в Encyclopedia of Pharmaceutical Technology, vol.2, 1989.
Препараты, подходящие для местного или офтальмологического введения, включают в себя жидкие или полужидкие препараты, такие как жидкие мази, лосьоны, гели, пластыри, эмульсии масло-в-воде или вода-в-масле, такие как кремы, мази или пасты; или растворы или суспензии, такие как капли.
Препараты, подходящие для назального или буккального ведения, включают в себя порошок, самораспыляющиеся и спреевые препараты, такие как аэрозоли и пульверизаторы.
Пролекарства настоящего изобретения можно также доставлять при использовании моноклональных антител, с которыми связаны молекулы соединения.
Помимо указанных выше ингредиентов, препараты соединения формулы I могут содержать один или более дополнительных ингредиентов, таких как разбавители, буферные агенты, ароматизаторы, красители, поверхностно-активные агенты, загустители, консерванты, например метилгидроксибензоат (включая антиоксиданты), эмульгирующие агенты и так далее.
Кроме того, указанные препараты могут также содержать другие терапевтически активные соединения, обычно используемые для лечения упомянутых выше заболеваний. Примеры подобных соединений включают в себя фосфатные связывающие вещества, стероиды и антипролиферативные агенты.
В еще одном аспекте изобретение относится к использованию соединения формулы I, необязательно, вместе с другим терапевтически активным соединением для производства лекарственного средства, предназначенного для лечения аномальной дифференцировки клеток и/или пролиферации клеток, рака, лейкемии, рака груди, глиального рака мозга, остеосаркомы, меланомы, миелосклероза, псориаза, первичного гиперпаратиреоидизма, s-PTH, s-PTH, связанного с почечной недостаточностью, сахарного диабета, дискоидной и системной красной волчанки, хронических дерматитов аутоиммунного типа, гипертензии, угрей, алопеции, старения кожи, СПИДа, нейродегенеративных нарушений, болезни Альцгеймера, реакций хозяина против трансплантата и трансплантата против хозяина, отторжения трансплантатов, вызванной стероидами атрофии кожи и остеопороза, и для вызывания остеогенеза. Указанное другое терапевтически активное соединение можно просто выбрать, например, из числа фосфатных связывающих веществ, стероидов и антипролиферативных агентов.
Соединение формулы I можно получить из промежуточных соединений 1 по реакционной схеме 1.
Схема 1
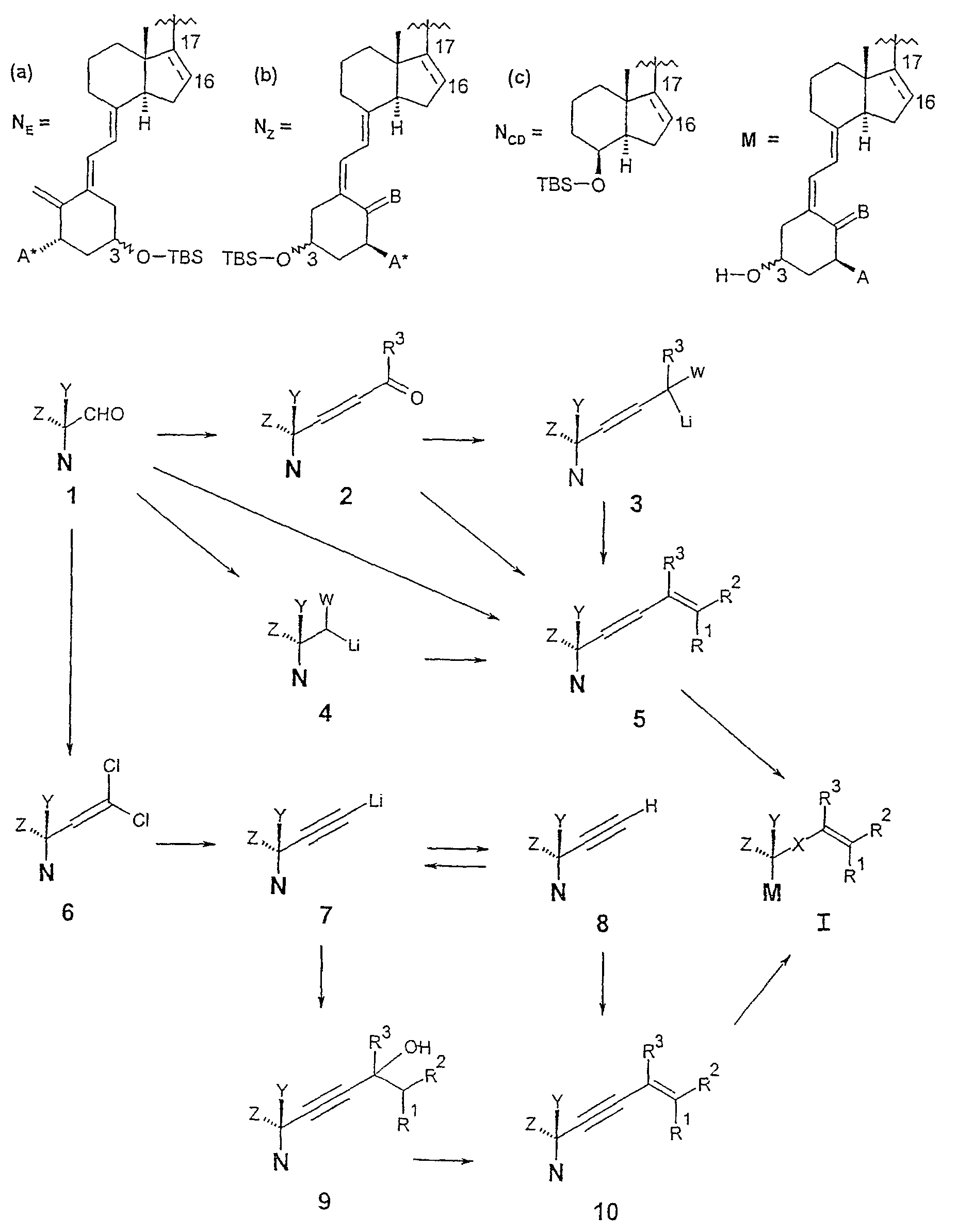
Символ * использован на схеме 1 для указания того, что группа А* в промежуточном соединении может либо быть идентична группе А, находящейся в соединении I (например, фтор в NZ), либо, альтернативно, может являться группой, которую можно преобразовать в нее на любой последующей стадии данного синтеза (например, гидроксил, защищенный силиловым эфиром, в NZ). Хотя это формально и не указано таким образом, аналогичная ситуация может также относится к переменным R1, R2, R3, Y и Z на схеме 1. Кроме того, идентичность N (то есть NE, NZ или NCD) и/или одной или более переменной группы(групп) может изменяться от промежуточного соединения к промежуточному соединению по ходу последовательности реакций. Однако действительная идентичность будет очевидна из конкретного контекста. Следует отметить, что хотя Cl и Li являются атомными символами (как С, Н и О), в качестве аббревиатуры функциональной группы или элемента, стабилизирующего литийорганические вещества, используют букву W. Конфигурацию (Е или Z) двойной связи (которая станет Х = этилен в конечных соединениях I) оставляют неопределенной в схеме 1 (рисуя линейное расположение), но определяют в случае необходимости.
Исходные соединения типа 1 и некоторые примеры промежуточных соединений типа 2, 4, 6, 7 и 8 хорошо известны специалисту в данной области техники и были описаны в литературе, например, G.-D. Zhu and W.H. Okamura в Chem. Rev. 1995, 95, 1877-1952. Суффиксы а, b и с устанавливают структуру группы N, определенной вверху схемы 1.
В общих чертах предполагаемые реакции, которые все хорошо известны химику-синтетику, специализирующемуся в области химии витамина D, проводят следующим образом. В данном описании используют стандартные сокращения, например, Ас = ацетил, водн. = водный, DCM = дихлорметан, Et = этил, эфир = диэтиловый эфир, ч = час(ы), LDA = диизопропиламид лития, Ме = метил, PDC = дихромат пиридиния, ТВА = тетра(н-бутил)аммоний, TBS = трет-бутилдиметилсилил, TMS = триметилсилил, Ts = п-тозил, DIBAL = гидрид диизобутилалюминия, Ph = фенил, ТГФ = тетрагидрофуран, v = объем.
1→2 Реакция Виттига или Водсворта-Эммонса [например, Виттига с Ph3P=CH-C(O)R3 (для R3= Н, через промежуточное соединение R3= ОМе, из которого его получают последовательным восстановлением DIBAL и PDC или окислением перйодинаном Десс-Мартина)]. Конфигурация двойной связи, установленная в данной реакции, обычно Е (однако часто можно выделить небольшие количества промежуточного соединения Z), но можно выбрать условия для получения увеличенной доли промежуточного соединения Z, например, модификацию реакции Водсворта-Эммонса с использованием (CF3CH2O)2P(O)-CH2C(O)OMe. Е-конфигурацию можно альтернативно преобразовать в Z при помощи фотоизомеризации на стадии промежуточного соединения 2. Выделение требуемого изомера из смеси Е- и Z-изомеров можно осуществить на данной или более поздней стадии, например, хроматографией или кристаллизацией.
1→4 Для промежуточных соединений, у которых W = S(O2)Ph или W = SeMe, в литературеописаны способы, такие как у M.J. Calverly, Tetrahedron Letters 1987, 28, 1337-1340.
1→5 Например, по реакции Виттига с Ph3P=CH-C(R3)=CR1R2. Образующиеся в данной реакции Е- и Z-изомеры можно необязательно разделить, например, хроматографией или кристаллизацией на этой стадии или на любой более поздней стадии данного синтеза.
1→6→7→8→7 Вместо показанного дихлорпромежуточного соединения (6) можно использовать дибромпромежуточное соединение в данной части хорошо известной последовательности реакции получения алкинов, описанной ранее, например, W.G. Salmond et al., Tetrahedron Letters 1977, 14, 1239-1240.
2→3 Для R3= Н (в 3): Последовательное восстановление DIBAL [для R3= ОМе (или Н) в 2 (см. 1→2), преобразование спирта в уходящую группу (например, Cl или OTs), которую затем замещают для введения W (например, -P(O)Ph2 или -S(O2)Ph), либо непосредственно, либо путем окисления более низкого состояния окисления -PPh2 или -SPh, при этом все они доступны в виде солей] и литиирование (например, при действии n-BuLi или LDA).
2→5 Реакция Виттига, например, с Ph3P=CR1R2, или реакция Водсворта-Эммонса, например, с использованием (EtO)2P(O)-CR1R2. Разделение 24-Е- и 24-Z-изомеров, образующихся в данной реакции, можно необязательно осуществить, например, хроматографией или кристаллизацией на этой стадии или на любой более поздней стадии данного синтеза.
3→5 Реакция сочетания с карбонильным соединением, например, реакцией Хорнера при W = P(O)Ph2 или реакцией Джулиа при W = S(O2)Ph (сопровождаемой в последней реакции восстановительным элиминированием W наряду с оксигруппой). Разделение образующихся 24-Е- и 24-Z-изомеров можно необязательно осуществить, например, хроматографией или кристаллизацией на этой стадии или на любой более поздней стадии данного синтеза.
4→5 Реакция сочетания с карбонильным соединением с последующим элиминированием W и оксигруппы. Выделение требуемого изомера из смеси Е- и Z-изомеров можно осуществить на этой или на более поздней удобной стадии.
7→9 Реакция сочетания с карбонильным соединением.
8→10 Катализируемое палладием кросс-сочетание с терминальным ацетиленом или с винильным или ацетиленовым производным, таким как галогенид (например, бромид). Реакции включают в себя, но не ограничиваются реакциями типа Хека, Сузуки, Кадиот-Ходкиевского, Негиши, Соногашира и Штилле.
9→10 Дегидратация при помощи сульфуранового реагента Мартина.
5 или 10→I "N→M": см. ниже. Кроме того, А*, R1, R2, R3, Y и/или Z могут быть модифицированы или переведены в производные при помощи способов и общих методик, которые хорошо известны специалисту в данной области техники, например, описанных в "Comprehensive Organic Transformations" R.C. Larock, VCH 1989.
NCD→М: Последовательное десилилированием при действии HF с получением спирта, окисление перйодинаном Десс-Мартина до кетона и сочетание по Хорнеру-Виттигу с литиевым производным требуемого известного А-циклического фосфиноксида формулы II с получением NZ. Затем десилилирование при помощи HF или ТВА-фторида.

NЕ→М: Преобразование в NZ (В = СН2) при помощи триплетчувствительной фотоизомеризации, затем десилилирование при помощи HF или ТВА-фторида.
NZ→М: Десилилирование при помощи HF или ТВА-фторида.
Далее изобретение проиллюстрировано следующими получениями и примерами: приведенные в качестве примеров соединения формулы I представлены в таблице 1, тогда как исходные вещества и промежуточные соединения общих формул с 1 по 10 (схема 1) приведены в таблице 2.
Получения и примеры
Реакции обычно (если не указано иначе) проводили при перемешивании в атмосфере аргона при добавлении реагента (жидкого или в растворе) по каплям из шприца. При обычной методике обработки органический слой отделяли, последовательно промывали водой и насыщенным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали в вакууме, получая сырой продукт, который затем очищали хроматографией. Всю препаративную и аналитическую (ТСХ) хроматографию проводили на силикагеле с использованием градиента от 1 до 50% (об./об.) эфира (то есть диэтилового эфира) в петролейном эфире в качестве элюента, или от 30% (об./об.) этилацетата в петролейном эфире до чистого этилацетата. В общих методиках переменные пункты начинают с красной строки (отдельных строк) и затем перечислены в конкретных получениях наряду с подробностями, при необходимости, в случае какого-либо отклонения от общей методики, которые были фактически использованы. Однако пропорциональное масштабирование количеств непеременных реагентов и растворителей по отношению к молярным количествам, указанным в каждом получении, считают доказанным и, таким образом, не считают отклонением, требующим точных деталей.
Соединения охарактеризовывали спектроскопически: в случае спектров ядерного магнитного резонанса1Н (300 МГц) и13С-ЯМР (75,6 МГц) приведены величины химических сдвигов (δ) (в м.д.), если не указано иначе, для растворов дейтерохлороформа относительно внутреннего тетраметилсилана (добавленного,1Н-ЯМР: δ=0,00 м.д.,13С-ЯМР: δ=0,00 м.д.) или хлороформа (остаточного,1Н-ЯМР: δ=7,25 м.д.), или дейтерохлороформа (13С-ЯМР: δ=76,81 м.д.). Значение для мультиплета (1Н-ЯМР) либо разрешенного [дублет (д), триплет (т), квартет (кв)], либо нет (м) дано при приблизительной средней точке, если не приведен интервал (с = синглет, уш = уширенный). В некоторых случаях, только выбранных, характеристические сигналы могут быть приведены для промежуточных соединений, то есть соединений из таблицы 2.
Общая методика 1 (получения 1-7 и 27-28) [2→5] (получения 29-30) [1→5]
К раствору или суспензии соли алкилтрифенилфосфония (7 ммоль) в сухом ТГФ (50 мл), находящейся примерно при -70°С, добавляли н-бутиллитий (1,6 М в гексане, 4,36 мл, 7 ммоль). Затем реакционную смесь оставляли нагреваться до температуры 0°С в течение 20 минут, после чего возобновляли охлаждение до -70°С для добавления промежуточного соединения 1 или 2 (4 ммоль), растворенного в сухом ТГФ (8 мл). Через 30 минут при той же температуре медленного отогревания и 70 минут при комнатной температуре смесь распределяли между насыщенным раствором хлорида аммония и этилацетатом и обрабатывали в соответствии со стандартной методикой обработки, приведенной выше, получая промежуточное соединение 5.
Получение 1: соединение 501
Соль алкилтрифенилфосфония: йодид изопропилтрифенилфосфония (3,16 г, 7,3 ммоль)
Промежуточное соединение 2: 202 (2,39 г).
Очистка соединения 502 из сырого продукта непосредственной кристаллизацией из метанола, опуская стадию хроматографии:13С-ЯМР: δ = 153,5, 143,1, 138,1, 135,2, 132,5, 125,1, 124,1, 121,5, 116,3, 106,4, 70,0, 67,1, 56,3, 56,2, 45,7, 43,8, 40,4, 40,3, 36,4, 28,8, 27,7, 25,7, 25,6, 23,3, 22,0, 20,6, 18,1, 18,0, 17,9, 12,1, -4,9, -5,1 м.д.
Получение 2: соединение 522
Соль алкилтрифенилфосфония: йодид изопропилтрифенилфосфония (1,55 г, 3,6 ммоль)
Промежуточное соединение 2: 206 (получено из 102 по аналогии с описанным получением 202 из 101 в WO9100855 (0,7 г, 2 ммоль).
Соединение 522:13С-ЯМР: δ = 138,5, 132,3, 125,1, 123,8, 69,3, 56,4, 52,9, 42,0, 40,5, 39,7, 34,3, 29,2, 25,7, 25,6, 22,8, 20,3, 18,0, 17,8, 17,5, 13,8, -5,0, -5,3 м.д.
Получение 3: соединение 503
Соль алкилтрифенилфосфония: йодид изопропилтрифенилфосфония (1,47 г, 3,4 ммоль)
Промежуточное соединение 2: 203 (1 г, 1,67 ммоль).
Очистка соединения 503 хроматографией (2% об.:об., эфир в петролейном эфире).
Соединение 503:13С-ЯМР: δ = 153,4, 143,3, 138,5, 135,1, 132,3, 125,1, 124,0, 121,6, 116,1, 106,4, 70,1, 67,0, 56,7, 56,1, 45,8, 43,8, 40,6, 39,6, 36,4, 28,8, 27,1, 25,7, 25,7, 25,6, 23,3, 21,9, 21,3, 18,1, 17,9, 12,1, -4,9, -5,1 м.д.
Получение 4: соединение 504
Соль алкилтрифенилфосфония: бромид циклопропилтрифенилфосфония (0,76 г, 2 ммоль)
Промежуточное соединение 2: 202 (0,60 г, 1 ммоль).
Очистка соединения 504 хроматографией (5% об.:об., эфир в петролейном эфире).
Соединение 504:13С-ЯМР: δ = 6,45 (д, J=12 Гц, 1H), 6,33 (уш.д, J=10 Гц, 1H), 6,12 (дд, J=15 Гц, J=10 Гц, 1H), 5,81 (д, J=12 Гц, 1H), 5,55 (дд, J=9 Гц, J=15 Гц, 1H), 4,97 (м, 1H), 4,93 (м, 1H), 4,53 (м, 1H), 4,23 (м, 1H), 2,86 (м, 1H), 2,55 (дд, 1H), 2,30 (уш.д, 1H), 2,20-1,15 (м, 14H), 1,15-1,0 (м, 14H), 1,07 (д, J=7 Гц, 3H), 0,89 (с, 9H), 0,86 (с, 9H), 0,57 (с, 3H), 0,05 (м, 12H) м.д.
Получение 5: соединение 505
Соль алкилтрифенилфосфония: бромид циклопропилтрифенилфосфония (1,53 г, 4 ммоль)
Промежуточное соединение 2: 203 (0,56 г, 0,93 ммоль).
Очистка соединения 505 хроматографией (5% об.:об., эфир в петролейном эфире).
Соединение 505:13С-ЯМР: δ = 6,44 (д, J=11,4 Гц, 1H), 6,35 (уш.д, J=10,3 Гц, 1H), 6,08 (дд, J=10,3 Гц, J=15,3, 1H), 5,81 (д, J=11,4 Гц, 1H), 5,55 (дд, J=9,5 Гц, J=15,3, 1H), 4,97 (уш.т, 1H), 4,93 (уш.т, 1H), 4,52 (м, 1H), 4,21 (м, 1H), 2,84 (м, 1H), 2,54 (дд, J=5,3 Гц, J=14,5 Гц, 1H), 2,31 (уш.д, J=13,7 Гц, 1H), 2,2-1,0 (м, 18H), 0,97 (д, J=6,5 Гц, 3H), 0,89 (с, 9H), 0,86 (с, 9H), 0,52 (с, 3H), 0,05 (с, 12H) м.д.
Получение 6: соединение 506
Соль алкилтрифенилфосфония: бромид циклобутилтрифенилфосфония (0,80 г, 2 ммоль)
Промежуточное соединение 2: 202 (0,60 г, 1 ммоль).
Очистка соединения 506 хроматографией (1% об.:об., эфир в петролейном эфире).
Соединение 506:13С-ЯМР: δ = 153,5, 143,1, 142,5, 137,1, 135,2, 123,6, 121,5, 120,8, 116,3, 106,4, 70,0, 67,0, 56,3, 56,2, 45,7, 43,8, 40,3, 40,3, 36,4, 31,1, 29,7, 28,7, 27,7, 25,7, 25,6, 23,3, 22,0, 20,5, 18,1, 17,9, 17,0, 12,0, -4,9, -5,0, -5,1 м.д.
Получение 7: соединение 507
Соль алкилтрифенилфосфония: бромид циклобутилтрифенилфосфония (1,33 г, 3,34 ммоль)
Промежуточное соединение 2: 203 (1 г, 1,67 ммоль).
Очистка соединения 507 хроматографией (1% об.:об., эфир в петролейном эфире).
Хроматография: 1% эфира в петролейном эфире.
Соединение 507:13С-ЯМР: δ = 153,4, 143,3, 142,4, 137,4, 135,1, 123,6, 121,6, 120,9, 116,1, 106,4, 70,1, 67,0, 56,8, 56,1, 45,8, 43,8, 40,6, 39,6, 36,4, 31,1, 29,7, 28,8, 27,1, 25,7, 25,6, 23,3, 21,9, 21,3, 18,1, 17,9, 16,9, 12,1, -4,9, -5,1 м.д.
Получение 8: соединение 502 [4→5]
К находящемуся примерно при -70°С раствору литиевого производного 403 (таблица 2, пункт 14) (полученного из 0,75 г, 1 ммоль селено-ацетального производного 101 в сухом ТГФ (5 мл)) прибавляли по каплям структурное звено боковой цепи - 3-метилкротоновый альдегид (0,10 г, 1,2 ммоль). После перемешивания при той же температуре в течение 30 минут реакцию гасили сырым ТГФ и распределяли смесь между эфиром и водой и получали промежуточный аддукт в виде смеси диастереоизомеров. К его раствору в сухом DCM (15 мл) и триэтиламине (2 мл), находящемуся примерно при 5°С, прибавляли метансульфонилхлорид (1,5 ммоль). После перемешивания при той же температуре в течение 30 минут реакционную смесь распределяли между эфиром и водой. В результате стандартной обработки, описанной выше, получали соединение 502:13С-ЯМР: δ = 153,5, 143,1, 136,0, 135,2, 134,4, 121,7, 121,5, 120,4, 116,3, 106,4, 70,0, 67,0, 56,5, 56,3, 45,7, 43,8, 40,4, 40,3, 36,4, 28,8, 27,3, 25,7, 25,6, 23,4, 22,0, 20,6, 18,0, 17,9, 12,2, -4,9, -5,0, -5,1 м.д.
Общая методика 2 (получения 9, 10) [2→5]
К находящемуся примерно при 20°С раствору промежуточного соединения 2 (0,76 ммоль) в DCM (5 мл) прибавляли триэтил 2-фосфонопропионат (0,45 г, 1,9 ммоль), 50%-ный водный раствор NaOH (5 мл) и гидросульфат ТВА (0,11 г). После энергичного перемешивания в течение 105 минут, реакционную смесь распределяли между водой и этилацетатом. В результате стандартной обработки, описанной выше (хроматография 2-5% об:об этилацетат в петролейном эфире в качестве элюента), получали промежуточное соединение 5.
Получение 9: соединение 508 и 509
Промежуточное соединение 2: 202 (0,46 г).
Первый элюированный продукт: соединение 509:13С-ЯМР: δ = 167,6, 153,5, 147,6, 142,8, 141,1, 135,3, 125,3, 123,8, 121,5, 116,4, 106,3, 70,0, 67,0, 59,9, 56,2, 55,8, 45,8, 43,8, 40,3, 40,3, 36,4, 28,7, 27,5, 25,7, 25,6, 23,3, 22,1, 20,4, 20,0, 18,1, 17,9, 14,1, 12,1, -0,5, -5,1 м.д.; второй элюированный продукт: соединение 508:13С-ЯМР: δ = 168,5, 153,5, 148,7, 142,7, 138,7, 135,4, 124,9, 123,5, 121,5, 116,4, 106,4, 70,0, 67,0, 60,2, 56,1, 55,7, 45,8, 43,8, 40,8, 40,2, 36,4, 28,7, 27,5, 25,7, 25,6, 23,3, 22,1, 20,0, 18,1, 17,9, 14,1, 12,4, 12,1, -5,0, -5,1 м.д.
Получение 10: соединение 512 и 513
Промежуточное соединение 2: 203 (1 г, 1,68 ммоль).
Первый элюированный продукт: соединение 513:13С-ЯМР: δ = 167,6, 153,4, 148,1, 143,0, 140,8, 135,2, 125,2, 123,8, 121,5, 116,2, 106,4, 70,0, 67,0, 59,9, 56,6, 56,0, 45,8, 43,8, 40,7, 39,6, 36,4, 28,7, 27,0, 25,7, 25,6, 23,2, 21,8, 20,6, 20,5, 18,1, 17,9, 14,1, 12,1, -4,9, -5,1 м.д.; второй элюированный продукт: соединение 512:13С-ЯМР: δ = 168,5, 153,4, 149,3, 142,9, 138,5, 135,3, 124,9, 123,4, 121,5, 116,3, 106,5, 70,1, 67,0, 60,2, 56,5, 56,0, 45,7, 43,8, 41,1, 39,6, 36,4, 28,7, 27,0, 25,7, 25,6, 23,2, 21, 8, 20,7, 18,0, 17,9, 14,2, 12,4, 12,2, -5,0, -5,1, -5,1 м.д.
Общая методика 3 (получения 11-14) [5→5']
К находящемуся примерно при -70°С раствору сложного эфира 5 (0,34 ммоль) в сухом ТГФ (5 мл) прибавляли DIBAL (1 М в гексане, 1 мл, 1 ммоль). Через 30 минут при той же температуре смеси давали нагреться до температуры -20°С в течение 1 часа, после чего возобновляли охлаждение до -70°С для добавления метанола (0,5 мл), чтобы погасить реакцию. Затем смесь распределяли между водой и этилацетатом и обрабатывали в соответствии со стандартной методикой, приведенной выше, получая спирт 5'.
Получение 11: соединение 510
Промежуточное соединение 5: 508 (0,23 г).
Соединение 510:13С-ЯМР: δ = 153,5, 142,9, 141,2, 135,3, 134,5, 125,4, 123,3, 121,5, 116,3, 106,4, 70,0, 68,6, 67,0, 56,2, 56,1, 45,7, 43,8, 40,4, 40,3, 36,4, 28,7, 27,7, 25,7, 25,6, 23,3, 22,0, 20,4, 18,1, 17,9, 13,9, 12,1, -4,9, -5,1 м.д.
Получение 12: соединение 511
Промежуточное соединение 5: 509 (0,18 г, 0,26 ммоль).
Соединение 511:13С-ЯМР: δ = 153,5, 142,9, 140,8, 135,3, 134,0, 128,3, 122,7, 121,5, 116,3, 106,4, 70,1, 67,0, 61,7, 56,2, 56,1, 45,7, 43,8, 40,3, 36,4, 28,7, 27,6, 25,7, 25,6, 25,4, 23,3, 22,0, 21,2, 20,3, 18,0, 17,9, 12,1, -5,0, -5,1 м.д.
Получение 13: соединение 514
Промежуточное соединение 5: 512 (0,36 г, 0,53 ммоль).
Соединение 514:13С-ЯМР: δ = 153,4, 143,1, 141,6, 135,1, 134,3, 125,4, 123,2, 121,5, 116,2, 106,5, 70,1, 68,6, 67,0, 56,7, 56, 1, 45,8, 43,8, 40,7, 39,6, 36,4, 28,8, 27,1, 25,7, 25,6, 23,2, 21,9, 21,1, 18,0, 17,9, 13,9, 12,1, -5,0, -5,1 м.д.
Получение 14: соединение 515
Промежуточное соединение 5: 513 (0,23 г).
Соединение 515:13С-ЯМР: δ = 153,4, 143,1, 141,3, 135,2, 133,9, 128,3, 122,6, 121,5, 116,2, 106,5, 70,1, 67,0, 61,7, 56,7, 56,1, 45,8, 43,8, 40,6, 39,6, 36,4, 28,8, 27,1, 25,7, 25,6, 23,2, 21,9, 21,2, 21,0, 18,0, 17,9, 12,1, -4,9, -5,1 м.д.
Общая методика 4 (получение 15) [5→ 5']
К находящемуся примерно при -70°С раствору сложного эфира 5 (0,6 ммоль) в сухом ТГФ (5 мл) прибавляли алкиллитий. Спустя час при той же температуре реакцию гасили метанолом (0,5 мл) и распределяли смесь между эфиром и водой. В результате стандартной обработки получали спирт 5.
Получение 15: соединение 516 [5→5']
Промежуточное соединение 5: 508 (0,4 г).
Алкиллитий: этиллитий (0,8 М в диэтиловом эфире, 2 мл).
Соединение 516:13С-ЯМР: δ = 153,5, 143,0, 140,1, 137,3, 135,2, 124,4, 123,8, 121,5, 116,3, 106,4, 78,2, 70,1, 67,0, 56,3, 56,2, 45,8, 43,8, 40,4, 40,3, 36,4, 31,6, 28,8, 27,6, 25,7, 25,6, 23,3, 22,0, 20,4, 18,1, 17,9, 13,3, 12,1, 7,4, -4,9, -5,1 м.д.
Получение 16: соединение 517 [2→5]
К находящемуся примерно при 5°С раствору/суспензии соединения 204 (0,32 г, 0,5 ммоль) и бромида метилтрифенилфосфония (0,59 г, 1,57 ммоль) в сухом ТГФ (5 мл) прибавляли трет-бутилат калия (1 М раствор в ТГФ, 1,4 мл). Через 2 часа при той же температуре смесь распределяли между водой и эфиром и обрабатывали стандартным образом, получая соединение 517, перекристаллизованное из смеси эфир-метанол:13С-ЯМР: δ = 153,5, 147,6, 143,0, 136,8, 135,3, 129,6, 121,5, 116,3, 110,3, 106,4, 70,0, 67,0, 56,3, 45,8, 43,8, 40,3, 40,2, 36,4, 28,8, 27,5, 25,7, 25,6, 23,3, 22,0, 20,4, 18,1, 17,9, 12,6, 12,1, 5,3, 5,2, -5,0, -5,1 м.д.
Получение 17: соединение 518 [2→5]
Тетрабромметан (288, 0,87 ммоль) растворяли в сухом ТГФ (3,6 мл). Добавляли трифенилфосфин (456 мг, 1,74 ммоль) и перемешивали реакционную смесь в течение 30 минут при комнатной температуре. Прибавляли раствор соединения 203 (261 мг; 0,435 ммоль) и триэтиламин (0,06 мл; 0,43 ммоль) в ТГФ (3,2 мл). Реакционную смесь перемешивали 90 минут при комнатной температуре, гасили водой (15 мл) и фильтровали через декалитовый фильтрующий материал. Фильтр промывали пентаном (2×25 мл). Фильтрат экстрагировали водой (3×15 мл) и насыщенным водным раствором хлорида натрия (15 мл), сушили и концентрировали в вакууме. Остаток очищали хроматографией (0,5% эфира в петролейном эфире). 518:13С-ЯМР: δ = 153,4, 145, 7, 142,8, 137,0, 135,3, 124,6, 121,5, 116,3, 106,5, 88,1, 70,1, 67,0, 56,4, 56,0, 45,7, 43,8, 40,8, 39,6, 36,4, 29,5, 28,7, 27,0, 25,7, 25,6, 25,4, 23,1, 21,8, 20,5, 18,1, 17,9, 12,1, -5,0, -5,1 м.д.
Общая методика 5 (получения 18, 19, 20) [6→7→9→10, включая 6→7→8]
К находящемуся примерно при -70°С раствору дихлорпромежуточного соединения 6 (1 ммоль) в сухом ТГФ (5 мл) прибавляли н-бутиллитий (1,33 мл, 1,5 М раствор в гексане, 2 молярных экв.). После этого температуре смеси давали мгновенно подняться до 0°С для гарантии эффективной конверсии в промежуточное литиевое производное 7. В результате гашения распределением между насыщенным раствором хлорида аммония и эфиром и обработки смеси на этой стадии получали промежуточное соединение 8. Альтернативно, возобновляли охлаждение раствора 7 до -70°С и производили добавление карбонильного соединения (1,5 ммоль). Через 30 минут при той же температуре и медленного нагревания до комнатной температуры смесь распределяли между насыщенным раствором хлорида аммония и эфиром и обрабатывали стандартным образом, получая соединение 9.
К находящемуся примерно при 5°С раствору данного промежуточного спирта 9 (приблизительно 0,4 ммоль) в сухом дихлорметане (8 мл) прибавляли сульфуран Мартина (0,54 г, 2 мольных экв.). После перемешивания при той же температуре в течение 1 часа, реакционную смесь распределяли между эфиром и 20%-ным раствором гидроксида натрия. В результате стандартной обработки получали продукт 10.
Получение 18: соединение 1001 через промежуточное соединение 701 и соединение 901
Промежуточное соединение 6: 601 (0,62 г, 0, 97 ммоль).
Карбонильное соединение: изобутиральдегид (0,13 мл).
Соединение 901:13С-ЯМР: δ = 153,5, 142,6, 135,4, 121,4, 116,4, 106,4, 90,4, 80,3, 70, 0, 68,0, 67,0, 55,9, 55,8, 45,6, 43,8, 39,5, 36,4, 34,5, 28,7, 27,6, 26,3, 25,7, 25,6, 23,1, 22,0, 21,4, 18,1, 18,0, 17,9, 17,2, 12,4, -5,0, -5,1 м.д.
Промежуточное соединение 9: 901 (0,27 г).
Продукт 10 дополнительно очищали кристаллизацией из смеси эфир-метанол.
Соединение 1001:13С-ЯМР: δ = 153,4, 146,0, 142,8, 135,3, 121,5, 116, 4, 106,5, 105,4, 96,5, 78,9, 70,1, 67,0, 56,1, 56,0, 45,6, 43,8, 39,6, 36,4, 28,7, 28,4, 26,4, 25,7, 25,6, 24,4, 23,1, 22,1, 21,6, 20,6, 18,1, 17,9, 12,3, -5,0, -5,1, -5,1 м.д.
Получение 19: соединение 801 через промежуточное соединение 701
Промежуточное соединение 6: 601 (0,64 г).
Соединение 801:13С-ЯМР: δ = 153,4, 142,6, 135,4, 121,4, 116,5, 106,5, 89,0, 70,1, 68,4, 67,0, 55,9, 55,5, 45,6, 43,8, 39,6, 36,4, 28,7, 27,6, 26,4, 25,7, 25,6, 23,1, 22,0, 21,2, 18,1, 17,9, 12,1, -4,9, -5,1, -5,1 м.д.
Получение 20: соединение 802 через промежуточное соединение 702
Промежуточное соединение 6: 602 (0,66 г).
Соединение 802:13 С-ЯМР: δ = 153,4, 142,9, 135,3, 121,5, 116,3, 106,5, 89,1, 70,1, 69,0, 67,1, 56,0, 55,4, 45,8, 43,8, 39,5, 36,4, 28,8, 27,3, 25,7, 25,6, 23,2, 21,7, 20,8, 18,1, 17,9, 12,1, -4,9, -5,1, -5,1 м.д.
1-бром-3-гидрокси-3-этилпентин
К раствору 3-гидрокси-3-этил-1-пентина (20 ммоль) в сухом ТГФ (40 мл) при комнатной температуре прибавляли н-бутиллитий (42 ммоль, 1,6 М в гексане) в течение 10 минут. После перемешивания в течение 30 минут раствор охлаждали до -40°С и в течение 20 минут прибавляли раствор брома (1,13 мл, 3,52 г, 22 ммоль) в сухом ТГФ (20 мл), также охлажденный до -40°С, после чего повторно нагревали до 25°С примерно в течение 1 часа. В результате стандартной обработки после добавления эфира и воды (хроматография: 0%-10% эфира в петролейном эфире) получали указанное в заголовке соединение.
1-бром-3-гидрокси-3-метил-1-бутин
При использовании 3-гидрокси-3-метил-1-бутина в качестве исходного соединения в приведенном выше получении продукт представлял собой 1-бром-3-гидрокси-3-метил-1-бутин. Его также получали из 3-гидрокси-3-метил-1-бутина обработкой ацетонового раствора нитратом серебра (0,3 экв.) при комнатной температуре, а затем, через 20 минут, N-бромсукцинимидом (1 мольный эквивалент). Через 12 часов добавляли эфир, раствор фильтровали, а фильтрат обрабатывали стандартным образом, получая масло, которое перегоняли (т.кип. 67°С/18 мм рт.ст.):13С-ЯМР: δ = 31,0, 31,0, 42,6, 66,1, 84,3 м.д.
Общая методика 6 (получения 21-23) [8→10]
К находящемуся примерно при 25°С раствору промежуточного соединения 8 (0,2 ммоль) в сухом пирролидине (5 мл) прибавляли структурное звено боковой цепи (0,8 ммоль; 4 мольных экв.), CuI (4 мг; 0,1 молярного экв.) и дихлорид бис-трифенилфосфинпалладия (7 мг; 0,05 мольного экв.). После перемешивания при той же температуре в течение 17 ч реакционную смесь распределяли между эфиром и насыщенным раствором хлорида аммония и обрабатывали стандартным образом, получая 10.
Получение 21: соединение 1003
Промежуточное соединение 8: 802 (66 мг, 0,11 ммоль).
Структурное звено боковой цепи: 1-бром-3-гидрокси-3-метил-1-бутин (75 мг).
Соединение 1003:13С-ЯМР: δ = 153,4, 142,7, 135,4, 121,4, 116,3, 106,5, 85,6, 80,4, 70,1, 67,2, 67,0, 65,4, 65,2, 55,8, 55, 4, 45,7, 43,8, 39,2, 36,4, 31,0, 28,8, 28,0, 27,1, 25,7, 25,6, 23,3, 21,7, 20,3, 18,1, 17,9, 12,2, -5,0, -5,1, -5,1 м.д.
Получение 22: соединение 1005
Промежуточное соединение 8: 801 (114 мг).
Структурное звено боковой цепи: 1-бром-3-гидрокси-3-этил-1-пентин.
Соединение 1005:13С-ЯМР: δ = 153,4, 142,4, 135,5, 121,4, 116,5, 106,5, 85,0, 78,5, 72,5, 70,1, 69,3, 67,0, 64,9, 55,8, 55,6, 45,7, 43,7, 39,5, 36,4, 34,1, 28,6, 28,3, 26,3, 25,7, 25,6, 23,1, 22,0, 20,7, 18,1, 17,9, 12,2, 8,3, -5, 0, -5,1, -5,1 м.д.
Получение 23: соединение 1007
Промежуточное соединение 8: 802 (118 мг).
Структурное звено боковой цепи: 1-бром-3-гидрокси-3-этил-1-пентин.
Соединение 1007:13С-ЯМР: δ = 153,4, 142,7, 135,4, 121,4, 116,3, 106,5, 85,0, 78,8, 72,5, 70,1, 69,2, 67,0, 65,4, 55,8, 55,4, 45,7, 43,8, 39,2, 36,4, 34,1, 28,8, 27,9, 27,1, 25,7, 25,6, 23,3, 21,7, 20,2, 18,1, 17,9, 12,2, 8,3, -5,0, -5,1, -5,1 м.д.
Получение 24: соединение 536 [2→5]
Тетрабромметан (8789 мг, 2,65 ммоль) растворяли в сухом ТГФ (9 мл). Добавляли трифенилфосфин (1800 мг, 6,8 ммоль) и перемешивали реакционную смесь в течение 30 минут при комнатной температуре. Прибавляли раствор соединения 202 (794 мг, 1,32 ммоль) и триэтиламин (0,18 мл; 1,4 ммоль) в ТГФ (8 мл). Реакционную смесь перемешивали 90 минут при комнатной температуре, гасили насыщенным раствором гидрокарбоната натрия (15 мл) и фильтровали через декалитовый фильтрующий материал. Фильтр промывали пентаном (2×25 мл). Фильтрат экстрагировали водой (3×15 мл) и насыщенным водным раствором хлорида натрия (15 мл), сушили и концентрировали в вакууме. Остаток очищали хроматографией (1,5% эфира в петролейном эфире) и кристаллизовали из смеси эфир-метанол.
Соединение 536:1Н-ЯМР: δ = 6,86 (д, 1H, J=9,9 Гц), 6,45 (д, 1H), 6,02 (дд, 1H, J=9,9 Гц и 15,3 Гц), 5,82 (д, 1H), 5,76 (дд, 1H, J=8,8 Гц и 15,3 Гц), 4,98 (м, 1H), 4,94 (м, 1H), 4,53 (м, 1H), 4,21 (м, 1H), 2,87 (м, 1H), 2,55 (дд, 1H), 2,30 (уш.д, 1H), 2,18 (м, 1H), 2,10-1,00 (м, 13H), 1,07 (д, 3H), 0,89 (с, 9H), 0,86 (с, 9H), 0,56 (с, 3H), 0,08-0,01 (м, 12H) м.д.
Получение 25: соединение 538 [2→5]
Соединение 202 (599 мг, 1 ммоль) и бромтрихлорметан (0,095 мл, 1 ммоль) растворяли в DCM (30 мл) и охлаждали до -20°С. Поддерживая температуру в интервале от -20°С до -10°С, прибавляли по каплям раствор трис(диметиламино)фосфина (0,40 мл, 2,2 ммоль) в DCM (30 мл). После перемешивания в течение 30 минут при комнатной температуре добавляли пентан (150 мл) и воду (30 мл). Органический слой отделяли, промывали водой (3×25 мл) и насыщенным водным раствором хлорида натрия (25 мл), сушили, концентрировали в вакууме и очищали хроматографией (1% эфира в петролейном эфире).
Соединение 538:1Н-ЯМР: δ = 6,45 (д, 1H), 6,34 (д, 1Н, J=10,3 Гц), 6,10 (дд, 1Н, J=10,3 Гц и 15,0 Гц), 5,82 (д, 1H), 5,69 (дд, 1Н, J=8,8 Гц и 15,0 Гц), 4,98 (м, 1H), 4,94 (м, 1H), 4,53 (м, 1H), 4,21 (м, 1H), 2,87 (м, 1H), 2,55 (дд, 1H), 2,30 (уш.д, 1H), 2,19 (м, 1H), 2,10-1, 13 (м, 13H), 1,07 (д, 3H), 0,89 (с, 9H), 0,86 (с, 9H), 0,56 (с, 3H), 0,08-0,02 (м, 12H) м.д.
Получение 26: соединение 540 [2→5]
Бромид циклобутилтрифенилфосфония (516 мг, 1,3 ммоль) суспендировали в сухом ТГФ (4,5 мл) и охлаждали до -6°С. Прибавляли раствор н-бутиллития (1,6 М в гексане, 1,0 мл, 1,6 ммоль) и перемешивали реакционную смесь в течение 20 минут при комнатной температуре, а затем вновь охлаждали до -6°С. Прибавляли раствор соединения 205 (400 мг, 0,65 ммоль) и трис(2-(2-метоксиэтокси)этил)амина (42 мкл, 0,13 ммоль) и перемешивали реакционную смесь при комнатной температуре в течение 3 часов. Добавляли воду (20 мл) и петролейный эфир (100 мл). Органический слой отделяли, промывали водой (3× 20 мл) и насыщенным водным раствором хлорида натрия (20 мл), сушили, концентрировали в вакууме и очищали хроматографией (0,5% эфира в петролейном эфире).
Соединение 540:1 Н-ЯМР: δ = 6,46 (д, 1H), 6,00 (д, 1Н, J=15,7 Гц), 5,81 (д, 1H), 5,33 (дд, 1Н, J=8,8 Гц и 15,7 Гц), 4,98 (т, 1H), 4,93 (т, 1H), 4,53 (м, 1H), 4,21 (м, 1H), 2,87 (м, 1H), 2,73 (м, 4H), 2,55 (дд, 1H), 2,30 (м, 1H), 2,22-1,00 (м, 16H), 1,56 (уш.с, 3H), 1,05 (д, 3H), 0,89 (с, 9H), 0,86 (с, 9H), 0,56 (с, 3H), 0,10-0,02 (м, 12H) м.д.
Получение 27: соединение 542
Соль алкилтрифенилфосфония: бромид циклопентилтрифенилфосфония (1,40 г, 3,4 ммоль)
Промежуточное соединение 2: 202 (1 г, 1,67 ммоль).
Очистка соединения 542 хроматографией (2% об.:об., эфир в петролейном эфире).
Соединение 542:1Н-ЯМР: δ = 6,45 (д, 1H), 6,02 (дд, 1Н, J=11,1 Гц и 14,9 Гц), 5,87 (м, 1H), 5,81 (д, 1H), 5,37 (дд, 1Н, J=8,8 Гц и 11,1 Гц), 4,98 (т, 1H), 4,94 (т, 1H), 4,53 (м, 1H), 4,21 (м, 1H), 2,87 (м, 1H), 2,55 (дд, 1H), 2,37-2,24 (м, 5H), 2,20-1,86 (м, 4H), 1,83-0,80 (м, 14H), 1,05 (д, 3H), 0,90 (с, 9H), 0,86 (с, 9H), 0,56 (с, 3H), 0,08-0,03 (м, 12H) м.д.
Получение 28: соединение 544
Соль алкилтрифенилфосфония: бромид циклогексилтрифенилфосфония (1,44 г, 3,4 ммоль)
Промежуточное соединение 2: 202 (1 г, 1,67 ммоль).
Очистка соединения 544 хроматографией (2% об.:об., эфир в петролейном эфире).
Соединение 544:1Н-ЯМР: δ = 6,45 (д, 1H), 6,20 (дд, 1Н, J=10,7 Гц и 14,9 Гц), 5,81 (д, 1H), 5,70 (д, 1Н, J=10,7 Гц), 5,43 (дд, 1Н, J=8,4 Гц и 14,9 Гц), 4,97 (м, 1H), 4,93 (м, 1H), 4,53 (м, 1H), 4,21 (м, 1H), 2,86 (м, 1H), 2,56 (дд, 1H), 2,35-0,80 (м, 25H), 1,04 (д, 3H), 0,89 (с, 9H), 0,86 (с, 9H), 0,56 (с, 3H), 0,08-0,02 (м, 12H) м.д.
Получение 29: соединение 546
Соль алкилтрифенилфосфония: бромид циклопропилтрифенилфосфония (766 мг, 2 ммоль)
Промежуточное соединение 1: соединение 103 (573 мг, 1 ммоль).
При очистке хроматографией (2% об.:об., эфир в петролейном эфире) получали 1(S),3(R)-бис(трет-бутилдиметилсилилокси)-20(R)-циклопропилиденметил-9, 10-секопрегна-5(Е),7(Е),10(19)-триен (соединение 546).
Соединение 546:13С-ЯМР: δ = 153,4, 143,3, 135,0, 125,0, 121,6, 117,7, 116,1, 106,4, 70,1, 67,0, 56,8, 56,0, 45, 7, 43,8, 39,7, 39,6, 36,4, 28,8, 27,1, 25,7, 25,6, 23,3, 21,9, 20,7, 18,0, 17,9, 12,2, 1,8, 1,7, -4,9, -5,0, -5,1, -5,1 м.д.
Получение 30: соединение 548
Соль алкилтрифенилфосфония: бромид циклопропилтрифенилфосфония (606 мг, 1,6 ммоль)
Промежуточное соединение 1: соединение 101 (458 мг, 0,8 ммоль).
При очистке хроматографией (2% об:об, эфир в петролейном эфире) получали 1(S),3(R)-бис(трет-бутилдиметилсилилокси)-20(S)-циклопропилиденметил-9,10-секопрегна-5(Е),7(Е),10(19)-триен (соединение 548).
Соединение 548:13С-ЯМР: δ = 153,4, 143,2, 135,1, 124,4, 121,6, 118,2, 116,2, 106,4, 70,1, 67,0, 56,6, 56,3, 45,7, 43,8, 40,2, 39,6, 36,4, 28,8, 27,4, 25,7, 25,6, 23,4, 22, 1, 20,3, 18,1, 17,9, 12,0, 2,2, 1,7, -4,9, -5,0, -5,1 м.д.
Получение 31: соединение 550
К находящемуся примерно при -70°С раствору литиевого производного 302 (полученного из предшественника 24-дифенилфосфиноил-1(S),3(R)-ди-TBS-окси-9,10-секохола-5(Е),7(Е),10(19),22(Е)-тетраена (0,21 г, 0,27 ммоль) и н-бутиллития (0,55 мл) в сухом ТГФ (2 мл)), прибавляли по каплям раствор диэтилкетона (0,03 мл) в сухом ТГФ (0,3 мл). После перемешивания при той же температуре в течение 30 минут реакционную смесь выдерживали при комнатной температуре в течение 2 часов, затем гасили сырым ТГФ, распределяли между эфиром и водой и обрабатывали стандартным образом, получая соединение 550:
1Н-ЯМР: δ (CDCl3) = 6,45 (д, 1H), 6,18 (дд, 1H), 5,81 (д, 1H), 5,71 (д, 1H), 5,43 (дд, 1H), 4,98 (м, 1H), 4,93 (м, 1H), 4,53 (м, 1H), 4,21 (м, 1H), 2,87 (д, 1H), 2,54 (дд, 1H), 2,30 (уш.д, 1H), 2, 20-1,10 (м, 18H), 1,05 (д, 3H), 1,00 (м, 6H), 0,88 (с, 9H), 0,86 (с, 9H), 0,56 (с, 3H), 0,05 (уш.с, 12H) м.д.
Получение 32: соединение 303
Раствор 24-дифенилфосфиноил-1(S),3(R)-ди-TBS-окси-9,10-секохола-5(Е),7(Е),10(19),22(Е)-тетраена (см. получение 33) (2,4 г, 3,1 ммоль) в DCM (5 мл) быстро охлаждали на бане с сухим льдом для прибавления жидкой двуокиси серы (10 мл). Смесь перемешивали при кипении (охлаждаемый сухим льдом пальчиковый холодильник) без дальнейшего охлаждения в течение 30 минут, после чего растворители удаляли в вакууме и кристаллизовали продукт из эфира, получая основного изомера аддукта 24-дифенилфосфиноил-1(S),3(R)-ди-TBS-окси-9,10-секохола-5(Е),7(Е),10(19),22(Е)-тетраена и двуокиси серы:
1 Н-ЯМР: δ (CDCl3) = 7,80-7,65 (м, 4H), 7,55-7,40 (м, 6H), 5,34 (м, 2H), 4,60 (м, 2H), 4,36 (м, 1H), 4,18 (м, 1H), 3,92 (м, 1H), 3,58 (уш.д, 1H), 3,04 (м, 2H), 2,56 (м, 1H), 2,14 (уш.д, 1H), 2,05-1,00 (м, 15H), 0,88 (д, 3H), 0,87 (уш.с, 18H), 0,55 (с, 3H), 0,05 (уш.с, 12H) м.д.
К находящемуся примерно при 5°С раствору данного аддукта (1,8 г, 2,1 ммоль) в сухом DCM (30 мл) при перемешивании прибавляли по каплям эфират трехфтористого бора (1,2 мл). Через 16 часов при 3-5°С добавляли 5%-ный водн. раствор гидрокарбоната натрия, затем разбавляли эфиром и осуществляли стандартную обработку (хроматография: 25% об.:об. ацетона в DCM), получая в качестве основного продукта один изомер аддукта 24-дифенилфосфиноил-3(R)-гидрокси-1(S)-TBS-окси-9, 10-секохола-5(Е),7(Е),10(19),22(Е)-тетраена с двуокисью серы:
1Н-ЯМР: δ (CDCl3) = 7,75-7,67 (м, 4H), 7,48-7,42 (м, 6H), 5,34 (м, 2H), 4,68 (м, 2H), 4,36 (уш.т, 1H), 4,21 (м, 1H), 3,92 (уш.д, 1H), 3,58 (уш.д, 1H), 3,04 (м, 2H), 2,57 (м, 1H), 2,24 (уш.д, 1H), 2,00-0,95 (м, 16H), 0,89 (д, 3H), 0,87 (с, 9H), 0,54 (с, 3H), 0,08 (с, 3H), 0,07 (с, 3H) м.д.
Находящийся примерно при 5°С раствор данного спирта (0,61 г, 0,84 ммоль) в сухом DCM (10 мл) при перемешивании обрабатывали перйодинаном Десс-Мартина (0,5 г). Через 30 минут добавляли 5%-ный водн. раствор гидрокарбоната натрия и 10%-ный раствор тиосульфата натрия и продолжали перемешивание в течение 10 минут, затем разбавляли эфиром и осуществляли стандартную обработку (хроматография: 25% об.:об. ацетон в DCM), получая один изомер аддукта 24-дифенилфосфиноил-3-оксо-1(S)-TBS-окси-9,10-секохола-5(Е),7(Е),10(19),22(Е)-тетраена с двуокисью серы. Данный кетон (0,53 г, 0,72 ммоль) растворяли в смеси ТГФ-метанол (2+5 мл) и обрабатывали боргидридом натрия (43 мг) при перемешивании на бане со льдом. По завершении восстановления (15 минут) реакционную смесь распределяли между этилацетатом и водой. В результате стандартной обработки (без хроматографии) получали 3(S)-гидроксисоединение с примесью небольшого количества уже описанного 3(R)-гидроксисоединения. Продукт нагревали при кипении в смеси толуол (10 мл)/вода (10 мл), содержащей суспендированный гидрокарбонат натрия (1,2 г) в течение 1 часа. После охлаждения, распределения между эфиром и водой и последующей стандартной обработки (без хроматографии) получали 24-дифенилфосфиноил-3(S)-гидрокси-1(S)-TBS-окси-9,10-секохола-5(Е),7(Е),10(19),22(Е)-тетраен с примесью небольшого количества 3(R)-гидроксисоединения. Продукт подвергали способу общей методики 7 (без хроматографии) с использованием 9-ацетилантрацена (0,02 г) и DCM, получая 5(Z)-изомер. К охлажденному льдом раствору данного продукта в сухом DCM (10 мл) и 2,6-лутидина (0,2 мл) при перемешивании прибавляли TBS трифлат (0,3 мл) и после оставления для взаимодействия на 1 час смесь распределяли между водой и эфиром и обрабатывали стандартным способом (хроматография: 25% об.:об. ацетона в DCM), получая 24-дифенилфосфиноил-1(S),3(S)-ди-TBS-окси-9,10-секохола-5(Е),7(Е),10(19),22(Е)-тетраен:
1Н-ЯМР: δ (CDCl3) = 7,80-7,65 (м, 4H), 7,50-7,40 (м, 6H), 6,23 (д, 1H), 5,94 (д, 1H), 5,37 (уш.т, 1H), 5,34 (м, 2H), 4,91 (уш.т, 1H), 3,93 (м, 1H), 3,68 (м, 1H), 3,05 (м, 2H), 2,78 (дд, 1H), 2,41 (уш.д, 1H), 2,25-0,90 (м, 15H), 0,93 (с, 9H), 0,87 (с, 9H), 0,86 (д, 3H), 0,46 (с, 3H), 0,10 (с, 3H), 0,07 (с, 3H), 0,06 (с, 3H), 0,05 (с, 3H) м.д.
Литиевое производное 303 получали, как полагается, из данного предшественника, добавлением по каплям н-бутиллития (1,6 М в гексане, 1 молярный экв.) при перемешивании к раствору в сухом ТГФ, находящемуся примерно при -70°С, и выдерживании при той же температуре в течение 15 минут.
Получение 33: соединение 302
К раствору 1(S), 3(R)-ди-TBS-окси-9,10-секохола-5(Е),7(Е),10(19),22(Е)-тетраен-24-ола (1,17 г, 1,94 ммоль) в сухом ТГФ (15 мл) при комнатной температуре добавляли трифосген (0,43 г), а затем по каплям пиридин (0,5 мл). Через 90 минут при той же температуре смесь распределяли между водой и эфиром и обрабатывали стандартным образом (хроматография: 1% об.:об. эфира в петролейном эфире), получая 24-хлор-1(S), 3(R)-ди-TBS-окси-9,10-секохола-5(Е),7(Е),10(19),22(Е)-тетраен:
13С-ЯМР: δ (CDCl3) = 153,5, 142,8, 141,8, 135,4, 123,5, 121,5, 116,4, 106,4, 70,0, 67,0, 56, 2, 55,7, 45,7, 45,5, 43,8, 40,2, 39,6, 36,4, 28,7, 27,4, 25,7, 25,6, 23,3, 22,0, 19,9, 18,1, 17,9, 12,1, -5,0, -5,1 м.д.
К находящемуся примерно при -70°С раствору данного хлорида (0,81 г) в сухом ТГФ (7 мл) при перемешивании прибавляли по каплям раствор дифенилфосфида лития (0,4 М в сухом ТГФ, 3,5 мл). После этого прибавляли несколько капель воды, затем нагревали до комнатной температуры и концентрировали в вакууме, получая масло. Его растворяли в DCM (15 мл) и энергично перемешивали с 5%-ной перекисью водорода (водн., 12 мл) в течение 30 минут. Смесь распределяли между водой и эфиром и обрабатывали стандартным образом (хроматография: 66% об.:об. этилацетата в петролейном эфире), получая 24-дифенилфосфиноил-1(S),3(R)-ди-TBS-окси-9,10-секохола-5(Е), 7(Е),10(19),22(Е)-тетраен:
1Н-ЯМР: δ (CDCl3) = 7,8-7,6 (м, 4H), 7,5-7,4 (м, 6H), 6,42 (д, 1H), 5,77 (д, 1H), 5,45-5,25 (м, 2H), 4,96 (уш.с, 1H), 4,92 (уш.с, 1H), 4,52 (м, 1H), 4,20 (м, 1H), 3,07 (д, 1H), 3,02 (д, 1H), 2,84 (уш.д, 1H), 2,55 (дд, 1H), 2,27 (уш.д, 1H), 2,05-0,90 (м, 14H), 0,88 (с, 9H), 0,87 (д, 3H), 0,86 (с, 9H), 0,47 (с, 3H), 0,05 (с, 12H) м.д.
Литиевое производное 302 получали, как полагается, из данного предшественника добавлением по каплям н-бутиллития (1,6 М в гексане, 1 молярный экв.) при перемешивании к раствору в сухом ТГФ, находящемуся примерно при -70°С, и выдерживании при той же температуре в течение 15 минут.
Получение 34: соединение 534
К находящемуся примерно при -70°С раствору литиевого производного 302 (полученного из предшественника 24-дифенилфосфиноил-1(S),3(R)-ди-TBS-окси-9,10-секохола-5(Е),7(Е),10(19),22(Е)-тетраена (0,71 г, 0,88 ммоль) и н-бутиллития (0,55 мл) в сухом ТГФ (8 мл) прибавляли по каплям раствор гексафторацетона (1 мл приблизительно 1 М раствора в сухом ТГФ). После перемешивания при той же температуре в течение 4 часов реакционную смесь выдерживали при комнатной температуре в течение 4 часов, затем гасили сырым ТГФ, распределяли между эфиром и водой и обрабатывали стандартным образом (хроматография: 5% об:об эфира в петролейном эфире), получая соединение 534:
13С-ЯМР: δ (CDCl3) = 157,3, 153,5, 142,3, 142,2, 135,6, 121,5, 121,4, 121,3, 120,5, 116,6, 106, 5, 70,0, 67,0, 56,0, 55,3, 46,0, 43,8, 40,9, 40,2, 36,4, 28,7, 27,4, 25,7, 25,6, 23,2, 22,1, 19,4, 18,1, 17,9, 12,1, -4,9, -5,0, -5,1, -5,1 м.д.
Получение 35: соединение 205 [1→2]
Смесь соединения 101 (5,00 г, 8,7 ммоль), 1-(трифенилфосфоранилиден)-2-пропанона (8,32 г, 26,1 ммоль) и толуола (100 мл) перемешивали в течение 18 часов при 110°С. Реакционную смесь охлаждали до комнатной температуры, фильтровали и концентрировали в вакууме. Остаток растворяли в пентане (75 мл), перемешивали в течение 45 минут при комнатной температуре и фильтровали через декалитовый фильтрующий материал. Фильтрат концентрировали в вакууме и очищали хроматографией (0-5% об.:об. эфира в петролейном эфире).
Соединение 205:1Н-ЯМР: δ = 6,66 (дд, 1Н, J=8,8 Гц и 16,1 Гц), 6,44 (д, 1H), 6,00 (д, 1Н, 3=16,1 Гц), 5,81 (д, 1H), 4,98 (м, 1H), 4,93 (м, 1H), 4,53 (м, 1H), 4,21 (м, 1H), 2,88 (м, 1H), 2,54 (дд, 1H), 2,38-2,16 (м, 2H), 2,22 (с, 3H), 2,10-1,85 (м, 3H), 1,82-1,18 (м, 10H), 1,11 (д, 3H), 0,89 (с, 9H), 0,86 (с, 9H), 0,57 (с, 3H), 0,08-0,02 (м, 12H).
Общая методика 7 (получения 101-126, 128) [a→b (B = CH2)]
Раствор промежуточного соединения 5Е-витамина D типа а (0,1 ммоль), триплетного сенсибилизатора (0,01 г) и триэтиламина (0,05 мл) в растворителе (5 мл) в пирексовой колбе облучали светом ультрафиолетовой лампы высокого давления, тип TQ180Z2 (Hanau) примерно при 20°С в течение 30 минут (время пропорционально масштабировали в соответствии с количеством промежуточного соединения а). Реакционную смесь (после фильтрования в случае использования антрацена) частично концентрировали в вакууме и очищали хроматографией, получая продукт промежуточного соединения типа b.
Получение 101: соединение 519
Промежуточное соединение типа а: 501 (1,29 г, 2,06 ммоль).
Сенсибилизатор: антрацен (0,65 г).
Растворитель: DCM (100 мл).
Облучение: использовали лампу TQ718Z2 в течение 30 минут.
Соединение 519:1Н-ЯМР: δ = 6,23 (д, 1H), 6,13 (дд, 1Н, 3=11,1 Гц и 14,9 Гц), 6,00 (д, 1H), 5,75 (д, 1Н, J=11,1 Гц), 5,40 (дд, 1Н, J=8,8 Гц и 14,9 Гц), 5,17 (м, 1H), 4,85 (м, 1H), 4, 36 (м, 1H), 4,18 (м, 1H), 2,82 (м, 1H), 2,44 (дд, 1H), 2,21 (дд, 1H), 2,11 (м, 1H), 1,74 (уш.с, 3H), 1,73 (уш.с, 3H), 2,03-1,14 (м, 13H), 1,04 (д, 3H), 0,87 (с, 18H), 0,55 (с, 3H), 0,05 (м, 12H) м.д.
Получение 102: соединение 521
Промежуточное соединение типа а: 502 (63 мг).
Сенсибилизатор: 9-ацетилантрацен.
Растворитель: DCM.
Соединение 521:1Н-ЯМР в соответствии со структурой.
Получение 103: соединение 523
Промежуточное соединение типа а: 503 (0,38 г).
Сенсибилизатор: антрацен (0,32 г).
Растворитель: DCM.
Очистка соединения 523 хроматографией (0,5% об.:об., эфир в петролейном эфире).
Соединение 523:1Н-ЯМР: δ = 6,22 (д, J=11,2 Гц, 1H), 6,11 (дд, 3=14,9 Гц, J=10,7 Гц, 1H), 6,00 (д, J=11,2 Гц, 1H), 5,76 (д, J=10,7 Гц, 1H), 5,41 (дд, J=9,6 Гц, J=14,9 Гц, 1H), 5,17 (м, 1H), 4,86 (м, 1H), 4,36 (м, 1H), 4,18 (м, 1H), 2,80 (м, 1H), 2,43 (дд, J=3,8 Гц, J=13,0 Гц, 1H), 2,20 (дд, J=7,5 Гц, J=13,0 Гц, 1H), 2,15-1,0 (м, 14H), 1,75 (уш.с, 3H), 1,72 (уш.с, 3H), 0,93 (д, J=6,5 Гц, 3H), 0,87 (с, 9H), 0,86 (с, 9H), 0,49 (с, 3H), 0,05 (уш.с, 12H) м.д.
Получение 104: соединение 524
Промежуточное соединение типа а: 504 (61 мг).
Сенсибилизатор: антрацен (0,05 г).
Растворитель: DCM.
Очистка соединения 524 хроматографией (0-2% об.:об., эфир в петролейном эфире).
Соединение 524:1Н-ЯМР: δ = 6,33 (уш.д, J=10,3 Гц, 1H), 6,22 (д, J=11,2 Гц, 1H), 6,11 (дд, J=10,3 Гц, J=15,3 Гц, 1H), 6,01 (д, J=11,2 Гц, 1H), 5,55 (дд, J=15,3 Гц, J=8,8 Гц, 1H), 5,17 (уш.с, 1H), 4,86 (уш.с, 1H), 4,18 (м, 1H), 2,81 (м, 1H), 2,44 (м, 1H), 2,25-1,0 (м, 20H), 1,06 (д, J=6,8 Гц, 3H), 0,87 (с, 18H), 0,55 (с, 3H), 0,05 (уш.с, 12H) м.д.
Получение 105: соединение 525
Промежуточное соединение типа а: 505 (0,24 г).
Сенсибилизатор: антрацен (0,23 г).
Растворитель: DCM.
Очистка соединения 525 хроматографией (0-2% об.:об., эфир в петролейном эфире).
Соединение 525:1Н-ЯМР: δ = 6,35 (уш.д, J=10,3 Гц, 1H), 6,22 (уш.д, J=11,5 Гц, 1H), 6,08 (дд, J=10,3 Гц, J=15,4 Гц, 1H), 6,00 (д, J=11,5 Гц, 1H), 5,55 (дд, J=9,4 Гц, J=15,4 Гц, 1H), 5,17 (уш.д, 1H), 4,86 (уш.д, 1H), 4,36 (м, 1H), 4,18 (м, 1H), 2,80 (уш.д, J=12,2 Гц, 1H), 2,43 (дд, J=3,6, J=13,0 Гц, 1H), 2,20 (дд, J=7,3 Гц, J=13,0 Гц, 1H), 2,15-1,0 (м, 18H), 0,97 (д, J=6,8 Гц, 3H), 0,87 (с, 9H), 0,87 (с, 9H), 0,50 (с, 3H), 0,05 (уш.с, 12H) м.д.
Получение 106: соединение 526
Промежуточное соединение типа а: 506 (0,4 г).
Сенсибилизатор: антрацен (0,34 г).
Растворитель: DCM.
Очистка соединения 526 хроматографией (0-2% об.:об., эфир в петролейном эфире).
Соединение 526:1Н-ЯМР: δ = 6,22 (д, J=11, 2 Гц, 1H), 6,00 (д, J=11,2 Гц, 1H), 5,84 (дд, J=15 Гц, J=10,7 Гц, 1H), 5,65 (м, 1H), 5,34 (дд, J=15 Гц, 3=8,7 Гц, 1H), 5,17 (уш.с, 1H), 4,85 (уш.с, 1H), 4,36 (м, 1H), 4,18 (м, 1H), 2,69 (м, 5H), 2,44 (м, 1H), 2,25-1,10 (м, 17H), 1,03 (д, J=6,7 Гц, 3H), 0,87 (с, 18H), 0,54 (с, 3H), 0,05 (уш.с, 12H) м.д.
Получение 107: соединение 527
Промежуточное соединение типа а: 507 (0,38 г).
Сенсибилизатор: антрацен (0,32 г).
Растворитель: DCM.
Очистка соединения 527 хроматографией (0,5% об.:об., эфир в петролейном эфире).
Соединение 527:13С-ЯМР: δ = 148,2, 142,3, 140,9, 137,5, 134,7, 123,5, 123,0, 120,9, 117,6, 110,9, 71,9, 67,3, 56,7, 56,0, 45,8, 45,7, 44, 6, 40,6, 39,7, 31,0, 29,7, 28,7, 27,1, 25,7, 25,6, 23,2, 21,8, 21,3, 18,0, 17,9, 16,9, 12,0, -4,9, -5,0, -5,3 м.д.
Получение 108: соединение 528
Промежуточное соединение типа а: 510 (0,15 г).
Сенсибилизатор: 9-ацетилантрацен (0,02 г).
Растворитель: DCM.
Соединение 528:1Н-ЯМР в соответствии со структурой.
Получение 109: соединение 529
Промежуточное соединение типа а: 511 (24 мг, 0,04 ммоль).
Сенсибилизатор: 9-ацетилантрацен.
Растворитель: толуол.
Соединение 529:1Н-ЯМР в соответствии со структурой.
Получение 110: соединение 530
Промежуточное соединение типа а: 514 (125 мг, 0,2 ммоль).
Сенсибилизатор: 9-ацетилантрацен.
Растворитель: DCM.
Соединение 530:1Н-ЯМР в соответствии со структурой.
Получение 111: соединение 531
Промежуточное соединение типа а: 515 (17 мг).
Сенсибилизатор: антрацен (0,01 г).
Растворитель: толуол (2 мл).
Соединение 531:1Н-ЯМР в соответствии со структурой.
Получение 112: соединение 532
Промежуточное соединение типа а: 516 (90 мг).
Сенсибилизатор: 9-ацетилантрацен.
Растворитель: DCM.
Соединение 532:1Н-ЯМР в соответствии со структурой.
Получение 113: соединение 533
Промежуточное соединение типа а: 517 (0, 10 г, 0,16 ммоль).
Сенсибилизатор: 9-ацетилантрацен.
Растворитель: DCM.
Соединение 533:1Н-ЯМР: δ = 6,23 (д, 1H), 6,03 (д, 1Н, J=15,6 Гц), 6,01 (д, 1H), 5,88 (дд, 1Н, J=8,4 Гц и 15,6 Гц), 5,17 (м, 1H), 4,86 (м, 1H), 4,78 (м, 1H), 4,72 (м, 1H), 4,37 (м, 1H), 4,18 (м, 1H), 2,83 (м, 1H), 2,45 (дд, 1H), 2,30-2,06 (м, 2H), 2,05-1,95 (м, 2H), 1,07 (д, 3H), 0,87 (с, 18H), 1,93-0,80 (м, 12H), 0,67 (м, 2Н), 0,56 (с, 3H), 0,41 (м, 2Н), 0,05 (м, 6H), 0,04 (м, 6H) м.д.
Получение 114: соединение 520
Промежуточное соединение типа а: 518 (57 мг).
Сенсибилизатор: антрацен (0,05 г).
Растворитель: DCM.
Очистка соединения 520 хроматографией (0,5% об.:об., эфир в петролейном эфире).
Соединение 520:1Н-ЯМР: δ = 6,87 (д, J=9,9 Гц, 1H), 6,22 (д, J=11,2 Гц, 1H), 6,00 (д, J=11,2 Гц, 1H), 6,01 (дд, J=9,9 Гц, J=15,3 Гц, 1H), 5,81 (дд, J=15,3 Гц, J=9,5 Гц, 1H), 5,17 (уш.м, 1H), 4,85 (уш.м, 1H), 4,36 (м, 1H), 4,19 (м, 1H), 2,81 (уш.м, 1H), 2,44 (дд, 1H), 2,2-1,0 (м, 15H), 0,95 (д, J=6,6 Гц, 3H), 0,87 (уш.с, 18H), 0,50 (с, 3H), 0,05 (уш.с, 12H) м.д.
Получение 115: соединение 1002
Промежуточное соединение типа а: 1001 (104 мг, 0,17 ммоль).
Сенсибилизатор: 9-ацетилантрацен.
Растворитель: метил-трет-бутиловый эфир
Соединение 1002:1Н-ЯМР в соответствии со структурой.
Получение 116: соединение 1004
Промежуточное соединение типа а: 1003 (41 мг).
Сенсибилизатор: 9-ацетилантрацен (10 мг).
Растворитель: толуол (4 мл).
Соединение 1004:1Н-ЯМР: δ = 6,23 (д, 1H), 6,00 (д, 1H), 5,17 (м, 1H), 4,85 (м, 1H), 4,37 (м, 1H), 4,18 (м, 1H), 2,82 (м, 1H), 2,44 (дд, 1H), 1,52 (с, 6H), 1,17 (д, 3H), 0,87 (с, 18H), 2,38-0,80 (м, 16H), 0,56 (с, 3H), 0,05 (с, 6H), 0,04 (с, 6H) м.д.
Получение 117: соединение 1006
Промежуточное соединение типа а: 1005 (70 мг, 0,1 ммоль).
Сенсибилизатор: антрацен (80 мг).
Растворитель: DCM.
Соединение 1006:13С-ЯМР: δ = 148,1, 140,0, 135,2, 122,8, 118,0, 111,0, 85,1, 78,4, 72,5, 71,7, 69,3, 67,3, 64,8, 55,7, 55,5, 45,8, 45,5, 44,6, 39,5, 34,1, 28,6, 28,3, 26,4, 25,6, 25,6, 23,0, 21,9, 20,7, 18,0, 17,9, 12,2, 8,3, -4,9, -5,0, -5,3 м.д.
Получение 118: соединение 1008
Промежуточное соединение типа а: 1007 (68 мг, 0,1 ммоль).
Сенсибилизатор: 9-ацетилантрацен.
Растворитель: DCM.
Соединение 1008:1Н-ЯМР: δ = 6,23 (д, 1H), 6,00 (д, 1H), 5,17 (м, 1H), 4,85 (м, 1H), 4,37 (м, 1H), 4,18 (м, 1H), 2,83 (м, 1H), 2,44 (дд, 1H), 1,17 (д, 3H), 1,03 (т, 6H), 0,87 (с, 18H), 2,38-0,80 (м, 20H), 0,56 (с, 3H), 0,05 (м, 6H), 0,04 (м, 6H) м.д.
Получение 119: соединение 537
Промежуточное соединение типа а: 536 (150 мг).
Сенсибилизатор: антрацен (0,112 г).
Растворитель: DCM.
Очистка соединения 537 хроматографией (0-2% об.:об., эфир в петролейном эфире).
Соединение 537:1Н-ЯМР в соответствии со структурой.
Получение 120: соединение 539
Промежуточное соединение типа а: 538 (76 мг).
Сенсибилизатор: антрацен (60 мг).
Растворитель: DCM.
Очистка соединения 539 хроматографией (0-2% об.:об., эфир в петролейном эфире).
Соединение 539:1Н-ЯМР: δ = 6,34 (д, 1Н, J=10,3 Гц), 6,22 (д, 1H), 6,09 (дд, 1Н, J=10,3 Гц и 14,9 Гц), 6,01 (д, 1H), 5,69 (дд, 1Н, J=8,8 Гц и 14,9 Гц), 5,17 (м, 1H), 4,85 (д, 1H), 4,36 (м, 1H), 4,18 (м, 1H), 2,82 (м, 1H), 2,44 (дд, 1H), 2,25-2,10 (м, 2H), 2,05-1,10 (м, 13H), 1,06 (д, 3H), 0,87 (с, 9H), 0,87 (с, 9H), 0,55 (с, 3H), 0,07-0,03 (м, 12H) м.д.
Получение 121: соединение 541
Промежуточное соединение типа а: 540 (120 мг).
Сенсибилизатор: антрацен (115 мг).
Растворитель: DCM.
Очистка соединения 541 хроматографией (0-2% об.:об., эфир в петролейном эфире).
Соединение 541:1Н-ЯМР: δ = 6,23 (д, 1H), 6,00 (д, 1H), 5,99 (д, 1Н, J=15,6 Гц), 5,33 (дд, 1Н, J=8,8 Гц и 15,6 Гц), 5,17 (м, 1H), 4,85 (уш.д, 1H), 4,36 (м, 1H), 4,18 (м, 1H), 2,87-2,60 (м, 5H), 2,44 (дд, 1H), 2,21 (дд, 1H), 2,16-1,10 (м, 16H), 1,55 (уш.с, 3H), 1,04 (д, 3H), 0,87 (уш.с, 18H), 0,55 (с, 3H), 0,07-0,03 (м, 12H) м.д.
Получение 122: соединение 543
Промежуточное соединение типа а: 542 (300 мг).
Сенсибилизатор: антрацен (200 мг).
Растворитель: DCM.
Очистка соединения 543 хроматографией (0-2% об.:об., эфир в петролейном эфире).
Соединение 543:1Н-ЯМР: δ = 6,23 (д, 1H), 6,01 (д, 1H), 6,01 (дд, 1H, J=11,1 Гц и 14,9 Гц), 5,86 (м, 1H), 5, 36 (дд, 1Н, J=8,8 Гц и 14,9 Гц), 5,16 (м, 1H), 4,85 (д, 1H), 4,36 (м, 1H), 4,18 (м, 1H), 2,82 (м, 1H), 2,44 (дд, 1H), 2,37-0,80 (м, 23H), 1,04 (д, 3H), 0,87 (с, 18H), 0,55 (с, 3H), 0,07-0,03 (м, 12H) м.д.
Получение 123: соединение 545
Промежуточное соединение типа а: 544 (214 мг).
Сенсибилизатор: антрацен (150 мг).
Растворитель: DCM.
Очистка соединения 543 хроматографией (0-2% об.:об., эфир в петролейном эфире).
Соединение 545:1Н-ЯМР: δ = 6,23 (д, 1H), 6,19 (дд, 1Н, J=10,7 Гц и 14,9 Гц), 6,00 (д, 1H), 5,69 (д, 1Н, J=10,7 Гц), 5,43 (дд, 1Н, J=8,4 Гц и 14,9 Гц), 5,17 (м, 1H), 4,85 (д, 1H), 4,36 (м, 1H), 4,18 (м, 1H), 2,81 (м, 1H), 2,44 (дд, 1H), 2, 32-0,80 (м, 25H), 1,04 (д, 3H), 0,87 (с, 18H), 0,54 (с, 1H), 0,07-0,03 (м, 12H) м.д.
Получение 124: соединение 547
Промежуточное соединение типа а: 546 (217 мг).
Сенсибилизатор: антрацен (214 мг).
Растворитель: DCM.
В результате очистки хроматографией (0-2% об.:об., эфир в петролейном эфире) получали 1(S),3(R)-бис(трет-бутилдиметилсилилокси)-20(R)-циклопропилиденметил-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 547).
Соединение 547:1Н-ЯМР: δ = 6, 22 (д, 1H), 6,00 (д, 1H), 5,62 (м, 1H), 5,17 (м, 1H), 4,86 (уш.д, 1H), 4,36 (м, 1H), 4,18 (м, 1H), 2,79 (м, 1H), 2,44 (дд, 1H), 2,28 (м, 1H), 2,20 (дд, 1H), 2,02-0,80 (м, 17H), 0,96 (д, 3H), 0,87 (с, 9H), 0,87 (с, 9H), 0,45 (с, 3H), 0,09-0,02 (м, 12H) м.д.
Получение 125: соединение 549
Промежуточное соединение типа а: 546 (175 мг).
Сенсибилизатор: антрацен (157 мг).
Растворитель: DCM.
В результате очистки хроматографией (0-2% об.:об., эфир в петролейном эфире) получали 1(S), 3(R)-бис(трет-бутилдиметилсилилокси)-20(S)-циклопропилиденметил-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 549).
Соединение 549:1Н-ЯМР: δ = 6,23 (д, 1H), 6, 01 (д, 1H), 5,61 (м, 1H), 5,17 (м, 1H), 4,86 (уш.д, 1H), 4,37 (м, 2H), 4,19 (м, 1H), 2,82 (м, 1H), 2,44 (дд, 1H), 2,32 (м, 1H), 2,21 (дд, 1H), 2,06-0,80 (м, 17H), 1,07 (д, 3H), 0,87 (с, 9H), 0,87 (с, 9H), 0,56 (с, 3H), 0,07-0,03 (м, 12H) м.д.
Получение 126: соединение 551
Промежуточное соединение типа а: 550 (0,07 г).
Сенсибилизатор: 9-ацетилантрацен (0,01 г).
Растворитель: DCM (7 мл).
Соединение 551:1Н-ЯМР (CDCl3): δ = 6,22 (д, 1H), 6,17 (дд, 1H), 6,00 (д, 1H), 5,70 (д, 1H), 5,43 (дд, 1H), 5,16 (уш.д, 1H), 4,85 (уш.д, 1H), 4,36 (м, 1H), 4,18 (м, 1H), 2,79 (дд, 1H), 2,43 (дд, 1H), 2,25-1,15 (м, 19H), 1,04 (д, 3H), 1,00 (м, 6H), 0,86 (уш.с, 18H), 0,54 (с, 3H), 0,05 (уш.с, 12H) м.д.
Получение 127: соединение 552
К находящемуся примерно при -70°С раствору литиевого производного 303 (полученного из предшественника 24-дифенилфосфиноил-1(S),3(S)-ди-TBS-окси-9,10-секохола-5(Е),7(Е),10(19),22(Е)-тетраена (0,13 г, 0,16 ммоль) и н-бутиллития (0,1 мл) в сухом ТГФ (2 мл)) прибавляли по каплям раствор диэтилкетона (0,025 мл) в сухом ТГФ (0,25 мл). После перемешивания при той же температуре в течение 30 минут реакционную смесь выдерживали при комнатной температуре 2 часа, а затем при 40°С в течение 1 часа, затем гасили сырым ТГФ, распределяли между эфиром и водой и обрабатывали стандартным образом (хроматография: 20% об.:об. толуола в петролейном эфире), получая соединение 552:1Н-ЯМР в соответствии со структурой.
Получение 128: соединение 535
Промежуточное соединение типа а: 534 (0,09 г).
Сенсибилизатор: 9-ацетилантрацен (0,01 г).
Растворитель: DCM (7 мл).
535:1Н-ЯМР (CDCl3): δ = 6,96 (д, 1H), 6,43 (т, 1H), 6,22 (д, 1H), 6, 19 (дд, 1H), 6,01 (д, 1H), 5,15 (м, 1H), 4,84 (д, 1H), 4,36 (м, 1H), 4,18 (м, 1H), 2,82 (д, 1H), 2,41 (дд, 1H), 2,40-2,15 (м, 2H), 2,0-1,15 (м, 13H), 1,15 (д, 3H), 0,87 (с, 9H), 0,86 (с, 9H), 0,57 (с, 3H), 0,05 (с, 6H), 0,04 (с, 6H) м.д.
Общая методика 8 (примеры 4, 14-18, 23, 25-27, 29 и 36)
К находящейся примерно при 25°С смеси раствора этилацетата (примерно 0,3 мл) соответствующего силилзащищенного промежуточного соединения (приблизительно 0,1 ммоль) и ацетонитрила (4 мл) прибавляли (из пластиковой пипетки) 40%-ную водную фтористо-водородную кислоту (0,5 мл, приблизительно 10 ммоль). После энергичного перемешивания при той же температуре в течение 1 часа реакционную смесь распределяли между этилацетатом и 3 н. раствором гидроксида натрия (до щелочной реакции по рН индикаторной бумаге), затем проводили стандартную обработку, получая соединение I.
Общая методика 9 (примеры 1-3, 5-13, 28, 30-33)
К раствору соответствующего силилзащищенного промежуточного соединения (0,1 ммоль) в ТГФ (4 мл) прибавляли твердый тригидрат ТВА-фторида (0,13 г, приблизительно 0,4 ммоль) и нагревали раствор при 60°С в течение одного часа. После охлаждения (и частичного концентрирования в вакууме, в случае, когда объем ТГФ по масштабной методике превышал 30 мл) добавляли 0,2 М водный раствор гидрокарбоната натрия и этилацетат. В результате стандартной обработки получали соединение I.
Пример 1: 1(S), 3(R)-дигидрокси-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 1)
Раствор 519 (2,1 г, 3,36 ммоль) и тригидрата фторида тетра-н-бутиламмония (5,42 г, 17,2 ммоль) в тетрагидрофуране (70 мл) нагревали при 60°С в атмосфере аргона в течение 60 минут. После охлаждения и концентрирования в вакууме реакционную смесь распределяли между этилацетатом и водным бикарбонатом натрия. Органическую фазу промывали водой и насыщенным раствором соли, сушили и концентрировали. Остаток очищали хроматографией (50% этилацетата в петролейном эфире). Фракции, содержащие указанное в заголовке соединение, концентрировали в вакууме, получая масло, которое выпало в виде бесцветных кристаллов из метилформиата. Соединение 1:13С-ЯМР: δ = 147,7, 143,1, 138, 2, 132,9, 132,8, 125,3, 125,0, 124,3, 117,1, 111,8, 70,8, 66,9, 56,4, 45,9, 45,3, 42,9, 40,5, 40,4, 29,1, 27,8, 25,9, 23,6, 22,3, 20,8, 18,2, 12,3 м.д.
Пример 2: 1(S), 3(R)-дигидрокси-9,10-секохолеста-5(Z),7(E),10(19),22(Z),24-пентаен (соединение 2)
Силилзащищенное промежуточное соединение: 521 (32 мг, 0,05 ммоль).
Соединение 2:13С-ЯМР: δ = 147,7, 143,1, 136,0, 134,8, 132,9, 125,0, 121,9, 120,6, 117,1, 111,7, 70,8, 66,9, 56,6, 56,4, 45,9, 45,3, 42,9, 40,5, 34,7, 29,1, 27,4, 26,4, 23,6, 22,3, 20,8, 18,1, 12, 4 м.д.
Пример 3: 1(S),3(R)-дигидрокси-9,10-секо-20(S)-холеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 3)
Силилзащищенное промежуточное соединение: 523 (135 мг, 0,22 ммоль).
Очистка соединения 3 хроматографией (40% об.:об., этилацетат в петролейном эфире).
Соединение 3:13С-ЯМР: δ = 147,7, 143,4, 138,6, 132,8, 132,5, 125,3, 125,0, 124,3, 116,9, 111,8, 70,9, 66,9, 56,9, 56,2, 46,0, 45,3, 42,9, 40,9, 39,7, 29,1, 27,3, 25,9, 23,5, 22,1, 21,5, 18,3, 12,2 м.д.
Пример 4: 1(S),3(R)-дигидрокси-9,10-секо-26,27-циклохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 4)
Силилзащищенное промежуточное соединение: 524 (36 мг).
Очистка соединения 4 хроматографией (50% об.:об., этилацетат в петролейном эфире).
Соединение 4:1Н-ЯМР: δ = 6,37 (д, J=11 Гц, 1H), 6,34 (уш.д, J=10 Гц, 1H), 6,11 (дд, J=10 Гц, J=15 Гц, 1H), 6,01 (д, J=11 Гц, 1H), 5,56 (дд, J=9 Гц, J=15 Гц, 1H), 5,32 (уш.с, 1H), 5,00 (уш.с, 1H), 4,43 (м, 1H), 4,23 (м, 1H), 2,83 (дд, J=4 Гц, J=11 Гц, 1H), 2,59 (дд, J=4 Гц, J=13 Гц, 1H), 2,31 (дд, J=6 Гц, J=13 Гц, 1H), 2,2-1,2 (м, 16H), 1,10 (м, 4H), 1,07 (д, J=7 Гц, 3H), 0,58 (с, 3H) м.д.
Пример 5: 1(S),3(R)-дигидрокси-9, 10-секо-26,27-цикло-20(S)-холеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 5)
Силилзащищенное промежуточное соединение: 525 (165 мг, 0,26 ммоль).
Очистка соединения 5 хроматографией (50% об.:об., этилацетат в петролейном эфире).
Соединение 5:13С-ЯМР: δ = 147,7, 143,2, 139,5, 132,9, 127,1, 125,0, 123,9, 119,1, 117,0, 111,8, 70,8, 66,8, 56,9, 56,2, 46,0, 45,3, 42,9, 40,7, 39,8, 29,1, 27,3, 23,5, 22,1, 21,3, 12,3, 2,4, 2,2 м.д.
Пример 6: 1(S),3(R)-дигидрокси-9,10-секо-26, 27-метанохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 6)
Силилзащищенное промежуточное соединение: 526 (348 мг, 0,55 ммоль).
Выделение из сырого продукта непосредственной кристаллизацией из метилформиата, опуская стадию хроматографии.
Соединение 6:13С-ЯМР: δ = 147,6, 143,1, 142,8, 137,2, 133,0, 125,0, 123,9, 121,0, 117,1, 111,8, 70,8, 66,9, 56,4, 56,4, 45,9, 45,3, 42,9, 40,4, 40,4, 31,3, 29,9, 29,1, 27,8, 23,6, 22,2, 20,8, 17,2, 12,3 м.д.
Пример 7: 1(S),3(R)-дигидрокси-9, 10-секо-26,27-метано-20(S)-холеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 7)
Силилзащищенное промежуточное соединение: 527 (150 мг, 0,23 ммоль).
Очистка соединения 7 хроматографией (40% об.:об., этилацетат в петролейном эфире).
Соединение 7:13С-ЯМР: δ = 147,7, 143,3, 142,6, 137,6, 132,8, 125,0, 123,8, 121,1, 116,9, 111,8, 70,9, 66,9, 56,9, 56,2, 46,0, 45,3, 42,9, 40,8, 39,8, 31,3, 29,9, 29,1, 27,3, 23,5, 22,1, 21,5, 17,1, 12,2 м.д.
Пример 8: 1(S),3(R),26-тригидрокси-9, 10-секохолеста-5(Z),7(E),10(19),22(Е),24(Е)-пентаен (соединение 9)
Силилзащищенное промежуточное соединение: 528 (148 мг, 0,23 ммоль).
Очистка соединения 9 кристаллизацией из метилформиата.
Соединение 9:1Н-ЯМР: (в гексадейтериоацетоне) δ = 6,29 (д, 1H), 6,25 (дд, 1Н, J=11,1 Гц и 15,1 Гц), 6,09 (д, 1H), 5,99 (д, 1Н, J=11, 1 Гц), 5,52 (дд, 1Н, J=8,8 Гц и 15,1 Гц), 5,31 (м, 1H), 4,86 (м, 1H), 4,39 (м, 1H), 4,17 (м, 1H), 3,96 (д, 2H), 3,86 (д, OH), 3,68 (т, OH), 3,62 (д, OH), 2,87 (м, 1H), 2,50 (дд, 1H), 2,29 (дд, 1H), 2, 20 (м, 1H), 1,72 (уш.с, 3H), 2,10-1,20 (м, 13H), 1,08 (д, 3H), 0,60 (с, 3H) м.д.
Пример 9: 1(S),3(R),26-тригидрокси-9,10-секо-20(S)-холеста-5(Z),7(E),10(19),22(Е), 24(Е)-пентаен (соединение 10)
Силилзащищенное промежуточное соединение: 529 (0,126 г, 0,2 ммоль).
Соединение 10:13С-ЯМР: δ = 147,7, 143,2, 141,8, 134,5, 132,9, 125,5, 125,0, 123,4, 117,0, 111,8, 70,9, 68,7, 66,8, 56,8, 56,2, 46,0, 45,3, 42,9, 41,0, 39,8, 29,1, 27,2, 23,5, 22,1, 21,3, 14,2, 12,3 м.д.
Пример 10: 1(S),3(R),26-тригидрокси-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24(Z)-пентаен (соединение 11)
Силилзащищенное промежуточное соединение: 530 (24 мг, 0,04 ммоль).
Соединение 11:1Н-ЯМР: δ = 6,38 (д, 1H), 6,22 (дд, 1Н, J=11,1 Гц и 14,9 Гц), 6,01 (д, 1H), 5,88 (д, 1Н, J=11,1 Гц), 5,51 (дд, 1Н, J=8,8 Гц и 14,9 Гц), 5,32 (м, 1H), 5,00 (м, 1H), 4, 43 (м, 1H), 4,24 (с, 2H), 4,22 (м, 1H), 2,83 (м, 1H), 2,60 (дд, 1H), 2,31 (дд, 1H), 2,13 (м, 1H), 1,85 (уш.с, 3H), 1,05 (д, 3H), 2,08-0,80 (м, 16H), 0,56 (с, 3H) м.д.
Пример 11: 1(S),3(R),26-тригидрокси-9,10-секо-20(S)-холеста-5(Z),7(E),10(19),22(Е),24(Z)-пентаен (соединение 12)
Силилзащищенное промежуточное соединение: 531 (17 мг, 0,03 ммоль).
Соединение 12:1H-ЯМР: δ = 6,37 (д, 1H), 6,20 (дд, 1Н, J=11,1 Гц и 14,9 Гц), 6,01 (д, 1H), 5,89 (д, 1Н, J=11,1 Гц), 5,52 (дд, 1Н, J=9,5 Гц и 14,9 Гц), 5,33 (м, 1H), 5,00 (м, 1H), 4,43 (м, 1H), 4,24 (с, 2H), 4,22 (м, 1H), 2,81 (м, 1H), 2,60 (дд, 1H), 2,31 (дд, 1H), 1,86 (уш.с, 3H), 0,94 (д, 3H), 2,20-0,80 (м, 17H), 0,50 (с, 3H) м.д.
Пример 12: 1(S),3(R)-дигидрокси-20(R)-(4-метил-5-этил-5-гидрокси-1(Е),3(Е)-гептадиенил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 13)
Силилзащищенное промежуточное соединение: 532 (90 мг, 0,13 ммоль).
Соединение 13:13С-ЯМР: δ = 147,7, 143,0, 140,2, 137,5, 133,0, 125,0, 124,6, 124,0, 117,1, 111,8, 78,4, 70,8, 66,8, 56,4, 56,4, 46,0, 45,3, 42,9, 40,5, 40,4, 31,8, 29,1, 27,7, 23,6, 22,3, 20,6, 14,2, 13,5, 12,3, 7,7 м.д.
Пример 13: 1(S),3(R)-дигидрокси-20(R)-(3-циклопропил-1(Е), 3-бутадиенил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 14)
Силилзащищенное промежуточное соединение: 533 (0,10 мг, 0,16 ммоль).
Очистка соединения 14 кристаллизацией из метилформиата.
Соединение 14:13С-ЯМР: δ = 147,8, 147,7, 143,1, 137,0, 133,0, 129,9, 125,0, 117,1, 111,8, 110,5, 70,8, 66,9, 56,5, 56,4, 46,0, 45,3, 42,9, 40,4, 40,3, 29,1, 27,6, 23,6, 22,2, 20,6, 12,8, 12,3, 5,5 м.д.
Пример 14: 1(S),3(R)-дигидрокси-9,10-секохолеста-5(Z),7(E),10(19),24-тетраен (соединение 15)
Силилзащищенное промежуточное соединение: 1002 (100 мг, 0,16 ммоль).
Очистка соединения 15 хроматографией (50% об.:об., этилацетат в петролейном эфире).
Соединение 15:13С-ЯМР: δ = 147,4, 146,1, 142,6, 132,9, 124,7, 117,0, 111,6, 105,4, 96,4, 78,9, 70,6, 66,6, 56,1, 55,8, 45,6, 45,1, 42,7, 39,5, 28,8, 28,3, 26,3, 24,4, 23,2, 22,1, 21,6, 20,5, 12,3 м.д.
Пример 15: 1(S),3(R)-дигидрокси-20(R)-(5-метил-5-гидрокси-1,3-гексадиинил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 16)
Силилзащищенное промежуточное соединение: 1004 (41 мг, 0,06 ммоль).
Соединение 16:13С-ЯМР: δ = 147,7, 142,7, 133,2, 124,9, 117,1, 111,8, 85,8, 80,6, 70, 8, 67,4, 66,8, 65,6, 65,4, 55,9, 55,6, 45,9, 45,2, 42,9, 39,3, 31,2, 29,1, 28,2, 27,3, 23,5, 21,9, 20,5, 12,4 м.д.
Пример 16: 1(S), 3(R)-дигидрокси-20(S)-(5-этил-5-гидрокси-1,3-гептадиинил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 17)
Силилзащищенное промежуточное соединение: 1006 (66 мг, 0,1 ммоль).
Соединение 17:13С-ЯМР: δ = 147,6, 142,4, 133,4, 124,8, 117,4, 111,9, 85,1, 78,8, 72,7, 70,9, 69,4, 66,9, 65,3, 55,9, 55,8, 45,9, 45,3, 42,9, 39,6, 34,3, 29,0, 28,4, 26,3, 23,3, 22,2, 21,0, 12,5, 8,5 м.д.
Пример 17: 1(S),3(R)-дигидрокси-20(R)-(5-этил-5-гидрокси-1,3-гептадиинил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 18)
Силилзащищенное промежуточное соединение: 1008 (69 мг, 0,1 ммоль).
Соединение 18:13С-ЯМР: δ = 147,7, 142,7, 133,2, 124,9, 117,1, 111,8, 85,2, 79,0, 72,7, 70,8, 69,4, 66,9, 65,6, 55,9, 55,6, 45,9, 45,3, 42,9, 39,3, 34,3, 29,1, 28,2, 27,3, 23,5, 22,0, 20,4, 12,4, 8,5 м.д.
Пример 18: 1(S), 3(R)-дигидрокси-20(S)-(4,4-дибром-1,3-бутадиен-1-ил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 8)
Силилзащищенное промежуточное соединение: 520 (75 мг, 0,1 ммоль).
Очистка соединения 8 хроматографией (50% об.:об., этилацетат в петролейном эфире).
Соединение 8:13С-ЯМР: δ = 147,4, 145,7, 142,6, 137,0, 132,9, 124,7, 124, 7, 116,9, 111,6, 88,1, 70,6, 66,6, 56,4, 55,9, 45,7, 45,0, 42,7, 40,7, 39,5, 28,8, 26,9, 23,2, 21,8, 20,5, 12,1 м.д.
Пример 19: 1(S)-фтор-3(R)-гидрокси-9, 10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 21)
По общей методике 8 (но увеличивая продолжительность реакции до 5 часов) соединение 522 (0,8 г, 2,1 ммоль) десилилировали до соответствующего спирта, 8-бетагидрокси-дезАВ-холеста-22(Е),24-диена. Раствор данного спирта (0,39 г, 1,5 ммоль) в сухом DCM (10 мл), находящийся примерно при 5°С, при перемешивании обрабатывали перйодинаном Десс-Мартина (0,7 г). Через 30 минут добавляли 5%-ный раствор гидрокарбоната натрия и 10%-ный водн. раствор тиосульфата натрия и продолжали перемешивание в течение 10 минут, затем разбавляли эфиром и осуществляли стандартную обработку, получая соответствующий кетон, 8-оксо-дезАВ-холеста-22(Е),24-диен. Данный кетон (67 мг, 0,25 ммоль) медленно прибавляли в ТГФ (3 мл) к находящемуся примерно при -70°С раствору литиевого производного (полученного in situ при действии 1 экв. n-BuLi) фосфиноксида II (A = F, B = CH2) (0,5 ммоль) в сухом ТГФ (4 мл). После перемешивания при той же температуре в течение 2 часов и нагревания до комнатной температуры смесь гасили сырым эфиром и обрабатывали стандартным образом (хроматография: 2% об.:об. эфира в петролейном эфире), получая TBS производное соединения 21. Его десилилировали по общей методике 9, получая соединение 21.
Соединение 21:1Н-ЯМР в соответствии со структурой.
Пример 20: 1(S),3(R)-дигидрокси-19-нор-9,10-секохолеста-5,7(E),22(Е),24-тетраен (соединение 22)
По общей методике 8 (но увеличивая продолжительность реакции до 5 часов) соединение 522 (0,8 г, 2,1 ммоль) десилилировали до соответствующего спирта, 8-бетагидрокси-дезАВ-холеста-22(Е),24-диена. Раствор данного спирта (0, 39 г, 1,5 ммоль) в сухом DCM (10 мл), находящийся примерно при 5°С, при перемешивании обрабатывали перйодинаном Десс-Мартина (0,7 г). Через 30 минут добавляли 5%-ный раствор гидрокарбоната натрия и 10%-ный водн. раствор тиосульфата натрия и продолжали перемешивание в течение 10 минут, затем разбавляли эфиром и осуществляли стандартную обработку, получая соответствующий кетон, 8-оксо-дезАВ-холеста-22(Е),24-диен. Данный кетон (67 мг, 0,25 ммоль) медленно прибавляли в ТГФ (3 мл) к находящемуся примерно при -70°С раствору литиевого производного (полученного in situ при действии 1 экв. n-BuLi) фосфиноксида II (A = O-TBS, B=H2) (0,5 ммоль) в сухом ТГФ (4 мл). После перемешивания при той же температуре в течение 2 часов и нагревания до комнатной температуры смесь гасили сырым эфиром и обрабатывали стандартным образом (хроматография: 2% об.:об. эфира в петролейном эфире), получая ди-TBS производное соединения 22. Его десилилировали по общей методике 9, получая соединение 22.
Соединение 22:1Н-ЯМР в соответствии со структурой.
Пример 21: 1(S),3(S)-дигидрокси-9, 10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 23)
Данное соединение получали аналогично соединению 29, используя промежуточное соединение типа 5, которое получали по аналогии с соединением 552, заменяя ацетон на диэтилкетон.
Соединение 23:1Н-ЯМР в соответствии со структурой.
Пример 22: 1(S), 3(R)-дигидрокси-9,10-секохолеста-5(Z),7(E),10(19),16,22(Е),24-гексаен (соединение 24)
Данное соединение получали аналогично соединению 1 (пример 1), но начиная последовательность (получения 1 и 101) с использованием промежуточного соединения типа 2а, которое получали из 104 по аналогии с описанным получением 202 из 101 в WO9100855.
Соединение 24:1 Н-ЯМР в соответствии со структурой.
Пример 23: 1(S),3(R)-дигидрокси-26,26,26,27,27,27-гексафтор-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 25)
Силилзащищенное промежуточное соединение: 535 (55 мг).
Хроматография: 50% об.:об. этилацетата в петролейном эфире.
Соединение 25:1Н-ЯМР (CDCl3): δ = 6,96 (д, 1H), 6,43 (т, 1H), 6,35 (д, 1H), 6,18 (дд, 1H), 6,01 (д, 1H), 5,31 (уш.с, 1H), 4,98 (уш.с, 1H), 4,41 (м, 1H), 4,22 (м, 1H), 2,80 (дд, 1H), 2,57 (дд, 1H), 2,30 (м, 2H), 2,05-1,20 (м, 8H), 1,10 (д, 3H), 0,58 (с, 3H) м.д.
Пример 24: капсулы, содержащие соединение 1
Соединение 1 растворяли в арахисовом масле до конечной концентрации 10 мкг соединения 1/мл масла. 10 массовых частей желатина, 5 массовых частей глицерина, 0,08 массовых частей сорбата калия и 14 массовых частей дистиллированной воды смешивали при нагревании и формовали в мягкие желатиновые капсулы. Затем каждую из них наполняли 100 мкл соединения 1 в виде раствора в масле таким образом, чтобы каждая капсула содержала 1 мкг соединения 1.
Пример 25: 1(S),3(R)-дигидрокси-20(R)-(4,4-дибром-1,3-бутадиен-1-ил)-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 27)
Силилзащищенное промежуточное соединение: 537 (101 мг, 0,13 ммоль).
Очистка соединения 27 хроматографией (50% об.:об., этилацетат в петролейном эфире).
Соединение 27:13 С-ЯМР: δ = 147,7, 145,3, 142,7, 137,3, 133,2, 125,0, 124,9, 117,3, 111,8, 88,3, 70,8, 66,9, 56,2, 55,8, 46,0, 45,3, 42,9, 40,6, 40,3, 29,0, 27,6, 23,5, 22,3, 20,0, 12,3 м.д.
Пример 26: 1(S),3(R)-дигидрокси-26,27-диметил-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 28)
Силилзащищенное промежуточное соединение: 551 (70 мг).
Очистка соединения 28 хроматографией: 50% об.:об. этилацетата в петролейном эфире.
Соединение 28:13С-ЯМР (CDCl3): δ = 147,4, 143,9, 142,9, 138,4, 132,7, 124,8, 123,9, 122,7, 116,9, 111,6, 70,6, 66,7, 56,2, 56,2, 45,7, 45,1, 42,7, 40,3, 40,2, 29,3, 28,9, 27,6, 23,6, 23,4, 22,1, 20,6, 13,2, 12,4, 12,1 м.д.
Пример 27: 1(S),3(S)-дигидрокси-26,27-диметил-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 29)
Силилзащищенное промежуточное соединение: 552 (25 мг).
Очистка соединения 30 хроматографией (50% об.:об. этилацетата в петролейном эфире).
Соединение 29:1Н-ЯМР: δ = 6,42 (д, 1H), 6,17 (дд, 1H), 6,00 (д, 1H), 5,70 (д, 1H), 5,43 (дд, 1H), 5,28 (уш.д, 1H), 4,98 (д, 1H), 4,29 (м, 1H), 4,03 (м, 1H), 2,84 (дд, 1H), 2,64 (уш.д, 1H), 2,55 (дд, 1H), 2,43 (дд, 1H), 2,20-1,15 (м, 19H), 1,04 (д, 3H), 1,00 (м, 6H), 0,56 (с, 3H) м.д.
Пример 28: 1(S),3(R)-дигидрокси-24-метил-26,27-метано-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 30)
Силилзащищенное промежуточное соединение: 541 (47 мг, 0,072 ммоль).
Очистка соединения 30 хроматографией (50% об.:об., этилацетат в петролейном эфире).
Соединение 30:1Н-ЯМР: δ = 6,38 (д, 1H), 6,01 (д, 1H), 5,99 (д, 1Н, J=15,7 Гц), 5,33 (м, 1H), 5,32 (м, 1H), 5,00 (м, 1H), 4,43 (м, 1H), 4,23 (м, 1H), 2,83 (дд, 1H), 2,79-2,65 (м, 4H), 2,60 (дд, 1H), 2,31 (дд, 1H), 2,22-1,16 (м, 18H), 1,56 (уш.с, 3H), 1,05 (д, 3H), 0,57 (с, 3H) м.д.
Пример 29: 1(S),3(R)-дигидрокси-20(R)-(4,4-дихлор-1,3-бутадиен-1-ил)-9, 10-секопрегна-5(Z),7(E),10(19)-триен (соединение 31)
Силилзащищенное промежуточное соединение: 539 (70 мг, 0,10 ммоль).
Очистка соединения 31 хроматографией (50% об.:об., этилацетат в петролейном эфире).
Соединение 31:13С-ЯМР: δ = 147,7, 144,6, 142,6, 133,2, 129,2, 124,9, 122,4, 118,9, 117,3, 111,8, 70,8, 66,9, 56,3, 55,9, 46, 0, 45,3, 42,9, 40,6, 40,3, 29,0, 27,6, 23,5, 22,3, 20,2, 12,3 м.д.
Пример 30: 1(S),3(R)-дигидрокси-26,27-этано-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 32)
Силилзащищенное промежуточное соединение: 543 (300 мг, 0,46 ммоль).
Очистка соединения 32 хроматографией (50% об.:об., этилацетат в петролейном эфире).
Соединение 32:13С-ЯМР: δ = 147,6, 145,1, 143,1, 137,6, 132,9, 125,7, 125,0, 120,4, 117,1, 111,8, 70,8, 66,8, 56,4, 45,9, 45,2, 42,8, 40,5, 40,4, 33,9, 29,3, 29,1, 27,8, 26,4, 26,3, 23,6, 22,2, 20,8, 12,3 м.д.
Пример 31: 1(S),3(R)-дигидрокси-26,27-пропано-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 33)
Силилзащищенное промежуточное соединение: 545 (200 мг, 0,30 ммоль).
Очистка соединения 22 хроматографией (50% об.:об., этилацетат в петролейном эфире).
Соединение 33:13С-ЯМР: δ = 147,6, 143,1, 140,9, 138,5, 132,9, 125,0, 123,6, 122,1, 117,1, 111,8, 70,8, 66,9, 56,5, 56,4, 46,0, 45,3, 42,9, 40,4, 37,2, 29,2, 29,1, 28,4, 27, 8, 27,7, 26,9, 23,6, 22,3, 20,7, 12,3 м.д.
Пример 32: 1(S),3(R)-дигидрокси-20(S)-циклопропилиденметил-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 34)
Силилзащищенное промежуточное соединение: 547 (143 мг, 0,24 ммоль).
Очистка соединения 34 хроматографией (50% об.:об., этилацетат в петролейном эфире).
Соединение 34:13С-ЯМР: δ = 147,7, 143,4, 132,8, 125,1, 125,0, 118,0, 116,9, 111,8, 70,9, 66,9, 56,9, 56,1, 46,0, 45,3, 42,9, 39,9, 39,8, 29,2, 27,3, 23,6, 22,1, 20,9, 12,4, 2,1, 1,9 м.д.
Пример 33: 1(S),3(R)-дигидрокси-20(R)-циклопропилиденметил-9,10-секопрегна-5(Z),7(E),10(19)-триен (соединение 35)
Силилзащищенное промежуточное соединение: 549 (111 мг, 0,18 ммоль).
Очистка соединения 35 хроматографией (50% об.:об., этилацетат в петролейном эфире).
Соединение 35:13 С-ЯМР: δ = 147,7, 143,2, 132,9, 125,0, 124,5, 118,5, 117,0, 111,7, 70,8, 66,9, 56,8, 56,4, 45,9, 45,3, 42,9, 40,4, 39,7, 29,1, 27,5, 23,6, 22,3, 20,5, 12,2, 2,3, 1,9 м.д.
Пример 36: 20-эпи-1(S),3(R)-дигидрокси-26,26,26,27,27,27-гексафтор-9,10-секохолеста-5(Z),7(E),10(19),22(Е),24-пентаен (соединение 36)
Данное соединение получали аналогично соединению 25 (пример 23), но начиная последовательность (получений 34 и 128) с 20-эпи-1(S),3(R)-ди-TBS-окси-9,10-секохола-5(Z),7(E),10(19),22(Е)-тетраен-24-ола.
Соединение 36:1Н-ЯМР в соответствии со структурой.
Реферат
Изобретение относится к аналогам витамина D общей формулы I, где R1 и R2 - галоген, C1-С6 углеводородный радикал, возможно замещенный 1, 2 -ОН группами, 1, 2 атомами F, или R1 и R2 - вместе - С3-С6 карбоцикл, или R1 и R2 - вместе - прямая связь, или R1 и R2 - Н, R3 - Н или C1-С3-углеводородный радикал, Х - (Е)-этилен, (Z)-этилен, этинилен или связь, Y и Z - Н, СН3; А - ОН, F или Н; В - -СН2- или Н2, при условии, что соединение I не является 3(S)-гидрокси-9,10-секохолеста-5(Z),7(Е),10(19),22(Е),24-пентаеном. Соединения проявляют сильное супрессорное действие на секрецию паратиреоидного гормона и полезны для лечения вторичного гиперпаратиреоидизма, возможно связанного с почечной недостаточностью. 4 н. и 15 з.п. ф-лы, 2 табл.
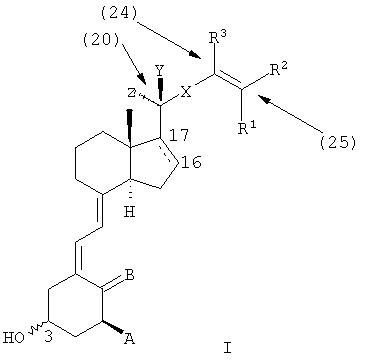
Формула


Комментарии