Полиморфная форма гиодезоксихолата натрия (nahdc) и способ ее получения - RU2669785C2
Код документа: RU2669785C2
Чертежи














Описание
Объектом настоящего изобретения является новая безводная полиморфная кристаллическая форма гиодезоксихолата натрия (NaHDC), названная формой II (FII), и способ ее получения.
Данный способ дает возможность получать гиодезоксихолат натрия в безводной полиморфной кристаллической форме II (FII) с высокой химической и полиморфной чистотой.
Изобретение также характеризует безводные полиморфные кристаллические формы NaHDC, названные формой I (FI) и формой III (FIII), гидратированные формы NaHDC, названные SI и SII, кристаллические формы NaHDC, гидратированные соответственно четырьмя и восемью молекулами воды, и аморфную форму.
Гиодезоксихолат натрия, т.е. 3α,6α-дигидрокси-5β-холан-24-оат натрия, который имеет указанную ниже химическую формулу (формулу I) и CAS RN 10421-49-5, особенно полезен в лечении и/или предупреждении атеросклеротического заболевания, как описано, например, в US8304383, выданном компании AtheroNova Operations Inc.:
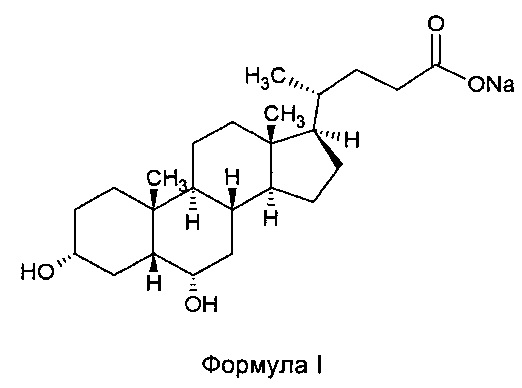
Соответствующая кислота, т.е. 3α,6α-дигидрокси-5β-холан-24-овая кислота формулы II, обычно именуемая гиодезоксихолевой кислотой (HDCA), является самой важной желчной кислотой, присутствующей в свиной желчи в количестве, в процентах относительного содержания, около 40% масс. относительно общего количества желчных кислот, присутствующих в свиной желчи.
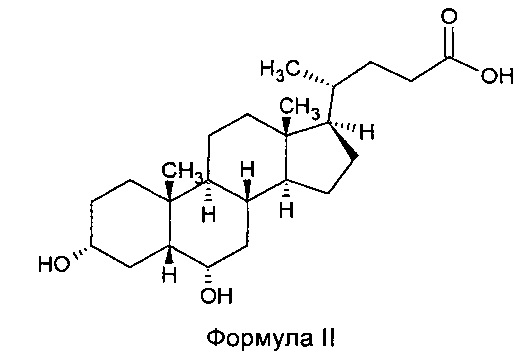
В настоящее время HDCA экстрагируют из свиной желчи способом, который предусматривает различные стадии: в первую очередь осуществляют процесс омыления желчи, т.е. основной гидролиз желчи в водном растворе, необходимый для деконъюгирования желчных кислот, которые в норме присутствуют в желчи в форме гликопроизводных и тауропроизводных.
Затем следует стадия отделения желчных кислот, которые в этой точке присутствуют в растворе в форме свободных карбоновых кислот, от жирных кислот: эту стадию "удаления жира" проводят с использованием растворителей, таких как кетоны, ацетаты, углеводороды, смеси углеводородов, такие как петролейный эфир, смеси алканов, алкенов, ароматических углеводородов и т.д.
После этого HDCA выделяют путем осаждения водным раствором или водно-спиртовым раствором в форме магниевой соли или других солей. Спиртами, подходящими для выделения этих солей, являются спирты с цепью С1-С5, такие как, например, метанол, этанол, 1-пропиловый спирт (1-пропанол), изопропиловый спирт, 2-пропанол, 1-бутанол, 2-бутанол, 2-пентанол и т.д.
Магниевая соль гиодезоксихолевой кислоты формулы III, сокращенно (HDC)2Mg, должна быть затем очищена путем проведения различных стадий переосаждения водными или водно-спиртовыми растворами, такими как те, которые описаны выше, с получением, после подкисления, HDCA с химической чистотой от 80 до 90%.
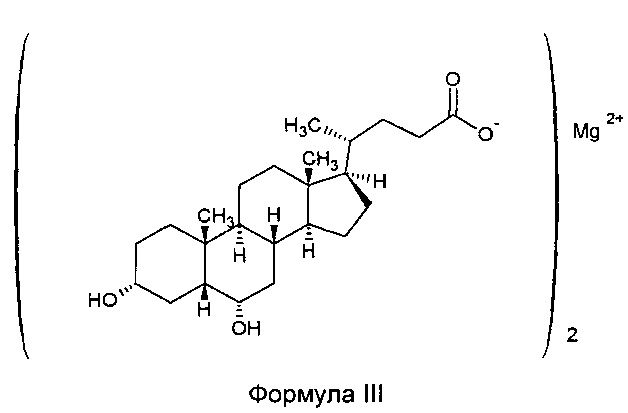
Эта методика и аналогичные способы описаны в патентных документах US 4186143 (Canada Packers Ltd); US 5349074 (Erregierre Industrie Chimica S.p.A); US 7982062B2 (Dipharma S.p.A.); WO 2007/069814 A1 и WO 2007/078039 A1 (оба Woong Pharma).
В предшествующем уровне техники никогда не были описаны кристаллические формы HDCA или ее солей, и, в частности, даже не было опубликовано никакой информации о существовании полиморфизма для натриевой соли гиодезоксихолевой кислоты. Например, в статье Nonappa et al., Crystal Growth & Design, Vol 9, N. 11 (2009) p. 4710-4719 охарактеризованы некоторые полиморфы, которые обнаружены в природных желчных кислотах, но с указанием, что для образцов HDCA, имеющихся в продаже, полиморфы не обнаружены.
Задачей настоящего изобретения, следовательно, является получение новой стабильной полиморфной формы натриевой соли гиодезоксихолевой кислоты (полиморфной формы FII) и создание способа ее получения, способного обеспечить получение указанной формы NaHDC с высокой химической и полиморфной чистотой.
Полиморфная форма FII, в отличие от других описанных форм NaHDC, имеет очень высокую стабильность в цикле сорбции влаги в изотерме при 25°C и при 40°C (смотри Фиг. 10, 11, 12 и 13). Полиморфная форма FII имеет негигроскопическую природу в отличие от всех других обнаруженных полиморфных форм (смотри Фиг. 27, 28 и 58): она очень стабильна, и ее нетрудно хранить. Такая природа является абсолютно необычной для других натриевых солей желчных кислот, которые имеют общую проблему высокой гигроскопичности и, следовательно, трудности хранения вследствие их нестабильности.
Полиморфная форма FII имеет очень высокую и неожиданную стабильность по отношению к влаге в изотерме при 25°C и при 40°C.
Действительно, при сорбции при 25°C образец стабилен вплоть до 70% RH (относительная влажность) (при 70% RH он показывает увеличение массы менее 2%). После 70% RH он абсорбирует влагу и при 90% RH происходит изменение массы, составляющее примерно на 35%. Ниже будут указаны результаты исследований влагоустойчивости этой полиморфной формы FN.
По результатам анализа DVS (динамическая сорбция пара) при 25°C полиморфная форма FI менее стабильна, чем полиморфная форма FII: полиморфная форма FII стабильна при сорбции при 25°C вплоть до 70% RH, тогда как полиморфная форма FI уже при 20% RH показывает изменение массы, составляющее примерно 2% (смотри Фиг. 27). Также по результатам анализа DVS при 40°C полиморфная форма FI менее стабильна, чем полиморфная форма FII: полиморфная форма FII стабильна при сорбции при 40°C вплоть до 70% RH, тогда как полиморфная форма FI уже при 30% RH показывает изменение массы, составляющее примерно 2% (смотри Фиг. 28). Кроме того, смесь NaHDC (смесь разных полиморфных форм, которые получены перед конечным переосаждением, проведенным, например, в безводном ацетоне) по результатам анализа DVS при 25°C менее стабильна, чем полиморфная форма FII (смотри Фиг. 58). Полиморфная форма FII стабильна при сорбции вплоть до 70% RH, тогда как смесь NaHDC уже при 20% RH показывает изменение массы, составляющее примерно 3%.
Способ по изобретению дает возможность получать полиморфную форму FII NaHDC с определенным размером частиц (гранулометрическим составом) и оптимальными физико-химическими характеристиками для использования NaHDC в качестве фармацевтического активного ингредиента, в частности в лечении и/или предупреждении атеросклеротического заболевания.
Дополнительными преимуществами способа по настоящему изобретению являются его воспроизводимость, его потенциал масштабирования и возможность получения активного ингредиента в полиморфной форме FII в виде порошка с оптимальной морфологией (габитус кристалла) для всех рабочих параметров, которые могут влиять на конечную биодоступность, таких как объемная плотность (кажущаяся плотность), плотность после уплотнения (насыпная плотность), прессуемость, скорость растворения, текучесть и гигроскопичность порошка.
Поскольку способ по изобретению дает возможность получать полиморфную форму FII гиодезоксихолата натрия с желаемым гранулометрическим составом, операции, такие как измельчение и микронизация активного ингредиента, которые обычно проводят для улучшения его биодоступности за счет увеличения скорости его растворения, могут быть исключены, что является преимуществом.
Этим путем, а также за счет очевидного энергосбережения можно исключить операции, которые могут влиять на химическую и/или полиморфную чистоту продукта, такие как, например, микронизация, которая потенциально может приводить к варьированию процентному содержанию аморфного вещества в уже образованных кристаллических формах (известный процесс аморфизации).
Наконец, способ по настоящему изобретению дает возможность получать полиморфную форму FII гиодезоксихолата натрия с высоким выходом.
Суммарный выход процесса превращения 3α,6α-дигидрокси-5β-холан-24-овой кислоты (HDCA) формулы II (гиодезоксихолевая кислота, HDCA), имеющей химическую чистоту от 80 до 90%, в натриевую соль гиодезоксихолевой кислоты (NaHDC), имеющую химическую чистоту 99,5%-99,9% и находящуюся в полиморфно чистой форме, полиморфной форме FII, составляет 65,0%-85,0% (масс./масс.) и 62,0%-80,0% (моль/моль).
HDCA очищают посредством солеобразования с магниевыми солями в деионизированной/питьевой воде или водно-спиртовом растворе: (HDC)2Mg выпадает в осадок, а соли примесей остаются в растворе. Кислотную функциональную группу возвращают путем подкисления водной суспензии (HDC)2Mg. Процесс многократно повторяют до достижения чистоты 99,5%-99,9% с выходами 90%-95% (масс./масс., моль/моль) для первого процесса солеобразования и с выходами 95%-98% (масс./масс., моль/моль) для последующих процессов солеобразования. HDCA, очищенную таким образом, растворяют в водном растворе гидроксида натрия и затем осаждают ацетоном с выходом 85%-95% (масс./масс.) и 80%-90% (моль/моль). Этот продукт (NaHDC) сразу после сушки суспендируют в ацетоне при нагревании до образования полиморфной формы FII с выходами 90%-95% (масс./масс., моль/моль). Суммарный выход способа составляет 65%-85% (масс./масс.) и 62%-80% (моль/моль).
Полиморфная форма по настоящему изобретению, т.е. полиморфная форма FII, является безводной и наиболее термодинамически стабильной формой при комнатной температуре и не подвергается взаимопревращению в другие формы в условиях способа по настоящему изобретению. Кроме того, когда она включена в композицию медицинского продукта, она является стабильной длительное время, поскольку никакого взаимопревращения в другие полиморфные формы гиодезоксихолата натрия, которые будут описаны ниже, не наблюдается. Как уже указано, в отличие от других форм, она имеет очень сильную и неожиданную стабильность по отношению к влажности, имея негигроскопическую природу в отличие от всех остальных ее форм, что является неожиданным для натриевой соли, относящейся к категории солей желчных кислот.
Термин "кристаллический полиморф" или "полиморф" в настоящем изобретении относится к конкретной кристаллической форме фармацевтического активного ингредиента, которая может быть охарактеризована аналитическими методами, такими как дифракция рентгеновских лучей на порошке (XPRD), FT-IR/ATR спектроскопия (инфракрасная спектроскопия с Фурье-преобразованием/спектроскопия нарушенного полного внутреннего отражения), FT-RAMAN спектроскопия (рамановская спектроскопия с Фурье-преобразованием), дифференциальная сканирующая калориметрия (DSC), термогравиметрический анализ (TGA) и анализ динамической сорбции пара (DVS) в изотерме при 25°C и при 40°C.
В настоящем изобретении полиморфная форма FII в одинаковой мере может именоваться одним из следующих терминов:
- полиморфная форма II, или
- полиморфная форма II (FII), или
- кристаллическая полиморфная форма II, или
- кристаллическая полиморфная форма II (FII), или
- безводная кристаллическая полиморфная форма II, или
- безводная кристаллическая полиморфная форма II (FII), или
- кристаллическая форма FII, или
- безводная кристаллическая форма FII.
Полиморфная форма FI в одинаковой мере может именоваться одним из следующих терминов:
- полиморфная форма I, или
- полиморфная форма I (FI), или
- кристаллическая полиморфная форма I, или
- кристаллическая полиморфная форма I (FI), или
- безводная кристаллическая полиморфная форма I, или
- безводная кристаллическая полиморфная форма I (FI), или
- кристаллическая форма FI, или
- безводная кристаллическая форма FI.
Полиморфная форма FIII в одинаковой мере может именоваться одним из следующих терминов:
- полиморфная форма III, или
- полиморфная форма III (FIII), или
- кристаллическая полиморфная форма III, или
- кристаллическая полиморфная форма III (FIII), или
- безводная кристаллическая полиморфная форма III, или
- безводная кристаллическая полиморфная форма III (FIII), или
- кристаллическая форма FIII, или
- безводная кристаллическая форма FIII.
Аналогично, для гидратированной полиморфной формы, использованной в качестве примера SI, возможно использование, в одинаковой мере, термина типа:
- гидратированная полиморфная форма SI, или
- гидратированная кристаллическая полиморфная форма SI.
Для гидратированной полиморфной формы, использованной в качестве примера SII, возможно использование, в одинаковой мере, термина типа:
- гидратированная полиморфная форма SII, или
- гидратированная кристаллическая полиморфная форма SII.
Краткое описание графических материалов
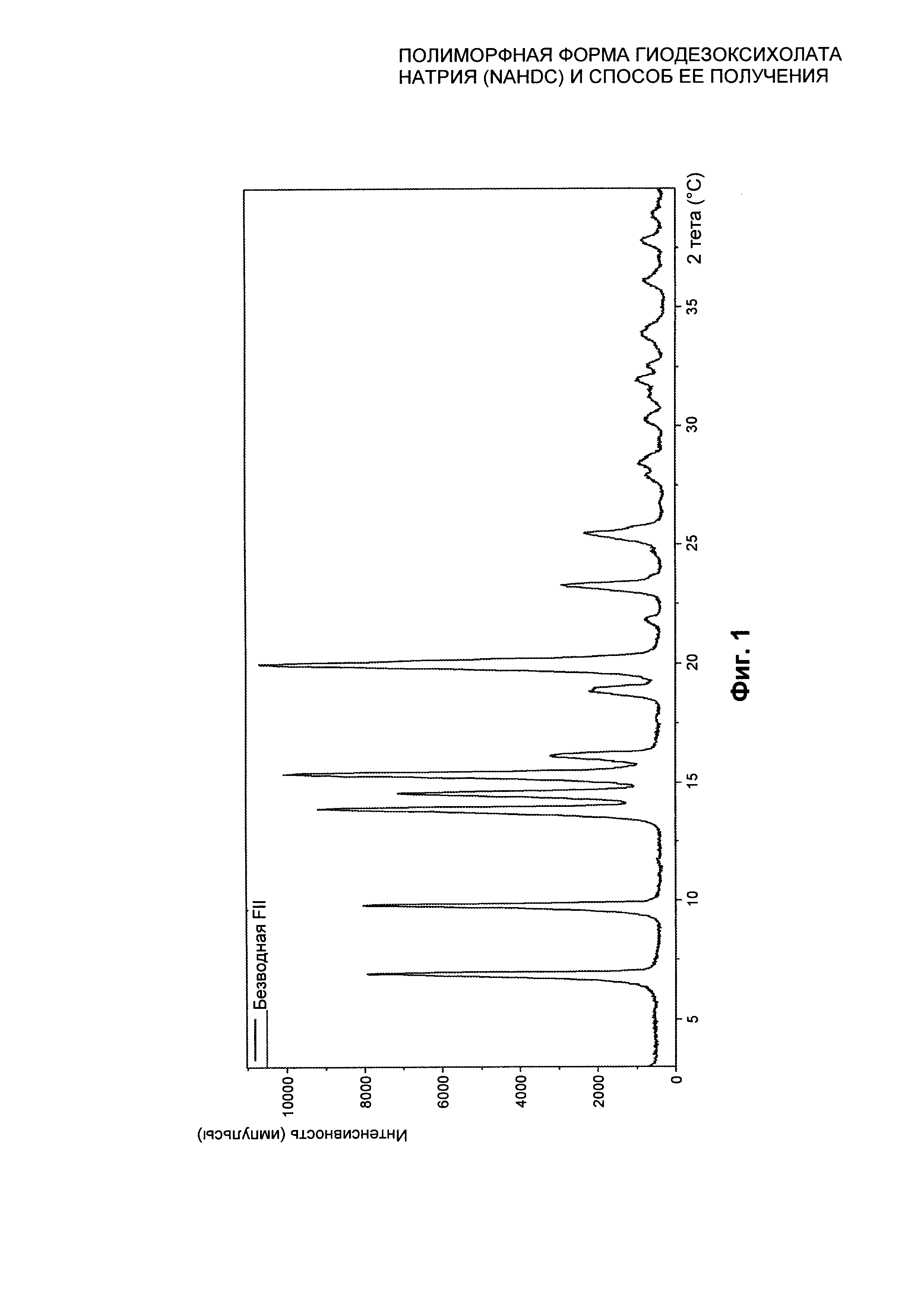
На Фиг. 1 представлена рентгеновская дифрактограмма на порошке (XPRD) безводной кристаллической формы II (FII) NaHDC.
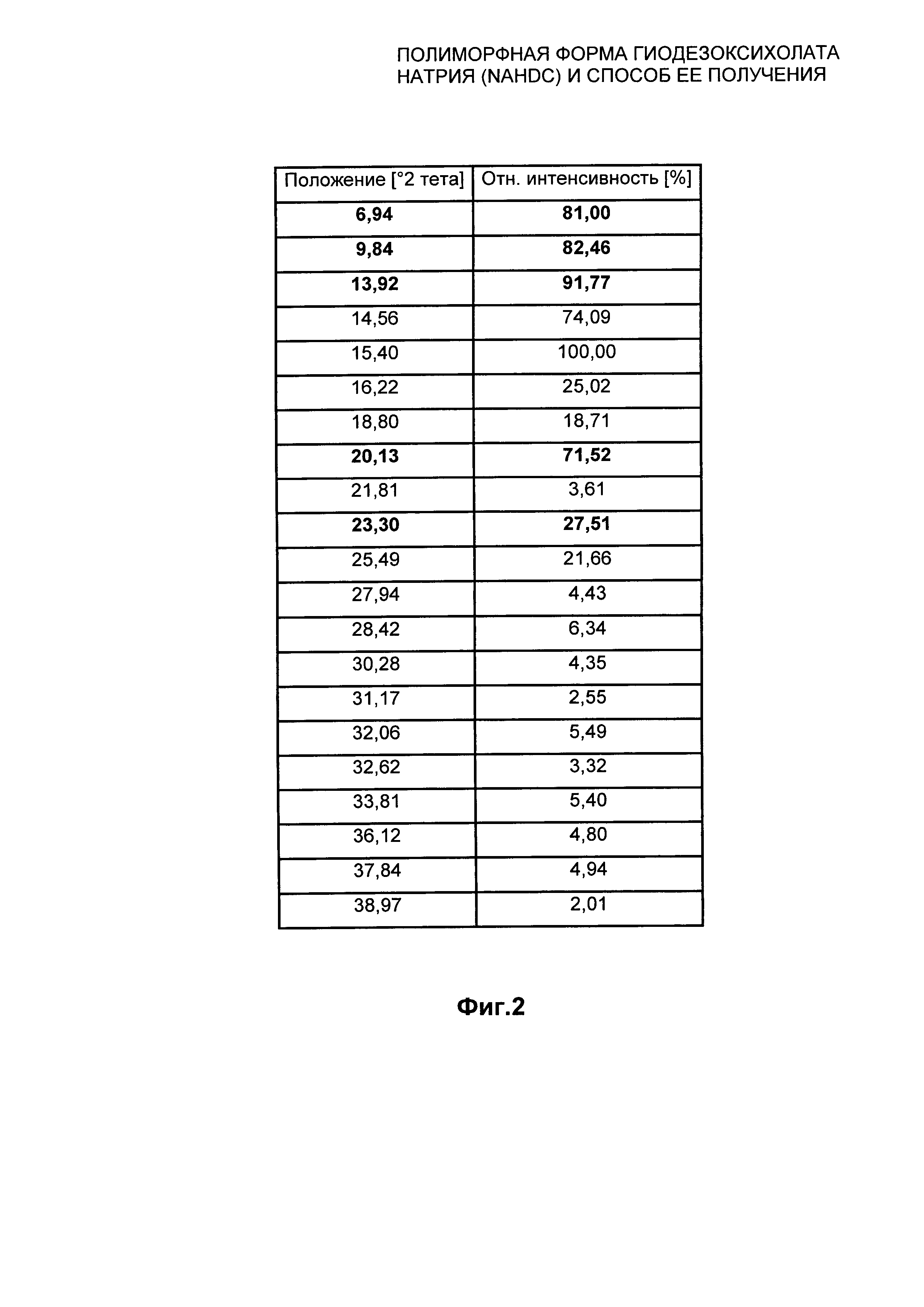
На Фиг. 2 представлены значения 2 тета пиков XPRD, представленной на Фиг. 1, для безводной кристаллической формы II (FII) вместе с соответствующей относительной интенсивностью. Пики, выделенные жирным шрифтом, являются характеристическими пиками формы FII.
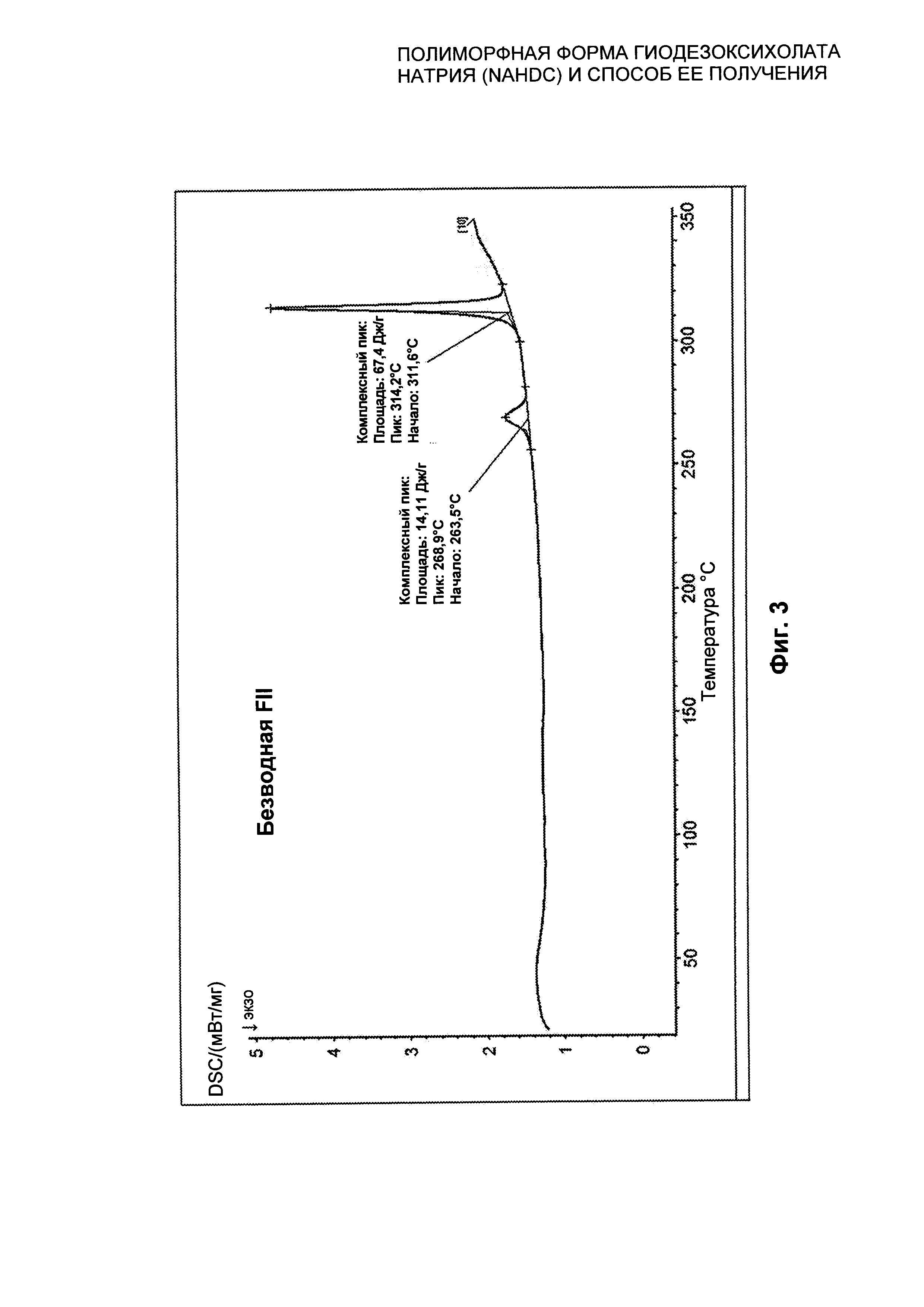
На Фиг. 3 представлен профиль дифференциальной сканирующей калориметрии (DSC) безводной кристаллической формы II (FII) NaHDC.
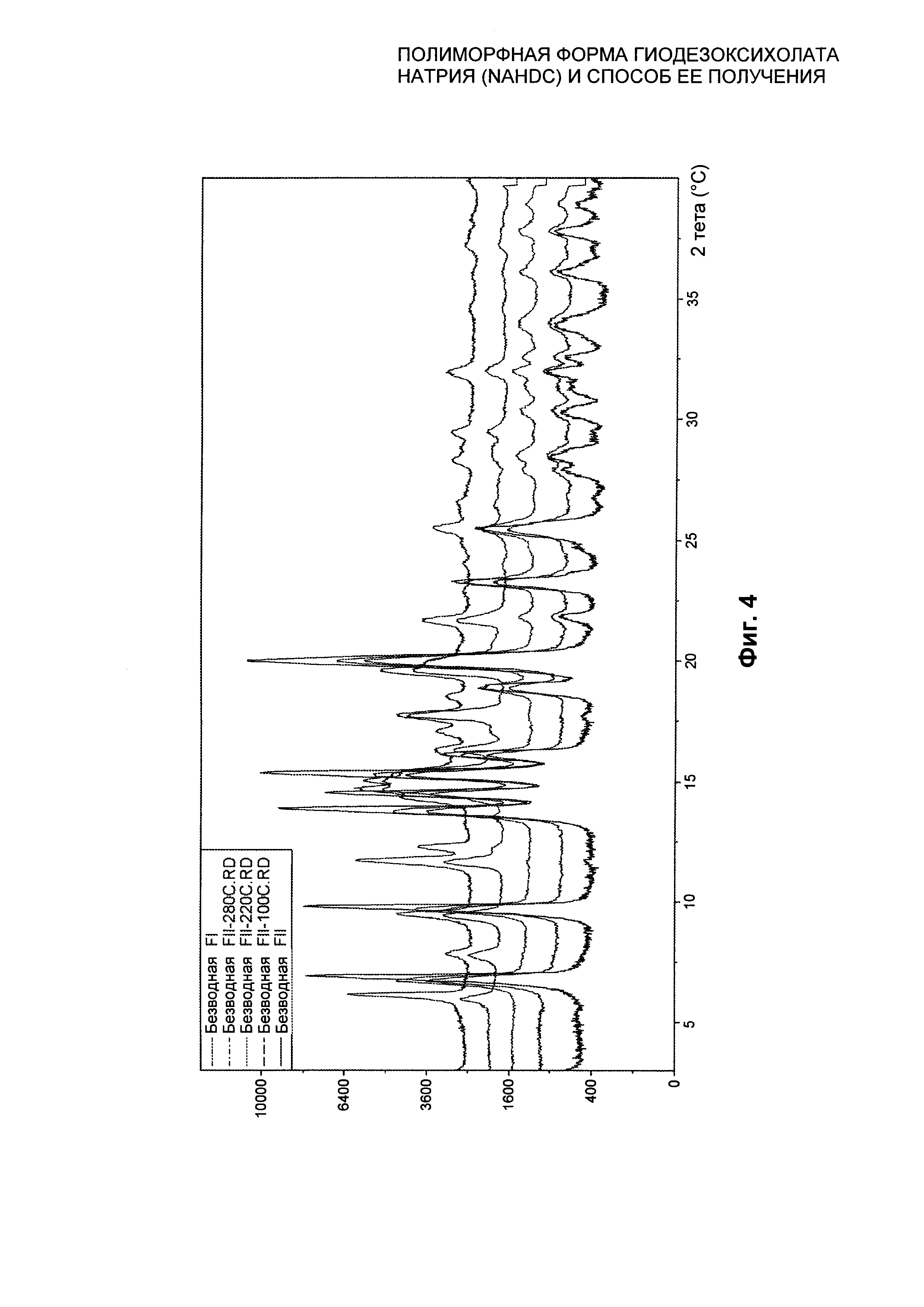
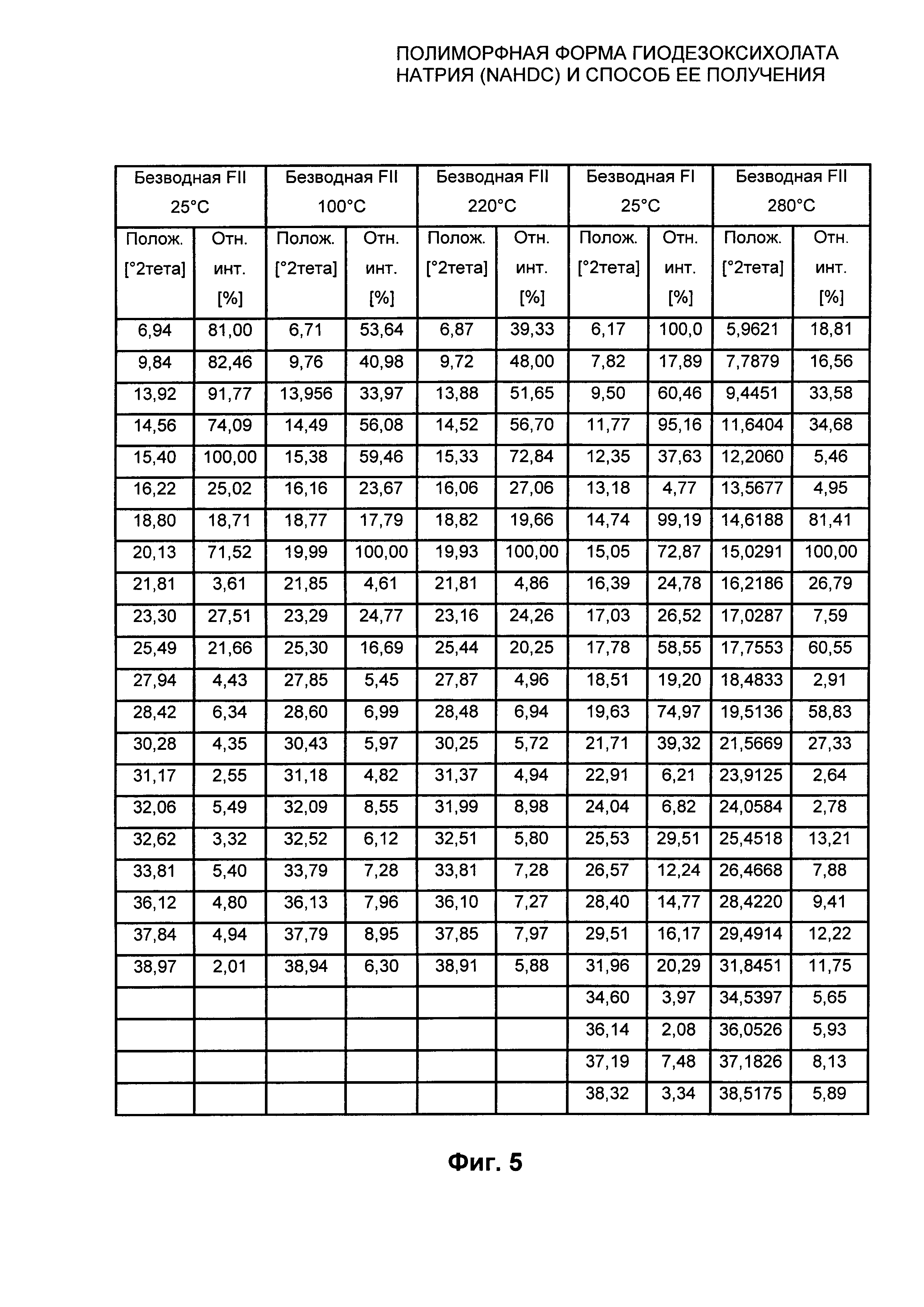
На Фиг. 4 представлено сравнение XRPD безводной формы FII NaHDC при 25°C, XRPD безводной формы FII NaHDC при 100°C, XRPD безводной формы FII NaHDC при 220°C, XRPD безводной формы FII NaHDC при 280°C с безводной формой I (FI) NaHDC при 25°C.
На Фиг. 5 представлено сравнение перечня пиков XRPD безводной формы FII NaHDC при 25°C, безводной формы FII NaHDC при 100°C, безводной формы FII NaHDC при 220°C, безводной формы FII NaHDC при 280°C с перечнем пиков XPRD безводной формы FI NaHDC при 25°C из Фиг. 4.
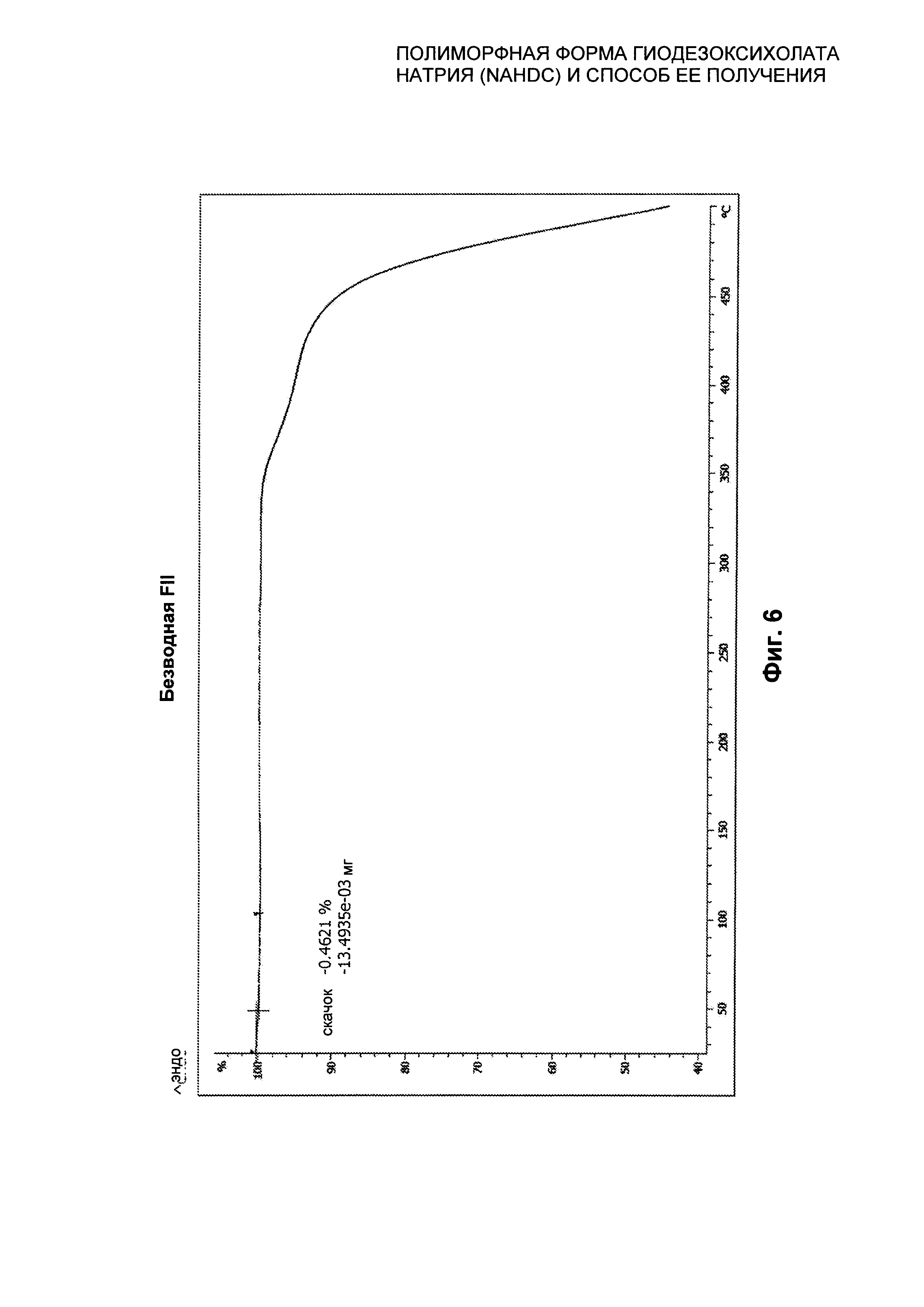
На Фиг. 6 представлен термогравиметрический профиль (TGA) безводной кристаллической формы FII NaHDC.
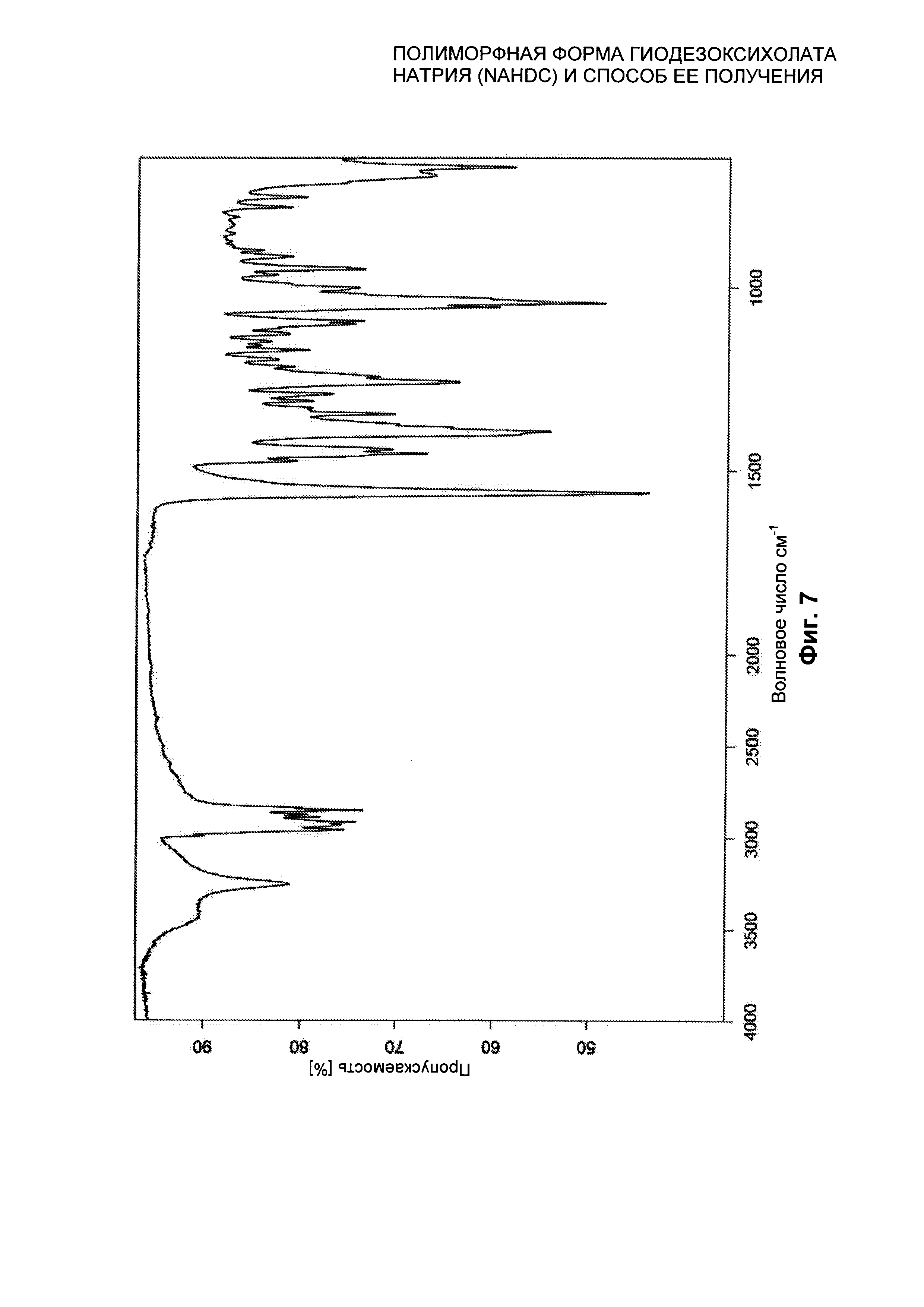
На Фиг. 7 представлен FT-IR/ATR спектр полиморфной формы FII NaHDC.
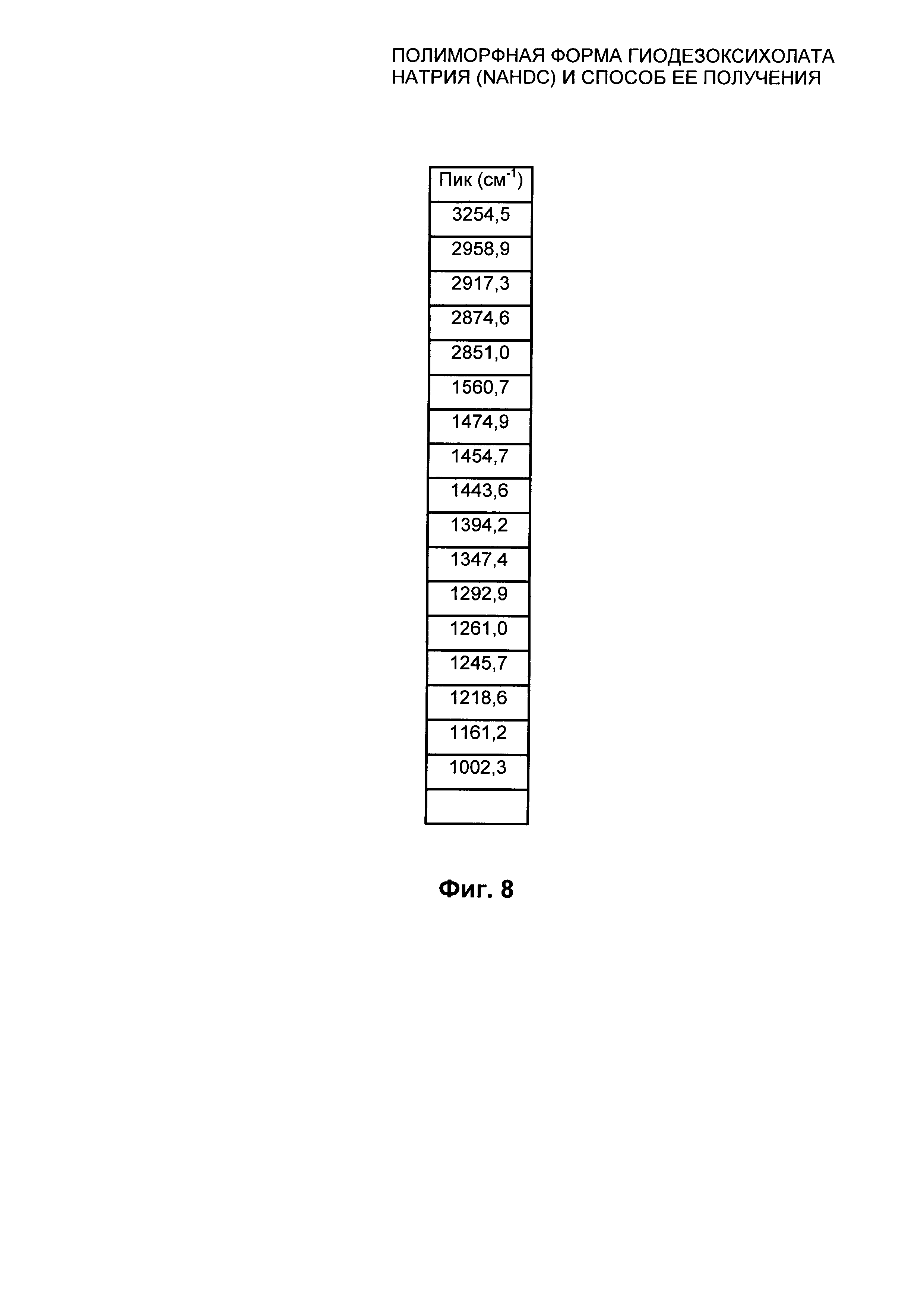
На Фиг. 8 представлены значения в см-1 характеристических пиков FT-IR/ATR из Фиг. 7 для безводной кристаллической формы FII NaHDC.
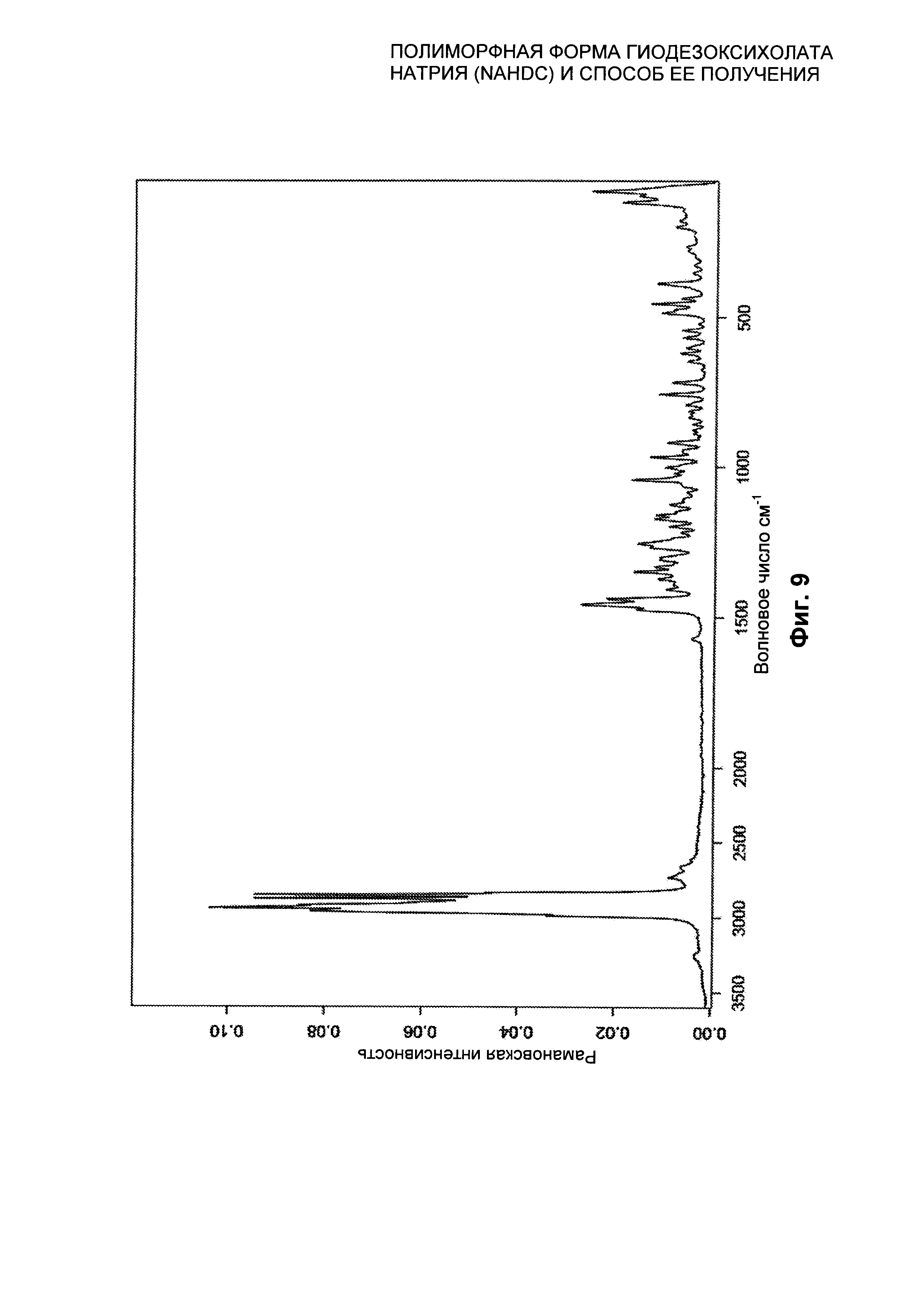
На Фиг. 9 представлен FT-RAMAN спектр безводной кристаллической формы FII NaHDC.
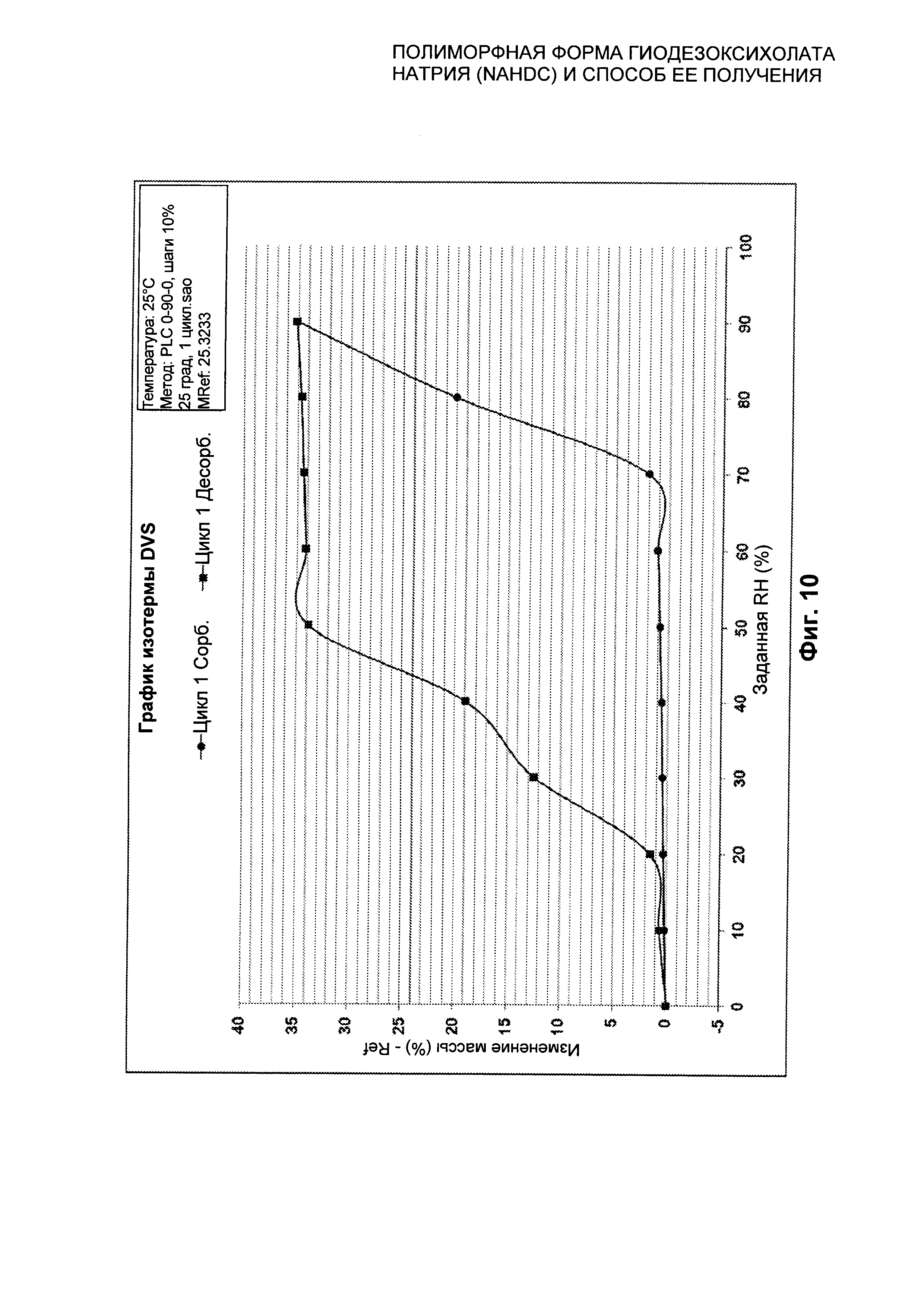
На Фиг. 10 представлена изотерма при 25°C безводной кристаллической формы FII NaHDC.
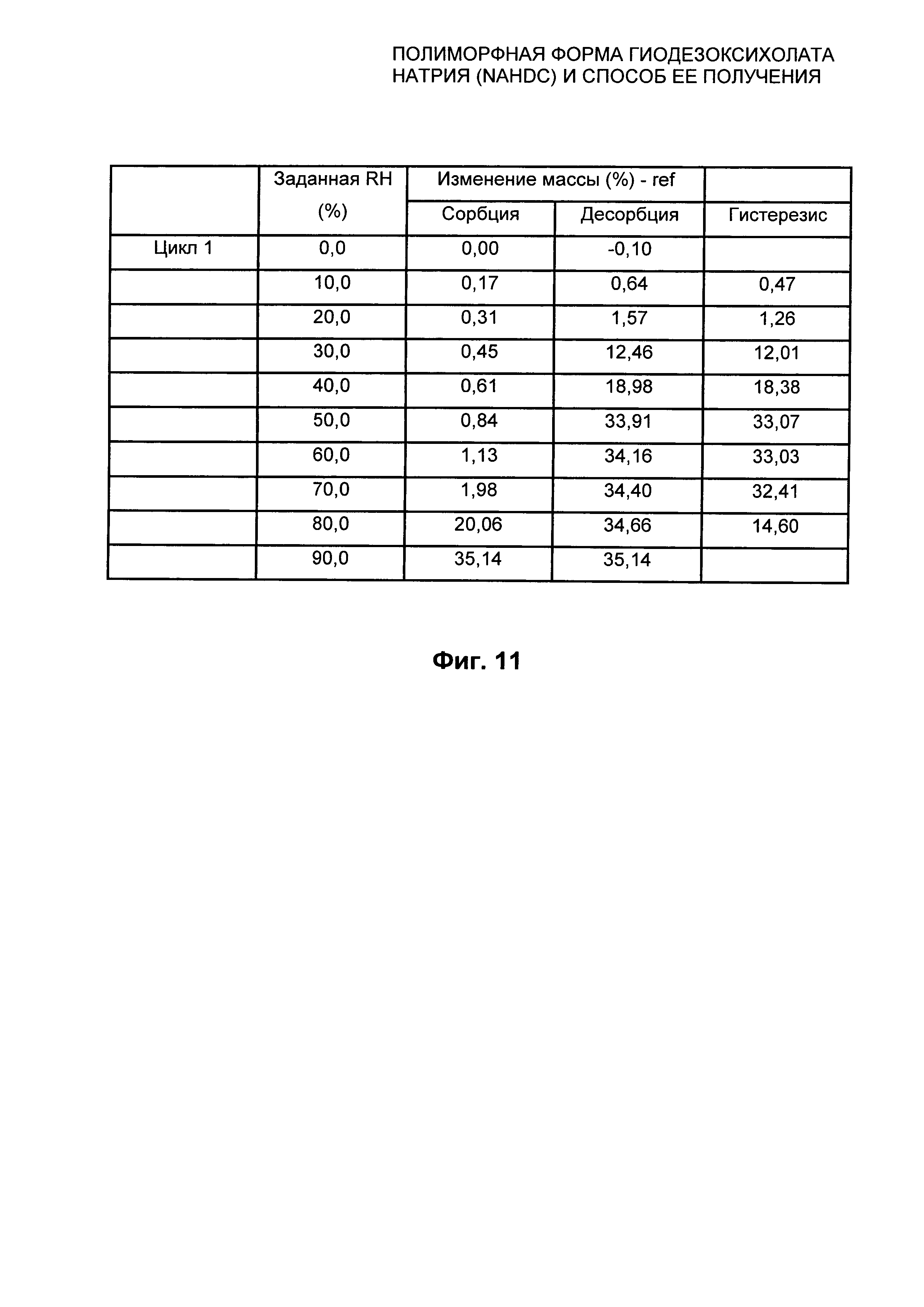
На Фиг. 11 представлены относительные показатели изотермы при 25°C из Фиг. 10 безводной кристаллической формы FII NaHDC.
На Фиг. 12 представлена изотерма при 40°C безводной кристаллической формы FII NaHDC.
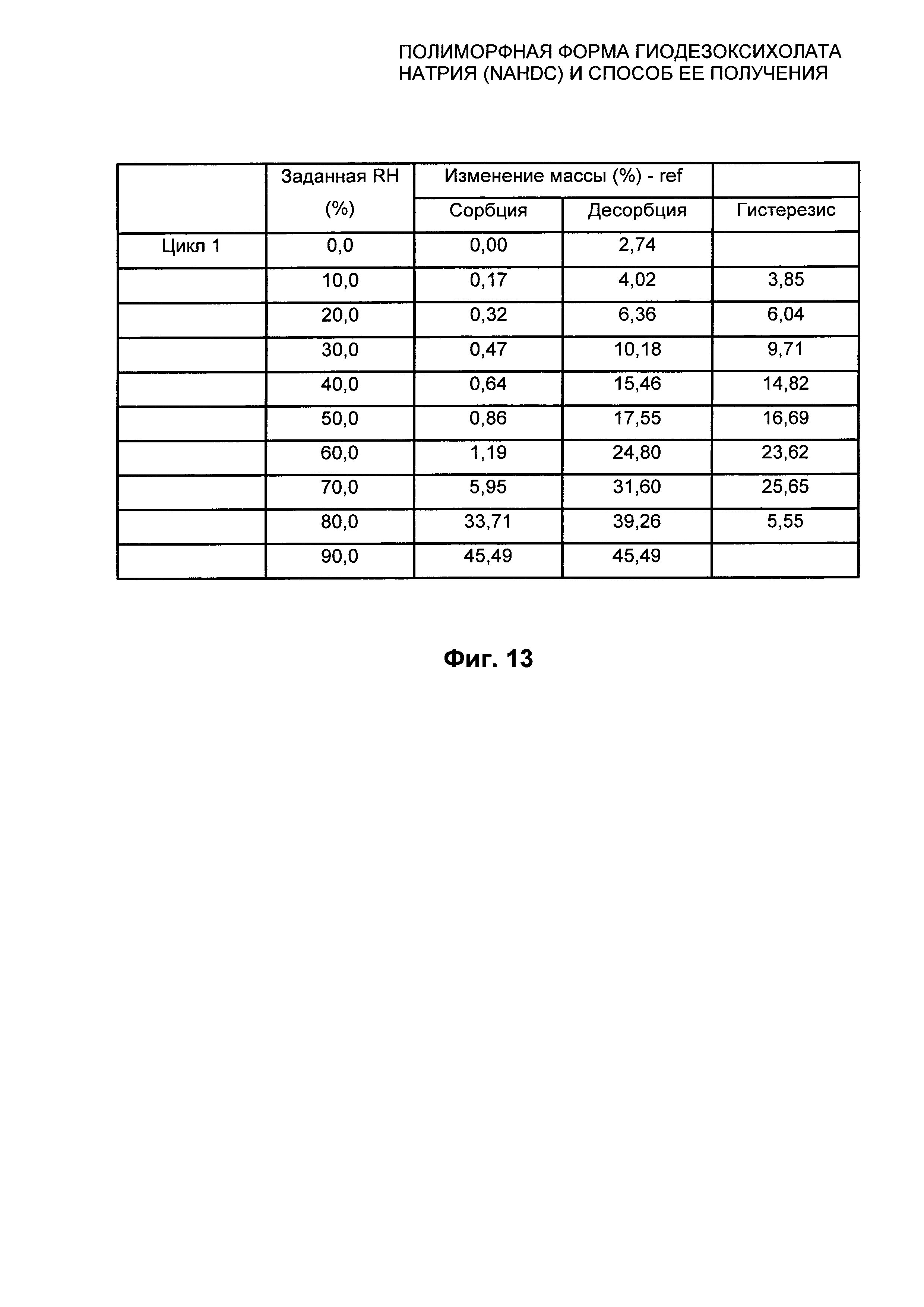
На Фиг. 13 представлены относительные показатели изотермы при 40°C из Фиг. 12 безводной кристаллической формы FII NaHDC.
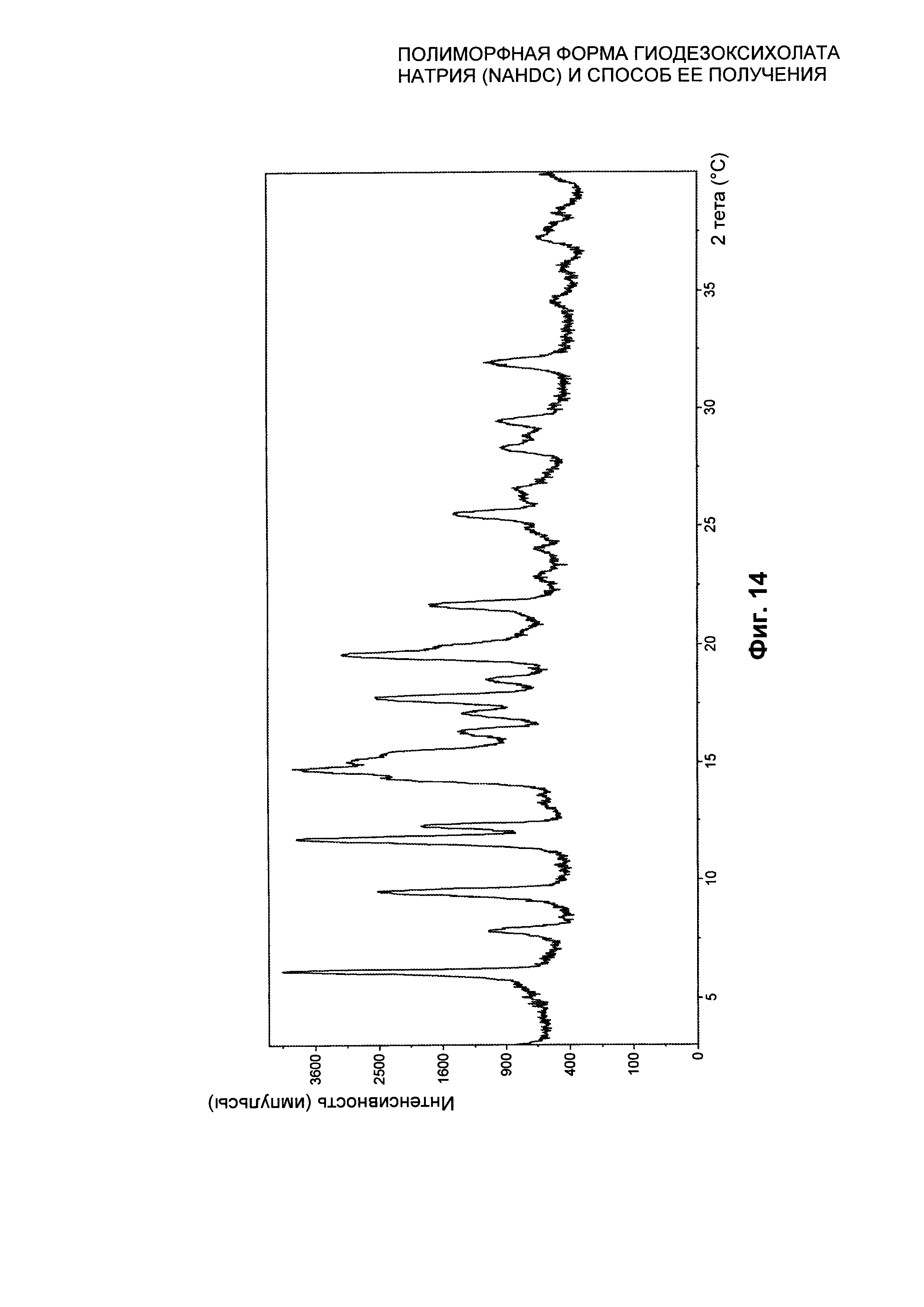
На Фиг. 14 представлена рентгеновская дифрактограмма на порошке (XPRD) безводной кристаллической формы FI NaHDC.
На Фиг. 15 представлены значения 2 тета пиков XPRD из Фиг. 14 для безводной кристаллической формы FI вместе с соответствующей относительной интенсивностью. Пики, выделенные жирным шрифтом, могут быть определены как характеристические пики Формы I (FII).
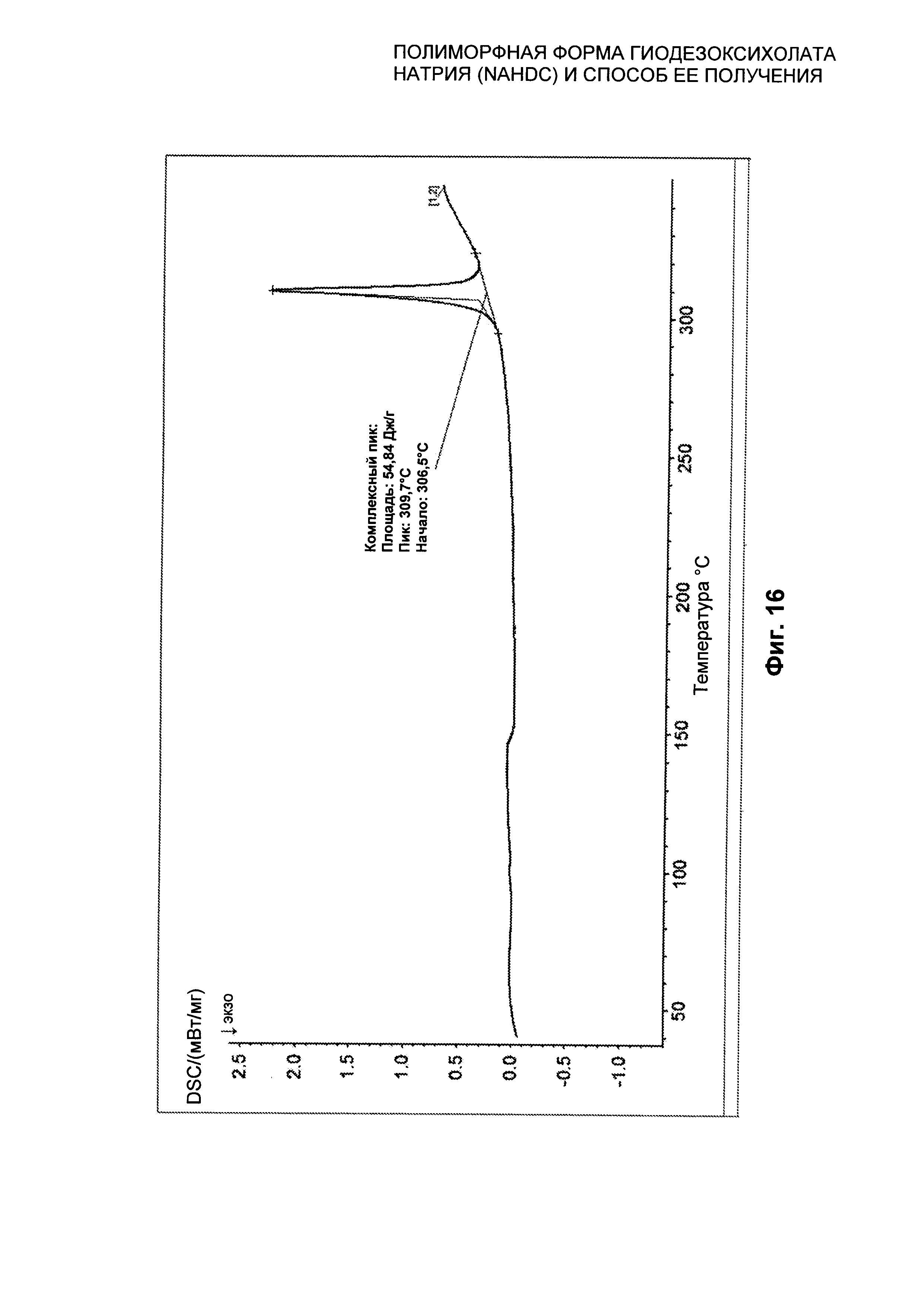
На Фиг. 16 представлен профиль дифференциальной сканирующей калориметрии (DSC) безводной кристаллической формы FI NaHDC.
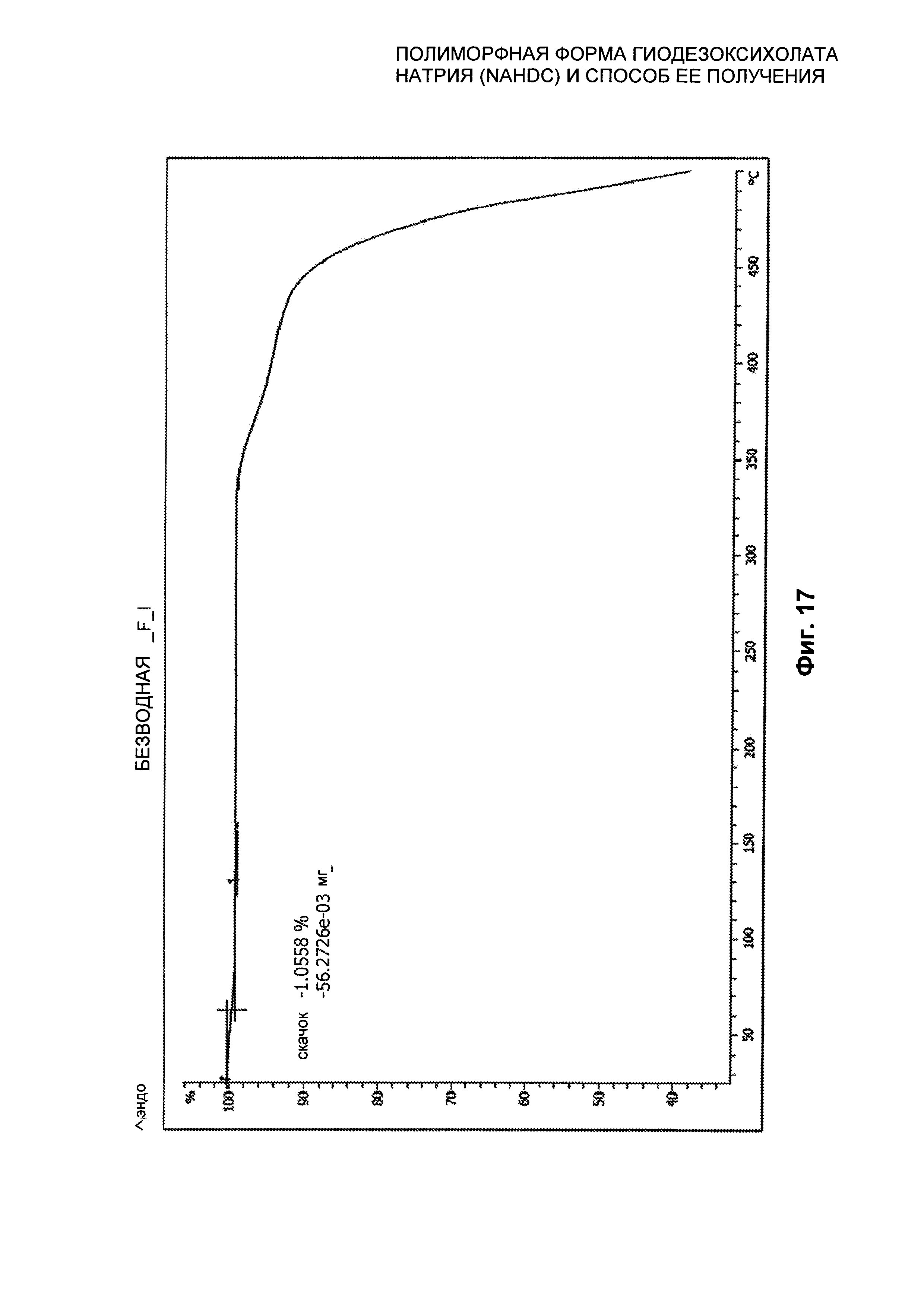
На Фиг. 17 представлен термогравиметрический профиль (TGA) безводной кристаллической формы FI NaHDC.
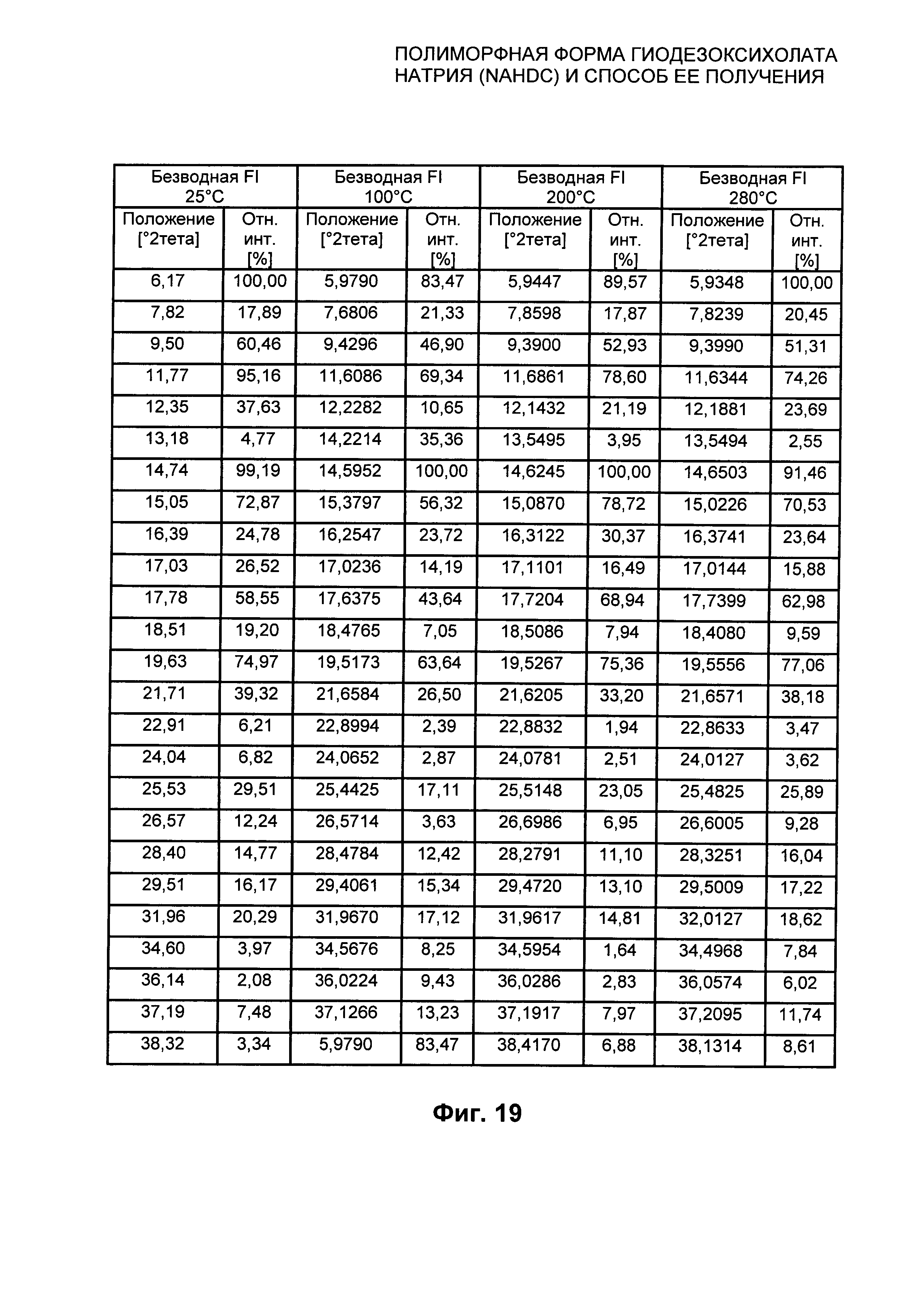
На Фиг. 18 представлено сравнение XRPD безводной кристаллической формы FI NaHDC при 25°C, XRPD безводной кристаллической формы FI NaHDC при 100°C, XRPD безводной кристаллической формы FI NaHDC при 200°C и XRPD безводной кристаллической формы FI NaHDC при 280°C.
На Фиг. 19 представлено сравнение перечней пиков безводной формы FI NaHDC, XRPD безводной формы FI NaHDC при 25°C, XRPD безводной формы FI NaHDC при 100°C, XRPD безводной формы FI NaHDC при 200°C, XRPD безводной формы FI NaHDC при 280°C из Фиг. 18.
На Фиг. 20 представлен FT-IR/ATR спектр безводной кристаллической формы FI NaHDC.
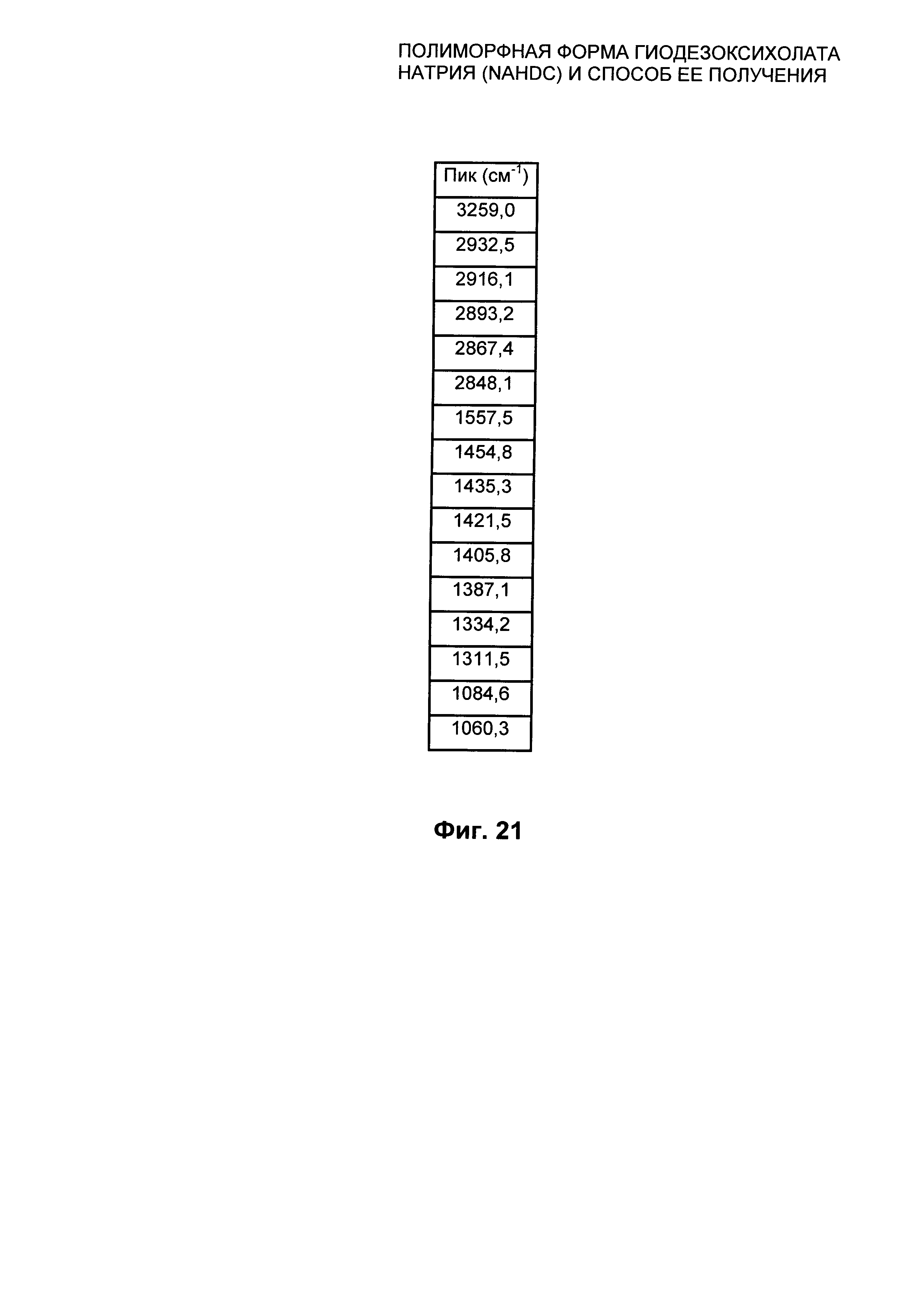
Фиг. 21 представлены значения в см-1 характеристических пиков FT-IR/ATR из Фиг. 20 для безводной кристаллической формы FI NaHDC.
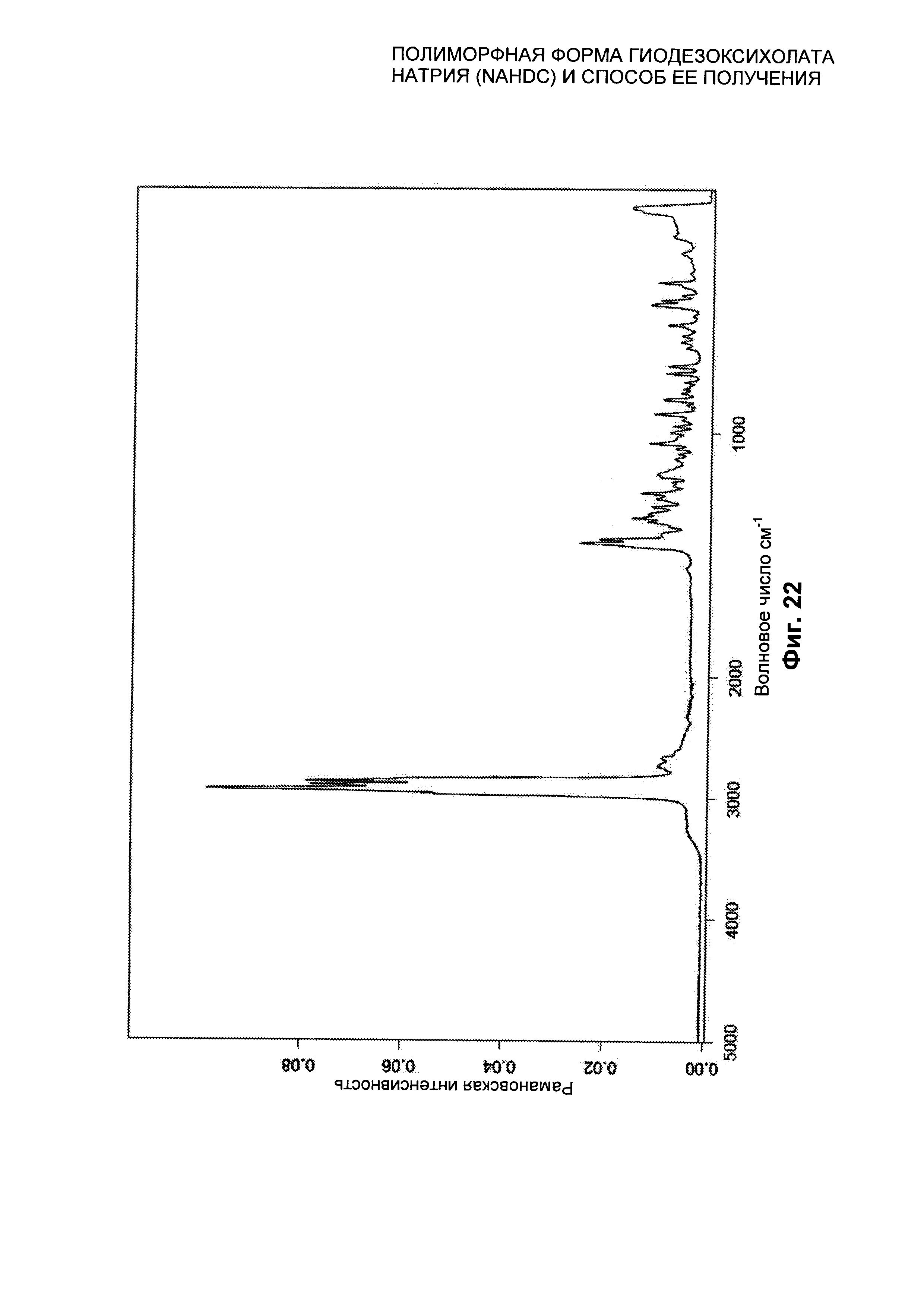
На Фиг. 22 представлен FT-RAMAN спектр безводной кристаллической формы FI NaHDC.
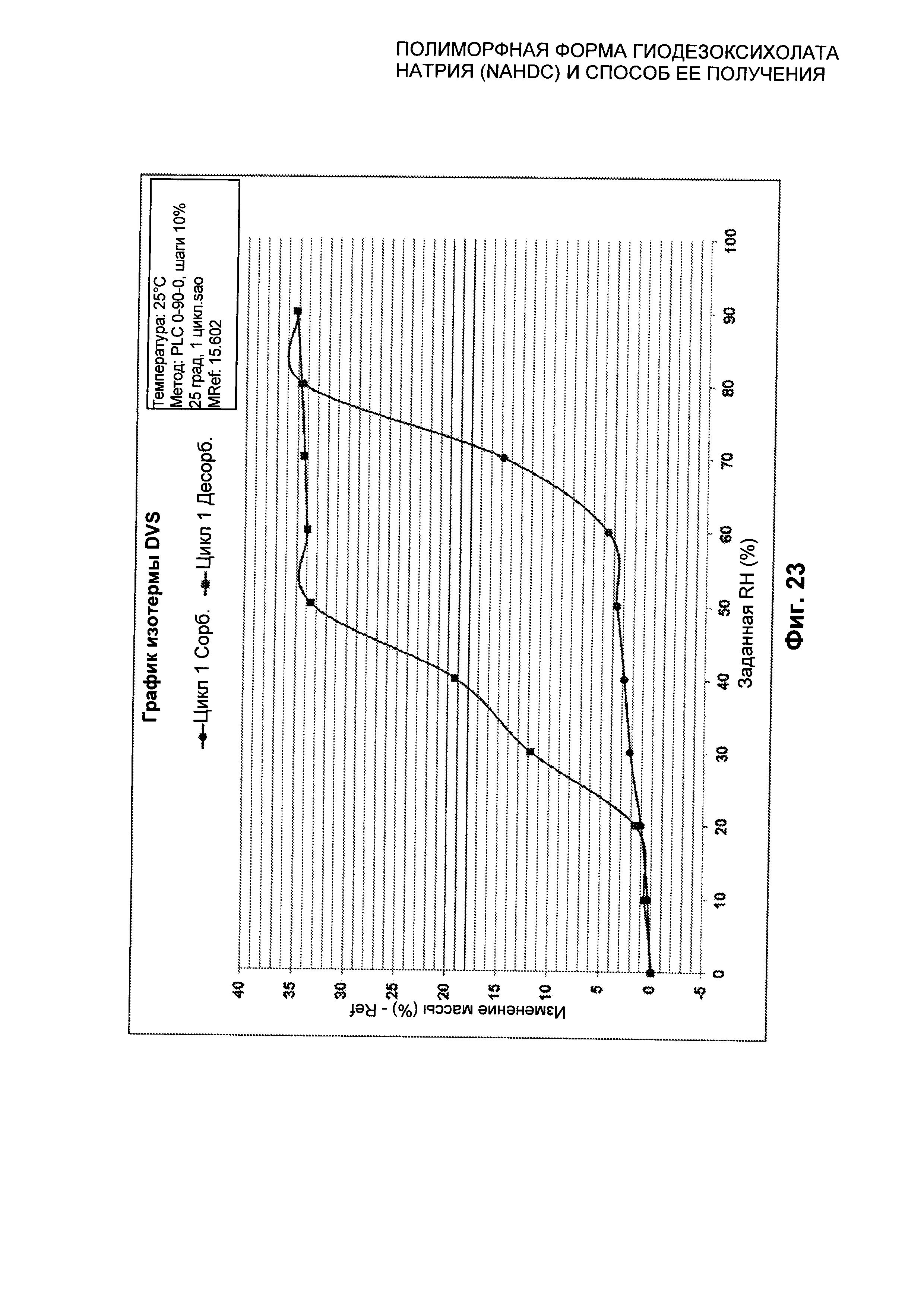
На Фиг. 23 представлена изотерма при 25°C безводной кристаллической формы FI NaHDC.
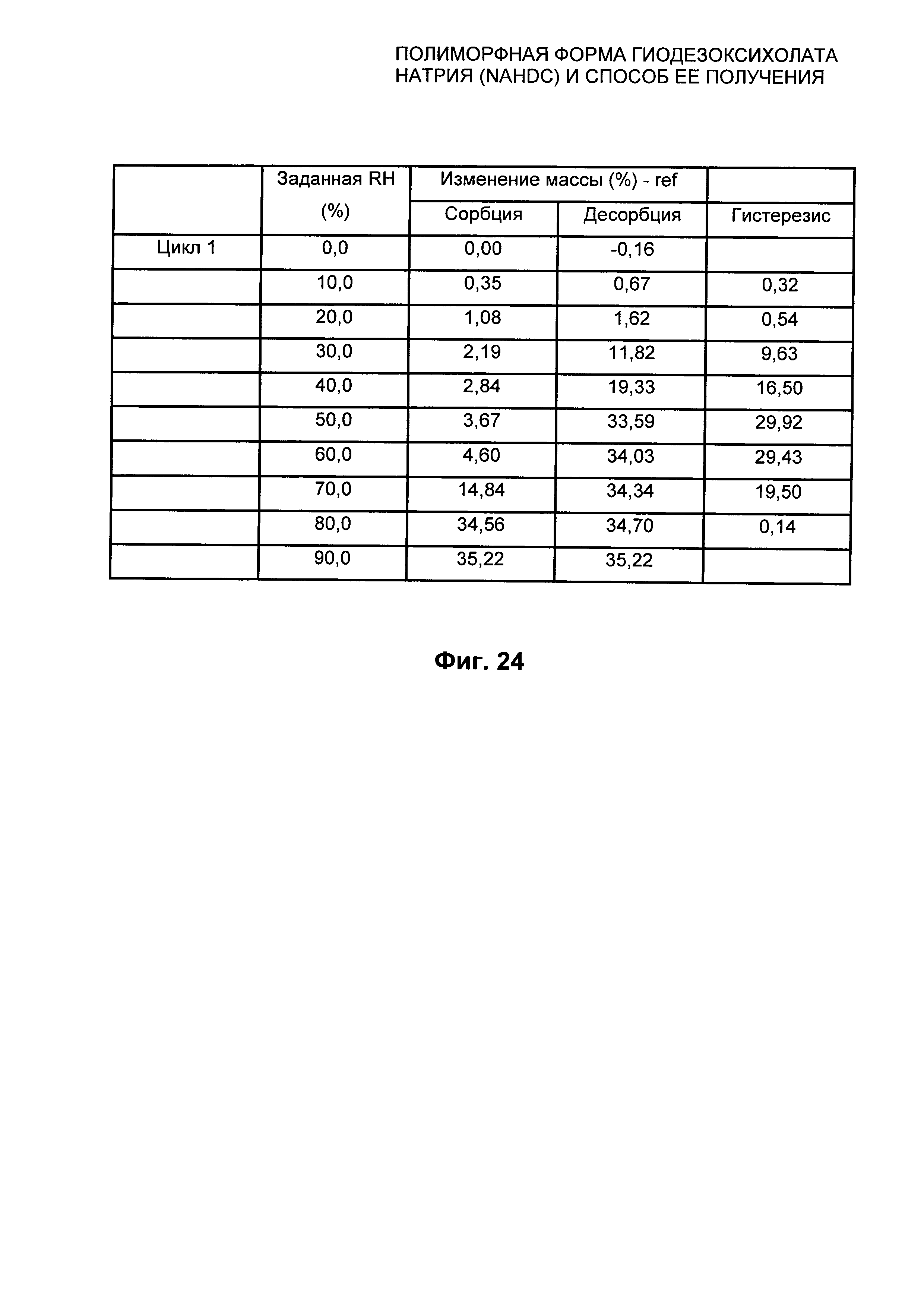
На Фиг. 24 представлены относительные показатели изотермы при 25°C из Фиг. 23 безводной кристаллической формы FI NaHDC.
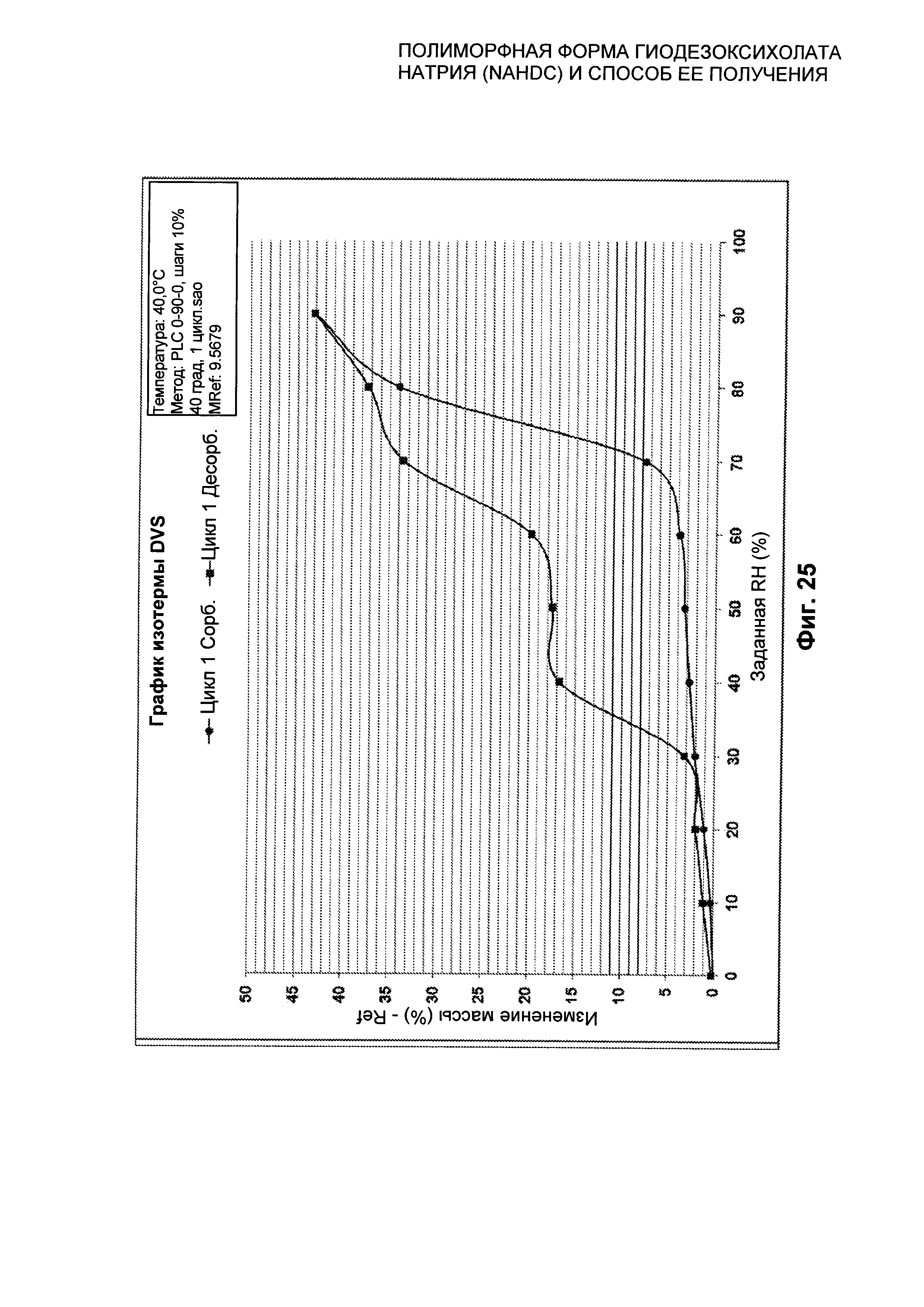
На Фиг. 25 представлена изотерма при 40°C безводной кристаллической формы FI NaHDC.
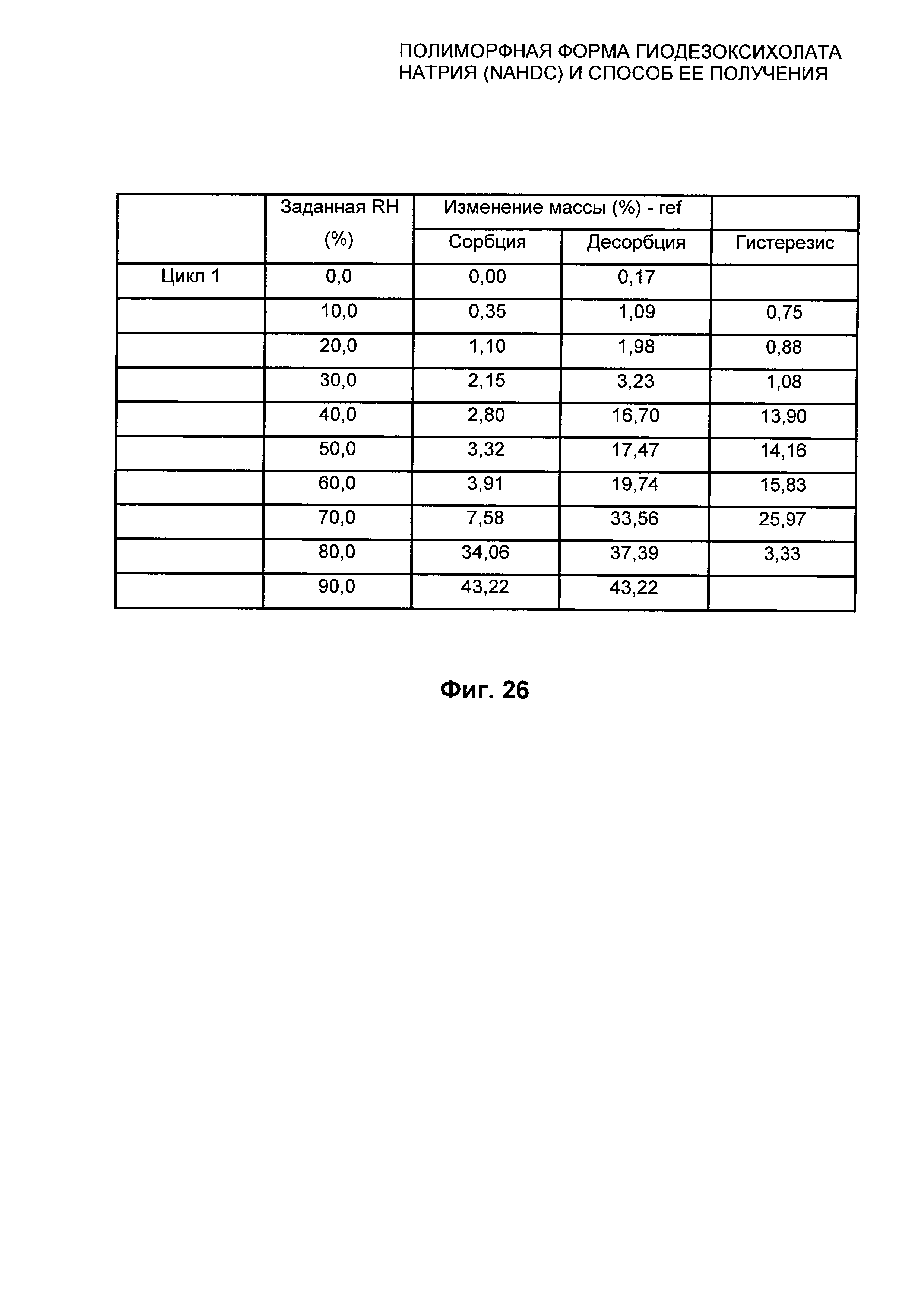
На Фиг. 26 представлены относительные показатели изотермы при 40°C из Фиг. 25 безводной кристаллической формы FI NaHDC.
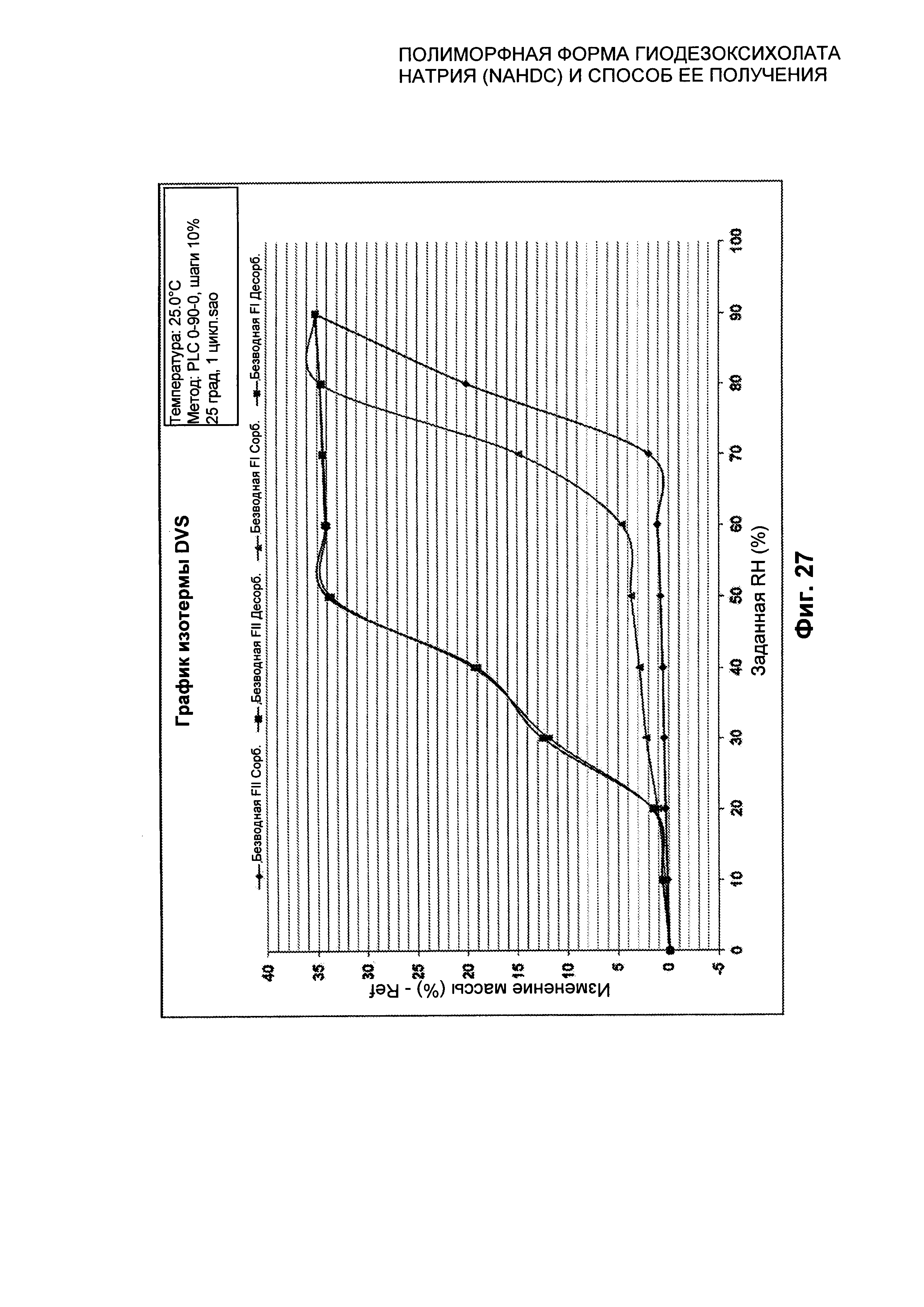
На Фиг. 27 представлено сравнение изотерм при 25°C безводной формы FI NaHDC и безводной формы FII NaHDC.
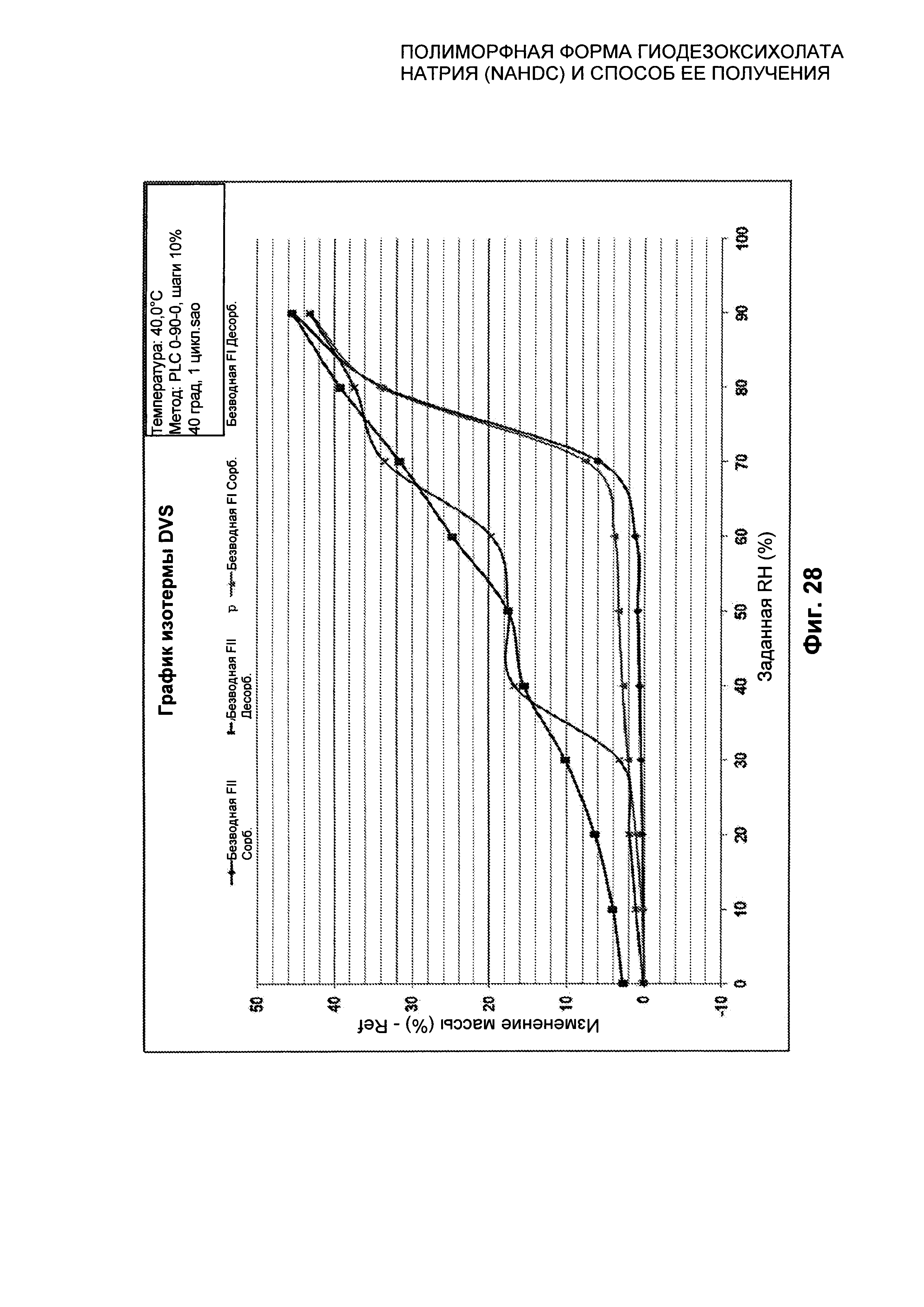
Фиг. 28: представлено сравнение изотерм при 40°C безводной формы FI NaHDC и безводной формы FII NaHDC.
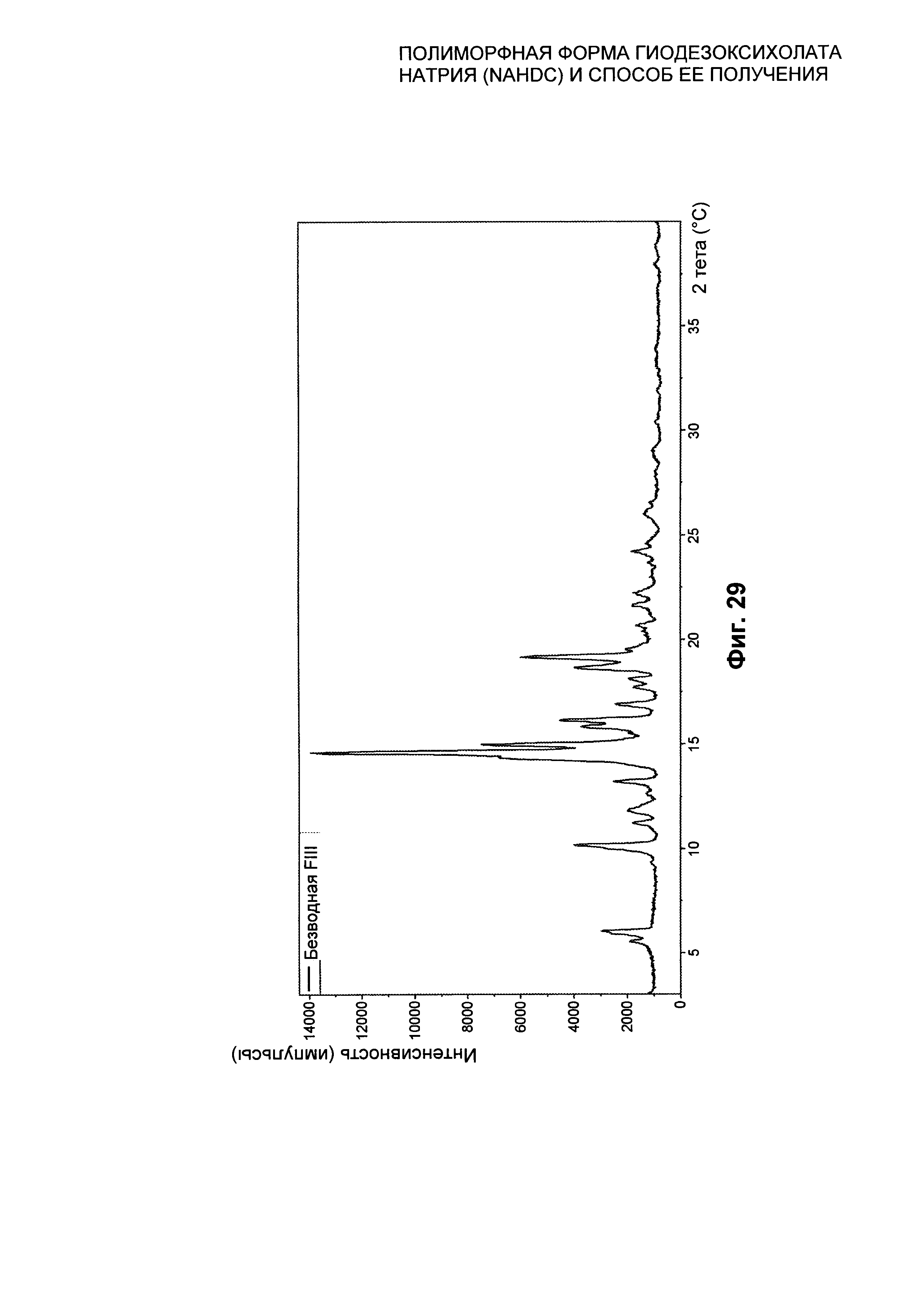
На Фиг. 29 представлена рентгеновская дифрактограмма на порошке (XPRD) безводной кристаллической формы III (FIII) NaHDC.
На Фиг. 30 представлены значения 2 тета пиков XPRD из Фиг. 29 для безводной кристаллической формы FIII вместе с соответствующей относительной интенсивностью. Пики, выделенные жирным шрифтом, могут быть определены как характеристические пики Формы III (FIII).
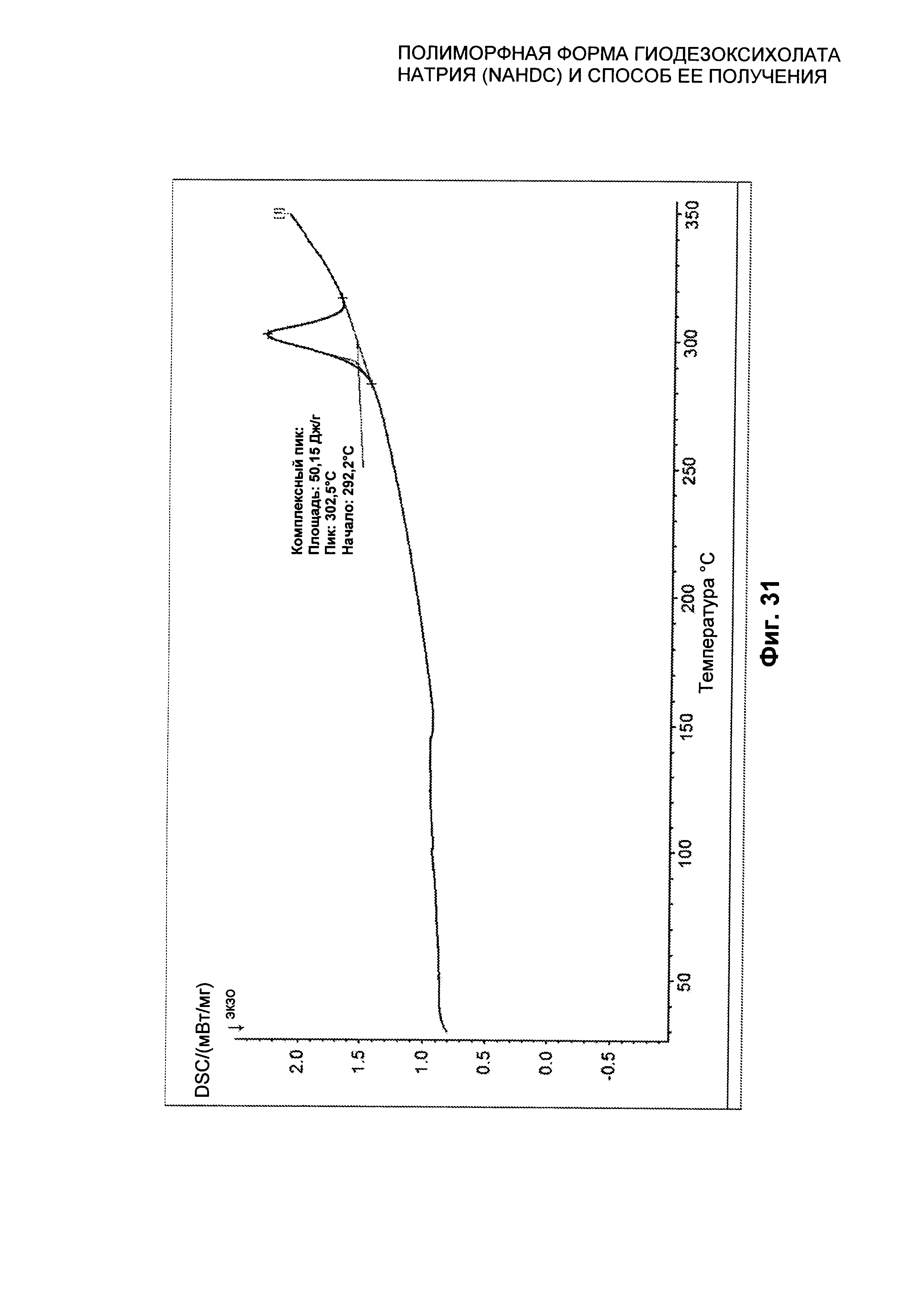
На Фиг. 31 представлен профиль дифференциальной сканирующей калориметрии (DSC) безводной кристаллической формы FIII NaHDC.
На Фиг. 32 представлен термогравиметрический профиль (TGA) безводной кристаллической формы FIII NaHDC.
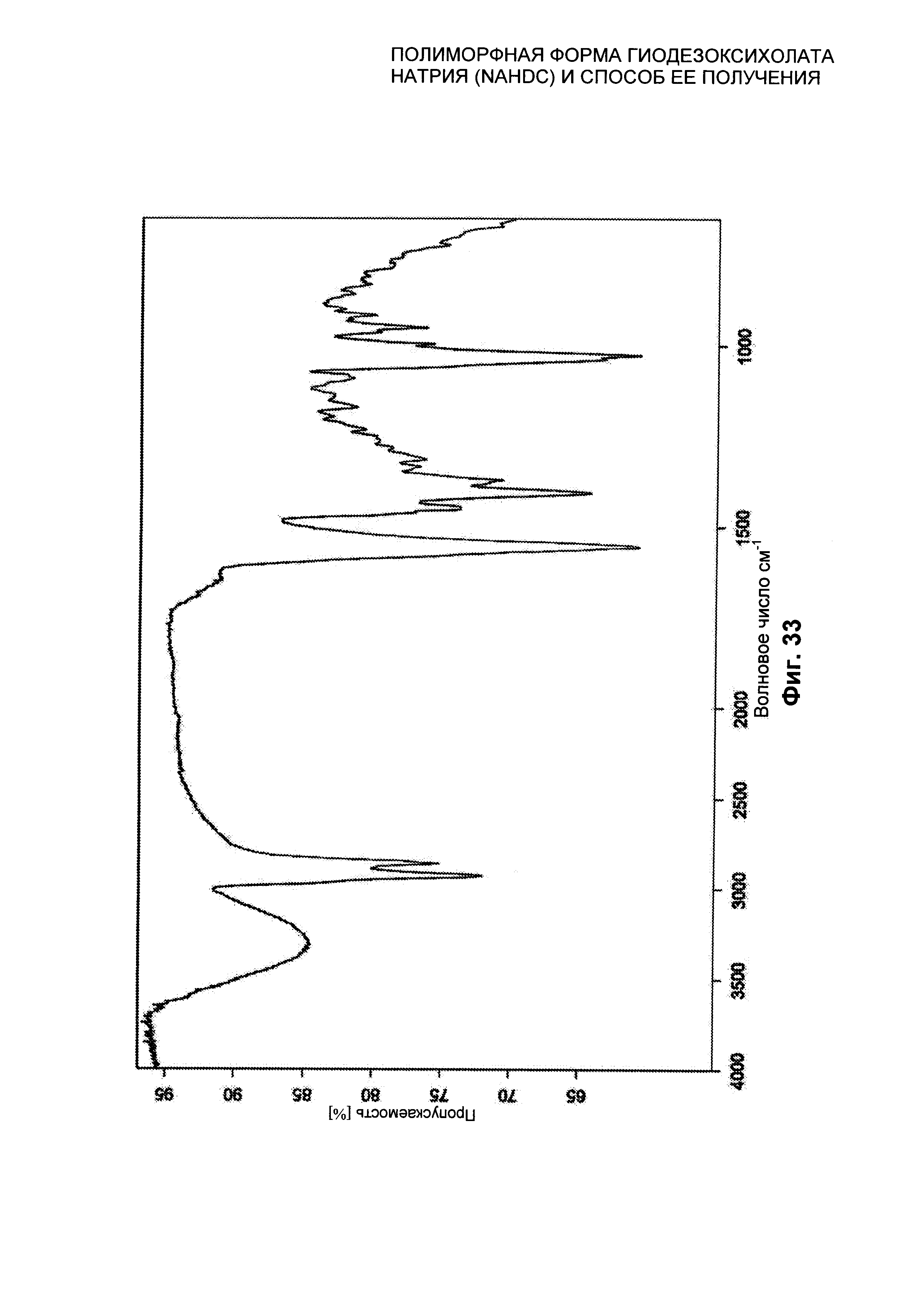
На Фиг. 33 представлен FT-IR/ATR спектр безводной кристаллической формы FIII NaHDC.
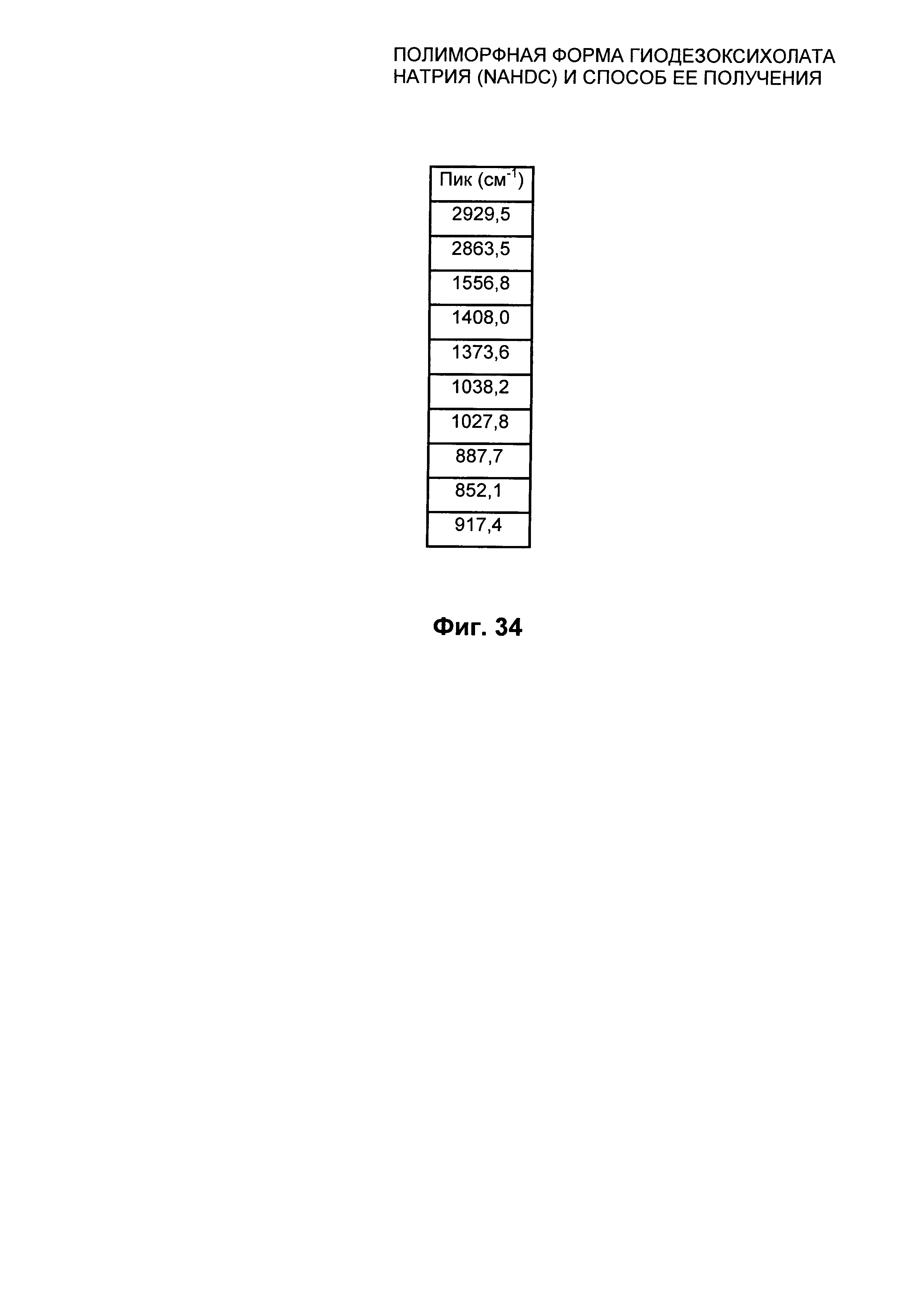
На Фиг. 34 представлены значения в см-1 характеристических пиков FT-IR/ATR из Фиг. 33 для безводной кристаллической формы FIII NaHDC.
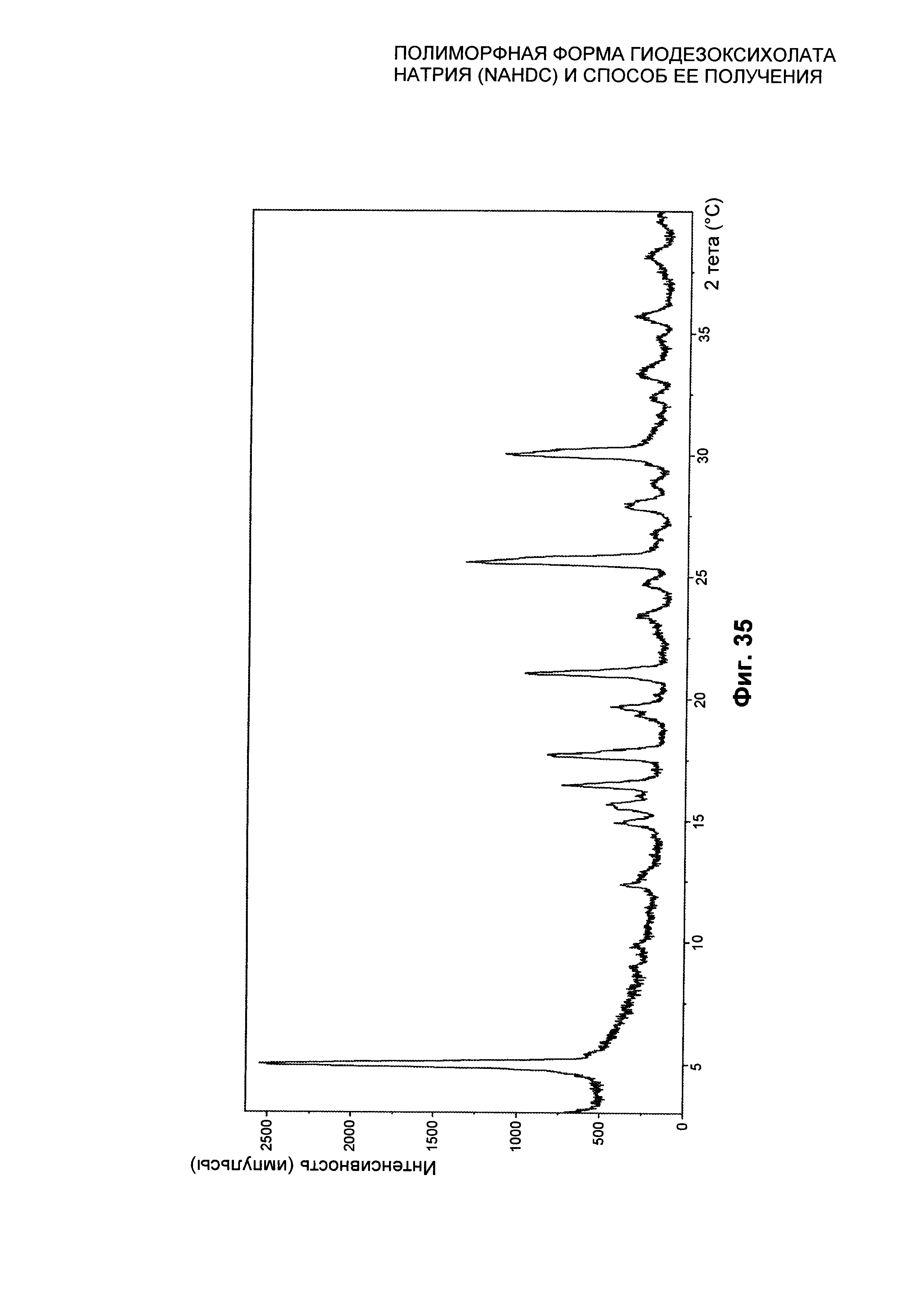
На Фиг. 35 представлена рентгеновская дифрактограмма на порошке (XPRD) гидратированной кристаллической формы SI NaHDC.
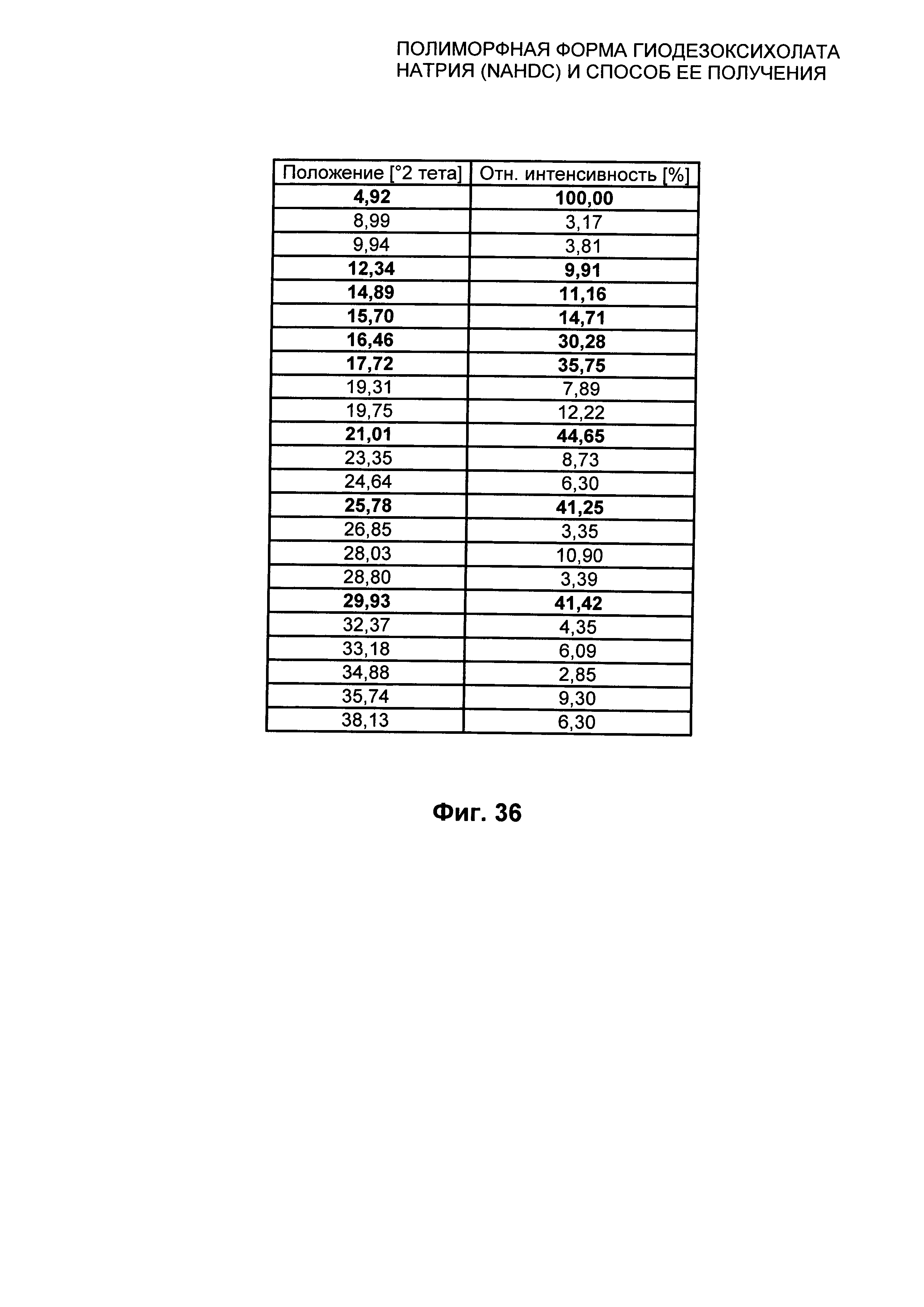
На Фиг. 36 представлены значения 2 тета пиков XPRD из Фиг. 35 для гидратированной кристаллической формы SI вместе с соответствующей относительной интенсивностью. Пики, выделенные жирным шрифтом, могут быть определены как характеристические пики Формы SI (SI).
На Фиг. 37 представлен профиль дифференциальной сканирующей калориметрии (DSC) гидратированной кристаллической формы SI (SI) NaHDC.
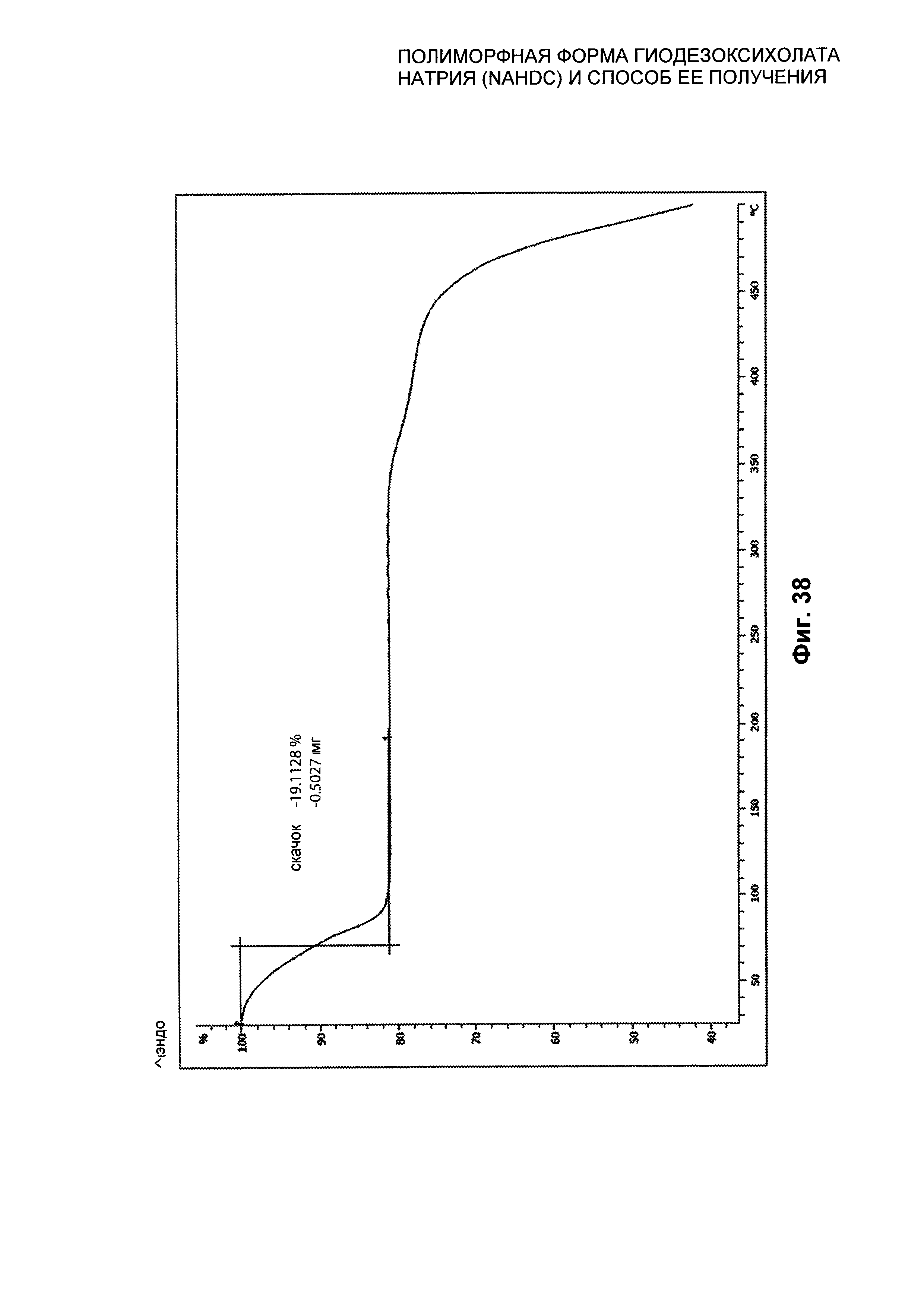
На Фиг. 38 представлен термогравиметрический профиль (TGA) гидратированной кристаллической формы SI NaHDC.
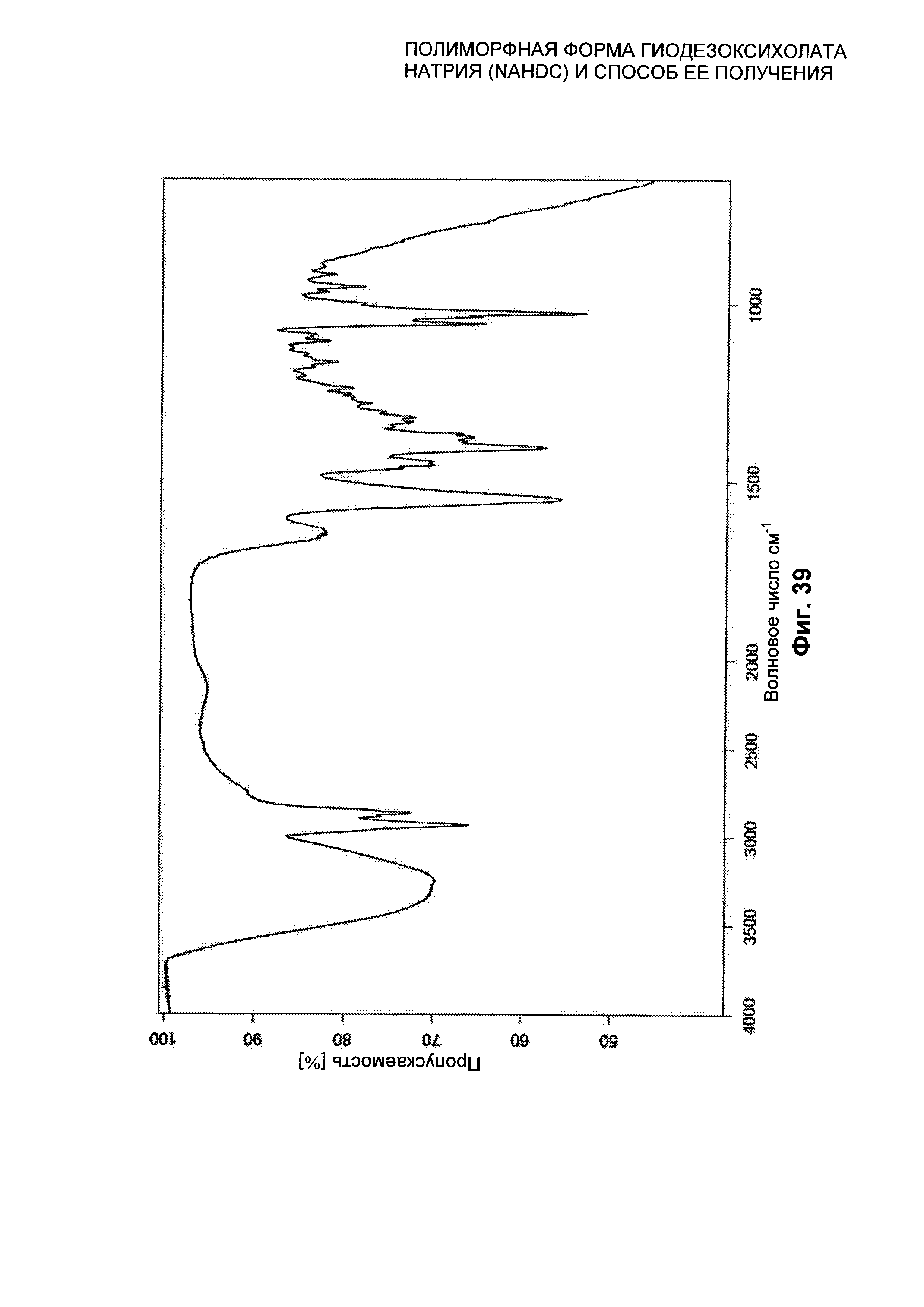
На Фиг. 39 представлен FT-IR/ATR спектр гидратированной кристаллической формы SI NaHDC.
На Фиг. 40 представлена рентгеновская дифрактограмма на порошке (XPRD) гидратированной кристаллической формы SII (SII) NaHDC.
На Фиг. 41 представлены значения 2 тета пиков XPRD из Фиг. 40 для гидратированной кристаллической формы SII вместе с соответствующей относительной интенсивностью. Пики, выделенные жирным шрифтом, могут быть определены как характеристические пики Формы SII (SII).
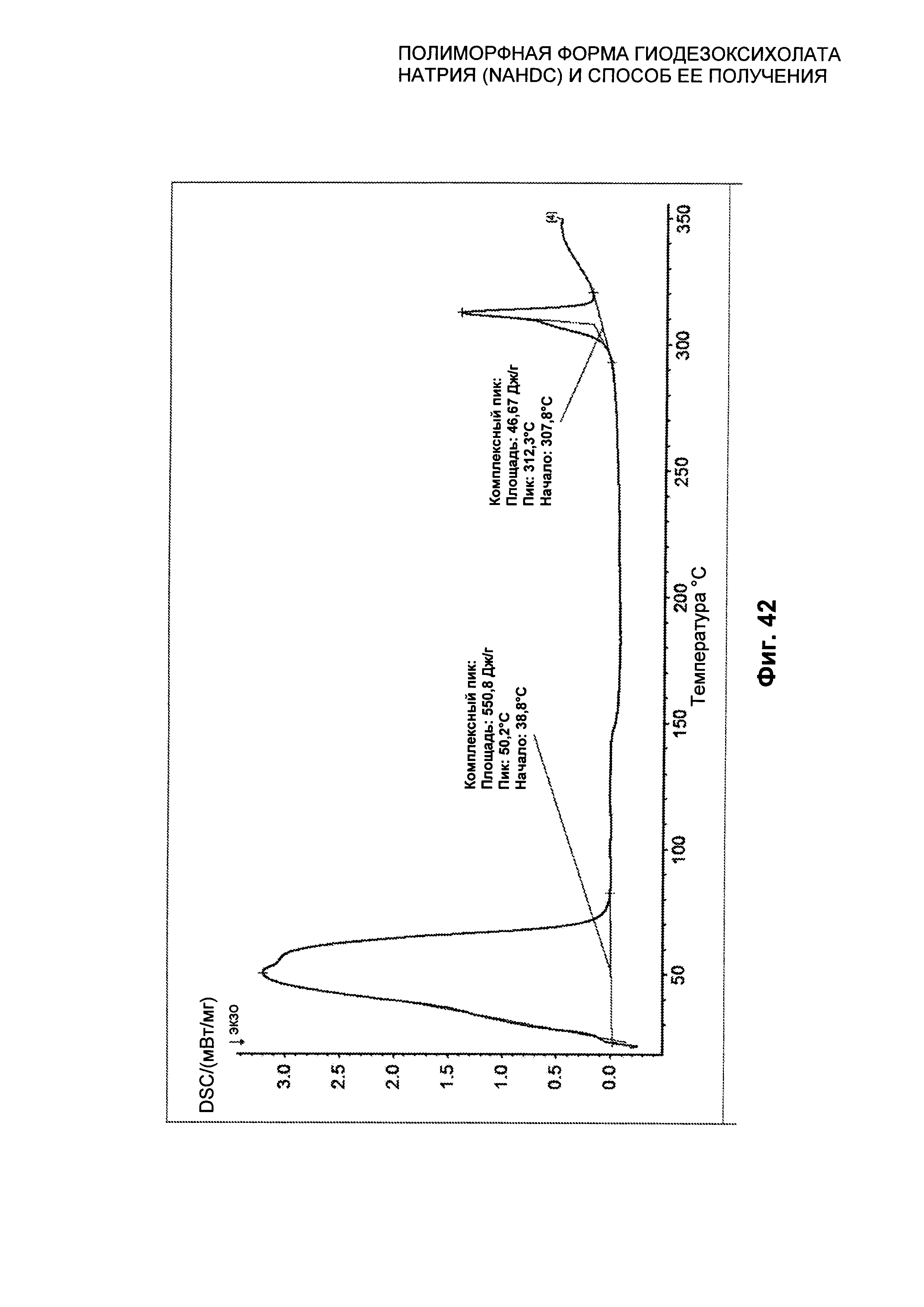
На Фиг. 42 представлен профиль дифференциальной сканирующей калориметрии (DSC) гидратированной кристаллической формы SII NaHDC.
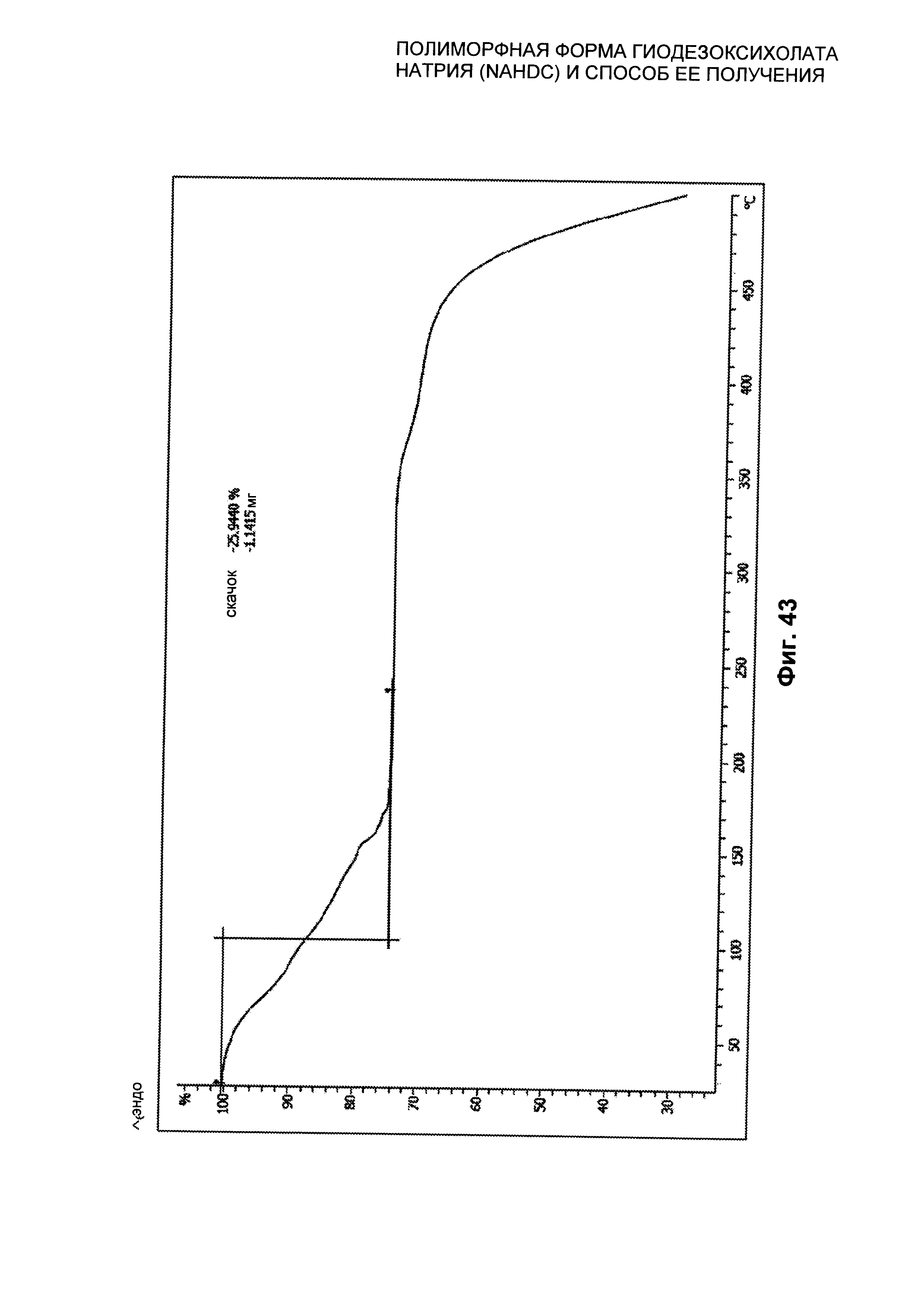
На Фиг. 43 представлен термогравиметрический профиль (TGA) гидратированной кристаллической формы SII NaHDC.
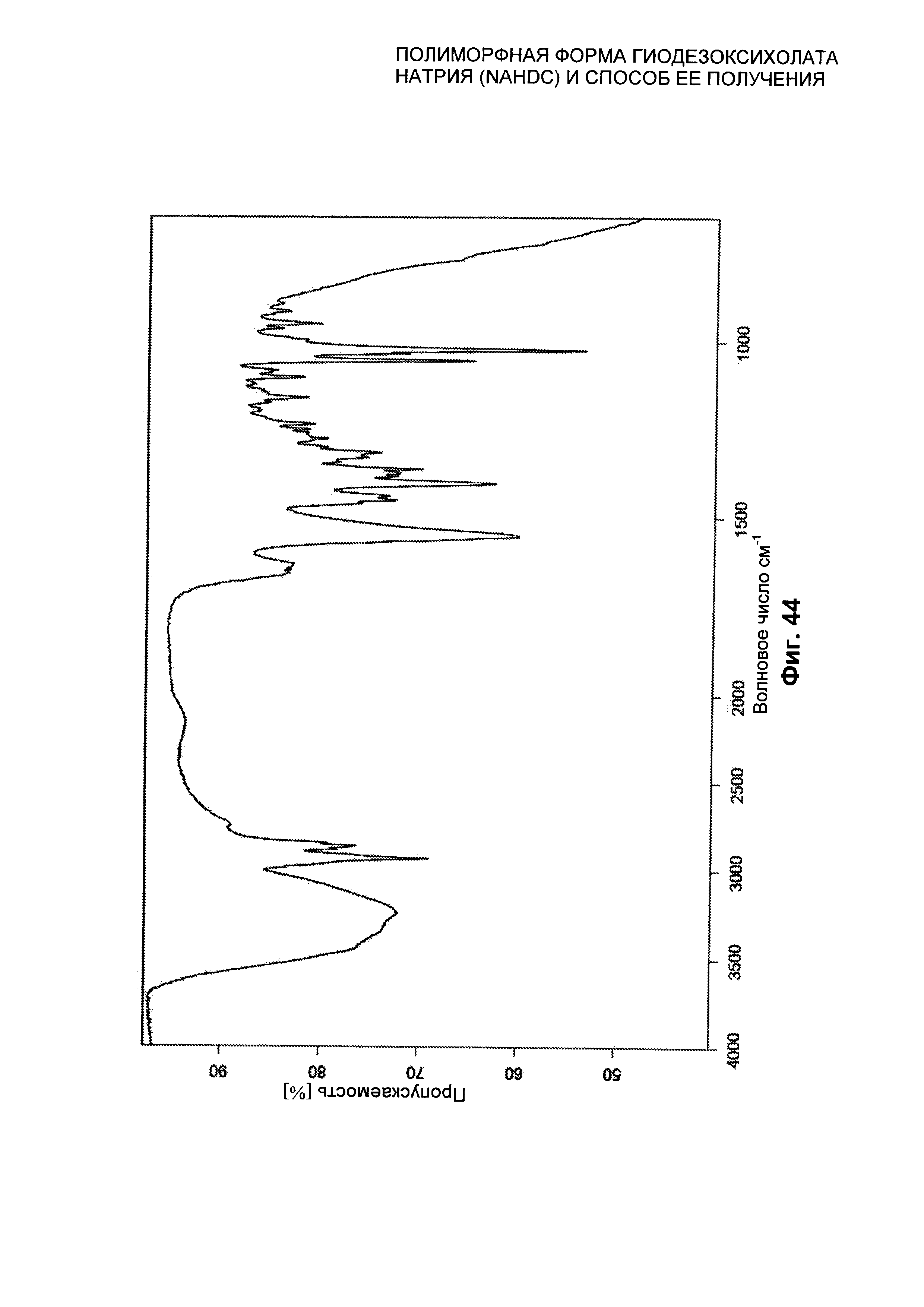
На Фиг. 44 представлен FT-IR/ATR спектр гидратированной кристаллической формы SII (SII) NaHDC.
На Фиг. 45 представлена рентгеновская дифрактограмма на порошке (XPRD) аморфной формы NaHDC.
На Фиг. 46 представлены значения 2 тета пиков XPRD из Фиг. 45 для аморфной формы NaHDC вместе с соответствующей относительной интенсивностью. Пики, выделенные жирным шрифтом, могут быть определены как характеристические пики аморфной формы.
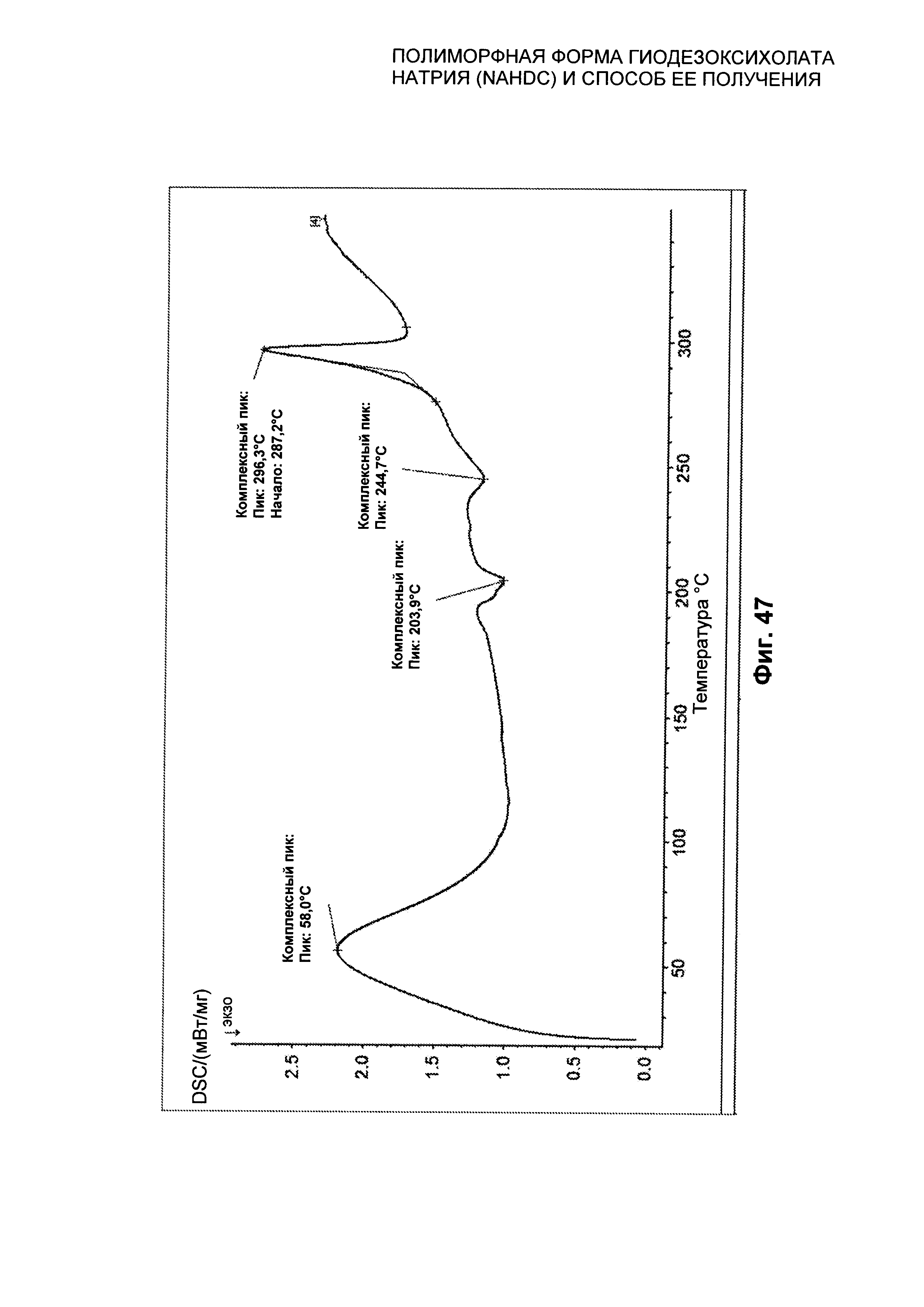
На Фиг. 47 представлен профиль дифференциальной сканирующей калориметрии (DSC) аморфной формы NaHDC.
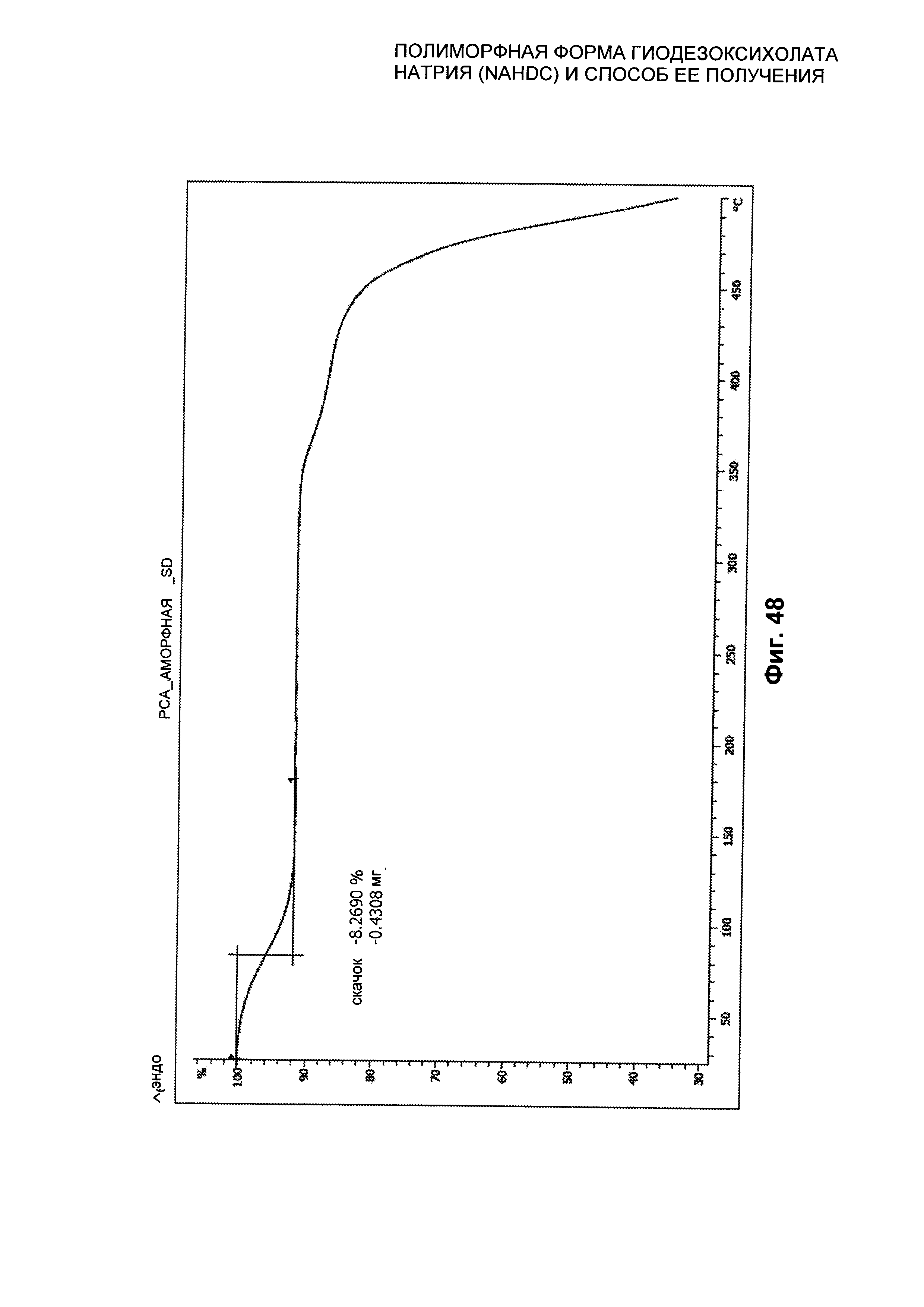
На Фиг. 48 представлен термогравиметрический профиль (TGA) аморфной формы NaHDC.
На Фиг. 49 представлен FT-IR/ATR спектр аморфной формы NaHDC.
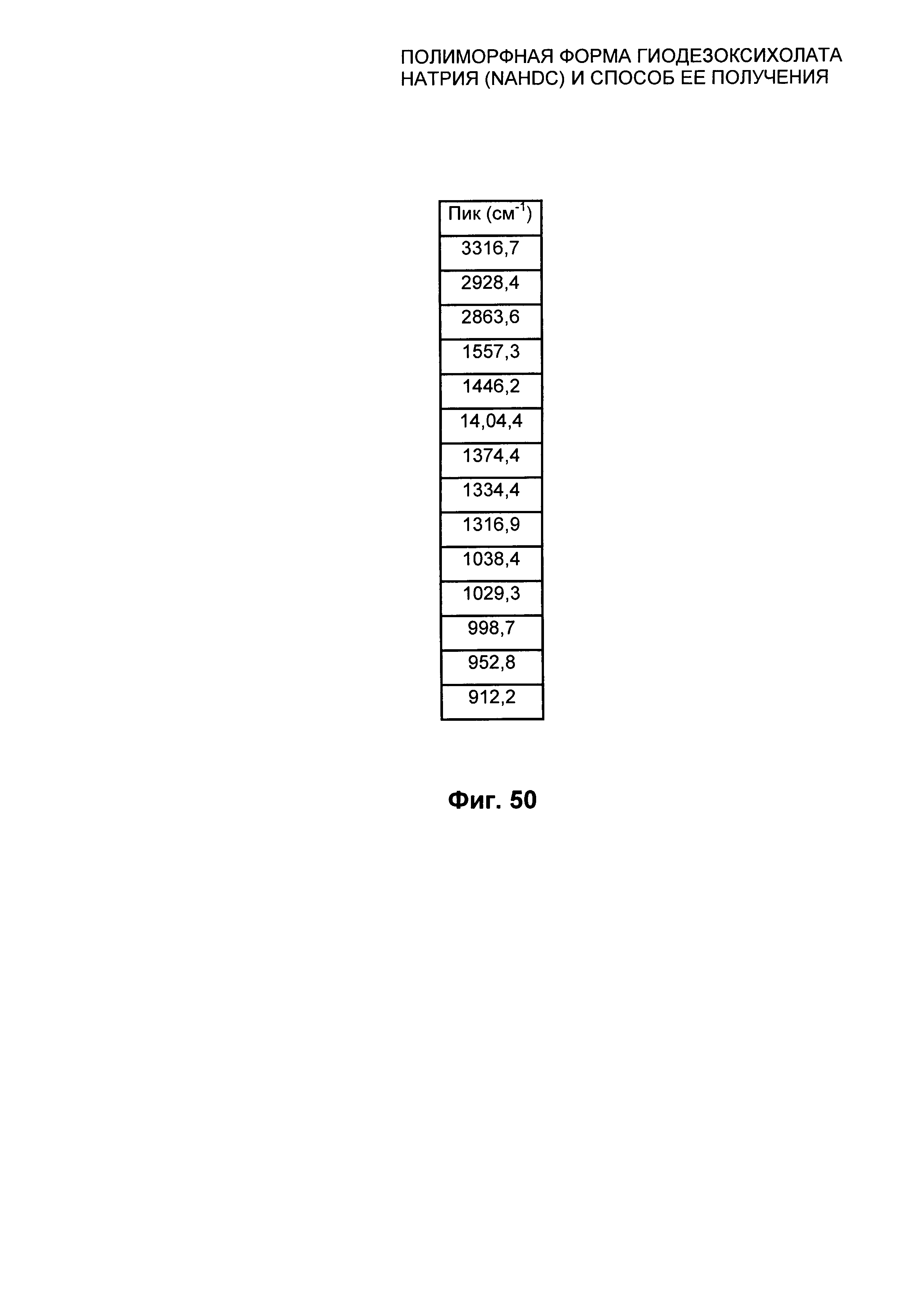
На Фиг. 50 представлены значения в см-1 характеристических пиков FT-IR/ATR из Фиг. 49 для аморфной формы NaHDC.
На Фиг. 51 представлена изотерма при 25°C аморфной формы NaHDC.
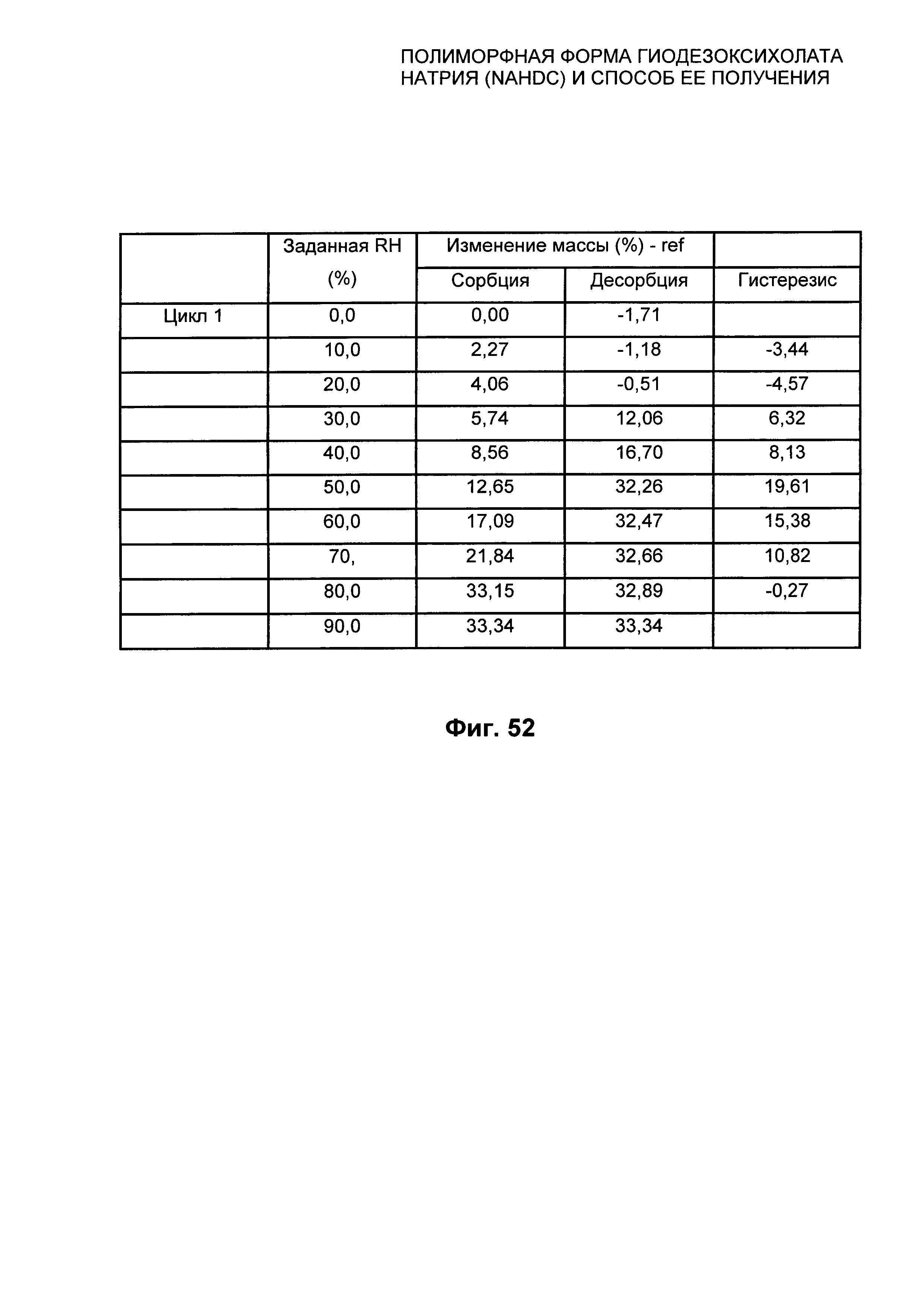
На Фиг. 52 представлены относительные показатели изотермы при 25°C из Фиг. 51 аморфной формы NaHDC.
На Фиг. 53 представлена рентгеновская дифрактограмма на порошке (XPRD) смеси NaHDC.
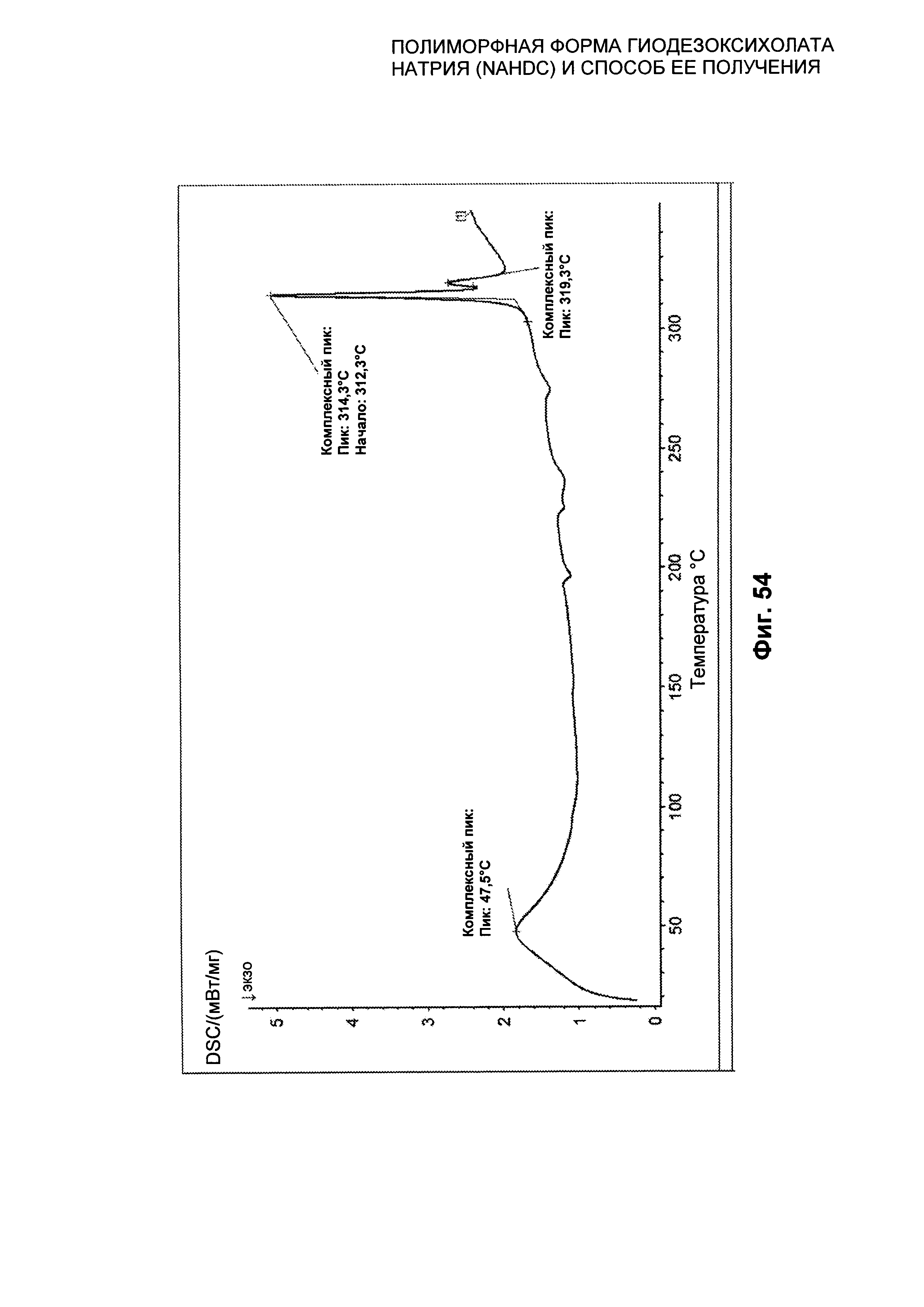
На Фиг. 54 представлен профиль дифференциальной сканирующей калориметрии (DSC) смеси NaHDC.
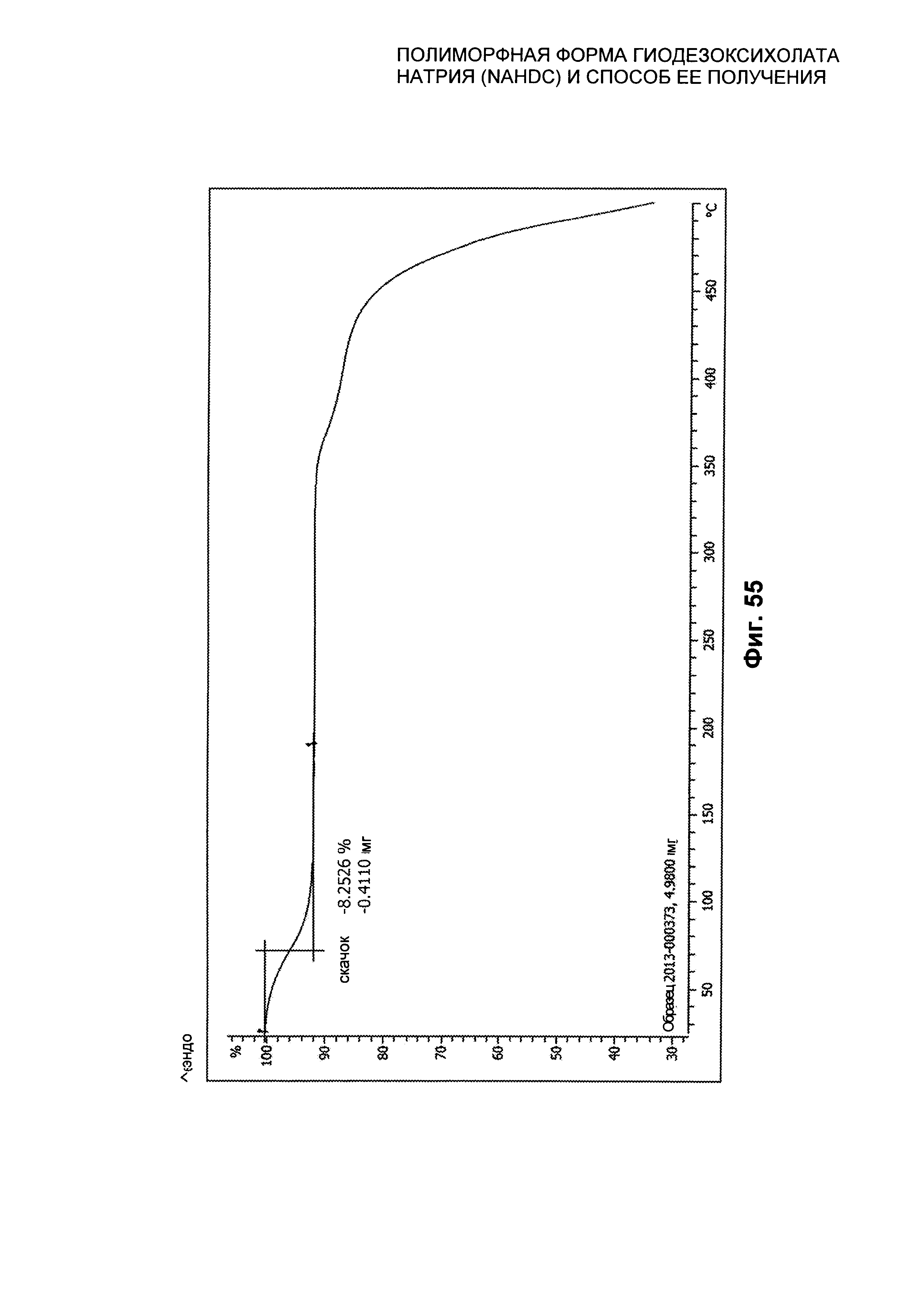
На Фиг. 55 представлен термогравиметрический профиль (TGA) смеси NaHDC.
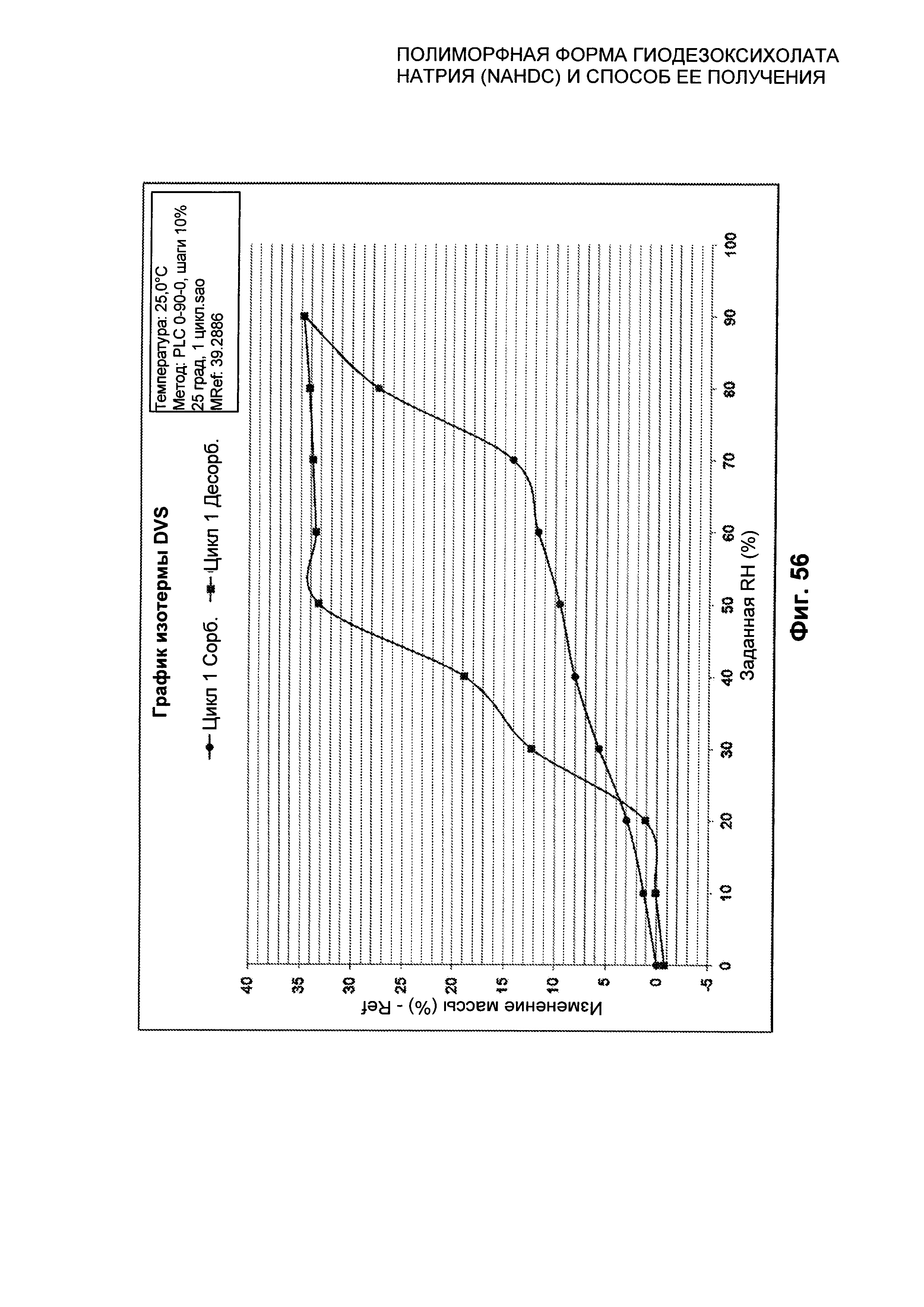
На Фиг. 56 представлена изотерма при 25°C смеси NaHDC.
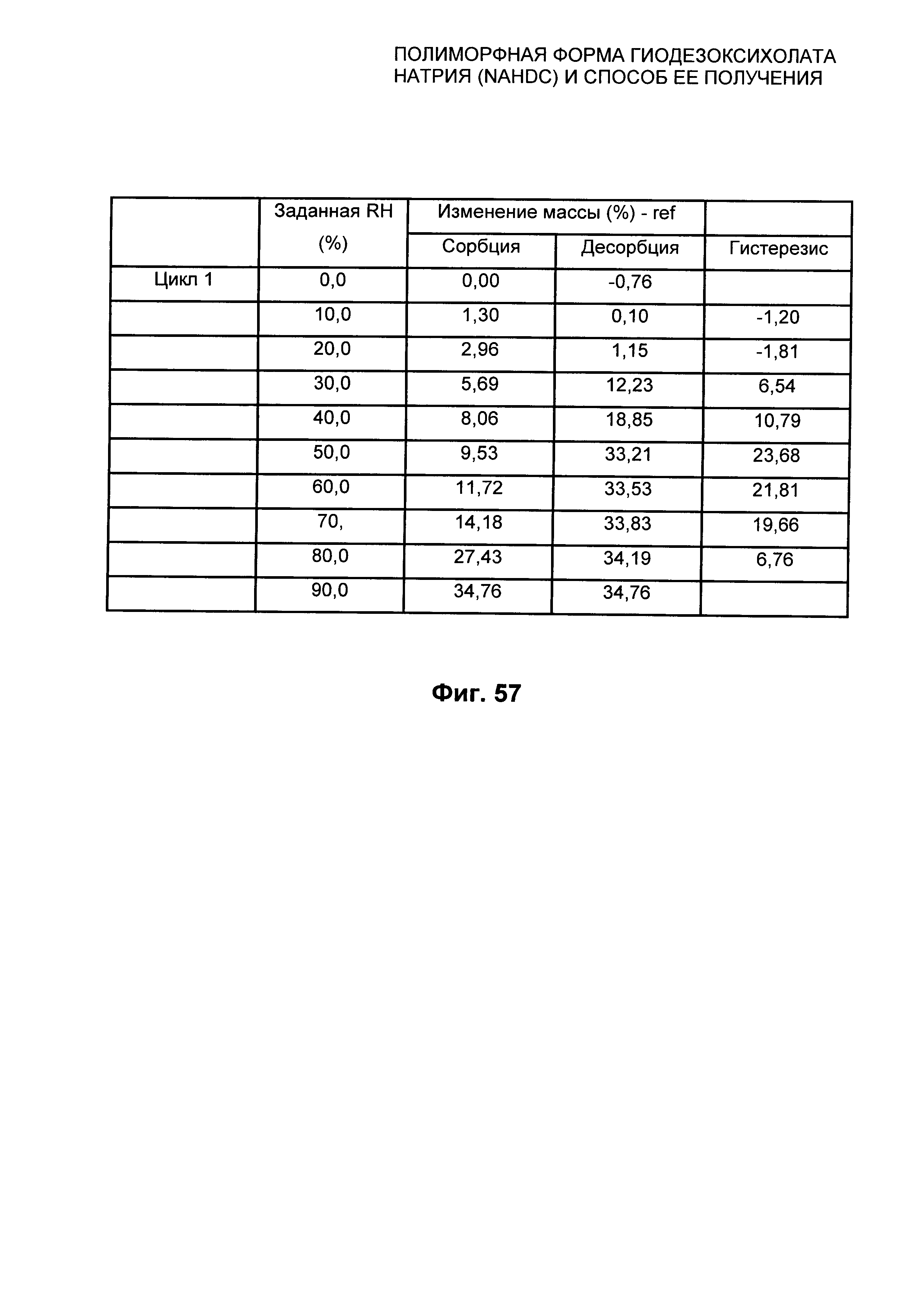
На Фиг. 57 представлены относительные показатели изотермы при 25°C из Фиг. 56 смеси NaHDC.
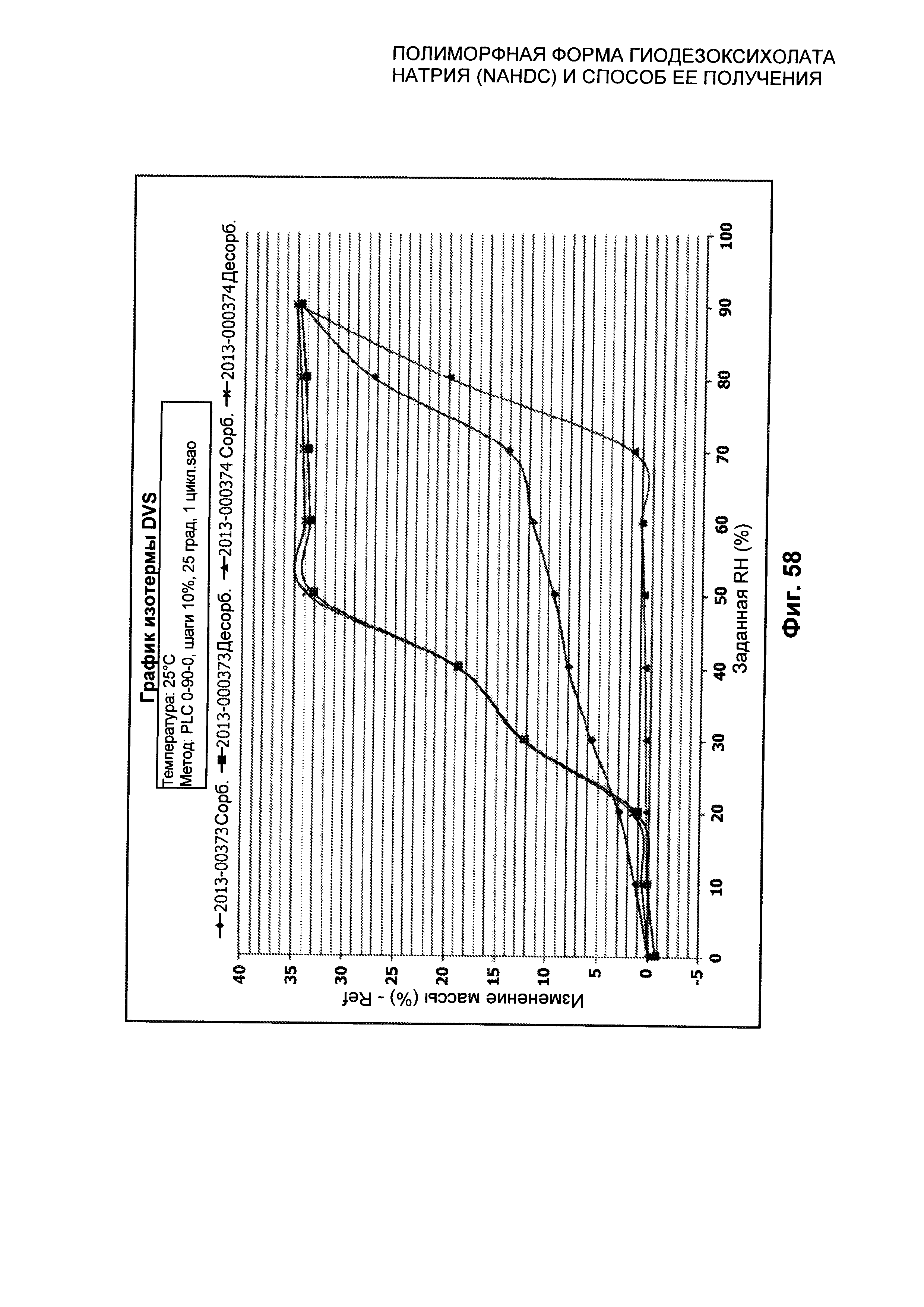
На Фиг. 58 представлено сравнение изотерм при 25°C смеси NaHDC и безводной формы FII NaHDC.
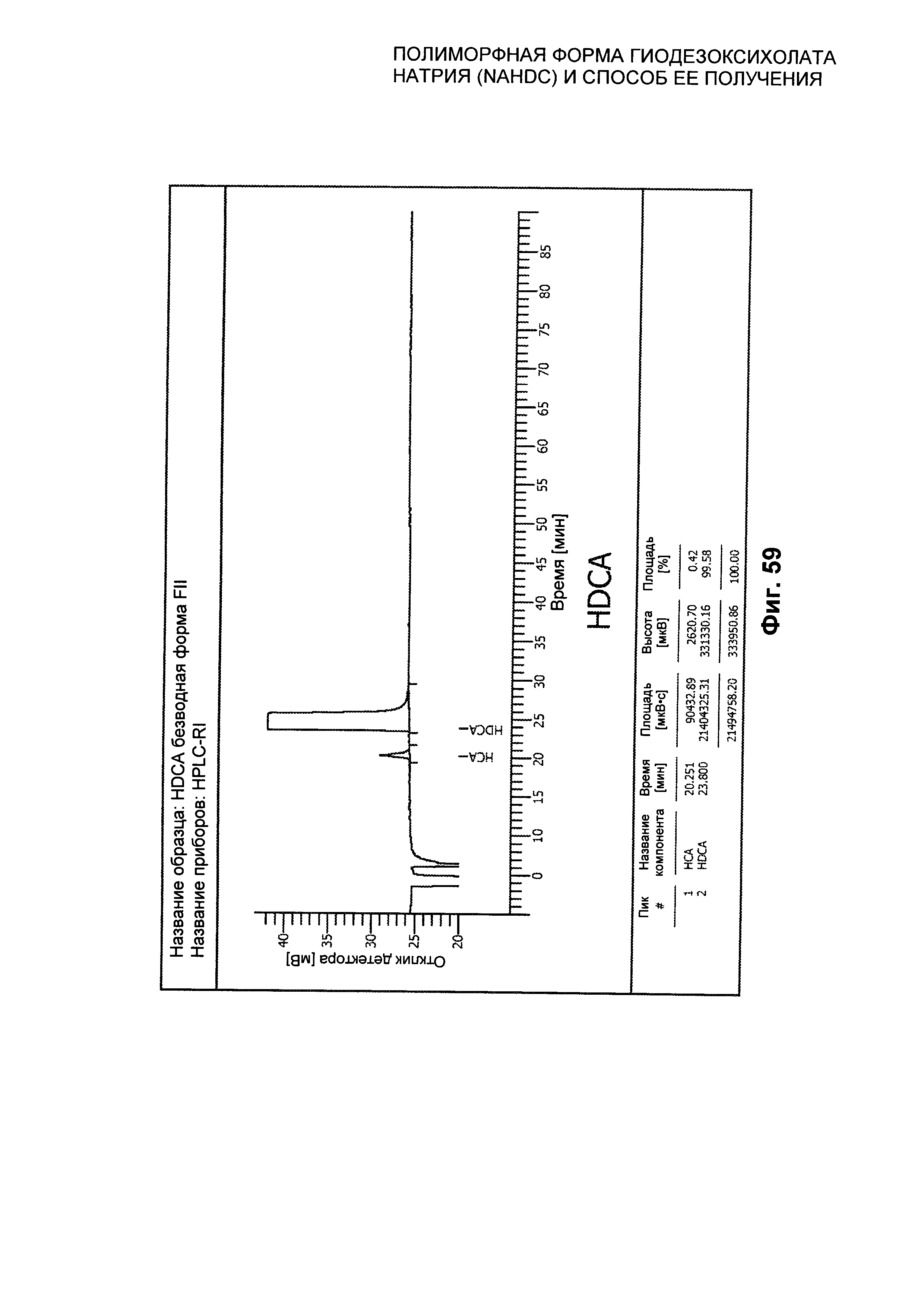
На Фиг. 59 представлен профиль HPLC (хроматограмма) полиморфной формы FN NaHDC в кислотной форме в виде HDCA.
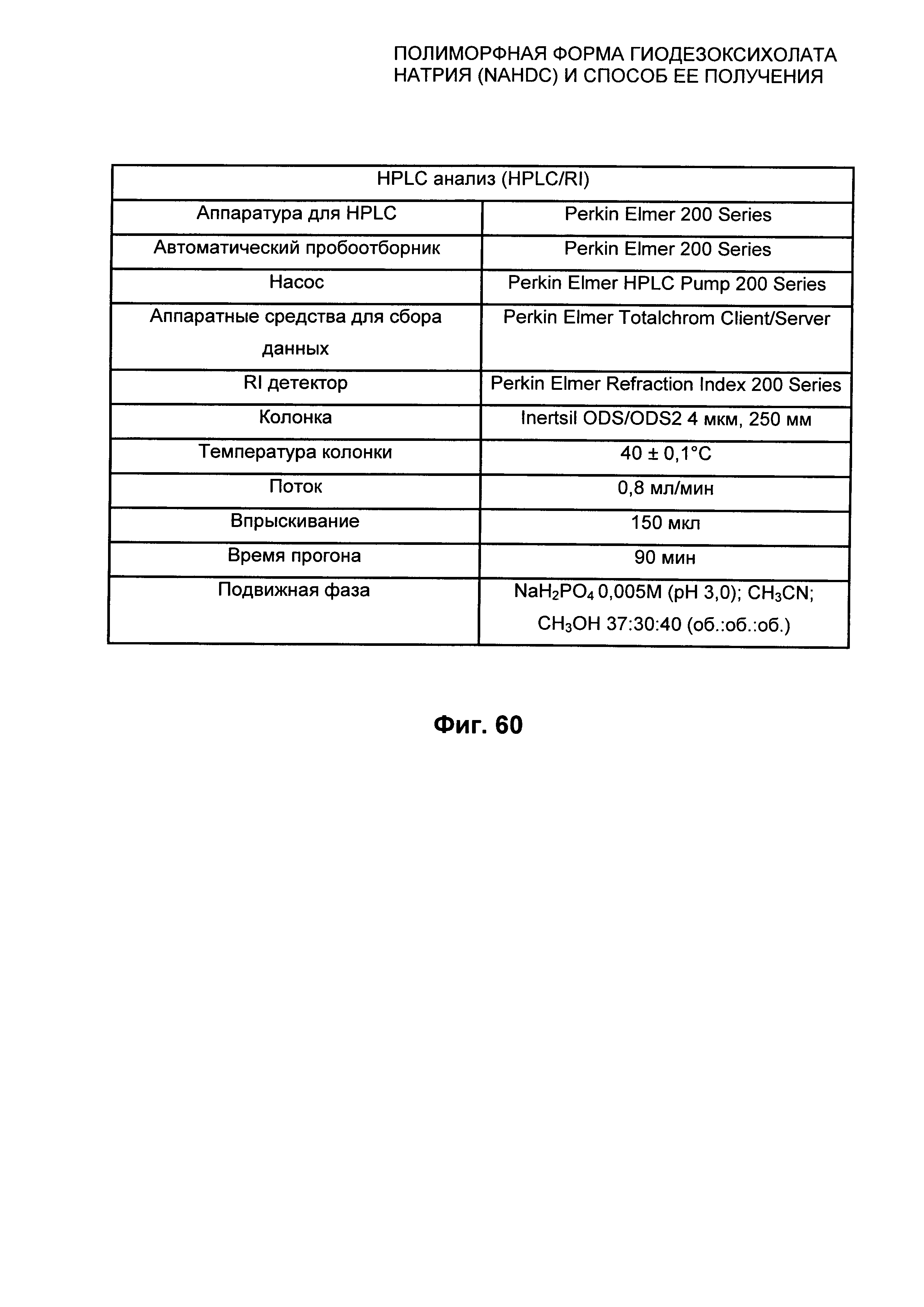
На Фиг. 60 представлен метод HPLC-анализа чистоты полиморфной формы FII NaHDC в кислотной форме в виде HDCA и приборы.
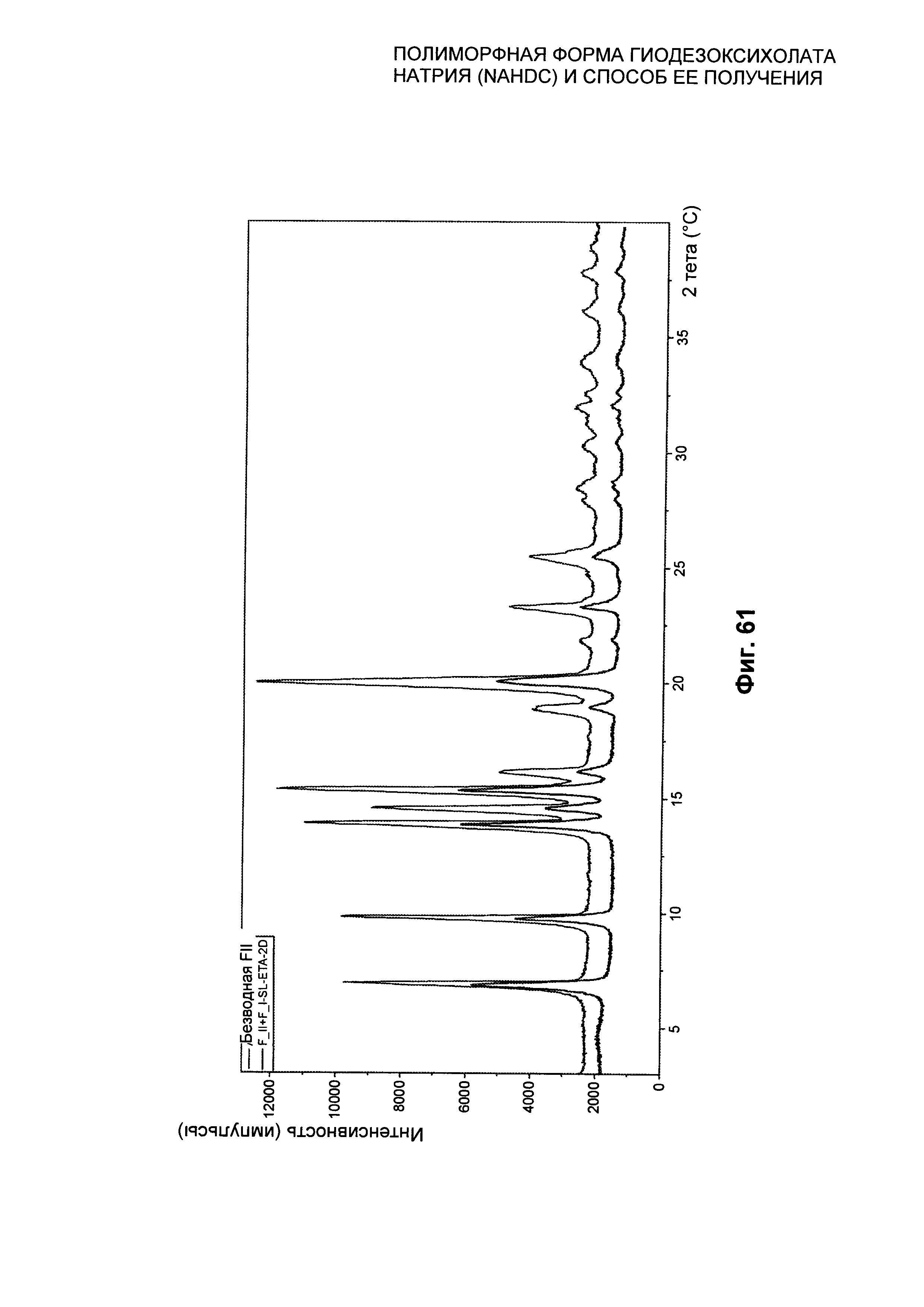
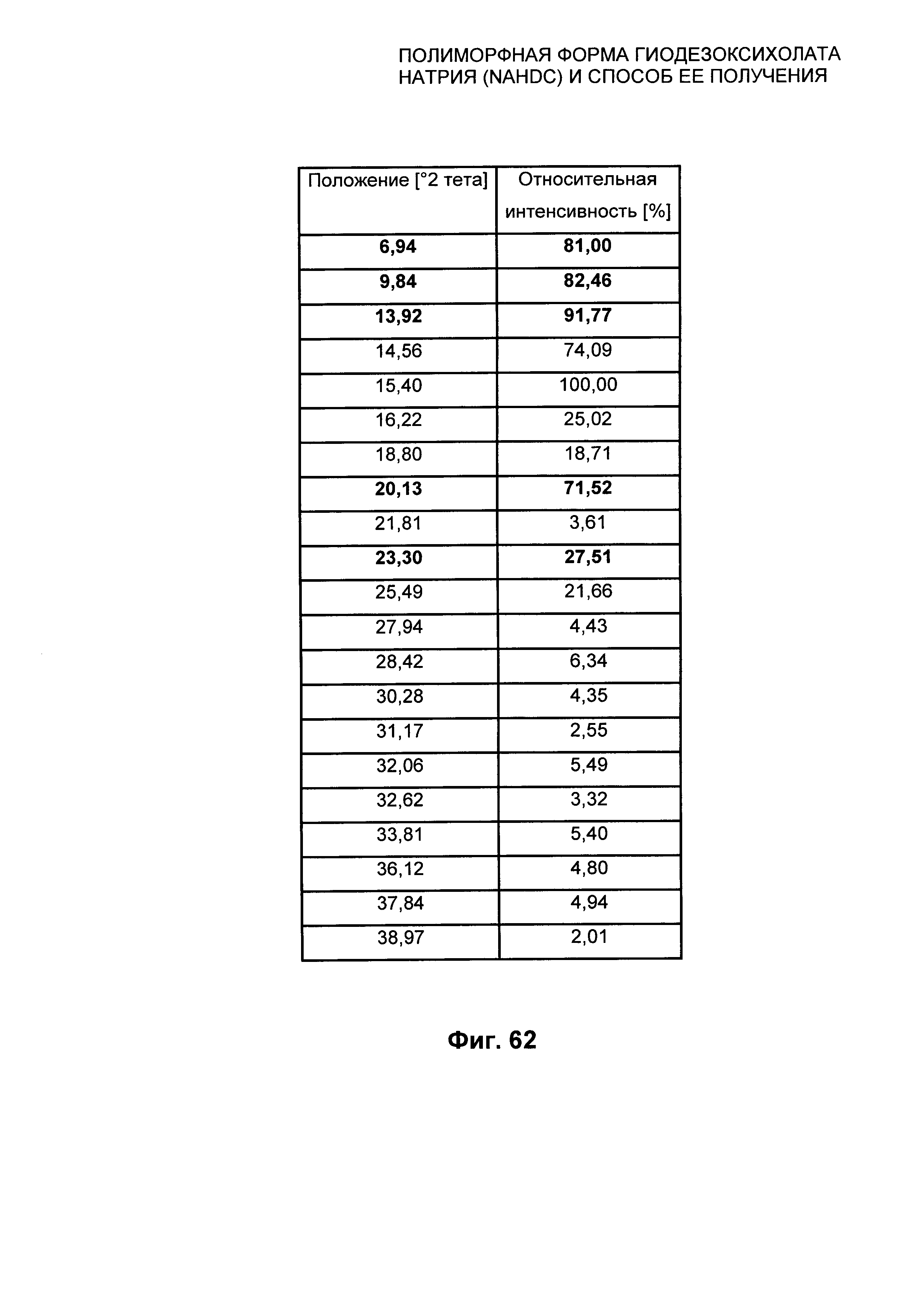
На Фиг. 61 представлена рентгеновская дифрактограмма на порошке (XPRD) полиморфной формы FII NaHDC, полученной путем смешивания полиморфной формы FI NaHDC и полиморфной формы FII NaHDC в соотношении 1:1 (масс./масс.) после переосаждения в этилацетате в течение 48 часов при температуре 25°C.
На Фиг. 62 представлены значения 2 тета пиков XPRD из Фиг. 61 для полиморфной формы FII NaHDC вместе с соответствующей относительной интенсивностью. Пики, выделенные жирным шрифтом, могут быть определены как характеристические пики Формы II (FII).
Таким образом, объектом настоящего изобретения является гиодезоксихолат натрия в полиморфной форме FII. Количество воды в кристалле полиморфной формы FII NaHDC составляет менее 1%, предпочтительно менее 0,6%, и еще более предпочтительно оно составляет менее 0,4%, где указанные проценты являются процентами относительно общей массы кристалла.
Полиморфная форма FII NaHDC характеризуется профилем рентгеновской дифрактограммы на порошке (XPRD), который представлен в качестве примера на Фиг. 1, и/или профилем дифференциальной сканирующей калориметрии (DSC), который представлен в качестве примера на Фиг. 3, и/или термогравиметрическим профилем (TGA), который представлен в качестве примера на Фиг. 6, и/или FT-IR/ATR спектром, который представлен на Фиг. 7, FT-RAMAN спектром, который представлен в качестве примера на Фиг. 9, анализом динамической сорбции пара (DVS) в изотерме при 25°C, который представлен в качестве примера на Фиг. 10, и анализом динамической сорбции пара (DVS) в изотерме при 40°C, который представлен в качестве примера на Фиг. 12.
Полиморфная форма FII NaHDC характеризуется XPRD профилем, представленным на Фиг. 1, характеристические пики которого находятся в следующих положениях 2 тета на Фиг. 2: 6,94; 9,84; 13,92; 20,13; 23,30 градусов, с пределом погрешности для значения, указанного для каждого пика, ±0,20 градусов 2 тета.
На Фиг. 2 указаны значения вышеупомянутых пиков XPRD полиморфной формы FII вместе с соответствующей относительной интенсивностью.
Полиморфная форма FII NaHDC характеризуется профилем DSC, представленным на Фиг. 3. На этом графике можно видеть эндотермический пик при 260°C с началом Пика при 263,5°C, Пиком при 268,9°C и энтальпией, равной 14,11 Дж/г, вследствие твердофазового перехода полиморфной формы FII NaHDC в полиморфную форму FI, что подтверждено анализом дифракции рентгеновских лучей на порошке (XPRD) при вариабельной температуре (смотри Фиг. 4 и 5). Следовательно, полиморфная форма FII не плавится и является стабильной вплоть до 260°C и при 280°C превращается в кристаллическую форму FI, которая будет описана ниже. Второй пик, который можно видеть на Фиг. 3, является эндотермическим пиком вследствие плавления полиморфной формы FI NaHDC при 310°C с началом Пика при 311,6°C, Пиком при 314,2°C и энтальпией плавления, равной 67,4 Дж/г.
Полиморфная форма FII NaHDC характеризуется профилем TGA, представленным на Фиг. 6. Профиль TGA демонстрирует начальную потерю массы примерно при 40°C, составляющую приблизительно 0,4%, которую можно отнести к поглощению воды, после чего потеря массы больше не наблюдается вплоть до 350°C, и это экспериментально подтверждает тот факт, что такая форма находится в ее "безводной" форме.
Полиморфная форма FII NaHDC характеризуется FT-IR/ATR спектром, представленным на Фиг. 7, характеристические пики которого находятся при следующих частотах на Фиг.8: 3254,5; 2958,9; 2917,3; 2874,6; 2851,0; 1560,7; 1474,9; 1454,7; 1443,6; 1394,2; 1347,4; 1292,9; 1261,0; 1245,7; 1218,6; 1161,2; 1002,3 см-1, с пределом погрешности для значения, указанного для каждого пика, ±1 см-1.
Полиморфная форма FII NaHDC характеризуется FT-RAMAN спектром, представленным на Фиг.9.
Полиморфная форма FII NaHDC характеризуется графиком DVS в изотерме при 25°C±0,1, который представлен в качестве примера на Фиг. 10, и соответствующими значениями, выраженными в %, которые указаны на Фиг. 11.
Полиморфная форма FII NaHDC характеризуется графиком DVS в изотерме при 40°C±0,1 который представлен в качестве примера на Фиг.12, и соответствующими значениями, выраженными в %, которые указаны на Фиг. 13.
Полиморфная форма FII в отличие от других описанных форм NaHDC имеет очень высокую стабильность в цикле сорбции влаги в изотерме при 25°C и при 40°C (смотри Фиг. 10, 11, 12 и 13). Как уже указано выше, полиморфная форма FII имеет негигроскопическую природу в отличие от всех остальных обнаруженных полиморфных форм (смотри Фиг. 27, 28 и 58) и, следовательно, она очень стабильна, и ее нетрудно хранить. Эта природа является абсолютно неожиданной для других натриевых солей желчных кислот, которые имеют общую проблему высокой гигроскопичности и, следовательно, трудности хранения вследствие их нестабильности.
Полиморфная форма FII имеет очень высокую и неожиданную стабильность по отношению к влажности в изотерме при 25°C и при 40°C.
Действительно, при сорбции при 25°C образец стабилен вплоть до 70% RH (при 70% RH он демонстрирует увеличение массы менее 2%). После 70% RH он абсорбирует влагу и при 90% RH происходит изменение массы, составляющее примерно 35%. При десорбции при 25°C образец стабилен вплоть до 50% RH, сохраняя изменение массы, составляющее примерно 34% (которое соответствует примерно 8 молекулам воды). При приблизительно 40% RH можно видеть точку перегиба, и в этой точке видно, что образец все еще содержит примерно 18% воды (что соответствует примерно 4 молекулам воды). При 0% RH изменение массы равно нулю. При сорбции при 40°C образец стабилен вплоть до 60% RH (при 70% RH он демонстрирует увеличение массы менее 2%). При 90% RH происходит изменение массы, составляющее примерно 45% (вероятно, образец расплывается за счет поглощения влаги). При десорбции при 40°C при 50-40% RH кривая демонстрирует плато, вероятно при затвердевании образца. При 0% RH изменение массы равно примерно 6%.
По результатам анализа DVS при 25°C полиморфная форма FI менее стабильна, чем полиморфная форма FII: полиморфная форма FII стабильна при сорбции при 25°C вплоть до примерно 70% RH, а полиморфная форма FI уже при 20% RH демонстрирует изменение массы, составляющее приблизительно 2% (смотри Фиг. 27). По результатам анализа DVS при 40°C полиморфная форма FI менее стабильна, чем полиморфная форма FII: полиморфная форма FII стабильна при сорбции при 40°C вплоть до примерно 70% RH, а полиморфная форма FI уже при 30% RH демонстрирует изменение массы, составляющее примерно 2% (смотри Фиг. 28). Кроме того, смесь NaHDC (смесь разных полиморфных форм, которую получают перед финальным переосаждением, например в безводном ацетоне), по результатам анализа DVS при 25°C менее стабильна, чем полиморфная форма FII (смотри Фиг. 58). Полиморфная форма FII стабильна при сорбции вплоть до примерно 70% RH, а смесь NaHDC уже при 20% RH демонстрирует изменение массы, составляющее примерно 3%.
Гиодезоксихолат натрия в полиморфной форме FI является другой безводной кристаллической формой. Количество воды в кристалле составляет менее 1%, предпочтительно менее 0,6%, и еще более предпочтительно оно составляет менее 0,4%, где указанные проценты являются процентами относительно общей массы кристалла.
Полиморфная кристаллическая форма FI NaHDC характеризуется профилем рентгеновской дифрактограммы на порошке (XPRD), который представлен в качестве примера на Фиг. 14, и/или профилем дифференциальной сканирующей калориметрии (DSC), который представлен в качестве примера на Фиг. 16, и/или термогравиметрическим профилем (TGA), который представлен в качестве примера на Фиг. 17, и/или FT-IR/ATR спектром, который представлен на Фиг. 20, FT-RAMAN спектром, который представлен в качестве примера на Фиг. 22, анализом динамической сорбции пара (DVS) в изотерме при 25°C, который представлен в качестве примера на Фиг. 23, и анализом динамической сорбции пара (DVS) в изотерме при 40°C, который представлен в качестве примера на Фиг. 25.
Кроме того, представлено сравнение анализа динамической сорбции пара (DVS) в изотерме при 25°C и при 40°C полиморфной формы FI и полиморфной формы FII, которое представлено в качестве примера на Фиг. 27 и 28.
Полиморфная форма FI NaHDC характеризуется профилем XPRD, представленным на Фиг. 14, характеристические пики которого находятся при следующих положениях 2 тета на Фиг. 15: 6,17; 7,82; 9,50; 11,77; 12,35; 17,03; 17,78; 19,63; 21,71; 25,53 градусов, с пределом погрешности для значения, указанного для каждого пика, ±0,20 градусов 2 тета.
На Фиг. 15 представлены значения вышеупомянутых пиков XPRD полиморфной формы FI вместе с соответствующей относительной интенсивностью.
Полиморфная форма FI NaHDC характеризуется профилем DSC, представленным на Фиг. 16. На этом графике эндотермический пик можно видеть при 310°C с началом Пика при 306,5°C, Пиком при 309,7°C и энтальпией плавления, равной 54,84 Дж/г, вследствие плавления безводной формы FI. Кроме того, анализ дифракции (XPRD) был проведен при вариабельной температуре (смотри Фиг. 18 и 19) и доказал стабильность вплоть до 280°C.
Полиморфная форма FI NaHDC характеризуется профилем TGA, представленным на Фиг. 17. Профиль TGA показывает начальную потерю массы при примерно 50°C, составляющую примерно 1%, обусловленную поглощением воды, и потеря массы больше не наблюдается вплоть до 350°C, и это экспериментально подтверждает тот факт, что эта форма находится в ее "безводной" форме. Это подтверждено анализом дифракции (XPRD) при вариабельной температуре. Полиморфная форма FI стабильна вплоть до 280°C, как показано на Фиг. 18 и 19, как уже сказано выше, и затем плавится, как показано на Фиг. 16.
Полиморфная форма FI NaHDC характеризуется FT-IR/ATR спектром, представленным на Фиг. 20, характеристические пики которого находятся при следующих частотах на Фиг. 21: 3259,0; 2932,5; 2916,1; 2893,2; 2867,4; 2848,1; 1557,5; 1454,8; 1435,3; 1421,5; 1405,8; 1387,1; 1334,2; 1311,5; 1084,6; 1060,3 см-1, с пределом погрешности для значения, указанного для каждого пика, ±1 см-1.
Полиморфная форма FI NaHDC характеризуется FT-RAMAN спектром, представленным на Фиг. 22.
Полиморфная форма FI NaHDC характеризуется графиком DVS в изотерме при 25°C±0,1, который представлен в качестве примера на Фиг. 23, и соответствующими значениями, выраженными в %, как показано на Фиг. 24.
При сорбции образец демонстрирует изменение массы, составляющее примерно 2% при 30% RH и 15% при 70% RH. При 90% RH происходит изменение массы, составляющее примерно 35%.
При десорбции образец стабилен вплоть до 50% RH, сохраняя изменение массы примерно 34% (что соответствует примерно 8 молекулам воды).
При примерно 40% RH можно видеть точку перегиба, и в этой точке образец, по-видимому, все еще содержит примерно 18% воды (что соответствует примерно 4 молекулам воды). При 0% RH изменение массы равно нулю.
Полиморфная форма FI NaHDC характеризуется графиком DVS в изотерме при 40°C±0,1 который представлен в качестве примера на Фиг. 25, и соответствующими значениями, выраженными в %, как показано на Фиг. 26.
При сорбции, при 30% RH, образец показывает изменение массы, составляющее примерно 2% и 8% при 70% RH. При 90% RH происходит изменение массы, составляющее примерно 43%. При десорбции при 50-40% RH кривая показывает плато, и образец демонстрирует изменение массы, составляющее примерно 17%. При 0% RH изменение массы равно нулю.
Кроме того, произведено сравнение в изотерме при 25°C и при 40°C полиморфной формы FI и полиморфной формы FII NaHDC, как показано на Фиг. 27 и 28.
Кроме того, полиморфными формами NaHDC, охарактеризованными в настоящем изобретении, являются также полиморфная форма FIII, гидратированные полиморфные формы NaHDC, названные SI и SII, которые являются формами NaHDC, гидратированными соответственно четырьмя и восемью молекулами воды, и аморфная форма.
Гиодезоксихолат натрия в полиморфной форме FIII является еще одной безводной кристаллической формой. Количество воды в кристалле составляет менее 1%, предпочтительно менее 0,6% и еще более предпочтительно оно составляет менее 0,4%, где указанные проценты являются процентами относительно общей массы кристалла.
Полиморфная форма FIII NaHDC характеризуется профилем рентгеновской дифрактограммы на порошке (XPRD), который представлен в качестве примера на Фиг. 29, и/или профилем дифференциальной сканирующей калориметрии (DSC), который представлен в качестве примера на Фиг. 31, и/или термогравиметрическим профилем (TGA), который представлен в качестве примера на Фиг. 32, и/или FT-IR/ATR спектром, который представлен на Фиг. 33.
Полиморфная форма FIII NaHDC характеризуется профилем XPRD, представленным на Фиг. 29, характеристические пики которого находятся при следующих положениях 2 тета на Фиг. 30: 5,54; 10,20; 11,24; 12,63; 14,63; 14,96; 15,78; 16,91; 18,13; 18,62; 19,16; 22,22; 24,24 градусов, с пределом погрешности для значения, указанного для каждого пика, ±0,20 градусов 2 тета.
На Фиг. 30 представлены значения вышеупомянутых пиков XPRD полиморфной формы FIII вместе с соответствующей относительной интенсивностью.
Полиморфная форма FIII NaHDC характеризуется профилем DSC, представленным на Фиг. 31. На этом графике можно видеть эндотермический пик при 290°C с началом Пика при 292,2°C, Пиком при 302,5°C и энтальпией плавления, равной 50,15 Дж/г, вследствие плавления безводной формы FIII.
Полиморфная форма FIII NaHDC характеризуется профилем TGA, представленным на Фиг. 32. Профиль TGA показывает начальную потерю массы при примерно 50°C, составляющую примерно 1%, обусловленную поглощением воды, после чего никаких потерь массы больше не наблюдается вплоть до 350°C, и это экспериментально подтверждает тот факт, что такая форма находится в ее "безводной" форме.
Полиморфная форма FIII NaHDC характеризуется FT-IR/ATR спектром, представленным на Фиг. 33, характеристические пики которого находятся при следующих частотах на Фиг. 34: 2929,5; 2863,5; 1556,8; 1408,0; 1373,6; 1038,2; 1027,8; 997,7; 852,1; 917,4 см-1, с пределом погрешности для значения, указанного для каждого пика, ±1 см-1.
Гиодезоксихолат натрия в гидратированной полиморфной форме SI является гидратированной формой, гидратированной примерно четырьмя молекулами воды.
Гидратированная полиморфная форма SI NaHDC характеризуется профилем рентгеновской дифрактограммы на порошке (XPRD), который представлен в качестве примера на Фиг. 35, и/или профилем дифференциальной сканирующей калориметрии (DSC), который представлен в качестве примера на Фиг. 37, и/или термогравиметрическим профилем (TGA), который представлен в качестве примера на Фиг. 38, и/или FT-IR/ATR спектром, который представлен на Фиг. 39.
Гидратированная полиморфная форма SI NaHDC характеризуется профилем XPRD, представленным на Фиг. 35, характеристические пики которого находятся при следующих положениях 2 тета на Фиг. 36: 4,92; 12,34; 14,89; 15,70; 16,46; 17,72; 21,01; 25,78; 29,93 градусов, с пределом погрешности для значения, указанного для каждого пика, ±0,20 градусов 2 тета.
На Фиг. 36 представлены значения вышеупомянутых пиков XPRD гидратированной полиморфной формы SI вместе с соответствующей относительной интенсивностью.
Гидратированная полиморфная форма SI NaHDC характеризуется профилем DSC, представленным на Фиг. 37. На этом графике можно видеть эндотермическое событие при примерно 50-70°C (комплексный Пик 54,9°C и 78,6°C), связанное с потерей воды, и эндотермический пик при примерно 310°C с началом Пика при 310,4°C, Пиком при 316,2°C и энтальпией плавления, равной 68,23 Дж/г, вследствие плавления безводной формы FI, в которую гидратированная форма SI взаимопревращается.
Гидратированная полиморфная форма SI NaHDC характеризуется профилем TGA, представленным на Фиг. 38. Профиль TGA показывает начальную потерю массы при примерно 70°C, составляющую примерно 19%, обусловленную потерей воды такой формой.
Гидратированная полиморфная форма SI NaHDC характеризуется FT-IR/ATR спектром, представленным на Фиг. 39.
Гиодезоксихолат натрия в гидратированной полиморфной форме SII является гидратированной формой, гидратированной примерно восемью молекулами воды.
Гидратированная полиморфная форма SII NaHDC характеризуется профилем рентгеновской дифрактограммы на порошке (XPRD), который представлен в качестве примера на Фиг. 40, и/или профилем дифференциальной сканирующей калориметрии (DSC), который представлен в качестве примера на Фиг. 42, и/или термогравиметрическим профилем (TGA), который представлен в качестве примера на Фиг. 43, и/или FT-IR/ATR спектром, который представлен на Фиг. 44.
Гидратированная полиморфная форма SII NaHDC характеризуется профилем XPRD, представленным на Фиг. 40, характеристические пики которого находятся при следующих положениях 2 тета на Фиг. 41: 4,88; 8,81; 12,82; 15,30; 15,47; 16,24; 17,45; 19,12; 19,52; 20,05; 20,83; 21,68; 22,32; 22,95; 25,30; 26,64; 27,33; 27,64; 28,07; 29,75 градусов, с пределом погрешности для значения, указанного для каждого пика, ±0,20 градусов 2 тета.
На Фиг. 41 представлены значения вышеупомянутых пиков XPRD гидратированной полиморфной формы SII вместе с соответствующей относительной интенсивностью.
Гидратированная полиморфная форма SII NaHDC характеризуется профилем DSC, представленным на Фиг. 42. На этом графике можно видеть эндотермическое событие при примерно 50°C (начало Комплексного Пика 38,8°C, Пик 50,2°C и энтальпия 550,8 Дж/г, связанная с потерей воды, и эндотермический пик при примерно 310°C с началом Пика при 307,8°C, Пиком при 312,3°C и энтальпией плавления, равной 46,67 Дж/г, вследствие плавления безводной формы FI, в которую гидратированная форма SII взаимопревращается.
Гидратированная полиморфная форма SII NaHDC характеризуется профилем TGA, представленным на Фиг. 43. Профиль TGA профиль показывает начальную потерю массы при примерно 100°C, составляющую примерно 25%, обусловленную потерей воды такой формой.
Гидратированная полиморфная форма SII NaHDC характеризуется FT-IR/ATR спектром, представленным на Фиг. 44.
Гиодезоксихолат натрия в аморфной форме.
Аморфная форма NaHDC характеризуется профилем рентгеновской дифрактограммы на порошке (XPRD), который представлен в качестве примера на Фиг. 45, и/или профилем дифференциальной сканирующей калориметрии (DSC), который представлен в качестве примера на Фиг. 47, и/или термогравиметрическим профилем (TGA), который представлен в качестве примера на Фиг. 48, и/или FT-IR/ATR спектром, который представлен на Фиг. 49, анализом динамической сорбции пара (DVS) в изотерме при 25°C, который представлен в качестве примера на Фиг. 51.
Аморфная форма NaHDC характеризуется профилем XPRD, представленным на Фиг. 45, характеристические пики которого находятся при следующих положениях 2 тета на Фиг. 46: 5,54; 15,58 градусов, с пределом погрешности для значения, указанного для каждого пика, ±0,20 градусов 2 тета.
На Фиг. 46 представлены значения вышеупомянутых пиков XPRD аморфной формы вместе с соответствующей относительной интенсивностью.
Аморфная форма NaHDC характеризуется профилем DSC, представленным на Фиг. 47. На этом графике можно видеть эндотермическое событие при примерно 50°C (Комплексный Пик 56,0°C, связанный с потерей воды). Кроме того, он имеет два экзотермических пика (Комплексный Пик 203,9°C и 244,7°C) после 200°C, вероятно связанный с перекристаллизацией аморфного вещества, и эндотермическое событие при примерно 300°C с началом Пика при 287,2°C, Пиком при 296,3°C вследствие плавления.
Аморфная форма NaHDC характеризуется профилем TGA, представленным на Фиг. 48. Профиль TGA показывает начальную потерю массы при примерно 80°C, составляющую примерно 8%, обусловленную потерей воды.
Аморфная форма NaHDC характеризуется FT-IR/ATR спектром, представленным на Фиг. 49, характеристические пики которого находятся при следующих частотах на Фиг. 50: 3316,7; 2928,4; 2863,6; 1557,3; 1446,2; 1404,4; 1374,4; 1334,4; 1316,9; 1038,4; 1029,3; 998,7; 952,8; 912,2 см-1 с пределом погрешности для значения, указанного для каждого пика, ±1 см-1.
Аморфная форма NaHDC характеризуется графиком DVS в изотерме при 25°C±0,1, который представлен в качестве примера на Фиг. 51, и соответствующими значениями, выраженными в %, как показано на Фиг. 52.
При сорбции, при 30% RH, образец показывает изменение массы, составляющее примерно 6% и составляющее 22% при 70% RH. При 90% RH происходит изменение массы, составляющее примерно 35%. При десорбции образец стабилен вплоть до 50% RH, сохраняя изменение массы примерно 34% (что соответствует примерно 8 молекулам воды). При примерно 40% RH можно видеть точку перегиба, и при в этой точке образец, по-видимому, все еще содержит примерно 17% воды (что соответствует примерно 4 молекулам воды). При 0% RH образец показывает массу, которая меньше исходной массы.
Гиодезоксихолат натрия, полученный перед последней стадией переосаждения, которая происходит, например, в ацетоне при нагревании, представляет собой смесь разных форм, которые описаны.
Количество воды в кристалле смеси NaHDC составляет менее 5%, предпочтительно менее 3%, и еще более предпочтительно оно составляет менее 2%, где указанные проценты являются процентами относительно общей массы кристалла.
Такая смесь NaHDC характеризуется профилем рентгеновской дифрактограммы на порошке (XPRD), который представлен в качестве примера на Фиг. 53, и/или профилем дифференциальной сканирующей калориметрии (DSC), который представлен в качестве примера на Фиг. 54, и/или термогравиметрическим профилем (TGA), который представлен в качестве примера на Фиг. 55, и/или анализом динамической сорбции пара (DVS) в изотерме при 25°C, который представлен в качестве примера на Фиг. 56. Кроме того, есть описание сравнения анализа динамической сорбции пара (DVS) в изотерме при 25°C смеси разных форм и безводной кристаллической формы FII, которое представлено в качестве примера на Фиг. 58.
Такая смесь форм NaHDC характеризуется профилем XPRD, представленным на Фиг. 53.
Смесь форм NaHDC характеризуется профилем DSC, представленным на Фиг. 54. На этом графике можно видеть эндотермическое событие при примерно 50°C, связанное с потерей воды (Комплексный Пик 47,5°C), два экзотермических события после 200°C, вероятно связанных с перекристаллизацией аморфного вещества, и эндотермическое событие, характеризующееся двойным пиком при температуре выше 310°C вследствие плавления (начало Комплексного Пика 312,3°C, Пик 314,3°C, Пик 319,3°C).
Смесь форм NaHDC характеризуется профилем TGA, представленным на Фиг. 55. Профиль TGA профиль показывает начальную потерю массы при примерно 70°C, составляющую примерно 8%, приписываемую воде.
Смесь форм NaHDC характеризуется графиком DVS в изотерме при 25°C±0,1 который представлен в качестве примера на Фиг. 56, и соответствующими значениями, выраженными в %, как показано на Фиг. 57.
При сорбции при 20% RH образец показывает изменение массы, составляющее примерно 3% и составляющее 15% при 70% RH. При 90% RH происходит изменение массы, составляющее примерно 35%. При десорбции образец стабилен вплоть до 50% RH, имея увеличение массы, составляющее примерно 34% (что соответствует примерно 8 молекулам воды); после примерно 40% RH можно видеть точку перегиба, и образец, по-видимому, содержит примерно 18% воды (что соответствует примерно 4 молекулам воды).
Кроме того, было проведено сравнение в изотерме при 25°C смеси форм NaHDC и полиморфной формы FII NaHDC, как показано на Фиг. 58. В целях сравнения на Фиг. 58 представлен профиль DVS неочищенного NaHDC, который, как объясняется, представляет собой комплекс и невоспроизводимую смесь разных форм, которая имеет химическую чистоту 99,5%. Эту смесь получают в промышленности перед финальным переосаждением при нагревании реакционной массы, например в ацетоне, в условиях дефлегмации.
Такой неочищенный NaHDC представляет собой смесь безводных и гидратированных полиморфных форм и потенциально с неизмеримыми процентными содержаниями аморфной части. Смеси полиморфных форм, гидратированных форм и аморфной формы не могут быть приготовлены с получением однозначного продукта, предназначенного для использования в клинических испытаниях, которые проводят перед коммерческим использованием в медицине. Следовательно, настоящее изобретение имеет преимущество в том, что предлагает новую стабильную безводную полиморфную форму NaHDC, т.е. полиморфную форму FII, с высокой химической и полиморфной чистотой, пригодную для изготовления фармацевтического средства.
В соответствии с примером, приведенным в экспериментальной части, полиморфная форма FII является предпочтительной формой для применения в качестве активного ингредиента, благодаря также ее стабильности в течение длительного времени и устойчивости к температуре (стабильна вплоть до 260°C): она представляет собой форму, которая является самой термодинамически стабильной при комнатной температуре (как уже описано) и самой стабильной по отношению к влажности, имея неожиданную и непредсказуемую стабильность по отношению к влажности как при 25°C, так и при 40°C, что продемонстрировано тестами, проведенными согласно руководящим указаниям Международной конференции по гармонизации ICH Q1A (версия 4, 6 февраля 2003) для проведения тестов на стабильность новых фармацевтических соединений при 25°C/60% RH и 40°C/75% RH.
Кроме того, способ синтеза новой полиморфной формы FII NaHDC, описанный ниже, дает возможность получать такой активный ингредиент с оптимальным размером частиц для приготовления фармацевтических средств, исключая необходимость в процессах контролирования размера частиц, таких как измельчение, микронизация или просеивание, которые могут подвергать риску полиморфную чистоту и химическую чистоту полиморфной формы FII из-за большого количества энергии, задействованной в этих операциях.
Способ синтеза полиморфной формы FII NaHDC по настоящему изобретению включает конечную стадию переосаждения органическим растворителем, выбранным из кетонного растворителя, растворителя, относящегося к категории сложных эфиров, спирта, растворителя, относящегося к категории нитрилов, или их смеси.
Предпочтительно, кетонный растворитель имеет цепь C3-C6, растворитель, относящийся к категории сложных эфиров, имеет цепь C2-C5 спиртовый растворитель имеет цепь C1-C5 и/или растворитель, относящийся к категории нитрилов, имеет цепь C2-C3.
Более предпочтительно, кетонный растворитель выбран из ацетона, метил-изобутил-кетона (MIBK), метил-этил-кетона (МЕК) или их смесей, растворителя, относящегося к категории сложных эфиров, выбранного из этилацетата, этилформиата, пропилацетата или их смесей, спиртового растворителя, выбранного из метанола, этанола, 1-пропилового спирта (1-пропанола), изопропилового спирта (2-пропанола), 1-бутанола, 2-бутанола, 2-пентанола или их смесей, и/или растворителя, относящегося к категории нитрилов, выбранного из ацетонитрила, пропионитрила или их смесей.
Предпочтительными органическими растворителями являются кетоны, и еще более предпочтительными является ацетон при нагревании.
Предпочтительной температурой, при которой проводят переосаждение безводной кристаллической формы II NaHDC, является температура в диапазоне от 55 до 120°C. Обычно предпочтительно использовать температуру, близкую к температуре дефлегмации каждого растворителя.
При использовании ацетона предпочтительной является температура от 55 до 60°C, и еще более предпочтительной является температура от 55 до 56°C.
Переосаждение происходит за период времени, составляющий от 6 до 10 часов, более предпочтительно от 6 до 8 часов.
Кетонные растворители являются предпочтительными, и среди них предпочтительным растворителем является ацетон.
В частности, предпочтительное соотношение NaHDC и растворителя, которым предпочтительно является кетонный растворитель, еще более предпочтительно безводный ацетон, составляет 1 к 8 (масса NaHDC к объему растворителя) и еще более предпочтительно 1 к 6 (масса NaHDC к объему растворителя).
В предпочтительном воплощении способ по изобретению включает следующие стадии:
а) по меньшей мере одна стадия очистки гиодезоксихолевой кислоты формулы II, которую проводят путем получения соли гиодезоксихолевой кислоты с щелочно-земельным металлом и ее последующего подкисления с получением очищенной гиодезоксихолевой кислоты;
b) получение гиодезоксихолата натрия путем обработки очищенной гиодезоксихолевой кислоты NaOH до pH от 8,5 до 9,5;
c) получение полиморфной формы FII гиодезоксихолата натрия путем переосаждения органическим растворителем, выбранным из кетонного растворителя, растворителя, относящегося к категории сложных эфиров, спирта, растворителя, относящегося к категории нитрилов, или их смеси.
Предпочтительно, на описанной выше стадии (с) кетонный растворитель имеет цепь C3-C6, растворитель, относящийся к категории сложных эфиров, имеет цепь С2-C5, спиртовый растворитель имеет цепь C1-C5, и/или растворитель, относящийся к категории нитрилов, имеет цепь C2-C3.
Более предпочтительно, на описанной выше стадии (с) кетонный растворитель выбран из ацетона, метил-изобутил-кетона (MIBK), метил-этил-кетона (МЕК) или их смесей, растворителя, относящегося к категории сложных эфиров, выбранного из этилацетата, этилформиата, пропилацетата или их смесей, спиртового растворителя, выбранного из метанола, этанола, 1-пропилового спирта (1-пропанола), изопропилового спирта (2-пропанола), 1-бутанола, 2-бутанола, 2-пентанола или их смесей, и/или растворителя, относящегося к категории нитрилов, выбранного из ацетонитрила, пропионитрила или их смесей.
В более предпочтительном воплощении способа по изобретению, указанного выше, стадию (с) проводят при температуре от 55 до 120°C в течение времени от 6 до 10 часов.
Предпочтительной солью гиодезоксихолевой кислоты с щелочноземельным металлом, которую используют на стадии (а), является магниевая соль гиодезоксихолевой кислоты формулы III ((HDC)2Mg).
Очистку на стадии (а) проводят путем образования соли HDCA с основанием с получением соли гиодезоксихолевой кислоты с щелочноземельным металлом, предпочтительно формулы III ((HDC)2Mg), и ее подкисления с получением очищенной HDCA.
Предпочтительно, исходная HDCA для стадии (а) имеет химическую чистоту от 80 до 90%, и она может быть получена способами предшествующего уровня техники.
Предпочтительно, HDCA, полученная по окончании стадии (а), имеет конечную химическую чистоту от 99,5% до 99,9%.
Стадию (а) предпочтительно повторяют дважды.
В этом последнем случае, исходя из химической чистоты HDCA, составляющей от 80 до 90%, после первой очистки получают химическую чистоту HDCA от 98,5% до 99,0%, и после второй очистки получают химическую чистоту от 99,5% до 99,9%.
На стадии (b) получают NaHDC предпочтительно с химической чистотой от 99,5% до 99,9%.
На стадии (с) получают полиморфную форму FII NaHDC предпочтительно с химической чистотой от 99,5% до 99,9%.
На стадии (а) основаниями, используемыми в данном изобретении, являются предпочтительно неорганические основания, такие как, например, NaOH, КОН, NH3, или органические основания, такие как, например, первичный, вторичный или третичный амин, такой как, например, изопропиламин, диметиламин, триэтиламин и т.д.
В предпочтительном воплощении способа по изобретению, исходную HDCA на стадии (а) добавляют в деионизированную или питьевую воду, саму или в смеси со спиртами с цепью С1-С5, такими как, например, метанол, этанол, 1-пропиловый спирт (1-пропанол), изопропиловый спирт (2-пропанол), 1-бутанол, 2-бутанол, 2-пентанол и т.д., предпочтительно этанол.
Смеси воды и спиртов, предпочтительно смеси воды и этанола, имеют соотношение, которое может варьировать от 7 к 2 объем/объем.
В этих смесях воды и спиртов, предпочтительно смесях воды и этанола, соотношение массы HDCA к общему объему растворителя (вода и спирты) варьирует от 1:9 до 1:25. Указанные смеси воды и спиртов предпочтительно используют при комнатной температуре (20-25°C).
Затем добавляют основание, которое, как указано выше, может быть неорганическим или органическим основанием.
На стадии (а) основание добавляют в стехиометрическом количестве, предпочтительно составляющем от 1 до 1,3 эквивалентов на каждый эквивалент HDCA и еще более предпочтительно от 1,0 и 1,1 эквивалентов на каждый эквивалент исходной HDCA.
Суспензию, полученную с HDCA и выбранным основанием, можно добавлять к воде, одной или в смеси со спиртами, как указано выше, перемешивают в течение периода времени предпочтительно от 30 до 60 минут при температуре предпочтительно от 60 до 90°C до получения прозрачного раствора, именуемого "Раствор A", с pH предпочтительно от 6,5 до 8,5, еще более предпочтительно 7,5.
В другом реакторе стехиометрическое количество соли щелочноземельного металла, предпочтительно магния, предпочтительно составляющее от 1 до 1,3 эквивалентов на каждый эквивалент исходной HDCA и еще более предпочтительно от 1 до 1,1 эквивалентов, добавляют к количеству воды, составляющему от 10 до 15 объемов деионизированной или питьевой воды, в расчете на сухую массу соли щелочно-земельного металла, при комнатной температуре. В результате получают раствор, именуемый "Раствором B".
Соль щелочно-земельного металла, предпочтительно магния, которую добавляют к воде, может представлять собой, например, сульфатную соль или гидрохлоридную соль, например гептагидрат сульфата магния, хлорид магния и т.д.
Добавление раствора B к раствору A предпочтительно проводят при температуре от 60 до 90°C в течение предпочтительно от 20 до 50 минут, и это дает возможность получать водную или водно-спиртовую суспензию соли щелочно-земельного металла, предпочтительно магния, гиодезоксихолевой кислоты.
Конечный pH этой суспензии предпочтительно составляет от 5 до 7.
После выдерживания этой суспензии при температуре 60-90°C в течение еще 30-60 минут ее охлаждают до комнатной температуры в течение периода времени 2-4 часа, и соль щелочно-земельного металла, предпочтительно магния, гиодезоксихолевой кислоты выделяют в виде белого твердого вещества, например фильтрованием.
Последующее суспендирование в воде соли гиодезоксихолевой кислоты с щелочно-земельным металлом, предпочтительно магниевой соли формулы III, в соотношении от 1 к 5 до 1 к 10 (масса HDCA к объему воды) с последующим слабым нагреванием при перемешивании, предпочтительно вплоть до 60-80°C, и добавлением минеральной кислоты до pH от 1 до 2 дает возможность получать после охлаждения до комнатной температуры за период времени 1-2 часа очищенную HDCA в виде белого твердого вещества, например путем фильтрования.
Особенно предпочтительными минеральными кислотами являются соляная кислота, серная кислота или фосфорная кислота и т.д., и предпочтительное количество используемой минеральной кислоты составляет от 1 до 1,5 эквивалентов на каждый эквивалент магниевой соли формулы III, еще более предпочтительно от 1 до 1,3 эквивалентов.
Очищенную HDCA выделяют предпочтительно фильтрованием, и остаток на фильтре промывают водой до нейтрального pH для удаления остаточной кислотности.
После первой очистки, в случае исходной HDCA с химической чистотой от 80 до 90%, получают HDCA с химической чистотой от 98,5% до 99,0%.
Повторение стадии (а), которое проводят предпочтительно в ее предпочтительной форме, с использованием HDCA с химической чистотой от 98,5% до 99,0%, полученной после первой очистки, дает возможность получать конечную HDCA на стадии (а) с химической чистотой от 99,5% до 99,9%.
Следующая стадия, т.е. стадия (b), предусматривает получение NaHDC путем обработки очищенной HDCA основанием. Предпочтительно, очищенная HDCA, поступающая со стадии (а), имеет химическую чистоту от 99,5% до 99,9%.
В предпочтительном воплощении способа по изобретению очищенную HDCA, поступающую со стадии (а), добавляют в воду, предпочтительно деионизированную, при перемешивании при комнатной температуре (20-25°C), где вода присутствует в соотношении от 1 к 4 до 1 к 8 (масса HDCA к объему воды).
Использование на этой стадии деионизированной воды дает возможность получать NaHDC в соответствии с техническими условиями, требуемыми для классификации активного фармацевтического ингредиента (API).
На стадии (b) основание NaOH добавляют в стехиометрическом количестве, составляющем предпочтительно от 1 до 1,1 эквивалентов на каждый эквивалент HDCA.
Полученную суспензию перемешивают в течение периода времени, составляющего предпочтительно от 30 до 60 минут, при температуре от 40 до 70°C до получения прозрачного раствора с конечным значением pH от 8,5 до 9,5.
Вакуумную отгонку присутствующей воды проводят при -1/-0.9 бар относительно давления окружающей среды до получения вязкого маслянистого остатка.
Затем к маслянистому остатку добавляют органический растворитель за период времени, составляющий от 3 до 6 часов, в соотношении от 1 к 6 до 1 к 8 (масса HDCA к объему растворителя), предпочтительно в соотношении 1 к 6 (масса HDCA к объему растворителя), при температуре предпочтительно от 45 до 50°C, с получением в результате слегка мутного раствора.
Предпочтительно, растворителем, который используют в этой части стадии (b), является органический растворитель, такой как, например, кетонный растворитель, предпочтительно с цепью C3-C6, такой как, например, ацетон, метил-изобутил-кетон (MIBK), метил-этил-кетон (МЕК) и т.д., растворитель, относящийся к категории сложных эфиров, предпочтительно с цепью C2-C5, такой как, например, этилацетат, этилформиат, пропилацетат и т.д., спирт, предпочтительно с цепью C1-C5, такой как, например, метанол, этанол, 1-пропиловый спирт (1-пропанол), изопропиловый спирт (2-пропанол), 1-бутанол, 2-бутанол, 2-пентанол и т.д., нитрил с цепью C2-C3, такой как, например, ацетонитрил, пропионитрил и т.д.
Предпочтительной температурой, при которой происходит осаждение NaHDC, является температура в диапазоне от 55 до 120°C.
Предпочтительным растворителем является безводный ацетон, и в этом случае предпочтительная температура составляет от 55 до 60°C, и еще более предпочтительно она составляет от 55 до 56°C.
После слабого нагревания раствор охлаждают до комнатной температуры в течение периода времени, составляющего от 3 до 6 часов.
Затем происходит осаждение NaHDC, поскольку используемый растворитель, предпочтительно кетонный, не является растворителем для этого соединения, в течение периода времени, составляющего от 8 до 10 часов.
Продукт NaHDC выделяют фильтрованием, и остаток на фильтре промывают раствором ацетон/вода 80:20 (об./об.), предпочтительно ацетон/вода 90:10 (об./об.) и более предпочтительно безводный ацетон, затем его подвергают сушке.
Полученный в результате NaHDC представляет собой смесь шести полиморфных форм, описанных выше, т.е. полиморфных форм FI, FII, FIII, SI, SII и аморфной формы, и в дальнейшем эта смесь сокращенно именуется "смесь NaHDC".
Количество воды, присутствующей в смеси NaHDC после сушки составляет менее 5%, предпочтительно менее 3%, и еще более предпочтительно оно составляет менее 2%, где указанные проценты являются процентами относительно общей массы кристалла смеси NaHDC.
Предпочтительно, смесь NaHDC, полученная по окончании стадии (b), имеет химическую чистоту от 99,5% до 99,9%.
На Фиг. 54 представлен профиль DSC смеси NaHDC, полученной в результате осаждения в случае, когда используемым кетонным растворителем является безводный ацетон, без проведения дополнительного конечного переосаждения высушенного продукта, представляющего собой смесь NaHDC.
Полиморфную форму FII NaHDC получают на стадии (с) путем обработки смеси NaHDC, полученной в точке (b), органическим растворителем, предпочтительно кетонным.
Примерами органических растворителей, используемых для переосаждения полиморфной формы FII NaHDC, т.е. которые действуют как нерастворители, являются, например, органические растворители, выбранные из кетонных растворителей, предпочтительно с цепью C3-C6, таких как, например, ацетон, метил-изобутил-кетон (MIBK) и метил-этил-кетон (МЕК), сложноэфирных растворителей, предпочтительно с цепью С2-С5, таких как, например, этилацетат, этилформиат и пропилацетат, спиртовых растворителей, предпочтительно с цепью C1-C5, таких как, например, метанол, этанол, 1-пропиловый спирт (1-пропанол), изопропиловый спирт (2-пропанол), 1-бутанол, 2-бутанол и 2-пентанол, и/или растворителей, относящихся к категории нитрилов, предпочтительно с цепью C2-C3, таких как, например, ацетонитрил и пропионитрил.
Предпочтительной температурой, при которой проводят переосаждение безводной кристаллической формы II NaHDC, является температура в диапазоне от 55 до 120°C.
При использовании ацетона предпочтительная температура составляет от 55 до 60°C, и еще более предпочтительно она составляет от 55 до 56°C.
Переосаждение происходит за период времени, составляющий от 6 до 10 часов, более предпочтительно от 6 до 8 часов.
Кетонные растворители являются предпочтительными, и среди них предпочтительным растворителем является ацетон.
В частности, предпочтительное соотношение NaHDC и растворителя, которым предпочтительно является кетонный растворитель и еще более предпочтительно безводный ацетон, составляет 1 к 8 (масса NaHDC к объему растворителя) и еще более предпочтительно 1 к 6 (масса NaHDC к объему растворителя).
Получают суспензию, которую медленно нагревают до температуры дефлегмации растворителя.
В том случае, когда растворителем является ацетон, суспензию нагревают до температуры от 55 до 60°C, предпочтительно 55-56°C.
Суспензию затем охлаждают до 25°C за период времени, составляющий от 3 до 6 часов.
Продукт выделяют фильтрованием, и остаток на фильтре промывают раствором ацетон/вода 80:20 (об./об.), предпочтительно ацетон/вода 90:10 (об./об.) и более предпочтительно безводным ацетоном.
Полученный в результате NaHDC представляет собой безводную полиморфную форму FII NaHDC с химической чистотой предпочтительно от 99,5% до 99,9%.
Количество воды в кристалле формы FII NaHDC составляет менее 1%, предпочтительно менее 0,6%, и еще более предпочтительно оно составляет менее 0,4%, где указанные проценты являются процентами относительно общей массы кристалла.
Предпочтительно, полиморфная форма FII NaHDC по настоящему изобретению не содержит аморфный NaHDC.
Кроме того, полиморфная форма FII NaHDC по настоящему изобретению не содержит никаких других полиморфных форм NaHDC, описанных выше.
Безводная полиморфная форма FNII NaHDC представляет собой чистый полиморф, где термин "чистый" означает, что безводная полиморфная форма FII NaHDC предпочтительно имеет содержание примесей менее 1%, еще более предпочтительно менее 0,7% и еще более предпочтительно менее 0,5%, где указанные проценты являются процентами относительно общей массы кристалла.
Предпочтительно, количество каждой отдельной примеси в полиморфе FII NaHDC составляет менее 0,5%, более предпочтительно менее 0,3% и еще более предпочтительно менее 0,1%, где указанные проценты являются процентами относительно общей массы кристалла.
Примеси в полиморфе FII NaHDC были определены, как указано в Таблице 1, и было доказано, что они являются известными примесями, такими как хенодезоксихолевая кислота (3α,7α-дигидрокси-5β-холан-24-овая кислота, сокращенно CDCA) и гиохолевая кислота (3α,6α,7α-тригидрокси-5β-холан-24-овая кислота, сокращенно НСА), указанные в Таблице 1, и неизвестными примесями, процентное содержание которых составляет менее 0,01% или в пределах обнаружимости относительно общей массы кристалла.
Профиль химической чистоты представлен на Фиг. 59.
Чистоту полиморфной формы FII NaHDC, полученной способом по настоящему изобретению, оценивали методом HPLC/RI (высокоэффективная жидкостная хроматография/детектор показателя преломления), аналитическим методом, описанным на Фиг. 60, с получением результатов, указанных в приведенной ниже Таблице 1.

Другие полиморфные формы, описанные выше, были получены способами, изложенными ниже.
Полиморфная форма FI была получена способом лиофилизации с использованием лиофилизатора SPascal, модель LIO100P.
В частности, смесь NaHDC, полученную на стадиях, описанных выше в пунктах (а) и (b), растворяют в деионизированной воде при температуре от 30 до 40°C с получением прозрачного раствора, который остается таковым после 24 часов при температуре 25°C. Раствор затем лиофилизируют при постоянной температуре -20°C в течение периода времени 72 часа, применяя давление 5×10-2 мбар в конце лиофилизации. Посредством лиофилизации кристаллическую форму FI NaHDC получают в виде очень тонкодисперсного белого кристаллического твердого вещества. Такая кристаллическая форма I NaHDC была охарактеризована анализами, описанными выше.
Полиморфная форма FIII была получена путем растворения смеси NaHDC, полученной на стадиях, описанных выше в пунктах (а) и (b), в деионизированной воде при температуре 50°C. Полученный прозрачный раствор медленно охлаждают до комнатной температуры. Получают белый осадок, который фильтруют и сушат в сушильной камере при 230°C в течение 15 часов. Такой осадок был охарактеризован как кристаллическая форма III NaHDC анализами, описанными выше.
Гидратированная полиморфная форма SI была получена путем растворения смеси NaHDC, полученной на стадиях, описанных выше в пунктах (а) и (b), в деионизированной воде при температуре 50°C. Полученный прозрачный раствор медленно охлаждают до комнатной температуры. Получают белый осадок, который фильтруют и сушат в течение 24 часов на воздухе. Такой осадок был охарактеризован как кристаллическая форма SI NaHDC анализами, описанными выше.
Гидратированная полиморфная форма SII была получена путем выдерживания смеси NaHDC, полученной на стадиях, описанных выше в пунктах (а) и (b), при постоянной температуре 25°C и при относительной влажности (RH) 90% в течение двух суток.
Такая гидратированная полиморфная форма SII NaHDC была охарактеризована анализами, описанными выше.
Аморфная форма NaHDC была получена путем растворения смеси NaHDC, полученной на стадиях, описанных выше в пунктах (а) и (b), в деионизированной воде при комнатной температуре.
Порошок был получен в результате распыления и сушки раствора с использованием распылительной сушилки Buchi mini spray dryer B-290.
Было установлено, что гидратированные полиморфные формы SI и SII взаимопревращаются в полиморфную форму FI при нагревании до температуры выше 310°C.
Было также установлено, как показано в примере 6, что смесь полиморфной формы FI с полиморфной формой FII (1:1 масс./масс.) в результате переосаждения в этилацетате после 48 часов при комнатной температуре (20-25°C) полностью превращается в полиморфную форму FII. Таким образом, по результатам анализов, как уже указано выше, указанная форма является самой термодинамически стабильной формой при комнатной температуре и вплоть до 260°C.
Таким образом, способ по настоящему изобретению дает возможность преимущественно получать новую полиморфную форму FII NaHDC, которая является чистой как химически, так и полиморфно.
Преимущество способа по настоящему изобретению заключается в получении полиморфной формы FII NaHDC с определенным размером частиц (гранулометрическим составом) и оптимальными физико-химическими характеристиками для использования NaHDC в качестве активного фармацевтического ингредиента, в частности в лечении и/или предупреждении атеросклеротического заболевания.
Следовательно, как уже указано выше, нет никакой необходимости в процессах гомогенизации или в определении размера частиц, которые могут изменять интересующую полиморфную форму.
Порошковая полиморфная форма FII NaHDC, полученная способом по настоящему изобретению, имеет гранулометрический состав от 25 мкм до 425 мкм, предпочтительно от 25 мкм до 250 мкм и еще более предпочтительно от 75 мкм до 250 мкм.
В частности, 60-80% масс. порошковой полиморфной формы FN NaHDC, полученной способом по настоящему изобретению, имеет гранулометрический состав от 75 мкм до 425 мкм, 15-20% масс. имеет гранулометрический состав менее 250 мкм, и 95% масс. имеет гранулометрический состав выше 25 мкм.
Объектом настоящего изобретения являются также фармацевтические композиции, которые содержат полиморф FII NaHDC, предпочтительно для перорального, парентерального, подкожного, внутривенного, внутримышечного, назального, местного (например трансдермального или трансмукозального) или ректального введения.
В частности, предпочтительными являются фармацевтические формы для перорального введение, такие как, например, порошки, гранулы, капсулы, пилюли, болюсы, таблетки, каплетки, облатки, жидкие препараты, предпочтительно в форме растворов, сиропов, суспензий, эмульсий.
Композиции по изобретению могут содержать полиморф FII NaHDC вместе с одним или более фармацевтически приемлемыми эксципиентами.
Полиморф FII NaHDC пригоден для использования в лечении и/или предупреждении атеросклеротического заболевания.
Следовательно, дополнительным объектом по настоящему изобретению являются фармацевтические композиции для применения в лечении и/или предупреждении атеросклеротического заболевания, содержащие полиморфную форму FII NaHDC.
МАТЕРИАЛЫ И МЕТОДЫ
Термические свойства описанных полиморфных форм определяли методом дифференциальной сканирующей калориметрии (DSC). Профили DSC были получены на приборе с тепловым потоком DSC 200 F3 Maia® (Netzsch). Прибор DSC 200 F3 Maia® был откалиброван по температуре и энтальпии с использованием индиевого стандарта (точка плавления: 156,6°C; ΔHf=28,45 Дж-1). Образцы анализировали согласно следующим условиям:
- температурный диапазон: 25-350°C;
- скорость нагревания: 10°C/мин;
- держатель образа: перфорированный алюминиевый тигель;
- газ: безводный азот при скорости потока 60 мл/мин.
Потерю массы описанных полиморфных форм, обусловленную растворителями и/или водой (Н20), определяли методом термогравиметрического анализа (TGA), используя термовесы TGA/DSC 1 Stare System Mettler Toledo. Для каждого образца % изменения массы измеряли в зависимости от температуры. TGA/DSC 1 Stare System Mettler Toledo калибровали в отношении температуры с использованием индия и алюминия.
Образцы анализировали методами TGA/DSC согласно следующим условиям:
- температурный диапазон: 25-450°C;
- скорость нагревания: 10°C/мин;
- держатель образца: перфорированный алюминиевый тигель;
- газ: безводный азот при скорости потока 100 мл/мин.
Для определения профилей дифракции рентгеновских лучей на порошке (XPRD) использовали дифрактометр Panalytical X'Pert Pro, оснащенный детектором X'Celerator и рентгеновской трубкой (PW3373/00 Cu LFF DK312503), при силе тока 40 мА и напряжении 40 кВ. Прибор калибровали с использованием в качестве стандарта кремниевого порошка PANalytical640. Образец устанавливали на стеклянном держателе образца и анализировали, используя следующие параметры:
ИК-спекты получали, используя спектрометр Nicolet FT-IR 6700 ThermoFischer. Спектры снимали в режиме ATR (нарушенное полное внутреннее отражение) на кристалле ZnSe с измерением следующих параметров:
Рамановские спектры регистрировали на спектрометре FT-Raman Bruker MultiRam, оснащенном Ge-диодным детектором, охлаждаемым жидким азотом. Источником возбуждения является лазер Nd3+-YAG (1064 нм) в конфигурации обратного рассеяния (180°). Диаметр сфокусированного лазерного луча равен примерно 100 мкм, и спектральное разрешение равно 4 см-1. Спектры регистрировали при мощности лазера примерно 60 мВт.
Для проверки стабильности образов измерения DVS (динамическая сорбция пара) выполняли с использованием прибора DVS Intrinsic SMS. Определяли изменение массы образца, связанное с изменением влажности в камере при постоянной температуре. Каждый образец взвешивали в пределах от 1 г до 4 г, с изменением массы, равным ±150 мг, и массовым разрешением, равным ±0,1 мкг, и размещали в приборе и анализировали при 25°C ±0,1 и 40°C ±0,1 в диапазоне относительной влажности от 0% RH до 90% RH с увеличением по 10% RH, с точностью ±1% RH. Кроме того, образец анализировали, доводя влажность от 0 до 90 и до 0% RH ступенями по 10% RH. Продолжительность этих ступеней является функцией стабилизации массы: если изменение массы остается менее 0,002 dm(%)/dt(мин) в течение 10 минут, то переходят на следующую ступень этап. Однако стабилизация для каждого этапа не может длиться более 6 часов, и в этом случае прибор проходит на следующую ступень этап. Последняя ступень предусматривает стабилизацию образца при 0% RH в течение 4 часов.
В качестве примера, но не для ограничения настоящего изобретения, ниже приведены Примеры, относящиеся к настоящему изобретению.
ПРИМЕРЫ
ПРИМЕР 1
Получение полиморфной формы FII NaHDC путем переосаждения в ацетоне
В 2-литровый реактор с рубашкой загружают 900 мл ацетона (6 объемов в расчете на загружаемую сухую твердую смесь NaHDC), запускают механическую мешалку, установив скорость 200 об/мин, и затем медленно добавляют 150 г (0,362 моль) смеси NaHDC. Смесь нагревают до температуры дефлегмации 56°C и перемешивают в течение 4 часов.
Охлаждение в течение 3 часов используют, чтобы довести температуру смеси с 56°C до 25°C.
Смесь фильтруют на воронке Бюхнера, и полученное белое твердое вещество промывают 150 мл смеси ацетон/вода 80-20 об./об. (1 объем в расчете на загруженную сухую твердую смесь NaHDC). Масса полученного твердого вещества во влажном состоянии равна 195,6 г, его сушат в сушильном шкафу при 50°C в течение 15 часов (в этом случае твердое вещество не размягчается во время сушки, как в случае получения смеси NaHDC).
Масса полученного твердого вещества в сухом состоянии равна 141,0 г, что соответствует выходу в % масс./масс., равному 94,0% масс./масс. и 93,9% в молях.
Твердое вещество имеет содержание воды, равное 0,59% масс./масс. Это твердое вещество было охарактеризовано как полиморфная форма FII методами, описанными в тексте и в графических материалах настоящей патентной заявки.
ПРИМЕР 2
Получение полиморфной формы FII NaHDC путем переосаждения в метил-изобутил-кетоне (MIBK)
В 2-литровый реактор с рубашкой загружают 900 мл метил-изобутил-кетона (MIBK) (6 объемов в расчете на загружаемую сухую твердую смесь NaHDC), запускают механическую мешалку, установив скорость 200 об/мин, и затем медленно добавляют 150 г (0,362 моль) смеси NaHDC. Смесь нагревают до температуры дефлегмации 110°C и перемешивают в течение 4 часов.
Охлаждение в течение 3 часов используют, чтобы довести температуру смеси с 110°C до 25°C.
Смесь фильтруют на воронке Бюхнера, и полученное белое твердое вещество промывают 150 мл MIBK (1 объем в расчете на загруженную сухую твердую смесь NaHDC).
Масса полученного твердого вещества во влажном состоянии равна 188,2 г; его сушат в сушильном шкафу при 50°C в течение 15 часов (в этом случае твердое вещество не размягчается во время сушки, как в случае получения смеси NaHDC).
Масса полученного твердого вещества в сухом состоянии равна 140,3 г, что соответствует выходу в % масс./масс. равному 93,5% масс./масс. и 93,4% в молях.
Полученное твердое вещество представляет собой полиморфную форму FII, и оно имеет содержание воды, равное 0,5% масс./масс. Это твердое вещество было охарактеризовано как полиморфная форма FII методами, описанными в тексте и в графических материалах настоящей патентной заявки.
ПРИМЕР 3
Получение полиморфной формы FII NaHDC путем переосаждения в изопропиловом спирте (2-пропаноле)
В 2-литровый реактор с рубашкой загружают 900 мл изопропилового спирта (2-пропанола (IPA)) (6 объемов в расчете на загружаемую сухую твердую смесь NaHDC), запускают механическую мешалку, установив скорость 200 об/мин, и затем медленно добавляют 150 г (0,362 моль) смеси NaHDC. Смесь нагревают до температуры дефлегмации 80°C и перемешивают в течение 4 часов.
Охлаждение в течение 3 часов используют, чтобы довести температуру смеси с 80°C до 25°C.
Смесь фильтруют на воронке Бюхнера, и полученное белое твердое вещество промывают 150 мл смеси IPA/Н2O 80-20 об./об. (1 объем в расчете на загруженную сухую твердую смесь NaHDC). Вода, содержащаяся в промывочном растворе, имеет тенденцию растворять профильтрованное твердое вещество (в этом случае твердое вещество не размягчается во время сушки, как в случае получения смеси NaHDC).
Масса полученного твердого вещества во влажном состоянии равна 128,0 г, и его сушат в сушильном шкафу при 50°C в течение 15 часов.
Масса полученного твердого вещества в сухом состоянии равна 94,1 г, что соответствует выходу в % масс./масс., равному 62,7% масс./масс. и 62,7% в молях.
Полученное твердое вещество представляет собой полиморфную форму FII, и оно имеет содержание воды, равное 0,27% масс./масс. Это твердое вещество было охарактеризовано как полиморфная форма FII методами, описанными в тексте и в графических материалах настоящей патентной заявки.
ПРИМЕР 4
Получение полиморфной формы FN NaHDC путем переосаждения в этилацетате (EtOAc)
В 2-литровый реактор с рубашкой загружают 900 мл этилацетата (EtOAc) (6 объемов в расчете на загружаемую сухую твердую смесь NaHDC), запускают механическую мешалку, установив скорость 200 об/мин, и затем медленно добавляют 150 г (0,362 моль) смеси NaHDC. Смесь нагревают до температуры дефлегмации 74°C и перемешивают в течение 4 часов.
Охлаждение в течение 3 часов используют, чтобы довести температуру смеси с 74°C до 25°C.
Смесь фильтруют на воронке Бюхнера, и полученное белое твердое вещество промывают 150 мл EtOAc (1 объем в расчете на загруженную сухую твердую смесь NaHDC).
Масса полученного твердого вещества во влажном состоянии равна 218,4 г, и его сушат в сушильном шкафу при 50°C в течение 15 часов (в этом случае твердое вещество не размягчается во время сушки, как в случае получения смеси NaHDC).
Масса полученного твердого вещества в сухом состоянии равна 145,7 г, что соответствует выходу в % масс./масс., равному 97,1% масс./масс. и 97,0% в молях.
Полученное твердое вещество представляет собой полиморфную форму FII, и оно имеет содержание воды, равное 0,24% масс./масс. Это твердое вещество было охарактеризовано как полиморфная форма FII методами, описанными в тексте и в графических материалах настоящей патентной заявки.
ПРИМЕР 5
Получение полиморфной формы FII NaHDC путем переосаждения в ацетонитриле (ACN)
В 2-литровый реактор с рубашкой загружают 900 мл ацетонитрила (ACN) (6 объемов в расчете на загружаемую сухую твердую смесь NaHDC), запускают механическую мешалку, установив скорость 200 об/мин, и затем медленно добавляют 150 г (0,362 моль) смеси NaHDC. Смесь нагревают до температуры дефлегмации 80°C и перемешивают в течение 4 часов.
Охлаждение в течение 3 часов используют, чтобы довести температуру смеси с 80°C до 25°C.
Смесь фильтруют на воронке Бюхнера, и полученное белое твердое вещество промывают 150 мл ACN (1 объем в расчете на загруженную сухую твердую смесь NaHDC).
Масса полученного твердого вещества во влажном состоянии равна 226,2 г, и его сушат в сушильном шкафу при 50°C в течение 15 часов (в этом случае твердое вещество не размягчается во время сушки, как в случае получения смеси NaHDC).
Масса полученного твердого вещества в сухом состоянии равна 146,2 г, что соответствует выходу в % масс./масс., равному 97,5% масс./масс. и 97,5% в молях.
Полученное твердое вещество представляет собой полиморфную форму FII, и оно имеет содержание воды, равное 0,47% масс./масс. Это твердое вещество было охарактеризовано как полиморфная форма FII методами, описанными в тексте и в графических материалах настоящей патентной заявки.
ПРИМЕР 6
Получение полиморфной формы FII NaHDC путем переосаждения в этилацетате (EtOAc) смеси полиморфной формы FI и полиморфной формы FII 1:1 (масс./масс.) при комнатной температуре (20-25°C) в течение 48 часов
В 2-литровый реактор с рубашкой загружают 1000 мл этилацетата (EtOAc), запускают механическую мешалку, установив скорость 200 об/мин, и затем медленно добавляют 25 г полиморфной формы FI и 25 г полиморфной формы FII. Смесь перемешивают в течение 48 часов при температуре 25°C.
Смесь фильтруют на воронке Бюхнера, и полученное белое твердое вещество промывают 50 мл EtOAc (1 объем в расчете на общую массу загруженной сухой твердой полиморфной формы FI NaHDC и полиморфной формы FII NaHDC).
Масса полученного твердого вещества во влажном состоянии равна 75,1 г, и его сушат в сушильном шкафу при 50°C в течение 15 часов (в этом случае твердое вещество не размягчается во время сушки, как в случае получения смеси NaHDC).
Масса полученного твердого вещества в сухом состоянии равна 48,5 г, что соответствует выходу в % масс./масс., равному 97,0% масс./масс. и 96,7% в молях.
Твердое вещество имеет содержание воды, равное 0,26% масс./масс. Анализ порошка показывает картину XPRD безводной формы FII (смотри Фиг. 61 и 62).
Таким образом, было продемонстрировано, что этим путем полиморфная форма FI взаимопревращается в полиморфную форму FII, т.е. в наиболее термодинамически стабильную форму при комнатной температуре.
ПРИМЕР 7
Получение смеси NaHDC путем переосаждения в безводном ацетоне (3 часа кипячения при температуре дефлегмации и 3 часа охлаждения)
В 2-литровый реактор с рубашкой загружают 300 мл деионизированной воды (2 объема в расчете на загружаемую сухую твердую смесь NaHDC), запускают механическую мешалку, установив скорость 180 об/мин, и затем медленно добавляют 150 г (0,362 моль) смеси NaHDC. Смесь нагревают до температуры 60°C и перемешивают до тех пор, пока твердое вещество не растворится полностью. Полученный в результате желтоватый вязкий раствор подвергают вакуумной дистилляции, пока в реакторе не останется очень вязкий маслянистый остаток с содержанием воды, равным 135 мл, и общей массой 285 г.
Температура дистилляции не превышает 60°C. После окончания дистилляции температуру понижают до 45°-50°C и по каплям добавляют 900 мл ацетона (6 объемов в расчете на загруженный сухой твердый NaHDC) за период времени 3 часа. Смесь нагревают до температуры дефлегмации, равной 56°C, и перемешивают в течение 3 часов. Охлаждение в течение 3 часов используют, чтобы довести температуру смеси с 56°C до 25°C. Смесь фильтруют на воронке Бюхнера, и полученное белое твердое вещество промывают 150 мл смеси ацетон/вода 80-20 об./об. (1 объем в расчете на загруженную сухую твердую смесь NaHDC).
Масса полученного твердого вещества во влажном состоянии равна 232,6 г, и его сушат в сушильном шкафу в вакууме при температуре 25°C в течение 15 часов, затем температуру увеличивают до 30°C в течение 4 часов и затем поднимают до 50°C в течение 15 часов.
Масса полученного твердого вещества в сухом состоянии равна 135,7 г, что соответствует выходу в % масс./масс., равному 90,5% масс./масс. и 90,3% в молях. Твердое вещество имеет содержание воды, равное 2,17% масс./масс. Это твердое вещество представляет собой смесь разных полиморфных форм, как указано на Фиг. 53, 54, 55, 56, 57, 58, 59 и 60.
ПРИМЕР 8
Получение смеси NaHDC путем переосаждения в безводном ацетоне (30 минут кипячения при температуре дефлегмации и 6 часов охлаждения)
В 2-литровый реактор с рубашкой загружают 300 мл деионизированной воды (2 объема в расчете на загружаемую сухую твердую смесь NaHDC), запускают механическую мешалку, установив скорость 180 об/мин, и затем медленно добавляют 150 г (0,362 моль) смеси NaHDC. Смесь нагревают до температуры 60°C и перемешивают до тех пор, пока твердое вещество не растворится полностью. Полученный в результате желтоватый вязкий раствор подвергают вакуумной дистилляции, пока в реакторе не останется очень вязкий маслянистый остаток с содержанием воды, равным 135 мл, и общей массой 285 г.
Температура дистилляции не превышает 60°C.
После окончания дистилляции температуру понижают до 45°C-50°C и по каплям добавляют 900 мл ацетона (6 объемов в расчете на загруженный твердый NaHDC) за период времени 3 часа. Смесь нагревают до температуры дефлегмации, равной 56°C, и перемешивают в течение 30 минут.
Охлаждение в течение 6 часов используют, чтобы довести температуру смеси с 56°C до 25°C.
Смесь фильтруют на воронке Бюхнера, и полученное белое твердое вещество промывают 150 мл смеси ацетон/вода 80-20 об./об. (1 объем в расчете на загруженную сухую твердую смесь NaHDC).
Масса полученного твердого вещества во влажном состоянии равна 191,3 г, и его сушат в сушильном шкафу в вакууме при температуре 25°C в течение 15 часов, увеличивают температуру до 30°C в течение 4 часов и затем поднимают до 50°C в течение 15 часов.
Масса полученного твердого вещества в сухом состоянии равна 136,1 г, что соответствует выходу в % масс./масс., равному 90,7% масс./масс. и 90,6% в молях.
Твердое вещество, которое имеет содержание воды 2,13% масс./масс., представляет собой смесь разных полиморфных форм, как указано на Фиг. 53, 54, 55, 56, 57, 58, 59 и 60.
ПРИМЕР 9
Сравнительный пример анализа динамической сорбции пара (DVS) в изотерме при 25°C±0,1 полиморфной Формы FII и полиморфной формы FI
Для проверки стабильности образцов проводили измерения DVS (динамическая сорбция пара), используя прибор DVS Intrinsic SMS. Определяли изменение массы образца, связанное с изменением влажности в камере при постоянной температуре. Каждый образец размещали в приборе и анализировали при 25°C±0,1 в диапазоне влажности от 0% до 90% RH с увеличением влажности на 10% RH, с точностью, равной ±1% RH. Образец стабилизировали при 0% RH в течение 4 часов. Продолжительность отдельных ступеней является функцией стабилизации массы: если изменение массы остается менее 0,002 dm(%)/dt(мин) в течение 10 минут, то переходят на следующую ступень. Стабилизация не может длиться больше 6 часов, и в этом случае переходят на следующую ступень. Последняя ступень предусматривает стабилизацию образца при 0% RH в течение 4 часов.
4 г полиморфной формы FII NaHDC точно взвешивают, изменение массы равно ±150 мг, и разрешение по массе равно ±0,1 мкг, и помещают в камеру при постоянной температуре 25°C±0,1, после чего регистрируют изменение массы по мере изменения % относительной влажности (RH). Как можно видеть из графика на Фиг. 10 и 27 и из значений, выраженных в %, на Фиг. 11, образец является неожиданно стабильным вплоть до 70% RH. Действительно, при сорбции при 25°C±0,1 полиморфная форма FII стабильна вплоть до 70% RH (при 70% RH она демонстрирует увеличение массы менее 2%). После 70% RH она абсорбирует влагу и при 90% RH происходит изменение массы, составляющее примерно 35%.
Напротив, образец полиморфной формы FI при сорбции при 25°C уже при 30% RH показывает изменение массы, составляющее примерно 2% и 15% при 70% RH. При 90% RH происходит изменение массы, составляющее примерно 35%.
При десорбции при 25°C±0,1 полиморфная форма FII стабильна вплоть до 50% RH, сохраняя изменение массы примерно 34% (что соответствует примерно 8 молекулам воды). При примерно 40% RH можно видеть точку перегиба, и в этой точке образец, по-видимому, все еще содержит примерно 18% воды (что соответствует примерно 4 молекулам воды). При 0% RH изменение массы равно нулю.
При десорбции при 25°C±0,1 полиморфная форма FI стабильна вплоть до 50% RH, сохраняя изменение массы примерно 34% (что соответствует примерно 8 молекулам воды). При примерно 40% RH можно видеть точку перегиба, и в этой точке образец, по-видимому, все еще содержит примерно 18% воды (что соответствует примерно 4 молекулам воды).
При 0% RH изменение массы равно нулю.
Из анализа DVS при 25°C±0,1 следует, что полиморфная форма FI менее стабильна, чем полиморфная форма FII: полиморфная форма FII стабильна при сорбции при 25°C вплоть до примерно 70% RH, тогда как полиморфная форма FI уже при 20% RH демонстрирует изменение массы примерно 2%, а при 70% RH она имеет весьма более высокое увеличение, примерно 15% воды (смотри Фиг. 23, 24 и 27).
ПРИМЕР 10
Сравнительный пример анализа динамической сорбции пара (DVS) в изотерме при 40°C±0,1 полиморфной формы FII и полиморфной формы FI
Для проверки стабильности образцов проводили измерения DVS (динамическая сорбция пара), используя прибор DVS Intrinsic SMS. Определяли изменение массы образца, связанное с изменением влажности в камере при постоянной температуре. Каждый образец размещали в приборе и анализировали при 40°C±0,1 в диапазоне влажности от 0% до 90% RH с шагом 10% RH, с точностью, равной ±1% RH. Образец стабилизировали при 0% RH в течение 4 часов. Продолжительность отдельных ступеней является функцией стабилизации массы: если изменение массы остается менее 0,002 dm(%)/dt(мин) в течение 10 минут, то переходят на следующую ступень. Стабилизация не может длиться больше 6 часов, и в этом случае переходят на следующую ступень. Последняя ступень предусматривает стабилизацию образца при 0% RH в течение 4 часов.
4 г полиморфной формы FII NaHDC точно взвешивают, изменение массы равно ±150 мг, и разрешение по массе равно ±0,1 мкг, и размещают в камере при постоянной температуре 40°C±0,1, после чего регистрируют изменение массы по мере изменения % относительной влажности (RH). Как можно видеть из графика на Фиг. 12 и 28 и из значений, выраженных в %, на Фиг. 13, образец является неожиданно стабильным вплоть до 70% RH. При сорбции при 40°C±0,1 полиморфная форма FII стабильна вплоть до 60% RH (при 70% RH она демонстрирует увеличение массы менее 2%). При 90% RH происходит изменение массы, составляющее примерно 45% (вероятно образец расплывается за счет поглощения влаги). Напротив, при сорбции при 40°C±0,1 образец полиморфной формы FI уже при 30% RH показывает изменение массы, составляющее примерно 2% и 8% при 70% RH.
При 90% RH происходит изменение массы, составляющее примерно 43%.
При десорбции при 40°C±0,1 кривая полиморфной формы FII при 50-40% RH показывает плато, вероятно при затвердевании образца. При 0% RH изменение массы составляет примерно 6%. При десорбции при 40°C кривая полиморфной формы FI при 50-40% RH показывает плато, и образец демонстрирует изменение массы примерно 17%.
При 0% RH изменение массы равно нулю.
Из анализа DVS при 40°C±0,1 следует, что форма FI менее стабильна, чем форма FII: форма FII стабильна при сорбции вплоть до примерно 70% RH, тогда как форма FI уже при 30% RH демонстрирует изменение массы примерно 2%.
ПРИМЕР 11
Сравнительный пример анализа динамической сорбции пара (DVS) в изотерме при 25°C±0,1 полиморфной формы FII и смеси NaHDC
Для проверки стабильности образцов проводили измерения DVS (динамическая сорбция пара), используя прибор DVS Intrinsic SMS. Определяли изменение массы образца, связанное с изменением влажности в камере при постоянной температуре. Каждый образец размещали в приборе и анализировали при 25°C±0,1 в диапазоне влажности от 0% до 90% RH с шагом 10% RH, с точностью, равной ±1% RH. Образец стабилизировали при 0% RH в течение 4 часов. Продолжительность отдельных ступеней является функцией стабилизации массы: если изменение массы остается менее 0,002 dm(%)/dt(мин) в течение 10 минут, то переходят на следующую ступень. Стабилизация не может длиться больше 6 часов, и в этом случае переходят на следующую ступень. Последняя ступень предусматривает стабилизацию образца при 0% RH в течение 4 часов.
4 г полиморфной формы FII NaHDC точно взвешивают, изменение массы равно ±150 мг, и разрешение по массе равно ±0,1 мкг, и размещают в камере при постоянной температуре 25°C±0,1, после чего регистрируют изменение массы по мере изменения % относительной влажности (RH). Как можно видеть из графика на Фиг. 10 и 58 и из значений, выраженных в %, на Фиг. 11, образец является неожиданно стабильным вплоть до 70% RH.
Действительно, при сорбции при 25°C±0,1 полиморфная форма FII стабильна вплоть до 70% RH (при 70% RH она демонстрирует увеличение массы менее 2%). После 70% RH она абсорбирует влагу и при 90% RH происходит изменение массы, составляющее примерно 35%. Напротив, образец смеси NaHDC при сорбции при 25°C±0,1 уже при 20% RH показывает изменение массы, составляющее примерно 3% и 15% при 70% RH. При 90% RH происходит изменение массы, составляющее примерно 35%.
При десорбции при 25°C±0,1 полиморфная форма FII стабильна вплоть до 50% RH, сохраняя изменение массы примерно 34% (что соответствует примерно 8 молекулам воды). При примерно 40% RH можно видеть точку перегиба, и в этой точке образец, по-видимому, все еще содержит примерно 18% воды (что соответствует примерно 4 молекулам воды). При 0% RH изменение массы равно нулю.
При десорбции смесь NaHDC стабильна вплоть до 50% RH, имея увеличение массы примерно 34% (что соответствует примерно 8 молекулам воды), и после примерно 40% RH можно видеть точку перегиба, когда образец, по-видимому, содержит примерно 18% воды (что соответствует примерно 4 молекулам воды).
Из анализа DVS при 25°C±0,1 следует, что смесь NaHDC менее стабильна, чем полиморфная форма FII: полиморфная форма FII стабильна при сорбции при 25°C±0,1 вплоть до примерно 70% RH, тогда как смесь NaHDC уже при 20% RH демонстрирует изменение массы примерно 3%, а при 70% RH она имеет весьма более высокое увеличение, примерно 15% воды (смотри Фиг. 56, 57 и 58).
ПРИМЕР 12
Получение полиморфной Формы FI
Форму FI получали путем лиофилизации.
Использовали лиофилизатор 5Pascal model LIO100P.
5 г смеси NaHDC растворяли в 95 мл деионизированной H2O при температуре 30-40°C, получая прозрачный раствор, который остается таковым через 24 часа при температуре 25°C.
Раствор лиофилизировали при постоянной температуре -20°C в течение 72 часов, применяя давление 5,10-2 мбар в конце лиофилизации. Было получено очень тонкодисперсное кристаллическое твердое вещество, которое было охарактеризовано как полиморфная форма FI методами, описанными в тексте и в графических материалах настоящей патентной заявки.
ПРИМЕР 13
Получение полиморфной формы FIII
Полиморфную форму FIII получали путем растворения 1,5 г смеси NaHDC в 3,5 мл деионизированной Н2O при температуре 50°C. Полученный прозрачный раствор медленно охлаждали до температуры 25°C. Был получен белый осадок, который отфильтровывали и сушили в сушильном шкафу при 230°C в течение 15 часов.
Указанный осадок был охарактеризован как полиморфная форма FIII методами, описанными в тексте и в графических материалах настоящей патентной заявки.
ПРИМЕР 14
Получение гидратированной полиморфной формы SI
Гидратированную полиморфную форму SI получали путем растворения 1,5 г смеси NaHDC в 3,5 мл деионизированной Н2O при температуре 50°C. Прозрачный раствор медленно охлаждали до комнатной температуры 25°C. Был получен белый осадок, который отфильтровывали и сушили в течение 24 часов на воздухе.
Указанный осадок был охарактеризован как гидратированная полиморфная форма SI методами, описанными в тексте и в графических материалах настоящей патентной заявки.
ПРИМЕР 15
Получение гидратированной полиморфной формы SII
Гидратированную полиморфную форму SII получали путем выдерживания 1 г смеси NaHDC в изотерме при комнатной температуре 25°C и при относительной влажности (RH) 90% в течение двух суток.
ПРИМЕР 16
Получение аморфной формы NaHDC
Аморфную форму получали путем растворения 2 г смеси NaHDC в 500 мл деионизированной H2O при комнатной температуре. Порошок получали посредством распыления и сушки раствора с использованием распылительной сушилки Buchi mini spray dryer B-290. Применяли температуру на входе 140°C, температуру на выходе 60°C, поток воздуха 473 л/ч и скорость нагнетания 9 мл/мин.
Реферат
Изобретение относится к гиодезоксихолату натрия в полиморфной форме FII, имеющему спектр дифракции рентгеновских лучей на порошке, имеющий следующие пики ± 0,20 градуса (2 тета): 6,94; 9,84; 13,92; 20,13; 23,30. Изобретение также относится к способу получения гиодезоксихолата натрия в полиморфной форме FII. Технический результат: получен гиодезоксихолат натрия в безводной полиморфной форме II (FII) с высокой химической и полиморфной чистотой. 2 н. и 16 з.п. ф-лы, 62 ил., 1 табл., 16 пр.
Формула
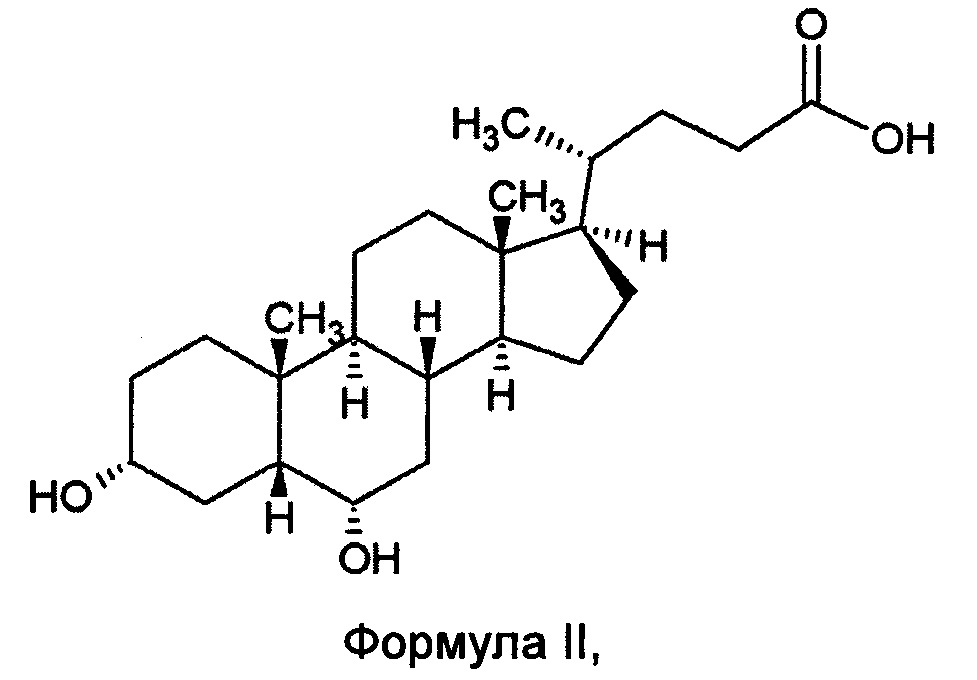


Комментарии