Способ лечения сахарного диабета, включая состояния, ассоциированные с сахарным диабетом, и осложнения сахарного диабета - RU2334518C2
Код документа: RU2334518C2
Чертежи







Описание
ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к способам лечения сахарного диабета у животных, в частности, у людей.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Сахарный диабет представляет собой гетерогенное первичное нарушение углеводного обмена с многочисленными этиологическими факторами, которые, как правило, включают дефицит инсулина или инсулинорезистентность, или и то, и другое. Диабет типа 1, или ювенильный диабет (развивающийся, в основном, у лиц молодого возраста), или инсулинозависимый сахарный диабет, имеется у больных с малой способностью секреции эндогенного инсулина или с абсолютным ее отсутствием. У указанных больных развивается крайняя гипергликемия (накопление глюкозы в кровяном русле) и они полностью пожизненно зависят от экзогенной инсулинотерапии. Диабет типа 2, поражающий, в основном, людей в зрелом и старческом возрасте, или инсулинонезависимый сахарный диабет ("ИНСД", "NIDDM"), имеет место у больных, у которых сохраняется некоторая способность секреции эндогенного инсулина, однако большая часть указанных больных страдает как от дефицита инсулина (относительный дефицит инсулина), так и инсулинорезистентности. Инсулинорезистентность может быть обусловлена недостаточной экспрессией инсулиновых рецепторов, снижением сродства к связыванию инсулина (снижение числа и аффинности инсулиновых рецепторов) или любой аномальностью на любой стадии пути передачи сигнала инсулина (1).
В общем, в Соединенных Штатах распространенность сахарного диабета среди населения составляет, вероятно, 2-4 процента, причем диабет типа 1 составляет 7-10 процентов всех больных сахарным диабетом. Вторичные осложнения сахарного диабета характеризуются серьезными клиническими проявлениями. Приблизительно 25 процентов всех новых случаев проявления терминальной почечной недостаточности имеют место у больных сахарным диабетом. Около 20000 ампутаций (пальцы стоп, стопы и нижние конечности) проводится у больных, больных сахарным диабетом, что составляет приблизительно половину ампутаций нетравматического характера, осуществляемых в Соединенных Штатах. Кроме того, сахарный диабет является основной причиной новых случаев слепоты, при этом приблизительно 5000 новых случаев происходит каждый год.
Углеводы из пищи разрушаются в кишечнике до глюкозы и других простых сахаров. Эти сахара всасываются в кровоток и поступают (наряду с другими питательными веществами) во все клетки тела. Однако для того чтобы поглотить глюкозу из крови, клеткам необходим инсулин - гормон, продуцируемый в поджелудочной железе. Поджелудочная железа, большая железа, расположенная позади желудка, выполняет множество функций. Она продуцирует пищеварительные ферменты - белки, которые способствуют расщеплению пищи в кишечнике. Кроме того, она содержит специализированные группы клеток, называемые "островками Лангерганса". Клетки этих островков представляют несколько типов, причем каждый тип клеток продуцирует конкретный гормон. Существует два основных гормона, которые регулируют уровни глюкозы в крови - инсулин и глюкагон. Оба продуцируются в островках Лангерганса - глюкагон альфа-клетками, а инсулин бета-клетками.
По мере того, как глюкоза поступает в кровоток после приема пищи, повышающийся уровень глюкозы в крови сигнализирует бета-клеткам секретировать инсулин. Инсулин (вместе с глюкозой) переносится кровотоком в клетки по всему телу. Разные ткани тела, в частности мышечная, печеночная и жировая ткань, имеют на поверхностях своих клеток специализированные молекулы, называемые рецепторами инсулина. Инсулин связывается с этими рецепторами, подобно ключу в замке - открывая каналы, которые позволяют глюкозе проникнуть в клетки.
После того как глюкоза попадет внутрь клеток, она может быть использована в качестве источника энергии (химической энергии, высвобождаемой в процессе катаболизма), необходимой для биологической работы клеток и роста организма. Избыток глюкозы хранится в печени в форме сложного углевода, называемого гликогеном. Тем временем, по мере того как уровни глюкозы в крови падают, секреция инсулина замедляется. Когда уровень глюкозы в крови начинает сильно снижаться (ниже физиологического уровня), это служит сигналом альфа-клеткам секретировать глюкагон. Глюкагон, в свою очередь, передает сигнал печени превращать гликоген обратно в глюкозу - процесс, называемый гликогенолизом. Это предотвращает падение уровня глюкозы в крови до слишком низкого значения, тем самым обеспечивая клетки организма устойчивым снабжением глюкозой между приемами пищи. Кроме того, глюкагон стимулирует получение новой глюкозы печенью из других (неуглеводных) питательных веществ, таких как аминокислоты (блоки, составляющие белок), способом, называемым глюконеогенезом, тем самым гарантируя резервный (дублирующий) источник глюкозы до следующего приема пищи.
Взаимодействие глюкозы, инсулина и глюкагона обычно гарантирует пребывание уровней глюкозы в крови внутри определенных пределов (физиологический уровень). В случае диабетиков, однако, это тонкое равновесие нарушается.
На сегодняшний день инсулинотерапия представляет собой основной способ лечения для всех больных диабетом типа 1 и для многих больных, страдающих диабетом типа 2. В зависимости от числа инъекций в день и типа(ов) применяемого инсулина схема лечения может быть более или менее интенсивной. Наиболее интенсивный способ лечения включает постоянную подачу инсулина в подкожное место брюшной стенки при помощи устройства доставки с разомкнутым контуром, состоящего из небольшого насоса с инсулином, которое больной должен носить, по существу, 24 часа ежедневно. Пероральные гипогликемические средства, такие как сульфомочевины, являются эффективными для больных диабетом типа 2, однако приблизительно от 10 до 20 больных (из них) не реагируют или прекращают реагировать через 12-24 мес, после начала лечения указанными средствами.
Эффективного контроля за уровнем глюкозы на протяжении длительных периодов времени трудно достичь даже в случае наиболее тщательного режима инсулинотерапии у наиболее сознательных больных. В качестве потенциально возможного лечения продолжает интенсивно исследоваться трансплантация поджелудочной железы или островковых клеток, которые в норме продуцируют инсулин. Кроме того, продолжаются работы, направленные на разработку новейших и более подходящих устройств наружного применения или имплантируемых устройств доставки инсулина, интегрированных (со встроенным) сенсором глюкозы.
Диабет типа 2 обычно наблюдается у лиц зрелого и старческого возраста (обычно в возрасте после 40 лет), но также он может иметь место у более молодых людей. Как правило, у людей, страдающих этим состоянием, поджелудочная железа продуцирует инсулин, однако клетки (тканей) тела не способны эффективно реагировать на него. Это состояние называют инсулинорезистентностью. Человек может иметь инсулинорезистентность без диабета, пока имеется достаточно инсулина для того, чтобы преодолеть резистентность. Однако, если резистентность к инсулину будет продолжать расти и/или продуцирование инсулина упадет ниже уровня, необходимого для достижения компенсации, может развиться диабет.
Большая часть диабетиков типа 2 могут лечиться пероральными лекарственными средствами, которые увеличивают секрецию инсулина поджелудочной железой и/или снижают инсулинорезистентность. Но через какое-то время панкреатические бета-клетки могут становиться все менее и менее чувствительными, при этом секретируя меньше инсулина, в то время как уровни глюкозы в крови высоки. В конечном счете человеку могут потребоваться инъекции инсулина для того, чтобы обеспечить контроль уровней глюкозы в крови.
Поскольку устойчивая гипергликемия может препятствовать заживлению ткани и проявлению иммунитета, у некоторых людей первым признаком проявления сахарного диабета могут быть медленно заживающие язвы (раны), частые инфекции или болезнь десен. Или первыми манифестирующими симптомами могут быть симптомы поражения органов, такие как, например, болезнь сердца или нейропатия. Общие симптомы диабетической нейропатии включают покалывание (онемение), потерю чувствительности или жгучую боль в области стоп и нижних конечностей. Хотя точные причины не установлены, сахарный диабет, по-видимому, является следствием взаимодействия генов и факторов образа жизни.
Одним из наиболее важных факторов риска заболеваемости сахарным диабетом является избыточный вес (2). Исследование показало, что наличие избыточного веса и диета с повышенным содержанием жира связаны с развитием инсулинорезистентности (3). Это особенно справедливо, когда избыточная жировая ткань локализуется в верхней части тела, вокруг брюшной полости - "форма яблока" (в противоположность "форме груши" с избыточным жиром ниже талии). Хотя причины этого еще не выяснены, исследователи считают, что инсулинорезистентность увеличивается гормонами (такими как лептин и резистин), которые секретируются жировыми клетками.
В пределах данной области продолжается активное исследование с целью разработки безопасных и эффективных способов лечения диабета. Цель настоящего изобретения состоит в устранении или смягчении недостатков и недостаточностей, известных в данной области.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способу лечения сахарного диабета и состояний, ассоциированных с сахарным диабетом, у животного, причем указанный способ включает введение нетоксичного и терапевтически эффективного количества одного или нескольких из нижеследующих соединений:

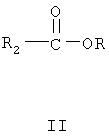
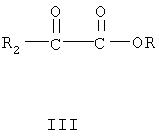
где R представляет собой часть фитостерола или фитостанола, R2 получен из аскорбиновой кислоты, R3 представляет собой водород или любой металл, щелочноземельный металл или щелочной металл, и всех их солей.
Кроме того, настоящее изобретение относится к применению указанных соединений для регулирования сывороточных уровней глюкозы, для повышения клеточной чувствительности к инсулину и для повышения чувствительности к глюкозе и уровня секреций инсулина панкреатическими бета-клетками.
Соединения настоящего изобретения, как было установлено, оказались неожиданно эффективными в повышении толерантности к глюкозе у животных. До сих пор не существовало никакой оценки этих типов соединений, касающейся проявления ими вышеупомянутых воздействий.
Одним существенным преимуществом применения конкретных соединений настоящего изобретения для этой цели является их растворимость в воде. В частности, было обнаружено, что растворимость в водных растворах, таких как вода, является превосходной, тем самым допуская пероральное введение per se без каких-либо дополнительных усовершенствований или модификаций. В соответствии с этим соединения настоящего изобретения можно получить и использовать как таковые или они могут быть легко включены в пищевые продукты, напитки, фармацевтические препараты и нутрицевтики независимо от того, являются ли эти "наполнители" основанными на воде. Эта повышенная растворимость обычно трансформируется в более низкие дозы соединений для введения, необходимые для достижения желательного терапевтического или профилактического действия.
Эти эффекты и другие существенные преимущества описаны более подробно ниже.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Настоящее изобретение иллюстрируется посредством нижеследующих не ограничивающих его чертежей, в которых:
Фиг.1 - схематическое представление способа получения фитостанолфосфатаскорбата и его натриевой соли;
Фиг.2 - схематическое представление способа получения фитостанолкарбонатаскорбата и его натриевой соли;
Фиг.3 - схематическое представление способа получения фитостанолоксалатаскорбата и его натриевой соли;
Фиг.4 - график, показывающий влияние лечения ситостанолфосфориласкорбатом ("FM-VP4") на массу тела у (на животной модели) тощих и тучных крыс линии Zucker. Данные представлены как среднее ± стандартное отклонение; в каждой группе, подвергнутой лечению, n=6. *p<0,05 против тучных;
Фиг.5 - график, показывающий влияние лечения ситостанолфосфориласкорбатом ("FM-VP4") на утренние уровни глюкозы в крови у тощих и тучных крыс линии Zucker. Данные представлены как среднее ± стандартное отклонение; в каждой группе, подвергнутой лечению, n=6. *p<0,05 против тучных;
Фиг.6 - график, показывающий действие FM-VP4 после 30-дневного лечения на уровни лептина в плазме у тощих и тучных крыс линии Zucker. Данные представлены как среднее ± стандартное отклонение; в каждой группе, подвергнутой лечению, n=6. *p<0,05 против ДО (лечения);
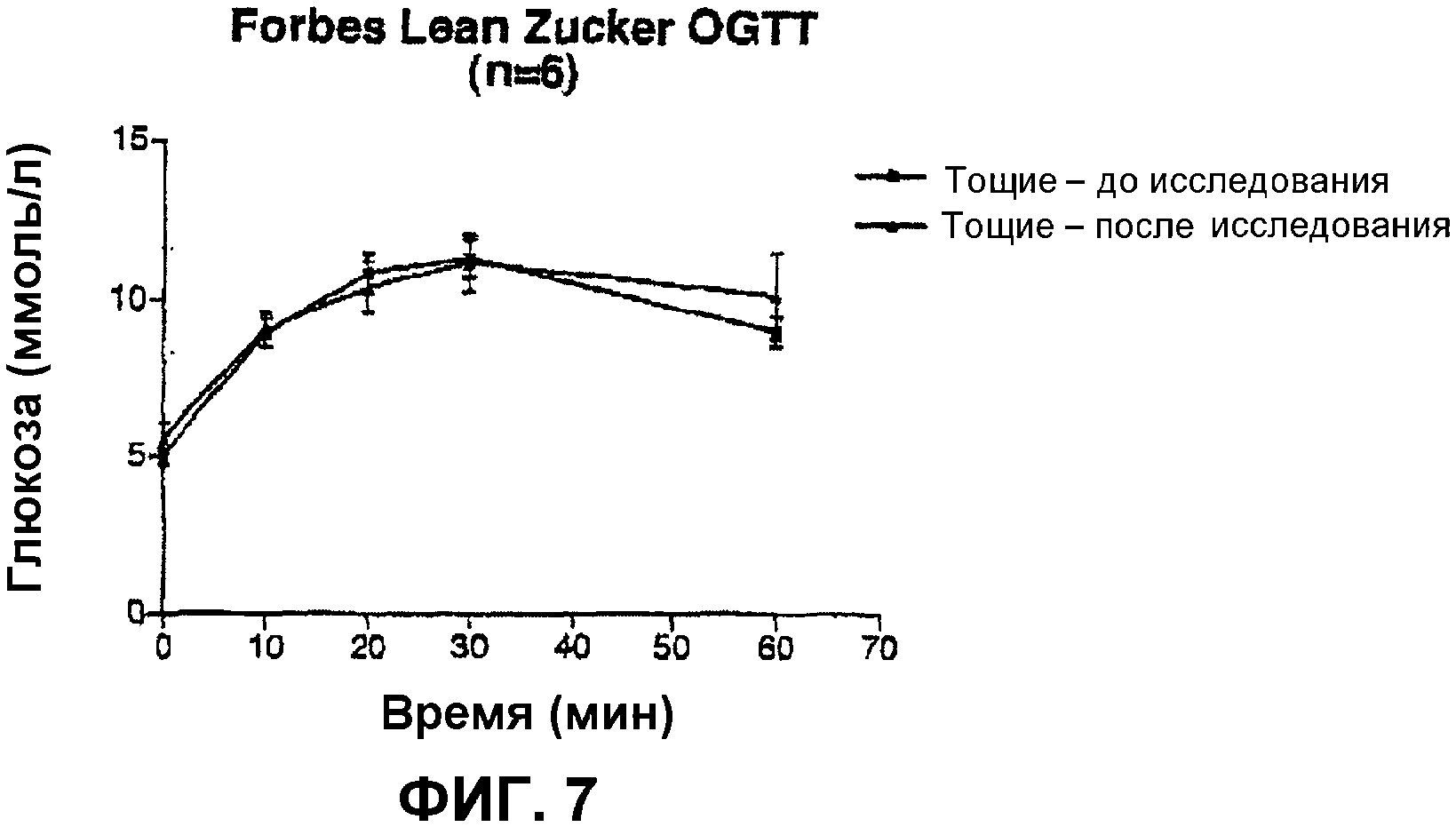
Фиг.7 - график, показывающий действие FM-VP4 после 30-дневного лечения на толерантность к глюкозе у тощих крыс линии Zucker. Данные представлены как среднее ± стандартное отклонение; в каждой группе, подвергнутой лечению, n=6. *p<0,05 против Тощего контроля;
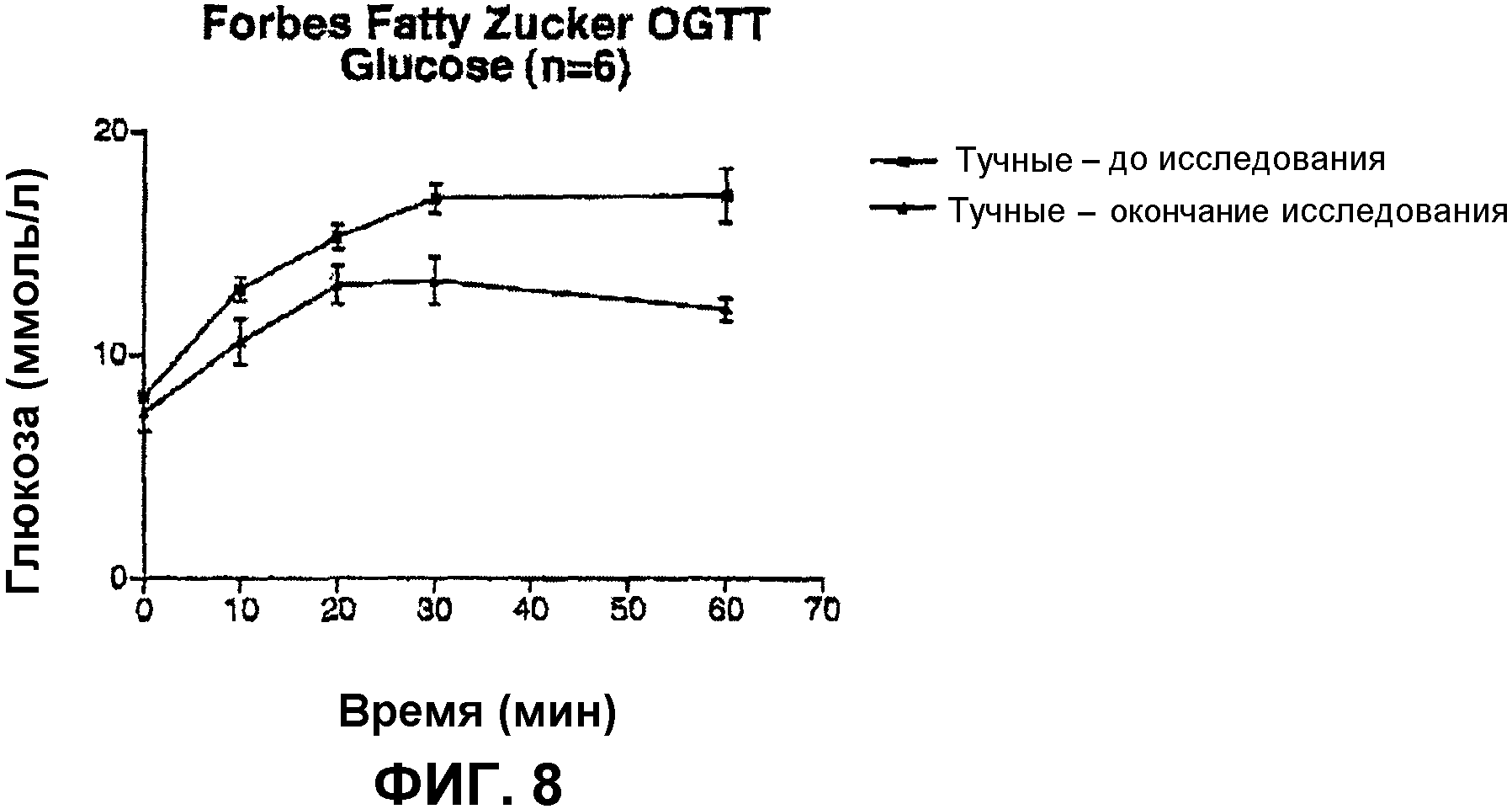
Фиг.8 - график, показывающий действие FM-VP4 после 30-дневного лечения на толерантность к глюкозе у тучных крыс линии Zucker (VDF). Данные представлены как среднее ± стандартное отклонение; в каждой группе, подвергнутой лечению, n=6. *p<0,05 против VDF контроля;
Фиг.9 - график, показывающий влияние FM-VP4 после 30-дневного лечения на инсулин OGTT у тощих крыс линии Zucker. Данные представлены как среднее ± стандартное отклонение; в каждой группе, подвергнутой лечению, n=6. *p<0,05 против Тощего контроля; и
Фиг.10 - график, показывающий влияние FM-VP4 после 30-дневного лечения на инсулин OGTT у тучных крыс линии Zucker. Данные представлены как среднее ± стандартное отклонение; в каждой группе, подвергнутой лечению, n=6. *p<0,05 против тучных.
ПРЕДПОЧТИТЕЛЬНЫЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
Нижеследующее подробное описание предлагается для того, чтобы помочь специалистам в данной области в осуществлении на практике настоящего изобретения. Однако это подробное описание не следует рассматривать как какое-либо ограничение объема настоящего изобретения. В изложенные здесь варианты осуществления изобретения специалистами средней квалификации в данной области могут быть внесены различные модификации и изменения, не выходя за рамки существа или объема настоящего изобретения.
В соответствии с настоящим изобретением предлагается способ лечения сахарного диабета и состояний, ассоциированных с сахарным диабетом, у животного, причем этот способ включает введение нетоксичного и терапевтически эффективного количества одного или нескольких нижеследующих соединений:



где R представляет собой часть фитостерола или фитостанола, R2 получен из аскорбиновой кислоты, R3 представляет собой водород или любой металл, щелочноземельный металл или щелочной металл, и всех их солей.
Подразумевается, что термин "терапевтически эффективный" определяет количество вводимого соединения(ий), необходимое для того, чтобы достичь одной или нескольких из нижеследующих целей:
а) лечение состояний, ассоциированных с сахарным диабетом, таких как гипергликемия и инсулинорезистентность, включая приобретенную инсулинорезистентность;
b) лечение осложнений сахарного диабета, таких как инсулинорезистентность, включая врожденную инсулинорезистентность, нарушенную толерантность к глюкозе и гиперинсулинемию;
с) лечение состояний, ассоциированных с инсулинорезистентностью, включая синдром поликистоза яичников, стероид-индуцированную инсулинорезистентность и сахарный диабет беременных;
d) лечение осложнений, ассоциированных с сахарным диабетом, включая почечные болезни, особенно почечную болезнь, связанную с диабетом типа 2, нейропатию и ретинопатию. Почечные болезни, связанные с диабетом типа 2, включая нефропатию, гломерулонефрит, гломерулосклероз, гипертензивный нефросклероз и почечную болезнь конечной (поздней) стадии. Дополнительные почечные болезни, ассоциированные с диабетом типа 2, включая нефротический синдром;
е) улучшение толерантности к глюкозе;
f) регулирование (контролирование) сывороточных уровней глюкозы;
g) повышение клеточной чувствительности к инсулину;
h) повышение чувствительности (восприимчивости) к глюкозе и уровня секреций инсулина панкреатическими бета-клетками;
i) лечение состояний, предшествующих диабету.
Сахарный диабет представляет (в настоящем описании) предпочтительно сахарный диабет типа 2.
Ниже будут более подробно описаны составные части соединений. Следует отметить, что, на всем протяжении данного описания, термины "соединение", "производное", "структура" и "аналог" могут использоваться взаимозаменяемо для описания вышеупомянутых структур, которые связывают как фитостерол или фитостанол, так и аскорбиновую кислоту и которые, как было обнаружено, являются эффективными в лечении сахарного диабета, состояний, ассоциированных с сахарным диабетом, и осложнений, ассоциированных с сахарным диабетом.
Фитостеролы/Фитостанолы
Используемый здесь термин "фитостерол" включает все фитостеролы, без ограничения, например ситостерол, кампестерол, стигмастерол, брассикастерол, десмостерол, халиностерол, пориферастерол, клионастерол, и все его природные или синтетические формы и его производные, включая изомеры. Термин "фитостанол" включает все насыщенные или гидрированные фитостеролы и все его природные или синтетические формы и его производные, включая изомеры. Необходимо иметь в виду, что модификации в отношении фитостеролов и фитостанолов, т.е. включение боковых цепей, также не выходят за рамки границ (объема) данного изобретения. Кроме того, необходимо иметь в виду, что, при возникновении сомнения по поводу употребления указанных выше двух терминов на всем протяжении настоящего описания, термин "фитостерол" заключает в себе как фитостерол, так и фитостанол, т.е. данные термины могут использоваться взаимозаменяемо, если не оговорено особо.
Фитостеролы и фитостанолы, используемые для получения производных в соответствии с данным изобретением, могут быть извлечены из ряда природных источников. Например, они могут быть получены при переработке растительных масел (включая масла водных растений), таких как кукурузное масло и другие растительные масла, жир зародышей пшеницы, экстракт сои, экстракт риса, рисовые отруби, рапсовое масло, подсолнечное масло, кунжутное масло и жиры рыб (и жиры других источников, относящихся к морскому миру). Настоящее изобретение не должно быть ограничено каким-либо одним источником фитостеролов. Патент США №4420427 раскрывает получение стеролов из растительного масличного фуза (баковый отстой), используя растворители, такие как метанол. Альтернативно, фитостеролы и фитостанолы можно получить из смолы таллового масла (жирная смесь омыляющихся веществ) или мыла, побочных продуктов переработки лесоводческой продукции, как описано в патенте США №5770749, который входит в настоящее описание в виде ссылки.
В одной предпочтительной форме производное настоящего изобретения получают с бета-ситостеролом, кампестанолом, ситостанолом и кампестеролом, природного происхождения или синтетически полученных, и каждое из этих производных, полученных таким образом, затем может быть вмешано в композицию до доставки в различных соотношениях. В другой предпочтительной форме производное настоящего изобретения получают с ситостанолом, природного происхождения или полученного синтетическим путем, или с кампестанолом, природного происхождения или полученного синтетическим путем, или их смесями.
В предпочтительной форме ситостанол представляет собой фитостанол. В наиболее предпочтительной форме соединение представляет собой любой фитостанолфосфориласкорбат или его соли.
R2
R2 включает аскорбиновую кислоту или любое ее производное. То, что достигнуто в пределах объема настоящего изобретения, это создание новой структуры или соединения, где часть фитостерола или фитостанола химически связана с аскорбиновой кислотой. Объединение приносит пользу и улучшает обе (составные) части этой новой структуры. Часть фитостерола, прежде плохо растворимая, становится, как часть нового производного, существенно более легко растворимой в водной или неводной среде, такой как масла и жиры. Соответственно становится возможным введение фитостерола без каких-либо дальнейших усовершенствований, связанных с его модификацией, для обеспечения его доставки в организм.
R3
R3 может представлять водород или может превратить исходное соединение в соль. Соображение, от которого зависит выбор соответствующей соли, состоит в том, что эти соли должны быть приемлемыми фармацевтически, нутрицевтически или приемлемыми для использования в пищевых продуктах, напитках и т.п. Такие соли должны иметь приемлемый анион или катион. В пределах объема настоящего изобретения, подходящие кислотно-аддитивные соли включают соли, полученные из неорганических кислот, таких как хлористоводородная, бромистоводородная, фосфорная, метафосфорная, азотная, сульфоновая и серная кислота, и органических кислот, таких как уксусная, бензолсульфоновая, бензойная, лимонная, этансульфоновая, фумаровая, глюконовая, гликоновая, гликолевая, изотионовая, молочная, лактобионовая, малеиновая, яблочная, метансульфоновая, янтарная, толуолсульфоновая и винная.
Подходящие соли основания включают соли аммония или любую соль металла, щелочноземельного металла или щелочного металла. Предпочтительно R3 выбран из: кальция, магния, марганца, меди, цинка, натрия, калия и лития. Наиболее предпочтительно R3 представляет собой натрий.
В наиболее предпочтительной форме настоящего изобретения соединение имеет структуру 1, отмеченную выше, фитостанол представляет собой ситостанол, R3 представляет собой натрий.
Получение производного
a) Получение сложного эфира
Существует много способов, с помощью которых можно получить структуры, включающие фитостеролы и/или фитостанолы и аскорбиновую кислоту. В общем, выбранный фитостерол или станол (или его галогенфосфат-, галогенкарбонат- или галогеноксалатные производные) и аскорбиновую кислоту смешивают вместе в соответствующих реакционных условиях, которые позволяют осуществить конденсацию "кислотной" части со "спиртом" (фитостерол). Эти условия являются такими же, которые используют в обычных реакциях эстерификации, таких как способ эстерификации по Фишеру, в котором кислотный компонент и спиртовой компонент подвергают взаимодействию непосредственно или в присутствии подходящего кислотного катализатора, такого как неорганическая (минеральная) кислота, серная кислота, фосфорная кислота, п-толуолсульфокислота. Органические растворители, обычно используемые в таких реакциях эстерификации, представляют собой простые эфиры, такие как диэтиловый эфир, тетрагидрофуран, или бензол, толуол или подобные ароматические растворители, и температуры могут варьироваться от комнатной до повышенных температур, в зависимости от реакционной способности реагирующих веществ, подвергающихся взаимодействию.
В предпочтительном варианте осуществления способ получения сложноэфирного производного включает "защиту" гидроксильных групп аскорбиновой кислоты или ее производных в виде сложных эфиров (например, в виде ацетатных сложных эфиров) или простых эфиров (например, метиловые эфиры) и затем конденсацию защищенной аскорбиновой кислоты с галогенфосфат-, галогенкарбонат- или галогеноксалатфитостерол/фитостанолом в подходящих условиях проведения реакции. В общем, вышеуказанные реакции конденсации проводят в органическом растворителе, таком как диэтиловый эфир, тетрагидрофуран, или бензоле, толуоле или подобных ароматических растворителях. В зависимости от природы и реакционной способности реагирующих веществ температуры реакции могут изменяться от низкой (-15°C) до повышенных температур.
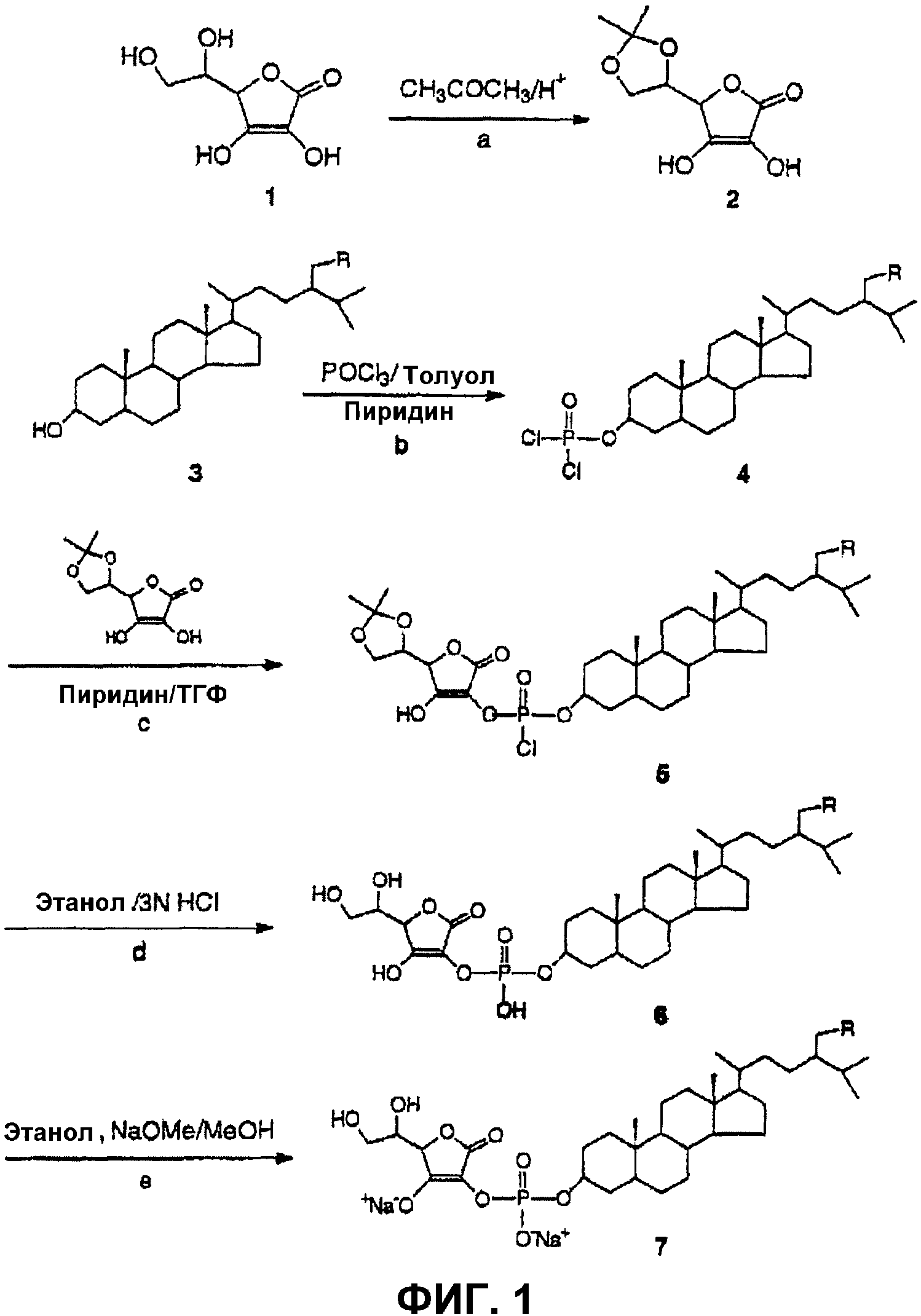
Фиг.1 - схематическое представление получения "защищенной" аскорбиновой кислоты (стадия a), получения промежуточного продукта, производного хлорфосфат/станола (стадия b), и реакции конденсации (альтернативно, стадии с или d) с получением одного из новых производных настоящего изобретения, отвечающего формуле I: фитостанолфосфатаскорбата (указанного как структура 6).
Более подробно, способ, представленный на Фиг.1, заключается в следующем: сначала аскорбиновую кислоту защищают от разложения посредством образования 5,6-изопропилиденаскорбиновой кислоты (структура 2). Это может быть достигнуто смешением ацетона с аскорбиновой кислотой и кислотным катализатором, таким как серная кислота или хлористоводородная кислота, в подходящих реакционных условиях (ссылка на пример 1 ниже). Хлорфосфатфитостанол (структура 4) получают путем получения раствора фитостанола в толуоле и пиридина (хотя альтернативно могут быть использованы другие азотсодержащие основания, такие как алифатические и ароматические амины) и обработки полученного раствора производным фосфора, таким как оксихлорид фосфора. Остаток, полученный после фильтрации и концентрирования маточного раствора, представляет собой хлорфосфатфитостанол (структура 4). Затем последний смешивают с 5,6-изопропилиденаскорбиновой кислотой и после добавления подходящего спирта, такого как этанол, и HCl (стадия d) концентрируют. Альтернативно, можно добавить смесь пиридин/ТГФ(THF) (стадия c) и продукт сконцентрировать. После окончательной промывки и сушки (стадия е) полученный новый продукт обеих стадий c или d представляет собой фитостанолфосфатаскорбат (структура 6).
Альтернативно, аскорбиновую кислоту защищают по гидроксильным группам, но не в виде 5,6-изопропилиденаскорбиновой кислоты, а в виде сложных эфиров (например, в виде ацетатов, фосфатов и т.п.). Затем последнюю конденсируют с фитостеролами или фитостанолами, дериватизируют, как описано выше, используя известные способы эстерификации, в конечном счете, получая структуры по данному изобретению. Образование моно- и дифосфатов аскорбиновой кислоты основательно описано в литературе. Например, в патенте США №4939128, содержание которого входит (составной частью) в описание настоящего изобретения в виде ссылки, Kato и др. раскрывают получение сложных эфиров фосфорной кислоты и аскорбиновой кислоты (phosphoric acid esters of ascorbic acid). Аналогично, патент США №4999437, выданный Dobler et al., содержание которого входит в описание настоящего изобретения в полном объеме в виде ссылки, описывает получение 2-фосфата аскорбиновой кислоты. У Dobler и др. основная реакция фосфорилирования аскорбиновой кислоты или производных аскорбиновой кислоты при помощи POCl3 в присутствии третичных аминов (описано в выложенной заявке на выдачу патента Германии (German Laid Open Application) DOS 2719303) усовершенствована добавлением в реакционный раствор соединения магния, предпочтительно водного раствора соединения магния. Любое из вышеупомянутых известных производных аскорбиновой кислоты может быть использовано в пределах объема настоящего изобретения.
Фиг.2 - схематическое представление получения "защищенной" аскорбиновой кислоты (стадия a), получения промежуточного производного хлоркарбонат/станола (стадия b) и реакции конденсации (необязательно стадии c или d) с получением структуры 9 (10 является такой же), одного из производных настоящего изобретения, отвечающего формуле II: фитостанолкарбонатаскорбата. Указанные хлоркарбонатные производные можно получить таким же способом, как подробно изложено выше согласно Фиг.1; однако оксихлорид фосфора заменяют (как показано на стадии b Фиг.2) на фосген.
Фиг.3 - схематическое представление получения "защищенной" аскорбиновой кислоты (стадия a), получения промежуточного производного хлороксалат/станола (стадия b) и реакции конденсации (необязательно стадии c или d) с получением новой структуры 13 (такая же, как 14), одного из производных настоящего изобретения, отвечающего формуле III: фитостанолоксалатаскорбата (указанной как структура 14). Указанные хлороксалатные производные можно получить таким же способом, как подробно изложено выше согласно Фиг.1; однако оксихлорид фосфора заменяют (как показано на стадии b Фиг.3) на оксалилхлорид.
b) Получение соли
Настоящее изобретение охватывает не только исходные (родоначальные) структуры, включающие фитостеролы или фитостанолы и аскорбиновую кислоту (например, предпочтительные структуры, представленные как структуры 5 и 6 на Фиг.1; структуры 9 и 10 на Фиг.2 и структуры 13 и 14 на Фиг.3), но также и их соли. Указанные соли являются даже более растворимыми в воде, чем соответствующие исходные соединения, и поэтому их эффективность и (объективная) оценка как in vitro, так и in vivo условиях значительно улучшена.
Образование солей производных настоящего изобретения можно легко осуществить обработкой исходного соединения рядом оснований (например, метоксидом натрия или алкоксидами других металлов) с получением соответствующих солей щелочных металлов. Соли других металлов, кальция, магния, марганца, меди, цинка и т.п., можно генерировать взаимодействием исходного соединения с алкоксидами соответствующих металлов. Что касается формулы I, R3 представляет собой либо водород (исходное соединение), либо любой металл, щелочно-земельный или щелочной металл (соль).
c) Восстановление каталитическими (гидрогенизация) и химическими способами
Необязательно, производные фитостерола настоящего изобретения или их составные части (либо фитостерол, либо аскорбиновая кислота) до или после получения производного могут быть гидрированными или насыщенными. Гидрогенизация гетероциклических структур в частично и полностью восстановленные аналоги представляет собой известный способ. Например, каталитическое и/или химическое восстановление цикла аскорбиновой кислоты в соответствующий дигидро-аналог легко осуществляют в атмосфере водорода и в присутствии металлического катализатора, такого как платина, палладий или никель Ренея. В общем, указанную реакцию проводят в органическом растворителе, таком как этанол, этилацетат, или аналогичных средах и либо при атмосферном давлении, либо при низком давлении (3-5 фунт/дюйм2) при комнатной температуре или слегка повышенных температурах.
Химические восстановления указанных систем включают восстановление семейством "гидридных" реагентов, таких как натрийборгидрид, литийалюминийгидрид и их аналоги. Указанные реакции восстановления обычно осуществляют в безводной инертной среде, включая этиловый эфир, тетрагидрофуран, диоксан или бензол, толуол или подобные ароматические растворители, при температурах от комнатной до температуры образования флегмы.
Подобные каталитические или химические способы (модификации) могут быть применены ко всем аналогам фитостерола настоящего изобретения. Соответственно соединения, используемые в рамках способов настоящего изобретения, включают все полностью или частично восстановленные производные, где цикл аскорбиновой кислоты является частично или полностью восстановленным и/или где часть фитостерола полностью или частично гидрогенизирована.
Производные
Настоящее изобретение включает способ лечения сахарного диабета и состояний, ассоциированных с сахарным диабетом, у животного, способ регулирования (контроля) сывороточных уровней глюкозы и повышения клеточной чувствительности к инсулину и способ повышения чувствительности к глюкозе и уровня секреций инсулина панкреатическими бета-клетками, и этот способ включает введение одного или нескольких из производных, содержащих фитостерол и/или фитостанол и аскорбиновую кислоту, включая их соли, представленных общими формулами:



где R представляет собой часть фитостерола или фитостанола; R2 получен из аскорбиновой кислоты, R3 представляет водород или любой металл, щелочно-земельный металл или щелочной металл. Наиболее предпочтительно соединения представляют собой производные галогенфосфат-, галогенкарбонат- и галогеноксалат/фитостанол/аскорбата, иллюстрированные на Фиг.1-3 в виде структур 5, 6, 7, 9, 10, 11, 13, 14 и 15. Должно быть совершенно очевидно, однако, что указанные структуры представляют собой лишь вариант выборки из многих новых производных, которые не выходят за рамки границ (объема), охватываемых формулами I, II и III, и которые могут быть использованы в соответствии со способами настоящего изобретения. Кроме того, необходимо иметь в виду, что хотя структурами 7, 11 и 15 (см. Фиг.1-3) представлены натриевые соли заявляемых (исходных) соединений, в объем изобретения также входят и другие соли, как это описано выше.
Механизм действия
Не углубляясь в какую-либо теорию относительно обоснования различных терапевтических эффективностей описанных здесь соединений, кажется, что многое опирается на улучшенную толерантность к глюкозе, предоставляемую этими соединениями.
Данные, предоставленные в примерах ниже, показывают, что имеет место весьма значительное улучшение в толерантности к глюкозе в группе тучных животных, которые демонстрируют кривую глюкозотолерантности, присущую диабетикам. Хотя ответ инсулина на пероральную глюкозу не показывает никакого существенного изменения у недиабетических тощих животных, в группе тучных животных наблюдается изменение в профиле секреции инсулина после лечения FM-VP4. Тучные животные являются крайне инсулинорезистентными и гиперинсулинемическими. Полагают, что гиперинсулинемия представляет собой попытку скомпенсировать недостаток эффективности инсулина на его тканях-мишенях (инсулинорезистентность). Эти животные также характеризуются притупленным ответом инсулина на глюкозу. Это доказывается почти плоским ответом инсулина на пероральную глюкозу, видным на Фиг.5 (группа до исследования). Очевидно, что соединения настоящего изобретения улучшают толерантность к глюкозе у тучных (генетически) диабетических крыс.
Способы использования
Желательные воздействия, описанные здесь, могут быть достигнуты различными способами. Указанные соединения можно вводить любым обычным способом, пригодным для использования в сочетании с фармацевтическими препаратами, нутрицевтиками, пищевыми продуктами, напитками и т.п.
Количество соединения, которое необходимо для достижения желательных воздействий, будет, конечно, зависеть от ряда факторов, таких как конкретное выбранное соединение, способ введения и состояние больного.
Соединения настоящего изобретения можно вводить больному либо как таковые, либо в фармацевтических композициях, где они смешаны с подходящими носителями или наполнителями.
Использование фармацевтически приемлемых носителей для формулирования заявляемых здесь соединений для осуществления данного изобретения на практике в лекарственные формы (dosage form), подходящие для системного введения, находится в пределах объема данного изобретения. В отношении соответствующего выбора носителя и подходящего способа получения, соединения настоящего изобретения, в частности соединения, формулированные в виде растворов, можно вводить парентерально, как например путем внутривенной инъекции. Соединения могут быть легко формулированы, используя хорошо известные в данной области фармацевтически приемлемые носители, в лекарственные формы, подходящие для перорального введения. Такие носители дают возможность сформулировать соединения данного изобретения в виде таблеток, пилюль, капсул, жидкостей, гелей, сиропов, взвесей, суспензий и т.п. для проглатывания больным (прием внутрь пероральным путем), который подлежит лечению.
Фармацевтические композиции, включающие одно или несколько соединений настоящего изобретения, включают композиции, в которых активные компоненты содержатся в эффективном количестве, достаточном для достижения предопределенной цели. Определение эффективных количеств находится в компетенции квалифицированных специалистов в данной области, особенно в свете представленного здесь подробного описания изобретения.
Помимо активных компонентов, указанные фармацевтические композиции могут содержать подходящие фармацевтически приемлемые носители, включая наполнители и вспомогательные вещества, которые облегчают переработку активных соединений в препараты, которые могут быть использованы фармацевтически. Препараты, формулированные для перорального приема, могут быть в форме таблеток, драже, капсул или растворов.
Фармацевтические композиции настоящего изобретения могут быть получены способом, который сам по себе является известным, например посредством обычного смешения, растворения, грануляции, приготовления драже, растирания в порошок, эмульгирования, инкапсулирования, способами улавливания (захватывания) или лиофилизации.
Фармацевтические составы для парентерального введения включают водные растворы активных соединений в водно-растворимой форме. Дополнительно, можно получить суспензии активных соединений в виде соответствующих маслянистых суспензий для инъекции.
Подходящие липофильные растворители или наполнители включают жирные масла, такие как кунжутное масло, или синтетические сложные эфиры жирных кислот, такие как этилолеат или триглицериды, или липосомы. Водные суспензии для инъекций могут содержать вещества, которые повышают вязкость суспензий, такие как карбоксиметилцеллюлоза, сорбит или декстран. Необязательно, суспензия может дополнительно содержать подходящие стабилизаторы или средства, которые увеличивают растворимость соединений, допуская получение высококонцентрированных растворов.
Фармацевтические препараты для перорального применения можно получить путем объединения активных соединений с твердым наполнителем, необязательно измельчения полученной смеси, и переработки смеси гранул, после добавления подходящих вспомогательных веществ, если это требуется, чтобы получить таблетки или ядра драже. Подходящими наполнителями являются, в частности, такие наполнители как сахара, включая лактозу, сахарозу, маннит или сорбит; целлюлозные препараты, такие как, например, кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, трагакантовая камедь, метилцеллюлоза, гидроксипропилметилцеллюлоза, натрий карбоксиметилцеллюлоза, и/или поливинилпирролидон (PVP). Если необходимо, могут быть добавлены дезинтегрирующие средства, такие как сшитый поливинилпирролидон, агар или альгиновая кислота или ее соль, такая как альгинат натрия.
Ядра драже обеспечиваются подходящими покрытиями. Для этой цели можно использовать концентрированные растворы сахаров, которые могут необязательно содержать аравийскую камедь, тальк, поливинилпирролидон, карбопол гель (carbopol gel), полиэтиленгликоль, и/или диоксид титана, растворы лака и подходящие органические растворители или смеси растворителей. Красящие вещества (красители) или пигменты могут быть добавлены в составы для покрытий таблеток или драже для идентификации или для того, чтобы охарактеризовать различные комбинации доз активного соединения.
Фармацевтические препараты, которые можно использовать перорально, включают (твердые) капсулы с разъемом для наполнения (push-fit), приготовленные из желатина, а также мягкие, герметизированные капсулы, полученные из желатина и пластификатора, такого как глицерин или сорбит. Твердые капсулы могут содержать активные компоненты в смеси с наполнителем, таким как лактоза, связующими средствами, такими как крахмалы, и/или смазками, такими как тальк или стеарат магния, и, необязательно, стабилизаторами. В мягких капсулах активные соединения могут быть растворены или суспендированы в подходящих жидкостях, таких как жирные (нелетучие) масла, жидкий парафин или жидкие полиэтиленгликоли. Кроме того, могут быть добавлены стабилизаторы.
Пероральные жидкие препараты могут быть в форме, например, эмульсий, сиропов или эликсиров или они могут быть представлены в виде сухого продукта, подлежащего воссозданию с водой или другим подходящим наполнителем перед использованием. Указанные жидкие препараты могут содержать обычные добавки, такие как суспендирующие средства, например сорбит, сироп, метилцеллюлозу, желатин, гидроксиэтилцеллюлозу, карбоксиметилцеллюлозу, гель стеарата алюминия, гидрогенизированные годные в пищу жиры; эмульгирующие средства, например лецитин, сорбитмоноолеат или акация; неводные наполнители (которые могут включать годные в пищу масла), например миндальное масло, фракционированное кокосовое масло, маслянистые сложные эфиры, такие как сложные эфиры глицерина, пропиленгликоля, или этиловый спирт; консерванты, например метил- или пропил п-гидроксибензоат или сорбиновая кислота; и, если требуется, обычные ароматизирующие средства или красители.
В другой форме настоящего изобретения соединения по данному изобретению могут быть введены при помощи пищевых продуктов, напитков и нутрицевтиков, включая, без ограничения, нижеследующее:
1) молочные продукты - такие как сыры, масло, молоко и другие молочные напитки, пастообразные и молочные смеси, мороженое и йогурт;
2) продукты на основе жиров - такие как маргарины, пасты, майонез, шортенинги, кулинарные жиры и масла для жарки и заправки (приправы);
3) продукты на основе злаков - включая зерновые культуры (например, хлеб и макаронные изделия), независимо от того являются ли эти изделия (пищевые продукты) вареными, печеными или полученными в результате другой обработки;
4) кондитерские изделия - такие как шоколад, сладости (конфеты), жевательная резинка, десерты (сладкое блюдо), сливки немолочного происхождения (например, Cool Whip™), щербеты, глазури и другие кондитерские начинки;
5) напитки - независимо от того являются ли они алкогольными или не содержат алкоголя, включая колас (газированные) и другие безалкогольные напитки, соки (нектары), пищевые добавки и жидкие заменители еды, такие как, например, продаваемые под торговыми марками Boost™ и Ensure™; и
6) смешанные (разнородные) продукты - включая яйца и продукты с добавлением яиц; пищевые продукты, подвергшиеся обработке, такие как супы, предварительно приготавливаемые соусы для макаронных блюд, полуфабрикаты (предварительно приготовленная еда) и т.п.
Соединения по данному изобретению могут быть включены непосредственно и без дополнительного изменения в пищу, используя такие способы как смешение, вливание, впрыскивание, диспергирование, эмульгирование, погружение, разбрызгивание (напыление) и замешивание (сбивание). Альтернативно, соединения могут применяться непосредственно на пищевой продукт или в напиток потребителем до глотания (приема внутрь). Вышеуказанные варианты являются простыми и экономичными способами доставки заявляемых соединений.
ПРИМЕРЫ
Настоящее изобретение описывается нижеследующими примерами, которые являются лишь его иллюстрацией, но не ограничением.
Пример 1
Защита аскорбиновой кислоты
Олеум (24%, 8,3 г) добавляют по каплям к ацетону (50 мл). Аскорбиновую кислоту (12 г) вводят в смесь при 0°C и реакционную смесь перемешивают при 0°C в течение 6 часов. Полученные кристаллы отфильтровывают путем отсасывания и фильтрованный осадок отжимают досуха и затем промывают ацетоном (30 мл). Получают продукт, 5,6-изопропилиденаскорбиновую кислоту (14 г).
Пример 2
Присоединение к фитостанолам
Раствор смеси (25 г) фитостанолов (кампестанол: 36,4%; ситостанол: 62,3%) в толуоле (500 мл) и пиридина (25 мл) добавляют по каплям к смеси фосфористого оксихлорида (9 мл) в толуоле (200 мл) при 0°C. Смесь перемешивают при комнатной температуре в течение 3 часов. Гидрохлорид пиридина отфильтровывают и маточный раствор концентрируют, чтобы извлечь толуол. Остаток растворяют в сухом ТГФ (THF) (100 мл) и добавляют по каплям при 0°C раствор вышеполученной защищенной аскорбиновой кислоты (14 г) в сухом ТГФ (THF) (400 мл). Перемешивание при комнатной температуре поддерживают в течение 1 часа. Раствор концентрируют, чтобы удалить растворитель. Добавляют этанол (400 мл) и 3N HCl (200 мл), смесь нагревают до 50°C в течение 30 мин и концентрируют. Добавляют этилацетат (600 мл), полученный раствор промывают водой (3×300 мл), сушат над сульфатом натрия, концентрируют и получают 22 г продукта (фитостанолфосфатаскорбат) в виде белого порошка.
Пример 3
Превращение в натриевую соль
Вышеполученную кислоту (17 г) растворяют в этаноле (100 мл) и добавляют при перемешивании и при комнатной температуре раствор метоксида натрия (2,7 г) в этаноле (50 мл). Перемешивание поддерживают в течение 30 мин после добавления. Полученный белый осадок отфильтровывают, сушат и взвешивают, получая 20 г белого порошка (фитостанолфосфатаскорбат натрий).
Пример 4
Исследование на тучных крысах (fa/fa) линии Zucker
Взрослых тучных (fa/fa) и тощих крыс-самцов линии Zucker (весом 340-410 г) использовали как в лечении на протяжении 4-х недель по протоколу, так и в исследованиях по абсорбции (всасыванию) в желудочно-кишечном тракте (ЖК, GI) [3H]-холестерина. Крыса представляла собой соответствующую животную модель для исследования всасывания холестерина в ЖК (GI) после перорального введения из-за сходств в интестинальных характеристиках (т.е. анатомических, метаболических и биохимических характеристиках) и в интестинальной обработке и абсорбции диетического холестерина между крысами и людьми. Аналогичная обработка и абсорбция диетического (вводимого с пищей) холестерина наблюдается у крыс линии Zucker.
Определение концентраций глюкозы, инсулина, лептина и липидов в плазме
Глюкозу определяют, используя систему мониторинга уровня глюкозы в крови Surestep (Lifescan Canada). Уровни инсулина и лептина измеряют радиоиммуноанализом (наборы RIA LINCO corp). Содержание холестерина и триглицеридов в плазме определяют, используя наборы ферментов (Sigma, St. Louis, MO), как описано ранее.
Построение исследования. В этом исследовании используют группу меченых тучных крыс-самцов (n=6) и тощих крыс VDF (n=6), возраста 12 лет. До введения одного из соединений настоящего изобретения, обозначенного как "FM-VP4" (ситостанолфосфатаскорбат), животных взвешивают и подвергают голоданию на протяжении ночи, отбирают пробы крови (натощак) для определения: глюкозы, инсулина, лептина, холестерина и триглицеридов. Затем животных обрабатывают 250 мг/кг FM-VP4 дважды в день путем кормления через желудочный зонд в течение 30 дней (используя 2% раствор FM-VP4, растворенного в питьевой воде). Каждые два дня животных взвешивают и определяют у них утренние уровни глюкозы в крови. По окончании 30 дней всех животных подвергают голоданию на протяжении ночи и проводят второй пероральный глюкозотолерантный тест (ПГТТ). У всех животных отбирают пробы крови натощак на определение глюкозы, инсулина и лептина. За этим следует пероральный глюкозотолерантный тест (ПГТТ, OGTT), выполняемый на находящихся в сознании, естественно себя ведущих животных, как описано ранее. Животные получали глюкозу (1 г/кг в виде 40% раствора), используя кормление через желудочный зонд, и отбирали пробы крови на 10, 20, 30, 60 и 120 минутах на определение глюкозы и инсулина.
Концентрация [3H]-холестерина в плазме после введения FM-VP4
Разработка состава FM-VP4-[3H]-холестерин для кормления через пероральный зонд. Составы состояли из 25 мкКи [3H]-холестерина (соответствующее 227,3 нг холестерина, исходя из специфической активности 110 мКи/мг; Amersham, Mississauga, ON, Canada), 1 мг немеченого (радиоактивным изотопом) холестерина (6,7) и возрастающих количеств FM-VP4 (1-20 мг). Составы смешивают с 1 мл Intralipid® (Clintec Nutritional Company; Deerfield, IL, USA) в день исследования и осторожно встряхивают. Intralipid® представляет собой стерильную, не содержащую пирогена, жировую эмульсию, полученную для введения в качестве источника калорий и необходимых жирных кислот и которую используют в качестве наполнителя для солюбилизации и совместного введения с экзогенным [3H]-холестерином и FM-VP4 в осязаемом (palpable) пероральном составе. Анализ комплексным методом, представляющим собой сочетание жидкостной хроматографии и масс-спектрометрии, обнаружил минимальное общее содержание холестеринов и содержание растительных станолов в пределах 10% Intralipid® до введения экзогенного холестерина (меченого и немеченого) и FM-VP4, как опубликовано ранее.
Различия в массе тела, глюкозы в крови, уровней лептина, глюкозы и инсулина в плазме после перорального глюкозотолерантного теста и абсорбции в ЖК [3H]-холестерина между группами, подвергнутыми лечению, и контрольными группами определяли, используя дисперсионный анализ (PCANOVA; Human Dynamic Systems). Статистические различия определяли, используя Newman Keuls post-hoc тест. Различия считали значимыми, если p<0,05. Все данные выражены как среднее ± стандартное отклонение.
Результаты
Масса тела. Профили массы тела на протяжении 30-дневного периода лечения лекарственным средством (Фиг.4) не показывают после лечения никакого существенного изменения массы тела ни в группе тощих крыс, ни в группе тучных крыс.
Утреннее содержание глюкозы в крови. Профили утреннего содержания глюкозы в крови на протяжении 30-дневного периода лечения лекарственным препаратом (Фиг.5) не показывают после лечения никакого существенного изменения в утреннем уровне глюкозы в крови (определяемом не в голодном состоянии) ни в группе тощих крыс, ни в группе тучных крыс. Всегда существует изменчивость (переменность) в этих показаниях, так как животные могут различаться по состоянию питания относительно времени измерения глюкозы (8 ч утра). Однако в этих исследованиях уровни глюкозы в крови остаются относительно согласованными на всем протяжении исследования. Кроме того, лечение FM-VP4 не вносит изменения в ежедневный рацион питания и/или потребление воды тощих и тучных крыс линии Zucker (данные не показаны).
Уровни лептина в плазме. Уровни satiety гормона-лептина существенно не изменились после лечения лекарственным препаратом ни в одной группе (Фиг.6). Следует отметить, что у тучных крыс линии Zucker имело место первичное нарушение, заключающее в мутации центральных рецепторов лептина, приводящее к аномальной регуляции аппетита через гипоталамус. Как следствие fa/fa, тучные животные имеют крайне повышенные уровни лептина. Имеются данные, указывающие на снижение уровней лептина после лечения FM-VP4 у тучных животных, однако эти различия не значительны.
Данные по глюкозе согласно пероральному глюкозотолерантному тесту (ПГТТ, OGTT). На фиг.7 и 8 представлены данные по глюкозе согласно ПГТТ (OGTT) для тощих и тучных животных соответственно до и после лечения FM-VP4. В то время как для группы недиабетических, с нормальной гликемией, тощих крыс не наблюдается изменения в толерантности к глюкозе, в группе тучных животных, которые демонстрируют кривую глюкозотолерантности, присущую диабетикам, имеет место весьма существенное улучшение толерантности к глюкозе (Фиг.8).
Данные по инсулину согласно пероральному глюкозотолерантному тесту (ПГТТ, OGTT). На фиг.9 и 10 представлены данные по инсулину согласно ПГТТ для тощих и тучных животных соответственно до и после лечения FM-VP4. Ответ инсулина на пероральную глюкозу не претерпевает никакого существенного изменения у недиабетических тощих животных (Фиг.9), в то время как в группе тучных животных после лечения FM-VP4 имеет место изменение в профиле секреции инсулина (Фиг.10).
Обсуждение
Цель этих исследований заключалась в определении воздействий фитостанолфосфориласкорбата (FM-VP4) на инсулинорезистентность и гипергликемию у тучных (fa/fa) и тощих крыс линии Zucker. Лечение (FM-VP4) не изменило массы тела, утренние уровни глюкозы и лептина. Полученные данные свидетельствуют о том, что FM-VP4 не вносит изменений в системный и (наследственно) генетически предрасположенный метаболизм глюкозы и гормонально регулируемый аппетит.
Кроме того, в то время как для группы недиабетических, с нормальной гликемией, тощих крыс не наблюдается изменение в толерантности к глюкозе, в группе тучных животных, которые демонстрируют кривую глюкозотолерантности, присущую диабетикам, имеет место весьма значительное улучшение толерантности к глюкозе. Однако, хотя ответ инсулина на пероральную глюкозу не претерпевает никакого существенного изменения у недиабетических тощих животных, в группе тучных животных имеет место изменение в профиле секреции инсулина после лечения FM-VP4. Тучные животные являются крайне инсулинорезистентными и гиперинсулинемическими. Полагают, что гиперинсулинемия представляет собой попытку скомпенсировать недостаток эффективности инсулина на его тканях-мишенях (инсулинорезистентность). Эти животные характеризуются притупленным ответом инсулина на глюкозу. Последнее проявляется в почти плоском ответе инсулина на пероральную глюкозу, как это видно на Фиг.8 (группа до исследования).
Интересно, что ранний пик секреции инсулина на 10-минутном периоде времени после введения пероральной глюкозы сопровождается улучшением толерантности к глюкозе у указанных животных после лечения FM-VP4. Это указывает на повышение чувствительности к глюкозе панкреатической бета-клетки, секретирующей инсулин, у этих животных в результате такого лечения. Потеря глюкозостимулируемой секреции инсулина ранней фазы является критерием (признаком) возникновения диабета типа 2 (начало диабета у лиц зрелого возраста) у людей и животных моделей диабета типа 2, включая используемую в исследовании колонию тучных крыс линии Zucker. Независимо от механизма улучшения толерантности к глюкозе при лечении by FM-VP4 (не из-за анорексии или потери массы тела, см. Фиг.4), снижение гипергликемии, вероятно, оказывает действие на снижение степени тяжести инсулинорезистентности, а это, в свою очередь, снижает потребность в инсулине и приводит к более чувствительному (реактивному) функционированию поджелудочной железы.
В заключение, введение FM-VP4 вызывает существенное улучшение толерантности к глюкозе в пределах тучных крыс линии Zucker без изменения массы тела и утренних уровней глюкозы, инсулина и лептина как у тощих, так и тучных крыс.
ССЫЛКИ
1. Olefsky, 1988, in "Cecil Textbook of Medicine", 18th Ed., 2:1360-81.
2. De Fronzo R.A. Ferrannini E. Insulin resistance: A multifaceted syndrome response for NIDDM, obesity, hypertension, dyslipidemia and atherolsclerotic cardiovascular disease. Diabetes Care:14:173; 1991.
3. Beck-Nielsen H., Pedersen O., Sorensen N.S. Effects of dietary changes on cellular insulin binding and in vivo insulin sensitivity. Metabolism 29:482: 1994.
Реферат
Изобретение относится к медицине, в частности к эндокринологии, и касается лечения сахарного диабета, ассоциированных с ним состояний и осложнений. Для этого вводят терапевтически эффективные количества фитостанола, охарактеризованного общей формулой I. Введение этих соединений в разработанных терапевтических дозах обеспечивает эффективное лечение сахарного диабета за счет повышения клеточной чувствительности к глюкозе и инсулину и усиления секреции инсулина бета-клетками поджелудочной железы. 4 н. и 14 з.п. ф-лы, 10 ил.
Формула




Документы, цитированные в отчёте о поиске
Способ выделения композиции фитостеролов, композиции, терапевтический продукт

Комментарии