Антитела против рецептора фолиевой кислоты 1, их иммуноконъюгаты и использование - RU2610663C2
Код документа: RU2610663C2
Чертежи





























































































Описание
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка претендует на приоритет заявки на патент США №61/307797, поданной 24 февраля 2010, заявки на патент США №61/346595, поданной 20 мая 2010, и заявки на патент США №61/413172, поданной 12 ноября 2010, содержание которых включено в данную заявку посредством ссылки во всей полноте.
ОБЛАСТЬ ТЕХНИКИ
[0002] Область техники настоящего изобретения в целом относится к антителам, их антиген-связывающим фрагментам, полипептидам, иммуноконъюгатам, соединяющимся с человеческим рецептором фолиевой кислоты 1, а также к способам использования антител и иммуноконъюгатов для терапии заболеваний, например, онкологических заболеваний.
УРОВЕНЬ ТЕХНИКИ
[0003] Онкологические заболевания - одна из основных причин смертности в развитых странах; за один год только в США диагноз онкологического заболевания ставится более чем одному миллиону людей, а умирает по причине онкологических заболеваний 500000 людей. По оценкам более чем у 1 человека из 3-х разовьется онкологическое заболевание в течение жизни. Известно более 200 различных видов рака, четыре из которых - молочной железы, легкого, колоректальный и рак простаты - отмечаются в более чем половине новых случаев рака (Jemal et al., 2003, Cancer J. Clin. 53:5-26).
[0004] Рецептор фолиевой кислоты 1 (FOLR1), также известный как альфа-рецептор фолиевой кислоты или фолат-связывающий белок, представляет собой N-гликозилированный белок, который экспрессируется на плазматической мембране клеток. FOLR1 обладает высокой аффинностью к фолиевой кислоте и ряду ее восстановленным производным. FOLR1 опосредует доставку физиологического фолата 5-метилтетрагидрофолата внутрь клеток.
[0005] FOLR1 избыточно экспрессируется при большинстве видов онкологических заболеваний яичника, а также при множестве онкологических заболеваний матки, эндометрия, поджелудочной железы, почек, легких и молочной железы, в то время как в нормальных тканях FOLR1 экспрессируется лишь в апикальной мембране эпителиальных клеток проксимальных канальцев почек, альвеолярных пневмоцитах легких, в мочевом пузыре, яичках, хориоидном сплетении и в щитовидной железе (Weitman SD, et al., Cancer Res 52: 3396-3401 (1992); Antony AC, Annu Rev Nutr 16: 501-521 (1996); Kalli KR, et al. Gynecol Oncol 108: 619-626 (2008)). Благодаря этой схеме экспрессии, FOLR1 является подходящей мишенью для FOLR1-направленной противоопухолевой терапии.
[0006] Поскольку рак яичника, как правило, протекает бессимптомно вплоть до поздней стадии, его часто диагностируют на поздней стадии с плохим прогнозом при терапии доступными в настоящее время процедурами, - как правило, химиотерапией после циторедуктивного хирургического вмешательства (von Gruenigen V et al., Cancer 112: 2221-2227 (2008); Ayhan A et al., Am J Obstet Gynecol 196: 81 е81-86 (2007); Harry VN et al., Obstet Gynecol Surv 64: 548-560 (2009)). Таким образом, имеется четкая неудовлетворенная медицинская потребность в более эффективных средствах лечения онкологических заболеваний яичника.
[0007] В качестве потенциальных противоопухолевых лекарственных средств были изучены три антитела против FOLR1. Мышиные моноклональные антитела Movl8 и Mov19 были выделены в в поздних 1980-х гг. (Miotti S et al., Int J Cancer 39: 297-303 (1987)), была подтверждена их аффинность против FOLR1 (Coney LR et al., Cancer Res 51: 6125-6132 (1991)), а затем они были протестированы в доклинических исследованиях на способность в виде конъюгатов с цитотоксическми белком, инактивирующим рибосомы, ликвидировать антиген-экспрессирующие раковые клетки (Conde FP et al., Eur J Biochem 178:795-802 (1989)).
[0008] Mov19 было протестировано в качестве биспецифического антитела, нацеленного на цитотоксические Т-клетки и клетки-натуральные киллеры (Mezzanzanica D et al., Int J Cancer 41: 609-615 (1988); Fen-mi S et al., Int J Cancer Suppi 4: 53-55 (1989); Ferrini S et al., Int J Cancer 48: 227-233 (1991)), а также в виде слитого белка, состоящего из одноцепочечного Fv (scFv) Mov19 и интерлейкина-2 in vivo (Melani С et al., Cancer Res 58: 4146-4154 (1998)). Для химерных (мышиная вариабельная/человеческая константная) антител против FOLR1 Movl8 и Mov19 была изучена доклинически способность опосредовать цитотоксическую иммунную клеточнозависимую гибель клеток опухолей, экспрессирующих FOLR1 in vitro (Coney LR et al., Cancer Res 54: 2448-2455 (1994)), химерное Movl8-IgE было протестировано в IgE-зависимых иммунотерапевитических доклинических моделях (Karagiannis SN et al., J Immunol 179: 2832-2843 (2007); Gould HJ et al., EurJImmunol 29: 3527-3537 (1999)).
[0009] Movl8 в виде конъюгатов с различными радионуклидами прошло доклинические исследования, а в начале 1990-х гг. - и клинические (Zacchetti A et al., Nucl Med Biol 36: 759-770 (2009)), по результатам которых ни один препарат не был утверджен.
[0010] МОКАЬОО3-гуманизированная форма мышиного моноклонального антитела против FOLR1 LK.26 - прошла доклиническое исследование в виде немодфицированного антитела (Ebel W et al., Cancer Immun 7:6 (2007)) и в виде конъюгата с радионуклидом111In (Smith-Jones PM et al., Nucl Med Biol 35: 343-351 (2008)), и в настоящее время проходит клинические исследования как немодифицированное антитело (D.K. Armstrong et al. J. Clin. Oncol. 26:2008, May 20 suppi; abstract 5500).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0011] В настоящем изобретении предлагаются новые антитела, связывающиеся с человеческим рецептором фолиевой кислоты 1, иммуноконъюгаты, содержащие эти антитела, а также способы их применения. Помимо этого, в настоящем изобретении предлагаются новые полипептиды, например, антитела, связывающиеся с человеческим рецептором фолиевой кислоты 1, фрагменты таких антител и иные полипептиды, связанные с такими антителами. Также предлагаются полинуклеотиды, содержащие нуклеотидные последовательности, кодирующие полипептиды, и векторы, содержащие полинуклеотиды. Помимо этого, предлагаются клетки, содержащие полипептиды и/или полинуклеотиды по изобретению. Также предлагаются композиции (например, фармацевтические композиции), содержащие новые антитела против рецептора фолиевой кислоты 1. Помимо этого, предлагаются способы получения и применения новых антител против рецептора фолиевой кислоты 1 или иммуноконъюгатов, например, способы, в которых новые антитела против рецептора фолиевой кислоты 1 или иммуноконъюгаты используются для ингибирования роста опухоли и/или для лечения рака.
[0012] Таким образом, в одном аспекте в изобретении предлагается гуманизированное антитело или его антиген-связывающий фрагмент, которые специфически связываются с рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит (a) CDR1 тяжелой цепи, содержащую GYFMN (SEQ ID NO:1); CDR2 тяжелой цепи, содержащую RIHPYDGDTFYNQXaa1FXaa2Xaa3 (SEQ ID NO:56); и CDR3 тяжелой цепи, содержащую YDGSRAMDY (SEQ ID NO:3); и (б) CDR1 легкой цепи, содержащую KASQSVSFAGTSLMH (SEQ ID NO:7); CDR2 легкой цепи, содержащую RASNLEA (SEQ ID NO:8); CDR3 легкой цепи, содержащую QQSREYPYT (SEQ ID NO:9); где Xaa1 выбран из К, Q, Н и R; Хаа2 выбран из Q, Н, N и R; и Хаа3 выбран из G, Е, Т, S, А и V. В определенном варианте воплощения гуманизированное антитело или его антиген-связывающий фрагмент связываются с человеческим рецептором фолиевой кислоты 1 с практически такой же аффинностью, что и химерное антитело Mov19. В определенном варианте воплощения гуманизированное антитело или его антиген-связывающий фрагмент содержит последовательность CDR2 тяжелой цепи RIHPYDGDTFYNQKFQG (SEQ ID NO:2).
[0013] В определенном варианте воплощения связывающую способность измеряют способом проточной цитометрии, Biacore или радиоиммунологическим анализом.
[0014] В ином варианте воплощения в изобретении предлагается гуманизированное антитело или его антиген-связывающий фрагмент, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (a) CDR1 тяжелой цепи, содержащую GYFMN (SEQ ID NO:1), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; CDR2 тяжелой цепи, содержащую RIHPYDGDTFYNQKFQG (SEQ ID NO:2), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и CDR3 тяжелой цепи, содержащую YDGSRAMDY (SEQ ID NO:3), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или (б) CDR1 тяжелой цепи, содержащую KASQSVSFAGTSLMH (SEQ ID NO:7), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; CDR2 тяжелой цепи, содержащую RASNLEA (SEQ ID NO:8), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; CDR3 тяжелой цепи, содержащую QQSREYPYT (SEQ ID NO:9), либо ее вариант, включающий 1,2,3 или 4 консервативных аминокислотных замены.
[0015] В определенном варианте воплощения в изобретении предлагается гуманизированное антитело или его антиген-связывающий фрагмент, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, содержащие тяжелую цепь с SEQ ID NO:6. В другом варианте воплощения гуманизированное антитело или его антиген-связывающий фрагмент кодируются плазмидной ДНК, депонированной в АТСС 7 апреля 2010 под номерами депонентов АТСС РТА-10772 и РТА-10773 или 10774.
[0016] В определенном варианте воплощения в изобретении предлагается гуманизированное антитело или его антиген-связывающий фрагмент, которые конкурируют по связыванию с FOLR1 с антителом, содержащим (а) CDR1 тяжелой цепи, содержащую GYFMN (SEQ ID NO:1); CDR2 тяжелой цепи, содержащую RIHPYDGDTFYNQXaa1FXaa2Xaa3 (SEQ ID NO:56); и CDR3 тяжелой цепи, содержащую YDGSRAMDY (SEQ ID NO:3); и (б) CDR1 легкой цепи, содержащую KASQSVSFAGTSLMH (SEQ ID NO:7); CDR2 легкой цепи, содержащую RASNLEA (SEQ ID NO:8); CDR3 легкой цепи, содержащую QQSREYPYT (SEQ ID NO:9); где Xaa1 выбран из K, Q, Н и R; Xaa2 выбран из Q, Н, N и R; и Хаа3 выбран из G, Е, Т, S, А и V. В определенном варианте воплощения гуманизированное антитело содержит последовательность CDR2 тяжелой цепи RIHPYDGDTFYNQKFQG (SEQ ID NO:2).
[0017] В определенном варианте воплощения в изобретении предлагается полипептид, гуманизированное антитело или его антиген-связывающий фрагмент, содержащие вариабельный домен тяжелой цепи, по меньшей мере на приблизительно 90% идентичный SEQ ID NO:4, и вариабельный домен легкой цепи, по меньшей мере на приблизительно 90% идентичный SEQ ID NO:10 или SEQ ID NO:11. В ином варианте воплощения гуманизированное антитело или его антиген-связывающий фрагмент содержат вариабельный домен тяжелой цепи, по меньшей мере на приблизительно 95% идентичный SEQ ID NO:4, и вариабельный домен легкой цепи, по меньшей мере на приблизительно 95% идентичный SEQ ID NO:10 или SEQ ID NO:11. В еще одном варианте воплощения гуманизированное антитело содержит вариабельный домен тяжелой цепи, по меньшей мере на приблизительно 99% идентичный SEQ ID NO:4, и вариабельный домен легкой цепи, по меньшей мере на приблизительно 99% идентичный SEQ ID NO:10 или SEQ ID NO:11. В определенном варианте воплощения гуманизированное антитело содержит вариабельный домен тяжелой цепи последовательности SEQ ID NO:4, и вариабельный домен легкой цепи последовательности SEQ ID NO:10 или SEQ ID NO:11. В определенных вариантах воплощения в изобретении предлагается полипептид, антитело или антиген-связывающий фрагмент, содержащие вариабельный домен тяжелой цепи, по меньшей мере на приблизительно 90% идентичный SEQ ID NOs:88-119. В определенных вариантах воплощения в изобретении предлагается полипептид, антитело или антиген-связывающий фрагмент, содержащие вариабельный домен тяжелой цепи, по меньшей мере на приблизительно 95% идентичный SEQ ID NOs:88-119. В определенных вариантах воплощения в изобретении предлагается полипептид, антитело или антиген-связывающий фрагмент, содержащие вариабельный домен тяжелой цепи, по меньшей мере на приблизительно 99% идентичный SEQ ID NOs:88-119.
[0018] В определенном варианте воплощения в изобретении предлагается гуманизированное антитело или его антиген-связывающий фрагмент, которые в клетках эукариотов экспрессируются по меньшей мере более чем в десять раз интенсивнее по сравнению с chMov19. В определенном варианте воплощения эукариотные клетки - клетки HEK-293Т.
[0019] В определенных вариантах воплощения в изобретении предлагается антитело или его антиген-связывающий фрагмент, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (a) CDR1 тяжелой цепи, содержащую SSYGMS (SEQ ID NO:30); CDR2 тяжелой цепи, содержащую TISSGGSYTY (SEQ ID NO:31); и/или CDR3 тяжелой цепи, содержащую DGEGGLYAMDY (SEQ ID NO:32); и/или (б) CDR1 легкой цепи, содержащую KASDHINNWLA (SEQ ID NO:27); CDR2 легкой цепи, содержащую GATSLET (SEQ ID NO:28); и CDR3 легкой цепи, содержащую QQYWSTPFT (SEQ ID NO:29). В другом варианте воплощения в изобретении предлагается антитело или его антиген-связывающий фрагмент, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (а) CDR1 тяжелой цепи, содержащую TNYWMQ (SEQ ID NO:60); CDR2 тяжелой цепи, содержащую AIYPGNGDSR (SEQ ID NO:61); и/или CDR3 тяжелой цепи, содержащую RDGNYAAY (SEQ ID NO:62); и/или (б) CDR1 легкой цепи, содержащую RASENIYSNLA (SEQ ID NO:57); CDR2 легкой цепи, содержащую AATNLAD (SEQ ID NO:58); и CDR3 легкой цепи, содержащую QHFWASPYT (SEQ ID NO:59). В ином варианте воплощения в изобретении предлагается антитело или его антиген-связывающий фрагмент, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (а) CDR1 тяжелой цепи, содержащую TNYWMY (SEQ ID NO:66); CDR2 тяжелой цепи, содержащую AIYPGNSDTT (SEQ ID NO:67); и/или CDR3 тяжелой цепи, содержащую RHDYGAMDY (SEQ ID NO:68); и/или (б) CDR1 легкой цепи, содержащую RASENIYTNLA (SEQ ID NO:63); CDR2 легкой цепи, содержащую TASNLAD (SEQ ID NO:64); и CDR3 легкой цепи, содержащую QHFWVSPYT (SEQ ID NO:65). В другом варианте воплощения в изобретении предлагается антитело или его антиген-связывающий фрагмент, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (а) CDR1 тяжелой цепи, содержащую SSFGMH (SEQ ID NO:72); CDR2 тяжелой цепи, содержащую YISSGSSTIS (SEQ ID NO:73); и/или CDR3 тяжелой цепи, содержащую EAYGSSMEY (SEQ ID NO:74); и/или (б) CDR1 легкой цепи, содержащую RASQNINNNLH (SEQ ID NO:69); CDR2 легкой цепи, содержащую YVSQSVS (SEQ ID NO:70); и CDR3 легкой цепи, содержащую QQSNSWPHYT (SEQ ID NO:71). В ином варианте воплощения в изобретении предлагаются антитело или его антиген-связывающий фрагмент, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (а) CDR1 тяжелой цепи, содержащую TSYTMH (SEQ ID NO:78); CDR2 тяжелой цепи, содержащую YINPISGYTN (SEQ ID NO:79); и/или CDR3 тяжелой цепи, содержащую GGAYGRKPMDY (SEQ ID NO:80); и/или (б) CDR1 легкой цепи, содержащую KASQNVGPNVA (SEQ ID NO:75); CDR2 легкой цепи, содержащую SASYRYS (SEQ ID NO:76); и CDR3 легкой цепи, содержащую QQYNSYPYT (SEQ ID NO:77).
[0020] В определенных вариантах воплощения полипептиды по изобретению являются полноразмерными антителом или антиген-связывающими фрагментами. В определенных вариантах воплощения антитела или антиген-связывающие фрагменты являются Fab, Fab’, F(ab’)2, Fd, одноцепочечным Fv или scFv, дисульфидно-связанным Fv, доменом V-NAR, IgNar, интрателом, IgGACH2, минителом, F(ab’)3, тетрателом, триателом, диателом, однодоменным антителом, DVD-Ig, Fcab, mAb2, (scFv)2 либо scFv-Fc.
[0021] В определенных вариантах воплощения антитело или полипептид по изобретению связываются с человеческим рецептором фолиевой кислоты 1 с Kd от приблизительно 1,0 до приблизительно 10 нМ. В одном варианте воплощения антитело или полипептид по изобретению связываются с человеческим рецептором фолиевой кислоты 1 с Kd приблизительно 1,0 нМ или лучше. В определенном варианте воплощения связывающую способность измеряют способом проточной цитометрии, Biacore или радиоиммунологическим анализом.
[0022] В изобретении также предлагается способ получения антитела по изобретению, заключающйся в культивировании клетки, экспрессирующей указанное антитело; и (б) выделении антитела из указанной культивированной клетки. В определенном варианте воплощения клетка является эукариотной клеткой. [0023] В изобретении также предлагается иммуноконъюгат с формулой (A)-(L)-(C), где: (А) - антитело, антиген-связывающий фрагмент или полипептид согласно изобретению, (L) - линкер, и (С) - цитотоксический агент, причем упомянутый линкер (L) соединяет (А) с (С).
[0024] В одном варианте воплощения линкер выбран из группы, состоящей из расщепляемого линкера, нерасщепляемого линкера, гидрофильного линкера и линкера, основывающегося на двухосновной карбоновой кислоте. В еще одном варианте воплощения линкер выбран из группы, состоящей из: N-сукцинимидил 4-(2-пиридилдитио)пентаноата (SPP) или N-сукцинимидил 4-(2-пиридилдитио)-2-сульфопентаноата (sulfo-SPP), N-сукцинимидил 4-(2-пиридилдитио)бутаноата (SPDB) или N-сукцинимидил 4-(2-пиридилдитио)-2-сульфобутаноата (sulfo-SPDB), N-сукцинимидил 4-(малеимидометил) циклогексанкарбоксилата (SMCC), N-сульфосукцинимидил 4-(малеимидометил) циклогексанкарбоксилата (sulfoSMCC), N-сукцинимидил-4-(иодацетил)-аминобензоата (SIAB) и N-сукцинимидил-[(N-малеимидопропионамидо)-тетраэтиленгликолевого] эфира (NHS-PEG4-малеимида). В определенном варианте воплощения линкер представляет собой N-сукцинимидил-[(N-малеимидопропионамидо)-тетраэтиленгликолевым] эфир (NHS-PEG4-малеимид).
[0025] В одном варианте воплощения иммунокнъюгаты содержат цитотоксический агент, который выбран из группы, состоящей из майтансиниода, аналога майтансиноида, бензодиазепина, таксоида, СС-1065, аналога СС-1065, дуокармицина, аналога дуокармицина, калихеамицина, доластатина, аналога доластатина, ауристатина, производного томаимицина и производного лептомицина либо пролекарственной формы агента. В еще одном варианте воплощения цитотоксический агент является майтансиноидом. В ином варианте воплощения цитотоксический агент может быть N(2’)-деацетил-N(2’)-(3-меркапто-1-оксопропил)-майтансином или N(2’)-деацетил-N2-(4-меркапто-4-метил-1-оксопентил)-майтансином.
[0026] В одном варианте воплощения в изобретении предлагается иммуноконъюгат, содержащий: (А) гуманизированное антитело, содержащее вариабельный домен тяжелой цепи с последовательностью SEQ ID NO:4 и вариабельный домен легкой цепи с последовательностью SEQ ID NO:10 или SEQ ID NO:11; (L) N-сукцинимидил-[(N-малеимидопропионамидо)-тетраэтиленгликолевый] эфир (NHS-PEG4-малеимида); и (С) N(2’)-деацетил-N2-(4-меркапто-4-метил-1-оксопентил)-майтансин; где (L) связывает (А) и (С).
[0027] В одном варианте воплощения в изобретении предлагается иммуноконъюгат, содержащий: (А) гуманизированное антитело, содержащее вариабельный домен тяжелой цепи с последовательностью SEQ ID NO:4 и вариабельный домен легкой цепи с последовательностью SEQ ID NO:10 или SEQ ID NO:11; (L) N-сукцинимидил 4-(2-пиридилдитио)бутаноат (SPDB); и (С) N(2’)-деацетил-N2-(4-меркапто-4-метил-1-оксопентил)-майтансин; где (L) связывает (А) и (С).
[0028] В одном варианте воплощения в изобретении предлагается иммуноконъюгат, содержащий: (А) гуманизированное антитело, содержащее вариабельный домен тяжелой цепи с последовательностью SEQ ID NO:4 и вариабельный домен легкой цепи с последовательностью SEQ ID NO:10 или SEQ ID NO:11; (L) N-сукцинимидил 4-(2-пиридилдитио)2-сульфобутаноат (sulfo-SPDB); и (С) N(2’)-деацетил-N2-(4-меркапто-4-метил-1-оксопентил)-майтансин; где (L) связывает (А) и (С).
[0029] В одном варианте воплощения в изобретении предлагается иммуноконъюгат, содержащий: (А) гуманизированное антитело, содержащее вариабельный домен тяжелой цепи с последовательностью SEQ ID NO:4 и вариабельный домен легкой цепи с последовательностью SEQ ID NO:10 или SEQ ID NO:11; (L) N-сукцинимидил 4-(2-пиридилдитио)-2-сульфопентаноат (sulfo-SPP); и (С) N(2’)-деацетил-N(2’)-(3-меркапто-1-оксопропил)-майтансин; где (L) связывает (А) и (С).
[0030] В одном варианте воплощения в изобретении предлагается иммуноконъюгат, содержащий: (А) гуманизированное антитело, содержащее вариабельный домен тяжелой цепи с последовательностью SEQ ID NO:4 и вариабельный домен легкой цепи с последовательностью SEQ ID NO:10 или SEQ ID NO:11; (L) N-сукцинимидил 4-(2-пиридилдитио)пентаноат (SPP); и (С) N(2’)-деацетил-N(2’)-(3-меркапто-1-оксопропил)-майтансин; где (L) связывает (А) и (С).
[0031] В изобретении также предлагается фармацевтическая композиция, содержащая антитело, антиген-связывающий фрагмент, полипептид или иммуноконъюгат, согласно изобретению, и фармацевтически приемлемый носитель. В определенном варианте воплощения фармацевтическая композиция, помимо этого, содержит второй противоопухолевый агент.
[0032] В изобретении также предлагается диагностический реактив, содержащий меченые антитело, антиген-связывающий фрагмент, полипептид или иммуноконъюгат согласно изобретению. В одном варианте воплощения метка выбрана из группы, состоящей из радиометки, флуорофора, хромофора, визуализирующего средства и иона металла.
[0033] В изобретении также предлагается набор, содержащий антитело, антиген-связывающий фрагмент, полипептид или иммуноконъюгат согласно изобретению.
[0034] В изобретении также предлагается способ ингибирования роста опухоли у субъекта, включающий введение субъекту терапевтически эффективного количества антитела, антиген-связывающего фрагмента, полипептида, иммуноконъюгата или фармацевтической композиции согласно изобретению. В определенном варианте воплощения в изобретении предлагается способ ингибирования роста опухоли у субъекта, включающий введение субъекту терапевтически эффективного количества иммуноконъюгата с формулой (A)-(L)-(C), где: (А) - антитело или антиген-связывающий фрагмент, которые специфически связываются с человеческим рецептором фолиевой кислоты 1; (L) - линкер; и (С) - цитотоксин, выбранный из группы, состоящей из майтансиноида и аналога майтансиноида; причем линкер (L) соединяет (А) с (С), а иммуноконъюгат уменьшает средний объем опухоли на модели ксенотрансплантата KB по меньшей мере в два раза. В определенном варианте воплощения способ включает введение антитела или его антиген-связывающего фрагмента, содержащих (a) CDR1 тяжелой цепи, содержащую GYFMN (SEQ ID NO:1); CDR2 тяжелой цепи, содержащую RIHPYDGDTFYNQXaa1FXaa2Xaa3 (SEQ ID NO:56); и CDR3 тяжелой цепи, содержащую YDGSRAMDY (SEQ ID NO:3); и (6) CDR1 легкой цепи, содержащую KASQSVSFAGTSLMH (SEQ ID NO:7); CDR2 легкой цепи, содержащую RASNLEA (SEQ ID NO:8); CDR3 легкой цепи, содержащую QQSREYPYT (SEQ ID NO:9); где Xaa1 выбран из K, Q, Н и R; Хаа2 выбран из Q, Н, N и R; и Хаа3 выбран из G, Е, Т, S, А и V. В еще одном варианте воплощения антитело содержит последовательность CDR2 тяжелой цепи, содержащую RIHPYDGDTFYNQKFQG (SEQ ID NO:2).
[0035] В определенном варианте воплощения в изобретении предлагается способ ингибирования роста опухоли, содержащий введение антитела или его антиген-связывающего фрагмента, кодированного плазмидной ДНК, депонированной в АТСС 7 апреля 2010 под номерами депонентов АТСС РТА-10772 и РТА-10773 или 10774.
[0036] В ином варианте воплощения в способе предлагается введение иммуноконъюгата, содержащего гуманизированное антитело, которое содержит вариабельный домен тяжелой цепи с последовательностью SEQ ID NO:4 и вариабельный домен легкой цепи с последовательностью SEQ ID NO:10 или SEQ ID NO:11; (L) N-сукцинимидил-[(N-малеимидопропионамидо)-тетраэтиленгликолевый] эфир (NHS-PEG4-малеимида); и (С) N(2’)-деацетил-N2-(4-меркапто-4-метил-1-оксопентил)-майтансин.
[0037] В ином варианте воплощения в способе предлагается введение иммуноконъюгата, содержащего (А) гуманизированное антитело, которое содержит вариабельный домен тяжелой цепи с последовательностью SEQ ID NO:4 и вариабельный домен легкой цепи с последовательностью SEQ ID NO:10 или SEQ ID NO:11; (L) N-сукцинимидил 4-(2-пиридилдитио)бутаноат (SPDB); и (С) N(2’)-деацетил-N2-(4-меркапто-4-метил-1-оксопентил)-майтансин; где (L) связывает (А) и (С).
[0038] В ином варианте воплощения в способе предлагается введение иммуноконъюгата, содержащего (А) гуманизированное антитело, которое содержит вариабельный домен тяжелой цепи с последовательностью SEQ ID NO:4 и вариабельный домен легкой цепи с последовательностью SEQ ID NO:10 или SEQ ID NO:11; (L) N-сукцинимидил 4-(2-пиридилдитио)2-сульфобутаноат (sulfo-SPDB); и (С) N-(2’)-деацетил-N2-(4-меркапто-4-метил-1-оксопентил)-майтансин; где (L) связывает (А) и (С).
[0039] В ином варианте воплощения в способе предлагается введение иммуноконъюгата, содержащего (А) гуманизированное антитело, которое содержит вариабельный домен тяжелой цепи с последовательностью SEQ ID NO:4 и вариабельный домен легкой цепи с последовательностью SEQ ID NO:10 или SEQ ID NO:11; (L) N-сукцинимидил 4-(2-пиридилдитио)-2-сульфопентаноат (sulfo-SPP); и (С) N(2’)-деацетил-N(2’)-(3-меркапто-1-оксопропил)-майтансин; где (L) связывает (А) и (С).
[0040] В ином варианте воплощения в способе предлагается введение иммуноконъюгата, содержащего (А) гуманизированное антитело, которое содержит вариабельный домен тяжелой цепи с последовательностью SEQ ID NO:4 и вариабельный домен легкой цепи с последовательностью SEQ ID NO:10 или SEQ ID NO:11; (L) N-сукцинимидил 4-(2-пиридилдитио)пентаноат (SPP); и (С) N(2’)-деацетил-N(2’)-(3-меркапто-1-оксопропил)-майтансин; где (L) связывает (А) и (С).
[0041] В другом варианте воплощения способ включает введение иммуноконъюгата, содержащего антитело huFR-1-21, депонированное в АТСС 7 апреля 2010 под номерами депонентов АТСС РТА-10775 и РТА-10776. В определенном варианте воплощения антитело huFR-1-21 включает (a) CDR1 тяжелой цепи, содержащую SSYGMS (SEQ ID NO:30); CDR2 тяжелой цепи, содержащую TISSGGSYTY (SEQ ID NO:31); и CDR3 тяжелой цепи, содержащую DGEGGLYAMDY (SEQ ID NO:32); и (б) CDR1 легкой цепи, содержащую KASDHINNWLA (SEQ ID NO:27); CDR2 легкой цепи, содержащую GATSLET (SEQ ID NO:28); и CDR3 легкой цепи, содержащую QQYWSTPFT (SEQ ID NO:29). В определенных вариантах воплощения способ включает введение иммуноконъюгата, содержащего антитело, являющееся антителом huFR1-48, которое содержит: (а) CDR1 тяжелой цепи, содержащую TNYWMQ (SEQ ID NO:60); CDR2 тяжелой цепи, содержащую AIYPGNGDSR (SEQ ID NO:61); и CDR3 тяжелой цепи, содержащую RDGNYAAY (SEQ ID NO:62); и (б) CDR1 легкой цепи, содержащую RASENIYSNLA (SEQ ID NO:57); CDR2 легкой цепи, содержащую AATNLAD (SEQ ID NO:58); и CDR3 легкой цепи, содержащую QHFWASPYT (SEQ ID NO:59). В определенных вариантах воплощения способ включает введение иммуноконъюгата, содержащего антитело, являющееся антителом huFR1-49, которое содержит: (а) CDR1 тяжелой цепи, содержащую TNYWMY (SEQ ID NO:66); CDR2 тяжелой цепи, содержащую AIYPGNSDTT (SEQ ID NO:67); и CDR3 тяжелой цепи, содержащую RHDYGAMDY (SEQ ID NO:68); и (б) CDR1 легкой цепи, содержащую RASENIYTNLA (SEQ ID NO:63); CDR2 легкой цепи, содержащую TASNLAD (SEQ ID NO:64); и CDR3 легкой цепи, содержащую QHFWVSPYT (SEQ ID NO:65). В определенных вариантах воплощения способ включает введение иммуноконъюгата, содержащего антитело, являющееся антителом huFR1-57, которое содержит: (а) CDR1 тяжелой цепи, содержащую SSFGMH (SEQ ID NO:72); CDR2 тяжелой цепи, содержащую YISSGSSTIS (SEQ ID NO:73); и CDR3 тяжелой цепи, содержащую EAYGSSMEY (SEQ ID NO:74); и (б) CDR1 легкой цепи, содержащую RASQNINNNLH (SEQ ID NO:69); CDR2 легкой цепи, содержащую YVSQSVS (SEQ ID NO:70); и CDR3 легкой цепи, содержащую QQSNSWPHYT (SEQ ID NO:71). В определенных вариантах воплощения способ включает введение иммуноконъюгата, содержащего антитело, являющееся антителом huFR1-65, которое содержит: (a) CDR1 тяжелой цепи, содержащую TSYTMH (SEQ ID NO:78); CDR2 тяжелой цепи, содержащую YINPISGYTN (SEQ ID NO:79); и CDR3 тяжелой цепи, содержащую GGAYGRKPMDY (SEQ ID NO:80); и (б) CDR1 легкой цепи, содержащую KASQNVGPNVA (SEQ ID NO:75); CDR2 легкой цепи, содержащую SASYRYS (SEQ ID NO:76); и CDR3 легкой цепи, содержащую QQYNSYPYT (SEQ ID N0:77).
[0042] В одном варианте воплощения способ ингибирует рост опухоли яичника, опухоли головного мозга, опухоли молочной железы, опухоли матки, опухоли эндометрия, опухоли поджелудочной железы, опухоли почки или опухоли легкого. В определенном варианте воплощения способ ингибирует рост опухоли яичника. В ином варианте воплощения, согласно изобретению, происходит ингибирование роста опухоли легкого. В определенном варианте воплощения ингибирование роста опухоли используется для лечения онкологического заболевания. В еще одном варианте воплощения способ содержит введение второго противоопухолевого препарата субъекту. В определенном варианте воплощения второй противоопухолевый агент является химиотерапевтическим агентом.
[0043] В изобретении также предлагается изолированная клетка, продуцирующая антитело, антиген-связывающий фрагмент или полипептид согласно изобретению.
[0044] В изобретении также предлагается изолированный полинуклеотид, содержащий последовательность, по меньшей мере на 90% идентичную последовательности, выбранной из группы, состоящей из SEQ ID NOs:5, 14, 15, 37, 38, 43, 44, 47, 48 и 120-127. В определенном варианте воплощения изолированный полинуклеотид по меньшей мере на 95% идентичен последовательности, выбранной из группы, состоящей из SEQ ID NOs:5, 14, 15, 37, 38, 43, 44, 47, 48 и 120-127. В ином варианте воплощения изолированный полинуклеотид по меньшей мере на 99% идентичен последовательности, выбранной из группы, состоящей из SEQ ID NOs:5, 14, 15, 37, 38, 43, 44, 47, 48 и 120-127. В изобретении также предлагается вектор, содержащий любой полинуклеотид с SEQ ID NOs:5, 14, 15, 37, 38, 43, 44, 47, 48 и 120-127. В ином варианте воплощения в изобретении предлагается клетка-хозяин, содержащая вектор, включающий полинуклеотид с SEQ ID NOs:5, 14, 15, 37, 38, 43, 44, 47, 48 и 120-127.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0045] Фигура 1. Поверхностные остатки мышиного (muMov19) и гуманизированного (huMov19) Mov19. (А) Поверхностные остатки легкой цепи мышиного и гуманизированного Mov19. Представлены поверхностные вариабельные остатки каркасной области легких цепей мышиного и гуманизированного Mov19, и номер позиции (система Kabat). Человеческие остатки, которые отличаются от оригинальных мышиных последовательностей подчеркнуты. *Положение 74 не является поверхностным положением, но для того, чтобы избавиться от консенсусного N-связанного сайта гликозилирования в версии 1.00, это положение было заменено на Треонин (самый частый человеческий остаток в этом положении), в результате чего была получена версия 1.60. (В) Поверхностные остатки тяжелых цепей мышиного и человеческого Mov19. Представлены поверхностные вариабельные остатки тяжелых цепей каркасной области мышиного и гуманизированного Mov19 и номер позиции (система Kabat). Человеческие остатки, отличающиеся от исходных мышиных последовательностей, подчеркнуты. Аналогичные поверхностные остатки представлены для FR1-21 (С) и (D).
[0046] Фигура 2. Выравнивание вариабельных доменов тяжелой и легкой цепей химерного Mov19 и huMov19 и вариабельных доменов тяжелой и легкой цепей muFRl-21 и huFRl-21. Выравнивание перестроенных последовательностей вариабельных областей Mov19 и Frl-21 с их мышиными эквивалентами. А) и С) вариабельные домены легкой цепи; В) и D) вариабельный домен тяжелой цепи. Черточками «-» показаны идентичные с мышиной последовательностью остатки. Определяющие комплементарность области (определение Kabat) подчеркнуты.
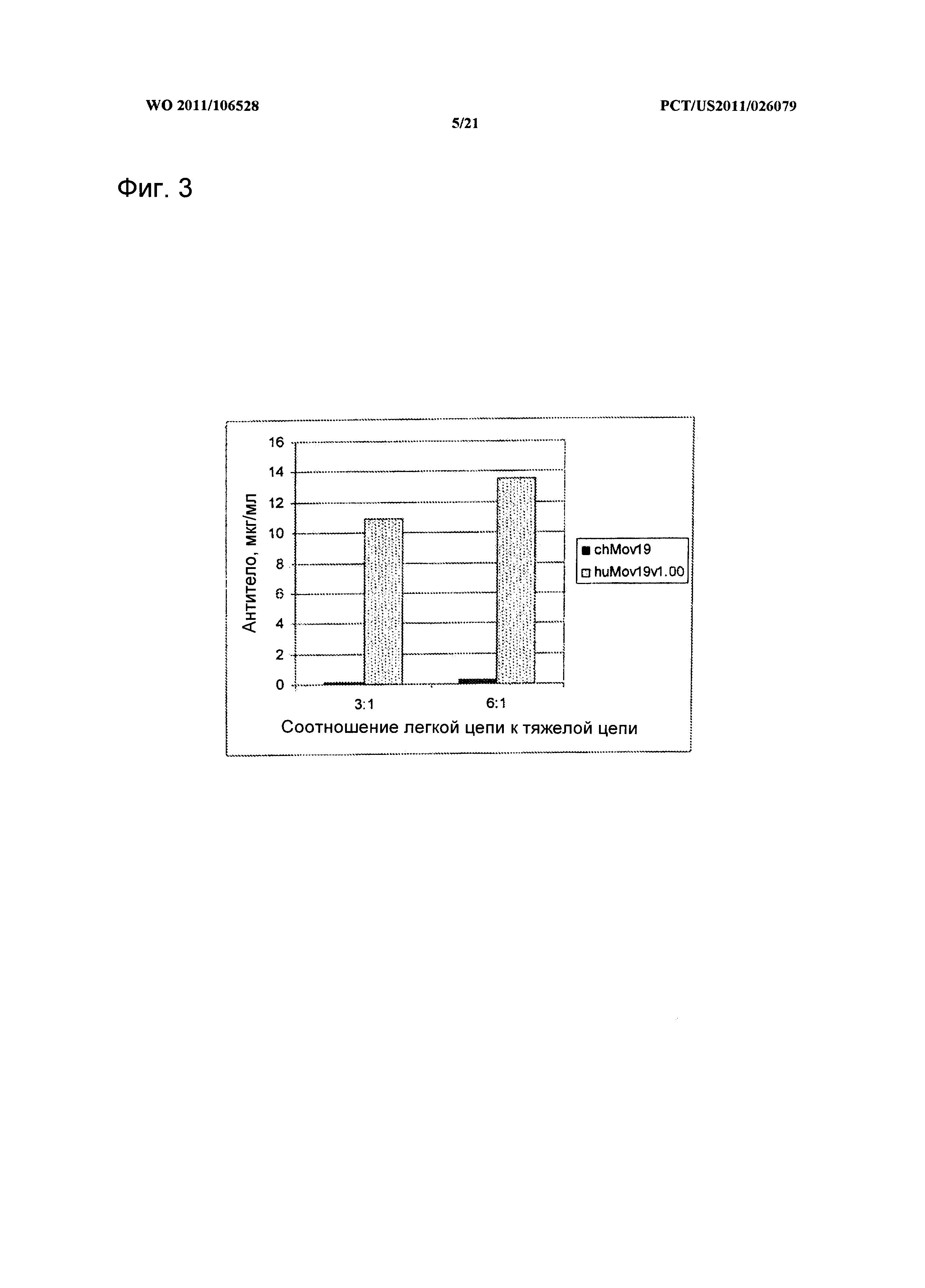
[0047] Фигура 3. Экспрессия химерного Mov199 и huMov19 в клетках НЕК. Плазмиды экспрессии химерного и человеческого Mov19 были транзиентно трансфицированы в суспензию клеток НЕК293-Т, собраны спустя 7 дней, экспрессированное антитело было определено способом количественного ИФА. Плазмиды легкой цепи и тяжелой цепи были трансфицированы в соотношении либо 3:1, либо 6:1, соответственно.
[0048] Фигура 4. Специфичность связывания антител против FOLR1, определенная по их связыванию с FOLR1-экспрессирующим клетками 300-19. Связывание huMov19 с клетками 300-19-FOLR1 согласно проточной цитометрии. Родительские клетки 300-19, экспрессирующие FOLR-1. Сплошная серая заливка показывает клеточную собственную флуоресценцию; черные пунктирные линии показывают клетки, инкубированные с вторичным анти-человеческим антителом, конъюгированным с FITC; черные сплошные линии показывают клетки, инкубированные с антителом huMov-19 и вторичным античеловеческим антителом, конъюгированным с FITC.
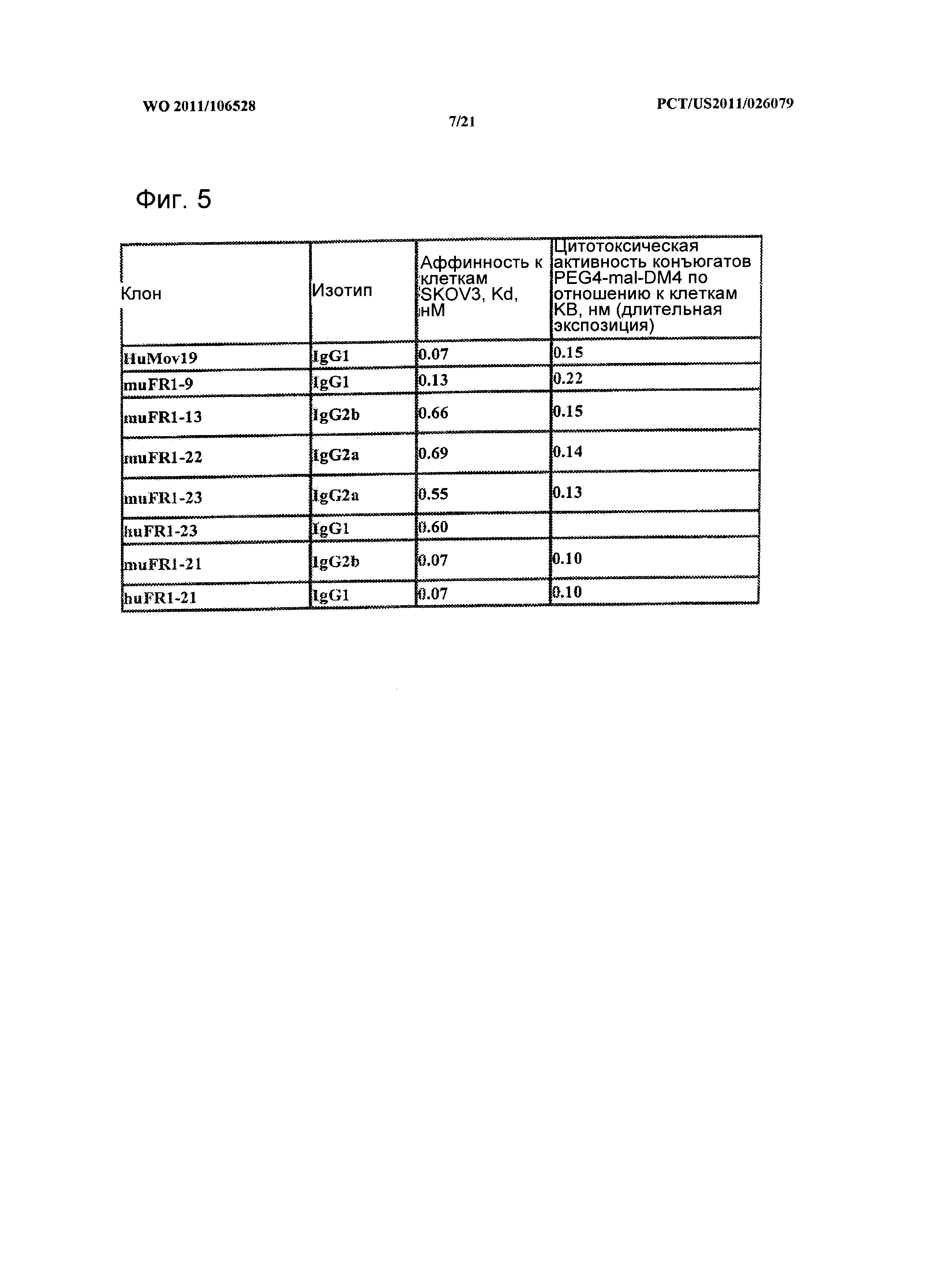
[0049] Фигура 5. Связывающая способность и цитотоксическая активность in vitro антител против FOLR1 и иммуноконъюгатов. Связывающая способность huMov19 и различных мышиных и гуманизированных антител FR-1 была определена на клетках SKOV3. Также измерялась цитотоксическая активность in vitro конъюгатов PEG4-Mal-DM4 с перечисленными антителами.
[0050] Фигура 6. Антитело-зависимая клеточная цитотоксичность иммуноконъюгатов. АЗКЦ-активность huMov19, huFR1-21 и Mor003 определялась на клетках Igrov1. Igrov 1 были инкубированы при 15000 клеток/лунку с соотношением клеток- мишеней:НК-клеток 1:4.
[0051] Фигура 7. Цитотоксическая активность при продолжительном экспонировании huFR1-21-PEG4-mal-DM4 и huMov19-PEG4-mal-DM4 на клетки КВ. Избыток неконъюгированных антител подавлял активность иммуноконъюгатов при их совместном инкубировании в присутствии клеток KB, что свидетельствует о антиген-зависимом характере цитотоксической активности.
[0052] Фигура 8. Эффективность in vivo конъюгатов, нацеленных на huMov19 в модели ксенотрансплантата КВ. На установленной ксенотрансплантатной модели клеток KB, имплантированных подкожно мышам с ТКИН, были протестированы FOLR1-нацеленный расщепляемый конъюгат huMov19-SPDB-DM4 (В) в сравнении с ненацеленным на FOLR1 huC242-SPDB-DM4 (D), а также нерасщепляемый конъюгат huMov19-PEG4-Mal-DM4 (С) в сравнении с ненацеленным huC242-PEG4Mal-DM4 (Е). Нацеливание FOLR1 нa huMov19 приводило к существенному уменьшение среднего объема опухоли.
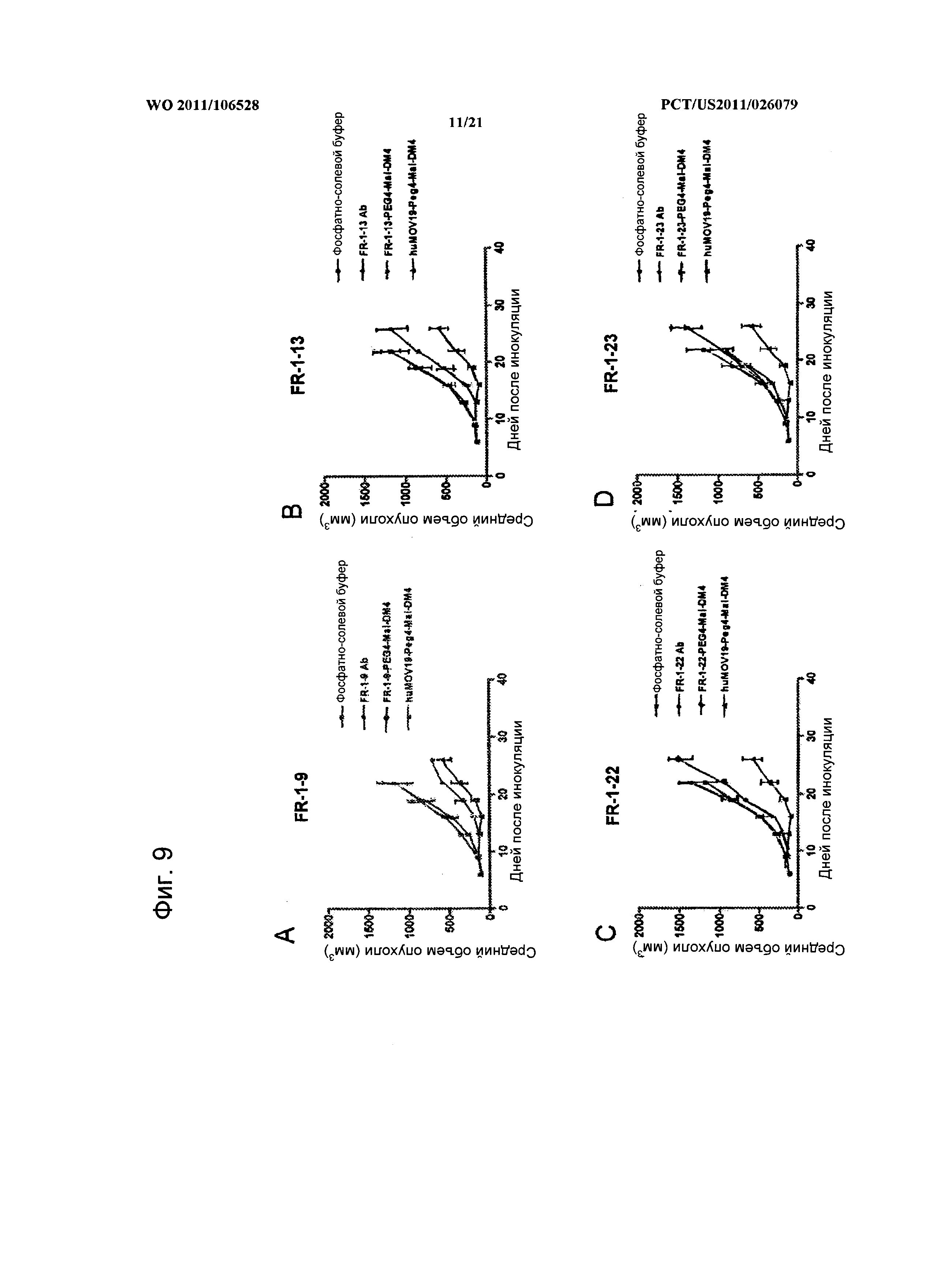
[0053] Фигура 9. Эффективность in vivo huMov19-PEG4-Mal-DM4 в сравнении с мышиными антителами против FOLR1 FR-1 в модели ксенотрансплантата КВ. Серия антител FR-1, как неконъюгированных, так и конъюгированных с PEG4-Mal-DM4, была протестирована на способность понижать средний объем опухоли в сравнении с huMov19-PEG4-Mal-DM4 в модели ксенотрансплантатной опухоли КВ. (A) FR-1-9, (В) FR-1-13, (С) FR-1-22 и (D)FR-1-23.
[0054] Фигура 10. Эффективность in vivo конъюгатов huMov19-PEG4-Mal-DM4 и huFR1-21-PEG4-Mal-DM4 в модели ксенотрансплантата КВ. На 6 день после инокуляции проводились однократные инъекции по 10 мг/кг huMov19-PEG4-Mal-DM4 и huFR1-21-PEG4-Mal-DM4. И huMov19-PEG4-Mal-DM4, и huFR1-21-PEG4-Mal-DM4 приводили к существенному уменьшению среднего объема опухоли. «Средний ОО»обозначает средний объем опухоли.
[0055] Фигура 11. HuMov19-PEG4-mal-DM4 проявляет дозозависимую активность в модели ксенотрансплантата КВ. Дозозависимая активность иммуноконъюгата оценивалась для интервала проверенных доз. При введении раз в неделю наблюдалось повышение противоопухолевой активности. Высокие нагрузки препарата лишь немного повышали активность в группах дозирования 10 мг/кг, в группах меньших дозировок антивность снижалась. 3,7 DAR обозначает 3,7 молекул препарата на антитело.
[0056] Фигура 12. Эффективность in vivo huMov19, конъюгированного с DM1 и DM4 через различные линкеры. huMov19 было конъюгировано с SMCC-DM1 при 3,9 молекул препарата на антитело; sulfo-mal-DM4 - при 3,7 молекул препарата на антитело (В), a sulfo-mal-DM4 - при 8,23 молекул препарата на антитело (С), затем была исследована их способность понижать средний объем опухоли при различных концентрациях в сравнении с huMov19-PEG4-mal-DM4.
[0057] Фигура 13. Эффективность in vivo huMov19, конъюгированного с DM1 и DM4 через различные линкеры. huMov19 было конъюгировано с SPP-DM1 при 4,3 молекул препарата на антитело; sulfo-SPDB-DM4 - при 3,8 молекул препарата на антитело, a SPDB-DM4 - при 3,8 молекул препарата на антитело, и с sulfo-SPDB-DM4 - при 6,8 молекул препарата на антитело; затем была исследоавана их способность понижать средний объем опухоли. Мыши получали по 5 мг/кг (А) и 2,5 мг/кг (В) одного из конъюгатов, приведенных выше, либо только фосфатно-солевой буфер.
[0058] Фигура 14. Эффективность in vivo huMov19-sulfo-SPDB-DM4 в модели ксенотрансплантатной опухоли OVCAR-3. Мыши получали по 25, 50 или 100 мкг/кг huMov19-sulfo-SPDB-DM4 либо только фосфатно-солевой буфер.
[0059] Фигура 15. Эффективность in vivo huMov19-sulfo-SPDB-DM4 в модели ксенотрансплантатной опухоли IGROV-1. Мыши получали по 25, 50 или 100 мкг/кг huMov19-sulfo-SPDB-DM4 либо только фосфатно-солевой буфер.
[0060] Фигура 16. Эффективность in vivo huMov19-sulfo-SPDB-DM4 в модели ксенотрансплантатной опухоли OV-90. Мыши получали по 25, 50 или 100 мкг/кг huMov19-sulfo-SPDB-DM4 либо только фосфатно-солевой буфер.
[0061] Фигура 17. Воздействие расщепляемых и нерасшепляемых линкеров на эффективность иммуноконъгатов в ксенотрансплантатных моделях КВ.
[0062] Фигура 18. Воздействие расщепляемых линкеров на эффективность иммуноконъгатов в (А) ксенотрансплантатной модели KB, (В) ксенотрансплантатной модели OVCAR-3.
[0063] Фигура 19. Эффективность in vitro и in vivo huFR1-48, huFR1-49, huFR1-57 и huFR1-65-SMCC-DM1 в ксенотрансплантатных моделях опухоли КВ. Мыши получали 200 мкг/кг однократно.
ДЕТАЛЬНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0064] В настоящем изобретении предлагаются новые агенты, включая такие полипептиды как антитела и иммуноглобулины, которые соединяются с человеческим рецептором фолиевой кислоты 1 (FOLR1), не ограничиваясь перечисленным. Также предлагаются родственные полипептиды и полинуклеотиды, композиции, содержащие FOLR1-связывающие агенты, и способы получения FOLR1-связывающих агентов. Помимо этого, предлагаются способы использования новых FOLR1-связывающих агентов, такие как способы ингибирования опухолевого роста и/или лечения онкологического заболевания.
I. Определения
[0065] Для облегчения понимания настоящего изобретения ниже даны определения ряда терминов и оборотов.
[0066] Термины «человеческий рецептор фолиевой кислоты I» или «FOLR1» при использовании здесь относятся к любому нативному человеческому FOLR1, если не указано иное. Термин «FOLR1» охватывает «полноразмерный» непроцессированный FOLR1, а также любую форму FOLR1, получающуюся при процессинге в клетке. Термин также охватывает природные варианты FOLR1, например, сплайс-варианты, аллельные варианты и изоформы. Полипептиды FOLR1, описанные здесь, могут быть выделены из множества источников, например, из человеческих тканей или из иных источников, либо быть получены рекомбинантными или синтетическими способами. Примерами последовательностей FOLR1 служат, не ограничиваясь перечисленным, идентификационные номера NCBI P15328, NP_001092242.1, ААХ29268.1, ААХ37119.1, NP_057937.1 HNP_057936.1.
[0067] Термин «антитело» обозначает молекулу иммуноглобулина, которая распознает и специфически связывается с мишенью, например, белком, полипептидом, пептидом, углеводом, полинуклеотидом, липидом или комбинацией перечисленного, через по меньшей мере один сайт распознавания антигена в вариабельнойобласти молекулы иммуноглобулина. При использовании здесь термин «антитело» охватывает неизмененные поликлональные антитела, неизмененные моноклональные антитела, фрагменты антител (например, фрагменты Fab, Fab’, F(ab’)2 и Fv), одноцепочечные мутанты Fv (scFv), мультиспецифические антитела, например, биспецифические антитела, полученные по меньшей мере из двух неизмененных антител, химерные антитела, гуманизированные антитела, человеческие антитела, слитые белки, содержащие антиген-определяющую часть антитела, и иные модифицированные молекулы иммуноглобулинов, содержащие антигенраспознающий сайт, при условии проявления антителами желаемой биологической активности. Антитело может принадлежать к одному из пяти основных классов иммуноглобулинов: IgA, IgD, IgE, IgG и IgM либо их подклассов (изотипов) (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2), в зависимости от типа константных доменов тяжелой цепи, называемых альфа, дельта, эпсилон, гамма и мю, соответственно. Различные классы иммуноглобулинов обладают различными и хорошо известными структурами субъединиц и трехмерными конфигурациями. Антитела могут быть свободными либо конъюгированными с иными молекулами, например, токсинами, радиоизотопами и т.д.
[0068] «Блокирующее» антитело или «антитело-антагонист» - антитело, которое ингибирует или уменьшает биологическую активность антигена, который оно связывает, например, FOLR1. В некоторых вариантах воплощения блокирующие антитела или антитела-антагонисты частично или полностью ингибируют биологическую активность антигена. Желательно, чтобы биологическая активность была уменьшена на 10%, 20%, 30%, 50%, 70%, 80%, 90%, 95% или даже 100%.
[0069] Термины «антитело против FOLR1» или «антитело, которое связывается с FOLR1» относятся к антителу, которое способно связывать FOLR1 с аффинностью, достаточной для использования антитела в диагностических или терапевтических целях по отношению к FOLR1. Излишнее связывание антитела против FOLR1 с несоответствующим белком, не являющимся FOLR1, составляет менее чем приблизительно 10% от связывания антитела с FOLR1 по данным, например, радиоиммунологического анализа (РИА). В определенных вариантах воплощения антитело, которое связывается с FOLR1, обладает константой диссоциации (Kd)≤1 мкМ, ≤100 нМ, ≤10 нМ, ≤1 нМ либо ≤0,1 нМ.
[0070] Термин «фрагмент антитела» относится к части неизмененного антитела и относится к антиген-определяющим вариабельным областяминтактного антитела. Примерами фрагментов антител служат, не ограничиваясь перечисленным, фрагменты Fab, Fab’, F(ab’)2 и Fv, линейные антитела, одноцепочечные антитела, мультиспецифические антитела, образованные из фрагментов антител.
[0071] «Моноклональное антитело» относится к гомогенной популяции антител, вовлеченной в высокоспецифическое распознавание и связывание одной антигенной детерминанты - эпитопа. Этим они отличаются от поликлональных антител, которые обычно включают различные антитела, направленные против разных антигенных детерминант. Термин «моноклональное антитело» охватывает неизмененные полноразмерные антитела, а также фрагменты антител (например, фрагменты Fab, Fab’, F(ab’)2 и Fv), одноцепочечные мутанты (scFv), слитые белки, содержащие часть антитела и иные модифицированные молекулы иммуноглобулинов, содержащие антиген-распознающий сайт. Кроме того, «моноклональное антитело» относится к таким антителам, изготовленным любым количеством способов, включая, но не ограничиваясь перечисленным, использование гибридом, фаговой селекции, рекомбинантной экспрессии и трансгенных животных.
[0072] Термин «гуманизированное антитело» относится к формам нечеловеческих (например, мышиных) антител, являющихся специфическими иммуноглобулиновыми цепями, химерными иммуноглобулинами или их фрагментами, содержащими минимальные нечеловеческие (например, мышиные) последовательности. Как правило, гуманизированные антитела являются человеческими иммуноглобулинами, у которых остатки из определяющей комплементарность области (CDR) заменены на остатки CDR нечеловеческого вида (например, мыши, крысы, кролика, хомячка), обладающие желательными специфичностью, аффинностью, способностью (Jones et al., 1986, Nature, 321:522-525; Riechmann et al., 1988, Nature, 332:323-327; Verhoeyen et al., 1988, Science, 239:1534-1536). В некоторых случаях остатки Fv-каркаснойобласти (FR) человеческого иммуноглобулина заменены на соответствующие остатки антитела нечеловеческого вида, обладающие желательной специфичностью, аффинностью и способностью. Гуманизированное антитело может быть далее модифицировано замещением дополнительных остатков в Fv-каркаснойобласти и/или в заменяемых нечеловеческих остатках для улучшения и оптимизации специфичности, аффинности и/или способности антитела. В общем гуманизированное антитело содержит все из по меньшей мере одного, а как правило - двух или трех вариабельных доменов, содержащих все или практически все CDR-области, которые соответствуют нечеловеческому иммуноглобулину, в которых практически все из FR-областей происходят от человеческой консенсусной последовательности иммуноглобулина. Гуманизированное антитело также может содержать по меньшей мере часть константнойобласти или домена иммуноглобулина (Fc), как правило, человеческого иммуноглобулина. Примеры и способы получения гуманизированных антител описаны в патентах США 5225539 или 5639641.
[0073] «Вариабельнаяобласть» антитела относится к вариабельнойобласти легкой цепи антитела или вариабельнойобласти тяжелой цепи, по отдельности или в комбинации. Вариабельные области тяжелой и легкой цепей состоят из четырех каркасных областей (FR), соединенных тремя областями, определяющими комплементарность (CDR), также известных как гипервариабельные области. Области, определяющие комплементарность, в каждой цепи держатся близко с каркасными областями и с областями, опеределяющими комплементарность, другой цепи, образуя антигенсвязывающий сайт антитела Известно по меньшей мере две техники определения CDR: (1) подход, основанный на перекрестно-видовой вариабельности последовательностей (например, Kabat et al., Sequences of Proteins of Immunological Interest, (5th ed., 1991, National Institutes of Health, Bethesda Md.)); и (2) подход, основанный на кристаллографическом исследовании комплексов антиген-антитело (Al-lazikani et al., (1997) J. Molec. Biol. 273:927-948)). Помимо этого, для определения CDR в данной области техники иногда применяются эти подходы в комбинации.
[0074] Система нумерации Kabat, как правило, используется для обозначения остатка в вариабельном домене (приблизительно остатки 1-107 легкой цепи и остатки 1-113 тяжелой цепи) (например, Kabat et al., Sequences of Immunological Interest. 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md. (1991)). [0075] Нумерация позиций аминокислот Kabat относится к системе нумерации, использующейся для вариабельных доменов тяжелой цепи или вариабельных доменов легкой цепи в обзоре антител Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Вифезда, Мэриленд. (1991). При использовании этой системы нумерации актуальная линейная аминокислотная последовательность может содержать меньшее количество аминокислот или дополнительные аминокислоты, что соответствует укорачиванию или внедрению в FR или CDR вариабельного домена. К примеру, вариабельный домен тяжелой цепи может содержать вставку одной аминокислоты (остаток 52а согласно Kabat) после остатка 52 Н2 и внедренные остатки (например, остатки 82а, 82b и 82 с, и т.д., согласно Kabat) после 82 остатка FR. Нумерация остатков Kabat может быть определена для заданного антитела путем выравнивания последовательности в гомологических участках с антителом со «стандартной» нумерацией последовательности Kabat. Система Chothia использует вместо этого расположение структурных петель (Chothia, Lesk J. Mol. Biol. 196:901-917 (1987)). Конец петли Chothia CDR-H1 по нумерации Kabat соответствует Н32-Н34, в зависимости от длины петли (потому что в системе нумерации Kabat вставки располагаются между Н35А и Н35 В; если 35А и 35 В отсутствуют, петля кончается на 32; если присутствует только 35А, петля кончается на 33; если присутствуют и 35А, и 35 В, петля кончается на 34). Гипервариабельные области АЬМ представляют компромисс между CDR Kabat и структурными петлями Chothia и используются ПО моделирования антител Oxford Molecular’s AbM.
[0076] Термин «человеческое антитело» обозначает антитело, продуцируемое человеком, или антитело с аминокислотной последовательностью, соответствующей антителу, продуцируемому человеком, изготовленному по любой технике, известной в данной области техники. Это определение человеческого антитела включает неизмененные или полноразмерные антитела, их фрагменты и/или антитела, содержащие по меньшей мере один полипептид человеческой тяжелой и/или легкой цепей, например, антитело, содержащее полипептиды мышиной легкой цепи и человеческой тяжелой цепи.
[0077] Термин «химерные антитела» относится к антителам, у которых аминокислотная последовательность молекулы иммуноглобулина происходит от двух и более видов. Как правило, вариабельные области легкой и тяжелой цепей соответствуют вариабельным областям антител, полученных от одного вида млекопитающих (например, мыши, крысы, кролика и т.д.), с желательной специфичностью, аффинностью и активностью, в то время как константные областигомологичны последовательностям антител, полученных от другого вида (обычно человека) для исключения формирования иммунного ответа у этого вида.
[0078] Термины «эпитоп» или «антигенная детерминанта» используются здесь взаимозаменяемо и относятся к той части антигена, которая может быть распознана и специфически связана с конкретным антителом. Если антиген является полипептидом, эпитопы могут быть образованы как последовательными аминокислотами, так и непоследовательными, но расположенными рядом в третичной структуре белка. Эпитопы, образованные последовательными аминокислотами, как правило, сохраняются при денатурации белка, в то время как эпитопы, образующиеся в третичной структуре белка, как правило, не сохраняются при денатурации белка. Эпитоп, как правило, включает по меньшей мере 3, а чаще - по меньшей мере 5 или 8-10 аминокислот в уникальной пространственной конформации.
[0079] «Связывающая способность» в общем относится к суммарной силе всех нековалентных взаимодействий между одиночным связывающим сайтом молекулы (например, антитела) и ее партнером в связывании (например, антигеном). Если не указано иное, при использовании здесь, «связывающая способность» обозначает природную связывающую способность, отражающую 1:1 взаимодействие между членами связывающейся пары (например, антитела и антигена). Аффинность молекулы Х к ее партнеру Y может быть охарактеризована константой диссоциации (Kd). Аффинность может быть измерена обычными способами, известными в данной области техники, включая те, которые описаны здесь. Низкоаффинные антитела, как правило, связывают антиген медленно и легко диссоциируют, в то время как высокоаффинные антитела, как правило, быстро связывают антиген и остаются связанными дольше. В данной области техники известно множество способов измерения связывающей аффинности, любой из которых может использоваться для целей настоящего изобретения. Специфические иллюстративные варианты воплощения описаны ниже.
[0080] «Или лучше», при использовании здесь, относится к более сильному связыванию между молекулой и ее партнером по связыванию. «Или лучше», при использовании здесь, относится к более сильному связыванию, что характеризуется меньшим численным значением величины Kd. К примеру, у антитела, обладающего аффинностью к антигену <0,6 нМ или лучше», аффинность антитела к антигену составляет 0,6 нМ, например, 0,59 нМ, 0,58 нМ, 0,57 нМ или любую величину, меньшую 0,6 нМ.
[0081] Фразы «практически одинаковый» или «практически такой же» при использовании здесь обозначают значительно высокую степень сходства двух цифровых величин (как правило, одной, характеризующей антитело по изобретению, и другой, характеризующей референтное антитело или антитело сравнения), такую, что специалист в данной области техники сочтет разность между двумя величинами малой или не имеющей биологического и/или статистического значения в контексте биологических характеристик, измеряющихся упомянутыми величинами (например, Kd-величинами). Разность между указанными двумя величинами равна меньше чем приблизительно 50%, меньше чем приблизительно 40%, меньше чем приблизительно 30%, меньше чем приблизительно 20% либо меньше чем приблизительно 10% относительно величины референтного антитела или антитела сравнения.
[0082] Полипептид, антитело, полинуклеотид, вектор, клетка или композиция, которые «изолированы» - полипептид, антитело, полинуклеотид, вектор, клетка или композиция, которые находятся в форме, необнаруживаемой в природе. Изолированные полипептиды, антитела, полинуклеотиды, векторы, клетки или композиции включают те, которые были очищены до такой степени, что они более не присутствуют в форме, обнаруживаемой в природе. В некоторых вариантах воплощения изолированные антитело, полинуклеотид, вектор, клетка или композиция являются практически чистыми.
[0083] При использовании здесь термин «практически чистый» относится к материалу, которыйпо меньшей мере на 50% чист (то есть свободен от примесей), по меньшей мере на 90% чист, по меньшей мере на 95% чист, по меньшей мере на 98% чист либо по меньшей мере на 99% чист.
[0084] Термин «иммуноконъюгат» или «конъюгат» при использовании здесь относится к соединению или производному, которое связано с агентом, соединяющимся с клеткой (например, с антителом против FOLR1 или его фрагментом), и определяется общей формулой: C-L-A, где С = цитотоксин, L = линкер, А = агент, соединяющийся с клеткой, либо антитело против FOLR1 или его фрагмент. Иммуноконъюгаты также могут быть определены обратной общей формулой: A-L-C.
[0085] «Линкер» - любая химическая группа, которая может стабильно, ковалентно связывать соединение, как правило, препарат, например, майтансиноид, с агентом, соединяющимся с клеткой, например, антителом против FOLR1 или его фрагментом. Линкеры могут быть чувствительны или частично устойчивы к кислотному расщеплению, световому расщеплению, пептидазному расщеплению, эстеразному расщеплению, расщеплению дисульфидных связей в условиях, при которых соединение или антитело остается активным. Подходящие линкеры хорошо известны в данной области техники и включают, к примеру, дисульфидные группы, тиоэфирные группы, кислото-лабильные группы, фотолабильные группы, пептидаза-лабильные группы и эстераза-лабильные группы. Линкеры также включают заряженные линкеры и их гидрофильные формы, как описано здесь и известно в данной области техники.
[0086] Термины «онкологическое заболевание» и «раковый» относятся к или описывают физиологическое состояние у млекопитающих, при котором популяция клеток характеризуется нерегулируемым клеточным ростом. Примеры онкологических заболеваний включают, не ограничиваясь перечисленным, карциному, лимфому, бластому, саркому, лейкемию. Более конкретными примерами таких онкологических заболеваний служат сквамозно-клеточный рак, мелкоклеточный рак легкого, немелкоклеточный рак легкого, аденокарцинома легкого, сквамозная карцинома легкого, рак брюшины, печеночно-клеточный рак, рак желудочно-кишечного тракта, рак поджелудочной железы, глиобластома, рак цервикального канала, рак яичника, рак печени, рак мочевого пузыря, гепатома, рак молочной железы, рак толстого кишечника, колоректальный рак, карцинома эндометрия или матки, карцинома слюнной железы, рак почки, рак печени, рак предстательной железы, рак вульвы, рак щитовидной железы, карцинома печени и различные типы опухолей головы и шеи.
[0087] «Опухоль» и «новообразование» относятся к любому количеству ткани, возникшей вследствие избыточного клеточного роста или пролиферации, как доброкачественного (неракового), так и злокачественного (ракового), включая предраковые поражения.
[0088] Термины «раковая клетка», «опухолевая клетка» и их грамматические эквиваленты относятся к общей популяции клеток, происходящих от опухолевого или предракового поражения, включающих как неопухолегенные клетки, содержащие популяцию опухолевых клеток, так и опухолегенные стволовые клетки (раковые стволовые клетки). При использовании здесь термин «опухолевая клетка» будет заменен на термин «неопухолегенный» в случае обозначения лишь тех опухолевых клеток, которые не могут обновляться, чтобы отличать их от опухолевых клеток из стволовых раковых клеток.
[0089] Термин «субъект» относится к любому животному (например, млекопитающему), включая, но не ограничиваясь перечисленным, людей, нечеловекообразных приматов, грызунов и т.п., являющемуся реципиентом конкретного лечения. Как правило, термины «субъект» и «пациент» используются здесь взаимозаменяемо по отношению к человеческому субъекту.
[0090] Введение «в комбинации с» одним и более дополнительных терапевтических агентов включает одновременное (сопутствующее) и последовательное введение в любом порядке.
[0091] Термин «фармацевтическая композиция» относится к такой форме препарата, в которой эффективно проявляется биологическая активность активного ингредиента и который не содержит дополнительных компонентов с неприемлемой токсичностью по отношению к субъекту, которому вводится композиция. Такая композиция может быть стерильной.
[0092] «Эффективное количество» антитела здесь понимается как количество, достаточное для достижения нужной цели. «Эффективное количество» может быть определено эмпирически обычным способом в зависимости от установленной цели.
[0093] Термин «терапевтически эффективное количество» относится к количеству антитела или иного препарата, эффективному для «лечения» заболевания или нарушения у субъекта или млекопитающего. В случае рака терапевтически эффективное количество препарата может уменьшать количество раковых клеток, уменьшать размер опухоли, ингибировать (например, замедлять до некоторой степени и, в некоторых вариантах воплощения, останавливать) инфильтрацию раковых клеток в периферические органы, ингибировать (например, замедлять до некоторой степени и, в некоторых вариантах воплощения, останавливать) метастазирование опухоли, ингибировать, до некоторой степени, опухолевый рост и/или ослаблять, до некоторой степени, один или более симптомов, ассоциированных с раком. См. определение термина «лечение», приведенное здесь. В случае, если препарат способен предотвращать рост и/или убивать существующие опухолевые клетки, он может быть цитостатическим и/или цитотоксическим. «Профилактически эффективное количество» относится к такому количеству, которое, при необходимых дозировках и периодах введения, эффективно для достижения желаемого профилактического результата. Как правило, но не обязательно, если профилактическая доза используется у субъектов до развития заболевания или на его ранних стадия, профилактически эффективное количество ниже терапевтически эффективного количества.
[0094] Слово «метка», при использовании здесь, относится к детектируемому соединению или композиции, которые конъюгируются прямо или косвенно с антителом, образуя «меченое» антитело. Метка может быть детектируема прямо (например, радиоизотопные или флуоресцентные метки) либо, в случае ферментной метки, может катализировать химическое изменение субстрата или вещества, или композиции, которые уже являются детектируемыми.
[0095] «Химиотерапевтический агент» - химическое соединение, подходящее для лечения онкологического заболевания, независимо от механизма действия. Классы химиотерапевтических агентов включают, не ограничиваясь перечисленным: алкилирующие агенты, антиметаболиты, растительные алкалоиды, являющиеся веретенными ядами, цитотоксические/противоопухолевые антибиотики, ингибиторы топоизомеразы, антитела, фотосенсибилизаторы и ингибиторы киназы. Химиотерапевтические агенты включают соединения, используемые в «нацеленной терапии» и в обычной химиотерапии.
[0096] Такие термины как «лечение» или «терапия», или «лечить», или «облегчение», или «облегчать» относятся к обоим пунктам, включающим: 1) терапевтические меры, которые излечивают, замедляют, ослабляют симптомы и/или останавливают прогрессирование диагностированного патологического состояния или нарушения, и 2) профилактические или предотвращающие меры, которые предотвращают и/или замедляют развитие целевого патологического состояния или нарушения. Таким образом, к нуждающимся в терапии относятся те лица, у которых уже наблюдается заболевание; те лица, которые предрасположены к развитию заболевания; и те лица, у которых заболевание необходимо предотвратить. В определенных вариантах воплощения субъект успешно «лечится» от онкологического заболевания, согласно способам настоящего изобретения, если у пациента наблюдается одно или более из следующего: уменьшение количества раковых клеток или полное их отсутствие; уменьшение размера опухоли; ингибирование или отсутствие инфильтрации раковых клеток в периферические органы, включая, к примеру, распространение рака в мягкие ткани и кости; ингибирование или отсутствие метастазов опухолей; ингибирование или отсутствие роста опухоли; ослабление одного или более симптомов, ассоциированных со специфическим онкологическим заболеванием; понижение заболеваемости и смертности; повышение качества жизни; понижение опухолегенности, опухолегенной частоты или опухолегенной емкости опухоли; понижение количества стволовых раковых клеток в опухоли; дифференциация опухолегенных клеток в неопухолегенное состояние; или какая-либо комбинация эффектов.
[0097] «Полинуклеотид» и «нуклеиновая кислота» здесь используются взаимозаменяемо и относятся к полимерам нуклеотидов любой длины, включая ДНК и РНК. Нуклеотиды могут быть дезоксирибонуклеотидами, рибонуклеотидами, модифицированными нуклеотидами или основаниями и/или их аналогами, либо любым субстратом, который может быть внедрен в полимер ДНК- или РНК-полимеразой. Полинуклеотид может содержать модифицированные нуклеотиды, например, метилированные нуклеотиды и их аналоги. Если они присутствуют, то изменения в структуре нуклеотидов могут быть внесены до или после их соединения в полимер. Последовательность нуклеотидов может прерываться ненуклеотидными компонентами. Полинуклеотид может быть, помимо этого, модифицирован после полимеризации, например, конъюгированием с компонентом-меткой. Другие типы модификаций включают, к примеру, «кэпы», замещение одного и более встречающихся в природе нуклеотидов на аналоги, межнуклеотидные модификации, например, с незаряженными связями (например, метилфосфонаты, фосфотриэфиры, фосфоамидаты, кабаматы и т.д.) и с заряженными связями (например, фосфоротиоаты, фосфородитиоаты и т.д.), со свободными фрагментами, например, белками (например, нуклеазами, токсинами, антителами, сигнальными пептидами, ply-L-лизином и т.д.), с интеркаляторами (например, акридином, псораленом и т.д.), с хелаторами (например, металлами, радиоактивными металлами, бором, металлами-окислителями и т.д.), с алкиляторами, например, модифицированными связями (например, альфа-аномерными нуклеиновыми кислотами и т.д.), а также с немодифицированными формами полинуклеотида(ов). Помимо этого, любая гидроксильная группа, обычно присутствующая в сахарах, может быть заменена, например, на фосфонатные группы, фосфатные группы, защищенные стандартными защитными группами, либо может быть активирована для того, чтобы получить дополнительные связи с дополнительными нуклеотидами, или может быть конъюгирована с твердыми подложками. 5’- и 3’-терминальные ОН могут быть фосфорилированы или замещены на амины, или кэпированы органическими фрагментами, содержащими 1-20 атомов углерода. Также другие гидроксилы могут быть замещены на стандартные защитные группы. Полинуклеотиды также могут содержать аналоги рибозы или дезоксирибозы, хорошо известные в данной области техники, к примеру, 2’-O-метил-, 2’-O-аллил, 2’-фтор- или 2’-азидо-рибозу, карбоциклические аналоги сахаров, .альфа.-аномерные сахара, эпимерные сахара, например, арабинозу, ксилозу или ликсозу, пиранозные сахара, фуранозные сахара, седогептулозы, ациклические аналоги и нуклеозидные аналоги с удаленными азотистыми основаниями, например, метилрибозид. Одна и более фосфодиэфирных связей может быть заменена на альтернативные связывающие группы. Данные альтернативные связывающие группы включают, не ограничиваясь перечисленным, варианты воплощения, в которых фосфат замещен на P(O)S («тиоат»), P(S)S («дитиоат»), «(O)NR2 («амидат»), P(O)R, P(O)OR’, CO или СН2 («формацеталь»), где каждый R или R’ является, независимо, Н или замещенным или незамещенным алкилом (1-20 С), необязательно содержащим простую эфирную (-O-) связь, арильную, алкенильную, циклоалкильную, циклоалкенильную или аральдильную. Не все связи в полинуклеотиде должны быть идентичными. Предшествующее описание относится ко всем полинуклеотидам, упоминающимся здесь, включая РНК и ДНК.
[0098] Термин «вектор» обозначает конструкцию, которая способна доставлять и, необязательно, экспрессировать один или более интересующих генов или последовательностьей в клетке-хозяине. Примеры векторов включают, не ограничиваясь перечисленным, вирусные векторы, свободные ДНК- или РНК-векторы экспрессии, плазмиды, космиды или фаговые векторы, ДНК- или РНК-векторы экспрессии, соединенные с катионными конденсирующими агентами, ДНК- или РНК-векторы экспрессии, помещенные в липосомы, определенные эукариотные клетки, например, клетки-продуценты.
[0099] Термины «полипептид», «пептид» и «белок» используются взаимозаменяемо для обозначения полимеров аминокислот любой длины. Полимер может быть линейным или разветвленным, он может содержать модифицированные аминокислоты и может содержать вставки, отличные от аминокислотных. Термины также охватывают аминокислотный полимер, который был модифицирован природно или по изобретению, к примеру, с образованием дисульфидной связи, гликозилированием, липидированием, ацетилированием, фосфорилированием или иной манипуляцией либо модификацией, например, конъюгированием с компонентом-меткой. Также в определение включены, к примеру, полипептиды, содержащие один или более аналогов аминокислот (включая, к примеру, неприродные аминокислоты и т.д.), а также иные модификации, известные в данной области техники. Следует понимать, что, поскольку полипептиды по настоящему изобретению основываются на антителах, в некоторых вариантах воплощения полипептиды могут присутствовать в виде одинарных цепей или связанных цепей.
[0100] Термины «идентичный» или процентная «идентичность», в контексте двух или более нуклеиновых кислот или полипептидов, относятся к двум или более последовательностей, которые одинаковы или обладают определенным процентным количеством одинаковых нуклеотидов или аминокислот при сравнении и выравнивании (при необходимости - с введением брешей) для максимального соответствия, причем консервативные аминокислотные замены не рассматриваются как идентичные. Процентная идентичность может быть измерена при помощи ПО или алгоритмов для сравнения последовательностей либо ручным подсчетом. В данной области техники известны различные алгоритмы и ПО, которые могут быть использованы для выравнивания нуклеотидных или аминокислотных последовательностей. Один нелимитирующий пример алгоритма выравнивания последовательностей - алгоритм, описанный в Karlin et al., 1990, Proc. Natl. Acad. Sci., 87:2264-2268, с изменениями согласно Karlin et al., 1993, Proc. Natl. Acad. Sci., 90:5873-5877, который используется в программах NBLAST и XBLAST (Altschul et al., 1991, Nucleic Acids Res., 25:3389-3402). В некоторых вариантах воплощения может использоваться Gapped BLAST согласно Altschul et al., 1997, Nucleic Acids Res. 25:3389-3402. BLAST-2, WU-BLAST-2 (Altschul et al., 1996, Methods in Enzymology, 266:460-480), ALIGN, ALIGN-2 (Genentech, South San Francisco, California) и Megalign (DNASTAR) - дополнительные свободные программы, которые могут использоваться для выравнивания последовательностей. В определенных вариантах воплощения процентная идентичность двух нуклеотидных последовательностей определяется при помощи программы GAP в ПО GCG (например, с использованием показателей NWSgapdna. CMP matrix и gap weight, равных 40, 50, 60, 70 или 90, показателя length weight, равного 1, 2, 3, 4, 5 или 6). В определенных альтернативных вариантах воплощения программа GAP в пакете GCG, в которой используется алгоритм Needleman и Wunsch (J. Mol. Biol. (48):444-453 (1970)), может применяться для определения процентной идентичности двух аминокислотных последовательностей (например, с использованием либо матрицы Blossum 62, либо матрицы РАМ250 и показателя gap weight, равного 16, 14, 12, 10, 8, 6 или 4, а также показателя length weight, равного 1, 2, 3, 4, 5). Альтернативно в определенных вариантах воплощения процентная идентичность нуклеотидных или аминокислотных последовательностей определяется по алгоритму Myers и Miller (CABIOS, 4:11-17 (1989)). К примеру, процентная идентичность может быть определена при помощи программы ALIGN (версии 2.0) и использовании РАМ 120 с таблицей остатков, параметрм gap length penalty, равным 12, и gap penalty, равным 4. Параметры, подходящие для максимального выравнивания в конкретном ПО для выравнивания, могут быть определены специалистом в данной области техники. В определенных вариантах воплощения применяются параметры по умолчанию, определенные в ПО для выравнивания. В определенных вариантах воплощения процентная идентичность «X» первой аминокислотной последовательности со второй аминокислотной последовательностью рассчитывается по формуле 100×(Y/Z), где Y - количество аминокислотных остатков, определенных как идентичные в выравнивании первой и второй последовательностей (при ручном выравнивании или конкретной программой выравнивания последовательностей), a Z - общее количество остатков во второй последовательности. Если длина первой последовательности больше длины второй, процентная идентичность первой последовательности со второй будет выше процентной идентичности второй последовательности с первой.
[0101] В качестве неограничивающего примера, наличие определенной процентной идентичности (например, по меньшей мере 80% идентичности, по меньшей мере 85% идентичности, по меньшей мере 90% идентичности, а в некоторых вариантах воплощения - по меньшей мере 95%, 96%, 97%, 98% или 99% идентичности) конкретного полипептида с референтной последовательностью в определенных вариантах воплощения может быть установлено при помощи программы Bestfit (Пакет Wisconsin Sequence Analysis Package, Версия 8 для Unix, Genetics Computer Group, University Research Park, 575 Science Drive, Madison, WI 53711). В BESTFIT используется алгоритм «локальной гомологии» Smith и Waterman, Advances in Applied Mathematics 2: 482-489 (1981) для поиска наилучшегосегмента гомологии между двумя последовательностями. При использовании Bestfit или иной программы выравнивания последовательностей для определения того, идентична ли конкретная последовательность, например, на 95% референтной последовательности по настоящему изобретению, параметры устанавливаются так, чтобы процентная идентичность рассчитывалась по полной длине референтной нуклеотидной последовательности и чтобы были разрешены бреши в гомологичности вплоть до 5% от общего количества нуклеотидов референтной последовательности.
[0102] В некоторых вариантах воплощения две нуклеиновые кислоты или два полипептида по изобретению в значительной степени идентичны, обладая по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, а в некоторых вариантах воплощения - по меньшей мере 95%, 96%, 97%, 98%, 99% нуклеотидной или аминокислотной идентичностью при сравнении и максимальном выравнивании, согласно алгоритму сравнения последовательностей или ручному подсчету. В определенных вариантах воплощения идентичность наблюдается в области последовательности, имеющей по меньшей мере приблизительно 10, приблизительно 20, приблизительно 40-60 остатков или любую целую величину в этом интервале, либо в области последовательности более чем 60-80 остатков, по меньшей мере приблизительно 90-100 остатков, либо же последовательности практически идентичны по всей длине сравниваемых последовательностей, к примеру, могут быть идентичны кодирующие области нуклеотидной последовательности.
[0103] «Консервативная аминокислотная замена» это такая замена, при которой одна аминокислота заменяется на другую аминокислоту с похожей боковой цепью. Семейства аминокислотных остатков по схожести боковых цепей определены в данной области техники и включают основные боковые цепи (например, лизин, аргинин, гистидин), кислотные боковые цепи (например, аспарагиновая кислота, глутаминовая кислота), незаряженные полярные боковые цепи (например, аспарагин, глутамин, серии, треонин, тирозин, цистеин), неполярные боковые цепи (например, глицин, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан), бета-разветвленные боковые цепи (например, треонин, валин, изолейцин) и ароматические боковые цепи (например, тирозин, фенилаланин, триптофан, гистидин). К примеру, замена фенилиаланина на тирозин является консерватиной заменой. В определенных вариантах воплощения консервативные замены в последовательностях полипептидов и антител по изобретению не приводят к исчезновению связывания полипептида или антитела, содержащего аминокислотную последовательность, с антигеном(ами), с которым(и) они обычно связываются, например, с FOLR1. Способы идентификации нуклеотидных и аминокислотных консервативных замен, не приводящих к исчезновению связывания с антигеном, хорошо известны в данной области техники (см., например, Brummell et al., Biochem.32: 1180-1187 (1993); Kobayashi et al., Protein Eng. 12(10):879-884 (1999); и Burks et al., Proc. Natl. Acad. Sci. USA 94:412-417 (1997)).
[0104] При использовании в настоящей заявке и формуле изобретения формы единственного числа включают и формы множественного числа, если из контекста явно не следует иное.
[0105] Следует понимать, что какие-либо варианты воплощения, описанные здесь с употреблением слова «содержащий», есть аналогами вариантов воплощения, описанных терминами «состоящий из» и/или «преимущественно состоящий из».
[0106] Термин «и/или» при использовании здесь во фразе типа «А и/или В» включает и «А и В», и «А или В», и «А» и «В». Аналогично термин «и/или» в такой фразе как «А, В, и/или С» охватывает каждое из следующих вариантов воплощений: А, В и С; А, В или С; А или С; А или В; В или С; А и С; А и В; В и С; А (одно), В (одно) и С (одно).
II. FOLR1-связывающие агенты
[0107] В настоящем изобретении предлагаются агенты, которые специфически связываются с человеческим FOLR1. Эти агенты называются здесь «FOLR1 -связывающими агентами». Полноразмерные аминокислотные (аа) и нуклеотидные (nt) последовательности для FOLR1 известны в данной области техники и представлены здесь в SEQ ID NOs:25 и 26, соответственно.
[0108] В определенных вариантах воплощения FOLR1-связывающие агенты являются антителами, иммуноконъюгатами или полипептидами. В некоторых вариантах воплощения FOLR1-связывающие агенты являются гуманизированными антителами. В определенных вариантах воплощения FOLR1-связывающие агенты являются гуманизированными версиями мышиного антитела Mov19 (вариабельные тяжелая и легкая цепи представлены в SEQ ID NOs:17 и 18, соответственно).
[0109] В определенных вариантах воплощения FOLR1-связывающие агенты оказывают один или более из следующих эффектов: ингибирование пролиферации опухолевых клеток, уменьшение опухолегенности опухоли путем уменьшения частотности раковых стволовых клеток в опухоли, ингибирование роста опухоли, повышение выживаемости, запуск клеточной смерти опухолевых клеток, дифференциация опухолегенных клеток в неопухолевое состояние либо предотвращение метастазирования опухолевых клеток.
[ОНО] В определенных вариантах воплощения иммуноконъюгаты или иные агенты, которые специфически связываются с человеческим FOLR1, запускают клеточную смерть посредством цитотоксического агента. К примеру, в некоторых вариантах воплощения антитело против человеческого FOLR1 конъюгировано с майтансиноидом, который активируется в опухолевых клетках, экспрессирующих FOLR1, при интернализации белка. В определенных альтернативных вариантах воплощения агент или антитело не конъюгированы.
[0111] В определенных вариантах воплощения FOLR1-связывающие агенты способны ингибировать рост опухоли. В определенных вариантах воплощения FOLR1-связывающие агенты способны ингибировать рост опухоли in vivo (например, в ксенотрансплантатной мышиной модели и/или у людей, страдающих раком). В определенных вариантах воплощения FOLR1-связывающие агенты способны ингибировать рост опухоли у человека.
[0112] Таким образом, в изобретении предлагаются гуманизированное антитело или его антиген-связывающий фрагмент, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, причем антитело содержит: (a) CDR1 тяжелой цепи, содержащую GYFMN (SEQ ID NO:1); CDR2 тяжелой цепи, содержащую RIHPYDGDTFYNQXaaiFXaa2Xaa3 (SEQ ID NO:56); и CDR3 тяжелой цепи, содержащую YDGSRAMDY (SEQ ID NO:3); и (б) CDR1 легкой цепи, содержащую KASQSVSFAGTSLMH (SEQ ID NO:7); CDR2 легкой цепи, содержащую RASNLEA (SEQ ID NO:8); CDR3 легкой цепи, содержащую QQSREYPYT (SEQ ID NO:9); где Xaa1 выбран из К, Q, И и R; Хаа2, выбран из Q, Н, N и R; и Хаа3 выбран из G, Е, Т, S, А и V. В определенных вариантах воплощения антитело является антителом huMov19, которое является описанным выше антителом, содержащим CDR2 тяжелой цепи RIHPYDGDTFYNQKFQG (SEQ ID NO:2).
[0113] В определенных вариантах воплощения в изобретении предлагаются гуманизированные антитела или антиген-связывающие фрагменты, которые специфически связываются с FOLR1, включающие определяющие комплементарность области huMov19, которые содержат до четырех (т.е. 0, 1, 2, 3 или 4) консервативных аминокислотных замен на определяющую комплементарность область. Таким образом, в определенных вариантах воплощения в изобретении предлагаются гуманизированные антитела или антиген-связывающие фрагменты, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (а) CDR1 тяжелой цепи, содержащую GYFMN (SEQ ID NO:1), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; CDR2 тяжелой цепи, содержащую RIHPYDGDTFYNQKFQG (SEQ ID NO:2), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и CDR3 тяжелой цепи, содержащую YDGSRAMDY (SEQ ID NO:3), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или (б) CDR1 легкой цепи, содержащую KASQSVSFAGTSLMH (SEQ ID NO:7), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; CDR2 легкой цепи, содержащую RASNLEA (SEQ ID NO:8), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; CDR3 легкой цепи, содержащую QQSREYPYT (SEQ ID NO:9), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены.
[0114] В изобретении также предлагается гуманизированное антитело (huFR1-21) или его антиген-связывающий фрагмент, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (а) CDR1 тяжелой цепи, содержащую SSYGMS (SEQ ID NO:30); CDR2 тяжелой цепи, содержащуюй TISSGGSYTY (SEQ ID NO:31); и CDR3 тяжелой цепи, содержащую DGEGGLYAMDY (SEQ ID NO:32); и/или (б) CDR1 легкой цепи, содержащую KASDHINNWLA (SEQ ID NO:27); CDR2 легкой цепи, содержащую GATSLET (SEQ ID NO:28); и CDR3 легкой цепи, содержащую QQYWSTPFT (SEQ ID NO:29).
[0115] В определенных вариантах воплощения в изобретении предлагаются гуманизированные антитела или антиген-связывающие фрагменты, которые специфически связываются с FOLR1, включающие определяющие комплементарность области huFR1-21, которые содержат до четырех (т.е. 0, 1, 2, 3 или 4) консервативных аминокислотных замен на определяющую комплементарность область. Таким образом, в определенных вариантах воплощения в изобретении предлагаются гуманизированные антитела или антиген-связывающие фрагменты, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (а) CDR1 тяжелой цепи, содержащую SSYGMS (SEQ ID NO:30), либо ее вариант, включающий 1,2,3 или 4 консервативных аминокислотных замены; и/или CDR2 тяжелой цепи, содержащую TISSGGSYTY (SEQ ID NO:31), либо ее вариант, включающий 1,2,3 или 4 консервативных аминокислотных замены; и/или CDR3 тяжелой цепи, содержащую DGEGGLYAMDY (SEQ ID NO:32), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или (б) CDR1 легкой цепи, содержащую KASDHINNWLA (SEQ ID NO:27), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR2 легкой цепи, содержащую GATSLET (SEQ ID NO:28), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR3 легкой цепи, содержащую QQYWSTPFT (SEQ ID NO:29), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены.
[0116] В определенных вариантах воплощения в изобретении предлагаются гуманизированные антитела или антиген-связывающие фрагменты, которые специфически связываются с FOLR1, включающие определяющие комплементарность области huFR1-48, которые содержат до четырех (т.е. 0, 1, 2, 3 или 4) консервативных аминокислотных замен на определяющую комплементарность область. Таким образом, в определенных вариантах воплощения в изобретении предлагаются гуманизированные антитела или антиген-связывающие фрагменты, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (a) CDR1 тяжелой цепи, содержащую TNYWMQ (SEQ ID NO:60), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR2 тяжелой цепи, содержащую IYPGNGDSR (SEQ ID NO:61), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR3 тяжелой цепи, содержащую RDGNYAAY (SEQ ID NO:62), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или (б) CDR1 легкой цепи, содержащую RASENIYSNLA (SEQ ID NO:57), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR2 легкой цепи, содержащую AATNLAD (SEQ ID NO:58), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR3 легкой цепи, содержащую QHFWASPYT (SEQ ID NO:59), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены.
[0117] В определенных вариантах воплощения в изобретении предлагаются гуманизированные антитела или антиген-связывающие фрагменты, которые специфически связываются с FOLR1, включающие определяющие комплементарность области huFR1-49, которые содержат до четырех (т.е. 0, 1, 2, 3 или 4) консервативных аминокислотных замен на определяющую комплементарность область. Таким образом, в определенных вариантах воплощения в изобретении предлагаются гуманизированные антитела или антиген-связывающие фрагменты, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (а) CDR1 тяжелой цепи, содержащую TNYWMY (SEQ ID NO:66), либо его вариант, включающий 1,2,3 или 4 консервативных аминокислотных замены; и/или CDR2 тяжелой цепи, содержащий AIYPGNSDTT (SEQ ID NO:67), либо ее вариант, включающий 1,2,3 или 4 консервативных аминокислотных замены; и/или CDR3 тяжелой цепи, содержащую RHDYGAMDY (SEQ ID NO:68), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или (б) CDR1 легкой цепи, содержащую RASENIYTNLA (SEQ ID NO:63), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR2 легкой цепи, содержащую TASNLAD (SEQ ID NO:64), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR3 легкой цепи, содержащую QHFWVSPYT (SEQ ID NO:65), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены.
[0118] В определенных вариантах воплощения в изобретении предлагаются гуманизированные антитела или антиген-связывающие фрагменты, которые специфически связываются с FOLR1, включающие определяющие комплементарность области huFR1-57, которые содержат до четырех (т.е. 0, 1, 2, 3 или 4) консервативных аминокислотных замен на определяющую комплементарность область. Таким образом, в определенных вариантах воплощения в изобретении предлагаются гуманизированные антитела или антиген-связывающие фрагменты, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (a) CDR1 тяжелой цепи, содержащую SSFGMH (SEQ ID NO:72), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR2 тяжелой цепи, содержащую YISSGSSTIS (SEQ ID NO:73), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR3 тяжелой цепи, содержащую EAYGSSMEY (SEQ ID NO:74), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или (б) CDR1 легкой цепи, содержащую RASQNINNNLH (SEQ ID NO:69), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR2 легкой цепи, содержащую YVSQSVS (SEQ ID NO:70), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR3 легкой цепи, содержащую QQSNSWPHYT (SEQ ID NO:71), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены.
[0119] В определенных вариантах воплощения в изобретении предлагаются гуманизированные антитела или антиген-связывающие фрагменты, которые специфически связываются с FOLR1, включающие определяющие комплементарность области huFR1-65, которые содержат до четырех (т.е. 0, 1, 2, 3 или 4) консервативных аминокислотных замены на определяющую комплементарность область. Таким образом, в определенных вариантах воплощения в изобретении предлагаются гуманизированные антитела или антиген-связывающие фрагменты, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, отличающиеся тем, что антитело содержит: (а) CDR1 тяжелой цепи, содержащую TSYTMH (SEQ ID NO:78), либо ее вариант, включающий 1,2,3 или 4 консервативных аминокислотных замены; и/или CDR2 тяжелой цепи, содержащую YINPISGYTN (SEQ ID NO:79), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR3 тяжелой цепи, содержащую GGAYGRKPMDY (SEQ ID NO:80), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или (б) CDR1 легкой цепи, содержащую KASQNVGPNVA (SEQ ID NO:75), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR2 легкой цепи, содержащую SASYRYS (SEQ ID NO:76), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены; и/или CDR3 легкой цепи, содержащую QQYNSYPYT (SEQ ID NO:77), либо ее вариант, включающий 1, 2, 3 или 4 консервативных аминокислотных замены.
[0120] Помимо этого, предлагаются полипептиды, содержащие одну из индивидуальных легких цепей или тяжелых цепей, описанных здесь, а также полипептиды (например, антитела), содержащие как легкую, так и тяжелую цепи. Полипептиды с SEQ ID NOs:4 и 6 содержат вариабельный домен тяжелой цепи huMov19 и тяжелую цепь huMov19, соответственно. Полипептиды с SEQ ID NOs:10-13 содержат вариабельный домен легкой цепи версии 1.00, вариабельный домен легкой цепи версии 1.60, легкую цепь версии 1.00 и легкую цепь версии 1.60 huMov19, соответственно. Полипептиды с SEQ ID NOs:42 и 46 содержат вариабельный домен тяжелой цепи huFR1-21 и тяжелую цепь huFR1-21, соответственно. Полипептиды с SEQ ID NOs:41 и 45 содержат вариабельный домен легкой цепи и легкую цепь huFR1-21, соответственно. Полипептиды с SEQ ID NOs:97 и 113 содержат вариабельный домен тяжелой цепи huFR1-48 и тяжелую цепь huFR1-48, соответственно. Полипептиды с SEQ ID NOs:96 и 112 содержат вариабельный домен легкой цепи и легкую цепь huFR1-48, соответственно. Полипептиды с SEQ ID NOs:99 и 115 содержат вариабельный домен тяжелой цепи huFR1-49 и тяжелую цепь huFR1-49, соответственно. Полипептиды с SEQ ID NOs:98 и 114 содержат вариабельный домен легкой цепи и легкую цепь huFR1-49, соответственно. Полипептиды с SEQ ID NOs:101 и 117 содержат вариабельный домен тяжелой цепи huFR1-57 и тяжелую цепь huFR1-57, соответственно. Полипептиды с SEQ ID NOs:100 и 116 содержат вариабельный домен легкой цепи и легкую цепь huFR1-57, соответственно. Полипептиды с SEQ ID NOs:103 и 119 содержат вариабельный домен тяжелой цепи huFR1-65 и тяжелую цепь huFR1-65, соответственно. Полипептиды с SEQ ID NOs:102 и 118 содержат вариабельный домен легкой цепи и легкую цепь huFR1-65, соответственно.
[0121] Также предлагаются полипептиды, которые содержат: (а) полипептид, обладающий по меньшей мере приблизительно 90% идентичностью последовательности с SEQ ID NO:4 или 6; и/или (б) полипептид, обладающий по меньшей мере приблизительно 90% идентичностью последовательности с SEQ ID NOs:10-13. Также предлагаются полипептиды, которые содержат: (а) полипептид, обладающий приблизительно 90% идентичностью последовательности с SEQ ID NO:42 или 46; и/или (б) полипептид, обладающий по меньшей мере приблизительно 90% идентичностью последовательности с SEQ ID NOs:41 и 45. Также предлагаются полипептиды, которые содержат: (а) полипептид, обладающий по меньшей мере приблизительно 90% идентичностью последовательности с SEQ ID NOs:97 или 113; и/или (б) полипептид, обладающий по меньшей мере приблизительно 90% идентичностью последовательности с SEQ ID NOs:96 или 112. Также предлагаются полипептиды, которые содержат: (а) полипептид, обладающий по меньшей мере приблизительно 90% идентичностью последовательности с SEQ ID NOs:99 или 115; и/или (б) полипептид, обладающий по меньшей мере приблизительно 90% идентичностью последовательности с SEQ ID NOs:98 или 114. Также предлагаются полипептиды, которые содержат: (а) полипептид, обладающий по меньшей мере приблизительно 90% идентичностью последовательности с SEQ ID NOs:101 или 117; и/или (б) полипептид, обладающий по меньшей мере приблизительно 90% идентичностью последовательности с SEQ ID NOs:100 или 116. Также предлагаются полипептиды, которые содержат: (а) полипептид, обладающий по меньшей мере приблизительно 90% идентичностью последовательности с SEQ ID NOs:103 или 119; и/или (б) полипептид, обладающий по меньшей мере приблизительно 90% идентичностью последовательности с SEQ ID NOs:102 или 118. В определенных вариантах воплощения полипептид содержит полипептид, который обладает по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98% либо по меньшей мере приблизительно 99% идентичностью последовательности с SEQ ID NOs:4, 6, 10-13, 41, 42, 45 или 46. Таким образом, в определенных вариантах воплощения полипептид содержит (а) полипептид с по меньшей мере приблизительно 95% идентичностью последовательности с SEQ ID NOs:4 или 6, и/или (б) полипептид с по меньшей мере приблизительно 95% идентичностью последовательности с SEQ ID NOs:10-13. В определенных вариантах воплощения полипептид содержит (а) полипептид с по меньшей мере приблизительно 95% идентичностью последовательности с SEQ ID NOs:42 или 46; и/или (б) полипептид с по меньшей мере приблизительно 95% идентичностью последовательности с SEQ ID NOs:41 или 45. Также предлагаются полипептиды, которые содержат: (а) полипептид, обладающий по меньшей мере приблизительно 95% идентичностью последовательности с SEQ ID NOs:97 или 113; и/или (б) полипептид, обладающий по меньшей мере приблизительно 95% идентичностью последовательности с SEQ ID NOs:96 или 112. Также предлагаются полипептиды, которые содержат: (а) полипептид, обладающий по меньшей мере приблизительно 95% идентичностью последовательности с SEQ ID NOs:99 или 115; и/или (б) полипептид, обладающий по меньшей мере приблизительно 95% идентичностью последовательности с SEQ ID NOs:98 или 114. Также предлагаются полипептиды, которые содержат: (а) полипептид, обладающий по меньшей мере приблизительно 95% идентичностью последовательности с SEQ ID NOs:101 или 117; и/или (б) полипептид, обладающий по меньшей мере приблизительно 95% идентичностью последовательности с SEQ ID NOs:100 или 116. Также предлагаются полипептиды, которые содержат: (а) полипептид, обладающий по меньшей мере приблизительно 95% идентичностью последовательности с SEQ ID NOs:103 или 119; и/или (б) полипептид, обладающий по меньшей мере приблизительно 95% идентичностью последовательности с SEQ ID NOs:102 или 118. В определенных вариантах воплощения полипептид содержит (а) полипептид с аминокислотной последовательностью SEQ ID NO:4; и/или (б) полипептид с аминокислотной последовательностью SEQ ID N0:10 или SEQ ID NO:11. В определенных вариантах воплощения полипептид содержит (а) полипептид с аминокислотной последовательностью SEQ ID NO:45; и/или (б) полипептид с аминокислотной последовательностью SEQ ID NO:46. В определенных вариантах воплощения полипептид содержит (а) полипептид с аминокислотной последовательностью SEQ ID NO:6; и/или (б) полипептид с аминокислотной последовательностью SEQ ID NO:12 или SEQ ID NO:13. В определенных вариантах воплощения полипептид является антителом и/или полипептидом, специфически связывающимся с человеческим рецептором фолиевой кислоты 1. В определенных вариантах воплощения полипептид является гуманизированным антителом, специфически связывающимся с человеческим рецептором фолиевой кислоты 1. К примеру, в изобретении предлагается антитело или гуманизированное антитело, которое специфически связывается с человеческим FOLR1, которое содержит (а) полипептид с аминокислотной последовательностью SEQ ID NO:4; и (б) полипептид с аминокислотной последовательностью SEQ ID NO:10 или SEQ ID NO:11. В определенных вариантах воплощения полипептид, содержащий SEQ ID NO:4, представляет собой вариабельную область тяжелой цепи. В определенных вариантах воплощения полипептид, содержащий SEQ ID NO:10 или 11, представляет собой вариабельную область легкой цепи. В изобретении также предлагается антитело или гуманизированное антитело, которое специфически связывается с человеческим FOLR1, которое содержит (а) полипептид с аминокислотной последовательностью SEQ ID NO:6 и (б) полипептид с аминокислотной последовательностью SEQ ID NO:12 или SEQ ID NO:13. В изобретении также предлагается антитело или гуманизированное антитело, которое специфически связывается с человеческим FOLR1, которое содержит (а) полипептид с аминокислотной последовательностью SEQ ID NO:45 и (б) полипептид с аминокислотной последовательностью SEQ ID NO:46. В изобретении также предлагается антитело или гуманизированное антитело, которое специфически связывается с человеческим FOLR1, которое содержит (а) полипептид с аминокислотной последовательностью SEQ ID NO:112 и (б) полипептид с аминокислотной последовательностью SEQ ID NO:113. В изобретении также предлагается антитело или гуманизированное антитело, которое специфически связывается с человеческим FOLR1, которое содержит (а) полипептид с аминокислотной последовательностью SEQ ID NO:114 и (б) полипептид с аминокислотной последовательностью SEQ ID NO:115. В изобретении также предлагается антитело или гуманизированное антитело, которое специфически связывается с человеческим FOLR1, которое содержит (а) полипептид с аминокислотной последовательностью SEQ ID NO:116 и (б) полипептид с аминокислотной последовательностью SEQ ID NO:117. В изобретении также предлагается антитело или гуманизированное антитело, которое специфически связывается с человеческим FOLR1, которое содержит (а) полипептид с аминокислотной последовательностью SEQ ID NO:118 и (б) полипептид с аминокислотной последовательностью SEQ ID NO:119. В определенных вариантах воплощения полипептид с определенной процентной идентичностью последовательности с SEQ ID NOs:4, 6, 10-13, 41, 42, 45, 46, 96-103 и 112-119 отличается от SEQ ID NO:4, 6, 10-13, 41, 42, 45, 46, 96-103 и 112-119 только консервативными заменами аминокислот.
[0122] В определенных вариантах воплощения FOLR1-связывающий агент содержит, преимущественно состоит, исключительно состоит или состоит из антитела против FOLR1, выбранного из группы, состоящей из антител huMov19, FR-1-21, FR1-48, FR1-49, FR1-57 и FR1-65.
[0123] В определенных вариантах воплощения антитело huMov19 закодировано плазмидами, депонированными в Американской Коллекции Типовых Культур (АТСС) 7 апреля 2010 под номерами депонентов АТСС РТА-10772 и РТА-10773 или 10774.
[0124] В определенных вариантах воплощения антитело FR-1-21 закодировано плазмидами, депонированными в АТСС 7 апреля 2010 под номерами депонентов РТА-10775 и 10776.
[0125] В определенных воплощениях гуманизированные антитела связывают FOLR1 с практически такой же аффинностью, что и химерное антитело Mov19. Аффинность или авидность антитела к антигену может быть определена экспериментально при помощи любого способа, хорошо известного в данной области техники, например, проточной цитометрии, энзим-связанного иммуносорбентного способа исследования (ELISA), радиоиммунного анализа (RIA) либо кинетического анализа (например, анализа BIACORE™). Анализы в формате прямого связывания, а также конкурентного связывания могут быть легко выполнены. (См., к примеру, Berzofsky, et al., "Antibody-Antigen Interactions," In Fundamental Immunology, Paul, W.E., Ed., Raven Press: New York, N.Y. (1984); Kuby, Janis Immunology, W.H. Freeman and Company: New York, N.Y. (1992) и способы, описанные здесь. Измеренная аффинность конкретного взаимодействия антитело-антиген может варьироваться при выполнении измерений в различных условиях (концентрации соли, рН, температуре). Таким образом, измерения аффинности и других антиген-связывающих параметров (например, KD или Kd, Kon, Koff) следует делать со стадартизованными растворами антитела и антигена в стандартизованном буфере, как принято в данной области техники, например, можно использовать буфер, описанный здесь.
[0126] В одном аспекте анализы связывания могут проводиться с использованием проточной цитометрии на клетках, экспрессирующих антиген FOLR1 на поверхности. К примеру, FOLR1-положительные клетки, такие как SKOV3, были инкубированы с различными концентрациями антител против FOLR1 с использованием 1×105 клеток на образец в 100 мкл буфера FACS (среда RPMI-1640 с добавкой 2% нормальной козьей сыворотки). Затем клетки были осаждены, промыты и инкубированы 1 ч с 100 мкл FITC-конъюгированных козьих анти-мышиных или козьих анти-человеческих IgG-антител (например, доступны в продаже у Jackson Laboratory, 6 мкг/мл в буфере FACS). Клетки были вновь осаждены, промыты буфером FACS и ресуспендированы в 200 мкл фосфатно-солевого буфера, содержащего 1% формальдегид. Образцы были собраны, к примеру, при помощи проточного цитометра FACSCalibur с многолуночным самплером HTS и проанализированы при помощи CellQuest Pro (все оборудование от BD Biosciences, Сан-Диего, США). Для каждого образца снималась средняя интенсивность флуоресценции для FL1 (MFI), после чего строилась кривая связывания в виде полулогарифмического графика зависимости интенсивности от концентрации антитела. Сигмовидную кривую дозовой зависимости сопоставляют с кривыми связывания при помощи GraphPad Prism v4 (GraphPad software, Сан-Диего, Калифорния) с параметрами по умолчанию и рассчитывают величины ЕС50. Величины ЕС50 могут использоваться для измерения кажущейся константы диссоциации «Kd» или «KD» для каждого антитела.
[0127] Моноклональные антитела могут быть приготовлены гибридомными способами, например, описанными Kohler и Milstein (1975) Nature 256:495. Используя гибридомный способ, мышь, хомячок или иное подходящее животное-носитель иммунизируется так, как описано выше, для того, чтобы достичь выделения лимфоцитами антител, которые специфически связываются с иммунизирующим антигеном. Лимфоциты также могут быть иммунизированы in vitro. После иммунизации лимфоциты выделяют и сливают с подходящей миеломной клеточной линией, используя, к примеру, полиэтиленгликоль, для образования гибридомных клеток, которые затем могут быть отделены от неслившихся лимфоцитов и миеломных клеток. Гибридомы, которые продуцируют моноклональные антитела, направленные специфически против выбранного антигена, согласно данным иммунопреципитации, иммуноблоттинга либо анализа связывания in vitro (например, радиоиммунологического анализа (РИА); энзим-связанного иммуносорбентного анализа (ELISA)), могут затем быть размножены в культуре in vitro стандартными способами (Coding, Monoclonal Antibodies: Principles and Practice, Academic Press, 1986) или in vivo в виде асцитных опухолей у животных. Моноклональные антитела затем могут быть очищены из питательной среды или асцитной жидкости так, как описано выше для поликлональных антител.
[0128] Альтернативно моноклональные антитела могут также быть изготовлены способами, использующими рекомбинантную ДНК, как описано в патенте США 4816567. Полинуклеотиды, кодирующие моноклональное антитело, выделяют из зрелых В-клеток или клеток гибридомы, например, способом ОТ-ПЦР с использованием олигонуклеотидных праймеров, которые специфически усиливают гены, кодирующие тяжелые и легкие цепи антитела, а их последовательности определяют обычными процедурами. Изолированные полинуклеотиды, кодирующие тяжелую и легкую цепи, затем клонируют в подходящие вектора экспрессии, которыми трансфицируют клетки-хозяева, например, клетки Е. coli, клетки COS, клетки яичника китайского хомячка (СНО), либо миеломные клетки, которые в иных случаях не продуцируют иммуноглобулиновых белков, моноклональные антитела образуются клетками-хозяевами. Также рекомбинантные моноклональные антитела желаемых видов или их фрагменты могут быть изолированы из фаговых дисплейных библиотек, экспрессирующих определяющие комплементарность области желаемых видов, как было описано (McCafferty et al., 1990, Nature, 348:552-554; Clackson et al., 1991, Nature, 352:624-628; и Marks et al., 1991, J. Mol. Biol., 222:581-597).
[0129] Полинуклеотид(ы), кодирующие моноклональное антитело могут, помимо этого, быть модифицированы множеством различных способов с использованием технологии рекомбинантных ДНК для получения альтернативных антител. В некоторых вариантах воплощения константные домены легкой и тяжелой цепей, например, мышиного моноклонального антитела, могут быть замещены 1) на области, к примеру, человеческого антитела - для получения химерного антитела или 2) на неиммуноглобулиновый полипептид - для получения слитого антитела. В некоторых вариантах воплощения константные области усечены или удалены для получения желательного фрагмента моноклонального антитела. Сайт-направленный или высокоплотный мутагенез вариабельнойобласти может применяться для оптимизации специфичности, аффинности и т.д. моноклонального антитела.
[0130] В некоторых вариантах воплощения моноклональное антитело против человеческого FOLR1 является гуманизированным антителом. В определенных вариантах воплощения подобные антитела используются терапевтически для уменьшения антигенности и ответов НАМА (человеческое анти-мышиное антитело) при введении человеческому субъекту.
[0131] Также могут применяться способы конструирования, гуманизации и перестройки нечеловеческих и человеческих антител, которые хорошо известны в данной области техники. Гуманизированное, перестроенное или аналогичным образом сконструированное антитело может иметь один или более аминокислотных остатков нечеловеческого происхождения, например, но не ограничиваясь перечисленным, от мыши, крысы, кролика, нечеловекообразных приматов или иных млекопитающих. Эти нечеловеческие аминокислотные остатки заменяются остатками, часто называемыми «импортными» остатками, которые обычно берутся из «импортного» вариабельного, константного или иного домена известной человеческой последовательности.
[0132] Подобные импортированные последовательности могут использоваться для уменьшения иммуногенности, уменьшения, усиления или изменения связывания, аффинности, скорости ассоциации, скорости диссоциации, авидности, специфичности, периода полужизни и иных подходящих характеристик, известных в данной области техники. В общем остатки областей, определяющих комплементарность, прямо и наиболее существенно влияют на FOLR1-связывание. Соответственно, часть всех нечеловеческих или человеческих последовательностей областей, определяющих комплементарность, сохраняется, в то время как нечеловеческие последовательности вариабельных и константных областей могут быть заменены на человеческие или иные аминокислоты.
[0133] Антитела, необязательно, могут быть гуманизированы, перестроены, конструированы в человеческие антитела с высокой аффинностью к антигену FOLR1 и иными предпочтительными биологическими свойствами. Для достижения этой цели гуманизированные (или человеческие) или сконструированные антитела против FOLR1 и перестроенные антитела, необязательно, могут быть изготовлены по процессу анализа родительских последовательностей и различных концептуальных гуманизированных и сконструированных продуктов с применением трехмерных моделей родительских, конструированных и гуманизированных последовательностей. Трехмерные модели иммуноглобулинов широкодоступны и известны специалистам в данной области техники. Имеются компьютерные программы, которые иллюстрируют и показывают вероятные трехмерные конформационные структуры выбранных кандидатных последовательностей иммуноглобулинов. Изучение этих проявлений позволяет провести анализ вероятной роли остатков в функционировании кандидатной иммуноглобулиновой последовательности, то есть анализ остатков, влияющих на способность кандидатного иммуноглобулина связываться с его антигеном, например, FOLR1. Таким образом, каркасные остатки (FR) могут быть выбраны и скомбинированы из консенсусных и импортных последовательностей так, чтобы получить желаемые характеристики антитела, например, повышенную аффинность к целевому(ым) антигену(ам).
[0134] Гуманизирование, перестраивание и конструирование антител по настоящему изобретению могут осуществляться в соответствии с любым известным способом, например, но не ограничиваясь перечисленным, способом описанным в Winter (Jones et al., Nature 321:522 (1986); Riechmann et al., Nature 332:323 (1988); Verhoeyen et al., Science 239:1534 (1988)), Sims et al., J. Immunol. 151: 2296 (1993); Chothia and Lesk, J. Mol. Biol. 196:901 (1987), Carter et al., Proc. Natl. Acad. Sci. U.S.A. 89:4285 (1992); Presta et al., J. Immunol. 151:2623 (1993), Патентах США под номерами 5639641, 5723323, 5976862, 5824514, 5817483, 5814476, 5763192, 5723323, 5766886, 5714352, 6204023, 6180370, 5693762, 5530101, 5585089, 5225539, 4816567, PCT/: US 98/16280, US 96/18978, US 91/09630, US 91/05939, US 94/01234, GB 89/01334, GB 91/01134, GB 92/01755, WO 90/14443, WO 90/14424, WO 90/14430, ЕР 229246, 7557189, 7538195 и 7342110, причем каждый источник включен во всей полноте в настоящий документ посредством ссылки, включая упомянутые в них источники.
[0135] В определенных альтернативных вариантах воплощения антитело против FOLR1 является человеческим антителом. Человеческие антитела могут быть прямо получены с использованием различных техник, известных в данной области техники. Иммортализованные человеческие В-лимфоциты иммунизированы in vitro или выделены от иммунизированого индивидуума, который образует антитело против антигена-мишени (See, e.g., Cole et al., Monoclonal Antibodies and Cancer Therapy, Alan R. Liss, p.77 (1985); Boemer et al., 1991, J. Immunol., 147 (1):86-95; и Патент США 5750373). Также человеческое антитело может быть выбрано из фаговой библиотеки, в которой экспрессируются человеческие антитела, например, согласно Vaughan et al., 1996, Nat. Biotech., 14:309-314, Sheets et al., 1998, Proc. Nat’1. Acad. Sci., 95:6157-6162, Hoogenboom и Winter, 1991, J. Mol. BioL, 227:381, и Marks et al., 1991, J. Mol. Biol., 222:581). Техники получения и использования фаговых библиотек антител также представлены в патентах США под номерами 5969108, 6172197, 5885793, 6521404, 6544731, 6555313, 6582915, 6593081, 6300064, 6653068, 6706484 и 7264963 и Rothe et al., 2007, J. Mol. Bio., doi:10.1016/j.jmb.2007.12.018 (каждый источник включен во всей полноте путем ссылки). Также в данной области техники известны стратегии созревания аффинности и перетасовки цепей (Marks et al., 1992, Bio/Technology 10:779-783, включено во всей полноте путем ссылки), которые могут использоваться для получения высокоаффинных человеческих антител.
[0136] Гуманизированные антитела также могут быть получены в трансгенных мышах, содержащих локусы человеческих иммуноглобулинов, которые после иммунизации способны производить полный репертуар человеческих антител в отсутствие эндогенной продукции иммуноглобулина. Этот подход описан в патентах США 5545807, 5545806, 5569825, 5625126, 5633425 и 5661016.
[0137] Изобретение также охватывает биспецифические антитела, которые специфически распознают человеческий рецептор фолиевой кислоты 1. Биспецифические антитела - антитела, которые способны специфически распознавать и связываться с по меньшей мере двумя различными эпитопами. Различные эпитопы могут находиться или в одной и той же молекуле (например, в человеческом рецепторе фолиевой кислоты 1), или в разных молекулах, к примеру, антитела могут специфически распознавать и связываться с человеческим рецептором фолиевой кислоты 1, а также, к примеру, 1) с эффекторной молекулой лейкоцита, например, Т-клеточным рецептором (например, CD3) или Fc-рецептором (например, CD64, CD32 или CD 16) или 2) с цитотоксическим агентом, что детально описано ниже.
[0138] Примерные биспецифические антитела могут связываться с двумя различными эпитопами, по меньшей мере один из которых происходит от полипептида по изобретению. Альтернативно анти-антигенное плечо молекулы иммуноглобулина может быть комбинировано с плечом, связывающимся с триггерной молекулой лейкоцита, например, Т-клеточной рецепторной молекулой (например, CD2, CD3, CD28 или В7) либо с Fc-рецепторами к IgG, так, чтобы оказывать направленное действие на механизмы клеточной защиты клетки, экспрессирующей конкретный антиген. Биспецифические антитела также могут использоваться для локализации цитотоксических агентов у клеток, экспрессирующих конкретный антиген. Данные антитела обладают антиген-связывающим плечом и плечом, связывающим цитотоксический агент или радионуклидный хелатор, например, EOTUBE, DPTA, DOTA или ТЕТА. Техники получения биспецифических антител хорошо известны в данной области техники (Millstein et al., 1983, Nature 305:537-539; Brennan et al., 1985, Science 229:81; Suresh et al, 1986, Methods in Enzymol. 121:120; Traunecker et al., 1991, EMBO J. 10:3655-3659; Shalaby et al., 1992, J. Exp. Med. 175:217-225; Kostelny et al., 1992, J. Immunol. 148:1547-1553; Gruber et al., 1994, J. Immunol. 152:5368; патент США 5731168). Также охватываются антитела с более чем двумя валентностями. К примеру, могут быть получены триспецифические антитела (Tutt et al., J. Immunol. 147:60 (1991)). Таким образом, в определенных вариантах воплощения антитела против FOLR1 мультиспецифичны.
[0139] В определенных вариантах воплощения фрагмент антитела предлагается для повышения проникновения в опухоль. Для получения фрагментов антител известны различные техники. Традиционно подобные фрагменты получали посредством протеолитического расщепления целых антител (см, например, Morimoto et al., 1993, Journal of Biochemical and Biophysical Methods 24:107-117; Brennan et al., 1985, Science, 229:81). В определенных вариантах воплощения фрагменты антител получают рекомбинантными способами. Фрагменты Fab, Fv и scFv могут быть экспрессированы и секретированы из Е. coli или иных клеток-хозяев, что позволяет выделять большие количества данных фрагментов. Подобные фрагменты антител могут быть выделены из библиотек антител фагов, обсуждавшихся выше. К примеру, фрагмент антитела может являться линейным антителом, описанным в патенте США 5641870, атакже может быть моноспецифическим или биспецифическим. Иные техники получения фрагментов антител очевидны опытному специалисту.
[0140] Техники могут быть адаптированы, согласно настоящему изобретению, для получения одноцепочечных антител, специфических к человеческому рецептору фолиевой кислоты 1 (см. патент США №4946778). Помимо этого, способы могут быть адаптированы для конструирования библиотек экспрессии Fab (Huse, et al., Science 246:1275-1281 (1989)) для быстрой и эффективной идентификации моноклональных Fab-фрагментов с желаемой специфичностью к рецептору фолиевой кислоты 1 либо их производных, фрагментов или гомологов. Фрагменты антител могут быть получены способами, известными в данной области техники, включая, но не ограничиваясь перечисленным: (а) фрагмент F(ab’)2, полученный при расщеплении молекулы антитела пепсином; (б) фрагмент Fab, образованный восстановлением дисульфидных мостиков фрагмента F(ab’)2, (в) фрагмент Fab, полученный обработкой молекулы антитела папином и восстановителем, и (г) фрагменты Fv.
[0141] Помимо этого, может быть желательным, особенно - в случае фрагментов антител, модифицировать антитело, чтобы увеличить его период полужизни в сыворотке. Это может быть достигнуто, к примеру, внедрением эпитопа связывания спасательного рецептора во фрагмент антитела мутированием соответствующейобласти фрагмента антитела или внедрением эпитопа в пептидный тег, который затем сливается с фрагментом антитела на любом конце или всередине (например, ДНК-синтезом или пептидным синтезом).
[0142] Настоящим изобретением также охватываются гетероконъюгатные антитела. Гетероконъюгатные антитела составлены двумя ковалентно связанными антителами. Подобные антитела были предложены для нацеливания иммунных клеток на нежелательные клетки (патент США №4676980). Предполагается, что антитела могут быть приготовлены in vitro способами, известными в синтетической химии белков, включая способы, в которых применяются перекрестносшивающие агенты. К примеру, иммунотоксины могут быть сконструированы с использованием дисульфидной обменной реакции или путем образования тиоэфирной связи. Примерами реактивов, пригодных для этой цели, служат иминотиолят и метил-4-меркаптобутиримидат.
[0143] Для целей настоящего изобретения следует отметить, что модифицированные антитела могут содержать любой тип вариабельнойобласти, который предлагается для связывания антитела с полипептидами человеческого FOLR1. В этой связи вариабельнаяобласть может содержать или может происходить от любого типа млекопитающего, у которого может быть индуцирован гуморальный ответ и могут быть образованы иммуноглобулины против желательного ассоциированного с опухолью антигена. В силу этого вариабельнаяобласть модифицированных антител может, к примеру, происходить от человека, мыши, нечеловекообразных приматов (например, яванских обезьян, макаков и т.д.) либо волков. В некоторых вариантах воплощения и вариабельная, и константная области модифицированных иммуноглобулинов являются человеческими. В иных вариантах воплощения вариабельные области сравнимых антител (обычно происходящих из нечеловеческих источников) могут быть сконструированы или специфически приспособлены так, чтобы улучшить связывающую способность или понизить иммуногенность молекулы. В этой связи вариабельные области, используемые в настоящем изобретении, могут быть гуманизированы или изменены иным образом посредством внедрения импортируемых аминокислотных последовательностей.
[0144] В определенных вариантах воплощения вариабельные домены и в тяжелой, и в легкой цепях изменены по меньшей мере частичной заменой одной или более областей, определяющих комплементарность, и, при необходимости, заменой каркаснойобласти и изменением последовательности. Хотя определяющие комплементарность области могут происходить от антитела того же класса или даже подкласса, что и антитело, от которого происходит каркасная область, предусматривается, что определяющие комплементарность области будут происходить от антитела иного класса и, в некоторых вариантах воплощения, от антитела другого вида. Может не быть необходимо заменять все определяющие комплементарность области полной определяющей комплементарность областью от донорской вариабельнойобласти, чтобы передать антиген-связывающую способность одного вариабельного домена другому. Вместо этого может быть необходимо только перенести те остатки, которые необходимы для поддержания активности антиген-связывающего сайта. Пояснения представлены в патентах США под номерами 5585089, 5693761 и 5693762; в компетенции специалиста в данной области техники проводить обычные эксперименты или исследования и тесты ошибок для получения функционального антитела с пониженной иммуногенностью.
[0145] Несмотря на изменения в вариабельнойобласти, специалисту в данной области техники понятно, что модифицированные антитела по настоящему изобретению охватывают антитела (например, полноразмерные антитела или их иммунореактивные фрагменты), в которых по меньшей мере часть одного или более константных доменов была удалена или иным образом изменена для получения желаемых биохимических характеристик, например, повышения локализации опухолии или понижения времени полужизни в сыворотке в сравнении с антителом с приблизительно такой же иммуногенностью, обладающим нативной или неизмененной константнойобластью. В некоторых вариантах воплощения константнаяобласть модифицированного антитела содержит человеческую константнуюобласть. Модификации константнойобласти, совместимые с данным изобретением, включают вставки, делеции или замещения одной или более аминокислот в одном или более доменов. Иными словами, модифицированные антитела, описанные здесь, могут содержать изменения или модификации одного или более из трех константных доменов тяжелой цепи (СН1, СН2 или СН3) и/или константных доменов легкой цепи (CL). В некторых вариантах воплощения подразумеваются модифицированные константные области, в которых один или более доменов частично или полностью удалены. В некоторыхвариантах воплощения модифицированные антитела содержат конструкции или варианты с удаленными доменами, в которых был полностью удален домен СН2 (ΔСН2-конструкции). В некоторых вариантах воплощения отсутствующий константный домен замещен коротким аминокислотным спейсером (например, с 10 остатками), который обеспечивает некоторую молекулярную гибкость, обычно придаваемую отсутствующей константнойобластью.
[0146] Помимо конфигурирования, в данной области техники известно, что константнаяобласть опосредует некоторые эффекторные функции. К примеру, связывание С 1-компонента комплемента с антителом запускает систему комплемента. Активация комплемента важна для опсонизации и лизиса клеточных патогенов. Активация комплемента также стимулирует воспалительный ответ и может быть вовлечена в аутоиммунную гиперчувствительность. Помимо этого, антитела связываются через Fc-область посредством Fc-рецепторного сайта в Fc-области, связывающегося с Fc-рецептором (FcR) на клетке. Имеется ряд Fc-рецепторов, специфических для различных классов антител, включая IgG (гамма-рецепторы), IgE (эта-рецепторы), IgA (альфа-рецепторы) и IgM (мю-рецепторы). Связывание антитела с Fc-рецепторами на клеточных поверхностях запускает множество важных и разнообразных биологических ответов, включая поглощение и расщепление покрытых антителом частиц, выведение иммунных комплексов, лизис покрытых антителом клеток клетками-киллерами (называемый антитело-зависимой клеточно-опосредованной цитотоксичностью или АЗКЦ), высвобождение воспалительных медиаторов, плацентарный перенос и контроль продукции иммуноглобулинов.
[0147] В определенных вариантах воплощения FOLR1-связывающие антитела обеспечивают измененные эффекторные функции, что, в свою очередь, влияет на биологический профиль вводимого антитела. К примеру, делеция или инактивация (через точечные мутации или иные способы) домена константнойобласти может уменьшать Fc-рецепторное связывание циркулирующего модифицированного антитела, повышая локализацию опухоли. В других случаях модифицирование константных областей, согласно изобретению, может изменять связывание с комплементом, уменьшая период полужизни в сыворотке и приводя к неспецифическому ассоциированию конъюгированного цитотоксина. Могут использоваться и иные модификации константнойобласти для удаления дисульфидных связей или олигосахаридных фрагментов, повышающие локализацию вследствие повышения антигенной специфичности или гибкости антитела. Аналогично модификации константнойобласти, в соответствии с настоящим изобретением, могут быть легко сделаны известными биохимическими техниками или техниками молекулярного инжиниринга, известными опытному специалисту.
[0148] В определенных вариантах воплощения FOLR1-связывающий агент, который является антителом, не обладает одной или более эффекторных функций. К примеру, в некоторых вариантах воплощения антитело не проявляет антитело-зависимой клеточной цитотоксичности (АЗКЦ) и/или не проявляет комплемент-зависимой цитотоксичности (КЗЦ). В определенных вариантах воплощения антитело не связывается с Fc-рецептором и/или факторами комплемента. В определенных вариантах воплощения антитело не обладает эффекторной функцией.
[0149] Следует заметить, что в некоторых вариантах воплощения модифицированные антитела могут быть сконструированы таким образом, что СН3-домен слит непосредственно с шарнирнойобластью соответствующих модифицированных антител. В других конструкциях может быть желательно внедрять пептидный спейсер между шарнирнойобластью и модифицированными доменами СН2 и/или СН3. К примеру, совместимые конструкции могут экспрессироваться с удаленным СН2-доменом и сохраненным СН3-доменом (модифицированным или немодифицированным), присоединенным к шарнирнойобласти через спейсер, содержащий 5-20 аминокислот. Подобный спейсер может быть добавлен, к примеру, для того, чтобы регуляторные элементы константного домена оставались свободными и доступными или для того, чтобы шарнирнаяобласть оставалась гибкой. Однако, следует заметить, что аминокислотные спейсеры могут в некоторых случаях быть иммуногенными и вызывать нежелательный иммунный ответ против конструкции. Соответственно, в определенных вариантах воплощения любой спейсер, добавленный к конструкции, будет относительно неиммуногенным или даже полностью неиммуногенным, чтобы обеспечить желательные биохимические свойства модифицированных антител.
[0150] Помимо делеции целых доменов константных областей, следует принять во внимание, что антитела по настоящему изобретению могут быть получены частичной делецией или заменой нескольких или даже одной аминокислоты. К примеру, мутация одной аминокислоты в выбранных областях СН2-домена может быть достаточна для частичного уменьшения Fc-связывания и, как следствие, для повышения локализации в опухоль. Аналогично может быть желательным удалить ту часть одного или более доменов константных областей, которая контролирует модулируемую эффекторную функцию (например, C1Q-связывание с комплементом). Подобные частичные делеции константных областей могут улучшать выбранные характеристики антитела (период полужизни в сыворотке), не затрагивая иные желательные функции, ассоциированные с доменом константнойобласти субъекта. Более того, как показано выше, константные области предлагаемых антител могут быть модифицированы посредством мутирования или замещения одной или более аминокислот, улучшая профиль полученной конструкции. В этой связи возможно нарушить активность, обеспечиваемую сохраненным сайтом связывания (например, Fc-связывание), частично сохранив конфигурацию и иммуногенный профиль модифицированного антитела. Некоторые воплощения могут включать добавление одной или более аминокислот в константнуюобласть для улучшения желаемых характеристик, например, для понижения или повышения эффекторной функции или для присоединения большего количества цитотоксинов или углеводов. В таких вариантах воплощения может быть желательным внедрять или реплицировать специфические последовательности, происходящие из выбранных доменов константных областей.
[0151] Настоящее изобретение, помимо этого, охватывает варианты и эквиваленты, которые в значительной степени гомологичны химерным, гуманизированным и человеческим антителам или их фрагментам, описанным далее. Они могут содержать, к примеру, мутации консервативного замещения, то есть замещение одной или более аминокислот на родственные. К примеру, консервативное замещение относится к замещению аминокислоты на другую аминокислоту, относящуюся к тому же классу, например, одну кислотную аминокислоту на другую кислотную аминокислоту, одну основную аминокислоту на другую основную аминокислоту или одну нейтральную аминокислоту на другую нейтральную аминокислоту. То, что понимается под консервативным замещением аминокислоты, хорошо известно в данной области техники.
[0152] Полипептиды по настоящему изобретению могут быть рекомбинантными полипептидами, натуральными полипептидами или синтетическими полипептидами, содержащими антитело против человеческого FOLR1 или его фрагмент. Некоторые аминокислотные последовательности по изобретению могут вариьроваться без существенного влияния на структуру и функцию белка. Таким образом, изобретение, помимо этого, включает вариации полипептидов с выраженной активностью или вариации, содержащие области антитела против белка человеческого рецептора фолиевой кислоты. Такие мутанты содержат делеции, вставки, инверсии, повторы и типовые замены.
[0153] Полипептиды и аналоги могут быть далее модифицированы с внедрением дополнительных химических групп, которые обычно не входят в состав белков. Эти дериватизированные группы могут улучшать растворимость, биологический период полужизни или абсорбцию белка. Группы также могут понижать или устранятьнежелательные побочные эффекты белков и т.п. Обзор таких групп представлен в REMINGTON’SPHARMACEUTICALSCIENCES, 20thed., MackPublishingCo., Easton, PA (2000).
[0154] Изолированные Полипептиды, описанные здесь, могут изготавливаться любым подходящим способом, известным в данной области техники. Такие способы варьируются от способов прямого синтеза белка до конструирования ДНК-последовательности, кодирующей изолированные полипептидные последовательности и экспрессирующей эти последовательности в подходящем трансформированном носителе. В некоторых вариантах воплощения ДНК-последовательность конструируется по рекомбинантной технологии с выделением или синтезом ДНК-последовательности, кодирующей интересующий белок дикого типа. Необязательно последовательность может быть мутагенизирована сайт-специфическим мутагенезом для получения ее функциональных аналогов. См., например, Zoeller et al., Proc. Nat’l. Acad. Sci. USA 81:5662-5066 (1984) и патент США №4588585.
[0155] В некоторых вариантах воплощения ДНК-последовательность, кодирующая интересующий полипептид, конструируется химическим синтезом с использованием олигонуклеотидного синтезатора. Такие олигонуклеотиды могут быть разработаны на основании аминокислотной последовательности желаемого полипептида с выбором тех кодонов, которые предпочтительны у клетки-хозяина, в которой производится интересующий рекомбинантный полипептид. Могут использоваться стандартные способы синтеза изолированной полинуклеотидной последовательности, кодирующей интересующий изолированный полипептид. К примеру, для конструирования обратно-транслируемого гена может использоваться полная аминокислотная последовательность. Помимо этого, может быть синтезирован ДНК-олигомер, содержащий нуклеотидную последовательность, кодирующую отдельный изолированный полипептид. К примеру, могут быть синтезированы, а затем связаны несколько малых олигонуклеотидов, кодирующих части желаемого полипептида. Индивидуальные олигонуклеотиды, как правило, содержат 5’- или 3’-липкие концы для комплементарного соединения.
[0156] После сборки (синтезом, сайт-направленным мутагенезом или иным способом) полинуклеотидные последовательности, кодирующие конкретный интересующий полипептид, будут внедрены в вектор экспрессии и оперативно связаны с последовательностью контроля экспрессии, необходимой для экспрессии белка в желаемом хозяине. Правильность сборки может быть подтверждена секвенированием нуклеотидной последовательности, рестрикционным картированием и экспрессией биологически активного полипептида в подходящем хозяине. Как известно в данной области техники, чтобы достичь высоких уровней экспрессии трансфицированного гена у хозяина, ген должен быть оперативно связан с последовательностями контроля транскрипции и трансляции, функциональных у выбранного хозяина.
[0157] В определенных вариантах воплощения для амплификации и экспрессии ДНК, кодирующей антитела против человеческого FOLR1 или их фрагменты, используются рекомбинантные векторы экспрессии. Рекомбинантные векторы экспрессии реплицируемые ДНК-конструкции, содержащие синтетические или полученные из кДНК фрагменты ДНК, кодирующие полипептидную цепь антитела против FOLR1 или его фрагмент, оперативно связанные с подходящими транскрипционными или трансляционными регуляторными элементами, происходящими из генов млекопитающих, микробов, вирусов или насекомых. Транскрипционная единица, как правило, содержит объединение (1) генетического элемента или элементов, обладающих регуляторной ролью при экспрессии гена, к примеру, транскрипционные промоторы или энхансеры, (2) структурной или кодирующей последовательности, транскрибируемой в мРНК и транслируемой в белок, и (3) подходящих последовательностей запуска и останова транскрипции и трансляции, как детально описано ниже. Подобные регуляторные элементы могут включать операторную последовательность для контроля транскрипции. Дополнительно могут предусматриваться: способность к репликации в хозяине, обусловленная, как правило, источником репликации, и селекционный ген для облегчения распознавания трансформантов. ДНК-области оперативно связаны, если они функционально относятся друг к другу. К примеру, ДНК сигнального пептида (секреторного лидера) оперативно связана с ДНК полипептида, если она экспрессируется в виде прекурсора, который участвует в секреции полипептида; промотор оперативно связан с кодирующей последовательностью, если он контролирует транскрипцию последовательности; либо рибосомный связывающий сайт оперативно связан с кодирующей последовательностью, если он расположен таким образом, чтобы позволять трансляцию. Структурные элементы, предназначенные для использования в системе экспрессии дрожжей, включают лидерную последовательность, позволяющую внеклеточную секрецию клеткой-хозяином транслируемого белка. Альтернативно, если рекомбинантный белок экспрессируется без лидерной или транспортной последовательностей, он может содержать N-терминальный остаток метионина. Этот остаток может затем отщепляться от экспрессируемого рекомбинантного белка для получения конечного продукта.
[0158] Выбор последовательности, контролирующей экспрессию, и вектора экспрессии зависит от выбора хозяина. Может использоваться большое количество комбинаций хозяев и векторов экспрессии. Пригодные векторы экспрессии для эукариотных хозяев включают, к примеру, векторы, содержащие контрольные последовательности экспрессии из SV40, бычьего вируса папилломы, аденовируса и цитомегаловируса. Пригодные векторы экспрессии в бактериальных хозяевах включают известные бактериальные плазмиды, например, плазмиды из Esherichia coli, включая pCR 1, pBR322, pMB9 и их производные, более широкий интервал плазмид, например, М13 и одноцепочечные ДНК нитчатых фагов.
[0159] Подходящие клетки-хозева для экспрессии FOLR1-связывающего полипептида или антитела (или FOLR1-белка для использования в качестве антигена) включают клетки прокариотов, дрожжей, насекомых и клетки высших эукариотов под контролем соответствующих промоторов. Прокариоты включают грамотрицательные и грамположительные организмы, к примеру, Е. coli или бациллы. Высшие эукариотные клетки включают установленные линии клеток млекопитающих, описанные выше. Также могут использоваться бесклеточные системы трансляции. Подходящие векторы клонирования и экспрессии для использования с клетками-хозяевами бактерий, грибов, дрожжей, млекопитающих были описаны в источнике Pouwels et al. (Cloning Vectors: A Laboratory Manual, Elsevier, N.Y., 1985), сущность которого включена в настоящий документ во всей полноте путем ссылки. Дополнительная информация о способах получения белков, включая получение антител, доступна, к примеру, в патентной заявке США №2008/0187954, патентах СШАпод номерами 6413746 и 6660501, а также в международной патентной заявке №WO 04009823, каждая из которых включена в настоящий документ во всей полноте путем ссылки.
[0160] Для экспрессии рекомбинантного белка также могут успешно использоваться различные культуры клеток млекопитающих или насекомых. Экспрессия рекомбинантных белков в клетках млекопитающих может проводиться потому, что такие белки подвергаются правильному фолдингу, модифицированию и полностью функциональны. Примерами подходящих клеток-хозяев млекопитающих служат линии НЕК-293 и HEK-293Т, COS-7 клеток почки обезьяны, описанные Gluzman (Cell 23:175, 1981), другие клеточные линии, включая, к примеру, L-клетки, С 127, ЗТЗ, клетки яичника китайского хомячка (СНО), клеточные линии HeLa и ВНК. Векторы экспрессии у млекопитающих могут содержать нетранскрибируемые элементы, например, точку начала репликации, подходящие промотор и энхансер, связанные с экспрессируемым геном, другие 5’ или 3’ фланкирующие нетранскрибируемые последовательности и 5’ или 3’ нетранслируемые последовательности, например, необходимые сайты связывания с рибосомами, сайт полиаденилирования, донорный и акцепторный сайты сплайсинга и транскрипционные последовательности останова. Обзор бакуловирусных систем производства гетерологических белков в клетках насекомых представлен в Luckow и Summers, Bio/Technology 6:47 (1988).
[0161] Белки, продуцируемые трансформированным хозяином, могут быть очищены любым подходящим способом. Такие стандартные способы включают хроматографию (например, ионный обмен, аффинную и эксклюзионную колонную хроматографию), центрифугирование, дифференциальную растворимость или иные стандартные техники очистки белков. Для облегчения очистки в аффинной колонке к белку могут быть присоединены аффинные метки, например, гексагистидин, связывающий мальтозу домен, поверхностная последовательность вируса гриппа и глутатион-3-трансфераза. Изолированные белки могут быть исследованы физическими способами с использованием таких техник, как протеолиз, ядерный магнитный резонанс и рентгеновская кристаллография.
[0162] К примеру, супернатанты из систем, выделяющих рекомбинантный белок в питательную среду, могут быть вначале сконцентрированы с использованием доступного в продаже фильтра для концентрации белков, к примеру, установок ультрафильтрации Amicon или Millipore Pellicon. После этапа концентрации концентрат может быть нанесен на подходящий матрикс для очистки. Альтернативно может использоваться анионообменная смола, например, матрикс или субстрат со свободными диэтиламиноэтильными группами (ДЭАЭ). Матриксы могут быть акриламидного, агарозного, декстранового, целлюлозного или иного типа, обычно используемого при очистке белков. Альтернативно может применяться этап катионного обмена. Подходящие катионообменные агенты включают различные нерастворимые матриксы, содержащие сульфопропильные или карбоксиметильные группы. Наконец, для дальнейшей очистки FOLR1 -связывающего агента может применяться один или более этапов высокоэффективной жидкостной хроматографии с обратными фазами (ОФ-ВЭЖХ) с использованием гидрофобной ОФ-ВЭЖХ среды, например, силикагеля со свободными метальными или иными алифатическими группами. Некоторые или все из изложенных выше этапов очистки в различных комбинациях также могут применяться для получения гомогенного рекомбинантного белка.
[0163] Рекомбинантный белок, продуцируемый в бактериальной культуре, может быть выделен, к примеру, первичной экстракцией из клеточных гранул с последующими одним и более этапов концентрирования, высаливания, ионного обмена в водном растворе или эксклюзионной хроматографии. Для окончательной очистки может применяться высокоэффективная жидкостная хроматография (ВЭЖХ). Микробные клетки, участвующие в экспрессии рекомбинантного белка могут быть разрушены любым удобным способом, включая циклическое замораживание-оттаивание, разрушение ультразвуком, механическое разрушение или использование агентов, расщепляющих клетки.
[0164] Известные в данной области техники способы очистки антител и иных белков также включают способы, описанные в патентных заявках США №2008/0312425, 2008/0177048 и 2009/0187005, каждая из которых включена в настоящий документ во всей полноте посредством ссылки.
[0165] В определенных вариантах воплощения FOLR1-связывающий агент - полипептид, не являющийся антителом. В данной области техники известно множество способов идентифицирования и продуцирования полипептидов, не являющихся антителами, но связывающихся с высокой аффиностью с белками-мишенями. См., например, Skerra, Curr. Opin. Biotechnol., 18:295-304 (2007), Hosse et al., Protein Science, 15:14-27 (2006), Gill et al., Curr. Opin. BiotechnoL, 17:653-658 (2006), Nygren, FEBS J., 275:2668-76 (2008) и Skerra, FEBS J., 27 5:2677-S3 (2008), каждый источник включен в настоящий документ во всей полноте посредством ссылки. В определенных вариантах воплощения для идентификации и продуцирования FOLR1-связывающего полипептида применяют технологию фагового дисплея. В определенных вариантах воплощения полипептид содержит каркасный белок, относящийся к типу, выбранному из группы, состоящей из белка А, липокалина, домена фрибронектина, консенсусного повторного домена анкирина и тиоредоксина.
[0166] В некоторых вариантах воплощения агент является небелковой молекулой. В некоторых вариантах воплощения агент является малой молекулой. Комбинаторные химические библиотеки и техники, подходящие для идентификации небелковых FOLR1-связывающих агентов, известны специалистам в данной области техники. См., например, Kennedy et al., J. Comb. Chem, 10:345-354 (2008), Dolle et al, J. Comb. Chem., 9:855-902 (2007) и Bhattacharyya, Curr. Med. Chem., 8:1383-404 (2001), которые включены в настоящий документ во всей полноте посредством ссылки. Еще в некоторых вариантах воплощения агент является углеводом, гликозаминогликаном, гликопротеином или протеогликаном.
[0167] В некоторых вариантах воплощения агент является аптамером нуклеиновой кислоты. Аптамеры это полинуклеотидные молекулы, выбранные (например, из случайных или мутагенизированных пулов) на основании их способности связываться с другой молекулой. В некоторых вариантах воплощения аптамер содержит ДНК-полинуклеотид. В определенных альтернативных вариантах воплощения аптамер содержит РНК-полинуклеотид. В определеных вариантах воплощения аптамер содержит один или более модифицированных остатков нуклеиновых кислот. Способы получения и скрининга аптамеров нуклеиновых кислот на связывание с белками хорошо известны в данной области техники. См., например, патент США №5270163, патент США №5683867, патент США №5763595, патент США №6344321, патент США №7368236, патент США №5582981, патент США №5756291, патент США №5840867, патент США №7312325, патент США №7329742, Международную Патентную Публикацию №WO 02/077262, Международную Патентную Публикацию №WO 03/070984, Патентную Заявку США №2005/0239134, Патентную Заявку США №2005/0124565 и Патентную Заявку США №2008/0227735; каждый источник включен в настоящий документ во всей полноте путем ссылки.
III. Иммуноконъюгаты
[0168] Настоящее изобретение также направлено на конъюгаты (также называемые здесь иммуноконъюгатами), содержащие антитела против FOLR1, фрагменты антител, функциональные эквиваленты, улучшенные антитела и их аспекты, описанные здесь, связанные или конъюгированные с цитотоксином (препаратом) или его пролекарством. Таким образом, в определенном варианте воплощения в изобретении предлагается иммуноконъюгат, содержащий гуманизированное антитело или его антиген-связывающий фрагмент, которые специфически связываются с человеческим рецептором фолиевой кислоты 1, причем антитело содержит: (a) CDR1 тяжелой цепи, содержащую GYFMN (SEQ ID NO:1); CDR2 тяжелой цепи, содержащую RIHPYDGDTFYNQXaa1FXaa2Xaa3 (SEQ ID NO:56); и CDR3 тяжелой цепи, содержащую YDGSRAMDY (SEQ ID NO:3); и (б) CDR1 легкой цепи, содержащую KASQSVSFAGTSLMH (SEQ ID NO:7); CDR2 легкой цепи, содержащую RASNLEA (SEQ ID NO:8); CDR3 легкой цепи, содержащую QQSREYPYT (SEQ ID NO:9); где Xaa1 выбран из K, Q, Н и R; Хаа2 выбран из Q, Н, N и R; и Хаа3 выбран из G, Е, Т, S, А и V. В определенных вариантах воплощения антитело является антителом huMov19, которое является описанным выше антителом, содержащим CDR2 тяжелой цепи RIHPYDGDTFYNQKFQG (SEQ ID NO:2). В иных вариантах воплощения антитело является FR1-21 и содержит (а) CDR1 тяжелой цепи, содержащую SSYGMS (SEQ ID NO:30); CDR2 тяжелой цепи, содержащую TISSGGSYTY (SEQ ID NO:31); и/или CDR3 тяжелой цепи, содержащую DGEGGLYAMDY (SEQ ID NO:32); и (б) CDR1 легкой цепи, содержащую KASDHINNWLA (SEQ ID NO:27); CDR2 легкой цепи, содержащую GATSLET (SEQ ID NO:28); и CDR3 легкой цепи, содержащую QQYWSTPFT (SEQ ID NO:29). В иных вариантах воплощения антитело является FR1-48 и содержит: (а) CDR1 тяжелой цепи, содержащую TNYWMQ (SEQ ID NO:60); CDR2 тяжелой цепи, содержащую AIYPGNGDSR (SEQ ID NO:61); и/или CDR3 тяжелой цепи, содержащую RDGNYAAY (SEQ ID NO:62); и/или (б) CDR1 легкой цепи, содержащую RASENIYSNLA (SEQ ID NO:57); CDR2 легкой цепи, содержащую AATNLAD (SEQ ID NO:58); и CDR3 легкой цепи, содержащую QHFWASPYT (SEQ ID NO:59). В иных вариантах воплощения антитело является FR1-49 и содержит: (a) CDR1 тяжелой цепи, содержащую TNYWMY (SEQ ID NO:66); CDR2 тяжелой цепи, содержащую AIYPGNSDTT (SEQ ID NO:67); и/или CDR3 тяжелой цепи, содержащую RHDYGAMDY (SEQ ID NO:68); и/или (б) CDR1 легкой цепи, содержащую RASENIYTNLA (SEQ ID NO:63); CDR2 легкой цепи, содержащую TASNLAD (SEQ ID NO:64); и CDR3 легкой цепи, содержащую QHFWVSPYT (SEQ ID NO:65). В иных вариантах воплощения антитело является FR1-57 и содержит: (а) CDR1 тяжелой цепи, содержащую SSFGMH (SEQ ID NO:72); CDR2 тяжелой цепи, содержащую YISSGSSTIS (SEQ ID NO:73); и/или CDR3 тяжелой цепи, содержащую EAYGSSMEY (SEQ ID NO:74); и/или (б) CDR1 легкой цепи, содержащую RASQNINNNLH (SEQ ID NO:69); CDR2 легкой цепи, содержащую YVSQSVS (SEQ ID NO:70); и CDR3 легкой цепи, содержащую QQSNSWPHYT (SEQ ID NO:71). В еще одном варианте воплощения антитело является FR1-65 и содержит: (а) CDR1 тяжелой цепи, содержащую TSYTMH (SEQ ID NO:78); CDR2 тяжелой цепи, содержащую YINPISGYTN (SEQ ID NO:79); и/или CDR3 тяжелой цепи, содержащую GGAYGRKPMDY (SEQ ID NO:80); и/или (б) CDR1 легкой цепи, содержащую KASQNVGPNVA (SEQ ID NO:75); CDR2 легкой цепи, содержащую SASYRYS (SEQ ID NO:76); и CDR3 легкой цепи, содержащую QQYNSYPYT (SEQ ID NO:77).
[0169] Подходящие препараты и их пролекарства известны в данной области техники. В определенных вариантах воплощения препараты или пролекарства являются цитотоксическими агентами. Цитотоксический агент, используемый в цитотоксическом конъюгате согласно настоящему изобретению, может быть любым соединением, приводящим клетку к гибели или индуцирующим гибель клетки, или некоторым образом уменьшающим жизнеспособность клетки, и может включать, к примеру, майтансиноиды и аналоги майтансиноидов, бензодиазепины, таксоиды, СС-1065 и аналоги СС-1065, дуокармицин и аналоги дуокармицина, энедиины, например, калихеамицины, доластатин и аналоги доластатина, включая ауристатины, производные томаимицина, производные лептомицина, метотрексат, цисплатин, карбоплатин, даунорубицин, доксорубицин, винкристин, винбластин, мелфалан, митомицин С, хлорамбуцил и морфолино-доксорубицин. В определенных вариантах воплощения цитотоксические агенты являются майтансиноидами и аналогами майтансиноидов.
[0170] Такие конъюгаты могут быть получены с использованием сшивающей группы, чтобы соединить препарат либо его пролекарство с антителом или его функциональным эквивалентом. Подходящие сшивающие группы хорошо известны в данной области техники и включают, к примеру, дисульфидные группы, тиоэфирные группы, кислото-лабильные группы, фотолабильные группы, пептидаза-лабильные группы и эстераза-лабильные группы.
[0171] Препарат или его пролекарство могут быть, например, соединены с антителом против FOLR1 или его фрагментом через дисульфидную связь. Сшивающая молекула или перекрестносшивающий агент содержат реактивную химическую группу, которая может взаимодействовать с антителом против FOLR1 или его фрагментом. В определенных вариантах воплощения реактивными химическими группами для взаимодействия с агентом, связывающимся с клеткой, являются N-сукцинимидиловые сложные эфиры и N-сульфосукцинимидиловые сложные эфиры. Дополнительно сшивающая молекула содержит реактивную химическую группу, в некоторых воплощениях дитиопиридильную группу, способную к взаимодействию с препаратом с образованием дисульфидной связи. В определенных вариантах воплощения сшивающие молекулы включают, к примеру, N-сукцинимидил 3-(2-пиридилдитио) пропионат (SPDP) (см., например, Carlsson et al., Biochem. J., 173: 723-737 (1978)), N-сукцинимидил 4-(2-пиридилдитио)бутаноат (SPDB) (см., например, патент США №4563304), N-сукцинимидил 4-(2-пиридилдитио)2-сульфобутаноат (sulfo-SPDB) (см. публикацию США №20090274713), N-сукцинимидил 4-(2-пиридилдитио) пентаноат (SPP) (см., например, CAS 341498-08-6), 2-иминотиолан или уксусноянтарный ангидрид. К примеру, антитело или агент, связывающий клетку, может быть модифицирован перекрестносшивающими реагентами, и антитело или агент, связывающий клетку, содержащий свободные или защищенные тиоловые группы, затем взаимодействует с дисульфид- или тиол-содержащим майтансиноидом с образованием конъюгатов. Конъюгаты могут быть очищены хроматографией, включая, но не ограничиваясь перечисленным, ВЭЖХ, эксклюзионную, адсорбционную, ионообменную и аффинную хроматографию, либо фильтрацией в тангенциальном потоке. В определенных вариантах воплощения антитело против FOLR1 связано с цитотоксином через линкер SPDB или sulfo-SPDB. В определенном воплощении антитело huMov19 связано с цитотоксином через линкер SPDB или sulfo-SPDB.
[0172] В ином аспекте настоящего изобретения антитело против FOLR1 соединено с цитотоксическими препаратами через дисульфидные связи и полиэтиленгликолевый спейсер для увеличения активности, растворимости или эффективности иммуноконъюгата. Подобные расщепляемые гидрофильные линкеры описаны в WO 2009/0134976. Дополнительным преимуществом такого типа линкеров является желаемое высокое количество мономеров и минимальная агрегация конъюгатов антитело-препарат. В данном аспекте специфически рассматриваются конъюгаты агентов, связывающих клетки, и препаратов, соединенных через дисульфидную группу (-S-S-), несущие полиэтиленгликолевые спейсеры ((CH2CH2O)n=1-14) с узким интервалом нагрузки препаратом в 2-8, которые обладают относительной высокой активностью против опухолевых клеток и обладают желаемыми биохимическими свойствами, а именно -высоким выходом конъюгации и высоким содержанием мономера с минимальной агрегацией белка.
[0173] В данном аспекте специфически рассматривается конъюгат антитела против FOLR1 и препарата формулы (I) или конъюгат формулы (Г):


где:
А обозначает антитело против FOLR1 или его фрагмент;
С обозначает цитотоксин или препарат;
Х обозначает алифатическую, ароматическую или гетероциклическую единицу, присоединенную к агенту, связывающемуся с клеткой через тиоэфирную связь, амидную связь, карбаматную связь или эфирную связь;
Y обозначает алифатическую, ароматическую или гетероциклическую единицу, присоединенную к препарату через дисульфидную связь;
1 равно 0 или 1;
m является целым числом от 2 до 8; и
n является целым числом от 1 до 24.
В определенных вариантах воплощения m является целым числом от 2 до 6.
В определенных вариантах воплощения m является целым числом от 3 до 5.
[0174] В определенных вариантах воплощения n является целым числом от 2 до 8. Альтернативно, как показано, например, в патентах США под номерами 6441163 и 7368565, препарат вначале может быть модифицирован с внедрением реактивной сложноэфирной группы, способной взаимодействовать с агентом, связывающимся с клеткой. Взаимодействие данных препаратов, содержащих активированный сшивающий фрагмент, с агентом, связывающимся с клеткой - еще один метод получения конъюгата агента, связывающегося с клеткой, и препарата. Майтансиноиды также могут быть сшиты с антителом против FOLR1 или его фрагментом при помощи сшивающих групп ПЭГ, как описано, например, в патенте США 6716821. Данные нерасщепляемые ПЭГ-группы растворимы в воде и неводных растворителях и могут использоваться для соединения одного и более цитотоксических агентов с агентом, связывающимся с клеткой. Примерами ПЭГ-связывающих групп служат гетеробифункциональные ПЭГ-линкеры, реагирующие с цитотоксическими агентами и агентами, связывающимися с клеткой на противоположных концах линкеров - через функциональную сульфгидрильную или дисульфидную группу на одном конце и активную сложноэфирную группу на другом конце. В качестве общего примера синтеза цитотоксического конъюгата с использованием ПЭГ-линкерных групп, дается ссылка на патент США 6716821, который включен в настоящий документ во всей полноте путем ссылки. Синтез начинается со взаимодействия одного или более цитотоксических агентов, несущих реактивный ПЭГ-фрагмент с агентом, связывающимся с клеткой, что приводит к замещению терминальной активной сложноэфирной группы каждого реактивного ПЭГ-фрагмента на аминокислотный остаток агента, связывающегося с клеткой, с образованием цитотоксического конъюгата, содержащего один или более цитотоксических агентов, ковалентно связанных с агентом, связывающимся с клеткой через ПЭГ-линкерную группу. Альтернативно клеточное связывание может быть модифицировано бифункциональным ПЭГ-перекрестно-сшивающим агентом для введения реактивного дисульфидного фрагмента (например, пиридилдисульфида), который затем может быть обработан тиол-содержащим майтансиноидом с образованием конъюгата. В ином способе клеточное связывание может быть модифицировано бифункциональным ПЭГ-перекрестно-сшивающим агентом для введения тиолового фрагмента, который затем может быть обработан реактивным дисульфид-содержащим (например, пиридилдисульфид-содержащим) майтансиноидом с образованием конъюгата.
[0175] Также могут быть получены конъюгаты антитело-майтансиноид с нерасщепляемыми связями. Подобные перекрестно-сшивающие агенты описаны в данной области техники (см. Thermo Scientific Pierce Crosslinking Technical Handbook и публикацию США №2005/0169933) и включают, не ограничиваясь перечисленным, N-сукцинимидил-4-(малеимидометил) циклогексанкарбоксилат (SMCC), N-сукцинимидил-4-(N-малеидометил)-циклогексан-1-карбокси-(6-амидокапроат), который является «длинноцепочечным» аналогом SMCC (LC-SMCC), □-малеимидоундекановой кислоты N-сукцинимидиловый сложный эфир (KMUA), β-малеимидопропановой кислоты N-сукцинимидиловый сложный эфир (BMPS), □-малеимидобутановой кислоты N-сукцинимидиловый сложный эфир (GMBS), □-малеимидокапроновой кислоты N-гидроксисукцинимидиловый сложный эфир (EMCS), m-малеимидобензоил-N-гидроксисукцинимидиловый сложный эфир (MBS), N-(□-малеимидоацетокси)-сукцинимидный сложный эфир (AMAS), сукцинимидил-6-(□-малеимидопропионамидо)гексаноат (SMPH), N-сукцинимидил 4-(р-малеимидофенил)-бутират (SMPB) и N-(р-малеимидофенил)изоцианата (PMPI), N-сукцинимидил-4-(иодоацетил)-аминобензоат (SIAB), N-сукцинимидил иодоацетат (SIA), N-сукцинимидил бромацетат (SBA) и N-сукцинимидил 3-(бромацетамидо)пропионат (SBAP). В определенных вариантах воплощения антитело модифицировано перекрестносшивающими реагентами, например, сукцинимидил 4-(N-малеимидометил)-циклогексан-1-кабоксилатом (SMCC), сульфо-SMCC, малеимидобензоил-N-гидроксисукцинимидным сложным эфиром (MBS), сульфо-MBS или сукцинимидил-иодоацетатом, как описано в литературе, для внедрения 1-10 реактивных групп (Yoshitake et al, Eur. J. Biochem., 101:395-399 (1979); Hashida et al., J. Applied Biochem., 56-63 (1984); и Liu et al., Biochem., 18:690-697 (1979)). Модифицированное антитело затем взаимодействует с тиол-содержащим производным майтансиноида с получением конъюгата. Конъюгат может быть очищен путем гель-фильтрации через колонку Sephadex G25 или диализом, или фильтрацией в тангенциальном потоке. Модифицированные антитела обрабатывают тиол-содержащим майтансиноидом (1-2 молярных эквивалента/малеимидную группу), конъюгаты антитело-майтансиноид очищают гель-фильтрацией через колонку Sephadex G-25, хроматографией на керамической колонке с гидроксиапатитом, диализом или фильтрацией в тангенциальном потоке, или при помощи комбинации способов. Обычно к одному антителу присоединяется 1-10 майтансиноидов. Один способ заключается в модификации антител с сукцинимидил 4-(N-малеимидометил)-циклогексан-1-карбоксилатом (SMCC) для внедрения малеимидных групп с последующим взаимодействием модифицированного антитела с тиол-содержащим майтансиноидом с образованием тиоэфир-связанного конъюгата. В нем также получаются конъюгаты, содержащие 1-10 молекул препарата на одну молекулу антитела. Конъюгаты майтансиноидов с антителами, фрагментами антител, белковыми гормонами, белковыми факторами роста и другими белками получают аналогичным образом.
[0176] В другом аспекте изобретения FOLR1-антитело (например, huMov19, FR1-21, FR1-48, FR1-49, FR1-57 или FR1-65) соединено с препаратом через нерасщепляемую связь, посредством ПЭГ-спейсера. Подходящие перекрестносшивающие реактивы, содержащие гидрофильные цепи ПЭГ, образующие сшивки между препаратом и антителом против FOLR1, хорошо известны в данной области техники или доступны в продаже (к примеру, у Quanta Biodesign, Пауэлл, Огайо). Подходящие перекрестносшивающие реактивы, содержащие ПЭГ, также могут быть синтезированы из доступных в продаже ПЭГ с использованием стандартных техник химического синтеза, известных специалистам в данной области техники. Препараты могут взаимодействовать с бифункциональными ПЭГ-содержащими линкерами с образованием соединений следующей формулы: Z-X1-(-CH2-CH2-O-)n-Yp-D способами, подробными описанным в патентной публикации США 20090274713 и в WO 2009/0134976, которые затем могут взаимодействовать с агентом, связывающимся с клеткой с образованием конъюгата. Альтернативно клеточное связывание может быть модифицировано бифункциональным ПЭГ-перекрестносшивающим агентом для введения тиол-реактивной группы (например, малеимидной или галоацетамидной), который затем может быть обработан тиол-содержащим майтансиноидом с образованием конъюгата. В ином способе клеточное связывание может быть модифицировано бифункциональным ПЭГ-перекрестносшивающим агентом для введения тиол-реактивного майтансиноида (например, майтансиноида, несущего малеимидную или галоацетамидную группу) с образованием конъюгата.
[0177] Соответственно, иной аспект настоящего изобретения - конъюгат антитела против FOLR1 формулы (II) или формулы (II’):


где А обозначает антитело против FOLR1 или его фрагмент;
С обозначает цитотоксин или препарат;
Х обозначает алифатическую, ароматическую или гетероциклическую единицу, присоединенную к агенту, связывающемуся с клеткой через тиоэфирную связь, амидную связь, карбаматную связь или простую эфирную связь;
Y обозначает алифатическую, ароматическую или гетероциклическую единицу, присоединенную к препарату через ковалентную связь, выбранную из группы, состоящей из тиоэфирной связи, амидной связи, карбаматной связи, простой эфирной связи, аминной связи, углерод-углеродной связи и гидразоновой связи;
1 равно 0 или 1;
р равно 0 или 1;
m является целым числом от 2 до 15; и
n является целым числом от 1 до 2000.
В определенном варианте воплощения m является целым числом от 2 до 8; и
В определенном варианте воплощения п является целым числом от 1 до 24.
В определенном варианте воплощения m является целым числом от 2 до 6.
В некоторых вариантах воплощения п является целым числом от 2 до 8.
[0178] В некоторых вариантах воплощения m является целым числом от 3 до 5. В определенном варианте воплощения антитело является huMov19. В ином варианте воплощения антитело является FR-1-21. В ином варианте воплощения антитело является FR-1-48. В ином варианте воплощения антитело является FR-1-49. В ином варианте воплощения антитело является FR-1-57. В ином варианте воплощения антитело является FR-1-65.
Примерами подходящих ПЭГ-содержащих линкеров служат линкеры, обладающие N-сукцинимидил сложноэфирнымили N-сульфосукцинимидил сложноэфирным фрагментом, способные взаимодействовать с антителом против FOLR1 или с его фрагментом, а также малеимидный или галоацетиловый фрагмент дляреакции с соединением. ПЭГ-спейсер может быть внедрен в любой перекрестносшивающий агент, известный в данной области техники, способами, описаннымиздесь.
[0179] Множество линкеров подробно описаны в патентных публикациях СШАпод номерами 20050169933 и 20090274713, а также в WO 2009/0134976, содержимое которых включено в настоящий документ во всей полноте путем ссылки.
[0180] Настоящее изобретение включает аспекты, в которых от примерно 2 до примерно 8 молекул препарата («нагрузка препарата»), к примеру, майтансиноида, присоединены к антителу против FOLR1 или его фрагменту, причем противоопухолевый эффект конъюгата гораздо более высок, чем в случае нагрузки препарата меньшим или большим количеством молекул препарата, присоединенных к такому же агенту, соединяющемуся с клеткой. «Нагрузка препарата», при использовании здесь, относится к количеству молекул препарата (например, майтансиноида), которые могут быть присоединены к агенту, связывающемуся с клеткой (например, с антителом против FOLR1 или его фрагментом). В одном аспекте количество молекул препарата, которые могут быть присоединены к агенту, связывающемуся с клеткой, может быть равно в среднем от приблизительно 2 до приблизительно 8 (например, 1,9, 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9, 3,0, 3,1, 3,2, 3,3, 3,4, 3,5, 3,6, 3,7, 3,8, 3,9, 4,0, 4,1, 4,2, 4,3, 4,4, 4,5, 4,6, 4,7, 4,8, 4,9, 5,0, 5,1, 5,2, 5,3, 5,4, 5,5, 5,6, 5,7, 5,8, 5,9, 6,0, 6,1, 6,2, 6,3, 6,4, 6,5, 6,6, 6,7, 6,8, 6,9, 7,0, 7,1, 7,2, 7,3, 7,4, 7,5, 7,6, 7,7, 7,8, 7,9, 8,0, 8,1). В определенных вариантах воплощения препарат является N2’-деацетил-N2’-(3-меркапто-1-оксопропил)-майтансином (DM1) или N2’-деацетил-N2’-(4-меркапто-4-метил-1-оксопентил) майтансином (DM4). Таким образом, в определенном варианте воплощения антитело huMov19 конъюгировано с DM1 или DM4. В ином варианте воплощения антитело FR-1-21 конъюгировано с DM1 или DM4. В ином варианте воплощения антитело FR-1-48 конъюгировано с DM1 или DM4. В ином варианте воплощения антитело FR-1-49 конъюгировано с DM1 или DM4. В ином варианте воплощения антитело FR-1-57 конъюгировано с DM1 или DM4. В ином варианте воплощения антитело FR-1-65 конъюгировано с DM1 или DM4.
[0181] Таким образом, в одном аспекте иммуноконъюгат содержит 1 майтансиноид на антитело. В другом аспекте иммуноконъюгат содержит 2 майтансиноида на антитело. В другом аспекте иммуноконъюгат содержит 3 майтансиноида на антитело. В другом аспекте иммуноконъюгат содержит 4 майтансиноида на антитело. В другом аспекте иммуноконъюгат содержит 5 майтансиноидов на антитело. В другом аспекте иммуноконъюгат содержит 6 майтансиноидов на антитело. В другом аспекте иммуноконъюгат содержит 7 майтансиноидов на антитело. В другом аспекте иммуноконъюгат содержит 8 майтансиноидов на антитело.
[0182] В одном аспекте иммуноконъюгат содержит от примерно 1 до примерно 8 майтансиноидов на антитело. В другом аспекте иммуноконъюгат содержит от примерно 2 до примерно 7 майтансиноидов на антитело. В другом аспекте иммуноконъюгат содержит от примерно 2 до примерно 6 майтансиноидов на антитело. В другом аспекте иммуноконъюгат содержит от примерно 2 до примерно 5 майтансиноидов на антитело. В другом аспекте иммуноконъюгат содержит от примерно 3 до примерно 5 майтансиноидов на антитело. В другом аспекте иммуноконъюгат содержит от примерно 3 до примерно 4 майтансиноидов на антитело.
[0183] В одном аспекте в композиции, содержащей иммуноконъюгаты, содержится в среднем от приблизительно 2 до приблизительно 8 (например, 1,9, 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9, 3,0, 3,1, 3,2, 3,3, 3,4, 3,5, 3,6, 3,7, 3,8, 3,9, 4,0, 4,1, 4,2, 4,3, 4,4, 4,5, 4,6, 4,7, 4,8, 4,9, 5,0, 5,1, 5,2, 5,3, 5,4, 5,5, 5,6, 5,7, 5,8, 5,9, 6,0, 6,1, 6,2, 6,3, 6,4, 6,5, 6,6, 6,7, 6,8, 6,9, 7,0, 7,1, 7,2, 7,3, 7,4, 7,5, 7,6, 7,7, 7,8, 7,9, 8,0, 8,1) молекул препарата (например, майтансиноидов), присоединенных к антителу. В одном аспекте в композиции, содержащей иммуноконъюгаты, содержится в среднем от приблизительно 1 до приблизительно 8 молекул препарата (например, майтансиноидов) на антитело. В одном аспекте в композиции, содержащей иммуноконъюгаты, содержится в среднем от приблизительно 2 до приблизительно 7 молекул препарата (например, майтансиноидов) на антитело. В одном аспекте в композиции, содержащей иммуноконъюгаты, содержится в среднем от приблизительно 2 до приблизительно 6 молекул препарата (например, майтансиноидов) на антитело. В одном аспекте в композиции, содержащей иммуноконъюгаты, содержится в среднем от приблизительно 2 до приблизительно 5 молекул препарата (например, майтансиноидов) на антитело. В одном аспекте в композиции, содержащей иммуноконъюгаты, содержится в среднем от приблизительно 3 до приблизительно 5 молекул препарата (например, майтансиноидов) на антитело. В одном аспекте в композиции, содержащей иммуноконъюгаты, содержится в среднем от приблизительно 3 до приблизительно 4 молекул препарата (например, майтансиноидов) на антитело. В одном аспекте композиция, содержащая иммуноконъюгаты, содержит от приблизительно 3,5 до приблизительно 4 молекул препарата (например, майтансиноидов) на антитело.
[0184] В одном аспекте в композиции, содержащей иммуноконъюгаты, содержится в среднем приблизительно 2±0,5, приблизительно 2,5±0,5, приблизительно 3±0,5, приблизительно 3,5±0,5, приблизительно 4±0,5, приблизительно 4,5±0,5, приблизительно 5±0,5, приблизительно 5,5±0,5, приблизительно 6±0,5, приблизительно 6,5±0,5, приблизительно 7±0,5, приблизительно 7,5±0,5 или приблизительно 8±0,5 молекул препарата (например, майтансиноидов), присоединенных к антителу. В одном аспекте в композиции, содержащей иммуноконъюгаты, содержится в среднем приблизительно 3,5±0,5 молекул препарата (например, майтансиноидов) на антитело.
[0185] Антитело против FOLR1 или его фрагмент могут быть модифицированы при взаимодействии антитела против FOLR1 или его фрагмента с бифункциональным перекрестносшивающим реагентом, образуя ковалентно связанную молекулу линкера с антителом против FOLR1 или его фрагментом. При использовании здесь термин «бифункциональный перекрестносшивающий реагент» - любой химический фрагмент, который ковалентно соединяет агент, соединяющийся с клетокой, с препаратом, например, препаратом, описанным здесь. В другом способе часть связывающего фрагмента предоставляется препаратом. В этой связи препарат содержит связывающий фрагмент, являющийся частью большей молекулы линкера, который используется для сочленения агента, соединяющегося с клеткой, с препаратом. К примеру, для образования майтансиноида DM1, боковая цепь С-3-гидроксильной группы майтансина модифицируется таким образом, чтобы в ней содержалась свободная сульфгидрильная группа (SH). Данная тиолированная форма майтансина может взаимодействовать с модифицированным агентом, связывающимся с клеткой, с образованием конъюгата. Таким образом, в итоге линкер состоит из двух компонентов: одного, предоставленного перекрестносшивающим реактивом, и второго, предоставленного боковой цепью DM1.
[0186] Молекулы препаратов также могут быть связаны с молекулами антител через промежуточную молекулу-носителя, например, альбумина сыворотки.
[0187] При использовании здесь выражение «связанный с агентом, соединяющимся с клеткой» или «связанный с антителом против FOLR1 или его фрагментом» относится к конъюгатной молекуле, содержащей по меньшей мере одно производное препарата, связанное с агентом, соединяющимся с клеткой, антителом против FOLR1 или его фрагментом через подходящую сшивающую группу или ее прекурсор. В определенных вариантах воплощения сшивающая группа - SMCC.
[0188] В определенных вариантах воплощения цитотоксические агенты, использующиеся в настоящем изобретении,- майтансиноиды и аналоги майтансиноидов. Примеры подходящих майтансиноидов включают сложные эфиры майтансинола и аналоги майтансинола. Также включены любые препараты, ингибирующие образование микротрубочек, высокотоксичные для клеток млекопитающих, такие как майтансинол и его аналоги.
[0189] Примерами подходящих сложных эфиров майтансинола служат эфиры с модифицированным ароматическим кольцом и эфиры с модификациями в других позициях. Такие подходящие майтансиноиды описаны в патентах США под номерами 4424219, 4256746, 4294757, 4307016, 4313946, 4315929, 4331598, 4361650, 4362663, 4364866, 4450254, 4322348, 4371533, 5208020, 5416064, 5475092, 5585499, 5846545, 6333410, 7276497 и 7473796.
[0190] В определенном варианте воплощения в иммуноконъюгатах по настоящему изобретению в качестве цитотоксического агента используется тиолсодержащий майтансиноид (DM1), который по номенклатуре называется N2’-деацетил-N2’-(3-меркапто-1-оксопропил)-майтансином. DM1 имеет следующую структурную формулу (III):

[0191] В ином варианте воплощения в конъюгатах по настоящему изобретению в качестве цитотоксического агента используется N2’-деацетил-N2’(4-метил-4-меркапто-1-оксопентил)-майтансин (например, DM4). DM4 имеет следующую структурную формулу (IV):

[0192] Иным майтансиноидом, содержащим боковую цепь со стерической тиоловой связью, является.^V2-деацетил-//-2(4-меркапто-l-оксопентил)-майтансин (называемый DM3), обладающий следующей структурной формулой (V):

[0193] Любой майтансиноид, описанный в патентах США под номерами 5208020 и 7276497, может использоваться в конъюгате по настоящему изобретению. В этой связи раскрытие 5208020 и 7276697 полностью включено в настоящий документ путем ссылки.
[0194] Множество положений в майтансиноидах может служить для химического связывания с линкером. К примеру, ожидается, что подходящим будет положение С-3 с гидроксильной группой, положение С-14, модифицированное гидроксиметильной группой, положение С-15, модифицированное гидроксильной группой, и положение С-20 с гидроксильной группой. В определенных вариантах воплощения используется положение С-3. В определенных вариантах воплощения используется положение С-3 майтансинола.
[0195] Структуры определенных конъюгатов показаны ниже:








В определенном варианте воплощения антитело является huMov19. В ином варианте воплощения антитело является FR1-21.
[0196] Ряд описаний получения подобных конъюгатов антитело-майтансиноид представлен в патентах США под номерами 6333410, 6441163, 6716821 и 7368565, каждый из которых включен в настоящий документ во всей полноте.
[0197] В общем раствор антитела в водном буфере может быть инкубирован с молярным избытком майтансиноидов с дисульфидной группой, несущей реактивную группу. Реакция может быть остановлена добавлением избытка амина (например, этаноламина, таурина и т.д.). Конъюгат майтансиноид-антитело затем может быть очищен гель-фильтрацией. Число молекул майтансиноида, связавшихся с молекулой антитела, может быть определено спектрофотометрическим измерением соотношения абсорбции на 252 нм и 280 нм. В среднем используется 1-10 молекул майтансиноида/молекулу антитела, в определенных воплощених используется в среднем 2-5. Среднее количество молекул майтансиноида/антитело может составлять, к примеру, приблизительно 1-10, 2-5, 3-4, 3,5-4 или 3,5. В одном аспекте среднее количество молекул майтансиноида/антитело равно приблизительно 3,5±0,5. В одном аспекте среднее количество молекул майтансиноида/антитело равно приблизительно 3,5-4.
[0198] Конъюгаты антител с майтансиноидными препаратами могут быть оценены на их способность подавлять пролиферацию различных нежелательных клеток in vitro. К примеру, для оценивания цитотоксичности данных соединений с легкостью может использоваться человеческая клеточная линия КВ. Исследуемые клетки могут быть подвергнуты воздействию веществ в течение 4-5 дней, выжившие фракции клеток измеряют прямым анализом известными способами. Затем по данным анализов могут быть вычислены величины IC50.
[0199] Также для получения конъюгатов с антителами против FOLR1 могут применяться бензодиазепиновые соединения, описанные, к примеру, в Патентной публикации США №2010/0203007 (например, индолинобензодиазепины или оксазолидинобензодиазепины), их производные и интермедиаты.
[0200] Подходящие бензодиазепины включают соединения с формулами (XIV), (XV) и (XVI), в которых димерные соединения, необязательно, несут связывающую группу, позволяющую связывание с агентами, связывающимися с клетками.



где двойная линия

R1, R2, R3, R4, R1’, R2’, R3’ и R4’, каждый независимо, выбраны из Н, замещенного или незамещенного линейного, разветвленного или циклического алкила, алкенила или алкинила с 1-10 атомами углерода, полиэтиленгликолевой единицы (-ОСН2СН2)n, где n - целое число от 1 до 2000, или заместителя, выбранного из галогена, гуанидия [-NH(C=NH)NH2], OR7, NR8R9, NO2, NRCOR’, SR10, сульфоксида вида SOR’, сульфона вида -SO2R’, сульфита -SO3, бисульфита -OSO3, сульфонамида вида SO2NRR’, циано-, азидо-, -COR11, OCOR11 или OCONR11R12, в которых R7, R8, R9, R10, R11 и R12, каждый независимо, выбран из Н, линейного, разветвленного или циклического алкила, алкенила или алкинила с 1-10 атомами углерода, полиэтиленгликолевой единицы (-OCH2CH2)n, где n - целое число от 1 до 2000, арила с 6-10 атомами углерода, гетероциклического кольца с 3-10 атомами углерода, необязательно R10 - SR13 или COR13, где R13 выбран из линейного, разветвленного или циклического алкила, алкенила или алкинила с 1-10 атомами углерода, полиэтиленгликолевой единицы (-ОСН2СН2)n, где n - целое число от 1 до 2000, арила с 6-10 атомами углерода, гетероциклического кольца с 3-10 атомами углерода, необязательно R11-OR14, где R14 имеет такое же значение, как и R, необязательно любой из R1, R2, R3, R4, R1’, R2’, R3’ или R4’ является сшивающей группой, позволяющей связать агент, соединяющийся с клеткой через ковалентную связь или выбран из полипирроло, поли-индолил, поли-имидазолил, полипирроло-имидазолил, поли-пирроло-индолил или полиимидазоло-индолил единиц, необязательно несущих сшивающую группу, позволяющую связывание с агентом, соединяющимся с клеткой;
Z выбран из (СН2)n, где n - 1, 2 или 3, CR15R16, NR17, О или S, где R15, R16 и R17, каждый независимо, выбран из Н, линейного, разветвленного или циклического алкила c 1-10 атомами углерода, полиэтиленгликолевой единицы (-ОСН2СН2)n, где n - целое число от 1 до 2000;
R6 - OR, SR или NRR’, где R и R’ имеют такое же значение, как определено выше;
X’ выбран из СН2, NR, CO, BH, SO ил SO2, где R имеет такое же значение, как определено выше;
Y’ - О, СН2, NR или S, где R имеет такое же значение, как определено выше;
Z’ - СН2 или (СН2)n, где n равно 2, 3 или 4, причем X’, Y’ и Z’ не являются СН2 одновременно;
А и А’ одинаковы или различны и выбраны из О, -CRR’O, S, -CRR’S, -NR15 или CRR’NHR15, где R и R’ имеют такое же значение, как определено выше, и где R15 имеет такое же значение, как определено выше для R;
D и D’ - одинаковы или различны и независимо выбраны из линейного, разветвленного или циклического алкила, алкенила или алкинила с 1-10 атомами углерода, необязательно замещенного галогеном, OR7, NR8R9, NO2, NRCOR’, SR10, сульфоксида вида SOR’, сульфона вида -SO2R’, сульфита -SO3, бисульфита -OSO3, сульфонамида вида SO2NRR’, циано-, азидо-, -COR11, OCOR11 или OCONR11R12, в которых R7, R8, R9, R10, R11 и R12 таковы, как определено выше, полиэтиленгликолевой единицы (-ОСН2СН2)n, где n - целое число от 1 до 2000;
L - необязательная фенильная группа или гетероциклическое кольцо с 3-10 атомами углерода, необязательно замещенные, где заместитель представляет собой связывающую группу, позволяющую связывание с агентом, соединяющимся с клеткой через ковалентную связь, либо выбраны из линейного, разветвленного или циклического алкила, алкенила или алкинила с 1-10 атомами углерода, необязательно замещенного галогеном, OR7, NR8R9, NO2, NRCOR’, SR10, сульфоксида вида SOR’, сульфона вида -SO2R’, сульфита -SO3, бисульфита -OSO3, сульфонамида вида SO2NRR’, циано-, азидо-, -COR11, OCOR11 или OCONR11R12, в которых R7, R8, R9, R10, R11 и R12 таковы, как определено выше, полиэтиленгликолевой единицы (-ОСН2СН2)n, где n - целое число от 1 до 2000; необязательно L само по себе является связывающей группой, позволяющей связывание с агентом, соединяющимся с клеткой через ковалентную связь; либо их фармацевтически приемлемыми сольватами, солями, гидратами или гидратированными солями, их оптическими изомерами, рацематами, диастереомерами, энантиомерами или полиморфными кристаллическими структурами этих соединений; причем соединение имеет не более одной связывающей группы, позволяющей связывание с агентом, соединяющимся с клеткой через ковалентную связь.
[0201] В одном аспекте двойная линия

Y выбран из -OR, NR’R", сульфита -SO3 или бисульфита -OSO3, причем R выбран из Н, линейного, разветвленного или циклического алкила с 1-10 атомами углерода, полиэтиленгликолевой единицы (-ОСН2СН2)n, где n - целое число от 1 до 2000, арила с 6-10 атомами углерода, гетероциклического кольца с 3-10 атомами углерода;
W-C=O, CH2 или SO2;
R1, R2, R3, R4, R1’, R2’, R3’ и R4’, каждый независмо, выбран из Н, NO2 или связывающей группы, позволяющей связывание с агентом, соединяющимся с клеткой через ковалентную связь;
R6-OR18, где R18 имеет такое же значение, как R;
Z выбран из (СН2)n, где n - 1, 2 или 3, CR15R16, NR17, O или S, где R15, R16 и R17, каждый независимо, выбран из Н, линейного, разветвленного или циклического алкила с 1-10 атомами углерода, полиэтиленгликолевой единицы (-ОСН2СН2)n, где n - целое число от 1 до 2000;
X’ выбран из СН2 или С=O;
Y’ - О, NR или S, где R имеет такое же значение, как определено выше;
Z’ - СН2или (СН2)2;
А и А’ оба - О;
D и D’ одинаковы или различны и независимо выбраны из линейного, разветвленного или циклического алкила, алкенила или алкенила с 1-10 атомами углерода;
L - необязательная фенильная группа или гетероциклическое кольцо с 3-10 атомами углерода, необязательно замещенные, где заместитель представляет собой связывающую группу, позволяющую связывание с агентом, соединяющимся с клеткой через ковалентную связь, либо выбраны из линейного, разветвленного или циклического алкила, алкенила или алкинила c 1-10 атомами углерода, необязательно замещенного галогеном, OR7, NR8R9, NO2, NRCOR’, SR10, сульфоксида вида SOR’, сульфона вида -SO2R’, сульфита -SO3, бисульфита -OSO3, сульфонамида вида SOzNRR’, циано-, азидо-, -CORii, OCORu или OCONR11R12, полиэтиленгликолевой единицы (-ОСН2СН2)n где n - целое число от 1 до 2000; необязательно L само по себе является связывающей группой, позволяющей связывание с агентом, соединяющимся с клеткой через ковалентную связь; либо их фармацевтически приемлемыми сольватами, солями, гидратами или гидратированными солями, их оптическими изомерами, рацематами, диастереомерами, энантиомерами или полиморфными кристаллическими структурами этих соединений.
[0202] В другом аспекте соединение описывается формулой (XVII):

где двойная линия

один из R2, R3 является связывающей группой, позволяющей связывание с агентом, соединяющимся с клеткой через ковалентную связь, а другой является Н;
один из L’, L" или L’" является связывающей группой, позволяющей связывание с агентом, соединяющимся с клеткой, а остальные являются Н; L’ может быть связывающей группой, a G - СН или N. Иные примеры описаны в патентной заявке США №61/150201, которая включена в настоящий документ в полном объеме посредством ссылки. Таким образом, в определенном варианте воплощения антитело huMov19 конъюгировано с бензодиазепином, обаладающим структурой, показанной на XIX-XXII выше. В ином варианте воплощения антитело FR-1-21 конъюгировано с бензодиазепином, обладающим структурой, показанной на XIX-XXII выше.
IV. Полинуклеотиды
[0203] В определенных вариантах воплощения изобретение охватывает полинуклеотиды, которые кодируют полипептид, специфически связывающийся с человеческим рецептором FOLR1 или фрагментом этого полипептида. К примеру, в изобретении предлагается полинуклеотид, содержащий нуклеиновую последовательность, кодирующую антитело к человеческому FOLR1 или фрагмент такого антитела. Полинуклеотиды по изобретению могут быть в виде РНК или ДНК. ДНК включает кДНК, геномную ДНК и синтетическую ДНК и может быть двуцепочечной или одноцепочечной, в последнем случае цепочка может быть кодирующей или некодирующей (антисмысловой).
[0204] В определенных вариантах воплощения полинуклеотиды изолированы. В определенных вариантах воплощения полинуклеотиды в значительной степени очищены.
[0205] В изобретении предлагается полинуклеотид, содержащий полинуклеотид, кодирующий последовательность, выбранную из группы, состоящей из SEQ ID NOs:4, 10, 11, 41, 42 и 88-103. Также предлагается полинуклеотид, кодирующий полипептид, обладающий по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности с SEQ ID NOs:4, 10, 11, 41, 42 и 88-103.
[0206] Полинуклеотиды с SEQ ID NOs:5, 14 и 15 содержат кодирующую последовательность вариабельного домена тяжелой цепи huMov19, вариабельного домена легкой цепи версии 1.00 и вариабельного домена легкой цепи версии 1.60, соответственно.
[0207] Помимо этого, в изобретении предлагается полинуклеотид, включающий последовательность, выбранную из группы, состоящей из SEQ ID NOs:5, 14, 15, 37, 38, 43, 44, 47, 48 и 120-127. Также предлагается полинуклеотид с по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% либо с по меньшей мере 99% идентичностью последовательности с SEQ ID NOs:5, 14, 15, 37, 38, 43, 44, 47, 48 и 120-127. Таким образом, в определенных вариантах воплощения полинуклеотид содержит (а) полинуклеотид с по меньшей мере 95% идентичностью последовательности с SEQ ID NO:5; и/или (б) полинуклеотид с по меньшей мере 95% идентичностью последовательности с SEQ ID NO:14 или 15. В определенных вариантах воплощения полинуклеотид содержит (а) полинуклеотид с аминокислотной последовательностью SEQ ID NO:5; и/или (б) полинуклеотид с аминокислотной последовательностью SEQ ID NO:14 или SEQ ID NO:15.
[0208] В определенных вариантах воплощения полинуклеотиды содержат кодирующую последовательность зрелого полипептида, слитого в одной рамке считывания с полинуклеотид ом, способствующим, к примеру, экспрессии и секреции полипептида из клетки-хозяина (например, с лидерной последовательностью, которая работает в качестве секреторной последовательности для контролируемого транспорта полипептида из клетки). Полипептид с лидерной последовательностью - белок-предшественник и может обладать лидерной последовательностью, отщепляемой клеткой-хозяином от зрелой формы полипептида. Полинуклеотиды также могут кодировать пропротеин, который представляет собой зрелый белок с дополнительными 5’-аминокислотными остатками. Зрелый белок с пропоследовательностью - пропротеин, являющийся неактивной формой протеина. При отщеплении пропоследовательности остается зрелый активный белок.
[0209] В определенных вариантах воплощения полинуклеотиды содержат кодирующую последовательность зрелого полипептида, слитого в одной рамке считывания с маркерной последовательностью, способствующей, к примеру, очистке кодируемого полипептида. К примеру, в случае бактериального хозяина маркерная последовательность может быть гексагистидиновым тегом от вектора pQE-9, предназначенным для очистки зрелого полипептида, слитого с маркером, а в случае использования в качестве хозяев клеток млекопитающих (например, клеток COS-7) маркерная последовательность может быть гемагглютининовым тегом (НА), полученным из гемагглютинина вируса гриппа.
[0210] Настоящее изобретение, помимо этого, относится к вариантам описанных выше полинуклеотидов, кодирующих, к примеру, фрагменты, аналоги и производные.
[0211] Полинуклеотидные варианты могут содержать изменения в кодирующих областях, некодирующих областях или в обоих типах областей. В некоторых вариантах воплощения полинуклеотидные варианты содержат изменения, которые приводят к молчащим заменам, вставкам или делениям, не влияющим на свойства или активность кодируемого полипептида. В некоторых вариантах воплощения нуклеотидные варианты продуцируются молчащими заменами, обусловленными вырожденностью генетического кода. Полинуклеотидные варианты могут быть получены по множеству причин, например, для оптимизации экспрессии кодонов у конкретного хозяина (изменение кодонов человеческой мРНК на те, которые предпочтительны для бактериального хозяина типа Е. coli).
[0212] Также предлагаются векторы и клетки, содержащие описанные здесь полинуклеотиды.
V. Способы применения и фармацевтические композиции
[0213] FOLR1-связывающие агенты (включая антитела, иммуноконъюгаты и полипептиды) по изобретению пригодны для использования во множестве приложений, включая, но не ограничиваясь перечисленным, терапевтические способы, такие каклечение рака. В определенных вариантах воплощения агенты полезны для ингибирования роста опухоли, включая стимулирование дифференциации, уменьшение объема опухоли и/или уменьшение опухолегенности опухоли. Используемые способы могут быть способами in vitro, ex vivo или in vivo. В определенных вариантах воплощения FOLR1-связывающий агент или антитело, или иммуноконъюгат, или полипептид являются антагонистами к человеческому FOLR1, с которым они связываются.
[0214] В одном аспекте антитела против FOLR1 и иммуноконъюгаты по изобретению полезны для определения присутствия FOLR1 в биологическом образце. Термин «детектирование», при использовании здесь, охватывает качественное или количественное детектирование. В определенных вариантах воплощения биологический образец содержит клетку или ткань. В определенных вариантах воплощения подобные ткани включают нормальные и/или раковые ткани, которые экспрессируют FOLR1 в большей степени, нежели другие ткани. В определенных вариантах воплощения избыточная экспрессия FOLR1 позволяет выявить наличие рака яичника, рака легкого, рака головного мозга, рака молочной железы, рака матки, рака почки или рака поджелудочной железы.
[0215] В одном аспекте в изобретении предлагается способ определения присутствия FOLR1 в биологическом образце. В определенных вариантах воплощения способ включает контактирование биологического образца и антитела против FOLR1 в условиях, позволяющих связывание антитела против FOLR1 с FOLR1, и детектирование образования комплекса между антителом против FOLR1 и FOLR1.
[0216] В одном аспекте в изобретении предлагается способ диагностирования нарушения, ассоциированного с повышенной экспрессией FOLR1. В определенных вариантах воплощения способ содержит контактирование тестируемой клетки с антителом против FOLR1, определение уровня экспрессии (количественно или качественно) FOLR1 тестируемой клеткой путем определения связывания антитела против FOLR1 с FOLR1, и сравнивание уровня экспрессии FOLR1 тестируемой клеткой с уровнем экспрессии FOLR1 контрольной клеткой (например, нормальной клеткой из той же ткани, что и тестируемая клетка, или клеткой, экспрессирующей FOLR1 на уровнях, сравнимых с нормальными клетками), причем больший уровень экспрессии FOLR1 тестируемой клеткой относительно контрольной клетки свидетельствует о наличии нарушения, связанного с повышенной экспрессией FOLR1. В определенных вариантах воплощения тестируемая клетка получена от субъекта, у которого подозревается нарушение, связанное с повышенной экспрессией FOLR1. В определенных вариантах воплощения нарушение является клеточным пролиферативным нарушением, например, раком или опухолью.
[0217] В определенных вариантах воплощения способ диагностики или детектирования, например, описанный выше, содержит детектирование связывания антитела против FOLR1 с FOLR1, экспрессируемым на поверхности клетки или содержащимся в препарате мембраны, полученном из клетки, экспрессирующей FOLR1 на ее поверхности. В определенных вариантах воплощения способ включает контактирование клетки и антитела против FOLR1 в условиях, позволяющих связывание антитела против FOLR1 с FOLR1, и детектирование образования комплекса между антителом против FOLR1 и FOLR1 на клеточной поверхности. Пример анализа, предназначенного для детектирования связывания антитела против FOLR1 с FOLR1, экспрессируемым на поверхности клетки, - анализ «FACS».
[0218] Для детектирования связывания антител против FOLR1 с FOLR1 могут использоваться и другие способы. Подобные способы включают, не ограничиваясь перечисленным, анализы связывания антигенов, хорошо известные в данной области техники, например, вестерн-блоттинг, радиоиммунологические анализы, ELISA (энзим-связанный иммуносорбентный анализ), «сандвич »-иммуноанализы, анализы иммунопреципитации, флуоресцентные иммуноанализы, иммуноанализы с протеином А и иммуногистохимический способ (IHC).
[0219] В определенных вариантах воплощения антитела против FOLR1 помечены. Метки включают, не ограничиваясь перечисленным, метки или фрагменты, которые детектируются непосредственно (например, флуоресцентные, хромофорные, электронноплотные, хемилюминесцентные и радиоактивные), а также фрагменты, например, ферменты или лиганды, которые детектируются косвенно, например, посредством ферментной реакции или молекулярного взаимодействия. [0220] В определенных вариантах воплощения антитела против FOLR1 иммобилизированы на нерастворимом матриксе. Иммобилизация приводит к отделению антитела против FOLR1 от любого FOLR1, остающегося свободным в растворе. Как правило, это осуществляется либо переведением антитела против FOLR1 в нерастворимую форму перед анализом, либо адсорбцией на водонерастворимом матриксе или поверхности (Bennich et al., Патент США №3720760), либо ковалентным спариванием (к примеру, с использованием глутаральдегидного перекрестного сшивания), либо переведением антитела против FOLR1 в нерастворимую форму после образования комплекса антитела против FOLR1 и FOLR1, например, иммунопреципитацией.
[0221] Любое из перечисленных выше воплощений диагностики или детектирования может осуществляться с использованием иммуноконъюгата по изобретению вместо антитела против FOLR1 или вместе с ним.
[0222] В определенных вариантах воплощения заболевание, которое подвергается терапии с FOLR1-связывающим агентом или антигонистом (например, антителом huMov19 или иммуноконъюгатом), - онкологическое заболевание. В определенных вариантах воплощения онкологическое заболевание характеризуется наличием опухолей, экспрессирующих рецептор фолиевой кислоты 1, с которыми связывается FOLR1-связывающий агент (например, антитело).
[0223] В настоящем изобретении предлагаются способы терапии онкологического заболевания, включающие введение терапевтически эффективного количества FOLR1-связывающего агента субъекту (например, субъекту, нуждающемуся в терапии). В некоторых вариантах воплощения онкологическое заболевание выбрано из группы, состоящей из колоректального рака, рака поджелудочной железы, рака легкого, рака яичника, рака печени, рака молочной железы, рака головного мозга, рака почки, рака предстательной железы, рака желудочно-кишечного тракта, меланомы, рака цервикального канала, рака мочевого пузыря, глиобластомы и онкологического заболевания головы и шеи. В определенных вариантах воплощения онкологическое заболевание является раком яичника. В определенных вариантах воплощения онкологическое заболевание является раком легкого. В некоторых вариантах воплощения субъект является человеком.
[0224] В настоящем изобретении, помимо этого, предлагаются способы ингибирования роста опухолей, в которых применяются антитела или иные агенты, описанные здесь. В определенных вариантах воплощения способ ингибирования роста опухоли включает контактирование клетки с FOLR1-связывающим агентом (например, антителом) in vitro. К примеру, иммортализированная клеточная линия или линия раковых клеток, экспрессирующая FOLR1, культивируются в среде, к которой добавляются антитело или иной агент, ингибирующие рост опухоли. В некоторых вариантах воплощения опухолевые клетки выделены от такого образца, взятого у пациента, как, например, биоптат тканей, плевральная эффузия или образец крови, и культивированы в среде, к которой добавлен FOLR1-связывающий агент для ингибирования роста опухоли.
[0225] В некоторых вариантах воплощения способ ингибирования роста опухоли включает контактирование опухоли или опухолевых клеток с FOLR1-связывающим агентом (например, антителом) in vivo. В определенных вариантах воплощения контактирование опухоли или опухолевой клетки с FOLR1-связывающим агентом осуществляется в животной модели. К примеру, FOLR1-связывающие агенты могут вводиться в ксенотрансплантаты, экспрессирующие один или более FOLR1, выращенных у иммунокомпрометированных мышей (например, мышей NOD/ТКИН) для ингибирования роста опухоли. В некоторых вариантах воплощения раковые стволовые клетки выделены от такого образца, взятого у пациента, как, например, биоптат тканей, плевральная эффузия или образец крови, и введены иммунокопрометированным мышам, которым затем вводится FOLR1-связывающий агент для ингибирования роста клеток опухоли. В некоторых вариантах воплощения FOLR1-связывающий агент вводится одновременно или спустя небольшое время после введения опухолегенных клеток животному для предотвращения роста опухоли. В некоторых вариантах воплощения FOLR1-связывающий агент вводится в качестве терапевтического средства после того, как опухолегенные клетки доросли до определенного размера.
[0226] В определенных вариантах воплощения способ ингибирования роста опухоли включает введение субъекту терапевтически эффективного количества FOLR1 -связывающего агента. В некоторых вариантах воплощения субъект является человеком. В некоторых вариантах воплощения у субъекта имеется опухоль либо субъект имел опухоль, которая была впоследствии удалена.
[0227] В определенных вариантах воплощения опухоль экспрессирует рецептор фолиевой кислоты, с которым связывается FOLR1-связывающий агент или антитело. В определенных вариантах воплощения опухоль избыточно экспрессирует FOLR1.
[0228] В некоторых вариантах воплощения опухоль выбрана из группы, состоящей из опухоли головного мозга, колоректальной опухоли, опухоли поджелудочной железы, опухоли легкого, опухоли яичника, опухоли печени, опухоли молочной железы, опухоли почки, опухоли предстательной железы, опухоли желудочно-кишечного тракта, меланомы, опухоли цервикального канала, опухоли мочевого пузыря, глиобластомы и опухоли головы и шеи. В определенных вариантах воплощения опухоль является опухолью яичника.
[0229] Помимо этого, в изобретении предлагается способ понижения опухолегенности опухоли у субъекта, включающий введение терапевтически эффективного количества FOLR1-связывающего агента субъекту. В определенных вариантах воплощения опухоль содержит раковые стволовые клетки. В определенных вариантах воплощения уровень раковых стволовых клеток в опухоли понижается при введении агента.
[0230] Таким образом, в определенных вариантах воплощения изобретения предлагаются способы терапии онкологического заболевания с использованием антитела huMov19 и иммуноконъюгатов. В определенных вариантах воплощения иммуноконъюгат huMov19 является huMov19-SPDB-DM4, huMov19-sulfo-SPP-DM1, huMov19-SPP-DM1 либо huMov19-PEG4-Mal-DM4.
[0231] Помимо этого, в изобретении предлагаются способы дифференцирования опухолегенных клеток в неопухолегенные клетки, включающий контактирование опухолегенных клеток с FOLR1-связывающим агентом (к примеру, введение FOLR1 - связывающего агента субъекту с опухолью, содержащей опухолегенные клетки, или субъекту, имевшему такую опухоль, которая была впоследствии удалена). В определенных вариантах воплощения опухолегенные клетки представляют собой клетки опухоли яичника.
[0232] Помимо этого, в настоящем изобретении также предлагаются способы снижения активации миофибробластов в строме солидной опухоли, включающие контактирование стромы с эффективным количеством FOLR1-связывающего агента, полипептида или антитела
[0233] В настоящем изобретении, помимо этого, предлагаются фармацевтические композиции, содержащие один или более FOLR1-связывающих агентов, описанных здесь. В определенных вариантах воплощения фармацевтические композиции, помимо этого, содержат фармацевтически приемлемый носитель. Данные фармацевтические композиции применяются для ингибирования роста опухолей и лечения рака у людей.
[0234] В определенных вариантах воплощения композиции изготавливаются для хранения и применения путем комбинирования очищенного антитела или агента по настоящему изобретению с фармацевтически приемлемым носителем (например, средой, добавкой) (Remington, The Science and Practice of Pharmacy 20th Edition Mack Publishing, 2000). Подходящие фармацевтически приемлемые носители включают, не ограничиваясь перечисленным, нетоксичные буферы, например, фосфатный, нитратный и на базе других органических солей; соли, например, натрия хлорид; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (например, октадецилдиметилбензиламмония хлорид; гексаметония хлорид; бензалкония хлорид; бензетония хлорид; фенол, бутиловый или бензиловый спирт; алкилпарабены, например, метил- или пропилпарабен; пирокатехин; резорцин; циклогексанол; 3-пентанол; и м-крезол); низкомолекулярные полипептиды (например, содержащие менее 10 аминокислотных остатков); белки, например, альбумин сыворотки, желатин или иммуноглобулины; гидрофильные полимеры, например, поливинилпирролидон; аминокислоты, например, глицин, глутамин, аспарагин, гистидин, аргинин или лизин; углеводы, например, моносахариды, дисахариды, глюкозу, маннозу или декстрины; хелатирующие агенты, например, ЭДТА; сахара, например, сахарозу, маннитол, трегалозу или сорбитол; солеобразующие противоионы, например, натрий; комплексы металлов (например, комплексы Zn-белок); и неионные ПАВ, например, TWEEN или полиэтиленгликоль (ПЭГ).
[0235] Фармацевтические композиции по настоящему изобретению могут вводиться любым количеством путей как для местной, так и для системной терапии. Введение может осуществляться местно (например, через слизистые оболочки, включая вагинальный и ректальный пути), например, трансдермальными пластырями, мазями, лосьонами, кремами, гелями, каплями, суппозиториями, спреями, жидкостями и порошками; через легкие (например, ингаляцией или инсуффляцией порошков или аэрозолей, включая небулайзеры; интратрахеально, интраназально, эпидермально и трансдермально); перорально; либо парентерально, включая внутривенное, внутриартериальное, подкожное, внутрибрюшинное или внутримышечное введения или инфузии; либо интракраниально (например, интратекально или интравентрикулярно).
[0236] Антитело или иммуноконъюгат по изобретению могут быть комбинированы в фармацевтической комбинированной композиции либо в режиме дозирования, например, в виде комбинированной терапии, со вторым соединением, обладающим противоопухолевыми свойствами. Второе соединение в фармацевтической комбинированной композиции или в режиме дозирования, предпочтительно, обладает синергичным эффектом с конъюгатом антитело-препарат в комбинации, не влияя отрицательно друг на друга. Также предлагаются фармацевтические композиции, содержащие FOLR1-связывающий агент и второй противоопухолевый агент.
[0237] При лечении заболевания нужная доза антитела или агента по настоящему изобретению зависит от типа заболевания, от тяжести и течения заболевания, от чувствительности заболевания, от того, вводятся ли антитела или конъюгаты в профилактических или терапевтических целях, от предыдущей терапии, анамнеза пациента и ответа на лечение и т.д., а также от суждений лечащего врача. Антитело или агент могут вводиться однократно или несколько раз в течение периода времени от нескольких дней до нескольких месяцев или вплоть до излечения либо уменьшения выраженности заболевания (например, уменьшения размера опухоли). Оптимальные режимы дозирования могут быть рассчитаны, исходя из измерений аккумуляции препарата в организме пациента, и будут зависеть от относительной активности индивидуального антитела или агента. Лечащий врач может с легкостью определить оптимальные дозировки, принципы дозирования и частоту введений. В определенных вариантах воплощения дозировка находится в пределах 0,01 мкг-100 мг/кг массы тела, и препарат может вводиться один или более раз в день, неделю, месяц или год. В определенных вариантах воплощения антитело или иной FOLR1-связывающий агент вводится один раз в две недели или один раз в три недели. В определенных вариантах воплощения дозировка антитела или иного FOLR1-связывающего агента находится в пределах от приблизительно 0,1 мг до приблизительно 20 мг на кг массы тела. Лечащий врач может оценить частоту введений на основании измеренных времени выведения и концентраций препарата в тканях или жидкостях тела.
[0238] Комбинированная терапия может проявлять «синергию» и быть «синергической», то есть проявляться в том, что эффект при совместном использовании активных компонентов выше, чем эффект, оказываемый при раздельном использовании соединений. Синергический эффект может быть достигнут, если активные компоненты: (1) находятся в одной композиции и вводятся или доставляются одновременно в комбинированной единичной дозированной формуле; (2) доставляются чередованием или параллельным введением отдельных формул, либо (3) иным режимом. При чередующейся терапии синергический эффект может быть достигнут, если соединения вводятся или доставляются последовательно, например, различными инъекциями отдельными шприцами. В общем при чередующейся терапии эффективная доза каждого активного компонента вводится последовательно, например, серийно, в то время как при комбинированной терапии эффективные дозы двух или более активных компонентов вводятся совместно.
VI. Наборы, содержащие FOLR1-связывающие агенты
[0239] В настоящем изобретении предлагаются наборы, которые содержат антитела, иммуноконъюгаты или иные агенты, описанные здесь, и которые могут использоваться способами, описаннымиздесь. В определенных вариантах воплощениянабор содержит по меньшей мере одно очищенное антитело против человеческого рецептора фолиевой кислоты 1 в одном или более контейнеров. В некоторых вариантах воплощения наборы содержат все компоненты, нужные и/или достаточные для проведения анализа детектирования, включая все контрольные образцы, указания по проведению анализов и любое ПО, необходимое для анализа и представления результатов. Специалист в данной области техники легко поймет, что предложенные по настоящему изобретению антитела, иммуноконъюгаты или иные агенты могут быть с легкостью встроены в один из установленных форматов наборов, хорошо известных в данной области техники.
[0240] Помимо этого, предлагаются наборы, содержащие FOLR1-связывающий агент (например, FOLR1-связывающее антитело), а также второй противоопухолевый агент.В определенных вариантах воплощения второй противоопухолевый агент является химиотерапевтическим агентом (например, гемцитабином или иринотеканом).
[0241] Варианты воплощения настоящего изобретения могут быть, помимо этого, определены ссылкой на следующие нелимитирующие примеры, в которых подробно описывается получение определенных антител по настоящему раскрытию и способы применения антител по настоящему раскрытию. Специалисту в данной области техникибудет понятно, что может быть внесено множество изменений как в материалы, так и в способы без отклонения от объема настоящего изобретения.
ПРИМЕРЫ
[0242] Следует понимать, что примеры и варианты воплощения, описанные здесь, предназначены лишь для иллюстративных целей и что множество модификаций или изменений, предложенных специалистами в данной области техники, соответствуют духу и находятся в пределах охвата настоящей заявки.
Пример 1
Химеризация мышиного моноклонального антитела Mov19
[0243] Аминокислотные последовательности вариабельной области Mov19 были получены из базы данных NCBI (номера доступа САА68253 для легкой цепи (SEQ ID NO:24) и САА68252 для тяжелой цепи (SEQ ID NO:23)), а затем кодон-оптимизированы и синтезированы Blue Heron Biotechnology. Вариабельная область легкой цепи была клонирована в сайты EcoRI и BsiWI плазмиды pAbKZeo, вариабельная область тяжелой цепи была клонирована в сайты HindIII и Apal плазмиды pAbGlNeo.
Пример 2
Гуманизация мышиных моноклональных антител Mov19 и FR1-21
[0244] Антитело Mov19 было гуманизировано, согласно методам перестраивания, описанным ранее (Roguska M. et. al., Proc. Natl. Acad. Sci. USA 1994 Feb; 91:969-973) и (Roguska et al., Protein Eng. 9(10):895-904 (1996)). Вкратце, средняя доступность растворителя к каждому каркасному остатку вариабельной области была рассчитана при помощи близкородственных исследованных структур антител из базы данных PDB, а позиции с более чем 30% средней доступностью были определены как поверхностные остатки (Pedersen J.T. et al., J. Mol. Biol. 1994; 235: 959-973). Человеческая поверхностная заместительная последовательность была выбрана путем выравнивания поверхностных позиций последовательностей мышиного антитела с соответствующими позициями человеческих зародышевых последовательностей антител в базе данных Kabat (Johnson, G. and Wu, Т. Т. (2001) Nucleic Acids Research, 29: 205-206). Наиболее гомологичная поверхностная вариабельная область человеческой легкой цепи (клон DPK19, локус IMGT IGKV2D-30*01 для Mov19 и локус IMGT IGKV1/OR2-0*01 для FR1-21) и наиболее гомологичная поверхностная вариабельная область человеческой тяжелой цепи (клон 8М27, локус IMGT IGHV1-69*08 для Mov19 и локус IMGT IGHV5-51*02 для FR1-21) были выбраны для замены каркасных поверхностных положений мышиного Mov19 с оставлением 6 CDR (Таблица 1) неизмененными. Мышиные и человеческие поверхностные последовательности Mov19 и FR1-21, а также остатки представлены на Фигурах 1A-D.
[0245] Ни одно изменение остатков не влияло на взаимодействие CDR Mov19 или FR1-21 с их эпитопами-мишенями в рецепторе фолиевой кислоты 1, поэтому в гуманизированные последовательности обоих антител обратные поверхностные мутации не вносились. В перестроенной последовательности Mov19 присутствовал консенсусный сайт N-связанного гликозилирования в N74 легкой цепи (легкая цепь версии 1.00), поэтому была изготовлена вторая версия гуманизированной легкой цепи, лишенная этого сайта. Просмотр базы данных Kabat человеческих последовательностей легкой цепи показал, что в позиции 74 легкой цепи чаще всего встречается треонин, поэтому легкая цепь версии 1.60 гуманизированного Mov19 была построена с треонином в положении 74. Положение 74 не является поверхностным, поэтому замена этого остатка не влияет на гуманизацию при перестраивании. Выравнивание последовательностей вариабельной области мышиного и гуманизированного Mov19 и FR1-21 представлено на Фигуре 2.
[0246] Последовательности вариабельных областей гуманизированных Mov19 и FR1-21 были кодон-оптимизированы и синтезированы Blue Heron Biotechnology. Последовательности фланкированы сайтами ферментативной рестрикции для облегчения клонирования внутри рамки считывания с соответствующими константными последовательностями в одноцепочечных плазмидах экспрессии млекопитающих. Вариабельная область легкой цепи была клонирована в сайты EcoRI и BsiWI плазмиды pAbKZeo. Результирующие плазмидные ДНК, кодирующие легкую цепь huMov19, были депонированы в АТСС под номерами депонентов АТСС РТА-10773 и РТА-10774, а результирующая плазмидная ДНК, кодирующая легкую цепь huFR1-21, была депонирована под номером депонента АТСС РТА-10776. Вариабельная область тяжелой цепи была клонирована в сайты HindIII и ApaI плазмиды pAbG1Neo. Результирующая плазмидная ДНК, кодирующая тяжелую цепь huMov19, была депонирована в АТСС под номером депонента АТСС РТА-10772, а результирующая плазмидная ДНК, кодирующая тяжелую цепь huFR1-21, была депонирована под номером депонента АТСС РТА-10775. Затем эти плазмиды были трансфицированы так, как описано в примере 3, чтобы получить huMov19. Плазмида, кодирующая любую из легких цепей huMov19 (например, депонированную в АТСС под номером депонента РТА-10773 или РТА-10774), может быть спарена с плазмидой, кодирующей тяжелую цепь huMov19, чтобы получить антитело huMov19 согласно способам, предложенным здесь, а также способам, известным обычному специалисту в данной области техники.
Пример 3
Экспрессия рекомбинантного антитела
[0247] Химерные и гуманизированные конструкции антител были транзиентно продуцированы либо в адгезивных клетках HEK-293Т по стандартной кальций-фосфатной процедуре (BD Biosciences, CalPhos Mammalian Transfection Kit, Cat №631312), либо в суспендированных клетках HEK-293Т по модифицированной процедуре ПЭИ [Durocher Y, Perret S, Kamen A High-level and high-throughput recombinant protein production by transient transfection of suspension-growing human 293-EBNA1 cells. Nucleic Acids Res. 2002 Jan 15; 30(2):E9] в роллерных колбах. ПЭИ-транзиентные трансфекции проводились так, как описано ранее (Durocher, Y. et al., Nucleic Acids Res. 30(2):E9 (2002)), за исключением того, что клетки HEK-293Т были выращены в Freestyle 293 (Invitrogen), а объем культуры не разбавляли после добавления комплексов ПЭИ-ДНК. И адгезивная, и суспензионная транзиентные трансфекции были инкубированы в течение недели, затем осветленный супернатант был очищен в колонке с Протеином А с последующей СМ колонной ионообменной хроматографией, так, как описано ниже. Как показано на Фигуре 3, в трансфицированных клетках экспрессия huMov19 была по меньшей мере в 10 раз выше экспрессии химерного Mov19.
Пример 4
Выделение антител
[0248] Антитела были выделены из осветленных супернатантов клеточной культуры с использованием стандартных методов, например, хроматографии с протеином А или G (HiTrap Protein А или G HP, 1 мл, Amersham Biosciences). Вкратце, супернатант был подготовлен для хроматографии путем добавления 1/10 объема 1 М Трис/HCl буфера, рН 8,0. рН-скорректированный супернатант был профильтрован через фильтровальную мембрану 0,22 мкм и загружен в колонку, уравновешенную связывающим буфером (фосфатно-солевой буфер, рН 7,3). Колонка была промыта связывающим буфером до достижения стабильного уровня фона без абсорбции на 280 нм. Антитела были элюированы 0,1 М буфером с уксусной кислотой, содержащим 0,15 М NaCl, рН 2,8, на скорости потока 0,5 мл/мин. Фракции объемом приблизительно 0,25 мл были собраны и нейтрализованы путем добавления 1/10 объема 1М Трис/HCl, рН 8,0. Пиковая(ые) фракция(и) была диализирована в течение ночи дважды относительно 1×фосфатно-солевого буфера и стерилизована фильтрованием через 0,2 мкм фильтровальную мембрану. Количество очищенных антител определяли, судя по абсорбции на А280.
[0249] Фракции, очищенные с протеином А, были потом доочищены способами ионообменной хроматографии (IEX) и хроматографии с сорбентом с карбоксиметильными группами (СМ). Вкратце, образцы, очищенные с протеином А, были обменены в стартовом буфере (10 мМ калия фосфата, 10 мМ натрия хлорида, рН 7,5) и профильтрованы через фильтр калибра 0,22 мкм. Подготовленный образец был затем загружен на смолу CM (GE Lifesciences), уравновешенную со стартовым буфером при потоке 120 см/ч. Размер колонки подбирался таким образом, чтобы связать все антитела в образце. Затем колонка была промыта связывающим буфером до достижения стабильного уровня фона без абсорбции на 280 нм. Антитела элюировали градиентом от 10 мМ до 500 мМ натрия хлорида в количестве 20 объемов колонки (ОК). Собирали фракции с величиной UV более 50 mAu относительно главного пика. Чистота (процентное содержание мономера и растворимых высокомолекулярных агрегатов) оценивалась эксклюзионной хроматографией (SEC) на геле TSK G3000SWXL в колонке 7,8×300 мм с предохранительной колонкой SWXL, 6,0х40 мм (Tosoh Bioscience, Монтгомеривилль, Пенсильвания) с использованием ВЭЖХ-системы Agilent HPLC 1100 (Agilent, Санта-Клара, Калифорния). Фракции с желаемой чистотой (>95%) были объединены, буфер был заменен на фосфатно-солевой буфер (рН 7,4), используя систему TFF, а затем стерилизованы фильтрованием через фильтр с мембраной 0,2 мкм. Чистота очищенных антител была далее определена спсобом эксклюзионной хроматографии, концентрация IgG была определена измерением абсорбции при 280 нМ с коэффициентом затухания 1,47. При необходимости делали разведение. Альтернативно для доочистки как мышиных, так и гуманизированных антител с повышенной селективностью, может применяться керамический гидроксиапатит (СНТ). Смола СНТ II типа с размером частиц 40 мкм (Bio-Rad Laboratories) применялась для доочистки антител аналогично методике для ионообменной хроматографии. В качестве стартового буфера для СНТ использовали 20 мМ натрия фосфата, рН 7,0, а антитела элюировали градиентом 20-160 мМ натрия фосфата количеством в 20 ОК.
Пример 5
Разработка мышиных антител против FOLR1
[0250] Имелось две различные серии иммунизации/скрининга. Первая серия дала образование клона FR1-21, вторая привела к образованию клонов FR1-48, FR1-49, FR1-57 и FR1-65. В первой серии мыши проходили подкожную иммунизацию приблизительно 5×106 FOLR1-экспрессирующих клеток KB (Американская Коллекция Культур Тканей, АТСС CCL-17). Во второй серии клетки 300-19, экспрессирующие на своей поверхности человеческий FOLR1, применялись для иммунизации мышей. Для создания этих клеток была получена аминокислотная последовательность человеческого FOLR1 с веб-сайта NCBI (номер доступа NP_057937), затем она была кодон-оптимизирована и синтезирована компанией Blue Heron biotechnologies, фланкирована сайтами рестрикции EcoRI и XbaI для облегчения клонирования в вектор экспрессии млекопитающих pSRa. Клетки 300-19 - пре-В-клеточная линия, полученная от мышей Balb/c (Reth et al., Nature, 317: 353-355 (1985)), - были подвергнуты трансфекции плазмидой экспрессии pSRa-FolR1 для стабильного экспрессирования высоких уровней человеческого FOLR1 на клеточной поверхности. Для обеих серий использовались стандартные протоколы иммунизации, используемые в ImmunoGen, Inc. Иммунизированные мыши были подвергнуты бустингу антигеном за три дня до умерщвления для получения гибридомы. Селезенки мышей были собраны согласно стандартным протоколам по работе с животными, например, перетиранием тканей между двумя стерильными замороженными микроскопными стеклами до получения отдельноклеточной суспензии в среде RPMI-1640. Клетки селезенки были центрифугированы, осадок был отделен, промыт и соединен с клетками миеломы мыши, например, P3X63Ag8.653 (Kearney et al., J Immunol, 123: 1548-1550 (1979)) с использованием полиэтиленгликоля-1500 (Roche 783 641). Слитые клетки были ресуспендированы в селекционной среде RPMI-1640, содержащей гипоксантин-аминоптерин-тимидин (HAT) (Sigma H-0262), и селектированы по росту в 96-луночных культуральных планшетах с плоским дном (Corning-Costar 3596, 0,2 мл клеточной суспензии на лунку) при 37°С с 5% СО2. Спустя 5 дней инкубации 0,1 мл супернатанта культуры было извлечено из каждой лунки и заменено на 0,1 мл среды RPMI-1640, содержащей добавку гипоксантина-тимидина (НТ) (Sigma H-0137). Инкубирование при 37°С с 5% СО2 продолжалось до тех пор, пока клоны гибридомы не были готовы для скрининга антител. Также могут использоваться иные методики иммунизации и получения антител, включая те, которые описаны у Langone et al. (Eds., "Immunochemical Techniques, Part I", Methods in Enzymology, Academic Press, volume 121, Florida) и yHarlow et al. ("Antibodies: A Laboratory Manual"; Cold Spring Harbor Laboratory Press, New York (1988)).
Пример 6
Скрининг и селекция гибридом
[0251] Клетки FOLR1-300-19, трансфицированные человеческими клетками FOLR1 и KB, использовались в скринингах первой и второй серии, соответственно. Супернатанты культур гибридомы были подвергнуты скринингу методом проточной цитометрии на предмет секреции мышиных моноклональных антител, связывающихся с FOLR1 -положительными клетками, например, FOLR1-экспрессирующими клетками 300-19 или клетками KB, но не с FOLR1-отрицательными клетками, например, нетрансфицированными клетками 300-19. 0,1 мл супернатанта гибридомы было инкубировано 3 ч либо с FOLR1-положительными клетками 300-19, либо с нетрансфицированными клетками 300-19 (1×105 клеток в образце) в 0,1 мл буфера FACS (среда RPMI-1640 с добавкой 2% нормальной козьей сыворотки). Затем клетки были центрифугированы, осаждены, промыты и инкубированы 1 час с 0,1 мл РЕ-конъюгированных козьих анти-мышиных IgG-антител (например, доступных в продаже у Jackson Laboratory, 6 мкг/мл в буфере FACS). Клетки были центрифугированы, вновь осаждены, промыты буфером FACS и ресуспендированы в 0,2 мл фосфатно-солевого буфера, содержащего 1% формальдегида. Связанная с клетками флуоресценция была измерена при помощи проточного цитометра FACSCalibur с многолуночным самплером HTS или матричного проточного цитометра FACS и проанализирована при помощи CellQuest Pro (все оборудование от BD Biosciences, Сан-Диего, США). Клоны, положительные по гибридоме, были субклонированы ограниченным разведением. Для последующего анализа было выбрано по одному субклону каждой гибридомы, обладавшему такой же реактивностью против FOLR1, как и родительские клетки, согласно проточной цитометрии. Стабильные субклоны были культивированы, изотип каждого секретируемого антитела против FOLR1 определялся при помощи изотипирующих реагентов, доступных в продаже (Roche 1493027). Мышиные антитела были выделены с протеином А из осветленной среды гибридомы, так, как описано выше. Эти антитела были обозначены как антитела FR-1.
Пример 7
Выделение мышиных моноклональных антител
[0252] Антитела были выделены из субклоновых супернатантов гибридомы с использованием стандартных методов, например, хроматографии с протеином А или G (HiTrap Protein А или G HP, 1 мл, Amersham Biosciences). Вкратце, супернатант был подготовлен для хроматографии путем добавления 1/10 объема 1 М Трис/HCl буфера, рН 8,0. рН-скорректированный супернатант был профильтрован через фильтровальную мембрану 0,22 мкм и загружен в колонку, уравновешенную связывающим буфером (фосфатно-солевой буфер, рН 7,3). Колонка была промыта связывающим буфером до достижения стабильного уровня фона без абсорбции на 280 нм. Антитела были элюированы 0,1 М буфером с уксусной кислотой, содержащим 0,15 М NaCl, рН 2,8, на скорости потока 0,5 мл/мин. Фракции объемом приблизительно 0,25 мл были собраны и нейтрализованы путем добавления 1/10 объема 1М Трис/HCl, рН 8,0. Пиковая(ые) фракция(и) была диализирована в течение ночи дважды относительно 1× фосфатно-солевого буфера и стерилизована фильтрованием через 0,2 мкм фильтровальную мембрану. Количество антител определяли, судя по абсорбции на А280.
Пример 8
Определение характеристик связывания способом проточной цитометрии
[0253] Специфичность связывания определялась способом проточной цитометрии с использованием очищенных антител. Диаграммы FACS, демонстрирующие связывание антител против FOLR1 с FOLR1-экспрессирующими клетками 300-19 в отсутствие связывания с родительскими клетками 300-19, показаны на Фигуре 4. Каждое антитело было инкубировано 3 часа либо с FOLR1-экспрессирующими клетками 300-19, либо нетрансфицированными клетками 300-19 (1×105 клеток в образце) в 0,1 мл буфера FACS (среда RPMI-1640 с добавкой 2% нормальной козьей сыворотки). Затем клетки были осаждены, промыты и инкубированы 1 час с 0,1 мл FITC-конъюгированных козьих антимышиных IgG-антител (например, доступных в продаже у Jackson Laboratory, 6 мкг/мл в буфере FACS). Клетки были вновь осаждены, промыты буфером FACS и ресуспендированы в 200 мкл фосфатно-солевого буфера, содержащего 1% формальдегида. Образцы были собраны при помощи проточного цитометра FACSCalibur с многолуночным самплером HTS или матричного проточного цитометра FACS и проанализированы при помощи CellQuest Pro (все оборудование от BD Biosciences, Сан-Диего, США). FACS-гистограммы антител против FOLR1 показали сдвиг флуоресценции, а родительские клетки 300-19 его не показали. Также при инкубировании любой из этих клеточных линий только с FITC-конъюгированным козьим анти-человеческим IgG-антителом существенного сдвига флуоресценции не наблюдалось.
Пример 9
Клонирование и секвенирование VL- и VH-областей антитела muFR1-21
[0254] Тотальная клеточная РНК была приготовлена из 5×106 клеток гибрид омы с использованием набора RNeasy (QIAgen) согласно рекомендациям производителя. кДНК затем была синтезирована из тотальной РНК с использованием набора для синтеза кДНК Superscript II (Invitrogen). Процедура первого раунда ПЦР с вырожденными праймерами на кДНК, происходящей из клеток гибридомы, основывалась на способах, описанных в Wang et al. ((2000) J Immunol Methods. Jan 13; 233(1-2):167-77) и Со et al. ((1992) J Immunol. Feb 15; 148(4): 1149-54). VH-последовательности были амплифицированы ПЦР с использованием следующих вырожденных праймеров: ЕсоМН1 CTTCCGGAATTCSARGTNMAGCTGSAGSAGTC (SEQ ID NO:50), EcoMH2 CTTCCGGAATTCSARGTNMAGCTGSAGSAGTCWGG (SEQ ID NO:51) и BamIgG1 GGAGGATCCATAGACAGATGGGGGTGTCGTTTTGGC (SEQ ID NO:52). VL-последовательности были амплифицированы ПЦР с использованием следующих вырожденных праймеров: SacIMK GGAGCTCGAYATTGTGMTSACMCARWCTMCA (SEQ ID NO:53) и HindKL TATAGAGCTCAAGCTTGGATGGTGGGAAGATGGATACAGTTGGTGC (SEQ ID NO:54). (Смешанные основания обозначаются следующим образом: N=G+A+T+C, S=G+C, Y=C+T, M=A+C, R=A+G, W=A+T).
[0255] ПЦР-реакционные смеси были затем выдержаны на 1% легкоплавком агарозном геле, цепочки с 300-400 парами оснований были вырезаны, выделены с использованием мини колонок Zymo ДНК, а затем направлены в Agencourt Biosciences для секвенирования. Соответствующие 5’ и 3’ ПЦР-праймеры использовались как секвенирующие праймеры для получения вариабельной области кДНК с обоих направлений. Аминокислотные последовательности VH- и VL-областей были определены транслированием результатов ДНК-секвенирования при помощи ПО VectorNTI.
[0256] Для идентификации 5’-конечных артефактов секвенирования праймеров в предварительных последовательностях кДНК вариабельной области использовался сайт NCBI IgBlast (www.ncbi.nlm.nih.gov/igblast/) для поиска с целью выявления зародышевых мышиных последовательностей, от которых происходили антитела. Очищенные последовательности вариабельных областей затем совмещались с референтными последовательностями NCBI константных областей специфических антител для получения ожидаемой полноразмерной последовательности мышиного антитела. Затем рассчитывали FR1-21 молекулярную массу ожидаемых легкой и тяжелой цепей мышиного антитела и сравнивали с массой, измеренной согласно анализу жидкостной хроматографией/масс-спектрометрией (ЖХ/МС). Тяжелая цепь мышиного FR1-21 соответствовала измеренной массе, в то время как для легкой цепи потребовалось секвеирование для определения последовательности 5’-конца. ПЦР-праймер CD37-I1LClead1 (ttttgaattcgccaccatgaagtttccttctcaacttct) был разработан для отжига с зародышевой лидерной последовательностью мышиного антитела таким образом, чтобы новая ПЦР-реакция давала полную вариабельную область последовательности кДНК, не измененную праймерами. ПЦР-реакции, зональная очистка и секвенирование проводились так, как описано выше; масса новой полной последовательности, кодирующей легкую цепь, соответствующую легкой цепи FR1-21, была определена способом ЖХ/МС.
Пример 10
Экспрессия референтных антител
[0257] Аминокислотная последовательность антитела против FOLR1 Morphotech MorAb-003 (Фарлетузумаба) была получена из Международного Перечня Непроприетарных Наименований Фармацевтических Субстанций (INN) Всемирной Организации Здравоохранения (ВОЗ), кодон-оптимизирована и синтезирована Blue Heron Biotechnology. Последовательность вариабельной области легкой цепи фланкирована сайтами ферментативной рестрикции EcoRI и BsiWI, последовательность вариабельной области тяжелой цепи фланкирована сайтами ферментативной рестрикции HindIII и Apal для клонирования в рамке считывания с соответствующими константными последовательностями в одноцепочечной плазмиде экспрессии млекопитающих. Клонирование, экспрессия и очистка проводились так, как это описано для гуманизированных Mov19 и FR1-21 выше.
Пример 11
АЗКЦ активность huMov19
[0258] Анализ высвобождения лактатдегидрогеназы (LDH) использовался для измерения антитело-зависимой клеточно-опосредованной цитотоксичности (АЗКЦ) линий опухолевых клеток с использованием свежевыделенных клеток-натуральных киллеров (НК) в качестве эффекторных клеток (например. Shields, J. Biol. Chem., 276(9):6591-6604 (2001)). НК-клетки были вначале выделены из человеческой крови здорового донора (Research Blood Components, Inc., Брайтон, Миннесота) по модифицированному протоколу, использующемуся для NK Isolation Kit II (Miltenyi Biotech, 130-091-152). Кровь была в 2 раза разбавлена 1х фосфатно-солевым буфером. 25 мл разбавленной крови было осторожно налито поверх 25 мл Ficoll Paque в 50 мл коническую пробирку и центрифугировано на 400 г 45 минут при комнатной температуре. Мононуклеарные клетки периферической крови (МКПК) были отобраны из границы раздела, перенесены в новую коническую пробирку вместимостью 50 мл и однократно промыты 1х фосфатно-солевым буфером. МКПК были ресуспендированы в 2 мл НК-изолирующего буфера (1х фосфатно-солевого буфера, 0,5% альбумина бычьей сыворотки, 2 мМ ЭДТА), затем к клеточной суспензии было добавлено 500 мкл коктейля биотин-антитело. Коктейль биотин-антитело содержит биотинилированные антитела, связывающиеся с лимфоцитами, за исключением НК-клеток, что дает отрицательную селекцию НК-клеток. Смесь инкубировали при 4°С 10 минут, затем добавляли 1,5 мл НК-изолирующего буфера и 1 мл микрогранул Anti-Biotin Micro Beads. Смесь клеток и антител инкубировали еще 15 минут при 4°С. Затем клетки были один раз промыты 50 мл НК-изолирующего буфера и ресуспендированы в 3 мл НК-изолирующего буфера. Затем в сепаратор autoMACS (Miltenyi Biotech) была установлена колонка MACS LS, которую предварительно промыли 3 мл НК-изолирующего буфера. Клеточную суспензию автоматически вводили в колонку, промывали, выходящую фракцию с немечеными НК-клетками собирали в новую коническую пробирку вместимостью 50 мл. Полученные NK-клетки высевали в 30 мл полной среды RPMI (RPMI-1640 с добавками 5% фетальной телячьей сыворотки, 1% пенициллина-стрептомицина, 1 мМ HEPES, 1 мМ натрия пирувата, 1% 100× MEM раствора незаменимых аминокислот) и выдерживали в течение ночи. Последующие анализы и разбавления проводились в среде RHBP (RPMI-1640 с добавками 20 мМ HEPES, рН 7,4, 0,1% альбумина бычьей сыворотки и 1% пенициллинастрептомицина). Различные концентрации растворов антител в среде RHBP были аликвотированы в двух повторностях по 50 мкл/лунку в 96-луночный круглодонный планшет. Клетки-мишени были ресуспендированы по 106 клеток/мл в среде RHBP и добавлены по 100 мкл/лунку в каждую лунку с разведениями антител. Планшет с клетками-мишенями и разведениями антител инкубировали 30 минут при 37°С. Затем в лунки с клетками-мишенями добавляли НК-клетки по 50 мкл/лунку. Типичное соотношение составляло приблизительно 1 клетка-мишень на 3-4 НК-клетки. Для каждого эксперимента применялись по меньшей мере следующие контроли: только ПК-клетки, только клетки-мишени (спонтанное высвобождение LDH), клетки-мишени с НК-клетками (антитело-независимое высвобождение LDH), клетки-мишени с 10% TritonX-100 (максимальное высвобождение LDH). Смеси инкубировали при 37°С 4 часа для лизиса клеток. Планшеты центрифугировали 10 минут при 1200 оборотов/мин., 100 мкл супернатанта осторожно переносили в новый 96-луночный плоскодонный планшет. В каждую лунку добавляли LDH-реакционную смесь (100 мкл/лунку) из набора Cytotoxicity Detection Kit (Roche 1644793), инкубировали при комнатной температуре 5-30 мин. Оптическую плотность образцов измеряли на 490 нм (OD490). Процентный специфический лизис каждого образца определяли по следующей формуле: процентный специфический лизис = (величина образца - спонтанное высвобождение)/(максимальное высвобождение - спонтанное высвобождение)*100.
[0259] При инкубировании с huMov19 наблюдалась выраженная АЗКЦ-активность против клеток IGROV-1 в присутствии человеческих эффекторных НК-клеток. АЗКЦ-активность против клеток IGROV-1 сравнивалась для huMov19, huFR-1-21, Mor003 и chTK1 (изотипный контроль) (Фигура 6). При обработке 0,9 нг/мл huMov19 наблюдался лизис приблизительно 30% клеток IGROV-1, что аналогично активности, наблюдавшейся у других антител против FOLR1. АЗКЦ-активность huMov19 характеризовалась величиной ЕС50 равной 0,20 нг/мл, huFr-1-21 - EC50 0,11 нг/мл, МогОО3-0,16 нг/мл, а chTK1 не обладало активностью против клеток IGROV-1.
Пример 12
Получение иммуноконъюгатов против FOLR1
Получение huMOV19v1.6-sulfo-SPDB-DM4
[0260] Линкер 2-sulfo-SPDB был растворен в ДМА. Антитело huMOV19vl.6 было инкубировано в концентрации 8 мг/мл с 12-кратным молярным избытком линкера 2-sulfo-SPDB в течение приблизительно 2 часов при 25°С при уровне рН 7,5. Реакционная смесь была очищена с использованием колонки SEPHADEX™ G25F, уравновешенной 50 мМ калий-фосфатным буфером, содержащим 50 мМ NaCl, 2 мМ ЭДТА, с рН 6,5. Майтансиноид DM4 был растворен в диметилацетамиде (DMA, конечная концентрация 5%), затем по каплям был добавлен его 1,7-кратный молярный избыток относительно линкера к sulfb-SPDB-модифицированному антителу. рН реакционной смеси был подкорректирован до 7,5 при помощи 1 м буфера HEPES. После инкубирования в течение ночи при комнатной температуре конъюгированное антитело было очищено хроматографией на SEPHADEX™ G25F, уравновешенной 10 мМ гистидина, 250 мМ глицина, 1% сахарозы, рН 5,5. Количество молекул DM4, присоединенных к одной молекуле антитела, определялось с использованием описанных ранее коэффициентов ослабления для антитела и майтансиноида (Widdison, WC, et al., J Med Chem, 49:4392-4408 (2006)). Процентное содержание свободных майтансиноидов определялось так, как описано выше. Были получены конъюгаты с 3,5-4 молекул DM4 на антитело huMov19v1.6, присутствовало <1% неконъюгированных майтансиноидов.
Получение huMOV19v1.6-SPP-DM1
[0261] Линкер N-сукцинимидил 4-(2-пиридилдитио)пентаноат (SPP) был растворен в этаноле. Антитело huMOV19v1.6 было инкубировано в концентрации 8 мг/мл с 6,5-6-кратным молярным избытком линкера SPP в течение приблизительно 2 часов при комнатной температуре в 50 мМ калий-фосфатном буфере (рН 6,5), содержащем 50 мМ NaCl, 2 мМ ЭДТА и 5% этанола. SPP-модифицированное антитело было разбавлено 2-кратно фосфатно-солевым буфером, рН 6,5, и модифицировано 1,5-кратным молярным избытком майтансиноида DM1 путем добавления концентрированного раствора (15-30 мМ) DM1 в диметилацетамиде (ДМА). Концентрация ДМА была подкорректирована до 5%, и после инкубирования в течение ночи при комнатной температуре конъюгированное антитело было очищено хроматографией на SEPHADEX™ G25F, уравновешенной 10 мМ, 250 мМ глицина, 1% сахарозы с рН 5,5. Количество молекул DM1, присоединенных к одной молекуле антитела определялось с использованием описанных ранее коэффициентов ослабления для антитела и DM1 (Liu et al., Proc. Natl. Acad. Sci. USA, 93, 8618-8623 (1996)). Процентное количество свободного майтансиноида, присутствующего после реакции конъюгации, определялось путем инжектирования 20-50 мкг конъюгата в колонку HiSepTM, уравновешенную 25% ацетонитрила в 100 мМ аммоний-ацетатном буфере, рН 7,0, с последующим элюированием ацетонитрилом. Площадь пика общих свободных майтансиноидов разных видов (элюированных в градиенте и идентифицированных сравнением времени элюирования с известными эталонами) измерялась с использованием детектора абсорбции, настроенного на длину волны 252 нм, затем она сравнивалась с пиком, обусловленным связанным майтансиноидом (элюированным в пике конъюгата в проточных фракциях), и рассчитывалось процентное содержание свободных майтансиноидов. Были получены конъюгаты с 3,5-4 молекулами DM1 на молекулу huMov19v1.6, присутствовало <1% неконъюгированных майтансиноидов.
Получение huMOV19v1.6 SPDB-DM4
[0262] Примерный линкер N-сукцинимидил 4-(2-пиридилдитио)бутаноат (SPDB) был растворен в этаноле. Антитело huMOV19v1.6 было инкубировано в концентрации 8 мг/мл с 5,5-5-кратным молярным избытком линкера SPDB в течение приблизительно 2 часов при комнатной температуре в 50 мМ калий-фосфатном буфере (рН 6,5), содержащем 50 мМ NaCl, 2 мМ ЭДТА и 3% этанола. SPDB-модифицированное антитело было разбавлено 2-кратно фосфатно-солевым буфером, рН 6,5 и модифицировано 1,5-кратным молярным избытком майтансиноида DM4 путем добавления концентрированного раствора (15-30 мМ) DM4 в диметилацетамиде (ДМА). После инкубирования в течение ночи при комнатной температуре конъюгированное антитело было очищено хроматографией на SEPHADEX™ G25F, уравновешенной буфером, содержащим 10 мМ гистидина, 250 мМ глицина, 1% сахарозы с рН 5,5. Количество молекул DM4, присоединившихся к молекуле антитела, определялось с использованием описанных ранее коэффициентов ослабления для антитела и майтансиноида (Widdison, WC, et al., J Med Chem, 49:4392-4408 (2006)). Процентное содержание свободных майтансиноидов определялось так, как описано выше. Были получены конъюгаты с 3,5-4 молекулами DM4 на антитело huMov19v1.6, присутствовало <1% неконъюгированных майтансиноидов.
Получение huMOV19v1.0-3-sulfb-mal-DM4
[0263] Линкер NHS-3-sulfo-mal и DM4 были по отдельности растворены в ДМА. Линкер и тиоло-DM4 были смешаны друг с другом в растворе ДМА, содержащем до 40% 200 мМ сукцинатного буфера, 2 мМ ЭДТА, с рН 5,0, в молярном соотношении DM4 к линкеру, равном 1,6:1, с конечной концентрацией DM4, равной 10 мМ. Смесь взаимодействовала 2 часа при 25°С. Без очистки реакционную смесь добавляли таким образом, чтобы достичь эквивалента 9,6-молярного избытка линкера к антителу в растворе антитела huMOV19v1.0 в фосфатном буфере (рН7,5) в конечных условиях конъюгирования 4 мг/мл антитела, 90% фосфатного буфера/10% ДМА, рН 7,5, (объем/объем). После инкубирования в течение ночи при комнатной температуре конъюгированная смесь была очищена хроматографией на SEPHADEX™ G25, уравновешенной фосфатно-солевым буфером, рН 7,5. Затем huMOV19v1.0-3-sulfo-mal-DM4 был подвергнут диализу в буфере, содержащем 9,55 мМ фосфата, 139,6 мМ NaCl, pH 6,5. Количество молекул DM4, присоединенных к одной молекуле антитела, определялось с использованием описанных ранее коэффициентов ослабления для антитела и майтансиноида (Widdison, WC, et al., J. Med Chem, 49:4392-4408 (2006)). Процентное содержание свободных майтансиноидов определялось так, как описано выше. Были получены конъюгаты с 3,5-4 молекул DM4 на антитело huMov19v1.0, присутствовало <1% неконъюгированных майтансиноидов.
Получение huMOV19v1.0-SMCC-DM1
[0264] Линкер NHS-sulfo-SMCC и DM1 были по отдельности растворены в ДМА. Линкер и тиоло-DM1 были смешаны друг с другом в растворе ДМА, содержащем до 40% 200 мМ сукцинатного буфера, 2 мМ ЭДТА, с pH 5,0, в молярном соотношении DM1 к линкеру, равном 1,2:1, с конечной концентрацией DM1, равной 3,75 мМ. Смесь взаимодействовала 75 минут при 20°С. Без очистки реакционную смесь добавляли таким образом, чтобы достичь эквивалента 6,4-молярного избытка линкера к антителу в растворе антитела huMOV19v1.0 в фосфатном буфере (рН7,5) в конечных условиях конъюгирования 4 мг/мл антитела, 88% 50 мМ калия фосфата, 50 мМ NaCl, 2 мМ ЭДТА, pH 7,5/12% ДМА, pH 7,5, (объем/объем). После 2 часов инкубирования при 20°С конъюгированная смесь была очищена хроматографией на SEPHADEX™ G25, уравновешенной фосфатно-солевым буфером, pH 7,5. Конъюгат huMOV19v1.0-SMCC-DM1 затем был диализирован в буфере, содержащем 250 мМ глицина, 10 мМ гистидина, pH 5,5. Количество молекул DM1, присоединенных к одной молекуле антитела определялось с использованием описанных ранее коэффициентов ослабления для антитела и майтансиноида (Widdison, WC, et al., J Med Chem, 49:4392-4408 (2006)). Процентное содержание свободных майтансиноидов определялось так, как описано выше. Были получены конъюгаты с 3,5-4 молекулами DM1 на антитело huMov19v1.0, присутствовало <2,8% неконъюгированных майтансиноидов.
Получение huMOV19v1.0-PEG4-mal-DM1
[0265] Реактив 1 этапа NHS-PEG4-mal-DM1 был растворен в ДМА. Антитело huMov19v1.0 было инкубировано в концентрации 5 мг/мл с 5,7-кратным молярным избытком NHS-PEG4-mal-DM1 в течение ночи при 25°С в 50 мМ KPi, 50 мМ NaCl, 2 мМ ЭДТА, pH 7,5 и 10% ДМА по объему. Реакционная смесь была очищена на SEPHADEX G25, уравновешенной фосфатно-солевым буфером, рН 7,5. Конъюгат huMOV19v1.0-PEG4-mal-DM1 был диализирован в буфере, содержащем 250 мМ глицина, 10 мМ гистидина, рН 5,5. Количество молекул DM1, присоединенных к одной молекуле антитела определялось с использованием описанных ранее коэффициентов ослабления для антитела и майтансиноида (Widdison, WC, et al., J Med Chem, 49:4392-4408 (2006)). Процентное содержание свободных майтансиноидов определялось так, как описано выше. Были получены конъюгаты с 3,5-4 молекулами DM1 на антитело huMov19v1.0, присутствовало <1,1% неконъюгированных майтансиноидов.
Пример 13
Связывающая способность антител и конъюгатов
[0266] Связывающая способность антител против FOLR1 и их конъюгатов с SPDB-DM4, PEG4Mal-DM4, SMCC-DM1 или против FOLR1-sulfo-SPDB-DM4 исследовалась способом проточной цитометрии. FOLR1-экспрессирующие клетки SKOV3 были инкубированы с различными концентрациями антител против FOLR1 или их конъюгатов и обработаны так, как описано выше для анализа способом проточной цитометрии. Анализ данных проводился с использованием CellQuest Pro (BD Biosciences, Сан-Диего, США), для каждого образца снималась средняя интенсивность флуоресценции для FL1 (MFI), после чего строился полулогарифмический график ее зависимости от концентрации антитела. Кривая зависимости эффекта от дозы была построена нелинейной регрессией, и величины кажущейся равновесной константы диссоциации (Кд) исследуемых образцов при связывании с клетками SKOV3 были рассчитаны при помощи GraphPad Prism v4 (GraphPad software, Сан-Диего, Калифорния) и представлены на Фигуре 5. Результаты показывают, что конъюгирование как с DM1, так и с DM4 посредством любого использованного линкера не влияет значимым образом на аффинность каждого антитела (например, huMov19).
Пример 14
Анализы цитотоксичности in vitro
[0267] Способность примерных конъюгатов muFR1-9, muFR1-13, muFR1-22, muFR1-23, huFR1-23, muFR1-21 и huFR1-21 ингибировать клеточный рост измерялась с использованием анализов цитотоксичности in vitro способами, описанными Kovtun YV et al. (Cancer Res 66: 3214-3221 (2006)). Конъюгат PEG4-mal-DM4 был добавлен в различных концентрациях к FOLR1-экспрессирующим клеткам KB в 96-луночном планшете, находящимся по 1000 клеток на лунку в 100 мкл полной среды RPMI (RPMI-1640, 10% фетальной телячьей сыворотки, 2 мМ глутамина, 1% гентамицина, все реактивы от Invitrogen). Антитела и конъюгаты были разбавлены полной средой RPMI с использованием серий 3-кратного разбавления и добавлены по 100 мкл в лунку. Итоговая концентрация, как правило, варьировалась от 3×10-8 М до 4,6×10-12 М. На каждом планшете были контрольные лунки, содержащие клетки и среду, но не содержащие конъюгатов, а также лунки, содержащие только среду. Планшеты были инкубированы от четырех до шести дней при 37°С в инкубаторе с увлажненной атмосферой, содержащей 5% СО2. Затем в лунки был добавлен реактив WST-8, 10% объем/объем (Dojindo Molecular Technologies, Gaithersburg, Мэриленд, США), планшеты были инкубированы при 37°С 2-6 часов. WST-8 восстанавливался дегидрогеназами живых клеток до оранжевого цвета (максимальный формазановый продукт, растворимый в питательной среде). Количество образующегося формазана прямо зависело от количества живых клеток. Планшеты были проанализированы путем измерения абсорбции на 450 нм (А450) и на 650 нм (А650) в многолучном планшет-ридере. Вначале фоновую опалесценцию клеток (А650) вычитали из А650. Полученную величину А*450 затем использовали для определения выжившей фракции клеток. За фоновую абсорбцию А*450 принимали абсорбцию лунок, содержащих только среду и WST-8. Выжившую фракцию рассчитывали следующим образом: Процентная выживаемость=100×(А*450 обработанного образца - А*450 фоновая)/(А*450 необработанного образца - А*450 фоновая). Для каждой обработки были построены полулогарифмические графики зависимости величины выжившей фракции от концентрации антитела или конъюгата. Исходя из этих данных, были определены величины IC50 при помощи GraphPad Prism v4 (GraphPad software, Сан-Диего, Калифорния), которые показаны на Фигуре 5. Результаты, показанные на Фигуре 5, демонстрируют, что все конъюгаты примерно одинаковы по своей цитотоксической активности против FOLR1-экспрессирующих клеток КВ. Для дальнейшего подтверждения специфичности конъюгатов антител против FOLR1 с майтансиноидами против FOLR1 величины их активности оценивались в присутствии избытка неконъюгированных антител против клеток КВ. При добавлении избытка конкурирующего неконъюгированного антитела к конъюгатам наблюдалось подавление их цитоткосичности, что показано на Фигуре 7. Эти данные свидетельствуют о том, что конъюгаты обуславливают гибель клеток KB антиген-зависимым образом. Дополнительные данные показали, что huMov19-SPDB-DM4 индуцировало останов клетокчного цикла в фазе G2/M для клеток KB при исследованиях in vitro.
Пример 15
Эффективность in vivo конъюгатов huMov19-PEG4Mal-DM4 и huMov19-SPDB-DM4 в сравнении со схожими ненацеленными конъюгатами на модели ксенотрансплантата KB
[0268] На установленной ксенотрансплантатной модели клеток KB, имплантированных подкожно мышам с ТКИН, был протестирован FOLR1-нацеленный расщепляемый конъюгат huMov19-SPDB-DM4 в сравнении с ненацеленным huC242-SPDB-DM4, а также нерасщепляемый конъюгат huMov19-PEG4-Mal-DM4 в сравнении с ненацеленным huC242-PEG4Mal-DM4. Мыши были рандомизированы по весу тела в терапевтические группы и получали терапию либо однократно (конъюгаты SPDB) на 3 день после инокуляции клеток, либо три раза еженедельно на 3, 10 и 17 день после инокуляции клеток по 5 и 10 мг/кг конъюгата, соответственно. Медианный объем опухоли в различных терапевтических группах показан на Фигуре 8. При терапии huMov19-SPDB-DM4 или huMov19-PEG4Mal-DM4 наблюдалось уменьшение медианного объема опухоли в сравнении с контрольной терапией фосфатно-солевым буфером, в то время как при терапии ненацеленным конъюгатом значимого эффекта не наблюдалось.
Пример 16
Эффективность in vivo конъюгатов против FOLR1-PEG4Mal-DM4 на модели ксенотрансплантата KB
[0269] Конъюгаты PEG4Mal-DM4 примерных антител против FOLR1 huMov19, muFR-1-9, muFR-1-13, muFR-1-22, muFR-1-23 и huFR-1-21 были протестированы с использованием установленной ксенотрансплантатной модели клеток KB, имплантированных подкожно мышам с ТКИН. Мыши были рандомизированы по весу тела в терапевтические группы и получали однократно на 3 день после инокуляции клеток по 10 мг/кг одного из вышеперечисленных конъюгатов либо только фосфатно-солевой буфер. Как было показано выше, huMov19-PEG4Mal-DM4 по цитотоксической активности in vitro схож с конъюгатами PEG4Mal-DM4 и muFR-1-9, muFR-1-13, muFR-1-22, muFR-1-23, huFR-1-21. HuMov19-PEG4Mal-DM4 и huFR-1-21-PEG4Mal-DM4 были существенно более активны in vivo, чем любой из других конъюгатов, обеспечивая более выраженное уменьшение медианного объема опухоли (Фигуры 9 и 10). Как было показано, активность имеет дозозависимый характер (Фигра 11), также на нее влияет выбор линкера (Фигуры 12 и 13).
Пример 17
Эффективность in vivo конъюгатов против FOLR1-sulfo-SPDB-DM4 на моделях ксенотрансплантатов
[0270] Конъюгаты против FOLR1 huMov19-sulfo-SPDB-DM4 были протестированы на трех ксенотрансплантатах серозной аденокарциномы яичника: OVCAR-3, IGROV-1 и OV-90. В каждой из этих ксенотрансплантатных опухолей наблюдались уровни экспрессии FOLR1, сравнимые с опухолями у пациентов при измерении с использованием способа калиброванного иммуногистохимического окрашивания (IHC) зафиксированных в формалине залитых парафином срезов. Мыши с установленными подкожными ксенотрансплантатными опухолями (приблизительно 100 мм3) получали однократную внутривенную инъекцию конъюгата huMov19-sulfo-SPDB-DM4 по 1,2, 2,5 и 5,0 мг/кг (основываясь на концентрации антител; на Фигурах 14-16 показана концентрация майтансиноидного конъюгата в мкг/кг). Конъюгат был активен во всех трех исследованных моделях. Для ксенотрансплантатов OVCAR-3 минимальная эффективная доза (МЭД) составляла 1,2 мг/кг (Фигура 14). Более высокие уровни доз были высокоактивны, приводя к полным регрессиям (ПР) у 4/6 и 2/6 мышей в терапевтических группах 2,5 и 5,0 мг/кг, соответственно. При терапии конъюгатом наблюдалась сильная противоопухолевая активность для обеих моделей ксенотрансплататов IGROV-1 и OV-90 с МЭД при однократном введении 2,5 мг/кг (Фигуры 15 и 16). Эти данные свидетельствуют о сильной противоопухолевой активности конъюгатов huMov19-sulfo-SPDB-DM4 против ксенотрансплантатных опухолей яичника с уровнями экспрессии FOLR1, сравнимыми с опухолями пациентов.
Пример 18
Влияние линкеров на эффективность иммуноконъюгата
[0271] Антитело huMov19 против FOLR1 было соединено с DM1 или DM4 через дисульфид-содержащие расщепляемые линкеры SPP, SPDB или sulfo-SPDB либо через нерасщепляемый линкер SMCC. Изучалась цитотоксическая активность in vitro этих конъюгатов на клеточных линиях KB, IGROV-1 и JEG-3. Анализ FACS показал, что клетки KB (цервикальные) обладали >2000000 антитело-связывающих сайтов на клетку. Клетки IGROV-1 (яичника) имели 260000 антитело-связывающих сайтов на клетку, а клетки JEG-3 (хориокарциономы) имели 40000 антитело-связывающих сайтов на клетку. Результаты изучения цитотоксичности in vitro представлены в Таблице 2 ниже. У расщепляемых конъюгатов наблюдалась существенно большая активность in vitro в сравнении с SMCC-конъюгатом.
[0272] Также была определена активность конъюгатов in vivo на моделях FOLR1-положительных KB- и О VCAR-3-опухолей. Результаты, представленные на Фигуре 17, свидетельствуют о более очевидном действии расщепляемых конъюгатов SPDB-DM4 и sulfo-SPDB-DM4 в сравнении с нерасщепляемыми конъюгатами SMCC-DM1 in vivo. Помимо этого, среди расщепляемых конъюгатов конъюгат SPP-DM1 был менее активен, чем конъюгаты SPDB-DM4 или sulfo-SPDB-DM4 в обеих ксенотрансплантатных моделях (Фигура 18). Два последних конъюгата обладали приблизительно одинаковой активностью против опухолей KB, в то время как в модели OVCAR-3 был более активен конъюгат sulfo-SPDB-DM4. Данные, полученные с использованием модели OVCAR-3, представлены в Таблице 3 ниже.
[0273] Эти данные свидетельствуют о том, что иммуноконъюгаты, содержащие расщепляемый линкер, обладают повышенной эффективностью как in vitro, так и in vivo, и что иммуноконъюгаты против FOLR1, содержащие sulfo-SPDB, высокоактивны на опухолевых моделях.
Пример 19
Эффективность конъюгата антитела huFR1 с SMCC-DM1 in vitro и in vivo
[0274] Антитела против FOLR1 huFR1-48, huFR1-49, huFR1-57 и huFR1-65 были конъюгированы с линкером SMCC и DM1, при помощи описанных выше ксенотрансплантатных моделей анализировались эффекты на клетки KB и in vivo, так, как это описано выше. Хотя каждое из антител обладало приблизительно одинаковой эффективностью в моделей клеток KB, иммуноконъюгаты huFR1-48, huFR1-49, huFR1-57 и huFR1-65 проявляли различную, но выраженную эффективность in vivo при дозе 200 мкг/кг в ксенотрансплантатной модели (Таблица 4 и Фигура 19).
[0275] Все публикации, патенты, патентные заявки, интернет-сайты и номера доступа/последовательности в базе данных (включая как полинуклеотидные, так и полипептидные последовательности), упомянутые здесь, включены посредством ссылки во всей полноте для всех целей и в пределах такого же охвата, что и каждая индивидуальная публикация, патент, патентная заявка, интернет-сайт или номер доступа/последовательности в базе данных, специфически и индивидуально указанные как включенная посредством ссылки.
Реферат
Изобретение относится к области биотехнологии и иммунологии. Предложено гуманизированное антитело и его антиген-связывающий фрагмент, специфически связывающиеся с рецептором фолиевой кислоты 1 (FOLR1) человека и охарактеризованные аминокислотными последовательностями участков, определяющих комплементарность с антигеном (CDR). Также предложен способ получения гуманизированного антитела по изобретению; иммуноконъюгаты с цитотоксическим средством; фармацевтические композиции; диагностическая композиция; наборы; способы ингибирования роста опухоли и способ лечения рака. Рассмотрены выделенные полинуклеотиды, кодирующие вариабельные домены антитела по изобретению; содержащие их векторы и клетки-хозяева. Антитело по изобретению является гуманизированной формой мышиного антитела Mov19 и может найти дальнейшее применение в терапии заболеваний, характеризующихся повышенной экспрессией FOLR1. 20 н. и 49 з.п. ф-лы, 19 ил., 4 табл., 19 пр.

Комментарии