Производные хиназолинона, применимые в качестве модуляторов fgfr киназы - RU2701517C2
Код документа: RU2701517C2
Описание
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к новым соединениям производным хиназолинона, к фармацевтическим композициям, содержащим указанные соединения, к способам получения указанных соединений и к применению указанных соединений в лечении заболеваний, например рака.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Согласно первому аспекту изобретения предложены соединения формулы (I):
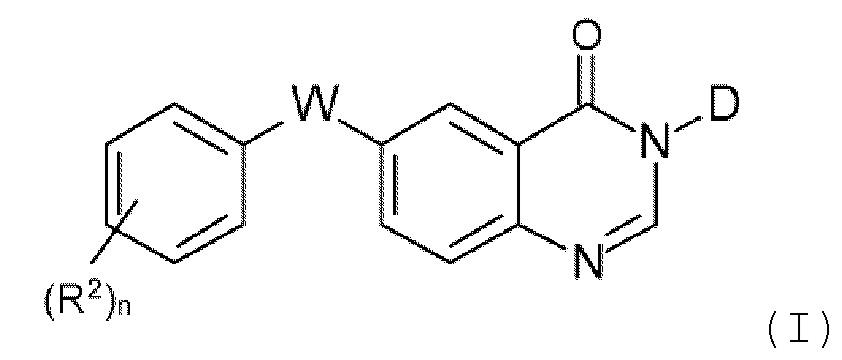
включая их любую таутомерную или стереохимически изомерную форму, где:
W представляет собой -N(R3)- или -C(R3aR3b)-;
каждый R2 независимо выбран из гидроксила, галогена, циано, C1-4алкила, C2-4алкенила, C2-4алкинила, C1-4алкокси, гидроксиC1-4алкила, гидроксиC1-4алкокси, галоC1-4алкила, галоC1-4алкокси, гидроксигалоC1-4алкила, гидроксигалоC1-4алкокси, C1-4алкоксиC1-4алкила, галоC1-4алкоксиC1-4алкила, C1-4алкоксиC1-4алкила, где каждый C1-4алкил необязательно может быть замещен одной или двумя гидроксильными группами, гидроксигалоC1-4алкоксиC1-4алкила, R13, C1-4алкила, который замещен R13, C1-4алкила, который замещен -C(=O)-R13, C1-4алкокси, который замещен R13, C1-4алкокси, который замещен -C(=O)-R13, -C(=O)-R13, C1-4алкила, который замещен -NR7R8, C1-4алкила, который замещен -C(=O)-NR7R8, C1-4алкокси, который замещен -NR7R8, C1-4алкокси, который замещен -C(=O)-NR7R8, -NR7R8 и -C(=O)-NR7R8; или когда две группы R2 присоединены к соседним атомам углерода, они могут быть объединены с образованием радикала формулы:
-O-(C(R17)2)p-O-;
-X-CH=CH-; или
-X-CH=N-; где R17 является водородом или фтором, p представляет собой 1 или 2, и X представляет собой O или S;
D представляет собой 3-12-членный моноциклический или бициклический карбоциклил или 3-12-членный моноциклический или бициклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, O или S, где каждый указанный карбоциклил и гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1;
R1 представляет собой водород, галоген, циано, C1-6алкил, C1-6алкокси, -C(=O)-O-C1-6алкил, C2-4алкенил, гидроксиC1-6алкил, галоC1-6алкил, гидроксигалоC1-6алкил, цианоC1-4алкил, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, -NR4R5, C1-6алкил, который замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен -NR4R5, -C(=O)-NR4R5, -C(=O)-C1-6алкил-NR4R5, C1-6алкил, который замещен -C(=O)-NR4R5, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NH-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, R6, C1-6алкил, который замещен R6, -C(=O)-R6, C1-6алкил, который замещен -C(=O)-R6, гидроксиC1-6алкил, который замещен R6, C1-6алкил, который замещен -Si(CH3)3, C1-6алкил, который замещен-P(=O)(ОH)2, или C1-6алкил, который замещен -P(=O)(OC1-6алкилом)2;
R3a представляет собой -NR10R11, гидроксил, C1-6алкокси, гидроксиC1-6алкокси, C1-6алкокси, который замещен -NR10R11, C1-6алкил, C2-6алкенил, C2-6алкинил, галоC1-6алкил, необязательно замещенный -O-C(=O)-C1-6алкилом, гидроксиC1-6алкил, необязательно замещенный -O-C(=O)-C1-6алкилом, гидроксиC2-6алкенил, гидроксиC2-6алкинил, гидроксигалоC1-6алкил, цианоC1-6алкил, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -C(=O)-C1-6алкилом, C1-6алкил, который замещен-C(=O)-O-C1-6алкилом, C1-6алкил, который замещен C1-6алкоксиC1-6алкил-O-C(=O)-, C1-6алкил, который замещен C1-6алкоксиC1-6алкил-C(=O)-, C1-6алкил, который замещен -O-C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами или -O-C(=O)-C1-6алкилом, C2-6алкенил, который замещен C1-6алкокси, C2-6алкинил, который замещен C1-6алкокси, C1-6алкил, который замещен R9 и который необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен -C(=O)-R9, C1-6алкил, который замещен гидроксилом и R9, C2-6алкенил, который замещен R9, C2-6алкинил, который замещен R9, C1-6алкил, который замещен -NR10R11, C2-6алкенил, который замещен -NR10R11, C2-6алкинил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя галогенами и -NR10R11, -C1-6алкил-C(R12)=N-O-R12, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -O-C(=O)-NR10R11, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, R13, C1-6алкил, который замещен -P(=O)(ОH)2, или C1-6алкил, который замещен -P(=O)(OC1-6алкилом)2;
R3b представляет собой водород или гидроксил; при условии, что если R3a представляет собой -NR10R11, то R3b представляет собой водород; или
R3a и R3b объединены с образованием =O, с образованием =NR10, с образованием циклопропила вместе с атомом углерода, к которому они присоединены, с образованием =CH-C0-4алкила, замещенного R3c, или с образованием

R3c представляет собой водород, гидроксил, C1-6алкокси, R9, -NR10R11, циано, -C(=O)-C1-6алкил или -CH(ОН)-C1-6алкил;
R3 представляет собой гидроксил, C1-6алкокси, гидроксиC1-6алкокси, C1-6алкокси, который замещен -NR10R11, C1-6алкил, C2-6алкенил, C2-6алкинил, галоC1-6алкил, необязательно замещенный -O-C(=O)-C1-6алкил, гидроксиC1-6алкил, необязательно замещенный -O-C(=O)-C1-6алкилом, гидроксиC2-6алкенил, гидроксиC2-6алкинил, гидроксигалоC1-6алкил, цианоC1-6алкил, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -C(=O)-C1-6алкилом, C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, C1-6алкил, который замещен C1-6алкоксиC1-6алкил-O-C(=O)-, C1-6алкил, который замещен C1-6алкоксиC1-6алкил-C(=O)-, C1-6алкил, который замещен -O-C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами или -O-C(=O)-C1-6алкилом, C2-6алкенил, который замещен C1-6алкокси, C2-6алкинил, который замещен C1-6алкокси, C1-6алкил, который замещен R9 и который необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен -C(=O)-R9, C1-6алкил, который замещен гидроксилом и R9, C2-6алкенил, который замещен R9, C2-6алкинил, который замещен R9, C1-6алкил, который замещен -NR10R11, C2-6алкенил, который замещен -NR10R11, C2-6алкинил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя галогенами и -NR10R11, -C1-6алкил-C(R12)=N-O-R12, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -O-C(=O)-NR10R11, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, R13, C1-6алкил, который замещен -P(=O)(ОH)2, или C1-6алкил, который замещен -P(=O)(OC1-6алкилом)2;
каждый R4 и R5 независимо представляет собой водород, C1-6алкил, C1-6алкил, который замещен -NR14R15, гидроксиC1-6алкил, галоC1-6алкил, гидроксигалоC1-6алкил, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, -C(=O)-NR14R15, -C(=O)-O-C1-6алкил, -C(=O)-R13, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NH-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-NR14R15, R13 или C1-6алкил, который замещен R13;
R6 представляет собой C3-8циклоалкил, C3-8циклоалкенил, фенил, 4-7-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, O или S, при этом указанный C3-8циклоалкил, C3-8циклоалкенил, фенил, 4-7-членный моноциклический гетероциклил необязательно, и каждый независимо, могут быть замещены 1, 2, 3, 4 или 5 заместителями, где каждый заместитель независимо выбран из циано, C1-6алкила, цианоC1-6алкила, гидроксила, карбоксила, гидроксиC1-6алкила, галогена, галоC1-6алкила, гидроксигалоC1-6алкила, C1-6алкокси, C1-6алкоксиC1-6алкила, C1-6алкил-O-C(=O)-, -NR14R15, -C(=O)-NR14R15, C1-6алкила, который замещен -NR14R15, C1-6алкила, который замещен -C(=O)-NR14R15, -S(=O)2-C1-6алкила, -S(=O)2-галоC1-6алкила, -S(=O)2-NR14R15, C1-6алкила, который замещен -S(=O)2-C1-6алкилом, C1-6алкила, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкила, который замещен -S(=O)2-NR14R15, C1-6алкила, который замещен -NH-S(=O)2-C1-6алкилом, C1-6алкила, который замещен -NH-S(=O)2-галоC1-6алкилом, или C1-6алкила, который замещен -NH-S(=O)2-NR14R15;
каждый R7 и R8 независимо представляет собой водород, C1-6алкил, гидроксиC1-6алкил, галоC1-6алкил, гидроксигалоC1-6алкил или C1-6алкоксиC1-6алкил;
R9 представляет собой C3-8циклоалкил, C3-8циклоалкенил, фенил, нафтил или 3-12-членный моноциклический или бициклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, O или S, где указанный C3-8циклоалкил, C3-8циклоалкенил, фенил, нафтил или 3-12-членный моноциклический или бициклический гетероциклил, каждый необязательно и каждый независимо, замещены 1, 2, 3, 4 или 5 заместителями, причем каждый заместитель независимо выбран из =O, C1-4алкила, гидроксила, карбоксила, гидроксиC1-4алкила, циано, цианоC1-4алкила, C1-4алкил-O-C(=O)-, C1-4алкила, который замещен C1-4алкил-O-C(=O)-, C1-4алкил-C(=O)-, C1-4алкоксиC1-4алкила, где каждый C1-4алкил необязательно может быть замещен одной или двумя гидроксильными группами, галогеном, галоC1-4алкила, гидроксигалоC1-4алкила, -NR14R15, -C(=O)-NR14R15, C1-4алкила, который замещен -NR14R15, C1-4алкила, который замещен -C(=O)-NR14R15, C1-4алкокси, -S(=O)2-C1-4алкила, -S(=O)2-галоC1-4алкила, -S(=O)2-NR14R15, C1-4алкила, который замещен -S(=O)2-NR14R15, C1-4алкила, который замещен -NH-S(=O)2-C1-4алкилом, C1-4алкила, который замещен -NH-S(=O)2-галоC1-4алкилом, C1-4алкила, который замещен -NH-S(=O)2-NR14R15, R13, -C(=O)-R13, C1-4алкила, который замещен R13, фенила, который необязательно замещен R16, фенилC1-6алкила, где фенил необязательно замещен R16, 5 или 6-членного ароматического моноциклического гетероциклила, содержащего по меньшей мере один гетероатом, выбранный из N, O или S, где указанный гетероциклил необязательно замещен R16; или когда два из заместителей R9 присоединены к одному и тому же атому, они вместе могут формировать 4-7-членный насыщенный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, O или S;
каждый R10 и R11 независимо представляет собой водород, карбоксил, C1-6алкил, цианоC1-6алкил, C1-6алкил, который замещен -NR14R15, C1-6алкил, который замещен -C(=O)-NR14R15, галоC1-6алкил, гидроксиC1-6алкил, гидроксигалоC1-6алкил, C1-6алкокси, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, R6, C1-6алкил, который замещен R6, -C(=O)-R6, -C(=O)-C1-6алкил, -C(=O)-гидроксиC1-6алкил, -C(=O)-галоC1-6алкил, -C(=O)-гидроксигалоC1-6алкил, C1-6алкил, который замещен -Si(CH3)3, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NH-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен карбоксилом, или C1-6алкил, который замещен -NH-S(=O)2-NR14R15;
R12 представляет собой водород или C1-4алкил, который необязательно замещен C1-4алкокси;
R13 представляет собой C3-8циклоалкил или насыщенный 4-6-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, O или S, где указанный C3-8циклоалкил или моноциклический гетероциклил необязательно замещены 1, 2 или 3 заместителями, каждый из которых независимо выбран из галогена, гидроксила, C1-6алкила, галоC1-6алкила, =O, циано, -C(=O)-C1-6алкила, C1-6алкокси или -NR14R15;
каждый R14 и R15 независимо представляет собой водород или галоC1-4алкил, или C1-4алкил, который необязательно замещен заместителем, выбранным из гидроксила, C1-4алкокси, амино или моно- или ди(C1-4алкил)амино;
R16 представляет собой гидроксил, галоген, циано, C1-4алкил, C1-4алкокси, -NR14R15 или -C(=O)NR14R15;
n независимо представляет собой целое число, равное 0, 1, 2, 3 или 4;
их N-оксиды, фармацевтически приемлемые соли или сольваты.
WO2012/118492, WO2006/092430, WO2008/003702, WO01/68047, WO2005/007099, WO2004/098494, WO2009/141386, WO2004/030635, WO2008/141065, WO2011/026579, WO2011/028947, WO2007/003419, WO00/42026, WO2012/154760, WO2011/047129, WO2003/076416, WO2002/096873, WO2000/055153, EP548934, US4166117, WO2011/135376 и WO2012/073017, в которых раскрыт ряд гетероциклильных производных.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Если из контекста не следует иное, ссылки на формулу (I) во всех разделах настоящего документа (включая применения, способы и другие аспекты изобретения) включают ссылки на все другие подформулы (например, Ia), подгруппы, предпочтения, варианты осуществления и примеры, как определено в настоящем описании.
Префикс "Cx-y" (где x и y являются целыми числами), при использовании в настоящем описании, относится к количеству атомов углерода в данной группе. Таким образом, С1-6алкильная группа содержит от 1 до 6 атомов углерода, С3-6циклоалкильная группа содержит от 3 до 6 атомов углерода, С1-4алкоксигруппа содержит от 1 до 4 атомов углерода и так далее.
Термин "гало" или "галоген", при использовании в настоящем описании, относится к атому фтора, хлора, брома или иода.
Термин "C1-4алкил" или "C1-6алкил", при использовании в настоящем описании для обозначения группы или части группы, относится к нормальной или разветвленной насыщенный углеводородной группе, содержащей от 1 до 4 или от 1 до 6 атомов углерода. Примеры таких групп включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил или гексил и т.п.
Термин "С2-4алкенил" или "С2-6алкенил", при использовании в настоящем описании для обозначения группы или части группы, относится к нормальной или разветвленной углеводородной группе, содержащей от 2 до 4 или от 2 до 6 атомов углерода и содержащей углерод-углеродную двойную связь.
Термин "С2-4алкинил" или "С2-6алкинил", при использовании в настоящем описании для обозначения группы или части группы, относится к нормальной или разветвленной углеводородной группе, содержащей от 2 до 4 или от 2 до 6 атомов углерода и содержащей углерод-углеродную тройную связь.
Термин "С1-4алкокси" или "С1-6алкокси", при использовании в настоящем описании для обозначения группы или части группы, относится к -O-C1-4алкильной группе или -O-C1-6алкильной группе, где C1-4алкил и C1-6алкил являются такими, как определено в настоящем описании. Примеры таких групп включают метокси, этокси, пропокси, бутокси и т.п.
Термин "С1-4алкоксиC1-4алкил" или "С1-6алкоксиC1-6алкил", при использовании в настоящем описании для обозначения группы или части группы, относится к C1-4алкил-O-C1-4алкильной группе или C1-6алкил-O-C1-6алкильной группе, где C1-4алкил и C1-6алкил являются такими, как определено в настоящем описании. Примеры таких групп включают метоксиэтил, этоксиэтил, пропоксиметил, бутоксипропил и т.п.
Термин "C3-8циклоалкил", при использовании в настоящем описании, относится к насыщенному моноциклическому углеводородному кольцу, содержащему 3-8 атомов углерода. Примеры таких групп включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил или циклооктил и т.п.
Термин "C3-8циклоалкенил", при использовании в настоящем описании, относится к моноциклическому углеводородному кольцу, содержащему 3-8 атомов углерода, имеющему углерод-углеродную двойную связь.
Термин "гидроксиC1-4алкил" или "гидроксиC1-6алкил", при использовании в настоящем описании для обозначения группы или части группы, относится к C1-4алкильной или C1-6алкильной группе, как определено в настоящем описании, где один или более одного атома водорода заменены гидроксильной группой. Таким образом, термины "гидроксиC1-4алкил" или "гидроксиC1-6алкил" включают моногидроксиC1-4алкил, моногидроксиC1-6алкил, а также полигидроксиC1-4алкил и полигидроксиC1-6алкил. Один, два, три или более атомов водорода могут быть заменены гидроксильной группой, при этом гидроксиC1-4алкил или гидроксиC1-6алкил могут иметь одну, две, три или более гидроксильные группы. Примеры таких групп включают гидроксиметил, гидроксиэтил, гидроксипропил и т.п.
Термин "галогенC1-4алкил" или "галогенC1-6алкил", при использовании в настоящем описании для обозначения группы или части группы, относится к C1-4алкильной или C1-6алкильной группе, как определено в настоящем описании, где один или более одного атома водорода заменены галогеном. Таким образом, термин "галогенC1-4алкил" или "галогенC1-6алкил" включает моногалогенC1-4алкил, моногалогенC1-6алкил, а также полигалогенC1-4алкил и полигалогенC1-6алкил. Один, два, три или более атомов водорода могут быть заменены галогеном, при этом галогенC1-4алкил или галогенC1-6алкил могут иметь один, два, три или более атомов галогена. Примеры таких групп включают фторэтил, фторметил, трифторметил или трифторэтил и т.п.
Термин "гидроксигалогенC1-4алкил" или "гидроксигалогенC1-6алкил", при использовании в настоящем описании для обозначения группы или части группы, относится к C1-4алкильной или C1-6алкильной группе, как определено в настоящем описании, где один или более одного атома водорода заменены гидроксильной группой и один или более одного атома водорода заменены галогеном. Таким образом, термин "гидроксигалогенC1-4алкил" или "гидроксигалогенC1-6алкил" относится к C1-4алкильной или C1-6алкильной группе, где один, два, три или более атомов водорода заменены гидроксильной группой и один, два, три или более атомов водорода заменены галогеном.
Термин "гидроксиС1-4алкокси" или "гидроксиС1-6алкокси", при использовании в настоящем описании для обозначения группы или части группы, относится к -O-C1-4алкильной группе или -O-C1-6алкильной группе, где C1-4алкильная и C1-6алкильная группа является такой, как определено выше, и один или более одного атома водорода C1-4алкильной и C1-6алкильной группы заменены гидроксильной группой. Таким образом, термин "гидроксиС1-4алкокси" или "гидроксиС1-6алкокси" включает моногидроксиС1-4алкокси, моногидроксиС1-6алкокси, а также полигидроксиС1-4алкокси и полигидроксиС1-6алкокси. Один, два, три или более атомов водорода могут быть заменены гидроксильной группой, при этом гидроксиС1-4алкоксигруппа или гидроксиС1-6алкоксигруппа может содержать одну, две, три или более гидроксильных групп. Примеры таких групп включают гидроксиметокси, гидроксиэтокси, гидроксипропокси и т.п.
Термин "галогенС1-4алкокси" или "галогенС1-6алкокси", при использовании в настоящем описании для обозначения группы или части группы, относится к -O-C1-4алкильной группе или -O-C1-6алкильной группе, как определено в настоящем описании, где один или более одного атома водорода заменены галогеном. Таким образом, термины "галогенС1-4алкокси" или "галогенС1-6алкокси" включают моногалогенС1-4алкокси, моногалогенС1-6алкокси, а также полигалогенС1-4алкокси и полигалогенС1-6алкокси. Один, два, три или более атомов водорода могут быть заменены галогеном, так что галогенC1-4алкокси или галогенC1-6алкокси могут иметь один, два, три или более атомов галогена. Примеры таких групп включают фторэтилокси, дифторметокси или трифторметокси и т.п.
Термин "гидроксигалогенС1-4алкокси", при использовании в настоящем описании для обозначения группы или части группы, относится к -O-C1-4алкильной группе, где C1-4алкильная группа является такой, как определено в настоящем описании, и где один или более одного атома водорода заменены гидроксильной группой, и один или более одного атома водорода заменены галогеном. Таким образом, термин "гидроксигалогенС1-4алкокси" относится к -O-C1-4алкильной группе, где один, два, три или более атомов водорода заменены гидроксильной группой и один, два, три или более атомов водорода заменены галогеном.
Термин "галогенС1-4алкоксиC1-4алкил", при использовании в настоящем описании для обозначения группы или части группы, относится к C1-4алкил-O-C1-4алкильной группе, где C1-4алкил является таким, как определено в настоящем описании, и где в одной или в обеих C1-4алкильных группах один или более одного атома водорода заменены галогеном. Таким образом, термин "галогенС1-4алкоксиC1-4алкил" относится к C1-4алкил-O-C1-4алкильной группе, где в одной или в обеих C1-4алкильных группах один, два, три или более атомов водорода заменены галогеном, и где C1-4алкил является таким, как определено в настоящем описании. Предпочтительно, в одной из C1-4алкильных групп один или более одного атома водорода заменены галогеном. Предпочтительно, галогенС1-4алкоксиC1-4алкил означает C1-4алкил, замещенный галогенC1-4алкоксигруппой.
Термин "гидроксигалогенС1-4алкоксиC1-4алкил", при использовании в настоящем описании, относится к C1-4алкил-O-C1-4алкильной группе, где C1-4алкил является таким, как определено в настоящем описании, и где в одной или в обеих C1-4алкильных группах один или более одного атома водорода заменены гидроксильной группой и один или более одного атома водорода заменены галогеном. Таким образом, термин "гидроксигалогенС1-4алкоксиC1-4алкил" относится к C1-4алкил-O-C1-4алкильной группе, где в одной или в обеих C1-4алкильных группах один, два, три или более атомов водорода заменены гидроксильной группой, и один, два, три или более атомов водорода заменены галогеном и где C1-4алкил является таким, как определено в настоящем описании.
Термин "гидроксиС2-6алкенил", при использовании в настоящем описании, относится к С2-6алкенильной группе, где один или более одного атома водорода заменены гидроксильной группой и где С2-6алкенил является таким, как определено в настоящем описании.
Термин "гидроксиС2-6алкинил", при использовании в настоящем описании, относится к С2-6алкинильной группе, где один или более одного атома водорода заменены гидроксильной группой, и где С2-6алкинил является таким, как определено в настоящем описании.
Термин "фенилС1-6алкил", при использовании в настоящем описании, относится к С1-6алкильной группе, как определено в настоящем описании, которая замещена одной фенильной группой.
Термин "цианоC1-4алкил" или "цианоC1-6алкил", при использовании в настоящем описании, относится к C1-4алкильной или C1-6алкильной группе, как определено в настоящем описании, которая замещена одной цианогруппой.
Термин "гетероциклил", при использовании в настоящем описании, должен, если из контекста не следует иное, включать как ароматические, так и неароматические кольцевые системы. Таким образом, например, термин "гетероциклильная группа" включает в пределах своего объема ароматические, неароматические, ненасыщенные, частично насыщенные и полностью насыщенные гетероциклильные кольцевые системы. В общем, если из контекста не следует иное, такие группы могут быть моноциклическими или бициклическими и могут содержать, например, от 3 до 12 членов в кольце, еще чаще от 5 до 10 членов в кольце. Примеры групп, содержащих от 4 до 7 членов в кольце, включают 4, 5, 6 или 7 атомов в кольце, и примеры групп, содержащих от 4 до 6 членов в кольце, включают 4, 5 или 6 атомов в кольце. Примерами моноциклических групп являются группы, содержащие 3, 4, 5, 6, 7 и 8 членов в кольце, еще чаще от 3 до 7, и предпочтительно 5, 6 или 7 членов в кольце, более предпочтительно 5 или 6 членов в кольце. Примерами бициклических групп являются группы, содержащие 8, 9, 10, 11 и 12 членов в кольце, и еще чаще 9 или 10 членов в кольце. В случае отсылки к гетероциклильным группам, гетероциклильное кольцо, если из контекста не следует иное, необязательно может быть замещено (т.е. не замещено или замещено) одним или более заместителями, как обсуждается в настоящем описании.
Гетероциклильные группы могут быть гетероарильными группами, содержащими от 5 до 12 членов в кольце, еще чаще от 5 до 10 членов в кольце. Термин "гетероарил" используют в описании для обозначения гетероциклильной группы, имеющей ароматический характер. Термин "гетероарил" охватывает полициклические (например, бициклические) кольцевые системы, где одно или более колец являются неароматическими, при условии, что по меньшей мере одно кольцо является ароматическим. В таких полициклических системах группа может быть присоединена ароматическим кольцом или неароматическим кольцом.
Примерами гетероарильных групп являются моноциклические и бициклические группы, содержащие от пяти до двенадцати членов в кольце, и еще чаще от пяти до десяти членов в кольце. Гетероарильная группа может представлять собой, например, пятичленное или шестичленное моноциклическое кольцо или бициклическую структуру, образованную из конденсированных пятичленных и шестичленных колец или двух конденсированных шестичленных колец или двух конденсированных пятичленных колец. Каждое кольцо может содержать до приблизительно пяти гетероатомов, обычно выбранных из атомов азота, серы и кислорода. Как правило, гетероарильное кольцо содержит до 4 гетероатомов, точнее до 3 гетероатомов, еще чаще до 2, например, один гетероатом. В одном варианте осуществления изобретения гетероарильное кольцо содержит по меньшей мере один атом азота в кольце. Атомы азота в гетероарильных кольцах могут быть основными, как в случае имидазола или пиридина, или по существу не основными, как в случае азота индола или пиррола. В большинстве случаев количество основных атомов азота, присутствующих в гетероарильной группе, включающей любые заместители аминогруппы кольца, составляет менее пяти.
Примеры пятичленных гетероарильных групп включают, без ограничения, пиррольные, фурановые, тиофеновые, имидазольные, фуразановые, оксазольные, оксадиазольные, оксатриазольные, изоксазольные, тиазольные, тиадиазольные, изотиазольные, пиразольные, триазольные и тетразольные группы.
Примеры шестичленных гетероарильных групп включают, без ограничения, пиридин, пиразин, пиридазин, пиримидин и триазин.
Бициклическая гетероарильная группа может быть, например, группой, выбранной из:
а) бензольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1, 2 или 3 гетероатома в кольце;
b) пиридинового кольца, конденсированного с 5- или 6-членным кольцом, содержащим 0, 1, 2 или 3 гетероатома в кольце;
c) пиримидинового кольца, конденсированного с 5- или 6-членным кольцом, содержащим 0, 1 или 2 гетероатома в кольце;
d) пиррольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 0, 1, 2 или 3 гетероатома в кольце;
e) пиразольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 0, 1 или 2 гетероатома в кольце;
f) имидазольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 0, 1 или 2 гетероатома в кольце;
g) оксазольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 0, 1 или 2 гетероатома в кольце;
h) изоксазольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 0, 1 или 2 гетероатома в кольце;
i) тиазольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 0, 1 или 2 гетероатома в кольце;
j) изотиазольного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 0, 1 или 2 гетероатома в кольце;
k) тиофенового кольца, конденсированного с 5- или 6-членным кольцом, содержащим 0, 1, 2 или 3 гетероатома в кольце;
l) фуранового кольца, конденсированного с 5- или 6-членным кольцом, содержащим 0, 1, 2 или 3 гетероатома в кольце;
m) циклогексильного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1, 2 или 3 гетероатома в кольце; и
n) циклопентильного кольца, конденсированного с 5- или 6-членным кольцом, содержащим 1, 2 или 3 гетероатома в кольце.
Конкретные примеры бициклических гетероарильных групп, содержащих пятичленное кольцо, конденсированное с другим пятичленным кольцом, включают, без ограничения, имидазотиазол (например, имидазо[2,1-b]тиазол) и имидазоимидазол (например, имидазо[1,2-a]имидазол).
Конкретные примеры бициклических гетероарильных групп, содержащих шестичленное кольцо, конденсированное с пятичленным кольцом, включают, без ограничения, бензофурановые, бензотиофеновые, бензимидазольные, бензоксазольные, изобензоксазольные, бензизоксазольные, бензотиазольные, бензизотиазольные, изобензофурановые, индольные, изоиндольные, индолизиновые, индолиновые, изоиндолиновые, пуриновые (например, адениновые, гуаниновые), индазольные, пиразолопиримидиновые (например, пиразоло[1,5-a]пиримидиновые), триазолопиримидиновые (например, [1,2,4]триазоло[1,5-a]пиримидиновые), бензодиоксольные, имидазопиридиновые и пиразолопиридиновые (например, пиразоло[1,5-a]пиридиновые) группы.
Конкретные примеры бициклических гетероарильных групп, содержащих два конденсированных шестичленных кольца, включают, без ограничения, хинолиновые, изохинолиновые, хромановые, тиохромановые, хроменовые, изохроменовые, изохромановые, бензодиоксановые, хинолизиновые, бензоксазиновые, бензодиазиновые, пиридопиридиновые, хиноксалиновые, хиназолиновые, циннолиновые, фталазиновые, нафтиридиновые и птеридиновые группы.
Примеры полициклических гетероарильных групп, содержащих ароматическое кольцо и неароматическое кольцо, включают тетрагидроизохинолиновые, тетрагидрохинолиновые, дигидробензтиеновые, дигидробензофурановые, 2,3-дигидробензо[1,4]диоксиновые, бензо[1,3]диоксольные, 4,5,6,7-тетрагидробензофурановые, тетрагидротриазолопиразиновые (например, 5,6,7,8-тетрагидро-[1,2,4]триазоло[4,3-a]пиразиновые), индолиновые и индановые группы.
Азотсодержащее гетероарильное кольцо должно содержать по меньшей мере один атом азота в кольце. Каждое кольцо может, кроме того, содержать до приблизительно четырех других гетероатомов, обычно выбираемых из атомов азота, серы и кислорода. Как правило, гетероарильное кольцо должно содержать до 3 гетероатомов, например 1, 2 или 3, еще чаще до 2 атомов азота, например, один атом азота. Атомы азота в гетероарильных кольцах могут быть основными, как в случае имидазола или пиридина, или по существу не основными, как в случае азота индола или пиррола. В большинстве случаев, число основных атомов азота, присутствующих в гетероарильной группе, включая любые заместители аминогруппы в кольце, составляет менее пяти.
Примеры азотсодержащих гетероарильных групп включают, без ограничения, пиридил, пирролил, имидазолил, оксазолил, оксадиазолил, тиадиазолил, оксатриазолил, изоксазолил, тиазолил, изотиазолил, фуразанил, пиразолил, пиразинил, пиримидинил, пиридазинил, триазинил, триазолил (например, 1,2,3-триазолил, 1,2,4-триазолил), тетразолил, хинолинил, изохинолинил, бензимидазолил, бензоксазолил, бензизоксазол, бензтиазолил и бензизотиазол, индолил, 3H-индолил, изоиндолил, индолизинил, изоиндолинил, пуринил (например, аденин [6-аминопурин], гуанин [2-амино-6-гидроксипурин]), индазолил, хинолизинил, бензоксазинил, бензодиазинил, пиридопиридинил, хиноксалинил, хиназолинил, циннолинил, фталазинил, нафтиридинил и птеридинил.
Примеры азотсодержащих полициклических гетероарильных групп, содержащих ароматическое кольцо и неароматическое кольцо, включают тетрагидроизохинолинил, тетрагидрохинолинил и индолинил.
Термин "неароматическая группа", если из контекста не следует иное, охватывает ненасыщенные кольцевые системы без ароматического характера, частично насыщенные и полностью насыщенные гетероциклильные кольцевые системы. Термины "ненасыщенные" и "частично насыщенные" относятся к кольцам, кольцевая структура(ы) которых содержит атомы, имеющие более одной общей валентной связи, т.е. кольцо содержит по меньшей мере одну кратную связь, например, связь C=C, C≡C или N=C. Термин "полностью насыщенные" относится к кольцам, в которых нет кратных связей между атомами кольца. Насыщенные гетероциклильные группы включают пиперидин, морфолин, тиоморфолин, пиперазин. Частично насыщенные гетероциклильные группы включают пиразолины, например, 2-пиразолин и 3-пиразолин.
Примерами неароматических гетероциклильных групп являются группы, содержащие от 3 до 12 членов в кольце, еще чаще от 5 до 10 членов в кольце. Такие группы могут быть, например, моноциклическими или бициклическими и обычно содержат от 1 до 5 гетероатомных членов в кольце (еще чаще 1, 2, 3 или 4 гетероатомных члена в кольце), обычно выбранные из атомов азота, кислорода и серы. Гетероциклильные группы могут содержать, например, циклические эфирные группы (например, как в тетрагидрофуране и диоксане), циклические тиоэфирные группы (например, как в тетрагидротиофене и дитиане), циклические аминные группы (например, как в пирролидине), циклические амидные группы (например, как в пирролидоне), циклические тиоамиды, циклические тиоэфиры, циклические мочевины (например, как в имидазолидин-2-оне), циклические сложноэфирные группы (например, как в бутиролактоне), циклические сульфоны (например, как в сульфолане и сульфолене), циклические сульфоксиды, циклические сульфонамиды и их комбинации (например, тиоморфолин).
Конкретные примеры включают морфолин, пиперидин (например, 1-пиперидинил, 2-пиперидинил, 3-пиперидинил и 4-пиперидинил), пиперидон, пирролидин (например, 1-пирролидинил, 2-пирролидинил и 3-пирролидинил), пирролидон, азетидин, пиран (2H-пиран или 4H-пиран), дигидротиофен, дигидропиран, дигидрофуран, дигидротиазол, тетрагидрофуран, тетрагидротиофен, диоксан, тетрагидропиран (например, 4-тетрагидропиранил), имидазолин, имидазолидинон, оксазолин, тиазолин, 2-пиразолин, пиразолидин, пиперазон, пиперазин и N-алкилпиперазины, такие как N-метилпиперазин. Как правило, предпочтительные неароматические гетероциклильные группы включают насыщенные группы, такие как пиперидин, пирролидин, азетидин, морфолин, пиперазин и N-алкилпиперазины.
В азотсодержащем неароматическом гетероциклильном кольце, кольцо должно содержать по меньшей мере один атом азота. Гетероциклильные группы могут содержать, например, циклические аминогруппы (например, как в пирролидине), циклические амиды (такие как пирролидинон, пиперидон или капролактам), циклические сульфонамиды (такие как изотиазолидин, 1,1-диоксид, [1,2]тиазинан 1,1-диоксид или [1,2]тиазепан 1,1-диоксид) и их комбинации. Конкретные примеры азотсодержащих неароматических гетероциклильных групп включают азиридин, морфолин, тиоморфолин, пиперидин (например, 1-пиперидинил, 2-пиперидинил, 3-пиперидинил и 4-пиперидинил), пирролидин (например, 1-пирролидинил, 2-пирролидинил и 3-пирролидинил), пирролидон, дигидротиазол, имидазолин, имидазолидинон, оксазолин, тиазолин, 6H-1,2,5-тиадиазин, 2-пиразолин, 3-пиразолин, пиразолидин, пиперазин и N-алкилпиперазины, такие как N-метилпиперазин.
Гетероциклильные группы могут быть полициклическими конденсированными кольцевыми системами или кольцевыми системами с внутренним мостиком, такими как окса- и аза-аналоги бициклоалканов, трициклоалканов (например, адамантан и оксаадамантан). По поводу разъяснения отличий между конденсированными и мостиковыми кольцевыми системами, см. AdvancedOrganicChemistry, Jerry March, 4th Edition, Wiley Interscience, pages 131-133, 1992.
Каждая гетероциклильная группа может быть не замещена или замещена одной или более группами-заместителями. Например, гетероциклильные группы могут быть не замещены или замещены 1, 2, 3 или 4 заместителями. В случае, когда гетероциклильная группа является моноциклической или бициклической, она обычно не замещена или имеет 1, 2 или 3 заместителя.
Термин "карбоциклил", при использовании в настоящем описании, если из контекста не следует иное, должен включать как ароматические, так и неароматические кольцевые системы. Таким образом, например, термин "карбоциклильная группа" включает, в пределах своего объема, ароматические, неароматические, ненасыщенные, частично насыщенные и полностью насыщенные кольцевые карбоциклильные системы. Как правило, если из контекста не следует иное, такие группы могут быть моноциклическими или бициклическими и могут содержать, например, от 3 до 12 членов в кольце, чаще от 5 до 10 членов в кольце. Ссылка на 4-7 членов в кольце включает 4, 5, 6 или 7 атомов в кольце, а ссылка на 4-6 членов в кольце включает 4, 5 или 6 атомов в кольце. Примерами моноциклических групп являются группы, содержащие 3, 4, 5, 6, 7 и 8 членов в кольце, чаще 3-7, и предпочтительно 5, 6 или 7 членов в кольце, более предпочтительно 5 или 6 членов в кольце. Примерами бициклических групп являются группы, которые содержат 8, 9, 10, 11 и 12 членов в кольце, и чаще 9 или 10 членов в кольце. В случае отсылки к карбоциклильным группам, карбоциклильное кольцо, если из контекста не следует иное, необязательно может быть замещено (т.е. не замещено или замещено) одним или более заместителями, как обсуждается в настоящем описании.
Термин карбоциклил включает арил, C3-8циклоалкил, C3-8циклоалкенил.
Термин "арил", при использовании в настоящем описании, относится к карбоциклильным ароматическим группам, включая фенильные, нафтильные, инденильные и тетрагидронафтильные группы.
Во всех случаях, при использовании выше или далее, когда такие заместители могут быть независимо выбраны из списка многочисленных определений, предполагаются все возможные комбинации, которые являются химически возможными. Во всех случаях, при использовании выше или далее, когда такой конкретный заместитель дополнительно замещен двумя или более группами, такими как, например, гидроксигалогенC1-4алкил, гидроксигалогенC1-4алкокси, предполагаются все возможные комбинации, которые являются химически возможными.
В одном варианте осуществления D представляет собой ароматическое кольцо.
В одном варианте осуществления D представляет собой 5-12-членный моноциклический или бициклический карбоциклил, или 5-12-членный моноциклический или бициклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный карбоциклил и гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой ароматический 3-12, в особенности ароматический 5-12-членный моноциклический или бициклический карбоциклил, или ароматический 3-12, в особенности ароматический 5-12-членный моноциклический или бициклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный карбоциклил и гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой ароматический 3-12 (например, 5-10) -членный моноциклический или бициклический карбоциклил, где указанный карбоциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой фенил или нафтил, где каждый указанный фенил или нафтил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой 5-12-членный моноциклический или бициклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой ароматический 5-12-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждая указанная гетероциклильная группа необязательно может быть замещена одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой 5 или 6-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой ароматический 5 или 6-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой 5-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой 5-членный моноциклический ароматический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой пиразолил (например, пиразол-4-ил), где каждый указанный пиразолил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой 6-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой 6-членный моноциклический ароматический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой 12-членный бициклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой 12-членный бициклический ароматический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой

В одном варианте осуществления D представляет собой

В одном варианте осуществления D не является пиразолилом, в частности D является пиридинилом, фенилом, пиролилом, имидазолилом, триазолилом, пиролопиридинилом, 1,3-бензодиоксолилом, индолилом, тиазолилом, тетразолилом, оксазолилом, пиримидинилом, тиадиазолилом, оксадиазолилом, где указанные кольца необязательно замещены. Указанные дополнительные заместители могут представлять собой галоген, циано, C1-6алкил, C1-6алкокси, -C(=O)-O-C1-6алкил, гидроксиC1-6алкил, -NR4R5, C1-6алкил, который замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен -NR4R5, -C(=O)-NR4R5, -C(=O)-C1-6алкил-NR4R5, R6, C1-6алкил, который замещен R6.
В одном варианте осуществления D необязательно замещен 4-пиразолилом. В одном варианте осуществления D является 4-пиразолилом, замещенным в положении 1 C1-6алкилом, например метилом.
В одном варианте осуществления D является 1-пиразолилом или 2-пиразолилом, которые необязательно могут быть замещены.
В одном варианте осуществления D является необязательно замещенным пиразолилом.
В одном варианте осуществления D не является пиразолилом, в особенности D является пиридинилом, фенилом, пиролилом, имидазолилом, триазолилом, пиролопиридинилом, 1,3-бензодиоксолилом, индолилом, тиазолилом, тетразолилом, оксазолилом, пиримидинилом, где указанные кольца необязательно замещены.
В одном варианте осуществления D является необязательно замещенным фенилом.
В одном варианте осуществления D является фенилом.
В одном варианте осуществления D является фенилом или необязательно замещенным пиразолилом.
В одном варианте осуществления D является 3-12-членным моноциклическим или бициклическим карбоциклилом или 3-12-членным моноциклическим или бициклическим гетероциклилом, содержащим по меньшей мере один гетероатом, выбранный из N, О или S, где указанный карбоциклил и гетероциклил замещены одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D является замещенным фенилом или замещенным пиразолилом.
В одном варианте осуществления D представляет собой 3-12-членный моноциклический или бициклический карбоциклил или 3-12-членный моноциклический или бициклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где указанный карбоциклил и гетероциклил замещены одной или более (например, 1, 2 или 3) группами R1;
R1 представляет собой C1-4алкил.
В одном варианте осуществления D является пиразолилом или фенилом, каждый из которых необязательно замещен C1-4алкилом; в особенности D является пиразолилом, который необязательно замещен C1-4алкилом.
В одном варианте осуществления D является пиразолилом или фенилом, каждый из которых необязательно замещен C1-4алкилом; W является -N(R3)- или -C(=O)-; R3 является C1-6алкилом, который замещен R9, или C1-6алкилом, который замещен -NR10R11.
В одном варианте осуществления D является пиразолилом или фенилом, каждый из которых необязательно замещен C1-4алкилом; W является -N(R3)-; R3 является C1-6алкилом, который замещен R9, или C1-6алкилом, который замещен -NR10R11.
В одном варианте осуществления D является пиразолилом, который необязательно замещен C1-4алкилом; W является -N(R3)-; R3 является C1-6алкилом, который замещен R9, или C1-6алкилом, который замещен -NR10R11.
В одном варианте осуществления D является пиразолилом, который замещен C1-4алкилом; W является -N(R3)-; R3 является C1-6алкилом, который замещен R9; R9 является имидазолилом.
В одном варианте осуществления D является пиразолилом, который замещен C1-4алкилом; W является -N(R3)-.
В одном варианте осуществления D представляет собой 3-12-членный моноциклический или бициклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный карбоциклил и гетероциклил могут быть необязательно замещены одной или более (например, 1, 2 или 3) группами R1; W является -N(R3)-.
В одном варианте осуществления R1 представляет собой водород, C1-6алкил, C2-4алкенил, гидроксиC1-6алкил, галоC1-6алкил, гидроксигалоC1-6алкил, цианоC1-4алкил, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, C1-6алкил, который замещен -NR4R5, C1-6алкил, который замещен -C(=O)-NR4R5, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NH-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, R6, C1-6алкил, который замещен R6, C1-6алкил, который замещен -C(=O)-R6, гидроксиC1-6алкил, который замещен R6, C1-6алкил, который замещен -Si(CH3)3, C1-6алкил, который замещен -P(=O)(ОH)2, или C1-6алкил, который замещен -P (=O)(OC1-6алкилом)2.
В одном варианте осуществления R1 представляет собой водород, C1-6алкил, C2-4алкенил, гидроксиC1-6алкил, галоC1-6алкил, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, C1-6алкил, который замещен -NR4R5, C1-6алкил, который замещен -C(=O)-NR4R5, -S(=O)2-C1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -С(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-C1-6алкилом, R6, C1-6алкил, который замещен R6, C1-6алкил, который замещен -C(=O)-R6, гидроксиC1-6алкил, который замещен R6, или C1-6алкил, который замещен -Si(CH3)3.
В одном варианте осуществления R1 представляет собой водород, галоген, циано, C1-6алкил, C1-6алкокси, -C(=O)-O-C1-6алкил, C2-4алкенил, гидроксиC1-6алкил, галоC1-6алкил, гидроксигалоC1-6алкил, цианоC1-4алкил, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, C1-6алкил, который замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен -NR4R5, -C(=O)-C1-6алкил-NR4R5, C1-6алкил, который замещен -C(=O)-NR4R5, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NH-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, R6, C1-6алкил, который замещен R6, -C(=O)-R6, C1-6алкил, который замещен -C(=O)-R6, гидроксиC1-6алкил, который замещен R6, C1-6алкил, который замещен -Si(CH3)3, C1-6алкил, который замещен -P(=O)(ОH)2, или C1-6алкил, который замещен -P (=O)(OC1-6алкилом)2.
В одном варианте осуществления R1 представляет собой водород.
В одном варианте осуществления R1 представляет собой C1-6алкил. В одном варианте осуществления R1 представляет собой метил.
В одном варианте осуществления R1 не является C1-6алкилом, который замещен R6.
В одном варианте осуществления R1 представляет собой водород, галоген, циано, C1-6алкил, C1-6алкокси, -C(=O)-O-C1-6алкил, C2-4алкенил, гидроксиC1-6алкил, галоC1-6алкил, гидроксигалоC1-6алкил, цианоC1-4алкил, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, -NR4R5, C1-6алкил, который замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен -NR4R5, -C(=O)-NR4R5, -C(=O)-C1-6алкил-NR4R5, C1-6алкил, который замещен -C(=O)-NR4R5, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NH-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, R6, -C(=O)-R6, C1-6алкил, который замещен -C(=O)-R6, гидроксиC1-6алкил, который замещен R6, C1-6алкил, который замещен -Si(CH3)3, C1-6алкил, который замещен -P(=O)(ОH)2, или C1-6алкил, который замещен -P (=O)(OC1-6алкилом)2.
В одном варианте осуществления R1 представляет водород, галоген, циано, C1-6алкил, C1-6алкокси, -C(=O)-O-C1-6алкил, C2-4алкенил, гидроксиC1-6алкил, галоC1-6алкил, гидроксигалоC1-6алкил, цианоC1-4алкил, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, C1-6алкил, который замещен -O-C(=O)-C1-6алкил, C1-6алкил, который замещен -NR4R5, -C(=O)-C1-6алкил-NR4R5, C1-6алкил, который замещен -C(=O)-NR4R5, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NH-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, R6, -C(=O)-R6, C1-6алкил, который замещен -C(=O)-R6, гидроксиC1-6алкил, который замещен R6, C1-6алкил, который замещен -Si(CH3)3, C1-6алкил, который замещен -P(=O)(ОH)2, или C1-6алкил, который замещен -P(=O) (OC1-6алкилом)2.
В одном варианте осуществления каждый R2 независимо выбран из гидроксила, галогена, циано, C1-4алкила, C2-4алкенила, C1-4алкокси, гидроксиC1-4алкила, гидроксиC1-4алкокси, галоC1-4алкила, галоC1-4алкокси, C1-4алкоксиC1-4алкила, R13, C1-4алкокси, который замещен R13, -C(=O)-R13, C1-4алкила, который замещен NR7R8, C1-4алкокси, который замещен NR7R8, -NR7R8 и -C(=O)-NR7R8; или когда две группы R2 присоединены к смежным атомам углерода, они вместе могут формировать радикал формулы -O-(C(R17)2)p-O-, где R17 представляет собой водород или фтор, а p обозначает 1 или 2.
В одном варианте осуществления каждый R2 независимо выбран из гидроксила, галогена, циано, C1-4алкила, C2-4алкенила, C1-4алкокси, гидроксиC1-4алкила, гидроксиC1-4алкокси, галоC1-4алкокси, C1-4алкоксиC1-4алкила, R13, C1-4алкокси, который замещен R13, -C(=O)-R13, C1-4алкила, который замещен NR7R8, C1-4алкокси, который замещен NR7R8, -NR7R8 или -C(=O)-NR7R8.
В одном варианте осуществления один или более R2 представляет собой C1-4алкокси, например CH3O-, или галоген, например фтор.
В одном варианте осуществления один или более R2 представляет собой C1-4алкокси, например CH3O-.
В одном варианте осуществления n равно 0. В одном варианте осуществления n равно 1. В одном варианте осуществления n равно 2. В одном варианте осуществления n равно 3. В одном варианте осуществления n равно 4.
В одном варианте осуществления n равно 1, 2, 3 или 4.
В одном варианте осуществления n равно 1, 2, 3 или 4, в частности 4, и по меньшей мере один R2 представляет собой C1-4алкилокси, например CH3O-.
В одном варианте осуществления n равно 2, 3 или 4.
В одном варианте осуществления n 4.
В одном варианте осуществления n равно 2, и один R2 присутствует в 3 положении, а другой присутствует в 5 положении.
В одном варианте осуществления n равно 2, и один R2 присутствует в 3 положении, а другой присутствует в 5 положении, и каждый R2 представляет собой C1-4алкокси, например, каждый R2 представляет собой CH3O-.
В одном варианте осуществления n равно 3, и один R2 присутствует в 2 положении, один R2 присутствует в 3 положении, и один R2 присутствует в 5 положении.
В одном варианте осуществления n равно 3 и один R2 присутствует в 3 положении и представляет собой C1-4алкокси, например CH3O-; один R2 присутствует в 5 положении и представляет собой C1-4алкокси, например CH3O-; один R2 присутствует во 2 положении и представляет собой галоген, например фтор.
В одном варианте осуществления n равно 4, и один R2 присутствует во 2 положении, один R2 присутствует в 3 положении, один R2 присутствует в 5 положении, и один R2 присутствует в 6 положении.
В одном варианте осуществления n равно 4, и один R2 присутствует в 3 положении и представляет собой C1-4алкокси, например CH3O-; один R2 присутствует в 5 положении и представляет собой C1-4алкокси, например CH3O-; один R2 присутствует во 2 положении и представляет собой галоген, например фтор, и один R2 присутствует в 6 положении и представляет собой галоген, например фтор.
В одном варианте осуществления R3 представляет собой C1-6алкил, гидроксиC1-6алкил, гидроксигалоC1-6алкил, гидроксиC2-6алкинил, галоC1-6алкил, галоC1-6алкил, необязательно замещенный (например, замещенный) -O-C(=O)-C1-6алкилом, C1-6алкил, замещенный -C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами или -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен R9, C1-6алкил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя галогенами и -NR10R11, C1-6алкил, который замещен -C(=O)-O-C1-6алкил, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -O-C(=O)-NR10R11, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, C1-6алкил, который замещен R9 и необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен гидроксилом и R9, -C1-6алкил-C(R12)=N-O-R12, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -C(=O)-R9, C2-6алкенил, который замещен R9, C2-6алкинил, который замещен R9, гидроксиC1-6алкокси, C2-6алкенил, C2-6алкинил, R13, C1-6алкил, который замещен C1-6алкоксиC1-6алкил-C(=O)-, или C1-6алкил, замещенный -P(=O)(OC1-6алкилом)2.
В одном варианте осуществления R3 представляет собой C1-6алкил, гидроксиC1-6алкил, гидроксигалоC1-6алкил, галоC1-6алкил, галоC1-6алкил, необязательно замещенный (например, замещенный) -O-C(=O)-C1-6алкилом, C1-6алкил, замещенный -C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами или -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен R9, C1-6алкил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя галогенами и -NR10R11, C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -O-C(=O)-NR10R11, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, C1-6алкил, который замещен R9 и необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен гидроксилом и R9, -C1-6алкил-C(R12)=N-O-R12, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -C(=O)-R9, C2-6алкенил, который замещен R9, гидроксиC1-6алкокси, C2-6алкенил, R13, C1-6алкил, который замещен C1-6алкоксиC1-6алкил-C(=O)-, или C1-6алкил, который замещен -P(=O)(OC1-6алкилом)2.
В одном варианте осуществления R3 представляет собой C1-6алкил, гидроксиC1-6алкил, гидроксигалоC1-6алкил, галоC1-6алкил, C1-6алкил, который замещен -C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, C1-6алкил, который замещен R9, C1-6алкил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя галогенами и -NR10R11, C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -O-C(=O)-NR10R11, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, C1-6алкил, который замещен гидроксилом и R9, -C1-6алкил-C(R12)=N-O-R12, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -C(=O)-R9, C2-6алкинил, который замещен R9, гидроксиC1-6алкокси, C2-6алкенил, C2-6алкинил, R13 или C1-6алкил, который замещен C1-6алкоксиC1-6алкил-C(=O)-.
В одном варианте осуществления R3 представляет собой C1-6алкил, гидроксиC1-6алкил, галоC1-6алкил, галоC1-6алкил, который необязательно замещен -O-C(=O)-C1-6алкилом, гидроксигалоC1-6алкил, гидроксиC2-6алкинил, C1-6алкил, который замещен -C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами или -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен R9, цианоC1-6алкил, C1-6алкил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя атомами галогена и -NR10R11, C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, C1-6алкил, который замещен C1-6алкоксиC1-6алкил-C(=O)-, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -C(=O)-NR14R15, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -O-C(=O)-NR10R11, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, C1-6алкил, который замещен R9 и замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен гидроксилом и R9, -C1-6алкил-C (R12)=N-O-R12, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -C(=O)-R9, C2-6алкенил, который замещен R9, C2-6алкинил, который замещен R9, C1-6алкилоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, C2-6алкенил, C2-6алкинил, R13, или C1-6алкил, который замещен -P(=O)(OC1-6алкилом)2.
В одном варианте осуществления R3 представляет собой C1-6алкил, гидроксиC1-6алкил, гидроксигалоC1-6алкил, галоC1-6алкил, C1-6алкил, который замещен -C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, C1-6алкил, который замещен R9, C1-6алкил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя галогенами и -NR10R11, C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, C1-6алкил, который замещен -O-C(=O)-NR10R11, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкил, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, C1-6алкил, который замещен гидроксилом и R9, -C1-6алкил-C(R12)=N-O-R12, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -C(=O)-R9, C2-6алкинил, который замещен R9, гидроксиC1-6алкокси, C2-6алкенил, C2-6алкинил или R13.
В одном варианте осуществления R3 представляет собой C1-6алкил, гидроксиC1-6алкил, гидроксигалоC1-6алкил, галоC1-6алкил, C1-6алкил, который замещен -C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, C1-6алкил, который замещен R9, C1-6алкил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя галогенами и -NR10R11, C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, C1-6алкил, который замещен -O-C(=O)-NR10R11, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, C1-6алкил, который замещен гидроксилом и R9, -C1-6алкил-C(R12)=N-O-R12, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -C(=O)-R9, гидроксиC1-6алкокси, C2-6алкенил или R13.
В одном варианте осуществления R3 представляет собой гидроксиC1-6алкил, галоC1-6алкил или C1-6алкил, который замещен R9.
В одном варианте осуществления R3 представляет собой гидроксиC1-6алкил, C1-6алкил, который замещен -NR10R11, или C1-6алкил, который замещен R9.
В одном варианте осуществления R3 представляет собой гидроксиC1-6алкил, галоC1-6алкил, C1-6алкил, который замещен -NR10R11, или C1-6алкил, который замещен R9.
В одном варианте осуществления R3 представляет гидроксиC1-6алкил, галоC1-6алкил, C1-6алкил, который замещен -NR10R11, или C1-6алкил, который замещен R9; каждый R10 и R11 независимо представляют собой водород или C1-6алкил.
В одном варианте осуществления R3 представляет гидроксиC1-6алкил, гидроксигалоC1-6алкил, галоC1-6алкил, C1-6алкил, который замещен R9, C1-6алкил, который замещен -NR10R11, C2-6алкинил, который замещен R9, или C2-6алкинил.
В одном варианте осуществления R3 представляет собой гидроксиC1-6алкил, галоC1-6алкил, C1-6алкил, который замещен R9, C1-6алкил, который замещен -NR10R11, C1-6алкоксиC1-6алкил или C2-6алкинил.
В одном варианте осуществления R3 представляет собой гидроксиC1-6алкил, гидроксигалоC1-6алкил, C1-6алкил, который замещен R9, C1-6алкил, который замещен -NR10R11, C2-6алкинил, который замещен R9, или C2-6алкинил.
В одном варианте осуществления R3 представляет собой C1-6алкил (например, C1-4алкил), который замещен R9.
В одном варианте осуществления, когда R3 представляет собой C1-6алкил (например, C1-4алкил), который замещен R9, R9 представляет собой необязательно замещенный насыщенный или ароматический 5 или 6-членный моноциклический гетероциклил, например, необязательно замещенный изоксазолидинил, пиримидинил, имидазолил или пирролидинил, в частности необязательно замещенный имидазолил (например, имидазол-2-ил). В одном варианте осуществления имидазолил замещен -S(=O)2-NR14R15 (например, -S(=O)2-N(CH3)2. В одном варианте осуществления R9 представляет собой незамещенный имидазолил (например, имидазол-2-ил).
В одном варианте осуществления, когда R3 представляет собой C1-6алкил (например, C1-4алкил), который замещен R9, R9 представляет собой необязательно замещенный ароматический 6-членный моноциклический гетероциклил, содержащий один или два гетероатома азота, например, пиримидинил или пиридинил.
В одном варианте осуществления, когда R3 представляет собой C1-6алкил (например, C1-4алкил), который замещен R9, R9 представляет собой необязательно замещенный 5-членный ароматический гетероцикл, такой как, например, имидазолил. Необязательные заместители могут представлять собой -S(=O)2-NR14R15.
В одном варианте осуществления, когда R3 представляет собой C1-6алкил (например, C1-4алкил), который замещен R9, R9 представляет собой замещенный 5-членный ароматический гетероцикл, такой как, например, имидазолил.
В одном варианте осуществления, когда R3 представляет собой C1-6алкил (например, C1-4алкил), который замещен R9, R9 представляет собой необязательно замещенный насыщенный 5 или 6-членный моноциклический гетероциклил, например, необязательно замещенный изоксазолидинил или пирролидинил, в частности необязательно замещенный пирролидинил. В одном варианте осуществления пирролидинил замещен оксогруппой. В одном варианте осуществления пирролидинил, который замещен оксогруппой, является пирролидин-2-илом, который замещен оксогруппой.
В одном варианте осуществления, когда R3 представляет собой C1-6алкил (например, метил или н-пропил), который замещен R9, R9 представляет собой C3-8циклоалкил, например, циклопропил.
В одном варианте осуществления R3 представляет собой C1-6алкил, который замещен гидроксилом, галогеном и/или -NR10R11. В одном варианте осуществления R3 представляет собой C1-6алкил, который замещен гидроксилом, галогеном или -NR10R11, где C1-6алкильная группа является алкильной группой с нормальной цепью, например, 2-этилом, н-пропилом. В другом варианте осуществления R3 представляет собой C1-6алкил, который замещен гидроксилом или галогеном.
В одном варианте осуществления R3 представляет собой гидроксиC1-6алкил. R3 может представлять собой -CH2CH2OH или -CH2CH2CH2OH.
В одном варианте осуществления R3 представляет собой гидроксигалоC1-6алкил, например, R3 может представлять собой -CH2CHOHCF3.
В одном варианте осуществления R3 представляет собой галоC1-6алкил, например, R3 может представлять собой -CH2CH2CH2Cl.
В одном варианте осуществления R3 представляет собой C1-6алкил, который замещен -NR10R11.
В одном варианте осуществления R3 представляет собой C1-4алкил, который замещен -NR10R11. В одном варианте осуществления R3 представляет собой C1-4алкил, замещенный -NR10R11, где C1-4алкильная группа является алкильной группой с нормальной цепью, например, 2-этилом, н-пропилом. В одном варианте осуществления R3 представляет собой C1-4алкил, который замещен -NR10R11, где C1-4алкильная группа является этиленовой группой (-CH2CH2-).
В одном варианте осуществления, когда R3 представляет собой C1-6алкил (например, 2-этил, н-пропил), который замещен -NR10R11, R10 и R11 независимо выбраны из водорода, C1-6алкила и галоC1-6алкила (например, водорода, изопропила или -CH2CF3).
В одном варианте осуществления R3 является гидроксиC1-6алкилом, C1-6алкилом, который замещен R9, или C1-6алкилом, который замещен -NR10R11; в частности, R3 является C1-6алкилом, который замещен R9, или C1-6алкилом, который замещен -NR10R11; более конкретно R3 является C1-6алкилом, который замещен R9.
В одном варианте осуществления R3a представляет собой -NR10R11, гидроксил, C1-6алкил, гидроксиC1-6алкил, гидроксигалоC1-6алкил, галоC1-6алкил, C1-6алкил, который замещен -C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами, C1-6алкил, который замещен R9, C1-6алкил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя галогенами и -NR10R11, C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, C1-6алкил, который замещен -O-C(=O)-NR10R11, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -O-C(=O)-NR10R11, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, C1-6алкил, который замещен гидроксилом и R9, -C1-6алкил-C(R12)=N-O-R12, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -C(=O)-R9, C2-6алкинил, который замещен R9, гидроксиC1-6алкокси, C2-6алкенил, C2-6алкинил, R13 или C1-6алкил, который замещен C1-6алкоксиC1-6алкил-C(=O)-.
В одном варианте осуществления R3a является -NR10R11, гидроксилом, гидроксиC1-6алкилом, цианоC1-6алкилом, C1-6алкилом, который замещен -C(=O)-C1-6алкилом, C1-6алкилом, который замещен -C(=O)-O-C1-6алкилом, C1-6алкилом, который замещен R9, C1-6алкилом, который замещен -NR10R11, C1-6алкилом, который замещен гидроксилом и -NR10R11, или C1-6алкилом, который замещен -C(=O)-NR10R11.
В одном варианте осуществления R3a является гидроксилом, C1-6алкилом, гидроксиC1-6алкилом, C1-6алкилом, который замещен -C(=O)-O-C1-6алкилом, C1-6алкилом, который замещен R9.
В одном варианте осуществления R3a является C1-6алкилом, который замещен R9.
В одном варианте осуществления R3a является C1-6алкилом, который замещен -C(=O)-O-C1-6алкилом, например, -CH2-C(=O)-O-CH3.
В одном варианте осуществления R3a представляет собой гидроксил.
В одном варианте осуществления R3b представляет собой водород.
В одном варианте осуществления R3b представляет собой гидроксил.
В одном варианте осуществления R3a представляет собой гидроксил, и R3b представляет собой водород.
В одном варианте осуществления R3a и R3b объединены с образованием =O, с образованием =NR10, с образованием циклопропила вместе с атомом углерода, к которому они присоединены, с образованием =CH-C0-4алкила, который замещен R3c, или с образованием
В одном варианте осуществления R3a и R3b объединены с образованием =O, с образованием циклопропила вместе с атомом углерода, к которому они присоединены, с образованием =CH-C0-4алкила, который замещен R3c, или с образованием

В одном варианте осуществления R3a и R3b объединены с образованием =O.
В одном варианте осуществления R3a и R3b объединены с образованием циклопропила вместе с атомом углерода, к которому они присоединены.
В одном варианте осуществления R3a и R3b объединены с образованием =CH-C0-4алкила, который замещен R3c, например, =CH-CH2-R3c или =CH-R3c.
В одном варианте осуществления R3c представляет собой водород.
В одном варианте осуществления R3c представляет собой гидроксил, C1-6алкокси, R9, -NR10R11, -C(=O)-NR14R15, циано, -C(=O)-C1-6алкил или -CH(OH)-C1-6алкил.
В одном варианте осуществления R3c представляет собой гидроксил, -C(=O)-NR14R15, -NR10R11, циано или -C(=O)-C1-6алкил.
В одном варианте осуществления R3a и R3b объединены с образованием =CH-C0-4алкила (например, =CH-CH2- или =CH-), который замещен R3c, где R3c представляет собой гидроксил или -C(=O)-NR14R15, например, -C (=O)NH(CH3).
В одном варианте осуществления R3a и R3b объединены с образованием =CH-C1-4алкила в Z конфигурации.
В одном варианте осуществления R3a и R3b объединены с образованием =CH-C1-4алкила в E конфигурации.
В одном варианте осуществления R3a представляет собой -NR10R11, гидроксил, C1-6алкокси, гидроксиC1-6алкокси, C1-6алкокси, который замещен -NR10R11, C1-6алкил, C2-6алкинил, галоC1-6алкил, который необязательно замещен -O-C(=O)-C1-6алкилом, гидроксиC1-6алкил, который необязательно замещен -O-C(=O)-C1-6алкилом, гидроксиC2-6алкинил, гидроксигалоC1-6алкил, цианоC1-6алкил, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -C(=O)-C1-6алкилом, C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, C1-6алкил который замещен C1-6алкоксиC1-6алкил-O-C(=O)-, C1-6алкил который замещен C1-6алкоксиC1-6алкил-C(=O)-, C1-6алкил, который замещен -O-C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами или -O-C(=O)-C1-6алкилом, C2-6алкинил, который замещен C1-6алкокси, C1-6алкил, который замещен R9 и необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен -C(=O)-R9, C1-6алкил, который замещен гидроксилом и R9, C1-6алкинил, который замещен R9, C1-6алкил, который замещен -NR10R11, C2-6алкинил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя галогенами и -NR10R11, -C1-6алкил-C(R12)=N-O-R12, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -O-C(=O)-NR10R11, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкил, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, R13, C1-6алкил, который замещен -P(=O)(ОH)2, или C1-6алкил, который замещен -P(=O)(OC1-6алкилом)2;
R3b представляет собой водород или гидроксил; при условии, что если R3a представляет собой -NR10R11, то R3b представляет собой водород; или
R3a и R3b объединены с образованием =O, с образованием =NR10, с образованием циклопропила вместе с атомом углерода, к которому они присоединены, с образованием =CH-C0-4алкила, который замещен R3c, или с образованием

В одном варианте осуществления R3a представляет собой -NR10R11, гидроксил, C1-6алкокси, гидроксиC1-6алкокси, C1-6алкокси, который замещен -NR10R11, C1-6алкил, C2-6алкенил, галоC1-6алкил, который необязательно замещен -O-C(=O)-C1-6алкилом, гидроксиC1-6алкил, который необязательно замещен -O-C(=O)-C1-6алкилом, гидроксиC2-6алкенил, гидроксигалоC1-6алкил, цианоC1-6алкил, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -C(=O)-C1-6алкилом, C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, C1-6алкил, который замещен C1-6алкоксиC1-6алкил-O-C(=O)-, C1-6алкил, который замещен C1-6алкоксиC1-6алкил-C(=O)-, C1-6алкил, который замещен -O-C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами или -O-C(=O)-C1-6алкилом, C2-6алкенил, который замещен C1-6алкокси, C1-6алкил, который замещен R9 и необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен -C(=O)-R9, C1-6алкил, который замещен гидроксилом и R9, C1-6алкенил, который замещен R9, C1-6алкил, который замещен -NR10R11, C2-6алкенил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя галогенами и -NR10R11, -C1-6алкил-C(R12)=N-O-R12, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -O-C(=O)-NR10R11, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, R13, C1-6алкил, который замещен -P(=O)(ОH)2 или C1-6алкил, который замещен -P(=O)(OC1-6алкилом)2;
R3b представляет собой водород или гидроксил; при условии, что если R3a представляет собой -NR10R11, то R3b представляет собой водород; или
R3a и R3b объединены с образованием =O, с образованием =NR10, с образованием циклопропила вместе с атомом углерода, к которому они присоединены, с образованием =CH-C0-4алкила, который замещен R3c, или с образованием

В одном варианте осуществления R3a представляетсобой -NR10R11, гидроксил, C1-6алкокси, гидроксиC1-6алкокси, C1-6алкокси, который замещен -NR10R11, C1-6алкил, галоC1-6алкил, который необязательно замещен -O-C(=O)-C1-6алкилом, гидроксиC1-6алкил, который необязательно замещен -O-C(=O)-C1-6алкилом, гидроксигалоC1-6алкил, цианоC1-6алкил, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -C(=O)-C1-6алкилом, C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, C1-6алкил который замещен C1-6алкоксиC1-6алкил-O-C(=O)-, C1-6алкил, который замещен C1-6алкоксиC1-6алкил-C(=O)-, C1-6алкил, который замещен -O-C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами или -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен R9 и необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен -C(=O)-R9, C1-6алкил, который замещен гидроксилом и R9, C1-6алкил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя галогенами и -NR10R11, -C1-6алкил-C(R12)=N-O-R12, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -O-C(=O)-NR10R11, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, R13, C1-6алкил, который замещен -P(=O)(ОH)2, или C1-6алкил, который замещен -P(=O)(OC1-6алкилом)2;
R3b представляет собой водород или гидроксил; при условии, что если R3a представляет собой -NR10R11, то R3b представляет собой водород; или
R3a и R3b объединены с образованием =O, с образованием =NR10, с образованием циклопропила вместе с атомом углерода, к которому они присоединены, с образованием =CH-C0-4алкила, который замещен R3c, или с образованием

В одном варианте осуществления R3a не является алкенилом или замещенным алкенилом.
В одном варианте осуществления R3a не является алкинилом или замещенным алкинилом.
В одном варианте осуществления R3a не является алкенилом, замещенным алкенилом, алкинилом или замещенным алкинилом.
В одном варианте осуществления R9 выбран из:
необязательно замещенного C3-8циклоалкила,
необязательно замещенного ароматического 5-членного моноциклического гетероциклила,
необязательно замещенного насыщенного 6-членного моноциклического гетероциклила,
насыщенного или ароматического 3, 4, 5 или 6-членного моноциклического гетероциклила, содержего один или два гетероатома кислорода,
необязательно замещенного 4-членного гетероциклила, содержащего один гетероатом кислорода,
необязательно замещенного ароматического 6-членного моноциклического гетероцикла, содержащего один или два гетероатома азота,
частично насыщенного 6-членного моноциклического гетероциклила, содержащего один гетероатом азота, который необязательно может быть замещен,
необязательно замещенного насыщенного 4-членного моноциклического гетероциклила, содержащего один гетероатом азота,
насыщенного 5-членного моноциклического гетероциклила, содержащего один гетероатом азота,
насыщенного 6-членного моноциклического гетероциклила, содержащего один гетероатом азота,
бициклического гетероциклила, содержащего бензольное кольцо, конденсированное с 5- или 6-членным кольцом, содержащим 1, 2 или 3 гетероатома,
4, 5 или 6-членного моноциклического насыщенного гетероцикла, замещенного двумя заместителями, которые присоединены к одному и тому же атому и которые объединены с образованием 4- к 7-членного насыщенного моноциклического гетероциклила, содержащего по меньшей мере один гетероатом, выбранный из N, О или S,
необязательно замещенного ароматического 5-членного моноциклического гетероциклила, содержащего один гетероатом серы,
необязательно замещенного ароматического 5-членного моноциклического гетероциклила, содержащего один гетероатом серы и один гетероатом азота,
насыщенного 6-членного моноциклического гетероциклила, содержащего два гетероатома азота,
ароматического 5-членного моноциклического гетероциклила, содержащего четыре гетероатома азота,
ароматического 5-членного моноциклического гетероциклила, содержащего один гетероатом кислорода и два гетероатома азота,
необязательно замещенного ароматического 5-членного моноциклического гетероциклила, содержащего два гетероатома азота,
необязательно замещенного ароматического 5-членного моноциклического гетероциклила, содержащего три гетероатома азота,
насыщенного 5-членного моноциклического гетероциклила, содержащего один гетероатом азота и один гетероатом кислорода,
насыщенного 6-членного моноциклического гетероциклила, содержащего один гетероатом азота и один гетероатом серы,
насыщенного 7-членного моноциклического гетероциклила, содержащего два гетероатома азота,
насыщенного 7-членного моноциклического гетероциклила, содержащего один гетероатом азота и один гетероатом кислорода, и
фенила или нафтила, в частности фенила.
В одном варианте осуществления R9 представляет собой необязательно замещенный 5-членный ароматический или насыщенный гетероцикл, такой как, например, имидазолил, пирролидинил, изоксазолидинил. Дополнительные заместители могут представлять собой =O, 5 или 6-членный ароматический моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где указанный гетероциклил необязательно замещен R16; или -S(=O)2-NR14R15.
В одном варианте осуществления R9 представляет собо C3-6циклоалкил, такой как, например, циклопропил, 3-членный насыщенный гетероциклил, такой как, например, оксиранил, необязательно замещенный 5-членный насыщенный гетероцикл, такой как, например, пирролидинонил, необязательно замещенный 6-членный ароматический или насыщенный гетероцикл, такой как, например, пиридил, пиримидинил, пиразинил, пиперазинил или морфолинил, необязательно замещенный бициклический гетероцикл, такой как, например, 1H-изоиндол-1,3-дион. Необязательные заместители могут представлять собой =O, C1-4алкокси, C1-4алкил, который замещен -NR14R15, гидроксиC1-4алкил или C1-4алкил-C(=O)-.
В одном варианте осуществления R9 представляет собой необязательно замещенный 5-членный ароматический гетероцикл, такой как, например, имидазолил, или необязательно замещенный 6-членный ароматический гетероцикл, такой как, например, пиридил, пиримидинил или пиразинил. Необязательные заместители могут представлять собой C1-4алкокси или -S(=O)2-NR14R15.
В одном варианте осуществления R9 представляет собой необязательно замещенный 5-членный ароматический гетероцикл, такой как, например, имидазолил. Необязательные заместители могут представлять собой -S(=O)2-NR14R15.
В одном варианте осуществления R9 представляет собой необязательно замещенный 6-членный ароматический гетероцикл, такой как, например, пиридинил или пиримидинил. Необязательные заместители могут представлять собой C1-4алкокси.
В одном варианте осуществления R9 представляет собой необязательно замещенный 5-членный ароматический или насыщенный гетероцикл, такой как, например, имидазолил, пирролидинил, оксазолидинил. Необязательные заместители могут представлять собой =O, 5- или 6-членный ароматический моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где указанный гетероциклил необязательно замещен R16; или -S(=O)2-NR14R15.
В одном варианте осуществления R9 представляет собой C3-6циклоалкил, такой как, например, циклопропил, 3-членный насыщенный гетероциклил, такой как, например, оксиранил, необязательно замещенный 5-членный насыщенный гетероцикл, такой как, например, пирролидинонил, необязательно замещенный 6-членный ароматический или насыщенный гетероцикл, такой как, например, пиридил, пиримидинил, пиразинил, пиперазинил или морфолинил, необязательно замещенный бициклический гетероцикл, такой как, например, 1H-изоиндол-1,3-дион. Необязательные заместители могут представлять собой =O, C1-4алкокси, C1-4алкил, который замещен -NR14R15, гидроксиC1-4алкил или C1-4алкил-C(=O)-.
В одном варианте осуществления R9 является имидазолилом, в частности 2-имидазолилом, который необязательно замещен -S(=O)2-NR14R15; в частности R9 является имидазолилом, в частности 2-имидазолилом.
В одном варианте осуществления R10 представляет собой водород или C1-6алкил.
В одном варианте осуществления R10 является водородом.
В одном варианте осуществления R11 представляет собой водород, C1-6алкил, галоC1-6алкил, -C(=O)-C1-6алкил, -S(=O)2-C1-6алкил, -S(=O)2-NR14R15, гидроксиC1-6алкил, -C(=O)-гидроксигалоC1-6алкил, -C(=O)-R6, цианоC1-6алкил, R6, -C(=O)-R6, C1-6алкил, который замещен R6, -C(=O)-галоC1-6алкил, C1-6алкил, который замещен -Si(CH3)3, C1-6алкил, который замещен -NR14R15, C1-6алкил, который замещен -C(=O)-NR14R15, C1-6алкокси, гидроксигалоC1-6алкил, карбоксил или C1-6алкоксиC1-6алкил.
В одном варианте осуществления R10 и R11 представляют собой водород или C1-6алкил.
В одном варианте осуществления R6 представляет собой 6-членный моноциклический насыщенный гетероциклил, который необязательно замещен. Например, пиперазинил или морфолинил или тетрагидропиранил, который необязательно замещен галогеном, C1-6алкилом или C1-6алкил-O-C(=O)-.
В одном варианте осуществления R6 представляет собой 6-членный моноциклический ароматический гетероциклил, который необязательно замещен. Например, пиридинил, который необязательно замещен галогеном, C1-6алкилом или C1-6алкил-O-C(=O)-.
В одном варианте осуществления R6 представляет собой необязательно замещенный насыщенный 4-7-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, такой как, например, тетрагидропиран.
В одном варианте осуществления R6 представляет собой C3-8циклоалкил, C3-8циклоалкенил, 4-7-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S; указанный C3-8циклоалкил, C3-8циклоалкенил, 4-7-членный моноциклический гетероциклил, необязательно и каждый независимо, замещен 1, 2, 3, 4 или 5 заместителями, при этом каждый заместитель независимо выбиран из циано, C1-6алкила, цианоC1-6алкила, гидроксил, карбоксила, гидроксиC1-6алкила, галогена, галоC1-6алкила, гидроксигалоC1-6алкила, C1-6алкокси, C1-6алкоксиC1-6алкила, C1-6алкил-O-C(=O)-NR14R15, -C(=O)-NR14R15, C1-6алкила, который замещен -NR14R15, C1-6алкила, который замещен -C(=O)-NR14R15, -S(=O)2-C1-6алкила, -S(=O)2-галоC1-6алкила, -S(=O)2-NR14R15, C1-6алкила, который замещен -S(=O)2-C1-6алкилом, C1-6алкила, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкила, который замещен -S(=O)2-NR14R15, C1-6алкила, который замещен -NH-S(=O)2-C1-6алкилом, C1-6алкила, который замещен -NH-S(=O)2-галоC1-6алкилом, или C1-6алкила, который замещен -NH-S(=O)2-NR14R15.
В одном варианте осуществления R12 представляет собой водород или C1-4алкил, который необязательно замещен C1-4алкилокси.
В одном варианте осуществления R13 представляет собой насыщенный 4-6-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N или O.
В одном варианте осуществления каждый R14 и R15 независимо представляет собой водород или C1-4алкил.
В одном варианте осуществления W является -N(R3)-.
В одном варианте осуществления W является -C(R3aR3b)-.
В одном варианте осуществления W является -C(=O)-.
В одном варианте осуществления W является -N(R3)- или -C(R3aR3b)-, где R3a и R3b не объединены с образованием =O.
В одном варианте осуществления W является -N(R3)- или -C(R3aR3b)-, где R3a представляет собой -NR10R11, гидроксил, C1-6алкокси, гидроксиC1-6алкокси, C1-6алкокси, который замещен -NR10R11, C1-6алкил, C2-6алкенил, C2-6алкинил, галоC1-6алкил, который необязательно замещен -O-C(=O)-C1-6алкилом, гидроксиC1-6алкил, который необязательно замещен -O-C(=O)-C1-6алкилом, гидроксиC2-6алкенил, гидроксиC2-6алкинил, гидроксигалоC1-6алкил, цианоC1-6алкил, C1-6алкил, который замещен карбоксилом, C1-6алкил, который замещен -C(=O)-C1-6алкилом, C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, C1-6алкил, который замещен C1-6алкоксиC1-6алкил-O-C(=O)-, C1-6алкил, который замещен C1-6алкоксиC1-6алкил-C(=O)-, C1-6алкил который замещен -O-C(=O)-C1-6алкилом, C1-6алкоксиC1-6алкил, где каждый C1-6алкил необязательно может быть замещен одной или двумя гидроксильными группами или -O-C(=O)-C1-6алкилом, C2-6алкенил, который замещен C1-6алкокси, C2-6алкинил, который замещен C1-6алкокси, C1-6алкил, который замещен R9 и необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен -C(=O)-R9, C1-6алкил, который замещен гидроксилом и R9, C2-6алкенил, который замещен R9, C2-6алкинил, который замещен R9, C1-6алкил, который замещен -NR10R11, C2-6алкенил, который замещен -NR10R11, C2-6алкинил, который замещен -NR10R11, C1-6алкил, который замещен гидроксилом и -NR10R11, C1-6алкил, который замещен одним или двумя галогенами и -NR10R11,-C1-6алкил-C(R12)=N-O-R12, C1-6алкил, который замещен -C(=O)-NR10R11, C1-6алкил, который замещен -O-C(=O)-NR10R11, -S(=O)2-C1-6алкил, -S(=O)2-галоC1-6алкил, -S(=O)2-NR14R15, C1-6алкил, который замещен -S(=O)2-C1-6алкилом, C1-6алкил, который замещен -S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -S(=O)2-NR14R15, C1-6алкил, который замещен -NR12-S(=O)2-C1-6алкилом, C1-6алкил, который замещен -NH-S(=O)2-галоC1-6алкилом, C1-6алкил, который замещен -NR12-S(=O)2-NR14R15, R13, C1-6алкил, который замещен -P(=O)(ОH)2, или C1-6алкил, который замещен -P(=O)(OC1-6алкилом)2;
R3b представляет собой водород или гидроксил; при условии, что если R3a представляет собой -NR10R11, то R3b представляет собой водород; или
R3a и R3b объединены с образованием =NR10, с образованием циклопропила вместе с атомом углерода, к которому они присоединены, с образованием =CH-C0-4алкила, который замещен R3c, или с образованием

В одном варианте осуществления W является -N(R3)- или -C(R3aR3b)-, где R3a и R3b не объединены вместе.
В одном варианте осуществления W является -N(R3)- или -C(=O)-; в частности W является -N(R3)-; R3 представляет собой гидроксиC1-6алкил, который необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен R9 и который необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен -NR10R11.
В одном варианте осуществления W является -N(R3)-, D является 5- или 6-членным моноциклическим ароматическим карбоциклилом или гетероциклилом, где указанный карбоциклил или гетероциклил могут быть необязательно замещены одной или более (например, 1, 2 или 3) группами R1; n равно 2 или 4; R2 является C1-6алкилокси или галогеном; R3 является гидроксиC1-6алкилом, галоC1-6алкилом или C1-6алкилом, который замещен R9. В одном варианте осуществления W является -N(R3)-, D является фенилом или пиразолилом, который замещен C1-6алкилом; n равно 2 или 4; R2 является C1-6алкилокси или галогеном; R3 является гидроксиC1-6алкилом, галоC1-6алкилом или C1-6алкилом, который замещен R9.
В одном варианте осуществления W является -N(R3)-, D является 5- или 6-членным моноциклическим ароматическим карбоциклилом или гетероциклилм, где указанный карбоциклил или гетероциклил могут быть необязательно замещены одной или более (например, 1, 2 или 3) группами R1; n равно 2, 3 или 4; R2 является C1-6алкилокси или галогеном; R3 является гидроксиC1-6алкилом, галоC1-6алкилом, C1-6алкилом, который замещен -NR10R11, или C1-6алкилом, который замещен R9; каждый R10 и R11 независимо представляет собой водород или C1-6алкил.
В одном варианте осуществления W является -N(R3)-, D является фенилом или пиразолилом, который замещен C1-6алкилом; n равно 2, 3 или 4; R2 является C1-6алкилокси или галогеном; R3 является гидроксиC1-6алкилом, галоC1-6алкилом, C1-6алкилом, который замещен -NR10R11, или C1-6алкилом, который замещен R9; каждый R10 и R11 независимо представляет собой водород или C1-6алкил.
В одном варианте осуществления W является -N(R3)-, D является 5- или 6-членным моноциклическим ароматическим карбоциклилом или гетероциклилом, где указанный карбоциклил или гетероциклил могут быть необязательно замещены одной или более (например, 1, 2 или 3) группами R1, в частности D является фенилом или пиразолилом, который необязательно замещен C1-6алкилом, более конкретно D является фенилом или пиразолилом, который необязательно замещен C1-6алкилом, и n равно 2 или 4; еще более конкретно D является фенилом или пиразолилом, который необязательно замещен C1-6алкилом; n равно 2 или 4, R2 является C1-6алкилокси или галогеном; еще более конкретно D является фенилом или пиразолилом, который необязательно замещен C1-6алкилом; n равно 2 или 4; R2 является C1-6алкилокси или галогеном, и указанный R2 расположен в положении 2, 3, 5 или 6; еще более конкретно D является фенилом или пиразолилом, который необязательно замещен C1-6алкилом; n равно 2; R2 является C1-6алкилокси, и указанный R2 расположен в положении 3 или 5; и R3 является гидроксиC1-6алкилом, галоC1-6алкилом или C1-6алкилом, который замещен R9.
В одном варианте осуществления W является -C(R3aR3b)-, D является 5- или 6-членным моноциклическим ароматическим карбоциклилом или гетероциклилом, где указанный карбоциклил или гетероциклил могут быть необязательно замещены одной или более (например, 1, 2 или 3) группами R1; n равно 2 или 4; R2 является C1-6алкилокси или галогеном; R3 является гидроксиC1-6алкилом, галоC1-6алкилом или C1-6алкилом, который замещен R9. В одном варианте осуществления W является -C(R3aR3b)-, D является фенилом или пиразолилом, который замещен C1-6алкилом; n равно 2 или 4; R2 является C1-6алкилокси или галогеном; R3 является гидроксиC1-6алкилом, галоC1-6алкилом или C1-6алкилом, который замещен R9.
В одном варианте осуществления W является -C(R3aR3b)-, D является 5- или 6-членным моноциклическим ароматическим карбоциклилом или гетероциклилом, где указанный карбоциклил или гетероциклил могут быть необязательно замещены одной или более (например, 1, 2 или 3) группами R1; в частности D является фенилом или пиразолилом, который необязательно замещен C1-6алкилом, более конкретно D является фенилом или пиразолилом, который необязательно замещен C1-6алкилом, и n равно 2 или 4; еще более конкретно D является фенилом или пиразолилом, который необязательно замещен C1-6алкилом; n равно 2 или 4; R2 является C1-6алкилокси или галогеном; еще более конкретно D является фенилом или пиразолилом, который необязательно замещен C1-6алкилом; n равно 2 или 4; R2 является C1-6алкилокси, и указанный R2 расположен в положении 2, 3, 5 или 6; еще более конкретно D является фенилом или пиразолилом, который необязательно замещен C1-6алкил; n равно 2 или 4; R2 является C1-6алкилокси, и указанный R2 расположен в положении 2, 3, 5 или 6; и R3 является гидроксиC1-6алкилом, галоC1-6алкилом или C1-6алкилом, который замещен R9.
В одном варианте осуществления n представляет собой целое число, равное 2 или 4; R2 представляет собой C1-4алкокси или галоген, например CH3O- или фтор; R3 представляет собой гидроксиC1-6алкил, галоC1-6алкил или C1-6алкил, который замещен R9, D представляет собой пиразолил, в частности пиразол-4-ил, который замещен C1-6алкилом; W является -N(R3)-.
В одном варианте осуществления
D является пиразолилом или фенилом, каждый из которых необязательно замещен C1-4алкилом;
W является -N(R3)- или -C(=O)-;
R3 является гидроксиC1-6алкилом, C1-6алкилом, который замещен R9, или C1-6алкилом, который замещен -NR10R11;
R9 является имидазолилом, который необязательно замещен -S(=O)2-NR14R15;
каждый R10 и R11 независимо представляет собой водород или C1-6алкил;
R14 и R15 представляют собой C1-4алкил.
В одном варианте осуществления
D является пиразолилом или фенилом, каждый из которых необязательно замещен C1-4алкилом;
W является -N(R3)-;
R3 является гидроксиC1-6алкилом, C1-6алкилом, который замещен R9, или C1-6алкилом, который замещен -NR10R11;
R9 является имидазолилом, который необязательно замещен -S(=O)2-NR14R15;
каждый R10 и R11 независимо представляет собой водород или C1-6алкил;
R14 и R15 представляют собой C1-4алкил.
В одном варианте осуществления
W является -N(R3)- или -C(=O)-; в частности W является -N(R3)-;
каждый R2 является галогеном или C1-4алкокси;
D представляет собой 5-6-членный моноциклический карбоциклил или 5-6-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный карбоциклил и гетероциклил могут быть необязательно замещены одной или более (например, 1, 2 или 3) группами R1;
R1 представляет собой C1-6алкил;
R3 представляет собой гидроксиC1-6алкил, C1-6алкил, который замещен R9, или C1-6алкил, который замещен -NR10R11;
R9 представляет собой 5-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где указанны 5-членный моноциклический гетероциклил необязательно замещен -S(=O)2-NR14R15;
каждый R10 и R11 независимо представляет собой водород или C1-6алкил;
R14 и R15 представляют собой C1-4алкил;
n независимо представляет собой целое число, равное 1, 2, 3 или 4.
В одном варианте осуществления
W является -N(R3)- или -C(=O)-; в частности W является -N(R3)-;
каждый R2 является галогеном или C1-4алкокси;
D представляет собой 5-6-членный моноциклический карбоциклил или 5-6-членный моноциклический гетероциклил, содержащий по меньшей мере один атом N, где каждый указанный карбоциклил и гетероциклил необязательно может быть замещен одной группой R1;
R1 представляет собой C1-6алкил;
R3 представляет собой гидроксиC1-6алкил, C1-6алкил, который замещен R9, или C1-6алкил, который замещен -NR10R11;
R9 представляет собой 5-членный моноциклический гетероциклил, содержащий по меньшей мере один атом N, где указанный 5-членный моноциклический гетероциклил необязательно замещен -S(=O)2-NR14R15;
каждый R10 и R11 независимо представляет собой водород или C1-6алкил;
R14 и R15 представляют собой C1-4алкил;
n независимо представляет собой целое число, равное 1, 2, 3 или 4.
В одном варианте осуществления
W является -N(R3)- или -C(=O)-; в частности W является -N(R3)-;
каждый R2 является фтором, хлором или метокси;
D представляет собой фенил или пиразолил, который замещен метилом по NH-группе;
R1 представляет собой метил;
R3 представляет собой оксиэтил, метил, который замещен R9, или этил, который замещен -NR10R11;
R9 представляет собой имидазолил, который необязательно замещен -S(=O)2-NR14R15;
каждый R10 и R11 независимо представляет собой водород, этил или изопропил;
R14 и R15 представляют собой метил; n независимо представляет собой целое число, равное 1, 2, 3 или 4.
В одном варианте осуществления
W является -N(R3)- или -C(=O)-; в частности W является -N(R3)-;
каждый R2 является галогеном или C1-4алкокси;
D представляет собой 3-12-членный моноциклический или бициклический карбоциклил или 3-12-членный моноциклический или бициклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный карбоциклил и гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1;
R1 представляет собой C1-6алкил;
R3 представляет собой гидроксиC1-6алкил, который необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен R9 и который необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен -NR10R11;
R9 представляет собой 3-12-членный моноциклический или бициклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где указанный 3-12-членный моноциклический или бициклический гетероциклил необязательно замещен -S(=O)2-NR14R15;
каждый R10 и R11 независимо представляет собой водород или C1-6алкил;
каждый R14 и R15 представляет собой C1-4алкил;
n независимо представляет собой целое число, равное 1, 2, 3 или 4.
В одном варианте осуществления
W является -N(R3)- или -C(R3aR3b)-; в частности W является -N(R3)-;
каждый R2 является галогеном или C1-4алкокси;
D представляет собой 5-6-членный моноциклический карбоциклил или 5-6-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный карбоциклил и гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1;
R1 представляет собой C1-6алкил или -C(=O)-O-C1-6алкил;
R3 представляет собой гидроксиC1-6алкил, C1-6алкил, который замещен R9, или C1-6алкил, который замещен -NR10R11;
R3a и R3b объединены с образованием =O или =CH-C0-4алкила, который замещен R3c; R3c является цианогруппой;
R9 представляет собой 5-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где указанный 5-членный моноциклический гетероциклил необязательно замещен -S(=O)2-NR14R15;
каждый R10 и R11 независимо представляет собой водород или C1-6алкил;
R14 и R15 представляют собой C1-4алкил;
n независимо представляет собой целое число, равное 1, 2, 3 или 4.
В одном варианте осуществления
W является -N(R3)- или -C(R3aR3b)-; в частности W является -N(R3)-;
каждый R2 является галогеном или C1-4алкокси;
D представляет собой 5-6-членный моноциклический карбоциклил или 5-6-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N или O, где каждый указанный карбоциклил и гетероциклил необязательно может быть замещен одной группой R1;
R1 представляет собой C1-6алкил или -C(=O)-O-C1-6алкил;
R3 представляет собой гидроксиC1-6алкил, C1-6алкил, который замещен R9, или C1-6алкил, который замещен -NR10R11;
R3a и R3b объединены с образованием =O или =CH-C0-4алкила, который замещен R3c; R3c является цианогруппой;
R9 представляет собой 5-членный моноциклический гетероциклил, содержащий по меньшей мере один атом N, где указанный 5-членный моноциклический гетероциклил необязательно замещен -S(=O)2-NR14R15;
каждый R10 и R11 независимо представляет собой водород или C1-6алкил;
R14 и R15 представляют собой C1-4алкил;
n независимо представляет собой целое число, равное 1, 2, 3 или 4.
В одном варианте осуществления
W является -N(R3)- или -C(R3aR3b)-; в частности W является -N(R3)-;
каждый R2 является фтором, хлором или метоксигруппой;
D представляет собой фенил, пиридинил, пиперидинил, тетрагидро-2H-пиранил, пиримидинил или пиразолил, где пиразолил или пиперидинил необязательно замещены метилом или трет-бутоксикарбонилом по NH-группе;
R3 представляет собой 2-оксиэтил, 3-гидроксипропил, -(CH2)2-NR10R11, -(CH2)3-NR10R11 или метил, который замещен R9;
R3a и R3b объединены с образованием =O или =CH-CN;
R9 представляет собой имидазолил, который необязательно замещен -S(=O)2-NR14R15;
каждый R10 и R11 независимо представляет собой водород, метил, этил или изопропил;
R14 и R15 представляют собой метил;
n независимо представляет собой целое число, равное 1, 2, 3 или 4.
В одном варианте осуществления
W является -N(R3)- или -C(R3aR3b)-; в частности W является -N(R3)-;
каждый R2 является галогеном или C1-4алкокси;
D представляет собой 3-12-членный моноциклический или бициклический карбоциклил или 3-12-членный моноциклический или бициклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный карбоциклил и гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1;
R1 представляет собой C1-6алкил или -C(=O)-O-C1-6алкил;
R3 представляет собой гидроксиC1-6алкил, который необязательно замещен -O-C(=O)-C1-6алкилом, C1-6алкил, который замещен R9 и который необязательно замещен -O-C(=O)-C1-6алкилом, или C1-6алкил, который замещен -NR10R11;
R3a и R3b объединены с образованием =O или =CH-C0-4алкила, который замещен R3c;
R3c является цианогруппой;
R9 представляет собой 3-12-членный моноциклический или бициклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где указанный 3-12-членный моноциклический или бициклический гетероциклил необязательно замещен -S(=O)2-NR14R15;
каждый R10 и R11 независимо представляет собой водород или C1-6алкил;
каждый R14 и R15 представляет собой C1-4алкил;
n независимо представляет собой целое число, равное 1, 2, 3 или 4.
В одном варианте осуществления
W является -N(R3)-;
каждый R2 является фтором или метоксигруппой;
D представляет собой пиперидинил или тетрагидро-2H-пиранил, в частности 4-пиперидинил или тетрагидро-2H-пиран-4-ил;
R3 представляет собой C1-4алкил, который замещен -NR10R11;
каждый R10 и R11 независимо представляет собой водород, метил, этил или изопропил;
n независимо представляет собой целое число, равное 3 или 4.
В одном варианте осуществления
W является -N(R3)-;
каждый R2 является фтором или метоксигруппой;
D представляет собой пиперидинил, тетрагидро-2H-пиранил, или пиразолил, где пиразолил или пиперидинил необязательно замещены метилом по NH-группе;
R3 представляет собой -(CH2)2-NR10R11, -(CH2)3-NR10R11 или метил, который замещен R9;
R9 представляет собой имидазолил, который необязательно замещен -S(=O)2-NR14R15;
каждый R10 и R11 независимо представляет собой водород, метил, этил или изопропил;
R14 и R15 представляют собой метил;
n независимо представляет собой целое число, равное 3 или 4.
В одном варианте осуществления R3 представляет собой гидроксиC2-6алкил, C1-6алкил, который замещен R9, или C2-6алкил, который замещен -NR10R11.
В одном варианте осуществления соединение формулы (I) является соединением формулы (Ia),

включая его любую таутомерную или стереохимически изомерную форму;
где n, R1, R2 и R3 являются такими, как определено в настоящем описании;
их N-оксидами, фармацевтически приемлемыми солями или сольватами.
В одном варианте осуществления соединение формулы (I) является соединением формулы (Iab),

включая его любую таутомерную или стереохимически изомерную форму;
где R3 и D являются такими, как определено в настоящем описании;
их N-оксидами, фармацевтически приемлемыми солями или сольватами.
В одном варианте осуществления соединение формулы (I) является соединением формулы (Iab),

включая его любую таутомерную или стереохимически изомерную форму;
где R3 представляет собой этил, который замещен -NR10R11;
каждый R10 и R11 независимо представляет собой водород, этил или изопропил;
D представляет собой пиразолил, который замещен метилом;
их N-оксидами, фармацевтически приемлемыми солями или сольватами.
В одном варианте осуществления D представляет собой фенил, 3-пиридинил, 4-пиридинил, 4-пиперидинил, тетрагидро-2H-пиран-4-ил, 5-пиримидинил, или пиразол-4-ил, где пиразол-4-ил или 4-пиперидинил необязательно замещены метилом или трет-бутоксикарбонилом по NH-группе.
В одном варианте осуществления D представляет собой неароматический 5- или 6-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N, О или S, где каждый указанный гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1.
В одном варианте осуществления D представляет собой неароматический 6-членный моноциклический гетероциклил, содержащий по меньшей мере один гетероатом, выбранный из N или O, где каждый указанный гетероциклил необязательно может быть замещен одной или более (например, 1, 2 или 3) группами R1; в частности D не замещен.
В другом варианте осуществления D представляет собой пиперидинил или тетрагидро-2H-пиранил, в частности 4-пиперидинил или тетрагидро-2H-пиран-4-ил.
В одном варианте осуществления соединение формулы (I) является соединением формулы (Ia),
включая его любую таутомерную или стереохимически изомерную форму; где:
R1 представляет собой C1-6алкил;
R2 представляет собой C1-4алкокси, например CH3O-, или галоген, например фтор;
n=2 или 4; и
R3 представляет собой гидроксиC1-6алкил, галоC1-6алкил или C1-6алкил, который замещен R9;
их N-оксидами, фармацевтически приемлемыми солями или сольватами.
В одном варианте осуществления соединение формулы (I) является любым из следующих соединений:

их N-оксидом, фармацевтически приемлемой солью или сольватом; в частности их фармацевтически приемлемой солью или сольватом.
В одном варианте осуществления соединение формулы (I) является любым из следующих соединений:

В одном варианте осуществления соединение формулы (I) является любым из следующих соединений:

их N-оксидом, фармацевтически приемлемой солью или сольватом; в частности фармацевтически приемлемой солью или сольватом.
В одном варианте осуществления соединение формулы (I) является любым из следующих соединений:
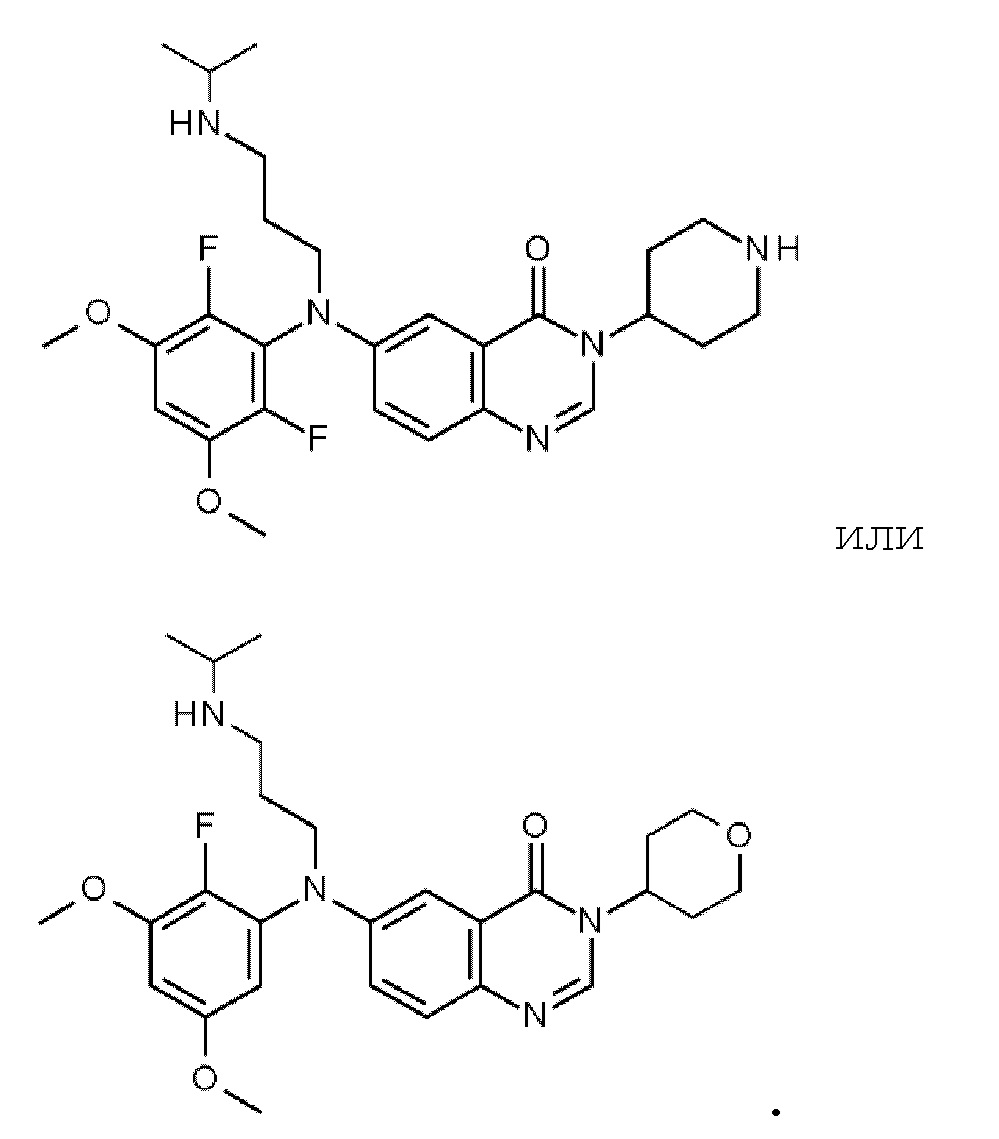
Во избежание неправильного толкования, следует понимать, что каждое общее и конкретное предпочтение, вариант осуществления изобретения и пример для одного заместителя могут быть комбинированы, при наличии возможности, с каждым общим и конкретным предпочтением, вариантом осуществления изобретения и примером для одного или более, и предпочтительно всех других заместителей, как определено в описании, и что все такие варианты осуществления изобретения охвачены настоящей заявкой.
Способы получения соединений формулы (I)
В данном разделе, как и во всех других разделах настоящей заявки, если из контекста не следует иное, отсылки к формуле (I) также включают все другие ее подгруппы и примеры, как определено в описании.
В общем, соединения формулы (I), в которых W является -N(R3)-, где указанные соединения представлены формулой (Ia), могут быть получены согласно следующей Схеме реакции 1.
Схема 1

В Схеме 1 применены следующие условия реакции:
1: в присутствии подходящего основания, такого как, например, гидрид натрия или Cs2CO3, и подходящего растворителя, такого как, например, N,N-диметилформамид, N,N-диметилацетамид, тетрагидрофуран или ацетонитрил, и где W1 представляет собой подходящую уходящую группу, такую как, например, галоген, например бром, хлор и т.п., или -O-S(=O)2-CH3, а R3d представляет собой необязательно замещенный C1-6алкил, такой как, например, -CН2-С3Н5;
2: в присутствии подходящего основания, такого как, например, гидрид натрия, Cs2CO3 или гидроксид калия, и подходящего растворителя, такого как, например, N,N-диметилформамид, N,N-диметилацетамид или ацетонитрил, и где R' представляет собой необязательно замещенный C1-4алкил, а R" представляет собой водород или необязательно замещенный C1-4алкил;
3: в присутствии подходящего агента фазового переноса, такого как, например, бромид тетрабутиламмония, подходящего основания, такого как, например, гидроксид калия, и подходящего растворителя, такого как, например, 2-метилтетрагидрофуран и вода. В случае, когда промежуточное соединение формулы (II) реагирует с промежуточным соединением формулы W1-C1-6алкил-N цикл; могут быть применены следующие условия: подходящее основание, такое как, например, гидрид натрия, и подходящий растворитель, такой как, например, N,N-диметилформамид или N,N-диметилацетамид.
4: в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, например, N,N-диметилформамида или N,N-диметилацетамида, и где P представляет собой подходящую защитную группу, такую как, например, -C(=O)-O-C(CH3)3;
5: в присутствии подходящей кислоты, такой как, например, HCl или трифторуксусная кислота, и подходящего растворителя, такого как, например, дихлорметан или спирт, например метанол;
6: в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, такого как, например, N,N-диметилформамид или N,N-диметилацетамид, или тетрагидрофуран, и где W2 представляет собой подходящую уходящую группу, такую как, например, галоген, например бром, и где Rx и Ry представляют собой C1-4алкил, и Rz представляет собой C1-4алкил или фенил, например Rx и Ry представляют собой CH3, а Rz представляет собой C(CH3)3 или фенил;
7: в присутствии подходящего растворителя, такого как, например, тетрагидрофуран. Данный тип реакции может быть также выполнен в присутствии подходящей кислоты, такой как, например, уксусная кислота или HCl, и подходящего растворителя, такого как, например, диоксан;
8: в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, такого как, например, N,N-диметилформамид или N,N-диметилацетамид, и где W3 представляет собой подходящую уходящую группу, такую как, например, галоген, например, бром и т.п.;
9: в присутствии подходящей кислоты, такой как, например, HCl, и подходящего растворителя, такого как, например, спирт, например метанол или изопропанол;
10: в присутствии подходящего основания, такого как, например, триэтиламин или диизопропилэтанамин, и подходящего растворителя, такого как, например, дихлорметан или тетрагидрофуран.
Во время этой реакции также может быть получено соединение формулы (Ib-1-4):

11: необязательно в присутствии подходящего основания, такого как, например, триэтиламин, K2CO3, Na2CO3 или гидрид натрия, и, необязательно, подходящего растворителя, такого как, например, ацетонитрил, тетрагидрофуран, диоксан, N,N-диметилформамид, 1-метил-пирролидинон. Данный тип реакции может быть также выполнен с подходящей солью NHR10R11, например, HCl солью NHR10R11, или может быть выполнен в присутствии иодида калия. Таким способом могут быть получены соединения, в которых R3 представляет собой иодC1-6алкил.
12: в присутствии подходящего растворителя, такого как, например, ацетонитрил, 1-метил-2-пирролидинон, необязательно в присутствии иодида калия или подходящего основания, такого как, например, Na2CO3, K2CO3 или триэтиламин. Данная реакция также может быть выполнена с подходящей солью

13: в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, такого как, например, диметилацетамид, и где P представляет собой подходящую защитную группу, такую как, например, -C(=O)-O-C(CH3)3.
Промежуточные соединения формулы (II), используемые в Схеме 1 выше, могут быть получены согласно следующей Схеме 2 реакции.
Схема 2

В Схеме 2, где W1 представляет собой подходящую уходящую группу, такую как, например, галоген, например бром, хлор и т.п., применены следующие условия реакции:
1: в присутствии триэтилортоформиата в подходящем растворителе, таком как, например, толуол;
2: в присутствии подходящего катализатора, такого как, например, хлор[2-(дициклогексилфосфино)-3,6-диметокси-2'-4'-6'-триизопропил-1,1'-бифенил][2-(2-аминоэтил)фенил]палладий (II), подходящего основания, такого как, например, карбонат цезия, в подходящем растворителе, таком как, например, толуол; или в присутствии подходящего катализатора, такого как, например, трис(дибензилиденацетон)дипалладий (0) (Pd2dba3), в присутствии подходящего лиганда, такого как, например, [1,1'-бинафталин]-2,2'-диилбис[дифенилфосфин] (BINAP), и подходящего основания, такого как, например, карбонат цезия, в подходящем растворителе, таком как, например, диоксан.
В общем, соединения формулы (I), где W является -C(R3aR3b)-, где указанные соединения представлены формулой (Ic-1), могут быть получены согласно следующей Схеме 3 реакции.
Схема 3

В Схеме 3, где W1 представляет собой подходящую уходящую группу, такую как, например, галоген, например бром, хлор и т.п., применены следующие условия реакции:
1: в присутствии подходящего катализатора, такого как, например, [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий (PdCl2dppf), и подходящего растворителя, такого как, например, тетрагидрофуран (ТГФ);
2: в присутствии подходящего основания, такого как, например, бутиллитий, и подходящего растворителя, такого как, например, ТГФ, и R3d представляет собой необязательно замещенный C1-6алкил. Данная реакция может быть также выполнена с защищенной формой реагента, а именно W1-R3d-P, где P является подходящей защитной группой, такой как, например, трет-бутилдиметилсилильная группа, с последующей подходящей реакцией снятия защиты, например, в присутствии подходящего десилилирующего реагента, такого как, например, фторид тетрабутиламмония, в подходящем растворителе, таком как, например, тетрагидрофуран, или, например, в присутствии подходящей кислоты, такой как, например, HCl или трифторуксусная кислота (ТФУ), и подходящего растворителя, такого как, например, спирт, например метанол, или дихлорметан.
Соединения формулы (I), где W является -C(R3aR3b)-, где указанные соединения представлены формулой (Ic-1), могут быть также получены согласно следующей Схеме 4 реакции.
Схема 4

В Схеме 4 применены следующие условия реакции:
1,2,3: необязательно в присутствии подходящего основания, такого как, например, триэтиламин, изопропиламин, карбонат калия, карбонат натрия или гидрид натрия, и, необязательно, подходящего растворителя, такого как, например, ацетонитрил, тетрагидрофуран, N,N-диметилформамид, подходящего спирта, например, 1-бутанола и т.п., и где P представляет собой подходящую защитную группу, такую как, например, -C(=O)-OC(CH3)3;
Стадия 1 может быть также выполнена с подходящей солью
4: в присутствии подходящей кислоты, такой как, например, HCl или ТФУ, и подходящего растворителя, такого как, например, дихлорметан, или спирта, например метанола.
Соединения формулы (I), где W является -C(R3aR3b)-, где указанные соединения представлены формулой (Ic-1), (Id) или (Ie), могут быть получены согласно следующей Схеме 5 реакции.
Схема 5

В Схеме 5 применены следующие условия реакции:
1: в присутствии монооксида углерода, подходящего палладиевого катализатора, такого как, например, ацетат палладия (II) (Pd(OAc)2), подходящего лиганда, такого как, например, трициклогексилфосфин, подходящего основания, такого что, например, триэтиламин, в подходящем растворителе, таком как, например, толуол
2: в подходящем растворителе, таком как, например, толуол
3: в присутствии подходящей кислоты Льюиса, такой как, например, триметилалюминий, и подходящего растворителя, такого как, например, толуол;
4: в присутствии подходящего катализатора, такого как, например, тетракис(трифенилфосфин)палладий (Pd(PPh3)4), подходящего растворителя, такого как, например, толуол, и подходящей кислоты, такой как хлороводород
5: в присутствии подходящего растворителя, такого как, например, тетрагидрофуран.
Соединение формулы (Ie-2а)

может быть получено согласно методике реакции, аналогичной используемой для синтеза промежуточного соединения формулы (XIII).
Соединения формулы (I), где W является -C(R3aR3b)-, где указанные соединения представлены формулой (Ic-2), могут быть получены согласно следующей Схеме 6 реакции.
Схема 6

В Схеме 6 применены следующие условия реакции:
1: в присутствии подходящего восстановителя, такого как, например, борогидрид натрия, и в присутствии подходящего растворителя, такого как, например, метанол;
2: в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, такого как, например, N,N-диметилформамид или N,N-диметилацетамид, и где Rx и Ry представляют собой C1-4алкил, и где Rz представляет собой C1-4алкил или фенил, например Rx и Ry представляют собой CH3, а Rz представляет собой C(CH3)3 или фенил, и где W2 представляет собой подходящую уходящую группу, такую как, например, галоген, например бром;
3: в присутствии подходящей кислоты, такой как, например, ТФУ, и подходящего растворителя, такого как, например, тетрагидрофуран. Данная реакция может быть также выполнена с фторидом тетрабутиламмония в присутствии подходящего растворителя, такого как, например, тетрагидрофуран.
Соединения формулы (Ib), где R3 представляет собой необязательно замещенный C2-6алкинил, где указанные соединения представлены формулой (Ib-2), могут быть получены согласно Схеме 7 реакции.
Схема 7

В Схеме 7 применены следующие условия реакции:
в присутствии подходящего основания, такого как, например, NaH, и подходящего растворителя, такого как, например, N,N-диметилформамид, и где R3e представляет собой необязательно замещенный C2-6алкинил, а W6 представляет собой подходящую уходящую группу, такую как, например, галоген, например хлор, или -O-S(=O)2-CH3. Промежуточное соединение W6-R3e, в котором W6 представляет собой -O-S(=O)2-CH3, может быть получено в реакции соответствующего спиртового производного с метансульфонилхлоридом в присутствии подходящего основания, такого как, например, триэтиламин или 4-диметиламинопиридин, и подходящего растворителя, такого как, например, дихлорметан.
Соединения формулы (Ib-2), где R3e представляет собой C2-6алкинил, который замещен гидроксилом, где указанные соединения представлены формулой (Ib-2-1), могут быть получены согласно следующей Схеме 8 реакции.
Схема 8

В Схеме 8 применены следующие условия реакции:
1: в присутствии подходящего основания, такого как, например, NaH, и подходящего растворителя, такого как, например, N,N-диметилформамид, и где Rx, Ry и Rz являются такими, как определено выше;
2: в присутствии подходящей кислоты, такой как, например, трифторуксусная кислота, и подходящего растворителя, такого как, например, тетрагидрофуран. Данная реакция может быть также выполнена с фторидом тетрабутиламмония в присутствии подходящего растворителя, такого как, например, тетрагидрофуран.
В альтернативе, вместо промежуточного соединения формулы (XVI), может также использоваться гало-C2-6алкинил-O-Si(Rx)(Ry)(Rz).
Соединения формулы (Ib-2), где R3e представляет собой C2-6алкинил, где указанные соединения представлены формулой (Ib-2-2), могут быть получены согласно следующей Схеме 9 реакции.
Схема 9
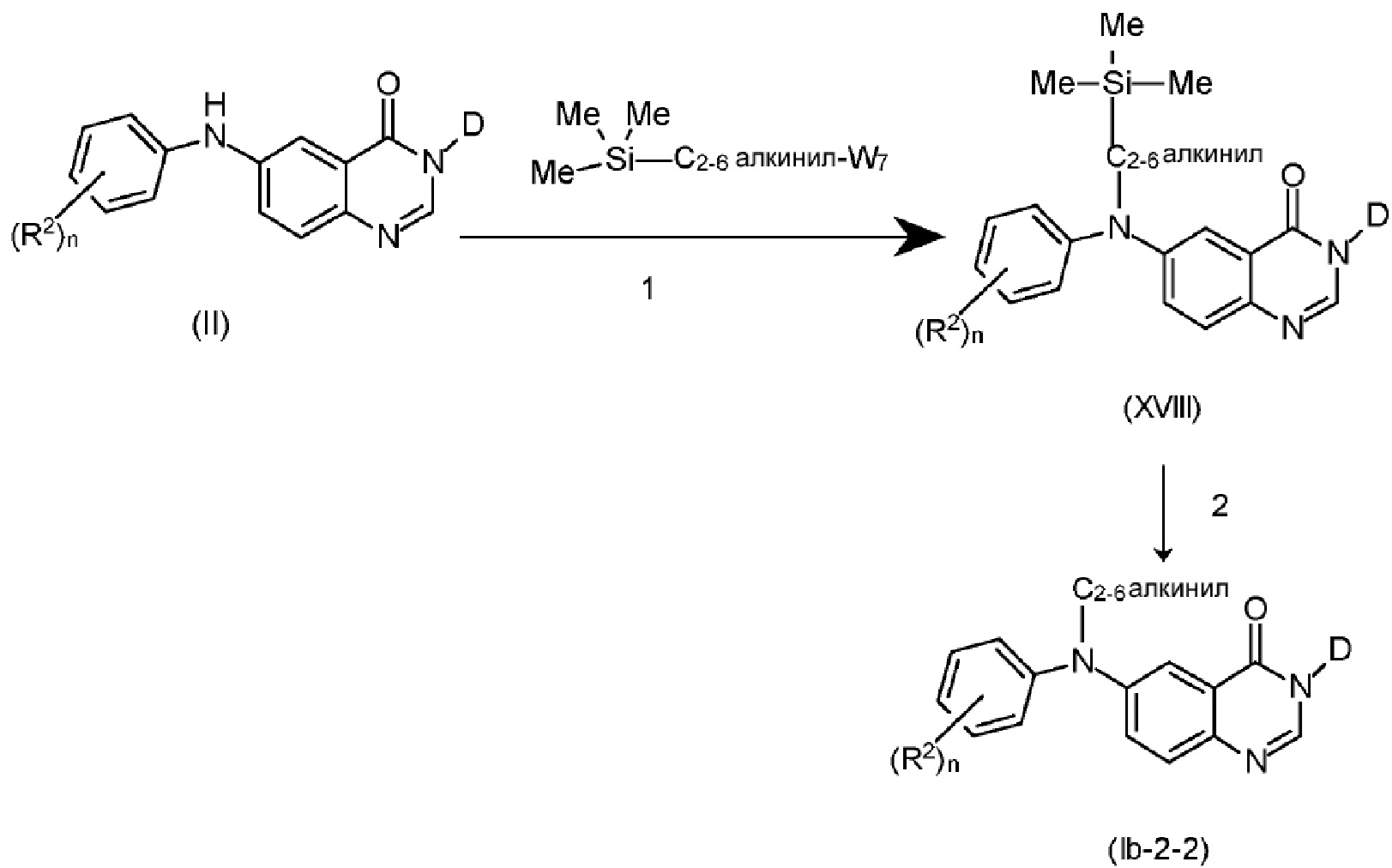
В Схеме 9 применены следующие условия реакции:
1: в присутствии подходящего основания, такого как, например, NaH, и подходящего растворителя, такого как, например, N,N-диметилформамид, и где W7 является подходящей уходящей группой, такой как, например, галоген;
2: в присутствии подходящего основания, такого как, например, K2CO3, и подходящего растворителя, такого как, например, спирт, например метанол и т.п.
Соединения формулы (Ib), где R3 представляет собой этил, который замещен -P(=O)(OC1-6алкилом)2, где указанные соединения представлены формулой (Ib-1-7), могут быть получены согласно следующей Схеме 10 реакции.
Схема 10

В Схеме 10 применены следующие условия реакции:
в присутствии подходящего катализатора, такого как, например, три-N-бутилфосфин, и подходящего растворителя, такого как, например, ацетонитрил.
Промежуточные соединения формулы (IV), в которой D являются кольцевой группой, содержащей атом азота, как представлено на Схеме 11, могут далее реагировать согласно следующей Схеме 11 реакции. На Схеме 11 R6b определен как 4-7-членный моноциклический гетероциклил, который присоединен к остальной части молекулы через атом N, и который необязательно содержит по меньшей мере один дополнительный гетероатом, выбранный из N, О или S.
Схема 11

На Схеме 11 группа D'N представляет собой группу -D, где кольцевая группа D содержит атом азота, при этом применены следующие условия реакции:
1: в реакции с W8-C1-6алкил-галогеном, где W8 представляет собой подходящую уходящую группу, такую как, например, галоген, например, например хлор, в присутствии подходящего основания, такого как, например, NaH, и подходящего растворителя, такого как, например, N,N-диметилформамид;
2: в реакции с R6b в присутствии подходящего основания, такого как, например, K2CO3, и подходящего растворителя, такого как, например, ацетонитрил;
3: в случае, когда в промежуточном соединении формулы (IV'-c) R6b несет гидроксильную группу, как в промежуточном соединении формулы (IV-c-1), то указанная гидроксильная группа может быть защищена подходящей защитной группой P, такой как, например, -O-C(=O)-C1-6алкил, в реакции с C1-6алкил-C(=O)-W9, где W9 представляет собой подходящую уходящую группу, такую как, например, галоген, например хлор, в присутствии подходящего основания, такого как, например, триэтиламин, 4-диметиламинопиридин, и подходящего растворителя, такого как, например, дихлорметан;
4: в реакции с фторидом тетрабутиламмония (TBAF) в присутствии подходящего растворителя, такого как, например, тетрагидрофуран;
5: в реакции с метансульфонилхлоридом в присутствии подходящего основания, такого как, например, триэтиламин, и подходящего растворителя, такого как, например, дихлорметан, и где Ru представляет собо -SO2CH3;
6: в реакции с промежуточным соединением формулы NHR10R11 в подходящем растворителе, таком как, например, ацетонитрил;
7: в присутствии подходящего основания, такого как, например, K2CO3, и подходящего растворителя, такого как, например, спирт, например метанол и т.п. Предполагается, что специалисту в данной области будет известно, для каких других кольцевых групп D могут также применяться описанные реакции.
Промежуточные соединения формулы (IV) и (XX) могут также реагировать с получением соединений настроящего изобретения согласно схемам реакции, как представлено на Схеме 1. Предполагается, что специалисту в данной области будет известно, при каких условиях и для каких определений R1 на кольцевой группе D может подходить защитная группа в проводимых реакциях. Например, гидроксильная группа в рамках определения R1 может быть защищена трет-бутилдиметилсилильной группой; группа NH в рамках определения R1 может быть защищена группой -C(=O)-O-C(CH3)3.
Предполагается, что специалисту в данной области будут известны подходящие реакции снятия защиты.
Соединения формулы (Ib), в которых R3 является C1-6алкилом, который замещен 3,3-диметилморфолином, может быть получен согласно Схеме 12 реакции ниже.
Схема 12

В Схеме 12 применены следующие условия реакции:
1: реакция с 2-амино-2-метил-1-пропанолом в присутствии подходящего основания, такого как, например, NaH, и в присутствии подходящего растворителя, такого как, например, N,N-диметилформамид;
2: реакция, например, с ди-трет-бутил-дикарбонатом в присутствии подходящего растворителя, такого как, например, диоксан, и подходящего основания, такого как, например, NaHCO3, и где P является подходящей защитной группой P, такой как, например, -C(=O)-O-C(CH3)3;
3: реакция с метансульфонилхлоридом в присутствии подходящего растворителя, такого как, например, дихлорметан, и подходящего основания, такого как, например, триэтиламин;
4: реакция с подходящей кислотой, такой как, например, трифторуксусная кислота, в присутствии подходящего растворителя, такого как, например, дихлорметан;
5: в присутствии подходящего основания, такого как, например, N,N-диизопропилэтиламин и триэтиламин, и подходящего растворителя, такой как, например, спирт, например метанол.
Соединения формулы (Ib), где R3 является C1-6алкилом, который замещен 5-амино-1,3,4-оксадиазолилом, могут быть получены согласно Схеме 13 реакции ниже.
Схема 13

В Схеме 13 применены следующие условия реакции:
1: в присутствии подходящего растворителя, такого как, например, спирт, например этанол;
2: в присутствии подходящего основания, такого как, например, NaHCO3, и подходящего растворителя, такого как, например, вода или диоксан, и где W10 представляет собой подходящую уходящую группу, такую как, например, галоген, например бром.
Предполагается, что специалисту в данной области будет известно, при каких условиях и на какой части молекулы может потребоваться защитная группа. Например, защитная группа на заместителе R1 или на группе D, или защитная группе на заместителе R3 или на заместителе R2, или их комбинации. Специалист, как предполагают, также сумеет подобрать наиболее подоходящую защитную группу, такой как, например, -C(=O)-O-C1-4алкил или

Специалисту, как предполагают, также будет известно, что в тех случаях, когда R1 представляет собой C(=O)-морфолинил, указанный R1 может быть получен из -C(=O)-NH-CH2-CH2-O-CH2-CH2-O-SO2-4-метилфенила, в присутствии гидрида натрия и подходящего растворителя, такого как, например, N,N-диметилформамид. Или что в тех случаях, когда R1 представляет собой -NH-C(=O)-морфолинил, указанный R1 может быть получен из -NH-C(=O)-O-C(CH3)3 в присутствии морфолина, и подходящего растворителя, такого как, например, 1-метил-2-пирролидинон. Или что в тех случаях, когда R1 представляет собой гидроксиC1-6алкил, например, -CH2-CH2-OH, указанный R1 может быть получен из соответствующего промежуточного алкоксикарбонильного соединения, например, -СН2-С(=O)-O-СН2-СН3, в присутствии 1M Dibal-H в гексане и подходящем растворителе, таком как, например, тетрагидрофуран.
Настоящее изобретение также включает дейтерированные соединения. Указанные дейтерированные соединения могут быть получены при использовании подходящих дейтерированных промежуточных соединений в процессе синтеза. Например, представленное ниже промежуточное соединение


Соединения формулы (I) могут также быть превращены друг в друга посредством известных в уровне техники реакций или превращений функциональных групп.
Например, соединения формулы (I), в которых R1 представляет собой тетрагидропиранил, могут быть превращены в соединение формулы (I), в котором R1 представляет собой водород, в реакции с подходящей кислотой, такой как, например, HCl или трифторуксусная кислота, в присутствии подходящего растворителя, такого как, например, дихлорметан, диоксан, или спирта, например метанола, изопропанола и т.п.
Соединения формулы (I), в которых R1 или R3 представляют собой моногалоалкил, могут быть превращены в соединение формулы (I), в котором R1 или R3 представляют собой C1-6алкил, который замещен кольцевой группой, как определено выше, и связанный с C1-6алкильной группой через атом азота, в реакции с подходящей кольцевой группой, необязательно в присутствии подходящего основания, такого как, например, триэтиламин или K2CO3, или гидрид натрия, и, необязательно, в присутствии подходящего растворителя, такого как, например, ацетонитрил, N,N-диметилформамид или 1-метил-2-пирролидинон.
Соединения формулы (I), в которых R1 или R3 представляют собой C1-6алкил-OH, могут быть превращены в соединение формулы (I), в котором R1 или R3 представляют собой C1-6алкил-F, в реакции с трифторидом диэтиламиносеры в присутствии подходящего растворителя, такого как, например, дихлорметан, и в присутствии каталитического количества спирта, такого как, например, этанол. Аналогичным образом, соединение формулы (I), в котором R1 или R3 представляют собой C1-6алкил, который замещен R6 или R9, где указанный R6 или R9 замещены OH, может быть превращено в соединение формулы (I), в котором R1 или R3 представляют собой C1-6алкил, который замещен R6 или R9, где указанные R6 или R9 замещены F, в реакции трифторидом диэтиламиносеры в присутствии подходящего растворителя, такого как, например, дихлорметан.
Соединения формулы (I), в которых R1 или R3 представляют собой C1-6алкил, который замещен R6 или R9, где указанные R6 или R9 замещены -C(=O)-O-C1-6алкилом, могут быть превращены в соединение формулы (I), в котором R1 или R3 представляют собой C1-6алкил, который замещен R6 или R9, где указанные R6 или R9 замещены -CH2-OH, в реакции с подходящим восстановителем, таким как, например, LiAlH4, в присутствии подходящего растворителя, такого как, например, тетрагидрофуран.
Соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен 1,3-диоксо-2H-изоиндол-2-илом, могут быть превращены в соединение формулы (I), в котором R3 представляет собой C1-6алкил, который замещен аминогруппой, в реакции с моногидратом гидразина в присутствии подходящего растворителя, такого как, например, спирт, например этанол. Соединения формулы (I), в которых R1 или R3 представляют собой C1-6алкил, который замещен аминогруппой, могут быть превращены в соединение формулы (I), в котором R1 или R3 представляют собой C1-6алкил, который замещен -NH-S(=O)2-C1-6алкилом, в реакцией с Cl-S(=O)2-C1-6алкилом в присутствии подходящего основания, такого как, например, триэтиламин, и подходящего растворителя, такого как, например, дихлорметан.
Соединения формулы (I), в которых R1 или R3 представляют собой C1-6алкил, который замещен галогеном, могут быть превращены в соединение формулы (I), в котором R1 или R3 представляют собой C1-6алкил, который замещен NR4R5 или NR10R11, в реакции с NHR4R5 или NHR10R11 или использовании такого амина в большом избытке или в присутствии подходящего основания, такого как, например, K2CO3, и подходящего растворителя, такого как, например, ацетонитрил, N,N-диметилацетамид или 1-метил-пирролидинон.
Соединения формулы (I), в которых R1 представляет собой водород, могут быть превращены в соединение формулы (I), в котором R1 представляет собой полигалоC1-6алкил или полигидроксиC1-6алкил, или C1-6алкил, или -S(=O)2-NR14R15, или -S(=O)2-C1-6алкил, в реакции с полигалоC1-6алкил-W или полигидроксиC1-6алкил-W, или C1-6алкил-W, или W-S(=O)2-NR14R15, или W-S(=O)2-C1-6алкилом, где W представляет собой подходящую уходящую группу, такую как, например, галоген, например, бром и т.п., в присутствии подходящего основания, такого как, например, гидрид натрия или K2CO3, или триэтиламин, или 4-диметиламино-пиридин, или диизопропиламин, и подходящего растворителя, такого как, например, N,N-диметилформамид или ацетонитрил, или дихлорметан. Соединения формулы (I), в которых R1 представляет собой водород, могут быть также превращены в соединение формулы (I), в котором R1 представляет собой C1-6алкил-OH, в реакции с W-C1-6алкил-O-Si(CH3)2(C(CH3)3) в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, такого как, например, N,N-диметилформамид. Специалисту будет очевидно, что эта стадия сопровождается реакцией с подходящей кислотой, такой как, например, трифторуксусная кислота, в подходящем растворителе, таком как, например, тетрагидрофуран, или реакцией с фторидом тетрабутиламмония в присутствии подходящего растворителя, такого как, например, тетрагидрофуран.
Соединения формулы (I), в которых R1 представляет собой водород, могут быть также превращены в соединение формулы (I), в котором R1 представляет собой этил, замещенный -S(=O)2-C1-6алкилом, в реакции с C1-6алкил-винилсульфоном в присутствии подходящего основания, такого как, например, триэтиламин, и подходящего растворителя, такого как, например, спирт, например метанол, или в реакции с C1-6алкил-2-бромэтилсульфоном в присутствии подходящего депротонирующего агента, такого как, например, NaH, и подходящего растворителя, такого как, например, диметилформамид.
Соединения формулы (I), в которых R1 представляет собой водород, могут быть также превращены в соединение формулы (I), в котром R1 представляет собой



Соединения формулы (I), в которых R1 представляет собой C1-6алкил, который замещен R6, где указанный R6 замещен -C(=O)-O-C1-6алкилом или -S(=O)2-NR14R15, или где R3 представляет собой C1-6алкил, который замещен R9, где указанный R9 замещен -C(=O)-O-C1-6алкилом или -S(=O)2-NR14R15, могут быть превращены в соединение формулы (I), в котором R6 или R9 не замещены, в реакции с подходящей кислотой, такой как, например, HCl, и подходящим растворителем, таким как, например, диоксан, ацетонитрил или спирт, например изопропиловый спирт.
Соединения формулы (I), в которых R1 представляет собой C1-6алкил, который замещен R6, где указанный R6 является кольцевой группой, включающей атом азота, который замещен -CH2-OH, или где R3 представляет собой C1-6алкил, который замещен R9, где указанный R9 является кольцевой группой, включающей атом азота, который замещен -CH2-OH, могут быть превращены в соединение формулы (I), в котором R6 или R9 не замещены, в реакции с гидроксидом натрия в присутствии подходящего растворителя, такого как, например, тетрагидрофуран. Соединения формулы (I), в которых R1 представляет собой C1-6алкил, который замещен R6, или R3 представляет собой C1-6алкил, который замещен R9, где указанный R6 или указанный R9 не замещены, могут быть превращены в соединение формулы (I), в котором указанный R6 или указанный R9 замещен C1-6алкилом, в реакции с W-C1-6алкилом, где W является таким, как определено выше, в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, такого как, например, N,N-диметилформамид. Соединения формулы (I), в которых R1 или R3 представляют собой гидроксиC1-6алкил, могут быть превращены в соответствующее карбонильное соединение в реакции с периодинаном Десса-Мартина в присутствии подходящего растворителя, такого как, например, дихлорметан.
Соединения формулы (I), в которых R1 представляет собой C1-6алкил, который замещен R6, или R3 представляет собой C1-6алкил, который замещен R9, где указанный R6 или указанный R9 замещен C1-6алкил-галогеном, могут быть превращены в соединение формулы (I), в котором указанный R6 или указанный R9 замещен C1-6алкил-CN, в реакции с цианидом натрия в присутствии подходящего растворителя, такого как, например, вода или спирт, например этанол. Соединения формулы (I), в которых R1 представляет собой C1-6алкил, который замещен R6, где указанный R6 не замещен, или где R3 представляет собой C1-6алкил, который замещен R9, где указанный R9 не замещен, могут быть превращены в соединение формулы (I), в котором R6 или R9 замещены -CH3 или -CH(CH3)2, в реакции с формальдегидом или ацетоном и NaBH3CN в присутствии подходящего растворителя, такого как, например, тетрагидрофуран или спирт, например метанол.
Соединения формулы (I), в которых R1 содержит заместитель R6, который замещен OH, или где R3 содержит заместитель R9, который замещен OH, могут быть превращены в соединение формулы (I), в котором заместители R6 или R9 замещены C1-6алкилоксигруппой, в реакции с W-C1-6алкилом в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, такого как, например, N,N-диметилформамид. Соединения формулы (I), в которых R1 содержат заместитель R6, который замещен C1-6алкилоксигруппой, или где R3 содержит заместитель R9, который замещен C1-6алкилоксигруппой, могут быть превращены в соединение формулы (I), в котором заместители R6 или R9 замещены -OH, в реакции с подходящей кислотой, такой как, например, соляная кислота. Соединения формулы (I), в которых R1 содержит заместитель R6, который замещен галогеном, или где R3 содержит заместитель R9, который замещен галогеном, могут быть превращены в соединение формулы (I), в котором заместители R6 или R9 замещены -NR14R15, в реакции с NHR14R15 в подходящем растворителе, таком как, например, 1-метил-пирролидинон. Соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, могут быть превращены в соединение формулы (I), в котором R3 представляет собой C1-6алкил, который замещен COOH, в реакции с LiOH в присутствии подходящего растворителя, такого как, например, тетрагидрофуран. Указанные соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен COOH, могут быть превращены в соединение формулы (I), в котором R3 представляет собой C1-6алкил, который замещен -C(=O)-NH2 или -C(=O)-NHCH3 или -C(=O)NR10R11, в реакции с NH(Si(CH3)3)2 или MeNH3+Cl- или NHR10R11 в присутствии подходящих реагентов для синтеза пептидов, таких как, например, 1-(3-диметиламинопропил)-3-этилкарбодиимид HCl и 1-гидроксибензотриазол, подходящего основания, такого как, например, триэтиламин, и подходящего растворителя, такого как, например, дихлорметан или N,N-диметилформамид.
Соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен -C(=O)-O-C1-6алкилом, могут быть также превращены в соединение формулы (I), в котором R3 представляет собой C1-6алкил, который замещен 4,5-дигидро-имидазол-2-илом, в реакции под N2 с этилендиамином и триметилалюминием в присутствии подходящего растворителя, такого как, например, толуол и гептан. Соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен COOH, могут быть также превращены в соединение формулы (I), в котором R3 представляет собой C1-6алкил, который замещен -C(=O)-N(CH3)(OCH3), в реакции с диметилгидроксиламином в присутствии карбонилдиимидазола и подходящего растворителя, такого как, например, дихлорметан.
Соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен


Соединения формулы (I), в которых R3 представляет собой C1-3алкил, который замещен -C(=O)-O-C1-6алкилом, могут быть превращены в соединение формулы (I), в котором R3 представляет собой C1-3алкил, который замещен -C(CH3)2-OH, в реакции с иодметаном и порошком Mg в присутствии подходящего растворителя, такого как, например, диэтиловый эфир или тетрагидрофуран. Соединения формулы (I), в которых R3 представляет собой C1-5алкил, который замещен -C(=O)-O-C1-6алкилом, могут быть превращены в соединение формулы (I), в котором R3 представляет C1-6алкил, который замещен -OH, в реакции с подходящим восстановителем, таким как, например, LiAlH4, в подходящем растворителе, таком как, например, тетрагидрофуран.
Соединения формулы (I), в которых R3 представляет собой C1-5алкил, который замещен -OH, могут быть превращены в соединение формулы (I), в котором R3 представляет собой C1-5алкил, который замещен -O-C(=O)-C1-6алкилом, в реакции с Cl-C(=O)-C1-6алкилом в присутствии подходящего основания, такого как, например, NaH, и подходящего растворителя, такого как, например, тетрагидрофуран.
Соединения формулы (I), в которых R3 представляет собой -CH2-CH=CH2, могут быть превращены в соединение формулы (I), в котором R3 представляет собой -CH2-CHOH-CH2-OH, в реакции с пермарнганатом калия и подходящим растворителем, таким как, например, ацетон или вода. Соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен -C(=O)-C1-4алкилом, могут быть превращены в соединение формулы (I), в котором R3 представляет собой C1-6алкил, который замещен -C(C1-4алкил)=N-OH, в реакции с гидроксиламином в присутствии подходящего основания, такого как, например, пиридин, и подходящего растворителя, такого как, например, спирт, например этанол.
Соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен NH2, могут быть превращены в соединение формулы (I), в котором R3 представляет собой C1-6алкил, который замещен -NH-C(=O)-R6 или -NH-C(=O)-C1-6алкилом, или -NH-C(=O)-полигидроксиC1-6алкилом, или -NH-C(=O)-полигалоC1-6алкилом, или -NH-C(=O)-полигидроксиполигалоC1-6алкилом, в реакции с соответствующим COOH аналогом, например, R6-COOH или CF3-C(CH3)(OH)-COOH и т.п., в присутствии подходящих реагентов для синтеза пептидов, таких как 1-гидрокси-бензотриазол и 1-(3-диметиламино)пропил)карбодиимид, необязательно в присутствии подходящего основания, такого как, например, триэтиламин. Указанные соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен NH2, могут быть также превращены в соединение формулы (I), в котором R3 представляет собой C1-6алкил, который замещен NH-C(=O)-CF3, в реакции с трифторуксусным ангидридом в присутствии подходящего основания, такого как, например, триэтиламин, и подходящего растворителя, такого как, например, тетрагидрофуран. Указанные соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен NH2, могут быть также превращены в соединение формулы (I), в котором R3 представляет собой C1-6алкил, который замещен -NH-полигалоC1-6алкилом, например -NH-CH2-CH2-F, в реакции с полигалоC1-6алкил-W, где W определен выше, например, иод-2-фторэтаном, в присутствии подходящего основания, такого как, например, K2CO3, и подходящего растворителя, такого как, например, N,N-диметилформамид или диоксан.
Соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен цианогруппой, могут быть превращены в соединение формулы (I), в котором R3 представляет собой C1-6алкил, который замещен тетразолилом, в реакции с азидом натрия и NH4+Cl- в присутствии подходящего растворителя, такого как, например, N,N-диметилформамид.
Соединения формулы (I), в которых R3 представляет собой -CH2-C≡CH, могут быть превращены в соединение формулы (I), в котором R3 представляет собой

Соединения формулы (I), в которых R3 представляет собой -CH2-C≡CH, могут быть превращены в соединение формулы (I), в котором R3 представляет собой

Соединения формулы (I), в которых R3 представляет собой C2-6алкинил, могут быть превращены в соединение формулы (I), в котором R3 представляет собой C2-6алкинил, который замещен R9, в реакции с W-R9, где W является таким, как определено выше, в присутствии подходящего катализатора, такого как, например, дихлорбис(трифенилфосфин)палладий, подходящего сокатализатора, такого как CuI, подходящего основания, такого как, например, триэтиламин, и подходящего растворителя, такого как, например, диметилсульфоксид.
Соединения формулы (I), в которых R3 включает R9, который замещен галогеном, могут быть превращены в соединение формулы (I), в котором R3 включает R9, который замещен -NR14R15, в реакции с NHR14R15 в присутствии подходящего растворителя, такого как, например, 1-метил-2-пирролидинон.
Соединения формулы (I), в которых R3 включает C2-6алкинил, могут быть гидрированы с получением соединения формулы (I), в котором R3 включает C2-6алкил, в присутствии подходящего катализатора, такого как, например, палладий на активированном угле, и подходящего растворителя, такого как, например, этилацетат.
Соединения формулы (I), в которых R3 включает C2-6алкинил, могут быть гидрированы с получением соединения формулы (I), в котором R3 включает C2-6алкенил, в присутствии подходящего катализатора, такого как, например, катализатор Линдлара, и подходящего растворителя, такого как, например, этилацетат.
Соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен -P (=O)(OC1-6алкилом)2, могут быть превращены в соединение формулы (I), в котором R3 представляет собой C1-6алкил, который замещен -P(=O)(ОH)2, в реакции с бромтриметилсиланом в присутствии подходящего растворителя, такого как, например, дихлорметан.
Соединения формулы (I), в которых заместитель R9 замещен =O, могут быть превращены в соответствующий восстановленный заместитель R9 в реакции с подходящим восстановителем, таким как, например, NaBH4, в подходящем растворителе, таком как, например, тетрагидрофуран.
Соединения формулы (I), в которых R3 включает -NHR10, могут быть превращены в соединение формулы (I), в котором R3 включает -NR10-(C=O)-необязательно замещенный C1-6алкил, реакцией с соответствующим W-(C=O)-необязательно замещенным C1-6алкилом, где W представляет собой подходящую уходящую группу, такую как, например, галоген, например хлор и т.п., в присутствии подходящего основания, такого как, например, триэтиламин, и подходящего растворителя, такого как, например, ацетонитрил.
Соединения формулы (I), в которых R3 представляет собой C1-6алкил, который замещен NR10(бензилом), могут быть превращены в соединение формулы (I), в котором R3 представляет собой C1-6алкил, который замещен NHR10, в реакции с 1-хлорэтилхлорформиатом в присутствии подходящего растворителя, такого как, например, дихлорметан.
Соединения формулы (I), в которых R1 представляет собой незамещенный пиперидин, могут быть превращены в соединение формулы (I), в котором R1 представляет собой 1-метил-пиперидин, в реакции с иодметаном в присутствии подходящего основания, такого как, например, карбонат калия, и подходящего растворителя, такого как, например, ацетонитрил. Соединения формулы (I), в которых R1 представляет собой водород, могут быть превращены в соединение формулы (I), в котором R1 представляет собой необязательно замещенный C1-6алкил, в реакции с необязательно замещенным C1-6алкил-W, где W представляет собой подходящую уходящую группу, такую как, например, галоген, например бром и т.п., в присутствии подходящего основания, такого как, например, карбонат калия, и подходящего растворителя, такого как, например, ацетонитрил.
Соединения формулы (I), в которых R2 представляет собой галоген, например бром, могут быть превращены в соединение формулы (I), в котором R2 представляет собой цианогруппу, в реакции с цианидом цинка в присутствии подходящего катализатора, такого как, например, Pd2(dba)3, и подходящего лиганда, такого как, например, 1,1-бис(дифенилфосфино)ферроцен, в присутствии подходящего растворителя, такого как, например, N,N-диметилформамид. Указанный заместитель R2, являющийся цианогруппой, может быть превращен в -CH2-NH2 путем гидрирования в присутствии NH3 и никеля.
Соединения формулы (I), в которых R2 представляет собой -OCH3, могут быть превращены в соединения формулы (I), в которых R2 представляет собой -OH, в реакции с трибромидом бора в присутствии подходящего растворителя, такого как, например, дихлорметан. Соединения формулы (I), в которых R2 представляет собой -OH, могут быть превращены в соединения формулы (I), в которых R2 представляет собой -OCH3, в реакции с метилиодидом в присутствии подходящего основания, такого как, например, карбонат калия, и подходящего растворителя, такого как, например, N,N-диметилформамид.
Соединения формулы (I), в которых R2 представляет собой водород, могут быть превращены в соединение формулы (I), в котором R2 представляет собой -CHOH-CF3, в реакции с метил-полукеталем трифторацетальдегида.
Предполагается, что специалисту будут известны вышеуказанные реакции превращения, также применимые к заместителю R3a.
Другим аспектом изобретения является способ получения соединения формулы (I), как определено в настоящем описании, включающий: (i) реакцию промежуточного соединения формулы

(a) W1-R3d в присутствии подходящего основания, такого как, например, гидрид натрия или Cs2CO3, и подходящего растворителя, такого как, например, N,N-диметилформамид, N,N-диметилацетамид, тетрагидрофуран или ацетонитрил, и где W1 представляет собой подходящую уходящую группу, такую как, например, галоген, например бром, хлор и т.п., или -O-S(=O)2-CH3, а R3d представляет собой необязательно замещенный C1-6алкил, такой как, например, -CH2-C3H5; или
(b)

(c) W1-C1-6алкил-NHR10 в присутствии подходящего реагента фазового переноса, такого как, например, бромид тетрабутиламмония, подходящего основания, такого как, например, гидроксид калия, и подходящего растворителя, такого как, например, 2-метилтетрагидрофуран и вода;
(d) W1-C1-6алкил-N циклом в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, такого как, например, N,N-диметилформамид или N,N-диметилацетамид;
(ii) снятие защиты с промежуточного соединения формулы

(iii) реакцию промежуточного соединения формулы

(iv) реакцию промежуточного соединения формулы

(a) NHR10R11, необязательно в присутствии подходящего основания, такого как, например, триэтиламин, K2CO3, Na2CO3 или гидрид натрия, и, необязательно, подходящего растворителя, такого как, например, ацетонитрил, тетрагидрофуран, диоксан, N,N-диметилформамид или 1-метил-пирролидинон. Данный тип реакции может быть также выполнен с подходящей солью NHR10R11, например, HCl солью NHR10R11, или может быть выполнен в присутствии иодида калия. Таким способом могут быть получены соединения, в которых R3 представляет собой иодC1-6алкил; или
(b)

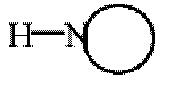
(c) NHR10P в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, такого как, например, диметилацетамид, и где P представляет собой подходящую защитную группу, такую как, например, -C(=O)-O-C(CH3)3, с последующей подходящей реакцией снятия защиты;
(v) реакцию промежуточного соединения формулы

(vi) реакцию промежуточного соединения формулы
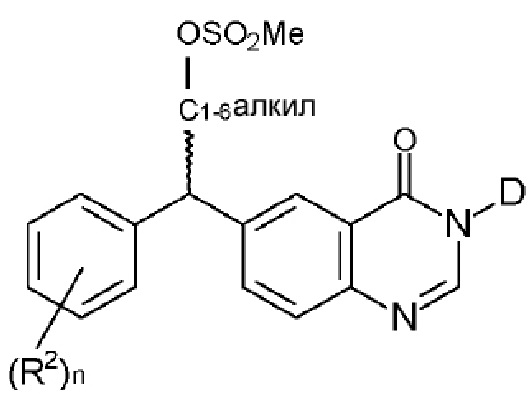
(a) NHR10R11, необязательно в присутствии подходящего основания, такого как, например, триэтиламин, карбонат калия, карбонат натрия или гидрид натрия, и, необязательно, подходящего растворителя, такого как, например, ацетонитрил, тетрагидрофуран, N,N-диметилформамид; или
(b)


(c) NHR10P: в присутствии подходящего основания, такого как, например, гидрид натрия, и подходящего растворителя, такого как, например, диметилацетамид, и где P представляет собой подходящую защитную группу, такую как, например, -C(=O)-O-C(CH3)3, с последующей подходящей реакцией снятия защиты;
(vii) снятие защиты с промежуточного соединения формулы

(viii) реакцию промежуточного соединения формулы (XIII), где Ra определен как -CO2Et, где указанные промежуточные соединения представлены формулой (XIII-a)
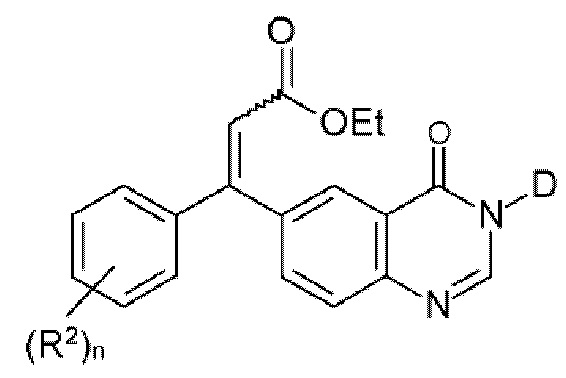
(ix) реакцию промежуточного соединения формулы
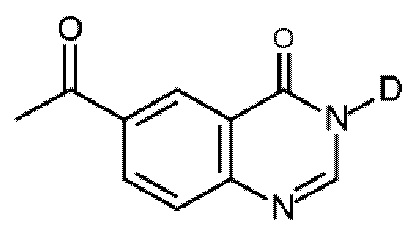
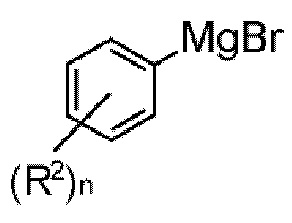
(x) снятие защиты с промежуточного соединения формулы

(xi) реакцию промежуточного соединения формулы

(xii) реакцию промежуточного соединения формулы

(xiii) реакцию промежуточного соединения формулы

(xiv) реакцию промежуточного соединения формулы

(xv) снятие защиты с промежуточного соединения формулы

(xvi) реакцию промежуточного соединения формулы

(xvii) реакцию промежуточного соединения формулы

где переменные являются такими, как определено в настоящем описании; и, необязательно, с последующим превращением одного соединения формулы (I) в другое соединение формулы (I).
Другим вариантом осуществления является способ синтеза соединения формулы (II), где:

промежуточное соединение формулы (VIII) реагирует с

Фармацевтическиприемлемые соли, сольваты или производные соединений
В данном разделе, как и во всех других разделах настоящей заявки, если из контекста не следует иное, ссылки на формулу (I) включают ссылки на все другие подгруппы, предпочтения, варианты осуществления и примеры, как определено в настоящем описании.
Если не указано иное, отсылка к конкретному соединению также включает ионные формы, соли, сольваты, изомеры, таутомеры, N-оксиды, сложные эфиры, пролекарства, изотопы и защищенные формы соединения, например, как описано ниже; предпочтительно ионные формы, или соли, или таутомеры, или изомеры, или N-оксиды, или сольваты соединения; и более предпочтительно ионные формы или соли, или таутомеры, или сольваты, или защищенные формы соединения, еще более предпочтительно соли или таутомеры или сольваты соединения. Многие соединения формулы (I) могут существовать в виде солей, например, кислотно-аддитивных солей, или, в некоторых случаях, в виде солей органических или неорганических оснований, таких как карбоксилатные, сульфонатные и фосфатные соли. Все такие соли включены в объем настоящего изобретения, и ссылки на соединения формулы (I) включают солевые формы соединений. Следует принять во внимание, что ссылки на "производные" включают ссылки на ионные формы, соли, сольваты, изомеры, таутомеры, N-оксиды, сложные эфиры, пролекарства, изотопы и защищенные формы соединений.
Согласно одному аспекту изобретения предложено соединение, как определено в описании, или его соль, таутомер, N-оксид или сольват. Согласно другому аспекту изобретения предложено соединение, как определено в описании, или его соль или сольват. Ссылки на соединения формулы (I) и их подгруппы, как определено в описании, включают в свой объем соли или сольваты, или таутомеры, или N-оксиды соединений.
Соединения в форме солей согласно настоящему изобретению обычно являются фармацевтически приемлемыми солями, при этом примеры фармацевтически приемлемых солей обсуждаются в публикации Berge et al. (1977) "Pharmaceutically Acceptable Salts", J. Pharm. Sci., Vol. 66, pp. 1-19. Однако соли, которые не являются фармацевтически приемлемыми солями, также могут быть получены в форме промежуточных соединений, которые затем могут быть превращены в фармацевтически приемлемые соли. Такие, не являющиеся фармацевтически приемлемыми, солевые формы, которые могут оказаться пригодными, например, при очистке или разделении соединений согласно изобретению, также составляют часть изобретения.
Соли согласно настоящему изобретению могут быть синтезированы из исходного соединения, которое содержит основную или кислотную группу, с помощью стандартных химических способов, таких как способы, описанные в PharmaceuticalSalts:Properties,Selection,andUse, P. Heinrich Stahl (Editor), Camille G. Wermuth (Editor), ISBN: 3-90639-026-8, Hardcover, 388 pages, August 2002. Как правило, такие соли могут быть получены при взаимодействии указанных соединений в форме свободной кислоты или основания с соответствующим основанием или кислотой в воде или в органическом растворителе, или в их смеси; обычно используют неводные среды, такие как эфир, этилацетат, этанол, изопропанол или ацетонитрил. Соединения согласно изобретению могут существовать в виде моно- или ди-солей в зависимости от pKa кислоты, из которой образуется соль.
Соли присоединения кислот могут быть образованы с использованием целого ряда кислот, как неорганических, так и органических. Примеры кислотно-аддитивных солей включают соли, образованные с кислотой, выбранной из группы, состоящей из уксусной, 2,2-дихлоруксусной, адипиновой, альгиновой, аскорбиновой (например, L-аскорбиновой), L-аспарагиновой, бензолсульфоновой, бензойной, 4-ацетамидобензойной, бутановой, (+)камфорной, камфорсульфоновой, (+)-(1S)-камфор-10-сульфоновой, каприновой, капроновой, каприловой, коричной, лимонной, цикламовой, додецилсерной, этан-1,2-дисульфоновой, этансульфоновой, 2-гидроксиэтансульфоновой, муравьиной, фумаровой, галактаровой, гентизиновой, глюкогептоновой, D-глюконовой, глюкуроновой (например, D-глюкуроновой), глутаминовой (например, L-глутаминовой), α-оксоглутаровой, гликолевой, гиппуровой, бромистоводородной, хлористоводородной, иодистоводородной, изетионовой, молочной (например, (+)-L-молочной, (±)-DL-молочной), лактобионовой, малеиновой, яблочной, (-)-L-яблочной, малоновой, (±)-DL-миндальной, метансульфоновой, нафталинсульфоновой (например, нафталин-2-сульфоновой), нафталин-1,5-дисульфоновой, 1-гидрокси-2-нафтойной, никотиновой, азотной, олеиновой, оротовой, щавелевой, пальмитиновой, памовой, фосфорной, пропионовой, L-пироглутаминовой, пировиноградной, салициловой, 4-аминосалициловой, себациновой, стеариновой, янтарной, серной, танниновой, (+)-L-винной, тиоциановой, толуолсульфоновой (например, п-толуолсульфоновой), ундециленовой и валериановой кислот, а также ацилированных аминокислот и катионообменных смол.
Одна отдельная группа солей состоит из солей, образованных из уксусной, хлористоводородной, иодистоводородной, фосфорной, азотной, серной, лимонной, молочной, янтарной, малеиновой, яблочной, изетионовой, фумаровой, бензолсульфоновой, толуолсульфоновой, метансульфоновой (мезилат), этансульфоновой, нафталинсульфоновой, валериановой, уксусной, пропановой, бутановой, малоновой, глюкуроновой и лактобионовой кислот. Другая группа кислотно-аддитивных солей включает соли, образованные из уксусной, адипиновой, аскорбиновой, аспарагиновой, лимонной, DL-молочной, фумаровой, глюконовой, глюкуроновой, гиппуровой, хлористоводородной, глутаминовой, DL-яблочной, метансульфоновой, себациновой, стеариновой, янтарной и винной кислот.
Если соединение является анионным или имеет функциональную группу, которая может быть анионной (например, -COOH может быть -COO-), тогда соль может быть образована с подходящим катионом. Примеры подходящих неорганических катионов включают, без ограничения, ионы щелочных металлов, такие как Na+ и K+, катионы щелочноземельных металлов, такие как Ca2+ и Мg2+, и другие катионы, такие как Al3+. Примеры подходящих органических катионов включают, без ограничения, ион аммония (т.e. NH4+) и ионы замещенного аммония (например, NH3R+, NH2R2+, NHR3+, NR4+).
Примерами некоторых подходящих ионов замещенного аммония являются такие ионы, которые получены из этиламина, диэтиламина, дициклогексиламина, триэтиламина, бутиламина, этилендиамина, этаноламина, диэтаноламина, пиперазина, бензиламина, фенилбензиламина, холина, меглумина и трометамина, а также аминокислот, таких как лизин и аргинин. Примером обычного иона четвертичного аммония является N(CH3)4+.
В случаях, когда соединения формулы (I) содержат функциональную аминогруппу, такие соединения могут образовывать соли четвертичного аммония, например, в результате реакции с алкилирующим агентом, согласно способам, хорошо известным специалистам. Такие соединения четвертичного аммония включены в объем формулы (I). Соединения формулы (I), содержащие функциональную аминогруппу, также могут образовывать N-оксиды. Ссылка в описании на соединение формулы (I), которое содержит функциональную аминогруппу, также включает N-оксид. В случае, когда соединение содержит несколько функциональных аминогрупп, один или более одного атомов азота могут быть окислены с образованием N-оксида. Конкретными примерами N-оксидов являются N-оксиды третичного амина или атома азота азотсодержащего гетероцикла. N-оксиды могут быть образованы при обработке соответствующего амина окислителем, таким как пероксид водорода или перкислота (например, пероксикарбоновая кислота), см., например, AdvancedOrganicChemistry, Jerry March, 4th Edition, Wiley Interscience, pages. Более конкретно, N-оксиды могут быть получены способом, описанным L.W. Deady (Syn.Comm. (1977), 7, 509-514), в котором аминосоединение подвергают взаимодействию с м-хлорпероксибензойной кислотой (МХПБК), например, в инертном растворителе, таком как дихлорметан.
Соединения согласно изобретению могут образовывать сольваты, например, с водой (т.e. гидраты) или с обычными органическими растворителями. При использовании в настоящем описании, термин "сольват" означает физическую ассоциацию соединений согласно настоящему изобретению с одной или более молекулами растворителя. Указанная физическая ассоциация включает различные степени ионного и ковалентного связывания, включая водородное связывание. В некоторых случаях сольват можно будет выделять, например, когда одна или более молекул растворителя включены в кристаллическую решетку твердого кристаллического вещества. Термин "сольват" охватывает как сольваты в фазе раствора, так и выделяемые сольваты. Неограничивающие примеры подходящих сольватов включают соединения согласно изобретению в комбинации с водой, изопропанолом, этанолом, метанолом, ДМСО, этилацетатом, уксусной кислотой или этаноламином и подобным. Соединения согласно изобретению могут производить свои биологические эффекты, когда они находятся в растворе.
Сольваты хорошо известны в фармацевтической химии. Они могут играть важную роль в способах получения вещества (например, в отношении его очистки, хранения вещества (например, его стабильности) и легкости обращения с веществом) и часто образуются как часть стадий выделения или очистки химического синтеза. Специалист в данной области сможет определить посредством стандартных и длительно используемых методик, образовался ли гидрат или другой сольват в условиях выделения или условиях очистки, применяемых для получения данного соединения. Примеры таких методик включают термогравиметрический анализ (ТГА), дифференциальную сканирующую калориметрию (ДСК), рентгеновскую кристаллографию (например, рентгеновскую кристаллографию монокристаллов или порошковую рентгеновскую дифракцию) и ЯМР твердого тела (ЯМР-ТТ, также известный как ЯМР с вращением образца под магическим углом или ЯМР-ВМУ). Такие методики представляют собой такую же часть стандартного аналитического инструментального набора опытного химика, как и ЯМР, ИК, ВЭЖХ и МС. В альтернативе, специалист в данной области может получить сольват искусственно, при использовании условий кристаллизации, которые включают количество растворителя, требуемое для конкретного сольвата. Далее описанные выше стандартные методы могут быть использованы для установления факта образования сольватов. Также формула (I) охватывает любые комплексы (например, комплексы включения или клатраты с соединениями, такими как циклодекстрины, или комплексы с металлами) соединений.
Кроме того, соединения согласно настоящему изобретению могут иметь одну или более полиморфных (кристаллических) или аморфных форм и в таком качестве должны быть включены в объем изобретения.
Соединения формулы (I) могут существовать в виде ряда различных геометрических изомерных и таутомерных форм, при этом ссылки на соединения формулы (I) включают все такие формы. Во избежание неопределенности, если соединение может существовать в одной из нескольких геометрических изомерных и таутомерных форм, и при этом только одна конкретно описана или показана, все остальные охвачены формулой (I). Другие примеры таутомерных форм включают, например, кето-, енольные и енолятные формы, как, например, в следующих таутомерных парах: кето/енол (представлены ниже), имин/енамин, амид/иминоспирт, амидин/ендиамины, нитрозо/оксим, тиокетон/ентиол и нитро/ацинитро.

В случаях, когда соединения формулы (I) содержат один или более хиральных центров и могут существовать в виде двух или более оптических изомеров, ссылки на соединения формулы (I) включают все их оптические изомерные формы (например, энантиомеры, эпимеры и диастереоизомеры), либо в виде индивидуальных оптических изомеров, либо в виде смесей (например, рацемических смесей) двух или более оптических изомеров, если из контекста не требуется иное. Оптические изомеры могут быть охарактеризованы и идентифицированы по их оптической активности (т.e. как + и - изомеры, или d и l изомеры), или они могут быть охарактеризованы на основе их абсолютной стереохимии, с использованием "R и S" номенклатуры, разработанной Каном, Ингольдом и Прелогом, см. AdvancedOrganicChemistry, Jerry March, 4th Edition, John Wiley & Sons, New York, 1992, pages 109-114, а также см. Cahn, Ingold & Prelog (1966) Angew.Chem. Int. Ed. Engl., 5, 385-415. Оптические изомеры могут быть разделены с помощью ряда методик, включающих хиральную хроматографию (хроматографию на хиральной подложке), при этом такие методики хорошо известны специалисту в данной области. В качестве альтернативы к хиральной хроматографии, оптические изомеры могут быть разделены путем образования диастереоизомерных солей с хиральными кислотами, такими как (+)-винная кислота, (-)-пироглутаминовая кислота, (-)-ди-толуоил-L-винная кислота, (+)-миндальная кислота, (-)-яблочная кислота и (-)-камфорсульфоновая кислота, разделения диастереоизомеров предпочтительной кристаллизацией, а затем диссоциации солей с получением индивидуального энантиомера свободного основания.
В случаях, когда соединения формулы (I) существуют в виде двух или более оптических изомерных форм, один энантиомер в паре энантиомеров может проявлять преимущества над другим энантиомером, например, в отношении биологической активности. Таким образом, в некоторых случаях может оказаться желательным использовать в качестве терапевтического средства только один из пары энантиомеров или только один из множества диастереоизомеров. Соответственно, в изобретении предложены композиции, содержащие соединение формулы (I), имеющее один или более хиральных центров, где по меньшей мере 55% (например, по меньшей мере 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95%) соединения формулы (I) присутствует в виде одиночного оптического изомера (например, энантиомера или диастереоизомера). В одном общем варианте осуществления 99% или более (например, по существу все) от общего количества соединения формулы (I) может присутствовать в виде одиночного оптического изомера (например, энантиомера или диастереоизомера). Если изомерная форма идентифицирована (например, S конфигурация или E изомер), это означает, что указанная изомерная форма в значительной степени свободна от изомера(ов), т.е. изомерная форма присутствует в количестве по меньшей мере 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или больше (например, по существу все) от общего количества соединения согласно изобретению.
Выше или далее, некоторые соединения включают следующую связь

Соединения согласно изобретению включают соединения с одним или более изотопными замещениями, при этом ссылка на конкретный элемент включает в себя все изотопы элемента. Например, ссылка на водород включает в себя1H,2H (D) и3H (T). Аналогично, ссылки на углерод и кислород включают в себя соответственно12C,13C и14C и16О и18О. Изотопы могут быть радиоактивными и нерадиоактивными. В одном варианте осуществления изобретения соединения не содержат радиоактивные изотопы. Такие соединения являются предпочтительными для терапевтического применения. Впрочем, в другом варианте осуществления изобретения соединение может содержать один или более радиоизотопов. Соединения, содержащие такие радиоизотопы, могут применяться в контексте диагностики.
Сложные эфиры, такие как эфиры карбоновых кислот и ацилоксиэфиры соединений формулы (I), несущих карбоксильную группу или гидроксильную группу, также охвачены формулой (I). В одном варианте осуществления изобретения формула (I) включает в себя сложные эфиры соединений формулы (I), несущих карбоксильную группу или гидроксильную группу. В другом варианте осуществления изобретения формула (I) не включает в себя сложные эфиры соединений формулы (I), несущих карбоксильную группу или гидроксильную группу. Примерами сложных эфиров являются соединения, содержащие группу -C(=O)OR, где R является сложноэфирным заместителем, например, С1-6алкильной группой, гетероциклильной группой или C5-20арильной группой, предпочтительно С1-6алкильной группой. Конкретные примеры сложноэфирных групп включают, без ограничения, -C(=O)OCH3, -C(=O)OCH2CH3, -C(=O)OC(CH3)3 и -C(=O)OPh. Примеры ацилоксигрупп (обратимых сложноэфирных групп) представлены -OC(=O)R, где R является ацилокси-заместителем, например, C1-7алкильной группой, C3-20гетероциклильной группой или C5-20арильной группой, предпочтительно C1-7алкильной группой. Конкретные примеры ацилоксигрупп включают, без ограничения, -OC(=O)CH3 (ацетокси), -OC(=O)CH2CH3, -OC(=O)C(CH3)3, -OC(=O)Ph и -OC(=O)CH2Ph.
Например, некоторые пролекарства являются сложными эфирами активного соединения (например, физиологически приемлемым метаболически лабильным сложным эфиром). Под "пролекарствами" подразумевают, например, любое соединение, которое invivo превращается в биологически активное соединение формулы (I). В процессе метаболизма сложноэфирная группа (-C(=O)OR) расщепляется с получением активного лекарственного вещества. Такие сложные эфиры могут быть образованы при этерификации, например, любой из карбоксильных групп (-C(=O)OH) в исходном соединении, с предварительной защитой, в случае необходимости, любых других реакционноспособных групп, присутствующих в исходном соединении, и последующим удалением защитной группы, при необходимости.
Примеры таких метаболически лабильных сложных эфиров включают эфиры формулы -C(=O)OR, в которой R является: C1-6алкилом (например, -Me, -Et, -nPr, -iPr, -nBu, -sBu, -iBu, -tBu); C1-6аминоалкилом [например, аминоэтилом; 2-(N,N-диэтиламино)этилом; 2-(4-морфолино)этилом); и ацилокси-C1-7алкилом [например, ацилоксиметилом; ацилоксиэтилом; пивалоилоксиметилом; ацетоксиметилом; 1-ацетоксиэтилом; 1-(1-метокси-1-метил)этилкарбонилоксиэтилом; 1-(бензоилокси)этилом; изопропоксикарбонилоксиметилом; 1-изопропоксикарбонилоксиэтилом; циклогексилкарбонилоксиметилом; 1-циклогексилкарбонилоксиэтилом; циклогексилоксикарбонилоксиметилом; 1-циклогексилоксикарбонил-оксиэтилом; (4-тетрагидропиранилокси)-карбонилоксиметилом; 1-(4-тетрагидропиранилокси)-карбонилоксиэтилом; (4-тетрагидропира-нил)карбонилоксиметилом; и 1-(4-тетрагидропиранил)-карбонилоксиэтилом]. Кроме того, некоторые пролекарства активируются энзиматически с образованием активного соединения или соединения, которое в результате дальнейшей химической реакции превращается в активное соединение (например, как в антиген-направленной терапии с использованием фермента и пролекарства (ADEPT), ген-направленной терапии с использованием фермента и пролекарства (GDEPT) и лиганд-направленной терапии с использованием фермента и пролекарства (LIDEPT) и т.д.). Например, пролекарство может быть производным сахара или другим гликозидным конъюгатом или может быть сложноэфирным производным аминокислоты.
Тирозиновая протеинкиназа (PTK)
Соединения согласно изобретению, представленные в описании, ингибируют или модулируют активность некоторых тирозинкиназ, и, следовательно, соединения будут пригодны в лечении или профилактике, в частности лечении заболеваний или состояний, опосредованных указанными тирозинкиназами, в частности FGFR.
FGFR
Семейство протеинтирозинкиназных (PTK) рецепторов фактора роста фибробластов (FGF) регулирует различные типы физиологических функций, включающих митогенез, заживление ран, дифференцировку клеток, ангиогенез и развитие. Как нормальный, так и злокачественный рост клеток, а также пролиферация находятся под воздействием изменений в локальной концентрации факторов FGF, молекул внеклеточной сигнализации, которые действуют как аутокринные, а также паракринные факторы. Аутокринная сигнализация FGF может быть особенно важной в развитии раковых опухолей, зависимых от стероидных гормонов, до гормононезависимого состояния. Факторы FGF и их рецепторы экспрессируются при повышенных уровнях в нескольких линиях тканей и клеток, при этом повышенная экспрессия, как полагают, вносит вклад в злокачественный фенотип. Кроме того, ряд онкогенов являются гомологами генов, кодирующих рецепторы факторов роста, и существует вероятность аномальной активации FGF-зависимой сигнализации при раке поджелудочной железы человека (Knights et al., Pharmacology and Therapeutics 2010 125:1 (105-117); Korc М. et al Current Cancer Drug Targets 2009 9:5 (639-651)).
Двумя типичными представителями являются кислотный фактор роста фибробластов (aFGF или FGF1) и основный фактор роста фибробластов (bFGF или FGF2), и на сегодняшний день идентифицированы по меньшей мере двадцать различных представителей семейства FGF. Клеточный ответ на факторы FGF передается через четыре типа трансмембранных протеинтирозин-киназных рецепторов факторов роста фибробластов (FGFR) с высоким сродством, обозначенных номерами от 1 до 4 (от FGFR1 до FGFR4).
Прерывание сигнального пути FGFR1 должно влиять на пролиферацию опухолевых клеток, поскольку данная киназа активируется во многих типах опухолей в добавление к пролиферирующим эндотелиальным клеткам. Повышенная экспрессия и активация FGFR1 в опухолеассоциированной сосудистой сети указывает на роль этих молекул в ангиогенезе опухоли.
Недавнее исследование продемонстрировало связь между экспрессией FGFR1 и онкогенностью в классических лобулярных карциномах (CLC). Карциномы CLC являются причиной 10-15% всех опухолей молочной железы и, как правило, недостатка экспрессии p53 и Her2 при сохранении экспрессии рецептора эстрогена. Амплификация гена 8p12-p11.2 была продемонстрирована в ~50% случаев CLC, причем было показано, что она связана с повышенной экспрессией FGFR1. Предварительные исследования с миРНК, направленными против FGFR1, или низкомолекулярным ингибитором рецептора показали, что клеточные линии, имеющие указанную амплификацию, особенно чувствительны к ингибированию данного сигнального пути. Рабдомиосаркома (RMS) является наиболее распространенной саркомой мягких тканей у детей, которая, вероятно, возникает в результате нарушения пролиферации и дифференцировки в течение миогенеза скелета. Рецептор FGFR1 сверхэкспрессирован в первичных рабдомиосаркомах и ассоциирован с гипометилированием 5'CpG-островков и нарушенной экспрессией генов AKT1, NOG и BMP4. Рецептор FGFR1 также связывали с плоскоклеточным раком легкого, колоректальным раком, глиобластомой, астроцитомой, раком предстательной железы, мелкоклеточным раком легкого, меланомой, раковыми опухолями головы и шеи, раком щитовидной железы, раком матки.
Рецептор 2 фактора роста фибробластов проявляет высокое сродство к кислотному и/или основному факторам роста фибробластов, а также к лигандам фактора роста кератиноцитов. Рецептор 2 фактора роста фибробластов также распространяет мощные остеогенные эффекты факторов FGF в процессе роста и дифференцировки остеобластов. Мутации в рецепторе 2 фактора роста фибробластов, приводящие к сложным функциональным изменениям, как было показано, вызывают аномальное окостенение черепных швов (краниосиностоз), что свидетельствует о главной роли FGFR сигнализации в костеобразовании в соединительнотканной мембране. Например, при синдроме Апера (AP), который характеризуется преждевременным окостенением черепных швов, большинство случаев связано с точечными мутациями, приводящими к приобретению новой и патологической функции в рецепторе 2 фактора роста фибробластов. Кроме того, скрининг мутаций у больных с синдромным краниосиностозом указывает на то, что повторные мутации FGFR2 служат причиной тяжелых форм синдрома Пфейфера. Конкретные мутации FGFR2 включают W290C, D321A, Y340С, C342R, C342S, C342W, N549H, K641R в FGFR2.
Несколько тяжелых нарушений в развитии скелета человека, включая синдромы Апера, Крузона, Джексона-Вейсса, Бира-Стивенсона (синдром сморщенной кожи) и Пфейфера, ассоциированы с наличием мутаций в рецепторе 2 фактора роста фибробластов. Большинство случаев, если не все, синдрома Пфейфера (PS) также вызваны de novo мутацией гена рецептора 2 фактора роста фибробластов, и недавно было показано, что мутации в рецепторе 2 фактора роста фибробластов нарушают один из критериев, обусловливающих лигандную специфичность. А именно, две мутантные сплайс-формы рецептора фактора роста фибробластов, FGFR2c и FGFR2b, приобретают способность связывать атипичные лиганды FGF и активироваться ими. Такая потеря лигандной специфичности приводит к нарушению сигнализации, и, как полагают, тяжелый фенотип указанных синдромов заболевания является результатом эктопической лиганд-зависимой активации рецептора 2 фактора роста фибробластов.
Генетические аберрации рецепторной тирозинкиназы FGFR3, такие как хромосомные транслокации или точечные мутации, приводят к эктопически экспрессируемым или нерегулируемым конститутивно активным FGFR3-рецепторам. Такие нарушения связаны с подгруппой множественных миелом и наблюдаются при карциноме мочевого пузыря, гепатоклеточной карциноме, плоскоклеточной карциноме полости рта и цервикальных карциномах. Соответственно, ингибиторы FGFR3 могут применяться в лечении множественной миеломы, карциномы мочевого пузыря и цервикальной карциномы. Экспрессия FGFR3 также повышена при раке мочевого пузыря, в частности, при инвазивном раке мочевого пузыря. Рецептор FGFR3 часто активирован при мутациях в уротелиальной карциноме (UC). Повышенную экспрессию ассоциировали с мутацией (85% опухолей с мутациями обнаружили высокий уровень экспрессии), но также 42% опухолей без обнаружимой мутации показывали сверхэкспрессию, включая многие мышечно-инвазивные опухоли. Рецептор FGFR3 также связан с раком эндометрия и щитовидной железы.
Повышенную экспрессию FGFR4 связывали с карциномами предстательной железы и щитовидной железы. Кроме того, зародышевый полиморфизм (Gly388Arg) ассоциирован с повышением частоты возникновения рака легкого, молочной железы, толстой кишки, печени (HCC) и предстательной железы. Кроме того, усеченная форма FGFR4 (включающая киназный домен), как было обнаружено, также присутствует в 40% опухолей гипофиза, но не присутствует в нормальной ткани. Повышенную экспрессию FGFR4 наблюдали в опухолях печени, толстой кишки и легкого. Рецептор FGFR4 связан с колоректальным раком и раком печени, где экспрессия его лиганда FGF19 часто повышена. Рецептор FGFR4 также связан с астроцитомами, рабдомиосаркомой.
Фиброзные состояния представляют главную медицинскую проблему, возникающую в результате аномального или избыточного отложения фиброзной ткани. Такие отложения встречаются при многих заболеваниях, включая цирроз печени, гломерулонефрит, легочный фиброз, системный фиброз, ревматоидный артрит, а также при естественном процессе заживления ран. Механизмы развития фиброза не полностью изучены, но, как полагают, он возникает в результате действий различных цитокинов (включающих фактор некроза опухоли (TNF), факторы роста фибробластов (FGF), фактор роста тромбоцитов (PDGF) и трансформирующий фактор роста бета). Фактор (TGFβ) вовлечен в пролиферацию фибробластов и отложение белков внеклеточного матрикса (включающих коллаген и фибронектин). Это приводит к изменению структуры ткани и функции и последующей патологии.
Ряд доклинических исследований продемонстрировал активацию факторов роста фибробластов в доклинических моделях фиброза легкого. Как было показано, TGFβ1 и PDGF вовлечены в процесс фиброгенеза, и в последующей опубликованной работе предполагается, что повышение факторов FGF и последующее усиление пролиферации фибробластов могут происходить в ответ на повышение TGFβ1. Потенциальный терапевтический эффект, направленный на фиброзный механизм при таких состояниях, как идиопатический легочный фиброз (IPF), предполагается на основе описанного клинического эффекта противофиброзного средства пирфенидона. Идиопатический легочный фиброз (также называемый криптогенным фиброзирующим альвеолитом) является прогрессирующим заболеванием, включающим рубцевание легкого. Постепенно альвеолярные мешочки легких замещаются фиброзной тканью, которая становится толще, что вызывает необратимую потерю способности ткани переносить кислород в кровоток. Симптомы заболевания включают одышку, хронический сухой кашель, утомляемость, боль в груди и потерю аппетита, приводящую к быстрой потере массы тела. Заболевание является крайне серьезным, с приблизительно 50% смертности после 5 лет.
В таком качестве, соединения, которые ингибируют FGFR-рецептор, будут пригодными в представлении средств для предотвращения роста опухолей или индуцирования апоптоза в опухолях, в особенности путем ингибирования ангиогенеза. Поэтому ожидается, что соединения окажутся полезными в лечении или предотвращении пролиферативных нарушений, таких как рак. В частности, опухоли с активирующими мутантными формами рецепторных тирозинкиназ или апрегуляцией рецепторных тирозинкиназ могут быть особенно чувствительными к ингибиторам. Больные с активирующими мутантными формами любой из изоформ специфических RTK, представленных в описании, могут также найти лечение ингибиторами RTK особенно благоприятным.
Фактор роста эндотелия сосудов (VEGFR)
Хронические пролиферативные заболевания часто сопровождаются сложным ангиогенезом, который может вносить вклад или поддерживать воспалительное и/или пролиферативное состояние, или приводит к деструкции ткани посредством инвазивной пролиферации кровеносных сосудов.
Ангиогенез обычно используется для описания развития новых или замены кровеносных сосудов или неоваскуляризации. Он представляет собой необходимый и физиологически нормальный процесс, при котором сосудистая система развивается в эмбрионе. Ангиогенез не происходит, как правило, в большинстве тканей взрослых в норме, за исключением участков овуляции, менструаций и заживления ран. Многие заболевания, впрочем, характеризуются постоянным и нерегулируемым ангиогенезом. Например, при артритах новые капиллярные кровеносные сосуды прорастают в сустав и разрушают хрящ. При диабете (и при многих болезнях глаз) новые сосуды заполняют желтое пятно или сетчатку или другие структуры глаза и могут вызывать слепоту. Процесс атеросклероза связывали с ангиогенезом. Рост опухоли и метастазирование, как было найдено, являются ангиогенез-зависимыми.
Распознавание участия ангиогенеза в основных заболеваниях сопровождается исследованием с целью идентификации и разработки ингибиторов ангиогенеза. Указанные ингибиторы обычно классифицируют исходя из ответа на отдельные мишени в каскаде реакций ангиогенеза, таких как активация эндотелиальных клеток под действием ангиогенного сигнала; синтез и высвобождение деструктивных ферментов; миграция эндотелиальных клеток; пролиферация эндотелиальных клеток; и образование капиллярных трубочек. Следовательно, ангиогенез протекает на многих стадиях, и предпринимаются попытки открытия и создания соединений, которые действуют путем блокирования ангиогенеза на указанных различных стадиях.
Опубликованные работы свидетельствуют о том, что ингибиторы ангиогенеза, функционирующие посредством различных механизмов, являются эффективными при таких заболеваниях, как рак и метастазирование, болезни глаз, артрит и гемангиома.
Фактор роста эндотелия сосудов (VEGF), полипептид, является митогенным в отношении эндотелиальных клеток invitro и стимулирует ангиогенные ответы invivo. Фактор VEGF также связывали с нарушенным ангиогенезом. Рецепторы VEGFR представляют собой тирозиновые протеинкиназы (PTK). PTK-киназы катализируют фосфорилирование специфических остатков тирозина в белках, участвующих в клеточной функции, и, таким образом, регулируют рост клеток, их выживание и дифференцировку.
Было идентифицировано три рецептора PTK для VEGF: VEGFR-1 (Flt-1), VEGFR-2 (Flk-1 или KDR) и VEGFR-3 (Flt-4). Указанные рецепторы вовлечены в ангиогенез и участвуют в сигнальной трансдукции. Особый интерес представляет рецептор VEGFR-2, который является трансмембранной рецепторной PTK, экспрессируемой в основном в эндотелиальных клетках. Активация VEGFR-2 посредством VEGF является критической стадией пути передачи сигнала, которая инициирует ангиогенез опухоли. Экспрессия VEGF может быть конститутивной по отношению к опухолевым клеткам и может быть также апрегулирована в ответ на некоторые стимулы. Одним таким стимулом является гипоксия, при которой экспрессия VEGF апрегулируется как в опухолевых, так и ассоциированных тканях хозяина. Лиганд VEGF активирует VEGFR-2 путем связывания с его внеклеточным VEGF связывающим сайтом. Такое связывание приводит к димеризации рецепторов VEGFR и аутофосфорилированию остатков тирозина на внутриклеточном киназном домене VEGFR-2. Киназный домен функционирует, перенося фосфат от АТФ к остаткам тирозина, представляя, таким образом, сайты связывания для сигнальных белков, активируемых ниже по каскаду после VEGFR-2, что, в конечном счете, приводит к инициации ангиогенеза.
Ингибирование сайта связывания киназного домена VEGFR-2 может блокировать фосфорилирование остатков тирозина и способствовать нарушению инициации ангиогенеза.
Ангиогенез является физиологическим процессом образования новых кровеносных сосудов, который опосредован различными цитокинами, называемыми ангиогенными факторами. Хотя возможную патофизиологическую роль ангиогенеза в солидных опухолях широко изучали в течение более чем трех десятилетий, совсем недавно было выявлено усиление ангиогенеза при хроническом лимфолейкозе (CLL) и при других злокачественных гематологических нарушениях. Повышенный уровень ангиогенеза был подтвержден различными экспериментальными методами, как в костном мозге, так и в лимфоузлах больного CLL. Хотя роль ангиогенеза в патофизиологии указанного заболевания сохраняется полностью проясненной, исходя из экспериментальных данных предположили, что несколько ангиогенных факторов играют роль в прогрессировании заболевания. Биологические маркеры ангиогенеза, как было показано, также представляют собой прогностическое значение при CLL. Из этого следует, что ингибиторы VEGFR-рецептора также могут приносить пользу больным лейкозом, таким как CLL.
Для того чтобы масса опухоли выходила за пределы критического размера, она должна развить ассоциированную сосудистую сеть. Было сделано предположение, что направленное воздействие на сосудистую сеть опухоли должно ограничить экспансию опухоли, и может оказаться пригодным в качестве терапии рака. Наблюдения за ростом опухоли показали, что небольшие массы опухолей могут сохраняться в ткани без какой-либо опухолеспецифической сосудистой сети. Остановку роста неваскуляризированных опухолей связывали с эффектами гипоксии в центре опухоли. Недавно был идентифицирован ряд проангиогенных и антиангиогенных факторов, и была изложена концепция "ангиогенного переключения", процесса, в котором нарушение нормального соотношения ангиогенных стимулов и ингибиторов в массе опухоли создает возможность автономной васкуляризации. Ангиогенное переключение, по-видимому, регулируется под действием одних и тех же генетических изменений, которые запускают злокачественную трансформацию: активацию онкогенов и потерю генов-супрессоров опухолей. Несколько факторов роста действуют как положительные регуляторы ангиогенеза. Основными из них являются фактор роста эндотелия сосудов (VEGF), основный фактор роста фибробластов (bFGF) и ангиогенин. Белки, такие как тромбоспондин (Tsp-1), ангиостатин и эндостатин, функционируют как отрицательные регуляторы ангиогенеза.
Ингибирование VEGFR2, но не VEGFR1, в значительной степени нарушает ангиогенное переключение, устойчивый ангиогенез и начальный рост опухоли в модели на мышах. На поздней стадии роста опухоли появляется фенотипическая устойчивость к блокированию VEGFR2, поскольку опухоли снова растут в процессе терапии после первоначального периода подавления роста. Такая устойчивость к блокированию VEGF вызывает реактивацию ангиогенеза опухоли, независимого от VEGF и ассоциированного с гипоксия-опосредованной индукцией других проангиогенных факторов, которые включают представителей семейства FGF. Указанные другие проангиогенные сигналы функционально причастны к реваскуляризации и к восстановлению роста опухолей в фазе эвазии, поскольку блокировка FGF уменьшает прогрессирование на фоне ингибирования VEGF.
Имеются данные о нормализации кровеносных сосудов глиобластом у больных, проходивших лечение ингибитором пан-VEGF-рецепторной тирозинкиназы, AZD2171, в фазе 2 исследования. Определение нормализации сосудов с помощью МРТ в сочетании с определением циркулирующих биомаркеров дает возможность эффективными способами оценить ответ на антиангиогенные средства.
PDGFR
Злокачественная опухоль является результатом неконтролируемой пролиферации клеток. Рост клеток контролируется посредством хрупкого баланса между стимулирующими рост и ингибирующими рост факторами. В нормальной ткани продукция и активность указанных факторов приводит к дифференцированным клеткам, растущим в контролируемых и регулируемых условиях, которые поддерживают нормальную целостность и функционирование органа. Злокачественная клетка избегает этого контроля; природный баланс нарушается (посредством различных механизмов) и становится нерегулируемым, происходит аберрантный рост клеток. Фактором роста, играющим важную роль в развитии опухоли, является фактор роста тромбоцитов (PDGF), который включает семейство пептидных факторов роста, которые передают сигнал посредством тирозинкиназных рецепторов клеточной поверхности (PDGFR) и стимулируют различные клеточные функции, включая рост, пролиферацию и дифференцировку.
Преимущества селективного ингибитора
Разработка ингибиторов FGFR киназ с профилем дифференциальной селективности дает новую возможность применения указанных направленных средств в подгруппах больных, заболевание которых обусловлено нарушением регуляции FGFR. Соединения, которые оказывают сниженное ингибиторное воздействие на дополнительные киназы, в частности VEGFR2 и PDGFR-бета, обеспечивают дифференцированный профиль побочных эффектов или токсичности и в таком качестве предоставляют возможность более эффективного лечения этих показаний. Ингибиторы VEGFR2 и PDGFR-бета ассоциируют с такими токсическими явлениями, как гипертензия или отек, соответственно. В случае ингибиторов VEGFR2, указанный гипертензивный эффект оказывается часто дозолимитирующим, может быть противопоказан в некоторых группах пациентов и требует клинического контроля.
Биологическая активность и применение в терапевтических целях
Соединения согласно изобретению, а также их подгруппы, проявляют ингибирующую или модулирующую активность в отношении рецептора фактора роста фибробластов (FGFR) и/или ингибирующую или модулирующую активность в отношении рецептора фактора роста эндотелия сосудов (VEGFR), и/или ингибирующую или модулирующую активность в отношении рецептора фактора роста тромбоцитов (PDGFR), и которые могут применяться в предотвращении или лечении заболеваний или состояний, описанных в настоящей заявке. Кроме того, соединения согласно изобретению, а также их подгруппы, могут применяться в предотвращении или лечении заболеваний или состояний, опосредуемых киназами. Ссылки на предотвращение или профилактику или лечение заболевания или состояния, такого как рак, включают в рамках их объема ослабление или уменьшение частоты заболеваемости раком.
Используемый в описании термин "модуляция", применительно к активности киназы, определяет изменение уровня биологической активности протеинкиназы. Таким образом, модуляция охватывает физиологические изменения, которые вызывают увеличение или уменьшение соответствующей протеинкиназной активности. В последнем случае модуляция может быть описана как "ингибирование". Модуляция может проявляться прямо или косвенно, и может быть опосредована любым механизмом и на любом физиологическом уровне, в том числе, например, на уровне экспрессии генов (включая, например, транскрипцию, трансляцию и/или посттрансляционную модификацию), на уровне экспрессии генов, кодирующих регуляторные элементы, которые прямо или косвенно влияют на уровни киназной активности. Таким образом, модуляция может выражаться в повышенной/подавленной экспрессии или в сверх- или недостаточной экспрессии киназы, включая амплификацию гена (т.е. множество копий гена) и/или повышенную или пониженную экспрессию под влиянием транскрипционного эффекта, а также гипер- (или гипо-) активность и (де)активацию протеинкиназы(киназ) (включая (де)активацию) под действием мутации(ий). Термины "модулированный", "модулирующий" и "модулировать" следует интерпретировать соответственным образом.
Используемый в описании термин "опосредованный", при использовании в связи с киназой (и применяемый, например, к различным физиологическим процессам, заболеваниям, статусам, состояниям, терапиям, лечениям или вмешательствам), предназначен для ограничительного использования в силу того, что различные процессы, заболевания, симптомы, состояния, лечения и вмешательства, к которым термин применяется, являются такими, в которых киназа играет биологическую роль. В случаях, когда термин применяют к заболеванию, симптому или состоянию, биологическая роль, которую играет киназа, может быть прямой или косвенной и может быть необходимой и/или достаточной для проявления симптомов заболевания или состояния (или его этиологии или развития). Таким образом, активность киназы (и в частности аберрантные уровни активности киназы, например, сверхэкспрессия киназы) необязательно должна быть ближайшей причиной заболевания или состояния: скорее ожидается, что опосредованные киназой заболевания, симптомы или состояния включают такие, которые имеют многофакторные этиологии и сложное развитие, в которых рассматриваемая киназа участвует только частично. В случаях, когда термин применяют к лечению, профилактике или вмешательству, роль, которую киназа играет, может быть прямой или косвенной и может быть необходимой и/или достаточной для проведения лечения, профилактики или исхода вмешательства. Таким образом, заболевание или состояние, опосредованное киназой, включает развитие устойчивости к любому конкретному лекарственному средству или лечению рака.
Таким образом, например, соединения согласно изобретению могут применяться в ослаблении или уменьшении частоты заболеваемости раком.
Более конкретно, соединения формул (I) и их подгрупп являются ингибиторами FGFR-рецепторов. Например, соединения согласно изобретению проявляют активность против FGFR1, FGFR2, FGFR3 и/или FGFR4 и, в частности, против FGFR, выбранных из FGFR1, FGFR2 и FGFR3; или, в частности, соединения формулы (I) и их подгрупп являются ингибиторами FGFR4.
Предпочтительными соединениями являются соединения, которые ингибируют один или более рецепторов FGFR, выбранных из FGFR1, FGFR2, FGFR3 и FGFR4. Предпочтительными соединениями согласно изобретению являются соединения, которые имеют значения IC50 менее 0,1 мкΜ.
Соединения согласно изобретению также проявляют активность против VEGFR.
Кроме того, многие из соединений согласно изобретению проявляют селективность по отношению к FGFR 1, 2 и/или 3, и/или 4, по сравнению с VEGFR (в частности VEGFR2) и/или PDGFR, и такие соединения представляют собой один предпочтительный вариант осуществления изобретения. В частности, соединения проявляют селективность в отношении VEGFR2. Например, многие соединения согласно изобретению имеют значения IC50 против FGFR1, 2 и/или 3 и/или 4, которые составляют диапазон между десятой и сотой от IC50 против VEGFR (в частности, VEGFR2) и/или PDGFR B. В частности, предпочтительные соединения согласно изобретению имеют по меньшей мере в 10 раз более высокую активность против FGFR или ингибирование FGFR, в частности FGFR1, FGFR2, FGFR3 и/или FGFR4, чем VEGFR2. Более предпочтительно, соединения согласно изобретению имеют, по меньшей мере, в 100 раз более высокую активность против FGFR или ингибирование FGFR, в частности FGFR1, FGFR2, FGFR3 и/или FGFR4, чем VEGFR2. Это можно определить, используя методы, представленные в описании.
Как результат их активности в модулировании или ингибировании киназ FGFR и/или VEGFR, соединения могут применяться в предоставлении средств предотвращения роста или индукции апоптоза неоплазий, в особенности путем ингибирования ангиогенеза. Таким образом, следует ожидать, что соединения окажутся полезными в лечении или предотвращении пролиферативных нарушений, таких как рак. Кроме того, соединения согласно изобретению могут быть пригодными в лечении заболеваний, при которых имеется нарушение пролиферации, апоптоза или дифференцировки.
В частности, опухоли с активирующими мутациями VEGFR или положительной регуляцией VEGFR и пациенты с повышенными уровнями лактатдегидрогеназы в сыворотке могут быть особенно чувствительными к соединениям согласно изобретению. Пациенты с активирующими мутациями любой из изоформ специфических RTK, представленных в описании, также могут проходить лечение соединениями согласно изобретению особенно благоприятно. Например, сверхэкспрессия VEGFR в лейкозных клетках при остром лейкозе, когда клон клеток-предшественников может экспрессировать VEGFR. Кроме того, отдельные опухоли с активирующими мутациями или положительной регуляцией или сверхэкспрессией любой из изоформ FGFR-рецептора, такой как FGFR1, FGFR2 или FGFR3 или FGFR4, могут быть особенно чувствительными к соединениям согласно изобретению, и, таким образом, пациенты, как описано в настоящей заявке, с такими конкретными опухолями также могут проходить лечение соединениями согласно изобретению как особенно благоприятное. Может оказаться предпочтительным, что лечение связано с или направлено на мутантную форму одной из рецепторных протеинкиназ, таких как обсуждаемые в настоящем описании. Диагностику опухолей с такими мутациями можно осуществлять с использованием методов, известных специалисту в данной области и описанных в настоящей заявке, таких как RTPCR и FISH.
Примеры типов рака, которые можно лечить (или ингибировать), включают, без ограничения, карциному, например, карциному мочевого пузыря, молочной железы, толстой кишки (например, колоректальные карциномы, такие как аденокарциному толстой кишки и аденому толстой кишки), почки, уротелиальную, матки, эпидермиса, печени, легкого (например, аденокарциному, мелкоклеточный рак легкого и немелкоклеточные карциномы легких, плоскоклеточный рак легкого), пищевода, головы и шеи, желчного пузыря, яичника, поджелудочной железы (например, карциному экзокринного отдела поджелудочной железы), желудка, желудочно-кишечный (также называемый рак ЖКТ) рак (например, желудочно-кишечные стромальные опухоли), шейки матки, эндометрия, щитовидной железы, предстательной железы или кожи (например, плоскоклеточную карциному или возвышающуюся дерматофибросаркому); рак гипофиза, гемобластоз лимфоидного происхождения, например, лейкоз, острый лимфолейкоз, хронический лимфолейкоз, B-клеточную лимфому (например, диффузную В-крупноклеточную лимфому), T-клеточную лимфому, лимфому Ходжкина, неходжкинскую лимфому, волосатоклеточную лимфому или лимфому Беркитта; гемобластоз миелоидного происхождения, например, острые и хронические миелогенные лейкозы, хронический миеломоноцитарный лейкоз (СМML), миелопролиферативное нарушение, миелопролиферативный синдром, миелодиспластический синдром или промиелоцитарный лейкоз; множественную миелому; фолликулярный рак щитовидной железы; гепатоцеллюлярный рак, опухоль мезенхимального происхождения (например, саркому Юинга), например, фибросаркому или рабдомиосаркому; опухоль центральной или периферической нервной системы, например, астроцитому, нейробластому, глиому (такую как мультиформная глиобластома) или шванному; меланому; семиному; тератокарциному; остеосаркому; ретикуллярный прогрессирующий меланоз; кератоакантому; фолликулярный рак щитовидной железы или саркому Капоши. В частности, плоскоклеточный рак легких, рак молочной железы, колоректальный рак, глиобластому, астроцитомы, рак предстательной железы, мелкоклеточный рак легких, меланому, раковые опухоли головы и шеи, рак щитовидной железы, рак матки, рак желудка, гепатоцеллюлярный рак, рак шейки матки, множественную миелому, рак мочевого пузыря, рак эндометрия, уротелиальный рак, рак толстой кишки, рабдомиосаркому, рак гипофиза.
Некоторые типы рака являются резистентными к лечению определенными лекарственными средствами. Это может быть обусловлено типом опухоли или может возникать вследствие лечения соединением. В этой связи, ссылки на множественную миелому включают чувствительную к бортезомибу множественную миелому или рефрактерную форму множественной миеломы. Подобным образом, ссылки на хронический миелогенный лейкоз включают чувствительный к иматинибу хронический миелогенный лейкоз и рефрактерную форму хронического миелогенного лейкоза. Хронический миелогенный лейкоз также известен как хронический миелобластный лейкоз, хронический гранулоцитарный лейкоз или CML. Аналогично, острый миелогенный лейкоз также назван как острый миелобластный лейкоз, острый гранулоцитарный лейкоз, острый нелимфоцитарный лейкоз или AML.
Соединения согласно изобретению также могут применяться в лечении заболеваний системы кроветворения с нарушенной клеточной пролиферацией, будь то предзлокачественные или стабильные заболевания, такие как миелопролиферативные заболевания. Миелопролиферативные заболевания ("MPD") представляют собой группу заболеваний костного мозга, в котором продуцируются избыточные клетки. Они связаны с и могут переходить в миелодиспластический синдром. Миелопролиферативные заболевания включают истинную полицитемию, эссенциальную тромбоцитемию и первичный миелофиброз. Другим гематологическим нарушением является гиперэозинофильный синдром. Т-клеточные лимфопролиферативные заболевания включают такие, которые связаны с натуральными киллерными клетками.
Кроме того, соединения согласно изобретению могут применяться для лечения желудочно-кишечного рака (также называемого как рак ЖКТ), например, гастроинтестинальных стромальных опухолей. Желудочно-кишечный рак относится к злокачественным состояниям желудочно-кишечного тракта, включающего пищевод, желудок, печень, билиарную систему, поджелудочную железу, кишечник и анус.
Таким образом, в фармацевтических композициях, применениях или способах данного изобретения для лечения заболевания или состояния, включающего аномальный рост клеток, заболеванием или состоянием, включающим аномальный рост клеток, в одном варианте осуществления является рак.
Конкретные подклассы рака включают множественную миелому, карциномы мочевого пузыря, шейки матки, предстательной железы и щитовидной железы, рак легкого, молочной железы и толстой кишки.
Другой подкласс рака включает множественную миелому, карциномы мочевого пузыря, гепатоклеточную карциному, плоскоклеточную карциному полости рта и карциномы шейки матки.
Соединение согласно изобретению, обладающее ингибиторной активностью по отношению к FGFR-рецептору, такому как FGFR1, может быть особенно полезным в лечении или предотвращении рака молочной железы, в частности, классических лобулярных карцином (CLC).
Поскольку соединения согласно изобретению проявляют активность по отношению к FGFR4, они также будут применяться в лечении рака предстательной железы или гипофиза, или они будут применяться в лечении рака молочной железы, рака легкого, рака предстательной железы, рака печени (НСС).
В частности, соединения согласно изобретению, в качестве ингибиторов FGFR, пригодны в лечении множественной миеломы, миелопролиферативных нарушений, рака эндометрия, рака предстательной железы, рака мочевого пузыря, рака легкого, рака яичника, рака молочной железы, рака желудка, колоректального рака и плоскоклеточной карциномы полости рта.
Другими подклассами рака являются множественная миелома, рак эндометрия, рак мочевого пузыря, рак шейки матки, рак предстательной железы, рак легкого, рак молочной железы, колоректальный рак и карциномы щитовидной железы.
В частности, соединения согласно изобретению являются пригодными в лечении множественной миеломы (в частности, множественной миеломы с транслокацией t(4;14) или повышенной экспрессией FGFR3), рака предстательной железы (гормон-рефрактерные карциномы предстательной железы), рака эндометрия (в частности, опухолей эндометрия с активирующими мутациями в FGFR2) и рака молочной железы (в частности, лобулярный рак молочной железы).
В частности, соединения изобретения обладают активностью против опухолей с FGFR3-TACC3 транслокацией, в частности опухолей мочевого пузыря или мозга с FGFR3-TACC3 транслокацией.
В частности, соединения являются пригодными в лечении лобулярных карцином, таких как CLC (классическая лобулярная карцинома).
Поскольку соединения проявляют активность против FGFR3, они будут пригодны в лечении множественной миеломы и рака мочевого пузыря.
В частности, соединения являются пригодными в лечении множественной миеломы с t(4;14)-положительной транслокацией.
В одном варианте осуществления изобретения соединения могут применяться для лечения саркомы. В одном варианте осуществления изобретения соединения могут применяться для лечения рака легкого, например, плоскоклеточной карциномы.
Поскольку соединения проявляют активность против FGFR2, они могут применяться в лечении рака эндометрия, яичника, желудка, гепатоцеллюлярного рака, рака матки, шейки матки и колоректального рака. FGFR2 также сверхэкспрессирован при эпителиальном раке яичников, поэтому соединения согласно изобретению могут быть особенно полезными в лечении рака яичников, такого как эпителиальный рак яичников.
В одном варианте осуществления соединения могут применяться для лечения рака легкого, в частности, NSCLC, плоскоклеточной карциномы, рака печени, рака почки, рака молочной железы, рака толстой кишки, колоректального рака, рака предстательной железы.
Соединения согласно изобретению также могут применяться в лечении опухолей, предварительно обработанных ингибитором VEGFR2 или антителом VEGFR2 (например, авастином).
В частности, соединения согласно изобретению могут применяться в лечении VEGFR2-резистентных опухолей. Ингибиторы и антитела VEGFR2 применяют в лечении карциномы щитовидной железы и почечно-клеточной карциномы, поэтому соединения согласно изобретению могут применяться в лечении VEGFR2-резистентной карциномы щитовидной железы и почечно-клеточной карциномы.
Типы рака могут быть такими, которые являются чувствительными к ингибированию любого одного или более рецепторов FGFR, выбранных из FGFR1, FGFR2, FGFR3, FGFR4, например, одного или более FGFR, выбранных из FGFR1, FGFR2 или FGFR3.
Является ли конкретный тип рака или нет тем типом рака, который проявляет чувствительность к торможению передачи сигнала от FGFR или VEGFR, можно определить посредством анализа роста клеток, как описано ниже, или способом, представленным в разделе, озаглавленном "Методы диагностики".
Соединения согласно изобретению и, в частности, такие соединения, которые проявляют ингибиторную активность по отношению к FGFR или VEGFR, могут быть особенно полезными в лечении или предотвращении рака, ассоциированного с наличием или характеризующегося наличием повышенных уровней FGFR или VEGFR, например, раковых опухолей, упоминаемых в этом контексте во вводном разделе настоящей заявки.
Соединения согласно настоящему изобретению могут применяться в лечении взрослой популяции. Соединения согласно настоящему изобретению могут применяться для лечения популяции детей.
Было обнаружено, что некоторые ингибиторы FGFR могут применяться в комбинации с другими противораковыми средствами. Например, комбинирование ингибитора, индуцирующего апоптоз, с другим средством, которое действует по другому механизму, регулируя рост клеток, может оказаться благоприятным, обеспечивая, таким образом, воздействие на две из характерных особенностей развития рака. Примеры таких комбинаций представлены ниже.
Соединения согласно изобретению могут применяться в лечении других состояний, которые возникают в результате нарушений пролиферации, таких как диабет II типа или инсулинонезависимый сахарный диабет, аутоиммунные заболевания, травма головы, инсульт, эпилепсия, нейродегенеративные заболевания, такие как болезнь Альцгеймера, заболевание двигательных нейронов, прогрессирующий надъядерный паралич, кортико-базальная дегенерация и болезнь Пика, например, аутоиммунные заболевания и нейродегенеративные заболевания.
Одна подгруппа болезненных состояний и заболеваний, для которой могут применяться соединения согласно изобретению, состоит из воспалительных заболеваний, сердечно-сосудистых заболеваний и заживления ран.
Также известно, что FGFR и VEGFR играют роль в апоптозе, ангиогенезе, пролиферации, дифференцировке и транскрипции, и поэтому соединения согласно изобретению могут применяться в лечении следующих заболеваний, отличных от рака: хронических воспалительных заболеваний, например, системной красной волчанки, аутоиммунного опосредованного гломерулонефрита, ревматоидного артрита, псориаза, воспалительного заболевания кишечника, аутоиммунного сахарного диабета, реакций гиперчувствительности в виде экземы, астмы, COPD, ринита и заболевания верхних дыхательных путей; сердечно-сосудистых заболеваний, например, гипертрофии сердца, рестеноза, атеросклероза; нейродегенеративных нарушений, например, болезни Альцгеймера, СПИД-ассоциированной деменции, болезни Паркинсона, амиотрофического бокового склероза, пигментного ретинита, спинальной мышечной атрофии и мозжечковой дегенерации; гломерулонефрита; миелодиспластических синдромов, ассоциированного с ишемическим повреждением инфаркта миокарда, инсульта и реперфузионного повреждения, аритмии, атеросклероза, заболеваний печени, индуцированных токсином и связанных с алкоголем, гематологических заболеваний, например, хронической анемии и гипопластической анемии; дегенеративных заболеваний костно-мышечной системы, например, остеопороза и артрита, аспирин-чувствительного риносинусита, фиброзно-кистозной дегенерации, рассеянного склероза, заболеваний почек и боли при раке.
Кроме того, мутации FGFR2 ассоциированы с несколькими тяжелыми нарушениями в развитии скелета человека, и, таким образом, соединения согласно изобретению могут быть пригодными в лечении нарушений развития скелета человека, включающих аномальную оссификацию черепных швов (краниосиностоз), синдром Апера (АР), синдром Крузона, синдром Джексона-Вейсса, синдром сморщенных кожных покровов Бира-Стивенсона и синдром Пфейффера.
Соединение согласно изобретению, проявляющее ингибиторную активность по отношению к рецептору FGFR, такому как FGFR2 или FGFR3, может быть наиболее пригодным в лечении или предотвращении заболеваний скелета. Конкретными заболеваниями скелета являются ахондроплазия или танатофорная карликовость (также известная как танатофорная дисплазия).
Соединение согласно изобретению, проявляющее ингибиторную активность по отношению к рецептору FGFR, такому как FGFR1, FGFR2 или FGFR3, может быть наиболее пригодным в лечении или предотвращении патологий, в которых прогрессирующий фиброз является симптомом. Фибротические состояния, при которых соединения согласно изобретению могут применяться в лечении, включают заболевания, характеризующиеся аномальным или избыточным отложением фиброзной ткани, например, при циррозе печени, гломерулонефрите, фиброзе легких, системном фиброзе, ревматоидном артрите, а также при естественном процессе заживления ран. В частности, соединения согласно изобретению могут также применяться в лечении фиброза легких, в частности, идиопатического легочного фиброза.
Сверхэкспрессия и активация рецепторов FGFR и VEGFR в опухолеассоциированной сосудистой сети также свидетельствует о роли соединений согласно изобретению в предотвращении и разрушении инициации ангиогенеза в опухоли. В частности, соединения согласно изобретению могут применяться в лечении рака, метастазирования, лейкозов, таких как CLL, заболеваний глаз, таких как возрастная макулодистрофия, в частности, влажная форма возрастной макулодистрофии, ишемические пролиферативные ретинопатии, такие как ретролентальная фиброплазия (ROP) и диабетическая ретинопатия, ревматоидный артрит и гемангиома.
Активность соединений согласно изобретению в качестве ингибиторов FGFR1-4, VEGFR и/или PDGFR A/B можно измерить посредством анализов, представленных в примерах ниже, а уровень активности, проявляемой данным соединением, можно определить в значениях IC50. Предпочтительными соединениями согласно настоящему изобретению являются соединения, имеющие значения IC50 меньше чем 1 мкΜ, более предпочтительно меньше чем 0,1 мкΜ.
В изобретении предложены соединения, которые проявляют ингибирующую или модулирующую активность в отношении FGFR, и которые могут применяться в предотвращении или лечении болезненных состояний или заболеваний, опосредованных FGFR-киназами.
В одном варианте осуществления предложено соединение, как определено в описании, для применения в терапии, для применения в качестве лекарственного препарата. В другом варианте осуществления изобретения предложено соединение, как определено в описании, для применения в профилактике или лечении, в частности, в лечении заболевания или состояния, опосредованного FGFR-киназой.
Таким образом, например, соединения согласно изобретению могут применяться в ослаблении или уменьшении частоты возникновения рака. Следовательно, в другом варианте осуществления предложено соединение, как определено в описании, для применения в профилактике или лечении, в частности в лечении рака. В одном варианте осуществления соединение, как определено в описании, предложено для применения в профилактике или лечении FGFR-зависимого рака. В одном варианте осуществления соединение, как определено в описании, предложено для применения в профилактике или лечении рака, опосредованного FGFR-киназами.
Таким образом, в изобретении предложены в том числе:
- Способ профилактики или лечения заболевания или состояния, опосредованного FGFR-киназой, включающий введение субъекту, нуждающемуся в этом, соединения формулы (I), как определено в настоящем описании.
- Способ профилактики или лечения заболевания или состояния, как определено в настоящем описании, включающий введение субъекту, нуждающемуся в этом, соединения формулы (I), как определено в настоящем описании.
- Способ профилактики или лечения рака, включающий введение субъекту, нуждающемуся в этом, соединения формулы (I), как определено в настоящем описании.
- Способ ослабления или уменьшения частоты возникновения заболевания или состояния, опосредованного FGFR-киназой, включающий введение субъекту, нуждающемуся в этом, соединения формулы (I), как определено в настоящем описании.
- Способ ингибирования FGFR-киназы, включающий контакт киназы с ингибирующим киназу соединением формулы (I), как определено в настоящем описании.
- Способ модулирования клеточного процесса (например, клеточное деление) путем ингибирования активности FGFR-киназы с использованием соединения формулы (I), как определено в настоящем описании.
- Соединение формулы (I), как определено в настоящем описании, для применения его в качестве модулятора клеточного процесса (например, деления клеток) путем ингибирования активности FGFR-киназы.
- Соединение формулы (I), как определено в настоящем описании, для применения его в профилактике или лечении рака, в частности лечении рака.
- Соединение формулы (I), как определено в настоящем описании, для применения его в качестве модулятора (например, ингибитора) FGFR.
- Применение соединения формулы (I), как определено в настоящем описании, для получения лекарственного средства, предназначенного для профилактики или лечения заболевания или состояния, опосредованного FGFR-киназой, соединения формулы (I), как определено в настоящем описании.
- Применение соединения формулы (I), как определено в настоящем описании, для получения лекарственного средства, предназначенного для профилактики или лечения заболевания или состояния, как описано в настоящей заявке.
- Применение соединения формулы (I), как определено в настоящем описании, для получения лекарственного средства, предназначенного для профилактики или лечения, в частности, лечения рака.
- Применение соединения формулы (I), как определено в настоящем описании, для получения лекарственного средства, предназначенного для модулирования (например, ингибирования) активности FGFR.
- Применение соединения формулы (I), как определено в настоящем описании, для получения лекарственного средства, предназначенного для модулирования клеточного процесса (например, деления клеток) путем ингибирования активности FGFR-киназы.
- Применение соединения формулы (I), как определено в настоящем описании, для получения лекарственного средства, предназначенного для профилактики или лечения заболевания или состояния, характеризующегося положительной регуляцией FGFR-киназы (например, FGFR1 или FGFR2, или FGFR3, или FGFR4).
- Применение соединения формулы (I), как определено в настоящем описании, для получения лекарственного средства, предназначенного для профилактики или лечения рака, рака, который характеризуется апрегуляцией FGFR-киназы (например, FGFR1 или FGFR2, или FGFR3, или FGFR4).
- Применение соединения формулы (I), как определено в настоящем описании, для получения лекарственного средства, предназначенного для профилактики или лечения рака у больного, выбранного из субпопуляции, обладающей генетическими аберрациями FGFR3-киназы.
- Применение соединения формулы (I), как определено в настоящем описании, для получения лекарственного средства, предназначенного для профилактики или лечения рака у больного, который согласно поставленному диагнозу является частью субпопуляции, обладающей генетическими аберрациями FGFR3-киназы.
- Способ профилактики или лечения заболевания или состояния, характеризующегося апрегуляцией FGFR-киназы (например, FGFR1 или FGFR2, или FGFR3, или FGFR4), включающий введение соединения формулы (I), как определено в настоящем описании.
- Способ облегчения или уменьшения частоты заболевания или состояния, характеризующегося апрегуляцией FGFR-киназы (например, FGFR1 или FGFR2, или FGFR3, или FGFR4), включающий введение соединения формулы (I), как определено в настоящем описании.
- Способ профилактики или лечения (или облегчения или уменьшения числа случаев) рака у пациента, страдающего от рака или у которого подозревают рак; включающий (i) прохождение пациентом диагностического исследования с целью определения, имеет ли пациент генетические аберрации гена FGFR3; и (ii) в случае присутствия у пациента указанного варианта, впоследствии введение пациенту соединения формулы (I), как определено в настоящем описании, проявляющего ингибиторную активность по отношению к FGFR3-киназе.
- Способ профилактики или лечения (или облегчения или уменьшения числа случаев) заболевания или состояния, характеризующегося апрегуляцией FGFR-киназы (например, FGFR1 или FGFR2, или FGFR3, или FGFR4), включающий (i) прохождение пациентом диагностического исследования с целью определения маркера, характерного для апрегуляции FGFR-киназы (например, FGFR1 или FGFR2, или FGFR3, или FGFR4), и (ii) в случае, где результат диагностического исследования свидетельствует об апрегуляции FGFR-киназы, впоследствии введение пациенту соединения формулы (I), как определено в настоящем описании, проявляющего ингибиторную активность по отношению к FGFR-киназе.
В одном варианте осуществления заболеванием, опосредованным FGFR-киназами, является связанное с онкологией заболевание (например, рак). В одном варианте осуществления заболеванием, опосредованным FGFR-киназами, является несвязанное с онкологией заболевание (например, любое представленное в описании заболевание, исключая рак). В одном варианте осуществления заболеванием, опосредованным FGFR-киназами, является состояние, описанное в настоящей заявке. В одном варианте осуществления изобретения заболеванием, опосредованным FGFR-киназами, является патологическое состояние скелета, представленное в описании. Конкретные нарушения развития скелета человека включают нарушение оссификации черепных швов (краниосиностоз), синдром Апера (AP), синдром Крузона, синдром Джексона-Вейсса, синдром сморщенных кожных покровов Бира-Стивенсона, синдром Пфейффера, ахондроплазию и танатофорную карликовость (также известную как танатофорная дисплазия).
Мутантные киназы
Лекарственно-устойчивые мутации киназы могут возникать в популяции больных, которые проходили лечение ингибиторами киназы. Такие мутации образуются, отчасти, в областях белка, которые связываются или взаимодействуют с конкретным ингибитором, используемым в терапии. Такие мутации снижают или повышают способность ингибитора связываться и ингибировать данную киназу. Эти мутации могут появляться по любым аминокислотным остаткам, которые взаимодействуют с ингибитором или представляют важность для поддержания связывания указанного ингибитора с мишенью. Ингибитор, который связывается с мишенью-киназой без необходимости взаимодействия с мутировавшим аминокислотным остатком, вероятно, не будет зависеть от мутации, и будет оставаться эффективным ингибитором фермента.
Изучение образцов, взятых у больных раком желудка, показало наличие двух мутаций в FGFR2, Ser167Pro в экзоне IIIa и мутацию сайта сплайсинга 940-2A-G в экзоне IIIc. Указанные мутации идентичны зародышевым активирующим мутациям, которые вызывают синдромы краниосиностоза, и которые наблюдали в 13% исследованных тканях первичного рака желудка. Кроме того, активирующие мутации в FGFR3 наблюдали в 5% образцов, взятых у исследуемых пациентов, при этом повышенная экспрессия рецепторов FGFR коррелировала с неблагоприятным прогнозом в данной группе пациентов.
Кроме того, существуют хромосомные транслокации или точковые мутации, которые наблюдали в FGFR, которые приводят к приобретению новой функции белкового продукта гена, повышенной экспрессии или конститутивно активным биологическим состояниям.
Таким образом, соединения согласно изобретению должны найти конкретное применение в отношении раковых опухолей, которые экспрессируют мутантную молекулярную мишень, такую как FGFR. Диагностику опухолей с такими мутациями можно осуществить, используя методы, известные специалисту в данной области и представленные в описании, такие как RTPCR и FISH.
Было сделано предположение, что мутации консервативного остатка треонина у АТФ-связывающего сайта FGFR должны приводить к устойчивости к ингибиторам. Аминокислотный остаток валин 561 был мутирован до метионина в FGFR1, что соответствует ранее сообщенным данным о мутациях, найденных в Abl (T315) и EGFR (T766), которые, как было показано, придают устойчивость к селективным ингибиторам. Данные анализа FGFR1 V561M показали, что указанная мутация придавала устойчивость к ингибитору тирозинкиназного рецептора по сравнению с диким типом.
Методы диагностики
До введения соединения формулы (I), пациент может быть подвергнут скринингу с целью определения, является ли заболевание или состояние, которым пациент страдает или может страдать, заболеванием или состоянием, которое должно быть чувствительным к лечению соединением, обладающим активностью, направленной против FGFR и/или VEGFR.
Например, биологический образец, полученный от пациента, может быть проанализирован с целью определения, является ли заболевание или состояние, такое как рак, которым пациент страдает или может страдать, заболеванием или состоянием, которое характеризуется генетическим нарушением или аномальной белковой экспрессией, что приводит к апрегуляции уровней или активности FGFR и/или VEGFR или к сенсибилизации пути до нормальной активности FGFR и/или VEGFR, или к апрегуляции указанных путей внутриклеточной сигнализации, связанных с фактором роста, таких как уровни лиганда фактора роста или активность лиганда фактора роста, или к апрегуляции биохимического пути, следующего после активации FGFR и/или VEGFR.
Примеры таких нарушений, которые приводят к активации или сенсибилизации сигнала от FGFR и/или VEGFR, включают потерю или ингибирование апоптических путей, апрегуляцию рецепторов или лигандов или присутствие мутантных вариантов рецепторов или лигандов, например, вариантов PTK. Опухоли с мутациями в FGFR1, FGFR2 или FGFR3, или FGFR4, или апрегуляцией, в частности сверхэкспрессией FGFR1, или мутанты FGFR2 или FGFR3 с приобретением новой функции, могут быть особенно чувствительными к ингибиторам FGFR.
Например, точковые мутации с приобретением новой функции в FGFR2 были идентифицированы при ряде заболеваний. В частности, активирующие мутации в FGFR2 были идентифицированы в 10% опухолей эндометрия.
Кроме того, генетические аберрации рецепторной тирозинкиназы FGFR3, такие как хромосомные транслокации или точковые мутации, приводящие к эктопически экспрессированным или нерегулируемым, конститутивно активным рецепторам FGFR3, были идентифицированы и связаны с подгруппой множественных миелом, карцином мочевого пузыря и шейки матки. Конкретная мутация T674I рецептора PDGF была идентифицирована у пациентов, проходивших лечение иматинибом. Кроме того, амплификация гена 8p12-p11.2 была продемонстрирована в ~50% случаев лобулярного рака молочной железы (CLC), и, как было показано, она была связана с повышенной экспрессией FGFR1. Предварительные исследования с миРНК, направленными против FGFR1, или низкомолекулярным ингибитором рецептора, выявили клеточные линии, делающие такую амплификацию особенно чувствительной к ингибированию данного сигнального пути.
В альтернативе, биологический образец, полученный от пациента, может быть проанализирован на предмет потери негативного регулятора или супрессора FGFR или VEGFR. В настоящем контексте термин "потеря" охватывает делецию гена, кодирующего регулятор или супрессор, усечение гена (например, в результате мутации), усечение транскрибируемого продукта гена или инактивацию транскрибируемого продукта (например, в результате токовой мутации) или секвестрацию другим генным продуктом.
Термин апрегуляция включает повышенную экспрессию или сверхэкспрессию, включающую амплификацию гена (т.е. множественные копии генов) и повышенную экспрессию посредством транскрипционного эффекта, а также гиперактивность и активацию, включающую активацию в результате мутаций. Таким образом, больной может быть подвергнут диагностическому исследованию с целью определения маркера, характерного для апрегуляции FGFR и/или VEGFR. Термин диагностика включает скрининг. Под маркером подразумеваются генетические маркеры, включающие, например, измерение состава ДНК для идентификации мутаций FGFR и/или VEGFR. Термин маркер также включает маркеры, характерные для апрегуляции FGFR и/или VEGFR, включая ферментативную активность, уровни фермента, состояние фермента (например, фосфорилированное или нет) и уровни мРНК указанных выше белков.
Диагностические испытания и скрининги обычно проводят на биологическом образце, выбранном из биопсийных образцов опухоли, образцов крови (выделение и обогащение выделенных опухолевых клеток), образцов кала, мокроты, анализа хромосом, плевральной жидкости, перитонеальной жидкости, соскоба щеки, биоптата и мочи.
Методы идентификации и анализ мутаций и апрегуляции белков известны специалисту в данной области. Методы скрининга могут включать, без ограничения, стандартные методы, такие как полимеразную цепную реакцию с обратной транскриптазой (ОТ-ПЦР) или гибридизацию insitu, такую как флуоресцентная гибридизация insitu (FISH).
Идентификация индивида, несущего мутацию в FGFR и/или VEGFR, может означать, что больной может быть особенно подходящим для лечения ингибитором FGFR и/или VEGFR. Опухоли могут предпочтительно подвергнуты скринингу на присутствие варианта FGFR и/или VEGFR до лечения. Способ скрининга обычно включает прямое секвенирование, анализ с олигонуклеотидными чипами или мутант-специфичным антителом. Кроме того, диагностика опухолей с такими мутациями может быть осуществлена с использованием методов, известных специалисту в данной области и представленных в описании, таких как ОT-ПЦР и FISH.
Кроме того, мутантные формы, например, FGFR или VEGFR2, могут быть идентифицированы путем прямого секвенирования, например, опухолевых биопсий при использовании ПЦР и методов прямого секвенирования продуктов ПЦР, как описано в тексте выше. Специалисту в данной области будет очевидно, что все такие хорошо известные методы определения сверхэкспрессии, активации или мутаций указанных выше белков могут быть применимы к данному случаю.
В скрининге с помощью ОT-ПЦР, уровень мРНК в опухоли оценивают путем создания кДНК копии мРНК с последующей амплификацией кДНК с помощью ПЦР. Методы ПЦР амплификации, выбор праймеров и условия амплификации хорошо известны специалисту в данной области. Манипуляции с нуклеиновой кислотой и ПЦР осуществляют стандартными способами, как описано, например, в руководстве Ausubel, F.M. et al., eds. (2004) Current Protocols in Molecular Biology, John Wiley & Sons Inc., или Innis, M.A. et al., eds. (1990) PCR Protocols: a guide to methods and applications, Academic Press, San Diego. Реакции и манипуляции, включающие методы исследования нуклеиновых кислот, также описаны в руководстве Sambrook et al., (2001), 3rd Ed, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press. В альтернативе, может быть использован коммерчески доступный набор для ОТ-ПЦР (например, Roche Molecular Biochemicals) или методики, описанные в патентах США 4666828; 4683202; 4801531; 5192659, 5272057, 5882864 и 6218529 и включенные в настоящее описание посредством отсылки. Примером способа гибридизации insitu для оценки экспрессии мРНК может быть флуоресцентная гибридизация insitu (FISH) (см., Angerer (1987) Meth. Enzymol., 152:649).
В общем, гибридизация insitu включает следующие основные стадии: (1) фиксацию анализируемой ткани; (2) предварительную гибридизацию образца для повышения доступности заданной нуклеиновой кислоты и снижения неспецифического связывания; (3) гибридизацию смеси нуклеиновых кислот с нуклеиновой кислотой в биологической структуре или ткани; (4) промывки после гибридизации для удаления фрагментов нуклеиновой кислоты, не связавшихся при гибридизации, и (5) детектирование гибридизованных фрагментов нуклеиновой кислоты. Зонды, используемые в таких способах, обычно являются меченными, например, радиоизотопами или флуоресцентными репортерами. Предпочтительные зонды являются достаточно длинными, например, приблизительно от 50, 100 или 200 нуклеотидов до 1000 или более нуклеотидов, для осуществления специфической гибридизации с заданной нуклеиновой кислотой(ами) в жестких условиях. Стандартные методы осуществления метода FISH описаны в руководстве Ausubel, F.M. et al., eds. (2004) Current Protocols in Molecular Biology, John Wiley & Sons Inc and Fluorescence In Situ Hybridization: Technical Overview by John M. S. Bartlett in Molecular Diagnosis of Cancer, Methods and Protocols, 2nd ed.; ISBN: 1-59259-760-2; March 2004, pps. 077-088; Series: Methods in Molecular Medicine.
Методы анализа уровня экспрессии генов описаны в DePrimo et al. (2003), BMC Cancer, 3:3. Кратко, протокол анализа следующий: двухцепочечную кДНК синтезируют из суммарной РНК с использованием олигомера (dT)24 для праймирования синтеза первой цепи кДНК с последующим синтезом второй цепи кДНК со случайными гексамерными праймерами. Двухнитевую кДНК используют в качестве матрицы для invitro транскрипции кРНК с применением биотинилированных рибонуклеотидов. кРНК химически фрагментируют согласно методикам, описанным Affymetrix (Santa Clara, CA, USA), а затем подвергают гибридизации в течение ночи на чипах с генами человека.
В альтернативе, белковые продукты, экспрессированные из мРНК, могут быть проанализированы с помощью иммуногистохимического анализа образцов опухоли, твердофазного иммуноферментного анализа с микротитровальными планшетами, Вестерн блоттинга, 2-мерного электрофореза в полиакриламидном геле с SDS, ELISA, проточной цитометрии и других методов, известных в данной области для определения специфических белков. Методы определения могут включать сайтспецифические антитела. Специалисту в данной области будет очевидно, что все такие хорошо известные методы определения апрегуляции FGFR и/или VEGFR, или определения вариантов FGFR и/или VEGFR, или их мутаций могут быть применимы к данному случаю.
Аномальные уровни белков, таких как FGFR или VEGFR, могут быть измерены при использовании стандартных ферментных анализов, например, таких анализов, которые описаны в настоящей заявке. Активацию или сверхэкспрессию также можно определять в образце ткани, например, в ткани опухоли. При измерении активности тирозинкиназы с помощью такого анализа, как анализ Chemicon International, тирозинкиназа, представляющая интерес, должна быть иммунопреципитирована из лизата образца, и ее активность измерена.
Альтернативные методы измерения сверхэкспрессии или активации FGFR или VEGFR, включая их изоформы, включают измерение плотности микрососудистой сети. Плотность можно измерить, например, с помощью методов, описанных Orre and Rogers (Int J Cancer (1999), 84(2) 101-8). Методы анализа также включают использование маркеров, например, в случае VEGFR, такие маркеры включают CD31, CD34 и CD105.
Таким образом, все перечисленные методы также могут быть использованы для идентификации опухолей, особенно подходящих для лечения соединениями согласно изобретению.
Соединения согласно изобретению являются наиболее пригодными в лечении пациента с мутантным вариантом FGFR. Мутацию G697C в FGFR3 наблюдают в 62% плоскоклеточных карцином полости рта, при этом она вызывает конститутивную активацию активности киназы. Активирующие мутации FGFR3 также были идентифицированы в случаях карциномы мочевого пузыря. Указанные мутации состояли из 6 видов с различными степенями распространенности: R248C, S249C, G372C, S373C, Y375C, K652Q. Кроме того, полиморфизм Gly388Arg в FGFR4, как было обнаружено, ассоциирован с повышением числа случаев и агрессивностью рака предстательной железы, толстой кишки, легкого, печени (НСС) и молочной железы.
Таким образом, в другом аспекте изобретение включает применение соединения согласно изобретению с целью получения лекарственного препарата для лечения или профилактики заболевания или состояния у пациента, у которого в результате скрининга было выявлено, что он страдает или подвергается риску развития заболевания или состояния, которое может быть чувствительным к лечению соединением, обладающим активностью против FGFR.
Конкретные мутации, на наличие которых пациент проходит скрининг, включают G697C, R248C, S249C, G372C, S373C, Y375C, K652Q в FGFR3 и полиморфизм Gly388Arg в FGFR4.
В другом аспекте изобретение включает соединение согласно изобретению для применения в профилактике или лечении рака у пациента, выбранного из субпопуляции, обладающей вариантом гена FGFR (например, мутация G697C в FGFR3 и полиморфизм Gly388Arg в FGFR4).
Определение нормализации сосудов с помощью МРТ (например, с использованием МРТ градиентного эха, спинового эха и повышения контрастности для измерения объема крови, относительного размера сосуда и сосудистой проницаемости) в сочетании с циркулирующими биомаркерами (циркулирующие клетки-предшественники (CPC), CEC, SDF1 и FGF2) также может быть использовано с целью идентификации VEGFR2-устойчивых опухолей для лечения соединением согласно изобретению.
Фармацевтические композиции и комбинации
Исходя из полезных фармакологических свойств соединений, рассматриваемые соединения могут быть включены в различные фармацевтические формы в целях введения.
В одном варианте осуществления фармацевтическая композиция (например, препарат) содержит по меньшей мере одно активное соединение согласно изобретению вместе с одним или более фармацевтически приемлемыми носителями, адъювантами, эксципиентами, разбавителями, наполнителями, буферами, стабилизаторами, консервантами, лубрикантами или другими материалами, хорошо известными специалистам в данной области, и, необязательно, другими терапевтическими или профилактическими средствами.
Для получения фармацевтической композиции согласно изобретению, эффективное количество соединения согласно настоящему изобретению, в качестве активного ингредиента, объединяют с фармацевтически приемлемым носителем в виде однородной смеси, причем носитель может иметь различные формы в зависимости от формы препарата, требуемого для введения. Фармацевтические композиции могут быть получены в любой форме, подходящей для перорального, парентерального, местного, интраназального, офтальмологического, ушного, ректального, внутривагинального или чрескожного введения. Указанные фармацевтические композиции желательно находятся в единичной дозированной форме, подходящей, предпочтительно, для введения перорально, ректально, подкожно или посредством парентеральной инъекции. Например, для получения композиции в дозированной форме для перорального применения, может быть использована любая из обычных фармацевтических сред, такая как, например, вода, гликоли, масла, спирты и тому подобное в случае пероральных жидких препаратов, таких как суспензии, сиропы, эликсиры и растворы; или твердые носители, такие как крахмалы, сахара, каолин, лубриканты, связующие вещества, дезинтегранты и тому подобное в случае порошков, пилюль, капсул и таблеток.
Благодаря легкости введения, таблетки и капсулы представляют собой наиболее благоприятную пероральную единичную дозированную форму, в случае которой, безусловно, используются твердые фармацевтические носители. Относительно парентеральных композиций, носитель, как правило, будет содержать стерильную воду, по меньшей мере, в значительной степени, хотя могут быть включены другие ингредиенты, например, для увеличения растворимости. Например, могут быть приготовлены растворы для инъекций, в которых носитель включает физиологический раствор, раствор глюкозы или смесь физиологического раствора и раствора глюкозы. Также могут быть получены суспензии для инъекций, в случае которых могут быть использованы соответствующие жидкие носители, суспендирующие средства и тому подобное. В композициях, подходящих для подкожного введения, носитель необязательно представляет собой вещество, усиливающее проникновение, и/или подходящее увлажняющее вещество, необязательно в комбинации с подходящими добавками любой природы в малых пропорциях, не оказывающими значительного повреждающего действия на кожу. Указанные добавки могут облегчать введение в кожу и/или могут быть полезными для получения требуемых композиций. Указанные композиции могут быть введены различными путями, например, в виде чрескожного пластыря, в виде капель, в виде мази. Они являются наиболее благоприятными для получения указанных выше фармацевтических композиций в единичной дозированной форме благодаря легкости введения и однородности дозировки. Единичная дозированная форма, при использовании в настоящем описании и формуле изобретения, относится к физически дискретным единицам, подходящим в качестве единичных дозировок, при этом каждая единица содержит заданное количество активного ингредиента, рассчитанное на достижение желаемого терапевтического эффекта, в сочетании с требуемым фармацевтическим носителем. Примерами таких единичных дозированных форм являются таблетки (включающие таблетки с насечками или таблетки с оболочкой), капсулы, пилюли, пакеты с порошком, облатки, растворы или суспензии для инъекций, чайные ложки, столовые ложки и тому подобное, и их раздельное множество.
Наиболее предпочтительно получать вышеуказанные фармацевтические композиции в единичной дозированной форме для легкости введения и однородности дозировки. Единичная дозированная форма, при использовании в описании и формуле изобретения, относится к физически дискретным единицам, подходящим в качестве единичных дозировок, при этом каждая единица содержит заданное количество активного ингредиента, рассчитанное на достижение желаемого терапевтического эффекта, в сочетании с требуемым фармацевтическим носителем. Примерами таких единичных дозированных форм являются таблетки (включающие таблетки с насечками или таблетки с оболочкой), капсулы, пилюли, пакеты с порошком, облатки, растворы или суспензии для инъекций, чайные ложки, столовые ложки и тому подобное, и их раздельное множество.
Соединение согласно изобретению вводят в количестве, достаточном для проявления его противоопухолевой активности.
Специалисты в данной области смогут легко определить эффективное количество, исходя из результатов тестирования, представленных ниже. В общем, предполагается, что терапевтически эффективное количество должно составлять от 0,005 мг/кг до 100 мг/кг массы тела, и, в частности, от 0,005 мг/кг до 10 мг/кг массы тела. Указанное количество может быть соответствующим введению требуемой дозы как единственной, в виде двух, трех, четырех или более субдоз при соответствующих интервалах в течение дня. Указанные субдозы могут быть получены в виде единичных дозированных форм, например, содержащих от 0,5 до 500 мг, в частности, от 1 мг до 500 мг, более конкретно, от 10 мг до 500 мг активного ингредиента на единичную дозированную форму.
В зависимости от способа введения, фармацевтическая композиция предпочтительно будет содержать от 0,05 до 99% по массе, более предпочтительно от 0,1 до 70% по массе, даже более предпочтительно от 0,1 до 50% по массе соединения согласно настоящему изобретению, и, от 1 до 99,95% по массе, более предпочтительно от 30 до 99,9% по массе, даже более предпочтительно от 50 до 99,9% по массе фармацевтически приемлемого носителя, где все проценты основаны на общей массе композиции.
В качестве другого аспекта настоящего изобретения предусматривают комбинацию соединения согласно настоящему изобретению с другим противораковым средством, в особенности для применения в качестве лекарственного средства, более конкретно для применения в лечении рака или связанных с раком заболеваний.
Для лечения указанных выше состояний, соединения согласно изобретению могут эффективно применяться в комбинации с одним или более лекарственными средствами, более конкретно с другими противораковыми средствами или адъювантами, используемыми в терапии рака. Примеры противораковых средств или адъювантов (поддерживающих средств в терапии) включают, без ограничения:
- комплексные соединения платины, например, цисплатин, необязательно в комбинации с амифостином, карбоплатином или оксалиплатином;
- соединения таксана, например, паклитаксел, частицы паклитаксела, связанного с белком (Abraxane™) или доцетаксел;
- ингибиторы топоизомеразы I, такие как соединения камптотецина, например, иринотекан, SN-38, топотекан, топотекан hcl;
- ингибиторы топоизомеразы II, такие как противоопухолевые эпиподофиллотоксины или производные подофиллотоксина, например, этопозид, этопозида фосфат или тенипозид;
- противоопухолевые алкалоиды барвинка, например, винбластин, винкристин или винорелбин;
- противоопухолевые нуклеозидные производные, например, 5-фторурацил, лейковорин, гемцитабин, гемцитабин hcl, капецитабин, кладрибин, флударабин, неларабин;
- алкилирующие средства, такие как азотистый иприт или нитрозомочевина, например, циклофосфамид, хлорамбуцил, кармустин, тиотепа, мефалан (мелфалан), ломустин, алтретамин, бусульфан, дакарбазин, эстрамустин, ифосфамид необязательно в комбинации с месна, пипоброман, прокарбазин, стрептозоцин, телозоломид, урацил;
- противоопухолевые производные антрациклина, например, даунорубицин, доксорубицин, необязательно в комбинации с дексразоксаном, доксил, идарубицин, митоксантрон, эпирубицин, эпирубицин hcl, валрубицин;
- молекулы, направленно воздействующие на рецептор IGF-1, например, пикроподофиллин;
- производные тетракарцина, например, тетракарцин A;
- глюкокортикоид, например, преднизон;
- антитела, например, трастузумаб (антитело HER2), ритуксимаб (антитело СD20), гемтузумаб, гемтузумаб озогамицин, цетуксимаб, пертузумаб, бевацизумаб, алемтузумаб, экулизумаб, ибритумомаб тиуксетан, нофетумомаб, панитумумаб, тозитумомаб, CNTO 328;
- антагонисты рецепторов эстрогена или селективные модуляторы рецепторов эстрогена или ингибиторы синтеза эстрогена, например, тамоксифен, фулвестрант, торемифен, дролоксифен, фазлодекс, ралоксифен или летрозол;
- ингибиторы ароматазы, такие как эксеместан, анастрозол, летразол, тестолактон и ворозол;
- средства, влияющие на дифференцировку, такие как ретиноиды, витамин D или ретиноевая кислота, и средства, блокирующие метаболизм ретиноевой кислоты (RAMBA), например, аккутан;
- ингибиторы ДНК-метилтрансферазы, например, азацитидин или децитабин;
- антифолаты, например, преметрексед динатрия;
- антибиотики, например, актиномицин D, блеомицин, митомицин C, дактиномицин, карминомицин, дауномицин, левамизол, пликамицин, митрамицин;
- антиметаболиты, например, клофарабин, аминоптерин, цитозина арабинозид или метотрексат, азацитидин, цитарабин, флоксуридин, пентостатин, тиогуанин;
- средства, индуцирующие апоптоз, и антиангиогенные средства, такие как ингибиторы Bcl-2, например, YC 137, BH 312, ABT 737, госсипол, HA 14-1, TW 37 или декановая кислота;
- тубулинсвязывающие средства, например, комбрестатин, колхицины или нокодазол;
- ингибиторы киназы (например, ингибиторы EGFR (рецептор фактора роста эпителия), MTKI (многонаправленные ингибиторы киназы), ингибиторы mTOR), например, флавоперидол, иматиниба мезилат, эрлотиниб, гефитиниб, дасатиниб, лапатиниб, лапатиниба дитозилат, сорафениб, сунитиниб, сунитиниба малеат, темсиролимус;
- ингибиторы фарнесилтрансферазы, например, типифарниб;
- ингибиторы гистондеацетилазы (HDAC), например, бутират натрия, субероиланилид гидроксамовой кислоты (SAHA), депсипептид (FR 901228), NVP-LAQ824, R306465, JNJ-26481585, трихостатин A, вориностат;
- ингибиторы убиквитин-протеасомного пути, например, PS-341, MLN .41 или бортезомиб;
- ионделис;
- ингибиторы теломеразы, например, теломестатин;
- ингибиторы матриксных металлопротеиназ, например, батимастат, маримастат, приностат или метастат.
- рекомбинантные интерлейкины, например, алдеслейкин, денилейкина дифтитокс, интерферон альфа 2a, интерферон альфа 2b, пегинтерферон альфа 2b
- ингибиторы MAPK
- ретиноиды, например, алитретиноин, бексаротен, третиноин
- триоксид мышьяка
- аспарагиназа
- стероиды, например, дромостанолона пропионат, мегестрола ацетат, нандролон (деканоат, фенпропионат), дексаметазон
- агонисты или антагонисты гонадотропин-рилизинг гормона, например, абареликс, гозерелина ацетат, гистрелина ацетат, лейпролида ацетат
- талидомид, леналидомид
- меркаптопурин, митотан, памидронат, пегадемас, пегаспаргаза, расбуриказа
- миметики ВH3, например, ABT-737
- ингибиторы MEK, например, PD98059, AZD6244, CI-1040
- аналоги колониестимулирующего фактора, например, филграстим, пегфилграстим, сарграмостим; эритропоэтин или его аналоги (например, дарбепоэтин альфа); интерлейкин 11; опрелвекин; золедронат; золедроновая кислота; фентанил; бисфосфонат; палифермин.
- стероидный ингибитор цитохром Р450 17-альфа-гидроксилазы-17,20-лиазы (CYP17), например, абиратерон, абиратерона ацетат.
Соединения согласно настоящему изобретению также имеют терапевтические применения в сенсибилизации опухолевых клеток для радиотерапии и химиотерапии.
Поэтому соединения согласно настоящему изобретению могут применяться в качестве "радиосенсибилизатора" и/или "хемосенсибилизатора" или могут быть представлены в комбинации с другим "радиосенсибилизатором" и/или "хемосенсибилизатором".
Термин "радиосенсибилизатор", используемый в настоящем описании, определяют как молекулу, предпочтительно молекулу низкой молекулярной массы, вводимую животным в терапевтически эффективных количествах для повышения чувствительности клеток к ионизирующему излучению и/или эффективности лечения заболеваний, поддающихся лечению ионизирующим излучением.
Термин "хемосенсибилизатор", используемый в настоящем описании, определяют как молекулу, предпочтительно молекулу низкой молекулярной массы, вводимую животным в терапевтически эффективных количествах для повышения чувствительности клеток к химиотерапии и/или эффективности лечения заболеваний, поддающихся лечению химиотерапией.
Некоторые механизмы способа действия радиосенсибилизаторов были предложены и описаны в литературе, включая: гипоксические клеточные радиосенсибилизаторы (например, соединения 2-нитроимидазола и соединения бензотриазина диоксида), имитирующие кислород, или, альтернативно, ведущие себя подобно биовосстановительным средствам при гипоксии; негипоксические клеточные радиосенсибилизаторы (например, галогенированные пиримидины) могут быть аналогами оснований ДНК и предпочтительно включаться в ДНК раковых клеток и, тем самым, стимулировать индуцированное излучением разрушение молекул ДНК и/или предотвращать механизмы репарации ДНК до нормы; и различные другие потенциальные механизмы действия были предположены для радиосенсибилизаторов в лечении заболевания.
В настоящее время во многих методиках лечения рака применяют радиосенсибилизаторы в сочетании с рентгеновским излучением. Примеры радиосенсибилизаторов, активированных рентгеновским излучением, включают, без ограничения, следующие соединения: метронидазол, мизонидазол, десметилмизонидазол, пимонидазол, этанидазол, ниморазол, митомицин C, RSU 1069, SR 4233, EО9, RB 6145, никотинамид, 5-бромдезоксиуридин (BUdR), 5-иоддезоксиуридин (IUdR), бромдезоксицитидин, фтордезоксиуридин (FudR), гидроксимочевину, цисплатин и терапевтически эффективные аналоги и производные перечисленных соединений.
Фотодинамическая терапия (ФДТ) рака использует видимый свет в качестве радиационного активатора сенсибилизирующего средства. Примеры фотодинамических радиосенсибилизаторов включают, без ограничения, следующие соединения: производные гематопорфирина, фотофрин, производные бензопорфирина, этиопорфирин олова, феоборбид-a, бактериохлорофилл-a, нафталоцианины, фталоцианины, фталоцианин цинка и терапевтически эффективные аналоги и производные перечисленных соединений.
Радиосенсибилизаторы могут быть введены в сочетании с терапевтически эффективным количеством одного или более других соединений, включающих, без ограничения: соединения, которые способствуют включению радиосенсибилизаторов в клетки-мишени; соединения, которые регулируют поток терапевтических средств, питательных веществ и/или кислорода к клеткам-мишеням; химиотерапевтические средства, которые действуют на опухоль с дополнительным излучением или без него; или другие терапевтически эффективные соединения, предназначенные для лечения рака или других заболеваний.
Хемосенсибилизаторы могут быть введены в сочетании с терапевтически эффективным количеством одного или более других соединений, включающих, без ограничения: соединения, которые способствуют включению хемосенсибилизаторов в клетки-мишени; соединения, которые регулируют поток терапевтических средств, питательных веществ и/или кислорода к клеткам-мишеням; химиотерапевтические средства, которые действуют на опухоль, или другие терапевтически эффективные соединения, предназначенные для лечения рака или других заболеваний. Антагонисты кальция, например, верапамил, как было обнаружено, могут применяться в комбинации с антинеопластическими средствами для достижения чувствительности к химиотерапевтическим препаратам в опухолевых клетках, устойчивых к общепринятым химиотерапевтическим средствам, и усиления эффективности таких соединений в чувствительных к лекарственным средствам злокачественных опухолях.
Исходя из их полезных фармакологических свойств, компоненты комбинаций согласно изобретению, т.е. одно или более других лекарственных средств и соединение согласно настоящему изобретению, могут быть включены в различные фармацевтические формы в целях введения. Компоненты могут быть включены раздельно в индивидуальные фармацевтические композиции или в одну фармацевтическую композицию, содержащую все компоненты.
Таким образом, настоящее изобретение также относится к фармацевтической композиции, содержащей одно или более других лекарственных средств и соединение согласно настоящему изобретению вместе с фармацевтическим носителем.
Настоящее изобретение также относится к применению комбинации согласно изобретению в получении фармацевтической композиции, направленной на ингибирование роста опухолевых клеток.
Настоящее изобретение также относится к продукту, содержащему в качестве первого активного ингредиента соединение согласно изобретению, а в качестве второго активного ингредиента - одно или более противораковых средств, как комбинированному препарату для одновременного, раздельного или последовательного применения в лечении пациентов, страдающих раком.
Одно или более других лекарственных средств и соединение согласно настоящему изобретению могут быть введены одновременно (например, в раздельных или единых композициях) или раздельно в любом порядке. В последнем случае, два или более соединений вводят в течение такого периода, в таком количестве и таким способом, которые достаточны для обеспечения достижения благоприятного или синергического эффекта. Следует отметить, что предпочтительный способ и порядок введения, а также соответствующие количества дозировки и схемы лечения для каждого компонента комбинации будут зависеть от другого конкретного лекарственного средства и соединения согласно настоящему изобретению, которые вводят, способа их введения, конкретной опухоли, подвергаемой лечению, и конкретного реципиента, подвергаемого лечению. Оптимальный способ и порядок введения, а также количества дозировки и схема лечения могут быть легко определены специалистами в данной области с использованием стандартных методов и с учетом информации, изложенной в настоящем описании.
Массовое отношение соединения согласно настоящему изобретению и одного или более других противораковых средств, в случае их применения в виде комбинации, может быть определено специалистом в данной области. Указанное отношение, точная дозировка и частота введения зависят от конкретного соединения согласно изобретению и другого применяемого противоракового средства (средств), конкретного состояния, подвергаемого лечению, тяжести состояния, подвергаемого лечению, возраста, массы тела, пола, питания, времени введения и общего физического состояния отдельного больного, способа введения, а также других лекарственных средств, которые может принимать индивид, как хорошо известно специалистам в данной области. Кроме того, очевидно, что эффективное суточное количество может быть уменьшено или увеличено в зависимости от реакции субъекта, подвергаемого лечению, и/или в зависимости от оценки врача, назначившего соединения согласно настоящему изобретению. Конкретное массовое отношение для настоящего соединения формулы (I) и другого противоракового средства может изменяться в пределах от 1/10 до 10/1, более конкретно от 1/5 до 5/1, еще конкретнее от 1/3 до 3/1.
Комплексное соединение платины предпочтительно вводят в дозировке, составляющей от 1 до 500 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 50 до 400 мг/м2, конкретно для цисплатина - в дозировке приблизительно 75 мг/м2, и для карбоплатина - приблизительно 300 мг/м2 на курс лечения.
Соединение таксана предпочтительно вводят в дозировке от 50 до 400 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 75 до 250 мг/м2, конкретно для паклитаксела - в дозировке приблизительно от 175 до 250 мг/м2, и для доцетаксела - приблизительно от 75 до 150 мг/м2 на курс лечения.
Соединение камптотецина предпочтительно вводят в дозировке от 0,1 до 400 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 1 до 300 мг/м2, конкретно для иринотекана - в дозировке приблизительно от 100 до 350 мг/м2 и для топотекана - приблизительно от 1 до 2 мг/м2 на курс лечения.
Противоопухолевое производное подофиллотоксина предпочтительно вводят в дозировке от 30 до 300 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 50 до 250 мг/м2, конкретно для этопозида - в дозировке приблизительно от 35 до 100 мг/м2, и для тенипозида - приблизительно от 50 до 250 мг/м2 на курс лечения.
Противоопухолевый алкалоид барвинка предпочтительно вводят в дозировке от 2 до 30 мг на квадратный метр (мг/м2) площади поверхности тела, конкретно для винбластина - в дозировке приблизительно от 3 до 12 мг/м2, для винкристина - в дозировке приблизительно от 1 до 2 мг/м2, и для винорелбина - в дозировке приблизительно от 10 до 30 мг/м2 на курс лечения.
Противоопухолевое нуклеозидное производное предпочтительно вводят в дозировке от 200 до 2500 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 700 до 1500 мг/м2, конкретно для - 5-FU в дозировке от 200 до 500 мг/м2, для гемцитабина - в дозировке приблизительно от 800 до 1200 мг/м2, и для капецитабина - приблизительно от 1000 до 2500 мг/м2 на курс лечения.
Алкилирующие средства, такие как азотистый иприт или нитрозомочевина, предпочтительно вводят в дозировке от 100 до 500 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 120 до 200 мг/м2, конкретно для циклофосфамида - в дозировке приблизительно от 100 до 500 мг/м2, для хлорамбуцила - в дозировке приблизительно от 0,1 до 0,2 мг/м2, для кармустина - в дозировке приблизительно от 150 до 200 мг/м2, и для ломустина - в дозировке приблизительно от 100 до 150 мг/м2 на курс лечения.
Противоопухолевое антрациклиновое производное предпочтительно вводят в дозировке от 10 до 75 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 15 до 60 мг/м2, конкретно для доксорубицина - в дозировке приблизительно от 40 до 75 мг/м2, для даунорубицина - в дозировке приблизительно от 25 до 45 мг/м2, и для идарубицина - в дозировке приблизительно от 10 до 15 мг/м2 на курс лечения.
Антиэстрогенное средство предпочтительно вводят в дозировке приблизительно от 1 до 100 мг ежедневно в зависимости от конкретного средства и состояния, подвергаемого лечению. Тамоксифен предпочтительно вводят перорально в дозировке от 5 до 50 мг, предпочтительно от 10 до 20 мг дважды в день, продолжая терапию в течение достаточного времени для достижения и сохранения терапевтического эффекта. Торемифен предпочтительно вводят перорально в дозировке приблизительно 60 мг один раз в день, продолжая терапию в течение достаточного времени для достижения и сохранения терапевтического эффекта. Анастрозол предпочтительно вводят перорально в дозировке приблизительно 1 мг один раз в день. Дролоксифен предпочтительно вводят перорально в дозировке приблизительно 20-100 мг один раз в день. Ралоксифен предпочтительно вводят перорально в дозировке приблизительно 60 мг один раз в день. Эксеместан предпочтительно вводят перорально в дозировке приблизительно 25 мг один раз в день.
Антитела предпочтительно вводят в дозировке приблизительно от 1 до 5 мг на квадратный метр (мг/м2) площади поверхности тела, или как известно в данной области, если есть различия. Трастузумаб предпочтительно вводят в дозировке от 1 до 5 мг на квадратный метр (мг/м2) площади поверхности тела, конкретно от 2 до 4 мг/м2 на курс лечения. Указанные дозировки могут быть введены, например, один раз, дважды или более на курс лечения, который может быть повторен, например, каждые 7, 14, 21 или 28 дней.
Соединения формулы (I), фармацевтически приемлемые соли присоединения, в частности фармацевтически приемлемые соли присоединения кислот, и их стереоизомерные формы могут проявлять значимые диагностические свойства, благодаря которым они могут применяться для определения или идентификации комплекса, образованного между меченым соединением и другими молекулами, пептидами, белками, ферментами или рецепторами.
В способах определения или идентификации могут применяться соединения, меченные такими метками, как радиоактивные изотопы, ферменты, флуоресцентные вещества, люминесцентные вещества и т.д. Примеры радиоактивных изотопов включают125I,131I,3H и14C. Ферменты обычно обнаруживают посредством конъюгирования соответствующего субстрата, который, в свою очередь, катализирует детектируемую реакцию. Соответствующие примеры включают, например, бета-галактозидазу, бета-глюкозидазу, щелочную фосфатазу, пероксидазу и малатдегидрогеназу, предпочтительно пероксидазу хрена. Люминесцентные вещества включают, например, люминол, производные люминола, люциферин, экворин и люциферазу.
Биологические образцы могут быть определены как ткань тела или физиологические жидкости. Примерами физиологических жидкостей являются спинномозговая жидкость, кровь, плазма, сыворотка, моча, мокрота, слюна и тому подобное.
Общие пути синтеза
Следующие примеры иллюстрируют настоящее изобретение, но представляют собой только примеры и не должны ограничивать объем формулы изобретения каким-либо способом.
Значения стехиометрии соли или содержания кислоты в соединениях, представленные в настоящем описании, получены экспериментально и могут отличаться в зависимости от используемого метода анализа (ЯМР для соединений 61', 62' и 73'). В случае если солевая форма не указана, соединение было получено в виде свободного основания.
В дальнейшем термин 'ДХМ' означает дихлорметан, 'Me' означает метил, 'Et' означает этил, 'MeOH' означает метанол, 'ДМФА' означает диметилформамид, 'Et2O' означает диэтиловый эфир, 'EtOAc' означает этилацетат, BrettPhos палладацикл: (CAS: 1148148-01-9) означает хлор[2-(дициклогексилфосфино)-3,6-диметокси-2'-4'-6'-триизопропил-1,1'-бифенил][2-(2-аминоэтил)-фенил]палладий (II), 'PdCl2dppf (CAS:72287-26-4) означает 1,1'-бис(дифенилфосфино)ферроцен дихлорпалладий (II), 'ТГФ' означает тетрагидрофуран, 'ACN' означает ацетонитрил, 'СКЖХ' означает сверкритическую жидкостную хроматографию, 'MgSO4' означает сульфат магния, 'q.s.' означает достаточное количество, 'тп' означает температуру плавления, 'iPrNH2' означает изопропиламин, 'ДСК' означает дифференциальную сканирующую калориметрию, 'ДИПЭ', означает диизопропиловый эфир, 'TBAF' фторид тетрабутиламмония, 'кт' означает комнатную температуру, 'Pd2dba3' означает трис(дибензилиденацетон)дипалладий (0), 'BINAP' означает [1,1'-бинафталин]-2,2'-диилбис[дифенилфосфин].
A. Получение промежуточных соединений
Пример A1:
Получение промежуточного соединения 1:

2-Амино-5-бромбензойную кислоту (50 г; 231,4 ммоль) растворяли в толуоле (500 мл). Добавляли триэтилортоформиат (58 мл; 347,2 ммоль), затем уксусную кислоту (1,3 мл; 23,1 ммоль). Смесь нагревали при 110°C в течение 2,5 часов. Реакцию охлаждали до комнатной температуры и добавляли анилин (21 мл; 231,4 ммоль). Смесь нагревали при 110°C еще в течение 20 часов. Полученную смесь охлаждали при комнатной температуре и фильтровали. Фильтрат кристаллизовали из петролейного эфира. Осадок отфильтровывали и перекристаллизовывали из смеси ДХМ и петролейного эфира с получением 15,6 г (22%) промежуточного соединения 1. Тп=178°C
Получение промежуточного соединения 2:

Смесь промежуточного соединения 1 (1,4 г; 4,6 ммоль), 2,6-дифтор-3,5-диметоксианилина (1,3 г; 6,9 ммоль), BrettPhos палладацикла (0,18 г; 0,23 ммоль) и карбоната цезия (4,5 г; 13,75 ммоль) в толуоле (60 мл) нагревали при 100°C в течение 5 часов. Смесь охлаждали, вливали в охлажденную воду и добавляли ДХМ. Раствор фильтровали через слой Celite® и экстрагировали фильтрат ДХМ. Органический слой сушили над MgSO4, фильтровали и выпаривали досуха.
Остаток (2,4 г) очищали с помощью хроматографии на силикагеле (нерегулярный SiOH 50 г; подвижная фаза: 99% ДХМ, 1% MeOH). Фракции, содержащие продукт, собирали и выпаривали досуха с получением 2,1 г промежуточного соединения, которое кристаллизовали из смеси MeOH и Et2O с получением 704 мг (38%) промежуточного соединения 2. Тп=156°C (ДСК)
Получение промежуточного соединения 5:

Промежуточное соединение 5 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 2,6-дихлор-3,5-диметоксианилина в качестве исходного соединения (выход: 59%).
Получение промежуточного соединения 7:

Промежуточное соединение 7 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 2-фтор-3,5-диметоксианилина в качестве исходного соединения (выход: 52%).
Получение промежуточного соединения 9:

Промежуточное соединение 9 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 3,5-диметоксианилина в качестве исходного соединения (выход: 45%).
Пример A2:
Получение промежуточного соединения 3:

Под N2 при 10°C гидрид натрия (60% в минеральном масле) (0,4 г; 9 ммоль) добавляли к раствору промежуточного соединения 2 (1,24 г; 3 ммоль) в ДМФА (12 мл). Раствор перемешивали при 10°C в течение 30 минут. Затем по каплям добавляли раствор (2-бромэтокси)-трет-бутилдиметилсилана (1,4 мл; 6,7 ммоль) в ДМФА (3 мл). Раствор оставляли медленно нагреваться до комнатной температуры в течение 5 часов. Раствор вливали в охлажденную воду и экстрагировали продукт EtOAc. Органический слой промывали водой, сушили над MgSO4, фильтровали и выпаривали досуха, получив 2 г промежуточного соединения 3, которое использовали в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 6:

Промежуточное соединение 6 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 3, при использовании промежуточного соединения 5 в качестве исходного соединения.
Получение промежуточного соединения 8:
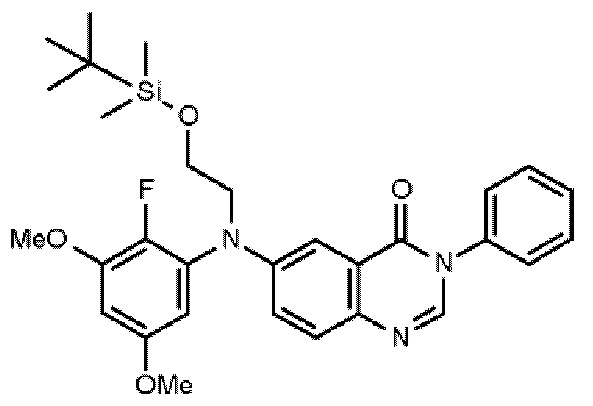
Промежуточное соединение 8 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 3, при использовании промежуточного соединения 7 в качестве исходного соединения.
Получение промежуточного соединения 10:
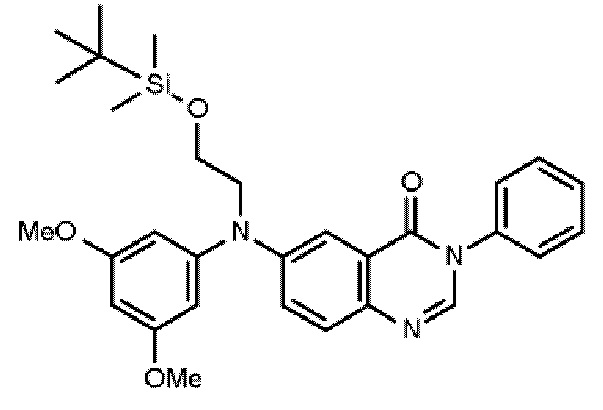
Промежуточное соединение 10 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 3, при использовании промежуточного соединения 9 в качестве исходного соединения.
Пример A3:
Получение промежуточного соединения 4:

Метансульфонилхлорид (0,3 мл; 3,75 ммоль) по каплям добавляли к раствору соединения 1 (0,43 г; 0,94 ммоль) и триэтиламина (0,65 мл; 4,7 ммоль) в ДХМ (20 мл) при 5°C под током N2. Реакционную смесь перемешивали при 5°C в течение 2 часов, затем вливали в воду со льдом и добавляли ДХМ (q.s.). Органический слой отделяли, сушили над MgSO4, фильтровали и растворитель выпаривали досуха при комнатной температуре, получив 0,5 г промежуточного соединения 4, которое использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Пример A4:
Получение промежуточного соединения 11:
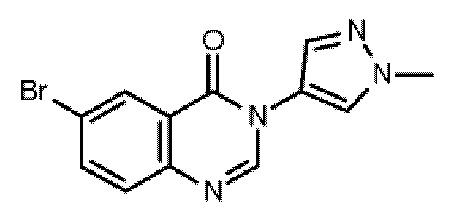
2-Амино-5-бромбензойную кислоту (33,4 г; 154,4 ммоль) растворяли в толуоле (2 л). Добавляли триэтилортоформиат (34 г; 231,7 ммоль), затем уксусную кислоту (2 мл). Смесь нагревали при 110°C в течение 2,5 часов. Реакцию охлаждали до комнатной температуры и добавляли 4-амино-1-метилпиразол (15 г; 154,4 ммоль). Смесь нагревали при 110°C еще в течение 20 часов. Полученную смесь охлаждали до комнатной температуры и фильтровали. Фильтрат кристаллизовали из смеси толуола и петролейного эфира. Осадок отфильтровывали и очищали с помощью хроматографии на силикагеле (нерегулярный SiOH; подвижная фаза: ДХМ/MeOH 80/1). Фракции, содержащие продукт, собирали и выпаривали досуха с получением 11 г (23%) промежуточного соединения 11.
Получение промежуточного соединения 22:

Смесь промежуточного соединения 11 (1,4 г; 4,6 ммоль), 2,6-дифтор-3,5-диметоксианилина (1,4 г; 7,3 ммоль), BrettPhos палладацикла (0,18 г; 0,23 ммоль) и карбоната цезия (4,5 г; 14 ммоль) в толуоле (60 мл) нагревали при 100°C в течение ночи. Смесь охлаждали, вливали в охлажденную воду и добавляли EtOAc. Раствор фильтровали через слой Celite® (кизельгур) и продукт экстрагировали EtOAc. Органический слой сушили над MgSO4, фильтровали и выпаривали досуха. Остаток (2,6 г) очищали с помощью хроматографии на силикагеле (нерегулярный SiOH, 300 г; подвижная фаза: 60% гептана, 5% MeOH, 35% EtOAc). Фракции, содержащие продукт, собирали и выпаривали досуха с получением 1,1 г промежуточного соединения, которое кристаллизовали из Et2O, получив 1,06 г (56%) промежуточного соединения 22. Тп=214°C (ДСК).
Получение промежуточного соединения 12:

Промежуточное соединение 12 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 22, при использовании м-анизидина в качестве исходного соединения (выход: 13%).
Получение промежуточного соединения 13:
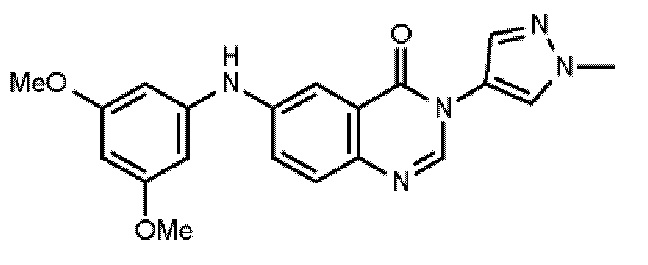
Промежуточное соединение 13 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 22, при использовании 3,5-диметоксианилина в качестве исходного соединения (выход: 50%).
Получение промежуточного соединения 16:
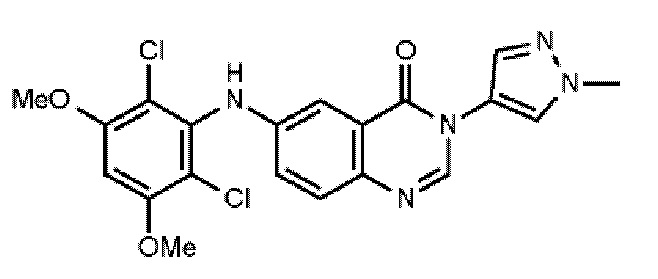
Промежуточное соединение 16 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 22, при использовании 2,6-дихлор-3,5-диметоксианилина в качестве исходного соединения (выход: 45%).
Получение промежуточного соединения 19:
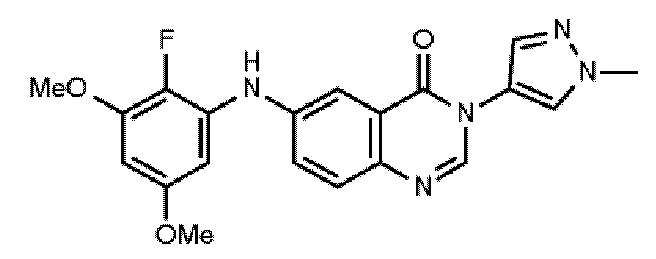
Промежуточное соединение 19 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 22, при использовании 2-фтор-3,5-диметоксианилина в качестве исходного соединения (выход: 7%).
Получение промежуточного соединения 23:

Под N2 при 10°C гидрид натрия (60% в минеральном масле) (0,26 г; 6,4 ммоль) добавляли к раствору промежуточного соединения 22 (0,88 г; 2ммоль) в ДМФА (12 мл). Раствор перемешивали при 10°C в течение 30 минут. Затем по каплям добавляли раствор (2-бромэтокси)-трет-бутилдиметилсилана (1 мл; 4,7 ммоль) в ДМФА (3 мл). Раствор оставляли медленно нагреваться до комнатной температуры в течение 5 часов. Раствор вливали в охлажденную воду, и продукт экстрагировали EtOAc. Органический слой промывали водой, сушили над MgSO4, фильтровали и выпаривали досуха, получив 1,65 г промежуточного соединения 23, которое использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 14:

Промежуточное соединение 14 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 23, при использовании промежуточного соединения 13 в качестве исходного соединения.
Получение промежуточного соединения 17:

Промежуточное соединение 17 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 23, при использовании промежуточного соединения 16 в качестве исходного соединения.
Получение промежуточного соединения 20:

Промежуточное соединение 20 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 23, при использовании промежуточного соединения 19 в качестве исходного соединения.
Пример A6:
Получение промежуточного соединения 24:

Метансульфонилхлорид (0,5 мл; 6,4 ммоль) по каплям добавляли к раствору соединения 18 (0,74 г; 1,6 ммоль) и триэтиламина (1,1 мл; 8 ммоль) в ДХМ (10 мл) при 5°C под током N2. Реакционную смесь перемешивали при 5°C в течение 2 часов. Реакционную смесь вливали в воду со льдом и добавляли ДХМ. Органический слой отделяли, сушили над MgSO4, фильтровали и досуха выпаривали растворитель при комнатной температуре, получив 0,8 г промежуточного соединения 24, которое использовали непосредственно в следующей стадии без дополнительной очистки.
Получение промежуточного соединения 15:
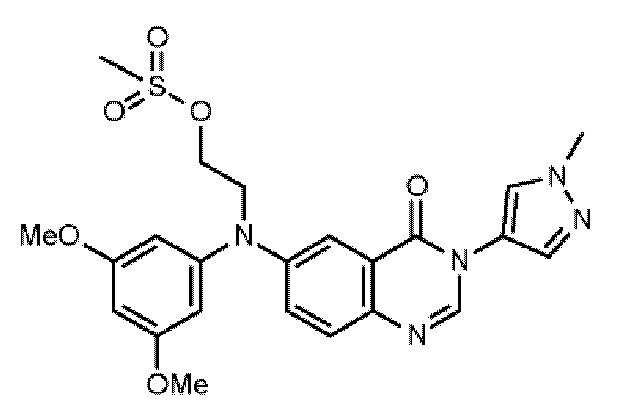
Промежуточное соединение 15 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 8 в качестве исходного соединения.
Получение промежуточного соединения 18:

Промежуточное соединение 18 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 10 в качестве исходного соединения.
Получение промежуточного соединения 21:

Промежуточное соединение 21 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 16 в качестве исходного соединения.
Пример A7:
Получение промежуточного соединения 25:

Промежуточное соединение 25 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 1, при использовании 4-аминопиперидин-1-карбоксилата в качестве исходного соединения (выход: 98%).
Получение промежуточного соединения 26:

Pd2dba3 (224 мг; 0,245 ммоль) и BINAP (305 мг; 0,49 ммоль) добавляли к раствору промежуточного соединения 25 (2 г; 4,9 ммоль), 2,6-дифтор-3,5-диметоксианилина (1,39 г; 7,35 ммоль) и Cs2CO3 (4,79 г; 14,69 ммоль) в диоксане (60 мл). Реакционную смесь нагревали в течение ночи при 80°C. Затем ее вливали в охлажденную воду, и водный слой экстрагировали ДХМ. Органический слой сушили над MgSO4, фильтровали и выпаривали растворитель. Полученный остаток кристаллизовали из ДИПЭ с получением 1,90 г промежуточного соединения 26 (75%). Тп=260°C (Kofler).
Получение промежуточного соединения 27:

Промежуточное соединение 27 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 3,5-диметоксианилина и промежуточного соединения 25 в качестве исходных соединений (выход: 84%). Тп=241°C (Kofler).
Получение промежуточного соединения 28:
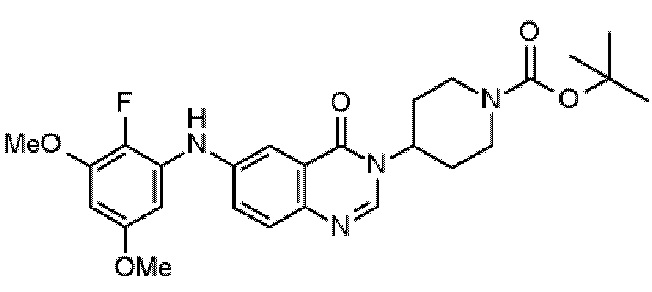
Промежуточное соединение 28 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 2-фтор-3,5-диметоксианилина и промежуточного соединения 25 в качестве исходных соединений (выход: 70%). Тп=263°C (Kofler).
Пример A8:
Получение промежуточного соединения 29:

Под N2 при -10°C гидрид натрия (60% в минеральном масле) (116 мг; 2,904 ммоль) добавляли к раствору промежуточного соединения 26 (500 мг; 0,968 ммоль) в ДМФА (15 мл). Реакционную смесь перемешивали при -10°C в течение 30 минут. Затем по каплям добавляли (2-бромэтокси)-трет-бутилдиметилсилан (0,455 мл; 2,13 ммоль). Реакционную смесь оставляли нагреваться до комнатной температуры в течение 2 часов. Раствор вливали в воду со льдом, и продукт экстрагировали EtOAc. Органический слой промывали рассолом, сушили над MgSO4, фильтровали и выпаривали досуха. Остаток очищали с помощью хроматографии на силикагеле (нерегулярный SiOH, 30 г; подвижная фаза: градиент с 0% MeOH, 100% ДХМ до 2% MeOH, 98% ДХМ). Фракции, содержащие продукт, собирали и выпаривали досуха с получением 436 мг (67%) промежуточного соединения 29.
Получение промежуточного соединения 30:

Промежуточное соединение 30 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 29, при использовании промежуточного соединения 28 в качестве исходного соединения (выход: 77%).
Получение промежуточного соединения 48:

Промежуточные 48 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 29, при использовании промежуточного соединения 27 в качестве исходного соединения (выход: 64%).
Пример A9:
Получение промежуточного соединения 31:

Промежуточное соединение 31 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 1, при использовании 3-аминопиридина в качестве исходного соединения (выход: 24%).
Получение промежуточного соединения 32:
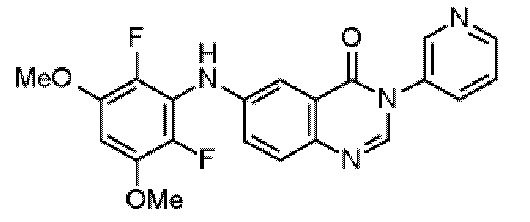
Промежуточное соединение 32 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 2,6-дифтор-3,5-диметоксианилина и промежуточного соединения 31 в качестве исходных соединений (выход: 51%). Тп=165°C (Kofler).
Получение промежуточного соединения 33:

Промежуточное соединение 33 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 2-дифтор-3,5-диметоксианилина и промежуточного соединения 31 в качестве исходных соединений (выход: 23%). Тп=162°C (Kofler).
Получение промежуточного соединения 34:

Промежуточное соединение 34 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 3,5-диметоксианилина и промежуточного соединения 31 в качестве исходных соединений (выход: 80%). Тп=176°C (Kofler).
Пример A10:
Получение промежуточного соединения 35:

Промежуточное соединение 35 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 23, при использовании промежуточного соединения 32 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 36:
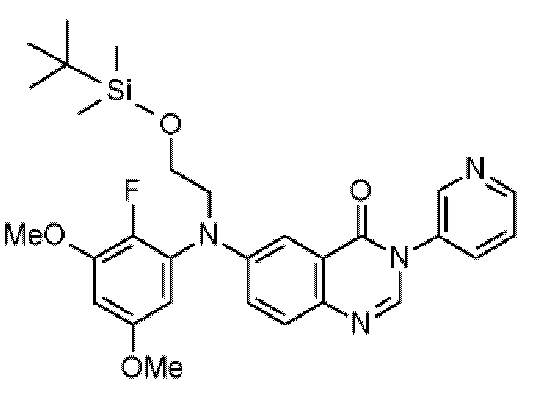
Промежуточное соединение 36 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 23, при использовании промежуточного соединения 33 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 37:

Промежуточное соединение 37 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 23, при использовании промежуточного соединения 34 в качестве исходного соединения (выход: 61%).
Пример A11:
Получение промежуточного соединения 38:

Промежуточное соединение 38 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 29 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 39:

Промежуточное соединение 39 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 30 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 40:

Промежуточное соединение 40 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 31 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Пример A12:
Получение промежуточного соединения 41:

Промежуточное соединение 41 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 1, при использовании 4-аминопиридина в качестве исходного соединения (выход: 29%).
Получение промежуточного соединения 42:
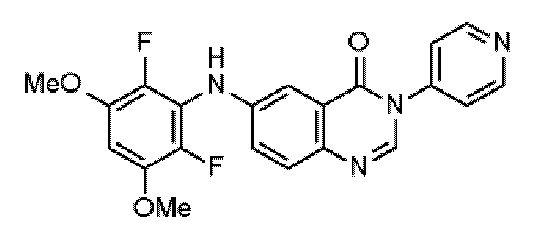
Промежуточное соединение 42 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 2,6-дифтор-3,5-диметоксианилина и промежуточного соединения 41 в качестве исходных соединений (выход: 19%).
100 мг промежуточного соединения 42 очищали с помощью ахиральной СКЖХ (неподвижная фаза: 2-этилпиридин 6 μм 150×21,2 мм), подвижная фаза: 80% CO2, 20% MeOH (0,3% iPrNH2)) с получением 84 мг промежуточного соединения 42 (Тп=248°C (Kofler)).
Получение промежуточного соединения 43:

Промежуточное соединение 43 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 2-дифтор-3,5-диметоксианилина и промежуточного соединения 41 в качестве исходных соединений (выход: 55%).
150 мг промежуточного соединения 43 перекристаллизовывали из MeOH и ДИПЭ, получив 107 мг промежуточного соединения 43 (Тп=215°C (Kofler)).
Получение промежуточного соединения 44:

Промежуточное соединение 44 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 3,5-диметоксианилина и промежуточного соединения 41 в качестве исходных соединений (выход: 23%). Тп=216°C (Kofler).
Пример A13:
Получение промежуточного соединения 45:

Промежуточное соединение 45 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 23, при использовании промежуточного соединения 42 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 46:

Промежуточное соединение 46 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 23, при использовании промежуточного соединения 43 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 47:

Промежуточное соединение 47 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 23, при использовании промежуточного соединения 44 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Пример A14:
Получение промежуточного соединения 49:
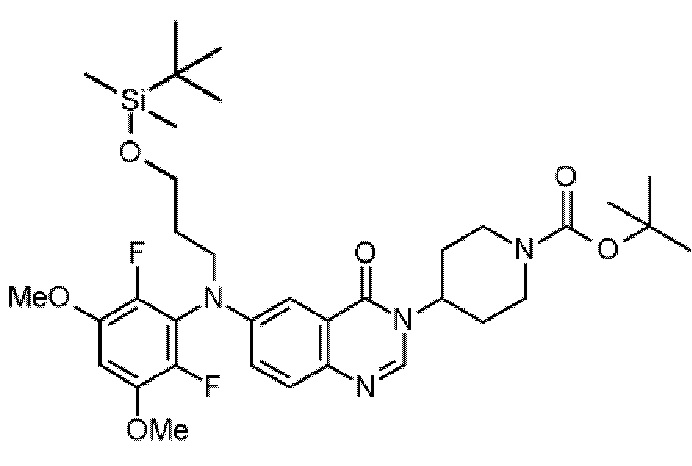
Гидрид натрия (60% в минеральном масле) (116 мг; 2,904 ммоль) при -10°C добавляли к раствору промежуточного соединения 26 (500 мг; 0,968 ммоль) в ДМФА (15 мл). Реакционную смесь перемешивали при -10°C в течение 30 минут. Затем по каплям добавляли (3-бромпропокси)-трет-бутилдиметилсилан (0,48 мл; 2,13 ммоль). Реакционную смесь оставляли нагреваться до 5°C в течение 2 часов. Раствор вливали в воду со льдом, и продукт экстрагировали EtOAc. Органический слой промывали рассолом, сушили над MgSO4, фильтровали и выпаривали досуха. Остаток кристаллизовали из Et2O, отфильтровывали осадок и сушили с получением 347 мг промежуточного соединения 49 (52%).
Получение промежуточного соединения 50:

Промежуточное соединение 50 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 49, при использовании промежуточного соединения 28 в качестве исходного соединения (выход: 73%).
Получение промежуточного соединения 51:

Промежуточное соединение 51 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 49, при использовании промежуточного соединения 27 в качестве исходного соединения (выход: 88%).
Пример A15:
Получение промежуточного соединения 52:
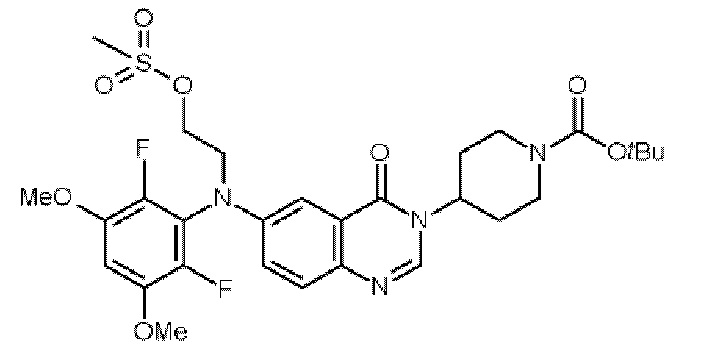
Промежуточное соединение 52 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 25 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 53:

Промежуточное соединение 53 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 26 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 54:

Промежуточное соединение 54 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 56 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Пример A16:
Получение промежуточного соединения 55:

Промежуточное соединение 55 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 50 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 56:

Промежуточное соединение 56 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 51 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 57:

Промежуточное соединение 57 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 52 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Пример A17:
Получение промежуточного соединения 58:

2-Амино-5-бромбензойную кислоту (30 г; 138,9 ммоль), триэтилортоформиат (30,9 г; 208,3 ммоль) и уксусную кислоту (0,9 мл) растворяли в толуоле (1,5 л). Смесь нагревали при 110°C в течение 2,5 часов. Затем добавляли тетрагидро-2H-пиран-4-амин (14.05 г; 138.9 ммоль) и реакционную смесь нагревали с обратным холодильником в течение 3 дней. Полученную смесь охлаждали при комнатной температуре и фильтровали. Фильтрат упаривали и кристаллизовали из смеси ДХМ и петролейного эфира с получением 26,9 г (62%) промежуточного соединения 58.
Получение промежуточного соединения 59:

Pd2dba3 (296 мг; 0,32 ммоль) и BINAP (403 мг; 0,65 ммоль) добавляли к раствору 2-фтор-3,5-диметоксианилина (1,66 г; 9,70 ммоль), промежуточного соединения 58 (2 г; 6,47 ммоль) и Cs2CO3 (6,32 г; 19,41 ммоль) в 1,4-диоксане (80 мл). Смесь нагревали при 80°C в течение ночи. Раствор вливали в охлажденную воду, продукт экстрагировали ДХМ. Органический слой промывали рассолом, сушили над MgSO4, фильтровали и выпаривали досуха. Остаток кристаллизовали из ДИПЭ. Осадок отфильтровывали с получением остатка промежуточного соединения (2,02 г, содержащего 81% промежуточного соединения 59 согласно ЖХ/МС). 150 мг этого остатка очищали с помощью флеш-хроматографии на силикагеле (15-40 μм, 4 г, ДХМ/MeOH: 98/2). Фракции, содержащие продукт, собирали и выпаривали досуха, получив 62 мг промежуточного соединения 59. Тп=240°C (Kofler).
Получение промежуточного соединения 60:

Промежуточное соединение 60 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 3,5-диметоксианилина и промежуточного соединения 58 в качестве исходных соединений (выход: 85%). Тп=205°C (Kofler).
Пример A18:
Получение промежуточного соединения 61:

Промежуточное соединение 61 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 29, при использовании промежуточного соединения 59 в качестве исходного соединения (выход: 31%).
Получение промежуточного соединения 62:
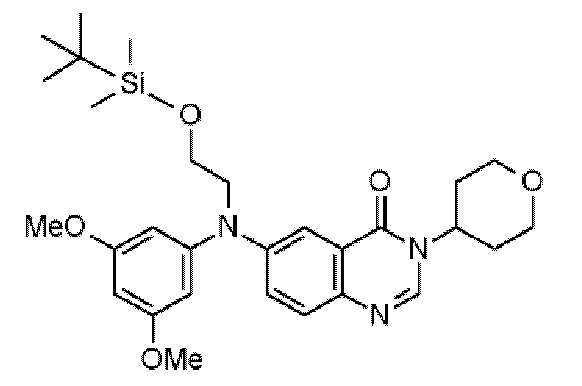
Промежуточное соединение 62 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 29, при использовании промежуточного соединения 60 в качестве исходного соединения (выход: 59%).
Получение промежуточного соединения 63:

Под N2 при 10°C гидрид натрия (60% в минеральном масле) (60 мг; 1,50 ммоль) добавляли к раствору промежуточного соединения 59 (200 мг; 0,50 ммоль) в ДМФА (12 мл). Раствор перемешивали при 10°C в течение 30 минут. Затем по каплям добавляли раствор (3-бромпропокси)-трет-бутилдиметилсилана (0,26 мл; 1,10 ммоль) в ДМФА (3 мл). Раствор перемешивали при 10°C в течение 5 часов. Раствор вливали в охлажденную воду, и продукт экстрагировали EtOAc. Органический слой промывали рассолом, сушили над MgSO4, фильтровали и выпаривали досуха. Остаток (367 мг) очищали с помощью флеш-хроматографии на силикагеле (15-40 μм, 12 г, ДХМ/MeOH: 99/1). Фракции, содержащие продукт, собирали и выпаривали досуха, получив 71 мг (26%) промежуточного соединения 63.
Получение промежуточного соединения 64:

Промежуточное соединение 64 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 49, при использовании промежуточного соединения 60 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Пример A20:
Получение промежуточного соединения 65:

Промежуточное соединение 65 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 63 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 66:

Промежуточное соединение 66 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 64 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Пример A21:
Получение промежуточного соединения 67:

Промежуточное соединение 67 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 65 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Получение промежуточного соединения 68:

Промежуточное соединение 68 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 24, при использовании соединения 66 в качестве исходного соединения. Это соединение использовали непосредственно в следующей стадии реакции без дополнительной очистки.
Пример A22:
Получение промежуточного соединения 69:
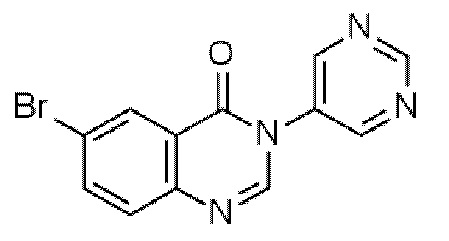
2-Амино-5-бромбензойную кислоту (19,8 г; 91,6 ммоль), растворяли в ксилоле (870 мл). Добавляли триэтилортоформиат (20,4 г; 137,5 ммоль) и нагревали смесь при 110°C в течение 2,5 часов. Реакцию охлаждали до комнатной температуры и добавляли 5-аминопиримидин (9,51 г; 100 ммоль). Смесь нагревали с обратным холодильником еще 48 часов. Полученную смесь охлаждали при комнатной температуре и выпаривали досуха. Остаток кристаллизовали из смеси метанола и 2-изопропоксипропана, и осадок отфильтровывали. Остаток очищали с помощью хроматографии на силикагеле (подвижная фаза: градиент от ДХМ/MeOH 100/1 до 50% ДХМ/50% MeOH). Фракции, содержащие продукт, собирали и выпаривали досуха, получив 6,1 г (22%) промежуточного соединения 69.
Получение промежуточного соединения 70:

Промежуточное соединение 70 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 2-фтор-3,5-диметоксианилина и промежуточного соединения 69 в качестве исходных соединений.
100 мг неочищенного промежуточного соединения 70 очищали м помощью флеш-хроматографии на силикагеле (15-40 μм, 4 г, ДХМ/MeOH: 98/2). Фракции, содержащие продукт, собирали и выпаривали досуха, получив 35 мг промежуточного соединения 70 (Тп=225°C (Kofler)).
Получение промежуточного соединения 72:

Промежуточное соединение 72 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 2, при использовании 2,6-дифтор-3,5-диметоксианилина и промежуточного соединения 69 в качестве исходных соединений (выход: 72%). Тп=187°C (Kofler).
Пример A23:
Получение промежуточного соединения 71:

Промежуточное соединение 71 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 29, при использовании промежуточного соединения 70 в качестве исходного соединения (выход: 35%).
Получение промежуточного соединения 73:

Промежуточное соединение 73 получали согласно методике, аналогичной описанной для синтеза промежуточного соединения 29, при использовании промежуточного соединения 72 в качестве исходного соединения (выход: 31%).
B. Получение конечных соединений
Пример B1:
Получение соединения 18:

При 10°C фторид тетрабутиламмония (13 мл; 43 ммоль) добавляли к раствору промежуточного соединения 23 (1,65 г; 3 ммоль) в ТГФ (50 мл) и перемешивали смесь при комнатной температуре в течение 8 часов. Раствор вливали в охлажденную воду, и продукт экстрагировали EtOAc. Органический слой сушили над MgSO4, фильтровали и выпаривали досуха. Остаток (1,3 г) очищали с помощью хроматографии на силикагеле (нерегулярный SiOH, 15-40 μм, 300 г, подвижная фаза: 97% ДХМ, 3% MeOH, 0,1% NH4OH). Фракции, содержащие продукт, собирали и выпаривали досуха. Остаток (0,43 г) кристаллизовали из смеси MeOH и Et2O. Осадок отфильтровывали и сушили с получением 0,394 г (30%) соединения 18 (Тп: 165°C (ДСК)).
Получение соединения 1:

Соединение 1 получали согласно методике, аналогичной описанной для синтеза соединения 18, при использовании промежуточного соединения 3 в качестве исходного соединения (выход: 34%; Тп: 169°C (ДСК)).
Получение соединения 5:

Соединение 5 получали согласно методике, аналогичной описанной для синтеза соединения 18, при использовании промежуточного соединения 6 в качестве исходного соединения (выход: 43%; Тп: 251°C (ДСК)).
Получение соединения 6:
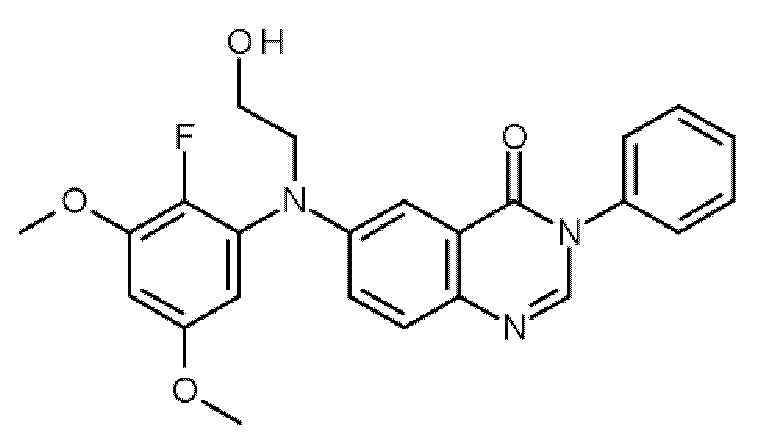
Соединение 6 получали согласно методике, аналогичной описанной для синтеза соединения 18, при использовании промежуточного соединения 8 в качестве исходного соединения (выход: 36%; Тп: 183°C (ДСК)).
Получение соединения 7:

Соединение 7 получали согласно методике, аналогичной описанной для синтеза соединения 18, при использовании промежуточного соединения 10 в качестве исходного соединения (выход: 20%; Тп: 171°C (ДСК)).
Получение соединения 8:

Соединение 8 получали согласно методике, аналогичной описанной для синтеза соединения 18, при использовании промежуточного соединения 14 в качестве исходного соединения (выход: 29%; Тп: 185°C (ДСК)).
Получение соединения 10:

Соединение 10 получали согласно методике, аналогичной описанной для синтеза соединения 18, при использовании промежуточного соединения 17 в качестве исходного соединения (выход: 55%; Тп: 223°C (ДСК)).
Получение соединения 16:
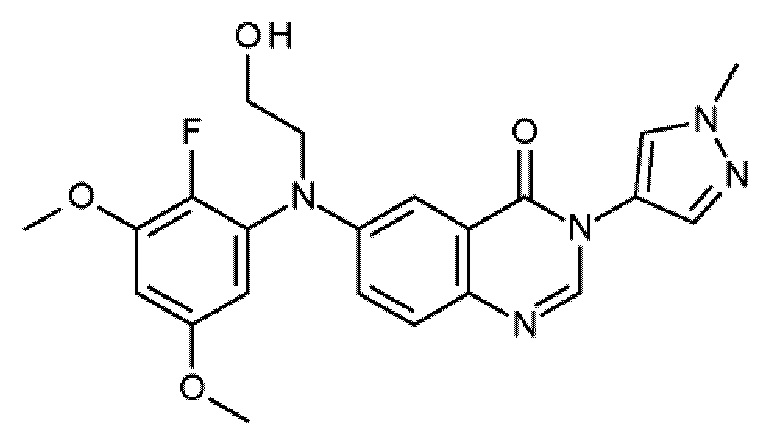
Соединение 16 получали согласно методике, аналогичной описанной для синтеза соединения 18, при использовании промежуточного соединения 20 в качестве исходного соединения (выход: 43%; тп: 164°C (ДСК)).
Получение соединения 25:

1M раствор фторида тетрабутиламмония в ТГФ (0,536 мл; 0,536 ммоль) при 5°C добавляли к раствору промежуточного соединения 29 (181 мг; 0,268 ммоль) в ТГФ и перемешивали реакционную смесь при комнатной температуре в течение 3 часов. Реакционную смесь разбавляли ДХМ и добавляли 10% водный раствор K2CO3. Органический слой фильтровали через Chromabond® и выпаривали досуха. Остаток очищали с помощью хроматографии на силикагеле (нерегулярный SiOH, 10 г; подвижная фаза: градиент от 0,2% NH4OH, 2% MeOH, 98% ДХМ до 0,4% NH4OH, 4% MeOH, 96% ДХМ). Фракции, содержащие продукт, собирали и выпаривали досуха с получением 148 мг (98%) соединения 25.
Получение соединения 26:

Соединение 26 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 30 в качестве исходного соединения (выход: 100%).
Получение соединения 56:

Соединение 56 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 48 в качестве исходного соединения (выход: 89%).
Получение соединения 29:
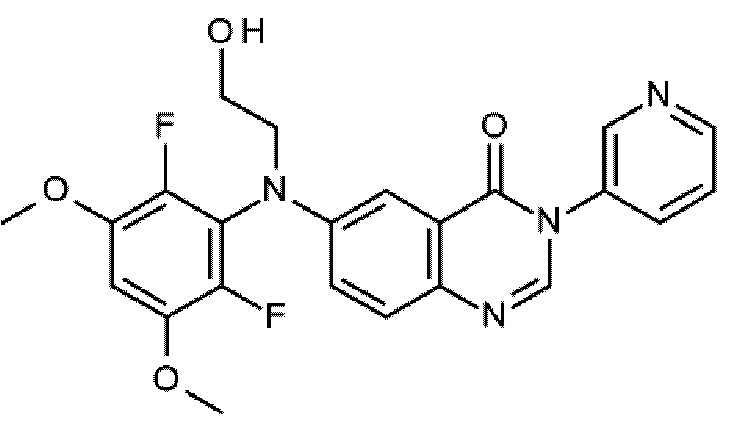
Соединение 29 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 35 в качестве исходного соединения (выход: 28%; Тп: 112°C (Kofler)).
Получение соединения 30:

Соединение 30 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 36 в качестве исходного соединения (выход: 39%; Тп: 186°C (Kofler)).
Получение соединения 31:

Соединение 31 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 37 в качестве исходного соединения (выход: 54%; Тп: 168°C (Kofler)).
Получение соединения 37:

Соединение 37 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 45 в качестве исходного соединения (выход: 37%; Тп: 198°C (Kofler)).
Получение соединения 38:

Соединение 38 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 46 в качестве исходного соединения (выход: 17%; Тп: 209°C (Kofler)).
Получение соединения 39:

Соединение 39 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 47 в качестве исходного соединения (выход: 18%; Тп: 177°C (Kofler)).
Получение соединения 63:
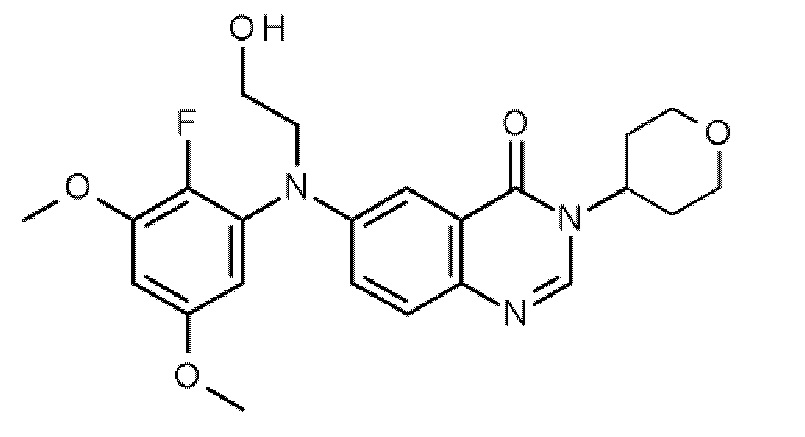
Соединение 63 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 61 в качестве исходного соединения. Очистка с помощью хроматографии на силикагеле (сферический немодифицированный силикагель 5 μм 150×30,0 мм, подвижная фаза: градиент от 0,2% NH4OH, 98% ДХМ, 2% MeOH до 0,8% NH4OH, 92% ДХМ, 8% MeOH). Чистые фракции собирали и выпаривали растворитель, получив 171 мг фракции А. Фракцию А очищали с помощью ахиральной СКЖХ (неподвижная фаза: CYANO 6 μм 150×21,2 мм, подвижная фаза: 70% CO2, 30% MeOH (0,3% iPrNH2). Фракции, содержащие продукт, собирали, и выпаривали растворитель, получив 124 мг фракции B. 18 мг этой фракции B промывали водой. Добавляли ДХМ и смесь фильтровали через фильтр для разделения фаз. Растворитель выпаривали с получением 8 мг соединения 63 (белое; Тп: 191°C (Kofler)).
Получение соединения 64:

Соединение 64 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 62 в качестве исходного соединения (выход: 88%; Тп: 204°C (Kofler)).
Получение соединения 74:
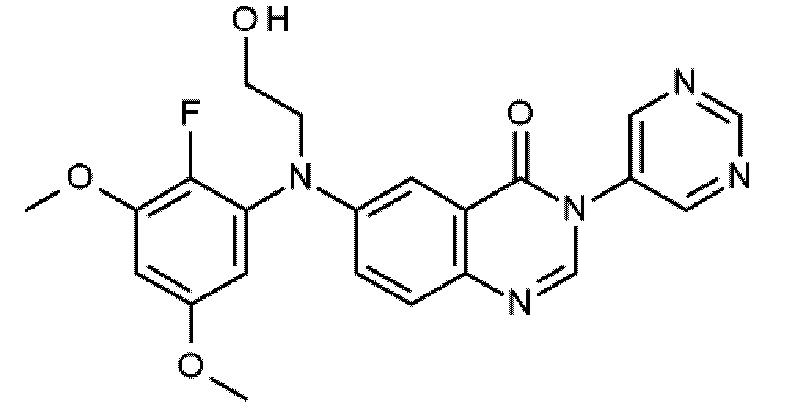
Соединение 74 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 71 в качестве исходного соединения (выход: 55%; Тп: 200°C (Kofler)).
Получение соединения 76:

Соединение 76 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 73 в качестве исходного соединения (выход: 86%; Тп: 178°C (Kofler)).
Пример B2:
Получение соединения 19:

Смесь промежуточного соединения 24 (0,37 г; 0,7 ммоль) и изопропиламина (1,8 мл; 20,5 ммоль) в ацетонитриле (10 мл) нагревали при 100°C в течение ночи в автоклаве. Раствор вливали в охлажденную воду, и продукт экстрагировали EtOAc. Органический слой сушили над MgSO4, фильтровали и выпаривали досуха. Остаток (0,68 г) очищали с помощью хроматографии на силикагеле (сферический силикагель, 5 μм, 150×30,0 мм, подвижная фаза: градиент от 0,2% NH4OH, 98% ДХМ, 2% MeOH до 0,8% NH4OH, 92% ДХМ, 8% MeOH). Фракции, содержащие продукт, собирали и выпаривали досуха. Остаток (0,26 г) кристаллизовали из смеси MeOH и Et2O. Осадок отфильтровывали и сушили с получением 0,190 г (56%) соединения 19 (Тп: 162°C (ДСК)).
Получение соединения 2:

Соединение 2 получали согласно методике, аналогичной описанной для синтеза соединения 19, при использовании промежуточного соединения 4 в качестве исходного соединения (выход: 33%; Тп: 124°C (ДСК)).
Получение соединения 9:

Соединение 9 получали согласно методике, аналогичной описанной для синтеза соединения 19, при использовании промежуточного соединения 15 в качестве исходного соединения (выход: 28%; Тп: 142°C (ДСК)).
Получение соединения 11:
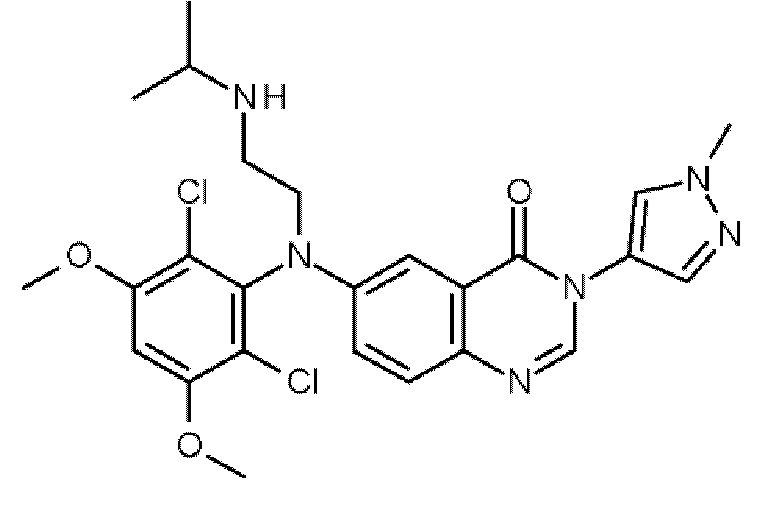
Соединение 11 получали согласно методике, аналогичной описанной для синтеза соединения 19, при использовании промежуточного соединения 18 в качестве исходного соединения (выход: 42%; Тп: 195°C (ДСК)).
Получение соединения 17:

Соединение 17 получали согласно методике, аналогичной описанной для синтеза соединения 19, при использовании промежуточного соединения 21 в качестве исходного соединения (выход: 64%; Тп: 132°C (ДСК)).
Получение соединения 32:

Соединение 32 получали согласно методике, аналогичной описанной для синтеза соединения 19, при использовании промежуточного соединения 38 в качестве исходного соединения (выход: 64%; Тп: 124°C (Kofler)).
Получение соединения 33:

Соединение 33 получали согласно методике, аналогичной описанной для синтеза соединения 19, при использовании промежуточного соединения 39 в качестве исходного соединения (выход: 44%; Тп: 133°C (Kofler)).
Получение соединения 34:

Соединение 34 получали согласно методике, аналогичной описанной для синтеза соединения 19, при использовании промежуточного соединения 40 в качестве исходного соединения (выход: 16%; Тп: 136°C (Kofler)).
Пример B3:
Получение соединения 20:

Смесь промежуточного соединения 24 (0,79 г; 1,48 ммоль) и метиламина (30 мл 2 М раствора в ТГФ; 59 ммоль) нагревали в автоклаве при 70°C в течение ночи. Раствор вливали в охлажденную воду, и продукт экстрагировали EtOAc. Органический слой сушили над MgSO4, фильтровали и выпаривали досуха. Остаток (0,54 г) очищали с помощью хроматографии на силикагеле (нерегулярный SiOH, 15-40 μм, 30 г, подвижная фаза: 0,1% NH4OH, 95% ДХМ, 5% MeOH). Фракции, содержащие продукт, собирали и выпаривали досуха. Остаток (0,19 г) кристаллизовали из смеси ACN и Et2O. Осадок отфильтровывали и сушили с получением 0,094 г (14%) соединения 20 (Тп: 141°C (ДСК)).
Получение соединения 57:

Смесь промежуточного соединения 52 (194 мг; 0,304 ммоль), метиламина (6 мл 2 М раствора в ТГФ; 12 ммоль) нагревали при 70°C в течение 18 часов в закрытой пробирке. Реакционную смесь выпаривали досуха. К раствору остатка в ДХМ (5 мл) при 5°C по каплям добавляли трифторуксусную кислоту (0,5 мл; 6,534 ммоль). Реакционную смесь оставляли медленно нагреваться до комнатной температуры и перемешивали в течение 18 часов. Реакционную смесь разбавляли ДХМ и добавляли 10% водный раствор K2CO3. Органический слой фильтровали через фильтр для разделения фаз и выпаривали досуха. Остаток очищали с помощью хроматографии на силикагеле (нерегулярный SiOH, 40 г; подвижная фаза: 1% NH4OH, 89% ДХМ, 10% MeOH). Фракции, содержащие продукт, собирали и выпаривали досуха. Остаток кристаллизовали из ДИПЭ, осадок отфильтровывали и сушили с получением 48 мг (33%) соединения 57 (Тп: смола 90°C (Kofler)).
Получение соединения 58:

Соединение 58 получали согласно методике, аналогичной описанной для синтеза соединения 57, при использовании промежуточного соединения 53 в качестве исходного соединения (выход: 41%; Тп: 176°C (Kofler)).
Получение соединения 59:

Соединение 59 получали согласно методике, аналогичной описанной для синтеза соединения 57, при использовании промежуточного соединения 54 в качестве исходного соединения (выход: 35%; Тп: 139°C (Kofler)).
Получение соединения 70:

Соединение 70 получали согласно методике, аналогичной описанной для синтеза соединения 20, при использовании промежуточного соединения 65 в качестве исходного соединения (выход: 18%, Тп=178°C (kofler)).
Получение соединения 71:

Соединение 71 получали согласно методике, аналогичной описанной для синтеза соединения 20, при использовании промежуточного соединения 66 в качестве исходного соединения (выход: 79%, Тп: 135°C (Kofler)).
Пример B4:
Получение соединения 21:

Под N2 при 10°C гидрид натрия (60% в минеральном масле) (0,29 г; 7,3 ммоль) добавляли к раствору промежуточного соединения 22 (1 г; 2,4 ммоль) в ДМФА (8 мл). Раствор перемешивали при 10°C в течение 30 минут. Затем по каплям добавляли раствор 2-(хлорметил)-N,N-диметил-1H-имидазол-сульфонамида (1 г; 4,9 ммоль) в ДМФА (3 мл) и реакционную смесь оставляли нагреваться до комнатной температуры в течение 5 часов. Раствор вливали в охлажденную воду, и продукт экстрагировали EtOAc. Органический слой промывали водой, сушили над MgSO4, фильтровали и выпаривали досуха с получением 1,8 г (количественный выход) соединения 21.
Получение соединения 3:

Соединение 3 получали согласно методике, аналогичной описанной для синтеза соединения 21, при использовании промежуточного соединения 2 в качестве исходного соединения (выход: 15%).
Получение соединения 12:

Соединение 12 получали согласно методике, аналогичной описанной для синтеза соединения 21, при использовании промежуточного соединения 16 в качестве исходного соединения (количественный выход).
Получение соединения 14:
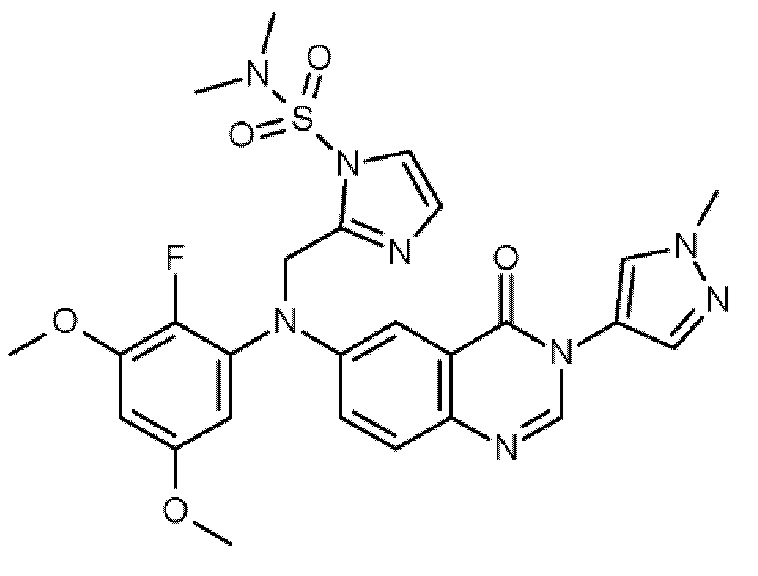
Соединение 14 получали согласно методике, аналогичной описанной для синтеза соединения 21, при использовании промежуточного соединения 19 в качестве исходного соединения (количественный выход).
Получение соединения 27:

Под N2 при -30°C гидрид натрия (60% в минеральном масле) (125 мг; 3,121 ммоль) добавляли к раствору промежуточного соединения 27 (500 мг; 1,04 ммоль) в ДМФА (15 мл). Реакционную смесь перемешивали при -10°C в течение 30 минут. Затем по каплям добавляли раствор 2-(хлорметил)-N,N-диметил-1H-имидазол-сульфонамида (512 мг; 2,289 ммоль) в ДМФА (5 мл). Реакционную смесь перемешивали при температуре ниже -10°C в течение 1 часа, затем 1 час при 0°C и позволяли нагреться до комнатной температуры (более 1 часа). Раствор вливали в воду со льдом, и продукт экстрагировали EtOAc. Органический слой промывали рассолом, сушили над MgSO4, фильтровали и выпаривали досуха. Остаток очищали с помощью хроматографии на силикагеле (нерегулярный SiOH, 30 г, 30 μм; подвижная фаза: градиент от 100% ДХМ до 0,2% NH4OH, 2% MeOH, 98% ДХМ). Фракции, содержащие продукт, собирали и выпаривали досуха с получением 325 мг (47%) соединения 27. Тп: смола, 100°C (Kofler).
Получение соединения 28:

Соединение 28 получали согласно методике, аналогичной описанной для синтеза соединения 27, при использовании промежуточного соединения 28 в качестве исходного соединения (выход: 73%; Тп: смола, 90°C (Kofler)).
Получение соединения 42:

Соединение 42 получали согласно методике, аналогичной описанной для синтеза соединения 27, при использовании промежуточного соединения 26 в качестве исходного соединения (выход: 52%; Тп: 168°C (Kofler)).
Получение соединения 35:

Соединение 35 получали согласно методике, аналогичной описанной для синтеза соединения 21, при использовании промежуточного соединения 32 в качестве исходного соединения (выход: 9%; Тп: 128°C (Kofler)).
Получение соединения 36:

Соединение 36 получали согласно методике, аналогичной описанной для синтеза соединения 21, при использовании промежуточного соединения 33 в качестве исходного соединения (выход: 11%; Тп: 108°C (Kofler)).
Получение соединения 40:

Соединение 40 получали согласно методике, аналогичной описанной для синтеза соединения 21, при использовании промежуточного соединения 42 в качестве исходного соединения (выход: 16%; Тп: 139°C (Kofler)).
Получение соединения 41:

Соединение 41 получали согласно методике, аналогичной описанной для синтеза соединения 21, при использовании промежуточного соединения 43 в качестве исходного соединения (выход: 13%; Тп: смола при 109°C (Kofler)).
Получение соединения 67:

Соединение 67 получали согласно методике, аналогичной описанной для синтеза соединения 27, при использовании промежуточного соединения 59 в качестве исходного соединения (выход: 11%; Тп: 189°C (Kofler)).
Получение соединения 68:

Соединение 68 получали согласно методике, аналогичной описанной для синтеза соединения 27, при использовании промежуточного соединения 60 в качестве исходного соединения. Очистка с помощью хроматографии на силикагеле (нерегулярный 20-45 μм 450 г SiOH, подвижная фаза: 40% гептан, 10% MeOH (+10% NH4OH), 50% EtOAc) дала 2 фракции соединения 68: 430 мг (26%, Тп: 182°C (Kofler)) и 910 мг (57%).
Пример B5:
Получение соединения 24:

Промежуточное соединение 11 (0,2 г; 0,66 ммоль), 3,5-диметоксифенил-бороновую кислоту (0,18 г; 0,98 ммоль), трициклогексилфосфин (0,018 г; 0,065 ммоль), ацетат палладия (II) (47% Pd) (0,015 г; 0,065 ммоль) и триэтиламин (0,183 мл; 1,31 ммоль) в толуоле (10 мл) перемешивали под монооксидом углерода (10 бар) при 100°C в течение 18 часов в автоклаве. Раствор охлаждали, вливали в охлажденную воду и добавляли EtOAc. Раствор фильтровали через слой Celite®. Фильтрат экстрагировали EtOAc, и органический слой промывали водой, сушили над MgSO4 и выпаривали досуха. Остаток (344 г) очищали с помощью хроматографии на силикагеле (сферический силикагель, 5 μм, 150×30,0 мм, подвижная фаза: градиент от 71% гептана, 1% MeOH (+10% NH4OH), 28% EtOAc до 0% гептана, 20% MeOH (+10% NH4OH), 80% EtOAc). Фракции, содержащие продукт, собирали и выпаривали досуха. Полученный остаток (56 мг) кристаллизовали из Et2O. Осадок отфильтровывали и сушили с получением 43 мг (17%) соединения 24 (Тп: 194°C (Kofler)).
Получение соединения 23:

Соединение 23 получали согласно методике, аналогичной описанной для синтеза соединения 24, при использовании промежуточного соединения 11 и 3-метоксифенил-бороновой кислоты в качестве исходных соединений (выход: 11%).
Пример B6:
Получение соединения 46:

Трифторуксусную кислоту (34 μл; 4,445 ммоль) при 5°C по каплям добавляли к раствору промежуточного соединения 29 (150 мг; 0,222 ммоль) в ДХМ (5 мл). Реакционную смесь оставляли медленно нагреваться до комнатной температуры и перемешивали в течение 48 часов. Реакционную смесь разбавляли ДХМ и добавляли 10% водный раствор K2CO3. Органический слой фильтровали через фильтр для разделения фаз и выпаривали досуха. Остаток очищали с помощью хроматографии на силикагеле (сферический немодифицированный силикагель 5 μм 150×30,0 мм; подвижная фаза: градиент от 0,4% NH4OH, 96% ДХМ, 4% MeOH до 1,7% NH4OH, 83% ДХМ, 17% MeOH). Фракции, содержащие продукт, собирали и выпаривали досуха с получением 40 мг соединения 46 (39%; Тп: 186°C (Kofler)).
Получение соединения 47:

Соединение 47 получали согласно методике, аналогичной описанной для синтеза соединения 46, при использовании промежуточного соединения 48 в качестве исходного соединения (выход: 14%; Тп: 165°C (Kofler)).
Получение соединения 48:
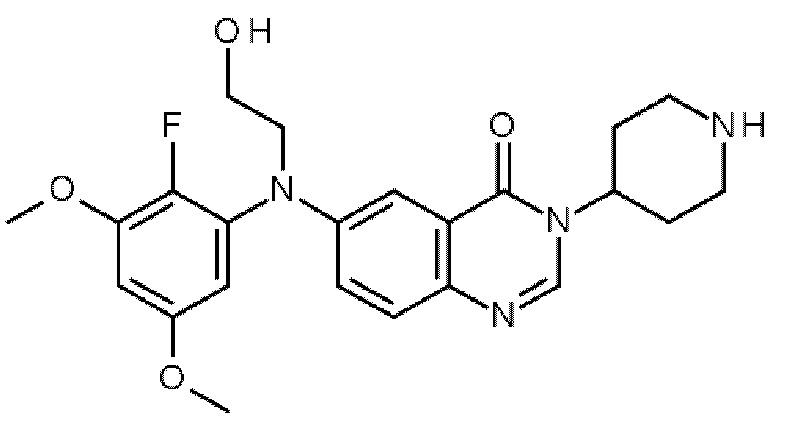
Соединение 48 получали согласно методике, аналогичной описанной для синтеза соединения 46, при использовании промежуточного соединения 30 в качестве исходного соединения (выход: 53%; Тп: 173°C (Kofler)).
Пример B7:
Получение соединения 50:

Соединение 50 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 49 в качестве исходного соединения (выход: 81%).
Получение соединения 51:

Соединение 51 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 50 в качестве исходного соединения (выход: 100%).
Получение соединения 52:

Соединение 52 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 51 в качестве исходного соединения (выход: 100%).
Получение соединения 65:

Соединение 65 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 63 в качестве исходного соединения (выход: 47%, Тп: 164°C (Kofler)).
Получение соединения 66:
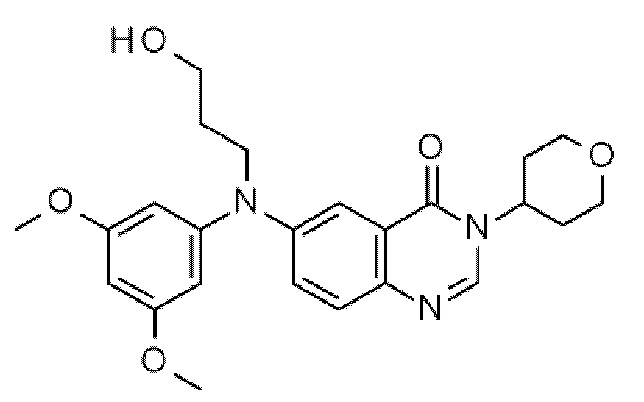
Соединение 66 получали согласно методике, аналогичной описанной для синтеза соединения 25, при использовании промежуточного соединения 64 в качестве исходного соединения (выход: 68%). Очистка с помощью хроматографии на силикагеле (нерегулярный SiOH 15-40 μм 300 г MERCK, подвижная фаза: 43% гептан, 7% MeOH (+10% NH4OH), 50% EtOAc) дала 2 фракции соединения 66: 228 мг (39%; Тп: 178°C (Kofler) и 162 мг (28%).
Получение соединения 53:

Соединение 53 получали согласно методике, аналогичной описанной для синтеза соединения 46, при использовании промежуточного соединения 49 в качестве исходного соединения (выход: 36%, Тп: 184°C (Kofler)).
Получение соединения 54:

Соединение 54 получали согласно методике, аналогичной описанной для синтеза соединения 46, при использовании промежуточного соединения 50 в качестве исходного соединения (выход: 53%, тп: 167°C (Kofler)).
Получение соединения 55:

Соединение 55 получали согласно методике, аналогичной описанной для синтеза соединения 46, при использовании промежуточного соединения 51 в качестве исходного соединения (выход: 34%, Тп: 167°C (Kofler)).
Пример B9:
Получение соединения 60:
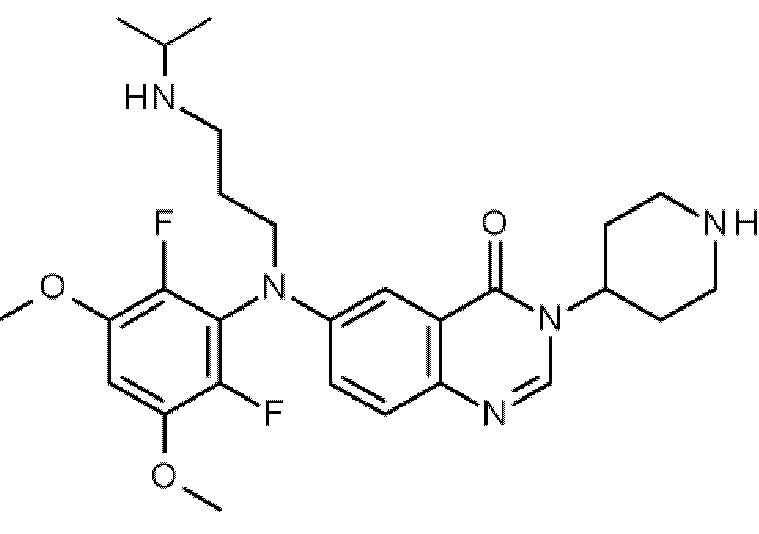
Смесь промежуточного соединения 55 (150 мг; 0,23 ммоль) и изопропиламина (0,6 мл; 6,9 ммоль) в ацетонитриле (6 мл) нагревали при 100°C в течение 2 часов в закрытой пробирке. Реакционную смесь выпаривали досуха. К раствору предыдущего остатка (140 мг) в ДХМ (10 мл) при 5°C по каплям добавляли трифторуксусную кислоту (1 мл; 13,07 ммоль). Реакционную смесь оставляли медленно нагреваться до комнатной температуры и перемешивали в течение 18 часов. Реакционную смесь разбавляли ДХМ и добавляли 10% водный раствор K2CO3. Органический слой фильтровали через фильтр для разделения фаз и выпаривали досуха. Остаток очищали с помощью хроматографии на силикагеле (нерегулярный SiOH, 40 г; подвижная фаза: 1% NH4OH, 89% ДХМ, 10% MeOH). Фракции, содержащие продукт, собирали и выпаривали досуха. Остаток (87 мг; 73%) кристаллизовали из ACN, осадок отфильтровывали и сушили с получением 22 мг (18%) соединения 60 (Тп: 126°C (Kofler)).
Получение соединения 61:

соединения 61'
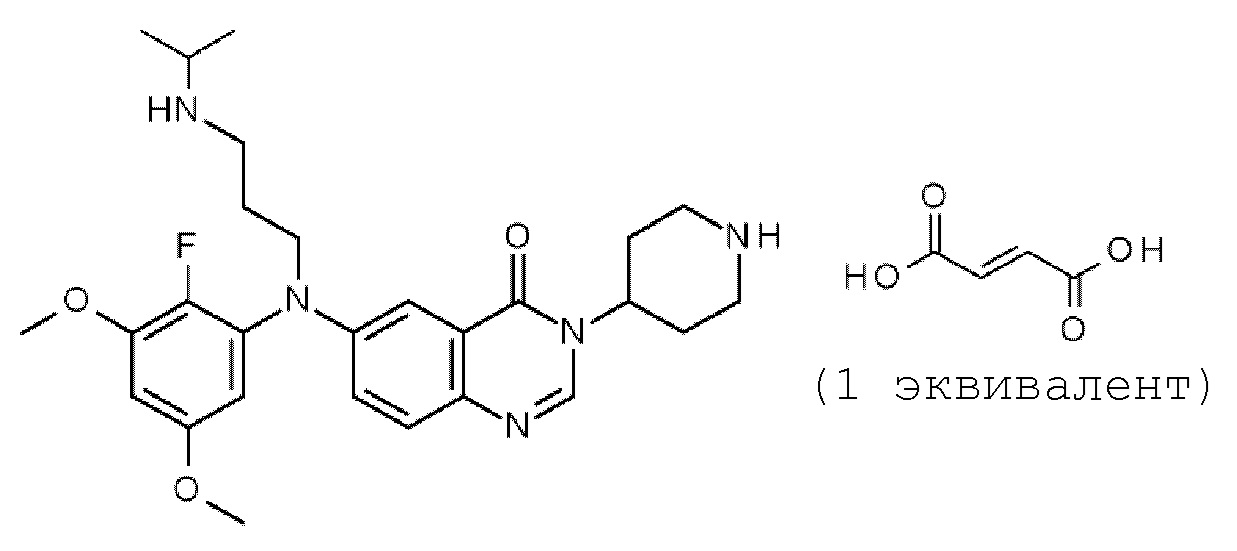
Соединение 61 получали согласно методике, аналогичной описанной для синтеза соединения 60, при использовании промежуточного соединения 56 в качестве исходного соединения (выход: 41%). Соединение 61 (97 мг; 0,19 ммоль) растворяли в ACN и добавляли фумаровую кислоту (23 мг; 0,195 ммоль). Продукт кристаллизовали из ACN. Осадок отфильтровывали и сушили с получением 104 мг (36%) соединения 61' (Тп: 140°C (смола, Kofler)).
Получение соединения 62:
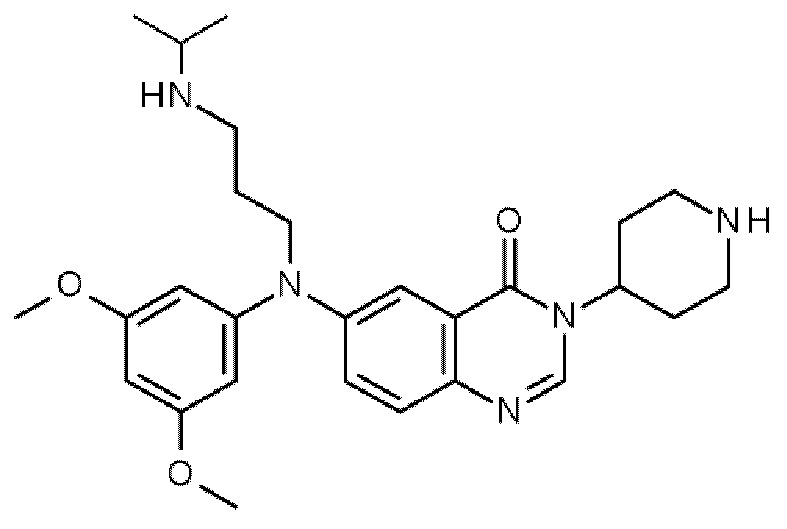
соединения 62'

Соединение 62 получали согласно методике, аналогичной описанной для синтеза соединения 60, при использовании промежуточного соединения 57 в качестве исходного соединения (выход: 63%). Соединение 62 (170 мг; 0,35 ммоль) растворяли в ACN и добавляли фумаровую кислоту (41 мг; 0,354 ммоль). Продукт кристаллизовали из ACN/EtOH. Осадок отфильтровывали и сушили с получением 180 мг (54%) соединения 62' (Тп: 255°C (Kofler)).
Получение соединения 72:
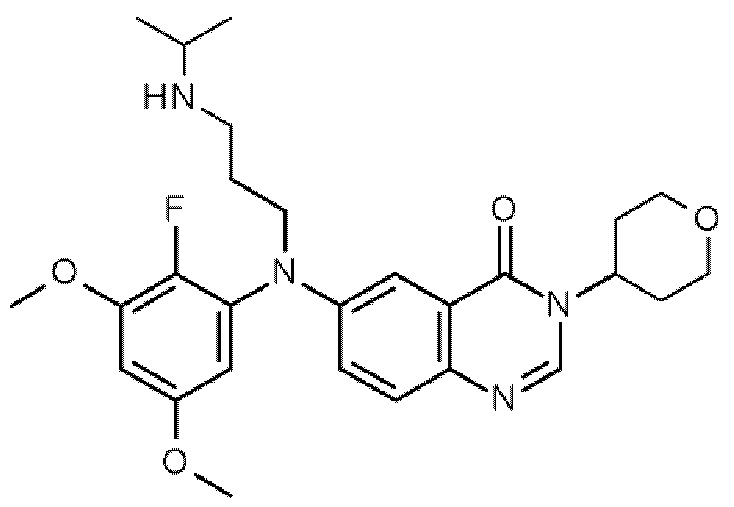
Соединение 72 получали согласно методике, аналогичной описанной для синтеза соединения 19, при использовании промежуточного соединения 67 в качестве исходного соединения (выход: 40%; Тп: смола, 80°C (Kofler)).
Получение соединения 73:


Соединение 73 получали согласно методике, аналогичной описанной для синтеза соединения 19, при использовании промежуточного соединения 68 в качестве исходного соединения (выход: 75%). Фумаровую кислоту (41 мг; 0,35 ммоль) добавляли к раствору соединения 73 (171 мг; 0,35 ммоль) в ацетоне (1 мл). Смесь перемешивали при кт в течение 2 часов. Осадок отфильтровывали, промывали небольшим количеством ацетона и сушили, получив 186 мг (48%) соединения 73' (Тп: 240°C (Kofler)).
Превращение C1:
Получение соединения 22:

Смесь соединения 21 (1,45 г; 2 ммоль) в 6 Н HCl (2,8 мл) и диоксане (10 мл) нагревали при 100°C в течение 2 часов. Раствор охлаждали до комнатной температуры, вливали в охлажденную воду, подщелачивали NH4OH и экстрагировали продукт EtOAc. Органический слой сушили над MgSO4, фильтровали и выпаривали досуха. Остаток (1,22 г) очищали с помощью хроматографии на силикагеле (нерегулярный SiOH, 15-40 μм, 40 г, подвижная фаза: 96% ДХМ, 4% MeOH, 0,1% NH4OH). Фракции, содержащие продукт, собирали и выпаривали досуха. Остаток (0,6 г) снова очищали с помощью хроматографии (нерегулярный SiOH, 15-40 μм, 40 г, подвижная фаза: 95% ДХМ, 5% MeOH, 0,5% NH4OH). Фракции, содержащие продукт, собирали и выпаривали досуха. Полученный остаток (0,4 г) очищали с помощью ахиральной СКЖХ (неподвижная фаза: 2-этилпиридин, 6 μм 150×21,2 мм), подвижная фаза: 80% CO2, 20% MeOH (0,3% iPrNH2)). Фракции, содержащие продукт, собирали и выпаривали досуха. Остаток (0,206 г) кристаллизовали из смеси ACN и Et2O. Осадок отфильтровывали и сушили с получением 0,17 г (17%) соединения 22 (Тп: 231°C (ДСК)).
Получение соединения 4:

Соединение 4 получали согласно методике, аналогичной описанной для синтеза соединения 22, при использовании соединения 3 в качестве исходного соединения (выход: 46%).
Получение соединения 13:

Соединение 13 получали согласно методике, аналогичной описанной для синтеза соединения 22, при использовании соединения 12 в качестве исходного соединения (выход: 20%).
Получение соединения 15:

Соединение 15 получали согласно методике, аналогичной описанной для синтеза соединения 22, при использовании соединения 14 в качестве исходного соединения (выход: 22%) Тп: 212°C (ДСК)).
Получение соединения 43:

Соединение 43 получали согласно методике, аналогичной описанной для синтеза соединения 22, при использовании соединения 42 в качестве исходного соединения (выход: 38%, Тп: 223°C (Kofler)).
Получение соединения 44:

Соединение 44 получали согласно методике, аналогичной описанной для синтеза соединения 22, при использовании соединения 27 в качестве исходного соединения (выход: 42%, Тп: 220°C (Kofler)).
Получение соединения 45:

Соединение 45 получали согласно методике, аналогичной описанной для синтеза соединения 22, при использовании соединения 28 в качестве исходного соединения (выход: 59%, Тп: 260°C (Kofler)).
Получение соединения 69:

Соединение 69 получали согласно методике, аналогичной описанной для синтеза соединения 22, при использовании соединения 68 в качестве исходного соединения (выход: 82%, Тп: 260°C (Kofler)).
Получение соединения 75:
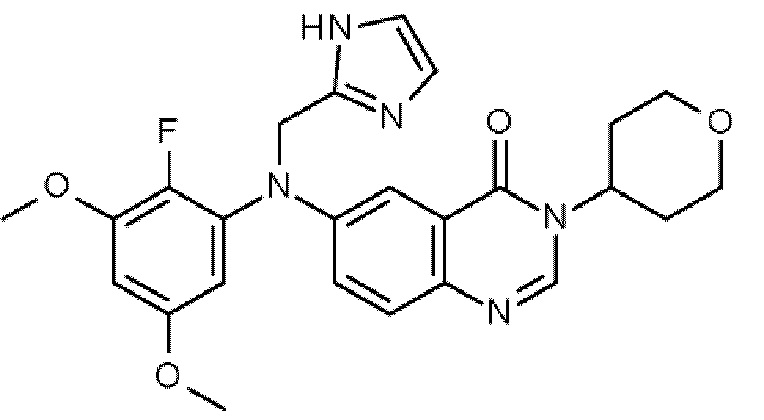
Соединение 75 получали согласно методике, аналогичной описанной для синтеза соединения 22, при использовании соединения 67 в качестве исходного соединения (выход: 37%, Тп: >260°C (Kofler)).
Превращение C2:
Получение соединения 49:

Смесь соединения 24 и (трифенилфосфоранилиден)ацетонитрила в толуоле нагревали с обратным холодильником в течение выходных. Реакционную смесь охлаждали до комнатной температуры, вливали в 10% водный раствор K2CO3 и экстрагировали EtOAc/MeOH. Органический слой отбирали, сушили над MgSO4, фильтровали и выпаривали досуха. Остаток очищали с помощью хроматографии на силикагеле (нерегулярный SiOH, 15-40 μм, 40 г; подвижная фаза: 42% гептан, 8% MeOH (+10% NH4OH), 50% EtOAc). Фракции, содержащие продукт, собирали и выпаривали досуха с получением остатка промежуточного соединения (22 мг), которое собирали в Et2O. Осадок отфильтровывали и сушили с получением 16 мг соединения 49 (8%, Тп: 217°C (Kofler)).
Аналитическая часть
Измерение ЖХ проводили при использовании системы UPLC (сверхэффективной жидкостной хроматографии) Acquity (Waters), включающей двухканальный насос с дегазатором, автосамплер, детектор на диодной матрице (DAD) и колонку, как указано в соответствующих способах ниже, температуру колонки поддерживали на уровне 40°С. Поток с колонки отводили на МС-детектор. МС-детектор был снабжен источником электрораспылительной ионизации. Напряжение на игле капилляра составляло 3 кВ, температуру источника поддерживали на уровне 130°С на Quattro (тройной квадрупольный масс-спектрометр производства Waters). В качестве газа в распылительном устройстве использовали азот. Регистрацию данных осуществляли с помощью системы Waters-Micromass MassLynx-Openlynx.
Обращенно-фазовую UPLC проводили на колонке С18 (1,7 μМ, 2,1×100 мм) Waters Acquity BEH (с гибридным мостиковым этилсилоксаном/силикагелем) со скоростью потока 0,343 мл/мин. Две подвижные фазы (подвижная фаза A: 95% 7 мМ ацетат аммония/5% ацетонитрил; подвижная фаза B: 100% ацетонитрил) использовали для создания условий градиента от 84,2% A и 15,8% B (удерживали в течение 0,49 минуты) до 10,5% A и 89,5% B за 2,18 минуты, удерживали в течение 1,94 мин и возвращались к исходным условиям за 0,73 мин, удерживали в течение 0,73 минут. Использовали вводимый объем 2 μл. Напряжение на конусе составляло 20 В для режима положительной и отрицательной ионизации. Масс-спектры получали при сканировании от 100 до 1000 за 0,2 секунды, используя задержку между каналами 0,1 секунды.
Температура плавления
Для ряда соединений значения температуры плавления (Тп) определяли с помощью DSC1 (Mettler-Toledo). Температуры плавления измеряли с температурным градиентом 10°C/минута. Максимальная температура составляла 350°C. Значения являются пиковыми значениями.
Для ряда соединений значения температуры плавления получали при использовании нагревательного столика Кофлера, состоящего из термостолика с линейным температурным градиентом, скользящего движка-указателя и температурной шкалы в градусах Цельсия.
ЯМР
Эксперименты ЯМР выполняли с использованием спектрометра Bruker Avance 500 III, при использовании внутренней дейтериевой стабилизации, снабженного реверсивной измерительной головкой для детектирования тройного резонанса (1H,13C,15N TXI). Химические сдвиги (δ) указаны в миллионных долях (м.д.)
Таблица: Н.с. означает номер соединения; Время удержания (Rt) указано в минутах; Тп означает температуру плавления (°C); разл. означает разложение; n.d. означает не определено.






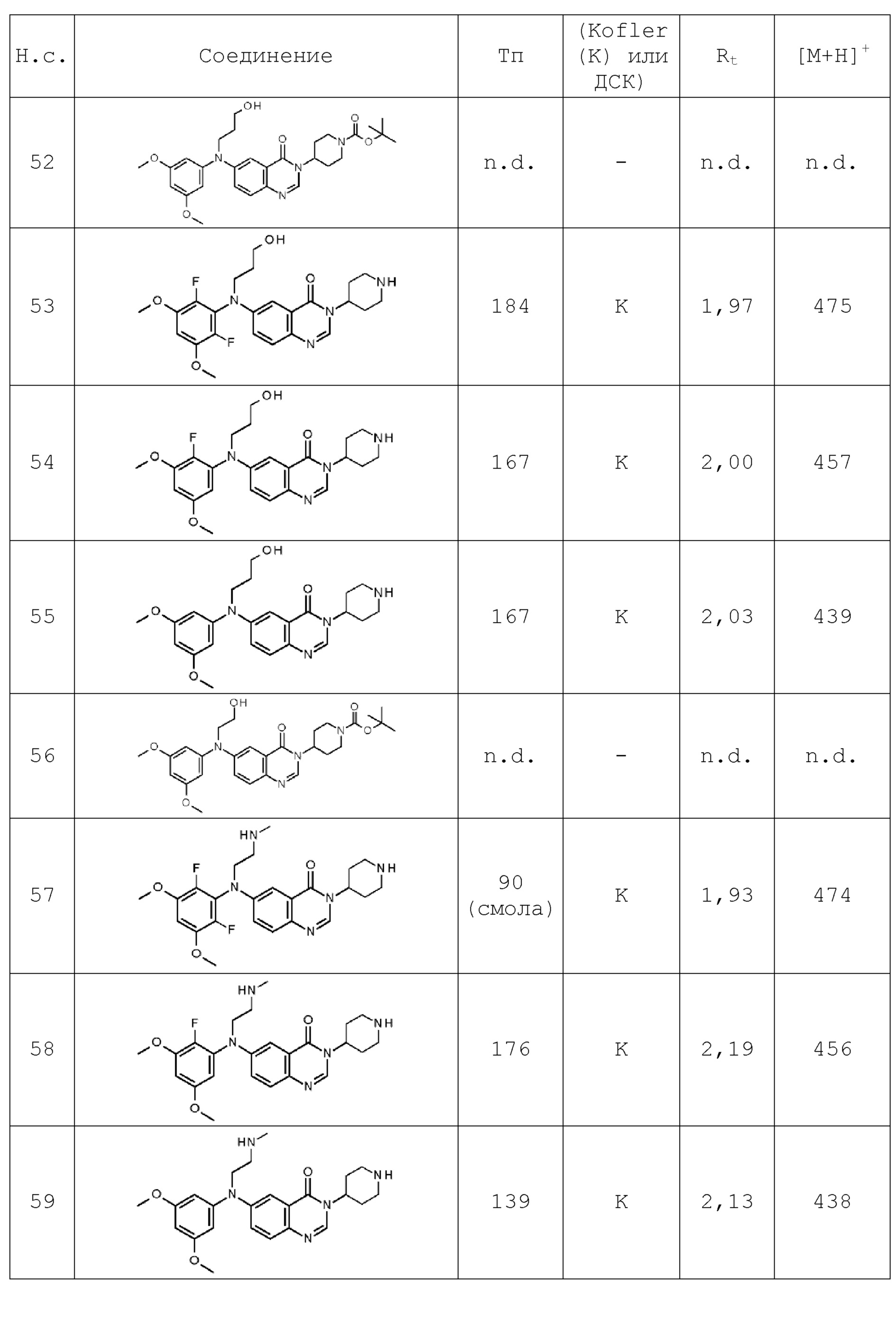




Соединение 19
1H-ЯМР (500 МГц, ДМСО-d6) δ 8,24 (с, 1H), 8,20 (с, 1H), 7,81 (с, 1H), 7,59 (д, J=9,1 Гц, 1H), 7,26 (д, J=2,8 Гц, 1H), 7,20 (дд, J=2,8, 9,1 Гц, 1H), 7,07 (т, J=8,0 Гц, 1H), 3,91 (с, 6H), 3,89 (с, 3H), 3,73 (т, J=7,2 Гц, 2H), 2,73 (т, J=7,2 Гц, 2H), 2,69-2,62 (м, 1H), 1,58 (ш. с., 1H), 0,92 (д, J=6,0 Гц, 6H).
Соединение 20
1H-ЯМР (500 МГц, ДМСО-d6) δ 8,24 (с, 1H), 8,20 (с, 1H), 7,81 (с, 1H), 7,59 (д, J=8,8 Гц, 1H), 7,26 (д, J=2,8 Гц, 1H), 7,21 (дд, J=2,8, 8,8 Гц, 1H), 7,08 (т, J=8,2 Гц, 1H), 3,92 (с, 6H), 3,89 (с, 3H), 3,75 (т, J=7,2 Гц, 2H), 2,71 (т, J=7,2 Гц, 2H), 2,34-2,21 (м, 4H).
Соединение 22
1H-ЯМР (500 МГц, ДМСО-d6) δ 11,87 (ш. с., 1H), 8,25 (с, 1H), 8,20 (с, 1H), 7,81 (с, 1H), 7,60 (д, J=8,8 Гц, 1H), 7,51 (дд, J=2,8, 8,8 Гц, 1H), 7,44 (д, J=2,8 Гц, 1H), 7,04 (т, J=8,0 гц, 1H), 7,00 (с, 1H), 6,81 (с, 1H), 4,85 (с, 2H), 3,89 (с, 9H).
Фармакологическая часть
Биологические исследования A
FGFR1 (ферментный анализ)
В конечном реакционном объеме 30 μл, FGFR1 (ч) (25 нг/мл) инкубировали с 50 мМ HEPES pH 7,5, 6 мМ MnCl2, 1 мМ DTT, 0,1 мМ Na3VO4, 0,01% Triton X-100, 500 нМ Btn-Flt3 и 5 μМ АТФ в присутствии соединения (конечная концентрация ДМСО 1%). После инкубирования в течение 60 минут при комнатной температуре, реакцию останавливали смесью 2,27 нМ EU-анти P-Tyr, 7 мМ ЭДТА, 31,25 нМ SA-XL-665 и 0,02% БСА, что продолжалось в течение 60 минут при комнатной температуре. После этого измеряли сигнал резонансного переноса энергии флуоресценции с временным разрешением (TR-FRET) (возбуждение 340 нм, эмиссия 620 нм, эмиссия 655 нм), и результаты выражали в RFU (относительных единицах флуоресценции). В данном анализе определяли ингибиторный эффект различных концентраций соединения (диапазон от 10 μМ до 0,1 нМ), и данные использовали для расчета значений IC50 (M) и pIC50 (-logIC50).
FGFR2 (ферментный анализ)
В конечном реакционном объеме 30 μл, FGFR2 (ч) (150 нг/мл) инкубировали с 50 мМ HEPES pH 7,5, 6 мМ MnCl2, 1 мМ DTT, 0,1 мМ Na3VO4, 0,01% Triton X-100, 500 нМ Btn-Flt3 и 0,4 μМ АТФ в присутствии соединения (конечная концентрация ДМСО 1%). После инкубирования в течение 60 минут при комнатной температуре, реакцию останавливали смесью 2,27 нМ EU-анти P-Tyr, 7 мМ ЭДТА, 31,25 нМ SA-XL-665 и 0,02% БСА, что продолжалось в течение 60 минут при комнатной температуре. После этого измеряли сигнал резонансного переноса энергии флуоресценции с временным разрешением (TR-FRET) (возбуждение 340 нм, эмиссия 620 нм, эмиссия 655 нм), и результаты выражали в RFU (относительных единицах флуоресценции). В данном анализе определяли ингибиторный эффект различных концентраций соединения (диапазон от 10 μМ до 0,1 нМ), и данные использовали для расчета значений IC50 (M) и pIC50 (-logIC50).
FGFR3 (ферментный анализ)
В конечном реакционном объеме 30 μл, FGFR3 (ч) (40 нг/мл) инкубировали с 50 мМ HEPES pH 7,5, 6 мМ MnCl2, 1 мМ DTT, 0,1 мМ Na3VО4, 0,01% Triton X-100, 500 нМ Btn-Flt3 и 25 μМ АТФ в присутствии соединения (конечная концентрация ДМСО 1%). После инкубирования в течение 60 минут при комнатной температуре, реакцию останавливали смесью 2,27 нМ EU-анти P-Tyr, 7 мМ ЭДТА, 31,25 нМ SA-XL-665 и 0,02% БСА, что продолжалось в течение 60 минут при комнатной температуре. После этого измеряли сигнал резонансного переноса энергии флуоресценции с временным разрешением (TR-FRET) (возбуждение 340 нм, эмиссия 620 нм, эмиссия 655 нм), и результаты выражали в RFU (относительных единицах флуоресценции). В данном анализе определяли ингибиторный эффект различных концентраций соединения (диапазон от 10 μМ до 0,1 нМ), и данные использовали для расчета значений IC50 (M) и pIC50 (-logIC50).
FGFR4 (ферментный анализ)
В конечном реакционном объеме 30 μл, FGFR4 (ч) (60 нг/мл) инкубировали с 50 мМ HEPES pH 7,5, 6 мМ MnCl2, 1 мМ DTT, 0,1 мМ Na3VО4, 0,01% Triton X-100, 500 нМ Btn-Flt3 и 5 μМ АТФ в присутствии соединения (конечная концентрация ДМСО 1%). После инкубирования в течение 60 минут при комнатной температуре, реакцию останавливали смесью 2,27 нМ EU-анти P-Tyr, 7 мМ ЭДТА, 31,25 нМ SA-XL-665 и 0,02% БСА, что продолжалось в течение 60 минут при комнатной температуре. После этого измеряли сигнал резонансного переноса энергии флуоресценции с временным разрешением (TR-FRET) (возбуждение 340 нм, эмиссия 620 нм, эмиссия 655 нм), и результаты выражали в RFU (относительных единицах флуоресценции). В данном анализе определяли ингибиторный эффект различных концентраций соединения (диапазон от 10 μМ до 0,1 нМ), и данные использовали для расчета значений IC50 (M) и pIC50 (-logIC50).
KDR (VEGFR2) (ферментный анализ)
В конечном объеме 30 μл, KDR (ч) (150 нг/мл) инкубировали с 50 мМ HEPES pH 7,5, 6 мМ MnCl2, 1 мМ DTT, 0,1 мМ Na3VО4, 0,01% Triton X-100, 500 нМ Btn-Flt3 и 3 μМ АТФ в присутствии соединения (конечная концентрация ДМСО 1%). После инкубирования в течение 120 минут при комнатной температуре, реакцию останавливали смесью 2,27 нМ EU-анти P-Tyr, 7 мМ ЭДТА, 31,25 нМ SA-XL-665 и 0,02% БСА, что продолжалось в течение 60 минут при комнатной температуре. После этого измеряли сигнал резонансного переноса энергии флуоресценции с временным разрешением (TR-FRET) (возбуждение 340 нм, эмиссия 620 нм, эмиссия 655 нм), и результаты выражали в RFU (относительных единицах флуоресценции). В данном анализе определяли ингибиторный эффект различных концентраций соединения (диапазон от 10 μМ до 0,1 нМ), и данные использовали для расчета значений IC50 (M) и pIC50 (-logIC50).
Ba/F3-FGFR1 (минус IL3 или плюс IL3) (анализ клеточной пролиферации)
В 384-луночном планшете 100 нл соединения, разведенного в ДМСО, вносили в лунки перед добавлением 50 μл среды культивирования клеток (без фенолового красного RPMI-1640, 10% FBS, 2 мМ L-глутамина и 50 μг/мл гентамицина), содержащей 20000 клеток на лунку Ba/F3-FGFR1-трансфицированных клеток. Клетки помещали в инкубатор при 37°С и 5% CO2. Через 24 часа в лунки добавляли 10 μл раствора Alamar Blue (0,5 мМ K3Fe(CN)6, 0,5 мМ K4Fe(CN)6, 0,15 мМ резазурина и 100 мМ фосфатного буфера) и инкубировали в течение 4 часов при 37°С и 5% СО2 до измерения RFU (относительные единицы флуоресценции) (возбуждение 540 нм, эмиссия 590 нм) в спектрофотометре для сканирования микропланшетов.
В данном анализе определяли ингибиторный эффект различных концентраций соединения (диапазон от 10 μМ до 0,1 нМ), и полученные данные использовали для расчета значений IC50 (M) и pIC50 (-logIC50). В качестве обратного скрининга, такой же эксперимент выполняли в присутствии 10 нг/мл мышиного IL3.
Ba/F3-FGFR3 (минус IL3 или плюс IL3) (анализ клеточной пролиферации)
В 384-луночном планшете 100 нл соединения, разведенного в ДМСО, вносили в лунки до добавления 50 μл среды культивирования клеток (без фенолового красного RPMI-1640, 10% FBS, 2 мМ L-глутамина и 50 μг/мл гентамицина), содержащей 20000 клеток на лунку Ba/F3-FGFR3-трансфицированных клеток. Клетки помещали в инкубатор при 37ºС и 5% CO2. Через 24 часа в лунки добавляли 10 μл раствора Alamar Blue (0,5 мМ K3Fe(CN)6, 0,5 мМ K4Fe(CN)6, 0,15 мМ резазурина и 100 мМ фосфатного буфера) и инкубировали в течение 4 часов при 37°С и 5% СО2 до измерения RFU (относительные единицы флуоресценции) (возбуждение 540 нм, эмиссия 590 нм) в спектрофотометре для сканирования микропланшетов.
В данном анализе определяли ингибиторный эффект различных концентраций соединения (диапазон от 10 μМ до 0,1 нМ), и полученные данные использовали для расчета значений IC50 (M) и pIC50 (-logIC50). В качестве обратного скрининга, такой же эксперимент выполняли в присутствии 10 нг/мл мышиного IL3.
Ba/F3-KDR (минус IL3 или плюс IL3) (анализ клеточной пролиферации)
В 384-луночном планшете 100 нл соединения, разведенного в ДМСО, вносили в лунки перед добавлением 50 μл среды культивирования клеток (без фенолового красного RPMI-1640, 10% FBS, 2 мМ L-глутамина и 50 μг/мл гентамицина), содержащей 20000 клеток на лунку Ba/F3-KDR-трансфицированных клеток. Клетки помещали в инкубатор при 37°С и 5% CO2. Через 24 часа в лунки добавляли 10 μл раствора Alamar Blue (0,5 мМ K3Fe(CN)6, 0,5 мМ K4Fe(CN)6, 0,15 мМ резазурина и 100 мМ фосфатного буфера) и инкубировали в течение 4 часов при 37°С и 5% СО2 до измерения RFU (относительные единицы флуоресценции) (возбуждение 540 нм, эмиссия 590 нм) в спектрофотометре для сканирования микропланшетов.
В данном анализе определяли ингибиторный эффект различных концентраций соединения (диапазон от 10 μМ до 0,1 нМ), и полученные данные использовали для расчета значений IC50 (M) и pIC50 (-logIC50). В качестве обратного скрининга, такой же эксперимент выполняли в присутствии 10 нг/мл мышиного IL3.
Ba/F3-FGFR4 (анализ клеточной пролиферации)
В 384-луночном планшете 100 нл соединения, разведенного в ДМСО, вносили в лунки перед добавлением 50 μл среды культивирования клеток (без фенолового красного RPMI-1640, 10% FBS, 2 мМ L-глутамина и 50 μг/мл гентамицина), содержащей 20000 клеток на лунку Ba/F3-FGFR4-трансфицированных клеток. Клетки помещали в инкубатор при 37°С и 5% CO2. Через 24 часа в лунки добавляли 10 μл раствора Alamar Blue (0,5 мМ K3Fe(CN)6, 0,5 мМ K4Fe(CN)6, 0,15 мМ резазурина и 100 мМ фосфатного буфера) и инкубировали в течение 4 часов при 37°С и 5% СО2 до измерения RFU (относительные единицы флуоресценции) (возбуждение 540 нм, эмиссия 590 нм) в спектрофотометре для сканирования микропланшетов.
В данном анализе определяли ингибиторный эффект различных концентраций соединения (диапазон от 10 μМ до 0,1 нМ), и полученные данные использовали для расчета значений IC50 (M) и pIC50 (-logIC50).
Данные для соединений согласно изобретению в представленных выше анализах приведены в таблице A1 (n.d. означает не определено).

Биологические исследования B
Анализы связывания фермента (KINOMEscan®)
Аффиности связывания фермента киназы соединений, раскрытых в настоящей заявке, определяли при использовании технологии KINOMEscan®, которую представила DiscoveRx Corporation, San Diego, California, USA (www.kinomescan.com). В Таблице B1 приведены полученные значения pKd (-log Kd; Kd (M) - константа связывания ингибитора):
Реферат
Изобретение относится к новому производному хиназолинона формулы (I), включая его любую таутомерную или стереохимически изомерную форму, или его фармацевтически приемлемой соли. Соединение обладает свойствами ингибитора FGFR киназ, в частности FGFR1, FGFR2, FGFR3 или FGFR4 или их мутаций. Соединения могут быть использованы для лечения рака опосредованного FGFR киназой, где рак выбран из множественной миеломы, в том числе множественной миеломы с транслокацией t(4;14), миелопролиферативных нарушений, рака эндометрия, рака простаты, рака мочевого пузыря, рака легких, рака яичников, рака молочной железы, рака желудка, рака толстой и прямой кишки и плоскоклеточной карциномы полости рта, плоскоклеточной карциномы, рака печени, рака почек, рака груди. В соединении формулы (I):(I)W является -N(R)- или -C(RR)-; каждый Rнезависимо выбран из галогена и Cалкокси; D представляет собой фенил или 5-6-членный моноциклический гетероциклил, содержащий 1 или 2 гетероатома, выбранный из N или О, где каждый указанный фенил и гетероциклил необязательно может быть замещен 1, 2 или 3 группами R; Rпредставляет собой водород, Cалкил или -C(=O)-O-Cалкил; Rи Rобъединены с образованием =O или с образованием =CH-Cалкила, который замещен R; Rпредставляет собой циано; Rпредставляет собой гидроксиСалкил, Cалкил, который замещен R, или Cалкил, который замещен -NRR; Rпредставляет собой 5- или 6-членный моноциклический гетероциклил, содержащий один или два N гетероатомов, указанный 5- или 6-членный моноциклический гетероциклил необязательно замещен одним -S(=O)-NRR; каждый Rи Rнезависимо представляет собой водород или Cалкил; каждый Rи Rнезависимо представляет собой водород или Cалкил; n независимо представляет собой целое число, равное 1, 2, 3 или 4. 5 н. и 26 з.п. ф-лы, 3 табл., 35 пр.
Формула
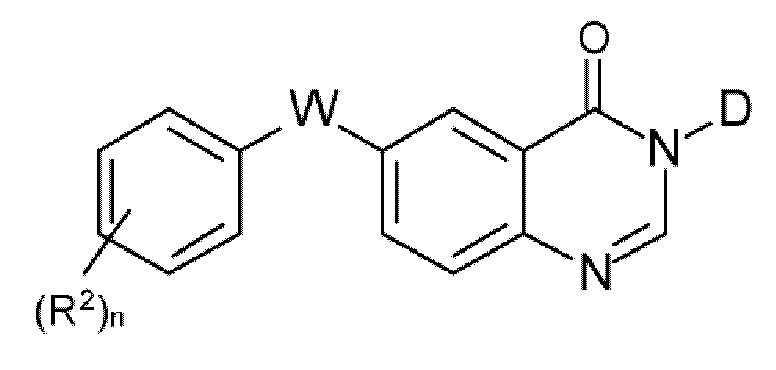

Документы, цитированные в отчёте о поиске
Новое сульфонамидное производное малоновой кислоты и его фармацевтическое применение

Комментарии