Положительные аллостерические модуляторы мускаринового ацетилхолинового рецептора m4 - RU2750935C2
Код документа: RU2750935C2
Чертежи


Описание
Перекрестная ссылка на родственные заявки
Настоящая заявка испрашивает приоритет по предварительной заявке на патент США №62/353447, поданной 22 июня 2016 г., предварительной заявке на патент США №62/418638, поданной 7 ноября 2016 г., и предварительной заявке на патент США №62/471281, поданной 14 марта 2017 г., каждая из которых включена в данный документ посредством ссылки во всей своей полноте.
Декларация государственного интереса
Настоящее изобретение выполнено при государственной поддержке посредством грантов №№ 5R01MH073676 и 1U19MH106839-01, присужденных Национальными институтами здравоохранения. Правительство обладает определенными правами на настоящее изобретение.
Область техники
Настоящее изобретение относится к соединениям, композициям и способам для лечения неврологических и психических расстройств, ассоциированных с нарушением функции мускаринового ацетилхолинового рецептора.
Уровень техники
Холинергическая нейропередача предусматривает активацию никотиновых ацетилхолиновых рецепторов (nAChR) или мускариновых ацетилхолиновых рецепторов (mAChR) путем связывания эндогенного ортостерического агониста ацетилхолина (ACh). Состояния, ассоциированные с когнитивным нарушением, такие как болезнь Альцгеймера, сопровождаются снижением содержания ацетилхолина в головном мозге. Считается, что это является результатом дегенерации холинергических нейронов в базальных отделах переднего мозга, которые широко иннервируют несколько областей головного мозга, включая ассоциативные зоны коры головного мозга и гиппокамп, которые играют критически важную роль в высших процессах. Клинические данные подтверждают, что холинергическая гипофункция вносит вклад в когнитивные дефициты у пациентов, страдающих шизофренией. Усилия по увеличению уровней ацетилхолина были направлены на увеличение уровней холина, предшественника в синтезе ацетилхолина, и на блокирование ацетилхолинэстеразы (AChE), фермента, который метаболизирует ацетилхолин. В результате этого ингибиторы ацетилхолинэстеразы (AChE), которые ингибируют гидролиз ACh, были одобрены в Соединенных Штатах для применения в паллиативном, но не изменяющем течение болезни лечении когнитивных дефицитов у пациентов с AD.
Попытки усиления центральной холинергической функции посредством введения холина или фосфатидилхолина не увенчались успехом. Ингибиторы AChE показали терапевтическую эффективность, однако было обнаружено, что они характеризуются частыми холинергическими побочными эффектами из-за периферической стимуляции ацетилхолина, включая резкую боль в животе, тошноту, рвоту и диарею. Такие побочные эффекты со стороны желудочно-кишечного тракта наблюдались у приблизительно трети пациентов, получавших лечение. Кроме того, также было обнаружено, что некоторые ингибиторы AChE, как например такрин, вызывают существенную гепатотоксичность, при этом повышенные уровни трансаминаз печени наблюдались у приблизительно 30% пациентов. Неблагоприятные эффекты ингибиторов AChE значительно ограничивают их клиническую применимость. Альтернативным подходом к фармакологическому нацеливанию на холинергическую гипофункцию является активация mAChR, которые широко экспрессируются во всем организме.
mAChR являются представителями класса А сопряженных с G-белком рецепторов (GPCR) и включают пять подтипов, обозначаемых М1-М5. Подтипы M1, М3 и M5 в основном сопряжены с Gq и активируют фосфолипазу С, тогда как подтипы М2 и М4 в основном сопряжены с Gi/o и ассоциированными эффекторными системами. Данные пять различных подтипов mAChR были идентифицированы в центральной нервной системе млекопитающих, где они преобладают и дифференциально экспрессируются. М1-М5 играют различные роли в когнитивных, сенсорных, моторных и вегетативных функциях. Таким образом, не ограничиваясь конкретной теорией, полагают, что селективные агонисты определенных подтипов mAChR, которые регулируют процессы, связанные с когнитивной функцией, могут показать превосходство над терапевтическими средствами для лечения психоза, шизофрении и связанных расстройств. Было показано, что мускариновый рецептор М4 играет главную роль в когнитивной обработке и, как полагают, играет главную роль в патофизиологии психотических расстройств, включая шизофрению.
Имеющиеся данные свидетельствуют о том, что наиболее выраженные нежелательные эффекты ингибиторов AChE и других холинергических средств опосредуются активацией периферических mAChR М2 и М3 и включают брадикардию, расстройство ЖКТ, повышенное слюноотделение и потоотделение. В отличие от этого М4 рассматривался как подтип, который наиболее вероятно опосредует эффекты нарушения функции мускаринового ацетилхолинового рецептора при психотических расстройствах, включая шизофрению, расстройства познавательной деятельности и нейропатическую боль. Поэтому значительное усилие было направлено на разработку селективных агонистов М4 для лечения таких расстройств. К сожалению, данные усилия не увенчались большим успехом из-за соединений, которые являются высокоселективными в отношении mAChR М4. Из-за этого агонисты mAChR, которые тестировали в клинических исследованиях, индуцировали ряд нежелательных явлений за счет активации периферических mAChR. Для полного понимания физиологических ролей отдельных подтипов mAChR и дополнительного изучения терапевтической пользы лигандов mAChR при психозе, включая шизофрению, расстройства познавательной деятельности и другие расстройства, может быть важно разработать соединения, которые являются высокоселективными активаторами mAChR М4 и других отдельных подтипов mAChR.
Предыдущие попытки открытия и разработки агонистов, которые являются высокоселективными в отношении отдельных подтипов mAChR, были неудачными из-за высокой консервативности ортостерического участка связывания ACh. Полагают, что разработка соединений, которые оказывают свое действие в аллостерических участках mAChR, которые отдалены от ортостерического участка и являются менее высококонсервативными, может преодолеть проблемы, ассоциированные с нацеливанием на высококонсервативный ортостерический участок связывания ACh. Данный подход оказался весьма успешным при разработке селективных лигандов для нескольких подтипов GPCR. В случае mAChR главная цель заключалась в разработке аллостерических лигандов, которые селективно увеличивают активность mAChR М4 или других подтипов mAChR. Аллостерические активаторы могут включать аллостерические агонисты, которые оказывают свое действие в участке, отдаленном от ортостерического участка, с непосредственной активацией рецептора в отсутствие ACh, а также положительные аллостерические модуляторы (РАМ), которые не активируют рецептор непосредственно, а потенцируют активацию рецептора с помощью эндогенного ортостерического агониста ACh. Также возможно, чтобы одна молекула обладала активностью как аллостерического потенциатора, так и аллостерического агониста.
Совсем недавно было показано, что мускариновые агонисты, включая ксаномелин, являются активными в животных моделях с профилями, подобными таковым у известных антипсихотических лекарственных средств, но не вызывают каталепсию (Bymaster et al., Eur. J. Pharmacol. 1998, 356, 109, Bymaster et al., Life Sci. 1999, 64, 527; Shannon et al., J. Pharmacol. Exp. Ther. 1999, 290, 901; Shannon et al, Schizophrenia Res. 2000, 42, 249). Более того, было показано, что ксаномелин снижает интенсивность психотических поведенческих симптомов, таких как приступы бреда, подозрительность, внезапные вскрикивания и галлюцинации, у пациентов с болезнью Альцгеймера (Bodick et al., Arch. Neurol. 1997, 54, 465), однако индуцируемые лечением побочные эффекты, например, эффекты со стороны желудочно-кишечного тракта, значительно ограничивали клиническую применимость данного соединения.
Несмотря на успехи в исследованиях мускаринового ацетилхолинового рецептора по-прежнему остается недостаток в соединениях, которые являются сильными эффективными и селективными активаторами mAChR М4, а также эффективными в лечении неврологических и психических расстройств, ассоциированных с холинергической активностью, и заболеваний, в которые вовлечен мускариновый рецептор М4.
Краткое описание
В одном аспекте раскрыты соединения формулы (I)

или их фармацевтически приемлемая соль, где:
В представляет собой О или S;
X представляет собой N или CR1;
Z представляет собой N или CR3;
R1 выбран из водорода, C1-C4-алкила, C1-C4-галогеналкила, галогена и -ORb;
R2 выбран из водорода, C1-C4-алкила, C1-C4-галогеналкила, C1-C4-гидроксиалкила, C1-C4-ацетоксиалкила, галогена и -ORb;
R3 выбран из водорода и C1-C4-алкила;
каждый из R4 и R5 независимо выбран из водорода, алкила, алкенила, алкинила, арила, гетероарила, циклоалкила, гетероалкила, гетероцикла и -(CRcRd)n-Y, каждый из которых может быть необязательно замещенным;
или R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют необязательно замещенное гетероциклическое кольцо;
R6 выбран из водорода и C1-C4-алкила;
каждый Y независимо выбран из галогена, -OR, -SR, -C(O)R, -C(O)OR, -S(O)R, -SO2R, -NR2, -C(O)NR2, -NRC(O)R, -S(O)2NR2, -NRS(O)2R, арила, гетероарила, циклоалкила и гетероцикла, каждый из которых может быть необязательно замещенным;
n равняется 1, 2, 3, 4, 5, 6, 7 или 8;
Rb выбран из водорода, C1-C4-алкила, C1-C4-галогеналкила, арила, гетероарила, циклоалкила и гетероцикла;
каждый из Rc и Rd независимо выбран из водорода, C1-C4-алкила, C1-C4-галогеналкила и галогена; и
каждый R независимо выбран из водорода, алкила, арила, арилалкила, циклоалкила, циклоалкилалкила, гетероцикла, гетероциклоалкила, гетероарила, гетероарилалкила и гетероалкила, каждый из которых может быть необязательно замещенным.
Также раскрыты фармацевтические композиции, содержащие соединения, способы получения соединений, наборы, содержащие соединения, и способы применения соединений, композиций и наборов для лечения расстройств, таких как неврологические и/или психические расстройства, ассоциированные с нарушением функции мускаринового ацетилхолинового рецептора, у млекопитающего.
Краткое описание графических материалов
На ФИГ. 1 показана схематическая иллюстрация лигандсвязывающих участков, включая ортостерический участок и аллостерический участок, на мускариновом ацетилхолиновом рецепторе.
На ФИГ. 2 показана некоторая биологическая активность иллюстративного соединения.
Подробное описание изобретения
В данном документе раскрыты положительные аллостерические модуляторы (т.е. потенциаторы) мускаринового ацетилхолинового рецептора М4 (mAChR М4), способы их получения, фармацевтические композиции, содержащие их, и способы лечения неврологических и психических расстройств, ассоциированных с нарушением функции мускаринового ацетилхолинового рецептора, с их применением. Соединения включают соединения, представляющие собой пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин, пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин, пиразино[2',3':4,5]тиено[3,2-d]пиримидин-4-амин, пиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин и пиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин.
Мускариновый ацетилхолиновый рецептор М4 человека (mAChR М4) представляет собой белок из 479 аминокислот, кодируемый геном CHRM4. Молекулярная масса негликозилированного белка составляет приблизительно 54 кДа, и он представляет собой трансмембранный GPCR. Как описано выше, mAChR М4 является представителем класса A GPCR или родопсин-подобных GPCR, которые характеризуются структурными особенностями, подобными родопсину, такими как семь трансмембранных сегментов. Мускариновые ацетилхолиновые рецепторы имеют N-конец, направленный по отношению к внеклеточной стороне мембраны, и С-конец, расположенный со стороны цитоплазмы. Схематическое изображение структуры mAChR М4 показано на фигуре 1, на которой трансмембранные сегменты показаны в виде цилиндрических форм (которые пронизывают липидный бислой клеточной мембраны). Ортостерическое связывание природного лиганда mAChR, ацетилхолина, происходит в кармане, расположенном между трансмембранными сегментами, изображенными на фигуре 1.
Предыдущие попытки открытия и разработки агонистов, которые являются высокоселективными в отношении отдельных подтипов mAChR, были неудачными из-за высокой консервативности ортостерического участка связывания ACh. Полагают, что разработка соединений, которые оказывают свое действие в аллостерических участках mAChR, которые отдалены от ортостерического участка и являются менее высококонсервативными, может преодолеть проблемы, ассоциированные с нацеливанием на высококонсервативный ортостерический участок связывания ACh. Не ограничиваясь конкретной теорией, полагают, что раскрытые соединения и продукты, полученные с помощью раскрытых способов, связываются с аллостерическим участком, отличающимся от ортостерического участка связывания. Например, раскрытое соединение может связываться в участке связывания, проиллюстрированном на фигуре 1.
1. Определения
Если не указано иное, все технические и научные термины, используемые в данном документе, имеют такое же значение, которое обычно понимает средний специалист в данной области техники. В случае противоречий следует руководствоваться настоящим документом, включая определения. Предпочтительные способы и материалы описаны ниже, хотя способы и материалы, аналогичные или эквивалентные описанным в данном документе, можно применять на практике или для тестирования настоящего изобретения. Все публикации, патентные заявки, патенты и другие ссылки, упомянутые в данном документе, включены посредством ссылки во всей своей полноте. Материалы, способы и примеры, раскрытые в данном документе, являются лишь иллюстративными и не предназначены для ограничения.
Подразумевается, что используемые в данном документе термины "содержат(содержит)", "включают(включает)", "имеющий", "имеет", "может", "состоят(состоит)" и их варианты представляют собой неограниченные переходные фразы, термины или слова, которые не исключают возможности дополнительных действий или структур. Формы единственного числа включают объекты во множественном числе, если в контексте явно не указано иное. В настоящем изобретении также предусматриваются другие варианты осуществления, "содержащие", "состоящие из" и "состоящие в основном из" вариантов осуществления или элементов, представленных в данном документе, независимо от того, изложены ли они явным образом или нет.
Модифицирующее слово "приблизительно", используемое по отношению к количеству, включает указанное значение и имеет значение, определяемое контекстом (например, предусматривает по меньшей мере некоторую долю погрешности, связанную с измерением конкретного количества). Модифицирующее слово "приблизительно" следует также рассматривать как раскрытие диапазона, определяемого абсолютными значениями двух конечных точек. Например, выражение "от приблизительно 2 до приблизительно 4" также раскрывает диапазон "от 2 до 4". Термин "приблизительно" может относиться к значению плюс или минус 10% от указанного числа. Например, "приблизительно 10%" может указывать диапазон от 9% до 11%, и "приблизительно 1" может означать от 0,9 до 1,1. Другие значения термина "приблизительно", такие как округление, могут быть очевидны из контекста, таким образом, например, "приблизительно 1" может также означать от 0,5 до 1,4.
Определения конкретных функциональных групп и химических терминов описаны более подробно ниже. Для целей настоящего изобретения химические элементы определены в соответствии с Периодической таблицей элементов версии CAS, Handbook of Chemistry and Physics, 75th Ed., внутри обложки, и конкретные функциональные группы обычно определяются, как описано в ней. Дополнительно общие принципы органической химии, а также определенные функциональные фрагменты и реакционная способность описаны в Organic Chemistry, Thomas Sorrell, University Science Books, Sausalito, 1999; Smith and March March's Advanced Organic Chemistry, 5th Edition, John Wiley & Sons, Inc., New York, 2001; Larock, Comprehensive Organic Transformations, VCH Publishers, Inc., New York, 1989; Carruthers, Some Modern Methods of Organic Synthesis, 3rd Edition, Cambridge University Press, Cambridge, 1987; полное содержание каждой из которых включено в данный документ посредством ссылки.
Термин "ацетоксиалкил", используемый в данном документе, означает по меньшей мере одну ацетокси-группу (-ОС(О)СН3), которая присоединена к основному молекулярному фрагменту посредством алкиленовой группы, определенной в данном документе.
Термин "алкокси", используемый в данном документе, относится к алкильной группе, определенной в данном документе, присоединенной к основному молекулярному фрагменту посредством атома кислорода. Иллюстративные примеры алкокси включают без ограничения метокси, этокси, пропокси, 2-пропокси, бутокси и трет-бутокси.
Термин "алкил", используемый в данном документе, означает прямую или разветвленную насыщенную углеводородную цепь, содержащую от 1 до 10 атомов углерода. Термин "низший алкил" или "C1-С6-алкил" означает углеводород с прямой или разветвленной цепью, содержащий от 1 до 6 атомов углерода. Термин "C1-С3-алкил" означает углеводород с прямой или разветвленной цепью, содержащий от 1 до 3 атомов углерода. Иллюстративные примеры алкила включают без ограничения метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, изопентил, неопентил, н-гексил, 3-метилгексил, 2,2-диметилпентил, 2,3-диметилпентил, н-гептил, н-октил, н-нонил и н-децил.
Термин "алкенил", используемый в данном документе, означает прямую или разветвленную углеводородную цепь, содержащую по меньшей мере одну углерод углеродную двойную связь и от 1 до 10 атомов углерода.
Термин "алкоксиалкил", используемый в данном документе, относится к алкоксигруппе, определенной в данном документе, присоединенной к основному молекулярному фрагменту посредством алкильной группы, определенной в данном документе.
Термин "алкоксифторалкил", используемый в данном документе, относится к алкоксигруппе, определенной в данном документе, присоединенной к основному молекулярному фрагменту посредством фторалкильной группы, определенной в данном документе.
Термин "алкилен", используемый в данном документе, относится к двухвалентной группе, полученной из углеводорода с прямой или разветвленной цепью, содержащего от 1 до 10 атомов углерода, например, от 2 до 5 атомов углерода. Иллюстративные примеры алкилена включают без ограничения -СН2СН2-, -CH2CH2CH2-, -СН2СН2СН2СН2- и -CH2CH2CH2CH2CH2-.
Термин "алкиламино", используемый в данном документе, означает по меньшей мере одну алкильную группу, определенную в данном документе, которая присоединена к основному молекулярному фрагменту посредством аминогруппы, определенной в данном документе.
Термин "амид", используемый в данном документе, означает -C(O)NR- или -NRC(O)-, где R может представлять собой водород, алкил, циклоалкил, арил, гетероарил, гетероцикл, алкенил или гетероалкил.
Термин "аминоалкил", используемый в данном документе, означает по меньшей мере одну аминогруппу, определенную в данном документе, которая присоединена к основному молекулярному фрагменту посредством алкиленовой группы, определенной в данном документе.
Термин "амино", используемый в данном документе, означает -NRxRy, где Rx и Ry могут представлять собой водород, алкил, циклоалкил, арил, гетероарил, гетероцикл, алкенил или гетероалкил. В случае аминоалкильной группы или любого другого фрагмента, где амино присоединяет вместе два других фрагмента, амино может представлять собой -NRx-, где Rx может представлять собой водород, алкил, циклоалкил, арил, гетероарил, гетероцикл, алкенил или гетероалкил.
Термин "арил", используемый в данном документе, относится к фенильной группе или бициклической конденсированной кольцевой системе. В качестве примера бициклических конденсированных кольцевых систем приводится фенильная группа, присоединенная к основному молекулярному фрагменту и конденсированная с циклоалкильной группой, определенной в данном документе, фенильной группой, гетероарильной группой, определенной в данном документе, или гетероциклом, определенным в данном документе. Иллюстративные примеры арила включают без ограничения индолил, нафтил, фенил, дигидробензофуран, дигидроизобензофуран и тетрагидрохинолинил.
Термин "цианоалкил", используемый в данном документе, означает по меньшей мере одну группу -CN, которая присоединена к основному молекулярному фрагменту посредством алкиленовой группы, определенной в данном документе.
Термин "цианофторалкил", используемый в данном документе, означает по меньшей мере одну группу -CN, которая присоединена к основному молекулярному фрагменту посредством фторалкильной группы, определенной в данном документе.
Термин "циклоалкокси", используемый в данном документе, относится к циклоалкильной группе, определенной в данном документе, присоединенной к основному молекулярному фрагменту посредством атома кислорода.
Термин "циклоалкил", используемый в данном документе, относится к карбоциклической кольцевой системе, содержащей от трех до десяти атомов углерода, при этом не содержащей гетероатомы и двойные связи. Иллюстративные примеры циклоалкила включают без ограничения циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклононил и циклодецил, а также бициклические циклоалкилы, как например бицикло[1.1.1]пентанил. Термин "циклоалкил" также включает карбоциклические кольцевые системы, в которых циклоалкильная группа присоединена к основному молекулярному фрагменту и конденсирована с арильной группой, определенной в данном документе (например, фенильной группой), гетероарильной группой, определенной в данном документе, или гетероциклом, определенным в данном документе. Иллюстративные примеры таких циклоалкильных групп включают без ограничения 2,3-дигидро-1H-инденил (например, 2,3-дигидро-1H-инден-1-ил и 2,3-дигидро-1H-инден-2-ил), 6,7-дигидро-5H-циклопента[b]пиридинил (например, 6,7-дигидро-5H-циклопента[b]пиридин-6-ил) и 5,6,7,8-тетрагидрохинолинил (например, 5,6,7,8-тетрагидрохинолин-5-ил).
Термин "циклоалкенил", используемый в данном документе, означает неароматическую моноциклическую или полициклическую кольцевую систему, содержащую по меньшей мере одну углерод-углеродную двойную связь и предпочтительно содержащую от 5 до 10 атомов углерода на кольцо. Иллюстративные моноциклические циклоалкенильные кольца включают циклопентенил, циклогексенил или циклогептенил.
Термин "фторалкил", используемый в данном документе, означает алкильную группу, определенную в данном документе, в которой один, два, три, четыре, пять, шесть, семь или восемь атомов водорода заменены фтором. Иллюстративные примеры фторалкила включают без ограничения 2-фторэтил, 2,2,2-трифторэтил, трифторметил, дифторметил, пентафторэтил и трифторпропил, такой как 3,3,3-трифторпропил.
Термин "фторалкокси", используемый в данном документе, означает по меньшей мере одну фторалкильную группу, определенную в данном документе, которая присоединена к основному молекулярному фрагменту посредством атома кислорода. Иллюстративные примеры фторалкокси включают без ограничения дифторметокси, трифторметокси и 2,2,2-трифторэтокси.
Термины "атом галогена" или "галоген", используемые в данном документе, означают Cl, Br, I или F.
Термин "галогеналкил", используемый в данном документе, означает алкильную группу, определенную в данном документе, в которой один, два, три, четыре, пять, шесть, семь или восемь атомов водорода заменены галогеном.
Термин "галогеналкокси", используемый в данном документе, означает по меньшей мере одну галогеналкильную группу, определенную в данном документе, которая присоединена к основному молекулярному фрагменту посредством атома кислорода.
Термин "галогенциклоалкил", используемый в данном документе, означает циклоалкильную группу, определенную в данном документе, в которой один или несколько атомов водорода заменены галогеном.
Термин "гетероалкил", используемый в данном документе, означает алкильную группу, определенную в данном документе, в которой один или несколько атомов углерода были заменены гетероатомом, независимо выбранным из S, О, Р и N. Иллюстративные примеры гетероалкилов включают без ограничения алкиловые эфиры, вторичные и третичные алкиламины, амиды и алкилсульфиды.
Термин "гетероарил", используемый в данном документе, относится к ароматическому моноциклическому кольцу или ароматической бициклической кольцевой системе. Ароматические моноциклические кольца представляют собой пяти- или шестичленные кольца, содержащие по меньшей мере один гетероатом, независимо выбранный из N, О и S (например, 1, 2, 3 или 4 гетероатома, независимо выбранные из О, S и N).
Пятичленные ароматические моноциклические кольца имеют две двойные связи, а шестичленные шестичленные ароматические моноциклические кольца имеют три двойные связи. В качестве примера бициклических гетероарильных групп приводится моноциклическое гетероарильное кольцо, присоединенное к основному молекулярному фрагменту и конденсированное с моноциклической циклоалкильной группой, определенной в данном документе, моноциклической арильной группой, определенной в данном документе, моноциклической гетероарильной группой, определенной в данном документе, или моноциклическим гетероциклом, определенным в данном документе. Иллюстративные примеры гетероарила включают без ограничения индолил, пиридинил (включая пиридин-2-ил, пиридин-3-ил, пиридин-4-ил), пиримидинил, пиразинил, пиридазинил, пиразолил, пирролил, бензопиразолил, 1,2,3-триазолил, 1,3,4-тиадиазолил, 1,2,4-тиадиазолил, 1,3,4-оксадиазолил, 1,2,4-оксадиазолил, имидазолил, тиазолил, изотиазолил, тиенил, бензимидазолил, бензотиазолил, бензоксазолил, бензоксадиазолил, бензотиенил, бензофуранил, изобензофуранил, фуранил, оксазолил, изоксазолил, пуринил, изоиндолил, хиноксалинил, индазолил, хиназолинил, 1,2,4-триазинил, 1,3,5-триазинил, изохинолинил, хинолинил, 6,7-дигидро-1,3-бензотиазолил, 6,7-дигидро-5Н-циклопента[b]пиридинил, имидазо[1,2-а]пиридинил, нафтиридинил, пиридоимидазолил, тиазоло[5,4-b]пиридин-2-ил, тиазоло[5,4-d]пиримидин-2-ил.
Термины "гетероцикл" или "гетероциклический", используемые в данном документе, означают моноциклический гетероцикл, бициклический гетероцикл или трициклический гетероцикл. Моноциклический гетероцикл представляет собой трех-, четырех-, пяти-, шести-, семи- или восьмичленное кольцо, содержащее по меньшей мере один гетероатом, независимо выбранный из О, N и S. Трех- или четырехчленное кольцо не содержит двойную связь или содержит одну двойную связь и один гетероатом, выбранный из О, N и S. Пятичленное кольцо не содержит двойную связь или содержит одну двойную связь и один, два или три гетероатома, независимо выбранных из О, N и S. Шестичленное кольцо не содержит двойную связь или содержит одну или две двойные связи и один, два или три гетероатома, независимо выбранных из О, N и S. Семи- и восьмичленные кольца не содержат двойную связь или содержат одну, две или три двойные связи и один, два или три гетероатома, независимо выбранных из О, N и S. Иллюстративные примеры моноциклических гетероциклов включают без ограничения азетидинил, азепанил, азиридинил, диазепанил, 1,3-диоксанил, 1,3-диоксоланил, 1,3-дитиоланил, 1,3-дитианил, имидазолинил, имидазолидинил, изотиазолинил, изотиазолидинил, изоксазолинил, изоксазолидинил, морфолинил, 2-оксо-3-пиперидинил, 2-оксоазепан-3-ил, оксадиазолинил, оксадиазолидинил, оксазолинил, оксазолидинил, оксетанил, оксепанил, оксоканил, пиперазинил, пиперидинил, пиранил, пиразолинил, пиразолидинил, пирролинил, пирролидинил, тетрагидрофуранил, тетрагидропиранил, тетрагидропиридинил, тетрагидротиенил, тиадиазолинил, тиадиазолидинил, 1,2-тиазинанил, 1,3-тиазинанил, тиазолинил, тиазолидинил, тиоморфолинил, 1,1-диоксидотиоморфолинил (тиоморфолинсульфон), тиопиранил и тритианил. Бициклический гетероцикл представляет собой моноциклический гетероцикл, конденсированный с фенильной группой, или моноциклический гетероцикл, конденсированный с моноциклическим циклоалкилом, или моноциклический гетероцикл, конденсированный с моноциклическим циклоалкенилом, или моноциклический гетероцикл, конденсированный с моноциклическим гетероциклом, или спирогетероциклическую группу, или соединенную мостиковой связью моноциклическую гетероциклическую кольцевую систему, в которой два несмежных атома кольца соединены алкиленовым мостиком из 1, 2, 3 или 4 атомов углерода или алкениленовым мостиком из двух, трех или четырех атомов углерода. Иллюстративные примеры бициклических гетероциклов включают без ограничения бензопиранил, бензотиопиранил, хроманил, 2,3-дигидробензофуранил, 2,3-дигидробензотиенил, 2,3-дигидроизохинолин, 2-азаспиро[3.3]гептан-2-ил, 2-оксаспиро[3.3]гептан-6-ил, 2-окса-6-азаспиро[3.3]гептан-6-ил, азабицикло[2.2.1]гептил (включая 2-азабицикло[2.2.1]гепт-2-ил), азабицикло[3.1.0]гексанил (включая 3-азабицикло[3.1.0]гексан-3-ил), 2,3-дигидро-1H-индолил, изоиндолинил, октагидроциклопента[c]пирролил, октагидропирролопиридинил и тетрагидроизохинолинил. В качестве примера трициклических гетероциклов приводятся бициклический гетероцикл, конденсированный с фенильной группой, или бициклический гетероцикл, конденсированный с моноциклическим циклоалкилом, или бициклический гетероцикл, конденсированный с моноциклическим циклоалкенилом, или бициклический гетероцикл, конденсированный с моноциклическим гетероциклом, или бициклический гетероцикл, в котором два несмежных атома бициклического кольца соединены алкиленовым мостиком из 1, 2, 3 или 4 атомов углерода или алкениленовым мостиком из двух, трех или четырех атомов углерода. Примеры трициклических гетероциклов включают без ограничения октагидро-2,5-эпоксипентален, гексагидро-2H-2,5-метаноциклопента[b]фуран, гексагидро-1H-1,4-метаноциклопента[с]фуран, азаадамантан(1-азатрицикло[3.3.1.13,7]декан) и оксаадамантан(2-оксатрицикло[3.3.1.13,7]декан). Моноциклические, бициклические и трициклические гетероциклы соединены с основным молекулярным фрагментом посредством любого атома углерода или любого атома азота, содержащихся в кольцах, и могут быть незамещенными или замещенными.
Термины "гидроксил" или "гидрокси", используемые в данном документе, означают группу -ОН.
Термин "гидроксиалкил", используемый в данном документе, означает по меньшей мере одну группу -ОН, которая присоединена к основному молекулярному фрагменту посредством алкиленовой группы, определенной в данном документе.
Термин "гидроксифторалкил", используемый в данном документе, означает по меньшей мере одну группу -ОН, которая присоединена к основному молекулярному фрагменту посредством фторалкильной группы, определенной в данном документе.
В некоторых случаях число атомов углерода в гидрокарбильном заместителе (например, алкиле или циклоалкиле) обозначается префиксом "Cx-Cy-", где x представляет собой минимальное число, а y представляет собой максимальное число атомов углерода в заместителе. Таким образом, например, "C1-С3-алкил" относится к алкильному заместителю, содержащему от 1 до 3 атомов углерода.
Термин "сульфонамид", используемый в данном документе, означает -S(O)2NRd- или -NRdS(O)-, где Rd может представлять собой водород, алкил, циклоалкил, арил, гетероарил, гетероцикл, алкенил или гетероалкил.
Термин "заместители" относится к группе, предусматривающей "замещение" арильной, гетероарильной, фенильной или пиридинильной группы по любому атому данной группы. Любой атом может быть замещенным.
Термин "замещенный" относится к группе, которая может быть дополнительно замещена одной или несколькими группами заместителей, отличных от водорода. Группы заместителей включают без ограничения галоген, =O (оксо), =S (тиоксо), циано, изоциано, нитро, фторалкил, алкоксифторалкил, фторалкокси, алкил, алкенил, алкинил, галогеналкил, галогеналкокси, гетероалкил, циклоалкил, циклоалкенил, арил, гетероарил, гетероцикл, циклоалкилалкил, гетероарилалкил, арилалкил, гидрокси, гидроксиалкил, алкокси, алкоксиалкил, алкилен, арилокси, фенокси, бензилокси, амино, алкиламино, ациламино, аминоалкил, ариламино, сульфониламино, сульфиниламино, сульфанил, сульфонил, алкилсульфонил, арилсульфонил, аминосульфонил, сульфинил, -СООН, кетон, амид, карбамат и ацил. Например, если группа описывается как "необязательно замещенная" (такая как алкильная, алкенильная, алкинильная, арильная, гетероарильная, циклоалкильная, гетероалкильная, гетероциклическая или другая группа, такая как R-группа), она может иметь 0, 1, 2, 3, 4 или 5 заместителей, независимо выбранных из галогена, =O (оксо), =S (тиоксо), циано, нитро, фторалкила, алкоксифторалкила, фторалкокси, алкила, алкенила, алкинила, галогеналкила, галогеналкокси, гетероалкила, циклоалкила, циклоалкенила, арила, гетероарила, гетероцикла, циклоалкилалкила, гетероарилалкила, арилалкила, гидрокси, гидроксиалкила, алкокси, алкоксиалкила, алкилена, арилокси, фенокси, бензилокси, амино, алкиламино, ациламино, аминоалкила, ариламино, сульфониламино, сульфиниламино, сульфонила, алкилсульфонила, арилсульфонила, аминосульфонила, сульфинила, -СООН, кетона, амида, карбамата и ацила.
Термин "



Для соединений, описанных в данном документе, группы и их заместители могут быть выбраны в соответствии с допустимой валентностью атомов и заместителей таким образом, что результаты выбора и замещения приводят к получению стабильного соединения, например, которое самопроизвольно не подвергается трансформации, например, посредством перегруппировки, циклизации, отщепления и т.д.
Термин "аллостерический участок", используемый в данном документе, относится к лигандсвязывающему участку, который с точки зрения топографии отличается от ортостерического участка связывания.
Термин "модулятор", используемый в данном документе, относится к молекулярной структуре (например, без ограничения лиганду и раскрытому соединению), которая модулирует активность целевого рецепторного белка.
Термин "лиганд", используемый в данном документе, относится к природной или синтетической молекулярной структуре, которая способна ассоциироваться или связываться с рецептором с образованием комплекса и опосредовать, предотвращать или модифицировать биологический эффект. Таким образом, термин "лиганд" охватывает аллостерические модуляторы, ингибиторы, активаторы, агонисты, антагонисты, природные субстраты и аналоги природных субстратов.
Термины "природный лиганд" и "эндогенный лиганд", используемые в данном документе, используются взаимозаменяемо и относятся к встречающемуся в природе лиганду, обнаруживаемому в природе, который связывается с рецептором.
Термин "ортостерический участок", используемый в данном документе, относится к основному участку связывания на рецепторе, который распознают эндогенный лиганд или агонист данного рецептора. Например, ортостерический участок рецептора mAChR М4 представляет собой участок, который связывает ацетилхолин.
Термин "положительный аллостерический модулятор рецептора mAChR М4", используемый в данном документе, относится к любому экзогенно вводимому соединению или средству, которые непосредственно или опосредовано усиливают активность рецептора mAChR М4 в присутствии или в отсутствие ацетилхолина или другого агониста у животного, в частности млекопитающего, например, человека. Например, положительный аллостерический модулятор рецептора mAChR М4 может увеличивать активность рецептора mAChR М4 в клетке в присутствии внеклеточного ацетилхолина. Клетка может представлять собой клетки яичника китайского хомячка (CHO-K1), трансфицированные с помощью mAChR М4 человека. Клетка может представлять собой клетки яичника китайского хомячка (CHO-K1), трансфицированные с помощью рецептора mAChR М4 крысы. Клетка может представлять собой клетки яичника китайского хомячка (CHO-K1), трансфицированные с помощью mAChR М4 млекопитающего. Термин "положительный аллостерический модулятор рецептора mAChR М4" включает соединение, которое представляет собой "аллостерический потенциатор рецептора mAChR М4" или "аллостерический агонист рецептора mAChR М4", а также соединение, которое обладает смешанной активностью, предусматривающей фармакологические свойства как "аллостерического потенциатора рецептора mAChR М4", так и "аллостерического агониста рецептора mAChR М4". Термин "положительный аллостерический модулятор рецептора mAChR М4" также включает соединение, которое представляет собой "аллостерический усилитель рецептора mAChR М4".
Термин "аллостерический потенциатор рецептора mAChR М4", используемый в данном документе, относится к любому экзогенно вводимому соединению или средству, которые непосредственно или опосредованно усиливают ответ, вызванный эндогенным лигандом (таким как ацетилхолин) при связывании эндогенного лиганда с ортостерическим участком рецептора mAChR М4, у животного, в частности млекопитающего, например, человека. Аллостерический потенциатор рецептора mAChR М4 связывается с участком, отличающимся от ортостерического участка, то есть аллостерическим участком, и положительно усиливает ответ рецептора на агонист или эндогенный лиганд. В некоторых вариантах осуществления аллостерический потенциатор не вызывает десенсибилизацию рецептора, при этом активность соединения в качестве аллостерического потенциатора рецептора mAChR М4 обеспечивает преимущества над применением чистого ортостерического агониста рецептора mAChR М4. Такие преимущества могут включать, например, увеличенный предел безопасности, более высокую переносимость, пониженную вероятность злоупотребления и сниженную токсичность.
Термин "аллостерический усилитель рецептора mAChR М4", используемый в данном документе, относится к любому экзогенно вводимому соединению или средству, которые непосредственно или опосредованно усиливают ответ, вызванный эндогенным лигандом (таким как ацетилхолин), у животного, в частности млекопитающего, например, человека. В некоторых вариантах осуществления аллостерический усилитель увеличивает аффинность природного лиганда или агониста в отношении ортостерического участка. В некоторых вариантах осуществления аллостерический усилитель увеличивает эффективность агониста. Аллостерический усилитель рецептора mAChR М4 связывается с участком, отличающимся от ортостерического участка, то есть аллостерическим участком, и положительно усиливает ответ рецептора на агонист или эндогенный лиганд. Аллостерический усилитель сам по себе не оказывает эффекта на рецептор, а требует присутствия агониста или природного лиганда для реализации эффекта в отношении рецептора.
Термин "аллостерический агонист рецептора mAChR М4", используемый в данном документе, относится к любому экзогенно вводимому соединению или средству, которые непосредственно активируют активность рецептора mAChR М4 в отсутствие эндогенного лиганда (такого как ацетилхолин) у животного, в частности млекопитающего, например, человека. Аллостерический агонист рецептора mAChR М4 связывается с участком, который отличается от ортостерического участка для ацетилхолина на рецепторе mAChR М4. Поскольку присутствие эндогенного лиганда не требуется, активность соединения в качестве аллостерического агониста рецептора mAChR М4 обеспечивает преимущества, если холинергический тонус в конкретном синапсе является низким.
Термин "нейтральный аллостерический лиганд рецептора mAChR М4", используемый в данном документе, относится к любому экзогенно вводимому соединению или средству, которые связываются с аллостерическим участком, не оказывая влияния на связывание или функцию агонистов или природного лиганда в ортостерическом участке у животного, в частности млекопитающего, например, человека. Однако нейтральный аллостерический лиганд может блокировать действие других аллостерических модуляторов, которые оказывают свое действие посредством одного и того же участка. Для перечисления числовых диапазонов в данном документе каждое промежуточное число в них явным образом предусматривается с одинаковой степенью точности. Например, для диапазона 6-9 числа 7 и 8 предусматриваются в дополнение к 6 и 9, а для диапазона 6,0-7,0 явным образом предусматриваются числа 6,0, 6,1, 6,2, 6,3, 6,4, 6,5, 6,6, 6,7, 6,8, 6,9 и 7,0.
2. Соединения
В одном аспекте раскрыто соединение формулы (I)

или его фармацевтически приемлемая соль, где:
В представляет собой О или S;
X представляет собой N или CR1;
Z представляет собой N или CR3;
R1 выбран из водорода, C1-C4-алкила, C1-C4-галогеналкила, галогена и -ORb;
R2 выбран из водорода, C1-C4-алкила, C1-C4-галогеналкила, C1-C4-гидроксиалкила, C1-C4-ацетоксиалкила, галогена и -ORb;
R3 выбран из водорода и C1-С4-алкила;
каждый из R4 и R5 независимо выбран из водорода, алкила, алкенила, алкинила, арила, гетероарила, циклоалкила, гетероалкила, гетероцикла и -(CRcRd)n-Y, каждый из которых может быть необязательно замещенным;
или R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют необязательно замещенное гетероциклическое кольцо;
R6 выбран из водорода и C1-C4-алкила;
каждый Y независимо выбран из галогена, -OR, -SR, -C(O)R, -C(O)OR, -S(O)R, -SO2R, -NR2, -C(O)NR2, -NRC(O)R, -S(O)2NR2, -NRS(O)2R, арила, гетероарила, циклоалкила и гетероцикла, каждый из которых может быть необязательно замещенным;
n равняется 1, 2, 3, 4, 5, 6, 7 или 8;
Rb выбран из водорода, C1-C4-алкила, C1-C4-галогеналкила, арила, гетероарила, циклоалкила и гетероцикла;
каждый из Rc и Rd независимо выбран из водорода, C1-C4-алкила, C1-C4-галогеналкила и галогена; и
каждый R независимо выбран из водорода, алкила, арила, арилалкила, циклоалкила, циклоалкилалкила, гетероцикла, гетероциклоалкила, гетероарила, гетероарилалкила и гетероалкила, каждый из которых может быть необязательно замещенным.
В некоторых вариантах осуществления Y выбран из галогена, -OR, -SR, -C(O)R, -C(O)OR, -S(O)R, -SO2R, -NR2, -C(O)NR2, -S(O)2NR2, арила, гетероарила, циклоалкила и гетероцикла, каждый из которых может быть необязательно замещенным.
В некоторых вариантах осуществления соединение представляет собой соединение формулы (Ia)

или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления соединение представляет собой соединение формулы (Ib)

или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления X представляет собой N.
В некоторых вариантах осуществления X представляет собой CR1. В некоторых вариантах осуществления R1 представляет собой водород. В некоторых вариантах осуществления R1 представляет собой C1-С4алкил. В некоторых вариантах осуществления R1 представляет собой метил.
В некоторых вариантах осуществления R2 выбран из водорода, C1-С4-алкила, C1-C4-галогеналкила, галогена и -ORb.
В некоторых вариантах осуществления R2 представляет собой водород.
В некоторых вариантах осуществления R2 выбран из C1-C4-алкила, C1-C4-галогеналкила, галогена и -ORb.
В некоторых вариантах осуществления R2 представляет собой C1-С4алкил. В некоторых вариантах осуществления R2 представляет собой метил.
В некоторых вариантах осуществления R2 представляет собой галоген. В некоторых вариантах осуществления R2 представляет собой хлор.
В некоторых вариантах осуществления R2 представляет собой -ORb. В некоторых вариантах осуществления Rb представляет собой C1-С4алкил. В некоторых вариантах осуществления Rb представляет собой метил.
В некоторых вариантах осуществления R2 представляет собой гидрокси-C1-C4-алкил. В некоторых вариантах осуществления R2 представляет собой гидроксиметил.
В некоторых вариантах осуществления R2 представляет собой ацетокси-C1-C4-алкил. В некоторых вариантах осуществления R2 представляет собой ацетоксиметил.
В некоторых вариантах осуществления R2 представляет собой водород.
В некоторых вариантах осуществления Z представляет собой CR3. В некоторых вариантах осуществления R3 представляет собой C1-С4алкил. В некоторых вариантах осуществления R3 представляет собой метил. В некоторых вариантах осуществления R3 представляет собой водород.
В некоторых вариантах осуществления Z представляет собой N.
В некоторых вариантах осуществления X представляет собой N, R2 представляет собой C1-С4алкил (например, метил), Z представляет собой CR3, и R3 представляет собой C1-С4алкил (например, метил).
В некоторых вариантах осуществления X представляет собой CR1, R1 представляет собой C1-С4алкил (например, метил), R2 представляет собой галоген (например, хлор), Z представляет собой CR3, и R3 представляет собой C1-С4алкил (например, метил).
В некоторых вариантах осуществления X представляет собой CR1, R1 представляет собой водород, R2 представляет собой C1-С4алкил (например, метил), Z представляет собой CR3, и R3 представляет собой водород.
В некоторых вариантах осуществления X представляет собой CR1, R1 представляет собой C1-С4алкил (например, метил), R2 представляет собой водород, Z представляет собой CR3, и R3 представляет собой C1-С4алкил (например, метил).
В некоторых вариантах осуществления X представляет собой CR1, R1 представляет собой водород, R2 представляет собой водород, и Z представляет собой N.
В некоторых вариантах осуществления X представляет собой N, R2 представляет собой галоген (например, хлор), Z представляет собой CR3, и R3 представляет собой C1-С4алкил (например, метил).
В некоторых вариантах осуществления X представляет собой CR1, R1 представляет собой водород, R2 представляет собой галоген (например, хлор), Z представляет собой CR3, и R3 представляет собой C1-С4алкил (например, метил).
В некоторых вариантах осуществления X представляет собой N, R2 представляет собой -ORb, Rb представляет собой С1-С4алкил (например, метил), Z представляет собой CR3, и R3 представляет собой С1-С4алкил (например, метил).
В некоторых вариантах осуществления X представляет собой N, R2 представляет собой C1-C4-гидроксиалкил (например, гидроксиметил), Z представляет собой CR3, и R3 представляет собой C1-С4алкил (например, метил).
В некоторых вариантах осуществления X представляет собой N, R2 представляет собой C1-C4-ацетоксиалкил (например, ацетоксиметил), Z представляет собой CR3, и R3 представляет собой C1-С4алкил (например, метил).
В некоторых вариантах осуществления R4 представляет собой водород или алкил, и R5 выбран из алкила, алкенила, алкинила, арила, гетероарила, циклоалкила, гетероалкила, гетероцикла и -(CRcRd)n-Y, любой из которых может быть необязательно замещенным. В некоторых вариантах осуществления R4 выбран из водорода и метила; R5 выбран из C1-С4алкила, С3-С6циклоалкила, 3-6-членного гетероцикла, имеющего один гетероатом, выбранный из N и О, и -(CRcRd)n-Y; при этом n равняется 1, 2 или 3; каждый из Rc и Rd представляет собой водород; Y выбран из -OR, арила, С3-С6циклоалкила, 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S, 3-6-членного гетероцикла, имеющего один или два гетероатома, независимо выбранных из N, О и S, сульфанила, -COR, -C(O)NR2 и -SO2R; где каждый алкил, арил, циклоалкил, гетероарил и гетероцикл независимо является незамещенным или замещенным 1 или 2 заместителями, независимо выбранными из C1-С4алкила, C1-С4гидроксиалкила, C1-С4алкокси, C1-C4-алкокси-C1-C4-алкила, C1-C4-аминоалкила, -CONR2, галогена, гидрокси, арила, С3-С6циклоалкила, 3-6-членного гетероцикла, имеющего один гетероатом, независимо выбранный из N и О, и 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S; и каждый R независимо выбран из водорода, C1-С4алкила, C1-С4гидроксиалкила, C1-С4галогеналкила, C1-С4-алкокси-C1-C4-алкила, С3-С6циклоалкила, 5-6-членной гетероарильной группы, имеющей 1, 2 или 3 гетероатома, независимо выбранных из N, S и О, 3-6-членного гетероцикла, имеющего один или два гетероатома, независимо выбранных из N и О, или бициклического гетероцикла, С3-С6циклоалкила.
В некоторых вариантах осуществления R4 выбран из водорода и метила; R5 выбран из C1-С4алкила, С3-С6циклоалкила, 3-6-членного гетероцикла, имеющего один гетероатом, выбранный из N и О, и -(CRcRd)n-Y; при этом n равняется 1, 2 или 3; каждый из Rc и Rd представляет собой водород; Y выбран из -OR, арила, С3-С6циклоалкила и 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S; и R представляет собой C1-С4алкил; где каждый из арила, циклоалкила, гетероарила и гетероцикла является независимо незамещенным или замещенным 1 или 2 заместителями, независимо выбранными из C1-С4алкила, C1-С4гидроксиалкила, C1-С4алкокси, галогена, гидрокси, арила, С3-С6циклоалкила, 3-6-членного гетероцикла, имеющего один гетероатом, выбранный из N и О, и 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S.
В некоторых вариантах осуществления R4 представляет собой алкил, и R5 выбран из алкила и гетероалкила. В некоторых вариантах осуществления R4 представляет собой метил, и R5 представляет собой метил. В некоторых вариантах осуществления R4 представляет собой метил, и R5 представляет собой 2-метоксиэтил.
В некоторых вариантах осуществления R4 представляет собой водород, и R5 выбран из циклоалкила, гетероцикла и -(CRcRd)n-Y, любой из который может быть необязательно замещенным.
В некоторых вариантах осуществления R4 представляет собой водород, и R5 представляет собой C1-С4алкил, например, метил, этил, н-пропил или изобутил.
В некоторых вариантах осуществления R4 представляет собой водород, и R5 представляет собой циклоалкильную группу, выбранную из циклопропила, циклобутила, циклопентила и циклогексила, любой из которых может быть необязательно замещенным. В некоторых вариантах осуществления R4 представляет собой водород, и R5 представляет собой циклоалкильную группу, выбранную из циклопропила, циклобутила, циклопентила и циклогексила, каждый из которых является незамещенным или замещенным 1 или 2 заместителями, независимо выбранными из C1-С4алкила, арила и галогена. Например, в некоторых вариантах осуществления R5 представляет собой циклопропил, который является незамещенным или замещенным 1 или 2 заместителями, независимо выбранными из C1-С4алкила, арила и галогена. В некоторых вариантах осуществления R5 представляет собой циклопропил, который замещен фенильной группой, где фенильная группа может быть необязательно замещенной. В некоторых вариантах осуществления R5 представляет собой циклопропил, который замещен фенильной группой, где фенильная группа замещена метоксигруппой или 1 или 2 атомами галогена (например, фтора). В некоторых вариантах осуществления R5 представляет собой циклобутил, который является незамещенным или замещенным 1 или 2 заместителями, независимо выбранными из галогена (например, фтора). В некоторых вариантах осуществления R5 представляет собой 2-оксаспиро[3.3]гептан-6-ил. В некоторых вариантах осуществления R5 представляет собой 2-азаспиро[3.3]гептан-6-ил, который может быть незамещенным или замещенным заместителем, выбранным из группы, состоящей из -C(O)R, 5-6-членной гетероарильной группы, имеющей 1,2 или 3 гетероатома, выбранных из N, S и О, и 3-6-членного гетероцикла, имеющего один гетероатом, выбранный из N и О, где R выбран из C1-С4алкила, C1-C4 галогеналкила, арила и 5-6-членной гетероарильной группы, имеющей 1, 2 или 3 гетероатома, независимо выбранных из N, S и О, где алкильная, арильная, гетероарильная и гетероциклическая группы могут быть необязательно дополнительно замещены (например, заместителем, выбранным из алкила и галогена).
В некоторых вариантах осуществления R4 представляет собой водород, и R5 представляет собой гетероцикл, выбранный из азетидинила, пирролидинила и тетрагидропиранила, любой из которых может быть необязательно замещенным. Например, в некоторых вариантах осуществления R5 представляет собой азетидинил, который замещен одним заместителем. В некоторых вариантах осуществления R5 представляет собой азетидинил, который замещен ацильной группой. В некоторых вариантах осуществления R5 представляет собой азетидинил, который замещен гетероарильной группой, где гетероарильная группа может быть необязательно замещенной. В некоторых вариантах осуществления R5 представляет собой азетидинил, который замещен 5-6-членной гетероарильной группой, имеющей 1, 2 или 3 гетероатома, независимо выбранных из N, S и О, где гетероарильная группа может быть необязательно замещенной. В некоторых вариантах осуществления R5 представляет собой азетидинил, который замещен пиридинильной группой или пиримидинильной группой, где пиридинильная группа или пиримидинильная группа являются незамещенными или замещенными одним или двумя заместителями, независимо выбранными из галогена, гидрокси, C1-С4алкила, С3-С6циклоалкила, C1-С4алкокси и C1-С4галогеналкила. В некоторых вариантах осуществления R5 представляет собой азетидинил, который замещен пиридинильной группой или пиримидинильной группой, где пиридинильная группа или пиримидинильная группа замещены одним или двумя заместителями, независимо выбранными из галогена, C1-С4алкокси и С1-С4галогеналкила. В некоторых вариантах осуществления R5 представляет собой азетидинил, который замещен пиридинильной группой или пиримидинильной группой, где пиридинильная группа или пиримидинильная группа замещены изопропокси-группой. В некоторых вариантах осуществления R5 представляет собой азетидинил, который замещен пиридинильной группой или пиримидинильной группой, где пиридинильная группа или пиримидинильная группа замещены трифторметильной группой. В некоторых вариантах осуществления R5 представляет собой пирролидинил, который замещен фенильной группой. В некоторых вариантах осуществления R5 представляет собой тетрагидропиранил.
В некоторых вариантах осуществления R4 представляет собой водород, и R5 представляет собой -(CRcRd)n-Y, где Y может быть необязательно замещенным. В некоторых вариантах осуществления Rc и Rd представляют собой водород, и n равняется 1, 2 или 3. В некоторых вариантах осуществления Rc и Rd представляют собой водород, и n равняется 1. В некоторых вариантах осуществления Rc представляет собой водород, Rd представляет собой метил, и n равняется 1.
В некоторых вариантах осуществления Y представляет собой арил, который может быть необязательно замещенным. В некоторых вариантах осуществления Y представляет собой фенил, который может быть необязательно замещенным. В некоторых вариантах осуществления Y представляет собой фенил, замещенный 0, 1, 2 или 3 заместителями, независимо выбранными из алкила, галогена, гидроксиалкила, арила, циклоалкила, гетероарила, гетероциклила, сульфанила, -OR, -SR, -C(O)R, -C(O)OR, -S(O)R, -SO2R, -NR2, -C(O)NR2 и -S(O)2NR2.
В некоторых вариантах осуществления Y представляет собой фенил, замещенный 0, 1, 2 или 3 заместителями, независимо выбранными из галогена (например, фтора или хлора); гидроксиалкила (например, гидрокси-С1-С6-алкила, например, гидроксиизопропила, такого как 2-гидроксиизопропил, или гидроксипентанила, такого как 3-гидроксипентан-3-ил); алкоксиалкила (например, C1-C4-алкокси-C1-C4-алкила, например, 1-метил-1-метоксиэтила); аминоалкила (например, амино-C1-C4-алкила, например, 1-амино-1-метилэтила); 5-6-членной гетероарильной группы, имеющей 1, 2 или 3 гетероатома, независимо выбранных из N, S и О (например, тиазолила, пиридила, пиримидинила, имидазолила, тиофенила, пирролила или пиразолила); 3-6-членного гетероцикла, имеющего один или два гетероатома, независимо выбранных из N, S и О (например, оксетанила, морфолино или пиперазинила); сульфанила, такого как пентафторсульфанил; -OR, где R выбран из водорода, алкила (например, C1-С4алкила, такого как метил), 5-6-членной гетероарильной группы, имеющей 1, 2 или 3 гетероатома, независимо выбранных из N, S и О (например, пиридила); -COR, где R выбран из 3-6-членного гетероцикла, имеющего один или два гетероатома, независимо выбранных из N и О (например, азетидинила, морфолино, пиперидинила или пирролидинила), или бициклического гетероцикла (например, 2-окса-6-азаспиро[3.3]гептан-6-ила); -C(O)NR2, где каждый R независимо выбран из водорода, алкила (например, C1-С4алкила, такого как метил, этил, изопропил или изобутил), галогеналкила (например, C1-С4галогеналкила, такого как трифторметил, 2,2,2-трифторэтил или 2,2,2-трифтор-1-метилэтил), гидроксиалкила (например, 3-гидрокси-1,2,2-триметилпропила), арила (например, фенила), арилалкила (например, бензила), циклоалкила (например, С3-С6циклоалкила, такого как циклопропил, циклобутил, циклопентил или циклогексил, или конденсированного циклоалкила, такого как 2-оксаспиро[3.3]гептан-6-ил), и гетероалкила (например, 2-метоксиэтила); и -SO2R, где R представляет собой С1-С4алкил (например, метил); и где каждая из алкильной, арильной, гетероарильной, гетероциклической или циклоалкильной групп необязательно дополнительно замещена, например, 1, 2, 3, 4 или 5 заместителями.
В некоторых вариантах осуществления Y представляет собой фенил, замещенный 0, 1 или 2 заместителями, независимо выбранными из галогена, алкокси, гидроксиалкила, циклоалкила и гетероарила. В некоторых вариантах осуществления Y представляет собой фенил, замещенный 0, 1 или 2 заместителями, независимо выбранными из галогена, алкокси и гетероарила. В некоторых вариантах осуществления Y представляет собой фенил, замещенный фтором и метокси. В некоторых вариантах осуществления Y представляет собой фенил, замещенный С3-С6циклоалкилом (например, циклобутилом), который является незамещенным или замещенным гидрокси. В некоторых вариантах осуществления Y представляет собой фенил, замещенный C1-С4гидроксиалкилом (например, гидроксиизопропилом, таким как 2-гидроксиизопропил). В некоторых вариантах осуществления Y представляет собой фенил, замещенный пиридильной группой, где пиридильная группа может быть необязательно замещенной (например, группой, представляющей собой атом галогена, такой как фтор).
В некоторых вариантах осуществления Y представляет собой гетероарил, который может быть необязательно замещенным. В некоторых вариантах осуществления Y представляет собой 5-6-членную гетероарильную группу, имеющую 1, 2 или 3 гетероатома, независимо выбранных из N, S и О, которая может быть необязательно замещенной. В некоторых вариантах осуществления Y выбран из пиридинила и пиримидинила, каждый из которых является независимо незамещенным или замещенным 1 или 2 заместителями, независимо выбранными из С1-С4алкила (например, метила), C1-С4гидроксиалкила (например, гидроксиизопропила, такого как 2-гидроксиизопропил), С1-С4галогеналкила (например, трифторметила), C1-С4галогеналкокси (например, дифторметокси) и изоциано. В некоторых вариантах осуществления Y выбран из пиридинила и пиримидинила, каждый из которых является независимо незамещенным или замещенным 1 или 2 заместителями, независимо выбранными из C1-С4алкила (например, метила) и С1-С4гидроксиалкила (например, гидроксиизопропила, такого как 2-гидроксиизопропил).
В некоторых вариантах осуществления Y представляет собой С3-С6циклоалкил (например, циклобутил или бицикло[1.1.1]пентанил), который может быть необязательно замещенным, например, заместителем, выбранным из галогена (например, фтора), -OR, где R представляет собой С1-С4алкил (например, метил), и -COOR, где R представляет собой C1-С4алкил (например, метил). В некоторых вариантах осуществления Y представляет собой 3-6-членный гетероцикл, имеющий один или два гетероатома, независимо выбранных из N и О (например, тетрагидрофуранил). В некоторых вариантах осуществления Y представляет собой -OR, где R представляет собой C1-С4алкил (например, метил).
В некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют азетидинильную, пирролидинильную, пиперидинильную или пиперазинильную группу, которая может быть необязательно замещена 1, 2 или 3 заместителями, независимо выбранными из алкила, алкенила, алкинила, арила, гетероарила, циклоалкила, гетероалкила, гетероцикла, циано, гидроксиалкила, алкоксиалкила и -(CRcRd)p-Y, где p равняется 0, 1, 2, 3, 4, 5, 6, 7 или 8. В некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют азетидинильную, пирролидинильную, пиперидинильную или пиперазинильную группу, которая может быть необязательно замещена 1, 2 или 3 заместителями, независимо выбранными из алкила, алкенила, алкинила, арила, гетероарила, циклоалкила, гетероалкила, гетероцикла и -(CRcRd)p-Y, где p равняется 0, 1, 2, 3, 4, 5, 6, 7 или 8.
В некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют азетидинильную, пирролидинильную, пиперидинильную или пиперазинильную группу, каждая из которых является независимо незамещенной или замещенной 1 или 2 заместителями, независимо выбранными из C1-С4алкила, С3-С6циклоалкила, арила, 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S, 3-6-членного гетероцикла, имеющего один гетероатом, независимо выбранный из N и О, оксо и -(CRcRd)p-Y; при этом p равняется 0 или 1; каждый из Rc и Rd представляет собой водород; каждый Y независимо выбран из С1-С4алкила, арила, -OR, -NR2; и каждый R независимо выбран из водорода, С1-С4алкила, арила и 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S; где каждый из арила, циклоалкила, гетероарила и гетероцикла является независимо незамещенным или замещенным 1 или 2 заместителями, независимо выбранными из C1-С4алкила, С1-С4галогеналкила, циано и галогена.
В некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют азетидинильную, пирролидинильную, пиперидинильную или пиперазинильную группу, каждая из которых является независимо незамещенной или замещенной 1 или 2 заместителями, независимо выбранными из С1-С4алкила, С3-С6циклоалкила, арила, 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S, 3-6-членного гетероцикла, имеющего один гетероатом, независимо выбранный из N и О, оксо и -(CRcRd)p-Y; при этом p равняется 0 или 1; каждый из Rc и Rd представляет собой водород или C1-С4алкил; Y выбран из C1-С4алкила, арила, -OR, -NR2, -C(O)OR, -C(O)NR2 и -NRC(O)R; и каждый R независимо выбран из водорода, C1-С4алкила, арила и 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S; где каждый из арила, циклоалкила, гетероарила и гетероцикл а является независимо незамещенным или замещенным 1 или 2 заместителями, независимо выбранными из C1-С4алкила, гидрокси, циано, C1-С4-галогеналкила и галогена.
В некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют азетидинильную, пирролидинильную, пиперидинильную или пиперазинильную группу, каждая из которых является независимо незамещенной или замещенной 1 или 2 заместителями, независимо выбранными из C1-С4алкила, С3-С6циклоалкила, арила, 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S, 3-6-членного гетероцикла, имеющего один гетероатом, независимо выбранный из N и О, оксо и -(CRcRd)p-Y; при этом p равняется 0 или 1; каждый из Rc и Rd представляет собой водород; Y выбран из C1-С4алкила, арила, -OR, -NR2; и каждый R независимо выбран из водорода и C1-С4алкила; где каждый из арила, циклоалкила, гетероарила и гетероцикла является независимо незамещенным или замещенным 1 или 2 заместителями, независимо выбранными из C1-С4алкила и галогена.
В некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют пиперидинильную группу. В некоторых вариантах осуществления пиперидинильная группа является незамещенной.
В некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют пиперазинильную группу, которая может быть необязательно замещенной. Например, пиперазинильное кольцо может быть замещено циклоалкильной группой, такой как циклопропил.
В некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют пирролидинильную группу, которая может быть необязательно замещенной. В некоторых вариантах осуществления пирролидинильная группа является незамещенной. В некоторых вариантах осуществления пирролидинильная группа может быть замещена 1 или 2 заместителями, независимо выбранными из галогена, арила и -(CRcRd)p-Y. В некоторых вариантах осуществления пирролидинильная группа замещена фенильной группой. В некоторых вариантах осуществления пирролидинильная группа замещена двумя группами, представляющими собой атом галогена (например, фтора). В некоторых вариантах осуществления пирролидинильная группа замещена одной группой, которая представляет собой -(CRcRd)p-Y, где p равняется 0, и Y представляет собой -NR2, и каждый R независимо представляет собой алкил (например, метил).
В некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют азетидинильную группу, которая может быть необязательно замещенной. В некоторых вариантах осуществления азетидинильная группа является незамещенной. В некоторых вариантах осуществления азетидинильная группа может быть замещенной 1 или 2 заместителями, независимо выбранными из алкила, галогена, гетероалкила, гетероарила, оксо и -(CRcRd)p-Y. В некоторых вариантах осуществления азетидинильная группа замещена гетероалкильной группой, такой как метоксиметильная группа. В некоторых вариантах осуществления азетидинильная группа замещена гетероарильной группой, такой как пиридинильная или пиримидинильная группа. В некоторых вариантах осуществления гетероарильная группа (такая как пиридинильная или пиримидинильная группа) является незамещенной или замещенной 1 или 2 заместителями, независимо выбранными из C1-С4алкила, галогена, галогеналкила, С3-С6циклоалкила и -OR, где R представляет собой водород или С1-С4алкил. В некоторых вариантах осуществления азетидинильная группа замещена оксогруппой. В некоторых вариантах осуществления азетидинильная группа замещена двумя группами, представляющими собой атом галогена (например, фтора). В некоторых вариантах осуществления азетидинильная группа замещена одной группой, которая представляет собой -(CRcRd)p-Y, где p равняется 0, и Y представляет собой -OR, где R представляет собой арил, который может быть необязательно замещенным. В некоторых вариантах осуществления R представляет собой незамещенный фенил. В некоторых вариантах осуществления R представляет собой фенил, замещенный одной группой, представляющей собой атом галогена (например, фтора). В некоторых вариантах осуществления азетидинильная группа замещена двумя заместителями, независимо выбранными из алкила (например, метила) и -(CRcRd)p-Y, где p равняется О, и Y представляет собой -OR, где R представляет собой водород.
В некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют конденсированную бициклическую гетероциклическую группу. Например, в некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют 3-азабицикло[3.1.0]гексан-3-ильную группу или изоиндолинильную группу, каждая из которых может быть необязательно замещенной.
В некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют спирогетероциклическую группу. Например, в некоторых вариантах осуществления R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют 2-окса-6-азаспиро[3.3]гептан-6-ильную группу или 2,6-диазаспиро[3.3]гептан-2-ильную группу.
В некоторых вариантах осуществления R6 представляет собой водород.
В другом аспекте соединение формулы (I) представляет собой соединение формулы (Ic)

или его фармацевтически приемлемую соль, где:
R2 выбран из C1-С4-алкила, C1-С4-галогеналкила, галогена и -ORb.
В другом аспекте соединение формулы (I) представляет собой соединение формулы (Id)
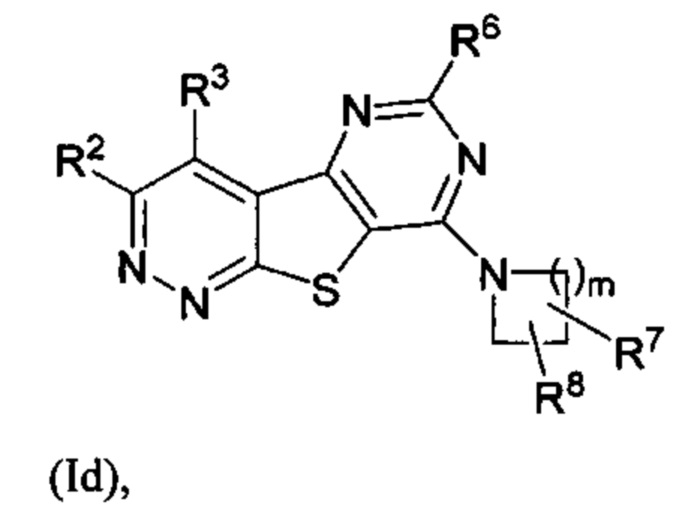
или его фармацевтически приемлемую соль, где:
R7 выбран из водорода, C1-С4алкила и галогена;
R8 представляет собой необязательно замещенный арил, гетероарил, арилокси или гетероарилокси; и
m равняется 1, 2 или 3.
В другом аспекте соединение формулы (I) представляет собой соединение формулы (Ie)
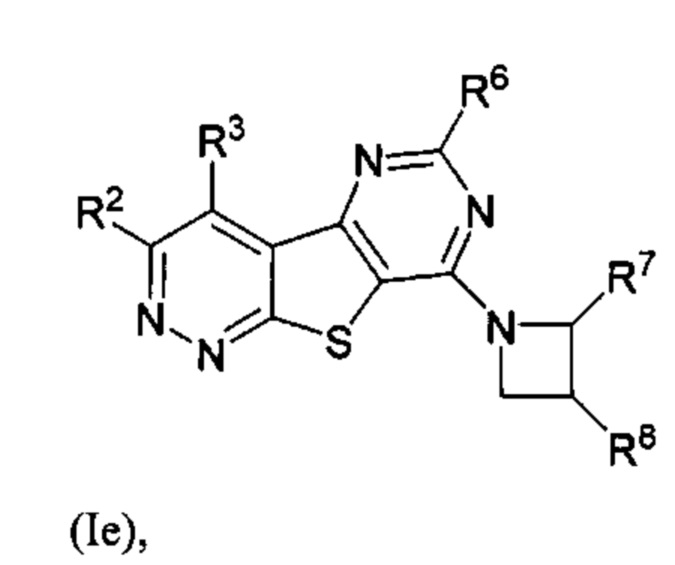
или его фармацевтически приемлемую соль, где:
R7 выбран из водорода, C1-С4алкила и галогена; и
R8 представляет собой необязательно замещенный арил или гетероарил.
В некоторых вариантах осуществления R8 представляет собой необязательно замещенный фенил.
В другом аспекте соединение формулы (I) представляет собой соединение формулы (If)

или его фармацевтически приемлемую соль, где:
А представляет собой 3-, 4-, 5-, 6- или 7-членный циклоалкил или гетероцикл; и
R9 представляет собой необязательно замещенный арил или гетероарил.
В другом аспекте соединение формулы (I) представляет собой соединение формулы (Ig)

или его фармацевтически приемлемую соль, где:
R1 представляет собой C1-C4-алкил;
R2 выбран из водорода и галогена; и
R3 представляет собой C1-C4-алкил.
В некоторых вариантах осуществления R1 представляет собой метил, R2 представляет собой хлор, и R3 представляет собой метил.
В другом аспекте соединение формулы (I) представляет собой соединение формулы (Ih)
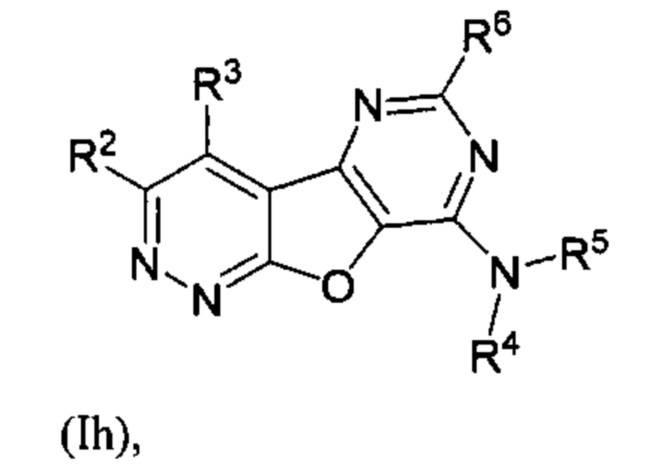
или его фармацевтически приемлемую соль, где:
R2 представляет собой C1-C4-алкил; и
R3 представляет собой C1-C4-алкил.
В другом аспекте соединение формулы (I) представляет собой соединение формулы (Ii)

или его фармацевтически приемлемую соль, где:
А выбран из арила, циклоалкила, гетероциклила или гетероарила;
q равняется 1, 2 или 3; и
каждый R9 независимо выбран из алкила, галогена, гидроксиалкила, алкоксиалкила, аминоалкила, арила, циклоалкила, гетероарила, гетероциклила, сульфанила, -(CRcRd)p-Y, -OR, -SR, -C(O)R, -C(O)OR, -S(O)R, -SO2R, -NR2, -C(O)NR2 и -S(O)2NR2, каждый из которых может быть необязательно замещенным.
В некоторых вариантах осуществления А выбран из фенила, С3-С6циклоалкила, 3-6-членного гетероцикла, имеющего один или два гетероатома, независимо выбранных из N, S и О, и 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S.
В некоторых вариантах осуществления А представляет собой фенил, и каждый R9 независимо выбран из галогена (например, фтора или хлора); гидроксиалкила (например, гидрокси-С1-С6-алкила, например, гидроксиизопропила, такого как 2-гидроксиизопропил, или гидроксипентанила, такого как 3-гидроксипентан-3-ил); алкоксиалкила (например, С1-С4-алкокси-С1-С4-алкила, например, 1-метил-1-метоксиэтила); аминоалкила (например, амино-C1-C4-алкила, например, 1-амино-1-метилэтила); 5-6-членной гетероарильной группы, имеющей 1, 2 или 3 гетероатома, независимо выбранных из N, S и О (например, тиазолила, пиридила, пиримидинила, имидазолила, тиофенила, пирролила или пиразолила); 3-6-членного гетероцикла, имеющего один или два гетероатома, независимо выбранных из N, S и О (например, оксетанила, морфолино или пиперазинила); сульфанила, такого как пентафторсульфанил; -OR, где R выбран из водорода, алкила (например, C1-С4алкила, такого как метил), 5-6-членной гетероарильной группы, имеющей 1, 2 или 3 гетероатома, независимо выбранных из N, S и О (например, пиридила); -COR, где R выбран из 3-6-членного гетероцикла, имеющего один или два гетероатома, независимо выбранных из N и О (например, азетидинила, морфолино, пиперидинила или пирролидинила), или бициклического гетероцикла (например, 2-окса-6-азаспиро[3.3]гептан-6-ила); -C(O)NR2, где каждый R независимо выбран из водорода, алкила (например, C1-С4алкила, такого как метил, этил, изопропил или изобутил), галогеналкила (например, C1-С4 галогеналкила, такого как трифторметил, 2,2,2-трифторэтил или 2,2,2-трифтор-1-метилэтил), гидроксиалкила (например, 3-гидрокси-1,2,2-триметилпропила), арила (например, фенила), арилалкила (например, бензила), циклоалкила (например, С3-С6циклоалкила, такого как циклопропил, циклобутил, циклопентил или циклогексил, или конденсированного циклоалкила, такого как 2-оксаспиро[3.3]гептан-6-ил), и гетероалкила (например, 2-метоксиэтила); и -SO2R, где R представляет собой C1-С4алкил (например, метил); и где каждая из алкильной, арильной, гетероарильной, гетероциклической или циклоалкильной групп необязательно дополнительно замещена, например, 1, 2, 3, 4 или 5 заместителями.
В некоторых вариантах осуществления А представляет собой фенил, и каждый R9 независимо выбран из C1-С6алкила, галогена, C1-С6гидроксиалкила, С1-С6-алкокси-С1-С6-алкила, фенила, С3-С6циклоалкила, 3-6-членного гетероцикла, имеющего один или два гетероатома, независимо выбранных из N, О и S, 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S, -(CRcRd)p-Y, -OR, -C(O)R, -C(O)NR2, -SO2R; при этом каждый Y независимо выбран из С3-С6циклоалкила, 3-6-членного гетероцикла, имеющего один или два гетероатома, независимо выбранных из N, О и S, и 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S; p равняется 1; Rc и Rd представляют собой водород; каждый R независимо выбран из водорода, C1-С6алкила, гидрокси, С3-С6циклоалкила, 3-6-членного гетероцикла, имеющего один или два гетероатома, независимо выбранных из N, О и S, и 5-6-членного гетероарила, имеющего 1 или 2 гетероатома, независимо выбранных из N, О и S; и каждый алкил, фенил, циклоалкил, гетероциклил и гетероарил является независимо незамещенным или замещенным 1, 2 или 3 заместителями, независимо выбранными из галогена, гидрокси, C1-С4алкила, C1-С4галогеналкила, С3-С6циклоалкила, C1-С4алкокси и C1-С4галогеналкокси.
Иллюстративные соединения формулы (I) включают без ограничения:
N,N,3,4-тетраметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-циклогексил-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-(тетрагидро-2Н-пиран-4-ил)пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-8-(пиперидин-1-ил)пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
N-циклобутил-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-8-(пирролидин-1-ил)пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-N-(1-(5-(трифторметил)пиримидин-2-ил)азетидин-3-ил)пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
8-(4-циклопропилпиперазин-1-ил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
8-(азетидин-1-ил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
8-(3-азабицикло[3.1.0]гексан-3-ил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)-N,N-диметилпирролидин-3-амин;
N-(2-метоксиэтил)-N,3,4-триметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
6-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)-2-окса-6-азаспиро[3.3]гептан;
8-(3-(метоксиметил)азетидин-1-ил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
8-метил-4-(пирролидин-1-ил)пиридо[3',2':4,5]тиено[3,2-d]пиримидин;
4-(3,3-дифторпирролидин-1-ил)-8-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
8-метил-N-(1-(5-(трифторметил)пиримидин-2-ил)азетидин-3-ил)пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
4-(азетидин-1-ил)-8-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
6-(8-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)-2-окса-6-азаспиро[3.3]гептан;
N-(1-(5-(трифторметил)пиримидин-2-ил)азетидин-3-ил)пиразино[2',3':4,5]тиено[3,2-d]пиримидин-4-амин;
8-(3,3-дифторазетидин-1-ил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-N-(1-(6-(трифторметил)пиридин-3-ил)азетидин-3-ил)пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-(1-фенилпирролидин-3-ил)пиримидо[4',5':4,5]тиено[2,3-с] пиридазин-8-амин;
3,4-диметил-8-(3-(пиридин-4-ил)азетидин-1-ил)пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
N-циклопропил-3,4-диметилпиримидо[4',5,:4,5]тиено[2,3-с]пиридазин-8-амин;
N-(2-(4-метоксифенил)циклопропил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-(3-фтор-4-метоксибензил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-8-(3-фенилпирролидин-1-ил)пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
N-(4-(2-фторпиридин-3-ил)бензил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
8-(3-(4-фторфенокси)азетидин-1-ил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
8-(3-(2-фторфенокси)азетидин-1-ил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
8-(3-(3-фторфенокси)азетидин-1-ил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-(3-феноксиазетидин-1-ил)пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)-3-метилазетидин-3-ол;
1-(3-((3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино)азетидин-1-ил)этан-1-он;
1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)азетидин-3-он;
8-хлор-N-(3,3-дифторциклобутил)-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-циклопропил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
2-[4-[[(8-хлор-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-ил)амино]метил]фенил]пропан-2-ол;
8-хлор-N-(2,2-диметилциклопропил)-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-(2-этилциклопропил)-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
4-(азетидин-1-ил)-8-хлор-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин;
8-хлор-N,N,7,9-тетраметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N,7,9-триметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-7,9-диметил-N-пропилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-изобутил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-этил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-7,9-диметил-4-пирролидин-1-илпиридо[3',2':4,5]фуро[3,2-d]пиримидин;
8-хлор-N-циклобутил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-циклопентил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-[2-(3,4-дифторфенил)циклопропил]-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-(циклобутилметил)-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-(3-метоксипропил)-7,9-диметилпиридо[3',2':4,5]фуро[3,2-s]пиримидин-4-амин;
8-хлор-7,9-диметил-N-[(2-метилпиримидин-5-ил)метил]пиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
N-циклобутил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
7,9-диметил-4-(2-окса-6-азаспиро[3.3]гептан-6-ил)пиридо[3',2':4,5]фуро[3,2-d]пиримидин;
2-[3-[[(7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-ил)амино]метил]фенил]пропан-2-ол;
N-[1-(5-изопропоксипиримидин-2-ил)азетидин-3-ил]-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
N-[1-(5-фторпиримидин-2-ил)азетидин-3-ил]-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
N-[1-(2,5-дихлор-4-пиридил)азетидин-3-ил]-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
N-[2-(3,4-дифторфенил)циклопропил]-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
N-циклопропил-7,9-диметилпиридо[3',2',:4,5]фуро[3,2-d]пиримидин-4-амин;
N-[1-(5-фторпиримидин-2-ил)азетидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
1-[4-[[(3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]фенил]циклобутанол;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол;
1-[3-[[(3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]фенил]циклобутанол;
2-[3-[[(3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол;
N-циклопропил-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
N-циклобутил-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
N-циклопентил-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
3,4-диметил-N-(2-оксаспиро[3.3]гептан-6-ил)пиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
N-(3,3-дифторциклобутил)-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
3,4-диметил-8-(2-окса-6-азаспиро[3.3]гептан-6-ил)пиримидо[4',5':4,5]фуро[2,3-с]пиридазин;
2-[5-[[(3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]-2-пиридил]пропан-2-ол;
N-[(3-фтор-4-метоксифенил)метил]-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол;
N-(2-(4-метоксифенил)циклопропил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-(3-фтор-4-метоксибензил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-(4-(2-фторпиридин-3-ил)бензил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)-3-метилазетидин-3-ол;
N-[1-(2,3-дифторфенил)пирролидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[1-(3-хлор-5-циклопропил-2-пиридил)азетидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[1-(6-циклопропил-2-метил-3-пиридил)азетидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[1-(5-фторпиримидин-2-ил)азетидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[1-(2,5-дихлор-4-пиридил)азетидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[1-(5-циклопропилпиразин-2-ил)азетидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
трет-бутил-3-[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]азетидин-1-карбоксилат;
N-(азетидин-3-ил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[1-(5-изопропоксипиримидин-2-ил)азетидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[[6-(дифторметокси)-3-пиридил]метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[[4-(циклопропилметокси)-3-фторфенил]метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[[4-(пентафтор-16-сульфанил)фенил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[(4-метилсульфонилфенил)метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[(3,4-диметоксифенил)метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)азетидин-3-амин;
N-[1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)азетидин-3-ил]ацетамид;
N-[1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)азетидин-3-ил]пиридин-4-карбоксамид;
1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)-3-метилазетидин-3-амин;
(3R)-1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)пирролидин-3-амин;
2-[4-[1-[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]этил]фенил]пропан-2-ол;
1-[4-[1-[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]этил]фенил]циклобутанол;
1-[3-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]циклобутанол;
3-циклопропил-1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)азетидин-3-ол;
1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)азетидин-3-карбоксамид;
8-(2,6-диазаспиро[3.3]гептан-2-ил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
2-[5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-пиридил]пропан-2-ол;
2-[4-[[(3,4-диметилпиримидо[4,5]тиено[1,2-с]пиридазин-8-ил)амино]метил]-3-фторфенил]пропан-2-ол;
3,4-диметил-N-[[4-(морфолинометил)фенил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[[4-(2-пиридил)фенил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[[4-(2-пиридилокси)фенил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[[4-(4-метилпиперазин-1-ил)фенил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фторфенил]пропан-2-ол;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]-1,1,1-трифторпропан-2-ол;
1-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]циклобутанол;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-3-фторфенил]бутан-2-ол;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]бутан-2-ол;
2-[1-[[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]метил]пирролидин-2-ил]пропан-2-ол;
3,4-диметил-N-[(4-пиперазин-1-илфенил)метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[2-(3,4-дифторфенил)циклопропил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[[4-[4-(2-метоксиэтил)пиперазин-1-ил]фенил]метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[(2,6-дифтор-4-метоксифенил)метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]пирролидин-1-илметанон;
[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]морфолинометанон;
[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]-(2-окса-6-азаспиро[3.3]гептан-6-ил)метанон;
[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]-(1-пиперидил)метанон;
3-азабицикло[3.1.0]гексан-3-ил-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]метанон;
[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]-[3-(метоксиметил)азетидин-1-ил]метанон;
[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]-[(3S)-3-фторпирролидин-1-ил]метанон;
[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]-[(3R)-3-фторпирролидин-1-ил]метанон;
(4,4-дифтор-1-пиперидил)-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]метанон;
азетидин-1-ил-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]метанон;
N-циклопропил-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-метилбензамид;
N-циклопропил-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бензамид;
(3,3-дифторпирролидин-1-ил)-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]метанон;
N-[(4-метоксифенил)метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[(3,5-дифтор-4-метоксифенил)метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)метиламино]метил]фенил]пропан-2-ол;
2-[1-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-3-бицикло[1.1.1]пентанил]пропан-2-ол;
N-(3-фтор-1-бицикло[1.1.1]пентанил)-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
метил-1-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бицикло[1.1.1]пентан-3-карбоксилат;
2-((1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)азетидин-3-ил)амино)никотинонитрил;
2-[2-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)изоиндолин-5-ил]пропан-2-ол;
1-циклопропил-1-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]этанол;
3-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]пентан-3-ол;
4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-метилбензамид;
3,4-диметил-N-[[6-(трифторметил)-3-пиридил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[(4,6-диметил-3-пиридил)метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[(5,6-диметил-3-пиридил)метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-(1-метилциклопропил)бензамид;
N-циклобутил-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бензамид;
4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-c]пиридазин-8-ил)амино]метил]-N-(3-фторциклобутил)бензамид;
N-(3,3-дифторциклобутил)-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бензамид;
N-циклопентил-4-[[3,4-диметилпиримидо[4',5':4,5]тиено[2,3-c]пиридазин-8-ил)амино]метил]бензамид;
4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-(2-оксаспиро[3.3]гептан-6-ил)бензамид;
4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-изопропилбензамид;
(3,3-дифторазетидин-1-ил)-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]метанон;
4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-[(1R)-2,2,2-трифтор-1-метилэтил]бензамид;
4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-(3-гидрокси-1,2,2-триметилпропил)бензамид;
N-цикклогексил-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-3-ил)амино]метил]бензамид;
N-(4,4-диметилциклогексил)-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бензамид;
N-[1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)азетидин-3-ил]-2,3-дифторпиридин-4-амин;
N-[2-(3,5-дихлор-2-пиридил)-2-азаспиро[3.3]гептан-6-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[2-(3-хлор-5-фтор-2-пиридил)-2-азаспиро[3.3]гептан-6-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[2-(5-хлор-3-фтор-2-пиридил)-2-азаспиро[3.3]гептан-6-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[2-(5-метилпиримидин-2-ил)-2-азаспиро[3.3]гептан-6-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[2-[(2-метилпиримидин-5-ил)метил]-2-азаспиро[3.3]гептан-6-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[2-[[2-(трифторметил)пиримидин-5-ил]метил]-2-азаспиро[3.3]гептан-6-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
1-[6-[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]-2-азаспиро[3.3]гептан-2-ил]-3,3,3-трифторпропан-1-он;
[6-[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]-2-азаспиро[3.3]гептан-2-ил]тетрагидропиран-4-илметанон;
1-[6-[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]-2-азаспиро[3.3]гептан-2-ил]гексан-1-он;
2-[1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)пирролидин-3-ил]пропан-2-ол;
[6-[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]-2-азаспиро[3.3]гептан-2-ил]-[4-(трифторметил)фенил]метанон;
1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)-N-[4-(трифторметил)фенил]пирролидин-3-карбоксамид;
1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)-N-(2-пиридил)пирролидин-3-карбоксамид;
2-[5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фторфенил]пропан-2-ол;
N-циклопропил-5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фторбензамид;
N-циклобутил-5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фторбензамид;
N-циклопентил-5-[[3,4-диметилпиримидо[4',5',4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фторбензамид;
5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фтор-N-изопропилбензамид;
5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фтор-N-изобутилбензамид;
N-(2,2-диметилциклопропил)-5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фторбензамид;
5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фтор-N-[(1R)-2,2,2-трифтор-1-метилэтил]бензамид;
5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фтор-N-(3-фторциклобутил)бензамид;
N-(3,3-дифторциклобутил)-5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фторбензамид;
5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фтор-N-(3-гидрокси-1,2,2-триметилпропил)бензамид;
5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фтор-N-(2-метоксиэтил)бензамид;
5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-фтор-N-метилбензамид;
2-[2-хлор-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол;
2-[3-хлор-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол;
3,4-диметил-N-[[4-(2-тиенил)фенил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[[4-(1Н-пиррол-2-ил)фенил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[[4-(1-метилпиразол-3-ил)фенил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-Диметил-N-[[4-(2-метилпиразол-3-ил)фенил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
4-[3-(метоксиметил)азетидин-1-ил]-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
6-(7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)-2-окса-6-азаспиро[3.3]гептан;
4-(3-азабицикло[3.1.0]гексан-3-ил)-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
4-(азетидин-1-ил)-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
4-(3,3-дифторазетидин-1-ил)-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
7,9-диметил-4-пирролидин-1-илпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
N-циклобутил-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
7,9-диметил-4-[3-(4-пиридил)азетидин-1-ил]пиридо[3',2':4,5]тиено[3,2-d]пиримидин;
N-[2-(4-метоксифенил)циклопропил]-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
N-[[6-(дифторметокси)-3-пиридил]метил]-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
7,9-диметил-N-[(4-метилсульфонилфенил)метил]пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
7,9-диметил-N-[(2-метилпиримидин-5-ил)метил]пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
2-[4-[[(7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)амино]метил]фенил]пропан-2-ол;
7,9-диметил-N-[1-[5-(трифторметил)пиримидин-2-ил]азетидин-3-ил]пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
1-[4-[3-[(7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)амино]азетидин-1-ил]-2-пиридил]циклобутанол;
3-хлор-4-метил-8-пирролидин-1-илпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3-хлор-N-циклобутил-4-метилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3-хлор-N-[6-(дифторметокси)-3-пиридил]метил]-4-метилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3-хлор-N-[(3-фтор-4-метоксифенил)метил]-4-метилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
2-[4-[[(3-хлор-4-метилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол;
3-хлор-4-метил-N-[1-[5-(трифторметил)пиримидин-2-ил]азетидин-3-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
8-хлор-9-метил-4-пирролидин-1-илпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
8-хлор-4-(3,3-дифторпирролидин-1-ил)-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
1-(8-хлор-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)азетидин-3-карбонитрил;
8-хлор-4-[3-(метоксиметил)азетидин-1-ил]-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
4-(3-азабицикло[3.1.0]гексан-3-ил)-8-хлор-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
8-хлор-4-(3-фторпирролидин-1-ил)-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
4-(азетидин-1-ил)-8-хлор-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
6-(8-хлор-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)-2-окса-6-азаспиро[3.3]гептан;
8-хлор-4-(3,3-дифторазетидин-1-ил)-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
8-хлор-9-метил-4-[3-(4-пиридил)азетидин-1-ил]пиридо[3',2':4,5]тиено[3,2-d]пиримидин;
8-хлор-N-[1-(5-фторпиримидин-2-ил)азетидин-3-ил]-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-9-метил-N-(1-метилциклопропил)пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-(2,2-диметилциклопропил)-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-циклобутил-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
4-[[(8-хлор-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)амино]метил]-N,N-диметилбензамид;
8-хлор-N-[(3,5-диметоксифенил)метил]-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-[1-(2,5-дихлор-4-пиридил)азетидин-3-ил]-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-9-метил-N-[[4-(морфолинометил)фенил]метил]пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-[(2,2-диметил-3H-бензофуран-5-ил)метил]-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-(1,3-дигидроизобензофуран-5-илметил)-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-(6,7-дигидро-5Н-циклопента[b]пиридин-3-илметил)-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-[2-(4-метоксифенил)циклопропил]-9-метилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-9-метил-N-[(4-метилсульфонилфенил)метил]пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-9-метил-N-[(2-метилпиримидин-5-ил)метил]пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
1-[4-[3-[(8-хлор-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)амино]азетидин-1-ил]-2-пиридил]циклобутанол;
2-[4-[[(8-хлор-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)амино]метил]фенил]пропан-2-ол;
8-хлор-7,9-диметил-N-[1-[5-(трифторметил)пиримидин-2-ил]азетидин-3-ил]пиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-7,9-диметил-4-пирролидин-1-илпиридо[3',2':4,5]фуро[3,2-d]пиримидин;
8-хлор-N-циклобутил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-(3,3-дифторциклобутил)-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-циклопропил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-циклопентил-7,9-диметилпиридо[3',2';4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-[2-(3,4-дифторфенил)циклопропил]-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-7,9-диметил-N-[(4-метилсульфонилфенил)метил]пиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-(циклобутилметил)-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-(3-метоксипропил)-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
2-[4-[[(8-хлор-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-ил)амино]метил]фенил]пропан-2-ол;
8-хлор-7,9-диметил-N-[(2-метилпиримидин-5-ил)метил]пиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-[(3-фтор-4-метоксифенил)метил]-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-7,9-диметил-4-пирролидин-1-илпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
8-хлор-4-(3,3-дифторпирролидин-1-ил)-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
1-(8-хлор-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)азетидин-3-карбонитрил;
4-(3-азабицикло[3.1.0]гексан-3-ил)-8-хлор-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
8-хлор-4-(3-фторпирролидин-1-ил)-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
4-(азетидин-1-ил)-8-хлор-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
6-(8-хлор-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)-2-окса-6-азаспиро[3.3]гептан;
8-хлор-4-(3,3-дифторазетидин-1-ил)-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин;
8-хлор-7,9-диметил-4-[3-(4-пиридил)азетидин-1-ил]пиридо[3',2':4,5]тиено[3,2-d]пиримидин;
8-хлор-N-[1-(5-фторпиримидин-2-ил)азетидин-3-ил]-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-7,9-диметил-N-(1-метилциклопропил)пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-(2,2-диметилциклопропил)-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-циклобутил-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-[(3,4-диметоксифенил)метил]-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-[(4-имидазол-1-илфенил)метил]-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-7,9-диметил-N-[[4-(морфолинометил)фенил]метил]пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-[(2,2-диметил-3Н-бензофуран-5-ил)метил]-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-7,9-диметил-N-[(2-метилпиримидин-5-ил)метил]пиридо[3',2':4,5]тиено[3,2-d] пиримидин-4-амин;
8-хлор-7,9-диметил-N-[1-[5-(трифторметил)пиримидин-2-ил]азетидин-3-ил]пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-7,9-диметил-N-(тетрагидрофуран-3-илметил)пиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-(3,3-дифторциклобутил)-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
8-хлор-N-циклопропил-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-амин;
1-[4-[[(8-хлор-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)амино]метил]фенил]циклобутанол;
1-[3-[[(8-хлор-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)амино]метил]фенил]циклобутанол;
2-[4-[[(8-хлор-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)амино]метил]-2-фторфенил]пропан-2-ол;
2-[4-[[(8-хлор-7,9-диметилпиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-ил)амино]метил]-3-фторфенил]пропан-2-ол;
2-[4-[[(3-метокси-4-метилпиримидо[4',5':4,5]тиено[2,3-c]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол;
3-метокси-4-метил-8-пирролидин-1-илпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3-метокси-4-метил-N-[1-[5-(трифторметил)пиримидин-2-ил]азетидин-3-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
8-хлор-N-(2,2-диметилциклопропил)-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-(2-этилциклопропил)-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-7,9-диметил-N-пропилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-изобутил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
8-хлор-N-этил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
2-[3-[[(8-хлор-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-ил)амино]метил]фенил]пропан-2-ол;
N-[1-(5-фторпиримидин-2-ил)азетидин-3-ил]-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
N-[1-(2,5-дихлор-4-пиридил)азетидин-3-ил]-7,9-диметилпиридо[3',2':4,5]фуро[3,1-d]пиримидин-4-амин;
7,9-диметил-N-[1-[5-(трифторметил)пиразин-2-ил]азетидин-3-ил]пиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
7,9-диметил-N-[(4-метилсульфонилфенил)метил]пиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
N-циклобутил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
N-[2-(3,4-дифторфенил)циклопропил]-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
N-циклопропил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин;
7,9-диметил-4-(2-окса-6-азаспиро[3.3]гептан-6-ил)пиридо[3',2':4,5]фуро[3,2-d]пиримидин;
1-[4-[[(3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]фенил]циклобутанол;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол;
1-[3-[[(3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]фенил]циклобутанол;
2-[3-[[(3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол;
N-циклопропил-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
N-циклобутил-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-c]пиридазин-8-амин;
N-циклопентил-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
3,4-диметил-N-(2-оксаспиро[3.3]гептан-6-ил)пиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
N-(3,3-дифторциклобутил)-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
3,4-диметил-8-(2-окса-6-азаспиро[3.3]гептан-6-ил)пиримидо[4',5':4,5]фуро[2,3-с]пиридазин;
2-[5-[[(3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]-2-пиридил]пропан-2-ол;
N-[(4-метоксифенил)метил]-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
N-[(2,6-дифтор-4-метоксифенил)метил]-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
N-[(3,5-дифтор-4-метоксифенил)метил]-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]фенил]-1,1,1-трифторпропан-2-ол;
N-[1-(3,4-дифторфенил)азетидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин;
2-хлор-N-циклопропил-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бензамид;
N-[1-(3,5-дихлор-2-пиридил)азетидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[1-(5-хлор-3-фтор-2-пиридил)азетидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
2-хлор-N-циклобутил-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бензамид;
2-хлор-N-циклопентил-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бензамид;
2-хлор-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-изопропилбензамид;
2-хлор-N-(2,2-диметилциклопропил)-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бензамид;
2-хлор-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-[(1R)-2,2,2-трифтор-1-метилэтил]бензамид;
2-хлор-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-(3-фторциклобутил)бензамид;
2-хлор-N-(3,3-дифторциклобутил)-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бензамид;
2-хлор-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-[1-[1-(гидроксиметил)циклопропил]этил]бензамид;
2-хлор-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-(2-метоксиэтил)бензамид;
2-хлор-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-N-метилбензамид;
3,4-диметил-N-[(4-тиазол-2-илфенил)метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[(3-пиримидин-2-илфенил)метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[(3-пиразол-1-илфенил)метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
8-[(3S)-3-[(2-хлор-4-пиридил)окси]пирролидин-1-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-[(3S)-3-[(2-метил-4-пиридил)окси]пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-[(3S)-3-[[2-(трифторметил)-4-пиридил]окси]пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-[(3S)-3-(3-пиридилокси)пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
5-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)(метил)амино]метил]-2-фтор-N-метилбензамид;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-2-метилфенил]пропан-2-ол;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-3-метилфенил]пропан-2-ол;
8-[(3R)-3-[(2-хлор-4-пиридил)окси]пирролидин-1-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-[(3R)-3-[[2-(трифторметил)-4-пиридил]окси]пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-[(3R)-3-[(2-метил-4-пиридил)окси]пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3-[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]-1-(4-фторфенил)циклобутанол;
3,4-диметил-8-[(3R)-3-(3-пиридилокси)пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-N-[[4-(1-метилпиррол-2-ил)фенил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[[4-(2,4-диметилпиразол-3-ил)фенил]метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[[4-(2-этилпиразол-3-ил)фенил]метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[[2-фтор-4-(2-метилпиразол-3-ил)фенил]метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
3,4-диметил-N-[(4-пиразол-1-илфенил)метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
8-[4-[(2-хлор-4-пиридил)окси]-1-пиперидил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
8-[3-[(2-хлор-4-пиридил)оксиметил]пирролидин-1-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
8-[3-[(2-хлор-4-пиридил)оксиметил]азетидин-1-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
8-[3-[(2-хлор-4-пиридил)окси]азетидин-1-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-(3-пиразин-2-илоксиазетидин-1-ил)пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
8-[3-[(4,6-диметил-3-пиридил)окси]азетидин-1-ил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
1,1,1,3,3,3-гексадейтерио-2-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол;
2-[(3R)-1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)пирролидин-3-ил]пропан-2-ол;
2-[(3S)-1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)пирролидин-3-ил]пропан-2-ол;
5-[1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)азетидин-3-ил]оксипиридин-2-карбонитрил;
3,4-диметил-8-[3-(3-пиридилокси)азетидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-[3-(1-метилпиразол-4-ил)оксиазетидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-[(3S,4R)-3-метил-4-[(2-метил-4-пиридил)окси]пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-[(3S)-3-(2-пиридилокси)пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-c]пиридазин;
3,4-диметил-8-[(3S)-3-[[5-(трифторметил)-2-пиридил]окси]пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-[(3S)-3-пиразин-2-илоксипирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-[(3S)-3-[[6-(трифторметил)-3-пиридил]окси]пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
4-[(3S)-1-(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)пирролидин-3-ил]оксибензонитрил;
3,4-диметил-8-[(3S)-3-[(6-метил-3-пиридил)окси]пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-[(2R,4S)-2-метил-4-[(2-метил-4-пиридил)окси]пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
3,4-диметил-8-[3-(4-пиридилокси)-3-(трифторметил)пирролидин-1-ил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин;
N-[[4-(1-метокси-1-метилэтил)фенил]метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]-3-фторфенил]-2-метилпропан-1-ол;
2-[4-[дидейтерио[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол;
3,4-диметил-N-[[4-[1-метил-1-(тридейтериометокси)этил]фенил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[[4-(1-амино-1-метилэтил)фенил]метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
N-[(1,1-диметил-3Н-изобензофуран-5-ил)метил]-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-1,2-диол;
3,4-диметил-N-[[4-(оксетан-3-ил)фенил]метил]пиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин;
2-[4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]-2-метилпропан-1-ол;
[8-[[4-(2-гидроксипропан-2-ил)бензил]амино]-4-метилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-3-ил]метилацетат и
2-[4-[[[3-(гидроксиметил)-4-метилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил]амино]метил]фенил]пропан-2-ол
или их фармацевтически приемлемую соль.
Названия соединений определяют с помощью алгоритма присваивания наименований Struct=Name, являющегося частью CHEMDRAW® ULTRA v. 12.0.
Соединение может существовать в виде стереоизомера, в котором присутствуют асимметричные или хиральные центры. Стереоизомер представляет собой "R" или "S"' в зависимости от конфигурации заместителей вокруг хирального атома углерода. Термины "R" и "S", используемые в данном документе, представляют собой конфигурации, определенные в IUPAC 1974 Recommendations for Section E, Fundamental Stereochemistry в Pure Appl. Chem., 1976, 45: 13-30. В настоящем изобретении предусмотрены различные стереоизомеры и их смеси, и они конкретно включены в объем настоящего изобретения. Стереоизомеры включают энантиомеры и диастереомеры и смеси энантиомеров или диастереомеров. Отдельные стереоизомеры соединений можно получить путем синтеза из коммерчески доступных исходных материалов, которые содержат асимметричные или хиральные центры, или путем получения рацемических смесей с последующим осуществлением способов разделения, хорошо известных средним специалистам в данной области техники. В качестве примеров данных способов разделения приводятся: (1) обеспечение присоединения смеси энантиомеров к хиральному вспомогательному реагенту, разделение полученной смеси диастереомеров посредством перекристаллизации или хроматографии и необязательное выделение оптически чистого продукта из вспомогательного реагента, как описано в Furniss, Hannaford, Smith, and Tatchell, "Vogel's Textbook of Practical Organic Chemistry", 5th edition (1989), Longman Scientific & Technical, Essex CM20 2JE, England, или (2) прямое разделение смеси оптических энантиомеров на хиральных хроматографических колонках, или (3) способы фракционной перекристаллизации.
Следует понимать, что соединение может иметь таутомерные формы, а также геометрические изомеры, и что они также составляют варианты осуществления настоящего изобретения.
В настоящее изобретение также включено меченное изотопом соединение, которое является идентичным указанному в формуле (I), за исключением того, что один или несколько атомов заменены атомом с атомной массой или массовым числом, отличными от атомной массы или массового числа, обычно встречающихся в природе. Примерами изотопов, пригодных для включения в соединения по настоящему изобретению, являются водород, углерод, азот, кислород, фосфор, сера, фтор и хлор, такие как без ограничения2H,3H,13С,14С,15N,18О,17О,31P,32P,35S,18F и36Cl соответственно. Замещение более тяжелыми изотопами, такими как дейтерий, т.е.2H, может обеспечивать определенные терапевтические преимущества вследствие более высокой устойчивости к инактивации в процессе метаболизма, например, увеличенного периода полувыведения in vivo или сниженных требований к дозе, и, следовательно, может быть предпочтительным в некоторых случаях. Соединение может включать позитронно-активные изотопы для медицинской визуализации и исследований с помощью позитронно-эмиссионной томографии (PET) для определения расположения рецепторов. Подходящими позитронно-активными изотопами, которые могут быть включены в соединения формулы (I), являются11С,13N,15O и18F. Меченные изотопом соединения формулы (I) обычно можно получить с помощью традиционных методик, известных специалистам в данной области техники, или с помощью способов, аналогичных способам, описанным в сопутствующих примерах с применением соответствующего меченного изотопом реагента вместо не меченного изотопом реагента.
В определенных вариантах осуществления в соединениях формулы (I) любой атом водорода может представлять собой дейтерий. В определенных вариантах осуществления R1 представляет собой дейтерий. В определенных вариантах осуществления R3 представляет собой дейтерий. В определенных вариантах осуществления R6 представляет собой дейтерий. В определенных вариантах осуществления R4 представляет собой водород, и R5 представляет собой -(CRcRd)n-Y, где Rc представляет собой дейтерий, и Rd представляет собой дейтерий. В определенных вариантах осуществления R4 представляет собой водород, и R5 представляет собой -(CRcRd)n-Y, при этом n равняется 1, и Y представляет собой фенил, который замещен C1-С4-гидроксиалкильной или С1-С4-алкокси-С1-С4-алкильной группой, где по меньшей мере один атом водорода в С1-С4-гидроксиалкильной или С1-С4-алкокси-С1-С4-алкильной группе представляет собой дейтерий.
а. Фармацевтически приемлемые соли
Раскрытые соединения могут существовать в виде фармацевтически приемлемых солей. Термин "фармацевтически приемлемая соль" относится к солям или цвиттер-ионам соединений, которые являются водорастворимыми или жирорастворимыми или диспергируемыми, пригодными для лечения расстройств без чрезмерной токсичности, раздражения и аллергической реакции, соответствующими приемлемому соотношению пользы/риска и эффективными для их предполагаемого применения. Соли можно получать во время окончательного выделения и очистки соединений или отдельно путем осуществления реакции аминогруппы соединений с подходящей кислотой. Например, соединение можно растворить в подходящем растворителе, таком как без ограничения метанол и вода, и обработать по меньшей мере одним эквивалентом кислоты, такой как хлористоводородная кислота. Полученная соль может выпадать в осадок, и ее можно выделять путем фильтрации и высушивать при пониженном давлении. В качестве альтернативы растворитель и избыток кислоты можно удалить при пониженном давлении с получением соли. Иллюстративные соли включают соль уксусной кислоты, соль адипиновой кислоты, соль альгиновой кислоты, соль лимонной кислоты, соль аспарагиновой кислоты, соль бензойной кислоты, бензолсульфонат, бисульфат, бутират, камфорат, камфорсульфонат, диглюконат, глицерофосфат, гемисульфат, гептаноат, гексаноат, соль муравьиной кислоты, изетионат, соль фумаровой кислоты, соль молочной кислоты, соль малеиновой кислоты, метансульфонат, нафтиленсульфонат, никотинат, соль щавелевой кислоты, памоат, пектинат, персульфат, 3-фенилпропионат, соль пикриновой кислоты, соль щавелевой кислоты, соль малеиновой кислоты, пивалат, пропионат, соль янтарной кислоты, соль винной кислоты, трихлорацетат, трифторацетат, глутамат, пара-толуолсульфонат, ундеканоат, хлористоводородную соль, бромистоводородную соль, сернокислую соль, фосфорнокислую соль и тому подобное. Аминогруппы соединений также могут быть кватернизованы с помощью алкилхлоридов, бромидов и йодидов, таких как метил, этил, пропил, изопропил, бутил, лаурил, миристил, стеарил и т.п.
Основные соли присоединения можно получать в ходе окончательного выделения и очистки раскрытых соединений путем осуществления реакции карбоксильной группы с подходящим основанием, таким как гидроксид, карбонат или бикарбонат катиона металла, такого как литий, натрий, калий, кальций, магний или алюминий, или органическим первичным, вторичным или третичным амином. Можно получать соли четвертичного амина, такие как соли, полученные из метиламина, диметиламина, триметиламина, триэтиламина, диэтиламина, этиламина, трибутиламина, пиридина, N,N-диметиланилина, N-метилпиперидина, N-метилморфолина, дициклогексиламина, прокаина, дибензиламина, N,N-дибензилфенэтиламина, 1-эфенамина и N,N'-дибензилэтилендиамина, этилендиамина, этаноламина, диэтаноламина, пиперидина, пиперазина и т.п.
В некоторых вариантах осуществления соединение, раскрытое в данном документе, может представлять собой хлористоводородную соль или дихлоргидратную соль. В некоторых вариантах осуществления соединение, раскрытое в данном документе, может представлять собой трифторацетатную соль.
b. Общий синтез
Соединения формулы (I) могут быть получены с помощью синтетических способов или метаболических способов. Получение соединений посредством метаболических способов включает способы, которые имеют место в организме человека или животного (in vivo), или способы, имеющие место in vitro.
Сокращения, которые используют в описаниях следующих схем, представляют собой: IPA означает изопропиловый спирт; АсОН означает уксусную кислоту; DCE означает 1,2-дихлорэтан; DIEA означает N,N-диизопропилэтиламин; HATU означает 1-[бис(диметиламино)метилен]-1H-1,2,3-триазоло[4,5-b]пиридиний-3-оксидгексафторфосфат; MeOH означает метанол; NMP означает N-метил-2-пирролидон; и MW означает микроволновой (в отношении микроволнового реактора).
Соединения формулы (I), в частности соединения формулы (Ia), могут быть синтезированы как показано на схеме 1.

Как показано на схеме 1, в результате реакции соединения I и этилтиогликолята II можно получить соединение III. В результате реакции соединения III с ацетатом формамидина получают соединение IV, и в результате реакции с оксихлоридом фосфора получают соединение V. В результате реакции сочетания соединения V с соединением VI, представляющим собой подходящий амин, получают соединение VII, которое соответствует соединению формулы (I), где R6 представляет собой водород.
Соединения формулы (I) также можно синтезировать как показано на схеме 2.


Как показано на схеме 2, в результате реакции соединения III с основанием с последующей реакцией сочетания хлорида аммония со средством для реакции сочетания, таким как HATU, получают соединение IIIA и в результате реакции с триэтилортоформиатом получают соединение IV. В результате реакции с оксихлоридом фосфора получают соединение V и в результате реакции сочетания соединения V с соединением VI, представляющим собой подходящий амин, получают соединение VII, которое соответствует соединению формулы (I), где R6 представляет собой водород. Соединения формулы (I), в частности соединения формулы (Ig), можно синтезировать как показано на схеме 3.

Как показано на схеме 3, в результате реакции соединения VIII (где R2 представляет собой водород или хлор) с этил-2-гидроксиацетатом можно получать соединение IX. В результате реакции соединения IX с ацетатом формамидина получают соединение X, которое можно вводить в реакцию с оксихлоридом фосфора с получением соединения XI. В результате реакции сочетания соединения XI с подходящим амином, с применением подходящего средства для реакции сочетания, получают соединение XII, которое соответствует соединению формулы (Ig), где R1 представляет собой метил, R2представляет собой водород или хлор, R3 представляет собой метил, и R6 представляет собой водород.
Соединения формулы (I), в частности соединения формулы (Ih), можно синтезировать как показано на схеме 4.

Как показано на схеме 4, в результате реакции соединения XIII и этил-2-гидроксиацетата можно получать соединение XIV. В результате реакции соединения XIV с ацетатом формамидина получают соединение XV. В результате реакции сочетания соединения XV с подходящим амином, с применением подходящего средства для реакции сочетания, получают соединение XVI, которое соответствует соединению формулы (Ih), где R2 представляет собой метил, R3 представляет собой метил, и R6представляет собой водород.
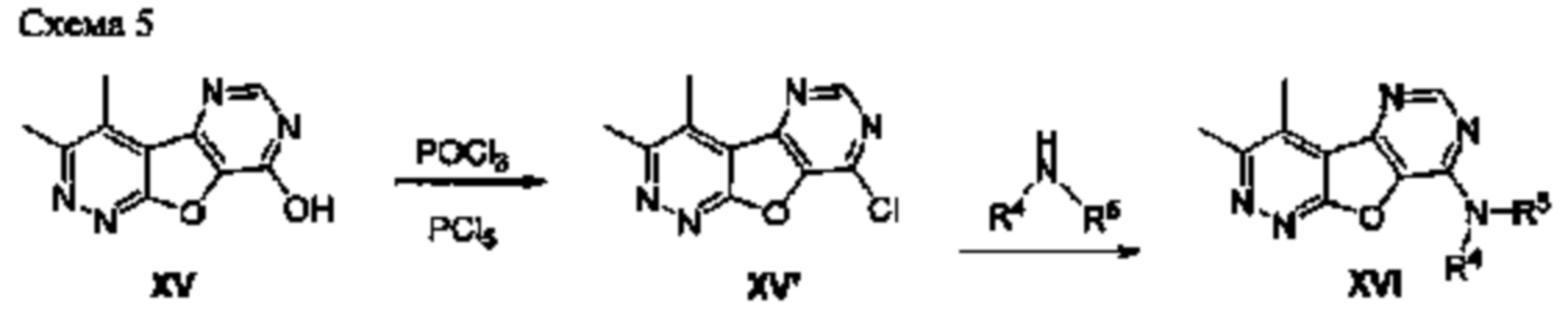
Как показано на схеме 5, другой путь получения соединения XVI включает реакцию соединения XV с оксихлоридом фосфора с получением соединения XV'. В результате реакции соединения XV' с подходящим амином, с применением подходящего средства для реакции сочетания, получают соединение XVI.
В каждой из приведенных выше схем можно использовать широкое разнообразие аминов HNR4R5. Такие амины могут быть коммерчески доступны или могут быть синтезированы с применением способов, известных средним специалистам в данной области техники.
Соединения и промежуточные соединения можно выделять и очищать с помощью способов, хорошо известных специалистам в области органического синтеза. Примеры традиционных способов выделения и очистки соединений могут включать без ограничения хроматографию на твердых носителях, таких как силикагель, оксид алюминия или диоксид кремния, дериватизированный с помощью алкилсилановых групп, путем перекристаллизации при высокой или низкой температуре с необязательной предварительной обработкой активированным углем, тонкослойную хроматографию, дистилляцию при различных значениях давления, сублимацию под вакуумом и растирание, как описано, например, в "Vbgel's Textbook of Practical Organic Chemistry," 5th edition (1989), by Furniss, Hannaford, Smith, and Tatchell, pub. Longman Scientific & Technical, Essex CM20 2JE, England.
Раскрытое соединение может характеризоваться по меньшей мере одним азотистым основанием, посредством которого соединение можно обработать кислотой с получением желаемой соли. Например, соединение можно подвергать реакции с кислотой при комнатной температуре или выше с получением желаемой соли, которую осаждают и собирают с помощью фильтрации после охлаждения. Примеры кислот, пригодных для осуществления реакции, включают без ограничения винную кислоту, молочную кислоту, янтарную кислоту, а также миндальную, атролактиновую, метансульфоновую, этансульфоновую, толуолсульфоновую, нафталенсульфоновую, бензолсульфоновую, карбоновую, фумаровую, малеиновую, глюконовую, уксусную, пропионовую, салициловую, хлористоводородную, бромистоводородную, фосфорную, серную, лимонную, гидроксимасляную, камфорсульфоновую, яблочную, фенилуксусную, аспарагиновую или глутаминовую кислоты и т.п.
Условия реакции и периоды времени реакции для каждой отдельной стадии могут варьировать в зависимости от конкретных используемых реагентов и заместителей, присутствующих в используемых реагентах. Конкретные способы представлены в разделе примеров. Реакционные смеси могут быть обработаны традиционным способом, например, путем удаления растворителя из остатка и дальнейшей очистки в соответствии с методиками, обычно известными из уровня техники, такими как без ограничения кристаллизация, дистилляция, экстракция, растирание и хроматография. Если не указано иное, исходные материалы и реагенты являются либо коммерчески доступными, либо могут быть получены специалистом в данной области техники из коммерчески доступных материалов с применением способов, описанных в химической литературе. Исходные материалы, если они не являются коммерчески доступными, могут быть получены с помощью способов, выбранных из стандартных методик органической химии, методик, аналогичных для синтеза известных структурно сходных соединений, или методик, которые аналогичны описанным выше схемам или способам, описанным в разделе примеров синтеза.
Проведение обычных экспериментов, в том числе соответствующее управление условиями реакции, реагентами и последовательностью способа синтеза, защита любой химической функциональности, которая не может быть совместима с условиями реакции, и снятие защиты в подходящей точке реакционной последовательности способа включены в объем настоящего изобретения. Подходящие защитные группы и способы защиты разных заместителей и снятия защиты с них с применением таких подходящих защитных групп хорошо известны специалистам в данной области; примеры которых можно найти в PGM Wuts и TW Greene, в книге Greene под названием Protective Groups in Organic Synthesis (4th ed.), John Wiley & Sons, NY (2006), которая включена в данный документ посредством ссылки в полном объеме. Синтез соединений по настоящему изобретению можно осуществлять с помощью способов, аналогичных описанным в схемах синтеза, которые описаны в данном документе выше, и в конкретных примерах.
Когда требуется оптически активная форма раскрытого соединения, ее можно получить осуществлением одного из способов, описанных в данном документе, с применением оптически активного исходного материала (полученного, например, путем асимметричной индукции подходящей стадии реакции) или путем разделения смеси стереоизомеров соединения или промежуточных соединений с применением стандартного способа (такого как хроматографическое разделение, перекристаллизация или ферментное разделение).
Подобным образом, когда требуется чистый геометрический изомер соединения, его можно получить осуществлением одного из вышеуказанных способов с применением чистого геометрического изомера в качестве исходного материала или путем разделения смеси геометрических изомеров соединения или промежуточных соединений с применением стандартного способа, такого как хроматографическое разделение.
Следует понимать, что схемы синтеза и конкретные примеры, которые описаны, являются иллюстративными и не должны рассматриваться как ограничивающие объем изобретения, как это определено в прилагаемой формуле изобретения. Все альтернативы, модификации и эквиваленты синтетических способов и конкретные примеры включены в объем формулы изобретения.
с. Активность мускаринового ацетилхолинового рецептора М4
В некоторых вариантах осуществления раскрытые соединения потенцируют реакцию mAChR M4 в отношении агониста (например, ацетилхолина). В некоторых вариантах осуществления раскрытые соединения усиливают реакцию mAChR M4 на немаксимальные концентрации агониста в присутствии соединения по сравнению с реакцией в отношении агониста в отсутствие соединения. Потенцирование активности mAChR M4 может быть продемонстрировано с помощью методики, известной из уровня техники. Например, активация активности mAChR M4 может быть определена путем измерения потока кальция в ответ на агонист, например ацетилхолин, в клетках с введенным чувствительным к Са2+ флуоресцентным красителем (например, Fluo-4), и совместной экспрессии химерного или неизбирательного белка G. В некоторых вариантах осуществления поток кальция измеряли как увеличение флуоресцентного статического соотношения. В некоторых вариантах осуществления активность положительного аллостерического модулятора анализировали как зависимое от концентрации усиление реакции при ЕС20 ацетилхолина (т.е. реакции mAChR M4 при концентрации ацетилхолина, которая обеспечивает 20% максимальной реакции).
В некоторых вариантах осуществления раскрытые соединения активируют реакцию mAChR M4 в виде повышения флуоресценции кальция в трансфицированных mAChR M4 клетках СНО-K1 в присутствии соединения по сравнению с реакцией эквивалентных клеток СНО-K1 в отсутствие соединения. В некоторых вариантах осуществления раскрытые соединения активируют реакцию mAChR M4 при ЕС50, составляющей менее приблизительно 10 мкМ, менее приблизительно 5 мкМ, менее приблизительно 1 мкМ, менее приблизительно 500 нМ, менее приблизительно 100 нМ или менее приблизительно 50 нМ. В некоторых вариантах осуществления трансфицированные mAChR M4 клетки СНО-K1 трансфицируют с помощью mAChR M4 человека. В некоторых вариантах осуществления трансфицированные mAChR M4 клетки СНО-K1 трансфицируют с помощью mAChR M4 крысы.
Раскрытые соединения могут проявлять положительную аллостерическую модуляцию реакции mAChR M4 на ацетилхолин в виде усиления реакции на немаксимальные концентрации ацетилхолина в клетках СНО-K1, трансфицированных с помощью mAChR M4, в присутствии соединения по сравнению с реакцией на ацетилхолин в отсутствие соединения. В некоторых вариантах осуществления раскрытые соединения проявляют положительную аллостерическую модуляцию реакции mAChR M4 на ацетилхолин с EC50, составляющей менее приблизительно 10 мкМ, менее приблизительно 5 мкМ, менее приблизительно 1 мкМ, менее приблизительно 500 нМ или менее приблизительно 100 нМ. В некоторых вариантах осуществления ЕС50 для положительной аллостерической модуляции определяют в клетках СНО-K1, которые трансфицированы с помощью mAChR M4. В некоторых вариантах осуществления трансфицированный mAChR M4 представляет собой mAChR M4 человека. В некоторых вариантах осуществления трансфицированный mAChR M4 представляет собой mAChR M4 крысы.
Раскрытые соединения могут активировать реакцию mAChR M4 в трансфицированных mAChR M4 клетках СНО-K1 с EC50, меньшей, чем ЕС50 для клеток СНО-K1, трансфицированных одним или несколькими из mAChR M1, M2, М3 или М5. То есть раскрытое соединение может обладать селективностью в отношении рецептора mAChR M4 по сравнению с одним или несколькими из рецепторов mAChR M1, M2, М3 или М5. Например, в некоторых вариантах осуществления раскрытое соединение может активировать реакцию mAChR M4 с EC50, составляющей приблизительно в 5 раз меньше, приблизительно в 10 раз меньше, приблизительно в 20 раз меньше, приблизительно в 30 раз меньше, приблизительно в 50 раз меньше, приблизительно в 100 раз меньше, приблизительно в 200 раз меньше, приблизительно в 300 раз меньше, приблизительно в 400 раз меньше или более чем приблизительно в 500 раз меньше, чем таковая в отношении mAChR M1. В некоторых вариантах осуществления раскрытое соединение может активировать реакцию mAChR M4 с EC50, составляющей приблизительно в 5 раз меньше, приблизительно в 10 раз меньше, приблизительно в 20 раз меньше, приблизительно в 30 раз меньше, приблизительно в 50 раз меньше, приблизительно в 100 раз меньше, приблизительно в 200 раз меньше, приблизительно в 300 раз меньше, приблизительно в 400 раз меньше или более чем приблизительно в 500 раз меньше, чем таковая в отношении mAChR M2. В некоторых вариантах осуществления раскрытое соединение может активировать реакцию mAChR M4 с ЕС50, составляющей приблизительно в 5 раз меньше, приблизительно в 10 раз меньше, приблизительно в 20 раз меньше, приблизительно в 30 раз меньше, приблизительно в 5 0 раз меньше, приблизительно в 100 раз меньше, приблизительно в 200 раз меньше, приблизительно в 300 раз меньше, приблизительно в 400 раз меньше или более чем приблизительно в 500 раз меньше, чем таковая в отношении mAChR М3. В некоторых вариантах осуществления раскрытое соединение может активировать реакцию mAChR M4 с ЕС50, составляющей приблизительно в 5 раз меньше, приблизительно в 10 раз меньше, приблизительно в 20 раз меньше, приблизительно в 30 раз меньше, приблизительно в 50 раз меньше, приблизительно в 100 раз меньше, приблизительно в 200 раз меньше, приблизительно в 300 раз меньше, приблизительно в 400 раз меньше или более чем приблизительно в 500 раз меньше, чем таковая в отношении mAChR M5. В некоторых вариантах осуществления раскрытое соединение может активировать реакцию mAChR M4 с EC50, составляющей в 5 раз меньше, приблизительно в 10 раз меньше, приблизительно в 20 раз меньше, приблизительно в 30 раз меньше, чем таковая в отношении рецепторов М2-М5, приблизительно в 50 раз меньше, приблизительно в 100 раз меньше, приблизительно в 200 раз меньше, приблизительно в 300 раз меньше, приблизительно в 400 раз меньше или более чем приблизительно в 500 раз меньше, чем таковая в отношении рецепторов mAChR M1, M2, М3 или M5.
Раскрытые соединения могут активировать реакцию mAChR M4 в трансфицированных M4 клетках СНО-K1 с EC50, составляющей менее приблизительно 10 мкМ, и проявлять селективность в отношении рецептора M4 по сравнению с одним или несколькими из рецепторов mAChR M1, M2, М3 или M5. Например, в некоторых вариантах осуществления соединение может характеризоваться EC50, составляющей менее приблизительно 10 мкМ, менее приблизительно 5 мкМ, менее приблизительно 1 мкМ, менее приблизительно 500 нМ, менее приблизительно 100 нМ или менее приблизительно 50 нМ; и соединение также может активировать реакцию mAChR M4 с ЕС50, составляющей приблизительно в 5 раз меньше, 10 раз меньше, 20 раз меньше, 30 раз меньше, 50 раз меньше, 100 раз меньше, 200 раз меньше, 300 раз меньше, 400 раз меньше или более чем приблизительно в 500 раз меньше, чем таковая в отношении mAChR M1. В некоторых вариантах осуществления соединение может характеризоваться ЕС50, составляющей менее приблизительно 10 мкМ, менее приблизительно 5 мкМ, менее приблизительно 1 мкМ, менее приблизительно 500 нМ, менее приблизительно 100 нМ или менее приблизительно 50 нМ; и соединение также может активировать реакцию mAChR M4 с EC50, составляющей приблизительно в 5 раз меньше, приблизительно в 10 раз меньше, приблизительно в 20 раз меньше, приблизительно в 30 раз меньше, приблизительно в 50 раз меньше, приблизительно в 100 раз меньше, приблизительно в 200 раз меньше, приблизительно в 300 раз меньше, приблизительно в 400 раз меньше или более чем приблизительно в 500 раз меньше, чем таковая в отношении mAChR M2. В некоторых вариантах осуществления соединение может характеризоваться EC50, составляющей менее приблизительно 10 мкМ, менее приблизительно 5 мкМ, менее приблизительно 1 мкМ, менее приблизительно 500 нМ, менее приблизительно 100 нМ или менее приблизительно 50 нМ; и соединение также может активировать реакцию mAChR M4 с ЕС50, составляющей приблизительно в 5 раз меньше, приблизительно в 10 раз меньше, приблизительно в 20 раз меньше, приблизительно в 30 раз меньше, приблизительно в 50 раз меньше, приблизительно в 100 раз меньше, приблизительно в 200 раз меньше, приблизительно в 300 раз меньше, приблизительно в 400 раз меньше или более чем приблизительно в 500 раз меньше, чем таковая в отношении mAChR М3. В некоторых вариантах осуществления соединение может характеризоваться ЕС50, составляющей менее приблизительно 10 мкМ, менее приблизительно 5 мкМ, менее приблизительно 1 мкМ, менее приблизительно 500 нМ, менее приблизительно 100 нМ или менее приблизительно 50 нМ; и соединение также может активировать реакцию mAChR M4 с ЕС50, составляющей приблизительно в 5 раз меньше, приблизительно в 10 раз меньше, приблизительно в 20 раз меньше, приблизительно в 30 раз меньше, приблизительно в 50 раз меньше, приблизительно в 100 раз меньше, приблизительно в 200 раз меньше, приблизительно в 300 раз меньше, приблизительно в 400 раз меньше или более чем приблизительно в 500 раз меньше, чем таковая в отношении mAChR M5. В некоторых вариантах осуществления соединение может характеризоваться EC50, составляющей менее приблизительно 10 мкМ, менее приблизительно 5 мкМ, менее приблизительно 1 мкМ, менее приблизительно 500 нМ, менее приблизительно 100 нМ или менее приблизительно 50 нМ; и соединение также может активировать реакцию mAChR M4 с ЕС50, составляющей в 5 раз меньше, приблизительно в 10 раз меньше, приблизительно в 20 раз меньше, приблизительно в 30 раз меньше, чем таковая в отношении рецепторов М2-М5, приблизительно в 50 раз меньше, приблизительно в 100 раз меньше, приблизительно в 200 раз меньше, приблизительно в 300 раз меньше, приблизительно в 400 раз меньше, рецепторов М2, М3или M5 или более чем приблизительно в 500 раз меньше, чем таковая в отношении рецепторов mAChR M1, M2, М3 или M5.
In vivo эффективность для раскрытых соединений может быть измерена в ряде доклинических крысиных моделей поведения, где при применении известных клинически применимых антипсихотиков проявляются подобные положительные реакции. Например, раскрытые соединения могут обращать вызванную амфетамином гиперлокомоцию у самцов крыс линии Sprague-Dawley в дозах, находящихся в диапазоне от 1 до 100 мг/кгр.о.
3. Фармацевтические композиции и составы
Раскрытые соединения можно включать в фармацевтические композиции, подходящие для введения субъекту (такому как пациент, который может представлять собой человека или пациента, отличного от человека). Раскрытые соединения также могут быть представлены в виде составов, таких как высушенные распылением дисперсионные составы.
Фармацевтические композиции и составы могут включать "терапевтически эффективное количество" или "профилактически эффективное количество" средства. "Терапевтически эффективное количество" относится к количеству, эффективному при дозах и в течение периодов времени, необходимых для достижения требуемого терапевтического результата. Терапевтически эффективное количество композиции может быть определено специалистом в данной области и может варьировать в зависимости от таких факторов, как, например, течение заболевания, возраст, пол и вес индивидуума и способность композиции вызывать требуемый ответ у индивидуума, Терапевтически эффективное количество также представляет собой таковое, при котором любые токсичные или вредные эффекты соединения по настоящему изобретению (например, соединения формулы (I)) перевешиваются терапевтически полезными эффектами. "Профилактически эффективное количество" относится к количеству, эффективному при дозах и в течение периодов времени, необходимых для достижения требуемого профилактического результата. Как правило, так как профилактическая доза применяется по отношению к субъектам перед заболеванием или на ранней стадии заболевания, профилактически эффективное количество будет составлять меньше, чем терапевтически эффективное количество.
Например, терапевтически эффективное количество соединения формулы (I) может составлять от приблизительно 1 мг/кг до приблизительно 1000 мг/кг, от приблизительно 5 мг/кг до приблизительно 950 мг/кг, от приблизительно 10 мг/кг до приблизительно 900 мг/кг, от приблизительно 15 мг/кг до приблизительно 850 мг/кг, от приблизительно 20 мг/кг до приблизительно 800 мг/кг, от приблизительно 25 мг/кг до приблизительно 750 мг/кг, от приблизительно 30 мг/кг до приблизительно 700 мг/кг, от приблизительно 35 мг/кг до приблизительно 650 мг/кг, от приблизительно 40 мг/кг до приблизительно 600 мг/кг, от приблизительно 45 мг/кг до приблизительно 550 мг/кг, от приблизительно 50 мг/кг до приблизительно 500 мг/кг, от приблизительно 55 мг/кг до приблизительно 450 мг/кг, от приблизительно 60 мг/кг до приблизительно 400 мг/кг, от приблизительно 65 мг/кг до приблизительно 350 мг/кг, от приблизительно 70 мг/кг до приблизительно 300 мг/кг, от приблизительно 75 мг/кг до приблизительно 250 мг/кг, от приблизительно 80 мг/кг до приблизительно 200 мг/кг, от приблизительно 85 мг/кг до приблизительно 150 мг/кг и от приблизительно 90 мг/кг до приблизительно 100 мг/кг.
Фармацевтические композиции и составы могут включать фармацевтически приемлемые носители. Термин "фармацевтически приемлемый носитель", используемый в данном документе, означает нетоксичный инертный твердый, полутвердый или жидкий наполнитель, разбавитель, материал для инкапсулирования или вспомогательный состав любого типа. Некоторые примеры материалов, которые могут выступать в качестве фармацевтически приемлемых носителей, представляют собой сахара, такие как без ограничения лактоза, глюкоза и сахароза; виды крахмала, такие как без ограничения кукурузный крахмал и картофельный крахмал; целлюлозу и ее производные, такие как без ограничения карбоксиметилцеллюлоза натрия, этилцеллюлоза и ацетатцеллюлоза; порошкообразный трагакант; солод; желатин; тальк; вспомогательные вещества, такие как без ограничения масло какао и виды воска для суппозиториев; масла, такие как без ограничения арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; гликоли, такие как пропиленгликоль; сложные эфиры, такие как без ограничения этилолеат и этиллаурат; агар; буферные средства, такие как без ограничения гидроксид магния и гидроксид алюминия; альгиновая кислота; апирогенная вода; изотонический раствор; раствор Рингера; этиловый спирт и фосфатно-буферные растворы, а также другие нетоксичные совместимые смазывающие средства, такие как без ограничения лаурилсульфат натрия и стеарат магния, а также окрашивающие средства, антиадгезивы, покрывающие средства, подсластители, вкусовые добавки и ароматизирующие средства, консерванты и антиоксиданты также могут присутствовать в композиции, в зависимости от решения специалиста в области составления.
Таким образом, соединения и их физиологически приемлемые соли могут быть составлены для введения, например, с помощью дозирования твердой лекарственной формы, глазных капель, в составе для местного применения на масляной основе, инъекции, ингаляции (либо через рот, либо через нос), имплантов или перорального, буккального, парентерального или ректального введения. Методики и составы, как правило, можно найти в "Remington's Pharmaceutical Sciences," (Meade Publishing Co., Easton, Pa.). Терапевтические композиции, как правило, должны быть стерильны и устойчивы в условиях производства и хранения.
Путь, посредством которого вводят раскрытые соединения, и форма композиции будут определять тип применяемого носителя. Композиция может быть представлена в различных формах, подходящих, например, для системного введения (например, перорального, ректального, назального, сублингвального, буккального, с помощью имплантов или парентерального) или местного введения (например, дермального, легочного, назального, ушного, глазного, с помощью системы доставки липосом или ионтофореза).
Носители для системного введения, как правило, включают по меньшей мере одно из разбавителей, смазывающих средств, связующих веществ, разрыхлителей, красящих веществ, вкусоароматических добавок, подсластителей, антиоксидантов, консервантов, веществ, способствующих скольжению, растворителей, суспендирующих средств, смачивающих веществ, поверхностно-активных веществ, их комбинаций и других. Все носители в композициях являются необязательными.
Подходящие разбавители включают сахара, такие как глюкоза, лактоза, декстроза и сахароза; диолы, такие как пропиленгликоль; карбонат кальция; карбонат натрия; сахароспирты, такие как глицерин; маннит и сорбит. Количество разбавителя(-ей) в композиции для системного или местного применения, как правило, составляет от приблизительно 50 до приблизительно 90%.
Подходящие смазывающие средства включают диоксид кремния, тальк, стеариновую кислоту и ее магниевые соли и кальциевые соли, сульфат кальция; и жидкие смазывающие средства, такие как полиэтиленгликоль, и растительные масла, такие как арахисовое масло, хлопковое масло, кунжутное масло, оливковое масло, кукурузное масло и масло какао. Количество смазывающего(-их) средства(средств) в композиции для системного или местного применения, как правило, составляет от приблизительно 5 до приблизительно 10%.
Подходящие связующие вещества включают поливинилпирролидон; алюмосиликат магния; виды крахмала, такие как кукурузный крахмал и картофельный крахмал; желатин; трагакант и целлюлозу и ее производные, такие как карбоксиметилцеллюлоза натрия, этилцеллюлоза, метилцеллюлоза, микрокристаллическая целлюлоза и карбоксиметилцеллюлоза натрия. Количество связующего(-их) вещества(веществ) в системной композиции, как правило, составляет от приблизительно 5 до приблизительно 50%.
Подходящие разрыхлители включают агар, альгиновую кислоту и ее натриевую соль, шипучие смеси, кроскармеллозу, кросповидон, карбоксиметилкрахмал натрия, крахмалгликолят натрия, глины и ионообменные смолы. Количество разрыхлителя(-ей) в композиции для системного или местного применения, как правило, составляет от приблизительно 0,1 до приблизительно 10%.
Подходящие красящие вещества включают такие красящие вещества, как краситель FD&C. Количество красящего вещества при применении в композиции для системного или местного применения, как правило, составляет от приблизительно 0,005 до приблизительно 0,1%.
Подходящие вкусоароматические добавки включают ментол, перечную мяту и фруктовые вкусоароматические добавки. Количество вкусоароматической(-их) добавки(добавок) при применении в композиции для системного или местного применения, как правило, составляет от приблизительно 0,1 до приблизительно 1,0%.
Подходящие подсластители включают аспартам и сахарин. Количество подсластителя(-ей) в композиции для системного или местного применения, как правило, составляет от приблизительно 0,001 до приблизительно 1%.
Подходящие антиоксиданты включают бутилированный гидроксианизол ("ВНА"), бутилированный гидрокситолуол ("ВНТ") и витамин Е. Количество антиоксиданта(-ов) в композиции для системного или местного применения, как правило, составляет от приблизительно 0,1 до приблизительно 5%.
Подходящие консерванты включают хлорид бензалкония, метилпарабен и бензоат натрия. Количество консерванта(-ов) в композиции для системного или местного применения, как правило, составляет от приблизительно 0,01 до приблизительно 5%. Подходящие вещества, способствующие скольжению, включают диоксид кремния. Количество вещества(веществ), способствующего(-их) скольжению, в композиции для системного или местного применения, как правило, составляет от приблизительно 1 до приблизительно 5%.
Подходящие растворители включают воду, изотонический раствор, этилолеат, глицерин, гидроксилированные касторовые масла, спирты, такие как этанол, и фосфатно-буферные растворы. Количество растворителя(-ей) в композиции для системного или местного применения, как правило, составляет от приблизительно 0 до приблизительно 100%.
Подходящие суспендирующие средства включают AVICEL RC-591 (от FMC Corporation в Филадельфии, Пенсильвания) и альгинат натрия. Количество суспендирующего(-их) средства(средств) в композиции для системного или местного применения, как правило, составляет от приблизительно 1 до приблизительно 8%.
Подходящие поверхностно-активные вещества включают лецитин, полисорбат 80, и лаурилсульфат натрия, и TWEENS от Atlas Powder Company в Уилмингтоне, Делавэр. Подходящие поверхностно-активные вещества включают те, которые раскрыты в C.T.F.A. Cosmetic Ingredient Handbook, 1992, pp. 587-592; Remington's Pharmaceutical Sciences, 15th Ed. 1975, pp. 335-337 и McCutcheon's Volume 1, Emulsifiers & Detergents, 1994, North American Edition, pp. 236-239. Количество поверхностно-активного(-ых) вещества(веществ) в композиции для системного или местного применения, как правило, составляет от приблизительно 0,1% до приблизительно 5%.
Хотя количества компонентов в композициях для системного применения могут варьировать в зависимости от типа получаемой композиции для системного применения, обычно композиции для системного применения содержат от 0,01% до 50% активного соединения (например, соединения формулы (I)) и от 50% до 99,99% одного или нескольких носителей. Композиции для парентерального введения, как правило, содержат от 0,1% до 10% активных веществ и от 90% до 99,9% носителя, в том числе разбавителя и растворителя.
Композиции для перорального введения могут иметь различные лекарственные формы. Например, твердые формы включают таблетки, капсулы, гранулы и нерасфасованные порошки. Данные лекарственные формы для перорального введения содержат безопасное и эффективное количество, обычно по меньшей мере приблизительно 5% и, более конкретно, от приблизительно 25% до приблизительно 50% активных веществ. Композиции с определенной дозой для перорального введения содержат от приблизительно 50% до приблизительно 95% носителей и, более конкретно, от приблизительно 50% до приблизительно 75%.
Таблетки можно спрессовывать, растирать в порошок, покрывать энтеросолюбильной оболочкой, покрывать сахарной оболочкой, покрывать пленочной оболочкой или спрессовывать многократно. Таблетки, как правило, содержат активный компонент и носитель, содержащий ингредиенты, выбранные из разбавителей, смазывающих средств, связующих веществ, разрыхлителей, красящих веществ, вкусоароматических добавок, подсластителей, веществ, способствующих скольжению, и их комбинаций. Конкретные разбавители включают карбонат кальция, карбонат натрия, маннит, лактозу и целлюлозу. Конкретные связующие вещества включают крахмал, желатин и сахарозу. Конкретные разрыхлители включают альгиновую кислоту и кроскармеллозу. Конкретные смазывающие средства включают стеарат магния, стеариновую кислоту и тальк. Конкретные красящие вещества представляют собой красители FD&C, которые можно добавлять для внешнего вида. Жевательные таблетки предпочтительно содержат подсластители, такие как аспартам и сахарин, или вкусоароматические добавки, такие как ментол, перечная мята, фруктовые вкусоароматические добавки, или их комбинацию.
Капсулы (включая импланты, составы с модифицированным высвобождением и составы с замедленным высвобождением), как правило, содержат активное соединение (например, соединение формулы (I)), и носитель, включающий один или несколько разбавителей, раскрытых выше, в капсуле, содержащей желатин. Гранулы, как правило, содержат раскрытое соединение и предпочтительно вещества, способствующие скольжению, такие как диоксид кремния, для улучшения свойств текучести. Импланты могут быть биоразлагающимися или небиоразлагающимися.
Выбор ингредиентов в носителе для композиций для перорального введения зависит от вторичных факторов, таких как вкус, стоимость и стабильность при хранении, которые не являются решающими для целей настоящего изобретения.
Твердые композиции можно покрывать посредством общепринятых способов, как правило, с помощью pH-зависимых или меняющихся со временем покрытий таким образом, что раскрытое соединение высвобождается в желудочно-кишечном тракте вблизи зоны необходимого применения или в различных местоположениях и в различные моменты времени для продления необходимого действия. Покрытия, как правило, содержат один или несколько компонентов, выбранных из ацетатфталата целлюлозы, фталата поливинилацетата, фталата гидроксипропилметилцеллюлозы, этилцеллюлозы, покрытий EUDRAGIT® (доступных от Evonik Industries в Эссене, Германия), видов воска и шеллака.
Композиции для перорального введения могут находиться в жидких формах. Например, подходящие жидкие формы включают водные растворы, эмульсии, суспензии, растворы, восстановленные из нешипучих гранул, суспензии, восстановленные из нешипучих гранул, шипучие препараты, восстановленные из шипучих гранул, крепкие настои, настойки, сиропы и т.д. Жидкие композиции для перорального введения, как правило, содержат раскрытое соединение и носитель, а именно носитель, выбранный из разбавителей, красящих веществ, вкусоароматических добавок, подсластителей, консервантов, растворителей, суспендирующих средств и поверхностно-активных веществ. Жидкие композиции для перорального введения предпочтительно содержат один или несколько ингредиентов, выбранных из красящих веществ, вкусоароматических добавок и подсластителей.
Другие композиции, применимые для достижения системной доставки исследуемых соединений, включают сублингвальные, буккальные и назальные лекарственные формы. Такие композиции, как правило, содержат одно или несколько растворимых веществ, представляющих собой наполнители, таких как разбавители, включая сахарозу, сорбит и маннит; и связующие вещества, такие как аравийская камедь, микрокристаллическая целлюлоза, карбоксиметилцеллюлоза и гидроксипропилметилцеллюлоза. Такие композиции могут дополнительно содержать смазывающие средства, красящие вещества, вкусоароматические добавки, подсластители, антиоксиданты и вещества, способствующие скольжению.
Раскрытые соединения можно вводить путем местного применения. Композиции для местного применения, которые можно локально наносить на кожу, могут быть в любой форме, включая твердые вещества, растворы, масла, кремы, мази, гели, лосьоны, шампуни, несмываемые и смываемые кондиционеры для волос, виды молочка, моющие средства, увлажнители, спреи, кожные пластыри и т.д. Композиции для местного применения содержат раскрытое соединение (например, соединение формулы (I)) и носитель. Носитель композиции для местного применения предпочтительно способствует проникновению соединений в кожу. Носитель может дополнительно содержать один или несколько необязательных компонентов.
Количество носителя, применяемого вместе с раскрытым соединением, является достаточным для обеспечения практического количества композиции для введения на единицу дозы соединения. Методики и композиции для получения лекарственных форм, применимых в способах по настоящему изобретению, описаны в следующих ссылках: Modem Pharmaceutics, Chapters 9 and 10, Banker & Rhodes, eds. (1979); Lieberman et al., Pharmaceutical Dosage Forms: Tablets (1981) и Ansel, Introduction to Pharmaceutical Dosage Forms, 2nd Ed, (1976).
Носитель может содержать один ингредиент или комбинацию из двух или более ингредиентов. В композициях для местного применения носитель включает носитель для местного применения. Подходящие носители для местного применения включают один или несколько ингредиентов, выбранных из фосфатно-буферного солевого раствора, изотонической воды, деионизованной воды, монофункциональных спиртов, симметричных спиртов, геля с алоэ вера, аллантоина, глицерина, масел с витаминами А и Е, минерального масла, пропиленгликоля, миристилпропионата PPG-2, диметилизосорбида, касторового масла, их комбинаций и т.п. Более конкретно, носители для средств применения на коже включают пропиленгликоль, диметилизосорбид и воду, и, еще более конкретно, фосфатно-буферный солевой раствор, изотоническую воду, деионизованную воду, монофункциональные спирты и симметричные спирты.
Носитель композиции для местного применения может дополнительно содержать один или несколько ингредиентов, выбранных из смягчающих средств, пропеллентов, растворителей, смачивающих средств, загустителей, порошков, ароматических добавок, пигментов и консервантов, все из которых являются необязательными.
Подходящие смягчающие средства включают стеариловый спирт, глицерилмонорицинолеат, глицерилмоностеарат, пропан-1,2-диол, бутан-1,3-диол, норковый жир, цетиловый спирт, изопропилизостеарат, стеариновую кислоту, изобутилпальмитат, изоцетилстеарат, олеиловый спирт, изопропиллаурат, гексиллаурат, децилолеат, октадекан-2-ол, изоцетиловый спирт, цетилпальмитат, ди-н-бутилсебацат, изопропилмиристат, изопропилпальмитат, изопропилстеарат, бутилстеарат, полиэтиленгликоль, триэтиленгликоль, ланолин, кунжутное масло, кокосовое масло, арахисовое масло, касторовое масло, ацетилированная спиртовая фракция ланолина, петролеум, минеральное масло, бутилмиристат, изостеариновую кислоту, пальмитиновую кислоту, изопропиллинолеат, лауриллактат, миристиллактат, децилолеат, миристилмиристат и их комбинации. Конкретные смягчающие средства для кожи включают стеариловый спирт и полидиметилсилоксан. Количество смягчающего(-их) средства(средств) в композиции для местного применения в отношении кожи, как правило, составляет от приблизительно 5% до приблизительно 95%.
Подходящие пропелленты включают пропан, бутан, изобутан, диметиловый эфир, диоксид углерода, оксид азота и их комбинации. Количество пропеллента(-ов) в композиции для местного применения, как правило, составляет от приблизительно 0% до приблизительно 95%.
Подходящие растворители включают воду, этиловый спирт, метиленхлорид, изопропанол, касторовое масло, моноэтиловый эфир этиленгликоля, монобутиловый эфир диэтиленгликоля, моноэтиловый эфир диэтиленгликоля, диметилсульфоксид, диметилформамид, тетрагидрофуран и их комбинации. Конкретные растворители включают этиловый спирт и гомотопные спирты. Количество растворителя(-ей) в композиции для местного применения, как правило, составляет от приблизительно 0% до приблизительно 95%.
Подходящие смачивающие средства включают глицерин, сорбит, 2-пирролидон-5-карбоксилат натрия, растворимый коллаген, дибутилфталат, желатин и их комбинации. Конкретные смачивающие средства включают глицерин. Количество смачивающего(-их) средства(средств) в композиции для местного применения, как правило, составляет от 0% до 95%.
Количество загустителя(-ей) в композиции для местного применения, как правило, составляет от приблизительно 0% до приблизительно 95%.
Подходящие порошки включают бета-циклодекстрины, гидроксипропилциклодекстрины, мел, тальк, фуллерову землю, каолин, крахмал, камеди, коллоидный диоксид кремния, полиакрилат натрия, тетраалкиламмониевые смектиты, триалкилариламмониевые смектиты, химически модифицированный алюмосиликат магния, органически модифицированную монтмориллонитовую глину, гидратированный алюмосиликат, пирогенный кремнезем, карбоксивиниловый полимер, карбоксиметилцеллюлозу натрия, этиленгликольмоностеарат и их комбинации. Количество порошка(-ов) в композиции для местного применения, как правило, составляет от 0% до 95%.
Количество ароматической добавки в композиции для местного применения, как правило, составляет от приблизительно 0% до приблизительно 0,5%, конкретно, от приблизительно 0,001% до приблизительно 0,1%.
Подходящие рН-регулирующие добавки включают HCl или NaOH в количествах, достаточных для регуляции рН фармацевтической композиции для местного применения.
Фармацевтические композиция или состав могут проявлять положительную аллостерическую модуляцию mAChR М4 с ЕС50, составляющей менее приблизительно 10 мкМ, менее приблизительно 5 мкМ, менее приблизительно 1 мкМ, менее приблизительно 500 нМ или менее приблизительно 100 нМ. Фармацевтические композиция или состав могут проявлять положительную аллостерическую модуляцию mAChR М4 с ЕС50, составляющей от приблизительно 10 мкМ до приблизительно 1 нМ, от приблизительно 1 мкМ до приблизительно 1 нМ, от приблизительно 100 нМ до приблизительно 1 нМ или от приблизительно 10 нМ до приблизительно 1 нМ.
а. Высушенные распылением дисперсионные составы
Раскрытые соединения можно составлять в виде дисперсии, высушенной распылением (SDD). SDD представляет собой однофазную, аморфную молекулярную дисперсию лекарственного средства в полимерной матрице. Она представляет собой твердый раствор с соединением, молекулярно "растворенным" в твердой матрице. SDD получают посредством растворения лекарственного средства и полимера в органическом растворителе и последующего высушивания раствора распылением. Применение высушивания распылением для фармацевтических средств применения может приводить к получению аморфных дисперсий с увеличенной растворимостью лекарственных средств класса II (высокая проницаемость, низкая растворимость) и класса IV (низкая проницаемость, низкая растворимость) согласно Биофармацевтической системе классификации (BCS). Условия составления и способа выбирают так, чтобы растворитель быстро испарялся из капель, таким образом обеспечивая недостаточное время для фазового разделения или кристаллизации. С помощью SDD продемонстрированы долгосрочная стабильность и технологичность. Например, с помощью SDD продемонстрированы показатели времени хранения более 2 лет. Преимущества SDD включают без ограничения повышенную биодоступность слаборастворимых в воде соединений при пероральном применении, доставку с применением традиционных твердых лекарственных форм (например, таблеток и капсул), воспроизводимый, контролируемый и масштабируемый способ производства и широкую применимость в отношении структурно различающихся нерастворимых соединений с широким диапазоном физических свойств.
Таким образом, в одном варианте осуществления настоящее изобретение может предусматривать высушенный распылением дисперсионный состав, содержащий соединение формулы (I).
4. Способы применения
Раскрытые соединения, фармацевтические композиции и составы можно применять в способах лечения расстройств, таких как неврологические и/или психические расстройства, ассоциированные с дисфункцией мускаринового ацетилхолинового рецептора. Раскрытые соединения и фармацевтические композиции также можно применять в способах потенцирования активности мускаринового ацетилхолинового рецептора у млекопитающего и в способах улучшения когнитивных функций у млекопитающего. Способы дополнительно включают котерапевтические способы улучшения исходов лечения в контексте когнитивной или поведенческой терапии. В способах применения, описанных в настоящем документе, дополнительное(-ые) терапевтическое(-ие) средство(-а) можно вводить одновременно или последовательно с раскрытыми соединениями и композициями.
а. Лечение расстройств
Раскрытые соединения, фармацевтические композиции и составы можно применять в способах лечения расстройств, таких как неврологические и/или психические расстройства, ассоциированные с дисфункцией мускаринового ацетилхолинового рецептора. Способы лечения могут предусматривать введение субъекту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (I) или фармацевтической композиции, содержащей терапевтически эффективное количество соединения формулы (I).
В некоторых вариантах осуществления в настоящем изобретении представлен способ улучшения когнитивных функций у млекопитающего, предусматривающий стадию введения млекопитающему терапевтически эффективного количества соединения формулы (I) или фармацевтической композиции, содержащей терапевтически эффективное количество соединения формулы (I).
Соединения и композиции, раскрытые в данном документе, могут быть применимы для лечения, предупреждения, смягчения, контролирования или снижения риска возникновения ряда расстройств, ассоциированных с активацией селективного рецептора mAChR М4. Например, лечение может предусматривать активацию селективного рецептора mAChR М4 до степени, эффективной для воздействия на холинергическую активность. Расстройство может быть ассоциировано с холинергической активностью, например холинергической гипофункцией. Таким образом, предусмотрен способ лечения или предупреждения расстройства у субъекта, предусматривающий стадию введения субъекту по меньшей мере одного раскрытого соединения или по меньшей мере одной раскрытой фармацевтической композиции в количестве, эффективном для лечения расстройства у субъекта.
Также предусмотрен способ лечения одного или нескольких расстройств, ассоциированных с активностью рецептора mAChR М4, у субъекта, предусматривающий стадию введения субъекту терапевтически эффективного количества соединения формулы (I) или фармацевтической композиции, содержащей терапевтически эффективное количество соединения формулы (I).
В некоторых вариантах осуществления в настоящем изобретении предусмотрен способ лечения расстройства, ассоциированного с дисфункцией мускаринового ацетилхолинового рецептора у млекопитающего, предусматривающий стадию введения млекопитающему эффективного количества по меньшей мере одного раскрытого соединения или его фармацевтически приемлемой соли или фармацевтической композиции, содержащей по меньшей мере одно раскрытое соединение или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления раскрытые соединения и композиции характеризуются полезностью при лечении ряда неврологических, психических и когнитивных расстройств, ассоциированных с рецептором mAChR М4, включающих одно или несколько из следующих состояний или заболеваний: шизофрении, психотического расстройства NOS, кратковременного психотического расстройства, шизофреноформного расстройства, шизоаффективного расстройства, бредового расстройства, индуцированного психотического расстройства, злокачественной шизофрении, послеродового психоза, психотической депрессии, психотической вспышки, позднего психоза, микседематозного психоза, производственного психоза, менструального психоза, вторичного психотического расстройства, биполярного расстройства I типа с психотическими признаками и психотического расстройства, вызванного употреблением психоактивных веществ. В некоторых вариантах осуществления психотическим расстройством является психоз, ассоциированный с заболеванием, выбранным из большого депрессивного расстройства, аффективного расстройства, биполярного расстройства, расстройства, связанного с аномальным уровнем электролитов, болезни Альцгеймера, неврологического расстройства, гипогликемии, AIDS, обыкновенной волчанки и посттравматического стрессового расстройства.
В некоторых вариантах осуществления расстройством является неврологическое расстройство, выбранное из опухоли головного мозга, деменции с тельцами Леви, рассеянного склероза, саркоидоза, болезни Лайма, сифилиса, болезни Альцгеймера, болезни Паркинсона, и анти-NMDA-рецепторного энцефалита.
В некоторых вариантах осуществления расстройством является психотическое расстройство, выбранное из шизофрении, кратковременного психотического расстройства, шизофреноформного расстройства, шизоаффективного расстройства, бредового расстройства и индуцированного психотического расстройства. В некоторых вариантах осуществления шизофрения выбрана из злокачественной шизофрении, кататонической шизофрении, параноидальной шизофрении, остаточной шизофрении, гебефренической шизофрении и недифференцированной шизофрении. В некоторых вариантах осуществления расстройство выбрано из шизоидного расстройства личности, шизотипического расстройства личности и параноидального расстройства личности. В некоторых вариантах осуществления психотическое расстройство вызвано соматическим заболеванием и вызвано употреблением психоактивных веществ или вызвано употреблением лекарственных средств (фенциклидином, кетамином и другими диссоциативными анестетиками, амфетаминами и другими психостимуляторами и кокаином).
В некоторых вариантах осуществления настоящее изобретение предусматривает способ лечения когнитивного расстройства, предусматривающий введение пациенту, нуждающемуся в нем, эффективного количества соединения или композиции по настоящему изобретению. В некоторых вариантах осуществления когнитивные расстройства включают деменцию (ассоциированную с болезнью Альцгеймера, ишемией, мультиинфарктной деменцией, травмой, сосудистыми проблемами или инсультом, заболеванием HIV, болезнью Паркинсона, болезнью Хантингтона, болезнью Пика, болезнью Крейтцфельдта-Якоба, перинатальной гипоксией, другими соматическими заболеваниями или злоупотреблением различными психоактивными веществами), делирий, амнестическое расстройство, вызванный употреблением психоактивных веществ сохраняющийся делирий, деменцию вследствие заболевания HIV, деменцию вследствие болезни Хантингтона, деменцию вследствие болезни Паркинсона, деменцию вследствие комплекса паркинсонизма-ALS, деменцию по типу болезни Альцгеймера, возрастное снижение когнитивных способностей и умеренные когнитивные нарушения.
Переработанное четвертое издание Диагностического и статистического руководства по расстройствам психической деятельности (DSM-IV-TR) (2000, American Psychiatric Association, Washington DC) предоставляет средство диагностики, которое предусматривает когнитивные расстройства, включая деменцию, делирий, амнестические расстройства и возрастное снижение когнитивных способностей. Пятое издание Диагностического и статистического руководства по расстройствам психической деятельности (DSM-5) (2013, American Psychiatric Association, Washington DC) предоставляет средство диагностики нейрокогнитивных расстройств (NCD), которые включают делирий, за которым следуют синдромы большого NCD, умеренного NCD и их этиологические подтипы. Подтипы большого или умеренного NCD включают NCD вследствие болезни Альцгеймера, сосудистое NCD, NCD с тельцами Леви, NCD вследствие болезни Паркинсона, лобно-височное NCD, NCD вследствие травматического повреждения головного мозга, NCD вследствие инфекции HIV, индуцированное веществом/лекарственным препаратом NCD, NCD вследствие болезни Хантингтона, NCD вследствие прионной болезни, NCD вследствие другого патологического состояния, NCD вследствие множественных этиологии и NCD неустановленного характера. Категория NCD в DSM-5 охватывает группу расстройств, при которых в когнитивной функции наблюдается первичное клиническое нарушение и которые приобретаются со временем в отличие от нарушений развития. Используемый в данном документе термин "когнитивные расстройства" включает лечение тех когнитивных расстройств и нейрокогнитивных расстройств, которые описаны в DSM-IV-TR или DSM-5. Квалифицированному специалисту будет понятно, что существуют альтернативные номенклатуры, нозологии и системы классификации для расстройств психической деятельности, и что данные системы развиваются вместе с медицинским и научным прогрессом. Таким образом, термин "когнитивные расстройства" предназначен для включения подобных расстройств, которые описаны в других диагностических источниках.
В некоторых вариантах осуществления настоящее изобретение предусматривает способ лечения шизофрении или психоза, предусматривающий введение пациенту, нуждающемуся в нем, эффективного количества соединения или композиции по настоящему изобретению. Конкретные патологии шизофрении или психоза представляют собой параноидальную, гебефреническую, кататоническую или недифференцированную шизофрению и психотическое расстройство, вызванное употреблением психоактивных веществ. DSM-IV-TR предоставляет средство диагностики, которое предусматривает параноидальную, гебефреническую, кататоническую, недифференцированную или остаточную шизофрению и психотическое расстройство, вызванное употреблением психоактивных веществ. В DSM-5 исключены подтипы шизофрении и вместо этого включен всесторонний подход к оценке тяжести главных симптомов шизофрении для охвата гетерогенности симптоматического типа и тяжести, проявляющихся среди индивидов с психотическими расстройствами. Используемый в данном документе термин "шизофрения или психоз" включает лечение тех расстройств психической деятельности, которые описаны в DSM-IV-TR или DSM-5. Квалифицированному специалисту будет понятно, что существуют альтернативные номенклатуры, нозологии и системы классификации для расстройств психической деятельности, и что данные системы развиваются вместе с медицинским и научным прогрессом. Таким образом, термин "шизофрения или психоз" предназначен для включения подобных расстройств, которые описаны в других диагностических источниках.
В некоторых вариантах осуществления настоящее изобретение предусматривает способ лечения боли, предусматривающий введение пациенту, нуждающемуся в нем, эффективного количества соединения или композиции по настоящему изобретению. Конкретные варианты осуществления, предусматривающие боль, представляют собой боль в костях и суставах (остеоартрит), повторяющуюся боль при движении, зубную боль, боль, связанную с раковым заболеванием, миофасциальный болевой синдром (мышечное повреждение, фибромиалгия), периоперационную боль (общая хирургия, гинекологическая), хроническую боль и нейропатическую боль.
Соединения и композиции могут быть дополнительно применимы в способе предупреждения, лечения, контроля, облегчения или снижения риска возникновения заболеваний, расстройств и состояний, упомянутых в данном документе. Соединения и композиция могут быть дополнительно применимы в способе предупреждения, лечения, контроля, облегчения или снижения риска возникновения вышеуказанных заболеваний, расстройств и состояний в комбинации с другими средствами.
При лечении состояний, при которых необходима активация mAChR М4, подходящий уровень дозы может составлять приблизительно от 0,01 до 500 мг на кг веса тела пациента в день, который можно вводить в однократных или многократных дозах. Уровень дозы может составлять от приблизительно 0,1 до приблизительно 250 мг/кг в день или от приблизительно 0,5 до приблизительно 100 мг/кг в день. Подходящий уровень дозы может составлять приблизительно от 0,01 до 250 мг/кг в день, приблизительно от 0,05 до 100 мг/кг в день или приблизительно от 0,1 до 50 мг/кг в день. В пределах данного диапазона доза может составлять от 0,05 до 0,5, от 0,5 до 5 или от 5 до 50 мг/кг в день. Для перорального введения композиции могут быть предоставлены в форме таблеток, содержащих от 1,0 до 1000 миллиграмм активного ингредиента, в частности 1,0, 5,0, 10, 15, 20, 25, 50, 75, 100, 150, 200, 250, 300, 400, 500, 600, 750, 800, 900 или 1000 миллиграмм активного ингредиента, для симптоматической корректировки дозы для пациента, подлежащего лечению. Соединения можно вводить в рамках режима от 1 до 4 раз в день, предпочтительно один или два раза в день. Данный режим доз можно корректировать с обеспечением наилучшего терапевтического ответа. Однако, будет понятно, что конкретные уровень дозы и частота введения доз для любого отдельного пациента могут варьировать и будут зависеть от ряда факторов, в том числе активности конкретного применяемого соединения, устойчивости к инактивации в процессе метаболизма и продолжительности действия такого соединения, возраста, веса тела, общего состояния здоровья, пола, рациона, способа и времени введения, скорости экскреции, комбинации с лекарственными средствами, тяжести отдельного состояния и уже проводимой терапии для пациента.
Таким образом, в некоторых вариантах осуществления настоящее изобретение относится к способу активации активности рецептора mAChR М4 по меньшей мере в одной клетке, предусматривающий стадию приведения в контакт по меньшей мере одной клетки по меньшей мере с одним раскрытым соединением или по меньшей мере с одним продуктом раскрытого способа в количестве, эффективном для активации mAChR М4 по меньшей мере в одной клетке. В некоторых вариантах осуществления клеткой является клетка млекопитающего, например человека. В некоторых вариантах осуществления клетка была выделена из субъекта перед стадией приведения в контакт. В некоторых вариантах осуществления приведение в контакт осуществляют путем введения субъекту.
В некоторых вариантах осуществления настоящее изобретение относится к способу активации активности mAChR М4 у субъекта, предусматривающему стадию введения субъекту по меньшей мере одного раскрытого соединения или по меньшей мере одного продукта раскрытого способа в дозе и количестве, эффективных для активации активности mAChR М4 у субъекта. В некоторых вариантах осуществления субъектом является млекопитающее, например человек. В некоторых вариантах осуществления у млекопитающего была диагностирована необходимость в агонизме mAChR М4 перед стадией введения. В некоторых вариантах осуществления у млекопитающего была диагностирована необходимость в активации mAChR М4 перед стадией введения. В некоторых вариантах осуществления способ дополнительно предусматривает стадию идентификации субъекта, нуждающегося в агонизме mAChR М4.
В некоторых вариантах осуществления настоящее изобретение относится к способу лечения расстройства, ассоциированного с селективной активацией mAChR М4, например расстройства, ассоциированного с холинергической активностью, у млекопитающего, предусматривающему стадию введения млекопитающему по меньшей мере одного раскрытого соединения или по меньшей мере одного продукта раскрытого способа в дозе и количестве, эффективных для лечения расстройства у млекопитающего. В некоторых вариантах осуществления млекопитающим является человек. В некоторых вариантах осуществления у млекопитающего была диагностирована необходимость в лечении расстройства перед стадией введения. В некоторых вариантах осуществления способ дополнительно предусматривает стадию идентификации субъекта, нуждающегося в лечении расстройства.
В некоторых вариантах осуществления расстройство может быть выбрано из психоза, шизофрении, кондуктивного расстройства, расстройства социального поведения, биполярного расстройства, психотических эпизодов тревожности, тревожности, ассоциированной с психозом, психотических расстройств настроения, таких как большое депрессивное расстройство тяжелой степени; расстройств настроения, ассоциированных с психотическими расстройствами, острого маниакального синдрома, депрессии, ассоциированной с биполярным расстройством, расстройств настроения, ассоциированных с шизофренией, поведенческих проявлений умственной отсталости, аутического расстройства, двигательных расстройств, синдрома Туретта, акинетико-ригидного синдрома, двигательных расстройств, ассоциированных с болезнью Паркинсона, поздней дискинезии, лекарственной дискинезии и дискинезии, вызванной нейродегенерацией, синдрома дефицита внимания и гиперактивности, когнитивных расстройств, форм деменции и расстройств памяти.
В некоторых вариантах осуществления расстройством является болезнь Альцгеймера.
b. Потенцирование активности мускаринового ацетилхолинового рецептора
В некоторых вариантах осуществления настоящее изобретение относится к способу потенцирования активности мускаринового ацетилхолинового рецептора у млекопитающего, предусматривающему стадию введения млекопитающему эффективного количества по меньшей мере одного раскрытого соединения или его фармацевтически приемлемой соли или фармацевтической композиции, содержащей по меньшей мере одно раскрытое соединение или его фармацевтически приемлемую соль. В некоторых вариантах осуществления потенцирование активности мускаринового ацетилхолинового рецептора повышает активность мускаринового ацетилхолинового рецептора. В некоторых вариантах осуществления потенцирование активности мускаринового ацетилхолинового рецептора представляет собой частичный агонизм мускаринового ацетилхолинового рецептора. В некоторых вариантах осуществления потенцирование активности мускаринового ацетилхолинового рецептора представляет собой положительную аллостерическую модуляцию мускаринового ацетилхолинового рецептора.
В некоторых вариантах осуществления вводимое соединение проявляет потенцирование mAChR М4 с ЕС50, составляющей менее приблизительно 10 мкМ, менее приблизительно 5 мкМ, менее приблизительно 1 мкМ, менее приблизительно 500 нМ или менее приблизительно 100 нМ. В некоторых вариантах осуществления вводимое соединение проявляет потенцирование mAChR М4 с ЕС50, составляющей от приблизительно 10 мкМ до приблизительно 1 нМ, от приблизительно 1 мкМ до приблизительно 1 нМ, от приблизительно 100 нМ до приблизительно 1 нМ или от приблизительно 10 нМ до приблизительно 1 нМ.
В некоторых вариантах осуществления млекопитающим является человек. В некоторых вариантах осуществления у млекопитающего была диагностирована необходимость в потенцировании активности мускаринового ацетилхолинового рецептора перед стадией введения. В некоторых вариантах осуществления способ дополнительно предусматривает стадию идентификации млекопитающего, нуждающегося в потенцировании активности мускаринового ацетилхолинового рецептора. В некоторых вариантах осуществления путем потенцирования активности мускаринового ацетилхолинового рецептора осуществляют лечение расстройства, ассоциированного с активностью мускаринового ацетилхолинового рецептора, у млекопитающего. В некоторых вариантах осуществления мускариновым ацетилхолиновым рецептором является mAChR М4.
В некоторых вариантах осуществления потенцирование активности мускаринового ацетилхолинового рецептора у млекопитающего ассоциировано с лечением неврологического и/или психического расстройства, ассоциированного с дисфункцией мускаринового рецептора, такого как неврологическое или психическое расстройство, раскрытое в данном документе. В некоторых вариантах осуществления мускариновым рецептором является mAChR М4.
В некоторых вариантах осуществления настоящее изобретение предусматривает способ потенцирования активности мускаринового ацетилхолинового рецептора в клетке, предусматривающий стадию приведения в контакт клетки с эффективным количеством по меньшей мере одного раскрытого соединения или его фармацевтически приемлемой соли. В некоторых вариантах осуществления клеткой является клетка млекопитающего (например, человека). В некоторых вариантах осуществления клетка была выделена из млекопитающего перед стадией приведения в контакт. В некоторых вариантах осуществления приведение в контакт осуществляют путем введения млекопитающему.
с. Улучшение когнитивных функций
В некоторых вариантах осуществления настоящее изобретение относится к способу улучшения когнитивных функций у млекопитающего, предусматривающему стадию введения млекопитающему эффективного количества по меньшей мере одного раскрытого соединения или его фармацевтически приемлемой соли, гидрата, сольвата или полиморфа.
В некоторых вариантах осуществления млекопитающим является человек. В некоторых вариантах осуществления у млекопитающего была диагностирована необходимость в улучшении когнитивных функций перед стадией введения. В некоторых вариантах осуществления способ дополнительно предусматривает стадию идентификации млекопитающего, нуждающегося в улучшении когнитивных функций. В некоторых вариантах осуществления необходимость в улучшении когнитивных функций ассоциирована с дисфункцией мускаринового рецептора. В некоторых вариантах осуществления мускариновым рецептором является mAChR М4.
В некоторых вариантах осуществления улучшение когнитивных функций представляет собой статистически значимое повышение степени распознавания новых объектов. В некоторых вариантах осуществления улучшение когнитивных функций представляет собой статистически значимое повышение степени выполнения Висконсинского теста сортировки карточек.
d. Котерапевтические способы
Настоящее изобретение дополнительно направлено на введение селективного активатора mAChR М4 для улучшения исходов лечения в контексте когнитивной или поведенческой терапии. Другими словами, в некоторых вариантах осуществления настоящее изобретение относится к котерапевтическому способу, предусматривающему стадию введения млекопитающему эффективных количества и дозы по меньшей мере одного раскрытого соединения или его фармацевтически приемлемой соли.
В некоторых вариантах осуществления введение улучшает исходы лечения в контексте когнитивной или поведенческой терапии. Введение в связи с осуществлением когнитивной или поведенческой терапии может быть непрерывным или прерывистым. Введение не обязательно должно быть одновременным с терапией и может проводиться перед, во время и/или после терапии. Например, когнитивную или поведенческую терапию можно проводить в пределах 1, 2, 3, 4, 5, 6, 7 дней до введения или после введения соединения. В качестве дополнительного примера когнитивную или поведенческую терапию можно проводить в пределах 1, 2, 3 или 4 недель до введения или после введения соединения. В качестве другого дополнительного примера когнитивную или поведенческую терапию можно проводить до введения или после введения в течение периодов времени, составляющих 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 периодов полувыведения введенного соединения.
Понятно, что раскрытые котерапевтические способы можно применять вместе с раскрытыми соединениями, композициями, наборами и путями применения.
e. Виды комбинированной терапии
В способах применения, описанных в настоящем документе, дополнительное(-ые) терапевтическое(-ие) средство(-а) можно вводить одновременно или последовательно с раскрытыми соединениями и композициями. Последовательное введение включает введение до или после раскрытых соединений и композиций. В некоторых вариантах осуществления дополнительное терапевтическое средство или дополнительные терапевтические средства можно вводить в той же композиции, что и раскрытые соединения. В других вариантах осуществления может иметь место некоторый интервал времени между введением дополнительного терапевтического средства и раскрытых соединений. В некоторых вариантах осуществления введение дополнительного терапевтического средства с раскрытым соединением может привести к более низким дозам других терапевтических средств и/или введению при менее частых интервалах. В случае применения в комбинации с одним или несколькими другими активными ингредиентами соединения по настоящему изобретению и другие активные ингредиенты можно применять при более низких дозах, нежели в случае применения каждого по отдельности. Соответственно, фармацевтические композиции по настоящему изобретению включают такие, которые содержат один или несколько других активных ингредиентов помимо соединения формулы (I). Вышеуказанные комбинации включают в себя комбинации соединения по настоящему изобретению не только с одним другим активным соединением, но также с двумя или более другими активными соединениями.
Раскрытые соединения можно применять в качестве самостоятельных средств или в комбинации с одним или несколькими другими лекарственными средствами при лечении, предупреждении, контроле, облегчении или снижении риска возникновения вышеуказанных заболеваний, расстройств и состояний, для которых соединение или другие лекарственные средства обладают полезностью, где комбинация лекарственных средств вместе является более безопасной или более эффективной, чем каждое лекарственное средство отдельно. Другое(-ие) лекарственное(-ые) средство(-а) можно вводить путем и в количестве, обычно применяемых для этого, одновременно или последовательно с раскрытым соединением. В случае, если раскрытое соединение применяют одновременно с одним или несколькими другими лекарственными средствами, можно применять фармацевтическую композицию в стандартной лекарственной форме, содержащей такие лекарственные средства и раскрытое соединение. Однако, комбинированную терапию также можно проводить по перекрывающимся графикам. Также предполагается, что комбинация одного или нескольких активных ингредиентов и раскрытого соединения может быть более действенной, чем каждое из них как отдельное средство. Таким образом, когда применяют в комбинации с одним или несколькими другими активными ингредиентами, раскрытые соединения и другие активные ингредиенты можно применять при более низких дозах, нежели в случае применения каждого по отдельности.
Фармацевтические композиции и способы по настоящему изобретению могут дополнительно содержать другие терапевтически активные соединения, как указано в данном документе, которые обычно применяют при лечении вышеуказанных патологических состояний.
Вышеуказанные комбинации включают в себя комбинации раскрытого соединения не только с одним другим активным соединением, но также с двумя или более другими активными соединениями. Точно так же раскрытые соединения можно применять в комбинации с другими лекарственными средствами, которые применяют при предупреждении, лечении, контроле, облегчении или снижении риска возникновения заболеваний или состояний, для лечения которых раскрытые соединения применимы. Такие другие лекарственные средства можно вводить путем и в количестве, обычно применяемых для этого, одновременно или последовательно с соединением по настоящему изобретению. В случае, если соединение по настоящему изобретению применяют одновременно с одним или несколькими другими лекарственными средствами, предпочтительной является фармацевтическая композиция, содержащая такие другие лекарственные средства в дополнение к раскрытому соединению. Соответственно, фармацевтические композиции включают те, которые также содержат один или несколько других активных ингредиентов помимо соединения по настоящему изобретению.
Весовое соотношение раскрытого соединения ко второму активному ингредиенту может варьировать и будет зависеть от эффективной дозы каждого ингредиента. Обычно будет применяться эффективная доза каждого из них. Таким образом, например, если соединение по настоящему изобретению объединяют с другим средством, весовое соотношение раскрытого соединения к другому средству обычно будет находиться в диапазоне от приблизительно 1000:1 до приблизительно 1:1000, предпочтительно от приблизительно 200:1 до приблизительно 1:200. Комбинации соединения по настоящему изобретению и других активных ингредиентов обычно также будут находиться в пределах вышеупомянутого диапазона, но в каждом случае необходимо применять эффективную дозу каждого активного ингредиента.
В таких комбинациях раскрытое соединение и другие активные средства можно вводить по отдельности или вместе. Кроме того, введение одного элемента можно проводить до введения, одновременно с введением или после введения другого(-их) средства(средств).
Соответственно, раскрытые соединения можно применять отдельно или в комбинации с другими средствами, которые, как известно, являются преимущественными в связи с показаниями, имеющимися у субъекта, или другими лекарственными средствами, которые воздействуют на рецепторы или ферменты, которые либо увеличивают эффективность, безопасность, удобство применения, либо уменьшают нежелательные побочные эффекты или токсичность раскрытых соединений. Исследуемое соединение и другое средство можно вводить совместно, либо при сопутствующей терапии, либо в составе фиксированной комбинации.
В некоторых вариантах осуществления соединение можно применять в комбинации со средствами против болезни Альцгеймера, ингибиторами бета-секретазы, холинергическими средствами, ингибиторами гамма-секретазы, ингибиторами HMG-СоА редуктазы, аллостерическими агонистами M1, положительными аллостерическими модуляторами M1, NSAID, в том числе ибупрофеном, витамином Е и антителами к амилоиду. В другом варианте осуществления исследуемое соединение можно применять в комбинации с успокоительными средствами, снотворными средствами, транквилизаторами, антипсихотиками (типичными и нетипичными), противотревожными средствами, циклопирролонами, имидазопиридинами, пиразолопиримидинами, малыми транквилизаторами, агонистами и антагонистами мелатонина, мелатонергетическими средствами, бензодиазепинами, барбитуратами, антагонистами 5НТ-2 и т.п., такими как адиназолам, аллобарбитал, алонимид, алпразолам, амисульприд, амитриптилин, амобарбитал, амоксапин, арипипразол, бентазепам, бензоктамин, бротизолам, бупропион, буспирон, бутабарбитал, буталбитал, капурид, карбоклорал, хлоралбетаин, хлоралгидрат, кломипрамин, клоназепам, клоперидон, клоразепат, хлордиазепоксид, хлоретат, хлорпромазин, клозапин, ципразепам, дезипрамин, декскламол, диазепам, дихлоралфеназон, дивальпроекс, дифенгидрамин, доксепин, эстазолам, этхлорвинол, этомидат, фенобам, флунитразепам, флупентиксол, флуфеназин, флуразепам, флувоксамин, флуоксетин, фозазепам, глютетимид, галазепам, галоперидол, гидроксизин, имипрамин, литий, лоразепам, лорметазепам, мапротилин, меклоквалон, мелатонин, мефобарбитал, мепробамат, метаквалон, мидафлур, мидазолам, нефазодон, низобамат, нитразепам, нортриптилин, оланзапин, оксазепам, паральдегид, пароксетин, пентобарбитал, перлапин, перфеназин, фенелзин, фенобарбитал, празепам, прометазин, пропофол, протриптилин, квазепам, кветиапин, реклазепам, рисперидон, ролетамид, секобарбитал, сертралин, супроклон, темазепам, тиоридазин, тиотиксен, траказолат, транилципромин, тразодон, триазолам, трепипам, трицетамид, триклофос, трифлуоперазин, триметозин, тримипрамин, ульдазепам, венлафаксин, залеплон, зипрасидон, золазепам, золпидем и их соли, и их комбинациями и т.п., или исследуемое соединение можно вводить в сочетании с применением физических способов, таких как фототерапия или электростимуляция.
В некоторых вариантах осуществления соединение можно применять в комбинации с леводопой (с селективным экстрацеребральным ингибитором декарбоксилазы, например карбидопой или бенсеразидом, или без него), антихолинергическими средствами, такими как бипериден (необязательно в виде его хлористоводородной соли или соли молочной кислоты) и хлористоводородным тригексифенидилом (бензгексол), ингибиторами СОМТ, такими как энтакапон, ингибиторами МОА-В, антиоксидантами, антагонистами аденозинового рецептора А2а, холинергическими агонистами, антагонистами рецептора NMDA, антагонистами рецептора серотонина и агонистами рецептора дофамина, такими как алентемол, бромокриптин, фенолдопам, лизурид, наксаголид, перголид и прамипексол. Следует понимать, что агонист дофамина может быть в форме фармацевтически приемлемой соли, например гидробромида алентемола, мезилата бромокриптина, мезилата фенолдопама, гидрохлорида наксаголида и мезилата перголида. Лизурид и прамипексол широко используются в форме, отличной от соли.
В некоторых вариантах осуществления соединение можно использовать в комбинации с соединением из таких классов нейролептических средств, как фенотиазин, тиоксантен, гетероциклический дибензазепин, бутирофенон, дифенилбутилпиперидин и индолон. Подходящие примеры фенотиазинов включают хлорпромазин, мезоридазин, тиоридазин, ацетофеназин, флуфеназин, перфеназин и трифлуоперазин. Подходящие примеры тиоксантенов включают хлорпротиксен и тиотиксен. Пример дибензазепина представляет собой клозапин. Пример бутирофенона представляет собой галоперидол. Пример дифенилбутилпиперидина представляет собой пимозид. Пример индолона представляет собой молиндолон. Другие нейролептические средства включают локсапин, сульпирид и рисперидон. Следует понимать, что нейролептические средства при применении в комбинации с исследуемым соединением могут быть в форме фармацевтически приемлемой соли, например, гидрохлорида хлорпромазина, безилата мезоридазина, гидрохлорида тиоридазина, малеината ацетофеназина, гидрохлорида флуфеназина, энантата флуфеназина, деканоата флуфеназина, гидрохлорида трифлуоперазина, гидрохлорида тиотиксена, деканоата галоперидола, сукцината локсапина и гидрохлорида молиндона. Перфеназин, хлорпротиксен, клозапин, галоперидол, пимозид и рисперидон широко используются в форме, отличной от соли.
Таким образом, исследуемое соединение можно применять в комбинации с ацетофеназином, алентемолом, арипипразолом, амисульпридом, бензгексолом, бромокриптином, бипериденом, хлорпромазином, хлорпротиксеном, клозапином, диазепамом, фенолдопамом, флуфеназином, галоперидолом, леводопой, леводопой с бенсеразидом, леводопой с карбидопой, лизуридом, локсапином, мезоридазином, молиндолоном, наксаголидом, оланзапином, перголидом, перфеназином, пимозидом, прамипексолом, кветиапином, рисперидоном, сульпиридом, тетрабеназином, тригексифенидилом, тиоридазином, тиотиксеном, трифлуоперазином или зипрасидоном.
В некоторых вариантах осуществления соединение можно применять в комбинации с антидепрессантом или противотревожным средством, в том числе ингибиторами обратного захвата норэпинефрина (включая третичные трициклические амины и вторичные трициклические амины), селективными ингибиторами обратного захвата серотонина (SSRI), ингибиторами моноаминоксидазы (MAOI), обратимыми ингибиторами моноаминоксидазы (RIMA), ингибиторами обратного захвата серотонина и норадреналина (SNRI), антагонистами кортикотропин-рилизинг фактора (CRF), антагонистами α-адренорецепторов, антагонистами рецептора нейрокинина-1, нетипичными антидепрессантами, бензодиазепинами, агонистами или антагонистами 5-НТ1А, особенно частичными агонистами 5-НТ1А и антагонистами кортикотропин-рилизинг фактора (CRF). Конкретные средства включают: амитриптилин, кломипрамин, доксепин, имипрамин и тримипрамин; амоксапин, дезипрамин, мапротилин, нортриптилин и протриптилин; флуоксетин, флувоксамин, пароксетин и сертралин; изокарбоксазид, фенелзин, транилципромин и селегилин; моклобемид; венлафаксин; дулоксетин; апрепитант; бупропион, литий, нефазодон, тразодон и вилоксазин; алпразолам, хлордиазепоксид, клоназепам, клоразепат, диазепам, галазепам, лоразепам, оксазепам и празепам; буспирон, флесиноксан, гепирон и ипсапирон и их фармацевтически приемлемые соли.
В некоторых вариантах осуществления соединения можно совместно вводить с ортостерическими мускариновыми агонистами, мускариновыми потенциаторами или ингибиторами холинэстеразы. В некоторых вариантах осуществления соединения можно совместно вводить с ингибиторами GlyT1 и т.п., такими как без ограничения: рисперидон, клозапин, галоперидол, флуоксетин, празепам, ксаномелин, литий, фенобарбитол и их соли и их комбинации.
f. Способы введения
Способы лечения могут включать любое количество способов введения раскрытой композиции. Способы введения могут включать таблетки, пилюли, драже, твердые и мягкие желатиновые капсулы, гранулы, пеллеты, водные, липидные, масляные или другие растворы, эмульсии, такие как эмульсии по типу масло в воде, липосомы, водные или масляные суспензии, сиропы, крепкие настои, твердые эмульсии, твердые дисперсии или диспергируемые порошки. Для получения фармацевтических композиций для перорального введения средство можно смешивать с общеизвестными и широко используемыми добавками и вспомогательными веществами, такими как, например, аравийская камедь, тальк, крахмал, сахара (такие как, например, маннитоза, метилцеллюлоза, лактоза), желатин, поверхностно-активные средства, стеарат магния, водные или неводные растворители, парафиновые производные, сшивающие средства, диспергирующие средства, эмульгаторы, смазывающие средства, консервирующие средства, вкусовые добавки (например, эфирные масла), вещества, усиливающие растворимость (например, бензилбензоат или бензиловый спирт), или вещества, увеличивающие биодоступность (например, Gelucire.TM.). В фармацевтической композиции средство также можно диспергировать в композиции на основе микрочастиц, например в композиции на основе наночастиц.
Для парентерального введения средство может быть растворенным или суспендированным в физиологически приемлемом разбавителе, таком как, например, вода, буфер, масла с солюбилизаторами или без них, поверхностно-активные средства, диспергирующие средства или эмульгаторы. В качестве масел, например и без ограничения, можно использовать оливковое масло, арахисовое масло, хлопковое масло, соевое масло, касторовое масло и кунжутное масло. Если говорить в общем, для парентерального введения средство может быть в форме водного, липидного, масляного раствора или раствора другого вида или суспензии или даже может вводиться в форме липосом или наносуспензий.
Термин "парентерально", используемый в данном документе, относится к способам введения, которые включают внутривенную, внутримышечную, интраперитонеальную, внутригрудинную, подкожную и внутрисуставную инъекцию и инфузию.
5. Наборы
В одном аспекте настоящее изобретение предусматривает наборы, содержащие по меньшей мере одно раскрытое соединение или его фармацевтически приемлемую соль и одно или несколько из:
(a) по меньшей мере одного средства, которое, как известно, повышает активность mAChR М4;
(b) по меньшей мере одного средства, которое, как известно, снижает активность mAChR М4;
(c) по меньшей мере одного средства, с помощью которого, как известно, осуществляют лечение расстройства, ассоциированного с холинергической активностью;
(d) инструкций касательно лечения расстройства, ассоциированного с холинергической активностью;
(e) инструкций касательно лечения расстройства, ассоциированного с активностью рецептора М4; или
(f) инструкций касательно введения соединения в связи с осуществлением когнитивной или поведенческой терапии.
В некоторых вариантах осуществления по меньшей мере одно раскрытое соединение и по меньшей мере одно средство совместно составлены. В некоторых вариантах осуществления по меньшей мере одно раскрытое соединение и по меньшей мере одно средство совместно упакованы. Наборы также могут содержать соединения и/или продукты, совместно упакованные, совместно составленные и/или совместно доставляемые с другими компонентами. Например, изготовитель лекарственных средств, лицо, осуществляющее перепродажу лекарственных средств, медик, производственная аптека или фармацевт могут предоставить набор, содержащий раскрытое соединение и/или продукт и другой компонент для доставки пациенту.
Раскрытые наборы можно применять по отношению к раскрытым способам применения.
Наборы могут содержать информацию, инструкции или и то, и другое, так что применение набора обеспечит лечение патологических состояний у млекопитающих (в частности, людей). Информация и инструкции могут быть в форме слов, рисунков или и того, и другого и т.п. В дополнение или в качестве альтернативы набор может содержать соединение, композицию или и то, и другое; и информацию, инструкции или и то, и другое в отношении способов применения соединения или композиции предпочтительно с благоприятным эффектом лечения или предупреждения патологических состояний у млекопитающих (например, людей).
Соединения и способы по настоящему изобретению будет легче понять с помощью ссылок на следующие примеры, которые предназначены для иллюстрации и не ограничивают объем настоящего изобретения.
6. Примеры
Все спектры ЯМР регистрировали на ЯМР-спектрометре АМХ Bruker 400 МГц. Химические сдвиги1Н в сторону слабого поля представлены в значениях δ в ppm с дейтерированным растворителем в качестве внутреннего стандарта. Данные представлены следующим образом: химический сдвиг, мультиплетность (s = синглет, bs = широкий синглет, d = дублет, t = триплет, q = квартет, dd = дублет дублетов, m = мультиплет, ABq = АВ квартет), константа взаимодействия, интеграция. Анализ с помощью обращенно-фазовой LCMS выполняли с применением системы Agilent 1200, содержащей насос для двухкомпонентных смесей с дегазатором, высокоэффективный автоматический дозатор, отсек для термостатируемой колонки, колонку С18, детектор на диодной матрице (DAD) и Agilent 6150 MSD со следующими параметрами. Градиентные условия были следующими: от 5% до 95% ацетонитрила с водной фазой, содержащей 0,1% TFA в воде, на протяжении 1,4 минуты. Образцы разделяли на колонке Waters Acquity UPLC ВЕН С18 (1,7 мкм, 1,0×50 мм) при 0,5 мл/мин. с поддержанием температуры колонки и растворителя при 55°С. DAD настраивали на сканирование от 190 до 300 нм, и применяемые сигналы составляли 220 нм и 254 нм (оба с шириной полосы 4 нм). MS-детектор сконфигурирован таким образом, что он имеет источник ионизации электрораспылением, и масс-спектры с низкой разрешающей способностью получали посредством сканирования от 140 до 700 AMU с размером шага 0,2 AMU при 0,13 циклов/секунда и с шириной пика 0,008 минуты. Поток высушивающего газа устанавливали на 13 литров в минуту при 300°С и давление распылителя устанавливали на 30 фунтов/кв. дюйм. Напряжение капиллярной иглы устанавливали на 3000 В, и напряжение фрагментора устанавливали на 100 В. Сбор данных проводили с помощью программного обеспечения Agilent Chemstation и Analytical Studio Reviewer.
Сокращения, которые были использованы в описаниях следующих примеров, представляют собой: IPA означает изопропиловый спирт; АсОН означает уксусную кислоту; ВОР означает гексафторфосфат (бензотриазол-1-илокси)трис(диметиламино)фосфония; DBU означает 1,8-диазабицикло(5.4.0)ундец-7-ен; DCM означает дихлорметан; DEAD означает диэтилазодикарбоксилат (номер по CAS 1972-28-7); DIEA означает N,N-диизопропилэтиламин; DMF означает N,N-диметилформамид; DMSO означает диметилсульфоксид; EtOAc означает этилацетат; EtOH означает этанол; HATU означает гексафторфосфат 1-[бис(диметиламино)метилен]-1H-1,2,3-триазоло[4,5-b]пиридиний-3-оксида; МеОН означает метанол; NMP означает N-метил-2-пирролидон; MW означает микроволновой (подразумевается микроволновой реактор); RBF означает круглодонную колбу; к.т. означает комнатную температуру; и THF означает тетрагидрофуран.
Пример 1. Общий синтез аминов
Последующее представляет собой иллюстративные синтезы некоторых аминов, применяемых для получения соединений, раскрытых в данном документе.

4-(1-Метокси-1-метилэтил)бензонитрил (X1). К раствору 4-(1-гидрокси-1-метилэтил)бензонитрила (700 мг, 4,34 ммоль, 1,0 экв.) в DMF (16,4 мл) при 5°С добавляли гидрид натрия (60% в минеральном масле, 260 мг, 6,51 ммоль, 1,5 экв.). После 1 ч. при 5°С добавляли йодметан (0,30 мл, 4,78 ммоль, 1,1 экв.). Обеспечивали нагревание смеси до к.т. После 2 ч. добавляли воду (20 мл), а затем EtOAc (30 мл). Слои разделяли. Водный слой экстрагировали с помощью EtOAc (2×30 мл). Объединенные органические слои промывали солевым раствором, высушивали (Na2SO4), фильтровали и концентрировали. Остаток очищали с помощью колоночной флэш-хроматографии на силикагеле (0-50% EtOAc/гексаны) с получением указанного в заголовке соединения в виде вязкого масла (600 мг, выход 79%). ES-MS [М+1]+: 176,6;1Н ЯМР (400 МГц, DMSO-d6) δ 7,82 (ddd, J=8,6, 1,8, 1,8 Гц, 2Н), 7,58 (ddd, J=8,6, 1,8, 1,8 Гц, 2Н), 7,58 (ddd)
[4-(1-Метокси-1-метилэтил)фенил]метанамин (Х2). К раствору X1 (600 мг, 3,42 ммоль, 1,0 экв.) в THF (17 мл) добавляли по каплям раствор алюмогидрида лития (1,0 М в THF, 10,27 мл, 10,27 ммоль, 3,0 экв.) при 0°С. После 30 мин. при 0°С ледяную баню убирали и реакционную смесь нагревали до температуры флегмы. После 30 мин. образовывалась кремообразная паста. Нагревание прекращали. При 0°С медленно добавляли насыщенный раствор сегнетовой соли (7,0 мл), а затем МеОН (7,0 мл). Смесь перемешивали при к.т. в течение 1 ч. и фильтровали через подушку из целита, которую дополнительно промывали с помощью 10% МеОН в DCM. Собранный фильтрат высушивали (MgSO4), фильтровали и концентрировали. Остаток очищали с помощью колоночной флэш-хроматографии на силикагеле с применением раствора DCM/MeOH/NH4OH (89:10:1) с DCM в качестве сорастворителя с получением указанного в заголовке соединения в виде вязкого масла (350 мг, выход 57%). ES-MS [М+1]+: 163,4;1Н ЯМР (400 МГц, DMSO-d6) δ 7,32-7,28 (m, 4Н), 3,70 (s, 2Н), 2,95 (s, 3Н), 1,43 (s, 6Н).
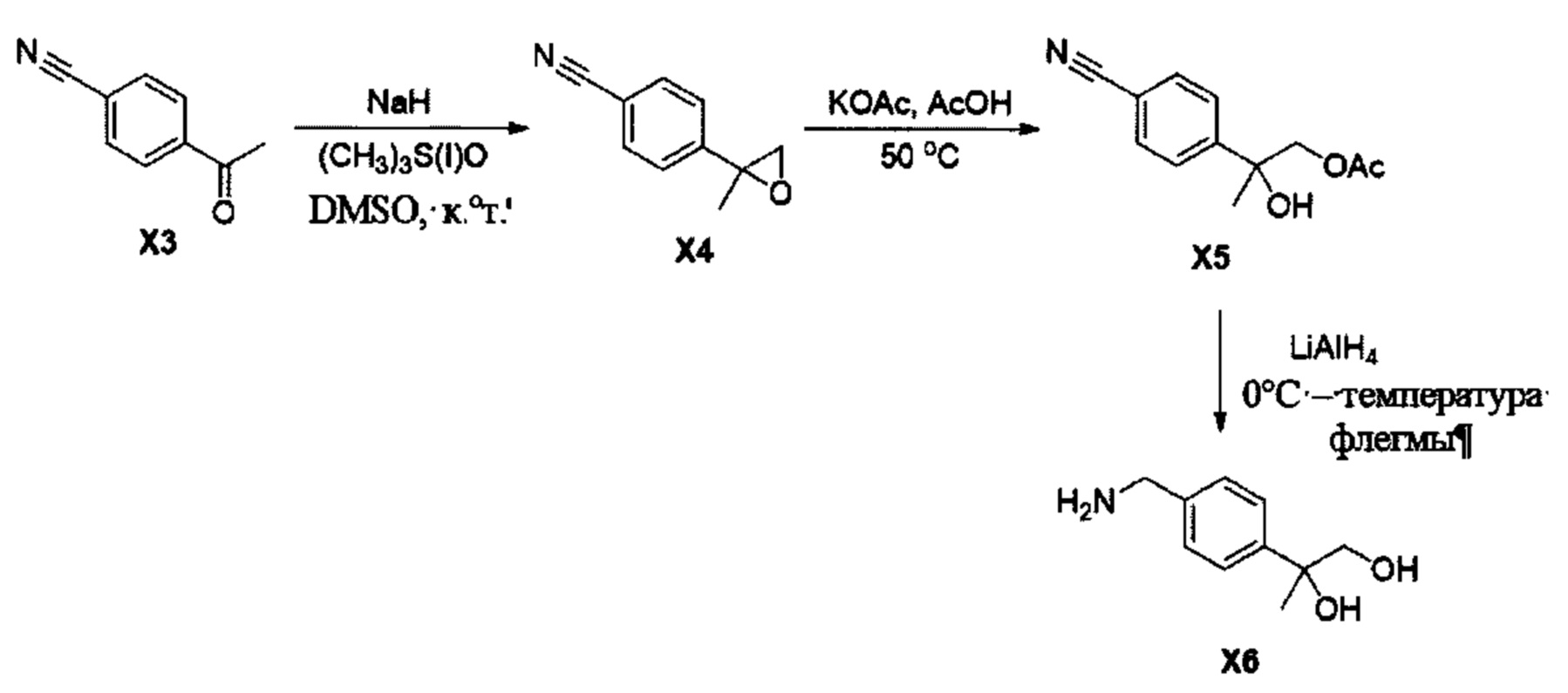
4-(2-Метилоксиран-2-ил)бензонитрил (Х4). К суспензии йодида триметилсульфоксония (1,82 г, 8,27 ммоль, 1,2 экв.) в DMSO (9,2 мл) при к.т. небольшими порциями добавляли гидрид натрия (60% в минеральном масле, 330 мг, 8,27 ммоль, 1,2 экв.). После 1 ч. добавляли раствор 4-ацетилбензонитрила, Х3 (1,0 г, 6,89 ммоль, 1,0 экв.) в DMSO (2,21 мл). После 16 ч. при к.т. реакционную смесь выливали в ледяную воду (100 мл) и экстрагировали с помощью EtOAc (3×100 мл). Объединенные органические слои промывали солевым раствором, высушивали (Na2SO4), фильтровали и концентрировали. Остаток очищали с помощью колоночной флэш-хроматографии на силикагеле (0-30% EtOAc/гексаны) с получением указанного в заголовке соединения в виде вязкого масла (900 мг, выход 74%). ES-MS [М+1]+: 160,2;1Н ЯМР (400 МГц, DMSO-d6) δ 7,83 (ddd, J=8,6, 1,8, 1,8 Гц, 2Н), 7,55 (ddd, J=8,6, 1,8, 1,8 Гц, 2Н), 7,55 (ddd, J=5,2 Гц, 1Н), 2,80 (dd, J=5,7. 0,5 Гц, 1Н), 1,68 (s, 3Н).
[2-(4-Цианофенил)-2-гидроксипропил]ацетат (Х5). К раствору Х4 (159 мг, 1,0 ммоль, 1,0 экв.) в уксусной кислоте (4,0 мл) добавляли ацетат калия (588 мг, 6,0 ммоль, 3,0 экв.). После 30 мин. при 80°С реакционную смесь концентрировали до сухого состояния при пониженном давлении. Остаток повторно растворяли в смеси DCM и насыщенного раствора NaHCO3 (1:1, об./об.). Органический слой отделяли и концентрировали. Неочищенный материал очищали с помощью колоночной флэш-хроматографии на силикагеле с применением 0-60% EtOAc/гексаны с получением указанного в заголовке соединения в виде вязкого масла (160 мг, выход 73%). ES-MS [М+1]+: 202,4;1Н ЯМР (400 МГц, DMSO-d6) δ 7,79 (ddd, J=8,6, 1,8, 1,8 Гц, 2Н), 7,69 (ddd, J=8,6, 1,9, 1,9 Гц, 2Н), 5,61 (s, 1Н), 4,11 (dd, J=11,2, 11,2 Гц, 2Н), 1,94 (s, 3Н), 1,46 (s, 3Н).
2-[4-(Аминометил)фенил]пропан-1,2-диол (Х6). К раствору Х5 (183 мг, 0,835 ммоль, 1,0 экв.) в THF (4,2 мл) по каплям добавляли раствор алюмогидрида лития (1,0 М в THF, 2,50 мл, 2,50 ммоль, 3,0 экв.) при 0°С. После 30 мин при 0°С ледяную баню убирали и реакционную смесь нагревали до температуры флегмы. После 15 мин. образовывалась кремообразная паста. Нагревание прекращали. При 0°С медленно добавляли насыщенный раствор сегнетовой соли (2,0 мл), а затем МеОН (3,0 мл). Смесь перемешивали при к.т. в течение 1 ч. и фильтровали через подушку из целита, которую дополнительно промывали с помощью 10% МеОН в DCM. Собранный фильтрат пропускали через фазовый сепаратор и концентрировали с получением указанного в заголовке соединения в виде вязкого масла, которое использовали на следующей стадии в неочищенном виде. ES-MS [М+1]+: 182,2.

3-(Гидроксиметил)-4-(1-гидрокси-1-метилэтил)бензонитрил (Х8). К раствору 1-оксо-3Н-изобензофуран-5-карбонитрила, Х7 (1,0 г, 6,28 ммоль, 1,0 экв.) в THF (31,5 мл) при -30°С добавляли раствор метилмагнийбромида (3 М в THF, 12,57 мл, 37,7 ммоль, 6,0 экв.). После 1 ч. при -30°С добавляли насыщенный раствор NH4Cl. Смесь экстрагировали с помощью EtOAc (3×100 мл). Объединенные органические слои промывали солевым раствором, высушивали (Na2SO4), фильтровали и концентрировали. Остаток очищали с помощью колоночной флэш-хроматографии на силикагеле (0-50% EtOAc/гексаны) с получением указанного в заголовке соединения в виде вязкого масла (1,05 г, выход 87%). ES-MS [М+1]+: 174,2;1Н ЯМР (400 МГц, DMSO-d6) δ 7,94 (d, J=1,7 Гц, 1H), 7,64 (dd, J=8,2, 1,9 Гц, 1Н), 7,53 (d, J=8,2 Гц, 1Н), 5,30-5,28 (m, 2Н), 4,86 (d, J=5,6 Гц, 2Н), 1,50 (s, 6Н).
1,1-Диметил-3Н-изобензофуран-5-карбонитрил (Х9). К раствору Х8 (1,05 г, 5,49 ммоль, 1,0 экв.) в толуоле (11,0 мл) при 0°С добавляли смесь ортофосфорной кислоты (5,0 мл) и воды (1,0 мл). После перемешивания в течение 16 ч. при к.т. слой толуола отделяли. Водный слой экстрагировали с помощью толуола (2×10 мл). Объединенные органические слои промывали с помощью насыщенного раствора NaHCO3 и воды, высушивали (Na2SO4), фильтровали и концентрировали. Неочищенный материал очищали с помощью колоночной флэш-хроматографии на силикагеле (0-60% EtOAc/гексаны) с получением указанного в заголовке соединения в виде бесцветного масла (730 мг, выход 76%). ES-MS [М+1]+: 174,2;1Н ЯМР (400 МГц, DMSO-d6) δ 7,77-7,76 (m, 2Н), 7,50 (d, J=8,2 Гц, 1Н), 4,99 (s, 2Н), 1,44 (s, 6Н).
(1,1-Диметил-3Н-изобензофуран-5-ил)метанамин (Х10). К раствору Х9 (730 мг, 4,21 ммоль, 1,0 экв.) в THF (28 мл) по каплям добавляли раствор алюмогидрида лития (1,0 М в THF, 12,64 мл, 12,64 ммоль, 3,0 экв.) при 5°С. После 30 мин. при 5°С ледяную баню убирали и реакционную смесь нагревали до температуры флегмы. После 30 мин. образовывалась кремообразная паста. Нагревание прекращали. При 0°С медленно добавляли насыщенный раствор сегнетовой соли (5,0 мл), а затем МеОН (5,0 мл). Смесь перемешивали при к.т. в течение 1 ч. и фильтровали через подушку из целита, которую дополнительно промывали с помощью 10% МеОН в DCM. Собранный фильтрат высушивали (Na2SO4), фильтровали и концентрировали. Остаток очищали с помощью колоночной флэш-хроматографии на силикагеле с применением раствора DCM/MeOH/NH4OH (89:10:1) с DCM в качестве сорастворителя с получением указанного в заголовке соединения в виде твердого вещества (450 мг, выход 60%). ES-MS [М+1]+: 178,4;1Н ЯМР (400 МГц, DMSO-d6) δ 7,23-7,20 (m, 2Н), 7,15 (d, J=7,5 Гц, 1Н), 4,93 (s, 2Н), 3,70 (s, 2Н), 1,39 (s, 6Н).

4-(Оксетан-3-ил)бензонитрил (Х12). Смесь 4-цианофенилбороновой кислоты, X11 (294 мг, 2,0 ммоль, 2,0 экв.), йодида никеля (II) (31,5 мг, 0,10 ммоль, 0,10 экв.), гексаметилдисилазана натрия (366,7 мг, 2,0 ммоль, 2,0 экв.) и гидрохлорида транс-2-аминоциклогексанола (15,2 мг, 0,10 ммоль, 0,10 экв.) в изопропаноле (4,0 мл) перемешивали в атмосфере азота. После 10 мин. добавляли раствор 3-йодоксетана (184 мг, 1,0 ммоль, 1,0 экв.) в изопропаноле (0,25 мл). Полученную смесь подвергали воздействию микроволнового реактора при 80°С. После 30 мин. смесь разбавляли EtOH и фильтровали через подушку из целита, которую тщательно промывали EtOH. Фильтрат концентрировали при пониженном давлении. Неочищенный материал очищали с помощью колоночной флэш-хроматографии на силикагеле (0-60% EtOAc/гексаны) с получением указанного в заголовке соединения в виде кристаллического твердого вещества (120 мг, выход 79%). ES-MS [М+1]+: 160,2;1Н ЯМР (400 МГц, DMSO-d6) 7,77 (ddd, J=8,4, 1,8, 1,8 Гц, 2Н), 7,50 (ddd, J=8,2 Гц, 1,8, 1,8 Гц, 2Н), 4,88 (dd, J=8,3, 6,0 Гц, 2Н), 4,53 (dd, J=6,4, 6,4 Гц, 1Н), 4,27 (m, 1Н).
[4-(Оксетан-3-ил)фенил]метанамин (Х13). К раствору Х12 (125 мг, 0,785 ммоль, 1,0 экв.) в THF (5,2 мл) по каплям добавляли раствор алюмогидрида лития (1,0 М в THF, 2,35 мл, 2,35 ммоль, 3,0 экв.) при 0°С. После 30 мин. при 0°С ледяную баню убирали и реакционную смесь нагревали до температуры флегмы. После 15 мин. образовывалась кремообразная паста. Нагревание прекращали. При 0°С медленно добавляли насыщенный раствор сегнетовой соли (5,0 мл), а затем МеОН (5,0 мл). Смесь перемешивали при к.т. в течение 1 ч. и фильтровали через подушку из целита, которую дополнительно промывали с помощью 10% МеОН в DCM. Собранный фильтрат концентрировали. Остаток очищали с помощью колоночной флэш-хроматографии на силикагеле с применением раствора DCM/MeOH/NH4OH (89:10:1) с DCM в качестве сорастворителя с получением указанного в заголовке соединения в виде вязкого масла (95 мг, выход 74%, чистота 67% согласно 1Н ЯМР). ES-MS [М+1]+: 164,2;1Н ЯМР (400 МГц, DMSO-d6) δ 7,34-7,30 (m, 4Н), 4,93 (dd, J=8,4, 5,8 Гц, 2Н), 4,60 (dd, J=6,8, 5,8 Гц, 2Н), 4,21 (m, 1Н).

Этил-2-(4-цианофенил)-2-метилпропаноат (Х15). Раствор этил-2-(4-цианофенил)ацетата (1,32 г, 7,0 ммоль, 1,0 экв.) в THF (22,5 мл) добавляли по каплям к суспензии гидрида натрия (60% в минеральном масле, 588 мг, 14,7 ммоль, 2,1 экв.) в THF (60 мл) при 0°С. После 30 мин. при 0°С обеспечивали нагревание реакционной смеси до к.т. После 15 мин. ее охлаждали до 0°С и добавляли йодметан (0,92 мл, 14,7 ммоль, 2,1 экв.). После перемешивания в течение 1 ч. реакционную смесь подкисляли с помощью раствора 1 М HCl и экстрагировали с помощью EtOAc (3×100 мл). Объединенные органические слои промывали солевым раствором, высушивали (Na2SO4), фильтровали и концентрировали. Остаток очищали с помощью колоночной флэш-хроматографии на силикагеле (0-60% EtOAc/гексаны) с получением указанного в заголовке соединения в виде вязкого масла (750 мг, выход 49%). ES-MS [М+1]+: 218,2;1Н ЯМР (400 МГц, DMSO-d6) δ 7,82 (ddd, J=8,2, 1,7, 1,7 Гц, 2Н), 7,52 (ddd, J=8,2, 1,7, 1,7 Гц, 2Н), 7,52 (ddd)
[4-(1-Метокси-1-метилэтил)фенил]метанамин (Х16). К раствору Х15 (750 мг, 3,45 ммоль, 1,0 экв.) в THF (23 мл) по каплям добавляли раствор алюмогидрида лития (1,0 М в THF, 10,36 мл, 10,36 ммоль, 3,0 экв.) при 0°С. После 30 мин. при 0°С ледяную баню убирали и реакционную смесь нагревали до температуры флегмы. После 30 мин. образовывалась кремообразная паста. Нагревание прекращали. При 0°С медленно добавляли насыщенный раствор сегнетовой соли (7,0 мл), а затем МеОН (7,0 мл). Смесь перемешивали при к.т. в течение 1 ч. и фильтровали через подушку из целита, которую дополнительно промывали с помощью 10% МеОН в DCM. Собранный фильтрат концентрировали. Остаток очищали с помощью колоночной флэш-хроматографии на силикагеле с применением раствора DCM/MeOH/NH4OH (89:10:1) с DCM в качестве сорастворителя с получением указанного в заголовке соединения в виде вязкого масла (400 мг, выход 65%). ES-MS [М+1]+: 163,4 (фрагментация посредством элиминации);1Н ЯМР (400 МГц, DMSO-d6) δ 7,28 (dd, J=8,4, 1,9 Гц, 2Н), 7,22 (dd, J=8,4, 1,8 Гц, 2Н), 4,62 (s, 1Н), 3,66 (s, 2Н), 3,39 (s, 2Н), 1,21 (s, 6Н).

4-(2-Гидроксипропан-2-ил)бензонитрил (Х18). К раствору 4-йодбензонитрила Х17 (10,0 г, 43,7 ммоль, 1,0 экв.) в THF (218 мл) при -78°С по каплям добавляли н-бутиллитий (2,5 М в гексанах, 22,7 мл, 56,8 ммоль, 1,3 экв.) с поддержанием температуры ниже -70°С. После 1 ч. добавляли ацетон (32,0 мл, 436,6 ммоль, 10,0 экв.) поддерживая температуру ниже -70°С. Баню с сухим льдом удаляли. После 16 часов при к.т. добавляли насыщенный раствор NH4Cl (100 мл), а затем EtOAc (250 мл). Слои разделяли. Водный слой экстрагировали с помощью EtOAc (2×200 мл). Объединенные органические слои промывали солевым раствором, высушивали (Na2SO4), фильтровали и концентрировали. Остаток очищали с помощью колоночной флэш-хроматографии на силикагеле (0-60% EtOAc/гексаны) с получением указанного в заголовке соединения в виде вязкого масла (4,88 г, выход 69%). ES-MS [М+1]+: 162,4;1Н ЯМР (400 МГц, DMSO-d6) δ 7,76 (dd, J=10, 2 Гц, 2Н), 7,66 (dd, J=8,6, 2 Гц, 2Н), 5,28 (s, 1Н), 1,43 (s, 6Н).
2-(4-(Аминометил)фенил)пропан-2-ол (Х19). К раствору 4-(2-гидроксипропан-2-ил)бензонитрила (4,88 г, 30,3 ммоль, 1,0 экв.) в THF (200 мл) по каплям добавляли раствор алюмогидрида лития (2,0 М в THF, 45,4 мл, 90,8 ммоль) при 0°С. После 30 мин. при 0°С ледяную баню убирали и реакционную смесь нагревали до температуры флегмы. После 30 мин. образовывалась кремообразная паста. Нагревание прекращали. При 0°С медленно добавляли насыщенный раствор сегнетовой соли (50 мл), а затем МеОН (50 мл). Смесь перемешивали при к.т. в течение 1 ч. и фильтровали через подушку из целита, которую дополнительно промывали с помощью 15% МеОН в DCM. Собранный фильтрат высушивали (MgSO4), фильтровали и концентрировали. Остаток очищали с помощью колоночной флэш-хроматографии на силикагеле с применением раствора DCM/MeOH/NH4OH (89:10:1) с DCM в качестве сорастворителя с получением указанного в заголовке соединения в виде белого кристаллического твердого вещества (4,25 г, выход 85%). ES-MS [М+1]+: 166,3;1Н ЯМР (400 МГц, DMSO-d6) δ 7,38 (d, J=8,3 Гц, 2Н), 7,24 (d, J=8,4 Гц, 2Н), 4,93 (bs, 1Н), 3,68 (s, 2 Н), 1,41 (s, 6Н);13С ЯМР (100 МГц, DMSO-d6) δ 148,9, 142,1, 126,9, 124,7, 71, 45,9, 32,5.
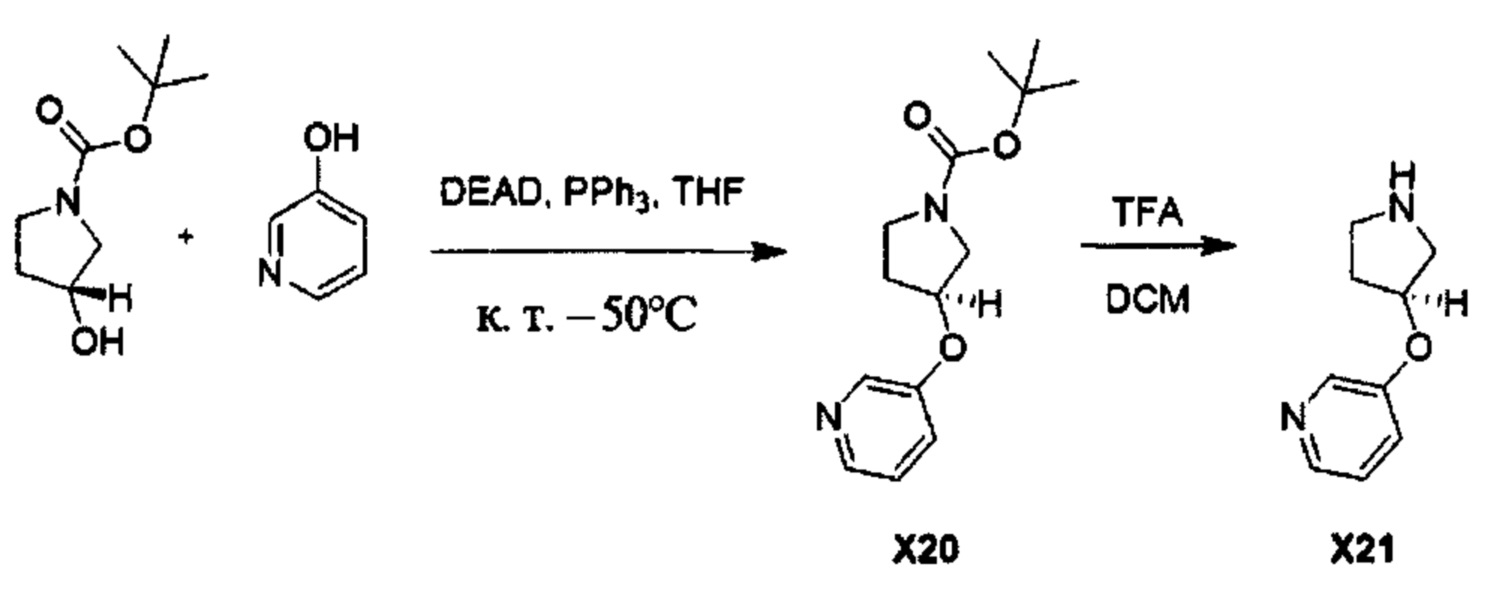
Трет-бутил-(S)-3-(пиридин-3-илокси)пирролидин-1-карбоксилат (Х20). К раствору DEAD (139,5 мг, 0,80 ммоль, 1,5 экв.) и PPh3 (210,1 мг, 0,80 ммоль, 1,5 экв.) в THF (4 мл) при комнатной температуре добавляли (R)-(-)-Boc-3-пирролидинол (100 мг, 0,53 ммоль, 1,0 экв.). После 10 мин. добавляли по каплям 3-пиридинол (0,063 мл, 0,80 ммоль, 1,5 экв.) и реакционную смесь нагревали до 50°С. За ходом реакции следили посредством LCMS и после 12 ч. реакционную смесь фильтровали через шприцевой фильтр. Растворитель удаляли под вакуумом. Неочищенный остаток растворяли в DMSO (4 мл) и очищали с помощью Gilson HPLC (50×250 мм, 30-70% MeCN/H2O вес/0,1% TFA). Необходимые фракции концентрировали с получением трет-бутил-(S)-3-(пиридин-3-илокси)пирролидин-1-карбоксилата. ES-MS [М+1]+: 265,4.
(S)-3-(Пирролидин-3-илокси)пиридин (Х21). К раствору трет-бутил-(S)-3-(пиридин-3-илокси)пирролидин-1-карбоксилата в DCM (10 мл) добавляли TFA (2,0 мл) по каплям при 0°С. Ледяную баню убирали и после 30 мин. при к.т. LCMS подтверждала отсутствие исходного материала. Реакционную смесь концентрировали с получением (S)-3-(пирролидин-3-илокси)пиридина (173,1 мг, выход 83% за 2 стадии). ES-MS [М+1]+: 165,2.

Трет-бутил-4-((2-хлорпиридин-4-ил)окси)пиперидин-1-карбоксилат (Х22). К раствору DEAD (97,4 мг, 0,56 ммоль, 1,5 экв.) и PPh3 (146,6 мг, 0,56 ммоль, 1,5 экв.) в THF (4 мл) при комнатной температуре добавляли 1-Boc-4-гидроксипиперидин (75 мг, 0,37 ммоль, 1,0 экв.). После 10 мин. добавляли 2-хлор-4-гидроксипиридин (72,4 мг, 0,56 ммоль, 1,5 экв.) и реакционную смесь нагревали до 50°С. За ходом реакции следили посредством LCMS и после 12 ч. реакционную смесь фильтровали через шприцевой фильтр. Растворитель удаляли под вакуумом. Неочищенный остаток растворяли в DMSO (3 мл) и очищали с помощью Gilson HPLC (30×100 мм, 40-100% MeCN/H2O вес/0,1% TFA). Необходимые фракции концентрировали с получением трет-бутил-4-((2-хлорпиридин-4-ил)окси)пиперидин-1-карбоксилата. ES-MS [М+1]+: 313,2.
2-Хлор-4-(пиперидин-4-илокси)пиридин (Х23). К раствору трет-бутил-4-((2-хлорпиридин-4-ил)окси)пиперидин-1-карбоксилата в DCM (10 мл) добавляли по каплям TFA (2,0 мл) при 0°С. Ледяную баню убирали и после 30 мин. при к.т. LCMS подтверждала отсутствие исходного материала. Реакционную смесь концентрировали с получением 2-хлор-4-(пиперидин-4-илокси)пиридина (80,5 мг, выход 49%). ES-MS [М+1]+: 213,4.

Трет-бутил-3-(((2-хлорпиридин-4-ил)окси)метил)азетидин-1-карбоксилат (Х24). К раствору DEAD (104,6 мг, 0,60 ммоль, 1,5 экв.) и PPh3 (157,6 мг, 0,60 ммоль, 1,5 экв.) в THF (4 мл) при комнатной температуре добавляли трет-бутил-3-(гидроксиметил)азетидин-1-карбоксилат (75 мг, 0,40 ммоль, 1,0 экв.). После 10 мин. добавляли 2-хлор-4-гидроксипиридин (77,8 мг, 0,60 ммоль, 1,5 экв.) и реакционную смесь нагревали до 50°С. За ходом реакции следили посредством LCMS и после 12 ч. реакционную смесь фильтровали через шприцевой фильтр. Растворитель удаляли под вакуумом. Неочищенный остаток растворяли в DMSO (3 мл) и очищали с помощью Gilson HPLC (30×100 мм, 40-90% MeCN/Н2О вес/0,1% TFA). Необходимые фракции концентрировали с получением трет-бутил-3-(((2-хлорпиридин-4-ил)окси)метил)азетидин-1-карбоксилата. ES-MS [М+1]+: 299,2.
2-Хлор-4-(пиперидин-4-илокси)пиридин (Х25). К раствору трет-бутил-(S)-3-(пиридин-3-илокси)пирролидин-1-карбоксилата в DCM (5 мл) добавляли по каплям TFA (1,0 мл) при 0°С. Ледяную баню убирали и после 30 мин. при к.т. LCMS подтверждала отсутствие исходного материала. Реакционную смесь концентрировали с получением 2-хлор-4-(пиперидин-4-илокси)пиридина (69 мг, выход 40%). ES-MS [М+1]+: 199,2.

Трет-бутил-3-(пиразин-2-илокси)азетидин-1-карбоксилат (Х26). К раствору 1-Вос-3-йодазетидина (75 мг, 0,26 ммоль, 1,5 экв.) и Cs2CO3 (434,2 мг, 1,32 ммоль, 5,0 экв.) в NMP (3 мл) добавляли 2-гидроксипиразин (38 мг, 0,40 ммоль, 1,5 экв.). Реакционную смесь нагревали до 50°С и после 12 ч. реакционную смесь фильтровали через шприцевой фильтр. Раствор очищали с помощью Gilson HPLC (30×100 мм, 15-60% MeCN/Н2О вес/0,1% TFA). Необходимые фракции концентрировали с получением трет-бутил-3-(пиразин-2-илокси)азетидин-1-карбоксилата. ES-MS [М+1]+: 252,2.
2-(Азетидин-3-илокси)пиразин (Х27). К раствору трет-бутил-3-(пиразин-2-илокси)азетидин-1-карбоксилата в DCM (5 мл) добавляли по каплям TFA (1,0 мл) при 0°С. Ледяную баню убирали и после 30 мин. при к.т. LCMS подтверждала отсутствие исходного материала. Реакционную смесь концентрировали с получением 2-(азетидин-3-илокси)пиразина (88 мг, выход 88%). ES-MS [М+1]+: 152,2.
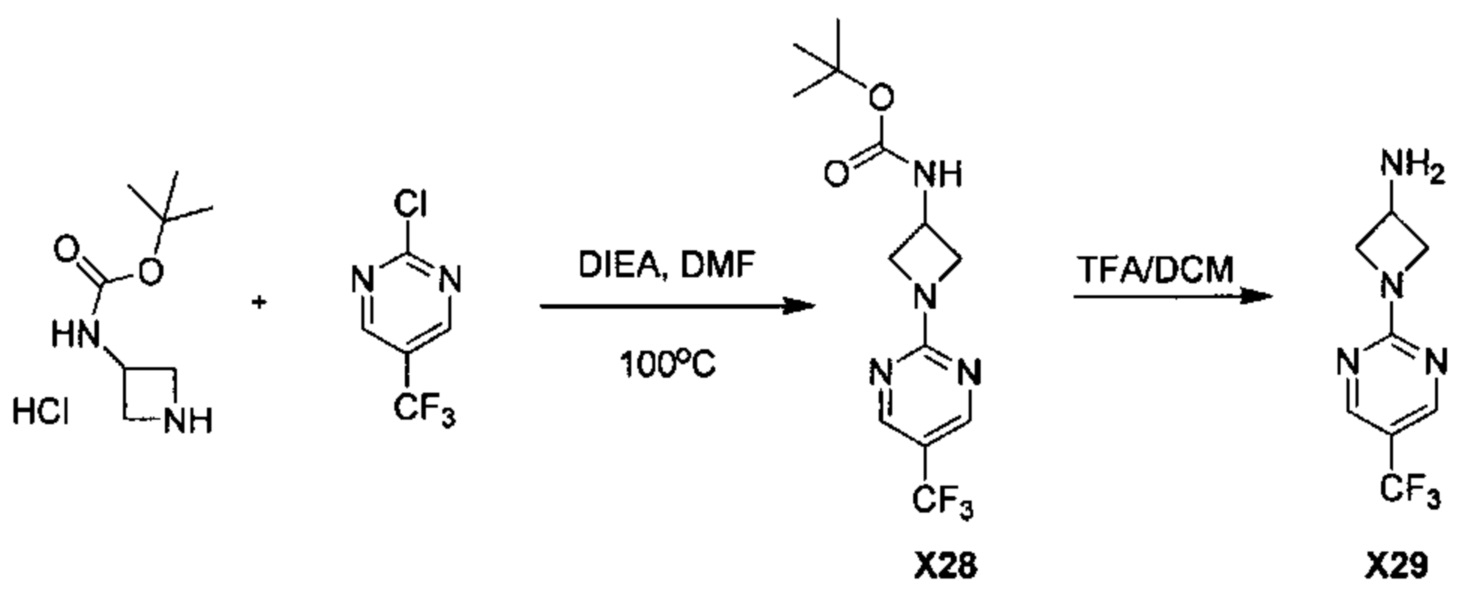
Трет-бутил-(1-(5-(трифторметил)пиримидин-2-ил)азетидин-3-ил)карбамат (Х28). Во флакон для микроволнового реактора добавляли гидрохлорид 3-Вос-аминоазетидина (1 экв.), 2-хлор-5-(трифторметил)пиримидин (1,1 экв.), DIEA (3 экв.) и DMF (0,5 М). Реакционную смесь нагревали до 100°С в течение ночи. LCMS подтверждала полное превращение. К реакционной смеси добавляли EtOAc : Н2О (1:1). Органический слой отделяли и промывали с помощью воды (2х). Водные слои повторно экстрагировали с помощью EtOAc (3х). Собранные органические слои высушивали (MgSO4), фильтровали и концентрировали in vacuo. Неочищенный материал очищали с использованием системы Biotage (загрузка твердой фазой, колонка 120G, 0-40% EtOAc/гексаны, время прогона 25 мин.). Необходимые фракции концентрировали. ES-MS [М+1]+: 319,2.
1-(5-(Трифторметил)пиримидин-2-ил)азетидин-3-амин (Х29). ВОС-защищенный амин растворяли в DCM (0,2 М) и трифторуксусной кислоте (10 экв.) и перемешивали в течение 2 часов. LCMS показала завершение реакции. Растворитель удаляли и неочищенный образец загружали в МеОН на картриджи, смоченные МеОН (SCX, 10G). Картриджи промывали с помощью МеОН (3х) для элюирования примесей, затем с помощью 2 н. NH3/МеОН (2х) для элюирования амина. Растворитель удаляли с получением требуемого продукта в виде свободного основания амина (выход 65-76%). ES-MS [М+1]+: 219,2.
Пример 2. N,N,3,4-Тетраметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин (соединение 1)

Этил-5-амино-3,4-диметилтиено[2,3-с]пиридазин-6-карбоксилат (А). Во флакон для микроволнового реактора объемом 20 мл добавляли 3-хлор-5,6-диметилпиридазин-4-карбонитрил (1,20 г, 7,16 ммоль), карбонат калия (1,98 г, 14,3 ммоль), IPA (15 мл) и этилтиогликолят (0,87 мл, 7,88 ммоль). После 20 мин. при 105°С в микроволновом реакторе реакционную смесь охлаждали до комнатной температуры и добавляли к воде (150 мл). Твердые вещества фильтровали и промывали с помощью воды 3 раза с получением А в виде зеленого порошка (1,42 г, выход 79%). ES-MS [М+1]+: 252,2;1Н ЯМР (400 МГц, CDCl3) δ 6,18 (s, 2Н), 4,41 (q, J=7 Гц, 2Н), 2,85 (s, 3Н), 2,77 (s, 3Н), 1,44 (t, J=7,12 Гц, 3Н).
3,4-Диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ол (В). Раствор А (1,41 г, 5,61 ммоль) в формамиде (10 мл, 252 ммоль) нагревали в открытом сосуде до 150°С. К реакционной смеси добавляли ацетат формамидина (1,75 г, 16,8 ммоль). При 150°С каждые 30 мин. в течение 2,5 ч. к реакционной смеси добавляли ацетат формамидина (1,75 г, 16,8 ммоль). Реакционную смесь убирали из колбонагревателя и медленно разбавляли холодной водой. Раствор частично концентрировали in vacuo. Остаток разбавляли водой и твердые вещества фильтровали, и промывали с помощью воды 3 раза, и высушивали в течение ночи в вакуумной печи. Фильтрат частично концентрировали in vacuo и разбавляли водой. Твердые вещества фильтровали и промывали с помощью воды 3 раза. Твердые вещества объединяли с получением В (877 мг, выход 67,2%). ES-MS [М+1]+: 233,2;1Н ЯМР (400 МГц, d6-DMSO) δ 8,48 (s, 1Н), 2,98 (s, 3Н), 2,80 (s, 3Н).
8-Хлор-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин (С). Гетерогенный раствор В (876 мг, 3,77 ммоль) в оксихлориде фосфора (18 мл, 193 ммоль) разделяли на три флакона для микроволнового реактора объемом 20 мл. Каждый реакционный сосуд нагревали до 150°С в микроволновом реакторе в течение 45 мин. Реакционные смеси разбавляли в DCM, и переносили в круглодонную колбу, и концентрировали in vacuo с получением указанного в заголовке соединения в виде липкого коричневого/черного остатка. Остаток суспендировали в NMP (20 мл) и использовали для дальнейших реакций в виде неочищенного раствора С (~40 мг/мл). Отбирали небольшую аликвоту и очищали с помощью обращенно-фазовой HPLC в градиенте MeCN : вода (0,5 мл NH4OH/1 л воды) с получением очищенного образца для тестирования in vitro и получения спектральных данных. ES-MS [М+1]+: 251,3;1Н ЯМР (400 МГц, CDCl3) δ 9,19 (s, 1Н), 3,10 (s, 3Н), 2,93 (s, 3Н).
N,N,3,4-тетраметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-амин (соединение 1). К раствору С (40 мг, 0,16 ммоль) в NMP (1 мл) добавляли N,N-диизопропилэтиламин (7087-68-5) (0,1 мл, 0,57 ммоль) и диметиламин (0,10 мл, 0,20 ммоль). После 15 мин. при 180°С в микроволновом реакторе фракции разделяли с помощью обращенно-фазовой HPLC в градиенте MeCN : вода (0,5 мл NH4OH/1 л воды). Фракции концентрировали с получением соединения 1 (3,4 мг, выход 8,2%). ES-MS [М+1]+: 260,2;1Н ЯМР (400 МГц, CDCl3) δ 8,73 (s, 1Н), 3,52 (s, 6H), 3,11 (s, 3Н), 2,90 (s, 3Н).
Пример 3. 2-[4-[[(3,4-Диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол (соединение 76)
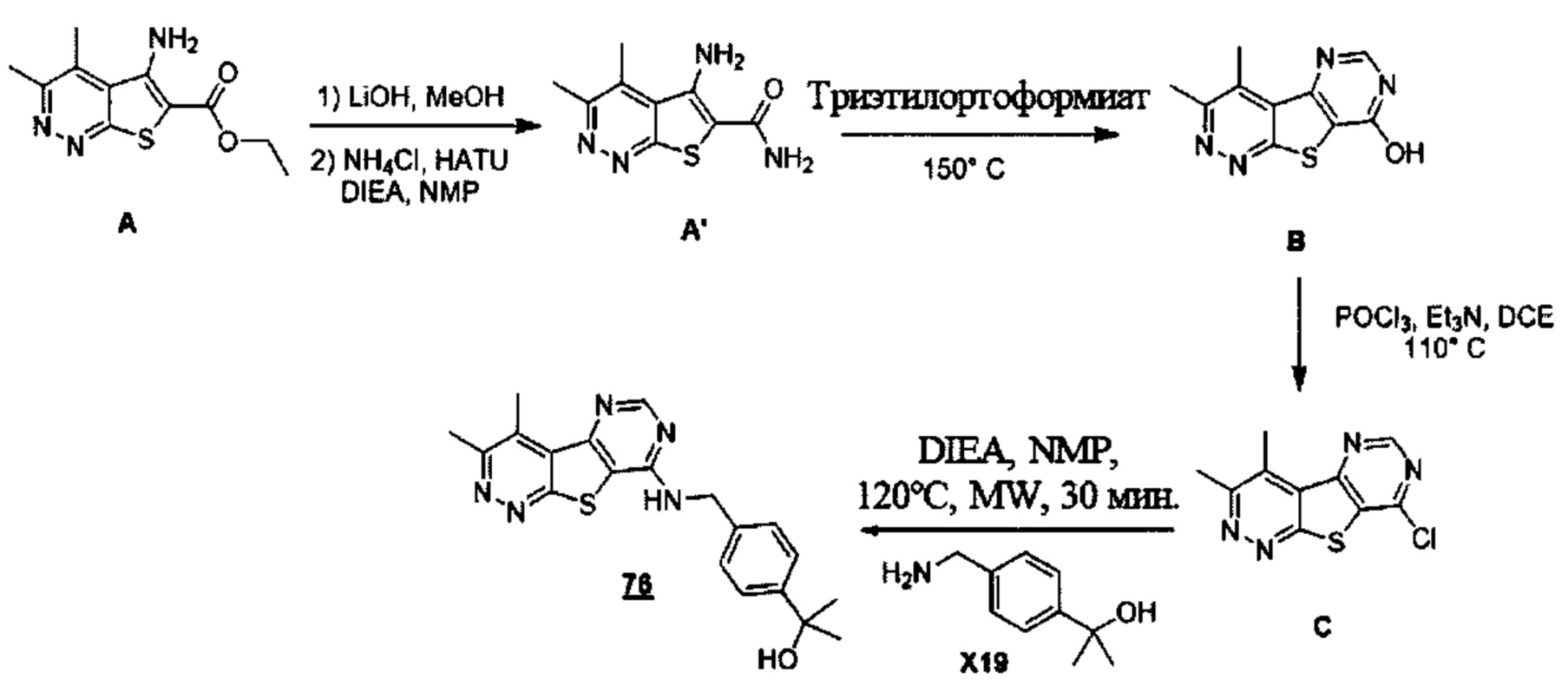
5-Амино-3,4-диметилтиено[2,3-с]пиридазин-6-карбоксамид (А'). К суспензии этил-5-амино-3,4-диметилтиено[2,3-с]пиридазин-6-карбоксилата (А, полученного, как описано в примере 2) (5,0 г, 19,9 ммоль, 1,0 экв.) в THF (33,0 мл) и МеОН (10,0 мл) добавляли водный раствор LiOH (1 М, 99,5 мл, 5,0 экв.). После 16 часов при комнатной температуре LCMS подтверждала убыль исходного материала. Реакционную смесь охлаждали до 0°С и твердое вещество желтого цвета фильтровали. Твердое вещество высушивали под вакуумом с получением карбоксилата лития (4,6 г) в виде желтого порошка. ES-MS [М+1]+: 224,4;1Н ЯМР (400 МГц, DMSO-d6) δ 6,37 (s, 2Н), 2,65 (s, 6). Фильтрат подкисляли с помощью 4 М HCl в диоксане с получением соответствующей карбоновой кислоты (950 мг). ES-MS [М+1]+: 224,3;1Н ЯМР (400 МГц, DMSO-d6) δ 7,01 (bs, 2Н), 2,73 (s, 3Н), 2,71 (s, 3Н).
К раствору карбоксилата лития (4,6 г, 20,0 ммоль, 1,0 экв.), HATU (9,16 г, 24,1 ммоль, 1,1 экв.) и DIEA (10,5 мл, 60,2 ммоль, 3,0 экв.) в NMP (73 мл, 2,75 М) добавляли хлорид аммония (1,61 г, 30,0 ммоль, 1,5 экв.). После 16 часов при комнатной температуре смесь медленно добавляли в ледяную воду (300 мл), и образовывался желтый осадок. Осадок собирали посредством фильтрации и промывали с помощью воды (2×50 мл). После высушивания под вакуумом получали оранжево-желтый порошок (3,5 г, выход 78% за 2 стадии). ES-MS [М+1]+: 223,0;1Н ЯМР (400 МГц, DMSO-d6) δ 7,49 (bs, 2Н), 6,95 (s, 2Н), 2,72 (s, 3Н), 2,70 (s, 3Н).
3,4-Диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ол (В). Суспензию соединения А' (3,5 г, 15,7 ммоль) в триэтилортоформиате (100 мл, 600 ммоль) нагревали до температуры флегмы в круглодонной колбе объемом 500 мл. После 6 часов LCMS показывала неполное превращение, и реакционную смесь концентрировали. К остатку добавляли дополнительное количество триэтилортоформиата (100 мл, 600 ммоль), и реакционную смесь нагревали с обратным холодильником. После 16 часов LCMS показала полное превращение. Реакционную смесь концентрировали до сухого состояния при пониженном давлении и подвергали азеотропной перегонке с толуолом (2×100 мл). Материал использовали в дальнейшем без дополнительной очистки (3,5 г). ES-MS [М+1]+: 233,2;1Н ЯМР (400 МГц, DMSO-d6) δ 8,43 (s, 1Н), 2,92 (s, 3Н), 2,77 (s, 3Н).
8-Хлор-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин (С). К суспензии соединения В (3,0 г, 11,6 ммоль, 1,0 экв.) в 1,2-дихлорэтане (58 мл) добавляли триэтиламин (2,4 мл, 17,4 ммоль, 1,5 экв.) с последующим медленным добавлением оксихлорида фосфора (35 мл, 375,5 ммоль, 32,3 экв.). Реакционную смесь нагревали до температуры флегмы. После 16 часов реакционную смесь охлаждали до к.т. и концентрировали под вакуумом. Остаток суспендировали в DCM (150 мл) и добавляли триэтиламин (5 мл). Полученный раствор фильтровали для удаления нерастворимых фосфатных солей. Фильтрат концентрировали при пониженном давлении с получением темно-коричневого остатка, который очищали с применением флэш-хроматографии на силикагеле (0-50% EtOAc/DCM) с получением указанного в заголовке соединения в виде рыхлого порошка (1,63 г, выход 56%). ES-MS [М+1]+: 251,0;1Н ЯМР (400 МГц, DMSO-d6) δ 9,33 (s, 1Н), 3,02 (s, 3Н), 2,83 (s, 3Н);13C ЯМР (100 МГц, CDCl3) δ 162,4, 157,5, 157,1, 155,8, 154,6, 136,2, 132,9, 127,2, 19,9, 14,5.
2-[4-[[(3,4-Диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол (соединение 76). Раствор соединения С (1,98 г, 7,88 ммоль, 1,0 экв.), 2-(4-(аминометил)фенил)пропан-2-ола (Х19) (2,12 г, 10,24 ммоль, 1,3 экв.) и DIEA (5,49 мл, 31,5 ммоль, 4,0 экв.) в NMP (39,4 мл, 2 М) подвергали воздействию микроволнового реактора Biotage в течение 30 мин. при 120°С. После охлаждения при к.т. смесь разбавляли DMSO и фильтровали через шприцевой фильтр для удаления любых нерастворимых солей. Неочищенный материал очищали с применением обращенно-фазовой HPLC с получением указанного в заголовке соединения (1,78 г, выход 60%) в виде грязно-белого порошка. ES-MS [М+1]+: 380,0;1Н ЯМР (400 МГц, DMSO-d6) δ 8,68 (t, 1Н), 8,63 (s, 1H), 7,42 (d, J=8,2 Гц, 2H), 7,32 (d, J=8,3 Гц, 2H), 4,96 (s, 1H), 4,74 (d, J=5,8 Гц, 2H), 2,92 (s, 3H), 2,73 (s, 3H), 1,40 (s, 6H);13C ЯМР (100 МГц, DMSO-d6) δ 162,3, 157,5, 156,9, 155,6, 153,4, 149,8, 136,9, 135,1, 127,9, 127,4, 125,0, 116,5, 71,0, 43,9, 32,4, 19,9, 14,1
Пример 4. 2-Хлор-N-циклопропил-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бензамид (соединение 313)

2-Хлор-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бензойная кислота (N). К суспензии соединения М, которое получали аналогичным образом, что и соединение 76 (85 мг, 0,21 ммоль, 1,0 экв.) в THF (1,36 мл) и метаноле (0,68 мл), добавляли раствор гидроксида лития (1 н. вводе, 1,03 мл, 5,0 экв.). После 30 мин. при 50°С реакционную смесь охлаждали до 0°С и рН доводили до ~3-4 с применением раствора 4 М HCl в 1,4-диоксане. Ярко-желтую суспензию концентрировали до сухого состояния при пониженном давлении. Неочищенный материал использовали на следующей стадии в виде соли LiCl, предполагая получение количественного выхода. ES-MS [М+1]+: 400,2.
2-Хлор-N-циклопропил-4-[[(3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил)амино]метил]бензамид (соединение 313). К суспензии соединения N (10 мг, 0,025 ммоль, 1,0 экв.) в DMF (1,0 мл) добавляли HATU (24 мг, 0,063 ммоль, 2,5 экв.) и N,N-диизопропилэтиламин (60 мкл, 0,34 ммоль, 13,8 экв.). После 5 мин при к.т. добавляли циклопропиламин (8,7 мкл, 0,13 ммоль, 5,0 экв.). Полученную смесь перемешивали в течение 20 мин. Очищали с применением обращенно-фазовой HPLC (основной способ, 33-64% ACN/вода/0,05% NH4OH) с получением указанного в заголовке соединения в виде бледно-желтого твердого вещества (5,1 мг, выход 46%). ES-MS [М+1]+: 438,8;1Н ЯМР (400 МГц, DMSO-d6) δ 8,88 (d, J=6,6 Гц, 1Н), 8,84 (s, 1Н), 8,70 (s, 1Н), 7,51 (d, J=0,8 Гц, 1Н), 7,44-7,38 (m, 2Н), 4,80 (s, 2Н), 4,22-4,16 (m, 1Н), 3,02 (s, 3Н), 3,00-2,92 (m, 2Н), 2,79 (s, 3Н), 2,68-2,57 (m, 2Н).
Соединения, приведенные в таблице 1, получали аналогичным образом, что и соединения, представленные в примерах 2-4, с помощью подходящих исходных материалов.


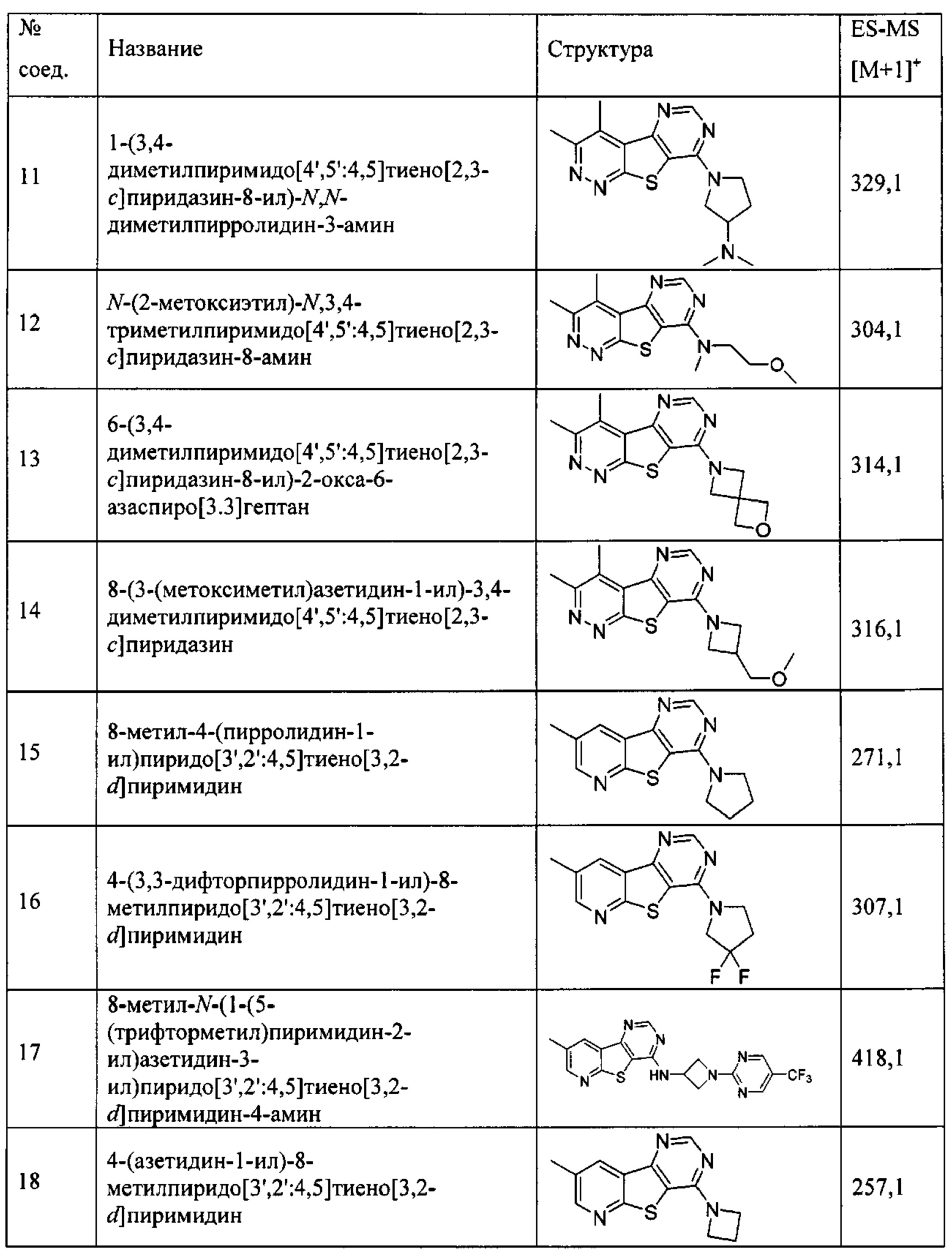

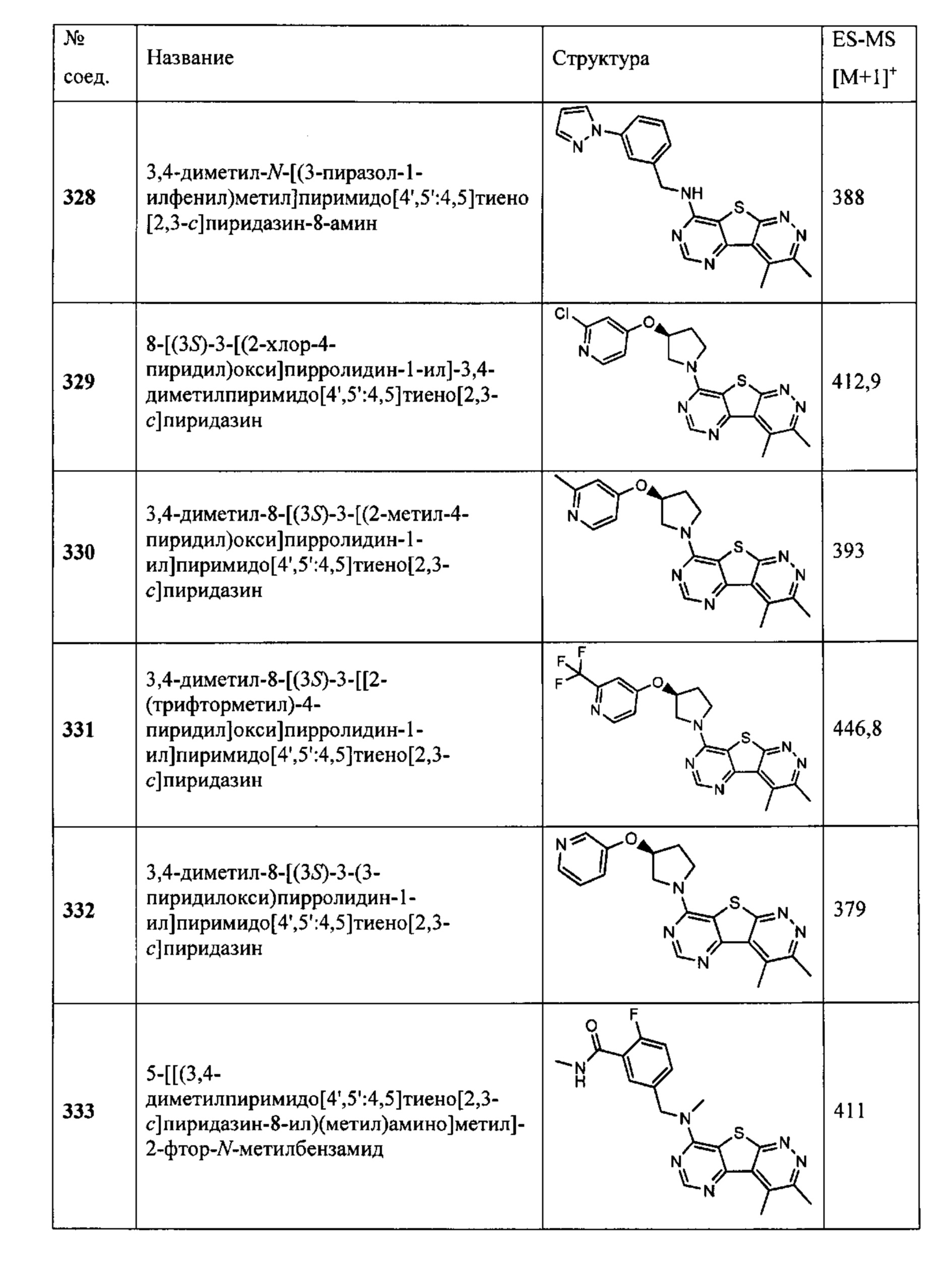









Пример 5. 8-хлор-N-(3,3-дифторциклобутил)-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин (соединение 37)
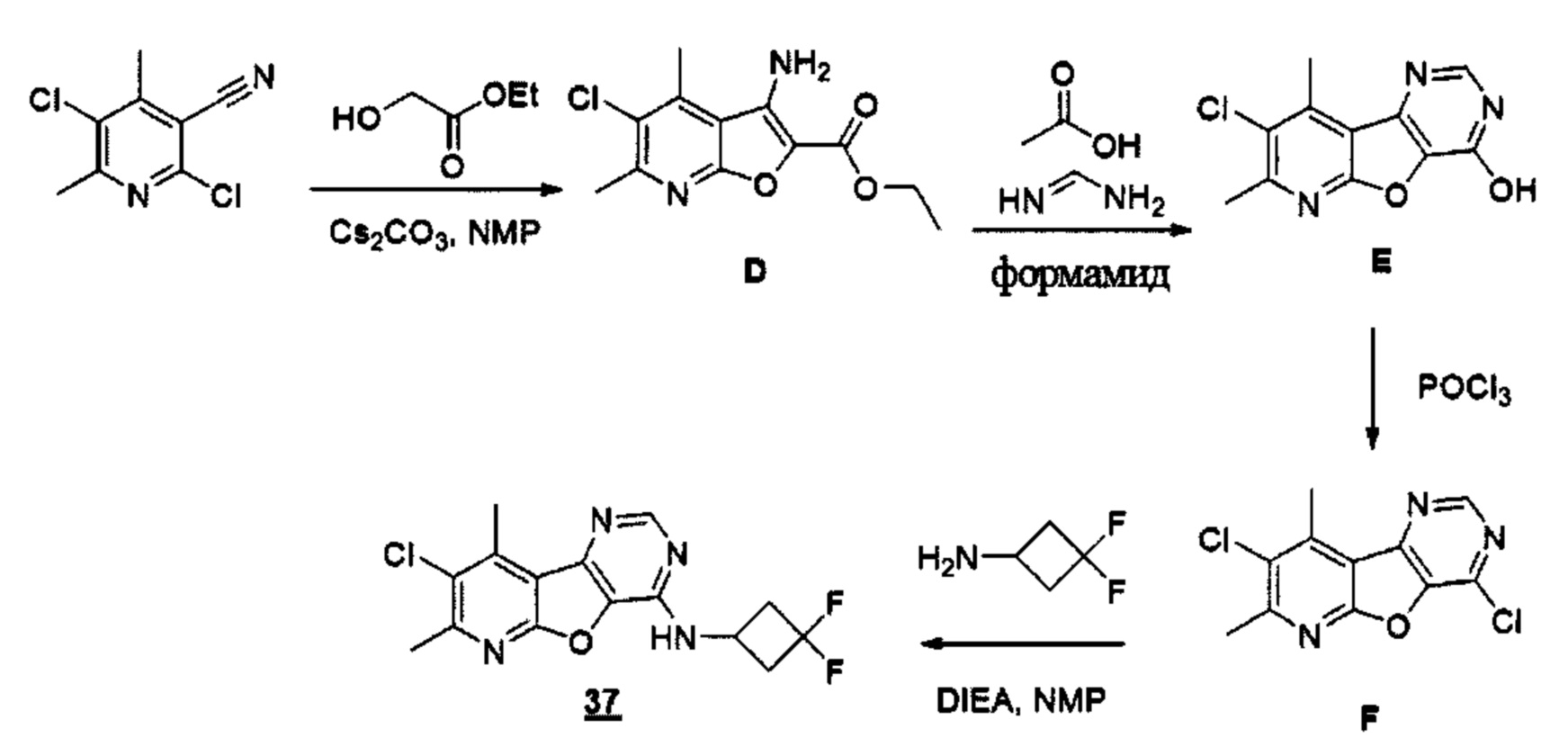
Этил-3-амино-5-хлор-4,6-диметилфуро[2,3-b]пиридин-2-карбоксилат (D). 2,5-хлор-4,6-диметилникотинолнитрил (1,0 г, 6,0 ммоль, 1,0 экв.), этилгликолят (0,6 мл, 6,6 ммоль, 1,1 экв.) и CS2CO3 (5,9 г, 18 ммоль, 3,0 экв.) добавляли к 100 мл RBF с NMP (9,23 мл) и обеспечивали перемешивание при 75°С в течение ночи. Реакционную смесь фильтровали через подушку из целита, которую ополаскивали с помощью DCM и EtOAc. Фильтрат концентрировали и очищали с помощью обращенно-фазовой HPLC с получением указанного в заголовке соединения (250 мг, 0,930 ммоль, выход 15,5%).1Н ЯМР (400 МГц, DMSO-d6): δ 6,09 (s, 2Н), 4,34 (q, J=7,0 Гц, 2Н), 2,72 (s, 3H), 2,61 (s, 3H), 1,34 (t, J=7,0 Гц, 3H); ES-MS [М+1]+: 269,2.
8-Хлор-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-ол (Е). Раствор соединения D (250 мг, 0,930 ммоль, 1,0 экв.) в формамиде (1,65 мл, 41,4 ммоль, 44,5 экв.) нагревали в закрытом сосуде до 150°С. При 150°С к реакционной смеси каждые 30 мин. в течение 1,5 ч. добавляли ацетат формамидина (290 мг, 2,79 ммоль, 3,0 экв.) в общем объеме, составляющем 9 эквивалентов. Реакционную смесь отводили от источника нагрева и охлаждали до к. т. К раствору добавляли Н2О и экстрагировали с помощью CHCl3/ изопропанола (3:1). Органические слои объединяли и концентрировали при пониженном давлении с получением указанного в заголовке соединения (230 мг, 0,921 ммоль, выход 99%) в виде коричневого твердого вещества. Его непосредственно применяли на следующей стадии без очистки. ES-MS [М+1]+: 250,2.
4,8-Дихлор-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин (F). Соединение Е (232 мг, 0,930 ммоль) и POCl3 (2,64 мл, 28,2 ммоль) загружали в RBF объемом 250 мл, оснащенную холодильником. Обеспечивали перемешивание реакционной смеси при 120°С до завершения реакции, что определяли с помощью LC-MS (4 часа). Охлаждали до комнатной температуры и переносили в большой химический стакан. Добавляли насыщ. NaHCO3 (100 мл), и медленно частями добавляли твердый K2CO3 с обеспечением контроля над газообразованием при интенсивном перемешивании. Когда рН смеси достигал 8, ее затем переносили в разделительную воронку. Добавляли воду, и необходимый продукт экстрагировали с помощью ЕА (3х). Органические слои собирали, высушивали с помощью Mg2SO4, фильтровали и концентрировали при пониженном давлении с получением указанного в заголовке соединения (200 мг, 0,746 ммоль, выход 80%) в виде коричневого твердого вещества.1Н ЯМР (400 МГц, DMSO-d6): δ 9,14 (s, 1Н), 2,98 (s, 3H), 2,77 (s, 3H); ES-MS [M+1]+: 268,2.
8-Хлор-N-(3,3-дифторциклобутил)-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амина гидрохлорид (37). Данное соединение получали таким же образом, как и соединение 55 (см. ниже) с получением указанного в заголовке соединения (10,5 мг, выход 55%) в виде соли HCl.1Н ЯМР (400 МГц, DMSO-d6): δ 8,75 (d, J=5,8 Гц, 1Н), 8,56 (s, 1Н), 4,54-4,51 (m, 1Н), 3,17-3,03 (m, 2Н), 3,00 (s, 3H), 2,89-2,77 (m, 2Н), 2,69 (s, 3H); ES-MS [М+1]+: 339,3.
Соединения, приведенные в таблице 2, получали аналогичным образом с помощью подходящих исходных материалов.
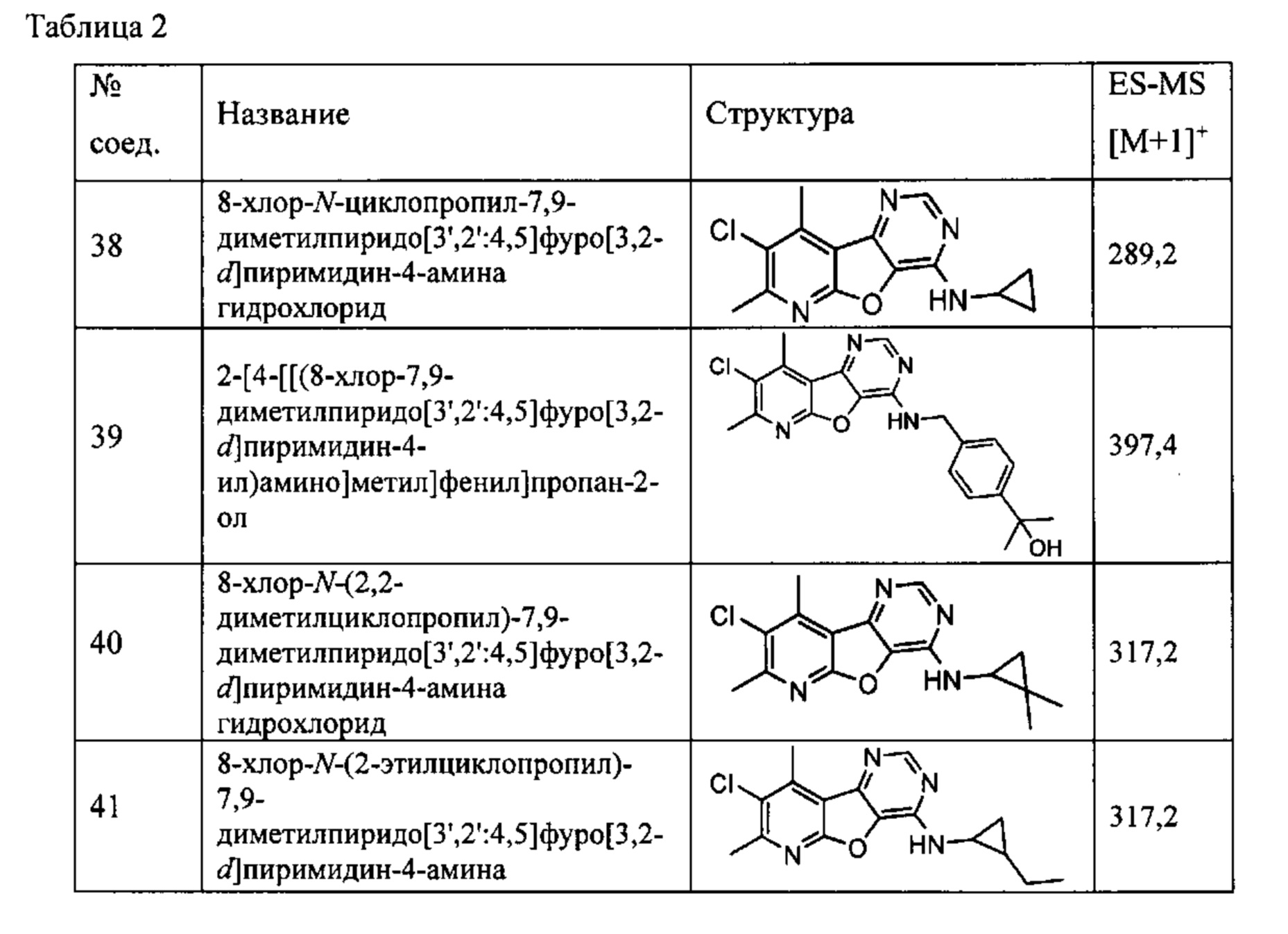

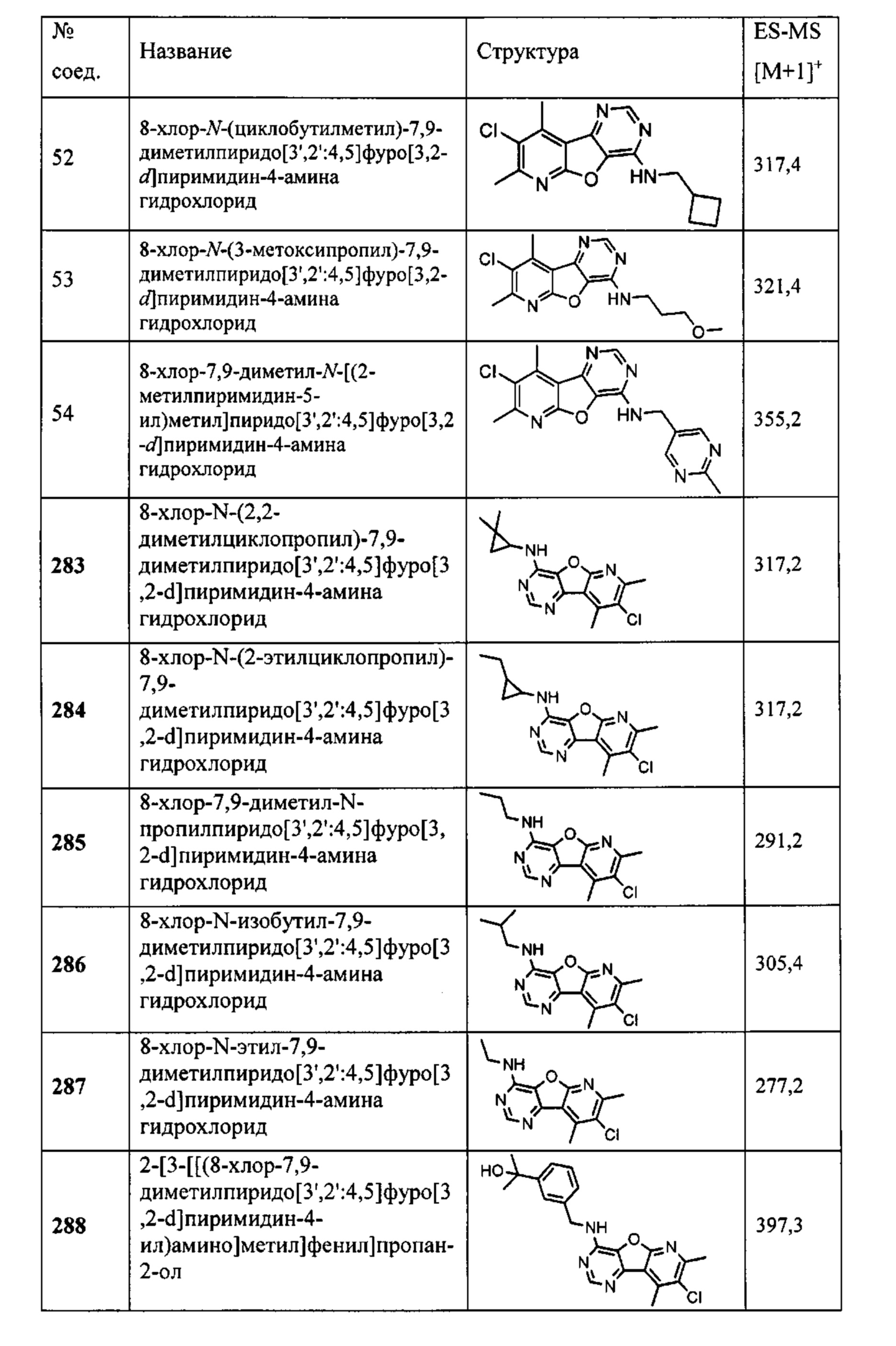
Пример 6. N-Циклобутил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амин (соединение 55)

Этил-3-амино-4,6-диметилфуро[2,3-b]пиридин-2-карбоксилат (G). 2-хлор-4,6-диметилникотинонитрил (1,0 г, 6,0 ммоль, 1,0 экв.), этилгликолят (0,6 мл, 6,6 ммоль, 1,1 экв.) и CS2CO3 (5,9 г, 18 ммоль, 3,0 экв.) совместно добавляли в RBF объемом 100 мл с NMP (9,23 мл, 0,2 М) и обеспечивали перемешивание при 75°С в течение ночи. Реакционную смесь фильтровали через подушку из целита, которую ополаскивали с помощью DCM и EtOAc. Фильтрат концентрировали и очищали с помощью обращенно-фазовой HPLC с получением указанного в заголовке соединения (501 мг, 2,14 ммоль, выход 35,6%).1Н ЯМР (400 МГц, DMSO-d6): δ 7,01 (s, 1Н), 6,00 (s, 2H), 4,33 (q, J=7,1 Гц, 2H), 2,65 (s, 3H), 2,48 (s, 3H), 1,34 (d, J=7,1 Гц, 2 H); ES-MS [M+1]+: 235,2.
7,9-Диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-ол (H). Раствор соединения G (361,79 мг, 1,54 ммоль, 1,0 экв.) в формамиде (2,73 мл, 68,77 ммоль, 44,5 экв.) нагревали в закрытом сосуде до 150°С. Каждые 30 мин. в течение 1,5 ч при 150°С к реакционной смеси добавляли ацетат формамидина (482,39 мг, 4,63 ммоль, 3,0 экв.) в общем объеме, составляющем 9 эквивалентов. Реакционную смесь отводили от источника нагрева и охлаждали до к.т. К раствору добавляли Н2О и экстрагировали с помощью CHCl3/изопропанола (3:1). Органические слои объединяли и концентрировали при пониженном давлении с получением указанного в заголовке соединения (842 мг, 1,53 ммоль, выход 98,8%) в виде коричневого твердого вещества. Его непосредственно применяли на следующей стадии без очистки. ES-MS [М+1]+: 216,3.
4-Хлор-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин (I). Соединение Н (330 мг, 1,53 ммоль) и POCl3 (4,35 мл, 46,54 ммоль) загружали в RBF объемом 250 мл, оснащенную холодильником. Обеспечивали перемешивание реакционной смеси при 120°С до завершения реакции, что определяли с помощью LC-MS. Нагревание прекращали. При достижении реакционной смесью комнатной температуры добавляли толуол, и реакционную смесь концентрировали при пониженном давлении для удаления POCl3. Затем в колбу добавляли холодную H2O, и смесь подвергали воздействию ультразвука и перемешивали с образованием твердого вещества светло-коричневого цвета. Гетерогенную смесь затем фильтровали in vacuo с получением указанного в заголовке соединения (358 мг, 1,53 ммоль, выход 99,9%) в виде светло-коричневого твердого вещества.1Н ЯМР (400 МГц, DMSO-d6): δ 9,08 (s, 1Н), 7,45 (s, 1H), 2,87 (s, 3H), 2,66 (s, 3H); ES-MS [M+1]+: 234,2.
N-Циклобутил-7,9-диметилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-4-амина гидрохлорид (55). В небольшой флакон добавляли суспензию соединения I (10 мг, 0,040 ммоль, 1,0 экв.) и DIEA (29,82 мкл, 0,170 ммоль, 4,25 экв.) в NMP (0,500 мл). Добавляли циклобутиламин (3,35 мг, 0,050 ммоль, 1,25 экв.) и обеспечивали перемешивание реакционной смеси при 50°С в течение 2 ч. Реакционную смесь затем охлаждали до к.т., и разбавляли DMSO (0,5 мл), и очищали с помощью обращенно-фазовой HPLC. Необходимые фракции собирали и концентрировали. Остаток растворяли в DCM (1,0 М), и добавляли 4 М HCl в диоксане (5 экв.). После 30 мин при к.т. растворитель удаляли с получением HCI-соли необходимого продукта (11,3 мг, 0,037 ммоль, выход 86,6%).1Н ЯМР (400 МГц, DMSO-d6): δ 8,50 (s, 1Н), 8,50 (s, 1H) 7,28 (s, 1H), 4,74-4,70 (m, 1H), 2,81 (s, 3H), 2,60 (s, 3H), 2,37-2,30 (m, 2H), 2,20-2,14 (m, 2H), 1,76-1,70 (m, 2H); ES-MS [M+1]+: 269,5.
Соединения, приведенные в таблице 3, получали аналогичным образом с помощью подходящих исходных материалов.



Пример 7. N-[1-(5-Фторпиримидин-2-ил)азетидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин (соединение 63)

Изопропил-5-амино-3,4-диметилфуро[2,3-с]пиридазин-6-карбоксилат (J). В каждый из двух флаконов для микроволнового реактора объемом 20 мл добавляли 3-хлор-5,6-диметилпиридазин-4-карбонитрил (500 мг, 2,985 ммоль, 1,1 экв.), K2CO3 (1,675 г, 11,935 ммоль, 4,0 экв.) и изопропанол (10 мл). Добавляли этилгликолят (310 мкл, 3,28 ммоль, 1,1 экв.), и флаконы закрывали и подвергали воздействию микроволнового реактора в течение 30 минут при 150°С. Реакционные смеси охлаждали до к.т. и разбавляли с помощью DCM, фильтровали через целит и промывали с помощью DCM и EtOAc. Фильтрат концентрировали при пониженном давлении с получением черного остатка. Неочищенный продукт очищали с применением колоночной флэш-хроматографии на силикагеле (0-75% DCM/EtOAc) с получением указанного в заголовке соединения (608 мг, 2,44 ммоль, выход 41%) в виде желтого порошка.1Н ЯМР (400 МГц, DMSO-d6): δ 6,19 (s, 2Н), 5,23 (m, 1Н), 2,67 (s, 3H), 2,63 (s, 3H), 1,36 (d, J=6,2 Гц, 6Н); ES-MS [М+1]+: 250,4.
3,4-Диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ол (K). Раствор соединения J (300 мг, 3,61 ммоль, 1,0 экв.) в формамиде (2,12 мл, 53,6 ммоль, 44,5 экв.) нагревали в закрытом сосуде до 150°С. При 150°С каждые 30 мин. в течение 1,5 ч. к реакционной смеси добавляли ацетат формамидина (376 мг, 3,61 ммоль, 3,0 экв.) в общем объеме, составляющем 9 эквивалентов. Реакционную смесь отводили от источника нагрева и охлаждали до к.т. К раствору добавляли Н2О и экстрагировали с помощью CHCl3/изопропанола (3:1). Органические слои объединяли и концентрировали при пониженном давлении с получением указанного в заголовке соединения (842 мг, 1,53 ммоль, выход 98,8%) в виде коричневого твердого вещества. Его непосредственно применяли на следующей стадии без дополнительный очистки. ES-MS [М+1]+: 217,3.
N-[1-(5-Фторпиримидин-2-ил)азетидин-3-ил]-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-амин (63). Во флакон совместно добавляли раствор соединения K (20 мг, 0,090 ммоль), ВОР (49,51 мг, 0,110 ммоль) и DBU (0,02 мл, 0,130 ммоль) в NMP (2 мл). Добавляли 1-(5-фторпиримидин-2-ил)азетидин-3-амин (21,7 мг, 0,130 ммоль) и реакционную смесь перемешивали при к.т. в течение ночи. Реакционную смесь фильтровали через шприцевой фильтр и очищали с помощью обращенно-фазовой HPLC с получением указанного в заголовке соединения (1,1 мг, 0,003 ммоль, выход 3,5%) в виде белого твердого вещества. ES-MS [М+1]+: 369,3.
Соединения, приведенные в таблице 4, получали аналогичным образом с помощью подходящих исходных материалов.

Пример 8. 2-[4-[[(3,4-Диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол (соединение 65)

8-Хлор-3,4-диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин (L). К суспензии соединения K (0,46 г, 2,12 ммоль, 1,0 экв.) в оксихлориде фосфора (4,0 мл) добавляли пентахлорид фосфора (89 мг, 0,43 ммоль, 0,20 экв.). Реакционную смесь нагревали до 120°С. После 16 часов реакционную смесь охлаждали до к.т. и концентрировали под вакуумом. К остатку добавляли толуол (100 мл) и растворитель удаляли при пониженном давлении. Остаток суспендировали в DCM (100 мл) и медленно добавляли триэтиламин (4 мл). К смеси добавляли воду (25 мл), и органический слой отделяли. Водный слой повторно экстрагировали с помощью DCM (3х), и объединенные органические слои фильтровали через гидрофобную фритту. Раствор концентрировали с получением промежуточного соединения L в виде коричневатого порошка, который использовали далее без дополнительной очистки. ES-MS [М+1]+: 235,4;1Н ЯМР (400 МГц, DMSO-d6) δ 9,24 (s, 1H), 2,91 (s, 3H), 2,81 (s, 3H).
2-[4-[[(3,4-Диметилпиримидо[4',5':4,5]фуро[2,3-с]пиридазин-8-ил)амино]метил]фенил]пропан-2-ол (соединение 65). Раствор промежуточного соединения L (12 мг, 0,05 ммоль, 1,0 экв.), 2-(4-(аминометил)фенил)пропан-2-ола (Х19) (41 мг, 0,25 ммоль, 5,0 экв.) и DIEA (44 мкл, 0,25 ммоль, 5,0 экв.) в NMP (0,5 мл, 0,1 М) нагревали до 60°С в течение 30 мин. или пока посредством LCMS не подтверждали убыль исходного материала. После охлаждения до к.т. смесь разбавляли DMSO и фильтровали через шприцевой фильтр для удаления любых нерастворимых солей. Неочищенный материал очищали с применением обращенно-фазовой HPLC с получением указанного в заголовке соединения (9,6 мг, выход 53%) в виде грязно-белого порошка. ES-MS [М+1]+: 364,2;1Н ЯМР (400 МГц, DMSO-d6) δ 9,10 (m, 1Н), 8,64 (s, 1Н), 7,48 (d, J=7,9 Гц, 2Н), 7,37 (d, J=8,0 Гц, 2Н), 5,02 (s, 1Н), 4,80 (d, J=5,8 Гц, 2Н), 2,90 (s, 3H), 2,80 (s, 3H), 1,45 (s, 6Н).
Соединения, приведенные в таблице 4, получали аналогичным образом с помощью подходящих исходных материалов.



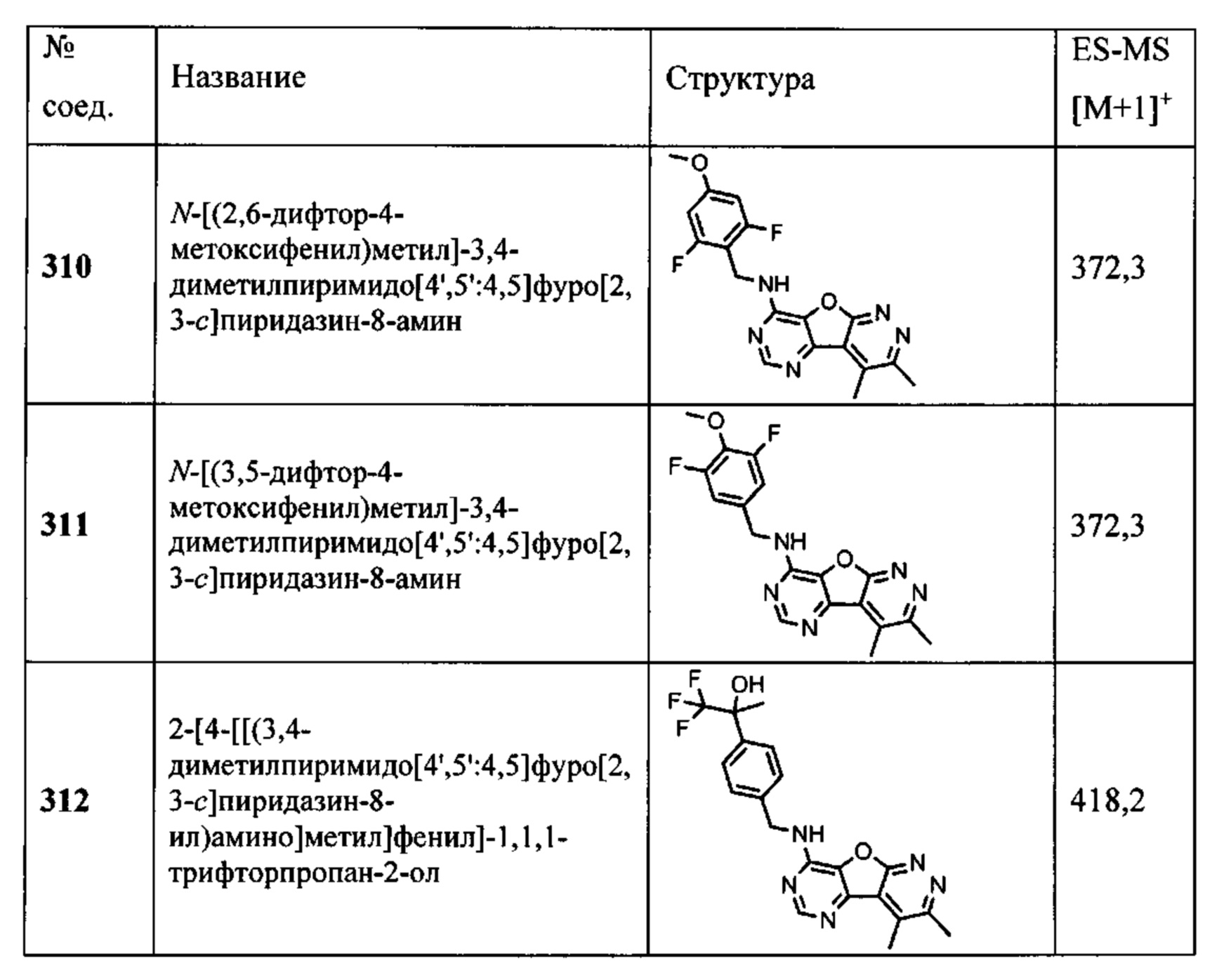
Пример 9. [8-[[4-(2-Гидроксипропан-2-ил)бензил]амино]-4-метилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-3-ил]метилацетат (соединение 376) и 2-[4-[[[3-(гидроксиметил)-4-метилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил]амино]метил]фенил]пропан-2-ол (соединение 377)
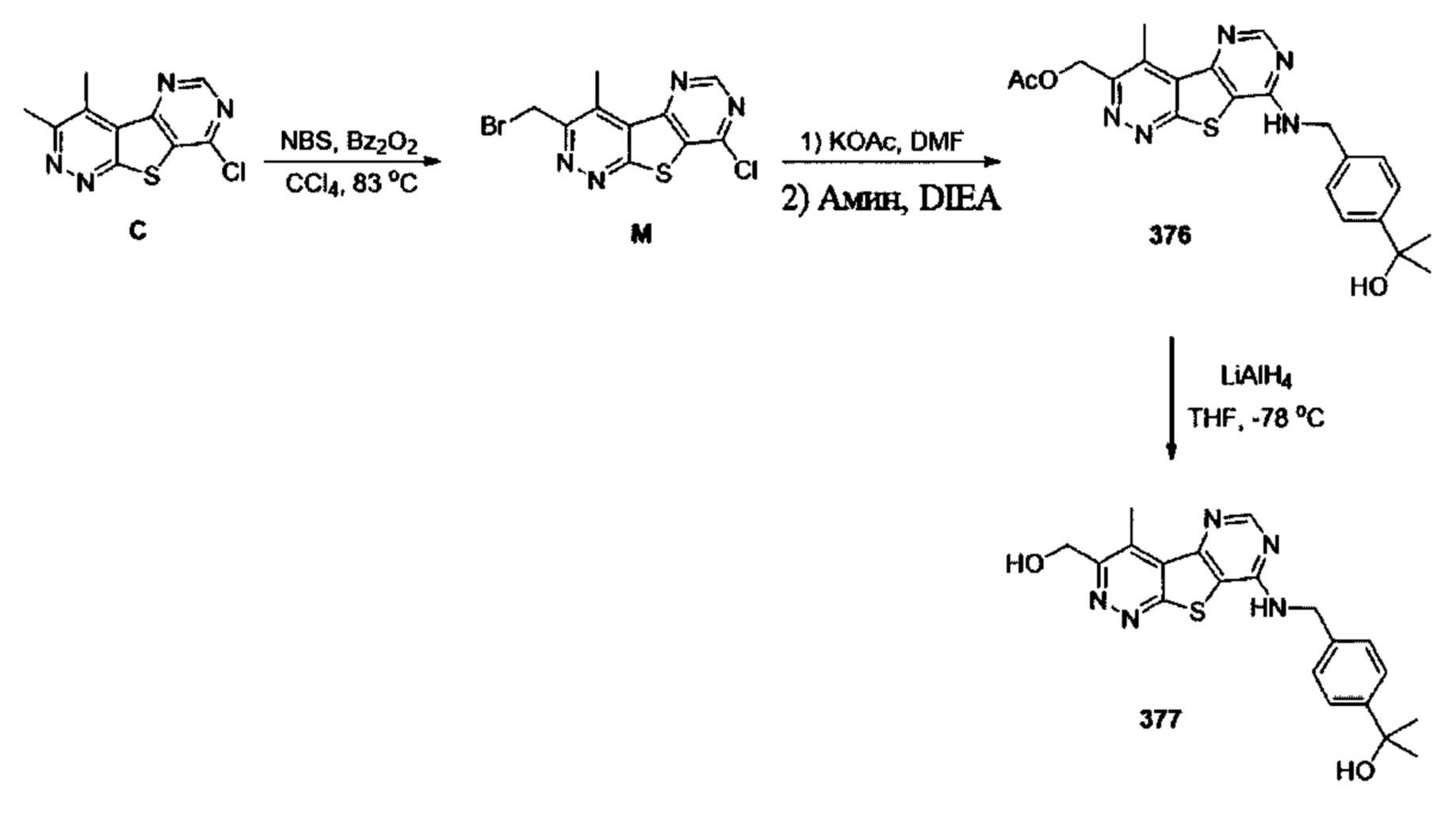
3-(Бромметил)-8-хлор-4-метилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин (М). К раствору 8-хлор-3,4-диметилпиримидо[4',5':4,5]тиено[2,3-с]пиридазина (соединение С) (100 мг, 0,40 ммоль, 1,0 экв.) и N-бромсукцинимида (78 мг, 0,44 ммоль, 1,1 экв.) в тетрахлорметане (4,0 мл) добавляли бензоилпероксид (13,3 мг, 0,06 ммоль, 0,14 экв.). После 2 ч. при 83°С реакционную смесь концентрировали. Неочищенный материал очищали посредством колоночной флэш-хроматографии на силикагеле (0-50% EtOAc/гексаны) с получением указанного в заголовке соединения, наряду с непрореагировавшим исходным материалом и побочным продуктом дибромирования, в виде лаймово-зеленого кристаллического твердого вещества (100 мг, выход 74%, с чистотой 66% 1Н ЯМР). ES-MS [М+1]+: 330,8;1Н ЯМР (400 МГц, DMSO-d6) δ 9,45 (s, 1H), 5,62 (s, 2H), 2,97 (s, 3H).
[8-[[4-(1-Гидрокси-1-метилэтил)фенил]метиламино]-4-метилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-3-ил]метилацетат (соединение 376). Смесь соединения М (50 мг, 0,152 ммоль, 1,0 экв.) и ацетата калия (22,3 мг, 0,228 ммоль, 1,5 экв.) в DMF (0,76 мл) перемешивали при к.т. После 45 мин. промежуточное соединение, представляющее собой ацетат, подтверждали с помощью LCMS (ES-MS [М+1]+: 308,9). Добавляли 2-[4-(аминометил)фенил]пропан-2-ол (27,6 мг, 0,17 ммоль, 1,1 экв.) и N,N-диизопропилэтиламин (52,8 мкл, 0,303 ммоль, 2,0 экв.). После 30 мин. при к.т. реакционную смесь разбавляли DMSO (2 мл) и фильтровали с применением шприцевого фильтра для удаления любых нерастворимых солей. Очистку проводили с использованием обращенно-фазовой HPLC с применением основного способа (35-65% MeCN/вода/0,05% NH4OH) с получением указанного в заголовке соединения в виде бледно-желтого порошка (40 мг, выход 60%).
2-[4-[[[3-(Гидроксиметил)-4-метилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-8-ил]амино]метил]фенил]пропан-2-ол (соединение 377). К раствору [8-[[4-(1-гидрокси-1-метилэтил)фенил]метиламино]-4-метилпиримидо[4',5':4,5]тиено[2,3-с]пиридазин-3-ил]метилацетата (376) (40 мг, 0,091 ммоль, 1,0 экв.) в THF (1,22 мл) по каплям добавляли раствор алюмогидрида лития (1,0 М в THF, 0,105 мл, 0,105 ммоль, 1,15 экв.) при -78°С. После 1 ч. при -78°С медленно добавляли МеОН. Смесь концентрировали до сухого состояния при пониженном давлении. Неочищенный материал суспендировали в DMSO (2,0 мл) и фильтровали через шприцевой фильтр для удаления нерастворимых солей. Очистку проводили с использованием обращенно-фазовой HPLC с применением основного способа (15-50% MeCN/вода/0,05% NH4OH) с получением указанного в заголовке соединения в виде бледно-желтого порошка (4,5 мг, выход 12%). ES-MS [М+1]+: 396,0;1Н ЯМР (400 МГц, CDCl3) δ 8,83 (s, 1Н), 7,49 (dd, J=8,3, 1,7, 2H), 7,43-7,35 (m, 3H), 5,53 (dd, J=5,0, 5,0 Гц, 1H), 5,26 (dd, J=7,2 Гц, 2H), 4,95 (dd, J=5,6 Гц, 2H), 2,99 (s, 3H), 1,80 (s, 1H), 1,62 (s, 6H).
Пример 10. Физико-химические свойства
Некоторые физико-химические свойства определяли для соединения 76 и они представлены в таблице 6.

Пример 11. Биологическая активность
A. Клеточные линии, экспрессирующие мускариновые ацетилхолиновые рецепторы
cDNA М4 человека, крысы, собаки и яванского макака ("cyno"), наряду с химерным G-белком Gqi5, трансфицировали в клетки яичника китайского хомячка (СНО-K1), приобретенные в Американской коллекции типовых культур, с применением Lipofectamine2000. Клетки hM4-Gqi5 выращивали в среде Хэма F-12, содержащей 10% инактивированной нагреванием фетальной бычьей сыворотки (FBS), 20 мМ HEPES, 50 мкг/мл сульфата G418 и 500 мкг/мл гигромицина В. Клетки rM4-Gqi5 выращивали в DMEM, содержащей 10% инактивированной нагреванием FBS, 20 мМ HEPES, 400 мкг/мл сульфата G418 и 500 мкг/мл гигромицина В.
B. Функциональный клеточный анализ активности мускариновых ацетилхолиновых рецепторов
Для высокопроизводительного измерения увеличения показателей уровня внутриклеточного кальция, вызванного агонистом, клетки СНО-K1, стабильно экспрессирующие мускариновые рецепторы, высевали в среду для выращивания, не содержащую G418 и гигромицин, при 15000 клеток/20 мкл/лунка в 384-луночных планшетах Greiner с черными стенками, (ТС)-обработанных для выращивания тканевой культуры, с прозрачным дном (VWR). Клетки инкубировали в течение ночи при 37°С и 5% СО2. На следующий день клетки промывали с применением ELX 405 (BioTek) посредством аналитического буфера; конечный объем затем отсасывали до 20 мкл. Далее в лунки добавляли 20 мкл 2,3 мкМ исходного раствора Fluo-4/сложного ацетоксиметилового эфира (Invitrogen, Карлсбад, Калифорния), полученного в виде 2,3 мМ исходного раствора в DMSO, и смешанного в соотношении 1:1 с 10% (вес/об.) Pluronic F-127, и разбавленного в аналитическом буфере, и клеточные планшеты инкубировали в течение 50 мин. при 37°С и 5% СО2. Краситель удаляли посредством промывания с помощью ELX 405, и конечный объем отсасывали до 20 мкл. Исходные планшеты с соединением форматировали в 11-точечном формате кривой концентрация-ответ (CRC) (разведения 1:3) в 100% DMSO с начальной концентрацией 10 мМ с применением жидкостного манипулятора BRAVO (Agilent). CRC тестируемого соединения затем переносили на дочерние планшеты (240 нл) с применением устройства для акустического переформатирования планшета Echo (Labcyte, Саннивейл, Калифорния) и затем разбавляли в аналитическом буфере (40 мкл) до 2× исходного раствора с применением Thermo Fisher Combi (Thermo Fisher Scientific, Уолтэм, Массачусетс).
Поток кальция измеряли с применением Functional Drug Screening System (FDSS) 6000 или 7000 (Hamamatsu Corporation, Токио, Япония) как увеличение статического соотношения флуоресценции. Соединения наносили на клетки (20 мкл, 2Х) с использованием автоматизированной системы FDSS на 2-4 с с начала протокола, и данные собирали при 1 Гц. На 144 с добавляли 10 мкл (5Х) агониста мускаринового рецептора ацетилхолина в концентрации ЕС20 с последующим добавлением 12 мкл ацетилхолина в концентрации EC80 на момент времени, составляющий 230 с (5Х). Активность агониста анализировали как зависимое от концентрации увеличение мобилизации кальция при добавлении соединения. Активность положительного аллостерического модулятора анализировали как зависимое от концентрации увеличение ответа на ацетилхолин в концентрации ЕС20. Активность антагониста анализировали как зависимое от концентрации уменьшение ответа на ацетилхолин в концентрации EC80. Кривые концентрации-ответа получали с применением четырехпараметрического логистического уравнения в программном обеспечении для подбора кривой XLFit (IDBS, Бриджуотер, Нью-Джерси) для Excel (Microsoft, Редмонд, Вашингтон) или Prism (GraphPad Software, Inc., Сан-Диего, Калифорния). Вышеописанный анализ также проводили во втором режиме, где к клеткам добавляли соединения по настоящему изобретению в подходящей фиксированной концентрации после установления исходного уровня флуоресценции в течение приблизительно 3 секунд, и измеряли ответ в клетках. Спустя 140 с добавляли агонист в подходящей концентрации и измеряли кальциевый ответ (максимальный-локальный минимальный ответ). Значения ЕС50 для агониста в присутствии тестируемого соединения определяли посредством подбора нелинейной кривой. Снижение значения ЕС50 агониста с увеличением концентраций соединений по настоящему изобретению (сдвиг влево кривой концентрации-ответа агониста) является показателем степени положительной аллостерической модуляции мускариновых рецепторов при данной концентрации соединения по настоящему изобретению. Повышение значения ЕС50 агониста с увеличением концентраций соединений по настоящему изобретению (сдвиг вправо кривой концентрации-ответа агониста) является показателем степени антагонизма мускариновых рецепторов при данной концентрации соединения по настоящему изобретению. Второй режим также показывает, влияют ли соединения по настоящему изобретению также и на максимальный ответ мускаринового рецептора в отношении агонистов.
С. Активность соединений в клеточном анализе mAChR М4
Соединения синтезировали как описано выше. Активность (ЕС50 и Emax) определяли в функциональном клеточном анализе mAChR М4, описанном выше, и данные показаны в таблицах 7-10. Номера соединений соответствуют номерам соединений, применяемым в таблицах 1-5.
Активность также определяли для соединения 76 в аналогичном анализе с применением М2 человека. Применительно к М2 человека соединение 76 имеет ЕС50=2800 нМ (48% Emax).
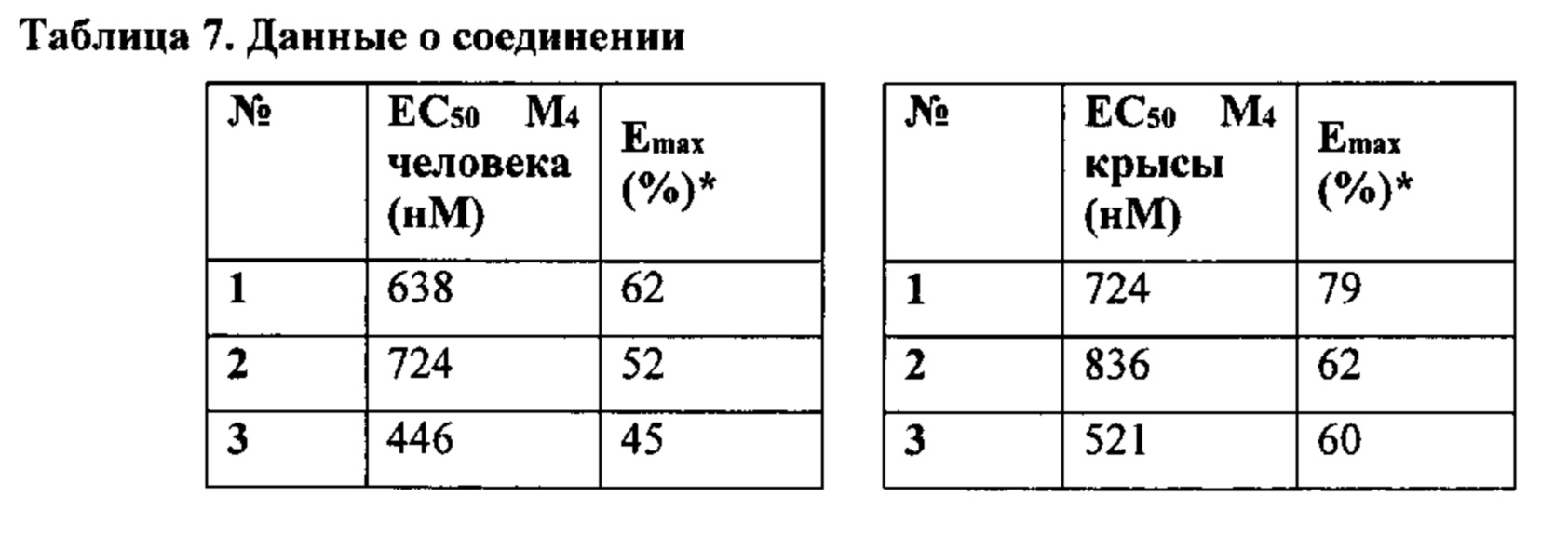


* %ACh максимум при 30 мкМ.
НО = не определено

* %ACh максимум при 30 мкМ.
НО = не определено
Таблица 9. Данные о соединении 76

* %ACh максимум при 30 мкМ.





* %ACh максимум при 30 мкМ.


* %ACh максимум при 30 мкМ.
D. Эффекты соединений в отношении индуцированной амфетамином гиперлокомоции у крыс
Способность соединения 76 обращать индуцированную амфетамином гиперлокомоцию в преклинической модели, прогнозирующей антипсихотик-подобную активность (Stanhope et al. (2001) J Pharmacol Exp Ther. 299:782-792), оценивали у самцов крыс Sprague-Dawley.
Лекарственные средства: d-амфетамина гемисульфат получали от Sigma (Сент-Луис, Миссури). Солевую поправку применяли для определения правильного количества формы d-амфетамина гемисульфата в миллиграммах для добавления в стерильную воду с целью получения 0,75 мг/мл раствора, который будут вводить в дозе 1 мл/кг веса тела каждого животного. Соединение 76 и сравниваемое соединение VU 0467154 (описанный mAChR М4 РАМ, Bubser et al. ACS Chem. Neurosci. 2014, 5(10):920-942) составляли в объемах, характерных для количества животных, которым каждый день вводили конкретную дозу. Растворы составляли таким образом, что животным вводили объем, равный 10 мл/кг веса тела для всех соединений. Подходящее количество в соответствии с дозой смешивали в 10% Tween 80 (Sigma) в стерильной воде. Смеси затем перемешали вихревым способом и хранили в ультразвуковой бане при 39°С в течение 1 часа, до образовании микросуспензии (за исключением самой высокой дозы, которая представляла собой суспензию).
Животные: использовали самцов крыс Sprague-Dawley весом 239-300 грамм и в среднем 265 г (Harlan, Inc., Индианаполис, Индиана). Их содержали в учреждении для ухода за животными, сертифицированном Американской ассоциацией по аккредитации ухода за лабораторными животными (AALAC), при 12-часовом цикле свет/темнота (включение света в 6 до полудня; выключение света в 6 после полудня), и они имели свободный доступ к пище и воде. Животных, применяемых в данном эксперименте, лишали пищи вечером перед проведением эксперимента с пероральным дозированием соединения/среды-носителя. Экспериментальные протоколы, осуществленные во время светового цикла были одобрены Институциональным комитетом по уходу за животными и их использованию Университета Вандербилта и соответствовали рекомендациям, установленным Руководством по содержанию и использованию лабораторных животных Национального научно-исследовательского совета.
Индуцированная амфетамином гиперлокомоция: Самцам крыс Harlan Sprague-Dawley давали привыкнуть к камерам для тестирования локомоторной активности Smart Open Field (Hamilton-Kinder, Сан-Диего, Калифорния), оснащенным 16×16 фотодатчиками для автоматической регистрации локомоторной активности. После 30 минут наблюдения животным с помощью перорального зонда вводили среду-носитель или соединение - либо соединение 76, либо VU0467154. За ними наблюдали в течение дополнительных 30 минут, и затем подкожно вводили среду-носитель или 1 мг/кг амфетамина. Затем за животными наблюдали в течение дополнительных 60 минут с общей продолжительностью, составляющей 120 минут. Данные выражали как изменения в количестве посещенных квадратов, определяемые как общее количество случаев прерывания лучей в течение интервала, составляющего 5 минут. Конечные образцы головного мозга и плазмы собирали в конце исследования для фармакокинетического анализа.
Анализ данных: данные о поведении анализировали с применением двухфакторного ANOVA с использованием основных эффектов обработки и времени. Апостериорный анализ проводили с применением t-критерия Даннета, при котором все экспериментальные группы сравнивали с VAMP-группой с использованием GraphPad Prism V.5.04 (GraphPad Software, Сан-Диего, Калифорния). Данные представляли в виде графика с использованием GraphPad Prism V.5.04 (GraphPad Software, Сан-Диего, Калифорния). Уровень вероятности p≤0,05 принимали в качестве уровня статистической значимости. Кроме того, рассчитывали и представляли в виде графика общее количество случаев прерывания лучей от момента введения амфетамина (65 мин.) до завершения исследования (120 мин.). Процент устранения рассчитывали с применением Microsoft Excel следующим образом: для каждого животного подсчитывали сумму общего количества посещенных квадратов в интервале от t=65 до t=120. Рассчитывали среднее значение каждой суммы для VAMP-группы. Затем для каждого животного рассчитывали процент устранения с использованием следующей формулы: Процент устранения = 100 - {[(общее количество посещенных квадратов для каждого животного в интервале от t=65 до t=120) / (среднее значение каждой суммы в интервале от t=65 до t=120 для VAMP-группы)] * 100}. Среднее значение процента устранения, а также среднюю квадратичную погрешность рассчитывали для каждой группы, получающей дозу, с применением GraphPad Prism V5.04.
Результаты: соединение 76, вводимое в дозах 0,1 мг/кг, 0,3 мг/кг, 0,56 мг/кг, 1 мг/кг, 3 мг/кг и 10 мг/кг, и VU0467154, вводимое в дозе 10 мг/кг, устраняли индуцированную амфетамином гиперлокомоцию со значениями процента устранения, составляющими 8,1%, 32,8%, %, 25,6%, 50,7%, 44,3%, 62,8% и 58,9% соответственно. Данные приведены на фигуре 2.
Выводы: системное введение соединения 76, являющегося РАМ М4, вызвало значительное и длительное устранение индуцированной амфетамином гиперлокомоции в аналогичной степени, что и сравниваемое соединение VU0467154, являющееся РАМ М4, при 10 мг/кг р.о., свидетельствуя о том, что такие соединения обладают антипсихотик-подобными эффектами в данной животной модели.
Пример 12. Вторичная фармакология и токсичность in vitro
Соединение 76 тестировали с применением LeadProfilingScreen® от Eurofins, который выявляет потенциальную неблагоприятную активность, дополнительную неожиданную активность и относительную селективность и специфичность. Скрининг включает 68 первичных молекулярных мишеней, включая несколько мишеней ЦНС, рекомендованных ЕМЕА для оценки способности вызывать лекарственную зависимость. Соединение 76 характеризовалось <50% ингибирования каждой мишени в LeadProfilingScreen® при 10 мкМ (связывание), за исключением аденозина А2а человека (50% ингибирования при 10 мкМ).
Соединение 76 дополнительно тестировали с использованием теста Эймса от Eurofins. Тест Эймса является широко применяемым анализом на бактериях для идентификации соединений, которые могут вызывать генные мутации, и он демонстрирует высокий уровень прогностичности в тестах на канцерогенность у грызунов. В тесте Эймса применялось четыре штамма Salmonella с предсуществующими мутациями, которые лишили бактерии способности синтезировать незаменимую аминокислоту гистидин и в результате способности расти в среде без гистидина. Если соединение вызывает мутации в этих конкретных генах, оно может восстановить функцию гена, позволяя клеткам восстановить способность синтезировать гистидин и следовательно расти в его отсутствии ("анализ на индукцию обратных мутаций"). Соединение 76 в количестве 5-100 мкМ успешно прошло тестирование в ходе данного анализа.
Наконец, соединение 76 тестировали посредством проведения анализа на цитотоксичность у бактерий. Соединение 76 в количестве 0,6-100 мкМ успешно прошло тестирование в ходе данного анализа.
Пример 13. Метаболизм и фармакокинетика лекарственного средства in vitro
Соединение 76 подвергали нескольким анализам in vitro для изучения как метаболизма, так и фармакокинетики. Данные анализы проводили в соответствии с известными способами, описанными в общих чертах в следующих ссылках: Conde-Ceide et al. ACS Med. Chem. Lett. 2015, 6, 716-720; Morris et al. J. Med. Chem. 2014, 57, 10192-10197; и Bubser et al. ACS Chem. Neurosci. 2014, 5, 920-942. Результаты представлены в таблице 11.


Пример 14. Метаболизм и фармакокинетика лекарственного средства in vivo
Соединение 76 подвергали нескольким анализам in vivo для изучения как метаболизма, так и фармакокинетики. Результаты представлены в таблице 12.


Следует понимать, что вышеизложенное подробное описание и сопутствующие примеры являются только иллюстративными и не должны рассматриваться как ограничивающие объем настоящего изобретения, который определяется только прилагаемой формулой изобретения и ее эквивалентами.
Различные изменения и модификации в отношении раскрытых вариантов осуществления будут очевидны специалистам в данной области техники. Такие изменения и модификации, включая без ограничения те, которые относятся к химическим структурам, заместителям, производным, промежуточным соединениям, синтезу, композициям, составам или способам применения изобретения, можно осуществлять без отклонения от их сущности и объема.
Реферат
Изобретение относится к трициклическим соединениям формулы (I), а также их фармацевтически приемлемым солям. Технический результат: получены новые соединения, а также фармацевтические композиции на их основе и способы лечения неврологического и/или психического расстройства, ассоциированного с нарушением функции мускаринового ацетилхолинового рецептора. 3 н. и 18 з.п. ф-лы, 11 табл., 12 пр., 2 ил.
Формула

Документы, цитированные в отчёте о поиске
Замещенные гидрированные тиено-пирроло [3,2-c] пиридины, лиганды, фармацевтическая композиция и способ их применения

Комментарии