Замещенные производные гуанидина - RU2733951C9
Код документа: RU2733951C9
Описание
ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящее изобретение относится к замещенным производным гуанидина, содержащей их фармацевтической композиции и конкретным замещенным производным гуанидина и содержащей их фармацевтической композиции для лечения заболеваний, предотвращаемых, облегчаемых и/или излечиваемых с помощью ингибирования VAP-1.
УРОВЕНЬ ТЕХНИКИ
[0002] Диабет типа 2 относится к типу болезней образа жизни, причем число пациентов с этим заболеванием в последние годы продолжает увеличиваться. Длительное гипергликемическое состояние постепенно разрушает микрососуды по всему телу, что приводит к риску причинения серьезного ущерба различным органам, включая глаза и почки. Серьезные повреждения таких типов называются диабетическими осложнениями, и при этом важными задачами становятся предотвращение начала и ингибирование прогрессирования трех основных диабетических осложнений, а именно диабетической невропатии, диабетической ретинопатии и диабетической нефропатии.
[0003] Хотя предотвращение начала и ингибирование прогрессирования диабетических осложнений в первую очередь основаны на контроле уровня глюкозы в крови, в последние годы у пациентов с диабетом наблюдали увеличение активности VAP-1 (белок сосудистой адгезии-1, также называемый семикарбазид-чувствительной аминоксидазой (SSAO)) в крови и ее корреляцию с уровнями гликозилированного гемоглобина в плазме. Этот фермент, который селективно расположен в сосудистой ткани, катализирует дезаминирование метиламина и аминоацетона, продуцируя, соответственно, формальдегид и метилглиоксаль в добавок к H2O2 и аммиаку. Поскольку каждое из этих веществ обладает цитотоксичностью, повышение уровня в VAP-1 в крови привлекает внимание как одна из причин начала воспалительных заболеваний или диабетических осложнений (смотри, например, непатентные документы 1 и 2).
[0004] На сегодняшний день сообщалось о различных ингибиторах фермента VAP-1. Описано, что соединение следующей формулы:

обладает активностью ингибирования VAP-1 и полезно для предотвращения и/или лечения связанных с VAP-1 заболеваний, включая воспалительные заболевания и диабетические осложнения различных типов и, в частности, диабетическую нефропатию или диабетический макулярный отек (смотри, например, патентный документ 1).
[0005] Кроме того, описано, что соединение следующей формулы:
обладает активностью ингибирования VAP-1 и полезно для предотвращения и/или лечения связанных с VAP-1 заболеваний, включая воспалительные заболевания и диабетические осложнения различных типов и, в частности, диабетическую нефропатию или диабетический макулярный отек (смотри, например, патентный документ 2).
[0006] С другой стороны, также сообщалось, что экспрессия VAP-1 увеличивается в печени пациентов с хроническим заболеванием печени, что концентрация растворимого VAP-1 в сыворотке и экспрессия VAP-1 в печени пациентов с неалкогольной жировой болезнью печени увеличиваются по сравнению с пациентами, не имеющими неалкогольной жировой болезни печени, и что существует корреляция между концентрацией растворимого VAP-1 в сыворотке и тяжестью фиброза на основании биопсии печени, осуществленной у пациентов с неалкогольной жировой болезнью печени (смотри, например, непатентный документ 3). По этой причине ожидается, что помимо вышеупомянутых диабетических осложнений ингибирование VAP-1 будет предотвращать, облегчать и/или излечивать неалкогольную жировую болезнь печени и особенно неалкогольный стеатогепатит.
ДОКУМЕНТЫ ПРЕДШЕСТВУЮЩЕГО УРОВНЯ ТЕХНИКИ
Патентные документы
[0007] Патентный документ 1: Международная публикация № WO 2011/034078
Патентный документ 2: Международная публикация № WO 2012/124696
Непатентные документы
[0008] Непатентный документ 1: Diabetologia (1997), 40: 1243-1250
Непатентный документ 2: Diabetologia (2002), 45: 1255-1262
Непатентный документ 3: The Journal of Clinical Investigation (2015), 2: 501-520
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Проблемы, решаемые изобретением
[0009] Настоящее изобретение предлагает полезное новое соединение для лечения заболеваний, предотвращаемых, облегчаемых и/или излечиваемых с помощью ингибирования VAP-1, и содержащую его фармацевтическую композицию.
Средства решения проблем
[0010] В результате проведения обширных исследований соединений, обладающих активностью ингибирования VAP-1, авторы настоящего изобретения обнаружили, что ряд замещенных производных гуанидина или их солей, имеющих оксимную структуру (=N-O-) в своей молекуле, обладают превосходной активностью ингибирования VAP-1 и полезны для лечения заболеваний, предотвращаемых, облегчаемых и/или излечиваемых с помощью ингибирования VAP-1, и особенно диабетической нефропатии и неалкогольного стеатогепатита, что приводит к выполнению настоящего изобретения.
[0011] Настоящее изобретение предлагает следующие изобретения с [1] по [34].
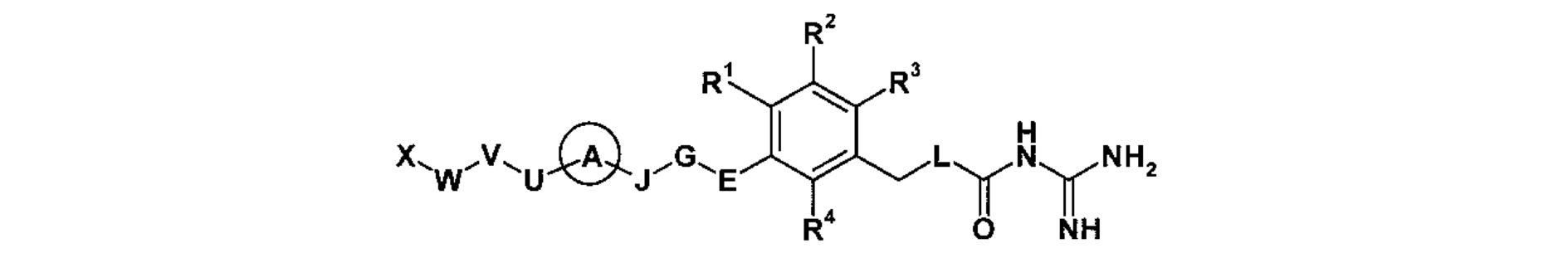
[1] Соединение общей формулы (I):

в котором
R1 представляет атом водорода, защитную группу, необязательно замещенную C1-C6 алкильную группу, необязательно замещенную C2-C6 алкенильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкокси-C1-C6 алкильную группу, -CONR11R12, необязательно замещенную гетероциклильную группу, необязательно замещенную гетероциклил-C1-C6 алкильную группу, необязательно замещенную арильную группу или необязательно замещенную C7-C16 аралкильную группу, и
X представляет N или C-R2,
причем R2 представляет атом водорода, атом галогена, необязательно замещенную C1-C6 алкильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкоксигруппу или цианогруппу, и
p и q, независимо друг от друга, представляют натуральное число от 1 до 3 при условии, что сумма p и q представляет собой натуральное число от 2 до 4,
причем термин "замещенный" означает замещенный по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, C1-C6 алкильной группы, C1-C6 алкоксигруппы, C1-C6 алкокси-C1-C6 алкильной группы, R13O-C1-C6 алкильной группы, галоген-C1-C6 алкильной группы, C7-C16 аралкильной группы, C1-C7 ацильной группы, цианогруппы, оксогруппы, -CONR11R12, -OR13, -COOR14, -NR15R16 и -S(O)nR17,
R11 и R12 независимо представляют атом водорода или C1-C6 алкильную группу, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R14 представляет атом водорода или C1-C6 алкильную группу, R15 и R16 независимо представляют атом водорода, C1-C6 алкильную группу, C7-C16 аралкильную группу, C1-C7 ацильную группу, -COOR14 или -S(O)nR17, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2;
или его фармакологически приемлемая соль.
[2] Соединение, описанное в [1], общей формулы (II):

в котором
R1 представляет атом водорода, защитную группу, необязательно замещенную C1-C6 алкильную группу, необязательно замещенную C2-C6 алкенильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкокси-C1-C6 алкильную группу, -CONR11R12, необязательно замещенную гетероциклильную группу, необязательно замещенную гетероциклил-C1-C6 алкильную группу, необязательно замещенную арильную группу или необязательно замещенную C7-C16 аралкильную группу, и
p и q, независимо друг от друга, представляют натуральное число от 1 до 3 при условии, что сумма p и q представляет собой натуральное число от 2 до 4,
причем термин "замещенный" означает замещенный по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, C1-C6 алкильной группы, C1-C6 алкоксигруппы, C1-C6 алкокси-C1-C6 алкильной группы, R13O-C1-C6 алкильной группы, галоген-C1-C6 алкильной группы, C7-C16 аралкильной группы, C1-C7 ацильной группы, цианогруппы, оксогруппы, -CONR11R12, -OR13, -COOR14, -NR15R16 и -S(O)nR17,
R11 и R12 независимо представляют атом водорода или C1-C6 алкильную группу, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R14 представляет атом водорода или C1-C6 алкильную группу, R15 и R16 независимо представляют атом водорода, C1-C6 алкильную группу, C7-C16 аралкильную группу, C1-C7 ацильную группу, -COOR14 или -S(O)nR17, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2;
или его фармакологически приемлемая соль.
[3] Соединение, описанное в [2], или его фармакологически приемлемая соль, в которых R1 представляет атом водорода, необязательно замещенную C1-C6 алкильную группу, C2-C6 алкенильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкокси-C1-C6 алкильную группу или необязательно замещенную гетероциклильную группу,
причем термин "замещенный" означает замещенный по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13 и -S(O)nR17, и
R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2.
[4] Соединение, описанное в [3], или его фармакологически приемлемая соль, в которых p и q представляют 1.
[5] Соединение, описанное в [4], или его фармакологически приемлемая соль, в которых R1 представляет C1-C4 алкильную группу, или C1-C4 алкильную группу, замещенную по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома фтора и гидроксильной группы.
[6] Соединение, описанное в [1], общей формулы (III):
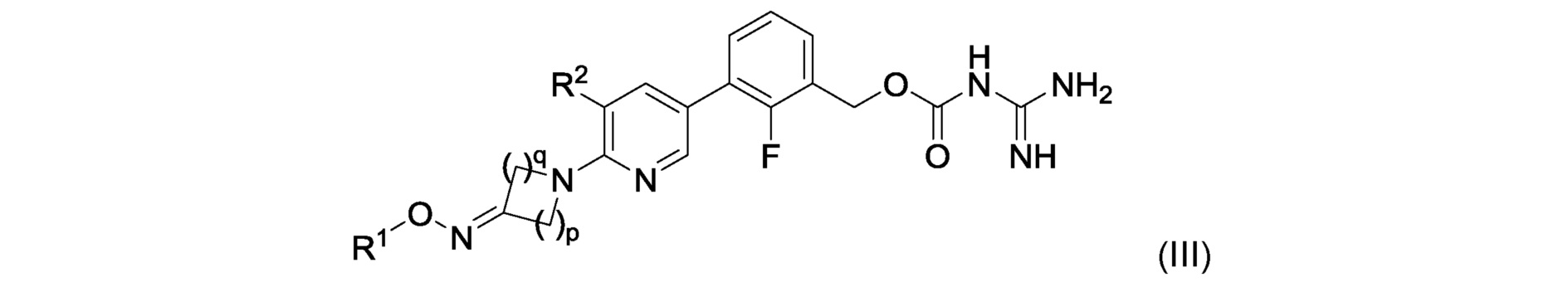
в котором
R1 представляет атом водорода, защитную группу, необязательно замещенную C1-C6 алкильную группу, необязательно замещенную C2-C6 алкенильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкокси-C1-C6 алкильную группу, -CONR11R12, необязательно замещенную гетероциклильную группу, необязательно замещенную гетероциклил-C1-C6 алкильную группу, необязательно замещенную арильную группу или необязательно замещенную C7-C16 аралкильную группу, и
R2 представляет атом водорода, атом галогена, необязательно замещенную C1-C6 алкильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкоксигруппу или цианогруппу, и
p и q, независимо друг от друга, представляют натуральное число от 1 до 3 при условии, что сумма p и q представляет собой натуральное число от 2 до 4,
причем термин "замещенный" означает замещенный по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, C1-C6 алкильной группы, C1-C6 алкоксигруппы, C1-C6 алкокси-C1-C6 алкильной группы, R13O-C1-C6 алкильной группы, галоген-C1-C6 алкильной группы, C7-C16 аралкильной группы, C1-C7 ацильной группы, цианогруппы, оксогруппы, -CONR11R12, -OR13, -COOR14, -NR15R16 и -S(O)nR17,
R11 и R12 независимо представляют атом водорода или C1-C6 алкильную группу, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R14 представляет атом водорода или C1-C6 алкильную группу, R15 и R16 независимо представляют атом водорода, C1-C6 алкильную группу, C7-C16 аралкильную группу, C1-C7 ацильную группу, -COOR14 или -S(O)nR17, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2;
или его фармакологически приемлемая соль.
[7] Соединение, описанное в [6], или его фармакологически приемлемая соль, в которых R1 представляет атом водорода, необязательно замещенную C1-C6 алкильную группу, C2-C6 алкенильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкокси-C1-C6 алкильную группу или необязательно замещенную гетероциклильную группу,
причем термин "замещенный" означает замещенный по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13 и -S(O)nR17,
R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2.
[8] Соединение, описанное в [7], или его фармакологически приемлемая соль, в которых R2 представляет атом галогена.
[9] Соединение, описанное в [8], или его фармакологически приемлемая соль, в которых R2 представляет атом фтора.
[10] Соединение, описанное в [9], или его фармакологически приемлемая соль, в которых p и q представляют 1.
[11] Соединение, описанное в [10], или его фармакологически приемлемая соль, в которых R1 представляет C1-C4 алкильную группу, или C1-C4 алкильную группу, замещенную по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома фтора и гидроксильной группы.
[12] Соединение, описанное в [1], или его фармакологически приемлемая соль, в которых данное соединение представляет собой:
2-фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
3-{2-[3-(этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
3-{2-{3-[(2,2-дифторэтокси)имино]азетидин-1-ил}пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(2,2,2-трифторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(3-фторпропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[3-({4-[(тетрагидропиран-2-ил)окси]бутокси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(2-метоксиэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]метилпивалат,
1-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-3-метоксипропан-2-илацетат,
4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутан-1,2-диилдиацетат,
2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилацетат,
2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилпропионат,
2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилбутират,
2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилбензоат,
2-фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{6-[3-(метоксиимино)азетидин-1-ил]-5-метилпиридин-3-ил}бензилкарбамимидоилкарбамат,
3-{5-циано-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат,
3-{5-хлор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат,
3-{5-(дифторметил)-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат,
3-{5-(циклопропил)-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат,
3-{5-этил-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-{6-[3-(метоксимино)азетидин-1-ил]-5-(метоксиметил)пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{5-метокси-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-(метоксимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
3-{2-[4-(этоксиимино)пиперидин-1-ил]пиридимин-5-ил}-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-(изопропоксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-(пропоксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
3-(2-{4-[(аллилокси)имино]пиперидин-1-ил}пиридимин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-({2-[(тетрагидропиран-2-ил)окси]этокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(2-метоксиэтокси)имино]пиперидин-1-ил}пиридимин-5-ил)бензилкарбамимидоилкарбамат,
2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этилацетат,
(E/Z)-2-фтор-3-{2-[3-(метоксиимино)пирролидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[3-(гидроксимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(2-гидроксиэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(3-гидроксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(4-гидроксибутокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[2-(2-гидроксиэтокси)этокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[3-фтор-2-(гидроксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(4-гидрокси-3-метоксибутокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилацетат,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилпропионат,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилбутират,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилизобутират,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилпивалат,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилгексаноат,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилбензоат,
2-фтор-3-{5-(2-гидроксипропан-2-ил)-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(2-гидроксиэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(3-гидроксипропокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(4-гидроксибутокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(3-гидрокси-2,2-диметилпропокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(3-гидрокси-3-метилбутокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(2-гидроксипропокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(3-гидрокси-2-метилпропокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[3-гидрокси-2-(гидроксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-(2-{3-[(2,3-дигидроксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
3-(2-{3-[(3,4-дигидроксибутокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
3-(6-{3-[(3,4-дигидроксибутокси)имино]азетидин-1-ил}-5-фторпиридин-3-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-{5-фтор-6-[3-{[3-гидрокси-2-(гидроксиметил)пропокси]имино}азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[3-гидрокси-2-(гидроксиметил)пропокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[3-гидрокси-2-(гидроксиметил)-2-метилпропокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-(2-{4-[(2,3-дигидроксипропокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[3-гидрокси-2-(метоксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(3-гидрокси-2-метоксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(2-фтор-3-гидроксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(5-фтор-6-{3-[(2-фтор-3-гидроксипропокси)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(2-гидрокси-3-метоксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-(гидроксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{5-фтор-6-[3-(гидроксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат,
трет-бутил-2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]ацетат,
2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]уксусную кислоту,
3-[2-(3-{[(диметилкарбамоил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[2-(метиламино)-2-оксоэтокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-(2-{3-[(3-амино-3-оксопропокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[3-(метиламино)-3-оксопропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
этил-4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутаноат,
4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутановую кислоту,
2-фтор-3-[2-(3-{[4-(метиламино)-4-оксобутокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(3-{[2-(диметиламино)этокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
3-{2-[3-{{2-[бензил(метил)амино]этокси}имино}азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат,
3-[2-(3-{[3-(ацетамидо-2-(гидроксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
3-[2-(3-{[3-(диметиламино)-2-(гидроксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
3-(2-{3-[(3-ацетамидо-2-метоксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[2-(пиперидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(морфолиноэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
3-[2-(3-{[2-(азетидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
3-[2-(3-{[2-(3,3-дифторазетидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[2-(3-фторазетидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[2-(3-метоксиазетидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[(4-метилморфолин-2-ил)метокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(3-{[(4-ацетилморфолин-2-ил)метокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[(5-оксотетрагидрофуран-2-ил)метокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]циклобутилацетат,
2-фтор-3-(2-{3-[(3-гидроксициклобутокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
3-(2-{3-[(бензилокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[(4-метоксибензил)окси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[(1-метилазетидин-3-ил)окси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(3-{[(1-ацетилазетидин-3-ил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
3-[2-(3-{[(1-бензилазетидин-3-ил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-{2-{3-({[1-(2,2,2-трифторэтил)азетидин-3-ил]окси}имино)азетидин-1-ил}пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[3-({[1-(метилсульфонил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
3-[2-(3-{[(1-этилазетидин-3-ил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
метил-3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-карбоксилат,
2-фтор-3-(2-{3-[(оксетан-3-илокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-{3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-ил}этилацетат,
2-фтор-3-{2-[3-({[1-(2-гидроксиэтил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[3-({[1-(2-метоксиэтил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[3-({[1-(2-фторэтил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
этил-3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]пропаноат,
3-(2-{4-[(3-амино-3-оксопропокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[3-(метиламино)-3-оксопропокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
этил-4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]бутаноат,
4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]бутановую кислоту,
3-[2-(4-{[3-(диметиламино)-3-оксопропокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
3-(2-{4-[(2-ацетамидоэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(N-метилацетамидо)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(N-метилметилсульфонамидо)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(метилсульфонамидо)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(4-{[2-(диметиламино)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(метиламино)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-(2-{4-[(2-аминоэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
3-(2-{4-[(2-цианоэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
3-(2-{4-[(3-цианопропокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(метилсульфонил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[3-(метилсульфонил)пропокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[1-(метил-1H-пиразол-3-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(4-{[(1H-пиразол-3-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-({[1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
3-[2-(4-{[(1H-пиразол-4-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[1-(метил-1H-пиразол-4-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(4-{[2-(1H-пиразол-1-ил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(пиридин-4-илметокси)имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(4-{[2-(2,5-диоксопирролидин-1-ил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(2-оксопирролидин-1-ил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(2-оксооксазолидин-3-ил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(3-оксоморфолино)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-(феноксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(пиримидин-5-илокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат или
2-фтор-3-(2-{4-[(пиримидин-2-илокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат.
[13] 2-фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат или его фармакологически приемлемая соль.
[14] 3-{2-[3-(этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат или его фармакологически приемлемая соль.
[15] 2-фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат или его фармакологически приемлемая соль.
[16] 2-фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил}бензилкарбамимидоилкарбамат или его фармакологически приемлемая соль.
[17] 2-фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат или его фармакологически приемлемая соль.
[18] 2-фтор-3-{5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил}бензилкарбамимидоилкарбамат или его фармакологически приемлемая соль.
[19] 3-(6-{3-[(3,4-дигидроксибутокси)имино]азетидин-1-ил}-5-фторпиридин-3-ил)-2-фторбензилкарбамимидоилкарбамат или его фармакологически приемлемая соль.
[20] 2-фтор-3-{5-фтор-6-[3-{[гидрокси-2-(гидроксиметил)пропокси]имино}азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат или его фармакологически приемлемая соль.
[21] 2-фтор-3-(2-{3-[(2-фтор-3-гидроксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат или его фармакологически приемлемая соль.
[22] 3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]циклобутилацетат или его фармакологически приемлемая соль.
[23] 2-фтор-3-(2-{3-[(3-гидроксициклобутокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат или его фармакологически приемлемая соль.
[24] 2-фтор-3-{2-[3-({[1-(метилсульфонил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат или его фармакологически приемлемая соль.
[25] 2-фтор-3-(2-{3-[(оксетан-3-илокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат или его фармакологически приемлемая соль.
[26] Соединение, описанное в любом из с [1] по [25], или его фармакологически приемлемая соль, в которых фармакологически приемлемая соль представляет собой соль органической кислоты.
[27] Соединение, описанное в любом из с [1] по [25], или его фармакологически приемлемая соль, в которых фармакологически приемлемая соль представляет собой соль дикарбоновой кислоты.
[28] Фармацевтическая композиция, содержащая соединение, описанное в любом из с [1] по [27], или его фармакологически приемлемую соль и фармакологически приемлемую добавку по меньшей мере одного типа.
[29] Фармацевтическая композиция, описанная в [28], для лечения заболевания, предотвращаемого, облегчаемого и/или излечиваемого с помощью ингибирования VAP-1.
[30] Фармацевтическая композиция, описанная в [29], причем заболевание представляет собой диабетическую нефропатию.
[31] Фармацевтическая композиция, описанная в [29], причем заболевание представляет собой неалкогольный стеатогепатит.
[32] Соединение, описанное в любом из с [1] по [27], или его фармакологически приемлемая соль для применения в лечении заболевания, предотвращаемого, облегчаемого и/или излечиваемого с помощью ингибирования VAP-1.
[33] Соединение, описанное в любом из с [1] по [27], или его фармакологически приемлемая соль для получения лекарственного средства для лечения заболевания, предотвращаемого, облегчаемого и/или излечиваемого с помощью ингибирования VAP-1.
[34] Способ лечения заболевания, предотвращаемого, облегчаемого и/или излечиваемого с помощью ингибирования VAP-1, который включает в себя введение терапевтически эффективного количества соединения, описанного в любом из с [1] по [27], или его фармакологически приемлемой соли нуждающемуся в этом пациенту.
Эффекты изобретения
[0012] Поскольку соединение настоящего изобретения общей формулы (I) или его фармакологически приемлемая соль обладают высокой активностью ингибирования VAP-1 и превосходными фармакокинетическими свойствами, они полезны в лечении заболевания, предотвращаемого, облегчаемого и/или излечиваемого с помощью ингибирования VAP-1, и обычно неалкогольных жировых заболеваний печени, таких как неалкогольный стеатогепатит, воспалительных заболеваний, таких как атопический дерматит или псориаз, диабетических осложнений, таких как диабетическая невропатия, диабетическая ретинопатия (и в частности диабетический макулярный отек) или диабетическая нефропатия, сосудистых заболеваний, таких как атеросклероз, заболеваний сердца, таких как инфаркт миокарда, и метаболических заболеваний, таких как ожирение.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0013] Значения терминов, используемых в настоящих описании и формуле изобретения, поясняются ниже. Термины, используемые в настоящих описании и формуле изобретения, имеют значения, указанные ниже, если специально не указано иное.
[0014] В настоящем описании числовые диапазоны, обозначенные символом "-", обозначают диапазон, который включает в себя значения, указанные до и после символа "-", в качестве минимального и максимального значений этого диапазона, соответственно.
[0015] В настоящем изобретении соединение общей формулы (I) включает его изотопные изомеры. А именно, все или часть атомов соединения общей формулы (I) могут быть замещены соответствующими изотопными атомами. Изотопный атом означает атом, имеющий другое массовое число, чем массовое число, встречающееся в природе. Примеры таких изотопных атомов включают атомы водорода (2H,3H), атомы углерода (13C,14C), атомы азота (15N) и атомы кислорода (17O,18O). В частности, атомы дейтерия (2H) могут быть представлены как "D". В таких случаях в соединении общей формулы (I), все атомы водорода в конкретных положениях, обозначенных D, замещены атомами дейтерия, и указывают на молекулярный вес, который отличается от молекулярного веса, рассчитанного по массовым числам, встречающимся в природе.
[0016] "Атом галогена" или "галоген" обозначает атом фтора, атом хлора, атом брома или атом йода либо отдельно, либо в комбинации с другими группами.
[0017] "C1-C6 алкильная группа" обозначает одновалентную группу линейного или разветвленного насыщенного алифатического углеводорода, содержащую 1-6 атомов углерода, либо отдельно, либо в комбинации с другими группами. Примеры C1-C6 алкильных групп включают метильную группу, этильную группу, пропильную группу, бутильную группу, пентильную группу и гексильную группу (включая различные их изомеры). Предпочтительным аспектом C1-C6 алкильной группы является C1-C4 алкильная группа, и ее примеры включают метильную группу, этильную группу, пропильную группу, изопропильную группу, бутильную группу, изобутильную группу, втор-бутильную группу и трет-бутильную группу.
[0018] "C1-C6 алкоксигруппа" обозначает группу -O-R4 (где R4 представляет вышеупомянутую C1-C6 алкильную группу) либо отдельно, либо в комбинации с другими группами. Примеры C1-C6 алкоксигрупп включают метоксигруппу, этоксигруппу, пропоксигруппу, бутилоксигруппу, пентилоксигруппу и гексилоксигруппу (включая различные их изомеры). Предпочтительным аспектом C1-C6 алкоксигруппы является C1-C4 алкоксигруппа, и ее примеры включают метоксигруппу, этоксигруппу, пропоксигруппу, изопропоксигруппу, бутилоксигруппу, изобутилоксигруппу, втор-бутилоксигруппу и трет-бутилоксигруппу.
[0019]"C1-C6 алкокси-C1-C6 алкильная группа" обозначает вышеупомянутую C1-C6 алкильную группу, замещенную вышеупомянутой C1-C6 алкоксигруппой. Примеры C1-C6 алкокси-C1-C6 алкильных групп включают метоксиметильную группу, этоксиметильную группу, пропоксиметильную группу, бутилоксиметильную группу, пентилоксиметильную группу, гексилоксиметильную группу, метоксиэтильную группу, этоксиэтильную группу, пропоксиэтильную группу, бутилоксиэтильную группу, пентилоксиэтильную группу, гексилоксиэтильную группу, метоксипропильную группу, этоксипропильную группу, пропоксипропильную группу и бутоксибутильную группу (включая различные их изомеры). Предпочтительным аспектом C1-C6 алкокси-C1-C6 алкильной группы является C1-C4 алкокси-C1-C4 алкильная группа, и ее примеры включают метоксиметильную группу, этоксиметильную группу, 2-метоксиэтильную группу, 2-этоксиэтильную группу, 3 -метоксипропильную группу, 2-метоксипропильную группу и 3-метоксибутильную группу.
[0020] "Галоген-C1-C6 алкильная группа" обозначает вышеупомянутую C1-C6 алкильную группу, замещенную по меньшей мере одним из вышеупомянутых одинаковых или различных атомов галогенов. Примеры галоген-C1-C6 алкильных групп включают линейные или разветвленные галоген-C1-C6 алкильные группы, такие как фторметильная группа, хлорметильная группа, бромметильная группа, дифторметильная группа, дихлорметильная группа, дибромметильная группа, трифторметильная группа, трихлорметильная группа, трибромметильная группа, 2-фторэтильная группа, 2-хлорэтильная группа, 2-бромэтильная группа, 2,2-дифторэтильная группа, 2,2-дихлорэтильная группа, 2,2-дибромэтильная группа, 2,2,2-трифторэтильная группа, 2,2,2-трихлорэтильная группа, 2,2,2-трибромэтильная группа, пентафторэтильная группа, пентахлорэтильная группа, пентабромэтильная группа, 3-фторпропильная группа, 3-хлорпропильная группа, 3-бромпропильная группа или 2,3-дифторпропильная группа.
[0021] "C3-C8 циклоалкильная группа" обозначает одновалентную группу циклического насыщенного алифатического углеводорода, содержащую 3-8 атомов углерода. Примеры C3-C8 циклоалкильных групп включают циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу, циклогептильную группу и циклооктильную группу. Предпочтительным аспектом C3-C8 циклоалкильной группы является C3-C6 циклоалкильная группа, и ее примеры включают циклопропильную группу, циклобутильную группу, циклопентильную группу и циклогексильную группу.
[0022] "C2-C6 алкенильная группа" обозначает одновалентную группу линейного или разветвленного ненасыщенного алифатического углеводорода, содержащую 2-6 атомом углерода и содержащую по меньшей мере одну двойную связь. Примеры C2-C6 алкенильных групп включают винильную группу, аллильную группу, изопропенильную группу, 1-бутенильную группу, 2-бутенильную группу, 1,3-бутадиенильную группу и 2-пентенильную группу. Предпочтительным аспектом C2-C6 алкенильной группы является C2-C4 алкенильная группа, и ее примеры включают винильную группу, аллильную группу, изопропенильную группу, 1-бутенильную группу, 2-бутенильную группу и 1,3-бутадиенильную группу.
[0023] "Арильная группа" обозначает одновалентную группу ароматического углеводород, содержащую 6-10 атомов углерода. Примеры арильных групп включают фенильную группу, 1-нафтильную группу и 2-нафтильную группу.
[0024] "C7-C16 аралкильная группа" обозначает вышеупомянутую C1-C6 алкильную группу, замещенную вышеупомянутой арильной группой. Примеры C7-C16 аралкильных групп включают бензильную группу, 1-фенилэтильную группу, 2-фенилэтильную группу, 1-нафтилметильную группу и 2-нафтилметильную группу.
[0025] "Гетероциклильная группа" обозначает одновалентную группу 4-7-членного насыщенного, частично ненасыщенного или ненасыщенного моноциклического гетероцикла, содержащую от одного до четырех гетероатомов, независимо выбранных из группы, состоящей из атома азота, атома кислорода и атома серы, или одновалентную группу бициклического гетероцикла, полученного конденсацией вышеупомянутого моноциклического гетероцикла с бензолом или циклогексаном. Примеры таких гетероциклильных групп включают группу моноциклического гетероцикла, в том числе азетидинильную группу, пирролидинильную группу, пирролинильную группу, пирролильную группу, пиперидильную группу, пиридильную группу, азепанильную группу, азепинильную группу, имидазолидинильную группу, имидазолинильную группу, имидазолильную группу, пиразолидинильную группу, пиразолинильную группу, пиразолильную группу, пиперазинильную группу, пиразинильную группу, пиримидинильную группу, пиридазинильную группу, триазолильную группу, тетразолильную группу, оксетанильную группу, тетрагидрофурильную группу, фурильную группу, пиранильную группу, тетрагидропиранильную группу, тиенильную группу, тиазолильную группу, изотиазолильную группу, оксазолидинильную группу, оксазолинильную группу, оксазолильную группу, изоксазолидильную группу, изоксазолинильную группу, изоксазолильную группу или морфолинильную группу, и группу бициклического гетероцикла, в том числе индолил, бензофуран, бензотиофен, хинолин, изохинолин, тетрагидрохинолин или тетрагидроизохинолин.
[0026] "Гетероциклил-C1-C6 алкильная группа" обозначает вышеупомянутую C1-C6 алкильную группу, замещенную вышеупомянутой гетероциклильной группой. Примеры гетероциклил-C1-C6 алкильных групп включают 2-(пиперидин-1-ил)этильную группу, 2-морфолиноэтильную группу, 2-(азетидин-1-ил)этильную группу, морфолин-2-илметильную группу, (тетрагидрофуран-2-ил)метильную группу, 1H-пиразол-3-илметильную группу, 1H-пиразол-4-илметильную группу, 2-(1H-пиразол-1-ил)этильную группу, пиридин-4-илметильную группу, пиридин-3-илметильную группу, пиридин-2-илметильную группу, 2-(пирролидин-1-ил)этильную группу, 2-(оксазолидин-3-ил)этильную группу, 2-(3-оксоморфолино)этильную группу и 2-(1H-тетразол-5-ил)этильную группу.
[0027] "C1-C7 ацильная группа" обозначает группу -CO-R5 (где R5 представляет атом водорода, вышеупомянутую C1-C6 алкильную группу или фенильную группу). Примеры C1-C7 ацильной группы включают формильную группу, ацетильную группу, пропионильную группу, бутирильную группу, изобутирильную группу, валерильную группу, изовалерильную группу, пивалоильную группу, гексаноильную группу и бензоильную группу.
[0028] "Защитная группа" обозначает защитную группу гидроксильной группы, и она может быть произвольным образом выбрана средним специалистом в данной области техники из защитных групп гидроксильной группы, описанных в известном уровне техники, например в документе Protective Groups in Organic Synthesis, 4th Edition, T. W. Greene and P. G. M. Wuts, ed., John Wiley & Sons Inc. (2006). Примеры защитных групп гидроксильной группы включают защитные группы на основе ацила, такие как C1-C7 ацильные группы (такие как формильная группа, ацетильная группа, пропионильная группа, бутирильная группа, изобутирильная группа, валерильная группа, изовалерильная группа, пивалоильная группа, гексаноил группа или бензоильная группа), защитные группы на основе ацеталя, такие как метоксиметильная группа, 1-этоксиэтильная группа, метилтиометильная группа, бензилоксиметильная группа, тетрагидропиранильная группа, защитные группы на основе силила, такие как три(C1-C4 алкил)силильная группа (такая как триметилсилильная группа, триэтилсилильная группа, триизопропилсилильная группа, диметилизопропилсилильная группа или трет-бутилдиметилсилильная группа), (C1-C4 алкил)диарилсилильная группа (такая как трет-бутилдифенилсилильная группа или дифенилметилсилильная группа), триарилсилильная группа (такая как трифенилсилильная группа) или трибензилсилильная группа, и защитные группы на основе бензила, такие как бензильная группа, п-метоксибензильная группа или трифенилметильная группа. Примеры предпочтительных аспектов защитных групп включают C1-C7 ацильную группу, тетрагидропиранильную группа, три(C1-C4 алкил)силильную группу, бензильную группа, п-метоксибензильную группу и трифенилметильную группу.
[0029] Кроме того, в случае, когда соединение общей формулы (I) содержит 1,2- или 1,3-диольную структуру, защитная группа может представлять собой циклический ацеталь, который защищает две гидроксильные группы в форме 5-членного или 6-членного циклического соединения. Примеры циклических ацеталей включают метиленацеталь, этилиденацеталь, ацетонид, бензилиденацеталь и п-метоксибензилиденацеталь. В случае, когда R1 замещен двумя группами -OR13, и присутствует 1,2- или 1,3-диольная структура, предпочтительным аспектом защитной группы является ацетонид.
[0030] В настоящем изобретении фраза "необязательно замещенный" обозначает некоторую группу, не замещенную или замещенную по меньшей мере одним заместителем, выбранным из группы указанных заместителей, такой как группа, состоящая из атома дейтерия, атома галогена, C1-C6 алкильной группы, C1-C6 алкоксигруппы, C1-C6 алкокси-C1-C6 алкильной группы, R13O-C1-C6 алкильной группы, галоген-C1-C6 алкильной группы, C7-C16 аралкильной группы, C1-C7 ацильной группы, цианогруппы, оксогруппы, -CONR11R12, -OR13, -COOR14, -NR15R16 и -S(O)nR17 (где R11 и R12 независимо представляют атом водорода или C1-C6 алкильную группу, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R14 представляет атом водорода или C1-C6 алкильную группу, R15 и R16 независимо представляют атом водорода, C1-C6 алкильную группу, C7-C16 аралкильную группу, C1-C7 ацильную группу, -COOR14 или -S(O)nR17, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2).
[0031] В настоящем изобретении предпочтительным аспектом "необязательно замещенной C1-C6 алкильной группы" является (незамещенная) C1-C6 алкильная группа или C1-C6 алкильная группа, замещенная по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, C1-C7 ацильной группы, цианогруппы, оксогруппы, -CONR11R12, -OR13, -COOR14, -NR15R16 и -S(O)nR17 (где R11 и R12 независимо представляют атом водорода или C1-C6 алкильную группу, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R14 представляет атом водорода или C1-C6 алкильную группу, R15 и R16 независимо представляют атом водорода, C1-C6 алкильную группу, C7-C16 аралкильную группу, C1-C7 ацильную группу, -COOR14 или -S(O)nR17, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2). Более предпочтительным аспектом "необязательно замещенной C1-C6 алкильной группы" является (незамещенная) C1-C6 алкильная группа или C1-C6 алкильная группа, замещенная по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, цианогруппы, -CONR11R12, -OR13, -COOR14, -NR15R16 и -S(O)nR17. Еще более предпочтительным аспектом "необязательно замещенной C1-C6 алкильной группы" является (незамещенная) C1-C6 алкильная группа или C1-C6 алкильная группа, замещенная по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13 и -S(O)nR17. Особенно предпочтительным аспектом "необязательно замещенной C1-C6 алкильной группы" является (незамещенная) C1-C6 алкильная группа или C1-C6 алкильная группа, замещенная по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома фтора и гидроксильной группы.
[0032] В настоящем изобретении предпочтительным аспектом "необязательно замещенной C2-C6 алкенильной группы" является (незамещенная) C2-C6 алкенильная группа или C2-C6 алкенильная группа, замещенная по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13 и -S(O)nR17 (где R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2). Более предпочтительным аспектом "необязательно замещенной C2-C6 алкенильной группы" является (незамещенная) C2-C6 алкенильная группа.
[0033] В настоящем изобретении предпочтительным аспектом "необязательно замещенной C3-C8 циклоалкильная группа" является (незамещенная) C3-C8 циклоалкильная группа или C3-C8 циклоалкильная группа, замещенная по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13 и -S(O)nR17 (где R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2). Более предпочтительным аспектом "необязательно замещенной C3-C8 циклоалкильной группы" является (незамещенная) C3-C8 циклоалкильная группа или C3-C8 циклоалкильная группа, замещенная по меньшей мере одной -OR13 группой.
[0034] В настоящем изобретении предпочтительным аспектом "необязательно замещенной C1-C6 алкокси-C1-C6 алкильной группы" является (незамещенная) C1-C6 алкокси-C1-C6 алкильная группа или C1-C6 алкокси-C1-C6 алкильная группа, замещенная по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13, -NR15R16 и -S(O)nR17 (где R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R15 и R16 независимо представляют атом водорода, C1-C6 алкильную группу, C7-C16 аралкильную группу, C1-C7 ацильную группу, -COOR14 или -S(O)nR17, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2). Более предпочтительным аспектом "необязательно замещенной C1-C6 алкокси-C1-C6 алкильной группы" является (незамещенная) C1-C6 алкокси-C1-C6 алкильная группа или C1-C6 алкокси-C1-C6 алкильная группа, замещенная по меньшей мере одним заместителем, выбранным из группы, состоящей из -OR13 и -NR15R16.
[0035] В настоящем изобретении предпочтительные аспекты "необязательно замещенной гетероциклильной группы" и "необязательно замещенной гетероциклил-C1-C6 алкильной группы" состоят из (незамещенной) гетероциклильной группы и (незамещенной) гетероциклил-C1-C6 алкильной группы или гетероциклильной группы и гетероциклил-C1-C6 алкильной группы, в которых гетероциклильный фрагмент замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, C1-C6 алкильной группы, C1-C6 алкоксигруппы, C1-C6 алкокси-C1-C6 алкильной группы, R13O-C1-C6 алкильной группы, галоген-C1-C6 алкильной группы, C7-C16 аралкильной группы, C1-C7 ацильной группы, оксогруппы, -COOR14 и -S(O)nR17 (где R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R14 представляет атом водорода или C1-C6 алкильную группу, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2). Более предпочтительные аспекты "необязательно замещенной гетероциклильной группы" и "необязательно замещенной гетероциклил-C1-C6 алкильной группы" состоят из (незамещенной) гетероциклильной группы и (незамещенной) гетероциклил-C1-C6 алкильной группы или гетероциклильной группы и гетероциклил-C1-C6 алкильной группы, в которых гетероциклильный фрагмент замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из атома галогена и -S(O)nR17.
[0036] В настоящем изобретении предпочтительным аспектом "необязательно замещенной арильной группы" является (незамещенная) арильная группа или арильная группа, замещенная по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13 и -S(O)nR17 (где R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2). Более предпочтительным аспектом "необязательно замещенной арильной группы" является (незамещенная) арильная группа.
[0037] Соединение настоящего изобретения общей формулы (I) включает его стереоизомеры (если такие стереоизомеры существуют). Стереоизомеры обозначают изомеры, имеющие различные пространственные конфигурации атомов, и их примеры включают оптические изомеры, такие как диастереомеры и энантиомеры, и геометрические изомеры. Например, в случае, когда соединение настоящего изобретения общей формулы (I) содержит один или несколько хиральных центров, соединение настоящего изобретения общей формулы (I) может присутствовать в форме оптически чистых энантиомеров, смеси энантиомеров, таких как рацематы, оптически чистые диастереомеры, смесь диастереомеров, рацематы диастереомеров или смесь рацематов диастереомеров. Кроме того, в случае, когда в соединении настоящего изобретения общей формулы (I) присутствует геометрический изомер на основе двойной связи, такой как двойная связь C=C или C=N, соединение настоящего изобретения общей формулы (I) может присутствовать в форме геометрического изомера чистых форм E и Z или смеси геометрических изомеров форм E и Z.
[0038] Примеры фармакологически приемлемых солей соединения настоящего изобретения общей формулы (I) включают соли неорганических кислот, такие как гидрохлориды, гидробромиды, гидройодиды, нитраты, сульфаты или фосфаты, и соли органических кислот, такие как ацетаты, трифторацетаты, бензоаты, оксалаты, малонаты, сукцинаты, малеаты, фумараты, тартраты, цитраты, метансульфонаты, этансульфонаты, трифторметансульфонаты, бензолсульфонаты, п-толуолсульфонаты, глутаматы или аспартаты. Предпочтительные аспекты солей органических кислот состоят из солей дикарбоновых кислот, таких как оксалаты, малонаты, сукцинаты, малеаты, фумараты и тартраты.
[0039] Другие примеры фармакологически приемлемых солей соединения настоящего изобретения общей формулы (I) включают соли металлов, такие как соли натрия, соли калия, соли кальция или соли магния, неорганические соли, такие как соли аммония, и соли органических аминов, такие как соли триэтиламина или соли гуанидина.
[0040] Соединение настоящего изобретения общей формулы (I) или его фармакологически приемлемая соль включают фармакологически приемлемые сольваты. Предпочтительным аспектом сольвата является гидрат. Кроме того, гидрат может представлять собой то, к чему приводит поглощение влаги соединением настоящего изобретения общей формулы (I) или его фармакологически приемлемой солью.
[0041] Соединение настоящего изобретения общей формулы (I) или его фармакологически приемлемая соль могут проявлять кристаллический полиморфизм в случае, если они являются кристаллами. Кристаллический полиморфизм обозначает одно и то же вещество, имеющее разные кристаллические структуры. Все кристаллы или их смеси в любом произвольном отношении включены в настоящее изобретение.
[0042] Ниже приводится подробное объяснение вариантов осуществления настоящего изобретения.
Настоящее изобретение относится к соединению общей формулы (I):

в котором
R1 представляет атом водорода, защитную группу, необязательно замещенную C1-C6 алкильную группу, необязательно замещенную C2-C6 алкенильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкокси-C1-C6 алкильную группу, -CONR11R12, необязательно замещенную гетероциклильную группу, необязательно замещенную гетероциклил-C1-C6 алкильную группу, необязательно замещенную арильную группу или необязательно замещенную C7-C16 аралкильную группу, и X представляет N или C-R2,
причем R2 представляет атом водорода, атом галогена, необязательно замещенную C1-C6 алкильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкоксигруппу или цианогруппу, и
p и q, независимо друг от друга, представляют натуральное число от 1 до 3 при условии, что сумма p и q представляет собой натуральное число от 2 до 4,
причем термин "замещенный" означает замещенный по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, C1-C6 алкильной группы, C1-C6 алкоксигруппы, C1-C6 алкокси-C1-C6 алкильной группы, R13O-C1-C6 алкильной группы, галоген-C1-C6 алкильной группы, C7-C16 аралкильной группы, C1-C7 ацильной группы, цианогруппы, оксогруппы, -CONR11R12, -OR13, -COOR14, -NR15R16 и -S(O)nR17,
R11 и R12 независимо представляют атом водорода или C1-C6 алкильную группу, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R14 представляет атом водорода или C1-C6 алкильную группу, R15 и R16 независимо представляют атом водорода, C1-C6 алкильную группу, C7-C16 аралкильную группу, C1-C7 ацильную группу, -COOR14 или -S(O)nR17, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2;
или его фармакологически приемлемой соли.
[0043] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (I) или его фармакологически приемлемой соли, в которых p и q представляют 1.
[0044] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (I) или его фармакологически приемлемой соли, в которых p представляет 1, и q представляет 2 (или p представляет 2, и q представляет 1).
[0045] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (I) или его фармакологически приемлемой соли, в которых p и q представляют 2.
[0046] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (I) или его фармакологически приемлемой соли, в которых p представляет 1, и q представляет 3 (или p представляет 3, и q представляет 1).
[0047] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (I) или его фармакологически приемлемой соли, в которых R1 представляет атом водорода, защитную группу, C1-C6 алкильную группу (которая может быть замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, цианогруппы, -CONR11R12, -OR13, -COOR14, -NR15R16 и -S(O)nR17), C2-C6 алкенильную группу, C3-C8 циклоалкильную группу (которая может быть замещена по меньшей мере одной группой -OR13), C1-C6 алкокси-C1-C6 алкильную группу (которая может быть замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из -OR13 и -NR15R16), -CONR11R12, гетероциклильную группу или гетероциклил-C1-C6 алкильную группу (в который гетероциклильный фрагмент может быть замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из атома галогена, C1-C6 алкильной группы, C1-C6 алкоксигруппы, C1-C6 алкокси-C1-C6 алкильной группы, R13O-C1-C6 алкильной группы, галоген-C1-C6 алкильной группы, C7-C16 аралкильной группы, C1-C7 ацильной группы, оксогруппы, -COOR14 и -S(O)nR17) или арильную группу; причем R11 и R12 независимо представляют атом водорода или C1-C6 алкильную группу, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R14 представляет атом водорода или C1-C6 алкильную группу, R15 и R16 независимо представляют атом водорода, C1-C6 алкильную группу, C7-C16 аралкильную группу, C1-C7 ацильную группу, -COOR14 или -S(O)nR17, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2.
[0048] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (I) или его фармакологически приемлемой соли, в которых R1 представляет атом водорода, необязательно замещенную C1-C6 алкильную группу, C2-C6 алкенильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкокси-C1-C6 алкильную группу или необязательно замещенную гетероциклильную группу, причем вышеупомянутый термин "замещенный" означает замещенный по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13 и -S(O)nR17, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, и R17 представляет C1-C6 алкильную группу.
[0049] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (I) или его фармакологически приемлемой соли, в которых R1 представляет атом водорода, C1-C6 алкильную группу (которая может быть замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13 и -S(O)nR17), C2-C6 алкенильную группу, C3-C8 циклоалкильную группу (которая может быть замещена по меньшей мере одной группой -OR13), C1-C6 алкокси-C1-C6 алкильную группу (которая может быть замещена по меньшей мере одной группой -OR13) или гетероциклильную группу (в которой гетероциклильный фрагмент может быть замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из атома галогена и -S(O)nR17); причем R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2.
[0050] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (I) или его фармакологически приемлемой соли, в которых R1 представляет C1-C4 алкильную группу или C1-C4 алкильную группу, замещенную по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома фтора и гидроксильной группы.
[0051] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (II) или его фармакологически приемлемой соли.
Общая формула (II):

В общей формуле (II) R1, p и q совпадают с определенными ранее в общей формуле (I).
[0052] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (II) или его фармакологически приемлемой соли, в которых p и q представляют 1.
[0053] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (II) или его фармакологически приемлемой соли, в которых p представляет 1, и q представляет 2 (или p представляет 2, и q представляет 1).
[0054] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (II) или его фармакологически приемлемой соли, в которых p и q представляют 2.
[0055] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (II) или его фармакологически приемлемой соли, в которых p представляет 1, и q представляет 3 (или p представляет 3, и q представляет 1).
[0056] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (II) или его фармакологически приемлемой соли, в которых R1 представляет атом водорода, защитную группу, C1-C6 алкильную группу (которая может быть замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, цианогруппы, -CONR11R12, -OR13, -COOR14, -NR15R16 и -S(O)nR17), C2-C6 алкенильную группу, C3-C8 циклоалкильную группу (которая может быть замещена по меньшей мере одной группой -OR13), C1-C6 алкокси-C1-C6 алкильную группу (которая может быть замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из -OR13 и -NR15R16), -CONR11R12, гетероциклильную группу или гетероциклил-C1-C6 алкильную группу (в которой гетероциклильный фрагмент может быть замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из атома галогена, C1-C6 алкильной группы, C1-C6 алкоксигруппы, C1-C6 алкокси-C1-C6 алкильной группы, R13O-C1-C6 алкильной группы, галоген-C1-C6 алкильной группы, C7-C16 аралкильной группы, C1-C7 ацильной группы, оксогруппы, -COOR14 и -S(O)nR17) или арильную группу; причем R11 и R12 независимо представляют атом водорода или C1-C6 алкильную группу, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R14 представляет атом водорода или C1-C6 алкильную группу, R15 и R16 независимо представляют атом водорода, C1-C6 алкильную группу, C7-C16 аралкильную группу, C1-C7 ацильную группу, -COOR14 или -S(O)nR17, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2.
[0057] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (II) или его фармакологически приемлемой соли, в которых R1 представляет атом водорода, необязательно замещенную C1-C6 алкильную группу, C2-C6 алкенильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкокси-C1-C6 алкильную группу или необязательно замещенную гетероциклильную группу, причем вышеупомянутый термин "замещенный" означает замещенный по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13 и -S(O)nR17, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, и R17 представляет C1-C6 алкильную группу.
[0058] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (II) или его фармакологически приемлемой соли, в которых R1 представляет атом водорода, C1-C6 алкильную группу (которая может быть замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13 и -S(O)nR17), C2-C6 алкенильную группу, C3-C8 циклоалкильную группу (которая может быть замещена по меньшей мере одной группой -OR13), C1-C6 алкокси-C1-C6 алкильную группу (которая может быть замещена по меньшей мере одной группой -OR13) или гетероциклильную группу (в которой гетероциклильный фрагмент может быть замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из атома галогена и -S(O)nR17); причем R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2.
[0059] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (II) или его фармакологически приемлемой соли, в которых R1 представляет C1-C4 алкильную группу или C1-C4 алкильную группу, замещенную по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома фтора и гидроксильной группы.
[0060] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (III) или его фармакологически приемлемой соли.
Общая формула (III):

В общей формуле (III) R1, R2, p и q совпадают с определенными ранее в общей формуле (I).
[0061] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (III) или его фармакологически приемлемой соли, в которых p и q представляют 1.
[0062] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (III) или его фармакологически приемлемой соли, в которых p представляет 1, и q представляет 2 (или p представляет 2, и q представляет 1).
[0063] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (III) или его фармакологически приемлемой соли, в которых p и q представляют 2.
[0064] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (III) или его фармакологически приемлемой соли, в которых p представляет 1, и q представляет 3 (или p представляет 3, и q представляет 1).
[0065] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (III) или его фармакологически приемлемой соли, в которых R2 представляет атом водорода, атом галогена, C1-C6 алкильную группу (которая может быть замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из атома галогена, -OR13 и C1-C6 алкоксигруппы), C3-C8 циклоалкильную группу, C1-C6 алкоксигруппу или цианогруппу, причем R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу.
[0066] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (III) или его фармакологически приемлемой соли, в которых R2 представляет атом водорода, атом фтора, атом хлора, C1-C4 алкильную группу, C1-C4 алкильную группу, замещенную по меньшей мере одним атомом фтора, C1-C4 алкильную группу, замещенную по меньшей мере одной гидроксильной группой, C1-C4 алкильную группу, замещенную по меньшей мере одной защищенной гидроксильной группой, C1-C4 алкильную группу, замещенную по меньшей мере одной C1-C4 алкоксигруппой, C3-C6 циклоалкильную группу, C1-C4 алкоксигруппу или цианогруппу.
[0067] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (III) или его фармакологически приемлемой соли, в которых R2 представляет атом водорода, атом фтора, атом хлора, метильную группу, этильную группу, дифторметильную группу, 2-[(тетрафторпиран-2-ил)окси]пропан-2-ильную группу, 2-гидроксипропан-2-ильную группу, метоксиметильную группу, циклопропильную группу, метоксигруппу или цианогруппу.
[0068] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (III) или его фармакологически приемлемой соли, в которых R2 представляет атом фтора.
[0069] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (III) или его фармакологически приемлемой соли, в которых R1 представляет атом водорода, защитную группу, C1-C6 алкильную группу (которая может быть замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, цианогруппы, -CONR11R12, -OR13, -COOR14, -NR15R16 и -S(O)nR17), C2-C6 алкенильную группу, C3-C8 циклоалкильную группу (которая может быть замещена по меньшей мере одной группой -OR13), C1-C6 алкокси-C1-C6 алкильную группу (которая может быть замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из -OR13 и -NR15R16), -CONR11R12, гетероциклильную группу или гетероциклил-C1-C6 алкильную группу (в которой гетероциклильный фрагмент может быть замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из атома галогена, C1-C6 алкильной группы, C1-C6 алкоксигруппы, C1-C6 алкокси-C1-C6 алкильной группы, R13O-C1-C6 алкильной группы, галоген-C1-C6 алкильной группы, C7-C16 аралкильной группы, C1-C7 ацильной группы, оксогруппы, -COOR14 и -S(O)nR17) или арильную группу; причем R11 и R12 независимо представляют атом водорода или C1-C6 алкильную группу, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R14 представляет атом водорода или C1-C6 алкильную группу, R15 и R16 независимо представляют атом водорода, C1-C6 алкильную группу, C7-C16 аралкильную группу, C1-C7 ацильную группу, -COOR14 или -S(O)nR17, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2.
[0070] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (III) или его фармакологически приемлемой соли, в которых R1 представляет атом водорода, необязательно замещенную C1-C6 алкильную группу, C2-C6 алкенильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкокси-C1-C6 алкильную группу или необязательно замещенную гетероциклильную группу, причем вышеупомянутый термин "замещенный" означает замещенный по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13 и -S(O)nR17, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, и R17 представляет C1-C6 алкильную группу.
[0071] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (III) или его фармакологически приемлемой соли, в которых R1 представляет атом водорода, C1-C6 алкильную группу (которая может быть замещена по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, -OR13 и -S(O)nR17), C2-C6 алкенильную группу, C3-C8 циклоалкильную группу (которая может быть замещена по меньшей мере одной группой -OR13), C1-C6 алкокси-C1-C6 алкильную группу (которая может быть замещена по меньшей мере одной группой -OR13) или гетероциклильную группу (в которой гетероциклильный фрагмент может быть замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из атома галогена и -S(O)nR17); причем R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2.
[0072] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (III) или его фармакологически приемлемой соли, в которых R1 представляет C1-C4 алкильную группу или C1-C4 алкильную группу, замещенную по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома фтора и гидроксильной группы.
[0073] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (III) или его фармакологически приемлемой соли, в которых R1 представляет C1-C4 алкильную группу или C1-C4 алкильную группу, замещенную по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома фтора и гидроксильной группы, и R2 представляет атом фтора.
[0074] В конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (I), (II) или (III) или его фармакологически приемлемой соли, в которых R1 представляет атом водорода, тетрагидропиран-2-ильную группу, трет-бутилдиметилсилильную группу, метильную группу, этильную группу, изопропильную группу, пропильную группу, аллильную группу, 2-метоксиэтильную группу, дейтерированную метильную группу, 2-фторэтильную группу, 2,2-дифторэтильную группу, 2,2,2-трифторэтильную группу, 3-фторпропильную группу, 2-гидроксиэтильную группу, 2-гидроксипропильную группу, 3-гидроксипропильную группу, 3-гидрокси-2-метилпропильную группу, 4-гидроксибутильную группу, 3-гидрокси-3-метилбутильную группу, 3-гидрокси-2,2-диметилпропильную группу, 2,3-дигидроксипропильную группу, 3-гидрокси-2-(гидроксиметил)-пропильную группу, 3-гидрокси-2-(гидроксиметил)-2-метилпропильную группу, 3,4-дигидроксибутильную группу, 3-фтор-2-(гидроксиметил)пропильную группу, 2-фтор-3-гидроксипропильную группу, 3-ацетилокси-2-(гидроксиметил)пропильную группу, 2-(гидроксиметил)-3-пропаноилоксипропильную группу, 3-бутаноилокси-2-(гидроксиметил)пропильную группу, 2-(гидроксиметил)-3-изобутирилоксипропильную группу, 2-(гидроксиметил)-3-пивалоилоксипропильную группу, 3-гексаноилокси-2-(гидроксиметил)пропильную группу, 3-бензоилокси-2-(гидроксиметил)пропильную группу, 3-фтор-2-{[(тетрагидропиран-2-ил)окси]метил}пропильную группу, 2-фтор-3-(тритилокси)пропильную группу, 2-[(тетрагидропиран-2-ил)окси]этильную группу, 2-[(тетрагидропиран-2-ил)окси]пропильную группу, 3-[(тетрагидропиран-2-ил)окси]пропильную группу, 2-метил-3-[(тетрагидропиран-2-ил)окси]пропильную группу, 4-[(тетрагидропиран-2-ил)окси]бутильную группу, 2,2-диметил-3-[(тетрагидропиран-2-ил)окси]пропильную группу, 3-метил-3-[(тетрагидропиран-2-ил)окси]бутильную группу, пивалоилоксиметильную группу, 2-(ацетилокси)этильную группу, 2-(пропаноилокси)этильную группу, 2-(бутаноилокси)этильную группу, 2-(бензоилокси)этильную группу, 3,4-ди(ацетилокси)бутильную группу, 2,2-диметил-1,3-диоксан-5-илметильную группу, 2,2-диметил-1,3-диоксолан-4-илметильную группу, 2-(2,2-диметил-1,3-диоксолан-4-ил)этильную группу, 2,2,5-триметил-1,3-диоксан-5-илметильную группу, 3-ацетилокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропильную группу, 3-пропаноилокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропильную группу, 3-бутаноилокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропильную группу, 3-изобутирилокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропильную группу, 3-пивалоилокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропильную группу, 3-гексаноилокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропильную группу, 3-бензоилокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропильную группу, 2-(2-гидроксиэтокси)этильную группу, 2-гидрокси-3-метоксипропильную группу, 3-гидрокси-2-метоксипропильную группу, 3-гидрокси-2-(метоксиметил)пропильную группу, 4-гидрокси-3-метоксибутильную группу, 2-метокси-3-(тритилокси)пропильную группу, 2-ацетилокси-3-метоксипропильную группу, 2-{2-[(тетрагидропиран-2-ил)окси]этокси}этильную группу, 3-метокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропильную группу или 3-метокси-4-[(тетрагидропиран-2-ил)окси]бутильную группу.
[0075] Кроме того, в конкретном варианте осуществления настоящее изобретение относится к соединению настоящего изобретения общей формулы (I), (II) или (III) или его фармакологически приемлемой соли, в которых R1 представляет 2-трет-бутокси-2-оксоэтильную группу, карбоксиметильную группу, диметилкарбамоильную группу, 2-(метиламино)-2-оксоэтильную группу, 3-амино-3-оксопропильную группу, 3-(метиламино-3-оксопропильную группу, 4-этокси-4-оксобутильную группу, 3-карбоксипропильную группу, 4-(метиламино)-4-оксобутильную группу, 2-(диметиламино)этильную группу, 2-[бензил(метил)амино]этильную группу, 3-ацетамидо-2-{[(тетрагидропиран-2-ил)окси]метил}пропильную группу, 3-ацетамидо-2-(гидроксиметил)пропильную группу, 3-(диметиламино)-2-{[(тетрагидропиран-2-ил)окси]метил}пропильную группу, 3-(диметиламино)-2-(гидроксиметил)пропильную группу, 3-ацетамидо-2-метоксипропильную группу, 2-(пиперидин-1-ил)этильную группу, 2-морфолиноэтильную группу, 2-(азетидин-1-ил)этильную группу, 2-(3,3-дифторазетидин-1-ил)этильную группу, 2-(3-фторазетидин-1-ил)этильную группу, 2-(3-метоксиазетидин-1-ил)этильную группу, (4-метилморфолин-2-ил)метильную группу, (4-ацетилморфолин-2-ил)метильную группу, (5-оксотетрагидрофуран-2-ил)метильную группу, 3-ацетилоксициклобутан-1-ильную группу, 3-гидроксициклобутан-1-ильную группу, бензильную группу, 4-метоксибензильную группу, 1-метилазетидин-3-ильную группу, 1-ацетилазетидин-3-ильную группу, 1-бензилазетидин-3-ильную группу, 1-(2,2,2-трифторэтил)азетидин-3-ильную группу, 1-(метилсульфонил)азетидин-3-ильную группу, 1-этилазетидин-3-ильную группу, 1-(метоксикарбонил)азетидин-3-ильную группу, оксетан-3-ильную группу, 1-[2-(ацетилокси)этил]азетидин-3-ильную группу, 1-(2-гидроксиэтил)азетидин-3-ильную группу, 1-(2-метоксиэтил)азетидин-3-ильную группу, 1-(2-фторэтил)азетидин-3-ильную группу, 3-этокси-3-оксопропильную группу, 3-амино-3-оксопропильную группу, 3-(метиламино)-3-оксопропильную группу, 3-(диметиламино)-3-оксопропильную группу, 2-ацетамидоэтильную группу, 2-(N-метилацетамидо)этильную группу, 2-(N-метилметилсульфонамидо)этильную группу, 2-[N-(трет-бутоксикарбонил)метилсульфонамидо]этильную группу, 2-(метилсульфонамидо)этильную группу, 2-[N-(трет-бутоксикарбонил)(метил)амино]этильную группу, 2-(метиламино)этильную группу, 2-[N-ди(трет-бутоксикарбонил)амино]этильную группу, 2- аминоэтильную группу, 2-цианоэтильную группу, 3-цианопропильную группу, 2-(метилсульфонил)этильную группу, 3-(метилсульфонил)пропильную группу, (1-метил-1H-пиразол-3-ил)метильную группу, [1-(тетрагидропиран-2-ил)-1H-пиразол-3-ил]метильную группу, (1H-пиразол-3-ил)метильную группу, [1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метильную группу, (1H-пиразол-4-ил)метильную группу, (1-метил-1H-пиразол-4-ил)метильную группу, 2-(1H-пиразол-1-ил)этильную группу, пиридин-4-илметильную группу, 2-(2,5-диоксопирролидин-1-ил)этильную группу, 2-(2-оксопирролидин-1-ил)этильную группу, 2-(2-оксооксазолидин-3-ил)этильную группу, 2-(3-оксоморофолино)этильную группу, фенильную группу, пиримидин-5-ильную группу или пиримидин-2-ильную группу.
[0076] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (I) или его фармакологически приемлемой соли, которое представляет собой
2-фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
3-{2-[3-(этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил}бензилкарбамимидоилкарбамат,
3-{2-{3-[(2,2-дифторэтокси)имино]азетидин-1-ил}пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(2,2,2-трифторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(3-фторпропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[3-({4-[(тетрагидропиран-2-ил)окси]бутокси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(2-метоксиэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]метилпивалат,
1-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-3-метоксипропан-2-илацетат,
4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутан-1,2-диилдиацетат,
2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилацетат,
2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилпропионат,
2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилбутират,
2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилбензоат,
2-фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{6-[3-(метоксиимино)азетидин-1-ил]-5-метилпиридин-3-ил}бензилкарбамимидоилкарбамат,
3-{5-циано-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат,
3-{5-хлор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат,
3-{5-(дифторметил)-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат,
3-{5-(циклопропил)-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат,
3-{5-этил-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-{6-[3-(метоксимино)азетидин-1-ил]-5-(метоксиметил)пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{5-метокси-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-(метоксимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
3-{2-[4-(этоксиимино)пиперидин-1-ил]пиридимин-5-ил}-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-(изопропоксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-(пропоксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
3-(2-{4-[(аллилокси)имино]пиперидин-1-ил}пиридимин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-({2-[(тетрагидропиран-2-ил)окси]этокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(2-метоксиэтокси)имино]пиперидин-1-ил}пиридимин-5-ил)бензилкарбамимидоилкарбамат,
2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этилацетат,
(E/Z)-2-фтор-3-{2-[3-(метоксиимино)пирролидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[3-(гидроксимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(2-гидроксиэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(3-гидроксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(4-гидроксибутокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[2-(2-гидроксиэтокси)этокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[3-фтор-2-(гидроксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(4-гидрокси-3-метоксибутокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилацетат,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилпропионат,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилбутират,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилизобутират,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилпивалат,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилгексаноат,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилбензоат,
2-фтор-3-{5-(2-гидроксипропан-2-ил)-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(2-гидроксиэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(3-гидроксипропокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(4-гидроксибутокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(3-гидрокси-2,2-диметилпропокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(3-гидрокси-3-метилбутокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(2-гидроксипропокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(3-гидрокси-2-метилпропокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[3-гидрокси-2-(гидроксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-(2-{3-[(2,3-дигидроксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
3-(2-{3-[(3,4-дигидроксибутокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
3-(6-{3-[(3,4-дигидроксибутокси)имино]азетидин-1-ил}-5-фторпиридин-3-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-{5-фтор-6-[3-{[гидрокси-2-(гидроксиметил)пропокси]имино}азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[3-гидрокси-2-(гидроксиметил)пропокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[3-гидрокси-2-(гидроксиметил)-2-метилпропокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-(2-{4-[(2,3-дигидроксипропокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[3-гидрокси-2-(метоксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(3-гидрокси-2-метоксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(2-фтор-3-гидроксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(5-фтор-6-{3-[(2-фтор-3-гидроксипропокси)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(2-гидрокси-3-метоксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-(гидроксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{5-фтор-6-[3-(гидроксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат,
трет-бутил-2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]ацетат,
2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]уксусную кислоту,
3-[2-(3-{[(диметилкарбамоил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[2-(метиламино)-2-оксоэтокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-(2-{3-[(3-амино-3-оксопропокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[3-(метиламино)-3-оксопропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
этил-4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутаноат,
4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутановую кислоту,
2-фтор-3-[2-(3-{[4-(метиламино)-4-оксобутокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(3-{[2-(диметиламино)этокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
3-{2-[3-{{2-[бензил(метил)амино]этокси}имино}азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат,
3-[2-(3-{[3-(ацетамидо-2-(гидроксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
3-[2-(3-{[3-(диметиламино)-2-(гидроксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
3-(2-{3-[(3-ацетамидо-2-метоксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[2-(пиперидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{3-[(морфолиноэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
3-[2-(3-{[2-(азетидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
3-[2-(3-{[2-(3,3-дифторазетидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[2-(3-фторазетидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[2-(3-метоксиазетидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[(4-метилморфолин-2-ил)метокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(3-{[(4-ацетилморфолин-2-ил)метокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[(5-оксотетрагидрофуран-2-ил)метокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]циклобутилацетат,
2-фтор-3-(2-{3-[(3-гидроксициклобутокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
3-(2-{3-[(бензилокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[(4-метоксибензил)окси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(3-{[(1-метилазетидин-3-ил)окси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(3-{[(1-ацетилазетидин-3-ил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
3-[2-(3-{[(1-бензилазетидин-3-ил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-{2-{3-({[1-(2,2,2-трифторэтил)азетидин-3-ил]окси}имино)азетидин-1-ил}пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[3-({[1-(метилсульфонил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
3-[2-(3-{[(1-этилазетидин-3-ил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
метил-3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-карбоксилат,
2-фтор-3-(2-{3-[(оксетан-3-илокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат,
2-{3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-ил}этилацетат,
2-фтор-3-{2-[3-({[1-(2-гидроксиэтил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[3-({[1-(2-метоксиэтил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[3-({[1-(2-фторэтил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
этил-3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]пропаноат,
3-(2-{4-[(3-амино-3-оксопропокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[3-(метиламино)-3-оксопропокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
этил-4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]бутаноат,
4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]бутановую кислоту,
3-[2-(4-{[3-(диметиламино)-3-оксопропокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
3-(2-{4-[(2-ацетамидоэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(N-метилацетамидо)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(N-метилметилсульфонамидо)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(метилсульфонамидо)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(4-{[2-(диметиламино)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(метиламино)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-(2-{4-[(2-аминоэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
3-(2-{4-[(2-цианоэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
3-(2-{4-[(3-цианопропокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(метилсульфонил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[3-(метилсульфонил)пропокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[1-(метил-1H-пиразол-3-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(4-{[(1H-пиразол-3-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-({[1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
3-[2-(4-{[(1H-пиразол-4-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[1-(метил-1H-пиразол-4-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(4-{[2-(1H-пиразол-1-ил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(пиридин-4-илметокси)имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
3-[2-(4-{[2-(2,5-диоксопирролидин-1-ил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(2-оксопирролидин-1-ил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(2-оксооксазолидин-3-ил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-[2-(4-{[2-(3-оксоморфолино)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат,
2-фтор-3-{2-[4-(феноксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат,
2-фтор-3-(2-{4-[(пиримидин-5-илокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат или
2-фтор-3-(2-{4-[(пиримидин-2-илокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат.
[0077] В конкретном варианте осуществления настоящее изобретение относится к 2-фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамату или его фармакологически приемлемой соли.
[0078] В конкретном варианте осуществления настоящее изобретение относится к 3-{2-[3-(этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамату или его фармакологически приемлемой соли.
[0079] В конкретном варианте осуществления настоящее изобретение относится к 2-фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату или его фармакологически приемлемой соли.
[0080] В конкретном варианте осуществления настоящее изобретение относится к 2-фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату или его фармакологически приемлемой соли.
[0081] В конкретном варианте осуществления настоящее изобретение относится к 2-фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамату или его фармакологически приемлемой соли.
[0082] В конкретном варианте осуществления настоящее изобретение относится к 2-фтор-3-{5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил}бензилкарбамимидоилкарбамату или его фармакологически приемлемой соли.
[0083] В конкретном варианте осуществления настоящее изобретение относится к 3-(6-{3-[(3,4-дигидроксибутокси)имино]азетидин-1-ил}-5-фторпиридин-3-ил)-2-фторбензилкарбамимидоилкарбамату или его фармакологически приемлемой соли.
[0084] В конкретном варианте осуществления настоящее изобретение относится к 2-фтор-3-{5-фтор-6-[3-{[3-гидрокси-2-(гидроксиметил)пропокси]имино}азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамату или его фармакологически приемлемой соли.
[0085] В конкретном варианте осуществления настоящее изобретение относится к 2-фтор-3-(2-{3-[(2-фтор-3-гидроксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату или его фармакологически приемлемой соли.
[0086] В конкретном варианте осуществления настоящее изобретение относится к 3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]циклобутилацетату или его фармакологически приемлемой соли.
[0087] В конкретном варианте осуществления настоящее изобретение относится к 2-фтор-3-(2-{3-[(3-гидроксициклобутокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату или его фармакологически приемлемой соли.
[0088] В конкретном варианте осуществления настоящее изобретение относится к 2-фтор-3-{2-[3-({[1-(метилсульфонил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамату или его фармакологически приемлемой соли.
[0089] В конкретном варианте осуществления настоящее изобретение относится к 2-фтор-3-(2-{3-[(оксетан-3-илокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату или его фармакологически приемлемой соли.
[0090] Конкретные примеры соединения настоящего изобретения общей формулы (I) также включают соединения, перечисленные в таблице 1 и таблице 2. Кроме того, в следующих таблицах 1 и 2 группа R1 представляет группу следующих формул A1-A90 или формул B1-B95. Кроме того, в следующих формулах A1-A90 D представляет атом дейтерия, и Ph представляет фенильную группу. Кроме того, в нижеследующей таблице 2 F представляет атом фтора, Cl представляет атом хлора, Br представляет атом брома, I представляет атом йода, Me представляет метильную группу, Et представляет этильную группу, nPr представляет н-пропильную группу, iPr представляет изопропильную группу, CH2F представляет фторметильную группу, CHF2 представляет дифторметильную группу, CF3 представляет трифторметильную группу, HOCH2 представляет гидроксиметильную группу, HOCHMe представляет 1-гидроксиэтильную группу, HOC(Me)2 представляет 2-гидроксипропан-2-ильную группу, THPOC(Me)2 представляет 2-[(тетрагидропиран-2-ил)окси]пропан-2-ильную группу, MeOCH2 представляет метоксиметильную группу, EtOCH2 представляет этоксиметильную группу, cPr представляет циклопропильную группу, cBu представляет циклобутильную группу, MeO представляет метоксигруппу, EtO представляет этоксигруппу, и NC представляет цианогруппу.
[0091]

[0092]

[0093] [Таблица 1]

[0094] [Таблица 2]

[0095] [Таблица 3]

[0096] [Таблица 4]
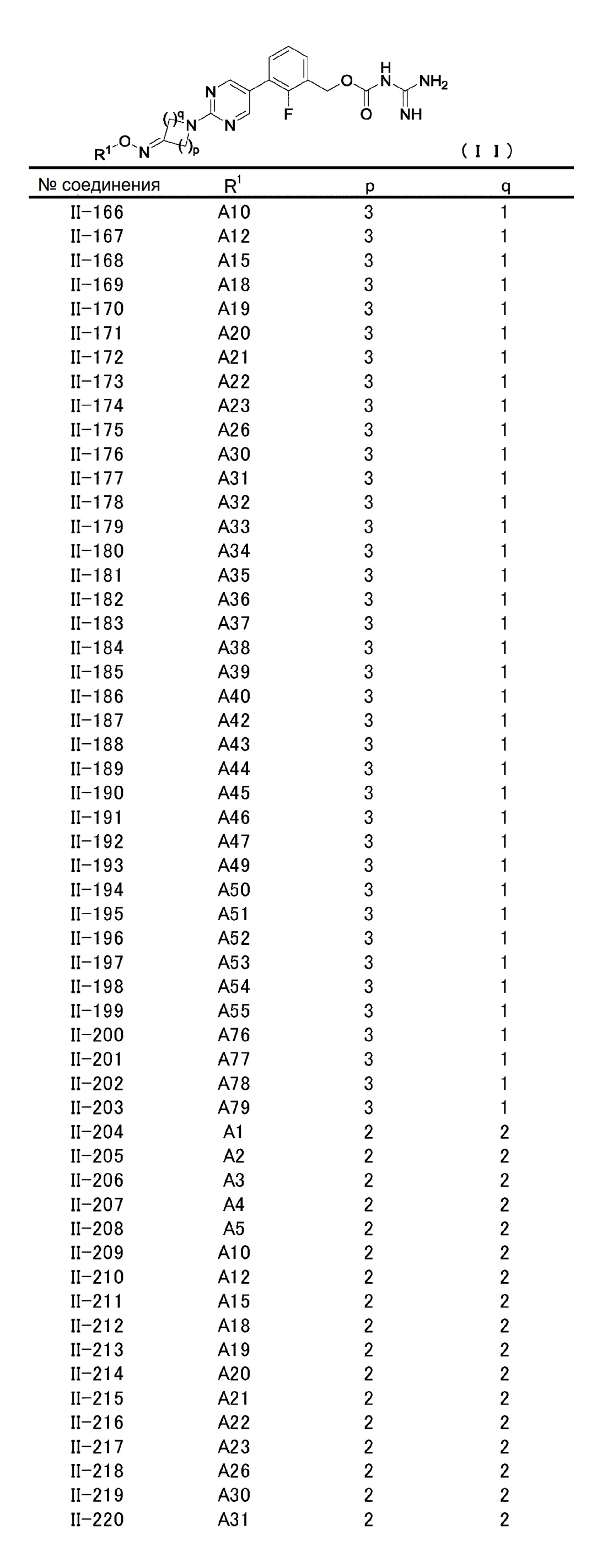
[0097] [Таблица 5]

[0098] [Таблица 6]
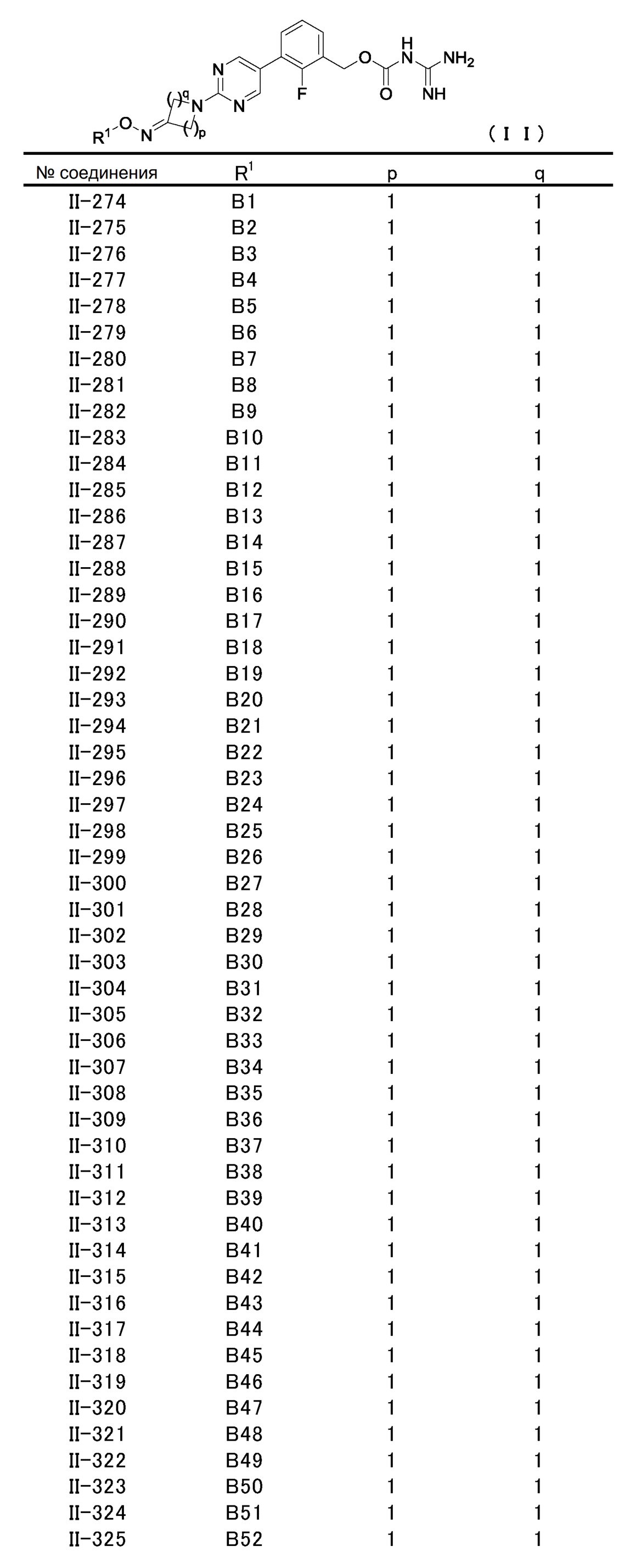
[0099] [Таблица 7]

[0100] [Таблица 8]

[0101] [Таблица 9]
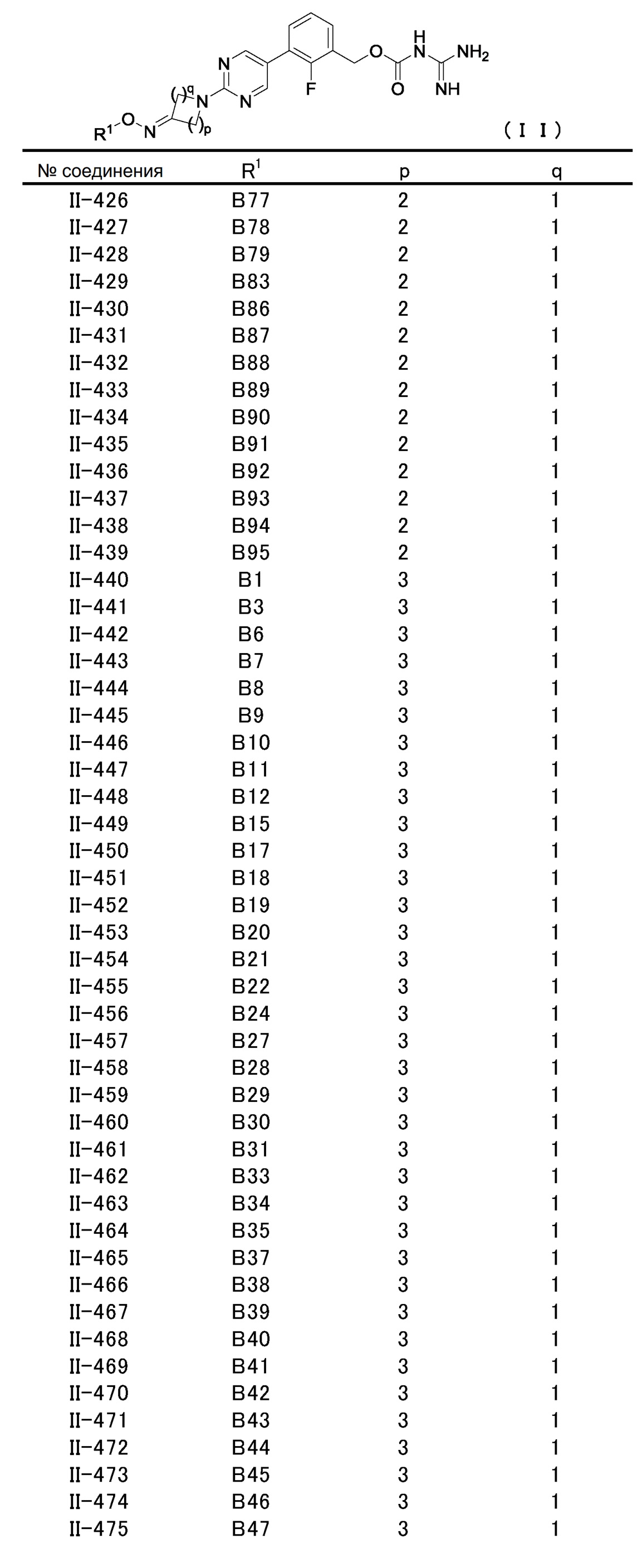
[0102] [Таблица 10]

[0103] [Таблица 11]
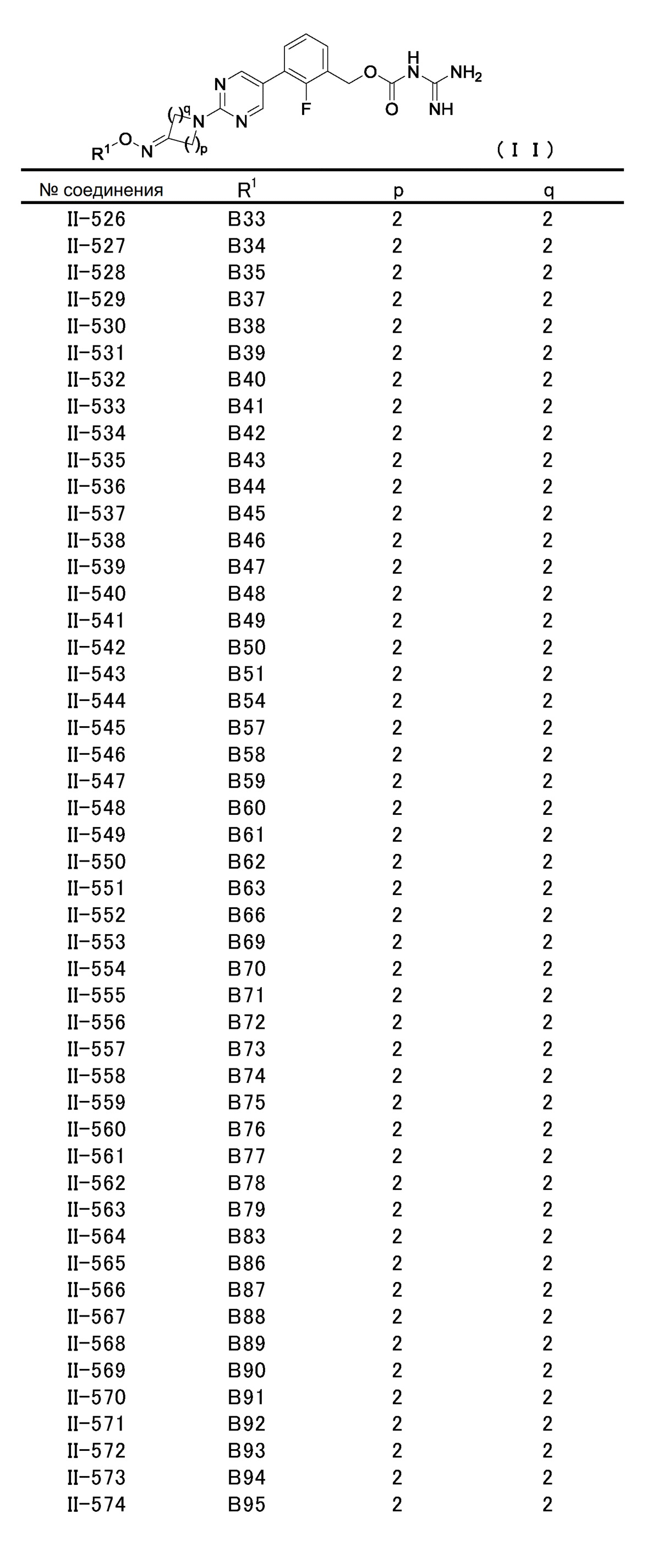
[0104] [Таблица 12]
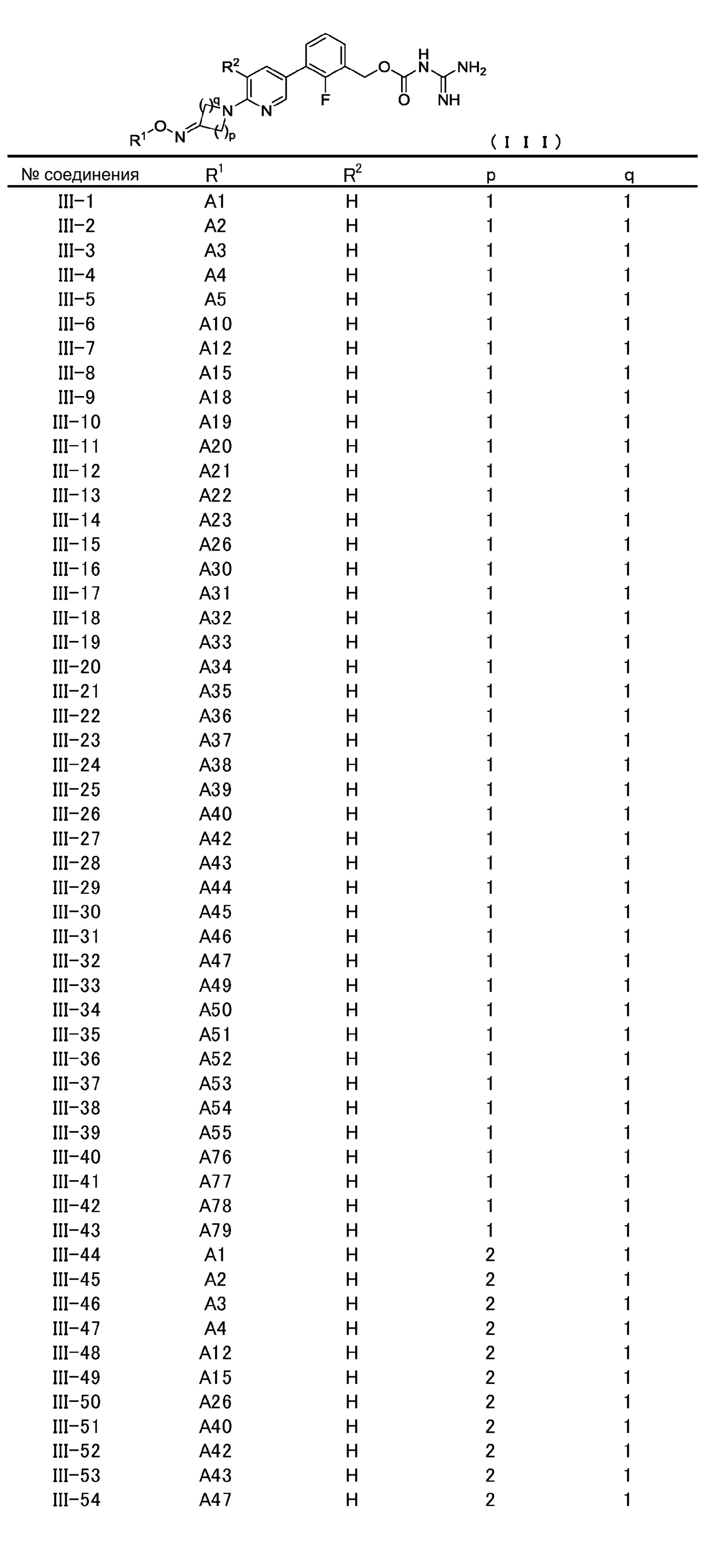
[0105] [Таблица 13]
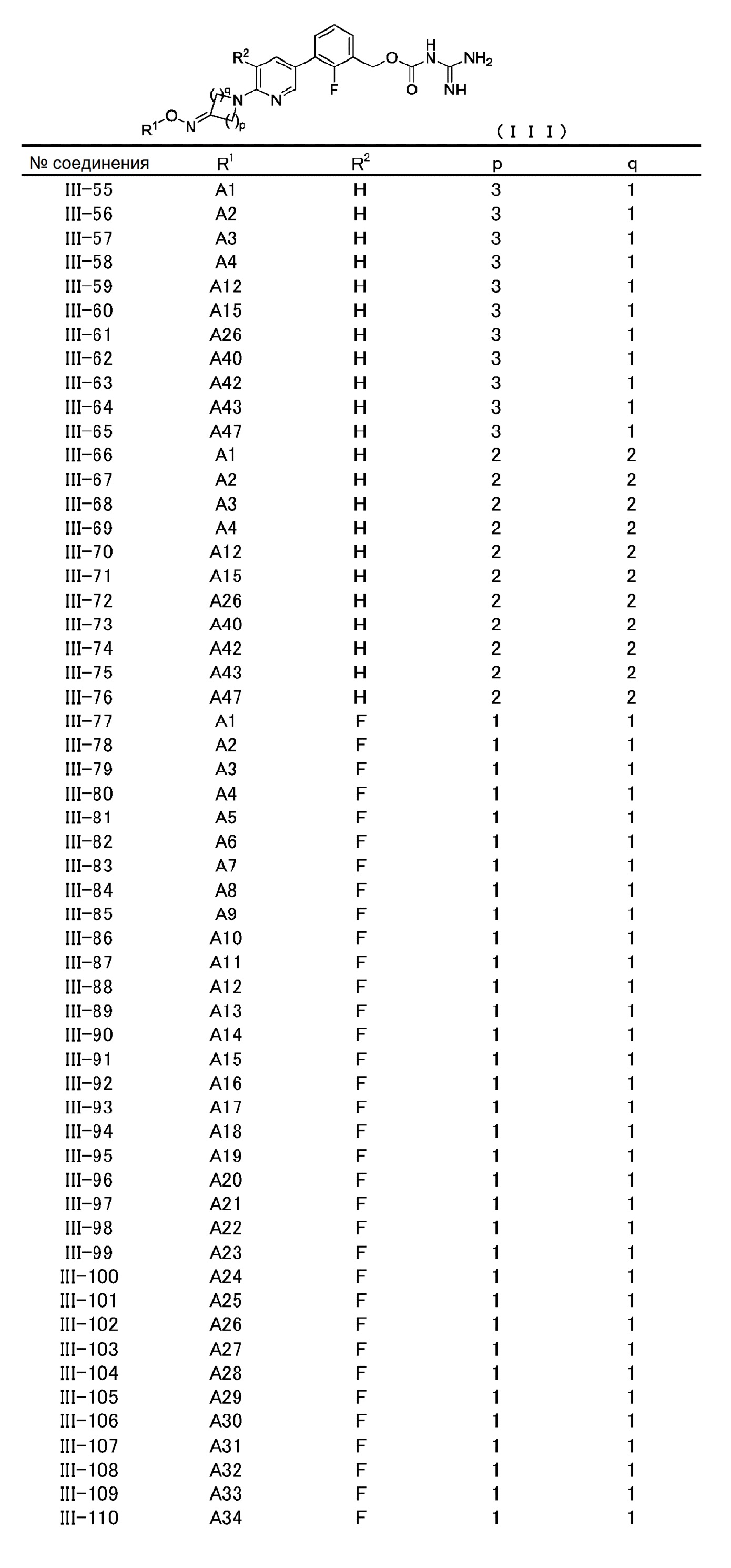
[0106] [Таблица 14]
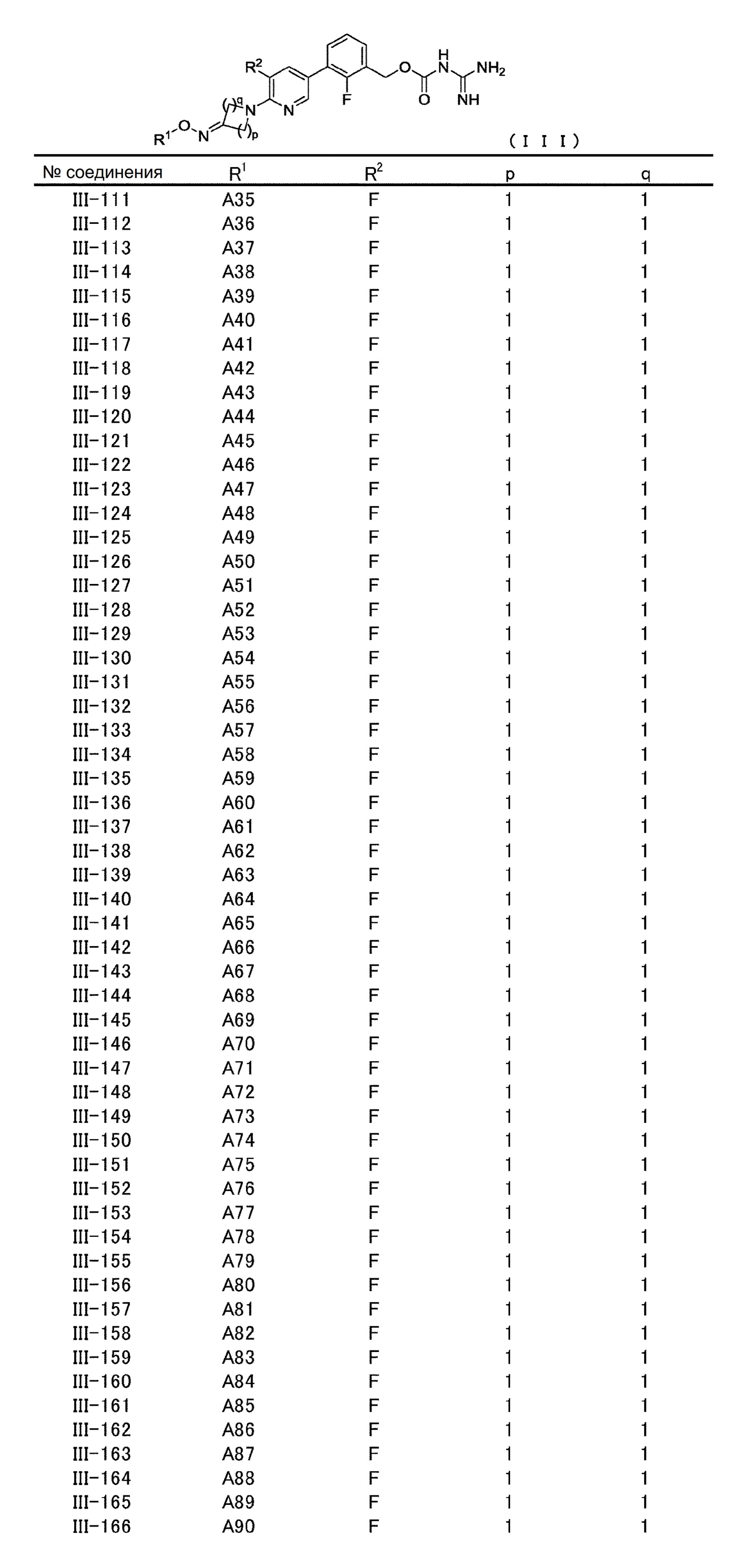
[0107] [Таблица 15]

[0108] [Таблица 16]

[0109] [Таблица 17]
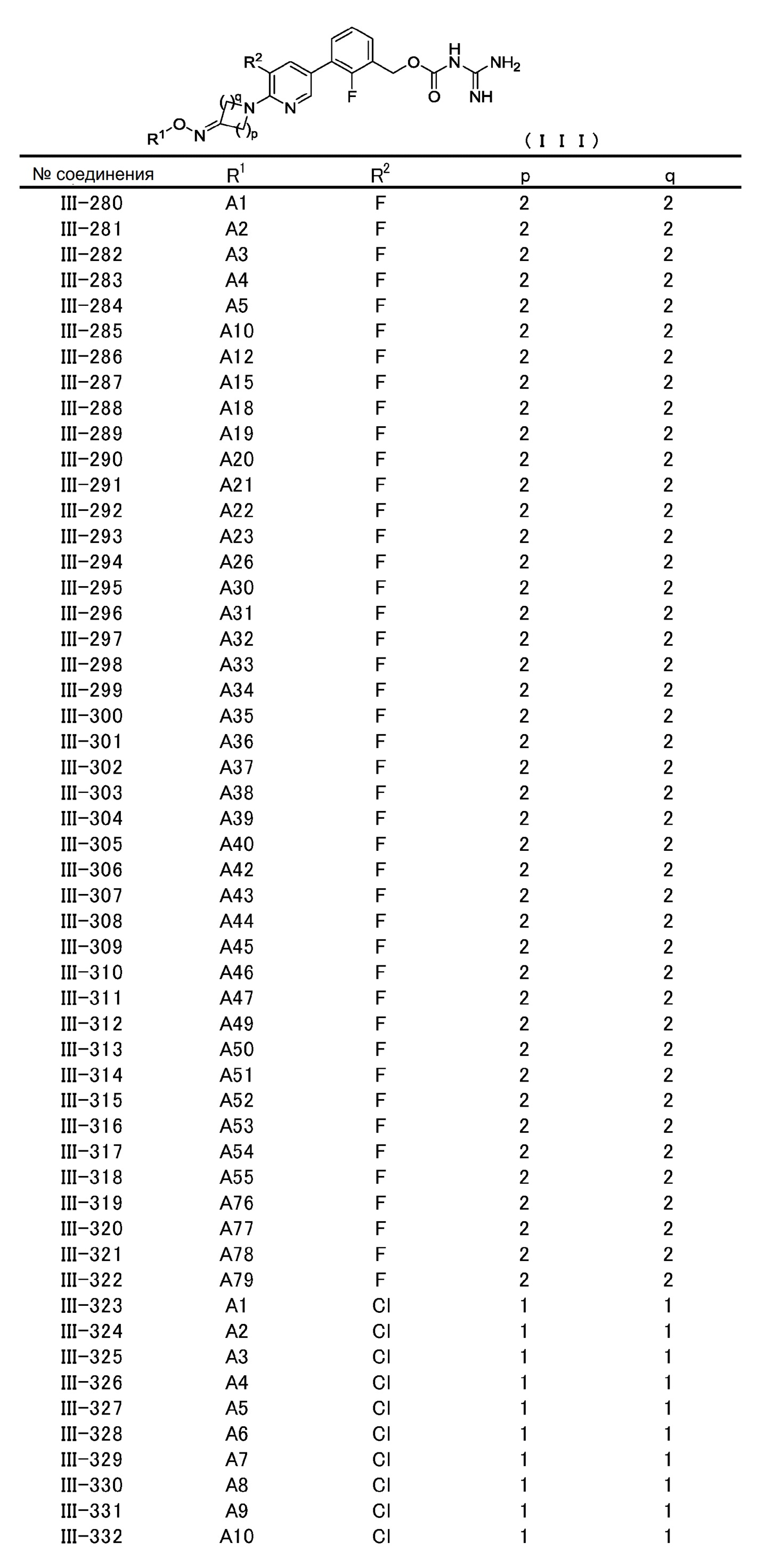
[0110] [Таблица 18]

[0111] [Таблица 19]

[0112] [Таблица 20]

[0113] [Таблица 21]

[0114] [Таблица 22]

[0115] [Таблица 23]

[0116] [Таблица 24]

[0117] [Таблица 25]
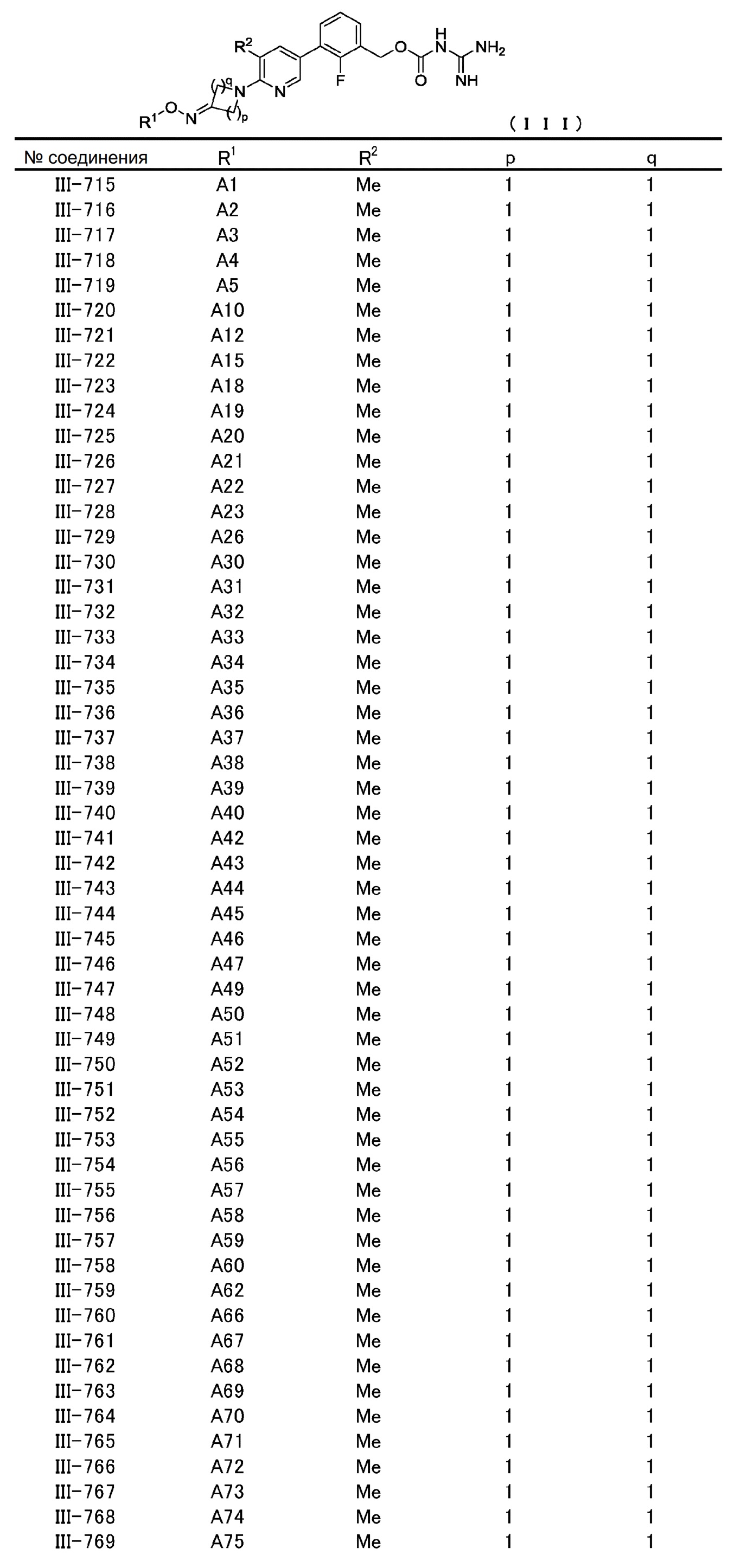
[0118] [Таблица 26]

[0119] [Таблица 27]

[0120] [Таблица 28]

[0121] [Таблица 29]

[0122] [Таблица 30]

[0123] [Таблица 31]
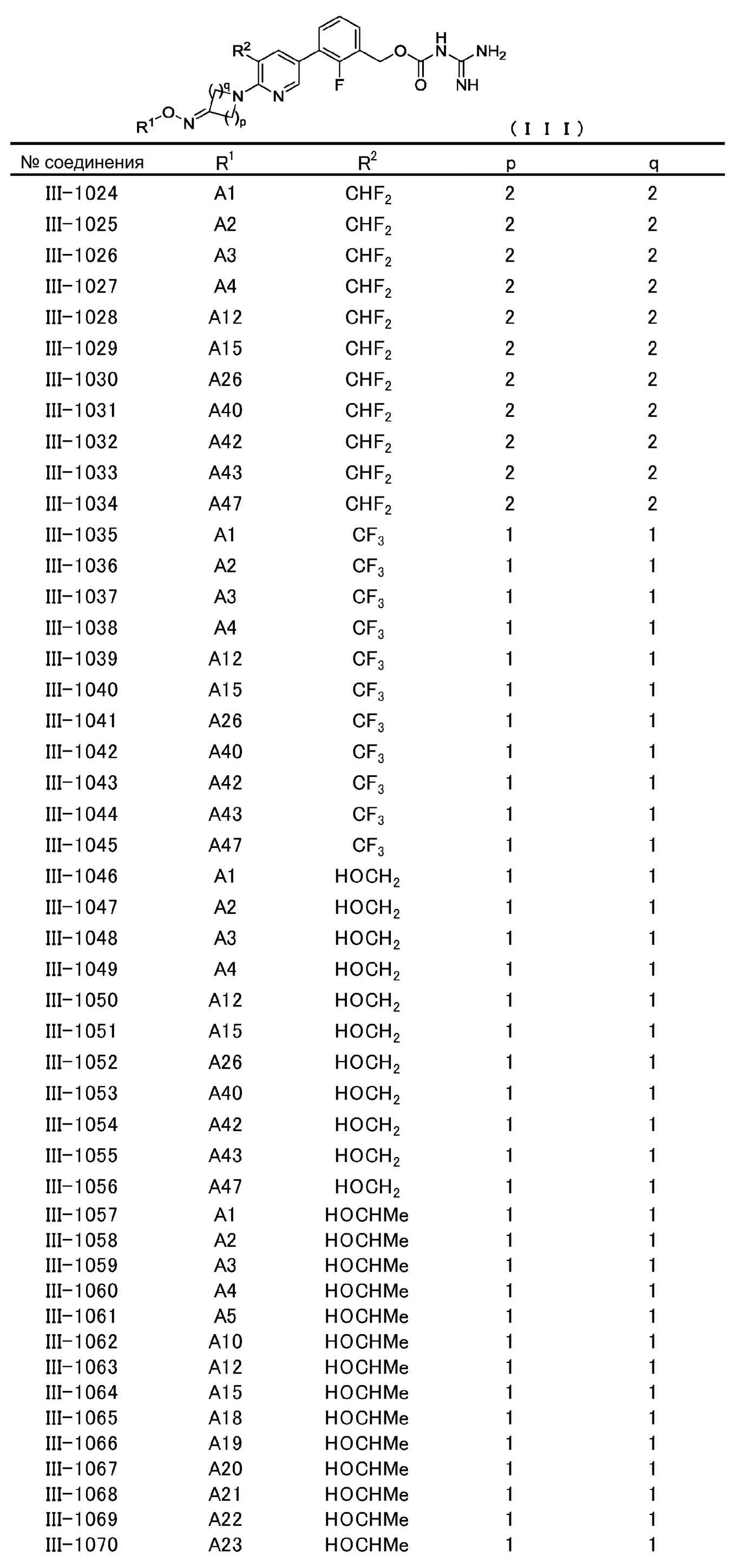
[0124] [Таблица 32]

[0125] [Таблица 33]

[0126] [Таблица 34]

[0127] [Таблица 35]

[0128] [Таблица 36]

[0129] [Таблица 37]
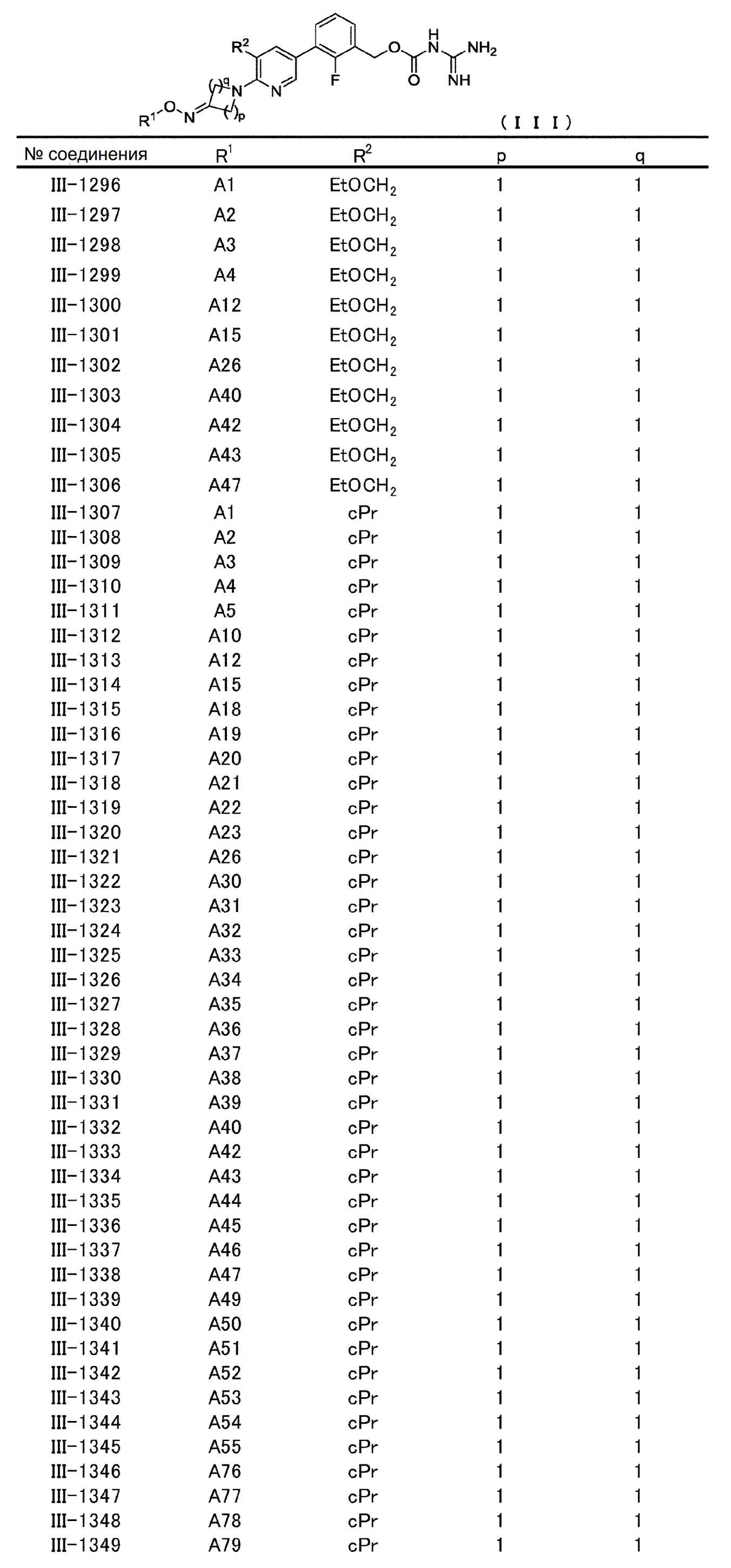
[0130] [Таблица 38]

[0131] [Таблица 39]

[0132] [Таблица 40]

[0133] [Таблица 41]
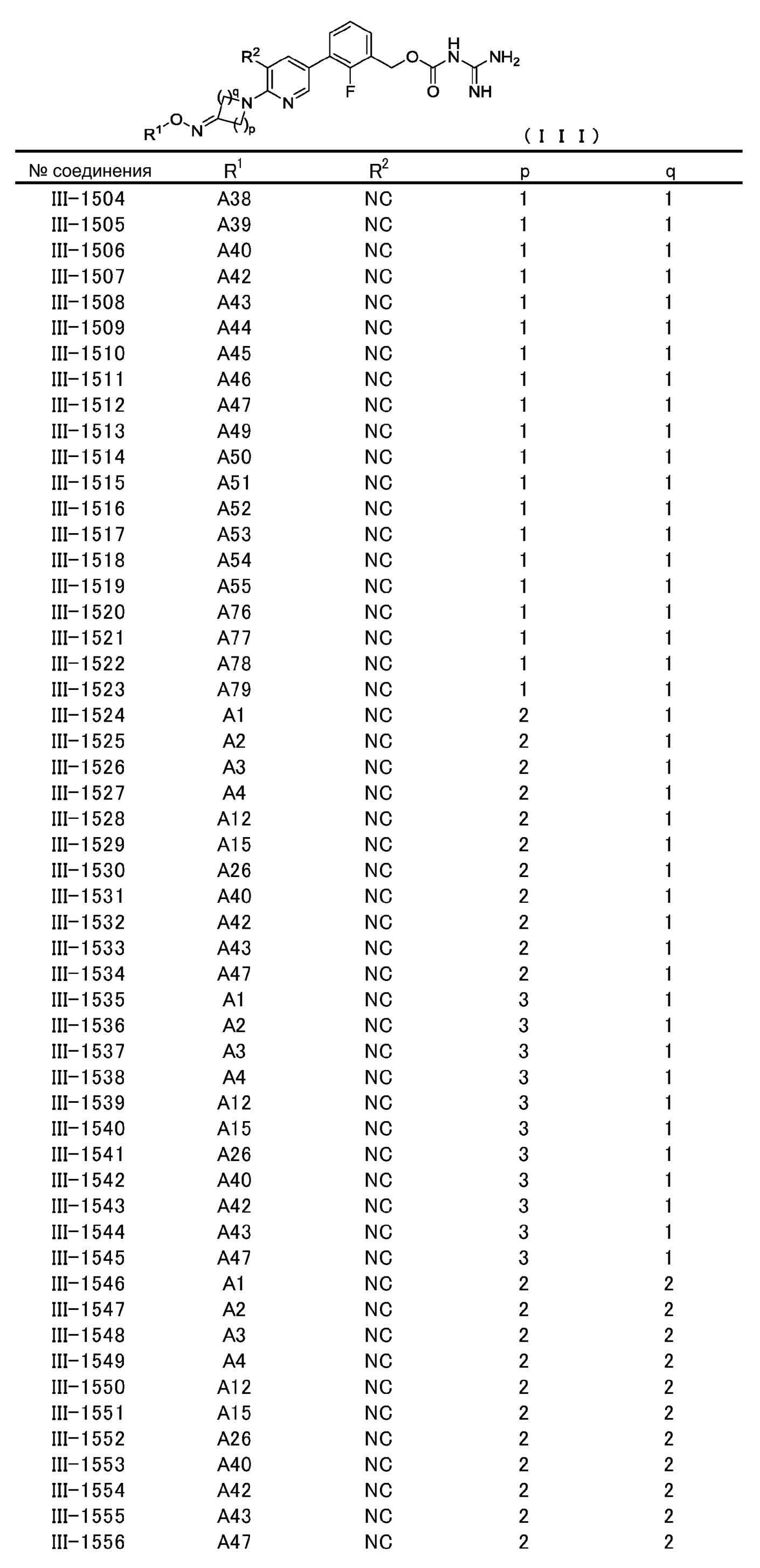
[0134] [Таблица 42]

[0135] [Таблица 43]

[0136] [Таблица 44]

[0137] [Таблица 45]

[0138] [Таблица 46]
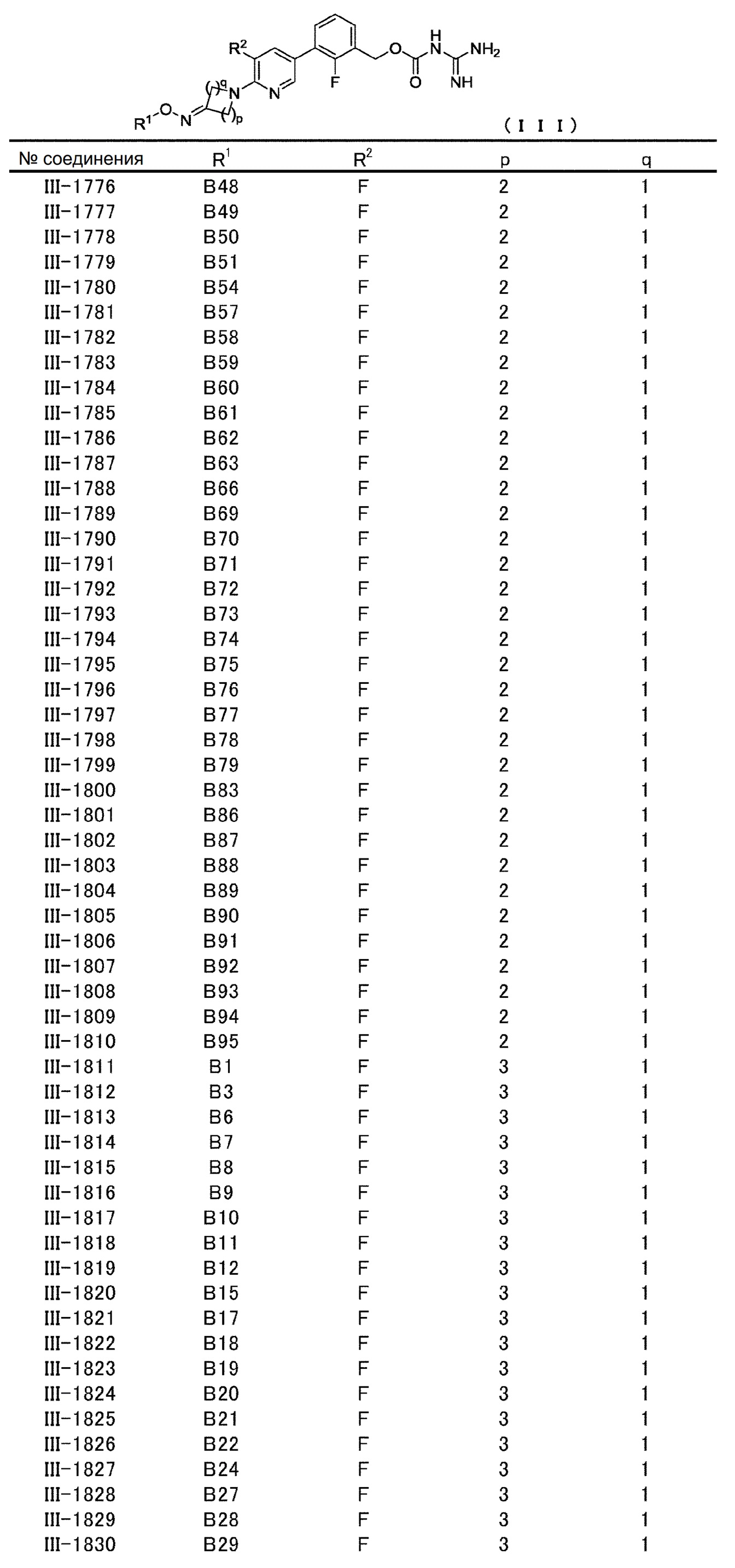
[0139] [Таблица 47]

[0140] [Таблица 48]

[0141] [Таблица 49]

[0142] [Таблица 50]
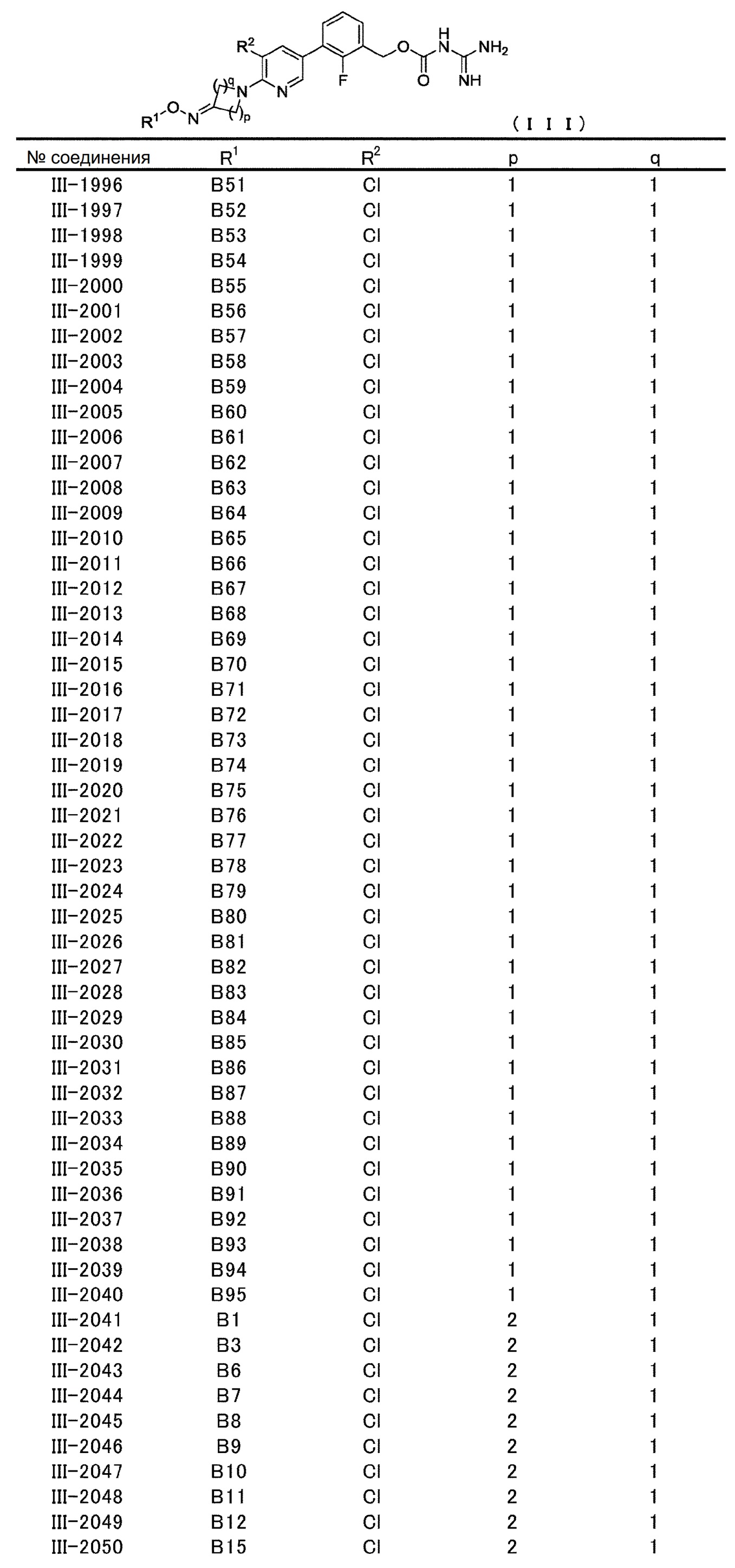
[0143] [Таблица 51]
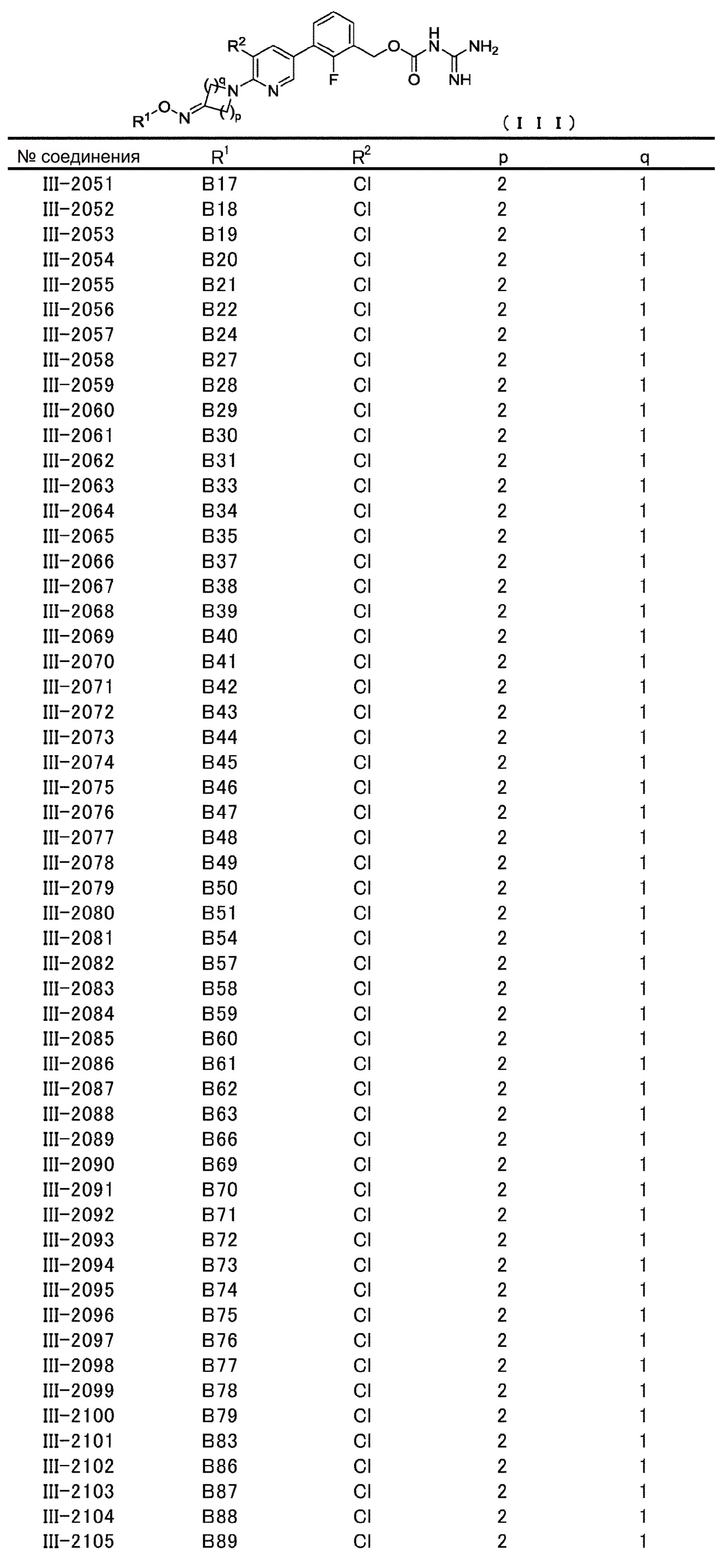
[0144] [Таблица 52]

[0145] [Таблица 53]
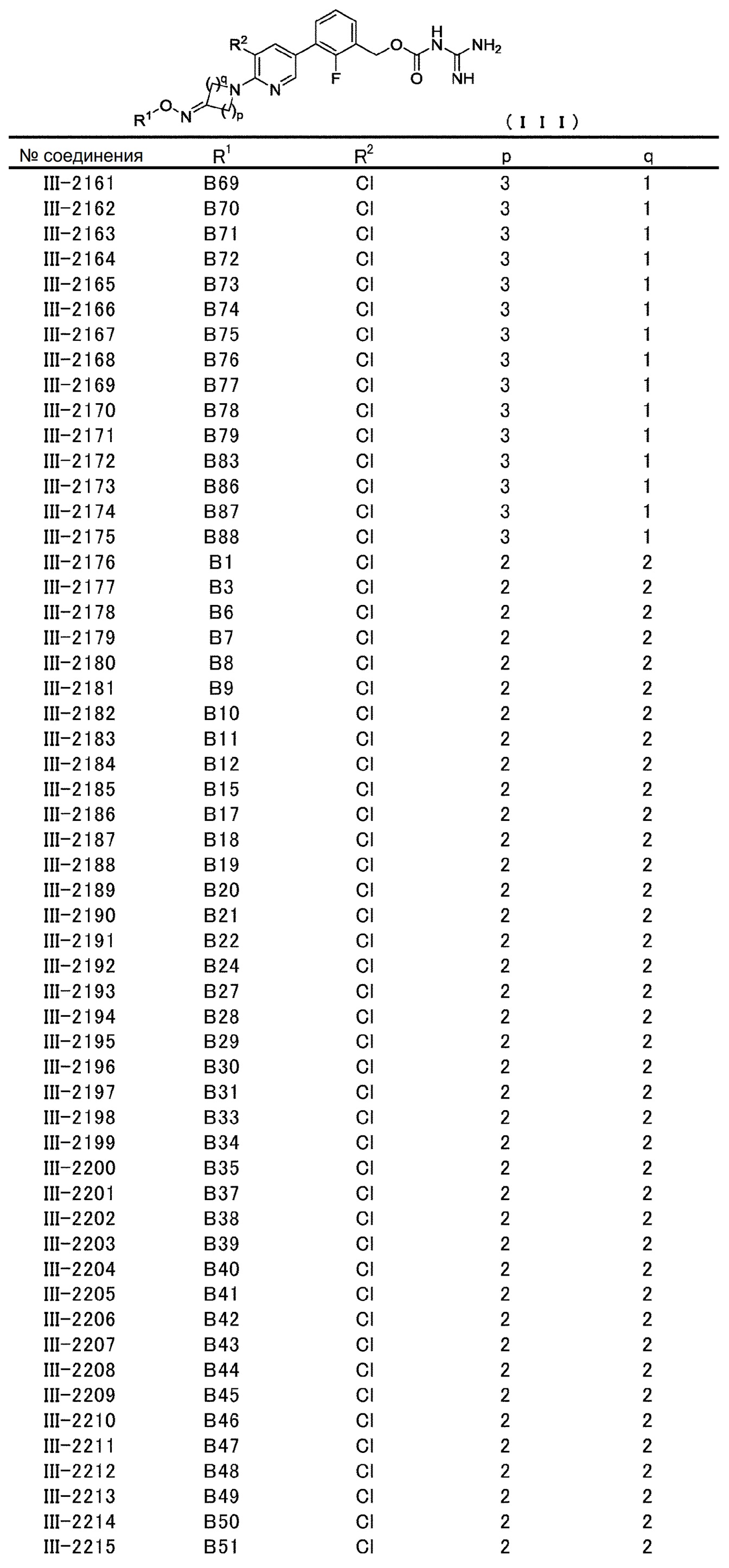
[0146] [Таблица 54]

[0147] [Таблица 55]
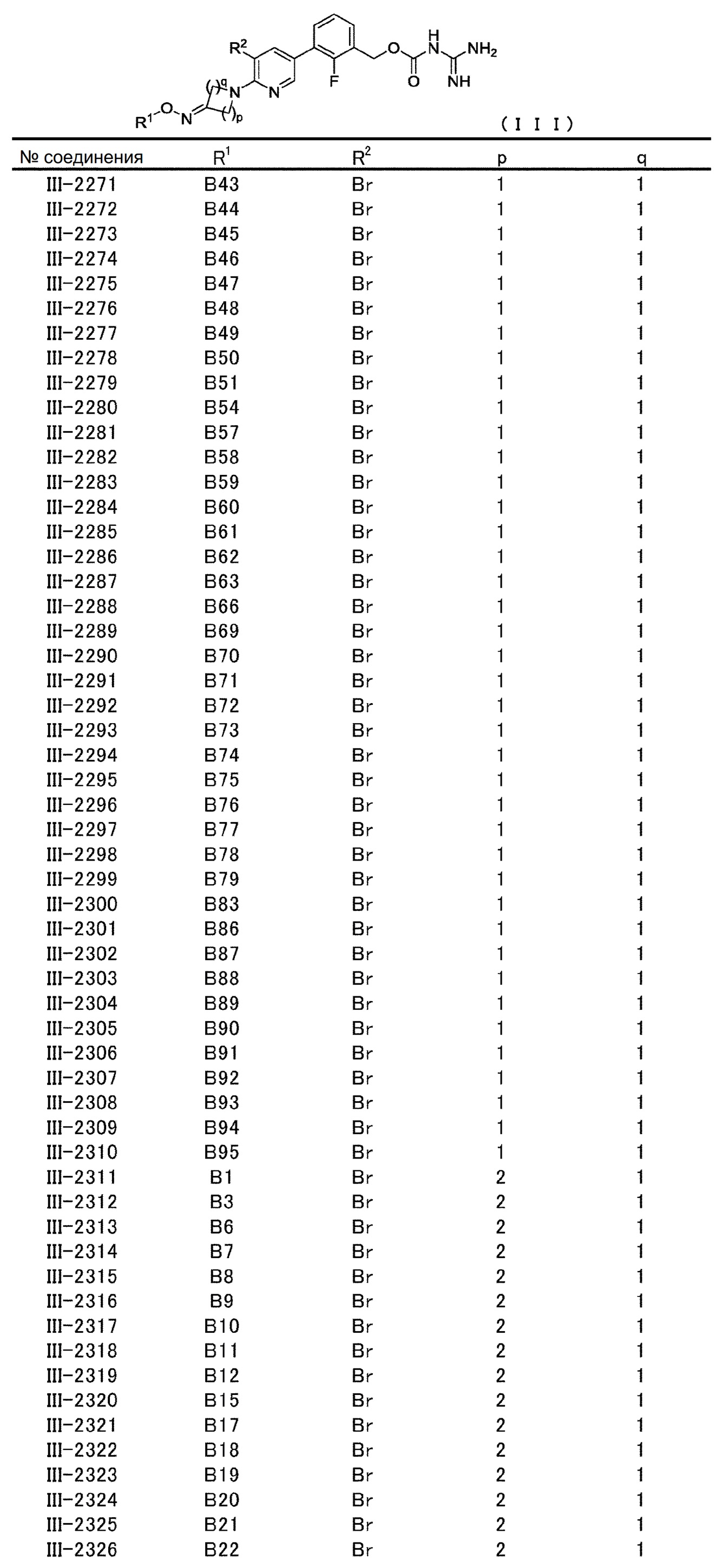
[0148] [Таблица 56]
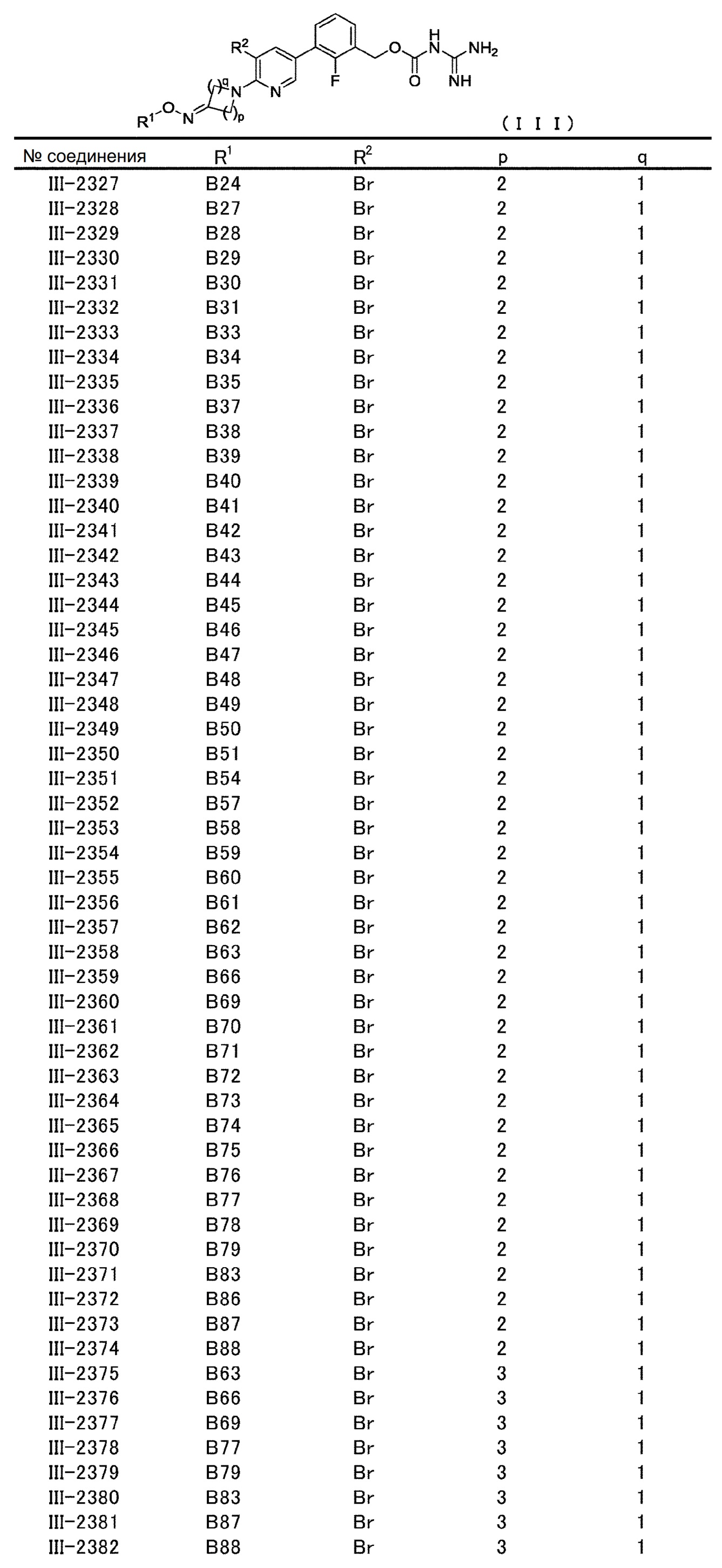
[0149] [Таблица 57]

[0150] [Таблица 58]

[0151] [Таблица 59]

[0152] [Таблица 60]
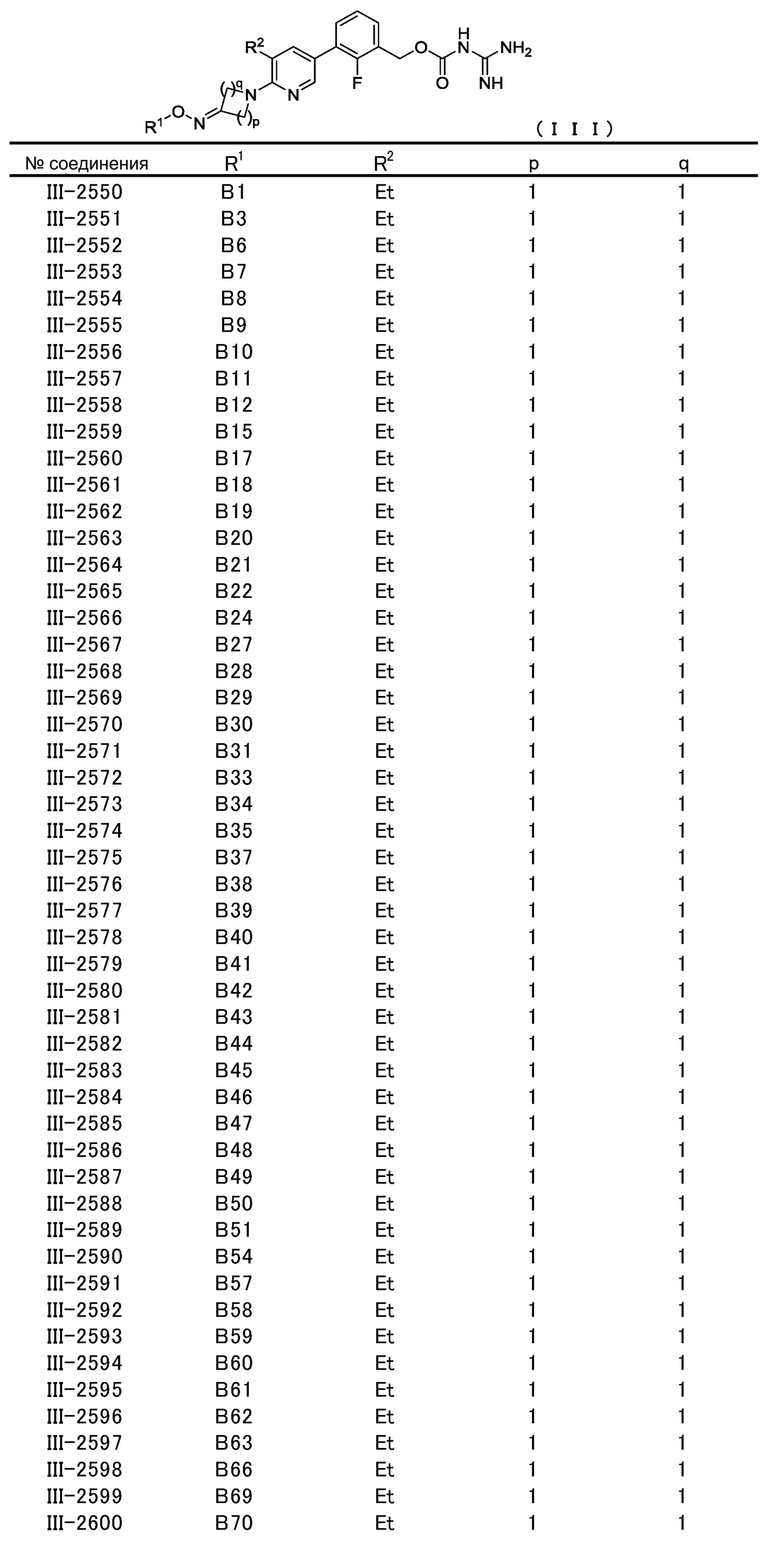
[0153] [Таблица 61]
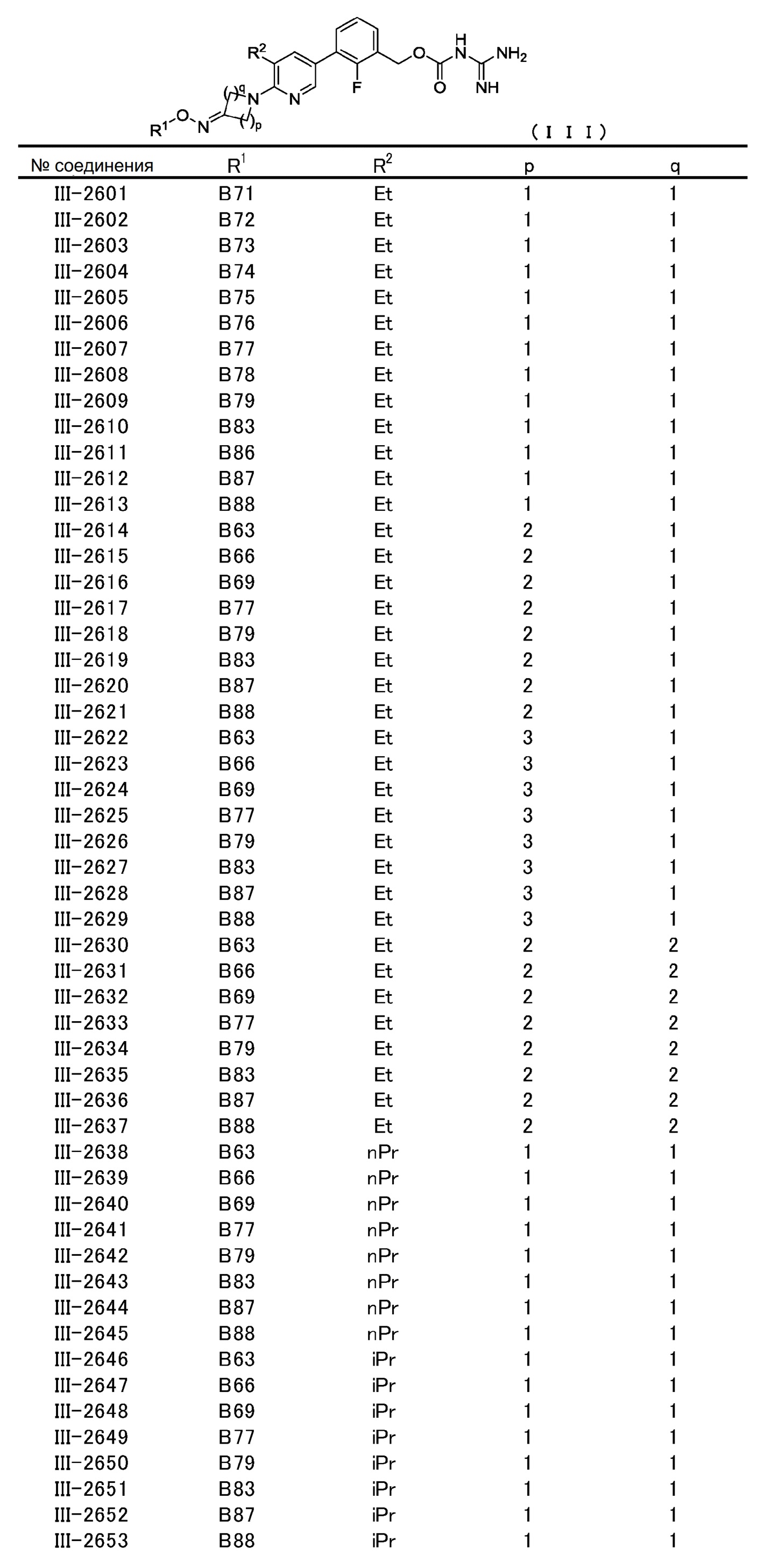
[0154] [Таблица 62]

[0155] [Таблица 63]

[0156] [Таблица 64]

[0157] [Таблица 65]

[0158] [Таблица 66]

[0159] [Таблица 67]

[0160] [Таблица 68]
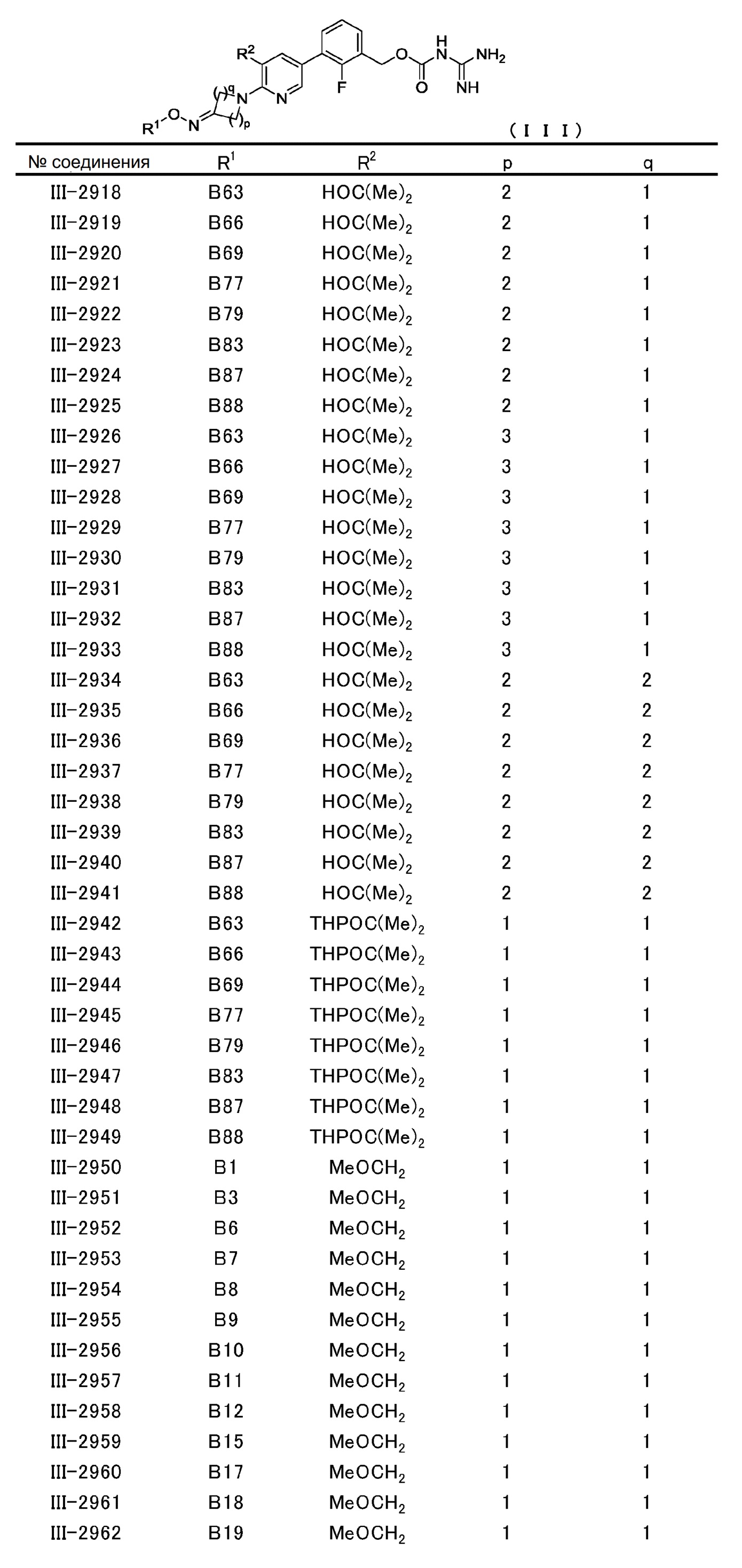
[0161] [Таблица 69]
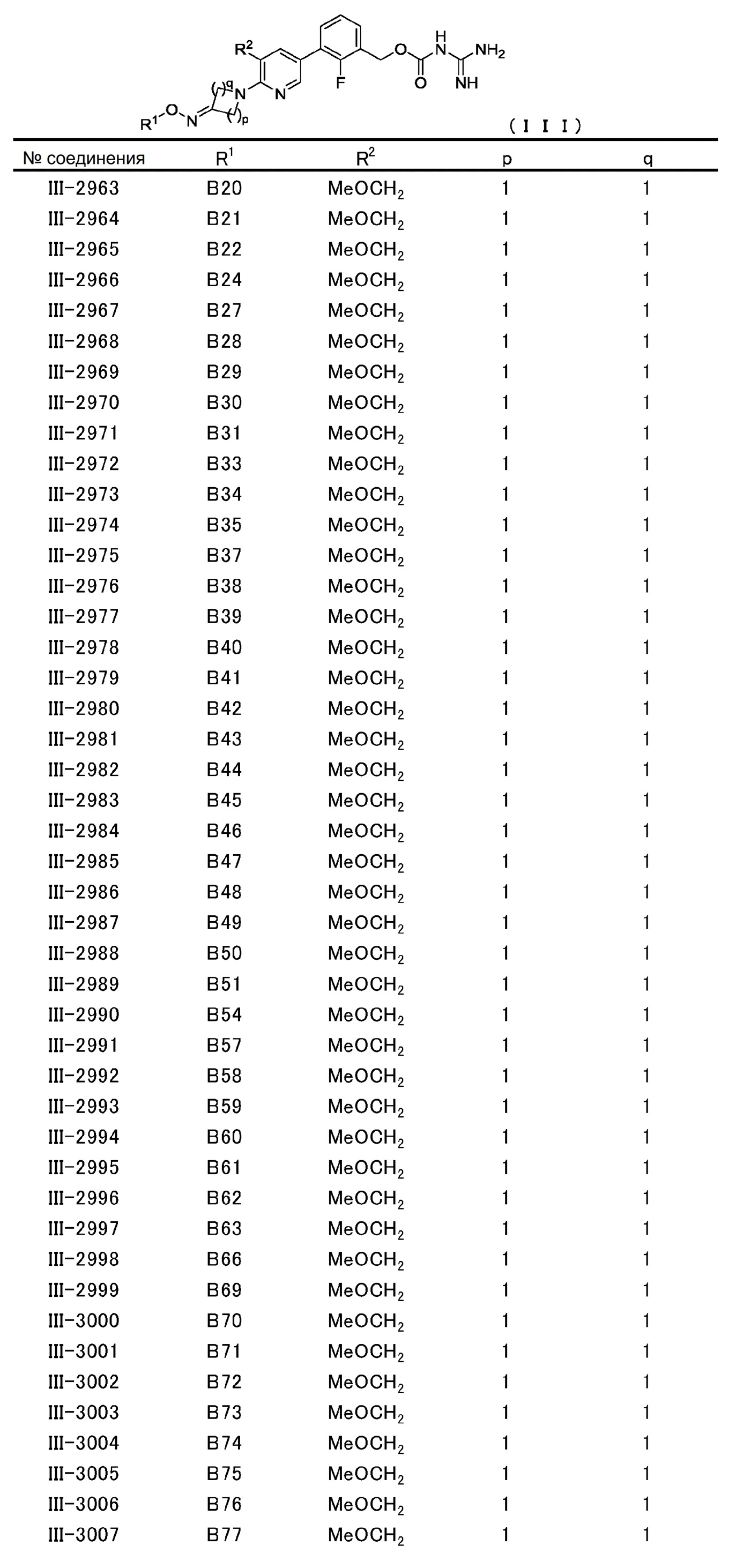
[0162] [Таблица 70]

[0163] [Таблица 71]

[0164] [Таблица 72]

[0165] [Таблица 73]

[0166] [Таблица 74]
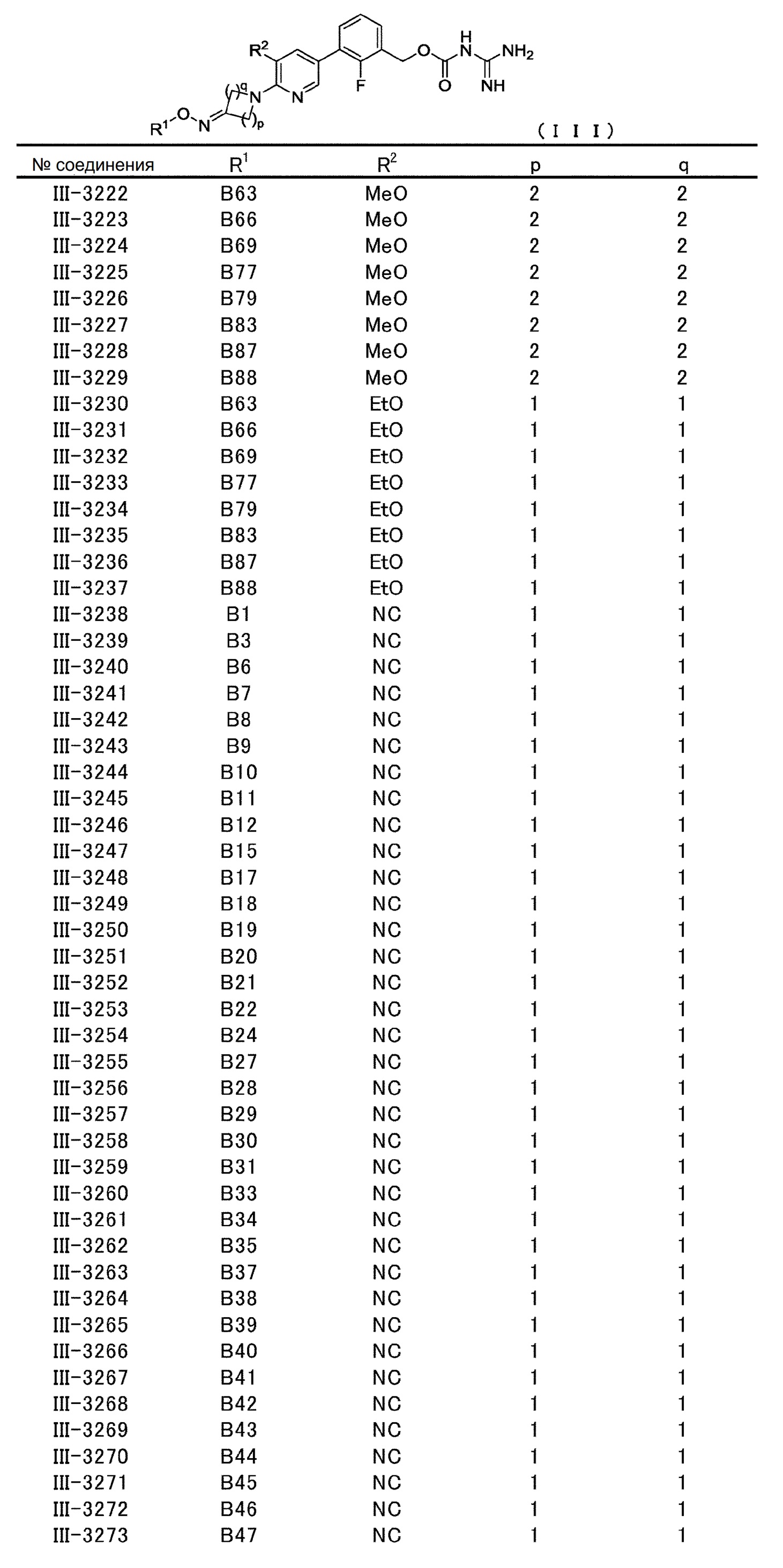
[0167] [Таблица 75]

[0168] Ниже приведен типичный способ получения соединения настоящего изобретения общей формулы (I) или его фармакологически приемлемой соли. При этом соединение настоящего изобретения или его фармакологически приемлемая соль не ограничены соединением или его фармакологически приемлемой солью, получаемыми в соответствии со способом получения, указанным ниже.
[0169] В способе получения, указанном ниже, в случае присутствия частичной структуры, которая ингибирует желаемую реакцию в соединении или подвергается побочной реакции (такой как гидроксильная группа, аминогруппа, карбонильная группа, карбоксильная группа, амидная группа или тиольная группа), желаемую реакцию можно проводить с помощью введения защитной группы в эту частичную структуру, а целевое соединение может быть получено путем последующего удаления защитной группы. Реакции для введения и удаления защитных групп можно проводить в соответствии со способами, обычно используемыми в синтетической органической химии (такими как способ, описанный в документе Protective Groups in Organic Synthesis, 4th Edition, T. W. Greene and P. G. M. Wuts, ed., John Wiley & Sons Inc. (2006)). Кроме того, конкретные способы получения отдельных соединений настоящего изобретения приведены в примерах, которые будут описаны ниже.
[0170] (Способ получения 1)

[0171] R1 представляет атом водорода, защитную группу, необязательно замещенную C1-C6 алкильную группу, необязательно замещенную C2-C6 алкенильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкокси-C1-C6 алкильную группу, -CONR11R12, необязательно замещенную гетероциклильную группу, необязательно замещенную гетероциклил-C1-C6 алкильную группу, необязательно замещенную арильную группу или необязательно замещенную C7-C16 аралкильную группу, и X представляет N или C-R2,
причем R2 представляет атом водорода, атом галогена, необязательно замещенную C1-C6 алкильную группу, необязательно замещенную C3-C8 циклоалкильную группу, необязательно замещенную C1-C6 алкоксигруппу или цианогруппу, и
p и q, независимо друг от друга, представляют натуральное число от 1 до 3 при условии, что сумма p и q представляет собой натуральное число от 2 до 4,
причем термин "замещенный" означает замещенный по меньшей мере одним заместителем, выбранным из группы, состоящей из атома дейтерия, атома галогена, C1-C6 алкильной группы, C1-C6 алкоксигруппы, C1-C6 алкокси-C1-C6 алкильной группы, R13O-C1-C6 алкильной группы, галоген-C1-C6 алкильной группы, C7-C16 аралкильной группы, C1-C7 ацильной группы, цианогруппы, оксогруппы, -CONR11R12, -OR13, -COOR14, -NR15R16 и -S(O)nR17, и
R11 и R12 независимо представляют атом водорода или C1-C6 алкильную группу, R13 представляет атом водорода, C1-C7 ацильную группу или защитную группу, R14 представляет атом водорода или C1-C6 алкильную группу, R15 и R16 независимо представляют атом водорода, C1-C6 алкильную группу, C7-C16 аралкильную группу, C1-C7 ацильную группу, -COOR14 или -S(O)nR17, R17 представляет C1-C6 алкильную группу, и n представляет 0, 1 или 2.
[0172] Этап 1 способа получения 1 является этапом приведения соединения (1) в реакцию с гуанидином или кислой солью гуанидина соединения (2) в растворителе в присутствии 1,1'-карбонилдиимидазола для получения соединения общей формулы (I).
Соединение (1) может быть получено в соответствии с синтезами 1-10, которые будут описаны ниже, и ссылочными примерами настоящего описания.
Примеры кислых солей гуанидина соединения (2) включают гидрохлорид гуанидина, сульфат гуанидина и карбонат гуанидина.
Соединение (2) известно и доступно от поставщика реагентов, такого как Tokyo Chemical Industry Co., Ltd. Количество гуанидина или кислой соли гуанидина, используемых на 1 моль соединения (1), обычно составляет от 0,9 до 5 молярных количеств и, предпочтительно, от 1,1 до 3 молярных количеств соединения (1).
Отсутствуют особые ограничения в отношении используемого растворителя, при условии что он не ингибирует реакцию и в определенной степени растворяет исходные материалы, и его примеры включают ароматические углеводороды, такие как бензол, толуол или ксилол, галогенированные алифатические углеводороды, такие как метиленхлорид, хлороформ или 1,2-дихлорэтан, простые эфиры, такие как тетрагидрофуран, 1,2-диметоксиэтан или 1,4-диоксан, нитрилы, такие как ацетонитрил или пропионитрил, амиды, такие как N,N-диметилформамид, N,N-диметилацетамид или N-метилпирролидон, и произвольную смесь этих растворителей. Предпочтительно, используют N,N-диметилформамид. Хотя конкретные ограничения в этом отношении отсутствуют, количество используемого растворителя обычно составляет от 1 до 20 и, предпочтительно, от 2 до 10 масс соединения (1).
Количество 1,1'-карбонилдиимидазола, используемого на 1 моль соединения (1), обычно составляет от 0,9 до 5 молярных количеств и, предпочтительно, от 1,1 до 3 молярных количеств соединения (1).
Несмотря на изменения в зависимости от таких факторов, как используемые типы и количества исходных материалов, растворителя и т.п., температура реакции обычно составляет от -20°C до 150°C и, предпочтительно, от 0°C до 40°C.
Несмотря на изменения в зависимости от таких факторов, как температура реакции, время реакции обычно составляет от 1 минуты до 24 часов и, предпочтительно, от 1 часа до 12 часов.
Хотя давление реакции при необходимости может быть установлено соответствующим образом, и реакция может быть проведена под давлением, при пониженном давлении или при атмосферном давлении, давление реакции, предпочтительно, представляет собой атмосферное давление. Хотя реакция может быть при необходимости проведена в соответствующим образом выбранной атмосфере, атмосфера реакции, предпочтительно, представляет собой воздушную атмосферу или атмосферу инертного газа, такую как атмосфера азота или аргона.
[0173] В случае, если в соединении (1) присутствует защитная группа, соединение (1) при необходимости может быть дополнительно подвергнуто этапу снятия защиты.
В случае, если соединение (1) содержит защитные группы по меньшей мере двух различных типов, выборочно может быть удалена защитная группа только одного типа с помощью выбора условий снятия защиты.
Условия снятия защиты могут быть соответствующим образом выбраны в соответствии со способом, обычно используемым в синтетической органической химии (таким как способ, описанный в документе Protective Groups in Organic Synthesis, 4th Edition, T. W. Greene and P. G. M. Wuts, ed., John Wiley & Sons Inc. (2006)), или примерами настоящего описания.
[0174] Вышеупомянутое соединение (1) может быть соответствующим образом получено в соответствии, например, со следующими синтезами 1-10 и ссылочными примерами настоящего описания.
(Синтез 1)
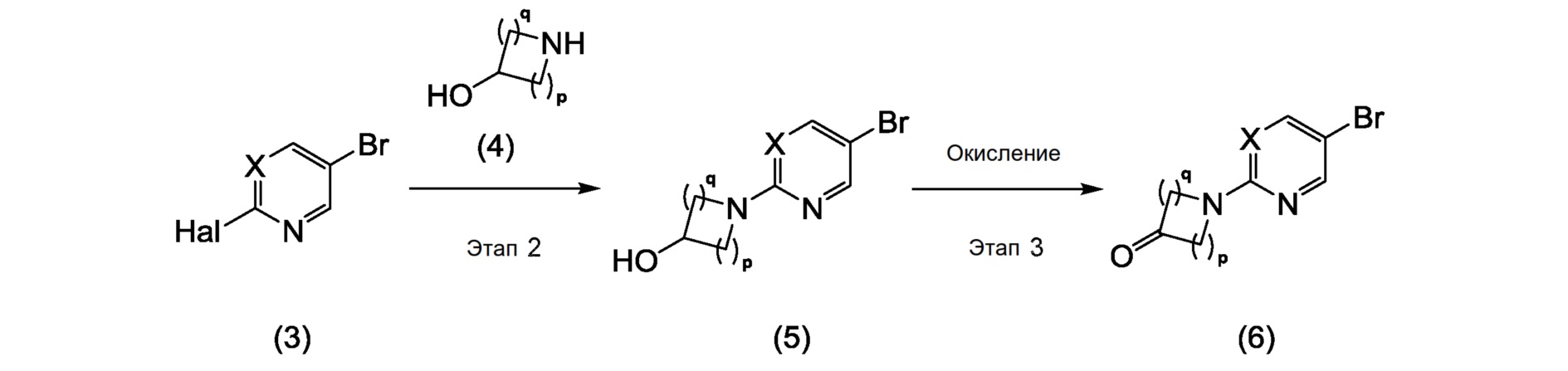
X, p и q соответствуют описанным выше, а Hal представляет атом галогена.
[0175] Этап 2 синтеза 1 представляет собой этап получения соединения (5) с помощью реакции соединения (3) и соединения (4) в растворителе и в присутствии основания.
Соединение (3) и соединение (4) известны или могут быть получены из известных соединений в соответствии с известными способами.
Примеры соединения (3) включают 5-бром-2-хлорпиридин, 5-бром-2-хлорпиримидин, 5-бром-2,3-дифторпиридин и 5-бром-2-фтор-3-метилпиридин.
Примеры соединения (4) включают азетидин-3-ол, пирролидин-3-ол, пиперидин-4-ол и их кислые соли.
Примеры кислых солей соединения (4) включают гидрохлориды, сульфаты и ацетаты.
Количество соединения (4), используемого на 1 моль соединения (3), обычно составляет от 0,9 до 5 молярных количеств и, предпочтительно, от 1,1 до 3 молярных количеств соединения (3).
Отсутствуют особые ограничения в отношении используемого растворителя, при условии что он не ингибирует реакцию и в определенной степени растворяет исходные материалы, и его примеры включают спирты, такие как метанол, этанол, пропанол или изопропанол, ароматические углеводороды, такие как бензол, толуол или ксилол, галогенированные алифатические углеводороды, такие как метиленхлорид, хлороформ или 1,2-дихлорэтан, простые эфиры, такие как тетрагидрофуран, 1,2-диметоксиэтан или 1,4-диоксан, нитрилы, такие как ацетонитрил или пропионитрил, амиды, такие как N,N-диметилформамид, N,N-диметилацетамид или N-метилпирролидон, сульфоксиды, такие как диметилсульфоксид, и произвольную смесь этих растворителей. Предпочтительно, используют спирты, такие как этанол, амиды, такие как N,N-диметилформамид или N-метилпирролидон, или сульфоксиды, такие как диметилсульфоксид. Хотя конкретные ограничения в этом отношении отсутствуют, количество используемого растворителя обычно составляет от 1 до 50 и, предпочтительно, от 5 до 20 масс соединения (3).
Примеры используемого основания включают ацетаты щелочных металлов, такие как ацетат натрия или ацетат калия, карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия или карбонат цезия, и органические основания, такие как триэтиламин или диизопропилэтиламин, причем предпочтительными являются карбонат калия, карбонат цезия, триэтиламин или диизопропилэтиламин. Количество основания, используемого на 1 моль соединения (3), обычно составляет от 0,9 до 10 молярных количеств и, предпочтительно, от 1 до 5 молярных количеств соединения (3).
Несмотря на изменения в зависимости от таких факторов, как используемые типы и количества исходных материалов, растворителя и т.п., температура реакции обычно составляет от 0°C до 150°C и, предпочтительно, от 40°C до 120°C.
Несмотря на изменения в зависимости от таких факторов, как температура реакции, время реакции обычно составляет от 1 минуты до 48 часов и, предпочтительно, от 0,5 часа до 24 часов.
Хотя давление реакции при необходимости может быть установлено соответствующим образом, и реакция может быть проведена под давлением, при пониженном давлении или при атмосферном давлении, давление реакции, предпочтительно, представляет собой атмосферное давление. Хотя реакция может быть при необходимости проведена в соответствующим образом выбранной атмосфере, атмосфера реакции, предпочтительно, представляет собой воздушную атмосферу или атмосферу инертного газа, такую как атмосфера азота или аргона.
[0176] Этап 3 синтеза 1 представляет собой этап получения соединения (6) путем окисления соединение (5) с помощью окисляющего средства в растворителе и, необязательно, в присутствии основания.
Примеры окисляющих средств включают диоксид марганца, хлорхромат пиридиния (PCC), дихлорид пиридиния (PDC) и 1,1,1-триацетокси-1,1-дигидро-1,2-бензойодохинол-3(1H)-он (перйодинан Десса-Мартина).
Отсутствуют особые ограничения в отношении используемого растворителя, при условии что он не ингибирует реакцию и в определенной степени растворяет исходные материалы, и его примеры включают галогенированные алифатические углеводороды, такие как метиленхлорид, хлороформ или 1,2-дихлорэтан, нитрилы, такие как ацетонитрил, и сложные эфиры, такие как метилацетат, этилацетат или изопропилацетат, причем предпочтительным является метиленхлорид.
Несмотря на изменения в зависимости от типа окисляющего средства, количество окисляющего средства, используемого на 1 моль соединения (5), обычно составляет от 0,9 до 100 молярных количеств и, предпочтительно, от 1 до 20 молярных количеств соединения (5).
Примеры используемого основания включают органические основания, такие как триэтиламин или пиридин, и неорганические основания, такие как бикарбонат натрия, бикарбонат калия, карбонат натрия или карбонат калия, причем предпочтительными являются пиридин или бикарбонат натрия. Количество основания, используемого на 1 моль соединения (5), обычно составляет от 0,9 до 20 молярных количеств и, предпочтительно, от 1 до 10 молярных количеств соединения (5).
Несмотря на изменения в зависимости от таких факторов, как используемые типы и количества исходных материалов, растворителя и т.п., температура реакции обычно составляет от 0°C до 150°C и, предпочтительно, от 0°C до 100°C.
Несмотря на изменения в зависимости от таких факторов, как температура реакции, время реакции обычно составляет от 30 минут до 24 часов и, предпочтительно, от 1 часа до 12 часов.
Хотя давление реакции при необходимости может быть установлено соответствующим образом, и реакция может быть проведена под давлением, при пониженном давлении или при атмосферном давлении, давление реакции, предпочтительно, представляет собой атмосферное давление. Хотя реакция может быть при необходимости проведена в соответствующим образом выбранной атмосфере, атмосфера реакции, предпочтительно, представляет собой воздушную атмосферу или атмосферу инертного газа, такую как атмосфера азота или аргона.
[0177] (Синтез 2)

X, Hal, p и q соответствуют описанным выше.
[0178] Этап 4 синтеза 2 представляет собой этап получения соединения (6) с помощью реакции соединения (3) и соединения (7) в растворителе и в присутствии основания.
Соединение (3) и соединение (7) известны или могут быть получены из известных соединений в соответствии с известным способом. Примеры соединения (3) соответствуют описанным выше.
Примеры соединения (7) включают азетидин-3-он, пирролидин-3-он, пиперидин-4-он и их кислые соли.
Примеры кислых солей соединения (7) включают гидрохлориды, сульфаты и ацетаты.
Этап 4 синтеза 2 может быть проведен с использованием тех же условий, что и этап 2 вышеупомянутого синтеза 1.
[0179] (Синтез 3)

X, Hal, p и q соответствуют описанным выше.
[0180] Этап 5 синтеза 3 представляет собой этап получения соединения (9) с помощью реакции соединения (3) и соединения (8) в растворителе и в присутствии основания.
Соединение (3) и соединение (8) известны или могут быть получены из известных соединений в соответствии с известным способом. Примеры соединения (3) соответствуют описанным выше.
Примеры соединения (8) включают 5,8-диокса-2-азаспиро[3.4]октан, 1,4-диокса-7-азаспиро[4.4]нонан, 1,4-диокса-8-азаспиро[4.5]декан и их кислые соли.
Примеры кислых солей соединения (8) включают гидрохлориды, сульфаты и ацетаты.
Этап 5 синтеза 3 может быть проведен с использованием тех же условий, что и этап 2 вышеупомянутого синтеза 1.
[0181] Этап 6 синтеза 3 включает этап получения соединения (6) путем снятия карбонильной защитной группы с соединения (9) в растворителе с помощью кислоты.
Примеры кислоты включают органические кислоты, такие как уксусная кислота, пара-толуолсульфоновая кислота или пара-толуолсульфонат пиридиния, и неорганические кислоты, такие как соляная кислота или хлорная кислота, причем предпочтительной является соляная кислота. Количество кислоты, используемой на 1 моль соединения (9), обычно составляет от 1 до 20 молярных количеств и, предпочтительно, от 1 до 10 молярных количеств соединения (9).
Отсутствуют особые ограничения в отношении используемого растворителя, при условии что он не ингибирует реакцию и в определенной степени растворяет исходные материалы, и его примеры включают воду, ароматические углеводороды, такие как бензол, толуол или ксилол, простые эфиры, такие как диэтиловый эфир, тетрагидрофуран, 1,4-диоксан или 1,2-диметоксиэтан, кетоны, такие как ацетон, метилэтилкетон, метилизобутилкетон или метил-трет-бутилкетон, и произвольную смесь этих растворителей, причем предпочтительным является ацетон. Хотя конкретные ограничения в этом отношении отсутствуют, количество используемого растворителя обычно составляет от 1 до 50 и, предпочтительно, от 5 до 20 масс соединения (9).
Несмотря на изменения в зависимости от таких факторов, как используемые типы и количества исходных материалов, растворителя и т.п., температура реакции обычно составляет от 0°C до 150°C и, предпочтительно, от 0°C до 100°C.
Несмотря на изменения в зависимости от таких факторов, как температура реакции, время реакции обычно составляет от 1 минуты до 48 часов и, предпочтительно, от 0,5 часа до 24 часов.
Хотя давление реакции при необходимости может быть установлено соответствующим образом, и реакция может быть проведена под давлением, при пониженном давлении или при атмосферном давлении, давление реакции, предпочтительно, представляет собой атмосферное давление. Хотя реакция может быть при необходимости проведена в соответствующим образом выбранной атмосфере, атмосфера реакции, предпочтительно, представляет собой воздушную атмосферу или атмосферу инертного газа, такую как атмосфера азота или аргона.
[0182] (Синтез 4)
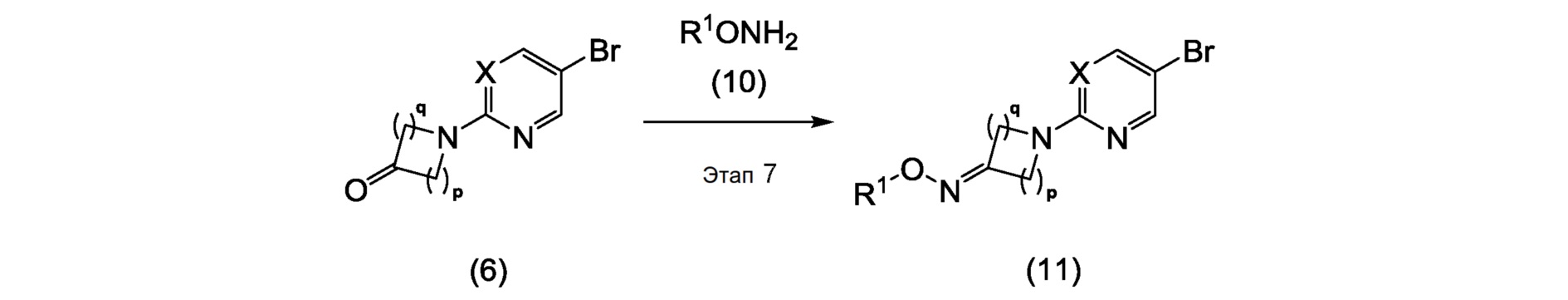
X, R1, p и q соответствуют описанным выше.
[0183] Этап 7 синтеза 4 представляет собой этап получения соединения (11) с помощью реакции соединения (6) и соединения (10) в растворителе и, необязательно, в присутствии основания.
Соединение (6) может быть получено в соответствии с любым из вышеупомянутых синтезов 1-3. Соединение (10) известно или может быть получено из известных соединений в соответствии с известным способом.
Соединение (10) известно или может быть получено из известных соединений в соответствии со ссылочными примерами настоящего описания, описанными ниже.
Соединение (10) может представлять собой кислую соль. Примеры кислых солей включают гидрохлориды, сульфаты и ацетаты.
Количество соединения (10), используемого на 1 моль соединения (6), обычно составляет от 0,9 до 10 молярных количеств и, предпочтительно, от 1,1 до 5 молярных количеств соединения (6).
Отсутствуют особые ограничения в отношении используемого растворителя, при условии что он не ингибирует реакцию и в определенной степени растворяет исходные материалы, и его примеры включают воду, спирты, такие как метанол, этанол, пропанол или изопропанол, простые эфиры, такие как тетрагидрофуран, 1,2-диметоксиэтан или 1,4-диоксан, нитрилы, такие как ацетонитрил или пропионитрил, и произвольную смесь этих растворителей. Предпочтительными являются вода, этанол, тетрагидрофуран или произвольная смесь этих растворителей. Хотя конкретные ограничения в этом отношении отсутствуют, количество используемого растворителя обычно составляет от 1 до 50 и, предпочтительно, от 5 до 30 масс соединения (6).
Примеры используемого основания включают ацетаты щелочных металлов, такие как ацетат натрия или ацетат калия, карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия или карбонат цезия, и органические основания, такие как триэтиламин или диизопропилэтиламин, причем предпочтительно используют карбонаты щелочных металлов, такие как карбонат натрия или карбонат калия. Количество основания, используемого на 1 моль соединения (6), обычно составляет от 0,9 до 10 молярных количеств и, предпочтительно, от 1 до 5 молярных количеств соединения (6).
Несмотря на изменения в зависимости от таких факторов, как используемые типы и количества исходных материалов, растворителя и т.п., температура реакции обычно составляет от 0°C до 150°C и, предпочтительно, от 20°C до 120°C.
Несмотря на изменения в зависимости от таких факторов, как температура реакции, время реакции обычно составляет от 1 минуты до 48 часов и, предпочтительно, от 0,5 часа до 24 часов.
Хотя давление реакции при необходимости может быть установлено соответствующим образом, и реакция может быть проведена под давлением, при пониженном давлении или при атмосферном давлении, давление реакции, предпочтительно, представляет собой атмосферное давление. Хотя реакция может быть при необходимости проведена в соответствующим образом выбранной атмосфере, атмосфера реакции, предпочтительно, представляет собой воздушную атмосферу или атмосферу инертного газа, такую как атмосфера азота или аргона.
[0184] (Синтез 5)

X, R1, p и q соответствуют описанным выше, а L представляет уходящую группу. Примеры уходящей группы L включают атом галогена, метансульфонилоксигруппу, трифторметансульфонилоксигруппу и пара-толуолсульфонилоксигруппу.
[0185] Этап 8 синтеза 5 представляет собой этап получения соединения (13) с помощью реакции соединения (6) с гидроксиламиновым соединением (12) или кислой солью гидроксиламина в растворителе.
Соединение (6) может быть получено в соответствии с любым из вышеупомянутых синтезов 1-3.
Примеры кислых солей гидроксиламиновых соединений (12) включают гидрохлорид гидроксиламина и сульфат гидроксиламина.
Гидроксиламиновые соединения (12) или кислые соли гидроксиламина известны и доступны у поставщика реагентов, такого как Tokyo Chemical Industry Co., Ltd. Количество гидрохлорида гидроксиламина, используемого на 1 моль соединения (6), обычно составляет от 0,9 до 5 молярных количеств и, предпочтительно, от 1,1 до 3 молярных количеств соединения (6).
Отсутствуют особые ограничения в отношении используемого растворителя, при условии что он не ингибирует реакцию и в определенной степени растворяет исходные материалы, и его примеры включают воду, спирты, такие как метанол, этанол, пропанол или изопропанол, простые эфиры, такие как тетрагидрофуран, 1,2-диметоксиэтан или 1,4-диоксан, нитрилы, такие как ацетонитрил или пропионитрил, и произвольную смесь этих растворителей. Предпочтительными являются вода, этанол, тетрагидрофуран или произвольная смесь этих растворителей. Хотя конкретные ограничения в этом отношении отсутствуют, количество используемого растворителя обычно составляет от 1 до 50 и, предпочтительно, от 5 до 30 масс соединения (6).
Несмотря на изменения в зависимости от таких факторов, как используемые типы и количества исходных материалов, растворителя и т.п., температура реакции обычно составляет от 0°C до 150°C и, предпочтительно, от 40°C до 120°C.
Несмотря на изменения в зависимости от таких факторов, как температура реакции, время реакции обычно составляет от 1 минуты до 48 часов и, предпочтительно, от 0,5 часа до 24 часов.
Хотя давление реакции при необходимости может быть установлено соответствующим образом, и реакция может быть проведена под давлением, при пониженном давлении или при атмосферном давлении, давление реакции, предпочтительно, представляет собой атмосферное давление. Хотя реакция может быть при необходимости проведена в соответствующим образом выбранной атмосфере, атмосфера реакции, предпочтительно, представляет собой воздушную атмосферу или атмосферу инертного газа, такую как атмосфера азота или аргона.
[0186] Этап 9 синтеза 5 представляет собой этап получения соединения (11) с помощью реакции соединения (13) и соединения (14) в растворителе и в присутствии основания.
Соединение (14) известно или может быть получено из известных соединений в соответствии со ссылочными примерами настоящего описания, приведенными ниже, и т.п. Количество соединения (14), используемого на 1 моль соединения (13), обычно составляет от 0,9 до 5 молярных количеств и, предпочтительно, от 1,1 до 3 молярных количеств соединения (13).
Отсутствуют особые ограничения в отношении используемого растворителя, при условии что он не ингибирует реакцию и в определенной степени растворяет исходные материалы, и его примеры включают ароматические углеводороды, такие как бензол, толуол или ксилол, галогенированные алифатические углеводороды, такие как метиленхлорид, хлороформ или 1,2-дихлорэтан, простые эфиры, такие как тетрагидрофуран, 1,2-диметоксиэтан или 1,4-диоксан, нитрилы, такие как ацетонитрил или пропионитрил, амиды, такие как N,N-диметилформамид, N,N-диметилацетамид или N-метилпирролидон, сульфоксиды, такие как диметилсульфоксид, и произвольную смесь этих растворителей. Предпочтительно, используют амиды, такие как N,N-диметилформамид или N-метилпирролидон. Хотя конкретные ограничения в этом отношении отсутствуют, количество используемого растворителя обычно составляет от 1 до 50 и, предпочтительно, от 5 до 30 масс соединения (13).
Примеры используемого основания включают ацетаты щелочных металлов, такие как ацетат натрия или ацетат калия, карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия или карбонат цезия, и органические основания, такие как триэтиламин или диизопропилэтиламин, причем предпочтительными являются карбонат калия, карбонат цезия, триэтиламин или диизопропилэтиламин. Количество основания, используемого на 1 моль соединения (13), обычно составляет от 0,9 до 10 молярных количеств и, предпочтительно, от 1 до 5 молярных количеств соединения (13).
Несмотря на изменения в зависимости от таких факторов, как используемые типы и количества исходных материалов, растворителя и т.п., температура реакции обычно составляет от 0°C до 150°C и, предпочтительно, от 20°C до 120°C.
Несмотря на изменения в зависимости от таких факторов, как температура реакции, время реакции обычно составляет от 1 минуты до 48 часов и, предпочтительно, от 0,5 часа до 24 часов.
Хотя давление реакции при необходимости может быть установлено соответствующим образом, и реакция может быть проведена под давлением, при пониженном давлении или при атмосферном давлении, давление реакции, предпочтительно, представляет собой атмосферное давление. Хотя реакция может быть при необходимости проведена в соответствующим образом выбранной атмосфере, атмосфера реакции, предпочтительно, представляет собой воздушную атмосферу или атмосферу инертного газа, такую как атмосфера азота или аргона.
[0187] (Синтез 6)

PG представляет защитную группу, и Y представляет группу бороновой кислоты или боронатный эфирный заместитель. Примеры боронатного заместителя Y включают диизопропилборонатную группу, пинаколборонатную группу, неопентилгликольборонатную группу и катехолборонатную группу.
[0188] Этап 10 синтеза 6 представляет собой этап получения соединения (16) путем введения защитной группы для гидроксильной группы соединения (15) в растворителе.
Соединение (15), а именно (2-бром-3-фторфенил)метанол, известно или может быть получено из известных соединений в соответствии с известным способом.
Введение защитной группы для гидроксильной группы может быть соответствующим образом осуществлено в соответствии с известным уровнем техники, например как описано в документе Protective Groups in Organic Synthesis, 4th Edition, T. W. Greene and P. G. M. Wuts, ed., John Wiley & Sons Inc., или примерах настоящего описания.
[0189] Этап 11 синтеза 6 представляет собой этап получения соединения (17) с помощью реакции соединения (16) с борилирующим реагентом в присутствии палладиевого катализатора и основания в растворителе и в атмосфере инертного газа для введения группы бороновой кислоты или боронатного эфирного заместителя.
Борилирующий реагент известен или может быть получен из известных соединений в соответствии с известным способом. Примеры борилирующих реагентов включают триметилборат, триизопропилборат, бис(пинаколато)диборан, бис(неопентилгликолято)диборан и бис(катехолато)диборан. Количество борилирующего реагента, используемого на 1 моль соединения (16), обычно составляет от 0,9 до 5 молярных количеств и, предпочтительно, от 1,1 до 3 молярных количеств соединения (16).
Отсутствуют особые ограничения в отношении используемого растворителя, при условии что он не ингибирует реакцию и растворяет исходные материалы, основание и катализатор в определенной степени, и его примеры включают ароматические углеводороды, такие как бензол или толуол, простые эфиры, такие как тетрагидрофуран, 1,2-диметоксиэтан или 1,4-диоксан, спирты, такие как метанол, этанол, пропанол или изопропанол, амиды, такие как N,N-диметилформамид, N,N-диметилацетамид или N-метилпирролидон, сульфоксиды, такие как диметилсульфоксид, нитрилы, такие как ацетонитрил, вода, и произвольную смесь этих растворителей, причем предпочтительными являются толуол, 1,4-диоксан, N,N-диметилформамид, диметилсульфоксид или ацетонитрил.
Примеры используемых инертных газов включают азот, гелий и аргон.
Примеры используемого палладиевого катализатора включают органические комплексы палладия, такие как тетракис(трифенилфосфин)палладий, дихлорид бис(трифенилфосфин)палладия или дихлорид 1,1'-бис(дифенилфосфино)ферроценпалладия, причем предпочтительным является дихлорид 1,1'-бис(дифенилфосфино)ферроценпалладия (II). Количество палладия, используемого как катализатор, на 1 моль соединения (16) обычно составляет от 0,0001 до 1 молярного количества и, предпочтительно, от 0,005 до 0,3 молярного количества соединения (16).
Примеры используемого основания включают ацетаты щелочных металлов, такие как ацетат натрия или ацетат калия, карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия или карбонат цезия, и органические основания, такие как триэтиламин или диизопропилэтиламин, причем предпочтительными являются ацетат натрия, ацетат калия или триэтиламин. Количество основания, используемого на 1 моль соединения (16), обычно составляет от 1 до 10 молярных количеств и, предпочтительно, от 1 до 5 молярных количеств соединения (16).
Несмотря на изменения в зависимости от таких факторов, как используемые типы и количества исходных материалов, растворителя и т.п., температура реакции обычно составляет от 0°C до 200°C и, предпочтительно, от 30°C до 150°C.
Несмотря на изменения в зависимости от таких факторов, как температура реакции, время реакции обычно составляет от 10 минут до 120 часов и, предпочтительно, от 0,5 часа до 48 часов.
Хотя давление реакции при необходимости может быть установлено соответствующим образом, и реакция может быть проведена под давлением, при пониженном давлении или при атмосферном давлении, давление реакции, предпочтительно, представляет собой атмосферное давление.
[0190] (Синтез 7)
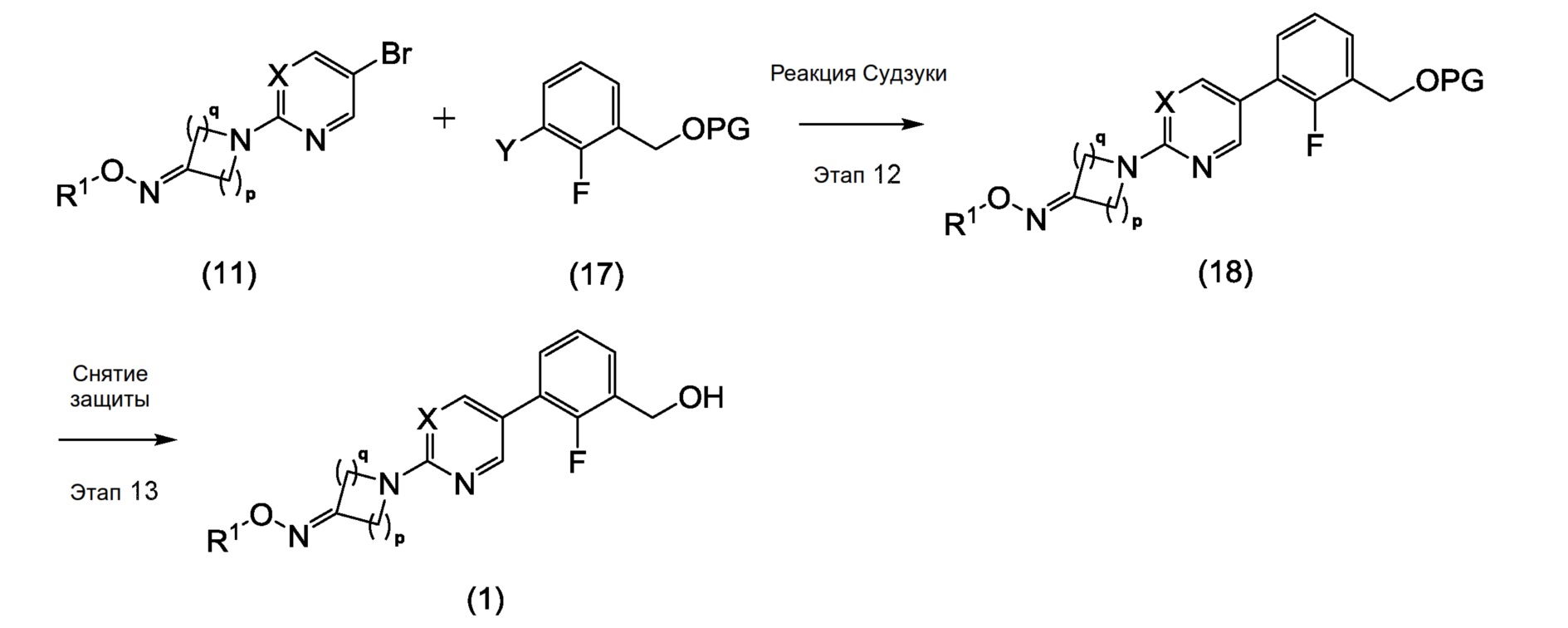
X, R1, Y, PG, p и q соответствуют описанным выше.
[0191] Этап 12 синтеза 7 представляет собой так называемую реакцию Судзуки для получения соединения (18) с помощью реакции соединения (11) и соединения (17) в растворителе и в присутствии основания или фторида и палладиевого катализатора в атмосфере инертного газа.
Соединение (11) может быть получено в соответствии с вышеупомянутым синтезом 4 или 5. Соединение (17) может быть получено в соответствии с вышеупомянутым синтезом 6. Количество соединения (17), используемого на 1 моль соединения (11), обычно составляет 0,8 до 3 молярных количеств и, предпочтительно, от 0,9 до 1,5 молярного количества соединения (11).
Отсутствуют особые ограничения в отношении используемого инертного растворителя, при условии что он не ингибирует реакцию и растворяет исходные материалы, катализатор и основание (или фторид) в определенной степени, и его примеры включают ароматические углеводороды, такие как бензол или толуол, простые эфиры, такие как тетрагидрофуран, 1,2-диметоксиэтан или 1,4-диоксан, спирты, такие как метанол, этанол, пропанол или изопропанол, амиды, такие как N,N-диметилформамид, N,N-диметилацетамид или N-метилпирролидон, сульфоксиды, такие как диметилсульфоксид, нитрилы, такие как ацетонитрил, воду и произвольную смесь этих растворителей, причем предпочтительными являются 1,2-диметоксиэтан, смешанный растворитель из 1,2-диметоксиэтана и воды, 1,4-диоксан, смешанный растворитель из 1,4-диоксана и воды, толуол, смешанный растворитель из толуола, этанола и воды или смешанный растворитель из толуола и воды.
Примеры используемого инертного газа включают азот, гелий и аргон.
Примеры используемого палладиевого катализатора включают металлические палладиевые катализаторы, такие как активированный палладием уголь или палладиевая сажа, органические комплексы палладия, такие как тетракис(трифенилфосфин)палладий, дихлорид бис(трифенилфосфин)палладия, дихлорид 1,1'-бис(дифенилфосфино)ферроценпалладия или трис(дибензилиденацетон)дипалладий, и соли палладия, такие как хлорид палладия или ацетат палладия, причем предпочтительным является тетракис(трифенилфосфин)палладий или ацетат палладия. Количество палладия, используемого как катализатор, на 1 моль соединения (11) обычно составляет от 0,0001 до 1 молярного количества и, предпочтительно, от 0,005 до 0,3 молярного количества соединения (11).
В случае использования как катализатора трис(дибензилиденацетон)дипалладия, хлорида палладия или ацетата палладия предпочтительно, чтобы также присутствовало органическое фосфиновое соединение. Примеры используемых органических фосфиновых соединений включают три-н-бутилфосфин, три-трет-бутилфосфин, трициклогексилфосфин, бутилди-1-адамантилфосфин, трифенилфосфин, три(о-толил)фосфин, 2-дициклогексилфосфино-2',6'-диметоксибифенил, 1,1'-бис(дифенилфосфино)ферроцен и 1,2,3,4,5-пентафенил-1'-(ди-трет-бутилфосфино)ферроцен, причем предпочтительными являются трициклогексилфосфин, бутилди-1-адамантилфосфин, трифенилфосфин или 2-дициклогексилфосфино-2',6'-диметоксибифенил. Количество органического фосфинового соединения, используемого на 1 моль палладия, обычно составляет от 1 до 5 молярных количеств и, предпочтительно, от 1,5 до 2,5 молярного количества палладия.
Примеры основания или фторида включают ацетаты щелочных металлов, такие как ацетат натрия или ацетат калия, карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия или карбонат цезия, фосфаты щелочных металлов, такие как фосфат тринатрия или фосфат трикалия, гидроксиды щелочных металлов, такие как гидроксид лития, гидроксид натрия или гидроксид калия, гидроксиды четвертичного аммония, такие как гидроксид тетраметиламмония, гидроксид тетраэтиламмония или гидроксид тетрабутиламмония, и фториды, такие как фторид цезия, фторид тетраметиламмония, фторид тетраэтиламмония или фторид тетрабутиламмония, причем предпочтительными являются карбонат натрия или фосфат трикалия. Количество основания или фторида, используемого на 1 моль соединения (11), обычно составляет от 1 до 10 молярных количеств и, предпочтительно, от 1,5 до 5 молярных количеств соединения (11).
Несмотря на изменения в зависимости от таких факторов, как используемые типы и количества исходных материалов, растворителя и т.п., температура реакции обычно составляет от 0°C до 200°C и, предпочтительно, от 50°C до 150°C.
Несмотря на изменения в зависимости от таких факторов, как температура реакции, время реакции обычно составляет от 10 минут до 120 часов и, предпочтительно, от 0,5 часа до 48 часов.
Хотя давление реакции при необходимости может быть установлено соответствующим образом, и реакция может быть проведена под давлением, при пониженном давлении или при атмосферном давлении, давление реакции, предпочтительно, представляет собой атмосферное давление.
[0192] Этап 13 синтеза 7 представляет собой этап получения соединения (1) путем подвергания соединения (18) снятию защиты для удаления его защитной группы PG.
Условия снятия защиты могут быть выбраны соответствующим образом в соответствии со способом, описанным в известном уровне техники, например в вышеупомянутом документе Protective Groups in Organic Synthesis, 4th Edition, T. W. Greene and P. G. M. Wuts, ed., John Wiley & Sons Inc., или примерах настоящего описания.
Кроме того, в случае, если соединение (18) содержит защитную группу, отличную от защитной группы PG, предпочтительно, удаляют только защитную группу PG с помощью соответствующего выбора условий снятия защиты.
[0193] (Синтез 8)

X, R1, Y, PG, p и q соответствуют описанным выше.
[0194] Этап 14 синтеза 8 представляет собой так называемую реакцию Судзуки для получения соединения (19) с помощью реакции соединения (6) и соединения (17) в растворителе и в присутствии основания или фторида и палладиевого катализатора в атмосфере инертного газа.
Соединение (6) может быть получено в соответствии с любым из вышеупомянутых синтезов 1-3. Соединение (17) может быть получено в соответствии с вышеупомянутым синтезом 6.
Этап 14 синтеза 8 может быть проведен с использованием тех же условий, что и этап 12 вышеупомянутого синтеза 7.
[0195] Этап 15 синтеза 8 представляет собой этап получения соединения (20) путем подвергания соединения (19) снятию защиты для удаления его защитной группы PG.
Условия снятия защиты могут быть выбраны соответствующим образом в соответствии со способом, описанным в известном уровне техники, например в вышеупомянутом документе Protective Groups in Organic Synthesis, 4th Edition, T. W. Greene and P. G. M. Wuts, ed., John Wiley & Sons Inc., или примерах настоящего описания.
Кроме того, в случае, если соединение (20) содержит защитную группу, отличную от защитной группы PG, предпочтительно, удаляют только защитную группу PG с помощью соответствующего выбора условий снятия защиты.
[0196] Этап 16 синтеза 8 представляет собой этап получения соединения (1) с помощью реакции соединения (20) и соединения (10) в присутствии растворителя и, необязательно, основания.
Этап 16 синтеза 8 может быть проведен с использованием тех же условий, что и этап 7 вышеупомянутого синтеза 4.
[0197] (Синтез 9)

X, R1, Y, PG, p и q соответствуют описанным выше.
[0198] Этап 17 синтеза 9 представляет собой так называемую реакцию Судзуки для получения соединения (21) с помощью реакции соединения (13) и соединения (17) в растворителе и в присутствии основания или фторида и палладиевого катализатора в атмосфере инертного газа.
Соединение (13) может быть получено в соответствии с этапом 8 вышеупомянутого синтеза 5. Соединение (17) может быть получено в соответствии с вышеупомянутым синтезом 6.
Этап 17 синтеза 9 может быть проведен с использованием тех же условий, что и этап 12 вышеупомянутого синтеза 7.
[0199] Этап 18 синтеза 9 представляет собой этап получения соединения (18) с помощью реакции соединения (21) и соединения (14) в растворителе и в присутствии основания.
Этап 18 синтеза 9 может быть проведен с использованием тех же условий, что и этап 9 вышеупомянутого синтеза 5.
[0200] Этап 19 синтеза 9 представляет собой этап получения соединения (1) путем подвергания соединения (18) снятию защиты для удаления его защитной группы PG, и он может быть проведен с использованием тех же условий, что и этап 13 вышеупомянутого синтеза 7.
[0201] (Синтез 10)

X, R1, Hal, Y, PG, p и q соответствуют описанным выше.
[0202] Этап 20 синтеза 10 представляет собой так называемую реакцию Судзуки для получения соединения (22) с помощью реакции соединения (3) и соединения (17) в растворителе и в присутствии основания или фторида и палладиевого катализатора в атмосфере инертного газа.
Соединение (3) известно или может быть получено из известных соединений в соответствии с известным способом. Соединение (17) может быть получено в соответствии с вышеупомянутым синтезом 6.
Этап 20 синтеза 10 может быть проведен с использованием тех же условий, что и этап 12 вышеупомянутого синтеза 7.
[0203] Этап 21 синтеза 10 представляет собой этап получения соединения (23) с помощью реакции соединения (22) и соединения (8) в растворителе и в присутствии основания.
Соединение (8) известно или может быть получено из известных соединений в соответствии с известным способом.
Этап 21 синтеза 10 может быть проведен с использованием тех же условий, что и этап 5 вышеупомянутого синтеза 3.
[0204] Этап 22 синтеза 10 представляет собой этап получения соединения (20) путем снятия защитной группы PG соединения (23) вместе с карбонильной защитной группой соединения (23) с помощью кислоты в растворителе.
Условия снятия защиты могут быть выбраны соответствующим образом в соответствии со способом, описанным в известном уровне техники, например в вышеупомянутом документе Protective Groups in Organic Synthesis, 4th Edition, T. W. Greene and P. G. M. Wuts, ed., John Wiley & Sons Inc., или ссылочных примерах настоящего описания.
[0205] Этап 23 синтеза 10 представляет собой этап получения соединения (1) с помощью реакции соединения (20) и соединения (10) в растворителе и в присутствии основания.
Этап 23 синтеза 10 может быть проведен с использованием тех же условий, что и этап 7 вышеупомянутого синтеза 4.
[0206] Соединение (1), используемое в способе получения 1, получают в соответствии с вышеупомянутыми синтезами 1-10. Однако соединение (1), используемое в способе получения 1, также может быть получено с помощью реакционной схемы, отличной от той, которая указана в вышеупомянутых синтезах 1-10, путем изменения подходящих комбинаций и/или подходящих порядков реакций в каждом из этапов и исходных материалов, указанных в вышеупомянутых синтезах 1-10, и путем введения и/или удаления подходящих защитных групп.
[0207] Хотя соединения, полученные на каждом этапе, могут быть выделены и очищены с помощью известных средств, эти соединения можно также использовать на следующем этапе как есть. Выделение и очистка могут быть проведены с использованием обычных фильтрации, экстракции, кристаллизации и различных процедур колоночной хроматографии.
[0208] В конкретном варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей соединение общей формулы (I), как указано в каждом из вышеупомянутых конкретных вариантов осуществления, или его фармакологически приемлемую соль, и, предпочтительно, относится к фармацевтической композиции, содержащей соединение общей формулы (I), как указано в каждом из вышеупомянутых конкретных вариантов осуществления, или его фармакологически приемлемую соль и фармакологически приемлемую добавку по меньшей мере одного типа.
[0209] В конкретном варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей соединение общей формулы (I), как указано в каждом из вышеупомянутых конкретных вариантов осуществления, или его фармакологически приемлемую соль, для лечения заболевания, предотвращаемого, облегчаемого и/или излечиваемого с помощью ингибирования VAP-1, и, предпочтительно, относится к фармацевтической композиции, содержащей соединение общей формулы (I), как указано в каждом из вышеупомянутых конкретных вариантов осуществления, или его фармакологически приемлемую соль и фармакологически приемлемую добавку по меньшей мере одного типа, для лечения заболевания, предотвращаемого, облегчаемого и/или излечиваемого с помощью ингибирования VAP-1.
[0210] В конкретном варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей соединение общей формулы (I), как указано в каждом из вышеупомянутых конкретных вариантов осуществления, или его фармакологически приемлемую соль, для лечения диабетической нефропатии и, предпочтительно, относится к фармацевтической композиции, содержащей соединение общей формулы (I), как указано в каждом из вышеупомянутых конкретных вариантов осуществления, или его фармакологически приемлемую соль и фармакологически приемлемую добавку по меньшей мере одного типа, для лечения диабетической нефропатии.
[0211] В конкретном варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей соединение общей формулы (I), как указано в каждом из вышеупомянутых конкретных вариантов осуществления, или его фармакологически приемлемую соль, для лечения неалкогольного стеатогепатита и, предпочтительно, относится к фармацевтической композиции, содержащей соединение общей формулы (I), как указано в каждом из вышеупомянутых конкретных вариантов осуществления, или его фармакологически приемлемую соль и фармакологически приемлемую добавку по меньшей мере одного типа, для лечения неалкогольного стеатогепатита.
[0212] Фармацевтическая композиция, содержащая соединение общей формулы (I) или его фармакологически приемлемую соль, может иметь форму соединения per se (форму нефасованного порошка), или может иметь форму препарата, такого как таблетка, капсула, порошок, сироп, гранула, зерно, пилюля, суспензия, эмульсия, чрескожный абсорбент, суппозиторий, мазь, лосьон, ингалятор, офтальмологический раствор или инъекция, получаемого смешиванием с подходящими фармакологически приемлемыми добавками и т.п., и может быть введена перорально или парентерально (в том числе с помощью внутривенного, внутримышечного, внутрибрюшинного, трансдермального, трансназального, транстрахеального, транспульмонарного, офтальмического, внутрикожного или подкожного введения).
Эти препараты получают известными способами с использованием таких добавок, как вспомогательные вещества, смазывающие вещества, связующие вещества, дезинтегрирующие средства, эмульгаторы, стабилизаторы, корректоры, разбавители, изотонические средства, буферы, регуляторы pH, солюбилизаторы, загустители, диспергаторы или консерванты (антисептики).
[0213] Примеры вспомогательных веществ включают органические вспомогательные вещества и неорганические вспомогательные вещества. Примеры органических вспомогательных веществ включают производные сахара, такие как лактоза, сахароза, глюкоза, маннит или сорбит, производные крахмала, такие как кукурузный крахмал, картофельный крахмал, α-крахмал или декстрин, производные целлюлозы, такие как кристаллическая целлюлоза, гуммиарабик, декстран и пуллулан. Примеры неорганических вспомогательных веществ включают легкую безводную кремниевую кислоту и сульфаты, такие как сульфат кальция.
[0214] Примеры смазывающих веществ включают стеариновую кислоту, стеараты металлов, такие как стеарат кальция или стеарат магния, тальк, коллоидный кремнезем, воски, такие как пчелиный воск или спермацет, борную кислоту, адипиновую кислоту, сульфаты, такие как сульфат натрия, гликоль, фумаровую кислоту, бензоат натрия, D,L-лейцин, лаурилсульфат натрия, кремниевые кислоты, такие как безводная кремниевая кислота или гидрат кремниевой кислоты, и производные крахмала, перечисленные в качестве примеров вышеупомянутых вспомогательных веществ.
[0215] Примеры связующих веществ включают гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, поливинилпирролидон, макрогол и соединения, перечисленные в качестве примеров вышеупомянутых вспомогательных веществ.
[0216] Примеры дезинтегрирующих средств включают производные целлюлозы, такие как низкозамещенная гидроксипропилцеллюлоза, карбоксиметилцеллюлоза, карбоксиметилцеллюлоза кальция или сшитая внутри карбоксиметилцеллюлоза кальция, сшитый поливинилпирролидон и химически модифицированные производные крахмала или целлюлозы, такие как карбоксиметилкрахмал или карбоксиметилкрахмал натрия.
[0217] Примеры эмульгаторов включают коллоидную глину, такую как бентонит или вигум, анионные поверхностно-активные вещества, такие как лаурилсульфат натрия, катионные поверхностно-активные вещества, такие как хлорид бензалкония, и неионогенные поверхностно-активные вещества, такие как полиоксиэтиленалкиловый эфир, сложный эфир полиоксиэтиленсорбитана и жирной кислоты или сложный эфир сахарозы и жирной кислоты.
[0218] Примеры стабилизаторов включают парагидроксибензоаты, такие как метилпарабен или пропилпарабен, спирты, такие как хлорбутанол, бензиловый спирт или фенилэтиловый спирт, хлорид бензалкония, фенолы, такие как фенол или крезол, тимеросал, уксусный ангидрид и сорбиновую кислоту.
[0219] Примеры корректоров включают подсластители, такие как сахарин натрия или аспартам, подкислители, такие как лимонная кислота, яблочная кислота или винная кислота, и ароматические вещества, такие как ментол, экстракт лимона или экстракт апельсина.
[0220] Примеры разбавителей включают воду, лактозу, маннит, глюкозу, сахарозу, сульфат кальция, гидроксипропилцеллюлозу, микрокристаллическую целлюлозу, воду, этанол, полиэтиленгликоль, пропиленгликоль, глицерин, крахмал, поливинилпирролидон и их смеси.
[0221] Примеры изотонических средств включают глицерин, пропиленгликоль, хлорид натрия, хлорид калия, сорбит и маннит.
[0222] Примеры буферов включают фосфорную кислоту, фосфаты, лимонную кислоту, уксусную кислоту и ε-аминокапроновую кислоту.
[0223] Примеры регуляторов рН включают соляную кислоту, лимонную кислоту, фосфорную кислоту, уксусную кислоту, гидроксид натрия, гидроксид калия, борную кислоту, буру, карбонат натрия и бикарбонат натрия.
[0224] Примеры солюбилизаторов включают полисорбат 80, полиоксиэтиленгидрированное касторовое масло 60 и макрогол 4000.
[0225] Примеры загустителей и диспергаторов включают целлюлозные полимеры, такие как гидроксипропилметилцеллюлоза или гидроксипропилцеллюлоза, поливиниловый спирт и поливинилпирролидон, тогда как примеры стабилизаторов включают эдетовую кислоту и эдетат натрия.
[0226] Примеры консервантов (антисептиков) включают сорбиновую кислоту общего назначения, сорбат калия, хлорид бензалкония, хлорид бензетония, метилпарагидроксибензоат, пропилпарагидроксибензоат и хлорбутанол, и эти консерванты также можно использовать в комбинации.
[0227] Также в соответствии с формой введения могут быть использованы другие подходящие добавки. Например, в случае, когда соединение настоящего изобретения общей формулы (I) или его фармакологически приемлемая соль имеют форму аэрозоля для трансназального или транстрахеального введения, в качестве пропеллента можно использовать диоксид углерода или хлорфторуглерод (CFC), такой как дихлордифторметан, трихлорфторметан или дихлортетрафторэтан.
[0228] Несмотря на возможность изменения в зависимости от таких условий, как симптомы, возраст или вес тела пациента, дозировка активного ингредиента фармацевтической композиции настоящего изобретения имеет нижний предел 0,001 мг/кг (и, предпочтительно, 0,01 мг/кг) и верхний предел 20 мг/кг (и, предпочтительно, 10 мг/кг) на введение в случае перорального введения, или нижний предел 0,0001 мг/кг (и, предпочтительно, 0,0005 мг/кг) и верхний предел 10 мг/кг (и, предпочтительно, 5 мг/кг) на введение в случае парентерального введения при введении взрослым от одного до шести раз в день в соответствии с симптомами.
[0229] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (I), как указано в каждом из вышеупомянутых конкретных вариантов осуществления, или его фармакологически приемлемой соли для применения в лечении заболевания, предотвращаемого, облегчаемого и/или излечиваемого с помощью ингибирования VAP-1.
[0230] В конкретном варианте осуществления настоящее изобретение относится к соединению общей формулы (I), как указано в каждом из вышеупомянутых конкретных вариантов осуществления, или его фармакологически приемлемой соли для получения лекарственного средства для лечения заболевания, предотвращаемого, облегчаемого и/или излечиваемого с помощью ингибирования VAP-1.
[0231] В конкретном варианте осуществления настоящее изобретение относится к способу лечения заболевания, предотвращаемого, облегчаемого и/или излечиваемого с помощью ингибирования VAP-1, который включает в себя введение терапевтически эффективного количества соединения общей формулы (I), как указано в каждом из вышеупомянутых конкретных вариантов осуществления, или его фармакологически приемлемой соли нуждающемуся в этом пациенту.
[0232] В настоящем изобретении термины "лечение" заболевания или "излечивание" заболевания включают в себя (1) предупреждение заболевания или, другими словами, не допущение появления клинических симптомов заболевания у субъекта, у которого, хотя есть вероятность того, что он подвергался воздействию заболевания или восприимчив к заболеванию, еще не проявляются или не обнаруживаются симптомы заболевания, (2) подавление заболевания или, другими словами, подавление возникновения заболевания или его клинических симптомов или (3) облегчение заболевания или, другими словами, индуцирование временного или постоянного ослабления заболевания или его клинических симптомов.
[0233] В настоящем изобретении "терапевтически эффективное количество" обозначает в случае введения субъекту количество соединения настоящего изобретения общей формулы (I), которое (i) лечит или предотвращает заболевание, (ii) ослабляет, облегчает или устраняет один или несколько симптомов заболевания или (iii) предотвращает или задерживает проявление одного или нескольких симптомов заболевания. Терапевтически эффективное количество изменяется в зависимости от используемого соединения настоящего изобретения общей формулы (I), подвергаемого лечению болезненного состояния, тяжести подвергаемого лечению заболевания, возраста и относительного состояния здоровья субъекта, способа и формы введения, решения проводящего обследование врача или ветеринара и других факторов.
Примеры
[0234] Силикагель DIOL в колоночной хроматографии на силикагеле обозначает CHROMATOREX (торговое наименование) DIOL MB 100-40/75 производства Fuji Silysia Chemical Ltd.
Силикагель DNH в колоночной хроматографии на силикагеле обозначает CHROMATOREX (торговое наименование) DNH MB 100-40/75 производства Fuji Silysia Chemical Ltd.
DUIS режима ионизации в масс-спектроскопии представляет собой смешанный режим ESI и APCI.
Если не указано иное, спектры1H-ЯМР приведены в химических сдвигах (δ) относительно тетраметилсилана как внутреннего стандарта (0 м.д.), а константы взаимодействия (значения J) указаны в единицах Гц. Варианты расщепления пиков указаны следующими сокращениями: s: синглет, d: дублет, t: триплет, q: квадруплет, quin: квинтиплет, sext: секситиплет, sep: септиплет, br s: уширенный синглет, m: мультиплет.
Сокращения, приведенные в примерах и ссылочных примерах, имеют общие значения, которые обычно используются в областях органической химии и фармацевтики. В частности, эти сокращения понимаются специалистами в данной области техники следующим образом.
TEA: триэтиламин
DIPEA: N,N-диизопропилэтиламин
DMF: N,N-диметилформамид
DMSO: диметилсульфоксид
THF: тетрагидрофуран
CDI: 1,1'-карбонилдиимидазол
TBME: трет-бутилметиловый эфир
DHP: 3,4-дигидро-2H-пиран
PPTS: пиридиния пара-толуолсульфонат
DMAP: N,N-диметил-4-аминопиридин
BAST: бис(2-метоксиэтил)аминосеры трифторид
NMP: N-метилпирролидон
TBS: трет-бутилдиметилсилил
THP: тетрагидропиран-2-ил
Соединения, использованные в примерах, синтезировали следующим образом.
[0235] [Примеры]
(Пример 1)
2-Фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-2)

CDI, 1,91 г (11,8 ммоль), добавляли к раствору в DMF (20 мл) 1-[5-(2-фтор-3-гидроксиметилфенил)пиримидин-2-ил]азетидин-3-она O-метилоксима, 1,78 г (5,89 ммоль), синтезированного таким же образом, как в ссылочном примере 7-1, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 2,12 г (11,8 ммоль), и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции к реакционной смеси добавляли воду, смесь перемешивали при комнатной температуре, и осажденное твердое вещество собирали с помощью фильтрации. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 50°C в течение 1 часа. Твердое вещество затем собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 2,09 г (5,40 ммоль, выход 92%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 388[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (br s, 2H), 7,54-7,47 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,85-4,78 (m, 4H), 3,83 (s, 3H).
[0236] (Пример 2)
3-{2-[3-(Этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат (соединение II-3)

DMF, 2,6 мл, добавляли к 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-этилоксиму, 80,5 мг (0,254 ммоль), синтезированному таким же образом, как в ссылочном примере 7-2, и CDI, 96,3 мг (0,594 ммоль). Смесь обрабатывали ультразвуком и перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 98,4 мг (0,546 ммоль), и смесь обрабатывали ультразвуком и перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли 15 мл метиленхлорида и 25 мл воды, и смесь перемешивали и охлаждали с помощью льда. Осажденное твердое вещество собирали с помощью фильтрации, промывали водой и диэтиловым эфиром и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 59,7 мг (0,149 ммоль, выход 58%) в виде сероватого белого твердого вещества.
Масс-спектр (DUIS, m/z): 402[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (s, 2H), 7,58-7,47 (m, 1H), 7,46-7,39 (m, 1H), 7,36-7,27 (m, 1H), 5,06 (s, 2H), 4,87-4,76 (m, 4H), 4,09 (q, J=7,0 Гц, 2H), 1,22 (t, J=7,0 Гц, 3H).
[0237] (Пример 3)
2-Фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-12)

CDI, 140 мг (0,863 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-метил-d3-оксима, 124 мг (0,406 ммоль), синтезированного таким же образом, как в ссылочном примере 7-3, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 150 мг (0,833 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 143 мг (0,366 ммоль, выход 90%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 391[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (br s, 2H), 7,55-7,47 (m, 1H), 7,46-7,38 (m, 1H), 7,34-7,25 (m, 1H), 5,06 (s, 2H), 4,86-4,76 (m, 4H).
[0238] (Пример 4)
3-[2-(3-{[(трет-Бутилдиметилсилил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-62)

DMF, 3 мл, добавляли к 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(трет-бутилдиметилсилил)оксиму, 129 мг (0,320 ммоль), синтезированному таким же образом, как в ссылочном примере 13-1, и CDI, 119 мг (0,734 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 125 мг (0,694 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли 20 мл воды, и смесь перемешивали. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 75°C. После естественного охлаждения добавляли диизопропиловый эфир, и смесь перемешивали при комнатной температуре. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 94,6 мг (0,194 ммоль, выход 61%) в виде белого твердого вещества.
Масс-спектр (DUIS, m/z): 488[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,55-7,47 (m, 1H), 7,45-7,37 (m, 1H), 7,32-7,26 (m, 1H), 5,06 (s, 2H), 4,89-4,78 (m, 4H), 0,92 (s, 9H), 0,16 (s, 6H).
[0239] (Пример 5)
2-Фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-15)

CDI, 160 мг (0,99 ммоль), добавляли к раствору в DMF (5 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(2-фторэтил)оксима, 150 мг (0,45 ммоль), синтезированного таким же образом, как в ссылочном примере 7-4, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 160 мг (0,89 ммоль), и смесь перемешивали при комнатной температуре в течение 2,5 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол) с получением указанного в заголовке соединения в количестве 63 мг (0,15 ммоль, выход 33%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 420[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,0 Гц, 2H), 7,55-7,47 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,88-4,80 (m, 4H), 4,73-4,55 (m, 2H), 4,34-4,21 (m, 2H).
[0240] (Пример 6)
3-(2-{3-[(2,2-Дифторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-18)

CDI, 74 мг (0,46 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(2,2-дифторэтил)оксима, 80 мг (0,23 ммоль), синтезированного таким же образом, как в ссылочном примере 7-5, и смесь перемешивали при комнатной температуре в течение 16 часов. Затем добавляли карбонат гуанидина, 82 мг (0,46 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 66 мг (0,15 ммоль, выход 65%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 438[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,66-8,61 (m, 2H), 7,55-7,47 (m, 1H), 7,46-7,38 (m, 1H), 7,34-7,26 (m, 1H), 6,25 (tt, J=3,6, 54,8 Гц, 1H), 5,06 (s, 2H), 4,89-4,81 (m, 4H), 4,32 (dt, J=3,6, 14,6 Гц, 2H).
[0241] (Пример 7)
2-Фтор-3-(2-{3-[(2,2,2-трифторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-19)

CDI, 120 мг (0,740 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(2,2,2-трифторэтил)оксима, 124 мг (0,335 ммоль), синтезированного таким же образом, как в ссылочном примере 7-6, и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли карбонат гуанидина, 120 мг (0,666 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 80,8 мг (0,177 ммоль, выход 53%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 456[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,4 Гц, 2H), 7,54-7,48 (m, 1H), 7,45-7,40 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,92-4,83 (m, 4H), 4,70 (q, J=9,0 Гц, 2H).
[0242] (Пример 8)
2-Фтор-3-(2-{3-[(3-фторпропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-20)

CDI, 89 мг (0,55 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(3-фторпропил)оксима, 96 мг (0,28 ммоль), синтезированного таким же образом, как в ссылочном примере 7-7, и смесь перемешивали при комнатной температуре в течение 17 часов. Затем добавляли карбонат гуанидина, 99 мг (0,55 ммоль), и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 0,10 г (0,23 ммоль, выход 82%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 434[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,66-8,60 (m, 2H), 7,54-7,48 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,86-4,79 (m, 4H), 4,54 (td, J=6,0, 47,2 Гц, 2H), 4,14 (t, J=6,3 Гц, 2H), 2,12-1,90 (m, 2H).
[0243] (Пример 9)
2-Фтор-3-{2-[3-({2-[(тетрагидропиран-2-ил)окси]этокси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-67)
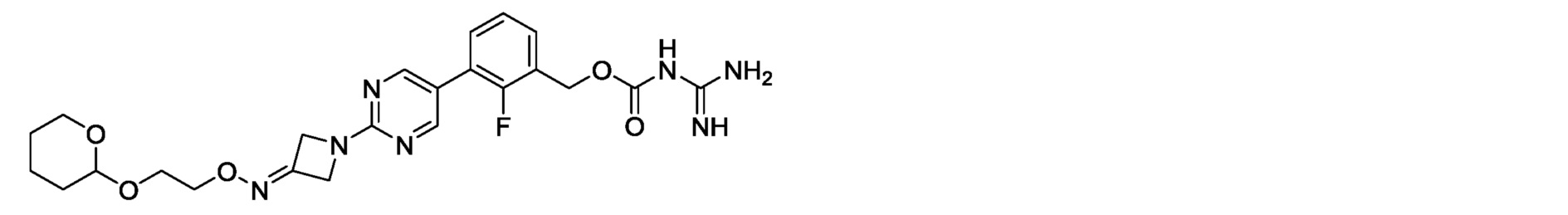
CDI, 74 мг (0,46 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-{2-[(тетрагидропиран-2-ил)окси]этил}оксима, 94 мг (0,23 ммоль), синтезированного таким же образом, как в ссылочном примере 7-8, и смесь перемешивали при комнатной температуре в течение 7 часов. Затем добавляли карбонат гуанидина, 81 мг (0,45 ммоль), и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 85 мг (0,17 ммоль, выход 74%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (d, J=1,3 Гц, 2H), 7,56-7,46 (m, 1H), 7,45-7,37 (m, 1H), 7,33-7,25 (m, 1H), 5,06 (s, 2H), 4,90-4,75 (m, 4H), 4,63-4,57 (m, 1H), 4,23-4,12 (m, 2H), 3,87-3,70 (m, 2H), 3,67-3,57 (m, 1H), 3,49-3,38 (m, 1H), 1,82-1,34 (m, 6H).
[0244] (Пример 10)
2-Фтор-3-{2-[3-({3-[(тетрагидропиран-2-ил)окси]пропокси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-68)

CDI, 136 мг (0,839 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-{3-[(тетрагидропиран-2-ил)окси]пропил}оксима, 180 мг (0,418 ммоль), синтезированного таким же образом, как в ссылочном примере 7-9, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 151 мг (0,838 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 145 мг (0,281 ммоль, выход 67%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,4 Гц, 2H), 7,57-7,47 (m, 1H), 7,46-7,39 (m, 1H), 7,34-7,24 (m, 1H), 5,07 (s, 2H), 4,86-4,78 (m, 4H), 4,62-4,48 (m, 1H), 4,11 (t, J=6,4 Гц, 2H), 3,81-3,63 (m, 2H), 3,52-3,37 (m, 2H), 1,87 (quin, J=6,4 Гц, 2H), 1,76-1,38 (m, 6H).
[0245] (Пример 11)
2-Фтор-3-{2-[3-({4-[(тетрагидропиран-2-ил)окси]бутокси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-69)

CDI, 160 мг (0,987 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-{4-[(тетрагидропиран-2-ил)окси]бутил}оксима, 190 мг (0,427 ммоль), синтезированного таким же образом, как в ссылочном примере 7-10, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 160 мг (0,888 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 50°C в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 166 мг (0,313 ммоль, выход 73%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 530[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,0 Гц, 2H), 7,54-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,86-4,77 (m, 4H), 4,56-4,52 (m, 1H), 4,09-4,01 (m, 2H), 3,77-3,31 (m, 4H), 1,76-1,36 (m, 10H).
[0246] (Пример 12)
2-Фтор-3-(2-{3-[(2-метоксиэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-26)

CDI, 62 мг (0,38 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(2-метоксиэтил)оксима, 66 мг (0,19 ммоль), синтезированного таким же образом, как в ссылочном примере 7-11, и смесь перемешивали при комнатной температуре в течение 7 часов. Затем добавляли карбонат гуанидина, 70 мг (0,39 ммоль), и смесь перемешивали при комнатной температуре в течение 19 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 73 мг (0,17 ммоль, выход 89%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 432[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,4 Гц, 2H), 7,54-7,47 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,86-4,78 (m, 4H), 4,18-4,12 (m, 2H), 3,60-3,54 (m, 2H), 3,27 (s, 3H).
[0247] (Пример 13)
2-Фтор-3-(2-{3-[(2-{2-[(тетрагидропиран-2-ил)окси]этокси}этокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-70)

CDI, 85 мг (0,52 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-{2-[(тетрагидропиран-2-ил)окси]этокси}этил]оксима, 105 мг (0,228 ммоль), синтезированного таким же образом, как в ссылочном примере 7-12, и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли карбонат гуанидина, 85 мг (0,47 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 98 мг (0,18 ммоль, выход 79%) в виде белой пены.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,54-7,48 (m, 1H), 7,46-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,86-4,78 (m, 4H), 4,60-4,56 (m, 1H), 4,18-4,12 (m, 2H), 3,78-3,38 (m, 8H), 1,76-1,34 (m, 6H).
[0248] (Пример 14)
[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]метилпивалат (соединение II-31)

CDI, 30 мг (0,19 ммоль), добавляли к раствору в DMF (2 мл) {[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}метилпивалата, 34 мг (0,084 ммоль), синтезированного таким же образом, как в ссылочном примере 7-13, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 30 мг (0,17 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: этилацетат:метанол) и (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 22 мг (0,045 ммоль, выход 54%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 488[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (s, 2H), 7,54-7,47 (m, 1H), 7,46-7,39 (m, 1H), 7,33-7,26 (m, 1H), 5,68 (s, 2H), 5,06 (s, 2H), 4,90-4,80 (m, 4H), 1,17 (s, 9H).
[0249] (Пример 15)
3-[2-(3-{[(2,2-Диметил-1,3-диоксан-5-ил)метокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-76)
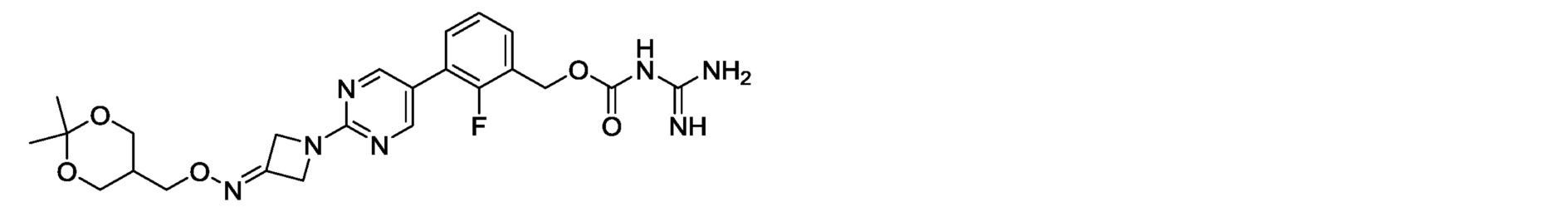
CDI, 183 мг (1,13 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксима, 147 мг (0,353 ммоль), синтезированного таким же образом, как в ссылочном примере 7-14, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 130 мг (0,722 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 90:10 (об/об)) с получением указанного в заголовке соединения в количестве 149 мг (0,297 ммоль, выход 84%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 502[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,1 Гц, 2H), 7,54-7,48 (m, 1H), 7,44-7,39 (m, 1H), 7,32-7,27 (m, 1H), 5,06 (s, 2H), 4,86-4,79 (m, 4H), 4,09 (d, J=7,0 Гц, 2H), 3,91 (dd, J=4,0, 11,9 Гц, 2H), 3,66 (dd, J=6,1, 11,9 Гц, 2H), 2,02-1,95 (m, 1H), 1,34 (s, 3H), 1,31 (s, 3H).
[0250] (Пример 16)
3-[2-(3-{[(2,2-Диметил-1,3-диоксолан-4-ил)метокси)]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-77)

CDI, 173 мг (1,07 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксима, 143 мг (0,355 ммоль), синтезированного таким же образом, как в ссылочном примере 7-15, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 128 мг (0,710 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 90:10 (об/об)) с получением указанного в заголовке соединения в количестве 137 мг (0,281 ммоль, выход 79%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 488[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,54-7,48 (m, 1H), 7,44-7,40 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,87-4,79 (m, 4H), 4,34-4,27 (m, 1H), 4,10-4,02 (m, 3H), 3,68 (dd, J=6,4, 8,4 Гц, 1H), 1,34 (s, 3H), 1,28 (s, 3H).
[0251] (Пример 17)
2-Фтор-3-(2-{3-[(3-метокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-80)

CDI, 92 мг (0,57 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(3-метокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксима, 134 мг (0,282 ммоль), синтезированного таким же образом, как в ссылочном примере 7-16, и смесь перемешивали при комнатной температуре в течение 4 часов. Затем добавляли карбонат гуанидина, 102 мг (0,566 ммоль), и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 129 мг (0,231 ммоль, выход 82%) в виде бесцветного масла.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,55-7,48 (m, 1H), 7,46-7,38 (m, 1H), 7,35-7,26 (m, 1H), 5,06 (s, 2H), 4,88-4,77 (m, 4H), 4,58-4,52 (m, 1H), 4,12-4,03 (m, 2H), 3,77-3,56 (m, 2H), 3,47-3,34 (m, 4H), 3,25 (s, 3H), 2,29-2,12 (m, 1H), 1,86-1,36 (m, 6H).
[0252] (Пример 18)
2-Фтор-3-[2-(3-{[2-метокси-3-(тритилокси)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-89)

CDI, 62 мг (0,38 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-метокси-3-(тритилокси)пропил]оксима, 0,12 г (0,19 ммоль), синтезированного таким же образом, как в ссылочном примере 7-17, и смесь перемешивали при комнатной температуре в течение 16 часов. Затем добавляли карбонат гуанидина, 68 мг (0,38 ммоль), и смесь перемешивали при комнатной температуре в течение 5 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 0,12 г (0,17 ммоль, выход 89%) в виде белой пены.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,65 (d, J=1,3 Гц, 2H), 7,57-7,19 (m, 18H), 5,07 (s, 2H), 4,85-4,77 (m, 2H), 4,73-4,53 (m, 2H), 4,18-4,06 (m, 2H), 3,66-3,59 (m, 1H), 3,34 (s, 3H), 3,21-2,98 (m, 2H).
[0253] (Пример 19)
3-[2-(3-{[2-(2,2-Диметил-1,3-диоксолан-4-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-78)

CDI, 70 мг (0,43 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксима, 90 мг (0,22 ммоль), синтезированного таким же образом, как в ссылочном примере 7-18, и смесь перемешивали при комнатной температуре в течение 6 часов. Затем добавляли карбонат гуанидина, 78 мг (0,43 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 0,10 г (0,20 ммоль, выход 91%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,55-7,48 (m, 1H), 7,46-7,39 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,86-4,78 (m, 4H), 4,17-4,05 (m, 3H), 4,02 (dd, J=6,0, 8,0 Гц, 1H), 3,61-3,44 (m, 1H), 1,95-1,78 (m, 2H), 1,32 (s, 3H), 1,27 (s, 3H).
[0254] (Пример 20)
1-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-3-метоксипропан-2-илацетат (соединение II-52)
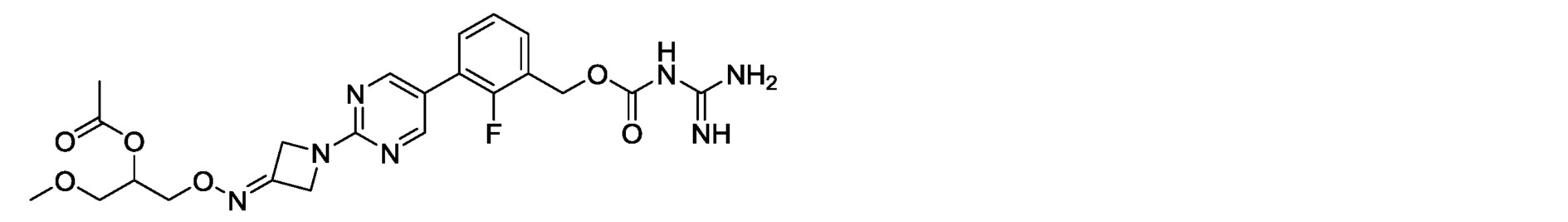
CDI, 52 мг (0,32 ммоль), добавляли к раствору в DMF (4 мл) 1-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-3-метоксипропан-2-илацетата, 66 мг (0,16 ммоль), синтезированного таким же образом, как в ссылочном примере 7-19, и смесь перемешивали при комнатной температуре в течение 17 часов. Затем добавляли карбонат гуанидина, 57 мг (0,32 ммоль), и смесь перемешивали при комнатной температуре в течение 6 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 58 мг (0,12 ммоль, выход 75%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 504[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,56-7,47 (m, 1H), 7,47-7,39 (m, 1H), 7,34-7,27 (m, 1H), 5,20-5,13 (m, 1H), 5,07 (s, 2H), 4,88-4,73 (m, 4H), 4,22-4,09 (m, 2H), 3,57-3,44 (m, 2H), 3,27 (s, 3H), 2,04 (s, 3H).
[0255] (Пример 21)
2-Фтор-3-(2-{3-[(3-фтор-2-{[(тетрагидропиран-2-ил)окси]метил}пропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-75)
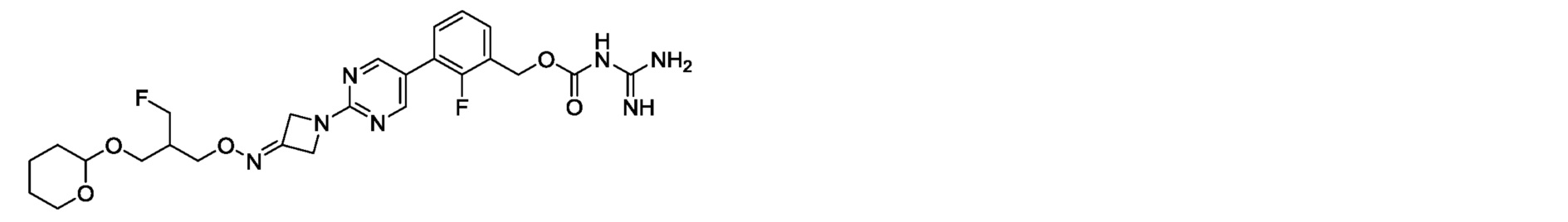
CDI, 68 мг (0,42 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(3-фтор-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксима, 65 мг (0,14 ммоль), синтезированного таким же образом, как в ссылочном примере 7-20, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли CDI, 30 мг (0,23 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. Затем добавляли карбонат гуанидина, 51 мг (0,28 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси три раза добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 90:10 (об/об)) с получением указанного в заголовке соединения в количестве 52 мг (0,095 ммоль, выход 68%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 548[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,4 Гц, 2H), 7,54-7,48 (m, 1H), 7,45-7,40 (m, 1H), 7,33-7,28 (m, 1H), 5,06 (s, 2H), 4,87-4,80 (m, 4H), 4,64-4,42 (m, 3H), 4,16-4,07 (m, 2H), 3,77-3,62 (m, 2H), 3,49-3,40 (m, 2H), 2,42-2,30 (m, 1H), 1,76-1,58 (m, 2H), 1,54-1,41 (m, 4H).
[0256] (Пример 22)
2-Фтор-3-[2-(3-{[2-фтор-3-(тритилокси)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-90)
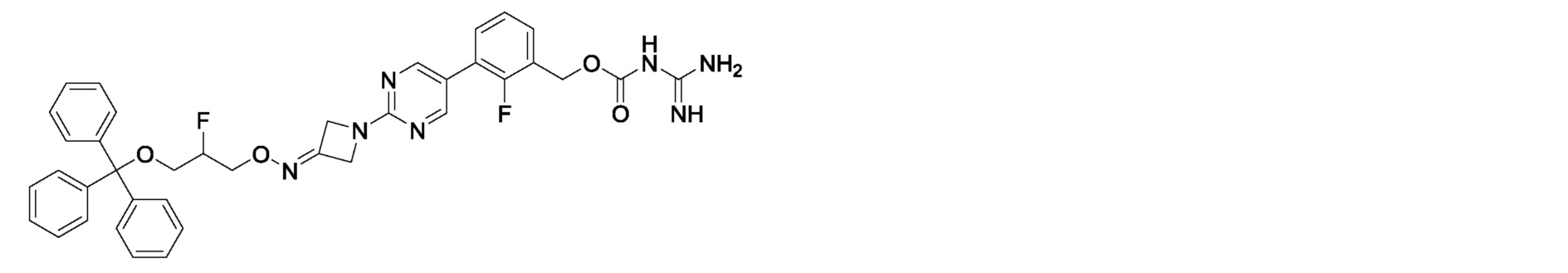
CDI, 1,0 г (6,2 ммоль), добавляли к раствору в DMF (16 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-фтор-3-(тритилокси)пропил]оксима, 1,7 г (2,8 ммоль), синтезированного таким же образом, как в ссылочном примере 7-21, и смесь перемешивали при комнатной температуре в течение 18 часов. Затем добавляли карбонат гуанидина, 1,1 г (6,1 ммоль), и смесь перемешивали при комнатной температуре в течение 20 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 1,9 г (2,7 ммоль, выход 96%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,65 (d, J=1,4 Гц, 2H), 7,58-7,22 (m, 18H), 5,08 (s, 2H), 5,04-4,85 (m, 1H), 4,84-4,78 (m, 2H), 4,76-4,62 (m, 2H), 4,47-4,14 (m, 2H), 3,37-3,13 (m, 2H).
[0257] (Пример 23)
2-Фтор-3-{2-[3-({3-метокси-4-[(тетрагидропиран-2-ил)окси]бутокси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-81)
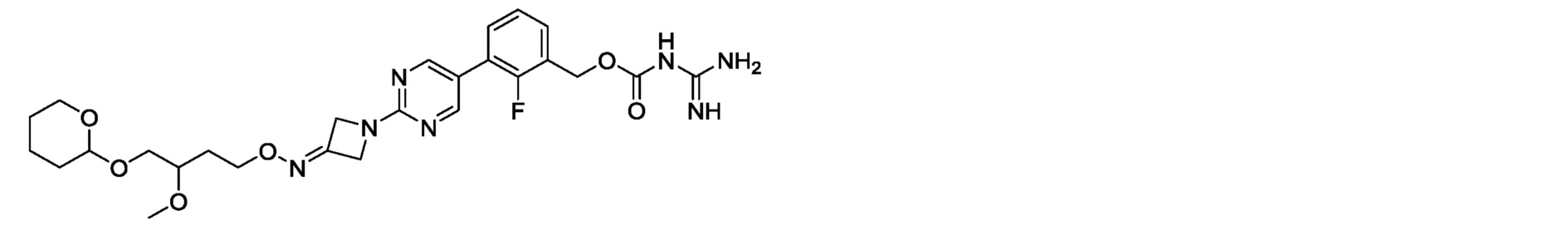
CDI, 108 мг (0,666 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-{3-метокси-4-[(тетрагидропиран-2-ил)окси]бутил}оксима, 79 мг (0,17 ммоль), синтезированного таким же образом, как в ссылочном примере 7-22, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 120 мг (0,666 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 62 мг (0,11 ммоль, выход 65%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 560[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,55-7,46 (m, 1H), 7,46-7,38 (m, 1H), 7,34-7,26 (m, 1H), 5,06 (s, 2H), 4,88-4,76 (m, 4H), 4,67-4,53 (m, 1H), 4,17-4,07 (m, 2H), 3,87-3,23 (m, 8H), 1,95-1,34 (m, 8H).
[0258] (Пример 24)
4-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутан-1,2-диилдиацетат (соединение II-53)
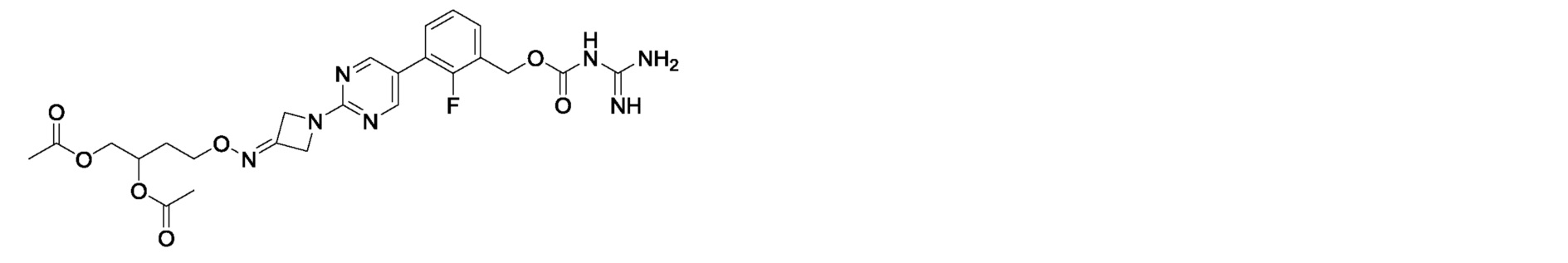
CDI, 47 мг (0,29 ммоль), добавляли к раствору в DMF (2 мл) 4-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}бутан-1,2-диилдиацетата, 53 мг (0,12 ммоль), синтезированного таким же образом, как в ссылочном примере 26, и смесь перемешивали при комнатной температуре в течение 6 часов. Затем добавляли карбонат гуанидина, 52 мг (0,29 ммоль), и смесь перемешивали при комнатной температуре в течение 18 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали. Осажденное твердое вещество собирали с помощью фильтрации. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 20 мг (0,037 ммоль, выход 31%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 546[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,4 Гц, 2H), 7,55-7,47 (m, 1H), 7,46-7,39 (m, 1H), 7,34-7,25 (m, 1H), 5,15-5,02 (m, 3H), 4,87-4,76 (m, 4H), 4,22 (dd, J=3,2, 12,0 Гц, 1H), 4,16-4,01 (m, 3H), 2,03 (s, 3H), 2,01 (s, 3H), 1,99-1,82 (m, 2H).
[0259] (Пример 25)
2-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилацетат (соединение II-36)
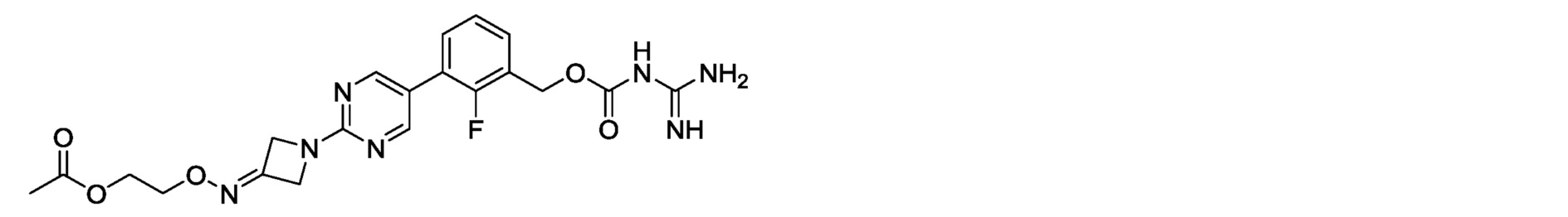
CDI, 24 мг (0,15 ммоль), добавляли к раствору в DMF (2 мл) 2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}этилацетата, 28 мг (0,075 ммоль), синтезированного таким же образом, как в ссылочном примере 7-23, и смесь перемешивали при комнатной температуре в течение 16 часов. Затем добавляли CDI, 12 мг (0,074 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 41 мг (0,23 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 8,0 мг (0,017 ммоль, выход 23%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 460[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,4 Гц, 2H), 7,54-7,47 (m, 1H), 7,46-7,38 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,88-4,76 (m, 4H), 4,27-4,20 (m, 4H), 2,04 (s, 3H).
[0260] (Пример 26)
2-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилпропионат (соединение II-37)

CDI, 70,0 мг (0,432 ммоль), добавляли к раствору в DMF (2 мл) 2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}этилпропионата, 82,2 мг (0,212 ммоль), синтезированного таким же образом, как в ссылочном примере 7-24, и смесь перемешивали при комнатной температуре в течение 4,25 часа. Затем добавляли 2 мл DMF и карбонат гуанидина, 94,2 мг (0,523 ммоль), и смесь перемешивали при комнатной температуре в течение 2,5 часа. После окончания реакции реакционную смесь выливали в 30 мл воды. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 85,4 мг (0,180 ммоль, выход 85%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 474[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,66-8,61 (m, 2H), 7,54-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,87-4,77 (m, 4H), 4,28-4,20 (m, 4H), 2,34 (q, J=7,5 Гц, 2H), 1,04 (t, J=7,5 Гц, 3H).
[0261] (Пример 27)
2-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилбутират (соединение II-38)

CDI, 79 мг (0,49 ммоль), добавляли к раствору в DMF (2 мл) 2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}этилбутирата, 93 мг (0,23 ммоль), синтезированного таким же образом, как в ссылочном примере 7-25, и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 91 мг (0,51 ммоль), и смесь перемешивали при комнатной температуре в течение 15 часов. После окончания реакции реакционную смесь выливали в 25 мл воды. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 104 мг (0,21 ммоль, выход 91%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 488[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,3 Гц, 2H), 7,54-7,48 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,86-4,77 (m, 4H), 4,28-4,20 (m, 4H), 2,30 (t, J=7,3 Гц, 2H), 1,55 (sext, J=7,3 Гц, 2H), 0,89 (t, J=7,3 Гц, 3H).
[0262] (Пример 28)
2-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилбензоат (соединение II-39)
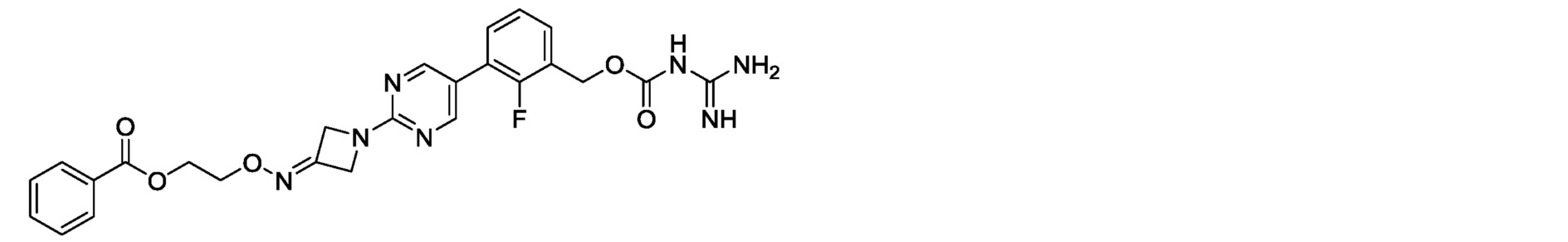
CDI, 68,2 мг (0,427 ммоль), добавляли к раствору в DMF (3 мл) 2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}этилбензоата, 90,9 мг (0,208 ммоль), синтезированного таким же образом, как в ссылочном примере 7-26, и смесь перемешивали при комнатной температуре в течение 4 часов. Затем добавляли 2 мл DMF и карбонат гуанидина, 91,3 мг (0,507 ммоль), и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции реакционную смесь выливали в 30 мл воды. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 90,7 мг (0,174 ммоль, выход 84%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 522[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,62 (d, J=0,8 Гц, 2H), 8,03-7,96 (m, 2H), 7,71-7,64 (m, 1H), 7,59-7,38 (m, 4H), 7,33-7,21 (m, 1H), 5,07 (s, 2H), 4,84-4,76 (m, 4H), 4,56-4,50 (m, 2H), 4,41-4,34 (m, 2H).
[0263] (Пример 29)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилацетат (соединение II-82)

CDI, 65 мг (0,40 ммоль), добавляли к раствору в DMF (4 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилацетата, 90 мг (0,18 ммоль), синтезированного таким же образом, как в ссылочном примере 7-27, и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли карбонат гуанидина, 65 мг (0,36 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 114 мг (включая примеси) в виде бесцветного масла.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,55-7,48 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,87-4,79 (m, 4H), 4,59-4,53 (m, 1H), 4,11-4,07 (m, 4H), 3,76-3,36 (m, 4H), 2-63-2,42 (m, 1H), 2,02 (s, 3H), 1,75-1,38 (m, 6H).
[0264] (Пример 30)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилпропионат (соединение II-83)

CDI, 60 мг (0,37 ммоль), добавляли к раствору в DMF (2 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилпропионата, 85 мг (0,17 ммоль), синтезированного таким же образом, как в ссылочном примере 7-28, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 60 мг (0,33 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 98 мг (включая примеси) в виде бесцветного масла.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,65-8,61 (m, 2H), 7,54-7,48 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,86-4,78 (m, 4H), 4,57-4,53 (m, 1H), 4,15-4,04 (m, 4H), 3,75-3,34 (m, 4H), 2,36-2,29 (m, 3H), 1,75-1,37 (m, 6H), 1,03 (t, J=7,5 Гц, 3H).
[0265] (Пример 31)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилбутират (соединение II-84)

CDI, 60 мг (0,37 ммоль), добавляли к раствору в DMF (2 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилбутирата, 89 мг (0,17 ммоль), синтезированного таким же образом, как в ссылочном примере 7-29, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 60 мг (0,33 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 92 мг (включая примеси) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,1 Гц, 2H), 7,54-7,48 (m, 1H), 7,45-7,39 (m, 1H), 7,34-7,27 (m, 1H), 5,06 (s, 2H), 4,87-4,77 (m, 4H), 4,57-4,53 (m, 1H), 4,16-4,03 (m, 4H), 3,75-3,64 (m, 2H), 3,47-3,35 (m, 2H), 2,37-2,32 (m, 1H), 2,29 (t, J=7,3 Гц, 2H), 1,74-1,38 (m, 8H), 0,88 (t, J=7,3 Гц, 3H).
[0266] (Пример 32)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилизобутират (соединение II-85)

CDI, 72,0 мг (0,444 ммоль), добавляли к раствору в DMF (4 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилизобутирата, 117 мг (0,221 ммоль), синтезированного таким же образом, как в ссылочном примере 7-30, и смесь перемешивали при комнатной температуре в течение 15 часов. Затем добавляли карбонат гуанидина, 80,0 мг (0,444 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 119 мг (0,193 ммоль, выход 88%) в виде белой пены.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,4 Гц, 2H), 7,54-7,48 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,87-4,78 (m, 4H), 4,62-4,49 (m, 1H), 4,16-4,02 (m, 4H), 3,74-3,58 (m, 2H), 3,49-3,33 (m, 2H), 2,55 (sep, J=7,0 Гц, 1H), 2,41-2,27 (m, 1H), 1,80-1,35 (m, 6H), 1,09 (d, J=7,0 Гц, 6H).
[0267] (Пример 33)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилпивалат (соединение II-86)
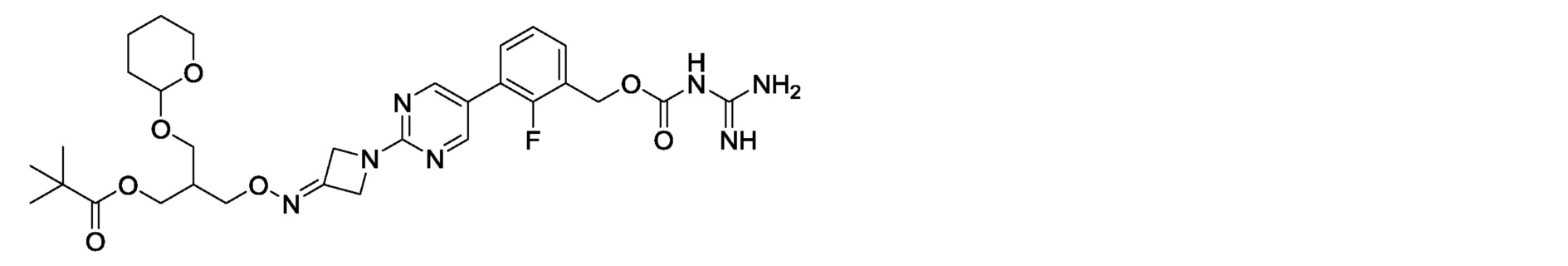
CDI, 65 мг (0,40 ммоль), добавляли к раствору в DMF (4 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилпивалата, 99 мг (0,18 ммоль), синтезированного таким же образом, как в ссылочном примере 7-31, и смесь перемешивали при комнатной температуре в течение 15 часов. Затем добавляли карбонат гуанидина, 70 мг (0,39 ммоль), и смесь перемешивали при комнатной температуре в течение 21 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 0,11 г (0,17 ммоль, выход 94%) в виде белой пены.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (d, J=1,3 Гц, 2H), 7,56-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,33-7,25 (m, 1H), 5,06 (s, 2H), 4,87-4,78 (m, 4H), 4,59-4,53 (m, 1H), 4,18-4,01 (m, 4H), 3,84-3,61 (m, 2H), 3,49-3,34 (m, 2H), 2,40-2,28 (m, 1H), 1,82-1,35 (m, 6H), 1,15 (s, 9H).
[0268] (Пример 34)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилгексаноат (соединение II-87)
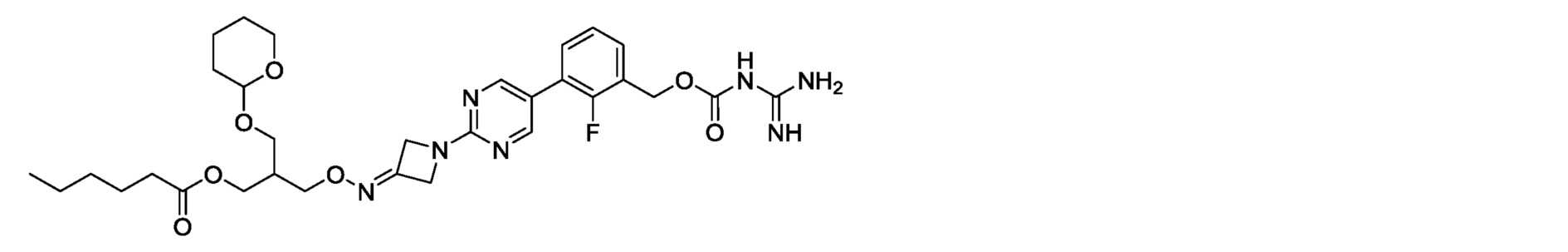
CDI, 109 мг (0,672 ммоль), добавляли к раствору в DMF (4 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилгексаноата, 188 мг (0,337 ммоль), синтезированного таким же образом, как в ссылочном примере 7-32, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 121 мг (0,672 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 163 мг (0,253 ммоль, выход 75%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 644[М+1]+.
[0269] (Пример 35)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилбензоат (соединение II-88)
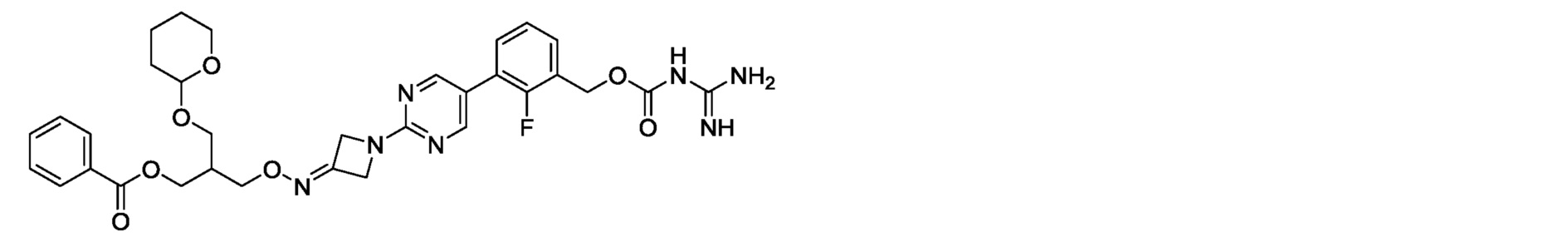
CDI, 65,2 мг (0,402 ммоль), добавляли к раствору в DMF (3 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилбензоата, 109 мг (0,193 ммоль), синтезированного таким же образом, как в ссылочном примере 7-33, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли CDI, 65,0 мг (0,401 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 70,0 мг (0,389 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 88:12 (об/об)) с получением указанного в заголовке соединения в количестве 102 мг (0,157 ммоль, выход 81%) в виде бесцветного масла.
Масс-спектр (ESI, m/z): 650[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,3 Гц, 2H), 8,00-7,96 (m, 2H), 7,66-7,61 (m, 1H), 7,54-7,48 (m, 3H), 7,44-7,39 (m, 1H), 7,32-7,27 (m, 1H), 5,06 (s, 2H), 4,82-4,75 (m, 4H), 4,61-4,57 (m, 1H), 4,42-4,35 (m, 2H), 4,26-4,16 (m, 2H), 3,82-3,74 (m, 1H), 3,74-3,67 (m, 1H), 3,53-3,36 (m, 2H), 2,54-2,45 (m, 1H), 1,75-1,53 (m, 2H), 1,51-1,39 (m, 4H).
[0270] (Пример 36)
2-Фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат (соединение III-78)

CDI, 1,4 г (8,6 ммоль), добавляли к раствору в DMF (15 мл) 1-{3-фтор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метилоксима, 1,22 г (3,82 ммоль), синтезированного таким же образом, как в ссылочном примере 7-34, и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли карбонат гуанидина, 1,4 г (7,8 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 50°C в течение 1 часа. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 1,31 г (3,24 ммоль, выход 85%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 405[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,19-8,15 (m, 1H), 7,78-7,71 (m, 1H), 7,53-7,46 (m, 1H), 7,44-7,37 (m, 1H), 7,31-7,24 (m, 1H), 5,06 (s, 2H), 4,90-4,83 (m, 4H), 3,82 (s, 3H).
[0271] (Пример 37)
2-Фтор-3-(5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамат (соединение III-88)

CDI, 110 мг (0,678 ммоль), добавляли к суспензии в DMF (4 мл) 1-{3-фтор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метил-d3-оксима, 99 мг (0,31 ммоль), синтезированного таким же образом, как в ссылочном примере 7-35, и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 110 мг (0,611 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 50°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 88 мг (0,22 ммоль, выход 71%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 408[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,20-8,15 (m, 1H), 7,79-7,70 (m, 1H), 7,53-7,47 (m, 1H), 7,43-7,37 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,90-4,82 (m, 4H).
[0272] (Пример 38)
3-[6-(3-{[2-(2,2-Диметил-1,3-диоксолан-4-ил)этокси]имино}азетидин-1-ил)-5-фторпиридин-3-ил]-2-фторбензилкарбамимидоилкарбамат (соединение III-154)

CDI, 215 мг (1,33 ммоль), добавляли к суспензии в DMF (6 мл) 1-{3-фтор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксима, 255 мг (0,588 ммоль), синтезированного таким же образом, как в ссылочном примере 7-36, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 215 мг (1,19 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 244 мг (0,471 ммоль, выход 80%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,20-8,15 (m, 1H), 7,79-7,71 (m, 1H), 7,53-7,46 (m, 1H), 7,44-7,38 (m, 1H), 7,31-7,25 (m, 1H), 5,06 (s, 2H), 4,91-4,83 (m, 4H), 4,17-4,05 (m, 3H), 4,05-3,99 (m, 1H), 3,53-3,46 (m, 1H), 1,91-1,79 (m, 2H), 1,32 (s, 3H), 1,27 (s, 3H).
[0273] (Пример 39)
3-[6-(3-{[(2,2-Диметил-1,3-диоксан-5-ил)метокси]имино}азетидин-1-ил)-5-фторпиридин-3-ил]-2-фторбензилкарбамимидоилкарбамат (соединение III-152)

CDI, 45 мг (0,28 ммоль), добавляли к суспензии в DMF (4 мл) 1-{3-фтор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксима, 54 мг (0,12 ммоль), синтезированного таким же образом, как в ссылочном примере 7-37, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 45 мг (0,25 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Полученное масло сушили при пониженном давлении с получением неочищенного продукта в количестве 116 мг, содержащего указанное в заголовке соединение в виде бесцветного масла.
[0274] (Пример 40)
2-Фтор-3-[5-фтор-6-(3-{[2-фтор-3-(тритилокси)пропокси]имино}азетидин-1-ил)пиридин-3-ил]бензилкарбамимидоилкарбамат (соединение III-166)

CDI, 300 мг (1,85 ммоль), добавляли к раствору в DMF (6 мл) 1-{3-фтор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-[2-фтор-3-(тритилокси)пропил]оксима, 576 мг (0,924 ммоль), синтезированного таким же образом, как в ссылочном примере 7-38, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 333 мг (1,85 ммоль), и смесь перемешивали при комнатной температуре в течение 15 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали насыщенным водным раствором гидрокарбоната натрия, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 631 мг (0,890 ммоль, выход 96%) в виде белой пены.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,24-8,18 (m, 1H), 7,84-7,74 (m, 1H), 7,56-7,46 (m, 1H), 7,44-7,22 (m, 17H), 5,06 (s, 2H), 5,03-4,66 (m, 5H), 4,43-4,15 (m, 2H), 3,31-3,12 (m, 2H).
[0275] (Пример 41)
2-Фтор-3-{6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат (соединение III-2)

CDI, 105 мг (0,648 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метилоксима, 49 мг (0,16 ммоль), синтезированного таким же образом, как в ссылочном примере 7-39, и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли карбонат гуанидина, 60 мг (0,33 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 88:12 (об/об)) с получением указанного в заголовке соединения в количестве 44 мг (0,11 ммоль, выход 69%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 387[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,32-8,29 (m, 1H), 7,81-7,77 (m, 1H), 7,49-7,33 (m, 2H), 7,31-7,23 (m, 1H), 6,71-6,66 (m, 1H), 5,06 (s, 2H), 4,76-4,69 (m, 4H), 3,82 (s, 3H).
[0276] (Пример 42)
2-Фтор-3-{6-[3-(метоксиимино)азетидин-1-ил]-5-метилпиридин-3-ил}бензилкарбамимидоилкарбамат (соединение III-716)

CDI, 175 мг (1,08 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]-3-метилпиридин-2-ил}азетидин-3-она O-метилоксима, 85 мг (0,27 ммоль), синтезированного таким же образом, как в ссылочном примере 7-40, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 194 мг (1,08 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали. Осажденное твердое вещество собирали с помощью фильтрации. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 21 мг (0,052 ммоль, выход 19%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 401[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,20-8,16 (m, 1H), 7,63-7,58 (m, 1H), 7,49-7,41 (m, 1H), 7,41-7,34 (m, 1H), 7,31-7,22 (m, 1H), 5,06 (s, 2H), 4,87-4,81 (m, 4H), 3,81 (s, 3H), 2,25 (s, 3H).
[0277] (Пример 43)
3-{5-Циано-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат (соединение III-1482)

CDI, 130 мг (0,802 ммоль), добавляли к раствору в DMF (6 мл) 5-[2-фтор-3-(гидроксиметил)фенил]-2-[3-(метоксиимино)азетидин-1-ил]никотинонитрила, 129 мг (0,395 ммоль), синтезированного таким же образом, как в ссылочном примере 7-41, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 150 мг (0,833 ммоль), и смесь перемешивали при комнатной температуре в течение 17 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали. Осажденное твердое вещество собирали с помощью фильтрации. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при комнатной температуре в течение 1 часа. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 98,0 мг (0,238 ммоль, выход 60%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 412[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59-8,54 (m, 1H), 8,26-8,22 (m, 1H), 7,55-7,47 (m, 1H), 7,46-7,39 (m, 1H), 7,34-7,25 (m, 1H), 5,06 (s, 2H), 5,03-4,99 (m, 4H), 3,84 (s, 3H).
[0278] (Пример 44)
3-{5-Хлор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат (соединение III-324)

CDI, 43 мг (0,27 ммоль), добавляли к суспензии в DMF (2 мл) 1-{3-хлор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метилоксима, 40 мг (0,12 ммоль), синтезированного таким же образом, как в ссылочном примере 7-42, и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 43 мг (0,24 ммоль), и смесь перемешивали при комнатной температуре в течение 2,5 часа. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 50°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 39 мг (0,093 ммоль, выход 78%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 421[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,34-8,28 (m, 1H), 7,93-7,88 (m, 1H), 7,54-7,47 (m, 1H), 7,44-7,39 (m, 1H), 7,31-7,25 (m, 1H), 5,06 (s, 2H), 4,96-4,89 (m, 4H), 3,82 (s, 3H).
[0279] (Пример 45)
3-{5-(Дифторметил)-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат (соединение III-960)

CDI, 125 мг (0,771 ммоль), добавляли к раствору в DMF (3 мл) 1-{3-(дифторметил)-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метилоксима, 108 мг (0,307 ммоль), синтезированного таким же образом, как в ссылочном примере 7-43, и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли CDI, 50 мг (0,31 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 112 мг (0,622 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре в течение 30 минут. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 104 мг (0,238 ммоль, выход 78%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 437[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,51-8,47 (m, 1H), 8,01-7,98 (m, 1H), 7,53-7,47 (m, 1H), 7,44-7,38 (m, 1H), 7,34-6,97 (m, 2H), 5,07 (s, 2H), 4,94-4,83 (m, 4H), 3,83 (s, 3H).
[0280] (Пример 46)
3-{5-Циклопропил-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат (соединение III-1308)

CDI, 200 мг (1,23 ммоль), добавляли к раствору в DMF (3 мл) 1-{3-циклопропил-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метилоксима, 121 мг (0,354 ммоль), синтезированного таким же образом, как в ссылочном примере 7-44, и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли карбонат гуанидина, 130 мг (0,722 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре в течение 30 минут. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 97,1 мг (0,228 ммоль, выход 64%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 427[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,20-8,13 (m, 1H), 7,47-7,40 (m, 2H), 7,40-7,35 (m, 1H), 7,29-7,22 (m, 1H), 5,05 (s, 2H), 4,94-4,90 (m, 4H), 3,82 (s, 3H), 1,98-1,82 (m, 1H), 0,98-0,91 (m, 2H), 0,75-0,69 (m, 2H).
[0281] (Пример 47)
3-{5-Этил-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}-2-фторбензилкарбамимидоилкарбамат (соединение III-851)

CDI, 195 мг (1,20 ммоль), добавляли к раствору в DMF (3 мл) 1-{3-этил-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метилоксима, 113 мг (0,343 ммоль), синтезированного таким же образом, как в ссылочном примере 7-45, и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли карбонат гуанидина, 124 мг (0,688 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре в течение 30 минут. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 96,0 мг (0,232 ммоль, выход 68%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 415[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,21-8,19 (m, 1H), 7,62-7,59 (m, 1H), 7,49-7,43 (m, 1H), 7,40-7,36 (m, 1H), 7,30-7,24 (m, 1H), 5,06 (s, 2H), 4,85-4,81 (m, 4H), 3,81 (s, 3H), 2,59 (q, J=7,4 Гц, 2H), 1,20 (t, J=7,5 Гц, 3H).
[0282] (Пример 48)
2-Фтор-3-{6-[3-(метоксиимино)азетидин-1-ил]-5-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-3-ил}бензилкарбамимидоилкарбамат (соединение III-1210)

CDI, 140 мг (0,863 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-2-ил}азетидин-3-она O-метилоксима, 189 мг (0,426 ммоль), синтезированного таким же образом, как в ссылочном примере 7-46, и смесь перемешивали при комнатной температуре в течение 6 часов. Затем добавляли карбонат гуанидина, 160 мг (0,888 ммоль), и смесь перемешивали при комнатной температуре в течение 20 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 175 мг (0,331 ммоль, выход 78%) в виде бесцветного масла.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,33-8,28 (m, 1H), 7,83-7,76 (m, 1H), 7,54-7,47 (m, 1H), 7,43-7,35 (m, 1H), 7,31-7,21 (m, 1H), 5,06 (s, 2H), 4,93-4,77 (m, 4H), 4,57-4,47 (m, 1H), 3,85-3,69 (m, 4H), 3,44-3,20 (m, 1H), 1,88-1,27 (m, 12H).
[0283] (Пример 49)
2-Фтор-3-{6-[3-(метоксиимино)азетидин-1-ил]-5-(метоксиметил)пиридин-3-ил}бензилкарбамимидоилкарбамат (соединение III-1221)

CDI, 150 мг (0,925 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]-3-(метоксиметил)пиридин-2-ил}азетидин-3-она O-метилоксима, 157 мг (0,455 ммоль), синтезированного таким же образом, как в ссылочном примере 7-47, и смесь перемешивали при комнатной температуре в течение 20 часов. Затем добавляли карбонат гуанидина, 170 мг (0,944 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре в течение 2 часов. После этого осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 164 мг (0,381 ммоль, выход 84%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 431[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,32-8,25 (m, 1H), 7,77-7,72 (m, 1H), 7,50-7,43 (m, 1H), 7,42-7,35 (m, 1H), 7,30-7,24 (m, 1H), 5,06 (s, 2H), 4,93-4,81 (m, 4H), 4,39 (s, 2H), 3,82 (s, 3H), 3,33 (s, 3H).
[0284] (Пример 50)
2-Фтор-3-{5-метокси-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат (соединение III-1395)

CDI, 153 мг (0,944 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]-3-метоксипиридин-2-ил}азетидин-3-она O-метилоксима, 104 мг (0,314 ммоль), синтезированного таким же образом, как в ссылочном примере 7-48, и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли карбонат гуанидина, 170 мг (0,944 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали. Осажденное твердое вещество собирали с помощью фильтрации. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 40°C. После этого твердое вещество собирали с помощью фильтрации и очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 13 мг (0,031 ммоль, выход 10%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 417[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 7,91-7,89 (m, 1H), 7,54-7,45 (m, 1H), 7,44-7,35 (m, 1H), 7,34-7,30 (m, 1H), 7,30-7,22 (m, 1H), 5,06 (s, 2H), 4,83-4,71 (m, 4H), 3,83 (s, 3H), 3,81 (s, 3H).
[0285] (Пример 51)
2-Фтор-3-{2-[4-(метоксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-205)

CDI, 112 мг (0,691 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-метилоксима, 100 мг (0,303 ммоль), синтезированного таким же образом, как в ссылочном примере 7-49, и смесь перемешивали при комнатной температуре в течение 6 часов. Затем добавляли карбонат гуанидина, 109 мг (0,605 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 117 мг (0,282 ммоль, выход 93%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 416[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,43-7,37 (m, 1H), 7,33-7,24 (m, 1H), 5,06 (s, 2H), 3,99-3,85 (m, 4H), 3,76 (s, 3H), 2,60-2,53 (m, 2H), 2,42-2,35 (m, 2H).
[0286] (Пример 52)
2-Фтор-3-[2-(4-{[(тетрагидропиран-2-ил)окси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-249)

CDI, 189 мг (0,117 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-тетрагидропиран-2-илоксима, 210 мг (0,524 ммоль), синтезированного таким же образом, как в ссылочном примере 61, и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 190 мг (0,105 ммоль), и смесь перемешивали при комнатной температуре в течение 11 часов. После окончания реакции реакционную смесь выливали в 20 мл воды, и смесь перемешивали в течение 20 минут. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 151 мг (0,311 ммоль, выход 59%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 486[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,0 Гц, 2H), 7,54-7,48 (m, 1H), 7,44-7,37 (m, 1H), 7,33-7,26 (m, 1H), 5,18-5,14 (m, 1H), 5,07 (s, 2H), 4,01-3,87 (m, 4H), 3,78-3,73 (m, 1H), 3,52-3,43 (m, 1H), 2,71-2,60 (m, 2H), 2,45-2,38 (m, 2H), 1,91-1,37 (m, 6H).
[0287] (Пример 53)
3-{2-[4-(Этоксиимино)пиперидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат (соединение II-206)

CDI, 110 мг (0,678 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-этилоксима, 100 мг (0,290 ммоль), синтезированного таким же образом, как в ссылочном примере 62-1, и смесь перемешивали при комнатной температуре в течение 6 часов. Затем добавляли карбонат гуанидина, 113 мг (0,627 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 114 мг (0,265 ммоль, выход 91%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 430[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,0 Гц, 2H), 7,56-7,46 (m, 1H), 7,44-7,36 (m, 1H), 7,32-7,23 (m, 1H), 5,06 (s, 2H), 4,02 (q, J=7,1 Гц, 2H), 3,95-3,89 (m, 4H), 2,60-2,54 (m, 2H), 2,41-2,35 (m, 2H), 1,19 (t, J=7,1 Гц, 3H).
[0288] (Пример 54)
2-Фтор-3-{2-[4-(Изопропоксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-208)

CDI, 79,6 мг (0,491 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-изопропилоксима, 77,1 мг (0,215 ммоль), синтезированного таким же образом, как в ссылочном примере 62-2, и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 80,8 мг (0,448 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции к реакционной смеси добавляли метиленхлорид и воду с последующей экстракцией метиленхлоридом. Органический слой сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 68:32 (об/об)). К полученному твердому веществу добавляли этилацетат, и смесь обрабатывали ультразвуком. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 45,3 мг (0,102 ммоль, выход 47%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,55-7,47 (m, 1H), 7,43-7,37 (m, 1H), 7,32-7,22 (m, 1H), 5,06 (s, 2H), 4,22 (sep, J=6,2 Гц, 1H), 3,98-3,87 (m, 4H), 2,60-2,54 (m, 2H), 2,43-2,36 (m, 2H), 1,18 (d, J=6,2 Гц, 6H).
[0289] (Пример 55)
2-Фтор-3-{2-[4-(пропоксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-207)

CDI, 100 мг (0,617 ммоль), добавляли к раствору в DMF (2,5 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-пропилоксима, 88,8 мг (0,248 ммоль), синтезированного таким же образом, как в ссылочном примере 62-3, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 100 мг (0,555 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли толуол, который затем концентрировали при пониженном давлении, и эту операцию повторяли несколько раз. К полученному твердому веществу добавляли этилацетат, и смесь обрабатывали ультразвуком. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 106 мг (0,239 ммоль, выход 96%) в виде белого твердого вещества.
Масс-спектр (DUIS, m/z): 444[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,54-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 3,96-3,89 (m, 6H), 2,61-2,55 (m, 2H), 2,41-2,34 (m, 2H), 1,60 (sext, J=7,3 Гц, 2H), 0,89 (t, J=7,3 Гц, 3H).
[0290] (Пример 56)
3-(2-{4-[(Аллилокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-209)

CDI, 100 мг (0,617 ммоль), добавляли к раствору в DMF (2,5 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-аллилоксима, 92,7 мг (0,260 ммоль), синтезированного таким же образом, как в ссылочном примере 63, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 100 мг (0,555 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли толуол, который затем концентрировали при пониженном давлении, и эту операцию повторяли несколько раз. К полученному твердому веществу добавляли этилацетат, и смесь обрабатывали ультразвуком. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 107 мг (0,242 ммоль, выход 93%) в виде белого твердого вещества.
Масс-спектр (DUIS, m/z): 442[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,60 (d, J=1,4 Гц, 2H), 7,58-7,44 (m, 1H), 7,42-7,33 (m, 1H), 7,31-7,23 (m, 1H), 6,02-5,92 (m, 1H), 5,31-5,24 (m, 1H), 5,21-5,16 (m, 1H), 5,06 (s, 2H), 4,53-4,48 (m, 2H), 3,97-3,89 (m, 4H), 2,64-2,56 (m, 2H), 2,42-2,34 (m, 2H).
[0291] (Пример 57)
2-Фтор-3-{2-[4-({2-[(тетрагидропиран-2-ил)окси]этокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-250)
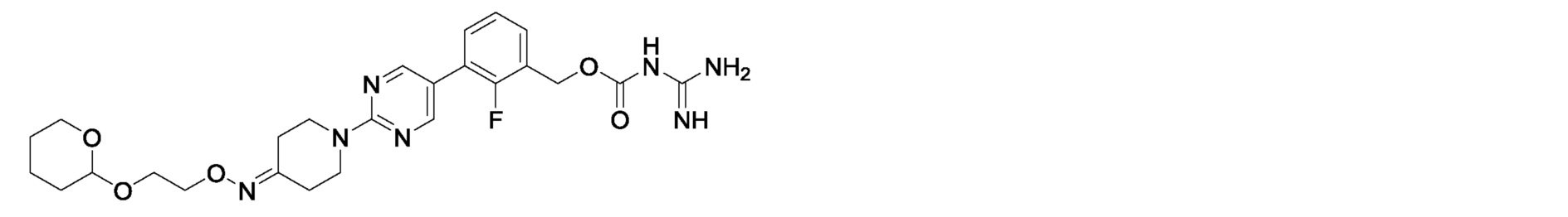
CDI, 35 мг (0,22 ммоль), добавляли к раствору в DMF (1 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{2-[(тетрагидропиран-2-ил)окси]этил}оксима, 38 мг (0,085 ммоль), синтезированного таким же образом, как в ссылочном примере 65, и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 32 мг (0,18 ммоль), и смесь перемешивали при комнатной температуре в течение 11 часов. После окончания реакции реакционную смесь выливали в 10 мл воды с последующей экстракцией смешанным растворителем метиленхлорид:метанол=80:20 (об/об). Органический слой сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: этилацетат:метанол=от 100:0 до 90:10 (об/об)) с получением указанного в заголовке соединения в количестве 43 мг (0,081 ммоль, выход 95%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 530[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (s, 2H), 7,54-7,46 (m, 1H), 7,43-7,36 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,61-4,56 (m, 1H), 4,16-4,07(m, 2H), 3,97-3,87 (m, 4H), 3,85-3,70 (m, 2H), 3,63-3,55 (m, 1H), 3,42-3,37 (m, 1H), 2,63-2,54 (m, 2H), 2,43-2,36 (m, 2H), 1,80-1,36 (m, 6H).
[0292] (Пример 58)
2-Фтор-3-{2-[4-({3-[(тетрагидропиран-2-ил)окси]пропокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-251)
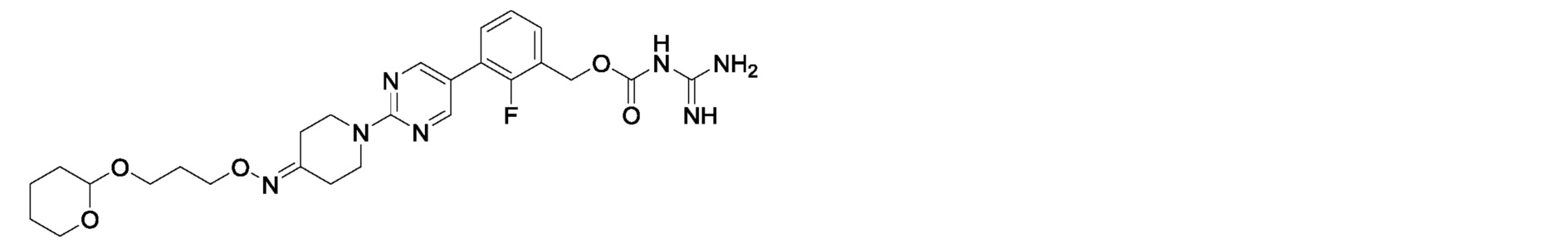
CDI, 69 мг (0,43 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{3-[(тетрагидропиран-2-ил)окси]пропил}оксима, 97 мг (0,21 ммоль), синтезированного таким же образом, как в ссылочном примере 7-51, и смесь перемешивали при комнатной температуре в течение 8 часов. Затем добавляли карбонат гуанидина, 77 мг (0,43 ммоль), и смесь перемешивали при комнатной температуре в течение 22 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 92 мг (0,17 ммоль, выход 81%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,58-7,47 (m, 1H), 7,44-7,37 (m, 1H), 7,32-7,24 (m, 1H), 5,06 (s, 2H), 4,59-4,51 (m, 1H), 4,11-4,00 (m, 2H), 3,98-3,86 (m, 4H), 3,78-3,64 (m, 2H), 3,47-3,35 (m, 2H), 2,63-2,54 (m, 2H), 2,46-2,36 (m, 2H), 1,97-1,79 (m, 2H), 1,78-1,39 (m, 6H).
[0293] (Пример 59)
2-Фтор-3-{2-[4-({4-[(тетрагидропиран-2-ил)окси]бутокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-252)
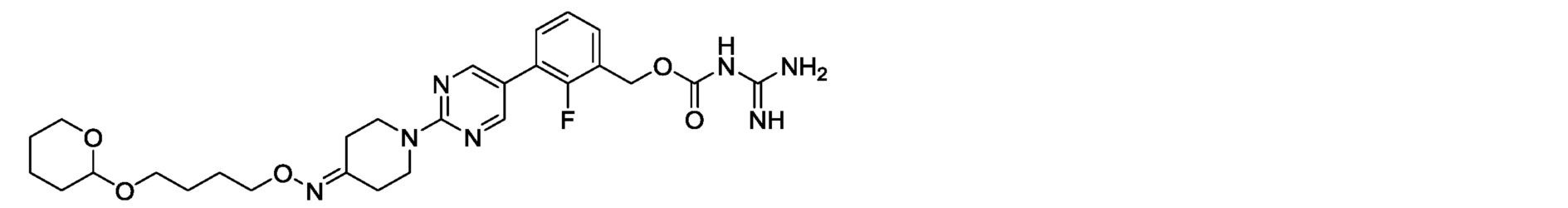
CDI, 84,0 мг (0,518 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{4-[(тетрагидропиран-2-ил)окси]бутил}оксима, 123 мг (0,260 ммоль), синтезированного таким же образом, как в ссылочном примере 7-52, и смесь перемешивали при комнатной температуре в течение 7 часов. Затем добавляли карбонат гуанидина, 94,0 мг (0,522 ммоль), и смесь перемешивали при комнатной температуре в течение 21 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 112 мг (0,201 ммоль, выход 77%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,54-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,33-7,24 (m, 1H), 5,06 (s, 2H), 4,56-4,52 (m, 1H), 4,02-3,95 (m, 2H), 3,95-3,87 (m, 4H), 3,77-3,69 (m, 1H), 3,68-3,60 (m, 1H), 3,45-3,30 (m, 2H), 2,62-2,55 (m, 2H), 2,42-2,34 (m, 2H), 1,79-1,36 (m, 10H).
[0294] (Пример 60)
2-Фтор-3-(2-{4-[(2-метоксиэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-218)

CDI, 107 мг (0,660 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-(2-метоксиэтил)оксима, 124 мг (0,331 ммоль), синтезированного таким же образом, как в ссылочном примере 7-53, и смесь перемешивали при комнатной температуре в течение 5 часов. Затем добавляли карбонат гуанидина, 119 мг (0,661 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 126 мг (0,274 ммоль, выход 83%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 460[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,4 Гц, 2H), 7,53-7,47 (m, 1H), 7,42-7,36 (m, 1H), 7,31-7,25 (m, 1H), 5,06 (s, 2H), 4,11-4,07 (m, 2H), 3,96-3,89 (m, 4H), 3,57-3,52 (m, 2H), 3,26 (s, 3H), 2,63-2,55 (m, 2H), 2,42-2,33 (m, 2H).
[0295] (Пример 61)
3-{2-[4-({2,2-Диметил-3-[(тетрагидропиран-2-ил)окси]пропокси}имино)пиперидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат (соединение II-254)
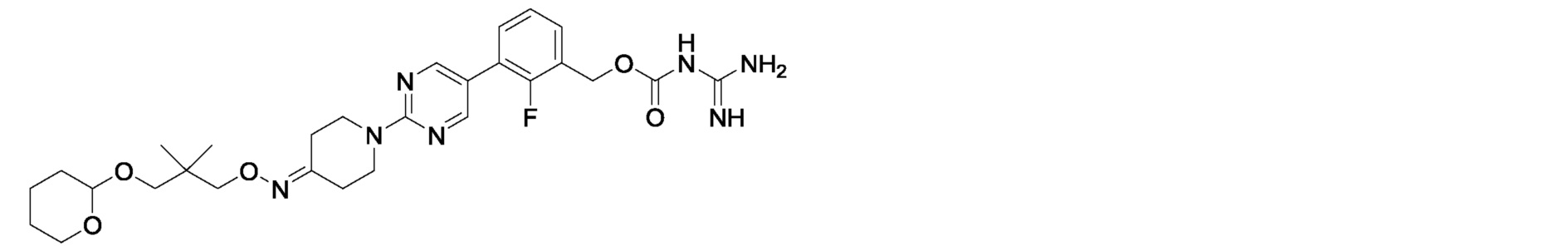
CDI, 100 мг (0,617 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{2,2-диметил-3-[(тетрагидропиран-2-ил)окси]пропил}оксима, 131 мг (0,269 ммоль), синтезированного таким же образом, как в ссылочном примере 7-54, и смесь перемешивали при комнатной температуре в течение 4 часов. Затем добавляли карбонат гуанидина, 100 мг (0,555 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 50°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 121 мг (0,212 ммоль, выход 79%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 572[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,53-7,47 (m, 1H), 7,43-7,37 (m, 1H), 7,31-7,26 (m, 1H), 5,06 (s, 2H), 4,54-4,50 (m, 1H), 3,96-3,88 (m, 4H), 3,83 (s, 2H), 3,76-3,66 (m, 1H), 3,47-3,37 (m, 2H), 3,07 (d, J=9,2 Гц, 1H), 2,63-2,56 (m, 2H), 2,43-2,35 (m, 2H), 1,77-1,36 (m, 6H), 0,91 (s, 3H), 0,91 (s, 3H).
[0296] (Пример 62)
2-Фтор-3-{2-[4-({3-метил-3-[(тетрагидропиран-2-ил)окси]бутокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-255)

CDI, 160 мг (0,987 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{3-метил-3-[(тетрагидропиран-2-ил)окси]бутил}оксима, 193 мг (0,397 ммоль), синтезированного таким же образом, как в ссылочном примере 7-55, и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли карбонат гуанидина, 145 мг (0,805 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли этилацетат, и смесь перемешивали при 70°C в течение 1 часа и при комнатной температуре в течение 14 часов. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 186 мг (0,325 ммоль, выход 82%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 572[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,53-7,48 (m, 1H), 7,42-7,37 (m, 1H), 7,31-7,26 (m, 1H), 5,06 (s, 2H), 4,77 (dd, J=2,7, 5,5 Гц, 1H), 4,13-4,04 (m, 2H), 3,95-3,88 (m, 4H), 3,84-3,77 (m, 1H), 3,44-3,37 (m, 1H), 2,60-2,52 (m, 2H), 2,43-2,36 (m, 2H), 1,86-1,68 (m, 3H), 1,59-1,32 (m, 5H), 1,19 (s, 3H), 1,18 (s, 3H).
[0297] (Пример 63)
2-Фтор-3-{2-[4-({2-[(тетрагидропиран-2-ил)окси]пропокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-256)

CDI, 49 мг (0,30 ммоль), добавляли к раствору в DMF (1,2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{2-[(тетрагидропиран-2-ил)окси]пропил}оксима, 57 мг (0,12 ммоль), синтезированного таким же образом, как в ссылочном примере 7-56, и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли карбонат гуанидина, 52 мг (0,29 ммоль), и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции к реакционной смеси три раза добавляли воду с последующей экстракцией метиленхлоридом. Органический слой сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли толуол, который затем концентрировали при пониженном давлении, и эту операцию повторяли несколько раз. Добавляли диизопропиловый эфир, и смесь обрабатывали ультразвуком. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 49 мг (0,090 ммоль, выход 75%) в виде белого твердого вещества.
Масс-спектр (DUIS, m/z): 544[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,61-8,57 (m, 2H), 7,54-7,46 (m, 1H), 7,43-7,37 (m, 1H), 7,33-7,24 (m, 1H), 5,06 (s, 2H), 4,79-4,61 (m, 1H), 4,10-3,73 (m, 8H), 3,45-3,34 (m, 1H), 2,63-2,56 (m, 2H), 2,44-2,34 (m, 2H), 1,86-1,36 (m, 6H), 1,17-1,03 (m, 3H).
[0298] (Пример 64)
2-Фтор-3-{2-[4-({2-метил-3-[(тетрагидропиран-2-ил)окси]пропокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-257)

CDI, 135 мг (0,833 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{2-метил-3-[(тетрагидропиран-2-ил)окси]пропил)}оксима, 175 мг (0,370 ммоль), синтезированного таким же образом, как в ссылочном примере 7-57, и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли карбонат гуанидина, 135 мг (0,749 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 50°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 117 мг (0,210 ммоль, выход 57%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 558[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63-8,56 (m, 2H), 7,54-7,47 (m, 1H), 7,42-7,36 (m, 1H), 7,31-7,25 (m, 1H), 5,06 (s, 2H), 4,56-4,51 (m, 1H), 4,02-3,80 (m, 6H), 3,77-3,67 (m, 1H), 3,63-3,37 (m, 2H), 3,34-3,18 (m, 1H), 2,63-2,55 (m, 2H), 2,43-2,36 (m, 2H), 2,11-2,01 (m, 1H), 1,76-1,37 (m, 6H), 0,97-0,87 (m, 3H).
[0299] (Пример 65)
3-[2-(4-{[(2,2-Диметил-1,3-диоксан-5-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-259)

CDI, 252 мг (1,55 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксима, 345 мг (0,776 ммоль), синтезированного таким же образом, как в ссылочном примере 7-58, и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли карбонат гуанидина, 280 мг (1,55 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 88:12 (об/об)). К полученному твердому веществу добавляли 5 мл этилацетата, и смесь перемешивали при 70°C в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 393 мг (0,742 ммоль, выход 96%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 530[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,53-7,47 (m, 1H), 7,44-7,36 (m, 1H), 7,34-7,24 (m, 1H), 5,06 (s, 2H), 4,02 (d, J=7,0 Гц, 2H), 3,97-3,85 (m, 6H), 3,77-3,45 (m, 2H), 2,62-2,55 (m, 2H), 2,43-2,37 (m, 2H), 2,03-1,94 (m, 1H), 1,33 (s, 3H), 1,32 (s, 3H).
[0300] (Пример 66)
2-Фтор-3-[2-(4-{[(2,2,5-триметил-1,3-диоксан-5-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-262)

CDI, 80 мг (0,49 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[(2,2,5-триметил-1,3-диоксан-5-ил)метил]оксима, 97 мг (0,21 ммоль), синтезированного таким же образом, как в ссылочном примере 7-59, и смесь перемешивали при комнатной температуре в течение 4 часов. Затем добавляли карбонат гуанидина, 80 мг (0,44 ммоль), и смесь перемешивали при комнатной температуре в течение 15 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол) и (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 83 мг (включая примеси) в виде белой пены.
Масс-спектр (APCI, m/z): 544[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,54-7,47 (m, 1H), 7,42-7,36 (m, 1H), 7,31-7,25 (m, 1H), 5,06 (s, 2H), 4,01 (s, 2H), 3,97-3,89 (m, 4H), 3,61 (d, J=11,7 Гц, 2H), 3,52 (d, J=11,7 Гц, 2H), 2,63-2,57 (m, 2H), 2,42-2,36 (m, 2H), 1,35 (s, 3H), 1,29 (s, 3H), 0,85 (s, 3H).
[0301] (Пример 67)
3-[2-(4-{[(2,2-Диметил-1,3-диоксолан-4-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-260)

CDI, 100 мг (0,617 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксима, 130 мг (0,302 ммоль), синтезированного таким же образом, как в ссылочном примере 7-60, и смесь перемешивали при комнатной температуре в течение 15 часов. Затем добавляли карбонат гуанидина, 110 мг (0,611 ммоль), и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 118 мг (0,229 ммоль, выход 76%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,5 Гц, 2H), 7,55-7,46 (m, 1H), 7,44-7,37 (m, 1H), 7,32-7,24 (m, 1H), 5,06 (s, 2H), 4,33-4,21 (m, 1H), 4,06-3,98 (m, 3H), 3,96-3,89 (m, 4H), 3,67 (dd, J=6,5, 8,3 Гц, 1H), 2,62-2,55 (m, 2H), 2,42-2,36 (m, 2H), 1,33 (s, 3H), 1,28 (s, 3H).
[0302] (Пример 68)
2-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этилацетат (соединение II-225)

CDI, 56 мг (0,35 ммоль), добавляли к раствору в DMF (4 мл) 2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этилацетата, 69 мг (0,17 ммоль), синтезированного таким же образом, как в ссылочном примере 7-61, и смесь перемешивали при комнатной температуре в течение 8 часов. Затем добавляли карбонат гуанидина, 62 мг (0,34 ммоль), и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 62 мг (0,13 ммоль, выход 76%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 488[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,1 Гц, 2H), 7,55-7,46 (m, 1H), 7,44-7,36 (m, 1H), 7,32-7,23 (m, 1H), 5,06 (s, 2H), 4,25-4,13 (m, 4H), 3,96-3,89 (m, 4H), 2,63-2,55 (m, 2H), 2,44-2,36 (m, 2H), 2,03 (s, 3H).
[0303] (Пример 69)
(E/Z)-2-фтор-3-{2-[3-(метоксиимино)пирролидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-92)

CDI, 52,4 мг (0,323 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пирролидин-3-она O-метилоксима, EZ-смесь, 51,1 мг (0,162 ммоль), синтезированного таким же образом, как в ссылочном примере 76, и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли карбонат гуанидина, 64,2 мг (0,356 ммоль), и смесь перемешивали при комнатной температуре в течение 13 часов. После окончания реакции реакционную смесь выливали в 20 мл воды, и смесь перемешивали при комнатной температуре в течение 5 минут. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 41,5 мг (0,103 ммоль, выход 64%) в виде коричневого твердого вещества.
Масс-спектр (ESI, m/z): 402[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63-8,59 (m, 2H), 7,53-7,46 (m, 1H), 7,43-7,37 (m, 1H), 7,33-7,24 (m, 1H), 5,06 (s, 2H), 4,26-4,20 (m, 2H), 3,87-3,77 (m, 5H), 2,87-2,80 (m, 2H).
[0304] (Пример 70)
2-Фтор-3-{2-[3-(гидроксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-1)

Раствор 1 М тетрабутиламмония фторида в THF, 230 мкл (0,230 ммоль), добавляли к суспензии в THF (5 мл) 3-[2-(3-{[(трет-бутилдиметилсилил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамата, 91,6 мг (0,188 ммоль), синтезированного таким же образом, как в примере 4, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении, и добавляли воду. Осажденное твердое вещество собирали с помощью фильтрации и промывали водой и диэтиловым эфиром. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 75°C в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол=от 99:1 до 50:50 (об/об)) с получением указанного в заголовке соединения в количестве 19,9 мг (0,0533 ммоль, выход 28%) в виде белого твердого вещества.
Масс-спектр (DUIS, m/z): 374[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (s, 2H), 7,57-7,47 (m, 1H), 7,46-7,38 (m, 1H), 7,34-7,24 (m, 1H), 5,06 (s, 2H), 4,88-4,70 (m, 4H).
[0305] (Пример 71)
2-Фтор-3-(2-{3-[(2-гидроксиэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата гидрохлорид (соединения II-21 гидрохлорид)

При 0°C раствор 2 М хлорида водорода в этаноле, 1 мл (2 ммоль), добавляли к суспензии в этаноле (2 мл) 2-фтор-3-{2-[3-({2-[(тетрагидропиран-2-ил)окси]этокси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата, 85 мг (0,17 ммоль), синтезированного таким же образом, как в примере 9, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. К концентрированному остатку добавляли TBME, и твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 59 мг (0,13 ммоль, выход 76%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 418[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,1 Гц, 2H), 7,67-7,59 (m, 1H), 7,58-7,50 (m, 1H), 7,40-7,31 (m, 1H), 5,37 (s, 2H), 4,86-4,80 (m, 4H), 4,05 (t, J=5,2 Гц, 2H), 3,61 (t, J=5,2 Гц, 2H).
[0306] (Пример 72)
2-Фтор-3-(2-{3-[(3-гидроксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-22)

При комнатной температуре раствор 2 М хлорида водорода в этаноле, 2 мл (4 ммоль), добавляли к 2-фтор-3-{2-[3-({3-[(тетрагидропиран-2-ил)окси]пропокси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамату, 145 мг (0,281 ммоль), синтезированному таким же образом, как в примере 10, и смесь перемешивали при комнатной температуре в течение 30 минут. После окончания реакции реакционную смесь концентрировали при пониженном давлении. К концентрированному остатку добавляли метиленхлорид, TEA и воду, и смесь перемешивали. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 69 мг (0,16 ммоль, выход 57%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 432[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,56-7,46 (m, 1H), 7,45-7,35 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,85-4,77 (m, 4H), 4,48 (t, J=5,1 Гц, 1H), 4,10 (t, J=6,5 Гц, 2H), 3,52-3,44 (m, 2H), 1,76 (quin, J=6,5 Гц, 2H).
[0307] (Пример 73)
2-Фтор-3-(2-{3-[(4-гидроксибутокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-23)

Раствор 2 М хлорида водорода в этаноле, 0,3 мл (0,6 ммоль), добавляли к суспензии в метиленхлориде (2 мл) 2-фтор-3-{2-[3-({4-[(тетрагидропиран-2-ил)окси]бутокси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата, 90 мг (0,17 ммоль), синтезированного таким же образом, как в примере 11, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол) с получением указанного в заголовке соединения в количестве 63 мг (0,14 ммоль, выход 82%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 446[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,66-8,60 (m, 2H), 7,54-7,47 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,86-4,77 (m, 4H), 4,07-4,01 (m, 2H), 3,44-3,38 (m, 2H), 1,69-1,59 (m, 2H), 1,53-1,43 (m, 2H).
[0308] (Пример 74)
2-Фтор-3-[2-(3-{[2-(2-гидроксиэтокси)этокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-30)

Раствор 2 М хлорида водорода в этаноле, 0,20 мл (0,40 ммоль), добавляли к раствору в этаноле (2 мл) 2-фтор-3-(2-{3-[(2-{2-[(тетрагидропиран-2-ил)окси]этокси}этокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата, 70 мг (0,13 ммоль), синтезированного таким же образом, как в примере 13, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли TEA, 55 мкл (0,40 ммоль), и реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол). К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 50°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 52 мг (0,11 ммоль, выход 85%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 462[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (s, 2H), 7,54-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,88-4,76 (m, 4H), 4,64-4,56 (m, 1H), 4,20-4,11 (m, 2H), 3,69-3,60 (m, 2H), 3,55-3,40 (m, 4H).
[0309] (Пример 75)
2-Фтор-3-[2-(3-{[3-фтор-2-(гидроксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-50)
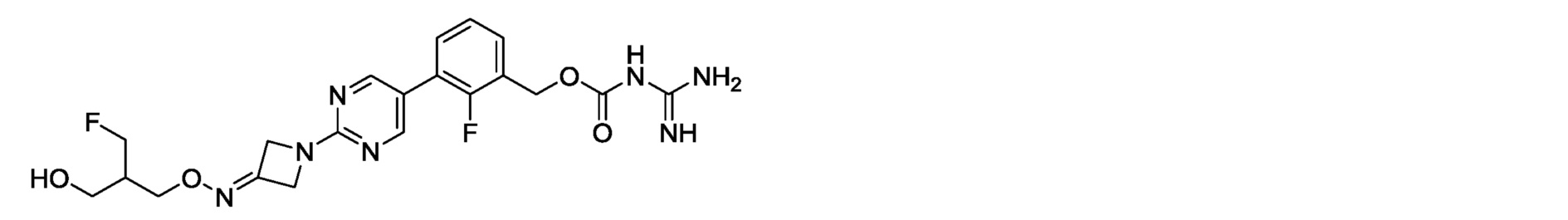
Раствор 2 М хлорида водорода в этаноле, 0,10 мл (0,20 ммоль), добавляли к раствору в метиленхлориде (0,10 мл) 2-фтор-3-(2-{3-[(3-фтор-2-{[(тетрагидропиран-2-ил)окси]метил}пропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата, 52 мг (0,095 ммоль), синтезированного таким же образом, как в примере 21, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли TEA и насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 88:12 (об/об)) с получением указанного в заголовке соединения в количестве 25 мг (0,054 ммоль, выход 57%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 464[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,1 Гц, 2H), 7,54-7,49 (m, 1H), 7,45-7,40 (m, 1H), 7,33-7,28 (m, 1H), 5,07 (s, 2H), 4,87-4,80 (m, 4H), 4,52 (dd, J=5,2 Гц, J=47,4 Гц, 2H), 4,14-4,02 (m, 2H), 3,53-3,44 (m, 2H), 2,25-2,12 (m, 1H).
[0310] (Пример 76)
2-Фтор-3-(2-{3-[(4-гидрокси-3-метоксибутокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-51)

При 0°C раствор 2 М хлорида водорода в этаноле, 0,56 мл (1,1 ммоль), добавляли к раствору в этаноле (2 мл) 2-фтор-3-{2-[3-({3-метокси-4-[(тетрагидропиран-2-ил)окси]бутокси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата, 63 мг (0,11 ммоль), синтезированного таким же образом, как в примере 23, и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли TEA и воду. Осажденное твердое вещество собирали с помощью фильтрации, промывали водой и этилацетатом и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 20 мг (0,042 ммоль, выход 38%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 476[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,69-8,60 (m, 2H), 7,67-7,57 (m, 1H), 7,56-7,47 (m, 1H), 7,42-7,31 (m, 1H), 5,31 (s, 2H), 4,90-4,76 (m, 4H), 4,17-4,05 (m, 2H), 3,41 (d, J=5,0 Гц, 2H), 3,30 (s, 3H), 3,28-3,20 (m, 1H), 1,90-1,78 (m, 1H), 1,76-1,63 (m, 1H).
[0311] (Пример 77)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилацетат (соединение II-54)
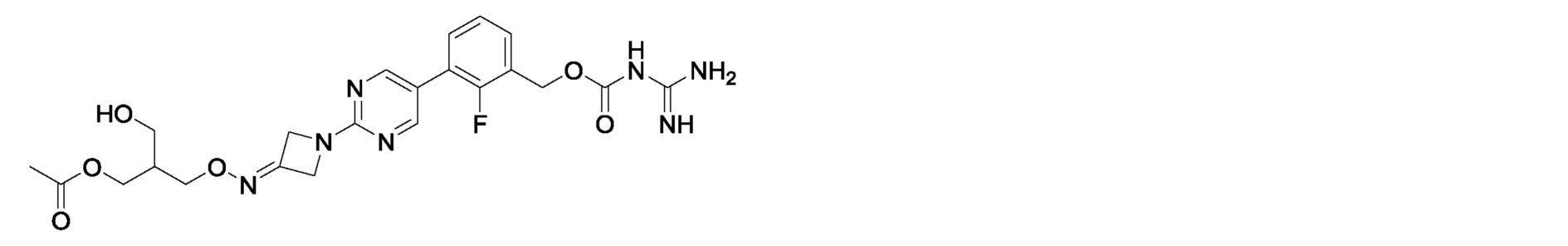
Раствор 2 М хлорида водорода в этаноле, 0,30 мл (0,60 ммоль), добавляли к раствору в этаноле (2 мл) 3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилацетата, 114 мг (0,194 ммоль), синтезированного таким же образом, как в примере 29, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли TEA, 0,20 мл (1,4 ммоль), и смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол). К полученному таким образом маслу добавляли гексан. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 44 мг (0,087 ммоль, выход 45%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 504[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,66-8,60 (m, 2H), 7,54-7,47 (m, 1H), 7,46-7,39 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,87-4,77 (m, 4H), 4,13-3,99 (m, 4H), 3,49-3,42 (m, 2H), 2,19-2,11 (m, 1H), 2,02 (s, 3H).
[0312] (Пример 78)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилпропионат (соединение II-55)
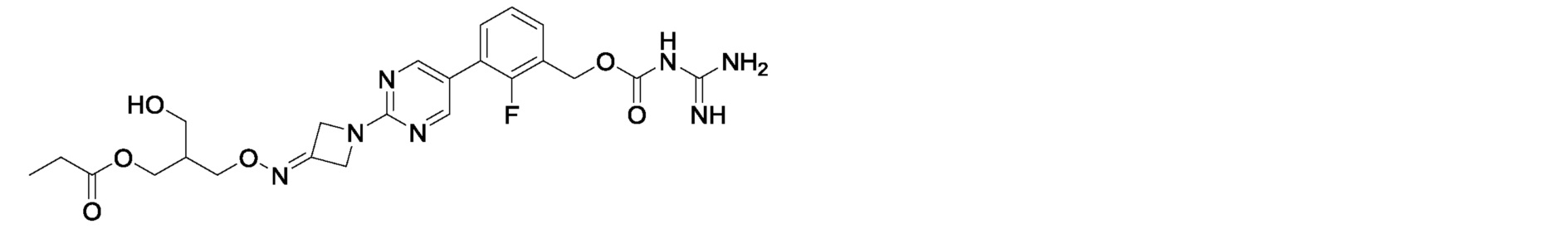
Раствор 2 М хлорида водорода в этаноле, 0,25 мл (0,50 ммоль), добавляли к раствору в этаноле (2 мл) 3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилпропионата, 98 мг (0,16 ммоль), синтезированного таким же образом, как в примере 30, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли TEA, 0,20 мл (1,4 ммоль), и смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол). К полученному таким образом маслу добавляли гексан. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 49 мг (0,095 ммоль, выход 59%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 518[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,67-8,57 (m, 2H), 7,54-7,48 (m, 1H), 7,44-7,37 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,87-4,77 (m, 4H), 4,66 (t, J=5,2 Гц, 1H), 4,14-3,99 (m, 4H), 3,52-3,40 (m, 2H), 2,32 (q, J=7,5 Гц, 2H), 2,19-2,10 (m, 1H), 1,03 (t, J=7,5 Гц, 3H).
[0313] (Пример 79)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилбутират (соединение II-56)
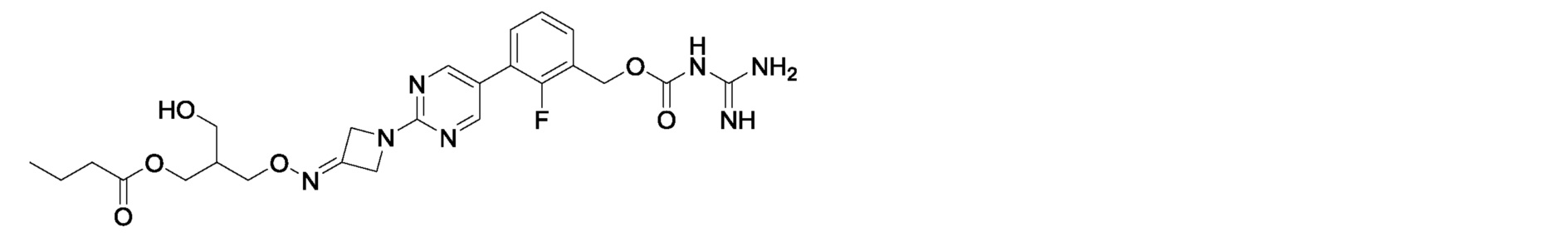
Раствор 2 М хлорида водорода в этаноле, 0,25 мл (0,50 ммоль), добавляли к раствору в этаноле (2 мл) 3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилбутирата, 92 мг (0,15 ммоль), синтезированного таким же образом, как в примере 31, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли TEA, 0,20 мл (1,4 ммоль), и смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол) с получением указанного в заголовке соединения в количестве 39 мг (0,073 ммоль, выход 49%) в виде белой пены.
Масс-спектр (ESI, m/z): 532[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,54-7,48 (m, 1H), 7,45-7,40 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,86-4,78 (m, 4H), 4,14-3,99 (m, 4H), 3,48-3,43 (m, 2H), 2,28 (t, J=7,3 Гц, 2H), 2,19-2,12 (m, 1H), 1,55 (sext, J=7,3 Гц, 2H), 0,88 (t, J=7,3 Гц, 3H).
[0314] (Пример 80)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилизобутират (соединение II-57)

При 0°C раствор 2 М хлорида водорода в этаноле, 1 мл (2 ммоль), добавляли к раствору в этаноле (2 мл) 3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилизобутирата, 0,12 г (0,19 ммоль), синтезированного таким же образом, как в примере 32, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли TEA и воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 53 мг (0,10 ммоль, выход 53%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 532[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,71-8,57 (m, 2H), 7,56-7,47 (m, 1H), 7,47-7,39 (m, 1H), 7,36-7,25 (m, 1H), 5,09 (s, 2H), 4,86-4,78 (m, 4H), 4,15-4,00 (m, 4H), 3,57-3,35 (m, 2H), 2,54 (sep, J=7,0 Гц, 1H), 2,25-2,08 (m, 1H), 1,09 (d, J=7,0 Гц, 6H).
[0315] (Пример 81)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилпивалат (соединение II-58)

При 0°C раствор 2 М хлорида водорода в этаноле, 1 мл (2 ммоль), добавляли к раствору в этаноле (4 мл) 3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилпивалата, 0,11 г (0,17 ммоль), синтезированного таким же образом, как в примере 33, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли TEA и воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 53 мг (0,097 ммоль, выход 57%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 546[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,56-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,87-4,77 (m, 4H), 4,14-3,99 (m, 4H), 3,56-3,39 (m, 2H), 2,26-2,07 (m, 1H), 1,15 (s, 9H).
[0316] (Пример 82)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилгексаноат (соединение II-59)

Раствор 2 М хлорида водорода в этаноле, 1,26 мл (2,52 ммоль), добавляли к раствору в этаноле (2,5 мл) 3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилгексаноата, 163 мг (0,253 ммоль), синтезированного таким же образом, как в примере 34, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли TEA, 0,35 мл (2,5 ммоль), и смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 62 мг (0,11 моль, выход 43%) в виде светло-желтого твердого вещества.
Масс-спектр (ESI, m/z): 560[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,1 Гц, 2H), 7,55-7,47 (m, 1H), 7,46-7,38 (m, 1H), 7,34-7,25 (m, 1H), 5,06 (s, 2H), 4,87-4,77 (m, 4H), 4,15-3,98 (m, 4H), 3,56-3,38 (m, 2H), 2,29 (t, J=7,4 Гц, 2H), 2,21-2,09 (m, 1H), 1,58-1,47 (m, 2H), 1,33-1,20 (m, 4H), 0,85 (t, J=6,8 Гц, 3H).
[0317] (Пример 83)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-(гидроксиметил)пропилбензоат (соединение II-60)

Раствор 2 М хлорида водорода в этаноле, 1,0 мл (2,0 ммоль), добавляли к раствору в этаноле (1 мл) 3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилбензоата, 102 мг (0,157 ммоль), синтезированного таким же образом, как в примере 35, и смесь перемешивали при комнатной температуре в течение 30 минут. После окончания реакции к реакционной смеси добавляли TEA и насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 88:12 (об/об)). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при комнатной температуре в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 65,0 мг (0,115 ммоль, выход 73%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 566[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (s, 2H), 8,01-7,96 (m, 2H), 7,68-7,57 (m, 1H), 7,55-7,48 (m, 3H), 7,46-7,39 (m, 1H), 7,34-7,27 (m, 1H), 5,07 (s, 2H), 4,84-4,71 (m, 4H), 4,35 (d, J=5,8 Гц, 2H), 4,25-4,11 (m, 2H), 3,62-3,53 (m, 2H), 2,41-2,30 (m, 1H).
[0318] (Пример 84)
2-Фтор-3-{5-(2-гидроксипропан-2-ил)-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат (соединение III-1134)

При 0°C раствор 2 М хлорида водорода в этаноле, 1,7 мл (3,4 ммоль), добавляли к раствору в этаноле (4 мл) 2-фтор-3-{6-[3-(метоксиимино)азетидин-1-ил]-5-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-3-ил}бензилкарбамимидоилкарбамата, 175 мг (0,331 ммоль), синтезированного таким же образом, как в примере 48, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли TEA и воду с последующей экстракцией метиленхлоридом. Органический слой промывали насыщенным водным раствором гидрокарбоната натрия, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 114 мг (0,256 ммоль, выход 77%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 445[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,32-8,25 (m, 1H), 7,80-7,74 (m, 1H), 7,51-7,44 (m, 1H), 7,42-7,35 (m, 1H), 7,34-7,22 (m, 1H), 5,06 (s, 2H), 4,88-4,79 (m, 4H), 3,81 (s, 3H), 1,56 (s, 6H).
[0319] (Пример 85)
2-Фтор-3-(2-{4-[(2-гидроксиэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-215)

Раствор 2 М хлорида водорода в этаноле, 1,0 мл (2,0 ммоль), добавляли к 2-фтор-3-{2-[4-({2-[(тетрагидропиран-2-ил)окси]этокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамату, 26 мг (0,049 ммоль), синтезированному таким же образом, как в примере 57, и смесь перемешивали при комнатной температуре в течение 20 минут. После окончания реакции реакционную смесь промывали насыщенным водным раствором гидрокарбоната натрия, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения в количестве 13 мг (0,029 ммоль, выход 59%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 446[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,55-7,48 (m, 1H), 7,43-7,36 (m, 1H), 7,33-7,24 (m, 1H), 5,06 (s, 2H), 4,01-3,96 (m, 2H), 3,96-3,90 (m, 4H), 3,63-3,55 (m, 2H), 2,62-2,55 (m, 2H), 2,42-2,33 (m, 2H).
[0320] (Пример 86)
2-Фтор-3-(2-{4-[(3-гидроксипропокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата гидрохлорид (соединения II-216 гидрохлорид)

Раствор 2 М хлорида водорода в этаноле, 1 мл (2 ммоль), добавляли к суспензии в этаноле (4 мл) 2-фтор-3-{2-[4-({3-[(тетрагидропиран-2-ил)окси]пропокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата, 92 мг (0,17 ммоль), синтезированного таким же образом, как в примере 58, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции осажденное твердое вещество собирали с помощью фильтрации, промывали TBME и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 53 мг (0,11 ммоль, выход 65%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 460[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (br s, 2H), 7,69-7,58 (m, 1H), 7,56-7,48 (m, 1H), 7,40-7,30 (m, 1H), 5,36 (s, 2H), 4,04 (t, J=6,5 Гц, 2H), 3,98-3,86 (m, 4H), 3,47 (t, J=6,4 Гц, 2H), 2,62-2,54 (m, 2H), 2,43-2,34 (m, 2H), 1,83-1,68 (m, 2H).
[0321] (Пример 87)
2-Фтор-3-(2-{4-[(4-гидроксибутокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата гидрохлорид (соединения II-217 гидрохлорид)

Раствор 2 М хлорида водорода в этаноле, 1 мл (2 ммоль), добавляли к раствору в этаноле (2 мл) 2-фтор-3-{2-[4-({4-[(тетрагидропиран-2-ил)окси]бутокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата, 0,11 г (0,20 ммоль), синтезированного таким же образом, как в примере 59, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции осажденное твердое вещество собирали с помощью фильтрации, промывали TBME и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 74 мг (0,15 ммоль, выход 75%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 474[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,3 Гц, 2H), 7,66-7,59 (m, 1H), 7,56-7,47 (m, 1H), 7,39-7,31 (m, 1H), 5,36 (s, 2H), 3,98 (t, J=6,6 Гц, 2H), 3,96-3,89 (m, 4H), 3,41 (t, J=6,5 Гц, 2H), 2,62-2,54 (m, 2H), 2,44-2,35 (m, 2H), 1,69-1,41 (m, 4H).
[0322] (Пример 88)
2-Фтор-3-(2-{4-[(3-гидрокси-2,2-диметилпропокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-221)

Раствор 2 М хлорида водорода в этаноле, 0,30 мл (0,60 ммоль), добавляли к суспензии в метиленхлориде (2 мл) 3-{2-[4-({2,2-диметил-3-[(тетрагидропиран-2-ил)окси]пропокси}имино)пиперидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамата, 90 мг (0,16 ммоль), синтезированного таким же образом, как в примере 61, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол) с получением указанного в заголовке соединения в количестве 56 мг (0,11 ммоль, выход 69%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 488[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (s, 2H), 7,54-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 3,97-3,87 (m, 4H), 3,78 (s, 2H), 3,18 (s, 2H), 2,63-2,56 (m, 2H), 2,41-2,34 (m, 2H), 0,84 (s, 6H).
[0323] (Пример 89)
2-Фтор-3-(2-{4-[(3-гидрокси-3-метилбутокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-222)

Раствор 2 М хлорида водорода в этаноле, 1,1 мл (2,2 ммоль), добавляли к суспензии в этаноле (0,57 мл) 2-фтор-3-{2-[4-({3-метил-3-[(тетрагидропиран-2-ил)окси]бутокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата, 130 мг (0,23 ммоль), синтезированного таким же образом, как в примере 62, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли TEA и насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 88:12 (об/об)) с получением указанного в заголовке соединения в количестве 95 мг (0,20 ммоль, выход 87%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 488[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,53-7,47 (m, 1H), 7,42-7,37 (m, 1H), 7,31-7,26 (m, 1H), 5,06 (s, 2H), 4,08 (t, J=7,3 Гц, 2H), 3,95-3,88 (m, 4H), 2,59-2,54 (m, 2H), 2,41-2,36 (m, 2H), 1,72 (t, J=7,3 Гц, 2H), 1,12 (s, 6H).
[0324] (Пример 90)
2-Фтор-3-(2-{4-[(2-гидроксипропокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-223)

Раствор 2 М хлорида водорода в этаноле, 0,4 мл (0,8 ммоль), добавляли к суспензии в этаноле (0,6 мл) 2-фтор-3-{2-[4-({2-[(тетрагидропиран-2-ил)окси]пропокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата, 47 мг (0,086 ммоль), синтезированного таким же образом, как в примере 63, и смесь перемешивали при комнатной температуре в течение 45 минут. После окончания реакции реакционную смесь концентрировали при пониженном давлении. К концентрированному остатку добавляли 3 мл насыщенного водного раствора гидрокарбоната натрия, и смесь перемешивали. Осажденное твердое вещество собирали с помощью фильтрации, промывали водой и диэтиловым эфиром и сушили при пониженном давлении. Полученное твердое вещество очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол=от 99:1 до 70:30 (об/об)). К полученному таким образом неочищенному продукту добавляли TBME, и смесь обрабатывали ультразвуком. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 12 мг (0,026 ммоль, выход 30%) в виде белого твердого вещества.
Масс-спектр (DUIS, m/z): 460[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,54-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 3,96-3,74 (m, 7H), 2,64-2,58 (m, 2H), 2,43-2,33 (m, 2H), 1,06 (d, J=6,1 Гц, 3H).
[0325] (Пример 91)
2-Фтор-3-(2-{4-[(3-гидрокси-2-метилпропокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-224)

Раствор 2 М хлорида водорода в этаноле, 0,40 мл (0,80 ммоль), добавляли к суспензии в метиленхлориде (2 мл) 2-фтор-3-{2-[4-({2-метил-3-[(тетрагидропиран-2-ил)окси]пропокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата, 100 мг (0,179 ммоль), синтезированного таким же образом, как в примере 64, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол) с получением указанного в заголовке соединения в количестве 65 мг (0,14 ммоль, выход 78%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 474[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,53-7,47 (m, 1H), 7,43-7,37 (m, 1H), 7,31-7,26 (m, 1H), 5,06 (s, 2H), 4,00-3,88 (m, 5H), 3,83-3,75 (m, 1H), 3,41-3,33 (m, 1H), 3,33-3,24 (m, 1H), 2,62-2,55 (m, 2H), 2,42-2,36 (m, 2H), 1,95-1,85 (m, 1H), 0,87 (d, J=6,9 Гц, 3H).
[0326] (Пример 92)
2-Фтор-3-[2-(3-{[3-гидрокси-2-(гидроксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-42)
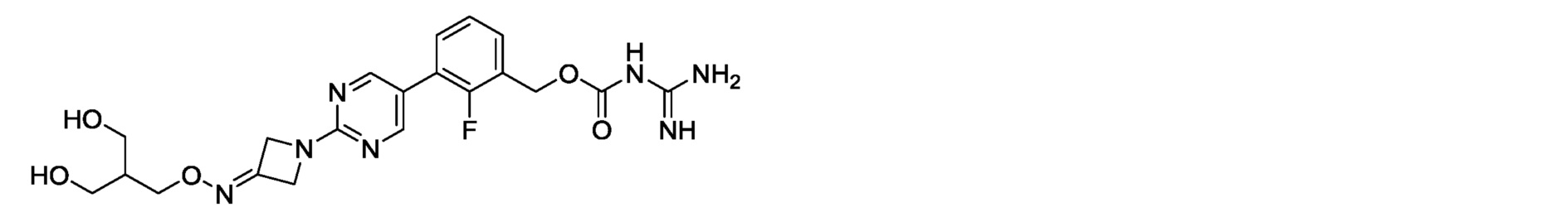
Раствор 2 М хлорида водорода в этаноле, 2,40 мл (4,80 ммоль), добавляли к суспензии в метиленхлориде (2 мл) 3-[2-(3-{[(2,2-диметил-1,3-диоксан-5-ил)метокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамата, 121 мг (0,241 ммоль), синтезированного таким же образом, как в примере 15, и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции к реакционной смеси добавляли TEA и воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 90:10 (об/об)). К полученному таким образом неочищенному продукту добавляли 5 мл этилацетата, и смесь перемешивали при 70°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 46,6 мг (0,101 ммоль, выход 42%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 462[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (s, 2H), 7,54-7,48 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,85-4,78 (m, 4H), 4,04 (d, J=6,4 Гц, 2H), 3,47-3,41 (m, 4H), 1,96-1,88 (m, 1H).
[0327] (Пример 93)
3-(2-{3-[(2,3-Дигидроксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-43)

Раствор 2 М хлорида водорода в этаноле, 1,0 мл (2,0 ммоль), добавляли к раствору в метиленхлориде (1,0 мл) 3-[2-(3-{[(2,2-диметил-1,3-диоксолан-4-ил)метокси)]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамата, 100 мг (0,21 ммоль), синтезированного таким же образом, как в примере 16, и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции к реакционной смеси добавляли TEA и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток два раза очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 88:12 (об/об)) с получением указанного в заголовке соединения в количестве 16 мг (0,036 ммоль, выход 17%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 448[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,65-8,61 (m, 2H), 7,54-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,86-4,79 (m, 4H), 4,07 (dd, J=4,5, 11,2 Гц, 1H), 3,92 (dd, J=6,7, 11,2 Гц, 1H), 3,75-3,60 (m, 1H), 3,36 (d, J=5,6 Гц, 2H).
[0328] (Пример 94)
3-(2-{3-[(3,4-Дигидроксибутокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-47)

Раствор 2 М хлорида водорода в этаноле, 1 мл (2 ммоль), добавляли к суспензии в этаноле (2 мл) 3-[2-(3-{[2-(2,2-диметил-1,3-диоксолан-4-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамата, 0,10 г (0,20 ммоль), синтезированного таким же образом, как в примере 19, и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции к реакционной смеси добавляли TEA и этанол. Смесь фильтровали, и фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 22 мг (0,048 ммоль, выход 24%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 462[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (br s, 2H), 7,56-7,47 (m, 1H), 7,46-7,39 (m, 1H), 7,34-7,26 (m, 1H), 5,06 (s, 2H), 4,90-4,73 (m, 4H), 4,13 (br t, J=6,5 Гц, 2H), 3,62-3,45 (m, 1H), 3,36-3,21 (m, 2H), 1,92-1,75 (m, 1H), 1,65-1,47 (m, 1H).
[0329] (Пример 95)
3-(6-{3-[(3,4-Дигидроксибутокси)имино]азетидин-1-ил}-5-фторпиридин-3-ил)-2-фторбензилкарбамимидоилкарбамат (соединение III-123)

Раствор 2 М хлорида водорода в этаноле, 0,71 мл (1,4 ммоль), добавляли к раствору в этаноле (5 мл) 3-[6-(3-{[2-(2,2-диметил-1,3-диоксолан-4-ил)этокси]имино}азетидин-1-ил)-5-фторпиридин-3-ил]-2-фторбензилкарбамимидоилкарбамата, 244 мг (0,471 ммоль), синтезированного таким же образом, как в примере 38, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли TEA, 0,20 мл (1,4 ммоль), и смесь концентрировали при пониженном давлении. К концентрированному остатку добавляли смешанный раствор метанол-метиленхлорид (5:95 (об/об)), и осажденное твердое вещество собирали с помощью фильтрации. Фильтрат концентрировали при пониженном давлении и очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол). Твердое вещество, полученное таким образом, и твердое вещество, полученное с помощью предыдущей фильтрации, объединяли, туда добавляли этилацетат, и смесь перемешивали при 50°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 123 мг (0,257 ммоль, выход 55%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 479[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,21-8,13 (m, 1H), 7,78-7,71 (m, 1H), 7,53-7,46 (m, 1H), 7,44-7,38 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,90-4,82 (m, 4H), 4,16-4,09 (m, 2H), 3,58-3,48 (m, 1H), 3,35-3,22 (m, 2H), 1,88-1,78 (m, 1H), 1,59-1,47 (m, 1H).
[0330] (Пример 96)
2-Фтор-3-{5-фтор-6-[3-{[3-гидрокси-2-(гидроксиметил)пропокси]имино}азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат (соединение III-118)
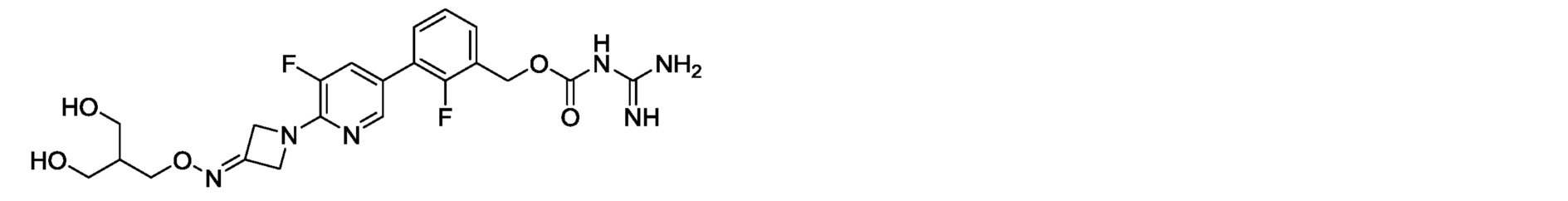
Раствор 2 М хлорида водорода в этаноле, 0,18 мл (0,36 ммоль), добавляли к раствору в этаноле (2 мл) 3-[6-(3-{[(2,2-диметил-1,3-диоксан-5-ил)метокси]имино}азетидин-1-ил)-5-фторпиридин-3-ил]-2-фторбензилкарбамимидоилкарбамата, 62 мг (0,12 ммоль), синтезированного таким же образом, как в примере 39, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли TEA, 50 мкл (0,36 ммоль), и смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол) с получением указанного в заголовке соединения в количестве 24 мг (0,050 ммоль, выход 42%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 479[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,22-8,13 (m, 1H), 7,79-7,71 (m, 1H), 7,53-7,47 (m, 1H), 7,44-7,38 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,90-4,83 (m, 4H), 4,04 (d, J=6,3 Гц, 2H), 3,47-3,43 (m, 4H), 1,96-1,86 (m, 1H).
[0331] (Пример 97)
2-Фтор-3-[2-(4-{[3-гидрокси-2-(гидроксиметил)пропокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-230)

Раствор 2 М хлорида водорода в этаноле, 1,41 мл (2,82 ммоль), добавляли к раствору в этаноле (0,3 мл) 3-[2-(4-{[(2,2-диметил-1,3-диоксан-5-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамата, 150 мг (0,283 ммоль), синтезированного таким же образом, как в примере 65, и смесь перемешивали при комнатной температуре в течение 30 минут. После окончания реакции к реакционной смеси добавляли TEA и насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол=от 100:0 до 92:8 (об/об)) с получением указанного в заголовке соединения в количестве 112 мг (0,229 ммоль, выход 81%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 490[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,53-7,47 (m, 1H), 7,42-7,37 (m, 1H), 7,31-7,26 (m, 1H), 5,06 (s, 2H), 3,98 (d, J=6,4 Гц, 2H), 3,96-3,89 (m, 4H), 3,47-3,39 (m, 4H), 2,61-2,55 (m, 2H), 2,43-2,36 (m, 2H), 1,93-1,85 (m, 1H).
[0332] (Пример 98)
2-Фтор-3-[2-(4-{[3-гидрокси-2-(гидроксиметил)-2-метилпропокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-232)

Раствор 2 М хлорида водорода в этаноле, 0,30 мл (0,60 ммоль), добавляли к раствору в метиленхлориде (2 мл) 2-фтор-3-[2-(4-{[(2,2,5-триметил-1,3-диоксан-5-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамата, 68 мг (0,13 ммоль), синтезированного таким же образом, как в примере 66, и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли TEA, 0,10 мл (0,72 ммоль), и смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол). К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 50°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 28 мг (0,056 ммоль, выход 43%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 504[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,53-7,47 (m, 1H), 7,42-7,37 (m, 1H), 7,31-7,25 (m, 1H), 5,06 (s, 2H), 3,96-3,89 (m, 4H), 3,86 (s, 2H), 3,28 (s, 4H), 2,61-2,55 (m, 2H), 2,40-2,35 (m, 2H), 0,81 (s, 3H).
[0333] (Пример 99)
3-(2-{4-[(2,3-Дигидроксипропокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-231)
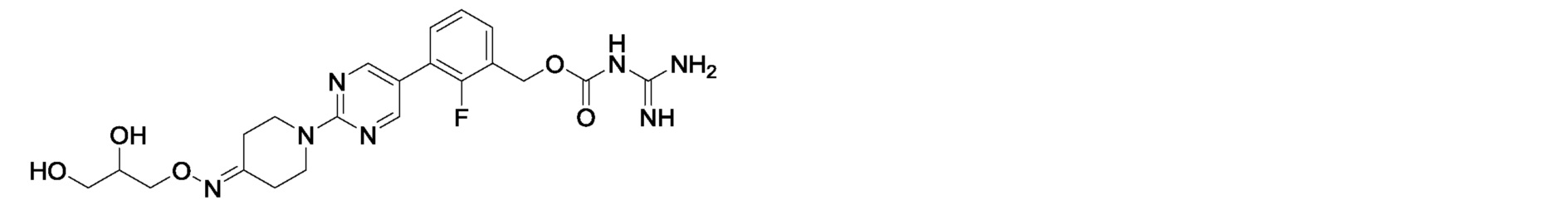
При 0°C раствор 2 М хлорида водорода в этаноле, 1 мл (2 ммоль), добавляли к 3-[2-(4-{[(2,2-диметил-1,3-диоксолан-4-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамату, 0,11 г (0,21 ммоль), синтезированному таким же образом, как в примере 67, и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции к реакционной смеси добавляли TEA и этанол. Смесь фильтровали, и фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 72 мг (0,15 ммоль, выход 71%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 476[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (br s, 2H), 7,56-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,07-3,82 (m, 6H), 3,76-3,64 (m, 1H), 3,41-3,31 (m, 2H), 2,65-2,55 (m, 2H), 2,44-2,35 (m, 2H).
[0334] (Пример 100)
2-Фтор-3-[2-(3-{[3-гидрокси-2-(метоксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-45)

Уксусную кислоту, 1,0 мл, добавляли к раствору в THF (2 мл) и воде (1 мл) 2-фтор-3-(2-{3-[(3-метокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата, 126 мг (0,225 ммоль), синтезированного таким же образом, как в примере 17, и смесь перемешивали при 60°C в течение 15 часов. После окончания реакции реакционную смесь очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 31 мг (0,065 ммоль, выход 29%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 476[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,26 (m, 1H), 5,07 (s, 2H), 4,90-4,71 (m, 4H), 4,12-3,84 (m, 2H), 3,44 (d, J=5,6 Гц, 2H), 3,39-3,32 (m, 2H), 3,23 (s, 3H), 2,12-2,00 (m, 1H).
[0335] (Пример 101)
2-Фтор-3-(2-{3-[(3-гидрокси-2-метоксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-46)

При 0°C раствор 2 М хлорида водорода в этаноле, 1 мл (2 ммоль), добавляли к раствору в этаноле (2 мл) 2-фтор-3-[2-(3-{[2-метокси-3-(тритилокси)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамата, 123 мг (0,175 ммоль), синтезированного таким же образом, как в примере 18, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли TEA. Смесь фильтровали, и фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 54 мг (0,12 ммоль, выход 69%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 462[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,56-7,48 (m, 1H), 7,46-7,39 (m, 1H), 7,34-7,25 (m, 1H), 5,06 (s, 2H), 4,87-4,79 (m, 4H), 4,19-3,96 (m, 2H), 3,48-3,40 (m, 3H), 3,34 (s, 3H).
[0336] (Пример 102)
2-Фтор-3-(2-{3-[(2-фтор-3-гидроксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-40)

При 0°C раствор 2 М хлорида водорода в этаноле, 9 мл (18 ммоль), добавляли к суспензии в этаноле (10 мл) 2-фтор-3-[2-(3-{[2-фтор-3-(тритилокси)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамата, 2,45 г (3,54 ммоль), синтезированного таким же образом, как в примере 22, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли TEA (6 мл), и смесь концентрировали при пониженном давлении. К концентрированному остатку добавляли воду, и осажденное твердое вещество собирали с помощью фильтрации. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при 50°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 1,20 г (2,67 ммоль, выход 75%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 450[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (s, 2H), 7,57-7,47 (m, 1H), 7,45-7,39 (m, 1H), 7,34-7,25 (m, 1H), 5,06 (s, 2H), 4,93-4,57 (m, 5H), 4,34-4,13 (m, 2H), 3,72-3,49 (m, 2H).
[0337] (Пример 103)
2-Фтор-3-(5-фтор-6-{3-[(2-фтор-3-гидроксипропокси)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамат (соединение III-116)

При 0°C раствор 2 М хлорида водорода в этаноле, 4,5 мл (9,0 ммоль), добавляли к раствору в этаноле (4 мл) 2-фтор-3-[5-фтор-6-(3-{[2-фтор-3-(тритилокси)пропокси]имино}азетидин-1-ил)пиридин-3-ил]бензилкарбамимидоилкарбамата, 631 мг (0,890 ммоль), синтезированного таким же образом, как в примере 40, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли TEA (2 мл) и воду с последующей экстракцией метиленхлоридом. Органический слой промывали насыщенным водным раствором гидрокарбоната натрия, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при комнатной температуре в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 332 мг (0,712 ммоль, выход 80%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 467[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,21-8,16 (m, 1H), 7,80-7,71 (m, 1H), 7,54-7,45 (m, 1H), 7,44-7,37 (m, 1H), 7,33-7,24 (m, 1H), 5,06 (s, 2H), 4,93-4,85 (m, 4H), 4,84-4,61 (m, 1H), 4,31-4,12 (m, 2H), 3,70-3,50 (m, 2H).
[0338] (Пример 104)
2-Фтор-3-(2-{3-[(2-гидрокси-3-метоксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-49)

Гидроксид лития, 4,0 мг (0,17 ммоль), добавляли к раствору в THF (2 мл) и воде (0,4 мл) 1-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-3-метоксипропан-2-илацетата, 43 мг (0,085 ммоль), синтезированного таким же образом, как в примере 20, и смесь перемешивали при 50°C в течение 2 часов. После окончания реакции к реакционной смеси добавляли уксусную кислоту, 10 мкл (0,17 ммоль). Смесь очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 42 мг (включая примеси) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 462[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,4 Гц, 2H), 7,58-7,48 (m, 1H), 7,45-7,37 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,86-4,79 (m, 4H), 4,04-3,90 (m, 2H), 3,89-3,81 (m, 1H), 3,37-3,28 (m, 2H), 3,27 (s, 3H).
[0339] (Пример 105)
2-Фтор-3-{2-[4-(гидроксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата гидрохлорид (соединения II-204 гидрохлорид)

Раствор 2 М хлорида водорода в этаноле, 3,0 мл (6,0 ммоль), добавляли к 2-фтор-3-[2-(4-{[(тетрагидропиран-2-ил)окси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамату, 117 мг (0,241 ммоль), синтезированному таким же образом, как в примере 52, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 106 мг (включая примеси) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 402[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,61 (d, J=1,4 Гц, 2H), 7,67-7,58 (m, 1H), 7,55-7,49 (m, 1H), 7,38-7,32 (m, 1H), 5,36 (s, 2H), 3,95-3,89 (m, 4H), 2,60-2,54 (m, 2H), 2,40-2,34 (m, 2H).
[0340] (Пример 106)
3-[6-(3-{[(трет-бутилдиметилсилил)окси]имино}азетидин-1-ил)-5-фторпиридин-3-ил]-2-фторбензилкарбамимидоилкарбамат (соединение III-138)
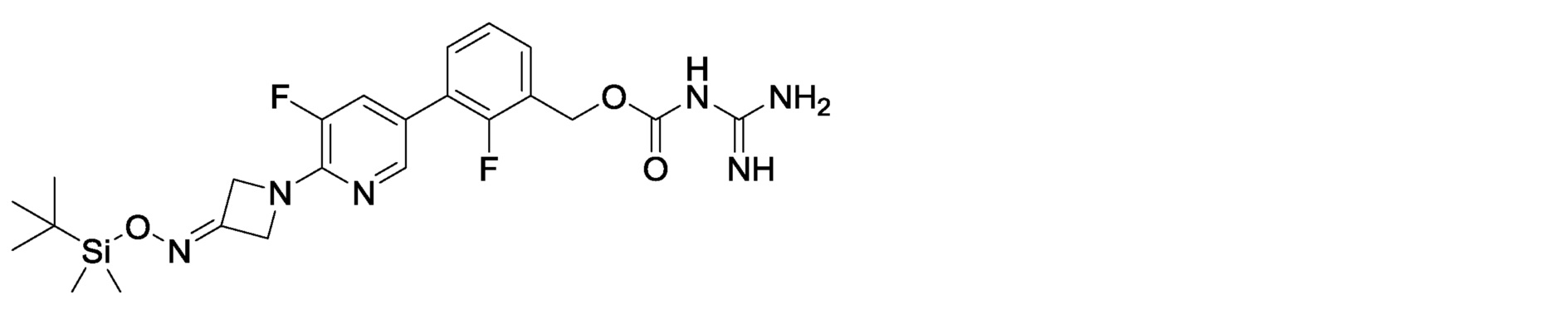
CDI, 350 мг (2,16 ммоль), добавляли к раствору в DMF (6 мл) 1-{3-фтор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-(трет-бутилдиметилсилил)оксима, 450 мг (1,07 ммоль), синтезированного таким же образом, как в ссылочном примере 13-2, и смесь перемешивали при комнатной температуре в течение 26 часов. Затем добавляли карбонат гуанидина, 580 мг (3,22 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 422 мг (0,836 ммоль, выход 78%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,25-8,18 (m, 1H), 7,84-7,75 (m, 1H), 7,58-7,50 (m, 1H), 7,49-7,41 (m, 1H), 7,38-7,28 (m, 1H), 5,10 (s, 2H), 4,95-4,89 (m, 4H), 0,96 (s, 9H), 0,20 (s, 6H).
[0341] (Пример 107)
2-Фтор-3-{5-фтор-6-[3-(гидроксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамат (соединение III-77)

Раствор 1 М тетрабутиламмония фторида в THF, 0,24 мл (0,24 ммоль), добавляли к раствору в THF (2 мл) 3-[6-(3-{[(трет-бутилдиметилсилил)окси]имино}азетидин-1-ил)-5-фторпиридин-3-ил]-2-фторбензилкарбамимидоилкарбамата, 100 мг (0,20 ммоль), синтезированного таким же образом, как в примере 106, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Затем добавляли этилацетат, и смесь перемешивали при комнатной температуре в течение 3 часов. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 35 мг (0,090 ммоль, выход 45%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 391[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,17 (s, 1H), 7,81-7,68 (m, 1H), 7,55-7,46 (m, 1H), 7,45-7,37 (m, 1H), 7,33-7,24 (m, 1H), 5,06 (s, 2H), 4,89-4,78 (m, 4H).
[0342] (Пример 108)
трет-Бутил-2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]ацетат (соединение II-279)

CDI, 82 мг (0,51 ммоль), добавляли к раствору в DMF (3 мл) трет-бутил-2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}ацетата, 92 мг (0,23 ммоль), синтезированного таким же образом, как в ссылочном примере 7-62, и смесь перемешивали при комнатной температуре в течение 2,5 часа. Затем добавляли карбонат гуанидина, 82 мг (0,46 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли толуол, который затем концентрировали при пониженном давлении, и эту операцию повторяли несколько раз. Добавляли этилацетат, и смесь обрабатывали ультразвуком. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 88 мг (0,18 ммоль, выход 78%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 488[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (s, 2H), 7,55-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,34-7,25 (m, 1H), 5,06 (s, 2H), 4,90-4,80 (m, 4H), 4,54 (s, 2H), 1,44 (s, 9H).
[0343] (Пример 109)
2-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]уксусной кислоты гидрохлорид (соединения II-274 гидрохлорид)
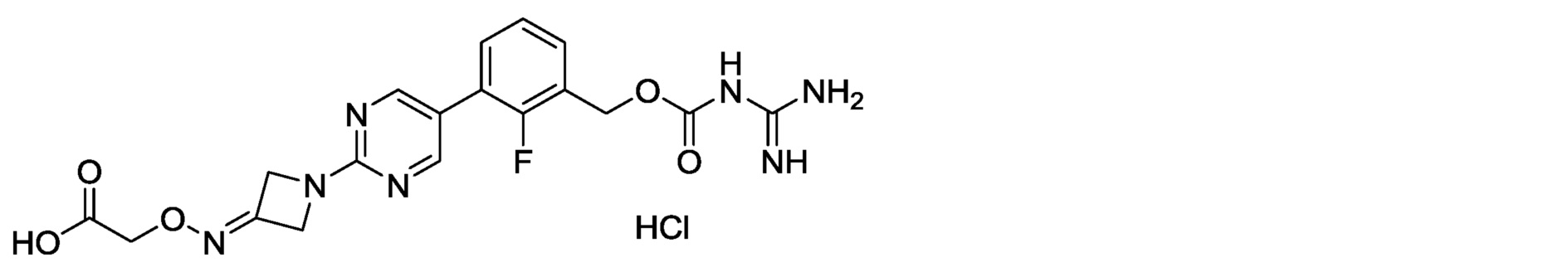
Раствор 4 М хлорида водорода в 1,4-диоксане, 500 мкл (2,00 ммоль), добавляли к суспензии в метиленхлориде (1 мл) трет-бутил-2-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]ацетата, 70 мг (0,14 ммоль), синтезированного таким же образом, как в примере 108, и смесь перемешивали при комнатной температуре в течение 20 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. К концентрированному остатку добавляли TBME, и смесь перемешивали при 50°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении. Водный раствор 1 н гидроксида натрия, 6,00 мл (6,00 ммоль), добавляли к раствору твердого вещества, полученного выше, в смешанном растворителе (2 мл) метиленхлорид:метанол=90:10 (об/об), и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции реакционную смесь нейтрализовывали добавлением 1 н соляной кислоты. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении. Раствор 4 М хлорида водорода в 1,4-диоксане, 1,00 мл (1,00 ммоль), добавляли к суспензии твердого вещества в метиленхлориде (1 мл), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции реакционную смесь концентрировали при пониженном давлении. К концентрированному остатку добавляли TBME, и смесь перемешивали при 50°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 25 мг (0,053 ммоль, выход 38%) в виде светло-желтого твердого вещества.
Масс-спектр (APCI, m/z): 432[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,65 (d, J=1,3 Гц, 2H), 7,67-7,60 (m, 1H), 7,57-7,51 (m, 1H), 7,40-7,33 (m, 1H), 5,37 (s, 2H), 4,89-4,82 (m, 4H), 4,59 (s, 2H).
[0344] (Пример 110)
3-[2-(3-{[(Диметилкарбамоил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-282)
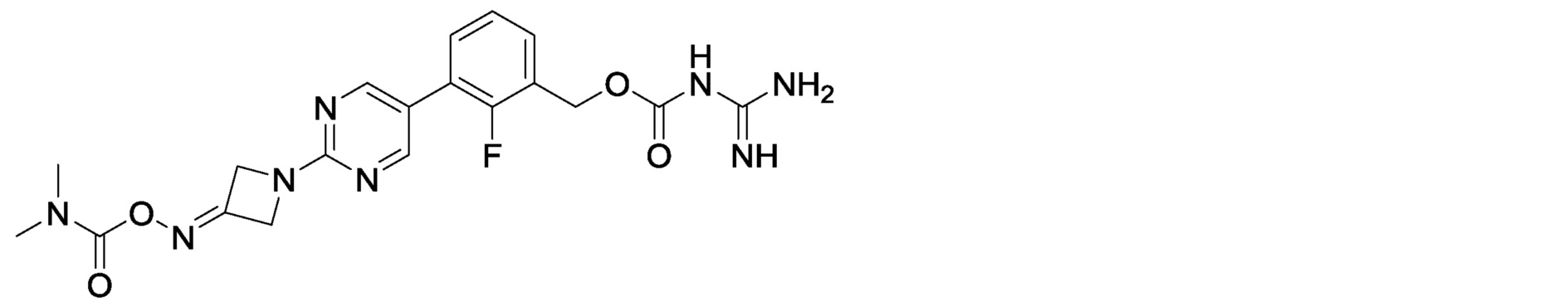
CDI, 41 мг (0,25 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-диметилкарбамоилоксима, 41 мг (0,11 ммоль), синтезированного таким же образом, как в ссылочном примере 7-63, и смесь перемешивали при комнатной температуре в течение 16 часов. Затем добавляли карбонат гуанидина, 41 мг (0,23 ммоль), и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. К твердому веществу добавляли этилацетат, и смесь перемешивали при комнатной температуре в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 22 мг (0,050 ммоль, выход 45%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 445[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,65 (d, J=1,1 Гц, 2H), 7,55-7,49 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,07 (s, 2H), 4,96 (s, 4H), 2,89 (s, 6H).
[0345] (Пример 111)
2-Фтор-3-[2-(3-{[2-(метиламино)-2-оксоэтокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-283)
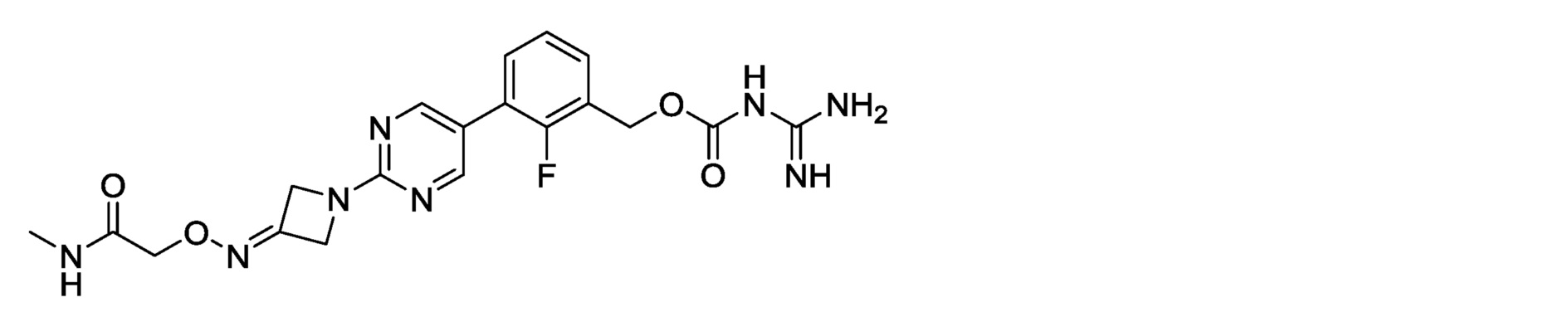
CDI, 60 мг (0,37 ммоль), добавляли к раствору в DMF (4 мл) 2-({[1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден]амино}окси)-N-метилацетамида, 58 мг (0,16 ммоль), синтезированного таким же образом, как ссылочное соединение 7-64, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 60 мг (0,33 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол). К полученному неочищенному продукту добавляли этилацетат, и смесь перемешивали при комнатной температуре. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении. Затем добавляли метанол, и смесь перемешивали. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении. Полученное таким образом твердое вещество очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). Полученный неочищенный продукт растворяли с помощью добавления смешанного растворителя метиленхлорид:метанол=90:10 (об/об). Раствор концентрировали при пониженном давлении, и концентрированный остаток сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 13 мг (0,029 ммоль, выход 18%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 445[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,65 (s, 2H), 7,66 (br d, J=4,3 Гц, 1H), 7,57-7,48 (m, 1H), 7,46-7,38 (m, 1H), 7,33-7,25 (m, 1H), 5,06 (s, 2H), 4,98-4,80 (m, 4H), 4,44 (s, 2H), 2,64 (d, J=4,5 Гц, 3H).
[0346] (Пример 112)
3-(2-{3-[(3-Амино-3-оксопропокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-284)

CDI, 226 мг (1,39 ммоль), добавляли к раствору в DMF (4 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}пропанамида, 165 мг (0,459 ммоль), синтезированного таким же образом, как в ссылочном примере 7-65, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 170 мг (0,944 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре в течение 30 минут. Осажденное твердое вещество собирали с помощью фильтрации. Полученное твердое вещество очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при 70°C в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 69,5 мг (0,156 ммоль, выход 34%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 445[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,3 Гц, 2H), 7,58-7,48 (m, 1H), 7,45-7,35 (m, 2H), 7,34-7,26 (m, 1H), 6,87 (br s, 1H), 5,06 (s, 2H), 4,92-4,68 (m, 4H), 4,22 (t, J=6,5 Гц, 2H), 2,42 (t, J=6,5 Гц, 2H).
[0347] (Пример 113)
2-Фтор-3-[2-(3-{[3-(метиламино)-3-оксопропокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-285)

CDI, 293 мг (1,81 ммоль), добавляли к раствору в DMF (4 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-N-метилпропанамида, 168 мг (0,450 ммоль), синтезированного таким же образом, как в ссылочном примере 7-66, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 165 мг (0,916 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при 70°C в течение 1 часа. После этого твердое вещество очищали путем сбора с помощью фильтрации и сушки при пониженном давлении с получением указанного в заголовке соединения в количестве 51,0 мг (0,111 ммоль, выход 25%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 459[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,83 (br d, J=4,3 Гц, 1H), 7,54-7,47 (m, 1H), 7,45-7,37 (m, 1H), 7,34-7,24 (m, 1H), 5,06 (s, 2H), 4,90-4,64 (m, 4H), 4,22 (t, J=6,5 Гц, 2H), 2,57 (d, J=4,3 Гц, 3H), 2,43 (t, J=6,5 Гц, 2H).
[0348] (Пример 114)
Этил-4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутаноат (соединение II-281)

CDI, 127 мг (0,783 ммоль), добавляли к раствору в DMF (6 мл) этил-4-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}бутаноата, 157 мг (0,390 ммоль), синтезированного таким же образом, как в ссылочном примере 7-67, и смесь перемешивали при комнатной температуре в течение 16 часов. Затем добавляли карбонат гуанидина, 141 мг (0,783 ммоль), и смесь перемешивали при комнатной температуре в течение 5 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 153 мг (0,314 ммоль, выход 81%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 488[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,46-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,87-4,77 (m, 4H),4,23-3,93 (m, 4H), 2,38 (t, J=7,3 Гц, 2H), 1,92-1,82 (m, 2H), 1,19 (t, J=7,1 Гц, 3H).
[0349] (Пример 115)
4-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутановая кислота (соединение II-276)

Гидроксид лития, 13 мг (0,543 ммоль), добавляли к суспензии в THF (4 мл) и воде (1 мл) этил-4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутаноата, 130 мг (0,267 ммоль), синтезированного таким же образом, как в примере 114, и смесь перемешивали при 50°C в течение 3 часов. После окончания реакции к реакционной смеси добавляли уксусную кислоту, 0,12 мл (2,10 ммоль), и воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Полученное твердое вещество сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 103 мг (0,224 ммоль, выход 84%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 460[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,49-7,37 (m, 2H), 7,31-7,20 (m, 1H), 5,09 (s, 2H), 4,86-4,74 (m, 4H), 4,05 (t, J=6,5 Гц, 2H),2,27 (t, J=7,3 Гц, 2H), 1,92-1,82 (m, 2H).
[0350] (Пример 116)
2-Фтор-3-[2-(3-{[4-(метиламино)-4-оксобутокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-290)

CDI, 110 мг (0,678 ммоль), добавляли к раствору в DMF (4 мл) 4-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-N-метилбутанамида, 116 мг (0,299 ммоль), синтезированного таким же образом, как ссылочное соединение 7-68, и смесь перемешивали при комнатной температуре в течение 30 минут. Затем добавляли карбонат гуанидина, 110 мг (0,611 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при 50°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 88,2 мг (0,187 ммоль, выход 63%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 473[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (d, J=1,4 Гц, 2H), 7,83-7,68 (m, 1H), 7,55-7,47 (m, 1H), 7,46-7,37 (m, 1H), 7,33-7,25 (m, 1H), 5,06 (s, 2H), 4,91-4,68 (m, 4H), 4,01 (t, J=6,5 Гц, 2H), 2,56 (d, J=4,6 Гц, 3H), 2,13 (t, J=7,5 Гц, 2H), 1,90-1,75 (m, 2H).
[0351] (Пример 117)
3-[2-(3-{[2-(Диметиламино)этокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-293)

CDI, 124 мг (0,765 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(диметиламино)этил]оксима, 55,0 мг (0,153 ммоль), синтезированного таким же образом, как в ссылочном примере 7-69, и смесь перемешивали при комнатной температуре в течение 16 часов. Затем добавляли карбонат гуанидина, 138 мг (0,766 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). Полученный таким образом неочищенный продукт промывали этилацетатом и водой и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 20,0 мг (0,0450 ммоль, выход 29%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 445[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,45-7,39 (m, 1H), 7,34-7,26 (m, 1H), 5,06 (s, 2H), 4,86-4,77 (m, 4H), 4,11 (t, J=6,0 Гц, 2H), 2,57-2,47 (m, 2H), 2,17 (s, 6H).
[0352] (Пример 118)
3-{2-[3-({2-[Бензил(метил)амино]этокси}имино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат (соединение II-294)

CDI, 62 мг (0,38 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-{2-[бензил(метил)амино]этил}оксима, 83 мг (0,19 ммоль), синтезированного таким же образом, как в ссылочном примере 7-70, и смесь перемешивали при комнатной температуре в течение 16 часов. Затем добавляли карбонат гуанидина, 69 мг (0,38 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Полученный таким образом неочищенный продукт промывали водой и этилацетатом и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 32 мг (0,061 ммоль, выход 32%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 521[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,0 Гц, 2H), 7,55-7,48 (m, 1H), 7,46-7,38 (m, 1H), 7,34-7,18 (m, 6H), 5,06 (s, 2H), 4,84-4,75 (m, 4H), 4,14(t, J=5,8 Гц, 2H), 3,59-3,40 (m, 2H), 2,62 (t, J=6,0 Гц, 2H), 2,20 (s, 3H).
[0353] (Пример 119)
3-(2-{3-[(3-Ацетамидо-2-{[(тетрагидропиран-2-ил)окси]метил}пропокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-362)

CDI, 67 мг (0,41 ммоль), добавляли к раствору в DMF (4 мл) N-(3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)ацетамида, 69 мг (0,14 ммоль), синтезированного таким же образом, как в ссылочном примере 7-71, и смесь перемешивали при комнатной температуре в течение 20 часов. Затем добавляли карбонат гуанидина, 50 мг (0,28 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 62 мг (0,11 ммоль, выход 79%) в виде белой пены.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,1 Гц, 2H), 7,91-7,84 (m, 1H), 7,54-7,47 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,87-4,78 (m, 4H), 4,57-4,52 (m, 1H), 4,09-3,99 (m, 2H), 3,78-3,58 (m, 2H), 3,48-3,40 (m,1H), 3,37-3,27 (m, 1H), 3,20-3,06 (m, 2H), 2,18-2,06 (m, 1H), 1,82 (s, 3H), 1,74-1,37 (m, 6H).
[0354] (Пример 120)
3-[2-(3-{[3-Ацетамидо-2-(гидроксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-302)
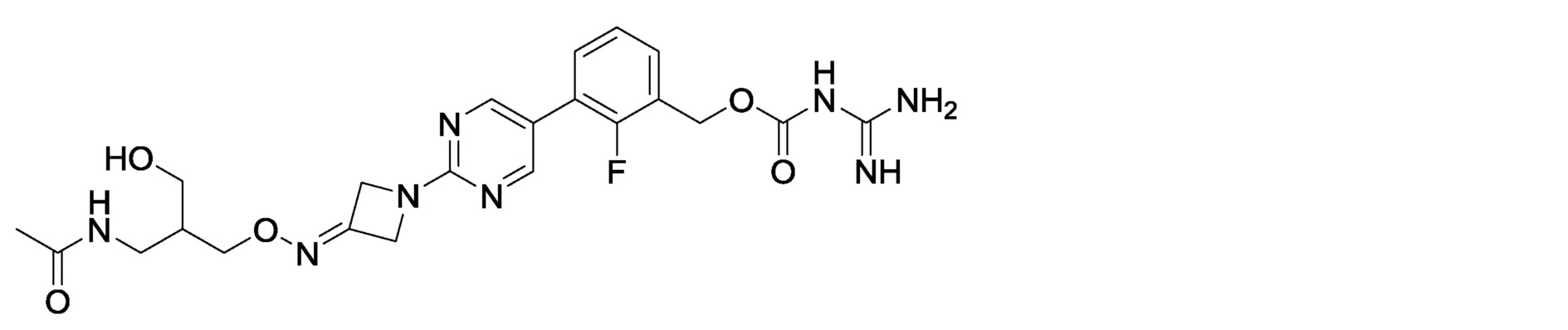
При 0°C раствор 2 М хлорида водорода в этаноле, 0,50 мл (1,0 ммоль), добавляли к раствору в этаноле (2 мл) 3-(2-{3-[(3-ацетамидо-2-{[(тетрагидропиран-2-ил)окси]метил}пропокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамата, 62 мг (0,11 ммоль), синтезированного таким же образом, как в примере 119, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли TEA. Смесь очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 41 мг (0,082 ммоль, выход 77%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 503[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,94-7,84 (m, 1H), 7,53-7,46 (m, 1H), 7,45-7,38 (m, 1H), 7,34-7,27 (m, 1H), 5,06 (s, 2H),4,86-4,78 (m, 4H), 4,07-3,94 (m, 2H), 3,44-3,35 (m, 2H), 3,17-3,04 (m, 2H), 1,99-1,90 (m, 1H), 1,82 (s, 3H).
[0355] (Пример 121)
3-{(2-[3-({3-(Диметиламино)-2-[(тетрагидропиран-2-илокси)метил]пропокси}имино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат (соединение II-363)

CDI, 50 мг (0,31 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(3-(диметиламино)-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксима, 50 мг (0,10 ммоль), синтезированного таким же образом, как в ссылочном примере 7-72, и смесь перемешивали при комнатной температуре в течение 19 часов. Затем добавляли карбонат гуанидина, 37 мг (0,21 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 48 мг (0,084 ммоль, выход 84%) в виде бесцветного масла.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,87-4,74 (m, 4H), 4,59-4,51 (m, 1H), 4,12-4,01 (m, 2H), 3,78-3,60 (m, 2H), 3,49-3,28 (m, 2H), 2,30-2,19 (m, 2H), 2,18-2,09 (m, 7H), 1,76-1,37(m, 6H).
[0356] (Пример 122)
3-[2-(3-{[3-(Диметиламино)-2-(гидроксиметил)пропокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-303)
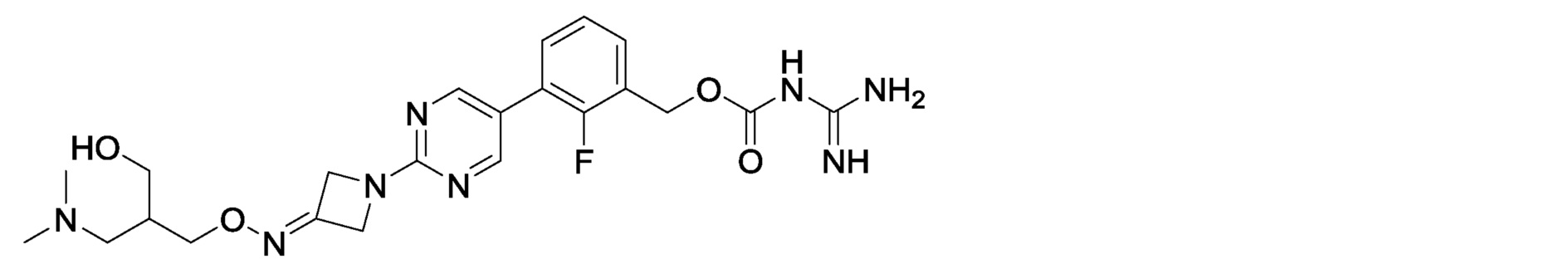
При 0°C раствор 2 М хлорида водорода в этаноле, 0,40 мл (0,80 ммоль), добавляли к раствору в этаноле (1 мл) 3-(2-{3-[(3-(диметиламино)-2-{[(тетрагидропиран-2-илокси)метил]пропокси}имино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамата, 48 мг (0,084 ммоль), синтезированного таким же образом, как в примере 121, и смесь перемешивали при комнатной температуре в течение 0,5 часа. После окончания реакции к реакционной смеси добавляли TEA. Смесь очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 20 мг (0,041 ммоль, выход 49%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 489[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,0 Гц, 2H), 7,54-7,46 (m, 1H), 7,45-7,35 (m, 1H), 7,34-7,25 (m, 1H), 5,06 (s, 2H), 4,86-4,77 (m, 4H), 4,57 (br s, 1H), 4,06-3,97 (m, 2H), 3,49-3,41 (m, 2H), 2,27-2,15 (m, 2H), 2,13 (s, 6H), 2,06-1,94 (m, 1H).
[0357] (Пример 123)
3-(2-{3-[(3-Ацетамидо-2-метоксипропокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-304)

CDI, 40 мг (0,25 ммоль), добавляли к раствору в DMF (4 мл) N-(3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-метоксипропил)ацетамида, 50 мг (0,12 ммоль), синтезированного таким же образом, как в ссылочном примере 7-73, и смесь перемешивали при комнатной температуре в течение 15 часов. Затем добавляли карбонат гуанидина, 45 мг (0,25 ммоль), и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 33 мг (0,066 ммоль, выход 55%) в виде светло-желтого твердого вещества.
Масс-спектр (ESI, m/z): 503[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (s, 2H), 7,89 (t, J=5,6 Гц, 1H), 7,57-7,46 (m, 1H), 7,46-7,36 (m, 1H), 7,35-7,22 (m, 1H), 5,06 (s, 2H), 4,88-4,77 (m, 4H), 4,13-3,95 (m, 2H), 3,51-3,44 (m, 1H), 3,34 (s, 3H), 3,26-3,08 (m, 2H), 1,82 (s, 3H).
[0358] (Пример 124)
2-Фтор-3-[2-(3-{[2-(пиперидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-311)

CDI, 94 мг (0,58 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(пиперидин-1-ил)этил]оксима, 77 мг (0,19 ммоль), синтезированного таким же образом, как в ссылочном примере 7-74, и смесь перемешивали при комнатной температуре в течение 16 часов. Затем добавляли карбонат гуанидина, 104 мг (0,58 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Полученный таким образом неочищенный продукт промывали водой и этилацетатом и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 45 мг (0,093 ммоль, выход 49%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 485[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,46-7,39 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,87-4,75 (m, 4H), 4,13 (t, J=6,1 Гц, 2H), 2,59-2,47 (m, 2H), 2,45-2,30 (m, 4H), 1,54-1,44 (m, 4H), 1,41-1,32 (m, 2H).
[0359] (Пример 125)
2-Фтор-3-(2-{3-[(2-морфолиноэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-312)

CDI, 126 мг (0,777 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(2-морфолиноэтил)оксима, 104 мг (0,259 ммоль), синтезированного таким же образом, как в ссылочном примере 7-75, и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли карбонат гуанидина, 95,2 мг (0,528 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 103 мг (0,212 ммоль, выход 82%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 487[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,53-7,48 (m, 1H), 7,45-7,39 (m, 1H), 7,34-7,26 (m, 1H), 5,06 (s, 2H), 4,87-4,76 (m, 4H), 4,15 (t, J=6,0 Гц, 2H), 3,60-3,55 (m, 4H), 2,59 (t, J=6,0 Гц, 2H), 2,46-2,39 (m, 4H).
[0360] (Пример 126)
3-[2-(3-{[2-(Азетидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-313)

CDI, 35 мг (0,22 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(азетидин-1-ил)этил]оксима, 27 мг (0,071 ммоль), синтезированного таким же образом, как в ссылочном примере 7-76, и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли CDI, 12 мг (0,074 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 26 мг (0,14 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 24 мг (0,053 ммоль, выход 74%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 457[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,46-7,39 (m, 1H), 7,33-7,28 (m, 1H), 5,07 (s, 2H), 4,85-4,77 (m, 4H), 3,98 (t, J=5,6 Гц, 2H), 3,17-3,10 (m, 4H), 2,60 (t, J=5,6 Гц, 2H), 1,99-1,92 (m, 2H).
[0361] (Пример 127)
3-[2-(3-{[2-(3,3-Дифторазетидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-315)

CDI, 22 мг (0,14 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(3,3-дифторазетидин-1-ил)этил]оксима 28 мг (0,069 ммоль), синтезированного таким же образом, как в ссылочном примере 7-77, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 25 мг (0,14 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Полученный таким образом неочищенный продукт промывали водой и этилацетатом и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 13 мг (0,026 ммоль, выход 38%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 493[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6+D2O) δ: 8,66-8,60 (m, 2H), 7,55-7,48 (m, 1H), 7,45-7,38 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,86-4,78 (m, 4H), 4,07 (t, J=5,3 Гц, 2H), 3,62 (t, J=12,5 Гц, 4H), 2,81 (t, J=5,3 Гц, 2H).
[0362] (Пример 128)
2-Фтор-3-[2-(3-{[2-(3-фторазетидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-314)

CDI, 38 мг (0,23 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(3-фторазетидин-1-ил)этил]оксима, 36 мг (0,092 ммоль), синтезированного таким же образом, как в ссылочном примере 7-78, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 42 мг (0,23 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). Полученный таким образом неочищенный продукт промывали TBME и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 22 мг (0,046 ммоль, выход 50%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 475[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,4 Гц, 2H), 7,55-7,48 (m, 1H), 7,46-7,39 (m, 1H), 7,33-7,26 (m, 1H), 5,25-5,02 (m, 3H), 4,87-4,76 (m, 4H), 4,03 (t, J=5,5 Гц, 2H), 3,67-3,49 (m, 2H), 3,21-3,07 (m, 2H), 2,71 (t, J=5,5 Гц, 2H).
[0363] (Пример 129)
2-Фтор-3-[2-(3-{[2-(3-метоксиазетидин-1-ил)этокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-316)
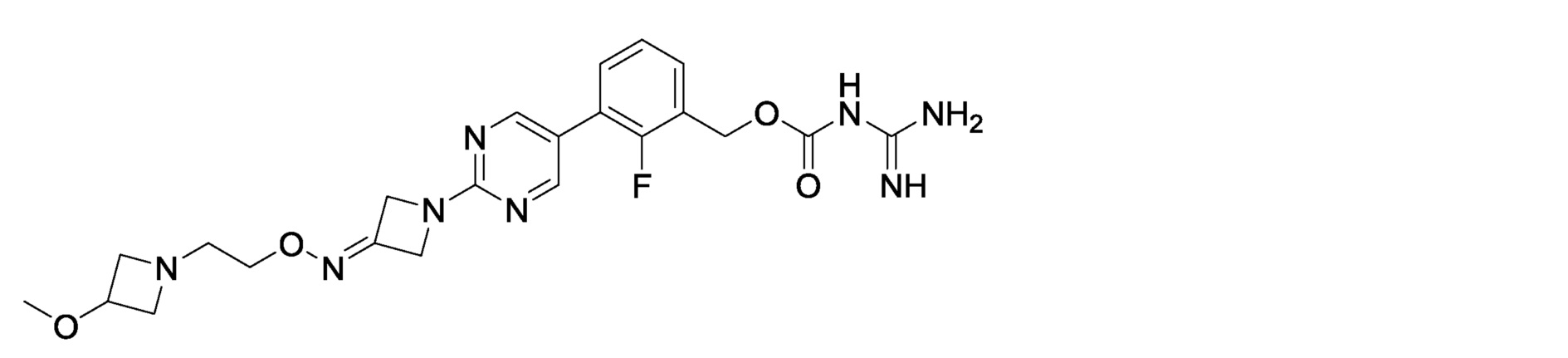
CDI, 40 мг (0,25 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(3-метоксиазетидин-1-ил)этил]оксима, 39 мг (0,097 ммоль), синтезированного таким же образом, как в ссылочном примере 7-79, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 44 мг (0,24 ммоль), и смесь перемешивали при комнатной температуре в течение 18 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Полученный таким образом неочищенный продукт промывали этилацетатом и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 21 мг (0,043 ммоль, выход 44%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 487[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,1 Гц, 2H), 7,55-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,34-7,25 (m, 1H), 5,06 (s, 2H), 4,87-4,76 (m, 4H), 4,05-3,88 (m, 3H), 3,62-3,36 (m, 2H), 3,14 (s, 3H), 2,88-2,79 (m, 2H), 2,71-2,62 (m, 2H).
[0364] (Пример 130)
2-Фтор-3-[2-(3-{[(4-метилморфолин-2-ил)метокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-317)

CDI, 130 мг (0,82 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[(4-метилморфолин-2-ил)метил]оксима 110 мг (0,27 ммоль), синтезированного таким же образом, как в ссылочном примере 7-80, и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли карбонат гуанидина, 100 мг (0,56 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 63 мг (0,13 ммоль, выход 47%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 487[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,55-7,47 (m, 1H), 7,45-7,37 (m, 1H), 7,33-7,25 (m, 1H), 5,06 (s, 2H), 4,87-4,77 (m, 4H), 4,08-3,91 (m, 2H), 3,80-3,74 (m, 1H), 3,73-3,65 (m, 1H), 3,54-3,44 (m, 1H), 2,75-2,68 (m, 1H), 2,60-2,55 (m, 1H), 2,17 (s, 3H), 2,00-1,91 (m, 1H), 1,78-1,69 (m, 1H).
[0365] (Пример 131)
3-[2-(3-{[(4-Ацетилморфолин-2-ил)метокси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-318)

CDI, 100 мг (0,62 ммоль), добавляли к раствору в DMF (3 мл) 1-[2-({[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}метил)морфолино]этанона, 88 мг (0,21 ммоль), синтезированного таким же образом, как в ссылочном примере 7-81, и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли карбонат гуанидина, 74 мг (0,41 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 87 мг (0,17 ммоль, выход 81%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 515[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,55-7,48 (m, 1H), 7,46-7,38 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,87-4,80 (m, 4H), 4,32-3,98 (m, 3H), 3,90-3,82 (m, 1H), 3,79-3,53 (m, 2H), 3,50-3,32 (m, 1H), 3,22-2,95 (m, 1H), 2,73-2,43 (m, 1H), 2,04-1,99 (m, 3H).
[0366] (Пример 132)
2-Фтор-3-[2-(3-{[(5-оксотетрагидрофуран-2-ил)метокси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-319)

CDI, 115 мг (0,709 ммоль), добавляли к раствору в DMF (4 мл) 5-({[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}метил)дигидрофуран-2(3H)-она, 121 мг (0,313 ммоль), синтезированного таким же образом, как ссылочное соединение 7-82, и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 115 мг (0,638 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Полученное твердое вещество очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при комнатной температуре. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 57,3 мг (0,122 ммоль, выход 39%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 472[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,4 Гц, 2H), 7,54-7,48 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,88-4,74 (m, 5H), 4,26-4,14 (m, 2H), 2,60-2,43 (m, 2H), 2,32-2,21 (m, 1H), 2,01-1,90 (m, 1H).
[0367] (Пример 133)
3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]циклобутилацетат (соединение II-339)

CDI, 53 мг (0,33 ммоль), добавляли к раствору в DMF (3 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}циклобутилацетата, 65 мг (0,16 ммоль), синтезированного таким же образом, как в ссылочном примере 7-83, и смесь перемешивали при комнатной температуре в течение 14 часов. Далее добавляли CDI, 26 мг (0,16 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 59 мг (0,33 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при 70°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 70 мг (0,14 ммоль, выход 88%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 486[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,34-7,26 (m, 1H), 5,09-5,01 (m, 3H), 4,87-4,79 (m, 5H), 2,50-2,44 (m, 2H), 2,40-2,32 (m, 2H), 2,01 (s, 3H).
[0368] (Пример 134)
2-Фтор-3-(2-{3-[(3-гидроксициклобутокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-336)

Гидроксид лития, 6,3 мг (0,26 ммоль), добавляли к раствору в THF (1 мл) и воде (1 мл) 3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]циклобутилацетата, 57 мг (0,12 ммоль), синтезированного таким же образом, как в примере 133, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 6,0 мг (0,014 ммоль, выход 12%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 444[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,0 Гц, 2H), 7,55-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,34-7,24 (m, 1H), 5,06 (s, 2H), 4,88-4,78 (m, 4H), 4,78-4,70 (m, 1H), 4,33-4,26 (m, 1H), 2,35-2,27 (m, 2H), 2,16-2,08 (m, 2H).
[0369] (Пример 135)
3-(2-{3-[(Бензилокси)имино]азетидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-334)

CDI, 58 мг (0,36 ммоль), добавляли к раствору в DMF (4 мл) 1-(5-(2-фтор-3-(гидроксиметил)фенил)пиримидин-2-ил)азетидин-3-она O-бензилоксима, 68 мг (0,18 ммоль), синтезированного таким же образом, как в ссылочном примере 7-84, и смесь перемешивали при комнатной температуре в течение 5 часов. Затем добавляли карбонат гуанидина, 65 мг (0,36 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов и оставляли стоять при комнатной температуре в течение 4 дней. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 66 мг (0,14 ммоль, выход 78%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 464[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,54-7,48 (m, 1H), 7,45-7,25 (m, 7H), 5,09 (s, 2H), 5,06 (s, 2H), 4,83 (s, 4H).
[0370] (Пример 136)
2-Фтор-3-[2-(3-{[(4-метоксибензил)окси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-335)

CDI, 110 мг (0,678 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(4-метоксибензил)оксима, 126 мг (0,309 ммоль), синтезированного таким же образом, как ссылочное соединение 7-85, и смесь перемешивали при комнатной температуре в течение 3 часов. Далее добавляли CDI, 40 мг (0,25 ммоль), и смесь перемешивали при комнатной температуре в течение 17 часов. Затем добавляли карбонат гуанидина, 110 мг (0,678 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Полученное твердое вещество очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при комнатной температуре. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 66,6 мг (0,135 ммоль, выход 44%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 494[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,62 (d, J=1,4 Гц, 2H), 7,54-7,47 (m, 1H), 7,45-7,39 (m, 1H), 7,36-7,26 (m, 3H), 6,96-6,90 (m, 2H), 5,06 (s, 2H), 5,01 (s, 2H), 4,85-4,77 (m, 4H), 3,76 (s, 3H).
[0371] (Пример 137)
2-Фтор-3-[2-(3-{[(1-метилазетидин-3-ил)окси]имино}азетидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-342)

CDI, 55 мг (0,34 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(1-метилазетидин-3-ил)оксима, 40 мг (0,11 ммоль), синтезированного таким же образом, как в ссылочном примере 7-86, и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 46 мг (0,26 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при 70°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 19 мг (0,043 ммоль, выход 39%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 443[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=0,6 Гц, 2H), 7,55-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 4,88-4,79 (m, 4H), 4,75-4,66 (m, 1H), 3,54-3,48 (m, 2H), 3,03-2,97 (m, 2H), 2,25 (s, 3H).
[0372] (Пример 138)
3-[2-(3-{[(1-Ацетилазетидин-3-ил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-350)

CDI, 89 мг (0,55 ммоль), добавляли к раствору в DMF (3 мл) 1-(3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}азетидин-1-ил)этанона, 70 мг (0,18 ммоль), синтезированного таким же образом, как в ссылочном примере 7-87, и смесь перемешивали при комнатной температуре в течение 5 часов. Затем добавляли карбонат гуанидина, 66 мг (0,37 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при 70°C в течение 1 часа. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 18 мг (0,038 ммоль, выход 21%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 487[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,46-7,38 (m, 1H), 7,34-7,26 (m, 1H), 5,06 (s, 2H), 5,01-4,91 (m, 1H), 4,90-4,83 (m, 4H), 4,41-4,34 (m, 1H), 4,15-4,06 (m, 2H), 3,83-3,77 (m, 1H), 1,78 (s, 3H).
[0373] (Пример 139)
3-[2-(3-{[(1-Бензилазетидин-3-ил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-344)

CDI, 21 мг (0,13 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(1-бензилазетидин-3-ил)оксима 28 мг (0,065 ммоль), синтезированного таким же образом, как в ссылочном примере 7-88, и смесь перемешивали при комнатной температуре в течение 3 часов. Далее добавляли CDI, 11 мг (0,068 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. Далее добавляли CDI, 11 мг (0,068 ммоль), и смесь перемешивали при комнатной температуре в течение 30 минут. Затем добавляли карбонат гуанидина, 23 мг (0,13 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 26 мг (0,050 ммоль, выход 77%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 519[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (br d, J=1,0 Гц, 2H), 7,55-7,46 (m, 1H), 7,45-7,36 (m, 1H), 7,34-7,21 (m, 6H), 5,06 (s, 2H), 4,87-4,75 (m, 5H), 3,60 (s, 2H), 3,55-3,39 (m, 2H), 3,13-3,02 (m, 2H).
[0374] (Пример 140)
2-Фтор-3-{2-[3-({[1-(2,2,2-трифторэтил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-346)

CDI, 19 мг (0,12 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[1-(2,2,2-трифторэтил)азетидин-3-ил]оксима, 25 мг (0,059 ммоль), синтезированного таким же образом, как в ссылочном примере 7-89, и смесь перемешивали при комнатной температуре в течение 2 часов. Далее добавляли CDI, 10 мг (0,062 ммоль), и смесь перемешивали при комнатной температуре в течение 30 минут. Затем добавляли карбонат гуанидина, 21 мг (0,12 ммоль), и смесь перемешивали при комнатной температуре в течение 40 минут. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 25 мг (0,049 ммоль, выход 83%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 511[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,46-7,38 (m, 1H), 7,34-7,25 (m, 1H), 5,06 (s, 2H), 4,87-4,79 (m, 5H), 3,74-3,63 (m, 2H), 3,37-3,30 (m, 2H), 3,25 (q, J=10,1 Гц, 2H).
[0375] (Пример 141)
2-Фтор-3-{2-[3-({[1-(метилсульфонил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-352)
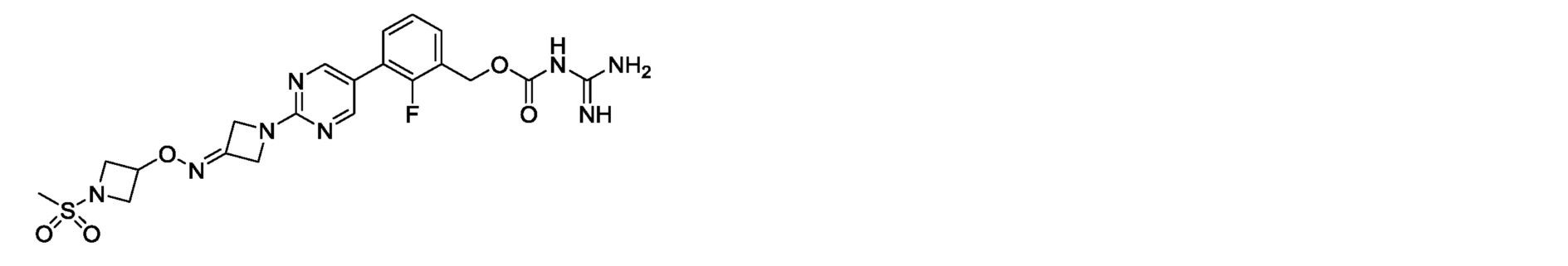
CDI, 31 мг (0,19 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[1-(метилсульфонил)азетидин-3-ил]оксима, 27 мг (0,064 ммоль), синтезированного таким же образом, как в ссылочном примере 7-90, и смесь перемешивали при комнатной температуре в течение 3 часов. Далее добавляли CDI, 11 мг (0,068 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 24 мг (0,13 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 14 мг (0,028 ммоль, выход 44%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 507[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,3 Гц, 2H), 7,56-7,47 (m, 1H), 7,46-7,38 (m, 1H), 7,35-7,24 (m, 1H), 5,06 (s, 2H), 5,01-4,93 (m, 1H), 4,90-4,84 (m, 4H), 4,18-4,11 (m, 2H), 3,95-3,89 (m, 2H), 3,04 (s, 3H).
[0376] (Пример 142)
3-[2-(3-{[(1-Этилазетидин-3-ил)окси]имино}азетидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-343)

CDI, 42 мг (0,26 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(1-этилазетидин-3-ил)оксима 30 мг (0,081 ммоль), синтезированного таким же образом, как в ссылочном примере 7-91, и смесь перемешивали при комнатной температуре в течение 4 часов. Далее добавляли CDI, 60 мг (0,37 ммоль), и смесь перемешивали при комнатной температуре в течение 17 часов. Затем добавляли карбонат гуанидина, 29 мг (0,16 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 28 мг (0,061 ммоль, выход 75%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 457[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,54-7,48 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,06 (s, 2H), 4,87-4,80 (m, 4H), 4,77-4,70 (m, 1H), 3,51-3,45 (m, 2H), 3,02-2,89 (m, 2H), 2,42 (q, J=7,2 Гц, 2H), 0,87 (t, J=7,2 Гц, 3H).
[0377] (Пример 143)
Метил-3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-карбоксилат (соединение II-351)

CDI, 90 мг (0,56 ммоль), добавляли к раствору в DMF (3 мл) метил-3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}азетидин-1-карбоксилата, 56 мг (0,14 ммоль), синтезированного таким же образом, как в ссылочном примере 7-92, и смесь перемешивали при комнатной температуре в течение 2,5 часа. Затем добавляли карбонат гуанидина, 50 мг (0,28 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 49 мг (0,10 ммоль, выход 71%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 487[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (d, J=1,0 Гц, 2H), 7,56-7,47 (m, 1H), 7,46-7,38 (m, 1H), 7,33-7,26 (m, 1H), 5,06 (s, 2H), 5,01-4,93 (m, 1H), 4,91-4,81 (m, 4H), 4,30-4,08 (m, 2H), 3,98-3,84 (m, 2H), 3,57 (s, 3H).
[0378] (Пример 144)
2-Фтор-3-(2-{3-[(оксетан-3-илокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-356)

CDI, 50 мг (0,31 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-оксетан-3-илоксима 50 мг (0,15 ммоль), синтезированного таким же образом, как в ссылочном примере 7-93, и смесь перемешивали при комнатной температуре в течение 5 часов. Затем добавляли карбонат гуанидина, 60 мг (0,33 ммоль), и смесь перемешивали при комнатной температуре в течение 15 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 30 мг (0,070 ммоль, выход 47%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 430[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,1 Гц, 2H), 7,56-7,48 (m, 1H), 7,46-7,40 (m, 1H), 7,34-7,28 (m, 1H), 5,25-5,18 (m, 1H), 5,07 (s, 2H), 4,91-4,83 (m, 4H), 4,81-4,74 (m, 2H), 4,60-4,54 (m, 2H).
[0379] (Пример 145)
2-{3-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-ил}этилацетат (соединение II-349)
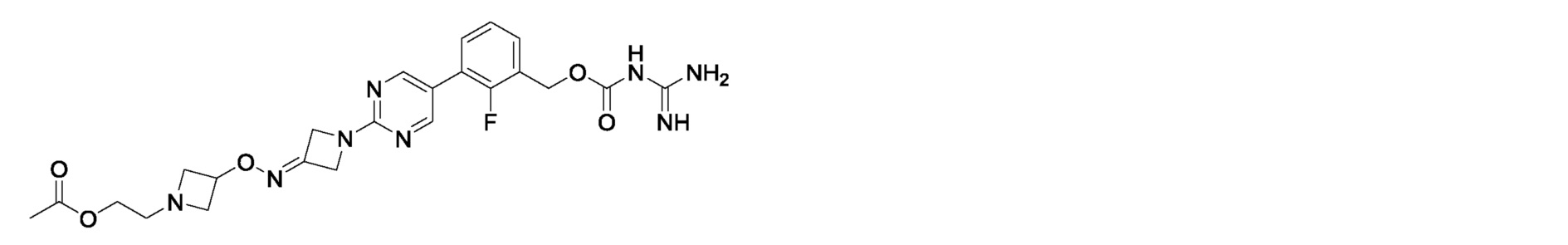
CDI, 68 мг (0,42 ммоль), добавляли к раствору в DMF (3 мл) 2-(3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}азетидин-1-ил)этилацетата, 43 мг (0,10 ммоль), синтезированного таким же образом, как в ссылочном примере 7-94, и смесь перемешивали при комнатной температуре в течение 3 часов. Далее добавляли CDI, 45 мг (0,28 ммоль), и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли карбонат гуанидина, 36 мг (0,20 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 42 мг (0,082 ммоль, выход 82%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 515[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (d, J=1,3 Гц, 2H), 7,55-7,46 (m, 1H), 7,45-7,37 (m, 1H), 7,33-7,25 (m, 1H), 5,06 (s, 2H), 4,88-4,80 (m, 4H), 4,80-4,72 (m, 1H), 3,96 (t, J=5,5 Гц, 2H), 3,59-3,52 (m, 2H), 3,10-3,04 (m, 2H), 2,65 (t, J=5,5 Гц, 2H), 2,00 (s, 3H).
[0380] (Пример 146)
2-Фтор-3-{2-[3-({[1-(2-гидроксиэтил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-347)
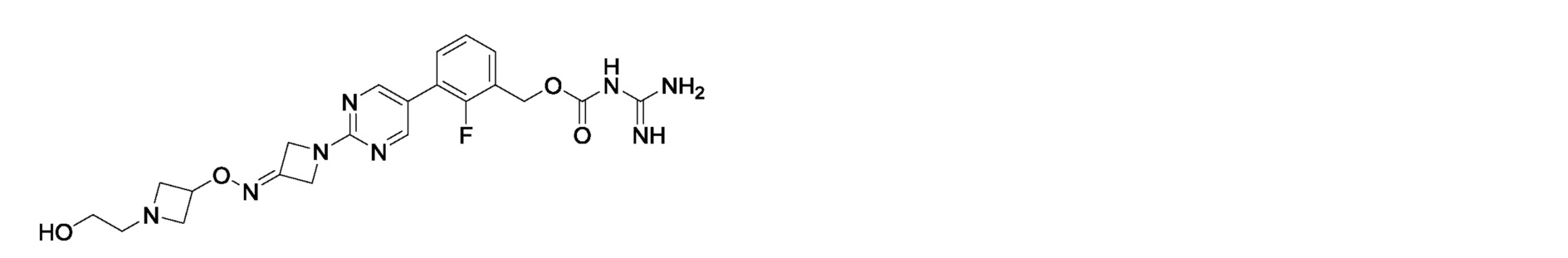
Гидроксид лития, 4,0 мг (0,167 ммоль), добавляли к раствору в THF (1 мл) и воде (1 мл) 2-{3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-ил}этилацетата, 35 мг (0,068 ммоль), синтезированного таким же образом, как в примере 145, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 4,8 мг (0,010 ммоль, выход 15%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 473[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=0,8 Гц, 2H), 7,55-7,47 (m, 1H), 7,46-7,38 (m, 1H), 7,34-7,26 (m, 1H), 5,06 (s, 2H), 4,90-4,68 (m, 5H), 3,58-3,46 (m, 2H), 3,35 (t, J=6,0 Гц, 2H), 3,12-2,97 (m, 2H), 2,59-2,45 (m, 2H).
[0381] (Пример 147)
2-Фтор-3-{2-[3-({[1-(2-метоксиэтил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-348)

CDI, 76 мг (0,47 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[1-(2-метоксиэтил)азетидин-3-ил]оксима, 47 мг (0,12 ммоль), синтезированного таким же образом, как в ссылочном примере 7-95, и смесь перемешивали при комнатной температуре в течение 14 часов. Далее добавляли CDI, 38 мг (0,23 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 42 мг (0,23 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 45 мг (0,093 ммоль, выход 78%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 487[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (d, J=1,4 Гц, 2H), 7,54-7,47 (m, 1H), 7,45-7,38 (m, 1H), 7,33-7,25 (m, 1H), 5,06 (s, 2H), 4,88-4,79 (m, 4H), 4,76-4,70 (m, 1H), 3,56-3,48 (m, 2H), 3,29 (t, J=5,8 Гц, 2H), 3,21 (s, 3H), 3,07-3,01 (m, 2H), 2,57 (t, J=5,8 Гц, 2H).
[0382] (Пример 148)
2-Фтор-3-{2-[3-({[1-(2-фторэтил)азетидин-3-ил]окси}имино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-345)
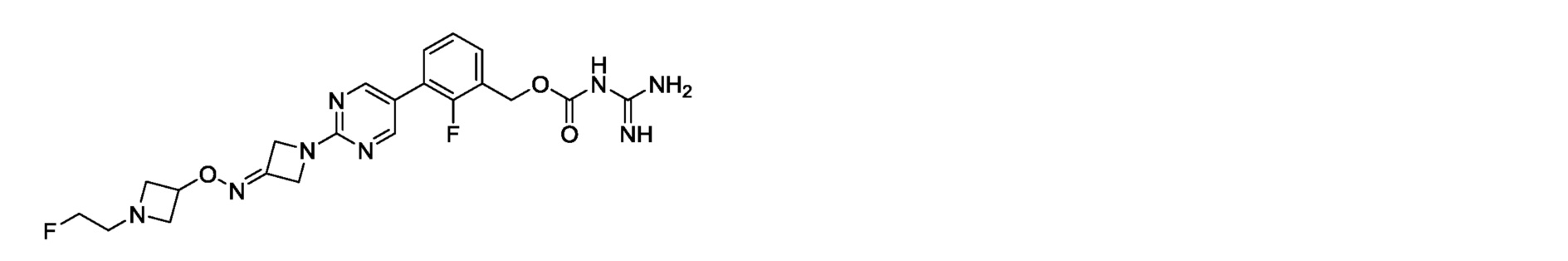
CDI, 81 мг (0,50 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[1-(2-фторэтил)азетидин-3-ил]оксима, 39 мг (0,10 ммоль), синтезированного таким же образом, как в ссылочном примере 7-96, и смесь перемешивали при комнатной температуре в течение 16 часов. Затем добавляли карбонат гуанидина, 36 мг (0,20 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду и насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 38 мг (0,080 ммоль, выход 80%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 475[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (br s, 2H), 7,54-7,47 (m, 1H), 7,45-7,37 (m, 1H), 7,34-7,25 (m, 1H), 5,06 (s, 2H), 4,88-4,74 (m, 5H), 4,50-4,28 (m, 2H), 3,62-3,52 (m, 2H), 3,16-3,06 (m, 2H), 2,85-2,61 (m, 2H).
[0383] (Пример 149)
Этил-3-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]пропанoат (соединение II-507)

CDI, 27 мг (0,17 ммоль), добавляли к раствору в DMF (2 мл) этил-3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}пропанoата, 34 мг (0,082 ммоль), синтезированного таким же образом, как в ссылочном примере 7-97, и смесь перемешивали при комнатной температуре в течение 16 часов. Затем добавляли карбонат гуанидина, 30 мг (0,17 ммоль), и смесь перемешивали при комнатной температуре в течение 6 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 20 мг (0,040 ммоль, выход 49%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 502[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,54-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,31-7,25 (m, 1H), 5,06 (s, 2H), 4,20 (t, J=6,1 Гц, 2H), 4,08 (q, J=7,1 Гц, 2H), 3,95-3,87 (m, 4H), 2,66-2,60 (m, 2H), 2,57-2,52 (m, 2H), 2,43-2,33 (m, 2H), 1,18 (t, J=7,1 Гц, 3H).
[0384] (Пример 150)
3-(2-{4-[(3-Амино-3-оксопропокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-511)
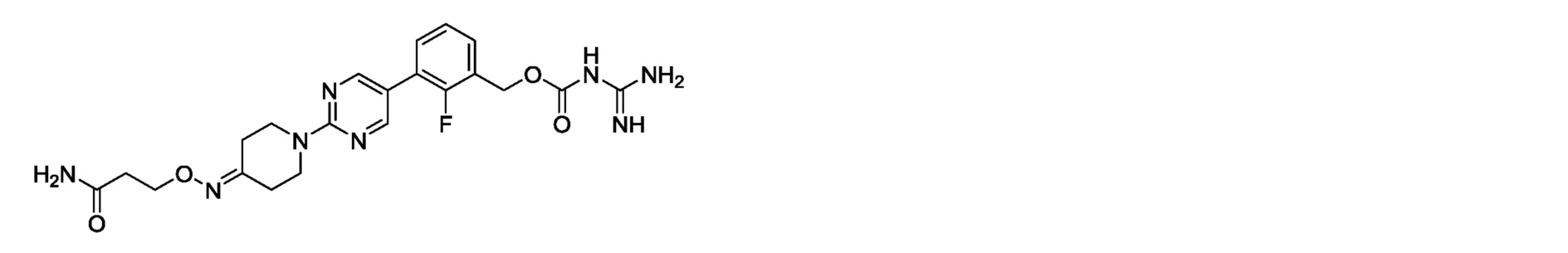
CDI, 59 мг (0,37 ммоль), добавляли к раствору в DMF (4 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}пропанамида, 65 мг (0,17 ммоль), синтезированного таким же образом, как в ссылочном примере 7-98, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 61 мг (0,34 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при 70°C в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 15 мг (0,031 ммоль, выход 18%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 473[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,54-7,46 (m, 1H), 7,42-7,32 (m, 2H), 7,30-7,24 (m, 1H), 6,83 (br s, 1H), 5,06 (s, 2H), 4,16 (t, J=6,6 Гц, 2H), 3,96-3,88 (m, 4H), 2,58-2,53 (m, 2H), 2,42-2,32 (m, 4H).
[0385] (Пример 151)
2-Фтор-3-[2-(4-{[3-(метиламино)-3-оксопропокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-512)
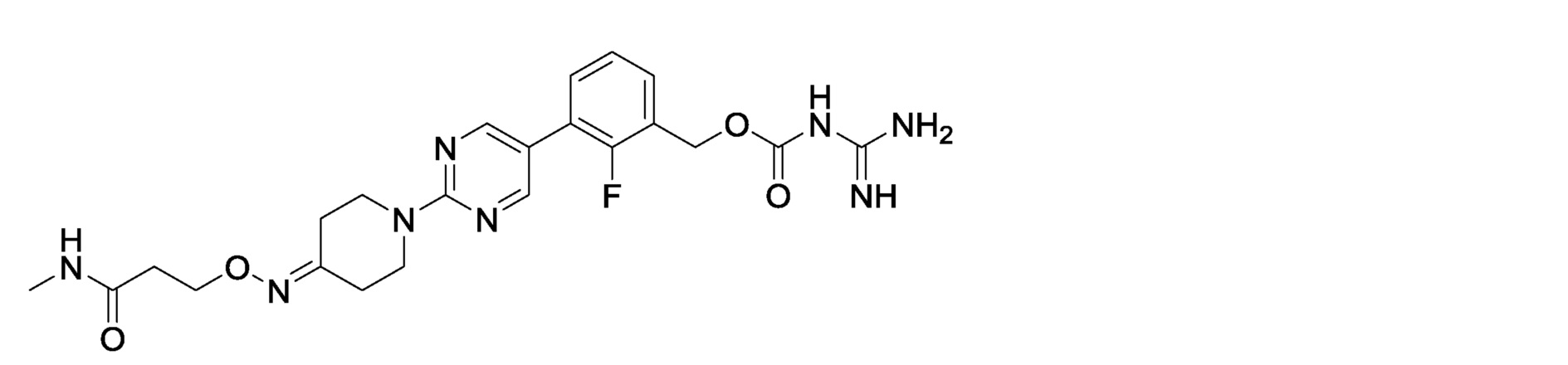
CDI, 65 мг (0,40 ммоль), добавляли к раствору в DMF (4 мл) неочищенного продукта, 80 мг, синтезированного таким же образом, как в ссылочном примере 7-99, который включал в себя 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}-N-метилпропанамид, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 72 мг (0,40 ммоль), и смесь перемешивали при комнатной температуре в течение 17 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол) с получением указанного в заголовке соединения в количестве 32 мг (0,066 ммоль) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 487[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (s, 2H), 7,53-7,47 (m, 1H), 7,42-7,36 (m, 1H), 7,31-7,25 (m, 1H), 5,06 (s, 2H), 4,16 (t, J=6,5 Гц, 2H), 3,96-3,87 (m, 4H), 2,60-2,53 (m, 5H), 2,44-2,34 (m, 4H).
[0386] (Пример 152)
Этил-4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]бутаноат (соединение II-508)

CDI, 85 мг (0,52 ммоль), добавляли к раствору в DMF (4 мл) этил-4-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}бутаноата, 0,11 г (0,26 ммоль), синтезированного таким же образом, как в ссылочном примере 7-100, и смесь перемешивали при комнатной температуре в течение 7 часов. Затем добавляли карбонат гуанидина, 95 мг (0,53 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 98 мг (0,19 ммоль, выход 73%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 516[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,55-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,32-7,23 (m, 1H), 5,06 (s, 2H), 4,05 (q, J=7,2 Гц, 2H), 3,98 (t, J=6,4 Гц, 2H), 3,95-3,89 (m, 4H), 2,61-2,54 (m, 2H), 2,44-2,32 (m, 4H), 1,90-1,81 (m, 2H), 1,18 (t, J=7,2 Гц, 3H).
[0387] (Пример 153)
4-[({1-[5-(3-{[(Карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]бутановая кислота (соединение II-505)

Гидроксид лития, 11 мг (0,46 ммоль), добавляли к суспензии в THF (6 мл) и воде (2 мл) этил-4-[({1-[5-(3-{[(карбамимидоилкарбамоил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]бутаноата, 85 мг (0,17 ммоль), синтезированного таким же образом, как в примере 152, и смесь перемешивали при 50°C в течение 6 часов. После окончания реакции к реакционной смеси добавляли уксусную кислоту 0,1 мл (1,7 ммоль) и воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Полученное твердое вещество сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 65 мг (0,13 ммоль, выход 77%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 488[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,54-7,47 (m, 1H), 7,43-7,37 (m, 1H), 7,32-7,26 (m, 1H), 5,06 (s, 2H), 3,98 (t, J=6,4 Гц, 2H),3,95-3,88 (m, 4H), 2,61-2,55 (m, 2H), 2,43-2,33 (m, 2H), 2,28 (t, J=7,3 Гц, 2H), 1,88-1,77 (m, 2H).
[0388] (Пример 154)
3-[2-(4-{[3-(Диметиламино)-3-оксопропокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-513)
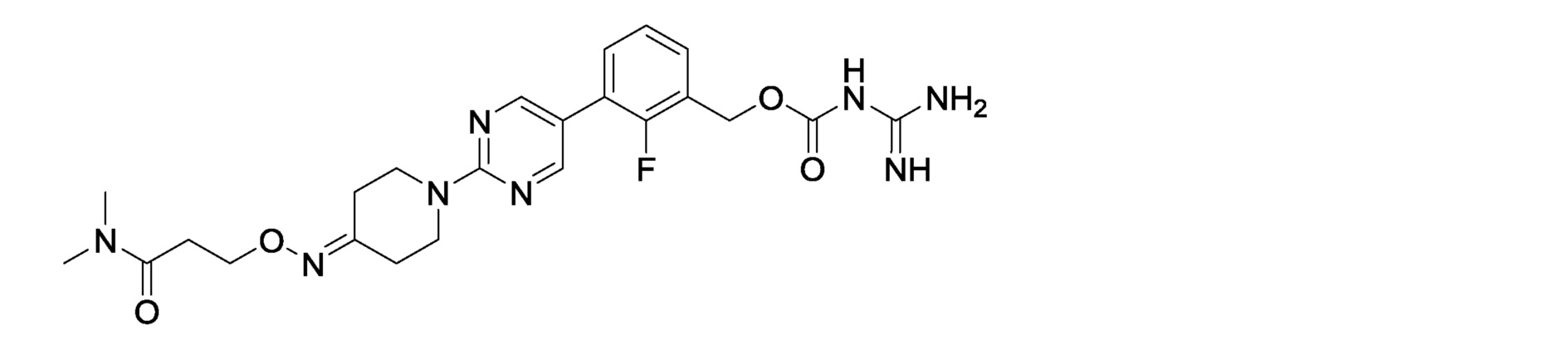
CDI, 117 мг (0,722 ммоль), добавляли к раствору в DMF (6 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}-N,N-диметилпропанамида, 150 мг (0,361 ммоль), синтезированного таким же образом, как в ссылочном примере 7-101, и смесь перемешивали при комнатной температуре в течение 7 часов. Затем добавляли карбонат гуанидина, 130 мг (0,722 ммоль), и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 123 мг (0,246 ммоль, выход 68%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 501[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,54-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,19 (t, J=6,7 Гц, 2H), 3,97-3,87 (m, 4H), 2,96 (s, 3H), 2,81 (s, 3H), 2,65 (t, J=6,7 Гц, 2H), 2,58-2,53 (m, 2H), 2,42-2,36 (m, 2H).
[0389] (Пример 155)
3-(2-{4-[(2-Ацетамидоэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-519)

CDI, 30 мг (0,19 ммоль), добавляли к раствору в DMF (4 мл) N-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)ацетамида, 37 мг (0,092 ммоль), синтезированного таким же образом, как в ссылочном примере 7-102, и смесь перемешивали при комнатной температуре в течение 7 часов. Затем добавляли карбонат гуанидина, 34 мг (0,19 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 37 мг (0,076 ммоль, выход 83%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 487[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,4 Гц, 2H), 7,56-7,47 (m, 1H), 7,44-7,37 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,01-3,89 (m, 6H), 3,33-3,26 (m, 2H), 2,64-2,56 (m, 3H), 2,43-2,36 (m, 2H), 1,82 (s, 3H).
[0390] (Пример 156)
2-Фтор-3-[2-(4-{[2-(N-метилацетамидо)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-520)
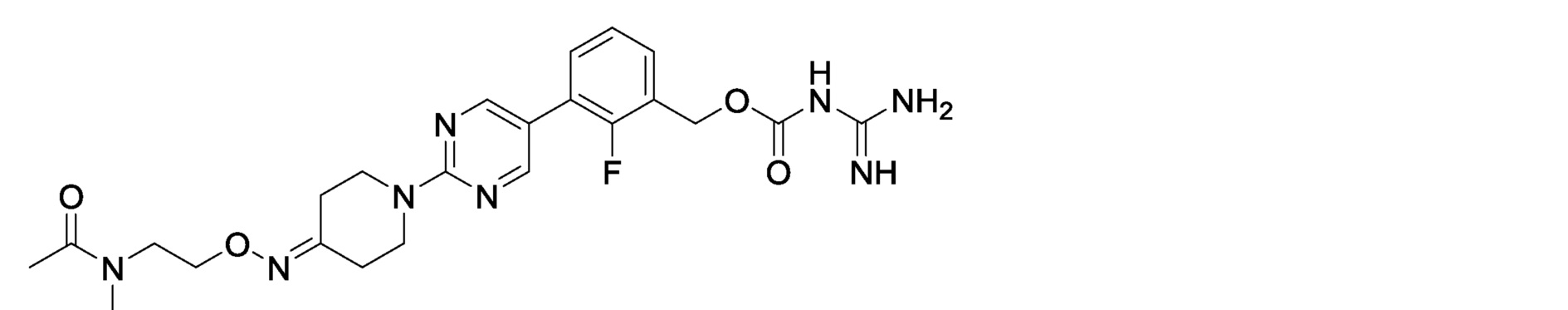
CDI, 75 мг (0,46 ммоль), добавляли к раствору в DMF (4 мл) N-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)-N-метилацетамида, 95 мг (0,23 ммоль), синтезированного таким же образом, как в ссылочном примере 7-103, и смесь перемешивали при комнатной температуре в течение 7 часов. Затем добавляли карбонат гуанидина, 83 мг (0,46 ммоль), и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 73 мг (0,15 ммоль, выход 65%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 501[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,4 Гц, 2H), 7,54-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,17-4,02 (m, 2H), 3,97-3,88 (m, 4H), 3,59-3,47 (m, 2H), 3,02-2,77 (m, 3H), 2,62-2,54 (m, 2H), 2,42-2,35 (m, 2H), 2,00-1,96 (m, 3H).
[0391] (Пример 157)
2-Фтор-3-[2-(4-{[2-(N-метилметилсульфонамидо)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамата гидрохлорид (соединения II-522 гидрохлорид)
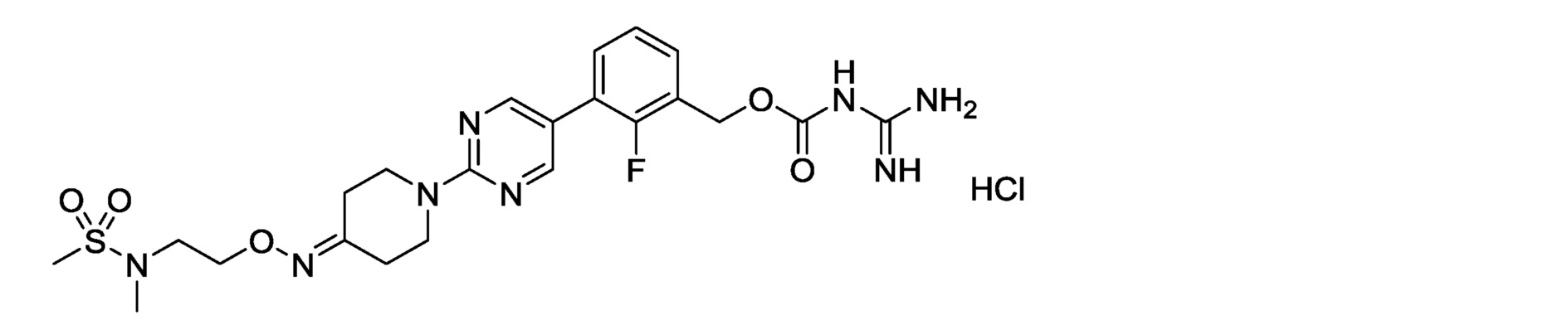
CDI, 59 мг (0,36 ммоль), добавляли к раствору в DMF (2,5 мл) N-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)-N-метилметансульфонамида, 55 мг (0,12 ммоль), синтезированного таким же образом, как в ссылочном примере 7-104, и смесь перемешивали при комнатной температуре в течение 17 часов. Затем добавляли карбонат гуанидина, 66 мг (0,37 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и промывали TBME. Полученный таким образом неочищенный продукт очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). Полученный неочищенный продукт растворяли в 2 н HCl в этаноле, и раствор концентрировали при пониженном давлении. Полученный таким образом неочищенный продукт промывали этилацетатом и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 51 мг (0,089 ммоль, выход 74%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 537[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6+D2O) δ: 8,61 (d, J=1,3 Гц, 2H), 7,67-7,59 (m, 1H), 7,55-7,49 (m, 1H), 7,39-7,32 (m, 1H), 5,36 (s, 2H), 4,16-4,08 (m, 2H), 3,98-3,89 (m, 4H), 3,38-3,30 (m, 2H), 2,88 (s, 3H), 2,81 (s, 3H), 2,63-2,56 (m, 2H), 2,44-2,38 (m, 2H).
[0392] (Пример 158)
3-{2-[4-({2-[N-(трет-бутоксикарбонил)метилсульфонамидо]этокси}имино)пиперидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат (соединение II-570)

CDI, 78 мг (0,48 ммоль), добавляли к раствору в DMF (3 мл) трет-бутил-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)(метилсульфонил)карбамата, 86 мг (0,16 ммоль), синтезированного таким же образом, как в ссылочном примере 7-105, и смесь перемешивали при комнатной температуре в течение 16 часов. Затем добавляли карбонат гуанидина, 86 мг (0,48 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 62 мг (0,10 ммоль, выход 63%) в виде бесцветного масла.
Масс-спектр (ESI, m/z): 623[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,33-7,23 (m, 1H), 5,06 (s, 2H), 4,14-4,08 (m, 2H), 3,97-3,82 (m, 6H), 3,34 (s, 3H), 2,62-2,46 (m, 2H), 2,43-2,35 (m, 2H), 1,47 (s, 9H).
[0393] (Пример 159)
2-Фтор-3-[2-(4-{[2-(метилсульфонамидо)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-521)

Раствор 2 М хлорида водорода в этаноле, (2 мл), добавляли к 3-{2-[4-({2-[N-(трет-бутоксикарбонил)метилсульфонамидо]этокси}имино)пиперидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамату, 62 мг (0,10 ммоль), синтезированному таким же образом, как в примере 158, и смесь перемешивали при комнатной температуре в течение 22 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток промывали TBME и фильтровали. Полученный таким образом неочищенный продукт растворяли в этаноле и нейтрализовывали триэтиламином. Полученный раствор очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 23 мг (0,044 ммоль, выход 44%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 523[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6+D2O) δ: 8,63-8,57 (m, 2H), 7,55-7,47 (m, 1H), 7,44-7,36 (m, 1H), 7,33-7,25 (m, 1H), 5,06 (s, 2H), 4,03 (t, J=5,7 Гц, 2H), 3,97-3,89 (m, 4H), 3,21 (t, J=5,7 Гц, 2H), 2,91 (s, 3H), 2,65-2,58 (m, 2H), 2,44-2,36 (m, 2H).
[0394] (Пример 160)
3-[2-(4-{[2-(Диметиламино)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-517)
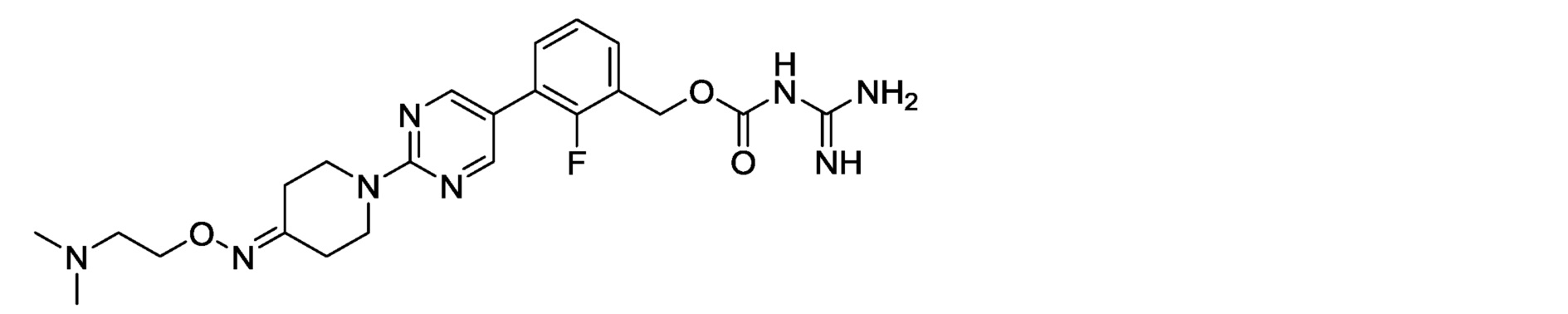
CDI, 28 мг (0,17 ммоль), добавляли к раствору в DMF (1,5 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[2-(диметиламино)этил]оксима, 14 мг (0,036 ммоль), синтезированного таким же образом, как в ссылочном примере 7-106, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 31 мг (0,17 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Полученный таким образом неочищенный продукт промывали TBME и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 14 мг (0,030 ммоль, выход 83%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 473[М+1]+.
1H-ЯМР(400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,55-7,46 (m, 1H), 7,43-7,37 (m, 1H), 7,33-7,24 (m, 1H), 5,06 (s, 2H), 4,06 (t, J=6,0 Гц, 2H), 3,96-3,88 (m, 4H), 2,63-2,45 (m, 4H), 2,42-2,36 (m, 2H), 2,17 (s, 6H).
[0395] (Пример 161)
3-{2-[4-({2-[(трет-Бутоксикарбонил)(метил)амино]этокси}имино)пиперидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат (соединение II-571)

CDI, 71,0 мг (0,438 ммоль), добавляли к раствору в DMF (2 мл) трет-бутил-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)(метил)карбамата, 103 мг (0,218 ммоль), синтезированного таким же образом, как в ссылочном примере 7-107, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 78,0 мг (0,433 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 87,0 мг (0,156 ммоль, выход 72%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 559[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6) δ: 8,60 (d, J=1,4 Гц, 2H), 7,54-7,47 (m, 1H), 7,43-7,35 (m, 1H), 7,32-7,24 (m, 1H), 5,06 (s, 2H), 4,10-4,01 (m, 2H), 3,98-3,87 (m, 4H), 3,45-3,37 (m, 2H), 2,86-2,75 (m, 2H), 2,63-2,45 (m, 2H), 2,43-2,36 (m, 2H), 1,38 (s, 9H).
[0396] (Пример 162)
2-Фтор-3-[2-(4-{[2-(метиламино)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамата дигидрохлорид (соединения II-516 дигидрохлорид)

Раствор 2 М хлорида водорода в этаноле, (3 мл), добавляли к 3-{2-[4-({2-[(трет-бутоксикарбонил)(метил)амино]этокси}имино)пиперидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамату, 87 мг (0,16 ммоль), синтезированному таким же образом, как в примере 161, и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток промывали TBME с получением указанного в заголовке соединения в количестве 66 мг (0,12 ммоль, выход 75%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 459[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6+D2O) δ: 8,61 (d, J=1,3 Гц, 2H), 7,66-7,58 (m, 1H), 7,56-7,48 (m, 1H), 7,39-7,30 (m, 1H), 5,36 (s, 2H), 4,26-4,18 (m, 2H), 4,00-3,90 (m, 4H), 3,24-3,16 (m, 2H), 2,69-2,62 (m, 2H), 2,60 (s, 3H), 2,46-2,38 (m, 2H).
[0397] (Пример 163)
3-{2-[4-({2-[(Ди-трет-бутоксикарбонил)амино]этокси}имино)пиперидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамат (соединение II-572)

CDI, 61,0 мг (0,376 ммоль), добавляли к раствору в DMF (2 мл) ди-трет-бутил-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)карбамата, 105 мг (0,188 ммоль), синтезированного таким же образом, как в ссылочном примере 7-108, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 68 мг (0,377 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 99,0 мг (0,154 ммоль, выход 82%) в виде бесцветного масла.
Масс-спектр (ESI, m/z): 645[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,53-7,46 (m, 1H), 7,42-7,36 (m, 1H), 7,31-7,24 (m, 1H), 5,06 (s, 2H), 4,11-4,05 (m, 2H), 3,95-3,87 (m, 4H), 3,79-3,73 (m, 2H), 2,58-2,47 (m, 2H), 2,42-2,35 (m, 2H), 1,43 (s, 18H).
[0398] (Пример 164)
3-(2-{4-[(2-Аминоэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-515)

Раствор 2 М хлорида водорода в этаноле, (3 мл), добавляли к 3-{2-[4-({2-[(ди-трет-бутоксикарбонил)амино]этокси}имино)пиперидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамату, 99 мг (0,15 ммоль), синтезированному таким же образом, как в примере 163, и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток промывали TBME и фильтровали. Полученный остаток растворяли в этаноле и нейтрализовывали триэтиламином. Полученный таким образом раствор очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: этилацетат:метанол). Полученный таким образом неочищенный продукт промывали TBME и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 43 мг (0,097 ммоль, выход 65%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 445[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,54-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 3,98-3,89 (m, 6H), 2,76-2,70 (m, 2H), 2,63-2,57 (m, 2H), 2,42-2,35 (m, 2H).
[0399] (Пример 165)
3-(2-{4-[(2-Цианоэтокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-526)

CDI, 53 мг (0,33 ммоль), добавляли к раствору в DMF (4 мл) 3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}пропаннитрила, 60 мг (0,16 ммоль), синтезированного таким же образом, как в ссылочном примере 7-109, и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли карбонат гуанидина, 59 мг (0,33 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 67 мг (0,15 ммоль, выход 91%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 455[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,4 Гц, 2H), 7,54-7,47 (m, 1H), 7,43-7,37 (m, 1H), 7,31-7,26 (m, 1H), 5,06 (s, 2H), 4,17 (t, J=6,0 Гц, 2H), 3,99-3,91 (m, 4H), 2,85 (t, J=6,0 Гц, 2H), 2,65-2,55 (m, 2H), 2,48-2,39 (m, 2H).
[0400] (Пример 166)
3-(2-{4-[(3-Цианопропокси)имино]пиперидин-1-ил}пиримидин-5-ил)-2-фторбензилкарбамимидоилкарбамат (соединение II-527)

CDI, 60 мг (0,37 ммоль), добавляли к раствору в DMF (4 мл) 4-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}бутаннитрила, 69 мг (0,18 ммоль), синтезированного таким же образом, как в ссылочном примере 7-110, и смесь перемешивали при комнатной температуре в течение 7 часов. Затем добавляли карбонат гуанидина, 65 мг (0,36 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 69 мг (0,15 ммоль, выход 83%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 469[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,55-7,47 (m, 1H), 7,44-7,36 (m, 1H), 7,33-7,25 (m, 1H), 5,06 (s, 2H), 4,05 (t, J=6,0 Гц, 2H), 3,97-3,89 (m, 4H), 2,64-2,49 (m, 4H), 2,44-2,37 (m, 2H), 1,96-1,85 (m, 2H).
[0401] (Пример 167)
2-Фтор-3-[2-(4-{[2-(метилсульфонил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-528)

CDI, 52 мг (0,29 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[2-(метилсульфонил)этил]оксима, 61 мг (0,14 ммоль), синтезированного таким же образом, как в ссылочном примере 7-111, и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли карбонат гуанидина, 47 мг (0,29 ммоль), и смесь перемешивали при комнатной температуре в течение 7 часов. После окончания реакции к реакционной смеси добавляли воду и метиленхлорид, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 19 мг (0,037 ммоль, выход 26%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 508[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,33-7,24 (m, 1H), 5,06 (s, 2H), 4,35 (t, J=5,8 Гц, 2H),3,96-3,87 (m, 4H), 3,52-3,43 (m, 2H), 2,99 (s, 3H), 2,63-2,56 (m, 2H), 2,46-2,38 (m, 2H).
[0402] (Пример 168)
2-Фтор-3-[2-(4-{[3-(метилсульфонил)пропокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-529)

CDI, 6,0 мг (0,037 ммоль), добавляли к раствору в DMF (1 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[3-(метилсульфонил)пропил]оксима, 8,0 мг (0,018 ммоль), синтезированного таким же образом, как в ссылочном примере 7-112, и смесь перемешивали при комнатной температуре в течение 14 часов. Далее добавляли CDI, 12 мг (0,074 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. Далее добавляли CDI, 12 мг (0,074 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 6,0 мг (0,033 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при 70°C в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 5,6 мг (0,011 ммоль, выход 61%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 522[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,1 Гц, 2H), 7,55-7,46 (m, 1H), 7,44-7,35 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,08 (t, J=6,3 Гц, 2H), 3,98-3,88 (m, 4H), 3,23-3,11 (m, 2H), 2,98 (s, 3H), 2,64-2,57 (m, 2H), 2,44-2,36 (m, 2H), 2,08-1,98 (m, 2H).
[0403] (Пример 169)
2-Фтор-3-[2-(4-{[(1-метил-1H-пиразол-3-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-541)
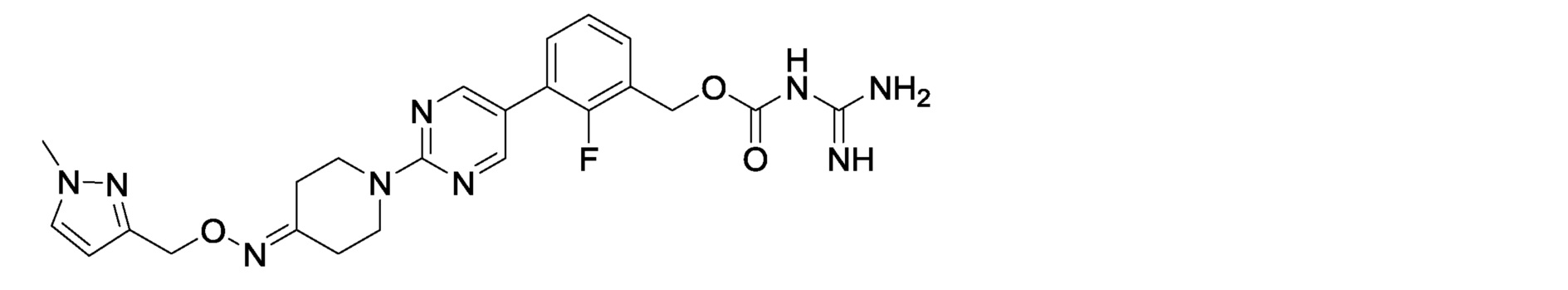
CDI, 73 мг (0,45 ммоль), добавляли к раствору в DMF (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[(1-метил-1H-пиразол-3-ил)метил]оксима, 83 мг (0,20 ммоль), синтезированного таким же образом, как ссылочное соединение 7-113, и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли карбонат гуанидина, 73 мг (0,41 ммоль), и смесь перемешивали при комнатной температуре в течение 3,5 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: 1,2-дихлорэтан:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь обрабатывали ультразвуком. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 55 мг (0,11 ммоль, выход 55%) в виде белого твердого вещества.
Масс-спектр (APCI, m/z): 496[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,61 (d, J=2,1 Гц, 1H), 7,53-7,47 (m, 1H), 7,42-7,36 (m, 1H), 7,31-7,25 (m, 1H), 6,23 (d, J=2,1 Гц, 1H), 5,06 (s, 2H), 4,93 (s, 2H), 3,95-3,87 (m, 4H), 3,80 (s, 3H), 2,60-2,48 (m, 2H), 2,42-2,35 (m, 2H).
[0404] (Пример 170)
2-Фтор-3-{2-[4-({[1-(тетрагидропиран-2-ил)-1H-пиразол-3-ил]метокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-573)

CDI, 16 мг (0,10 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-3-ил]метил}оксима, 23 мг (0,048 ммоль), синтезированного таким же образом, как в ссылочном примере 7-114, и смесь перемешивали при комнатной температуре в течение 14 часов. Далее добавляли CDI, 8,0 мг (0,049 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли карбонат гуанидина, 18 мг (0,10 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 27 мг (0,047 ммоль, выход 98%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 566[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,52 (d, J=1,4 Гц, 2H), 7,57 (d, J=2,4 Гц, 1H), 7,46-7,40 (m, 1H), 7,32-7,27 (m, 1H), 7,22-7,14 (m, 1H), 6,36 (d, J=2,4 Гц, 1H), 5,40-5,33 (m, 1H), 5,24 (s, 2H), 5,12 (s, 2H), 4,11-4,03 (m, 1H), 4,03-3,94 (m, 4H), 3,75-3,63 (m, 1H), 2,72-2,67 (m, 2H), 2,49-2,44 (m, 2H), 2,19-1,97 (m, 3H), 1,80-1,49 (m, 3H).
[0405] (Пример 171)
3-[2-(4-{[(1H-пиразол-3-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-539)

Раствор 2 М хлорида водорода в этаноле, (1,6 мл), добавляли к 2-фтор-3-{2-[4-({[1-(тетрагидропиран-2-ил)-1H-пиразол-3-ил]метокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамату 25 мг (0,044 ммоль), синтезированному таким же образом, как в примере 170, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли TEA и этанол при охлаждении льдом. Смесь перемешивали при комнатной температуре в течение 30 минут, и осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 9,9 мг (0,021 ммоль, выход 48%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 482[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,3 Гц, 2H), 7,67-7,46 (m, 2H), 7,43-7,35 (m, 1H), 7,31-7,25 (m, 1H), 6,27 (d, J=2,1 Гц, 1H), 5,06 (s, 2H), 5,00 (s, 2H), 3,97-3,86 (m, 4H), 2,60-2,54 (m, 2H), 2,42-2,36 (m, 2H).
[0406] (Пример 172)
2-Фтор-3-{2-[4-({[1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-574)

CDI, 65 мг (0,40 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-5-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метил}оксима, 89 мг (0,19 ммоль), синтезированного таким же образом, как в ссылочном примере 7-115, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 70 мг (0,39 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 91 мг (0,16 ммоль, выход 84%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 566[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (s, 2H), 7,89 (s, 1H), 7,53-7,47 (m, 2H), 7,42-7,36 (m, 1H), 7,31-7,25 (m, 1H), 5,38-5,33 (m, 1H), 5,06 (s, 2H), 4,90 (s, 2H), 3,95-3,87 (m, 5H), 3,65-3,55 (m, 1H), 2,59-2,53 (m, 2H), 2,44-2,33 (m, 2H), 2,14-1,82 (m, 3H), 1,74-1,43 (m, 3H).
[0407] (Пример 173)
3-[2-(4-{[(1H-пиразол-4-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-540)

Раствор 2 М хлорида водорода в этаноле, 2,0 мл (4,0 ммоль), добавляли к 2-фтор-3-{2-[4-({[1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метокси}имино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамату, 80 мг (0,14 ммоль), синтезированному таким же образом, как в примере 172, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. К концентрированному остатку добавляли метиленхлорид и TEA, и затем добавляли воду. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 41 мг (0,085 ммоль, выход 61%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 482[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,87-7,65 (m, 1H), 7,61-7,45 (m, 2H), 7,43-7,36 (m, 1H), 7,33-7,22 (m, 1H), 5,06 (s, 2H), 4,93 (s, 2H), 4,02-3,83(m, 4H), 2,59-2,53 (m, 2H), 2,45-2,37 (m, 2H).
[0408] (Пример 174)
2-Фтор-3-[2-(4-{[(1-метил-1H-пиразол-4-ил)метокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-542)
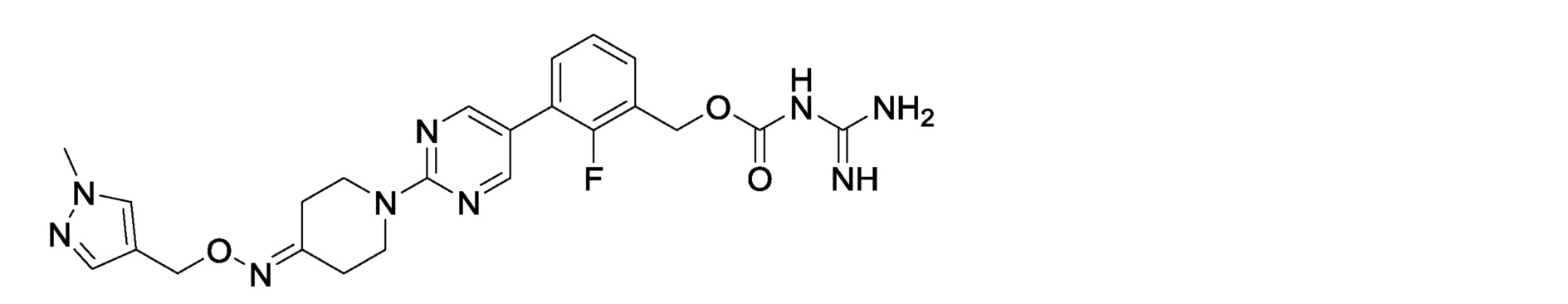
CDI, 84 мг (0,52 ммоль), добавляли к раствору в DMF (6 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[(1-метил-1H-пиразол-4-ил)метил]оксима 0,11 г (0,26 ммоль), синтезированного таким же образом, как в ссылочном примере 7-116, и смесь перемешивали при комнатной температуре в течение 15 часов. Затем добавляли карбонат гуанидина, 93 мг (0,52 ммоль), и смесь перемешивали при комнатной температуре в течение 5 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 78 мг (0,16 ммоль, выход 62%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 496[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,70 (s, 1H), 7,54-7,47 (m, 1H), 7,42 (s, 1H), 7,42-7,37 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,87 (s, 2H), 3,95-3,87 (m, 4H), 3,81 (s, 3H), 2,57-2,53 (m, 2H), 2,43-2,33 (m, 2H).
[0409] (Пример 175)
3-[2-(4-{[2-(1H-пиразол-1-ил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-543)
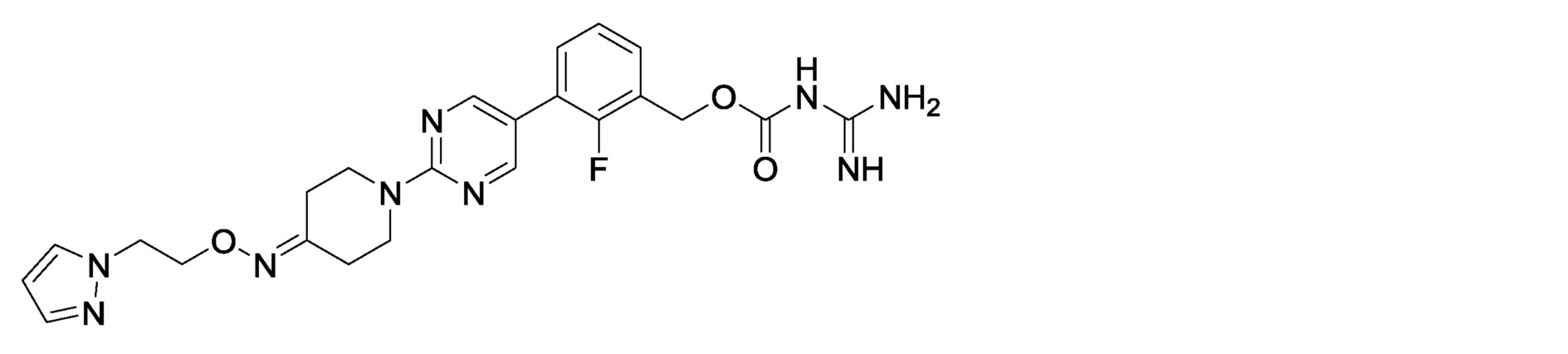
CDI, 24 мг (0,15 ммоль), добавляли к раствору в DMF (1 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[2-(1H-пиразол-1-ил)этил]оксима 30 мг (0,073 ммоль), синтезированного таким же образом, как в ссылочном примере 7-117, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли карбонат гуанидина, 26 мг (0,15 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Полученный таким образом неочищенный продукт промывали TBME и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 16 мг (0,032 ммоль, выход 44%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 496[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,4 Гц, 2H), 7,67 (dd, J=0,6, 2,3 Гц, 1H), 7,54-7,47 (m, 1H), 7,45 (dd, J=0,6, 1,9 Гц, 1H), 7,43-7,36 (m, 1H), 7,32-7,25 (m, 1H), 6,23 (dd, J=1,9, 2,3 Гц, 1H), 5,06 (s, 2H), 4,39-4,32 (m, 2H), 4,32-4,25 (m, 2H), 3,97-3,85 (m, 4H), 2,56-2,46 (m, 2H), 2,42-2,36 (m, 2H).
[0410] (Пример 176)
2-Фтор-3-(2-{4-[(пиридин-4-илметокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-544)
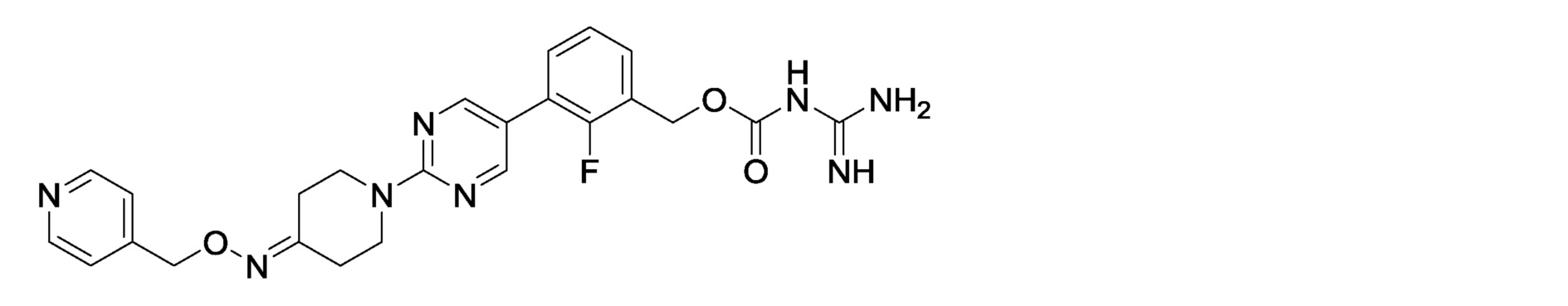
CDI, 95 мг (0,586 ммоль), добавляли к раствору в DMF (4 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-пиридин-4-илметилоксима, 104 мг (0,255 ммоль), синтезированного таким же образом, как ссылочное соединение 7-118, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли карбонат гуанидина, 95 мг (0,527 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. К полученному твердому веществу добавляли этилацетат, и смесь перемешивали при комнатной температуре. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 99,5 мг (0,202 ммоль, выход 79%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 493[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,0 Гц, 2H), 8,56-8,51 (m, 2H), 7,54-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,36-7,32 (m, 2H), 7,31-7,25 (m, 1H), 5,11 (s, 2H), 5,06 (s, 2H), 4,00-3,88 (m, 4H), 2,73-2,66 (m, 2H), 2,43-2,36 (m, 2H).
[0411] (Пример 177)
3-[2-(4-{[2-(2,5-Диоксопирролидин-1-ил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]-2-фторбензилкарбамимидоилкарбамат (соединение II-545)

CDI, 101 мг (0,62 ммоль), добавляли к раствору в DMF (4 мл) 1-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)пирролидин-2,5-диона, 138 мг (0,31 ммоль), синтезированного таким же образом, как в ссылочном примере 7-119, и смесь перемешивали при комнатной температуре в течение 4 часов. Затем добавляли карбонат гуанидина, 115 мг (0,64 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол). К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при 70°C в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 93 мг (0,18 ммоль, выход 58%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 527[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,60 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,43-7,36 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,11-4,05 (m, 2H), 3,95-3,86 (m, 4H), 3,67-3,55 (m, 2H), 2,63 (s, 4H), 2,52-2,47 (m, 2H), 2,40-2,32 (m, 2H).
[0412] (Пример 178)
2-Фтор-3-[2-(4-{[2-(2-оксопирролидин-1-ил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-546)

CDI, 61 мг (0,38 ммоль), добавляли к раствору в DMF (2 мл) 1-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)пирролидин-2-она, 80 мг (0,19 ммоль), синтезированного таким же образом, как в ссылочном примере 7-120, и смесь перемешивали при комнатной температуре в течение 4 часов. Затем добавляли карбонат гуанидина, 67 мг (0,37 ммоль), и смесь перемешивали при комнатной температуре в течение 15 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 82 мг (0,16 ммоль, выход 84%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 513[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (d, J=1,1 Гц, 2H), 7,55-7,47 (m, 1H), 7,44-7,36 (m, 1H), 7,33-7,24 (m, 1H), 5,06 (s, 2H), 4,11-4,04 (m, 2H), 3,96-3,87 (m, 4H), 3,45-3,36 (m, 4H), 2,60-2,54 (m, 2H), 2,48-2,36 (m, 2H), 2,25-2,16 (m, 2H), 2,00-1,83 (m, 2H).
[0413] (Пример 179)
2-Фтор-3-[2-(4-{[2-(2-оксооксазолидин-3-ил)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-547)
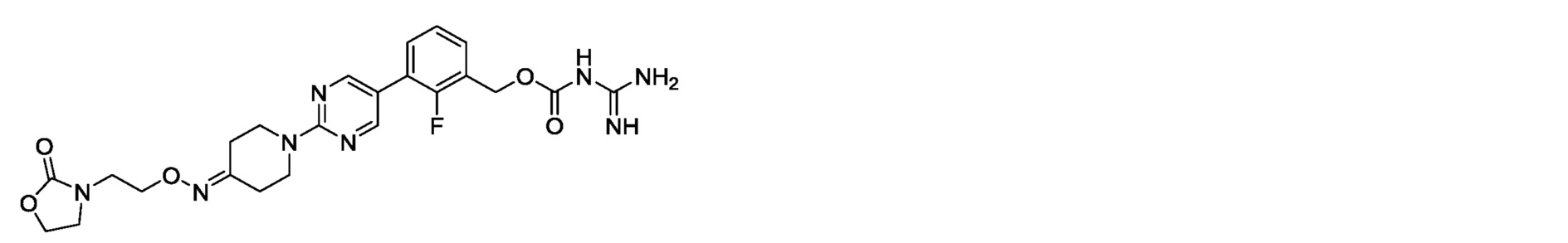
CDI, 76 мг (0,47 ммоль), добавляли к раствору в DMF (4 мл) 3-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)оксазолидин-2-она, 67 мг (0,16 ммоль), синтезированного таким же образом, как в ссылочном примере 7-121, и смесь перемешивали при комнатной температуре в течение 14 часов. Далее добавляли CDI, 25 мг (0,15 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли карбонат гуанидина, 58 мг (0,32 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 62 мг (0,12 ммоль, выход 75%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 515[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,59 (br s, 2H), 7,55-7,46 (m, 1H), 7,43-7,36 (m, 1H), 7,32-7,25 (m, 1H), 5,06 (s, 2H), 4,29-4,21 (m, 2H), 4,17-4,07 (m, 2H), 3,97-3,87 (m, 4H), 3,64-3,55 (m, 2H), 3,44-3,38 (m, 2H), 2,60-2,54 (m, 2H), 2,43-2,36 (m, 2H).
[0414] (Пример 180)
2-Фтор-3-[2-(4-{[2-(3-оксоморфолино)этокси]имино}пиперидин-1-ил)пиримидин-5-ил]бензилкарбамимидоилкарбамат (соединение II-548)

CDI, 130 мг (0,802 ммоль), добавляли к раствору в DMF (4 мл) 4-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)морфолин-3-она, 118 мг (0,266 ммоль), синтезированного таким же образом, как в ссылочном примере 7-122, и смесь перемешивали при комнатной температуре в течение 4 часов. Затем добавляли карбонат гуанидина, 106 мг (0,588 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 106 мг (0,201 ммоль, выход 76%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 529[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,60 (d, J=1,4 Гц, 2H), 7,55-7,47 (m, 1H), 7,42-7,35 (m, 1H), 7,31-7,24 (m, 1H), 5,06 (s, 2H), 4,17-4,08 (m, 2H), 4,02 (s, 2H), 3,96-3,89 (m, 4H), 3,84-3,76 (m, 2H), 3,60-3,52 (m, 2H), 3,43-3,35 (m, 2H), 2,60-2,52 (m, 2H), 2,43-2,36 (m, 2H).
[0415] (Пример 181)
2-Фтор-3-{2-[4-(феноксиимино)пиперидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамат (соединение II-565)
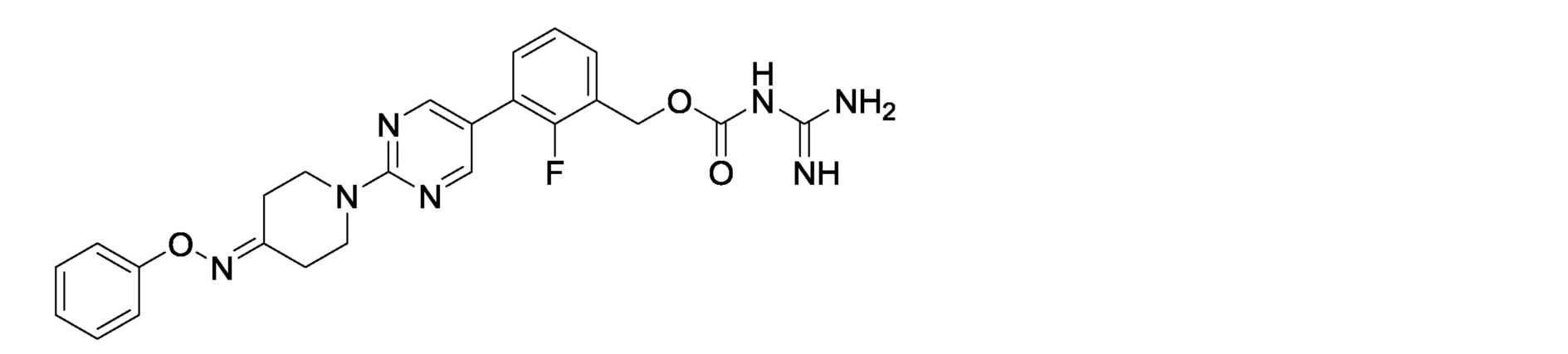
CDI, 69 мг (0,43 ммоль), добавляли к раствору в DMF (1 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-фенилоксима 68 мг (0,17 ммоль), синтезированного таким же образом, как в ссылочном примере 120, и смесь перемешивали при комнатной температуре в течение 1 часа. Далее добавляли 1 мл DMF. Затем добавляли карбонат гуанидина, 67 мг (0,37 ммоль), и смесь перемешивали при комнатной температуре в течение 11 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Полученное твердое вещество очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: этилацетат:метанол). Полученный фракцию, включающую в себя целевое соединение, концентрировали при пониженном давлении. К концентрированному остатку добавляли этанол, и смесь перемешивали при 65°C в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 58 мг (0,11 ммоль, выход 65%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 478[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,62 (s, 2H), 7,55-7,48 (m, 1H), 7,43-7,27 (m, 4H), 7,20-7,13 (m, 2H), 7,05-6,97 (m, 1H), 5,07 (s, 2H), 4,07-3,98 (m, 4H), 2,86-2,80 (m, 2H), 2,61-2,54 (m, 2H).
[0416] (Пример 182)
2-Фтор-3-(2-{4-[(пиримидин-5-илокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-566)
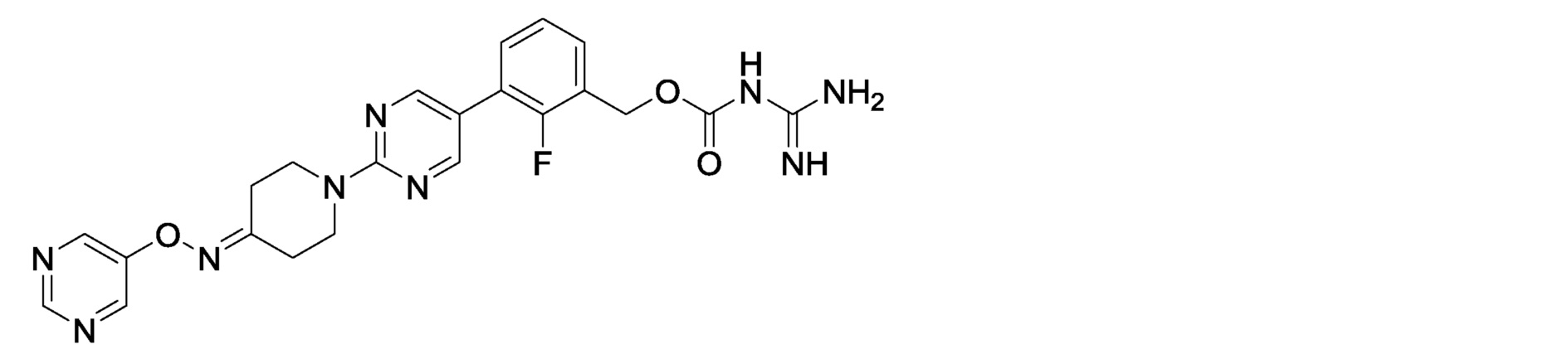
CDI, 36 мг (0,22 ммоль), добавляли к раствору в DMF (2 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-пиримидин-5-илоксима, 44 мг (0,11 ммоль), синтезированного таким же образом, как в ссылочном примере 7-123, и смесь перемешивали при комнатной температуре в течение 3,5 часа. Далее добавляли CDI, 18 мг (0,11 ммоль), и смесь перемешивали при комнатной температуре в течение 3,5 часа. Затем добавляли карбонат гуанидина, 50 мг (0,28 ммоль), и смесь перемешивали при комнатной температуре в течение 19 часов. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации. Полученное твердое вещество очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: этилацетат:метанол) и затем очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 17 мг (0,035 ммоль, выход 32%) в виде светло-желтого твердого вещества.
Масс-спектр (ESI, m/z): 480[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,89 (d, J=1,3 Гц, 1H), 8,74 (d, J=1,0 Гц, 2H), 8,65-8,61 (m, 2H), 7,55-7,49 (m, 1H), 7,44-7,38 (m, 1H), 7,33-7,27 (m, 1H), 5,07 (s, 2H), 4,09-4,00 (m, 4H), 2,91-2,84 (m, 2H), 2,64-2,56 (m, 2H).
[0417] (Пример 183)
2-Фтор-3-(2-{4-[(пиримидин-2-илокси)имино]пиперидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамат (соединение II-567)

CDI, 13,6 мг (0,084 ммоль), добавляли к раствору в DMF (1 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-пиримидин-2-илоксима, 15,4 мг (0,039 ммоль), синтезированного таким же образом, как в ссылочном примере 7-124, и смесь перемешивали при комнатной температуре в течение 3,5 часа. Далее добавляли CDI, 4,1 мг (0,025 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли карбонат гуанидина, 18,1 мг (0,10 ммоль), и смесь перемешивали при комнатной температуре в течение 18,5 часа. После окончания реакции к реакционной смеси добавляли воду, и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 13,6 мг (0,028 ммоль, выход 72%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 480[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,67 (d, J=4,8 Гц, 2H), 8,63 (d, J=1,3 Гц, 2H), 7,57-7,48 (m, 1H), 7,45-7,36 (m, 1H), 7,32-7,21 (m, 2H), 5,07 (s, 2H), 4,09-3,98 (m, 4H), 2,87-2,80 (m, 2H), 2,63-2,57 (m, 2H).
[0418] (Пример 184)
2-Фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата 1/2 L-тартрат (соединения II-2 1/2 L-тартрат)

DMSO (5 мл) добавляли к 2-фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамату (соединение II-2), 500 мг (1,29 ммоль), синтезированному таким же образом, как в примере 1, и смесь нагревали до 50°C с получением раствора. Затем добавляли L-винную кислоту, 198 мг (1,32 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 545 мг (1,18 ммоль, выход 91%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 388[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,4 Гц, 2H), 7,56-7,48 (m, 1H), 7,48-7,38 (m, 1H), 7,35-7,24 (m, 1H), 5,09 (s, 2H), 4,85-4,78 (m, 4H), 4,19 (s, 1H), 3,83 (s, 3H).
[0419] (Пример 185)
2-Фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата 1/2 D-тартрат (соединения II-2 1/2 D-тартрат)

DMSO (5 мл) добавляли к 2-фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамату (соединение II-2), 500 мг (1,29 ммоль), синтезированному таким же образом, как в примере 1, и смесь нагревали до 50°C с получением раствора. Затем добавляли D-винную кислоту, 201 мг (1,34 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 558 мг (1,21 ммоль, выход 94%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 388[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,4 Гц, 2H), 7,57-7,49 (m, 1H), 7,47-7,40 (m, 1H), 7,37-7,25 (m, 1H), 5,10 (s, 2H), 4,87-4,76 (m, 4H), 4,20 (s, 1H), 3,83 (s, 3H).
[0420] (Пример 186)
2-Фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата малеат (соединения II-2 малеат)

DMSO (5 мл) добавляли к 2-фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамату (соединение II-2), 500 мг (1,29 ммоль), синтезированному таким же образом, как в примере 1, и смесь нагревали до 50°C с получением раствора. Затем добавляли малеиновую кислоту, 152 мг (1,31 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 556 мг (1,10 ммоль, выход 85%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 388[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,1 Гц, 2H), 7,66-7,57 (m, 1H), 7,56-7,49 (m, 1H), 7,39-7,31 (m, 1H), 6,08 (s, 2H), 5,33 (s, 2H), 4,87-4,77 (m, 4H), 3,83 (s, 3H).
[0421] (Пример 187)
2-Фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамата 1/2 сукцинат (соединения II-2 1/2 сукцинат)
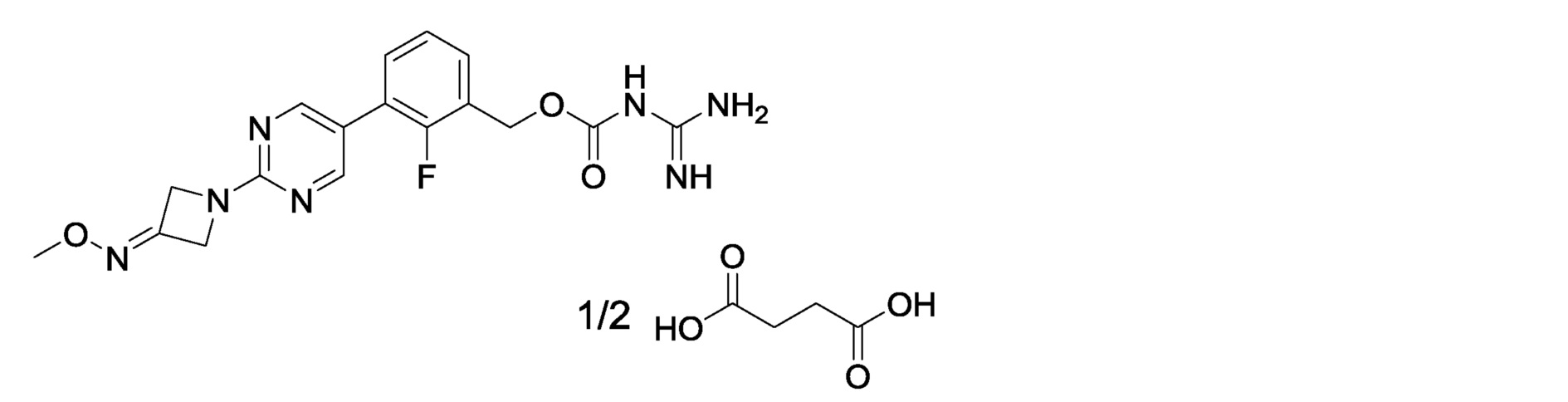
DMSO (5 мл) добавляли к 2-фтор-3-{2-[3-(метоксиимино)азетидин-1-ил]пиримидин-5-ил}бензилкарбамимидоилкарбамату (соединение II-2), 500 мг (1,29 ммоль), синтезированному таким же образом, как в примере 1, и смесь нагревали до 50°C с получением раствора. Затем добавляли янтарную кислоту, 153 мг (1,30 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 506 мг (1,13 ммоль, выход 88%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 388[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,54-7,38 (m, 2H), 7,34-7,26 (m, 1H), 5,07 (s, 2H), 4,86-4,77 (m, 4H), 3,83 (s, 3H), 2,41 (s, 2H).
[0422] (Пример 188)
3-{2-[3-(Этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамата 1/2 L-тартрат (соединения II-3 1/2 L-тартрат)

DMSO (5 мл) добавляли к 3-{2-[3-(этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамату (соединение II-3), 500 мг (1,25 ммоль), синтезированному таким же образом, как в примере 2, и смесь нагревали до 50°C с получением раствора. Затем добавляли L-винную кислоту, 190 мг (1,27 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 561 мг (1,18 ммоль, выход 94%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 402[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,57-7,48 (m, 1H), 7,47-7,39 (m, 1H), 7,34-7,25 (m, 1H), 5,09 (s, 2H), 4,87-4,75 (m, 4H), 4,19 (s, 1H), 4,08 (q, J=7,0 Гц, 2H), 1,22 (t, J=7,0 Гц, 3H).
[0423] (Пример 189)
3-{2-[3-(Этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамата 1/2 D-тартрат (соединения III-3 1/2 D-тартрат)
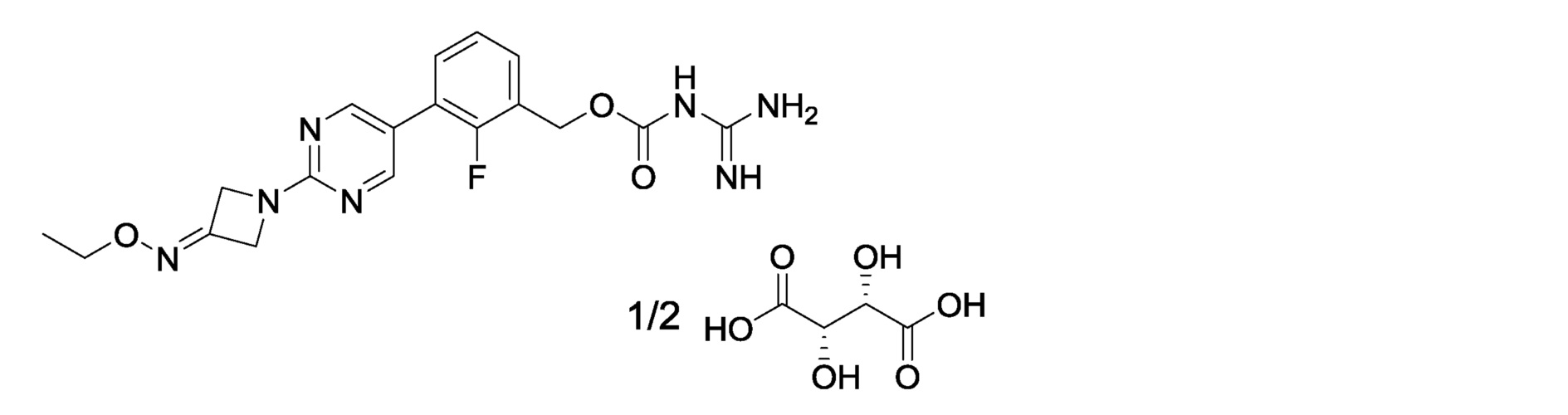
DMSO (5 мл) добавляли к 3-{2-[3-(этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамату (соединение II-3), 500 мг (1,25 ммоль), синтезированному таким же образом, как в примере 2, и смесь нагревали до 50°C с получением раствора. Затем добавляли D-винную кислоту, 188 мг (1,25 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 534 мг (1,12 ммоль, выход 90%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 402[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,58-7,48 (m, 1H), 7,46-7,39 (m, 1H), 7,35-7,25 (m, 1H), 5,08 (s, 2H), 4,89-4,74 (m, 4H), 4,17 (s, 1H), 4,08 (q, J=7,1 Гц, 2H), 1,22 (t, J=0,1 Гц, 3H).
[0424] (Пример 190)
3-{2-[3-(Этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамата малеат (соединения II-3 малеат)

DMSO (5 мл) добавляли к 3-{2-[3-(этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамату (соединение II-3), 500 мг (1,25 ммоль), синтезированному таким же образом, как в примере 2, и смесь нагревали до 50°C с получением раствора. Затем добавляли малеиновую кислоту, 151 мг (1,30 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 597 мг (1,15 ммоль, выход 92%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 402[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,1 Гц, 2H), 7,66-7,56 (m, 1H), 7,56-7,48 (m, 1H), 7,39-7,32 (m, 1H), 6,07 (s, 2H), 5,30 (s, 2H), 4,93-4,74 (m, 4H), 4,09 (q, J=7,0 Гц, 2H), 1,22 (t, J=7,0 Гц, 3H).
[0425] (Пример 191)
3-{2-[3-(Этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамата 1/2 сукцинат (соединения II-3 1/2 сукцинат)

DMSO (5 мл) добавляли к 3-{2-[3-(этоксиимино)азетидин-1-ил]пиримидин-5-ил}-2-фторбензилкарбамимидоилкарбамату (соединение II-3), 500 мг (1,25 ммоль), синтезированному таким же образом, как в примере 2, и смесь нагревали до 50°C с получением раствора. Затем добавляли янтарную кислоту, 147 мг (1,25 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 560 мг (1,22 ммоль, выход 98%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 402[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,67-8,59 (m, 2H), 7,55-7,48 (m, 1H), 7,46-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,07 (s, 2H), 4,88-4,76 (m, 4H), 4,08 (q, J=7,0 Гц, 2H), 2,42 (s, 2H), 1,22 (t, J=7,0 Гц, 3H).
[0426] (Пример 192)
2-Фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата 1/2 L-тартрат (соединения II-12 1/2 L-тартрат)

DMSO (5 мл) добавляли к 2-фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату (соединение II-12), 500 мг (1,28 ммоль), синтезированному таким же образом, как в примере 3, и смесь нагревали до 50°C с получением раствора. Затем добавляли L-винную кислоту, 199 мг (1,33 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 573 мг (1,23 ммоль, выход 96%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 391[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (s, 2H), 7,56-7,49 (m, 1H), 7,46-7,40 (m, 1H), 7,33-7,26 (m, 1H), 5,10 (s, 2H), 4,87-4,77 (m, 4H), 4,19 (s, 1H).
[0427] (Пример 193)
2-Фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата 1/2 D-тартрат (соединения II-12 1/2 D-тартрат)

DMSO (5 мл) добавляли к 2-фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату (соединение II-12), 500 мг (1,28 ммоль), синтезированному таким же образом, как в примере 3, и смесь нагревали до 50°C с получением раствора. Затем добавляли D-винную кислоту, 194 мг (1,29 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 555 мг (1,19 ммоль, выход 93%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 391[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,1 Гц, 2H), 7,57-7,49 (m, 1H), 7,47-7,40 (m, 1H), 7,34-7,27 (m, 1H), 5,09 (s, 2H), 4,85-4,78 (m, 4H), 4,18 (s, 1H).
[0428] (Пример 194)
2-Фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата малеат (соединения II-12 малеат)

DMSO (5 мл) добавляли к 2-фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату (соединение II-12), 500 мг (1,28 ммоль), синтезированному таким же образом, как в примере 3, и смесь нагревали до 50°C с получением раствора. Затем добавляли малеиновую кислоту, 151 мг (1,30 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 543 мг (1,07 ммоль, выход 84%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 391[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,1 Гц, 2H), 7,65-7,57 (m, 1H), 7,56-7,49 (m, 1H), 7,39-7,32 (m, 1H), 6,08 (s, 2H), 5,32 (s, 2H), 4,85-4,78 (m, 4H).
[0429] (Пример 195)
2-Фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата 1/2 сукцинат (соединения II-12 1/2 сукцинат)
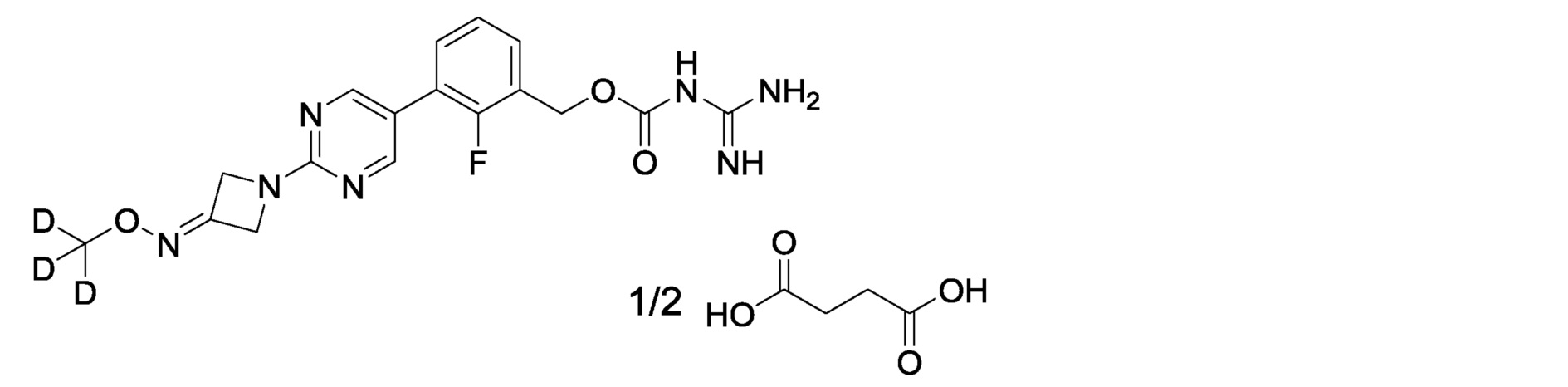
DMSO (5 мл) добавляли к 2-фтор-3-(2-{3-[(метокси-d3)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату (соединение II-12), 500 мг (1,28 ммоль), синтезированному таким же образом, как в примере 3, и смесь нагревали до 50°C с получением раствора. Затем добавляли янтарную кислоту, 153 мг (1,30 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 506 мг (1,13 ммоль, выход 88%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 391[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,3 Гц, 2H), 7,54-7,47 (m, 1H), 7,45-7,39 (m, 1H), 7,33-7,27 (m, 1H), 5,07 (s, 2H), 4,85-4,78 (m, 4H), 2,41 (s, 2H).
[0430] (Пример 196)
2-Фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата 1/2 L-тартрат (соединения II-15 1/2 L-тартрат)
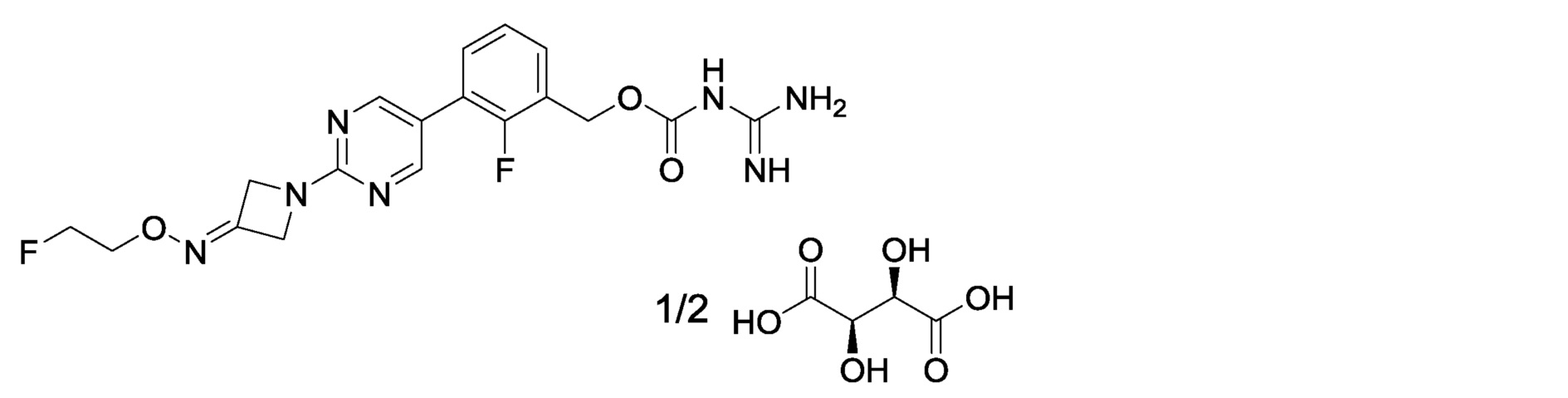
DMSO (5 мл) добавляли к 2-фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату (соединение II-15), 500 мг (1,19 ммоль), синтезированному таким же образом, как в примере 5, и смесь нагревали до 50°C с получением раствора. Затем добавляли L-винную кислоту, 179 мг (1,20 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 541 мг (1,09 ммоль, выход 92%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 420[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,3 Гц, 2H), 7,58-7,49 (m, 1H), 7,48-7,40 (m, 1H), 7,36-7,27 (m, 1H), 5,10 (s, 2H), 4,90-4,80 (m, 4H), 4,75-4,55 (m, 2H), 4,36-4,22 (m, 2H), 4,18 (s, 1H).
[0431] (Пример 197)
2-Фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата 1/2 D-тартрат (соединения II-15 1/2 D-тартрат)

DMSO (5 мл) добавляли к 2-фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату (соединение II-15), 500 мг (1,19 ммоль), синтезированному таким же образом, как в примере 5, и смесь нагревали до 50°C с получением раствора. Затем добавляли D-винную кислоту, 181 мг (1,21 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 529 мг (1,07 ммоль, выход 90%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 420[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,3 Гц, 2H), 7,58-7,48 (m, 1H), 7,47-7,40 (m, 1H), 7,34-7,27 (m, 1H), 5,09 (s, 2H), 4,89-4,80 (m, 4H), 4,74-4,54 (m, 2H), 4,37-4,20 (m, 2H), 4,17 (s, 1H).
[0432] (Пример 198)
2-Фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата малеат (соединения II-15 малеат)

DMSO (5 мл) добавляли к 2-фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату (соединение II-15), 500 мг (1,19 ммоль), синтезированному таким же образом, как в примере 5, и смесь нагревали до 50°C с получением раствора. Затем добавляли малеиновую кислоту, 138 мг (1,19 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 48 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 518 мг (0,967 ммоль, выход 81%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 420[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (d, J=1,3 Гц, 2H), 7,65-7,58 (m, 1H), 7,56-7,49 (m, 1H), 7,40-7,33 (m, 1H), 6,08 (s, 2H), 5,32 (s, 2H), 4,90-4,81 (m, 4H), 4,74-4,55 (m, 2H), 4,35-4,20 (m, 2H).
[0433] (Пример 199)
2-Фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамата 1/2 сукцинат (соединения II-15 1/2 сукцинат)
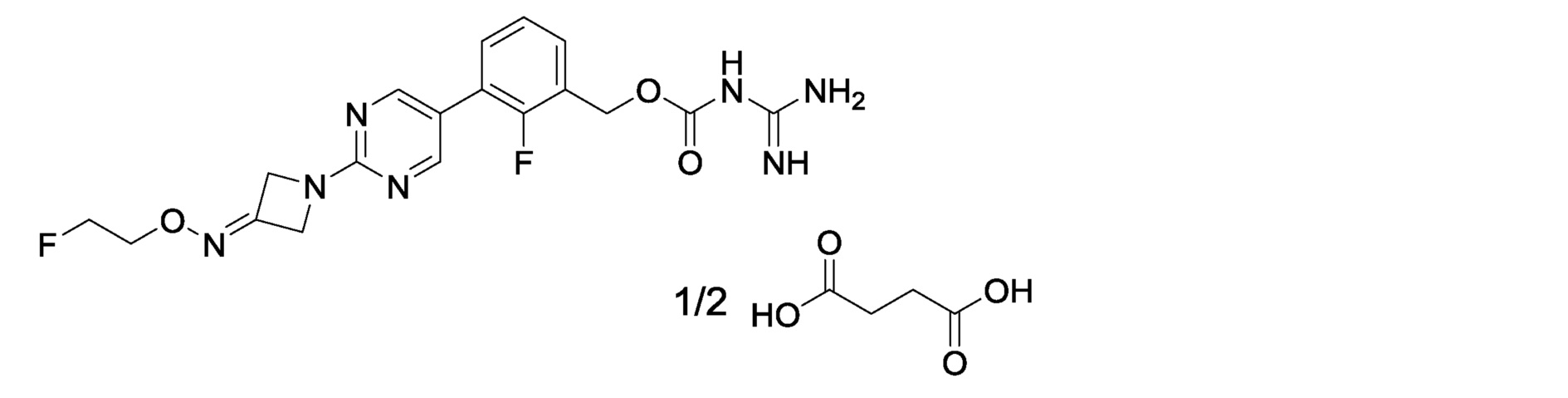
DMSO (5 мл) добавляли к 2-фтор-3-(2-{3-[(2-фторэтокси)имино]азетидин-1-ил}пиримидин-5-ил)бензилкарбамимидоилкарбамату (соединение II-15), 500 мг (1,19 ммоль), синтезированному таким же образом, как в примере 5, и смесь нагревали до 50°C с получением раствора. Затем добавляли янтарную кислоту, 145 мг (1,23 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 20 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 492 мг (1,03 ммоль, выход 87%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 420[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,64 (s, 2H), 7,54-7,48 (m, 1H), 7,45-7,39 (m, 1H), 7,35-7,24 (m, 1H), 5,07 (s, 2H), 4,88-4,80 (m, 4H), 4,75-4,54 (m, 2H), 4,36-4,20 (m, 2H), 2,41 (s, 2H).
[0434] (Пример 200)
2-Фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамата 1/2 L-тартрат (соединения III-78 1/2 L-тартрат)

DMSO (5 мл) добавляли к 2-фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамату (соединение III-78), 500 мг (1,24 ммоль), синтезированному таким же образом, как в примере 36, и смесь нагревали до 50°C с получением раствора. Затем добавляли L-винную кислоту, 188 мг (1,25 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 515 мг (1,07 ммоль, выход 86%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 405[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,21-8,15 (m, 1H), 7,79-7,72 (m, 1H), 7,55-7,48 (m, 1H), 7,45-7,38 (m, 1H), 7,33-7,25 (m, 1H), 5,09 (s, 2H), 4,90-4,82 (m, 4H), 4,19 (s, 1H), 3,82 (s, 3H).
[0435] (Пример 201)
2-Фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамата 1/2 D-тартрат (соединения III-78 1/2 D-тартрат)

DMSO (5 мл) добавляли к 2-фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамату (соединение III-78), 500 мг (1,24 ммоль), синтезированному таким же образом, как в примере 36, и смесь нагревали до 50°C с получением раствора. Затем добавляли D-винную кислоту, 186 мг (1,24 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 525 мг (1,10 ммоль, выход 89%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 405[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,22-8,15 (m, 1H), 7,79-7,72 (m, 1H), 7,55-7,47 (m, 1H), 7,46-7,38 (m, 1H), 7,32-7,25 (m, 1H), 5,09 (s, 2H), 4,92-4,80 (m, 4H), 4,20 (s, 1H), 3,82 (s, 3H).
[0436] (Пример 202)
2-Фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамата малеат (соединения III-78 малеат)

DMSO (5 мл) добавляли к 2-фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамату (соединение III-78), 500 мг (1,24 ммоль), синтезированному таким же образом, как в примере 36, и смесь нагревали до 50°C с получением раствора. Затем добавляли малеиновую кислоту, 150 мг (1,29 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 40 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 455 мг (0,874 ммоль, выход 71%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 405[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,21-8,17 (m, 1H), 7,81-7,70 (m, 1H), 7,63-7,56 (m, 1H), 7,56-7,47 (m, 1H), 7,40-7,28 (m, 1H), 6,07 (s, 2H), 5,32 (s, 2H), 4,90-4,84 (m, 4H), 3,82 (s, 3H).
[0437] (Пример 203)
2-Фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамата 1/2 сукцинат (соединения III-78 1/2 сукцинат)
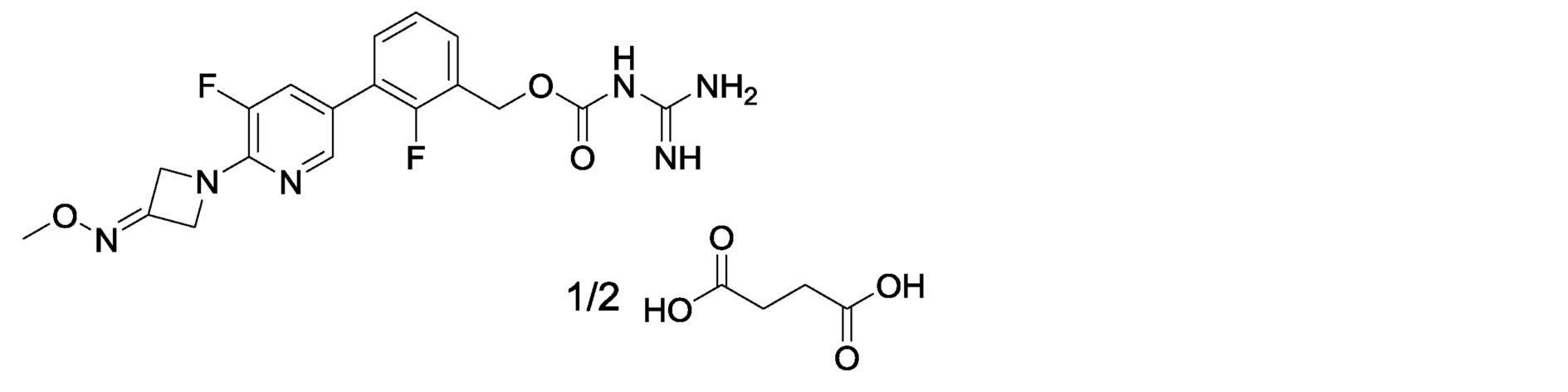
DMSO (4 мл) добавляли к 2-фтор-3-{5-фтор-6-[3-(метоксиимино)азетидин-1-ил]пиридин-3-ил}бензилкарбамимидоилкарбамату (соединение III-78), 500 мг (1,24 ммоль), синтезированному таким же образом, как в примере 36, и смесь нагревали до 50°C с получением раствора. Затем добавляли янтарную кислоту, 150 мг (1,27 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 20 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 488 мг (1,05 ммоль, выход 85%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 405[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,22-8,13 (m, 1H), 7,81-7,70 (m, 1H), 7,55-7,45 (m, 1H), 7,44-7,37 (m, 1H), 7,33-7,23 (m, 1H), 5,06 (s, 2H), 4,90-4,83 (m, 4H), 3,82 (s, 3H), 2,40 (s, 2H).
[0438] (Пример 204)
2-Фтор-3-(5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамата 1/2 L-тартрат (соединения III-88 1/2 L-тартрат)

DMSO (5 мл) добавляли к 2-фтор-3-(5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамату (соединение III-88), 500 мг (1,23 ммоль), синтезированному таким же образом, как в примере 37, и смесь нагревали до 50°C с получением раствора. Затем добавляли L-винную кислоту, 185 мг (1,23 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 567 мг (1,18 ммоль, выход 96%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 408[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,20-8,16 (m, 1H), 7,78-7,72 (m, 1H), 7,55-7,47 (m, 1H), 7,46-7,39 (m, 1H), 7,36-7,22 (m, 1H), 5,10 (s, 2H), 4,90-4,82 (m, 4H), 4,20 (s, 1H).
[0439] (Пример 205)
2-Фтор-3-(5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамата 1/2 D-тартрат (соединения III-88 1/2 D-тартрат)
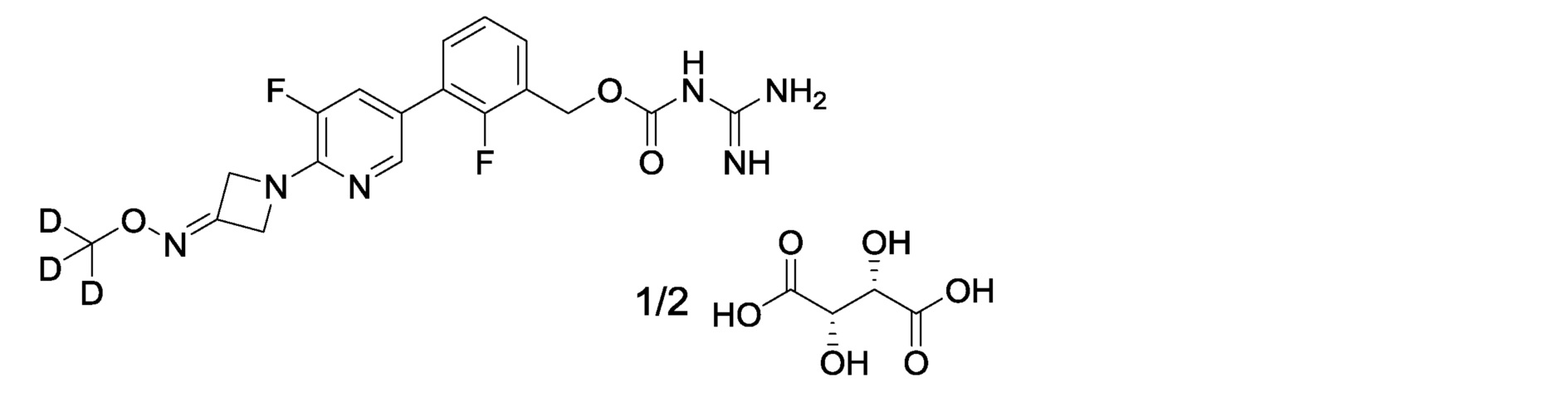
DMSO (5 мл) добавляли к 2-фтор-3-(5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамату (соединение III-88), 500 мг (1,23 ммоль), синтезированному таким же образом, как в примере 37, и смесь нагревали до 50°C с получением раствора. Затем добавляли D-винную кислоту, 184 мг (1,23 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 573 мг (1,19 ммоль, выход 97%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 408[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,20-8,15 (m, 1H), 7,80-7,71 (m, 1H), 7,55-7,48 (m, 1H), 7,46-7,38 (m, 1H), 7,34-7,25 (m, 1H), 5,10 (s, 2H), 4,90-4,83 (m, 4H), 4,20 (s, 1H).
[0440] (Пример 206)
2-Фтор-3-(5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамата малеат (соединения III-88 малеат)

DMSO (5 мл) добавляли к 2-фтор-3-(5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамату (соединение III-88), 500 мг (1,23 ммоль), синтезированному таким же образом, как в примере 37, и смесь нагревали до 50°C с получением раствора. Затем добавляли малеиновую кислоту, 148 мг (1,28 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 16 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 527 мг (1,01 ммоль, выход 82%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 408[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,20-8,17 (m, 1H), 7,80-7,71 (m, 1H), 7,63-7,57 (m, 1H), 7,54-7,48 (m, 1H), 7,37-7,31 (m, 1H), 6,08 (s, 2H), 5,32 (s, 2H), 4,90-4,84 (m, 4H).
[0441] (Пример 207)
2-Фтор-3-(5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамата 1/2 сукцинат (соединения III-88 1/2 сукцинат)

DMSO (5 мл) добавляли к 2-фтор-3-(5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамату (соединение III-88), 500 мг (1,23 ммоль), синтезированному таким же образом, как в примере 37, и смесь нагревали до 50°C с получением раствора. Затем добавляли янтарную кислоту, 146 мг (1,24 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (20 мл), и смесь перемешивали при комнатной температуре в течение 20 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 497 мг (1,07 ммоль, выход 87%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 408[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,19-8,16 (m, 1H), 7,78-7,72 (m, 1H), 7,53-7,46 (m, 1H), 7,44-7,37 (m, 1H), 7,32-7,25 (m, 1H), 5,07 (s, 2H), 4,89-4,83 (m, 4H), 2,42 (s, 2H).
[0442] (Пример 208)
2-Фтор-3-(5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамата моносукцинат (соединения III-88 сукцинат)

DMSO (0,4 мл) добавляли к 2-фтор-3-(5-фтор-6-{3-[(метокси-d3)имино]азетидин-1-ил}пиридин-3-ил)бензилкарбамимидоилкарбамату (соединение III-88) 100 мг (0,245 ммоль), синтезированному таким же образом, как в примере 37, и смесь нагревали до 60°C с получением раствора. Затем добавляли янтарную кислоту, 29 мг (0,246 ммоль), и смесь охлаждали до комнатной температуры. В нее по каплям вливали этилацетат (2 мл), и смесь перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 123 мг (0,234 ммоль, выход 96%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 408[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,20-8,16 (m, 1H), 7,79-7,72 (m, 1H), 7,54-7,46 (m, 1H), 7,44-7,37 (m, 1H), 7,33-7,24 (m, 1H), 5,07 (s, 2H), 4,90-4,83 (m, 4H), 2,42 (s, 4H).
[0443] [Ссылочные примеры]
(Ссылочный пример 1)
1-(5-Бромпиримидин-2-ил)азетидин-3-ол (ссылочное соединение 1)

TEA, 54 мл (0,39 моль), добавляли к раствору в этаноле (300 мл) 5-бром-2-хлорпиримидина, 25 г (0,13 моль), и гидрохлорида азетидин-3-ола 16 г (0,15 моль), и смесь перемешивали при 60°C в течение 4 часов. После окончания реакции растворитель реакционной смеси концентрировали при пониженном давлении до приблизительно половины объема. Добавляли 200 мл воды, и смесь перемешивали при комнатной температуре в течение 3 часов. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 28 г (0,12 моль, выход 92%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 230, 232[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,43 (s, 2H), 5,73 (d, J=6,5 Гц, 1H), 4,59-4,51 (m, 1H), 4,25-4,18 (m, 2H), 3,79-3,73 (m, 2H).
[0444] (Ссылочный пример 2)
1-(5-Бромпиримидин-2-ил)азетидин-3-он (ссылочное соединение 2)

Перйодинан Десса-Мартина, 50 г (120 ммоль), и гидрокарбонат натрия, 10 г (120 ммоль), добавляли к суспензии метиленхлорида (400 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-ола 19 г (83 ммоль), синтезированного таким же образом, как в ссылочном примере 1, и смесь перемешивали при комнатной температуре в течение 20 часов. После окончания реакции к реакционной смеси добавляли тиосульфат натрия пентагидрат и насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией метиленхлоридом. Органический слой промывали насыщенным водным раствором гидрокарбоната натрия, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли диизопропиловый эфир. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 16 г (70 ммоль, выход 84%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 228, 230[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,58 (s, 2H), 4,87 (s, 4H).
[0445] Указанное в заголовке соединение также синтезировали следующим образом.
TEA 3,0 мл (22 ммоль), добавляли к раствору в этаноле (10 мл) 5-бром-2-хлорпиримидина, 2,0 г (10 ммоль), и гидрохлорида азетидин-3-она, 1,0 г (9,3 ммоль), и смесь перемешивали при 80°C в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:этилацетат) с получением указанного в заголовке соединения в количестве 0,55 г (2,4 ммоль, выход 24%) в виде бесцветного масла.
[0446] Указанное в заголовке соединение также синтезировали следующим образом.
Азадол, 7,0 мг (0,046 ммоль), и диацетат йодбензола, 0,40 г (1,2 ммоль), добавляли к раствору в метиленхлориде (5 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-ола, 0,20 г (0,87 ммоль), синтезированного таким же образом, как в ссылочном примере 1, и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия и 20% водный раствор тиосульфата натрия, и смесь перемешивали в течение 1 часа с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли гексан, и смесь перемешивали при 50°C. Твердое вещество собирали с помощью фильтрации с получением указанного в заголовке соединения в количестве 0,19 г (0,82 ммоль, выход 94%) в виде белого твердого вещества.
[0447] (Ссылочный пример 3-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1)

O-метилгидроксиламина гидрохлорид, 1,5 г (18 ммоль), добавляли к раствору в THF (40 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она, 2,0 г (8,8 ммоль), синтезированного таким же образом, как в ссылочном примере 2, и смесь перемешивали при 50°C в течение 12 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия. Осажденное твердое вещество собирали с помощью фильтрации, промывали TBME и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 1,5 г (5,8 ммоль, выход 66%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 257, 259[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,54 (s, 2H), 4,80-4,66 (m, 4H), 3,81 (s, 3H).
[0448] (Ссылочный пример 3-2)
1-(5-Бромпиридин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-2)

O-метилгидроксиламина гидрохлорид, 38 мг (0,46 ммоль), добавляли к раствору в THF (4 мл) 1-(5-бромпиридин-2-ил)азетидин-3-она, 52 мг (0,23 ммоль), синтезированного таким же образом, как в ссылочном примере 32-2, и смесь перемешивали при 50°C в течение 8 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:этилацетат) с получением указанного в заголовке соединения в количестве 55 мг (0,22 ммоль, выход 96%) в виде белого твердого вещества.
[0449] (Ссылочный пример 3-3)
1-(5-Бром-3-метилпиридин-2-ил)азетидин-3-она O-метилоксима (ссылочное соединение 3-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 3-2, за исключением того, что 1-(5-бромпиридин-2-ил)азетидин-3-он (ссылочное соединение 32-2) заменяли на 1-(5-бром-3-метилпиридин-2-ил)азетидин-3-он, синтезированный таким же образом, как в ссылочном примере 32-3, и температура реакции была равна температуре окружающей среды. В результате указанное в заголовке соединение (выход 81%) было получено в виде светло-коричневого твердого вещества.
Масс-спектр (ESI, m/z): 270, 272[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,09 (d, J=2,1 Гц, 1H), 7,65-7,60 (m, 1H), 4,77 (s, 4H), 3,79 (s, 3H), 2,17 (s, 3H).
[0450] (Ссылочный пример 3-4)
1-(5-Бром-3-хлорпиридин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 3-2, за исключением того, что 1-(5-бромпиридин-2-ил)азетидин-3-он (ссылочное соединение 32-2) заменяли на 1-(5-бром-3-хлорпиридин-2-ил)азетидин-3-он, синтезированный таким же образом, как в ссылочном примере 32-4. В результате указанное в заголовке соединение (выход 75%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 290, 292[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,12 (d, J=2,1 Гц, 1H), 7,63 (d, J=2,1 Гц, 1H), 4,92-4,84 (m, 4H), 3,89 (s, 3H).
[0451] (Ссылочный пример 3-5)
1-[5-Бром-3-(дифторметил)пиридин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 3-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 3-2, за исключением того, что 1-(5-бромпиридин-2-ил)азетидин-3-он (ссылочное соединение 32-2) заменяли на 1-[5-бром-3-(дифторметил)пиридин-2-ил]азетидин-3-он, синтезированный таким же образом, как в ссылочном примере 32-5, и температуру реакции изменяли на 70°C. В результате указанное в заголовке соединение (выход 87%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 306, 308[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,42-8,39 (m, 1H), 7,99-7,96 (m, 1H), 7,07 (t, J=54,2 Гц, 1H), 4,85-4,80 (m, 4H), 3,81 (s, 3H).
[0452] (Ссылочный пример 3-6)
1-(5-Бром-3-циклопропилпиридин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-6)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 3-2, за исключением того, что 1-(5-бромпиридин-2-ил)азетидин-3-он (ссылочное соединение 32-2) заменяли на 1-(5-бром-3-циклопропилпиридин-2-ил)азетидин-3-он, синтезированный таким же образом, как в ссылочном примере 32-6, и температуру реакции изменяли на 70°C. В результате указанное в заголовке соединение (выход 37%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 296, 298[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,08-8,05 (m, 1H), 7,41 (dd, J=0,7, 2,3 Гц, 1H), 4,88-4,83 (m, 4H), 3,80 (s, 3H), 1,88-1,79 (m, 1H), 0,95-0,86 (m, 2H), 0,78-0,69 (m, 2H).
[0453] (Ссылочный пример 3-7)
1-(5-Бром-3-этилпиридин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-7)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 3-2, за исключением того, что 1-(5-бромпиридин-2-ил)азетидин-3-он (ссылочное соединение 32-2) заменяли на 1-(5-бром-3-этилпиридин-2-ил)азетидин-3-он, синтезированный таким же образом, как в ссылочном примере 32-7, и температуру реакции изменяли на 70°C. В результате указанное в заголовке соединение (выход 84%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 284, 286[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,10 (d, J=2,3 Гц, 1H), 7,63-7,59 (m, 1H), 4,80-4,72 (m, 4H), 3,80 (s, 3H), 2,58-2,42 (m, 2H), 1,15 (t, J=7,5 Гц, 3H).
[0454] (Ссылочный пример 3-8)
1-[5-Бром-3-(метоксиметил)пиридин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 3-8)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 3-2, за исключением того, что 1-(5-бромпиридин-2-ил)азетидин-3-он (ссылочное соединение 32-2) заменяли на 1-[5-бром-3-(метоксиметил)пиридин-2-ил]азетидин-3-он, синтезированный таким же образом, как в ссылочном примере 50-2. В результате указанное в заголовке соединение (выход 76%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 300, 302[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,19 (d, J=2,4 Гц, 1H), 7,71 (d, J=2,4 Гц, 1H), 4,82-4,78 (m, 4H), 4,31 (s, 2H), 3,80 (s, 3H), 3,31 (s, 3H).
[0455] (Ссылочный пример 4)
[(3-Бром-2-фторбензил)окси](трет-бутил)диметилсилан (ссылочное соединение 4)

(трет-Бутил)диметилсилилхлорид 22 г (0,15 моль) и имидазол 14 г (0,21 моль) добавляли к раствору в THF (200 мл) (3-бром-2-фторфенил)метанола, 25 г (0,12 моль), и смесь перемешивали при комнатной температуре в течение 5 часов и оставляли стоять при комнатной температуре в течение 2 дней. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 35 г (0,11 моль, выход 92%) в виде бесцветного масла.
Масс-спектр (CI, m/z): 319, 321[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,65-7,59 (m, 1H), 7,48-7,42 (m, 1H), 7,22-7,15 (m, 1H), 4,78 (s, 2H), 0,90 (s, 9H), 0,09 (s, 6H).
[0456] (Ссылочный пример 5)
трет-Бутил{[2-фтор-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил]окси}диметилсилан (ссылочное соединение 5)

Раствор в 1,4-диоксане (100 мл) [(3-бром-2-фторбензил)окси](трет-бутил)диметилсилана, 14,4 г (45,0 ммоль), синтезированного таким же образом, как в ссылочном примере 4, бис(пинаколато)диборана, 12,6 г (49,6 ммоль), и ацетата калия, 6,00 г (61,1 ммоль), дегазировали и продували азотом. Затем добавляли [1,1'-бис(дифенилфосфино)ферроцен]палладия(II) дихлорид, 1,84 г (2,25 ммоль). Смесь перемешивали под струей аргона при 100°C в течение 20 часов. После окончания реакции реакционную смесь фильтровали через целит, добавляли воду, и затем экстрагировали этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 9,64 г (26,3 ммоль, выход 43%) в виде светло-желтого масла.
Масс-спектр (CI, m/z): 367[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,60-7,52 (m, 2H), 7,25-7,17 (m, 1H), 4,74 (s, 2H), 1,29 (s, 12H), 0,90 (s, 9H), 0,09 (s, 6H).
[0457] (Ссылочный пример 6-1)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1)

Суспензию в 1,2-диметоксиэтане (70 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксима, 2,00 г (7,78 ммоль), синтезированного таким же образом, как в ссылочном примере 3-1, трет-бутил{[2-фтор-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил]окси}диметилсилана, 2,85 г (7,78 ммоль), синтезированного таким же образом, как в ссылочном примере 5, и 2 М водного раствора карбоната натрия, 12 мл (24 ммоль), дегазировали и продували азотом. Затем добавляли тетракис(трифенилфосфин)палладий (0) 1,35 г (1,17 ммоль). Смесь перемешивали под струей аргона при 80°C в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:этилацетат) с получением указанного в заголовке соединения в количестве 2,75 г (6,60 ммоль, выход 85%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 417[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,4 Гц, 2H), 7,55-7,42 (m, 2H), 7,35-7,27 (m, 1H), 4,84-4,78 (m, 6H), 3,83 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0458] (Ссылочный пример 6-2)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-этилоксим, синтезированный таким же образом, как в ссылочном примере 8. В результате указанное в заголовке соединение (выход 82%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 431[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,5 Гц, 2H), 7,53-7,42 (m, 2H), 7,35-7,29 (m, 1H), 4,85-4,77 (m, 6H), 4,08 (q, J=7,0 Гц, 2H), 1,22 (t, J=7,0 Гц, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0459] (Ссылочный пример 6-3)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метил-d3-оксим (ссылочное соединение 6-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метил-d3-оксим, синтезированный таким же образом, как в ссылочном примере 10-1. В результате указанное в заголовке соединение (выход 77%) было получено в виде серого твердого вещества.
Масс-спектр (CI, m/z): 420[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,4 Гц, 2H), 7,52-7,42 (m, 2H), 7,35-7,27 (m, 1H), 4,85-4,77 (m, 6H), 0,91 (s, 9H), 0,11 (s, 6H).
[0460] (Ссылочный пример 6-4)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2-фторэтил)оксим (ссылочное соединение 6-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(2-фторэтил)оксим, синтезированный таким же образом, как в ссылочном примере 10-2. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 449[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,0 Гц, 2H), 7,56-7,47 (m, 1H), 7,31-7,19 (m, 2H), 4,93-4,87 (m, 4H), 4,85 (s, 2H), 4,75-4,59 (m, 2H), 4,40-4,28 (m, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0461] (Ссылочный пример 6-5)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она оксим (ссылочное соединение 6-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она оксим, синтезированный таким же образом, как в ссылочном примере 9-1. В результате указанное в заголовке соединение (выход 83%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 403[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,5 Гц, 2H), 7,54-7,48 (m, 1H), 7,30-7,20 (m, 2H), 7,15 (s, 1H), 4,95-4,88 (m, 4H), 4,85 (s, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0462] (Ссылочный пример 6-6)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-фторпропил)оксим (ссылочное соединение 6-6)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-фторпропил)оксим, синтезированный таким же образом, как в ссылочном примере 10-3. В результате указанное в заголовке соединение (выход 70%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 463[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,53-7,43 (m, 2H), 7,36-7,26 (m, 1H), 4,85-4,79 (m, 6H), 4,53 (td, J=6,0, 47,3 Гц, 2H), 4,13 (t, J=6,3 Гц, 2H), 2,08-1,93 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0463] (Ссылочный пример 6-7)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-{2-[(тетрагидропиран-2-ил)окси]этил}оксим (ссылочное соединение 6-7)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-{2-[(тетрагидропиран-2-ил)окси]этил}оксим, синтезированный таким же образом, как в ссылочном примере 10-4, и температуру реакции изменяли на 85°C. В результате указанное в заголовке соединение (выход 72%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 531[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,54-7,41 (m, 2H), 7,38-7,22 (m, 1H), 4,88-4,77 (m, 6H), 4,63-4,58 (m, 1H), 4,22-4,12 (m, 2H), 3,87-3,70 (m, 2H), 3,67-3,57 (m, 1H), 3,49-3,38 (m, 1H), 1,81-1,41 (m, 6H), 0,91 (s, 9H), 0,11 (s, 6H).
[0464] (Ссылочный пример 6-8)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-{3-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 6-8)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-{3-[(тетрагидропиран-2-ил)окси]пропил}оксим, синтезированный таким же образом, как в ссылочном примере 10-5. В результате указанное в заголовке соединение (выход 66%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 545[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,52-7,44 (m, 2H), 7,35-7,28 (m, 1H), 4,89-4,73 (m, 6H), 4,59-4,51 (m, 1H), 4,18-4,05 (m, 2H), 3,80-3,63 (m, 2H), 3,48-3,37 (m, 2H), 1,91-1,79 (m, 2H), 1,78-1,39 (m, 6H), 0,91 (s, 9H), 0,11 (s, 6H).
[0465] (Ссылочный пример 6-9)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-{4-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 6-9)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-{4-[(тетрагидропиран-2-ил)окси]бутил}оксим, синтезированный таким же образом, как в ссылочном примере 10-6. В результате указанное в заголовке соединение (выход 93%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 559[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,56 (d, J=1,4 Гц, 2H), 7,54-7,46 (m, 1H), 7,30-7,19 (m, 2H), 4,89-4,86 (m, 4H), 4,85 (s, 2H), 4,61-4,56 (m, 1H), 4,20-4,10 (m, 2H), 3,92-3,73 (m, 2H), 3,55-3,37 (m, 2H), 1,88-1,47 (m, 10H), 0,96 (s, 9H), 0,14 (s, 6H).
[0466] (Ссылочный пример 6-10)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2-метоксиэтил)оксим (ссылочное соединение 6-10)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(2-метоксиэтил)оксим, синтезированный таким же образом, как в ссылочном примере 10-7, и температуру реакции изменяли на 85°C. В результате указанное в заголовке соединение (выход 66%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 461[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,55-7,42 (m, 2H), 7,37-7,20 (m, 1H), 4,85-4,78 (m, 6H), 4,16-4,13 (m, 2H), 3,58-3,54 (m, 2H), 3,27 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0467] (Ссылочный пример 6-11)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2-{2-[(тетрагидропиран-2-ил)окси]этокси}этил)оксим (ссылочное соединение 6-11)
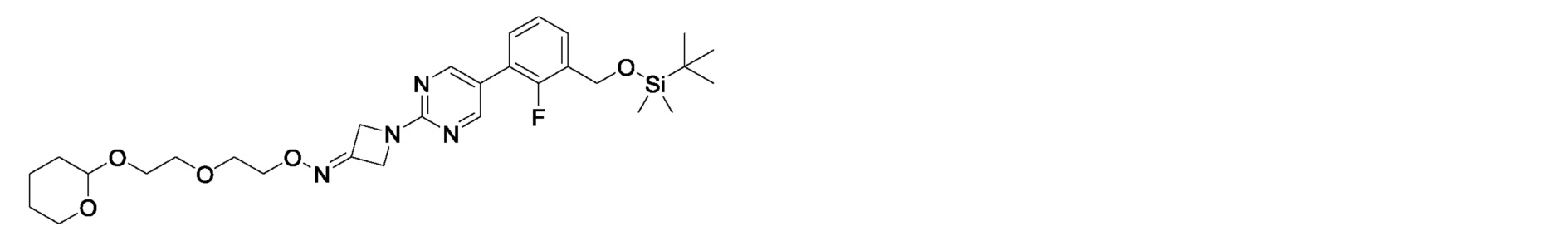
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(2-{2-[(тетрагидропиран-2-ил)окси]этокси}этил)оксим, синтезированный таким же образом, как в ссылочном примере 16. В результате указанное в заголовке соединение (выход 80%) было получено в виде желтого масла.
Масс-спектр (CI, m/z): 575[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,56 (d, J=1,5 Гц, 2H), 7,54-7,47 (m, 1H), 7,29-7,19 (m, 2H), 4,91-4,87 (m, 4H), 4,85 (s, 2H), 4,67-4,63 (m, 1H), 4,29-4,24 (m, 2H), 3,91-3,84 (m, 2H), 3,80-3,76 (m, 2H), 3,72-3,68 (m, 2H), 3,66-3,59 (m, 1H), 3,54-3,47(m, 1H), 1,90-1,41 (m, 6H), 0,96 (s, 9H), 0,14 (s, 6H).
[0468] (Ссылочный пример 6-12)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим (ссылочное соединение 6-12)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 10-8. В результате указанное в заголовке соединение (выход 89%) было получено в виде белого твердого вещества.
[0469] (Ссылочный пример 6-13)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим (ссылочное соединение 6-13)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 10-9. В результате указанное в заголовке соединение (выход 94%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 517[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,53-7,42 (m, 2H), 7,36-7,27 (m, 1H), 4,85-4,78 (m, 6H), 4,34-4,26 (m, 1H), 4,10-4,01 (m, 3H), 3,68 (dd, J=6,4, 8,4 Гц, 1H), 1,33 (s, 3H), 1,28 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0470] (Ссылочный пример 6-14)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-метокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 6-14)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-метокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим, синтезированный таким же образом, как в ссылочном примере 19-1. В результате указанное в заголовке соединение (выход 85%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 589[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,59-7,40 (m, 2H), 7,37-7,26 (m, 1H), 4,86-4,77 (m, 6H), 4,60-4,33 (m, 1H), 4,16-4,01 (m, 2H), 3,80-3,63 (m, 2H), 3,48-3,33 (m, 4H), 3,24 (s, 3H), 2,27-2,13 (m, 1H), 1,81-1,36 (m, 6H), 0,91 (s, 9H), 0,11 (s, 6H).
[0471] (Ссылочный пример 6-15)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-метокси-3-(тритилокси)пропил]оксим (ссылочное соединение 6-15)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[2-метокси-3-(тритилокси)пропил]оксим, синтезированный таким же образом, как в ссылочном примере 19-2. В результате указанное в заголовке соединение (выход 84%) было получено в виде светло-желтой пены.
Масс-спектр (CI, m/z): 733[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,65 (d, J=1,5 Гц, 2H), 7,52-7,21 (m, 18H), 4,87-4,76 (m, 4H), 4,75-4,53 (m, 2H), 4,21-4,05 (m, 2H), 3,67-3,58 (m, 1H), 3,34 (s, 3H), 3,18-2,98 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0472] (Ссылочный пример 6-16)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксим (ссылочное соединение 6-16)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 10-10. В результате указанное в заголовке соединение (выход 98%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 531[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,52-7,43 (m, 2H), 7,38-7,24 (m, 1H), 4,85-4,77 (m, 6H), 4,18-4,05 (m, 3H), 4,02 (dd, J=6,1, 8,0 Гц, 1H), 3,49 (dd, J=7,3, 8,0 Гц, 1H), 1,91-1,79 (m, 2H), 1,31 (s, 3H), 1,27 (s, 3H), 0,90 (s, 9H), 0,11 (s, 6H).
[0473] (Ссылочный пример 6-17)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-фтор-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 6-17)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-фтор-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим, синтезированный таким же образом, как в ссылочном примере 23. В результате указанное в заголовке соединение (выход 97%) было получено в виде светло-желтого масла.
Масс-спектр (ESI, m/z): 577[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,54-7,39 (m, 2H), 7,37-7,26 (m, 1H), 4,86-4,79 (m, 6H), 4,65-4,41 (m, 3H), 4,17-4,07 (m, 2H), 3,78-3,67 (m, 2H), 3,48-3,38 (m, 2H), 2,43-2,30 (m, 1H), 1,77-1,57 (m, 2H), 1,53-1,41 (m, 4H), 0,91 (s, 9H), 0,11 (s, 6H).
[0474] (Ссылочный пример 6-18)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-фтор-3-(тритилокси)пропил]оксим (ссылочное соединение 6-18)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[2-фтор-3-(тритилокси)пропил]оксим, синтезированный таким же образом, как в ссылочном примере 24-1. В результате указанное в заголовке соединение (выход 60%) было получено в виде белой пены.
Масс-спектр (ESI, m/z): 721[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (d, J=1,4 Гц, 2H), 7,51-7,24 (m, 18H), 5,03-4,84 (m, 1H), 4,83-4,78 (m, 4H), 4,76-4,59 (m, 2H), 4,42-4,15 (m, 2H), 3,33-3,13 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0475] (Ссылочный пример 6-19)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-{3-метокси-4-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 6-19)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-{3-метокси-4-[(тетрагидропиран-2-ил)окси]бутил}оксим, синтезированный таким же образом, как в ссылочном примере 19-3, и температуру реакции изменяли на 70°C. В результате указанное в заголовке соединение (выход 92%) было получено в виде светло-желтого масла.
Масс-спектр (ESI, m/z): 589[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,31-7,18 (m, 2H), 4,91-4,86 (m, 4H), 4,85 (s, 2H), 4,68-4,60 (m, 1H), 4,27-4,18 (m, 2H), 3,92-3,83 (m, 1H), 3,83-3,73 (m, 1H), 3,58-3,37 (m, 6H), 2,03-1,46 (m, 8H), 0,96 (s, 9H), 0,14 (s, 6H).
[0476] (Ссылочный пример 6-20)
4-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутан-1,2-диилдиацетат (ссылочное соединение 6-20)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 4-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)бутан-1,2-диилдиацетат, синтезированный таким же образом, как в ссылочном примере 25, и температуру реакции изменяли на 70°C. В результате указанное в заголовке соединение (выход 35%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (ESI, m/z): 575[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,56 (d, J=1,4 Гц, 2H), 7,54-7,47 (m, 1H), 7,30-7,19 (m, 2H), 5,24-5,17 (m, 1H), 4,87 (s, 4H), 4,85 (s, 2H), 4,29 (dd, J=3,3, 12,0 Гц, 1H), 4,22-4,12 (m, 2H), 4,09 (dd, J=6,2, 12,0 Гц, 1H), 2,08 (s, 3H), 2,07 (s, 3H), 2,06-1,94 (m, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0477] (Ссылочный пример 6-21)
2-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилацетат (ссылочное соединение 6-21)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 2-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)этилацетат, синтезированный таким же образом, как в ссылочном примере 10-11. В результате указанное в заголовке соединение (выход 80%) было получено в виде бесцветного масла.
Масс-спектр (ESI, m/z): 489[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,31-7,19 (m, 2H), 4,94-4,87 (m, 4H), 4,85 (s, 2H), 4,38-4,25 (m, 4H), 2,10 (s, 3H), 0,96 (s, 9H), 0,14 (s, 6H).
[0478] (Ссылочный пример 6-22)
2-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилпропионат (ссылочное соединение 6-22)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 2-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)этилпропионат, синтезированный таким же образом, как в ссылочном примере 28-1. В результате указанное в заголовке соединение (выход 38%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 503[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,56-7,46 (m, 1H), 7,32-7,18 (m, 2H), 4,90-4,86 (m, 4H), 4,85 (s, 2H), 4,36-4,27 (m, 4H), 2,38 (q, J=7,6 Гц, 2H), 1,16 (t, J=7,6 Гц, 3H), 0,96 (s, 9H), 0,14 (s, 6H).
[0479] (Ссылочный пример 6-23)
2-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилбутират (ссылочное соединение 6-23)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 2-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)этилбутират, синтезированный таким же образом, как в ссылочном примере 28-2, и продукт очищали разделением с помощью ВЭЖХ. В результате указанное в заголовке соединение (выход 65%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 517[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,54-7,48 (m, 1H), 7,29-7,20 (m, 2H), 4,91-4,86 (m, 4H), 4,85 (s, 2H), 4,36-4,26 (m, 4H), 2,33 (t, J=7,4 Гц, 2H), 1,67 (sext, J=7,4 Гц, 2H), 0,99-0,93 (m, 12H), 0,14 (s, 6H).
[0480] (Ссылочный пример 6-24)
2-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилбензоат (ссылочное соединение 6-24)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 2-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)этилбензоат, синтезированный таким же образом, как в ссылочном примере 28-3. В результате указанное в заголовке соединение (выход 72%) было получено в виде светло-желтого масла.
Ссылочное соединение 6-24
Масс-спектр (CI, m/z): 551[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,56 (d, J=1,4 Гц, 2H), 8,12-7,97 (m, 2H), 7,60-7,54 (m, 1H), 7,53-7,42 (m, 3H), 7,28-7,22 (m, 2H), 4,88 (s, 4H), 4,85 (s, 2H), 4,62-4,51 (m, 2H), 4,47-4,39 (m, 2H), 0,96 (s, 9H), 0,13 (s, 6H).
[0481] (Ссылочный пример 6-25)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 6-25)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим, синтезированный таким же образом, как в ссылочном примере 18-1. В результате указанное в заголовке соединение (выход 91%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 575[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,54-7,48 (m, 1H), 7,29-7,20 (m, 2H), 4,89-4,86 (m, 4H), 4,85 (s, 2H), 4,62-4,57 (m, 1H), 4,27-4,16 (m, 2H), 3,92-3,70 (m, 4H), 3,63-3,49(m, 2H), 2,56-2,46 (m, 1H), 2,34-2,23 (m, 1H), 1,84-1,48 (m, 6H), 0,96 (s, 9H), 0,14 (s, 6H).
[0482] (Ссылочный пример 6-26)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-фторпиридин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-26)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 33-1. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 434[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,17-8,14 (m, 1H), 7,53-7,43 (m, 2H), 7,31-7,18 (m, 2H), 4,90-4,88 (m, 4H), 4,84 (s, 2H), 3,91 (s, 3H), 0,96 (s, 9H), 0,13 (s, 6H).
[0483] (Ссылочный пример 6-27)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-фторпиридин-2-ил]азетидин-3-она O-метил-d3-оксим (ссылочное соединение 6-27)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-она O-метил-d3-оксим, синтезированный таким же образом, как в ссылочном примере 33-2. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 437[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,17-8,13 (m, 1H), 7,53-7,43 (m, 2H), 7,31-7,24 (m, 1H), 7,24-7,16 (m, 1H), 4,91-4,87 (m, 4H), 4,84 (s, 2H), 0,96 (s, 9H), 0,13 (s, 6H).
[0484] (Ссылочный пример 6-28)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-фторпиридин-2-ил]азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксим (ссылочное соединение 6-28)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 34-1. В результате указанное в заголовке соединение (включая примеси) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 548[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,17-8,13 (m, 1H), 7,53-7,42 (m, 2H), 7,31-7,17 (m, 2H), 4,91-4,88 (m, 4H), 4,84 (s, 2H), 4,26-4,15 (m, 3H), 4,12-4,06 (m, 1H), 3,61-3,55 (m, 1H), 2,01-1,92 (m, 2H), 1,42 (s, 3H), 1,37 (s, 3H), 0,96 (s, 9H), 0,13 (s, 6H).
[0485] (Ссылочный пример 6-29)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-фторпиридин-2-ил]азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим (ссылочное соединение 6-29)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 34-2. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 548[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,17-8,14 (m, 1H), 7,76-7,18 (m, 4H), 4,91-4,87 (m, 4H), 4,85 (s, 2H), 4,18 (d, J=6,9 Гц, 2H), 4,01 (dd, J=4,0, 12,0 Гц, 2H), 3,76 (dd, J=5,9, 12,0 Гц, 2H), 2,14-2,06 (m, 1H), 1,45 (s, 3H), 1,42 (s, 3H), 0,96 (s, 9H), 0,14 (s, 6H).
[0486] (Ссылочный пример 6-30)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-фторпиридин-2-ил]азетидин-3-она O-[2-фтор-3-(тритилокси)пропил]оксим (ссылочное соединение 6-30)
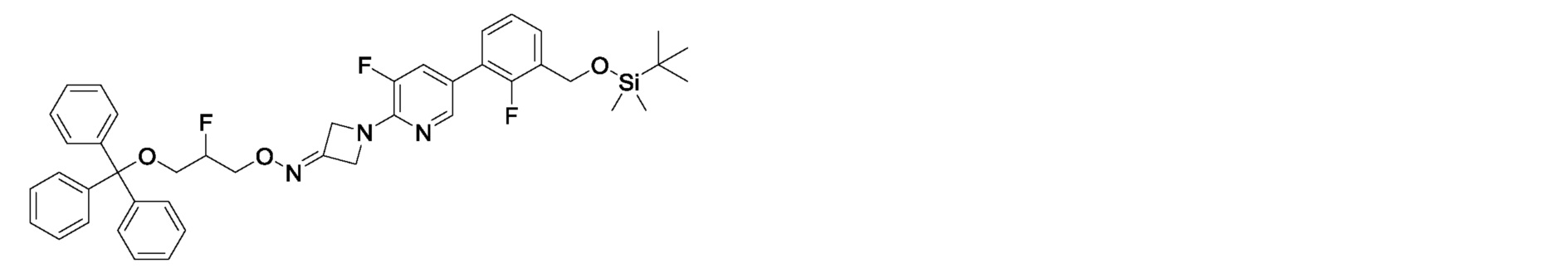
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-она O-[2-фтор-3-(тритилокси)пропил]оксим, синтезированный таким же образом, как в ссылочном примере 24-2. В результате указанное в заголовке соединение (выход 81%) было получено в виде бесцветной пены.
Масс-спектр (CI, m/z): 738[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,21-8,18 (m, 1H), 7,79-7,73 (m, 1H), 7,51-7,17 (m, 18H), 5,02-4,67 (m, 7H), 4,39-4,14 (m, 2H), 3,31-3,13 (m, 2H), 0,91(s, 9H), 0,11 (s, 6H).
[0487] (Ссылочный пример 6-31)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиридин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-31)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиридин-2-ил)азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 3-2. В результате указанное в заголовке соединение (выход 97%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 416[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,32-8,29 (m, 1H), 7,80-7,75 (m, 1H), 7,45-7,39 (m, 2H), 7,31-7,25 (m, 1H), 6,69-6,65 (m, 1H), 4,81 (s, 2H), 4,76-4,65 (m, 4H), 3,82 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0488] (Ссылочный пример 6-32)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-метилпиридин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-32)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бром-3-метилпиридин-2-ил)азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 3-3. В результате указанное в заголовке соединение (выход 58%) было получено в виде желтого масла.
Масс-спектр (ESI, m/z): 430[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,27-8,23 (m, 1H), 7,53-7,49 (m, 1H), 7,49-7,43 (m, 1H), 7,31-7,24 (m, 1H), 7,23-7,16 (m, 1H), 4,89-4,82 (m, 6H), 3,90 (s, 3H), 2,27 (s, 3H), 0,96 (s, 9H), 0,13 (s, 6H).
[0489] (Ссылочный пример 6-33)
5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-2-[3-(метоксиимино)азетидин-1-ил]никотинонитрил (ссылочное соединение 6-33)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 5-бром-2-[3-(метоксиимино)азетидин-1-ил]никотинонитрил, синтезированный таким же образом, как в ссылочном примере 39, и температуру реакции изменяли на 85°C. В результате указанное в заголовке соединение (выход 50%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 441[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,58-8,54 (m, 1H), 8,24 (dd, J=0,9, 2,3 Гц, 1H), 7,54-7,41 (m, 2H), 7,36-7,25 (m, 1H), 5,06-4,96 (m, 4H), 4,80 (s, 2H), 3,83 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0490] (Ссылочный пример 6-34)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-хлорпиридин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-34)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бром-3-хлорпиридин-2-ил)азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 3-4. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 450[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,29-8,27 (m, 1H), 7,74-7,71 (m, 1H), 7,52-7,46 (m, 1H), 7,29-7,18 (m, 2H), 4,99-4,94 (m, 4H), 4,84 (s, 2H), 3,90 (s, 3H), 0,96 (s, 9H), 0,13 (s, 6H).
[0491] (Ссылочный пример 6-35)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-(дифторметил)пиридин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-35)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-[5-бром-3-(дифторметил)пиридин-2-ил]азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 3-5. В результате указанное в заголовке соединение (выход 89%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 466[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,51-8,47 (m, 1H), 8,00-7,97 (m, 1H), 7,50-7,43 (m, 2H), 7,36-6,99 (m, 2H), 4,93-4,86 (m, 4H), 4,81 (s, 2H), 3,83 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0492] (Ссылочный пример 6-36)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-циклопропилпиридин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-36)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бром-3-циклопропилпиридин-2-ил)азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 3-6. В результате указанное в заголовке соединение (выход 90%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 456[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,18-8,15 (m, 1H), 7,44-7,38 (m, 3H), 7,31-7,23 (m, 1H), 4,94-4,90 (m, 4H), 4,80 (s, 2H), 3,81 (s, 3H), 1,94-1,86 (m, 1H), 0,98-0,85 (m, 11H), 0,75-0,69 (m, 2H), 0,11 (s, 6H).
[0493] (Ссылочный пример 6-37)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-этилпиридин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-37)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бром-3-этилпиридин-2-ил)азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 3-7. В результате указанное в заголовке соединение (выход 83%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 444[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,22-8,17 (m, 1H), 7,61-7,59 (m, 1H), 7,46-7,40 (m, 2H), 7,32-7,25 (m, 1H), 4,85-4,79 (m, 6H), 3,81 (s, 3H), 2,63-2,53 (m, 2H), 1,19 (t, J=7,4 Гц, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0494] (Ссылочный пример 6-38)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-38)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бром-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-2-ил)азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 51. В результате указанное в заголовке соединение (выход 85%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 558[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,32-8,28 (m, 1H), 7,82-7,75 (m, 1H), 7,56-7,37 (m, 2H), 7,35-7,24 (m, 1H), 4,87-4,80 (m, 6H), 4,54-4,50 (m, 1H), 3,85-3,72 (m, 4H), 3,40-3,23 (m, 1H), 1,83-1,28 (m, 12H), 0,91 (s, 9H), 0,11 (s, 6H).
[0495] (Ссылочный пример 6-39)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-(метоксиметил)пиридин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-39)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-[5-бром-3-(метоксиметил)пиридин-2-ил]азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 3-8. В результате указанное в заголовке соединение (выход 81%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 460[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,31-8,25 (m, 1H), 7,76-7,70 (m, 1H), 7,49-7,38 (m, 2H), 7,34-7,24 (m, 1H), 4,89-4,84 (m, 4H), 4,81 (s, 2H), 4,39 (s, 2H), 3,81 (s, 3H), 3,33 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0496] (Ссылочный пример 6-40)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-3-метоксипиридин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-40)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бром-3-метоксипиридин-2-ил)азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 57. В результате указанное в заголовке соединение (включая примеси) было получено в виде желтого масла.
Масс-спектр (ESI, m/z): 446[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,92-7,89 (m, 1H), 7,50-7,40 (m, 2H), 7,34-7,26 (m, 2H), 4,81 (s, 2H), 4,79-4,74 (m, 4H), 3,82 (s, 3H), 3,80 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0497] (Ссылочный пример 6-41)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-он (ссылочное соединение 6-41)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-он, синтезированный таким же образом, как в ссылочном примере 59. В результате указанное в заголовке соединение (выход 91%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 416[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,53-7,41 (m, 2H), 7,37-7,24 (m, 1H), 4,82 (s, 2H), 4,14-4,07 (m, 4H), 2,48-2,43 (m, 4H), 0,92 (s, 9H), 0,11 (s, 6H).
[0498] (Ссылочный пример 6-42)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{3-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 6-42)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-{3-[(тетрагидропиран-2-ил)окси]пропил}оксим, синтезированный таким же образом, как в ссылочном примере 67-1. В результате указанное в заголовке соединение (выход 72%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 573[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,52-7,38 (m, 2H), 7,34-7,26 (m, 1H), 4,83 (s, 2H), 4,57-4,54 (m, 1H), 4,08-4,02 (m, 2H), 3,97-3,87 (m, 4H), 3,76-3,62 (m, 2H), 3,47-3,35 (m, 2H), 2,61-2,54 (m, 2H), 2,42-2,36 (m, 2H), 1,93-1,32 (m, 8H), 0,91 (s, 9H), 0,11 (s, 6H).
[0499] (Ссылочный пример 6-43)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{4-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 6-43)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-{4-[(тетрагидропиран-2-ил)окси]бутил}оксим, синтезированный таким же образом, как в ссылочном примере 67-2. В результате указанное в заголовке соединение (выход 80%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 587[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,53-7,41 (m, 2H), 7,34-7,24 (m, 1H), 4,81 (s, 2H), 4,64-4,47 (m, 1H), 4,02-3,96 (m, 2H), 3,95-3,86 (m, 4H), 3,77-3,57 (m, 2H), 3,46-3,34 (m, 2H), 2,60-2,54 (m, 2H), 2,41-2,35 (m, 2H), 1,86-1,36 (m, 10H), 0,91 (s, 9H), 0,11 (s, 6H).
[0500] (Ссылочный пример 6-44)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-(2-метоксиэтил)оксим (ссылочное соединение 6-44)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-(2-метоксиэтил)оксим, синтезированный таким же образом, как в ссылочном примере 67-3, и температуру реакции изменяли на 85°C. В результате указанное в заголовке соединение (выход 75%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 489[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,51-7,39 (m, 2H), 7,34-7,23 (m, 1H), 4,83 (s, 2H), 4,13-4,05 (m, 2H), 3,98-3,89 (m, 4H), 3,59-3,50 (m, 2H), 3,26 (s, 3H), 2,62-2,54 (m, 2H), 2,40-2,35 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0501] (Ссылочный пример 6-45)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{2,2-диметил-3-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 6-45)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-{2,2-диметил-3-[(тетрагидропиран-2-ил)окси]пропил}оксим, синтезированный таким же образом, как в ссылочном примере 67-4. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 601[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,5 Гц, 2H), 7,51-7,45 (m, 1H), 7,30-7,18 (m, 2H), 4,85 (s, 2H), 4,60-4,56 (m, 1H), 4,03-3,97 (m, 4H), 3,93-3,91 (m, 2H), 3,90-3,80 (m, 1H), 3,56 (d, J=9,3 Гц, 1H), 3,53-3,45 (m, 1H), 3,12 (d, J=9,3 Гц, 1H), 2,73-2,67 (m, 2H), 2,50-2,43 (m, 2H), 1,90-1,46 (m, 6H), 0,98 (s, 3H), 0,97 (s, 3H), 0,96 (s, 9H), 0,14 (s, 6H).
[0502] (Ссылочный пример 6-46)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{3-метил-3-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 6-46)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-{3-метил-3-[(тетрагидропиран-2-ил)окси]бутил}оксим, синтезированный таким же образом, как в ссылочном примере 69-1. В результате указанное в заголовке соединение (выход 84%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 601[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,52 (d, J=1,5 Гц, 2H), 7,51-7,45 (m, 1H), 7,31-7,18 (m, 2H), 4,85 (s, 2H), 4,81-4,75 (m, 1H), 4,24-4,16 (m, 2H), 4,04-3,92 (m, 5H), 3,57-3,38 (m, 1H), 2,70-2,64 (m, 2H), 2,49-2,44 (m, 2H), 1,97-1,80 (m, 3H), 1,72-1,41 (m, 5H), 1,28 (s, 3H), 1,26 (s, 3H), 0,96 (s, 9H), 0,14 (s, 6H).
[0503] (Ссылочный пример 6-47)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{2-метил-3-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 6-47)
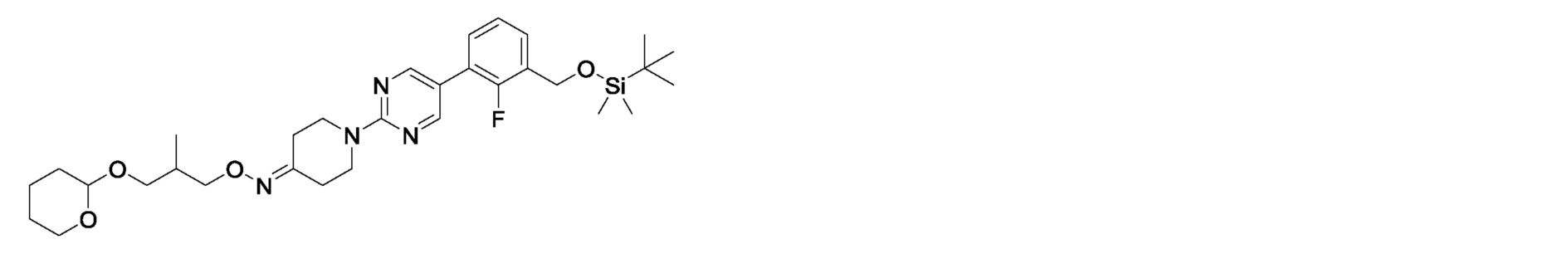
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-{2-метил-3-[(тетрагидропиран-2-ил)окси]пропил}оксим, синтезированный таким же образом, как в ссылочном примере 67-6. В результате указанное в заголовке соединение (включая примеси) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 587[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,4 Гц, 2H), 7,51-7,44 (m, 1H), 7,30-7,18 (m, 2H), 4,85 (s, 2H), 4,61-4,55 (m, 1H), 4,22-3,23 (m, 10H), 2,72-2,65 (m, 2H), 2,50-2,44 (m, 2H), 2,23-2,10 (m, 1H), 1,88-1,46 (m, 6H), 1,04-0,98 (m, 3H), 0,96 (s, 9H), 0,14 (s, 6H).
[0504] (Ссылочный пример 6-48)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим (ссылочное соединение 6-48)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 67-7. В результате указанное в заголовке соединение (выход 96%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 559[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,4 Гц, 2H), 7,51-7,45 (m, 1H), 7,30-7,18 (m, 2H), 4,85 (s, 2H), 4,16-4,07 (m, 2H), 4,04-3,95 (m, 6H), 3,77 (dd, J=6,5, 11,9 Гц, 2H), 2,70-2,64 (m, 2H), 2,48-2,42 (m, 2H), 2,19-2,10 (m, 1H), 1,44 (s, 3H), 1,42 (s, 3H), 0,96 (s, 9H), 0,14 (s, 6H).
[0505] (Ссылочный пример 6-49)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[(2,2,5-триметил-1,3-диоксан-5-ил)метил]оксим (ссылочное соединение 6-49)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-[(2,2,5-триметил-1,3-диоксан-5-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 67-8. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 346[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,4 Гц, 2H), 7,51-7,45 (m, 1H), 7,29-7,18 (m, 2H), 4,85 (s, 2H), 4,11 (s, 2H), 4,03-3,97 (m, 4H), 3,78-3,73 (m, 2H), 3,60-3,55 (m, 2H), 2,71-2,66 (m, 2H), 2,49-2,45 (m, 2H), 1,44 (s, 3H), 1,42 (s, 3H), 0,96 (s, 9H), 0,95 (s, 3H), 0,14 (s, 6H).
[0506] (Ссылочный пример 6-50)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим (ссылочное соединение 6-50)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 67-9. В результате указанное в заголовке соединение (выход 80%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 545[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,52-7,40 (m, 2H), 7,37-7,28 (m, 1H), 4,81 (s, 2H), 4,34-4,19 (m, 1H), 4,06-3,98 (m, 3H), 3,96-3,88 (m, 4H), 3,67 (dd, J=6,5, 8,3 Гц, 1H), 2,62-2,55 (m, 2H), 2,42-2,32 (m, 2H), 1,33 (s, 3H), 1,28 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0507] (Ссылочный пример 6-51)
2-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этилацетат (ссылочное соединение 6-51)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этилацетат, синтезированный таким же образом, как в ссылочном примере 29-3. В результате указанное в заголовке соединение (выход 85%) было получено в виде светло-коричневого твердого вещества.
Масс-спектр (CI, m/z): 517[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,52-7,41 (m, 2H), 7,35-7,24 (m, 1H), 4,81 (s, 2H), 4,31-4,12 (m, 4H), 3,97-3,86 (m, 4H), 2,62-2,55 (m, 2H), 2,43-2,34 (m, 2H), 2,03 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0508] (Ссылочный пример 6-52)
трет-Бутил-2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]ацетат (ссылочное соединение 6-52)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на трет-бутил-2-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)ацетат, синтезированный таким же образом, как в ссылочном примере 10-12. В результате указанное в заголовке соединение (включая примеси) было получено в виде желтого масла.
Масс-спектр (CI, m/z): 517[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,55-7,47 (m, 1H), 7,29-7,20 (m, 2H), 4,99-4,89 (m, 4H), 4,85 (s, 2H), 4,52 (s, 2H), 1,50 (s, 9H), 0,96 (s, 9H), 0,14 (s, 6H).
[0509] (Ссылочный пример 6-53)
2-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-N-метилацетамид (ссылочное соединение 6-53)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 2-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)-N-метилацетамид, синтезированный таким же образом, как в ссылочном примере 77. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 474[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,58 (d, J=1,4 Гц, 2H), 7,58-7,43 (m, 1H), 7,29-7,21 (m, 2H), 6,16 (br s, 1H), 4,85 (s, 2H), 4,58 (s, 2H), 2,91 (d, J=4,9 Гц, 3H), 0,96 (s, 9H), 0,14 (s, 6H).
[0510] (Ссылочный пример 6-54)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]пропанамид (ссылочное соединение 6-54)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 3-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)пропанамид, синтезированный таким же образом, как в ссылочном примере 78-1. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 474[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,52-7,43 (m, 2H), 7,37 (br s, 1H), 7,34-7,27 (m, 1H), 6,87 (br s, 1H), 4,87-4,72 (m, 6H), 4,22 (t, J=6,5 Гц, 2H), 2,42 (t, J=6,5 Гц, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0511] (Ссылочный пример 6-55)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-N-метилпропанамид (ссылочное соединение 6-55)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 3-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)-N-метилпропанамид, синтезированный таким же образом, как в ссылочном примере 78-2. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 488[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,90-7,77 (m, 1H), 7,52-7,42 (m, 2H), 7,36-7,25 (m, 1H), 4,87-4,71 (m, 6H), 4,22 (t, J=6,5 Гц, 2H), 2,57 (d, J=4,5 Гц, 3H), 2,43 (t, J=6,5 Гц, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0512] (Ссылочный пример 6-56)
Этил-4-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутаноат (ссылочное соединение 6-56)
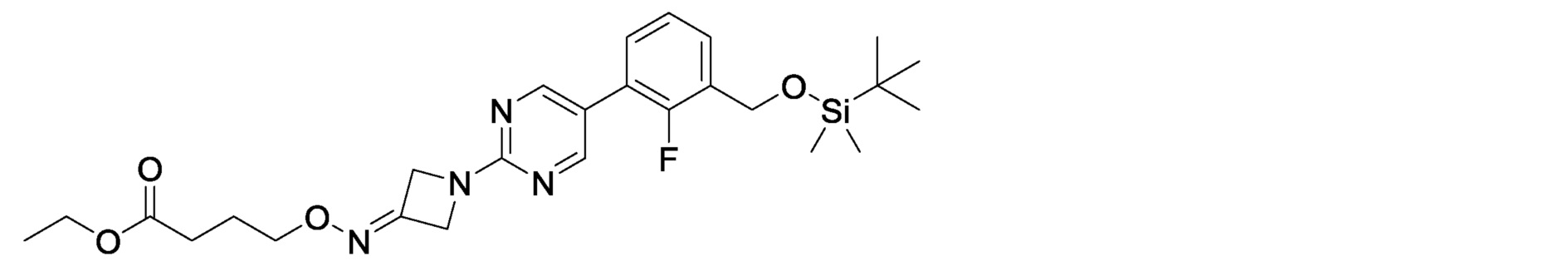
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на этил-4-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)бутаноат, синтезированный таким же образом, как в ссылочном примере 10-13. В результате указанное в заголовке соединение (выход 86%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 517[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,54-7,43 (m, 2H), 7,35-7,27 (m, 1H), 4,85-4,77 (m, 6H), 4,10-4,01 (m, 4H), 2,38 (t, J=7,4 Гц, 2H), 1,93-1,82 (m, 2H), 1,18 (t, J=7,2 Гц, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0513] (Ссылочный пример 6-57)
4-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-N-метилбутанамид (ссылочное соединение 6-57)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 4-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)-N-метилбутанамид, синтезированный таким же образом, как в ссылочном примере 80. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 502[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,5 Гц, 2H), 7,58-7,43 (m, 1H), 7,29-7,20 (m, 2H), 5,48 (br s, 1H), 4,91-4,82 (m, 6H), 4,13 (t, J=6,1 Гц, 2H), 2,83 (d, J=4,8 Гц, 3H), 2,28 (t, J=7,4 Гц, 2H), 2,08-1,99 (m, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0514] (Ссылочный пример 6-58)
2-{3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропил}изоиндолин-1,3-дион (ссылочное соединение 6-58)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 2-[3-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)-2-{[(тетрагидропиран-2-ил)окси]метил}пропил]изоиндолин-1,3-дион, синтезированный таким же образом, как в ссылочном примере 85-1. В результате указанное в заголовке соединение (выход 73%) было получено в виде желтого масла.
Масс-спектр (EI, m/z): 703[М]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,3 Гц, 2H), 7,88-7,83 (m, 2H), 7,80-7,74 (m, 2H), 7,52-7,44 (m, 2H), 7,35-7,29 (m, 1H), 4,82 (s,2H), 4,77-4,62 (m, 2H), 4,57-4,46 (m, 3H), 4,17-4,04 (m, 2H), 3,76-3,60 (m, 4H), 3,43-3,35 (m, 2H), 2,60-2,47 (m, 1H), 1,70-1,22 (m, 6H), 0,91 (s, 9H), 0,11 (s, 6H).
[0515] (Ссылочный пример 6-59)
2-{3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-метоксипропил}изоиндолин-1,3-дион (ссылочное соединение 6-59)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 2-[3-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)-2-метоксипропил]изоиндолин-1,3-дион, синтезированный таким же образом, как в ссылочном примере 85-2. В результате указанное в заголовке соединение (выход 80%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 620[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,63 (d, J=1,4 Гц, 2H), 7,91-7,85 (m, 2H), 7,85-7,80 (m, 2H), 7,55-7,41 (m, 2H), 7,37-7,24 (m, 1H), 4,82 (s, 2H),4,79-4,68 (m, 4H), 4,17-4,07 (m, 2H), 3,87-3,64 (m, 3H), 3,32 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0516] (Ссылочный пример 6-60)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2-морфолиноэтил)оксим (ссылочное соединение 6-60)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(2-морфолиноэтил)оксим, синтезированный таким же образом, как в ссылочном примере 90-1. В результате указанное в заголовке соединение (выход 83%)) было получено в виде темно-коричневого твердого вещества.
Масс-спектр (CI, m/z): 516[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,4 Гц, 2H), 7,51-7,43 (m, 2H), 7,35-7,28 (m, 1H), 4,85-4,77 (m, 6H), 4,15 (t, J=6,0 Гц, 2H), 3,61-3,52(m, 4H), 2,58 (t, J=6,0 Гц, 2H), 2,45-2,38 (m, 4H), 0,91 (s, 9H), 0,11 (s, 6H).
[0517] (Ссылочный пример 6-61)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(азетидин-1-ил)этил]оксим (ссылочное соединение 6-61)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[2-(азетидин-1-ил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 90-2. В результате указанное в заголовке соединение (выход 74%) было получено в виде бесцветного масла.
Масс-спектр (ESI, m/z): 486[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,4 Гц, 2H), 7,50-7,44 (m, 2H), 7,34-7,29 (m, 1H), 4,85-4,76 (m, 6H), 3,97 (t, J=5,7 Гц, 2H), 3,16-3,09(m, 4H), 2,59 (t, J=5,7 Гц, 2H), 1,99-1,89 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0518] (Ссылочный пример 6-62)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[(4-метилморфолин-2-ил)метил]оксим (ссылочное соединение 6-62)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[(4-метилморфолин-2-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 92-1. В результате указанное в заголовке соединение (включая примеси) было получено в виде коричневого масла.
Масс-спектр (ESI, m/z): 516[М+1]+.
[0519] (Ссылочный пример 6-63)
1-(2-{[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]метил}морфолино)этанон (ссылочное соединение 6-63)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-{2-[({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)метил]морфолино}этанон, синтезированный таким же образом, как в ссылочном примере 87-3. В результате указанное в заголовке соединение (включая примеси) было получено в виде коричневого масла.
Масс-спектр (ESI, m/z): 544[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,3 Гц, 2H), 7,52-7,42 (m, 2H), 7,36-7,28 (m, 1H), 4,86-4,78 (m, 6H), 4,32-3,98 (m, 3H), 3,90-3,82 (m, 1H), 3,79-3,53 (m, 2H), 3,50-3,39 (m, 1H), 3,22-2,89 (m, 1H), 2,70-2,40 (m, 1H), 2,03-1,99 (m, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0520] (Ссылочный пример 6-64)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]циклобутилацетат (ссылочное соединение 6-64)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 3-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)циклобутилацетат, синтезированный таким же образом, как в ссылочном примере 29-4. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 515[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,3 Гц, 2H), 7,53-7,41 (m, 2H), 7,37-7,27 (m, 1H), 5,12-4,98 (m, 1H), 4,90-4,75 (m, 7H), 2,54-2,44 (m, 2H), 2,40-2,29 (m, 2H), 2,01 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0521] (Ссылочный пример 6-65)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-бензилоксим (ссылочное соединение 6-65)
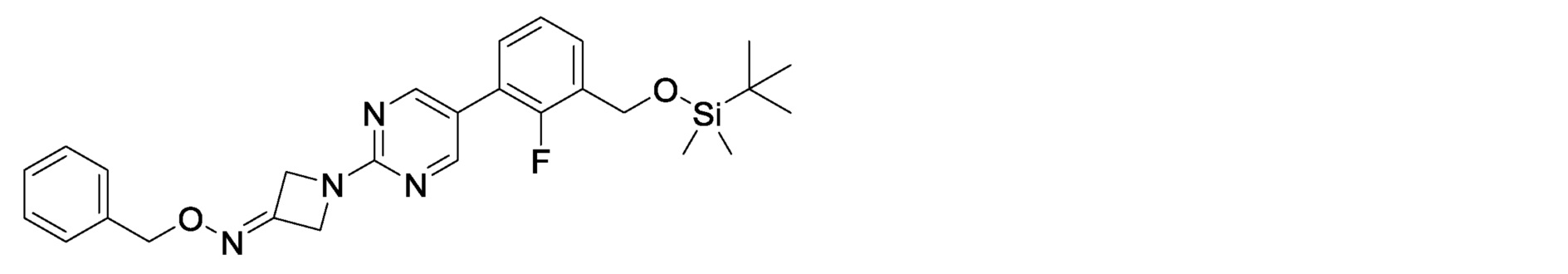
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-бензилоксим, синтезированный таким же образом, как в ссылочном примере 98. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 493[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,4 Гц, 2H), 7,52-7,27 (m, 8H), 5,09 (s, 2H), 4,85-4,79 (m, 6H), 0,91 (s, 9H), 0,11 (s, 6H).
[0522] (Ссылочный пример 6-66)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(1-метилазетидин-3-ил)оксим (ссылочное соединение 6-66)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(1-метилазетидин-3-ил)оксим, синтезированный таким же образом, как в ссылочном примере 92-2. В результате указанное в заголовке соединение (включая примеси) было получено в виде коричневого масла.
Масс-спектр (ESI, m/z): 472[М+1]+.
[0523] (Ссылочный пример 6-67)
1-{3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-ил}этанон (ссылочное соединение 6-67)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-[3-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)азетидин-1-ил]этанон, синтезированный таким же образом, как в ссылочном примере 87-4. В результате указанное в заголовке соединение (включая примеси) было получено в виде коричневого масла.
Масс-спектр (ESI, m/z): 500[М+1]+.
[0524] (Ссылочный пример 6-68)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(1-бензилазетидин-3-ил)оксим (ссылочное соединение 6-68)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(1-бензилазетидин-3-ил)оксим, синтезированный таким же образом, как в ссылочном примере 100-1. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого масла.
Масс-спектр (ESI, m/z): 548[М+1]+.
[0525] (Ссылочный пример 6-69)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[1-(2,2,2-трифторэтил)азетидин-3-ил]оксим (ссылочное соединение 6-69)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[1-(2,2,2-трифторэтил)азетидин-3-ил]оксим, синтезированный таким же образом, как в ссылочном примере 101-1. В результате указанное в заголовке соединение (включая примеси) было получено в виде бесцветного масла.
Масс-спектр (ESI, m/z): 540[М+1]+.
[0526] (Ссылочный пример 6-70)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[1-(метилсульфонил)азетидин-3-ил]оксим (ссылочное соединение 6-70)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[1-(метилсульфонил)азетидин-3-ил]оксим, синтезированный таким же образом, как в ссылочном примере 102-1. В результате указанное в заголовке соединение (включая примеси) было получено в виде бесцветного масла.
[0527] (Ссылочный пример 6-71)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(1-этилазетидин-3-ил)оксим (ссылочное соединение 6-71)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(1-этилазетидин-3-ил)оксим, синтезированный таким же образом, как в ссылочном примере 100-2. В результате указанное в заголовке соединение (включая примеси) было получено в виде коричневого масла.
Масс-спектр (ESI, m/z): 486[М+1]+.
[0528] (Ссылочный пример 6-72)
Метил-3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-карбоксилат (ссылочное соединение 6-72)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на метил-3-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)азетидин-1-карбоксилат, синтезированный таким же образом, как в ссылочном примере 102-2. В результате указанное в заголовке соединение (выход 81%) было получено в виде бесцветного масла.
Масс-спектр (ESI, m/z): 516[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,50-7,45 (m, 2H), 7,36-7,24 (m, 1H), 5,02-4,91 (m, 1H), 4,89-4,83 (m, 4H), 4,81 (s, 2H), 4,27-4,08 (m, 2H), 4,01-3,79 (m, 2H), 3,57 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0529] (Ссылочный пример 6-73)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-оксетан-3-илоксим (ссылочное соединение 6-73)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-оксетан-3-илоксим, синтезированный таким же образом, как в ссылочном примере 10-15. В результате указанное в заголовке соединение (выход 51%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 459[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (d, J=1,4 Гц, 2H), 7,53-7,43 (m, 2H), 7,35-7,28 (m, 1H), 5,26-5,17 (m, 1H), 4,90-4,84 (m, 4H), 4,81 (s, 2H), 4,79-4,74 (m, 2H), 4,59-4,53 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0530] (Ссылочный пример 6-74)
2-{3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-ил}этилацетат (ссылочное соединение 6-74)
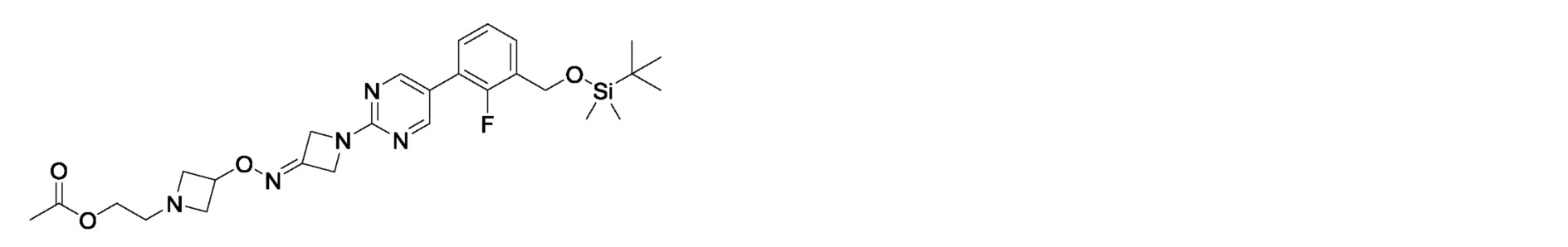
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 2-[3-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)азетидин-1-ил]этилацетат, синтезированный таким же образом, как в ссылочном примере 29-5. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
[0531] (Ссылочный пример 6-75)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[1-(2-метоксиэтил)азетидин-3-ил]оксим (ссылочное соединение 6-75)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[1-(2-метоксиэтил)азетидин-3-ил]оксим, синтезированный таким же образом, как в ссылочном примере 101-2. В результате указанное в заголовке соединение (включая примеси) было получено в виде коричневого масла.
Масс-спектр (ESI, m/z): 516[М+1]+.
[0532] (Ссылочный пример 6-76)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[1-(2-фторэтил)азетидин-3-ил]оксим (ссылочное соединение 6-76)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[1-(2-фторэтил)азетидин-3-ил]оксим, синтезированный таким же образом, как в ссылочном примере 101-3. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого масла.
[0533] (Ссылочный пример 6-77)
Этил-3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]пропанoат (ссылочное соединение 6-77)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на этил-3-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)пропанoат, синтезированный таким же образом, как в ссылочном примере 104. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 531[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,51-7,41 (m, 2H), 7,33-7,27 (m, 1H), 4,81 (s, 2H), 4,20 (t, J=6,1 Гц, 2H), 4,07 (q, J=7,1 Гц, 2H), 3,96-3,86 (m, 4H), 2,65-2,61 (m, 2H), 2,56-2,51 (m, 2H), 2,41-2,35 (m, 2H), 1,18 (t, J=7,1 Гц, 4H), 0,91 (s, 9H), 0,11 (s, 6H).
[0534] (Ссылочный пример 6-78)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]пропанамид (ссылочное соединение 6-78)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 3-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)пропанамид, синтезированный таким же образом, как в ссылочном примере 105-1. В результате указанное в заголовке соединение (включая примеси) было получено в виде белой пены.
Масс-спектр (ESI, m/z): 502[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,4 Гц, 2H), 7,51-7,43 (m, 2H), 7,26-7,19 (m, 1H), 5,86 (br s, 1H), 5,31 (br s, 1H), 4,85 (s, 2H), 4,33 (t, J=5,9 Гц, 2H), 4,04-3,96 (m, 4H), 2,73-2,59 (m, 4H), 2,50-2,44 (m, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0535] (Ссылочный пример 6-79)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]-N-метилпропанамид (ссылочное соединение 6-79)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 3-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)-N-метилпропанамид, синтезированный таким же образом, как в ссылочном примере 105-2. В результате указанное в заголовке соединение (выход 88%) было получено в виде серого твердого вещества.
Масс-спектр (CI, m/z): 516[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,86-7,76 (m, 1H), 7,68-7,40 (m, 2H), 7,34-7,25 (m, 1H), 4,81 (s, 2H), 4,16 (t, J=6,5 Гц, 2H),3,97-3,87 (m, 4H), 2,59-2,52 (m, 5H), 2,43-2,35 (m, 4H), 0,92 (s, 9H), 0,11 (s, 6H).
[0536] (Ссылочный пример 6-80)
Этил-4-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]бутаноат (ссылочное соединение 6-80)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на этил-4-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)бутаноат, синтезированный таким же образом, как в ссылочном примере 67-11. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого масла.
[0537] (Ссылочный пример 6-81)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]-N,N-диметилпропанамид (ссылочное соединение 6-81)
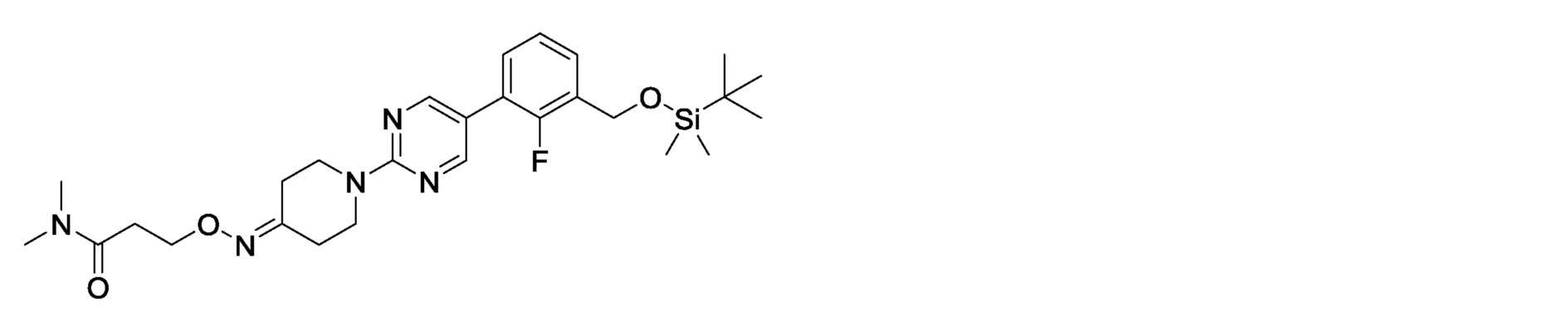
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 3-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)-N,N-диметилпропанамид, синтезированный таким же образом, как в ссылочном примере 105-3. В результате указанное в заголовке соединение (выход 95%) было получено в виде серого твердого вещества.
Масс-спектр (CI, m/z): 530[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,51-7,41 (m, 2H), 7,34-7,26 (m, 1H), 4,81 (s, 2H), 4,19 (t, J=6,8 Гц, 2H), 3,96-3,89 (m, 4H), 2,96 (s, 3H), 2,81 (s, 3H), 2,68-2,62 (m, 2H), 2,57-2,53 (m, 2H), 2,41-2,36 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0538] (Ссылочный пример 6-82)
2-{2-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}изоиндолин-1,3-дион (ссылочное соединение 6-82)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 2-[2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этил]изоиндолин-1,3-дион, синтезированный таким же образом, как в ссылочном примере 85-3. В результате указанное в заголовке соединение (выход 84%) было получено в виде темно-коричневого масла.
Масс-спектр (CI, m/z): 604[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,58 (d, J=1,4 Гц, 2H), 7,91-7,82 (m, 4H), 7,52-7,39 (m, 2H), 7,34-7,26 (m, 1H), 4,81 (s, 2H), 4,26-4,16 (m, 2H), 3,87-3,82 (m, 4H), 3,79-3,68 (m, 2H), 2,48-2,39 (m, 2H), 2,19-2,08 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0539] (Ссылочный пример 6-83)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[2-(диметиламино)этил]оксим (ссылочное соединение 6-83)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-{5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил}азетидин-3-она O-[2-(диметиламино)этил]оксим, синтезированный таким же образом, как в ссылочном примере 110-1. В результате указанное в заголовке соединение (выход 86%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 502[М+1]+.
[0540] (Ссылочный пример 6-84)
трет-Бутил-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}(метил)карбамат (ссылочное соединение 6-84)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на трет-бутил-[2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этил](метил)карбамат, синтезированный таким же образом, как в ссылочном примере 109-2. В результате указанное в заголовке соединение (выход 84%) было получено в виде белой пены.
Масс-спектр (ESI, m/z): 588[М+1]+.
1H-ЯМР(400 МГц, CDCl3) δ: 8,53 (d, J=1,4 Гц, 2H), 7,52-7,44 (m, 1H), 7,30-7,16 (m, 2H), 4,85 (s, 2H), 4,23-4,10 (m, 2H), 4,06-3,95 (m, 4H), 3,56-3,42 (m, 2H), 2,95-2,86 (m, 3H), 2,71-2,65 (m, 2H), 2,51-2,43 (m, 2H), 1,46 (s, 9H), 0,96 (s, 9H), 0,14 (s, 6H).
[0541] (Ссылочный пример 6-85)
Ди-трет-бутил-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}карбамат (ссылочное соединение 6-85)
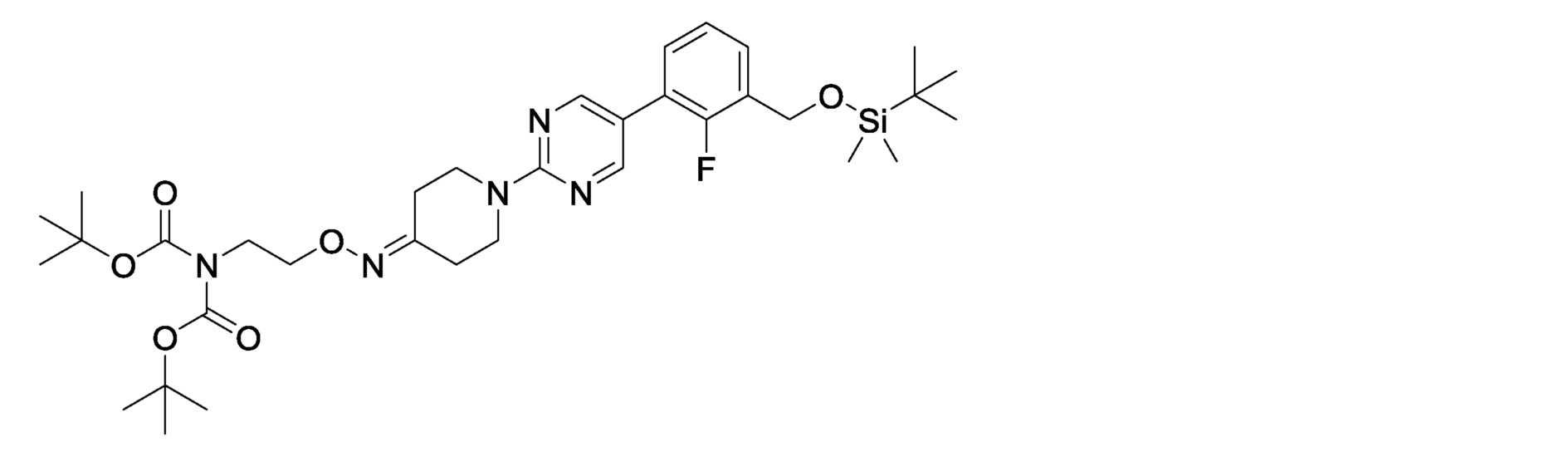
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на ди-трет-бутил-[2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этил]карбамат, синтезированный таким же образом, как в ссылочном примере 111. В результате указанное в заголовке соединение (выход 95%) было получено в виде бесцветного масла.
Масс-спектр (ESI, m/z): 674[М+1]+.
[0542] (Ссылочный пример 6-86)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил)]пиперидин-4-илиден}амино)окси]пропаннитрил (ссылочное соединение 6-86)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 3-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)пропаннитрил, синтезированный таким же образом, как в ссылочном примере 112. В результате указанное в заголовке соединение (выход 87%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 484[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,5 Гц, 2H), 7,52-7,45 (m, 1H), 7,29-7,20 (m, 2H), 4,85 (s, 2H), 4,25 (t, J=6,3 Гц, 2H), 4,04-3,98 (m, 4H), 2,74 (t, J=6,3 Гц, 2H), 2,73-2,68 (m, 2H), 2,48-2,43 (m, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0543] (Ссылочный пример 6-87)
4-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]бутаннитрил (ссылочное соединение 6-87)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 4-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)бутаннитрил, синтезированный таким же образом, как в ссылочном примере 67-12. В результате указанное в заголовке соединение (выход 72%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 498[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,52-7,41 (m, 2H), 7,34-7,25 (m, 1H), 4,81 (s, 2H), 4,04 (t, J=6,0 Гц, 2H), 3,96-3,89 (m, 4H), 2,63-2,53 (m, 4H), 2,42-2,36 (m, 2H), 1,93-1,86 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0544] (Ссылочный пример 6-88)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[2-(метилсульфонил)этил]оксим (ссылочное соединение 6-88)
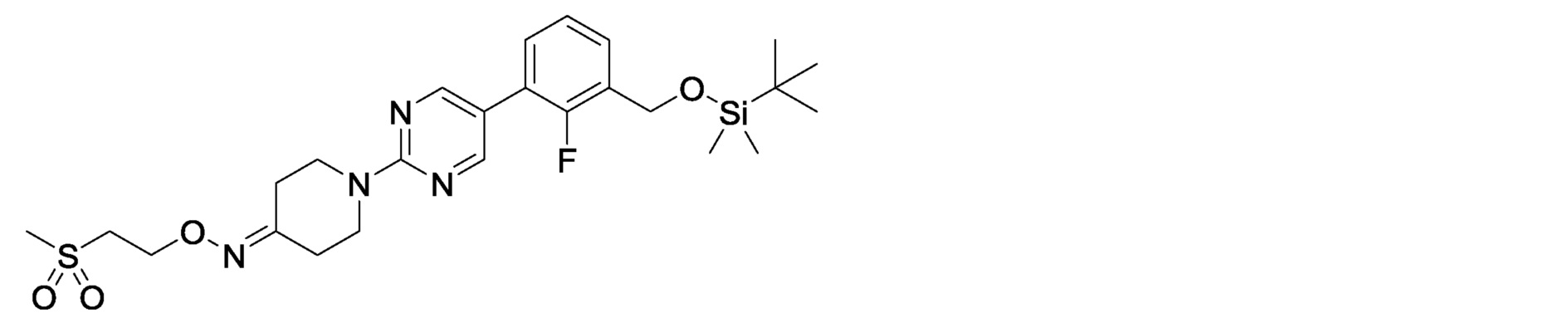
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-[2-(метилсульфонил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 113. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
[0545] (Ссылочный пример 6-89)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[3-(метилсульфонил)пропил]оксим (ссылочное соединение 6-89)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-[3-(метилсульфонил)пропил]оксим, синтезированный таким же образом, как в ссылочном примере 67-13. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
[0546] (Ссылочный пример 6-90)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[(1-метил-1H-пиразол-3-ил)метил]оксим (ссылочное соединение 6-90)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-[(1-метил-1H-пиразол-3-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 67-14. В результате указанное в заголовке соединение (выход 74%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 525[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,52 (d, J=1,5 Гц, 2H), 7,51-7,44 (m, 1H), 7,32 (d, J=2,1 Гц, 1H), 7,29-7,18 (m, 2H), 6,30 (d, J=2,1 Гц, 1H), 5,09 (s, 2H), 4,85 (s, 2H), 4,03-3,93 (m, 4H), 3,90 (s, 3H), 2,74-2,67 (m, 2H), 2,51-2,45 (m, 2H), 0,96 (s, 9H), 0,13 (s, 6H).
[0547] (Ссылочный пример 6-91)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-3-ил]метил}оксим (ссылочное соединение 6-91)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-3-ил]метил}оксим, синтезированный таким же образом, как в ссылочном примере 67-15. В результате указанное в заголовке соединение (включая примеси) было получено в виде бесцветного масла.
Масс-спектр (ESI, m/z): 595[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,52 (d, J=1,4 Гц, 2H), 7,57 (d, J=2,4 Гц, 1H), 7,50-7,44 (m, 1H), 7,27-7,16 (m, 2H), 6,36 (d, J=2,4 Гц, 1H), 5,36 (dd, J=2,7, 9,6 Гц, 1H), 5,12 (s, 2H), 4,85 (s, 2H), 4,11-4,04 (m, 1H), 4,02-3,93 (m, 4H), 3,77-3,59 (m, 1H), 2,72-2,67 (m, 2H), 2,50-2,45 (m, 2H), 2,20-1,96 (m, 3H), 1,76-1,52 (m, 3H), 0,96 (s, 9H), 0,13 (s, 6H).
[0548] (Ссылочный пример 6-92)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метил}оксим (ссылочное соединение 6-92)
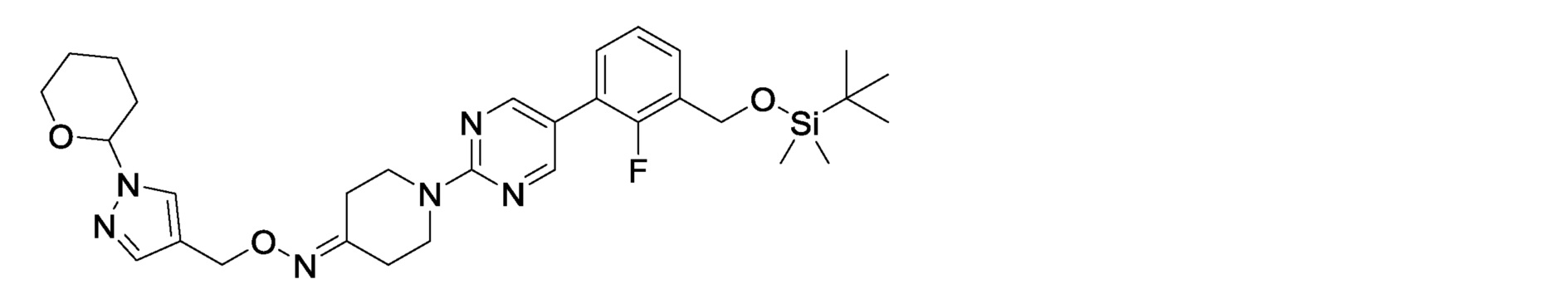
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метил}оксим, синтезированный таким же образом, как в ссылочном примере 67-16. В результате указанное в заголовке соединение (выход 76%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 595[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,58 (d, J=1,5 Гц, 2H), 7,90 (s, 1H), 7,53-7,40 (m, 3H), 7,34-7,26 (m, 1H), 5,36 (dd, J=2,3, 10,1 Гц, 1H), 4,89 (s, 2H), 4,80 (s, 2H), 3,98-3,86 (m, 5H), 3,68-3,56 (m, 1H), 2,59-2,52 (m, 2H), 2,43-2,36 (m, 2H), 2,11-1,46 (m, 6H), 0,91 (s, 9H), 0,11 (s, 6H).
[0549] (Ссылочный пример 6-93)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[(1-метил-1H-пиразол-4-ил)метил]оксим (ссылочное соединение 6-93)
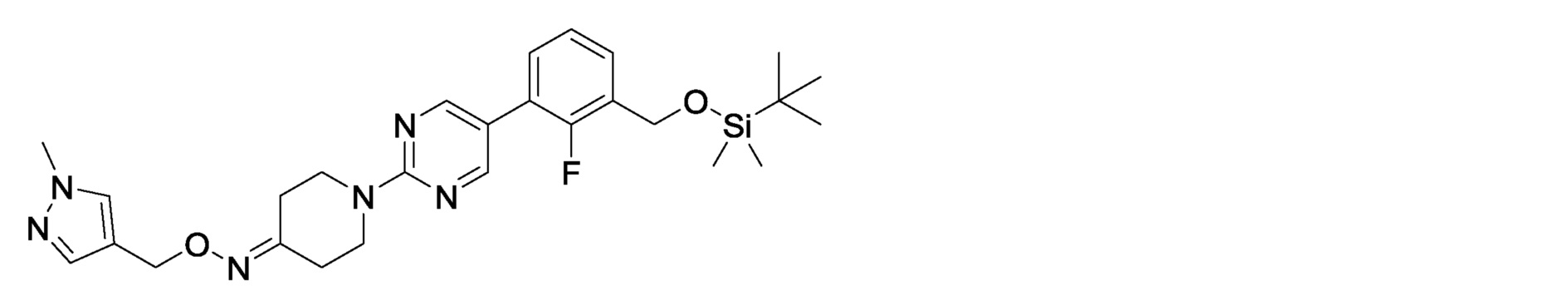
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-[(1-метил-1H-пиразол-4-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 116. В результате указанное в заголовке соединение (выход 70%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 525[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,58 (d, J=1,4 Гц, 2H), 7,70 (s, 1H), 7,50-7,41 (m, 3H), 7,33-7,26 (m, 1H), 4,87 (s, 2H), 4,81 (s, 2H), 3,95-3,87 (m,4H), 3,81 (s, 3H), 2,56-2,52 (m, 2H), 2,42-2,36 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0550] (Ссылочный пример 6-94)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[2-(1H-пиразол-1-ил)этил]оксим (ссылочное соединение 6-94)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-[2-(1H-пиразол-1-ил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 110-3. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 525[М+1]+.
[0551] (Ссылочный пример 6-95)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-пиридин-4-илметилоксим (ссылочное соединение 6-95)
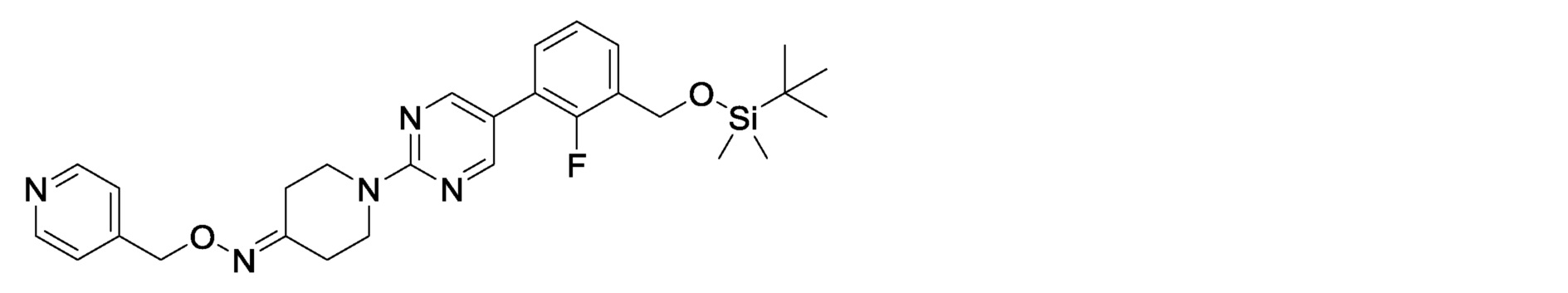
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-пиридин-4-илметилоксим, синтезированный таким же образом, как в ссылочном примере 117. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 522[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,61-8,56 (m, 2H), 8,53 (d, J=1,4 Гц, 2H), 7,58-7,43 (m, 1H), 7,32-7,18 (m, 4H), 5,11 (s, 2H), 4,85 (s, 2H), 4,07-3,96 (m, 4H), 2,81-2,73 (m, 2H), 2,50-2,42 (m, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0552] (Ссылочный пример 6-96)
1-{2-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}пирролидин-2,5-дион (ссылочное соединение 6-96)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-[2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден)амино]окси}этил)пирролидин-2,5-дион, синтезированный таким же образом, как в ссылочном примере 118. В результате указанное в заголовке соединение (выход 88%) было получено в виде светло-коричневого масла.
Масс-спектр (CI, m/z): 556[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,52 (d, J=1,4 Гц, 2H), 7,52-7,43 (m, 1H), 7,32-7,16 (m, 2H), 4,85 (s, 2H), 4,25-4,16 (m, 2H), 4,04-3,95 (m, 4H), 3,86-3,77 (m, 2H), 2,71 (s, 4H), 2,64-2,55 (m, 2H), 2,46-2,41 (m, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0553] (Ссылочный пример 6-97)
1-{2-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}пирролидин-2-он (ссылочное соединение 6-97)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 1-[2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этил]пирролидин-2-он, синтезированный таким же образом, как в ссылочном примере 119-1. В результате указанное в заголовке соединение (включая примеси) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 542[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,51-7,42 (m, 2H), 7,33-7,27 (m, 1H), 4,81 (s, 2H), 4,09-4,04 (m, 2H), 3,97-3,86 (m, 4H), 3,44-3,36 (m, 4H), 2,59-2,53 (m, 2H), 2,42-2,35 (m, 2H), 2,24-2,13 (m, 2H), 1,98-1,84 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0554] (Ссылочный пример 6-98)
3-{2-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}оксазолидин-2-он (ссылочное соединение 6-98)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 3-[2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этил]оксазолидин-2-он, синтезированный таким же образом, как в ссылочном примере 119-2. В результате указанное в заголовке соединение (включая примеси) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 544[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,51-7,42 (m, 2H), 7,34-7,26 (m, 1H), 4,81 (s, 2H), 4,28-4,21 (m, 2H), 4,15-4,08 (m, 2H), 3,96-3,88 (m, 4H), 3,64-3,54 (m, 2H), 3,44-3,38 (m, 2H), 2,60-2,52 (m, 2H), 2,43-2,35 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0555] (Ссылочный пример 6-99)
4-{2-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}морфолин-3-он (ссылочное соединение 6-99)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 6-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 3-1) заменяли на 4-[2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этил]морфолин-3-он, синтезированный таким же образом, как в ссылочном примере 119-3. В результате указанное в заголовке соединение (включая примеси) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 558[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,51-7,41 (m, 2H), 7,35-7,25 (m, 1H), 4,81 (s, 2H), 4,15-4,09 (m, 2H), 4,02 (s, 2H), 3,95-3,89 (m, 4H), 3,85-3,78 (m, 2H), 3,59-3,53 (m, 2H), 3,42-3,36 (m, 2H), 2,60-2,52 (m, 2H), 2,42-2,34 (m, 2H), 1,99 (s, 1H), 0,91 (s, 9H), 0,11 (s, 6H).
[0556] (Ссылочный пример 7-1)
1-[5-(2-Фтор-3-гидроксиметилфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 7-1)

Раствор 1 М тетрабутиламмония фторида в THF, 8,0 мл (8,0 ммоль), добавляли к раствору в THF (30 мл) 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксима, 2,75 г (6,60 ммоль), синтезированного таким же образом, как в ссылочном примере 6-1, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли TBME, и смесь перемешивали при комнатной температуре. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 1,78 г (5,89 ммоль, выход 89%) в виде серого твердого вещества.
Масс-спектр (CI, m/z): 303[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,5 Гц, 2H), 7,53-7,41 (m, 2H), 7,32-7,26 (m, 1H), 5,33 (t, J=5,6 Гц, 1H), 4,84-4,77 (m, 4H), 4,60 (d, J=5,6 Гц, 2H), 3,83 (s, 3H).
[0557] (Ссылочный пример 7-2)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-этилоксим (ссылочное соединение 7-2)

Раствор 1 М тетрабутиламмония фторида в THF, 0,38 мл (0,38 ммоль), добавляли к раствору в THF (2,6 мл) 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксима, 130 мг (0,302 ммоль), синтезированного таким же образом, как в ссылочном примере 6-2, и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:метанол) с получением указанного в заголовке соединения в количестве 83,6 мг (0,264 ммоль, выход 87%) в виде светло-желтого твердого вещества.
Масс-спектр (DUIS, m/z): 317[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,4 Гц, 2H), 7,54-7,41 (m, 2H), 7,32-7,26 (m, 1H), 5,34 (t, J=5,7 Гц, 1H), 4,85-4,76 (m, 4H), 4,60 (d, J=5,7 Гц, 2H), 4,08 (q, J=7,0 Гц, 2H), 1,22 (t, J=7,0 Гц, 3H).
[0558] (Ссылочный пример 7-3)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-метил-d3-оксим (ссылочное соединение 7-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метил-d3-оксим, синтезированный таким же образом, как в ссылочном примере 6-3. В результате указанное в заголовке соединение (выход 83%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 306[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,4 Гц, 2H), 7,54-7,40 (m, 2H), 7,34-7,25 (m, 1H), 5,34 (br s, 1H), 4,86-4,76 (m, 4H), 4,60 (br s, 2H).
[0559] (Ссылочный пример 7-4)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(2-фторэтил)оксим (ссылочное соединение 7-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2-фторэтил)оксим, синтезированный таким же образом, как в ссылочном примере 6-4. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 335[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3)δ: 8,57 (d, J=1,0 Гц, 2H), 7,51-7,41 (m, 1H), 7,35-7,20 (m, 2H), 4,94-4,88 (m, 4H), 4,84 (d, J=6,1 Гц, 2H), 4,74-4,58 (m, 2H), 4,39-4,28 (m, 2H), 1,85 (t, J=6,1 Гц, 1H).
[0560] (Ссылочный пример 7-5)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(2,2-дифторэтил)оксим (ссылочное соединение 7-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2,2-дифторэтил)оксим, синтезированный таким же образом, как в ссылочном примере 15-1. В результате указанное в заголовке соединение (выход 83%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 353[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (d, J=1,4 Гц, 2H), 7,53-7,41 (m, 2H), 7,33-7,26 (m, 1H), 6,25 (tt, J=3,8, 54,8 Гц, 1H), 5,34 (t, J=5,2 Гц, 1H), 4,90-4,80 (m, 4H), 4,60 (d, J=5,2 Гц, 2H), 4,31 (dt, J=3,8, 14,7 Гц, 2H).
[0561] (Ссылочный пример 7-6)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(2,2,2-трифторэтил)оксим (ссылочное соединение 7-6)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2,2,2-трифторэтил)оксим, синтезированный таким же образом, как в ссылочном примере 15-2. В результате указанное в заголовке соединение (выход 90%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 371[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,58 (d, J=1,4 Гц, 2H), 7,49-7,42 (m, 1H), 7,34-7,22 (m, 2H), 4,94-4,89 (m, 4H), 4,84 (d, J=6,1 Гц, 2H), 4,45 (q, J=8,5 Гц, 2H), 1,85 (t, J=6,1 Гц, 1H).
[0562] (Ссылочный пример 7-7)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(3-фторпропил)оксим (ссылочное соединение 7-7)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-фторпропил)оксим, синтезированный таким же образом, как в ссылочном примере 6-6. В результате указанное в заголовке соединение (выход 80%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 349[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,53-7,40 (m, 2H), 7,33-7,25 (m, 1H), 5,34 (t, J=5,7 Гц, 1H), 4,85-4,79 (m, 4H), 4,64-4,44 (m, 4H), 4,13 (t, J=6,3 Гц, 2H), 2,10-1,92 (m, 2H).
[0563] (Ссылочный пример 7-8)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-{2-[(тетрагидропиран-2-ил)окси]этил}оксим (ссылочное соединение 7-8)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-{2-[(тетрагидропиран-2-ил)окси]этил}оксим, синтезированный таким же образом, как в ссылочном примере 6-7. В результате указанное в заголовке соединение (выход 80%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 417[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,54-7,40 (m, 2H), 7,34-7,24 (m, 1H), 5,36 (br s, 1H), 4,92-4,74 (m, 4H), 4,66-4,52 (m, 3H), 4,26-4,08 (m, 2H), 3,88-3,70 (m, 2H), 3,69-3,56 (m, 1H), 3,49-3,38 (m, 1H), 1,84-1,35 (m, 6H).
[0564] (Ссылочный пример 7-9)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-{3-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 7-9)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-{3-[(тетрагидропиран-2-ил)окси]пропил}оксим, синтезированный таким же образом, как в ссылочном примере 6-8. В результате указанное в заголовке соединение (выход 97%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 431[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,53-7,41 (m, 2H), 7,32-7,26 (m, 1H), 5,34 (t, J=5,5 Гц, 1H), 4,85-4,77 (m, 4H), 4,60 (d, J=5,5 Гц, 2H), 4,58-4,55 (m, 1H), 4,11 (t, J=6,5 Гц, 2H), 3,78-3,64 (m, 2H), 3,49-3,39 (m, 2H), 1,87 (quin, J=6,5 Гц, 2H), 1,78-1,39 (m, 6H).
[0565] (Ссылочный пример 7-10)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-{4-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 7-10)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-{4-[(тетрагидропиран-2-ил)окси]бутил}оксим, синтезированный таким же образом, как в ссылочном примере 6-9. В результате указанное в заголовке соединение (выход 88%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 445[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,48-7,41 (m, 1H), 7,35-7,21 (m, 2H), 4,91-4,86 (m, 4H), 4,84 (d, J=6,1 Гц, 2H), 4,61-4,58 (m, 1H), 4,16-4,11 (m, 2H), 3,91-3,83 (m, 1H), 3,83-3,74 (m, 1H), 3,55-3,47 (m, 1H), 3,47-3,39 (m, 1H), 1,88-1,47 (m, 10H).
[0566] (Ссылочный пример 7-11)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(2-метоксиэтил)оксим (ссылочное соединение 7-11)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2-метоксиэтил)оксим, синтезированный таким же образом, как в ссылочном примере 6-10. В результате указанное в заголовке соединение (выход 75%) было получено в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,52-7,41 (m, 2H), 7,32-7,26 (m, 1H), 5,34 (t, J=5,1 Гц, 1H), 4,87-4,77 (m, 4H), 4,60 (d, J=5,1 Гц, 2H), 4,19-4,12 (m, 2H), 3,59-3,53 (m, 2H), 3,27 (s, 3H).
[0567] (Ссылочный пример 7-12)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(2-{2-[(тетрагидропиран-2-ил)окси]этокси}этил)оксим (ссылочное соединение 7-12)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2-{2-[(тетрагидропиран-2-ил)окси]этокси}этил)оксим, синтезированный таким же образом, как в ссылочном примере 6-11. В результате указанное в заголовке соединение (выход 86%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 461[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,56 (d, J=1,4 Гц, 2H), 7,48-7,42 (m, 1H), 7,34-7,20 (m, 2H), 4,91-4,87 (m, 4H), 4,83 (d, J=5,9 Гц, 2H), 4,66-4,63 (m, 1H), 4,29-4,24 (m, 2H), 3,91-3,84 (m, 2H), 3,80-3,76 (m, 2H), 3,72-3,69 (m, 2H), 3,66-3,59 (m, 1H), 3,54-3,47(m, 1H), 1,91 (t, J=5,9 Гц, 1H), 1,88-1,46 (m, 6H).
[0568] (Ссылочный пример 7-13)
{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}метилпивалат (ссылочное соединение 7-13)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на [({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]метилпивалат, синтезированный таким же образом, как в ссылочном примере 15-3. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 403[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,5 Гц, 2H), 7,49-7,42 (m, 1H), 7,42-7,20 (m, 2H), 5,73 (s, 2H), 4,92-4,88 (m, 4H), 4,84 (d, J=5,9 Гц, 2H), 1,83 (t, J=5,9 Гц, 1H), 1,24 (s, 9H).
[0569] (Ссылочный пример 7-14)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим (ссылочное соединение 7-14)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 6-12. В результате указанное в заголовке соединение (выход 88%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 417[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,51-7,42 (m, 2H), 7,32-7,26 (m, 1H), 5,34 (br s, 1H), 4,85-4,79 (m, 4H), 4,60 (s, 2H), 4,08 (d, J=7,0 Гц, 2H), 3,91 (dd, J=4,0, 11,8 Гц, 2H), 3,65 (dd, J=6,1, 11,8 Гц, 2H), 2,02-1,95 (m, 1H), 1,34 (s, 3H), 1,31 (s, 3H).
[0570] (Ссылочный пример 7-15)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим (ссылочное соединение 7-15)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 6-13. В результате указанное в заголовке соединение (выход 93%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 403[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,51-7,42 (m, 2H), 7,33-7,25 (m, 1H), 5,34 (t, J=5,7 Гц, 1H), 4,86-4,78 (m, 4H), 4,60 (d, J=5,7 Гц, 2H), 4,34-4,26 (m, 1H), 4,10-4,00 (m, 3H), 3,68 (dd, J=6,4, 8,4 Гц, 1H), 1,33 (s, 3H), 1,28 (s, 3H).
[0571] (Ссылочный пример 7-16)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(3-метокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 7-16)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил)азетидин-3-она O-(3-метокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим, синтезированный таким же образом, как в ссылочном примере 6-14. В результате указанное в заголовке соединение (выход 90%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 475[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,54-7,40 (m, 2H), 7,34-7,21 (m, 1H), 5,34 (t, J=5,6 Гц, 1H), 4,88-4,76 (m, 4H), 4,60 (d, J=5,6 Гц, 2H), 4,57-4,52 (m, 1H), 4,12-3,93 (m, 2H), 3,79-3,63 (m, 2H), 3,47-3,33 (m, 4H), 3,24 (s, 3H), 2,28-2,16 (m, 1H), 1,78-1,37 (m, 6H).
[0572] (Ссылочный пример 7-17)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-метокси-3-(тритилокси)пропил]оксим (ссылочное соединение 7-17)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-метокси-3-(тритилокси)пропил]оксим, синтезированный таким же образом, как в ссылочном примере 6-15. В результате указанное в заголовке соединение (выход 80%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 619[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,65 (d, J=1,4 Гц, 2H), 7,53-7,21 (m, 18H), 5,34 (t, J=5,7 Гц, 1H), 4,82-4,79 (m, 2H), 4,74-4,44 (m, 4H), 4,18-4,06 (m, 2H), 3,69-3,57 (m, 1H), 3,34 (s, 3H), 3,23-2,96 (m, 2H).
[0573] (Ссылочный пример 7-18)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксим (ссылочное соединение 7-18)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 6-16. В результате указанное в заголовке соединение (выход 55%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 417[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,53-7,40 (m, 2H), 7,35-7,24 (m, 1H), 5,34 (t, J=5,7 Гц, 1H), 4,86-4,77 (m, 4H), 4,60 (d, J=5,7 Гц, 2H), 4,16-4,07 (m, 3H), 4,02 (dd, J=6,0, 8,0 Гц, 1H), 3,49 (dd, J=7,2, 8,0 Гц, 1H), 1,93-1,77 (m, 2H), 1,31 (s, 3H), 1,27 (s, 3H).
[0574] (Ссылочный пример 7-19)
1-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-3-метоксипропан-2-илацетат (ссылочное соединение 7-19)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-3-метоксипропан-2-илацетат синтезированный таким же образом, как в ссылочном примере 22. В результате указанное в заголовке соединение (выход 60%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 419[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,3 Гц, 2H), 7,52-7,41 (m, 2H), 7,35-7,25 (m, 1H), 5,34 (t, J=5,6 Гц, 1H), 5,22-5,09 (m, 1H), 4,87-4,73 (m, 4H), 4,60 (d, J=5,6 Гц, 2H), 4,22-4,07 (m, 2H), 3,54-3,44 (m, 2H), 3,27 (s, 3H), 2,04 (s, 3H).
[0575] (Ссылочный пример 7-20)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(3-фтор-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 7-20)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-фтор-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим, синтезированный таким же образом, как в ссылочном примере 6-17. В результате указанное в заголовке соединение (выход 36%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 463[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,53-7,40 (m, 2H), 7,32-7,26 (m, 1H), 5,33 (t, J=5,7 Гц, 1H), 4,87-4,79 (m, 4H), 4,66-4,41 (m, 5H), 4,16-4,05 (m, 2H), 3,76-3,68 (m, 2H), 3,47-3,38 (m, 2H), 2,43-2,29 (m, 1H), 1,76-1,57 (m, 2H), 1,53-1,41 (m, 4H).
[0576] (Ссылочный пример 7-21)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-фтор-3-(тритилокси)пропил]оксим (ссылочное соединение 7-21)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-фтор-3-(тритилокси)пропил]оксим, синтезированный таким же образом, как в ссылочном примере 6-18, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 90%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 607[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (d, J=1,4 Гц, 2H), 7,55-7,19 (m, 18H), 5,34 (t, J=5,6 Гц, 1H), 5,04-4,84 (m, 1H), 4,83-4,77 (m, 2H), 4,76-4,63 (m, 2H), 4,61 (d, J=5,6 Гц, 2H), 4,43-4,15 (m, 2H), 3,31-3,11 (m, 2H).
[0577] (Ссылочный пример 7-22)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-{3-метокси-4-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 7-22)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-{3-метокси-4-[(тетрагидропиран-2-ил)окси]бутил}оксим, синтезированный таким же образом, как в ссылочном примере 6-19. В результате указанное в заголовке соединение (выход 96%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 475[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,50-7,41 (m, 1H), 7,35-7,28 (m, 1H), 7,28-7,19 (m, 1H), 4,93-4,86 (m, 4H), 4,83 (d, J=5,4 Гц, 2H), 4,69-4,59 (m, 1H), 4,31-4,16 (m, 2H), 4,00-3,73 (m, 2H), 3,60-3,36 (m, 6H), 2,03-1,46 (m, 9H).
[0578] (Ссылочный пример 7-23)
2-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}этилацетат (ссылочное соединение 7-23)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилацетат, синтезированный таким же образом, как в ссылочном примере 6-21. В результате указанное в заголовке соединение (выход 61%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 375[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,49-7,42 (m, 1H), 7,35-7,21 (m, 2H), 4,92-4,87 (m, 4H), 4,84 (d, J=6,1 Гц, 2H), 4,37-4,26 (m, 4H), 2,10 (s, 3H), 1,83 (t, J=6,1 Гц, 1H).
[0579] (Ссылочный пример 7-24)
2-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}этилпропионат (ссылочное соединение 7-24)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилпропионат, синтезированный таким же образом, как в ссылочном примере 6-22. В результате указанное в заголовке соединение (выход 88%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 389[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,53-7,39 (m, 2H), 7,34-7,25 (m, 1H), 5,34 (t, J=5,5 Гц, 1H), 4,87-4,76 (m, 4H), 4,60 (d, J=5,5 Гц, 2H), 4,28-4,19 (m, 4H), 2,34 (q, J=7,5 Гц, 2H), 1,03 (t, J=7,5 Гц, 3H).
[0580] (Ссылочный пример 7-25)
2-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}этилбутират (ссылочное соединение 7-25)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилбутират, синтезированный таким же образом, как в ссылочном примере 6-23. В результате указанное в заголовке соединение (выход 89%) было получено в виде бесцветной пены.
Масс-спектр (CI, m/z): 403[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,1 Гц, 2H), 7,56-7,38 (m, 2H), 7,34-7,24 (m, 1H), 5,34 (t, J=5,0 Гц, 1H), 4,90-4,70 (m, 4H), 4,60 (d, J=5,0 Гц, 2H), 4,34-4,17 (m, 4H), 2,30 (t, J=7,3 Гц, 2H), 1,55 (sext, J=7,3 Гц, 2H), 0,89 (t, J=7,3 Гц, 3H).
[0581] (Ссылочный пример 7-26)
2-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}этилбензоат (ссылочное соединение 7-26)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилбензоат, синтезированный таким же образом, как в ссылочном примере 6-24. В результате указанное в заголовке соединение (выход 82%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 437[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,4 Гц, 2H), 8,02-7,92 (m, 2H), 7,73-7,63 (m, 1H), 7,59-7,40 (m, 4H), 7,33-7,23 (m, 1H), 5,34 (t, J=5,5 Гц, 1H), 4,90-4,72 (m, 4H), 4,60 (d, J=5,5 Гц, 2H), 4,56-4,49 (m, 2H), 4,41-4,34 (m, 2H).
[0582] (Ссылочный пример 7-27)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилацетат (ссылочное соединение 7-27)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилацетат, синтезированный таким же образом, как в ссылочном примере 29-1. В результате указанное в заголовке соединение (выход 79%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 503[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,5 Гц, 2H), 7,48-7,42 (m, 1H), 7,35-7,21 (m, 2H), 4,90-4,86 (m, 4H), 4,83 (d, J=6,0 Гц, 2H), 4,62-4,57 (m, 1H), 4,25-4,13 (m, 4H), 3,87-3,76 (m, 2H), 3,58-3,47 (m, 1H), 3,47-3,39 (m, 1H), 2,46-2,38 (m, 1H), 2,07 (s, 3H), 1,89 (t, J=6,0 Гц, 1H), 1,84-1,48 (m, 6H).
[0583] (Ссылочный пример 7-28)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилпропионат (ссылочное соединение 7-28)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилпропионат, синтезированный таким же образом, как в ссылочном примере 29-2. В результате указанное в заголовке соединение (выход 89%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 517[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,48-7,42 (m, 1H), 7,35-7,21 (m, 2H), 4,90-4,86 (m, 4H), 4,83 (d, J=6,0 Гц, 2H), 4,61-4,57 (m, 1H), 4,25-4,13 (m, 4H), 3,87-3,78 (m, 2H), 3,56-3,48 (m, 1H), 3,47-3,38 (m, 1H), 2,46-2,39 (m, 1H), 2,35 (q, J=7,6 Гц, 2H), 1,86 (t, J=6,0 Гц, 1H), 1,83-1,47 (m, 6H), 1,15 (t, J=7,6 Гц, 3H).
[0584] (Ссылочный пример 7-29)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилбутират (ссылочное соединение 7-29)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилбутират, синтезированный таким же образом, как в ссылочном примере 30-1. В результате указанное в заголовке соединение (выход 85%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 531[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,5 Гц, 2H), 7,49-7,42 (m, 1H), 7,35-7,21 (m, 2H), 4,90-4,85 (m, 4H), 4,83 (d, J=6,1 Гц, 2H), 4,61-4,57 (m, 1H), 4,24-4,14 (m, 4H), 3,87-3,77 (m, 2H), 3,55-3,48 (m, 1H), 3,46-3,38 (m, 1H), 2,46-2,38 (m, 1H), 2,30 (t, J=7,4 Гц, 2H), 1,88 (t, J=6,1 Гц, 1H), 1,85-1,47 (m, 8H), 0,95 (t, J=7,4 Гц, 3H).
[0585] (Ссылочный пример 7-30)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилизобутират (ссылочное соединение 7-30)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилизобутират, синтезированный таким же образом, как в ссылочном примере 30-2, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 82%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 531[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,54-740 (m, 2H), 7,35-7,24 (m, 1H), 5,40 (br. s, 1H), 4,88-4,77 (m, 4H), 4,61 (br. s, 2H), 4,58-4,54 (m, 1H), 4,20-4,01 (m, 4H), 3,77-3,61 (m, 2H), 3,48-3,35 (m, 2H), 2,55 (sep, J=7,0 Гц, 1H), 2,39-2,26 (m, 1H), 1,78-1,38 (m, 6H), 1,09 (d, J=7,0 Гц, 6H).
[0586] (Ссылочный пример 7-31)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилпивалат (ссылочное соединение 7-31)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилпивалат, синтезированный таким же образом, как в ссылочном примере 30-3, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 89%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 545[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,52-7,41 (m, 2H), 7,32-7,26 (m, 1H), 5,34 (t, J=5,1 Гц, 1H), 4,87-4,77 (m, 4H), 4,60 (d, J=5,1 Гц, 2H), 4,58-4,53 (m, 1H), 4,19-4,02 (m, 4H), 3,78-3,65 (m, 2H), 3,48-3,34 (m, 2H), 2,40-2,28 (m, 1H), 1,79-1,38 (m, 6H), 1,15 (s, 9H).
[0587] (Ссылочный пример 7-32)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилгексаноат (ссылочное соединение 7-32)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилгексаноат, синтезированный таким же образом, как в ссылочном примере 30-4. В результате указанное в заголовке соединение (выход 98%) было получено в виде бесцветного масла.
Масс-спектр (ESI, m/z): 559[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,5 Гц, 2H), 7,49-7,42 (m, 1H), 7,36-7,20 (m, 2H), 4,92-4,86 (m, 4H), 4,84 (d, J=5,3 Гц, 2H), 4,62-4,56 (m, 1H), 4,25-4,15 (m, 4H), 3,87-3,77 (m, 2H), 3,56-3,48 (m, 1H), 3,47-3,38 (m, 1H), 2,48-2,38 (m, 1H), 2,32 (t, J=7,5 Гц, 2H), 1,92-1,75 (m, 2H), 1,75-1,47 (m, 7H), 1,39-1,24 (m, 4H), 0,90 (t, J=7,0 Гц, 3H).
[0588] (Ссылочный пример 7-33)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропилбензоат (ссылочное соединение 7-33)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилбензоат, синтезированный таким же образом, как в ссылочном примере 30-5. В результате указанное в заголовке соединение (выход 96%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 565[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,4 Гц, 2H), 8,00-7,96 (m, 2H), 7,66-7,60 (m, 1H), 7,54-7,42 (m, 4H), 7,32-7,26 (m, 1H), 5,33 (t, J=5,2 Гц, 1H), 4,83-4,73 (m, 4H), 4,63-4,57 (m, 3H), 4,43-4,34 (m, 2H), 4,26-4,16 (m, 2H), 3,82-3,67 (m, 2H), 3,52-3,36 (m, 2H), 1,75-1,55 (m, 2H), 1,52-1,38 (m, 4H).
[0589] (Ссылочный пример 7-34)
1-{3-Фтор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метилоксим (ссылочное соединение 7-34)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-фторпиридин-2-ил]азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 6-26. В результате указанное в заголовке соединение (выход 79%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 320[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,17-8,14 (m, 1H), 7,50-7,40 (m, 2H), 7,36-7,30 (m, 1H), 7,25-7,19 (m, 1H), 4,92-4,88 (m, 4H), 4,83 (d, J=5,9 Гц, 2H), 3,91 (s, 3H), 1,86 (t, J=5,9 Гц, 1H).
[0590] (Ссылочный пример 7-35)
1-{3-Фтор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метил-d3-оксим (ссылочное соединение 7-35)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-фторпиридин-2-ил]азетидин-3-она O-метил-d3-оксим, синтезированный таким же образом, как в ссылочном примере 6-27. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 323[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,19-8,12 (m, 1H), 7,50-7,40 (m, 2H), 7,36-7,30 (m, 1H), 7,25-7,20 (m, 1H), 4,92-4,87 (m, 4H), 4,83 (d, J=6,2 Гц, 2H), 1,86-1,81 (m, 1H).
[0591] (Ссылочный пример 7-36)
1-{3-Фтор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксим (ссылочное соединение 7-36)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-фторпиридин-2-ил]азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 6-28. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 434[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,17-8,13 (m, 1H), 7,50-7,40 (m, 2H), 7,37-7,28 (m, 1H), 7,25-7,19 (m, 1H), 4,91-4,87 (m, 4H), 4,85-4,80 (m, 2H), 4,26-4,16 (m, 3H), 4,12-4,06 (m, 1H), 3,61-3,55 (m, 1H), 2,00-1,90 (m, 3H), 1,42 (s, 3H), 1,37 (s, 3H).
[0592] (Ссылочный пример 7-37)
1-{3-Фтор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим (ссылочное соединение 7-37)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-фторпиридин-2-ил]азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 6-29. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 434[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,17-8,14 (m, 1H), 7,51-7,40 (m, 2H), 7,37-7,29 (m, 1H), 7,25-7,19 (m, 1H), 4,91-4,87 (m, 4H), 4,83 (d, J=6,0 Гц, 2H), 4,19 (d, J=6,9 Гц, 2H), 4,01 (dd, J=4,1, 12,0 Гц, 2H), 3,76 (dd, J=5,9, 12,0 Гц, 2H), 2,14-2,06 (m, 1H), 1,82 (t, J=6,0 Гц, 1H), 1,45 (s, 3H), 1,42 (s, 3H).
[0593] (Ссылочный пример 7-38)
1-{3-Фтор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-[2-фтор-3-(тритилокси)пропил]оксим (ссылочное соединение 7-38)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-фторпиридин-2-ил]азетидин-3-она O-[2-фтор-3-(тритилокси)пропил]оксим, синтезированный таким же образом, как в ссылочном примере 6-30, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 80%) было получено в виде белой пены.
Масс-спектр (ESI, m/z): 624[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,22-8,15 (m, 1H), 7,81-7,73 (m, 1H), 7,54-7,21 (m, 18H), 5,34 (t, J=5,1 Гц, 1H), 5,06-4,67 (m, 5H), 4,61 (d, J=5,1 Гц, 2H), 4,39-4,11 (m, 2H), 3,33-3,12 (m, 2H).
[0594] (Ссылочный пример 7-39)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метилоксим (ссылочное соединение 7-39)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиридин-2-ил]азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 6-31. В результате указанное в заголовке соединение (выход 83%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 302[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,32-8,29 (m, 1H), 7,80-7,75 (m, 1H), 7,47-7,35 (m, 2H), 7,29-7,23 (m, 1H), 6,69-6,64 (m, 1H), 5,30 (t, J=5,6 Гц, 1H), 4,76-4,68 (m, 4H), 4,60 (d, J=5,6 Гц, 2H), 3,82 (s, 3H).
[0595] (Ссылочный пример 7-40)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]-3-метилпиридин-2-ил}азетидин-3-она O-метилоксим (ссылочное соединение 7-40)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-метилпиридин-2-ил]азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 6-32. В результате указанное в заголовке соединение (выход 84%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 316[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,27-8,22 (m, 1H), 7,55-7,50 (m, 1H), 7,44-7,37 (m, 1H), 7,37-7,29 (m, 1H), 7,24-7,16 (m, 1H), 4,89-4,84 (m, 4H), 4,82 (s, 2H), 3,90 (s, 3H), 2,27 (s, 3H).
[0596] (Ссылочный пример 7-41)
5-[2-Фтор-3-(гидроксиметил)фенил]-2-[3-(метоксиимино)азетидин-1-ил]никотинонитрил (ссылочное соединение 7-41)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-2-[3-(метоксиимино)азетидин-1-ил]никотинонитрил, синтезированный таким же образом, как в ссылочном примере 6-33, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 78%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 327[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59-8,54 (m, 1H), 8,24 (dd, J=1,0, 2,3 Гц, 1H), 7,53-7,42 (m, 2H), 7,31-7,26 (m, 1H), 5,33 (t, J=5,6 Гц, 1H), 5,03-4,98 (m, 4H), 4,60 (d, J=5,6 Гц, 2H), 3,83 (s, 3H).
[0597] (Ссылочный пример 7-42)
1-{3-Хлор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метилоксим (ссылочное соединение 7-42)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-хлорпиридин-2-ил]азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 6-34. В результате указанное в заголовке соединение (выход 80%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 336[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,29-8,27 (m, 1H), 7,75-7,72 (m, 1H), 7,46-7,40 (m, 1H), 7,35-7,29 (m, 1H), 7,25-7,19 (m, 1H), 4,99-4,93 (m, 4H), 4,83 (d, J=6,0 Гц, 2H), 3,90 (s, 3H), 1,81 (t, J=6,0 Гц, 1H).
[0598] (Ссылочный пример 7-43)
1-{3-(Дифторметил)-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метилоксим (ссылочное соединение 7-43)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-(дифторметил)пиридин-2-ил]азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 6-35. В результате указанное в заголовке соединение (выход 87%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 352[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,50-8,47 (m, 1H), 8,00-7,97 (m, 1H), 7,50-7,42 (m, 2H), 7,33-6,97 (m, 2H), 5,36-5,28 (m, 1H), 4,92-4,86 (m, 4H), 4,64-4,58 (m, 2H), 3,83 (s, 3H).
[0599] (Ссылочный пример 7-44)
1-{3-Циклопропил-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метилоксим (ссылочное соединение 7-44)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-циклопропилпиридин-2-ил]азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 6-36. В результате указанное в заголовке соединение (выход 92%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 342[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,18-8,15 (m, 1H), 7,46-7,36 (m, 3H), 7,28-7,21 (m, 1H), 5,33-5,25 (m, 1H), 4,94-4,90 (m, 4H), 4,62-4,56 (m, 2H), 3,81 (s, 3H), 1,94-1,86 (m, 1H), 0,97-0,91 (m, 2H), 0,75-0,69 (m, 2H).
[0600] (Ссылочный пример 7-45)
1-{3-Этил-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-метилоксим (ссылочное соединение 7-45)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-этилпиридин-2-ил]азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 6-37. В результате указанное в заголовке соединение (выход 53%) было получено в виде бесцветной пены.
Масс-спектр (ESI, m/z): 330[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,21-8,19 (m, 1H), 7,61-7,59 (m, 1H), 7,47-7,38 (m, 2H), 7,28-7,24 (m, 1H), 5,34-5,28 (m, 1H), 4,84-4,80 (m, 4H), 4,62-4,58 (m, 2H), 3,81 (s, 3H), 2,58 (q, J=7,5 Гц, 2H), 1,19 (t, J=7,5 Гц, 3H).
[0601] (Ссылочный пример 7-46)
1-(5-[2-Фтор-3-(гидроксиметил)фенил]-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 7-46)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-2-ил]азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 6-38, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 80%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 444[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,33-8,28 (m, 1H), 7,81-7,76 (m, 1H), 7,51-7,39 (m, 2H), 7,33-7,21 (m, 1H), 5,33 (br s, 1H), 4,93-4,76 (m, 4H), 4,61 (br s, 2H), 4,55-4,48 (m, 1H), 3,85-3,72 (m, 4H), 3,41-3,22 (m, 1H), 1,87-1,28 (m, 12H).
[0602] (Ссылочный пример 7-47)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]-3-(метоксиметил)пиридин-2-ил}азетидин-3-она O-метилоксим (ссылочное соединение 7-47)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-(метоксиметил)пиридин-2-ил]азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 6-39. В результате указанное в заголовке соединение (выход 83%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 346[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,30-8,27 (m, 1H), 7,75-7,72 (m, 1H), 7,49-7,36 (m, 2H), 7,29-7,20 (m, 1H), 5,31 (t, J=5,6 Гц, 1H), 4,92-4,80 (m, 4H), 4,60 (d, J=5,6 Гц, 2H), 4,39 (s, 2H), 3,81 (s, 3H).
[0603] (Ссылочный пример 7-48)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]-3-метоксипиридин-2-ил}азетидин-3-она O-метилоксим (ссылочное соединение 7-48)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-3-метоксипиридин-2-ил]азетидин-3-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 6-40. В результате указанное в заголовке соединение (выход 84%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 332[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,92-7,88 (m, 1H), 7,48-7,40 (m, 2H), 7,34-7,30 (m, 1H), 7,29-7,23 (m, 1H), 5,31 (t, J=5,4 Гц, 1H), 4,80-4,72 (m, 4H), 4,60 (d, J=5,4 Гц, 2H), 3,82 (s, 3H), 3,80 (s, 3H).
[0604] (Ссылочный пример 7-49)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-метилоксим (ссылочное соединение 7-49)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-метилоксим, синтезированный таким же образом, как в ссылочном примере 60. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 331[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,51-7,38 (m, 2H), 7,33-7,21 (m, 1H), 5,34 (br s, 1H), 4,60 (br s, 2H), 3,95-3,89 (m, 4H), 3,76 (s, 3H), 2,59-2,53 (m, 2H), 2,41-2,24 (m, 2H).
[0605] (Ссылочный пример 7-50)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-он (ссылочное соединение 7-50)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-он, синтезированный таким же образом, как в ссылочном примере 6-41, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого масла.
Масс-спектр (CI, m/z): 302[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,5 Гц, 2H), 7,52-7,41 (m, 1H), 7,36-7,29 (m, 1H), 7,28-7,22 (m, 1H), 4,84 (d, J=6,0 Гц, 2H), 4,22-4,17 (m, 4H), 2,58-2,52 (m, 4H), 1,90 (t, J=6,0 Гц, 1H).
[0606] (Ссылочный пример 7-51)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{3-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 7-51)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{3-[(тетрагидропиран-2-ил)окси]пропил}оксим, синтезированный таким же образом, как в ссылочном примере 6-42. В результате указанное в заголовке соединение (выход 85%) было получено в виде бесцветного масла.
[0607] (Ссылочный пример 7-52)
1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{4-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 7-52)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{4-[(тетрагидропиран-2-ил)окси]бутил}оксим, синтезированный таким же образом, как в ссылочном примере 6-43. В результате указанное в заголовке соединение (выход 77%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 473[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,52-7,39 (m, 2H), 7,32-7,21 (m, 1H), 5,33 (t, J=4,2 Гц, 1H), 4,60 (d, J=4,2 Гц, 2H), 4,56-4,51 (m, 1H), 4,02-3,96 (m, 2H), 3,95-3,88 (m, 4H), 3,77-3,68 (m, 1H), 3,67-3,60 (m, 1H), 3,46-3,34 (m, 2H), 2,62-2,55 (m, 2H), 2,42-2,34 (m, 2H), 1,80-1,34 (m, 10H).
[0608] (Ссылочный пример 7-53)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-(2-метоксиэтил)оксим (ссылочное соединение 7-53)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-(2-метоксиэтил)оксим, синтезированный таким же образом, как в ссылочном примере 6-44, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 79%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 375[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,49-7,41 (m, 2H), 7,31-7,24 (m, 1H), 5,33 (t, J=5,6 Гц, 1H), 4,60 (d, J=5,6 Гц, 2H), 4,13-4,05(m, 2H), 3,96-3,88 (m, 4H), 3,57-3,51 (m, 2H), 3,26 (s, 3H), 2,62-2,55 (m, 2H), 2,42-2,34 (m, 2H).
[0609] (Ссылочный пример 7-54)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{2,2-диметил-3-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 7-54)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{2,2-диметил-3-[(тетрагидропиран-2-ил)окси]пропил}оксим, синтезированный таким же образом, как в ссылочном примере 6-45. В результате указанное в заголовке соединение (выход 89%) было получено в виде белой пены.
Масс-спектр (CI, m/z): 487[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,5 Гц, 2H), 7,46-7,39 (m, 1H), 7,35-7,19 (m, 2H), 4,86-4,80 (m, 2H), 4,60-4,56 (m, 1H), 4,03-3,97 (m, 4H), 3,95-3,89 (m, 2H), 3,88-3,80 (m, 1H), 3,56 (d, J=9,3 Гц, 1H), 3,53-3,45 (m, 1H), 3,12 (d, J=9,3 Гц, 1H), 2,75-2,66 (m, 2H), 2,50-2,44 (m, 2H), 1,90-1,45 (m, 6H), 0,98 (s, 3H), 0,97 (s, 3H).
[0610] (Ссылочный пример 7-55)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{3-метил-3-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 7-55)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{3-метил-3-[(тетрагидропиран-2-ил)окси]бутил}оксим, синтезированный таким же образом, как в ссылочном примере 6-46. В результате указанное в заголовке соединение (выход 94%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 487[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,5 Гц, 2H), 7,45-7,40 (m, 1H), 7,34-7,27 (m, 1H), 7,25-7,21 (m, 1H), 4,83 (d, J=4,9 Гц, 2H), 4,80-4,77 (m, 1H), 4,25-4,15 (m, 2H), 4,07-3,89 (m, 5H), 3,51-3,41 (m, 1H), 2,71-2,64 (m, 2H), 2,50-2,43 (m, 2H), 1,97-1,80 (m, 4H), 1,74-1,60 (m, 1H), 1,55-1,40 (m, 4H), 1,28 (s, 3H), 1,26 (s, 3H).
[0611] (Ссылочный пример 7-56)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{2-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 7-56)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{2-[(тетрагидропиран-2-ил)окси]пропил}оксим, синтезированный таким же образом, как в ссылочном примере 71. В результате указанное в заголовке соединение (выход 94%) было получено в виде светло-желтой пены.
Масс-спектр (DUIS, m/z): 459[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,55-8,51 (m, 2H), 7,46-7,40 (m, 1H), 7,35-7,29 (m, 1H), 7,25-7,20 (m, 1H), 4,83 (s, 2H), 4,81-4,73 (m, 1H), 4,19-4,07 (m, 2H), 4,07-3,90 (m, 6H), 3,62-3,42 (m, 1H), 2,75-2,65 (m, 2H), 2,50-2,43 (m, 2H), 1,93-1,44 (m, 7H), 1,26-1,11 (m, 3H).
[0612] (Ссылочный пример 7-57)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{2-метил-3-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 7-57)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{2-метил-3-[(тетрагидропиран-2-ил)окси]пропил}оксим, синтезированный таким же образом, как в ссылочном примере 6-47. В результате указанное в заголовке соединение (выход 78%) было получено в виде белой пены.
Масс-спектр (CI, m/z): 473[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,5 Гц, 2H), 7,45-7,39 (m, 1H), 7,35-7,20 (m, 2H), 4,83 (d, J=6,0 Гц, 2H), 4,61-4,58 (m, 1H), 4,12-3,24 (m, 10H), 2,73-2,65 (m, 2H), 2,50-2,43 (m, 2H), 2,24-2,13 (m, 1H), 1,89-1,46 (m, 7H), 1,04-0,98 (m, 3H).
[0613] (Ссылочный пример 7-58)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим (ссылочное соединение 7-58)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 6-48. В результате указанное в заголовке соединение (выход 85%) было получено в виде белого твердого вещества.
Масс-спектр (EI, m/z): 444[М]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,5 Гц, 2H), 7,45-7,40 (m, 1H), 7,34-7,28 (m, 1H), 7,26-7,21 (m, 1H), 4,83 (d, J=6,1 Гц, 2H), 4,12 (d, J=6,9 Гц, 2H), 4,03-3,96 (m, 6H), 3,77 (dd, J=6,5, 12,0 Гц, 2H), 2,70-2,65 (m, 2H), 2,48-2,43 (m, 2H), 2,19-2,10 (m, 1H), 1,82 (t, J=6,1 Гц, 1H), 1,44 (s, 3H), 1,42 (s, 3H).
[0614] (Ссылочный пример 7-59)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[(2,2,5-триметил-1,3-диоксан-5-ил)метил]оксим (ссылочное соединение 7-59)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[(2,2,5-триметил-1,3-диоксан-5-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 6-49. В результате указанное в заголовке соединение (выход 76%) было получено в виде белой пены.
Масс-спектр (CI, m/z): 459[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,4 Гц, 2H), 7,45-7,39 (m, 1H), 7,35-7,21 (m, 7H), 4,86-4,80 (m, 2H), 4,11 (s, 2H), 4,03-3,97 (m, 4H), 3,75 (d, J=11,9 Гц, 2H), 3,58 (d, J=11,9 Гц, 2H), 2,71-2,66 (m, 2H), 2,51-2,44 (m, 2H), 1,85-1,78 (m, 1H), 1,44 (s, 3H), 1,42 (s, 3H), 0,95 (s, 3H).
[0615] (Ссылочный пример 7-60)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим (ссылочное соединение 7-60)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 6-50. В результате указанное в заголовке соединение (выход 81%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 431[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,49-7,41 (m, 2H), 7,31-7,24 (m, 1H), 5,32 (t, J=5,7 Гц, 1H), 4,60 (d, J=5,7 Гц, 2H), 4,31-4,25(m, 1H), 4,07-3,97 (m, 3H), 3,97-3,88 (m, 4H), 3,67 (dd, J=6,5. 8,3 Гц, 1H), 2,62-2,55 (m, 2H), 2,43-2,33 (m, 2H), 1,33 (s, 3H), 1,28 (s, 3H).
[0616] (Ссылочный пример 7-61)
2-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этилацетат (ссылочное соединение 7-61)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этилацетат, синтезированный таким же образом, как в ссылочном примере 6-51. В результате указанное в заголовке соединение (выход 81%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 403[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,49-7,41 (m, 2H), 7,30-7,25 (m, 1H), 5,33 (t, J=5,3 Гц, 1H), 4,60 (d, J=5,3 Гц, 2H), 4,27-4,12 (m, 4H), 3,96-3,89 (m, 4H), 2,64-2,54 (m, 2H), 2,44-2,32 (m, 2H), 2,03 (s, 3H).
[0617] (Ссылочный пример 7-62)
трет-Бутил-2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}ацетат (ссылочное соединение 7-62)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на трет-бутил-2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]ацетат, синтезированный таким же образом, как в ссылочном примере 6-52. В результате указанное в заголовке соединение (выход 46%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 403[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,48-7,42 (m, 1H), 7,34-7,21 (m, 2H), 4,99-4,88 (m, 4H), 4,83 (br s, 2H), 4,52 (s, 2H), 1,50 (s, 9H).
[0618] (Ссылочный пример 7-63)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-диметилкарбамоилоксим (ссылочное соединение 7-63)
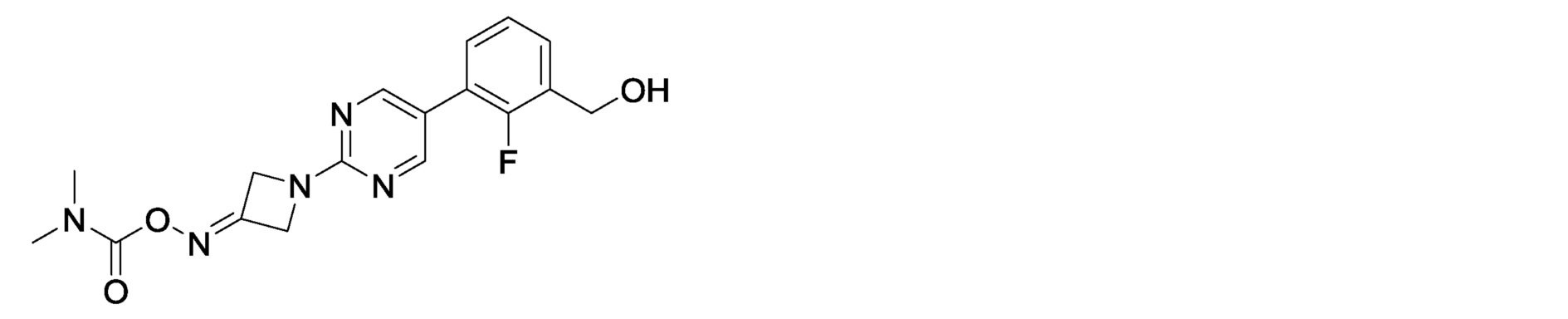
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-диметилкарбамоилоксим, синтезированный таким же образом, как в ссылочном примере 15-4. В результате указанное в заголовке соединение (выход 49%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 360[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,58 (d, J=1,4 Гц, 2H), 7,50-7,44 (m, 1H), 7,35-7,23 (m, 2H), 5,04-4,95 (m, 4H), 4,84 (s, 2H), 3,02 (br s, 3H), 2,96 (br s, 3H).
[0619] (Ссылочный пример 7-64)
2-({[1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден]амино}окси)-N-метилацетамид (ссылочное соединение 7-64)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-N-метилацетамид, синтезированный таким же образом, как в ссылочном примере 6-53. В результате указанное в заголовке соединение (выход 64%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 360[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,59 (d, J=1,5 Гц, 2H), 7,50-7,43 (m, 1H), 7,35-7,22 (m, 2H), 6,16 (br s, 1H), 4,96-4,90 (m, 4H), 4,84 (d, J=5,8 Гц, 2H), 4,58 (s, 2H), 2,91 (d, J=4,9 Гц, 3H), 1,86 (t, J=5,8 Гц, 1H).
[0620] (Ссылочный пример 7-65)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил)пиримидин-2-ил)азетидин-3-илиден]амино}окси)пропанамид (ссылочное соединение 7-65)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]пропанамид, синтезированный таким же образом, как в ссылочном примере 6-54, что не проводили очистку с помощью колоночной хроматографии на силикагеле, и что к продукту добавляли этилацетат, и смесь перемешивали при комнатной температуре и после этого фильтровали с получением твердого вещества. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого твердого вещества.
Масс-спектр (ESI, m/z): 360[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,3 Гц, 2H), 7,55-7,47 (m, 1H), 7,47-7,36 (m, 2H), 7,31-7,25 (m, 1H), 6,86 (br s, 1H), 4,85-4,74 (m, 4H), 4,59 (s, 2H), 4,22 (t, J=6,5 Гц, 2H), 2,42 (t, J=6,5 Гц, 2H).
[0621] (Ссылочный пример 7-66)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-N-метилпропанамид (ссылочное соединение 7-66)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-N-метилпропанамид, синтезированный таким же образом, как в ссылочном примере 6-55, и не проводили очистку с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,5 Гц, 2H), 8,05-7,88 (m, 1H), 7,53-7,47 (m, 1H), 7,46-7,38 (m, 1H), 7,32-7,23 (m, 1H), 4,86-4,73 (m, 4H), 4,59 (s, 2H), 4,22 (t, J=6,5 Гц, 2H), 2,57 (d, J=3,4 Гц, 3H), 2,43 (t, J=6,5 Гц, 2H).
[0622] (Ссылочный пример 7-67)
Этил-4-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}бутаноат (ссылочное соединение 7-67)
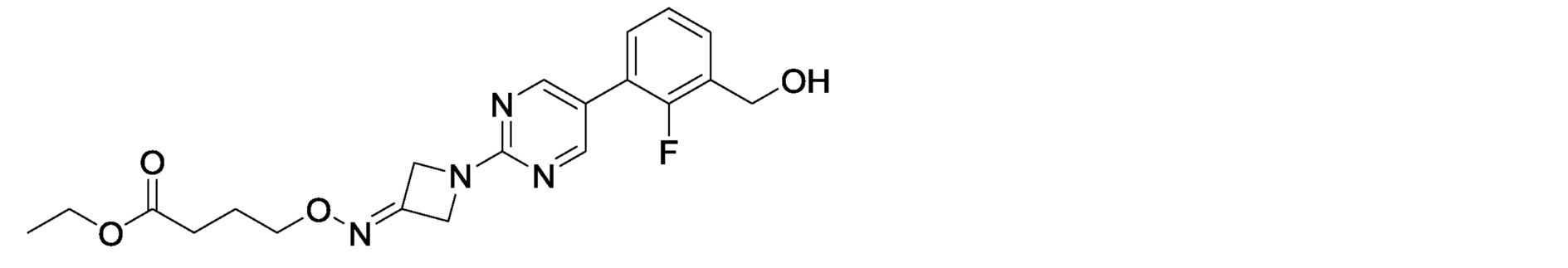
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на этил-4-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутаноат, синтезированный таким же образом, как в ссылочном примере 6-56. В результате указанное в заголовке соединение (выход 82%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 403[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,52-7,41 (m, 2H), 7,31-7,26 (m, 1H), 5,34 (t, J=4,1 Гц, 1H), 4,90-4,74 (m, 4H), 4,60 (d, J=4,1 Гц, 2H), 4,11-4,01 (m, 4H), 2,38 (t, J=7,3 Гц, 2H), 1,92-1,82 (m, 2H), 1,18 (t, J=7,2 Гц, 3H).
[0623] (Ссылочный пример 7-68)
4-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-N-метилбутанамид (ссылочное соединение 7-68)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 4-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-N-метилбутанамид, синтезированный таким же образом, как в ссылочном примере 6-57, и что к концентрированному остатку вместо TBME добавляли этилацетат, и смесь перемешивали при комнатной температуре. В результате указанное в заголовке соединение (выход 64%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 388[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,5 Гц, 2H), 7,48-7,43 (m, 1H), 7,34-7,21 (m, 2H), 5,48 (br s, 1H), 4,92-4,79 (m, 6H), 4,13 (t, J=6,1 Гц, 2H), 2,83 (d, J=4,9 Гц, 3H), 2,31-2,25 (m, 2H), 2,08-1,99 (m, 2H), 1,90 (br s, 1H).
[0624] (Ссылочный пример 7-69)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(диметиламино)этил]оксим (ссылочное соединение 7-69)
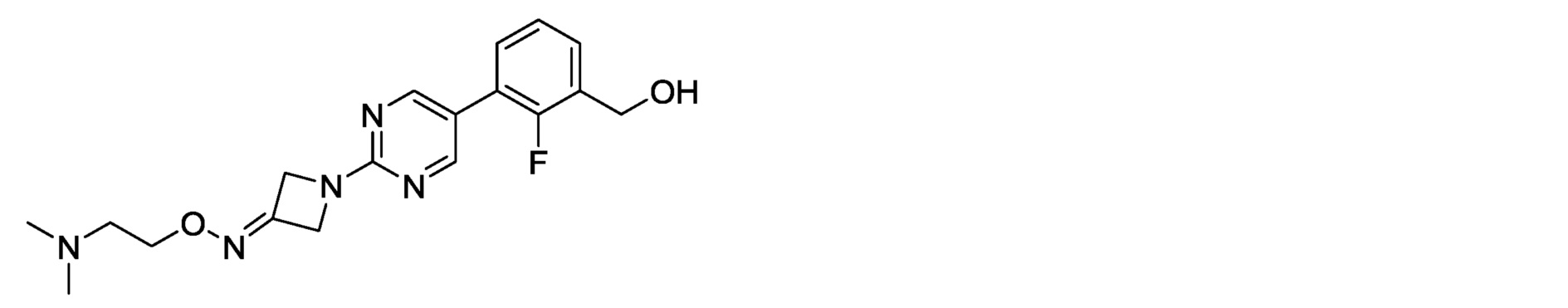
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(диметиламино)этил]оксим, синтезированный таким же образом, как в ссылочном примере 83, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 16%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 360[М+1]+.
[0625] (Ссылочный пример 7-70)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-{2-[бензил(метил)амино]этил}оксим (ссылочное соединение 7-70)
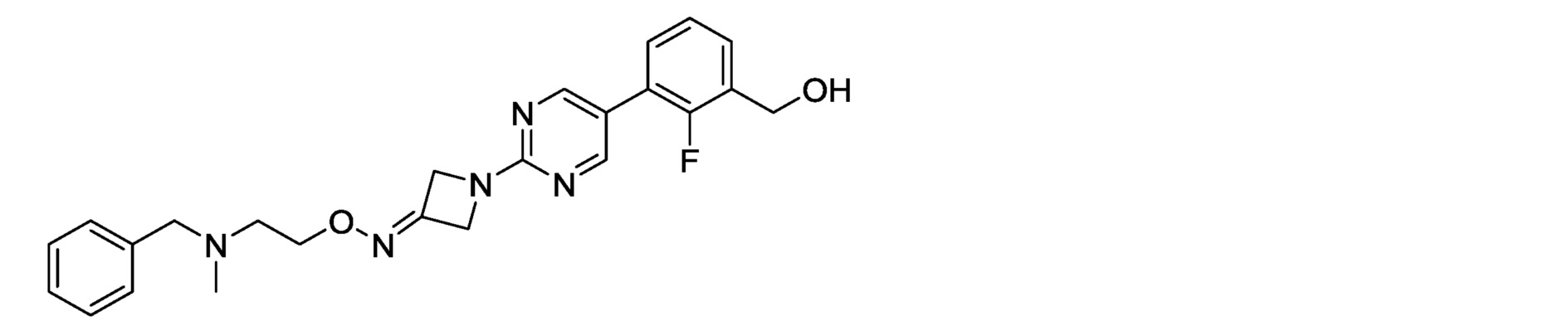
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси)метил)-2-фторфенил)пиримидин-2-ил)азетидин-3-она O-{2-[бензил(метил)амино]этил}оксим, синтезированный таким же образом, как в ссылочном примере 84-1. В результате указанное в заголовке соединение (с количественным выходом) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 436[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,53-7,41 (m, 2H), 7,35-7,17 (m, 6H), 5,34 (t, J=5,6 Гц, 1H), 4,82-4,75 (m, 4H), 4,60 (d, J=5,6 Гц, 2H), 4,14 (t, J=6,0 Гц, 2H), 3,52 (s, 2H), 2,62 (t, J=6,0 Гц, 2H), 2,20 (s, 3H).
[0626] (Ссылочный пример 7-71)
N-(3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)ацетамид (ссылочное соединение 7-71)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на N-{3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропил}ацетамид, синтезированный таким же образом, как в ссылочном примере 87-1. В результате указанное в заголовке соединение (выход 97%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 502[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,88-7,80 (m, 1H), 7,52-7,41 (m, 2H), 7,34-7,26 (m, 1H), 5,34 (t, J=5,6 Гц, 1H), 4,89-4,76(m, 4H), 4,60 (d, J=5,6 Гц, 2H), 4,56-4,52 (m, 1H), 4,13-3,95 (m, 2H), 3,80-3,55 (m, 2H), 3,48-3,26 (m, 2H), 3,17-3,08 (m, 2H), 2,17-2,05 (m, 1H), 1,81 (s, 3H), 1,77-1,39 (m, 6H).
[0627] (Ссылочный пример 7-72)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[3-(диметиламино)-2-{[(тетрагидропиран-2-ил)окси]метил}пропил]оксим (ссылочное соединение 7-72)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[3-(диметиламино)-2-{[(тетрагидропиран-2-ил)окси]метил}пропил]оксим, синтезированный таким же образом, как в ссылочном примере 88. В результате указанное в заголовке соединение (выход 38%) было получено в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,52-7,41 (m, 2H), 7,32-7,26 (m, 1H), 5,40-5,28 (m, 1H), 4,91-4,74 (m, 4H), 4,63-4,59 (m,2H), 4,57-4,52 (m, 1H), 4,10-4,02 (m, 2H), 3,81-3,57 (m, 2H), 3,47-3,34 (m, 2H), 2,30-2,19 (m, 2H), 2,18-2,09 (m, 7H), 1,81-1,39 (m, 6H).
[0628] (Ссылочный пример 7-73)
N-(3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}-2-метоксипропил)ацетамид (ссылочное соединение 7-73)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на N-{3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-метоксипропил}ацетамид, синтезированный таким же образом, как в ссылочном примере 87-2. В результате указанное в заголовке соединение (выход 68%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 418[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,1 Гц, 2H), 7,88 (t, J=5,5 Гц, 1H), 7,54-7,37 (m, 2H), 7,34-7,23 (m, 1H), 5,32 (t, J=5,7 Гц, 1H), 4,89-4,77(m, 4H), 4,60 (d, J=5,7 Гц, 2H), 4,13-3,95 (m, 2H), 3,54-3,43 (m, 1H), 3,34 (s, 3H), 3,25-3,08 (m, 2H), 1,83 (s, 3H).
[0629] (Ссылочный пример 7-74)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(пиперидин-1-ил)этил]оксим (ссылочное соединение 7-74)
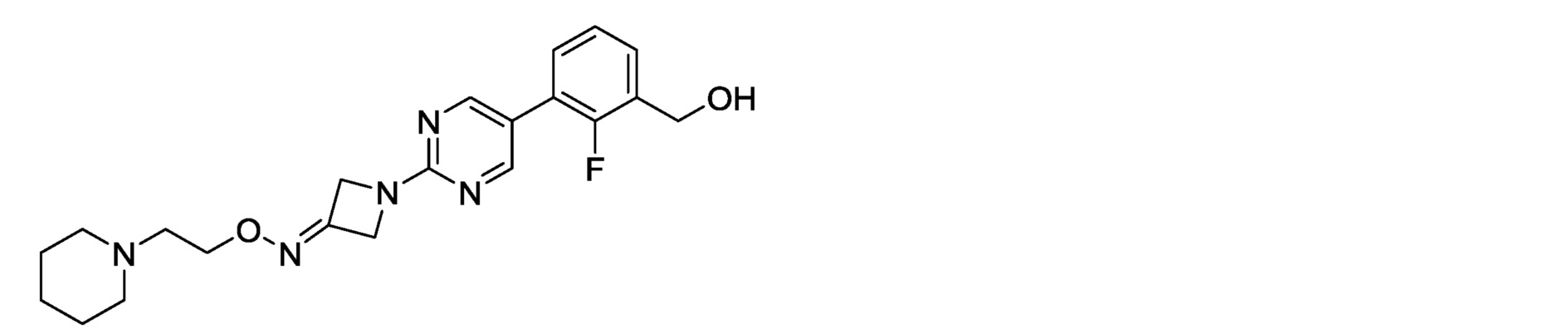
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(пиперидин-1-ил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 84-2. В результате указанное в заголовке соединение (выход 94%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 400[М+1]+.
1H-ЯМР (400 МГц, CDCl3) δ: 8,57 (d, J=1,5 Гц, 2H), 7,49-7,42 (m, 1H), 7,35-7,21 (m, 2H), 4,91-4,86 (m, 4H), 4,83 (s, 2H), 4,25 (t, J=6,0 Гц, 2H), 2,67 (t, J=6,0 Гц, 2H), 2,53-2,42 (m, 4H), 1,69-1,39 (m, 6H).
[0630] (Ссылочный пример 7-75)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(2-морфолиноэтил)оксим (ссылочное соединение 7-75)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2-морфолиноэтил)оксим, синтезированный таким же образом, как в ссылочном примере 6-60. В результате указанное в заголовке соединение (выход 99%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 402[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,51-7,42 (m, 2H), 7,31-7,27 (m, 1H), 5,34 (t, J=5,3 Гц, 1H), 4,84-4,77 (m, 4H), 4,60 (d, J=5,3 Гц, 2H), 4,15 (t, J=6,0 Гц, 2H), 3,59-3,54 (m, 4H), 2,58 (t, J=6,0 Гц, 2H), 2,46-2,38 (m, 4H).
[0631] (Ссылочный пример 7-76)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(азетидин-1-ил)этил]оксим (ссылочное соединение 7-76)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(азетидин-1-ил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 6-61. В результате указанное в заголовке соединение (выход 78%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 372[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,4 Гц, 2H), 7,51-7,42 (m, 2H), 7,32-7,26 (m, 1H), 5,34 (t, J=5,5 Гц, 1H), 4,85-4,75 (m, 4H), 4,60 (d, J=5,5 Гц, 2H), 3,97 (t, J=5,8 Гц, 2H), 3,16-3,09 (m, 4H), 2,59 (t, J=5,8 Гц, 2H), 2,07-1,78 (m, 2H).
[0632] (Ссылочный пример 7-77)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(3,3-дифторазетидин-1-ил)этил]оксим (ссылочное соединение 7-77)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(3,3-дифторазетидин-1-ил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 84-3. В результате указанное в заголовке соединение (выход 72%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 408[М+1]+.
1H-ЯМР (400 МГц, CDCl3) δ: 8,57 (d, J=1,5 Гц, 2H), 7,49-7,42 (m, 1H), 7,36-7,21 (m, 2H), 4,93-4,80 (m, 6H), 4,17 (t, J=5,3 Гц, 2H), 3,66 (t, J=12,0 Гц, 4H), 2,88 (t, J=5,3 Гц, 2H).
[0633] (Ссылочный пример 7-78)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(3-фторазетидин-1-ил)этил]оксим (ссылочное соединение 7-78)
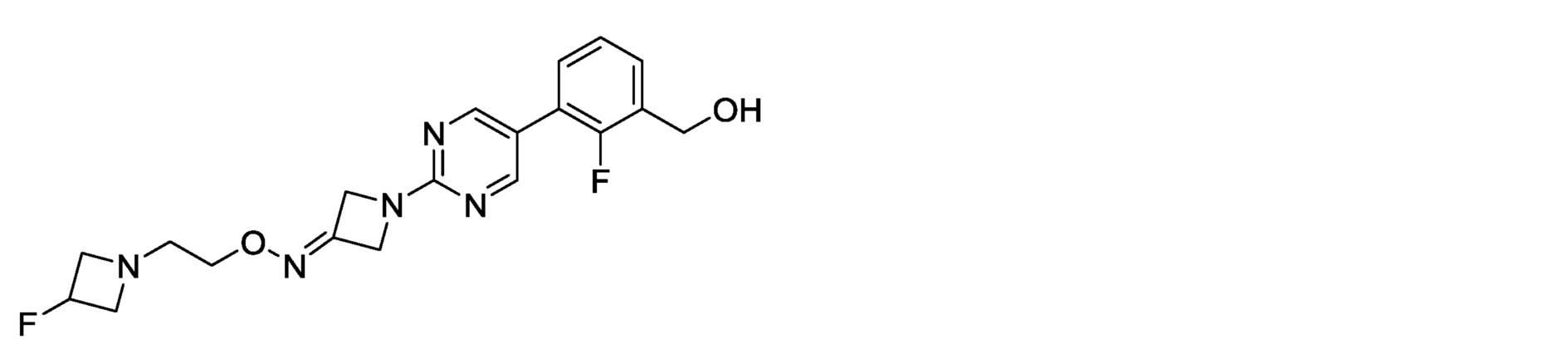
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(3-фторазетидин-1-ил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 84-4. В результате указанное в заголовке соединение (выход 78%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 390[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,52-7,41 (m, 2H), 7,32-7,25 (m, 1H), 5,33 (t, J=5,7 Гц, 1H), 5,24-5,02 (m, 1H), 4,88-4,75 (m, 4H), 4,60 (d, J=5,7 Гц, 2H), 4,02 (t, J=5,5 Гц, 2H), 3,65-3,53 (m, 2H), 3,20-3,05 (m, 2H), 2,71 (t, J=5,5 Гц, 2H).
[0634] (Ссылочный пример 7-79)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[2-(3-метоксиазетидин-1-ил)этил]оксим (ссылочное соединение 7-79)
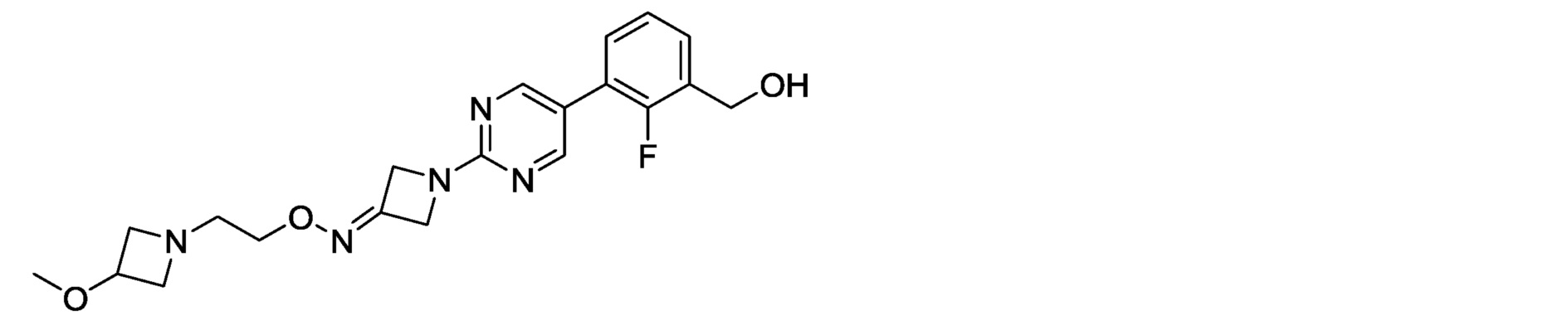
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(3-метоксиазетидин-1-ил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 84-5. В результате указанное в заголовке соединение (выход 66%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 402[М+1]+.
1H-ЯМР(400 МГц, DMSO-d6) δ: 8,62 (d, J=1,4 Гц, 2H), 7,52-7,40 (m, 2H), 7,32-7,25 (m, 1H), 5,33 (t, J=5,7 Гц, 1H), 4,86-4,75 (m, 4H), 4,60 (d, J=5,7 Гц, 2H), 4,03-3,88 (m, 3H), 3,55-3,48 (m, 2H), 3,13 (s, 3H), 2,86-2,78 (m, 2H), 2,69-2,61 (m, 2H).
[0635] (Ссылочный пример 7-80)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[(4-метилморфолин-2-ил)метил]оксим (ссылочное соединение 7-80)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[(4-метилморфолин-2-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 6-62. В результате указанное в заголовке соединение (выход 79%) было получено в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,51-7,42 (m, 2H), 7,32-7,26 (m, 1H), 5,34 (t, J=5,5 Гц, 1H), 4,86-4,78 (m, 4H), 4,60 (d, J=5,5 Гц, 2H), 4,06-3,93 (m, 2H), 3,80-3,74 (m, 1H), 3,74-3,66 (m, 1H), 3,53-3,45 (m, 1H), 2,73-2,68 (m, 1H), 2,60-2,53 (m, 1H), 2,17 (s, 3H), 2,00-1,92 (m, 1H), 1,77-1,71 (m, 1H).
[0636] (Ссылочный пример 7-81)
1-[2-({[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино)окси]метил)морфолино}этанон (ссылочное соединение 7-81)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-(2-{[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]метил}морфолино)этанон, синтезированный таким же образом, как в ссылочном примере 6-63. В результате указанное в заголовке соединение (выход 74%) было получено в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,51-7,42 (m, 2H), 7,32-7,26 (m, 1H), 5,34 (t, J=5,7 Гц, 1H), 4,86-4,79 (m, 4H), 4,60 (d, J=5,7 Гц, 2H), 4,33-3,98 (m, 3H), 3,88-3,82 (m, 1H), 3,79-3,52 (m, 2H), 3,49-3,26 (m, 1H), 3,21-2,92 (m, 1H), 2,73-2,45 (m, 1H), 2,03-1,98 (m,3H).
[0637] (Ссылочный пример 7-82)
5-({[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}метил)дигидрофуран-2(3H)-он (ссылочное соединение 7-82)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 5-{[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]метил}дигидрофуран-2(3H)-он, синтезированный таким же образом, как в ссылочном примере 15-5. В результате указанное в заголовке соединение (выход 72%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 387[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,49-7,43 (m, 1H), 7,35-7,21 (m, 2H), 4,92-4,86 (m, 4H), 4,86-4,76 (m, 3H), 4,33-4,20 (m, 2H), 2,60-2,53 (m, 2H), 2,41-2,31 (m, 1H), 2,16-2,04 (m, 1H), 1,89-1,81 (m, 1H).
[0638] (Ссылочный пример 7-83)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}циклобутилацетат (ссылочное соединение 7-83)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]циклобутилацетат, синтезированный таким же образом, как в ссылочном примере 6-64, и температуру реакции изменяли на 0°C. В результате указанное в заголовке соединение (выход 82%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 401[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,51-7,42 (m, 2H), 7,32-7,27 (m, 1H), 5,34 (t, J=5,7 Гц, 1H), 5,08-5,01 (m, 1H), 4,86-4,79 (m, 5H), 4,60 (d, J=5,7 Гц, 2H), 2,51-2,44 (m, 2H), 2,40-2,31 (m, 2H), 2,01 (s, 3H).
[0639] (Ссылочный пример 7-84)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-бензилоксим (ссылочное соединение 7-84)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-бензилоксим, синтезированный таким же образом, как в ссылочном примере 6-65. В результате указанное в заголовке соединение (выход 68%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 379[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,5 Гц, 2H), 7,51-7,26 (m, 8H), 5,34 (t, J=5,6 Гц, 1H), 5,09 (s, 2H), 4,83 (s, 4H), 4,60 (d, J=5,6 Гц, 2H).
[0640] (Ссылочный пример 7-85)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(4-метоксибензил)оксим (ссылочное соединение 7-85)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил)азетидин-3-она O-(4-метоксибензил)оксим, синтезированный таким же образом, как в ссылочном примере 15-6. В результате указанное в заголовке соединение (выход 98%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 409[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,55 (d, J=1,5 Гц, 2H), 7,48-7,41 (m, 1H), 7,35-7,20 (m, 4H), 6,93-6,87 (m, 2H), 5,05 (s, 2H), 4,90-4,80 (m, 6H), 3,82 (s, 3H), 1,84 (t, J=5,9 Гц, 1H).
[0641] (Ссылочный пример 7-86)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(1-метилазетидин-3-ил)оксим (ссылочное соединение 7-86)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(1-метилазетидин-3-ил)оксим, синтезированный таким же образом, как в ссылочном примере 6-66. В результате указанное в заголовке соединение (включая примеси) было получено в виде коричневого масла.
Масс-спектр (ESI, m/z): 358[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,54-7,37 (m, 2H), 7,35-7,20 (m, 1H), 4,87-4,79 (m, 4H), 4,75-4,65 (m, 1H), 4,59 (s, 2H), 3,58-3,46 (m, 2H), 3,04-2,92 (m, 2H), 2,25 (s, 3H).
[0642] (Ссылочный пример 7-87)
1-(3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}азетидин-1-ил)этанон (ссылочное соединение 7-87)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-{3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-ил}этанон, синтезированный таким же образом, как в ссылочном примере 6-67. В результате указанное в заголовке соединение (включая примеси) было получено в виде желтого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,55-7,37 (m, 2H), 7,33-7,21 (m, 1H), 5,01-4,92 (m, 1H), 4,90-4,83 (m, 4H), 4,60 (s, 2H), 4,42-4,32 (m, 1H), 4,15-4,03 (m, 2H), 3,83-3,72 (m, 1H), 1,78 (s, 3H).
[0643] (Ссылочный пример 7-88)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(1-бензилазетидин-3-ил)оксим (ссылочное соединение 7-88)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(1-бензилазетидин-3-ил)оксим, синтезированный таким же образом, как в ссылочном примере 6-68. В результате указанное в заголовке соединение (выход 82%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 434[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,51-7,42 (m, 2H), 7,33-7,21 (m, 6H), 5,34 (t, J=5,5 Гц, 1H), 4,86-4,75 (m, 5H), 4,60 (d, J=5,5 Гц, 2H), 3,60 (s, 2H), 3,55-3,47 (m, 2H), 3,11-3,03 (m, 2H).
[0644] (Ссылочный пример 7-89)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[1-(2,2,2-трифторэтил)азетидин-3-ил]оксим (ссылочное соединение 7-89)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[1-(2,2,2-трифторэтил)азетидин-3-ил]оксим, синтезированный таким же образом, как в ссылочном примере 6-69. В результате указанное в заголовке соединение (выход 81%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 426[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,51-7,42 (m, 2H), 7,32-7,26 (m, 1H), 5,34 (t, J=5,7 Гц, 1H), 4,86-4,78 (m, 5H), 4,60 (d, J=5,7 Гц, 2H), 3,71-3,65 (m, 2H), 3,37-3,30 (m, 2H), 3,25 (q, J=10,1 Гц, 2H).
[0645] (Ссылочный пример 7-90)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[1-(метилсульфонил)азетидин-3-ил]оксим (ссылочное соединение 7-90)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[1-(метилсульфонил)азетидин-3-ил]оксим, синтезированный таким же образом, как в ссылочном примере 6-70. В результате указанное в заголовке соединение (выход 79%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 422[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (d, J=1,4 Гц, 2H), 7,54-7,40 (m, 2H), 7,33-7,25 (m, 1H), 5,34 (t, J=5,5 Гц, 1H), 4,96 (tt, J=4,6, 6,7 Гц, 1H), 4,90-4,83 (m, 4H), 4,60 (d, J=5,5 Гц, 2H), 4,14 (dd, J=6,7, 9,9 Гц, 2H), 3,92 (dd, J=4,6, 9,9 Гц, 2H), 3,04 (s, 3H).
[0646] (Ссылочный пример 7-91)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(1-этилазетидин-3-ил)оксим (ссылочное соединение 7-91)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(1-этилазетидин-3-ил)оксим, синтезированный таким же образом, как в ссылочном примере 6-71. В результате указанное в заголовке соединение (выход 78%) было получено в виде коричневого масла.
Масс-спектр (CI, m/z): 372[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,51-7,42 (m, 2H), 7,32-7,26 (m, 1H), 5,34 (t, J=5,4 Гц, 1H), 4,87-4,80 (m, 4H), 4,77-4,69 (m, 1H), 4,60 (d, J=5,4 Гц, 2H), 3,51-3,44 (m, 2H), 2,97-2,90 (m, 2H), 2,41 (q, J=7,2 Гц, 2H), 0,87 (t, J=7,2 Гц, 3H).
[0647] (Ссылочный пример 7-92)
Метил-3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}азетидин-1-карбоксилат (ссылочное соединение 7-92)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на метил-3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-карбоксилат, синтезированный таким же образом, как в ссылочном примере 6-72. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 402[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,53-7,40 (m, 2H), 7,34-7,22 (m, 1H), 5,35 (t, J=5,3 Гц, 1H), 5,00-4,93 (m, 1H), 4,89-4,82 (m, 4H), 4,60 (d, J=5,3 Гц, 2H), 4,25-4,10 (m, 2H), 3,97-3,83 (m, 2H), 3,57 (s, 3H).
[0648] (Ссылочный пример 7-93)
1-(5-(2-Фтор-3-(гидроксиметил)фенил)пиримидин-2-ил)азетидин-3-она O-оксетан-3-илоксим (ссылочное соединение 7-93)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-оксетан-3-илоксим, синтезированный таким же образом, как в ссылочном примере 6-73. В результате указанное в заголовке соединение (выход 59%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 345[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64 (d, J=1,1 Гц, 2H), 7,53-7,41 (m, 2H), 7,33-7,25 (m, 1H), 5,34 (t, J=5,7 Гц, 1H), 5,25-5,18 (m, 1H), 4,91-4,83(m, 4H), 4,80-4,72 (m, 2H), 4,60 (d, J=5,7 Гц, 2H), 4,58-4,52 (m, 2H).
[0649] (Ссылочный пример 7-94)
2-(3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}азетидин-1-ил)этилацетат (ссылочное соединение 7-94)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 2-{3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]азетидин-1-ил}этилацетат, синтезированный таким же образом, как в ссылочном примере 6-74, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 91%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 430[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,51-7,42 (m, 2H), 7,32-7,26 (m, 1H), 5,33 (t, J=5,5 Гц, 1H), 4,88-4,79 (m, 4H), 4,79-4,71 (m, 1H), 4,60 (d, J=5,5 Гц, 2H), 3,96 (t, J=5,6 Гц, 2H), 3,58-3,52 (m, 2H), 3,10-3,04 (m, 2H), 2,65 (t, J=5,6 Гц, 2H), 2,00 (s, 3H).
[0650] (Ссылочный пример 7-95)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[1-(2-метоксиэтил)азетидин-3-ил]оксим (ссылочное соединение 7-95)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[1-(2-метоксиэтил)азетидин-3-ил]оксим, синтезированный таким же образом, как в ссылочном примере 6-75, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 71%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 402[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,51-7,42 (m, 2H), 7,32-7,26 (m, 1H), 5,33 (t, J=5,4 Гц, 1H), 4,85-4,80 (m, 4H), 4,77-4,70 (m, 1H), 4,60 (d, J=5,4 Гц, 2H), 3,56-3,48 (m, 2H), 3,29 (t, J=5,8 Гц, 2H), 3,21 (s, 3H), 3,08-3,01 (m, 2H), 2,57 (t, J=5,8 Гц, 2H).
[0651] (Ссылочный пример 7-96)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-[1-(2-фторэтил)азетидин-3-ил]оксим (ссылочное соединение 7-96)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[1-(2-фторэтил)азетидин-3-ил]оксим, синтезированный таким же образом, как в ссылочном примере 6-76, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 71%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 390[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,51-7,42 (m, 2H), 7,32-7,26 (m, 1H), 5,34 (t, J=5,3 Гц, 1H), 4,87-4,80 (m, 4H), 4,80-4,72 (m, 1H), 4,60 (d, J=5,3 Гц, 2H), 4,40 (td, J=4,8, 47,7 Гц, 2H), 3,61-3,53 (m, 2H), 3,15-3,05 (m, 2H), 2,71 (td, J=4,8, 29,1 Гц, 2H).
[0652] (Ссылочный пример 7-97)
Этил-3-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}пропанoат (ссылочное соединение 7-97)
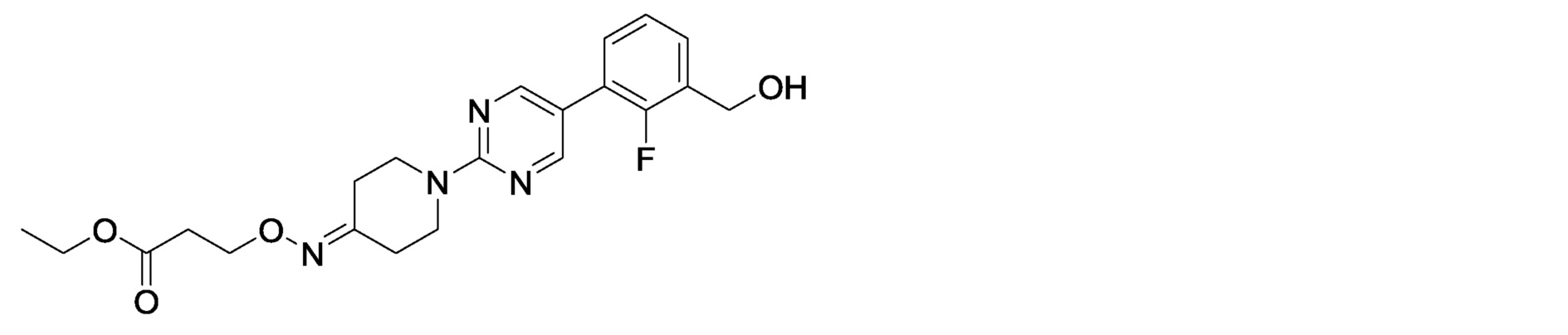
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на этил-3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]пропанoат, синтезированный таким же образом, как в ссылочном примере 6-77. В результате указанное в заголовке соединение (выход 39%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 417[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,51-7,41 (m, 2H), 7,32-7,24 (m, 1H), 7,32-7,24 (m, 1H), 5,37-5,30 (m, 1H), 4,63-4,57 (m, 2H), 4,20 (t, J=6,1 Гц, 2H), 4,07 (q, J=7,2 Гц, 2H), 3,95-3,87 (m, 4H), 2,65-2,60 (m, 2H), 2,53 (t, J=6,1 Гц, 2H), 2,41-2,35 (m, 2H), 1,18 (t, J=7,2 Гц, 3H).
[0653] (Ссылочный пример 7-98)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}пропанамид (ссылочное соединение 7-98)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]пропанамид, синтезированный таким же образом, как в ссылочном примере 6-78. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 388[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,5 Гц, 2H), 7,48-7,38 (m, 1H), 7,36-7,18 (m, 2H), 5,86 (br s, 1H), 5,31 (br s, 1H), 4,83 (s, 2H), 4,37-4,30 (m, 2H), 4,04-3,96 (m, 4H), 2,70-2,62 (m, 4H), 2,50-2,44 (m, 2H).
[0654] (Ссылочный пример 7-99)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}-N-метилпропанамид (ссылочное соединение 7-99)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]-N-метилпропанамид, синтезированный таким же образом, как в ссылочном примере 6-79, и не проводили очистку с помощью колоночной хроматографии на силикагеле. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде светло-желтого твердого вещества.
[0655] (Ссылочный пример 7-100)
Этил-4-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}бутаноат (ссылочное соединение 7-100)
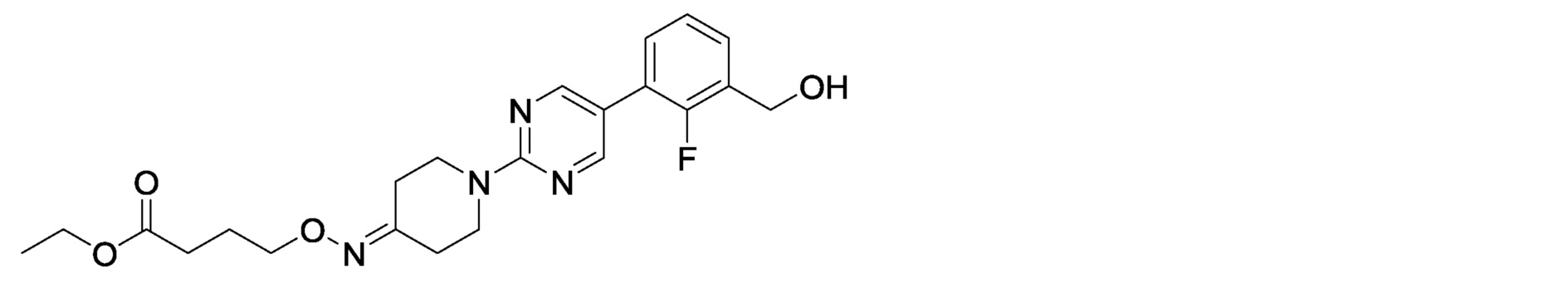
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на этил-4-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]бутаноат, синтезированный таким же образом, как в ссылочном примере 6-80. В результате указанное в заголовке соединение (выход 70%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 431[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,49-7,41 (m, 2H), 7,31-7,24 (m, 1H), 5,33 (t, J=5,7 Гц, 1H), 4,60 (d, J=5,7 Гц, 2H), 4,05 (q, J=7,2 Гц, 2H), 3,98 (t, J=6,4 Гц, 2H), 3,95-3,89 (m, 4H), 2,59-2,54 (m, 2H), 2,41-2,32 (m, 4H), 1,89-1,81 (m, 2H), 1,18 (t, J=7,2 Гц, 3H).
[0656] (Ссылочный пример 7-101)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}-N,N-диметилпропанамид (ссылочное соединение 7-101)
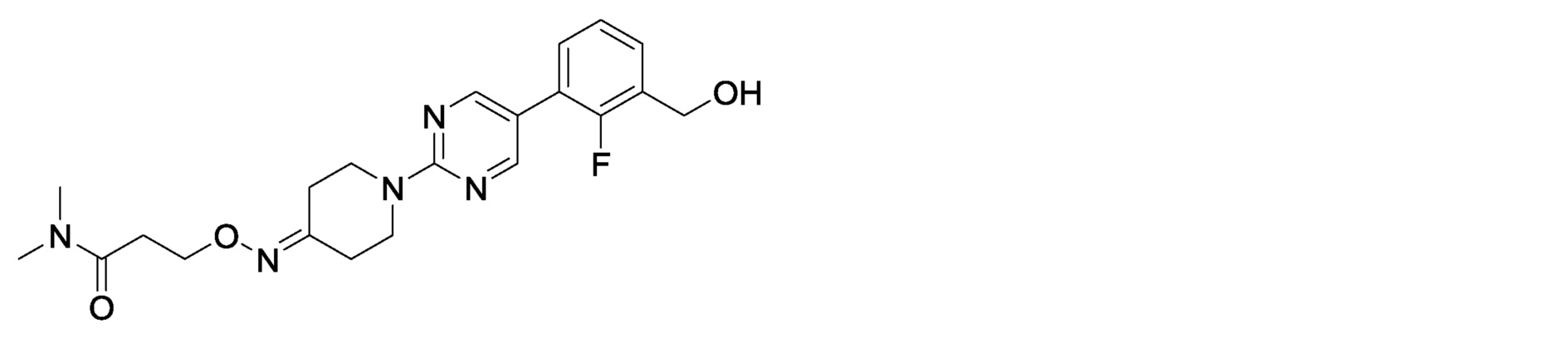
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]-N,N-диметилпропанамид, синтезированный таким же образом, как в ссылочном примере 6-81. В результате указанное в заголовке соединение (выход 71%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 416[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,49-7,41 (m, 2H), 7,31-7,24 (m, 1H), 5,36-5,31 (m, 1H), 4,63-4,57 (m, 2H), 4,19 (t, J=6,8 Гц, 2H), 3,95-3,89 (m, 4H), 2,96 (s, 3H), 2,81 (s, 3H), 2,65 (t, J=6,8 Гц, 2H), 2,58-2,52 (m, 2H), 2,41-2,36 (m, 2H).
[0657] (Ссылочный пример 7-102)
N-(2-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)ацетамид (ссылочное соединение 7-102)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на N-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}ацетамид, синтезированный таким же образом, как в ссылочном примере 87-5. В результате указанное в заголовке соединение (выход 94%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 402[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,96-7,89 (m, 1H), 7,51-7,40 (m, 2H), 7,32-7,24 (m, 1H), 5,34 (br. s, 1H), 4,60 (s, 2H), 4,05-3,83 (m, 6H), 3,32-3,22 (m, 2H),2,63-2,56 (m, 2H), 2,43-2,36 (m, 2H), 1,81 (s, 3H).
[0658] (Ссылочный пример 7-103)
N-(2-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)-N-метилацетамид (ссылочное соединение 7-103)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на N-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}-N-метилацетамид, синтезированный таким же образом, как в ссылочном примере 106. В результате указанное в заголовке соединение (с количественным выходом) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 416[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,50-7,41 (m, 2H), 7,31-7,24 (m, 1H), 5,33 (t, J=5,6 Гц, 1H), 4,60 (d, J=5,6 Гц, 2H), 4,17-4,02 (m, 2H), 3,96-3,88 (m, 4H), 3,58-3,47 (m, 2H), 3,01-2,77 (m, 3H), 2,60-2,54 (m, 2H), 2,42-2,35 (m, 2H), 2,00-1,96 (m, 3H).
[0659] (Ссылочный пример 7-104)
N-(2-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)-N-метилметансульфонамид (ссылочное соединение 7-104)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на N-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}-N-метилметансульфонамид, синтезированный таким же образом, как в ссылочном примере 108, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 83%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 452[М+1]+.
[0660] (Ссылочный пример 7-105)
трет-Бутил-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)(метилсульфонил)карбамат (ссылочное соединение 7-105)
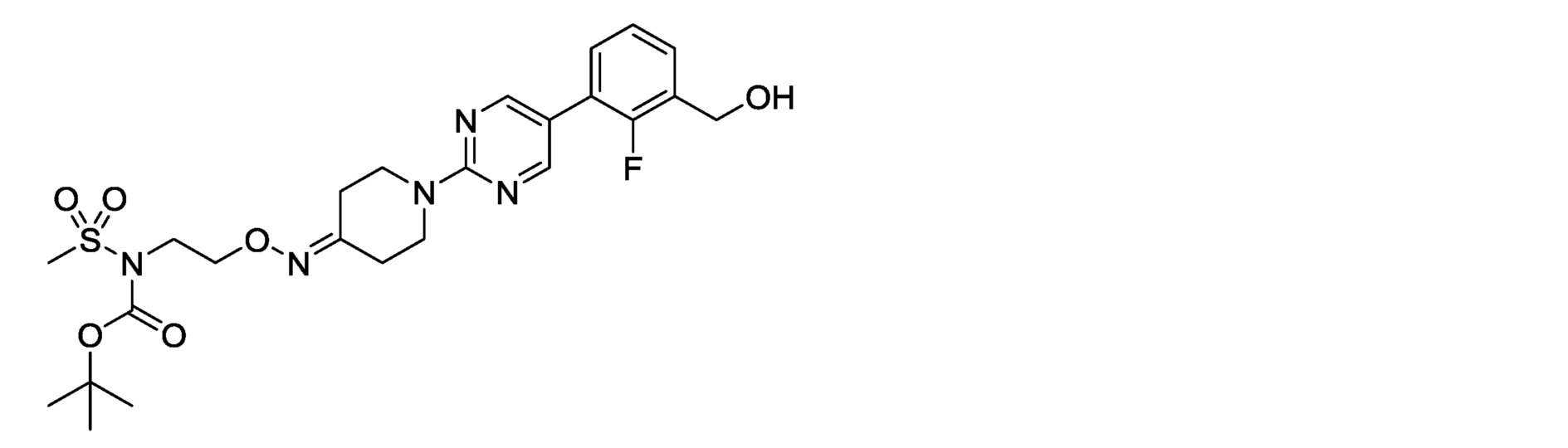
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на трет-бутил-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}(метилсульфонил)карбамат, синтезированный таким же образом, как в ссылочном примере 109-1. В результате указанное в заголовке соединение (выход 87%) было получено в виде бесцветного масла.
Масс-спектр (ESI, m/z): 538[М+1]+.
1H-ЯМР(400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,50-7,40 (m, 2H), 7,31-7,23 (m, 1H), 4,60 (s, 2H), 4,16-4,07 (m, 2H), 3,97-3,80 (m, 6H), 3,50-3,14 (m, 3H), 2,61-2,54 (m, 2H), 2,41-2,34 (m, 2H), 1,47 (s, 9H).
[0661] (Ссылочный пример 7-106)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[2-(диметиламино)этил]оксим (ссылочное соединение 7-106)
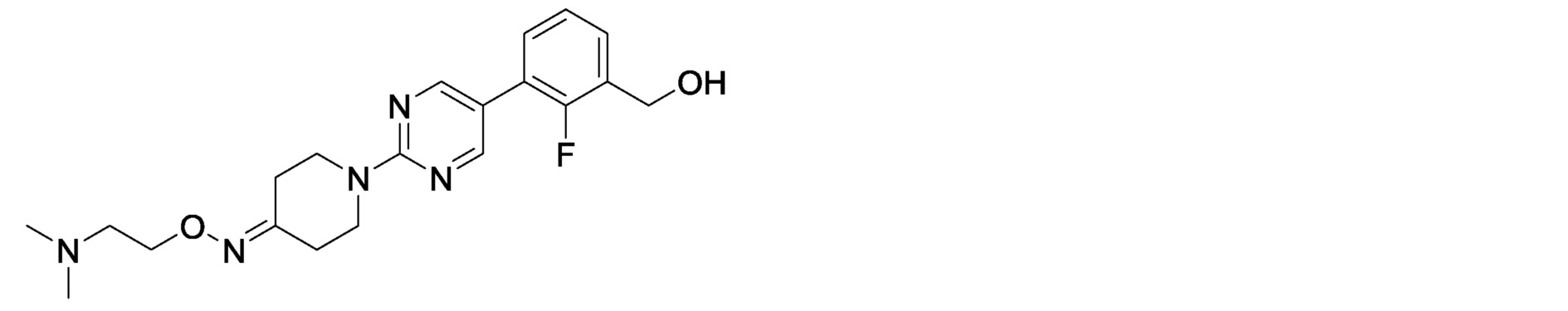
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[2-(диметиламино)этил]оксим, синтезированный таким же образом, как в ссылочном примере 6-83, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 16%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 388[М+1]+.
1H-ЯМР(400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,49-7,41 (m, 2H), 7,31-7,24 (m, 1H), 5,40-5,25 (m, 1H), 4,63-4,57 (m, 2H), 4,05 (t, J=6,1 Гц, 2H), 3,95-3,88 (m, 4H), 2,61-2,44 (m, 4H), 2,41-2,35 (m, 2H), 2,16 (s, 6H).
[0662] (Ссылочный пример 7-107)
трет-Бутил-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)(метил)карбамат (ссылочное соединение 7-107)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на трет-бутил-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}(метил)карбамат, синтезированный таким же образом, как в ссылочном примере 6-84. В результате указанное в заголовке соединение (выход 71%) было получено в виде бесцветного масла.
Масс-спектр (ESI, m/z): 474[М+1]+.
1H-ЯМР(400 МГц, CDCl3) δ: 8,53 (d, J=1,5 Гц, 2H), 7,47-7,39 (m, 1H), 7,35-7,29 (m, 1H), 7,28-7,20 (m, 1H), 4,83 (d, J=4,8 Гц, 2H), 4,21-4,09 (m, 3H), 4,05-3,95 (m, 4H), 3,55-3,43 (m, 2H), 2,96-2,85 (m, 3H), 2,72-2,64 (m, 2H), 2,51-2,43 (m, 2H), 1,46 (s, 9H).
[0663] (Ссылочный пример 7-108)
Ди-трет-бутил-(2-{[(1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)карбамат (ссылочное соединение 7-108)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на ди-трет-бутил-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}карбамат, синтезированный таким же образом, как в ссылочном примере 6-85. В результате указанное в заголовке соединение (выход 70%) было получено в виде бесцветного масла.
Масс-спектр (ESI, m/z): 560[М+1]+.
1H-ЯМР (400 МГц, CDCl3) δ: 8,53 (d, J=1,5 Гц, 2H), 7,46-7,40 (m, 1H), 7,35-7,28 (m, 1H), 7,28-7,20 (m, 1H), 4,83 (d, J=6,0 Гц, 2H), 4,22-4,16 (m, 2H), 4,04-3,94 (m, 4H), 3,94-3,86 (m, 2H), 2,69-2,63 (m, 2H), 2,49-2,42 (m, 2H), 1,85 (t, J=6,0 Гц, 1H), 1,51 (s, 18H).
[0664] (Ссылочный пример 7-109)
3-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}пропаннитрил (ссылочное соединение 7-109)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил)]пиперидин-4-илиден}амино)окси]пропаннитрил, синтезированный таким же образом, как в ссылочном примере 6-86. В результате указанное в заголовке соединение (выход 45%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 370[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,54 (d, J=1,5 Гц, 2H), 7,47-7,40 (m, 1H), 7,35-7,29 (m, 1H), 7,27-7,21 (m, 1H), 4,83 (d, J=6,0 Гц, 2H), 4,25 (t, J=6,3 Гц, 2H), 4,05-3,98 (m, 4H), 2,74 (t, J=6,3 Гц, 2H), 2,73-2,66 (m, 2H), 2,49-2,43 (m, 2H), 1,83 (t, J=6,0 Гц, 1H).
[0665] (Ссылочный пример 7-110)
4-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}бутаннитрил (ссылочное соединение 7-110)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 4-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]бутаннитрил, синтезированный таким же образом, как в ссылочном примере 6-87. В результате указанное в заголовке соединение (выход 78%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 384[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,50-7,41 (m, 2H), 7,30-7,25 (m, 1H), 5,38-5,30 (m, 1H), 4,64-4,56 (m, 2H), 4,04 (t, J=6,0 Гц, 2H), 3,96-3,90 (m, 4H), 2,63-2,58 (m, 2H), 2,55 (t, J=7,1 Гц, 2H), 2,43-2,35 (m, 2H), 1,95-1,84 (m, 2H).
[0666] (Ссылочный пример 7-111)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[2-(метилсульфонил)этил]оксим (ссылочное соединение 7-111)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[2-(метилсульфонил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 6-88. В результате указанное в заголовке соединение (выход 99%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 423[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,51-7,40 (m, 2H), 7,31-7,24 (m, 1H), 5,33 (t, J=5,5 Гц, 1H), 4,60 (d, J=5,5 Гц, 2H), 4,35 (t, J=5,8 Гц, 2H), 3,97-3,90 (m, 4H), 3,48 (t, J=5,8 Гц, 2H), 2,99 (s, 3H), 2,62-2,55 (m, 2H), 2,43-2,37 (m, 2H).
[0667] (Ссылочный пример 7-112)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[3-(метилсульфонил)пропил]оксим (ссылочное соединение 7-112)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[3-(метилсульфонил)пропил]оксим, синтезированный таким же образом, как в ссылочном примере 6-89. В результате указанное в заголовке соединение (выход 67%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 437[М+1]+.
1H-ЯМР спектр (400 МГц,CDCl3) δ: 8,54 (d, J=1,5 Гц, 2H), 7,47-7,39 (m, 1H), 7,35-7,20 (m, 2H), 4,83 (d, J=6,0 Гц, 2H), 4,17 (t, J=6,0 Гц, 2H), 4,06-3,95 (m, 4H), 3,17-3,12 (m, 2H), 2,93 (s, 3H), 2,70-2,63 (m, 2H), 2,50-2,42 (m, 2H), 2,30-2,18 (m, 2H), 1,81 (t, J=6,3 Гц, 1H).
[0668] (Ссылочный пример 7-113)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[(1-метил-1H-пиразол-3-ил)метил]оксим (ссылочное соединение 7-113)
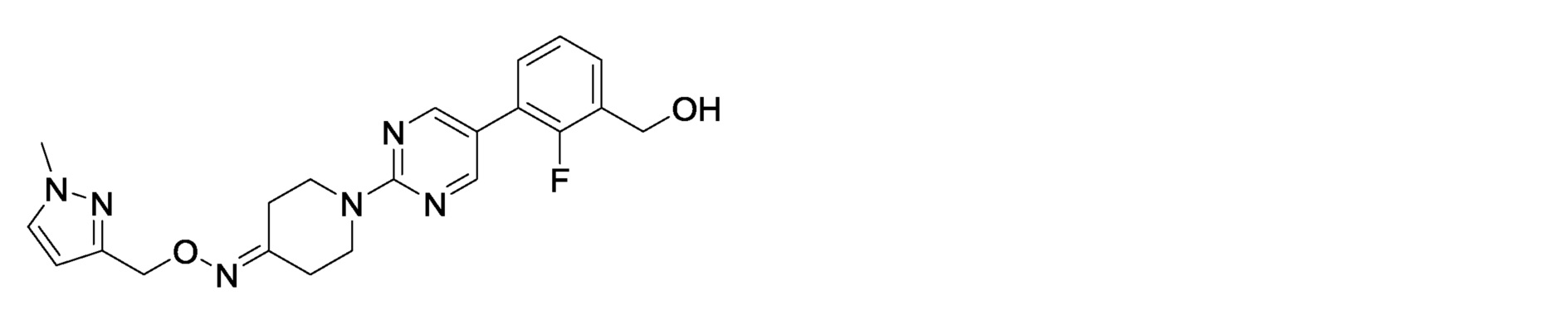
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[(1-метил-1H-пиразол-3-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 6-90. В результате указанное в заголовке соединение (выход 91%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 411[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,52 (d, J=1,5 Гц, 2H), 7,45-7,39 (m, 1H), 7,35-7,19 (m, 3H), 6,30 (d, J=2,3 Гц, 1H), 5,09 (s, 2H), 4,83 (d, J=6,1 Гц, 2H), 4,03-3,94 (m, 4H), 3,90 (s, 3H), 2,74-2,67 (m, 2H), 2,51-2,45 (m, 2H), 1,84 (t, J=6,1 Гц, 1H).
[0669] (Ссылочный пример 7-114)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-3-ил]метил}оксим (ссылочное соединение 7-114)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-3-ил]метил}оксим, синтезированный таким же образом, как в ссылочном примере 6-91. В результате указанное в заголовке соединение (выход 66%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 481[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,52 (d, J=1,5 Гц, 2H), 7,57 (d, J=2,4 Гц, 1H), 7,45-7,39 (m, 1H), 7,34-7,27 (m, 1H), 7,25-7,21 (m, 1H), 6,36 (d, J=2,4 Гц, 1H), 5,36 (dd, J=2,8, 9,5 Гц, 1H), 5,12 (s, 2H), 4,83 (br d, J=4,5 Гц, 2H), 4,11-4,04 (m, 1H), 4,04-3,95 (m, 4H), 3,74-3,65 (m, 1H), 2,72-2,67 (m, 2H), 2,50-2,45 (m, 2H), 2,17-2,00 (m, 3H), 1,83 (br t, J=4,5 Гц, 1H), 1,75-1,46 (m, 3H).
[0670] (Ссылочный пример 7-115)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метил}оксим (ссылочное соединение 7-115)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метил}оксим, синтезированный таким же образом, как в ссылочном примере 6-92. В результате указанное в заголовке соединение (выход 60%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 481[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,58 (d, J=1,4 Гц, 2H), 7,90 (s, 1H), 7,51 (s, 1H), 7,49-7,40 (m, 2H), 7,32-7,23 (m, 1H), 5,36 (dd, J=2,2, 10,1 Гц, 1H), 5,32 (t, J=5,3 Гц, 1H), 4,89 (s, 2H), 4,60 (d, J=5,3 Гц, 2H), 3,97-3,83 (m, 5H), 3,69-3,55 (m, 1H), 2,57-2,52 (m, 2H), 2,41-2,36 (m, 2H), 2,14-1,46 (m,6H).
[0671] (Ссылочный пример 7-116)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[(1-метил-1H-пиразол-4-ил)метил]оксим (ссылочное соединение 7-116)
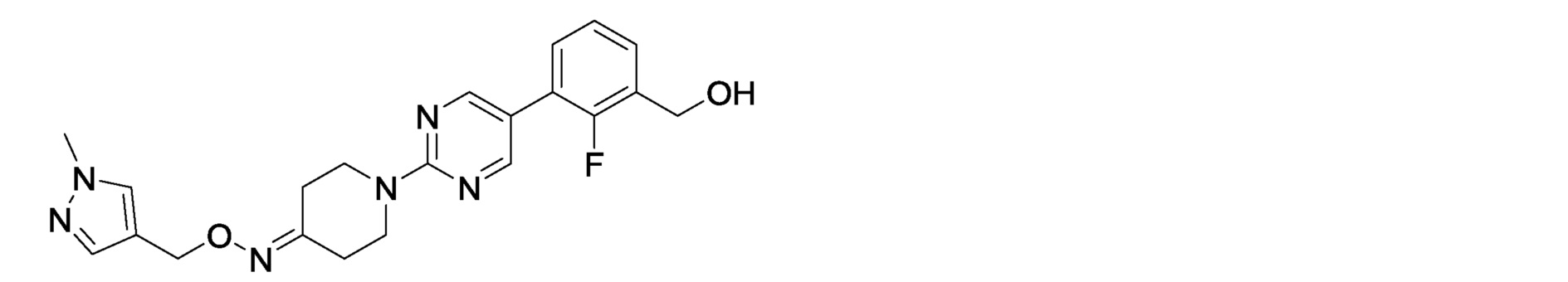
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[(1-метил-1H-пиразол-4-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 6-93. В результате указанное в заголовке соединение (с количественным выходом) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 411[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,58 (d, J=1,5 Гц, 2H), 7,70 (s, 1H), 7,49-7,40 (m, 3H), 7,31-7,23 (m, 1H), 5,32 (t, J=5,3 Гц, 1H), 4,87 (s, 2H), 4,60 (d, J=5,3 Гц, 2H), 3,95-3,87 (m, 4H), 3,81 (s, 3H), 2,56-2,52 (m, 2H), 2,41-2,35 (m, 2H).
[0672] (Ссылочный пример 7-117)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-[2-(1H-пиразол-1-ил)этил]оксим (ссылочное соединение 7-117)
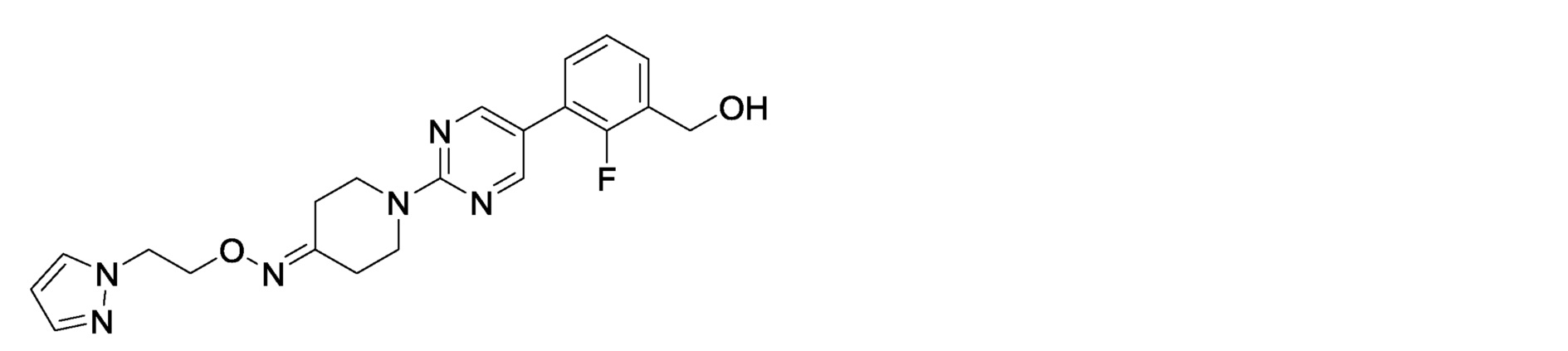
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-метилоксим (ссылочное соединение 6-1) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-[2-(1H-пиразол-1-ил)этил]оксим, синтезированный таким же образом, как в ссылочном примере 6-94, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 32%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 411[М+1]+.
[0673] (Ссылочный пример 7-118)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-пиридин-4-илметилоксим (ссылочное соединение 7-118)
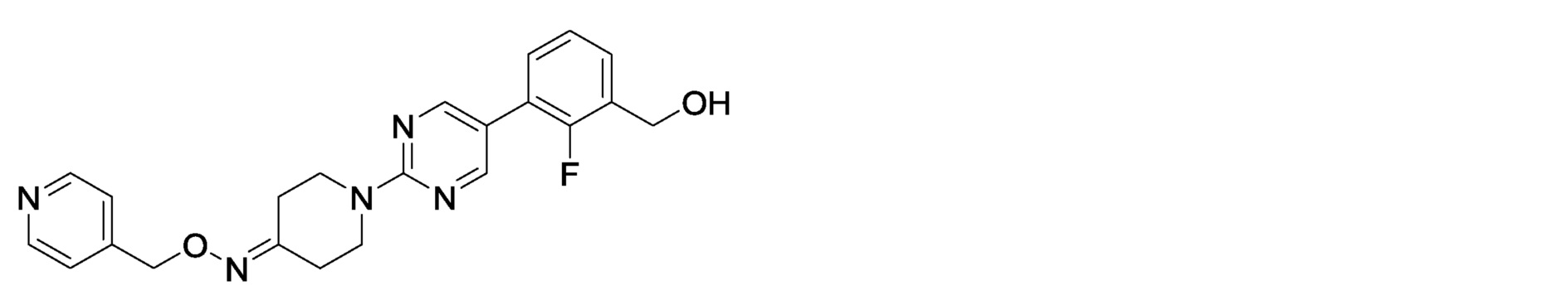
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-пиридин-4-илметилоксим, синтезированный таким же образом, как в ссылочном примере 6-95. В результате указанное в заголовке соединение (включая примеси) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 408[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,60-8,56 (m, 2H), 8,54 (d, J=1,5 Гц, 2H), 7,51-7,39 (m, 1H), 7,35-7,20 (m, 4H), 5,11 (s, 2H), 4,84 (br s, 2H), 4,07-3,97 (m, 4H), 2,81-2,73 (m, 2H), 2,50-2,43 (m, 2H), 1,96-1,85 (m, 1H).
[0674] (Ссылочный пример 7-119)
1-(2-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)пирролидин-2,5-дион (ссылочное соединение 7-119)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}пирролидин-2,5-дион, синтезированный таким же образом, как в ссылочном примере 6-96. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 442[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,5 Гц, 2H), 7,46-7,39 (m, 1H), 7,35-7,28 (m, 1H), 7,26-7,21 (m, 1H), 4,83 (d, J=5,7 Гц, 2H), 4,24-4,17 (m, 2H), 4,05-3,95 (m, 4H), 3,85-3,78 (m, 2H), 2,71 (s, 4H), 2,63-2,56 (m, 2H), 2,47-2,40 (m, 2H), 1,84 (br t, J=5,7 Гц, 1H).
[0675] (Ссылочный пример 7-120)
1-(2-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)пирролидин-2-он (ссылочное соединение 7-120)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}пирролидин-2-он, синтезированный таким же образом, как в ссылочном примере 6-97. В результате указанное в заголовке соединение (выход 69%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 428[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,49-7,42 (m, 2H), 7,31-7,22 (m, 1H), 5,32 (t, J=5,7 Гц, 1H), 4,60 (d, J=5,7 Гц, 2H), 4,11-4,01 (m, 2H), 3,96-3,88 (m, 4H), 3,44-3,35 (m, 4H), 2,59-2,53 (m, 2H), 2,41-2,35 (m, 2H), 2,25-2,14 (m, 2H), 1,97-1,86 (m, 2H).
[0676] (Ссылочный пример 7-121)
3-(2-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)оксазолидин-2-он (ссылочное соединение 7-121)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 3-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}оксазолидин-2-он, синтезированный таким же образом, как в ссылочном примере 6-98. В результате указанное в заголовке соединение (выход 72%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 430[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,49-7,42 (m, 2H), 7,30-7,25 (m, 1H), 5,33 (br t, J=4,9 Гц, 1H), 4,60 (br d, J=4,9 Гц, 2H), 4,29-4,21 (m, 2H), 4,15-4,08 (m, 2H), 3,96-3,89 (m, 4H), 3,63-3,55 (m, 2H), 3,45-3,36 (m, 2H), 2,60-2,54 (m, 2H), 2,41-2,36 (m, 2H).
[0677] (Ссылочный пример 7-122)
4-(2-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-илиден)амино]окси}этил)морфолин-3-он (ссылочное соединение 7-122)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 4-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}морфолин-3-он, синтезированный таким же образом, как в ссылочном примере 6-99. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 444[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,49-7,42 (m, 2H), 7,31-7,25 (m, 1H), 5,32 (t, J=5,6 Гц, 1H), 4,60 (d, J=5,6 Гц, 2H), 4,16-4,08 (m, 2H), 4,02 (s, 2H), 3,96-3,88 (m, 4H), 3,85-3,75 (m, 2H), 3,62-3,50 (m, 2H), 3,43-3,34 (m, 2H), 2,60-2,53 (m, 2H), 2,42-2,36 (m, 2H).
[0678] (Ссылочный пример 7-123)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-пиримидин-5-илоксим (ссылочное соединение 7-123)
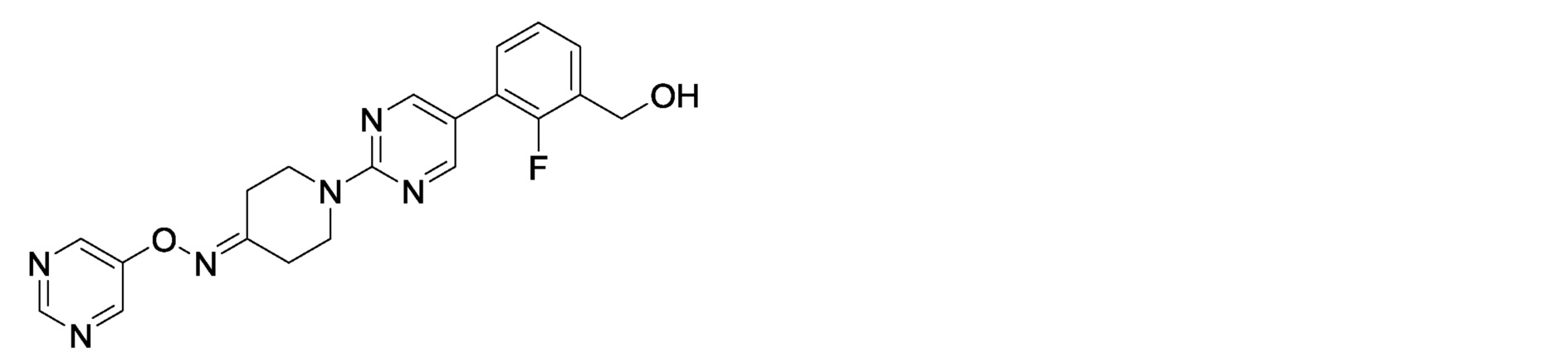
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-пиримидин-5-илоксим, синтезированный таким же образом, как в ссылочном примере 121. В результате указанное в заголовке соединение (выход 92%) было получено в виде темно-коричневого твердого вещества.
Масс-спектр (CI, m/z): 395[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,90 (s, 1H), 8,73 (s, 2H), 8,62 (d, J=1,4 Гц, 2H), 7,50-7,43 (m, 2H), 7,32-7,25 (m, 1H), 5,34 (t, J=5,4 Гц, 1H), 4,61 (d, J=5,4 Гц, 2H), 4,10-4,00 (m, 4H), 2,90-2,84 (m, 2H), 2,63-2,57 (m, 2H).
[0679] (Ссылочный пример 7-124)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-пиримидин-2-илоксим (ссылочное соединение 7-124)
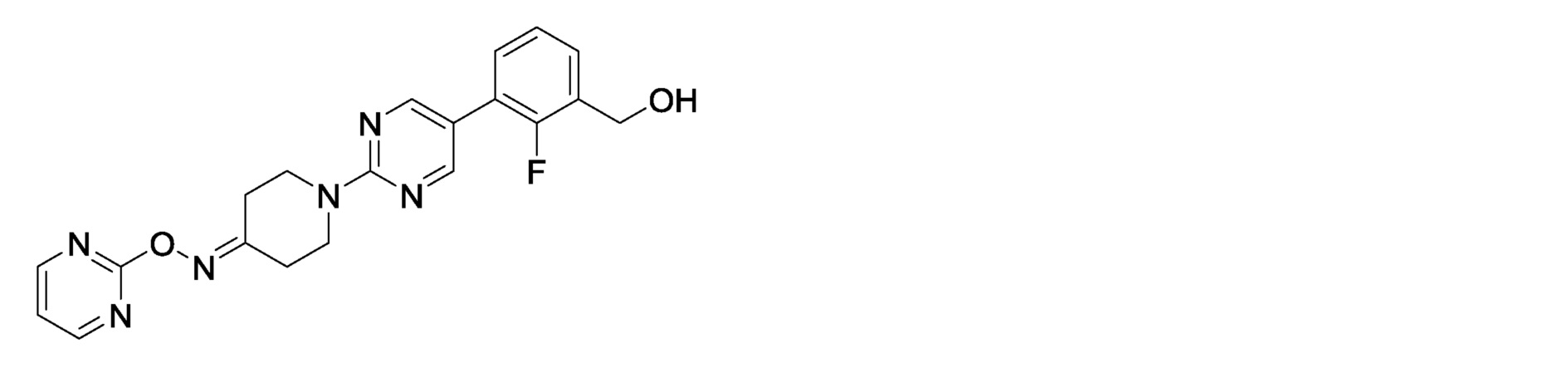
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 7-2, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-этилоксим (ссылочное соединение 6-2) заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-пиримидин-2-илоксим, синтезированный таким же образом, как в ссылочном примере 74-2. В результате указанное в заголовке соединение (выход 93%) было получено в виде темно-коричневого твердого вещества.
Масс-спектр (CI, m/z): 395[М+1]+.
1H-ЯМР спектр (400 МГц,DMSO-d6) δ: 8,67 (d, J=4,8 Гц, 2H), 8,62 (d, J=1,4 Гц, 2H), 7,51-7,43 (m, 2H), 7,31-7,23 (m, 2H), 5,38-5,30 (m, 1H), 4,64-4,58 (m, 2H), 4,07-3,99 (m, 4H), 2,86-2,80 (m, 2H), 2,63-2,56 (m, 2H).
[0680] (Ссылочный пример 8)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-этилоксим (ссылочное соединение 8)

Карбонат натрия, 70 мг (0,66 ммоль), и O-этилгидроксиламина гидрохлорид, 48 мг (0,49 ммоль), добавляли к раствору в THF, (1 мл), этаноле, (2 мл), и воде, (1 мл), 1-(5-бромпиримидин-2-ил)азетидин-3-она, 0,10 г (0,44 ммоль), синтезированного таким же образом, как в ссылочном примере 2. Смесь перемешивали при 50°C в течение 2 часов, оставляли спокойно стоять при комнатной температуре в течение ночи, и перемешивали при 50°C в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:этилацетат) с получением указанного в заголовке соединения в количестве 0,10 г (0,37 ммоль, выход 84%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 270, 272[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,54 (s, 2H), 4,77-4,71 (m, 4H), 4,06 (q, J=7,0 Гц, 2H), 1,20 (t, J=7,0 Гц, 3H).
[0681] (Ссылочный пример 9-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она оксим (ссылочное соединение 9-1)

Гидроксиламина гидрохлорид, 12,1 г (174 ммоль), добавляли при перемешивании к суспензии в THF (300 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она, 15,9 г (69,7 ммоль), синтезированного таким же образом, как в ссылочном примере 2, и смесь перемешивали при 55°C в течение 10 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 18,0 г (включая примеси) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 243, 245[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 10,95 (br s, 1H), 8,54 (s, 2H), 4,75-4,67 (m, 4H).
[0682] (Ссылочный пример 9-2)
1-(5-Бром-3-фторпиридин-2-ил)азетидин-3-она оксим (ссылочное соединение 9-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 9-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-он (ссылочное соединение 2) заменяли на 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-он, синтезированный таким же образом, как в ссылочном примере 32-1, что экстракцию проводили этилацетатом, и что продукт очищали перекристаллизацией из метиленхлорида. В результате указанное в заголовке соединение (выход 89%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 260, 262[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,03 (dd, J=0,8, 1,9 Гц, 1H), 7,38 (dd, J=1,9, 10,7 Гц, 1H), 7,33 (s, 1H), 4,90-4,82 (m, 4H).
[0683] (Ссылочный пример 9-3)
2-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)уксусная кислота (ссылочное соединение 9-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 9-1, за исключением того, что гидроксиламина гидрохлорид заменяли на карбоксиметоксиламина гемигидрохлорид, что температура реакции всегда была равна температуре окружающей среды, и что после окончания реакции реакционную смесь концентрировали при пониженном давлении. В результате было получено указанное в заголовке соединение (включая примеси).
[0684] (Ссылочный пример 9-4)
3-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)пропионовая кислота (ссылочное соединение 9-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 9-1, за исключением того, что гидроксиламина гидрохлорид заменяли на гидрохлорид 3-(аминоокси)пропионовой кислоты, и что после окончания реакции реакционную смесь концентрировали при пониженном давлении. В результате было получено указанное в заголовке соединение (включая примеси).
[0685] (Ссылочный пример 10-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-метил-d3-оксим (ссылочное соединение 10-1)

Йодметан-d3, 0,10 мл (1,6 ммоль), и карбонат цезия, 0,80 г (2,5 ммоль), добавляли к раствору в DMF (6,0 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она оксима, 0,20 г (0,82 ммоль), синтезированного таким же образом, как в ссылочном примере 9-1, и смесь перемешивали при комнатной температуре в течение 18 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:этилацетат) с получением указанного в заголовке соединения в количестве 0,17 г (0,65 ммоль, выход 79%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 260, 262[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,52 (s, 2H), 4,80-4,70 (m, 4H).
[0686] (Ссылочный пример 10-2)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(2-фторэтил)оксим (ссылочное соединение 10-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на 2-фторэтилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-1, и температуру реакции изменяли на 90°C. В результате указанное в заголовке соединение (выход 81%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 289, 291[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,37 (s, 2H), 4,85-4,79 (m, 4H), 4,74-4,57 (m, 2H), 4,39-4,25 (m, 2H).
[0687] (Ссылочный пример 10-3)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(3-фторпропил)оксим (ссылочное соединение 10-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на 3-фторпропилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-3, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (выход 60%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 303, 305[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,79-4,72 (m, 4H), 4,62-4,41 (m, 2H), 4,12 (t, J=6,3 Гц, 2H), 2,06-1,92 (m, 2H).
[0688] (Ссылочный пример 10-4)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-{2-[(тетрагидропиран-2-ил)окси]этил}оксим (ссылочное соединение 10-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на 2-(2-бромэтокси)тетрагидропиран, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (выход 79%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 371, 373[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,79-4,70 (m, 4H), 4,63-4,53 (m, 1H), 4,23-4,11 (m, 2H), 3,86-3,69 (m, 2H), 3,65-3,56 (m, 1H), 3,50-3,38 (m, 1H), 1,89-1,24 (m, 6H).
[0689] (Ссылочный пример 10-5)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-{3-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 10-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на 2-(3-бромпропокси)тетрагидропиран, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 385,387[М+1]+.
1H-ЯМР спектр (400 МГц,DMSO-d6) δ: 8,54 (s, 2H), 4,81-4,68 (m, 4H), 4,59-4,51 (m, 1H), 4,19-4,03 (m, 2H), 3,77-3,63 (m, 2H), 3,48-3,36 (m, 2H), 1,89-1,80 (m, 2H), 1,75-1,39 (m, 6H).
[0690] (Ссылочный пример 10-6)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-{4-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 10-6)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на 2-(4-бромбутокси)тетрагидропиран, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (выход 89%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 399,401[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,54 (s, 2H), 4,80-4,71 (m, 4H), 4,57-4,50 (m, 1H), 4,07-4,01 (m, 2H), 3,78-3,58 (m, 2H), 3,47-3,33 (m, 2H), 1,84-1,36 (m, 10H).
[0691] (Ссылочный пример 10-7)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(2-метоксиэтил)оксим (ссылочное соединение 10-7)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на 2-бромэтилметиловый эфир, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (выход 89%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 301, 303[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,79-4,71 (m, 4H), 4,17-4,10 (m, 2H), 3,58-3,51 (m, 2H), 3,26 (s, 3H).
[0692] (Ссылочный пример 10-8)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим (ссылочное соединение 10-8)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на (2,2-диметил-1,3-диоксан-5-ил)метилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-4, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (выход 74%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 371, 373[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,79-4,72 (m, 4H), 4,07 (d, J=7,2 Гц, 2H), 3,89 (dd, J=4,0, 11,9 Гц, 2H), 3,64 (dd, J=6,1, 11,9 Гц, 2H), 2,01-1,93 (m, 1H), 1,33 (s, 3H), 1,30 (s, 3H).
[0693] (Ссылочный пример 10-9)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим (ссылочное соединение 10-9)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на (2,2-диметил-1,3-диоксолан-4-ил)метилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-5, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (выход 66%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 357, 359[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,79-4,72 (m, 4H), 4,33-4,24 (m, 1H), 4,09-4,00 (m, 3H), 3,66 (dd, J=6,5, 8,3 Гц, 1H), 1,32 (s, 3H), 1,27 (s, 3H).
[0694] (Ссылочный пример 10-10)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксим (ссылочное соединение 10-10)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на 2-(2,2-диметил-1,3-диоксолан-4-ил)этилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-6, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (выход 82%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 371, 373[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,54 (s, 2H), 4,79-4,70 (m, 4H), 4,17-4,03 (m, 3H), 4,01 (dd, J=6,0, 8,0 Гц, 1H), 3,48 (dd, J=7,2, 8,0 Гц, 1H), 1,89-1,79 (m, 2H), 1,31 (s, 3H), 1,26 (s, 3H).
[0695] (Ссылочный пример 10-11)
2-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)этилацетат (ссылочное соединение 10-11)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на 2-бромэтилацетат, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (выход 65%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 329, 331[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,37 (s, 2H), 4,85-4,75 (m, 4H), 4,35-4,24 (m, 4H), 2,09 (s, 3H).
[0696] (Ссылочный пример 10-12)
трет-Бутил-2-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)ацетат (ссылочное соединение 10-12)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на трет-бутилбромацетат. В результате указанное в заголовке соединение (выход 83%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 357, 359[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,37 (s, 2H), 4,89-4,81 (m, 4H), 4,51 (s, 2H), 1,49 (s, 9H).
[0697] (Ссылочный пример 10-13)
Этил-4-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)бутаноат (ссылочное соединение 10-13)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на этил-4-бромбутират, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (выход 90%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 357, 359[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,78-4,70 (m, 4H), 4,09-4,00 (m, 4H), 2,36 (t, J=7,4 Гц, 2H), 1,92-1,79 (m, 2H), 1,18 (t, J=7,1 Гц, 3H).
[0698] (Ссылочный пример 10-14)
трет-Бутил-2-[({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)метил]морфолин-4-карбоксилат (ссылочное соединение 10-14)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на трет-бутил-2-{[(метилсульфонил)окси]метил}морфолин-4-карбоксилат, синтезированный таким же образом, как в ссылочном примере 14-9, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (выход 50%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 442, 444[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,80-4,72 (m, 4H), 4,08-3,98 (m, 2H), 3,88-3,76 (m, 2H), 3,76-3,65 (m, 1H), 3,63-3,53 (m, 1H), 3,45-3,33 (m, 1H), 2,97-2,77 (m, 1H), 2,76-2,54 (m, 1H), 1,40 (s, 9H).
[0699] (Ссылочный пример 10-15)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-оксетан-3-илоксим (ссылочное соединение 10-15)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 10-1, за исключением того, что йодметан-d3 заменяли на оксетан-3-ил-4-метилбензолсульфонат, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 299, 301[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,56 (s, 2H), 5,23-5,16 (m, 1H), 4,83-4,78 (m, 4H), 4,78-4,73 (m, 2H), 4,57-4,52 (m, 2H).
[0700] (Ссылочный пример 11-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(трет-бутилдиметилсилил)оксим (ссылочное соединение 11-1)

TEA, 300 мкл (2,15 ммоль), добавляли к суспензии в DMF (3 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она оксима, 261 мг (1,07 ммоль), синтезированного таким же образом, как в ссылочном примере 9-1. Затем туда по каплям вливали раствор в DMF (2 мл) трет-бутилхлордиметилсилана, 244 мг (1,62 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. Далее добавляли TEA, 300 мкл (2,15 ммоль), и трет-бутилхлордиметилсилан, 204 мг (1,35 ммоль), и смесь перемешивали при 60°C в течение 1 часа. После окончания реакции реакционную смесь разбавляли толуолом, последовательно промывали насыщенным водным раствором гидрокарбоната натрия и рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 296 мг (0,828 ммоль, выход 77%) в виде светло-желтого твердого вещества.
Масс-спектр (DUIS, m/z): 357, 359[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,81-4,72 (m, 4H), 0,91 (s, 9H), 0,15 (s, 6H).
[0701] (Ссылочный пример 11-2)
1-(5-Бром-3-фторпиридин-2-ил)азетидин-3-она O-(трет-бутилдиметилсилил)оксим (ссылочное соединение 11-2)

(трет-Бутил)диметилсилилхлорид, 350 мг (2,32 ммоль), и имидазол, 172 мг (2,53 ммоль), добавляли к раствору в THF (10 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-гидрокси-2-метоксипропил)оксима, 500 мг (1,92 ммоль), синтезированного таким же образом, как в ссылочном примере 9-2, и смесь перемешивали при комнатной температуре в течение 26 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Экстракт концентрировали, и остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 643 мг (выход 89%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,11-8,09 (m, 1H), 7,93-7,87 (m, 1H), 4,86-4,78 (m, 4H), 0,91 (s, 9H), 0,15 (s, 6H).
[0702] (Ссылочный пример 12)
[2-Фтор-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]метанол (ссылочное соединение 12)

Раствор 1 М тетрабутиламмония фторида в THF, 1,35 мл (1,35 ммоль), добавляли к раствору в THF (10 мл) трет-бутил{[2-фтор-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил]окси}диметилсилана, 302 мг (0,824 ммоль), синтезированного таким же образом, как в ссылочном примере 5, и смесь перемешивали при комнатной температуре в течение 2,5 часа. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 172 мг (0,682 ммоль, выход 83%) в виде бесцветного масла.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 7,74-7,64 (m, 1H), 7,56-7,49 (m, 1H), 7,20-7,10 (m, 1H), 4,76 (s, 2H), 1,37 (s, 12H).
[0703] (Ссылочный пример 13-1)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-она O-(трет-бутилдиметилсилил)оксим (ссылочное соединение 13-1)

Через суспензию в воде (0,8 мл) и 1,4-диоксане (4,0 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(трет-бутилдиметилсилил)оксима, 180 мг (0,504 ммоль), синтезированного таким же образом, как в ссылочном примере 11-1, [2-фтор-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]метанола, 164 мг (0,651 ммоль), синтезированного таким же образом, как в ссылочном примере 12, и фосфата трикалия, 278 мг (1,31 ммоль), пропускали газообразный азот в течение 15 минут. Затем добавляли тетракис(трифенилфосфин)палладий(0), 31,1 мг (0,0269 ммоль). Смесь подавали в микроволновое реакционное устройство и перемешивали при 120°C в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:метанол=от 99:1 до 99:4 (об/об)) с получением указанного в заголовке соединения в количестве 131 мг (0,325 ммоль, выход 64%) в виде белого твердого вещества.
Масс-спектр (DUIS, m/z): 403[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,66-7,42 (m, 2H), 7,32-7,26 (m, 1H), 5,34 (t, J=5,6 Гц, 1H), 4,88-4,73 (m, 4H), 4,61 (d, J=5,6 Гц, 2H), 0,93 (s, 9H), 0,16 (s, 6H).
[0704] (Ссылочный пример 13-2)
1-{3-Фтор-5-[2-фтор-3-(гидроксиметил)фенил]пиридин-2-ил}азетидин-3-она O-(трет-бутилдиметилсилил)оксим (ссылочное соединение 13-2)

Раствор в 1,4-диоксане (10 мл) и воде (5 мл) 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-она O-(трет-бутилдиметилсилил)оксима, 642 мг (1,72 ммоль), синтезированного таким же образом, как в ссылочном примере 11-2, [2-фтор-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]метанола, 487 мг (1,93 ммоль), синтезированного таким же образом, как в ссылочном примере 12, и карбоната натрия, 545 мг (5,14 ммоль), дегазировали и продували азотом. Затем добавляли тетракис(трифенилфосфин)палладий(0), 99 мг (0,086 ммоль). Смесь перемешивали под струей аргона при 80°C в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 450 мг (1,07 ммоль, выход 62%) в виде светло-желтого твердого вещества.
Масс-спектр (ESI, m/z): 420[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,19-8,15 (m, 1H), 7,78-7,69 (m, 1H), 7,50-7,37 (m, 2H), 7,32-7,25 (m, 1H), 4,91-4,77 (m, 4H), 4,60 (s, 2H), 0,92 (s, 9H), 0,16 (s, 6H).
[0705] (Ссылочный пример 14-1)
2-Фторэтилметансульфонат (ссылочное соединение 14-1)

TEA, 4,4 мл (32 ммоль), и метансульфонилхлорид, 1,4 мл (18 ммоль), добавляли к раствору в метиленхлориде (30 мл) этиленфторгидрина, 1,0 г (16 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении с получением неочищенного продукта в количестве 2,23 г, содержащего указанное в заголовке соединение в виде светло-желтого масла.
Масс-спектр (CI, m/z): 143[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 4,76-4,60 (m, 2H), 4,53-4,41 (m, 2H), 3,08 (s, 3H).
[0706] (Ссылочный пример 14-2)
2,2-Дифторэтилметансульфонат (ссылочное соединение 14-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на 2,2-дифторэтанол. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт.
[0707] (Ссылочный пример 14-3)
3-Фторпропилметансульфонат (ссылочное соединение 14-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на 3-фторпропан-1-ол. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде коричневого масла.
[0708] (Ссылочный пример 14-4)
(2,2-Диметил-1,3-диоксан-5-ил)метилметансульфонат (ссылочное соединение 14-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на (2,2-диметил-1,3-диоксан-5-ил)метанол. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде желтого масла.
[0709] (Ссылочный пример 14-5)
(2,2-Диметил-1,3-диоксолан-4-ил)метилметансульфонат (ссылочное соединение 14-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на (2,2-диметил-1,3-диоксолан-4-ил)метанол. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде коричневого масла.
[0710] (Ссылочный пример 14-6)
2-(2,2-Диметил-1,3-диоксолан-4-ил)этилметансульфонат (ссылочное соединение 14-6)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на 2-(2,2-диметил-1,3-диоксолан-4-ил)этанол. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде коричневого масла.
[0711] (Ссылочный пример 14-7)
3-Гидрокси-3-метилбутилметансульфонат (ссылочное соединение 14-7)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на 3-метилбутан-1,3-диол. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде бесцветного масла.
[0712] (Ссылочный пример 14-8)
(2,2,5-Триметил-1,3-диоксан-5-ил)метилметансульфонат (ссылочное соединение 14-8)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на (2,2,5-триметил-1,3-диоксан-5-ил)метанол. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде оранжевого масла.
Масс-спектр (CI, m/z): 239[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 4,34 (s, 2H), 3,71-3,59 (m, 4H), 3,04 (s, 3H), 1,45 (s, 3H), 1,40 (s, 3H), 0,88 (s, 3H).
[0713] (Ссылочный пример 14-9)
трет-Бутил-2-{[(метилсульфонил)окси]метил}морфолин-4-карбоксилат (ссылочное соединение 14-9)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на трет-бутил-2-(гидроксиметил)морфолин-4-карбоксилат. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт.
[0714] (Ссылочный пример 14-10)
(5-Оксотетрагидрофуран-2-ил)метилметансульфонат (ссылочное соединение 14-10)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на дигидро-5-(гидроксиметил)-2(3H)-фуранон. В результате было получено указанное в заголовке соединение (включая примеси).
Масс-спектр (CI, m/z): 195[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 4,83-4,74 (m, 1H), 4,48-4,27 (m, 2H), 3,09 (s, 3H), 2,71-2,53 (m, 2H), 2,46-2,11 (m, 2H).
[0715] (Ссылочный пример 14-11)
3-(Метилсульфонил)пропилметансульфонат (ссылочное соединение 14-11)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на 3-(метилсульфонил)пропан-1-ол. В результате указанное в заголовке соединение (включая примеси) было получено в виде желтого твердого вещества.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 4,48-4,36 (m, 2H), 3,23-3,16 (m, 2H), 3,06 (s, 3H), 2,97 (s, 3H), 2,44-2,25 (m, 2H).
[0716] (Ссылочный пример 14-12)
(1-Метил-1H-пиразол-3-ил)метилметансульфонат (ссылочное соединение 14-12)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на (1-метил-1H-пиразол-3-ил)метанол, синтезированный таким же образом, как в ссылочном примере 114-1, и продукт очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 22%) было получено в виде бесцветного масла.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 7,31 (d, J=2,2 Гц, 1H), 6,30 (d, J=2,2 Гц, 1H), 4,60 (s, 2H), 3,89 (s, 3H).
[0717] (Ссылочный пример 14-13)
3-(Хлорметил)-1-(тетрагидропиран-2-ил)-1H-пиразол (ссылочное соединение 14-13)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на [1-(тетрагидропиран-2-ил)-1H-пиразол-3-ил]метанол, синтезированный таким же образом, как в ссылочном примере 114-2. В результате указанное в заголовке соединение (выход 66%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 201[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 7,56 (d, J=2,5 Гц, 1H), 6,37 (d, J=2,5 Гц, 1H), 5,34 (dd, J=2,9, 9,4 Гц, 1H), 4,62 (s, 2H), 4,11-4,03 (m, 1H), 3,74-3,65 (m, 1H), 2,16-1,99 (m, 3H), 1,86-1,42 (m, 3H).
[0718] (Ссылочный пример 14-14)
[1-(Тетрагидропиран-2-ил)-1H-пиразол-4-ил]метилметансульфонат (ссылочное соединение 14-14)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 14-1, за исключением того, что этиленфторгидрин заменяли на [1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метанол, синтезированный таким же образом, как в ссылочном примере 114-3. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт.
[0719] (Ссылочный пример 15-1)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2,2-дифторэтил)оксим (ссылочное соединение 15-1)

2,2-Дифторэтилметансульфонат, 298 мг (1,86 ммоль), синтезированный таким же образом, как в ссылочном примере 14-2, и карбонат цезия, 607 мг (1,86 ммоль), добавляли к раствору в DMF (1 мл) 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она оксима, 150 мг (0,373 ммоль), синтезированного таким же образом, как в ссылочном примере 6-5, и смесь перемешивали при комнатной температуре в течение 15 часов и при 70°C в течение 3 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 128 мг (0,274 ммоль, выход 74%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 467[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,55-7,47 (m, 1H), 7,31-7,19 (m, 2H), 6,01 (tt, J=4,2, 55,3 Гц, 1H), 4,92-4,88 (m, 4H), 4,85 (s, 2H), 4,26 (dt, J=4,2, 13,3 Гц, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0720] (Ссылочный пример 15-2)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2,2,2-трифторэтил)оксим (ссылочное соединение 15-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 15-1, за исключением того, что 2,2-дифторэтилметансульфонат (ссылочное соединение 14-2) заменяли на 2,2,2-трифторэтилтрифторметансульфонат, температура реакции всегда была равна температуре окружающей среды, и не проводили очистку с помощью колоночной хроматографии на силикагеле. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 485[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,56-7,45 (m, 1H), 7,32-7,20 (m, 2H), 4,94-4,89 (m, 4H), 4,85 (s, 2H), 4,45 (q, J=8,5 Гц, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0721] (Ссылочный пример 15-3)
[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]метилпивалат (ссылочное соединение 15-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 15-1, за исключением того, что 2,2-дифторэтилметансульфонат (ссылочное соединение 14-2) заменяли на хлорметилпивалат, и температура реакции всегда была равна температуре окружающей среды. В результате указанное в заголовке соединение (выход 25%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 517[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,5 Гц, 2H), 7,54-7,48 (m, 1H), 7,30-7,20 (m, 2H), 5,73 (s, 2H), 4,93-4,88 (m, 4H), 4,85 (s, 2H), 1,24 (s, 9H), 0,96 (s, 9H), 0,14 (s, 6H).
[0722] (Ссылочный пример 15-4)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-диметилкарбамоилоксим (ссылочное соединение 15-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 15-1, за исключением того, что 2,2-дифторэтилметансульфонат (ссылочное соединение 14-2) заменяли на диметилкарбамоилхлорид, и температура реакции всегда была равна температуре окружающей среды. В результате указанное в заголовке соединение (выход 63%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 474[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,58 (d, J=1,4 Гц, 2H), 7,56-7,46 (m, 1H), 7,32-7,21 (m, 2H), 5,05-4,94 (m, 4H), 4,85 (s, 2H), 3,01 (br s, 3H), 2,95 (br s, 3H), 0,96 (s, 9H), 0,14 (s, 6H).
[0723] (Ссылочный пример 15-5)
5-{[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]метил}дигидрофуран-2(3H)-он (ссылочное соединение 15-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 15-1, за исключением того, что 2,2-дифторэтилметансульфонат (ссылочное соединение 14-2) заменяли на (5-оксотетрагидрофуран-2-ил)метилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-10, и температура реакции всегда была равна температуре окружающей среды. В результате указанное в заголовке соединение (выход 53%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 501[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,55-7,47 (m, 1H), 7,31-7,19 (m, 2H), 4,93-4,76 (m, 7H), 4,34-4,20 (m, 2H), 2,64-2,48 (m, 2H), 2,42-2,30 (m, 1H), 2,16-2,02 (m, 1H), 0,96 (s, 9H), 0,16-0,11 (m, 6H).
[0724] (Ссылочный пример 15-6)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил)азетидин-3-она O-(4-метоксибензил)оксим (ссылочное соединение 15-6)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 15-1, за исключением того, что 2,2-дифторэтилметансульфонат (ссылочное соединение 14-2) заменяли на p-метоксибензилбромид, и температура реакции всегда была равна температуре окружающей среды. В результате указанное в заголовке соединение (выход 85%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 523[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,55 (d, J=1,3 Гц, 2H), 7,54-7,46 (m, 1H), 7,35-7,29 (m, 2H), 7,28-7,19 (m, 2H), 6,93-6,88 (m, 2H), 5,05 (s, 2H), 4,89-4,82 (m, 6H), 3,82 (s, 3H), 0,96 (s, 9H), 0,13 (s, 6H).
[0725] (Ссылочный пример 16)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(2-{2-[(тетрагидропиран-2-ил)окси]этокси}этил)оксим (ссылочное соединение 16)

При перемешивании при 0°C 55% гидрид натрия, 50 мг (1,1 ммоль), добавляли по частям к суспензии в THF (6 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(2-гидроксиэтил)оксима, 160 мг (0,557 ммоль), синтезированного таким же образом, как в ссылочном примере 27, и смесь перемешивали при 0°C в течение 30 минут. Затем в нее по каплям вливали 2-(2-бромэтокси)тетрагидропиран, 0,253 мл (1,67 ммоль), при 0°C, и смесь перемешивали при комнатной температуре в течение 1 часа. Добавляли 6 мл DMF, и смесь перемешивали при 60°C в течение 2,5 часа. После естественного охлаждения смеси до комнатной температуры в нее по каплям вливали 2-(2-бромэтокси)тетрагидропиран, 0,253 мл (1,67 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции к реакционной смеси добавляли ледяную воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 138 мг (0,332 ммоль, выход 60%) в виде светло-желтого масла.
Масс-спектр (CI, m/z): 415, 417[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,37 (s, 2H), 4,82-4,78 (m, 4H), 4,66-4,62 (m, 1H), 4,27-4,23 (m, 2H), 3,91-3,83 (m, 2H), 3,79-3,74 (m, 2H), 3,71-3,67 (m, 2H), 3,65-3,58 (m, 1H), 3,54-3,47(m, 1H), 1,89-1,45 (m, 6H).
[0726] (Ссылочный пример 17-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[3-гидрокси-2-(гидроксиметил)пропил]оксим (ссылочное соединение 17-1)

Раствор 2 М хлорида водорода в этаноле, 22,0 мл (44,0 ммоль), добавляли к суспензии в метиленхлориде (11 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксима, 3,30 г (8,89 ммоль), синтезированного таким же образом, как в ссылочном примере 10-8, и смесь перемешивали при комнатной температуре в течение 30 минут. После окончания реакции к реакционной смеси добавляли TEA и воду при охлаждении льдом, и смесь концентрировали при пониженном давлении. К концентрированному остатку добавляли 30 мл воды, и смесь перемешивали при комнатной температуре в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 2,11 г (6,37 ммоль, выход 72%) в виде розового твердого вещества.
Масс-спектр (ESI, m/z): 331, 333[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,79-4,70 (m, 4H), 4,42 (t, J=5,2 Гц, 2H), 4,02 (d, J=6,4 Гц, 2H), 3,49-3,38 (m, 4H), 1,95-1,92 (m, 1H).
[0727] (Ссылочный пример 17-2)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(3,4-дигидроксибутил)оксим (ссылочное соединение 17-2)

Раствор 2 М хлорида водорода в этаноле, 20 мл (40 ммоль), добавляли к раствору в этаноле (67 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксима 2,5 г (6,7 ммоль), синтезированного таким же образом, как в ссылочном примере 10-10, и смесь перемешивали при 70°C в течение 4 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. К концентрированному остатку добавляли этилацетат. Смесь нейтрализовывали водным раствором гидрокарбоната натрия. Осажденное твердое вещество собирали с помощью фильтрации, промывали этилацетатом, и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 2,3 г (6,9 ммоль, количественный выход) в виде бежевого твердого вещества.
Масс-спектр (ESI, m/z): 331, 333[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6+D2O) δ: 8,54 (s, 2H), 4,79-4,69 (m, 4H), 4,17-4,08 (m, 2H), 3,59-3,44 (m, 1H), 3,31 (dd, J=5,8, 10,8 Гц, 1H), 3,24 (dd, J=5,5, 10,8 Гц, 1H), 1,88-1,76 (m, 1H), 1,59-1,47 (m, 1H).
[0728] (Ссылочный пример 18-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 18-1)

DHP, 0,65 мл (7,7 ммоль), и PPTS, 0,16 г (0,64 ммоль), добавляли к суспензии в метиленхлориде (10 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[3-гидрокси-2-(гидроксиметил)пропил]оксима, 2,1 г (6,3 ммоль), синтезированного таким же образом, как в ссылочном примере 17-1, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли 14 мл DMF, и смесь перемешивали при комнатной температуре в течение 25 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве (включая примеси) 1,35 г в виде светло-желтого масла.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,78-4,71 (m, 4H), 4,56-4,50 (m, 2H), 4,10-4,00 (m, 2H), 3,79-3,60 (m, 2H), 3,51-3,34 (m, 4H), 2,19-2,01 (m, 1H), 1,83-1,31 (m, 6H).
[0729] (Ссылочный пример 18-2)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-{3-гидрокси-4-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 18-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 18-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[3-гидрокси-2-(гидроксиметил)пропил]оксим (ссылочное соединение 17-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3,4-дигидроксибутил)оксим, синтезированный таким же образом, как в ссылочном примере 17-2. В результате указанное в заголовке соединение (выход 46%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 415, 417[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,54 (s, 2H), 4,80-4,70 (m, 4H), 4,70-4,66 (m, 1H), 4,61-4,51 (m, 1H), 4,13 (t, J=6,6 Гц, 2H), 3,80-3,65 (m, 2H), 3,59-3,45 (m, 1H), 3,44-3,19 (m, 2H), 1,91-1,33 (m, 8H).
[0730] (Ссылочный пример 19-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(3-метокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 19-1)

При 0°C йодметан, 0,037 мл (0,59 ммоль), и 55% гидрид натрия, 25 мг (0,57 ммоль), добавляли к раствору в THF (6 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксима, 0,16 г (0,39 ммоль), синтезированного таким же образом, как в ссылочном примере 18-1, и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 0,16 г (0,37 ммоль, выход 95%) в виде бесцветного масла.
Масс-спектр (CI, m/z): 429, 431[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,79-4,71 (m, 4H), 4,55-4,51 (m, 1H), 4,09-4,00 (m, 2H), 3,78-3,61 (m, 2H), 3,47-3,32 (m, 4H), 3,23 (s, 3H), 2,27-2,15 (m, 1H), 1,79-1,41 (m, 6H).
[0731] (Ссылочный пример 19-2)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[2-метокси-3-(тритилокси)пропил]оксим (ссылочное соединение 19-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 19-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 18-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[2-гидрокси-3-(тритилокси)пропил]оксим, синтезированный таким же образом, как в ссылочном примере 21-1. В результате указанное в заголовке соединение (выход 85%) было получено в виде белой пены.
Масс-спектр (CI, m/z): 573, 575[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,57 (s, 2H), 7,44-7,20 (m, 15H), 4,77-4,71 (m, 2H), 4,66-4,47 (m, 2H), 4,18-4,05 (m, 2H), 3,66-3,56 (m, 1H), 3,33 (s, 3H), 3,17-2,96 (m, 2H).
[0732] (Ссылочный пример 19-3)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-{3-метокси-4-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 19-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 19-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 18-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-{3-гидрокси-4-[(тетрагидропиран-2-ил)окси]бутил}оксим, синтезированный таким же образом, как в ссылочном примере 18-2. В результате указанное в заголовке соединение (выход 39%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 451, 453[М+Na]+.
[0733] (Ссылочный пример 20-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(2,3-дигидроксипропил)оксим (ссылочное соединение 20-1)

PPTS, 1,0 г (4,0 ммоль), добавляли к суспензии в метаноле (100 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксима, 6,6 г (18 ммоль), синтезированного таким же образом, как в ссылочном примере 10-9, и смесь перемешивали при 70°C в течение 15 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали водой три раза, сушили над безводным сульфатом магния и фильтровали. Фильтрат оставляли при пониженном давлении с получением неочищенного продукта в количестве 5,1 г, содержащего указанное в заголовке соединение в виде светло-коричневого твердого вещества.
Масс-спектр (ESI, m/z): 317, 319[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,80-4,72 (m, 5H), 4,57 (t, J=5,7 Гц, 1H), 4,09-3,98 (m, 1H), 3,93-3,87 (m, 1H), 3,74-3,65 (m, 1H), 3,35 (d, J=5,6 Гц, 2H).
[0734] Указанное в заголовке соединение также синтезировали следующим образом.
Уксусную кислоту, 3,0 мл (52 ммоль), добавляли к суспензии в воде (3 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксима, 790 мг (2,12 ммоль), синтезированного таким же образом, как в ссылочном примере 10-9, и смесь перемешивали при 80°C в течение 1 часа. После окончания реакции к реакционной смеси добавляли толуол. Смесь концентрировали при пониженном давлении с получением неочищенного продукта в количестве 701 мг, содержащего указанное в заголовке соединение в виде светло-красного твердого вещества.
[0735] (Ссылочный пример 20-2)
1-(5-Бром-3-фторпиридин-2-ил)азетидин-3-она O-(2,3-дигидроксипропил)оксим (ссылочное соединение 20-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 20-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим (ссылочное соединение 10-9) заменяли на 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим, синтезированный таким же образом, как в ссылочном примере 34-3, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 70%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 334, 336[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,10 (dd, J=1,0, 1,9 Гц, 1H), 7,91 (dd, J=1,9, 11,3 Гц, 1H), 4,85-4,78 (m, 4H), 4,75 (d, J=5,1 Гц, 1H), 4,57 (t, J=5,7 Гц, 1H), 4,04 (dd, J=4,5, 11,0 Гц, 1H), 3,89 (dd, J=6,6, 11,0 Гц, 1H), 3,74-3,62 (m, 1H), 3,35 (t, J=5,6 Гц, 2H).
[0736] (Ссылочный пример 21-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[2-гидрокси-3-(тритилокси)пропил]оксим (ссылочное соединение 21-1)

TEA, 7,7 мл (55 ммоль), DMAP, 0,45 г (3,7 ммоль), и тритилхлорид, 7,7 г (28 ммоль), добавляли к раствору в DMF (50 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(2,3-дигидроксипропил)оксима, 5,8 г (18 ммоль), синтезированного таким же образом, как в ссылочном примере 20-1, и смесь перемешивали при 60°C в течение 8 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток два раза очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 5,4 г (9,7 ммоль, выход 54%) в виде светло-желтого твердого вещества.
Масс-спектр (ESI, m/z): 559, 561[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,57 (s, 2H), 7,43-7,20 (m, 15H), 5,06 (br s, 1H), 4,80-4,68 (m, 2H), 4,67-4,47 (m, 1H), 4,09-3,96 (m, 2H), 3,66-3,86 (m, 1H), 2,96 (d, J=5,3 Гц, 2H).
[0737] Указанное в заголовке соединение также синтезировали следующим образом.
Тритилхлорид, 677 мг (2,43 ммоль), и TEA, 0,615 мл (4,41 ммоль), добавляли к суспензии в метиленхлориде (15 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(2,3-дигидроксипропил)оксима, 700 мг (2,21 ммоль), синтезированного таким же образом, как в ссылочном примере 20-1, и смесь перемешивали при комнатной температуре в течение 23 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:этилацетат) с получением указанного в заголовке соединения в количестве 420 мг (0,751 ммоль, выход 34%) в виде коричневой пены.
[0738] (Ссылочный пример 21-2)
1-(5-Бром-3-фторпиридин-2-ил)азетидин-3-она O-[2-гидрокси-3-(тритилокси)пропил]оксим (ссылочное соединение 21-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 21-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(2,3-дигидроксипропил)оксим (ссылочное соединение 20-1) заменяли на 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-она O-(2,3-дигидроксипропил)оксим, синтезированный таким же образом, как в ссылочном примере 20-2. В результате указанное в заголовке соединение (выход 80%) было получено в виде светло-коричневой пены.
Масс-спектр (ESI, m/z): 576, 578[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,12 (dd, J=0,9, 2,0 Гц, 1H), 7,92 (dd, J=2,0, 11,3 Гц, 1H), 7,55-7,13 (m, 15H), 5,06 (d, J=5,1 Гц, 1H), 4,85-4,74 (m, 2H), 4,73-4,52 (m, 2H), 4,11-3,96 (m, 2H), 3,96-3,81 (m, 1H), 3,04-2,87 (m, 2H).
[0739] (Ссылочный пример 22)
1-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-3-метоксипропан-2-илацетат (ссылочное соединение 22)

DMSO, 1 мл, глицидиловый метиловый эфир, 0,17 мл (1,9 ммоль), и 1-(5-бромпиримидин-2-ил)азетидин-3-она оксим, 0,30 г (1,2 ммоль), синтезированный таким же образом, как в ссылочном примере 9-1, добавляли к раствору в воде (1 мл) гидроксида калия, 0,10 г (1,8 ммоль), и смесь перемешивали при комнатной температуре в течение 20 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония, и осажденное твердое вещество собирали с помощью фильтрации. Фильтрат экстрагировали метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат объединяли с твердым веществом, собранным с помощью предыдущей фильтрации, и смесь концентрировали при пониженном давлении. Концентрированный остаток сушили при пониженном давлении с получением неочищенного продукта в количестве 0,41 г, содержащего 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(2-гидрокси-3-метоксипропил)оксим, в виде белого твердого вещества.
Затем уксусный ангидрид, 0,17 мл (1,8 ммоль), и TEA, 0,34 мл (2,4 ммоль), добавляли к раствору в метиленхлориде (8 мл) и THF (4 мл) полученного выше неочищенного продукта, 0,40 г, содержащего 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(2-гидрокси-3-метоксипропил)оксим, и смесь перемешивали при комнатной температуре в течение 96 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением неочищенного продукта в количестве 167 мг, содержащего 1-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)-3-метоксипропан-2-илацетат, в виде белого твердого вещества.
Затем полученный выше неочищенный продукт, 0,17 г, содержащий 1-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)-3-метоксипропан-2-илацетат, трет-бутил{[2-фтор-3-(4,4,5,5,-тетраметил-1,3,2-диоксаборолан-2-ил)бензил]окси}диметилсилан, 0,16 г (0,45 ммоль), синтезированный таким же образом, как в ссылочном примере 5, и 2 М водный раствор карбоната натрия, 0,70 мл (1,4 ммоль), суспендировали в 1,2-диметоксиэтане (6 мл). Суспензию дегазировали и продували азотом. Затем добавляли тетракис(трифенилфосфин)палладий(0), 78 мг (0,067 ммоль). Смесь перемешивали под струей аргона при 80°C в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 0,14 г (0,27 ммоль, выход 23% [три этапа]) в виде светло-желтого масла.
Масс-спектр (CI, m/z): 533[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,52-7,42 (m, 2H), 7,34-7,28 (m, 1H), 5,28-5,07 (m, 1H), 4,89-4,74 (m, 6H), 4,26-4,07 (m, 2H), 3,57-3,42 (m, 2H), 3,27 (s, 3H), 2,04 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0740] (Ссылочный пример 23)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(3-фтор-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 23)

Метансульфонилхлорид, 51 мкл (0,65 ммоль), добавляли к раствору в метиленхлориде (6 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксима, 210 мг (0,506 ммоль), синтезированного таким же образом, как в ссылочном примере 18-1. Затем при охлаждении льдом добавляли TEA, 106 мкл (0,761 ммоль), и смесь перемешивали при комнатной температуре в течение 15 минут. Затем добавляли метансульфонилхлорид, 51 мкл (0,65 ммоль), и TEA, 106 мкл (0,761 ммоль), и смесь перемешивали при комнатной температуре в течение 10 минут. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор карбоната натрия с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Раствор 1 М тетрабутиламмония фторида в THF, 1,15 мл (1,15 ммоль), добавляли к раствору в THF (6 мл) концентрированного остатка, и смесь перемешивали при 60°C в течение 8 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 137 мг (0,328 ммоль, выход 65% [два этапа]) в виде бесцветного масла.
Масс-спектр (CI, m/z): 417, 419[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,80-4,73 (m, 4H), 4,64-4,40 (m, 3H), 4,17-4,03 (m, 2H), 3,76-3,66 (m, 2H), 3,47-3,35 (m, 2H), 2,47-2,28 (m, 1H), 1,76-1,54 (m, 2H), 1,53-1,41 (m, 4H).
[0741] (Ссылочный пример 24-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[2-фтор-3-(тритилокси)пропил]оксим (ссылочное соединение 24-1)

При 0°C BAST, 5,9 мл (29 ммоль), добавляли к раствору в метиленхлориде (60 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[2-гидрокси-3-(тритилокси)пропил]оксима, 5,4 г (9,7 ммоль), синтезированного таким же образом, как в ссылочном примере 21-1, и смесь перемешивали при комнатной температуре в течение 24 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли 30 мл TBME, и смесь перемешивали при комнатной температуре в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 3,0 г (5,3 ммоль, выход 55%) в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 561, 563[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,57 (s, 2H), 7,45-7,19 (m, 15H), 5,03-4,84 (m, 1H), 4,78-4,71 (m, 2H), 4,69-4,55 (m, 2H), 4,41-4,11 (m, 2H), 3,33-3,11(m, 2H).
[0742] (Ссылочный пример 24-2)
1-(5-Бром-3-фторпиридин-2-ил)азетидин-3-она O-[2-фтор-3-(тритилокси)пропил]оксим (ссылочное соединение 24-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 24-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[2-гидрокси-3-(тритилокси)пропил]оксим (ссылочное соединение 21-1) заменяли на 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-она O-[2-гидрокси-3-(тритилокси)пропил]оксим, синтезированный таким же образом, как в ссылочном примере 21-2, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 50%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 578, 580[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,12 (dd, J=0,9, 1,9 Гц, 1H), 7,92 (dd, J=1,9, 11,2 Гц, 1H), 7,46-7,16 (m, 15H), 5,03-4,82 (m, 1H), 4,82-4,76 (m, 2H), 4,76-4,59 (m, 2H), 4,36-4,15 (m, 2H), 3,33-3,10 (m, 2H).
[0743] (Ссылочный пример 25)
4-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)бутан-1,2-диилдиацетат (ссылочное соединение 25)

TEA, 4,0 мл (29 ммоль), и уксусный ангидрид, 0,80 мл (8,5 ммоль), добавляли к раствору в DMF (58 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3,4-дигидроксибутил)оксима, 1,92 г (5,80 ммоль), синтезированного таким же образом, как в ссылочном примере 17-2, и смесь перемешивали при комнатной температуре в течение 24 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 340 мг (0,819 ммоль, выход 14%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 415, 417[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 5,12-5,03 (m, 1H), 4,81-4,68 (m, 4H), 4,20 (dd, J=3,3, 12,0 Гц, 1H), 4,13-4,00 (m, 3H), 2,02 (s, 3H), 2,01 (s, 3H), 1,98-1,82 (m, 2H).
[0744] (Ссылочный пример 26)
4-{[(1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}азетидин-3-илиден)амино]окси}бутан-1,2-диилдиацетат (ссылочное соединение 26)

2 н соляную кислоту, 60 мкл (0,13 ммоль), добавляли к раствору в THF (2 мл) 4-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]бутан-1,2-диилдиацетата, 72 мг (0,13 ммоль), синтезированного таким же образом, как в ссылочном примере 6-20, и смесь перемешивали при комнатной температуре в течение 20 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 53 мг (0,12 ммоль, выход 92%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 461[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,53-7,41 (m, 2H), 7,33-7,26 (m, 1H), 5,34 (t, J=5,6 Гц, 1H), 5,13-5,05 (m, 1H), 4,86-4,75 (m, 4H), 4,60 (d, J=5,6 Гц, 2H), 4,21 (dd, J=3,2, 12,0 Гц, 1H), 4,14-4,01 (m, 3H), 2,03 (s, 3H), 2,01 (s, 3H), 1,99-1,83 (m, 2H).
[0745] (Ссылочный пример 27)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(2-гидроксиэтил)оксим (ссылочное соединение 27)

Раствор 2 М хлорида водорода в этаноле, 16 мл (32 ммоль), добавляли к 1-(5-бромпиримидин-2-ил)азетидин-3-она O-{2-[(тетрагидропиран-2-ил)окси]этил}оксиму, 1,79 г (4,82 ммоль), синтезированному таким же образом, как в ссылочном примере 10-4, и смесь перемешивали при комнатной температуре в течение 8 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении, и к концентрированному остатку добавляли TBME (5 мл). Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 1,10 г (3,83 ммоль, выход 79%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 287, 289[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,38 (s, 2H), 4,85-4,79 (m, 4H), 4,24-4,19 (m, 2H), 3,93-3,86 (m, 2H), 2,05 (t, J=6,0 Гц, 1H).
[0746] (Ссылочный пример 28-1)
2-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)этилпропионат (ссылочное соединение 28-1)

TEA, 750 мкл (5,38 ммоль), добавляли к суспензии в метиленхлориде (3 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(2-гидроксиэтил)оксима, 303 мг (1,06 ммоль), синтезированного таким же образом, как в ссылочном примере 27, и смесь перемешивали в течение 10 минут при охлаждении льдом. Затем в нее по каплям вливали пропионилхлорид, 182 мкл (2,09 ммоль), при охлаждении льдом, и смесь перемешивали при комнатной температуре в течение 30 минут. Затем добавляли метиленхлорид, (7 мл), TEA, 750 мкл (5,38 ммоль), и пропионилхлорид, 182 мкл (2,09 ммоль), при охлаждении льдом, и смесь перемешивали при комнатной температуре в течение 15 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией метиленхлоридом. Органический слой сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат=от 87:13 до 66:34 (об/об)) с получением указанного в заголовке соединения в количестве 273 мг (0,796 ммоль, выход 75%) в виде светло-желтого масла.
Масс-спектр (CI, m/z): 343, 345[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,37 (s, 2H), 4,84-4,76 (m, 4H), 4,36-4,24 (m, 4H), 2,37 (q, J=7,6 Гц, 2H), 1,15 (t, J=7,6 Гц, 3H).
[0747] (Ссылочный пример 28-2)
2-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)этилбутират (ссылочное соединение 28-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 28-1, за исключением того, что пропионилхлорид заменяли на бутирилхлорид. В результате указанное в заголовке соединение (выход 41%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 357, 359[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,37 (s, 2H), 4,82-4,77 (m, 4H), 4,35-4,25 (m, 4H), 2,32 (t, J=7,4 Гц, 2H), 1,66 (sext, J=7,4 Гц, 2H), 0,95 (t, J=7,4 Гц, 3H).
[0748] (Ссылочный пример 28-3)
2-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)этилбензоат (ссылочное соединение 28-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 28-1, за исключением того, что пропионилхлорид заменяли на бензоилхлорид. В результате указанное в заголовке соединение (выход 41%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 391, 393[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,36 (s, 2H), 8,07-8,04 (m, 2H), 7,61-7,54 (m, 1H), 7,47-7,42 (m, 2H), 4,80 (s, 4H), 4,60-4,53 (m, 2H), 4,45-4,38 (m, 2H).
[0749] (Ссылочный пример 29-1)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилацетат (ссылочное соединение 29-1)

TEA, 32 мкл (0,34 ммоль), и уксусный ангидрид, 103 мкл (0,731 ммоль), добавляли к раствору в метиленхлориде (4 мл) 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксима, 140 мг (0,244 ммоль), синтезированного таким же образом, как в ссылочном примере 6-25, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли TEA, 118 мкл (1,25 ммоль), и уксусный ангидрид, 207 мкл (1,48 ммоль), и смесь перемешивали при комнатной температуре в течение 13 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 139 мг (0,225 ммоль, выход 93%) в виде бесцветного масла.
Масс-спектр (CI, m/z): 617[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,56 (d, J=1,4 Гц, 2H), 7,54-7,48 (m, 1H), 7,30-7,19 (m, 2H), 4,90-4,86 (m, 4H), 4,85 (s, 2H), 4,61-4,57 (m, 1H), 4,25-4,09 (m, 4H), 3,88-3,77 (m, 2H), 3,57-3,48 (m, 1H), 3,47-3,38 (m, 1H), 2,47-2,39 (m, 1H), 2,07 (s, 3H), 1,86-1,47 (m, 6H), 0,96 (s, 9H), 0,14 (s, 6H).
[0750] (Ссылочный пример 29-2)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилпропионат (ссылочное соединение 29-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 29-1, за исключением того, что уксусный ангидрид заменяли на пропановый ангидрид. В результате указанное в заголовке соединение (выход 76%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 631[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,53-7,47 (m, 1H), 7,30-7,20 (m, 2H), 4,90-4,86 (m, 4H), 4,85 (s, 2H), 4,61-4,57 (m, 1H), 4,24-4,13 (m, 4H), 3,89-3,78 (m, 2H), 3,56-3,48 (m, 1H), 3,47-3,39 (m, 1H), 2,46-2,30 (m, 3H), 1,85-1,40 (m, 6H), 1,19-1,12 (m, 3H), 0,96 (s, 9H), 0,14 (s, 6H).
[0751] (Ссылочный пример 29-3)
2-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этилацетат (ссылочное соединение 29-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 29-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 6-25) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-(2-гидроксиэтил)оксим, синтезированный таким же образом, как в ссылочном примере 72. В результате указанное в заголовке соединение (выход 79%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 357, 359[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,49 (s, 2H), 4,24-4,11 (m, 4H), 3,92-3,77 (m, 4H), 2,57-2,51 (m, 2H), 2,39-2,32 (m, 2H), 2,02 (s, 3H).
[0752] (Ссылочный пример 29-4)
3-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)циклобутилацетат (ссылочное соединение 29-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 29-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 6-25) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-гидроксициклобутил)оксим, синтезированный таким же образом, как в ссылочном примере 96-1, и добавляли DMAP. В результате указанное в заголовке соединение (выход 98%) было получено в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 5,08-4,99 (m, 1H), 4,84-4,71 (m, 5H), 2,49-2,41 (m, 2H), 2,39-2,28 (m, 2H), 2,01 (s, 3H).
[0753] (Ссылочный пример 29-5)
2-[3-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)азетидин-1-ил]этилацетат (ссылочное соединение 29-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 29-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 6-25) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[1-(2-гидроксиэтил)азетидин-3-ил]оксим, синтезированный таким же образом, как в ссылочном примере 96-2. В результате указанное в заголовке соединение (выход 88%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 384, 386[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,79-4,70 (m, 5H), 3,96 (t, J=5,5 Гц, 2H), 3,58-3,50 (m, 2H), 3,10-3,01 (m, 2H), 2,64 (t, J=5,6 Гц, 2H), 1,99 (s, 3H).
[0754] (Ссылочный пример 30-1)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилбутират (ссылочное соединение 30-1)
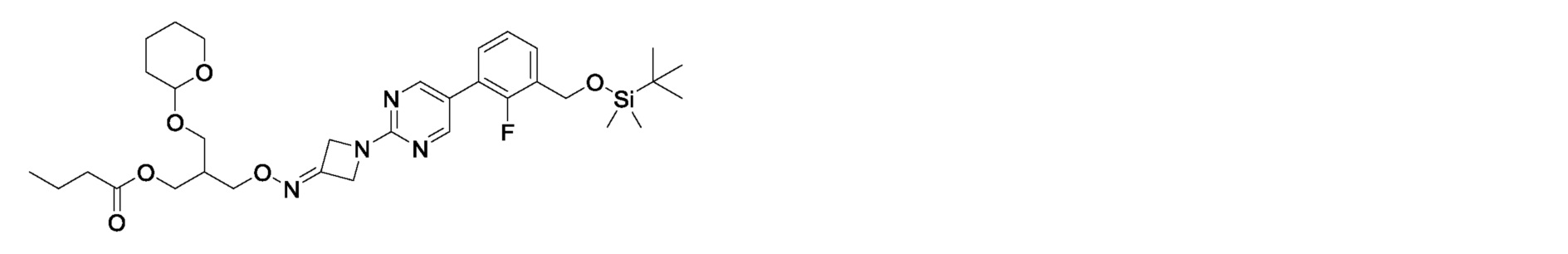
Масляный ангидрид, 60 мкл (0,37 ммоль), TEA, 80 мкл (0,57 ммоль), и DMAP, 4,0 мг (0,033 ммоль), добавляли к раствору в метиленхлориде (6 мл) 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксима, 0,16 г (0,28 ммоль), синтезированного таким же образом, как в ссылочном примере 6-25, и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 0,13 г (0,20 ммоль, выход 71%) в виде бесцветного масла.
Масс-спектр (CI, m/z): 645[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,3 Гц, 2H), 7,53-7,42 (m, 2H), 7,36-7,27 (m, 1H), 4,92-4,73 (m, 6H), 4,62-4,50 (m, 1H), 4,17-3,99 (m, 4H), 3,81-3,60 (m, 2H), 3,51-3,23 (m, 2H), 2,39-2,20 (m, 3H), 1,84-1,33 (m, 8H), 0,91 (s, 9H), 0,88 (t, J=7,4 Гц, 3H), 0,11 (s, 6H).
[0755] (Ссылочный пример 30-2)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилизобутират (ссылочное соединение 30-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 30-1, за исключением того, что масляный ангидрид заменяли на изомасляный ангидрид. В результате указанное в заголовке соединение (выход 82%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 645[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,53-7,42 (m, 2H), 7,34-7,29 (m, 1H), 4,88-4,76 (m, 6H), 4,60-4,52 (m, 1H), 4,16-4,04 (m, 4H), 3,77-3,65 (m, 2H), 3,48-3,34 (m, 2H), 2,55 (sep, J=7,0 Гц, 1H), 2,40-2,27 (m, 1H), 1,79-1,38 (m, 6H), 1,09 (d, J=7,0 Гц, 6H), 0,91 (s, 9H), 0,11 (s, 6H).
[0756] (Ссылочный пример 30-3)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилпивалат (ссылочное соединение 30-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 30-1, за исключением того, что масляный ангидрид заменяли на триметилуксусный ангидрид. В результате указанное в заголовке соединение (выход 73%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 659[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,3 Гц, 2H), 7,52-7,42 (m, 2H), 7,35-7,28 (m, 1H), 4,85-4,79 (m, 6H), 4,59-4,53 (m, 1H), 4,20-4,04 (m, 4H), 3,78-3,63 (m, 2H), 3,47-3,34 (m, 2H), 2,39-2,29 (m, 1H), 1,75-1,37 (m, 6H), 1,15 (s, 9H), 0,91 (s, 9H), 0,11 (s, 6H).
[0757] (Ссылочный пример 30-4)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилгексаноат (Ссылочный пример 30-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 30-1, за исключением того, что масляный ангидрид заменяли на гексановый ангидрид. В результате указанное в заголовке соединение (выход 82%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 673[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,55-7,43 (m, 2H), 7,36-7,28 (m, 1H), 4,90-4,74 (m, 6H), 4,61-4,51 (m, 1H), 4,19-4,00 (m, 4H), 3,76-3,56 (m, 2H), 3,49-3,26 (m, 2H), 2,40-2,20 (m, 3H), 1,83-1,16 (m, 12H), 0,91 (s, 9H), 0,85 (t, J=7,1 Гц, 3H), 0,11 (s, 6H).
[0758] (Ссылочный пример 30-5)
3-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропилбензоат (ссылочное соединение 30-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 30-1, за исключением того, что масляный ангидрид заменяли на бензойный ангидрид. В результате указанное в заголовке соединение (выход 78%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 679[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,62 (d, J=1,4 Гц, 2H), 8,03-7,93 (m, 2H), 7,67-7,59 (m, 1H), 7,57-7,43 (m, 4H), 7,35-7,26 (m, 1H), 4,90-4,69 (m, 6H), 4,63-4,53 (m, 1H), 4,43-4,32 (m, 2H), 4,26-4,12 (m, 2H), 3,87-3,64 (m, 2H), 3,57-3,34 (m, 2H), 1,81-1,32 (m, 6H), 0,91 (s, 9H), 0,11 (s, 6H).
[0759] (Ссылочный пример 31-1)
1-(5-Бром-3-фторпиридин-2-ил)азетидин-3-ол (ссылочное соединение 31-1)

Карбонат цезия, 19 г (58 ммоль), и гидрохлорид азетидин-3-ола, 4,0 г (37 ммоль), добавляли к раствору в NMP (15 мл) 5-бром-2,3-дифторпиридина, 2,85 г (14,7 ммоль), и смесь перемешивали при 110°C в течение 1 часа. После окончания реакции реакционную смесь охлаждали естественным образом до комнатной температуры. К ней добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 2,63 г (10,7 ммоль, выход 73%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 247, 249[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 7,96 (dd, J=0,9, 2,0 Гц, 1H), 7,30 (dd, J=2,0, 10,9 Гц, 1H), 4,83-4,74 (m, 1H), 4,43-4,36 (m, 2H), 4,01-3,95 (m, 2H), 2,31 (d, J=6,3 Гц, 1H).
[0760] Указанное в заголовке соединение также синтезировали следующим образом.
TEA, 14 мл (100 моль), добавляли к раствору в этаноле (70 мл) 5-бром-2,3-дифторпиридина, 7,56 г (39,0 ммоль), и гидрохлорида азетидин-3-ола, 5,00 г (45,6 моль), и смесь перемешивали при 55°C в течение 3 часов. После окончания реакции к реакционной смеси добавляли 70 мл воды. Растворитель концентрировали при пониженном давлении до приблизительно половины объема, и остаток перемешивали при комнатной температуре. Осажденное твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 8,06 г (32,6 моль, выход 84%) в виде белого твердого вещества.
[0761] (Ссылочный пример 31-2)
1-(5-Бром-3-хлорпиридин-2-ил)азетидин-3-ол (ссылочное соединение 31-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 31-1, за исключением того, что 5-бром-2,3-дифторпиридин заменяли на 5-бром-3-хлор-2-фторпиридин. В результате указанное в заголовке соединение (выход 80%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 263, 265[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,15 (d, J=2,1 Гц, 1H), 7,91 (d, J=2,1 Гц, 1H), 5,63 (d, J=6,1 Гц, 1H), 4,54-4,45 (m, 1H), 4,38-4,31 (m, 2H), 3,89-3,82 (m, 2H).
[0762] (Ссылочный пример 31-3)
1-(3-Метоксипиридин-2-ил)азетидин-3-ол (ссылочное соединение 31-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 31-1, за исключением того, что 5-бром-2,3-дифторпиридин заменяли на 2-фтор-3-метоксипиридин, синтезированный таким же образом, как в ссылочном примере 55, что NMP заменяли на DMSO, и что температуру реакции изменяли на 100°C. В результате указанное в заголовке соединение (выход 37%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 181[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,64 (dd, J=1,4, 5,0 Гц, 1H), 7,07 (dd, J=1,4, 7,8 Гц, 1H), 6,64 (dd, J=5,0, 7,8 Гц, 1H), 5,46 (br s, 1H), 4,53-4,42 (m, 1H), 4,20-4,12 (m, 2H), 3,74-3,67 (m, 5H).
[0763] (Ссылочный пример 32-1)
1-(5-Бром-3-фторпиридин-2-ил)азетидин-3-он (ссылочное соединение 32-1)

При 0°C перйодинан Десса-Мартина, 5,9 г (14 ммоль), добавляли к суспензии в метиленхлориде (30 мл) 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-ола, 2,63 г (10,7 ммоль), синтезированного таким же образом, как в ссылочном примере 31-1, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции водный раствор тиосульфата натрия и насыщенный водный раствор гидрокарбоната натрия добавляли к реакционной смеси, и смесь перемешивали в течение 30 минут с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении с получением неочищенного продукта в количестве 2,55 г, содержащего указанное в заголовке соединение в виде коричневого твердого вещества.
Масс-спектр (CI, m/z): 245, 247[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,07 (dd, J=0,8, 1,9 Гц, 1H), 7,43 (dd, J=1,9, 10,5 Гц, 1H), 4,92-4,89 (m, 4H).
[0764] Указанное в заголовке соединение также синтезировали следующим образом.
Азадол, 40 мг (0,26 ммоль), и йодбензола диацетат, 1,80 г (5,59 ммоль), добавляли к раствору в метиленхлориде (10 мл) 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-ола, 1,00 г (4,05 ммоль), синтезированного таким же образом, как в ссылочном примере 31-1, и смесь перемешивали при комнатной температуре в течение 22 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия и тиосульфат натрия, и смесь перемешивали в течение 1 часа с последующей экстракцией этилацетатом. Органический слой промывали насыщенным водным раствором бикарбоната натрия, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли TBME и гексан, и смесь перемешивали при комнатной температуре. Твердое вещество собирали с помощью фильтрации. В результате указанное в заголовке соединение 504 мг (2,06 ммоль, выход 51%) было получено в виде белого твердого вещества.
[0765] (Ссылочный пример 32-2)
1-(5-Бромпиридин-2-ил)азетидин-3-он (ссылочное соединение 32-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 32-1, за исключением того, что 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-ол (ссылочное соединение 31-1) заменяли на 1-(5-бромпиридин-2-ил)азетидин-3-ол, синтезированный таким же образом, как в ссылочном примере 35, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:этилацетат). В результате указанное в заголовке соединение (выход 27%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 227, 229[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,25-8,23 (m, 1H), 7,79 (dd, J=2,5, 8,8 Гц, 1H), 6,65-6,61 (m, 1H), 4,79 (s, 4H).
[0766] (Ссылочный пример 32-3)
1-(5-Бром-3-метилпиридин-2-ил)азетидин-3-он (ссылочное соединение 32-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 32-1, за исключением того, что 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-ол (ссылочное соединение 31-1) заменяли на 1-(5-бром-3-метилпиридин-2-ил)азетидин-3-ол, синтезированный таким же образом, как в ссылочном примере 36. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт.
[0767] (Ссылочный пример 32-4)
1-(5-Бром-3-хлорпиридин-2-ил)азетидин-3-он (ссылочное соединение 32-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 32-1, за исключением того, что 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-ол (ссылочное соединение 31-1) заменяли на 1-(5-бром-3-хлорпиридин-2-ил)азетидин-3-ол, синтезированный таким же образом, как в ссылочном примере 31-2. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде коричневого твердого вещества.
Масс-спектр (CI, m/z): 261, 263[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,17 (d, J=2,1 Гц, 1H), 7,70 (d, J=2,1 Гц, 1H), 4,96 (s, 4H).
[0768] (Ссылочный пример 32-5)
1-[5-Бром-3-(дифторметил)пиридин-2-ил]азетидин-3-он (ссылочное соединение 32-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 32-1, за исключением того, что 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-ол (ссылочное соединение 31-1) заменяли на 1-[5-бром-3-(дифторметил)пиридин-2-ил]азетидин-3-ол, синтезированный таким же образом, как в ссылочном примере 43-2, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат). В результате указанное в заголовке соединение (выход 83%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 277, 279[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,46-8,42 (m, 1H), 8,05-8,01 (m, 1H), 7,09 (t, J=54,2 Гц, 1H), 4,95 (s, 4H).
[0769] (Ссылочный пример 32-6)
1-(5-Бром-3-циклопропилпиридин-2-ил)азетидин-3-он (ссылочное соединение 32-6)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 32-1, за исключением того, что 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-ол (ссылочное соединение 31-1) заменяли на 1-(5-бром-3-циклопропилпиридин-2-ил)азетидин-3-ол, синтезированный таким же образом, как в ссылочном примере 43-1, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат). В результате указанное в заголовке соединение (выход 87%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 267, 269[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,10 (d, J=2,3 Гц, 1H), 7,45 (dd, J=0,6, 2,3 Гц, 1H), 4,97 (s, 4H), 1,88-1,81 (m, 1H), 0,96-0,87 (m, 2H), 0,77-0,72 (m, 2H).
[0770] (Ссылочный пример 32-7)
1-(5-Бром-3-этилпиридин-2-ил)азетидин-3-он (ссылочное соединение 32-7)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 32-1, за исключением того, что 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-ол (ссылочное соединение 31-1) заменяли на 1-(5-бром-3-этилпиридин-2-ил)азетидин-3-ол, синтезированный таким же образом, как в ссылочном примере 43-3, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат). В результате указанное в заголовке соединение (выход 79%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 255, 257[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,14 (d, J=2,4 Гц, 1H), 7,66-7,64 (m, 1H), 4,88 (s, 4H), 2,59-2,45 (m, 2H), 1,17 (t, J=7,5 Гц, 3H).
[0771] (Ссылочный пример 33-1)
1-(5-Бром-3-фторпиридин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 33-1)

Карбонат цезия, 6,2 г (19 ммоль), и йодметан, 0,90 мл (14 ммоль), добавляли к раствору в DMF (8 мл) 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-она оксима, 1,65 г (6,34 ммоль), синтезированного таким же образом, как в ссылочном примере 9-2, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 1,33 г (4,85 ммоль, выход 76%) в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 274, 276[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,02 (dd, J=0,8, 1,9 Гц, 1H), 7,37 (dd, J=1,9, 10,7 Гц, 1H), 4,83-4,81 (m, 4H), 3,89 (s, 3H).
[0772] Указанное в заголовке соединение также синтезировали следующим образом.
O-метилгидроксиламина гидрохлорид 160 мг (1,92 ммоль), добавляли к раствору в THF (8 мл) 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-она, 226 мг (0,922 ммоль), синтезированного таким же образом, как в ссылочном примере 32-1, и смесь перемешивали при 50°C в течение 8 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:этилацетат) с получением указанного в заголовке соединения в количестве 129 мг (0,471 ммоль, выход 51%) в виде белого твердого вещества.
[0773] (Ссылочный пример 33-2)
1-(5-Бром-3-фторпиридин-2-ил)азетидин-3-она O-метил-d3-оксим (ссылочное соединение 33-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 33-1, за исключением того, что йодметан заменяли на йодметан-d3. В результате указанное в заголовке соединение (выход 70%) было получено в виде белого твердого вещества.
Масс-спектр (EI, m/z): 276[М]+, 278[М]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,02 (dd, J=0,9, 1,9 Гц, 1H), 7,37 (dd, J=1,9, 10,7 Гц, 1H), 4,85-4,77 (m, 4H).
[0774] (Ссылочный пример 34-1)
1-(5-Бром-3-фторпиридин-2-ил)азетидин-3-она O-[2-(2,2-диметил-1,3-диоксолан-4-ил)этил]оксим (ссылочное соединение 34-1)

Карбонат цезия, 1,10 г (3,38 ммоль), и 2-(2,2-диметил-1,3-диоксолан-4-ил)этилметансульфонат, 570 мг (2,54 ммоль), синтезированный таким же образом, как в ссылочном примере 14-6, добавляли к раствору в DMF (2 мл) 1-(5-бром-3-фторпиридин-2-ил)азетидин-3-она оксима, 220 мг (0,846 ммоль), синтезированного таким же образом, как в ссылочном примере 9-2, и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 265 мг (0,683 ммоль, выход 81%) в виде бесцветного масла.
Масс-спектр (CI, m/z): 388, 340[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,02 (dd, J=0,9, 1,9 Гц, 1H), 7,37 (dd, J=1,9, 10,7 Гц, 1H), 4,83-4,80 (m, 4H), 4,24-4,13 (m, 3H), 4,10-4,05 (m, 1H), 3,60-3,54 (m, 1H), 1,99-1,91 (m, 2H), 1,41 (s, 3H), 1,36 (s, 3H).
[0775] (Ссылочный пример 34-2)
1-(5-Бром-3-фторпиридин-2-ил)азетидин-3-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим (ссылочное соединение 34-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 34-1, за исключением того, что 2-(2,2-диметил-1,3-диоксолан-4-ил)этилметансульфонат (ссылочное соединение 14-6) заменяли на (2,2-диметил-1,3-диоксан-5-ил)метилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-4. В результате указанное в заголовке соединение (включая примеси) было получено в виде светло-желтого твердого вещества.
Масс-спектр (EI, m/z): 387[М]+, 389[М]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,02 (dd, J=0,8, 1,9 Гц, 1H), 7,37 (dd, J=1,9, 10,7 Гц, 1H), 4,83-4,79 (m, 4H), 4,17 (d, J=6,9 Гц, 2H), 4,00 (dd, J=4,0, 12,0 Гц, 2H), 3,75 (dd, J=5,8, 12,0 Гц, 2H), 2,13-2,04 (m, 1H), 1,45 (s, 3H), 1,41 (s, 3H).
[0776] (Ссылочный пример 34-3)
1-(5-Бром-3-фторпиридин-2-ил)азетидин-3-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим (ссылочное соединение 34-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 34-1, за исключением того, что 2-(2,2-диметил-1,3-диоксолан-4-ил)этилметансульфонат (ссылочное соединение 14-6) заменяли на (2,2-диметил-1,3-диоксолан-4-ил)метилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-5, и температуру реакции изменяли на 80°C. В результате указанное в заголовке соединение (выход 41%) было получено в виде желтого твердого вещества.
Масс-спектр (CI, m/z): 374, 376[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,10 (dd, J=0,9, 2,0 Гц, 1H), 7,91 (dd, J=2,0, 11,3 Гц, 1H), 4,85-4,77 (m, 4H), 4,32-4,23 (m, 1H), 4,07-4,00 (m, 3H), 3,66 (dd, J=6,4, 8,4 Гц, 1H), 1,32 (s, 3H), 1,27 (s, 3H).
[0777] (Ссылочный пример 35)
1-(5-Бромпиридин-2-ил)азетидин-3-ол (ссылочное соединение 35)

DIPEA, 2,72 мл (15,6 ммоль), добавляли к суспензии в DMF (10 мл) 5-бром-2-хлорпиридина, 1,00 г (5,20 ммоль), и гидрохлорида азетидин-3-ола, 712 мг (6,50 ммоль), и смесь перемешивали при 120°C в течение 22 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией толуолом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 200 мг (0,873 ммоль, выход 17%) в виде бесцветного масла.
Масс-спектр (CI, m/z): 229, 231[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,11 (dd, J=0,6, 2,7 Гц, 1H), 7,65 (dd, J=2,7, 8,8 Гц, 1H), 6,36 (dd, J=0,6, 8,8 Гц, 1H), 5,66 (d, J=6,4 Гц, 1H), 4,59-4,52 (m, 1H), 4,16-4,10 (m, 2H), 3,67-3,62 (m, 2H).
[0778] (Ссылочный пример 36)
1-(5-Бром-3-метилпиридин-2-ил)азетидин-3-ол (ссылочное соединение 36)

Гидрохлорид азетидин-3-ола, 1,2 г (11 ммоль), и карбонат цезия, 5,1 г (16 ммоль), добавляли к раствору в DMF (10 мл) 5-бром-2-фтор-3-метилпиридина, 1,0 г (5,3 ммоль), и смесь перемешивали при комнатной температуре в течение 15 часов и при 100°C в течение 5 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 0,50 г (2,1 ммоль, выход 40%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 243, 245[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,01 (d, J=2,4 Гц, 1H), 7,54-7,49 (m, 1H), 5,55 (d, J=4,8 Гц, 1H), 4,54-4,44 (m, 1H), 4,24-4,17 (m, 2H), 3,81-3,69 (m, 2H), 2,12 (s, 3H).
[0779] (Ссылочный пример 37-1)
трет-Бутил-3-(метоксиимино)азетидин-1-карбоксилат (ссылочное соединение 37-1)

O-метилгидроксиламина гидрохлорид, 3,0 г (36 ммоль), и карбонат натрия, 5,6 г (53 ммоль), добавляли к раствору в этаноле (30 мл) и воде (8 мл) трет-бутил-3-оксоазетидин-1-карбоксилата, 3,0 г (17 ммоль), и смесь перемешивали при 70°C в течение 12 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении с получением неочищенного продукта в количестве 3,3 г, содержащего указанное в заголовке соединение.
Масс-спектр (CI, m/z): 201[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 4,61-4,47 (m, 4H), 3,78 (s, 3H), 1,40 (s, 9H).
[0780] (Ссылочный пример 37-2)
трет-Бутил-3-[(бензилокси)имино]азетидин-1-карбоксилат (ссылочное соединение 37-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 37-1, за исключением того, что O-метилгидроксиламина гидрохлорид заменяли на O-бензилгидроксиламина гидрохлорид. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде светло-желтого масла.
[0781] (Ссылочный пример 38)
Азетидин-3-она O-метилоксима гидрохлорид (ссылочное соединение 38)

При 0°C раствор 2 М хлорида водорода в этаноле, 30 мл (60 ммоль), добавляли к раствору в этаноле (30 мл) неочищенного продукта, 3,3 г, из ссылочного примера 37-1, который включал в себя трет-бутил-3-(метоксиимино)азетидин-1-карбоксилат, и смесь перемешивали при комнатной температуре в течение 7 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении с получением неочищенного продукта в количестве 1,26 г, содержащего указанное в заголовке соединение.
Масс-спектр (CI, m/z): 101[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 9,81 (br s., 2H), 4,83-4,70 (m, 4H), 3,82 (s, 3H).
[0782] (Ссылочный пример 39)
5-Бром-2-[3-(метоксиимино)азетидин-1-ил]никотинонитрил (ссылочное соединение 39)

TEA, 0,65 мл (4,7 ммоль), добавляли к суспензии в этаноле (8 мл) неочищенного продукта, 0,25 г, из ссылочного примера 38, который включал в себя азетидин-3-она O-метилоксима гидрохлорид, и 5-бром-2-хлорникотинонитрила, 0,20 г (0,92 ммоль), и смесь перемешивали при 70°C в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 0,12 г (включая примеси) в виде светло-коричневого твердого вещества.
Масс-спектр (CI, m/z): 281, 283[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (d, J=2,4 Гц, 1H), 8,36 (d, J=2,4 Гц, 1H), 4,96-4,92 (m, 4H), 3,82 (s, 3H).
[0783] (Ссылочный пример 40)
1-[3-(Дифторметил)пиридин-2-ил]азетидин-3-ол (ссылочное соединение 40)

Гидрохлорид азетидин-3-ола, 1,13 г (10,3 ммоль), и DIPEA, 4,20 мл (24,1 ммоль), добавляли к раствору в DMSO (10 мл) 2-хлор-3-(дифторметил)пиридина, 1,32 г (8,07 ммоль), и смесь перемешивали при 110°C в течение 13 часов. Затем добавляли карбонат цезия, 7,89 г (24,2 ммоль), и гидрохлорид азетидин-3-ола, 1,13 г (10,3 ммоль), и смесь перемешивали при 110°C в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 1,03 г (5,15 ммоль, выход 64%) в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 201[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,24-8,20 (m, 1H), 7,74-7,70 (m, 1H), 7,01 (t, J=54,9 Гц, 1H), 6,75 (dd, J=4,9, 7,5 Гц, 1H), 5,63 (d, J=3,6 Гц, 1H), 4,59-4,50 (m, 1H), 4,31-4,24 (m, 2H), 3,88-3,82 (m, 2H).
[0784] (Ссылочный пример 41)
1-(3-Йодпиридин-2-ил)азетидин-3-ол (ссылочное соединение 41)

Гидрохлорид азетидин-3-ола, 1,22 г (11,1 ммоль), и DIPEA, 4,64 мл (26,6 ммоль), добавляли к раствору в DMSO (10 мл) 2-фтор-3-йодпиридина, 1,98 г (8,88 ммоль), и смесь перемешивали при 100°C в течение 9 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией толуолом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 1,66 г (6,01 ммоль, выход 68%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 277[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,12 (dd, J=1,6, 4,7 Гц, 1H), 8,00 (dd, J=1,6, 7,5 Гц, 1H), 6,52 (dd, J=4,7, 7,5 Гц, 1H), 5,56 (s, 1H), 4,46-4,36 (m, 3H), 3,87-3,81 (m, 2H).
[0785] (Ссылочный пример 42)
1-(3-Циклопропилпиридин-2-ил)азетидин-3-ол (ссылочное соединение 42)

Циклопропилбороновую кислоту, 443 мг (5,16 ммоль), 2 М водный раствор карбоната натрия, 5,16 мл (10,3 ммоль), ацетат палладия(II), 30 мг (0,13 ммоль), и 2-дициклогексилфосфино-2',6'-диметокси-1,1'-бифенил, 106 мг (0,258 ммоль), добавляли к раствору в толуоле (20 мл) 1-(3-йодпиридин-2-ил)азетидин-3-ола, 712 мг (2,58 ммоль), синтезированного таким же образом, как в ссылочном примере 41. Смесь дегазировали, продували азотом и перемешивали при 110°C в течение 2 часов под струей аргона. Затем добавляли ацетат палладия(II), 30 мг (0,13 ммоль), и 2-дициклогексилфосфино-2',6'-диметокси-1,1'-бифенил, 100 мг (0,244 ммоль). Смесь дегазировали, продували азотом и перемешивали при 110°C в течение 5 часов под струей аргона. Затем добавляли ацетат палладия(II), 60 мг (0,27 ммоль), и 2-дициклогексилфосфино-2',6'-диметокси-1,1'-бифенил, 200 мг (0,487 ммоль). Смесь дегазировали, продували азотом и перемешивали при 110°C в течение 4 часов под струей аргона. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией толуолом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 276 мг (1,45 ммоль, выход 56%) в виде желтого масла.
Масс-спектр (CI, m/z): 191[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,93-7,90 (m, 1H), 7,19-7,16 (m, 1H), 6,61 (dd, J=4,9, 7,3 Гц, 1H), 5,49 (br s, 1H), 4,54-4,47 (m, 1H), 4,32-4,27 (m, 2H), 3,87-3,83 (m, 2H), 1,80-1,73 (m, 1H), 0,89-0,84 (m, 2H), 0,63-0,58 (m, 2H).
[0786] (Ссылочный пример 43-1)
1-(5-Бром-3-циклопропилпиридин-2-ил)азетидин-3-ол (ссылочное соединение 43-1)

При охлаждении льдом N-бромсукцинимид, 326 мг (1,83 ммоль), добавляли к раствору в ацетонитриле (10 мл) 1-(3-циклопропилпиридин-2-ил)азетидин-3-ола, 332 мг (1,75 ммоль), синтезированного таким же образом, как в ссылочном примере 42, и смесь перемешивали при 0°C в течение 30 минут. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 383 мг (1,42 ммоль, выход 82%) в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 269, 271[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,00-7,97 (m, 1H), 7,30 (dd, J=0,8, 2,3 Гц, 1H), 5,56 (br s, 1H), 4,55-4,47 (m, 1H), 4,35-4,28 (m, 2H), 3,88-3,83 (m, 2H), 1,81-1,73 (m, 1H), 0,91-0,85 (m, 2H), 0,70-0,65 (m, 2H).
[0787] (Ссылочный пример 43-2)
1-[5-Бром-3-(дифторметил)пиридин-2-ил]азетидин-3-ол (ссылочное соединение 43-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 43-1, за исключением того, что 1-(3-циклопропилпиридин-2-ил)азетидин-3-ол (ссылочное соединение 42) заменяли на 1-[3-(дифторметил)пиридин-2-ил]азетидин-3-ол, синтезированный таким же образом, как в ссылочном примере 40, и температура реакции была равна температуре окружающей среды. В результате указанное в заголовке соединение (выход 95%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 279, 281[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,33-8,29 (m, 1H), 7,88-7,85 (m, 1H), 6,96 (t, J=54,6 Гц, 1H), 5,68 (d, J=5,4 Гц, 1H), 4,59-4,50 (m, 1H), 4,32-4,25 (m, 2H), 3,88-3,82 (m, 2H).
[0788] (Ссылочный пример 43-3)
1-(5-Бром-3-этилпиридин-2-ил)азетидин-3-ол (ссылочное соединение 43-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 43-1, за исключением того, что 1-(3-циклопропилпиридин-2-ил)азетидин-3-ол (ссылочное соединение 42) заменяли на 1-(3-этилпиридин-2-ил)азетидин-3-ол, синтезированный таким же образом, как в ссылочном примере 45. В результате указанное в заголовке соединение (выход 86%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 257, 259[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,03 (d, J=2,3 Гц, 1H), 7,51-7,48 (m, 1H), 5,57 (d, J=4,1 Гц, 1H), 4,54-4,46 (m, 1H), 4,22-4,16 (m, 2H), 3,78-3,72 (m, 2H), 2,50-2,42 (m, 2H), 1,11 (t, J=7,5 Гц, 3H).
[0789] (Ссылочный пример 43-4)
1-[5-Бром-3-(метоксиметил)пиридин-2-ил]азетидин-3-ол (ссылочное соединение 43-4)

При охлаждении льдом N-бромсукцинимид, 900 мг (5,06 ммоль), добавляли к раствору в ацетонитриле (10 мл) 1-[3-(метоксиметил)пиридин-2-ил]азетидин-3-ола, 890 мг (4,58 ммоль), синтезированного таким же образом, как в ссылочном примере 54, и смесь перемешивали при 0°C в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли воду. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 690 мг (2,53 ммоль, выход 55%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 273, 275[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,10 (d, J=2,4 Гц, 1H), 7,61 (d, J=2,4 Гц, 1H), 5,59 (d, J=6,0 Гц, 1H), 4,60-4,45 (m, 1H), 4,27-4,20 (m, 4H), 3,85-3,78 (m, 2H), 3,28 (s, 3H).
[0790] (Ссылочный пример 43-5)
1-(5-Бром-3-метоксипиридин-2-ил)азетидин-3-ол (ссылочное соединение 43-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 43-1, за исключением того, что 1-(3-циклопропилпиридин-2-ил)азетидин-3-ол (ссылочное соединение 42) заменяли на 1-(3-метоксипиридин-2-ил)азетидин-3-ол, синтезированный таким же образом, как в ссылочном примере 31-3, и температура реакции была равна температуре окружающей среды. В результате указанное в заголовке соединение (выход 76%) было получено в виде светло-желтого масла.
Масс-спектр (ESI, m/z): 259, 261[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,72 (d, J=2,0 Гц, 1H), 7,25 (d, J=2,0 Гц, 1H), 5,52 (d, J=5,6 Гц, 1H), 4,52-4,44 (m, 1H), 4,22-4,14 (m, 2H), 3,75 (s, 3H), 3,74-3,68 (m, 2H).
[0791] (Ссылочный пример 44)
1-(3-Винилпиридин-2-ил)азетидин-3-ол (ссылочное соединение 44)

Винилтрифторборат калия, 582 мг (4,34 ммоль), и TEA, 530 мкл (3,80 ммоль), добавляли к раствору в 1-пропаноле (30 мл) 1-(3-йодпиридин-2-ил)азетидин-3-ола, 1,00 г (3,62 ммоль), синтезированного таким же образом, как в ссылочном примере 41. Смесь дегазировали и продували азотом. Добавляли дихлорид 1,1'-бис(дифенилфосфино)ферроценпалладия(II), 53,0 мг (0,072 ммоль), и смесь перемешивали при 100°C в течение 2 часов под струей аргона. Затем добавляли дихлорид 1,1'-бис(дифенилфосфино)ферроценпалладия(II), 100 мг (0,137 ммоль). Смесь перемешивали под струей аргона при 100°C в течение 10 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. К водному слою добавляли насыщенный водный раствор карбоната натрия с последующей экстракцией этилацетатом. Органические слои объединяли, промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 370 мг (2,10 ммоль, выход 58%) в виде коричневого масла.
Масс-спектр (CI, m/z): 177[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,04 (dd, J=1,8, 4,8 Гц, 1H), 7,61 (dd, J=1,8, 7,4 Гц, 1H), 6,76-6,67 (m, 2H), 5,60 (dd, J=1,4, 17,4 Гц, 1H), 5,53 (br s, 1H), 5,27 (dd, J=1,4, 11,0 Гц, 1H), 4,52-4,46 (m, 1H), 4,23-4,18 (m, 2H), 3,77-3,72 (m, 2H).
[0792] (Ссылочный пример 45)
1-(3-Этилпиридин-2-ил)азетидин-3-ол (ссылочное соединение 45)

Палладированный уголь (10% порошок Pd-угля (водный) типа PE (торговое наименование), производства N.E. CHEMCAT, содержащий 54% воды), 38 мг, добавляли к раствору в THF (4 мл) и этаноле (8 мл) 1-(3-винилпиридин-2-ил)азетидин-3-ола, 370 мг (2,10 ммоль), синтезированного таким же образом, как в ссылочном примере 44. При пониженном давлении атмосферу продували водородом, и смесь перемешивали при комнатной температуре в течение 30 минут. После окончания реакции реакционную смесь фильтровали через целит. Фильтрат концентрировали при пониженном давлении с получением неочищенного продукта в количестве 388 мг, содержащего указанное в заголовке соединение в виде светло-желтого масла.
[0793] (Ссылочный пример 46)
Метил-5-бром-2-фторникотинат (ссылочное соединение 46)

Йодметан, 0,75 мл (12 ммоль), и карбонат калия, 2,5 г (18 ммоль), добавляли к раствору в DMF (8 мл) 5-бром-2-фторникотиновой кислоты, 2,0 г (9,1 ммоль), и смесь перемешивали при комнатной температуре в течение 20 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 1,7 г (7,3 ммоль, выход 80%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 234, 236[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,66 (dd, J=1,3, 2,6 Гц, 1H), 8,56 (dd, J=2,6, 8,2 Гц, 1H), 3,89 (s, 3H).
[0794] (Ссылочный пример 47)
2-(5-Бром-2-фторпиридин-3-ил)пропан-2-ол (ссылочное соединение 47)

Раствор в THF (10 мл) метил-5-бром-2-фторникотината, 1,65 г (7,05 ммоль), синтезированного таким же образом, как в ссылочном примере 46, дегазировали и продували азотом. При 0°C добавляли 1,4 М раствор метилмагния бромида в THF и толуоле, 12,6 мл (17,6 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 1,71 г (включая примеси) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 234, 236[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,26 (d, J=1,6, 2,6 Гц, 1H), 8,19 (d, J=2,6, 8,8 Гц, 1H), 5,60 (s, 1H), 1,51-1,43 (m, 6H).
[0795] (Ссылочный пример 48)
5-Бром-2-фтор-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин (ссылочное соединение 48)

PPTS, 0,37 г (1,5 ммоль), и DHP, 3,1 мл (37 ммоль), добавляли к раствору в метиленхлориде (10 мл) 2-(5-бром-2-фторпиридин-3-ил)пропан-2-ола, 1,7 г (7,3 ммоль), синтезированного таким же образом, как в ссылочном примере 47, и смесь перемешивали при комнатной температуре в течение 20 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 2,1 г (6,6 ммоль, выход 90%) в виде бесцветного масла.
Масс-спектр (CI, m/z): 318, 320[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,30 (dd, J=1,6, 2,4 Гц, 1H), 8,12 (dd, J=2,4, 8,8 Гц, 1H), 4,76-4,72 (m, 1H), 3,85-3,71 (m, 1H), 3,42-3,32 (m, 1H), 1,85-1,33 (m, 12H).
[0796] (Ссылочный пример 49)
1-(5-Бром-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-2-ил)азетидин-3-ол (ссылочное соединение 49)

Карбонат калия, 3,61 г (26,1 ммоль), и гидрохлорид азетидин-3-ола, 1,43 г (13,1 ммоль), добавляли к раствору в DMSO (10 мл) 5-бром-2-фтор-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридина, 2,08 г (6,54 ммоль), синтезированного таким же образом, как в ссылочном примере 48, и смесь перемешивали при 90°C в течение 10 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 846 мг (2,28 ммоль, выход 35%) в виде бесцветной пены.
Масс-спектр (CI, m/z): 371, 373[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,13 (d, J=2,3 Гц, 1H), 7,61 (d, J=2,3 Гц, 1H), 5,46 (br s, 1H), 4,46-4,35 (m, 2H), 4,30-4,13 (m, 2H), 3,88-3,71 (m, 3H), 3,41-3,22 (m, 1H), 1,87-1,29 (m, 12H).
[0797] (Ссылочный пример 50-1)
1-(5-Бром-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-2-ил)азетидин-3-он (ссылочное соединение 50-1)

Перйодинан Десса-Мартина, 1,45 г (3,42 ммоль), и гидрокарбонат натрия, 300 мг (3,57 ммоль), добавляли к раствору в метиленхлориде (20 мл) 1-(5-бром-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-2-ил)азетидин-3-ола, 846 мг (2,28 ммоль), синтезированного таким же образом, как в ссылочном примере 49, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду и тиосульфат натрия с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 554 мг (1,50 ммоль, выход 66%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 369, 371[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,24 (d, J=2,4 Гц, 1H), 7,77 (d, J=2,4 Гц, 1H), 4,95-4,82 (m, 4H), 4,58-4,48 (m, 1H), 3,81-3,67 (m, 1H), 3,36-3,28 (m, 1H), 1,87-1,24 (m, 12H).
[0798] (Ссылочный пример 50-2)
1-[5-Бром-3-(метоксиметил)пиридин-2-ил]азетидин-3-он (ссылочное соединение 50-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 50-1, за исключением того, что 1-(5-бром-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-2-ил)азетидин-3-ол (ссылочное соединение 49) заменяли на 1-[5-бром-3-(метоксиметил)пиридин-2-ил]азетидин-3-ол, синтезированный таким же образом, как в ссылочном примере 43-4. В результате указанное в заголовке соединение (выход 80%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 271, 273[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,23 (d, J=2,4 Гц, 1H), 7,76 (d, J=2,4 Гц, 1H), 4,92 (s, 4H), 4,33 (s, 2H), 3,31 (s, 3H).
[0799] (Ссылочный пример 51)
1-(5-Бром-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 51)

Карбонат натрия, 350 мг (3,30 ммоль), и O-метилгидроксиламина гидрохлорид, 251 мг (3,01 ммоль), добавляли к суспензия в этаноле (10 мл), THF (10 мл) и воде (6 мл) 1-(5-бром-3-{2-[(тетрагидропиран-2-ил)окси]пропан-2-ил}пиридин-2-ил)азетидин-3-она, 554 мг (1,50 ммоль), синтезированного таким же образом, как в ссылочном примере 50-1, и смесь перемешивали при 60°C в течение 4 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:этилацетат) с получением указанного в заголовке соединения в количестве 565 мг (включая примеси) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 398, 400[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,20 (d, J=2,2 Гц, 1H), 7,71 (d, J=2,2 Гц, 1H), 4,86-4,70 (m, 4H), 4,51-4,45 (m, 1H), 3,80 (s, 3H), 3,78-3,69 (m, 1H), 3,42-3,22 (m, 1H), 1,85-1,26 (m, 12H).
[0800] (Ссылочный пример 52)
(2-Фторпиридин-3-ил)метанол (ссылочное соединение 52)

Борогидрид натрия, 1,0 г (26 ммоль), добавляли к раствору в этаноле (14 мл) 2-фторникотинальдегида, 1,6 мл (16 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения в количестве 1,3 г (10 ммоль, выход 63%) в виде бесцветного масла.
[0801] (Ссылочный пример 53)
2-Фтор-3-(метоксиметил)пиридин (ссылочное соединение 53)

При 0°C 55% гидрид натрия, 0,70 г (16 ммоль), добавляли по частям к раствору в THF (20 мл) (2-фторпиридин-3-ил)метанола, 1,3 г (10 ммоль), синтезированного таким же образом, как в ссылочном примере 52, и йодметана, 6,6 мл (110 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 0,89 г (6,3 ммоль, выход 63%) в виде бесцветного масла.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,23-8,14 (m, 1H), 8,02-7,92 (m, 1H), 7,40-7,35 (m, 1H), 4,46 (s, 2H), 3,33 (s, 3H).
[0802] (Ссылочный пример 54)
1-[3-(Метоксиметил)пиридин-2-ил]азетидин-3-ол (ссылочное соединение 54)

Гидрохлорид азетидин-3-ола, 1,4 г (13 ммоль), и карбонат цезия, 6,1 г (19 ммоль), добавляли к раствору в DMSO (10 мл) 2-фтор-3-(метоксиметил)пиридина, 0,89 г (6,3 ммоль), синтезированного таким же образом, как в ссылочном примере 53, и смесь перемешивали при 100°C в течение 10 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 0,89 г (4,6 ммоль, выход 73%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 195[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,03 (dd, J=1,8, 4,9 Гц, 1H), 7,44 (dd, J=1,8, 7,3 Гц, 1H), 6,66 (dd, J=4,9, 7,3 Гц, 1H), 5,54 (br s, 1H), 4,59-4,44 (m, 1H), 4,26 (s, 2H), 4,24-4,14 (m, 2H), 3,84-3,78 (m, 2H), 3,27 (s, 3H).
[0803] (Ссылочный пример 55)
2-Фтор-3-метоксипиридин (ссылочное соединение 55)

Йодметан, 1,7 мл (27 ммоль), и карбонат цезия, 4,3 г (13 ммоль), добавляли к раствору в DMSO (20 мл) 2-фторпиридин-3-ола, 1,0 г (8,8 ммоль), и смесь перемешивали при 60°C в течение 1 часа. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения в количестве 1,1 г (8,7 ммоль, выход 99%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,76-7,69 (m, 1H), 7,65 (ddd, J=1,5, 8,0, 10,7 Гц, 1H), 7,31 (ddd, J=0,9, 4,8, 8,0 Гц, 1H), 3,88 (s, 3H).
[0804] (Ссылочный пример 56)
1-(5-Бром-3-метоксипиридин-2-ил)азетидин-3-он (ссылочное соединение 56)

Пиридин, 0,055 мл (0,68 ммоль), и перйодинан Десса-Мартина, 110 мг (0,26 ммоль), добавляли к раствору в метиленхлориде (2 мл) 1-(5-бром-3-метоксипиридин-2-ил)азетидин-3-ола, 50 мг (0,19 ммоль), синтезированного таким же образом, как в ссылочном примере 43-5, и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции реакционную смесь разбавляли этилацетатом, последовательно промывали насыщенным водным раствором тиосульфата натрия и рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 20 мг (0,078 моль, выход 40%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 257, 259[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,84 (d, J=1,9 Гц, 1H), 7,41 (d, J=1,9 Гц, 1H), 4,82 (s, 4H), 3,81 (s, 3H).
[0805] (Ссылочный пример 57)
1-(5-Бром-3-метоксипиридин-2-ил)азетидин-3-она O-метилоксим (ссылочное соединение 57)

O-метилгидроксиламина гидрохлорид, 60 мг (0,72 ммоль), и карбонат калия, 130 мг (0,94 ммоль), добавляли к раствору в THF (4 мл) 1-(5-бром-3-метоксипиридин-2-ил)азетидин-3-она, 61 мг (0,24 ммоль), синтезированного таким же образом, как в ссылочном примере 56, и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 45 мг (0,16 ммоль, выход 67%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 286, 288[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,80 (d, J=2,0 Гц, 1H), 7,37 (d, J=2,0 Гц, 1H), 4,73-4,67 (m, 4H), 3,79 (s, 3H), 3,79 (s, 3H).
[0806] (Ссылочный пример 58)
8-(5-Бромпиримидин-2-ил)-1,4-диокса-8-азаспиро[4.5]декан (ссылочное соединение 58)

1,4-Диокса-8-азаспиро[4.5]декан, 0,74 мл (5,8 ммоль), и DIPEA, 1,8 мл (10 ммоль), добавляли к раствору в DMF (10 мл) 5-бром-2-хлорпиримидина, 1,0 г (5,2 ммоль), и смесь перемешивали при 100°C в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 1,5 г (5,0 ммоль, выход 96%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 300, 302[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,42 (s, 2H), 3,92 (s, 4H), 3,84-3,75 (m, 4H), 1,66-1,59 (m, 4H).
[0807] (Ссылочный пример 59)
1-(5-Бромпиримидин-2-ил)пиперидин-4-он (ссылочное соединение 59)

6 н соляную кислоту, 4,0 мл (24 ммоль), добавляли к раствору в ацетоне (20 мл) 8-(5-бромпиримидин-2-ил)-1,4-диокса-8-азаспиро[4.5]декана, 1,5 г (5,0 ммоль), синтезированного таким же образом, как в ссылочном примере 58, и смесь перемешивали при комнатной температуре в течение 20 часов и при 50°C в течение 6 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 1,0 г (3,9 ммоль, выход 78%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 256, 258[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,35 (s, 2H), 4,22-3,97 (m, 4H), 2,57-2,41 (m, 4H).
[0808] (Ссылочный пример 60)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-метилоксим (ссылочное соединение 60)

Карбонат натрия, 242 мг (2,28 ммоль), и O-метилгидроксиламина гидрохлорид, 188 мг (2,25 ммоль), добавляли к суспензии в этаноле (8 мл), THF (6 мл) и воде (1 мл) 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она, 440 мг (1,06 ммоль), синтезированного таким же образом, как в ссылочном примере 6-41, и смесь перемешивали при 50°C в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой и рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 392 мг (0,882 ммоль, выход 83%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 445[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,52-7,41 (m, 2H), 7,35-7,25 (m, 1H), 4,81 (s, 2H), 3,95-3,89 (m, 4H), 3,76 (s, 3H), 2,58-2,53 (m, 2H), 2,42-2,32 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0809] (Ссылочный пример 61)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-тетрагидропиран-2-илоксим (ссылочное соединение 61)

Карбонат натрия, 115 мг (1,09 ммоль), и O-(тетрагидропиран-2-ил)гидроксиламин, 90,4 мг (0,772 ммоль), добавляли к раствору в THF (3 мл), этаноле (4 мл) и воде (0,5 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она, 150 мг (0,498 ммоль), синтезированного таким же образом, как в ссылочном примере 7-50, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли O-(тетрагидропиран-2-ил)гидроксиламин, 53,1 мг (0,453 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат=от 53:47 до 37:73 (об/об)) с получением указанного в заголовке соединения в количестве 215 мг (включая примеси) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 401[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,5 Гц, 2H), 7,46-7,40 (m, 1H), 7,35-7,29 (m, 1H), 7,25-7,20 (m, 1H), 5,26-5,22 (m, 1H), 4,83(d, J=5,8 Гц, 2H), 4,06-3,97 (m, 4H), 3,97-3,88 (m, 1H), 3,67-3,56 (m, 1H), 2,79-2,74 (m, 2H), 2,59-2,48 (m, 2H), 1,92-1,50 (m, 7H).
[0810] (Ссылочный пример 62-1)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-этилоксим (ссылочное соединение 62-1)

Карбонат натрия, 220 мг (2,08 ммоль), и O-этилгидроксиламина гидрохлорид, 192 мг (1,97 ммоль), добавляли к раствору в этаноле (8 мл), THF (6 мл) и воде (1 мл) 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она, 410 мг (0,987 ммоль), синтезированного таким же образом, как в ссылочном примере 6-41, и смесь перемешивали при 50°C в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой и рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:этилацетат) с получением указанного в заголовке соединения в количестве 272 мг (0,790 ммоль, выход 80%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 345[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,50-7,40 (m, 2H), 7,32-7,23 (m, 1H), 5,33 (t, J=5,2 Гц, 1H), 4,60 (d, J=5,2 Гц, 2H), 4,02 (q, J=7,0 Гц, 2H), 3,95-3,88 (m, 4H), 2,60-2,54 (m, 2H), 2,41-2,35 (m, 2H), 1,19 (t, J=7,0 Гц, 3H).
[0811] (Ссылочный пример 62-2)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-изопропилоксим (ссылочное соединение 62-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 62-1, за исключением того, что O-этилгидроксиламина гидрохлорид заменяли на 2-(аминоокси)пропана гидрохлорид. В результате указанное в заголовке соединение (выход 92%) было получено в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,53 (d, J=1,5 Гц, 2H), 7,47-7,38 (m, 1H), 7,35-7,29 (m, 1H), 7,26-7,20 (m, 1H), 4,83 (d, J=6,1 Гц, 2H), 4,31 (sep, J=6,3 Гц, 1H), 4,03-3,97 (m, 4H), 2,72-2,66 (m, 2H), 2,50-2,45 (m, 2H), 1,85-1,81 (m, 1H), 1,25 (d, J=6,3 Гц, 6H).
[0812] (Ссылочный пример 62-3)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-пропилоксим (ссылочное соединение 62-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 62-1, за исключением того, что O-этилгидроксиламина гидрохлорид заменяли на O-пропилгидроксиламина гидрохлорид, и температура реакции была равна температуре окружающей среды. В результате указанное в заголовке соединение (выход 87%) было получено в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,49-7,42 (m, 2H), 7,30-7,25 (m, 1H), 5,33 (t, J=5,5 Гц, 1H), 4,60 (d, J=5,5 Гц, 2H), 3,96-3,88 (m, 6H), 2,61-2,55 (m, 2H), 2,43-2,33 (m, 2H), 1,60 (sext, J=7,3 Гц, 2H), 0,89 (t, J=7,3 Гц, 3H).
[0813] (Ссылочный пример 63)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-аллилоксим (ссылочное соединение 63)

O-аллилгидроксиламина гидрохлорид, 67,2 мг (0,613 ммоль), и карбонат натрия, 62,4 мг (0,589 ммоль), добавляли к раствору в THF (1,7 мл), этаноле (2,2 мл) и воде (0,3 мл) 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она, 124 мг (0,298 ммоль), синтезированного таким же образом, как в ссылочном примере 6-41, и смесь перемешивали при комнатной температуре в течение 13,5 часа. Реакционную смесь фильтровали и промывали этилацетатом. После этого фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли этанол, 2 мл, и уксусную кислоту, 0,4 мл, и смесь перемешивали при комнатной температуре в течение 1,5 часа. Затем добавляли уксусную кислоту, 1 мл, и смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении. К концентрированному остатку добавляли этанол, 3 мл, и раствор 2 М хлорида водорода в этаноле, 0,15 мл (0,30 ммоль), и смесь перемешивали при комнатной температуре в течение 4,5 часа. После окончания реакции к реакционной смеси добавляли карбонат натрия, 33,6 мг (0,317 ммоль), и воду (0,2 мл), и смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь фильтровали и промывали этилацетатом, и фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 95,7 мг (0,269 ммоль, выход 90%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,49-7,42 (m, 2H), 7,30-7,25 (m, 1H), 6,02-5,92 (m, 1H), 5,33 (t, J=5,6 Гц, 1H), 5,31-5,25 (m, 1H), 5,20-5,16 (m, 1H), 4,60 (d, J=5,6 Гц, 2H), 4,53-4,48 (m, 2H), 3,96-3,89 (m, 4H), 2,63-2,57 (m, 2H), 2,41-2,34 (m, 2H).
[0814] (Ссылочный пример 64)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она оксим (ссылочное соединение 64)

TEA, 0,28 мл (2,0 ммоль), добавляли к суспензии в THF (4 мл) гидроксиламина гидрохлорида, 92 мг (1,2 ммоль), и смесь перемешивали при комнатной температуре в течение 5 минут. Затем туда добавляли раствор в THF (4 мл) 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она, 0,28 г (0,67 ммоль), синтезированного таким же образом, как в ссылочном примере 6-41, и смесь перемешивали при комнатной температуре в течение 1 часа и при 50°C в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 0,26 г (0,60 ммоль, выход 90%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 431[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO) δ: 10,47 (s, 1H), 8,59 (d, J=1,5 Гц, 2H), 7,54-7,40 (m, 2H), 7,35-7,27 (m, 1H), 4,81 (s, 2H), 3,95-3,86 (m, 4H), 2,60-2,53 (m, 2H), 2,39-2,33 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0815] (Ссылочный пример 65)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-{2-[(тетрагидропиран-2-ил)окси]этил}оксим (ссылочное соединение 65)

Карбонат цезия, 168 мг (0,516 ммоль), и 2-(2-бромэтокси)тетрагидропиран, 55 мкл (0,36 ммоль), добавляли к раствору в DMF (2 мл) 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она оксима, 101 мг (0,235 ммоль), синтезированного таким же образом, как в ссылочном примере 64, и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли 2 мл DMF, и смесь перемешивали при комнатной температуре в течение 2,5 часа. Затем добавляли 1 мл метанола, и смесь перемешивали при комнатной температуре в течение 1,5 часа и при 85°C в течение 3 часов. После окончания реакции реакционную смесь очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) и затем очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: этилацетат:метанол=от 72:28 до 38:62 (об/об)) с получением указанного в заголовке соединения в количестве 39,4 мг (0,089 ммоль, выход 38%) в виде бесцветного масла.
Масс-спектр (ESI, m/z): 445[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,4 Гц, 2H), 7,51-7,33 (m, 2H), 7,32-7,14 (m, 1H), 5,33 (t, J=5,6 Гц, 1H), 4,62-4,56 (m, 3H), 4,16-4,08(m, 2H), 3,95-3,85 (m, 4H), 3,84-3,69 (m, 2H), 3,64-3,55 (m, 1H), 3,46-3,37 (m, 1H), 2,63-2,56 (m, 2H), 2,41-2,36 (m, 2H), 1,78-1,36 (m, 6H).
[0816] (Ссылочный пример 66)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она оксим (ссылочное соединение 66)

Карбонат натрия, 3,4 г (3,2 ммоль), и гидроксиламина гидрохлорид, 1,7 г (25 ммоль), добавляли к суспензии в THF (30 мл), этаноле (30 мл) и воде (10 мл) 1-(5-бромпиримидин-2-ил)пиперидин-4-она, 4,0 г (16 ммоль), синтезированного таким же образом, как в ссылочном примере 59, и смесь перемешивали при 50°C в течение 1 часа. После окончания реакции осажденное твердое вещество собирали из реакционной смеси с помощью фильтрации. К фильтрату добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Твердое вещество, собранное ранее, добавляли к фильтрату, и смесь концентрировали при пониженном давлении с получением указанного в заголовке соединения в количестве 2,5 г (9,8 ммоль, выход 61%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 271, 273[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 10,40 (br s, 1H), 8,48 (s, 2H), 3,84-3,78 (m, 4H), 2,55-2,50 (m, 2H), 2,36-2,29 (m, 2H).
[0817] (Ссылочный пример 67-1)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-{3-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 67-1)

Карбонат цезия, 288 мг (0,884 ммоль), и 2-(3-бромпропокси)тетрагидропиран, 0,120 мл (0,708 ммоль), добавляли к раствору в DMF (4 мл) 1-(5-бромпиримидин-2-ил)пиперидин-4-она оксима, 120 мг (0,443 ммоль), синтезированного таким же образом, как в ссылочном примере 66, и смесь перемешивали при 80°C в течение 9 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 143 мг (0,346 ммоль, выход 78%) в виде бесцветного масла.
Масс-спектр (CI, m/z): 413, 415[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 4,59-4,49 (m, 1H), 4,08-3,98 (m, 2H), 3,88-3,60 (m, 6H), 3,48-3,36 (m, 2H), 2,58-2,50 (m, 2H), 2,38-2,30 (m, 2H), 1,93-1,77 (m, 2H), 1,75-1,32 (m, 6H).
[0818] (Ссылочный пример 67-2)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-{4-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 67-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бромпропокси)тетрагидропиран заменяли на 2-(4-бромбутокси)тетрагидропиран. В результате указанное в заголовке соединение (выход 95%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 427, 429[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 4,65-4,41 (m, 1H), 4,02-3,92 (m, 2H), 3,88-3,79 (m, 4H), 3,76-3,57 (m, 2H), 3,49-3,34 (m, 2H), 2,56-2,50 (m, 2H), 2,39-2,31 (m, 2H), 1,85-1,31 (m, 10H).
[0819] (Ссылочный пример 67-3)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-(2-метоксиэтил)оксим (ссылочное соединение 67-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бромпропокси)тетрагидропиран заменяли на 2-бромэтилметиловый эфир, и температуру реакции изменяли на 85°C. В результате указанное в заголовке соединение (выход 77%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 329, 331[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 4,10-4,04 (m, 2H), 3,85-3,79 (m, 4H), 3,56-3,50 (m, 2H), 3,25 (s, 3H), 2,56-2,52 (m, 2H), 2,38-2,32 (m, 2H).
[0820] (Ссылочный пример 67-4)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-{2,2-диметил-3-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 67-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бром-пропокси)тетрагидропиран заменяли на 2-(3-бром-2,2-диметилпропокси)тетрагидропиран, синтезированный таким же образом, как в ссылочном примере 68-1. В результате указанное в заголовке соединение (выход 49%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 441, 443[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,30 (s, 2H), 4,59-4,55 (m, 1H), 3,94-3,80 (m, 7H), 3,55 (d, J=9,3 Гц, 1H), 3,51-3,45 (m, 1H), 3,11 (d, J=9,3 Гц, 1H), 2,68-2,63 (m, 2H), 2,45-2,39 (m, 2H), 1,89-1,46 (m, 6H), 0,97 (s, 3H), 0,96 (s, 3H).
[0821] (Ссылочный пример 67-5)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-(3-гидрокси-3-метилбутил)оксим (ссылочное соединение 67-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бромпропокси)тетрагидропиран заменяли на 3-гидрокси-3-метилбутилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-7. В результате указанное в заголовке соединение (выход 88%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 357, 359[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,31 (s, 2H), 4,26 (t, J=6,3 Гц, 2H), 3,94-3,86 (m, 4H), 2,64-2,58 (m, 2H), 2,46-2,40 (m, 2H), 2,24 (s, 1H), 1,89 (t, J=6,3 Гц, 2H), 1,28 (s, 6H).
[0822] (Ссылочный пример 67-6)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-{2-метил-3-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 67-6)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бром-пропокси)тетрагидропиран заменяли на 2-(3-бром-2-метилпропокси)тетрагидропиран, синтезированный таким же образом, как в ссылочном примере 68-2, и температуру реакции изменяли на 90°C. В результате указанное в заголовке соединение (с количественным выходом) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 427, 429[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,31 (s, 2H), 4,62-4,54 (m, 1H), 4,23-3,23 (m, 10H), 2,68-2,61 (m, 2H), 2,45-2,39 (m, 2H), 2,21-2,09 (m, 1H), 1,90-1,44 (m, 6H), 1,04-0,93 (m, 3H).
[0823] (Ссылочный пример 67-7)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-[(2,2-диметил-1,3-диоксан-5-ил)метил]оксим (ссылочное соединение 67-7)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бромпропокси)тетрагидропиран заменяли на (2,2-диметил-1,3-диоксан-5-ил)метилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-4. В результате указанное в заголовке соединение (выход 87%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 399, 401[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,31 (s, 2H), 4,11 (d, J=6,9 Гц, 2H), 3,99 (dd, J=4,3, 12,0 Гц, 2H), 3,92-3,86 (m, 4H), 3,75 (dd, J=6,5, 12,0 Гц, 2H), 2,66-2,59 (m, 2H), 2,44-2,38 (m, 2H), 2,18-2,09 (m, 1H), 1,44 (s, 3H), 1,42 (s, 3H).
[0824] (Ссылочный пример 67-8)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-[(2,2,5-триметил-1,3-диоксан-5-ил)метил]оксим (ссылочное соединение 67-8)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бром-пропокси)тетрагидропиран заменяли на (2,2,5-триметил-1,3-диоксан-5-ил)метилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-8. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
[0825] (Ссылочный пример 67-9)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-[(2,2-диметил-1,3-диоксолан-4-ил)метил]оксим (ссылочное соединение 67-9)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бромпропокси)тетрагидропиран заменяли на (2,2-диметил-1,3-диоксолан-4-ил)метилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-5. В результате указанное в заголовке соединение (выход 71%) было получено в виде бесцветного масла.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 4,20-4,33 (m, 1H), 3,93-4,06 (m, 3H), 3,77-3,89 (m, 4H), 3,59-3,71 (m, 1H), 2,52-2,59 (m, 2H), 2,31-2,39 (m, 2H), 1,32 (s, 3H), 1,27 (s, 3H).
[0826] (Ссылочный пример 67-10)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-{2-[(тетрагидропиран-2-ил)окси]этил}оксим (ссылочное соединение 67-10)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бромпропокси)тетрагидропиран заменяли на 2-(2-бромэтокси)тетрагидропиран. В результате указанное в заголовке соединение (выход 79%) было получено в виде светло-желтого масла.
Масс-спектр (CI, m/z): 399, 401[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 4,61-4,54 (m, 1H), 4,15-4,06 (m, 2H), 3,88-3,68 (m, 6H), 3,63-3,53 (m, 1H), 3,45-3,37 (m, 1H), 2,59-2,52 (m, 2H), 2,39-2,32 (m, 2H), 1,79-1,31 (m, 6H).
[0827] (Ссылочный пример 67-11)
Этил-4-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)бутаноат (ссылочное соединение 67-11)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бромпропокси)тетрагидропиран заменяли на этил-4-бромбутират. В результате указанное в заголовке соединение (выход 80%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 385, 387[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 4,04 (q, J=7,2 Гц, 2H), 3,97 (t, J=6,4 Гц, 2H), 3,85-3,78 (m, 4H), 2,55-2,51 (m, 2H), 2,38-2,32 (m, 4H), 1,89-1,79 (m, 2H), 1,17 (t, J=7,2 Гц, 3H).
[0828] (Ссылочный пример 67-12)
4-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)бутаннитрил (ссылочное соединение 67-12)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бромпропокси)тетрагидропиран заменяли на 4-бромбутиронитрил. В результате указанное в заголовке соединение (выход 85%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 338, 340[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,49 (s, 2H), 4,03 (t, J=6,1 Гц, 2H), 3,87-3,79 (m, 4H), 2,61-2,52 (m, 4H), 2,39-2,32 (m, 2H), 1,94-1,83 (m, 2H).
[0829] (Ссылочный пример 67-13)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-[3-(метилсульфонил)пропил]оксим (ссылочное соединение 67-13)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бромпропокси)тетрагидропиран заменяли на 3-(метилсульфонил)пропилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-11, и температуру реакции изменяли на 100°C. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 391, 393[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,31 (s, 2H), 4,16 (t, J=6,0 Гц, 2H), 3,97-3,84 (m, 4H), 3,17-3,10 (m, 2H), 2,93 (s, 3H), 2,66-2,57 (m, 2H), 2,44-2,38 (m, 2H), 2,29-2,17 (m, 2H).
[0830] (Ссылочный пример 67-14)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-[(1-метил-1H-пиразол-3-ил)метил]оксим (ссылочное соединение 67-14)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бромпропокси)тетрагидропиран заменяли на (1-метил-1H-пиразол-3-ил)метилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-12, и температуру реакции изменяли на 50°C. В результате указанное в заголовке соединение (выход 57%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 365, 367[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,30 (s, 2H), 7,31 (d, J=2,2 Гц, 1H), 6,29 (d, J=2,2 Гц, 1H), 5,08 (s, 2H), 3,92-3,84 (m, 7H), 2,69-2,63 (m, 2H), 2,46-2,41 (m, 2H).
[0831] (Ссылочный пример 67-15)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-3-ил]метил}оксим (ссылочное соединение 67-15)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бромпропокси)тетрагидропиран заменяли на 3-(хлорметил)-1-(тетрагидропиран-2-ил)-1H-пиразол, синтезированный таким же образом, как в ссылочном примере 14-13. В результате указанное в заголовке соединение (выход 62%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 435, 437[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,30 (s, 2H), 7,56 (d, J=2,5 Гц, 1H), 6,35 (d, J=2,5 Гц, 1H), 5,36 (dd, J=2,8, 9,7 Гц, 1H), 5,11 (s, 2H), 4,13-4,04 (m, 1H), 3,92-3,83 (m, 4H), 3,77-3,63 (m, 1H), 2,68-2,62 (m, 2H), 2,46-2,40 (m, 2H), 2,17-2,00 (m, 3H), 1,75-1,47 (m, 3H).
[0832] (Ссылочный пример 67-16)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метил}оксим (ссылочное соединение 67-16)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 67-1, за исключением того, что 2-(3-бромпропокси)тетрагидропиран заменяли на [1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метилметансульфонат, синтезированный таким же образом, как в ссылочном примере 14-14, и температура реакции была равна температуре окружающей среды. В результате указанное в заголовке соединение (выход 24%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 435, 437[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 7,89 (s, 1H), 7,49 (s, 1H), 5,36 (dd, J=2,3, 10,1 Гц, 1H), 4,88 (s, 2H), 3,95-3,87 (m, 1H), 3,85-3,76 (m,4H), 3,66-3,56 (m, 1H), 2,54-2,48 (m, 2H), 2,42-2,32 (m, 2H), 2,14-1,81 (m, 3H), 1,74-1,42 (m, 3H).
[0833] (Ссылочный пример 68-1)
2-(3-Бром-2,2-диметилпропокси)тетрагидропиран (ссылочное соединение 68-1)

PPTS, 0,3 г (1 ммоль), и DHP, 0,90 мл (10 ммоль), добавляли к раствору в метиленхлориде (20 мл) 3-бром-2,2-диметил-1-пропанола, 1,0 г (6,0 ммоль), и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 1,5 г (6,0 ммоль, выход 100%) в виде бесцветного масла.
Масс-спектр (CI, m/z): 251, 253[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 4,62-4,58 (m, 1H), 3,90-3,83 (m, 1H), 3,58 (d, J=9,4 Гц, 1H), 3,55-3,49 (m, 1H), 3,46-3,36 (m, 2H), 3,16 (d, J=9,4 Гц, 1H), 1,88-1,45 (m, 6H), 1,06 (s, 3H), 1,03 (s, 3H).
[0834] (Ссылочный пример 68-2)
2-(3-Бром-2-метилпропокси)тетрагидропиран (ссылочное соединение 68-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 68-1, за исключением того, что 3-бром-2,2-диметил-1-пропанол заменяли на 3-бром-2-метилпропан-1-ол. В результате указанное в заголовке соединение (выход 97%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 237, 239[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 4,63-4,56 (m, 1H), 3,90-3,82 (m, 1H), 3,73-3,63 (m, 1H), 3,57-3,42 (m, 3H), 3,37-3,26 (m, 1H), 2,18-2,06 (m, 1H), 1,88-1,47 (m, 6H), 1,08-1,01 (m, 3H).
[0835] (Ссылочный пример 69-1)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-{3-метил-3-[(тетрагидропиран-2-ил)окси]бутил}оксим (ссылочное соединение 69-1)

DHP, 89 мкл (0,98 ммоль), и PPTS, 25 мг (0,099 ммоль), добавляли к суспензии в метиленхлориде (5 мл) 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-(3-гидрокси-3-метилбутил)оксима, 175 мг (0,490 ммоль), синтезированного таким же образом, как в ссылочном примере 67-5, и смесь перемешивали при комнатной температуре в течение 14 часов. Затем добавляли DHP, 89 мкл (0,98 ммоль), и PPTS, 25 мг (0,099 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 227 мг (включая примеси) в виде бесцветного масла.
Масс-спектр (CI, m/z): 441, 443[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,30 (s, 2H), 4,80-4,75 (m, 1H), 4,23-4,11 (m, 2H), 3,99-3,83 (m, 5H), 3,50-3,37 (m, 1H), 2,66-2,59 (m, 2H), 2,46-2,40 (m, 2H), 1,97-1,78 (m, 3H), 1,75-1,47 (m, 5H), 1,27 (s, 3H), 1,25 (s, 3H).
[0836] (Ссылочный пример 69-2)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-{2-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 69-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 69-1, за исключением того, что 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-(3-гидрокси-3-метилбутил)оксим (ссылочное соединение 67-5) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-(2-гидроксипропил)оксим, синтезированный таким же образом, как в ссылочном примере 70. В результате указанное в заголовке соединение (включая примеси) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 357, 359[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,31 (s, 2H), 4,26 (t, J=6,3 Гц, 2H), 3,94-3,86 (m, 4H), 2,64-2,58 (m, 2H), 2,46-2,40 (m, 2H), 2,24 (s, 1H), 1,89 (t, J=6,3 Гц, 2H), 1,28 (s, 6H).
[0837] (Ссылочный пример 70)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-(2-гидроксипропил)оксим (ссылочное соединение 70)

55% Гидрид натрия, 98,0 мг (2,25 ммоль), добавляли к суспензии в DMF (3 мл) 1-(5-бромпиримидин-2-ил)пиперидин-4-она оксима, 302 мг (1,11 ммоль), синтезированного таким же образом, как в ссылочном примере 66, и смесь перемешивали при комнатной температуре в течение 45 минут. Затем добавляли 1-бромпропан-2-ол, 100 мкл (1,13 ммоль). Смесь перемешивали при комнатной температуре в течение 14 часов, при 50°C в течение 10 часов, при 80°C в течение 1 часа и при 100°C в течение 9 часов. После окончания реакции к реакционной смеси добавляли воду и 1 н соляную кислоту, для того чтобы довести pH до 7. Реакционную смесь фильтровали и промывали водой. К фильтрату добавляли рассол с последующей экстракцией этилацетатом. Органический слой сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 48,8 мг (0,148 ммоль, выход 13%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 4,62 (d, J=4,3 Гц, 1H), 3,88-3,72 (m, 7H), 2,60-2,53 (m, 2H), 2,38-2,31 (m, 2H), 1,04 (d, J=6,1 Гц, 3H).
[0838] (Ссылочный пример 71)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-{2-[(тетрагидропиран-2-ил)окси]пропил}оксим (ссылочное соединение 71)

1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-{2-[(тетрагидропиран-2-ил)окси]пропил}оксим, 59,1 мг (0,143 ммоль), синтезированный таким же образом, как в ссылочном примере 69-2, трет-бутил{[2-фтор-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил]окси}диметилсилан, 99,4 мг (0,271 ммоль), синтезированный таким же образом, как в ссылочном примере 5, и фосфат трикалия, 80,3 мг (0,378 ммоль), суспендировали в воде (0,2 мл) и 1,4-диоксане (1 мл). Через суспензию пропускали газообразный азот в течение 15 минут. Затем добавляли тетракис(трифенилфосфин)палладий(0), 10,3 мг (0,00891 ммоль). Смесь подавали в микроволновое реакционное устройство и перемешивали при 120°C в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 83,7 мг (включая примеси) в виде светло-желтого масла.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,55-8,51 (m, 2H), 7,51-7,45 (m, 1H), 7,28-7,21 (m, 2H), 4,85 (s, 2H), 4,82-4,73 (m, 1H), 4,23-4,07 (m, 2H), 4,04-3,90 (m, 6H), 3,54-3,44 (m, 1H), 2,75-2,65 (m, 2H), 2,49-2,44 (m, 2H), 1,91-1,44 (m, 6H), 1,26-1,14 (m, 3H), 0,96 (s, 9H), 0,14 (s, 6H).
[0839] (Ссылочный пример 72)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-(2-гидроксиэтил)оксим (ссылочное соединение 72)

Раствор 2 М хлорида водорода в этаноле, 2,0 мл (4,0 ммоль), добавляли к раствору в диоксане (6 мл) и этаноле (6 мл) 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-{2-[(тетрагидропиран-2-ил)окси]этил}оксима, 0,45 г (1,1 ммоль), синтезированного таким же образом, как в ссылочном примере 67-10, и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли TEA при 0°C. Затем добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 0,30 г (0,95 ммоль, выход 84%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 315, 317[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,50 (s, 2H), 4,62 (t, J=5,6 Гц, 1H), 4,01-3,95 (m, 2H), 3,87-3,76 (m, 4H), 3,62-3,55 (m, 2H), 2,59-2,53 (m, 2H), 2,38-2,31 (m, 2H).
[0840] (Ссылочный пример 73)
5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)-2-хлорпиримидин (ссылочное соединение 73)

трет-Бутил{[2-фтор-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензил]окси}диметилсилан, 1,81 г (4,94 ммоль), синтезированный таким же образом, как в ссылочном примере 5, и 5-бром-2-хлорпиримидин, 1,17 г (6,05 ммоль), суспендировали в 1,4-диоксане (20 мл) и воде (5,0 мл). К суспензии добавляли фосфат трикалия n-гидрат, 4,02 г (15,1 ммоль), и через суспензию пропускали газообразный аргон в течение 5 минут. Затем добавляли тетракис(трифенилфосфин)палладий(0), 284 мг (0,246 ммоль), и смесь перемешивали при 100°C в течение 1,5 часа под струей аргона. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 1,22 г (3,46 ммоль, выход 70%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 417[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,81 (d, J=1,4 Гц, 2H), 7,66-7,60 (m, 1H), 7,34-7,28 (m, 2H), 4,86 (s, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0841] (Ссылочный пример 74-1)
7-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]-1,4-диокса-7-азаспиро[4.4]нонан (ссылочное соединение 74-1)

TEA, 0,50 мл (3,6 ммоль), и 1,4-диокса-7-азаспиро[4.4]нонан, 156 мг (1,21 ммоль), добавляли к суспензии в этаноле (5 мл) 5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-2-хлорпиримидина, 369 мг (1,05 ммоль), синтезированного таким же образом, как в ссылочном примере 73, и смесь перемешивали при 100°C в течение 1,75 часа. После окончания реакции реакционную смесь концентрировали при пониженном давлении. К ней добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения в количестве 472 мг (включая примеси) в виде светло-желтого масла.
Масс-спектр (CI, m/z): 446[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,52 (d, J=1,4 Гц, 2H), 7,52-7,41 (m, 1H), 7,26-7,18 (m, 2H), 4,85 (s, 2H), 4,07-3,99 (m, 4H), 3,80 (t, J=7,3 Гц, 2H), 3,71 (s, 2H), 2,24 (t, J=7,3 Гц, 2H), 0,96 (s, 9H), 0,13 (s, 6H).
[0842] (Ссылочный пример 74-2)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-пиримидин-2-илоксим (ссылочное соединение 74-2)

TEA, 57 мкл (0,41 ммоль), добавляли к суспензии в этаноле (2 мл) пиперидин-4-она O-пиримидин-2-илоксима, 19 мг (0,099 ммоль), синтезированного таким же образом, как в ссылочном примере 123, и 5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)-2-хлорпиримидина, 30 мг (0,085 ммоль). Смесь перемешивали при 80°C в течение 10 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве (включая примеси) в виде темно-коричневого твердого вещества.
Масс-спектр (CI, m/z): 509[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,64 (d, J=4,8 Гц, 2H), 8,55 (d, J=1,4 Гц, 2H), 7,52-7,46 (m, 1H), 7,30-7,20 (m, 2H), 7,08-7,05 (m, 1H), 4,85 (s, 2H), 4,15-4,08 (m, 4H), 3,02-2,98 (m, 2H), 2,76-2,71 (m, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0843] (Ссылочный пример 75)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пирролидин-3-он (ссылочное соединение 75)

2 н серную кислоту, 0,01 мл (0,02 ммоль), добавляли к раствору в THF (10 мл) 7-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]-1,4-диокса-7-азаспиро[4.4]нонана, 460 мг (1,03 ммоль), синтезированного таким же образом, как в ссылочном примере 74-1, и смесь перемешивали при 80°C в течение 11 часов. После окончания реакции осажденное твердое вещество собирали с помощью фильтрации. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток объединяли с собранным ранее твердым веществом. Очистка с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) давала указанное в заголовке соединение в количестве 174 мг (0,606 ммоль, выход 59%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 288[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,3 Гц, 2H), 7,52-7,40 (m, 2H), 7,33-7,24 (m, 1H), 5,33 (t, J=5,6 Гц, 1H), 4,61 (d, J=5,6 Гц, 2H), 3,98-3,92 (m, 4H), 2,77-2,69 (m, 2H).
[0844] (Ссылочный пример 76)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пирролидин-3-она O-метилоксим, EZ-смесь (ссылочное соединение 76)

THF, 5 мл, метиленхлорид, 10 мл, и O-метилгидроксиламина гидрохлорид, 50,2 мг (0,601 ммоль), добавляли к суспензии в метаноле (3 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пирролидин-3-она, 170 мг (0,592 ммоль), синтезированного таким же образом, как в ссылочном примере 75, и смесь перемешивали при комнатной температуре в течение 15 минут. Затем добавляли O-метилгидроксиламина гидрохлорид, 152 мг (1,82 ммоль), и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции реакционный раствор концентрировали при пониженном давлении. Добавляли насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией смешанным растворителем метиленхлорид:метанол=90:10 (об/об). Органический слой сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат:метанол) с получением указанного в заголовке соединения в количестве 51,1 мг (0,162 ммоль, выход 27%) в виде светло-желтого твердого вещества.
Масс-спектр (ESI, m/z): 317[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63-8,57 (m, 2H), 7,51-7,39 (m, 2H), 7,33-7,25 (m, 1H), 5,33 (br s, 1H), 4,60 (s, 2H), 4,27-4,19 (m, 2H), 3,87-3,76 (m, 5H), 2,92-2,76 (m, 2H).
[0845] (Ссылочный пример 77)
2-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)-N-метилацетамид (ссылочное соединение 77)

CDI, 360 мг (2,22 ммоль), добавляли к раствору в DMF (6 мл) 2-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)уксусной кислоты, 264 мг (0,877 ммоль), синтезированной таким же образом, как в ссылочном примере 9-3, и смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли 2,0 М раствор метиламина в THF, 4,30 мл (8,60 ммоль), и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 140 мг (0,446 ммоль, выход 51%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 314,316[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,39 (s, 2H), 6,13 (br s, 1H), 4,89-4,81 (m, 4H), 4,56 (s, 2H), 2,90 (d, J=5,0 Гц, 3H).
[0846] (Ссылочный пример 78-1)
3-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)пропанамид (ссылочное соединение 78-1)

CDI, 221 мг (1,36 ммоль), добавляли к суспензии в DMF (4 мл) 3-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)пропановой кислоты гидрохлорида, 201 мг (0,572 ммоль), синтезированного таким же образом, как в ссылочном примере 9-4, и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли 0,4 М раствор аммиака в THF, 8,00 мл (3,20 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции реакционную смесь концентрировали при пониженном давлении. К концентрированному остатку добавляли толуол, который затем концентрировали при пониженном давлении, и эту операцию повторяли несколько раз. К концентрированному остатку добавляли этилацетат, и смесь перемешивали при комнатной температуре в течение 30 минут. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением неочищенного продукта в количестве 179 мг, содержащего указанное в заголовке соединение в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H) 7,39 (s, 1H), 6,85 (s, 1H), 4,80-4,66 (m, 4H), 4,20 (t, J=6,5 Гц, 2H), 2,41 (t, J=6,5 Гц, 2H).
[0847] (Ссылочный пример 78-2)
3-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)-N-метилпропанамид (ссылочное соединение 78-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 78-1, за исключением того, что 0,4 М раствор аммиака в THF заменяли на 2 М раствор метиламина в THF. В результате указанное в заголовке соединение (выход 69%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 328, 330[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 7,93-7,71 (m, 1H), 4,87-4,55 (m, 4H), 4,20 (t, J=6,5 Гц, 2H), 2,56 (d, J=4,6 Гц, 3H), 2,42 (t, J=6,5 Гц, 2H).
[0848] (Ссылочный пример 79)
4-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)бутановая кислота (ссылочное соединение 79)

Гидроксид лития моногидрат, 130 мг (3,10 ммоль), добавляли к суспензии в метаноле (6 мл) этил-4-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)бутаноата, 268 мг (0,750 ммоль), синтезированного таким же образом, как в ссылочном примере 10-13, и смесь перемешивали при комнатной температуре в течение 15 часов и после этого концентрировали при пониженном давлении. К концентрированному остатку добавляли THF (6 мл) и воду (3 мл), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции THF отгоняли при пониженном давлении. К концентрированному остатку добавляли 1 н соляную кислоту для того чтобы довести pH до 3, и осажденное твердое вещество собирали с помощью фильтрации. Собранное твердое вещество сушили при пониженном давлении. Далее фильтрат экстрагировали этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Осажденное твердое вещество объединяли с твердым веществом, собранным с помощью предыдущей фильтрации. Таким образом, указанное в заголовке соединение в количестве 214 мг (0,650 ммоль, выход 87%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 329, 331[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,38 (s, 2H), 4,82-4,76 (m, 4H), 4,14 (t, J=6,1 Гц, 2H), 2,47 (t, J=7,3 Гц, 2H), 2,02 (quin, J=6,6 Гц, 2H).
[0849] (Ссылочный пример 80)
4-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)-N-метилбутанамид (ссылочное соединение 80)

CDI, 270 мг (1,67 ммоль), добавляли к раствору в DMF (6 мл) 4-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)бутановой кислоты, 214 мг (0,650 ммоль), синтезированной таким же образом, как в ссылочном примере 79, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли 2,0 М раствор метиламина в THF, 3,25 мл (6,50 ммоль), и смесь перемешивали при комнатной температуре в течение 20 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли этилацетат, и смесь обрабатывали ультразвуком. Твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении. Фильтрат концентрировали при пониженном давлении, и концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: этилацетат:метанол). Концентрированную при пониженном давлении фракцию, включающую в себя целевое соединение, объединяли с твердым веществом, собранным с помощью предыдущей фильтрации. В результате указанное в заголовке соединение 170 мг (0,497 ммоль, выход 76%) было получено в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 342, 344[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,37 (s, 2H), 5,46 (br s, 1H), 4,82-4,76 (m, 4H), 4,12 (t, J=6,1 Гц, 2H), 2,82 (d, J=4,8 Гц, 3H), 2,26 (t, J=7,3 Гц, 2H), 2,06-1,98 (m, 2H).
[0850] (Ссылочный пример 81)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2-гидроксиэтил)оксим (ссылочное соединение 81)

Гидроксид лития, 25,5 мг (1,06 ммоль), добавляли к раствору в THF (2 мл) и воде (1 мл) 2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилацетата, 260 мг (0,532 ммоль), синтезированного таким же образом, как в ссылочном примере 10-11, и смесь перемешивали при 70°C в течение 5 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 170 мг (0,381 ммоль, выход 72%) в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 447[М+1]+.
[0851] (Ссылочный пример 82-1)
2-[({1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилметансульфонат (ссылочное соединение 82-1)

TEA, 0,159 мл (1,14 ммоль), и метансульфонилхлорид, 0,0591 мл (0,758 ммоль), добавляли к раствору в метиленхлориде (3 мл) 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2-гидроксиэтил)оксима, 170 мг (0,381 ммоль), синтезированного таким же образом, как в ссылочном примере 81, и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении с получением неочищенного продукта в количестве 199 мг, содержащего указанное в заголовке соединение в виде желтого масла.
Масс-спектр (ESI, m/z): 525[М+1]+.
[0852] (Ссылочный пример 82-2)
2-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)этилметансульфонат (ссылочное соединение 82-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 82-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2-гидроксиэтил)оксим (ссылочное соединение 81) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(2-гидроксиэтил)оксим, синтезированный таким же образом, как в ссылочном примере 27. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,81-4,74 (m, 4H), 4,46-4,36 (m, 2H), 4,32-4,23 (m, 2H), 3,19 (s, 3H).
[0853] (Ссылочный пример 82-3)
2-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этилметансульфонат (ссылочное соединение 82-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 82-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(2-гидроксиэтил)оксим (ссылочное соединение 81) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-(2-гидроксиэтил)оксим, синтезированный таким же образом, как в ссылочном примере 72. В результате указанное в заголовке соединение (выход 96%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 393, 395[М+1]+.
1H-ЯМР (400 МГц, CDCl3) δ: 8,31 (s, 2H), 4,51-4,43 (m, 2H), 4,33-4,25 (m, 2H), 3,95-3,86 (m, 4H), 3,03 (s, 3H), 2,69-2,61 (m, 2H), 2,45-2,37 (m, 2H).
[0854] (Ссылочный пример 83)
1-{5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил}азетидин-3-она O-[2-(диметиламино)этил]оксим (ссылочное соединение 83)
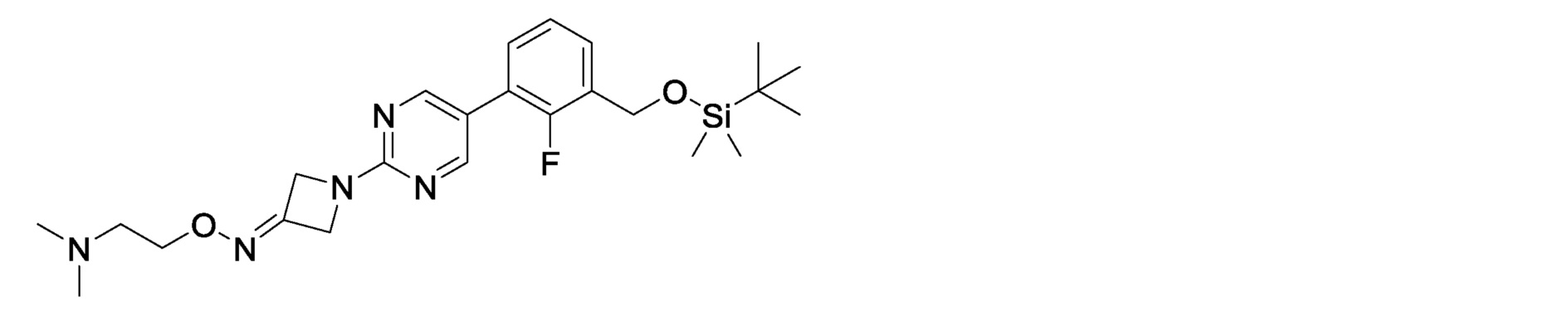
2 М раствор диметиламина в THF, 1,4 мл (2,8 ммоль), добавляли к раствору в DMF (5 мл) 2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилметансульфоната, 100 мг (0,19 ммоль), синтезированного таким же образом, как в ссылочном примере 82-1. Смесь подавали в микроволновое реакционное устройство и перемешивали при 80°C в течение 2 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 67 мг (0,14 ммоль, выход 74%) в виде светло-желтого масла.
Масс-спектр (ESI, m/z): 474[М+1]+.
[0855] (Ссылочный пример 84-1)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-{2-[бензил(метил)амино]этил}оксим (ссылочное соединение 84-1)

N-метил-1-фенилметанамин, 0,0737 мл (0,572 ммоль), добавляли к раствору в DMF (2 мл) 2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]этилметансульфоната, 100 мг (0,191 ммоль), синтезированного таким же образом, как в ссылочном примере 82-1, и смесь перемешивали при 70°C в течение 7 часов и при комнатной температуре в течение 17 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 104 мг (0,189 ммоль, выход 99%) в виде светло-желтого масла.
Масс-спектр (ESI, m/z): 550[М+1]+.
1H-ЯМР (400 МГц, CDCl3) δ: 8,57 (d, J=1,5 Гц, 2H), 7,54-7,48 (m, 1H), 7,36-7,20 (m, 7H), 4,89-4,82 (m, 6H), 4,23 (t, J=5,8 Гц, 2H), 3,57 (s, 2H), 2,72 (t, J=5,8 Гц, 2H), 2,31 (s, 3H), 0,96 (s, 9H), 0,14 (s, 6H).
[0856] (Ссылочный пример 84-2)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(пиперидин-1-ил)этил]оксим (ссылочное соединение 84-2)
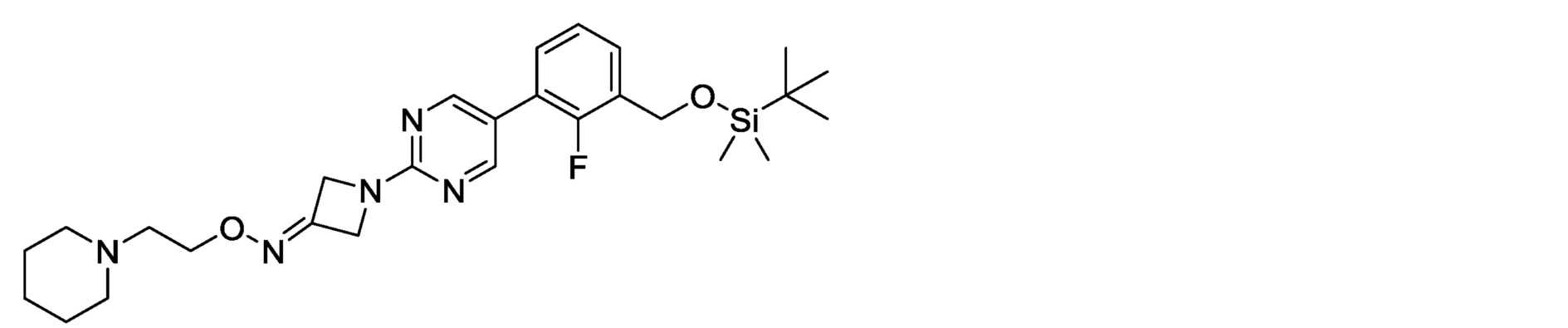
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 84-1, за исключением того, что N-метил-1-фенилметанамин заменяли на пиперидин. В результате указанное в заголовке соединение (с количественным выходом) было получено в виде желтого твердого вещества.
Масс-спектр (ESI, m/z): 514[М+1]+.
[0857] (Ссылочный пример 84-3)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(3,3-дифторазетидин-1-ил)этил]оксим (ссылочное соединение 84-3)
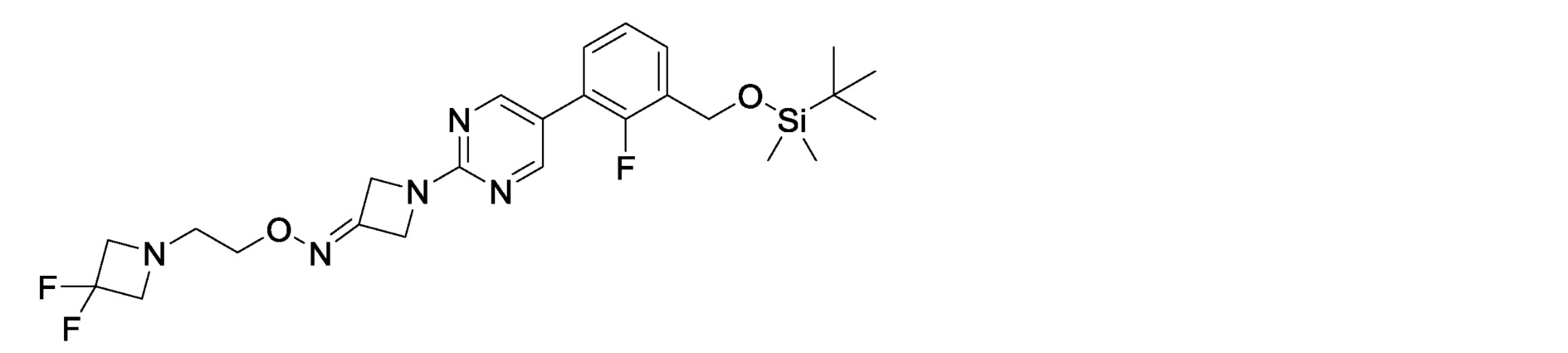
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 84-1, за исключением того, что N-метил-1-фенилметанамин заменяли на 3,3-дифторазетидина гидрохлорид, и добавляли TEA. В результате указанное в заголовке соединение (выход 52%) было получено в виде бесцветного масла.
Масс-спектр (ESI, m/z): 522[М+1]+.
1H-ЯМР (400 МГц, CDCl3) δ: 8,57 (d, J=1,4 Гц, 2H), 7,55-7,47 (m, 1H), 7,30-7,20 (m, 2H), 4,91-4,82 (m, 6H), 4,21-4,14 (m, 2H), 3,66 (t, J=12,0 Гц, 4H), 2,92-2,84 (m, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0858] (Ссылочный пример 84-4)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(3-фторазетидин-1-ил)этил]оксим (ссылочное соединение 84-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 84-1, за исключением того, что N-метил-1-фенилметанамин заменяли на 3-фторазетидина гидрохлорид, что добавляли TEA, и что температуру реакции изменяли на 60°C. В результате указанное в заголовке соединение (включая примеси) было получено в виде желтого масла.
Масс-спектр (ESI, m/z): 504[М+1]+.
[0859] (Ссылочный пример 84-5)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[2-(3-метоксиазетидин-1-ил)этил]оксим (ссылочное соединение 84-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 84-1, за исключением того, что N-метил-1-фенилметанамин заменяли на 3-метоксиазетидина гидрохлорид, и добавляли TEA. В результате указанное в заголовке соединение (включая примеси) было получено в виде желтого масла.
Масс-спектр (ESI, m/z): 516[М+1]+.
[0860] (Ссылочный пример 85-1)
2-[3-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)-2-{[(тетрагидропиран-2-ил)окси]метил}пропил]изоиндолин-1,3-дион (ссылочное соединение 85-1)

Фталимид, 0,19 г (1,3 ммоль), 1,1'-азобис(N,N-диметилформамид), 0,22 г (1,3 ммоль), и трибутилфосфин, 0,32 мл (1,3 ммоль), добавляли к раствору в THF (8 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксима, 0,36 г (0,87 ммоль), синтезированного таким же образом, как в ссылочном примере 18-1, и смесь перемешивали при комнатной температуре в течение 17 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 0,45 г (0,83 ммоль, выход 95%) в виде бесцветного масла.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,54 (s, 2H), 7,89-7,82 (m, 2H), 7,81-7,75 (m, 2H), 4,73-4,56 (m, 2H), 4,54-4,40 (m, 3H), 4,14-4,00 (m, 2H), 3,77-3,61 (m, 4H), 3,43-3,33 (m, 3H), 1,67-1,22 (m, 6H).
[0861] (Ссылочный пример 85-2)
2-[3-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)-2-метоксипропил]изоиндолин-1,3-дион (ссылочное соединение 85-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 85-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 18-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-гидрокси-2-метоксипропил)оксим, синтезированный таким же образом, как в ссылочном примере 89. В результате указанное в заголовке соединение (выход 73%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 460, 462[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 7,90-7,78 (m, 4H), 4,76-4,60 (m, 4H), 4,17-4,03 (m, 2H), 3,84-3,62 (m, 3H), 3,31 (s, 3H).
[0862] (Ссылочный пример 85-3)
2-[2-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этил]изоиндолин-1,3-дион (ссылочное соединение 85-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 85-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(3-гидрокси-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 18-1) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-(2-гидроксиэтил)оксим, синтезированный таким же образом, как в ссылочном примере 72. В результате указанное в заголовке соединение (выход 79%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 444, 446[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 7,90-7,80 (m, 4H), 4,25-4,14 (m, 2H), 3,86-3,80 (m, 2H), 3,78-3,72 (m, 2H), 3,70-3,60 (m, 2H), 2,46-2,33 (m, 2H), 2,17-1,99 (m, 2H).
[0863] (Ссылочный пример 86-1)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-амино-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 86-1)

Гидразина моногидрат, 0,35 мл (7,2 ммоль), добавляли к раствору в метиленхлориде (4 мл) и этаноле (6 мл) 2-{3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропил}изоиндолин-1,3-диона, 465 мг (0,661 ммоль), синтезированного таким же образом, как в ссылочном примере 6-58, и смесь перемешивали при комнатной температуре в течение 18 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении с получением неочищенного продукта в количестве 360 мг, содержащего указанное в заголовке соединение в виде коричневого масла.
[0864] (Ссылочный пример 86-2)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-амино-2-метоксипропил)оксим (ссылочное соединение 86-2)
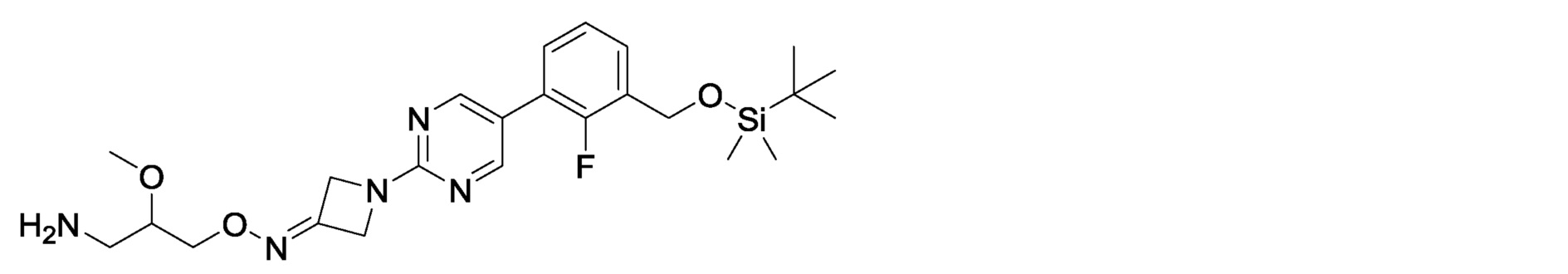
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 86-1, за исключением того, что 2-{3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропил}изоиндолин-1,3-дион (ссылочное соединение 6-58) заменяли на 2-{3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-метоксипропил}изоиндолин-1,3-дион, синтезированный таким же образом, как в ссылочном примере 6-59. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде светло-желтого масла.
Масс-спектр (CI, m/z): 490[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,67-7,40 (m, 2H), 7,35-7,27 (m, 1H), 4,93-4,76 (m, 6H), 4,19-3,95 (m, 2H), 3,94-3,76 (m,1H), 3,34 (s, 3H), 2,69-2,54 (m, 2H), 0,91 (s, 9H), 0,11 (s, 6H).
[0865] (Ссылочный пример 86-3)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-(2-аминоэтил)оксим (ссылочное соединение 86-3)
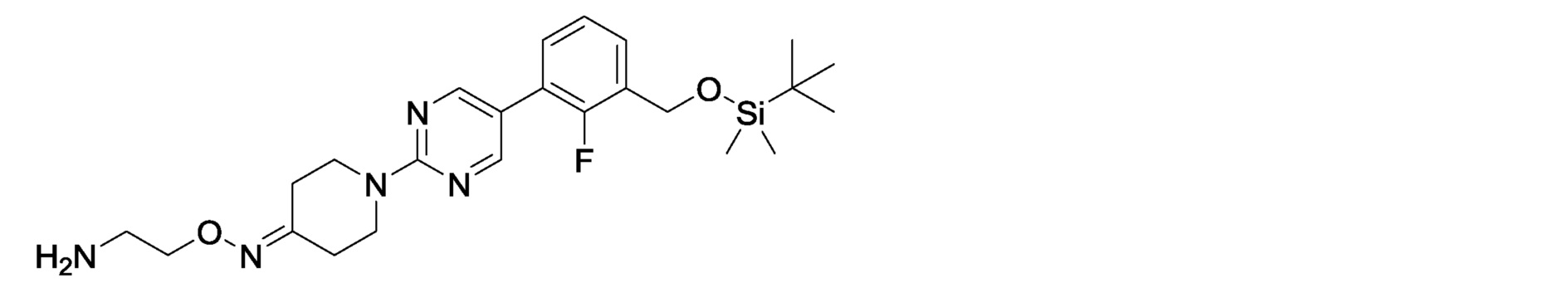
Данную реакцию проводили с помощью способа, описанного в ссылочном примере 86-1, за исключением того, что 2-{3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропил}изоиндолин-1,3-дион (ссылочное соединение 6-58) заменяли на неочищенный продукт, синтезированный таким же образом, как в ссылочном примере 6-82, который включал в себя 2-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}изоиндолин-1,3-дион, что реакционным растворителем являлся только этанол, и что температуру реакции изменяли на 60°C. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде коричневого масла.
[0866] (Ссылочный пример 87-1)
N-{3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-{[(тетрагидропиран-2-ил)окси]метил}пропил}ацетамид (ссылочное соединение 87-1)

TEA, 0,075 мл (0,54 ммоль), и уксусный ангидрид, 0,050 мл (0,53 ммоль), добавляли к раствору в метиленхлориде (6 мл) неочищенного продукта, 0,15 г, синтезированного таким же образом, как в ссылочном примере 86-1, который включал в себя 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-амино-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 0,087 г (0,14 ммоль) в виде бесцветного масла.
Масс-спектр (CI, m/z): 616[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,3 Гц, 2H), 7,89-7,80 (m, 1H), 7,54-7,42 (m, 2H), 7,36-7,28 (m, 1H), 4,86-4,78 (m, 6H), 4,56-4,52 (m,1H), 4,08-3,99 (m, 2H), 3,77-3,57 (m, 2H), 3,45-3,37 (m,2H), 3,15-3,10 (m, 2H), 2,16-2,08 (m, 1H), 1,82 (s, 3H), 1,77-1,29 (m, 6H), 0,91 (s, 9H), 0,11 (s, 6H).
[0867] (Ссылочный пример 87-2)
N-{3-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-илиден}амино)окси]-2-метоксипропил}ацетамид (ссылочное соединение 87-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 87-1, за исключением того, что неочищенный продукт, содержащий 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-амино-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 86-1), заменяли на 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-амино-2-метоксипропил)оксим, синтезированный таким же образом, как в ссылочном примере 86-2. В результате указанное в заголовке соединение (выход 47%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 532[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,4 Гц, 2H), 7,89 (t, J=5,8 Гц, 1H), 7,52-7,43 (m, 2H), 7,35-7,28 (m, 1H), 4,88-4,76 (m, 6H), 4,11-3,97(m, 2H), 3,52-3,45 (m, 1H), 3,34 (s, 3H), 3,26-3,08 (m, 2H), 1,82 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0868] (Ссылочный пример 87-3)
1-{2-[({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)метил]морфолино}этанон (ссылочное соединение 87-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 87-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-амино-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 86-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-морфолин-2-илметилоксим, синтезированный таким же образом, как в ссылочном примере 91. В результате указанное в заголовке соединение (выход 94%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 384, 386[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,80-4,72 (m, 4H), 4,28-4,09 (m, 1H), 4,08-3,98 (m, 2H), 3,88-3,80 (m, 1H), 3,77-3,51 (m, 2H), 3,49-3,28 (m, 1H), 3,19-2,90 (m, 1H), 2,73-2,42 (m, 1H), 2,01-1,99 (m, 3H).
[0869] (Ссылочный пример 87-4)
1-[3-({[1-(5-Бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)азетидин-1-ил]этанон (ссылочное соединение 87-4)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 87-1, за исключением того, что 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-амино-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 86-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-азетидин-3-илоксим, синтезированный таким же образом, как в ссылочном примере 99. В результате указанное в заголовке соединение (выход 88%) было получено в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,56 (s, 2H), 4,99-4,90 (m, 1H), 4,84-4,75 (m, 4H), 4,39-4,32 (m, 1H), 4,12-4,03 (m, 2H), 3,81-3,74 (m, 1H), 1,77 (s, 3H).
[0870] (Ссылочный пример 87-5)
N-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}ацетамид (ссылочное соединение 87-5)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 87-1, за исключением того, что неочищенный продукт, содержащий 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-амино-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим (ссылочное соединение 86-1) заменяли на неочищенный продукт, синтезированный таким же образом, как в ссылочном примере 86-3, который включал в себя 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-(2-аминоэтил)оксим. В результате указанное в заголовке соединение (выход 82%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 516[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,98-7,87 (m, 1H), 7,53-7,41 (m, 2H), 7,36-7,26 (m, 1H), 4,81 (s, 2H), 4,01-3,88 (m, 6H), 3,30-3,22 (m, 2H), 2,62-2,56 (m, 2H), 2,42-2,33 (m, 2H), 1,81 (s, 3H), 0,91 (s, 9H), 0,11 (s, 6H).
[0871] (Ссылочный пример 88)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-[3-(диметиламино)-2-{[(тетрагидропиран-2-ил)окси]метил}пропил]оксим (ссылочное соединение 88)
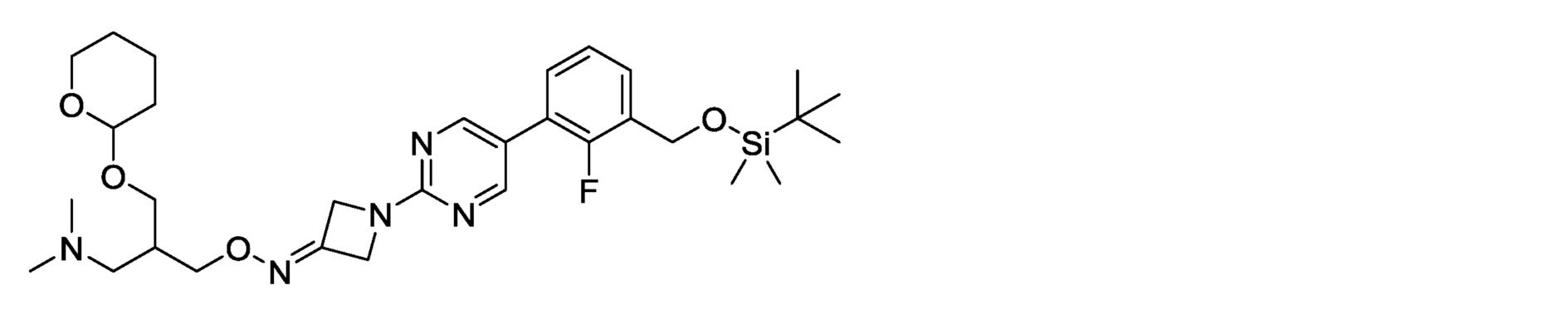
36% Водный раствор формальдегида, 0,84 мл (11 ммоль), и натрия триацетоксиборогидрид, 0,19 г (0,90 ммоль), добавляли к раствору в метаноле (6 мл) неочищенного продукта, 0,21 г, синтезированного таким же образом, как в ссылочном примере 86-1, который включал в себя 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]азетидин-3-она O-(3-амино-2-{[(тетрагидропиран-2-ил)окси]метил}пропил)оксим, и смесь перемешивали при комнатной температуре в течение 1,5 часа. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 0,16 г (включая примеси) в виде бесцветного масла.
Масс-спектр (CI, m/z): 602[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,63 (d, J=1,5 Гц, 2H), 7,54-7,41 (m, 2H), 7,36-7,27 (m, 1H), 4,89-4,75 (m, 6H), 4,57-4,50 (m, 1H), 4,11-3,95 (m,2H), 3,78-3,57 (m, 2H), 3,50-3,35 (m, 2H), 2,30-2,02 (m, 9H), 1,80-1,35 (m, 6H), 0,91 (s, 9H), 0,11 (s, 6H).
[0872] (Ссылочный пример 89)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(3-гидрокси-2-метоксипропил)оксим (ссылочное соединение 89)

При 0°C раствор 2 М хлорида водорода в этаноле, 1,0 мл (2,0 ммоль), добавляли к раствору в этаноле (6 мл) и THF (2 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-[2-метокси-3-(тритилокси)пропил]оксима, 0,46 г (0,80 ммоль), синтезированного таким же образом, как в ссылочном примере 19-2, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли TEA и воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 0,25 г (0,75 ммоль, выход 94%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 331, 333[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,80-4,72 (m, 4H), 4,70-4,64 (m, 1H), 4,15-3,97 (m, 2H), 3,47-3,39 (m, 3H), 3,33 (s, 3H).
[0873] (Ссылочный пример 90-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(2-морфолиноэтил)оксим (ссылочное соединение 90-1)

DMF (2 мл) добавляли к 2-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)этилметансульфонату, 150 мг (0,411 ммоль), синтезированному таким же образом, как в ссылочном примере 82-2, и морфолину, 179 мг (2,06 ммоль), и смесь перемешивали при 80°C в течение 4 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: гексан:этилацетат) и затем с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 116 мг (0,326 ммоль, выход 79%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 356, 358[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,80-4,69 (m, 4H), 4,13 (t, J=6,0 Гц, 2H), 3,58-3,52 (m, 4H), 2,57 (t, J=6,0 Гц, 2H), 2,43-2,37 (m, 4H).
[0874] (Ссылочный пример 90-2)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[2-(азетидин-1-ил)этил]оксим (ссылочное соединение 90-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 90-1, за исключением того, что морфолин заменяли на азетидин, и температуру реакции изменяли на 50°C. В результате указанное в заголовке соединение (выход 26%) было получено в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,54 (s, 2H), 4,78-4,69 (m, 4H), 3,95 (t, J=5,8 Гц, 2H), 3,16-3,04 (m, 4H), 2,57 (t, J=5,8 Гц, 2H), 1,98-1,89 (m, 2H).
[0875] (Ссылочный пример 91)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-морфолин-2-илметилоксим (ссылочное соединение 91)

Раствор 2 М хлорида водорода в этаноле, 5,00 мл (10,0 ммоль), добавляли к раствору в этаноле (2,5 мл) трет-бутил-2-[({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)метил]морфолин-4-карбоксилата, 440 мг (0,995 ммоль), синтезированного таким же образом, как в ссылочном примере 10-14, и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения в количестве 260 мг (0,760 ммоль, выход 76%) в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 342, 344[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,86-4,65 (m, 4H), 4,00-3,86 (m, 2H), 3,75-3,65 (m, 1H), 3,64-3,52 (m, 1H), 3,46-3,35 (m, 1H), 2,83-2,74 (m, 1H), 2,72-2,55 (m, 2H), 2,41-2,30 (m, 1H).
[0876] (Ссылочный пример 92-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[(4-метилморфолин-2-ил)метил]оксим (ссылочное соединение 92-1)

37% Водный раствор формальдегида, 0,13 мл (1,7 ммоль), и натрия триацетоксиборогидрид, 16 мг (0,075 ммоль), добавляли к раствору в метаноле (1 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-морфолин-2-илметилоксима, 20 мг (0,058 ммоль), синтезированного таким же образом, как в ссылочном примере 91, и смесь перемешивали при комнатной температуре в течение 15 минут. Аналогичным образом, 37% водный раствор формальдегида, 0,64 мл (8,6 ммоль), и натрия триацетоксиборогидрид, 75 мг (0,35 ммоль), добавляли к раствору в метаноле (5 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-морфолин-2-илметилоксима, 100 мг (0,29 ммоль), синтезированного таким же образом, как в ссылочном примере 91, и смесь перемешивали при комнатной температуре в течение 15 минут. После окончания реакции реакционные смеси объединяли вместе. К ним добавляли насыщенный водный раствор карбоната натрия и воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении с получением неочищенного продукта в количестве 130 мг, содержащего указанное в заголовке соединение в виде белого твердого вещества.
Масс-спектр (CI, m/z): 356, 358[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,81-4,66 (m, 4H), 4,11-3,86 (m, 2H), 3,79-3,72 (m, 1H), 3,72-3,64 (m, 1H), 3,54-3,41 (m, 1H), 2,72-2,66 (m, 1H), 2,60-2,53 (m, 1H), 2,16 (s, 3H), 2,00-1,91 (m, 1H), 1,76-1,69 (m, 1H).
[0877] (Ссылочный пример 92-2)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(1-метилазетидин-3-ил)оксим (ссылочное соединение 92-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 92-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-морфолин-2-илметилоксим (ссылочное соединение 91) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-азетидин-3-илоксим, синтезированный таким же образом, как в ссылочном примере 99, и продукт очищали с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 56%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 312,314[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,81-4,73 (m, 4H), 4,72-4,64 (m, 1H), 3,53-3,46 (m, 2H), 3,00-2,94 (m, 2H), 2,24 (s, 3H).
[0878] (Ссылочный пример 93-1)
2-{3-[(трет-Бутилдиметилсилил)окси]циклобутокси}изоиндолин-1,3-дион (ссылочное соединение 93-1)

Трифенилфосфин, 190 мг (0,724 ммоль), и 40% раствор диизопропилазодикарбоксилата в толуоле, 0,383 мл (0,728 ммоль), добавляли к суспензии в THF (5 мл) 3-[(трет-бутилдиметилсилил)окси]циклобутанола, 108 мг (0,534 ммоль), и 2-гидроксиизоиндолин-1,3-диона, 80,0 мг (0,490 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель, растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 121 мг (0,349 ммоль, выход 71%) в виде бесцветного масла.
Масс-спектр (CI, m/z): 348[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,87 (s, 4H), 4,91-4,83 (m, 1H), 4,71-4,61 (m, 1H), 2,50-2,43 (m, 2H), 2,20-2,10 (m, 2H), 0,86 (s, 9H), 0,04 (s, 6H).
[0879] (Ссылочный пример 93-2)
трет-Бутил-3-[(1,3-диоксоизоиндолин-2-ил)окси]азетидин-1-карбоксилат (ссылочное соединение 93-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 93-1, за исключением того, что 3-[(трет-бутилдиметилсилил)окси]циклобутанол заменяли на трет-бутил-3-гидроксиазетидин-1-карбоксилат, и что продукт очищали с помощью колоночной хроматографии на силикагеле, к полученному таким образом твердому веществу добавляли TBME, смесь перемешивали при комнатной температуре, и твердое вещество собирали с помощью фильтрации. В результате указанное в заголовке соединение (выход 82%) было получено в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,91-7,85 (m, 4H), 5,02-4,97 (m, 1H), 4,19-4,08 (m, 2H), 4,02-3,91 (m, 2H), 1,39 (s, 9H).
[0880] (Ссылочный пример 93-3)
2-(Пиридин-4-илметокси)изоиндолин-1,3-дион (ссылочное соединение 93-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 93-1, за исключением того, что 3-[(трет-бутилдиметилсилил)окси]циклобутанол заменяли на 4-пиридинметанол, и что после окончания реакции реакционную смесь концентрировали при пониженном давлении, к концентрированному остатку добавляли метанол, не проводя очистку концентрированного остатка с помощью колоночной хроматографии на силикагеле, и смесь перемешивали и фильтровали с получением твердого вещества. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 255[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,64-8,59 (m, 2H), 7,89-7,86 (m, 4H), 7,56-7,52 (m, 2H), 5,25 (s, 2H).
[0881] (Ссылочный пример 94-1)
O-{3-[(трет-бутилдиметилсилил)окси]циклобутил}гидроксиламин (ссылочное соединение 94-1)

Гидразина моногидрат, 0,168 мл (3,46 ммоль), добавляли к раствору в метиленхлориде (2 мл) 2-{3-[(трет-бутилдиметилсилил)окси]циклобутокси}изоиндолин-1,3-диона, 120 мг (0,345 ммоль), синтезированного таким же образом, как в ссылочном примере 93-1, и смесь перемешивали при комнатной температуре в течение 15 часов. После окончания реакции реакционную смесь фильтровали. Фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения в количестве 73,8 мг (0,339 ммоль, выход 98%) в виде бесцветного масла.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 5,83 (s, 2H), 4,48-4,34 (m, 1H), 4,16-4,05 (m, 1H), 2,30-2,20 (m, 2H), 2,00-1,88 (m, 2H), 0,85 (s, 9H), 0,01 (s, 6H).
[0882] (Ссылочный пример 94-2)
трет-Бутил-3-(аминоокси)азетидин-1-карбоксилат (ссылочное соединение 94-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 94-1, за исключением того, что 2-{3-[(трет-бутилдиметилсилил)окси]циклобутокси}изоиндолин-1,3-дион (ссылочное соединение 93-1) заменяли на трет-бутил-3-[(1,3-диоксоизоиндолин-2-ил)окси]азетидин-1-карбоксилат, синтезированный таким же образом, как в ссылочном примере 93-2. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде бесцветного масла.
Масс-спектр (CI, m/z): 189[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 6,16 (s, 2H), 4,40-4,24 (m, 1H), 3,98-3,82 (m, 2H), 3,78-3,65 (m, 2H), 1,37 (s, 9H).
[0883] (Ссылочный пример 94-3)
O-(пиридин-4-илметил)гидроксиламина дигидрохлорид (ссылочное соединение 94-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 94-1, за исключением того, что 2-{3-[(трет-бутилдиметилсилил)окси]циклобутокси}изоиндолин-1,3-дион (ссылочное соединение 93-1) заменяли на 2-(пиридин-4-илметокси)изоиндолин-1,3-дион, синтезированный таким же образом, как в ссылочном примере 93-3, и что после окончания реакции реакционную смесь фильтровали, к фильтрату добавляли насыщенный водный раствор бикарбоната натрия с последующей экстракцией метиленхлоридом, органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали, фильтрат концентрировали при пониженном давлении, диэтиловый эфир и 4 н раствор хлорида водорода в 1,4-диоксане добавляли к концентрированному остатку, и осажденное твердое вещество собирали с помощью фильтрации. В результате указанное в заголовке соединение (выход 47%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 125[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,93-8,87 (m, 2H), 7,97-7,92 (m, 2H), 5,36 (s, 2H).
[0884] (Ссылочный пример 95-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-{3-[(трет-бутилдиметилсилил)окси]циклобутил}оксим (ссылочное соединение 95-1)

O-{3-[(трет-бутилдиметилсилил)окси]циклобутил}гидроксиламин, 72 мг (0,33 ммоль), синтезированный таким же образом, как в ссылочном примере 94-1, добавляли к суспензии в этаноле (2 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она, 69 мг (0,30 ммоль), синтезированного таким же образом, как в ссылочном примере 2, и смесь перемешивали при 50°C в течение 3 часов и при 100°C в течение 8 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель, растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 100 мг (0,23 ммоль, выход 77%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 427, 429[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,80-4,65 (m, 5H), 4,54-4,42 (m, 1H), 2,41-2,31 (m, 2H), 2,21-2,08 (m, 2H), 0,85 (s, 9H), 0,02 (s, 6H).
[0885] (Ссылочный пример 95-2)
трет-Бутил-3-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)азетидин-1-карбоксилат (ссылочное соединение 95-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 95-1, за исключением того, что O-{3-[(трет-бутилдиметилсилил)окси]циклобутил}гидроксиламин (ссылочное соединение 94-1) заменяли на трет-бутил-3-(аминоокси)азетидин-1-карбоксилат, синтезированный таким же образом, как в ссылочном примере 94-2, что температура реакции всегда составляла 100°C, и что после окончания реакции осажденное твердое вещество собирали с помощью фильтрации. В результате указанное в заголовке соединение (выход 49%) было получено в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,56 (s, 2H), 4,96-4,85 (m, 1H), 4,82-4,76 (m, 4H), 4,16-4,02 (m, 2H), 3,88-3,74 (m, 2H), 1,38 (s, 9H).
[0886] (Ссылочный пример 96-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(3-гидроксициклобутил)оксим (ссылочное соединение 96-1)

Раствор 1 М тетрабутиламмония фторида в THF, 0,30 мл (0,30 ммоль), добавляли к раствору в THF (3 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-{3-[(трет-бутилдиметилсилил)окси]циклобутил}оксима, 99 мг (0,23 ммоль), синтезированного таким же образом, как в ссылочном примере 95-1, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 69 мг (0,22 ммоль, выход 96%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 313, 315[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 5,08 (d, J=5,0 Гц, 1H), 4,81-4,67 (m, 5H), 4,34-4,22 (m, 1H), 2,32-2,23 (m, 2H), 2,15-2,04 (m, 2H).
[0887] (Ссылочный пример 96-2)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[1-(2-гидроксиэтил)азетидин-3-ил]оксим (ссылочное соединение 96-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 96-1, за исключением того, что 1-(5-бромпиримидин-2-ил)азетидин-3-она O-{3-[(трет-бутилдиметилсилил)окси]циклобутил}оксим (ссылочное соединение 95-1) заменяли на 1-(5-бромпиримидин-2-ил)азетидин-3-она O-(1-{2-[(трет-бутилдиметилсилил)окси]этил}азетидин-3-ил)оксим, синтезированный таким же образом, как в ссылочном примере 100-3. В результате указанное в заголовке соединение (выход 57%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 342, 344[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,79-4,69 (m, 5H), 4,38 (t, J=5,5 Гц, 1H), 3,55-3,47 (m, 2H), 3,36-3,29 (m, 2H), 3,05-2,99 (m, 2H), 2,47 (t, J=6,0 Гц, 2H).
[0888] (Ссылочный пример 97)
Азетидин-3-она O-бензилоксима гидрохлорид (ссылочное соединение 97)

Раствор 4 М хлорида водорода в 1,4-диоксане, 4,0 мл (16 ммоль), добавляли к раствору в метаноле (30 мл) неочищенного продукта, 1,61 г, синтезированного таким же образом, как в ссылочном примере 37-2, который включал в себя трет-бутил-3-[(бензилокси)имино]азетидин-1-карбоксилат, и смесь перемешивали при комнатной температуре в течение 24 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток сушили при пониженном давлении с получением неочищенного продукта в количестве 1,86 г, содержащего указанное в заголовке соединение в виде белого твердого вещества.
[0889] (Ссылочный пример 98)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-бензилоксим (ссылочное соединение 98)

5-Бром-2-хлорпиримидин, 300 мг (1,55 ммоль), и DIPEA, 1,00 мл (5,74 ммоль), добавляли к раствору в ацетонитриле (8 мл) неочищенного продукта 330 мг, синтезированного таким же образом, как в ссылочном примере 97, который включал в себя азетидин-3-она O-бензилоксима гидрохлорид, и смесь перемешивали при 60°C в течение 2 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:этилацетат) с получением указанного в заголовке соединения в количестве 117 мг (0,351 ммоль) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 333, 335[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,54 (s, 2H), 7,40-7,29 (m, 5H), 5,07 (s, 2H), 4,76 (s, 4H).
[0890] (Ссылочный пример 99)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-азетидин-3-илоксим (ссылочное соединение 99)

TFA, 5,00 мл (64,9 ммоль), добавляли к раствору в метиленхлориде (10 мл) трет-бутил-3-{[(1-(5-бромпиримидин-2-ил)азетидин-3-илиден)амино]окси)азетидин-1-карбоксилата, 1,04 г (2,61 ммоль), синтезированного таким же образом, как в ссылочном примере 95-2, и смесь перемешивали при комнатной температуре в течение 15 часов. После окончания реакции к реакционной смеси добавляли TEA и воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения в количестве 759 мг (2,55 ммоль, выход 98%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 298, 300[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,56 (s, 2H), 4,98-4,91 (m, 1H), 4,86-4,72 (m, 4H), 3,86-3,78 (m, 2H), 3,73-3,66 (m, 2H).
[0891] (Ссылочный пример 100-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(1-бензилазетидин-3-ил)оксим (ссылочное соединение 100-1)

Бензальдегид, 0,034 мл (0,34 ммоль), и натрия триацетоксиборогидрид, 53 мг (0,25 ммоль), добавляли к раствору в метиленхлориде (2 мл) и MeOH (0,5 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-азетидин-3-илоксима, 50 мг (0,17 ммоль), синтезированного таким же образом, как в ссылочном примере 99, и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом и сушили над безводным сульфатом натрия. Смесь концентрировали, и остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель, растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 41 мг (0,11 ммоль, выход 65%) в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 7,33-7,21 (m, 5H), 4,80-4,73 (m, 5H), 3,59 (s, 2H), 3,53-3,46 (m, 2H), 3,10-3,01 (m, 2H).
[0892] (Ссылочный пример 100-2)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(1-этилазетидин-3-ил)оксим (ссылочное соединение 100-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 100-1, за исключением того, что бензальдегид заменяли на ацетальдегид. В результате указанное в заголовке соединение (выход 35%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 326, 328[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,79-4,68 (m, 5H), 3,51-3,42 (m, 2H), 2,97-2,88 (m, 2H), 2,40 (q, J=7,2 Гц, 2H), 0,86 (t, J=7,2 Гц, 3H).
[0893] (Ссылочный пример 100-3)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-(1-{2-[(трет-бутилдиметилсилил)окси]этил}азетидин-3-ил)оксим (ссылочное соединение 100-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 100-1, за исключением того, что бензальдегид заменяли на 2-[(трет-бутилдиметилсилил)окси]ацетальдегид. В результате указанное в заголовке соединение (выход 71%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 456, 458[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,79-4,69 (m, 5H), 3,59-3,48 (m, 4H), 3,12-2,97 (m, 2H), 2,57-2,46 (m, 2H), 0,86 (s, 9H), 0,02 (s, 6H).
[0894] (Ссылочный пример 101-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[1-(2,2,2-трифторэтил)азетидин-3-ил]оксим (ссылочное соединение 101-1)

2,2,2-Трифторэтилтрифторметансульфонат, 0,029 мл (0,20 ммоль), и DIPEA, 0,086 мл (0,50 ммоль), добавляли к суспензии в DMF (1 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-азетидин-3-илоксима, 50 мг (0,17 ммоль), синтезированного таким же образом, как в ссылочном примере 99, и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом и сушили над безводным сульфатом магния. Смесь концентрировали, и остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель, растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 39 мг (0,10 ммоль, выход 59%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 380, 382[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,83-4,75 (m, 5H), 3,69-3,64 (m, 2H), 3,37-3,29 (m, 2H), 3,25 (q, J=10,2 Гц, 2H).
[0895] (Ссылочный пример 101-2)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[1-(2-метоксиэтил)азетидин-3-ил]оксим (ссылочное соединение 101-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 101-1, за исключением того, что 2,2,2-трифторэтилтрифторметансульфонат заменяли на 2-бромэтилметиловый эфир, и температуру реакции изменяли на 70°C. В результате указанное в заголовке соединение (выход 43%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 356, 358[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,80-4,68 (m, 5H), 3,54-3,46 (m, 2H), 3,28 (t, J=5,8 Гц, 2H), 3,20 (s, 3H), 3,08-2,97 (m, 2H), 2,56 (t, J=5,8 Гц, 2H).
[0896] (Ссылочный пример 101-3)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[1-(2-фторэтил)азетидин-3-ил]оксим (ссылочное соединение 101-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 101-1, за исключением того, что 2,2,2-трифторэтилтрифторметансульфонат заменяли на 2-фторэтил-4-метилбензолсульфонат, и температуру реакции изменяли на 100°C, а затем на 120°C. В результате указанное в заголовке соединение (включая примеси) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 344, 346[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,55 (s, 2H), 4,81-4,71 (m, 5H), 4,39 (td, J=4,8, 47,7 Гц, 2H), 3,60-3,51 (m, 2H), 3,13-3,03 (m, 2H), 2,70 (td, J=4,8, 29,0 Гц, 2H).
[0897] (Ссылочный пример 102-1)
1-(5-Бромпиримидин-2-ил)азетидин-3-она O-[1-(метилсульфонил)азетидин-3-ил]оксим (ссылочное соединение 102-1)

Метансульфонилхлорид, 0,026 мл (0,34 ммоль), и TEA, 0,077 мл (0,55 ммоль), добавляли к раствору в метиленхлориде (1 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она O-азетидин-3-илоксима, 82 мг (0,28 ммоль), синтезированного таким же образом, как в ссылочном примере 99, и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом и сушили над безводным сульфатом магния. Смесь концентрировали, и остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель, растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 58 мг (0,15 ммоль, выход 54%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 376, 378[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,56 (s, 2H), 4,99-4,87 (m, 1H), 4,83-4,77 (m, 4H), 4,13 (dd, J=6,7, 9,7 Гц, 2H), 3,90 (dd, J=4,6, 9,7 Гц, 2H), 3,03 (s, 3H).
[0898] (Ссылочный пример 102-2)
Метил-3-({[1-(5-бромпиримидин-2-ил)азетидин-3-илиден]амино}окси)азетидин-1-карбоксилат (ссылочное соединение 102-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 102-1, за исключением того, что метансульфонилхлорид заменяли на метилхлорформиат. В результате указанное в заголовке соединение (выход 78%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 356, 358[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,56 (s, 2H), 4,98-4,92 (m, 1H), 4,84-4,74 (m, 4H), 4,24-4,09 (m, 2H), 3,95-3,82 (m, 2H), 3,56 (s, 3H).
[0899] (Ссылочный пример 103)
3-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)пропановой кислоты гидрохлорид (ссылочное соединение 103)

3-(Аминоокси)пропановой кислоты гидрохлорид, 67 мг (0,47 ммоль), добавляли к раствору в THF (2 мл) и этаноле (2 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она, 0,10 г (0,39 ммоль), синтезированного таким же образом, как в ссылочном примере 2, и смесь перемешивали при 50°C в течение 2 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток сушили при пониженном давлении с получением неочищенного продукта в количестве 0,13 г, содержащего указанное в заголовке соединение в виде белого твердого вещества.
[0900] (Ссылочный пример 104)
Этил-3-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)пропанoат (ссылочное соединение 104)

Карбонат калия, 0,11 г (0,80 ммоль), и йодэтан, 0,050 мл (0,62 ммоль), добавляли к раствору в DMF (4 мл) неочищенного продукта, 0,13 г, синтезированного таким же образом, как в ссылочном примере 103, который включал в себя 3-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)пропановую кислоту, и смесь перемешивали при комнатной температуре в течение 4 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 99 мг (0,27 ммоль) в виде бесцветного масла.
Масс-спектр (CI, m/z): 371, 373[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 4,19 (t, J=6,1 Гц, 2H), 4,07 (q, J=7,2 Гц, 2H), 3,87-3,76 (m, 4H), 2,66-2,58 (m, 2H), 2,38-2,32 (m, 2H), 1,17 (t, J=7,2 Гц, 3H).
[0901] (Ссылочный пример 105-1)
3-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)пропанамид (ссылочное соединение 105-1)

CDI, 168 мг (1,04 ммоль), добавляли к раствору в THF (4 мл) 3-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)пропановой кислоты гидрохлорида, 175 мг (0,461 ммоль), синтезированного таким же образом, как в ссылочном примере 103, и смесь перемешивали при комнатной температуре в течение 4 часов. Затем добавляли 28% водный раствор аммиака, 0,965 мл (51,0 ммоль), при охлаждении льдом. Смесь перемешивали в течение 15 минут при охлаждении льдом. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. К неочищенному продукту, полученному таким образом, добавляли этилацетат, и смесь перемешивали при комнатной температуре. После этого твердое вещество собирали с помощью фильтрации и сушили при пониженном давлении с получением указанного в заголовке соединения в количестве 93,9 мг (0,274 ммоль, выход 59%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 342, 344[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,31 (s, 2H), 5,83 (br s, 1H), 5,30 (br s, 1H), 4,32 (t, J=6,0 Гц, 2H), 3,95-3,85 (m, 4H), 2,68-2,57 (m, 4H), 2,47-2,39 (m, 2H).
[0902] (Ссылочный пример 105-2)
3-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)-N-метилпропанамид (ссылочное соединение 105-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 105-1, за исключением того, что 28% водный раствор аммиака заменяли на 2 М раствор метиламина в THF, что THF заменяли на DMF, и что продукт очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: этилацетат:метанол), и полученный таким образом неочищенный продукт промывали TBME. В результате указанное в заголовке соединение (выход 36%) было получено в виде белого твердого вещества.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 7,84-7,74 (m, 1H), 4,14 (t, J=6,6 Гц, 2H), 3,88-3,77 (m, 4H), 2,56 (d, J=4,5 Гц, 3H), 2,43-2,29 (m, 4H).
[0903] (Ссылочный пример 105-3)
3-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)-N,N-диметилпропанамид (ссылочное соединение 105-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 105-1, за исключением того, что 28% водный раствор аммиака заменяли на 2 М раствор диметиламина в THF, что THF заменяли на DMF, и что продукт очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: этилацетат:метанол). В результате указанное в заголовке соединение (выход 18%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 370, 372[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 4,17 (t, J=6,8 Гц, 2H), 3,87-3,77 (m, 4H), 2,95 (s, 3H), 2,80 (s, 3H), 2,64 (t, J=6,7 Гц, 2H), 2,54-2,48 (m, 2H), 2,39-2,31 (m,2H).
[0904] (Ссылочный пример 106)
N-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}-N-метилацетамид (ссылочное соединение 106)

При 0°C 55% гидрид натрия, 16 мг (0,37 ммоль), добавляли к раствору в THF (4 мл) N-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}ацетамида, 0,12 г (0,23 ммоль), синтезированного таким же образом, как в ссылочном примере 87-5, и смесь перемешивали при 0°C в течение 10 минут. Затем добавляли йодметан, 0,030 мл (0,48 ммоль), при 0°C, и смесь перемешивали при комнатной температуре в течение 14 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 0,11 г (0,21 ммоль, выход 91%) в виде светло-желтого масла.
Масс-спектр (CI, m/z): 530[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,59 (d, J=1,5 Гц, 2H), 7,51-7,41 (m, 2H), 7,33-7,27 (m, 1H), 4,81 (s, 2H), 4,16-4,02 (m, 2H), 3,96-3,89 (m, 4H), 3,59-3,46 (m, 2H), 3,00-2,79 (m, 3H), 2,60-2,53 (m, 2H), 2,42-2,36 (m, 2H), 2,00-1,96 (m, 3H), 0,92 (s, 9H), 0,11 (s, 6H).
[0905] (Ссылочный пример 107)
N-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}метансульфонамид (ссылочное соединение 107)

При 0°C TEA, 0,11 мл (0,79 ммоль), и метансульфонилхлорид, 0,054 мл (0,69 ммоль), добавляли к раствору в метиленхлориде (3 мл) 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-(2-аминоэтил)оксима, 300 мг (0,63 ммоль), синтезированного таким же образом, как в ссылочном примере 86-3, и смесь перемешивали при комнатной температуре в течение 16 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве (включая примеси) 100 мг в виде желтого масла.
Масс-спектр (ESI, m/z): 552[М+1]+.
1H-ЯМР (400 МГц, CDCl3) δ: 8,53 (d, J=1,4 Гц, 2H), 7,53-7,44 (m, 1H), 7,30-7,18 (m, 2H), 4,85 (s, 2H), 4,83-4,74 (m, 1H), 4,23-4,15 (m, 2H), 4,06-3,96 (m, 4H), 3,50-3,42 (m, 2H), 2,99 (s, 3H), 2,72-2,63 (m, 2H), 2,49-2,42 (m, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0906] (Ссылочный пример 108)
N-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}-N-метилметансульфонамид (ссылочное соединение 108)
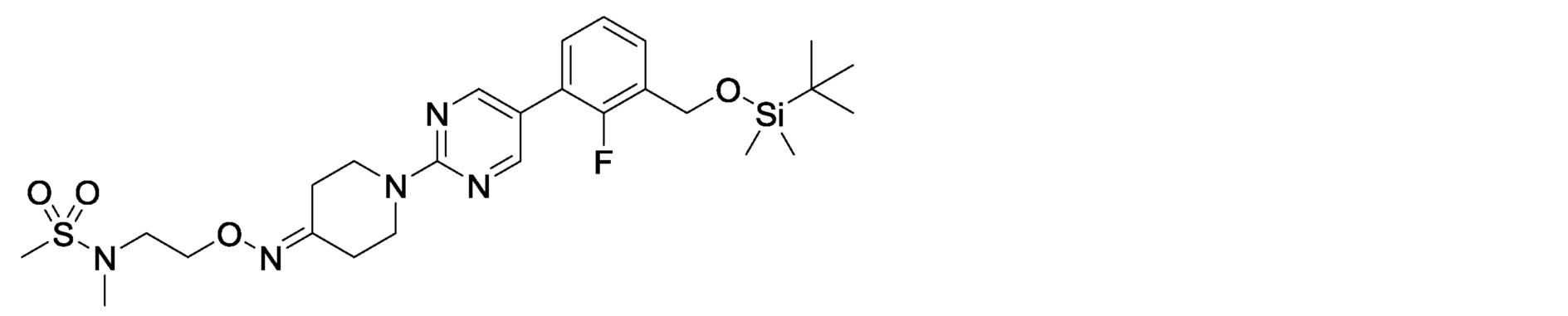
Йодметан, 0,056 мл (0,90 ммоль), и карбонат калия, 50 мг (0,36 ммоль), добавляли к раствору в метиленхлориде (3 мл) N-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}метансульфонамида, 100 мг (0,18 ммоль), синтезированного таким же образом, как в ссылочном примере 107, и смесь перемешивали при комнатной температуре в течение 66 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве (включая примеси) 83 мг в виде желтого масла.
Масс-спектр (ESI, m/z): 566[М+1]+.
[0907] (Ссылочный пример 109-1)
трет-Бутил-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}(метилсульфонил)карбамат (ссылочное соединение 109-1)
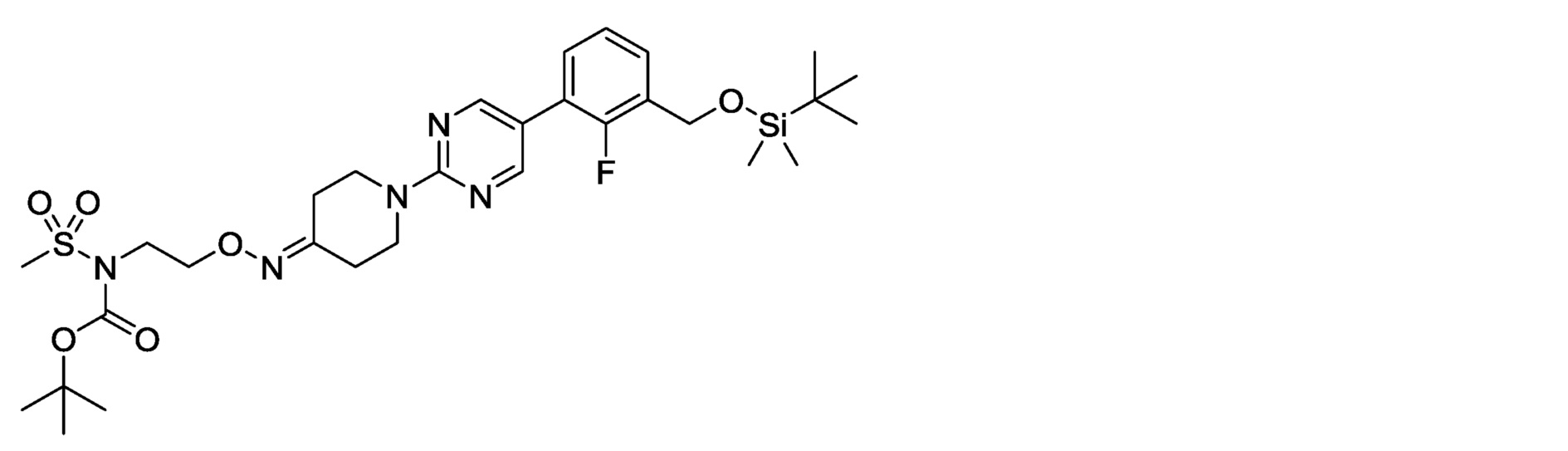
Ди-трет-бутилкарбонат, 0,088 мл (0,38 ммоль), TEA, 0,079 мл (0,057 ммоль), и DMAP, 3,5 мг (0,029 ммоль), добавляли к раствору в метиленхлориде (3 мл) N-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}метансульфонамида, 100 мг (0,19 ммоль), синтезированного таким же образом, как в ссылочном примере 107, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 120 мг (0,18 ммоль, выход 95%) в виде желтого масла.
Масс-спектр (ESI, m/z): 652[М+1]+.
[0908] (Ссылочный пример 109-2)
трет-Бутил-[2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этил](метил)карбамат (ссылочное соединение 109-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 109-1, за исключением того, что N-{2-[({1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-илиден}амино)окси]этил}метансульфонамид (ссылочное соединение 107) заменяли на 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-[2-(метиламино)этил]оксим, синтезированный таким же образом, как в ссылочном примере 110-2. В результате указанное в заголовке соединение (выход 92%) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 428,430[М+1]+.
1H-ЯМР (400 МГц, DMSO-d6) δ: 8,48 (s, 2H), 4,09-3,99 (m, 2H), 3,87-3,78 (m, 4H), 3,45-3,36 (m, 2H), 2,86-2,74 (m, 3H), 2,60-2,45 (m, 2H), 2,41-2,30 (m, 2H), 1,37 (s, 9H).
[0909] (Ссылочный пример 110-1)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-[2-(диметиламино)этил]оксим (ссылочное соединение 110-1)

2 М раствор диметиламина в THF, 1,27 мл (2,54 ммоль), добавляли к раствору в DMF (3 мл) 2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этилметансульфоната, 100 мг (0,254 ммоль), синтезированного таким же образом, как в ссылочном примере 82-3. Смесь подавали в микроволновое реакционное устройство и перемешивали при 80°C в течение 1 часа. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 78,0 мг (0,228 ммоль, выход 90%) в виде бесцветного масла.
Масс-спектр (ESI, m/z): 342, 344[М+1]+.
1H-ЯМР (400 МГц, CDCl3) δ: 8,30 (s, 2H), 4,16 (t, J=5,8 Гц, 2H), 3,94-3,84 (m, 4H), 2,69-2,58 (m, 4H), 2,46-2,38 (m, 2H), 2,30 (s, 6H).
[0910] (Ссылочный пример 110-2)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-[2-(метиламино)этил]оксим (ссылочное соединение 110-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 110-1, за исключением того, что 2 М раствор диметиламина в THF заменяли на 1 М раствор метиламина в THF, что растворители не использовали, что смесь перемешивали при температуре реакции 90°C в течение 1 часа и при температуре реакции 110°C в течение 1 часа, и что не проводили очистку с помощью хроматографии на силикагеле. В результате был получен содержащий указанное в заголовке соединение неочищенный продукт в виде желтого масла.
Масс-спектр (ESI, m/z): 328, 330[М+1]+.
[0911] (Ссылочный пример 110-3)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-[2-(1H-пиразол-1-ил)этил]оксим (ссылочное соединение 110-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 110-1, за исключением того, что 2 М раствор диметиламина в THF заменяли на 1H-пиразол, что добавляли карбонат цезия, и что микроволновое реакционное устройство заменяли на масляную баню. В результате указанное в заголовке соединение (включая примеси) было получено в виде белого твердого вещества.
Масс-спектр (ESI, m/z): 365, 367[М+1]+.
1H-ЯМР (400 МГц, CDCl3) δ: 8,31 (s, 2H), 7,54-7,50 (m, 1H), 7,40-7,36 (m, 1H), 6,23 (t, J=2,1 Гц, 1H), 4,45-4,36 (m, 4H), 3,93-3,84 (m, 4H), 2,60-2,54 (m, 2H), 2,45-2,39 (m, 2H).
[0912] (Ссылочный пример 111)
Ди-трет-бутил-[2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этил]карбамат (ссылочное соединение 111)

Карбонат цезия, 436 мг (1,34 ммоль), добавляли к раствору в DMF (3 мл) 2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этилметансульфоната, 263 мг (0,669 ммоль), синтезированного таким же образом, как в ссылочном примере 82-3, и ди-трет-бутил иминокарбоксилата, 174 мг (0,801 ммоль), и смесь перемешивали при 80°C в течение 5 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 358 мг (включая примеси) в виде желтого масла.
Масс-спектр (ESI, m/z): 514, 516[М+1]+.
1H-ЯМР(400 МГц, CDCl3) δ: 8,30 (s, 2H), 4,20-4,14 (m, 2H), 3,94-3,84 (m, 6H), 2,65-2,57 (m, 2H), 2,45-2,37 (m, 2H), 1,55 (s, 9H), 1,48 (s, 9H).
[0913] (Ссылочный пример 112)
3-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)пропаннитрил (ссылочное соединение 112)

Пиридин 0,290 мл (3,59 ммоль), добавляли к раствору в метиленхлориде (20 мл) 3-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)пропанамида, 558 мг (1,63 ммоль), синтезированного таким же образом, как в ссылочном примере 105-1, и смесь перемешивали при комнатной температуре. Затем добавляли трифторуксусный ангидрид, 0,345 мл (2,44 ммоль), при охлаждении льдом. Смесь перемешивали в течение 1 часа при охлаждении льдом. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией метиленхлоридом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 442 мг (1,36 ммоль, выход 83%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 324, 326[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,31 (s, 2H), 4,24 (t, J=6,3 Гц, 2H), 3,94-3,88 (m, 4H), 2,73 (t, J=6,3 Гц, 2H), 2,69-2,63 (m, 2H), 2,45-2,39 (m, 2H).
[0914] (Ссылочный пример 113)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-[2-(метилсульфонил)этил]оксим (ссылочное соединение 113)

Метил-(2-хлорэтил)сульфон, 95 мг (0,67 ммоль), карбонат цезия, 0,29 г (0,89 ммоль), и йодид натрия, 15 мг (0,10 ммоль), добавляли к раствору в DMF (4 мл) 1-(5-бромпиримидин-2-ил)азетидин-3-она оксима, 0,12 г (0,44 ммоль), синтезированного таким же образом, как в ссылочном примере 66, и смесь перемешивали при 80°C в течение 8 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 0,11 г (0,29 ммоль, выход 66%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 377, 379[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,49 (s, 2H), 4,34 (t, J=5,8 Гц, 2H), 3,88-3,79 (m, 4H), 3,47 (t, J=5,8 Гц, 2H), 2,98 (s, 3H), 2,59-2,52 (m, 2H), 2,42-2,35 (m, 2H).
[0915] (Ссылочный пример 114-1)
(1-Метил-1H-пиразол-3-ил)метанол (ссылочное соединение 114-1)

При 0°C натрия борогидрид, 360 мг (9,52 ммоль), добавляли к раствору в этаноле (30 мл) 1-метил-1H-пиразол-3-карбальдегида, 1,00 г (9,08 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 860 мг (7,67 ммоль, выход 84%) в виде бесцветного масла.
Масс-спектр (CI, m/z): 113[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 7,31 (d, J=2,2 Гц, 1H), 6,23 (d, J=2,2 Гц, 1H), 4,67 (s, 2H), 3,88 (s, 3H).
[0916] (Ссылочный пример 114-2)
[1-(Тетрагидропиран-2-ил)-1H-пиразол-3-ил]метанол (ссылочное соединение 114-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 114-1, за исключением того, что 1-метил-1H-пиразол-3-карбальдегид заменяли на 1-(тетрагидропиран-2-ил)-1H-пиразол-3-карбальдегид, синтезированный таким же образом, как в ссылочном примере 115-1, что этанол заменяли на метанол, что после окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом, и что не проводили очистку с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 93%) было получено в виде бесцветного масла.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 7,56 (d, J=2,5 Гц, 1H), 6,30 (d, J=2,5 Гц, 1H), 5,34 (dd, J=2,4, 9,9 Гц, 1H), 4,71 (d, J=6,0 Гц, 2H), 4,13-4,03 (m, 1H), 3,79-3,64 (m, 1H), 2,19-2,00 (m, 3H), 1,92 (t, J=6,0 Гц, 1H), 1,78-1,38 (m, 3H).
[0917] (Ссылочный пример 114-3)
[1-(Тетрагидропиран-2-ил)-1H-пиразол-4-ил]метанол (ссылочное соединение 114-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 114-1, за исключением того, что 1-метил-1H-пиразол-3-карбальдегид заменяли на 1-(тетрагидропиран-2-ил)-1H-пиразол-4-карбальдегид, синтезированный таким же образом, как в ссылочном примере 115-2, что этанол заменяли на метанол, что после окончания реакции к реакционной смеси добавляли рассол и последующей экстракцией этилацетатом, и что не проводили очистку с помощью колоночной хроматографии на силикагеле. В результате указанное в заголовке соединение (выход 85%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 183[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 7,74-7,71 (m, 1H), 7,41-7,38 (m, 1H), 5,33 (dd, J=2,4, 10,0 Гц, 1H), 4,84 (t, J=5,5 Гц, 1H), 4,34 (d, J=5,4 Гц, 2H), 3,97-3,82 (m, 1H), 3,71-3,52 (m, 1H), 2,13-1,80 (m, 3H), 1,73-1,42 (m, 3H).
[0918] (Ссылочный пример 115-1)
1-(Тетрагидропиран-2-ил)-1H-пиразол-3-карбальдегид (ссылочное соединение 115-1)

пара-Толуолсульфоновую кислоту, 206 мг (1,08 ммоль), и DHP, 1,85 мл (21,8 ммоль), добавляли к суспензии в THF (30 мл) 1H-пиразол-3-карбальдегида, 1,05 г (10,9 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. Затем добавляли 30 мл метиленхлорида, и смесь перемешивали при комнатной температуре в течение 4,5 часа и при 60°C в течение 5 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве (включая примеси).
[0919] (Ссылочный пример 115-2)
1-(Тетрагидропиран-2-ил)-1H-пиразол-4-карбальдегид (ссылочное соединение 115-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 115-1, за исключением того, что 1H-пиразол-3-карбальдегид заменяли на 1H-пиразол-4-карбальдегид, что THF заменяли на метиленхлорид, и что температура реакции была равна температуре окружающей среды. В результате указанное в заголовке соединение (выход 86%) было получено в виде бесцветного масла.
Масс-спектр (CI, m/z): 181[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 9,83 (s, 1H), 8,64 (s, 1H), 8,02 (s, 1H), 5,50 (dd, J=2,5, 9,8 Гц, 1H), 3,99-3,90 (m, 1H), 3,72-3,59 (m, 1H), 2,16-1,86 (m, 3H), 1,75-1,47 (m, 3H).
[0920] (Ссылочный пример 116)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-[(1-метил-1H-пиразол-4-ил)метил]оксим (ссылочное соединение 116)

Раствор 2 М хлорида водорода в этаноле, 2,0 мл (4,0 ммоль), добавляли к 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-{[1-(тетрагидропиран-2-ил)-1H-пиразол-4-ил]метил}оксиму, 0,18 г (0,41 ммоль), синтезированному таким же образом, как в ссылочном примере 67-16, и смесь перемешивали при комнатной температуре в течение 2 часов. После окончания реакции к реакционной смеси добавляли TEA и воду с последующей экстракцией этилацетатом. Органический слой промывали насыщенным водным раствором бикарбоната натрия, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. К концентрированному остатку добавляли 4 мл DMF. При перемешивании при комнатной температуре добавляли карбонат цезия, 0,26 г (0,80 ммоль), и йодметан, 0,040 мл (0,64 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 17 часов. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали водой, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: 1,2-дихлорэтан:этилацетат) с получением указанного в заголовке соединения в количестве 0,14 г (0,38 ммоль, выход 93%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 366, 368[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,47 (s, 2H), 7,69 (s, 1H), 7,41 (s, 1H), 4,86 (s, 2H), 3,84-3,78 (m, 7H), 2,52-2,47 (m, 2H), 2,39-2,32 (m, 2H).
[0921] (Ссылочный пример 117)
1-(5-Бромпиримидин-2-ил)пиперидин-4-она O-пиридин-4-илметилоксим (ссылочное соединение 117)

Карбонат натрия, 210 мг (1,98 ммоль), и O-(пиридин-4-илметил)гидроксиламина дигидрохлорид, 260 мг (1,32 ммоль), синтезированный таким же образом, как в ссылочном примере 94-3, добавляли к раствору в THF (6 мл) 1-(5-бромпиримидин-2-ил)пиперидин-4-она, 170 мг (0,664 ммоль), синтезированного таким же образом, как в ссылочном примере 59, и смесь перемешивали при комнатной температуре в течение 13 часов и при 50°C в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 113 мг (0,312 ммоль, выход 47%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 362, 364[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,60-8,56 (m, 2H), 8,31 (s, 2H), 7,27-7,22 (m, 2H), 5,10 (s, 2H), 3,95-3,88 (m, 4H), 2,74-2,69 (m, 2H), 2,45-2,39 (m, 2H).
[0922] (Ссылочный пример 118)
1-[2-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден)амино]окси}этил)пирролидин-2,5-дион (ссылочное соединение 118)

Трибутилфосфин, 0,150 мл (0,608 ммоль), и N,N,N',N'-тетраметилазодикарбоксамид, 150 мг (0,595 ммоль), добавляли к раствору в THF (3 мл) 1-(5-бромпиримидин-2-ил)пиперидин-4-она O-(2-гидроксиэтил)оксима, 125 мг (0,397 ммоль), синтезированного таким же образом, как в ссылочном примере 72, и пирролидин-2,5-диона, 58,2 мг (0,587 ммоль), и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли воду с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 144 мг (0,364 ммоль, выход 92%) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 396, 398[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,30 (s, 2H), 4,24-4,15 (m, 2H), 3,94-3,85 (m, 4H), 3,84-3,76 (m, 2H), 2,70 (s, 4H), 2,58-2,52 (m, 2H), 2,42-2,36 (m, 2H).
[0923] (Ссылочный пример 119-1)
1-[2-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этил]пирролидин-2-он (ссылочное соединение 119-1)

55% Гидрид натрия, 25 мг (0,57 ммоль), добавляли к раствору в DMF (3 мл) пирролидин-2-она, 48 мг (0,56 ммоль), и смесь перемешивали при комнатной температуре в течение 30 минут. Затем добавляли неочищенный продукт, 149 мг, синтезированный таким же образом, как в ссылочном примере 82-2, который включал в себя 2-({[1-(5-бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этилметансульфонат. Смесь перемешивали при комнатной температуре в течение 14 часов и при 60°C в течение 2 часов. Затем добавляли пирролидин-2-он, 16 мг (0,19 ммоль), и смесь перемешивали при 60°C в течение 1 часа. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор хлорида аммония с последующей экстракцией этилацетатом. Органический слой промывали рассолом, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: гексан:этилацетат) с получением указанного в заголовке соединения в количестве 100 мг (0,265 ммоль) в виде белого твердого вещества.
Масс-спектр (CI, m/z): 384, 386[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,31 (s, 2H), 4,21-4,14 (m, 2H), 3,94-3,86 (m, 4H), 3,62-3,53 (m, 2H), 3,50-3,41 (m, 2H), 2,66-2,58 (m, 2H), 2,44-2,35 (m, 4H), 2,06-1,98 (m, 2H).
[0924] (Ссылочный пример 119-2)
3-[2-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этил]оксазолидин-2-он (ссылочное соединение 119-2)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 119-1, за исключением того, что пирролидин-2-он заменяли на оксазолидин-2-он. В результате указанное в заголовке соединение (выход 57%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 384, 386[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,31 (s, 2H), 4,37-4,28 (m, 2H), 4,27-4,17 (m, 2H), 3,95-3,85 (m, 4H), 3,69-3,62 (m, 2H), 3,59-3,53 (m, 2H), 2,66-2,56 (m, 2H), 2,45-2,37 (m, 2H).
[0925] (Ссылочный пример 119-3)
4-[2-({[1-(5-Бромпиримидин-2-ил)пиперидин-4-илиден]амино}окси)этил]морфолин-3-он (ссылочное соединение 119-3)

Данную реакцию проводили с помощью способа, описанного в ссылочном примере 119-1, за исключением того, что пирролидин-2-он заменяли на морфолин-3-он, и температуру реакции изменяли на 40°C. В результате указанное в заголовке соединение (выход 76%) было получено в виде белого твердого вещества.
Масс-спектр (CI, m/z): 398, 400[М+1]+.
1H-ЯМР спектр (400 МГц, DMSO-d6) δ: 8,49 (s, 2H), 4,14-4,09 (m, 2H), 4,01 (s, 2H), 3,84-3,77 (m, 6H), 3,58-3,51 (m, 2H), 3,40-3,36 (m, 2H), 2,56-2,51 (m, 2H), 2,38-2,33 (m, 2H).
[0926] (Ссылочный пример 120)
1-{5-[2-Фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она O-фенилоксим (ссылочное соединение 120)
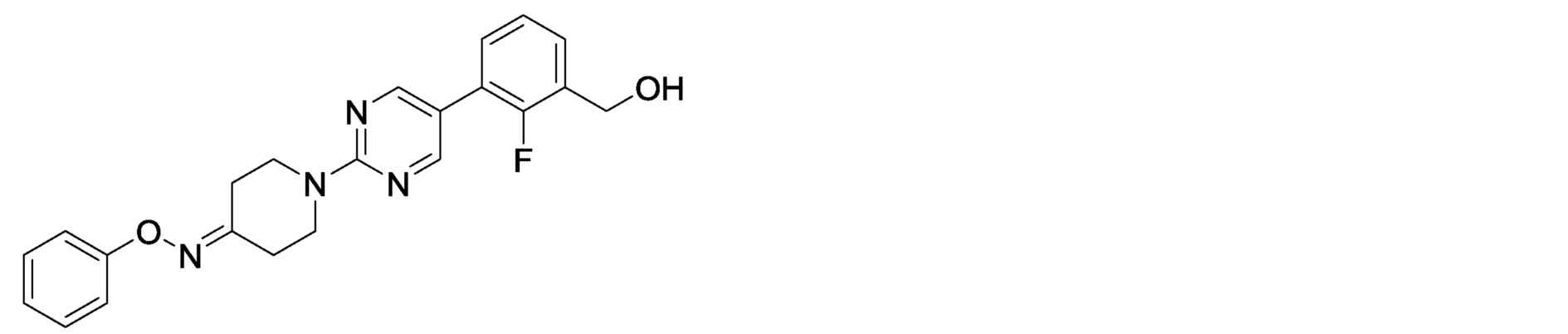
O-фенилгидроксиламина гидрохлорид, 36 мг (0,25 ммоль), добавляли к раствору в этаноле (1 мл) 1-{5-[2-фтор-3-(гидроксиметил)фенил]пиримидин-2-ил}пиперидин-4-она, 61 мг (0,20 ммоль), синтезированного таким же образом, как в ссылочном примере 7-50, и смесь перемешивали при комнатной температуре в течение 1 часа. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия с последующей экстракцией этилацетатом. Органический слой сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: 1,2-дихлорэтан: этилацетат) с получением указанного в заголовке соединения в количестве 61 мг (0,16 ммоль, выход 80%) в виде светло-желтого твердого вещества.
Масс-спектр (CI, m/z): 393[М+1]+.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,55 (d, J=1,5 Гц, 2H), 7,48-7,39 (m, 1H), 7,36-7,28 (m, 3H), 7,25-7,17 (m, 3H), 7,05-6,98 (m, 1H), 4,84(d, J=6,1 Гц, 2H), 4,12-4,05 (m, 4H), 2,93-2,88 (m, 2H), 2,65-2,59 (m, 2H), 1,83 (t, J=6,1 Гц, 1H).
[0927] (Ссылочный пример 121)
1-[5-(3-{[(трет-Бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она O-пиримидин-5-илоксим (ссылочное соединение 121)

Суспензию в толуоле (1 мл) 5-бромпиримидина, 42 мг (0,26 ммоль), 2-(ди-трет-бутилфосфино)-2',4',6'-триизопропил-3,6-диметокси-1,1'-бифенила, 13 мг (0,027 ммоль), димера хлорида аллилпалладия, 2,7 мг (0,0074 ммоль), и карбоната цезия, 0,12 г (0,37 ммоль), перемешивали при продувании аргоном, и добавляли 1-[5-(3-{[(трет-бутилдиметилсилил)окси]метил}-2-фторфенил)пиримидин-2-ил]пиперидин-4-она оксим, 109 мг (0,25 ммоль), синтезированный таким же образом, как в ссылочном примере 64. Смесь перемешивали при 65°C в течение 5 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия с последующей экстракцией этилацетатом. Органический слой промывали насыщенным водным раствором бикарбоната натрия, сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DIOL, растворитель для элюирования: 1,2-дихлорэтан: этилацетат) с получением указанного в заголовке соединения в количестве 74 мг (0,15 ммоль, выход 58%) в виде светло-желтого твердого вещества.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,91 (s, 1H), 8,68 (s, 2H), 8,56 (d, J=1,5 Гц, 2H), 7,53-7,46 (m, 1H), 7,30-7,20 (m, 2H), 4,86 (s, 2H), 4,15-4,07 (m, 4H), 2,94-2,87 (m, 2H), 2,66-2,59 (m, 2H), 0,96 (s, 9H), 0,14 (s, 6H).
[0928] (Ссылочный пример 122)
трет-Бутил-4-[(пиримидин-2-илокси)имино]пиперидин-1-карбоксилат (ссылочное соединение 122)

Карбонат цезия, 288 мг (0,882 ммоль), добавляли к раствору в DMF (1 мл) трет-бутил-4-(гидроксиимино)пиперидин-1-карбоксилата, 148 мг (0,689 ммоль), и 2-хлорпиримидина, 51,9 мг (0,453 ммоль), и смесь перемешивали при 85°C в течение 4 часов. После окончания реакции к реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия с последующей экстракцией этилацетатом. Органический слой сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве 37,1 мг (0,127 ммоль, выход 28%) в виде темно-коричневого твердого вещества.
1H-ЯМР спектр (400 МГц, CDCl3) δ: 8,63 (d, J=4,8 Гц, 2H), 7,08-7,04 (m, 1H), 3,69-3,49 (m, 4H), 2,95-2,85 (m, 2H), 2,71-2,52 (m, 2H), 1,49 (s, 9H).
[0929] (Ссылочный пример 123)
Пиперидин-4-она O-пиримидин-2-илоксим (ссылочное соединение 123)

2,6-Диметилпиридин, 28 мкл (0,24 ммоль), добавляли к раствору в метиленхлориде (1 мл) трет-бутил-4-[(пиримидин-2-илокси)имино]пиперидин-1-карбоксилата, 35 мг (0,12 ммоль), синтезированного таким же образом, как в ссылочном примере 122, и смесь перемешивали при комнатной температуре в течение 3 минут. Затем добавляли триметилсилила трифторметансульфонат, 33 мкл (0,18 ммоль), и смесь перемешивали при комнатной температуре в течение 17 часов. Затем добавляли 2,6-диметилпиридин, 42 мкл (0,36 ммоль), и триметилсилила трифторметансульфонат, 44 мкл (0,24 ммоль), и смесь перемешивали при комнатной температуре в течение 3 часов. После окончания реакции реакционную смесь концентрировали при пониженном давлении. Концентрированный остаток очищали с помощью колоночной хроматографии на силикагеле (силикагель DNH, растворитель для элюирования: этилацетат:метанол) с получением указанного в заголовке соединения в количестве (включая примеси) в виде темно-коричневого масла.
[0930] (Пример тестирования 1)
Тест ингибирования человеческого фермента VAP-1
Этот тест проводили путем модификации способа P. H. Yu et al. (Diabetologia 40 1243 (1997)). Человеческий фермент VAP-1 (R&D Systems, Inc.) предварительно инкубировали в 96-луночном планшете с соединением, растворенным в диметилсульфоксиде при комнатной температуре в течение 20 минут. Затем раствор доводили до конечного объема 200 мкл, реакционный раствор с ферментом инкубировали с14C-бензиламином (конечная концентрация 100 мкМ) при 37°C в течение 1 часа. Реакцию останавливали добавлением к реакционному раствору 100 мкл 2 М раствора лимонной кислоты. Окислительный продукт экстрагировали с помощью смеси толуол/этилацетат, и измеряли радиоактивность жидкостным сцинцилляционным счетчиком. Относительное ингибирование соединения рассчитывали с помощью следующего уравнения.
Относительное ингибирование={1 - [активность фермента VAP-1 после обработки соединением]/[активность фермента VAP-1 в присутствии только диметилсульфоксида без соединения]} × 100
[0931] В этом тесте соединения настоящего изобретения показали отличную активность ингибирования человеческого VAP-1. Например, относительное ингибирование на 50% или больше получали с помощью соединений, 30 нМ каждое, из примеров 1, 2, 3, 5, 6, 7, 8, 12, 20, 25, 36, 37, 41, 42, 43, 44, 45, 46, 47, 49, 50, 57, 60, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 85, 86, 87, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 107, 108, 110, 111, 112, 113, 114, 115, 116, 117, 118, 120, 122, 123, 124, 125, 126, 128, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 146, 147, 148, 150, 151, 152, 153, 154, 155, 156, 157, 159, 162, 164, 165, 166, 167, 168, 169, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 182, 183, 184, 185, 186, 187, 188, 189, 190, 191, 192, 193, 194, 195, 196, 197, 198, 199, 200, 201, 202, 203, 204, 205, 206, 207 и 208.
[0932] (Пример тестирования 2)
Тест ингибирования человеческого VAP-1 в плазме
Этот тест проводили путем модификации способа P. H. Yu et al. (Diabetologia 40 1243 (1997)). Человеческую кровь собирали от здорового донора в пробирку с гепарином и центрифугировали при 3000 об/мин и 4°C в течение 10 минут для получения плазмы. Плазму предварительно инкубировали в 96-луночном микропланшете с соединением, растворенным в диметилсульфоксиде, и паргилином (конечная концентрация 100 мкМ) при комнатной температуре в течение 20 минут. Затем раствор доводили до конечного объема 200 мкл, реакционный раствор с плазмой инкубировали с14C-бензиламином (конечная концентрация 50 мкМ) при 37°C в течение 1 часа. Реакцию останавливали добавлением к реакционному раствору 100 мкл 2 М раствора лимонной кислоты. Окислительный продукт экстрагировали с помощью смеси толуол/этилацетат, и измеряли радиоактивность жидкостным сцинцилляционным счетчиком. Относительное ингибирование соединения рассчитывали с помощью следующего уравнения.
Относительное ингибирование={1 - [активность VAP-1 после обработки соединением]/[активность VAP-1 в присутствии только диметилсульфоксида без соединения]} × 100
[0933] (Пример тестирования 3)
Тест ингибирования крысиного VAP-1 в плазме
Этот тест проводили путем модификации способа P. H. Yu et al. (Diabetologia 40 1243 (1997)). Кровь собирали у самцов крыс SD возраста 7-12-недель в пробирки с гепарином и центрифугировали при 3000 об/мин и 4°C в течение 10 минут для получения плазмы. Плазму предварительно инкубировали в 96-луночном микропланшете с соединением, растворенным в диметилсульфоксиде, и паргилином (конечная концентрация 100 мкМ) при комнатной температуре в течение 20 минут. Затем раствор доводили до конечного объема 200 мкл, реакционный раствор с плазмой инкубировали с14C-бензиламином (конечная концентрация 2,5 мкМ) при 37°C в течение 3 часов. Реакцию останавливали добавлением к реакционному раствору 100 мкл 2 М раствора лимонной кислоты. Окислительный продукт экстрагировали с помощью смеси толуол/этилацетат, и измеряли радиоактивность жидкостным сцинцилляционным счетчиком. Относительное ингибирование соединения рассчитывали с помощью следующего уравнения.
Относительное ингибирование={1 - [активность VAP-1 после обработки соединением]/[активность VAP-1 в присутствии только диметилсульфоксида без соединения]} × 100
[0934] (Пример тестирования 4)
(Ex vivo) тест ингибирования крысиного VAP-1 в плазме после перорального введения соединения
Соединение перорально вводили (0,3-10 мг/кг) самцам крыс SD возраста 7-12-недель не натощак. Под анестезией кровь собирали в пробирки с гепарином из яремной вены перед введением и через 3, 8 и 24 часа после введения. Кровь центрифугировали при 14000 об/мин в течение 10 минут для получения плазмы. Активность фермента VAP-1 в плазме измеряли с помощью радиохимического ферментного анализа.
Радиохимический ферментный анализ проводили путем модификации способа P. H. Yu et al. (Diabetologia 40 1243 (1997)). К полученной плазме добавляли14C-бензиламин (2,5 мкМ) и инкубировали при 37°C в течение 3 часов. Реакцию останавливали добавлением к реакционному раствору 100 мкл 2 М раствора лимонной кислоты. Окислительный продукт экстрагировали с помощью смеси толуол/этилацетат, и измеряли радиоактивность жидкостным сцинцилляционным счетчиком. Относительное ингибирование соединения рассчитывали с помощью следующего уравнения.
Относительное ингибирование={1 - [активность VAP-1 в плазме после введение соединения]/[активность VAP-1 в плазме перед введением]} × 100
В этом тесте соединения настоящего изобретения показали отличную активность ингибирования VAP-1. Например, относительное ингибирование на 50% или больше получали через 3 часа после введения соединений, в дозе 0,3 мг/кг каждое, из примеров 1, 2, 3, 5, 12, 20, 36, 37, 41, 42, 51, 53, 57, 60, 68, 69, 70, 72, 83, 85, 86, 87, 90, 91, 94, 95, 96, 97, 98, 99, 101, 102, 105, 133, 134, 141, 144, 149, 150, 151, 153, 154, 155, 156, 159, 165, 166, 167, 168, 169, 171, 173, 174, 175, 176, 177, 178, 182 и 183.
[0935] (Пример тестирования 5)
Влияние на альбуминурию диабетических крыс
Диабет индуцировали вызван внутривенной инъекцией стрептозотоцина (STZ) 50 мг/мл на кг в 2 мМ буферном растворе лимонной кислоты (pH 4,5) крысам SD возрастом 7-8 недель (вес 180-250 г). В то же время нормальным крысам вводили такое же количество 2 мМ буферного раствора лимонной кислоты (pH 4,5) в качестве контроля. Уровень глюкозы в крови измеряли способом ферментных электродов. На четвертый день после инъекции крыс с уровнем глюкозы в крови выше 350 мг/дл классифицировали как модель диабета. Соединение вводили ежедневно в течение 4 недель с дня инъекции STZ. После лечения с помощью соединения в течение 4 недель собирали мочу в течение 24 часов с помощью метаболической клетки, и измеряли концентрацию альбумина в моче.
[0936] (Пример тестирования 6)
Влияние на печень в моделях неалкогольного стеатогепатита (NASH)
Это исследование проводили с использованием мышей с моделью NASH/мышей с моделью STAM (зарегистрированный торговое наименование) (Medical Molecular Morphology 46 141 (2013)) от Stelic Institute & Co., Inc.
Мышей C57BL6J/JcL с беременностью четырнадцать дней (CLEA Japan, Inc.) кормили и давали им возможность родить. Двухдневным мышам подкожно вводили стрептозотоцин (SIGMA-ALDRICH JAPAN) в физиологическом растворе (Japanese Pharmacopoeia, Otsuka Pharmaceutical Co., Ltd.) один раз в их спины. После достижения возраста 4 недель мышей кормили диетой с высоким содержанием жиров (High Fat Diet 32 (стерилизовано облучением, CLEA Japan, Inc.) до конца эксперимента.
Соединение перорально вводили ежедневно с возраста 5 или 6 недель. В возрасте 9 или 11 недель животных умерщвляли под анестезией. Печени собирали и измеряли их вес во влажном состоянии. Из части печеней получали парафиновые срезы или замороженные срезы, их исследовали гистопатологически, и измеряли показатель активности NAFLD. Далее из части печеней экстрагировали РНК, и измеряли экспрессию маркерного гена фиброза с помощью метода количественной ПЦР. Результаты статистически анализировали с помощью EXSUS или Prism 4 (производства GraphPad Software).
[0937] (Пример тестирования 7)
Тест ингибирования цитотоксичности в человеческих нормальных гломерулярных эндотелиальных клетках микрососудов
Человеческие нормальные гломерулярные эндотелиальные клетки микрососудов высевали по 6000 клеток на лунку в 96-луночный культуральный планшет с коллагеновым покрытием. После одного дня культивирования среду в каждой лунке полностью удаляли аспирированием и заменяли на 50 мкл раствора соединения, разбавленного базальной средой. В контрольные лунки добавляли базальную среду, содержащую 0,1% DMSO. Затем планшет инкубировали в инкубаторе с CO2 в течение 30 минут. В каждую лунку отрицательного контроля (ингибирование 0%), а также лунку, содержащую соединение, добавляли пятьдесят микролитров 2 мМ метиламина, разбавленного базальной средой (конечная концентрация 1 мМ), и в каждую лунку положительного контроля (ингибирование 100%) добавляли 50 мкл базальной среды. Планшет инкубировали в инкубаторе с CO2 в течение 2 дней. В каждую лунку добавляли десять микролитров CCK-8, и смеси инкубировали в инкубаторе для планшетов при 37°C в течение приблизительно 2 часов после перемешивания с помощью встряхивателя для планшетов. Поглощение смесей на 450 нм измеряли с помощью мультпланшетного ридера. Относительное ингибирование цитотоксичности для соединения рассчитывали с помощью следующего уравнения.
Относительное ингибирование={[Среднее поглощение лунок, содержащих соединение] - [Среднее поглощение лунок с отрицательным контролем]}/{[Среднее поглощение лунок с положительным контролем] - [Среднее поглощение лунок с отрицательным контролем]} × 100
В этом тесте соединения настоящего изобретения показали отличный эффект ингибирования цитотоксичности в человеческих нормальных гломерулярных эндотелиальных клетках микрососудов. Например, относительное ингибирование на 50% или больше получали с помощью соединений, 100 нМ каждое, из примеров 1, 2, 3, 5, 36, 37, 95, 96, 102, 133, 134, 141 и 144.
[0938] (Пример тестирования 8)
Тест ингибирования цитотоксичности в человеческих нормальных эндотелиальных клетках подобных печеночному синусоиду микрососудов
Человеческие нормальные эндотелиальные клетки подобных печеночному синусоиду микрососудов высевали по 6000 клеток на лунку в 96-луночный культуральный планшет с коллагеновым покрытием. После одного дня культивирования среду в каждой лунке полностью удаляли аспирированием и заменяли на 50 мкл раствора соединения, разбавленного базальной средой. В контрольные лунки добавляли базальную среду, содержащую 0,1% DMSO. Затем планшет инкубировали в инкубаторе с CO2 в течение 30 минут. В каждую лунку отрицательного контроля (ингибирование 0%), а также лунку, содержащую соединение, добавляли пятьдесят микролитров 2 мМ метиламина, разбавленного базальной средой (конечная концентрация 1 мМ), и в каждую лунку положительного контроля (ингибирование 100%) добавляли 50 мкл базальной среды. Планшет инкубировали в инкубаторе с CO2 в течение 2 дней. В каждую лунку добавляли десять микролитров CCK-8, и смеси инкубировали в инкубаторе для планшетов при 37°C в течение приблизительно 2 часов после перемешивания с помощью встряхивателя для планшетов. Поглощение смесей на 450 нм измеряли с помощью мультпланшетного ридера. Относительное ингибирование цитотоксичности для соединения рассчитывали с помощью следующего уравнения.
Относительное ингибирование={[Среднее поглощение лунок, содержащих соединение] - [Среднее поглощение лунок с отрицательным контролем]}/{[Среднее поглощение лунок с положительным контролем] - [Среднее поглощение лунок с отрицательным контролем]} × 100
В этом тесте соединения настоящего изобретения показали отличный эффект ингибирования цитотоксичности в человеческих нормальных гломерулярных эндотелиальных клетках микрососудов. Например, относительное ингибирование на 50% или больше получали с помощью соединений, 300 нМ каждое, из примеров 1, 2, 3, 5, 36, 37, 95, 96, 102, 133, 134, 141 и 144.
[0939] (Пример тестирования 9)
Фармакокинетическое (PK) исследование на крысах (концентрация соединения в плазме после перорального введения)
Крысам SD возрастом от семи до восьми недель (вес 180-250 г) перорально вводили суспензию соединения в 0,5 вес/об% растворе метилцеллюлозы 400. Под анестезией кровь собирали из яремной вены в пробирки с ЭДТА через 0,25, 0,5, 1, 2, 4, 6, 8 и 24 часа после введения соединения. Кровь центрифугировали при 4°C и 6000 g в течение 3 минут с получением плазмы. К плазме добавляли ацетонитрил, и смесь перемешивали с помощью встряхивателя при 750 об/мин в течение 3 минут и депротеинизировали центрифугированием при 3700 об/мин в течение 2 минут. Полученный таким образом образец анализировали с помощью ЖХ/МС в следующих условиях.
Концентрацию соединения в плазме в каждый момент забора крови определяли по методу внутреннего стандарта, и все AUC (площадь под кривой) рассчитывали по методу трапеций.
Для измерения использовали следующие системы ЖХ и МС.
ЖХ: CBM 30 series производства Shimadzu Corporation
Колонка: Phenomenex Kinetex C18 (50×2,1 мм, 2,6 мкм)
Температура колонки: 40°C
Скорость потока: 0,3 мл/мин
Мобильная фаза A: 0,1% водный раствор муравьиной кислоты, мобильная фаза B: 0,1% муравьиная кислота, 50% смесь ацетонитрил/метанол
Градиент: 0-2 минуты: A/B=от 90/10 до 10/90, 2-3 минуты: A/B=10/90, 3-3,01 минуты: A/B=от 10/90 до 90/10
МС: 3200 производства SCIEX
Ионизация: ESI
Режим: положительный
В данном исследовании соединения настоящего изобретения показали отличную PK. Например, 1000 нг·ч/мл или большую AUC получали с помощью соединений из примеров 1, 36, 37, 95, 96 и 102 в дозе 3 мг/кг.
[Промышленная применимость]
[0940] Соединения настоящего изобретения общей формулы (I) или их фармакологически приемлемые соли обладают высокой активностью ингибирования VAP-1 и отличными фармакокинетическими характеристиками, и поэтому они полезны для лечения заболеваний, предотвращаемых, облегчаемых и/или излечиваемых с помощью ингибирования VAP-1, типичными представителями которых являются неалкогольные жировые болезни печени, такие как неалкогольный стеатогепатит; воспалительные заболевания, такие как атопический дерматит и псориаз; диабетические осложнения, такие как диабетическая невропатия, диабетическая ретинопатия (в частности, диабетический макулярный отек) и диабетическая нефропатия; заболевания сосудов, такие как атеросклероз; заболевания сердца, такие как инфаркт миокарда; и метаболические нарушения, такие как ожирение.
Реферат
Изобретение относится к соединению формулы (I)в котором R1 представляет собой: атом водорода, C1-C6алкильную группу, необязательно замещенную атомом(-ами) дейтерия, атомом(-ами) галогена, группой(-ами) -OR13, -NR15R16, -COOR14, циано, -CONR11R12или -S(O)nR17, C3-C8циклоалкильную группу, необязательно замещенную -OR13, C1-C6алкокси-C1-C6алкильную группу, необязательно замещенную -OR13, -CONR11R12, 4-6-членную гетероциклильную группу, содержащую 1-2 атома азота или атом кислорода в кольце, необязательно замещенную C1-C6алкильной группой, C1-C6алкокси-C1-C6алкильной группой, галоген-C1-C6алкильной группой, бензильной группой, C1-C7ацильной группой, -COOR14, R13O-C1-C6алкильной группой, -S(O)nR17, 4-6-членную гетероциклил-C1-C6алкильную группу, содержащую 1-2 гетероатома в кольце, выбранных из атома азота и кислорода, необязательно замещенную атомом галогена, C1-C6алкильной группой, C1-C7ацильной группой, оксогруппой или защитной группой, выбранной из тетрагидропиранила, бензильную группу, необязательно замещенную C1-C6алкоксигруппой; и X представляет N или C-R2, причем R2представляет собой: атом водорода, атом галогена, C1-C6алкильную группу, необязательно замещенную атомом галогена или C1-C6алкоксигруппой, C3-C8циклоалкильную группу, C1-C6алкоксигруппу или цианогруппу; p и q, независимо друг от друга, представляют натуральное число от 1 до 3 при условии, что сумма p и q представляет собой натуральное число от 2 до 4; R11и R12независимо представляют собой атом водорода или C1-C6алкильную группу; R13представляет собой атом водорода, C1-C7ацильную группу или защитную группу, выбранную из тетрагидропиранила; R14представляет собой атом водорода или C1-C6алкильную группу; R15и R16независимо представляют собой атом водорода, C1-C6алкильную группу, бензильную группу, C1-C7ацильную группу или -S(O)nR17; R17представляет собой C1-C6алкильную группу; и n представляет собой 2; или его фармакологически приемлемой соли, которое является ингибитором VAP-1. 16 н. и 18 з.п. ф-лы, 75 табл., 122 пр.
Формула
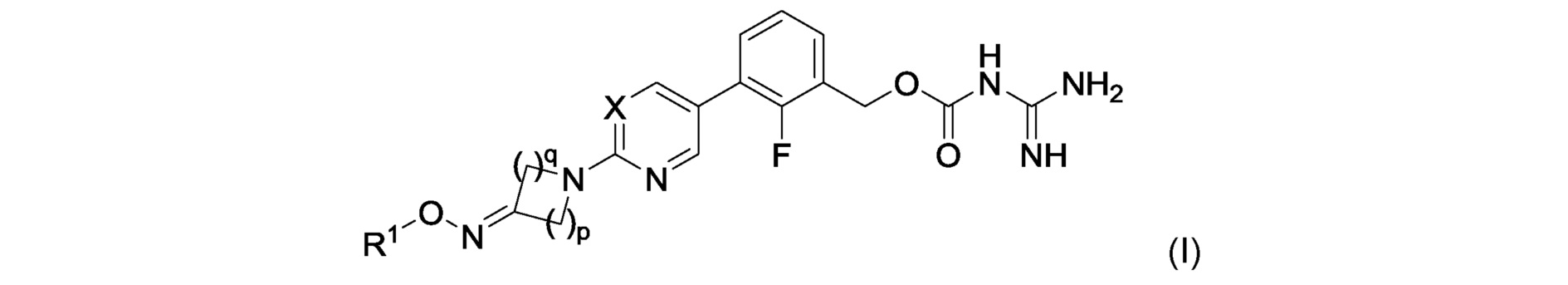


Документы, цитированные в отчёте о поиске
Новые аналоги пиридина

Комментарии