Композиция противораковой вакцины, содержащая пептид wt1, для трансдермального введения - RU2685933C2
Код документа: RU2685933C2
Чертежи




Описание
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к противораковой вакцине для трансдермального введения, содержащей пептид WT1 и/или модифицированный пептид WT1 и стимулятор индукции клеточного иммунитета.
УРОВЕНЬ ТЕХНИКИ
Существует противораковая вакцина, которая предотвращает вирусную инфекцию, тем самым предотвращая развитие злокачественной опухоли, вызванное вирусом, и противораковая вакцина, которая приводит к такому результату, что злокачественные клетки подвергаются специфичной атаке иммунной системой за счет распознавания специфичного для злокачественной опухоли антигена иммунным механизмом, в частности клеточным иммунным механизмом, в котором важную роль играют цитотоксические T-клетки (CTL). Первая совсем не эффективна в случае злокачественной опухоли, в которой вирус не принимает участия. Последняя позволяет осуществлять терапию злокачественной опухоли, основанную на целенаправленном воздействии на антиген, которым обладает сама злокачественная клетка. Полагают, что последняя эффективна против широкого круга злокачественных опухолей, имеющих антиген, за счет точного определения антигена. Наряду с прочим, противораковой вакциной, основанная на принципах последней вакцины, можно лечить опухоли, которые трудно удалять посредством хирургической операции из-за их размера, и она вызывает меньше побочных эффектов по сравнению с обычной терапией, такой как химиотерапия и лучевая терапия.
Ген WT1 (опухоли Вильмса 1) сверхэкспрессируется во многих гематопоэтических опухолях и солидных злокачественных опухолях, например, при остром миелоцитарном лейкозе, остром лимфоцитарном лейкозе, хроническом миелоцитарном лейкозе, миелодиспластическом синдроме, множественной миеломе, неходжкинской лимфоме, раке легких, раке молочной железы, раке желудка, раке толстой/прямой кишки, раке поджелудочной железы, раке желчных протоков, плоскоклеточном раке головы и шеи, раке щитовидной железы, раке почек, раке простаты, раке яичника, раке матки, саркоме мягких тканей и костей, злокачественной меланоме, злокачественной мезотелиоме, опухоли половых клеток яичка и злокачественной глиоме. Такие злокачественные опухоли сверхпродуцируют белок WT1. Белок WT1 фрагментируется в злокачественной опухоли с образованием неполных пептидов, состоящих из 8-12 аминокислот. Пептид WT1 является одним из пептидных фрагментов, который был связан с молекулой MHC класса I в злокачественной клетке, перемещен к поверхности злокачественной клетки и презентирован в виде антигена, связанного с молекулой MHC класса I на поверхности злокачественной клетки. Пептид WT1 становится маркером злокачественной клетки. Аминокислотная последовательность пептида WT1 соответствует типу молекулы MHC класса I клетки. Например, в случае клетки, имеющей MHC HLA-A*0201-типа, образуется пептид WT1, ограниченный MHC HLA-A*0201-типа, такой как пептид Db126, состоящий из 9 аминокислот, а в случае клетки, имеющей MHC HLA-A*2402-типа, образуется пептид WT1, ограниченный MHC HLA-A*2402-типа, такой как пептид Db235, состоящий из 9 аминокислот. В случае клетки, имеющей другой MHC, такой как MHC HLA-A26-типа (WO 2005/095598), HLA-A*3303-типа (WO 2007/097358) или HLA-A*1101-типа (WO 2008/081701), образуется пептид WT1, ограниченный по каждому из указанных типов MHC. Когда пептид WT1 или модифицированный пептид WT1, в котором часть аминокислот пептида WT1 заменена или модифицирована, вводят в живой организм в качестве антигена (в данном случае пептид WT1 или модифицированный пептид WT1, который вводят в качестве антигена, называют «антигенным пептидом WT1»), антигенный пептид WT1 связывается с молекулой MHC класса на поверхности дендритной клетки, которая является антигенпрезентирующей клеткой, или антигенный пептид WT1 захватывается дендритной клеткой, связывается с молекулой MHC класса I дендритной клетки и затем перемещается к поверхности дендритной клетки, и таким образом презентируется в виде антигена, связанного с молекулой MHC класса I, на поверхности дендритной клетки. Активированная дендритная клетка, имеющая комплекс антигенный пептид WT1/молекула MHC класса, перемещается в регионарный лимфатический узел и активирует CD8-позитивный T-лимфоцит, который распознает комплекс антигенный пептид WT1/молекула MHC класса I, при этом происходит дифференцировка и пролиферация клетки в цитотоксическую T-клетку (CTL). CTL распознает опухолевые клетки, имеющие комплекс пептида WT1 (полученного из эндогенного белка WT1) с такой же аминокислотной последовательностью, как и у антигенного пептида WT1, и молекулы MHC класса I, или опухолевую клетку, имеющую комплекс пептида WT1 (полученного из эндогенного белка WT1) с аминокислотной последовательностью, обладающей перекрестной иммунореактивностью с антигенным пептидом WT1, и молекулы MHC класса I, и атакует распознаваемые опухолевые клетки. Таким образом, указанные выше различные MHC-ограниченные пептиды WT1, такие как пептид Db126 и пептид Db235, и модифицированные пептиды WT1, в которых часть аминокислот заменена или модифицирована, применимы в качестве противораковых вакцин (непатентный документ 1).
Также известно, что адъювант используют для того, чтобы усилить действие пептида WT1 и/или модифицированного пептида WT1 в качестве противораковой вакцины. В качестве адъюванта для пептида WT1 и/или модифицированного пептида WT1 известны, например, минеральные гели, такие как гидроксид алюминия; поверхностно-активные вещества, такие как лизолецитин, и полиолы типа плюроников; полианионы; пептиды; или масляные эмульсии (патентный документ 1), и GM-CSF, BCG-CWS и монтанид ISA51 (непатентный документ 1). В дополнение к указанному было известно множество вакцинных адъювантов, включая циклические динуклеотидные аналоги (патентный документ 3 и патентный документ 4), такие как 1H-имидазо[4,5-c]хинолин-4-амин, имихимод (патентный документ 2) и циклический ди-GMP (c-ди-GMP) и лиганды TLR2, 3, 7, 8 и 9 (патентный документ 5). Кроме того, также известно, что иммунитет, индуцированный трансдермальным введением пептида, содержащего имихимод, дополнительно усиливается добавлением пептида-25 (непатентный документ 2).
В общем, вакцины вводят посредством подкожной или интрадермальной инъекции. В дополнение к указанным путям было проведено испытание индукции иммунитета с использованием различных путей введения, например, трансдермального введения (патентный документ 5 и непатентный документ 2), буккального введения, назального введения и подъязычного введения (непатентный документ 3, патентный документ 6 и патентный документ 7).
СПИСОК ДОКУМЕНТОВ
[патентный документ 1] патент Японии №4422903;
[патентный документ 2] JP 7-505883 A;
[патентный документ 3] JP 2007-529531 A;
[патентный документ 4] публикация заявки на выдачу патента США № 2008/0286296;
[патентный документ 5] публикация заявки на выдачу патента США № 2008/0193487;
[патентный документ 6] JP 2002-531415 A;
[патентный документ 7] публикация заявки на выдачу патента США № 2008/0112974.
[Непатентные документы]
[непатентный документ 1] Yoshihiro Oka et al., Current Opinion in Immunology, 20: 211-220 (2008);
[непатентный документ 2] Hosoi Akihiro et al., Cancer Research, 68, 3941-3949 (2008);
[непатентный документ 3] Zhengrong Cui et al., Pharmaceutical Research, Vol. 19, № 7, 947-953 (2002).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Хорошо известно, что адъювант применяют для усиления эффективности вакцины. Подходящие адъюванты обычно варьируют, например, в зависимости от вида антигена, пути введения и иммунного ответа, который требуется индуцировать (т.е. клеточного иммунитета или гуморального иммунитета). Кроме того, в дополнение к адъюванту существует множество веществ, которые стимулируют индукцию иммунитета. Таким образом, целью настоящего изобретения является получение композиции для применения в качестве противораковой вакцины с более высокой эффективностью и удобной для применения.
Микроорганизм или вирус сами по себе или их часть входят в состав широко применяемой вакцины, и вакцину вводят для индукции иммунного ответа. Обычно в связи с тем что инвазии микроорганизма или вируса препятствует кожа вследствие их размера, необходимо инвазивное введение вакцины в организм. Поэтому вакцины обычно вводят посредством инъекции. Однако инъекция имеет несколько проблем, включая боль, страх, след на месте инъекции и последующее рубцевание. Другим людям, не являющимся медицинскими работниками, не разрешено осуществлять инъекцию. Интрадермальная инъекция, которая может вызывать более сильный иммунный ответ, является трудным способом введения. Существует риск случайной инфекции медицинских работников вследствие повреждения в результате укола иглой. Пациенты вынуждены много раз посещать лечебное учреждение, когда введение осуществляют многократно. Образуются медицинские отходы, которые требуют специальной утилизации, такие как иглы для инъекций. С точки зрения указанных выше проблем инъекция не является обязательным оптимальным путем введения.
Пептид WT1 и/или модифицированный пептид WT1 может активировать CTL (цитотоксические T-клетки) посредством молекулы MHC класса I, то есть, пептид может индуцировать клеточный иммунитет. Пептид WT1 и/или модифицированный пептид WT1 представляет собой молекулу, имеющую молекулярную массу примерно от 700 до примерно 1600, и состоящую из 8-12 аминокислот, и имеющую значительно меньшие размеры, чем сами микроорганизмы или вирусы, хотя они не считаются низкомолекулярным веществом. Возможно, что их можно вводить другим путем, отличным от инъекции. Однако препарат для введения пептидной вакцины другим путем, отличным от инъекции, еще не был разработан. Это обусловлено многими причинами, например: подходящее вещество, которое может стимулировать индукцию клеточного иммунитета, не было известно; также было неизвестно, может ли быть доставлен антиген в ткань, подходящую для индукции клеточного иммунитета. В частности, вещество, которое может стимулировать индукцию клеточного иммунитета, которое можно применять вместе с антигеном при введении другим путем, отличным от инъекции, не было известно.
Было обнаружено, что при трансдермальном введении можно получить эффект индукции клеточного иммунитета, который эквивалентен или превышает такой эффект при инъекции. Поэтому проводили поиски вещества, подходящего для индукции клеточного иммунитета при трансдермальном введении пептида WT1 и/или модифицированного пептида WT1 и в результате было обнаружено, что применение фармакологически приемлемой кислоты или ее фармакологически приемлемая соли является наиболее приемлемым. Кроме того, было обнаружено, что подходящим является совместное использование фармакологически приемлемой кислоты с одним или несколькими видами стимуляторов индукции клеточного иммунитета, выбранных из группы, состоящей из лиганда TLR, циклического динуклеотида, хелперного пептида, иммуномодулирующего низкомолекулярного лекарственного средства, ингибитора циклооксигеназы, антагониста рецептора простагландина, агониста рецептора простагландина, ингибитора продукции TSLP, ингибитора аденилатциклазы, омега-3 жирной кислоты, агониста PPAR, антагониста рецептора дофамина, агониста рецептора дофамина, агониста рецептора гистамина, антагониста рецептора гистамина, агониста рецептора серотонина, антагониста рецептора серотонина, антагониста рецептора вазопрессина, агониста рецептора вазопрессина, антагониста мускаринового рецептора, агониста мускаринового рецептора, антагониста рецептора адреналина, агониста рецептора адреналина, агониста рецептора ангиотензина, агониста рецептора ГАМК, антагониста рецептора тромбина, агониста рецептора тромбина, агониста опиоидного рецептора, агониста рецептора АДФ, антагониста рецептора лейкотриена, агониста рецептора лейкотриена, агониста рецептора мелатонина, агониста рецептора соматостатина, агониста рецептора каннабиноида, агониста рецептора сфингозин-1-фосфата, агониста метаботропного рецептора глутамата, ингибитора фосфолипазы A2, ингибитора продукции TGF-β и ингибитора цитокина Th2. В особенно применимом аспекте клеточный иммунитет заметно усиливается сочетанием фармакологически приемлемой кислоты и лиганда TLR, или сочетанием фармакологически приемлемой кислоты, лиганда TLR и хелперного пептида. Кроме того, было обнаружено, что при введении в условиях слабого раздражения получают высокий эффект в отношении индукции клеточного иммунитета. В частности, высокий эффект в отношении индукции клеточного иммунитета получают в случае выбора условия слабого раздражения, когда трансэпидермальная потеря влаги (TEWL) (г/час⋅м2), которая является показателем для кожи модельного животного при оценке раздражения кожи, перед введением композиции противораковой вакцины для трансдермального введения составляет 50 или меньше, и введения композиции противораковой вакцины для трансдермального введения. Альтернативно высокий эффект в отношении индукции клеточного иммунитета также получают, придавая композиции противораковой вакцины для трансдермального введения свойство такого слабого раздражения кожи, так что уровень TSLP в коже (пг/мг белка) у модельного животного в случае оценки раздражения кожи при осуществлении введения становится равным 10000 или меньше.
Таким образом, настоящее изобретение в первом аспекте относится к аспектам, перечисленным ниже:
(1) Композиция противораковой вакцины для трансдермального введения для индукции клеточного иммунитета, содержащая:
(i) пептид WT1 и/или модифицированный пептид WT1; и
(ii) фармакологически приемлемую кислоту в качестве первого стимулятора индукции клеточного иммунитета или ее фармакологически приемлемую соль.
(2) Композиция противораковой вакцины для трансдермального введения по п. (1), где фармакологически приемлемая кислота или ее фармакологически приемлемая соль представляют собой органическую кислоту или ее фармакологически приемлемую соль.
(3) Композиция противораковой вакцины для трансдермального введения по п. (2), где органическая кислота или ее фармакологически приемлемая соль представляют собой органическое соединение, содержащее карбоксильную группу, или органическое соединение, содержащее сульфонатную группу, или ее фармакологически приемлемая соль.
(4) Композиция противораковой вакцины для трансдермального введения по п. (2), где органическая кислота или ее фармакологически приемлемая соль является насыщенной или ненасыщенной жирной кислотой с прямой или разветвленной цепью, в которой насыщенная часть прямой цепи имеет от 8 до 20 атомов углерода, молочной кислотой, яблочной кислотой, салициловой кислотой, малеиновой кислотой, лимонной кислотой, или органическим соединением, содержащим сульфонатную группу, или ее фармакологически приемлемой солью.
(5) Композиция противораковой вакцины для трансдермального введения по п. (2), где органическая кислота или ее фармакологически приемлемая соль является жирной кислотой, выбранной из группы, состоящей из декановой кислоты, лауриновой кислоты, миристиновой кислоты, изостеариновой кислоты и олеиновой кислоты или молочной кислоты, салициловой кислоты, лимонной кислоты или метансульфоновой кислоты, или их фармакологически приемлемой соли.
(6) Композиция противораковой вакцины для трансдермального введения по любому из пп. (1)-(5), дополнительно содержащая второй стимулятор индукции клеточного иммунитета, выбранный из лиганда TLR, циклического динуклеотида, хелперного пептида, иммуномодулирующего низкомолекулярного лекарственного средства, ингибитора циклооксигеназы, антагониста рецептора простагландина, агониста рецептора простагландина, ингибитора продукции TSLP, ингибитора аденилатциклазы, омега-3 жирной кислоты, агониста PPAR, антагониста рецептора дофамина, агониста рецептора дофамина, агониста рецептора гистамина, антагониста рецептора гистамина, агониста рецептора серотонина, антагониста рецептора серотонина, антагониста рецептора вазопрессина, агониста рецептора вазопрессина, антагониста мускаринового рецептора, агониста мускаринового рецептора, антагониста рецептора адреналина, агониста рецептора адреналина, агониста рецептора ангиотензина, агониста рецептора ГАМК, антагониста рецептора тромбина, агониста рецептора тромбина, агониста опиоидного рецептора, агониста рецептора АДФ, антагониста рецептора лейкотриена, агониста рецептора лейкотриена, агониста рецептора мелатонина, агониста рецептора соматостатина, агониста рецептора каннабиноида, агониста рецептора сфингозин-1-фосфата, агониста метаботропного рецептора глутамата, ингибитора фосфолипазы A2, ингибитора продукции TGF-β и ингибитора цитокина Th2 и сочетания двух или более указанных видов.
(7) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является лиганд TLR.
(8) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является циклический динуклеотид.
(9) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является иммуномодулирующее низкомолекулярное лекарственное средство.
(10) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является ингибитор циклооксигеназы.
(11) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является антагонист рецептора простагландина, и кроме того, антагонист рецептора простагландина представляет собой антагонист рецептора EP2, антагонист рецептора EP4, антагонист рецептора DP или антагонист рецептора IP.
(12) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора простагландина, и кроме того, агонист рецептора простагландина представляет собой агонист рецептора EP3.
(13) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является ингибитор продукции TSLP.
(14) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является ингибитор аденилатциклазы.
(15) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является омега-3 жирная кислота.
(16) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист PPAR, и кроме того, агонист PPAR представляет собой агонист PPAR-α, агонист PPAR-δ или агонист PPAR-γ.
(17) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является антагонист рецептора дофамина, и кроме того, антагонист рецептора дофамина представляет собой антагонист рецептора D1 или антагонист рецептора D5.
(18) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора дофамина, и кроме того, агонист рецептора дофамина представляет собой агонист рецептора D2, агонист рецептора D3 или агонист рецептора D4.
(19) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является антагонист рецептора гистамина, и кроме того, антагонист рецептора гистамина представляет собой антагонист рецептора H1 или антагонист рецептора H2.
(20) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора гистамина, и кроме того, агонист рецептора гистамина представляет собой агонист рецептора H1, агонист рецептора H3 или агонист рецептора H4.
(21) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является антагонист рецептора серотонина, и кроме того, антагонистом рецептора серотонина является антагонист рецептора 5-HT2, антагонист рецептора 5-HT4, антагонист рецептора 5-HT6 или антагонист рецептора 5-HT7.
(22) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора серотонина, и кроме того, агонист рецептора серотонина представляет собой агонист рецептора 5-HT1 или агонист рецептора 5-HT2.
(23) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является антагонист рецептора вазопрессина, и кроме того, антагонист рецептора вазопрессина представляет собой антагонист рецептора V2.
(24) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора вазопрессина, и кроме того, агонист рецептора вазопрессина представляет собой агонист рецептора V1.
(25) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является антагонист мускаринового рецептора, и кроме того, антагонист мускаринового рецептора представляет собой антагонист рецептора M1, антагонист рецептора M3 или антагонист рецептора M5.
(26) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист мускаринового рецептора, и кроме того, агонист мускаринового рецептора представляет собой агонист рецептора M1, агонист рецептора M2, агонист рецептора M3, агонист рецептора M4 или агонист рецептора M5.
(27) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является антагонист рецептора адреналина, и кроме того, антагонист рецептора адреналина представляет собой антагонист рецептора α1, антагонист рецептора β1, антагонист рецептора β2 или антагонист рецептора β3.
(28) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора адреналина, и кроме того, агонист рецептора адреналина представляет собой агонист рецептора α1 или агонист рецептора α2.
(29) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора ангиотензина, и кроме того, агонист рецептора ангиотензина представляет собой агонист рецептора AT2.
(30) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора ГАМК и кроме того, агонист рецептора ГАМК представляет собой агонист рецептора ГАМКВ.
(31) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является антагонист рецептора тромбина, и кроме того, антагонист рецептора тромбина представляет собой антагонист рецептора PAR-1.
(32) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора тромбина, и кроме того, агонист рецептора тромбина представляет собой агонист рецептора PAR-1.
(33) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист опиоидного рецептора.
(34) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является антагонист рецептора лейкотриена, и кроме того, антагонист рецептора лейкотриена представляет собой антагонист рецептора CysLT1 или антагонист рецептора CysLT2.
(35) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора лейкотриена, и кроме того, агонист рецептора лейкотриена представляет собой агонист рецептора BLT.
(36) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора мелатонина.
(37) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора соматостатина.
(38) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора каннабиноида.
(39) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора сфингозин-1-фосфата.
(40) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист метаботропного рецептора глутамата, и кроме того, агонист метаботропного рецептора глутамата представляет собой агонист рецептора mGluR2, агонист рецептора mGluR3, агонист рецептора mGluR4, агонист рецептора mGluR6, агонист рецептора mGluR7 или агонист рецептора mGluR8.
(41) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является агонист рецептора АДФ.
(42) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является ингибитор фосфолипазы A2.
(43) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является ингибитор продукции TGF-β.
(44) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является ингибитор цитокина Th2.
(45) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является хелперный пептид.
(46) Композиция противораковой вакцины для трансдермального введения по п. (6), где вторым стимулятором индукции клеточного иммунитета является сочетание одного или нескольких видов, выбранных из группы, состоящей из лиганда TLR, циклического динуклеотида, иммуномодулирующего низкомолекулярного лекарственного средства, ингибитора циклооксигеназы, антагониста рецептора простагландина, агониста рецептора простагландина, ингибитора продукции TSLP, ингибитора аденилатциклазы, омега-3 жирной кислоты, агониста PPAR, антагониста рецептора дофамина, агониста рецептора дофамина, агониста рецептора гистамина, антагониста рецептора гистамина, агониста рецептора серотонина, антагониста рецептора серотонина, антагониста рецептора вазопрессина, агониста рецептора вазопрессина, антагониста мускаринового рецептора, агониста мускаринового рецептора, антагониста рецептора адреналина, агониста рецептора адреналина, агониста рецептора ангиотензина, агониста рецептора ГАМК, антагониста рецептора тромбина, агониста рецептора тромбина, агониста опиоидного рецептора, агониста рецептора АДФ, антагониста рецептора лейкотриена, агониста рецептора лейкотриена, агониста рецептора мелатонина, агониста рецептора соматостатина, агониста рецептора каннабиноида, агониста рецептора сфингозин-1-фосфата, агониста метаботропного рецептора глутамата, ингибитора фосфолипазы A2, ингибитора продукции TGF-β и ингибитора цитокина Th2 с хелперным пептидом.
(47) Композиция противораковой вакцины для трансдермального введения по любому из пп. (1)-(46), которая имеет форму препарата в форме крема.
(48) Композиция противораковой вакцины для трансдермального введения по любому из пп. (1)-(46), которая имеет форму жидкого препарата.
(49) Композиция противораковой вакцины для трансдермального введения по любому из пп. (1)-(48), которую вводят в условиях слабого раздражения.
(50) Композиция противораковой вакцины для трансдермального введения по п. (49), где условие слабого раздражения представляет собой условие, при котором трансэпидермальная потеря влаги (TEWL) перед введением модельному животному в случае оценки раздражения кожи составляет 50 г/час⋅м2 или меньше.
(51) Композиция противораковой вакцины для трансдермального введения по п. (49) или (50), где условие слабого раздражения представляет собой условие, при котором уровень TSLP кожи при осуществлении введения модельному животному в случае оценки раздражения кожи составляет 10000 пг/мг белка или меньше.
В другом аспекте противораковую вакцину согласно настоящему изобретению можно применять для лечения или профилактики злокачественной опухоли. Таким образом, настоящее изобретение также относится к перечисленным ниже аспектам:
(52) Способ лечения или профилактики злокачественной опухоли, включающий в себя трансдермальное введение субъекту терапевтически эффективного количества (i) пептида WT1 и/или модифицированного пептида WT1, и (ii) фармакологически приемлемой кислоты или ее фармакологически приемлемой соли.
(53) Способ лечения или профилактики злокачественной опухоли, включающий в себя трансдермальное введение субъекту терапевтически эффективного количества (i) пептида WT1 и/или модифицированного пептида WT1, (ii) фармакологически приемлемой кислоты в качестве первого стимулятора индукции клеточного иммунитета или ее фармакологически приемлемой соли, и (iii) второго стимулятора индукции клеточного иммунитета, выбранного из лиганда TLR, циклического динуклеотида, хелперного пептида, иммуномодулирующего низкомолекулярного лекарственного средства, ингибитора циклооксигеназы, антагониста рецептора простагландина, агониста рецептора простагландина, ингибитора продукции TSLP, ингибитора аденилатциклазы, омега-3 жирной кислоты, агониста PPAR, антагониста рецептора дофамина, агониста рецептора дофамина, агониста рецептора гистамина, антагониста рецептора гистамина, агониста рецептора серотонина, антагониста рецептора серотонина, антагониста рецептора вазопрессина, агониста рецептора вазопрессина, антагониста мускаринового рецептора, агониста мускаринового рецептора, антагониста рецептора адреналина, агониста рецептора адреналина, агониста рецептора ангиотензина, агониста рецептора ГАМК, антагониста рецептора тромбина, агониста рецептора тромбина, агониста опиоидного рецептора, агониста рецептора АДФ, антагониста рецептора лейкотриена, агониста рецептора лейкотриена, агониста рецептора мелатонина, агониста рецептора соматостатина, агониста рецептора каннабиноида, агониста рецептора сфингозин-1-фосфата, агониста метаботропного рецептора глутамата, ингибитора фосфолипазы A2, ингибитора продукции TGF-β, ингибитора цитокина Th2 и сочетания двух или более указанных видов.
(54) Способ лечения или профилактики злокачественной опухоли, включающий в себя введение субъекту терапевтически эффективного количества композиции противораковой вакцины для трансдермального введения по любому из пп. (1)-(51).
(55) Фармакологически приемлемая кислота или ее фармакологически приемлемая соль для применения в качестве стимулятора индукции клеточного иммунитета в случае трансдермального введения пептида WT1 и/или модифицированного пептида WT1; и
(56) Сочетание (i) фармакологически приемлемой кислоты или ее фармакологически приемлемой соли и (ii) одного или нескольких видов веществ, выбранных из группы, состоящей из лиганда TLR, циклического динуклеотида, хелперного пептида, иммуномодулирующего низкомолекулярного лекарственного средства, ингибитора циклооксигеназы, антагониста рецептора простагландина, агониста рецептора простагландина, ингибитора продукции TSLP, ингибитора аденилатциклазы, омега-3 жирной кислоты, агониста PPAR, антагониста рецептора дофамина, агониста рецептора дофамина, агониста рецептора гистамина, антагониста рецептора гистамина, агониста рецептора серотонина, антагониста рецептора серотонина, антагониста рецептора вазопрессина, агониста рецептора вазопрессина, антагониста мускаринового рецептора, агониста мускаринового рецептора, антагониста рецептора адреналина, агониста рецептора адреналина, агониста рецептора ангиотензина, агониста рецептора ГАМК, антагониста рецептора тромбина, агониста рецептора тромбина, агониста опиоидного рецептора, агониста рецептора АДФ, антагониста рецептора лейкотриена, агониста рецептора лейкотриена, агониста рецептора мелатонина, агониста рецептора соматостатина, агониста рецептора каннабиноида, агониста рецептора сфингозин-1-фосфата, агониста метаботропного рецептора глутамата, ингибитора фосфолипазы A2, ингибитора продукции TGF-β и ингибитор цитокина Th2, для применения в качестве стимулятора индукции клеточного иммунитета в случае трансдермального введения пептида WT1 и/или модифицированного пептида WT1.
(57) Способ индукции клеточного иммунитета, включающий в себя трансдермальное введение субъекту (i) пептида WT1 и/или модифицированного пептида WT1 и (ii) фармакологически приемлемой кислоты или ее фармакологически приемлемой соли в качестве первого стимулятора индукции клеточного иммунитета.
(58) Фармакологически приемлемая кислота или ее фармакологически приемлемая соль для применения с целью ускорения индукции клеточного иммунитета при трансдермальном введении пептида WT1 и/или модифицированного пептида WT1.
(59) Сочетание (i) фармакологически приемлемой кислоты или ее фармакологически приемлемой соли и (ii) одного или нескольких веществ, выбранных из группы, состоящей из лиганда TLR, циклического динуклеотида, хелперного пептида, иммуномодулирующего низкомолекулярного лекарственного средства, ингибитора циклооксигеназы, антагониста рецептора простагландина, агониста рецептора простагландина, ингибитора продукции TSLP, ингибитора аденилатциклазы, омега-3 жирной кислоты, агониста PPAR, антагониста рецептора дофамина, агониста рецептора дофамина, агониста рецептора гистамина, антагониста рецептора гистамина, агониста рецептора серотонина, антагониста рецептора серотонина, антагониста рецептора вазопрессина, агониста рецептора вазопрессина, антагониста мускаринового рецептора, агониста мускаринового рецептора, антагониста рецептора адреналина, агониста рецептора адреналина, агониста рецептора ангиотензина, агониста рецептора ГАМК, антагониста рецептора тромбина, агониста рецептора тромбина, агониста опиоидного рецептора, агониста рецептора АДФ, антагониста рецептора лейкотриена, агониста рецептора лейкотриена, агониста рецептора мелатонина, агониста рецептора соматостатина, агониста рецептора каннабиноида, агониста рецептора сфингозин-1-фосфата, агониста метаботропного рецептора глутамата, ингибитора фосфолипазы A2, ингибитора продукции TGF-бета и ингибитора цитокина Th2, для применения с целью ускорения индукции клеточного иммунитета при трансдермальном введении пептида WT1 и/или модифицированного пептида WT1.
(60) Сочетание (i) пептида WT1 и/или модифицированного пептида WT1 и (ii) фармакологически приемлемой кислоты или ее фармакологически приемлемой соли в качестве первого стимулятора индукции клеточного иммунитета для применения с целью индукции клеточного иммунитета при трансдермальном введении пептида WT1 и/или модифицированного пептида WT1.
(61) Сочетание (i) пептида WT1 и/или модифицированного пептида WT1 и (ii) фармакологически приемлемой кислоты или ее фармакологически приемлемой соли для применения при лечении или профилактике злокачественной опухоли, при этом сочетание вводят трансдермально; и
(62) Применение (i) пептида WT1 и/или модифицированного пептида WT1 и (ii) фармакологически приемлемой кислоты или ее фармакологически приемлемой соли в качестве первого стимулятора индукции клеточного иммунитета для производства композиции противораковой вакцины для трансдермального введения, предназначенной для индукции клеточного иммунитета.
Так как композицию противораковой вакцины согласно настоящему изобретению можно вводить трансдермально, она обладает следующими преимуществами: прекрасное соответствие требованиям, например, неинвазивное введение, нет боли и освобождение от страха перед инъекцией; пациент может вводить композицию противораковой вакцины сам/сама, так как введение является простым; можно избежать риска случайной инфекции вследствие повреждения в результате укола иглой для медицинского персонала; в случае многократного введения частота амбулаторных посещений может быть снижена и это может вносить вклад в улучшение качества жизни пациента; и медицинские отходы, которые требуют специальной утилизации, такие как иглы для инъекций, не образуются. Кроме того, если композиция противораковой вакцины имеет форму препарата в виде пластыря, такого как препарат для компресса или препарат в виде ленты, то конечно можно вводить предварительно определяемую дозу, можно произвольно контролировать скорость высвобождения лекарственного средства, и композиция противораковой вакцины не прилипает к другой стороне при введении. Кроме того, так как препарат в виде пластыря можно легко отлепить, то в случае, когда возникает побочный эффект, пациент сам/сама может мгновенно остановить введение, удалив пластырь с места нанесения. Кроме того, также существует преимущество, которое заключается в том, что эффективность композиции противораковой вакцины согласно настоящему изобретению заметно улучшена по сравнению с введением пептида WT1 и/или модифицированного пептида WT1 отдельно. Кроме того, также существует преимущество, которое заключается в том, что при использовании фармакологически приемлемой кислоты или ее фармакологически приемлемой соли эффективность композиции противораковой вакцины для трансдермального введения повышена. Кроме того, композиция противораковой вакцины согласно настоящему изобретению также имеет преимущество, состоящее в том, что трансдермальное введение композиции индуцирует более сильный клеточный иммунитет по сравнению с инъекционным введением.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[Фиг. 1]. На фиг. 1 представлено изображение, показывающее эффект индукции клеточного иммунитета препаратом в виде ПИБ-пленки с разными включенными в нее кислотами.
[Фиг. 2]. На фиг. 2 представлено изображение, показывающее влияние добавления кислоты в разные пленочные препараты.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Сначала будут определены термины, используемые в настоящем описании, чтобы настоящее изобретение можно было легче понять. Термины, которым не дано определение, имеют значение, которые обычно подразумевает специалист в данной области, в частности в области медицины, фармации, иммунологии, клеточной биологии, биохимии, химии полимеров и тому подобных, если контекст не требует иного.
I. Определения
В используемом в настоящем описании смысле термин «пептид WT1» означает неполный пептид, состоящий примерно из 8-15, предпочтительно примерно из 8-12 аминокислот, который получает в результате фрагментации белка WT1, который является продуктом ракового гена WT1 (опухоль Вильмса), и включает в себя пептид Db126, пептид Db235 и тому подобные. Кроме того, неполный пептид продукта WT1, раскрытый в WO 2000/06602, полученный из WT1 пептид ракового антигена, связывающий HLA-A26, описанный в WO 2005/095598, ограниченный по HLA-A*3303 пептид WT1, описанный в WO 2007/097358, и ограниченный по HLA-A*1101 пептид WT1, описанный в WO 2008/081701, также включены в термин «пептид WT1» согласно настоящему изобретению.
Термин «пептид Db126» означает пептид WT1, состоящий из последовательности Arg Met Phe Pro Asn Ala Pro Tyr Leu (SEQ ID NO: 1). Термин «пептид Db235» означает пептид WT1, состоящий из последовательности Cys Met Thr Trp Asn Gln Met Asn Leu (SEQ ID NO: 2) (патентный документ 1).
В используемом в настоящем описании смысле термин «модифицированный пептид WT1» означает пептид, в котором все или часть аминокислот пептида WT1 модифицированы заменой, модификацией или тому подобным.
Модифицированный пептид WT1 включает, например,
(a) пептид, состоящий из аминокислотной последовательности, в которой от одной до нескольких, например, 1, 2, 3, 4 или 5 аминокислот заменены, делетированы или добавлены в аминокислотной последовательности пептида WT1; и
(b) пептид, состоящий из аминокислотной последовательности, в которой все или часть аминокислот, например, одна или больше, например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 аминокислот модифицированы в аминокислотной последовательности пептида WT1.
Примеры «модификации» аминокислоты, которая может быть присутствовать в модифицированном пептиде WT1, включают без ограничения модификацию за счет добавления алифатической цепи, такую как алкилирование, такое как ацетилирование и метилирование, гликозилирование, гидроксилирование, карбоксилирование, введение альдегидной группы, фосфорилирование, сульфонилирование, формилирование, миристоилирование, пальмитоилирование и стеарилирование, октаноилирование, этерефикацию, амидирование, дезамидирование, модификацию за счет образования дисульфидной связи, такую как модификацию цистеином, модификацию глутатионом и модификацию тиогликолевой кислотой, гликирование, убиквитинилирование, образование сукцинимида, глутамилирование, пренилирование и тому подобное. Модифицированный пептид WT1 может содержать сочетание замены, делеции или добавления одной или нескольких аминокислот и модификацию одной или нескольких аминокислот.
В качестве конкретного примера, пептид Db235m, в котором часть пептида Db235 модифицирована, представляет собой модифицированный пептид WT1, состоящий из последовательности Cys Tyr Thr Trp Asn Gln Met Asn Leu (SEQ ID NO: 3) (WO 2002/079253), и включен в термин «модифицированный пептид WT1» согласно настоящему изобретению. Пептид WT1, относящийся к типу пептидов с заменами, описанный в WO 2004/026897, производное пептида WT1235-243, раскрытое в WO 2007/063903 A1, и HLA-A24-ограниченный пептид ракового антигена, раскрытый в WO 2003/106682, также включены в термин «модифицированный пептид WT1» в настоящем изобретении. Конкретные примеры HLA-A24-ограниченного модифицированного пептида WT1, описанного в WO 2003/106682, включают пептид RYF с последовательностью Arg Tyr Phe Pro Asn Ala Pro Tyr Leu (SEQ ID NO: 4) и пептид AYL с последовательностью Ala Tyr Leu Pro Ala Val Pro Ser Leu (SEQ ID NO: 5).
Пептид WT1 и/или модифицированный пептид WT1 могут быть в свободной форме или в форме любой фармакологически приемлемой соли, например, в форме солей кислот (соль уксусной кислоты, соль ТФУ, соль хлористоводородной кислоты, соль серной кислоты, соль фосфорной кислоты, соль молочной кислоты, соль винной кислоты, соль малеиновой кислоты, соль фумаровой кислоты, соль щавелевой кислоты, соль бромистоводородной кислоты, соль янтарной кислоты, соль азотной кислоты, соль яблочной кислоты, соль лимонной кислоты, соль олеиновой кислоты, соль пальмитиновой кислоты, соль пропионовой кислоты, соль муравьиной кислоты, соль бензойной кислоты, соль пикриновой кислоты, соль бензолсульфоновой кислоты, соль додецилсерной кислоты, соль метансульфоновой кислоты, соль п-толуолсульфоновой кислоты, соль глутаровой кислоты, соли различных аминокислот и т.д.), солей металлов (соли щелочных металлов (например, соль натрия, соль калия), солей щелочноземельных металлов (например, соль кальция, соль магния, соль алюминия и т.д.) или солей аминов (соль триэтиламина, соль бензиламина, соль диэтаноламина, соль трет-бутиламина, соль дициклогексиламина, соль аргинина, соль диметиламмония, соль аммония и т.д.). Предпочтительной фармакологически приемлемой солью является соль уксусной кислоты или соль ТФУ. Можно использовать пептид WT1 и/или модифицированный пептид WT1, который был синтезирован или получен и выделен и очищен хорошо известным способом.
В используемом в настоящем описании смысле, термин «стимулятор индукции клеточного иммунитета» означает любое вещество, которое может усиливать клеточный иммунный ответ, индуцированный антигеном, который вводят вместе с веществом, по сравнению иммунным ответом, индуцированным антигеном без вещества. Стимулятор индукции клеточного иммунитета может включать вещества, подробно описанные в настоящей публикации, хотя стимулятор не ограничен механизмом действия, посредством которого происходит стимуляция индукции клеточного иммунитета.
В используемом в настоящем описании смысле термин «лиганд TLR» означает лиганд Toll-подобного рецептора (TLR) и включает, например, лиганды TLR 1-9. Примеры лиганда TLR включают лиганд TLR1/2, лиганд TLR2/6, лиганд TLR2 и дектина-1, лиганд TLR3, лиганд TLR4, лиганд TLR5, лиганд TLR7 и/или TLR8, лиганд TLR9 и тому подобные. В предпочтительном аспекте настоящего изобретения лигандом TLR является лиганд TLR1/2, лиганд TLR2 и дектина-1, лиганд TLR3, лиганд TLR4, лиганд TLR7 и/или TLR8 и/или лиганд TLR9.
В используемом в настоящем описании смысле термин «лиганд TLR1/2» означает лиганд гетеродимера Toll-подобного рецептора (TLR) 1 и Toll-подобного рецептора (TLR) 2 и включает, например, триацилированный липопротеин, полученный из клеточной стенки бактерии, и его соль, которые могут представлять собой экстракт, продукт или синтетический продукт и не ограничены указанным.
В предпочтительном аспекте настоящего изобретения лигандом TLR1/2 является Pam3CSK4. Pam3CSK4 имеет формулу:
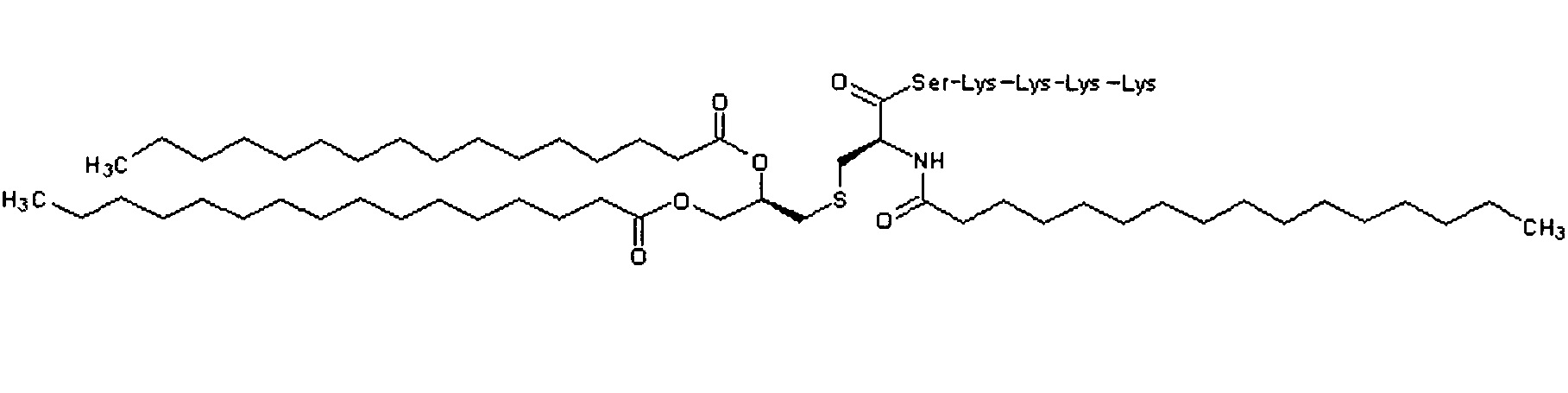
В используемом в настоящем описании смысле термин «лиганд TLR2 и дектина-1» означает лиганд Toll-подобного рецептора (TLR) 2 и рецептора β1,3-глюкана (дектина-1) и включает, например, β1,3-глюкан, полученный из клеточной стенки гриба, и его соль, которые могут представлять собой экстракт, продукт или синтетический продукт, и не ограничены указанным. В предпочтительном аспекте настоящего изобретения лигандом TLR2 и дектина-1 является зимозан, полученный из клеточной стенки дрожжей.
В используемом в настоящем описании смысле термин «лиганд TLR3» означает лиганд Toll-подобного рецептора (TLR) 3 и включает, например, двунитевую РНК (днРНК), полученную из вируса, и ее соль, и они могут представлять собой экстракт, продукт или синтетический продукт и не ограничены указанным. В предпочтительном аспекте настоящего изобретения лигандом TLR3 является полиинозиновая-полицитидиловая кислота (поли(I:C)), которая является синтетическим продуктом, и/или ее соль.
В используемом в настоящем описании смысле термин «лиганд TLR4» означает лиганд Toll-подобного рецептора (TLR) 4 и включает, например, липополисахарид (LPS), полученный из бактерии или растения, в частности, производное липида A, например, монофосфориллипид A, 3-деацилированный монофосфориллипид A (3D-MPL), OM174, OM 294 DP или OM 197 MP-Ac DP и тому подобные, алкилглюкозаминидфосфат (AGP), например, AGP, раскрытый в WO 98/50399 или US 6303347, или соль AGP, которая раскрыта в US 6764840, и липополисахарид, глюкопиранозиллипид и гиалуронат натрия, полученные из бактерии Pantoea, но не ограничен указанным.
В предпочтительном аспекте настоящего изобретения предпочтительными в качестве лиганда TLR4 являются липополисахариды, полученные из рода Acetobacter (например, Acetobacter aceti, Acetobacter xylinum, Acetobacter orientalis и т.д.), рода Zymomonas (например, Zymomonas mobilis и т.д.), рода Xanthomonas (например, Xanthomonas campestris и т.д.), рода Enterobacter (например, Enterobacter cloacae и т.д.) и рода Pantoea (например, Pantoea agglomerans и т.д.). Экстракты, полученные из таких липополисахаридов, или очищенные липополисахариды могут быть использованы как таковые. Кроме того, например, липополисахариды (IP-PA1), полученные из Pantoea agglomerans, можно приобрести от компании Funakoshi. Кроме того, в предпочтительном аспекте настоящего изобретения лигандом TLR4 является липополисахарид, глюкопиранозиллипид и/или гиалуронат натрия, полученные из бактерии Pantoea bacterium.
В используемом в настоящем описании смысле термин «лиганд TLR7 и/или TLR8» означает лиганд Toll-подобного рецептора (TLR) 7 и/или TLR8 и включает, например, однонитевую РНК, имихимод, резихимод (R848), TLR7-II и другие соединения, например, локсорибин и бропиримин, но не ограничен указанным.
В предпочтительном аспекте настоящего изобретения лигандом TLR7 и/или TLR8 является имихимод. Имихимод представляет собой 1-(2-метилпропил)-1H-имидазо[4,5-c]хинолин-4-амин формулы:

и его характеристики и способ получения описаны, например, в JP 7-505883 A (патентный документ 2).
В другом предпочтительном аспекте лигандом TLR7 и/или TLR8 является резихимод. Резихимод представляет собой 4-амино-2-(этоксиметил)-α,α-диметил-1H-имидазо[4,5-c]хинолин-1-этанол формулы:

В другом предпочтительном аспекте лигандом TLR7 и/или TLR8 является TLR7-II. TLR7-II представлен формулой:
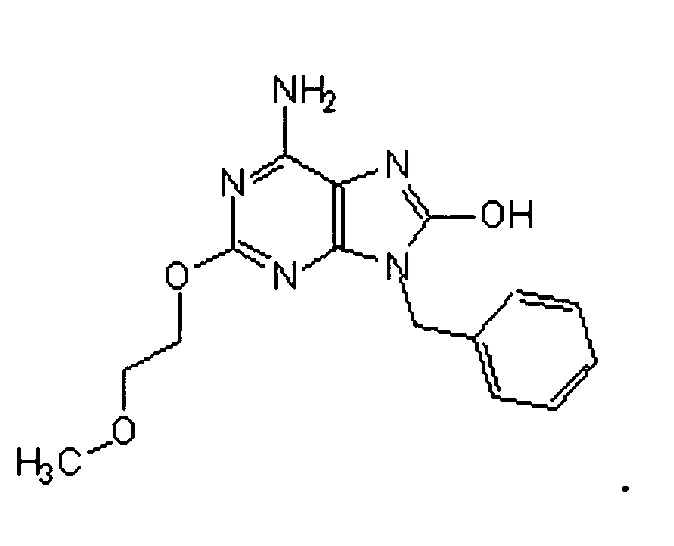
В другом предпочтительном аспекте лигандом TLR7 и/или TLR8 является бропиримин. Бропиримин представлен формулой:
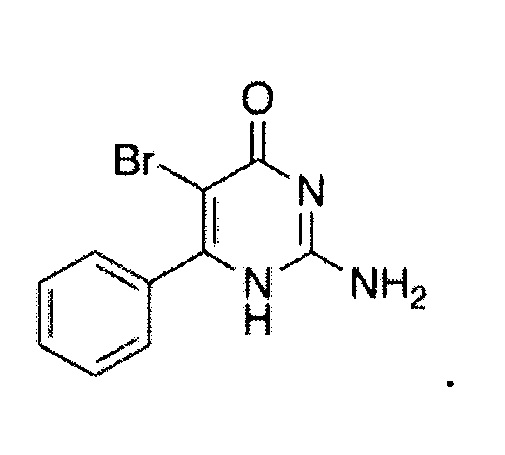
В используемом в настоящем описании смысле термин «лиганд TLR9» означает лиганд Toll-подобного рецептора (TLR) 9 и включает, например, ODN1826 и тому подобные. Лиганд TLR9, используемый в настоящем изобретении, может представлять собой экстракт, продукт или синтетический продукт и не ограничен указанным. В предпочтительном аспекте настоящего изобретения лигандом TLR9 является ODN1826.
ODN1826 является олигодезоксинуклеотидом, состоящим из следующей последовательности (SEQ ID NO: 6).
5’-tccatgacgttcctgacgtt-3’
В используемом в настоящем описании смысле термин «лиганд TLR2/6» означает лиганд гетеродимера Toll-подобного рецептора (TLR) 2 и Toll-подобного рецептора (TLR) 6 и включает, например, диацилированный липопротеин, полученный из клеточной стенки микоплазмы, и его соль, которые могут представлять собой экстракт, продукт или синтетический продукт, и не ограничены указанным. В предпочтительном аспекте настоящего изобретения лигандом TLR2/6 является Pam2CSK4, MALP-2 и/или FSL-1.
Pam2CSK4 представлен следующей формулой.

FSL-1 представлен следующей формулой.
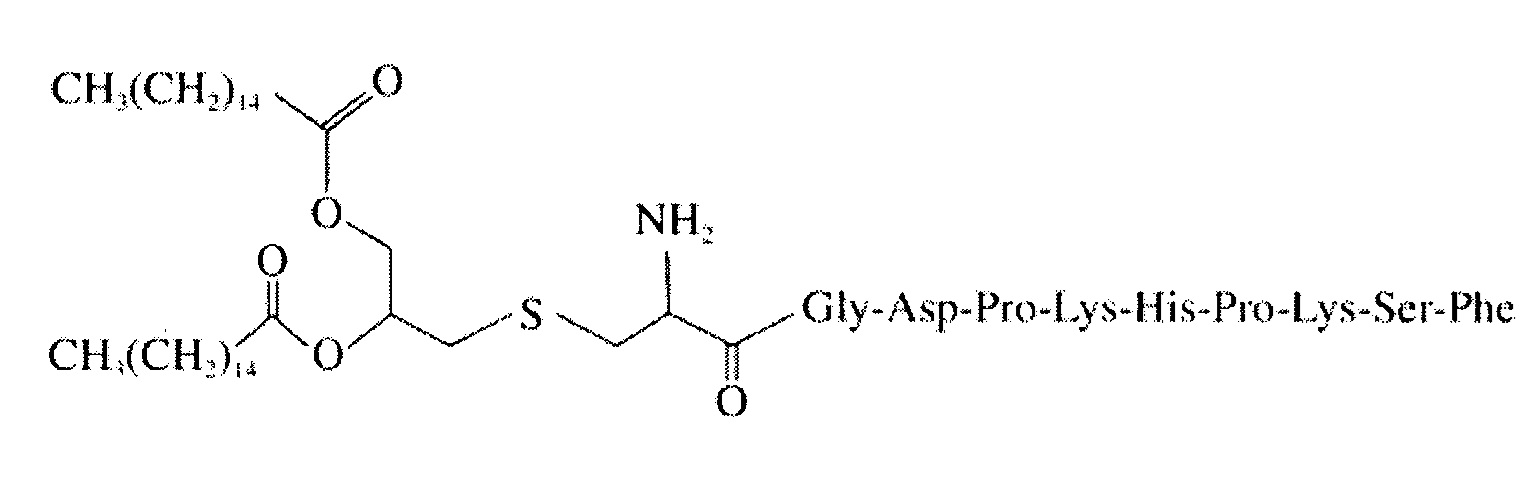
В используемом в настоящем описании смысле термин «лиганд TLR5» означает лиганд Toll-подобного рецептора (TLR) 5 и включает, например, флагеллин и тому подобные. Лиганд TLR5, используемый в настоящем изобретении, может представлять собой экстракт, продукт или синтетический продукт, и не ограничен указанным. В предпочтительном аспекте настоящего изобретения лигандом TLR5 является флагеллин.
Toll-подобные рецепторы (TLR) составляют семейство трансмембранных белков I-типа, которые инициируют врожденный иммунный ответ, в котором принимают участие специфичный цитокин, специфичный хемокин и фактор роста, за счет их активации in vivo. Все TLR могут активировать определенную молекулу передачи внутриклеточного сигнала, например, ядерный фактор κB (NF-κB) и активируемую митогенами протеинкиназу (MAP-киназу) или тому подобные, хотя каждому TLR, по-видимому, соответствуют конкретные популяции цитокинов и хемокинов, которые высвобождаются. TLR3, 7, 8 и 9 включены в подсемейство TLR, которое присутствует во фракции эндосом или фракции лизосом иммунной клетки (например, дендритной клетки и моноцита). В частности, TLR3 экспрессируется широким кругом клеток, таких как дендритная клетка и фибробласт, TLR7 экспрессируется дендритной клеткой, подобной плазматической клетке, и в меньшей степени экспрессируется моноцитом, TLR8 экспрессируется моноцитом, а также полученной из моноцита дендритной клеткой и миелогенной дендритной клеткой, и TLR9 экспрессируется дендритной клеткой, подобной плазматической клетке. Такое подсемейство опосредует распознавание нуклеиновой кислоты микроорганизма (однонитевой РНК, двунитевой РНК, однонитевой ДНК и т.д.). Агонисты TLR3, TLR7 и/или TLR8 и TLR9 стимулируют продукцию различных воспалительных цитокинов (включая, например, интерлейкин-6, интерлейкин-12, TNF-α и интерферон-γ). Такие агонисты также стимулируют повышение экспрессии костимулирующей молекулы (например, CD40, CD80 и CD86), молекулы главного комплекса гистосовместимости и рецептора хемокина. Интерфероны I-типа (IFNα и IFNβ) продуцируются клеткой при активации агонистами TLR7 и/или TLR8.
В используемом в настоящем описании смысле термин «циклический динуклеотид» означает молекулу, в которой две группы OH в представленной сахаром части двух нуклеотидов, образуют сложный эфир c каждой молекулой фосфорной кислоты, и при этом происходит циклизация нуклеотидов, и ее аналог, и включает, например, циклический ди-АМФ (ц-ди-АМФ), циклический ди-ГМФ (ц-ди-ГМФ), c-dGpGp, c-dGpdGp, c-GpAp, c-GpCp, c-GpUp и тому подобные, но не ограничен указанным. Циклический динуклеотид активирует дендритную клетку или T-клетку. Дополнительные примеры циклического динуклеотида, их применение в качестве адъюванта и способ их получения описаны в JP 2007-529531 A (патентный документ 3). В предпочтительном аспекте настоящего изобретения циклическим динуклеотидом является циклический ди-ГМФ и/или циклический ди-АМФ. Циклический ди-ГМФ имеет формулу:

и способ его синтеза описаны Kawai et al., Nucleic Acids Research Suppl. 3: 103-4.
В используемом в настоящем описании смысле термин «хелперный пептид» означает любой пептид, который активирует хелперную T-клетку, и включает, например, полученный из туберкулезной бациллы хелперный пептид, полученный из вируса кори хелперный пептид, полученный из вируса гепатита B хелперный пептид, полученный из вируса гепатита C хелперный пептид, полученный из Chlamydia trachomatis хелперный пептид, полученный из спорозоита Plasmodium falciparum хелперный пептид, полученный из гемоцианина морского блюдечка «замочная скважина» хелперный пептид, полученный из столбнячного токсина хелперный пептид, полученный их коклюшного токсина хелперный пептид, полученный из дифтерийного токсина хелперный пептид, полученный из злокачественной клетки хелперный пептид (например, хелперный пептид WT1_332-347 (описанный в патенте Японии № 4621142 «WT1-derived HLA-DR binding Antigen Peptide»), хелперный пептид hWT135, хелперный пептид hWT186, хелперный пептид hWT1294 (все три вида описаны в WO 2010/123065 «Cancer Antigen Helper Peptide»), хелперный пептид IMA-MMP-001, хелперный пептид CEA-006, хелперный пептид MMP-001, хелперный пептид TGFBI-004, хелперный пептид HER-2/neu (а/к 776-790), хелперный пептид AE36, хелперный пептид AE37, хелперный пептид MET-005, хелперный пептид BIR-002 и т.д.), и универсальный хелперный аналог (например, PADRE). В предпочтительном аспекте настоящего изобретения хелперный пептид состоит из 10-20 аминокислот, предпочтительно из 12-19 аминокислот, более предпочтительно из 13-18 аминокислот. В предпочтительном аспекте настоящего изобретения хелперным пептидом является пептид-25, hWT135, PADRE или WT1_332-347. Пептид-25 представляет собой пептид из 15 аминокислот, состоящий из последовательности Phe Gln Asp Ala Tyr Asn Ala Ala Gly Gly His Asn Ala Val Phe (SEQ ID NO: 7), соответствующий аминокислотным остаткам 240-254 Ag85B, который является одним из основных белков, секретируемых туберкулезной бациллой человека (Mycobacterium tuberculosis). Кроме того, hWT135 представляет собой пептид из 18 аминокислот, состоящий из последовательности Trp Ala Pro Val Leu Asp Phe Ala Pro Pro Gly Ala Ser Ala Tyr Gly Ser Leu (показанной в виде SEQ ID NO: 8 в настоящей заявке), описанный в WO 2010/123065 «Cancer Antigen Helper Peptide». PADRE представляет собой пептид из 13 аминокислот, состоящий из последовательности D-Ala Lys циклогексил-Ala Val Ala Ala Trp Thr Leu Lys Ala Ala D-Ala (показанной в виде SEQ ID NO: 9 в настоящей заявке). WT1_332-347 представляет собой пептид из 16 аминокислот, состоящий из последовательности Lys Arg Tyr Phe Lys Leu Ser His Leu Gln Met His Ser Arg Lys His (показанной в виде SEQ ID NO: 10 в настоящей заявке), описанный в патенте Японии № 4621142 «WT1-derived HLA-DR binding Antigen Peptide».
Кроме того, в настоящем изобретении вместо вышеуказанных хелперных пептидов или в сочетании с ними также могут быть использованы пептиды, в которых все или часть аминокислот хелперных пептидов модифицированы заменой, модификацией или тому подобным (далее называемые «модифицированными хелперными пептидами»).
Модифицированный хелперный пептид включает, например,
(a) пептид, состоящий из аминокислотной последовательности, в которой от одной до нескольких, например, 1, 2, 3, 4 или 5 аминокислот заменены, делетированы или добавлены в аминокислотной последовательности исходного хелперного пептида; и
(b) пептид, состоящий из аминокислотной последовательности, в которой все или часть аминокислот, например, одна или несколько, например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 или 18 аминокислот модифицированы в аминокислотной последовательности исходного хелперного пептида.
Одним примером модифицированного хелперного пептида является пептид-25B. Пептид-25B является одним из примеров модифицированного пептида-25, в котором часть аминокислот пептида-25 модифицирована, чтобы усилить эффект иммуностимуляции, и представляет собой пептид из 15 аминокислот, состоящий из последовательности Phe Gln Asp Ala Tyr Asn Ala Val His Ala Ala His Ala Val Phe (SEQ ID NO: 11).
Примеры «модификации» аминокислоты, которую может иметь модифицированный хелперный пептид, включают без ограничения модификацию посредством добавления алифатической цепи, такую как ацетилирование, алкилирование, такое как метилирование, гликозилирование, гидроксилирование, карбоксилирование, введение альдегидной группы, фосфорилирование, сульфонилирование, формилирование, добавление жирной кислоты, такое как миристоилирование, пальмитоилирование и стеарилирование, октаноилирование, этерефикацию, амидирование, дезамидирование, модификацию за счет образования дисульфидной связи, такую как модификацию цистеином, модификацию глутатионом и модификацию тиогликолевой кислотой, гликирование, убиквитинилирование, образование сукцинимида, глутамилирование, пренилирование и тому подобное. Кроме того, модифицированный хелперный пептид может содержать сочетание замены, делеции или добавления одной или нескольких аминокислот и модификацию одной или нескольких аминокислот.
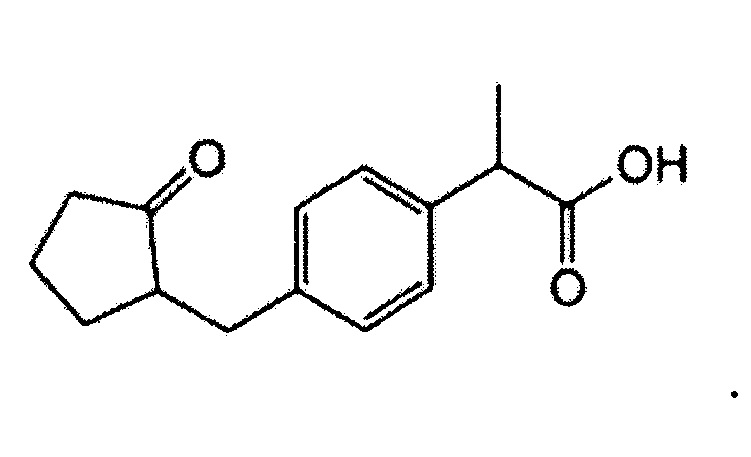
В используемом в настоящем описании смысле термин «ингибитор циклооксигеназы» означает вещество, которое ингибирует функцию циклооксигеназы (ЦОГ). Далее его также называют «ингибитор ЦОГ». В качестве ингибиторов ЦОГ существуют ингибитор ЦОГ, который избирательно действует на конкретную циклооксигеназу (например, ЦОГ-1 или ЦОГ-2), и ингибитор ЦОГ, не обладающий избирательностью. Примеры ингибиторов ЦОГ, которые можно использовать в настоящем изобретении, включают этодолак, локсопрофен, целекоксиб, вальдекоксиб, парекоксиб, лумиракоксиб, мелоксикам, теноксикам, диклофенак, мефенамовую кислоту, толфенамовую кислоту, флуфенамовую кислоту, меклофенамовую кислоту, нифлумовую кислоту, бензидамин, индобуфен, трифлусал, толметин, фенопрофен, тиапрофеновую кислоту, фелбинак, непафенак, амфенак, правадолин, залтопрофен, сулиндак, набуметон, дифлунисал, пироксикам, ибупрофен, напроксен, фенопрофен, аспирин, метилсалицилат, салициламид, салсалат, алоксиприн, толметин, индометацин, проглуметацин, ацеметацин, флурбипрофен, пранопрофен, ацетаминофен, флоктафенин, лорноксикам, теноксикам, тиапрофеновую кислоту, оксапрозин, кетопрофен, декскетопрофен, дексибупрофен, алминопрофен, кеторолак, мофезолак, фенилбутазон, оксифенилбутазон, кетофенилбутазон, фепразон, фенбутазон, этензамид, тиарамид, тиноридин, эпиризол, эморфазон и их производное, а также их фармакологически приемлемую соль. В предпочтительном аспекте настоящего изобретения ингибитором ЦОГ является этодолак и/или локсопрофен.
Локсопрофен представлен формулой:
В используемом в настоящем описании смысле термин «антагонист рецептора простагландина» означает вещество, обладающее функцией предотвращения действия простагландина на рецептор, и включает, например, антагонист рецептора EP2, антагонист рецептора EP4, антагонист рецептора DP и антагонист рецептора IP.
В используемом в настоящем описании смысле термин «антагонист рецептора EP2» означает вещество, обладающее функцией предотвращения действия простагландина E2 на рецептор EP2. Примеры антагониста рецептора EP2 включают AH6809 и его производное, а также его фармакологически приемлемую соль.
AH6809 представлен формулой:

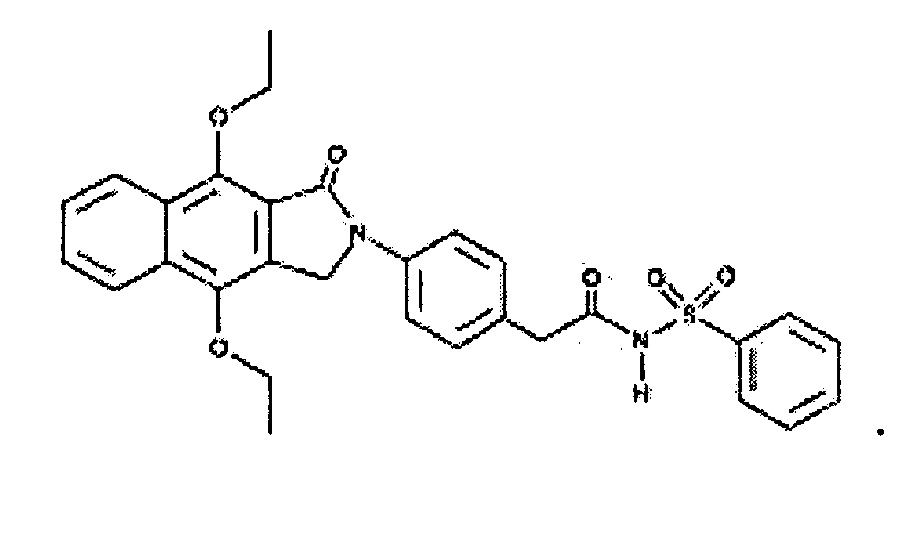
В используемом в настоящем описании смысле термин «антагонист рецептора EP4» означает вещество, обладающее функцией предотвращения действия простагландина E2 на рецептор EP4. Примеры антагониста рецептора EP4 включают GW627368X и его производное, а также его фармакологически приемлемую соль.
GW627368X представлен формулой:
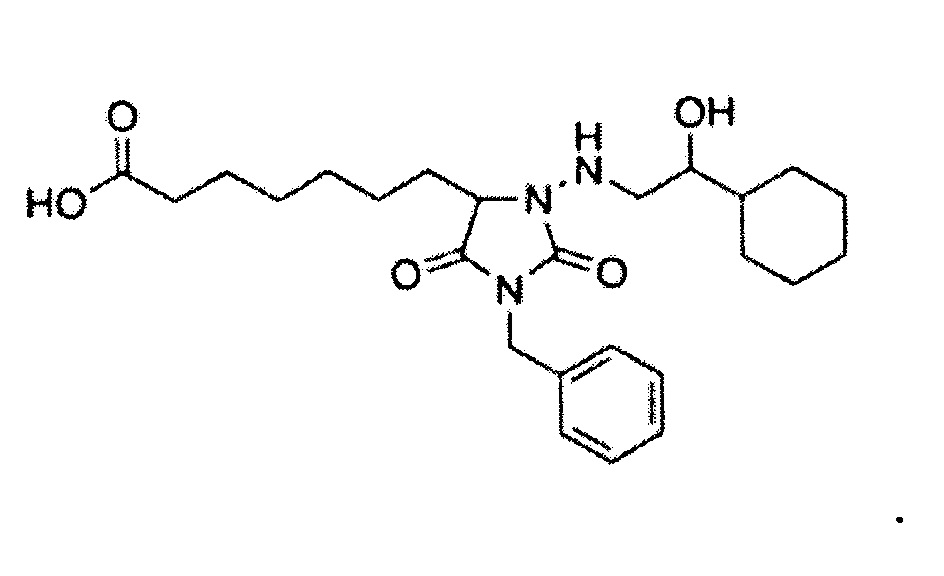
В используемом в настоящем описании смысле термин «антагонист рецептора DP» означает вещество, обладающее функцией предотвращения действия простагландин f D2 на рецептор DP. Примеры антагониста рецептора DP включают S-5751, BWA868C и их производное, а также их фармакологически приемлемую соль.
BWA868C представлен формулой:
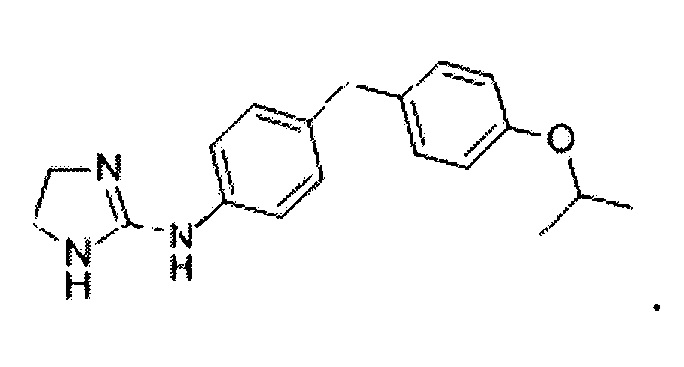
В используемом в настоящем описании смысле термин «антагонист рецептора IP» означает вещество, обладающее функцией предотвращения действия простагландина I2 на рецептор IP. Примеры антагониста рецептора IP включают RO1138452 и его производное, а также его фармакологически приемлемую соль.
RO1138452 представлен формулой:
В используемом в настоящем описании смысле термин «агонист рецептора простагландина» означает вещество, обладающее функцией действия на рецептор простагландина, и включает, например, агонист рецептора EP3.
В используемом в настоящем описании смысле термин «агонист рецептора EP3» означает вещество, обладающее функцией действия на рецептор EP3. Примеры агониста рецептора EP3 включают сульпростон, GR63799, клопростенол, ONO-AE-248, карбациклин и их производное, а также их фармакологически приемлемую соль.
Сульпростон представлен формулой:
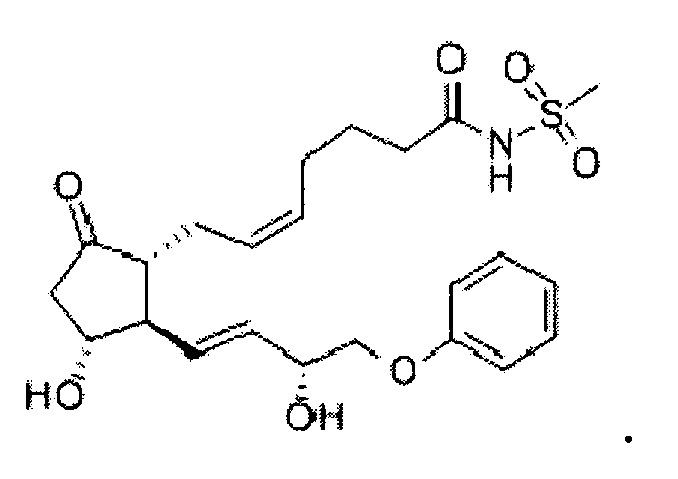
В используемом в настоящем описании смысле термин «ингибитор продукции TSLP» означает вещество, обладающее функцией ингибирования продукции TSLP. Так как считается, что лекарственное средство, которое ингибирует NF-κB, опосредованно ингибирует продукцию TSLP, то его включают в указанную категорию. Примеры ингибитора продукции TSLP включают нарингенин, берберин, ресвератрол, лютеолин, апигенин, хризоэриол, велутин, рутин, гесперидин, кверцетин, дайдзеин, генистеин, носкапин, дииндолилметан, ксантон, партенолид и их производное, а также их фармакологически приемлемую соль.
Берберин представлен формулой:
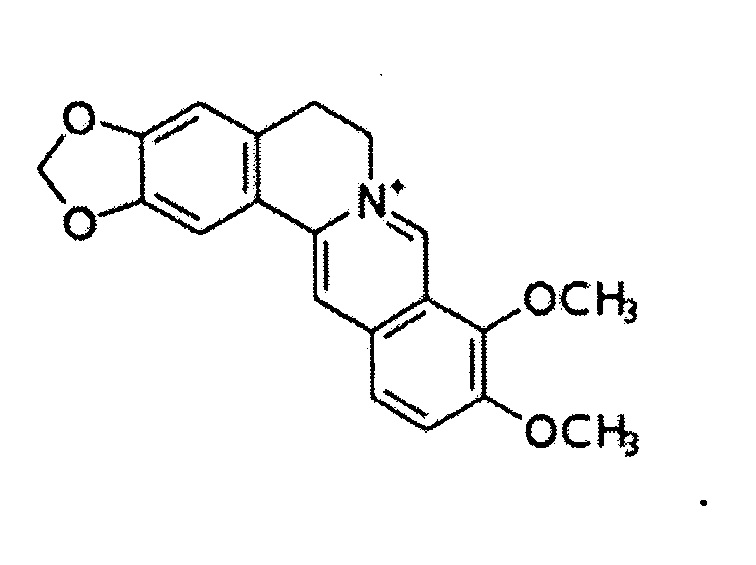
В используемом в настоящем описании смысле термин «ингибитор аденилатциклазы» означает вещество, обладающее функцией ингибирования активности аденилатциклазы. Примеры ингибитора аденилатциклазы включают 2’,5’-дидезоксиаденозин, ниацин, инсулин и их производное, а также их фармакологически приемлемую соль.
2’,5’-Дидезоксиаденозин представлен формулой:
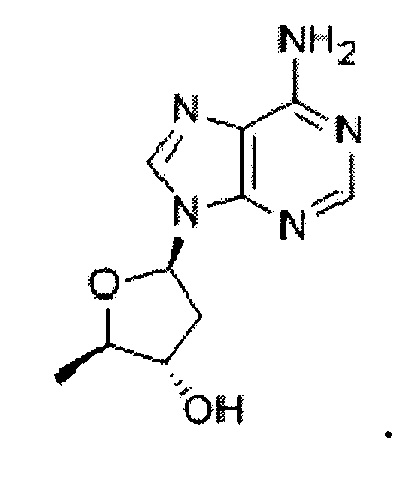
В используемом в настоящем описании смысле термин «омега-3 жирная кислота» относится к ненасыщенной жирной кислоте, имеющей углерод-углеродную двойную связь в положении ω-3. Примеры омега-3 жирной кислоты включают эйкозапентаеновую кислоту, α-линоленовую кислоту, докозагексаеновую кислоту и их производное, а также их фармакологически приемлемую соль.
Эйкозапентаеновая кислота представлена формулой:

В используемом в настоящем описании смысле термин «агонист PPAR» означает вещество, обладающее функцией действия на активируемый пролифератором пероксисом рецептор, и включает, например, агонист PPAR-α, агонист PPAR-δ и агонист PPAR-γ.
В используемом в настоящем описании смысле термин «агонист PPAR-α» означает вещество, обладающее функцией действия на активируемый пролифератором пероксисом рецептор типа α. Термин «агонист PPAR-δ» означает вещество, обладающее функцией действия на активируемый пролифератором пероксисом рецептор типа δ. Термин «агонист PPAR-γ» означает вещество, обладающее функцией действия на активируемый пролифератором пероксисом рецептор типа γ. Примеры агониста PPAR-α и/или агониста PPAR-δ и/или агониста PPAR-γ включают клофибрат, фенофибрат, безафибрат, ципрофибрат, этофибрат, телмисартан, олеилэтаноламид, тетрадецилтиоуксусную кислоту, троглитазон, пиоглитазон, росиглитазон, балаглитазон, ривоглитазон, циглитазон, дарглитазон, эдаглитазон, нетоглитазон, индеглитазар, тесаглитазар, мураглитазар, алеглитазар и их производное, а также их фармакологически приемлемую соль.
Клофибрат представлен формулой:

В используемом в настоящем описании смысле термин «антагонист рецептора дофамина» означает вещество, обладающее функцией предотвращения действия дофамина на рецептор, и включает, например, антагонист рецептора D1 и антагонист рецептора D5.
В используемом в настоящем описании смысле термин «антагонист рецептора D1» означает вещество, обладающее функцией предотвращения действия дофамина на рецептор D1. Примеры антагониста рецептора D1 включают бензазепин, фенолдопам, лоркасерин, SCH23390, SCH39166, LE300 и их производное, а также их фармакологически приемлемую соль.
Бензазепин представлен формулой:

В используемом в настоящем описании смысле термин «антагонист рецептора D5» означает вещество, обладающее функцией предотвращения действия дофамина на рецептор D5. Примеры антагониста рецептора D5 включают SCH39166 и его производное, а также его фармакологически приемлемую соль.
SCH39166 представлен формулой:

В используемом в настоящем описании смысле термин «агонист рецептора дофамина» означает вещество, обладающее функцией действия на рецептор дофамина, и включает, например, агонист рецептора D2, агонист рецептора D3 и агонист рецептора D4.
В используемом в настоящем описании смысле термин «агонист рецептора D2» означает вещество, обладающее функцией действия на рецептор D2. Примеры агониста рецептора D2 включают каберголин, бромкриптин, перголид, ропинирол, талипексол, арипипразол, луразидон и их производное, а также их фармакологически приемлемую соль.
Ропинирол представлен формулой:
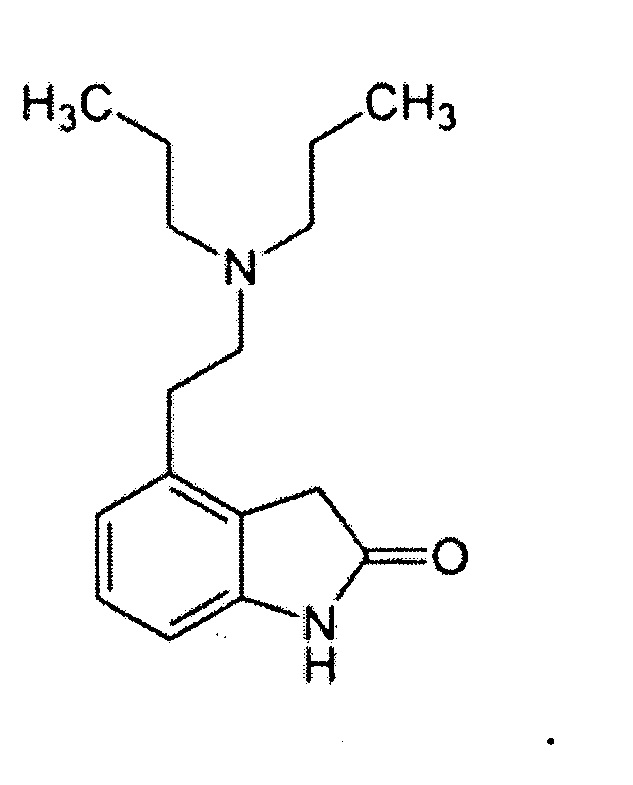
В используемом в настоящем описании смысле термин «агонист рецептора D3» означает вещество, обладающее функцией действия на рецептор D3. Примеры агониста рецептора D3 включают пирибедил, ротиготин, PD1289077, OH-DPAT и их производное, а также их фармакологически приемлемую соль.
Ротиготин представлен формулой:
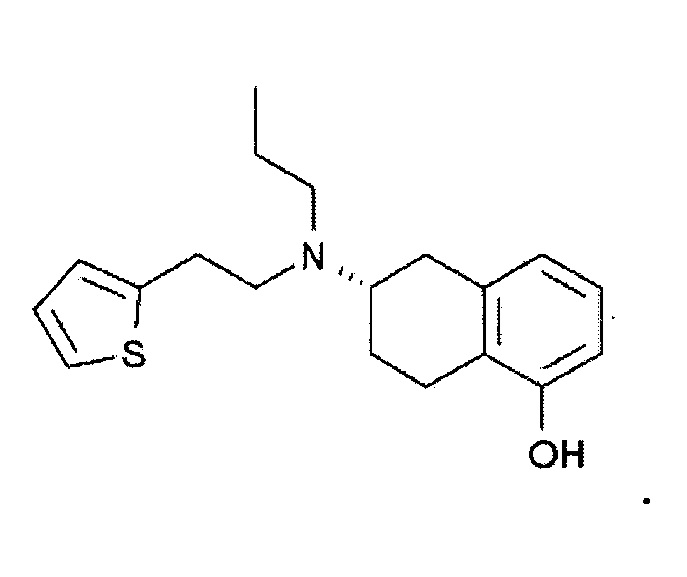
В используемом в настоящем описании смысле термин «агонист рецептора D4» означает вещество, обладающее функцией действия на рецептор D4. Примеры агониста рецептора D4 включают флибансерин, ABT724, PD168077, CP226269 и их производное, а также их фармакологически приемлемую соль.
Флибансерин представлен формулой:

В используемом в настоящем описании смысле термин «антагонист рецептора гистамина» означает вещество, обладающее функцией предотвращения действия гистамина на рецептор, и включает, например, антагонист рецептора H1 и антагонист рецептора H2.
В используемом в настоящем описании смысле термин «антагонист рецептора H1» означает вещество, обладающее функцией предотвращения действия гистамина на рецептор H1. Примеры антагониста рецептора H1 включают кетансерин, тонзиламин, мепирамин, трипеленамин, диметинден, клемастин, бамипин, изотипендил, хлорфеноксамин, диметотиазин, хлорпромазин, гидроксизин, опипрамол, бетагистин, циннаризин, левокабастин, антазолин, дифенилпиралин, карбиноксамин, доксиламин, алимемазин, циклизин, меклозин, левоцетиризин, ципрогептадин, фениндамин, трипролидин, азатадин, астемизол, терфенадин, акривастин, эбастин, деслоратадин, рупатадин, биластин, мизоластин, ноберастин, рокастин, темеластин, бепотастин, дифенгидрамин, хлорфенирамин, кетотифен, прометазин, ципрогептадин, эпинастин, олопатадин, бепотастин, астемизол, эмедастин, меквитазин, оксатомид, лоратадин, фексофенадин, цетиризин, азеластин и их производное, а также их фармакологически приемлемую соль.
Дифенгидрамин представлен формулой:
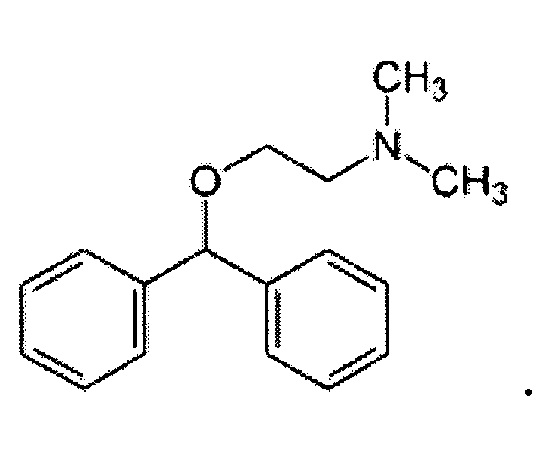
В используемом в настоящем описании смысле термин «антагонист рецептора H2» означает вещество, обладающее функцией предотвращения действия гистамина на рецептор H2. Примеры антагониста рецептора H2 включают циметидин, ранитидин, фамотидин, низатидин, роксатидин, лафутидин и их производное, а также их фармакологически приемлемую соль.
Фамотидин представлен формулой:

В используемом в настоящем описании смысле термин «агонист рецептора гистамина» означает вещество, обладающее функцией действия на рецептор гистамина, и включает, например, агонист рецептора H1, агонист рецептора H3 и агонист рецептора H4.
В используемом в настоящем описании смысле термин «агонист рецептора H1» означает вещество, обладающее функцией действия на рецептор H1. Примеры агониста рецептора H1 включают 2-пиридилэтиламин, 2-тиазолилэтиламин и их производное, а также их фармакологически приемлемую соль.
2-Пиридилэтиламин представлен формулой:
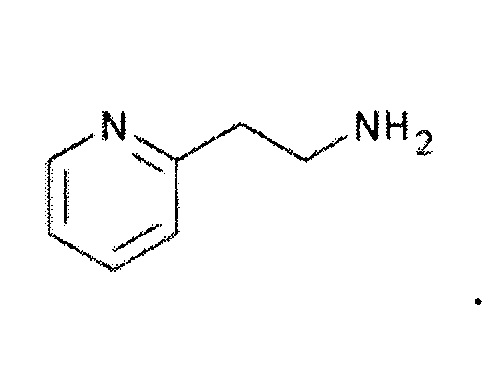
В используемом в настоящем описании смысле термин «агонист рецептора H3» означает вещество, обладающее функцией действия на рецептор H3. Примеры агониста рецептора H3 включают иметридин, иметит, иммепип, α-метилгистамин, проксифан и их производное, а также их фармакологически приемлемую соль.
Проксифан представлен формулой:
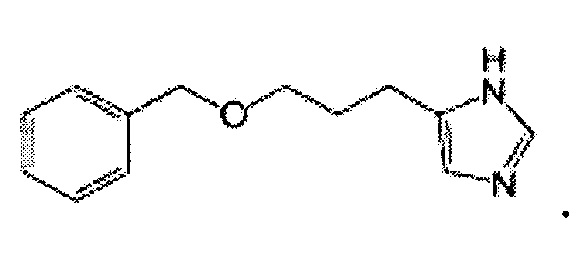
В используемом в настоящем описании смысле термин «агонист рецептора H4» означает вещество, обладающее функцией действия на рецептор H4. Примеры агониста рецептора H4 включают 4-метилгистамин, VUF8430, иммепип и их производное, а также их фармакологически приемлемую соль.
4-Метилгистамин представлен формулой:

В используемом в настоящем описании смысле термин «антагонист рецептора серотонина» означает вещество, обладающее функцией предотвращения действия серотонина на рецептор, и включает, например, антагонист рецептора 5-HT2, антагонист рецептора 5-HT4, антагонист рецептора 5-HT6 и антагонист рецептора 5-HT7.
В используемом в настоящем описании смысле термин «антагонист рецептора 5-HT2» означает вещество, обладающее функцией предотвращения действия серотонина на рецептор 5-HT2. Примеры антагониста рецептора 5-HT2 включают пизотифен, рисперидон, оланзапин, кветиапин, арипипразол, блонансерин, клозапин, палиперидон, ритансерин, йохимбин, месулергин, агомелатин, циклобензаприн, сарпогрелат, метисергид, кетансерин и их производное, а также их фармакологически приемлемую соль.
Оланзапин представлен формулой:

В используемом в настоящем описании смысле термин «антагонист рецептора 5-HT4» означает вещество, обладающее функцией предотвращения действия серотонина на рецептор 5-HT4. Примеры антагониста рецептора 5-HT4 включают пибосерод, GR113808, GR125487, RS39604, SB204070 и их производное, а также их фармакологически приемлемую соль.
Пибосерод представлен формулой:
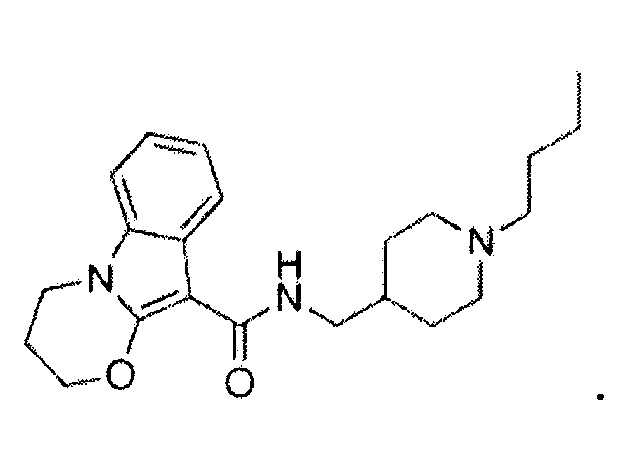
В используемом в настоящем описании смысле термин «антагонист рецептора 5-HT6» означает вещество, обладающее функцией предотвращения действия серотонина на рецептор 5-HT6. Примеры антагониста рецептора 5-HT6 включают церлапирдин, клозапин и их производное, а также их фармакологически приемлемую соль.
Церлапирдин представлен формулой:
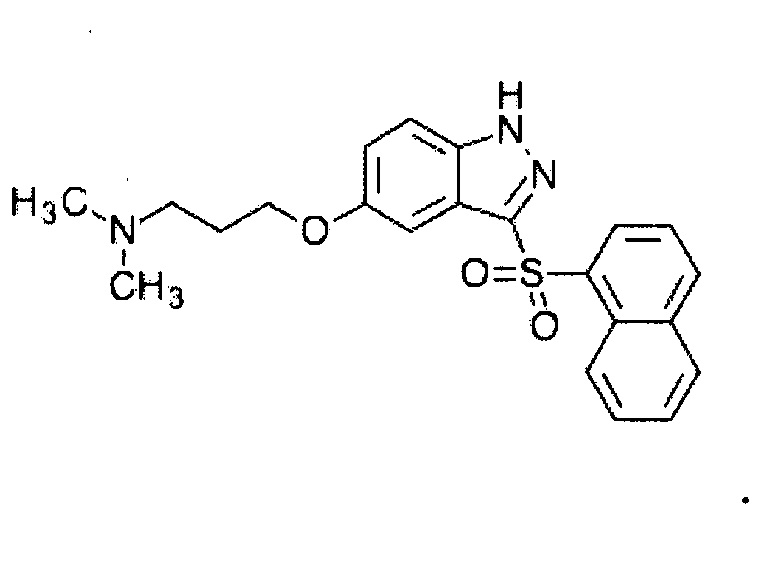
В используемом в настоящем описании смысле термин «антагонист рецептора 5-HT7» означает вещество, обладающее функцией предотвращения действия серотонина на рецептор 5-HT7. Примеры антагониста рецептора 5-HT7 включают лурасидон, метерголин и их производное, а также их фармакологически приемлемую соль.
Метерголин представлен формулой:

В используемом в настоящем описании смысле термин «агонист рецептора серотонина» означает вещество, обладающее функцией действия на рецептор серотонина, и включает, например, агонист рецептора 5-HT1 и агонист рецептора 5-HT2.
В используемом в настоящем описании смысле термин «агонист рецептора 5-HT1» означает вещество, обладающее функцией действия на рецептор 5-HT1. Примеры агониста рецептора 5-HT1 включают пиклозотан, тандоспирон, суматриптан, золмитриптан, элетриптан, ризатриптан, наратриптан, алмотриптан, фроватриптан, авитриптан, эрготамин, алкалоид спорыньи и их производное, а также их фармакологически приемлемую соль.
Золмитриптан представлен формулой:

В используемом в настоящем описании смысле термин «агонист рецептора 5-HT2» означает вещество, обладающее функцией действия на рецептор 5-HT2. Примеры агониста рецептора 5-HT2 включают α-метил-5-HT, агомелатин, норфенфлурамин, мета-хлорфенилпиперазин и их производное, а также их фармакологически приемлемую соль.
Агомелатин представлен формулой:

В используемом в настоящем описании смысле термин «антагонист рецептора вазопрессина» означает вещество, обладающее функцией предотвращения действия вазопрессина на рецептор, и включает, например, антагонист рецептора V2.
В используемом в настоящем описании смысле термин «антагонист рецептора V2» означает вещество, обладающее функцией предотвращения действия вазопрессина на рецептор V2. Примеры антагониста рецептора V2 включают толваптан, мозаваптан, кониваптан, ликсиваптан и их производное, а также их фармакологически приемлемую соль.
Мозаваптан представлен формулой:
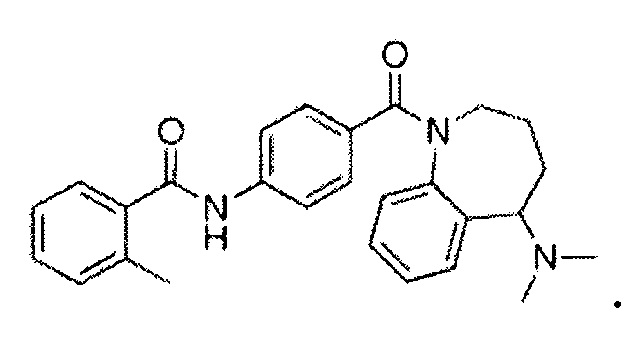
В используемом в настоящем описании смысле термин «агонист рецептора вазопрессина» означает вещество, обладающее функцией действия на рецептор вазопрессина, и включает, например, агонист рецептора V1.
В используемом в настоящем описании смысле термин «агонист рецептора V1» означает вещество, обладающее функцией действия на рецептор V1. Примеры агониста рецептора V1 включают вазопрессин, фелипрессин, десмопрессин, липрессин, терлипрессин, орнипрессин, аргипрессин и их производное, а также их фармакологически приемлемую соль.
Десмопрессин представлен формулой:

В используемом в настоящем описании смысле термин «антагонист мускаринового рецептора» означает вещество, обладающее функцией действия на мускариновый рецептор, и включает, например, антагонист рецептора M1, антагонист рецептора M3 и антагонист рецептора M5.
В используемом в настоящем описании смысле термин «антагонист рецептора M1» означает вещество, обладающее функцией предотвращения действия ацетилхолина на рецептор M1. Термин «антагонист рецептора M3» означает вещество, обладающее функцией предотвращения действия ацетилхолина на рецептор M3. Термин «антагонист рецептора M5» означает вещество, обладающее функцией предотвращения действия ацетилхолина на рецептор M5. Примеры антагониста рецептора M1 и/или антагониста рецептора M3 и/или антагониста рецептора M5 включают пирензепин, атропин, тримебутин, пиперидолат, оксибутинин, тропикамид, пропиверин, толтеродин, солифенацин, дарифенацин, имидафенацин, оксифенциклимин, бромид тиотропия, эзоксибутинин, тиквизий и их производное, а также их фармакологически приемлемую соль.
Оксибутинин представлен формулой:

В используемом в настоящем описании смысле термин «агонист мускаринового рецептора» означает вещество, обладающее функцией действия на мускариновый рецептор, и включает, например, агонист рецептора M1, агонист рецептора M2, агонист рецептора M3, агонист рецептора M4 и агонист рецептора M5.
В используемом в настоящем описании смысле термин «агонист рецептора M1» означает вещество, обладающее функцией действия на рецептор M1. Термин «агонист рецептора M2» означает вещество, обладающее функцией действия на рецептор M2. Термин «агонист рецептора M3» означает вещество, обладающее функцией действия на рецептор M3. Термин «агонист рецептора M4» означает вещество, обладающее функцией действия на рецептор M4. Термин «агонист рецептора M5» означает вещество, обладающее функцией действия на рецептор M5. Примеры агониста рецептора M1 и/или агониста рецептора M2, и/или агониста рецептора M3, и/или агониста рецептора M4, и/или агониста M5 включают ацетилхолин, ацеклидин, алвамелин, талсаклидин, ксаномелин, пилокарпин, цевимелин, бетанехол, мазатикол, мускарин и их производное, а также их фармакологически приемлемую соль.
Бетанехол представлен формулой:
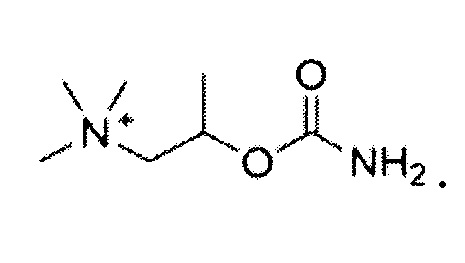
В используемом в настоящем описании смысле термин «антагонист рецептора адреналина» означает вещество, обладающее функцией предотвращения действия адреналина на рецептор, и включает, например, антагонист рецептора α1, антагонист рецептора β1, антагонист рецептора β2 и антагонист рецептора β3.
В используемом в настоящем описании смысле термин «антагонист рецептора α1» означает вещество, обладающее функцией предотвращения действия адреналина на рецептор α1. Примеры антагониста рецептора α1 включают празолин, доксазозин, буназозин, тримазозин, алфузозин, силодозин, теразозин, тамсулозин и их производное, а также их фармакологически приемлемую соль.
Тамсулозин представлен формулой:
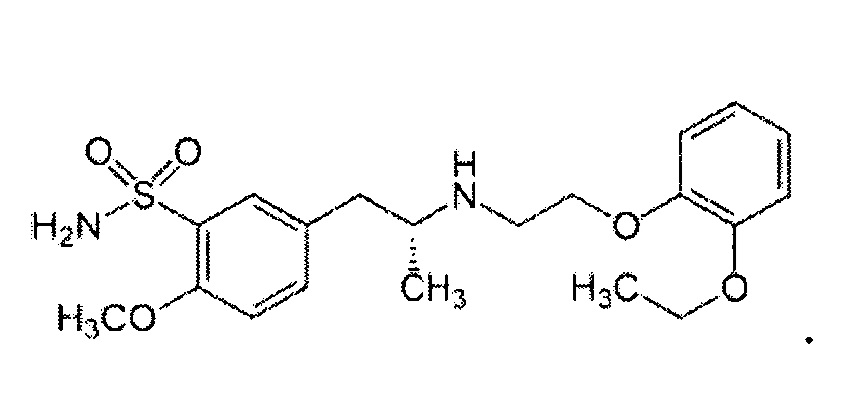
В используемом в настоящем описании смысле термин «антагонист рецептора β1» означает вещество, обладающее функцией предотвращения действия адреналина на рецептор β1. Термин «антагонист рецептора β2» означает вещество, обладающее функцией предотвращения действия адреналина на рецептор β2. Термин «антагонист рецептора β3» означает вещество, обладающее функцией предотвращения действия адреналина на рецептор β3. Примеры антагониста рецептора β1 и/или антагониста рецептора β2, и/или антагониста рецептора β3 включают бопиндолол, пиндолол, тимолол, дихлоризопреналин, алпренолол, картеолол, инденолол, бунитролол, пенбутолол, пропранолол, надолол, нипрадилол, тилизолол, ацебутолол, целипролол, метопролол, атенолол, бисопролол, бетаксолол, практолол, бевантолол, бутоксамин, карведилол, амосулалол, аротинолол, лабеталол и их производное, а также их фармакологически приемлемую соль.
Пропранолол представлен формулой:

В используемом в настоящем описании смысле термин «агонист рецептора ангиотензина» означает вещество, обладающее функцией действия на рецептор ангиотензина, и включает, например, агонист рецептора AT2.
В используемом в настоящем описании смысле термин «агонист рецептора адреналина» означает вещество, обладающее функцией действия на рецептор адреналина, и включает, например, агонист рецептора α1 и агонист рецептора α2.
В используемом в настоящем описании смысле термин «агонист рецептора α1» означает вещество, обладающее функцией действия на рецептор α1. Термин «агонист рецептора α2» означает вещество, обладающее функцией действия на рецептор α2. Примеры агониста рецептора α1 и/или агониста рецептора α2 включают норэпинефрин, норфенефрин, этилефрин, нафазолин, фенилэфрин, мидодрин, метоксамин, окседрин, метараминол, арбутамин, эфедрин, оксиметазолин, тетризолин, ксилометазолин, трамазолин, псевдоэфидрин, дипивефрин, амидефрин, метилэфедрин, рилменидин, бримонидин, медетомидин, ксилазин, тизанидин, кванфацин, метилдопа, кванабенз и их производное, а также их фармакологически приемлемую соль.
Ксилазин представлен формулой:
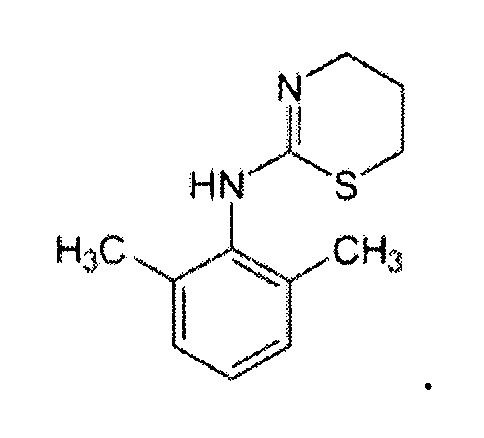
В используемом в настоящем описании смысле термин «агонист рецептора ангиотензина» означает вещество, обладающее функцией действия на рецептор ангиотензина, и включает, например, агонист рецептора AT2.
В используемом в настоящем описании смысле термин «агонист рецептора AT2» означает вещество, обладающее функцией действия на рецептор AT2. Примеры агониста рецептора AT2 включают новокинин, ангиотензин и их производное, а также их фармакологически приемлемую соль.
Ангиотензин представлен формулой:
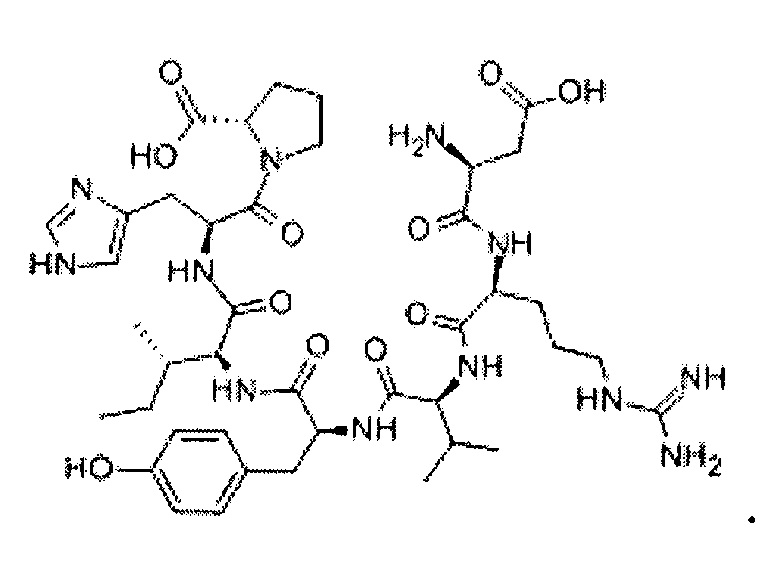
В используемом в настоящем описании смысле термин «агонист рецептора ГАМК» означает вещество, обладающее функцией действия на рецептор ГАМК, и включает, например, агонист рецептора ГАМКВ.
В используемом в настоящем описании смысле термин «агонист рецептора ГАМКВ» означает вещество, обладающее функцией действия на рецептор ГАМКВ. Примеры агониста рецептора ГАМКВ включают баклофен, γ-аминомасляную кислоту, арбаклофен и их производное, а также их фармакологически приемлемую соль.
Баклофен представлен формулой:
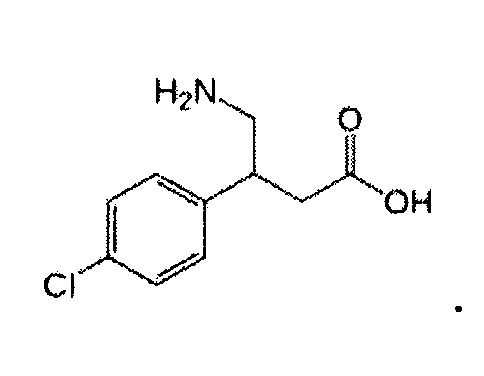
В используемом в настоящем описании смысле термин «антагонист рецептора тромбина» означает вещество, обладающее функцией предотвращения действия тромбина на рецептор, и включает, например, антагонист рецептора PAR-1.
В используемом в настоящем описании смысле термин «антагонист рецептора PAR-1» означает вещество, обладающее функцией предотвращения действия тромбина на рецептор PAR-1. Примеры антагониста рецептора PAR-1 включают ворапаксар, атопаксар, FR171113, RWJ56110, дабигатран, этексилат дабигатрана, мелагатран, ксимелагатран, гирудин, гирулог, аргатробан и их производное, а также их фармакологически приемлемую соль.
Ворапаксар представлен формулой:
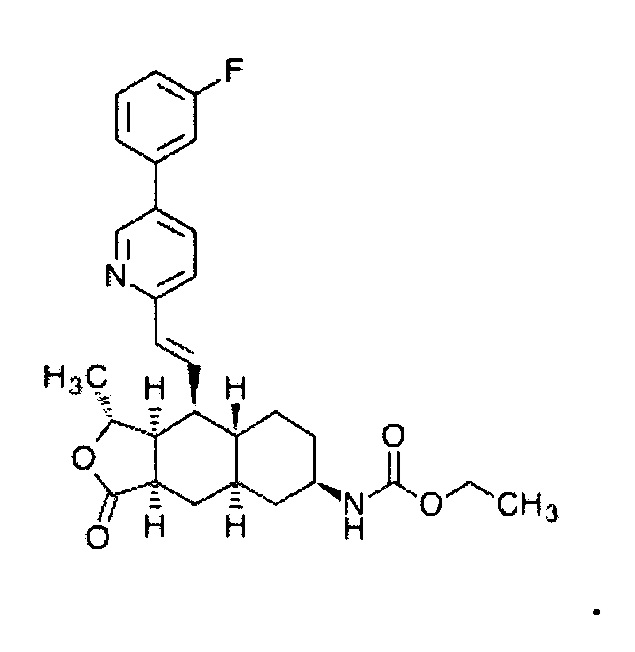
В используемом в настоящем описании смысле термин «агонист рецептора тромбина» означает вещество, обладающее функцией действия на рецептор тромбина, и включает, например, агонист рецептора PAR-1.
В используемом в настоящем описании смысле термин «агонист рецептора PAR-1» означает вещество, обладающее функцией действия на рецептор PAR-1. Примеры агониста рецептора PAR-1 включают TRAP-6, TRAP-14, NAT6-NH2 и их производное, а также их фармакологически приемлемую соль.
TRAP-6 представлен формулой:
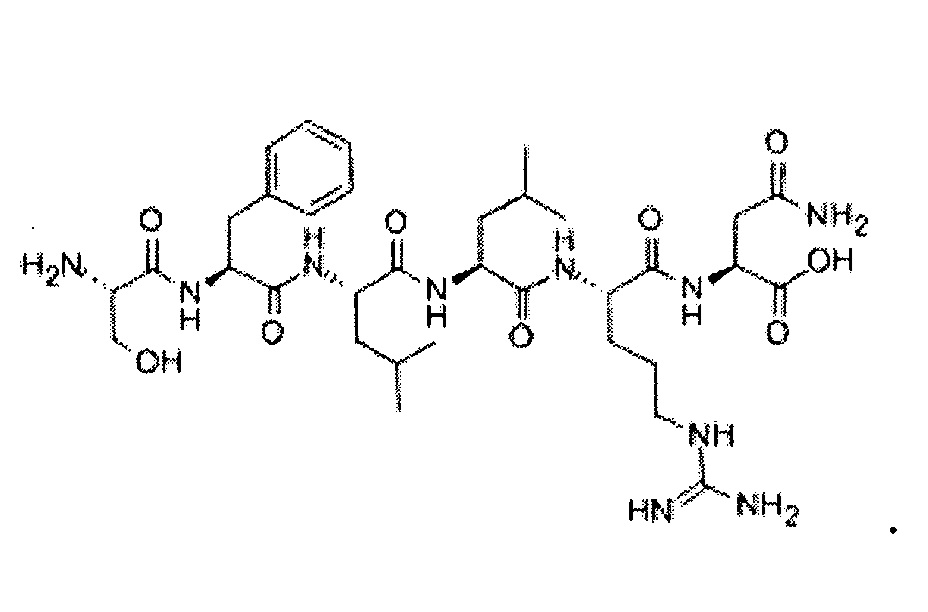
В используемом в настоящем описании смысле термин «агонист опиоидного рецептора» означает вещество, обладающее функцией действия на опиоидный рецептор. Примеры агониста опиоидного рецептора включают тримебутин, алвимопан, морфин, оксикодон, дигидрокодеин, диаморфин, петидин, пентазоцин, бупренорфин, буторфанол, налбуфин, тилидин, дезоцин, мептазинол, тапентадол, налтрексон, метадон, этилморфин, гидрокодон, ацетилдигидрокодеин, налорфин, лоперамид, ремоксиприд, опипрамол, и их производное, а также их фармакологически приемлемую соль.
Бупренорфин представлен формулой:

В используемом в настоящем описании смысле термин «антагонист рецептора лейкотриена» означает вещество, обладающее функцией предотвращения действия лейкотриена на рецептор, и включает, например, антагонист рецептора CysLT1 и антагонист рецептора CysLT2.
В используемом в настоящем описании смысле термин «антагонист рецептора CysLT1» означает вещество, обладающее функцией предотвращения действия лейкотриена на рецептор CysLT1. Термин «антагонист рецептора CysLT2» означает вещество, обладающее функцией предотвращения действия лейкотриена на рецептор CysLT2. Примеры антагониста рецептора CysLT1 и/или антагониста рецептора CysLT2 включают монтелукаст, зафирлукаст, пранлукаст, и их производное, а также их фармакологически приемлемую соль. Примеры фармакологически приемлемой соли монтелукаста включают монтелукаст натрия и тому подобные.
Монтелукаст натрия представлен формулой:
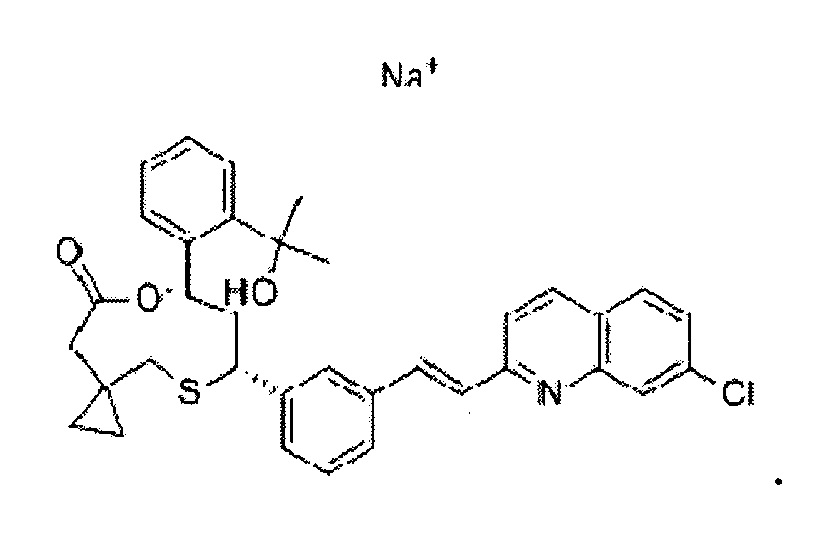
В используемом в настоящем описании смысле термин «агонист рецептора лейкотриена» означает вещество, обладающее функцией действия на рецептор лейкотриена, и включает, например, агонист рецептора BLT.
В используемом в настоящем описании смысле термин «агонист рецептора BLT» означает вещество, обладающее функцией действия на рецептор BLT. Примеры агониста рецептора BLT включают лейкотриен B4, CAY10583 и их производное, а также их фармакологически приемлемую соль.
Лейкотриен B4 представлен формулой:

В используемом в настоящем описании смысле термин «агонист рецептора АДФ» означает вещество, обладающее функцией действия на рецептор АДФ. Примеры агониста рецептора АДФ включают аденозиндифосфат и его производное, а также его фармакологически приемлемую соль.
Аденозиндифосфат представлен формулой:
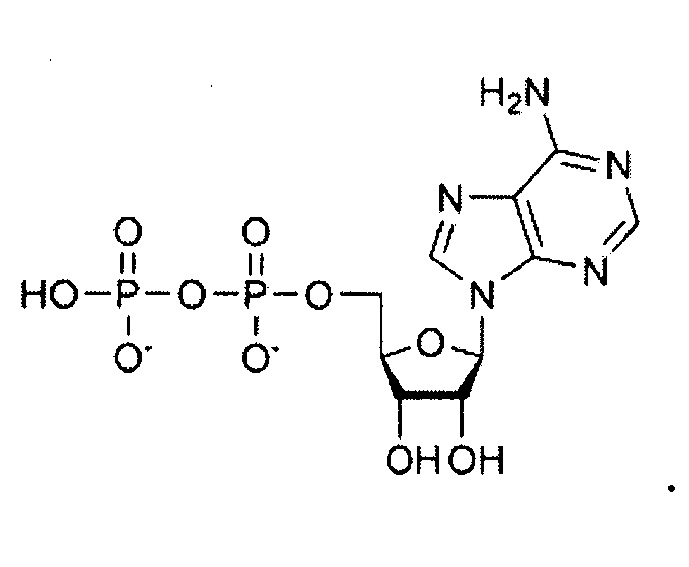
В используемом в настоящем описании смысле термин «агонист рецептора мелатонина» означает вещество, обладающее функцией действия на рецептор мелатонина. Примеры агониста рецептора мелатонина включают мелатонин, перлапин, тасимелтеон и их производное, а также их фармакологически приемлемую соль.
Мелатонин представлен формулой:
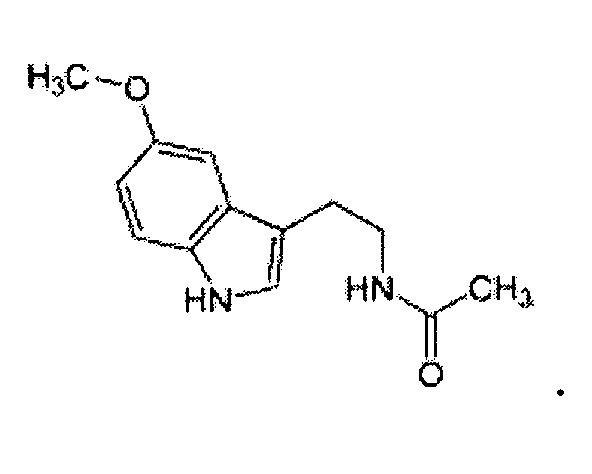
В используемом в настоящем описании смысле термин «агонист рецептора соматостатина» означает вещество, обладающее функцией действия на рецептор соматостатина. Примеры агониста рецептора соматостатина включают соматостатин, соматостатин-14, октреотид и их производное, а также их фармакологически приемлемую соль.
Октреотид представлен формулой:
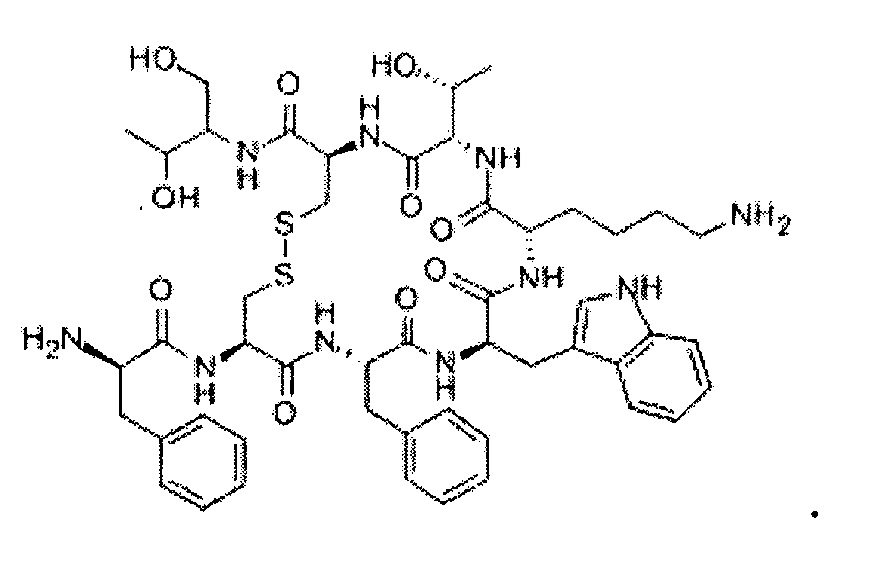
В используемом в настоящем описании смысле термин «агонист рецептора каннабиноида» означает вещество, обладающее функцией действия на рецептор каннабиноида. Примеры агониста рецептора каннабиноида включают дронабинол, набилон, левонантрадол, отенабант, GW833972A, GW405833 и их производное, а также их фармакологически приемлемую соль.
Дронабинол представлен формулой:

В используемом в настоящем описании смысле термин «агонист рецептора сфингозин-1-фосфата» означает вещество, обладающее функцией действия на рецептор сфингозин-1-фосфата. Примеры агониста рецептора сфингозин-1-фосфата включают финголимод, понесимод, RPC-1063, ONO-4641, SEW2871, сфингозин-1-фосфат и их производное, а также их фармакологически приемлемую соль.
Финголимод представлен формулой:

В используемом в настоящем описании смысле термин «агонист метаботропного рецептора глутамата» означает вещество, обладающее функцией действия на метаботропный рецептор глутамата, и включает, например, агонист рецептора mGluR2, агонист рецептора mGluR3, агонист рецептора mGluR4, агонист рецептора mGluR6, агонист рецептора mGluR7 и агонист рецептора mGluR8.
В используемом в настоящем описании смысле термин «агонист рецептора mGluR2» означает вещество, обладающее функцией действия на рецептор mGluR2. Термин «агонист рецептора mGluR3» означает вещество, обладающее функцией действия на рецептор mGluR3. Термин «агонист рецептора mGluR4» означает вещество, обладающее функцией действия на рецептор mGluR4. Термин «агонист рецептора mGluR6» означает вещество, обладающее функцией действия на рецептор mGluR6. Термин «агонист рецептора mGluR7» означает вещество, обладающее функцией действия на рецептор mGluR7. Термин «агонист рецептора mGluR8» означает вещество, обладающее функцией действия на рецептор mGluR8. Примеры агониста рецептора mGluR2 и/или агониста рецептора mGluR3, и/или агониста рецептора mGluR4, и/или агониста рецептора mGluR6, и/или агониста рецептора mGluR7, и/или агониста рецептора mGluR8 включают VU0361737, VU0155041, бифенилинданон A, PBDA, L-AP4, и их производное, а также их фармакологически приемлемую соль.
VU0361737 представлен формулой:

В используемом в настоящем описании смысле термин «ингибитор фосфолипазы A2» означает вещество, обладающее функцией ингибирования активности фосфолипазы A2. Примеры ингибитора фосфолипазы A2 включают глицирризиновую кислоту, глицирретиновую кислоту и их производное, а также их фармакологически приемлемую соль.
Глицирретиновая кислота представлена формулой:

В используемом в настоящем описании смысле термин «ингибитор продукции TGF-β» означает вещество, обладающее функцией ингибирования продукции TGF-β. Примеры ингибитора продукции TGF-β включают пирфенидон, траниласт и их производное, а также их фармакологически приемлемую соль.
Пирфенидон представлен формулой:
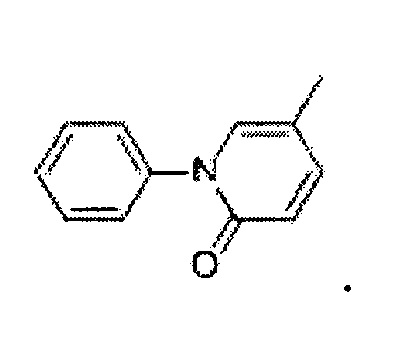
В используемом в настоящем описании смысле термин «ингибитор цитокина Th2» означает вещество, обладающее функцией ингибирования продукции цитокина Th2, такое как IL-4 и IL-5. Примеры ингибитор цитокина Th2 включают суплатаст и его производное, а также его фармакологически приемлемую соль. Примеры фармакологически приемлемой соли суплатаста включают тозилат суплатаста. В предпочтительном аспекте настоящего изобретения ингибитором цитокина Th2 является тозилат суплатаста.
Тозилат суплатаста представлен формулой:
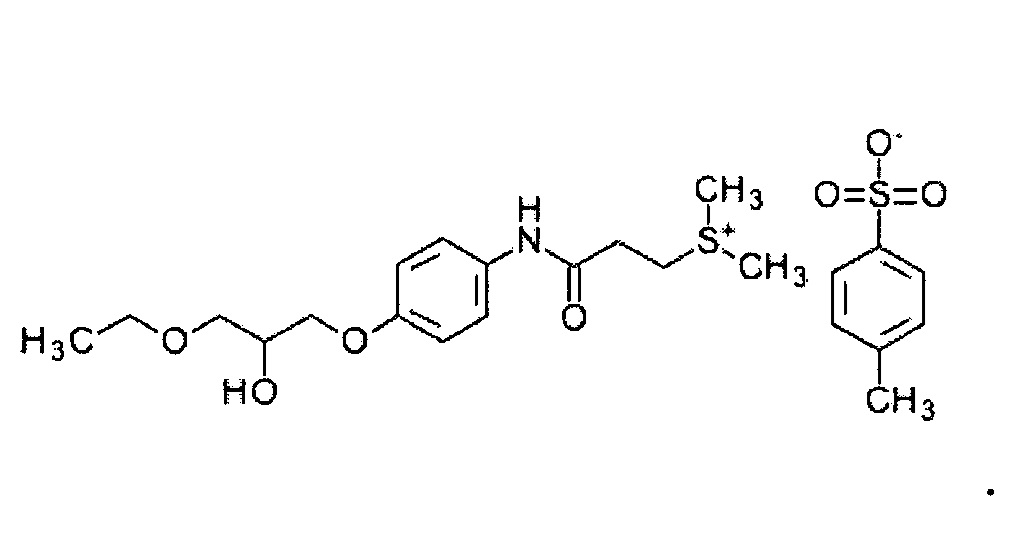
В используемом в настоящем описании смысле термин «кислота» означает кислоту Бронстеда и включает неорганические кислоты и органическое кислоты, предпочтительно карбоновые кислоты, например, жирную кислоту и молочную кислоту. В используемом в настоящем описании смысле термин «фармакологически приемлемая кислота» в качестве первого стимулятора индукции клеточного иммунитета, которая может входить в состав композиции согласно настоящему изобретению, означает кислоту, которая не оказывает вредного влияния на субъект, которому вводят композицию, и не приводит к потере фармакологической активности ингредиентов в композиции. В предпочтительном аспекте настоящего изобретения фармакологически приемлемой кислотой является органическая кислота, более предпочтительно органическое соединение, содержащее карбоксильную группу, или органическое соединение, содержащее сульфонатную группу, более предпочтительно насыщенная или ненасыщенная жирная кислота с прямой или разветвленной цепью, в которой часть, представленная насыщенной прямой цепью, имеет от 8 до 20 атомов углерода, молочная кислота, яблочная кислота, салициловая кислота, малеиновая кислота, лимонная кислота, или органическое соединение, содержащее сульфонатную группу, более предпочтительно насыщенная или ненасыщенная жирная кислота с прямой или разветвленной цепью, в которой часть, представленная насыщенной прямой цепью, имеет от 8 до 16 атомов углерода, молочная кислота, яблочная кислота, салициловая кислота, малеиновая кислота, лимонная кислота, или органическое соединение, содержащее сульфонатную группу, более предпочтительно жирная кислота, выбранная из группы, состоящей из декановой кислоты, лауриновой кислоты, миристиновой кислоты, изостеариновой кислоты и олеиновой кислоты, или молочной кислоты, салициловой кислоты, лимонной кислоты или метансульфоновой кислоты.
В используемом в настоящем описании смысле «фармакологически приемлемая соль», которая может входить в состав композиции согласно настоящему изобретению, означает соль, которая не оказывает вредного влияния на субъекта, которому вводят композицию, и не приводит к утрате фармакологической активности ингредиентов в композиции, и включает соли неорганических кислот (например, гидрохлорид и фосфат), соли органических кислот (например, ацетат, фталат и соль ТФУ), соли металлов (соли щелочных металлов (например, соль натрия и соль калия), соли щелочноземельных металлов (например, соль кальция и соль магния), соль алюминия и т.д.), соли аминов (соль триэтиламина, соль бензиламина, соль диэтаноламина, соль трет-бутиламина, соль дициклогексиламина, соль аргинина, соль диметиламмония, соль аммония и т.д.), но не ограничена указанными солями.
В используемом в настоящем описании смысле термин «иммуномодулирующее низкомолекулярное лекарственное средство» означает вещество, которое активирует или подавляет иммунные клетки, такие как T-клетка, NK-клетка, макрофаг и тому подобные, и которое не соответствует ни одному из указанных выше веществ: лиганду TLR, циклическому динуклеотиду, хелперному пептиду, иммуномодулирующему низкомолекулярному лекарственному средству, ингибитору циклооксигеназы, антагонисту рецептора простагландина, агонисту рецептора простагландина, ингибитору продукции TSLP, ингибитору аденилатциклазы, омега-3 жирной кислоте, агонисту PPAR, антагонисту рецептора дофамина, агонисту рецептора дофамина, агонисту рецептора гистамина, антагонисту рецептора гистамина, агонисту рецептора серотонина, антагонисту рецептора серотонина, антагонисту рецептора вазопрессина, агонисту рецептора вазопрессина, антагонисту мускаринового рецептора, агонисту мускаринового рецептора, антагонисту рецептора адреналина, агонисту рецептора адреналина, агонисту рецептора ангиотензина, агонисту рецептора ГАМК, антагонисту рецептора тромбина, агонисту рецептора тромбина, агонисту опиоидного рецептора, агонисту рецептора АДФ, антагонисту рецептора лейкотриена, агонисту рецептора лейкотриена, агонисту рецептора мелатонина, агонисту рецептора соматостатина, агонисту рецептора каннабиноида, агонисту рецептора сфингозин-1-фосфата, агонисту метаботропного рецептора глутамата, ингибитору фосфолипазы A2, ингибитору продукции TGF-β и ингибитору цитокина Th2. Примеры иммуномодулирующего низкомолекулярного лекарственного средства включают бестатин, пидотимод, левамизол, голотимод, форфеникинол и их производное, а также их фармакологически приемлемую соль. Примеры фармакологически приемлемой соли левамизола включают гидрохлорид левамизола и тому подобные.
Бестатин представлен формулой:

Пидотимод представлен формулой:

Гидрохлорид левамизола представлен формулой:
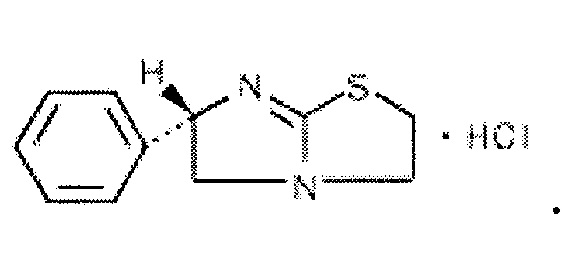
В настоящем изобретении иммуномодулирующим низкомолекулярным лекарственным средством обычно является соединение, имеющее молекулярную массу менее 1000, предпочтительно менее 500. В предпочтительном аспекте настоящего изобретения иммуномодулирующим низкомолекулярным лекарственным средством является одно или несколько соединений, выбранных из группы, состоящей из бестатина, пидотимода и гидрохлорида левамизола.
Как описано выше, авторы настоящего изобретения обнаружили, что среди множества стимуляторов индукции клеточного иммунитета лиганд TLR, циклический динуклеотид, хелперный пептид, иммуномодулирующее низкомолекулярное лекарственное средство, ингибитор циклооксигеназы, антагонист рецептора простагландина, агонист рецептора простагландина, ингибитор продукции TSLP, ингибитор аденилатциклазы, омега-3 жирная кислота, агонист PPAR, антагонист рецептора дофамина, агонист рецептора дофамина, агонист рецептора гистамина, антагонист рецептора гистамина, агонист рецептора серотонина, антагонист рецептора серотонина, антагонист рецептора вазопрессина, агонист рецептора вазопрессина, антагонист мускаринового рецептора, агонист мускаринового рецептора, антагонист рецептора адреналина, агонист рецептора адреналина, агонист рецептора ангиотензина, агонист рецептора ГАМК, антагонист рецептора тромбина, агонист рецептора тромбина, агонист опиоидного рецептора, агонист рецептора АДФ, антагонист рецептора лейкотриена, агонист рецептора лейкотриена, агонист рецептора мелатонина, агонист рецептора соматостатина, агонист рецептора каннабиноида, агонист рецептора сфингозин-1-фосфата, агонист метаботропного рецептора глутамата, ингибитор фосфолипазы A2, ингибитор продукции TGF-β и ингибитор цитокина Th2 являются особенно применимыми для трансдермального введения пептидного антигена WT1 и/или модифицированного пептидного антигена WT1, и следовательно, в одном аспекте второй стимулятор индукции клеточного иммунитета, который можно применять вместе с фармакологически приемлемой кислотой или ее фармакологически приемлемой солью в настоящем изобретении, выбран из одного или нескольких таких видов. В качестве способа количественного измерения индукции клеточного иммунитета разработано множество способов, и можно использовать один или несколько таких способов, например, способ ELISPOT, описанный в примерах.
В используемом в настоящем описании смысле неинвазивное введение означает введение без активного причинения физического раздражения и/или химического раздражения, предпочтительно, без физического раздражения (например, без раздражения при соскобе липкой лентой или раздражения микроиглой) кожи.
В используемом в настоящем описании смысле термин «условие слабого раздражения» означает условие, в случае которого раздражение, причиняемое коже, меньше, чем раздражение, обычно причиняемое, чтобы улучшить проницаемость кожи для антигена, находящегося в обычных вакцинах, или условие, в случае которого кожа вообще не получает раздражения. В общем, физическую и/или химическую стимуляцию кожи осуществляют перед или одновременно с трансдермальным введением обычной вакцинной композиции так, чтобы антиген мог проникнуть через кожу. В предпочтительном аспекте настоящего изобретения примеры условия слабого раздражения включают условие слабого физического раздражения и условие слабого химического раздражения. Условие слабого физического раздражения представляет собой, например, условие, при котором трансэпидермальная потеря влаги (TEWL) (г/час⋅м2) у модельного животного при оценке раздражения кожи составляет 50 или меньше, предпочтительно 45 или меньше, более предпочтительно 40 или меньше, еще более предпочтительно 35 или меньше, и еще более предпочтительно 30 или меньше. Так как уровень TEWL составляет примерно 2 (г/час⋅м2) в необработанной коже, то уровень TEWL перед введением составляет 2 (г/час⋅м2) или больше. Условием слабого химического раздражения является, например, условие, при котором уровень тимусного стромального лимфопоэтина (TSLP) (пг/мл белка) в коже модельного животного при оценке раздражения кожи составляет 10000 или меньше, предпочтительно 9000 или меньше, более предпочтительно 8000 или меньше, еще более предпочтительно 7000 или меньше. Так как уровень TSLP составляет 1 (пг/мг белка) в необработанной коже, то уровень TSLP при осуществлении введения вакцинной композиции превышает 1 (пг/мг белка), предпочтительно превышает 2 (пг/мг белка), более предпочтительно превышает 3 (пг/мг белка). «Тимусный стромальный лимфопоэтин (TSLP)» является цитокином, который принимает участие в дифференцировке и рекрутинге T-клеток и который может быть использован в качестве показателя степени раздражения кожи в настоящем изобретении. Более высокое значение TSLP означает более сильное раздражение кожи. Примеры средств достижения условия слабого физического раздражения включают исключение проведения обычной предварительной обработки кожи перед введением, например, исключение соскоба липкой лентой, пункции микроиглой или тому подобного перед введением. Примеры средств достижения условия слабого химического раздражения включают избегание введения раздражающего химического ингредиента, такого как этанол, поверхностно-активное вещество или тому подобного в определенном или большем количестве. Способ достижения условия слабого раздражения можно определить, используя модельное животное для оценки раздражения кожи, и определяемый при этом способ можно применять на субъекте, которому необходимо лечение вакцинной композицией, например, человеке.
В используемом в настоящем описании смысле термин «злокачественная опухоль» означает злокачественную опухоль, ассоциированную с аномальной экспрессией, например, сверхэкспрессией гена WT1. Примеры злокачественной опухоли могут включать гематопоэтические опухоли или солидные злокачественные опухоли. Примеры гематопоэтических опухолей, ассоциированных с аномальной экспрессией гена WT1, включают без ограничения лейкоз, такой как острый миелоцитарный лейкоз, острый лимфоцитарный лейкоз и хронический миелоцитарный лейкоз, миелодиспластический синдром, множественную миелому, а также злокачественную лимфому, такую как неходжкинская лимфома. Примеры солидных злокачественных опухолей, ассоциированных с аномальной экспрессией гена WT1, включают без ограничения, рак легкого, рак молочной железы, рак желудка, рак толстой/прямой кишки, рак половых клеток, рак печения, рак кожи, рак поджелудочной железы, рак желчных протоков, плоскоклеточный рак головы и шеи, рак щитовидной железы, рак почек, рак мочевого пузыря, рак простаты, рак яичника, рак матки, рак шейки матки, саркому мягких тканей и костей, злокачественную меланому, злокачественную мезотелиому, опухоль половых клеток яичка и злокачественную глиому.
В используемом в настоящем описании смысле термин «аномальная экспрессия гена» означает, что уровень экспрессии гена в клетке заметно повышен или понижен, например, в 2 раза или больше, например в 4 раза или больше, по сравнению с другими клетками в той же ткани. Термин «сверхэкспрессия» означает, что аномальная экспрессия представляет собой повышение уровня экспрессия. Уровень экспрессии гена можно легко измерить, используя любой хорошо известный в данной области способ.
В используемом в настоящем описании смысле термин «субъект» означает любое животное, имеющее ген WT1, иммунный ответ которого может быть индуцирован посредством трансдермального введения композиции противораковой вакцины для трансдермального введения на практической стадии. Обычно субъектом может быть млекопитающее, такое как человек, мышь, крыса, собака, кошка, кролик, лошадь, корова, овца, свинья, коза, мартышка, шимпанзе или тому подобные. Особенно предпочтительным субъектом является человек.
В используемом в настоящем описании смысле термин «модельное животное для иммунологической оценки» означает модельное животное для оценки свойства композиции противораковой вакцины для трансдермального введения индуцировать иммунитет. В частности, термин означает модельное животное для оценки свойства индуцировать клеточный иммунитет. Модельное животное для иммунологической оценки следует выбирать с точки зрения совместимости между антигеном в композиции вакцины, которую необходимо оценить, и молекулой MHC класса 1 животного. Следует использовать животную модель, подходящую для оценки свойства композиции вакцины индуцировать клеточный иммунитет. Например, в случае композиции вакцины, содержащей пептид класса 1, ограниченный по MHC типа HLA-A*24, свойство можно оценивать на мыши BALB/c. В случае композиции вакцины, содержащей пептид, ограниченный по MHC типа HLA-A*02, свойство можно оценивать на генетически модифицированной мыши, на которой можно оценивать индукцию иммунитета пептидом, ограниченным по MHC типа HLA-A*02. В случае композиции вакцины, содержащей пептид, ограниченный по MHC другого HLA-типа, свойство оценивают на животном, на котором можно оценивать индукцию иммунитета пептидом, ограниченным по MHC данного HLA-типа. В случае композиции вакцины, содержащей белковый антиген, свойство оценивают на животном, имеющем MHC, совместимый с эпитопом класса 1, используемым для индукции иммунитета, из числа различных эпитопов класса 1, включенных в состав аминокислотной последовательности белкового антигена. Кроме того, в случае композиции противораковой вакцины для трансдермального введения, в которой использован пептид Db126, который совместим не только с типом HLA-A*02, но также с типом MHC-H-2Db, в качестве модельного животного для иммунологической оценки можно использовать не только генетически модифицированную мышь, у которой можно оценивать индукцию иммунитета пептидом, ограниченным MHC типа HLA-A*0201, но также и мышь C57BL/6, которая является животным, имеющим тип MHC-H-2Db. В случае срезания волос животного при подготовке места для трансдермального введения животное следует использовать после заживления у него повреждения кожи, вызванного срезанием волос.
В используемом в настоящем описании смысле термин «модельное животное для оценки раздражения кожи» означает модельное животное для оценки трансэпидермальной потери влаги (TEWL) в качестве показателя физического раздражения кожи или модельное животное для оценки TSLP в качестве показателя свойства раздражения кожи композицией противораковой вакцины для трансдермального введения. Независимо от вида антигена, входящего в состав композиции противораковой вакцины для трансдермального введения, мышь C57BL/6 можно использовать в качестве модельного животного для оценки раздражения кожи. В случае срезания волос животного при подготовке места для трансдермального введения животное следует использовать после заживления у него повреждения кожи, вызванного срезанием волос.
II. Композиция противораковой вакцины для трансдермального введения
Ранее уже было показано, что пептиды WT1 и/или модифицированные пептиды WT1 применимы в качестве противораковой вакцины (например, патентный документ 1).
В используемом в настоящем описании смысле композиция «для трансдермального введения» может быть представлена в виде любого препарата или препаративной формы, которую обычно используют для трансдермального введения, например, в виде жидкого препарата для наружного применения, такого как препарат в виде линимента или препарат для примочки, препарата в виде спрея для наружного применения, такого как аэрозольный препарат, препарата в виде мази, препарата в виде наклейки, препарата в форме крема, гелевого препарата или препарата в виде пластыря, такого как препарат в форме клейкой ленты, или препарата для горячего компресса. Группы, определения, природа, способ получения и тому подобное в отношении таких препаратов или препаративных форм хорошо известны в данной области. Например, смотри Фармакопею Японии, 16-е издание. Композиция для трансдермального введения, подходящая для настоящего изобретения, имеет форму препарата в форме крема, жидкого препарата для наружного применения или препарата в форме клейкой ленты.
Примеры основы для препарата линимента включают воду; спирты, такие как этанол и пропиленгликоль; жирные масла, такие как твердый парафин, мягкий парафин, жидкий парафин, глицерин, парафиновое масло, пчелиный воск и металлическое мыло; клейкое вещество; природные масла (например, миндальное масло, кукурузное масло, арахисовое масло, касторовое масло, оливковое масло или их производное (такое как полиоксилированное касторовое масло)); бараний жир или его производное, жирные кислоты и/или сложные эфиры (например, стеариновую кислоту, олеиновую кислоту, изопропилмиристат), а также их смесь.
Препарат в форме примочки представляет собой препарат, в котором активный ингредиент тонко и гомогенно диспергирован в водной жидкости, и существуют суспензионный препарат для примочки и эмульгированный препарат для примочки. Примеры суспендирующего средства включают аравийскую камедь, альгинат натрия, натрий-карбоксиметилцеллюлозу, метилцеллюлозу, бентонит и тому подобное. Примеры эмульгирующего средства включают лаурилсульфат натрия, сложный эфир сорбитана и жирной кислоты и тому подобные.
Например, в качестве основы для мази обычно можно использовать гидрофобную основу, такую как жиры или масла, воски и углеводородные соединения. В частности, примеры основы для мазей включают минеральные основы, такие как желтый вазелин, белый вазелин, парафин, жидкий парафин, пластибейз, силикон и тому подобное, и животные или растительные основы, такие как пчелиный воск, животный жир или растительное масло и тому подобное.
Примеры основы для препарата в форме крема включают основы типа вода/масло, такие как гидрофильная мазь, быстро впитывающийся крем и тому подобные; и основы типа масло/вода, такие как гидрофильный вазелин, очищенный ланолин, аквахол, эуцерин, неоцерин, водный ланолин, кольдкрем, гидрофильная основа пластибейз и тому подобные.
В качестве основы геля можно использовать, например, следующие основы: карбоксивиниловый полимер, гелевую основу, не содержащую жира мазь, поливинилпирролидон, поливиниловый спирт, полиакрилат натрия, карбоксиметилцеллюлозу, крахмал, ксантановую камедь, камедь карайи, альгинат натрия, метилцеллюлозу, гидроксипропилцеллюлозу, фталат гидроксипропилметилцеллюлозы (HPMCP), ацетат-фталат целлюлозы (CAP), карбоксиметилэтилцеллюлозу (CMEC), этилцеллюлозу, гидроксиэтилцеллюлозу, гидроксипропилметилцеллюлозу, карбоксивиниловый полимер, трагакантовую камедь, аравийскую камедь, камедь тары, камедь семян тамаринда, камедь семян подорожника, агар, геллановую камедь, глюкоманнан, камедь бобов рожкового дерева, гуаровую камедь, каррагинан, декстрин, декстран, амилозу, калий-карбоксиметилцеллюлозу, натрий-карбоксиметилцеллюлозу, кальций-карбоксиметилцеллюлозу, пуллулан, хитозан, натрий-карбоксиметилкрахмал, оболочку семян подорожника, галактоманнан, сополимер аминоалкилметакрилата E, сополимер аминоалкилметакрилата RS, сополимер метакриловой кислоты L, сополимер метакриловой кислоты LD, сополимер метакриловой кислоты S, сополимер метилакрилат/метакриловая кислота/метилметакрилат, сополимер этилакрилат/метилметакрилат, диэтиламиноацетат поливинилацеталя, казеин, сложный алкиловый эфир альгиновой кислоты, желатин, полиэтиленгликоль и тому подобное в виде основы гидрогеля.
Примеры основы препарата для горячего компресса включают желатин, натрий-карбоксиметилцеллюлозу, метилцеллюлозу, полиакрилат натрия, каолин, поливиниловый спирт, поливинилпирролидон, глицерин, пропиленгликоль, воду и тому подобное.
Например, препарат в форме клейкой ленты имеет липкий слой, содержащий акриловый адгезив, природный каучуковый адгезив, синтетический каучуковый адгезив (включая каучуковый эластомер, такой как синтетический изопреновый каучук, полиизобутилен (PIB), стирол-бутадиеновый каучук, стирол-изопрен-стирольный (SIS) каучук и т.д.), силиконовый адгезив, адгезив на основе сложного винилового эфира, адгезив на основе простого винилового эфира или тому подобное, и подложку, которая поддерживает адгезивный слой. Необязательно препарат может дополнительно содержать защитную удаляемую пленку, которая покрывает адгезивный слой, чтобы избежать его обнажения до применения, и которую можно легко снять с адгезивного слоя при использовании.
Количество пептида WT1 и/или модифицированного пептида WT1, фармакологически приемлемой кислоты или ее фармакологически приемлемой соли и стимулятора индукции клеточного иммунитета в композиции противораковой вакцины для трансдермального введения согласно настоящему изобретению особым образом не ограничено. В одном аспекте композиция противораковой вакцины для трансдермального введения согласно настоящему изобретению содержит пептид WT1 и/или модифицированный пептид WT1 предпочтительно в количестве от 0,01 до 40% масс., более предпочтительно от 0,1 до 30% масс. в расчете на общую массу композиции. В одном аспекте композиция противораковой вакцины для трансдермального введения согласно настоящему изобретению содержит фармакологически приемлемую кислоту или ее фармакологически приемлемую соль предпочтительно в количестве от 0,001 до 30% масс., более предпочтительно от 0,01 до 20% масс. в расчете на общую массу композиции. Когда композиция противораковой вакцины для трансдермального введения согласно настоящему изобретению содержит стимулятор индукции клеточного иммунитета, стимулятор индукции клеточного иммунитета предпочтительно содержится в количестве от 0,001 до 30% масс., более предпочтительно от 0,01 до 20% масс. в расчете на общую массу композиции.
Когда композиция противораковой вакцины для трансдермального введения согласно настоящему изобретению представлена препаратом в форме клейкой ленты, адгезивный слой препарата в форме клейкой ленты (далее также называемого «препаратов в форме клейкой ленты согласно настоящему изобретению») содержит антиген и, необязательно, дополнительно содержит стимулятор индукции клеточного иммунитета. В одном аспекте адгезивный слой препарата в форме клейкой ленты согласно настоящему изобретению содержит антиген предпочтительно в количестве от 0,01 до 40% масс., более предпочтительно от 0,1 до 30% масс. в расчете на общую массу адгезивного слоя. Когда адгезивный слой препарата в форме клейкой ленты согласно настоящему изобретению содержит стимулятор индукции клеточного иммунитета, стимулятор индукции клеточного иммунитета предпочтительно содержится в количестве от 0,001 до 30% масс., более предпочтительно от 0,01 до 20% масс. в расчете на общую массу адгезивного слоя.
Адгезив, который должен образовывать адгезивный слой препарата в форме клейкой ленты согласно настоящему изобретению, особым образом не ограничен, и его примеры включают акриловые адгезивы, состоящие из акрилового полимера; каучуковые адгезивы, содержащие каучуковый эластомер, такой как стирол-диен-стироловый блок-сополимер (например, стирол-изопрен-стироловый блок-сополимер, стирол-бутадиен-стироловый блок-сополимер и т.д.), полиизопрен, полиизобутилен, бутилкаучук, полибутадиен и тому подобные; силиконовые адгезивы, такие как силиконовый каучук, диметилсилоксановая основа, дифенилсилоксановая основа и тому подобные; адгезивы на основе простого винилового эфира, такие как простой поливинилметиловый эфир, простой поливинилэтиловый эфир, простой поливинилизобутиловый эфир и тому подобные; адгезивы на основе сложного винилового эфира, такие как сополимер винилацетат-этилен и тому подобные; и сложные полиэфирные адгезивы, состоящие из компонента карбоновой кислоты, такого как диметилтерефталат, диметилизофталат, диметилфталат, и компонента многоатомного спирта, такого как этиленгликоль. Особенно предпочтительным адгезивом является акриловый адгезив, каучуковый адгезив и силиконовый адгезив. Такие адгезивы находятся в адгезивном слое предпочтительно в количестве от 10 до 90% масс., более предпочтительно от 20 до 80% масс., в виде твердого вещества в расчете на общую массу адгезивного слоя.
Примеры акрилового адгезива включают адгезив на основе сложного эфира акриловой кислоты, содержащий в качестве основного компонента полимер, содержащий сложный C2-C18-алкиловый эфир (мет)акриловой кислоты в качестве первого мономера. Примеры сложного алкилового эфира (мет)акриловой кислоты (первого мономера) включают сложные алкиловые эфиры (мет)акриловой кислоты, в которых алкильной группой является алкильная группа с прямой цепью, разветвленной цепью или циклическая алкильная группа, имеющая от 1 до 18 атомов углерода (например, метил, этил, пропил, бутил, пентил, гексил, циклогексил, гептил, октил, 2-этилгексил, нонил, децил, ундецил, додецил, тридецил и т.д.). Предпочтительными являются сложные алкиловые эфиры (мет)акриловой кислоты, в которых алкильной группой является алкильная группа с прямой цепью, разветвленной цепью или циклическая алкильная группа, имеющая от 4 до 18 атомов углерода (например, бутил, пентил, гексил, циклогексил, гептил, октил, 2-этилгексил, нонил, децил, ундецил, додецил, тридецил и т.д.). Кроме того, так как применение мономерного компонента, который снижает температуру стеклования полимера, является подходящим для придания адгезивности при комнатной температуре, более предпочтительными являются сложные алкиловый эфиры (мет)акриловой кислоты, в которых алкильной группой является алкильная группа с прямой цепью, разветвленной цепью или циклическая алкильная группы, имеющая от 4 до 8 атомов углерода (например, бутил, пентил, гексил, циклогексил, гептил, октил, 2-этилгексил и т.д., предпочтительно бутил, 2-этилгексил и циклогексил, особенно предпочтительно 2-этилгексил). В частности, более предпочтительными являются бутилакрилат, 2-этилгексилакрилат, 2-этилгексилметакрилат, циклогексилакрилат, циклогексилметакрилат и тому подобные, и среди них наиболее предпочтительным является 2-этилгексилакрилат. Такие сложные алкиловые эфиры (мет)акриловой кислоты (первый мономерный компонент) можно использовать отдельно или их можно использовать, сочетая по два или больше.
Кроме того, акриловый адгезив может содержать второй мономер сополимеризуемый со сложным алкиловым эфиром (мет)акриловой кислоты, и примеры второго мономера включают мономеры, имеющие функциональную группу, которая может стать точкой поперечного сшивания при использовании поперечно сшивающего агента. Примеры функциональной группы, которая может принимать участие в реакции образования поперечной сшивки, включают гидроксигруппу, карбоксильную группу, группу винила и тому подобные, и предпочтительными являются гидроксигруппа и карбоксильная группа. Конкретные примеры мономера (второго мономерного компонента) включают сложный гидроксиэтиловый эфир (мет)акриловый кислоты, сложный гидроксипропиловый эфир (мет)акриловый кислоты, N-гидроксиалкил(мет)акриламид, (мет)акриловую кислоту, итаконовую кислоту, малеиновую кислоту, малеиновый ангидрид, мезаконовую кислоту, цитраконовую кислоту, глютаконовую кислоту и тому подобные. Среди них наиболее предпочтительными с точки зрения легкой доступности являются акриловая кислота, метакриловая кислота и сложный гидроксиэтиловый эфир акриловой кислоты (в частности, 2-гидроксиэтилакрилат), и наиболее предпочтительной является акриловая кислота. Такие мономеры (второй мономерный компонент) можно использовать отдельно или их можно использовать, сочетая по два или больше.
Кроме того, акриловый адгезив необязательно может содержать третий мономер дополнительно ко второму мономеру. Примеры третьего мономера (третьего мономерного компонента) включают сложные виниловые эфиры, такие как винилацетат, винилпропионат и тому подобные; простые виниловые эфиры, такие как метилвиниловый эфир, этилвиниловый эфир и тому подобные; виниламиды, такие как N-винил-2-пирролидон, N-винилкапролактам и тому подобные; сложные алкоксиэфиры (мет)акриловой кислоты, такие как метоксиэтиловый эфир (мет)акриловой кислоты, этоксиэтиловый эфир (мет)акриловой кислоты, тетрагидрофурфуриловый эфир (мет)акриловой кислоты и тому подобные; содержащие гидроксигруппу мономеры (при использовании в качестве третьего мономерного компонента не является точкой образования поперечной сшивки), такие как гидроксипропил(мет)акрилат, α-гидроксиметилакрилат и тому подобные; производные (мет)акриловой кислоты, имеющие амидную группу, такие как (мет)акриламид, диметил(мет)акриламид, N-бутил(мет)акриламид, N-метилол(мет)акриламид и тому подобные; сложные аминоалкиловые эфиры (мет)акриловой кислоты, такие как аминоэтиловый эфир (мет)акриловой кислоты, диметиламиноэтиловый эфир (мет)акриловой кислоты, трет-бутиламиноэтиловый эфир (мет)акриловой кислоты и тому подобные; сложные алкоксиалкиленгликолевые эфиры (мет)акриловой кислоты, такие как метоксиэтиленгликолевый эфир (мет)акриловой кислоты, метоксидиэтиленгликолевый эфир (мет)акриловой кислоты, метоксиполиэтиленгликолевый эфир (мет)акриловой кислоты, метоксиполипропиленгликолевый эфир (мет)акриловой кислоты и тому подобные; (мет)акрилонитрилы; мономеры, имеющие сульфоновую кислоту, такие как стиролсульфоновая кислота, аллилсульфоновая кислота, сульфопропил(мет)акрилат, (мет)акрилоилоксинафталинсульфоновая кислота, акриламидметилсульфоновая кислота и тому подобные; и мономеры, содержащие группу винила, такие как винилпиперидон, винилпиримидин, винилпиперазин, винилпиррол, винилимидазол, винилоксазол, винилморфолин и тому подобные. Среди них предпочтительными являются сложные виниловые эфиры и виниламиды, при этом винилацетат является предпочтительным среди сложных виниловых эфиров, и N-винил-2-пирролидон является предпочтительным среди виниламидов. Такие мономеры (третий мономерный компонент) можно использовать отдельно или их можно использовать, сочетая по два или больше.
Когда акриловым адгезивом является сополимер сложного алкилового эфира (мет)акриловой кислоты (первого мономерного компонента) и винилового мономера, имеющего функциональную группу, которая может принимать участие в реакции образования поперечной сшивки (второго мономерного компонента), сложный алкиловый эфир (мет)акриловой кислоты и виниловый мономер, имеющий функциональную группу, которая может принимать участие в реакции образования поперечной сшивки подвергают сополимеризации смешиванием компонентов в массовом соотношении сложный алкиловый эфир (мет)акриловой кислоты:виниловый мономер, имеющий функциональную группу, которая может принимать участие в реакции образования поперечной сшивки, предпочтительно, 99-85:1-15, более предпочтительно 99-90:1-10.
Кроме того, когда акриловым адгезивом является сополимер сложного алкилового эфира (мет)акриловой кислоты (первого мономерного компонента), винилового мономера, имеющего функциональную группу, которая принимает участие в реакции образования поперечной сшивки (второго мономерного компонента) и другого мономера, отличного от первых двух (третьего мономерного компонента), сложный алкиловый эфир (мет)акриловой кислоты, виниловый мономер, имеющий функциональную группу, которая принимает участие в реакции образования поперечной сшивки, и другой мономер, отличный от первых двух подвергают сополимеризации, смешивая компоненты в массовом соотношении сложный алкиловый эфир (мет)акриловой кислоты : виниловый мономер, имеющий функциональную группу, которая принимает участие в реакции образования поперечной сшивки : другой мономер, отличный от первых двух, предпочтительно 40-94:1-15:5-50, более предпочтительно 50-89:1-10:10-40.
Компоненты можно полимеризовать известным способом. Например, мономеры в растворителе, таком как этилацетат, можно подвергать взаимодействию в присутствии инициатора полимеризации (например, бензоилпероксида, азобисизобутиронитрила и т.д.) при 50-70°C в течение 5-48 часов.
Особенно предпочтительными акриловыми адгезивами в настоящем изобретении являются, например, сополимер сложный 2-этилгексиловый эфир акриловой кислоты/акриловая кислота/N-винил-2-пирролидон, сополимер сложный 2-этилгексиловый эфир акриловой кислоты/N-(2-гидроксиэтил)акриламид/N-винил-2-пирролидон, сополимер сложный 2-этилгексиловый эфир акриловой кислоты/сложный 2-гидроксиэтиловый эфир акриловой кислоты/винилацетат и сополимер сложный 2-этилгексиловый эфир акриловой кислоты/акриловая кислота и более предпочтителен сополимер сложный 2-этилгексиловый эфир акриловой кислоты/акриловая кислоты/N-винил-2-пирролидон.
Необязательно такие акриловые адгезивы могут быть подвергнуты физической обработке для образования поперечных сшивок с использованием ультрафиолетового облучения или радиационного облучения, такого как облучение электронным пучком, или химической обработки для образования поперечных сшивок с использованием различных поперечно сшивающих агентов, таких как соединение изоцианата, такое как трехфункциональный изоцианат, органический пероксид, металлоорганическая соль, алкоголят металла, хелатирующее металлы соединение, полифункциональное соединение (полифункциональный агент, образующий внешние поперечные сшивки, мономер для полифункционального внутреннего поперечного сшивания, такой как диакрилат и диметакрилат).
Примеры каучукового адгезива включают каучуковые адгезивы, в которых смешивают каучуковый эластомер, такой как полиизобутилен/полибутеновый эластомер, стирол/диен/стироловый блок-сополимер, стирол/бутадиеновый эластомер, нитриловый эластомер, хлоропреновый эластомер, винилпиридиновый эластомер, полиизобутиленовый эластомер, бутиловый эластомер или изопрен/изобутиленовый эластомер. Из них, с точки зрения растворимости пептида и стимулятора индукции клеточного иммунитета в адгезиве и адгезивности кожи, предпочтительно используют полиизобутилен (PIB), стирол/диен/стироловый блок-сополимер (например, стирол/бутадиен/стироловый блок-сополимер (SBS), стирол/изопрен/стироловый блок-сополимер (SIS) и т.д.) и тому подобные. Также можно использовать смесь из двух или более таких адгезивов.
Кроме того, чтобы достичь подходящей силы адгезии и растворимости лекарственного средства в случае каучукового адгезива, каучуковый адгезив может представлять собой смесь двух или более каучуковых эластомеров из одинаковых или разных мономерных компонентов, которые имеют разные средние молекулярные массы. Например, что касается полиизобутилена, то предпочтительной является смесь полиизобутилена с высокой молекулярной массой, имеющего среднюю молекулярную массу от 150000 до 5500000, полиизобутилена со средней молекулярной массой, имеющего среднюю молекулярную массу от 10000 до 150000, и/или полиизобутилена с низкой молекулярной массой, имеющего среднюю молекулярную массу от 500 до 4000. В данном случае предпочтительно смешивание полиизобутиленов с высокой молекулярной массой, средней молекулярной массой и низкой молекулярной массой в массовом соотношении с высокой молекулярной массой:средней молекулярной массой:низкой молекулярной массой=10-80, предпочтительно 20-70:0-90, предпочтительно 10-80:0-80, предпочтительно 10-60.
В используемом в настоящем описании смысле средняя молекулярная масса означает средневязкостную молекулярную массу, вычисленную из выражения вязкости по Флори, и ее получают, вычисляя индекс Штаудингера (J0), исходя из времени истечения через капилляр 1 вискозиметра Уббелоде при 20°C, используя выражение Шульца-Блашке и используя такое значение J0 в следующем выражении.
(Формула)
J0=ηsp/c(1+0,31 ηsp) (уравнение Шульца-Блашке)
ηsp=t/t0-1
t: время истечения раствора (согласно формуле поправки Хагенбаха-Куэтта)
t0: Время истечения раствора (согласно формуле поправки Хагенбаха-Куэтта)
c: Концентрация раствора (г/см3)

Чтобы придать подходящую адгезивность, в каучуковый адгезив может быть примешан, например, агент, придающий клейкость, такой как канифольная смола, политерпеновая смола, кумарон-инденовая смола, нефтяная смола, терпен-фенольная смола, ксиленовая смола, алициклическая насыщенная углеводородная смола или тому подобные. В смесь могут быть введены один, два или больше видов агентов, придающих клейкость, в количестве 50% масс. или меньше, предпочтительно от 5 до 40% масс. в расчете на общую массу каучукового адгезива.
Примеры силиконового адгезива включают силиконовые адгезивы, состоящие из полиорганосилоксанового адгезива, полидиметилсилоксанового адгезива, полидиметилдифенилсилоксанового адгезива. Наряду с прочими предпочтительно используют коммерчески доступный силиконовый адгезив, такой как BIO PSA из Dow Corning Corporation.
Подложка, которая поддерживает адгезивный слой, особым образом не ограничена, и используют подложку, которая по существу непроницаема для пептида и стимулятора индукции клеточного иммунитета, так что пептид, стимулятор индукции клеточного иммунитета, добавки или тому подобное, которые находятся в адгезивном слое, не будут проходить через подложку и просачиваться на задней поверхности.
В качестве подложки можно использовать, например, одну пленку из полиэфира, полиамида, поли(винилиденхлорида), полиэтилена, полипропилена, поли(винилхлорида), сополимера этилена-этилакрилата, политетрафторэтилена, иономерной смолы, металлической фольги или тому подобного, или многослойную пленку из указанных пленок. В том числе, чтобы получить хорошую адгезивность (способность к заякориванию) между подложкой и адгезивным слоем, предпочтительно, чтобы подложка представляла собой многослойную пленку из непористой полимерной пленки и пористой пленкой, изготовленной из указанного выше материала. В данном случае желательно, чтобы адгезивный слой был образован со стороны пористой пленки. В качестве такой пористой пленки выбрана пористая пленка, которая улучшает заякоривание на адгезивном слое, и конкретные примеры такой пленки включают лист бумаги, тканое полотно, нетканое полотно, трикотажное полотно, лист, который был механически обработан с целью перфорирования, и тому подобные. С точки зрения осуществления технологической обработки и тому подобного из них особенно предпочтительными являются бумажный лист, тканое полотно и нетканое полотно. В качестве пористой пленки, с точки зрения улучшения заякоривания, мягкости и простоты приклеивания препарата в форме клейкой ленты и тому подобного, выбрана пористая пленка, имеющая толщину в диапазоне от 1 до 200 мкм. Кроме того, в случае использования в качестве пористой пленки тканого полотна или нетканого полотна, масса на единицу площади предпочтительно составляет от 5 до 30 г/м2, более предпочтительно от 6 до 15 г/м2.
Примеры наиболее подходящей подложки включают многослойную пленку из полиэфирной пленки (предпочтительно, полиэтилентерефталатной пленки), имеющей толщину от 1,5 до 6 мкм, и нетканого полотна из полиэфира (предпочтительно, полиэтилентерефталата), имеющего массу на единицу площади от 6 до 15 г/м2.
В препарате в форме клейкой ленты согласно настоящему изобретению для того, чтобы защитить поверхность адгезивного слоя до использования, желательно, чтобы на адгезивную поверхность была нанесена защитная удаляемая пленка. Защитная удаляемая пленка особым образом не ограничена, так как ее обрабатывают так, чтобы она обладала свойством, позволяющим ее снимать, и ее можно было снимать с приложением достаточно небольшой силы для отделения. Например, пленка из полиэфира, поли(винилхлорида), поли(винилиденхлорида), полиэтилентерефталата или тому подобного, бумаги, такой как очищенная бумага, пергамин и тому подобная, или многослойная пленка из очищенной бумаги или пергамина и полиолефина может быть обработана адгезивным слоем и использована в качестве защитной удаляемой пленки. Толщина защитной удаляемой пленки предпочтительно составляет от 10 до 200 мкм, более предпочтительно от 25 до 100 мкм. В качестве защитной удаляемой снимаемой пленки с точки зрения изоляционного свойства и стоимости предпочтительным является полиэфирный слой, в частности, слой полиэтилентерефталата. Кроме того, с точки зрения свойств, способствующих облечению обработки, в данном случае предпочтительной является защитная удаляемая пленка, имеющая толщину примерно от 25 до 100 мкм.
Предпочтительно введение субъекту композиции согласно настоящему изобретению в условиях слабого раздражения. Введение в условиях слабого раздражения может быть достигнуто, например, (i) введением субъекту композиции согласно настоящему изобретению в таких условиях введения, когда трансэпидермальная потеря влаги (TEWL) (г/час⋅м2), оцениваемая у модельного животного в случае оценки раздражения кожи, составляет 50 или меньше, (ii) введением субъекту композиции, обеспечивающей уровень TSLP в коже (пг/мг белка) 10000 или меньше, оцениваемый у модельного животного в случае оценки раздражения кожи.
Кроме того, композиция согласно настоящему изобретению при необходимости может содержать добавку. Добавка выбрана, например, из средств для обеспечения изотоничности, антисептиков/бактерицидных средств, антиоксидантов, противовоспалительных средств, солюбилизаторов, суспендирующих средств, наполнителей, средств для корректировки pH, стабилизаторов, стимуляторов всасывания, средств, контролирующих скорость высвобождения, красителей, пластификаторов, поперечно сшивающих агентов, адгезивов и тому подобного, или сочетания двух или более видов указанных средств, в зависимости от совместимости с основным ингредиентом основы, пептидом WT1 и/или модифицированным пептидом WT1 и стимулятором индукции клеточного иммунитета, планируемой схемы введения и тому подобного. Кроме того, в том случае, когда композиция согласно настоящему изобретению представляет собой препарат в форме клейкой ленты, препарат в форме клейкой ленты может содержать в качестве добавки усилитель проницаемости кожи.
В используемом в настоящем описании смысле термин «усилитель проницаемости кожи» означает любое вещество, которое может повысить эффективность проникновения трансдермально вводимого антигена через кожу, по сравнению с эффективностью, получаемой без такого вещества. Усилитель проницаемости кожи особым образом не ограничен, при условии, что он представляет собой жидкость при комнатной температуре (25°C), то есть обладает текучестью при такой температуре и оказывает действие, усиливающее всасывание. Когда усилитель проницаемости кожи представляет собой смесь двух или более веществ, смесь является жидкостью при комнатной температуре (25°C) и оказывает действие, усиливающее всасывание. Усилитель проницаемости кожи может представлять собой органическую жидкость и предпочтительно гидрофобную жидкость с точки зрения ее совместимости с адгезивным слоем.
Примеры усилителей проницаемости кожи включают высшие спирты, такие как олеиловый спирт, октилдодеканол и тому подобные; многоатомные спирты, такие как глицерин, этиленгликоль, полипропиленгликоль и тому подобные; высшие жирные кислоты, такие как олеиновая кислота, каприловая кислота и тому подобные; сложные эфиры жирных кислот, такие как изопропилмиристат, изопропилпальмитат, этилолеат и тому подобные; сложные эфиры многоосновных кислот, такие как диэтилсебацат, диизопропиладипат и тому подобные; сложные эфиры многоатомных спиртов и жирных кислот, такие как диглицерилтриизостеарат, эфир моноолеиновой кислоты и сорбитана, эфир дикаприловой кислоты и пропиленгликоля, эфир монолауриновой кислоты и полиэтиленгликоля, эфир тетраолеиновой кислоты и полиоксиэтиленсорбита и тому подобные; простые алкиловые эфиры полиоксиэтилена, такие как лауриловый эфир полиоксиэтилена и тому подобные; углеводороды, такие как сквалан, жидкий парафин и тому подобные; растительные масла, такие как оливковое масло, касторовое масло и тому подобные; силиконовые масла; пирролидоны, такие как N-метилпирролидон, N-додецилпирролидон и тому подобные; сульфоксиды, такие как децилметилсульфоксид и тому подобные, и такие усилители можно использовать отдельно или их можно использовать в виде смесей двух или более видов усилителей.
При использовании каучукового или акрилового адгезива можно применять второй усилитель проницаемости кожи. Конкретные примеры второго усилителя проницаемости кожи включают поливинилпирролидон, кросповидон, полипропиленгликоль, поливиниловый спирт, карбоксивиниловый полимер, гидроксипропилцеллюлозу и тому подобное или их смесь, но не ограничены указанным. В предпочтительном аспекте вторым усилителем проницаемости кожи согласно настоящему изобретению является поливинилпирролидон, кросповидон и/или полипропиленгликоль.
С точки зрения усиления проницаемости кожи для пептида WT1 и/или модифицированного пептида WT1, в качестве усилителя проницаемости кожи предпочтительно используют высший спирт, более конкретно, высший спирт, имеющий от 8 до 18 (предпочтительно от 8 до 14) атомов углерода, сложный эфир жирной кислоты, более конкретно, сложный эфир жирной кислоты, имеющей от 8 до 18 (предпочтительно от 12 до 16) атомов углерода, и одноатомного спирта, имеющего от 1 до 18 атомов углерода, сложный эфир многоатомного спирта и жирной кислоты или тому подобные, в частности, предпочтительно в качестве усилителя проницаемости кожи используют сложный эфир жирной кислоты, в частности, изопропилмиристат, изопропилпальмитат или диэтилсебацат. Количество такого усилителя проницаемости кожи предпочтительно составляет от 0,1% масс. до 70% масс., более предпочтительно от 1% масс. до 65% масс., более предпочтительно от 5% масс. до 60% масс. в расчете на общее количество адгезивного слоя. Когда количество усилителя проницаемости кожи составляет 0,1% масс. или больше, может быть получен высокий эффект стимуляции трансдермального всасывания. Когда количество составляет 70% масс. или меньше, может быть получена высокая способность к трансдермальному всасыванию с подавлением при этом снижения силы адгезии или силы когезии всего адгезивного слоя, и поэтому использование такого количества имеет преимущества.
Терапевтически эффективное количество пептида WT1 и/или модифицированного пептида WT1 может широко варьировать, в зависимости от тяжести заболевания, возраста и относительного состояния здоровья субъекта, а также других известных факторов. В общем, удовлетворительный результат может быть получен в случае суточной дозы примерно от 0,1 мкг до 1 г/кг массы тела. Фармакологически приемлемую кислоту или ее фармакологически приемлемую соль вводят одновременно с антигеном или последовательно, и предпочтительным является одновременное введение. Эффективное количество фармакологически приемлемой кислоты или ее фармакологически приемлемой соли может широко варьировать, в зависимости от конкретной используемой кислоты или соли, присутствия или отсутствия совместно используемого стимулятора индукции клеточного иммунитета и тому подобного, и удовлетворительный результат получают в случае дозы от 0,01 мкг до 1 г/кг массы тела. Когда совместно используют стимулятор индукции клеточного иммунитета, стимулятор индукции клеточного иммунитета вводят одновременно с пептидом WT1 и/или модифицированным пептидом WT1 или последовательно, и предпочтительным является одновременное введение. Эффективное количество стимулятора индукции клеточного иммунитета может широко варьировать, в зависимости от конкретного используемого стимулятора индукции клеточного иммунитета, присутствия или отсутствия другого стимулятора индукции клеточного иммунитета и тому подобного, и удовлетворительный результат получают в случае дозы от 0,01 мкг до 1 г/кг массы тела. Эффективное количество хелперного пептида может широко варьировать, в зависимости от другого конкретного используемого ингредиента, его количества и тому подобного, и удовлетворительный результат получают в случае дозы от 0,01 мкг до 1 г/кг массы тела. Суточную дозу можно вводить в виде однократной дозы или несколькими дробными порциями несколько раз, например два раза или больше, например, два, три, четыре или пять раз. Композицию можно применять непрерывно в течение периода времени от 1 минуты до 7 дней на одно введение. Интервал введения соответственно выбран из интервалов от ежедневного введения до введения раз в год (например, ежедневно, раз в 2 дня, раз в 3 дня, раз в 1 неделю, раз в 2 недели, раз в 1 месяц, раз в 3 месяца, раз в 6 месяцев, раз в 1 год) и более длительных интервалов, в зависимости состояния пациента, тяжести злокачественной опухоли, в зависимости от того, с какой целью осуществляют введение: терапевтической или профилактической. В общем, в целях лечения пациента, действительно имеющего тяжелую форму злокачественной опухоли, пептид WT1 и/или модифицированный пептид WT1 вводят с более высокой частотой и в более высокой дозе, а в целях профилактики пациенту, не имеющему злокачественной опухоли, пептид WT1 и/или модифицированный пептид WT1 вводят с более низкой частотой и в более низкой дозе.
В настоящем изобретении физическое раздражение означает любое физическое раздражение, которое вызывает повреждение рогового слоя, включая царапину и соскобы. Например, процедура соскоба липкой лентой, которая удаляет роговой слой, при использовании адгезивной ленты или тому подобного, процедура нанесения повреждения кожи при использовании режущего инструмента и процедура, в которой используют микроиглу, такая как перфорирование рогового слоя тонкой иглой, также относятся к физическому раздражению.
Трансэпидермальная потеря влаги означает количество воды (г), испаряемой с 1 м2 кератина в час. Трансэпидермальную потерю влаги можно легко измерить с помощью устройства для измерения потери влаги в течение короткого периода времени, и такое измерение широко используют в качестве показателя в случае оценки степени повреждения кожи. Также в настоящем изобретении трансэпидермальную потерю влаги используют в качестве показателя уровня физического раздражения.
TSLP (тимусный стромальный лимфопоэтин) является одним из IL-7-подобных цитокинов, которые продуцируются кератиноцитами кожи, тимусом и эпителиальными клетками слизистой оболочки, и как известно, вовлечен в созревание дендритных клеток и дифференцировку T-клеток. В настоящем изобретении TSLP используют в качестве показателя уровня химического раздражения, которое представляет собой раздражение, получаемое в результате действия лекарственного средства.
Настоящее изобретение будет объяснено более подробно и конкретно ниже с использованием примеров. Настоящее изобретение не ограничено объемом примеров.
ПРИМЕРЫ
Препарат в форме крема
Получили препарат в форме крема, содержащий ингредиенты, указанные в следующей далее таблице 2. В частности, пептид Db126 (ограниченный по MHC HLA-A*02-типа пептид) или пептид RYF (ограниченный по MHC HLA-A*24-типа пептид) или пептид AYL (ограниченный по MHC HLA-A*24-типа пептид), стимуляторы индукции клеточного иммунитета, отличные от хелперного пептида, хелперный пептид, фармакологически приемлемую кислоту и необязательно добавку взвешивали в количествах, точно указанных в таблице 2, затем в смесь добавляли 15 частей по массе ДМСО и добавляли основу (крем для основы) до 100 частей по массе, получая препарат в форме крема. В случае препаратов в форме крема согласно примерам или сравнительным примерам, для которых смешиваемые количества специально указаны в таблице 2, в таблице описаны смешиваемые количества соответствующих ингредиентов.
Крем для основы, указанный в таблице 2, готовили внесением в смесь и перемешиванием веществ в соответствии с соотношением, описанным в следующей таблице 1.
Белый вазелин, моностеарат сорбитана, бензиловый спирт, стеариловый спирт, полисорбат 60, концентрированный глицерин и диметилсульфоксид (ДМСО) приобретали из Wako Pure Chemical Industries, Ltd. ТФУ-соль антигенного пептида Db126, ТФУ-соль пептида RYF, ТФУ-соль пептида AYL, уксуснокислую соль антигенного пептида Db126, пептид-25 (Pep25) и пептид-25B (Pep25B) синтезировали химически, очищали, используя ВЭЖХ и использовали. Цетанол и имихимод (IMQ) приобретали из Tokyo Chemical Industry Co., Ltd. Циклический ди-ГМФ (ц-ди-ГМФ) и циклический ди-АМФ (ц-ди-АМФ) приобретали из Biolog Life Science Institute. Полученный из бактерий Pantoea липополисахарид производства MACROPHI Inc., Pam3CSK4 производства InvivoGen, глюкопиранозил-липид производства InvivoGen (MPLAs), зимозан производства Nacalai Tesque, Inc., поли(I:C) производства InvivoGen, бропиримин производства TOCRIS bioscience, R848 производства InvivoGen, гиалуронат натрия производства Kikkoman Biochemifa Company (микрогиалуроновая кислота FCH), ODN1826 производства InvivoGen, пидотимод производства Santa Cruz Biotechnology, Inc., бестатин производства Wako Pure Chemical Industries, Ltd., гидрохлорид левамизола производства MP Biomedicals, тозилат суплатаста производства TOCRIS bioscience, этодолак производства Wako Pure Chemical Industries, Ltd., и Na-локсопрофен производства Yoshindo Inc. использовали соответствующим образом.
Применяли следующие вещества:
Имихимод: Tokyo Chemical Industry Co., Ltd., клофибрат: производства LKT Laboratories, Inc., фенофибрат: производства Wako Pure Chemical Industries, Ltd., кверцетин: производства Cayman Chemical Company, берберин (n-гидрат хлорида берберина): производства Wako Pure Chemical Industries, Ltd., носкапин: производства Wako Pure Chemical Industries, Ltd., 3,3’-дииндолилметан: производства Wako Pure Chemical Industries, Ltd., ксантон: производства Wako Pure Chemical Industries, Ltd., партенолид: производства Wako Pure Chemical Industries, Ltd., этодолак: производства Wako Pure Chemical Industries, Ltd., локсопрофен (локсопрофен-Na): производства Yoshindo Inc., индометацин: производства Wako Pure Chemical Industries, Ltd., аспирин: производства Sigma-Aldrich, диклофенак (диклофенак натрия): производства Wako Pure Chemical Industries, Ltd., кетопрофен: производства Wako Pure Chemical Industries, Ltd., целекоксиб: производства TOCRIS bioscience, вальдекоксиб: производства TOCRIS bioscience, докозагексаеновую кислоту: производства Cayman Chemical Company, 2’,5’-дидезоксиаденозин: производства BIOMOL International, SCH23390: производства Wako Pure Chemical Industries, Ltd., ропинирол (ропинирол HCl): производства Ragactives, ротиготин: производства STARNASCENS, GW627368X: производства Cayman Chemical Company, сульпростон: производства Cayman Chemical Company, клопростенол: производства Wako Pure Chemical Industries, Ltd., BWA868C: производства Cayman Chemical Company, RO1138452: производства Cayman Chemical Company, лейкотриен B4: производства Cayman Chemical Company, монтелукаст (монтелукаст натрия): производства LG Life Sciences, зилейтон: производства Toronto Research Chemicals, Inc., никотиновую кислоту: производства Wako Pure Chemical Industries, Ltd., глицирризиновую кислоту (глицирризинат дикалия): производства Wako Pure Chemical Industries, Ltd., пирфенидон: производства TOCRIS bioscience, траниласт: производства Wako Pure Chemical Industries, Ltd., дифенгидрамин (гидрохлорид дифенгидрамина): производства Wako Pure Chemical Industries, Ltd., фамотидин: производства Wako Pure Chemical Industries, Ltd., иммепип (дигидробромид иммепипа): производства TOCRIS bioscience, проксифан: производства TOCRIS bioscience, азеластин (гидрохлорид азеластина): производства LKT Laboratories, Inc., циметидин: производства Wako Pure Chemical Industries, Ltd., 4-метилгистамин: производства TOCRIS bioscience, оланзапин: производства Wako Pure Chemical Industries, Ltd., йохимбин (гидрохлорид йохимбина): производства Wako Pure Chemical Industries, Ltd., ацетилхолин (хлорид ацетилхолина): производства Wako Pure Chemical Industries, Ltd., метерголин (сложный фенилметиловый эфир метерголина): производства TOCRIS bioscience, клозапин: производства Wako Pure Chemical Industries, Ltd., суматриптан: производства MYUNG IN PHARM. CO., LTD., золмитриптан: производства Cipla, толваптан: производства Sigma-Aldrich, десмопрессин: производства Sigma-Aldrich, оксибутинин (гидрохлорид оксибутинина): производства Sigma-Aldrich, пилокарпин (гидрохлорид пилокарпина): производства Wako Pure Chemical Industries, Ltd., тамсулозин (гидрохлорид тамсулазина): производства Cipla, мидодрин (гидрохлорид мидодрина): производства Wako Pure Chemical Industries, Ltd., пропранолол (гидрохлорид пропранолола): производства Wako Pure Chemical Industries, Ltd., ксилазин: производства Wako Pure Chemical Industries, Ltd., новокинин: производства Sigma-Aldrich, баклофен: производства Tokyo Chemical Industry Co., Ltd., TRAP-6: производства Bachem, аденозиндифосфат: производства MP Biomedicals, соматостатин-14: производства Bachem, GW405833: производства Sigma-Aldrich, SEW2871: производства Cayman Chemical Company, тримебутин (малеат тримебутина): производства Tokyo Chemical Industry Co., Ltd., лоперамид (гидрохлорид лоперамида): производства Wako Pure Chemical Industries, Ltd., мелатонин: производства LKT Laboratories, Inc., бифенилинданон A: производства Sigma-Aldrich, L-AP4 (L-2-амино-4-фосфономасляная кислота): производства Wako Pure Chemical Industries, Ltd.
Получали композитную подложку, в которой многослойный продукт ПЭТ-пленка/ПЭТ-нетканое полотно (площадью 0,7 см2) приклеивали к центральной части адгезивной ленты для фиксации, так чтобы сторона с ПЭТ-пленкой была со стороны ленты. Препарат в форме крема (4 мг) наносили на часть такой композитной подложки, состоящей из нетканого полотна, и полученный продукт использовали в качестве образца для введения в тесте по иммунизации.
Тест иммунизации мышей 1 (препарат в форме крема)
Тест по иммунизации мышей осуществляли, используя препараты в форме крема и модельное животное для иммунологической оценки. Оценку уровня индукции иммунитета осуществляли способом ELISPOT. В частности, на спине мыши выстригали волосы. Мышь оставляли вплоть до заживления у нее повреждения кожи вследствие срезания волос. Затем образец наносили на спину мыши на предварительно определяемый период времени и затем удаляли. Затем мышь оставляли на период времени, составляющий предварительно определяемое количество дней, и оценивали уровень антиген-специфичного клеточного иммунитета. После периода времени, составляющего предварительно определяемое количество дней, рассчитываемого от момента нанесения образца, выделяли селезенку и готовили суспензию клеток селезенки. Клетки селезенки (3×106 клеток/лунку) и антигенный пептид (100 мкМ) вместе со средой для культивирования помещали в лунку планшета ELISPOT, на котором были иммобилизованы антитела против IFN-γ мыши. Планшет культивировали в течение 20 часов в условиях 37°C и 5% CO2. Количество пятен, представляющих IFN-γ-продуцирующие клетки (количество пятен/3×106 клеток) оценивали способом ELISPOT. Во всех случаях 4 мг препарата в форме крема наносили один раз на 24 часа и селезенку выделяли через 6 дней после завершения нанесения.
В примере 3 делали соскоб кожи клейкой лентой (TS) десять раз, используя клейкую ленту DUNPLON (NITTO DENKO CS SYSTEM CORPORATION, No. 375), перед нанесением образца, и в примерах 4 и 5 кожу повреждали микрорезаком (MICRO FEATHER № 7330G, производства FEATHER) и микроиглой (длина иглы 750 мкм Micro Needle Roller System MR75, производства Ostar Beauty), соответственно, перед нанесением.
Кроме того, в некоторых группах также измеряли уровень TSLP в коже мыши после введения, трансэпидермальную потерю влаги у мыши перед введением и проницаемость кожи для антигенного пептида Db126 и имихимода. Мышью, используемой для оценки уровня TSLP, трансэпидермальной потери влаги и проницаемости кожи, была мышь C57BL/6.
(Способ измерения уровня TSLP)
После завершения нанесения образца кожу со спины мыши выделяли и кожу измельчали, используя гомогенизатор (Physcotron, Microtec Co., Ltd.), в растворителе для экстракции (раствор PBS, содержащий ингибитор протеаз (смесь ингибиторов протеаз для общего применения, Sigma-Aldrich) и 10 мкМ индометацина (производства Wako Pure Chemical Industries, Ltd.)). Измельченную кожу центрифугировали при 4°C и 9000 g в течение 10 минут, и надосадок извлекали. Количество TSLP в надосадке измеряли в ELISA (набор для ELISA TSLP Quantikine на мышах, R&D Systems). Кроме того, измеряли количество общего белка в надосадке способом BCA (набор для анализа белков Pierce BCA, Thermo Fisher Scientific K.K.), и количество TSLP делили на количество общего белка для стандартизации.
(Измерение трансэпидермальной потери влаги)
Трансэпидермальную потерю влаги измеряли с использованием портативного устройства для измерения потери влаги с системой переключения камер (производства Asahibiomed Co., Ltd., VAPO SCAN AS-VT100RS), осуществляя контакт кожи мыши с устройством в течение 5-15 секунд. Значение, которое измеряли через 10 минут после предварительной обработки кожи мыши, считали трансэпидермальной потерей влаги (TEWL) (г/час⋅м2).
(Тестирование проницаемости кожи мыши)
Проницаемость кожи для антигенного пептида Db126 и имихимода определяли, используя диффузионную ячейку Франца. Кусочек кожи выделяли со спины мыши, на которой волосы были сострижены заранее, закрепляли в диффузионной ячейке Франца (площадь нанесения 4,91 см2), в которой циркулировал фосфатный буфер (изотоничный буфер, pH 7,4) при 37°C. Препарат 0,7 см2 приклеивали на закрепленную кожу, и образец в ячейке собирали через 24 часа. Собранный образец подвергали высокоэффективной жидкостной хроматографии - тандемной масс-спектрометрии, и вычисляли количество антигенного пептида Db126, который проникал через кожу через 24 часа (проникающее количество антигенного пептида Db126, мкг/см2/24 час), и количество имихимода (проникающее количество имихимода, мкг/см2/24 час) на основании предварительно определенной калибровочной кривой.
Результаты теста по иммунизации и результаты измерения уровня TSLP и трансэпидермальной потери влаги показаны в следующей далее таблице 2, наряду с линией мышей, используемой в тесте по иммунизации. «Генетически модифицированная мышь» в таблице 2 означает генетически модифицированную мышь, на которой можно оценивать индукцию клеточного иммунитета пептидом, ограниченным по MHC HLA-A*0201-типа. Кроме того, результаты измерения проницаемости кожи показаны в таблице 3. Кроме того, для сравнения результаты иммунизации с использованием инъекционного препарата, описанного далее (сравнительные примеры 4-8), описаны в конце таблицы.

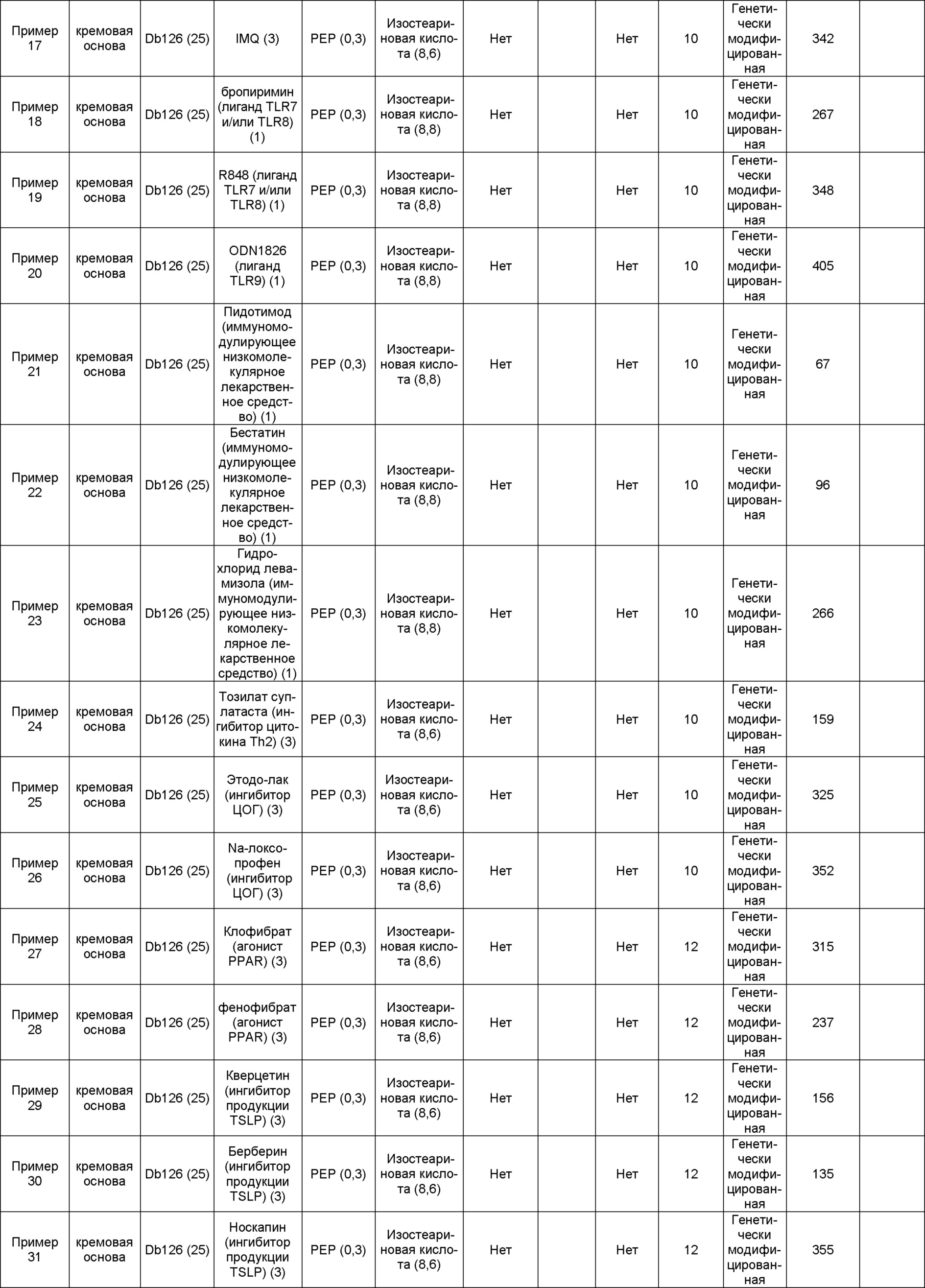
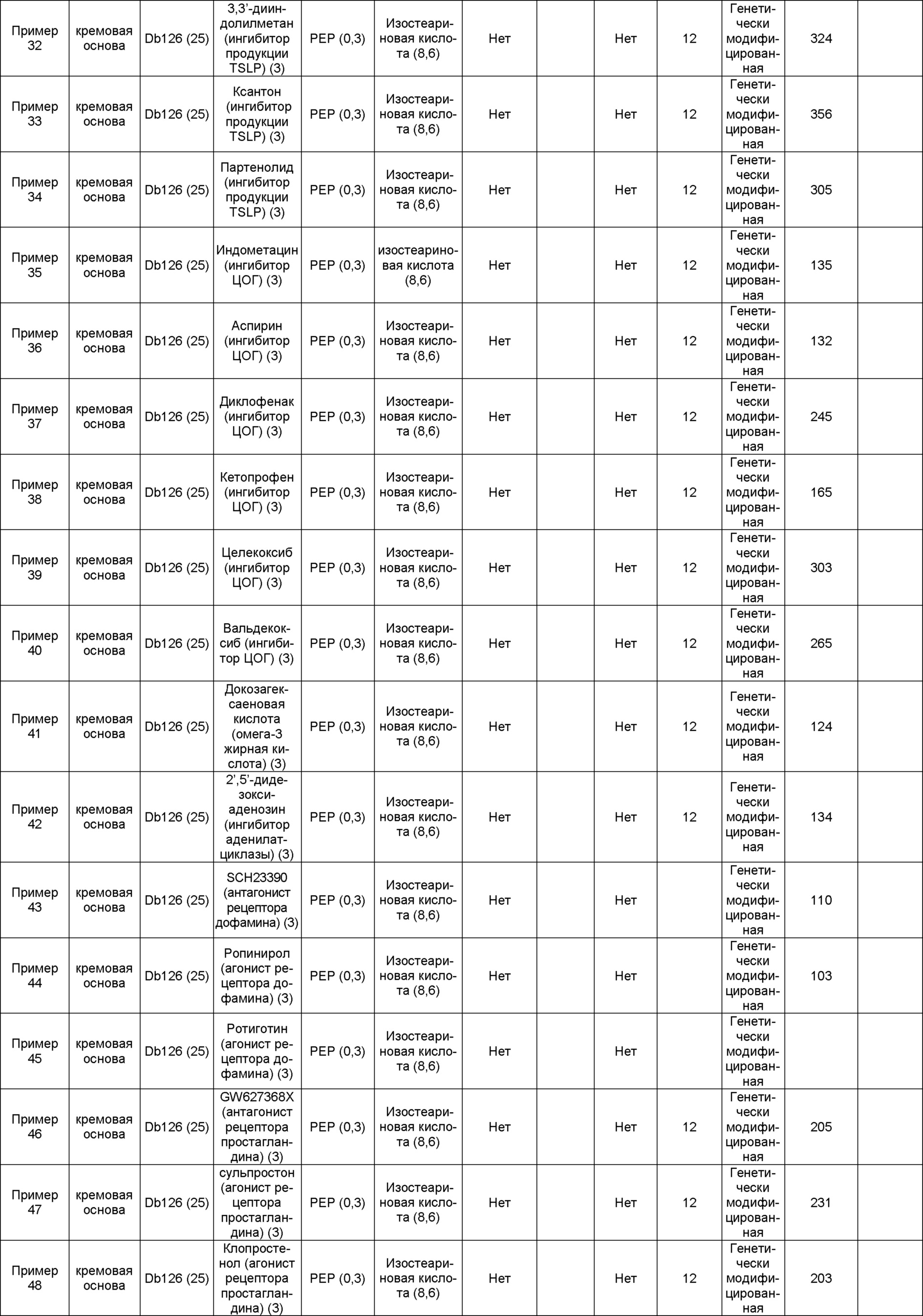
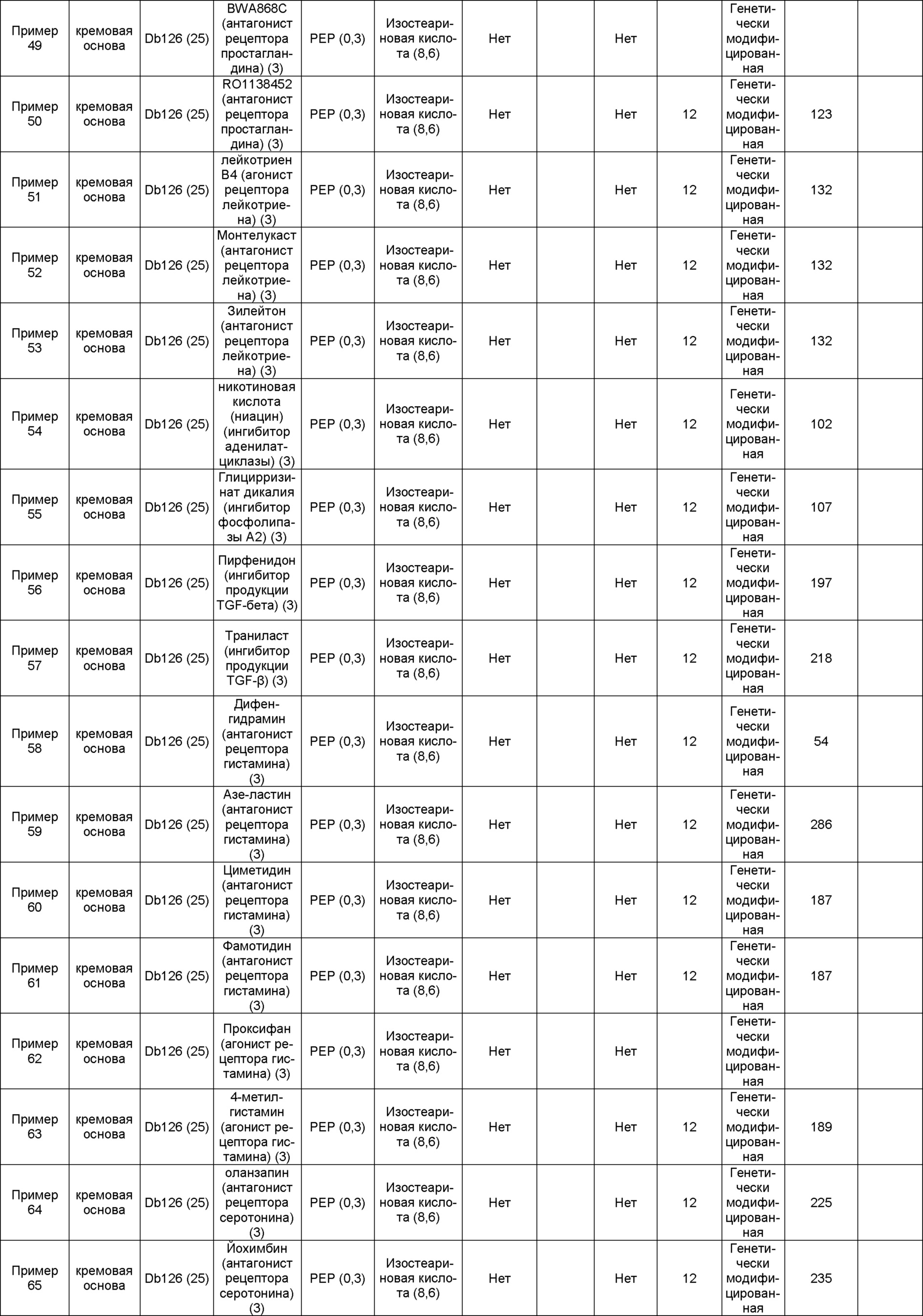



Препарат в форме клейкой ленты
Готовили адгезивы для препарата в форме клейкой ленты.
(Полимеризация акрилового адгезива A)
В атмосфере инертного газа 75 частей 2-этилгексилакрилата, 22 части N-винил-2-пирролидона, 3 части акриловой кислоты и 0,2 части азобисизобутиронитрила полимеризовали в растворе при 60°C в этилацетате, получая раствор акрилового адгезива A.
(Полимеризация акрилового адгезива B)
В атмосфере инертного газа 70 частей 2-этилгексилакрилата, 25 частей N-винил-2-пирролидона, 5 частей N-(2-гидроксиэтил)акриламида и 0,2 части азобисизобутиронитрила полимеризовали в растворе при 60°C в этилацетате, получая раствор акрилового адгезива B.
(Получение каучукового адгезива PIB)
В толуоле растворяли 24 части полиизобутилена (Oppanol B200, производства BASF), 36 частей полиизобутилена (Oppanol B12, производства BASF) и 40 частей алициклической нефтяной смолы (Arkon P-100, производства Arakawa Chemical Industries, Ltd.), получая раствор каучукового адгезива PIB.
(Получение SIS-адгезива A)
В толуоле растворяли 60 частей блок-сополимера стирол-изопрен-стирол (SIS5002, производства JSR Corporation) и 40 частей алициклической нефтяной смолы (Arkon P-100, производства Arakawa Chemical Industries, Ltd.), получая раствор SIS-адгезива А.
(Получение SIS-PIB-адгезива A)
В толуоле растворяли 30 частей блок-сополимера стирол-изопрен-стирол (SIS5002, производства JSR Corporation), 30 частей полиизобутилена (Oppanol B100, производства BASF) и 40 частей алициклической нефтяной смолы (Arkon P-100, производства Arakawa Chemical Industries, Ltd.), получая раствор SIS-PIB-адгезива A.
Получали препарат в форме клейкой ленты, показанный в следующей таблице 4. В частности, антигенный пептид Db126, стимулятор индукции клеточного иммунитета, фармакологически приемлемую кислоту и, необязательно, усилитель проницаемости кожи, раствор адгезива и органический растворитель (этилацетат, этанол, толуол и т.д.) в количествах, описанных в таблице 4, вносили в смесь, перемешивали и распределяли на защитной удаляемой пленке так, чтобы толщина после высушивания составляла примерно 80 мкм, и органический растворитель удаляли при высушивании, и приклеивали к подложке, получая препарат в виде клейкой ленты. Раствор адгезива добавляли в смесь так, чтобы в сумме соответствующие ингредиенты и адгезив после сушки для удаления органического растворителя составляли 100 частей по массе. В качестве подложки использовали полиэтилентерефталатную (ПЭТ) пленку (толщиной 25 мкм). Лист полиэтилентерефталата (ПЭТ) (толщиной 75 мкм), обработанный силиконом, использовали в качестве защитной удаляемой пленки. Такой препарат в виде клейкой ленты разрезали, получая кусочек 0,7 см2, и брали для теста иммунизации. Защитную удаляемую пленку снимали непосредственно перед нанесением препарата в форме клейкой ленты.
Источники, из которых приобретали антигенный пептид Db126, стимулятор индукции клеточного иммунитета и фармакологически приемлемую кислоту, были такими же, как в случае препарата в форме крема. Изопропилмиристат (IPM) приобретали из Croda, Япония. WT135 (хелперный пептид hWT135), PADRE (универсальный хелперный пептид) и WT1332 (хелперный пептид WT1332-347) синтезировали химически и очищали, используя ВЭЖХ, перед применением.
Тест иммунизации мышей 2 (препарат в форме клейкой ленты)
Используя полученный таким образом препарат в форме клейкой ленты, осуществляли тест 2 по иммунизации мышей таким же образом, как тест 1 по иммунизации мышей. Препарат наносили один раз на 24 часа/неделю и выделяли селезенку через 6 дней после введения. Генетически модифицированную мышь, которую можно применять для оценки способности индуцировать клеточный иммунитет пептида, ограниченного по MHC HLA-A*0201-типа, использовали в качестве модельного животного для иммунологической оценки.
В примере 69 кожу повреждали микрорезаком (MICRO FEATHER No. 7330G, производства FEATHER) перед нанесением препарата.
В некоторых группах уровень TSLP в коже после нанесения, трансэпидермальную потерю влаги до нанесения и проницаемость кожи для антигенного пептида Db126 и имихимода измеряли таким же образом, как и в тесте иммунизации мышей 1. Мышью, используемой для оценки уровня TSLP, трансэпидермальной потери влаги и проницаемости кожи, была мышь C57BL/6.
Результаты теста иммунизации и результаты измерения уровня TSLP и трансэпидермальной потери влаги показаны в следующей далее таблице 4. Кроме того, результаты измерения проницаемости кожи показаны в таблице 5.
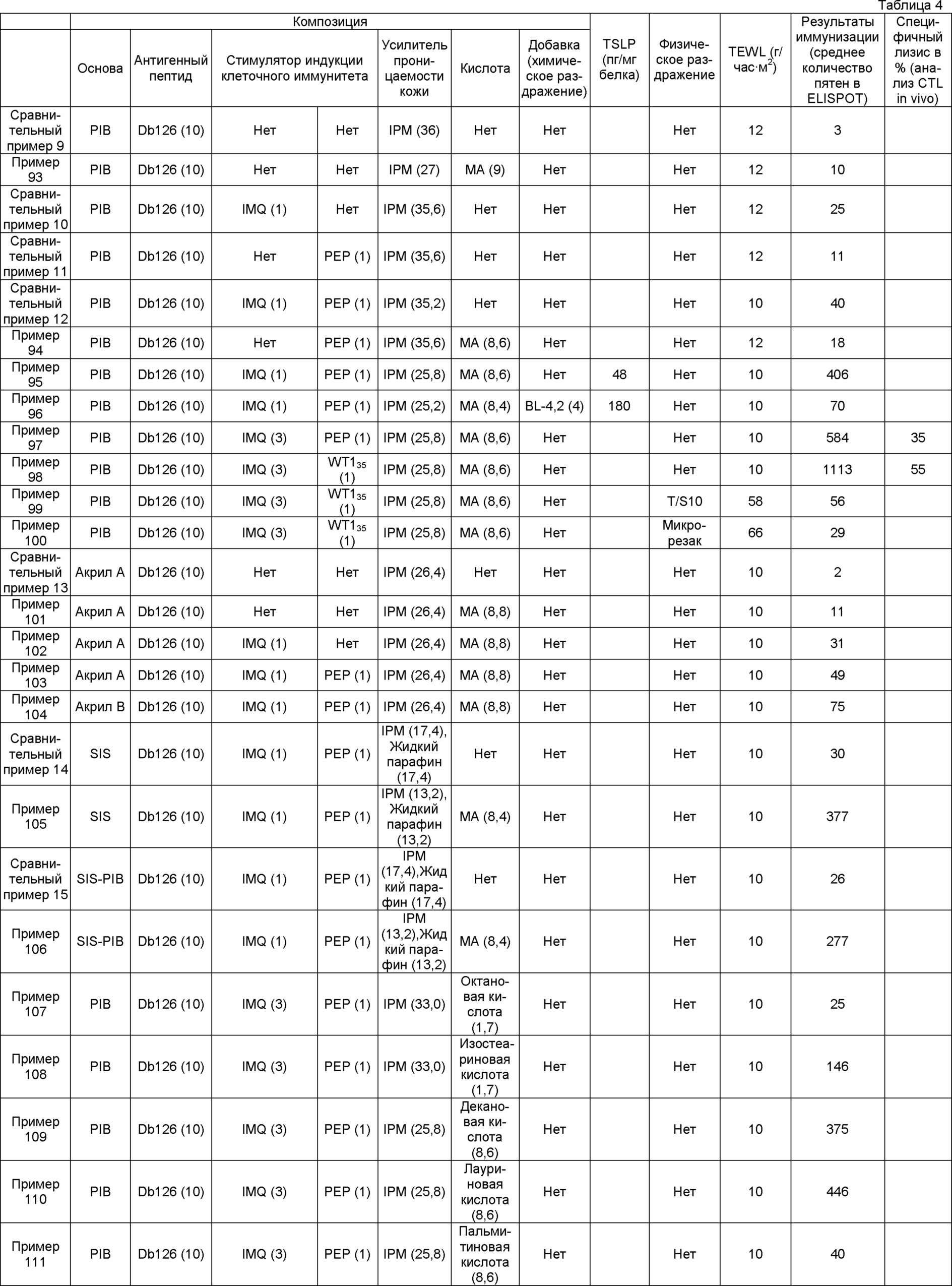
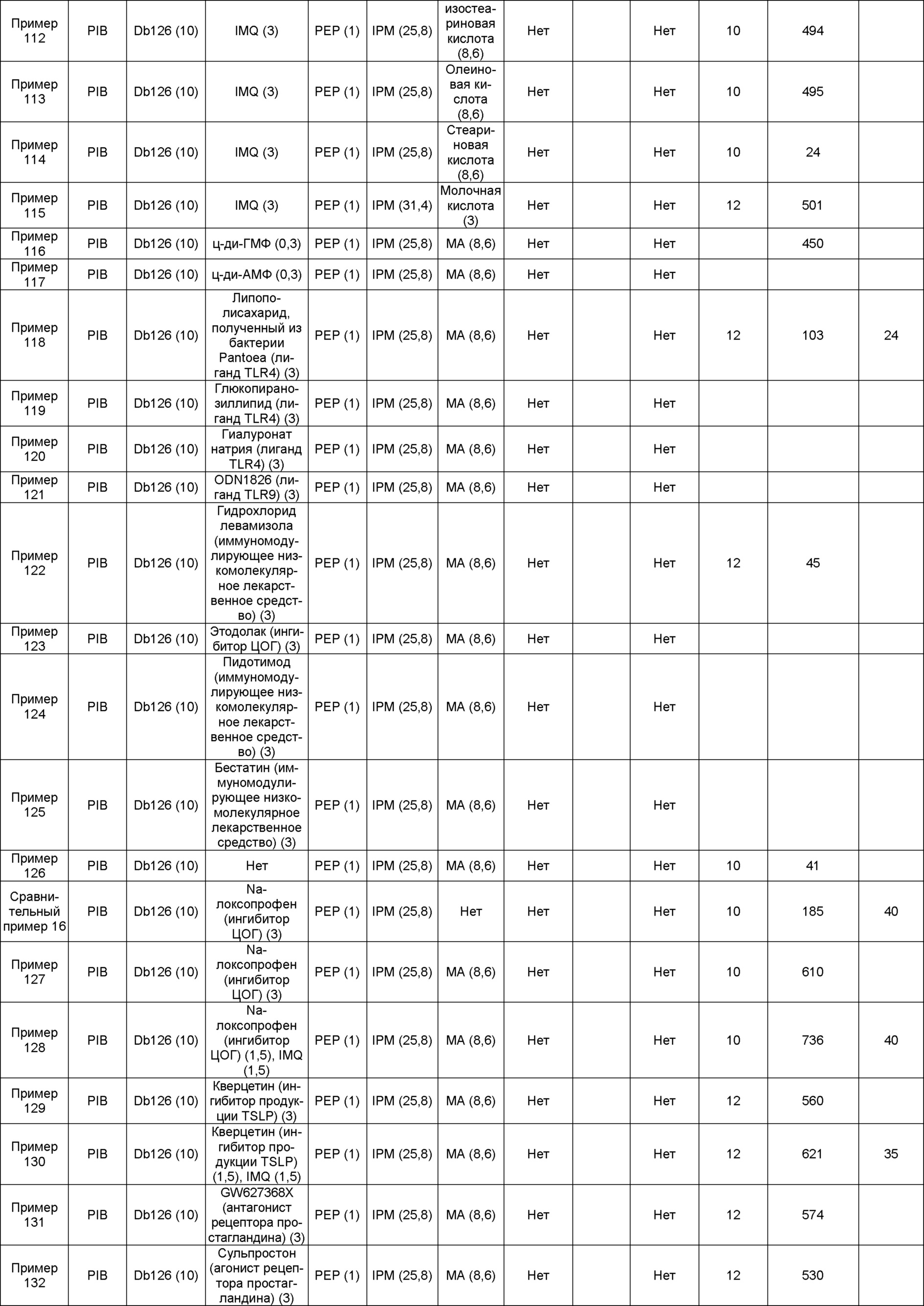

Жидкий препарат для наружного применения
Готовили жидкий препарат для наружного применения, содержащий композицию, указанную в следующей таблице 6. Антигенный пептид Db126, стимулятор индукции клеточного иммунитета и фармакологически приемлемую кислоту в количествах для смешивания, описанных в таблице 6, и 15 частей по массе ДМСО смешивали, добавляли основу так, чтобы в сумме получить 100 частей по массе, и вещества перемешивали, получая жидкий препарат для наружного применения. Пропиленгликоль (PG) и олеиловый спирт (OA) смешивали так, чтобы соотношение по массе соответствовало соотношению 98:2 или 90:10, получая основу. Получали композитную подложку, в которой часть, состоящая из целлюлозного нетканого полотна (площадью 0,8 см2) приклеивали к центральной части адгезивной ленты для фиксации. Часть композитной подложки, состоящую из нетканого полотна, пропитывали 67 мкл полученного жидкого препарата для наружного применения и использовали в тесте иммунизации.
Источники, из которых приобретали антигенный пептид Db126, стимулятор индукции клеточного иммунитета и фармакологически приемлемую кислоту, были такими же, как в случае препарата в форме крема. Молочную кислоту приобретали из Wako Pure Chemical Industries, Ltd.
Тест иммунизации мышей 3 (жидкий препарат для наружного применения)
Используя жидкий препарат для наружного применения, полученный как описано выше, тест по иммунизации мышей осуществляли таким же образом, как тест по иммунизации мышей 1. Использовали дозу 67 мкл, как описано выше. Жидкий препарат наносили один раз на 24 часа/неделю и селезенку выделяли через 6 дней после завершения нанесения. Использовали мышь C57BL/6.
В некоторых группах уровень TSLP в коже у мыши после нанесения, трансэпидермальную потерю влаги у мыши до нанесения измеряли, используя мышь C57BL/6 таким же образом, как и в тесте иммунизации мышей 1.
Результаты теста иммунизации, результаты измерения уровня TSLP и трансэпидермальной потери влаги показаны в следующей далее таблице 6 с указанием при этом каждой используемой мыши.
Инъекционный препарат
Готовили препараты для интрадермальной инъекции, содержащие композицию, описанную в следующей далее таблице 7. В частности, добавляли физиологический раствор в качестве основы к антигенному пептиду Db126 и монтаниду ISA51VG (производства Freund Corporation), используемому в качестве адъюванта, в количествах в смеси, описанных в таблице 7, получая в сумме 100 частей по массе, и вещества перемешивали, используя гомогенизатор, с получением инъекционного препарата.
Тест иммунизации мышей 4 (инъекционный препарат)
Используя инъекционный препарат, полученный, как описано выше, осуществляли тест по иммунизации мышей таким же образом, как и тест по иммунизации мышей 1. 30 мкл инъекционного препарата вводили один раз в область спины мыши посредством интрадермальной инъекции и выделяли селезенку через 6 дней после введения. Генетически модифицированную мышь, которую можно применять для оценки способности пептида, ограниченного MHC HLA-A*0201-типа, индуцировать клеточный иммунитет, использовали в качестве модельного животного. Результаты теста иммунизации показаны в следующей далее таблице 7.
Анализ CTL in vivo
Через семь дней после конечной иммунизации клетки селезенки (клетка-мишень или контрольная клетка) трансплантировали согласно следующему способу, селезенку выделяли через 18 часов. Значение специфичного лизиса в % получали, осуществляя измерение FACS.
Способ 1. Сбор клеток селезенки у нативной мыши
Использовали не подвергавшуюся обработке (нативную) мышь, которая представляла собой мышь того же вида, как и мышь, используемая в тесте иммунизации. Селезенку выделяли из нативной мыши и раздавливали, используя предметное стекло, в чашке Петри, содержащей среду RPMI1640. Раздавленную селезенку помещали в пробирку объемом 50 мл и центрифугировали при 10°C и 1100 об/мин в течение 5 минут. Надосадок отбрасывали. В пробирку добавляли 20 мл лизирующего буфера с последующей инкубацией при комнатной температуре в течение 5 минут. В пробирку добавляли 20 мл среды и затем пробирку центрифугировали. В пробирку добавляли среду и полученную смесь пропускали через сито, получая суспензию клеток.
Способ 2. Мечение клеток селезенки антигеном
Клетки селезенки, полученные согласно способу 1, центрифугировали при 10°C и 1100 об/мин в течение 5 минут, надосадок отбрасывали и добавляли буфер HBSS, получая суспензию клеток 2×107 клеток/мл. Суспензию клеток распределяли в две пробирки объемом 50 мл, добавляли 100 мкМ раствор антигена (антиген представлял собой такой же антиген, который использовали в тесте иммунизации) в одну из пробирок, содержащих раствор с клетками, так чтобы конечная концентрация достигала 10 мкМ, получая при этом клетки-мишени. Клетки в другой пробирке считали контрольными. Клетки в обеих пробирках инкубировали при 37°C в течение 1 часа, центрифугировали, надосадок отбрасывали и добавляли среду.
Способ 3. Мечение клеток селезенки CFSE
Клетки, меченые антигеном согласно способу 2, центрифугировали и добавляли 0,1% БСА-PBS до получения 1×107 клеток/мл. К раствору с клетками-мишенями добавляли 5 мМ раствор CFSE до конечной концентрации 10 мкМ, а к раствору с контрольными клетками добавляли 5 мМ раствор CFSE до конечной концентрации 1 мкМ и смесь встряхивали, затем инкубировали при 37°C в течение 10 минут. Затем осуществляли центрифугирование, надосадок отбрасывали и добавляли среду.
Способ 4. Трансплантация клеток селезенки
Клетки, меченые CFSE согласно способу 3, центрифугировали, надосадок отбрасывали и клетки доводили до концентрации 5×107 клеток/мл, используя буфер HBSS. Равные количества раствора с клетками-мишенями и раствора с контрольными клетками смешивали и вводили по 200 мкл иммунизированным мышам через глазничные вены (количество клеток для трансплантации: 1×107 клеток/животное).
Способ 5. Получение клеток селезенки от иммунизированной мыши и измерение FACS
Через восемнадцать часов после трансплантации клеток выделяли селезенку мыши и готовили суспензию клеток селезенки таким же образом, как в способе 1. Затем выявляли CFSE-позитивные клетки, используя FACS, и получали соотношение между клетками с высоким содержанием CFSE (клетки-мишени) и низким содержанием CFSE (контрольные клетки). Цитотоксическую активность оценивали по формуле, показанной ниже. Полученное значение может быть использовано в качестве показателя, свидетельствующего о способности антигенспецифичных клеток-киллеров, индуцированных в результате иммунизации вакцинной композицией, специфично атаковать клетки, которые презентируют антиген в живом организме. Было подтверждено, что композиция согласно настоящему изобретению может индуцировать сильный индуцируемый антигеном клеточный иммунитет.
r=(% клеток с низким содержанием CFSE)/(% клеток с высоким содержанием CFSE)
Специфичный лизис, %=(1-(r_неиммунизированные/r_иммунизированные))×100
В результате сравнения, осуществляемого между сравнительным примером 1 и примером 1, сравнения между сравнительным примером 2 и примером 7, сравнения между сравнительным примером 3 и примером 8, сравнения между сравнительным примером 12 и примером 95, сравнения между сравнительным примером 14 и примером 105, сравнения между сравнительным примером 15 и примером 106, сравнения между сравнительным примером 16 и примером 127, сравнения между сравнительным примером 17 и примерами 148-153 и сравнения между сравнительным примером 18 и примером 154, показано, что клеточный иммунитет был индуцирован и стимулирован при добавлении кислоты.
Кроме того, показано, что клеточный иммунитет был индуцирован разными препаратами в форме клейкой ленты в случае содержания кислоты в смеси (смотри таблицу 4 и фиг. 1 и 2). Показано, что октановая кислота, изостеариновая кислота, декановая кислота, лауриновая кислота, пальмитиновая кислота, изостеариновая кислота, олеиновая кислота, стеариновая кислота и молочная кислота являются предпочтительными, и что особенно сильный клеточный иммунитет был индуцирован при добавлении в смесь декановой кислоты, лауриновой кислоты, миристиновой кислоты, изостеариновой кислоты, олеиновой кислоты и молочной кислоты. Из них лауриновая кислота, миристиновая кислота, изостеариновая кислота, олеиновая кислота и молочная кислота давали особенно высокие результаты.
Также в случае трансдермальной иммунизации с использованием жидкого препарата добавление кислоты стимулировало индукцию иммунитета. Эффективными были молочная кислота, салициловая кислота, яблочная кислота, метансульфоновая кислота, малеиновая кислота и лимонная кислота. Особенно эффективными были молочная кислота, салициловая кислота, лимонная кислота и метансульфоновая кислота.
Кроме того, также показано, что клеточный иммунитет был сильнее, чем в случае иммунитета, индуцируемого при инъекции (смотри таблицы 4 и 7).
На основании описанных выше результатов было подтверждено, что композиция противораковой вакцины для трансдермального введения для индукции клеточного иммунитета, содержащая (i) пептид WT1 и/или модифицированный пептид WT1 и (ii) фармакологически приемлемую кислоту или ее фармакологически приемлемую соль в качестве первого стимулятора индукции клеточного иммунитета, была эффективной в индукции клеточного иммунитета.
Кроме того, в таблице 2, таблице 4 и таблице 6 также показано, что клеточный иммунитет ослабевает при нанесении физического повреждения на кожу в результате предварительной обработки, такой как соскоб липкой лентой или ранение кожи, или при наличии химического раздражения кожи, вызываемого использованием поверхностно-активного вещества или конкретного вида вещества основы.
Что касается препаратов в форме клейкой ленты, в которых были разные виды органических жирных кислот, то не было выявлено явного соответствия между проникающим через кожу количеством и уровнем индукции иммунитета. Кроме того, было подтверждено, что проникающее через кожу количество Db126 и имихимода увеличивалось в результате предварительной обработки кожи.
При проверке и сравнении с результатом, полученным при тестировании иммунитета, показано, что уровень TSLP, который является показателем раздражения кожи, был повыше, и уровень индукция клеточного иммунитета был снижен при повышении доли OA в жидком препарате PG/OA или добавлении поверхностно-активного вещества в клейкой ленте. На основании полученного результата показано, что важно индуцировать клеточный иммунитет в условиях слабого раздражения.
Показано, что уровень TEWL был повышен при предварительной обработке кожи, и кожный барьер нарушен при физическом раздражении. Полученный результат соответствует тому факту, что количество проникающих через кожу Db126 и имихимода было повышено в случае предварительно обработки кожи в тесте по оценке проницаемости кожи. Однако, несмотря на увеличение проникающего количества, клеточный иммунитет не был повышен, а скорее ослаблен. На основании полученного результата показано, что введение в условиях слабого раздражения более важно для индукции клеточного иммунитета, чем увеличение количества проникающего через кожу антигена и адъюванта.
Реферат
Изобретение относится к области биотехнологии, в частности к композиции противораковой вакцины для трансдермального введения для применения в индукции клеточного иммунитета, где рак сверхэкспрессирует WT-1. Вышеуказанная композиция содержит эффективное количество пептида WT1 и/или модифицированного пептида WT1, выбранного из группы, состоящей из пептида Db126, пептида RYF и пептида AYL. Также вышеуказанная композиция содержит эффективное количество первого стимулятора индукции клеточного иммунитета, который представляет собой фармакологически приемлемую кислоту или ее фармакологически приемлемую соль, где кислота выбрана из группы, состоящей из изостеариновой кислоты, декановой кислоты, миристиновой кислоты и яблочной кислоты. Изобретение позволяет эффективно индуцировать клеточный иммунитет против раковой опухоли. 8 з.п. ф-лы, 2 ил., 7 табл.

Комментарии