Ингибиторы гиразы бактерий и их применения - RU2262932C2
Код документа: RU2262932C2
Описание
Область изобретения
Данное изобретение касается в области медицинской химии и относится к соединениям и их фармацевтическим композициям, которые ингибируют гиразы бактерий. Соединения пригодны в качестве ингибиторов активности гираз бактерий. Настоящее изобретение также относится к способам лечения бактериальных инфекций у млекопитающих. Настоящее изобретение также относится к способам снижения числа бактерий в биологической пробе.
Предпосылки изобретения
Уже давно была установлена резистентность бактерий к антибиотикам, и в настоящее время она считается серьезной проблемой здравоохранения во всем мире. В результате резистентности некоторые бактериальные инфекции либо трудно лечить антибиотиками, либо они совсем не поддаются лечению. Эта проблема стала особенно серьезной после недавнего открытия множественной лекарственной устойчивости у некоторых штаммов бактерий таких, как Streptococcus pneumoniae (SP), Mycobacterium tuberculosis и Enterococcus. Особенно вызывающим тревогу стало появление устойчивого к ванкомицину энтерококка, поскольку ранее ванкомицин был единственным эффективным антибиотиком для лечения данной инфекции, и считался лекарством "последней надежды" в отношении многих инфекций. Несмотря на то, что многие другие резистентные к лекарствам бактерии не вызывают угрожающего для жизни заболевания, как энтерококки, имеется опасение того, что гены, индуцирующие резистентность, могут распространяться в более опасные микроорганизмы, такие как Staphylococcus aureus, у которых уже доминирующей является резистентность к метициллину (De Clerq et al., Current Opinion in Anti-infective Investigational Drugs, 1999, 1, 1; Levy "The Challenge of Antibiotic Resistance", Scientific American, March, 1998).
Другим вызывающим тревогу моментом является то, насколько быстро появляется резистентность к антибиотикам. Например, до 1960-х г.г. SP был универсально чувствительным к пенициллину, и в 1987 г. только 0,02% штаммов SP в США было резистентным. Однако в 1995 г. уже сообщалось, что резистентность SP к пенициллину составляла примерно 7%, и в некоторых районах США была высокой и равной 30% (Lewis, FDA Consumer magazine (September, 1995); Gershman in The Medical Reporter, 1997).
Больницы, в частности, служат центрами образования и передачи резистентных к лекарственным препаратам микроорганизмов. Инфекции, имеющие место в больницах, известные, как нозокомиальные (внутрибольничные) инфекции, становятся все более возрастающей проблемой. Из двух миллионов американцев, заражающихся в больницах каждый год, более половины из них заражены инфекциями, являющимися резистентными по меньшей мере к одному антибиотику. По данным Центра контроля заболеваний в 1992 г. более 13000 бывших на лечении в больнице пациентов умерло от бактериальных инфекций, возбудители которых были резистентными к лечению антибиотиками (Lewis, "The Rise of Antibiotic-Resistant Infections", FDA Consumer magazine, Sept, 1995).
В результате необходимости бороться с резистентными к лекарственным препаратам бактериями и все растущего отсутствия эффективности у доступных препаратов, имеется возрастающий интерес к разработке новых антибиотиков. Одна привлекательная стратегия для разработки новых антибиотиков заключается в ингибировании ДНК-гиразы, фермента бактерий, необходимого для репликации ДНК и, следовательно, необходимого для роста и деления бактериальных клеток. Активность гиразы также связана с событиями, имеющими место при транскрипции, репарации и рекомбинации ДНК.
Гираза является одной из топоизомераз, группы ферментов, которые катализируют взаимопревращение топологических изомеров ДНК (в основном см. Kornberg and Baker, DNA Replication, 2d Ed., Chapter 12, 1992, W.H.Freeman and Co.; Drlica, Molecular Microbiology, 1992, 6, 425; Drlica and Zhao, Microbiology and Molecular Biology Reviews, 1997, 61, 377). Сама по себе гираза контролирует суперспирализацию ДНК, и ослабляет топологический стресс, который имеет место, когда цепи ДНК исходного дуплекса раскручиваются во время репликации. Гираза также катализирует превращение релаксированного, замкнутого циклического ДНК-дуплекса в отрицательно суперскрученную форму, которая более благоприятна для рекомбинации. Механизм реакции суперспирализации включает упаковку гиразы вокруг области ДНК, разрыв двойной цепи в данной области, прохождение второй области ДНК через место разрыва и соединение разорванных цепей. Подобный механизм расщепления характерен для топоизомеразы типа II. Реакция суперспирализации стимулируется связыванием АТФ с гиразой. Затем АТФ гидролизуется во время реакции. Данное связывание и последующий гидролиз АТФ вызывают конформационные изменения в связанной с ДНК гиразе, которые необходимы для проявления ее активности. Также было установлено, что уровень суперспирализации ДНК (или релаксации) зависит от соотношения АТФ/АДФ. При отсутствии АТФ гираза способна только релаксировать суперспирализованную ДНК.
ДНК-гираза бактерий является белковым тетрамером массой 400 kDa, состоящим из двух субъединиц А (GyrA) и двух субъединиц В (GyrB). Связывание и расщепление ДНК связано с GyrA, в то время как АТФ связывается и гидролизуется белком GyrB. GyrB состоит из аминоконцевого домена, который обладает АТФ-азной активностью, и карбоксиконцевого домена, который взаимодействует с GyrA и ДНК. В противоположность, топоизомеразы типа II у эукариот являются гомодимерами, которые могут релаксировать отрицательные и положительные супервитки, но не могут вводить отрицательные супервитки. В идеале, антибиотики, механизм действия которых основан на ингибировании ДНК-гиразы бактерий, будут избирательными для данного фермента и относительно неактивны в отношении топоизомераз типа II у эукариот.
Широко применяемые хинолоновые антибиотики ингибируют ДНК-гиразу бактерий. Примеры хинолонов включают ранее появившиеся соединения, такие как налидиксовая кислота и оксолиновая кислота, а также появившиеся позднее, более эффективные фторхинолоны, такие как норфлоксацин, ципрофлоксацин и тровафлоксацин. Данные соединения связываются с GyrA и стабилизируют расщепленный комплекс, ингибируя, таким образом, функцию гиразы в целом, приводя к гибели клеток. Однако общепризнанной является резистентность к лекарственным препаратам, как проблема для данной группы соединений (WHO Report, "Use of Quinolones in Food Animals and Potential Impact on Human Health", 1998). Для хинолонов, как и других групп антибиотиков, является характерным то, что у бактерий, подвергшихся воздействию более ранних соединений, часто быстро развивается перекрестная резистентность к более эффективным соединениям, входящим в эту же группу.
Менее известны ингибиторы, которые связываются с GyrB. Примеры включают кумарины, новобиоцин и кумермицин А, циклотиалидин, цинодин и клероцидин. Было показано, что кумарины очень прочно связываются с GyrB. Например, новобиоцин образует сеть водородных связей с белком и несколько гидрофобных связей. Несмотря на то, что, как оказалось, новобиоцин и АТФ связываются внутри сайта связывания АТФ, имеется минимальное перекрытие в связанной ориентации двух соединений. Перекрывающиеся участки являются сахарной единицей новобиоцина и аденином АТФ (Maxwell, Trends in Microbiology, 1997, 5, 102).
Для резистентных к кумарину бактерий наиболее доминирующая точечная мутация находится на поверхности остатка аргинина, который связывается с карбонилом кумаринового кольца (Arg136 в GyrB E. coli). Несмотря на то, что ферменты с данной мутацией показывают более низкую суперспирализацию и активность АТФ-азы, они также менее чувствительны к ингибированию под действием кумариновых препаратов (Maxwell, Mol. Microbiol., 1993, 9, 681).
Несмотря на то, что кумарины являются сильными ингибиторами суперспирализации под действием гиразы, их не используют широко в качестве антибиотиков. В основном они не пригодны в таком качестве из-за их слабого проникновения в бактерии, эукариотической токсичности и низкой растворимости в воде (Maxwell, Trends in Microbiology, 1997, 5, 102). Было бы желательным иметь новый, эффективный ингибитор GyrB для преодоления этих недостатков, предпочтительно функционирующий не на основе связывания с Arg136 для проявления активности. Подобный ингибитор будет привлекательным потенциальным антибиотиком без наличия проблем с резистентностью, характерной для других групп антибиотиков.
Поскольку резистентность бактерий к антибиотикам стала серьезной проблемой здравоохранения, существует насущная потребность в разработке более новых и более эффективных антибиотиков. Конкретнее, имеется потребность в антибиотиках, которые представляют новую группу соединений, не используемых ранее для лечения бактериальной инфекции. Такие соединения будут, особенно пригодными для лечения нозокамиальных инфекций в больницах, где образование и распространение резистентных бактерий становится все более превалирующим.
Описание изобретения
В настоящее время было установлено, что соединения данного изобретения и их фармацевтические композиции пригодны для лечения бактериальных инфекций. Одно воплощение изобретения относится к способу лечения бактериальной инфекции у млекопитающего, нуждающегося в этом, включающему стадию введения указанному млекопитающему терапевтически эффективного количества соединения формулы I:

или его фармацевтически приемлемого производного или пролекарства, в которой:
Z представляет О или N-R4;
W представляет атом азота или CRа;
Rа выбран из атома водорода, атома галогена, -CF3, R7, -OR7 или -N(R7)2;
R1 представляет арильное или гетероарильное кольцо, где указанное кольцо необязательно замещено вплоть до четырех R9; где заместитель R9 в орто-положении R1, будучи взятый вместе с R2, может образовать конденсированное, ненасыщенное или частично ненасыщенное, необязательно замещенное 5-8-членное кольцо, содержащее 0-2 кольцевых гетероатома, выбранных из атомов азота, кислорода или серы;
R2 и R3 каждый независимо выбран из R6, атома галогена, CN, SR6, OR6, N(R6)2, NRCO2R6, NRCON(R6)2, CON(R6)2, NRCOR6, NRN(R6)2, COR6, CO2R6, COCOR6, SO2R6, SO2N(R6)2 или NRSO2 R6; или R2 и R3, будучи взятые вместе, образуют конденсированное, ненасыщенное или частично ненасыщенное, необязательно замещенное 5-8-членное кольцо, содержащее 0-2 кольцевых гетероатома, выбранных из атомов азота, кислорода или серы;
R4 выбран из R6, CON(R6), COR6, CO2R6, COCOR6, SO2R6, SO2N(R6)2 или (CH2)YR2;
y равно 1-6;
R5 выбран из R7, Ar, COAr, CON(R7)Ar, (CH2)YCO2R, (CH2)YN(R7)2, C(=NR10)-N(R7)2, C(=NR10)-NRCOR, C(=S)-N(R7)2, CON(R7)2, CO2R, COR, SO2R или SO2N(R7)2;
Ar представляет 5-членное гетероарильное, гетероциклическое или карбоциклическое кольцо, где указанное кольцо необязательно замещено вплоть до трех заместителями, выбранными из оксо, атома галогена, CN, NO2, R8, OR8, NHR8, NHCOR8, NHCONHR8, COR8, CONHR8, SO2R8, NHSO2NHR8 или SO2NHR8;
каждый R независимо выбран из водорода или необязательно замещенной алифатической группы, содержащей от одного до шести атомов углерода;
каждый R6 независимо выбран из R7 или необязательно замещенной группы, выбранной из алкокси, гидроксиалкила, гетероциклила, гетероциклилалкила, арила, аралкила, аралкокси, арилоксиалкила, гетероарила, гетероаралкила, гетероаралкокси или гетероароилоксиалкила;
каждый R7 независимо выбран из атома водорода или необязательно замещенной алифатической группы, содержащей от одного до шести атомов углерода, или два R7 при одном и том же атоме азота, будучи взятые вместе с атомом азота, необязательно образуют 4-6-членное, насыщенное или ненасыщенное гетероциклическое кольцо, содержащее от одного до трех гетероатомов;
R8 представляет С1-С4 алифатическую группу, где два R8 в смежных положениях Ar, или арильного или гетероарильного кольца, могут быть взяты вместе с их промежуточными атомами с образованием 3-6-членного конденсированного кольца;
каждый R9 независимо выбран из оксо, атома галогена, CN, NO2, Tn(галогеналкила), R6, SR6, OR6, OR8, N(R6 )2, CON(R6)2, CON(R)COR6, COR6, CO2R6, CO2N(R6)2, COCOR6, SO2R6, SO2N(R6)2, N(R)TnCO2R6, N(R)TnCON(R6)2, N(R)TnN(R6)2, N(R)TnNRCO2R6, N(R)TnNRCON(R6)2, N(R)TnCOR6, N(R)TnNRCOR6, N(R)TnSO2 N(R6)2, N(R)TnSO2R6, TnPO(OR7)2, TnOPO(OR7)2, TnSP(OR7 )2, TnPO(OR7)2 или TnNPO(OR7)2;
каждый Q независимо выбран из С1-С3 разветвленного или нормального алкила;
Т выбран из -Q- или -Qm-CH(Qm-R2)-;
каждый m и n независимо выбран из нуля или 1; и
R10 выбран из R7 или Ar.
В том смысле, в котором они используются в данном описании, если не указано иначе, будут применимы следующие определения. Кроме того, если не указано иначе, радикалы функциональных групп выбраны независимо.
Термин "алифатический" в том смысле, в котором он используется, означает нормальные, разветвленные или циклические С1 -С12 углеводороды, которые являются полностью насыщенными или содержат одну или более единиц ненасыщенности, но которые не являются ароматическими. Например, подходящие алифатические группы включают замещенный или незамещенный, нормальный, разветвленный или циклический алкил, алкенил, алкинил и их гибриды, такие как (циклоалкил)алкил, (циклоалкенил)алкил или (циклоалкил)алкенил. Термины "алкил", "алкокси", "гидроксиалкил", "алкоксиалкил" и "алкоксикарбонил", используемые одни или как часть более крупной группы, включают как нормальные, так и разветвленные цепи, содержащие 1-12 атомов углерода. Термины "алкенил" и "алкинил", используемые одни или как часть более крупной группы, будут включать как нормальные, так и разветвленные цепи, содержащие 2-12 атомов углерода. Термин "циклоалкил", используемый один или как часть более крупной группы, будет включать циклические С3-С12 углеводороды, которые полностью насыщены, или которые содержат одну или более единиц ненасыщенности, но которые не являются ароматическими.
Термины "галогеналкил", "галогеналкенил" и "галогеналкокси" означают алкил, алкенил или алкокси, которые могут быть замещены одним или более атомами галогена. Термин "галоген" означает F, Cl, Br или I.
Термин "гетероатом" означает атом N, O или S и включает любую окисленную форму азота и серы, и кватернизированную форму любого основного азота.
Термин "карбоцикл", "карбоциклил" или "карбоциклический" в том смысле, в котором он используется, означает алифатическую кольцевую систему, содержащую 3-14 членов. Термин "карбоцикл", "карбоциклил" или "карбоциклический", насыщенный или частично ненасыщенный, также относится к кольцам, которые необязательно замещены. Термины "карбоциклил" или "карбоциклический" также включают алифатические кольца, которые сконденсированы с одним и более ароматическими или неароматическими кольцами, так, как в декагидронафтиле или тетрагидронафтиле, где радикал или место присоединения находится в алифатическом кольце.
Термин "арил", используемый один или как часть более крупной группы, как в "аралкиле", "аралкокси" или "арилоксиалкиле", относится к ароматическим кольцевым группам, содержащим 5-14 членов, таким, как фенил, бензил, фенетил, 1-нафтил, 2-нафтил, 1-антрацил и 2-антрацил. Термин "арил" также относится к кольцам, которые необязательно замещены. Термин "арил" можно использовать взаимозаменяемо с термином "арильное кольцо". "Арил" также включает конденсированные полициклические ароматические кольцевые системы, в которых ароматическое кольцо сконденсировано с одним или более колец. Примеры включают 1-нафтил, 2-нафтил, 1-антрацил и 2-антрацил. Также включенной в объем термина "арил", в том смысле, в котором он используется в данном описании, является группа, в которой ароматическое кольцо сконденсировано с одним или более неароматическими кольцами так, как в инданиле, фенантридиниле или тетрагидронафтиле, где радикал или место присоединения находится в ароматическом кольце.
Термин "гетероцикл", "гетероциклил" или "гетероциклический", в том смысле, в котором он используется в данном описании, включает неароматические кольцевые системы, содержащие 5-14 членов, предпочтительно 5-10, в которых один или более кольцевых углеродов, предпочтительно от 1 до 4, заменены гетероатомом, таким как атом N, O или S. Примеры гетероциклических колец включают 3-1Н-бензимидазол-2-он, (1-замещенный)-2-оксобензимидазол-3-ил, 2-тетрагидрофуранил, 3-тетрагидрофуранил, 2-тетрагидротиофенил, 3-тетрагидротиофенил, 2-морфолинил, 3-морфолинил, 4-морфолинил, 2-тиоморфолинил, 3-тиоморфолинил, 4-тиоморфолинил, 1-пирролидинил, 2-пирролидинил, 3-пирролидинил, 1-пиперазинил, 2-пиперазинил, 1-пиперидинил, 2-пиперидинил, 3-пиперидинил, 4-пиперидинил, 4-тиазолидинил, диазолонил, N-замещенный диазолонил, 1-фталимидинил, бензоксанил, бензопирролидинил, бензопиперидинил, бензоксоланил, бензотиоланил и бензотианил. Также включенной в объем термина "гетероциклил" или "гетероциклический", в том смысле, в котором он используется в данном описании, является группа, в которой неароматическое, содержащее гетероатом кольцо, сконденсировано с одним или более ароматическими или неароматическими кольцами так, как в индолиниле, хроманиле, фенантридиниле или тетрагидрохинолиниле, где радикал или место присоединения находится в неароматическом, содержащем гетероатом кольце. Термин "гетероцикл", "гетероциклил" или "гетероциклический", насыщенный или частично ненасыщенный, также относится к кольцам, которые необязательно замещены.
Термин "гетероарил", используемый один или как часть более крупной группы, как в "гетероаралкиле" или "гетероарилалкокси", относится к гетероароматическим кольцевым группам, содержащим 5-14 членов. Примеры гетероарильных колец включают 2-фуранил, 3-фуранил, 3-фуразанил, N-имидазолил, 2-имидазолил, 4-имидазолил, 5-имидазолил, 3-изоксазолил, 4-изоксазолил, 5-изоксазолил, 2-оксадиазолил, 5-оксадиазолил, 2-оксазолил, 4-оксазолил, 5-оксазолил, 1-пирролил, 2-пирролил, 3-пирролил, 1-пиразолил, 3-пиразолил, 4-пиразолил, 2-пиридил, 3-пиридил, 4-пиридил, 2-пиримидил, 4-пиримидил, 5-пиримидил, 3-пиридазинил, 2-тиазолил, 4-тиазолил, 5-тиазолил, 5-тетразолил, 2-триазолил, 5-триазолил, 2-тиенил, 3-тиенил, карбазолил, бензимидазолил, бензотиенил, бензофуранил, индолил, хинолинил, бензотриазолил, бензотиазолил, бензооксазолил, бензимидазолил, изохинолинил, индолил, изоиндолил, акридинил или бензоизоксазолил. Также включенной в объем термина "гетероарил", в том смысле, в котором он используется в данном описании, является группа, в которой гетероароматическое кольцо сконденсировано с одним или более ароматическими или неароматическими кольцами, где радикал или место присоединения находится в гетероароматическом кольце. Примеры включают тетрагидрохинолин, тетрагидроизохинолин и пиридо[3,4-d]пиримидинил. Термин "гетероарил" также относится к кольцам, которые необязательно замещены. Термин "гетероарил" можно использовать взаимозаменяемо с термином "гетероарильное кольцо" или термином "гетероароматический".
Арил (включая аралкил, аралкокси, арилоксиалкил и тому подобное) или гетероарил (включая гетероаралкил и гетероарилалкокси и тому подобное) могут включать один или более заместителей. Примеры подходящих заместителей при ненасыщенном атоме углерода арила, гетероарила, аралкила или гетероаралкила включают атом галогена, -Rо, -ORо, -SRо, 1,2-метилендиокси, 1,2-этилендиокси, защищенный ОН (такой, как ацилокси), фенил (Ph), замещенный Ph, -О(Ph), замещенный -О(Ph), -СН2(Ph), замещенный -СН2(Ph), -СН2СН2(Ph), замещенный -СН2СН2(Ph), -NO2, -CN, -N(Ro)2, -NRoC(O)Ro, -NRoC(O)N(Ro)2, -NRoCO2Ro, -NRoNRoC(O)Ro, -NRo NRoC(O)N(Ro)2, -NRoNRoCO2Ro, -C(O)C(O)Ro, -C(O)CH2C(O)Ro, -CO2Ro, -C(O)Ro, -C(O)N(Ro)2, -OC(O)N(Ro)2, -S(O)2Ro, -SO2N(Ro)2, -S(O)Ro, -NRoSO2N(Ro)2, -NRoSO2Ro, -C(=S)N(Ro)2, -C(=NH)-N(Ro)2, -(CH2)Y NHC(O)Ro, -(CH2)YNHC(O)CH(V-Ro)(Ro), где Ro представляет Н, замещенную или незамещенную алифатическую группу, незамещенное гетероарильное или гетероциклическое кольцо, фенил (Ph), замещенный Ph, -О(Ph), замещенный -О(Ph), -СН2(Ph) или замещенный -СН2(Ph); y равно 0-6; и V представляет линкерную группу. Примеры заместителей в алифатической группе или фенильном кольце включают амино, алкиламино, диалкиламино, аминокарбонил, атом галогена, алкил, алкиламинокарбонил, диалкиламинокарбонил, алкиламинокарбонилокси, диалкиламинокарбонилокси, алкокси, нитро, циано, карбокси, алкоксикарбонил, алкилкарбонил, гидрокси, галогеналкокси или галогеналкил.
Алифатическая группа или неароматическое гетероциклическое кольцо может содержать один или более заместителей. Примеры подходящих заместителей при насыщенном атоме углерода алифатической группы или неароматического гетероциклического кольца включают таковые, перечисленные выше для ненасыщенного углерода арила или гетероарила, и являются следующими: =O, =S, =NNHR*, =NN(R*)2, =N-, =NNHC(O)R*, =NNHCO2(алкил), =NNHSO2(алкил) или =NR*, где каждый R* независимо выбран из атома водорода, незамещенной алифатической группы или замещенной алифатической группы. Примеры заместителей в алифатической группе включают амино, алкиламино, диалкиламино, аминокарбонил, атом галогена, алкил, алкиламинокарбонил, диалкиламинокарбонил, алкиламинокарбонилокси, диалкиламинокарбонилокси, алкокси, нитро, циано, карбокси, алкоксикарбонил, алкилкарбонил, гидрокси, галогеналкокси или галогеналкил.
Подходящие заместители при азоте ароматического или неароматического гетероциклического кольца включают -R+, -N(R+)2, -C(O)R+, -CO2R+, -C(O)C(O)R+, -C(O)CH2C(O)R+, -SO2R+, -SO2N(R+)2, -C(=S)N(R+)2, -C(=NH)N(R+)2 и -NR+SO2R+, где R+представляет Н, алифатическую группу, замещенную алифатическую группу, фенил (Ph), замещенный Ph, -О(Ph), замещенный -О(Ph), -СН2(Ph), замещенный -СН2(Ph) или незамещенное гетероарильное или гетероциклическое кольцо. Примеры заместителей в алифатической группе или фенильном кольце включают амино, алкиламино, диалкиламино, аминокарбонил, атом галогена, алкил, алкиламинокарбонил, диалкиламинокарбонил, алкиламинокарбонилокси, диалкиламинокарбонилокси, алкокси, нитро, циано, карбокси, алкоксикарбонил, алкилкарбонил, гидрокси, галогеналкокси или галогеналкил.
Термин "линкерная группа" или "линкер" означает органическую группу, которая связывает две части соединения. Обычно линкеры включают атом, такой как атом кислорода или атом серы, звено, такое как -NH-, -CH2-, -C(O)-, -C(O)NH- или цепь атомов такую, как алкилиден. Как правило, молекулярная масса линкера находится в пределах примерно 14-200. Примеры линкеров включают насыщенный или ненасыщенный С1-6алкилиден, который необязательно замещен, и в котором один или два насыщенных атома углерода цепи необязательно замещены -C(O)-, -C(O)C(O)-, -CONH-, -CONHNH-, -CO2-, -OC(O)-, -NHCO2-, -O-, -NHCONH-, -OC(O)NH-, -NHNH-, -NHCO-, -S-, -SO-, -SO2-, -NH-, -SO2NH- или -NHSO2-.
Термин "алкилиден" относится к необязательно замещенной, нормальной или разветвленной углеродной цепи, которая может быть полностью насыщенной или иметь одну или более единиц ненасыщенности. Необязательными заместителями являются описанные выше для алифатической группы.
Допустимо сочетание заместителей или переменных, если только такое сочетание приводит к образованию стабильного или химически возможного соединения. Стабильное или химически возможное соединение представляет собой такое соединение, которое в значительной степени не изменяется при температуре 40°С или ниже при отсутствии влаги или других химически реактивных условий по меньшей мере в течение недели.
Специалистам в данной области очевидно, что некоторые соединения данного изобретения могут находиться в таутомерных формах, все подобные таутомерные формы соединений входят в объем изобретения.
Если не указано иначе, то подразумевается, что структуры, представленные здесь, включают все стереохимические формы структуры, т.е. R- и S-конфигурации для каждого асимметричного центра. Следовательно, отдельные стереохимические изомеры, а также смеси энантиомеров и диастереоизомеров данных соединений входят в объем изобретения. Если не указано иначе, то также подразумевается, что структуры, описанные здесь, включают соединения, которые различаются только наличием одного или более изотопно обогащенных атомов. Например, соединения, имеющие данные структуры, за исключением замещения атома водорода дейтерием или тритием, или замещения атома углерода13С- или14С-углеродом, входят в объем данного изобретения.
Одно предпочтительное воплощение данного изобретения относится к способу лечения бактериальной инфекции у млекопитающего, нуждающегося в этом, включающему стадию введения указанному млекопитающему терапевтически эффективного количества соединения, имеющего формулу Ia или Ib.

или его фармацевтически приемлемого производного или пролекарства, где R1, R2, R3, R4 и R5 имеют значения, определенные выше.
Примеры предпочтительного R1 включают необязательно замещенный фенил, 2-пиридил, 3-пиридил, 4-пиридил, тиенил, пиримидил, имидазол-1-ил, имидазол-2-ил, пиразол-1-ил, аминопиримидинил, хинолинил, аминобензимидазол и индолил. Предпочтительный R9, если имеется в R1-арильном или гетероарильном кольце, включает атом галогена, CN, оксо, R6, SR6, OR6, N(R6)2, CON(R6)2, CO2R6, CON(R)COR6, N(R)TnCO2R6, N(R)TnNRCO2R6, N(R)TnN(R6)2, NO2, Tn(галогеналкил), CO2N(R6)2, COR6, SO2R6 или SO2N(R6)2. Примеры таких групп R9 включают, но не ограничиваются ими, пиррол-2,5-дион, NR2, OR, CO2H, NO2, OH, NHCOR, NHCO2R, NHCH2CO2R, NH(CH2)2NHCO2R, CH2CO2R, CF3, SO2R, NHCH(CH2OH)CO2H, N-SO2 Me-пиперидинил, SMe, NH(CH2)2NH2 и пиперидинил.
Предпочтительные группы R2 и R3включают атом галогена, CN, CO2R6, OR6 и R6. Примеры предпочтительных групп R3включают Br, F, Cl, COOH, CN, OMe, метил, этил, трет-бутил, CF3, OH и OBn.
Примеры предпочтительного R5 включают СО2 (алифатический), С(=NH)-NH2 и CON(R7)2, такой как СО(пиперидин-1-ил), CONHEt, CONHMe, CONH(циклопропил), CONH(изопропил), CONH(пропил), CONH(пирролидинил), CO2Et и CO2Me.
Предпочтительные соединения формулы Ia и Ib включают таковые, имеющие один или более, или наиболее предпочтительно все признаки, выбранные из группы, состоящей из:
(а) R1 представляет необязательно замещенное арильное или гетероарильное кольцо;
(b) R2 и R3 каждый независимо выбран из атома галогена, CN, CO2R6, OR6 или R6;
(с) R5 представляет CO2 R, COAr, COR, CON(R7)2, Ar, (CH2)YCO2R или (CH2)yN(R7)2; и
(d) R9 представляет атом галогена, CN, оксо, R6, SR6, OR6, N(R6)2, CON(R6)2, CO2R6, CON(R)COR6, N(R)TnCO2R6, N(R)TnNRCO2R6, N(R)TnN(R6)2, NO2, Tn(галогеналкил), CO2 N(R6)2, COR6, SO2R6 или SO2N(R6)2.
Более предпочтительные соединения формулы Ia и Ib включают таковые, имеющие один или более, или наиболее предпочтительно все признаки, выбранные из группы, состоящей из:
(а) R1 представляет необязательно замещенное кольцо, выбранное из фенила, 2-пиридила, 3-пиридила, 4-пиридила, тиенила, пиримидила, имидазол-1-ила, имидазол-2-ила, пиразол-1-ила, аминопиримидинила, хинолинила, аминобензимидазола или индолила;
(b) R2 представляет атом водорода, алкокси, аминоалкил или атом галогена;
(с) R3 представляет атом водорода, алкокси, аралкокси или атом галогена;
(d) R4 представляет атом водорода или (СН2)YR2;
(е) R5 представляет CON(R7)2, Ar, (CH2)Y CO2R или (CH2)YN(R7)2; и
(f) R9 представляет атом галогена, CN, оксо, R6, SR6, OR6, N(R6)2, CON(R6)2, CO2R6, CON(R)COR6 илиN(R)TnCO2R6.
Выбранные соединения формулы Ia представлены в таблице 1.
Выбранные соединения формулы Ib представлены в таблице 2.
Другое воплощение данного изобретения относится к соединениям формулы IIa или IIb.

или их фармацевтически приемлемому производному или пролекарству, в которой:
W представляет атом азота или CRa;
Rа выбран из атома водорода, атома галогена, -CF3, R7, -OR7 или -N(R7)2;
R1 представляет арильное или гетероарильное кольцо, где указанное кольцо необязательно замещено вплоть до четырех R9; где заместитель R9 в орто-положении R1, будучи взятый вместе с R2, может образовывать конденсированное, ненасыщенное или частично ненасыщенное, необязательно замещенное 5-8-членное кольцо, содержащее 0-2 кольцевых гетероатома, выбранных из атомов азота, кислорода или серы;
R2 и R3 каждый независимо выбран из R6, атома галогена, CN, SR6, OR6, N(R6)2, NRCO2R6, NRCON(R6)2, CON(R6)2, NRCOR6, NRN(R6)2, COR6, CO2R6 , COCOR6, SO2R6, SO2N(R6)2 или NRSO2R6; или R2 и R3, будучи взятые вместе, образуют конденсированное, ненасыщенное или частично ненасыщенное, необязательно замещенное 5-8-членное кольцо, содержащее 0-2 кольцевых гетероатома, выбранных из атомов азота, кислорода или серы;
R4 выбран из R6, CON(R6), COR6, CO2R6, COCOR6, SO2R6, SO2N(R6)2 или (CH2)YR2;
y равно 1-6;
каждый R независимо выбран из водорода или необязательно замещенной алифатической группы, содержащей от одного до шести атомов углерода;
Ar представляет 5-членное гетероарильное, гетероциклическое или карбоциклическое кольцо, где указанное кольцо необязательно замещено вплоть до трех заместителями, выбранными из оксо, атома галогена, CN, NO2, R8, OR8, NHR8, NHCOR8, NHCONHR8, COR8, CONHR8, SO2R8, NHSO2NHR8 или SO2NHR8;
каждый R6 независимо выбран из R7 или необязательно замещенной группы, выбранной из алкокси, гидроксиалкила, гетероциклила, гетероциклилалкила, арила, аралкила, аралкокси, арилоксиалкила, гетероарила, гетероаралкила, гетероаралкокси или гетероароилоксиалкила;
каждый R7 независимо выбран из атома водорода или необязательно замещенной алифатической группы, содержащей от одного до шести атомов углерода, или два R7 при одном и том же атоме азота, будучи взятые вместе с атомом азота, необязательно образуют 4-6-членное, насыщенное или ненасыщенное гетероциклическое кольцо, содержащее от одного до трех гетероатомов;
R8 представляет С1-С4 алифатическую группу, где два R8 в смежных положениях Ar, или арильного или гетероарильного кольца, могут быть взяты вместе с их промежуточными атомами с образованием 3-6-членного конденсированного кольца;
каждый R9 независимо выбран из оксо, атома галогена, CN, NO2, Tn (галогеналкила), R6, SR6, OR6, OR8, N(R6)2, CON(R6)2, CON(R)COR6, COR6, CO2 R6, CO2N(R6)2, COCOR6, SO2R6, SO2N(R6)2,N(R)TnCO2R6, N(R)TnCON(R6)2, N(R)TnN(R6)2, N(R)TnNRCO2R6, N(R)TnNRCON(R6)2, N(R)TnCOR6, N(R)TnNRCOR6, N(R)TnSO2N(R6)2, N(R)TnSO2R6, TnPO(OR7)2, TnOPO(OR7)2, TnSP(OR7)2, TnPO(OR7)2 или TnNPO(OR7)2;
каждый Q независимо выбран из С1-С3 разветвленного или нормального алкила;
Т выбран из -Q- или -Qm-CH(Qm-R2)-; и
каждый m и n независимо выбран из нуля или 1.
Примеры предпочтительного R1 включают необязательно замещенный фенил, 2-пиридил, 3-пиридил, 4-пиридил, тиенил, пиримидил, имидазол-1-ил, имидазол-2-ил, пиразол-1-ил, аминопиримидинил, хинолинил, аминобензимидазол и индолил. Предпочтительный R9, если имеется в R1 -арильном или гетероарильном кольце формул IIa или IIb, включает атом галогена, CN, оксо, R6, SR6, OR6, N(R6)2, CON(R6)2, CO2R6,CON(R)COR6 и N(R)TnCO2R6. Примеры групп R9 включают, но не ограничиваются ими, пиррол-2,5-дионом, NR2, OR, CO2H, NO2, OH, NHCOR, NHCO2R, NHCH2CO2R, NH(CH2)2NHCO2R, CH2CO2R, CF3, SO2R, NHCH(CH2OH)CO2H, N-SO2Me-пиперидинилом, SMe, NH(CH2)2NH2 и пиперидинилом.
Предпочтительные группы R2 и R3 включают атом галогена, CN, CO2R6, OR6 и R6. Примеры предпочтительных групп R3 включают Br, F, Cl, COOH, CN, OMe, метил, этил, трет-бутил, CF3, OH и OBn.
Предпочтительные соединения формулы IIa и IIb включают таковые, имеющие один или более, или наиболее предпочтительно все признаки, выбранные из группы, состоящей из:
(а) R1 представляет необязательно замещенное арильное или гетероарильное кольцо;
(b) R2 и R3 каждый независимо выбран из атома галогена, CN, CO2R6, OR6 или R6;
(с) R9 представляет атом галогена, CN, оксо, R6, SR6, OR6, N(R6)2, CON(R6)2, CO2R6, CON(R)COR6, N(R)TnCO2R6, N(R)TnNRCO2R6, N(R)TnN(R6)2, NO2, Tn(галогеналкил), CO2N(R6)2, COR6, SO2R6 или SO2N(R6)2;
Более предпочтительные соединения формулы IIa и IIb включают таковые, имеющие один или более, или наиболее предпочтительно все признаки, выбранные из группы, состоящей из:
(а) R1 представляет необязательно замещенное кольцо, выбранное из фенила, 2-пиридила, 3-пиридила, 4-пиридила, тиенила, пиримидила, имидазол-1-ила, имидазол-2-ила, пиразол-1-ила, аминопиримидинила, хинолинила, аминобензимидазола и индолила;
(b) R2 представляет атом водорода, алкокси, аминоалкил или атом галогена;
(с) R3 представляет атом водорода, алкокси, аралкокси или атом галогена;
(d) R4 представляет атом водорода или (СН2)YR2; и
(е) R9 представляет атом галогена, CN, оксо, R6, SR6, OR6, N(R6)2, CON(R6)2, CO2R6, CON(R)COR6 илиN(R)TnCO2R6.
Другое воплощение данного изобретения относится к соединениям формулы IIIa или IIIb:

или их фармацевтически приемлемому производному или пролекарству, в которой:
W представляет атом азота или CRa;
Rа выбран из атома водорода, атома галогена, -CF3, R7, -OR7 или -N(R7)2;
кольцо А необязательно замещено вплоть до трех R9; где, когда заместитель R9находится в орто-положении кольца А, то указанный заместитель R9 может быть взят вместе с R2 с образованием необязательно замещенного 5-7-членного кольца, содержащего 0-2 кольцевых гетероатома, выбранных из атомов азота, кислорода или серы;
R2 и R3 каждый независимо выбран из R6, атома галогена, CN, SR6, OR6, N(R6)2, NRCO2R6, NRCON(R6)2, CON(R6)2, NRCOR6, NRN(R6)2, COR6, CO2R6, COCOR6, SO2R6, SO2N(R6)2 или NRSO2R6; или R2 и R3, будучи взятые вместе, образуют конденсированное, ненасыщенное или частично ненасыщенное, необязательно замещенное 5-8-членное кольцо, содержащее 0-2 кольцевых гетероатома, выбранных из атомов азота, кислорода или серы;
R4 выбран из R6, CON(R6), COR6, CO2R6, COCOR6, SO2R6, SO2N(R6)2 или (CH2)YR2;
y равно 1-6;
R5 выбран из R7, Ar, COAr, CON(R7)Ar, (CH2)YCO2R, (CH2)YN(R7)2, C(=NR10)-N(R7)2, C(=NR10)-NRCOR, C(=S)-N(R7 )2, CON(R7)2, CO2R, COR, SO2R или SO2N(R7)2;
Ar представляет 5-членное гетероарильное, гетероциклическое или карбоциклическое кольцо, где указанное кольцо необязательно замещено вплоть до трех заместителями, выбранными из оксо, атома галогена, CN, NO2, R8, OR8, NHR8, NHCOR8, NHCONHR8, COR8, CONHR8, SO2R8, NHSO2NHR8 или SO2NHR8;
каждый R независимо выбран из водорода или необязательно замещенной алифатической группы, содержащей от одного до шести атомов углерода;
каждый R6 независимо выбран из R7 или необязательно замещенной группы, выбранной из алкокси, гидроксиалкила, гетероциклила, гетероциклилалкила, арила, аралкила, аралкокси, арилоксиалкила, гетероарила, гетероаралкила, гетероаралкокси или гетероароилоксиалкила;
каждый R7 независимо выбран из атома водорода или необязательно замещенной алифатической группы, содержащей от одного до шести атомов углерода, или два R7 при одном и том же атоме азота, будучи взятые вместе с атомом азота, необязательно образуют 4-6-членное, насыщенное или ненасыщенное гетероциклическое кольцо, содержащее от одного до трех гетероатомов;
R8 представляет С1-С4 алифатическую группу, где два R8 в смежных положениях Ar, или арильного или гетероарильного кольца, могут быть взяты вместе с их промежуточными атомами с образованием 3-6-членного конденсированного кольца;
каждый R9 независимо выбран из оксо, атома галогена, CN, NO2, Tn(галогеналкила), R6, SR6, OR6, OR8, N(R6)2, CON(R6)2, CON(R)COR6, COR6, CO2R6, CO2N(R6)2, COCOR6, SO2R6, SO2 N(R6)2,N(R)TnCO2R6, N(R)TnCON(R6)2, N(R)TnN(R6)2, N(R)TnNRCO2R6, N(R)TnNRCON(R6)2, N(R)TnCOR6, N(R)TnNRCOR6, N(R)TnSO2N(R6)2, N(R)TnSO2R6, TnPO(OR7)2, TnOPO(OR7)2, TnSP(OR7)2, TnPO(OR7)2 или TnNPO(OR7)2;
каждый Q независимо выбран из С1-С3 разветвленного или нормального алкила;
Т выбран из -Q- или -Qm-CH(Qm-R2)-; и
каждый m и n независимо выбран из нуля или 1; и
R10 выбран из R7 или Ar.
Предпочтительный R9, если имеется в кольце А формул IIIa и IIIb, включает атом галогена, CN, оксо, R6, SR6, OR6, N(R6)2, CON(R6)2, CO2R6, CON(R)COR6,N(R)TnCO2R6. Примеры таких групп R9 включают, но не ограничиваются ими, пиррол-2,5-дион, NR2, OR, CO2H, NO2, OH, NHCOR, NHCO2R, NHCH2CO2R, NH(CH2)2 NHCO2R, CH2CO2R, CF3, SO2R, NHCH(CH2OH)CO2H, N-SO2Me-пиперидинил, SMe, NH(CH2)2NH2 и пиперидинил.
Предпочтительные группы R2 и R3 включают атом галогена, CN, CO2R6, OR6 и R6. Примеры предпочтительных групп R3 включают Br, F, Cl, COOH, CN, OMe, метил, этил, трет-бутил, CF3, OH и OBn.
Примеры предпочтительного R5 включают СО2 (алифатический), С(=NH)-NH2 и CON(R7)2, такой как СО(пиперидин-1-ил), CONHEt, CONHMe, CONH(циклопропил), CONH(изопропил), CONH(пропил), CONH(пирролидинил), CO2Et и CO2Me.
Предпочтительные соединения формул IIIa и IIIb включают таковые, имеющие один или более, или наиболее предпочтительно все признаки, выбранные из группы, состоящей из:
(а) R2 и R3 каждый независимо выбран из атома галогена, CN, CO2R6, OR6 или R6;
(b) R5 представляет CO2R, COAr, COR, CON(R7)2, Ar, (CH2)YCO2R или (CH2)yN(R7)2; и
(с) R9 представляет атом галогена, CN, оксо, R6, SR6, OR6, N(R6)2, CON(R6)2, CO2 R6, CON(R)COR6, N(R)TnCO2R6, N(R)TnNRCO2R6, N(R)TnN(R6)2, NO2, Tn(галогеналкил), CO2N(R6)2, COR6, SO2R6 или SO2N(R6)2.
Более предпочтительные соединения формул IIIa и IIIb включают таковые, имеющие один или более, или наиболее предпочтительно все признаки, выбранные из группы, состоящей из:
(а) R2 представляет атом водорода, алкокси, аминоалкил или атом галогена;
(b) R3 представляет атом водорода, алкокси, аралкокси или атом галогена;
(c) R4 представляет атом водорода или (СН2)YR2;
(d) R5 представляет CON(R7)2, Ar, (CH2)YCO2R или (CH2)YN(R7)2; и
(e) R9 представляет атом галогена, CN, оксо, R6, SR6, OR6, N(R6)2, CON(R6)2, CO2R6, CON(R)COR6 илиN(R)TnCO2R6.
Соединения данного изобретения в основном можно получить способами, известными специалистам в данной области для аналогичных соединений, как показано на общих схемах I-VII ниже. Подробно условия, использованные для получения данных соединений, представлены ниже в примерах.

Реагенты и условия: (а) Ar-бороновая кислота, PdCl2 (dppf), K3PO4, ДМФА, 95°С, 18 ч; (b) 40 фунтов/кв. дюйм, 10% Pd/С, EtOAc; (c) ROCOCl, NaOH, H2O, 0°С; (d) p-TsOH, ROH, кипячение с обратным холодильником, 1 ч.
Соединения 2 получают обработкой раствора 4-бром-2-нитроанилина (1) в ДМФА арилбороновой кислотой (1,2 экв), фосфатом калия (1,3 экв) и дихлор(дифенилфосфиноферроцен)палладием (0,1 экв). Полученную смесь нагревают при 95°С в течение 18 ч, затем охлаждают до комнатной температуры и разбавляют этилацетатом. Неочищенный продукт выделяют обработкой водой, затем концентрируют в вакууме. Концентрат очищают хроматографией на силикагеле с получением соединения 2. Данной реакцией получают широкий ряд замещений в арильном кольце. Примеры подходящих замещенных и незамещенных арильных групп включают, но не ограничиваются ими, представлены в таблице 1 выше.
Соединение 3 получают обработкой раствора соединения 2 в этилацетате 10% палладием на углероде (0,1 г/ммоль) и полученную суспензию гидрируют при давлении 40 фунтов/кв. дюйм при одновременном встряхивании при комнатной температуре в течение 2 ч. Катализатор удаляют фильтрованием и фильтрат концентрируют в вакууме с получением соединения 3.
Соединения формулы 5 получают вначале получением раствора 2-метил-5-тиопсевдомочевины 4 (1 экв) и алкилхлорформиата (2 экв) в воде при 0°С. К раствору добавляют по каплям 25% водный раствор гидроксида натрия в течение 1 ч, пока значение рН не стабилизируется при 8. Затем добавляют уксусную кислоту для доведения рН до 5, затем добавляют тригидрат ацетата натрия (1 экв) и раствор соединения 3 (1 экв) в ROH. Добавляют п-толуолсульфоновую кислоту (каталитическое количество) и полученную смесь нагревают при температуре кипения с обратным холодильником в течение 1 ч. Затем реакционную смесь охлаждают до комнатной температуры и разбавляют этилацетатом. После обработки водой неочищенный продукт очищают препаративной ВЭЖХ с получением соединения 5.

Реагенты и условия: (а) бис(пинаколато)дибор, КОАс, PdCl2 (dppf), ДМСО, 80°С; (b) ArBr, K3PO4, PdCl2 (dppf), ДМСО, 95°С.
На схеме II выше показан альтернативный способ получения соединения 2. Исходное соединение 1 (1 экв) смешивают с бис(пинаколато)дибором (1,2 экв), PdCl2 (dppf) (0,1 экв) и КОАс (3 экв) в ДМСО и полученную смесь нагревают при 80°С в течение 18 ч. Реакционную смесь охлаждают до комнатной температуры, затем добавляют арилбромид (1,1 экв) с последующим добавлением К3РО4 (3 экв) и PdCl2 (dppf) (0,1 экв). Полученную смесь нагревают при 95°С еще в течение 72 ч, затем дают охладиться до комнатной температуры. Очистка хроматографией дает соединение 2.

Реагенты и условия: (а) BrCN, ТГФ, МеОН, вода, комнатная температура; (b) EtNCO, ТГФ, кипячение с обратным холодильником.
Используя получение соединения номер Ia-84 для иллюстрации, на схеме III выше показан общий способ, используемый для получения соединений формулы IIa. Исходное соединение 6 получают способом, описанным на схеме I на стадиях (а) и (b). Соединение 7 получают обработкой соединения 6 бромистым цианом в ацетонитриле при комнатной температуре в течение ночи. Обработка водой дает соединение 7. Соединение Ia-84 получают из соединения 7 обработкой этилизоцианатом в ТГФ при нагревании при температуре кипения с обратным холодильником в течение ночи. Неочищенный продукт очищают препаративной хроматографией с получением Ia-84.

Реагенты и условия: (а) EtOH, 80°С, 4 ч; (b) PdCl2 (dppf), K3PO4, 95°С, 48 ч; (с) Pd/C, H2, 50 фунтов/кв. дюйм, 6 ч; (d) 2-метил-2-тиопсевдомочевина (14), EtOCOCl, 80°С, 18 ч.
Используя получение соединения номер Ia-86 для иллюстрации, на схеме IV выше показан общий способ, который можно использовать для получения соединений формулы IIIa. Соединение 10 получают из 5-бром-2-хлорпиримидина (8) и N-Boc-этилендиамина (9) нагреванием смеси соединений 8 и 9 в этаноле при 80°С в течение 4 ч. Соединение 12 получают из соединений 10 и 11 способом, представленным на схеме II. Соединение 12 используют для получения Ia-86 на стадиях (с) и (d) по стадиям (b) и (c) схемы I.

Реагенты и условия: (а) BrCN, ТГФ, МеОН, вода, комнатная температура; (b) EtOCOCl, пиридин.
Используя получение соединения номер Ib-1 для иллюстрации, на схеме V выше показан общий способ, который можно использовать для получения соединений формулы Ib. Соединение 16 получают из соединения 15 способом, представленным на схеме III, стадия (а). Соединение Ib-1 получают обработкой соединения 16 этилхлорформиатом в пиридине.

Реагенты и условия: (а) (b) EtNCO, ТГФ, кипячение с обратным холодильником.
Используя получение соединения номер Ib-3 для иллюстрации, на схеме VI выше показан общий способ, который можно использовать для получения соединений формулы IIb. Соединение 16 обрабатывают этилизоцианатом в ТГФ при нагревании при температуре кипения с обратным холодильником по схеме III, стадия (b), с получением Ib-3.
Схема VII

Реагенты и условия: (а) NaH, ТГФ, 0°С; (b) Н2 (45 фунтов/кв. дюйм), Pd-C, MeOH; (c) BrCN, MeCN, MeOH, комнатная температура; (d) i EtNCO, ДМСО, 80°С; ii NH3, MeOH, 80°С.
На схеме VII выше представлен общий способ получения соединений данного изобретения, в которых R1 представляет имидазол-1-ил. На стадии (а) динитрофторбензол (17) смешивают с метил-4-имидазолкарбоксилатом (18) в ТГФ и обрабатывают гидридом натрия при 0°С. Через 3 ч реакционную смесь разбавляют толуолом и подкисляют HCl. Фазы разделяют и водную фазу промывают толуолом, охлаждают до 0°С и подщелачивают концентрированным NH4OH. Добавляют этилацетат и полученную смесь перемешивают до растворения всех твердых частиц. Фазы разделяют и органическую фазу промывают насыщенным раствором соли, сушат над Na2SO4, затем фильтруют и фильтрат концентрируют в вакууме. Смесь региоизомеров разделяют и очищают флэш-хроматографией (силикагель, в градиенте

Соединение 19 используют для получения соединения Ia-156, Ia-157 и Ia-170 способом, в основном аналогичным способам, описанным выше для схемы III.
Предпочтительное воплощение данного изобретения относится к способу лечения бактериальной инфекции у млекопитающего, нуждающегося в этом, включающему стадию введения указанному млекопитающему терапевтически эффективного количества соединения, имеющего формулу IIa или IIb:

или его фармацевтически приемлемого производного или пролекарства, в которой:
W представляет атом азота или CRa;
Rа выбран из атома водорода, атома галогена, -CF3, R7, -OR7 или -N(R7)2;
R1 представляет арильное или гетероарильное кольцо, где указанное кольцо необязательно замещено вплоть до четырех R9; где заместитель R9 в орто-положении R1, будучи взятый вместе с R2, может образовывать конденсированное, ненасыщенное или частично ненасыщенное, необязательно замещенное 5-8-членное кольцо, содержащее 0-2 кольцевых гетероатома, выбранных из атомов азота, кислорода или серы;
R2 и R3 каждый независимо выбран из R6, атома галогена, CN, SR6, OR6, N(R6)2, NRCO2R6, NRCON(R6)2, CON(R6)2, NRCOR6, NRN(R6)2, COR6, CO2R6 , COCOR6, SO2R6, SO2N(R6)2 или NRSO2R6; или R2 и R3, будучи взятые вместе, образуют конденсированное, ненасыщенное или частично ненасыщенное, необязательно замещенное 5-8-членное кольцо, содержащее 0-2 кольцевых гетероатома, выбранных из атомов азота, кислорода или серы;
R4 выбран из R6, CON(R6), COR6, CO2R6, COCOR6, SO2R6, SO2N(R6)2 или (CH2)YR2;
y равно 1-6;
каждый R независимо выбран из водорода или необязательно замещенной алифатической группы, содержащей от одного до шести атомов углерода;
Ar представляет 5-членное гетероарильное, гетероциклическое или карбоциклическое кольцо, где указанное кольцо необязательно замещено вплоть до трех заместителями, выбранными из оксо, атома галогена, CN, NO2, R8, OR8, NHR8, NHCOR8, NHCONHR8, COR8, CONHR8, SO2R8, NHSO2NHR8 или SO2NHR8;
каждый R6 независимо выбран из R7 или необязательно замещенной группы, выбранной из алкокси, гидроксиалкила, гетероциклила, гетероциклилалкила, арила, аралкила, аралкокси, арилоксиалкила, гетероарила, гетероаралкила, гетероаралкокси или гетероароилоксиалкила;
каждый R7 независимо выбран из атома водорода или необязательно замещенной алифатической группы, содержащей от одного до шести атомов углерода, или два R7 при одном и том же атоме азота, будучи взятые вместе с атомом азота, необязательно образуют 4-6-членное, насыщенное или ненасыщенное гетероциклическое кольцо, содержащее от одного до трех гетероатомов;
R8 представляет С1-С4 алифатическую группу, где два R8 в смежных положениях Ar, или арильного или гетероарильного кольца, могут быть взяты вместе с их промежуточными атомами с образованием 3-6-членного конденсированного кольца;
каждый R9 независимо выбран из оксо, атома галогена, CN, NO2, Tn (галогеналкила), R6, SR6, OR6, OR8, N(R6)2, CON(R6)2, CON(R)COR6, COR6, CO2 R6, CO2N(R6)2, COCOR6, SO2R6, SO2N(R6)2,N(R)TnCO2R6, N(R)TnCON(R6)2, N(R)TnN(R6)2, N(R)TnNRCO2R6, N(R)TnNRCON(R6)2, N(R)TnCOR6, N(R)TnNRCOR6, N(R)TnSO2N(R6)2, N(R)TnSO2R6, TnPO(OR7)2, TnOPO(OR7)2, TnSP(OR7)2, TnPO(OR7)2 или TnNPO(OR7)2;
каждый Q независимо выбран из С1-С3 разветвленного или нормального алкила;
Т выбран из -Q- или -Qm-CH(Qm-R2)-; и
каждый m и n независимо выбран из нуля или 1.
Другое предпочтительное воплощение данного изобретения относится к способу лечения бактериальной инфекции у млекопитающего, нуждающегося в этом, включающему стадию введения указанному млекопитающему терапевтически эффективного количества соединения формулы IIIa или IIIb:
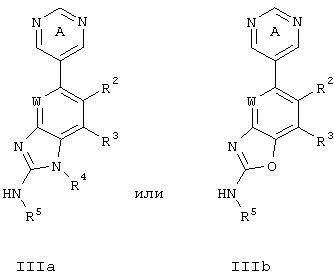
или его фармацевтически приемлемого производного или пролекарства, в которой:
W представляет атом азота или CRa;
Rа выбран из атома водорода, атома галогена, -CF3, R7, -OR7 или -N(R7)2;
кольцо А необязательно замещено вплоть до трех R9; где, когда заместитель R9находится в орто-положении кольца А, то указанный заместитель R9 может быть взят вместе с R2 с образованием необязательно замещенного 5-7-членного кольца, содержащего 0-2 кольцевых гетероатома, выбранных из атомов азота, кислорода или серы;
R2 и R3 каждый независимо выбран из R6, атома галогена, CN, SR6, OR6, N(R6)2, NRCO2R6, NRCON(R6)2, CON(R6)2, NRCOR6, NRN(R6)2, COR6, CO2R6, COCOR6, SO2R6, SO2N(R6)2 или NRSO2R6; или R2 и R3, будучи взятые вместе, образуют конденсированное, ненасыщенное или частично ненасыщенное, необязательно замещенное 5-8-членное кольцо, содержащее 0-2 кольцевых гетероатома, выбранных из атомов азота, кислорода или серы;
R4 выбран из R6, CON(R6), COR6, CO2R6, COCOR6, SO2R6, SO2N(R6)2 или (CH2)YR2;
y равно 1-6;
R5 выбран из R7, Ar, COAr, CON(R7)Ar, (CH2)YCO2R, (CH2)YN(R7 )2, C(=NR10)-N(R7)2, C(=NR10)-NRCOR, C(=S)-N(R7)2, CON(R7)2, CO2R, COR, SO2R или SO2N(R7)2;
Ar представляет 5-членное гетероарильное, гетероциклическое или карбоциклическое кольцо, где указанное кольцо необязательно замещено вплоть до трех заместителями, выбранными из оксо, атома галогена, CN, NO2, R8, OR8, NHR8, NHCOR8, NHCONHR8, COR8, CONHR8, SO2R8, NHSO2NHR8 или SO2NHR8;
каждый R независимо выбран из водорода или необязательно замещенной алифатической группы, содержащей от одного до шести атомов углерода;
каждый R6 независимо выбран из R7 или необязательно замещенной группы, выбранной из алкокси, гидроксиалкила, гетероциклила, гетероциклилалкила, арила, аралкила, аралкокси, арилоксиалкила, гетероарила, гетероаралкила, гетероаралкокси или гетероароилоксиалкила;
каждый R7 независимо выбран из атома водорода или необязательно замещенной алифатической группы, содержащей от одного до шести атомов углерода, или два R7 при одном и том же атоме азота, будучи взятые вместе с атомом азота, необязательно образуют 4-6-членное, насыщенное или ненасыщенное гетероциклическое кольцо, содержащее от одного до трех гетероатомов;
R8 представляет С1-С4 алифатическую группу, где два R8 в смежных положениях Ar, или арильного или гетероарильного кольца, могут быть взяты вместе с их промежуточными атомами с образованием 3-6-членного конденсированного кольца;
каждый R9 независимо выбран из оксо, атома галогена, CN, NO2, Tn(галогеналкила), R6, SR6, OR6, OR8, N(R6)2, CON(R6)2, CON(R)COR6, COR6, CO2R6, CO2N(R6)2, COCOR6, SO2R6, SO2N(R6)2,N(R)TnCO2R6, N(R)Tn CON(R6)2, N(R)TnN(R6)2, N(R)TnNRCO2R6, N(R)TnNRCON(R6)2, N(R)Tn COR6, N(R)TnNRCOR6, N(R)TnSO2N(R6)2, N(R)TnSO2R6, TnPO(OR7)2, TnOPO(OR7)2, TnSP(OR7)2, TnPO(OR7)2 или TnNPO(OR7)2;
каждый Q независимо выбран из С1-С3 разветвленного или нормального алкила;
Т выбран из -Q- или -Qm-CH(Qm-R2)-; и
каждый m и n независимо выбран из нуля или одного; и
R10 выбран из R7 или Ar.
По другому воплощению изобретение обеспечивает способ снижения числа бактерий в биологической пробе. Данный способ включает стадию контактирования указанной биологической пробы с соединением формулы I:

или его фармацевтически приемлемым производным или пролекарством, в которой:
Z представляет О или N-R4;
W представляет атом азота или CRа;
Rа выбран из атома водорода, атома галогена, -CF3, R7, -OR7 или -N(R7)2;
R1 представляет арильное или гетероарильное кольцо, где указанное кольцо необязательно замещено вплоть до четырех R9; где заместитель R9 в орто-положении R1, будучи взятый вместе с R2, могут образовывать конденсированное, ненасыщенное или частично ненасыщенное, необязательно замещенное 5-8-членное кольцо, содержащее 0-2 кольцевых гетероатома, выбранных из атомов азота, кислорода или серы;
R2 и R3 каждый независимо выбран из R6, атома галогена, CN, SR6, OR6, N(R6)2, NRCO2R6, NRCON(R6)2, CON(R6)2, NRCOR6, NRN(R6)2, COR6, СО2R6, COCOR6, SO2R6, SO2N(R6)2 или NRSO2R6; или R2 и R3, будучи взятые вместе, образуют конденсированное, ненасыщенное или частично ненасыщенное, необязательно замещенное 5-8-членное кольцо, содержащее 0-2 кольцевых гетероатома, выбранных из атомов азота, кислорода или серы;
R4 выбран из R6, CON(R6), COR6, CO2R6, COCOR6, SO2R6, SO2N(R6)2 или (CH2)YR2;
y равно 1-6;
R5 выбран из R7, Ar, COAr, CON(R7)Ar, (CH2)YCO2R, (CH2)YN(R7)2, C(=NR10)-N(R7)2, C(=NR10)-NRCOR, C(=S)-N(R7)2, CON(R7)2, CO2R, COR, SO2R или SO2N(R7)2;
Ar представляет 5-членное гетероарильное, гетероциклическое или карбоциклическое кольцо, где указанное кольцо необязательно замещено вплоть до трех заместителями, выбранными из оксо, атома галогена, CN, NO2, R8, OR8, NHR8, NHCOR8, NHCONHR8, COR8, CONHR8, SO2R8, NHSO2NHR8 или SO2NHR8;
каждый R независимо выбран из водорода или необязательно замещенной алифатической группы, содержащей от одного до шести атомов углерода;
каждый R6 независимо выбран из R7 или необязательно замещенной группы, выбранной из алкокси, гидроксиалкила, гетероциклила, гетероциклилалкила, арила, аралкила, аралкокси, арилоксиалкила, гетероарила, гетероаралкила, гетероаралкокси или гетероароилоксиалкила;
каждый R7 независимо выбран из атома водорода или необязательно замещенной алифатической группы, содержащей от одного до шести атомов углерода, или два R7 при одном и том же атоме азота, будучи взятые вместе с атомом азота, необязательно образуют 4-6-членное, насыщенное или ненасыщенное гетероциклическое кольцо, содержащее от одного до трех гетероатомов;
R8 представляет С1-С4 алифатическую группу, где два R8 в смежных положениях Ar, или арильного или гетероарильного кольца, могут быть взяты вместе с их промежуточными атомами с образованием 3-6-членного конденсированного кольца;
каждый R9 независимо выбран из оксо, атома галогена, CN, NO2, Tn(галогеналкила), R6, SR6, OR6, OR8, N(R6)2, CON(R6)2, CON(R)COR6, COR6, CO2R6, CO2N(R6)2, COCOR6, SO2 R6, SO2N(R6)2, N(R)TnCO2R6, N(R)TnCON(R6)2, N(R)TnN(R6)2, N(R)TnNRCO2R6, N(R)TnNRCON(R6)2, N(R)TnCOR6, N(R)TnNRCOR6, N(R)TnSO2 N(R6)2, N(R)TnSO2R6, TnPO(OR7)2, TnOPO(OR7)2, TnSP(OR7 )2, TnPO(OR7)2 или TnNPO(OR7)2;
каждый Q независимо выбран из С1-С3 разветвленного или нормального алкила;
Т выбран из -Q- или -Qm-CH(Qm-R2)-;
каждый m и n независимо выбран из нуля или 1; и
R10 выбран из R7 или Ar.
Термин "биологическая проба", в том смысле, в котором он здесь используется, включает культуры клеток или их экстракты; биопсийный материал, полученный от млекопитающего, или его экстракты; и кровь, слюну, мочу, фекалии, сперму, слезы или другие жидкости организма или их экстракты. Термин "биологическая проба" также включает живые организмы, где в данном случае "контактирование соединения данного изобретения с биологической пробой" является синонимом термина "введение указанного соединения (или композиции, содержащей указанное соединение) млекопитающему".
Предпочтительное воплощение включает контактирование указанной биологической пробы с соединением формулы Ia, Ib, IIa, IIb, IIIa, IIIb или соединением, входящим в перечень в таблицах 1 и 2. Фармацевтические композиции, пригодные для этих способов, описаны ниже.
Соединения данного изобретения являются эффективными ингибиторами гиразы, что определено ферментативным анализом. Также было показано, что данные соединения обладают антимикробной активностью в тесте антимикробной чувствительности. Подробно условия, используемые как для ферментативного анализа, так и теста антимикробной чувствительности, приведены в примерах ниже.
Ингибиторы гиразы данного изобретения или их фармацевтически приемлемые соли можно включить в фармацевтические композиции для введения животным или людям. Данные фармацевтические композиции, эффективные для лечения и профилактики бактериальной инфекции, содержащие ингибитор гиразы в количестве, достаточном для определяемого снижения числа бактерий, и фармацевтически приемлемый носитель, представляют другое воплощение настоящего изобретения. Термин "определяемое снижение числа бактерий" в том смысле, в котором он используется, означает определяемое изменение числа бактерий в пробе, содержащей указанный ингибитор, по сравнению с пробой, содержащей только бактерии.
Известны агенты, которые повышают чувствительность бактерий к антибиотикам. Например, в патенте США 5523288, патенте США 5783561 и патенте США 6140306 описаны способы использования бактерицидного/повышающего проницаемость белка (BPI) для увеличения чувствительности грамположительных и грамотрицательных бактерий к антибиотикам. Агенты, повышающие проницаемость внешней мембраны бактерий, описаны Vaara M. в Microbiological Reviews (1992), pp.395-411, и чувствительность грамотрицательных бактерий - описаны Tsubery et al. в J. Med. Chem. (2000), pp.3085-3092.
Другое предпочтительное воплощение данного изобретения относится к способу, как описано выше, лечения бактериальной инфекции у млекопитающего, нуждающегося в этом, дополнительно включающему стадию введения указанному млекопитающему агента, который повышает чувствительность бактерий к антибиотикам.
По другому предпочтительному воплощению изобретение обеспечивает способ, как описано выше, снижения числа бактерий в биологической пробе, дополнительно включающий стадию контактирования указанной биологической пробы с агентом, который повышает чувствительность бактерий к антибиотикам.
Фармацевтические композиции и способы данного изобретения будут в основном пригодны для борьбы с бактериальными инфекциями in vivo. Примеры бактерий, с которыми можно бороться с помощью композиций и способов данного изобретения включают, но не ограничиваются ими, следующие микроорганизмы: Streptococcus pneumoniae, Streptococcus pyrogenes, Enterococcus fecalis, Enterococcus faecium, Klebsiella pneumoniae, Enterobacter sps. Proteus sps. Pseudomonas aeruginosa, E.coli, Serratia marcesens, Staphylococcus aureus, Coag. Neg. Staph, Haemophilus influenzae, Bacillus anthracis, Mycoplasma pneumoniae и Staphylococcus epidermitidis. Следовательно, композиции и способы будут пригодны для борьбы, лечения и подавления прогрессирования, тяжести или действия нозокоминальных и ненозокоминальных инфекций. Примеры применений при патогенных инфекциях включают, но не ограничиваются ими, инфекции мочевых путей, пневмониюю, инфекции операционных ран и бактериемию. Примеры применений при внебольничных инфекциях включают, но не ограничиваются ими, инфекции мочевых путей, пневмонию, простатит, инфекции кожи и мягких тканей, инфекции в брюшной полости и лечение пациентов с лихорадочной нейтропенией.
В дополнении к соединениям данного изобретения также можно использовать фармацевтически приемлемые производные или пролекарства соединений данного изобретения в композициях для лечения или профилактики указанных выше нарушений.
"Фармацевтически приемлемое производное или пролекарство" означает фармацевтически приемлемую соль, сложный эфир, соль сложного эфира или другое производное соединения данного изобретения, которое при введении реципиенту способно обеспечить, прямо или опосредованно, соединение данного изобретения или его обладающий ингибирующей активностью метаболит или остаток. Особо предпочтительными производными или пролекарствами являются таковые, которые повышают биодоступность соединений данного изобретения при введении данных соединений млекопитающему (например, когда введенное перорально соединение легче всасывается в кровь) или которое повышает доставку исходного соединения в биологическую камеру (например, мозг или лимфатическую систему) по сравнению с исходными соединениями.
Фармацевтически приемлемые пролекарства соединений данного изобретения включают, но не ограничиваются ими, сложные эфиры, эфиры аминокислот, эфиры фосфорных кислот, соли металлов и эфиры сульфокислот.
Фармацевтически приемлемые соли соединений данного изобретения включают таковые, полученные из фармацевтически приемлемых неорганических и органических кислот и оснований. Примеры подходящих солей кислот включают ацетат, адипат, альгинат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, цитрат, камфорат, камфорсульфонат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, формиат, фумарат, глюкогептаноат, глицерофосфат, гликолят, гемисульфат, гептаноат, гексаноат, гидрохлорид, гидробромид, гидройодид, 2-гидроксиэтансульфонат, лактат, малеат, малонат, метансульфонат, 2-нафталинсульфонат, никотинат, нитрат, пальмоат, пектинат, персульфат, 3-фенилпропионат, фосфат, пикрат, пивалат, пропионат, салицилат, сукцинат, сульфат, тартрат, тиоцианат, тозилат и ундеканоат. Можно использовать другие кислоты, такие как щавелевая кислота, которые сами по себе не являются фармацевтически приемлемыми, для получения солей, пригодных в качестве промежуточных соединений при получении соединений по изобретению и их фармацевтически приемлемых аддитивных солей кислоты.
Соли, полученные из соответствующих оснований, включают соли щелочных металлов (например, натрия и калия), щелочноземельных металлов (например, магния), аммония и N+(С1-4 алкила)4. Данное изобретение также предусматривает кватернизацию любых основных азотсодержащих групп раскрываемых соединений. Подобной кватернизацией можно получить водорастворимые или растворимые в масле, или диспергируемые продукты.
Фармацевтические композиции данного изобретения содержат соединение формулы I или его фармацевтически приемлемую соль, и фармацевтически приемлемый носитель. Такие композиции могут необязательно содержать дополнительное терапевтическое средство. Подобные средства включают, но не ограничиваются ими, антибиотик, противовоспалительное средство, ингибитор матриксной металлопротеазы, ингибитор липоксигеназы, антагонист цитокинов, иммуносупрессор, противоопухолевое средство, противовирусное средство, цитокин, фактор роста, иммуномодулятор, простагландин или соединение против сосудистой гиперпролиферации.
Термин "фармацевтически приемлемый носитель" относится к нетоксичному носителю, который можно вводить пациенту вместе с соединением данного изобретения, и который не оказывает отрицательного влияния на его фармакологическую активность.
Фармацевтически приемлемые носители, которые можно использовать в фармацевтических композициях данного изобретения включают, но не ограничиваются ими, ионообменники, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как сывороточный альбумин человека, буферные вещества, такие как фосфаты, глицин, сорбиновую кислоту, сорбат калия, неполные глицеридные смеси насыщенных растительных жирных кислот, воду, соли или электролиты, такие как протамина сульфат, динатрийгидрофосфат, калийгидрофосфат, хлориднатрия, соли цинка, коллоидный диоксид кремния, трисиликат магния, поливинилпирролидон, соединения на основе целлюлозы, полиэтиленгликоль, натриевую соль карбоксиметилцеллюлозы, полиакрилаты, воски, блоксополимеры полиэтилен-полиоксипропилен, ланолин и самоэмульгирующимиеся системы доставки лекарственных препаратов (SEDDS), такие как α-токоферол, сукцинат полиэтиленгликоля 1000 или другие подобные полимерные матрицы для доставки.
Термин "фармацевтически эффективное количество" относится к количеству, эффективному для лечения или улучшение состояния при бактериальной инфекции у пациента. Термин "профилактически эффективное количество" относится к количеству, эффективному для профилактики и значительного подавления бактериальной инфекции у пациента.
В зависимости от конкретного состояния или заболевания, которое подвергается лечению или профилактике, вместе с ингибиторами данного изобретения можно вводить дополнительные терапевтические средства, которые обычно применяют для лечения или профилактики данного состояния. Такие терапевтические средства включают, но не ограничиваются ими, антибиотик, противовоспалительное средство, ингибор матриксной металлопротеазы, ингибитор липоксигеназы, антагонист цитокинов, иммунодепрессант, антинеопластическое средство, противовирусное средство, цитокин, фактор роста, иммуномодулятор, простагландин или соединение против сосудистой гиперпролиферации.
Соединения данного изобретения можно использовать обычным образом для борьбы с бактериальными инфекциями in vivo и для лечения или подавления прогрессирования, или тяжести эффектов, опосредуемых бактериями. Подобные способы лечения, их дозы и требования могут быть выбраны специалистами в данной области из имеющихся способов и методов.
Например, соединение данного изобретения можно сочетать с фармацевтически приемлемым адъювантом для введения пациенту, страдающему от бактериальной инфекции или заболевания, фармацевтически приемлемым образом и в количестве, эффективном для уменьшения тяжести данной инфекции или заболевания.
Альтернативно, соединения данного изобретения можно использовать в композициях и способах лечения или профилактики индивидуумов против бактериальных инфекций или заболеваний в течение продолжительного периода времени. Соединения можно применять в таких композициях либо как таковое, либо вместе с другими соединениями данного изобретения способом, совместимым с обычным применением ингибиторов ферментов в фармацевтических композициях. Например, соединение данного изобретения можно сочетать с фармацевтически приемлемыми адъювантами, обычно применяемыми в вакцинах и вводимых в эффективных для профилактики количествах для защиты индивидуумов в течение продолжительного периода времени против бактериальных инфекций или заболеваний.
Соединения формулы I также можно вводить совместно с другими антибиотиками для усиления терапевтического или профилактического действия в отношении различных бактериальных инфекций. Когда соединения данного изобретения вводят в комбинированной терапии с другими средствами, их можно вводить пациенту последовательно или одновременно. Альтернативно фармацевтические или профилактические композиции данного изобретения содержат комбинацию соединения формулы I и другого терапевтического или профилактического средства.
Дополнительные терапевтические средства, описанные выше, можно вводить отдельно, как часть множественной дозы, содержащей ингибитор композиции. Альтернативно, данные средства могут быть частью единичной дозированной формы, смешанной вместе с ингибитором в одной композиции.
Фармацевтические композиции данного изобретения можно вводить перорально, парентерально, ингаляционно, местно, ректально, интерназально, буккально, вагинально или посредством имплантированного резервуара. Фармацевтические композиции данного изобретения могут включать любые обычные нетоксичные, фармацевтически приемлемые носители, адъюванты или разбавители. В некоторых случаях рН композиции можно довести фармацевтически приемлемыми кислотами, основаниями или буферами для повышения стабильности включенного в состав композиции соединения или его формы для доставки. Термин "парентеральный" в том смысле, в котором он используется, включает подкожную, внутрикожную, внутривенную, внутримышечную, внутрисуставную, внутрисиновиальную, внутристернальную, интратекальную, в очаг поражения и внутричерепную инъекцию или инфузии.
Фармацевтические композиции могут быть в форме стерильного инъекционного препарата, например, в виде стерильной инъекционной водной или маслянистой суспензии. Данную суспензию можно получить с помощью методов, известных в данной области, с использованием диспергирующих или смачивающих агентов (таких, как, например, Твин-80), и суспендирующих агентов. Стерильный инъецируемый препарат может быть также стерильным инъекционным раствором или суспензией в нетоксичном, приемлемом для парентерального введения разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Среди приемлемых носителей и растворителей, которые можно использовать, находятся маннит, вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды обычно используются стерильные, жирные масла. Для данной цели можно применять любое мягкое жирное масло, включая синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота и ее глицеридные производные, пригодны для приготовления инъекционных препаратов, а также природные фармацевтически приемлемые масла, такие как оливковое масло или касторовое масло, особенно в их полиоксиэтилированных формах. Данные масляные растворы или суспензии могут также включать разбавитель или диспергатор, представляющий собой спирт с длинной цепью, такой, как описано в Фармакопее Helvetica, или подобный спирт.
Фармацевтические композиции данного изобретения можно вводить перорально в любой дозированной форме, приемлемой для перорального введения, включая, но не ограничиваясь ими, капсулы, таблетки, а также водные суспензии и растворы. В случае таблеток для перорального введения, носители, которые обычно используются, включают лактозу и кукурузный крахмал. Обычно также добавляют лубриканты, такие как стеарат магния. Для перорального введения в капсуле, пригодные разбавители включают лактозу и сухой кукурузный крахмал. Когда водные суспензии и растворы, и пропиленгликоль вводят перорально, активный ингредиент смешивают с эмульгирующими и суспендирующими агентами. Если желательно, можно добавить подсластители и/или ароматизаторы, и/или окрашивающие агенты.
Фармацевтические композиции данного изобретения можно также вводить в виде суппозиториев для ректального применения. Данные композиции можно получить смешиванием соединения данного изобретения с подходящим, не обладающим раздражающим действием эксципиентом, который находится в твердом состоянии при комнатной температуре, но становится жидким при ректальной температуре и, следовательно, будет расплавляться в прямой кишке с высвобождением активных компонентов. Подобные материалы включают, но не ограничиваются ими, масло какао, пчелиный воск и полиэтиленгликоли.
Местное применение фармацевтических композиций данного изобретения является особенно подходящим, когда желаемое лечение включает области или органы, легко доступные для местной аппликации. Для местной аппликации на кожу фармацевтическая композиция должна быть составлена с подходящей мазью, содержащей активные компоненты, суспендированные или растворенные в носителе. Носители для местного применения соединений данного изобретения включают, но не ограничиваются ими, минеральные масла, жидкий вазелин, белый вазелин, пропиленгликоль, производные полиоксиэтилена-полиоксипропилена, эмульгирующий воск и воду. Альтернативно, фармацевтическую композицию можно составить с подходящим лосьоном или кремом, содержащим активное соединение, суспендированное или растворенное в носителе. Подходящие носители включают, но не ограничиваются ими, минеральное масло, моностеарат сорбита, полисорбат-60, цетиловые эфиры воски, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и воду. Фармацевтические композиции данного изобретения можно также применять местно в нижний отдел кишечного тракта при введении суппозитория для ректального введения или с помощью подходящей клизмы. В данное изобретение также включены трансдермальные пластыри для местного применения.
Фармацевтические композиции данного изобретения можно вводить в виде назального аэрозоля или ингаляцией. Подобные композиции получают способами, хорошо известными в области фармацевтических композиций, и их можно получить в виде растворов в физиологическом растворе, используя бензиловый спирт и другие подходящие консерванты, вещества, способствующие всасыванию, для повышения биодоступности, фторуглероды и/или другие солюбилизирующие или диспергирующие агенты, известные в данной области.
Дозы, находящиеся в пределах примерно от 0,01 до примерно 100 мг/кг массы тела в день, предпочтительно от 0,5 до примерно 75 мг/кг массы тела в день и наиболее предпочтительно примерно от 1 до 50 мг/кг массы тела в день активного ингредиента, пригодны при монотерапии для профилактики и лечения бактериальных инфекций, вызванных бактериями, такими как Streptococcus pneumoniae, Streptococcus pyrogenes, Enterococcus fecalis, Enterococcus faecium, Klebsiella pneumoniae, Enterobacter sps. Proteus sps. Pseudomonas aeruginosa, E.coli, Serratia marcesens, S. aureus и Coag. Neg. Staph.
Как правило, фармацевтические композиции данного изобретения будут вводить примерно от 1 до 5 раз в день или, альтернативно, в виде продолжительной инфузии. Или, альтернативно, композиции настоящего изобретения можно вводить в композиции с пульсирующим высвобождением. Подобное введение можно использовать для длительной или кратковременной терапии. Количество активного ингредиента, которое можно смешать с носителями для получения единичной дозированной формы, будет варьироваться в зависимости от хозяина, который подвергается лечению, и конкретного пути введения. Типичный препарат будет содержать примерно от 5% до примерно 95% активного соединения (мас./мас.). Предпочтительно такие препараты содержат примерно от 20% до примерно 80% активного соединения.
Когда композиции данного изобретения содержат комбинацию соединения формулы I и одного или более дополнительных терапевтических или профилактических средств, то соединение и дополнительное средство должны находиться в дозах в пределах примерно от 10% до 80% от дозы, обычно вводимой при монотерапии.
При улучшении состояния пациента можно вводить поддерживающую дозу соединения, композиции или комбинации данного изобретения, если необходимо. Следовательно, дозу или частоту введения, или оба фактора можно снижать в зависимости от симптомов до уровня, при котором сохраняется улучшенное состояние, и когда симптомы подавлены до желаемого уровня, лечение прекращают. Для пациентов, однако, может быть необходимо прерывающееся лечение в течение продолжительного периода времени при любом рецидиве симптомов заболевания.
Специалистам в данной области, очевидно, понятно, что могут быть необходимы более низкие или более высокие дозы, чем представленные выше. Конкретная дозировка и схемы лечения для любого конкретного пациента будут зависеть от различных факторов, включая активность используемого определенного соединения, возраст, массу тела, общее состояние здоровья, пол, рацион, время введения, скорость выделения, комбинацию препаратов, тяжесть и течение заболевания, и предрасположенность пациента к заболеванию, а также мнение лечащего врача.
По другому воплощению изобретение обеспечивает способы лечения или профилактики бактериальной инфекции или заболевания, включающие стадию введения пациенту любого раскрываемого соединения, фармацевтической композиции или комбинации. Термин "пациент" в том смысле, в котором он используется, означает животное, предпочтительно, млекопитающее, и наиболее предпочтительно, человека.
Соединения данного изобретения также пригодны в качестве промышленно доступных реагентов, которые эффективно связываются с ферментом гиразой В. В качестве промышленно доступных реагентов, соединения настоящего изобретения и их производные можно использовать для блокирования активности гиразы В при постановке биохимических или клеточных тестов для гиразы бактерий или ее гомологов, или их можно преобразовать в их производные для связывания со стабильной смолой в качестве иммобилизованного субстрата для проведения аффинной хроматографии. Эти и другие применения, характеризующие промышленно доступные ингибиторы гиразы В, будут понятны специалистам в данной области.
Для того чтобы лучше понять данное изобретение, ниже приводятся следующие примеры. Данные примеры представлены только с целью иллюстрации, и ни коем образом не ограничивают объем изобретения.
Примеры
Пример 1

4-(Пиридин-3-ил)-2-нитроанилин (2): к раствору 4-бром-2-нитроанилина (217 мг, 1 ммоль) в ДМФА (6 мл) добавляли 3-пиридинбороновую кислоту (148 мг, 1,2 ммоль), фосфат калия (276 мг, 1,3 ммоль) и дихлор(дифенилфосфиноферроцен) палладий (75 мг, 0,1 ммоль). Полученную смесь нагревали при 95°С в течение 18 ч, затем охлаждали до комнатной температуры и разбавляли этилацетатом (80 мл). Полученный раствор последовательно промывали насыщенным водным раствором бикарбоната натрия, водой и насыщенным раствором соли, сушили над сульфатом магния, затем концентрировали в вакууме. Концентрат очищали хроматографией [силикагель, смесь этилацетат:гексан (1:3)→(1:2)] с получением соединения 2 (117 мг, 54%).1Н ЯМР (CDCl3) δ 8,8 (д, 1H), 8,55 (м, 1H), 8,35 (д, 1H), 7,85 (дд, 1H), 7,65 (дд, 1H), 7,35 (м, 1H), 6,95 (д, 1H), 6,25 (уш.с, 2H).
Пример 2

4-Пиридин-3-илбензол-1,2-диамин (3): к раствору соединения 2 (117 мг, 0,54 ммоль) в этилацетате (13 мл) добавляли 10% палладий на углероде (51 мг). Полученную суспензию помещали в аппарат Парра для гидрирования под давлением газообразного водорода 40 фунтов/кв. дюйм при встряхивании, при комнатной температуре в течение 2 ч. Катализатор удаляли фильтрованием и фильтрат концентрировали в вакууме с получением соединения 2 (115 мг, количественный выход).1Н ЯМР (CDCl3) δ 8,8 (м, 1H), 8,45 (м, 1H), 7,75 (м, 1H), 7,25 (м, 1H), 6,95 (м, 2H), 6,80 (м, 1H), 3,25 (уш.с, 4H).
Пример 3

Этиловый эфир (5-пиридин-3-ил-1Н-бензимидазол-2-ил) карбаминовой кислоты (Ia-11): к раствору 2-метил-2-тиопсевдомочевины (151 мг, 0,54 ммоль) и этилхлорформиата (0,103 мл, 1,08 ммоль) в воде (2 мл) при 0°С добавляли по каплям 25% водный раствор гидроксида натрия в течение 1 ч, пока значение рН не стабилизировалось при 8. Затем добавляли достаточное количество уксусной кислоты для доведения рН до 5, затем добавляли тригидрат ацетата натрия (74 мг, 0,54 ммоль) и раствор соединения 2 (0,54 ммоль) в этаноле (3 мл). Добавляли каталитическое количество п-толуолсульфоновой кислоты и полученную смесь нагревали при температуре кипения с обратным холодильником в течение 1 ч. Затем реакционную смесь охлаждали до комнатной температуры и разбавляли этилацетатом (50 мл). Органический раствор промывали водным раствором NaOH, водой и насыщенным раствором соли, затем сушили над сульфатом магния и концентрировали в вакууме. Неочищенный продукт очищали препаративной ВЭЖХ с получением соединения (Ia-11).1Н ЯМР (CDCL3) δ 9.1 (c, 1H), 8,75 (д, 1H), 8,5 (d, 1H), 7,9 (s, 1H), 7,8 (m, 1H), 7,65 (m, 2H), 4,3 (кв, 2H), 1,3 (т, 3H). (M+1) 283.
Пример 4

5-Фенил-1Н-бензимидазол-2-иламин (7): к раствору бифенил-3,4-диамина (0,99 мл) в смеси ТГФ:MeOH:вода (5 мл:10 мл: 10 мл) добавляли бромистый циан (5 М раствор в ацетонитриле, 1,06 ммоль). Полученную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь распределяли между EtOAc и водным раствором гидроксида натрия, и водный слой повторно экстрагировали EtAOc. Объединенные EtAOc-экстракты промывали водой, насыщенным раствором соли, сушили над MgSO4, затем концентрировали в вакууме с получением соединения 7 (147 мг, 71%) в виде не совсем белого твердого вещества.
Пример 5

1-Этил-3-(5-фенил-1Н-бензимидазол-2-ил) мочевина (Ia-84): к раствору соединения 7 (40 мг, 0,19 ммоль) в ТГФ (1 мл) добавляли этилизоцианат (27 мкл, 0,34 ммоль) в виде раствора в ТГФ (0,5 мл). Реакционную смесь нагревали при температуре кипения с обратным холодильником в течение ночи, затем концентрировали в вакууме. Неочищенный продукт очищали препаративной ВЭЖХ с получением Ia-84.
Пример 6
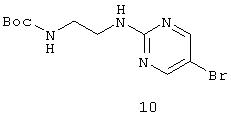
Трет-бутиловый эфир [2-(5-бромпиримидин-2-иламино)этил]карбаминовой кислоты (10): смесь 5-бром-2-хлорпиримидина (500 мг), N-Вос-этилендиамина (496 мг) и триэтиламина (1 мл) в этаноле (10 мл) нагревали при 80°С в течение 4 ч. Затем реакционную смесь концентрировали в вакууме и остаток очищали препаративной ВЭЖХ (смесь гексан: EtAOc, 60:40) с получением соединения 10 (700 мг) в виде белого твердого вещества.
Пример 7

Метиловый эфир 1-(3,4-динитрофенил)-1Н-имидазол-4-карбоновой кислоты (19): к перемешиваемому раствору 1, 2-динитро-4-фторбензола (325 мг, 1,74 ммоль) и метил-4-имидазолкарбоксилата (200 мг, 1,59 ммоль) в ТГФ (5 мл) при 0°С добавляли одной порцией NaH (70 мг, 1,74 ммоль). Полученную смесь перемешивали при 0°С в течение 3 ч, затем разбавляли толуолом и подкисляли 6 Н раствором HCl. Фазы разделяли и водную фазу промывали толуолом, охлаждали до 0°С и подщелачивали концентрированной NH4OH. Добавляли этилацетат и полученную смесь перемешивали до растворения всех твердых частиц. Фазы разделяли, органическую фазу промывали насыщенным раствором соли, сушили над Na2SO4, фильтровали и концентрировали в вакууме. Смесь региоизомеров разделяли и очищали флэш-хроматографией (силикагель, в градиенте

Пример 8

Метиловый эфир 1-[2-(3-этилуреидо)-3Н-бензимидазол-5-ил]-1Н-имидазол-4-карбоновой кислоты (Ia-156): смесь соединения 19 (225 мг, 0,770 ммоль) и 10% Pd-C (каталитическое количество) в MeOH (10 мл) помещали в атмосферу Н2 при давлении 45 фунтов/кв. дюйм (аппарат Парра) на ночь. Смесь фильтровали, концентрировали в вакууме, повторно разбавляли MeCN и MeOH (5 мл/5 мл) и обрабатывали бромистым цианом (168 мг, 1,54 ммоль) при комнатной температуре. Полученную смесь перемешивали в течение 4 ч (выпадает осадок), затем реакцию гасили добавлением 7Н NH3-MeOH. Сырую реакционную смесь концентрировали в вакууме и непосредственно подвергали флэш-хроматографии (силикагель, в градиенте 10%->35% 7H NH3 -MeOH/CH2Cl2) с получением чистого аминобензимидазола в виде белого твердого вещества.
Очищенный аминобензимидазол разбавляли в ДМСО (1 мл), обрабатывали избытком этилизоцианата (0,5 мл) и нагревали до 80°С в течение 3 ч. Реакционную смесь охлаждали до комнатной температуры, удаляли в вакууме избыток этилизоцианата, проводили азеотропную перегонку с MeOH (трижды), разбавляли МеОН (5 мл), обрабатывали NH4OH (2 мл) и нагревали при 80°С в течение 3 ч. Смесь охлаждали до комнатной температуры, концентрировали в вакууме, разбавляли смесью вода/насыщенный раствор соли 1/1 и дважды экстрагировали смесью этилацетат/этанол 4/1. Объединенные органические экстракты сушили над Na2SO4, фильтровали, концентрировали в вакууме и подвергали флэш-хроматографии (силикагель, в градиенте

Пример 9

1-[2-(3-Этилуреидо)-3Н-бензимидазол-5-ил]-1Н-имидазол-4-карбоновая кислота
1-[2-(Этилуреидо)-3Н-бензимидазол-5-ил]-1Н-имидазол-4-карбоновая кислота (Ia-157): раствор соединения Ia-156 (95 мг, 0,289 ммоль) в 6 Н HCl (2 мл) нагревали при температуре кипения с обратным холодильником в течение 6 ч. Затем раствор охлаждали до комнатной температуры, концентрировали в вакууме и последовательно проводили азеотропную перегонку с MeOH (дважды) и ацетоном (дважды). Полученные твердые частицы суспендировали в ацетоне, фильтровали и промывали ацетоном с последующим промыванием гексаном с получением соединения Ia-157 (115 мг, 100%) в виде белого твердого вещества.1H ЯМР (500 МГц, ДМСО-d6): 8,77 (1H, м); 8,52 (1H, м), 7,79 (1H, с); 7,72 (1H, м); 7,65 (2H, м); 5,6-4,0 (2H, уш.с); 3,20 (2H, дт); 1,11 (3H, т).
Пример 10

Раствор соединения Ia-157 (20 мг, 0,051 ммоль) и морфолина (0,050 мл, избыток) в ДМФА (1 мл) обрабатывали PyBrop (20 мг, избыток) при комнатной температуре. Полученную смесь перемешивали в течение ночи, затем разбавляли смесью этилацетат:этанол 4:1, промывали смесью насыщенный раствор соли: вода (5 раз), сушили над Na2SO4, фильтровали, подвергали флэш-хроматографии (силикагель, в градиенте

Пример 11
Были получены другие соединения формулы I способами, в основном аналогичными описанным в приведенных выше примерах 1-6 и представленным на схемах I-VI. Данные по характеристике данных соединений обобщены в таблице 3 ниже и включают масс-спектры (в виде М+1) и данные1Н ЯМР.
Данные1Н ЯМР обобщены в таблице 3 ниже, где приводится "Y", обозначающий данные1Н ЯМР, и было установлено, что они согласуются со структурой. Номера соединений соответствуют номерам соединений, перечисленным в таблице 1.
Пример 12
Анализ активности гиразы-АТФ-азы
Активность ДНК-гиразы в отношении гидролиза АТФ определяли сочетанием продуцирования АДР с участием пируваткиназы/лактатдегидрогеназы с окислением NADH. Данный метод описан ранее (Tamura and Gellert, 1990, J. Biol. Chem., 265, 21342).
Определение активности АТФ-азы проводили при 30°С в забуференных растворах, содержащих 100 мМ Трис, рН 7,6, 1,5 мМ MgCl2, 150 мМ KCl. Сочетающая система включала (конечные концентрации) 2,5 мМ фосфоенолпирувата, 200 мкм никотинамидадениндинуклеотида (NADH), 1 мМ DTT, 30 мкг/мл пируваткиназы и 10 мкг/мл лактатдегидрогеназы. Добавляли 40 нМ фермента (субъединица Gyr A2B2 массой 374 kDa из Staphylococcus aureus) и раствор ингибитора в ДМСО до конечной концентрации 4%, и реакционную смесь инкубировали в течение 10 мин при 30°С. Затем реакцию начинали добавлением АТФ до конечной концентрации 0,9 мМ и определяли скорость убывания NADH при 340 нм в течение 10 мин. Значения ингибирования в процентах определяли, исходя из скорости по отношению к концентрационному профилю, и выражали в виде среднего из двух значений.
В таблице 4 представлены данные по ингибирующей активности в процентах выбранных соединений данного изобретения в тесте ингибирования активности гиразы при концентрации 10 мкМ. Номера соединений соответствуют номерам соединений в таблице 1. Соединения, обладающие активностью и обозначенные "А", обеспечивали процент ингибирования ниже 50%; соединения, обладающие активностью и обозначенные "В", обеспечивали процент ингибирования между 50 и 75%, и соединения, обладающие активностью и обозначенные "С", обеспечивали процент ингибирования выше 75%.
Пример 13
Тестирование чувствительности в жидких средах
Соединения данного изобретения также тестировали на их антимикробную активность тестированием чувствительности в жидких средах. Подобный анализ проводили, следуя указаниям самого последнего документа NCCLS для практики: "M7-A5 Methods for dilution Antimicrobial Susceptibility Tests for Bacteria that Grow Aerobically; Approved Standard - Fifth Edition (2000)". Другие публикации, такие как "Antibiotics in Laboratory Medicine" (Edited by V.Lorian, Publishers Williams and Wilkins, 1996), обеспечивали основные практические методы при лабораторном тестировании антибиотиков. В основном, несколько отдельных колоний бактерий (3-7) с чашки со свежей культурой переносили в соответствующую насыщенную бульонную среду, такую как MHB, соответствующим образом обогащенную для более "требовательных" микроорганизмов. Их культивировали в течение ночи до высокой плотности с последующим разведением в 1000-2000 раз с получением плотности инокулята, находящейся в пределах 5×105-5×106 КОЕ на мл. Альтернативно, свежесобранные колонии можно инкубировать при 37°С в течение примерно 4-8 ч, пока культуры не достигают мутности, равной или превышающей 0,5 по стандарту McFarland (примерно 1,5×108 клеток на мл), и разбавляют с получением того же значения КОЕ на мл. Более удобным методом инокулят готовили с использованием промышленно доступного устройства (система BBL PROMPT), который включает соприкосновение пяти колоний непосредственно с палочкой, в основании которой находятся поперечно-нарезанные желобки, с последующим приготовлением суспензии бактерий в соответствующем объеме физиологического раствора. Разведение до соответствующей клеточной плотности инокулята проводили из данной клеточной суспензии. Бульон, использованный для тестирования, состоял из среды МНВ с добавлением 50 мг Са2+на л и 25 мг Mg2+на л. Готовили серии стандартных разведений контрольных антибиотиков и хранили, как описано в стандарте М7-А5 NCCLS, обычно ряд разведений находился в пределах от 128 мкг на мл до 0,015 мкг на мл (2-кратные серийные разведения). Испытуемые соединения растворяли и разбавляли в день проведения опытов; использовали такие же или подобные пределы концентраций, какие указаны выше. Испытуемые соединения и контроли помещали в многолуночный планшет и добавляли тестируемые бактерии таким образом, чтобы конечная концентрация инокулята составляла примерно 5×104 КОЕ на лунку, и конечный объем равнялся 100 мкл. Планшеты инкубировали при 35°С в течение ночи (16-20 ч) и визуально определяли мутность или проводили количественную оценку на ридере для многолуночных планшетов. Конечная минимальная ингибирующая концентрация (MIC) представляет самую низкую концентрацию препарата, при которой тестируемые микроорганизмы не росли. Результаты подобных определений сравнивали с соответствующими таблицами, имеющимися в двух указанных выше публикациях, для гарантии того, что пределы антибактериальной активности находятся в принятых пределах данного стандартизованного теста.
В таблице 5 представлены результаты теста по определению MIC для выбранных соединений данного изобретения. Номера соединений соответствуют номерам соединений в таблице 1. Соединения, обладающие активностью и обозначенные "А", обеспечивали MIC равную менее чем 10 мкг/мл; соединения, обладающие активностью и обозначенные "В", обеспечивали MIC, находящуюся в пределах 10-40 мкг/мл; соединения, обладающие активностью и обозначенные "С", обеспечивали MIC выше, чем 40 мкг/мл.
Несмотря на то, что описано ряд воплощений данного изобретения, является очевидным, что основные воплощения можно изменить с получением других воплощений, в которых используются продукты и способы данного изобретения.
Реферат
Изобретение относится к области медицины и фармакологии, и касается снижения числа бактерий в биологической пробе путем контактирования указанной пробы с соединением формулы I, способа лечения бактериальной инфекции с помощью соединений формулы I, соединений формулы I и фармацевтической композиции, содержащей соединения формулы I. Изобретение обеспечивает повышенную эффективность лечения. 5 н. и 49 з.п. ф-лы, 5 табл.

Формула




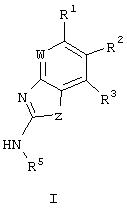
























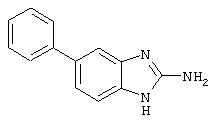





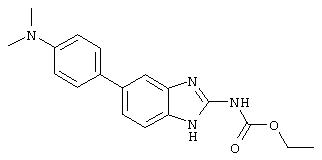


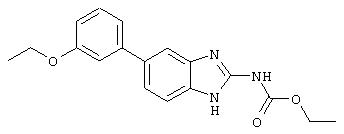











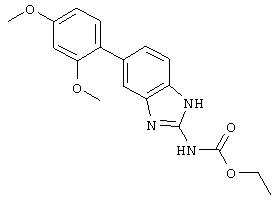





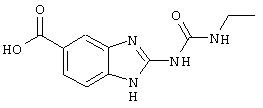











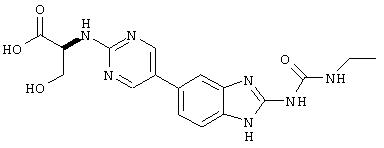






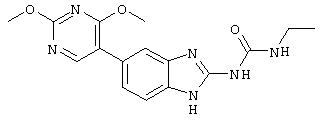







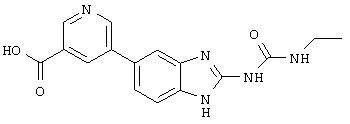




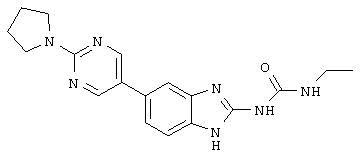









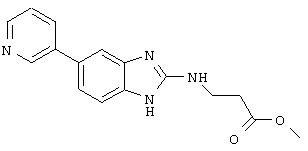



















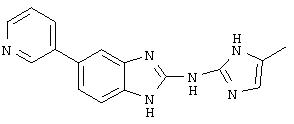















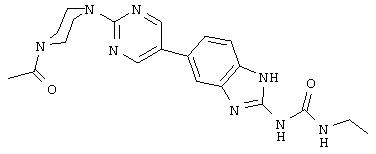




















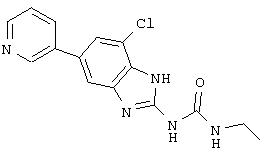








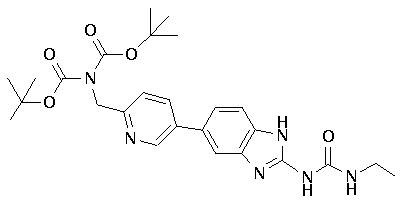





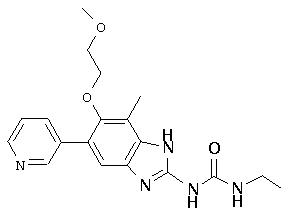



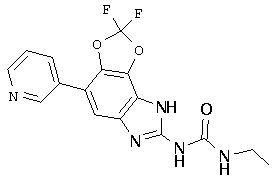





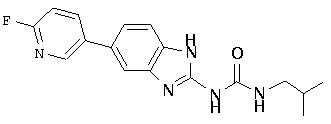


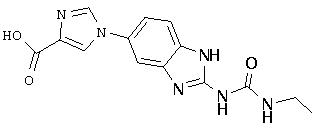









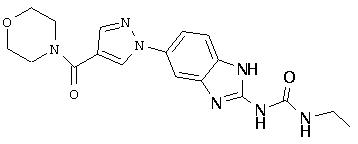















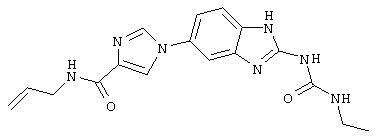

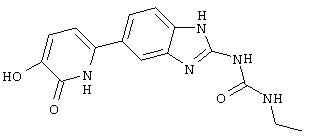





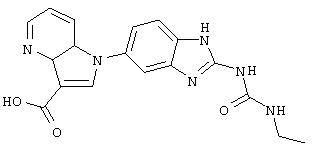









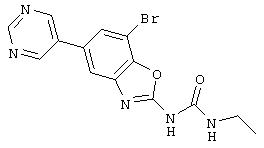

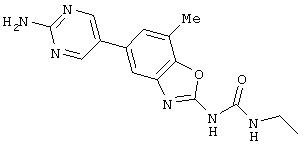

















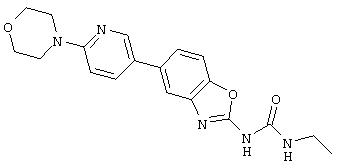



Комментарии