Фармацевтические комбинации ингибитора гистондеацетилаз и ингибитора протеасом или иммуномодулирующего лекарственного средства для лечения рака крови - RU2721409C1
Код документа: RU2721409C1
Чертежи


Описание
Область техники, к которой относится настоящее изобретение
Настоящее изобретение относится к фармацевтической комбинации для лечения рака крови, конкретнее, множественной миеломы, а именно, такого рака крови, который устойчив к стандартным терапиям; и, конкретнее, настоящее изобретение относится к фармацевтической комбинации для лечения миеломы, которая включает в себя ингибитор гистондеацетилаз, ингибитор протеасом или иммуномодулирующее лекарственное средство и противораковое стероидное средство.
Предшествующий уровень техники
Под миеломой, одним из типов рака крови, понимают опухоль, представленную клетками, которые, как правило, обнаруживаются в костном мозге. Более того, множественная миелома (ММ) означает диссеминированное злокачественное новообразование, состоящее из плазматических клеток, характеризующееся множественными миелоидными очагами и секрецией М-компонента (фрагмента моноклонального иммуноглобулина), с массовыми остеолитическими очагами, которые приводят к болям в костях, патологическим переломам, гиперкальциемии и нормоцитарной нормохромной анемии. Множественная миелома не поддается лечению традиционными схемами высокодозной химиотерапии.
В то же время в регуляции экспрессии генов важную роль играет статус ацетилирования нуклеосомных гистонов. Деацетилирование нуклеосомных гистонов опосредуется группой ферментов, деацетилаз гистонов (здесь и далее - HDAC), для которых известно 11 изоформ. Деацетилирование гистонов индуцирует конденсацию хроматина, что приводит к репрессии транскрипции, тогда как ацетилирование позволяет воздействовать на транскрипционный механизм, который облегчает транскрипцию за счет релаксации в определенных хромосомных участках. При попадании в опухолевые клетки селективные ингибиторы HDAC вызывают гиперацетилирование гистонов. О последнем известно, что оно изменяет регуляцию транскрипции подгруппы генов, включая те, которые кодируют опухолевые супрессоры, участвующие в контроле клеточного цикла, делении клетки и апоптозе. Кроме того, было показано in vivo, что ингибиторы HDAC подавляют опухолевый рост. Подавление опухолевого роста сопровождается гиперацетилированием гистонов и тубулина и может включать ряд других механизмов. Ингибиторы HDAC блокируют пролиферацию опухолевых клеток как in vitro, так и in vivo. Как упоминалось выше, известно, что ингибиторы HDAC эффективно подавляют рост раковых клеток при множественной миеломе, но при использовании лекарственных средств предшествующего поколения имеют место сложности, связанные с их высокой токсичностью.
С другой стороны, ингибиторы протеасом и иммуномодулирующие лекарственные средства хорошо известны как основные средства при лечении множественной миеломы.
При этом было показано, что лекарственные средства класса иммуномодуляторов (IMiD) обладают выраженными противомиеломными характеристиками для разных моделей множественной миеломы, а также значимой клинической эффективностью у пациентов с множественной миеломой. Среди них известен бортезомиб (также известный как велкейд или PS-341), о котором сообщалось, что он обладает активностью в отношении линий клеток NSCLS (немелкоклеточной карциномы легкого) в качестве низкомолекулярного ингибитора протеасом, одобренного FDA по показанию рефрактерная множественная миелома, и для которого было показано, что он индуцирует время-зависимый арест клеточного цикла в фазе G2/M.
Ввиду различных сложностей, связанных с лечением данными терапевтическими средствами, включая их токсичность, существует острая необходимость в комбинации и способе, которые были бы более эффективны и менее токсичны при лечении пациентов с множественной миеломой.
Краткое раскрытие настоящего изобретения
Техническая задача
С учетом изложенных обстоятельств авторы настоящего изобретения провели обширные исследования по поиску более эффективного и менее токсичного лекарственного средства против рака крови, а именно, множественной миеломы. В результате, после подтверждения, что таковой является комбинация соединения с химической формулой 1 в качестве ингибитора HDAC и ингибитора протеасом или иммуномодулирующего лекарственного средства и противоракового стероидного средства, было создано настоящее изобретение. Она позволяет добиться синергического противоракового действия с более низкой токсичностью и сопоставимым фармакологическим действием по сравнению с другими ингибиторами HDAC при множественной миеломе, которая в прошлом с трудом поддавалась эффективному лечению из-за различных сложностей, например, токсичности и т.д.
Таким образом, цель настоящего изобретения состоит в том, чтобы представить композицию для лечения миеломы, содержащую соединение с химической формулой 1 в качестве ингибитора гистондеацетилаз, ингибитор протеасом или иммуномодулирующее лекарственное средство и противораковое стероидное средство.
Техническое решение
В соответствии с одним вариантом осуществления, настоящее изобретение относится к фармацевтической комбинации для лечения рака крови, содержащей
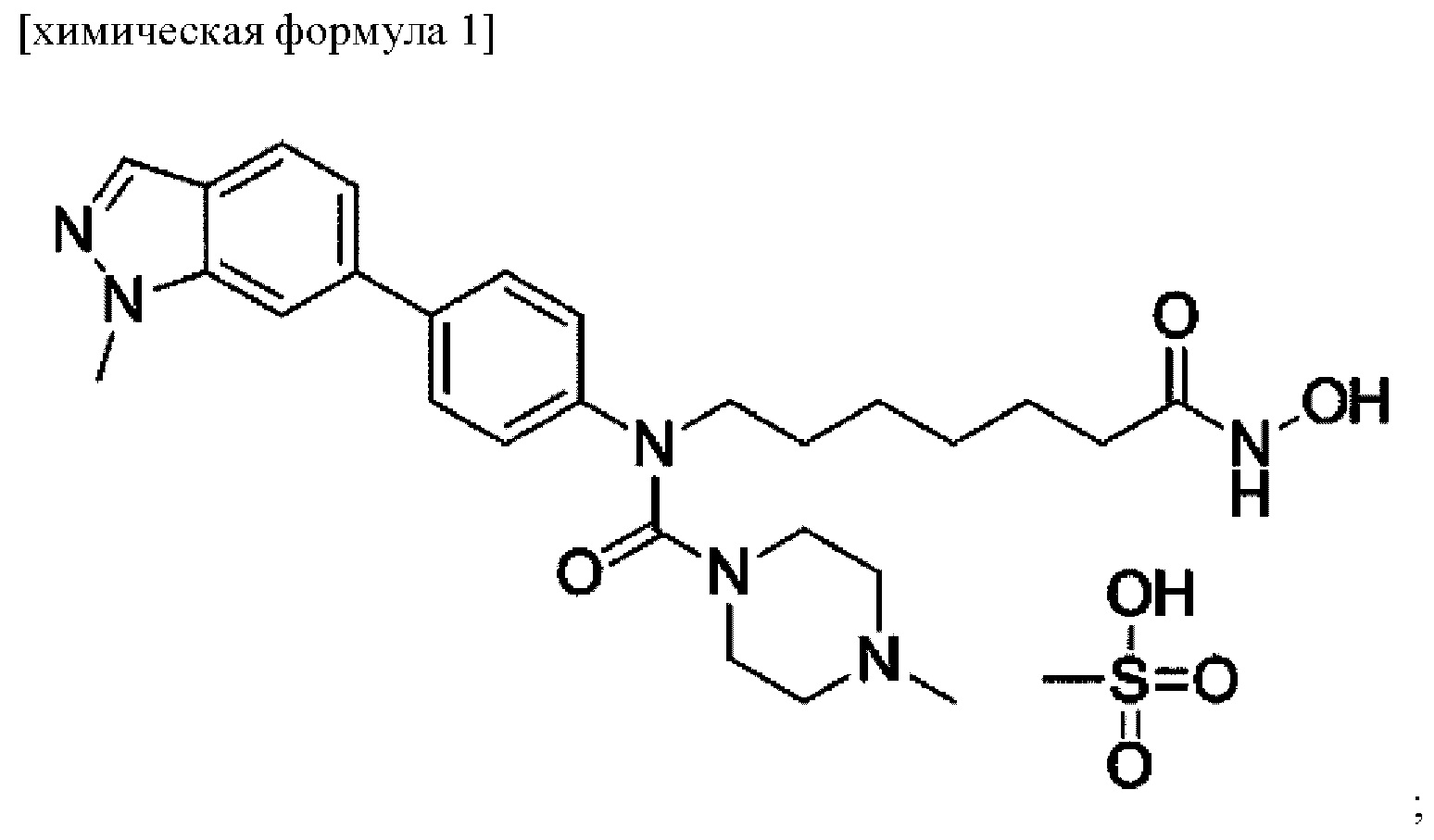
1) производное гидроксамовой кислоты, представленное химической формулой 1, метансульфонат N-(7-(гидроксиамино)-7-оксогептил)-4-метил-N-(4-(1-метил-1Н-индазол-6-ил)фенил)пиперазин-1-карбоксамида или его фармацевтически приемлемую соль в качестве первого активного ингредиента;
2) ингибитор протеасом или иммуномодулирующее лекарственное средство в качестве второго активного ингредиента; и
3) противораковое стероидное средство в качестве третьего активного ингредиента. Предпочтительно, чтобы рак крови был представлен множественной миеломой.
Химическая формула 1
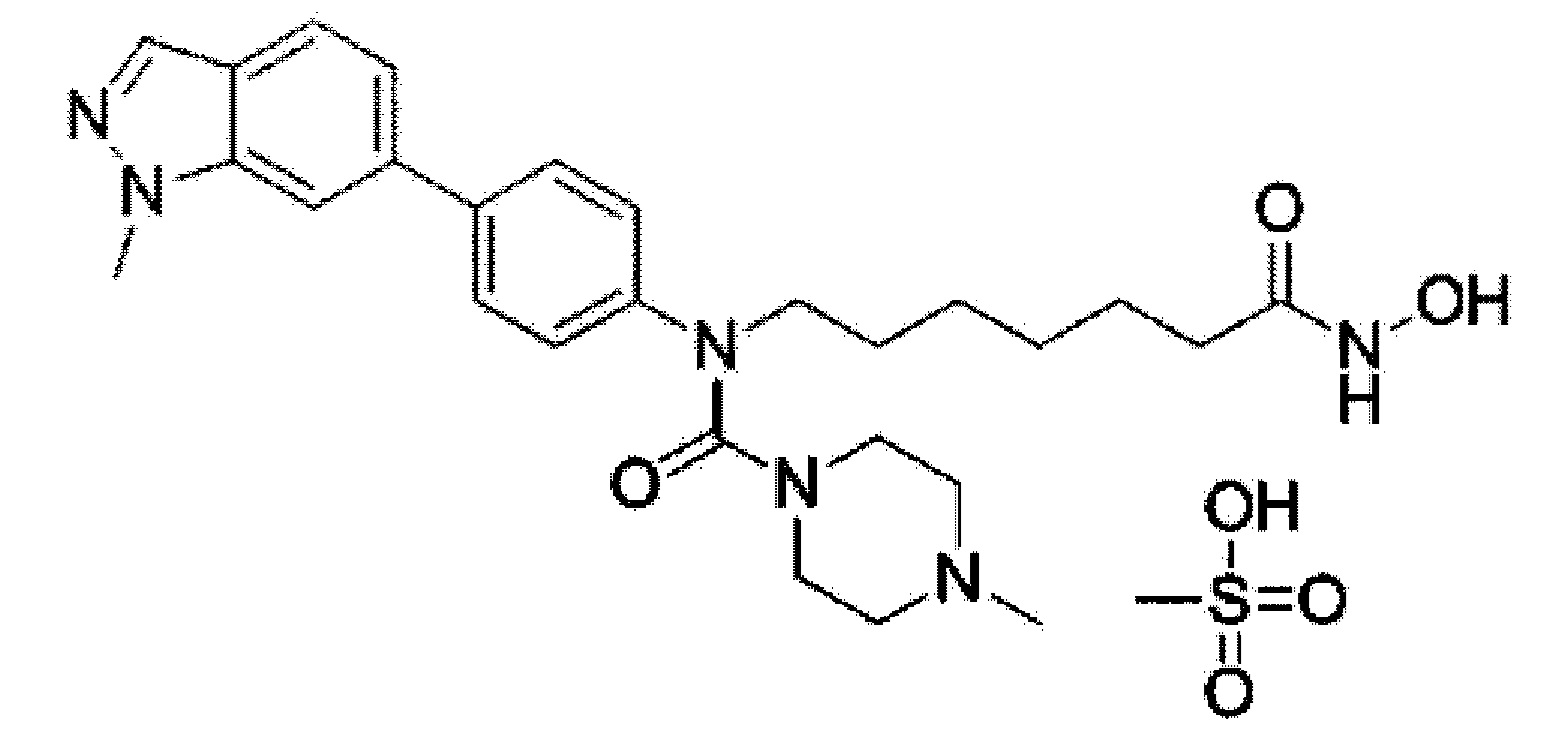
Полезные эффекты
Более высокая эффективность комбинации согласно настоящему изобретению может быть продемонстрирована путем измерения синергического терапевтического действия. Комбинация по настоящему изобретению обладает синергическим противораковым действием тогда, когда первый активный ингредиент, ингибитор HDAC, вводят в сочетании со вторым активным ингредиентом и третьим активным ингредиентом, и, как следствие, она характеризуется превосходной противораковой активностью против рака крови, в особенности множественной миеломы.
Краткое описание чертежей
Фиг. 1а представляет собой график опухолевого роста в контрольной группе и каждой из экспериментальных групп на модельных ксенографтах MM.1s у мышей.
Фиг. 1b представляет собой график изменения размера опухоли у каждой особи в каждой из экспериментальных групп на момент последнего дня исследования (день 57) на модельных ксенографтах MM.1s у мышей.
Фиг. 2а представляет собой график опухолевого роста в контрольной группе и каждой из экспериментальных групп на модельных ксенографтах MM.1s у мышей.
Фиг. 2b представляет собой график изменения размера опухоли у каждой особи в каждой из экспериментальных групп на момент последнего дня исследования (день 70) на модельных ксенографтах MM.1s у мышей.
Наилучший вариант осуществления
Теперь настоящее изобретение будет описано более подробно.
Первый активный ингредиент фармацевтической комбинации, согласно настоящему изобретению, представляет собой соединение с приведенной ранее химической формулой 1, которое обладает активностью в отношении гистондеацетилаз (HDAC). Описание и способ получения соединения с приведенной выше химической формулой 1 подробно изложены в международной патентной публикации № WO 2010-110545, которая включена в данный документ посредством ссылки. В настоящем изобретении соединение с приведенной выше химической формулой 1 может быть получено способом получения, раскрытым в указанном выше документе. В целом известно, что дозировка соединения с приведенной выше химической формулой 1 при введении людям может быть различной в зависимости от различных факторов, включая индивидуальные специфические факторы пациентов, но, например, его можно вводить в дозе 10-210 мг/м2.
В то же время второй активный ингредиент фармацевтической комбинации, согласно настоящему изобретению, представляет собой ингибитор протеасом или иммуномодулирующее лекарственное средство, где под ингибитором протеасом понимают соединение, ингибирующее активность протеасомы (клеточного комплекса, расщепляющего белок), тем самым обращая расщепление белка, регулирующего цикл клеточного деления; данный факт базируется на том, что нормальные клетки восстанавливают способность к делению даже в том случае, если активность протеасом была временно ингибирована, однако различные раковые клетки входят в процесс клеточной гибели, как только активность протеасом была временно ингибирована. Ингибитор протеасом, который может входить в состав фармацевтической комбинации настоящего изобретения, может принадлежать к различным классам известных ингибиторов протеасом. Например, в качестве представителя класса пептидов, содержащих боронатную группу, можно привести бортезомиб (МНН, PS0341; велкейд), который был одобрен в США для лечения рецидивирующей множественной миеломы. Существует также СЕР-18770, другой представитель класса пептидов, содержащих боронатную группу. Среди других классов ингибиторов протеасом выделяют пептиды с альдегидной группой (например, MG132), пептиды с винилсульфонной группой, пептиды с эпоксикетонной группой (например, эпоксимицин, карфилзомиб), ингибиторы р-лактонов (например, лактоцистин, MLN 519, NPI-0052, салиноспорамид А), соединение, которое приводит к образованию дитиокарбаматного комплекса металла (например, дисульфирам, который также используют для лечения хронического алкоголизма), и специфический антиоксидант (например, эпигаллокатехин-3-галлат, катехин-3-галлат и салиноспорамид А). Ингибитор протеасом, входящий в состав фармацевтической комбинации настоящего изобретения, это, предпочтительно, бортезомиб, представленный приведенной далее химической формулой 2, или его фармацевтически приемлемая соль. Бортезомиб можно вводить внутривенно или подкожно в дозе 0,3-1,5 мг/м2 1 или 2 раза в неделю в зависимости от схемы введения, но не ограничиваясь ею.
Химическая формула 2

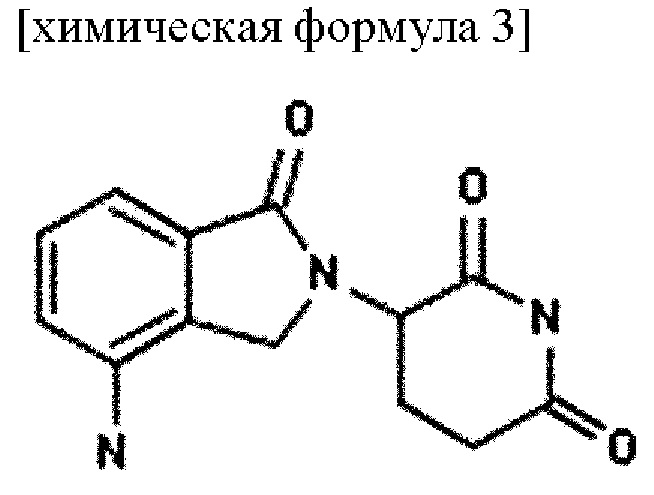
В то же время иммуномодулирующее лекарственное средство обладает такими действиями, как стимуляция экспансии иммунных клеток и гибели опухолевых, и т.д., а именно, регулирует иммунитет за счет улучшения ADCC (антителозависимой клеточноопосредованной цитотоксичности). В частности, иммуномодулирующее лекарственное средство, входящее в состав фармацевтической комбинации настоящего изобретения, может быть представлено талидомидом, леналидомидом, формалидомидом или фармацевтически приемлемой солью; предпочтительно, леналидомидом, представленным приведенной далее химической формулой 3, или его фармацевтически приемлемой солью. Леналидомид, как правило, принимают перорально в дозе от 10 до 30 мг в зависимости от схемы введения, но не ограничиваясь ею.
Химическая формула 3

Третьим активным ингредиентом фармацевтической комбинации, согласно настоящему изобретению, является противораковое стероидное средство, которое, например, может быть представлено без ограничения преднизолоном или дексаметазоном. Предпочтительно, оно представлено дексаметазоном, который представлен приведенной далее химической формулой 4, а именно (8S, 9R, 10S, 11S, 13S, 14S, 16R, 17R)-9-фтор-11,17-дигидрокси-17-(2-гидроксиацетил)-10,13,16-триметил-
6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-3-он или его изотопный вариант; или его фармацевтически приемлемая соль, гидрат или сольват. В одном варианте осуществления дексаметазон - это (8S, 9R, 10S, 11S, 13S, 14S, 16R, 17R)-9-фтор-11,17-дигидрокси-17-(2-гидроксиацетил)-10,13,16-триметил-
6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-3-он. В другом варианте осуществления дексаметазон - это (8S, 9R, 10S, 11S, 13S, 14S, 16R, 17R)-9-фтор-11,17-дигидрокси-17-(2-гидроксиацетил)-10,13,16-триметил-
6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-3-он, где атом водорода дейтерирован.
Химическая формула 4

В настоящем изобретении под фармацевтически приемлемой солью подразумевают соль, обычно используемую в медицинской промышленности; и, например, существуют соли с неорганическими ионами, полученные с использованием кальция, калия, натрия, магния и т.д.; соли неорганических кислот, полученные с использованием соляной кислоты, азотной кислоты, фосфорной кислоты, бромноватой кислоты, йодноватой кислоты, перхлорной кислоты, виноградной кислоты, серной кислоты и т.д.; соли органических кислот, полученные с использованием уксусной кислоты, трифторуксусной кислоты, лимонной кислоты, малеиновой кислоты, янтарной кислоты, щавелевой кислоты, бензойной кислоты, виноградной кислоты, фумаровой кислоты, миндальной кислоты, пропионовой кислоты, лимонной кислоты, молочной кислоты, гликолевой кислоты, глюконовой кислоты, галактуроновой кислоты, глутаминовой кислоты, глутаровой кислоты, глюкуроновой кислоты, аспарагиновой кислоты, аскорбиновой кислоты, угольной кислоты, ванилиновой кислоты, йодистоводородной кислоты и т.д.; соли аминокислот, полученные с использованием метансульфоновой кислоты, этансульфоновой кислоты, бензолсульфоновой кислоты, п-толуолсульфоновой кислоты и нафталинсульфоновой кислоты и т.д.; соли аминов, полученные с использованием триметиламина, триэтиламина, аммиака, пиридина, пиколина и т.д., но виды солей в настоящем изобретении не ограничиваются перечисленными.
В одном варианте осуществления содержание первого активного ингредиента, второго активного ингредиента и третьего активного ингредиента может быть представлено на 100 весовых частей всей фармацевтической комбинации. Если в качестве второго активного ингредиента применяют ингибитор протеасом, такой как бортезомиб, то комбинация включает 28,55-85,60 весовых частей первого активного ингредиента, 1,28-8,63 весовых частей второго активного ингредиента и 2,71-69,55 весовых частей третьего активного ингредиента. Если в качестве второго активного ингредиента применяют иммуномодулирующее лекарственное средство, такое как леналидомид, то комбинация включает 19,54-94,69 весовых частей первого активного ингредиента, 2,46-52,63 весовых частей второго активного ингредиента и 2,52-59,70 весовых частей третьего активного ингредиента.
Фармацевтическая комбинация может включать как 3 вида отдельных составов, так и может состоять из двух или одного состава.
Комбинацию по настоящему изобретению можно вводить перорально или парентерально (например, внутривенно, подкожно, внутрибрюшинно или местно). В настоящем изобретении первый и второй активные ингредиенты можно вводить перорально или парентерально и, предпочтительно, их можно вводить парентерально. Кроме того, третий активный ингредиент можно вводить парентерально или перорально и, предпочтительно, его вводят перорально.
Диапазон подходящих доз первого, второго и третьего активных ингредиентов в комбинации по настоящему изобретению варьирует в зависимости от массы тела, возраста, пола, состояния здоровья пациента, рациона, времени введения, способа введения, скорости выведения и степени тяжести заболевания и т.д. Суточная доза первого активного ингредиента составляет примерно 10-80 мг/кг, предпочтительно 20-60 мг/кг. Кроме того, суточная доза второго активного ингредиента по настоящему изобретению составляет примерно 0,1-5 мг/кг, предпочтительно 0,5-2 мг/кг.
Подходящий период введения первого активного ингредиента, второго активного ингредиента и третьего активного ингредиента в комбинации по настоящему изобретению может быть определен в зависимости от дозы. Например, если второй активный ингредиент по настоящему изобретению представляет собой ингибитор протеасом, то первый активный ингредиент можно вводить с частотой от одного раза в день до одного раза в две недели, предпочтительно один раз в неделю. Кроме того, второй активный ингредиент по настоящему изобретению можно вводить с частотой от одного раза в день до одного раза в неделю, предпочтительно два раза в неделю. Третий активный ингредиент по настоящему изобретению можно вводить с частотой от одного раза в день до одного раза в неделю, предпочтительно 4 раза в неделю. Кроме того, если в качестве второго активного ингредиента по настоящему изобретению выступает иммуномодулирующее лекарственное средство, то первый активный ингредиент по настоящему изобретению можно вводить с частотой от одного раза в день до одного раза каждые две недели, предпочтительно один раз в неделю; а второй активный ингредиент можно вводить с частотой от одного раза в день до одного раза в неделю, предпочтительно один раз в день; а третий активный ингредиент можно вводить с частотой от одного раза в день до одного раза в неделю, предпочтительно один раз в неделю.
Для фармацевтической комбинации согласно настоящему изобретению подтверждено объединенное действие первого активного ингредиента, который представляет собой ингибитор HDAC, второго активного ингредиента, который представляет собой ингибитор протеасом или иммуномодулирующее лекарственное средство, и третьего активного ингредиента, который представляет собой противораковое стероидное средство, выражающееся в превосходной противораковой активности.
Поэтому противораковую комбинацию согласно настоящему изобретению можно с пользой применять в качестве противораковой стратегии лечения, и она может быть особенно предпочтительна для лечения рака крови. Рак крови предпочтительно может быть представлен множественной миеломой.
В настоящем изобретении первый активный ингредиент, второй активный ингредиент и третий активный ингредиент, входящие в состав комбинации настоящего изобретения, могут быть соответственно представлены отдельной фармацевтической композицией; а фармацевтическая композиция может быть приготовлена либо в форме с однократной дозой, либо в виде множества доз, содержащихся в контейнере, путем составления ее с фармацевтически приемлемым носителем согласно способу, который может быть легко выполнен специалистом в данной области техники.
При составлении обычно применяют фармацевтически приемлемый носитель; к нему относятся лактоза, декстроза, сахароза, сорбит, маннит, крахмал, гуммиарабик, фосфат кальция, альгинат, желатин, силикат кальция, микрокристаллическая целлюлоза, поливинилпирролидон, целлюлоза, вода, патока, метилцеллюлоза, метилгидроксибензоат, пропилгидроксибензоат, тальк, стеарат магния и минеральное масло и т.д., но не ограничиваются ими. Фармацевтическая комбинация настоящего изобретения помимо вышеуказанных компонентов может содержать смазывающее средство, смачивающее средство, подсластитель, ароматизатор, эмульгатор, суспендирующее средство, консервант и т.д.. Подходящие фармацевтически приемлемые носители и составы подробно описаны в Remington's Pharmaceutical Sciences (19-е изд., 1995 г.).
В другом варианте осуществления настоящее изобретение относится к способу лечения рака, предусматривающему введение фармацевтической комбинации индивидууму, который нуждается в таком лечении. В настоящем изобретении под индивидуумом понимают млекопитающих, в частности людей.
Вариант осуществления настоящего изобретения
Теперь конфигурация и действие настоящего изобретения будут описаны более подробно с использованием примеров. Эти примеры приведены лишь для иллюстрации, объем настоящего изобретения ими не ограничивается.
Пример 1. Подтверждение противоракового действия комбинации по настоящему изобретению с применением бортезомиба в качестве второго активного ингредиента на модельных ксенографтах MM.1s
1-1) Методика эксперимента
a. Получение модели опухоли у животных
Линию клеток MM.1s множественной миеломы человека приобретали в Американской коллекции типовых культур (США). Линию клеток MM.1s культивировали с использованием среды RPMI1640 (Gibco, США), содержащей 10% эмбриональной телячьей сыворотки (Gibco, Гранд-Айленд, Нью-Йорк, США).
После этого клетки MM.1s смешивали с матригелем и вводили подкожно самцам мышей NOD.CB17-Prkdcscid/NCrHsd (2×107 клеток/животное) для формирования групп, в которых животные были бы равномерно распределены по размеру опухоли, а затем этих животных использовали в эксперименте.
b. Приготовление активных ингредиентов
Соединение с химической формулой 1 готовили в концентрации 4 мг/мл путем растворения в физиологическом растворе.
Бортезомиб готовили в концентрации 0,005 мг/мл путем растворения в физиологическом растворе.
Дексаметазон готовили в концентрации 0,05 мг/мл путем разведения исходного раствора с концентрацией 5 мг/мл в физиологическом растворе.
Используемый раствор готовили непосредственно в день использования, неиспользованный раствор утилизировали.
c. Подтверждение противораковой активности
Противораковое действие соединения с химической формулой 1, а также бортезомиба и дексаметазона оценивали на модельных ксенографтах MM.1s у мышей. Экспериментальных животных распределяли по следующим различным группам введения:
- контрольная группа, получавшая наполнитель;
- группа, получавшая соединение с химической формулой 1 (40 мг/кг, один раз в неделю, путь введения инъекционный);
- группа, получавшая комбинацию бортезомиба (0,05 мг/кг, два раза в неделю, путь введения инъекционный) и дексаметазона (0,5 мг/кг, 4 раза в неделю, путь введения инъекционный);
- группа, получавшая комбинацию соединения с химической формулой 1 (40 мг/кг, один раз в неделю, путь введения инъекционный), бортезомиба (0,05 мг/кг, два раза в неделю, путь введения инъекционный) и дексаметазона (0,5 мг/кг, 4 раза в неделю, путь введения инъекционный).
Животные во всех группах получали внутрибрюшинные введения в течение 57 дней. Проявления токсичности контролировали путем измерения веса мышей, и на протяжении всего эксперимента опухолевый рост измеряли с использованием калипера. Объем опухоли рассчитывали при помощи следующего уравнения 1:
Математическое уравнение 1
Объем опухоли = (длина × ширина2)/2
d. Статистический анализ
Все результаты, полученные для экспериментальных групп, сравнивали, исходя из предположения о нормальности данных, посредством параметрического множественного сравнения или непараметрического множественного сравнения; статистический анализ выполняли с использованием Prism 5.03 (GraphPad Software Inc., Сан-Диего, Калифорния, США); статистически значимыми считали результаты, для которых р-значение составляло менее 0,05.
1-2) Результаты эксперимента
Для оценки противоракового действия при совместном введении соединения с химической формулой 1 и бортезомиба с дексаметазоном ксенографтной мыши вводили каждое из веществ и контролировали вес животного и опухолевый рост на протяжении 57 дней.
В аспекте оценки ингибирующего опухолевый рост действия сравнивали размеры опухолей в группе, получавшей соединение с химической формулой 1, группе, получавшей комбинацию из бортезомиба и дексаметазона, группе, получавшей комбинацию из соединения с химической формулой 1, бортезомиба и дексаметазона, с группой, получавшей вспомогательное вещество, на протяжении всего эксперимента, при этом наблюдали сильное ингибирование опухолевого роста.
В группе, которая получала комбинацию из бортезомиба и дексаметазона, наблюдали незначительное уменьшение размера опухоли, при этом всего одно животное достигло полной ремиссии, а у большей части мышей было показано уменьшение размера опухоли менее чем на 50%. При этом в группе, которая получала комбинацию из соединения с химической формулой 1, бортезомиба и дексаметазона, полную ремиссию наблюдали у 3 мышей, тогда как у большей части мышей было показано уменьшение размера опухоли более чем на 50%. Достижение полной ремиссии рака было неожиданным результатом, а увеличение доли животных с полной ремиссией позволяет говорить о высокой эффективности комбинации данных лекарственных средств.
Полученные результаты дают основания предполагать исключительную эффективность противоракового действия, достигаемого с помощью комбинированной терапии 3-мя средствами, а именно соединением с химической формулой 1, бортезомибом и дексаметазоном.
Пример 2. Подтверждение противоракового действия комбинации по настоящему изобретению с применением леналидомида в качестве второго активного ингредиента на модельных ксенографтах MM.1s
2-1) Методика эксперимента
a. Получение модели опухоли у животных
Линию клеток MM.1s множественной миеломы человека приобретали в Американской коллекции типовых культур (США). Линию клеток MM.1s культивировали с использованием среды RPMI1640 (Gibco, США), содержащей 10% эмбриональной телячьей сыворотки (Gibco, Гранд-Айленд, Нью-Йорк, США).
После этого клетки смешивали с матригелем и вводили подкожно самцам мышей NOD.CB17-Prkdcscid/NCrHsd (2×107 клеток/животное) для формирования групп, в которых животные были бы равномерно распределены по размеру опухоли, а затем этих животных использовали в эксперименте.
b. Приготовление активных ингредиентов
Соединение с химической формулой 1 готовили в концентрации 6 мг/мл путем растворения в физиологическом растворе.
Леналидомид готовили в концентрации 1 мг/мл путем растворения в 1% соляной кислоте (HCl) в фосфатно-солевом буфере (ФСБ), а затем титрования до нейтрального значения рН.
Дексаметазон готовили в концентрации 0,2 мг/мл путем разведения исходного раствора с концентрацией 5 мг/мл в физиологическом растворе.
Используемый раствор готовили непосредственно в день использования, неиспользованный раствор утилизировали.
c. Подтверждение противораковой активности
Противораковое действие соединения с химической формулой 1, а также леналидомида и дексаметазона оценивали на модельных ксенографтах MM.1s у мышей. Экспериментальных животных распределяли по следующим различным группам введения:
- контрольная группа, получавшая наполнитель;
- группа, получавшая соединение с химической формулой 1 (60 мг/кг, один раз в неделю, путь введения инъекционный);
- группа, получавшая комбинацию леналидомида (10 мг/кг, один раз в день, путь введения инъекционный) и дексаметазона (2 мг/кг, один раз в неделю, путь введения инъекционный);
- группа, получавшая комбинацию соединения с химической формулой 1 (60 мг/кг, один раз в неделю, путь введения инъекционный), леналидомида (10 мг/кг, один раз в день, путь введения инъекционный) и дексаметазона (2 мг/кг, один раз в неделю, путь введения инъекционный).
Животные во всех группах получали внутрибрюшинные введения в течение 70 дней. Проявления токсичности контролировали путем измерения веса мышей, и на протяжении всего эксперимента опухолевый рост измеряли с использованием калипера. Объем опухоли рассчитывали при помощи математического уравнения 1, приведенного в примере 1.
d. Статистический анализ
Все результаты настоящего эксперимента, полученные для экспериментальных групп, сравнивали, исходя из предположения о нормальности данных, посредством параметрического множественного сравнения или непараметрического множественного сравнения; статистический анализ выполняли с использованием Prism 5.03 (GraphPad Software Inc., Сан-Диего, Калифорния, США); статистически значимыми считали результаты, для которых р-значение составляло менее 0,05.
2-2) Результаты эксперимента
Для оценки противоракового действия при совместном введении соединения с химической формулой 1 и леналидомида с дексаметазоном ксенографтной мыши вводили каждое вещество и контролировали вес животных и опухолевый рост на протяжении 70 дней.
В аспекте оценки ингибирующего опухолевый рост действия сравнивали размеры опухолей в группе, получавшей соединение с химической формулой 1, группе, получавшей комбинацию из леналидомида и дексаметазона, группе, получавшей комбинацию из соединения с химической формулой 1, леналидомида и дексаметазон, с группой, получавшей вспомогательное вещество, на протяжении всего эксперимента, при этом наблюдали сильное ингибирование опухолевого роста.
В группе, которая получала комбинацию из леналидомида и дексаметазона, наблюдали незначительное увеличение в размере первичной раковой опухоли, тогда как в группе, получавшей комбинацию из соединения с химической формулой 1, леналидомида и дексаметазона, у большей части мышей наблюдали уменьшение размера раковой опухоли вплоть до полной ремиссии.
Полученные результаты дают основания предполагать очень высокую эффективность противоракового действия, достигаемого с помощью комбинированной терапии 3-мя средства, а именно соединением с химической формулой 1, леналидомидом и дексаметазоном.
Реферат
Настоящее изобретение относится к фармацевтической комбинации для лечения рака крови, которая включает в себя ингибитор гистондеацетилазы (HDAC) с химической формулой 1, ингибитор протеасом или иммуномодулирующее лекарственное средство и противораковое стероидное средство. Фармацевтическая комбинация по настоящему изобретению может быть полезна при лечении рака крови, например множественной миеломы, за счет уменьшения токсичности, что является недостатком стандартных ингибиторов HDAC, и эквивалентного уровня фармакологического действия, обеспечиваемого сложным механизмом ингибирования ракового роста, который опосредован соединением с химической формулой 1 и его фармацевтически приемлемой солью, ингибитором протеасом или иммуномодулирующим лекарственным средством и противораковым стероидным средством. 10 з.п. ф-лы, 2 ил., 2 пр.
Формула



Комментарии