Ингибиторы сигма-рецептора - RU2404972C2
Код документа: RU2404972C2
Чертежи


Описание
Область изобретения
Настоящее изобретение относится к соединениям, имеющим фармакологическую активность в отношении сигма-рецептора, и, более конкретно, к некоторым производным пиразола, к способам получения таких соединений, к включающим в себя их фармацевтическим композициям и к их применению в лечении и профилактике, в частности, для лечения психоза.
Предшествующий уровень техники
Поиск новых терапевтических средств в последние годы сильно облегчен лучшим пониманием структуры белков и других биомолекул, ассоциированных с заболеваниями-мишенями. Одним из важнейших классов данных белков является сигма-рецептор, рецептор клеточной поверхности центральной нервной системы (ЦНС), который может быть связан с дисфорическими, галлюциногенными и кардиостимулирующими эффектами опиоидов. Из исследований биологии и функции сигма-рецепторов были представлены доказательства того, что лиганды сигма-рецептора могут использоваться в лечении психоза и нарушений движения, таких как дистония и поздняя дискинезия, и моторные нарушения, ассоциированные с хореей Гентингтона или синдромом Турета, или с болезнью Паркинсона (Walker, J.M. et al., Pharmacological Reviews, 1990, 42, 355). Имелись сообщения, что известный лиганд сигма-рецептора римказол в клинике характеризуется эффектами лечения психоза (Snyder, S.H., Largent, B. L. J. Neuropsychiatry 1989, 1, 7). Участки связывания сигма имеют предпочтительное сродство к правовращающим изомерам некоторых опиатных бензоморфанов, таких как (+)SKF 10047, (+)циклазоцин, и (+)пентазоцин, и также к некоторым нарколептикам, таким как галоперидол. Сигма-рецептор имеет, по меньшей мере, два субтипа, которые могут различаться стереоселективными изомерами данных фармакологически активных лекарственных средств. SKF 10047 имеет наномолярное сродство к участку сигма 1 и имеет микромолярное сродство к участку сигма 2. Галоперидол имеет сходное сродство в отношении обоих субтипов. Эндогенные лиганды сигма неизвестны, хотя предполагается, что одним из них является прогестерон. Возможные опосредованные сигма-участком эффекты лекарственных средств включают в себя модулирование функции глутаматного рецептора, нейротрансмиттерную реакцию, поведение и распознавание (Quirion, R. et al. Trends Pharmacol. Sci., 1992, 13:85-86). В большей части исследований предполагается, что участки связывания сигма (рецепторы) являются элементами каскада передачи сигнала, находящимися в плазмалемме. Лекарственные средства, о которых сообщается, что они являются селективными сигма-лигандами, оценивали в качестве антипсихотиков (Hanner, M. et al. Proc. Natl. Acad. Sci, 1996, 93:8072-8077). Существование сигма-рецепторов в ЦНС, иммунной и эндокринной системах указывает на возможность, что они могут служить в качестве связки между данными тремя системами.
В свете потенциальных терапевтических применений агонистов или антагонистов сигма-рецептора большие усилия направлены на поиск избирательных лигандов. Таким образом, предшествующий уровень техники раскрывает различные лиганды сигма-рецептора.
В заявке на выдачу Международного патента WO 91/09594, в общем, описан большой класс лигандов сигма-рецепторов, некоторые из которых представляют собой соединения 4-фенилпиперидина, тетрагидропиридина или пиперазина, имеющие заместитель кольцевого атома N - необязательно замещенный арил или гетероарил, алкил, алкенил, алкинил, алкокси или алкоксиалкил. Термины арил и гетероарил определяются путем указания числа таких заместителей.
В заявке на выдачу Европейского патента EP 0414289A1, в общем, описан класс производных 1,2,3,4-тетрагидро-спиро[нафталин-1,4'-пиперидина] и 1,4-дигидро-спиро[нафталин-1,4'-пиперидина], замещенных у атома N пиперидина углеводородной группой, с предполагаемой избирательной антагонистической активностью в отношении сигма-рецептора. Термин «углеводород», определенный в указанном патенте, покрывает все возможные неразветвленные, циклические, гетероциклические и другие группы. Однако конкретно описаны только соединения, имеющие бензил, фенэтил, циклоалкилметил, фурил или тиенилметил или низший алкил или алкенил в качестве углеводородных заместителей атома азота пиперидина. Доказано, что данные соединения вытесняют меченный тритием дитолилгуанидин (DTG) с сигма-участков, с константой лучше 200 нМ. 1'-бензил-1,2,3,4-тетрагидро-спиро[нафталин-1,4'-пиперидин] указан как особенно предпочтительное соединение.
В публикации Европейского патента EP 0445974A2, в общем, описаны соответствующие производные спиро[индан-1,4'-пиперидина] и спиро[бензоциклогептен-5,4'-пиперидина]. Опять доказано, что данные соединения лишь вытесняют меченный тритием дитолилгуанидин (DTG) из сигма-участков с константой больше 200 нМ.
Заявка на выдачу Европейского патента EP 0431943A2 относится к дальнейшему исключительно широкому классу соединений спиропиперидина, замещенных у атома N и заявленных как применимые в качестве противоаритмических средств и при ослабленной насосной функции сердца. В указанной заявке приводится пример нескольких соединений, большинство из которых содержат оксо- и/или сульфониламино-заместитель в спироциклической кольцевой системе. В остальных соединениях главный компонент имеет другой полярный заместитель, присоединенный к спиро-ядру, и/или они имеют некоторые полярные заместители в заместителе на атоме N пиперидина. Не дано каких-либо предположений или указаний на эффект данных соединений в отношении сигма-рецептора.
До сих пор сохраняется потребность в поиске соединений, которые имеют фармакологическую активность в отношении сигма-рецептора, эффективны и избирательны, имеют хорошие свойства «применимости в качестве лекарственных средств», т.е. хорошие фармацевтические свойства, связанные с введением, распределением, метаболизмом и экскрецией.
Сущность изобретения
В настоящее время авторами изобретения обнаружено семейство производных пиразола, которые являются особенно избирательными ингибиторами сигма-рецептора. Данные соединения содержат пиразольную группу, конденсированную с циклоалкильным кольцом, имеющим 5, 6 или 7 атомов углерода.
В одном из аспектов изобретение относится к соединению формулы I:

в котором
R1 выбран из группы, образованной водородом, замещенным или незамещенным алкилом, замещенным или незамещенным циклоалкилом, замещенным или незамещенным гетероциклилом, замещенным или незамещенным арилом, замещенным или незамещенным арилалкилом, и замещенным или незамещенным гетероциклилалкилом;
R2 выбран из группы, образованной водородом, замещенным или незамещенным алкилом, замещенным или незамещенным циклоалкилом, замещенным или незамещенным алкокси, замещенным или незамещенным арилом, замещенным или незамещенным гетероциклилом, замещенным или незамещенным арилалкилом, и замещенным или незамещенным гетероциклилалкилом;
R3 и R4 независимо выбраны из группы, образованной водородом, замещенным или незамещенным алкилом, замещенным или незамещенным циклоалкилом, замещенным или незамещенным гетероциклом, замещенным или незамещенным арилом, замещенным или незамещенным арилалкилом, и замещенным или незамещенным гетероциклилалкилом; или R3 и R4 вместе образуют 3-6-членное замещенное или незамещенное кольцо;
R5 и R6 независимо выбраны из группы, образованной водородом, замещенным или незамещенным алкилом, замещенным или незамещенным циклоалкилом, замещенным или незамещенным гетероциклом, замещенным или незамещенным арилом, замещенным или незамещенным арилалкилом, и замещенным или незамещенным гетероциклилалкилом; или R5 и R6 вместе образуют замещенную или незамещенную гетероциклическую группу, имеющую от 3 до 7 атомов в кольце;
n выбран из 0, 1 и 2;
m выбран из 0, 1, 2, 3 и 4;
пунктирная линия ---- представляет собой простую или двойную связь;
при условии, что когда R1 является фенилом, R2 является H, пунктирная линия ---- представляет собой двойную связь, m равен 1, а R5 и R6образуют 2,5-диоксопирролидин или 5-этокси-2-оксопирролидин; тогда R3 и R4 не могут одновременно быть H или метилом;
или к его фармацевтически приемлемой соли, изомеру, пролекарству или сольвату.
В одном из вариантов осуществления R2 предпочтительно представляет собой водород или алкил; более предпочтительно водород. Также предпочтительно, чтобы m представлял собой 1 или 2 и также чтобы n представлял собой 0 или 1. Более того, также предпочтительно, чтобы R3 и R4 оба представляли собой водород или алкил; более предпочтительно оба они представляли собой водород или метил; и наиболее предпочтительно оба они представляли собой водород. Далее, также предпочтительно, чтобы R1 был выбран из группы, образованной замещенным или незамещенным алкилом, замещенным или незамещенным циклоалкилом, замещенным или незамещенным гетероциклилом или замещенным или незамещенным арилом; более предпочтительно замещенным или незамещенным алкилом, незамещенным циклоалкилом, незамещенным арилом, и ароматическим гетероциклилом; и наиболее предпочтительно метилом, трет-бутилом, циклогексилом и фенилом. Более того, также предпочтительно, чтобы R5 и R6 вместе образовывали замещенный или незамещенный гетероциклил, имеющий от 3 до 7 атомов в кольце, в частности морфолин-4-ил, 2,6-диметилморфолин-4-ил, пиперидин-1-или, 4-фенилпиперидин-1-ил, 3-фенилпиперидин-1-ил, 4-бензилпиперазин-1-ил, 4-фенилпиперазин-1-ил, 2-[спиро[изобензофуран-1(3H), 4'-пиперидин]-1'-ил, азепан-1-ил, 1,2,3,4-тетрагидроизохинолин-2-ил, пирролидин-1-ил, 3-фенилпирролидин-1-ил, изоиндолин-2-ил или имидазол-1-ил; особенно, когда R2 представляет собой водород, m равен 1 и n равен 1; более особенно, когда R3 и R4 оба представляют собой водород; и даже более особенно, когда R1 является замещенным или незамещенным фенилом. Хорошие результаты получают, когда R5 представляет собой бензил и R6 представляет собой метил.
Приведенные выше варианты осуществления и предпочтения для R1-R6, n, m и пунктирной линии могут комбинироваться с получением дальнейших предпочтительных соединений.
В другом аспекте изобретение относится к способу получения соединения формулы (I), или его соли, изомера или сольвата.
В другом аспекте изобретение относится к фармацевтической композиции, содержащей соединение, определенное выше, или его фармацевтически приемлемую соль, энантиомер, пролекарство или сольват, и фармацевтически приемлемый носитель, адъювант или средство переноса.
В другом предпочтительном варианте осуществления изобретение относится к применению соединения, определенного выше, в производстве лекарственного средства для лечения диареи, нарушения баланса липопротеинов, гиперлипедемии, гипертриглицеридемии, гиперхолестеринемии, мигрени, избыточного веса, артрита, гипертензии, аритмии, глаукомы, язвенной болезни, дефицитов обучения, памяти и внимания, когнитивных расстройств, нейродегенеративных заболеваний, демиелинизирующих заболеваний, пристрастия к наркотикам и химическим веществам, включая кокаин, амфетамин, этанол и никотин; поздней дискинезии, ишемического инсульта, эпилепсии, инсульта, стресса, рака или психотических заболеваний, в частности депрессии, тревожности или шизофрении; воспалительных, аутоиммунных заболеваний; или для применения в качестве фармакологического инструмента, в качестве анксиолитика или иммунодепрессанта.
Краткое описание чертежей
На фиг.1 показан протокол для всех тестов, проведенных с филаментами фон Фрея.
На фиг.2 показан протокол для всех тестов, в которых показано, что имеется отличие в применении каррагинана вместо капсаицина и измерений Харгрива вместо филаментов фон Фрея.
Подробное описание изобретения
Типичные соединения по изобретению эффективно и избирательно ингибируют сигма-рецептор.
В приведенном выше определении соединений формулы (I) следующие термины имеют указанное значение.
«Алкил» относится к радикалу с неразветвленной или разветвленной углеводородной цепью, состоящему из атомов углерода и водорода, не содержащего ненасыщенности, имеющему от 1 до 8 углеродных атомов, и он присоединен к остальной части молекулы простой связью, например, метил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, и т.д. Алкильные радикалы могут необязательно замещаться одним или несколькими заместителями, такими как арил, галоген, гидрокси, алкокси, карбокси, циано, карбонил, ацил, алкоксикарбонил, амино, нитро, меркапто, алкилтио, и т.д. При замещении арилом имеет место радикал «аралкил», такой как бензил и фенэтил.
«Алкенил» относится к алкильному радикалу, имеющему, по меньшей мере, 2 атома углерода и имеющему один или несколько ненасыщенных связей. «Циклоалкил» относится к стабильному 3-10-членному моноциклическому или бициклическому радикалу, насыщенному или частично насыщенному, и он состоит исключительно из атомов углерода и водорода, например циклогексила или адамантила. Кроме обозначенных иначе случаев в спецификации, термин «циклоалкил» означает включение циклоалкильных радикалов, которые необязательно замещены одним или несколькими заместителями, такими как алкил, галоген, гидрокси, амино, циано, нитро, алкокси, карбокси, алкоксикарбонил, и т.д.
«Арил» относится к радикалам с одним или несколькими кольцами, включая радикалы с несколькими кольцами, которые содержат отдельные и/или конденсированные арильные группы. Типичные арильные группы содержат от 1 до 3 отдельных или конденсированных колец и от 6 до 18 кольцевых углеродных атомов, например радикалы фенил, нафтил, инденил, фенантрил или антрил. Арильный радикал может необязательно замещаться одним или несколькими заместителями, такими как гидрокси, меркапто, галоген, алкил, фенил, алкокси, галогеналкил, нитро, циано, диалкиламино, аминоалкил, ацил, алкоксикарбонил, и т.д.
«Гетероциклил» относится к стабильному 3-15-членному кольцевому радикалу, но не ароматическому, который состоит из углеродных атомов и от одного до пяти гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы, предпочтительно к 4-8-членному кольцу из одного или нескольких гетероатомов, более предпочтительно к 5- или 6-членному кольцу с одним или несколькими гетероатомами. Для целей изобретения гетероцикл может быть моноциклической, бициклической или трициклической кольцевой системой, которая может включать конденсированные кольцевые системы; и атомы азотa, углерода или серы в гетероциклическом радикале могут быть необязательно окислены; атом азота может необязательно быть четвертичным; и гетероциклический радикал может быть частично или полностью насыщенным или ароматическим. Неограничивающие примеры таких гетероциклов включают в себя азепины, бензимидазол, бензотиазол, фуран, изотиазол, имидазол, индол, пиперидин, пиперазин, пурин, хинолин, тридиазол, тетрагидрофуран, кумарин, морфолин; пиррозол, пиразол, оксазол, изоксазол, триазол, имидазол, и т.д. Кроме обозначенных иначе случаев в данной спецификации термин «гетероциклил», как подразумевается, включает гетероциклильные радикалы, необязательно замещенные одним или несколькими заместителями, такими как гидрокси, меркапто, галоген, алкил, фенил, алкокси, галогеналкил, нитро, циано, диалкиламино, аминоалкил, ацил, алкоксикарбонил, сульфонил, сульфониламино, алкил или арилсульфониламино, алкиларилсульфониламино, ациламино, ацетамидо, и т.д.
«Алкокси» относится к радикалу формулы -ORa, в котором Ra представляет алкильный радикал, определенный выше, например метокси, этокси, пропокси, и т.д.
«Алкоксикарбонил» относится к радикалу формулы -C(O)ORa, где Ra представляет собой алкильный радикал, определенный выше, например метоксикарбонил, этоксикарбонил, пропоксикарбонил, и т.д.
«Алкилтио» относится к радикалу формулы -SRa, где Ra представляет собой алкильный радикал, определенный выше, например метилтио, этилтио, пропилтио, и т.д.
«Амино» относится к радикалу формулы -NH2, -NHRa или -NRaRb, необязательно в виде четвертичного основания, в котором Ra и Rb независимо представляют собой алкильный радикал, определенный выше, например метиламино, этиламино, диметиламино, диэтиламино, пропиламино, и т.д.
«Галоген» или «гало» относится к брому, хлору, йоду, или фтору.
Приведенные здесь ссылки на замещенные группы соединений по настоящему изобретению относятся к конкретной группе, которая может замещаться в одном или нескольких доступных положениях одной или несколькими подходящими группами, например галогеном, таким как фтор, хлор, бром и йод; цианогруппой; гидроксилом; нитрогруппой; азидом; алканоилом, таким как C1-6-алканоильная группа, например ацил и тому подобное; карбоксамидом; алкильными группами, включающими такие группы, имеющие от примерно 1 до 12 углеродных атомов или примерно от 1 до 6 углеродных атомов и, более предпочтительно, 1-3 углеродных атома; алкенильными и алкинильными группами, включающими в себя группы, имеющие одну или несколько ненасыщенных связей, и примерно от 2 до 12 углеродных атомов или примерно от 2 до 6 углеродных атомов; алкоксигруппами, имеющими одну или несколько связей с кислородом и от 1 примерно до 12 углеродных атомов или от 1 примерно до 6 углеродных атомов; арилоксигруппой, например фенокси; алкилтиогруппами, включающими радикалы, имеющие одну или несколько тиоэфирных связей и от 1 примерно до 12 углеродных атомов или от 1 примерно до 6 углеродных атомов; алкилсульфинильными группами, включающими радикалы, имеющие одну или несколько сульфинильных связей и от 1 примерно до 12 углеродных атомов или от 1 примерно до 6 углеродных атомов; алкилсульфонильными группами, включающими радикалы, имеющие одну или несколько сульфонильных связей и от 1 примерно до 12 углеродных атомов или от 1 примерно до 6 углеродных атомов; аминоалкильными группами, такими как группы, имеющие один или несколько атомов N и от 1 примерно до 12 углеродных атомов или от 1 примерно до 6 углеродных атомов; карбоциклическим арилом, имеющим 6 или более углеродов, в особенности, фенилом или нафтилом, и аралкилом, таким как бензил. Кроме указанных иначе случаев, необязательно замещенная группа может иметь заместитель в каждом замещаемом положении группы, и каждая замена независима одна от другой.
Настоящее изобретение не относится к промежуточным продуктам синтеза, раскрытым в EP 276834A, соответствующим соединением общей формулы I, в которой R1 представляет собой метил, R3=R4=R2=H, R5=R6=метил, n=2, m=0, и пунктирная линия представляет собой двойную связь. Настоящее изобретение не относится к промежуточным продуктам синтеза, раскрытым Indian Journal of Chemistry, Section B, 1980, 19b, 243-45, соответствующим некоторым соединениям общей формулы I, в которой R5 и R6 вместе образуют группу 5-этокси-2-оксопирролидина или 5,2-диоксопирролидина.
Конкретные отдельные соединения по изобретению, соответствующие формуле (I), представляют собой перечисленные ниже соединения:
1. 4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазол,
2. 4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазола оксалат,
3. 1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазол,
4. 1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазола оксалат,
5. (E)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1H-индазол,
6. 1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1H-индазол,
7. 1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1H-индазола оксалат,
8. 4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазол,
9. 4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазола оксалат,
10. 4-(2-(4-бензилпиперазин-1-ил)этил)-4,5,6,7-тетрагидро-1-фенил-1H-индазол,
11. 4,5,6,7-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3H),4'-пиперидин]-1'-ил]этил)-1H-индазол,
12. 4,5,6,7-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3H),4'-пиперидин]-1'-ил]этил)-1H-индазола оксалат,
13. 4,5,6,7-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этил)-1H-индазол,
14. 4,5,6,7-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этил)-1H-индазола оксалат,
15. (E)-4-(2-(азепан-1-ил)этилиден)-4,5,6,7-тетрагидро-1-фенил-1H-индазол,
16. (E)-4-(2-(азепан-1-ил)этилиден)-4,5,6,7-тетрагидро-1-фенил-1H-индазола оксалат,
17. (E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперидин-1-ил)этилиден)-1H-индазол,
18. (E)-4,5,6,7-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3H),4'-пиперидин]-1'-ил]этилиден)-1H-индазол,
19. (E)-4,5,6,7-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3H),4'-пиперидин]-1'-ил]этилиден)-1H-индазола оксалат,
20. (E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперазин-1-ил)этилиден)-1H-индазол,
21. 1,2,3,4-тетрагидро-2-((E)-2-(6,7-дигидро-1-фенил-1H-индазол-4(5H)илиден)этил)изохинолин,
22. 1,2,3,4-тетрагидро-2-((E)-2-(6,7-дигидро-1-фенил-1H-индазол-4(5H)илиден)этил)изохинолина оксалат,
23. (E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(3-фенилпиперидин-1-ил)этилиден)-1H-индазол,
24. (E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(3-фенилпирролидин-1-ил)этилиден)-1H-индазол
25. (E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(3-фенилпирролидин-1-ил)этилиден)-1H-индазола оксалат,
26. (E)-4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этилиден)-1-фенил-1H-индазол,
27. (E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этилиден)-1H-индазол,
28. 1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперазин-1-ил)этил)-1H-индазол,
29. 1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперазин-1-ил)этил)-1H-индазола оксалат,
30. 1,4,5,6-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенилциклопента[c]пиразол,
31. 1,4,5,6-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенилциклопента[c]пиразола оксалат,
32. 4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперазин-1-ил)этил)-1H-индазол,
33. 4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперазин-1-ил)этил)-1H-индазола оксалат,
34. 2-(2-(1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол-4-ил)этил)изоиндолин,
35. 2-(2-(1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол-4-ил)этил)изоиндолина оксалат,
36. 1,4,5,6-тетрагидро-1-фенил-4-(2-(4-фенилпиперидин-1-ил)этил)циклопента[c]пиразол,
37. 1,4,5,6-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этил)циклопента[c]пиразол,
38. 1,4,5,6-тетрагидро-1-фенил-4-(2-(4-фенилпиперазин-1-ил)этил)циклопента[c]пиразол,
39. 1,4,5,6-тетрагидро-1-фенил-4-(2-(пирролидин-1-ил)этил)циклопента[c]пиразол,
40. 1,4,5,6-тетрагидро-1-фенил-4-(2-(пирролидин-1-ил)этил)циклопента[c]пиразола оксалат,
41. 4-(2-(4-бензилпиперазин-1-ил)этил)-1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол,
42. 4-(2-(4-бензилпиперазин-1-ил)этил)-1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразола диоксалат,
43. 1,2,3,4-тетрагидро-2-(2-(1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол-4-ил)этил)изохинолин,
44. 1,2,3,4-тетрагидро-2-(2-(1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол-4-ил)этил)изохинолина оксалат,
45. 4-(2-(1H-имидазол-1-ил)этил)-1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол,
46. цис-1,4,5,6-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1-фенилциклопента[c]пиразол,
47. цис-1,4,5,6-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1-фенилциклопента[c]пиразола оксалат,
48. цис-4,5,6,7-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1-фенил-1H-индазол,
49. цис-4,5,6,7-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1-фенил-1H-индазола оксалат,
50. 1,4,5,6-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3H),4'-пиперидин]-1'-ил]этил)циклопента[c]пиразол,
51. 1,4,5,6-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3H),4'-пиперидин]-1'-ил]этил)циклопента[c]пиразола оксалат,
52. N-бензил-2-(1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол-4-ил)-N-метил-этанамин,
53. Смесь диастереомеров 1,4,5,6-тетрагидро-1-фенил-4-(2-(3-фенилпиперидин-1-ил)этил)циклопента[c]пиразола,
54. N-бензил-2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)-N-метилэтанамин,
55. 4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1-фенил-1H-индазол,
56. 4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1-фенил-1H-индазола оксалат,
57. 4,5,6,7-тетрагидро-1-метил-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазол,
58. 4,5,6,7-тетрагидро-1-метил-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазола оксалат,
59. 4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1-метил-1H-индазол,
60. 4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1-метил-1H-индазола оксалат,
61. N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1H-индазол-4-ил)-N-метилэтанамин,
62. N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1H-индазол-4-ил)-N-метилэтанамина оксалат,
63. 4,5,6,7-тетрагидро-1-метил-4-(2-(морфолин-4-ил)этил)-1H-индазол,
64. 4,5,6,7-тетрагидро-1-метил-4-(2-(морфолин-4-ил)этил)-1H-индазола оксалат,
65. 1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1H-индазол,
66. 1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1H-индазола оксалат,
67. цис-1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1H-индазол,
68. цис-1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1H-индазола оксалат,
69. N-бензил-2-(1-(4-фторфенил)-4,5,6,7-тетрагидро-1H-индазол-4-ил)-N-метил-этанамин,
70. 1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1H-индазол,
71. 1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1H-индазола оксалат,
72. 1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазол,
73. (+)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазол,
74. (+)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазола оксалат,
75. (-)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазол,
76. (-)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазола оксалат,
77. (E)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1H-индазола оксалат
78. (E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этилиден)-1H-индазола оксалат,
79. (E)-N-бензил-2-(6,7-дигидро-1-фенил-1H-индазол-4(5H)-илиден)-N-метил-этанамин,
80. (E)-N-бензил-2-(6,7-дигидро-1-фенил-1H-индазол-4(5H)-илиден)-N-метил-этанамина оксалат,
81. (E)-4,5,6,7-тетрагидро-4-(2-(цис-2,6-диметилморфолин-4-ил)этилиден)-1-фенил-1H-индазол,
82. (E)-4,5,6,7-тетрагидро-4-(2-(цис-2,6-диметилморфолин-4-ил)этилиден)-1-фенил-1H-индазола оксалат,
83. (E)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(цис-2,6-диметилморфолино-4-ил)этилиден)-1H-индазол,
84. (E)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(цис-2,6-диметилморфолино-4-ил)этилиден)-1H-индазола оксалат,
85. (E)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(морфолино-4-ил)этилиден)-1H-индазол,
86. (E)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(морфолино-4-ил)этилиден)-1H-индазола оксалат,
87. (E)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(пиперидин-1-ил)этилиден)-1H-индазол,
88. (E)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(пиперидин-1-ил)этилиден)-1H-индазола оксалат,
89. (E)-4-(2-(N,N-диэтиламино)этилиден)-4,5,6,7-тетрагидро-1-фенил-1H-индазол,
90. (E)-4-(2-(N,N-диэтиламино)этилиден)-4,5,6,7-тетрагидро-1-фенил-1H-индазола оксалат,
91. (E)-4-(2-(4-циклогексилпиперазин-1-ил)этилиден)-4,5,6,7-тетрагидро-1-фенил-1H-индазол,
92. (E)-4,5,6,7-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этилиден)-1-фенил-1H-индазол,
93. 4,5,6,7-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенил-1H-индазол,
94. 4,5,6,7-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенил-1H-индазола оксалат,
95. 1,4,5,6-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этил)циклопента[c]пиразола оксалат,
96. 1,4,5,6-тетрагидро-1-фенил-4-[2-(тиоморфолин-4-ил)этил]циклопента[c]пиразол,
97. 1,4,5,6-тетрагидро-1-фенил-4-[2-(тиоморфолин-4-ил)этил]циклопента[c]пиразола оксалат,
98. 1,4,5,6-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенилциклопента[c]пиразол,
99. 1,4,5,6-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенилциклопента[c]пиразола оксалат,
100. 1,4,5,6-тетрагидро-4-(2-(4-метилпиперазин-1-ил)этил)-1-фенилциклопента[c]пиразол,
101. 4-(2-(4-циклогексилпиперазин-1-ил)этил)-1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол,
102. 4-(2-азепан-1-ил)этил)-4,5,6,7-тетрагидро-1-фенил-1Н-индазол,
103. N-бензил-2-(1-трет-бутил-4,5,6,7-тетрагидро-1Н-индазол-4-ил)-N-метилэтанамин,
104. 1-трет-бутил-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил-1Н-индазол,
105. 1-трет-бутил-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил-1Н-индазола оксалат,
106. (-)-N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1Н-индазол-4-ил)-N-метилэтанамин,
107. (+)-N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1Н-индазол-4-ил)-N-метилэтанамин,
108. N-(2-(4,5,6,7-тетрагидро-1-метил-1Н-индазол-4-ил)этил)-N-метилциклогексанамин,
109. 4,5,6,7-тетрагидро-4-(2-(4-гидрокси-4-фенилпиперидин-1-ил)этил)-1-метил-1Н-индазол,
110. 4,5,6,7-тетрагидро-1-метил-4-(2-(4-фенилпиперидин-1-ил)этил)-1Н-индазол,
111. N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1Н-индазол-4-ил)-N-метилэтанамин,
112. 4,5,6,7-тетрагидро-1-метил-4-(2-[спиро[изобензофуран-1(3Н),4'-пиперидин]-1'-ил]этил)-1Н-индазол.
Хотя здесь перечислены оксалаты, другие фармацевтически приемлемые соли также образуют часть данной группы предпочтительных соединений.
Кроме указанных иначе случаев, соединения по изобретению также, как подразумевается, включают соединения, которые отличаются только присутствием одного или несколько изотопно обогащенных атомов. Например, соединения, имеющие настоящие структуры, кроме замены водорода дейтерием или тритием, или замены углерода13C- или14C-обогащенным углеродом или15N-обогащенным азотом, входят в объем изобретения.
Термин «фармацевтически приемлемые соли, сольваты, пролекарства» относится к любой фармацевтически приемлемой соли, сложному эфиру, сольвату или любому другому соединению, которое после введения реципиенту способно предоставлять (непосредственно или опосредованно) описанное здесь соединение. Однако следует понимать, что фармацевтически не приемлемые соли также входят в объем изобретения, поскольку последние могут использоваться при получении фармацевтически приемлемых солей. Получение солей, пролекарств и производных может проводиться способами, известными в данной области.
Например, фармацевтически приемлемые соли предоставленных здесь соединений синтезируют из исходного соединения, которое содержит основной или кислый радикал общепринятыми химическими методами. В общем, данные соли, например, получают взаимодействием свободных кислот или оснований данных соединений со стехиометрическим количеством подходящего основания или кислоты в воде или в органическом растворителе или в их смеси. В общем, предпочтительны неводные среды, такие как эфир, этилацетат, этанол, изопропанол, ацетон или ацетонитрил. Примеры кислотно-аддитивных солей включают аддитивные соли минеральных кислот, такие как, например, гидрохлорид, гидробромид, гидройодид, сульфат, нитрат, фосфат, и аддитивные соли органических кислоты, такие как, например, ацетат, малеат, фумарат, цитрат, оксалат, сукцинат, тартрат, малат, манделат, метансульфонат и п-толуолсульфонат. Примеры щелочно-аддитивных солей включают в себя неорганические соли, такие как, например, соли натрия, калия, кальция, аммония, магния, алюминия и лития, и соли органических оснований, такие как, например, этилендиамин, этаноламин, N,N-диалкиленэтаноламин, триэтаноламин, глюкамин и соли основных аминокислот.
Особенно предпочтительные производные и пролекарство представляют собой те, которые повышают биологическую доступность соединений по изобретению при введении таких соединений пациенту (например, предоставляя перорально вводимому соединению легче всасываться в кровь) или которые усиливают доставку исходного соединения в биологический компартмент (например, головной мозг или лимфатическую систему) относительно исходного варианта.
Любое соединение, которое представляет собой пролекарство соединения формулы (I), входит в объем изобретения. Термин «пролекарство» применяется в его широчайшем смысле и охватывает те производные, которые преобразуются in vivo в соединения по изобретению. Такие производные хорошо известны специалистам в данной области и включают в себя в зависимости от функциональных групп, присутствующих в молекуле, и без ограничения следующие производные настоящих соединений: сложные эфиры, сложные эфиры аминокислот, сложные эфиры фосфатов, сложные эфиры сульфоната и солей металлов, карбаматы и амиды. Примеры хорошо известных способов получения пролекарства данного действующего соединения хорошо известны специалистам в данной области и могут быть найдены, например, в Krogsgaard-Larsen et al. "Textbook of Drug design and Discovery" Taylor & Francis (april 2002).
Соединения по изобретению могут быть в кристаллической форме, в виде свободных соединений или сольватов и подразумевается, что все эти формы входят в объем настоящего изобретения. Способы сольватации, в общем, известны в данной области. Подходящие сольваты представляют собой фармацевтически приемлемые сольваты. В конкретном варианте осуществления сольват представляет собой гидрат.
Соединения формулы (I) или их соли или сольваты предпочтительно находятся в фармацевтически приемлемой и, по существу, чистой форме. Под фармацевтически приемлемой формой подразумевается, среди прочего, наличие фармацевтически приемлемого уровня чистоты, без учета обычных фармацевтических добавок, таких как разбавители и носители, который исключает присутствие материалов, считающихся токсичными в нормальной дозировке. Уровни чистоты для лекарственного вещества предпочтительно составляют выше 50%, более предпочтительно выше 70%, наиболее предпочтительно выше 90%. В предпочтительном варианте осуществления чистота составляет выше 95% соединения формулы (I) или его солей, сольватов или пролекарств.
Соединения по настоящему изобретению, представленные описанной выше формулой (I), могут включать в себя энантиомеры в зависимости от присутствия хиральных центров или изомеры в зависимости от присутствия множественных связей (например, Z, E). Единичные изомеры, энантиомеры или диастереоизомеры и их смеси входят в объем настоящего изобретения.
Соединения формулы (I), определенные выше, могут быть получены доступными синтетическими процедурами. Например, соединение формулы (I) может быть получено присоединением соединения формулы (II):

в котором R1-R4, m и n соответствуют определенным выше в формуле (I), и X является уходящей группой, предпочтительно хлором или пиридинием, с соединением формулы (III):
HNR5R6(III),
в котором R5 и R6 соответствуют определенным выше в формуле (I). Взаимодействие соединений формул (II) и (III) предпочтительно проводится в апротонном растворителе, неограничивающим примером которого является диметилформамид (DMF), в присутствии неорганического основания, такого как K2CO3. Соединения формулы (III) коммерчески доступны или могут быть получены общепринятыми способами.
Следующие схемы от I до VI иллюстрируют некоторые способы получения соединений формулы (I):
Способ A
Соединения формулы (I), в частности соединения формулы (Ia), могут быть получены согласно синтетическому процессу описанному по схеме I:
Схема I



По способу A соединения формулы (VII) получают способами, известными из литературы. См., например, Schenone, P., Mosti, L. Menozzi, G., J. Heterocyclic Chem., 1982, 19, 1355-1361; Peet, N.P., Letourneau, E., Heterocycles, 1991, 32, 41-72; Mosti, L., et al. Il Farmaco, 1988, 43, 763-774; Trehan, I.R. et al. IndianJournal of Chemistry, Section B, 1980, 19b, 243-45.
По способу A соединения формулы (VIII) получают из предшественников формулы (VII) путем каталитического гидрирования в присутствии катализаторов, таких как Pd-C или PtO2, в растворителе, таком как метанол, этанол, N,N-диметилформамид или уксусная кислота. Сходным образом, соединения формулы (VIII), в которых n=0 и R1=H, могут быть получены способом, описанным в JP 5765369 A2.
По способу A соединения формулы (IX) получают из промежуточных соединений формулы (VIII) восстановлением сложноэфирной группы гидридом алюминия-лития или гидридом диизобутилалюминия в инертном растворителе, таком как этиловый эфир, тетрагидрофуран или толуол, при подходящей температуре, которая может составлять от -78°C до температуры флегмы растворителя.
Наконец, по способу A соединения формулы (IIa) получают из соединений формулы (IX) путем трансформации гидроксильной группы в уходящую группу, такой как хлорид, путем взаимодействия с тионилхлоридом в инертном растворителе, таком как толуол, при подходящей температуре, которая может составлять от комнатной температуры до температуры флегмы растворителя.
Способ B
Соединения формулы (I), в частности соединения формулы (Ib), могут быть получены согласно способу синтеза, описанному в схеме II:
Схема II
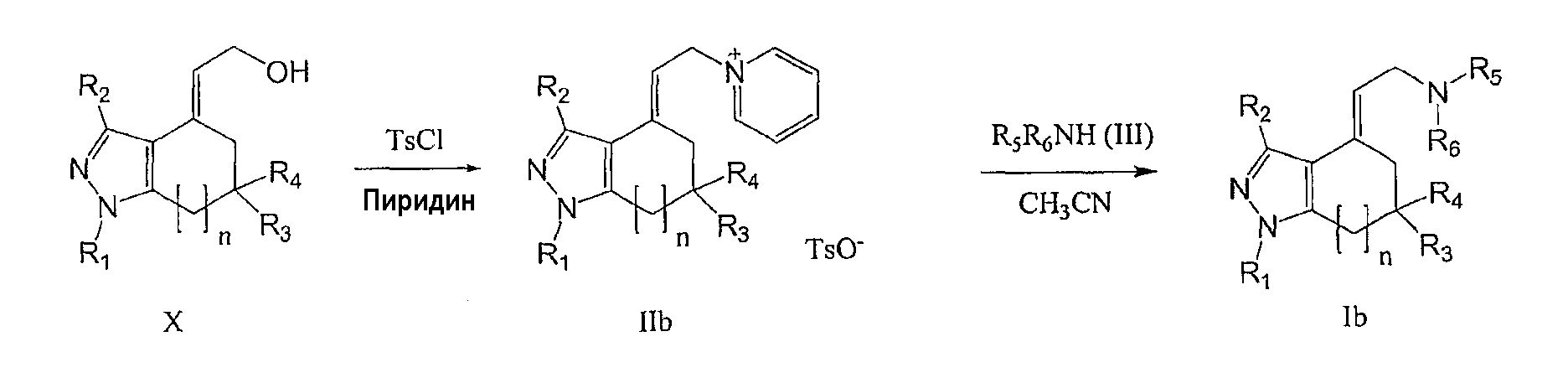
По способу B соединения формулы (X) получают в соответствии со способами, известными из литературы. См., например, Trehan, LR. et al. Indian Journal of Chemistry, Section B, 1980, 19b, 243-45.
По способу B соединения формулы (IIb) получают взаимодействием соединений формулы (X) с хлоридом тозила в пиридине при температуре от 0°C до комнатной температуры.
По способу B соединения формулы Ib получают взаимодействием соединений формулы IIb с аминами формулы R5R6NH (III) в ацетонитриле.
Способ C
Соединения формулы (I), в частности соединения формулы (Ib), могут быть получены синтетическим способом, описываемым схемой III:
Схема III


По способу C соединения формулы (XI) получают хорошо известными способами исходя из соединений формулы (VI). См., например, Mosti, L. et al., Il Farmaco, 1988, 43, 763-774.
По способу C соединения формулы (XII) получают из соединений формулы (XI) путем восстановления цианогруппы гидридом диизобутилалюминия в инертном растворителе, таком как тетрагидрофуран, толуол или метиленхлорид, и при подходящей температуре от -78°C до комнатной температуры.
Наконец, по способу C соединения формулы (Ib) получают восстановительным аминированием альдегидов формулы (XII) аминами формулы R5R6NH (III) в присутствии восстановительных агентов, таких как цианоборгидрид натрия (NaBH3CN) или боргидрид натрия (NaBH4), в растворителе, таком как метанол или этанол, и при подходящей температуре от 0°C до комнатной температуры.
Способ D
Соединения формулы (I), в частности соединения формулы (Ib), также могут быть получены синтетическим способом, описываемым схемой IV:
Схема IV


По способу D соединения формулы (XIII) получают из соединений формулы (VII) путем гидролиза сложноэфирной группы с основанием, таким как NaOH, KOH или LiOH, в смеси воды и спирта, такого как метанол или этанол, и при подходящей температуре от комнатной температуры до температуры флегмы растворителя.
По способу D соединения формулы (XIV) получают взаимодействием соединений формулы (XIII) с алкилхлорформиатом, таким как метилхлорформиат, этилхлорформиат, изопренилхлорформиат или изобутилхлорформиат, в присутствии основания, такого как триэтиламин, этилдиизопропиламин или N-метилморфолин, и последующей обработкой аминами формулы R5R6NH (III), в инертном растворителе, таком как метиленхлорид, тетрагидрофуран или N,N-диметилформамид, и при подходящей температуре от 0°C до комнатной температуры. Соединения формулы (XIV) могут также быть получены из соединений формулы (XIII) и аминов формулы R5R6NH (III) в присутствии реагентов, которые активируют карбонильные группы, таких как N,N'-дициклогексилкарбодиимид, 1-(3-диметиламинопропил)-3-этилкарбодиимид, гидрохлорид или диизопропилкарбодиимид. Данное взаимодействие также может проводиться с использованием карбодиимидов в присутствии 1-бензотриазола или N-гидроксисукцинимида. Соединения формулы (XIV) также могут быть получены из соединений формулы (XIII) и аминов формулы R5R6NH (III) в присутствии N,N'-карбонилдиимидазола.
По способу D соединения формулы (Ib) получают из соединений формулы (XIV) путем взаимодействия с восстанавливающими средствами, такими как гидрид алюминия и лития, гидрид диизобутилалюминия, или в две стадии с использованием тетрафторбората триэтилоксония и боргидрида натрия (E. Cereda, et al., Tetrahedron Letters, 21, 4977-4980, 1980).
Способ E
Соединения формулы (I), в частности соединения формулы (Ib), также могут быть получены синтетическим способом, описываемым схемой V:
Схема V

По способу E соединения формулы (Ia) получают из соединений формулы (Ib) путем каталитического гидрирования в присутствии катализаторов, таких как Pd-C или PtO2, в растворителе, таком как метанол, этанол, N,N-диметилформамид или уксусная кислота.
Способ F
Соединения формулы (I), в частности соединения формулы (Iа), также могут быть получены синтетическим способом, описываемым схемой VI:
Схема VI

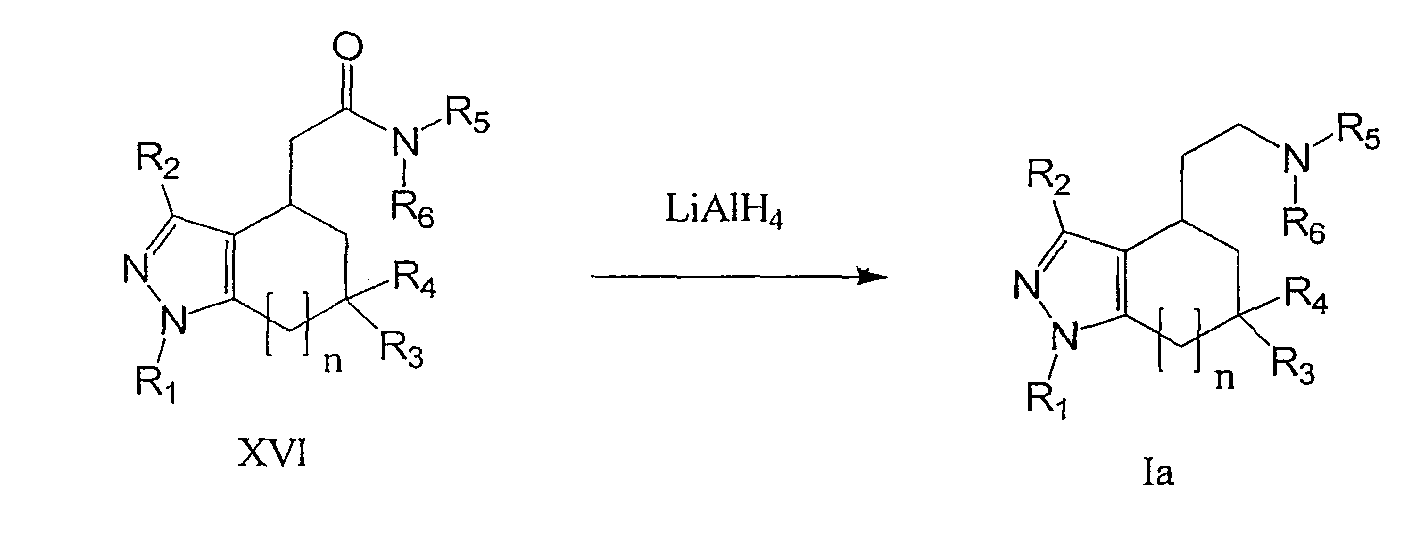
По способу F соединения формулы (XV) получают из соединений формулы (VIII) путем гидролиза сложноэфирной группы основанием, таким как NaOH, KOH или LiOH, в смеси с водой и спиртом, таким как метанол или этанол, и при подходящей температуре, которая может составлять от комнатной температуры до температуры флегмы растворителя.
По способу F соединения формулы (XVI) получают из соединений формулы (XV) и аминов формулы R5R6NH (III) в присутствии N,N'-карбонилдиимидазола. Соединения формулы (XVI) могут также быть получены взаимодействием соединений формулы (XV) с алкилхлорформиатом, таким как метилхлорформиат, этилхлорформиат, изопренилхлорформиат или изобутилхлорформиат, в присутствии основания, такого как триэтиламин, этилдиизопропиламин или N-метилморфолин, и последующей обработкой аминами формулы R5R6NH (III), в инертном растворителе, таком как метиленхлорид, тетрагидрофуран или N,N-диметилформамид, и при подходящей температуре от 0°C до комнатной температуры. Соединения формулы (XVI) могут также быть получены из соединений формулы (XV) и аминов формулы R5R6NH (III) в присутствии реагентов, которые активируют карбонильные группы, таких как N,N'-дициклогексилкарбодиимид, гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида, или диизопропилкарбодиимид. Данное взаимодействие также может проводиться с использованием карбодиимидов в присутствии 1-бензотриазола или N-гидроксисукцинимида.
По способу F соединения формулы (Ia) получают из соединений формулы (XVI) путем взаимодействия с восстанавливающими средствами, такими как гидрид алюминия и лития, гидрид диизобутилалюминия, или в две стадии с использованием тетрафторбората триэтилоксония и боргидрида натрия.
Полученные продукты взаимодействия могут, если требуется, быть очищены общепринятыми способами, такими как кристаллизация и хроматография. Там, где описанные выше процессы получения соединений по изобретению приводят к возникновению смесей стереоизомеров, данные изомеры могут разделяться общепринятыми способами, такими как препаративная хроматография. Если имеются хиральные центры, соединения могут быть получены в рацемической форме, или отдельные энантиомеры могут быть получены путем энантиоспецифичного синтеза или разрешения.
Одной из предпочтительных фармацевтически приемлемых форм является кристаллическая форма, причем такая форма включается в фармацевтическую композицию. В случае солей и сольватов дополнительные радикалы ионов и растворителей также не должны быть токсичными. Соединения по изобретению могут представлять собой различные полиморфные формы, подразумевается, что изобретение охватывает все такие формы.
Другой аспект изобретения относится к способу лечения или профилактики опосредованного сигма-рецептором заболевания, причем данный способ включает в себя введение нуждающемуся в таком лечении пациенту терапевтически эффективного количества определенного выше соединения формулы (I) или их фармацевтической композиции. Среди опосредованных сигма-рецепторов заболеваний, которые можно лечить, находятся диарея, связанные с липопротеинами нарушения, мигрень, избыточный вес, артрит, гипертензия, аритмия, язва, когнитивые расстройства, пристрастие к химическим веществам, например кокаиновая зависимость, поздняя дискинезия, ишемический инсульт, эпилепсия, инсульт, депрессия, стресс, боль, особенно невропатическая боль или аллодиния, состояние психоза. Соединения по изобретению также могут использоваться в качестве фармакологического инструмента или в качестве анксиолитика или иммунодепрессанта.
Настоящее изобретение далее относится к фармацевтическим композициям, содержащим соединение по изобретению или его фармацевтически приемлемую соль, производное, пролекарство или стереоизомеры, вместе с фармацевтически приемлемым носителем, адъювантом или несущим средством, для введения пациенту.
Примеры фармацевтических композиций включают любую твердую (таблетки, пилюли, капсулы, гранулы, и т.д.) и жидкую (растворы, суспензии или эмульсии) композицию для перорального, местного или парентерального введения.
В предпочтительном варианте осуществления фармацевтические композиции находятся в пероральной форме, твердом или жидком виде. Подходящие дозированные формы для перорального введения могут представлять собой таблетки, капсулы, сиропы, или растворы и могут содержать общепринятые наполнители, известные в данной области, такие как связующие средства, например сироп, гуммиарабик, желатин, сорбит, трагакант, или поливинилпирролидон; наполнители, например лактозу, сахар, кукурузный крахмал, фосфат кальция, сорбит или глицин; смазки для таблеток, например стеарат магния; дезинтегрирующие средства, например, крахмал, поливинилпирролидон, гликолят крахмала натрия или микрокристаллическая целлюлоза; или фармацевтически приемлемые увлажняющие средства, такие как лаурилсульфат натрия.
Твердые композиции для перорального введения могут быть получены общепринятыми способами смешивания, наполнения или таблетирования. Повторные операции перемешивания могут использоваться для распределения активного средства по данным композициям с использованием больших количеств наполнителей. Такие операции являются общепринятыми в данной области. Таблетки могут, например, быть получены влажным или сухим гранулированием и необязательно покрываться способами, хорошо известными в обычной фармацевтической практике, в частности, с внутренним покрытием.
Фармацевтические композиции могут также адаптироваться для парентерального введения, например, в виде стерильных растворов, суспензий и лиофилизованных продуктов в подходящей единичной дозированной форме. Могут использоваться адекватные наполнители, например наполнители, буферные средства или поверхностно-активные вещества.
Указанные препараты могут быть получены стандартными способами, такими как описанные в Фармакопее Испании или США и сходных справочных текстах, или ссылки на которые даны в этих источниках.
Введение соединения или композиций по настоящему изобретению может осуществляться любым принятым способом, таким как внутривенное вливание, пероральные препараты и внутрибрюшинное и внутривенное введение. Пероральное введение предпочтительно из-за удобства для пациента и хронического характера подлежащих лечению заболеваний.
В основном, эффективное введенное количество соединения по изобретению зависит от выбранного соединения, тяжести подлежащего лечению заболевания и массы тела пациента. Однако активные соединения обычно вводят один или несколько раз в сутки, например 1, 2, 3 или 4 раза в сутки, при обычно общей суточной дозе в интервале от 0,1 до 1000 мг/кг/сутки.
Соединения и композиции по изобретению могут использоваться с другими лекарственными средства для предоставления комбинированного лечения. Другие лекарственные средства образуют часть той же композиции или предоставляются в отдельной композиции для лечения в одно и то же время или в разное время.
Следующие примеры приводятся только в качестве дальнейшей иллюстрации изобретения, при этом они не могут использоваться для определения пределов изобретения.
ПРИМЕРЫ
Пример 1
Синтез 4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазол (1)
Стадия 1: Синтез этил-2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)ацетата

Pd-C (150 мг, 10%) добавляют к раствору E/Z-изомеров этил-(1,5,6,7-тетрагидро-1-фенил-4H-индазол-4-илиден)ацетата (1,6 г, 5,67 ммоль) в 50 мл EtOH и полученный в результате раствор перемешивают в атмосфере азота (50 фунтов на кв.дюйм) в гидрогенизаторе Парра в течение 18 часов. Реакционную смесь очищают азотом, фильтруют через целит и растворитель упаривают при пониженном давлении с получением этил-2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)ацетата (1,60 г, 5,63 ммоль, 99%, масло).
1H ЯМР (300 МГц, CDCl3): δ 1,29 (т, J=7,2 Гц, 3Н), 1,48 (м, 1H), 1,73 (м, 1H), 1,98 (м, 2H), 2,45 (дд, J=15,4 Гц, J'=8,0 Гц, 1H), 2,68 (м, 3Н), 3,26 (м, 1H), 4,20 (кв, J=7,2 Гц, 2H), 7,31 (м, 1H), 7,41-7,52 (м, 5H).
Стадия 2: синтез 2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)этанола

Раствор этил-2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)ацетата (1,40 г, 5,79 ммоль) в 5 мл THF добавляют на перемешиваемую суспензию гидрида алюминия-лития (300 мг, 7,9 ммоль) в 20 мл THF при комнатной температуре. Смесь инкубируют при перемешивании при комнатной температуре в течение 18 часов и затем кипятят с обратным холодильником в течение 1 часа. Смесь гидролизуют льдом и NaOH (10%), фильтруют через целит и упаривают растворитель при пониженном давлении с получением 2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)этанола (1,10 г, 4,55 ммоль, 79%, масло).
1H ЯМР (300 МГц, CDCl3): δ 1,45 (м, 1Н), 1,72 (м, 2H), 1,98 (м, 3H), 2,32 (ушир.с, 1H), 2,71 (м, 2H), 2,91 (м, 1H), 3,84 (т, J=6,7 Гц, 2H), 7,32 (м, 1H), 7,40-7,55 (м, 4H), 7,57 (с, 1H).
Стадия 3: Синтез 4-(2-хлорэтил)-4,5,6,7-тетрагидро-1-фенил-1H-индазола

Тионилхлорид (4 мл) медленно добавляют при комнатной температуре в раствор 2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)этанола (516 мг, 2,13 ммоль) в 25 мл толуола. Реакционную смесь нагревают при 90°C в течение 2 часов. Растворитель удаляют при пониженном давлении. Неочищенный продукт растворяют в этилацетате и дважды промывают раствором NaHCO3. Растворитель затем упаривают при пониженном давлении с получением 4-(2-хлорэтил)-4,5,6,7-тетрагидро-1-фенил-1H-индазола (423 мг, 1,62 ммоль, 76%, масло).
1H ЯМР (300 МГц, CDCl3): δ 1,45 (м, 1H), 1,73 (м, 1H), 1,94 (м, 3H), 2,18 (м, 1H), 2,71 (м, 2H), 3,00 (м, 1H), 3,70 (т, J=6,8 Гц, 2H), 7,32 (м, 1H), 7,47 (м, 4H), 7,55 (с, 1H).
Стадия 4: синтез 4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазол

Смесь 4-(2-хлорэтил)-4,5,6,7-тетрагидро-1-фенил-1H-индазола (423 мг, 1,62 ммоль), K2CO3 (336 мг, 2,43 ммоль), морфолина (0,42 мл, 4,87 ммоль) и каталитическое количество KI в 20 мл DMF нагревают до кипения с обратным холодильником в течение 18 час. Растворитель удаляют при пониженном давлении, неочищенный продукт растворяют в этилацетате, промывают водой и органическую фазу упаривают при пониженном давлении. Полученный в результате неочищенный продукт очищают хроматографией на силикагеле с получением 4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазола (384 мг, 1,23 ммоль, 76%, масло).
1H ЯМР (300 МГц, CDCl3): δ 1,42 (м, 1H), 1,67 (м, 2H), 1,92 (м, 3H), 2,40-2,60 (м, 6H), 2,69 (м, 2H), 2,77 (м, 1H), 3,74 (м, 4H), 7,29 (м, 1H), 7,44 (м, 4H), 7,51 (с, 1H).
Пример 2
Синтез 4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазола оксалат (2)

HO2CCO2H·2H2O (156 мг, 1,23 ммоль) добавляют к раствору 4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазола (380 мг, 1,22 ммоль) в 4 мл ацетона с получением оксалата 4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-Фенил-1H-индазола оксалата (318 мг, 0,79 ммоль, 65%, белое твердое вещество), т.пл.=150-151°C.
1Н ЯМР (300 МГц, ДМСО-d6, TFA): δ 1,36 (м, 1H), 1,60 (м, 1H), 1,71-1,93 (м, 3H), 2,04 (м, 1H), 2,56-2,77 (м, 3H), 3,03 (м, 2H), 3,21 (м, 2H), 3,44 (д, J=12,7 Гц, 2H), 3,62 (т, J=11,6 Гц, 2H), 3,92 (м, 2H), 7,29 (м, 1H), 7,38-7,49 (м, 4H), 7,62 (с, 1H), 9,69 (м, 1H).
Пример 3
Синтез 1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазола (3)
Стадия 1: синтез 1-(3,4-дихлорфенил)-1,5,6,7-тетрагидро-4H-индазол-4-она

Смесь гидрохлорида 1-(3,4-дихлорфенил)гидразина (6,78 г, 31,8 ммоль) и безводного ацетата натрия (2,60 г, 31,8 ммоль) в н-BuOH (20 мл) медленно добавляют к раствору 2-((диметиламино)метилен)циклогексан-1,3-диона (5,32 г, 31,8 ммоль) в н-BuOH (100 мл) и уксусной кислоте (5 мл). Полученную в результате смесь нагревают до кипения с обратным холодильником в течение 2 часов, контролируя реакцию посредством ТСХ. Растворитель упаривают при пониженном давлении, остаток разбавляют в AcOEt и промывают H2O. Затем растворитель еще раз упаривают и неочищенный продукт очищают хроматографией на силикагеле с получением 1-(3,4-дихлорфенил)-1,5,6,7-тетрагидро-4H-индазол-4-она (5,0 г, 17,79 ммоль, 56%, оранжевое твердое вещество).
1H ЯМР (300 МГц, CDCl3): δ 2,17 (м, 2H), 2,51 (м, 2H), 2,96 (т, J=6,1 Гц, 2H), 7,36 (т, J=8,6 Гц, J'=2,4 Гц, 1H), 7,54 (д, J=8,6 Гц, 1H), 7,64 (д, J=2,4 Гц, 1H), 8,02 (с, 1Н).
Стадия 2: синтез смеси E/Z-изомеров этил-(1-(3,4-дихлорфенил)-1,5,6,7-тетрагидро-4H-индазол-4-илиден)ацетата

Суспензию гидрида натрия (428 мг, 60% суспензия, 10,6 ммоль) добавляют в атмосфере азота к раствору триэтилфосфоноацетата (2,40 г, 10,6 ммоль) в THF (40 мл) и инкубируют при комнатной температуре в течение 10 минут. Далее 1-(3,4-дихлорфенил)-1,5,6,7-тетрагидро-4H-индазол-4-он (1,0 г, 3,56 ммоль) добавляют к полученному ранее раствору и смесь кипятят с обратным холодильником в течение 18 часов, контролируя реакцию путем ТСХ. Раствор выливают в воду и затем экстрагируют AcOEt. Органическую фазу затем упаривают при пониженном давлении с получение отвердевающего масла и неочищенный продукт очищают путем хроматографии на силикагеле с получением смеси E/Z-изомеров этил-(1-(3,4-дихлорфенил)-1,5,6,7-тетрагидро-4H-индазол-4-илиден)ацетата (1,2 г, 3,41 ммоль, 96%, оранжевое твердое вещество).
1H ЯМР (300 МГц, CDCl3): δ 1,31 (т, J=7,1 Гц, 3H), 1,96 (м, 2H), 2,56-3,16 (2м, 2H), 2,84 (м, 2H), 4,20 (м, 2H), 5,67-6,09 (2с, 1H), 7,35 (д, J=8,6 Гц, 1H), 7,53 (д, J=8,6 Гц, 1H), 7,64 (с, 1H), 7,90-8,83 (2с, 1H).
Стадия 3: Синтез этил-2-(1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-4-ил)ацетата

PtO2 (30 мг) добавляют к раствору смеси E/Z-изомеров этил-(1-(3,4-дихлорфенил)-1,5,6,7-тетрагидро-4H-индазол-4-илиден)ацетата (1,5 г, 4,27 ммоль) в уксусной кислоте (25 мл); смесь инкубируют при перемешивании под давлением 1 атм H2. Затем образец экстрагируют и проводят1Н-ЯМР. Затем смесь фильтруют, разбавляют AcOEt и промывают водой H2O и насыщенным раствором NaHCO3. Затем растворитель упаривают при пониженном давлении с получением этил 2-(1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-4-ил)ацетата (1,0 г, 2,83 ммоль, чистота 66%, масло).
1H ЯМР (300 МГц, CDCl3): δ 1,29 (т, J=7,2 Гц, 3Н), 1,45 (м, 1H), 1,74 (м, 1H), 1,98 (м, 2H), 2,44 (дд, J=15,4 Гц, J'=7,9 Гц, 1H), 2,61-2,73 (м, 3Н), 3,24 (м, 1H), 4,20 (кв, J=7,2 Гц, 2H), 7,36 (дд, J=8,8 Гц, J'=2,5 Гц, 1H), 7,50 (м, 2H), 7,64 (д, J=2,5 Гц, 1H).
Стадия 4: синтез 2-(1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-4-ил)этанола

Раствор DIBALH (1 M) в толуоле (13 мл, 13,0 ммоль) медленно добавляют, с поддержанием температуры взаимодействия ниже -65°C, к раствору этил-2-(1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-4-ил)ацетата (1,83 г, 5,2 ммоль) в 20 мл высушенного Cl2CH2, охлажденного при -75°C в атмосфере N2. Полученную в результате смесь инкубируют при перемешивании при -70°C в течение 30 минут, контролируя реакцию путем ТСХ. Затем температуру повышают до 0°С и добавляют 10 мл холодной воды, в то время как температура поддерживается при 0°C. Образуется осадок, который фильтруется и промывается Cl2CH2. Органическую фазу дважды промывают водой, сушат и упаривают при пониженном давлении. Полученный в результате неочищенный продукт очищают хроматографией на силикагеле с получением 2-(1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-4-ил)этанола (1,06 г, 3,41 ммоль, 66%, масло).
1H ЯМР (300 МГц, CDCl3): δ 1,43 (м, 1Н), 1,70 (м, 2H), 1,90-2,18 (м, 4H), 2,69 (м, 2H), 2,87 (м, 1H), 3,79 (т, J=6,6 Гц, 2H), 7,35 (дд, J=8,7 Гц, J'=2,5 Гц, 1H), 7,49 (д, J=8,7 Гц, 1H), 7,53 (с, 1H), 7,64 (д, J=2,5 Гц, 1H).
Стадия 5: Синтез 4-(2-хлорэтил)-4,5,6,7-тетрагидро-1-(3,4-дихлорфенил)-1H-индазола

Тионилхлорид (4 мл) медленно добавляют при комнатной температуре к раствору 2-(1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-4-ил)этанола (512 мг, 1,65 ммоль) в 20 мл толуола. Реакционную смесь нагревают при 90°C в течение 2 часов. Растворитель удаляют при пониженном давлении. Неочищенный продукт растворяют в этилацетате дважды промывают раствором NaHCO3. Затем растворитель упаривают при пониженном давлении с получением 4-(2- хлорэтил)-4,5,6,7-тетрагидро-1-(3,4-дихлорфенил)-1H-индазол (462 мг, 1,40 ммоль, 85%, масло).
1H ЯМР (300 МГц, CDCl3): δ 1,44 (м, 1H), 1,75 (м, 1H), 1,84-2,12 (м, 3H), 2,18 (м, 1H), 2,72 (м, 2H), 2,99 (м, 1H), 3,69 (т, J=7,0 Гц, 2H), 7,37 (дд, J=8,6 Гц, J'=2,5 Гц, 1H), 7,50 (д, J=8,6 Гц, 1H), 7,54 (с, 1H), 7,65 (д, J=2,5 Гц, 1H).
Стадия 6: синтез 1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазола

Смесь 4-(2-хлорэтил)-4,5,6,7-тетрагидро-1-(3,4-дихлорфенил)-1H-индазола (235 мг, 0,71 ммоль), K2CO3 (99 мг, 0,71 ммоль), 4-фенилпиперидина (97 мг, 0,71 ммоль) и каталитического количества KI в 5 мл DMF нагревают до кипения с обратным холодильником в течение 18 часов. Растворитель удаляют при пониженном давлении, неочищенный продукт растворяют в этилацетате, промывают водой и органическую фазу упаривают при пониженном давлении. Полученный в результате неочищенный продукт очищают хроматографией на силикагеле с получением 1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазола (146 мг, 0,32 ммоль, 45%, масло).
1H ЯМР (300 МГц, CDCl3): δ 1,36-2,30 (м, 12H), 2,50-2,83 (м, 6H), 3,20 (м, 2H), 7,18-7,40 (м, 6H), 7,51 (д, J=8,6 Гц, 1H), 7,55 (с, 1H), 7,66 (д, J=2,3 Гц, 1H).
Пример 4
Синтез оксалата 1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазола (4)
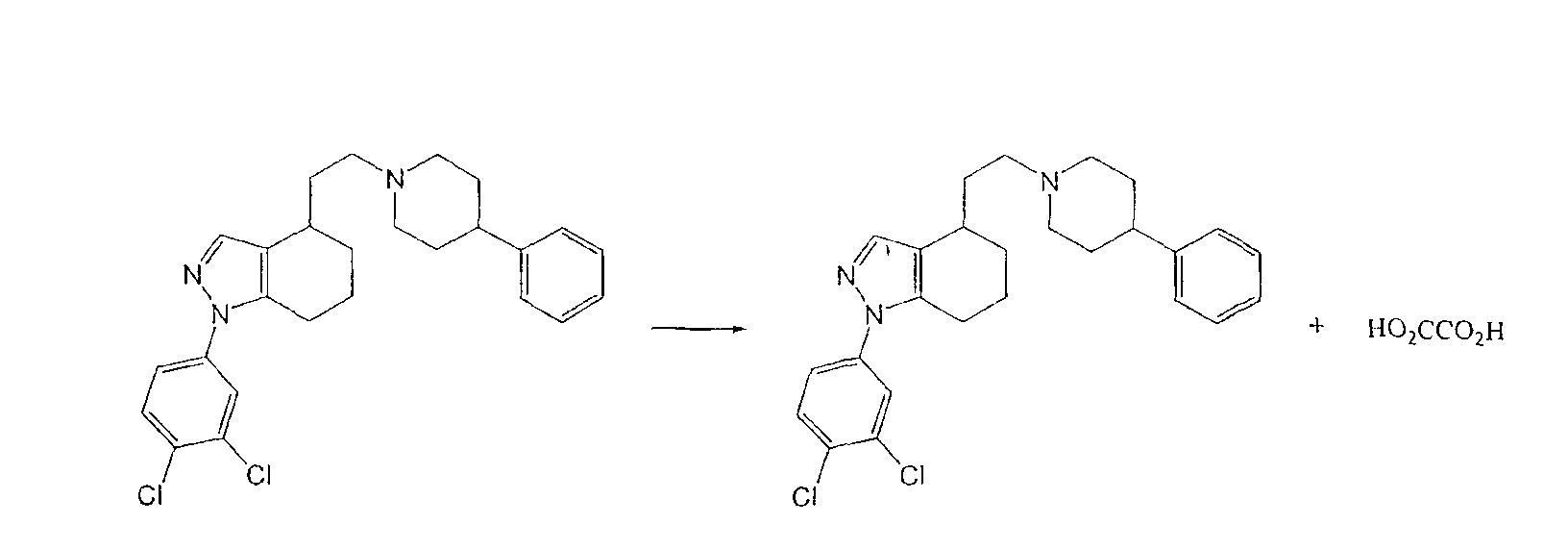
HO2CCO2H·2H2O (40 мг, 0,32 ммоль) добавляют к раствору 1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазола (140 мг, 0,31 ммоль) в 4 мл ацетона с получением оксалата 1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2- (4-фенилпиперидин-1-ил)этил)-1H-индазола (125 мг, 0,23 ммоль, 74%, белое твердое вещество), т.пл.=133-134°C.
Пример 5
Синтез (E)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1H-индазола (5)
Способ D
Стадия 1: Синтез E/Z-смеси 2-(1,5,6,7-тетрагидро-1-фенил-4H-индазол-4-илиден)уксусной кислоты

H2O (15 мл) и 10% NaOH (3 мл, 7,5 ммоль) добавляют к раствору смеси E/Z этил-2-(1,5,6,7-тетрагидро-1-фенил-4H-индазол-4-илиден)ацетата (2,06 г, 7,31 ммоль) в этаноле (30 мл) и кипятят с обратным холодильником в течение 3 часов, контролируя реакцию посредством ТСХ. Этанол упаривают при пониженном давлении и подкисляют 1н HCl и образованный осадок фильтруют, промывают H2O и сушат с получением смеси E/Z (85/15) 2-(1,5,6,7-тетрагидро-1-фенил-4H-индазол-4-илиден)уксусной кислоты (1,37 г, 5,39 ммоль, 74%).
1H ЯМР (300 МГц, CDCl3): δ 1,94 (м, 2H), 2,59 (2×м, (0,30+1,70)H), 2,86 (м, 2H), 5,70 и 6,12 (2×с, (0,15+0,85)H), 7,38 (м, 1H), 7,48 (м, 4H), 7,94 и 8,85 (2×с, (0,85+0,15)H).
Стадия 2: синтез (E/Z)-4-(2-(1-фенил-6,7-дигидро-1H-индазол-4(5H)илиден)ацетил)морфолина

Триэтиламин (0,054 мл, 0,39 ммоль) и этилхлорформиат (0,037 мл, 0,30 ммоль) добавляют к раствору смеси E/Z 2-(1,5,6,7-тетрагидро-1-фенил-4H-индазол-4-илиден)уксусной кислоты (100 мг, 0,39 ммоль) в CH2Cl2 (5 мл), охлаждают до 0°C и перемешивают в течение 45 минут при 0°C. Затем морфолин (0,034 мл, 0,39 ммоль) добавляют, контролируя реакцию посредством ТСХ. Раствор промывают разбавленным NaOH, органическую фазу отделяют, сушат и упаривают при пониженном давлении. Полученный в результате неочищенный продукт очищают посредством хроматографии на силикагеле с получением смеси E/Z (80/20) 4-(2-(1-фенил-6,7-дигидро-1H-индазол-4(5H)-илиден)ацетил)морфолина (40 мг, 0,12 ммоль, 32%).
1H ЯМР (300 МГц, CDCl3): δ 1,91 (м, 2H), 2,50 и 2,75-3,00 (2×м, (0,40+3,60)H), 3,50-3,90 (м, 8H), 5,67 и 6,24 (2×с, (0,20+0,80)H), 7,36 (м, 1H), 7,48 (м, 4H), 7,86 и 7,93 (2×с, (0,80+0,20)H).
Стадия 3: синтез (E)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1H-индазола

Смесь E/Z 4-(2-(1-фенил-6,7-дигидро-1H-индазол-4(5H)-илиден)ацетил)морфолина (398 мг, 1,23 ммоль) добавляют к смеси LiAlH4 (129 мг, 3,70 ммоль) в THF (10 мл), охлажденной до 0°С. Температуре реакционной смеси позволяют повыситься до комнатной температуры и смесь перемешивают в течение 4 часов, и затем реакционную смесь кипятят с обратным холодильником в течение 30 минут. Смесь охлаждают на ледяной бане и добавляют лед. Нерастворимое твердое вещество отфильтровывают и промывают AcOEt. Органическую фазу промывают H2O, сушат и упаривают при пониженном давлении с получением смеси E/Z 4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1H-индазола, который очищают посредством хроматографии на силикагеле с получением (E)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1H-индазола (118 мг, 0,38 ммоль, 31%) и смеси E/Z 4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1H-индазола (80,2 мг, 0,26 ммоль, 21%). Спектр1Н-ЯМР (300 МГц, CDCl3) (E)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1H-индазол совпадает со спектром соединения, полученного способом A.
Дальнейший синтез соединения (5):
Стадия 1: синтез толуол-4-сульфоната 1-[2-(1-фенил-1,5,6,7-тетрагидроиндазол-4-илиден)этил]пиридиния

П-толуолсульфонилхлорид (210 мг, 1,10 ммоль) добавляют к раствору (E)-2-(6,7-дигидро-1-фенил-1H-индазол-4(5H)-илиден)этанола (254 мг, 1,05 ммоль) в 10 мл пиридина, охлажденного до 0°С. Реакцию контролируют путем ТСХ. Затем растворитель упаривают, неочищенный продукт разбавляют CHCl3 и промывают разбавленным раствором NaHCO3. Органическую фазу упаривают при пониженном давлении с получением толуол-4-сульфоната 1-[2-(1-фенил-1,5,6,7-тетрагидроиндазол-4-илиден)этил]пиридиния (300 мг, 0,63 ммоль, 60%, желтое твердое вещество).
Стадия 2: синтез (E)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1H-индазола

Смесь толуол-4-сульфоната 1-[2-(1-фенил-l,5,6,7-тетрагидроиндазол-4-илиден)этил]пиридиния (290 мг, 0,63 ммоль) и морфолина (180 мг, 1,5 ммоль) в 15 мл ацетонитрила кипятят с обратным холодильником в течение 4 часов, контролируя реакцию путем ТСХ. Затем растворитель упаривают, неочищенный продукт разбавляют этилацетатом и промывают три раза водой. Затем органическую фазу упаривают при пониженном давлении. Неочищенный продукт, полученный таким образом, очищают путем хроматографии на силикагеле с получением (E)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1H-индазола (110 мг, 0,36 ммоль, 57%, бежевое твердое вещество, т.пл.=114-116°C).
1H ЯМР (300 МГц, CDCl3): δ 1,87 (м, 2H), 2,40-2,62 (м, 6H), 2,81 (т, J=6,1 Гц, 2Н), 3,18 (д, J=7,3 Гц, 2H), 3,75 (м, 4H), 5,81 (т, J=7,3 Гц, 1H), 7,33 (м, 1H), 7,47 (м, 4Н), 7,81 (с, 1H).
Следующие соединения получают сходным путем.
Пример 6
1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1H-индазол (6)

1H ЯМР (300 МГц, CDCl3): δ 1,41 (м, 1H), 1,66 (м, 2H), 1,93 (м, 3H), 2,47 (м, 6H), 2,62-2,79 (м, 3H), 3,71 (т, J=4,7 Гц, 4H), 7,34 (дд, J=8,7 Гц, J'=2,5 Гц, 1H), 7,48 (д, J=8,7 Гц, 1H), 7,49 (с, 1H), 7,63 (д, J=2,5 Гц, 1H), (65 мг, 0,17 ммоль, 23%, масло).
Пример 7
1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1H-индазола оксалат (7)

(45 мг, 0,10 ммоль, 59%, кремовое твердое вещество, т.пл.=148,0-149,8°C).
Пример 8
4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазол (8)

1H ЯМР (300 МГц, CDCl3): δ 1,44 (м, 1H), 1,70 (м, 1H), 1,79-2,11 (м, 8H), 2,23 (м, 2H), 2,48-2,85 (м, 6H), 3,22 (м, 2H), 7,16-7,35 (м, 6H), 7,40-7,52 (м, 4H), 7,54 (с, 1H), (106 мг, 0,28 ммoль, 28%, масло).
Пример 9
4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазола оксалат (9)

(47 мг, 0,10 ммоль, 36%, белое твердое вещество, т.пл.=124-125°C).
Пример 10
4-(2-(4-бензилпиперазин-1-ил)этил)-4,5,6,7-тетрагидро-1-фенил-1H-индазол (10)

1H ЯМР (300 МГц, CDCl3): δ 1,42 (м, 1H), 1,68 (м, 2H), 1,92 (м, 3H), 2,40-2,80 (м, 13H), 3,52 (с, 2H), 7,20-7,37 (м, 6H), 7,39-7,52 (м, 5), (110 мг, 0,27 ммоль, 23%, бежевое твердое вещество, т.пл.=98-101°C).
Пример 11
4,5,6,7-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3H),4'-пиперидин]-1'-ил]этил)-1H-индазол (11)

1H ЯМР (300 МГц, CDCl3): δ 1,40 (м, 1H), 1,60-1,80 (м, 4H), 1,88-2,05 (м, 5H), 2,40 (м, 2H), 2,57 (т, J=7,9 Гц, 2H), 2,67 (м, 2H), 2,74 (м, 1H), 2,90 (м, 2H), 5,04 (с, 2H), 7,10-7,30 (м, 5H), 7,37-7,48 (м, 4H), 7,51 (с, 1H), (163 мг, 0,39 ммоль, 34%, масло).
Пример 12
4,5,6,7-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3H),4'-пиперидин]-1'-ил]этил)-1H-индазола оксалат (12)
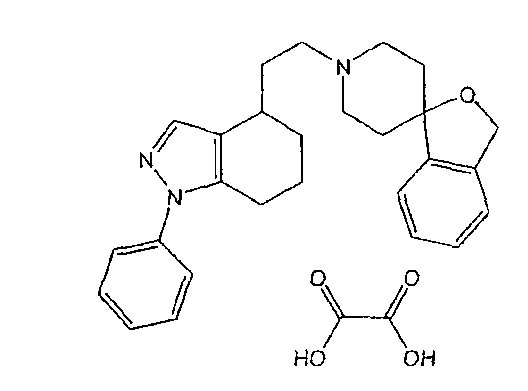
(148 мг, 0,29 ммоль, 74%, белое твердое вещество, т.пл.=133-135°C).
Пример 13
4,5,6,7-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этил)-1H-индазол (13)

1H ЯМР (300 МГц, CDCl3): δ 1,44 (м, 3Н), 1,69 (м, 6H), 1,95 (м, 3H), 2,55 (м, 6H), 2,69 (м, 2H), 2,76 (м, 1H), 7,30 (м, 1H), 7,40-7,50 (м, 4H), 7,51 (с, 1H), (83 мг, 0,27 ммоль, 23%, масло).
Пример 14
4,5,6,7-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этил)-1H-индазола оксалат (14)

(50 мг, 0,13 ммоль, 48%, белое твердое вещество, т.пл.=185-188°C).
Пример 15
(E)-4-(2-(азепан-1-ил)этилиден)-4,5,6,7-тетрагидро-1-фенил-1H-индазол (15)

1H ЯМР (300 МГц, CDCl3): δ 1,56-1,80 (м, 8H), 1,85 (м, 2H), 2,47 (м, 2H), 2,73 (м, 4H), 2,81 (т, J=6,1 Гц, 2H), 3,34 (д, J=7,1 Гц, 2H), 5,87 (т, J=7,1 Гц, 1H), 7,32 (м, 1H), 7,47 (м, 4H), 7,83 (с, 1H), (17 мг, 0,05 ммоль, 11%, масло).
Пример 16
(E)-4-(2-(азепан-1-ил)этилиден)-4,5,6,7-тетрагидро-1-фенил-1H-индазола оксалат (16)
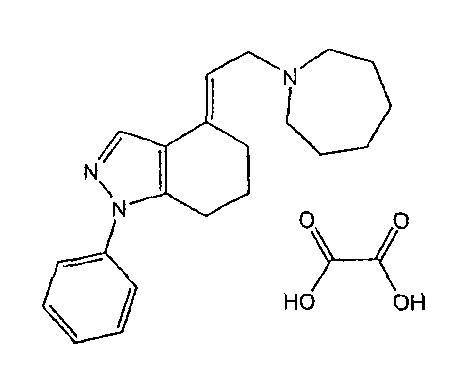
(15 мг, 0,04 ммоль, 80%, белое твердое вещество, т.пл.=171-173°C).
Пример 17
(E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперидин-1-ил)этилиден)-1H-индазол (17)

1H ЯМР (300 МГц, CDCl3): δ 1,90 (м, 4Н), 2,02 (м, 2H), 2,29 (м, 2H), 2,46 (м, 3Н), 2,82 (т, J=6,1 Гц, 2H), 3,26 (м, 2H), 3,36 (м, 2H), 5,90 (т, J=7,1 Гц, 1H), 7,18-7,38 (м, 6H), 7,47 (м, 4H), 7,85 (с, 1H), (30 мг, 0,08 ммоль, 16%, бежевое твердое вещество, т.пл.=110-112°C).
Пример 18
(E)-4,5,6,7-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3H),4'-пиперидин]-1'-ил]этилиден)-1H-индазол (18)

1H ЯМР (300 МГц, CDCl3): δ 1,78-1,97 (м, 4H), 2,20 (м, 2H), 2,48-2,70 (м, 4H), 2,82 (т, J=6,0 Гц, 2H), 3,08 (м, 2H), 3,36 (м, 2H), 5,08 (с, 2H), 5,91 (т, J=7,5 Гц, 1H), 7,18-7,38 (м, 5H), 7,47 (м, 4H), 7,86 (с, 1H), (50 мг, 0,12 ммоль, 24%, масло).
Пример 19
(E)-4,5,6,7-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3H),4'-пиперидин]-1'-ил]этилиден)-1H-индазола оксалат (19)

(18 мг, 0,04 ммоль, 36%, белое твердое вещество, т.пл.=155-157°C).
Пример 20
(E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперазин-1-ил)этилиден)-1H-индазол (20)

1H ЯМР (300 МГц, CDCl3): δ 1,89 (м, 2H), 2,51 (м, 2H), 2,73 (м, 4H), 2,83 (т, J=6,1 Гц, 2H), 3,28 (м, 6H), 5,87 (т, J=7,2 Гц, 1H), 6,86 (т, J=7,4 Гц, 1H), 6,94 (д, J=7,9 Гц, 2H), 7,22-7,37 (м, 3H), 7,48 (м, 4H), 7,84 (с, 1H), (20 мг, 0,05 ммоль, 10%, бежевое твердое вещество, т.пл.=114-116°C).
Пример 21
1,2,3,4-тетрагидро-2-((E)-2-(6,7-дигидро-1-фенил-1H-индазол-4(5H)-илиден)этил)изохинолин (21)

1H ЯМР (300 МГц, CDCl3): δ 1,90 (м, 2H), 2,52 (м, 2H), 2,83 (м, 4H), 2,95 (м, 2H), 3,38 (д, J=7,2 Гц, 2H), 3,75 (с, 2H), 5,93 (т, J=7,2 Гц, 1H), 7,03 (м, 1H), 7,12 (м, 3H), 7,33 (м, 1H), 7,42-7,52 (м, 4H), 7,84 (с, 1H), (60 мг, 0,17 ммоль, 34%, масло).
Пример 22
1,2,3,4-тетрагидро-2-((E)-2-(6,7-дигидро-1-фенил-1H-индазол-4(5H)-илиден)этил)изохинолина оксалат (22)

(25 мг, 0,06 ммоль, 40%, белое твердое вещество, т.пл.=217-218°C).
Пример 23
(E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(3-фенилпиперидин-1-ил)этилиден)-1H-индазол (23)

1H ЯМР (300 МГц, CDCl3): δ 1,40-2,20 (м, 9H), 2,46 (м, 2H), 2,80 (т, J=6,2 Гц, 2H), 2,85-3,38 (м, 4H), 5,87 (т, J=7,9 Гц, 1H), 7,18-7,38 (м, 6H), 7,46 (м, 4H), 7,83 (с, 1H), (46 мг, 0,12 ммоль, 24%, бежевое твердое вещество, т.пл.=136-138°C).
Пример 24
(E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(3-фенилпирролидин-1-ил)этилиден)-1H-индазол (24)

1H ЯМР (300 МГц, CDCl3): δ 1,82 (м, 2H), 1,92 (м, 1H), 2,32 (м, 1H), 2,45 (м, 2H), 2,57 (м, 1H), 2,75 (м, 3H), 3,01 (м, 1H), 3,23 (м, 1H), 3,38 (м, 3H), 5,83 (т, J=7,5 Гц, 1H), 7,09-7,30 (м, 6H), 7,34-7,46 (м, 4H), 7,77 (с, 1H), (60 мг, 0,16 ммоль, 32%, масло).
Пример 25
(E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(3-фенилпирролидин-1-ил)этилиден)-1H-индазола оксалат (25)

(46 мг, 0,10 ммоль, 67%, белое твердое вещество, т.пл.=178-181°C).
Пример 26
(E)-4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этилиден)-1-фенил-1H-индазол (26)

1H ЯМР (300 МГц, CDCl3): δ 1,91 (м, 2H), 2,52 (м, 2H), 2,83 (т, J=6,1 Гц, 2H), 3,70 (д, J=7,3 Гц, 2H), 4,20 (с, 4H), 5,93 (т, J=7,3 Гц, 1H), 7,20-7,50 (м, 9H), 7,83 (с, 1H), (20 мг, 0,06 ммоль, 12%, бежевое твердое вещество, т.пл.=130-131°C).
Пример 27
(E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этилиден)-1H-индазол (27)

1H ЯМР (300 МГц, CDCl3): δ 1,48 (м, 2H), 1,68 (м, 4H), 1,87 (м, 2H), 2,37-2,66 (м, 6Н), 2,81 (т, J=6,1 Гц, 2H), 3,22 (д, J=7,3 Гц, 2H), 5,86 (т, J=7,3 Гц, 1H), 7,32 (м, 1H), 7,41-7,50 (м, 4H), 7,83 (с, 1H), (60 мг, 0,20 ммоль, 40%, бежевое твердое вещество, т.пл.=101-104°C).
Пример 28
1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперазин-1-ил)этил)-1H-индазол (28)

1H ЯМР (300 МГц, CDCl3): δ 1,44 (м, 1H), 1,71 (м, 2H), 1,98 (м, 3Н), 2,55-2,85 (м, 9H), 3,29 (ушир, с, 4H), 6,83-6,95 (м, 3Н), 7,25 (м, 2H), 7,35 (дд, J=8,8 Гц, J'=2,5 Гц, 1H), 7,49 (м, 1H), 7,53 (с, 1H), 7,64 (д, J=2,5 Гц, 1H), (75 мг, 0,16 ммоль, 47%, масло).
Пример 29
1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперазин-1-ил)этил)-1H-индазола оксалат (29)

(50 мг, 0,09 ммоль, 60%, белое твердое вещество, т.пл.=183-184°C).
Пример 30
1,4,5,6-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенилциклопента[c]пиразол (30)
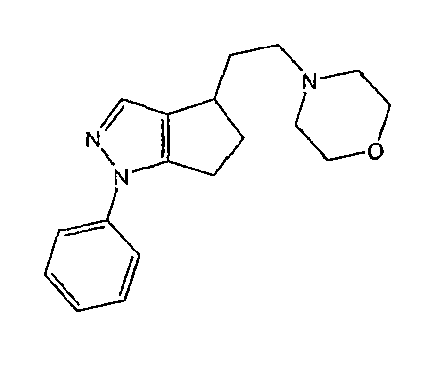
1H ЯМР (300 МГц, CDCl3): δ 1,82 (м, 2H), 2,25 (м, 1H), 2,59 (м, 6H), 2,80 (м, 1H), 2,89-3,12 (м, 3Н), 3,80 (ушир.с, 4H), 7,23 (м, 1H), 7,37 (с, 1H), 7,41 (м, 2H), 7,61 (д, J=8,2 Гц, 2H), (114 мг, 0,38 ммоль, 72%, масло).
Пример 31
1,4,5,6-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенилциклопента[c]пиразола оксалат (31)

(98 мг, 0,25 ммоль, 71%, бежевое твердое вещество, т.пл.=159,0-161,8).
Пример 32
4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперазин-1-ил)этил)-1H-индазол (32)

1H ЯМР (300 МГц, CDCl3): δ 1,44 (м, 1Н), 1,62-1,78 (м, 2Н), 1,99 (м, 3Н), 2,58 (м, 2H), 2,63-2,75 (м, 6H), 2,80 (м, 1H), 3,23 (м, 4H), 6,85 (т, J=7,3 Гц, 1H), 6,94 (д, J=8,8 Гц, 2H), 7,23-7,34 (м, 3H), 7,40-7,52 (м, 4H), 7,55 (с, 1H), (160 мг, 0,41 ммоль, 36%, масло).
Пример 33
4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперазин-1-ил)этил)-1H-индазола оксалат (33)

(150 мг, 0,31 ммоль, 76%, белое твердое вещество, т.пл.=177-180°C).
Пример 34
2-(2-(1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол-4-ил)этил)изоиндолин (34)

1H ЯМР (300 МГц, CDCl3): δ 1,97 (м, 2H), 2,30 (м, 1H), 2,85 (м, 1H), 3,01 (м, 4H), 3,17 (м, 1H), 4,16 (с, 4H), 7,23 (с, 5H), 7,23 (с, 1H), 7,42 (м, 2H), 7,63 (д, J=7,8 Гц, 2H), (93 мг, 0,28 ммоль, 70%, масло).
Пример 35
2-(2-(1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол-4-ил)этил)изоиндолина оксалат (35)

(35 мг, 0,08 ммоль, 33%, сероватое твердое вещество, т.пл.=195-197°C).
Пример 36
1,4,5,6-тетрагидро-1-фенил-4-(2-(4-фенилпиперидин-1-ил)этил)циклопента[c]пиразол (36)

1H ЯМР (300 МГц, CDCl3): δ 1,63 (м, 2H), 1,90-2,18 (м, 3Н), 2,35 (м, 2H), 2,52-3,20 (м, 9H), 3,69 (м, 2H), 7,20-7,46 (м, 9H), 7,61 (д, J=7,8 Гц, 2H), (41,8 мг, 0,11 ммоль, 27%, бежевое твердое вещество, т.пл.=83-86°C).
Пример 37
1,4,5,6-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этил)циклопента[c]пиразол (37)

1H ЯМР (300 МГц, CDCl3): δ 1,49 (м, 2H), 1,70 (м, 4H), 1,86 (м, 2H), 2,24 (м, 1H), 2,56 (м, 6H), 2,79 (м, 1H), 2,90-3,10 (м, 3H), 7,23 (м, 1H), 7,37 (с, 1H), 7,41 (м, 2H), 7,62 (д, J=7,9 Гц, 2H), (14 мг, 0,05 ммоль, 10%, оранжевое твердое вещество, т.пл.=213-219°C).
Пример 38
1,4,5,6-тетрагидро-1-фенил-4-(2-(4-фенилпиперазин-1-ил)этил)циклопента[c]пиразол (38)

1H ЯМР (300 МГц, CDCl3): δ 1,82 (м, 2H), 2,24 (м, 1H), 2,58 (м, 2H), 2,68 (м, 4H), 2,80 (м, 1H), 2,90-3,20 (м, 3H), 3,24 (м, 4H), 6,86 (м, 1H), 6,94 (д, J=8,1 Гц, 2H), 7,22-7,30 (м, 3H), 7,40 (с, 1H), 7,42 (м, 2H), 7,63 (д, J=8,1 Гц, 2H), (65 мг, 0,17 ммоль, 32%, бежевое твердое вещество, т.пл.=82,5-83,5°C).
Пример 39
1,4,5,6-тетрагидро-1-фенил-4-(2-(пирролидин-1-ил)этил)циклопента[c]пиразол (39)

1H ЯМР (300 МГц, CDCl3): δ 1,84 (м, 6H), 3,25 (м, 1H), 2,65 (м, 6H), 2,79 (м, 1H), 2,90-3,12 (м, 3H), 7,23 (м, 1H), 7,38 (с, 1H), 7,42 (м, 2H), 7,62 (д, J=7,8 Гц, 2H), (55 мг, 0,20 ммоль, 38%, масло).
Пример 40
1,4,5,6-тетрагидро-1-фенил-4-(2-(пирролидин-1-ил)этил)циклопента[c]пиразола оксалат (40)

(21,5 мг, 0,06 ммоль, 33%, белое твердое вещество, т.пл.=134,2-136°C).
Пример 41
4-(2-(4-бензилпиперазин-1-ил)этил)-1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол (41)

1H ЯМР (300 МГц, CDCl3): δ 1,76 (м, 2H), 2,22 (м, 1H), 2,38-2,65 (м, 10), 2,78 (м, 1H), 2,90-3,10 (м, 3H), 3,52 (с, 2H), 7,18-7,39 (м, 6H), 7,41 (с, 1H), 7,44 (м, 2H), 7,62 (д, J=7,8 Гц, 2H), (124 мг, 0,33 ммоль, 62%, масло).
Пример 42
4-(2-(4-бензилпиперазин-1-ил)этил)-1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразола диоксалат (42)

(149 мг, 0,26 ммоль, 87%, белое твердое вещество, т.пл.=215-218°C).
Пример 43
1,2,3,4-тетрагидро-2-(2-(1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол-4-ил)этил)изохинолин (43)

1H ЯМР (300 МГц, CDCl3): δ 1,86 (м, 2H), 2,28 (м, 1H), 2,65 (м, 2H), 2,70-3,18 (м, 8H), 3,66 (с, 2H), 7,03 (м, 1H), 7,11 (м, 3H), 7,23 (м, 1H), 7,41 (м, 3H), 7,63 (д, J=7,8 Гц, 2H), (73 мг, 0,21 ммоль, 39%, масло).
Пример 44
1,2,3,4-тетрагидро-2-(2-(l,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол-4-ил)этил)изохинолина оксалат (44)

(47,9 мг, 0,11 ммоль, 58%, бежевое твердое вещество, т.пл.=200,5-203,0°C).
Пример 45
4-(2-(1H-имидазол-1-ил)этил)-1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол (45)

1H ЯМР (300 МГц, CDCl3): δ 2,04 (м, 2H), 2,22 (м, 1H), 2,81 (м, 1H), 2,90-3,10 (м, 3H), 4,09 (м, 2H), 6,96 (с, 1H), 7,09 (с, 1H), 7,25 (м, 1H), 7,38 (с, 1H), 7,42 (м, 2H), 7,62 (м, 3H), (65,8 мг, 0,24 ммоль, 44%, оранжевое твердое вещество, т.пл.=102,9-105,7°C).
Пример 46
цис-1,4,5,6-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1-фенилциклопента[c]пиразол (46)

1H ЯМР (300 МГц, CDCl3): δ 1,17 (д, J=5,9 Гц, 6H), 1,78 (м, 4H), 2,23 (м, 1H), 2,48 (м, 2H), 2,82 (м, 3H), 3,02 (м, 3H), 3,74 (м, 2H), 7,23 (м, 1H), 7,38 (с, 1H), 7,42 (м, 2H), 7,62 (д, J=7,7 Гц, 2H), (220 мг, 0,68 ммоль, 64%, масло).
Пример 47
цис-1,4,5,6-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1-фенилциклопента[c]пиразола оксалат (47)

(193 мг, 0,46 ммоль, 68%, белое твердое вещество, т.пл.=160,2-161,5°C).
Пример 48
цис-4,5,6,7-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1-фенил-1H-индазол (48)

1H ЯМР (300 МГц, CDCl3): δ 1,70 (д, J=6,3 Гц, 6H), 1,42 (м, 1H), 1,56-1,84 (м, 4H), 1,94 (м, 3H), 2,51 (м, 2H), 2,62-2,90 (м, 5H), 3,74 (м, 2H), 7,30 (м, 1H), 7,40-7,52 (м, 5H), (200 мг, 0,59 ммоль, 51%, масло).
Пример 49
цис-4,5,6,7-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1-фенил-1H-индазола оксалат (49)

(150 мг, 0,35 ммоль, 61%, белое твердое вещество, т.пл.=186,6-190,0°C).
Пример 50
1,4,5,6-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-l(3H),4'-пиперидин]-1'-ил]этил)циклопента[c]пиразол (50)

1H ЯМР (300 МГц, CDCl3): δ 1,60-1,92 (м, 4H), 2,00 (м, 2H), 2,24 (м, 1Н), 2,43 (м, 2H), 2,57 (м, 2H), 2,70-3,12 (м, 6H), 5,06 (с, 2H), 7,05-7,30 (м, 5H), 7,40 (м, 3H), 7,62 (д, J=7,6 Гц, 2H), (159 мг, 0,40 ммоль, 74%, масло).
Пример 51
1,4,5,6-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3H),4'-пиперидин]-1'-ил]этил)циклопента[c]пиразола оксалат (51)

(48,6 мг, 0,10 ммоль, 25%, белое твердое вещество, т.пл.=170,5-173,6°C).
Пример 52
N-бензил-2-(1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол-4-ил)-N-метилэтанамин (52)

1H ЯМР (300 МГц, CDCl3): δ 1,82 (м, 2H), 2,21 (м, 1H), 2,32 (ушир, с, 3H), 2,61 (м, 2H), 2,77 (м, 1H), 2,97 (м, 2H), 3,08 (м, 1H), 3,64 (м, 2H), 7,20-7,45 (м, 9H), 7,61 (д, J=7,8 Гц, 2H), (60 мг, 0,18 ммоль, 37%, масло).
Пример 53
Смесь диастереомеров 1,4,5,6-тетрагидро-1-фенил-4-(2-(3-фенилпиперидин-1-ил)этил)циклопента[c]пиразола (53)

(128 мг, 0,35 ммоль, 65%, масло).
Пример 54
N-бензил-2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)-N-метилэтанамин (54)

1H ЯМР (300 МГц, CDCl3): δ 1,39 (м, 1H), 1,67 (м, 2H), 1,93 (м, 3H), 2,29 (с, 3H), 2,60 (м, 2H), 2,69 (м, 2H), 2,81 (м, 1H), 3,59 (м, 2H), 7,20-7,53 (м, 11Н), (149,7 мг, 0,43 ммоль, 45%, масло).
Пример 55
4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1-фенил-1H-индазол (55)

1H ЯМР (300 МГц, CDCl3): δ 1,48 (м, 1Н), 1,62-1,909 (м, 2H), 1,92-2,15 (м, 3H), 2,72 (ушир.с, 2H), 2,83-3,05 (м, 3H), 4,09 (с, 4H), 7,16-7,39 (м, 5H), 7,40-7,60 (м, 5H), (201 мг, 0,59 ммоль, 62%, масло).
Пример 56
4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1-фенил-1H-индазола оксалат (56)
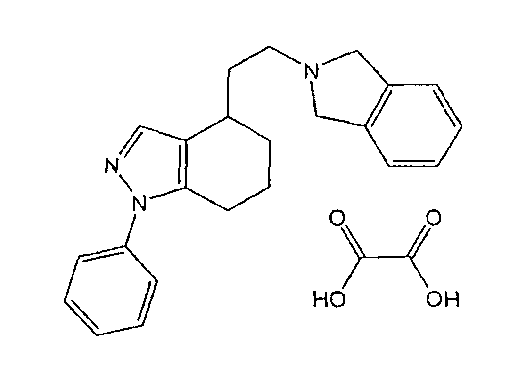
(146,9 мг, 0,34 ммоль, 60%, сероватое твердое вещество, т.пл.=195,7-200,0°C).
Пример 57
4,5,6,7-тетрагидро-1-метил-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазол (57)

1H ЯМР (300 МГц, CDCl3): δ 1,39 (м, 1H), 1,63-2,40 (м, 11H), 2,42-2,78 (м, 6H), 3,24 (м, 2H), 3,71 (с, 3H), 7,18-7,38 (м, 6H), (158 мг, 0,49 ммоль, 39%, белое твердое вещество, т.пл.=63-70°C).
Пример 58
4,5,6,7-тетрагидро-1-метил-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазола оксалат (58)
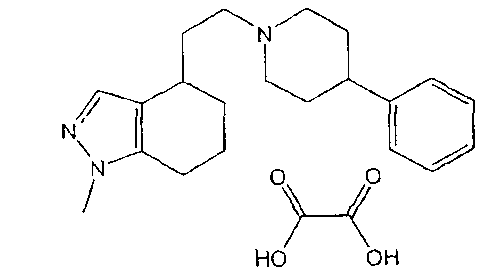
(77,5 мг, 0,19 ммоль, 40%, белое твердое вещество, т.пл.=117,3-120,5°C).
Пример 59
4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1-метил-1H-индазол (59)

1H ЯМР (300 МГц, CDCl3): δ 1,40 (м, 1H), 1,76 (м, 2H), 1,98 (м, 3H), 2,54 (ушир.с, 2H), 2,79 (м, 1H), 2,93 (м, 2H), 3,71 (с, 3H), 4,08 (м, 4H), 7,18-7,40 (м, 5H), (96,4 мг, 0,34 ммоль, 45%, масло).
Пример 60
4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1-метил-1H-индазола оксалат (60)

(51 мг, 0,14 ммоль, 45%, сероватое твердое вещество, т.пл.=150-151°C).
Пример 61
N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1H-индазол-4-ил)-N-метилэтанамин (61)

1H ЯМР (300 МГц, CDCl3): δ 1,30 (м, 1H), 1,68 (м, 2H), 1,92 (м, 3Н), 2,27 (с, 3H), 2,42-2,62 (м, 4H), 2,69 (м, 1H), 3,60 (м, 2H), 3,70 (с, 3H), 7,20-7,42 (м, 6H), (90,8 мг, 0,32 ммоль, 43%, масло).
Пример 62
N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1H-индазол-4-ил)-N-метилэтанамина оксалат (62)

(42,6 мг, 0,11 ммоль, 37%, белое твердое вещество, т.пл.=140,2-141,7°C).
Пример 63
4,5,6,7-тетрагидро-1-метил-4-(2-(морфолин-4-ил)этил)-1H-индазол (63)

1H ЯМР (300 МГц, CDCl3): δ 1,35 (м, 1H), 1,65 (м, 2H), 1,92 (м, 3H), 2,42-2,60 (м, 8H), 2,66 (м, 1H), 3,71 (с, 3H), 3,75 (м, 4H), 7,27 (с, 1H), (60,8 мг, 0,24 ммоль, 32%, масло).
Пример 64
4,5,6,7-тетрагидро-1-метил-4-(2-(морфолин-4-ил)этил)-1H-индазола оксалат (64)

(22 мг, 0,06 ммоль, 30%, белое твердое вещество, т.пл.=137,7-139,3°C).
Пример 65
1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1H-индазол (65)

1H ЯМР (300 МГц, CDCl3): δ 1,43 (м, 1H), 1,69 (м, 2H), 1,94 (м, 3H), 2,52 (м, 6H), 2,65 (м, 2H), 2,77 (м, 1H), 3,75 (м, 4H), 7,13 (м, 2H), 7,44 (дд, J=9,2 Гц, J'=4,8 Гц, 2H), 7,50 (с, 1H), (84 мг, 0,25 ммоль, 46%, масло).
Пример 66
1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1H-индазола оксалат (66)

(67 мг, 0,16 ммоль, 70%, белое твердое вещество, т.пл.=148-151°C).
Пример 67
цис-1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1H-индазол (67)

1H ЯМР (300 МГц, CDCl3): δ 1,17 (д, J=6,3 Гц, 6H), 1,41 (м, 1H), 1,60-1,81 (м, 4H), 1,94 (м, 3Н), 2,48 (т, J=7,7 Гц, 2H), 2,65 (м, 2H), 2,71-2,86 (м, 3H), 3,71 (м, 2H), 7,13 (м, 2H), 7,44 (дд, J=9,1 Гц, J'=4,8 Гц, 2H), 7,50 (с, 1H), (114 мг, 0,32 ммоль, 59%, масло).
Пример 68
цис-1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1H-индазола оксалат (68)

(86 мг, 0,19 ммоль, 63%, белое твердое вещество, т.пл.=164-169°C).
Пример 69
N-бензил-2-(1-(4-фторфенил)-4,5,6,7-тетрагидро-1H-индазол-4-ил)-N-метилэтанамин (69)

1H ЯМР (300 МГц, CD3OD): δ 1,42 (м, 1H), 1,70 (м, 2H), 1,96 (м, 3H), 2,29 (с, 3H), 2,54-2,67 (м, 4H), 2,57 (м, 1H), 3,59-3,61 (АВ cистема, JAB=12,8 Гц, 2H), 7,21-7,40 (м, 7H), 7,43-7,56 (м, 3H), (100 мг, 0,28 ммоль, 52%, масло).
Пример 70
1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1H-индазол (70)

1H ЯМР (300 МГц, CDCl3): δ 1,48 (м, 1H), 1,74 (м, 2H), 2,00 (м, 3H), 2,67 (м, 2H), 2,82-2,94 (м, 3H), 4,00 (с, 4H), 7,13 (м, 2H), 7,21 (м, 4H), 7,46 (дд, J=8,9 Гц, J'=4,8 Гц, 2H), 7,55 (с, 1H), (117 мг, 0,32 ммоль, 59%, масло).
Пример 71
1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1H-индазола оксалат (71)

(55 мг, 0,12 ммоль, 40%, сероватое твердое вещество, т.пл.=176-179°C).
Пример 72
1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазол (72)

1H ЯМР (300 МГц, CDCl3): δ 1,47 (м, 1H), 1,71 (м, 1H), 1,80-2,95 (м, 16H), 3,41 (м, 2H), 7,13 (м, 2H), 7,20-7,38 (м, 5H), 7,44 (дд, J=9,1 Гц, J'=4,8 Гц, 2H), 7,51 (с, 1H), (65 мг, 0,16 ммоль, 30%, бежевое твердое вещество, т.пл.=93-94,5°C).
Хиральное разделение соединений примера 1
Разделение энантиомеров рацемического соединения 4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазола (пример 1) проводят путем хиральной полупрепаративной ВЭЖХ с использованием колонки Chiralpak AS с размером частиц 10 мкм размером 25×2 см от Daicel. Используемая мобильная фаза представляет собой н-гексан/этанол 95/5 об./об. при скорости потока 13 мл/мин. Данные соединений:
- 1-ый пик: время удержания = 11,5 мин (примеры 73 и 74).
Пример 73
(+)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазол
Масло, [альфа]D20 + 4,3 (c=1, CHCl3), ee>99,9%.
Пример 74
(+)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазола оксалат
102 мг, белое твердое вещество, т.пл.=175-176°C, [альфа]D20 + 1,7 (c=1, MeOH), ee 99,5%.
- 2-ой пик: время удержания = 13,2 мин (примеры 75 и 76).
Пример 75
(-)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазол
Масло, [альфа]D20 -5,8 (c=1, CHCl3), ee>98,4%.
Пример 76
(-)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазола оксалат
104 мг, белое твердое вещество, т.пл.=175-176°C, [альфа]D20 -1,3 (c=1, MeOH), ee>98,4%).
Пример 77
(E)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1H-индазола оксалат (77)
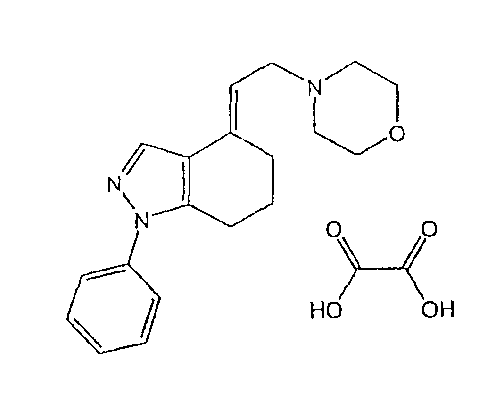
(127 мг, 0,32 ммоль, 16,7%, белое твердое вещество, т.з. (температура замерзания) = 156-157°C).
Пример 78
(E)-4,5,6,7-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этилиден)-1H-индазола оксалат (78)

(82 мг, 0,21 ммоль, 29,1%, белое твердое вещество, т.з.=188-189°C).
Пример 79
Синтез (E)-N-бензил-2-(6,7-дигидро-1-фенил-1H-индазол-4(5H)-илиден)-N-этилэтанамина (79)

Способ C
Стадия 1: синтез (E)-2-(1,5,6,7-тетрагидро-1-фенил-4H-индазол-4-илиден)ацетальдегида

Раствор 1M гидрида диизобутилалюминия в толуоле (0,7 мл, 0,7 ммоль) медленно добавляют к раствору (E)-2-(1,5,6,7-тетрагидро-1-фенил-4H-индазол-4-илиден)ацетонитрила (120 мг, 0,51 ммоль) в метиленхлориде (5 мл), охлажденному 0°C, и инкубируют при данной температуре в течение 3 часов, контролируя реакцию путем ТСХ. Добавляют воду и 0,5н раствор HCl и фильтруют нерастворимое твердое вещество. Смесь разбавляют в метиленхлориде и промывают водой и насыщенным раствором хлорида нaтрия. Фазу элиминируют при пониженном давлении и полученный в результате неочищенный продукт очищают посредством хроматографии на силикагеле с получением (E)-2-(1,5,6,7-тетрагидро-1-фенил-4H-индазол-4-илиден)ацетальдегида (74,5 мг, 0,31 ммоль, 61%, масло).
1H ЯМР (300 МГц, CDCl3): δ 2,02 (м, 2H), 2,91 (м, 2H), 3,05 (м, 2H), 6,31 (д, J=8,1 Гц, 1H), 7,35-7,55 (м, 5H), 7,93 (с, 1H), 10,11 (д, J=8,1 Гц, 1H).
Когда взаимодействие проводят со смесью E/Z-изомеров 2-(1,5,6,7-тетрагидро-1-фенил-4H-индазол-4-илиден)ацетонитрила, получают смесь E/Z-изомеров 2-(1,5,6,7-тетрагидро-1-фенил-4H-индазол-4-илиден)ацетальдегида.
Стадия 2: синтез (E)-N-бензил-2-(6,7-дигидро-1-фенил-1H-индазол-4(5H)-илиден)-N-метилэтанамина

Раствор (E)-2-(l,5,6,7-тетрагидро-1-фенил-4H-индазол-4-илиден)ацетальдегида (299 мг, 1,25 ммоль) и N-бензилметиламина (0,18 мл, 1,38 ммоль) в метаноле (20 мл), охлажденный до 0°C, оставляют перемешиваться в течение 20 минут. Затем добавляют цианоборгидрид натрия (213 мг, 3,39 ммоль) при 0°C и затем смеси дают нагреться до комнатной температуры, контролируя реакцию путем ТСХ. Растворитель упаривают при пониженном давлении, остаток разбавляют этилацетатом, промывают водой и насыщенным раствором хлорида натрия, сушат и упаривают при пониженном давлении. Полученный в результате неочищенный продукт очищают посредством хроматографии на силикагеле с получением (E)-N-бензил-2-(6,7-дигидро-1-фенил-1H-индазол-4(5H)-илиден)-N-метилэтанамина (158 мг, 0,46 ммоль, 36%, масло).
1H ЯМР (300 МГц, CDCl3): δ 1,87 (м, 2H), 2,27 (с, 3H), 2,45 (м, 2H), 2,81 (т, J=6,1 Гц, 2H), 3,23 (д, J=6,9 Гц, 2H), 3,59 (с, 2H), 5,88 (м, 1H), 7,20-7,50 (м, 10Н), 7,83 (с, 1H).
Когда взаимодействие проводят со смесью E/Z-изомеров 2-(1,5,6,7-тетрагидро-1-фенил-4H-индазол-4-илиден)ацетальдегида, получают смесь E/Z-изомеров N-бензил-2-(6,7-дигидро-1-фенил-1H-индазол-4(5H)-илиден)-N-метилэтанамин.
1H ЯМР (300 МГц, CDCl3): δ 1,87 (м, 2H), 2,27 (с, 3Н), 2,45 (м, 2H), 2,81 (т, J=6,1 Гц, 2H), 3,23 (д, J=6,9 Гц, 2H), 3,59 (с, 2H), 5,88 (м, 1H), 7,20-7,50 (м, 10Н), 7,83 (с, 1H), (158 мг, 0,46 ммоль, 26%, масло).
Пример 80
(E)-N-бензил-2-(6,7-дигидро-1-фенил-1H-индазол-4(5H)-илиден)-N-метилэтанамина оксалат (80)

(118 мг, 0,27 ммоль, 59%, т.з.=107-108°C, желтое твердое вещество).
Пример 81
(E)-4,5,6,7-тетрагидро-4-(2-(цис-2,6-диметилморфолин-4-ил)этилиден)-1-фенил-1H-индазол (81)

1H ЯМР (300 МГц, CDCl3): δ 1,17 (д, J=6,3 Гц, 6H), 1,80 (м, 4H), 2,48 (м, 2H), 2,84 (м, 4H), 3,19 (д, J=6,4 Гц, 2H), 3,77 (м, 2H), 5,82 (м, 1H), 7,35 (м, 1H), 7,46 (м, 4H), 7,83 (с, 1H), (84 мг, 0,25 ммоль, 15%, масло).
Пример 82
(E)-4,5,6,7-тетрагидро-4-(2-(цис-2,6-диметилморфолин-4-ил)этилиден)-1-фенил-1H-индазола оксалат (82)

(40 мг, 0,09 ммоль, 37%, т.з.=133-136°C, желтое твердое вещество).
Пример 83
(E)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(цис-2,6-диметилморфолино-4-ил)этилиден)-1H-индазол (83)

1H ЯМР (300 МГц, CDCl3): δ 1,15 (д, J=6,2 Гц, 6H), 1,87 (м, 4H), 2,45 (м, 2H), 2,75-2,93 (м, 4H), 3,21 (м, 2H), 3,79 (м, 2H), 5,81 (м, 1H), 7,35 (м, 1H), 7,49 (м, 1H), 7,62 (м, 1H), 7,81 (с, 1H), (95 мг, 0,23 ммоль, 72%, желтоватое масло).
Пример 84
(E)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(цис-2,6-диметилморфолино-4-ил)этилиден)-1H-индазола оксалат (84)
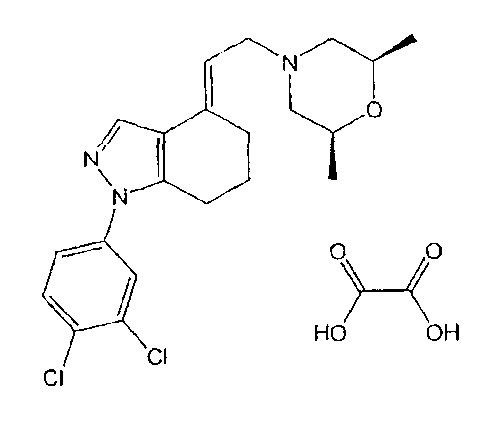
(59 мг, 0,12 ммоль, 51%, т.з.=129-130°C, белое твердое вещество).
Пример 85
(E)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(морфолино-4-ил)этилиден)-1H-индазол (85)

1H ЯМР (300 МГц, CDCl3): δ 1,89 (м, 2H), 2,40-2,63 (м, 6H), 2,81 (т, J=6,1 Гц, 2H), 3,21 (д, J=7,2 Гц, 2H), 3,78 (м, 4H), 5,82 (т, J=6,1 Гц, 1H), 7,35 (дд, J=8,6 Гц, J'=2,2 Гц, 1H), 7,52 (д, J=8,6 Гц, 1H), 7,64 (д, J=2,2 Гц, 1H), 7,81 (с, 1H), (97 мг, 0,26 ммоль, 79%, желтоватое масло).
Пример 86
(E)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(морфолино-4-ил)этилиден)-1H-индазола оксалат (86)

(66 мг, 0,14 ммоль, 54%, т.з.=170-172°C, белое твердое вещество).
Пример 87
(E)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(пиперидин-1-ил)этилиден)-1H-индазол (87)

(42 мг, 0,11 ммоль, 48%, желтоватое масло).
Пример 88
(E)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(пиперидин-1-ил)этилиден)-1H-индазола оксалат (88)

1H ЯМР (300 МГц, CD3OD): δ 1,40-2,05 (м, 8H), 2,62 (м, 2H), 2,88-3,10 (м, 4H), 3,53 (м, 2H), 3,90 (д, J=7,6 Гц, 2H), 5,86 (м, 1H), 7,51 (дд, J=8,6 Гц, J'=2,3 Гц, 1H), 7,70 (д, J=8,6 Гц, 1H), 7,78 (д, J=2,3 Гц, 1H), 8,01 (с, 1H), (12 мг, 0,03 ммоль, 16%, т.з.=100-102°C, белое твердое вещество).
Пример 89
(E)-4-(2-(N,N-диэтиламино)этилиден)-4,5,6,7-тетрагидро-1-фенил-1H-индазол (89)
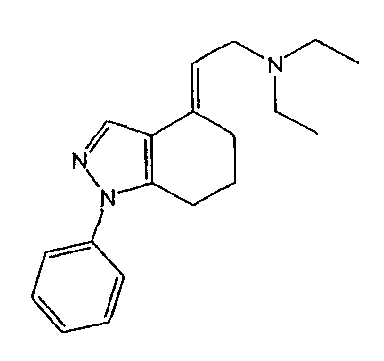
1H ЯМР (300 МГц, CDCl3): δ 1,14 (т, J=7,2 Гц, 6H), 1,89 (м, 2H), 2,49 (м, 2H), 2,67 (кв, J=7,2 Гц, 4H), 2,82 (т, J=6,0 Гц, 2H), 3,36 (д, J=7,0 Гц, 2H), 5,83 (т, J=7,0 Гц, 1H), 7,32 (м, 1H), 7,40-7,50 (м, 4H), 7,83 (с, 1H), (68,8 мг, 0,23 ммоль, 27,7%, масло).
Пример 90
(E)-4-(2-(N,N-диэтиламино)этилиден)-4,5,6,7-тетрагидро-1-фенил-1H-индазола оксалат (90)

(34,2 мг, 0,09 ммоль, 10,6%, т.з.=163-164°C, желтоватое твердое вещество).
Пример 91
(E)-4-(2-(4-циклогексилпиперазин-1-ил)этилиден)-4,5,6,7-тетрагидро-1-фенил-1H-индазол (91)

1H ЯМР (300 МГц, CDCl3): δ 1,05-1,32 (м, 5Н), 1,58-2,01 (м, 7Н), 2,30 (м, 1Н), 2,40-2,75 (м, 10Н), 2,81 (т, J=6,0 Гц, 2Н), 3,17 (д, J=7,3 Гц, 2Н), 5,83 (т, J=7,3 Гц, 1Н), 7,33 (м, 1Н), 7,47 (м, 4Н), 7,81 (с, 1Н), (81 мг, 0,21 ммоль, 25%, т.з.=124-130°C, желтоватое твердое вещество).
Пример 92
(E)-4,5,6,7-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этилиден)-1-фенил-1H-индазол (92)

1H ЯМР (300 МГц, CDCl3): δ 0,93 (д, J=6,0 Гц, 3Н), 1,28 (м, 3Н), 1,65 (м, 2Н), 1,82-2,03 (м, 4Н), 2,47 (м, 2Н), 2,81 (т, J=6,1 Гц, 2Н), 2,97 (м, 2Н), 3,14 (д, J=7,2 Гц, 2Н), 5,86 (т, J=7,2 Гц, 1Н), 7,53 (м, 1Н), 7,40-7,50 (м, 4Н), 7,82 (с, 1Н), (30 мг, 0,09 ммоль, 11%, т.з.=83-90°C, белое твердое вещество).
Пример 93
Синтез 4,5,6,7-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенил-1H-индазола (93)

Способ E
Pd-C (100 мг, 20%) добавляют к раствору смеси E/Z-изомеров 4,5,6,7-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этилиден)-1-фенил-1H-индазола (324 мг, 1,01 ммоль) в 75 мл EtOH и полученный в результате раствор перемешивают в атмосфере азота (45 фунтов на кв.дюйм) в гидрогенизаторе Парра в течение 18 часов. Реакционную смесь очищают азотом, фильтруют через целит и растворитель упаривают при пониженном давлении. Полученный в результате неочищенный продукт очищают посредством хроматографии на силикагеле с получением 4,5,6,7-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенил-1H-индазола (130 мг, 0,40 ммоль, 40%, масло).
1H ЯМР (300 МГц, CDCl3): δ 1,00 (д, J=6,3 Гц, 3Н), 1,40-2,25 (м, 11H), 2,50 (м, 2H), 2,69 (м, 2H), 2,80-3,00 (м, 3Н), 3,40 (м, 2H), 7,33 (м, 1H), 7,46 (м, 4H), 7,49 (с, 1H).
1H ЯМР (300 МГц, CDCl3): δ 1,00 (д, J=6,3 Гц, 3Н), 1,40-2,25 (м, 11H), 2,50 (м, 2H), 2,69 (м, 2H), 2,80-3,00 (м, 3Н), 3,40 (м, 2H), 7,33 (м, 1H), 7,46 (м, 4H), 7,49 (с, 1H), (130 мг, 0,40 ммоль, 40%, масло).
Пример 94
4,5,6,7-Тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенил-1H-индазола оксалат (94)

(55 мг, 0,13 ммоль, 33%, т.з.=201-203°C, бежевое твердое вещество).
Пример 95
1,4,5,6-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этил)циклопента[c]пиразола оксалат (95)

(75 мг, 0,19 ммоль, 68%, т.з.=166-169°C, бежевое твердое вещество).
Пример 96
1,4,5,6-тетрагидро-1-фенил-4-[2-(тиоморфолин-4-ил)этил]циклопента[c]пиразол (96)

1H ЯМР (300 МГц, CDCl3): δ 1,77 (м, 2H), 2,23 (м, 1Н), 2,54 (м, 2H), 2,65-2,90 (м, 9H), 3,01 (м, 3Н), 7,24 (м, 1H), 7,37 (с, 1H), 7,42 (м, 2H), 7,62 (д, J=8,5 Гц, 2H), (71 мг, 0,23 ммоль, 56%, масло).
Пример 97
1,4,5,6-тетрагидро-1-фенил-4-[2-(тиоморфолин-4-ил)этил]циклопента[c]пиразола оксалат (97)

(48 мг, 0,12 ммоль, 52%, т.з.=168-172°C, сероватое твердое вещество).
Пример 98
1,4,5,6-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенилциклопента[c]пиразол (98)
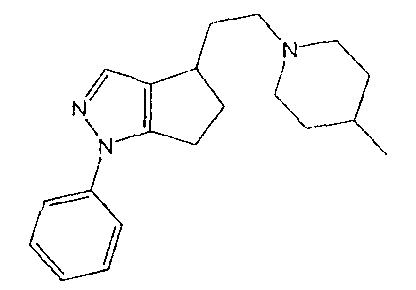
1H ЯМР (300 МГц, CDCl3): δ 0,93 (д, J=5,9 Гц, 3Н), 1,35 (м, 3H), 1,65 (м, 2H), 1,80 (м, 2H), 1,99 (м, 2H), 2,24 (м, 1H), 2,49 (м, 2H), 2,80 (м, 1H), 3,01 (м, 5H), 7,23 (м, 1H), 7,38 (с, 1H), 7,42 (м, 2H), 7,62 (д, J=8,2 Гц, 2H), (58 мг, 0,19 ммоль, 46%, т.з.=78-82°C, бежевое твердое вещество).
Пример 99
1,4,5,6-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенилциклопента[c]пиразола оксалат (99)

(45 мг, 0,11 ммоль, 58%, т.з=198-206°C, сероватое твердое вещество).
Пример 100
1,4,5,6-тетрагидро-4-(2-(4-метилпиперазин-1-ил)этил)-1-фенилциклопента[c]пиразол (100)

1H ЯМР (300 МГц, CDCl3): δ 1,76 (м, 2H), 2,25 (м, 1H), 2,30 (с, 3Н), 2,38-2,70 (м, 10Н), 2,80 (м, 1H), 3,01 (м, 3Н), 7,23 (м, 1H), 7,38 (с, 1H), 7,42 (м, 2H), 7,72 (д, J=7,6 Гц, 2H), (30 мг, 0,10 ммоль, 24%, т.з.=80-86°C, бежевое твердое вещество).
Пример 101
4-(2-(4-циклогексилпиперазин-1-ил)этил)-1,4,5,6-тетрагидро-1-фенилциклопента[c]пиразол (101)

1H ЯМР (300 МГц, CDCl3): δ 1,06-1,30 (м, 5H), 1,58-1,98 (м, 7H), 2,24 (м, 2H), 2,40-2,85 (м, 11H), 3,00 (м, 3H), 7,23 (м, 1H), 7,38 (с, 1H), 7,42 (м, 2H), 7,63 (м, 2H), (35 мг, 0,09 ммоль, 22%, т.з.=81-84°C, бежевое твердое вещество).
Пример 102
Синтез 4-(2-(азепан-1-ил)этил)-4,5,6,7-тетрагидро-1-фенил-1H-индазола (102)
Способ F
Стадия 1: синтез 2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)уксусной кислоты

LiOH·H2O (120 мг, 2,85 ммоль), растворенный в 1 мл воды, добавляют к раствору этил-2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)ацетата (808 мг, 2,85 ммоль) в метаноле (20 мл) и перемешивают при комнатной температуре в течение 1 часа, контролируя реакцию посредство ТСХ. Метанол упаривают при пониженном давлении, остаток суспендируют в воде и подкисляют разбавленной HCl с образованием массы, которую экстрагируют этилацетатом. Органическую фазу промывают водой, сушат и упаривают при пониженном давлении с получением 2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)уксусной кислоты (410 мг, 1,59 ммоль, 53%, твердое вещество).
1H ЯМР (300 МГц, CDCl3): δ 1,51 (м, 1H), 1,76 (м, 1H), 1,85-2,11 (м, 2H), 2,51 (дд, J=15,7 Гц, J'=8,1 Гц, 1H), 2,65-2,80 (м, 3H), 3,27 (м, 1H), 7,34 (м, 1H), 7,47 (м, 4H), 7,60 (с, 1H).
Стадия 2: синтез 1-(2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)ацетил)азепана

CDI (63,2 мг, 0,39 ммоль) добавляют к раствору 2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)уксусной кислоты (100 мг, 0,39 ммоль) в CH2Cl2 (20 мл), охлаждают на ледяной бане и нагревают до 45°C в течение 2,5 часов. Затем смесь охлаждают до 0°C и добавляют азациклогептан (38,7 мг, 0,39 ммоль), и нагревают при 45°C в течение 1 часа. Растворитель упаривают при пониженном давлении, остаток растворяют в AcOEt и промывают разбавленной HCl. Органическую фазу сушат и упаривают при пониженном давлении. Полученный в результате неочищенный продукт очищают посредством хроматографии на силикагеле с получением 1-(2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)ацетил)азепана (45 мг, 0,13 ммоль, 33%, масло).
1H ЯМР (300 МГц, CDCl3): δ 1,45 (м, 1H), 1,52-1,81 (м, 9H), 1,92 (м, 1H), 2,08 (м, 1H), 2,47 (дд, J=15,2 Гц, J'=7,6 Гц, 1H), 2,61-2,75 (м, 3H), 3,42 (м, 3H), 3,59 (м, 2H), 7,34 (м, 1H), 7,46 (м, 4H), 7,57 (с, 1H).
Стадия 3: синтез 4-(2-(азепан-1-ил)этил)-4,5,6,7-тетрагидро-1-фенил-1H-индазола

Раствор 1-(2-(4,5,6,7-тетрагидро-1-фенил-1H-индазол-4-ил)ацетил)азепана (60 мг, 0,18 ммоль) в безводном THF (2 мл) медленно добавляют к суспензии LiAlH4 (20 мг, 0,53 ммоль) в безводном THF (10 мл), охлажденной до 0°C. Смесь кипятят с обратным холодильником в течение 3 часов, контролируя реакцию путем ТСХ. Смесь охлаждают и добавляют воду и раствор NaOH, осадок фильтруют и промывают AcOEt. Органическую фазу отделяют, промывают водой и сушат с получением 4-(2-(азепан-1-ил)этил)-4,5,6,7-тетрагидро-1-фенил-1H-индазола (36 мг, 0,11 ммоль, 63%, масло).
1H ЯМР (300 МГц, CDCl3): δ 1,60-2,05 (м, 14H), 2,60-2,92 (м, 9H), 7,30 (м, 1H), 7,40-7,50 (м, 4H), 7,53 (с, 1H).
Пример 103
N-бензил-2-(1-трет-бутил-4,5,6,7-тетрагидро-1H-индазол-4-ил)-N-метилэтанамин (103)

1H ЯМР (300 МГц, CDCl3): δ 1,29 (м, 1H), 1,50-2,05 (м, 14H, (δ=1,60, с, 9H)), 2,26 (ушир, с, 3H), 2,45-2,90 (м, 5H), 3,59 (м, 2H), 7,20-7,43 (м, 6H).
Пример 104
1-трет-бутил-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазол (104)

1H ЯМР (300 МГц, CDCl3): δ 1,37 (м, 1H), 1,48-2,35 (м, 20H, (δ= 1,60, с, 9H)), 2,50-2,90 (м, 6H), 3,21 (м, 2H), 7,18-7,38 (м, 6H).
Пример 105
1-трет-бутил-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазола оксалат (105)

(36 мг, 0,08 ммоль, 37%, т.з.=122-124°C, белое твердое вещество).
Хиральное разделение соединений примера 61
Хиральное разделение рацемического N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1H-индазол-4-ил)-N-метилэтанамина (61) (257 мг) проводят путем хиральной полупрепаративной ВЭЖХ с использованием колонки Chiralpak AD-H с размером гранул 5 мкм размером 25×2 см от Daicel. Использованная мобильная фаза состояла из н-гексана/этанола/диэтиламина (90/10/0,2, об./об./об.) при потоке 17 мл/мин. Данные соединений:
1-ый пик: время удержания = 9,7 мин (соединение 106).
Пример 106
(-)-N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1H-индазол-4-ил)-N-метилэтанамин
97,1 мг, масло, [альфа]D20 - 9,1 (c=1, MeOH), ee (избыток энантиомера)>99,9%.
2-ой пик: время удержания = 12,9 мин (соединение 107).
Пример 107
(+)-N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1H-индазол-4-ил)-N-метилэтанамин
96,9 мг, масло, [альфа]D20 + 8,2 (c=1, MeOH), ee (избыток энантиомера)>99,9%.
Пример 108
N-(2-(4,5,6,7-тетрагидро-1-метил-1H-индазол-4-ил)этил)-N-метилциклогексанамин (108)

1H ЯМР (300 МГц, CDCl3): δ 1,03-1,40 (м, 6H), 1,55-2,03 (м, 10Н), 2,34 (с, 3H), 2,43-2,58 (м, 3H), 2,60-2,73 (м, 3H), 3,71 (с, 3H), 7,28 (с, 1H), (155 мг, 0,56 ммоль, 77%, масло).
Пример 109
4,5,6,7-тетрагидро-4-(2-(4-гидрокси-4-фенилпиперидин-1-ил)этил)-1-метил-1H-индазол (109)

1H ЯМР (300 МГц, CDCl3): δ 1,40 (м, 1H), 1,50-2,10 (м, 9H), 2,40-3,20 (м, 9H), 3,71 (с, 3H), 7,28 (м, 2H), 7,36 (м, 2H), 7,52 (м, 2H), (44 мг, 0,13 ммоль, 18%, т.з.=130-135°C, оранжевое твердое вещество).
Пример 110
4,5,6,7-тетрагидро-1-метил-4-(2-(4-фенилпиперидин-1-ил)этил)-1H-индазол (110)

1H ЯМР (300 МГц, CDCl3): δ 1,37 (м, 1H), 1,60-2,20 (м, 11H), 2,54 (м, 5H), 2,67 (м, 1H), 3,10 (м, 2H), 3,72 (с, 3H), 6,97 (м, 2H), 7,18 (м, 2H), 7,30 (с, 1H), (135 мг, 0,40 ммоль, 54%, т.з.= 47-54°C, оранжевый цвет).
Пример 111
N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1H-индазол-4-ил)-N-метилэтанамин (111)
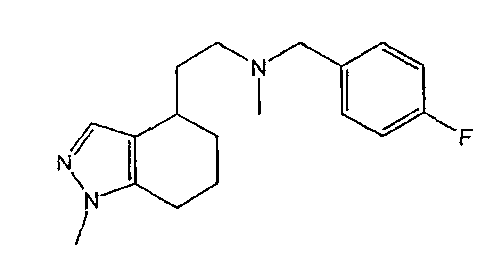
1H ЯМР (300 МГц, CDCl3): δ 1,30 (м, 1H), 1,50-2,02 (м, 5H), 2,27 (ушир.с, 3H), 2,40-2,72 (м, 5H), 3,56 (м, 2H), 3,71 (с, 3H), 7,02 (т, J=8,6 Гц, 2H), 7,23 (с, 1H), 7,34 (м, 2H), (68 мг, 0,23 ммоль, 31%, масло).
Пример 112
4,5,6,7-тетрагидро-1-метил-4-(2-[спиро]изобензофуран-1(3H),4'-пиперидин]-1'-ил]этил)-1H-индазол (112)

1H ЯМР (300 МГц, CDCl3): δ 1,38 (м, 1H), 1,42-2,10 (м, 9H), 2,40-2,80 (м, 7H), 3,04 (м, 2H), 3,72 (с, 3H), 5,07 (с, 2H), 7,17-7,37 (м, 5H), (154 мг, 0,44 ммоль, 60%, т.з.=95-100°C, бежевое твердое вещество).
ПРИМЕРЫ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ
Некоторые репрезентативные соединения по изобретению тестировали на их активность в качестве ингибиторов сигма (сигма-1 и сигма-2). При этом использовали следующие протоколы.
Сигма-1
Получение мембраны головного мозга и анализы связывания для σ-1-рецептора проводили, как описано (DeHaven-Hudkins et al., 1992), с некоторыми модификациями. В кратком изложении, препараты головного мозга морских свинок гомогенизировали в 10 объемах (масс./об.) Tris-HCl 50 мМ, 0,32 M сахарозы, pH 7,4, в устройстве Kinematica Polytron PT 3000 при 15000 об/мин в течение 30 с. Гомогенат центрифугировали при 1000×g в течение 10 мин при 4°C, и надосадочную жидкость собирали и центрифугировали опять при 48000×g в течение 15 мин при 4°C. Осадок ресуспендировали в 10 объемах буфера Tris-HCl (50 мМ, pH 7,4), инкубировали при 37°C в течение 30 мин и центрифугировали при 48000×g в течение 20 мин при 4°C. После этого осадок ресуспендировали в свежем буфере Tris-HCl (50 мМ, pH 7,4) и хранили на льду до применения.
Каждая пробирка для анализа содержала 10 мкл [3H](+)-пентазоцина (конечная концентрация 0,5 нМ), 900 мкл суспензии ткани до конечного объема анализа 1 мл и конечной концентрации ткани, примерно равной 30 мг массы нетто ткани/мл. Неспецифичное связывание определяли путем добавления конечной концентрации 1 мкМ галоперидола. Все пробирки инкубировали при 37°C в течение 150 мин перед окончанием взаимодействия путем быстрой фильтрации через стекловолоконный фильтр Schleicher & Schuell GF 3362 [предварительно вымоченный в растворе 0,5% полиэтиленимина в течение, по меньшей мере, 1 ч]. Затем фильтры промывали четыре раза 4 мл холодного буфера Tris-HCl (50 мМ, pH 7,4). После добавления сцинтилляционного коктейля образцам позволяли уравновешиваться в течение ночи. Количество связанной радиоактивности определяли путем жидкостной сцинтилляционной спектрометрии с использованием жидкостного сцинтилляционного счетчика Wallac Winspectral 1414. Концентрации белка определяли способом Lowry et al. (1951).
Ссылки
DeHaven-Hudkins, D. L., L.C. Fleissner, and F. Y. Ford-Rice, 1992, "Characterization of the binding of [3H](+)pentazocine to σ recognition sites in guinea pig brain", Eur. J. Pharmacol 227, 371-378.
Lowry, O.H., N.J. Rosebrough, A.L. Farr, and R.J. Randall, 1951, Protein measurement with the Folin phenol reagent, J. Biol. Chem, 193, 265.
Сигма-2
Исследования связывания с σ2-рецептором проводили, как описано (Radesca et al., 1991), с некоторыми модификациями. В кратком изложении, препараты головного мозга от нокаут-мышей по сигма-рецептору I типа (сигма-1) гомогенизировали в объеме 10 мл/г массы нетто ткани ледяного 10 мМ Tris-HCl, pH 7,4, содержащего 320 мМ сахарозы (Tris-сахарозный буфер) в гомогенизаторе Potter-Elvehjem (10 импульсов при 500 об/мин). Гомогенаты центрифугировали при 1000×g в течение 10 мин при 4°C, и надосадочную жидкость сохраняли. Осадок ресуспендировали перемешиванием на вортексе 2 мл/г ледяного Tris-сахарозного буфера и опять центрифугировали при 1000×g в течение 10 мин. Объединенные препараты надосадочной жидкости после центрифугирования при 1000×g центрифугировали при 31000×g в течение 15 мин при 4°C. Осадки ресуспендировали перемешиванием на вортексе в 3 мл/г 10 мM Tris-HCl, pH 7,4, и суспензию инкубировали при 25°C в течение 15 мин. После центрифугирования при 31000×g в течение 15 мин осадки ресуспендировали путем осторожной гомогенизации на устройстве Potter Elvehjem до объема 1,53 мл/г в 10 мМ Tris-HCl, pH 7,4.
Пробирки для анализа содержали 10 мкл [3H]-DTG (конечная концентрация 3 нМ), 400 мкл суспензии ткани (5,3 мл/г в 50 мМ Tris-HCl, pH 8,0) до конечного объема анализа 0,5 мл. Неспецифичное связывание определяли путем добавления конечной концентрации 1 мкМ галоперидола. Все пробирки инкубировали при 25°C в течение 120 мин перед окончанием взаимодействия путем быстрой фильтрации через стекловолоконный фильтр Schleicher & Schuell GF 3362 [предварительно вымоченный в растворе 0,5% полиэтиленимина в течение, по меньшей мере, 1 ч]. Затем фильтры промывали три раза 5 мл холодного буфера Tris-HCl (10 мМ, pH 8,0). После добавления сцинтилляционного коктейля образцам позволяли уравновешиваться в течение ночи. Количество связанной радиоактивности определяли путем жидкостной сцинтилляционной спектрометрии с использованием жидкостного сцинтилляционного счетчика Wallac Winspectral 1414. Концентрации белка определяли способом Lowry et al. (1951).
Ссылки
Radesca, L., W.D. Bowen, and L. Di Paolo, B.R. de Costa, 1991, Synthesis and Receptor Binding of Enantiomeric N-Substituted cis-N-[2-(3,4-Dichlorophenyl)ethyl]-2-(1-pyrrolidinyl)ciclohexylamines as High-Affinity σ Receptor Ligands, J. Med. Chem. 34, 3065-3074.
Langa, F., Codony X., Tovar V., Lavado A., Gimenez E., Cozar P., Cantero M., Dordal A., Hernandez E., Perez R., Monroy X., Zamanillo D., Guitart X., Montoliu LL, 2003, Generation and phenotypic analisis of sigma receptor type I (Sigma 1) knockout mice, European Journal of Neuroscience, Vol.18, 2188-2196.
Lowry, O. H., N.J. Rosebrough, A.L. Fair, and RJ. Randall, 1951, Protein measurement with the Folin phenol reagent, J. Biol. Chem, 193, 265.
Некоторые из полученных результатов показаны ниже в таблице (I).


Воздействие на развитие механической аллодинии за счет капсаицина
В данной модели используются филаменты фон Фрея, и она предназначена для тестирования эффектов и симптомов невропатической боли, аллодинии, и т.д.
Интерес в данной модели состоит в следующем.
- Инъекция 1 мкг капсаицина экспериментальным животным вызывает острую боль с последующей гипералгезией/аллодинией.
- Механизмы, вовлеченные в индуцируемую капсаицином острую боль и гипералгезию, хорошо известны (в основном, это активация периферических ноцицепторов и сенситизация нейронов спинного мозга, соответственно).
На фиг.1 показан протокол для всех тестов с филаментами фон Фрея. После расселения мышей вначале, согласно фиг.1, обрабатывают тестируемым соединением (или растворителем в контролях). Затем 1 мкг капсаицина (1% DMSO) инъецируют в их лапу, в результате чего в ней развивается боль. Затем подвергавшуюся воздействию лапу обрабатывают механическим стимулом и измеряют время ожидания до того, как лапа отдергивается.
С использованием данного фармакологического теста было показано, что соединения из примеров 2, 58, 62 и 77 имеют четкий эффект против аллодинии. В дозировке 32 мг/кг достигалось облегчение боли, равное, по меньшей мере, 50%, в то время как соединение по примеру 58, как наиболее действенное, достигало 100% обезболивания в дозе 2 мг/кг.
Эффект всех 4 тестируемых соединений может отменяться применением 40 мг/кг PRE084 (хорошо известный сигма-агонист), доказывая, что наблюдаемый эффект является следствием связывания сигма.
Воздействие на развитие тепловой гипералгезии вследствие действия каррагинана
Некоторые соединения также оценивали на предмет антиноцицептивной активности в модели индуцированной каррагинаном тепловой гипералгезии на мышах. В данной модели через два часа после инъекции каррагинана в лапу для оценки тепловой гипералгезии использовали плантарный тест по способу, описанному Hargreaves et al. (1988). Соединения были из примеров 58 и 62.
На фиг.2 показан протокол для всех тестов, который показывает, что различие состоит в применении каррагинана вместо капсаицина и измерения Харгривза вместо филаментов фон Фрея. Оба соединения обладали в данной модели высокой активностью, при том, что соединение из примера 58 характеризовалось примерно 90% обезболиванием при 10 мг/кг и 60% при 2,5 мг/кг. Соединение из примера 62 характеризовалось 90% обезболиванием при 40 мг/кг, 75% при 10 мг/кг и 40% при 2,5 мг/кг.
Эффект обоих соединений мог отменяться применением 40 мг/кг PRE084.
Седалищный нерв
Кроме того, значительное ингибирование механической аллодинии также доказано для соединения из примера 62 при 30 мг/кг подкожно в модели частичного лигирования седалищного нерва (Seltzer et al., 1990) с невропатической болью у мышей. Тест фон Фрея применяли для оценки механической аллодинии через 11-13 суток после операции.
Ссылки
Hargreaves K, Dubner R, Brown F, Flores C, Joris J. “A new and sensitive method for measuring thermal nociception in cutaneous hyperalgesia." Pain 1988; 32:77-88.
Seltzer Z, Dubner R, Shir Y. "A novel behavioral model of neuropathic pain disorders produced in rats by partial sciatic nerve injury." Pain 1990; 43:205-218.
Реферат
Изобретение относится к новым соединениям, имеющим фармакологическую активность в отношении сигма-рецептора, и, более конкретно, к производным пиразола формулы (I), в которой радикалы и символы имеют значения, определенные в п.1 формулы изобретения; к способу получения этих соединений; к включающей их фармацевтической композиции и к их применению для производства лекарственного средства для лечения и профилактики заболевания или состояния, опосредованного сигма-рецептором, в частности для лечения психотического заболевания, такого как депрессия, тревожность или шизофрения, и невропатической или воспалительной боли, включая аллодинию и/или гипералгезию. 5 н. и 6 з.п. ф-лы, 2 ил., 1 табл.
Формула

в котором R1 выбран из группы, образованной алкилом, имеющим от 1 до 8 атомов углерода, 3-10-членным циклоалкилом и фенилом, необязательно незамещенным 1 или 2 атомами галогена;
R2 представляет собой водород;
R3 и R4 представляют собой водород;
R5 и R6 независимо выбраны из группы, образованной водородом, алкилом, имеющим от 1 до 8 атомов углерода, 3-10-членным циклоалкилом, фенилом, фенил(С1-С2алкилом), где фенил необязательно замещен галогеном; или R5 и R6 вместе образуют гетероциклил, имеющий от 5 до 7 атомов в кольце, который необязательно замещен 1 или 2 группами, независимо выбранными из C1-6алкила, гидрокси, фенила, необязательно замещенного галогеном, бензила, циклогексила, или незамещенного гетероциклила, имеющего от 5 до 7 атомов в кольце, необязательно сконденсированного с бензольным кольцом, или необязательно спироконденсированного с (3Н)-изобензофураном;
n выбран из 0 и 1;
m выбран из 1, 2, 3 и 4;
пунктирная линия ---- представляет собой простую или двойную связь;
или его фармацевтически приемлемая соль или изомер.
в частности морфолин-4-ил, 2,6-диметилморфолин-4-ил, пиперидин-1-ил, 4-фенилпиперидин-1-ил, 3-фенилпиперидин-1-ил, 4-бензилпиперазин-1-ил, 4-фенилпиперазин-1-ил, 2-[спиро[изобензофуран-1(3Н),4'-пиперидин]-1'-ил, азепан-1-ил, 1,2,3,4-тетрагидроизохинолин-2-ил, пирролидин-1-ил, 3-фенилпирролидин-1-ил, изоиндолин-2-ил или имидазол-1-ил.
4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазол,
4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1H-индазола оксалат,
1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1Н-индазол,
1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1Н-индазола оксалат,
(Е)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1Н-индазол,
1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1Н-индазол,
1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1Н-индазола оксалат,
4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперидин-1-ил)этил)-1Н-индазол,
4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперидин-1-ил)этил)-1Н-индазола оксалат,
4-(2-(4-бензилпиперазин-1-ил)этил)-4,5,6,7-тетрагидро-1-фенил-1Н-индазол,
4,5,6,7-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3Н),4'-пиперидин]-1'-ил]этил)-1Н-индазол,
4,5,6,7-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3Н),4'-пиперидин]-1'-ил]этил)-1H-индазола оксалат,
4,5,6,7-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этил)-1Н-индазол,
4,5,6,7-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этил)-1 Н-индазола оксалат,
(Е)-4-(2-(азепан-1-ил)этилиден)-4,5,6,7-тетрагидро-1-фенил-1Н-индазол,
(Е)-4-(2-(азепан-1-ил)этилиден)-4,5,6,7-тетрагидро-1-фенил-1Н-индазола оксалат,
(Е)-4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперидин-1-ил)этилиден)-1Н-индазол,
(Е)-4,5,6,7-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3Н),4'-пиперидин]-1'-ил]этилиден)-1Н-индазол,
(Е)-4,5,6,7-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3Н),4'-пиперидин]-1'-ил]этилиден)-1Н-индазола оксалат,
(Е)-4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперазин-1-ил)этилиден)-1Н-индазол,
1,2,3,4-тетрагидро-2-((Е)-2-(6,7-дигидро-1-фенил-1Н-индазол-4(5Н)-илиден)этил)изохинолин,
1,2,3,4-тетрагидро-2-((Е)-2-(6,7-дигидро-1-фенил-1Н-индазол-4(5Н)-илиден)этил)изохинолина оксалат,
(Е)-4,5,6,7-тетрагидро-1-фенил-4-(2-(3-фенилпиперидин-1-ил)этилиден)-1Н-индазол,
(Е)-4,5,6,7-тетрагидро-1-фенил-4-(2-(3-фенилпирролидин-1-ил)этилиден)-1Н-индазол,
(Е)-4,5,6,7-тетрагидро-1-фенил-4-(2-(3-фенилпирролидин-1-ил)этилиден)-1H-индазола оксалат,
(Е)-4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этилиден)-1-фенил-1Н-индазол,
(Е)-4,5,6,7-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этилиден)-1Н-индазол,
1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперазин-1-ил)этил)-1Н-индазол,
1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперазин-1-ил)этил)-1Н-индазола оксалат,
1,4,5,6-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенилциклопента[с]пиразол,
1,4,5,6-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенилциклопента[с]пиразола оксалат,
4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперазин-1-ил)этил)-1Н-индазол,
4,5,6,7-тетрагидро-1-фенил-4-(2-(4-фенилпиперазин-1-ил)этил)-1Н-индазола оксалат,
2-(2-(1,4,5,6-тетрагидро-1-фенилциклопента[с]пиразол-4-ил)этил)изоиндолин,
2-(2-(1,4,5,6-тетрагидро-1-фенилциклопента[с]пиразол-4-ил)этил)изоиндолина оксалат,
1,4,5,6-тетрагидро-1-фенил-4-(2-(4-фенилпиперидин-1-ил)этил)циклопента[с] пиразол,
1,4,5,6-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этил)циклопента[с]пиразол,
1,4,5,6-тетрагидро-1-фенил-4-(2-(4-фенилпиперазин-1-ил)этил)циклопента[с]пиразол,
1,4,5,6-тетрагидро-1-фенил-4-(2-(пирролидин-1-ил)этил)циклопента[с]пиразол,
1,4,5,6-тетрагидро-1-фенил-4-(2-(пирролидин-1-ил)этил)циклопента[с]пиразола оксалат,
4-(2-(4-бензилпиперазин-1-ил)этил)-1,4,5,6-тетрагидро-1-фенилциклопента[с]пиразол,
4-(2-(4-бензилпиперазин-1-ил)этил)-1,4,5,6-тетрагидро-1-фенилциклопента[с]пиразола диоксалат,
1,2,3,4-тетрагидро-2-(2-(1,4,5,6-тетрагидро-1-фенилциклопента[с]пиразол-4-ил)этил)изохинолин,
1,2,3,4-тетрагидро-2-(2-(1,4,5,6-тетрагидро-1-фенилциклопента[с]пиразол-4-ил)этил)изохинолина оксалат,
4-(2-(1Н-имидазол-1-ил)этил)-1,4,5,6-тетрагидро-1-фенилциклопента[с] пиразол,
цис-1,4,5,6-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1-фенилциклопента[с] пиразол,
цис-1,4,5,6-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1-фенилциклопента[с]пиразола оксалат,
цис-4,5,6,7-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1-фенил-1Н-индазол,
цис-4,5,6,7-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1-фенил-1Н-индазола оксалат,
1,4,5,6-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3Н),4'-пиперидин]-1'-ил]этил)циклопента[с]пиразол,
1,4,5,6-тетрагидро-1-фенил-4-(2-[спиро[изобензофуран-1(3Н),4'-пиперидин]-1'-ил]этил)циклопента[с]пиразола оксалат,
N-бензил-2-(1,4,5,6-тетрагидро-1-фенилциклопента [с]пиразол-4-ил)-N-метилэтанамин,
смесь диастереомеров 1,4,5,6-тетрагидро-1-фенил-4-(2-(3-фенилпиперидин-1 -ил)этил)циклопента[с] пиразола,
N-бензил-2-(4,5,6,7-тетрагидро-1-фенил-1Н-индазол-4-ил)-N-метилэтанамин,
4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1-фенил-lH-индазол,
4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1-фенил-1Н-индазола оксалат,
4,5,6,7-тетрагидро-1-метил-4-(2-(4-фенилпиперидин-1-ил)этил)-1Н-индазол,
4,5,6,7-тетрагидро-1-метил-4-(2-(4-фенилпиперидин-1-ил)этил)-1Н-индазола оксалат,
4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1-метил-lH-индазол,
4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1-метил-1Н-индазола оксалат,
N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1Н-индазол-4-ил)-N-метилэтанамин,
N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1Н-индазол-4-ил)-N-метилэтанамина оксалат,
4,5,6,7-тетрагидро-1-метил-4-(2-(морфолин-4-ил)этил)-1Н-индазол,
4,5,6,7-тетрагидро-1-метил-4-(2-(морфолин-4-ил)этил)-1Н-индазола оксалат,
1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1Н-индазол,
1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1Н-индазола оксалат,
цис-1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1Н-индазол,
цис-1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(2,6-диметилморфолин-4-ил)этил)-1Н-индазола оксалат,
N-бензил-2-(1-(4-фторфенил)-4,5,6,7-тетрагидро-1Н-индазол-4-ил)-N-метилэтанамин,
1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1Н-индазол,
1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(изоиндолин-2-ил)этил)-1Н-индазола оксалат,
1-(4-фторфенил)-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил)-1Н-индазол,
(+)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1Н-индазол,
(+)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1Н-индазола оксалат,
(-)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1Н-индазол,
(-)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этил)-1-фенил-1Н-индазола оксалат,
(Е)-4,5,6,7-тетрагидро-4-(2-(морфолин-4-ил)этилиден)-1-фенил-1Н-индазола оксалат,
(Е)-4,5,6,7-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этилиден)-1Н-индазола оксалат,
(Е)-N-бензил-2-(6,7-дигидро-1-фенил-1Н-индазол-4(5Н)-илиден)-N-метилэтанамин,
(Е)-N-бензил-2-(6,7-дигидро-1-фенил-1Н-индазол-4(5Н)-илиден)-N-метилэтанамина оксалат,
(Е)-4,5,6,7-тетрагидро-4-(2-(цис-2,6-диметилморфолин-4-ил)этилиден)-1-фенил-3-Н-индазол,
(Е)-4,5,6,7-тетрагидро-4-(2-(цис-2,6-диметилморфолин-4-ил)этилиден)-1-фенил-1Н-индазола оксалат,
(Е)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(цис-2,6-диметилморфолино-4-ил)этилиден)-1Н-индазол,
(Е)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(цис-2,6-диметилморфолино-4-ил)этилиден)-1Н-индазола оксалат,
(Е)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(морфолино-4-ил)этилиден)-1Н-индазол,
(Е)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(морфолино-4-ил)этилиден)-1Н-индазола оксалат,
(Е)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(пиперидин-1-ил)этилиден)-1Н-индазол,
(Е)-1-(3,4-дихлорфенил)-4,5,6,7-тетрагидро-4-(2-(пиперидин-1-ил)этилиден)-1Н-индазола оксалат,
(Е)-4-(2-(N,N-диэтиламино)этилиден)-4,5,6,7-тетрагидро-1-фенил-1Н-индазол,
(Е)-4-(2-(N,N-диэтиламино)этилиден)-4,5,6,7-тетрагидро-1-фенил-1Н-индазола оксалат,
(Е)-4-(2-(4-циклогексилпиперазин-1-ил)этилиден)-4,5,6,7-тетрагидро-1-фенил-1Н-индазол,
(Е)-4,5,6,7-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этилиден)-1-фенил-1Н-индазол,
4,5,6,7-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенил-1Н-индазол,
4,5,6,7-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенил-1Н-индазола оксалат,
1,4,5,6-тетрагидро-1-фенил-4-(2-(пиперидин-1-ил)этил)циклопента[с] пиразола оксалат,
1,4,5,6-тетрагидро-1-фенил-4-[2-(тиоморфолин-4-ил)этил] циклопента[с] пиразол,
1,4,5,6-тетрагидро-1-фенил-4-[2-(тиоморфолин-4-ил)этил] циклопента[с] пиразола оксалат,
1,4,5,6-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенилциклопента[с] пиразол,
1,4,5,6-тетрагидро-4-(2-(4-метилпиперидин-1-ил)этил)-1-фенилциклопента[с] пиразола оксалат,
1,4,5,6-тетрагидро-4-(2-(4-метилпиперазин-1-ил)этил)-1-фенилциклопента[с] пиразол,
4-(2-(4-циклогексилпиперазин-1-ил)этил)-1,4,5,6-тетрагидро-1-фенилциклопента[с]пиразол,
4-(2-азепан-1-ил)этил)-4,5,6,7-тетрагидро-1-фенил-1Н-индазол, N-бензил-2-(1-трет-бутил-4,5,6,7-тетрагидро-1Н-индазол-4-ил)N-метилэтанамин,
1-трет-бутил-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил-1Н-индазол,
1-трет-бутил-4,5,6,7-тетрагидро-4-(2-(4-фенилпиперидин-1-ил)этил-1Н-индазола оксалат,
(-)-N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1Н-индазол-4-ил)-]-N-метилэтанамин,
(+)-N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1Н-индазол-4-ил)-N-метилэтанамин,
N-(2-(4,5,6,7-тетрагидро-1-метил-1Н-индазол-4-ил)этил)-N-метилциклогексанамин,
4,5,6,7-тетрагидро-4-(2-(4-гидрокси-4-фенилпиперидин-1-ил)этил)-1-метил-1Н-индазол,
4,5,6,7-тетрагидро-1-метил-4-(2-(4-фенилпиперидин-1-ил)этил)-1Н-индазол,
N-бензил-2-(4,5,6,7-тетрагидро-1-метил-1Н-индазол-4-ил)-N-метилэтанамин,
4,5,6,7-тетрагидро-1-метил-4-(2-[спиро[изобензофуран-1(3Н),4'-пиперидин]-1'-ил]этил)-lH-индазол,
или любая их фармацевтически приемлемая соль.

в котором R1-R4, m и n определены в п.1, и Х представляет собой уходящую группу, предпочтительно хлор или пиридиний, к соединению формулы (III):

в котором R5 и R6 определены в п.1.
Документы, цитированные в отчёте о поиске
Производные бензимидазола и способ их получения

Комментарии