Способ лечения глубокой депрессии у человека - RU2445973C2
Код документа: RU2445973C2
Описание
Перекрестные ссылки на родственные заявки
В настоящей заявке испрашивается приоритет по дате подачи предварительной заявки на патент US 60/747,843, находящейся на одновременном рассмотрении, поданной 22 мая 2006 года, которая, таким образом, полностью включена в настоящее описание в качестве ссылки.
Предпосылки создания изобретения
Область техники
Настоящее изобретение относится к медикаментозному лечению депрессивных заболеваний.
Уровень техники
От депрессивных расстройств только в США страдает около 20 миллионов взрослого населения. Если не лечить депрессивные расстройства, то они могут истощать организм, как эмоционально, так и физически.
Депрессивные расстройства охватывают группу симптомов, которые перечислены в буклете, опубликованном Национальным институтом здравоохранения США (NIMH), в разделе «Депрессия», таких как:
“Постоянное грустное, тревожное или «безразличное» настроение
Ощущение безысходности, пессимизм
Угрызения совести, бесполезность, беспомощность
Потеря интереса или удовольствия от увлечений и деятельности, которые раньше приносили наслаждение, включая секс
Снижение энергии, усталость, «заторможенное» существование
Трудности при концентрации, запоминании, принятии решений
Бессонница, очень ранее пробуждение или просыпание
Потеря аппетита и/или веса или переедание и увеличение веса
Мысли о смерти или суициде; попытки самоубийства
Беспокойность, раздражительность
Непрекращающиеся физические симптомы, которые не поддаются лечению, такие как головные боли, расстройства пищеварения и хроническая боль.”
В соответствии с буклетом NIMH, тремя самыми распространенными типами депрессивных заболеваний являются:
“Глубокая депрессия проявляется в виде комбинации симптомов (см. перечисленные симптомы), которые мешают работать, учиться, спать, кушать и получать удовольствие от активностей. Такой инвалидизирующий эпизод депрессии может встречаться только один раз, но чаще он встречается несколько раз в течение жизни.
Менее тяжелым типом депрессии, дистимии, являются продолжительные, хронические симптомы, которые не являются инвалидизирующими, но не позволяют человеку функционировать хорошо или чувствовать себя хорошо. Многие люди с дистимией также испытывают глубокие депрессивные эпизоды несколько раз в течение жизни.
Другим типом депрессии является биполярное расстройство, которое также называется маниакально-депрессивным психозом. В отличие от других форм депрессивных расстройств, биполярное расстройство характеризуется циклическими изменениями настроения: сильными повышениями (мания) и снижениями (депрессия). Иногда изменения настроения являются драматическими и быстрыми, но очень часто постепенными. В депрессивном цикле особь может иметь любой или все симптомы депрессивного расстройства. В маниакальном цикле особь может быть сверхактивной, излишне разговорчивой и иметь большое количество энергии. Мания часто оказывает влияние на мышление, здравый смысл и социальное поведение таким образом, что может вызвать серьезные проблемы и замешательство. Например, особь в маниакальной фазе может чувствовать себя в приподнятом настроении, наполненной крупномасштабными планами, которые могут изменяться от неблагоразумных деловых решений до романтических веселий. При отсутствии лечения мания может усугубиться развитием психоза.”
Соединение, которое в настоящем изобретении обозначается как МА-1, представляет собой (1R-транс)-N-[[2-(2,3-дигидро-4-бензофуранил)циклопропил]метил]пропанамид. Оно представляет собой опытный мелатонинергический агонист, который имеет высокое сродство к обоим рецепторам Мелатонин-1 (МТ-1) и Мелатонин-2 (МТ-2) и, следовательно, потенциально является природным для лечения бессонницы и нарушений сна циркадного ритма. МА-1 описан в патенте US №5,856,529, содержание которого полностью включено в данную заявку в качестве ссылки. Соединение, которое в настоящем изобретении обозначается как МА-2, представляет собой N-[1-(2,3-дигидробезофуран-4-ил)пирролидин-3-ил]-N-этилмочевину]. Оно также представляет собой опытный мелатонинергический агонист и описано в патенте US №6,211,225, содержание которого полностью включено в данную заявку в качестве ссылки.
Сущность изобретения
Способ по изобретению охватывает лечение одного или нескольких депрессивных расстройств у животного, а также лечение одного или нескольких симптомов депрессивного заболевания.
Способ по изобретению также охватывает лечение или предотвращение других нарушений, при лечении которых проявляют эффективность определенные антидепрессанты, например ингибиторы обратного захвата серотонина. Они включают, но не ограничиваясь только ими, невроз навязчивых состояний, паническое расстройство, социальное тревожное расстройство, социофобию, посттравматическое стрессовое расстройство, предменструальное дисфорическое расстройство и генерализированное тревожное расстройство.
Подробное описание изобретения
Настоящее изобретение, которое в дальнейшем описывается со ссылкой на иллюстративные варианты осуществления, охватывает применение агонистов мелатонина, которые в дальнейшем в данной заявке обозначаются как МА-1 и МА-2, включая их соли, пролекарства, сложные эфиры, метаболиты, сольваты, гидраты, энантиомеры, стереоизомеры и аморфные и кристаллические формы. МА-1 является белым или белым с желтоватым или сероватым порошком с точкой плавления приблизительно 78°С (ДСК) и имеет структуру, которая иллюстрируется формулой 1.
Формула 1: Химическая структура МА-1

Метаболиты МА-1 включают, например, описанные Vachharajani и др. в “Preclinical Pharmacokinetics and Metabolism of BMS-214778, a Novel Melatonin Receptor Agonist”, J. Pharmaceutical Sci., 92(4): 760-772, которая, таким образом, включена в данную заявку в качестве ссылки. Более предпочтительно эти метаболиты включают гидроксилированные и дегидрированные производные МА-1, а также глюкуронидные и диольные производные МА-1. Структура восьми таких метаболитов приведена на формулах 2-9.

Формула 2 - Гидроксилированный МА-1 метаболит 1
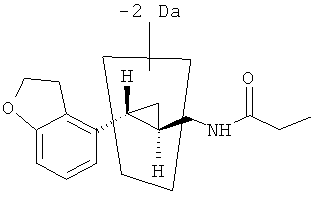
Формула 3 - Дегидрированный МА-1 метаболит 2

Формула 4 - Гидроксилированный МА-1 метаболит 3

Формула 5 - Гидроксилированный МА-1 метаболит 4

Формула 6 - Дегидрированный МА-1 метаболит 5

Формула 7 - Гидроксилированный МА-1 метаболит 6

Формула 8 - Глюкуроновый МА-1 метаболит

Формула 9 - Диольный МА-1 метаболит
Эффективное количество МА-1 или МА-2 можно вводить субъекту-животному (обычно человеку, но также можно лечить других животных, например сельскохозяйственных животных, домашних животных и гоночных животных) различными путями. Эффективное количество представляет собой количество, которое при осуществлении курса лечения будет обладать профилактическим или улучшающим действием на депрессивное расстройство или его симптом. Например, эффективное количество представляет собой количество, которое предотвращает появление или рецидив симптомов депрессивного расстройства в той же степени, что и другие антидепрессанты, например селективные ингибиторы обратного захвата серотонина, такие как флуоксетин, пароксетин, сертралин и др.
Эффективное количество, в количественном отношении, может изменяться, например, в зависимости от пациента, тяжести нарушения или симптома, подвергаемого лечению, и пути введения. Такая доза может быть определена с помощью стандартных исследований. В целом, для системного введения, например перорального введения, точкой отсчета для дозы является доза МА-1 или МА-2, которая применяется для лечения нарушений суточного ритма у людей, то есть от 1 до 500 мг/сутки при пероральном введении. Полагают, что МА-1 или МА-2 может вводиться взрослым людям в дозах от 1 до 500 мг/сутки, хотя, для избегания возможных побочных действий, предпочтительно использовать более низкие дозы, например 150, 100, 50, 25, 10 или 1 мг/сутки. В целом, доза МА-1 будет находиться в интервале от приблизительно 10 до приблизительно 150 мг/сутки, предпочтительно от приблизительно 10 до приблизительно 100 мг/сутки, в одной или нескольких стандартных лекарственных формах.
Следует принять во внимание, что протокол введения, включающий количество МА-1 или МА-2, вводимое в конкретном случае, будет определяться лечащим врачом с учетом значимых обстоятельств, включая, например, состояние, подвергаемое лечению, выбранный путь введения, возраст, вес и ответную реакцию конкретного пациента и тяжесть симптомов пациента. Пациенты обязательно должны находиться под наблюдением для обнаружения возможных побочных действий.
Для терапевтического или профилактического применения МА-1 или МА-2 обычно будет вводиться в виде фармацевтической композиции, содержащей в качестве основного активного компонента по меньшей мере одно такое соединение в комбинации с твердым или жидким фармацевтически приемлемым носителем и, необязательно, с фармацевтически приемлемыми адъювантами и наполнителями, применяемыми согласно стандартным и общепринятым методикам.
МА-1 очень хорошо растворяется или свободно растворяется в 95% этаноле, метаноле, ацетонитриле, этилацетате, изопропаноле, полиэтиленгликолях (PEG-300 и PEG-400) и только слабо растворяется в воде. Нативное pH насыщенного раствора МА-1 в воде составляет 8,5 и на его водную растворимость практически не влияет значение pH.
Фармацевтические композиции, пригодные согласно настоящему изобретению, включают подходящие дозированные формы для перорального, парентерального (включая подкожное, внутримышечное, внутрикожное и внутривенное), трансдермального, бронхиального или назального введения. Таким образом, если используется твердый носитель, то приготавливаемое лекарственное средство может быть таблетировано, помещено в твердую желатиновую капсулу в порошкообразной форме, или в форме пеллеты, или в форме пастилки или лепешки. Твердый носитель может содержать общепринятые наполнители, такие как связующие, вспомогательные вещества, замасливатели для таблеток, вещества, вызывающие дезинтеграцию, смачивающие вещества и другие. Если это является желательным, то таблетка может быть покрыта пленочным покрытием согласно общепринятым методикам. Если используется жидкий носитель, то лекарственное средство может находиться в виде сиропа, эмульсии, мягкой желатиновой капсулы, стерильного средства для инъекции, водной или неводной жидкой суспензии или может быть представлено в виде безводного продукта для восстановления водой или другим подходящим наполнителем перед использованием. Жидкие препараты могут содержать общепринятые вспомогательные вещества, такие как суспендирующие средства, эмульсификаторы, смачивающие вещества, неводные наполнители (включая пищевые масла), консерванты, а также ароматизаторы и/или красители. Для парентерального введения носитель обычно будет содержать стерильную воду, по меньшей мере в значительной степени, хотя также могут использоваться солевые растворы, растворы глюкозы и т.п. Также можно использовать суспензии для инъекций, в которых могут применяться общепринятые суспендирующие вещества. Также в парентеральные дозированные формы можно добавлять общепринятые консерванты, буферные вещества и др. Чрезвычайно полезным является введение соединения формулы 1 в виде пероральных дозированных лекарственных препаратов. Фармацевтические композиции могут приготавливаться с помощью общепринятых методик, подходящих для желательного лекарственного средства, содержащего подходящие количества МА-1 или МА-2. См., например, Remington's Pharmaceutical Sciences, Mack Publishing Company, Easton, Pa., 17-я редакция, 1985.
При приготовлении фармацевтических композиций для применения согласно изобретению активный компонент или активные компоненты обычно могут быть смешаны с носителем, или разведены носителем, или включены в носитель, который может находиться в форме капсулы, саше, бумажного или другого контейнера. Если носитель служит разбавителем, то он может представлять собой твердое, полутвердое или жидкое вещество, которое действует в качестве наполнителя, вспомогательного вещества или среды для активного компонента. Таким образом, композиция может находиться в форме таблеток, пилюль, порошков, лепешек, саше, капсул, эликсиров, суспензий, эмульсий, растворов, сиропов, аэрозолей (в виде твердой или жидкой среды), мазей, содержащей, например, вплоть до 10 мас.% активного соединения, мягких и твердых желатиновых капсул, суппозиториев, стерильных растворов для инъекций и стерильных упакованных порошков.
Некоторыми примерами подходящих носителей и разбавителей являются лактоза, декстроза, сахароза, сорбит, маннит, крахмалы, гуммиарабик, фосфат кальция, альгинаты, трагакантовая камедь, желатин, силикат кальция, микрокристаллическая целлюлоза, поливинилпирролидон, целлюлоза, вода, сироп, метилцеллюлоза, метил- и пропилгидроксибензоаты, тальк, стеарат магния и минеральное масло. Лекарственные препараты дополнительно могут содержать замасливатели, смачивающие вещества, эмульсификаторы и суспендирующие средства, консерванты, подсластители или ароматизаторы. Композиции по изобретению могут быть приготовлены таким образом, чтобы обеспечить быстрое, длительное или замедленное высвобождение активного компонента после введения пациенту.
Композиции предпочтительно приготавливают в стандартной лекарственной форме, каждая дозированная единица которой содержит от приблизительно 0,1 до приблизительно 100 мг активного компонента. Термин “стандартная лекарственная форма” относится к физически дискретным элементам, подходящим в виде единичных дозированных форм для людей и других млекопитающих, каждая единица содержит заранее определенное количество активного вещества, рассчитанное таким образом, чтобы получить желательное профилактическое или терапевтическое действие при осуществлении лечения, в сочетании с требуемым фармацевтическим носителем. Таким образом, например, взрослый пациент, страдающий от депрессивного расстройства, может принимать 1-4 таблетки, каждая из которых содержит 10-100 мг МА-1, которая может приниматься один раз, два раза или три раза в сутки и может обеспечивать улучшение его или ее состояний в течение от приблизительно одной до приблизительно 12 недель.
Типичная стандартная дозированная форма может представлять собой капсулу размера 0 или размера 1, содержащую 10, 20, 50 или 100 мг МА-1, а также безводную лактозу, микрокристаллическую целлюлозу, коллоидный диоксид кремния, кросскармеллозу натрия и стеарат магния. Рекомендуется хранить при температуре от 15 до 20°С, защищая от попадания влаги и солнечного света.
МА-1 также может быть приготовлен в виде лекарственного средства с контролируемым высвобождением, например замедленным, продолжительным, или пульсирующим высвобождением. МА-1 также может сопутствующе вводиться с другими терапевтическими лекарственными средствами, включая, но не ограничиваясь только ими, лечение другими антидепрессантами или лечение другими средствами для лечения других эмоциональных нарушений. Таким образом, изобретение охватывает, например, введение МА-1 или МА-2 в комбинации с другими мелатонинергическими агонистами или другими средствами, индуцирующими сон. Другие антидепрессанты включают, но не ограничиваясь только ими, следующие категории лекарственных средств:
- агонисты мелатонина
- селективные ингибиторы обратного захвата серотонина (SSRI)
○ 5-HT1A антагонисты
○ антагонист 5-НТ1А/β-адренорецептора
○ 5-НТ1B антагонисты
○ 5-НТ2C антагонисты
▪ Селективные и неселективные
○ 5-НТ2C агонисты
○ 5-НТ6 агонисты
○ α-2 адренергические антагонисты
- ингибиторы обратного захвата серотонина и норэпинефрина (SNRI)
- ингибиторы моноаминоксидазы (MAOI)
- трициклические антидепрессанты (ТСА)
- тройные моноаминовые усовершенствованные блокаторы
- бензодиазепины
- антагонисты NMDA рецептора
- Пирролиноны
- Бензотиадиазиды
- Бензоилпиперидины
- Биарилопропилсульфонамиды
- Метаботропные глутаматные рецепторы (mGluR)
- GABA антагонисты
- NK1 антагонисты
- NK2 антагонисты
- CRF1 антагонисты
- Аргинин вазопрессин V1b антагонисты
- антагонисты МСН рецептора
- NGF антагонисты
- BDNF антагонисты
- NT-3 антагонисты
- NT-4 антагонисты
- CREB антагонисты
Иллюстративными и неограничивающими примерами таких агентов являются:
мелатонинергические агонисты: мелатонин, агомелатин, (1R-транс)-N-[[2-(2,3-дигидро-4-бензофуранил)циклопропил]метил]пропанамид и N-[1-(2,3-дигидробезофуран-4-ил)пирролидин-3-ил]-N-этилмочевина], рамельтеон, 2-фенилмелатонин, 8-M-PDOT, 2-йодмелатонин, 6-хлормелатонин;
ингибиторы обратного захвата серотонина: пароксетин, флуоксетин, сертралин, венлаксафин, циталопрам, эсциталопрам, флувоксамин, тразадон, нефазодон, милнаципран, дезипрамин, дулоксетин, YM992;
SSRI/5-HT1A антагонисты: WAY-100635, Пиндолол;
SSRI/5-HT1В антагонисты: SB-224289;
SSRI/5-HT2C антагонисты;
Селективные: SB242084, RS102221;
Неселективные: Кетансерин, Ириндалон;
SSRI/5-HT2C агонисты: Org 37684, Ro 60-0175, WAY-161503, YM348, WAY-629, WAY-163909;
SSRI/5-HT6 агонисты: LY586713, WAY-466, WAY-1811187;
α-2 адренергические антагонисты: Миртазапин (Ремерон);
тройные моноаминовые усовершенствованные блокаторы: DOV 21,947;
антагонисты NMDA рецептора: МК-801, Мемантин, Кетамин, Фельбамат, Глицин, D-серин, D-циклосерин, L-глутамательфенпродил;
Пирролидионы: Пирацетам, Анирацетам;
трициклические: Амитриптилин, Кломипрамин, Дезипрамин, Дотиепин, Доксепин, Имипрамин, Лофепрамин, Нортриптилин, Протриптилин, Тримипрамин, Иприндол, Опипрамол;
тетрациклические: Мапротилин, Миансерин, Миртазапин, Амоксапин, Тразодон, Нефазодон;
усилители обратного захвата серотонина: тианептин;
ингибиторы моноаминоксидазы: Гармалин, Ниаламид, Селегилин, Изоксарбоксазид, Ипрониазид, Ипроклозид, Моклобемид, Фенелзин, Толоксатон, Транилципромин;
ингибиторы обратного захвата допамина: Бупропион, Аминептин, Метилфенидат, Фенметразин, Ваноксерин;
ингибиторы обратного захвата норэпинефрина: Атомоксетин, Ребоксетин, Вилоксазин, Мапротилин, Бупропион, Ребоксетин;
ингибиторы обратного захвата серотонина-норэпинефрина: Дезипрамин, Дулоксетин, Милнаципран, Нефазодон, Венлафаксин;
Бензотиадиазиды: Циклотиазид;
Бензоилпиперидины: СХ516, СХ546;
Биарилопропилсульфонамиды: LY392098, LY404187, LY451646;
Метаботропные глутаматные рецепторы (mGluR): 2-метил-6-(фенилэтинил)-пиридин (МРЕР), 3-[(2-метил-1,3-тиазол-4-ил)этинил]-пиридин (МТЕР), JNJ16259685, CPCOOEt, MGS0039, LY341495, LY354740, ACPT-1/L-SOP (L-серин-О-фосфат), HomoAMPA, N-фенил-7-(гидроксиимино) циклопропа[b] хромен-1а-карбоксамид;
GABA антагонисты: CGP36742, CGP56433, CGP56999;
NK1 антагонисты: GW823296, GW679769, GW597599 (Вестипитант), R673, СР-122,721, L-759274, GR205171, L733060;
NK2 антагонисты: SR48968;
CRF1 антагонисты: DMP696, DMP904, GW876008, AAG561, TS-041, СР-154,526 (анталармин), SSR125543, R278995/CRA0450, R121919;
Аргинин вазопрессин V1b антагонисты: SSR149415;
антагонисты МСН рецептора: Т-226296.
У некоторых пациентов, по имеющимся данным, является полезным дополнение лечения антидепрессантами литием или трийодтиронином.
Таким образом, в другом иллюстративном варианте осуществления изобретение охватывает набор, содержащий одну или несколько фармацевтических дозированных единиц МА-1 или МА-2 и одну или несколько фармацевтических дозированных единиц антидепрессанта, где любая или обе стандартные лекарственные формы МА-1 или МА-2 и дозированная единица антидепрессанта также могут содержать соответственно антидепрессант или антипсихотическое средство, и, необязательно, один или несколько дополнительных фармацевтически активных компонентов. В другом варианте осуществления изобретение охватывает введение МА-1 или МА-2 и другого средства или средств в различные промежутки времени таким образом, чтобы эффективное количество каждого средства поддерживалось в кровообращении пациента в подходящих количествах в течение подходящего времени. Такой набор может облегчать, например, введение МА-1 или МА-2 в различные периоды времени относительно введения другого средства или средств. В сопутствующем варианте осуществления набор содержит фармацевтические дозированные единицы только одного средства отдельно и другие фармацевтические дозированные единицы, содержащие оба средства. Таким образом, например, МА-1 или МА-2 можно принимать самостоятельно в течение дня и с другим средством или другими средствами вечером.
Если используются такие комбинации, то полагают, что доза каждого компонента будет приблизительно такой же или меньше, чем эффективное количество любого средства отдельно. Например, каждый фармацевтически активный компонент может вводиться в дозах, которые составляют от 20% до приблизительно 80% дозы, в которой каждый компонент будет вводиться отдельно.
Два (или больше) средства могут вводиться более или менее совместно, то есть одновременно (например, в течение от приблизительно 0 до приблизительно 5 минут друг от друга, предпочтительно в течение одной минуты), или они могут вводиться в различное время. Например, в одном аспекте изобретение обеспечивает фармацевтическую композицию, содержащую оба, антипсихотическое средство и другое средство или средства. Этот вариант осуществления, например, включает пилюлю или капсулу, содержащую оба активных фармацевтических компонента либо смешанные вместе или содержащую каждый активный фармацевтический компонент в раздельной порции пилюли или капсулы.
Стандартные лекарственные формы по изобретению, независимо от того, содержат ли они МА-1 или МА-2 или его активный метаболит в виде единственного активного фармацевтического компонента или в комбинации с другим средством, например антипсихотическим средством или антидепрессантом, также могут быть приготовлены в виде лекарственного средства с контролируемым высвобождением, например замедленным, продолжительным, или пульсирующим высвобождением. Из такой формы, в случае комбинаций, МА-1 или МА-2 или его активный метаболит может высвобождаться с одинаковой или различной скоростью и временем, как и другое средство или средства.
Примеры
Примеры, представленные ниже, являются иллюстративными и не ограничивают изобретение, а иллюстрируют полезность МА-1 для предотвращения и лечения симптомов депрессивных расстройств.
Примеры 1-3. МА-1 тестировали на следующих 3 моделях: (1) индуцированное стрессом повышение цГМФ, (2) тест принудительного плавания мышей и (3) тест принудительного плавания крыс. Ниже описаны использованные протоколы и результаты, полученные в этих исследованиях.
Индуцированное стрессом повышение цГМФ в клетках
Протокол: животных помещали в ударную камеру со стальным решетчатым полом и ударяли током 1 мА в течение 10 секунд. Через одну минуту после действия стресс-фактора животных помещали в пластмассовую замкнутую трубку и умертвляли с помощью микроволнового облучения (1,8 с при 3,5 кВ). Быстро удаляли мозжечок, быстро замораживали и хранили при -80°С до исследования цГМФ. Животных, которые не подвергались действию стресс-фактора, доставали непосредственно из их клеток и умертвляли с помощью микроволнового облучения и ткани обрабатывали аналогично. Дозирование лекарственного средства осуществляли за 30-60 минут до шокового стрессового воздействия на ступни. Для цГМФ исследования ткань гомогенизировали в 2 мл 1% прехлорной кислоты, используя Brinkman Polytron при установках #5 в течение ~15 с для каждого и помещали на лед до завершения гомогенизации всех образцов. После этого образцы помещали на водяную баню при 85°С в течение 5 минут, центрифугировали при 2500g в течение 15 минут и для анализа собирали ~0,5 мл супернатанта. Супернатант разводили 1:20 в натрий-ацетатном буфере согласно инструкциям производителя на 125I-цГМФ флеш-планшетах. Разведенные образцы инкубировали в течение ночи в лунках флеш-планшет с 125I-цГМФ, анализируя на счетчике гамма-излучения для прочтения планшетов, и превращали в пмоль цГМФ/мг ткани, используя стандартную кривую, полученную в аналогичном опыте.
Результаты: крысы, получавшие электрошок, проявляли ~2,5х повышение уровней цГМФ в мозжечке. Это повышение ослабляется на ~50% путем лечения МА-1 в дозах 0,1-10 мг/кг. Хотя действие, по-видимому, является максимальным независимо от дозы, более низкие дозы не испытывали.
Тест принудительного плавания мышей
Протокол: животных выдерживали при цикле день:ночь 12:12 и свет включали в 6.00 утра. Мышей помещали в комнату для тестирования по меньшей мере за один час до начала теста. Наполнитель, амитриптилин и МА-1 вводили согласно одному из трех условий: А) острое лечение, животным вводили дозу за 30 минут до тестирования; В) 4-дневное субхроническое AM лечение, где дозу вводили в течение раннего утреннего периода (09.00-11.00 ч), с конечной дозой, которую вводили за 30 минут до тестирования; и С) субхроническое РМ лечение, где дозу вводили в течение вечернего периода (17.30-18.00 ч, непосредственно перед выключением света), и тест принудительного плавания осуществляли на следующее утро. Животных тестировали в тесте принудительного плавания, используя модификацию протокола, изначально описанного Porsolt и др. (1978). Мышей помещали в химические стаканы объемом 1 л (KIMAX #14005), наполненные 800 мл воды (20-22°С) для плавания в течение 7 минут. Животных оценивали только в течение последних 5 минут теста и присваивали либо “0”, если они активно плавали, или “1”, если они были неподвижными, за исключением незначительных движений, необходимых для поддержания на поверхности. В течение 5-минутного оценочного периода было десять 30-секундных интервалов, в которых оценивали общий возможный балл 0-10 для каждой мыши. Данные выражали в виде серединного значения (вероятное отклонение). Каждое исследование осуществляли независимо с отдельными группами интактных мышей. Данные анализировали, используя Statview (SAS, Carу, NC) с анализом Крускала-Уоллиса, с последующим U-тестом Mann-Whitney с уровнем значимости, равным р<0,05.
Результаты: МА-1 тестировали для определения эффективности на модели принудительного плавания мышей в трех условиях, включая (А) острое лечение, с тестированием через 30 минут после введения дозы, (В) 4-дневное субхроническое лечение с введением дозы утром (AM) и тестированием через 30 минут после конечной дозы и (С) 4-дневное субхроническое лечение с введением дозы после обеда (РМ) и тестированием на следующее утро. В качестве положительного контроля в этом исследовании использовали амитриптилин, и он был активным в условиях А и В, но не проявлял активности в условиях С. Однако МА-1 не проявлял активности в этом исследовании в любом из тестируемых условий.
Тест принудительного плавания крыс
Протокол: животных тестировали в тесте принудительного плавания, используя протокол, изначально описанный Porsolt и др. (Eur. J. Pharmacol., 47, 379-391, 1978). Крыс индивидуально помещали в цилиндр (высота=40 см, диаметр=20 см), содержащий 13 см воды (25°С), в течение 15 минут в первый день эксперимента (Сессия 1) и затем возвращали в воду через 24 часа для проведения теста в течение 5 минут (Сессия 2). Измеряли продолжительность неподвижности в течение 5-минутного теста. На каждую группы исследовали 6 крыс. Тест осуществляли слепым. Сессию 1 и Сессию 2 проводили либо в течение цикла света, то есть в интервале от 2,5 до 5,5 часов после включения света, или в течение цикла темноты, то есть в интервале от 2,5 до 5,5 часов после выключения света. Таким образом, тесты в течение цикла света осуществляли в интервале от 9:30 утра и 12:30 утра, тогда как тесты в течение цикла темноты, в связи со сдвигом цикла света, осуществляли в интервале от 14:30 и 17:30.
Для возможности осуществления 2 фаз эксперимента (фаза света и фаза темноты) в один и тот же день одним и тем же лаборантом животных, которых тестировали в течение фазы темноты, подвергали сдвигу цикла света за 12 дней до первой сессии теста принудительного плавания, тогда как цикл света/темноты сдвигали вперед на 7 часов (свет включали в: 0:00 часов, выключали: 12:00 (полдень)). Полагают, что 12-дневный период является достаточным для животных для осуществления сдвига цикла темноты. Для привыкания животных к сдвигу цикла света животных цикла темноты подвергали сдвигу за 12 дней до Сессии 1. Другими словами, для обеспечения аналогичных условий между животными цикла света и животными цикла темноты всех животных, которых использовали в эксперименте, получали из одной доставленной партии и их помещали в опытные клетки в одно и то же время, то есть за 12 дней до Сессии 1.
Тестирование в течение фазы света осуществляли при нормальном лабораторном освещении и тестирование в течение фазы темноты осуществляли при инфракрасном освещении. МА-1, агомелатин и мелатонин оценивали при 2 пероральных (п.о.) дозах каждого, которые вводили дважды (за 24 часа и 1 час до Сессии 2). Первое введение осуществляли сразу после Сессии 1. В качестве сравнительного вещества использовали имипрамин (64 мг/кг п.о.), который вводили два раза в тех же самых экспериментальных условиях.
Результаты: крысам вводили дозы и тестировали либо в течение фазы темноты (таблица 1) или фазы света (таблица 2) 24-часового цикла, для исследования возможности чувствительности к циркадному времени. Тестируемые соединения включали имипрамин в качестве положительного контроля (64 мг/кг), мелатонин (10 и 50 мг/кг), агомелатин (10 и 50 мг/кг) и МА-1 (1 и 10 мг/кг). Дозы выбирали для согласования с интервалом, для которого в литературе описана активность для этого или других поведенческих исследований. Активность была более сильной в течение фазы темноты для всех агонистов мелатонина, где агомелатин проявляет снижение на 60% и 33% времени неподвижности при введении в дозах 10 и 50 мг/кг соответственно. МА-1 также проявляет значительное снижение времени неподвижности для обеих тестируемых доз, со снижением на 37% и 41% неподвижности, наблюдаемой при введении в дозах 1 и 10 мг/кг соответственно. Активность также наблюдали у животных, тестируемых в течение фазы света (таблица 2), хотя эффекты были более умеренными и менее согласованными с тестируемыми дозами.
Выводы: эти исследованы были осуществлены для тестирования того, проявляет ли МА-1 активность, аналогичную другим агонистам мелатонина на поведенческих моделях стресса и поведенческого отчаяния у грызунов. На тех моделях, в которых другие агонисты мелатонина проявляли активность, МА-1 был активным. Мелатонин и агомелатин в более ранних исследованиях проявляли активность в индуцированном стрессе анализе цГМФ (данные не представлены) на уровнях, аналогичных наблюдаемым для МА-1. Дополнительно, МА-1 проявляет активность у крыс FST (Porsolt labs), аналогичную по интенсивности активности, проявляемой агомелатином и мелатонином. Хотя МА-1 является неактивным на модели FST у мышей, нет проявления активности для других агонистов мелатонина в этом исследовании. Отсутствие влияния на модели FST у мышей по сравнению с анализом для крыс, проведенным с помощью Porsolt Labs, обусловлено не только разными видами, поскольку также не наблюдали активности для агонистов мелатонина на другой версии FST у крыс. Это подтверждает тот факт, что малозаметные отличия в структуре исследования, пути введения или времени дозирования могут быть решающими для проявления действия агонистами мелатонина в этом исследовании. В еще другом исследовании, не приведенном в данной заявке, МА-1 тестировали на крысах в тесте модифицированного принудительного плавания в дозах 5 мг/кг и 10 мг/кг и не обнаружили влияния на параметры подвижности, плавания или лазанья, которые были бы статистически достоверным по сравнению с наполнителем.
Реферат
Изобретение относится к области фармацевтики. Способ включает внутреннее введение человеку эффективного количества N-[[2-(2,3-дигидро-4-бензофуранил)циклопропил]метил]пропанамида. Глубокая депрессия включает по меньшей мере один симптом, выбранный из группы, включающей: постоянное грустное, тревожное или безразличное настроение; ощущение безысходности; пессимизм; угрызения совести, бесполезность или беспомощность; потеря интереса или удовольствия от увлечений и деятельности, которые раньше приносили наслаждение, включая секс; снижение энергии, усталость или заторможенное существование; трудности при концентрации, запоминании или принятии решений; бессонницу, очень раннее пробуждение или просыпание; потерю аппетита и/или веса или переедание и увеличение веса; мысли о смерти или суициде; попытки самоубийства; беспокойность; раздражительность; непрекращающиеся физические симптомы, которые не поддаются лечению, включая головные боли, расстройства пищеварения и хроническую боль, и любую их комбинацию. Способ позволяет эффективно предотвращать и лечить симптомы глубокой депрессии. 1 з.п. ф-лы, 2 табл., 3 пр.
Формула
Документы, цитированные в отчёте о поиске
Комбинация лекарственных препаратов, включающая миртазапин, для лечения депрессии и связанных расстройств

Комментарии