Применение 2-фенил-3-ароилбензотиофенов для ингибирования расстройств цнс у женщин в постменопаузе - RU2138261C1
Код документа: RU2138261C1
Описание
У женщин в климактерическом периоде ощущения тревоги, беспокойства, депрессии, напряжения и раздражительности начинаются еще в течение предменопаузы и могут коррелировать со снижением уровня эстрогенов в организме, в связи с чем для лечения этих симптомов рекомендована эстрогензамещающая терапия (Malleson J., Lancet, 2: 158, (1953); Wilson et. al., J. Am. Geriatric Soc., 11:347, (1963).
Механизм защитного действия эстрогена в данном случае неизвестен, хотя предпочтительно, может быть связан с потенциальным влиянием эстрогена на биогенные амины, такие как серотонин Aylward M., Int Res. Communications System Med. Sei., 1:30 (1973). Исходя из этой точки зрения, количество циркулирующего серотонина у женщин в постменопаузе редуцировано (Gonzales G., et. al., Maturitas 17, 23-29 (1993), и серотония (равно как и некоторые другие биогенные амины) играет вероятную роль в развитии состояния депрессии. Phillips and Sherwin (Psychoneuro-endocrinology. 17: 485-495 (1992)) сообщают, что у женщин с менопаузой, вызванной хирургическим вмешательством, получавших эстроген, показатели тестов на запоминание в кратковременной и долговременной памяти выше, чем у аналогичных женщин, нелеченных эстрогенов. Существует две предположительные гипотезы, объясняющие этот эффект. Имеются некоторые доказательства, что отдельные агонисты эстрогенов (или антиэстрогены), такие как тамоксифен, взаимодействуют с мускариновым рецептором (Ben-Baruch G. et/ al., Molec. Pharmacol., 21:287-293 (1982), а мускариновые агонисты (M2), как известно, оказывают положительное влияние в ряде задач на ассоциативную память и имеют показания к клиническому применению при болезни Альцгеймера. Вторая интересная гипотеза может быть связана с нейрокинами, такими как вещество P, которое, как известно, обладает нейротрофной функцией, а также свойством улучшения памяти (Thoenen H., Trends in Neuroscience, 14 : 165 - 170 (1991); Huston J. et al., Neurosei. Biobehav. Rev. 13 : 171 - 180 (1989), и таким образом, посредством воздействия либо на рецептор для нейротрансмиттера в ЦНС, либо на нейропептидный рецептор, селективный к ткани агонист/антагонист эстрогена может стимулировать память и оказывать усиливающее влияние на познавательные процессы. Указанная активность наиболее релевантно может быть оценена у человека, хотя для предклинических испытаний пригодны различные экспериментальные модели (т.е. обучение в лабиринте, затухание приобретенного рефлекса и.д.).
Вероятно, наиболее частым осложнением, связанным с ЦНС, у женщин в климатическом периоде являются приливы. Хотя они несомненно представляют собой соматический процесс, осуществляемый воздействием на микроциркуляцию, текущие данные представляют неоспоримые доказательства в пользу точки зрения об инициирующем воздействии ЦНС (Lomax P., et. al., Pharmac. Ther. 57 : 347 - 358 (1993)).
В связи с этим селективный к ткани агонист/антагонист эстрагена, подобный ралоксифену, может представлять идеальное средство терапии, оказывающее необходимый эффект при отсутствии нежелательных побочных осложнений на репродуктивную ткань.
Настоящее изобретение представляет способы ингибирования расстройств со стороны ЦНС у женщин в постменопаузе, включающие введение женщинами, нуждающимся в лечении, эффективного количества соединения, описанного формулой I.
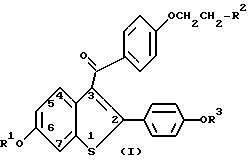
где R1 и R3 являются независимо водородом, -CH3,

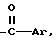
где Ar является необязательно замещенным фенилом;
R2 выбран из группы, состоящей из пирролидино-, гексаметиленимино- и пиперидино- и их фармацевтически приемлемых солей и сольватов.
Настоящее изобретение относится к открытию, что выбранная группа 2-фенил-3-ароилбензотиофенов (бензотиофены) формулы I пригодны для устранения расстройств ЦНС у женщин в стадии постменопаузы. Способ лечения, предлагаемые в данном изобретении, применимы на практике путем введения необходимой дозы соединения формулы I или его фармакологически приемлемой соли сольвата, которые эффективны для ингибирования одного или более расстройств ЦНС. Термин ингибирование обозначает его основное общепринятое значение, которое включает профилактическое лечение человеческого субъекта, подверженного описанным симптомам, позволяющее контролировать и/или лечить существующие симптомы. Как таковой, представленный метод включает оба похода - медицинское терапевтическое и/или профилактическое лечение в зависимости от показаний. К расстройствам ЦНС относятся наиболее известные нарушения, которые включены в определения профессионалами в данной области и которые наиболее часто поражают женщин в состоянии постменопаузы: тревога, депрессия, напряжение, раздражительность, колебания настроения, дефекты мотивации, понижение памяти и процессов заполнения.
Ралоксифен - соединение, описываемое в настоящем изобретении, является гидрохлоридом соединения формулы I, где R1 и R3 являются водородом, и R2 - 1-пиперидинилом, является ядро-регулирующей молекулой. Было показано, что ралоксифен связывается с рецептором эстрогена и является исходно молекулой, чьи функция и фармакология носят антиэстрогенный характер, благодаря чему он блокирует способность эстрогена активировать ткань матки и эстрогензависимую опухоль молочной железы. В действительности ралоксифен должен активировать действие эстрогена в нескольких видах клеток; однако в других типах клеток ралоксифен активирует те же самые гены, что и эстроген и проявляет сходные фармакологические свойства, например ингибирует разрежение костной ткани и снижение сывороточных липидов. В результате ралоксифен рассматривается как антиэстроген со смешанными свойствами агонист/антагониста. Уникальные свойства, которые проявляет ралоксифен и их отличие от таковых эстрогена, как теперь понятно, обусловлены уникальной активацией и/или супрессией различных функций генов ралоксифен-эстрогенным рецепторным комплексом в противоположность активации и/или супрессии генов эстроген-эстрогенным рецепторным комплексом. Поэтому, хотя ралоксифен и эстроген используют и конкурируют за один и тот же рецептор, фармакологический результат регуляции гена из двух возможных нелегко предсказуем и уникален для каждого вещества. Это не означает, что механизм действия непременно осуществляется целиком или частично посредством самого эстрогенного рецептора.
Как правило, соединение смешивают с общеизвестными наполнителями, растворителями или носителями, и прессуют в виде таблеток или готовят в виде эликсиров или растворов для удобного орального применения, либо для внутримышечного или внутривенного введения. Соединения также могут быть применены трансдермально или могут быть приготовлены в виде лекарственных форм, предназначенных для применения в виде дозированных препаратов с замедленным высвобождением, и тому подобное.
Соединения, используемые в настоящем изобретении, могут быть получены способами, которые подробно описаны в патентах США NOS 4133814; 4418068 и 4380635, приведенных в описании в качестве ссылок. Как правило процесс начинается с бензо(в) тиофена, имеющего 6-гидроксильную и 2-(4-гидроксифенильную) группы. Исходное соединение ацилировано или лишено защитных групп для получения соединений формулы I. Примеры получения таких соединений приведены в вышеуказанных патентах США. Замещенный фенил представляет собой фенил, замещенный одним или двумя следующими заместителями: C1-C6 алкил, C1-C4 алкокси, гидрокси, нитро хлор, фтор, трихлорметил или трифторметил.
Соединения, используемые в методах настоящего изобретения, образуют соли фармацевтически приемлемых кислот и оснований с разнообразными органическими и неорганическими кислотами и основаниями и включают, в том числе, физиологически приемлемые соли, которые часто используются в химико-фармацевтическом производства. Такие соли также являются частью настоящего изобретения. Типичные неорганические кислоты, применяемые для образования таких солей, включают: хлористоводородную, бромистоводородную, иодистоводородную, азотную, серную, фосфорную, фосфорноватую и тому подобное. Могут также применяться соли, полученные из органических кислот, таких как алифатические, моно- и дикарбоновые кислоты, фенилзамещенные алкановые кислоты, гидроксиалкановые и гидроксиалкилкандикарбоновые кислоты, ароматические кислоты, алифатические и ароматические сульфокислоты.
Таким образом, такие фармацевтически приемлемые соли включают: ацетат, фенилацетат, трифтор ацетат, акрилат, аскорбат, бензоат, хлоробензоат, динитробензоат, гидроксибензоат, метоксибензоат, метилбензоат, о-ацетоксибензоат, нафталин-2-бензоат, бромид, изобутират, фенилбутират, -гидроксибутират, -гидроксибутират, бутин-1,4-диоат, гексин-1,4-диоат, капронат, каприлат, хлорид, циннамат, нитрат, формиат, фумарат, гликоллят, гептаноат, гинпурат, лактан, малат, малеат, гидроксималеат, малонат, манделат, мезилат, никотинат, изоникатинат, нитрат, оксалат, фталат, терафталат, фосфат, дигидрофосфат, монософат, метафосфат, пирофосфат, пропиолят, пропионат, фенилпропионат, салицилат, себацинат, сукцинат, суберат, сульфат, бисульфат, пиросульфат, сульфит, бисульфит, сульфонат, бензолсульфонат, р-бромфенилсульфонат, хлорбензолсульфонат, этансульфонат, 2-гидроксиэтансульфонат, метансульфонат, нафталин-1-сульфонат, нафталин-2-сульфонат, р-толуолсульфонат, ксилолсульфонат, тартрат и тому подобное. Предпочтительной солью является гидрохлорид.
Фармацевтически приемлемые соли присоединения кислот обычно образуются путем реакции соединения формул I с эквимолярным или избыточным количеством кислоты. Реагенты, как правило, смешиваются в соответствующем растворителе, таком как диэтиловый эфир или бензол. Соль обычно осаждается из раствора в течение периода от 1 ч до 10 дней и может быть отделена фильтрованием, либо удалением растворителя стандартным способом.
Основания, обычно используемые для образования солей, включают: гидроксид аммония, гидроксиды щелочных и щелочноземельных металлов, карбонаты, а также алифатические первичные, вторичные и третичные амины, алифатические диамины. Наиболее пригодны для получения солей основания : гидроксид аммония, карбонат калия, метиламин, диэтиламин, этилендиамин и циклогексиламин.
Фармацевтически приемлемые соли, как правило, характеризуются повышенной растворимостью в сравнении с исходным соединением, и поэтому чаще всего пригодны для таких лекарственных форм, как жидкости и эмульсии.
Фармацевтические препараты готовятся с помощью хорошо известных методов. Например, соединения могут быть сформированы с применением общеизвестных наполнителей, растворителей или носителей в форме таблеток, капсул, взвесей, порошков и тому подобных. Примерами наполнителей, растворителей и носителей, которые пригодны для таких лекарственных форм, являются следующие вещества: наполнители и разбавители, такие как крахмал, сахара, маннит и кремнийсодержащие соединения; связывающие агенты, такие как карбоксиметилцеллюлоза и другие производные целлюлозы, алгинаты, желатин и поливинилпирролидон; увлажняющие агенты, такие как глицерин; дезинтегрирующие агенты, такие как карбонат кальция и бикарбонат натрия; агенты, замедляющие растворение, такие как парафин, и ускоряющие всасывание, такие как четвертичные соединения аммония, поверхностно активные агенты, такие как цетиловый спирт, моностеарат глицерина, адсорбенты, такие как каолин, бентонит и смазывающие, такие как тальк, стеараты кальция и магния, твердые полиэтиленгликоли.
Указанные соединения также могут быть приготовлены в виде элексиров или растворов для обычно орального применения, или в виде растворов для парэнтерального введения, например, внутримышечным, подкожным или внутривенным путем. Кроме того, эти соединения хорошо подходят для создания дозированных препаратов с замедленным высвобождением и тому подобное. Лекарственные формы могут быть составлены таким образом, что активные ингредиенты выделяются только или преимущественно в определенном участке кишечного тракта в определенный период времени. Из полимерных веществ или воска могут быть сделаны покрывающие и защитные оболочки.
В соответствии с настоящим изобретением индивидуальная дозировка соединения формулы I, необходимая для ингибирования одного или более нарушений ЦНС у женщин в постменопаузе, будет зависеть от тяжести состояния, способа введения и других связанных факторов, решение в отношении которых принимается лечащим врачом. Как правило, допустимые и эффективные суточные дозы колеблятся от 0,1 до 1000 мг/сут, и наиболее часто составляет от 50 до 200 мг/сут. Выбранные дозы вводятся женщине, нуждающейся в лечении, от одного до трех раз в сутки или чаще при необходимости более эффективного лечения патологической симптоматики.
Обычно более предпочтительно применять соединение формулы 1 в виде солей, присоединения кислоты как это принято при применении препаратов, несущих основную группу, такую как пиперидиновое кольцо. Существуют также преимущества введения таких соединений оральным путем у женщин в постменопаузе. Для целей орального применения пригодны следующие формы.
Препараты
В приводимых ниже лекарственных формах понятие "Активный ингредиент" означает соединение формулы I.
Лекарственная форма I:
Желатиновые капсулы
Твердые желатиновые капсулы готовятся с использованием следующим веществ:
Ингредиент - Количество (мг/капсулу)
Активный ингредиент - 0,1 - 1 000
Крахмал, NF - 0
- 650
Сыпучий крахмальный порошок - 0 - 650
Сликоновая жидкость 350 сантисток - 0 - 15
Ингридиенты смешивали, пропускали через сито размером N 45 меш США и заполняли смесью
твердые желатиновые капсулы.
Примеры капсул, приготовленных на основе ралоксифена, приведены ниже:
Лекарственная форма 2:
Капсула с ралоксифеном
Ингредиент
- Количество (мг/капсулу)
Ралоксифен - 1
Крахмал, NF - 112
Сыпучий крахмальный порошок - 225,3
Силиконовая жидкость 350 сантисток - 1,7
Лекарственная форма
3:
Капсула с ралоксифеном
Ингредиент - Количество (мг/капсулу)
Ралоксифен - 5
Крахмал, NF - 108
Сыпучий крахмальный порошок - 225,3
Силиконовая
жидкость 350 сантисток - 1,7
Лекарственная форма 4:
Капсула с ралоксифеном
Ингредиент - Количество (мг/капсулу)
Ралоксифен - 10
Крахмал, NF - 103
Сыпучий крахмальный порошок - 225,3
Силиконовая жидкость 350 сантисток - 1,7
Лекарственная форма 5:
Капсула с ралоксифеном
Ингредиент - Количество (мг/капсулу)
Ралоксифен - 50
Крахмал, NF - 150
Сыпучий крахмальный порошок - 397
Силиконовая жидкость 350 сантисток - 3,0
Вышеуказанные лекарственны формы могут быть
изменены в разумных пределах.
Таблетированные лекарственные формы готовят с использованием следующих ингредиентов:
Лекарственная форма 6:
Таблетки
Ингредиент
- Количество (мг/таблетку)
Активный ингредиент - 0,1 - 1 000
Микрокристаллическая целлюлоза - 0 - 650
Двуокись кремния - 0 - 650
Стеариновая кислота - 0 - 15
Компоненты смешиваются и прессуются в форме таблеток
В виде альтернативы таблетки, содержащие от 0,1 - до 1000 мг активного ингредиента каждая, готовятся следующим образом:
Лекарственная форма :
Таблетки
Ингредиент - Количество (мг/таблетку)
Активный ингредиент - 0,1 - 1 000
Крахмал - 45
Микрокристаллическая целлюлоза - 35
Поливинилпирролидон (в виде 10% водного раствора) - 4
Натрий-карбоксиметил целлюлоза - 4,5
Стеарат магния - 0,5
Тальк - 1,0
Активный ингредиент, крахмал и
целлюлоза пропускают через сито размером N 45 меш США и тщательно перемешиваются. Раствор поливинилпирролидона смешивали с полученным порошком и затем пропускали через сито N 14 меш США. Полученные
таким образом гранулы высушивали при 50-60oC и повторно пропускали через фильтр N 18 меш США. Натрий-карбоксиметил целлюлозу, стеарат магния и тальк, пропустив предварительно через фильтр N
60 меш, затем добавляли к гранулам, которые после тщательного прессовали в виде таблеток.
Суспензии содержащие каждая от 0,1 до 100 мг активного ингредиента в объеме 5 мл на одну дозу,
готовили следующим образом:
Лекарственная форма 8:
Суспензии
Ингредиент - Количество (мг/5 мл)
Активный ингредиент - 0,1 - 1000 мг
Натрий-карбоксиметилцеллюлоза - 50 мг
Сироп - 1,25 мл
Раствор бензойной кислоты - 0,10 мл
Ароматизатор - q.v.
Краситель - q.v.
Очищенная вода до - 5 мл.
Лекарственный препарат пропускали через сито меш США и смешивали с натрий карбоксиметилцеллюлозой и сиропом до образования равномерной пасты. Раствор бензойной кислоты, ароматизатор и краситель разводили с небольшим количеством воды, и вводили в массу при постоянном взбалтывания. Для получения требуемого объема ко всей взвеси добавляли необходимое количество воды.
Способ исследования
Для клинического излучения выбирали от 5 до 50 женщин. Все женщины находились в постменопаузе, т.е. не имели менструаций в течение 6-12 мес до начала
исследования, были как правило здоровы и жаловались на один или более из вышеперечисленных симптомов со стороны ЦНС. Ввиду идиосинкраического и субъективного характера указанных расстройств,
исследование включало контрольную группу женщин, получивших плацебо.
Таким образом, женщин делали на две группы, одна из которых получали активное соединение данного изобретения, и другая - плацебо. Женщины в подопытной группе получали перорально от 50 до 200 мг активного вещества в день. Такая терапия продолжалась от 3 до 12 месяцев. Точные протоколы учитывали количество и тяжесть вышеуказанных расстройств в обоих группах с последующим сравнением этих результатов в конце исследования. Сравнение результатов проводили между членами групп, а также для каждой женщины отдельно сравнивали симптоматику до и после лечения.
Эффективность соединений данного изобретения иллюстрируется положительным воздействием, которое они оказывают на одно или более расстройств ЦНС при описанной схеме лечения.
Реферат
Изобретение относится к медицине, конкретно - к гинекологии.
Предложено новое средство ингибирования одного или более расстройств ЦНС у женщин в постменопаузе, представляющее собой соединение формулы

где R1 и R3 являются независимо водородом -СН3,


где Ar является соответствующим образом замещенным фенилом;
R2 выбран из группы, состоящей из пирролидино-, гексаметиленимино-, и пиперидино-, или их фармацевтически приемлемых солей. Изобретение расширяет арсенал средств указанного назначения. 3 з.п. ф-лы.
Формула

где R1 и R3 являются независимо водородом, -CH3,
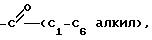

R2 выбран из группы, состоящей из пирролидино-, гексаметиленимино-, и пиперидино, или его фармацевтически приемлемых солей, для ингибирования одного или более расстройств ЦНС у женщин в периоде постменопаузы, включающих тревогу, депрессивное состояние, напряженность, раздражительность, мотивационные дефекты, снижение памяти и нарушение познавательной функции.
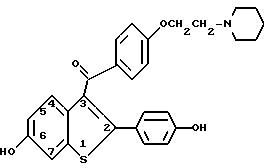
или его гидрохлоридом.
