(2s,4s)-4-амино-n-(4-фторфенил)пироглутаминовая кислота, обладающая церебропротекторным, ноотропным и антитромботическим действием - RU2769521C1
Код документа: RU2769521C1
Описание
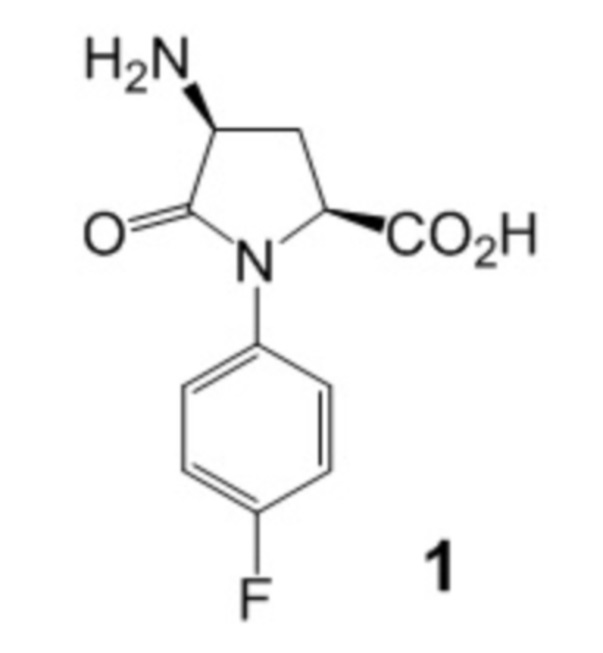
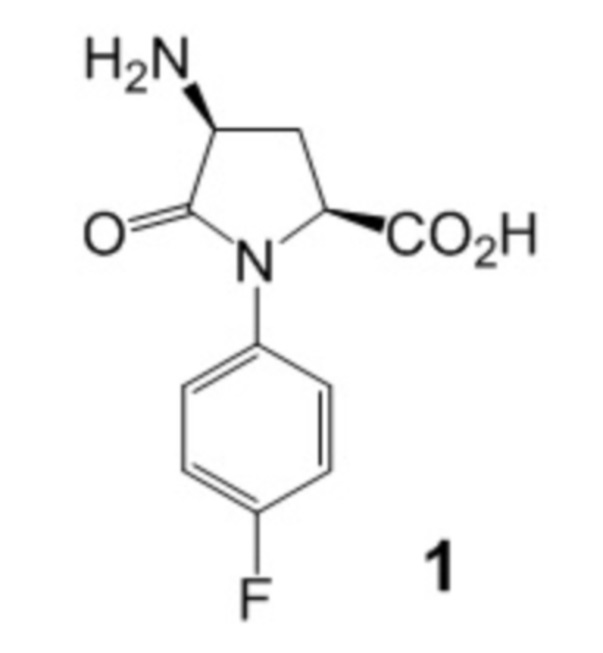
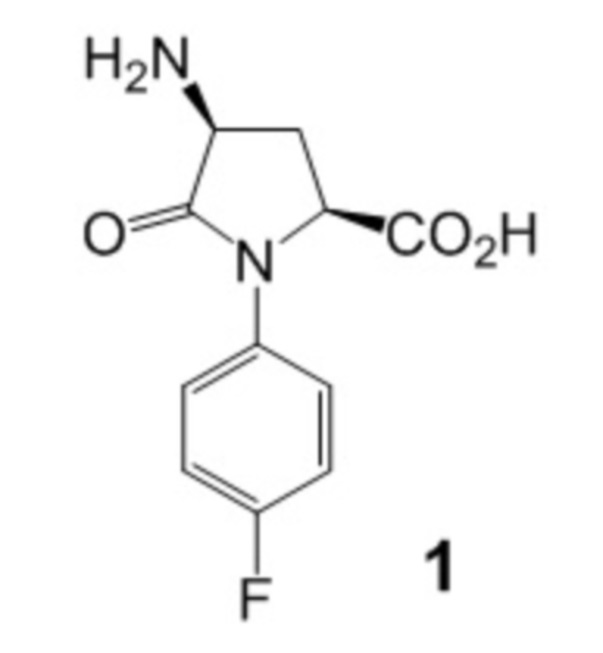
Изобретение относится к области медицины, производному пироглутаминовой кислоты, а именно, (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоте формулы 1 его способу получения и применения в качестве церебропротектора, которое может быть использовано для лечения последствий нарушений мозгового кровообращения и профилактики вторичных тромбозов.
Острые и хронические нарушения мозгового кровообращения (НМК) продолжают оставаться ведущей причиной инвалидизации и потери трудоспособности населения. Нарушения мелкой моторики, координации, памяти и обучаемости, развитие тревожно-депрессивных расстройств при нарушениях мозгового кровообращения снижают качество жизни и эффективность лечения пациента, являются целями фармакотерапии [Бойцов С.А., Шальнова С.А., Деев А.Д. Эпидемиологическая ситуация как фактор, определяющий стратегию действий по снижению смертности в Российской Федерации. Терапевтический архив. 2020;92(1):4-9].
Известно значительное число церебропротекторных средств и способов терапии и профилактики поражений головного мозга [Клинические рекомендации по ведению больных с ишемическим инсультом и транзиторными ишемическими атаками. Москва, 2017. 92 c.], в том числе препаратами с нейропротекторным действием, эффективность которых не всегда бывает достаточной [Путилина М.В. Комбинированное применение нейропротекторов в терапии цереброваскулярных заболеваний. Журнал неврологии и психиатрии им. C.C. Корсакова. 2016;116(11):58-63]. Поэтому имеется острая необходимость в разработке новых церебропротекторных средств, оказывающих нейропротекторное действие и положительно влияющих на реологические свойства крови в условиях нарушения мозгового кровообращения.
Среди производных пироглутаминовой кислоты известны препараты с противосудорожной, анксиолитической и ноотропной активностью (Таблица 1). При этом среди ближайших структурных аналогов (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоты о церебропротекторной активности в условиях нарушения мозгового кровообращения сведения отсутствуют.

Наиболее близким аналогом (прототипом) нашего технического решения является соединение фасорацетам, обладающее ноотропной активностью [Malykh A.G., Sadaie M.R. Piracetam and piracetam-like drugs: from basic science to novel clinical applications to CNS disorders. Drugs. 2010;70(3):287-312].
Аналогом исследуемого производного пироглутаминовой кислоты по фармакотерапевтическому действию является препарат цитиколин, который является компонентом фосфолипидов мембран клеток, а также предшественником ацетилхолина и применяется в острый и последующие периоды нарушения мозгового кровообращения с целью защиты нервной ткани и ускорения восстановления когнитивных функций [Сергеев Д.В., Домашенко М.А., Пирадов М.А. Цитиколин при ишемическом инсульте: от острого периода к реабилитации. Медицинский совет. 2015. № 18. С. 6-10].
Аналогом исследуемого соединения также является антиагрегантный препарат ацетилсалициловая кислота, который рекомендован для профилактики вторичных тромбозов в острый и последующие периоды инфаркта и инсульта [Клинические рекомендации по ведению больных с ишемическим инсультом и транзиторными ишемическими атаками. Москва, 2017. 92 c.].
Задача, которую решает предлагаемое изобретение, заключается в разработке нового соединения с высокой церебропротекторной активностью, которое реализуется за счет наличия у патентуемого средства ноотропной и антитромботической активности, что позволит расширить номенклатуру эффективных средств для лечения последствий нарушения мозгового кровообращения и профилактики повторных тромбозов.
Техническим результатом данного изобретения является создание нового химического соединения – (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоты (1):

Соединение 1, его физико-химические характеристики, биологическая активность, а также способ его получения в литературе не описаны.
Соединение формулы (1) может быть получено в две стадии из доступного [Krasnov V.P., Bukrina I.M., Zhdanova E.A., Kodess M.I., Korolyova M.A. Synthesis, 1994, 961–964] диметилового эфира (2S,4RS)-4-бром-N-фталоилглутаминовой кислоты (2).
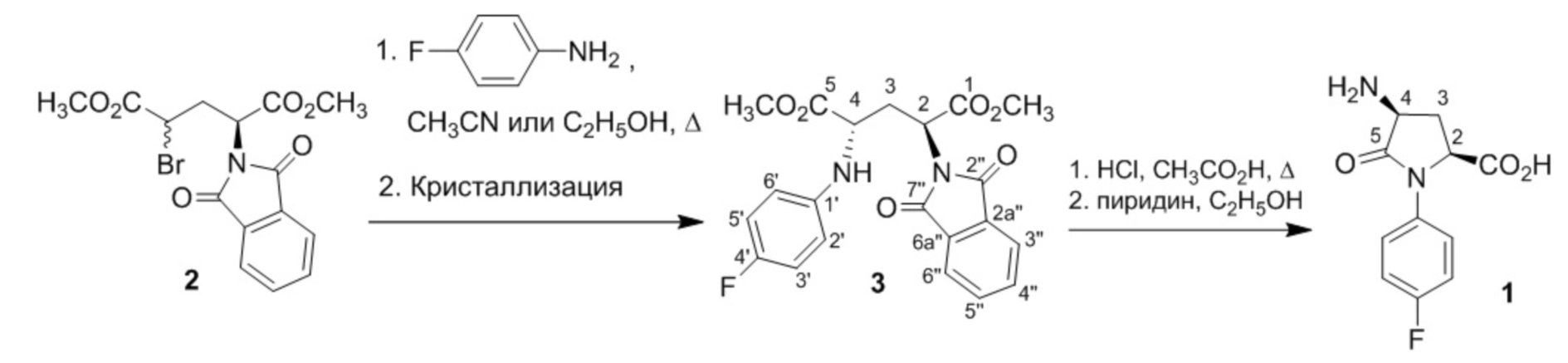
Соединение 2 вводят в реакцию с 4-фторанилином в ацетонитриле или этаноле. В результате выделяют диметиловый эфир (2S,4S)-4-(4-фторфенил)-N-фталоилглутаминовой кислоты (3), кислотный гидролиз которого в смеси соляной и уксусной кислот приводит к целевому соединению 1.
Характеристики нового соединения 1 приведены в примерах конкретного выполнения.
Структуру полученного соединения подтверждают методами спектроскопии ЯМР1H,13С,19F и элементного анализа. Индивидуальность соединения подтверждают методами ТСХ и ВЭЖХ.
Температуры плавления соединения 1 определены на приборе Stuart SMP3 (Barloworld Scientific).
Элементный анализ выполнен на автоматическом CHNS-O анализаторе РE 2400 серия II (Perkin Elmer).
Удельное вращение [(град·мл)/(г·дм)] определяли на поляриметре Perkin Elmer Model 341, концентрация раствора в г/100 мл.
Спектры ЯМР1H и13С зарегистрированы на приборе Bruker Avance 500 (500 МГц для1Н, 126 МГц для13С) при 24 °С в CDCl3 с Si(СН3)4 в качестве внутреннего стандарта (для соединения 3) и в D2O c триметилсилилпропансульфонатом натрия (DSS) в качестве внутреннего стандарта (для соединения 1). Спектры19F зарегистрированы на приборе Bruker Avance 500 (470 МГц) при 24 °С в CDCl3 с гексафторбензолом в качестве внутреннего стандарта (для соединения 3) и в D2O с гексафторбензолом в качестве внешнего стандарта (для соединения 1). Химические сдвиги (δ) приведены в миллионных долях (м.д.), а константы спин-спинового взаимодействия (J) в герцах (Гц).
Аналитическая ВЭЖХ выполнена на жидкостном хроматографе «Knauer Smartline-1100», колонка Reprosil (250×4,6 мм), детектирование при длинах волн 220 и 230 нм, элюирование системой гексан-изопропиловый спирт, 80 : 1. Скорость потока 1,0 мл/мин.
Для ТСХ использованы пластинки Sorbfil (OOO «Имид», Россия). Проявление в УФ свете.
Исследования in vitro и in vivo были выполнены с использованием беспородных крыс-самцов (Филиал «Столбовая» ГУ НЦБМТ РАМН, Московская обл.), которых содержали в стандартных условиях вивария со свободным доступом к воде и корму (ГОСТ Р 51849-2001). Для оценки фармакологических свойств, демонстрирующих церебропротекторный потенциал, а также непосредственно церебропротекторные свойства (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоты формулы 1 были использованы следующие методы [Руководство по проведению доклинических исследований лекарственных средств: под ред. А.Н. Миронова. Ч.1. М.: Гриф и К,2012.944 с.]:
I. Оценка антиагрегантной активности in vitro.
1. Оценка влияния исследуемых соединений на степень АДФ-индуцируемой агрегации тромбоцитов in vitro.
II. Оценка антитромботической активности in vivo при курсовом введении.
1. Оценка антитромботической активности на модели артериального тромбоза.
2. Оценка антитромботической активности на модели тромбоза глубоких вен.
III. Оценка психотропной активности, при однократном введении интактным животным.
1. Оценка влияния на двигательную и исследовательскую активность в тесте Открытое поле.
2. Оценка противотревожной активности в тесте Приподнятый крестообразный лабиринт» (ПКЛ).
3. Оценка ноотропной активности в тесте «экстраполяционного избавления» (ТЭИ).
IV. Оценка церебропротекторной активности при лечебном курсовом введении соединения 1 с экспериментальным нарушением мозгового кровообращения (НМК).
1. В тесте Открытое поле: оценка двигательной и исследовательской активности у животных с экспериментальным НМК.
2. В адгезивном тесте: оценка сенсорно-моторной функции.
3. В тесте Ротарод: оценка координации движений.
4. В тесте распознавание нового объекта (РНО) и тесте «экстраполяционного избавления» (ТЭИ): оценка когнитивной функции.
V. У животных с экспериментальным НМК определяли степень АДФ-индуцируемой агрегации тромбоцитов in vitro.
VI. Изучение острой токсичности исследуемого соединения.
Примеры конкретного выполнения
Пример 1. Синтез (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоты (1)
Раствор 11,08 г (28,84 ммоль) диметилового эфира (2S,4RS)-4-бром-N-фталоилглутаминовой кислоты (2) и 8,2 мл (86,52 ммоль, 3,0 экв.) 4-фторанилина кипятят в 65 мл ацетонитрила в течение 24 часов. После охлаждения до комнатной температуры отфильтровывают осадок гидробромида амина, фильтрат упаривают, остаток растворяют в хлороформе (250 мл), промывают 1 М HCl (3 раза по 80 мл) и водой (2 раза по 80 мл). Органический слой сушат над Na2SO4, упаривают, получают диметиловый эфир 4-(4-фторфенил)-N-фталоилглутаминовой кислоты (11,58 г, 97%) в виде смеси (2S,4S)- и (2S,4R)-изомеров в соотношении 3 : 1. ВЭЖХ: для (2S,4S)-изомера tR = 15,7 мин, для (2S,4R)-изомера tR = 14,1 мин.
Данную смесь кристаллизуют из 95% этилового спирта три раза. Получают 6,62 г (55% в расчёте на соединение 2) диметилового эфира (2S,4S)-4-(4-фторфенил)-N-фталоилглутаминовой кислоты (3) в виде светло-жёлтых кристаллов. Т пл. = 135–136 °С. [α]D20 = –35,2 (c 1; CHCl3). Найдено: С 60,94; Н 4,68; N 6,60; F 4,48. Вычислено для С21Н19N2О6F (М = 414,39): С 60,87; Н 4,62; N 6,76; F 4,58. Спектр ЯМР1Н (500 МГц, CDCl3): 2,67 (д.д.д, 1 Н, C3HB Glu, J = 14,5; 9,2; 4,2 Гц); 2,76 (д.д.д, 1 Н, C3HA, J = 14,5; 9,6; 4,2 Гц); 3,67 (c, 3 Н, CH3О); 3,74 (c, 3 Н, CH3О); 3,96 (уш. д.д, 1 Н, C4Н, J = 9,1; 4,3 Гц); 4,03 (уш. с, 1 Н, NH); 5,24 (д.д, 1 Н, С2H, J = 9,6; 4,1 Гц); 6,53 (м, 2 Н, C2’H, C6’H); 6,80 (м, 2 Н, C3’H, C5’H); 7,76 (м, 2 Н, Phth); 7,87 (м, 2 Н, Phth). Спектр ЯМР13С (126 МГц, CDCl3): 32,24 (C3); 48,87 (C2); 52,40 (С5О2СН3); 53,03 (С1О2СН3); 55,40 (C4); 115,68 (д, C2’, C6’, J = 7,6 Гц); 115,69 (д, C3’, C5’, J = 22,4 Гц); 123,65 (C3’’, C6’’); 131,69 (C2а’’, C6а’’); 134,32 (C4’’, C5’’); 142,56 (д, C1’, J = 2,0 Гц); 156,70 (д, C4’, J = 237,0 Гц); 167,38 (C2’’, C7’’); 169,38 (С1О2СН3); 173,47 (С5О2СН3). Спектр ЯМР19F (470 МГц, CDCl3): 35,97 (т.т, С4’F, J = 8,6; 4,3 Гц). ВЭЖХ: tR = 15,7 мин.
К 6,62 г (15,97 ммоль) диметилового эфира (2S,4S)-4-(4-фторфенил)-N-фталоилглутаминовой кислоты (3) приливают 30 мл конц. водн. HCl и 30 мл ледяной уксусной кислоты. Кипятят в течение 12 часов, упаривают досуха, остаток обрабатывают 20% HCl при перемешивании (30 мл), после выдерживания при 0…+10 °С в течение ночи отфильтровывают осадок фталевой кислоты, фильтрат упаривают досуха, остаток высушивают в вакууме, растворяют в 95% водном этиловом спирте (20 мл) и добавляют пиридин (1,4 мл). После охлаждения в холодильнике (0…+10 °С) в течение ночи отфильтровывают осадок, промывают на фильтре 95% водным этиловым спиртом, сушат в вакууме при 120 °С в течение 3 часов. Получают 2,49 г (65% в расчёте на соединение 3) соединения 1 в виде бесцветного твердого вещества. Т пл = 233–236 °С (с разл.). [α]D20 = –42,4 (c 1; H2O). Найдено: С 55,41; Н 4,61; N 11,71; F 7,77. Вычислено для С11Н11N2О3F (М = 238,22): С 55,46; Н 4,65; N 11,76; F 7,98. Спектр ЯМР1Н (500 МГц, D2O): 2,15 (д.д.д, 1 Н, C3HB, J = 13,2; 9,3; 8,4 Гц); 3,08 (д.д.д, 1 Н, C3HA, J = 13,2; 9,0; 7,2 Гц); 4,37 (т, 1 Н, C4H, J = 9,3 Гц); 4,77 (т, 1 Н, C2H, J = 7,4 Гц); 7,22 (м, 2 Н, C3’H, C5’H); 7,42 (м, 2 Н, C2’H, C6’H). Спектр ЯМР13С (126 МГц, D2O): 30,79 (C3); 53,46 (C4); 64,57 (C2); 118,81 (д, C3’, C5’, J = 23,0 Гц); 127,78 (д, C2’, C6’, J = 8,8 Гц); 135,33 (д, C1’, J = 2,9 Гц); 163,66 (д, C4’, J = 244,5 Гц); 172,78 (C5); 179,04 (CО2Н). Спектр ЯМР19F (470 МГц, D2O): 47,82 (т.т, С4’F, J = 8,7; 4,8 Гц).
Соединение 1 из 70% водного этилового спирта кристаллизуется в виде дигидрата. Найдено: С 48,49; Н 5,51; N 10,11. Вычислено для С11Н11N2О3F × 2 H2O (М = 274,25): С 48,18; Н 5,51; N 10,21. Спектры ЯМР1Н (500 МГц, D2O) и19F (470 МГц, D2O) идентичны спектрам безводной формы.
Пример 2. Влияние (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоты (1) на степень АДФ-индуцируемой агрегации тромбоцитов in vitro
Антиагрегантную активность оценивали по степени АДФ-индуцированной агрегации тромбоцитов после инкубации 270 мкл плазмы (богатой тромбоцитами) с изучаемым соединением (в объеме 30 мкл), в диапазоне его молярных конечных концентраций 1×10−5 М – 1×10−8 М, а также с препаратом сравнения (ацетилсалициловая кислота, АСК) в аналогичных концентрациях. Плазму получали из крови интактных крыс. В качестве контроля использовали дистиллированную воду. Препаратом сравнения выступала ацетилсалициловая кислота (АСК), как антиагрегантное средство, обладающее наиболее оптимальным соотношением эффективности и безопасности, и широко применяемое в клинической практике. Соединение 1 снижало степень агрегации тромбоцитов в концентрации 10−7 М на 30%, 10−6 М на 29,8% и 10−5 М на 37,8% относительно контроля, что сопоставимо с показателями препарата сравнения и даже их немного превышает (Таблица 2).

Пример 3. Оценка антитромботической активности (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоты (1) in vivo на модели артериального тромбоза и тромбоза глубоких вен
Антитромботическую активность производного пироглутаминовой кислоты оценивали на моделях артериального (аппликация хлорида железа (III) на адвентицию сонной артерии) и венозного (перевязкой нижней полой вены) тромбозов, при курсовом профилактическом (3 дня, 1 раз в сутки, последнее введение осуществляли за 60 минут до моделирования тромбоза) пероральном введении в дозе 27 мг/кг.
В условиях формирования артериального тромба в сонной артерии при аппликации FeCl3 было выявлено, что исследуемое производное пироглутаминовой кислоты 1 и препарат сравнения ацетилсалициловая кислота вызывали значительное пролонгирование формирования тромба (Таблица 3). При оценке массы венозного тромба через 24 часа, после перевязки нижней полой вены (выше слияния бедренных вен) было отмечено, что при предварительном введении соединения 1, а также препарата сравнения при перевязке нижней полой вены масса извлекаемого из сосуда тромба была меньше, чем в контрольной группе. Данные результаты полностью согласуются с полученными на предыдущем этапе и указывают на наличие антиагрегантной и антитромботической активности патентуемого соединения 1.

Пример 4. Оценка психотропной активности (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоты (1), при однократном введении интактным животным
Влияние соединения 1 на психоэмоциональное состояние интактных животных (двигательную и ориентировочно-исследовательскую активность) оценивали в тестах Открытое поле (ОП), на уровень тревоги в тесте «Приподнятый крестообразный лабиринт» (ПКЛ) и на сохранность памятного следа в «Тесте экстраполяционного избавления» (ТЭИ), после его однократного перорального введения в дозе 27 мг/кг.
Влияние на поведенческую активность
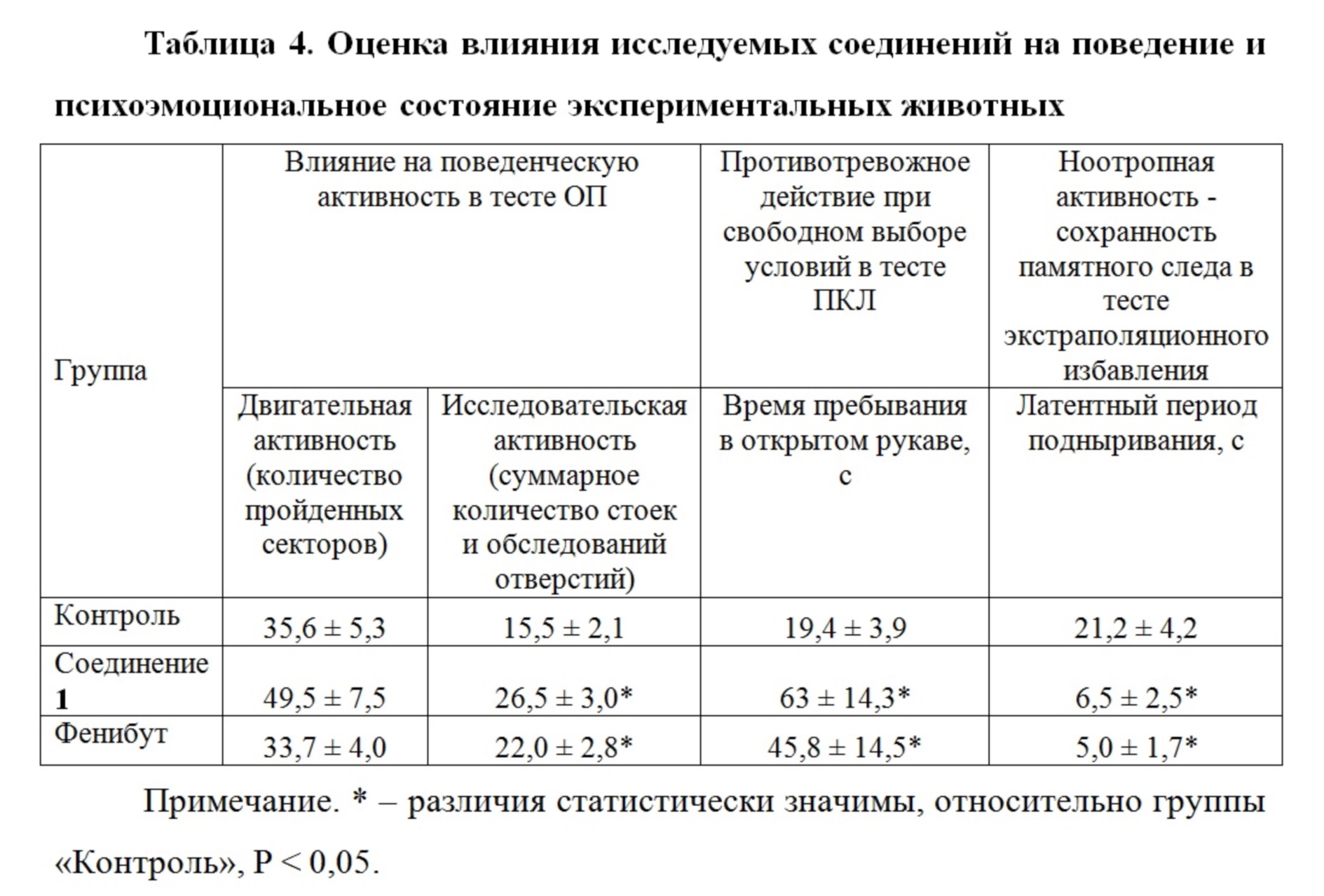
В тесте «Открытое поле» двигательная активность животных (количество пройденных секторов), которым вводили патентуемое соединение 1, значимо не отличалась от регистрируемой у животных контрольной группы, но их показатели ориентировочно-исследовательской активности (суммарное количество стоек и обследований отверстий) были выше, чем у контрольных животных (Таблица 4).
Противотревожное действие
Тест приподнятый крестообразный лабиринт (ПКЛ) используется для изучения поведения грызунов в условиях переменной стрессогенности (при свободном выборе комфортных условий), позволяет оценить уровень тревожности животного и применяется для выявления соединений с анксиолитической активностью. Животные, которым вводили соединение 1, более чем в 3 раза дольше пребывали в открытых рукавах установки в сравнении с контрольной группой (Таблица 4), что свидетельствует о снижении уровня тревоги и подавлении чувства страха.
Ноотропная активность
Результаты теста экстраполяционного избавления (ТЭИ) свидетельствуют о положительном влиянии соединения 1 на формирование и сохранение памятного следа. Животные, которым вводили патентуемое соединение 1, быстрее справлялись с решением экстраполяционной задачи и избавлялись от влияния аверсивной среды (на уровне препарат сравнения фенибут). Под действием соединения 1 латентный период подныривания сокращался на 69% относительно контрольной группы животных (Таблица 4), что позволяет предположить наличие ноотропной активности соединения 1.
Полученные результаты показывают наличие не только антитромботического, но и выраженного противотревожного и ноотропного действия у соединения 1. Можно предположить, что вещество с такими свойствами может оказаться эффективным при нарушении мозгового кровообращения, следствием которого часто являются когнитивные и тревожные расстройства.
Пример 5. Оценка церебропротекторной активности (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоты (1) при лечебном курсовом введении животным с нарушением мозгового кровообращения
Нарушение мозгового кровообращения (НМК) моделировали одномоментной необратимой окклюзией общих сонных артерий. Через 24 часа, после операции была проведена оценка уровня неврологического дефицита и распределение по группам. В исследование не включали животных, проявляющих выраженный неврологический дефицит по шкале Combs and D'Alecy. После распределения по группам, исследуемое соединение и референтные препараты вводили перорально в течение 7 дней.
Церебропротекторную активность (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоты (1) оценивали по двигательной и исследовательской активности, сенсорно-моторной и когнитивной функции после лечебного 7 дневного курсового введения у животных с нарушением мозгового кровообращения.
Оценка влияния на двигательную и исследовательскую активность в тесте Открытое поле.
В тесте Открытое поле животные контрольной группы двигались меньше ложнооперированных. Курсовое введение патентуемого соединения и препарата сравнения фасорацетам способствовало значительному повышению двигательной и исследовательской активностей в тесте Открытое поле (Таблица 5).

Оценка влияния на координацию движений в тесте Ротарод
Одномоментная окклюзия общих сонных артерий значительно нарушала координацию движений подопытных животных в тесте Ротарод: среднее время удержания на вращающемся стержне в контрольной группе было на 89% ниже, чем у ложнооперированных (Таблица 5). У животных, которым вводили соединение 1, время удержания на вращающемся стержне было статистически значимо выше (на уровне препаратов сравнения цитиколин и фасорацетам).
Оценка влияния на сенсорно-моторную функцию в адгезивном тесте
У животных с НМК отмечались выраженные сенсорно-моторные нарушения. Так, в адгезивном тесте, животные контрольной группы значительно дольше не обращали внимание на инородный объект (стикер) и не устраняли его с ладонной поверхности передних лап (в 9 и 8, раз соответственно), чем ложнооперированные (Таблица 5). Крысы с НМК, которым вводили соединение 1, значимо быстрее обнаруживали и удаляли инородный предмет (на уровне препарата сравнения цитиколина), что свидетельствует о лучшем восстановлении сенсорно-моторных функций у животных с НМК. Фасорацетам эффекта не давал.
Оценка влияния на когнитивную функцию в тесте распознавание нового объекта и тесте «экстраполяционного избавления» (ТЭИ)
В тесте распознавание нового объекта в ходе оценки индекса дискриминации, при повторном предъявлении старого объекта вместе с новым, животные с НМК без лечения практически в равной степени уделяли внимание обоим объектам (Таблица 5), что указывает на выраженные нарушения кратковременной памяти. В опытных группах те животные, которым вводили соединение 1, значимо большее время (по сравнению с контролем) уделяли изучению нового объекта (на уровне препарата сравнения цитиколина).
В тесте «экстраполяционного избавления», при воспроизведении выученного навыка через 7 дней после моделирования НМК оценивали влияние проведенной терапии на сохранность памятного следа (долговременную память). В контрольной группе (без лечения) крысы тратили значительное большее количество времени на решение экстраполяционной задачи, по сравнению с группой ложнооперированных (Таблица 5), и только в группе, которой вводили соединение 1, животные значимо быстрее решали задачу экстраполяционного избавления в стрессовых условиях. Это может быть связано с противотревожным действием патентуемого соединения.
Пример 6. Оценка влияния на степень агрегации тромбоцитов в условиях экспериментального нарушения мозгового кровообращения
После лечебного 7 дневного курсового введения (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоты (1) у животных с нарушением мозгового кровообращения оценивали степень АДФ-индуцируемой агрегации тромбоцитов.
АДФ-индуцируемая агрегация тромбоцитов у животных с нарушением мозгового кровообращения, была значительно выше, чем в группе без лечения (Таблица 6). Нормальная функция тромбоцитов наблюдалась только в группах, животным которых вводили соединение 1 или препарат сравнения – ацетилсалициловую кислоту.
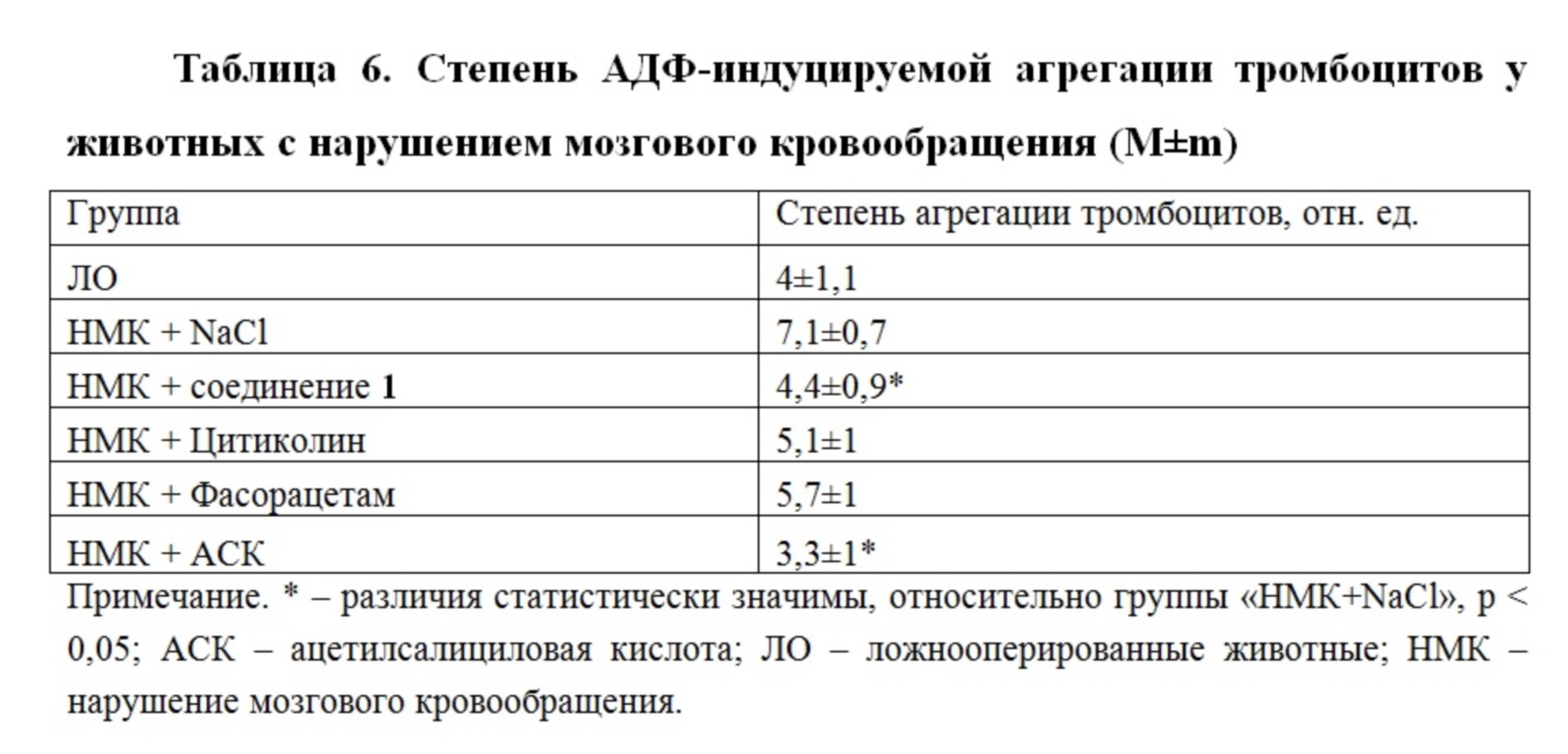
Таким образом (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовая кислота (1), обладает антиагрегантной, ноотропной и противотревожной активностью. В условиях экспериментального нарушения мозгового кровообращения проявляет выраженное церебропротекторное действие, которое превышает по выраженности таковое у препаратов сравнения – фасорацетама и цитиколина.
Пример 7. Исследование острой токсичности (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоты (1)
Острую токсичность, соединения 1 определяли при его однократном, внутрижелудочном введении в дозах 1000, 1500, 2000 и 3000 и 3500 мг/кг. Непрерывное наблюдение за животными осуществляли в течение нескольких часов, а затем мыши помещались в домашнюю клетку и в последующем осматривались 1 раз в день в течение 14 дней. Гибель 50% животных наблюдалось, только после введения патентуемого соединения в дозе 3500 мг/кг. Обозначенные результаты позволяют отнести патентуемое соединение к малотоксичным с большой широтой терапевтического эффекта (с учетом величины эффективной дозы в пределах 27 мг/кг).
Реферат
Изобретение относится новому производному пироглутаминовой кислоты - (2S,4S)-4-амино-N-(4-фторфенил)пироглутаминовой кислоте формулы 1. Технический результат: получено новое соединение, которое может быть применимо в качестве церебропротектора с ноотропной и антитромботической активностью. 6 табл., 7 пр.
Формула

Комментарии