(Гетеро)арилциклопропиламины в качестве ингибиторов lsd1 - RU2668952C2
Код документа: RU2668952C2
Описание
Настоящее изобретение относится к (гетеро)арилциклопропиламинам, предпочтительно к соединениям формулы I, Ia, Ia-1, Ib и Ic, более предпочтительно к соединениям формулы I и Iа, описанным и определенным в настоящем изобретении, и к их применению в терапии, включая, например, лечение или предупреждение рака, неврологического заболевания или патологического состояния или вирусной инфекции.
Общей характеристикой многих заболеваний человека является аберрантная экспрессия генов в пораженной ткани в отличие от нормальной ткани. Это относится к раку и неврологическим заболеваниям, которые характеризуются изменениями характера экспрессии генов. Характер экспрессии генов регулируется в клетке на многих уровнях. Регулирование экспрессии генов может происходить с помощью модификаций ДНК: метилирование промотора ДНК связано с подавлением экспрессии генов. Различные ингибиторы метилирования ДНК утверждены для клинического применения, включая мощное средство видазутм. Другой класс модификаций включает модификации гистонов, которые образуют белковый каркас, с которым обычно связана ДНК (обернута вокруг) в эукариотных клетках. Гистоны играют критическую роль в организации ДНК и регулируют обертывание ДНК вокруг гистонов и ее развертывание, что критически важно для регулирования экспрессии генов - обернутая ДНК обычно недоступна для транскрипции генов. Обнаружен целый ряд модификаций гистонов, включая продукты ацетилирования гистона, метилирования лизина гистона, метилирования аргинина гистона, убиквинилиривание гистона и сумоилирование гистона, многие из которых модифицируют доступность ассоциированной ДНК с помощью механизма клеточной транскрипции. Эти гистонные метки служат для рекрутинга различных комплексов белков, участвующих в транскрипции и репрессии. Все увеличивающееся количество исследований направлено на изображение того, как различные комбинации гистонных меток регулируют экспрессию генов клеточноспецифическим образом и для описания этого подхода предложен новый термин: гистонный код.
Прототипической гистонной меткой является ацетилирование гистона. Гистонацетилтрансфераза и гистондезацетилазы являются катализаторами, участвующими в модуляции этой гистонной метки, хотя обычно эти ферменты являются частями мультипротеиновых комплексов, содержащих другие белки, участвующие в считывании и модификации гистонных меток. Компоненты этих белковых комплексов обычно являются клеточноспецифическими и обычно представляют собой регуляторы транскрипции, репрессоры, сорепрессоры, рецепторы, связанные с модуляцией экспрессии генов (например, эстрогенный или андрогенный рецептор). Ингибиторы гистондезацетилазы меняют профиль ацетилирования хроматина гистона. В соответствии с этим показано, что ингибиторы гистондезацетилазы, такие как вориностат (САГК (субероиланилид гидроксамовой кислоты)), трихостатин A (TSA) и многие другие, меняют экспрессию генов в различных моделях на животных in vitro и in vivo. Клинически показано, что ингибиторы гистондезацетилазы обладают активностью при раке и исследовано их применение в онкологии, а также при неврологических патологических состояниях и других заболеваниях.
Другой модификацией, которая участвует в регуляции экспрессии генов, является метилирование гистона, включая метилирование лизина и аргинина. Недавно показано, что статус метилирования лизинов гистонов важен для динамической регуляции экспрессии генов.
В модификациях лизина гистона участвует группа ферментов, известных, как гистонлизинметилтрансферазы и гистонлизиндеметилазы. Недавно было установлено (Shi et al. (2004) Cell 119:941), что одна конкретная гистонлизиндеметилаза человека под названием лизинспецифическая деметилаза-1 (LSD1) участвует в этой критически важной модификации гистона. LSD1 характеризуется значительным структурным сходством и идентичности/гомологии аминокислот с полиаминоксидазами и моноаминоксидазами, каждая из которых (т.е. МАО-А, МАО-В и LSD1) является зависимой от флавина аминоксидазой, которые катализируют окисление связей азот-водород и/или связей азот-углерод. Установлено, что LSD1 представляет собой привлекательную мишень для разработки новых лекарственных средств, предназначенных для лечения рака, неврологических заболеваний и других патологических состояний.
Известно, что содержащие циклопропиламин соединения ингибируют целый ряд важных для медицины мишеней, включая аминоксидазы, такие как моноаминоксидаза А (МАО-А или МАОА), моноаминоксидаза В (МАО-В или МАОВ) и лизинспецифическая деметилаза-1 (LSD1). Известно, что транилципромин (также известный под названием 2-фенилциклопропиламин), который является активным ингредиентом препарата парнат® и одним из самых известных примеров циклопропиламина, ингибирует все эти ферменты. Поскольку ингибирование МАО-А может привести к нежелательным побочным эффектам, желательно выявить производные циклопропиламина, которые обладают высокой ингибирующей активностью по отношению к LSD1 и при этом не обладают или обладают значительно сниженной ингибирующей активностью по отношению к МАО-А.
Ввиду отсутствия адекватных средств лечения таких патологических состояний, как рак и нейродегенерация, настоятельно необходимы лекарственные средства, влияющие на заболеваний, и лекарственные средства, которые воздействуют путем ингибирования новых мишеней. Поэтому необходима разработка ингибиторов LSD1, в особенности таких, которые селективно ингибируют LSD1.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к выявлению соединений и их применению для лечения или предупреждения заболеваний. Настоящее изобретение относится к (гетеро)арилциклопропиламинам, включая соединения формулы I, Ia, Ia-1, Ib и Ic, и предпочтительно соединения формулы I, Ia и Ia-1, описанные и определенные в настоящем изобретении. Настоящее изобретение, в частности, относится к соединению формулы I, Ia, Ia-1, Ib и Ic, и предпочтительно к соединению формулы I, Ia и Ia-1, к фармацевтическим композициям, содержащим соединение формулы I, Ia, Ia-1, Ib или Ic, и предпочтительно соединение формулы I, Ia или Ia-1, и фармацевтически приемлемый носитель, и к их применению для лечения заболеваний. Одним применением соединения формулы I, Ia, Ia-1, Ib и Ic является применение для лечения или предупреждения рака. Другим применением соединения формулы I, Ia, Ia-1, Ib и Ic является ингибирование LSD1. Таким образом, настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic, и предпочтительно к соединению формулы I, Ia или Ia-1, предназначенному для применения для лечения или предупреждения заболевания человека. Настоящее изобретение также относится к соединению формулы I, Ia, Ia-1, Ib или Ic, и предпочтительно к соединению формулы I, Ia и Ia-1, предназначенному для применения для лечения или предупреждения рака. Настоящее изобретение также относится к соединению формулы I, Ia, Ia-1, Ib или Ic, и предпочтительно к соединению формулы I, Ia и Ia-1, предназначенному для применения для лечения или предупреждения неврологического заболевания. Настоящее изобретение также относится к соединению формулы I, Ia, Ia-1, Ib или Ic, и предпочтительно к соединению формулы I, Ia и Ia-1, предназначенному для применения для лечения или предупреждения вирусной инфекции.
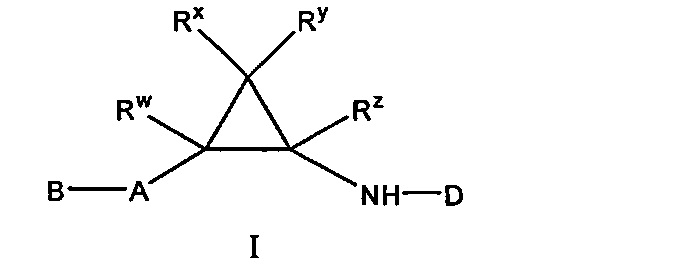
В соответствии с этим, настоящее изобретение относится к соединению формулы I:

в которой:
А обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R1;
B обозначает водород, R1 или -L-E;
E обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R2;
L обозначает связь, -O-, -NH-, -N(C1-C4-алкил)-, C1-C4-алкилен или гетеро-C1-C4-алкилен;
D обозначает циклоалкильную группу, содержащую от 4 до 7 атомов C, где указанная циклоалкильная группа содержит 1 или 2 заместителя R3 и дополнительно необязательно замещена одним или большим количеством R4 и где циклоалкильная группа необязательно:
(a) сконденсирована с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связана с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связана со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
каждый R1 независимо выбран из группы, включающей C1-C8-алкил, C2-C8-алкенил, C2-C8-алкинил, циклил, аминогруппу, амидную группу, гидроксигруппу, нитрогруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфинил, сульфонил, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, О-карбоксигруппу, С-карбоксигруппу, карбаматную группу и мочевинную группу;
каждый R2 независимо выбран из группы, включающей C1-C8-алкил, C2-C8-алкенил, C2-C8-алкинил, циклил, аминогруппу, амидную группу, гидроксигруппу, нитрогруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфинил, сульфонил, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, О-карбоксигруппу, С-карбоксигруппу, карбаматную группу и мочевинную группу;
каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -NR9SO2NR7R8, -OH, -CONR7R8, оксогруппу, -C1-C4-aлкилeн-NR7R8, -C1-C4-алкилен-NHOH, -C1-C4-aлкилeн-NR9COR10, -C1-C4-алкилен-NR9SO2R10, -C1-C4-алкилен-NR9COOR10, -C1-C4-aлкилeн-NR9CONR7R8, -C1-C4-алкилен-NR9SO2NR7R8, -C1-C4-алкилен-OH и -C1-C4-алкилен-CONR7R8;
каждый R4 и каждый R6 независимо выбран из группы, включающей C1-C8-алкил, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу и C1-C8-алкоксигруппу;
каждый R5 независимо выбран из группы, включающей C1-C8-алкил, C2-C8-алкенил, C2-C8-алкинил, циклил, аминогруппу, амидную группу, гидроксигруппу, нитрогруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфинил, сульфонил, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, О-карбоксигруппу, С-карбоксигруппу, карбаматную группу и мочевинную группу;
каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил и гидрокси-C1-C8-алкил, или R7 и R8 связаны друг с другом и вместе с атомом N, к которому они присоединены, образуют насыщенное 3-7-членное гетероциклическое кольцо, которое необязательно содержит один дополнительный гетероатом, выбранный из группы, включающей N, О и S, где один или большее количество атомов C указанного гетероциклического кольца необязательно окислены с образованием групп CO, где один или большее количество атомов S указанного гетероциклического кольца, если они содержатся, необязательно окислены с независимым образованием групп SO или групп SO2, и где указанное гетероциклическое кольцо необязательно замещено одним или большим количеством R11;
каждый R9 независимо выбран из группы, включающей водород и C1-C4-алкил; каждый R10 независимо выбран из группы, включающей C1-C8-алкил, галоген-C1-C8-алкил, циклил и циклил-C1-C8-алкил, где указанный циклил или циклильный фрагмент, содержащийся в указанном циклил-C1-C8-алкиле, необязательно замещен одним или большим количеством R14; каждый R11 независимо выбран из группы, включающей C1-C8-алкил, галоген, C1-C8-алкоксигруппу, гидроксигруппу и -NR12R13;
каждый R12 и каждый R13 независимо выбран из группы, включающей водород и C1-C8-алкил;
каждый R14 независимо выбран из группы, включающей C1-C8-алкил, C2-C8-алкенил, C2-C8-алкинил, аминогруппу, амидную группу, гидроксигруппу, нитрогруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфинил, сульфонил, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, О-карбоксигруппу, С-карбоксигруппу, карбаматную группу и мочевинную группу; и
каждый Rw, Rx, Ry и Rzнезависимо выбран из группы, включающей водород, галоген и C1-C4-алкил;
при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол.
Кроме того, предпочтительно, если исключен 2-((2-фенилциклопропил)амино)циклогексанол.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, в которой Rw, Rx, Ry и Rz все обозначают водород, т.е. к соединению формулы Iа:

в которой:
А обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R1;
B обозначает водород, R1 или -L-E;
E обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R;
L обозначает связь, -O-, -NH-, -N(C1-C4-алкил)-, C1-C4-алкилен или гетеро-C1-C4-алкилен;
D обозначает циклоалкильную группу, содержащую от 4 до 7 атомов C, где указанная циклоалкильная группа содержит 1 или 2 заместителя R3 и дополнительно необязательно замещена одним или большим количеством R4 и где циклоалкильная группа необязательно:
(a) сконденсирована с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связана с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связана со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
каждый R1 независимо выбран из группы, включающей C1-C8-алкил, C2-C8-алкенил, C2-C8-алкинил, циклил, аминогруппу, амидную группу, гидроксигруппу, нитрогруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфинил, сульфонил, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, О-карбоксигруппу, С-карбоксигруппу, карбаматную группу и мочевинную группу;
каждый R2 независимо выбран из группы, включающей C1-C8-алкил, C2-C8-алкенил, C2-C8-алкинил, циклил, аминогруппу, амидную группу, гидроксигруппу, нитрогруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфинил, сульфонил, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, О-карбоксигруппу, С-карбоксигруппу, карбаматную группу и мочевинную группу;
каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -OH, -CONR7R8, оксогруппу, -C1-C4-aлкилeн-NR7R8, -C1-C4-алкилен-NHOH, -C1-C4-aлкилeн-NR9COR10, -C1-C4-алкилен-NR9SO2R10, -C1-C4-алкилен-NR9COOR10, -C1-C4-алкилен-NR9CONR7R8, -C1-C4-алкилен-NR9SO2NR7R8, -C1-C4-алкилен-OH и -C1-C4-алкилен-CONR7R8;
каждый R4 и каждый R6 независимо выбран из группы, включающей C1-C8-алкил, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу и C1-C8-алкоксигруппу;
каждый R5 независимо выбран из группы, включающей C1-C8-алкил, C2-C8-алкенил, C2-C8-алкинил, циклил, аминогруппу, амидную группу, гидроксигруппу, нитрогруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфинил, сульфонил, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, О-карбоксигруппу, С-карбоксигруппу, карбаматную группу и мочевинную группу;
каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил и гидрокси-C1-C8-алкил, или R7 и R8 связаны друг с другом и вместе с атомом N, к которому они присоединены, образуют насыщенное 3-7-членное гетероциклическое кольцо, которое необязательно содержит один дополнительный гетероатом, выбранный из группы, включающей N, О и S, где один или большее количество атомов C указанного гетероциклического кольца необязательно окислены с образованием групп СО, где один или большее количество атомов S указанного гетероциклического кольца, если они содержатся, необязательно окислены с независимым образованием групп SO или групп SO2, и где указанное гетероциклическое кольцо необязательно замещено одним или большим количеством R11;
каждый R9 независимо выбран из группы, включающей водород и C1-C4-алкил;
каждый R10 независимо выбран из группы, включающей C1-C8-алкил, галоген-C1-C8-алкил, циклил и циклил-C1-C8-алкил, где указанный циклил или циклильный фрагмент, содержащийся в указанном циклил-C1-C8-алкиле, необязательно замещен одним или большим количеством R14;
каждый R11 независимо выбран из группы, включающей C1-C8-алкил, галоген, C1-C8-алкоксигруппу, гидроксигруппу и -NR12R13;
каждый R12 и каждый R13 независимо выбран из группы, включающей водород и C1-C8-алкил; и
каждый R14 независимо выбран из группы, включающей C1-C8-алкил, -C2-C8-алкенил, С2-С8-алкинил, аминогруппу, амидную группу, гидроксигруппу, нитрогруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфинил, сульфонил, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, О-карбоксигруппу, С-карбоксигруппу, карбаматную группу и мочевинную группу;
при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол.
Кроме того, предпочтительно, если исключен 2-((2-фенилциклопропил)амино)циклогексанол.
В другом варианте осуществления настоящее изобретение относится к соединению формулы Ia, определенной выше, в которой заместители -A-B и -NH-D циклопропильного фрагмента находятся в транс-конфигурации, т.е. к соединению формулы Ia-1:

где группы и переменные в формуле Ia-1, включая A, B, D, Е, L, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, R13 и R14, являются такими, как определено выше для соединения формулы Ia, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол.
Кроме того, предпочтительно, если исключен 2-((2-фенилциклопропил)амино)циклогексанол.
Приведенное выше изображение химической структуры соединения формулы Ia-1 предназначено не для указания абсолютной стереохимической конфигурации двух хиральных центров, содержащихся в циклопропильном кольце, а только для указания их относительной стереохимической конфигурации (которая является транс-конфигурацией). Таким образом, соединение формулы Ia-1 также можно представить следующим образом:

Поэтому соединение формулы Ia-1 означает отдельные оптически активные транс-изомеры, а также любые их смеси.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, определенной выше, в которой каждый Rw, Rx, Ry и Rz независимо выбран из группы, включающей водород, галоген и C1-C4-алкил, при условии, что по меньшей мере один из Rw, Rx, Ry и Rz нe обозначает водород; далее это соединение называется соединением формулы Ib. В более предпочтительном варианте осуществления Rw выбран из группы, включающей галоген и C1-C4-алкил, предпочтительно из группы, включающей фтор и метил, и каждый Rx, Ry и Rz обозначает водород. Соединение формулы I, в которой Rw выбран из группы, включающей галоген и C1-C4-алкил, предпочтительно из группы, включающей фтор и метил, и каждый Rx, Ry и Rz обозначает водород далее называется соединением формулы Ic.
В объем настоящего изобретения также входят все изомеры соединений формулы I, Ia, Ia-1, Ib и Ic (определенные в настоящем изобретении), включая все стереоизомеры и их смеси. В объем настоящего изобретения также входят все соли и все сольваты, предпочтительно фармацевтически приемлемые соли и сольваты, соединений формулы I, Ia, Ia-1, Ib и Ic. Кроме того, в объем настоящего изобретения также входят все физические формы (включая аморфные и кристаллические формы) любых таких соединений. Любое указание на соединение формулы I, Ia, Ia-1, Ib или Ic соответственно, если не указано иное, следует понимать как указание на соединение формулы I, Ia, Ia-1, Ib или Ic (соответственно), любой его изомер (включая любой его стереоизомер или любые их смеси), любую его соль (включая любую его фармацевтически приемлемую соль), любой его сольват (включая любой его фармацевтически приемлемый сольват) и любую его физическую форму.
Соединения формулы Ia, включая также соединения формулы Ia-1, являются особенно предпочтительными соединениями, предлагаемыми в настоящем изобретении. Наиболее предпочтительными соединениями, предлагаемыми в настоящем изобретении, являются соединения формулы Ia-1.
Любая химическая структура или формула, приведенная в настоящем изобретении, также характеризует немеченые формы, а также изотопно-меченые формы соединений, предлагаемых в настоящем изобретении. Изотопно-меченые соединения обладают структурами, описывающимися формулами, приведенными в настоящем изобретении, за исключением того, что один или большее количество атомов заменены на атомы, обладающими указанными атомными массами или массовыми числами. Примеры изотопов, которые можно вводить в соединения, предлагаемые в настоящем изобретении, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора, хлора и йода, такие как2H,3H,11С,13С,14С,15N,18О,17О,31Р,32Р,35S,18F,36Сl и125I соответственно. Такие изотопно-меченые соединения применимы для изучения метаболизма (предпочтительно содержащие14С), изучения кинетики реакций (содержащие, например,2Н или3Н), в методологиях детектирования и визуализации [таких как позитронная эмиссионная томография (ПЭТ) или однофотонная эмиссионная компьютерная томография (ОФЭКТ)], включая исследование распределения лекарственного средства или субстрата в тканях, или в лучевой терапии пациентов. В частности, меченое с помощью18F или11С соединение может быть особенно предпочтительным для исследований с помощью ПЭТ или ОФЭКТ. Кроме того, замещение более тяжелыми изотопами, предпочтительно дейтерием (т.е.2Н), может обеспечить некоторые терапевтические преимущества, обусловленные их более высокой метаболической стабильностью, например, увеличенной длительностью полувыведения in vivo или возможностью использования меньших доз. Особенно предпочтительными являются дейтерированные формы соединений, предлагаемых в настоящем изобретении, т.е. соединение формулы I, Ia, Ia-1, Ib и Ic, указанное выше, в котором один или большее количество атомов водорода заменены на дейтерий. Изотопно-меченые соединения, предлагаемые в настоящем изобретении, обычно можно получить по методикам, раскрытым в схемах или в примерах и синтезах, описанных ниже, путем замены не содержащего изотопа реагента на легко доступный изотопно-меченый реагент. В дополнение к немеченым формам в объем настоящего изобретения входят все изотопно-меченые формы соединений формулы I, Ia, Ia-1, Ib и Ic.
В соединении формулы I, Ia, Ib или Ic заместители -A-B и -NH-D циклопропильного фрагмента предпочтительно находятся в трансконфигурации.
Соединения формулы I, Ia, Ia-1, Ib и Ic являются активными ингибиторами LSD1 и поэтому они могут быть применимы для лечения или предупреждения любого заболевания, связанного с LSD1.
Таким образом, настоящее изобретение относится к фармацевтической композиции, содержащей соединение формулы I, Ia, Ia-1, Ib или Ic и фармацевтически приемлемый носитель.
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей соединение формулы I

где группы и переменные в формуле I, включая A, B, D, Rw, Rx, Ry и Rz, являются такими, как определено выше, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол;
и фармацевтически приемлемый носитель.
В другом варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей соединение формулы Ia

где группы и переменные в формуле Ia, включая А, В и D, являются такими, как определено выше, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол;
и фармацевтически приемлемый носитель.
В другом варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей соединение формулы Ia-1

где группы и переменные в формуле Ia-1, включая А, В и D, являются такими, как определено выше, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол;
и фармацевтически приемлемый носитель.
Предпочтительные варианты осуществления соединений формулы I, Ia, Ia-1, Ib и Ic, например, предназначенные для использования в композициях, предлагаемых в настоящем изобретении, более подробно определены и описаны ниже в настоящем изобретении.
Другим объектом настоящего изобретения является способ лечения или предупреждения заболевания, включающий введение пациенту (предпочтительно человеку), нуждающемуся в таком лечении или предупреждении, соединения формулы I, Ia, Ia-1, Ib или Ic (описанного выше или определенного в его вариантах осуществления, описанных ниже) в количестве, эффективном для лечения или предупреждения указанного заболевания. В одном варианте осуществления таким заболеванием является заболевание, связанное с LSD1.
Родственным объектом настоящего изобретения является соединение формулы I, Ia, Ia-1, Ib или Ic (описанное выше или определенное в его вариантах осуществления, описанных ниже), предназначенное для применения в качестве лекарственного средства. В более предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic, предназначенному для применения для лечения или предупреждения заболевания, связанного с LSD1.
Таким образом, в одном варианте осуществления настоящее изобретение относится к соединению формулы I

где группы и переменные в формуле I, включая A, B, D, Rw, Rx, Ry и Rz, являются такими, как определено выше, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол;
предназначенному для применения в качестве лекарственного средства.
В другом варианте осуществления настоящее изобретение относится к соединению формулы Ia

где группы и переменные в формуле Ia, включая А, В и D, являются такими, как определено выше, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол;
предназначенному для применения в качестве лекарственного средства.
В другом варианте осуществления настоящее изобретение относится к соединению формулы Ia-1

где группы и переменные в формуле Ia-1, включая А, В и D, являются такими, как определено выше, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол;
предназначенному для применения в качестве лекарственного средства.
Еще одним объектом настоящего изобретения является способ ингибирования активности LSD1, включающий введение пациенту, нуждающемуся в лечении, соединения формулы I, Ia, Ia-1, Ib или Ic в количестве, достаточном для ингибирования активности LSD1. Предпочтительно, если пациентом является человек. Родственным объектом настоящего изобретения является соединение формулы I, Ia, Ia-1, Ib или Ic, определенное в настоящем изобретении, предназначенное для применения в качестве ингибитора LSD1. Предпочтительными вариантами осуществления соединений формулы I, Ia, Ia-1, Ib или Ic, предназначенных для применения в настоящем изобретении, являются такие, как более подробно описанные ниже.
Другим объектом настоящего изобретения является способ лечения или предупреждения рака, включающий введение пациенту (предпочтительно человеку), нуждающемуся в таком лечении или предупреждении, соединения формулы I, Ia, Ia-1, Ib или Ic (определенного выше или определенного в вариантах осуществления, более подробно описанных в настоящем изобретении) в количестве, достаточном для лечения или предупреждения такого рака. Родственным объектом настоящего изобретения является способ лечения или предупреждения рака, в котором указанный рак выбран из группы, включающей рак молочной железы, рак легких, рак предстательной железы, колоректальный рак, рак головного мозга, рак кожи, рак крови (например, лейкоз, включая, например, острый миелолейкоз (ОМЛ), хронический миелолейкоз (ХМЛ), хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический лимфолейкоз (ХЛЛ), острый лимфобластный лейкоз (ОЛЛ) или волосатоклеточный лейкоз), лимфому и миелому, включающему введение пациенту (предпочтительно человеку), нуждающемуся в таком лечении или предупреждении, соединения формулы I, Ia, Ia-1, Ib или Ic (определенного выше или определенного в вариантах осуществления, более подробно описанных в настоящем изобретении) в количестве, достаточном для лечения или предупреждения такого рака. В еще более предпочтительном объекте указанный рак выбран из группы, включающей рак предстательной железы, рак головного мозга, колоректальный рак, рак легких, рак молочной железы, рак кожи и рак крови. В одном предпочтительном объекте раком является рак предстательной железы. В одном предпочтительном объекте раком является рак легких. В одном предпочтительном объекте раком является рак головного мозга. В одном предпочтительном объекте раком является рак крови (например, лейкоз, включая, например, острый миелолейкоз (ОМЛ), хронический миелолейкоз (ХМЛ), хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический лимфолейкоз (ХЛЛ), острый лимфобластный лейкоз (ОЛЛ) или волосатоклеточный лейкоз). В одном предпочтительном объекте раком является рак молочной железы. В одном предпочтительном объекте раком является колоректальный рак. В одном предпочтительном объекте раком является лимфома. В одном предпочтительном объекте раком является миелома. В предпочтительном варианте осуществления способ включает введение терапевтически эффективного количества соединения формулы I, Ia, Ia-1, Ib или Ic, достаточного для лечения или предупреждения указанного рака. В предпочтительном объекте терапевтически эффективное количество соединения формулы I, Ia, Ia-1, Ib или Ic является количеством, достаточным для ингибирования LSD1. В другом предпочтительном объекте терапевтически эффективное количество является количеством, достаточным для модулирования степени метилирования гистона. В другом предпочтительном объекте терапевтически эффективное количество является количеством, достаточным для модулирования степени метилирования гистон-3-лизина-4. В другом предпочтительном объекте терапевтически эффективное количество является количеством, достаточным для модулирования степени метилирования гистон-3-лизина-9. Несмотря на то, что настоящее изобретение относится и к лечению, и к предупреждению рака, лечение рака является особенно предпочтительным.
Таким образом, в одном варианте осуществления настоящее изобретение относится к способу лечения или предупреждения рака, включающему введение пациенту (предпочтительно человеку), нуждающемуся в таком лечении или предупреждении, некоторого количества соединения формулы I
где группы и переменные в формуле I, включая A, B, D, Rw, Rx, Ry и Rz, являются такими, как определено выше, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол.
В другом варианте осуществления настоящее изобретение относится к способу лечения или предупреждения рака, включающему введение пациенту (предпочтительно человеку), нуждающемуся в таком лечении или предупреждении, некоторого количества соединения формулы Ia

где группы и переменные в формуле Ia, включая А, В и D, являются такими, как определено выше, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол.
В другом варианте осуществления настоящее изобретение относится к способу лечения или предупреждения рака, включающему введение пациенту (предпочтительно человеку), нуждающемуся в таком лечении или предупреждении, некоторого количества соединения формулы Ia-1

где группы и переменные в формуле Ia-1, включая А, В и D, являются такими, как определено выше, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол.
Родственным объектом настоящего изобретения является соединение формулы I, Ia, Ia-1, Ib или Ic (определенное выше или определенное в вариантах осуществления, более подробно описанных в настоящем изобретении), предназначенное для применения для лечения или предупреждения рака. Другим родственным объектом настоящего изобретения является соединение формулы I, Ia, Ia-1, Ib или Ic, предназначенное для применения для лечения или предупреждения рака, где указанный рак выбран из группы, включающей рак молочной железы, рак легких, рак предстательной железы, колоректальный рак, рак головного мозга, рак кожи, рак крови (например, лейкоз, включая, например, острый миелолейкоз (ОМЛ), хронический миелолейкоз (ХМЛ), хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический лимфолейкоз (ХЛЛ), острый лимфобластный лейкоз (ОЛЛ) или волосатоклеточный лейкоз), лимфому и миелому. В более предпочтительном объекте указанный рак выбран из группы, включающей рак предстательной железы, рак головного мозга, колоректальный рак, рак легких, рак молочной железы, рак кожи и рак крови. В одном предпочтительном объекте раком является рак предстательной железы. В одном предпочтительном объекте раком является рак легких. В одном предпочтительном объекте раком является рак головного мозга. В одном предпочтительном объекте раком является рак крови (например, лейкоз, включая, например, острый миелолейкоз (ОМЛ), хронический миелолейкоз (ХМЛ), хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический лимфолейкоз (ХЛЛ), острый лимфобластный лейкоз (ОЛЛ) или волосатоклеточный лейкоз). В одном предпочтительном объекте раком является рак молочной железы. В одном предпочтительном объекте раком является колоректальный рак. В одном предпочтительном объекте раком является лимфома. В одном предпочтительном объекте раком является миелома. В предпочтительном варианте осуществления вводят терапевтически эффективное количество соединения формулы I, Ia, Ia-1, Ib или Ic, достаточное для лечения или предупреждения указанного рака. В предпочтительном объекте терапевтически эффективное количество соединения формулы I, Ia, Ia-1, Ib или Ic является количеством, достаточным для ингибирования LSD1. В другом предпочтительном объекте терапевтически эффективное количество является количеством, достаточным для модулирования степени метилирования гистона. В другом предпочтительном объекте терапевтически эффективное количество является количеством, достаточным для модулирования степени метилирования гистон-3-лизина-4. В другом предпочтительном объекте терапевтически эффективное количество является количеством, достаточным для модулирования степени метилирования гистон-3-лизина-9.
Таким образом, в одном варианте осуществления настоящее изобретение относится к соединению формулы I

где группы и переменные в формуле I, включая A, B, D, Rw, Rx, Ry и Rz, являются такими, как определено выше, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол;
предназначенному для применения для лечения или предупреждения рака.
В другом варианте осуществления настоящее изобретение относится к соединению формулы Ia

где группы и переменные в формуле Ia, включая А, В и D, являются такими, как определено выше, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол;
предназначенному для применения для лечения или предупреждения рака.
В другом варианте осуществления настоящее изобретение относится к соединению формулы Ia-1

где группы и переменные в формуле Ia-1, включая А, В и D, являются такими, как определено выше, при условии, что исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол;
предназначенному для применения для лечения или предупреждения рака.
Другим объектом настоящего изобретения является способ лечения или предупреждения неврологического заболевания (например, нейродегенеративного заболевания), включающий введение пациенту, нуждающемуся в таком лечении или предупреждении, соединения формулы 1,1а, Ia-1, Ib или Ic (определенного выше или в вариантах осуществления, более подробно описанных в настоящем изобретении) в количестве, достаточном для лечения или предупреждения указанного неврологического заболевания. Родственным объектом настоящего изобретения является способ лечения или предупреждения неврологического заболевания, в котором указанное неврологическое заболевание выбрано из группы, включающей депрессию, болезнь Альцгеймера, болезнь Гентингтона, болезнь Паркинсона, боковой амиотрофический склероз, слабоумие с тельцами Леви или лобно-височное слабоумие, предпочтительно из группы, включающей депрессию, болезнь Альцгеймера, болезнь Гентингтона, болезнь Паркинсона или слабоумие с тельцами Леви, включающему введение пациенту (предпочтительно человеку), нуждающемуся в таком лечении или предупреждении, соединения формулы I, Ia, Ia-1, Ib или Ic (определенного выше или определенного в вариантах осуществления, более подробно описанных в настоящем изобретении) в количестве, достаточном для лечения или предупреждения такого неврологического заболевания. В предпочтительном варианте осуществления способ включает введение терапевтически эффективного количества соединения формулы I, Ia, Ia-1, Ib или Ic, достаточного для лечения или предупреждения указанного неврологического заболевания. В предпочтительном объекте терапевтически эффективное количество соединения формулы I, Ia, Ia-1, Ib или Ic является количеством, достаточным для ингибирования LSD1. В другом предпочтительном объекте терапевтически эффективное количество является количеством, достаточным для модулирования степени метилирования гистона. В другом предпочтительном объекте терапевтически эффективное количество является количеством, достаточным для модулирования степени метилирования гистон-3-лизина-4. В другом предпочтительном объекте терапевтически эффективное количество является количеством, достаточным для модулирования степени метилирования гистон-3-лизина-9.
Другим родственным объектом настоящего изобретения является соединение формулы I, Ia, Ia-1, Ib или Ic (определенное выше или в вариантах осуществления, более подробно описанных в настоящем изобретении), предназначенное для применения для лечения или предупреждения неврологического заболевания (например, нейродегенеративного заболевания). В одном варианте осуществления указанное неврологическое заболевание выбрано из группы, включающей депрессию, болезнь Альцгеймера, болезнь Гентингтона, болезнь Паркинсона, боковой амиотрофический склероз, слабоумие с тельцами Леви и лобно-височное слабоумие, предпочтительно из группы, включающей депрессия, болезнь Альцгеймера, болезнь Гентингтона, болезнь Паркинсона и слабоумие с тельцами Леви. В предпочтительном варианте осуществления вводят терапевтически эффективное количество соединения формулы I, Ia, Ia-1, Ib или Ic, достаточное для лечения или предупреждения указанного неврологического заболевания. В предпочтительном объекте терапевтически эффективное количество соединения формулы I, Ia, Ia-1, Ib или Ic является количеством, достаточным для ингибирования LSD1. В другом предпочтительном объекте терапевтически эффективное количество является количеством, достаточным для модулирования степени метилирования гистона. В другом предпочтительном объекте терапевтически эффективное количество является количеством, достаточным для модулирования степени метилирования гистон-3-лизина-4. В другом предпочтительном объекте терапевтически эффективное количество является количеством, достаточным для модулирования степени метилирования гистон-3-лизина-9.
Другим объектом настоящего изобретения является способ лечения или предупреждения вирусной инфекции, включающий введение нуждающемуся в нем пациенту (предпочтительно человеку) соединения формулы I, Ia, Ia-1, Ib или Ic (определенного выше или в вариантах осуществления, более подробно описанных в настоящем изобретении) в количестве, достаточном для лечения или предупреждения указанной вирусной инфекции. Родственным объектом настоящего изобретения также является соединение формулы I, Ia, Ia-1, Ib или Ic (определенное выше или в вариантах осуществления, более подробно описанных в настоящем изобретении), предназначенное для применения для лечения или предупреждения вирусной инфекции. В одном предпочтительном варианте осуществления вирусной инфекцией является инфекция, вызванная вирусом герпеса. В более предпочтительном варианте осуществления инфекция, вызванная вирусом герпеса, вызвана и/или связана с вирусом герпеса, выбранным из группы, включающей HSV-1, HSV-2 и вирус Эпштейна-Барра. В другом варианте осуществления вирусная инфекция вызвана и/или связана с ВИЧ (вирус иммунодефицита человека). В другом варианте осуществления вирусная инфекция вызвана и/или связана с гепаднавирусом (т.е. вирусом семейства Hepadnaviridae), предпочтительно вирусом гепатита B (HBV). В другом варианте осуществления вирусная инфекция вызвана и/или связана с флавивирусом (т.е. вирусом семейства FIavivihdae), предпочтительно вирусом гепатита C (HCV), вирусом желтой лихорадки, вирусом Западного Нила, вирусом денге или вирусом японского энцефалита, и более предпочтительно HCV. В еще более предпочтительном варианте осуществления настоящее изобретение относится к способу лечения или предупреждения реактивации вируса после латентного периода, способ включает введение индивидууму (предпочтительно человеку) соединения формулы I, Ia, Ia-1, Ib или Ic (определенного выше или в вариантах осуществления, более подробно описанных в настоящем изобретении). В соответствии с этим, настоящее изобретение также относится к соединению формулы I, Ia, Ia-1, Ib или Ic (определенному выше или в вариантах осуществления, более подробно описанных в настоящем изобретении), предназначенному для применения для лечения или предупреждения реактивации вируса после латентного периода. В предпочтительном варианте осуществления вирусом, который реактивируется, является вирус герпеса. В более предпочтительном варианте осуществления вирус герпеса, который реактивируется, выбран из группы, включающей HSV-1, HSV-2 и вирус Эпштейна-Барра. В еще более предпочтительном варианте осуществления вирусом, который реактивируется, является HSV. В другом предпочтительном варианте осуществления вирусом, который реактивируется, является ВИЧ.
Еще одним объектом настоящего изобретения является применение соединения формулы I, Ia, Ia-1, Ib или Ic (определенного выше или в вариантах осуществления, более подробно описанных в настоящем изобретении) для приготовления лекарственного средства, предназначенного для лечения или предупреждения рака. В предпочтительном варианте осуществления указанный рак выбран из группы, включающей рак молочной железы, рак легких, рак предстательной железы, колоректальный рак, рак головного мозга, рак кожи, рак крови (например, лейкоз, включая, например, острый миелолейкоз (ОМЛ), хронический миелолейкоз (ХМЛ), хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический лимфолейкоз (ХЛЛ), острый лимфобластный лейкоз (ОЛЛ) или волосатоклеточный лейкоз), лимфому и миелому.
Еще одним объектом настоящего изобретения является применение соединения формулы I, Ia, Ia-1, Ib или Ic (определенного выше или в вариантах осуществления, более подробно описанных в настоящем изобретении) для приготовления лекарственного средства, предназначенного для лечения или предупреждения неврологического заболевания (например, нейродегенеративного заболевания). В предпочтительном варианте осуществления указанное неврологическое заболевание выбрано из группы, включающей депрессию, болезнь Альцгеймера, болезнь Гентингтона, болезнь Паркинсона, боковой амиотрофический склероз, слабоумие с тельцами Леви или лобно-височное слабоумие, предпочтительно из группы, включающей депрессию, болезнь Альцгеймера, болезнь Гентингтона, болезнь Паркинсона и слабоумие с тельцами Леви.
Еще одним объектом настоящего изобретения является применение соединения формулы I, Ia, Ia-1, Ib или Ic (определенного выше или в вариантах осуществления, более подробно описанных в настоящем изобретении) для приготовления лекарственного средства, предназначенного для лечения или предупреждения вирусной инфекции. В предпочтительном варианте осуществления указанной вирусной инфекцией является инфекция, вызванная вирусом герпеса (инфекция, вызванная вирусом герпеса, вызванная и/или связанная с вирусом герпеса, выбранным из группы, включающей HSV-1, HSV-2 и вирус Эпштейна-Барра), или вирусная инфекция вызвана и/или связана с ВИЧ. В другом предпочтительном варианте осуществления указанная вирусная инфекция вызвана и/или связана с гепаднавирусом, предпочтительно с вирусом гепатита B (HBV). В другом варианте осуществления указанная вирусная инфекция вызвана и/или связана с флавивирусом, предпочтительно с вирусом желтой лихорадки, вирусом Западного Нила, вирусом денге или вирусом японского энцефалита, и более предпочтительно с HCV.
Еще одним объектом настоящего изобретения является применение соединения формулы I, Ia, Ia-1, Ib или Ic (определенного выше или в вариантах осуществления, более подробно описанных в настоящем изобретении) для приготовления лекарственного средства, предназначенного для лечения или предупреждения реактивации вируса после латентного периода. В предпочтительном варианте осуществления вирусом, который реактивируется, является вирус герпеса (например, HSV-1, HSV-2 или вирус Эпштейна-Барра), HSV или ВИЧ.
Еще одним объектом настоящего изобретения является способ выявления соединения, которое является селективным ингибитором LSD1, способ включает выбор или получение соединения формулы I, Ia, Ia-1, Ib или Ic, определенного в настоящем изобретении, и определение способности указанного соединения ингибировать LSD1 и МАО-А и/или МАО-В, где соединение, которое ингибирует LSD1 в большей степени, чем МАО-А и/или МАО-В, идентифицируют, как селективный ингибитор. Соединение этого объекта, которое является ингибитором LSD1, можно применять для лечения заболевания, предпочтительно заболевания человека.
Другим объектом настоящего изобретения является способ получения соединения формулы I или его соли, который включает реакцию соединения формулы II

в которой A, В, Rw, Rx, Ry, Rz обладают значениями, раскрытыми выше для соединения формулы I, с соединением формулы III

в которой D обладает значением, раскрытым выше для соединения формулы I, и в которой группа (группы) R3, содержащаяся в кольце D, необязательно содержит защитную группу,
в присутствии восстановительного реагента с последующим удалением любой защитной группы, которая может содержаться. Восстановительным реагентом может являться, например, борогидрид, такой как борогидрид натрия или триацетоксиборогидрид натрия.
Если не приведено другое определение, то все технические и научные термины, использующиеся в настоящем изобретении, обладают такими же значениями, которые обычно известны специалисту с общей подготовкой в области техники, к которой относится настоящее изобретение. Хотя при практическом осуществлении или тестировании настоящего изобретения можно использовать методики и материалы, сходные с описанными в настоящем изобретении или эквивалентные им, подходящие методики и материалы описаны ниже. В случае противоречий необходимо руководствоваться настоящим описанием, включая определения. Кроме того, материалы, методики и примеры являются лишь иллюстративными и их не следует рассматривать в качестве ограничивающих.
Другие особенности и преимущества настоящего изобретения очевидны из приведенного ниже подробного описания и из формулы изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к выявлению соединений и их применению для лечения или предупреждения заболеваний. Настоящее изобретение относится к соединениям формулы I, Ia, Ia-1, Ib и Ic, фармацевтическим композициям, содержащим соединение формулы I, Ia, Ia-1, Ib или Ic и фармацевтически приемлемый носитель, и к их применению для лечения заболеваний. Одним применением соединений формулы I, Ia, Ia-1, Ib и Ic является применение для лечения рака.
Настоящее изобретение относится к соединению формулы I

В соединении формулы I каждый Rw, Rx, Ry и Rz независимо выбран из группы, включающей водород, галоген и C1-C4-алкил. В одном варианте осуществления каждый Rw, Rx, Ry и Rz независимо выбран из группы, включающей водород, фтор и C1-C4-алкил, предпочтительно из группы, включающей водород, фтор и метил. В другом варианте осуществления каждый Rw, Rx, Ry и Rz независимо выбран из группы, включающей водород и фтор. В другом варианте осуществления Rw обозначает фтор и каждый Rx, Ry и R2независимо выбран из группы, включающей водород, галоген и C1-C4-алкил; предпочтительно, если Rw обозначает фтор и каждый Rx, Ry и Rz обозначает водород. В другом варианте осуществления Rz обозначает фтор и каждый Rw, Rx и Ry независимо выбран из группы, включающей водород, галоген и C1-C4-алкил; предпочтительно, если Rz обозначает фтор и каждый Rw, Rx и Ryобозначает водород. В другом варианте осуществления Rw и Rz обозначают фтор и каждый Rx и Ryнезависимо выбран из группы, включающей водород, галоген и C1-C4-алкил; предпочтительно, если Rw и Rz обозначают фтор и каждый Rx и Ryобозначает водород. В предпочтительном варианте осуществления Rw выбран из группы, включающей водород, галоген и C1-C4-алкил, предпочтительно из группы, включающей водород, фтор и метил, и каждый Rx, Ry и Rz обозначает водород. В более предпочтительном варианте осуществления каждый Rw, Rx, Ry и Rz обозначает водород. Соединение формулы I, в которой каждый Rw, Rx, Ry и Rz обозначает водород, является соединением формулы Ia, которая может быть представлена следующим образом:

В другом варианте осуществления в соединении формулы I каждый Rw, Rx, Ry и Rz независимо выбран из группы, включающей водород, галоген и C1-C4-алкил при условии, что по меньшей мере один из них нE обозначает водород, этим соединением является соединение формулы Ib. В более предпочтительном варианте осуществления Rw выбран из группы, включающей галоген и C1-C4-алкил, предпочтительно фтор и метил, и каждый Rx, Ry и Rz обозначает водород. Соединение формулы I, в которой Rw выбран из группы, включающей галоген и C1-C4-алкил, предпочтительно фтор и метил, и каждый Rx, Ry и Rz обозначает водород, является соединением формулы Ic. Предпочтительно, если в соединении формулы Ic Rw обозначает метил.
В соединении формулы I, Ia, Ia-1, Ib или Ic группа A обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R1. В одном варианте осуществления A обозначает арил (предпочтительно фенил или нафтил), необязательно замещенный одним или большим количеством R1. В предпочтительном варианте осуществления A обозначает фенил, необязательно замещенный одним или большим количеством R1. В другом предпочтительном варианте осуществления A обозначает нафтил, необязательно замещенный одним или большим количеством R1. В другом варианте осуществления A обозначает гетероарил (предпочтительно моноциклический гетероарил), необязательно замещенный одним или большим количеством R1. В предпочтительном варианте осуществления A обозначает фенил, нафтил или моноциклический гетероарил, где указанный фенил, нафтил или моноциклический гетероарил необязательно замещен одним или большим количеством R1. Предпочтительно, если A обозначает моноциклический арил (т.е. фенил) или моноциклический гетероарил, где указанный моноциклический арил или указанный моноциклический гетероарил необязательно замещен одним или большим количеством R1. Более предпочтительно, если A обозначает фенил, пиридил, тиофенил, пирролил, фуранил или тиазолил, где A (т.е. указанный фенил, указанный пиридил, указанный тиофенил, указанный пирролил, указанный фуранил или указанный тиазолил) необязательно замещен одним или большим количеством R1. Более предпочтительно, если A обозначает фенил, пиридил, тиазолил или тиофенил, где A (т.е. указанный фенил, указанный пиридил, указанный тиазолил или указанный тиофенил) необязательно замещен одним или большим количеством R1. Еще более предпочтительно, если A обозначает фенил, пиридил или тиазолил, где A необязательно замещен одним или большим количеством R1. Еще более предпочтительно, если A обозначает фенил, 3-пиридил или 5-тиазолил, как это показано ниже:

где A необязательно замещен одним или большим количеством R1. В одном варианте осуществления A обозначает фенил или пиридил, предпочтительно фенил или 3-пиридил. В другом варианте осуществления A обозначает фенил. В другом варианте осуществления A обозначает пиридил, предпочтительно 3-пиридил. В другом варианте осуществления A обозначает тиазолил, предпочтительно 5-тиазолил. В одном варианте осуществления A содержит 0, 1 или 2 заместителя R1. В другом варианте осуществления A содержит 0 или 1 заместитель R1. В другом варианте осуществления A содержит 0 заместителей R1. В другом варианте осуществления A содержит 1 или 2 заместителя R1. В другом варианте осуществления A содержит 1 заместитель R1. В указанных выше вариантах осуществления, в которых A содержит 0, 1 или 2 заместителя R1, общее количество заместителей R1 определено, включая возможность того, что B может обозначать R1. Соответственно, если A содержит 0 заместителей R1, то B нe обозначает R1.
В соединении формулы I, Ia, Ia-1, Ib или Ic B обозначает водород, R1 или -L-E. В одном варианте осуществления B обозначает -L-E. В предпочтительном варианте осуществления B обозначает водород или R1. В другом предпочтительном варианте осуществления B обозначает водород. В другом варианте осуществления B обозначает R1.
В соединении формулы I, Ia, Ia-1, Ib или Ic E обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R2. В одном варианте осуществления E обозначает арильную группу (например, фенил, нафтил или антраценил), необязательно замещенную одним или большим количеством R2. В другом варианте осуществления E обозначает гетероарильную группу (например, пиридинил, тиофенил, пирролил, фуранил, тиазолил, оксазолил, изоксазолил, оксадиазолил, тиадиазолил, триазинил, пиридазинил, пиразинил, пиримидинил, хинолил, индолил, пиразолил, индазолил, имидазолил или бензимидазолил), необязательно замещенную одним или большим количеством R2. Предпочтительно, если E обозначает моноциклический арил (т.е. фенил) или моноциклический гетероарил, где указанный моноциклический арил или указанный моноциклический гетероарил необязательно замещен одним или большим количеством R2. В одном варианте осуществления E содержит 0, 1, 2 или 3 заместителя R2. В другом варианте осуществления E содержит 0, 1 или 2 заместителя R2. В другом варианте осуществления E содержит 0 или 1 заместитель R2. В другом варианте осуществления E содержит 0 заместителей R2. В другом варианте осуществления E содержит 1 заместитель R2. Предпочтительно, E обозначает фенил, необязательно замещенный одним или большим количеством R2. В одном варианте осуществления E обозначает фенил, необязательно замещенный с помощью 1, 2 или 3 R2. В другом варианте осуществления E обозначает фенил, необязательно замещенный с помощью 1 или 2 R2. В другом варианте осуществления E обозначает фенил, необязательно замещенный одним R2. В другом варианте осуществления E обозначает фенил. В другом варианте осуществления E обозначает фенил, замещенный с помощью 1, 2 или 3, предпочтительно с помощью 1 или 2 R2. В другом предпочтительном варианте осуществления E обозначает гетероарил, предпочтительно моноциклический гетероарил, необязательно замещенный одним или большим количеством (предпочтительно с помощью 1, 2 или 3) R2. В одном варианте осуществления E обозначает гетероарил, предпочтительно моноциклический гетероарил. В другом варианте осуществления E обозначает гетероарил (предпочтительно моноциклический гетероарил), замещенный с помощью 1, 2 или 3, предпочтительно с помощью 1 или 2 R2.
В соединении формулы I, Ia, Ia-1, Ib или Ic L обозначает связь, -O-, -NH-, -N(C1-C4-алкил)-, C1-C4-алкилен или гетеро-C1-C4-алкилен. Предпочтительно, если указанный гетеро-C1-C4-алкилен представляет собой -(CH2)x-NH- или -(CH2)х-O-, где х равно 1, 2, 3 или 4; еще более предпочтительно, если указанные группы -(CH2)x-NH- или -(CH2)х-O- связаны с кольцом A через атом N или О соответственно, и связаны с кольцом E через группу -(СН2)x-. Более предпочтительно, если указанный гетеро-C1-C4-алкилен представляет собой -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или О соответственно, и связаны с кольцом E через группу -CH2-.
В одном варианте осуществления L обозначает связь, -O-, -NH-, -N(C1-C4-алкил)-, -CH2-, CH2-CH2-, -CH2-NH- или -CH2-O-. В предпочтительном варианте осуществления L обозначает связь, -O-, -NH-, -N(C1-C4-алкил)-, -CH2-NH- или -CH2-O-. В более предпочтительном варианте осуществления L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-. В еще более предпочтительном варианте осуществления L обозначает связь или -CH2-O-. В другом предпочтительном варианте осуществления L обозначает связь. В другом варианте осуществления L обозначает -O-, -NH-, -N(C1-C4-алкил)-, C1-C4-алкилен или гетеро-C1-C4-алкилен; предпочтительно, если L обозначает -O-, -NH-, -N(C1-C4-алкил)-, -CH2-, CH2-CH2-, -CH2-NH- или -CH2-O-; более предпочтительно, если L обозначает -O-, -NH-, -N(C1-C4-алкил)-, -CH2-NH- или -CH2-O-; еще более предпочтительно, если L обозначает -O-, -NH-, -CH2-NH- или -CH2-O-; еще более предпочтительно, если L обозначает -NH-, -CH2-NH- или -CH2-O-; и наиболее предпочтительно, если L обозначает -CH2-O-. Предпочтительно, если во всех этих вариантах осуществления указанные группы -CH2-NH- или -CH2-O-связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-.
В одном варианте осуществления B обозначает -L-E; E обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R2; и L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или О соответственно, и связаны с кольцом E через группу -CH2-. В другом варианте осуществления B обозначает -L-E; E обозначает фенил, необязательно замещенный одним или большим количеством R2; и L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где группы -CH2-NH- и -CH2-O-связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. В другом варианте осуществления B обозначает -L-E; E обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R2; и L обозначает связь или -CH2-O-, где группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-. В другом варианте осуществления B обозначает -L-E; E обозначает фенил, необязательно замещенный одним или большим количеством R2; и L обозначает связь или -CH2-O-, где группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-. В другом варианте осуществления B обозначает -L-E; E обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R2; и L обозначает связь. В другом варианте осуществления B обозначает -L-E; E обозначает фенил, необязательно замещенный одним или большим количеством R2; и L обозначает связь. В другом варианте осуществления B обозначает -L-E; E обозначает гетероарил, необязательно замещенный одним или большим количеством R2; и L обозначает связь. В другом варианте осуществления B обозначает -L-E; E обозначает арил или гетероарил; и L обозначает связь. В другом варианте осуществления B обозначает -L-E; E обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R2; и L обозначает -CH2-O-, где группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-. В другом варианте осуществления B обозначает -L-E; E обозначает фенил, необязательно замещенный одним или большим количеством R2; и L обозначает -CH2-O-, где группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-. В другом варианте осуществления B обозначает -L-E; E обозначает гетероарил (предпочтительно моноциклический гетероарил, более предпочтительно пиридинил), где указанный гетероарил необязательно замещен одним или большим количеством R2; и L обозначает -CH2-O-, где группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-. В другом варианте осуществления B обозначает -L-E; E обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R2; и L обозначает -O-, -NH-, -N(C1-C4-алкил)-, C1-C4-алкилен или -CH2-NH-, и более предпочтительно, если L обозначает -O-, -NH- или -CH2-NH-, где группа -CH2-NH- связана с кольцом A через атом N и с кольцом E через группу -CH2-. В другом варианте осуществления B обозначает -L-E; E обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R2; и L обозначает -NH- или -CH2-NH-, где группа -CH2-NH- связана с кольцом A через атом N и с кольцом E через группу -CH2-.
В соединении формулы I, Ia, Ia-1, Ib или Ic каждый R1 независимо выбран из группы, включающей C1-C8-алкил, C2-C8-алкенил, C2-C8-алкинил, циклил, аминогруппу, амидную группу, гидроксигруппу, нитрогруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфинил, сульфонил, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, О-карбоксигруппу, С-карбоксигруппу, карбаматную группу и мочевинную группу. Если в кольце A в качестве заместителей содержится более одного R1, то они могут быть одинаковыми или разными. В одном варианте осуществления каждый R1 независимо выбран из группы, включающей C1-C8-алкил, циклил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом варианте осуществления каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом варианте осуществления каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), С1-С4 алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил), предпочтительно, если каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил) и C1-C4-алкоксигруппу (например, метоксигруппу). В другом варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В соединении формулы I, Ia, Ia-1, Ib или Ic каждый R2 независимо выбран из группы, включающей C1-C8-алкил, С2-С8-алкенил, C2-C8-алкинил, циклил, аминогруппу, амидную группу, гидроксигруппу, нитрогруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфинил, сульфонил, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, О-карбоксигруппу, С-карбоксигруппу, карбаматную группу и мочевинную группу. Если в кольце E в качестве заместителей содержится более одного R2, то они могут быть одинаковыми или разными. В одном варианте осуществления каждый R2 независимо выбран из группы, включающей C1-C8-алкил, циклил, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу и C1-C8-алкоксигруппу. Предпочтительно, если каждый R2 независимо выбран из группы, включающей C1-C8-алкил, циклил, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, N-сульфонамидную группу и C1-C8-алкоксигруппу; более предпочтительно, если каждый R2 независимо выбран из группы, включающей C1-C8-алкил, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, N-сульфонамидную группу и C1-C8-алкоксигруппу. В другом варианте осуществления каждый R2 независимо выбран из группы, включающей гидроксигруппу, галоген (например, фтор или хлор), галоген-C1-C8-алкил (например, трифторметил) и сульфонамидную группу (предпочтительно N-сульфонамидную группу). В другом варианте осуществления каждый R2 независимо выбран из группы, включающей гидроксигруппу, галоген, галоген-C1-C8-алкил и N-сульфонамидную группу. В другом варианте осуществления каждый R2 независимо выбран из группы, включающей гидроксигруппу, галоген, галоген-C1-C8-алкил и -NR'SO2R (где R и R' являются такими, как определено ниже в настоящем изобретении; предпочтительно, если R' обозначает Н и R обозначает C1-C8-алкил (например, метил, этил или изопропил), или R' обозначает Н и R2 обозначает необязательно замещенный фенил). В другом варианте осуществления каждый R2 независимо выбран из группы, включающей гидроксигруппу, галоген, галоген-C1-C8-алкил и -NHSO2R (где R обозначает C1-C8-алкил (например, метил, этил или изопропил), необязательно замещенный фенил (например, фенил, 2-цианофенил, 3-цианофенил, 4-цианофенил, 2-аминофенил, 3-аминофенил или 4-аминофенил), необязательно замещенный гетероциклоалкил (например, пиперазин-1-ил) или необязательно замещенный гетероарил (например, 3-пиридил или 6-амино-3-пиридил)). В другом варианте осуществления каждый R2 независимо выбран из группы, включающей гидроксигруппу, галоген и галоген-C1-C8-алкил. В другом варианте осуществления каждый R2 независимо выбран из группы, включающей гидроксигруппу, галоген и галоген-C1-C4-алкил. В другом варианте осуществления каждый R2 независимо выбран из группы, включающей гидроксигруппу, хлор, фтор или трифторметил. В другом варианте осуществления кольцо E замещено одним R2 и указанный R2 обозначает -NHSO2R, где R обозначает C1-C8-алкил (например, метил, этил или изопропил), необязательно замещенный фенил (например, фенил или 2-цианофенил), необязательно замещенный гетероциклоалкил (например, пиперазин-1-ил) или необязательно замещенный гетероарил (например, 3-пиридил или 6-амино-3-пиридил).
В соединении формулы I, Ia, Ia-l,Ib или Ic D обозначает циклоалкильную группу, содержащую от 4 до 7 атомов C, где указанная циклоалкильная группа содержит 1 или 2 заместителя R3 и дополнительно необязательно замещена одним или большим количеством R4 и где циклоалкильная группа необязательно:
(а) сконденсирована с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связана с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. образуется мостиковая структура), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связана со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец (т.е. образуется спироцикл), и где указанное второе кольцо необязательно замещено одним или большим количеством R6.
Таким образом, циклоалкильная группа, содержащаяся в D, всегда замещена одной или двумя группами R3, которые могут быть одинаковыми или разными и могут находиться в любом доступном положении циклоалкильной группы, предпочтительно на разных атомах C, но предпочтительно не на кольцевом атоме C, связывающем указанную циклоалкильную группу с остальной частью молекулы. Предпочтительно, если группа R3 (или 1 или 2 группы R3, если содержатся 2 группы R3) находится на атоме C, расположенном в положении, наиболее удаленном от атома С, связывающего циклоалкильную группу с остальной частью соединения формулы I, это означает расположение типа "1,4" - или "пара" - для циклобутильного и циклогексильного колец и расположение типа "1,3" - или "мета" - для циклопентильного и циклогептильного колец. В предпочтительном варианте осуществления в циклоалкильной группе содержится только одна группа R3. Указанная циклоалкильная группа может содержать один или большее количество дополнительных заместителей R4, которые могут быть одинаковыми или разными, и могут находиться в любом доступном положении циклоалкильной группы. Кроме того, циклоалкильная группа может быть сконденсирована со вторым кольцом или образовывать мостиковые структуры или спирановые структуры, как это более подробно определено выше.
В одном варианте осуществления D обозначает циклоалкильную группу, содержащую от 4 до 7 атомов C, предпочтительно циклогексильную группу, где указанная циклоалкильная группа (предпочтительно циклогексил) содержит 1 или 2 заместителя R3 и дополнительно необязательно замещена одним или большим количеством R4, и где циклоалкильная группа (предпочтительно, циклогексил) необязательно сконденсирована с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5.
В предпочтительном варианте осуществления D обозначает циклоалкильную группу, содержащую от 4 до 7 атомов C, предпочтительно циклогексильную группу, где указанная циклоалкильная группа (предпочтительно, циклогексил) содержит 1 или 2 заместителя R3 и дополнительно необязательно замещена одним или большим количеством R4.
В более предпочтительном варианте осуществления D обозначает циклоалкильную группу, содержащую от 4 до 7 атомов C, предпочтительно циклогексильную группу, где указанная циклоалкильная группа (предпочтительно циклогексил) содержит 1 заместитель R3 и дополнительно необязательно замещена одним или большим количеством R4.
В еще более предпочтительном варианте осуществления D обозначает циклоалкильную группу, содержащую от 4 до 7 атомов C, предпочтительно циклогексильную группу, где указанная циклоалкильная группа (предпочтительно циклогексил) содержит 1 заместитель R3.
В другом варианте осуществления D обозначает циклоалкильную группу, содержащую от 4 до 7 атомов C, предпочтительно циклогексильную группу, где указанная циклоалкильная группа (предпочтительно циклогексил) содержит 1 или 2 заместителя R3 и дополнительно необязательно замещена одним или большим количеством R4, и где циклоалкильная группа (предпочтительно циклогексил) сконденсирована с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5.
В другом варианте осуществления D обозначает циклоалкильную группу, содержащую от 4 до 7 атомов C, предпочтительно циклогексильную группу, где указанная циклоалкильная группа содержит 1 или 2 заместителя R3 и дополнительно необязательно замещена одним или большим количеством R4, и где циклоалкильная группа связана с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-С4-алкил.
В другом варианте осуществления D обозначает циклоалкильную группу, содержащую от 4 до 7 атомов C, предпочтительно циклогексильную группу, где указанная циклоалкильная группа содержит 1 или 2 заместителя R3 и дополнительно необязательно замещена одним или большим количеством R4, и где циклоалкильная группа связана со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6.
В предпочтительном варианте осуществления D выбран из группы, включающей D1, D2, D3 и D4:
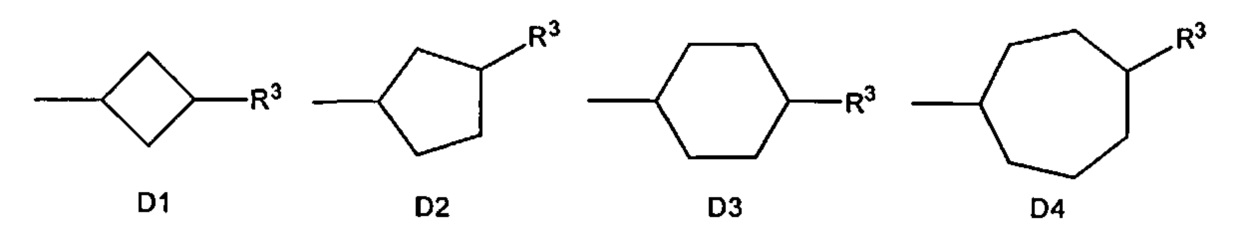
где циклобутильное кольцо, содержащееся в D1, циклопентильное кольцо, содержащееся в D2, циклогексильное кольцо, содержащееся в D3, и циклогептильное кольцо, содержащееся в D4, необязательно замещено одним дополнительным R3 и необязательно замещено одним или большим количеством R4,
где циклобутильное кольцо, содержащееся в D1, необязательно:
(a) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклобутильного кольца, содержащегося D1, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(b) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклобутильному кольцу, содержащемуся в D1, с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
и где циклопентильное кольцо, содержащееся в D2, циклогексильное кольцо, содержащееся в D3, и циклогептильное кольцо, содержащееся в D4, необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклопентильного кольца, содержащегося в D2, циклогексильного кольца, содержащегося в D3, или циклогептильного кольца, содержащегося в D4), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклопентильному кольцу, содержащемуся в D2, циклогексильному кольцу, содержащемуся в D3, или циклогептильному кольцу, содержащемуся в D4) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6.
Следует понимать, что связь, расположенная с противоположной стороны от R3, показанная в приведенных выше формулах D1, D2, D3 и D4, означает положение присоединения соответствующей группы Dl, D2, D3 или D4 к остальной части соединения формулы I, Ia, Ia-1, Ib или Ic.
В другом предпочтительном варианте осуществления D выбран из группы, включающей D1, D2, D3 и D4:

где циклобутильное кольцо, содержащееся в D1, циклопентильное кольцо, содержащееся в D2, циклогексильное кольцо, содержащееся в D3, и циклогептильное кольцо, содержащееся в D4, необязательно замещено одним дополнительным R3 и необязательно замещено одним или большим количеством R4.
В другом предпочтительном варианте осуществления D выбран из группы, включающей D1, D2, D3 и D4:

где циклобутильное кольцо, содержащееся в D1, циклопентильное кольцо, содержащееся в D2, циклогексильное кольцо, содержащееся в D3, и циклогептильное кольцо, содержащееся в D4, необязательно замещено одним или большим количеством R4.
В более предпочтительном варианте осуществления D обозначает

где циклогексильное кольцо, необязательно замещено одним дополнительным R3 и необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо, содержащееся в D, необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклогексильного кольца), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклогексильному кольцу) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6.
В еще более предпочтительном варианте осуществления D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклогексильного кольца), где p равно 1 или 2 и каждый R независимо обозначает водород или C1-C4-алкил; или
(с) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклогексильному кольцу) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6.
В еще более предпочтительном варианте осуществления D обозначает
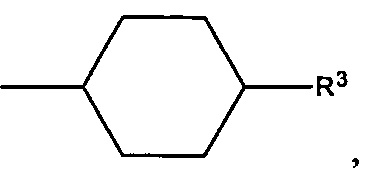
где циклогексильное кольцо необязательно замещено одним или большим количеством R4.
В особенно предпочтительном варианте осуществления D обозначает

В другом варианте осуществления D обозначает группу формулы

где циклогексильное кольцо необязательно замещено одним или большим количеством R4.
В другом варианте осуществления D обозначает группу формулы

В соединении формулы I, Ia, Ia-1, Ib или Ic каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -OH, -CONR7R8, оксогруппу, -C1-C4-алкилен-NR7R8, -C1-C4-алкилен-NHOH, -C1-C4-aлкилeн-NR9COR10, -C1-C4-алкилен-NR9SO2R10, -C1-C4-aлкилeн-NR9COOR10, -C1-C4-алкилен-NR9CONR7R8, -C1-C4-aлкилeн-NR9SO2NR7R8, -C1-C4-алкилен-ОН и -C1-C4-алкилен-CONR7R8. Если R3 обозначает оксогруппу (т.е. группу формулы =O), то в этом положении, т.е. на атоме C, к которому присоединена оксогруппа, может не содержаться дополнительный заместитель (R3, если содержится второй R3, или R4). Кроме того, следует понимать, что, если в любой из приведенных выше формул D1, D2, D3 или D4 R3 обозначает оксогруппу (т.е. =O), то эта оксогруппа присоединена к соответствующему циклоалкильному кольцу с помощью углерод-углеродной двойной связи. В предпочтительном варианте осуществления в соединении формулы I, Ia, Ia-1, Ib или Ic содержится только один R3.
В одном варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -CONR7R8, оксогруппу, -C1-C4-алкилен-NR7R8, -C1-C4-алкилен-NHOH, -C1-C4-алкилeн-NR9COR10, -C1-C4-алкилeн-NR9SO2R10, -C1-C4-алкилен-NR9COOR10, -C1-C4-алкилен-NR9CONR7R8, -C1-C4-алкилен-NR9SO2NR7R8, -C1-C4-алкилен-ОН и -C1-C4-алкилен-CONR7R8. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -ОН, оксогруппу, -C1-C4-алкилен-NR7R8, -C1-C4-алкилен-NHOH, -C1-C4-алкилен-NR9COR10, -C1-C4-алкилен-NR9SO2R10, -C1-C4-алкилен-NR9COOR10, -C1-C4-алкилен-NR9CONR7R8, -C1-C4-алкилен-NR9SO2NR7R8 и -C1-C4-алкилен-OH. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, оксогруппу, -C1-C4-алкилен-NR7R8, -C1-C4-алкилен-NHOH, -C1-C4-алкилен-NR9COR10, -C1-C4-алкилен-NR9SO2R10, -C1-C4-алкилен-NR9COOR10, -C1-C4-алкилен-NR9CONR7R8, -C1-C4-алкилен-NR9SO2NR7R8 и -C1-C4-алкилен-ОН. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -OH, -CONR7R8 и оксогруппу. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -CONR7R8 и оксогруппу. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -NR9SO2NR7R8, -ОН и оксогруппу. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR8CONR7R8, -NR9SO2NR7R8 и оксогруппу. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -OH, -CONR7R8 и оксогруппу. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -CONR7R8 и оксогруппу. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -ОН и оксогруппу. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей-NR7R8, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8 и оксогруппу. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -NR9COR10, -NR9SO2R10, -ОН и оксогруппу. В предпочтительном варианте осуществления содержится только один R3. В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -NR9COR10, -NR9SO2R10 и оксогруппу. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -ОН, оксогруппу, -C1-C4-aлкилeн-NR7R8 и -C1-C4-алкилен-ОН. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, оксогруппу, -C1-C4-алкилен-NR7R8 и -C1-C4-алкилен-ОН. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8, -ОН и оксогруппу. В предпочтительном варианте осуществления содержится только один R3.
В другом варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8 и -OH. В предпочтительном варианте осуществления содержится только один R3.
В предпочтительном варианте осуществления каждый R3 независимо выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8.
Предпочтительно, если указанный -C1-C4-aлкилeн-NR7R8 представляет собой -C1-C2-алкилен-NR7R8. В предпочтительном варианте осуществления содержится только один R3.
В более предпочтительном варианте осуществления каждый R3 независимо выбран из числа групп -NR7R8. В предпочтительном варианте осуществления содержится только один R3.
В соединении формулы I, Ia, Ia-1, Ib или Ic каждый R4 и каждый R6 независимо выбран из группы, включающей C1-C8-алкил, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу и C1-C8-алкоксигруппу.
Предпочтительно, если каждый R4 и каждый R6 независимо выбран из группы, включающей C1-C8-алкил, галоген и C1-C8-алкоксигруппу. Более предпочтительно, если каждый R4 и каждый R6 независимо выбран из группы, включающей C1-C4-алкил, галоген и C1-C4-алкоксигруппу.
В соединении формулы I, Ia, Ia-1, Ib или Ic каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил и гидрокси-C1-C8-алкил, или R7 и R8 связаны друг с другом и вместе с атомом N, к которому они присоединены, образуют насыщенное 3-7-членное гетероциклическое кольцо, которое необязательно содержит один дополнительный гетероатом, выбранный из группы, включающей N, О и S, где один или большее количество атомов C указанного гетероциклического кольца необязательно окислены с образованием групп СО, где один или большее количество атомов S указанного гетероциклического кольца, если они содержатся, необязательно окислены с независимым образованием групп SO или групп SO2, и где указанное гетероциклическое кольцо необязательно замещено одним или большим количеством R11. Предпочтительно, если указанные выше алкильные группы, в виде группы или части группы (например, R12R13N-C1-C8-алкильной или гидрокси-C1-C4-алкильной группы), представляют собой C1-C4-алкил, более предпочтительно C1-C4-алкил. В одном варианте осуществления каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил (предпочтительно H2N-C1-C8-алкил) и гидрокси-C1-C8-алкил; предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C4-алкил, R12R13N-C1-C4-алкил (предпочтительно H2N-C1-C4-алкил) и гидрокси-C1-C4-алкил, и более предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C2-алкил, R12R13N-C1-C2-алкил (предпочтительно Н2N-C1-C2-алкил) и гидрокси-C1-C2-алкил. В предпочтительном варианте осуществления R7 и R8 все обозначают водород.
В другом варианте осуществления R7 и R8 связаны друг с другом и вместе с атомом N, к которому они присоединены, образуют насыщенное 3-7-членное гетероциклическое кольцо, которое необязательно содержит один дополнительный гетероатом, выбранный из группы, включающей N, О и S, где один или большее количество атомов C указанного гетероциклического кольца необязательно окислены с образованием групп СО, где один или большее количество атомов S указанного гетероциклического кольца, если они содержатся, необязательно окислены с независимым образованием групп SO или групп SO2, и где указанное гетероциклическое кольцо необязательно замещено одним или большим количеством R11. В одном предпочтительном варианте осуществления -NR7R8 обозначает группу формулы:

В соединении формулы I, Ia, Ia-1, Ib или Ic каждый R9 независимо выбран из группы, включающей водород и C1-C4-алкил. В предпочтительном варианте осуществления каждый R9 обозначает водород.
В соединении формулы I, Ia, Ia-1, Ib или Ic каждый R10 независимо выбран из группы, включающей C1-C8-алкил, галоген-C1-C8-алкил, циклил и циклил-C1-C8-алкил, где указанный циклил или циклильный фрагмент, содержащийся в указанном циклил-C1-C8-алкиле (т.е. любая из указанных выше циклильных групп, включая также циклильную группу, образующую часть циклил-C1-C8-алкильной группы), необязательно замещен одним или большим количеством R14. В одном варианте осуществления каждый R10 выбран из группы, включающей C1-C8-алкил и циклил, необязательно замещенный одним или большим количеством R14, предпочтительно, если каждый R10 выбран из группы, включающей C1-C4-алкил (например, метил) и арил (предпочтительно фенил), необязательно замещенный одним или большим количеством R14. В другом варианте осуществления каждый R10 обозначает C1-C8-алкил, например, C1-C4-алкил. В другом варианте осуществления каждый R10 обозначает циклил, необязательно замещенный одним или большим количеством R14, например, арил, необязательно замещенный одним или большим количеством R14, предпочтительно фенил, необязательно замещенный одним или большим количеством R14. Указанные выше группы, необязательно замещенные одним или большим количеством R14, могут быть, например, замещены с помощью 1, 2 или 3 R14.
В другом варианте осуществления содержится один R3 и указанный R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8, где фрагмент -NR7R8, содержащийся в -NR7R8 и в -C1-C4-алкилен-NR7R8, представляет собой -NH2 или группу формулы:

В предпочтительном воплощении приведенного выше варианта осуществления содержится один R3 и указанный R3 выбран из группы, включающей -NH2 и -C1-C4-алкилен-NH2, предпочтительно из группы, включающей -NH2 и -C1-C2-алкилен-NH2 (например, -CH2-NH2, -CH2-CH2-NH2 или -CH(CH3)-NH2).
В другом варианте осуществления содержится один R3 и указанный R3 обозначает -NR7R8, где -NR7R8 представляет собой -NH2 или группу формулы:

В другом варианте осуществления содержится один R3 и указанный R3 обозначает -NH2.
В другом варианте осуществления содержится один R3 и указанный R3 обозначает группу формулы:

В приведенных выше вариантах осуществления, а также во всех вариантах осуществления соединений, предлагаемых в настоящем изобретении, описанных ниже, исключены следующие соединения:
2-((2-фенилциклопропил)амино)циклогептанол и
2-((2-фенилциклопропил)амино)циклопентанол.
Предпочтительно, если в приведенных выше вариантах осуществления, а также во всех вариантах осуществления соединений, предлагаемых в настоящем изобретении, описанных ниже, также исключен 2-((2-фенилциклопропил)амино)циклогексанол.
В соединении формулы I, Ia, Ib или Ic заместители -A-B и -NH-D циклопропильного фрагмента предпочтительно находятся в трансконфигурации. Таким образом, в одном варианте осуществления настоящее изобретение относится к соединению формулы I (включая соединение Ia, Ib или Ic), в котором группы -A-B и -NH-D находятся в транс-конфигурации. В предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы Ia, в котором группы -A-B и -NH-D находятся в трансконфигурации, которое является соединением формулы Ia-1:
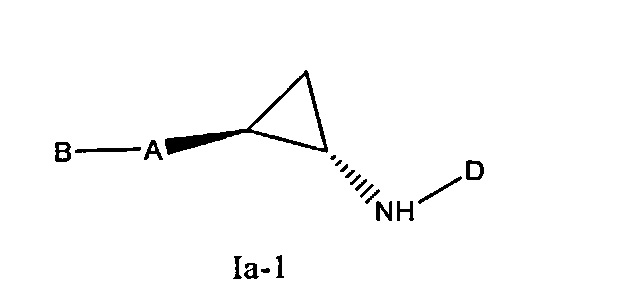
где группы и переменные в формуле Ia-1, включая A, B, D, Е, L, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, R13 и R14, являются такими, как определено выше для соединения формулы I и Ia и в различных предпочтительных вариантах осуществления соединения формулы I и Ia, описанных выше. Приведенное выше изображение химической структуры соединения формулы Ia-1 предназначено не для указания абсолютной стереохимической конфигурации двух хиральных центров, содержащихся в циклопропильном кольце, а только для указания их относительной стереохимической конфигурации (которая является транс-конфигурацией). Поэтому соединение формулы Ia-1 означает отдельные оптически активные транс-изомеры, а также смеси транс-изомеров.
В одном варианте осуществления настоящее изобретение относится к соединению формулы I, в которой каждый Rw, Rx, Ry и Rz независимо выбран из группы, включающей водород, фтор и С1-С4-алкил, предпочтительно из группы, включающей водород, фтор и метил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, в которой каждый Rw, Rx, Ry и Rz независимо выбран из группы, включающей водород и фтор.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, в которой Rw обозначает фтор и каждый Rx, Ry и Rz независимо выбран из группы, включающей водород, галоген и C1-C4-алкил; предпочтительно, если Rw обозначает фтор и каждый Rx, Ry и Rz обозначает водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, в которой Rz обозначает фтор и каждый Rw, Rx и Ry независимо выбран из группы, включающей водород, галоген и C1-C4-алкил; предпочтительно, если Rz обозначает фтор и каждый Rw, Rx и Ry обозначает водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, в которой Rw и Rz обозначают фтор и каждый Rx и Ry независимо выбран из группы, включающей водород, галоген и C1-C4-алкил; предпочтительно, если Rw и Rz обозначают фтор и каждый Rx и Ry обозначает водород.
В предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, в которой Rw выбран из группы, включающей водород, галоген и C1-C4-алкил, предпочтительно из группы, включающей водород, фтор и метил, и каждый Rx, Ry и Rz обозначает водород.
В более предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, в которой каждый Rw, Rx, Ry и Rz обозначает водород, т.е. к соединению формулы Ia:
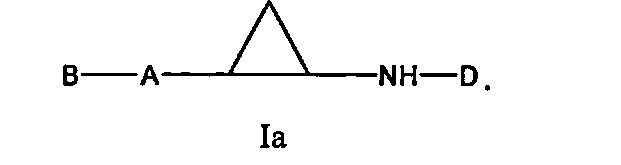
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, в которой каждый Rw, Rx, Ry и Rz независимо выбран из группы, включающей водород, галоген и C1-C4-алкил при условии, что по меньшей мере один из них нe обозначает водород, т.е. к соединению формулы Ib.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, в которой Rw выбран из группы, включающей галоген и C1-C4-алкил, предпочтительно из группы, включающей фтор и метил, и каждый Rx, Ry и Rz обозначает водород, т.е. к соединению формулы Ic. Предпочтительно, если в соединении формулы Ic Rw обозначает метил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой D выбран из группы, включающей D1, D2, D3 и D4:

где циклобутильное кольцо, содержащееся в D1, циклопентильное кольцо, содержащееся в D2, циклогексильное кольцо, содержащееся в D3, и циклогептильное кольцо, содержащееся в D4, необязательно замещено одним дополнительным R3 и необязательно замещено одним или большим количеством R4, и где циклобутильное кольцо, содержащееся в D1, циклопентильное кольцо, содержащееся в D2, циклогексильное кольцо, содержащееся в D3, и циклогептильное кольцо, содержащееся в D4, необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5 (возможность (а) применима только к D2, D3 и D4, но не к D1); или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклобутильного кольца, содержащегося в D1, циклопентильного кольца, содержащегося в D2, циклогексильного кольца, содержащегося в D3, или циклогептильного кольца, содержащегося в D4), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклобутильному кольцу, содержащемуся в D1, циклопентильному кольцу, содержащемуся в D2, циклогексильному кольцу, содержащемуся в D3, или циклогептильному кольцу, содержащемуся в D4) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6.
В предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой D обозначает

где циклогексильное кольцо, необязательно замещено одним дополнительным R3 и необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо, содержащееся в D, необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклогексильного кольца), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклогексильному кольцу) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6.
В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклогексильного кольца), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклогексильному кольцу) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6.
В более предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы 1а или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4.
В еще более предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы 1а или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой D обозначает

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой D обозначает

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -ОН, оксогруппу, -C1-C4-алкилен-NR7R8, -C1-C4-алкилен-NHOH, -C1-C4-aлкилeн-NR9COR10, -C1-C4-алкилен-NR9SO2R10, -C1-C4-алклен-NR9COOR10, -C1-C4-алкилен-NR9CONR7R8, -C1-C4-алкилен-NR9SO2NR7R8 и -C1-C4-алкилен-ОН.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, оксогруппу, -C1-C4-алкилен-NR7R8, -C1-C4-алкилен-NHOH, -C1-C4-алкилен-NR9COR10, -C1-C4-алкилен-NR9SO2R10, -C1-C4-алкилен-NR9COOR10, -C1-C4-алкилен-NR9CONR7R8, -C1-C4-алкилен-NR9SO2NR7R8 и -C1-C4-алкилен-ОН.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -ОН и оксогруппу.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8 и оксогруппу.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R3 независимо выбран из группы, включающей -NR7R8, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -ОН и оксогруппу. В более предпочтительном варианте осуществления каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил и гидрокси-C1-C8-алкил; предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C4-алкил, R12R13N-C1-C4-алкил и гидрокси-C1-C4-алкил, более предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C2-алкил, R12R13N-C1-C2-алкил и гидрокси-C1-C2-алкил, и еще более предпочтительно, если R7 и R8 все обозначают водород; и каждый R10 выбран из группы, включающей C1-C8-алкил и циклил, необязательно замещенный одним или большим количеством R14, предпочтительно, если каждый R10 выбран из группы, включающей C1-C4-алкил (например, метил) и арил (предпочтительно фенил), необязательно замещенный одним или большим количеством R14. Указанные выше группы, необязательно замещенные одним или большим количеством R14, могут быть, например, замещены с помощью 1, 2 или 3 R14.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R независимо выбран из группы, включающей -NR7R8, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8 и оксогруппу. В более предпочтительном варианте осуществления каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил и гидрокси-C1-C8-алкил; предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C4-алкил, R12R13N-C1-C4-алкил и гидрокси-C1-C4-алкил, более предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C2-алкил, R12R13N-C1-C2-алкил и гидрокси C1-C4-алкил, и еще более предпочтительно, если R7 и R8 все обозначают водород; и каждый R10 выбран из группы, включающей C1-C8-алкил и циклил, необязательно замещенный одним или большим количеством R14, предпочтительно, если каждый R10 выбран из группы, включающей C1-C4-алкил (например, метил) и арил (предпочтительно фенил), необязательно замещенный одним или большим количеством R14. Указанные выше группы, необязательно замещенные одним или большим количеством R14, могут быть, например, замещены с помощью 1, 2 или 3 R14.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R3 независимо выбран из группы, включающей -NR7R8, -NR9COR10, -NR9SO2R10, -ОН и оксогруппу. В более предпочтительном варианте осуществления каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил и гидрокси-C1-C8-алкил; предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C4-алкил, R12R13N-C1-C4-алкил и гидрокси-C1-C4-алкил, более предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C2-алкил, R12R13N-C1-C4-алкил и гидрокси-C1-C2-алкил, и еще более предпочтительно, если R7 и R8 все обозначают водород; и каждый R10 выбран из группы, включающей C1-C8-алкил и циклил, необязательно замещенный одним или большим количеством R14, предпочтительно, если каждый R10 выбран из группы, включающей C1-C4-алкил (например, метил) и арил (предпочтительно фенил), необязательно замещенный одним или большим количеством R14. Указанные выше группы, необязательно замещенные одним или большим количеством R14, могут быть, например, замещены с помощью 1, 2 или 3 R14.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R3 независимо выбран из группы, включающей -NR7R8, -NR9COR10, -NR9SO2R10 и оксогруппу. В более предпочтительном варианте осуществления каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил и гидрокси-C1-C8-алкил; предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C4-алкил, R12R13N-C1-C4-алкил и гидрокси-C1-C4-алкил, более предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C2-алкил, R12R13N-C1-C2-алкил и гидрокси-C1-C2-алкил, и еще более предпочтительно, если R7 и R8 все обозначают водород; и каждый R10 выбран из группы, включающей C1-C8-алкил и циклил, необязательно замещенный одним или большим количеством R14, предпочтительно, если каждый R10 выбран из группы, включающей C1-C4-алкил (например, метил) и арил (предпочтительно фенил), необязательно замещенный одним или большим количеством R14. Указанные выше группы, необязательно замещенные одним или большим количеством R14, могут быть, например, замещены с помощью 1, 2 или 3 R14.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R3 независимо выбран из группы, включающей -NR7R8, -ОН, оксогруппу, -C1-C4-алкилен-NR7R8 и - C1-C4-алкилен-ОН. В более предпочтительном варианте осуществления каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил и гидрокси-C1-C8-алкил; предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C4-алкил, R12R13N-C1-C4-алкил и гидрокси-C1-C4-алкил, более предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C2-алкил, R12R13N-C1-C2-алкил и гидрокси-C1-C2-алкил, и еще более предпочтительно, если R7 и R8 все обозначают водород. В другом предпочтительном варианте осуществления R7 и R8 связаны друг с другом и вместе с атомом N, к которому они присоединены, образуют насыщенное 3-7-членное гетероциклическое кольцо, которое необязательно содержит один дополнительный гетероатом, выбранный из группы, включающей N, О и S, где один или большее количество атомов C указанного гетероциклического кольца необязательно окислены с образованием групп СО, где один или большее количество атомов S указанного гетероциклического кольца, если они содержатся, необязательно окислены с независимым образованием групп SO или групп SO2, и где указанное гетероциклическое кольцо необязательно замещено одним или большим количеством (например, с помощью 1, 2 или 3) R11, и предпочтительно, если -NR7R8 обозначает группу формулы:

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R3 независимо выбран из группы, включающей -NR7R8, оксогруппу, -C1-C4-алкилен-NR7R8 и -C1-C4-алкилен-ОН. В более предпочтительном варианте осуществления каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил и гидрокси-C1-C8-алкил; предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C4-алкил, R12R13N-C1-C4-алкил и гидрокси-C1-C4-алкил, более предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-С2-алкил, R12R13N-C1-С2-алкил и гидрокси-C1-С2-алкил, и еще более предпочтительно, если R7 и R8 все обозначают водород. В другом предпочтительном варианте осуществления R7 и R8 связаны друг с другом и вместе с атомом N, к которому они присоединены, образуют насыщенное 3-7-членное гетероциклическое кольцо, которое необязательно содержит один дополнительный гетероатом, выбранный из группы, включающей N, О и S, где один или большее количество атомов C указанного гетероциклического кольца необязательно окислены с образованием групп СО, где один или большее количество атомов S указанного гетероциклического кольца, если они содержатся, необязательно окислены с независимым образованием групп SO или групп SO2, и где указанное гетероциклическое кольцо необязательно замещено одним или большим количеством (например, с помощью 1, 2 или 3) R11, и предпочтительно, если -NR7R8 обозначает группу формулы:

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R3 независимо выбран из группы, включающей -NR7R8 и -OH. В более предпочтительном варианте осуществления каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил и гидрокси-C1-C8-алкил; предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-С4-алкил, R12R13N-C1-С2-алкил и гидрокси-C1-C4-алкил, более предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-С2-алкил, R12R13N-C1-С2-алкил и гидрокси-C1-С2-алкил, и еще более предпочтительно, если R7 и R8 все обозначают водород. В другом предпочтительном варианте осуществления R7 и R8 связаны друг с другом и вместе с атомом N, к которому они присоединены, образуют насыщенное 3-7-членное гетероциклическое кольцо, которое необязательно содержит один дополнительный гетероатом, выбранный из группы, включающей N, О и S, где один или большее количество атомов C указанного гетероциклического кольца необязательно окислены с образованием групп СО, где один или большее количество атомов S указанного гетероциклического кольца, если они содержатся, необязательно окислены с независимым образованием групп SO или групп SO2, и где указанное гетероциклическое кольцо необязательно замещено одним или большим количеством (например, с помощью 1, 2 или 3) R11, и предпочтительно, если -NR7R8 обозначает группу формулы:

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R3 независимо выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8, предпочтительно из группы, включающей -NR7R8 и -C1-C2-aлкилeн-NR7R8. В более предпочтительном варианте осуществления каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил и гидрокси-C1-C8-алкил; предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C-алкил, R12R13N-C1-C4-алкил и гидрокси-C1-C4-алкил, более предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C2-алкил, R12R13N-C1-С2-алкил и гидрокси-C1-C2-алкил, и еще более предпочтительно, если R7 и R8 все обозначают водород. В другом предпочтительном варианте осуществления R7 и R8 связаны друг с другом и вместе с атомом N, к которому они присоединены, образуют насыщенное 3-7-членное гетероциклическое кольцо, которое необязательно содержит один дополнительный гетероатом, выбранный из группы, включающей N, О и S, где один или большее количество атомов C указанного гетероциклического кольца необязательно окислены с образованием групп СО, где один или большее количество атомов S указанного гетероциклического кольца, если они содержатся, необязательно окислены с независимым образованием групп SO или групп SO2, и где указанное гетероциклическое кольцо необязательно замещено одним или большим количеством (например, с помощью 1, 2 или 3) R11, и предпочтительно, если -NR7R8 обозначает группу формулы:

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой каждый R3 независимо выбран из числа групп -NR7R8. В более предпочтительном варианте осуществления каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C8-алкил, R12R13N-C1-C8-алкил и гидрокси-C1-C8-алкил; предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-C4-алкил, R12R13N-C1-C4-алкил и гидрокси-C1-C4-алкил, более предпочтительно, если каждый R7 и каждый R8 независимо выбран из группы, включающей водород, C1-С2-алкил, R12R13N-C1-С2-алкил и гидрокси-C1-C2-алкил, и еще более предпочтительно, если R7 и R8 все обозначают водород. В другом предпочтительном варианте осуществления R7 и R8 связаны друг с другом и вместе с атомом N, к которому они присоединены, образуют насыщенное 3-7-членное гетероциклическое кольцо, которое необязательно содержит один дополнительный гетероатом, выбранный из группы, включающей N, О и S, где один или большее количество атомов C указанного гетероциклического кольца необязательно окислены с образованием групп СО, где один или большее количество атомов S указанного гетероциклического кольца, если они содержатся, необязательно окислены с независимым образованием групп SO или групп SO2, и где указанное гетероциклическое кольцо необязательно замещено одним или большим количеством (например, с помощью 1, 2 или 3) R11, и предпочтительно, если -NR7R8 обозначает группу формулы:
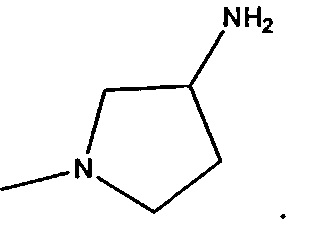
В предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Iс, включая соединение I, Ia, Ia-1, Ib или Iс, определенное в предпочтительных вариантах осуществления, раскрытых в настоящем изобретении, в которых в кольце D содержится только один заместитель R3.
В одном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D выбран из группы, включающей D1, D2, D3 и D4:

где циклобутильное кольцо, содержащееся в D1, циклопентильное кольцо, содержащееся в D2, циклогексильное кольцо, содержащееся в D3, и циклогептильное кольцо, содержащееся в D4, необязательно замещено одним дополнительным R3 и необязательно замещено одним или большим количеством R4, и где циклобутильное кольцо, содержащееся в D1, циклопентильное кольцо, содержащееся в D2, циклогексильное кольцо, содержащееся в D3, и циклогептильное кольцо, содержащееся в D4, необязательно:
(а) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5 (возможность (а) применима только к D2, D3 и D4, но не к D1); или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклобутильного кольца, содержащегося в D1, циклопентильного кольца, содержащегося в D2, циклогексильного кольца, содержащегося в D3, или циклогептильного кольца, содержащегося в D4), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклобутильному кольцу, содержащемуся в D1, циклопентильному кольцу, содержащемуся в D2, циклогексильному кольцу, содержащемуся в D3, или циклогептильному кольцу, содержащемуся в D4) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6; и каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -OH, -CONR7R8, оксогруппу, -C1-C4-алкилен-NR7R8, -C1-C4-алкилен-NHOH, -C1-C4-aлкилeн-NR9COR10, -C1-C4-алкилен-NR9SO2R10, -C1-C4-алкилен-NR9COOR10, -C1-C4-алкилен-NR9CONR7R8, - C1-C8-алкилен-NR9SO2NR7R8, -C1-C4-алкилен-ОН и -C1-C4-aлкилeн-CONR7R8. Более предпочтительно, если содержится только одна группа R3.
В одном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой: D выбран из группы, включающей D1, D2, D3 и D4:

где циклобутильное кольцо, содержащееся в D1, циклопентильное кольцо, содержащееся в D2, циклогексильное кольцо, содержащееся в D3, и циклогептильное кольцо, содержащееся в D4, необязательно замещено одним дополнительным R3 и необязательно замещено одним или большим количеством R4, и где циклобутильное кольцо, содержащееся в D1, циклопентильное кольцо, содержащееся в D2, циклогексильное кольцо, содержащееся в D3, и циклогептильное кольцо, содержащееся в D4, необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5 (возможность (а) применима только к D2, D3 и D4, но не к D1); или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклобутильного кольца, содержащегося в D1, циклопентильного кольца, содержащегося в D2, циклогексильного кольца, содержащегося в D3, или циклогептильного кольца, содержащегося в D4), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклобутильному кольцу, содержащемуся в D1, циклопентильному кольцу, содержащемуся в D2, циклогексильному кольцу, содержащемуся в D3, или циклогептильному кольцу, содержащемуся в D4) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6; и каждый R3 независимо выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8. Более предпочтительно, если содержится только одна группа R3. В предпочтительном варианте осуществления R7 и R8 все обозначают водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо, необязательно замещено одним дополнительным R3 и необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо, содержащееся в D, необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклогексильного кольца), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклогексильному кольцу) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6; и каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -OH, -CONR7R8, оксогруппу, -C1-C4-алкилeн-NR7R8, -C1-C4-алкилен-NHOH, -C1-C4-алкилен-NR9СOR10, -C1-C4-алкилен-NR9SO2R10, -C1-C4-алкилен-NR9COOR10, -C1-C4-алкилен-NR9CONR7R8, C1-C4-алкилен-NR9SO2NR7R8, -C1-C4-алкилен-ОН и -C1-C4-алкилен-CONR7R8. Более предпочтительно, если содержится только одна группа R3.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо, необязательно замещено одним дополнительным R3 и необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо, содержащееся в D, необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклогексильного кольца), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклогексильному кольцу) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6; и каждый R3 независимо выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -ОН и оксогруппу. Более предпочтительно, если содержится только одна группа R3.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо, необязательно замещено одним дополнительным R3 и необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо, содержащееся в D, необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклогексильного кольца), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклогексильному кольцу) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6; и каждый R3 независимо выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8. Более предпочтительно, если содержится только одна группа R3. В предпочтительном варианте осуществления R7 и R8 все обозначают водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклогексильного кольца), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклогексильному кольцу) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6; и R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -OH, -CONR7R8, оксогруппу, -C1-C4-алкилен-NR7R8, -C1-C4-алкилен-NHOH, - C1-C4-алкилен-NR9COR10, -C1-C4-aлкилeн-NR9SO2R10, -C1-C4-алкилен-NR9COOR10, -C1-C4-алкилен-NR9CONR7R8, -C1-C4-алкилен-NR9SO2NR7R8, -C1-C4-алкилен-ОН и -C1-C4-алкилен-CONR7R8.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает
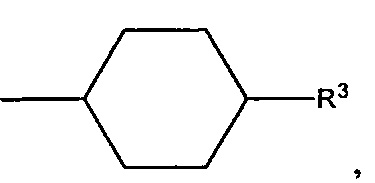
где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклогексильного кольца), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклогексильному кольцу) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6; и
R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -ОН и оксогруппу.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклогексильного кольца), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклогексильному кольцу) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6; и R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8. В предпочтительном варианте осуществления R7 и R8 все обозначают водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы (т.е. циклогексильного кольца), где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе (т.е. к циклогексильному кольцу) с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6; и R3 обозначает -NR7R8.
В приведенном выше варианте осуществления R3 предпочтительно обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4; и
R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -OH, -CONR7R8, оксогруппу, -C1-C4-aлкилeн-NR7R8, -C1-C4-алкилен-NHOH, -C1-C4-алкилен-NR9COR10, -C1-C4-aлкилeн-NR9SO2R10,-C1-C4-aлкилeн-NR9COOR10, -C1-C4-aлкилeн-NR9CONR7R8, -C1-C4-алкилен-NR9SO2NR7R8, -C1-C4-алкилен-ОН и -C1-C4-aлкилeн-CONR7R8.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4; и
R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -ОН и оксогруппу.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4; и
R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8. В предпочтительном варианте осуществления R7 и R8 все обозначают водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4; и
R3 обозначает -NR7R8.
В приведенном выше варианте осуществления R3 предпочтительно обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой: D обозначает
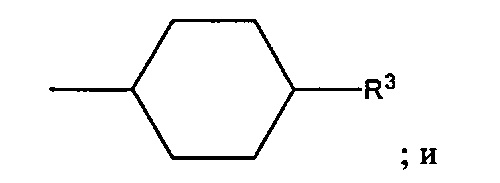
R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -OH, -CONR7R8, оксогруппу, -C1-C4-алкилен-NR7R8, -C1-C4-алкилен-NHOH, -C1-C4-алкилен-NR9COR10, -C1-C4-алкилен-NR9SO2R10, -C1-C4-алкилен-NR9COOR10, -C1-C4-алкилен-NR9CONR7R8, -C1-C4-алкилен-NR9SO2NR7R8, -C1-C4-алкилен-ОН и -C1-C4-алкилен-CONR7R8.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, NR9SO2NR7R8, -ОН и оксогруппу.
В предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8. В предпочтительном варианте осуществления R7 и R8 все обозначают водород.
В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы 1а-1), в которой:
D обозначает

R3 обозначает -NR7R8.
В приведенном выше варианте осуществления R3 предпочтительно обозначает -NH2. В другом предпочтительном варианте осуществления R3обозначает

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Iа-1), в которой:
D обозначает

где циклобутильное кольцо необязательно замещено одним или большим количеством R4; и
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8. В предпочтительном варианте осуществления R7 и R8 все обозначают водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклобутильное кольцо необязательно замещено одним или большим количеством R4; и
R3 обозначает -NR7R8. В этом варианте осуществления R3 предпочтительно обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает
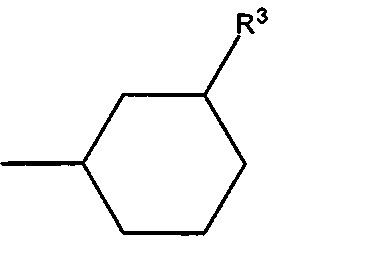
где циклогексильное кольцо необязательно замещено одним или большим количеством R4; и
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8. В предпочтительном варианте осуществления R7 и R8 все обозначают водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает
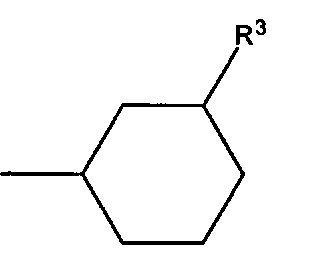
где циклогексильное кольцо необязательно замещено одним или большим количеством R4: и
R3 обозначает -NR7R8. В этом варианте осуществления R3 предпочтительно обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой A обозначает фенил, нафтил или моноциклический гетероарил, где указанный фенил, нафтил или моноциклический гетероарил необязательно замещен одним или большим количеством (например, с помощью 1 или 2) R1. В более предпочтительном варианте осуществления A обозначает фенил, нафтил, пиридил, тиофенил, пирролил, фуранил или тиазолил, где A необязательно замещен одним или большим количеством R1. Более предпочтительно, если A обозначает фенил, нафтил, пиридил или тиазолил, где A необязательно замещен одним или большим количеством R1. Еще более предпочтительно, если A обозначает фенил, 2-нафтил, 3-пиридил или 5-тиазолил, где A необязательно замещен одним или большим количеством R1. В одном варианте осуществления A обозначает фенил, необязательно замещенный одним или большим количеством R1. В другом варианте осуществления A обозначает нафтил, предпочтительно 2-нафтил, необязательно замещенный одним или большим количеством R1. В другом варианте осуществления A обозначает пиридил, предпочтительно 3-пиридил, необязательно замещенный одним или большим количеством R1. В другом варианте осуществления A обозначает тиазолил, предпочтительно 5-тиазолил, необязательно замещенный одним или большим количеством R1.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой A обозначает фенил или моноциклический гетероарил, где указанный фенил или указанный моноциклический гетероарил необязательно замещен одним или большим количеством (например, с помощью 1 или 2) R1. В более предпочтительном варианте осуществления A обозначает фенил, пиридил, тиофенил, пирролил, фуранил или тиазолил, где A необязательно замещен одним или большим количеством R1. Более предпочтительно, если A обозначает фенил, пиридил или тиазолил, где A необязательно замещен одним или большим количеством R1. В одном варианте осуществления A обозначает фенил. В другом варианте осуществления A обозначает 3-пиридил. В другом варианте осуществления A обозначает 5-тиазолил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой A обозначает фенил, необязательно замещенный одним или большим количеством R1.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой A обозначает нафтил (например, 2-нафтил), необязательно замещенный одним или большим количеством R1.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой A обозначает гетероарил, необязательно замещенный одним или большим количеством R1. Предпочтительно, если A обозначает моноциклический гетероарил, необязательно замещенный одним или большим количеством R1.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой: А обозначает фенил или моноциклический гетероарил (предпочтительно фенил, пиридил или тиазолил, более предпочтительно фенил, 3-пиридил или 5-тиазолил), где A необязательно замещен одним или большим количеством R1;
B обозначает водород, R1 или -L-E;
E обозначает фенил, необязательно замещенный одним или большим количеством R2; и
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. В более предпочтительном варианте осуществления L обозначает связь или -CH2-O-, где указанная группа -CH2-O-связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой: А обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R1; и
B обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой: где A обозначает фенил, нафтил или моноциклический гетероарил, где указанный фенил, указанный нафтил или указанный моноциклический гетероарил необязательно замещен одним или большим количеством R1; и B обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
А обозначает фенил или моноциклический гетероарил, где указанный фенил или указанный моноциклический гетероарил необязательно замещен одним или большим количеством R1; и
B обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-апкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где A необязательно замещен одним или большим количеством R1; и
B обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
А обозначает нафтил, необязательно замещенный одним или большим количеством R1; и
B обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
А обозначает фенил, нафтил или моноциклический гетероарил; и
B обозначает водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой: А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил); и B обозначает водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
А обозначает фенил; и
B обозначает водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
А обозначает нафтил; и
B обозначает водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой: А обозначает гетероарил, предпочтительно моноциклический гетероарил; и B обозначает водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Iа-1), в которой:
А обозначает фенил или моноциклический гетероарил (предпочтительно фенил, пиридил или тиазолил, и более предпочтительно фенил, 3-пиридил или 5-тиазолил), где указанный фенил или указанный моноциклический гетероарил необязательно замещен одним или большим количеством R1; и
B обозначает -L-E. В приведенном выше варианте осуществления предпочтительно, если L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. В более предпочтительном варианте осуществления E обозначает фенил, необязательно замещенный одним или большим количеством R, и L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O-связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
А обозначает фенил или пиридил (предпочтительно фенил или 3-пиридил), где A необязательно замещен одним или большим количеством R1; и
B обозначает -L-E. В приведенном выше варианте осуществления предпочтительно, если L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. В более предпочтительном варианте осуществления E обозначает фенил, необязательно замещенный одним или большим количеством R2, и L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
А обозначает фенил; и
B обозначает -L-E. В приведенном выше варианте осуществления предпочтительно, если L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. В более предпочтительном варианте осуществления E обозначает фенил, необязательно замещенный одним или большим количеством R2, и L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O-связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
А обозначает 3-пиридил; и
B обозначает -L-E. В приведенном выше варианте осуществления предпочтительно, если L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. В более предпочтительном варианте осуществления E обозначает фенил, необязательно замещенный одним или большим количеством R2, и L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O-связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
B обозначает -L-E;
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или О соответственно, и связаны с кольцом E через группу -CH2-; и
E обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R2. В предпочтительном варианте осуществления каждый R2 независимо выбран из группы, включающей гидроксигруппу, галоген, галоген-C1-C8-алкил и N-сульфонамидную группу.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает
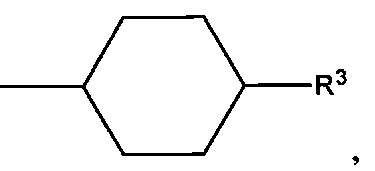
где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где A необязательно замещен одним или большим количеством R1;
B обозначает водород, R1 или -L-E;
E обозначает фенил, необязательно замещенный одним или большим количеством R2;
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
А обозначает арил или гетероарил, где A необязательно замещен одним или большим количеством R1; и
B обозначает водород или R.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(с) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где A необязательно замещен одним или большим количеством R1; и
B обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
А обозначает фенил, необязательно замещенный одним или большим количеством R1; и
B обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
А обозначает арил или гетероарил (предпочтительно фенил, нафтил, пиридил или тиазолил); и
B обозначает водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
А обозначает фенил; и
B обозначает водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
А обозначает фенил или пиридил (предпочтительно фенил или 3-пиридил), где A необязательно замещен одним или большим количеством R1; и
B обозначает -L-E. Предпочтительно, если L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. В более предпочтительном варианте осуществления E обозначает фенил, необязательно замещенный одним или большим количеством R2, и L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где A необязательно замещен одним или большим количеством R1;
B обозначает водород, R1 или -L-E;
E обозначает фенил, необязательно замещенный одним или большим количеством R2;
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NR7R8. Более предпочтительно, если R3 обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где A необязательно замещен одним или большим количеством R1;
В обозначает водород, R1 или -L-E;
Е обозначает фенил, необязательно замещенный одним или большим количеством R2;
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NR7R8. Более предпочтительно, если R3 обозначает -NH2.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(а) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8;
А обозначает арил или гетероарил, где A необязательно замещен одним или большим количеством R1; и
В обозначает водород или R1.
В предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NR7R8. Более предпочтительно, если R3 обозначает -NH2.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает
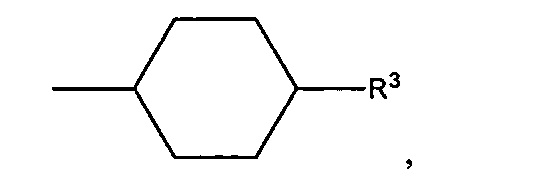
где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где A необязательно замещен одним или большим количеством R1; и
В обозначает водород или R1.
В предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NR7R8. Более предпочтительно, если R3 обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(а) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где A необязательно замещен одним или большим количеством R1; и
B обозначает водород или R1.
В предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NR7R8. Более предпочтительно, если R3 обозначает -NH2.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает
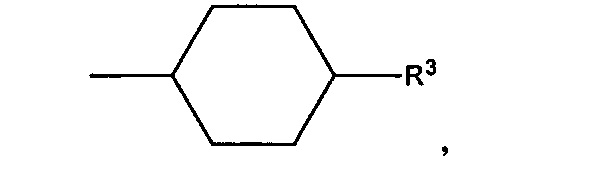
где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8;
А обозначает фенил, необязательно замещенный одним или большим количеством R1; и
В обозначает водород или R1.
В предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NR7R8. Более предпочтительно, если R3 обозначает -NH2.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8;
А обозначает фенил; и
B обозначает водород.
В предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NR7R8. Более предпочтительно, если R3 обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(а) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8;
А обозначает фенил; и
В обозначает водород.
В предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NR7R8. Более предпочтительно, если R3 обозначает -NH2.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(а) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8;
А обозначает фенил или пиридил (предпочтительно фенил или 3-пиридил), где A необязательно замещен одним или большим количеством R1; и
B обозначает -L-E. Предпочтительно, если L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. В более предпочтительном варианте осуществления E обозначает фенил, необязательно замещенный одним или большим количеством R2, и L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NR7R8. Более предпочтительно, если R3 обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4, и где циклогексильное кольцо необязательно:
(a) сконденсировано с фенильным или 5- или 6-членным ароматическим гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное конденсированное фенильное или указанное конденсированное ароматическое гетероциклическое кольцо необязательно замещено одним или большим количеством R5; или
(b) связано с мостиковой группой -(C(Ra)2)p-, соединяющей любые два несоседних кольцевых атома углерода циклоалкильной группы, где p равно 1 или 2 и каждый Ra независимо обозначает водород или C1-C4-алкил; или
(c) связано со вторым кольцом, которое является 3-7-членным насыщенным карбоциклическим кольцом или 3-7-членным насыщенным гетероциклическим кольцом, содержащим от 1 до 3 гетероатомов, независимо выбранных из группы, включающей N, О и S, где указанное второе кольцо присоединено к циклоалкильной группе с помощью одного атома углерода, общего для обоих колец, и где указанное второе кольцо необязательно замещено одним или большим количеством R6;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8;
А обозначает фенил или пиридил (предпочтительно фенил или 3-пиридил), где А необязательно замещен одним или большим количеством R1; и
B обозначает -L-E. Предпочтительно, если L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом А через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. В более предпочтительном варианте осуществления E обозначает фенил, необязательно замещенный одним или большим количеством R2, и L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом А через атом N или О соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CН2-O-, где указанная группа -СН2-О- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NR7R8. Более предпочтительно, если R3 обозначает -NH2.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Iс (предпочтительно к соединению формулы I, Iа или Ia-1, более предпочтительно к соединению формулы Iа или Iа-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -NR9SO2NR7R8, -OH, -CONR7R8, оксогруппу, -C1-С4-алкилен-NR7R8, -C1-С4-алкилен-NHOH, -C1-С4-алкилен-NR9COR10, -C1-С4-алкилен-NR9SO2R10, -C1-С4-алкилен-NR9СOOR10, -C1-С4-aлкилeн-NR9CONR7R8, -C1-С4-алкилен-NR9SO2NR7R8, -C1-С4-алкилен-ОН и -C1-С4-алкилен-CONR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где A необязательно замещен одним или большим количеством R1;
B обозначает водород, R1 или -L-E;
Е обозначает фенил, необязательно замещенный одним или большим количеством R2;
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -NR9SO2NR7R8, -OH, -CONR7R8, оксогруппу, -C1-С4-алкилен-NR7R8, -C1-С4-алкилен-NHOH, -C1-С4-алкилен-NR9COR10, -C1-С4-алкилен-NR9SO2R10, -C1-С4-алкилен-NR9СOOR10, -C1-С4-aлкилeн-NR9CONR7R8, -C1-С4-алкилен-NR9SO2NR7R8, -C1-С4-алкилен-ОН и -C1-С4-алкилен-CONR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где А необязательно замещен одним или большим количеством R1; и
B обозначает водород или R1.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -NR9SO2NR7R8, -OH, -CONR7R8, оксогруппу, -C1-С4-алкилен-NR7R8, -C1-С4-алкилен-NHOH, -C1-С4-алкилен-NR9COR10, -C1-С4-алкилен-NR9SO2R10, -C1-С4-алкилен-NR9СOOR10, -C1-С4-aлкилeн-NR9CONR7R8, -C1-С4-алкилен-NR9SO2NR7R8, -C1-С4-алкилен-ОН и -C1-С4-алкилен-CONR7R8;
А обозначает фенил; и
B обозначает водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -NR9SO2NR7R8, -OH, -CONR7R8, оксогруппу, -C1-С4-алкилен-NR7R8, -C1-С4-алкилен-NHOH, -C1-С4-алкилен-NR9COR10, -C1-С4-алкилен-NR9SO2R10, -C1-С4-алкилен-NR9СOOR10, -C1-С4-aлкилeн-NR9CONR7R8, -C1-С4-алкилен-NR9SO2NR7R8, -C1-С4-алкилен-ОН и -C1-С4-алкилен-CONR7R8;
А обозначает фенил или пиридил (предпочтительно фенил или 3-пиридил), где А необязательно замещен одним или большим количеством R1; и
В обозначает -L-E. Предпочтительно, если L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом А через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. В более предпочтительном варианте осуществления Е обозначает фенил, необязательно замещенный одним или большим количеством R2, и L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Iа-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -NR9SO2NR7R8, -ОН и оксогруппу;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где А необязательно замещен одним или большим количеством R1;
B обозначает водород, R1 или -L-E;
Е обозначает фенил, необязательно замещенный одним или большим количеством R2;
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -NR9SO2NR7R8, -ОН и оксогруппу;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где A необязательно замещен одним или большим количеством R1; и
B обозначает водород или R1.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Iа-1), в которой:
D обозначает
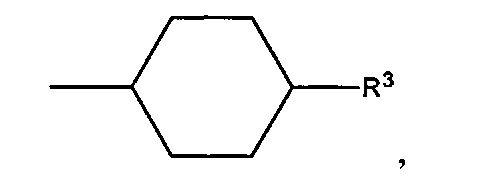
где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -NR9SO2NR7R8, -ОН и оксогруппу;
А обозначает фенил; и
B обозначает водород.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8, -NHOH, -NR9COR10, -NR9SO2R10, -NR9COOR10, -NR9CONR7R8, -NR9SO2NR7R8, -ОН и оксогруппу;
А обозначает фенил или пиридил (предпочтительно фенил или 3-пиридил), где А необязательно замещен одним или большим количеством R1; и
B обозначает -L-E. Предпочтительно, если L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. В более предпочтительном варианте осуществления E обозначает фенил, необязательно замещенный одним или большим количеством R2, и L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где A необязательно замещен одним или большим количеством R1;
В обозначает водород, R1 или -L-E;
Е обозначает фенил, необязательно замещенный одним или большим количеством R2;
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где А необязательно замещен одним или большим количеством R1;
В обозначает водород, R1 или -L-E;
Е обозначает фенил, необязательно замещенный одним или большим количеством R2;
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8;
А обозначает арил или гетероарил, где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R1; и
В обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В более предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где А необязательно замещен одним или большим количеством R1; и
В обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), С1-С4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В более предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает
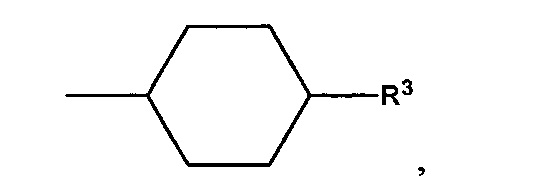
где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где A необязательно замещен одним или большим количеством R1; и
B обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В еще более предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Iа-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8;
А обозначает фенил, необязательно замещенный одним или большим количеством R1; и
В обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8;
А обозначает нафтил, необязательно замещенный одним или большим количеством R1; и
B обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), С1-С4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8;
А обозначает гетероарил, предпочтительно моноциклический гетероарил, необязательно замещенный одним или большим количеством R1; и
B обозначает водород или R1.
В приведенном выше варианте осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8;
А обозначает фенил; и
B обозначает водород.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-алкилен-NR7R8;
А обозначает фенил; и
B обозначает водород.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает
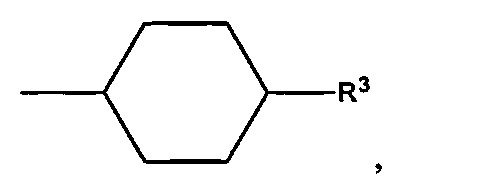
где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 выбран из группы, включающей -NR7R8 и -C1-C4-aлкилeн-NR7R8;
А обозначает фенил или пиридил (предпочтительно фенил или 3-пиридил), где А необязательно замещен одним или большим количеством R1; и
B обозначает -L-E. Предпочтительно, если L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом А через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. В более предпочтительном варианте осуществления Е обозначает фенил, необязательно замещенный одним или большим количеством R2, и L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-О- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает арил или гетероарил (например, фенил, нафтил или моноциклический гетероарил), где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R1; и
B обозначает водород, R1 или -L-E.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где А необязательно замещен одним или большим количеством R1; и
B обозначает водород, R1 или -L-E.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где А необязательно замещен одним или большим количеством R1;
B обозначает водород, R1 или -L-E;
Е обозначает фенил, необязательно замещенный одним или большим количеством R2;
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Ia или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где А необязательно замещен одним или большим количеством R1;
В обозначает водород, R1 или -L-E;
Е обозначает фенил, необязательно замещенный одним или большим количеством R2;
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-. Предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает арил или гетероарил (например, фенил, нафтил или моноциклический гетероарил), где указанный арил или указанный гетероарил необязательно замещен одним или большим количеством R1; и
В обозначает водород или R1.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В указанных выше вариантах осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.

В более предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где А необязательно замещен одним или большим количеством R1; и
B обозначает водород или R1.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В указанных выше вариантах осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В более предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил), где А необязательно замещен одним или большим количеством R1; и
B обозначает водород или R1.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В указанных выше вариантах осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил, необязательно замещенный одним или большим количеством R1; и
В обозначает водород или R1.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В указанных выше вариантах осуществления предпочтительно, если каждый R1 независимо выбран из группы, включающей C1-C8-алкил, аминогруппу, амидную группу, гидроксигруппу, галоген, галоген-C1-C8-алкил, галоген-C1-C8-алкоксигруппу, цианогруппу, сульфонамидную группу, C1-C8-алкоксигруппу, ацил, карбоксигруппу, карбаматную группу и мочевинную группу. В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил (например, метил), галоген-C1-C4-алкил (например, трифторметил), C1-C4-алкоксигруппу (например, метоксигруппу) и C3-C6-циклоалкил (например, циклопропил). В другом предпочтительном варианте осуществления каждый R1 независимо выбран из группы, включающей галоген, C1-C4-алкил и C3-C6-циклоалкил.
В особенно предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic, в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил, нафтил или моноциклический гетероарил; и
B обозначает водород.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В другом особенно предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic, в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил, пиридил или тиазолил (предпочтительно фенил, 3-пиридил или 5-тиазолил); и
B обозначает водород.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В другом особенно предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил; и
В обозначает водород.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом особенно предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил; и
В обозначает водород.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил или пиридил (предпочтительно фенил или 3-пиридил), где А необязательно замещен одним или большим количеством R1; и
В обозначает -L-E.
Предпочтительно, если L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-; более предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил или пиридил (предпочтительно фенил или 3-пиридил), где А необязательно замещен одним или большим количеством R1; и
B обозначает -L-E.
Предпочтительно, если L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-; более предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил или пиридил (предпочтительно фенил или 3-пиридил), где А необязательно замещен одним или большим количеством R1;
В обозначает -L-E;
Е обозначает фенил, необязательно замещенный одним или большим количеством R2; и
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-, и предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2. В другом предпочтительном варианте осуществления R3 обозначает

В другом предпочтительном варианте осуществления настоящее изобретение относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Iа-1), в которой:
D обозначает

где циклогексильное кольцо необязательно замещено одним или большим количеством R4;
R3 обозначает -NR7R8;
А обозначает фенил или пиридил (предпочтительно фенил или 3-пиридил), где А необязательно замещен одним или большим количеством R1;
B обозначает -L-E;
Е обозначает фенил, необязательно замещенный одним или большим количеством R2; и
L обозначает связь, -O-, -NH-, -CH2-NH- или -CH2-O-, где указанные группы -CH2-NH- и -CH2-O- связаны с кольцом A через атом N или O соответственно, и связаны с кольцом E через группу -CH2-, и предпочтительно, если L обозначает связь или -CH2-O-, где указанная группа -CH2-O- связана с кольцом A через атом O и с кольцом E через группу -CH2-.
В более предпочтительном воплощении приведенного выше варианта осуществления R3 обозначает -NH2.
В другом варианте осуществления настоящее изобретение относится к соединению формулы I, Ia или Ia-1, выбранному из группы, включающей:
N1-((транс)-2-фенилциклопропил)циклогексан-1,4-диамин;
(цис)-N1-((1S,2R)-2-фенилциклопропил)циклогексан-1,4-диамин;
(тpaнc)-N1-((1S,2R)-2-фeнилциклoпpoпил)циклoгeкcaн-1,4-диaмин;
(цис)-N1-((1R,2S)-2-фенилциклопропил)циклогексан-1,4-диамин;
(транс)-N1-((1R,2S)-2-фенилциклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(тиазол-5-ил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(пиридин-3-ил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(6-(3-(трифторметил)фенил)пиридин-3-ил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(4-(бензилокси)фенил)циклопропил)циклогексан-1,4-диамин;
4-(((транс)-2-(6-(3-(трифторметил)фенил)пиридин-3-ил)циклопропил)амино)циклогексанол;
4-(((транс)-2-(6-(3-(трифторметил)фенил)пиридин-3-ил)циклопропил)амино)циклогексанкарбоксамид;
N-(4-(((транс)-2-(6-(3-(трифторметил)фенил)пиридин-3-ил)циклопропил)амино)циклогексил)ацетамид;
N-(4-(((транс)-2-(6-(3-(трифторметил)фенил)пиридин-3-ил)циклопропил)амино)циклогексил)метансульфонамид;
(R)-1-(4-(((транс)-2-фенилциклопропил)амино)циклогексил)пирролидин-3-амин;
N1-((транс)-2-(4'-хлор-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(3'-хлор-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин;
4'-((транс)-2-((4-аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ол;
N-(4'-((транс)-2-((4-аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)метансульфонамид;
N1-((транс)-2-(4-((2-фторбензил)окси)фенил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(4-((3-фторбензил)окси)фенил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(4-((4-фторбензил)окси)фенил)циклопропил)циклогексан-1,4-диамин;
N1-метил-N4-((транс)-2-фенилциклопропил)циклогексан-1,4-диамин;
N1-метил-N4-((транс)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(4-(бензилокси)фенил)циклопропил)-N4-метилциклогексан-1,4-диамин;
N1-((транс)-2-фенилциклопропил)циклобутан-1,3-диамин;
N1-((транс)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклобутан-1,3-диамин;
N1-((транс)-2-(4-(бензилокси)фенил)циклопропил)циклобутан-1,3-диамин;
N1-((транс)-2-фенилциклопропил)-2,3-дигидро-1Н-инден-1,3-диамин;
N1-((транс)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)-2,3-дигидро-1Н-инден-1,3-диамин;
N1-((транс)-2-(4-(бензилокси)фенил)циклопропил)-2,3-дигидро-1Н-инден-1,3-диамин;
N1-((транс)-2-фтор-2-фенилциклопропил)циклогексан-1,4-диамин;
N1-((1S,2S)-2-фтор-2-фенилциклопропил)циклогексан-1,4-диамин;
N1-((1R,2R)-2-фтор-2-фенилциклопропил)циклогексан-1,4-диамин;
1-метил-N4-((транс)-2-фенилциклопропил)циклогексан-1,4-диамин;
4-(аминометил)-N-((транс)-2-фенилциклопропил)циклогексиламин;
N1-((транс)-2-фенилциклопропил)циклогексан-1,3-диамин;
N1-((цис)-2-фенилциклопропил)циклогексан-1,4-диамин;
трет-бутил-(4-(((транс)-2-фенилциклопропил)амино)циклогексил)карбамат;
1-этил-3-(4-(((транс)-2-фенилциклопропил)амино)циклогексил)мочевина;
4-морфолино-N-((транс)-2-фенилциклопропил)циклогексиламин;
N1-((транс)-2-(4-бромфенил)циклопропил)циклогексан-1,4-диамин;
N1-(2-(о-толил)циклопропил)циклогексан-1,4-диамин;
N1-(2-(4-(трифторметил)фенил)циклопропил)циклогексан-1,4-диамин
N1-(2-(4-метоксифенил)циклопропил)циклогексан-1,4-диамин;
4-(2-((4-аминоциклогексил)амино)циклопропил)фенол;
N1-(2-(2-фторфенил)циклопропил)циклогексан-1,4-диамин;
N1-(2-(3,4-дифторфенил)циклопропил)циклогексан-1,4-диамин;
N1-(2-(нафталин-2-ил)циклопропил)циклогексан-1,4-диамин;
N1-(2-метил-2-фенилциклопропил)циклогексан-1,4-диамин;
(R)-1-(4-(((транс)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)амино)циклогексил)пирролидин-3-амин;
(цис)-N1-((1S,2R)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин;
(транс)-N1-((1S,2R)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин;
(цис)-N1-((1R,2S)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин;
(транс)-N1-((1R,2S)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(4-циклопропилфенил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(4-(пиридин-3-ил)фенил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(4-(1Н-индазол-6-ил)фенил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(4-(1Н-пиразол-5-ил)фенил)циклопропил)циклогексан-1,4-диамин;
3-(5-((транс)-2-((4-аминоциклогексил)амино)циклопропил)тиофен-2-ил)фенол;
3-(5-((транс)-2-((4-аминоциклогексил)амино)циклопропил)тиазол-2-ил)фенол;
3-(5-((транс)-2-((4-аминоциклогексил)амино)циклопропил)пиридин-2-ил)-5-метоксибензонитрил;
5-(5-((транс)-2-((4-аминоциклогексил)амино)циклопропил)пиридин-2-ил)-2-метилфенол;
N-(4'-((транс)-2-((4-аминоциклогексил)амино)циклопропил)-6-метокси-[1,1'-бифенил]-3-ил)метансульфонамид;
N-(3-(5-((транс)-2-((4-аминоциклогексил)амино)циклопропил)тиазол-2-ил)фенил)-2-цианобензолсульфонамид;
N-(4'-((транс)-2-((4-аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)-2-цианобензолсульфонамид;
6-амино-N-(4'-((транс)-2-((4-аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)пиридин-3-сульфонамид;
N-(4'-((транс)-2-((4-аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)пиперазин-1-сульфонамид;
N1-((цис)-2-фтор-2-фенилциклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(4-((3-(пиперазин-1-ил)бензил)окси)фенил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(4-(пиридин-3-илметокси)фенил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(6-((3-метилбензил)амино)пиридин-3-ил)циклопропил)циклогексан-1,4-диамин;
3-((5-((транс)-2-((4-аминоциклогексил)амино)циклопропил)пиридин-2-ил)амино)бензонитрил;
N1-((транс)-2-(нафталин-2-ил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(о-толил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(4-(трифторметил)фенил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(4-метоксифенил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(2-фторфенил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-(3,4-дифторфенил)циклопропил)циклогексан-1,4-диамин;
N1-((транс)-2-метил-2-фенилциклопропил)циклогексан-1,4-диамин;
(цис)-N1-((1S,2R)-2-(пиридин-3-ил)циклопропил)циклогексан-1,4-диамин;
(транс)-N1-((1R,2S)-2-(пиридин-3-ил)циклопропил)циклогексан-1,4-диамин;
(цис)-N1-((1R,2S)-2-(пиридин-3-ил)циклопропил)циклогексан-1,4-диамин;
(транс)-N1-((1S,2R)-2-(пиридин-3-ил)циклопропил)циклогексан-1,4-диамин;
(цис)-N1-((1S,2R)-2-фенилциклопропил)циклобутан-1,3-диамин;
(транс)-N1-((1R,2S)-2-фенилциклопропил)циклобутан-1,3-диамин;
(цис)-N1-((1R,2S)-2-фенилциклопропил)циклобутан-1,3-диамин;
(транс)-N1-((1S,2R)-2-фенилциклопропил)циклобутан-1,3-диамин;
(цис)-N1-((1S,2R)-2-(3,4-дифторфенил)циклопропил)циклогексан-1,4-диамин;
(транс)-N1-((1R,2S)-2-(3,4-дифторфенил)циклопропил)циклогексан-1,4-диамин;
(цис)-N1-((1R,2S)-2-(3,4-дифторфенил)циклопропил)циклогексан-1,4-диамин;
(транс)-N1-((1S,2R)-2-(3,4-дифторфенил)циклопропил)циклогексан-1,4-диамин;
(цис)-N1-((1S,2R)-2-(нaфтaлин-2-ил)циклoпpoпил)циклoгeкcaн-1,4-диамин;
(транс)-N1-((1R,2S)-2-(нaфтaлин-2-ил)циклoпpoпил)циклoгeкcaн-1,4-диамин;
(цис)-N1-((1R,2S)-2-(нафталин-2-ил)циклопропил)циклогексан-1,4-диамин;
(транс)-N1-((1S,2R)-2-(нaфтaлин-2-ил)циклопропил)циклогексан-1,4-диамин;
(цис)-N1-((1S,2R)-2-(4-(1Н-пиразол-5-ил)фенил)циклопропил)циклогексан-1,4-диамин;
(тpaнc)-N1-((1R,2S)-2-(4-(1Н-пиразол-5-ил)фенил)циклопропил)циклогексан-1,4-диамин;
(цис)-N1-((1R,2S)-2-(4-(1Н-пиразол-5-ил)фенил)циклопропил)циклогексан-1,4-диамин;
(тpaнc)-N1-((1S,2R)-2-(4-(1H-пиpaзoл-5-ил)фeнил)циклoпpoпил)циклoгeкcaн-1,4-диамин;
N-(4'-((1R,2S)-2-(((циc)-4-aминoциклoгeкcил)aминo)циклoпpoпил)-[1,1'-бифенил]-3-ил)пиперазин-1-сульфонамид;
N-(4'-((1S,2R)-2-(((тpaнc)-4-aминoциклoгeкcил)aминo)циклoпpoпил)-[1,1'-бифенил]-3-ил)пиперазин-1-сульфонамид;
N-(4'-((1S,2R)-2-(((цис)-4-аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)пиперазин-1-сульфонамид;
N-(4'-((1R,2S)-2-(((тpaнc)-4-aминoциклoгeкcил)aминo)циклoпpoпил)-[1,1'-бифенил]-3-ил)пиперазин-1-сульфонамид;
(циc)-N1-((1S,2R)-2-(4-((2-фтopбeнзил)oкcи)фeнил)циклoпpoпил)циклoгeкcaн-1,4-диамин;
(транс)-N1-((1R,2S)-2-(4-((2-фтopбeнзил)oкcи)фeнил)циклoпpoпил)циклoгeкcaн-1,4-диамин;
(цис)-N1-((1R,2S)-2-(4-((2-фторбензил)окси)фенил)циклопропил)циклогексан-1,4-диамин;
(транс)-N1-((1S,2R)-2-(4-((2-фторбензил)окси)фенил)циклопропил)циклогексан-1,4-диамин;
а также их соли и сольваты (включая их фармацевтически приемлемые соли и сольваты).
Настоящее изобретение также относится к любому соединению или к любой подгруппе соединений, перечисленных выше. Настоящее изобретение также относится к фармацевтически приемлемой соли, предпочтительно гидрохлориду (такому как, например, моногидрохлорид, дигидрохлорид или, если это является подходящим, тригидрохлорид) любого из перечисленных выше соединений.
Предпочтительные варианты осуществления соединений формулы I, Ia, Iа-1, Ib и Iс, предназначенных для применения в композициях и способах, предлагаемых в настоящем изобретении, являются такими, как определено выше в настоящем изобретении.
Другим объектом настоящего изобретения является способ выявления соединения, которое является селективным ингибитором LSD1, способ включает выбор или получение соединения формулы I, Ia, Ia-1, Ib или Ic и определение способности указанного соединения ингибировать LSD1 и МАО-А и/или МАО-В с помощью таких исследований, как более подробно раскрытые ниже, где соединение, которое ингибирует LSD1 в большей степени, чем МАО-А и/или МАО-В, идентифицируют, как селективный ингибитор LSD1. Селективные ингибиторы LSD1 обладают значениями IC50 для LSD1, которые меньше, чем значение IC50 для МАО-А и/или МАО-В. Предпочтительно, если значения IC50 для LSD1 в два раза меньше, чем для МАО-А и/или МАО-В. В одном воплощении этого варианта осуществления значение IC50 для LSD1 по меньшей мере в 5 раз меньше, чем значение IC50 для МАО-А и/или МАО-В. В одном воплощении этого варианта осуществления значение IC50 для LSD1 по меньшей мере в 10 раз меньше, чем значение IC50 для МАО-А и/или МАО-В. Предпочтительно, если селективный ингибитор LSD1 обладает значением IC50 для LSD1, которое в >50 раз, предпочтительно в >100 раз меньше, чем значение IС50 для МАО-А и/или МАО-В.
В соединениях формулы I, Ia, Ia-1, Ib и Iс, раскрытых в настоящем изобретении, содержатся асимметрические центры. Следует понимать, что в объем настоящего изобретения входят все стереохимические изомерные формы, соединения формулы I, Ia, Ia-1, Ib и Iс, включая диастереоизомерные, энантиомерные и эпимерные формы, а также d-изомеры и l-изомеры ((+)-изомеры и (-)-изомеры), и любые их смеси, включая полностью или частично приведенные в равновесие смеси. Отдельные стереоизомеры соединений, предлагаемых в настоящем изобретении, можно получить синтетически из имеющихся в продаже хиральных исходных веществ или путем выделения из смесей стереоизомеров, так, как это также описано в примерах. Методики разделения смесей энантиомеров и диастереоизомеров хорошо известны специалисту в данной области техники. Например, смеси диастереоизомеров можно разделить с использованием обычных методик разделения, таких как перекристаллизация или хроматография. Смеси энантиомерных продуктов можно разделить путем превращения в смеси диастереоизомеров с последующим разделением с использованием перекристаллизации или хроматографических методик, прямого разделения энантиомеров на хиральных хроматографических колонках или по любой другой подходящей методике хирального разделения, известной в данной области техники. Исходные соединения, обладающие конкретной стереохимической конфигурацией, имеются в продаже или их можно получить и разделить по методикам, известным в данной области техники.
Кроме того, соединения, раскрытые в настоящем изобретении, могут существовать в виде геометрических изомеров. В объем настоящего изобретения входят все цис-, транс-, син-, анти-, (Е)- и (Z)-изомеры, а также их смеси.
Кроме того, соединения могут существовать в виде таутомеров; все таутомеры входят в объем настоящего изобретения.
Соединения, предлагаемые в настоящем изобретении, содержат один или большее количество основных атомов азота и поэтому они могут образовывать соли с органическими и неорганическими кислотами. Соединения, предлагаемые в настоящем изобретении, также могут содержать один или большее количество кислых протонов и поэтому они также могут образовывать соли с основаниями. Не существует ограничений на тип соли, которую можно использовать, при условии, что они являются фармацевтически приемлемыми при использовании для терапевтических целей. Соли соединения, предлагаемого в настоящем изобретении, можно получить в ходе конечного выделения и очистки соединений, предлагаемых в настоящем изобретении, или их можно получить путем обработки соединения формулы I, Ia, Ia-1, Ib или Ic достаточным количеством необходимой кислоты или основания по обычной методике и получить соответствующую соль. Все соли соединений формулы I, Ia, Ia-1, Ib и Iс, включая фармацевтически приемлемые соли, входят в объем настоящего изобретения. В одном варианте осуществления соединение формулы I, Ia, Ia-1, Ib или Ic находится в форме соли. В более предпочтительном варианте осуществления соединение формулы I, Iа и Ia-1 находится в форме фармацевтически приемлемой соли. В одном варианте осуществления такой фармацевтически приемлемой солью является гидрохлорид, например, моногидрохлорид, дигидрохлорид или тригидрохлорид.
Кроме того, соединения, раскрытые в настоящем изобретении, могут находиться в несольватированной, а также сольватированной формах с фармацевтически приемлемыми растворителями, такими как вода, этанол и т.п. Сольватированные формы, содержащие воду, известны, как гидраты. Обычно сольватированные формы считают эквивалентными несольватированным формам. Таким образом, настоящее изобретение относится к несольватированным и сольватированным формам соединений формулы I, Ia, Iа-1, Ib или Iс (или любой их соли).
Соединения формулы I, Ia, Ia-1, Ib и Iс могут находится в различных физических формах, т.е. аморфных и кристаллических формах. Кроме того, соединения, предлагаемые в настоящем изобретении, могут обладать способностью кристаллизоваться более, чем в одной форме, эта характеристика известна, как полиморфизм. Полиморфные формы можно различить на основании различия их физических характеристик, хорошо известных в данной области техники, таких как порошковая рентгенограмма, температура плавления или растворимость. Все физические формы соединений, предлагаемых в настоящем изобретении, включая все их полиморфные формы, входят в объем настоящего изобретения.
Кроме того, в объем настоящего изобретения входят все немеченые и изотопно меченые формы соединений формулы I, Ia, Ia-1, Ib и Ic. В одном варианте осуществления настоящее изобретение относится к дейтерированным формам соединений формулы I, Ia, Ia-1, Ib и Ic.
Настоящее изобретение также относится к соединению формулы I, Ia, Ia-1, Ib или Ic (предпочтительно к соединению формулы I, Ia или Ia-1, более предпочтительно к соединению формулы Iа или Ia-1, и наиболее предпочтительно к соединению формулы Ia-1), описанному и определенному в настоящем изобретении, в котором заместители -A-В и -NH-D циклопропильного фрагмента находятся в транс-конфигурации, и кроме того, где соединение является оптически активным. При использовании в настоящем изобретении термин "оптически активное" означает способность соединения вращать плоскость поляризованного света.
Другим объектом настоящего изобретения является в основном чистый оптически активный стереоизомер соединения формулы I, Ia, Ia-1, Ib или Ic, описанной и определенной в настоящем изобретении, в которой заместители -A-В и -NH-D циклопропильного фрагмента находятся в транс-конфигурации, или его фармацевтически приемлемая соль или сольват, а также его применение в качестве лекарственного средства. При использовании в настоящем изобретении "в основном чистый" означает, что содержится 90 мол. % или более искомого стереоизомера и 10 мол. % или менее любого другого стереоизомера, предпочтительно, если содержится 95 мол. % или более искомого стереоизомера и 5 мол. % или менее любого другого стереоизомера, более предпочтительно, если содержится 98 мол. % или более искомого стереоизомера и 2 мол. % или менее любого другого стереоизомера, еще более предпочтительно, если содержится 99 мол. % или более искомого стереоизомера и 1 мол. % или менее любого другого стереоизомера, и еще более предпочтительно, если содержится 99,5 мол. % или более искомого стереоизомера и 0,5 мол. % или менее любого другого стереоизомера. В основном чистый оптически активный стереоизомер соединения формулы I, Ia, Ia-1, Ib или Ic, описанной и определенной в настоящем изобретении, в которой заместители -A-B и -NH-D циклопропильного фрагмента находятся в транс-конфигурации, применим для лечения или предупреждения заболевания или нарушения, предпочтительно рака, неврологического заболевания или вирусной инфекции.
Определения:
Для описания сложной структурной группы любое определение, приведенное в настоящем изобретении, можно использовать в комбинации с любым другим определением. По определению, последним элементом любого такого определения является такой, который присоединен к исходному фрагменту. Например, сложная циклил-C1-C8-алкильная группа представляет собой циклильную группу, присоединенную к исходной молекуле через амидную группу, и термин алкоксиалкил означает алкоксигруппу, присоединенную к исходной молекуле через C1-C8-алкильную группу.
При использовании в настоящем изобретении термин "ацил" означает карбонил, присоединенный к алкенилу, алкилу, арилу, циклоалкилу, гетероарилу, гетероциклилу или любому другому фрагменту, в котором атомом, присоединенным к карбонилу, является атом углерода. Предпочтительно, если термин "ацил" означает группу формулы -C(=O)R'', в которой R'' обозначает алкенил, алкил, арил, циклоалкил, гетероарил или гетероциклил. "Ацетильная" группа означает группу -C(=O)CH3. "Алкилкарбонильная" или "алканоильная" группа означает алкильную группу, присоединенную к исходной молекуле через карбонильную группу. Примеры таких групп включают, но не ограничиваются только ими, метилкарбонил или этилкарбонил. Примеры ацильных групп включают, но не ограничиваются только ими, формил, алканоил или ароил.
При использовании в настоящем изобретении термин "алкенил" означает обладающую линейной цепью или разветвленной цепью углеводородную группу, содержащую одну или большее количество двойных связей и содержащую от 2 до 20 атомов углерода. C2-C8-Алкенил означает алкенильную группу, содержащую от 2 до 8 атомов углерода.
При использовании в настоящем изобретении термин "алкоксигруппа" означает простую алкильную эфирную группу (т.е. группу формулы алкил-O-), где термин алкил является таким, как определено ниже. Примеры подходящих простых алкильных эфирных групп включают, но не ограничиваются только ими, метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, н-бутоксигруппу, изобутоксигруппу, втор-бутоксигруппу, трет-бутоксигруппу или н-пентоксигруппу. Термин C1-Cz-алкоксигруппа означает алкоксигруппу, в которой алкильный фрагмент содержит от 1 до z атомов углерода; например, C1-C8-алкоксигруппа означает алкоксигруппу, в которой алкильным фрагментом является C1-C8-алкил, т.е. группу формулы C1-C8-алкил-O-.
При использовании в настоящем изобретении термин "алкил" означает обладающую линейной цепью или разветвленной цепью алкильную группу, содержащую от 1 до 20 атомов углерода. C1-Cz-Алкил означает алкил, содержащий от 1 до z атомов углерода; таким образом, C1-C8-алкил содержит от 1 до 8 атомов углерода, C1-C4-алкил содержит от 1 до 4 атомов углерода и C1-C2-алкил содержит от 1 до 2 атомов углерода. Примеры алкильных групп включают, но не ограничиваются только ими, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, изопентил, неопентил, изоамил, гексил, гептил, октил или нонил.
При использовании в настоящем изобретении термин "C1-C4-алкилен" означает C1-C4-алкильную группу, присоединенную в двух положениях, т.е. алкандиильную группу. Примеры включают, но не ограничиваются только ими, метилен (т.е. группу формулы -CH2-), этилен (включая этан-1,2-диил и этан-1,1-диил), пропилен (например, пропан-1,3-диил, пропан-1,2-диил и пропан-1,1-диил) и бутилен (например, бутан-1,4-диил, бутан-1,3-диил или бутан-1,1-диил). Соответственно, термин "C1-C4-алкилен" может означать обладающую линейной цепью или разветвленной цепью алкиленовую группу, содержащую от 1 до 4 атомов углерода.
При использовании в настоящем изобретении термин "алкинил" означает обладающую линейной цепью или разветвленной цепью углеводородную группу, содержащую одну или большее количество тройных связей и содержащую от 2 до 20 атомов углерода. C2-C8-Алкинил содержит от 2 до 8 атомов углерода. Примеры алкинильных групп включают, но не ограничиваются только ими, этинил, пропинил, гидроксипропинил, бутин-1-ил, бутин-2-ил, пентин-1-ил, 3-метилбутин-1-ил или гексин-2-ил.
При использовании в настоящем изобретении термин "амидная группа" означает аминогруппу, описанную ниже, присоединенную к исходному молекулярному фрагменту через карбонильную группу (например, -C(=O)NRR') или наоборот (-N(R)C(=O)R'). "Амидная группа" включает "C-амидную группу" и "N-амидную группу", определенную в настоящем изобретении. R и R' являются такими, как определено в настоящем изобретении.
При использовании в настоящем изобретении термин "С-амидная группа" означает группу -C(=O)NRR', в которой R и R' являются такими, как определено в настоящем изобретении.
При использовании в настоящем изобретении термин "N-амидная группа" означает группу -N(R)C(=O)R', в которой R и R' являются такими, как определено в настоящем изобретении.
При использовании в настоящем изобретении термин "аминогруппа" означает - -NRR', где R и R' независимо выбраны из группы, включающей водород, алкил, гетероалкил, арил, карбоциклил и гетероциклил. Кроме того, R и R' можно объединить с образованием гетероциклила. Типичные "аминогруппы" включают, но не ограничиваются только ими, -NH2, -NH(C1-C4-алкил) и -N(C1-C4-алкил)(C1-C4-алкил).
При использовании в настоящем изобретении термин "арил" означает карбоциклическую ароматическую систему, содержащую одно кольцо или два, или три кольца, сконденсированных друг с другом, в которой все кольцевые атомы являются атомами углерода. Термин "арильные" группы включает, но не ограничивается только ими, такие группы, как фенил, нафтил или антраценил. Термин "моноциклический арил" означает фенил.
При использовании в настоящем изобретении термин "арилоксигруппа" означает арильную группу, присоединенную к исходному молекулярному фрагменту через оксигруппу (-O-).
При использовании в настоящем изобретении термин "карбамат" означает О-карбамильную или N-карбамильную группу, определенную в настоящем изобретении. N-Карбамильная группа означает -NR-COOR', где R и R' являются такими, как определено в настоящем изобретении. О-Карбамильная группа означает -OCO-NRR', где R и R' являются такими, как определено в настоящем изобретении.
При использовании в настоящем изобретении термин "карбонил", когда он содержится в виде отдельной группы, включает формил -C(=O)Н, и в комбинации означает группу -C(=O)-.
При использовании в настоящем изобретении термин "карбоксил" или "карбоксигруппа" означает -C(=O)ОН или соответствующий "карбоксилатный" анион, такой как содержащийся в соли карбоновой кислоты.
"О-Карбоксигруппа" означает группу RC(=O)O-, в которой R является таким, как определено в настоящем изобретении.
"С-Карбоксигруппа" означает группы -C(=O)OR, в которых R является таким, как определено в настоящем изобретении.
При использовании в настоящем изобретении термин "цианогруппа" означает -CN.
При использовании в настоящем изобретении термин "карбоциклил" означает насыщенную или частично насыщенную моноциклическую или конденсированную бициклическую или трициклическую группу, где все кольцевые атомы циклической системы являются атомами углерода и где каждый циклический фрагмент содержит от 3 до 12 кольцевых атомов углерода. "Карбоциклил" включает бензол, сконденсированный с карбоциклильной кольцевой системой. Одна группа карбоциклилов содержит от 5 до 7 атомов углерода. Примеры карбоциклильных групп включают, но не ограничиваются только ими, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, тетрагидронафтил, инданил, октагидронафтил, 2,3-дигидро-1Н-инденил или адамантил.
При использовании в настоящем изобретении термин "циклоалкил", если не указано иное (как, например, в определении кольца D), означает насыщенную моноциклическую, бициклическую или трициклическую группу, где все кольцевые атомы циклической системы являются атомами углерода и где каждый циклический фрагмент содержит от 3 до 12 кольцевых атомов углерода. C3-C6-Циклоалкил означает циклоалкил, который содержит от 3 до 6 атомов углерода, т.е. циклопропил, циклобутил, циклопентил и циклогексил. Циклоалкил, содержащий от 4 до 7 атомов C включает циклобутил, циклопентил, циклогексил и циклогептил. Примеры циклоалкильных групп включают, но не ограничиваются только ими, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил или адамантил.
При использовании в настоящем изобретении термин "циклил" означает арильную, гетероциклильную или карбоциклильную группу, определенную в настоящем изобретении.
При использовании в настоящем изобретении термин "циклил-C1-C8-алкил" означает C1-C8-алкил, определенный выше, в котором один атом водорода в C1-C8-алкильной группе заменен на одну циклильную группу, определенную выше.
При использовании в настоящем изобретении термин "галоген" означает фтор, хлор, бром или йод.
При использовании в настоящем изобретении термин "галогеналкоксигруппа" означает галогеналкильную группу (определенную ниже), присоединенную к исходному молекулярному фрагменту через атом кислорода. Галоген-C1-C8-алкоксигруппа означает галогеналкоксигруппу, в которой галогеналкильный фрагмент содержит от 1 до 8 атомов С. Примеры галогеналкоксигрупп включают, но не ограничиваются только ими, трифторметоксигруппу, 2-фторэтоксигруппу, пентафторэтоксигруппу или 3-хлорпропоксигруппу.
При использовании в настоящем изобретении термин "галогеналкил" означает алкильную группу обладает значением, определенным выше, в которой один или большее количество атомов водорода заменены галогеном. Галоген-C1-C8-алкильная группа означает галогеналкильную группу, в которой алкильный фрагмент содержит от 1 до 8 атомов С. Термин предпочтительно включает моногалогеналкильные, дигалогеналкильные или полигалогеналкильные группы. В одном примере моногалогеналкильная группа, может содержать атом йода, брома, хлора или фтора в группе. Дигалогенидные или полигалогеналкильные группы могут содержать два или большее количество одинаковых атомов галогенов или комбинацию разных галогенидных групп. Примеры галогеналкильных групп включают, включают, но не ограничиваются только ими, фторметил, дифторметил, трифторметил, хлорметил, дихлорметил, трихлорметил, пентафторэтил, гептафторпропил, дифторхлорметил, дихлорфторметил, дифторэтил, дифторпропил, дихлорэтил или дихлорпропил.
При использовании в настоящем изобретении термин "гетероалкил" означает линейную или разветвленную алкильную цепь, в которой 1, 2 или 3 атома углерода, образующие алкильную цепь, заменены гетероатомом, независимо выбранным из группы, включающей О, N и S, и в которой гетероатом(ы) азота и/или серы (если содержатся) необязательно могут быть окислены и гетероатом(ы) азота (если содержатся) необязательно могут быть кватернизованы. Гетероатом(ы) О, N и S могут, например, находиться во внутреннем положении гетероалкильной группы, т.е. гетероалкил может быть связан с остальной частью молекулы через гетероатом или атом углерода. До двух гетероатомов могут располагаться рядом, как, например, в -CH2-NH-OCH3. Соответственно, другим примером "гетероалкильной" группы является линейная или разветвленная алкильная группа, в которой два соседних атома углерода заменены гетероатомами S и N, соответственно и гетероатом серы, кроме того, окислен с образованием таких фрагментов, как, например, -S(=O)2-NH2, -S(=O)2-NH(алкил) или -S(=O)2-N(алкил)(алкил).
При использовании в настоящем изобретении термин "гетеро-C1-C4-алкилен" означает линейную или разветвленную C1-C4-алкиленовую группу (т.е. линейную или разветвленную C1-C4-алкандиильную группу), связанную с одним гетероатомом, выбранным из группы, включающей O, N и S, и также означает линейную или разветвленную C1-C4-алкиленовую группу, в которой один или большее количество (например, 1, 2 (если содержатся) или 3 (если содержатся)) атомов углерода указанной алкиленовой группы заменены гетероатомом, независимо выбранным из группы, включающей O, N и S. Гетероатом(ы) азота и/или серы (если содержатся) необязательно могут быть окислены и гетероатом(ы) азота (если содержатся) необязательно могут быть кватернизованы. Гетероатом(ы) О, N и S могут находиться в концевом (концевых) и/или во внутреннем положении гетеро-C1-C4-алкиленовой группы. Следует понимать, что наличие атомов водорода зависит от валентности гетероатома, заменяющего соответствующий атом углерода. Если, например, атом углерода в группе -CH2- заменен на O или S, то полученной группой будет -O- или -S- соответственно и ей будет -N(H)-, если атом углерода заменен на N. Аналогичным образом, если центральный атом в группе -CH2-CH(-CH3)-CH2- заменен на N, то полученной группой будет -CH2-N(-СН3)-CH2-. Примером "гетеро-C1-C4-алкиленовой" группы является линейная или разветвленная C1-C4-алкиленовая группа, в которой два соседних атома углерода заменены гетероатомами S и N соответственно, и гетероатом серы, кроме того, окислен, то дает такие фрагменты, как, например, -S(=O)2-N(H)- или -S(=O)2-N(CH3)-.
При использовании в настоящем изобретении термин "гетероарил" означает 5-6-членное ненасыщенное моноциклическое кольцо, или конденсированную моноциклическую, бициклическую, или трициклическую кольцевую систему, в которой кольца являются ароматическими и в которой по меньшей мере одно кольцо содержит по меньшей мере один атом, выбранный из группы, включающей O, S и N. Предпочтительными гетероарильными группами являются 5-6-членные моноциклические или 9-10-членные бициклические гетероарильные группы. Примеры гетероарильных групп включают, но не ограничиваются только ими, пиридинил, имидазолил, имидазопиридинил, пиримидинил, пиразолил, триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксадиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофуранил, циннолинил, индазолил, индолизинил, фталазинил, пиридазинил, триазинил, изоиндолил, птеридинил, пуринил, оксадиазолил, триазолил, тиадиазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиазолил, бензоксазолил, хиназолинил, хиноксалинил, нафтиридинил или фуропиридинил.
При использовании в настоящем изобретении термин "гетероциклил" или "гетероцикл" каждый означает насыщенную, частично ненасыщенную или полностью ненасыщенную моноциклическую, бициклическую, или трициклическую гетероциклическую группу, содержащую по меньшей мере один гетероатом в качестве элемента кольца, где каждый указанный гетероатом может быть независимо выбран из группы, включающей азот, кислород и серу, где атомы азота или серы могут быть окислены (например, с образованием -N=O, -S(=O)- или -S(=O)2-). Кроме того, 1, 2 или 3 атома углерода гетероциклила могут быть необязательно окислены (например, с образованием оксогруппы или =O). Одна группа гетероциклилов содержит от 1 до 4 гетероатомов в качестве элементов кольца. Другая группа гетероциклилов содержит от 1 до 2 гетероатомов в качестве элементов кольца. Одна группа гетероциклилов содержит от 3 до 8 элементов кольца в каждом кольце. Еще одна группа гетероциклилов содержит от 3 до 7 элементов кольца в каждом кольце. И другая группа гетероциклилов содержит от 5 до 6 элементов кольца в каждом кольце. "Гетероциклил" включает гетероциклильную группу сконденсированную с карбоциклильной или бензольной кольцевыми системами. Примеры гетероциклильных групп включают, но не ограничиваются только ими, пирролидинил, тетрагидрофуранил, дигидрофуранил, тетрагидротиенил, тетрагидропиранил, дигидропиранил, тетрагидротиопиранил, пиперидиновую группу, морфолиновую группу, тиоморфолиновую группу, тиоксанил, пиперазинил, гомопиперазинил, азетидинил, оксетанил, тиетанил, гомопиперидинил, оксепанил, тиепанил, оксазепинил, диазепинил, тиазепинил, 2-пирролинил, 3-пирролинил, индолинил, 2Н-пиранил, 4Н-пиранил, диоксанил, 1,3-диоксоланил, пиразолинил, дитианил, дитиоланил, дигидропиранил, дигидротиенил, дигидрофуранил, пиразолидинилимидазолинил или имидазолидинил. Примеры гетероарилов, которые являются гетероциклилами, включают, но не ограничиваются только ими, пиридинил, имидазолил, имидазопиридинил, пиримидинил, пиразолил, триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксадиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофуранил, циннолинил, индазолил, индолизинил, фталазинил, пиридазинил, триазинил, изоиндолил, птеридинил, пуринил, оксадиазолил, триазолил, тиадиазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиазолил, бензоксазолил, хиназолинил, хиноксалинил, нафтиридинил или фуропиридинил.
При использовании в настоящем изобретении термин "гетероциклоалкил" означает гетероциклильную группу, которая не полностью насыщена, например, одна или большее количество кольцевых систем гетероциклоалкила не являются ароматическими. Примеры гетероциклоалкилов включают пиперазинил, морфолинил, пиперидинил или пирролидинил.
При использовании в настоящем изобретении термин "гидроксигруппа" означает -OH.
При использовании в настоящем изобретении термин "гидрокси-C1-C8-алкил" означает C1-C8-алкильную группу, в которой один или больше количество атомов водорода (предпочтительно 1 или 2) заменены гидроксигруппами.
При использовании в настоящем изобретении термин "R12R13N-C1-C8-алкил" означает C1-C8-алкильную группу, в которой один или больше количество атомов водорода (предпочтительно 1 или 2, более предпочтительно 1) заменены на -NR12R13.
При использовании в настоящем изобретении термин "низш.", если специально не приведено иного определения, означает фрагмент, содержащий от 1 включительно до 6 атомов углерода.
При использовании в настоящем изобретении термин "нитрогруппа" означает -NO2.
При использовании в настоящем изобретении термины "сульфонат", "сульфоновая кислота" и "сулфоновый" означает группу -SO3H и ее анион, в качестве сульфоновой кислоты использующийся для образования соли.
При использовании в настоящем изобретении термин "сульфинил" означает -S(=O)(R), где R является таким, как определено в настоящем изобретении.
При использовании в настоящем изобретении термин "сульфонил" означает -S(=O)2R, где R является таким, как определено в настоящем изобретении.
При использовании в настоящем изобретении термин "сульфонамидная группа" означает N-сульфонамидную группу или S-сульфонамидную группу, определенную в настоящем изобретении.
При использовании в настоящем изобретении термин "N-сульфонамидная группа" означает группу RS(=O)2N(R')-, в которой R и R' являются такими, как определено в настоящем изобретении. Предпочтительными N-сульфонамидными группами являются группы -NHSO2R, в которых R является таким, как определено в настоящем изобретении, предпочтительно, если R обозначает алкил, циклоалкил, гетероалкил, арил, гетероарил или гетероциклоалкил, более предпочтительно, если R обозначает алкил, арил, гетероарил или гетероциклоалкил, где указанный алкил, указанный циклоалкил, указанный гетероалкил, указанный арил, указанный гетероарил и указанный гетероциклоалкил все необязательно являются замещенными. Необязательные заместители указанного алкила, указанного циклоалкила, указанного гетероалкила, указанного арила, указанного гетероарила и указанного гетероциклоалкила могут быть независимо выбраны из группы, включающей низш. алкил, низш. алкенил, низш. алкинил, низш. алканоил, низш. гетероалкил, низш. гетероциклоалкил, низш. галогеналкил, низш. циклоалкил, фенил, арил, гетероарил, пиридил, арилоксигруппу, низш. алкоксигруппу, низш. галогеналкоксигруппу, оксогруппу, низш. ацилоксигруппу, карбонил, карбоксигруппу, низш. алкилкарбонил, низш. сложноэфирную карбоксигруппу, низш. карбоксамидную группу, цианогруппу, галоген, гидроксигруппу, аминогруппу, амидную группу, нитрогруппу, тиогруппу, низш. алкилтиогруппу, низш. галогеналкилтиогруппу, низш. пергалогеналкилтиогруппу, арилтиогруппу, сульфонатную группу, сульфоновую группу, тризамещенный силил, N3, SH, SCH3, С(O)CH3, CO2CH3, СО2Н, карбаматную группу и мочевинную группу. Предпочтительно, если необязательные заместители независимо выбраны из группы, включающей гидроксигруппу, галоген, алкил, алкоксигруппу, галогеналкил, галогеналкоксигруппу, -N(C1-C3-алкил)2, -NH(C1-C3-алкил), -NHC(=O)(C1-C3-алкил), -C(=O)ОН, -С(=O)O(C1-C3-алкил), -С(=O)(C1-C3-алкил), -C(=O)NH2, -С(=O)NH(C1-C3-алкил), -С(=O)NH(циклоалкил), -C(=O)N(C1-C3-алкил)2, -S(=O)2(C1-C3-алкил), -S(=O)2NH2, -S(=O)2N(C1-C3-алкил)2, -S(=O)2NH(C1-C3-алкил), -CHF2, -OCF3, -OCHF2, -SCF3, -CF3, -CN, -NH2, -NO2 или тетразолил. Особенно предпочтительными N-сульфонамидными группами являются группы -NHSO2R, в которых R обозначает алкил, циклоалкил, гетероалкил, арил, гетероарил или гетероциклоалкил, и предпочтительно, если R обозначает алкил, арил, гетероарил или гетероциклоалкил, и -NHSO2 (необязательно замещенный арил). Еще более предпочтительными N-сульфонамидными группами являются группы -NHSO2(алкил) и -NHSO2 (необязательно замещенный арил). Типичными неограничивающими N-сульфонамидными группами являются группы -NHSO2(алкил), такая как -NHSO2CH3, -NHSO2CH2CH3 или -NHSO2(изопропил), и -NHSO2 (необязательно замещенный арил), такая как -NHSO2-фенил, -NHSO2-(2-цианофенил), -NHSO2-(3-цианофенил), -NHSO2-(4-цианофенил), -NHSO2-(2-аминофенил), -NHSO2-(3-аминофенил) или -NHSO2-(4-аминофенил). Другими типичными N-сульфонамидными группами являются группы -NHSO2 (необязательно замещенный гетероциклоалкил), такая как -NHSO2-(пиперазин-1-ил), и -NHSO2 (необязательно замещенный гетероарил), такая как -NHSO2-(необязательно замещенный пиридил), например, -NHSO2- (3-пиридил) или -NHSO2-(6-амино-3-пиридил).
При использовании в настоящем изобретении термин "S-сульфонамидная группа" означает группу -S(=O)2NRR', в которой R и R' являются такими, как определено в настоящем изобретении.
При использовании в настоящем изобретении термин "мочевинная группы" означает группу -N(R)C(=O)N(R)(R'), в которой R и R' являются такими, как определено в настоящем изобретении.
Термин R или термин R', указанный сам по себе и без определения количества, если не приведено другое определение, означает фрагмент, выбранный из группы, включающей водород, алкил, циклоалкил, гетероалкил, арил, гетероарил и гетероциклоалкил. Термин включает и незамещенные, и замещенные формы указанных выше групп. Предпочтительно, если указанные группы являются незамещенными.
Независимо от того, содержит или не содержит группа R числовое обозначение, каждая группа R, включая R, R' и Rz, в которой z=(1, 2, 3, …z), каждый заместитель, и каждый термин следует считать независящими друг от друга в отношении выбора из группы. Если любая переменная, заместитель или термин (например, арил, гетероцикл, R и т.п.) встречается в формуле или родовой структуре более одного раза, то его определение в каждом случае не зависит от определения в каждом другом случае. Специалисты в данной области техники также должны понимать, что некоторые группы могут быть присоединены к исходной молекуле или могут занимать положение в цепи элементов на любом конце, как это обозначено. Таким образом, только в качестве примера, несимметричная группа, такая как -C(=O)N(R)-, может быть присоединена к исходному фрагменту по любому атому углерода или азота.
При использовании в настоящем изобретении термин "необязательно замещенная" означает предыдущую или предшествующую группу, которая может быть замещенной или незамещенной. Если она является замещенной и если не указано иное, то заместители "необязательно замещенной" группы могут включать, без наложения ограничений, один или большее количество заместителей независимо выбранных из числа следующих групп или специально указанного набора групп, по отдельности или в комбинации: низш. алкил, низш. алкенил, низш. алкинил, низш. алканоил, низш. гетероалкил, низш. гетероциклоалкил, низш. галогеналкил, низш. циклоалкил, фенил, арил, гетероарил, пиридил, арилоксигруппу, низш. алкоксигруппу, низш. галогеналкоксигруппу, оксогруппу, низш. ацилоксигруппу, карбонил, карбоксигруппу, низш. алкилкарбонил, низш. сложноэфирную карбоксигруппу, низш. карбоксамидную группу, цианогруппу, галоген, гидроксигруппу, аминогруппу, амидную группу, нитрогруппу, тиогруппу, низш. алкилтиогруппу, низш. галогеналкилтиогруппу, низш. пергалогеналкилтиогруппу, арилтиогруппу, сульфонатную группу, сульфоновую группу, тризамещенный силил, N3, SH, SCH3, С(O)CH3, CO2CH3, СО2H, карбаматную группу и мочевинную группу. Два заместителя могут быть связаны с образованием конденсированного 5-, 6- или 7-членного карбоциклического или гетероциклического кольца, содержащего от 0 до 3 гетероатомов, например, образующего метилендиоксигруппу или этилендиоксигруппу. Необязательно замещенная группа может быть незамещенной (например, -CH2CH3), полностью замещенной (например, -CF2CF3), монозамещенной (например, -CH2CH2F) или замещенной в диапазоне от полностью замещенной до монозамещенной (например, -CH2CF3). Если заместители указаны без определения степени замещения, то включены замещенные и незамещенные формы. Если заместитель указан, как "замещенный", то специально включена замещенная форма. Кроме того, при необходимости можно определить различные наборы необязательных заместителей конкретного фрагмента; в этих случаях необязательное замещение будет таким, как определено, часто сразу после выражения "необязательно замещенный с помощью". В одном предпочтительном определении необязательные заместители выбраны из группы, включающей гидроксигруппу, галоген, алкил, алкоксигруппу, галогеналкил, галогеналкоксигруппу, -N(C1-C3-алкил)2, -NH(C1-C3-алкил), -NHC(=O)(C1-C3-алкил), -С(=O)ОН, -C(=O)O(C1-C3-алкил), -С(=O)(C1-C3-алкил), -C(=O)NH2, -С(=O)NH(C1-C3-алкил), -С(=O)NH(циклоалкил), -С(=O)N(C1-C3-алкил)2, -S(=O)2(C1-C3-алкил), -S(=O)2NH2, -S(=O)2N(C1-C3-алкил)2, -S(=O)2NH(C1-C3-алкил), -CHF2, -OCF3, -OCHF2, -SCF3, -CF3, -CN, -NH2, -NO2 или тетразолил.
При использовании в настоящем изобретении термин "необязательный заместитель" означает, что соответствующий заместитель может содержаться или может отсутствовать. Соответственно, соединение, содержащее 1, 2 или 3 необязательных заместителя, может быть незамещенным или может содержать 1, 2 или 3 заместителя.
При использовании в настоящем изобретении термин "лечение заболевания" означает замедление или обращение прогрессирования заболевания. Лечение заболевания включает устранение симптома и/или ослабление симптомов заболевания.
При использовании в настоящем изобретении термин "предупреждение заболевания" означает замедление заболевания или начала развития заболевания или его симптомов. Предупреждение заболевания или нарушения может включать остановку развития заболевания или его симптомов.
При использовании в настоящем изобретении термин "разовая дозированная форма" означает отдельную порцию, такую как капсула или таблетка, пригодную для использования в качестве разовой дозы для пациентов-людей. Каждая порция содержит заранее заданное количество соединения формулы I, которое, как это установлено или предположено, приводит к необходимому фармакокинетическому профилю, который обеспечивает необходимый терапевтический эффект. Дозированная форма содержит соединение формулы I вместе по меньшей мере с одним фармацевтически приемлемым носителем, солью, инертным наполнителем или их комбинацией.
При использовании в настоящем изобретении термин "субъект" или "пациент", или "индивидуум", такой как субъект, нуждающийся в лечении или предупреждении, может представлять собой эукариота, животного, позвоночного животного, млекопитающего, грызуна (например, морскую свинку, хомяка, крысу, мышь), представителя семейства мышиных (например, мышь), представителя семейства собачьих (например, собаку), представителя семейства кошачьих (например, кошку), представителя семейства лошадиных (например, лошадь), примата, представителя семейства обезьяньих (например, обезьяну или человекообразную обезьяну), обезьяну (например, мартышку, бабуина), человекообразную обезьяну (например, гориллу, шимпанзе, орангутана, гиббона) или человека. Значения терминов "эукариот", "животное", "млекопитающее" и т.п. хорошо известно в данной области техники и определены, например, в публикации Wehner und Gehring (1995; Thieme Verlag). В контексте настоящего изобретения особо отмечается, что следует лечить животных, которые являются экономически, агрономически важными или важными с научной точки зрения. Важные с научной точки зрения организмы включают, но не ограничиваются только ими, мышей, крыс и кроликов. Низшие организмы, такие как, например, плодовые мушки, такие как Drosophila melagonaster, и нематоды, такие как Caenorhabditis elegans, также можно использовать в научных исследованиях. Неограничивающими примерами агрономически важных животных являются овцы, крупный рогатый скот и свиньи, тогда как, например, кошек и собак можно считать экономически важными животными. Предпочтительно, если субъект/пациент/индивидуум является млекопитающим; более предпочтительно, если субъект/пациент/индивидуум является человеком или млекопитающим, не являющимся человеком (таким как, например, морская свинка, хомяк, крыса, мышь, кролик, собака, кошка, лошадь, обезьяна, человекообразная обезьяна, мартышка, бабуин, горилла, шимпанзе, орангутан, гиббон, овца, крупный рогатый скот или свинья); еще более предпочтительно, если субъект/пациент/индивидуум является человеком.
При использовании в настоящем изобретении термин "доза" или "дозировка" означает количество активного ингредиента, который индивидуум принимает или которое вводят за один раз. Например, равная 40 мг доза соединения формулы I в случае режима введения два раза в сутки означает ситуацию, когда индивидуум принимает 40 мг соединения формулы I два раза в сутки, например, 40 мг утром и 40 мг вечером. Равную 40 мг дозу соединения формулы I можно разделить на 2 или большее количество доз, например, 2 дозы по 20 мг соединения формулы I в форме таблетки или 2 дозы по 20 мг соединения формулы I в форме капсулы.
При использовании в настоящем изобретении термин "терапевтически эффективное количество", такое как терапевтически эффективное количество соединения, предлагаемого в настоящем изобретении, означает количество, достаточное для обеспечения у субъекта необходимого биологического эффекта (например, терапевтического эффекта). Соответственно, терапевтически эффективное количество соединения может являться количеством, которое при введении субъекту, страдающему от такого заболевания или нарушения или подверженному такому заболеванию или нарушению, является достаточным для лечения или предупреждения заболевания или нарушения, и/или замедления начала развития или прогрессирования заболевания или нарушения, и/или облегчения одного или большего количества симптомов заболевания или нарушения.
При использовании в настоящем изобретении "фармацевтически приемлемое пролекарство" означает соединение, которое при физиологических условиях или путем сольволиза может превратиться в заданное соединение или в фармацевтически приемлемую соль такого соединения.
При использовании в настоящем изобретении "фармацевтически приемлемая соль" означает соль, которая сохраняет биологическую эффективность свободных кислот и оснований данного соединения и не является биологически или в ином отношении нежелательной. Соединение, предназначенное для применения в настоящем изобретении, может обладать достаточным количеством кислотных, достаточным количеством основных групп или обоими типами функциональных групп и соответствующим образом взаимодействовать с любым количеством неорганических или органических оснований и неорганических и органических кислот с образованием фармацевтически приемлемой соли. Типичные фармацевтически приемлемые соли включают соли, полученные по реакции соединений, предлагаемых в настоящем изобретении, с неорганической или органической кислотой или с неорганическим основанием, такие как гидрохлориды, гидробромиды, сульфаты, пиросульфаты, бисульфаты, сульфиты, бисульфиты, фосфаты, моногидрофосфаты, дигидрофосфаты, метафосфаты, пирофосфаты, хлориды, бромиды, йодиды, нитраты, ацетаты, пропионаты, деканоаты, каприлаты, акрилаты, формиаты, изобутираты, капроаты, гептаноаты, пропиолаты, оксалаты, малонаты, сукцинаты, субераты, себацинаты, фумараты, малеаты, бутин-1,4-диоаты, гексин-1,6-диоаты, бензоаты, хлорбензоаты, метилбензоаты, динитробензоаты, гидроксибензоаты, метоксибензоаты, фталаты, сульфонаты, ксилолсульфонаты, фенилацетаты, фенилпропионаты, фенилбутираты, цитраты, лактаты, гамма-гидроксибутираты, гликоляты, тартраты, метансульфонаты, этансульфонаты, пропансульфонаты, бензолсульфонаты, толуолсульфонаты, трифторметансульфонаты, нафталин-1-сульфонаты, нафталин-2-сульфонаты, манделаты, пируваты, стеараты, аскорбаты или салицилаты. Если соединения, предлагаемые в настоящем изобретении, содержат кислотный фрагмент, то их подходящие фармацевтически приемлемые соли могут включать соли щелочных металлов, например, соли натрия или калия; соли щелочноземельных металлов, например, соли кальция или магния; и соли, образованные с подходящими органическими лигандами, такими как аммиак, алкиламины, гидроксиалкиламины, лизин, аргинин, N-метилглюкамин, прокаин и т.п. Фармацевтически приемлемые соли хорошо известны в данной области техники.
При использовании в настоящем изобретении "фармацевтически приемлемый носитель" означает вещества, не являющиеся АФИ (АФИ означает активный фармацевтический ингредиент), такие как разрыхлители, связующие, наполнители и смазывающие вещества, использующиеся для приготовления фармацевтических продуктов. Они обычно являются безопасными при введении людям в соответствии с установленными правительственными стандартами, включая введенные в действие Управлением по контролю за качеством пищевых продуктов, медикаментов и косметических средств США и Европейским медицинским агентством. Фармацевтически приемлемые носители или инертные наполнители хорошо известны специалистам в данной области техники.
Специалист в данной области техники понимает, что некоторые переменные в перечне заместителей повторяются (разные названия для одного и того же заместителя), являются родовыми для других переменных перечня и/или по значению частично перекрываются с другими терминами. Специалист в данной области техники понимает, что в соединениях, предлагаемых в настоящем изобретении, заместители могут быть присоединены к остальной части молекулы в целом ряде положений и предпочтительными являются положения, указанные в примерах.
Соединения, предлагаемые в настоящем изобретении, неожиданно оказались активными и селективными ингибиторами LSD1. Исключение ингибирования других мишеней может исключить неожиданные или нежелательные побочные эффекты, такие как так называемый "эффект сыра", связанный с МАО-А. Таким образом, соединения, предлагаемые в настоящем изобретении, применимы для лечения или предупреждения любого заболевания или нарушения, связанного с LSD1. Они, в частности, включают неврологические заболевания и вирусные инфекции.
Предпочтительно, если соединения формулы I, включая соединения формулы Ia, Ia-1, Ib и Ic, а также любые их соли и сольваты, применяют для лечения или предупреждения рака, и наиболее предпочтительно для лечения рака. Типы рака, которые можно лечить (или предупреждать) с помощью соединений, предлагаемых в настоящем изобретении, включают, но не ограничиваются только ими, такие типы рака, как:
Раковое заболевание крови (в настоящем изобретении также называющееся раком крови), включая раковые заболевания крови, костного мозга и лимфатических узлов, такие как лейкозы (например, острый миелолейкоз (ОМЛ), острый промиелоцитарный лейкоз (ОПЛ), хронический миелолейкоз (ХМЛ), хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический лимфолейкоз (ХЛЛ), острый лимфобластный лейкоз (ОЛЛ) или волосатоклеточный лейкоз), миелодиспластический синдром, множественную миелому, миелодиспластический синдром и лимфомы (например, болезнь Ходжкина, неходжкинская лимфома (злокачественная лимфома));
Рак молочной железы, включая инвазивную карциному из эпителия протоков, преинвазивную дольковую карциному, дольковую карциному и смешанную карциному из эпителия протоков и дольковую карциному; Рак легких, такой как бронхогенная карцинома (плоскоклеточная, недифференцированная мелкоклеточная, недифференцированная крупноклеточная, аденокарцинома), альвеолярная (бронхиолярная) карцинома, аденома бронха, саркома, лимфома, хондроматозная гамартома и инезотелиома; Раковые заболевания желудочно-кишечного тракта, такие как рак пищевода (например, плоскоклеточная карцинома, аденокарцинома, лейомиосаркома, лимфома), желудка (например, карцинома, лимфома, лейомиосаркома), поджелудочной железы (например, протоковая аденокарцинома, инсулинома, глюкагонома, гастринома, карциноидные опухоли, випома), тонкой кишки (например, аденокарцинома, лимфома, карциноидные опухоли, саркома Капоши, лейомиома, гемангиома, липома, нейрофиброма, фиброма) и толстой кишки (например, аденокарцинома, ворсинчатая аденома, ворсинчатая аденома, гамартома, лейомиома);
Раковые заболевания мочеполового тракта, такие как рак почек (например, аденокарцинома, опухоль Вильмса (нефробластома), лимфома, лейкоз), рак мочевого пузыря и уретры (например, плоскоклеточная карцинома, переходно-клеточная карцинома, аденокарцинома), рак предстательной железы (например, аденокарцинома, саркома) и рак яичек (например, семинома, тератома, эмбриональная карцинома, тератокарцинома, хориокарцинома, саркома, интерстициально-клеточная карцинома, фиброма, фиброаденома, аденоматоидные опухоли, липома);
Рак печени, такой как гепатома (печеночно-клеточная карцинома), холангиокарцинома, гептобластома, ангиосаркома, печеночно-клеточная аденома и гемангиома;
Рак кости, такой как остеогенная саркома (остеосаркома), фибросаркома, злокачественная фиброзная гистиоцитома, хондросаркома, саркома Юинга, злокачественная лимфома (ретикулоклеточная саркома), множественная миелома, злокачественная гигантоклеточная опухоль хордома, остеохондрома (костно-хрящевые экзостозы), доброкачественная хондрома, хондробластома, хондромиксоидная фиброма, остеоид-остеома и гигантоклеточные опухоли; Раковые заболевания нервной системы, такие как рак черепа (например, остеома, гемангиома, гранулема, ксантома, деформирующий остит), рак оболочек головного мозга (например, менингиома, менингиосаркома, глиоматоз), рак головного мозга (например, астроцитома, медуллобластома, глиома, эпендимома, герминома (пинеалома), мультиформная глиобластома, олигодендроглиома, шваннома, ретинобластома, врожденные опухоли), нейрофиброма спинного мозга, менингиома, глиома и саркома; Гинекологические раковые заболевания, такие как рак матки (например, карцинома эндометрия), рак шейки матки (например, карцинома шейки матки, предопухолевая дисплазия шейки матки), рак яичников (например, карцинома яичников (серозная цистаденокарцинома, слизеобразующая цистаденокарцинома, неклассифицированная карцинома), гранулезотекаклеточные опухоли, опухоли из клеток Сертоли-Лейдига, дисгерминома, злокачественная тератома), рак вульвы (например, плоскоклеточная карцинома, внутриэпителиальная карцинома, аденокарцинома, фибросаркома, меланома), рак влагалища (например, светлоклеточная карцинома, плоскоклеточная карцинома, кистевидная саркома (эмбриональная рабдомиосаркома)) и рак фаллопиевых труб (карцинома);
Рак сердца, такой как саркома (например, ангиосаркома, фибросаркома, рабдомиосаркома, липосаркома), миксома, рабдомиома, фиброма, липома и тератома;
Рак кожи, такой как злокачественная меланома, базально-клеточная карцинома, плоскоклеточная карцинома и саркома Капоши; и Рак надпочечников, такой как нейробластома.
Соответственно, в одном варианте осуществления соединения, предлагаемые в настоящем изобретении, применяют для лечения или предупреждения рака, предпочтительно для лечения рака, где указанный рак выбран из группы, включающей рак крови, лейкоз, лимфому, рак молочной железы, рак легких, рак предстательной железы, колоректальный рак, рак головного мозга, нейробластому, рак мочевого пузыря, рак печени, саркому, миелому и рак кожи. В другом варианте осуществления соединения, предлагаемые в настоящем изобретении, применяют для лечения или предупреждения (предпочтительно для лечения) рака крови (также известного, как раковое заболевание крови), включая лейкозы (например, острый миелолейкоз (ОМЛ), хронический миелолейкоз (ХМЛ), хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический лимфолейкоз (ХЛЛ), острый лимфобластный лейкоз (ОЛЛ) или волосатоклеточный лейкоз), лимфомы и миеломы, рак предстательной железы, рак молочной железы, рак легких, колоректальный рак, рак головного мозга или рак кожи. В предпочтительном варианте осуществления соединения формулы I, включая соединения формулы Ia, Ia-1, Ib и Ic, применяют для лечения рака крови. Более предпочтительно, если соединения формулы I, включая соединения формулы Ia, Ia-1, Ib и Ic, применяют для лечения лейкоза, включая острый миелолейкоз (ОМЛ), хронический миелолейкоз (ХМЛ), хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический лимфолейкоз (ХЛЛ), острый лимфобластный лейкоз (ОЛЛ) и волосатоклеточный лейкоз.
Обычно соединения формулы I, Ia, Ia-1, Ib или Ic могут быть эффективны в количестве, составляющем от примерно 0,01 мкг/(кг сутки) до примерно 100 мг/(кг сутки) в пересчете на полную массу тела. Активный ингредиент можно вводить одной порцией или можно разделить на несколько меньших доз, вводимых через заранее заданные промежутки времени. Разовая доза, подходящая для каждого введения может составлять, например, от примерно 1 мкг до примерно 2000 мг, предпочтительно от примерно 5 мкг до примерно 1000 мг. Еще более предпочтительно, если количество вводимого активного ингредиента составляет от примерно 5 мкг до примерно 100 мг в сутки. Эти дозы зависят от фармакокинетических параметров конкретного соединения и других характеристик ВРМВ (всасывание, распределение, метаболизм и выведение), а также от эффективности соединения при конкретном состоянии заболевания.
Следует понимать, что указанные выше диапазоны доз являются лишь типичными и не ограничивают объем настоящего изобретения. Терапевтически эффективное количество каждого активного соединения может меняться от таких факторов, включая, но не ограничиваясь только ими, как активность использующегося соединения, стабильность активного соединения в организме пациента, тяжесть патологических состояний, протекание которых облегчают, полная масса подвергающегося лечению пациента, путь введения, легкость всасывания, распределения и выведения активного соединения из организма, возраст и чувствительность пациента по отношению к лечению и т.п., что должен понимать специалист в данной области техники. Вводимое количество можно регулировать, поскольку различные факторы меняются во времени.
Несмотря на то, что для применения в терапии соединение, предлагаемое в настоящем изобретении, можно вводить непосредственно само по себе, обычно его вводят в форме фармацевтической композиции, которая содержит указанное соединение в качестве активного фармацевтического ингредиента вместе с одним или большим количеством фармацевтически приемлемых инертных наполнителей или носителей.
Соединения, предлагаемые в настоящем изобретении, можно вводить любым путем, который соответствует их назначению. Примеры включают пероральный, парентеральный, внутривенный, подкожный или местный пути.
Для пероральной доставки активные соединения можно ввести в препарат, который включает фармацевтически приемлемые носители, такие как связующие (например, желатин, целлюлоза, трагакантовая камедь), инертные наполнители (например, крахмал, лактоза), смазывающие вещества (например, стеарат магния, диоксид кремния), разрыхлители (например, альгинат, примогель и кукурузный крахмал) и подсластитель и ароматизаторы (например, глюкоза, сахароза, сахарин, метилсалицилат и перечная мята). Препарат можно доставлять перорально в виде закрытых капсул из желатина или прессованных таблеток. Капсулы и таблетки можно изготовить по любым обычным методикам. На капсулы и таблетки также можно нанести различные покрытия, известные в данной области техники, для изменения аромата, вкуса, цвета и формы капсул и таблеток. Кроме того, в капсулы можно внести жидкие носители, такие как нелетучее жидкое масло.
Препараты, подходящие для перорального введения также могут находится в форме суспензии, сиропа, жевательной резинки, облатки, эликсира и т.п. При необходимости в них также можно включить обычные агенты, изменяющие аромат, вкус, цвет и форму этих специальных форм препаратов. Кроме того, для удобства введения с помощью зонда для искусственного кормления пациентов, которые не могут глотать, активные соединения можно растворить в приемлемом липофильном растительном масле в качестве разбавителя, таком как оливковое масло, кукурузное масло и сафлоровое масло.
Активные соединения также можно вводить парентерально в виде раствора или суспензии или в лиофилизированной форме, которую перед использованием можно превратить в раствор или суспензию. В таких препаратах можно использовать разбавители или фармацевтически приемлемые носители, такие как стерильная вода и буферный физиологический раствор. Можно включить другие обычные растворители, буферы для регулирования рН, стабилизаторы, антибактериальные средства, поверхностно-активные вещества и антиоксиданты. Например, применяющиеся компоненты включают хлорид натрия, ацетатные, цитратные или фосфатные буферы, глицерин, декстрозу, нелетучие масла, метилпарабены, полиэтиленгликоль, пропиленгликоль, бисульфат натрия, бензиловый спирт, аскорбиновую кислоту и т.п. Препараты для парентерального введения можно хранить в любых обычных контейнерах, таких как флаконы и ампулы.
Пути местного введения включают назальное, трансбуккальное, проводимое через слизистую оболочку, ректальное или вагинальное введение. Для местного введения активные соединения можно приготовить в виде лосьонов, кремов, мазей, гелей, порошков, суспензий, капель и аэрозолей. Так, в препараты можно включить один или большее количество загущающих агентов, влагоудерживающих веществ и стабилизирующих агентов. Примеры таких агентов включают, но не ограничиваются только ими, полиэтиленгликоль, сорбит, ксантановую камедь, вазелиновое масло, пчелиный воск или минеральное масло, ланолин, сквален и т.п. Специальным типом местной доставки является использование чрескожного пластыря. Методики изготовления чрескожных пластырей описаны, например, в публикации Brown, et al. (1988) Ann. Rev. Med. 39: 221-229, которая включена в настоящее изобретение в качестве ссылки.
Подходящим путем введения также может быть подкожная имплантация, предназначенная для пролонгированного высвобождения активных соединений. Она включает хирургические процедуры для имплантации активного соединения в любой подходящей композиции в подкожное пространство, например, под переднюю брюшную стенку. См., например, публикацию Wilson et al. (1984) J. Clin. Psych. 45: 242-247. Для пролонгированного высвобождения активных соединений в качестве носителя можно использовать гидрогели. Гидрогели в целом известны в данной области техники. Их обычно получают путем сшивки высокомолекулярных биологически совместимых полимеров в сетку, которая набухает в воде с образованием гелеобразного материала. Предпочтительно, если гидрогели являются биологически разлагающимися или биологически сорбирующимися. Для задач настоящего изобретения можно использовать гидрогели, приготовленные из полиэтиленгликолей, коллагена или сополимера гликоля с L-молочной кислотой. См., например, публикацию Phillips et al. (1984) J. Pharmaceut. Sci., 73: 1718-1720.
Активные соединения также можно конъюгировать с растворимым в воде неиммуногенным, непептидным обладающим большой молекулярной массой полимером с образованием конъюгата с полимером. Например, активное соединение ковалентно связывают с полиэтиленгликолем с образованием конъюгата. Обычно такой конъюгат обладает улучшенной растворимостью, стабильностью и пониженной токсичностью и иммуногенностью. Таким образом, при введении пациенту активное соединение в конъюгате может обладать более длительным периодом полувыведения из организма и большей эффективностью. См. публикацию Burnham (1994) Am. J. Hosp. Pharm. 15: 210-218. Пэгилированные (ПЭГ - полиэтиленгликоль) белки в настоящее время используются в белковозаместительной терапии и для других терапевтических целей. Например, пэгилированные интерферон (ПЭГ-ИНТРОН А®) используют для клинического лечения гепатита В. Пэгилированную аденозиндезаминазу (АДАГЕН®) используют для лечения тяжелого комбинированного иммунодефицита (SCIDS). Пэгилированную L-аспарагиназу (ОНКАПСПАР®) используют для лечения острого лимфобластного лейкоза (ОЛЛ). Предпочтительно, если ковалентная связь между полимером и активным соединением и/или в самом полимере гидролитически разрывается при физиологических условиях. Такие конъюгаты, известные в качестве "пролекарств", могут легко высвобождать активное соединение внутри организма. Регулируемое высвобождение активного соединения также можно обеспечить путем включения активного ингредиента в микрокапсулы, нанокапсулы или гидрогели, общеизвестные в данной области техники. Другие фармацевтически приемлемые пролекарства соединений, предлагаемых в настоящем изобретении, включают, но не ограничиваются только ими, сложные эфиры, карбонаты, тиокарбонаты, N-ацилпроизводные, N-ацилоксиалкилпроизводные, четвертичные производные третичных аминов, N-основания Манниха, шиффовы основания, конъюгаты аминокислот, фосфаты, соли металлов и сульфонаты.
В качестве носителей для активных соединений, предлагаемых в настоящем изобретении, также можно использовать липосомы. Липосомы являются мицеллами, образованными из различных липидов, таких как холестерин, фосфолипиды, жирные кислоты и их производные. Также можно использовать различные модифицированные липиды. Липосомы могут уменьшать токсичность активных соединений и повышать их стабильность. Методики приготовления липосомных суспензий, содержащих активные ингредиенты, общеизвестны в данной области техники. См., например, патент U.S. №4522811; Prescott, Ed., Methods in Cell Biology, Volume XIV, Academic Press, New York, N. Y. (1976).
Активные соединения также можно вводить в комбинации с другим активным средством, которое синергетически устраняет или предупреждаем такие же симптомы или эффективно для лечения другого заболевания или устранения симптома у подвергающегося лечению пациента, если другое активное средство не мешает активному соединению или неблагоприятно не влияет на воздействие активных соединений, предлагаемых в настоящем изобретении. Такие другие активные средства включают, но не ограничиваются только ими, противовоспалительные средства, противовирусные средства, антибиотики, фунгицидные средства, антитромботические средства, сердечнососудистые средства, средства, снижающие содержание холестерина, противораковые лекарственные средства, гипотензивные лекарственные средства и т.п.
Комбинированная терапия включает введение одного фармацевтического дозированного препарата, который содержит соединение, предлагаемое в настоящем изобретении, и одно или большее количество дополнительных активных средств, а также введение соединения, предлагаемого в настоящем изобретении, и каждого дополнительного активного средства в каждом случае в отдельном фармацевтическом дозированном препарате. Если их вводят по отдельности, то введение может быть одновременным, последовательным или раздельным и соединение, предлагаемое в настоящем изобретении, и дополнительное терапевтическое средство (средства) можно вводить одним и тем же путем или использовать разные пути введения, например, одно соединение можно вводить перорально и другое внутривенно.
В частности, если соединение формулы I, Ia, Ia-1, Ib или Ic применяют для лечения или предупреждения рака, то указанное соединение можно применять в комбинации с одним или большим количеством дополнительных средств, для которых известно, что они применимы для лечения или предупреждения рака, включая химиотерапию или лучевую терапию.
Обычно для комбинированной терапии вместе с соединением, предлагаемым в настоящем изобретении, можно использовать любое противоопухолевое средство, которое обладает активностью по отношению к раковому заболеванию, которое лечат или предупреждают с помощью соединения, предлагаемого в настоящем изобретении. Примеры противоопухолевых средств, которые можно использовать в комбинации с соединениями и способами, предлагаемыми в настоящем изобретении, обычно включают, если это является подходящим, алкилирующие средства, антиметаболиты, эпидофиллотоксины, противоопухолевые ферменты, ингибиторы топоизомеразы, прокарбазины, митоксантроны, координационные комплексы платины, модификаторы биологического ответа и ингибиторы роста, гормональные/антигормональные терапевтические средства и гематопоэтические факторы роста. Типичные классы противоопухолевых средств включают антрациклины, алкалоиды барвинка, митомицины, блеомицины, цитотоксические нуклеозиды, эпотилоны, дискодермолиды, птеридины, диинены и подофиллотоксины. Особенно полезные представители этих классов включают, например, карминомицин, даунорубицин, аминоптерин, метотрексат, метоптерин, дихлорметотрексат, митомицин С, порфиромицин, 5-фторурацил, 6-меркаптопурин, гемцитабин, цитозинарабинозид, подофиллотоксин или производные подофиллотоксина, такие как этопозид, этопозидфосфат или тенипозид, мелфалан, винбластин, винкристин, лейрозидин, виндезин, лейрозин, паклитаксел и т.п. Другие полезные противоопухолевые средства включают эстрамустин, карбоплатин, циклофосфамид, блеомицин, гемцитабин, ифосфамид, мелфалан, гексаметилмеламин, тиотепа, цитарабин, идатрексат, триметрексат, дакарбазин, L-аспарагиназа, камптотецин, СРТ-11, топотекан, ara-С, бикалутамид, флутамид, лейпролид, производные пиридобензоиндолы, интерфероны и интерлейкины.
Таким образом, соединение формулы I, Ia, Ia-1, Ib или Ic, предлагаемое в настоящем изобретении, можно использовать для лечения или предупреждения рака, где указанное соединение предназначено для введения в комбинации с одним или большим количеством противораковых средств. Противораковые средства, вводимые при комбинированной терапии, в зависимости от случая могут быть выбраны из группы, включающей: ингибитор ангиогенеза опухоли (например, ингибитор протеазы, ингибитор киназы рецептора эпидермального фактора роста или ингибитор киназы рецептора сосудистого эндотелиального фактора роста); цитотоксическое лекарственное средство (например, антиметаболит, такой как пуриновый и пиримидиновый аналоги антиметаболитов); антимитотическое средство (например, лекарственное средство, стабилизирующее микротрубочки или антимитотический алкалоид); координационный комплекс платины; противоопухолевый антибиотик; алкилирующее средство (например, азотистый иприт или нитрозомочевина); эндокринное средство (например, адренокортикостероид, андроген, антиандроген, эстроген, антиэстроген, ингибитор ароматазы, агонист гонадотропин-рилизинг гормона или аналог соматостатина); или соединение, которое направленно воздействует на фермент или рецептор, который сверхэкспрессируется и/или другим образом участвует в конкретном метаболическом пути, регуляция которого нарушена в опухолевой клетке (например, ингибиторы АТФ (аденозинтрифосфат) и ГТФ (гуанозинтрифосфат) фосфодиэстеразы, ингибиторы гистондезацетилазы, ингибиторы протеинкиназы (такие как ингибиторы серин-, треонин- и тирозинкиназы (например, протеинтирозинкиназы Абельсона)) и различные факторы роста, их рецепторы и ингибиторы их киназ (такие как ингибиторы киназы рецептора эпидермального фактора роста, ингибиторы киназы рецептора сосудистого эндотелиального фактора роста, ингибиторы фактора роста фибробластов, ингибиторы рецептора инсулиноподобного фактора роста и ингибиторы киназы рецептора тромбоцитарного фактора роста)); ингибиторы аминопептидазы; ингибиторы протеосомы; ингибиторы циклооксигеназы (например, ингибиторы циклооксигеназы-1 или циклооксигеназы-2); ингибиторы топоизомеразы (например, ингибиторы топоизомеразы I ингибиторы или топоизомеразы II); или средства, содержащие ретиноиды.
Алкилирующим средством, которое можно использовать в качестве противоракового лекарственного средства в комбинации с соединением, предлагаемым в настоящем изобретении, может быть, например, азотистый иприт (такой как циклофосфамид, мехлорэтамин (хлорметин), урамустин, мелфалан, хлорамбуцил, ифосфамид, бендамустин или трофосфамид), нитрозомочевина (такая как кармустин, стрептозоцин, фотемустин, ломустин, нимустин, преднимустин, ранимустин или семустин), алкилсульфонат (такой как бусульфан, манносульфан или треосульфан), азиридин (такой как гексаметилмеламин (алтретамин), триэтиленмеламин, тиотепа (N,N'N'-триэтилентиофосфорамид), карбоквон или триазиквон), гидразин (такой как прокарбазин), триазен (такой как дакарбазин) или имидазотетразины (такие как темозоломид).
Координационным комплексом платины, который можно использовать в качестве противоракового лекарственного средства в комбинации с соединением, предлагаемым в настоящем изобретении, может быть, например, цисплатин, карбоплатин, недаплатин, оксалиплатин, сатраплатин или триплатинтетранитрат.
Цитотоксическим лекарственным средством, которое можно использовать в качестве противоракового лекарственного средства в комбинации с соединением, предлагаемым в настоящем изобретении, может быть, например, антиметаболит, включая антиметаболиты - аналоги фолиевой кислоты (такие как аминоптерин, метотрексат, пеметрексед или ралтитрексед), антиметаболиты - аналоги пурина (такие как кладрибин, клофарабин, флударабин, 6-меркаптопурин (включая его пролекарственную форму азатиоприн), пентостатин или 6-тиогуанин) и антиметаболиты - аналоги пиримидина (такие как цитарабин, децитабин, 5-фторурацил (включая его пролекарственные формы капецитабин и тегафур), флоксуридин, гемцитабин, эноцитабин или сапацитабин).
Антимитотическим средством, которое можно использовать в качестве противоракового лекарственного средства в комбинации с соединением, предлагаемым в настоящем изобретении, может быть, например, таксан (такой как доцетаксел, ларотаксел, ортатаксел, паклитаксел/таксол или тесетаксел), алкалоид барвинка (такой как винбластин, винкристин, винфлунин, виндезин, винзолидин или винорелбин), эпотилон (такой как эпотилон А, эпотилон В, эпотилон С, эпотилон D, эпотилон Е или эпотилон F) или аналог эпотилона В (такой как иксабепилон/азаэпотилон В).
Противоопухолевым антибиотиком, который можно использовать в качестве противоракового лекарственного средства в комбинации с соединением, предлагаемым в настоящем изобретении, может быть, например, антрациклин (такой как акларубицин, даунорубицин, доксорубицин, эпирубицин, идарубицин, амрубицин, пирарубицин, валрубицин или зорубицин), антрацендион (такой как митоксантрон или пиксантрон) или противоопухолевый антибиотик, выделенный из Streptomyces (такой как актиномицин (включая актиномицин D), блеомицин, митомицин (включая митомицин С) или пликамицин).
Ингибитором тирозинкиназы, который можно использовать в качестве противоракового лекарственного средства в комбинации с соединением, предлагаемым в настоящем изобретении, может быть, например, акситиниб, босутиниб, цедираниб, дасатиниб, эрлотиниб, гефитиниб, иматиниб, лапатиниб, лестауртиниб, нилотиниб, семаксаниб, сорафениб, сунитиниб или вандетаниб.
Ингибитором топоизомеразы, который можно использовать в качестве противоракового лекарственного средства в комбинации с соединением, предлагаемым в настоящем изобретении, может быть, например, ингибитор топоизомеразы I (такой как иринотекан, топотекан, камптотецин, белотекан, рубитекан или ламелларин D) или ингибитор топоизомеразы II (такой как амсакрин, этопозид, этопозидфосфат, тенипозид или доксорубицин).
В комбинации с соединением, предлагаемым в настоящем изобретении, можно использовать другие противораковые лекарственные средства. Противораковые лекарственные средства могут включать биологические или химические молекулы, такие как родственный TNF индуцирующий апоптоз лиганд (TRAIL), тамоксифен, торемифен, флюоксиместерон, ралоксифен, diethylstibestrol, бикалутамид, нилутамид, флутамид, аминоглютетимид, анастрозол, тетразол, аналоги рилизинг-фактора лютеинизирующего гормона (LHRH), кетоконазол, госерелинацетат, лейпролид, мегэстролацетат, преднизон, мифепристон, амсакрин, бексаротен, эстрамустин, ирофульвен, трабектедин, цетуксимаб, панитумумаб, тозитумомаб, алемтузумаб, бевацизумаб, эдреколомаб, гемтузумаб, альвоцидиб, селициклиб, аминолевулиновая кислота, метиламинолевулинат, эфапроксирал, порфимер натрия, талапорфин, темопорфин, вертепорфин, анагрелид, триоксид мышьяка, атрасентан, бортезомиб, кармофур, целекоксиб, демеколцин, элескломол, элсамитруцин, этоглуцид, лонидамин, лукантон, мазопрокол, митобронитол, митогуазон, митотан, облимерсен, омацетаксин, ситимаген, цераденовек, тегафур, тестолактон, тиазофурин, типифарниб и вориностат.
Примеры средств, содержащих ретиноиды, включают все природные, рекомбинантные и синтетические производные или миметики витамина А, например, ретинилпальмитат, ретиноил-бета-глюкуронид (витамин А1-бета-глюкуронид), ретинилфосфат (витамин А1-фосфат), ретиниловые сложные эфиры, 4-оксоретинол, 4-оксоретинальдегид, 3-дегидроретинол (витамин А2), 11-цис-ретиналь (11-цис-ретинальдегид, 11-цис- или нео-b-витамин А1-альдегид), 5,6-эпоксиретинол (5,6-эпокси-витамин А1-спирт), ангидроретинол (ангидро-витамин А1) и 4-кеторетинол (4-кето-витамин А1-спирт), полностью-транс-ретиноевая кислота (ПТРК; третиноин; витамин А-кислота; 3,7-диметил-9-(2,6,6-триметил-1-циклогексен-1-ил)-2,4,6,8-нонатетраеноевая кислота [регистрационный №CAS 302-79-4]), липидные препараты полностью-транс-ретиноевой кислоты (например, ATRA-IV), 9-цис-ретиноевая кислота (9-цис-РК; алитретиноин; панретинтм; LGD1057), 13-цис-ретиноевая кислота (изотретиноин), (Е)-4-[2-(5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафталинил)-1-пропенил]бензойная кислота, 3-метил-(Е)-4-[2-(5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафталинил)-1-пропенил]бензойная кислота, фенретинид (N-(4-гидроксифенил)ретинамид; 4-HPR), этретинат (этиловый эфир (полностью-Е)-9-(4-метокси-2,3,6-триметилфенил)-3,7-диметил-2,4,6,8-нонатетраеноевой кислоты; тегизон), ацитретин ((полностью-Е)-9-(4-метокси-2,3,6-триметилфенил)-3,7-диметил-2,4,6,8-нонатетраеноевая кислота; Ro 10-1670; сориатан; неотигазон), тазаротен (этил-6-[2-(4,4-диметилтиохроман-6-ил)-этинил]никотинат; тазорак; аваге; зорак), токоретинат (9-цис-третиноин; токоферил), адапален (6-[3-(1-адамантил)-4-метоксифенил]-2-нафтойная кислота; дифферин), мотретинид (триметилметоксифенил-N-этилретинамид; тасмадерм), ретинальдегид (ретиналь), CD437 (6-[3-(1-адамантил)-4-гидроксифенил)-2-нафталинкарбоновая кислота; АГФН), CD2325, ST1926 ([Е-3-(4'-гидрокси-3'-адамантилбифенил-4-ил)акриловая кислота), ST1878 (метил-2-[3-[2-[3-(2-метокси-1,1-диметил-2-оксоэтокси)фенокси]этокси]фенокси]изобутират), ST2307, ST1898, ST2306, ST2474, ММ11453, ММ002 (3-Cl-АНРС), МХ2870-1, МХ3350-1, МХ84 и МХ90-1, докозагексаеновая кислота (ДГК), фитановая кислота (3,7,11,15-тетраметилгексадекановая кислота), MS6682 (метопреновая кислота), LG100268 (LG268), LG100324, SR11203 ([2-(4-карбоксифенил)-2-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафталинил)-1,3-дитиан), SR11217 (4-(2-метил-1-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафталинил)пропенил)бензойная кислота), SR11234, SR11236 (2-(4-карбоксифенил)-2-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафталинил)-1,3-диоксан), SR11246, AGN194204, производные 9-цис-РК, такие как LGD1069 (3-метил-TTNEB; бексаротен; таргретин®; 4-[1-(5,6,7,8-тетрагидро-3,5,5,8,8-пентаметил-2-нафталинил)этенил]бензойная кислота).
Примеры ингибиторов гистондезацетилазы включают, но не ограничиваются только ими, МС-275 (SNDX-275; энтиностат), FK228 (FR901228; депсипептид; ромидепсин), CI-994 (ацетилдиналин; тацединалин), апицидин (цикло[(2S-2-амино-8-оксодеканоил-L-метокси-L-триптофил-L-изолейцил-(2R)-2-пиперидинкарбонил]), А-161906 (7-[4-(4-цианофенил)фенокси]гидроксамовая кислота), скриптаид (гидроксиамид 6-(1,3-диоксо-1Н,3Н-бензо[де]изохинолин-2-ил)гексановой кислоты), PXD-101 (белиностат), CHAP (циклический пептид, содержащий гидроксамовую кислоту), LAQ-824 (дациностат), BML-EI319 (депудецин), O3139 (оксамфлатин), NSC 696085 (пироксамид), MW2796; MW2996, Т2580 (трапоксин A), AN-9 (пиванекс), W222305 (трибутирин) трихостатин А, трихостатин С, масляную кислоту, вальпроевую кислоту (ВПК), субероиланилид гидроксамовой кислоты (САГК; вориностат), бис-гидроксамид м-карбоксикоричной кислоты (ГАКК), салицил-бис-гидроксамовую кислоту (S607; СГК; SHAM); субероил-бис-гидроксамовую кислоту (СБГК); азелаин-бис-гидроксамовую кислоту (АБГК); азелаин-1-гидроксамат-9-анилид (ААГА); 3Cl-UCHA (6-(3-хлорфенилуреидо)гидроксамовая кислота); и бутират, 4-фенилбутират, фенилацетат, валерат, изовалерат, бутирамид, изобутирамид, 3-бромпропионат и вальпроат натрия.
Кроме того, в совместной терапии с соединениями, предлагаемыми в настоящем изобретении, также можно использовать биологические лекарственные средства, такие как антитела, фрагменты антител, конструкции антител (например, одноцепочечные конструкции) и/или модифицированные антитела (такие как привитые к CDR антитела, гуманизированные антитела, "полностью гуманизированные" антитела и т.п.), направленные на рак или опухоль маркеры/факторы/цитокины, участвующие в раковых заболеваниях. Примерами таких биологических молекул являются алемтузумаб, аполизумаб, азелизумаб, атлизумаб, бапиньюзумаб, бевацизумаб, биватузумабмертанзин, кантузумабмертанзин, цеделизумаб, цертолизумабпегол, цитфуситузумаб, цидтузумаб, даклизумаб, экулизумаб, эфализумаб, эпратузумаб, эрлизумаб, фелвизумаб, фонтолизумаб, гемтузумаб озогамицин, инотузумабозогамицин, ипилимумаб, лабетузумаб, линтузумаб, матузумаб, меполизумаб, мотавизумаб, мотовизумаб, натализумаб, нимотузумаб, ноловизумаб, нумавизумаб, окрелизумаб, омализумаб, паливизумаб, пасколизумаб, пекфуситузумаб, пектузумаб, пертузумаб, пекселизумаб, раливизумаб, ранибизумаб, ресливизумаб, реслизумаб, резивизумаб, ритуксимаб, ровелизумаб, ролизумаб, сибротузумаб, сиплизумаб, сонтузумаб, такатузумаб тетраксетан, тадоцизумаб, тализумаб, тефибазумаб, тоцилизумаб, торализумаб, трастузумаб, тукотузумабцелмолейкин, тукузитузумаб, умавизумаб, уртоксазумаб и визилизумаб.
Другие биологические средства включают, но не ограничиваются только ими, иммуномодулирующие белки, такие как цитокины (такие как интерлейкин-2 (IL-2, алдеслейкин), эпойетин-альфа; ЕРО), гранулоцит-CSF (G-CSF; филграстин) и гранулоцит-макрофаг-CSF (GM-CSF; сарграмостим), и интерфероны, (например, интерферон-альфа, интерферон-бета и интерферон-гамма), бацилла Кальмета-Герена, левамизол и октреотид, эндостатин, подавляющие опухоль гены (например, DPC4, NF-1, NF-2, RB, р53, WT1, BRCA1 и BRCA2) и противораковые вакцины (например, опухолевые специфические антигены, такие как ганглиозиды (GM2), специфический антиген простаты (САП), альфа-фетопротеин (AFP), карциноэмбриональный антиген (КЭА) (продуцируется при раке толстой кишки и других аденокарциномах, например, при раке молочной железы, легких, желудка и поджелудочной железы), связанные с меланомой антигены (MART-1, gap 100, МАGЕ-1,3-тирозиназа), фрагменты Е6 и Е7 папилломавируса, целые клетки или сегменты/лизаты аутологических опухолевых клеток и аллогенных опухолевых клеток.
Описание общего пути синтеза
Соединения формулы I можно синтезировать в соответствии или по аналогии с общими путями, описанными ниже. Если не указано иное, то в описанных ниже методиках значения различных заместителей в каждом синтетическом продукте и в каждом соединении формулы I являются значениями, описанными выше для соединения формулы I. Для получения соединений формулы I также можно использовать другие пути, известные специалисту с общей подготовкой в данной области техники, а также другие реагенты и промежуточные продукты. Приведенные ниже схемы реакций представляют собой только примеры осуществления настоящего изобретения и никоим образом не ограничивают настоящее изобретение. В некоторых методиках, описанных ниже, может быть необходимо или желательно защитить реакционноспособные или лабильные группы обычными защитными группами. Природа этих защитных групп и процедуры их введения и удаления хорошо известны в данной области техники (см., например, Greene TW and Wuts PGM "Greene's Protecting Groups in Organic Synthesis", 4th edition, Wiley, 2006). Когда содержится защитная группа, необходимо проведение последующей стадии удаления защитной группы, которую можно провести при стандартных условиях, хорошо известных в данной области техники, таких как описанные в приведенной выше публикации.
В общем случае соединения формулы I можно получить путем восстановительного алкилирования циклопропиламинопроизводного формулы II с использованием кетона формулы III, как это показано ниже на схеме 1:

Где А, В, D, Rw, Rx, Ry, Rz обладают значениями, раскрытыми выше для соединения формулы I.
Указанное восстановительное алкилирование можно провести при стандартных условиях проведения реакций восстановительного алкилирования, хорошо известных в данной области техники. Например, подходящим набором условий является введение в реакцию соединения II с соединением III с использованием восстановительного реагента, такого как борогидрид (например, триацетоксиборогидрид натрия или борогидрид натрия) в подходящем растворителе, таком как дихлорэтан или метанол, необязательно в присутствии кислоты, такой как уксусная кислота. Для проведения реакции необходимо защитить любую другую аминогруппу, которая может содержаться в соединении II или в соединении III, с использованием обычных защитных групп аминогруппы, чтобы избежать любых побочных реакций; если содержится такая защитная группа аминогруппы, то для получения соединения формулы I потребуется последующее проведение стадии удаления защитной группы. Можно использовать любую подходящую защитную группу аминогруппы, такую как, например, трет-бутоксикарбонильная группа (Boc). Если используют группу Boc, то удаление защитной группы можно провести при стандартных условиях, например, в кислой среде с использованием HCl в органическом растворителе, таком как диэтиловый эфир или 1,4-диоксан, или с использованием трифторуксусной кислоты (ТФК) в дихлорметане. Если на последней стадии синтеза используют HCl, соединения формулы I получают в виде гидрохлорида. Аналогичным образом, если используют ТФК, то соединения получают в виде трифторацетата.
Циклопропиламинопроизводные формулы II и кетоны формулы III имеются в продаже или их можно получить по методикам, раскрытым в литературе.
Методики получения соединений формулы I более подробно описаны ниже.
Соединения формулы I, в которой Rw, Rx, Ry, Rz=H, можно синтезировать, например, общим путем, представленным на схеме 2. Этот путь является особенно подходящим для получения соединений, в которых B=Н или R1, поскольку соответствующий альдегид (1) имеется в продаже или его можно легко получить. На приведенной ниже схеме 2 для схематического представления "В" не использовали.

Альдегиды формулы (1) вводят в реакцию Хорнера-Уодсворта-Эммонса с использованием триэтилфосфоноацетата и основания, предпочтительно трет-бутоксида калия, в подходящем растворителе, таком как тетрагидрофуран, и получают этилакрилатные производные формулы (2), которые затем вводят в реакцию циклопропанирования с использованием триметилсульфоксониййодида и гидрида натрия в диметилсульфоксиде в качестве растворителя и получают (транс)-этилциклопропанкарбоксилатные производные формулы (3) (получают в виде рацемической смеси транс-((1S,2R) и (1R,2S))). Гидролиз с получением соответствующих производных (транс)-циклопропанкарбоновой кислоты (4) можно провести в щелочной среде с использованием, например, NaOH в подходящем растворителе, таком как МеОН. Последующая реакция соединения (4) сначала с этилхлорформиатом и триэтиламином в ацетоне и затем с азидом натрия в воде приводит к образованию (транс)-циклопропанкарбонилазидных производных формулы (5). Реакция с трет-бутанолом приводит к образованию трет-бутил-(транс)-циклопропилкарбаматных производных формулы (6). Удаление защитной группы Boc в кислой среде, например, с использованием 2М раствора HCl в диэтиловом эфире в подходящем растворителе, таком как диэтиловый эфир, или с использованием HCl в 1,4-диоксане приводит к образованию (транс)-циклопропанаминовых производных формулы (7).
Альтернативно, (транс)-циклопропанаминовые производные формулы (7) можно синтезировать по реакции альдегидов формулы (1) с нитрометаном и ацетатом аммония с использованием тетрагидрофурана в качестве растворителя, что приводит к образованию нитростирола формулы (10). Последующая реакция циклопропанирования с использованием триметилсульфоксониййодида и трет-бутоксида калия приводит к образованию транс-нитроциклопропильных производных формулы (11) (получают в виде рацемической смеси транс-((1S,2R), (1R,2S))) и заключительное восстановление с использованием цинка в хлористоводородной кислоте дает (транс)-циклопропанаминовые производные формулы (7).
Восстановительное алкилирование производных формулы (7) с использованием кетонов формулы (8) при стандартных условиях, например, с использованием триацетоксиборогидрида натрия или борогидрида натрия в качестве восстановительного реагента, в подходящем растворителе, таком как дихлорэтан или метанол, приводит к образованию (транс)-циклопропиламинопроизводных формулы (9), которые соответствуют соединению формулы I, и, в частности формулы Iа, в которой Rw, Rx, Ry, Rz=H. В случае, если кетоны формулы (8) содержат защищенную аминогруппу, например, защищенную группой Boc аминогруппу (Boc: трет-бутоксикарбонил), то для получения соединения (9) необходимо провести дополнительную стадию реакции удаления защитной группы, которую можно провести в кислой среде, например, с использованием 2М раствора HCl в диэтиловом эфире в подходящем растворителе, таком как диэтиловый эфир, или с использованием HCl в 1,4-диоксане.
Альдегиды формулы (1) и кетоны формулы (8) имеются в продаже или их можно получить по хорошо известным методикам синтеза из легко доступных исходных веществ.
Соединения формулы I, в которой B=-L-E и Rw, Rx, Ry, Rz=H и L=-(CH2)х-O- (где х является таким, как определено выше), можно синтезировать, например, общим путем, представленным на схеме 3:

Алкилирование альдегидов формулы 1 (в которой R1=-ОН) с использованием бромпроизводных формулы (12) (также можно использовать другие галогенпроизводные) и основания, предпочтительно карбоната калия в подходящем растворителе, таком как N,N-диметилформамид, приводит к образованию производных альдегидов формулы (13). Их вводят в реакцию Хорнера-Уодсворта-Эммонса при таких же условиях, как раскрытые на схеме 2, и получают этилакрилатные производные формулы (14), которые затем вводят в реакцию циклопропанирования при таких же условиях, как раскрытые на схеме 2, и получают (транс)-этилциклопропанкарбоксилатные производные формулы (15). С использованием таких же условиях, как раскрытые на схеме 2 для превращения соединения (3) в соединение (7), соединение (15) превращают в (транс)-циклопропанаминовые производные формулы (19).
Альтернативно, (транс)-циклопропанаминовые производные формулы (19) можно синтезировать из альдегидов формулы (13) путем превращения в нитростирол (21), с последующим циклопропанированием и получением соединения (22) и восстановлением нитрогруппы при таких же условиях, как раскрытые на схеме 2 для превращения соединения (1) в соединение (7) через соединения (10) и (11).
Восстановительное алкилирование производных формулы (19) с использованием кетонов формулы (8) при таких же условиях, как раскрытые на схеме 1 или 2, дает соединение (20), которое соответствует соединению формулы I, в которой B=-L-E и Rw, Rx, Ry, Rz=Н и L=-(СН2)х-O-. В случае, если кетон формулы (8) содержат защищенную аминогруппу, например, защищенную группой Boc аминогруппу (Boc: трет-бутоксикарбонил), то для получения соединения (20), необходимо провести дополнительную стадию реакции удаления защитной группы, которую можно провести в кислой среде, например, с использованием 2М раствора HCl в диэтиловом эфире в подходящем растворителе, таком как диэтиловый эфир, или с использованием HCl в 1,4-диоксане.
Альдегиды формулы (1) (в которой R1=-ОН), бромпроизводные формулы (12) и кетоны формулы (8) имеются в продаже или их можно получить по хорошо известным методикам синтеза из легко доступных исходных веществ.
Соединения формулы I, в которой B=-L-E и Rw, Rx, Ry, Rz=Н и L=-O-, можно синтезировать, например, общим путем, представленным на схеме 4:

СХЕМА 4: ДХЭ (дихлорэтан), ДМСО (диметилсульфоксид), Pd2(dba)3 (трис(дибензилиденацетон)дипалладий(0)), ТГФ (тетрагидрофуран), Xantphos (4,5-бис(дифенилфосфино)-9,9-диметилксантен).
Альдегиды формулы (1) (в которой R1=Br) вводят в реакцию Хорнера-Уодсворта-Эммонса при таких же условиях, как раскрытые на схеме 2, и получают этилакрилатные производные формулы (2) (в которой R1=Br) которые затем вводят в реакцию циклопропанирования при таких же условиях, как раскрытые на схеме 2 для превращения соединения (2) в соединение (3), и получают (транс)-этилциклопропанкарбоксилатные производные формулы (3), в которой R1=Br. Соединения формулы (3) (в которой R1=Br) превращают в соответствующие производные (транс)-циклопропанкарбоновой кислоты формулы (4) (в которой R1=Br), которые затем превращают в (транс)-циклопропанкарбонилазидные производные формулы (5) (в которой R1=Br) и затем в трет-бутил-(транс)-циклопропилкарбаматные производные формулы (6) (в которой R1=Br) при таких же условиях, как раскрытые на схеме 2. Реакция соединений формулы (6) (в которой R1=Br) с гидроксипроизводными формулы (23) с использованием палладиевого катализатора, такого как трис(дибензилиденацетон)дипалладий(0), Xantphos и основания, такого как трет-бутоксид натрия, в подходящем растворителе, таком как диоксан, приводит к образованию трет-бутил-(транс)-циклопропилкарбаматных производных формулы (24). Удаление защитной группы Boc в кислой среде, например, с использованием 2М раствора HCl в диэтиловом эфире в подходящем растворителе, таком как диэтиловый эфир, приводит к образованию (транс)-циклопропанаминовых производных формулы (25). Восстановительное алкилирование с использованием кетонов формулы (8) при таких же условиях, как раскрытые на схеме 1 или 2, приводит к образованию (транс)-циклопропиламинопроизводных формулы (26), которые соответствуют соединению формулы I, в которой B=-L-E и Rw, Rx, Ry, Rz=Н и L обозначает О. В случае, если кетон формулы (8) содержат защищенную аминогруппу, например, защищенную группой Boc аминогруппу (Boc: трет-бутоксикарбонил), то для получения соединения (26), необходимо провести дополнительную стадию реакции удаления защитной группы, которую можно провести в кислой среде, например, с использованием 2М раствора HCl в диэтиловом эфире в подходящем растворителе, таком как диэтиловый эфир, или с использованием HCl в 1,4-диоксане.
Альдегиды формулы (1) (в которой R1=Br), гидроксипроизводные формулы (25) и кетоны формулы (8) имеются в продаже или их можно получить по хорошо известным методикам синтеза из легко доступных исходных веществ.
Соединения формулы I, в которой B=-L-E и Rw, Rx, Ry, Rz=Н и L=-NH- или -(CH2)x-NH- можно синтезировать, например, общим путем, представленным на схеме 5.

трет-Бутил-(транс)-циклопропилкарбаматные производные формулы (6) (в которой R1=Br), полученные по такой же методике, как раскрытая на схеме 4, превращают в (транс)-циклопропанаминовые производные формулы (7) (в которой R1=Br) путем удаления защитной группы Boc в кислой среде, например, с использованием 2М раствора HCl в диэтиловом эфире в подходящем растворителе, таком как диэтиловый эфир, или с использованием HCl в 1,4-диоксане. Восстановительное алкилирование соединений (7) (R1=Br) с использованием кетонов формулы (8) с использованием таких же условий, как раскрытые выше, например, с использованием триацетоксиборогидрида натрия или борогидрида натрия в качестве восстановительного реагента, в подходящем растворителе, таком как дихлорэтан или метанол, приводит к образованию (транс)-циклопропиламинопроизводных формулы (9) (в которой R1=Br). Реакция соединения формулы (9) (в которой R1=Br) с ди-трет-бутилдикарбонатом в щелочной среде с использованием, например, триэтиламина в подходящем растворителе, таком как тетрагидрофуран, дает содержащие защитную группу Boc производные формулы (27), которые затем вводят в реакцию с аминопроизводными формулы (28) с использованием палладиевого катализатора, такого как трис(дибензилиденацетон)дипалладий(0), Xantphos и основания, такого как трет-бутоксид натрия, в подходящем растворителе, таком как диоксан, и получают трет-бутил-(транс)-циклопропилкарбаматные производные формулы (29). Удаление защитной группы Boc у соединения (29) в вислой среде, например, с использованием 2М раствора HCl в диэтиловом эфире в подходящем растворителе, таком как диэтиловый эфир, приводит к образованию (транс)-циклопропанаминовых производных формулы (30), которые соответствуют соединению формулы I, в которой B=-L-E и Rw, Rx, Ry, Rz=Н и L=-NH- или -(CH2)x-NH-.
Альдегиды формулы (1) (в которой R1=Br), амины формулы (28) и кетоны формулы (8) имеются в продаже или их можно получить по хорошо известным методикам синтеза из легко доступных исходных веществ.
Соединения формулы I, в которой Rw=F, можно синтезировать, например, общим путем, представленным на схеме 6. Эта методика применима для получения соединений, обладающих транс- или цис-конфигурацией относительно циклопропильного кольца (т.е. где группы В-А- и -NH-D находятся в транс- или цис-конфигурации), или их смесей, поскольку использующаяся реакция циклопропанирования дает смесь цис/транс-изомеров, как это представлено с помощью волнистой линии на схеме 6, которую можно использовать без обработки и получить соединения, предлагаемые в настоящем изобретении, в виде смеси цис/транс-изомеров, или, при необходимости, ее можно разделить и получить в конце синтеза необходимые цис- или транс-продукты.

Бромфторирование производных формулы (31) с использованием N-бромсукцинимида и триэтиламинтригидрофторида в подходящем растворителе, таком как дихлорметан, приводит к образованию фторпроизводных формулы (32). Реакция отщепления с использованием основания, такого как, например, трет-бутоксид калия в подходящем растворителе, таком, как например, пентан, дает фторпроизводные формулы (33). Реакция циклопропанирования с использованием этилдиазоацетата и ацетилацетоната меди(II) в качестве катализатора в подходящем растворителе, таком как дихлорметан, дает смеси цис- и транс-производных формулы (34) состава 1:1. На этой стадии диастереоизомеры можно разделить хроматографически или после омыления (проводимого в щелочной среде с использованием, например, NaOH в подходящем растворителе, таком как МеОН) путем перекристаллизации соответствующих карбоновых кислот формулы (35). Разложение Курциуса содержащих защитную группу Boc циклопропиламинов формулы (36) можно провести с использованием основания, такого как, например, триэтиламин, дифенилфосфорилазид и ди-трет-бутилдикарбонат, в подходящем растворителе, таком как, например, трет-бутанол. Удаление защитной группы Boc в кислой среде, например, с использованием 2М раствора HCl в диэтиловом эфире в подходящем растворителе, таком как диэтиловый эфир, или HCl в 1,4-диоксане, приводит к образованию циклопропанаминовых производных формулы (37). Восстановительное алкилирование с использованием кетонов формулы (8) при таких же условиях, как раскрытые на схеме 1 или 2, приводит к образованию циклопропиламинопроизводных формулы (38), которые соответствуют соединению формулы I, в которой Rw=F. В случае, если кетоны формулы (8) содержат защищенную аминогруппу, например, защищенную группой Boc аминогруппу (Boc: трет-бутоксикарбонил), то для получения соединения (38), необходимо провести дополнительную стадию реакции удаления защитной группы, которую можно провести в кислой среде, например, с использованием 2М раствора HCl в подходящем растворителе, таком как диэтиловый эфир, или с использованием HCl в 1,4-диоксане.
Соединения формулы (31) и кетоны формулы (8) имеются в продаже или их можно получить по хорошо известным методикам синтеза из легко доступных исходных веществ.
Соединения формулы I, в которой Rw обозначает Н, фтор или C1-C4-алкил и Rx, Ry, Rz=Н, можно синтезировать, например, общим путем, представленным ниже на схеме 7. Эта методика применима для получения соединений, в которых Rw отличается от водорода, обладающих транс- или цис-конфигурацией относительно циклопропильного кольца (т.е. где группы В-А- и -NH-D находятся в транс- или цис-конфигурации), а также соединений формулы I, в которой Rw, Rx, Ry, Rz=Н (т.е. соединение формулы Iа), обладающих цис-конфигурацией, поскольку использующаяся реакция циклопропанирования дает смесь цис/транс-изомеров, как это представлено с помощью волнистой линии на схеме 7, которую можно разделить и получить искомые цис- или транс-соединения, предлагаемые в настоящем изобретении.

Производные формулы (39) подвергают циклопропанированию с использованием этилдиазоацетата и хлорида меди(1) в качестве катализатора в подходящем растворителе, таком как хлороформ, и получают смеси цис- и транс-производных состава формулы (40) 1:1. Альтернативно, можно использовать содержащий медь катализатор, раскрытый на схеме 6. На этой стадии диастереоизомеры можно разделить хроматографически или после омыления (проводимого в щелочной среде с использованием, например, NaOH в подходящем растворителе, таком как МеОН) путем перекристаллизации соответствующих карбоновых кислот формулы (41). Разложение Курциуса содержащих защитную группу Boc циклопропиламинов формулы (43) можно провести сначала с использованием этилхлорформиата и основания, такого как, например, триэтиламин, в подходящем растворителе, таком как, например, ацетон, и с последующей реакцией с азидом натрия в воде и получить циклопропанкарбонилазидные производные формулы (42). Реакция с трет-бутанолом приводит к образованию содержащих защитную группу Boc циклопропиламинов формулы (43).
Удаление защитной группы Boc в кислой среде, например, с использованием HCl в 1,4-диоксане в подходящем растворителе, таком как 1,4-диоксан, или HCl в Et2O с использованием Et2O в качестве растворителя приводит к образованию циклопропанаминовых производных формулы (44). Восcтановительное алкилирование с использованием кетонов формулы (8) при таких же условиях, как раскрытые на схеме 1, приводит к образованию циклопропиламинопроизводных, предлагаемых в настоящем изобретении, обозначенных на приведенной выше схеме, как соединения формулы (45). В случае, если кетон формулы (8) содержит защищенную аминогруппу, например, защищенную группой Boc аминогруппу (Boc: трет-бутоксикарбонил), то для получения соединения (45), необходимо провести дополнительную стадию реакции удаления защитной группы, которую можно провести в кислой среде, например, с использованием HCl в 1,4-диоксане в подходящем растворителе, таком как 1,4-диоксан, или HCl в Et2O с использованием Et2O в качестве растворителя.
Соединения формулы (39) и кетоны формулы (8) имеются в продаже или их можно получить по хорошо известным методикам синтеза из легко доступных исходных веществ.
Соединения формулы I, в которой B=-L-E и Rw, Rx, Ry, Rz=Н, и L=связь, можно синтезировать, например, общим путем, представленным на схеме 8.

трет-Бутил-(транс)-циклопропилкарбаматные производные формулы (6), полученные по такой же методике, как раскрытая на схеме 4, превращают в (транс)-циклопропанаминовые производные формулы (47) по реакции с производными бороновой кислоты или ее эфиров формулы (46) с использованием подходящего растворителя, такого как ацетонитрил и вода, основания, такого как, например, карбонат калия, и палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий(0). Удаление защитной группы Boc в кислой среде, например, с использованием HCl в 1,4-диоксане в подходящем растворителе, таком как 1,4-диоксан, приводит к образованию (транс)-циклопропанаминовых производных формулы (48). Восстановительное алкилирование с использованием кетонов формулы (8) при таких же условиях, как раскрытые на схеме 1, приводит к образованию (транс)-циклопропиламинопроизводных формулы (49), которые соответствуют соединениям формулы I, в которой B=-L-E и Rw, Rx, Ry, Rz=H и L=связь. Если кетоны формулы (8) содержат защищенную аминогруппу, например, защищенную группой Boc аминогруппу (Boc: трет-бутоксикарбонил), то для получения соединения (49), необходимо провести дополнительную стадию реакции удаления защитной группы. Удаление защитной группы можно провести в кислой среде, например, с использованием HCl в 1,4-диоксане в подходящем растворителе, таком как 1,4-диоксан, или HCl в Et2O с использованием Et2O в качестве растворителя.
Альтернативно, (транс)-циклопропиламинопроизводные формулы (49) можно синтезировать путем удаления группы Boc у трет-бутил-(транс)-циклопропилкарбаматных производных формулы (6) в кислой среде, например, с использованием HCl в подходящем растворителе, таком как 1,4-диоксан, и получить (транс)-циклопропанаминовые производные формулы (7). Восстановительное алкилирование соединений (7) с использованием кетонов формулы (8) при таких же условиях, как раскрытые на схеме 1 или 2, например, с использованием триацетоксиборогидрида натрия или борогидрида натрия в качестве восстановительного реагента в подходящем растворителе, таком как дихлорэтан или метанол, приводит к образованию (транс)-циклопропиламинопроизводных формулы (9). Реакция соединения (9) с ди-трет-бутилдикарбонатом в щелочной среде с использованием, например, триэтиламина в подходящем растворителе, таком как тетрагидрофуран, дает содержащие защитную группу Boc производные формулы (27). Их превращают в (транс)-циклопропанаминовые производные формулы (50) по реакции с имеющимися в продаже производными бороновых кислот или их эфиров формулы (46) с использованием подходящего растворителя, такого как ацетонитрил и вода, основания, такого как, например, карбонат калия, и палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий(0). Удаление защитной группы Boc в кислой среде, например, с использованием HCl в 1,4-диоксане в подходящем растворителе, таком как 1,4-диоксан, или HCl в Et2O с использованием Et2O в качестве растворителя, приводит к образованию (транс)-циклопропанаминовых производных формулы (49).
Альдегиды формулы (1), производные бороновых кислот или их эфиров формулы (46) и кетоны формулы (8) имеются в продаже или их можно получить по хорошо известным методикам синтеза из легко доступных исходных веществ.
Кроме того, некоторые соединения, предлагаемые в настоящем изобретении, можно получить из других соединений формулы I с использованием соответствующих реакций взаимопревращения функциональных групп, содержащихся в соединении формулы I, за одну или несколько стадий с использованием хорошо известных в органическом синтезе реакций при стандартных условиях проведения эксперимента. Указанные превращения можно провести для групп R1, R2 или R3 и они включают, например, замещение первичного или вторичного амина или спирта путем обработки алкилирующим реагентом, восстановление нитрогруппы до аминогруппы, превращение амина в амид, сульфонамид, сульфамид, карбамат или мочевину, катализируемое палладием перекрестное сочетание аминов с арилгалогенидами и т.п. Такие реакции взаимопревращения можно провести для соединения формулы I, а также для любого подходящего синтетического промежуточного продукта, описанного на приведенных выше схемах.
Соли соединения формулы I можно получить в ходе заключительных выделения и очистки соединений, предлагаемых в настоящем изобретении, или их можно получить обычным образом путем обработки соединения формулы I достаточным количеством необходимой кислоты (или основания) и получить соль.
На приведенных выше схемах 2-5 и 8 реакция циклопропанирования, проводимая при раскрытых условиях, всегда приводит к получению рацемической смеси транс-изомеров соединений (3), (11), (15) и (22). Если синтетические процедуры продолжают с использованием полученной таким образом транс-рацемической смеси, то соответствующие соединения формулы I получают в виде смесей транс-изомеров. Аналогичным образом, на схемах 6 и 7 реакция циклопропанирования, проводимая при раскрытых условиях, приводит к получению смеси цис/транс-изомеров соединений (34) и (40). Если синтетическую процедуру продолжают с использованием указанной смеси изомеров, то соответствующие соединения формулы I получают в виде смесей цис/транс-изомеров. При использовании в настоящем изобретении цис- и транс-означает расположение группы -A-B относительно группы -NH-D в циклопропильном кольце.
Если способы получения соединений, предлагаемых в настоящем изобретении, приводят к получению смесей стереоизомеров, то отдельные стереоизомеры соединения формулы I можно получить путем разделения соединения формулы I, полученного в виде смеси стереоизомеров, с использованием хорошо известных методик, таких как образование пар диастереоизомеров путем образования соли с оптически активной кислотой с последующей фракционной кристаллизацией и выделением свободного основания, или путем хиральной препаративной хроматографии. Альтернативно, на различных стадиях описанных выше процедур синтеза и с использованием любой известной методики хирального разделения можно получить оптически чистые или энантиомерно обогащенные синтетические промежуточные продукты, которые затем можно использовать без обработки на следующих стадиях. Предпочтительно, если хиральное разделение проводят для транс-циклопропиламинов формулы (7), (19), (25), (37) или (48). Разделение также можно провести на других стадиях процедуры, например, для соединения формулы (34) или (40). Подходящая методика получения энантиомеров транс-циклопропиламинов (7), (19), (25), (37) и (48) включает взаимодействие транс-замещенного циклопропиламина с хиральным реагентом для перекристаллизации в растворителе (предпочтительно при условиях, которые достаточны для кристаллизации соли хирального реагента для перекристаллизации и транс-замещенного циклопропиламина); и выделение закристаллизованой соли хирального реагента для перекристаллизации и транс-замещенного циклопропиламина; таким образом получают энантиомер транс-N-замещенного циклопропиламина. Подходящим для перекристаллизации хиральным реагентом является S-(+)-миндальная кислота, D-(-)-винная кислота, L-(+)-винная кислота, L-(-)-ди-п-толуоилвинная кислота или R-(-)-миндальная кислота. Подходящими растворителями являются тетрагидрофуран, этанол или их смеси с H2O.
Альтернативно, специалист в данной области техники с помощью хиральной хроматографии может получить оптически чистые или энантиомерно обогащенные конечные соединения (или синтетические промежуточные продукты).
Примеры
Если не указано иное, в соединениях, приведенных во всех примерах в настоящем описании, стереохимическая конфигурация определена химическим названием, указанным для соответствующего соединения, даже если изображенная структура может означать более конкретную конфигурацию. Тем не менее, настоящее изобретение относится к всем стереоизомерам соединений, описанных и определенных в настоящем изобретении. Соответственно, в объем настоящего изобретения входят соединения, описанные в примерах, определенные их химическими названиями, и, кроме того, также соответствующие соединения, обладающие абсолютной конфигурацией, указанной в соответствующих изображенных структурах.
Использовали следующие аббревиатуры:
АЦН: ацетонитрил, АсОН: уксусная кислота, Boc: трет-бутилоксикарбонил, (Вос)2O: ди-трет-бутилдикарбонат, brm: широкий мультиплет, brs: широкий синглет, Cu(acac)2: ацетилацетонат меди(II), d: дублет, ДХЭ: 1,2-дихлорэтан, ДХМ: дихлорметан, ДМФ: N,N-диметилформамид, ДМСО: диметилсульфоксид, ДФФА: дифенилфосфорилазид, Et2O: диэтиловый эфир, EtOAc: этилацетат, ВЭЖХ: высокоэффективная жидкостная хроматография, m: мультиплет, ММЭ: метоксиметиловый эфир, МеОН: метанол, NBS: N-бромсукцинимид, ЯМР: ядерный магнитный резонанс, Pd2(dba)3:
трис(дибензилиденацетон)дипалладий(0), q: квадруплет, Rf: коэффициент удержания, КТ: комнатная температура, s: синглет, t: триплет, ТЭА: триэтиламин, ТГФ: тетрагидрофуран, ТСХ: тонкослойная хроматография, Xantphos: 4,5-бис(дифенилфосфино)-9,9-диметилксантен.
Промежуточный продукт А: 1-(Бензилокси)-4-[(транс)-2-нитроциклопропил]бензол

Триметилсульфоксониййодид (0,62 г, 2,82 ммоля) порциями добавляли к раствору t-BuOK (0,32 г, 2,82 ммоля) в сухом ДМСО (5 мл). Через 10 мин через канюлю добавляли раствор 1-(бензилокси)-4-[(Е)-2-нитровинил]бензола (0,60 г, 2,35 ммоля) в ДМСО (5 мл) и смесь перемешивали при комнатной температуре в течение 6 ч. Реакционную смесь выливали в воду (10 мл) и экстрагировали с помощью Et2O (3×10 мл); органические слои промывали рассолом (2×15 мл), сушили над безводным Na2SO4 и фильтровали. После удаления растворителя оставшееся оранжевое масло очищали с помощью колоночной хроматографии на силикагеле (5% EtOAc/гексаны) и получали 0,16 г 1-(бензилокси)-4-[(транс)-2-нитроциклопропил]бензола [Rf=0,5 (20% EtOAc/гексаны), белое твердое вещество, выход 26%].
Промежуточный продукт В: транс-2-[4-(Бензилокси)фенил]циклопропанамин

Цинковую пыль (1,97 г, 30 молей) при энергичном перемешивании в течение 30 мин небольшими порциями добавляли к раствору 1-(бензилокси)-4-[(транс)-2-нитроциклопропил]бензола (промежуточный продукт A, 0,81 г, 3,0 ммоля) в i-PrOH (25 мл) и HCl (11 мл 2,7 н. водного раствора, 30 ммолей). Через 17 ч смесь фильтровали через слой целита, который промывали с помощью 10 мл метанола. Фильтрат концентрировали и добавляли 10 мл воды, промывали с помощью CH2Cl2 (3×15 мл). Органические слои сушили над безводным Na2SO4 и фильтровали. После удаления растворителя неочищенный продукт очищали с помощью колоночной хроматографии на силикагеле (10% МеОН/CH2Cl2) и получали 0,50 г (транс)-2-[4-(бензилокси)фенил]циклопропанамина [Rf=0,2 (10% МеОН/CH2Cl2), белое твердое вещество, выход 70%].
1H-ЯМР (МеОН, 250 МГц, δ): 7,45-7,27 (m, 5Н, ArH); 6,96 (d, J=8,5 Гц, 2Н, ArH); 6,86 (d, J=8,5 Гц, 2Н, ArH); 5,03 (s, 2Н, CH2); 2,41-2,34 (m, 1Н, СН); 1,86-1,76 (m, 1Н, СН); 0,98-0,85 (m, 2Н, СН2).
Промежуточный продукт C: 4-(Бензилокси)бензальдегид

Карбонат калия (678 г, 4,91 моля) добавляли к раствору 4-гидроксибензальдегида (200 г, 1,63 моля) в ДМФ (2 л), затем при 0°C добавляли бензилбромид (214 мл, 1,80 моля) и перемешивали при КТ в течение 18 ч. После завершения реакции реакционную смесь выливали в воду со льдом (3 л), твердое вещество отфильтровывали и сушили и получали 4-(бензилокси)бензальдегид (230 г, 66%).
Промежуточный продукт D: (Е)-Этил-3-(4-(бензилокси)фенил)акрилат
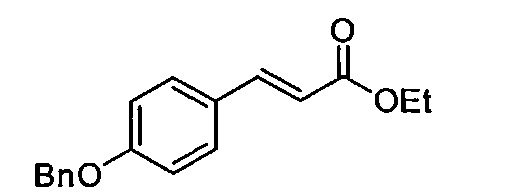
Триэтилфосфоноацетат (259 мл, 1,3 моля) при -5°C по каплям медленно добавляли к раствору трет-бутоксида калия (145 г, 1,29 моля) в сухом ТГФ (2 л) и перемешивали в течение 30-45 мин. Затем при -10°C в течение 15 мин медленно по каплям добавляли раствор 4-(бензилокси)бензальдегида (промежуточный продукт C, 230 г, 1,08 моля) в сухом ТГФ (1,5 л) и перемешивали в течение 30 мин. После завершения реакции реакционную смесь выливали в воду со льдом (1 л) и экстрагировали с помощью EtOAc (2×1,5 л). Объединенные органические экстракты промывали насыщенным раствором NaHCO3 (1 л), водой (1 л), рассолом (1 л), сушили над безводным Na2SO4, фильтровали и выпаривали и получали неочищенный (Е)-этил-3-(4-(бензилокси)фенил)акрилат (290 г, 95%). Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт Е: (транс)-Этил-2-(4-(бензилокси)фенил)циклопропанкарбоксилат

Триметилсульфоксониййодид (224 г, 1,02 моля) при КТ в течение 20 мин порциями добавляли к суспензии NaH (40,8 г, 1,02 моля) в сухом ДМСО (2 л) и перемешивали в течение 1 ч до образования прозрачного раствора. По каплям добавляли раствор (Е)-этил-3-(4-(бензилокси)фенил)акрилата (промежуточный продукт D, 240 г, 0,85 моля) в сухом ДМСО (2 л) и перемешивали при КТ в течение 30 мин. После завершения реакции реакционную смесь выливали в воду со льдом (2 л), экстрагировали с помощью EtOAc (2×1 л). Объединенные органические экстракты промывали водой со льдом (1 л), рассолом (1 л), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (транс)-этил-2-(4-(бензилокси)фенил)циклопропанкарбоксилат (142 г, 58,6%) в виде почти белого твердого вещества. Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт F: (транс)-2-(4-(Бензилокси)фенил)циклопропанкарбоновая кислота

4 н. Раствор NaOH (4 л) при 0°C добавляли к раствору (транс)-этил-2-(4-(бензилокси)фенил)циклопропанкарбоксилата (промежуточный продукт E, 250 г, 0,844 моля) в метаноле (1,2 л) и перемешивали при КТ в течение 4 ч. После завершения реакции растворитель выпаривали, остаток разбавляли водой (1 л), подкисляли 4 н. раствором HCl, экстрагировали с помощью EtOAc (2×2 л). Объединенные органические экстракты промывали водой (1 л), рассолом (1 л), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (транс)-2-(4-(бензилокси)фенил)циклопропанкарбоновую кислоту (190 г, 84%) в виде почти белого твердого вещества. Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт G: (транс)-2-(4-(Бензилокси)фенил)циклопропанкарбонилазид
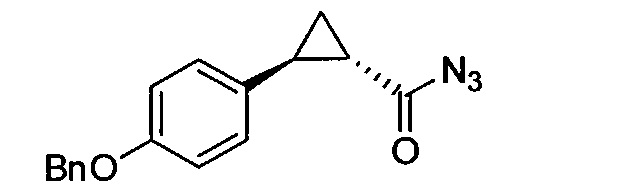
Этилхлорформиат (143 мл, 1,48 моля) при -20°C добавляли к раствору (транс)-2-(4-(бензилокси)фенил)циклопропанкарбоновой кислоты (промежуточный продукт F, 190 г, 0,70 моля), триэтиламина (229 мл, 1,63 моля) в ацетоне (2,8 л) и перемешивали в течение 1 ч, затем добавляли раствор NaN3 (138 г, 2,1 моля) в воде (200 мл) и перемешивали при КТ в течение 30 мин. После завершения реакции растворитель выпаривали, остаток растворяли в EtOAc (2 л), промывали водой (2 л), рассолом (1 л), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (транс)-2-(4-(бензилокси)фенил)циклопропанкарбонилазид (178 г, 85,9%).
Промежуточный продукт Н: трет-Бутил-((транс)-2-(4-(бензилокси)фенил)циклопропил)карбамат

Раствор (транс)-2-(4-(бензилокси)фенил)циклопропанкарбонилазида (промежуточный продукт G, 178 г, 0,64 моля) в трет-бутаноле (2,6 л) нагревали при 90°C в течение 16 ч. После завершения реакции растворитель выпаривали и неочищенный остаток очищали с помощью колоночной хроматографии (SiO2) с использованием смеси EtOAc:петролейный эфир (4:96) и получали трет-бутил-((транс)-2-(4-(бензилокси)фенил)циклопропил)карбамат (78 г, 37,8%) в виде почти белого твердого вещества.
Промежуточный продукт I: (Е)-Этил-3-(6-бромпиридин-3-ил)акрилат

Триэтилфосфоноацетат (26,6 г, 118,8 ммоля) при -5°C медленно по каплям добавляли к смеси трет-бутоксида калия (14,5 г, 129,6 ммоля) с сухим ТГФ (200 мл), перемешивали в течение 20 мин и затем при -5°C медленно по каплям добавляли раствор 6-бромпиридин-3-карбоксальдегида (20 г, 108 ммолей) в сухом ТГФ (100 мл) и перемешивали в течение 30 мин. После завершения реакции реакционную смесь выливали в воду со льдом (350 мл) и экстрагировали с помощью EtOAc (2×300 мл). Объединенные органические экстракты промывали насыщенным раствором NaHCO3 (250 мл), водой (250 мл) и рассолом (250 мл) и сушили над безводным Na2SO4, фильтровали и выпаривали и получали (Е)-этил-3-(6-бромпиридин-3-ил)акрилат (20 г, 72,9%) в виде коричневой жидкости. Его использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт J: (транс)-Этил-2-(6-бромпиридин-3-ил)циклопропанкарбоксилат

Триметилсульфоксониййодид (20,8 г, 94,7 ммоля) при КТ небольшими порциями добавляли к суспензии гидрида натрия (4 г, 170,6 ммоля) в сухом ДМСО (400 мл), перемешивали в течение 1 ч до образования прозрачного раствора. Добавляли раствор (E)-этил-3-(6-бромпиридин-3-ил)акрилата (промежуточный продукт I, 20 г, 78,7 ммоля) в сухом ДМСО (20 мл) и перемешивали в течение 4 ч. После завершения реакции реакционную смесь выливали в воду со льдом (700 мл), экстрагировали с помощью EtOAc (2×350 мл). Объединенные органические экстракты промывали водой (250 мл), рассолом (250 мл) и сушили над безводным Na2SO4, фильтровали и выпаривали и получали (транс)-этил-2-(6-бромпиридин-3-ил)циклопропанкарбоксилат (10 г, 47%) в виде коричневой жидкости.
Промежуточный продукт К: Гидрохлорид (транс)-2-(6-бромпиридин-3-ил)циклопропанкарбоновой кислоты
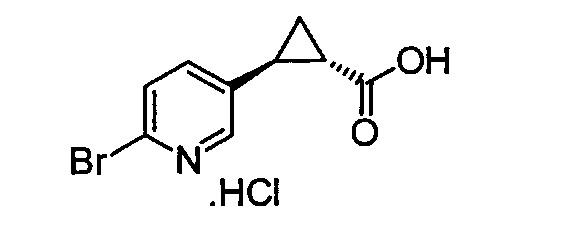
4 н. Раствор NaOH (60 мл) добавляли к раствору (транс)-этил-2-(6-бромпиридин-3-ил)циклопропанкарбоксилата (промежуточный продукт J, 10 г, 37,1 ммоля) в метаноле (100 мл) и реакционную смесь перемешивали при КТ в течение 4 ч. После завершения реакции растворитель выпаривали и остаток разбавляли водой со льдом (250 мл) и подкисляли 4 н. раствором HCl, водный слой экстрагировали с помощью EtOAc (2×350 мл). Объединенные органические экстракты промывали водой (250 мл), рассолом (250 мл) и сушили над безводным Na2SO4, фильтровали и выпаривали и получали гидрохлорид (транс)-2-(6-бромпиридин-3-ил)циклопропанкарбоновой кислоты (5 г, 55,8%) в виде светло-коричневого твердого вещества.
Промежуточный продукт L: (транс)-2-(6-Бромпиридин-3-ил)циклопропанкарбонилазид

Этилхлорформиат (5,8 мл, 62 ммоля) при -5°C добавляли к раствору гидрохлорида (транс)-2-(6-бромпиридин-3-ил)циклопропанкарбоновой кислоты (промежуточный продукт K, 5 г, 20,7 ммоля) и Et3N (14,2 мл, 103,7 ммоля) в ацетоне (100 мл), затем реакционную смесь перемешивали при -5°C в течение 1 ч, затем добавляли раствор NaN3 (2,7 г, 41,4 ммоля) в воде (10 мл) и перемешивали при КТ в течение 30 мин. После завершения реакции растворитель выпаривали в вакууме. Неочищенный остаток растворяли в этилацетате (200 мл), промывали водой (80 мл), рассолом (80 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (транс)-2-(6-бромпиридин-3-ил)циклопропанкарбонилазид (2,5 г, 45,5%) в виде коричневой вязкой жидкости.
Промежуточный продукт М: трет-Бутил-(транс)-2-(6-бромпиридин-3-ил)циклопропилкарбамат

Раствор (транс)-2-(6-бромпиридин-3-ил)циклопропанкарбонилазида (промежуточный продукт L, 2,5 г, 9,36 ммоля) в трет-бутаноле (80 мл) нагревали при 90°C в течение 16 ч. После завершения реакции растворитель выпаривали в вакууме и остаток переносили в воду (100 мл) и экстрагировали с помощью EtOAc (2×100 мл). Объединенные органические экстракты промывали водой (100 мл), рассолом (100 мл) и сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный остаток очищали с помощью колоночной флэш-хроматографии (SiO2) при элюировании смесью EtOAc:гексан (2:8) и получали трет-бутил-(транс)-2-(6-бромпиридин-3-ил)циклопропилкарбамат (1,1 г, 37,5%) в виде светло-желтого твердого вещества.
1Н-ЯМР (CDCl3) δ (част./млн): 1,16 (q, 1Н), 1,23 (квинтет, 1Н), 1,45 (s, 9Н), 2,01 (m, 1Н), 2,69 (m, 1H), 4,88 (br, 1Н), 7,36 (s, 2Н), 8,20 (s, 1Н).
Промежуточный продукт N: (Е)-Этил-3-(4-бромфенил)акрилат

Раствор триэтилфосфоноацетата (13,1 г, 0,0589 моля) при -5°C медленно добавляли (по каплям) к раствору трет-бутоксида калия (6,59 г, 0,0589 моля) в сухом ТГФ (150 мл), перемешивали при такой же температуре в течение 30-45 мин, затем при -5°C в течение 15 мин медленно по каплям добавляли раствор 4-бромбензальдегида (10 г, 0,054 моля), в сухом ТГФ (50 мл), реакционную смесь перемешивали при такой же температуре в течение 30 мин. После завершения реакции по данным ТСХ (тонкослойная хроматография) реакционную смесь выливали в воду со льдом (300 мл), экстрагировали с помощью EtOAc (2×200 мл). Объединенные органические экстракты промывали насыщенным раствором NaHCO3 (200 мл), водой (200 мл), рассолом (200 мл) и сушили над безводным Na2SO4, фильтровали и выпаривали и получали неочищенный (Е)-этил-3-(4-бромфенил)акрилат (10 г, 72%) в виде бледно-зеленой жидкости. Его использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт О: (транс)-Этил-2-(4-бромфенил)циклопропанкарбоксилат

Триметилсульфоксониййодид (5,19 г, 0,0236 моля) при КТ небольшими порциями в течение 20 мин медленно добавляли к суспензии гидрида натрия (0,44 г, 0,0236 моля) в сухом ДМСО (80 мл), перемешивали в течение 1 ч до образования прозрачного раствора. Затем медленно по каплям добавляли раствор (E)-этил-3-(4-бромфенил)акрилата (промежуточный продукт N, 5 г, 0,01968) в сухом ДМСО (20 мл), перемешивали при КТ в течение 30 мин. После завершения реакции по данным ТСХ реакционную смесь выливали в воду со льдом (200 мл), экстрагировали с помощью EtOAc (2×150 мл). Объединенные органические экстракты промывали водой со льдом (2×150 мл), рассолом (150 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (транс)-этил-2-(4-бромфенил)циклопропанкарбоксилат (4 г, 75,9%) в виде зеленой жидкости. Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт P: (транс)-2-(4-Бромфенил)циклопропанкарбоновая кислота

4 н. Раствор NaOH (20 мл) добавляли к раствору (транс)-этил-2-(4-бромфенил)циклопропанкарбоксилата (промежуточный продукт О, 4 г, 0,0149 моля) в метаноле (40 мл) и перемешивали при КТ в течение 2 ч. После завершения реакции по данным ТСХ растворитель выпаривали и остаток разбавляли водой (50 мл), подкисляли 4 н. раствором HCl, образовавшееся твердое вещество отфильтровывали и сушили и получали (транс)-2-(4-бромфенил)циклопропанкарбоновую кислоту (2,59 г, 72%) в виде белого твердого вещества.
Промежуточный продукт Q: (транс)-2-(4-Бромфенил)циклопропанкарбонилазид

Этилхлорформиат (1,9 мл) при -20°C добавляли к раствору (транс)-2-(4-бромфенил)циклопропанкарбоновой кислоты (промежуточный продукт Р, 4 г, 0,0165 моля) и Et3N (2,51 мл, 0,0199 моля) в ацетоне (60 мл), перемешивали при такой же температуре в течение 1 ч, затем добавляли раствор NaN3 (1,3 г, 0,0199 моля) в воде (5 мл) и перемешивали при КТ в течение 30 мин. После завершения реакции по данным ТСХ растворитель выпаривали и неочищенный остаток растворяли в этилацетате (100 мл), промывали водой (40 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (транс)-2-(4-бромфенил)циклопропанкарбонилазид (4 г). Неочищенный остаток использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт R: трет-Бутил-(транс)-2-(4-бромфенил)циклопропилкарбамат

Раствор (транс)-2-(4-бромфенил)циклопропанкарбонилазида (промежуточный продукт Q, 4 г) в трет-бутаноле (40 мл) нагревали при 90°C в течение 16 ч. После завершения реакции по данным ТСХ растворитель выпаривали, остаток выливали в воду (50 мл), экстрагировали с помощью EtOAc (2×50 мл). Объединенные органические экстракты промывали водой (50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2) при элюировании смесью EtOAc: петролейный эфир (2:98) и получали трет-бутил-(транс)-2-(4-бромфенил)циклопропилкарбамат (2,5 г, 48%, суммарный за 2 стадии) в виде белого твердого вещества.
1Н-ЯМР (CDCl3, 250 МГц) δ (част./млн): 1,07-1,19 (m, 2Н), 1,44 (s, 9Н); 2,05-1,94 (m, 1Н); 2,72-2,62 (m, 1Н); 4,85 (br, 1Н); 7,09-6,96 (m, 2Н); 7,44-7,33 (m, 2Н).
Промежуточный продукт S: (E)-Этил-3-(пиридин-3-ил)акрилат

Раствор триэтилфосфоноацетата (66,75 мл, 336,44 ммоля) при -5°C в течение 10 мин по каплям добавляли к раствору трет-бутоксида калия (37,7 г, 280,37 ммоля) в сухом ТГФ (300 мл) и перемешивали при 0°C в течение 30 мин. Затем при 0°C в течение 15 мин по каплям добавляли раствор никотинового альдегида (30 г, 280,37 ммоля) в сухом ТГФ (50 мл) и перемешивали при КТ в течение 2 ч. После завершения реакции реакционную смесь выливали в воду со льдом (150 мл) и экстрагировали с помощью EtOAc (2×300 мл). Объединенные экстракты промывали насыщенным раствором NaHCO3 (200 мл), водой (200 мл), рассолом (200 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали неочищенный жидкий (E)-этил-3-(пиридин-3-ил)акрилат (42 г, 84,67%). Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт Т: (транс)-Этил-2-(пиридин-3-ил)циклопропанкарбоксилат

Триметилсульфоксониййодид (14,90 г, 67,76 ммоля) при КТ в течение 20 мин порциями добавляли к суспензии NaH (2,71 г, 67,76 ммоля) в сухом ДМСО (100 мл) и перемешивали в течение 1 ч до образования прозрачного раствора. По каплям добавляли раствор (E)-этил-3-(пиридин-3-ил)акрилата (промежуточный продукт S, 10 г, 56,47 ммоля) в сухом ДМСО (50 мл) и перемешивали при КТ в течение 20 мин. После завершения реакции реакционную смесь выливали в воду со льдом (200 мл), экстрагировали с помощью EtOAc (2×200 мл). Объединенные органические экстракты промывали водой со льдом (150 мл), рассолом (150 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (транс)-этил-2-(пиридин-3-ил)циклопропанкарбоксилат (4 г, 37,07%) в виде бледно-коричневой жидкости. Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт U: (транс)-2-(Пиридин-3-ил)циклопропанкарбоновая кислота
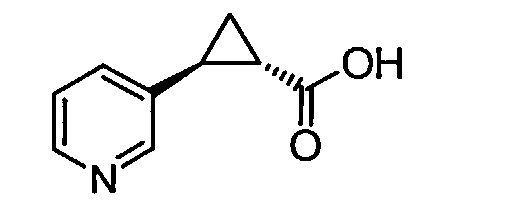
Раствор NaOH (7,116 г в 45 мл H2O, 177,92 ммоля) при 0°C добавляли к раствору (транс)-этил-2-(пиридин-3-ил)циклопропанкарбоксилата (промежуточный продукт T, 17 г, 88,96 ммоля) в метаноле (170 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции растворитель выпаривали, остаток разбавляли водой (50 мл), нейтрализовывали уксусной кислотой и экстрагировали с помощью EtOAc (4×100 мл). Объединенные экстракты промывали водой (100 мл), рассолом (100 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (транс)-2-(пиридин-3-ил)циклопропанкарбоновую кислоту (9 г, 62,06%) в виде почти белого твердого вещества. Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт V: (транс)-2-(Пиридин-3-ил)циклопропанкарбонилазид

Этилхлорформиат (6,89 мл, 71,15 ммоля) при -20°C добавляли к раствору (транс)-2-(пиридин-3-ил)циклопропанкарбоновой кислоты (промежуточный продукт U, 9 г, 55,194 ммоля) и триэтиламина (11,03 мл, 82,79 ммоля) в ацетоне (90 мл) и перемешивали в течение 1 ч, затем добавляли раствор NaN3 (5,38 г, 82,79 ммоля) в воде (25 мл) и перемешивали при КТ в течение 30 мин. После завершения реакции растворитель выпаривали, остаток растворяли в EtOAc (100 мл), промывали водой (2×50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (транс)-2-(пиридин-3-ил)циклопропанкарбонилазид (8,4 г, 81%). Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт W: трет-Бутил-((транс)-2-(пиридин-3-ил)циклопропил)карбамат

Раствор (транс)-2-(пиридин-3-ил)циклопропанкарбонилазида (промежуточный продукт V, 8,4 г, 44,66 ммоля) в трет-бутаноле (85 мл) нагревали при 90°C в течение 16 ч. После завершения реакции растворитель выпаривали и неочищенный остаток очищали с помощью колоночной хроматографии (SiO2) с использованием смеси EtOAc:петролейный эфир (25:75) и получали трет-бутил-(транс)-2-(пиридин-3-ил)циклопропилкарбамат (3,9 г, 37,32%) в виде бесцветной жидкости.
Промежуточный продукт X: (транс)-2-(Пиридин-3-ил)циклопропанамингидрохлорид

HCl в диоксане (10 мл) при 0°C добавляли к раствору трет-бутил-(транс)-2-(пиридин-3-ил)циклопропилкарбамата (промежуточный продукт W, 2 г, 8,541 ммоля) в 1,4-диоксане (10 мл) и перемешивали при КТ в течение 12 ч. После завершения реакции растворитель выпаривали и остаток растирали с диэтиловым эфиром (20 мл), затем с гексаном (20 мл) и получали (транс)-2-(пиридин-3-ил)циклопропанамингидрохлорид (1,2 г, 82,7%).
Промежуточный продукт Y: (E)-Этил-3-(тиазол-5-ил)акрилат

Раствор триэтилфосфоноацетата (11,88 г, 53,03 ммоля) при -5°C по каплям добавляли к раствору трет-бутоксида калия (5,94 г, 53,03 ммоля) в сухом ТГФ (100 мл) и перемешивали в течение 30 мин. Затем при -5°C в течение 15 мин по каплям добавляли раствор тиазол-5-карбальдегида (5 г, 44,19 ммоля) в сухом ТГФ (25 мл) и перемешивали в течение 30 мин. После завершения реакции реакционную смесь выливали в воду со льдом (150 мл), экстрагировали с помощью EtOAc (2×100 мл). Объединенные экстракты промывали насыщенным раствором NaHCO3 (100 мл), водой (100 мл), рассолом (100 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали неочищенный (E)-этил-3-(тиазол-5-ил)акрилат (10 г, 82,3%) в виде белого твердого вещества. Неочищенное вещество использовали на следующей стадии без дополнительной очистки
Промежуточный продукт Z: (транс)-Этил-2-(тиазол-5-ил)циклопропанкарбоксилат

Триметилсульфоксониййодид (14,40 г, 65,49 ммоля) при КТ в течение 20 мин порциями добавляли к суспензии NaH (2,61 г, 108,75 ммоля) в сухом ДМСО (200 мл) и перемешивали в течение 1 ч до образования прозрачного раствора. Затем по каплям добавляли раствор (E)-этил-3-(тиазол-5-ил)акрилата (промежуточный продукт Y, 10 г, 54,57 ммоля) в сухом ДМСО (50 мл) и перемешивали при КТ в течение 30 мин. После завершения реакции реакционную смесь выливали в воду со льдом (100 мл) и экстрагировали с помощью EtOAc (2×100 мл). Объединенные органические экстракты промывали водой (2×50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали транс-этил-2-(тиазол-5-ил)циклопропанкарбоксилат (8 г, 61,9%) в виде красновато-коричневой жидкости. Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт AА: (транс)-2-(Тиазол-5-ил)циклопропанкарбоновая кислота

4 н. Раствор NaOH (40 мл) добавляли к раствору транс-этил-2-(тиазол-5-ил)циклопропанкарбоксилата (промежуточный продукт Z, 8 г, 40,55 ммоля) в метаноле (80 мл) и перемешивали при КТ в течение 4 ч. После завершения реакции растворитель выпаривали, остаток разбавляли водой (50 мл), подкисляли уксусной кислотой и экстрагировали с помощью EtOAc (2×75 мл). Объединенные экстракты промывали водой (50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали транс-2-(тиазол-5-ил)циклопропанкарбоновую кислоту (4 г, 58,30%). Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт AВ: (транс)-2-(Тиазол-5-ил)циклопропанкарбонилазид

Этилхлорформиат (3,34 г, 30,76 ммоля) при -20°C добавляли к раствору транс-2-(тиазол-5-ил)циклопропанкарбоновой кислоты (промежуточный продукт AА, 4 г, 26,3 ммоля) и триэтиламина (3,62 г, 35,50 ммоля) в ацетоне (40 мл), перемешивали при такой же температуре в течение 1 ч. Затем добавляли раствор NaN3 (2,84 г, 47,33 ммоля) в воде (10 мл) и перемешивали при КТ в течение 30 мин. После завершения реакции растворитель выпаривали, неочищенный остаток растворяли в EtOAc (100 мл), промывали водой (50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали транс-2-(тиазол-5-ил)циклопропанкарбонилазид (3 г, 58,7%) в виде коричневой жидкости. Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт AС: трет-Бутил-((транс)-2-(тиазол-5-ил)циклопропил)карбамат

Раствор транс-2-(тиазол-5-ил)циклопропанкарбонилазида (промежуточный продукт AВ, 3 г, 15,44 ммоля) в трет-бутаноле (60 мл) нагревали при 90°C в течение 16 ч. После завершения реакции растворитель выпаривали и остаток переносили в воду (50 мл), экстрагировали с помощью EtOAc (2×50 мл). Объединенные органические экстракты промывали водой (50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2) с использованием смеси EtOAc: петролейный эфир (20:80) и получали трет-бутил-транс-2-(тиазол-5-ил)циклопропилкарбамат (1,1 г, 29,64%) в виде бледно-желтой жидкости.
Промежуточный продукт AD: (транс)-2-(Тиазол-5-ил)циклопропанамингидрохлорид

HCl в диоксане (10 мл) при 15°C добавляли к раствору трет-бутил-транс-2-(тиазол-5-ил)циклопропилкарбамата (промежуточный продукт AС, 1,1 г, 45,83 ммоля) в диоксане (10 мл) и перемешивали при КТ в течение 3 ч. После завершения реакции растворитель выпаривали, остаток растирали с EtOAc и получали транс-2-(тиазол-5-ил)циклопропанамингидрохлорид (600 мг, 74,8%) в виде бледно-желтого твердого вещества.
Промежуточный продукт AЕ: трет-Бутил-((транс)-2-(6-(3-(трифторметил)фенил)пиридин-3-ил)циклопропил)карбамат

Раствор трет-бутил-(транс)-2-(6-бромпиридин-3-ил)циклопропилкарбамата (промежуточный продукт М, 100 мг, 0,32 ммоля), карбонат калия (132 мг, 0,96 ммоля) и 3-трифторметилбензолбороновой кислоты (72 мг, 0,38 ммоля) в смеси CH3CN:H2O (4:1) (10 мл) дегазировали в течение 30 мин. Добавляли тетракис(трифенилфосфин)палладий (37 мг, 0,032 ммоля) и дегазировали в течение 10 мин и реакционную смесь кипятили с обратным холодильником в течение 2 ч. После завершения реакции реакционную смесь выливали в смесь воды со льдом (100 мл), экстрагировали этилацетатом (5×40 мл). Объединенный экстракт промывали водой (70 мл), рассолом (70 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2), с использованием смеси EtOAc: петролейный эфир (1:9) и получали трет-бутил-(транс)-2-(6-(3-(трифторметил)фенил)пиридин-3-ил)циклопропилкарбамат (70 мг, 58,3%) в виде белого твердого вещества.
1Н ЯМР (CDCl3) δ (част./млн): 1,26 (m, 2Н), 1,46 (s, 9Н), 2,10 (m, 1Н), 2,78 (m, 1H), 4,86 (br, 1Н), 7,55 (m, 2Н), 7,65 (t, 2Н), 8,14 (d, 1Н), 8,24 (s, 1Н), 8,54 (s, 1Н). МС (масс-спектрометрия) (М+Н): 379,1.
Промежуточный продукт AF: (транс)-2-(6-(3-(Трифторметил)фенил)пиридин-3-ил)циклопропанаминдигидрохлорид

HCl в диэтиловом эфире (5 мл) при 0°C в течение 10 мин медленно по каплям добавляли к раствору трет-бутил-(транс)-2-(6-(3-(трифторметил)фенил)пиридин-3-ил)циклопропилкарбамата (промежуточный продукт AЕ, 70 мг, 0,185 ммоля) в диэтиловом эфире (10 мл) и затем перемешивали в течение 2 ч. После завершения реакции реакционную смесь фильтровали в инертной атмосфере и промывали гексаном (10 мл), с помощью EtOAc (5 мл) и сушили при пониженном давлении и получали (транс)-2-(6-(3-(трифторметил)фенил)пиридин-3-ил)циклопропанаминдигидрохлорид (50 мг, 86,2%) в виде бледно-желтого порошкообразного вещества.
1Н ЯМР (D2O) δ (част./млн): 1,52 (q, 1Н), 1,63 (квинтет, 1Н), 2,66 (m, 1Н), 3,08 (m, 1Н), 7,72 (t, 1Н), 7,89 (d, 1Н), 7,98 (d, 1Н), 8,09 (s, 1Н), 8,14 (d, 1Н), 8,27 (d, 1Н), 8,61 (s, 1Н). МС (М+Н): 279,1.
Промежуточный продукт AG: трет-Бутил-((транс)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)карбамат

Раствор трет-бутил-(транс)-2-(4-бромфенил)циклопропилкарбамата (промежуточный продукт R, 1 г, 3,2 ммоля), карбоната калия (1,31 г, 9,6 ммоля) и 3-(трифторметил)фенилбороновой кислоты (0,73 г, 3,8 ммоля) в смеси ацетонитрил:вода (4:1) дегазировали в течение 30 мин. Затем добавляли тетракис(трифенилфосфин)палладий (36 мг, 0,032 ммоля), повторно дегазировали в течение 10 мин и реакционную смесь кипятили с обратным холодильником в течение 5 ч. После завершения реакции реакционную смесь выливали в смесь воды со льдом (50 мл) и экстрагировали этилацетатом (2×50 мл). Объединенные экстракты промывали водой (70 мл), рассолом (70 мл), сушили над безводным Na2SO4 и затем фильтровали и выпаривали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2), с использованием смеси EtOAc: петролейный эфир (2:8) и получали трет-бутил-((транс)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)карбамат (0,8 г, 66%) в виде белого твердого вещества.
Промежуточный продукт AН: (транс)-2-(3'-(Трифторметил)-[1,1'-бифенил]-4-ил)циклопропанамингидрохлорид

HCl в диэтиловом эфире (3 мл) при 10°C в течение 10 мин медленно по каплям добавляли к раствору трет-бутил-((транс)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)карбамата (промежуточный продукт AG, 200 мг, 0,53 ммоля) в диэтиловом эфире (5 мл) и затем перемешивали в течение 4 ч. После завершения реакции растворитель выпаривали и остаток растирали с гексаном (5 мл), диэтиловым эфиром (5 мл) и сушили при пониженном давлении и получали (транс)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропанамингидрохлорид (140 мг, 77,8%) в виде белого твердого вещества.
1Н ЯМР (ДМСО-d6) δ (част./млн): 1,27 (q, 1Н), 1,46 (квинтет, 1Н), 2,41 (m, 1Н), 2,86 (m, 1Н), 7,29 (d, 2Н), 7,69 (m, 4Н), 7,96 (m, 2Н), 8,53 (s, 1Н), 8,61 (br, 2Н). МС (М+Н): 278,3.
Промежуточный продукт AI: 4,4-Диметоксициклогексанкарбоксамид

HCl в метаноле (2 мл) при КТ добавляли к раствору этил-4-оксоциклогексанкарбоксилата (5 г, 29,41 ммоля) в метаноле (2 мл), перемешивали при КТ в течение 3 ч и затем добавляли водный раствор аммиака (30 мл) и нагревали в герметизированной пробирке при 90°C в течение 48 ч. После завершения реакции растворитель выпаривали. Неочищенное вещество очищали с помощью колоночной хроматографии (SiO2) и получали 4,4-диметоксициклогексанкарбоксамид (1,2 г, 31,8%) в виде белого твердого вещества.
Промежуточный продукт AJ: 4-Оксоциклогексанкарбоксамид

п-Толуолсульфоновую кислоту (500 мг, 2,90 ммоля) добавляли к раствору 4,4-диметоксициклогексанкарбоксамида (промежуточный продукт AI, 1,2 г, 7,36 ммоля) в смеси ацетон-вода (1:1) (20 мл) и нагревали при 60°C в течение 3 ч. После завершения реакции реакционную смесь выливали в воду со льдом (20 мл), экстрагировали 40% раствора изопропанола в хлороформе (3×30 мл). Объединенные экстракты промывали водой, рассолом, сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный продукт промывали 10% раствором дихлорметана в петролейном эфире и получали 4-оксоциклогексанкарбоксамид (410 мг, 45,55%) в виде белого твердого вещества.
Промежуточный продукт AК: 4-Аминоциклогексанонгидрохлорид

HCl в диоксане (1 мл) при 5°C по каплям добавляли к раствору трет-бутил-4-оксоциклогексилкарбамата (200 мг, 0,938 ммоля) в диоксане (2 мл) и перемешивали при КТ в течение 6 ч. После завершения реакции растворитель выпаривали, твердый остаток растирали с Et2O (10 мл) и сушили и получали 4-аминоциклогексанонгидрохлорид (150 мг, 100%) в виде почти белого твердого вещества. Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт AL: N-(4-Оксоциклогексил)метансульфонамид

Метансульфонилхлорид (1,83 г, 16,07 ммоля) по каплям добавляли к раствору 4-аминоциклогексанонгидрохлорида (промежуточный продукт AК, 1,5 г, 13,39 ммоля) и K2CO3 (6,46 г, 46,87 ммоля) в смеси АЦН-ТГФ (1:1) (30 мл) и затем перемешивали при КТ в течение 16 ч. После завершения реакции растворитель выпаривали, неочищенный остаток разбавляли водой (50 мл), экстрагировали с помощью EtOAc (2×50 мл). Объединенные экстракты промывали водой (50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали N-(4-оксоциклогексил)метансульфонамида (990 мг, 38,6%) в виде белого твердого вещества.
Промежуточный продукт AM: (R)-трет-Бутил-(1-(1,4-диоксаспиро[4.5]декан-8-ил)пирролидин-3-ил)карбамат

1,4-Диоксаспиро[4.5]декан-8-он (0,76 г, 4,88 ммоля) добавляли к раствору (R)-трет-бутилпирролидин-3-илкарбамата (1,0 г, 5,36 ммоля) в ДХЭ (65 мл) и перемешивали в течение 15 мин. Затем при 0°C добавляли триацетоксиборогидрид натрия (1,55 г, 7,32 ммоля) и перемешивали при КТ в течение 16 ч. После завершения реакции реакционную смесь разбавляли с помощью ДХМ (50 мл), промывали насыщенным раствором NaHCO3 (50 мл), водой (50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный остаток очищали с помощью колоночной хроматографии с использованием SiO2 при элюировании смесью гексан: метил-трет-бутиловый эфир (80:20) и получали (R)-трет-бутил-(1-(1,4-диоксаспиро[4.5]декан-8-ил)пирролидин-3-ил)карбамат (1,53 г, 96,8%).
Промежуточный продукт AN: (R)-4-(3-Аминопирролидин-1-ил)циклогексанон

HCl в 1,4 диоксане (5 мл) при 15°C добавляли к раствору (R)-трет-бутил-(1-(1,4-диоксаспиро[4.5]декан-8-ил)пирролидин-3-ил)карбамата (промежуточный продукт AM, 1,53 г, 8,39 ммоля) в диоксане (25 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции добавляли насыщенный раствор Na2CO3 (50 мл), растворитель выпаривали и остаток растирали с Et2O и сушили и получали (R)-4-(3-аминопирролидин-1-ил)циклогексанон (0,61 г, 71,5%).
Промежуточный продукт AО: (R)-трет-Бутил-(1-(4-оксоциклогексил)пирролидин-3-ил)карбамат

Ди-трет-бутилдикарбонат (1,77 г, 9,98 ммоля) добавляли к раствору (R)-4-(3-аминопирролидин-1-ил)циклогексанона (0,61 г, 3,34 ммоля) в воде (6 мл) и перемешивали при КТ в течение 2 ч. После завершения реакции реакционную смесь промывали с помощью ДХМ (50 мл) и AcOEt (50 мл). Затем органический слой промывали с помощью H2O (50 мл) и рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный остаток очищали с помощью колоночной хроматографии с использованием SiO2 при элюировании смесью гексан: метил-трет-бутиловый эфир (80:20) и получали (R)-трет-бутил-(1-(4-оксоциклогексил)пирролидин-3-ил)карбамат (0,23 г, 23,9%).
Промежуточный продукт AР: 1-Этил-3-(4-оксоциклогексил)мочевина

Изоцианатоэтан (237 мг, 3,34 ммоля) и триэтиламин (0,85 мл, 6,68 ммоля) добавляли к раствору 4-аминоциклогексанонгидрохлорида (промежуточный продукт AK, 500 мг, 3,34 ммоля) в толуоле (5 мл) и перемешивали при 110°C в течение 16 ч. После завершения реакции растворитель выпаривали, неочищенный остаток очищали с помощью колоночной хроматографии (SiO2) с использованием смеси EtOAc: петролейный эфир (3:7) и получали 1-этил-3-(4-оксоциклогексил)мочевину (600 мг, 98%) в виде коричневого твердого вещества.
Промежуточный продукт AQ: 4-((2-Метоксиэтокси)метокси)бензальдегид

4-Гидроксибензальдегид (50 г, 409 ммолей) в ТГФ (50 мл) при 0°C в течение 30 мин медленно по каплям добавляли к суспензии гидрида натрия (19,6 г, 817 ммолей) в ТГФ (750 мл) и перемешивали в течение 15 мин, затем при 0°C добавляли 1-(хлорметокси)-2-метоксиэтан (ММЭ-хлорид, 61,10 г, 490 ммолей). Реакционную смесь перемешивали при КТ в течение 30 мин и после завершения реакции выливали в воду со льдом (500 мл) и экстрагировали с помощью EtOAc (2×750 мл). Объединенные органические экстракты промывали водой со льдом (500 мл), рассолом (500 мл), сушили над безводным Na2SO4, фильтровали и концентрировали и получали 4-((2-метоксиэтокси)метокси)бензальдегид (52 г, 50%) в виде бледно-желтой жидкости. Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт AR: (транс)-2-(4-Бромфенил)циклопропанамин

К раствору трет-бутил-транс-2-(4-бромфенил)циклопропилкарбамата (промежуточный продукт R, 10 г, 32,05 ммоля) в 1,4-диоксане (100 мл) при 10°C добавляли HCl в диоксане (50 мл) и перемешивали при КТ в течение 20 ч. После завершения реакции растворитель выпаривали и остаток переносили в воду со льдом, подщелачивали насыщенным водным раствором NaHCO3 и экстрагировали с помощью EtOAc (2×100 мл). Объединенные экстракты промывали водой, рассолом, сушили над безводным Na2SO4, фильтровали и концентрировали и получали (транс)-2-(4-бромфенил)циклопропанамин (6,2 г, 91%). Неочищенный продукт использовали на следующей стадии без дополнительной очистки.
Промежуточный продукт AS: трет-Бутил-(4-(((транс)-2-(4-бромфенил)циклопропил)амино)циклогексил)карбамат

трет-Бутил-4-оксоциклогексилкарбамат (5 г, 23,58 ммоля) добавляли к раствору (транс)-2-(4-бромфенил)циклопропанамина (промежуточный продукт AR, 5 г, 23,58 ммоля) в ДХЭ (100 мл), затем добавляли АсОН (1,41 г, 23,58 ммоля). Смесь перемешивали в течение 5 мин и затем охлаждали до 0°C, затем добавляли триацетоксиборогидрид натрия (8,9 г, 42,45 ммоля). Реакционную смесь перемешивали при КТ в течение 16 ч и после завершения реакции выливали в насыщенный водный раствор NaHCO3 и экстрагировали с помощью ДХМ (2×100 мл). Объединенные экстракты промывали водой (100 мл), рассолом (100 мл), сушили над безводным Na2SO4, фильтровали и концентрировали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2, петролейный эфир/EtOAc 7:3) и получали трет-бутил-(4-(((транс)-2-(4-бромфенил)циклопропил)амино)циклогексил)карбамат (6,2 г, 64%).
Промежуточный продукт AT: трет-Бутил-((транс)-2-(4-бромфенил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамат

Раствор NaOH (1,96 г, 49 ммолей) добавляли к раствору трет-бутил-(4-(((транс)-2-(4-бромфенил)циклопропил)амино)циклогексил)карбамата (промежуточный продукт AS, 5 г, 12,25 ммоля) в смеси 1,4-диоксан/Н2O состава 9:1 (100 мл), затем добавляли Вос-ангидрид (4 г, 18,37 ммоля). Реакционную смесь перемешивали при КТ в течение 16 ч и после завершения реакции выливали в воду (50 мл) и экстрагировали с помощью EtOAc (2×50 мл). Объединенные экстракты промывали водой (50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и концентрировали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2, EtOAc/петролейный эфир 2:8) и получали трет-бутил-((транс)-2-(4-бромфенил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамат (5,2 г, 83%) в виде бесцветной жидкости.
Промежуточный продукт AU: (транс)-2-(6-Бромпиридин-3-ил)циклопропанамин

Это соединение синтезировали по методике, описанной для получения промежуточного продукта AR, и с использованием соответствующего исходного вещества (трет-бутил-((транс)-2-(6-бромпиридин-3-ил)циклопропил)карбамат); получали 1,2 г искомого соединения.
Промежуточный продукт AV: (2-Бром-1-фторэтил)бензол

Триэтиламинтригидрофторид (36,3 мл, 216,01 ммоля) и N-бромсукцинимид (30,75 г, 172,8 ммоля) при 0°C добавляли к раствору стирола (15 г, 144,0 ммоля) в ДХМ (150 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции реакционную смесь нейтрализовывали водным раствором NH4OH (150 мл) и экстрагировали с помощью ДХМ (2×200 мл). Объединенные экстракты промывали 0,1 н. раствором HCl (100 мл), 5% раствором NaHCO3 (100 мл), рассолом (100 мл) и сушили над безводным Na2SO4, фильтровали и концентрировали и получали (2-бром-1-фторэтил)бензол (25 г, 85%) в виде коричневой жидкости.
Промежуточный продукт AW: (1-Фторвинил)бензол

KOtBu (27,77 г, 247,54 ммоля) при 0°C порциями добавляли к раствору (2-бром-1-фторэтил)бензола (промежуточный продукт AV, 25 г, 123,7) в пентане (250 мл). Реакционную смесь перемешивали при кипячении с обратным холодильником в течение 1 ч и после завершения реакции охлаждали до КТ, затем выливали в воду со льдом (150 мл) и экстрагировали гексаном (2×200 мл). Объединенные экстракты промывали 5% раствором NaHCO3 (150 мл), 0,05 М раствором HCl (150 мл), водой (150 мл), рассолом (150 мл) и сушили над безводным Na2SO4, фильтровали и концентрировали и получали (1-фторвинил)бензол (13 г, 86%) в виде бледно-желтой жидкости.
Промежуточный продукт AХ: Этил-2-фтор-2-фенилциклопропанкарбоксилат (цис/транс)

Ацетилацетонат меди (II) (321 мг, 1,23 ммоля) растворяли в сухом ДХМ (10 мл) и перемешивали в течение нескольких минут, затем добавляли несколько капель фенилгидразина. Раствор перемешивали при КТ в течение 10 мин, затем добавляли раствор (1-фторвинил)бензола (промежуточный продукт AW, 5 г, 40,98 ммоля) в сухом ДХМ (50 мл). Смесь кипятили с обратным холодильником, затем в течение 60 мин медленно по каплям добавляли раствор этилдиазоацетата (6,46 мл, 61,47 ммоля) в CH2Cl2. Реакционную смесь перемешивали при кипячении с обратным холодильником в течение 14 ч и после завершения реакции охлаждали до комнатной температуры, разбавляли с помощью ДХМ (50 мл), промывали раствором Na2CO3 (25 мл), водой (25 мл), и рассолом (25 мл), сушили над безводным Na2SO4, фильтровали и концентрировали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2) с использованием смеси ДХМ:гексан (10:90) и получали этил-2-фтор-2-фенилциклопропанкарбоксилат (цис) (540 мг, 6,3%) и этил-2-фтор-2-фенилциклопропанкарбоксилат (транс) (480 мг, 5,6%)
Промежуточный продукт AY: (цис)-Этил-2-фенилциклопропанкарбоксилат

Этилдиазоацетат (10,09 мл, 96,01 ммоля) добавляли к раствору стирола (10 г, 96,01 ммоля) в сухом хлороформе (200 мл), затем добавляли Cu(I)Cl (каталитическое количество) и перемешивали при 60°C в течение 4 ч. После завершения реакции растворитель выпаривали и неочищенный остаток очищали с помощью колоночной хроматографии (SiO2, EtOAc/петролейный эфир 1:9) и получали (цис)-этил-2-фенилциклопропанкарбоксилат (1,7 г, 9,3%) в виде бесцветной жидкости.
Промежуточный продукт AZ: N-(3-Бром-4-метоксифенил)метансульфонамид
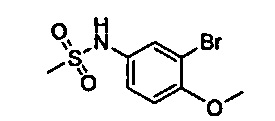
Метансульфонилхлорид (55,82 мл, 0,494 ммоля) добавляли к раствору 3-бром-4-метоксианилина (100 мг, 0,494 ммоля) в пиридине (1 мл) при 0°C и перемешивали при КТ в течение 2 ч. После завершения реакции реакционную смесь выливали в воду со льдом (10 мл) и экстрагировали с помощью EtOAc (2×15 мл). Объединенные экстракты промывали водой (3×10 мл), рассолом (15 мл) и сушили над безводным Na2SO4 фильтровали, и выпаривали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2) с использованием смеси EtOAc: гексан (3:7) и получали N-(3-бром-4-метоксифенил)метансульфонамид (137 мг, 99%) в виде белого твердого вещества
Промежуточный продукт ВА: N-(4-Метокси-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)метансульфонамид

Раствор N-(3-бром-4-метоксифенил)метансульфонамида (промежуточный продукт AZ, 136 мг, 0,485 ммоля), бис(пинаколято)дибора (147 мг, 0,58 ммоля) и КОАс (87,3 мг, 0,888 ммоля) в диоксане (5,5 мл) дегазировали в течение 30 мин, затем добавляли PdCl2(dppf)2 (17,7 мг, 0,020 ммоля) и реакционную смесь нагревали при 100°C в течение 3 ч. После завершения реакции реакционную смесь выливали в воду (10 мл), экстрагировали с помощью EtOAc (2×15 мл). Объединенные экстракты промывали водой (10 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2, EtOAc: петролейный эфир 1:9) и получали N-(4-метокси-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил) фенил)метансульфонамид (100 мг, 63%) в виде белого твердого вещества.
Промежуточный продукт BB: 3-Метокси-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензонитрил

Это соединение синтезировали по методике, описанной для получения промежуточного продукта ВА, и с использованием соответствующего исходного вещества (3-бром-5-метоксибензонитрил); получали 1,4 г искомого соединения в виде белого твердого вещества.
Промежуточные продукты BC ((транс)-этил-2-(5-бромтиофен-2-ил)циклопропанкарбоксилат), BD ((транс)-этил-2-(2-бромтиазол-5-ил)циклопропанкарбоксилат) и BE ((транс)-этил-2-(4-((2-метоксиэтокси)метокси)фенил)циклопропанкарбоксилат):
Эти промежуточные продукты синтезировали по такой же методике, как описанная для получения промежуточного продукта Т (никотиновый альдегид вводили в реакцию Хорнера-Уодсворта-Эммонса и получали промежуточный продукт S, который затем вводили в реакцию циклопропанирования и получали промежуточный продукт Т), с использованием в качестве исходных веществ соответствующих имеющихся в продаже альдегидов, приведенных ниже:

Промежуточные продукты BF ((транс)-2-(5-бромтиофен-2-ил)циклопропанамин), BG ((транс)-2-(2-бромтиазол-5-ил)циклопропанамин), ВН (4-((транс)-2-аминоциклопропил)фенол), BI ((цис)-2-фтор-2-фенилциклопропанамин), BJ ((транс)-2-фтор-2-фенилциклопропанамин)) и ВК ((цис)-2-фенилциклопропанамин):
Эти промежуточные продукты синтезировали по такой же методике, как описанная для получения промежуточного продукта X из промежуточного продукта Т (проводили гидролиз (транс)-этил-2-(пиридин-3-ил)циклопропанкарбоксилата и получали промежуточный продукт U, который затем вводили в реакцию Курциуса и получали сначала промежуточный продукт V и затем промежуточный продукт W, и, в заключение, удаляли защитную группу Вое и получали промежуточный продукт X), с использованием соответствующих промежуточных продуктов.
Промежуточные продукты BF, ВН и ВК получали в виде гидрохлоридов.
Промежуточные продукты BG, BI и ВJ обрабатывали кислотой для проведения стадии удаления защитной группы Воc, затем подщелачивали насыщенным водным раствором NaHCO3 и получали свободные основания.

Промежуточный продукт BL: трет-Бутил-((транс)-2-(4-гидроксифенил)циклопропил)карбамат

K2CO3 (20,36 г, 147,56 ммоля) и (Вос)2O (16,8 мл, 70,27 ммоля) добавляли к раствору 4-((транс)-2-аминоциклопропил)фенолгидрохлорида (промежуточный продукт BI, 13 г, 70,27 ммоля) в 1,4-диоксане (78 мл) и воде (195 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции реакционную смесь выливали в воду (300 мл) и экстрагировали с помощью EtOAc (2×200 мл). Объединенные экстракты промывали водой (75 мл), рассолом (75 мл), сушили над безводным Na2SO4, фильтровали и концентрировали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2, EtOAc/петролейный эфир 3:7) и получали трет-бутил-((транс)-2-(4-гидроксифенил)циклопропил)карбамат (14 г, 80%) в виде густой вязкой коричневой жидкости.
Промежуточные продукты ВМ (трет-бутил-(4-(((транс)-2-(6-бромпиридин-3-ил)циклопропил)амино)циклогексил)карбамат) BN (трет-бутил-(4-(((транс)-2-(5-бромтиофен-2-ил)циклопропил)амино)циклогексил)карбамат) и ВО (трет-бутил-(4-(((транс)-2-(2-бромтиазол-5-ил)циклопропил)амино)циклогексил)карбамат):
Эти промежуточные продукты синтезировали по такой же методике, как описанная для получения промежуточного продукта AS из промежуточного продукта AR (восстановительное алкилирование), с использованием в качестве исходных веществ соответствующих промежуточных продуктов.

Промежуточные продукты BP (трет-бутил-((транс)-2-(6-бромпиридин-3-ил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамат) и BQ (трет-бутил-((транс)-2-(2-бромтиазол-5-ил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамат):
Эти промежуточные продукты синтезировали по такой же методике, как описанная для получения промежуточного продукта AT из промежуточного продукта AS (удаление защитной группы Boc), с использованием в качестве исходных веществ соответствующих промежуточных продуктов.
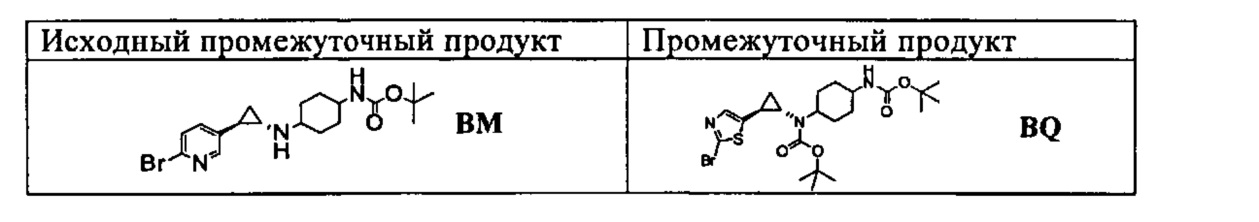

Промежуточный продукт BR: трет-Бутил-((транс)-2-(3'-амино-[1,1'-бифенил]-4-ил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамат
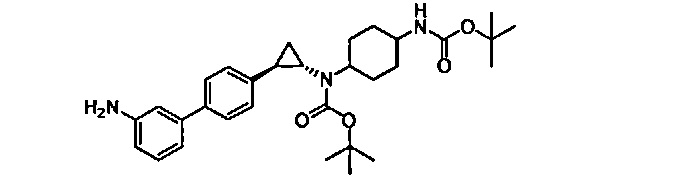
Раствор ((транс)-2-(4-бромфенил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамата (промежуточный продукт AT, 1,5 г, 3,32 ммоля), (3-аминофенил)бороновой кислоты (484 мг, 2,35 ммоля) и K2CO3 (805 мг, 5,88 ммоля) в смеси АЦН-H2O состава 8:2 (20 объемов) дегазировали в течение 15 мин, затем добавляли Pd(PPh3)4 (68 мг, 0,06 ммоля). Реакционную смесь перемешивали при 90°C в течение 16 ч и после завершения реакции выливали в воду со льдом и экстрагировали с помощью EtOAc (2×50 мл). Объединенные экстракты промывали водой (50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и концентрировали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2, EtOAc:петролейный эфир 3:7) и получали трет-бутил-((транс)-2-(3'-амино-[1,1'-бифенил]-4-ил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамат (1,23 г, 71%) в виде смолообразного твердого вещества.
Промежуточные продукты BS (N-(4'-((транс)-2-аминоциклопропил)-6-метокси-[1,1'-бифенил]-3-ил)метансульфонамид), ВТ (3-(5-((транс)-2-аминоциклопропил)пиридин-2-ил)-5-метоксибензонитрил) и BU (5-(5-((транс)-2-аминоциклопропил)пиридин-2-ил)-2-метилфенол):
Эти промежуточные продукты синтезировали по такой же методике, как описанная для получения промежуточного продукта R из промежуточного продукта АН (проводили реакцию сочетания Судзуки промежуточного продукта R с 3-(трифторметил)фенилбороновой кислотой и получали промежуточный продукт AG и затем удаляли защитную группу Вое и получали промежуточный продукт R), с использованием в качестве исходных веществ соответствующих промежуточных продуктов и имеющихся в продаже производных бороновых кислот или их эфиров, приведенных ниже.
Эти промежуточные продукты получали в виде гидрохлоридов.
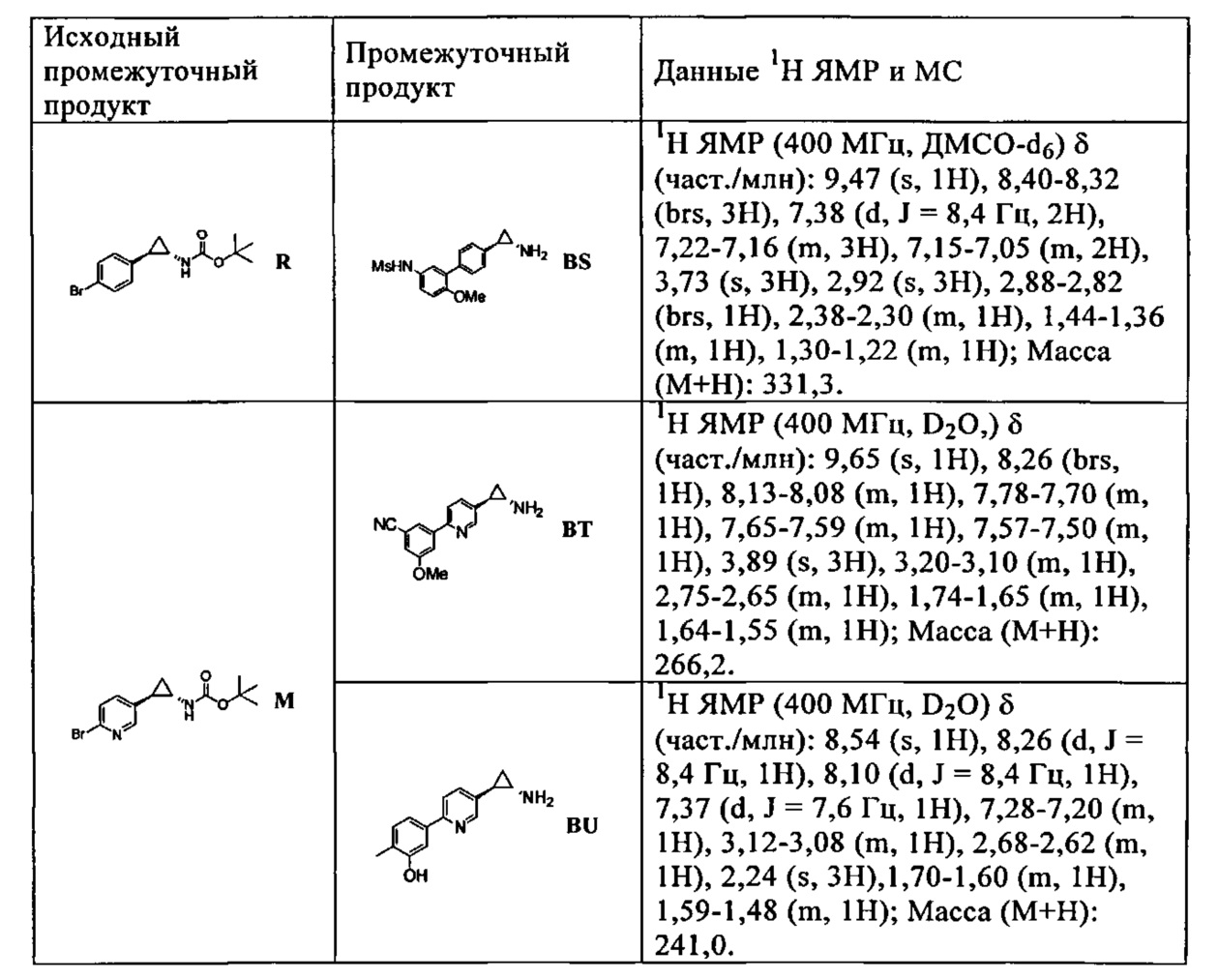
Пример 1: N1-((транс)-2-Фенилциклопропил)циклогексан-1,4-диаминдигидрохлорид
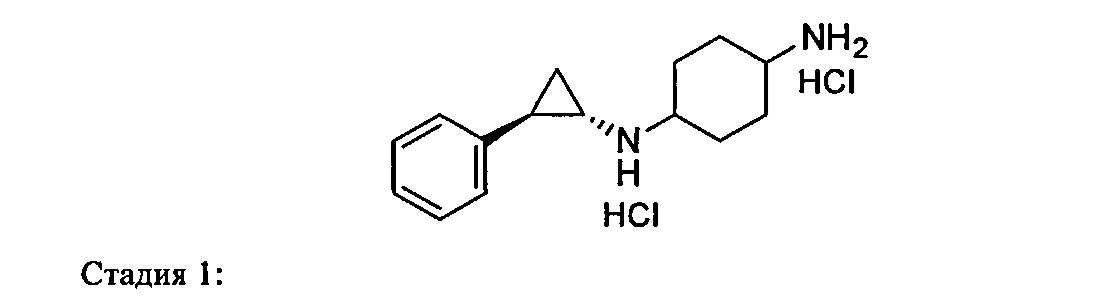
Уксусную кислоту (586 мг, 9,77 ммоля) добавляли к раствору транс-2-фенилциклопропанамина (1,3 г, 9,77 ммоля) и трет-бутил-4-оксоциклогексилкарбамата (2,08 г, 9,77 ммоля) в ДХЭ (26 мл) и перемешивали в течение 5 мин. Затем при 0°C добавляли триацетоксиборогидрид натрия (3,72 г, 17,5 ммоля) и перемешивали при КТ в течение 5 ч. После завершения реакции реакционную смесь разбавляли с помощью ДХМ (50 мл), водой (50 мл), рассолом (50 мл) сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный остаток очищали с помощью колоночной хроматографии с использованием SiO2 при элюировании смесью EtOAc:петролейный эфир (1:9) и получали трет-бутил-4-(транс-2-фенилциклопропиламино)циклогексилкарбамат (2,5 г, 77,6%) в виде бледно-желтой жидкости.
Стадия 2:
HCl в 1,4-диоксане (10 мл) добавляли к раствору трет-бутил-4-(транс-2-фенилциклопропиламино)циклогексилкарбамата (2,45 г, 7,57 ммоля) в диоксане (25 мл) при 15°C и перемешивали при КТ в течение 16 ч. После завершения реакции растворитель выпаривали и остаток растирали с Et2O и сушили и получали N1-((транс)-2-фенилциклопропил)циклогексан-1,4-диаминдигидрохлорид (1,5 г, 67,5%) в виде почти белого твердого вещества.
1Н ЯМР (400 МГц, ДМСО-d6) δ (част./млн): 9,66-9,56 (brd, 2Н), 8,15-8,11 (d, 3Н), 7,32-7,16 (m, 5Н), 3,33 (brs, 1Н), 3,24-3,16 (m, 1Н), 2,99 (brs, 1Н), 2,91 (brs, 1Н), 2,55 (brs, 1H), 2,17 (brs, 1Н), 2,0 (m, 1Н), 1,96-1,75 (m, 4Н), 1,63-1,43 (m, 2Н), 1,4-1,3 (m, 1Н), 1,29-1,26 (m, 1Н); Масса (М+Н): 231,34.
Полученный выше N1-((транс)-2-фенилциклопропил)циклогексан-1,4-диамин представлял собой смесь 4 изомеров, которые соответствовали комбинации двух разных (транс)-конформаций относительно циклопропильного кольца (которые представляли собой (1R,2S) и (1S,2R) соответственно) при цис- и транс-конформации относительно циклогексанового кольца. Синтез каждого из этих отдельных изомеров проводили следующим образом:
Пример 2: (цис)-N1-((1S,2R)-2-Фенилциклопропил)циклогексан-1,4-диамингидрохлорид
Стадия 1:
К раствору транс-2-фенилциклопропанамина (1,1 г, 8,2 ммоля) в EtOH (6 мл) при 0°C добавляли 0-(-)-винную кислоту (1,24 г, 8,2 ммоля) и перемешивали при КТ в течение 1 ч. После завершения реакции твердое вещество отфильтровывали и сушили и получали транс-2-фенилциклопропанамин в виде тартрата (2,15 г, 91,8%). Соль переносили в смесь изопропанол (ИПС): вода (3:1) (20 мл) и перемешивали при 70°C в течение 2 ч. Прозрачному раствору давали охладиться до КТ. Отделившееся твердое вещество собирали фильтрованием, переносили в воду (50 мл), подщелачивали раствором NaOH и экстрагировали с помощью EtOAc (2×50 мл). Объединенные экстракты промывали водой (50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (1S,2R)-2-фенилциклопропанамин (510 мг, 46,3%).
Стадия 2:
К раствору (1S,2R)-2-фенилциклопропанамина (450 мг, 3,38 ммоля), трет-бутил-4-оксоциклогексилкарбамата (792 мг, 3,72 ммоля) и уксусной кислоты (202 мг, 3,38 ммоля) в ДХЭ (10 мл) при 0°C добавляли триацетоксиборогидрид натрия (1,29 г, 6,09 ммоля) и перемешивали при КТ в течение 3 ч. После завершения реакции растворитель выпаривали, неочищенный остаток переносили в воду (25 мл), подщелачивали с помощью NaHCO3 экстрагировали с помощью EtOAc (2×25 мл). Объединенные экстракты промывали водой (25 мл), рассолом (25 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенное вещество очищали с помощью колоночной хроматографии с использованием SiO2 при элюировании смесью EtOAc: петролейный эфир (3:7) и получали трет-бутил-((транс)-4-(((1S,2R)-2-фенилциклопропил)амино)циклогексил)карбамат (210 мг, 18,8%) и трет-бутил-((цис)-4-(((1S,2R)-2-фенилциклопропил)амино)циклогексил)карбамат (280 мг, 25,1%).
Стадия 3:
К раствору трет-бутил-((цис)-4-(((1S,2R)-2-фенилциклопропил)амино)циклогексил)карбамата (190 мг, 0,57 ммоля) в 1,4-диоксане (2 мл) при 10°C по каплям добавляли HCl в 1,4 диоксане (2 мл) и перемешивали при КТ в течение 16 ч. После завершения растворитель выпаривали, твердое вещество перемешивали с Et2O, отфильтровывали и сушили и получали (цис)-N1-((1S,2R)-2-фенилциклопропил)циклогексан-1,4-диамингидрохлорид (110 мг, 71,89%) в виде почти белого твердого вещества.
1H ЯМР (400 МГц, ДМСО-d6) δ: 9,5 (brs, 2Н), 8,12 (brs, 3Н), 7,17-7,32 (m, 5Н), 3,24 (brs, 2Н), 2,98 (brs, 1Н), 2,57 (brs, 1Н), 1,98-1,74 (m, 8Н), 1,61 (brs, 1Н), 1,28 (m, 1Н); Масса (М+Н): 231,27; : +57,50 (С=0,54% в ДМСО).
Пример 3: (транс)-N1-((1S,2R)-2-Фенилциклопропил)циклогексан-1,4-диамингидрохлорид
Это соединение синтезировали по такой же методике, как описанная в примере 2, но защитную группу Воc удаляли у трет-бутил-((транс)-4-(((1S,2R)-2-фенилциклопропил)амино)циклогексил)карбамата, который получали на стадии 3 в качестве промежуточного продукта; получали 120 мг (выход=59,4%) соединения в виде почти белого твердого вещества.
1Н ЯМР (400 МГц, ДМСО-d6) δ (част./млн): 9,52 (brs, 2Н), 8,03 (brs, 3Н), 7,33-7,16 (m, 5Н), 3,17 (brs, 1Н), 2,9 (brm, 2Н), 2,16 (brs, 2Н), 2,03 (brd, 2Н), 1,54-1,25 (m, 6Н); Масса (М+Н): 231,28; : +67,04° (С=0,53% в ДМСО).
Пример 4: (цис)-N1-((1R,2S)-2-Фенилциклопропил)циклогексан-1,4-диамингидрохлорид
Стадия 1:
К раствору транс-2-фенилциклопропанамина (неочищенный, выделенный из маточных растворов после проведения реакции, описанной на стадии 1 примера 2) (0,8 г, 6,01 ммоля) в EtOH (5,4 мл) при 0°C добавляли L-(+)-винную кислоту (0,90 г, 6,01 ммоля) и перемешивали при КТ в течение 1 ч. После завершения реакции твердое вещество отфильтровывали и сушили и получали транс-2-фенилциклопропанамин в виде тартрата (1,5 г, 88,2%). Соль переносили в смесь ИПС: вода (3:1) (15 мл) и перемешивали при 70°C в течение 2 ч. Прозрачному раствору давали охладиться до КТ. Отделившееся твердое вещество собирали фильтрованием, переносили в воду (50 мл), подщелачивали раствором NaOH и экстрагировали с помощью EtOAc (2×50 мл). Объединенные экстракты промывали водой (50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (1R,2S)-2-фенилциклопропанамин (320 мг).
Стадия 2:
К раствору (1R,2S)-2-фенилциклопропанамина (280 мг, 1,21 ммоля), трет-бутил-4-оксоциклогексилкарбамата (309 мг, 1,45 ммоля) и уксусной кислоты (72 мг, 1,21 ммоля) в ДХЭ (8 мл) при 0°C добавляли триацетоксиборогидрид натрия (461 мг, 2,17 ммоля) и перемешивали при КТ в течение 3 ч. После завершения реакции растворитель выпаривали, неочищенный остаток переносили в воду (25 мл), обрабатывали с помощью NaHCO3 и экстрагировали с помощью EtOAc (2×25 мл). Объединенные экстракты промывали водой (25 мл), рассолом (25 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенное вещество очищали с помощью колоночной хроматографии с использованием SiO2 при элюировании смесью EtOAc:петролейный эфир (3:7) и получали трет-бутил-((цис)-4-(((1R,2S)-2-фенилциклопропил)амино)циклогексил)карбамат (180 мг, 25,35%) и трет-бутил-((транс)-4-(((1R,2S)-2-фенилциклопропил)амино)циклогексил)карбамат (210 мг, 29,5%).
Стадия 3:
К раствору трет-бутил-((цис)-4-(((111,28)-2-фенилциклопропил)амино)циклогексил)карбамата (160 мг, 0,48 ммоля) в 1,4-диоксане (2 мл) при 10°C по каплям добавляли HCl в 1,4-диоксане (2 мл) и перемешивали при КТ в течение 16 ч. После завершения растворитель выпаривали, твердое вещество перемешивали с Et2O, отфильтровывали и сушили и получали (цис)-N1-((1R,2S)-2-фенилциклопропил)циклогексан-1,4-диамингидрохлорид (80 мг, 58,3%) в виде почти белого твердого вещества.
1Н ЯМР (400 МГц, ДМСО-d6) δ: 9,54 (brs, 2Н), 8,14 (brs, 3Н), 7,35-7,15 (m, 5Н), 3,33 (brs, 1Н), 3,25 (brs, 2Н), 2,62-2,55 (m, 1Н), 2,03-1,67 (m, 8Н), 1,63-1,57 (m, 1Н), 1,28 (q, 1Н); Масса (М+Н): 231,27; : -65,70° (С=0,5% в ДМСО).
Пример 5: (транс)-N1-((1R,2S)-2-фенилциклопропил)циклогексан-1,4-диамингидрохлорид
Это соединение синтезировали по такой же методике, как описанная в примере 4, но на стадии 3 защитную группу Boc удаляли у трет-бутил-((транс)-4-(((1R,2S)-2-фенилциклопропил)амино)циклогексил)карбамата; получали 95 мг (выход=50,8%) соединения в виде почти белого твердого вещества.
1H ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ (част./млн): 7,32 (t, J=7,2 Гц, 2Н), 7,24 (t, J=7,2 Гц, 1Н), 7,17 (d, J=8 Гц, 2Н), 3,26-3,18 (m, 1Н), 3,05-2,89 (m, 2Н), 2,51-2,42 (m, 1Н), 2,22-2,10 (m, 2Н), 2,08-1,98 (m, 2Н), 1,57-1,28 (m, 6Н); Масса (М+Н): 231,25; : -60,19° (С=0,54% в ДМСО).
С использованием альтернативной методики (транс)-N1-((1R,2S)-2-фенилциклопропил)циклогексан-1,4-диамин получали следующим образом:
При энергичном перемешивании к раствору (1R,2S)-2-фенилциклопропанамина (0,752 г 5,64 ммоля) в метаноле (10 мл) при комнатной температуре (22-25°C) добавляли молекулярные сита (1,0 г), затем при 10°C добавляли трет-бутил-4-оксоциклогексилкарбамат (1,07 г, 5,0 ммоля) и перемешивали в течение 5 мин. К реакционной смеси при 0-5°C добавляли уксусную кислоту (0,028 мл, 0,5 ммоля) и перемешивали при комнатной температуре в течение 3 ч. Реакционную смесь охлаждали до -25 - -30°C и при такой же температуре порциями добавляли борогидрид натрия (0,229 г, 6,02 ммоля). Реакционную смесь перемешивали в течение 3 ч, позволяя температуре реакционной смеси повыситься до комнатной температуры.
За протеканием реакции следили с помощью ТСХ (EtOAc/гексан 8:2). После завершения реакции неорганические вещества отфильтровывали через целит. Фильтрат выпаривали и неочищенный остаток переносили в смесь воды (20 мл) и ДХМ (20 мл) и подщелачивали 5% водным раствором NaOH (до pH 10). Слой, содержащий ДХМ, отделяли и водный слой повторно экстрагировали с помощью ДХМ (20 мл). Объединенные органические экстракты промывали водой (20 мл) и 10% раствором рассола (20 мл), сушили над безводным сульфатом натрия, фильтровали и выпаривали полностью. Неочищенный продукт очищали путем перемешивания в 2% растворе EtOAc в гексане при комнатной температуре в течение 2 ч и получали трет-бутил-4-((1R,2S)-2-фенилциклопропиламино)циклогексилкарбамат в виде почти белого твердого вещества (0,90 г, 54%).
При энергичном перемешивании к раствору трет-бутил-4-((1R,2S)-2-фенилциклопропиламино)циклогексилкарбамата (0,8 г, 2,42 ммоля) в 1,4-диоксане (10 мл) при 10-15°C медленно добавляли 15% раствор HCl в диоксане (8 мл) и перемешивали при комнатной температуре в течение 20 ч. За протеканием реакции следили с помощью ВЭЖХ. После завершения реакции растворитель удаляли при пониженном давлении. Остаток суспендировали в диизопропиловом эфире (15 мл) и перемешивали при комнатной температуре в течение 1 ч, фильтровали и сушили в вакууме. Неочищенный продукт дополнительно очищали путем перемешивания в диизопропиловом эфире (15 мл) при комнатной температуре в течение 2 ч. Твердое вещество отфильтровывали и получали (транс)-N1-((1R,2S)-2-фенилциклопропил)циклогексан-1,4-диаминдигидрохлорид (0,57 г, 77%) (содержание дигидрохлорида определяли путем аргентометрии) в виде почти белого твердого вещества.
1Н ЯМР (400 МГц, ДМСО-d6) δ (част./млн): 9,74 (bs, 2Н), 8,18 (bs, 3H), 7,30 (m, 2Н), 7,24 (m, 1Н), 7,18 (m, 2Н), 3,15 (bs, 1Н), 2,94 (m, 2Н), 2,56 (m, 1Н), 2,18 (m, 2Н), 2,04 (m, 2Н), 1,58 (m, 3H), 1,44 (m, 2Н), 1,26 (m, 1Н); Масса (М+Н): 231,5.
Приведенные ниже соединения можно синтезировать по методике, описанной для получения соединения примера 1, с использованием соответствующих промежуточных продуктов. Стадию 2 проводили только в том случае, если промежуточный продукт, который использовали в реакции восстановительного алкилирования (стадия 1), содержал защитную группу Воc (трет-бутилоксикарбонил).
Пример 6: N1-((транс)-2-(Тиазол-5-ил)циклопропил)циклогексан-1,4-диамингидрохлорид

1Н ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ (част./млн): 8,95 (s, 1Н), 7,75 (s, 1Н), 3,3-3,18 (m, 1Н), 3,1-2,9 (m, 2Н), 2,85-2,72 (m, 1Н), 2,25-1,98 (brm, 3H), 1,7-1,35 (brm, 5Н); Масса (М+Н): 238,19.
Пример 7: N1-((транс)-2-(Пиридин-3-ил)циклопропил)циклогексан-1,4-диамингидрохлорид

1ЯМР (400 МГц, D2O) δ (част./млн): 8,64 (2Н, d), 8,32 (1H, d), 7,98 (1Н, t), 3,37 (2Н, m), 3,22 (2Н, m), 2,77-2,72 (1Н, m), 2,25-2,12 (3H, m), 1,92-1,46 (7Н, m), Масса (М+Н): 232,34.
Пример 8: N1-((транс)-2-(6-(3-(Трифторметил)фенил)пиридин-3-ил)циклопропил)циклогексан-1,4-диамингидрохлорид

1Н ЯМР (400 МГц, D2O) δ (част./млн): 8,60 (s, 1Н), 8,20-8,00 (m, 3H), 7,90 (d, J=12 Гц, 1Н), 7,76-7,72 (t, J=8 Гц, 1Н), 7,60-7,40 (br, 1Н), 3,60-3,40 (m, 2Н), 3,20 (m, 1Н), 2,70 (m, 1H), 2,30 (m, 1Н), 2,20-2,00 (m, 2Н), 1,97-1,67 (m, 5Н), 1,65 (m, 1Н), 1,60-1,40 (m, 1Н); Масса (М+Н): 376,3.
Пример 9: N1-((транс)-2-(3'-(Трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамингидрохлорид

1Н ЯМР (400 МГц, ДМСО-d6) δ: 9,65-9,48 (brd, 2Н), 8,1 (s, 3H), 7,95 (m, 2Н), 7,7 (m, 4Н), 7,3 (d, 2Н), 3,2 (brd, 1Н), 2,9 (brd, 2Н), 2,52 (m, 1Н), 2,2 (brd, 2Н), 2,05 (brd, 2Н), 1,86-1,76 (m, 2Н), 1,6-1,25 (m, 5Н); Масса (М+Н): 375,29.
Пример 10: N1-((транс)-2-(4-(Бензилокси)фенил)циклопропил)циклогексан-1,4-диамингидрохлорид

1H ЯМР (400 МГц, ДМСО-d6) δ: 9,64-9,45 (brd, 2Н), 8,2-8,05 (brd, 3H), 7,48-7,3 (m, 5Н), 7,15 (d, 2Н), 6,95 (d, 2Н), 5,08 (s, 2Н), 3,2-3,15 (brs, 1Н), 2,9 (brs, 1Н), 2,82 (brs, 1H), 2,45 (brs, 1Н), 2,18 (brd, 2Н), 2,05 (brd, 2Н), 1,9 (brs, 1Н), 1,58-1,27 (m, 4Н),1,22 (m, 1Н); Масса (М+Н): 337,31.
Пример 11: 4-(((транс)-2-(6-(3-(Трифторметил)фенил)пиридин-3-ил)циклопропил)амино)циклогексанол

1ЯМР ЯМР (400 МГц, D2O) δ (част./млн): 8,76 (s, 1Н), 8,37 (brs, 1Н), 8,32-8,26 (m, 2Н), 8,16 (m, 1Н), 8,06 (m, 1Н), 7,91 (t, J=8 Гц, 1Н), 4,11 (brs, 1Н), 3,84-3,65 (m, 1Н), 3,60-3,40 (m, 1Н), 3,33 (brs, 1Н), 2,87 (brs, 1Н), 2,28-2,03 (m, 3H), 1,90-1,70 (m, 4Н), 1,68-1,57 (m, 1Н), 1,55-1,40 (m, 1Н); Масса (М+Н): 377,2.
Пример 12: 4-(((транс)-2-(6-(3-(Трифторметил)фенил)пиридин-3-ил)циклопропил)амино)циклогексанкарбоксамидгидрохлорид

1Н ЯМР (400 МГц, D2O) δ (част./млн): 8,80 (brs, 1Н), 8,50-8,40 (brs, 1Н), 8,38-8,26 (1H, 2Н), 8,20-8,00 (m, 2Н), 7,95-7,83 (m, 1Н), 3,65-3,25 (m, 3H), 2,96-2,82 (m, 1Н), 2,75-2,54 (m, 1Н), 2,47-2,30 (m, 1Н), 2,20-1,80 (m, 7Н), 1,70-1,50 (m, 1Н); Масса (М+Н): 404,3.
Пример 13: N-(4-(((транс)-2-(6-(3-(Трифторметил)фенил)пиридин-3-ил)циклопропил)амино)циклогексил)ацетамидгидрохлорид
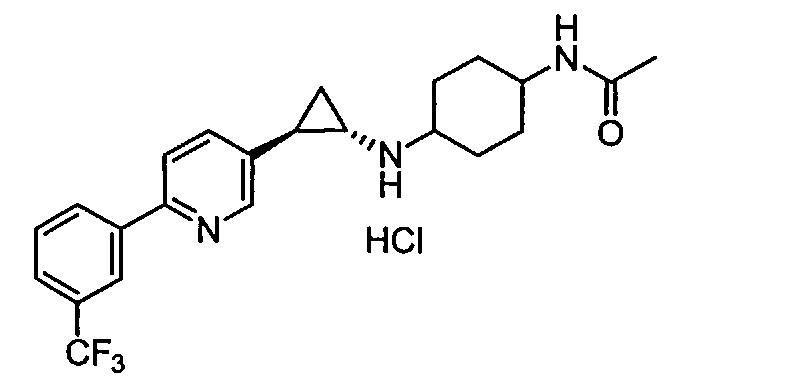
1Н ЯМР (400 МГц, D2O) δ (част./млн): 8,79 (s, 1Н), 8,39 (m, 1Н), 8,30 (m, 1Н), 8,24 (s, 1Н), 8,13 (m, 1Н), 8,11 (m, 1Н), 7,88 (t, J=8 Гц, 1Н), 3,70-3,62 (m, 1Н), 3,50-3,40 (m, 1Н), 3,38-3,24 (m, 1Н), 2,92-2,80 (m, 1Н), 2,34-2,24 (m, 2Н), 2,17-2,03 (m, 3H), 1,98 (s, 1Н), 1,94-1,72 (m, 4Н), 1,70-1,57 (m, 1Н), 1,50-1,35 (m, 2Н). Масса (М+Н): 418,2.
Пример 14: N-(4-(((транс)-2-(6-(3-(Трифторметил)фенил)пиридин-3-ил)циклопропил)амино)циклогексил)метансульфонамидгидрохлорид

1H ЯМР (400 МГц, D2O) δ (част./млн): 8,73 (s, 1Н), 8,41-8,32 (m, 1Н), 8,28-8,22 (m, 2Н), 8,12 (d, J=8 Гц, 1Н), 8,03 (d, J=8 Гц, 1Н), 7,88 (t, J=8 Гц, 1Н), 3,3,52-3,26 (m, 3H), 3,14 (s, 3H), 2,91-2,80 (m, 1Н), 2,36-1,96 (m, 4Н), 1,88-1,58 (m, 4Н), 1,56-1,42 (m, 2Н). Масса (М+Н): 454,1.
Пример 15: (R)-1-(4-(((транс)-2-Фенилциклопропил)амино)циклогексил)пирролидин-3-аминтригидрохлорид

1Н ЯМР (400 МГц, ДМСО-d6) δ (част./млн): 10,71-10,45 (m, 1Н), 9,61-9,50 (brs, 1Н), 9,49-9,34 (brs, 1Н), 8,09 (t, J=6 Гц, 3H), 7,98 (квинтет, 2Н), 4,85-4,20 (m, 7Н), 4,08-3,92 (m, 1Н), 3,82-3,65 (m, 1Н), 3,47-3,38 (m, 1H), 3,10-2,32 (m, 1H), 2,07 (q, 1Н). Масса (М+Н): 300,1.
Приведенные ниже соединения синтезировали по методике, описанной для получения соединения примера 1, с использованием соответствующих промежуточных продуктов и имеющихся в продаже реагентов. Стадию 2 проводили только в том случае, если промежуточный продукт, который использовали в реакции восстановительного алкилирования (стадия 1), содержал защитную группу Вое (трет-бутилоксикарбонил).
Пример 16: 1-Метил-N4-((транс)-2-фенилциклопропил)циклогексан-1,4-диамин

1Н ЯМР (400 МГц, D2O) δ: 7,45-7,30 (m, 3H), 7,24 (d, J=8 Гц, 2Н), 3,55-3,42 (m, 1Н), 3,05-2,98 (m, 1H), 2,62-2,52 (m, 1H), 2,28-2,20 (m, 2H), 2,18-1,98 (m, 2H), 1,87-1,64 (m, 4H), 1,62-1,44 (m, 2H), 1,41 (s, 3H); Масса (M+H): 245,33. Это соединение получали в виде гидрохлорида.
Пример 17: 4-(Аминометил)-N-((транс)-2-фенилциклопропил)циклогексиламин

1H ЯМР (400 МГц, CD3OD) δ: 7,33-7,25 (m, 2Н), 7,21-7,17 (m, 3H), 3,45 (brs, 1Н), 2,98 (d, J=8 Гц, 1Н), 2,95-2,92 (m, 1Н), 2,82 (d, J=7 Гц, 1Н), 2,57-2,55 (m, 1Н), 2,28-2,26 (m, 1H), 1,95-1,90 (m, 4H), 1,73-1,70 (m, 3H), 1,62-1,58 (m, 2H), 1,45-1,39 (m, 1H); Масса (M+H): 245,29. Это соединение получали в виде гидрохлорида.
Пример 18: N1-((транс)-2-Фенилциклопропил)циклогексан-1,3-диамин

1Н ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ (част./млн): 7,33 (t, J=7,4 Гц, 2Н), 7,26 (d, J=7,2 Гц, 1Н), 7,23 (t, J=8 Гц, 2Н), 4,1-4,0 (m, 1Н), 4,0-3,9 (m, 1Н), 2,96-2,86 (m, 1Н), 2,5-2,43 (m, 1Н), 2,10-1,90 (m, 2Н), 1,88-1,76 (m, 2Н), 1,75-1,63 (m, 3H), 1,62-1,48 (m, 2Н), 1,40-1,30 (m, 1Н); Масса (М+Н): 231,29. Это соединение получали в виде гидрохлорида.
Пример 19: N1-((транс)-2-Фенилциклопропил)циклобутан-1,3-диамин

1Н ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ (част./млн): 7,33 (t, J=8 Гц, 2Н), 7,25 (t, J=8 Гц, 1Н), 7,17 (d, J=8 Гц, 2Н), 4,1-4,0 (m, 1Н), 2,95-2,85 (m, 1Н), 2,74-2,60 (m, 2Н), 2,5-2,42 (m, 3H), 1,48 (квинтет, 1Н), 1,33 (q, 1Н); Масса (М+Н): 203,0. Это соединение получали в виде гидрохлорида.
Пример 20: N1-((транс)-2-Фенилциклопропил)-2,3-дигидро-1Н-инден-1,3-диамин

1Н ЯМР (400 МГц, D2O) δ: 7,70-7,53 (m, 4Н), 7,46-7,30 (m, 3H), 7,17 (d, J=8 Гц, 1Н), 7,03 (d, J=8 Гц, 1Н), 5,40-5,30 (m, 1Н), 5,14-5,04 (m,1Н), 3,05-2,93 (m, 2Н), 2,78-2,64 (m, 1Н), 2,54-2,32 (m, 1H), 1,62-1,42 (m, 2Н); Масса (М+Н): 265,3. Это соединение получали в виде гидрохлорида.
Пример 21: N1-((цис)-2-Фенилциклопропил)циклогексан-1,4-диамин

1Н ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 7,46-7,30 (m, 5Н), 3,03-2,88 (m, 2Н), 2,52-2,45 (m, 1Н), 2,27-2,20 (m, 1Н), 2,08-1,94 (m, 2Н), 1,94-1,58 (m, 3H), 1,54-1,20 (m, 5Н); Масса (М+Н): 231,18. Это соединение получали в виде гидрохлорида.
Пример 22: N1-Метил-N4-((транс)-2-фенилциклопропил)циклогексан-1,4-диамин

1ЯМР ЯМР (400 МГц, D2O) δ: 7,61-7,34 (m, 3H), 7,30-7,20 (m, 2Н), 3,70-3,58 (brs, 1Н), 3,53-3,33 (m, 1H), 3,22-2,95 (m, 1H), 2,82-2,70 (m, 3H), 2,63-2,47 (brs, 1H), 2,42-2,22 (m, 2H), 2,18-1,85 (m, 5H), 1,45-1,65 (m, 3H); Масса (M+H): 245,1. Это соединение получали в виде гидрохлорида.
Пример 23: трет-Бутил-(4-(((транс)-2-фенилциклопропил)амино)циклогексил)карбамат

1H ЯМР (400 МГц, CDCl3) δ (поворотные изомеры, 1:1): 7,28-7,23 (m, 2Н), 7,17-7,13 (m, 1Н), 7,02 (d, J=8 Гц, 2Н), 4,62 (brs, 0,5Н), 4,35 (brs, 0,5Н), 3,63 (brs, 0,5Н), 3,39 (brs, 0,5Н), 2,79 (brs, 0,5Н), 2,69-2,57 (m, 0,5Н), 2,38-2,22 (m, 1Н), 1,98-1,94 (m, 3H), 1,87-1,82 (m, 1Н), 1,75-1,60 (m, 2Н), 1,43 (s, 9Н), 1,33-1,00 (m, 5Н); Масса (М+Н): 331,27. Это соединение получали в виде свободного амина.
Пример 24: 1-Этил-3-(4-(((транс)-2-фенилциклопропил)амино)циклогексил)мочевина

1H ЯМР (400 МГц, DMCO-d6, обмен с D2O) δ: 7,33 (t, J=7,6 Гц, 2Н), 7,24 (t, J=7,2 Гц, 1Н), 7,18 (d, J=8 Гц, 2Н), 3,36-3,14 (m, 1Н), 3,04-2,92 (m, 3H), 2,50-2,40 (m, 2Н), 2,12-2,04 (m, 1Н), 1,93-1,81 (m, 2Н), 1,75-1,61 (m, 2Н), 1,60-1,40 (m, 3H), 1,39-1,30 (m, 1H), 1,20-1,13 (m, 1H), 1,03-0,94 (m, 3H); Масса (M+H): 302,26. Это соединение получали в виде гидрохлорида.
Пример 25: 4-Морфолино-N-((транс)-2-фенилциклопропил)циклогексиламин

1H ЯМР (400 МГц, CDCl3) δ: 7,28-7,22 (m, 2Н), 7,14 (t, J=8 Гц, 1Н), 7,02 (d, J=8 Гц, 2Н), 3,78-3,68 (m, 4Н), 2,94-2,85 (m, 1Н), 2,53 (brs, 4Н), 2,30-2,23 (m, 1Н), 2,22-2,16 (m, 1Н), 1,92-1,84 (m, 1Н), 1,70-1,62 (m, 2Н), 1,61-1,47 (m, 5Н), 1,10-1,02 (m, 1Н), 1,01-0,96 (m, 1Н); Масса (М+Н): 301,2. Это соединение получали в виде свободного амина.
Пример 26: N1-((транс)-2-(4-Бромфенил)циклопропил)циклогексан-1,4-диамин

1Н ЯМР (400 МГц, D2O) δ: 7,56 (d, J=8 Гц, 2Н), 7,14 (d, J=8 Гц, 2Н), 3,64-3,50 (m, 1Н), 3,48-3,38 (m, 1Н), 2,35-2,24 (m, 1Н), 3,05-2,97 (m, 1Н), 2,60-2,48 (m, 1Н), 2,40-2,19 (m, 2Н), 2,18 -1,84 (m, 3H), 1,70-1,44 (m, 4Н); Масса (М+Н): 309,06. Это соединение получали в виде гидрохлорида.
Пример 27: N1-(2-(о-Толил)циклопропил)циклогексан-1,4-диамин

1Н ЯМР (400 МГц, CD3OD) δ: 7,22-7,12 (m, 3H), 7,04-6,98 (m, 1Н), 3,60-3,40 (m, 1Н), 3,22-3,08 (m, 2Н), 2,72-2,49 (m, 1Н), 2,44 (s, 3H), 2,42-2,34 (m, 1Н), 2,25-2,16 (m, 1Н), 2,15-1,92 (m, 4Н), 1,70-1,50 (m, 3H), 1,32-1,24 (m, 1Н); Масса (М+Н): 245,22. Это соединение получали в виде гидрохлорида.
Пример 28: N1-(2-(4-(Трифторметил)фенил)циклопропил)циклогексан-1,4-диамин

1H ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 7,73-7,63 (m, 2Н), 7,50-7,36 (m, 2Н), 3,26-3,10 (m, 1Н), 3,07-2,92 (m, 1H), 2,48-2,41 (m, 1H), 2,20-2,09 (m, 2H), 2,08-1,98 (m, 1H), 1,90-1,67 (m, 5H), 1,60-1,32 (m, 4H); Масса (M+H): 299,24. Это соединение получали в виде гидрохлорида.
Пример 29: N1-(2-(4-Метоксифенил)циклопропил)циклогексан-1,4-диамин

1H ЯМР (400 МГц, CD3OD) δ: 7,16-7,08 (m, 2Н), 6,87 (d, J=8,8 Гц, 4Н), 3,76 (s, 3H), 3,44-3,38 (m, 1H), 3,22-3,12 (m, 0,5Н), 2,94-2,85 (m, 1Н), 2,52-2,44 (m, 0,5Н), 2,43-2,30 (m, 2Н), 2,24-2,14 (m, 1Н), 2,10-1,90 (m, 3H), 1,62-1,51 (m, 3 Н), 1,50-1,42 (m, 1Н), 1,37 (q, 1Н); Масса (М+Н): 261,26. Это соединение получали в виде гидрохлорида.
Пример 30: 4-(2-((4-Аминоциклогексил)амино)циклопропил)фенол

1Н ЯМР (400 МГц, ДМCO-d6, обмен с D2O) δ: 6,98 (d, J=8,4 Гц, 2Н), 6,71 (d, J=8,4 Гц, 2Н), 3,24-3,15 (m, 1Н), 3,07-2,95 (m, 1H), 2,87-2,78 (m, 1H), 2,45-2,36 (m, 1H), 2,22-2,11 (m, 2H), 2,09-1,98 (m, 2H), 1,94-1,75 (m, 1H), 1,58-1,34 (m, 4H), 1,26-1,18 (m, 1H); Масса (M+H): 247,22. Это соединение получали в виде гидрохлорида.
Пример 31: N1-(2-(2-Фторфенил)циклопропил)циклогексан-1,4-диамин

1H ЯМР (400 МГц, CD3OD) δ: 7,33-7,31 (m, 1Н), 7,29-7,26 (m, 3H), 3,52-3,30 (m, 2Н), 3,17-3,06 (m, 2Н), 2,73-2,61 (m, 1Н), 2,36-2,33 (m, 1Н), 2,17-2,20 (m, 1Н), 2,05-1,95 (m, 4H), 1,58-1,45 (m, 4H); Масса (М+Н): 249,23. Это соединение получали в виде гидрохлорида.
Пример 32: 1N-(2-(3,4-Дифторфенил)циклопропил)циклогексан-1,4-диамин

1H ЯМР (400 МГц, CD3OD) δ: 7,27-7,12 (m, 2Н), 7,08-7,00 (m, 1Н), 3,56-3,46 (m, 1Н), 3,46-3,34 (m, 1Н), 3,24-3,14 (m, 1Н), 3,05-2,97 (m, 1Н), 2,68-2,60 (m, 1Н), 2,58-2,48 (m, 1Н), 2,38-2,25 (m, 1Н), 2,38-2,25 (m, 1Н), 2,23-2,15 (m, 1Н), 2,14-1,90 (m, 4Н), 1,70-1,50 (m, 3H), 1,43 (q, 1 Н); Масса (М+Н): 267,21. Это соединение получали в виде гидрохлорида.
Пример 33: N1-(2-(Нафталин-2-ил)циклопропил)циклогексан-1,4-диамин

1Н ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 7,93-7,83 (m, 3H), 7,71 (s, 1Н), 7,50 (квинтет, 2Н), 7,34 (d, J=8,4 Гц, 1Н), 3,28-3,19 (m, 1H), 3,10-2,97 (m, 2H), 2,68-2,60 (m, 1H), 2,24-2,15 (m, 2H), 2,08-1,98 (m, 2H), 1,62-1,35 (m, 6H); Масса (M+H): 281,14. Это соединение получали в виде гидрохлорида.
Пример 34: N1-(2-Метил-2-фенилциклопропил)циклогексан-1,4-диамин
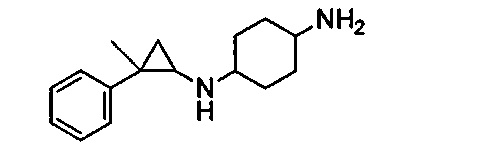
1H ЯМР (400 МГц, CD3OD) δ: 7,40-7,30 (m, 4Н), 7,27-7,21 (m, 1Н), 3,58-3,46 (m, 1Н), 2,95-2,85 (m, 1Н), 2,54-2,28 (m, 1Н), 2,25-2,18 (m, 1Н), 2,16-1,92 (m, 5Н), 1,67 (s, 3H), 1,62-1,52 (m, 2Н), 1,35-1,25 (m, 1Н); Масса (М+Н): 245,22. Это соединение получали в виде гидрохлорида.
Пример 35: (R)-1-(4-(((транс)-2-(3'-(Трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)амино)циклогексил)пирролидин-3-амин

1H ЯМР (400 МГц, D2O) δ: 7,98 (s, 1Н), 7,89 (d, J=8 Гц, 2H), 7,76-7,62 (m, 3H), 7,2 (d, J=8 Гц, 2H), 4,2 (brs, 2H), 4,06-3,96 (m, 2H), 3,72-3,62 (m, 2 H), 3,10-3,01 (m, 1H), 2,70-2,56 (m, 2H), 2,34-2,20 (m, 2H), 2,18-2,02 (m, 3H), 2,00-1,86 (m, 2H), 1,65-1,55 (m, 2H); Масса (M+H): 444,3. Это соединение получали в виде гидрохлорида.
Пример 36: (цис)-N1-((1S,2R)-2-(3'-(Трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин

Стадия 1:
L-(+)-Миндальную кислоту (2,7 г, 18,05 ммоля) добавляли к раствору (транс)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропанамина (свободный амин, полученный из промежуточного продукта АН, 5 г, 18,05 ммоля) в смеси ЕtOH/Н2O состава 1:9 (25 объемов) и кипятили с обратным холодильником в течение 2 ч. После образования прозрачного раствора реакционной смеси давали охладиться до КТ (16 ч). Осадившееся твердое вещество отфильтровывали, переносили в воду (100 мл), подщелачивали водным раствором NaHCO3 и экстрагировали с помощью EtOAc (2×100 мл). Объединенные экстракты промывали водой (100 мл), рассолом (100 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (1S,2R)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропанамин (1,3 г) в виде светло-желтого твердого вещества.
Стадия 2:
трет-Бутил-4-оксоциклогексилкарбамат (999 мг, 4,69 ммоля), уксусную кислоту (280 мг, 4,69 ммоля) и триацетоксиборогидрид натрия (1,78 г, 8,44 ммоля) при 0°C добавляли к раствору (1S,2R)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропанамина (1,3 г, 4,69 ммоля) в ДХЭ (10 мл) и перемешивали при КТ в течение 3 ч. После завершения реакции растворитель выпаривали и неочищенный остаток переносили в воду (25 мл), промывали с помощью NaHCO3 и экстрагировали с помощью EtOAc (2×25 мл). Объединенные экстракты промывали водой (25 мл), рассолом (25 мл), сушили над безводным Na2SO4, фильтровали и выпаривали.
Диастереоизомеры разделяли с помощью колоночной флэш-хроматографии с использованием SiO2 при элюировании смесью EtOAc: петролейный эфир (3:7). Сначала выделяли менее полярный трет-бутил-((цис)-4-(((1S,2R)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)амино)циклогексил)карбамат (460 мг), затем более полярный трет-бутил-((транс)-4-(((1S,2R)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)амино)циклогексил)карбамат (490 мг).
Стадия 3:
HCl в 1,4-диоксане (5 мл) при 15°C добавляли к раствору трет-бутил-((цис)-4-(((1S,2R)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)амино)циклогексил)карбамата (440 мг, 0,93 ммоля) в 1,4-диоксане (9 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции растворитель выпаривали. Остаток растирали с Et2O, отфильтровывали и сушили и получали (цис)-N1-((1S,2R)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин в виде гидрохлорида (320 мг), почти белое твердое вещество.
1H ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 8,02-7,92 (m, 2Н), 7,71 (d, J=8 Гц, 4Н), 7,32 (d, J=8 Гц, 2Н), 3,38 (brs, 1Н), 3,27 (brs, 1H), 3,06 (brs, 1H), 2,60 (brs, 1H), 2,0-1,73 (m, 8H), 1,62 (brs, 1H), 1,44-1,35 (m, 1H); Масса (M+H): 375,23; : +53,93° (C=0,53% в ДМСО).
Пример 37: (транс)-N1-((1S,2R)-2-(3'-(Трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин

Это соединение синтезировали по такой же методике, как описанная в примере 36, и получали содержащий группу Вое промежуточный трет-бутил-((транс)-4-(((1S,2R)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)амино)циклогексил)карбамат в качестве второго продукта стадии восстановительного алкилирования и в заключение получали 328 мг искомого соединения в виде гидрохлорида, бледно-коричневое твердое вещество.
1H ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 8,02-7,92 (m, 2Н), 7,71 (d, J=8 Гц, 4Н), 7,32 (d, J=8 Гц, 2Н), 3,30-3,20 (m, 1Н), 3,06-2,96 (m, 2H), 2,62-2,54 (m, 1H), 2,25-2,15 (m, 2H), 2,10-2,00 (m, 2H), 1,62-1,35 (m, 6H); Масса (M+H): 375,25; : +52,83° (С=0,53% в ДМСО).
Пример 38: (цис)-N1-((1R,2S)-2-(3'-(Трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин

Стадия 1:
D-(-)-Миндальную кислоту (2,7 г, 18,05 ммоля) добавляли к раствору (транс)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропанамина (свободный амин, полученный из промежуточного продукта АН, 5 г, 18,05 ммоля) в смеси ЕtOH/Н2O состава 1:9 (25 объемов) и кипятили с обратным холодильником в течение 2 ч. После образования прозрачного раствора реакционной смеси давали охладиться до КТ (16 ч). Осадившееся твердое вещество отфильтровывали, переносили в воду (100 мл), подщелачивали водным раствором NaНСО3 и экстрагировали с помощью EtOAc (2×100 мл). Объединенные экстракты промывали водой (100 мл), рассолом (100 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (1R,2S)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропанамин (900 мг) в виде светло-желтого твердого вещества.
Стадия 2:
трет-Бутил-4-оксоциклогексилкарбамат (692 мг, 3,2 ммоля), уксусную кислоту (194 мг, 3,2 ммоля) и триацетоксиборогидрид натрия (1,2 г, 5,76 ммоля) при 0°C добавляли к раствору (1R,2S)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропанамина (900 мг, 3,2 ммоля) в ДХЭ (10 мл) и перемешивали при КТ в течение 3 ч. После завершения реакции растворитель выпаривали. Остаток переносили в воду (25 мл), промывали с помощью NaHCO3 и экстрагировали с помощью EtOAc (2×25 мл). Объединенные экстракты промывали водой (25 мл), рассолом (25 мл), сушили над безводным Na2SO4, фильтровали и выпаривали.
Диастереоизомеры разделяли с помощью колоночной флэш-хроматографии с использованием SiO2 при элюировании смесью EtOAc:петролейный эфир (3:7). Сначала выделяли менее полярный изомер, трет-бутил-((цис)-4-(((1R,2S)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)амино)циклогексил)карбамат (390 мг), затем более полярный изомер, трет-бутил-((транс)-4-(((1R,2S)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)амино)циклогексил)карбамат (480 мг).
Стадия 3:
HCl в диоксане (4 мл) при 15°C добавляли к раствору трет-бутил-((цис)-4-(((1R,2S)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)амино)циклогексил)карбамата (380 мг, 0,801 ммоля) в 1,4-диоксане (8 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции растворитель выпаривали. Остаток растирали с Et2O, отфильтровывали и сушили и получали (цис)-N1-((1R,2S)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин в виде гидрохлорида (280 мг), белое твердое вещество.
1H ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 8,02-7,92 (m, 2Н), 7,71 (d, J=8 Гц, 4Н), 7,33 (d, J=8 Гц, 2Н), 3,39 (brs, 1H), 3,28 (brs, 1H), 3,05 (brs, 1H), 2,60 (brs, 1Н), 2,0-1,75 (m, 8H), 1,68-1,60 (m, 1H), 1,46-1,38 (m, 1H); Масса (M+H): 375,28; : -65,31° (C=0,53% в ДМСО)
Пример 39: (транс)-N1-((1R,2S)-2-(3'-(Трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклстексан-1,4-диамин

Это соединение синтезировали по такой же методике, как описанная в примере 38, и получали содержащий группу Воc промежуточный трет-бутил-((транс)-4-(((1R,2S)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)амино)циклогексил)карбамат в качестве второго продукта стадии восстановительного алкилирования и в заключение получали 350 мг искомого соединения в виде гидрохлорида, бледно-коричневое твердое вещество.
1H ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 8,02-7,92 (m, 2Н), 7,71 (d, J=8 Гц, 4Н), 7,32 (d, J=8 Гц, 2Н), 3,30-3,20 (m, 1Н), 3,06-2,96 (m, 2H), 2,62-2,54 (m, 1H), 2,25-2,15 (m, 2H), 2,10-2,00 (m, 2H), 1,62-1,35 (m, 6H); Масса (M+H): 375,24; : -48,30° (C=0,52% в ДМСО)
Пример 40: N1-((транс)-2-(4-Циклопропилфенил)циклопропил)циклогексан-1,4-диамин
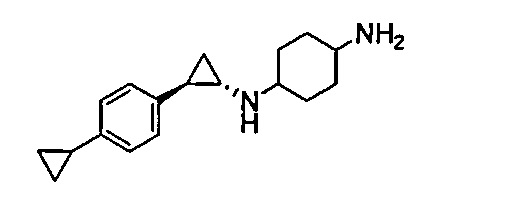
Стадия 1:
Раствор трет-бутил-((транс)-2-(4-бромфенил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамата (промежуточный продукт AT, 400 мг, 0,78 ммоля), циклопропилбороновой кислоты (81 мг, 0,94 ммоля) и К2CO3 (322 мг, 2,34 ммоля) в смеси АЦН/H2O состава 4:1 (8 мл) дегазировали в течение 30 мин. Добавляли Pd(PPh3)4 (45 мг, 0,039 ммоля) и смесь перемешивали при кипячении с обратным холодильником в течение 16 ч. После завершения реакции реакционную смесь выливали в воду и экстрагировали с помощью EtOAc (2×25 мл). Объединенные экстракты промывали водой (25 мл), рассолом (25 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенное вещество очищали с помощью колоночной хроматографии (SiO2) с использованием смеси EtOAc:петролейный эфир (3:7) и получали трет-бутил-(4-((трет-бутоксикарбонил)амино)циклогексил)((транс)-2-(4-циклопропилфенил)циклопропил)карбамат (160 мг) в виде белого твердого вещества.
Стадия 2:
HCl в диоксане (1 мл) при 10°C добавляли к раствору трет-бутил-(4-((трет-бутоксикарбонил)амино)циклогексил)((транс)-2-(4-циклопропилфенил)циклопропил)карбамата (160 мг, 0,33 ммоля) в диоксане (3 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции растворитель выпаривали. Твердое вещество растирали с Et2O, отфильтровывали и сушили и получали N1-((транс)-2-(4-циклопропилфенил)циклопропил)циклогексан-1,4-диамин в виде гидрохлорида (60 мг), белое твердое вещество.
1Н ЯМР (400 МГц, ДМСО-d6) δ: 9,50-9,43 (m, 2Н), 8,03 (brs, 3H), 7,02-6,98 (m, 4Н), 3,28-3,18 (m, 1Н), 2,97-2,80 (m, 1Н), 2,43 (brs, 1Н), 2,17 (brs, 1Н), 2,02-1,75 (m, 6Н), 1,58-1,20 (m, 5Н), 0,92-0,87 (m, 2Н), 0,61-0,57 (m, 2Н); Масса (М+Н): 271,24
Приведенные ниже соединения можно синтезировать по общим методикам, раскрытым в разделе "Описание общего пути синтеза", и, в частности, по методике, описанной в примере 40, и с использованием соответствующих промежуточных продуктов или имеющихся в продаже реагентов.
Пример 41: N1-((транс)-2-(4-(Пиридин-3-ил)фенил)циклопропил)циклогексан-1,4-диамин

1Н ЯМР (400 МГц, ДМСО-d6) δ: 9,82-9,69 (m, 2Н), 9,16 (m, J=12,8 Гц, 1Н), 8,78 (brs, 1Н), 8,68-8,63 (m, 1Н), 8,19-8,15 (m, 3H), 7,95-7,92 (m, 1Н), 7,81 (s, 2Н), 7,38 (s, 2Н), 3,28-3,08 (m, 2Н), 2,99 (brs, 1Н), 2,67 (brs, 1Н), 2,20 (brs, 1Н), 2,05-2,02 (m, 1H), 1,98-1,89 (m, 1H), 1,78-1,63 (m, 5H), 1,44-1,36 (m, 2H); Масса (M+H): 308,2. Это соединение получали в виде гидрохлорида.
Пример 42: N1-((транс)-2-(4-(1Н-Индазол-6-ил)фенил)циклопропил)циклогексан-1,4-диамин

1Н ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 8,11 (s, 1Н), 7,86 (d, J=8 Гц, 1H), 7,75 (s, 1H), 7,69 (d, J=8 Гц, 2H), 7,42 (d, J=8 Гц, 1H), 7,31 (d, J=8 Гц, 2H), 3,42 (brs, 1H), 3,36-3,20 (m, 1H), 3,10-2,98 (m, 1H), 2,24-2,15 (m, 1H), 2,10-2,00 (m, 1H), 1,90 (brs, 2H), 1,81 (brs, 2H), 1,63-1,35 (m, 4H); Масса (M+H): 347,2. Это соединение получали в виде гидрохлорида.
Пример 43: N1-((транс)-2-(4-(1Н-Пиразол-5-ил)фенил)циклопропил)циклогексан-1,4-диамин

1Н ЯМР (400 МГц, CD3OD) δ: 8,24-8,15 (m, 1Н), 7,80 (d, J=7,6 Гц, 2Н), 7,43-7,37 (m, 2Н), 7,09-7,02 (m, 1Н), 3,58-3,50 (m, 1Н), 3,46-3,40 (m, 1Н), 3,22-3,08 (m, 1Н), 2,77-2,59 (m, 1Н), 2,40-2,29 (m, 1Н), 2,24-2,15 (m, 1Н), 2,13-1,93 (m, 4Н), 1,80-1,48 (m, 4Н); Масса (М+Н): 297,32. Это соединение получали в виде гидрохлорида.
Пример 44: 3-(5-((транс)-2-((4-Аминоциклогексил)амино)циклопропил)тиофен-2-ил)фенол

1Н ЯМР (400 МГц, D2O) δ: 7,32-7,21 (m, 2Н), 7,20 (d, J=8 Гц, 1Н), 7,11 (s, 1H), 6,89-6,88 (m, 1H), 6,84 (d, J=7,6 Гц, 1H), 3,42-3,38 (m, 1H), 3,28-3,18 (m, 1H), 3,03-2,98 (m, 1H), 2,74-2,68 (m, 1H), 2,38-2,30 (m, 2H), 2,11-2,04 (m, 3H), 2,00-1,78 (m, 2H), 1,61-1,42 (m, 5H); Масса (M+H): 329,13. Это соединение получали в виде гидрохлорида.
Пример 45: 3-(5-((транс)-2-((4-Аминоциклогексил)амино)циклопропил)тиазол-2-ил)фенол

1H ЯМР (400 МГц, ДМСО-d6) δ: 9,79 (brs, 1Н), 9,70 (brs, 1Н), 8,10 (brs, 2Н), 7,72 (s, 1Н), 7,30 (s, 2Н), 6,86 (s, 1Н), 3,40-3,19 (m, 2Н), 3,18-2,95 (m, 2Н), 2,85 (brs, 1Н), 2,22-2,19 (m, 1Н), 2,08-1,62 (m, 5Н), 1,58-1,38 (m, 3H); Масса (М+Н): 330,2. Это соединение получали в виде гидрохлорида.
Пример 46: 3-(5-((транс)-2-((4-Аминоциклогексил)амино)циклопропил)пиридин-2-ил)-5-метоксибензонитрил

Стадия 1:
АсОН (12,9 мг, 0,215 ммоля) добавляли к раствору 3-(5-((транс)-2-аминоциклопропил)пиридин-2-ил)-5-метоксибензонитрила (промежуточный продукт ВТ, 65 мг, 0,245 ммоля) и трет-бутил-4-оксоциклогексилкарбамата (45,9 мг, 0,215 ммоля) в ДХЭ (2 мл) и перемешивали при КТ в течение 15 мин, затем при 0°C добавляли триацетоксиборогидрид натрия (82 мг, 0,387 ммоля) и перемешивали при КТ в течение 5 ч. После завершения реакции растворитель выпаривали. Неочищенный остаток переносили в воду (10 мл), подщелачивали с помощью NaHCO3 (10 мл) и экстрагировали с помощью ДХМ (2×10 мл). Объединенные экстракты промывали водой (10 мл), рассолом (10 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали трет-бутил-(4-(((транс)-2-(6-(3-циано-5-метоксифенил)пиридин-3-ил)циклопропил)амино)циклогексил)карбамат (110 мг). Неочищенный продукт использовали на следующей стадии без дополнительной очистки. Стадия 2:
HCl в диоксане (1 мл) при 10°C добавляли к раствору трет-бутил-(4-(((транс)-2-(6-(3-циано-5-метоксифенил)пиридин-3-ил)циклопропил)амино)циклогексил)карбамата (110 мг, 0,238 ммоля) в диоксане (2 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции растворитель выпаривали. Остаток растирали с Et2O, отфильтровывали и сушили и получали 3-(5-((транс)-2-((4-аминоциклогексил)амино)циклопропил)пиридин-2-ил)-5-метоксибензонитрил в виде гидрохлорида (20 мг), оранжевое твердое вещество.
1Н ЯМР (400 МГц, CD3OD) δ: 8,70 (s, 1Н), 8,07 (d, J=8,8 Гц, 1Н), 7,96 (d, J=7,2 Гц, 1Н), 7,93-7,88 (m, 1Н), 7,85-7,80 (m, 1Н), 7,46 (s, 1Н), 3,94 (s, 3H), 3,26-3,16 (m, 1Н), 2,77-2,68 (m, 1Н), 2,42-2,25 (m, 1Н), 2,24-2,10 (m, 1Н), 2,08-1,90 (m, 3H), 1,89-1,80 (m, 1Н), 1,78-1,27 (m, 6Н); Масса (М+Н): 363,30
Приведенные ниже соединения синтезировали по общим методикам, раскрытым в разделе "Описание общего пути синтеза", и, в частности, по методике, описанной в примере 46, и с использованием соответствующих промежуточных продуктов.
Пример 47: 5-(5-((транс)-2-((4-Аминоциклогексил)амино)циклопропил)пиридин-2-ил)-2-метилфенол
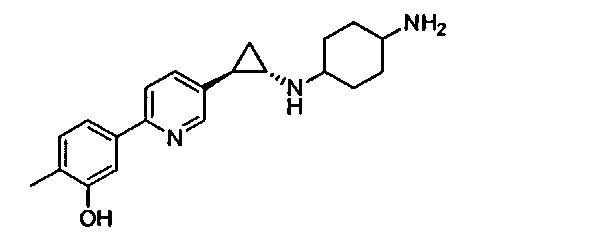
1H ЯМР (400 МГц, CD3OD) δ: 8,74 (s, 1Н), 8,33 (d, J=8,4 Гц, 1Н), 8,17 (d, J=8,4 Гц, 1Н), 7,35 (d, J=7,6 Гц, 1Н), 7,34-7,25 (m, 2Н), 3,50-3,42 (m, 1Н), 3,38-3,32 (m, 1H), 3,24-3,10 (m, 1H), 2,90-2,82 (m, 1Н), 2,43-2,31 (m, 2Н), 2,28 (s, 3H), 2,23-2,12 (m, 2Н), 1,84-1,78 (m, 1H), 1,76-1,50 (m, 5Н); Масса (М+Н): 338,32. Это соединение получали в виде гидрохлорида.
Пример 48: N-(4'-((транс)-2-((4-Аминоциклогексил)амино)циклопропил)-6-метокси-[1,1'-бифенил]-3-ил)метансульфонамид

1H ЯМР (400 МГц, CD3OD) δ: 7,45 (d, J=8 Гц, 2Н), 7,27-7,19 (m, 4Н), 7,10-7,02 (m, 1Н), 3,78 (s, 3H), 3,08-3,00 (m, 1Н), 2,91 (s, 3H), 2,55-2,47 (m, 1Н), 2,40-2,30 (m, 2Н), 2,24-2,14 (m, 2Н), 2,05-1,93 (m, 2Н), 1,66-1,46 (m, 6Н); Масса (М+Н): 430,22. Это соединение получали в виде гидрохлорида.
Пример 49: N-(3-(5-((транс)-2-((4-Аминоциклогексил)амино)циклопропил)тиазол-2-ил)фенил)-2-цианобензолсульфонамид
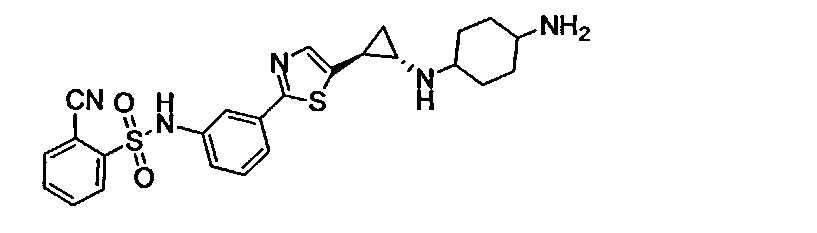
Стадия 1:
Раствор трет-бутил-((транс)-2-(2-бромтиазол-5-ил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамата (промежуточный продукт BQ, 1,25 г, 2,42 ммоля), 3-аминофенилбороновой кислоты (364 мг, 2,66 ммоля) и K2CO3 (1 г, 7,26 ммоля) в смеси АЦН-H2O (4:1) (12 мл) дегазировали в течение 30 мин. Добавляли Pd(PPh3)4 (27,9 мг, 0,024 ммоля) и смесь перемешивали при кипячении с обратным холодильником в течение 16 ч. После завершения реакции реакционную смесь выливали в воду и экстрагировали с помощью EtOAc (2×50 мл). Объединенные экстракты промывали водой (50 мл), рассолом (50 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенное вещество очищали с помощью колоночной хроматографии (SiO2, EtOAc/петролейный эфир 3:7) и получали трет-бутил-((транс)-2-(2-(3-аминофенил)тиазол-5-ил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамат (950 мг) в виде желтой смолообразной жидкости.
Стадия 2:
2-Цианобензол-1-сульфонилхлорид (361 мг, 1,799 ммоля) при 0°C добавляли к раствору трет-бутил-((транс)-2-(2-(3-аминофенил)тиазол-5-ил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамата (950 мг, 1,799 ммоля) в пиридине (5 мл) и перемешивали при КТ в течение 5 ч. После завершения реакции реакционную смесь выливали в воду и экстрагировали с помощью EtOAc (2×25 мл). Объединенные экстракты промывали водой (2×25 мл), рассолом, сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенное вещество очищали с помощью препаративной ВЭЖХ и получали трет-бутил-(4-((трет-бутоксикарбонил)амино)циклогексил)((транс)-2-(2-(3-(2-цианофенилсульфонамидо)фенил)тиазол-5-ил)циклопропил)карбамат (240 мг) в виде белого твердого вещества.
Стадия 3:
HCl в диоксане (1,2 мл) при 10°C добавляли к раствору трет-бутил-(4-((трет-бутоксикарбонил)амино)циклогексил)((транс)-2-(2-(3-(2-цианофенилсульфонамидо)фенил)тиазол-5-ил)циклопропил)карбамата (240 мг, 0,34 ммоля) в диоксане (2,4 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции растворитель выпаривали и остаток растирали с Et2O, отфильтровывали и сушили и получали N-(3-(5-((транс)-2-((4-аминоциклогексил)амино)циклопропил)тиазол-2-ил)фенил)-2-цианобензолсульфонамид в виде гидрохлорида (110 мг), светло-коричневое твердое вещество.
1Н ЯМР (400 МГц, ДМСО-d6) δ: 11,11 (s, 1Н), 9,81-9,71 (m, 2Н), 8,24-8,08 (brs, 2Н), 8,08 (dd, J=7,6 и 4,8 Гц, 2Н), 7,93 (t, J=8 Гц, 1Н), 7,83 (t, J=7,2 Гц, 1Н), 7,73 (s, 1Н), 7,66 (s, 1Н). 7,56 (d, J=7,2 Гц, 1Н), 7,38 (t, J=8 Гц, 1Н), 7,18 (d, J=8 Гц, 1Н), 3,4-3,18 (m, 2Н), 3,05-2,85 (m, 2Н), 2,2 (m, 1Н), 2,1-1,8 (m, 4Н), 1,75 (brd, 2Н), 1,42 (m, 3H); Масса (М+Н): 494,1
Приведенное ниже соединение синтезировали по общим методикам, раскрытым в разделе "Описание общего пути синтеза", и, в частности, по методике, описанной в примере 49, и с использованием соответствующих промежуточных продуктов или имеющихся в продаже реагентов.
Пример 50: N-(4'-((транс)-2-((4-Аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)-2-цианобензолсульфонамид

1Н ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 8,11 (d, J=8 Гц, 1Н), 8,06 (d, J=8 Гц, 1H), 7,93 (t, J=8 Гц, 1H), 7,83 (t, J=8 Гц, 1H), 7,72-7,60 (m, 1H), 7,48 (d, J=8 Гц, 2H), 7,40-7,31 (m, 2H), 7,30-7,24 (m, 2H), 7,07-7,01 (m, 1H), 3,39 (brs, 1H), 3,35-3,18 (m, 1H), 3,08-2,94 (m, 2H), 2,15 (brs, 1H), 2,10-2,00 (m, 1H), 1,88 (brs, 2H), 1,80 (brs, 2H), 1,62-1,35 (m, 4H); Масса (M+H): 487,27. Это соединение получали в виде гидрохлорида.
Пример 51: 6-Амино-N-(4'-((транс)-2-((4-аминоциклогексил)амино)циклопропил)- [1,1'-бифенил]-3-ил)пиридин-3-сульфонамид

Стадия 1:
6-Нитропиридин-3-сульфонилхлорид (223 мг, 1 ммоль) при 0°C добавляли к раствору трет-бутил-((транс)-2-(3'-амино-[1,1'-бифенил]-4-ил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамата (промежуточный продукт BR, 500 мг, 0,95 ммоля) в пиридине (10 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции реакционную смесь выливали в воду (25 мл) и экстрагировали с помощью EtOAc (2×25 мл). Объединенные экстракты промывали водой (3×25 мл), рассолом (25 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали трет-бутил-(4-((трет-бутоксикарбонил)амино)циклогексил)((транс)-2-(3'-(6-нитропиридин-3-сульфонамидо)-[1,1'-бифенил]-4-ил)циклопропил)карбамат (580 мг). Неочищенный продукт использовали на следующей стадии без дополнительной очистки.
Стадия 2:
Хлорид аммония (217 мг, 4,1 ммоля) добавляли к раствору трет-бутил-(4-((трет-бутоксикарбонил)амино)циклогексил)((транс)-2-(3'-(6-нитропиридин-3-сульфонамидо)-[1,1'-бифенил]-4-ил)циклопропил)карбамата (580 мг, 0,82 ммоля) в EtOH (12 мл), затем добавляли порошкообразное железо (229 мг, 4,1 ммоля) и реакционную смесь перемешивали при кипячении с обратным холодильником в течение 4 ч. После завершения реакции реакционную смесь фильтровали через слой целита, фильтрат концентрировали и остаток переносили в воду (25 мл) и экстрагировали с помощью EtOAc (2×25 мл). Объединенные экстракты промывали водой (25 мл), рассолом (25 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенное вещество очищали с помощью препаративной ВЭЖХ и получали трет-бутил-((транс)-2-(3'-(6-аминопиридин-3-сульфонамидо)-[1,1'-бифенил]-4-ил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамат (190 мг) в виде почти белого твердого вещества.
Стадия 3:
HCl в диоксане (1 мл) при 10°C по каплям добавляли к раствору трет-бутил-((транс)-2-(3'-(6-аминопиридин-3-сульфонамидо)-[1,1'-бифенил]-4-ил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамата (90 мг, 0,13 ммоля) в диоксане (2 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции растворитель выпаривали. Остаток растирали с Et2O, отфильтровывали и сушили и получали 6-амино-N-(4'-((транс)-2-((4-аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)пиридин-3-сульфонамид в виде гидрохлорида (60 мг), почти белое твердое вещество.
1Н ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 8,24 (s, 1Н), 7,72 (dd, J=8 Гц, 2,5 Гц, 1H), 7,50 (d, J=8 Гц, 2H), 7,38-7,32 (m, 3H), 7,28 (d, J=8 Гц, 1H), 7,10-7,05 (m, 1H), 6,57 (d, J=8 Гц, 2H), 3,30-3,19 (m, 1H), 3,05-2,98 (m, 2H), 2,54-2,46 (m, 1H), 2,23-2,13 (m, 2H), 2,10-2,00 (m, 2H), 1,59-1,36 (m, 6H); Масса (M+H): 478,06
Пример 52: N-(4'-((транс)-2-((4-Аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)пиперазин-1-сульфонамид

Это соединение синтезировали по такой же методике, как описанная в примере 51, используя трет-бутил-4-(хлорсульфонил)пиперазин-1-карбоксилат на стадии 1 и не проводя стадию 2. Конечное удаление защитной группы (удаление группы Boc, стадия 3) давало 80 мг искомого соединения в виде гидрохлорида, белое твердое вещество.
1H ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 7,57 (d, J=8 Гц, 2Н), 7,50-7,38 (m, 3H), 7,35-7,25 (m, 2Н), 7,24 (d, J=8 Гц, 1Н), 3,37 (brs, 4H), 3,36-3,20 (m, 2H), 3,37 (brs, 4H), 3,11 (brs, 3H), 3,05-2,96 (m, 2H), 2,23-2,15 (m, 1H), 2,10-2,0 (m, 1H),1,90 (brs, 2H), 1,81 (brs, 2H), 1,63-1,35 (m, 4H); Масса (M+H): 470,33
Пример 53: N1-((транс)-2-Фтор-2-фенилциклопропил)циклогексан-1,4-диамин

Стадия 1:
трет-Бутил-4-оксоциклогексилкарбамат (493 мг, 2,31 ммоля) добавляли к раствору (транс)-2-фтор-2-фенилциклопропанамина (промежуточный продукт BJ, 350 мг, 2,31 ммоля) в ДХЭ (7 мл). Смесь перемешивали при КТ в течение 10 мин и затем охлаждали до 0°C. Добавляли триацетоксиборогидрид натрия (978 мг, 4,62 ммоля) и перемешивание продолжали при КТ в течение 15 мин. После завершения реакционную смесь выливали в воду со льдом и экстрагировали с помощью ДХМ (2×25 мл). Объединенные экстракты промывали водой (10 мл), рассолом (10 мл) и сушили над безводным Na2SO4. Фильтрат не выпаривали и использовали на следующей стадии.
HCl в диоксане (1,6 мл) добавляли к раствору трет-бутил-(4-(((транс)-2-фтор-2-фенилциклопропил)амино)циклогексил)карбамата в ДХМ (3,2 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции растворитель выпаривали и неочищенный остаток растирали с диэтиловым эфиром (10 мл) и гексаном (10 мл) и получали N1-((транс)-2-фтор-2-фенилциклопропил)циклогексан-1,4-диамин в виде гидрохлорида (300 мг), желтое твердое вещество.
Стадия 2:
2 н. Раствор NaOH (5,8 мл) и (Вос)2O (0,54 мл, 2,26 ммоля) при 10°C добавляли к раствору N1-((транс)-2-фтор-2-фенилциклопропил)циклогексан-1,4-диамина (290 мг, 0,906 ммоля) в 1,4-диоксане (10 объемов) и перемешивали при комнатной температуре в течение 4 ч. После завершения реакции реакционную смесь разбавляли водой (10 мл) и экстрагировали с помощью EtOAc (2×15 мл). Объединенные экстракты промывали водой (10 мл), рассолом (10 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенное вещество очищали с помощью препаративной ВЭЖХ и получали трет-бутил-(4-((трет-бутоксикарбонил)амино)циклогексил)((транс)-2-фтор-2-фенилциклопропил)карбамат (140 мг) в виде белого твердого вещества
Стадия 3:
HCl в диоксане (0,7 мл) добавляли к раствору трет-бутил-(4-((трет-бутоксикарбонил)амино)циклогексил)((транс)-2-фтор-2-фенилциклопропил)карбамата (140 мг, 0,312 ммоля) в диоксане (1,4 мл) при 0°C и перемешивали при КТ в течение 6 ч. После завершения реакции растворитель выпаривали и остаток растирали с диэтиловым эфиром (5 мл), затем с н-пентаном (5 мл) и получали N1-((транс)-2-фтор-2-фенилциклопропил)циклогексан-1,4-диамин в виде гидрохлорида (80 мг), почти белое твердое вещество.
1H ЯМР (400 МГц, D2O) δ: 7,49 (s, 2Н), 7,42 (s, 3H), 3,60-3,43 (m, 2Н), 3,22-3,12 (m, 2Н), 2,33-2,18 (m, 3H), 1,98-1,91 (m, 3H), 1,68-1,45 (m, 3H), Масса (М+Н): 249,17
Пример 54: N1-((цис)-2-Фтор-2-фенилциклопропил)циклогексан-1,4-диамин

Это соединение синтезировали по такой же методике, как описанная в примере 53, с использованием в качестве исходного вещества (цис)-2-фтор-2-фенилциклопропанамина (промежуточный продукт BI); получали 80 мг соединения в виде гидрохлорида, почти белое твердое вещество.
1Н ЯМР (400 МГц, D2O) δ: 7,79 (s, 2Н), 7,62 (s, 3H), 3,69-3,53 (m, 2Н), 3,4-3,18 (m, 2Н), 2,39 (s, 1Н), 2,28-2,08 (m, 3H), 2,02-1,81 (m, 4H), 1,68-1,45 (m, 3H), Масса (M+H): 249,17
Пример 55: N1-((транс)-2-(4-((3-(Пиперазин-1-ил)бензил)окси)фенил)циклопропил)циклогексан-1,4-диамин

Стадия 1:
K2CO3 (1,1 г, 8,0 ммоля) при 0°C добавляли к раствору трет-бутил-((транс)-2-(4-гидроксифенил)циклопропил)карбамата (промежуточный продукт BL, 1 г, 4,0 ммоля) и 1-бром-3-(бромметил)бензола (997 мг, 4,0 ммоля) в ДМФ (10 мл) и перемешивали при КТ в течение 18 ч. После завершения реакции реакционную смесь выливали в воду со льдом (20 мл) и экстрагировали этилацетатом (2×20 мл). Объединенные экстракты промывали водой (20 мл), рассолом (20 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный продукт очищали с помощью колоночной хроматографии (SiO2, EtOAc/петролейный эфир 2:8) и получали трет-бутил-((транс)-2-(4-((3-бромбензил)окси)фенил)циклопропил)карбамат (1,2 г) в виде почти белого твердого вещества.
Стадия 2:
HCl в диоксане (10 мл) при 15°C по каплям добавляли к раствору трет-бутил-((транс)-2-(4-((3-бромбензил)окси)фенил)циклопропил)карбамата (1,2 г, 2,8 ммоля) в диоксане (5 мл) и перемешивали при КТ в течение 2 ч. После завершения реакции растворитель выпаривали. Остаток переносили в воду (15 мл), подщелачивали раствором NaHCO3 (5 мл) и экстрагировали с помощью EtOAc (2×20 мл). Объединенные экстракты промывали водой (20 мл), рассолом (20 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали (транс)-2-(4-((3-бромбензил)окси)фенил)циклопропанамин (800 мг). Неочищенное вещество использовали на следующей стадии без дополнительной очистки.
Стадия 3:
Уксусную кислоту (0,17 мл, 2,515 ммоля) добавляли к раствору (транс)-2-(4-((3-бромбензил)окси)фенил)циклопропанамина (800 мг, 2,51 ммоля) и трет-бутил-4-оксоциклогексилкарбамата (537 мг, 2,515 ммоля) в ДХЭ (20 мл). При 0°C добавляли триацетоксиборогидрид натрия (960 мг, 4,52 ммоля) и смесь перемешивали при КТ в течение 4 ч. После завершения реакции реакционную смесь разбавляли с помощью ДХМ (20 мл), промывали водным раствором NaHCO3, затем водой (10 мл), рассолом (10 мл). Органическую фазу сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный продукт очищали с помощью колоночной хроматографии (SiO2, EtOAc/петролейный эфир 6:4) и получали трет-бутил-(4-(((транс)-2-(4-((3-бромбензил)окси)фенил)циклопропил)амино)циклогексил)карбамат (900 мг).
Стадия 4:
NaOH (310 мг, 7,76 ммоля) при 10°C добавляли к раствору трет-бутил-(4-(((транс)-2-(4-((3-бромбензил)окси)фенил)циклопропил)амино)циклогексил)карбамата (1,0 г, 1,94 ммоля) в смеси 1,4-диоксан/вода (4:1). Затем добавляли Вос2О (830 мг, 3,88 ммоля) и смесь перемешивали при КТ в течение 18 ч. После завершения реакции реакционную смесь выливали в воду со льдом (20 мл) и экстрагировали этилацетатом (2×20 мл). Объединенные экстракты промывали водой (20 мл), рассолом (20 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный продукт очищали с помощью колоночной хроматографии (SiO2, EtOAc/петролейный эфир 3:7) и получали трет-бутил-((транс)-2-(4-((3-бромбензил)окси)фенил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамат (600 мг).
Стадия 5:
NaOtBu (141 мг, 1,46 ммоля) при КТ добавляли к раствору трет-бутил-((транс)-2-(4-((3-бромбензил)окси)фенил)циклопропил)(4-((трет-бутоксикарбонил)амино)циклогексил)карбамата (600 мг, 0,975 ммоля) и трет-бутилпиперазин-1-карбоксилата (363 мг, 1,95 ммоля) в диоксане (15 мл), который затем дегазировали аргоном в течение 15 мин. Добавляли Pd2(dba)3 (44,6 мг, 0,0487 ммоля), затем Xantphos (169 мг, 0,292 ммоля) и повторно дегазировали в течение 15 мин. Реакционную смесь перемешивали при кипячении с обратным холодильником в течение 18 ч. После завершения реакции смесь фильтровали через слой целита и фильтрат концентрировали. Остаток переносили в воду (20 мл) и экстрагировали этилацетатом (2×20 мл). Объединенные экстракты промывали водой (20 мл), рассолом (20 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный продукт очищали с помощью колоночной хроматографии (нейтральный диоксид алюминия, EtOAc/петролейный эфир 2:8) и получали трет-бутил-4-(3-((4-((транс)-2-((трет-бутоксикарбонил)(4-((трет-бутоксикарбонил)амино)циклогексил)амино)циклопропил)фенокси)метил)фенил)пиперазин-1-карбоксилат (260 мг) в виде белого твердого вещества.
Стадия 6:
HCl в диоксане (3 мл) при 10°C добавляли к раствору трет-бутил-4-(3-((4-((транс)-2-((трет-бутоксикарбонил)(4-((трет-бутоксикарбонил)амино)циклогексил)амино)циклопропил)фенокси)метил)фенил)пиперазин-1-карбоксилата (150 мг, 0,208 ммоля) в 1,4-диоксане (2 мл) и перемешивали при КТ в течение 6 ч. После завершения реакции растворитель выпаривали и остаток растирали с EtOAc (4 мл), затем с н-гексаном (2 мл) и получали N1-((транс)-2-(4-((3-(пиперазин-1-ил)бензил)окси)фенил)циклопропил)циклогексан-1,4-диамин в виде гидрохлорида (80 мг), бледно-желтое твердое вещество.
1Н ЯМР (400 МГц, D2O) δ: 7,40 (t, J=8 Гц, 1Н), 7,19 (s, 1H), 7,18-7,07 (m, 4H), 7,01 (d, J=8 Гц, 2H), 5,11 (s, 2H), 3,6-3,3 (m, 9H), 3,28-3,18 (m, 1H), 3,95-3,84 (m, 1H), 2,50-2,39 (m, 1H), 2,32-2,24 (m, 1H), 2,19-2,11 (m, 1H), 2,09-1,99 (m, 1H), 1,98-1,77 (m, 3H), 1,62-1,33 (m, 4H); Масса (M+H): 421,28
Приведенные ниже соединения можно синтезировать по общим методикам, раскрытым в разделе "Описание общего пути синтеза", и, в частности, по методике, описанной в примере 55, не проводя стадии 4 и 5, и с использованием соответствующих промежуточных продуктов или имеющихся в продаже реагентов.
Пример 56: N1-((транс)-2-(4-(Пиридин-3-илметокси)фенил)циклопропил)циклогексан-1,4-диамин

1H ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 8,79 (s, 1Н), 8,68 (s, 1Н), 8,31-8,24 (m, 1Н), 7,83-75 (m, 1Н), 7,20-7,10 (m, 2Н), 7,01 (d, J=8,4 Гц, 2Н), 5,23 (s, 2Н), 3,42-3,17 (m, 2Н), 3,08-2,95 (m, 1Н), 2,94-2,83 (m, 1Н), 2,48-2,35 (m, 1Н), 2,22-2,10 (m, 1H), 2,09-1,98 (m, 1Н), 1,97-1,72 (m, 3H), 1,55-1,38 (m, 3H), 1,37-1,25 (m, 1Н); Масса (М+Н): 338,19. Это соединение получали в виде гидрохлорида.
Пример 57: N1-((транс)-2-(4-((2-Фторбензил)окси)фенил)циклопропил)циклогексан-1,4-диамин

1H ЯМР (400 МГц, ДМСО-d6) δ: 9,55 (brd, 2Н), 8,1 (brs, 3H), 7,58 (t, 1Н), 7,62 (d, 1Н), 7,28 (m, 2Н), 7,18 (d, 2Н), 6,98 (d, 2Н), 5,1 (s, 2Н), 3,25-3,15 (m, 2Н), 2,88-2,81 (m, 2Н), 2,45 (brs, 1Н), 2,15 (brs, 1Н), 2,05-1,7 (m, 5Н), 1,6-1,3 (m, 3H), 1,25 (d, 1Н); Масса (М+Н): 355,25. Это соединение получали в виде гидрохлорида.
Пример 58: N1-((транс)-2-(6-((3-Метилбензил)амино)пиридин-3-ил)циклопропил)циклогексан-1,4-диамин

Стадия 1:
Раствор трет-бутил-((транс)-2-(6-бромпиридин-3-ил)циклопропил)(4-((Трет-бутоксикарбонил)амино)циклогексил)карбамата (промежуточный продукт BP, 300 мг, 0,58 ммоля), м-толилметанамина (78 мг, 0,64 ммоля), трет-бутоксида натрия (83 мг, 0,87 ммоля) и БИНАФ (2,2'-бис(дифенилфосфино)-1,1'-бинафтил) (108 мг, 0,17 ммоля) в 1,4-диоксане (6 мл) дегазировали в течение 10 мин. Добавляли трис(дибензилиденацетон)дипалладий(0) (26 мг, 0,029 ммоля) и реакционную смесь перемешивали при 100°C в течение 16 ч. После завершения реакции реакционную смесь выливали в охлажденную льдом воду (15 мл) и экстрагировали с помощью EtOAc (2×10 мл). Объединенные экстракты промывали водой (10 мл), рассолом (10 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2) с использованием смеси EtOAc:петролейный эфир (3:7) и получали трет-бутил-(4-((трет-бутоксикарбонил)амино)циклогексил)((транс)-2-(6-((3-метилбензил)амино)пиридин-3-ил)циклопропил)карбамат (100 мг) в виде белого твердого вещества.
Стадия 2:
HCl в 1,4-диоксане (1 мл) при 10°C добавляли к раствору трет-бутил-(4-((трет-бутоксикарбонил)амино)циклогексил)((транс)-2-(6-((3-метилбензил)амино)пиридин-3-ил)циклопропил)карбамата (100 мг, 0,181 ммоля) в диоксане (2 мл), и реакционную смесь перемешивали при КТ в течение 16 ч. После завершения реакции растворитель выпаривали. Твердый остаток растирали с Et2O и гексаном и получали N1-((транс)-2-(6-((3-метилбензил)амино)пиридин-3-ил)циклопропил)циклогексан-1,4-диамин в виде гидрохлорида (60 мг), коричневое твердое вещество.
1Н ЯМР (400 МГц, D2O) δ: 7,68 (d, J=9,6 Гц, 1Н), 7,63 (s, 1H), 7,30 (t, J=8 Гц, 1H), 7,24-7,16 (m, 3H), 6,99 (d, J=9,4 Гц, 2H), 4,56 (s, 2H), 3,58-3,47 (m, 1H), 3,42-3,31 (m, 1H), 3,27-3,17 (m, 1H), 3,05-2,95 (m, 1H), 2,52-2,41 (m, 1H), 2,30 (s, 3H), 2,27-2,23 (m, 1H), 2,20-2,12 (m, 2H), 2,00-1,80 (m, 2H), 1,64-1,39 (m, 4H); Масса (M+H): 351,41
Пример 59: 3-((5-((транс)-2-((4-Аминоциклогексил)амино)циклопропил)пиридин-2-ил)амино)бензонитрил

Стадия 1:
Раствор трет-бутил-(транс)-2-(6-бромпиридин-3-ил)циклопропилкарбамата (промежуточный продукт М, 250 мг, 0,798 ммоля), 3-аминобензонитрила (113 мг, 0,957 ммоля) и трет-бутоксида натрия (115 мг, 1,197 ммоля) в 1,4-диоксане (5 мл) дегазировали в течение 30 мин, затем добавляли трис(дибензилиденацетон)дипалладий(0) (36 мг, 0,039 ммоля) и 4,5-бис(дифенилфосфино)-9,9-диметилксантен (Xantphos) (138 мг, 0,238 ммоля) и реакционную смесь нагревали при 80°C в течение 1 ч. После завершения реакции растворитель выпаривали, остаток переносили в воду со льдом (10 мл) и экстрагировали с помощью EtOAc (2×20 мл). Объединенные экстракты промывали водой (10 мл), рассолом (10 мл), сушили над безводным Na2SO4, фильтровали и выпаривали. Неочищенный остаток очищали с помощью колоночной хроматографии (SiO2) с использованием смеси EtOAc:петролейный эфир (2:8) и получали трет-бутил-((транс)-2-(6-((3-цианофенил)амино)пиридин-3-ил)циклопропил)карбамат (100 мг) в виде желтого твердого вещества.
Стадия 2:
HCl в 1,4-диоксане (1 мл) при 0°C добавляли к раствору трет-бутил-((транс)-2-(6-((3-цианофенил)амино)пиридин-3-ил)циклопропил)карбамата (100 мг, 0,285 ммоля) в 1,4-диоксане (1 мл) и перемешивали при КТ в течение 4 ч. После завершения реакции растворитель выпаривали и остаток растирали с диэтиловым эфиром (5 мл), затем с н-пентаном (5 мл) и получали 3-((5-((транс)-2-аминоциклопропил)пиридин-2-ил)амино)бензонитрил в виде гидрохлорида (80 мг), бледно-желтое твердое вещество.
Стадия 3:
АсОН (11,46 мг, 0,191 ммоля) добавляли к раствору 3-((5-((транс)-2-аминоциклопропил)пиридин-2-ил)амино)бензонитрила (55 мг, 0,191 ммоля) и трет-бутил-4-оксоциклогексилкарбамата (40,68 мг, 0,191 ммоля) в ДХЭ (1 мл) и перемешивали при КТ в течение 15 мин, затем при 0°C добавляли триацетоксиборогидрид натрия (72,8 мг, 0,343 ммоля) и перемешивали при КТ в течение 5 ч. После завершения реакции растворитель выпаривали. Неочищенный остаток переносили в воду (10 мл), подщелачивали с помощью NaHCO3 (10 мл) и экстрагировали с помощью ДХМ (2×10 мл). Объединенные экстракты промывали водой (10 мл), рассолом (10 мл), сушили над безводным Na2SO4, фильтровали и выпаривали и получали трет-бутил-(4-(((транс)-2-(6-((3-цианофенил)амино)пиридин-3-ил)циклопропил)амино)циклогексил)карбамат (75 мг) в виде светло-желтого масла. Неочищенный продукт использовали на следующей стадии без дополнительной очистки.
Стадия 4:
HCl в 1,4-диоксане (1 мл) при 10°C добавляли к раствору трет-бутил-(4-(((транс)-2-(6-((3-цианофенил)амино)пиридин-3-ил)циклопропил)амино)циклогексил)карбамата (75 мг, 0,167 ммоля) в 1,4-диоксане (2 мл) и перемешивали при КТ в течение 16 ч. После завершения реакции растворитель выпаривали. Твердое вещество растирали с Et2O и сушили и получали неочищенный продукт. Неочищенное вещество очищали с помощью препаративной ВЭЖХ и получали 3-((5-((транс)-2-((4-аминоциклогексил)амино)циклопропил)пиридин-2-ил)амино)бензонитрил в виде гидрохлорида (28 мг), почти белое липкое твердое вещество.
1H ЯМР (400 МГц, ДМСО-d6, обмен с D2O) δ: 8,35 (s, 1Н), 8,15 (s, 1H), 7,78 (d, J=8 Гц, 1H), 7,54-7,42 (m, 2H), 7,31 (d, J=8 Гц, 1H), 6,85 (d, J=8,8 Гц, 1H), 3,45-3,17 (m, 2H), 3,08-2,93 (m, 2H), 2,44-2,34 (m, 1H), 2,22-2,10 (m, 1H), 2,09-1,98 (m, 1H), 1,97-1,70 (m, 3H), 1,55-1,32 (m, 4H); Масса (M+H): 348,20
Приведенные ниже соединения можно синтезировать по общим методикам, раскрытым в разделе "Описание общего пути синтеза", включая методологии, описанные на схемах 1, 2, 3, 4, 5, 6, 7 или 8 и в приведенных выше примерах.
Пример 60: N1-((транс)-2-(4'-Хлор-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин

Пример 61: N1-((транс)-2-(3'-Хлор-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин

Пример 62: 4'-((транс)-2-((4-Аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ол

Пример 63: N-(4'-((транс)-2-((4-Аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)метансульфонамид

Пример 64: N1-((транс)-2-(4-((3-Фторбензил)окси)фенил)циклопропил)циклогексан-1,4-диамин

Пример 65: N1-((транс)-2-(4-((4-Фторбензил)окси)фенил)циклопропил)циклогексан-1,4-диамин

Пример 66: N1-Метил-N4-((транс)-2-(3'-(трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклогексан-1,4-диамин
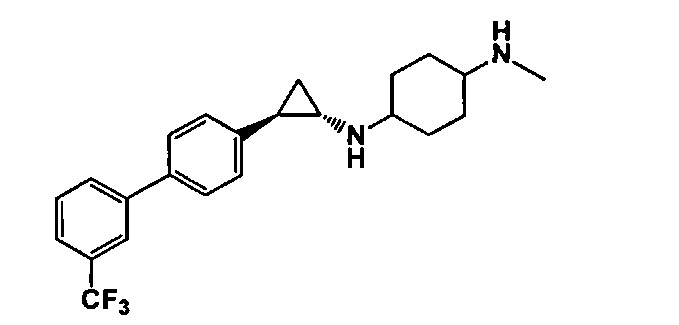
Пример 67: 1N-((транс)-2-(4-(Бензилокси)фенил)циклопропил)-N4-метилциклогексан-1,4-диамин

Пример 68: N1-((транс)-2-(3'-(Трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)циклобутан-1,3-диамин

Пример 69: N1-((транс)-2-(4-(Бензилокси)фенил)циклопропил)циклобутан-1,3-диамин

Пример 70: N1-((транс)-2-(3'-(Трифторметил)-[1,1'-бифенил]-4-ил)циклопропил)-2,3-дигидро-1Н-инден-1,3-диамин
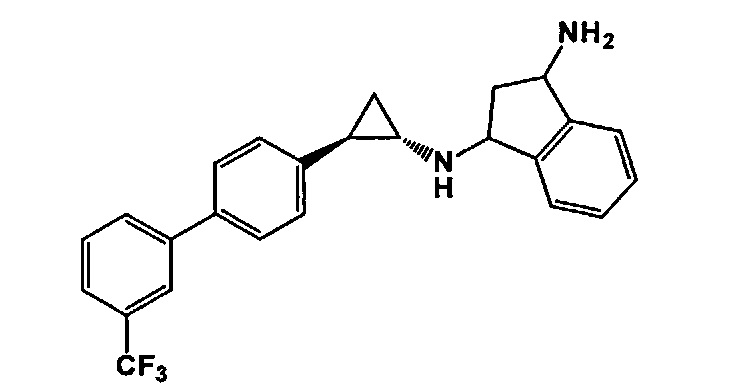
Пример 71: N1-((транс)-2-(4-(Бензилокси)фенил)циклопропил)-2,3-дигидро-1 Н-инден-1,3-диамин

Пример 72: N1-((1S,2S)-2-Фтор-2-фенилциклопропил)циклогексан-1,4-диамин

Пример 73: N1-((1S,2R)-2-Фтор-2-фенилциклопропил)циклогексан-1,4-диамин

Пример 74: N1-((транс)-2-(Нафталин-2-ил)циклопропил)циклогексан-1,4-диамин
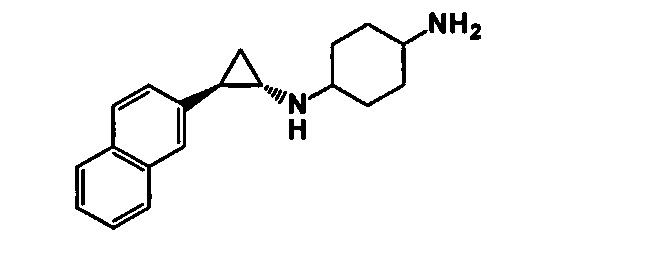
Пример 75: N1-((транс)-2-(о-Толил)циклопропил)циклогексан-1,4-диамин

Пример 76: N1-((транс)-2-(4-(Трифторметил)фенил)циклопропил)циклогексан-1,4-диамин

Пример 77: N1-((транс)-2-(4-Метоксифенил)циклопропил)циклогексан-1,4-диамин

Пример 78: N1-((транс)-2-(2-Фторфенил)циклопропил)циклогексан-1,4-диамин

Пример 79: N1-((транс)-2-(3,4-Дифторфенил)циклопропил)циклогексан-1,4-диамин
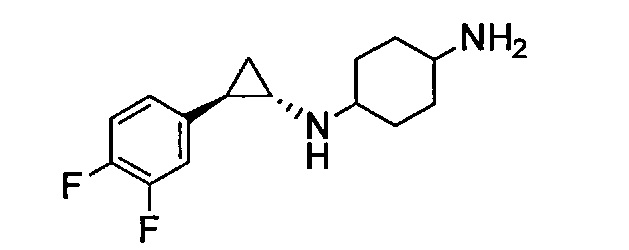
Пример 80: N1-((транс)-2-Метил-2-фенилциклопропил)циклогексан-1,4-диамин

Пример 81: (цис)-N1-((1S,2R)-2-(Пиридин-3-ил)циклопропил)циклогексан-1,4-диамин

Пример 82: (транс)-N1-((1R,2S)-2-(Пиридин-3-ил)циклопропил)циклстексан-1,4-диамин

Пример 83: (цис)-N1-((1R,2S)-2-(Пиридин-3-ил)циклопропил)циклогексан-1,4-диамин

Пример 84: (транс)-N1-((1S,2R)-2-(Пиридин-3-ил)циклопропил)циклогексан-1,4-диамин

Пример 85: (цис)-N1-((1S,2R)-2-Фенилциклопропил)циклобутан-1,3-диамин

Пример 86: (транс)-N1-((1R,2S)-2-Фенилциклопропил)циклобутан-1,3-диамин

Пример 87: (цис)-N1-((1R,2S)-2-Фенилциклопропил)циклобутан-1,3-диамин
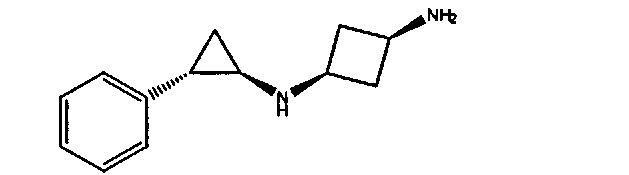
Пример 88: (транс)-N1-((1S,2R)-2-Фенилциклопропил)циклобутан-1,3-диамин
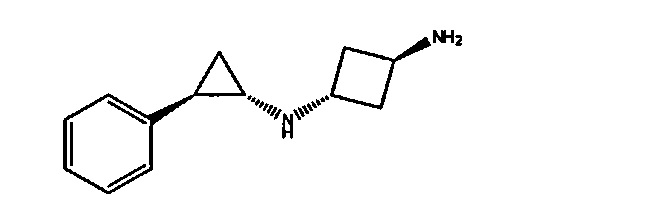
Пример 89: (цис)-N1-((1S,2R)-2-(3,4-Дифторфенил)циклопропил)циклогексан-1,4-диамин

Пример 90: (транс)-N1-((1R,2S)-2-(3,4-Дифторфенил)циклопропил)циклогексан-1,4-диамин

Пример 91: (цис)-N1-((1R,2S)-2-(3,4-Дифторфенил)циклопропил)циклогексан-1,4-диамин

Пример 92: (транс)-N1-((1S,2R)-2-(3,4-Дифторфенил)циклопропил)циклогексан-1,4-диамин
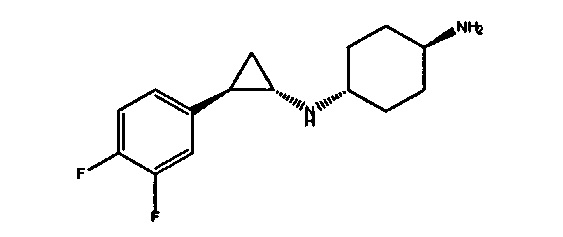
Пример 93: (цис)-N1-((1S,2R)-2-(Нафталин-2-ил)циклопропил)циклогексан-1,4-диамин

Пример 94: (транс)-N1-((1R,2S)-2-(Нафталин-2-ил)циклопропил)циклогексан-1,4-диамин

Пример 95: (цис)-N1-((1R,2S)-2-(Нафталин-2-ил)циклопропил)циклогексан-1,4-диамин

Пример 96: (транс)-N1-((1S,2R)-2-(Нафталин-2-ил)циклопропил)циклогексан-1,4-диамин

Пример 97: (цис)-N1-((1S,2R)-2-(4-(1Н-Пиразол-5-ил)фенил)циклопропил)циклогексан-1,4-диамин

Пример 98: (транс)-N1-((1R,2S)-2-(4-(1Н-Пиразол-5-ил)фенил)циклопропил)циклогексан-1,4-диамин
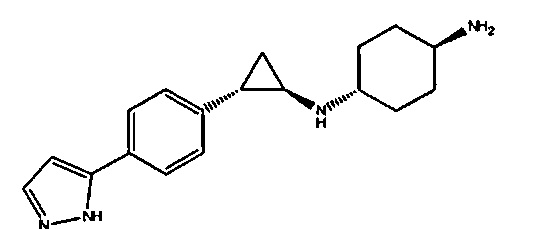
Пример 99: (цис)-N1-((1R,2S)-2-(4-(1Н-Пиразол-5-ил)фенил)циклопропил)циклогексан-1,4-диамин

Пример 100: (транс)-N1-((1S,2R)-2-(4-(1Н-Пиразол-5-ил)фенил)циклопропил)циклогексан-1,4-диамин

Пример 101: N-(4'-((1R,2S)-2-(((цис)-4-Аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)пиперазин-1-сульфонамид

Пример 102: N-(4'-((1S,2R)-2-(((транс)-4-Аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)пиперазин-1-сульфонамид

Пример 103: N-(4'-((1S,2R)-2-(((цис)-4-Аминоциклогексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)пиперазин-1-сульфонамид

Пример 104: N-(4'-((1R,2S)-2-(((транс)-4-Аминоциклстексил)амино)циклопропил)-[1,1'-бифенил]-3-ил)пиперазин-1-сульфонамид

Пример 105: (цис)-N1-((1S,2R)-2-(4-((2-Фторбензил)окси)фенил)циклопропил)циклогексан-1,4-диамин

Пример 106: (транс)-N1-((1R,2S)-2-(4-((2-Фторбензил)окси)фенил)циклопропил)циклогексан-1,4-диамин

Пример 107: (цис)-N1-((1R,2S)-2-(4-((2-Фторбензил)окси)фенил)циклопропил)циклогексан-1,4-диамин

Пример 108: (транс)-N1-((1S,2R)-2-(4-((2-Фторбензил)окси)фенил)циклопропил)циклогексан-1,4-диамин

Биологические исследования
Пример 109: Биологические исследования - ингибирование LSD1 Можно исследовать способность соединений, предлагаемых в настоящем изобретении, ингибировать LSD1. Способность соединений, предлагаемых в настоящем изобретении, ингибировать LSD1 можно изучить следующим образом. Рекомбинантный белок LSD1 человека приобретали у фирмы BPS Bioscience Inc (catalog reference number 50100: рекомбинантный белок LSD1 человека, GenBank accession no. NM_015013, аминокислоты 158-конец, содержит на N-конце метку GST, ММ (молекулярная масса): 103 кДа). Для изучения ферментативной активности LSD1 и/или степени его ингибирования рассматриваемым ингибитором (ингибиторами) в качестве субстрата выбран диметилированный пептид Н3-К4 (Anaspec). Активность деметилазы оценивали при анаэробных условиях путем определения количества H2O2, образовавшегося при каталитической реакции с использованием набора для исследования Amplex® Red пероксид/пероксидаза (Invitrogen).
Вкратце, методика заключалась в следующем: определенное количество LSD1 инкубировали на льду в течение 15 мин при отсутствии и/или в присутствии соответствующего ингибитора с использованием по меньшей мере восьми 3-кратных серийных разведений (например, от 0 до 75 мкМ, в зависимости от активности ингибитора). В качестве контроля для ингибирования использовали транилципромин (Biomol International). При проведении эксперимента каждую концентрацию ингибитора исследовали дважды. После введения фермента в реакцию с ингибитором в каждую реакционную смесь добавляли КM диметилированного пептида Н3-К4 и реакционную смесь выдерживали в темноте при 37°C в течение 1 ч. Реакции ферментов проводили в буфере, содержащем 50 мМ фосфат натрия, pH 7,4. После завершения инкубации к реакционной смеси добавляли реагент Amplex® Red и раствор пероксидазы хрена (ПРХ) в соответствии с инструкциями поставщика (Invitrogen) и инкубацию проводили в темноте комнатной температуре в течение еще 5 мин при. Для проверки эффективности набора использовали 1 мкМ раствор H2O2. За превращением реагента Amplex® Red в резоруфин вследствие наличия H2O2 в реакционной смеси следили по флуоресценции (возбуждение при 540 нм, испускание при 590 нм) с использованием считывающего устройства для микропланшетов (Infinite 200, Tecan). Для определения содержания H2O2, образовавшегося при отсутствии и/или в присутствии ингибитора использовали произвольные единицы.
Максимальная активность деметилазы по отношению к LSD1 наблюдалась при отсутствии ингибитора и вносили поправку на фоновую флуоресценцию при отсутствии LSD1. 3Hачение IC50 для каждого ингибитора определяли с помощью программного обеспечения GraphPad Prism.
В приведенной ниже таблице 1 представлены данные исследования по ингибированию LSD1 целым рядом соединений примеров. В таблице 2 приведены значения IC50 для всех соединений примеров, изученных в этом исследовании. Обнаружено, что парнат (транилципромин; т.е. 2-транс-фенилциклопропиламин) обладает значением IC50, равным 35±10 мкМ. Эти исследования показывают, что соединения, предлагаемые в настоящем изобретении, неожиданно активно ингибируют LSD1.
Пример 110: Биологические исследования - использование моноаминоксидазы для определения селективности соединений, предлагаемых в настоящем изобретении, по отношению к LSD1
Рекомбинантные белки моноаминоксидазы человека МАО-А и МАО-В приобретали у фирмы Sigma Aldrich. МАО катализируют окислительное дезаминирование первичных, вторичных и третичных аминов. Для определения ферментативной активности МАО и/или степени их ингибирования рассматриваемым ингибитором (ингибиторами) использовали скрининг ингибиторов на основе флуоресценции. В качестве субстрата выбрано нефлуоресцирующее соединение 3-(2-аминофенил)-3-оксопропанамин (кинураминдигидробромид, Sigma Aldrich). Кинурамин является неспецифическим субстратом для определения активности обоих МАО. При изучении окислительного дезаминирования с помощью МАО кинурамин превращается во флуоресцирующий продукт, 4-гидроксихинолин (4-HQ).
Активность моноаминоксидазы оценивали путем определения степени превращения кинурамина в 4-гидроксихинолин. Исследования проводили в черных 96-луночных планшетах с прозрачным дном (Corning) при конечном объеме, равном 100 мкл. Буфером для исследования являлся 100 мМ HEPES (N-2-гидроксиэтилпиперазин-N-2-этансульфоновая кислота), рН 7,5. Каждый эксперимент в каждой серии проводили дважды.
Вкратце, методика заключалась в следующем: определенное количество МАО (0,25 мкг МАО-А и 0,5 мкг МАО-В) инкубировали на льду в течение 15 мин в буфере для проведения реакции при отсутствии и/или в присутствии соединения с использованием в каждом случае по меньшей мере восьми 3-кратных серийных разведений (например, от 0 до 50 мкМ, в зависимости от активности ингибитора). В качестве контроля для специфического ингибирования МАО-А и МАО-В использовали клоргилин и депренил (Sigma Aldrich) соответственно.
После введения фермента (ферментов) в реакцию с ингибитором в каждую реакционную смесь добавляли Км кинурамина для исследования МАО-В и МАО-А соответственно и реакционную смесь выдерживали в темноте при 37°C в течение 1 ч. Окислительное дезаминирование субстрата останавливали путем добавления 50 мкл 2 н. раствора NaOH. За превращением кинурамина в 4-гидроксихинолин следили по флуоресценции (возбуждение при 320 нм, испускание при 360 нм) с использованием считывающего устройства для микропланшетов (Infinite 200, Tecan). Для определения интенсивности флуоресценции при отсутствии и/или в присутствии ингибитора использовали произвольные единицы.
Максимальная активность окислительного дезаминирования наблюдалась при определении содержания 4-гидроксихинолина, образовавшегося из кинурамина при отсутствии ингибитора с поправкой на фоновую флуоресценцию при отсутствии ферментов МАО. Значения IC50 для каждого ингибитора рассчитывали с помощью программного обеспечения GraphPad Prism.
Ниже приведены результаты, полученные для соединений, предлагаемых в настоящем изобретении, в биологических исследованиях, приведенных в примерах 109 и 110.

Диапазоны значений Ki, приведенные в таблице 1, составляют для МАО-А, МАО-В и LSD1:I = более 40 мкМ; II = от 1 мкМ до 40 мкМ; III от 0,1 мкМ до 1 мкМ; IV = от 0,001 мкМ до 0,1 мкМ. Термин "значение Ki" используют в настоящем изобретении для обозначения значения IC50, т.е. концентрации, необходимой для равного половине максимального (50%) ингибирования соответствующей мишени (МАО-А, МАО-В или LSD1).
В целом установлено, что соединения, предлагаемые в настоящем изобретении, обладают чрезвычайно низкими значениями IC50 для LSD1, по сравнению со значениями для МАО-А и МАО-В. Для некоторых соединений примеров значения IC50 для LSD1 составляли менее 0,1 мкМ.
Конкретные значение IC50, полученные для соединений, раскрытых в примерах, при их изучении в исследованиях, приведенных в примерах 109 (ингибирование LSD1) и 110 (ингибирование МАО-А и -В), приведены ниже в таблице 2:



Как видно из данных, представленных в приведенной ниже таблице, соединения, предлагаемые в настоящем изобретении, являются очень активными ингибиторами LSD1 и в некоторых случаях обладают значениями IC50, равными ниже 100 нМ или даже ниже 50 нМ. Кроме того, соединения обладают высокой селективностью по отношению к LSD1 по сравнению с селективностью по отношению к МАО-А и МАО-В, и обладают значениями IC50 для LSD1, обычно в ≥100 раз меньшими, чем соответствующие значения IC50 для МАО-А и МАО-В.
Пример 111: Исследование в клетках - индуцирования дифференциации лейкозных клеток ТНР-1
Острый миелолейкоз (ОМЛ) характеризуется наличием лейкозных клеток, созревание которых останавливается и они быстро делятся. При индуцировании конечной дифференцировки клетки ОМЛ утрачивают способность пролиферировать и гибнут без необходимости прямого цитотоксического воздействия.
С помощью анализа индуцирования мембранной экспрессии CD11b в клетках ТНР-1 в настоящем изобретении исследовали способность ингибиторов LSD1 индуцировать конечную моноцитарную дифференциацию клеток ОМЛ линии MLL-AF9.
Исследование проводили следующим образом:
Клетки ТНР-1 готовили из периферической крови мальчика в возрасте 1 год с рецидивом острого моноцитарного лейкоза в 1978 г. Они обладали хромосомной перестройкой t(9; 11)(p21; q23), что генерирует ген слияния MLL-MLLT3 (MLL-AF9). Клетки этой линии могут подвергаться моноцитарной дифференциации при обработке соответствующими стимулами. ТНР-1 приобретали у фирмы DSMZ GmbH (Deutsche Sammlung von Mikroorganismen und Zellkulturen) и выращивали в среде RPMI 1640, содержащей 10% фетальной бычьей сыворотки.
В этом исследовании в 6-луночные планшеты для выращивания культур тканей высевали 150000 клеток ТНР-1 в 1 мл полной культуральной среды. Серийные разведения соединений готовили в ДМСО и затем дополнительно разводили в полной среде и получали растворы, концентрация которых равнялась удвоенной конечной концентрации, при которой обрабатывали клетки. 1 мл Этих 2× концентрированных растворов добавляли к клеткам. Конечное содержание ДМСО должно быть одинаковым во всех клетках и поддерживаться равным ниже 0,1% об./об. (обычно 0,01-0,02% об./об.), поскольку при более высоком содержании ДМСО может индуцироваться дифференциация клеток ТНР-1.
Клетки выдерживали в присутствии исследуемого соединения в атмосфере, содержащей 5% СO2, при 37°C в течение 96 ч. После завершения обработки клетки собирали, дважды промывали буфером ЗФФ (забуференный фосфатом физиологический раствор) и помещали в 96-луночный планшет с V-образным дном. Каждый обработанный образец разделяли на две части. Одну часть окрашивали мечеными фикоэритрином антителами к CD11b (клон ICRF44, приобретали у фирмы eBiosciences) и другую часть окрашивали соответствующими мечеными фикоэритрином изотипами контрольных антител (мышиные антитела к IgG1, приобретали у фирмы eBiosciences). Образцы инкубировали в темноте при 4°C в течение 30-60 мин и трижды промывали буфером ЗФФ, содержащим 1% фетальной бычьей сыворотки.
Образцы анализировали с помощью проточного цитометра, снабженного синим лазером (488 нм). Испускание флуоресценции детектировали и интенсивность флуоресценции количественно определяли с использованием фильтра 575/30 нм. Выраженную в процентах долю клеток CD11b с положительной реакцией, как индикатора моноцитарной дифференциации, определяли путем сопоставления с клетками, окрашенные изотипами контрольных антител. Значения ЕС50 рассчитывали с помощью нелинейного регрессионного анализа.

Эти результаты показывают, что соединения, предлагаемые в настоящем изобретении, обладают очень высокой активностью в отношении индуцирования дифференциации лейкозных клеток ТНР-1 и это показывает, что эти соединения являются особенно подходящими для лечения или предупреждения лейкозов.
В предшествующих публикациях об LSD1 установлено, что она участвует в пролиферации и росте клеток. В некоторых исследованиях LSD1 рассматривалась в качестве мишени терапевтического воздействия при раке. В публикации Huang et al. (2007) PNAS 104: 8023-8028 установлено, что полиаминовые ингибиторы LSD1 в раковых клетках приводят к умеренной реэкспресии генов, которые в результате аберрации стали молчащими, в особенности при колоректальном раке (Huang et al. Clin Cancer Res. (2009) Dec1; 15 (23): 7217-28. Epub 2009 Nov 24. PMID: 19934284). В публикации Scoumanne et al. ((2007) J. Biol. Chem. May 25; 282 (21): 15471-5) установлено, что недостаток LSD1 приводит частичной остановке клеточного цикла в G2/M и сенсибилизированных клетках и усилению супрессии, вызванной повреждением ДНК. В публикации Kahl et al. ((2006) Cancer Res. 66 (23): 11341-7.) установлено, что экспрессия LSD1 коррелирует с агрессивностью рака предстательной железы. В публикации Metzger et al. ((2005) Nature, 437 (7057), 436-439) сообщают, что модулирование LSD1 с помощью siPHK и паргилина регулирует андрогенный рецептор (АР) и, вероятно, может использоваться для лечения типов рака, при которых играет роль АР, таких как рак предстательной железы, яичников и головного мозга. В публикации Lee et al. ((2006) Chem. Biol. 13: 563-567) сообщают, что в некоторых линиях раковых клеток транилципромин дерепрессирует ген Egr-1. Имеется много данных о том, что во многих случаях Egr-1 является геном-супрессором опухолей. Например, в публикации Calogero et al. (2004) Cancer Cell International 4:1, экзогенная экспрессия Egr-1 приводит к остановке роста и в конечном счете к гибели первичных линий раковых клеток; в публикации Lucerna et al. (2006) Cancer Research 66, 6708-6713, показано, что длительная экспрессия Egr-1 в некоторых моделях приводит к антиангиогенному эффекту и подавляет рост опухолей; в публикации Ferraro et al. ((2005) J. Clin. Oncol. Mar 20; 23 (9): 1921-6) сообщают, что Egr-1 подвергается понижающей регуляции у пациентов, страдающих раком легких с высоким риском рецидива, и может быть более устойчивым к терапии. Таким образом, усиление экспрессии Egr-1 путем ингибирования LSD1 является методикой лечения некоторых типов рака. В недавних исследованиях показано, что LSD1 также участвует в раке головного мозга (Schulte et al. (2009) Cancer Res. Mar 1; 69 (5): 2065-71). В других исследованиях показано, что LSD1 участвует в раке молочной железы (Lims et al. Carcinogenesis, (2010), 31 (3): 512-20, Epub 2009 Dec 30. [Epub ahead of print] PMID: 20042638), раке легких, раке мочевого пузыря и колоректальном раке (Hayami et al (2011), Int J Cancer, 128 (3): 574-86, PMID:20333681), и лейкозе (Binda et al (2010), J Am Chem Soc, 132 (19): 6827-33, PMID: 20415477).
Таким образом, большое количество данных показывает, что LSD1 участвует в целом ряде раковых заболеваний, что указывает на то, что LSD1 является мишенью терапевтического воздействия при раке. Авторы настоящего изобретения обнаружили класс ингибиторов LSD1, которые можно использовать для лечения заболеваний, в которых мишенью для лечения является LSD1, таких как рак. В соответствии с этим (гетеро)арилциклопропиламины, предлагаемые в настоящем изобретении, можно использовать для лечения таких заболеваний.
Недавние исследования показали, что LSD1 также участвует в вирусной инфекции и реактивации вируса. В частности, показано, что фармакологические ингибиторы LSD1, такие как парнат и siPHK, лишенная LSD1, приводят к уменьшенной вирулентности и уменьшают реактивацию после латентного периода (Liang et al. (2009) Nat. Med. 15: 1312-1317). Поэтому предполагается, что соединения, предлагаемые в настоящем изобретении, можно использовать для лечения или предупреждения вирусной инфекции. Кроме того, предполагается, что соединения, предлагаемые в настоящем изобретении, могут лечить или предупреждать реактивацию вируса после латентного периода.
Таким образом, если не ограничиваться теоретическими соображениями, то можно сделать вывод о том, согласно изобретению выявлен новый класс ингибиторов LSD1 на основе циклопропанамина, обладающие неожиданной активностью и селективностью по отношению к LSD1, биологически важной мишени при онкологических и других заболеваниях.
Все публикации и заявки на патенты включены в настоящее изобретение в качестве ссылки в такой же степени, как, если бы для каждой отдельной публикации или заявки на патент было специально и по отдельности указано, что она включена в настоящее изобретение в качестве ссылки. Простое указание на публикации и заявки на патенты необязательно является признанием того, что они являются предшествующим уровнем техники для настоящей заявки.
Хотя выше настоящее изобретение подробно описано в качестве иллюстрации и примера для облегчения понимания, очевидно, что в объеме прилагаемой формулы изобретения в него можно внести некоторые изменения и модификации.
Реферат
Изобретение относится к новому (гетеро)арилциклопропиламину формулы I или его фармацевтически приемлемой соли, где заместители -А-В и -NH-D циклопропильного фрагмента могут находиться в транс-конфигурации или соединение может быть оптически активным стереоизомером. Соединения обладают свойствами ингибитора лизинспецифической деметилазы-1 (LSD1) и могут найти применение для лечения рака, выбранного из группы, включающей рак молочной железы, рак легких, рак предстательной железы, колоректальный рак, рак головного мозга, рак кожи, рак крови, лейкоз, лимфому и миелому. При этом лейкоз может представлять собой острый миелолейкоз (ОМЛ), хронический миелолейкоз (ХМЛ), хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический лимфолейкоз (ХЛЛ), острый лимфобластный лейкоз (ОЛЛ) и волосатоклеточный лейкоз. Соединения также могут найти применение для лечения или предупреждения вирусной инфекции, в том числе для лечения или предупреждения реактивации вируса после латентного периода, который связан с LSD1. В соединении формулы IА обозначает фенил, нафтил, пиридил, тиофенил, пирролил, фуранил или тиазолил, где указанный фенил, указанный нафтил, указанный пиридил, указанный тиофенил, указанный пирролил, указанный фуранил или указанный тиазолил необязательно замещен одним или большим количеством R; В обозначает водород, Rили -L-E; Е обозначает фенил, пиридинил, пиразолил или индазолил, где указанный фенил, указанный пиридинил, указанный пиразолил или указанный индазолил необязательно замещен одним или большим количеством R; L обозначает связь, -О-, -NH-, -CH-NH- или -СН-О-, где указанные группы -CH-NH- и -СН-О- связаны с кольцом А через атом N или О соответственно и связаны с кольцом Е через группу -СН-, содержащуюся в указанных группах -CH-NH- и -СН-О-; D выбран из D1, D2, D3 и D4:где циклобутильное кольцо, содержащееся в D1, циклопентильное кольцо, содержащееся в D2, циклогексильное кольцо, содержащееся в D3, и циклогептильное кольцо, содержащееся в D4, необязательно замещено одним или большим количеством R; каждый Rнезависимо выбран из группы, включающей галоген, С-С-алкил, галоген-С-С-алкил, С-С-алкоксигруппу и С-С-циклоалкил; каждый Rнезависимо выбран из группы, включающей С-С-алкил, гидроксигруппу, галоген, галоген-С-С-алкил, галоген-С-С-алкоксигруппу, цианогруппу, N-сульфонамидную группу и C-C-алкоксигруппу; Rвыбран из группы, включающей -NRRи -C-C-алкилен-NRR; каждый Rнезависимо выбран из группы, включающей C-C-алкил, галоген, галоген-С-С-алкил, галоген-С-С-алкоксигруппу и С-С-алкоксигруппу; каждый Rи каждый Rнезависимо выбран из группы, включающей водород, C-C-алкил, RRN-C-C-алкил и гидрокси-С-С-алкил, или Rи Rсвязаны друг с другом и вместе с атомом N, к которому они присоединены, образуют насыщенное 3-7-членное гетероциклическое кольцо, которое необязательно содержит один дополнительный гетероатом, выбранный из группы, включающей N, О и S, где один или большее количество атомов С указанного гетероциклического кольца необязательно окислены с образованием групп СО, где один или большее количество атомов S указанного гетероциклического кольца, если они содержатся, необязательно окислены с независимым образованием групп SO или групп SO, и где указанное гетероциклическое кольцо необязательно замещено одним или большим количеством R; каждый Rнезависимо выбран из группы, включающей С-С-алкил, галоген, C-C-алкоксигруппу, гидроксигруппу и -NRR; каждый Rи каждый Rнезависимо выбран из группы, включающей водород и C-C-алкил; каждый R, R, Rи Rнезависимо выбран из группы, включающей водород, галоген и С-С-алкил. 15 н. и 73 з. п. ф-лы, 3 табл., 111 пр.
Формула




















Документы, цитированные в отчёте о поиске
Лизинспецифические ингибиторы деметилазы-1 и их применение
Лизинспецифические ингибиторы деметилазы-1 и их применение

Комментарии