Бензотиофеновые селективные блокаторы эстрогеновых рецепторов - RU2747802C2
Код документа: RU2747802C2
Чертежи

Описание
Ссылка на связанные заявки
Согласно настоящей заявке испрашивается приоритет в соответствии с предварительной заявкой США 62/264971, поданной 9 декабря 2015 г., и предварительной заявкой США 62/322878, поданной 15 апреля 2016 г. Содержимое этих заявок включено в настоящий документ посредством ссылки для всех целей.
Область техники, к которой относится настоящее изобретение
Настоящее изобретение предусматривает соединения и композиции, которые включают бензотиофеновые лиганды эстрогеновых рецепторов и применения этих соединений для лечения нарушений, связанных с эстрогенами.
Заявление о наличии конфликта интересов со стороны государства
Настоящее изобретение было выполнено при государственной поддержке согласно контракту №1R01CA188017-01A1, заключенному с Национальным институтом здоровья. Государство обладает определенными правами на настоящее изобретение.
Предшествующий уровень техники настоящего изобретения
Эстрогены представляют собой основные женские гормоны, ответственные за развитие и регуляцию женской половой системы и вторичных женских половых признаков. Эстрогены также выполняют многочисленные функции в синтезе белка, коагуляции, липидном балансе, водном балансе, регуляции меланина, функционировании желудочно-кишечного тракта, функционировании легких, когнитивной деятельности, иммунном ответе и сердечнососудистых заболеваниях, в числе прочего.
Эстрогеновый рецептор («ER») представляет собой активируемый лигандом транскрипционный регуляторный белок, который опосредует индукцию ряда биологических эффектов посредством своего взаимодействия с эндогенными эстрогенами, в том числе 17β-эстрадиолом и эстронами. Было обнаружено, что ER имеет две изоформы, ER-α и ER-β, и оба рецептора участвуют в регуляции и развитии женский половых путей.
ER и эстрогены регулируют биологические процессы посредством нескольких отдельных путей. Классический путь предусматривает связывание активированного лигандом ER со специфическим мотивом последовательности ДНК, называемым эстроген-активным элементом (ERE). ER могут также участвовать в неклассических путях, таких как ERE-независимая транскрипция генов посредством белок-белкового взаимодействия с другими факторами транскрипции, негеномных путях с быстрыми эффектами и лиганд-независимых путях, которые предусматривают активацию посредством других сигнальных путей. Такая передача сигнала при участии ER является определяющей не только для развития и функционирования женских половых органов, но также для метаболизма и массы костной ткани, метаболизма липидов, сердечно-сосудистой защиты и передачи сигналов в центральной нервной системе.
Исследования в данной области подтвердили огромную сложность видов активности эстрогена и ER. Целью разработки лекарственных средств было создание новых соединений, которые модулируют активность эстрогена, в результате функционирования либо в качестве антагониста или агониста, либо в качестве частичного антагониста либо частичного агониста.
Одной целью было выявление полных антиэстрогенов (полных антагонистов), которые имеют эффект подавления блокировки всей эстрогенной активности в организме. Фулвестрант представляет собой пример полного антагониста эстрогеновых рецепторов, при этом агонистичекая активность отсутствует. Он представляет собой селективный блокатор эстрогеновых рецепторов (SERD). Фулвестрант был раскрыт компанией Imperial Chemical Industries (ICI) в патенте США №4659516 и продается компанией AstraZeneca под названием фаздолекс. Он показан для лечения гормон-рецептор-положительной метастатической злокачественной опухоли молочной железы у женщин постменопаузального периода с прогрессированием заболевания после антиэстрогенной терапии. Фулвестрант имеет ограниченную водорастворимость и требует ежемесячных внутримышечных (IM) инъекций. Нерастворимость фулвестранта в воде создает проблему достижения и поддержания эффективных концентраций в сыворотке.
Другим классом антиэстрогенов являются селективные модуляторы эстрогеновых рецепторов (SERM), которые выступают в роли антагонистов или агонистов геноспецифическим или тканеспецифическим образом. Целью терапии SERM является выявление лекарственных средств со смешанными профилями, которые обеспечивают полезную целевую антиэстрогенную активность, а также либо не допускают побочные внецелевых эффектов, либо характеризуются случайными полезными эстрогеновыми побочными эффектами. Примером SERM является тамоксифен, изначально продаваемый компанией AstraZeneca под названием нолвадекс. Тамоксифен был также раскрыт компанией ICI в патенте США №4659516 (см. также патенты США №№6774122 и 7456160). Тамоксифен представляет собой пролекарственное средством, которое метаболизируется до 4-гидрокситамоксифена и N-десметил-4-гидрокситамоксифена, которые характеризуются высокой аффинностью связывания с эстрогеновым рецептором. Тамоксифен показан для предупреждения дальнейшего развития злокачественной опухоли молочной железы после лечения злокачественной опухоли молочной железы и для лечения злокачественной опухоли молочной железы с поражением лимфоузлов у женщин после мастектомии и лучевой терапии. Тамоксифен может влиять на состояние костной ткани. У женщин предменопаузального периода тамоксифен может вызывать истончение костей, в то время как может быть полезным для костной ткани у женщин в постменопаузальном периоде. Были отмечены серьезные побочные эффекты, в том числе повышенный риск злокачественной опухоли матки у женщин в постменопаузальном периоде и «опухолевые обострения» у женщин со злокачественной опухолью молочной железы, которая распространилась в костную ткань. Помимо этих побочных эффектов, некоторые женщины, которые изначально отвечали на тамоксифен, со временем испытывают приобретенную резистентность, и в некоторых случаях ER-положительная злокачественная опухоль молочной железы не только становится резистентной к тамоксифену, но тамоксифен становится агонистом, который индуцирует опухолевую пролиферацию.
Третья линия терапии злокачественной опухоли молочной железы предусматривает стероидные и нестероидные ингибиторы ароматазы, которые блокируют образование эстрогенов и, тем самым, блокируют ER-зависимый рост. Эти лекарственные средства, которые включают летрозол, анастрозол и эксеместан, характеризуются риском исключения всех эстрогенов из организма женщин после менопаузы, повышая риск истончения костей, остео пороза и переломов.
Был раскрыт ряд SERD, SERM и ингибиторов ароматазы. SERM ралоксифен был раскрыт компанией Eli Lilly в 1981 г. (патенты США №№4418068; 5478847; 5393763; и 5457117) для предупреждения злокачественной опухоли молочной железы и лечения остеопороза. В июне 2011 г. компания Aragon Pharmaceuticals раскрыла бензопирановые производные и аналоги аколбифена для лечения резистентной к тамоксифену злокачественной опухоли молочной железы (см. WO 2011/156518, патенты США №№8455534 и 8299112). Компания Aragon стала называться Seragon в 2013 г., а в 2014 г. был приобретен Genentech. См. также патенты США №№9078871; 8853423; 8703810; US 2015/0005286; и WO 2014/205138. В настоящее время компания Genentech разрабатывает бриланстрант (GDC-0810, ранее ARN-810) для лечения местнораспространенной или метастатической эстроген-рецептор-положительной злокачественной опухоли молочной железы.
Компания Genentech раскрыла ряд соединений на основе тетрагидропиридо[3,4-b]индол-1-ила с модулирующей активностью по отношению к эстрогеновым рецепторам в US 2016/0175289 и комбинированную терапию трех соединений, одним из которых был GDN-0810, для модулирования эстрогеновых рецепторов в US 2015/0258080.
Компания AstraZeneca в настоящее время разрабатывает AZD9496, новый селективный блокатор эстрогеновых рецепторов для перорального применения у пациентов с эстроген-рецептор-положительной злокачественной опухолью молочной железы (WO 2014/191726).
Дополнительные антиэстрогенные соединения раскрыты в WO 2012/084711; WO 2002/013802; WO 2002/004418; WO 2002/003992; WO 2002/003991; WO 2002/003990; WO 2002/003989; WO 2002/003988; WO 2002/003986; WO 2002/003977; WO 2002/003976; WO 2002/003975; WO 2006/078834; US 6821989; US 2002/0128276; US 6777424; US 2002/0016340; US 6326392; US 6756401; US 2002/0013327; US 6512002; US 6632834; US 2001/0056099; US 6583170; US 6479535; WO 1999/024027; US 6005102; EP 0802184; US 5998402; US 5780497 и US 5880137.
Компания J-Pharma в настоящее время разрабатывает бензотиофеновые соединения для лечения нарушений, связанных с транспортом уратов. См., например, WO 2012/048058.
Компания Bionomics LTD разрабатывает бензофураны, бензотиофены, бензоселенофены и индолы для лечения нарушений, связанных с полимеризацией тубулина. См., например, WO 2007/087684.
Дополнительные бензотиофеновые соединения раскрыты в WO 2010/127452, WO 2010/093578, WO 2009/013195, EP 1947085, JP 2005-129430, US 2007/0112009, WO 2005/016929, EP 0752421, EP 0622673, EP 0551849, EP 0545478, US 5491123 и WO 2006/084338.
Принимая во внимание часто разрушающие воздействия расстройств, модулирующих эстрогены, в том числе злокачественных опухолей, опухолей и, в частности, злокачественной опухоли молочной железы, сохраняется существенная необходимость в создании новых лекарственных средствах, которые обладают значительной антиэстрогенной эффективностью, при этом отсутствуют неприемлемые побочные эффекты.
Краткое раскрытие настоящего изобретения
Предусмотрены бензотиофеновые соединения и их фармацевтически приемлемые соли, которые характеризуются предпочтительной селективной модулирующей активностью по отношению к эстрогеновым рецепторам, и, в частности, антиэстрогенной активностью. Эти соединения можно применять для лечения пациента, обычно человека, с нарушением, связанным с эстрогенами, в том числе без ограничения злокачественной опухолью или опухолью, посредством введения эффективного количества пациенту, нуждающемуся в этом, необязательно в фармацевтически приемлемом носителе. В соответствии с определенными вариантами осуществления злокачественную опухоль выбирают из таковой молочной железы, яичника, эндометрия, почки и матки. В соответствии с другим вариантом осуществления злокачественная опухоль представляет собой метастатическую резистентную к эндокринной терапии злокачественную опухоль молочной железы. Альтернативно соединение или его фармацевтически приемлемую соль можно применять для предупреждения нарушения, опосредованного эстрогенами, в том числе без ограничения злокачественной опухоли или опухоли, в том числе таковых молочной железы, яичника, эндометрия, почки и матки. В соответствии с некоторыми вариантами осуществления соединение применяется после химиотерапии или лучевой терапии в целях избежания рецидива или вместо химиотерапии или лучевой терапии в качестве первичного лечения.
В соответствии с одним вариантом осуществления соединение по настоящему изобретению представляет собой селективный блокатор эстрогена (SERD). В соответствии с другим вариантом осуществления соединение по настоящему изобретению может представлять собой селективный блокатор смешанных эстрогеновых рецепторов (SMERD). В соответствии с одним вариантом осуществления соединение вызывает антагонизм E2 в эпителиальных клетках молочной железы и вызывает значительное разрушение ERα.
В соответствии с одним аспектом соединение по настоящему изобретению или его фармацевтически приемлемая соль или пролекарственное средство можно применять для лечения гормональной злокачественной опухоли или опухоли, которая метастазировала в головной мозг, костную ткань или другой орган. В соответствии с одним вариантом осуществления данного аспекта гормональная злокачественная опухоль является эстроген-опосредованной. В соответствии с другим вариантом осуществления эстроген-опосредованную злокачественную опухоль выбирают из таковой молочной железы, матки, яичника и эндометрия. В соответствии с другими вариантами осуществления соединение по настоящему изобретению или его фармацевтически приемлемая соль или пролекарственное средство можно применять для предупреждения гормональной злокачественной опухоли или опухоли от метастазирования в головной мозг, костную ткань или другой орган, в том числе гормональной злокачественной опухоли, которая является эстроген-опосредованной, например, таковой молочной железы, матки, яичника или эндометрия.
Согласно одному аспекту настоящее изобретение относится к соединению формулы А или его фармацевтически приемлемой соли:
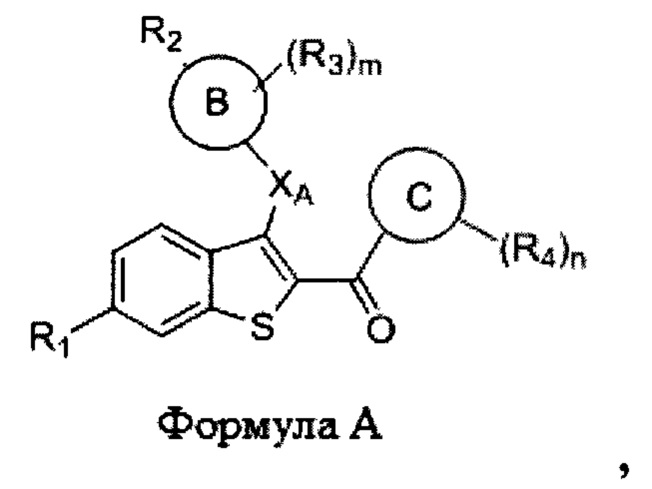
где:
m равно 0, 1, 2, 3 или 4;
n равно 0, 1, 2, 3 или 4;
XA выбран из -O-, -СН2-, -S-, -NH-, -NMe-, -CF2- и С3циклоалкила;
Кольцо В представляет собой фенил, нафтил, хинолинил, 5- или 6-членный моно циклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
Кольцо С представляет собой фенил, тиофенил (т.е., тиенил), 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
R1 выбран из гидроксила, водорода, галогена, -O(C1-C6 алкил), -OC(O)(C1-C6 алкил), -ОС(O)С6Н5, -ОС(O)O(C1-C6 алкил), -ОС(O)ОС6Н5 и -OSO2(C2-C6 алкил);
R2 выбран из -СН=СНСООН, -NH(CO)COOH, -СООН, -C2-C6алкенилен-СООН и -C2-C6алкинилен-СООН;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, -C1-C6алкила и -C1-C6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-С6алкила, -C1-C6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно другому аспекту настоящее изобретение включает в себя фармацевтическую композицию, которая включает в себя соединение формулы А и фармацевтически приемлемый носитель или наполнитель.
Согласно другому аспекту настоящее изобретение относится к способу лечения или предупреждения опухоли или злокачественной опухоли, который включает в себя введение субъекту, типично человеку, при необходимости такого лечения терапевтически эффективного количества соединения формулы А или его фармацевтически приемлемой соли.
Согласно другому аспекту настоящее изобретение относится к соединению формулы В или его фармацевтически приемлемой соли:
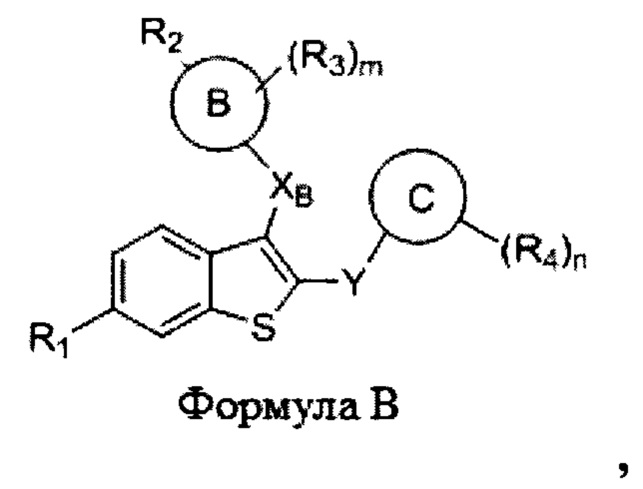
где:
m равно 0, 1, 2, 3 или 4;
n равно 0, 1, 2, 3 или 4;
XB выбран из -O-, -СН2-, -S-, -NH-, -NMe-, -CF2- и -С3циклоалкил-;
Y выбран из -С(O)-, -O-, -CF2- или -С3циклоалкил-, -СН2-, -S-, -NH- и -N(Me)-;
Кольцо В представляет собой фенил, нафтил, хинолинил, 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
Кольцо С представляет собой фенил, тиофенил (т.е., тиенил), 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
R1 выбран из гидроксила, водорода, галогена, -O(C1-C6 алкил), -OC(O)(C1-C6 алкил), -ОС(O)С6Н5, -ОС(O)O(C1-C6 алкил), -ОС(O)ОС6Н5 и -OSO2(C2-C6 алкил);
R2 выбран из -СН=СНСООН, -NH(CO)COOH, -COOH, -C2-C6алкенилен-СООН и -C2-C6алкинилен-СООН;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, -C1-C6алкила и -C1-C6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-С6алкила, -C1-C6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно другому аспекту настоящее изобретение включает в себя фармацевтическую композицию, которая включает в себя соединение формулы В и фармацевтически приемлемый носитель или наполнитель.
Согласно другому аспекту настоящее изобретение относится к способу лечения или предупреждения опухоли или злокачественной опухоли, который включает в себя введение субъекту, типично человеку, при необходимости такого лечения терапевтически эффективного количества соединения формулы В или его фармацевтически приемлемой соли.
Согласно другому аспекту настоящее изобретение относится к соединению формулы С:
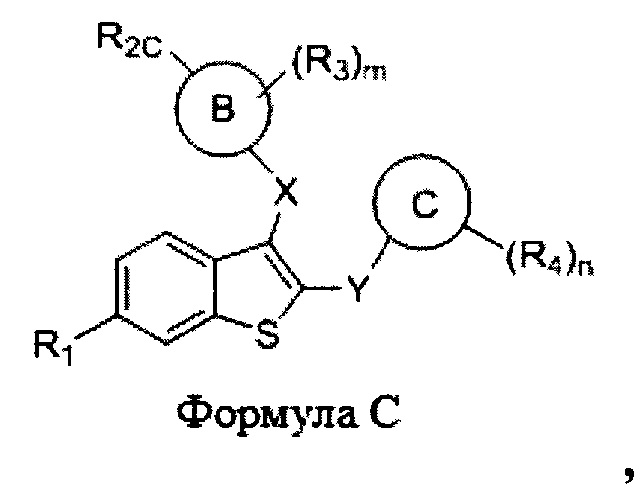
где:
m равно 0, 1, 2, 3 или 4;
n равно 0, 1, 2, 3 или 4;
X выбран из -O-, -С(O)-, -СН2-, -S-, -NH-, -NMe-, -CF2- и -С3циклоалкил-;
Y выбран из -С(O)-, -O-, -CF2- или -С3циклоалкил-, -СН2-, -S-, -NH- и -N(Me)-;
Кольцо В представляет собой фенил, нафтил, хинолинил, 5- или 6-членный моноциклический гетероарил, циклоалкил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
Кольцо С представляет собой фенил, тиофенил (т.е., тиенил), 5- или 6-членный моноциклический гетероарил, циклоалкил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
R1 выбран из гидроксила, водорода, галогена, -O(C1-C6 алкил), -OC(O)(C1-C6 алкил), -ОС(O)С6Н5, -ОС(O)O(C1-C6 алкил), -ОС(O)ОС6Н5 и -OSO2(C2-C6 алкил);
R2C выбран из -CH=СНСООН, -NH(CO)COOH, -циклоалкил(СООН), -C2-C6алкенилен-СООН и -C2-C6алкинилен-СООН.
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, -C1-С6алкила и -C1-C6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-C6алкила, -C1-C6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно другому аспекту настоящее изобретение включает в себя фармацевтическую композицию, которая включает в себя одно или несколько соединений формулы С и фармацевтически приемлемый носитель или наполнитель.
Согласно другому аспекту настоящее изобретение относится к способу лечения или предупреждения опухоли или злокачественной опухоли, который включает в себя введение субъекту, типично человеку, при необходимости такого лечения терапевтически эффективного количества соединения формулы С или его фармацевтически приемлемой соли.
Согласно одному аспекту настоящее изобретение относится к соединению формулы D, или его фармацевтически приемлемой соли:
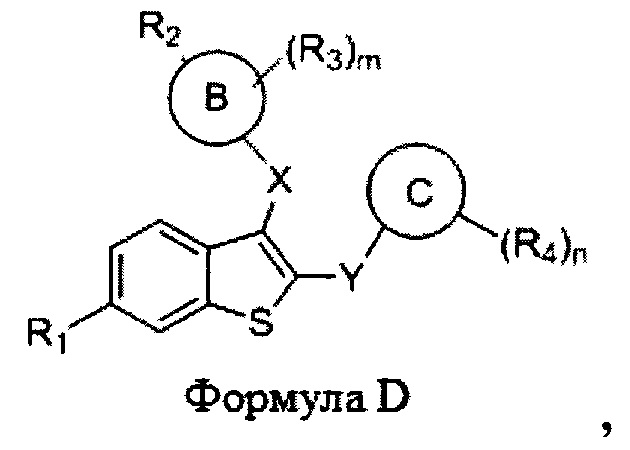
где:
m равно 0, 1, 2, 3 или 4;
n равно 0, 1, 2, 3 или 4;
X выбран из -O-, -С(O)-, -СН2-, -S-, -NH-, -NMe-, -CF2- и -С3циклоалкил-;
Y выбран из -С(O)-, -O-, -CF2- или -С3циклоалкил-, -СН2-, -S-, -NH- и -NMe-;
Кольцо В представляет собой фенил, нафтил, хинолинил, 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
Кольцо С представляет собой фенил, тиофенил (т.е., тиенил), 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
R1 выбран из гидроксила, водорода, галогена, -O(C1-C6 алкил), -OC(O)(C1-C6 алкил), -ОС(O)С6Н5, -ОС(O)O(C1-C6 алкил), -ОС(O)ОС6Н5 и -OSO2(C2-C6 алкил);
R2 выбран из -СН=СНСООН, -NH(CO)COOH, -COOH, C2-C6алкенилен-СООН и C2-C6алкинилен-СООН;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, C1-C6алкила и -C1-C6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-C6алкила, -C1-C6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно другому аспекту настоящее изобретение включает в себя фармацевтическую композицию, которая включает в себя одно или несколько соединений формулы D и фармацевтически приемлемый носитель или наполнитель.
Согласно другому аспекту настоящее изобретение относится к способу лечения или предупреждения злокачественной опухоли или опухоли, который включает в себя введение субъекту, типично человеку, при необходимости такого лечения терапевтически эффективного количества соединения формулы D или его фармацевтически приемлемой соли.
Согласно определенным вариантам осуществления соединение характеризуется структурой, выбранной из следующего, или представляет собой фармацевтически приемлемую соль:
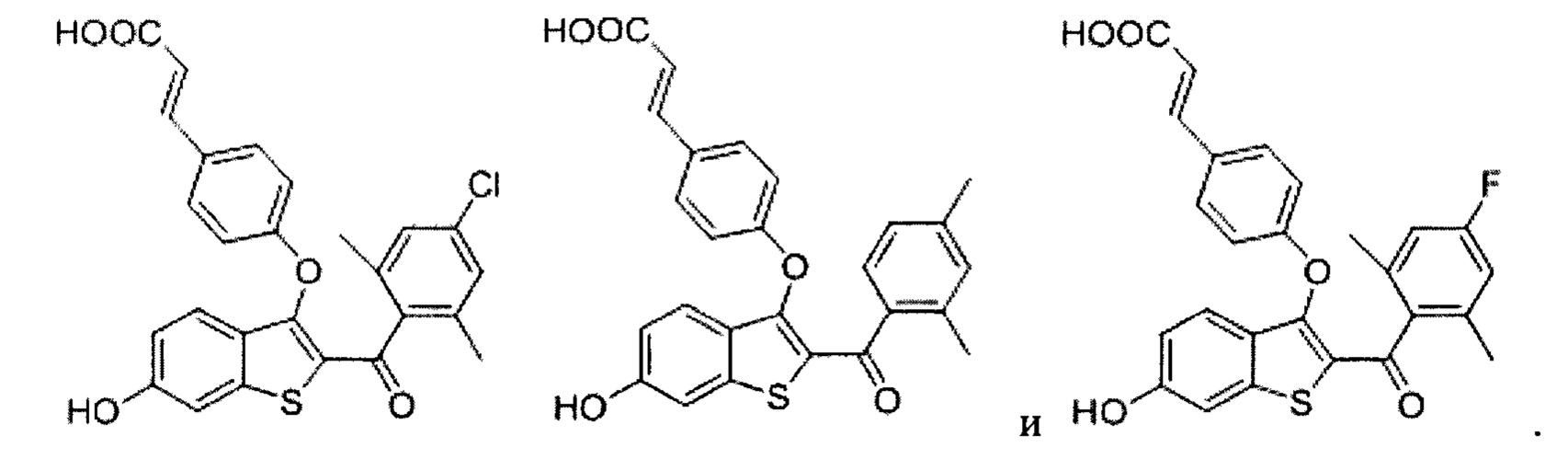
Согласно другим вариантам осуществления соединение выбрано из следующего или представляет собой фармацевтически приемлемую соль:
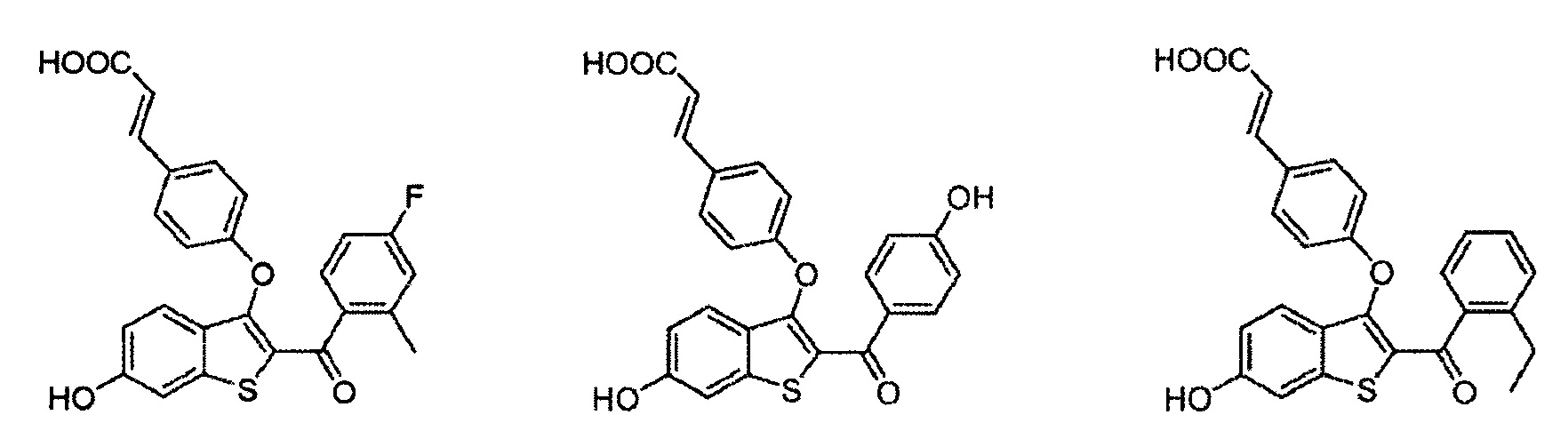
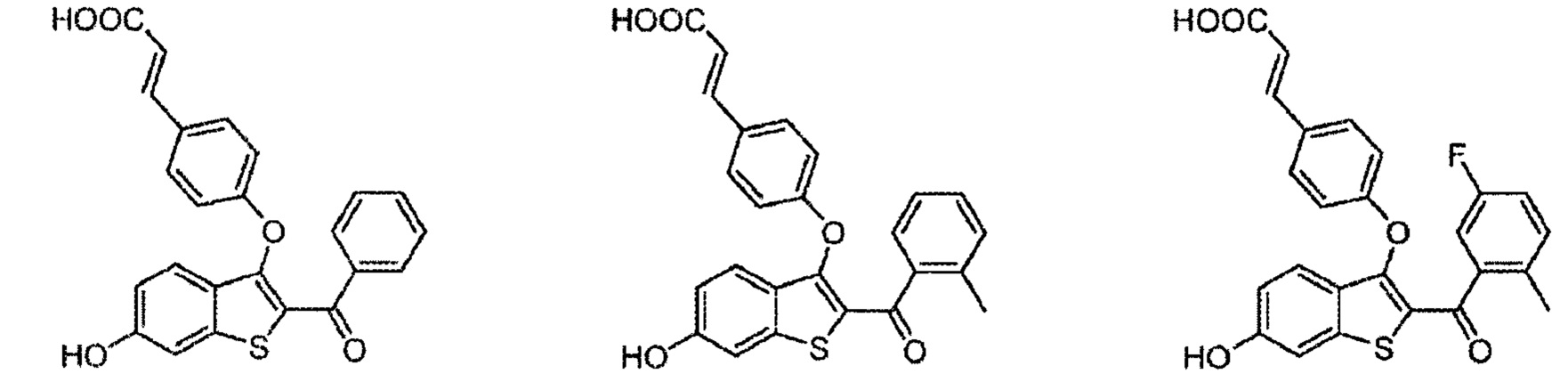
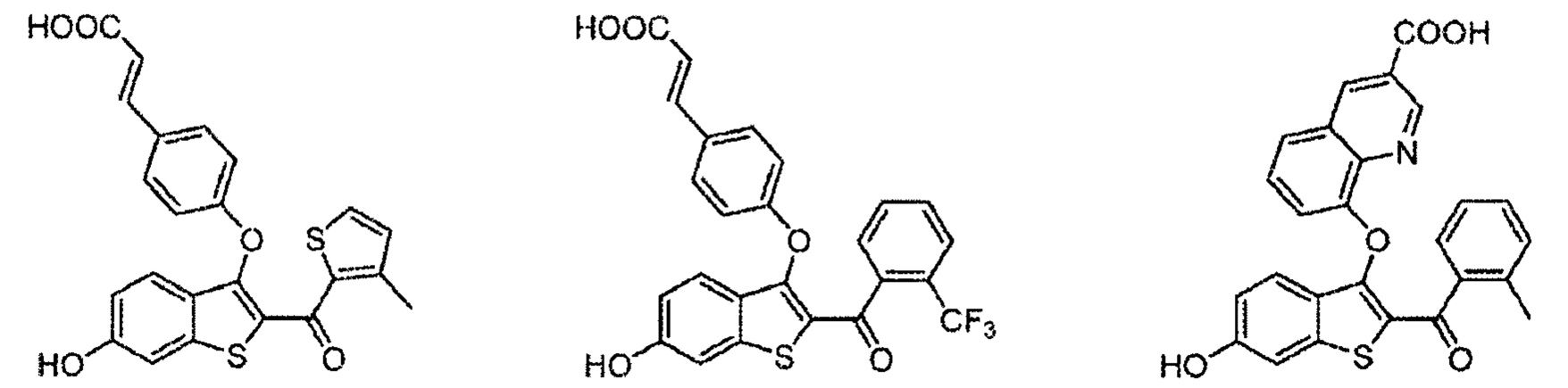
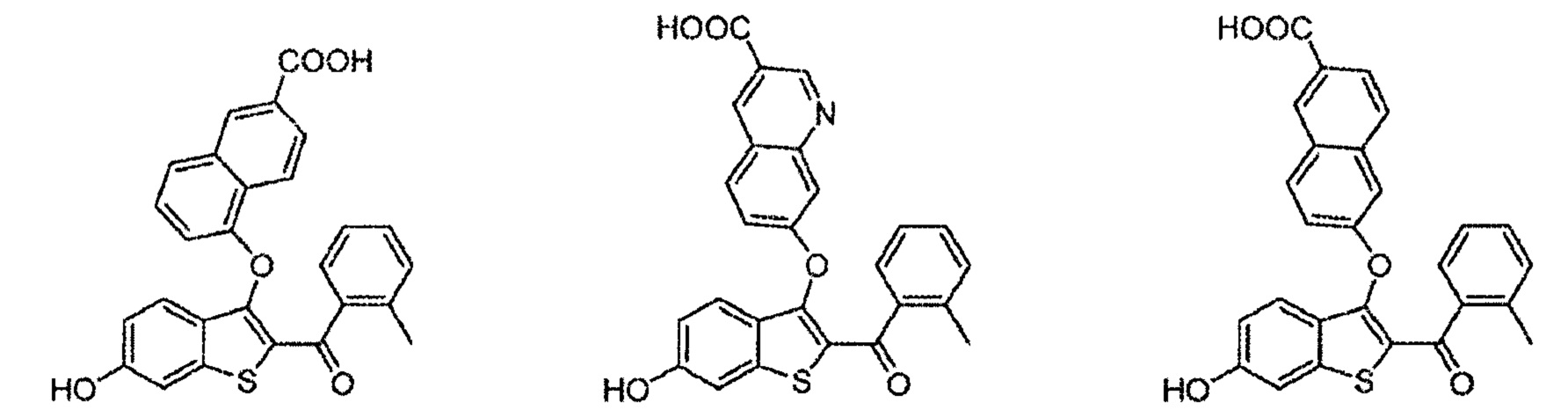
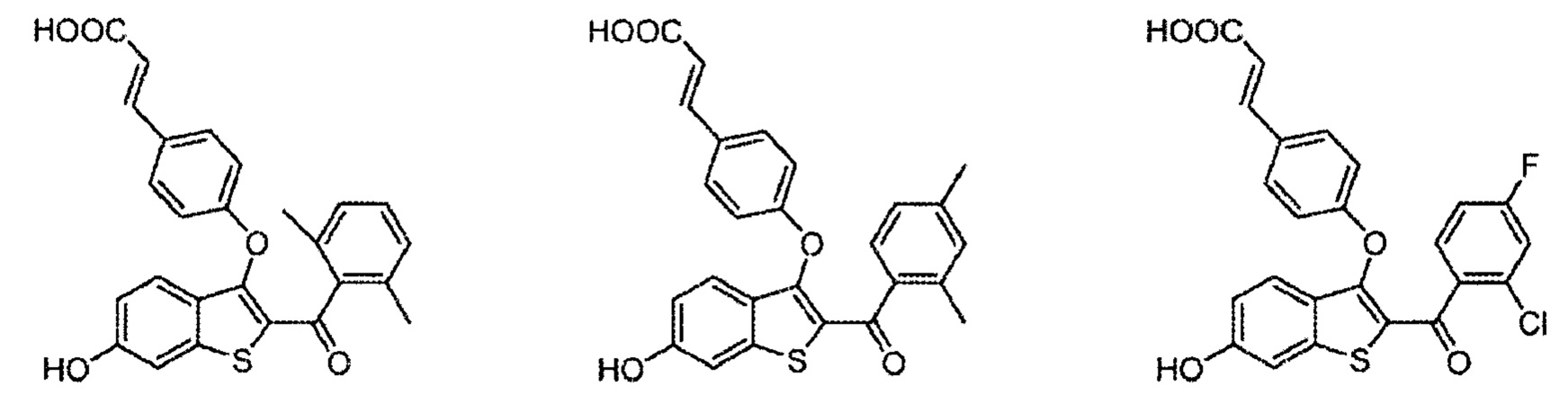
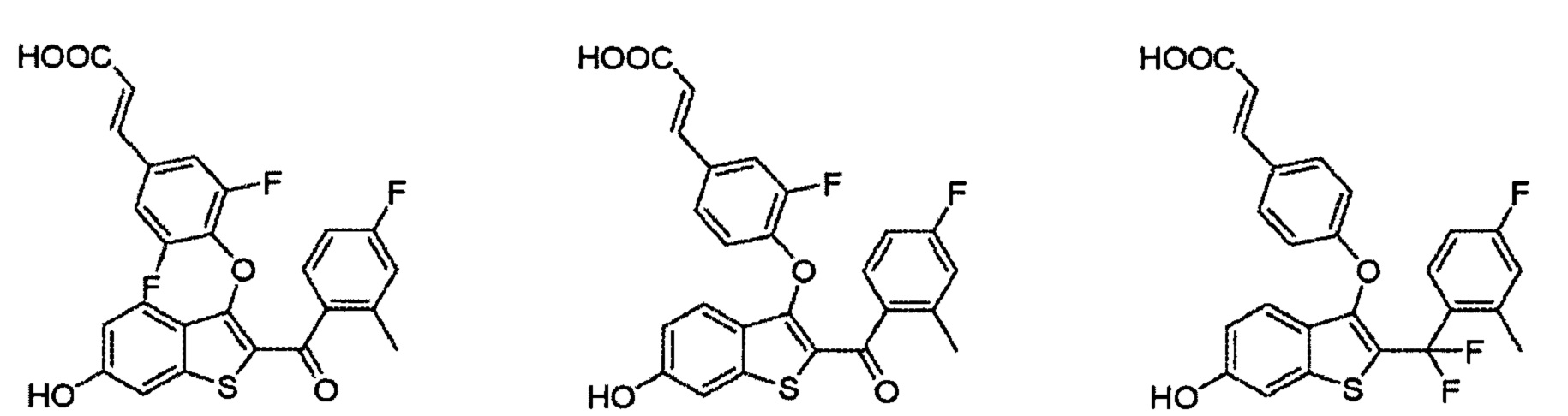
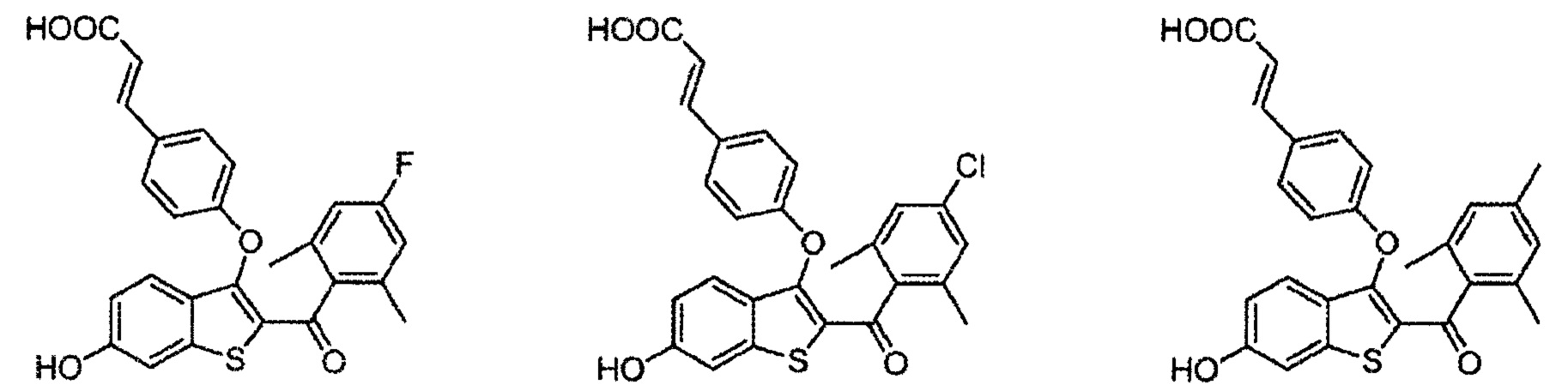
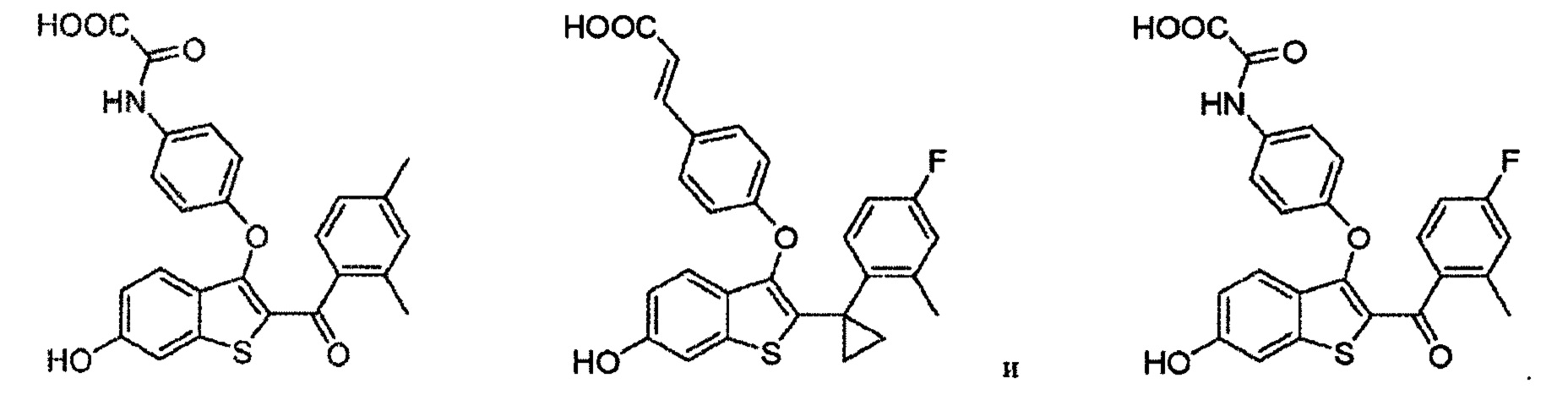
Согласно определенным вариантам осуществления вышеуказанных структур, которые содержат -CO2H, соединение может быт представлено, например, в виде сложноэфирного, амидного или эфирного пролекарства. Сложным эфиром может быть, например, -CO2R, где R представляет собой алкильный (включая циклоалкильный), гетероалкильный, алкенильный, алкинильный, арильный, гетероарильный, гетероциклический или любой другой фрагмент, который метаболизирован in vivo с получением исходного лекарственного средства.
Настоящее изобретение включает в себя по меньшей мере следующие признаки:
(a) соединение, как описано в настоящем изобретении, или его фармацевтически приемлемую соль или пролекарство;
(b) соединение, как описано в настоящем изобретении, или его фармацевтически приемлемую соль или пролекарство, что применимы при лечении или предупреждении связанного с эстрогеном нарушения, включая без ограничения опухоль или злокачественную опухоль;
(c) применение соединения, как описано в настоящем изобретении, или его фармацевтически приемлемой соли или пролекарства при изготовлении лекарственного препарата для лечения или предупреждения связанного с эстрогеном нарушения, включая без ограничения опухоль или злокачественную опухоль;
(d) способ изготовления лекарственного препарата для терапевтического применения для лечения или предупреждения нарушения аномальной клеточной пролиферации, включая без ограничения опухоль или злокачественную опухоль, отличающийся тем, что соединение по настоящему изобретению или его соль или пролекарство, как описано в настоящем изобретении, использовали при изготовлении;
(e) соединение, как описано в настоящем изобретении, или его фармацевтически приемлемую соль или пролекарство для применения при лечении или предупреждении злокачественной опухоли молочной железы, почки, матки, яичника или эндометрия;
(f) применение соединения, как описано в настоящем изобретении, или его фармацевтически приемлемой соли или пролекарства при изготовлении лекарственного препарата для лечения или предупреждения злокачественной опухоли молочной железы, почки, матки, яичника или эндометрия;
(g) способ изготовления лекарственного препарата для терапевтического применения для лечения или предупреждения злокачественной опухоли молочной железы, почки, матки, яичника или эндометрия, отличающийся тем, что соединение, как описано в настоящем изобретении, или его фармацевтически приемлемую соль или пролекарство использовали при изготовлении;
(h) соединение, как описано в настоящем изобретении, или его фармацевтически приемлемую соль или пролекарство для применения при лечении или предупреждении гормон-рецептор-положительной метастатической злокачественной опухоли молочной железы.
(i) применение соединения, как описано в настоящем изобретении, или его фармацевтически приемлемой соли или пролекарства при изготовлении лекарственного препарата для лечения или предупреждения гормон-рецептор-положительной метастатической злокачественной опухоли молочной железы;
(j) способ изготовления лекарственного препарата для лечения или предупреждения гормон-рецептор-положительной метастатической злокачественной опухоли молочной железы, отличающийся тем, что соединение, как описано в настоящем изобретении, или его фармацевтически приемлемую соль или пролекарство использовали при изготовлении;
(k) соединение, как описано в настоящем изобретении, или его фармацевтически приемлемую соль или пролекарство для применения при лечении или предупреждении разрежения кости, включая остеопороз;
(l) применение соединения, как описано в настоящем изобретении, или его фармацевтически приемлемой соли или пролекарства при изготовлении лекарственного препарата для лечения или предупреждения разрежения кости, включая остеопороз;
(m) способ изготовления лекарственного препарата для применения при лечении или предупреждении разрежения кости, включая остеопороз, отличающийся тем, что соединение, как описано в настоящем изобретении, использовали при изготовлении;
(n) фармацевтический состав, содержащий эффективное для лечения или предупреждения количество соединения, как описано в настоящем изобретении, или его фармацевтически приемлемой соли или пролекарства вместе с фармацевтически приемлемым носителем или разбавителем;
(о) соединение, как описано в настоящем изобретении, или его фармацевтически приемлемую соль или пролекарство в виде смеси энантиомеров или диастереомеров (соответственно), включая рацемат;
(р) соединение по настоящему изобретению, как описано в настоящем изобретении, в энантиомерно или диастереомерно (соответственно) обогащенной форме, включая выделенный энантиомер или диастереомер (т.е., более чем 85, 90, 95, 97 или 99% чистоты); и
(q) способ получения терапевтического продукта, который содержит эффективное количество соединения, как описано в настоящем изобретении, или его фармацевтически приемлемой соли или пролекарства.
Краткое описание чертежей
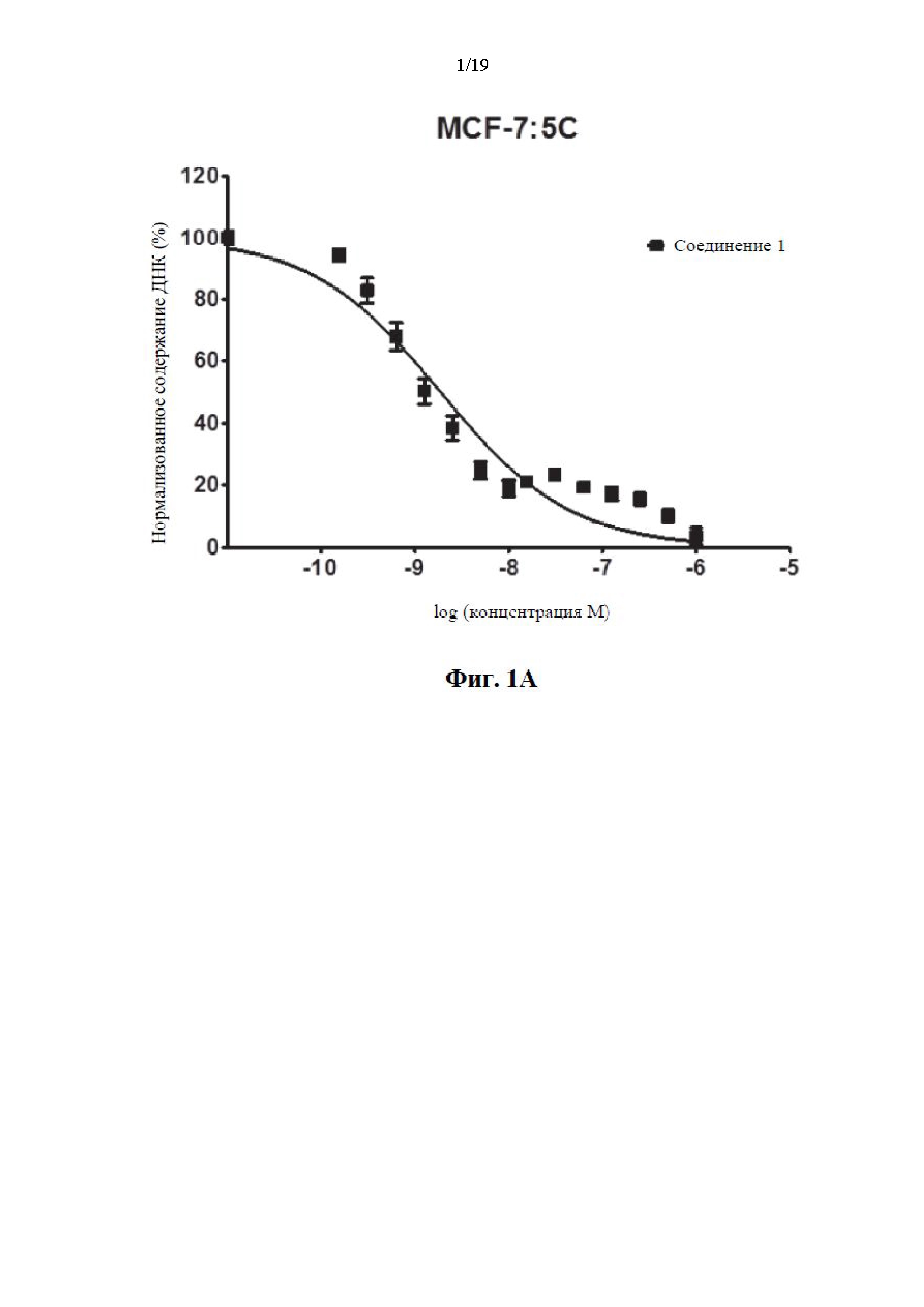
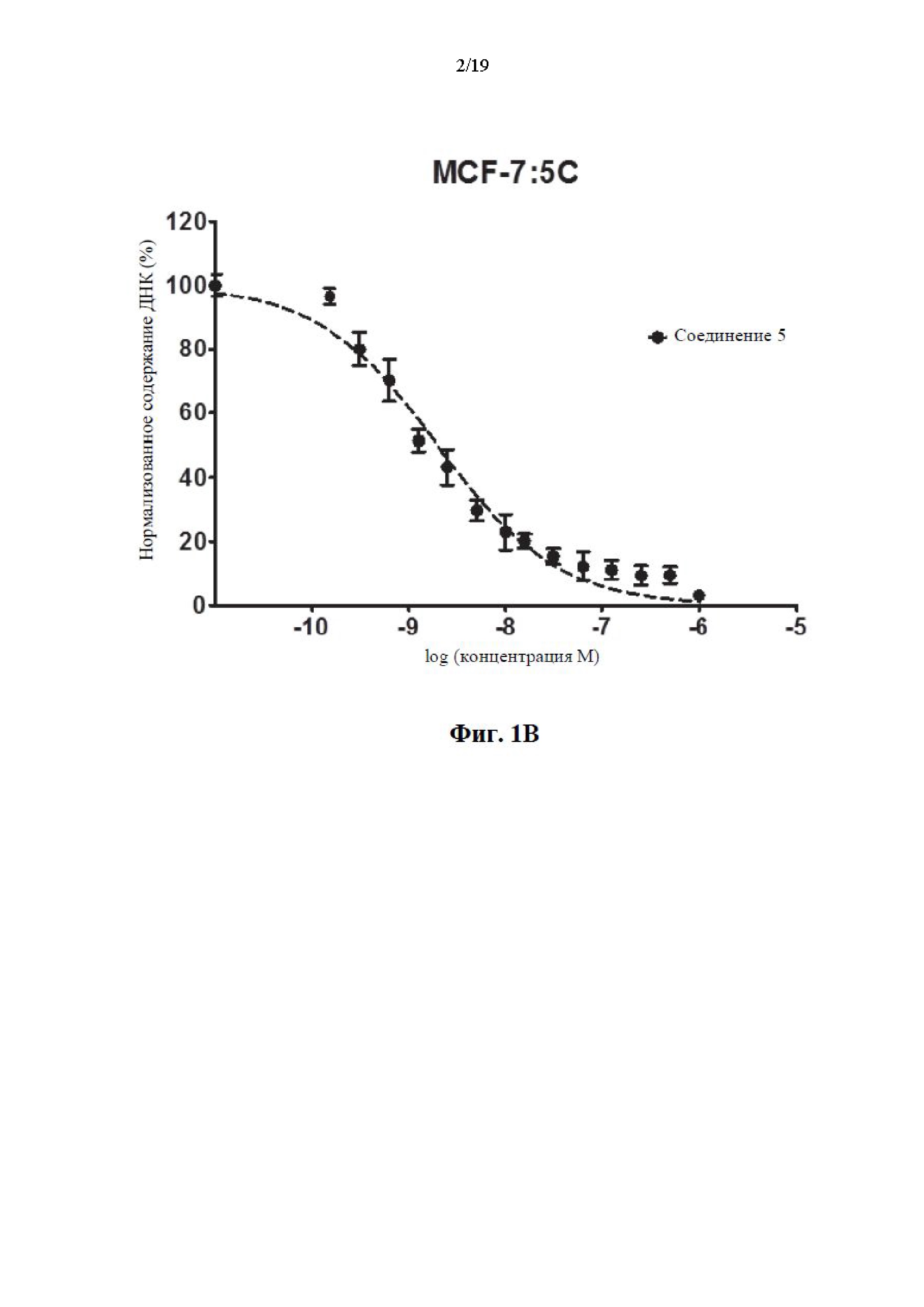
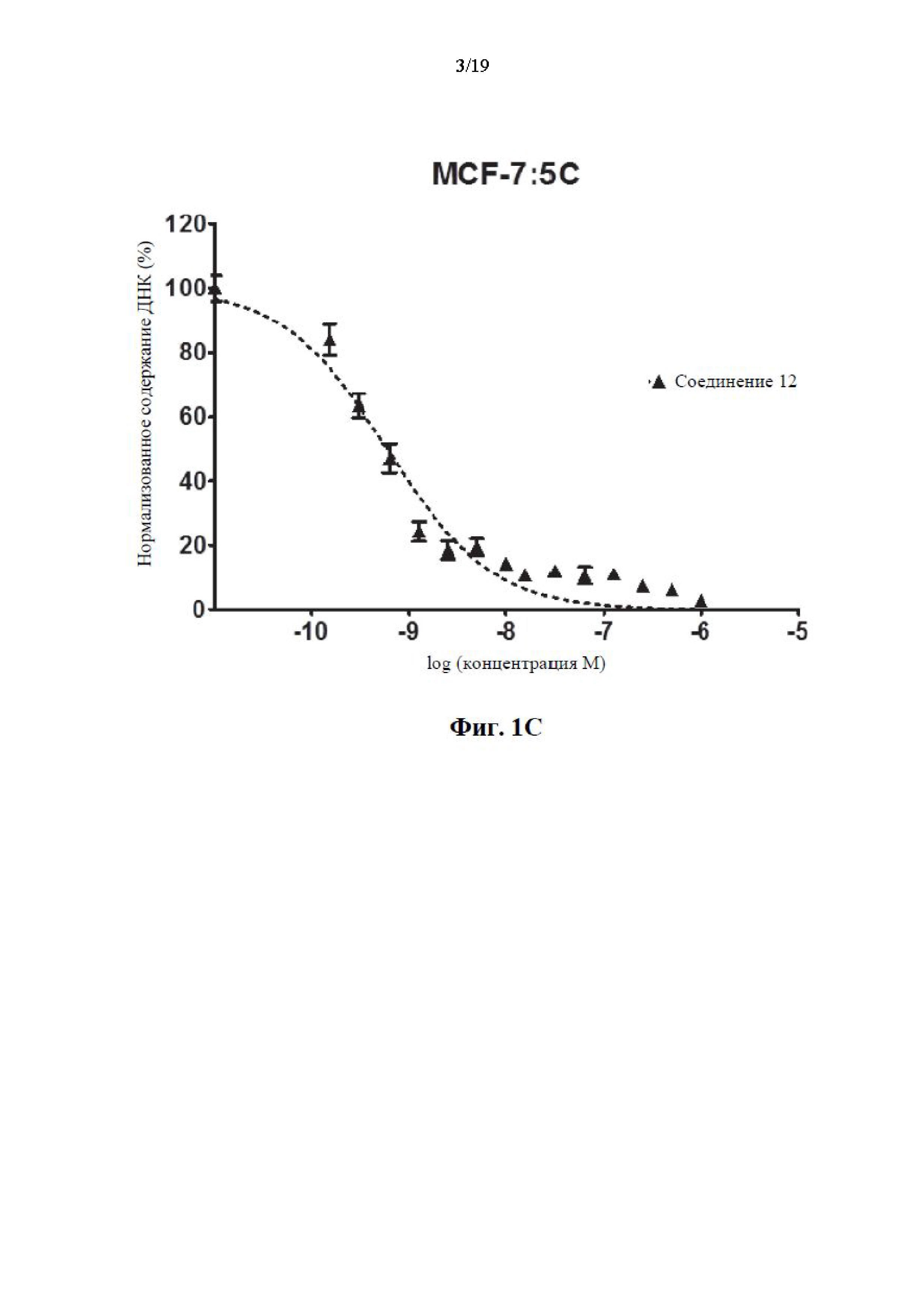
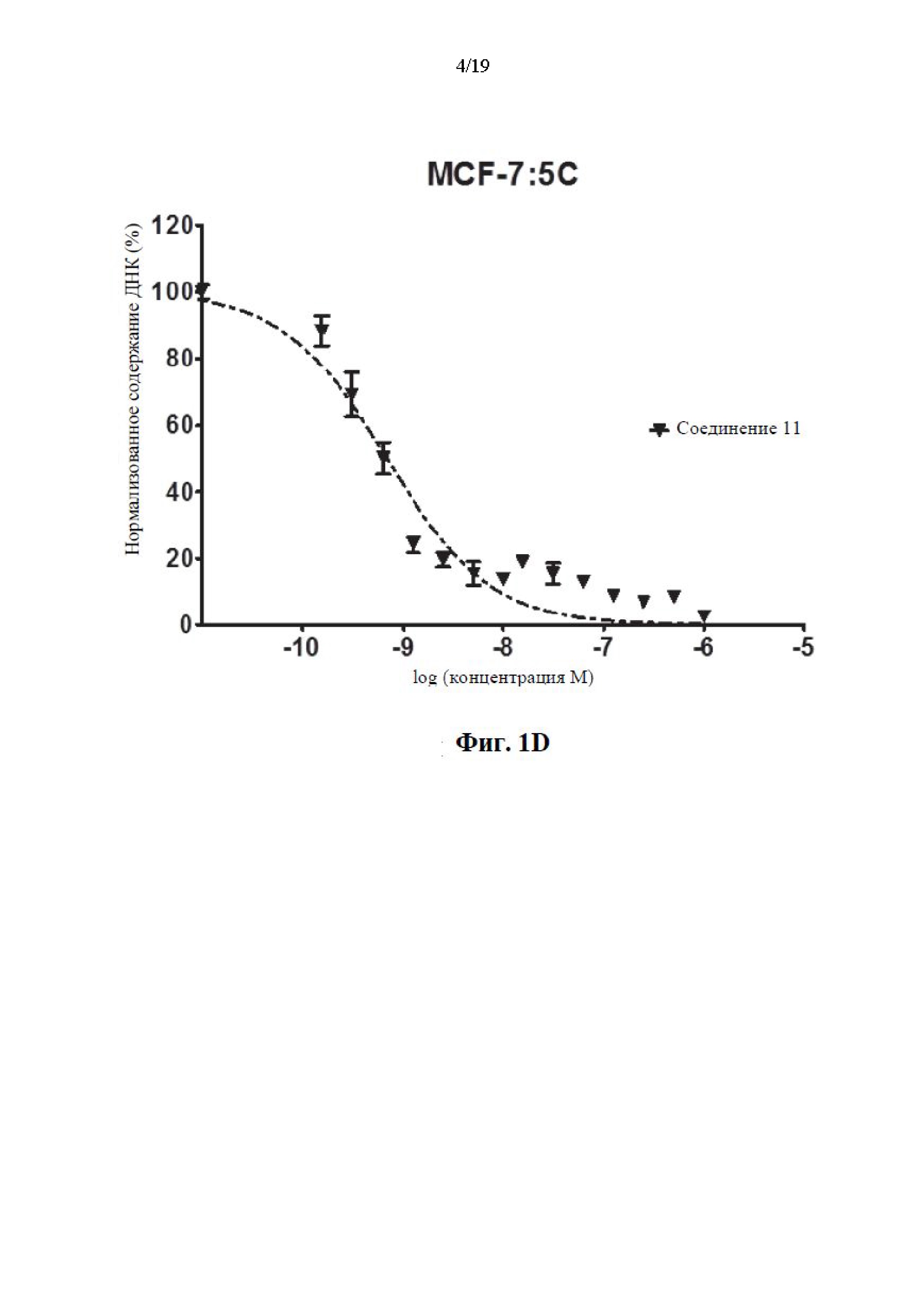
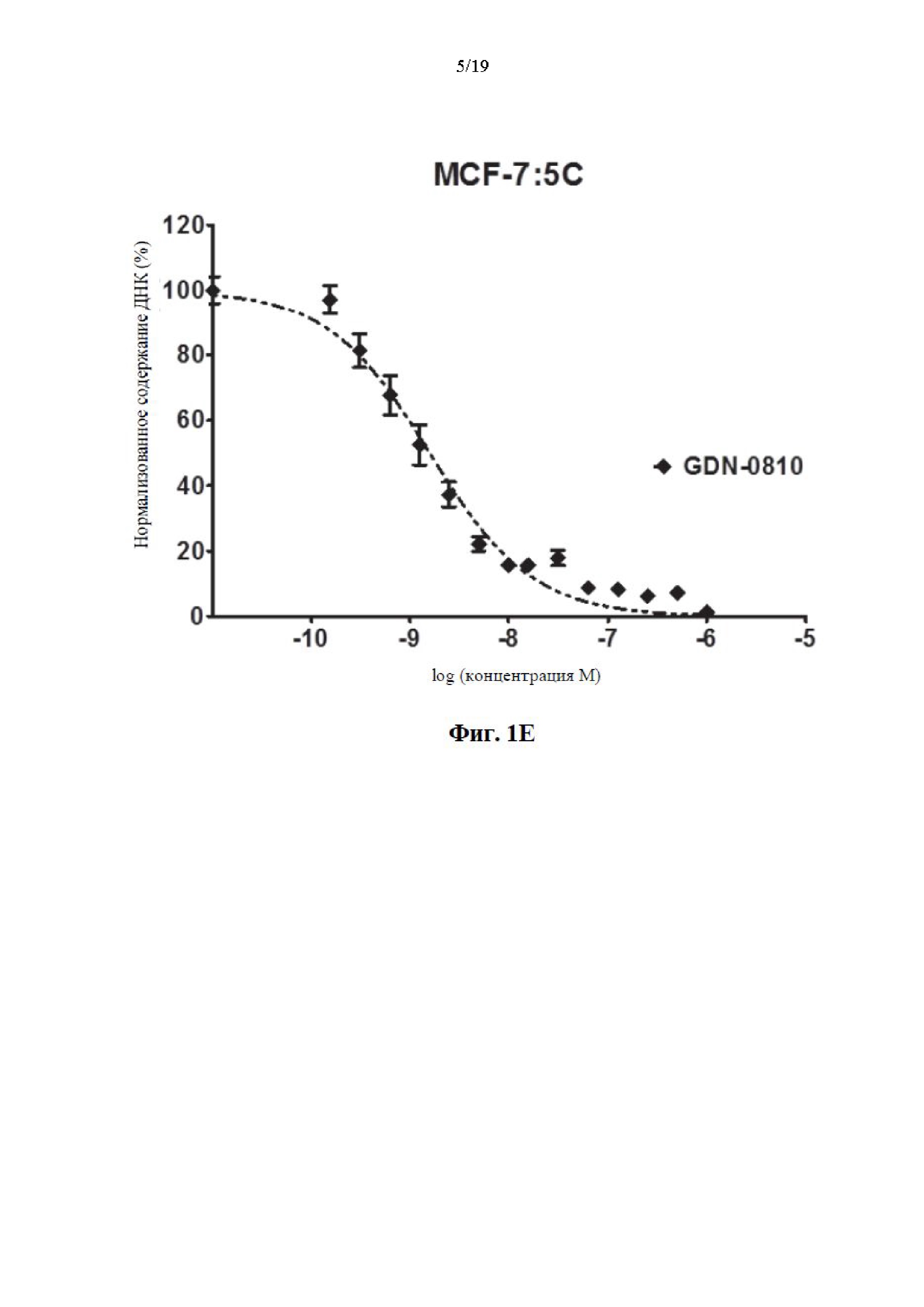
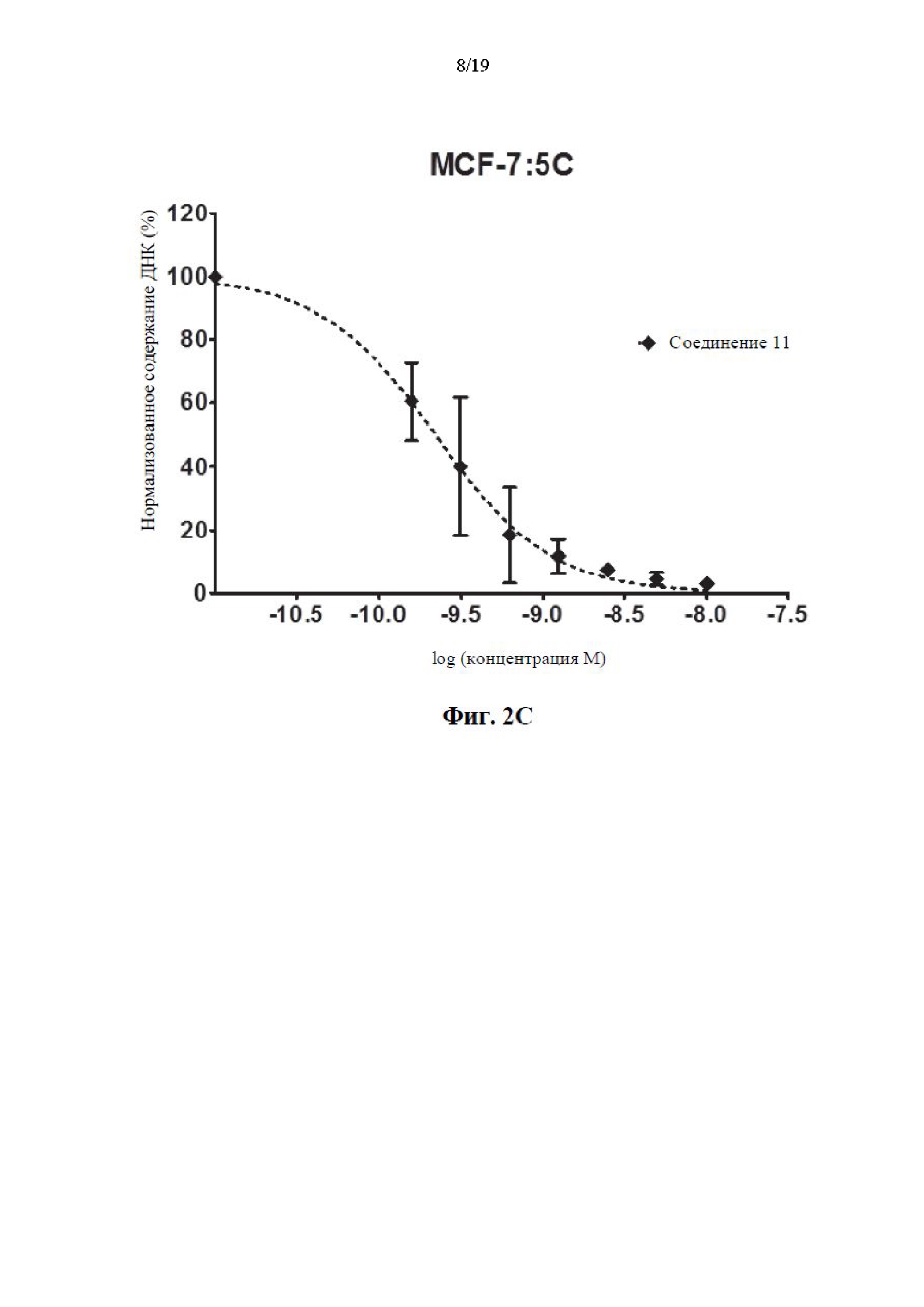
На фиг. 1А, фиг. 1В, фиг. 1C, фиг. 1D и фиг. 1Е представлены графики эффективности соединений 1, 5, 11 и 12 по сравнению с известным соединением GDN-0810 по отношению к резистентным к тамоксифену клеткам MCF-7:5С. Ось y представляет собой нормализованное содержание ДНК в процентах и ось x представляет собой концентрацию соединения, измеренного в log(молярных) единицах. На графике показано, что иллюстративные соединения характеризуются субнаномолярной эффективностью среди резистентных к тамоксифену клеток MCF-7:5C при применении анализа содержания ДНК.
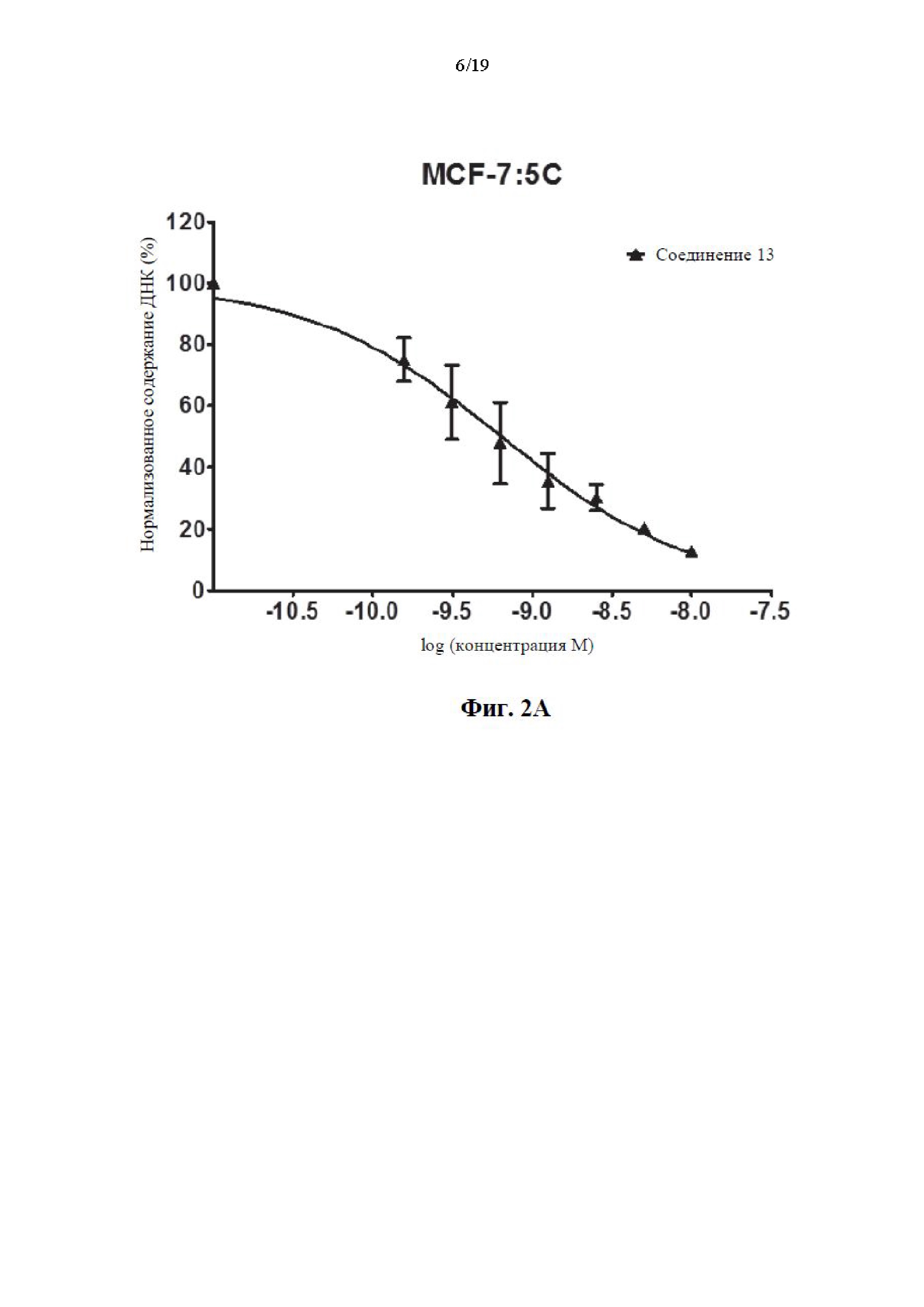
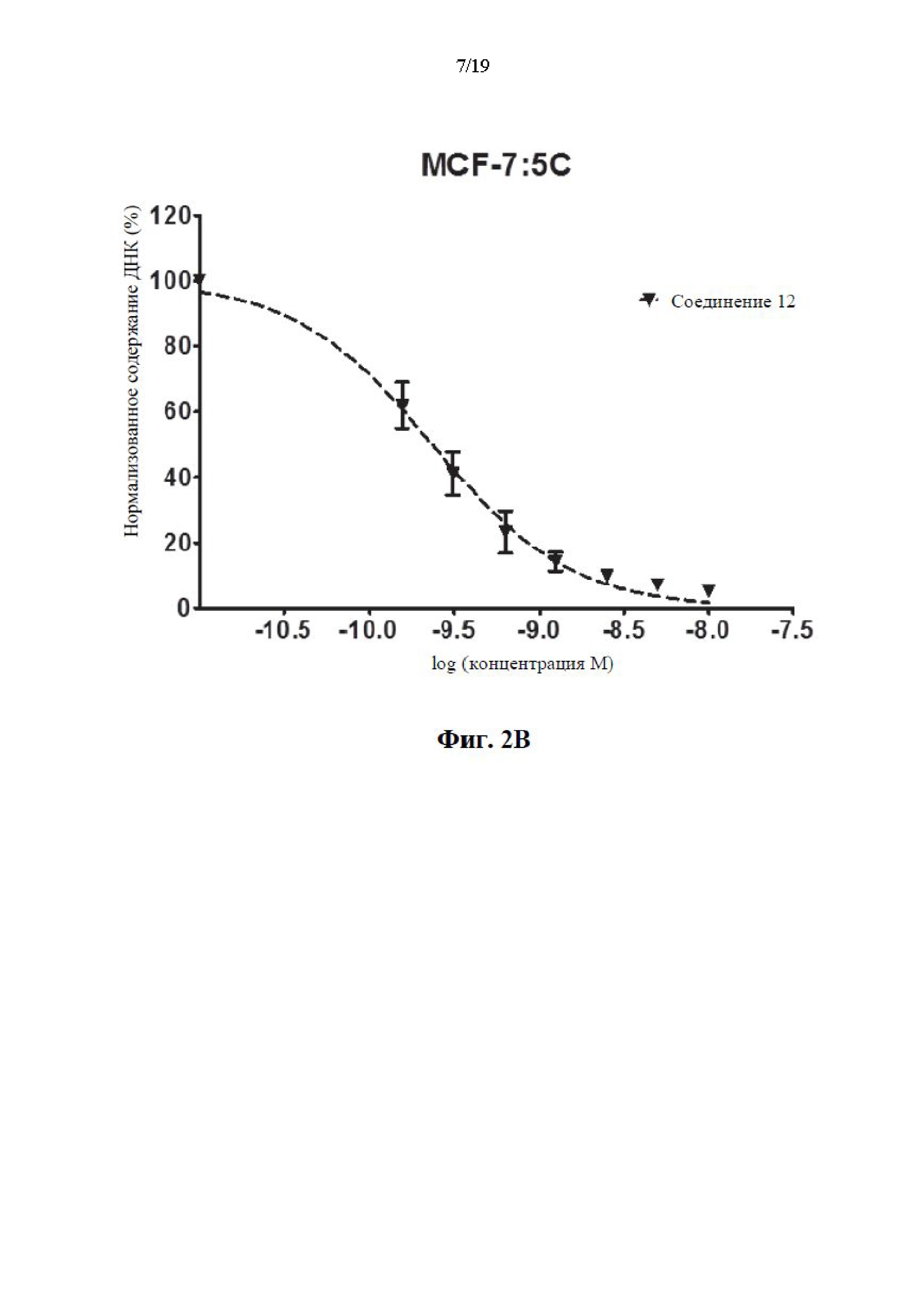
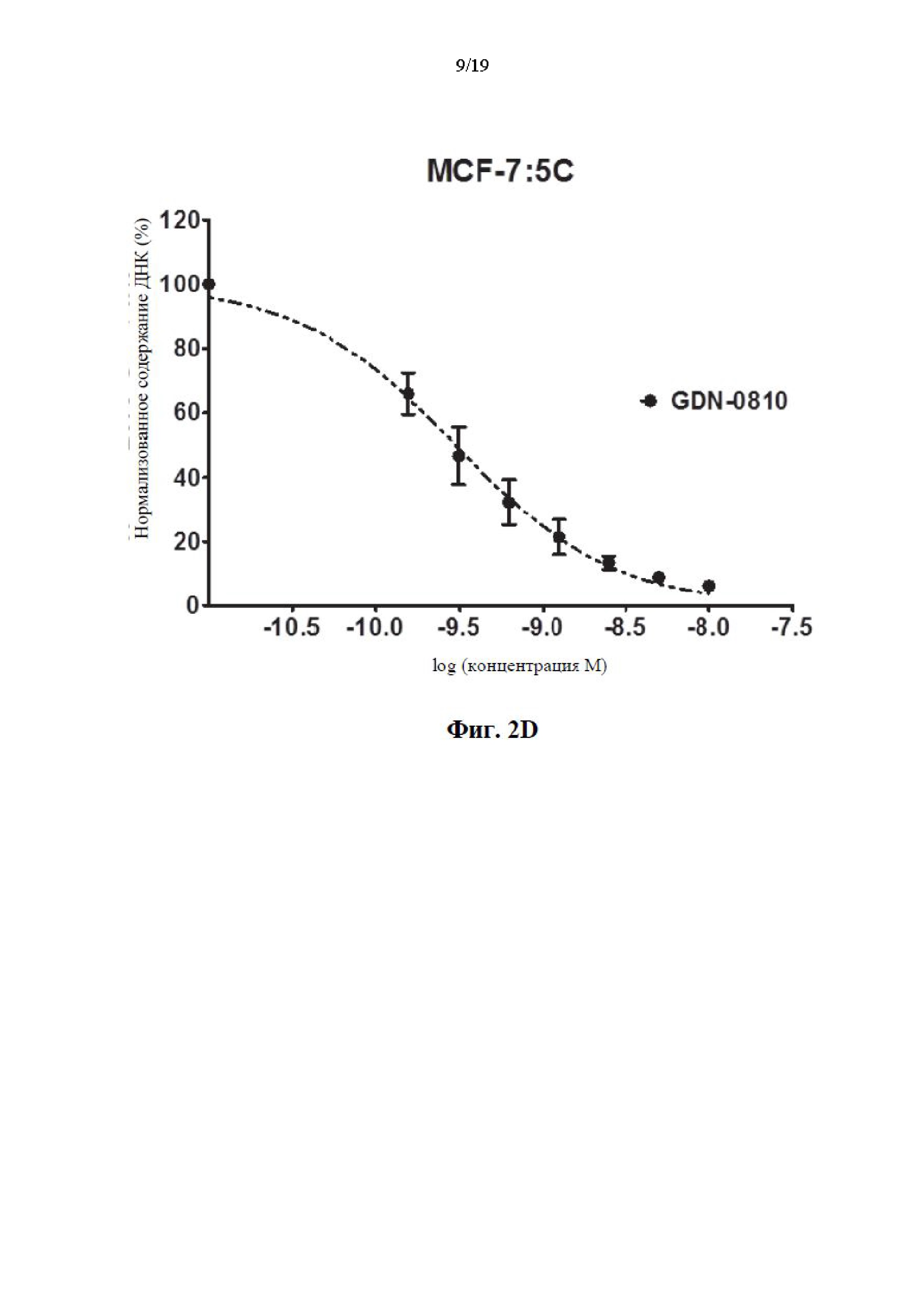
На фиг. 2А, фиг. 2В, фиг. 2С и фиг. 2D представлены графики эффективности соединений 11, 12 и 13 по сравнению с известным соединением GDN-0810 по отношению к резистентным к тамоксифену клеткам MCF-7:WS8. Ось y представляет собой нормализованное содержание ДНК в процентах и ось x представляет собой концентрацию соединения, измеренного в log(молярных) единицах. На графике показано, что типичные соединения характеризуются субнаномолярной эффективностью среди резистентных к тамоксифену клеток MCF-7:WS8 при применении анализа содержания ДНК.
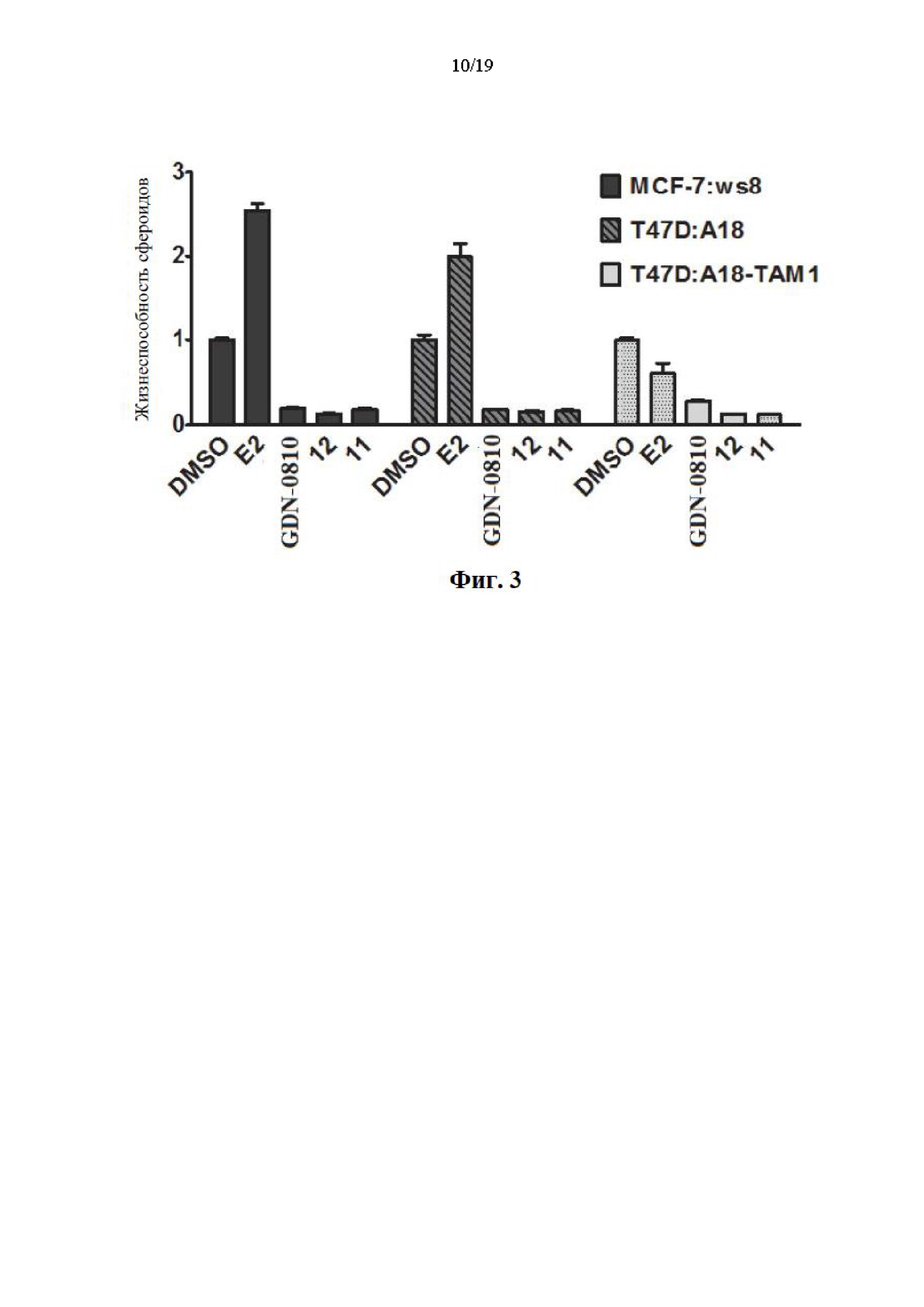
На фиг. 3 представлен график эффективности соединений 11 и 12 по сравнению с известным соединением GDN-0810 и простагландином Е2 по отношению к резистентным к тамоксифену сфероидным клеткам MCF-7:ws8, T47D:A18 и T47D:A18-TAM1. Ось y представляет собой нормализованную популяцию сфероидных клеток, где 1 представляет собой популяцию, подвергшуюся воздействию 100 нМ DMSO (контроль), а ось x представляет собой соединение, вводимое в концентрациях 100 нМ. На графике показано, что иллюстративные соединения по настоящему изобретению характеризуются эффективностью при 100 нМ среди нескольких резистентных и чувствительных 3D клеток.
На фиг. 4 представлен вестерн-блоттинг, который показывает блокировку эстрогеновых рецепторов при концентрациях 10 нМ соединений 1, 3, 4, 5, 6 и 7 по сравнению с известными соединениями GDN-0810 и ралоксифеном. При помощи анализа вестерн-блот показано, что все соединения 1, 3, 4, 5, 6 и 7 блокируют эстрогеновый рецептор при концентрациях 10 нМ.
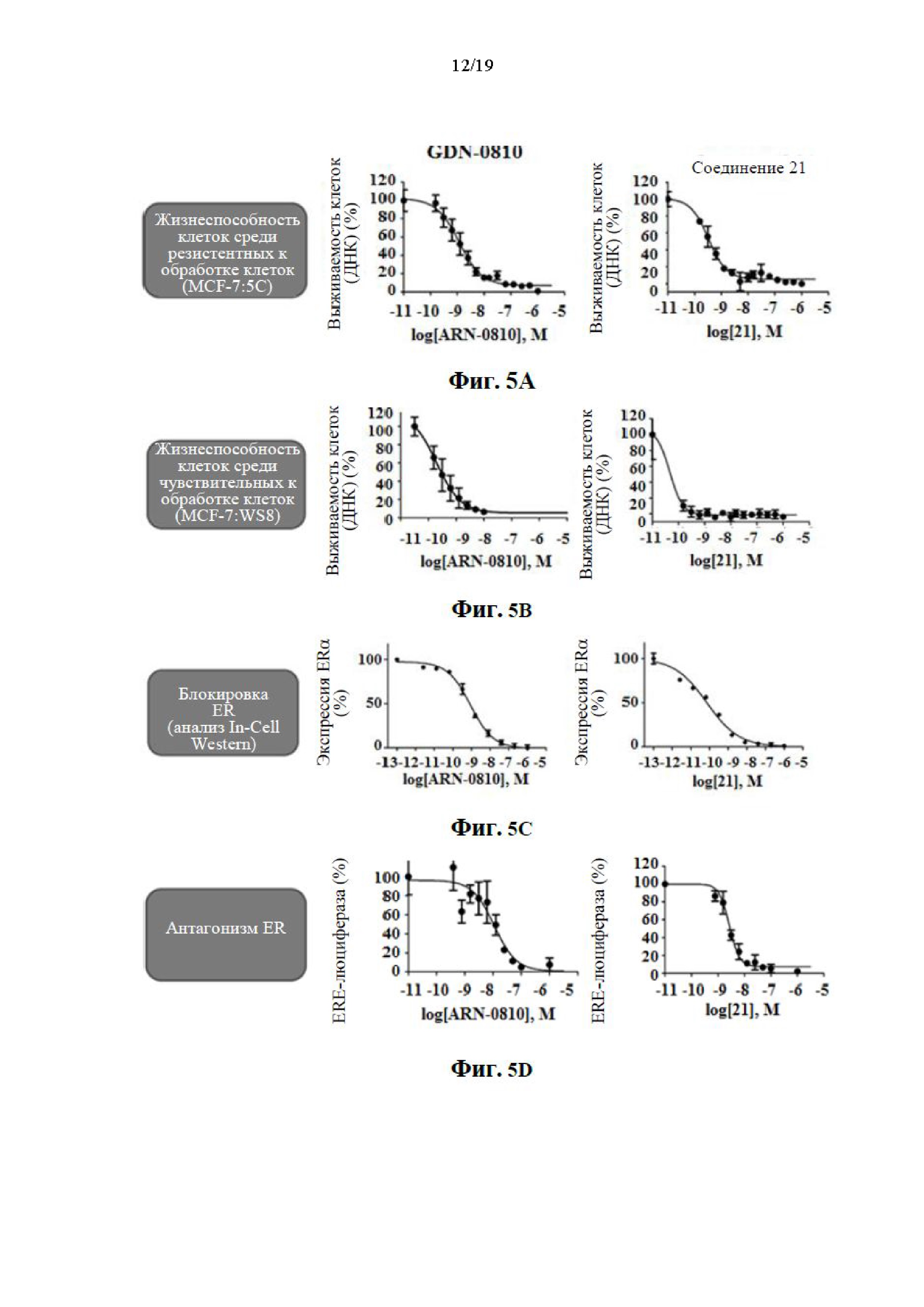
На фиг. 5А представлен график, показывающий жизнеспособность клеток среди резистентных к лечению клеток злокачественной опухоли молочной железы MCF-7:5C. Ось y представляет собой выживаемость клеток, измеряемую в процентах и нормализованную по отношению к исходным измерениям, а ось x представляет собой концентрацию GDN-0810 или соединения 21, измеряемую в log(молярных) единицах. Измерения выполняли через 4 дня после обработки и нормализовали по отношению к 100% дозы носителя.
На фиг. 5В представлен график, показывающий жизнеспособность клеток среди чувствительных к лечению клеток злокачественной опухоли молочной железы MCF-7:WS8. Ось y представляет собой выживаемость клеток, измеряемую в процентах и нормализованную по отношению к исходным измерениям, а ось x представляет собой концентрацию GDN-0810 или соединения 21, измеряемую в log(молярных) единицах. Измерения выполняли через 4 дня после обработки и нормализовали по отношению к 100% дозы носителя.
На фиг. 5С представлен график, показывающий уровень блокировки эстрогеновых рецепторов, измеряемый в экспериментах при помощи вестерн-блоттинга. Ось y представляет собой уровень экспрессии эстрогеновых рецепторов, измеряемый в процентах и нормализованный по отношению к исходным измерениям, а ось x представляет собой концентрацию GDN-0810 или соединения 21, измеряемую в log(молярных) единицах. Данные нормализовали по отношению к 1 мкМ GDN-0810 в качестве 0% и контроля DMSO в качестве 100%.
На фиг. 5D представлен график, показывающий уровень антагонизма эстрогеновых рецепторов, измеряемый в ERE-люциферазном анализе среди клеток MCF-7:WS8. Ось y представляет собой уровень ERE-люциферазы, измеряемый в процентах и нормализованный по отношению к исходным измерениям, а ось x представляет собой концентрацию GDN-0810 или соединения 21, измеряемую в log(молярных) единицах. Данные нормализовали по отношению к 1 мкМ GDN-0810 в качестве 0% и 0,1 нМ Е2 в качестве 100%. Данные показывают среднее и s.e.m., полученные по меньшей мере из 3 пассажей клеток.
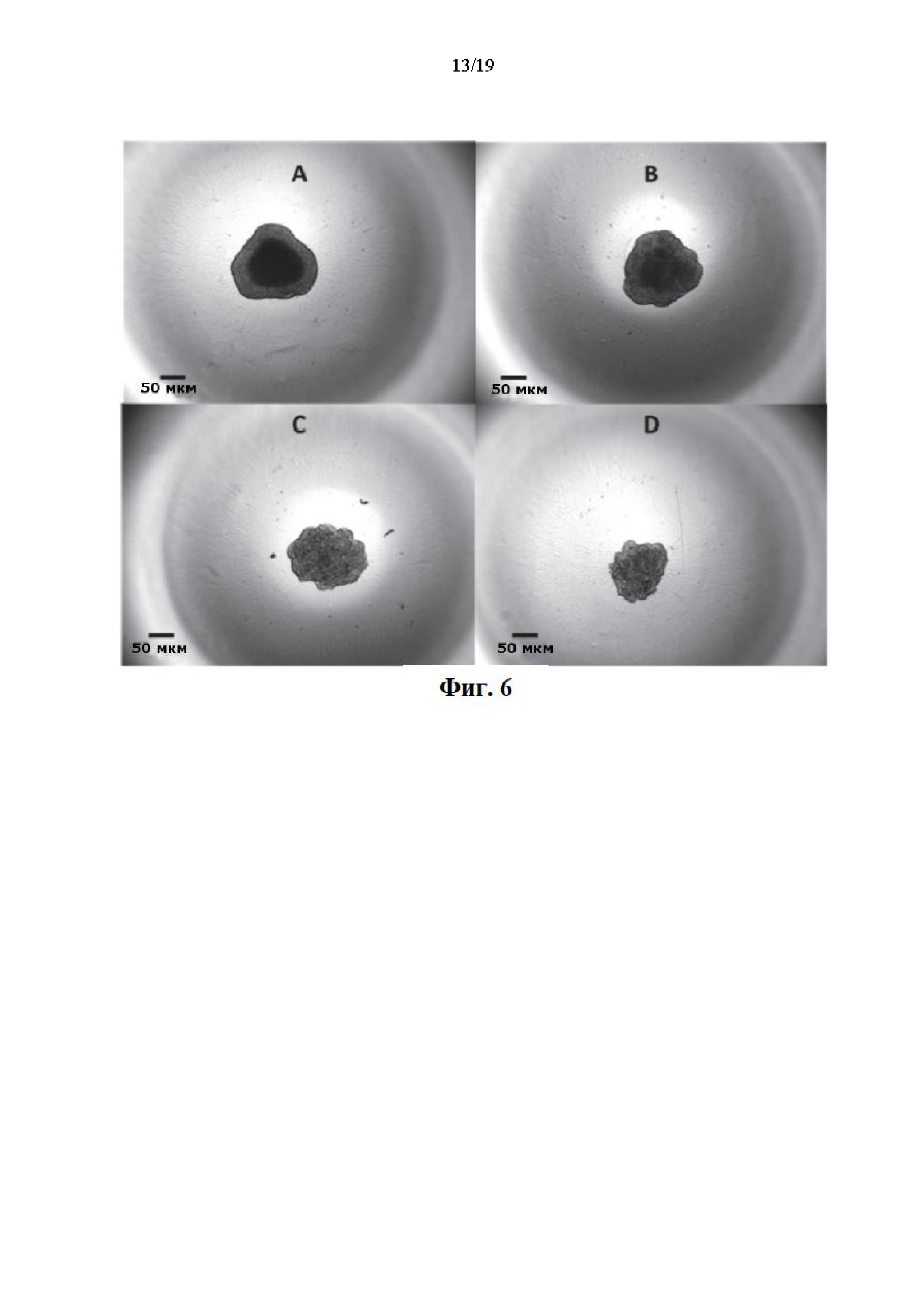
На фиг. 6 представлены изображения клеточной микроскопии, показывающие, что SERD ингибируют рост сфероидов MCF-7:TAM1 через 10 дней после обработки. На изображении А представлены сфероиды в DMSO. На изображении В представлены сфероиды в присутствии 1 нМ концентрации GDN-0810. На изображении С представлены сфероиды в присутствии 1 нМ концентрации соединения 21. На изображении D представлены сфероиды в присутствии 10 нМ концентрации соединения 21.
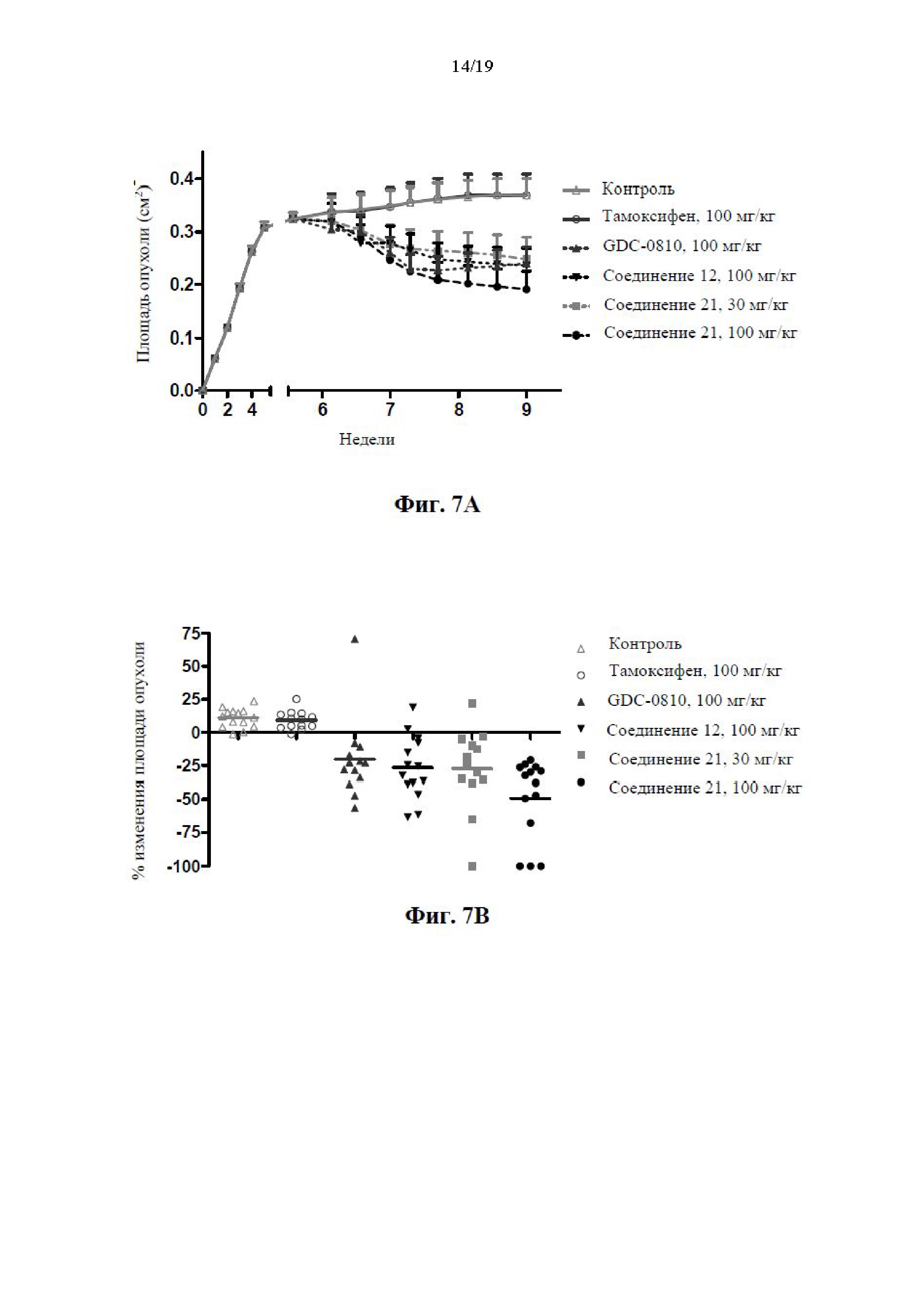
На фиг. 7А представлен график площади опухоли с применением опухолей MCF7:TAM1, которые выращивали до средней площади среза 0,32 см2. Ось y представляет собой площадь опухоли, измеряемой в см2, а ось x представляет собой время, измеряемое в неделях. Для данного исследования мышей рандомизировали на шесть групп обработки: контроль, тамоксифен (100 мг/кг), GDN-0810 (100 мг/кг), соединение 12 (10 мг/кг) и две дозы соединения 21 (30 мг/кг и 100 мг/кг). Соединения вводили ежедневно при помощи желудочного зонда.
На фиг. 7В представлен график площади опухоли с применением опухолей MCF7:TAM1, которые выращивали до средней площади среза 0,32 см2. Ось y представляет собой изменение площади опухоли, измеряемое в виде процента изменения на 23-й день, а ось x представляет собой идентичность соединения. Для данного исследования мышей рандомизировали на шесть групп обработки: контроль, тамоксифен (100 мг/кг), GDN-0810 (100 мг/кг), соединение 12 (10 мг/кг) и две дозы соединения 21 (30 мг/кг и 100 мг/кг). Соединения вводили ежедневно при помощи желудочного зонда.
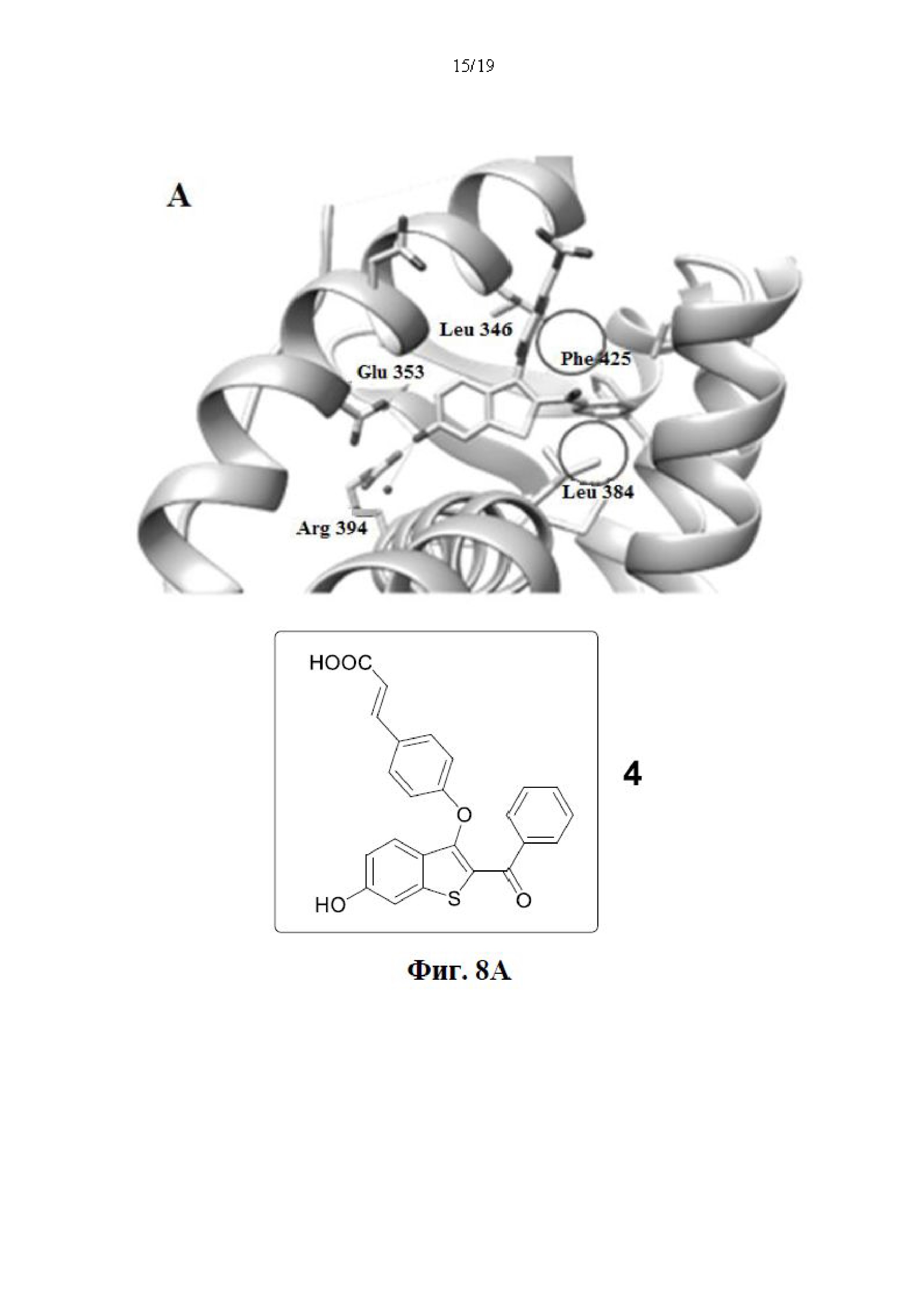
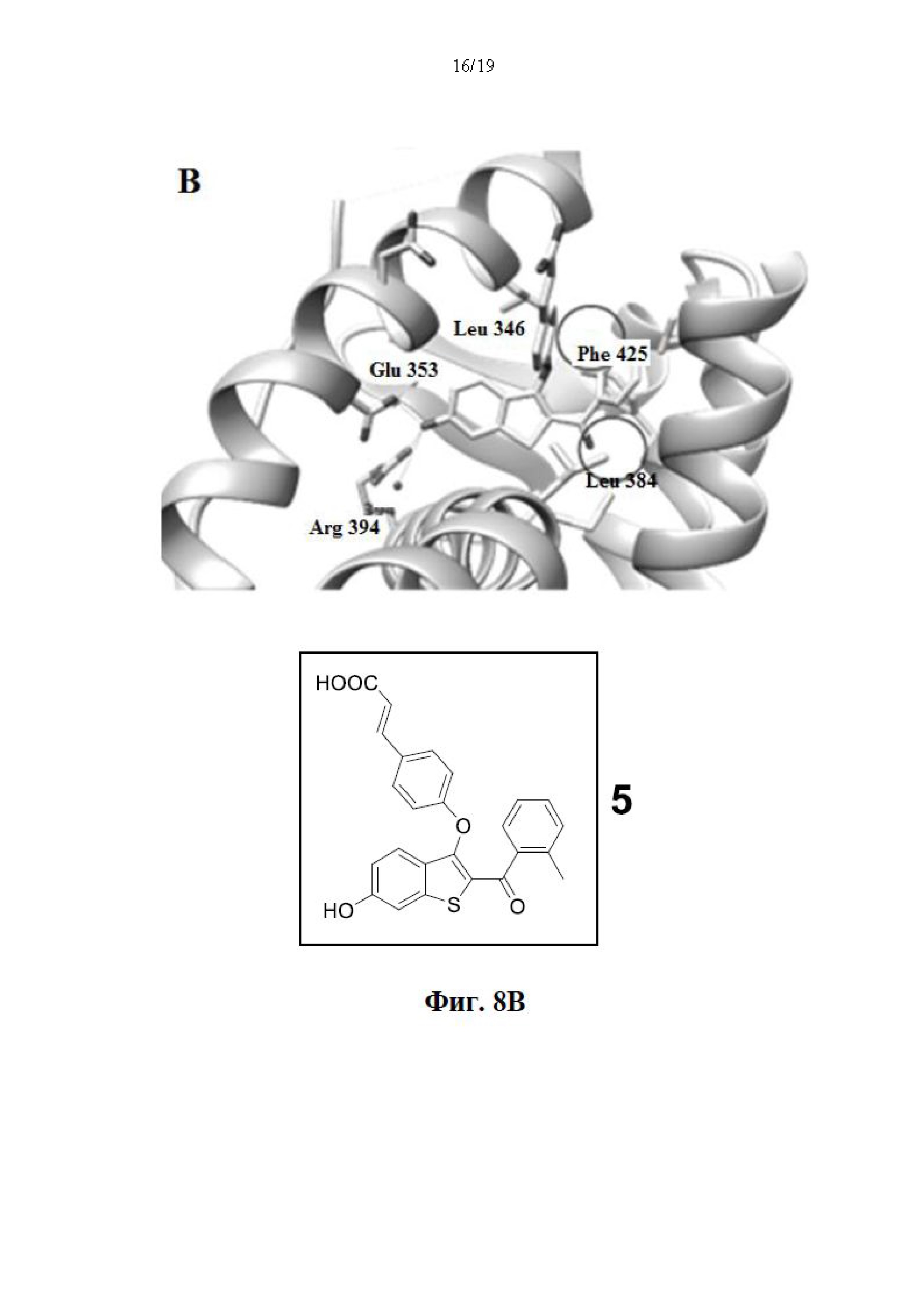
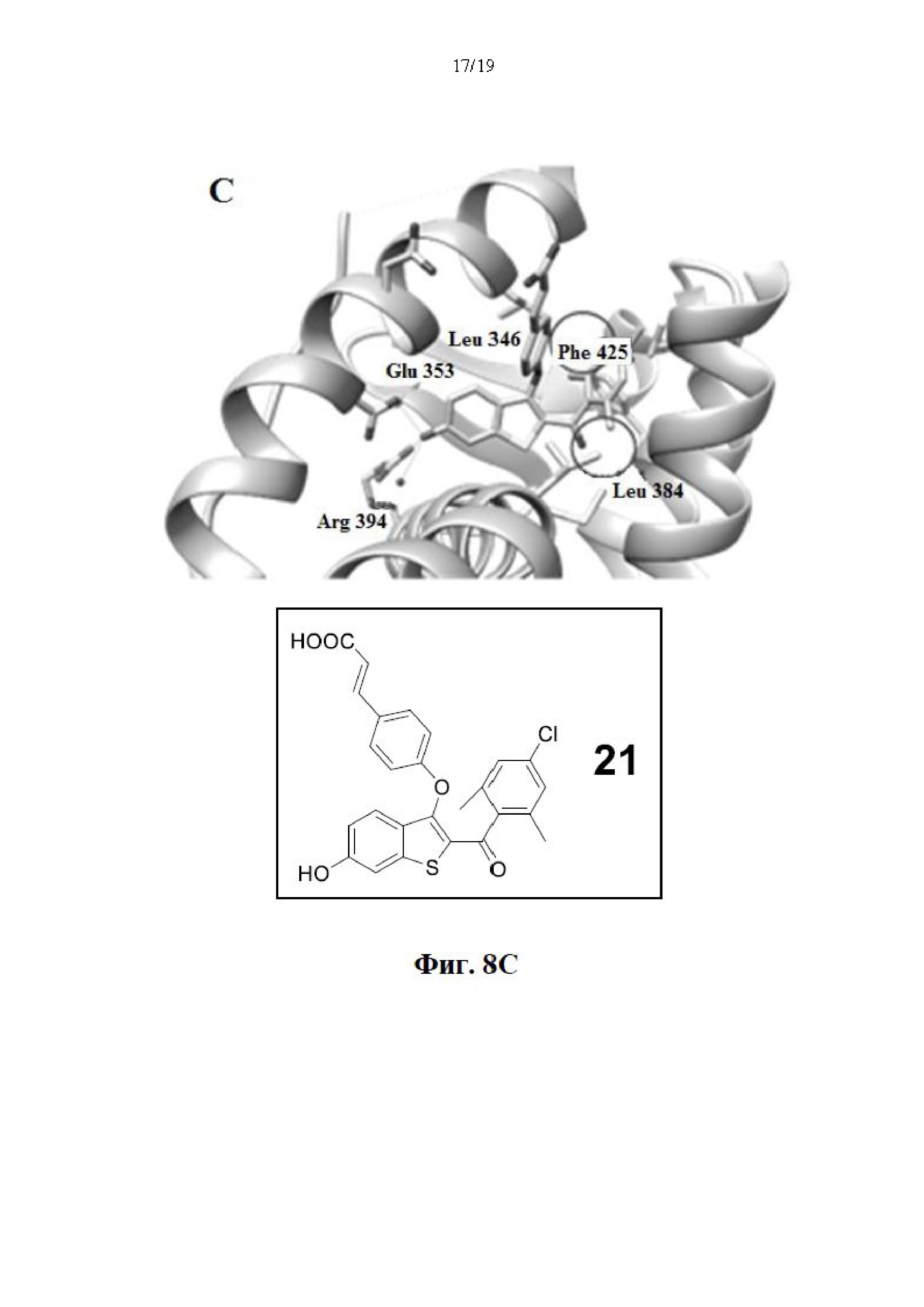
На фиг. 8А, фиг. 8В и фиг. С представлены маркированные изображения соединений 4, 5 и 21. Соединение 4 (А), 5 (В) и 21 (С) фиксировали по отношению к ER LBD (pdb ID: 5ak2). Соединение 4 имеет минимальный контакт с гидрофобными карманами (рядом с Phe 425 и Leu 384), в то время как соединение 5 и 21 имеет метальные группы, которые плотно прилегают в гидрофобную полость и соответствуют большей эффективности в анализах на жизнеспособность клеток.
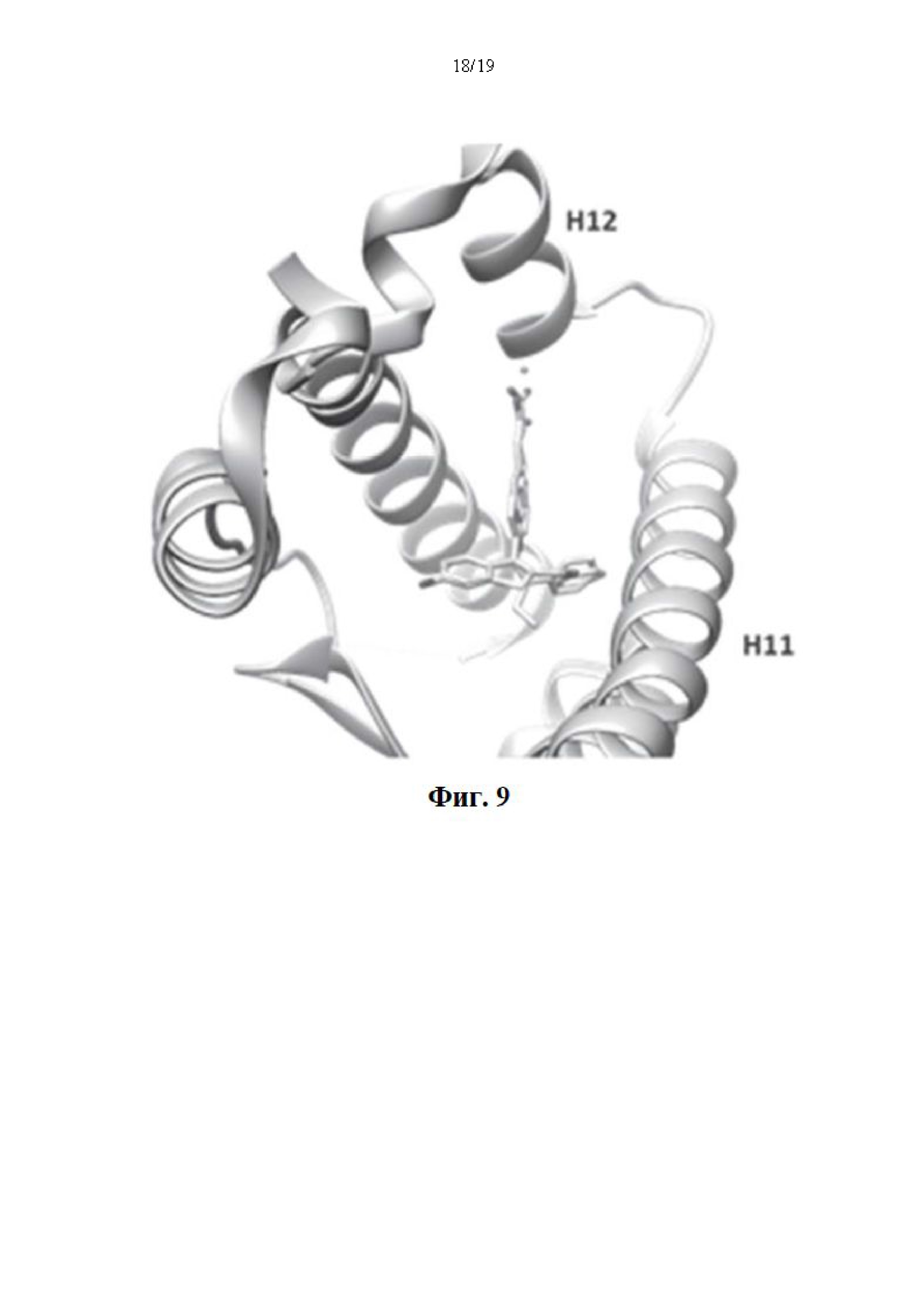
На фиг. 9 представлено фиксированное положение соединения 4, фиксированное по отношению к ERα LBD (pdb ID: 1R5K), показывающее аналогичную общую топологию по сравнению с комплексом GW5638-ER. Взаимодействие боковой цепи акрилата со спиралью 12 является основной структурной особенностью комплексов SERD-ER.
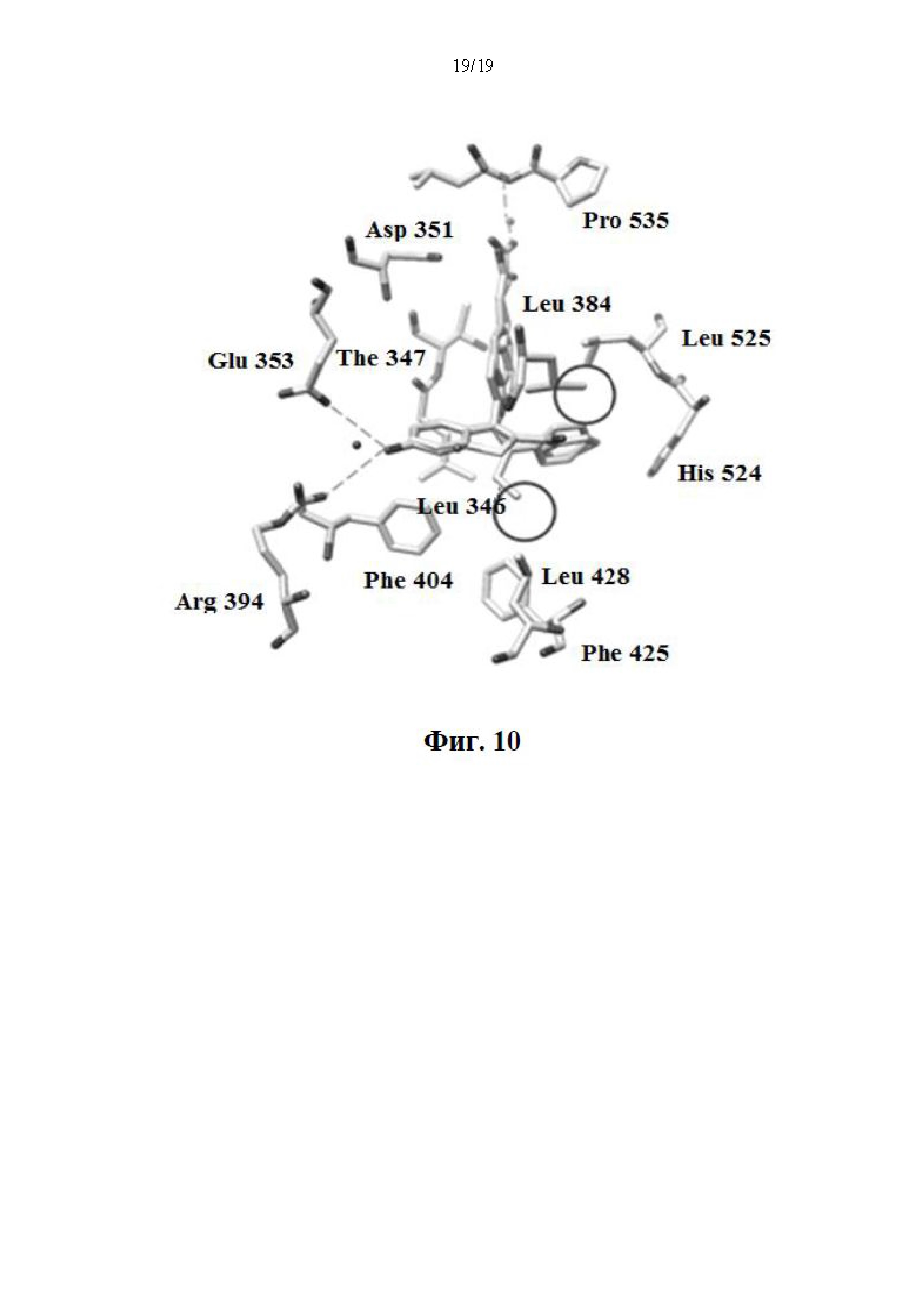
На фиг. 10 представлено фиксированное положение соединения 4, фиксированное по отношению к ERα LBD (pdb ID: 1R5K). Остатки в пределах 5
Подробное описание настоящено изобретения
Определения
Следующие используемые в настоящем описании термины и выражения характеризуются указанными значениями.
Используемым в настоящем описании терминам может предшествовать и/или следовать за ними простая черта, «-», или двойная черта, «=», для обозначения природы связи между указанным заместителем и его исходным фрагментом; простая черта означает простую связь, а двойная черта означает двойную связь. При отсутствии простой или двойной черты является понятным, что простая связь образована между заместителем и его исходным фрагментом; кроме того, подразумевается, что заместители читаются «слева направо», если черта не указывает на другое. Например, C1-C6алкоксикарбонилокси и -OC(O)C1-C6 алкил означают одинаковую функциональную группу; подобным образом, арилалкил и -алкиларил означают одинаковую функциональную группу.
«Алкенил» означает углеводород с неразветвленной или разветвленной цепью, содержащей от 2 до 10 атомов углерода, если не отмечено иное, и содержащей по меньшей мере одну двойную связь углерод-углерод. Типичные примеры алкенила включают в себя без ограничения этенил, 2-пропенил, 2-метил-2-пропенил, 3-бутенил, 4-пентенил, 5-гексенил, 2-гептенил, 2-метил-1-гептенил, 3-деценил и 3,7-диметилоокта-2,6-диенил.
«Алкокси» означает алкильную группу, как определено в настоящем описании, присоединенную к исходному молекулярному фрагменту через атом кислорода. Типичные примеры алкокси включают в себя без ограничения метокси, этокси, пропокси, 2-пропокси, бутокси, трет-бутокси, пентилокси и гексилокси.
«Алкил» означает углеводород с неразветвленной или разветвленной цепью, содержащей от 1 до 10 атомов углерода, если не отмечено иное. Типичные примеры алкила включают в себя без ограничения метил, этил, н-пропил, изо-пропил, н-бутил, втор-бутил, изо-бутил, трет-бутил, н-пентил, изопентил, неопентил, н-гексил, 3-метилгексил, 2,2-диметилпентил, 2,3-диметилпентил, н-гептил, н-октил, н-нонил и н-децил. Если «алкильная» группа является связывающей группой между двумя фрагментами, тогда она также может быть неразветвленной или разветвленной цепью; примеры включают в себя без ограничения -СН2-, -СН2СН2-, -СН2СН2СНС(СН3)- и -СН2СН(СН2СН3)СН2-.
«Алкинил» означает углеводородную группу с неразветвленной или разветвленной цепью, содержащую от 2 до 10 атомов углерода и содержащую по меньшей мере одну тройную связь углерод-углерод. Типичные примеры алкинила включают в себя без ограничения ацетиленил, 1-пропинил, 2-пропинил, 3-бутинил, 2-пентинил и 1-бутинил.
«Арил» означает фенильную (т.е. моноциклический арил) или бициклическую кольцевую систему, содержащую по меньшей мере одно фенильное кольцо или ароматическое бициклическое кольцо, содержащее только атомы углерода в ароматической бициклической кольцевой системе. Бициклическим арилом может быть азуленил, нафтил или фенил, конденсированный с моноциклическим циклоалкилом, моноциклическим циклоалкенилом или моноциклическим гетероциклилом. Бициклический арил присоединен к исходному молекулярному фрагменту через любой атом углерода, который содержится в фенильной части бициклической системы, или любой атом углерода в нафтильном или азуленильном кольце. Конденсированные моноциклические циклоалкильные или моноциклические гетероциклильные части бициклического арила необязательно замещены одной или двумя оксо и/или тиагруппами. Типичные примеры бициклических арилов включают в себя без ограничения азуленил, нафтил, дигидроинден-1-ил, дигидроинден-2-ил, дигидроинден-3-ил, дигидроинден-4-ил, 2,3-дигидроиндол-4-ил, 2,3-дигидроиндол-5-ил, 2,3-дигидроиндол-6-ил, 2,3-дигидроиндол-7-ил, индол-1-ил, индол-2-ил, индол-3-ил, индол-4-ил, дигидронафталин-2-ил, дигидронафталин-3-ил, дигидронафталин-4-ил, дигидронафталин-1-ил, 5,6,7,8-тетрагидронафталин-1-ил, 5,6,7,8-тетрагидронафталин-2-ил, 2,3-дигидробензофуран-4-ил, 2,3-дигидробензофуран-5-ил, 2,3-дигидробензофуран-6-ил, 2,3-дигидробензофуран-7-ил, бензо[d][1,3]диоксол-4-ил, бензо[d][1,3]диоксол-5-ил, 2Н-хромен-2-он-5-ил, 2H-хромен-2-он-6-ил, 2H-хромен-2-он-7-ил, 2H-хромен-2-он-8-ил, изоиндолин-1,3-дион-4-ил, изоиндолин-1,3-дион-5-ил, индол-1-он-4-ил, индол-1-он-5-ил, индол-1-он-6-ил, индол-1-он-7-ил, 2,3-дигидробензо[b][1,4]диоксан-5-ил, 2,3-дигидробензо[b][1,4]диоксан-6-ил, 2H-бензо[b][1,4]оксазин3(4H)-он-5-ил, 2Н-бензо[b][1,4]оксазин3(4H)-он-6-ил, 2H-бензо[b][1,4]оксазин3(4H)-он-7-ил, 2H-бензо[b][1,4]оксазин3(4H)-он-8-ил, бензо[d]оксазин-2(3Н)-он-5-ил, бензо[d]океазин-2(3H)-он-6-ил, бензо[d]оксазин-2(3H)-он-7-ил, бензо[d]оксазин-2(3Н)-он-8-ил, хиназолин-4(3H)-он-5-ил, хиназолин-4(3H)-он-6-ил, хиназолин-4(3H)-он-7-ил, хиназолин-4(3H)-он-8-ил, хиноксалин-2(1H)-он-5-ил, хиноксалин-2(1H)-он-6-ил, хиноксалин-2(1H)-он-7-ил, хиноксалин-2(1H)-он-8-ил, бензо[d]тиазол-2(3H)-он-4-ил, бензо[d]тиазол-2(3H)-он-5-ил, бензо[d]тиазол-2(3H)-он-6-ил и бензо[d]тиазол-2(3H)-он-7-ил. Согласно определенным вариантам осуществления бициклический арил представляет собой (i) нафтильное или (ii) фенильное кольцо, конденсированное с любым из 5- или 6-членного моноциклического циклоалкила, 5- или 6-членного моноциклического циклоалкенила или 5- или 6-членного моноциклического гетероциклила, где конденсированные циклоалкильные, циклоалкенильные и гетероциклильные группы необязательно замещены одной или двумя группами, которые независимо представляют собой оксо или тиа. Согласно определенным вариантам осуществления раскрытия арильной группой является фенил или нафтил. Согласно определенным другим вариантам осуществления арильной группой является фенил.
«Циано» и «нитрил» означает -CN группу.
«Гало» или «галоген» означает -Cl, -Br, -I или -F. Согласно определенным вариантам осуществления «гало» или «галоген» относится к -Cl или -F.
«Галогеналкил» означает по меньшей мере один галоген, как определено в настоящем описании, присоединенный к исходному молекулярному фрагменту через алкильную группу, как определено в настоящем описании. Типичные примеры галогеналкила включают в себя без ограничения хлорметил, 2-фторэтил, трифторметил, пентафторэтил и 2-хлор-3-фторпентил. Согласно определенным вариантам осуществления каждый «галогеналкил» представляет собой фторалкил, например, полифторалкил, такой как в основном перфторированный алкил.
«Гетероарил» означает моноциклическую гетероарильную или бициклическую кольцевую систему, содержащую по меньшей мере одно гетероароматическое кольцо. Моноциклический гетероарил может быть 5- или 6-членным кольцом. 5-членное кольцо состоит из двух двойных связей и одного, двух, трех или четырех атомов азота и необязательно одного атома кислорода или серы. 6-членное кольцо состоит из трех двойных связей и одного, двух, трех или четырех атомов азота. 5- или 6-членный гетероарил соединен с исходным молекулярным фрагментом через любой атом углерода или любой атом азота, который содержится в гетероариле. Типичные примеры моноциклического гетероарила включают в себя без ограничения фурил, имидазолил, изоксазолил, изотиазолил, оксадиазолил, оксазолил, пиридинил, пиридазинил, пиримидинил, пиразинил, пиразолил, пирролил, тетразолил, тиадиазолил, тиазолил, тиенил, триазолил и триазинил. Бициклический гетероарил состоит из моноциклического гетероарила, конденсированного с фенилом, моноциклического циклоалкила, моноциклического циклоалкенила, моноциклического гетероциклила или моноциклического гетероарила. Конденсированная циклоалкильная или гетероциклильная часть бициклическая гетероарильная группа необязательно замещена одной или двумя группами, которые независимо представляют собой оксо или тиа. Если бициклический гетероарил содержит конденсированное циклоалкильное, циклоалкенильное или гетероциклильное кольцо, тогда бициклическая гетероарильная группа соединена с исходным молекулярным фрагментом через любой атом углерода или азота, которые содержатся в моноциклической гетероарильной части бициклической кольцевой системы. Если бициклический гетероарил представляет собой моноциклический гетероарил, конденсированный с фенильным кольцом, тогда бициклическая гетероарильная группа соединена с исходным молекулярным фрагментом через любой атом углерода или азота, который содержится в бициклической кольцевой системе. Типичные примеры бициклического гетероарила включают в себя без ограничения бензимидазолил, бензофуранил, бензотиенил, бензоксадиазолил, бензоксатиадиазолил, бензотиазолил, циннолинил, 5,6-дигидрохинолин-2-ил, 5,6-дигидроизохинолин-1-ил, фуропиридинил, индазолил, индолил, изохинолинил, нафтиридинил, хинолинил, пуринил, 5,6,7,8-тетрагидрохинолин-2-ил, 5,6,7,8-тетрагидрохинолин-3-ил, 5,6,7,8-тетрагидрохинолин-4-ил, 5,6,7,8-тетрагидроизохинолин-1-ил, тиенопиридинил, 4,5,6,7-тетрагидробензо[с][1,2,5]оксадиазолил и 6,7-дигидробензо[с][1,2,5]оксадиазол-4(5H)-онил. Согласно определенным вариантам осуществления конденсированный бициклический гетероарил представляет собой 5- или 6-членное моноциклическое гетероарильное кольцо, конденсированное с любым из фенильного кольца, 5- или 6-членного моноциклического циклоалкила, 5- или 6-членного моноциклического циклоалкенила, 5- или 6-членного моноциклического гетероциклила или 5- или 6-членного моноциклического гетероарила, причем конденсированные циклоалкильные, циклоалкенильные и гетероциклильные группы необязательно замещены одной или двумя группами, которые независимо представляют собой оксо или тиа. Согласно определенным вариантам осуществления настоящего раскрытия гетероарильная группа представляет собой фурил, имидазолил, пиридинил, пиримидинил, пиразинил, пиразолил, пирролил, тиазолил, тиенил, триазолил, бензимидазолил, бензофуранил, индазолил, индолил или хинолинил.
«Гетероциклил» означает моноциклический гетероцикл или бициклический гетероцикл. Моноциклический гетероцикл представляет собой 3-, 4-, 5-, 6- или 7-членное кольцо, содержащее по меньшей мере один гетероатом, независимо выбранный из группы, состоящей из О, N и S, где кольцо является насыщенным или ненасыщенным, но не ароматическим. 3- или 4-членное кольцо содержит 1 гетероатом, выбранный из группы, состоящей из О, N и S. 5-членное кольцо может не содержать или содержать одну двойную связь и один, два или три гетероатома, выбранные из группы, состоящей из О, N и S. 6- или 7-членное кольцо не содержит или содержит одну или две двойные связи и один, два или три гетероатома, выбранные из группы, состоящей из О, N и S. Моноциклический гетероцикл соединен с исходным молекулярным фрагментом через любой атом углерода или любой атом азота, который содержится в моноциклическом гетероцикле. Типичные примеры моноциклического гетероцикла включают в себя без ограничения азетидинил, азепанил, азиридинил, диазепанил, 1,3-диоксанил, 1,3-диоксоланил, 1,3-дитиоланил, 1,3-дитианил, имидазолинил, имидазолидинил, изотиазолинил, изотиазолидинил, изоксазолинил, изоксазолидинил, морфолинил, оксадиазолинил, оксадиазолидинил, оксазолинил, оксазолидинил, пиперазинил, пиперидинил, пиранил, пиразолинил, пиразолиднил, пирролинил, пирролидинил, тетрагидрофуранил, тетрагидротиенил, тиадиазолинил, тиадиазолидинил, тиазолинил, тиазолидинил, тиоморфолинил, 1,1-диоксидотиоморфолинил (тиоморфолина сульфон), тиопиранил и тритианил. Бициклический гетероцикл представляет собой моноциклический гетероцикл, конденсированный с любым из фенила, моноциклического циклоалкила, моноциклического циклоалкенила, моноциклического гетероцикла или моноциклического гетероарила. Бициклический гетероцикл соединен с исходным молекулярным фрагментом через любой атом углерода или любой атом азота, который содержится в моноциклической гетероциклической части бициклической кольцевой системы. Типичные примеры бициклических гетероциклилов включают в себя без ограничений 2,3-дигидробензофуран-2-ил, 2,3-дигидробензофуран-3-ил, индолин-1-ил, индолин-2-ил, индолин-3-ил, 2,3-дигидробензотиен-2-ил, декагидрохинолинил, декагидроизохинолинил, октагидро-1H-индолил и октагидробензофуранил. Гетероциклильные группы необязательно замещены одной или двумя группами, которые независимо представляют собой оксо или тиа. Согласно определенным вариантам осуществления бициклический гетероциклил представляет собой 5- или 6-членное моноциклическое гетероциклильное кольцо, конденсированное с фенильным кольцом, 5- или 6-членным моноциклическим циклоалкилом, 5- или 6-членным моноциклическим циклоалкенилом, 5- или 6-членным моноциклическим гетероциклилом или 5- или 6-членным моноциклическим гетероарилом, где бициклический гетероциклил необязательно замещен одной или двумя группами, которые независимо представляют собой оксо или тиа. Согласно определенным вариантам осуществления настоящего раскрытия гетероциклил представляет собой пирролидинил, пиперидинил, пиперазинил или морфолинил.
«Насыщенный» означает, что упоминаемая химическая структура не содержит никаких многочисленных связей углерод-углерод. Например, насыщенная циклоалкильная группа, как определено в настоящем описании, включает в себя циклогексил, циклопропил и т.п.
«Ненасыщенный» означает, что упоминаемая химическая структура содержит по меньшей мере одну из многочисленных связей углерод-углерод, но не является ароматической. Например, ненасыщенная циклоалкильная группа, как определено в настоящем описании, включает в себя циклогексенил, циклопентенил, циклогексадианил и т.п.
«Фармацевтически приемлемая соль» относится и к кислотно-, и к основно-аддитивным солям.
«Модуляция» или «модулировать» относится к лечению, предупреждению, подавлению, усилению или вызыванию функционирования, состояния или нарушения.
«Лечение» или «терапия» относится к лечению заболевания или нарушения, описанных в настоящем изобретении, у субъекта, предпочтительно человека, и включает в себя:
i. ингибирование заболевания или нарушения, т.е., прекращение его развития;
ii. облегчение заболевания или нарушения, т.е., вызывание ослабления нарушения;
iii. замедление развития нарушения; и/или
iv. ингибирование, облегчение или замедление развития одного или нескольких симптомов заболевания или нарушения.
«Субъект» относится к теплокровному животному, такому как млекопитающее, предпочтительно человек или человеческий ребенок, который страдает от или у которого есть возможность быть пораженным одним или несколькими заболеваниями и нарушениями, описанными в настоящем изобретении.
«Пролекарство», как используется в настоящем описании, означает соединение, которое при введении хозяину in vivo превращается в исходное лекарственное средство. Используемый в настоящем описании термин «исходное лекарственное средство» означает любое из описанных в настоящем изобретении химических соединений. Пролекарства могут быть использованы для достижения любого требуемого эффекта, включая усиление свойств исходного лекарственного средства или улучшение фармацевтических или фармакокинетических свойств исходного. Неограничивающие примеры пролекарств включают в себя пролекарства с ковалентным присоединением удаляемых групп или удаляемых частей групп, например, без ограничения производные ацилирования, фосфорилирования, фосфонилирования, фосфорамидатные производные, производные амидирования, восстановления, окисления, эстерификации, алкилирования, другие карбоксипроизводные, сульфокси или сульфоновые производные, карбонилирования или ангидридные, среди прочих.
Описанные в настоящем изобретении вещества, соединения, композиции, изделия и способы могут пониматься более легко в соответствии со следующим подробным описанием конкретных аспектов раскрытого объекта изобретения и примеров и фигур. Является понятным, что описанные ниже аспекты не ограничены конкретными вариантами осуществления, которые, безусловно, могут варьировать, как известно специалистам настоящей области техники. Также является понятным, что используемая в настоящем описании терминология представлена только в целях описания конкретных аспектов и не предусмотрена для ограничения.
Соединения
Бензотиофеновые лиганды эстрогенового рецептора по настоящему изобретению включают в себя соединения формулы А или их фармацевтически приемлемые соли:
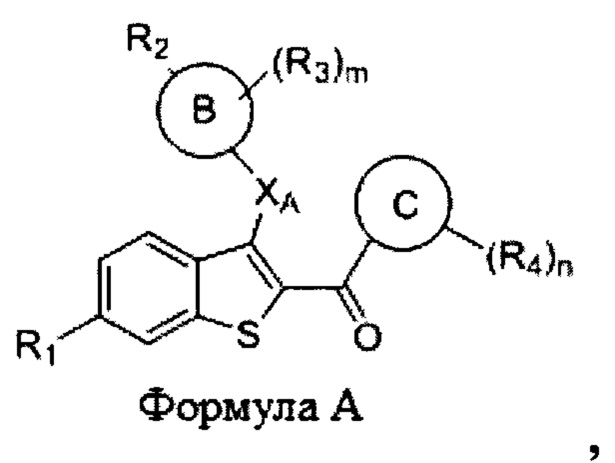
где:
m равно 0, 1, 2, 3 или 4;
n равно 0, 1, 2, 3 или 4;
XA выбран из -O-, -СН2-, -S-, -NH-, -NMe-, -CF2- и -С3циклоалкил-;
Кольцо В представляет собой фенил, нафтил, хинолинил, 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
Кольцо С представляет собой фенил, тиофенил (т.е., тиенил), 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
R1 выбран из гидроксила, водорода, галогена, -O(C1-C6 алкил), -OC(O)(C1-C6 алкил), -ОС(O)С6Н5, -OC(O)O(C1-C6 алкил), -ОС(O)ОС6Н5 и -OSO2(C2-C6 алкил);
R2 выбран из -СН=СНСООН, -NH(CO)COOH, -СООН, -C2-C6алкенилен-СООН и -C2-C6алкинилен-СООН;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, -C1-C6алкила и -C1-C6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-C6алкила, C1-C6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно другому аспекту настоящее изобретение включает в себя фармацевтическую композицию, содержащую одно или несколько соединений формулы А и фармацевтически приемлемый носитель или наполнитель.
Согласно другому аспекту настоящее изобретение относится к способу лечения или предупреждения злокачественной опухоли (включая злокачественную опухоль молочной железы, яичника, матки, почки или эндометрия) или опухоли, который включает в себя введение субъекту, типично человеку, при необходимости такого лечения терапевтически эффективного количества соединения формулы А или его фармацевтически приемлемой соли.
Согласно другому аспекту настоящее изобретение относится к соединению формулы В или его фармацевтически приемлемой соли:
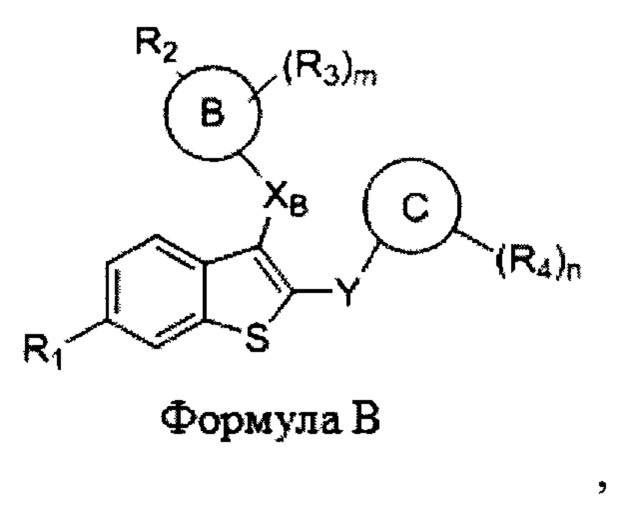
где:
m равно 0, 1, 2, 3 или 4;
b равно 0, 1, 2, 3 или 4;
XB выбран из -O-, -СН2-, -S-, -NH-, -NMe-, -CF2- и -С3циклоалкил-;
Y выбран из -С(O)-, -O-, -CF2- или -С3циклоалкил-, -СН2-, -S-, -NH- и -N(Me)-;
Кольцо В представляет собой фенил, нафтил, хинолинил, 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
Кольцо С представляет собой фенил, тиофенил (т.е., тиенил), 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
R1 выбран из гидроксила, водорода, галогена, -O(C1-C6 алкил), -OC(O)(C1-C6 алкил), -ОС(O)С6Н5, -ОС(O)O(C1-C6 алкил), -ОС(O)ОС6Н5 и -OSO2(C2-C6 алкил);
R2 выбран из -СН=СНСООН, -NH(CO)COOH, -COOH, -C2-C6алкенилен-СООН и -C2-C6алкинилен-СООН;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, -C1-C6алкила и -C1-C6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-C6алкила, -C1-C6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно другому аспекту настоящее изобретение включает в себя фармацевтическую композицию, содержащую одно или несколько соединений формулы В и фармацевтически приемлемый носитель или наполнитель.
Согласно другому аспекту настоящее изобретение относится к способу лечения или предупреждения злокачественной опухоли (включая злокачественную опухоль молочной железы, яичника, матки, почки или эндометрия) или опухоли, который включает в себя введение субъекту, такому как человек, при необходимости такого лечения терапевтически эффективного количества соединения формулы В или его фармацевтически приемлемой соли или пролекарства.
Согласно другому аспекту настоящее изобретение относится к соединению формулы С:
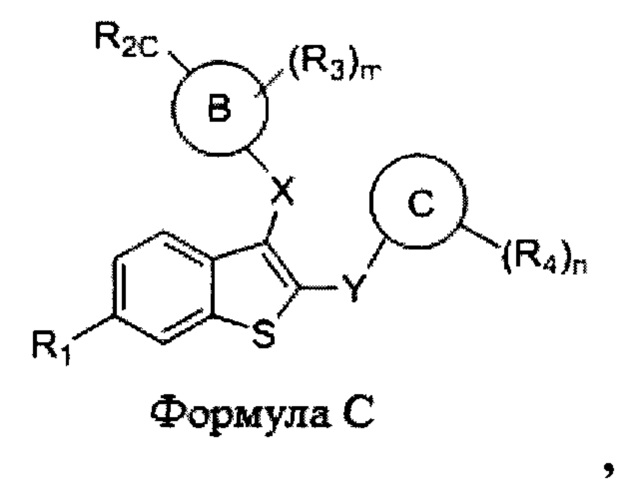
где:
m равно 0, 1, 2, 3 или 4;
n равно 0, 1, 2, 3 или 4;
X выбран из -O-, -С(O)-, -СН2-, -S-, -NH-, -NMe-, -CF2- и -С3циклоалкил-;
Y выбран из -С(O)-, -O-, -CF2- или С3циклоалкила, -СН2-, -S-, -NH- и -NMe-;
Кольцо В представляет собой фенил, нафтил, хинолинил, 5- или 6-членный моноциклический гетероарил, циклоалкил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
Кольцо С представляет собой фенил, тиофенил (т.е., тиенил), 5- или 6-членный моноциклический гетероарил, циклоалкил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
R1 выбран из гидроксила, водорода, галогена, -O(C1-C6 алкил), -OC(O)(C1-C6 алкил), -ОС(O)С6Н5, -ОС(O)O(C1-C6 алкил), -ОС(O)ОС6Н5 и -OSO2(C2-C6 алкил);
R2C выбран из -СН=СНСООН, -NH(CO)COOH, -C2-C6алкенилен-СООН и -C2-C6алкинилен-СООН;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, -C1-C6алкила и -C1-C6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-C6алкила, -C1-C6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно другому аспекту настоящее изобретение включает в себя фармацевтическую композицию, которая включает в себя одно или несколько соединений формулы С и фармацевтически приемлемый носитель или наполнитель.
Согласно другому аспекту настоящее изобретение относится к способу лечения или предупреждения злокачественной опухоли (включая злокачественную опухоль молочной железы, яичника, матки, почки или эндометрия) или опухоли, который включает в себя введение субъекту, типично человеку, при необходимости такого лечения терапевтически эффективного количества соединения формулы С или его фармацевтически приемлемой соли или пролекарства.
Согласно одному аспекту настоящее изобретение относится к соединению формулы D или его фармацевтически приемлемой соли:
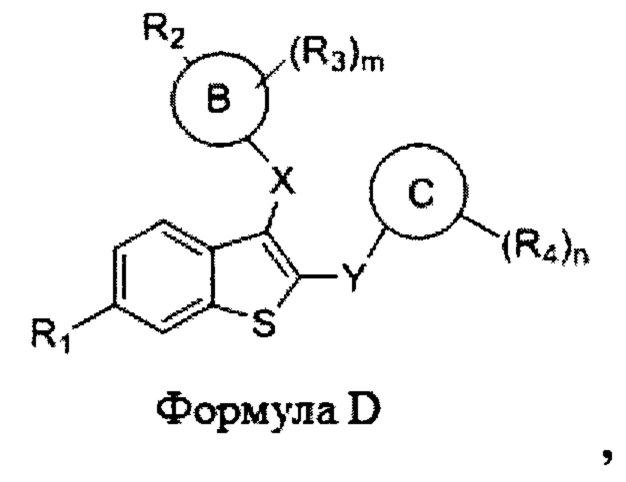
где:
m равно 0, 1, 2, 3 или 4;
n равно 0, 1, 2, 3 или 4;
X выбран из -O-, -С(O)-, -СН2-, -S-, -NH-, -NMe-, -CF2- и -С3циклоалкил-;
Y выбран из -С(O)-, -O-, -CF2- или -С3циклоалкила, -СН2-, -S-, -NH- и -NMe-;
Кольцо В представляет собой фенил, нафтил, хинолинил, 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
Кольцо С представляет собой фенил, тиофенил (т.е., тиенил), 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
R1 выбран из гидроксила, водорода, галогена, -O(C1-C6 алкил), -OC(O)(C1-C6 алкил), -ОС(O)С6Н5, -OC(O)O(C1-C6 алкил), -ОС(O)ОС6Н5 и -OSO2(C2-C6 алкил);
R2 выбран из -СН=СНСООН, -NH(CO)COOH, -COOH, -C2-C6алкенилен-СООН и -C2-C6алкинилен-СООН;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, -C1-C6алкила и -C1-C6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-C6алкила, -C1-C6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно другому аспекту настоящее изобретение включает в себя фармацевтическую композицию, которая включает в себя одно или несколько соединений формулы D или их фармацевтически приемлемую соль или пролекарство и фармацевтически приемлемый носитель или наполнитель.
Согласно другому аспекту настоящее изобретение относится к способу лечения или предупреждения злокачественной опухоли (включая злокачественную опухоль молочной железы, яичника, матки, почки или эндометрия), который включает в себя введение субъекту при необходимости такого лечения терапевтически эффективного количества соединения формулы D или его фармацевтически приемлемой соли или пролекарства.
Согласно одному варианту осуществления настоящего изобретения Х представляет собой -О-.
Согласно другому варианту осуществления Y представляет собой -С(O)-.
Согласно дополнительному варианту осуществления Х представляет собой -О- и Y представляет собой -С(O)-.
Согласно одному варианту осуществления R1 выбран из гидроксила и -O(C1-C6 алкил).
Согласно одному варианту осуществления R2 выбран из -СООН, -NH(CO)COOH и - СН=СНСООН.
Согласно одному варианту осуществления кольцо В представляет собой фенил, нафтил или хинолинил и кольцо С представляет собой фенил или тиенил.
Согласно одному варианту осуществления кольцо С представляет собой фенил.
Согласно одному варианту осуществления
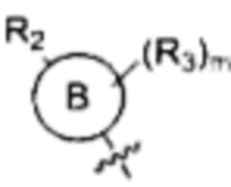
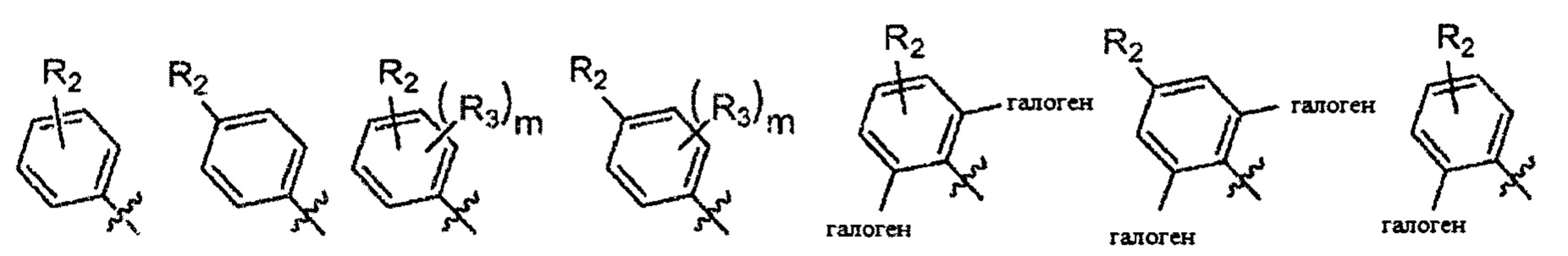
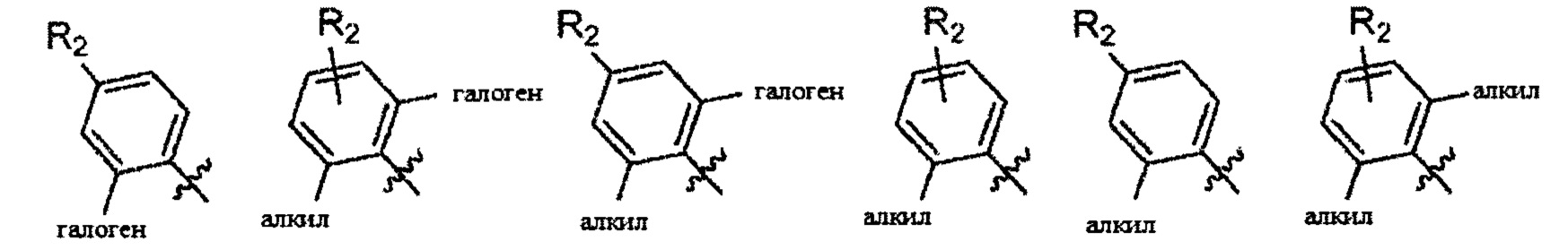
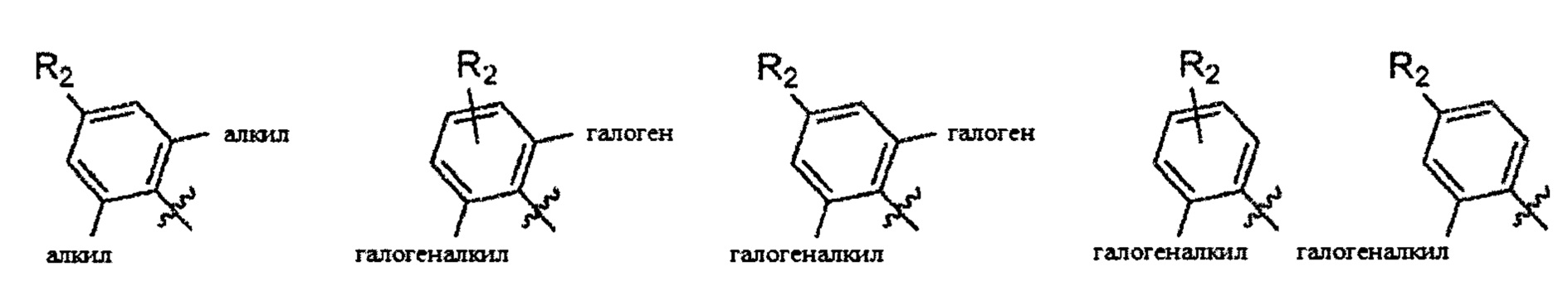

Согласно одному варианту осуществления вышеуказанных вариантов осуществления В-кольца алкил представляет собой метил. Согласно другому варианту осуществления вышеуказанных вариантов осуществления В-кольца алкил независимо представляет собой метил, этил, пропил или циклопропил. Согласно одному варианту осуществления вышеуказанных вариантов осуществления В-кольца галоген представляет собой фтор. Согласно другому варианту осуществления вышеуказанных В-колец галоген независимо представляет собой фтор или хлор, включая, что один галоген представляет собой фтор, а второй представляет собой хлор. Согласно одному варианту осуществления вышеуказанных вариантов осуществления В-кольца галогеналкил независимо представляет собой моно-, ди- или трифторметил.
Согласно другому варианту осуществления
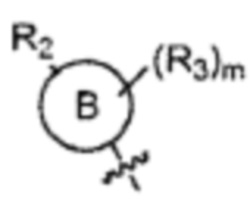
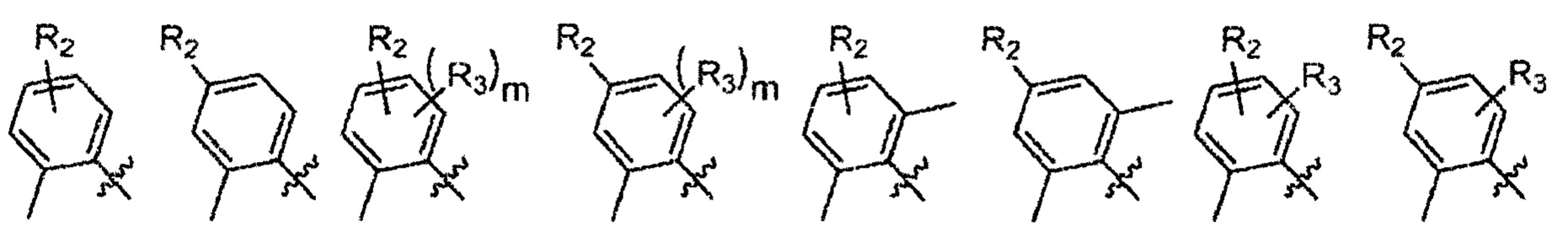
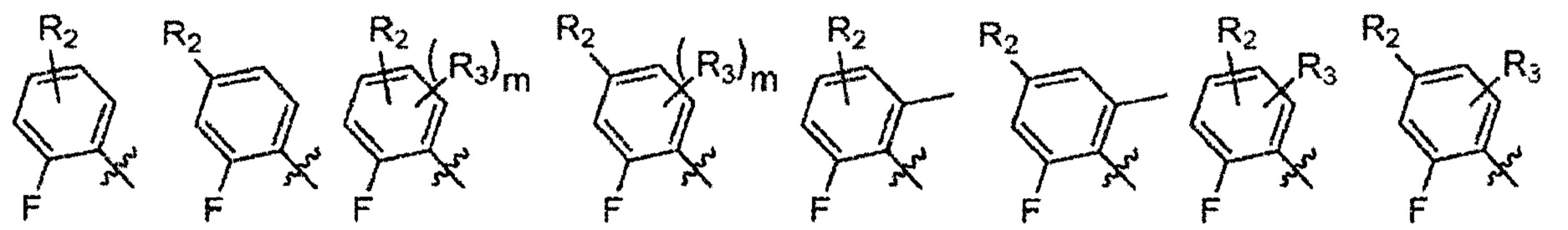
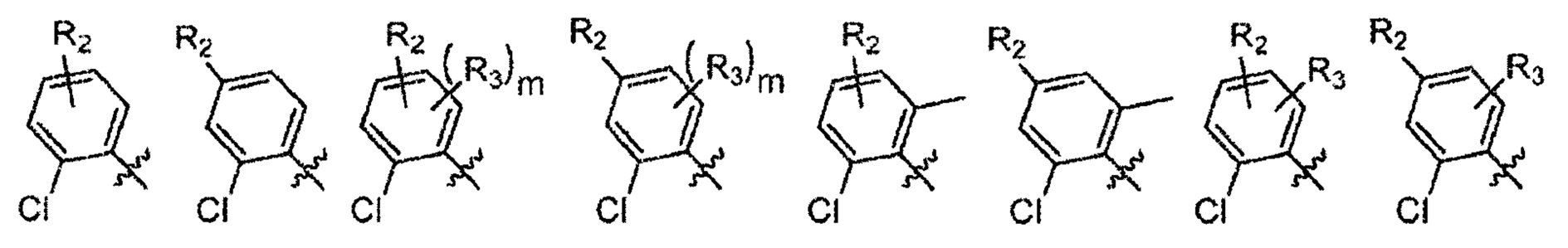
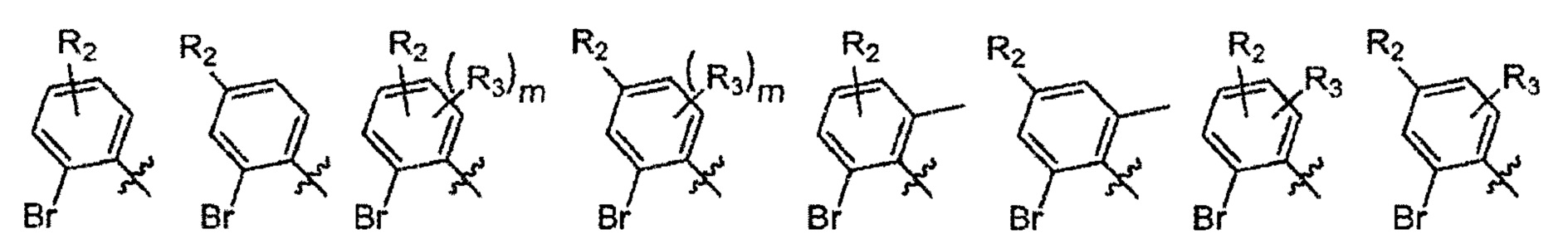
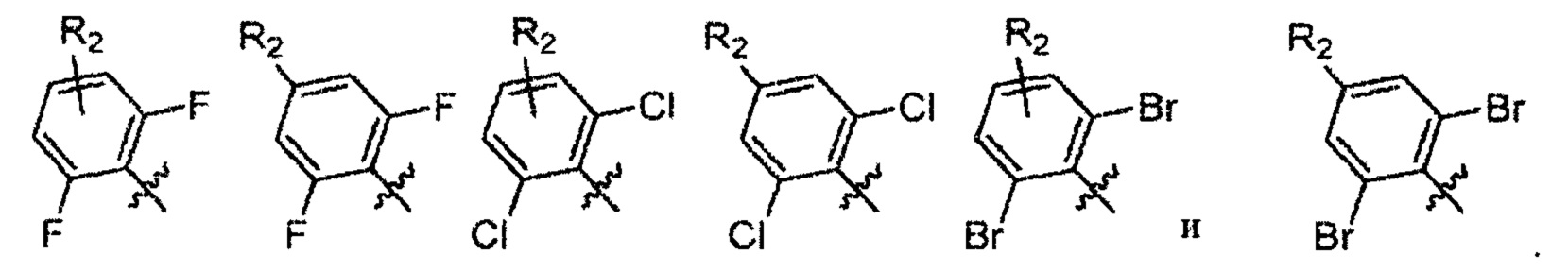
Согласно одному варианту осуществления
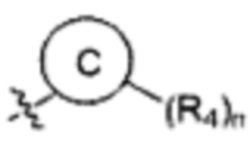
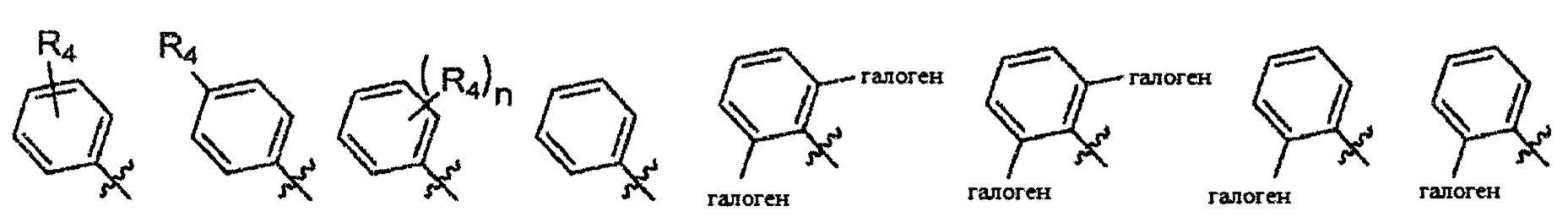
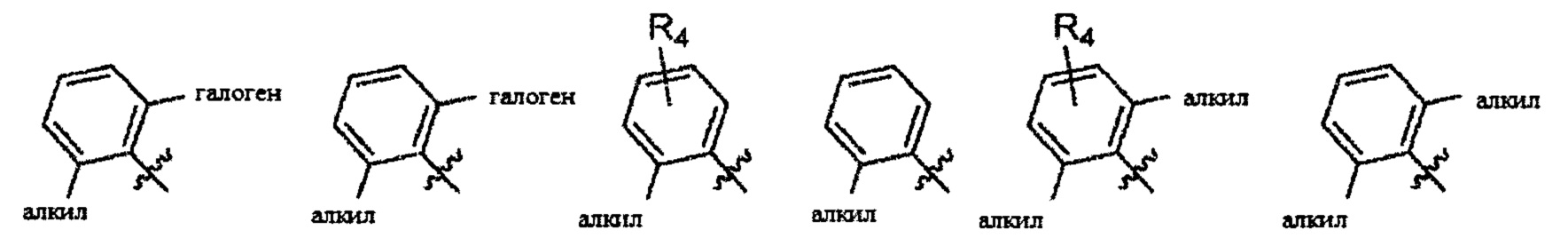
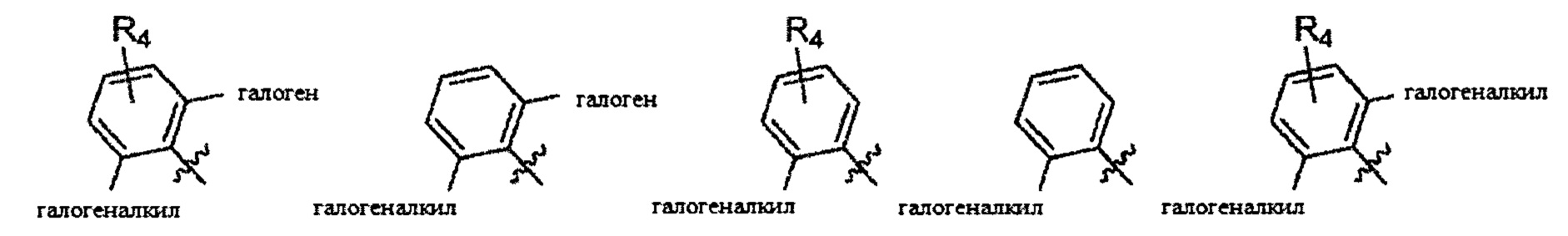
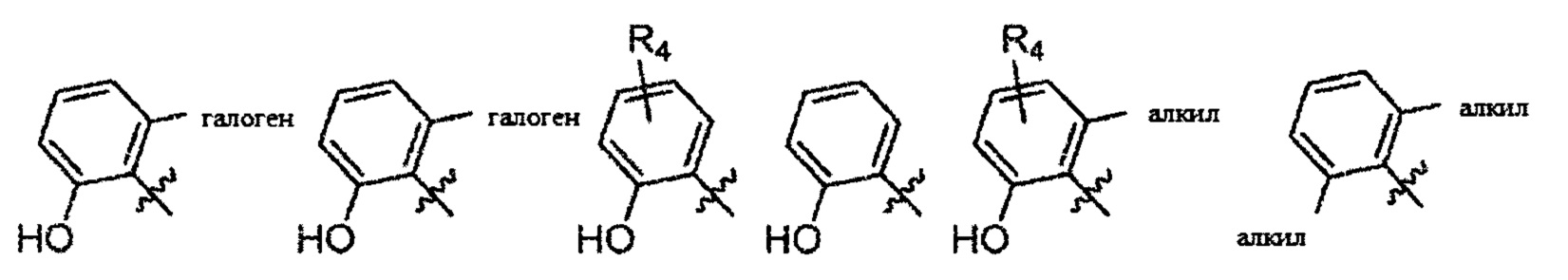
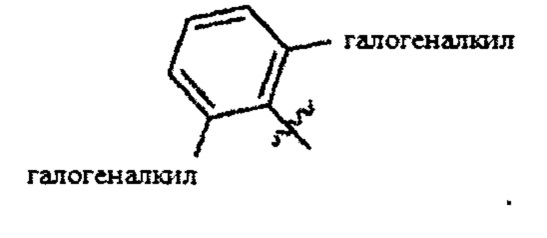
Согласно одному варианту осуществления вышеуказанных вариантов осуществления С-кольца алкил представляет собой метил. Согласно другому варианту осуществления вышеуказанных вариантов осуществления С-кольца алкил независимо представляет собой метил, этил, пропил или циклопропил. Согласно одному варианту осуществления вышеуказанных вариантов осуществления С-кольца галоген представляет собой фтор. Согласно другому варианту осуществления вышеуказанных С-колец галоген независимо представляет собой фтор или хлор, включая, что один галоген представляет собой фтор, а второй представляет собой хлор. Согласно одному варианту осуществления вышеуказанных вариантов осуществления В-кольца галогеналкил независимо представляет собой моно-, ди- или трифторметил.
Согласно другому варианту осуществления

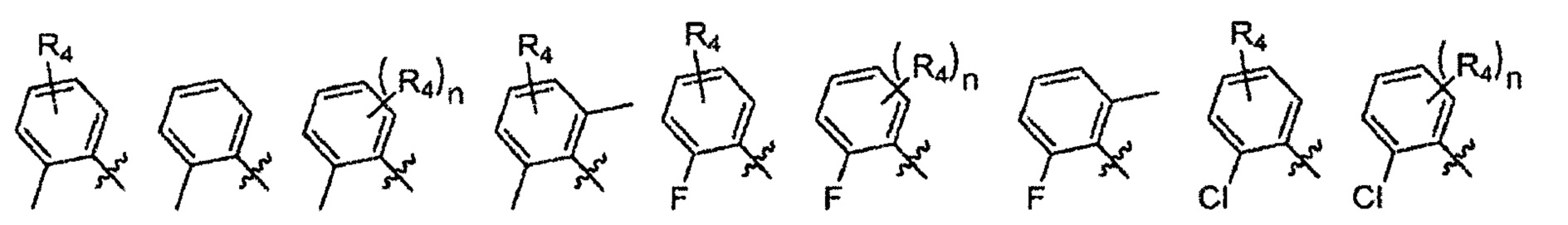
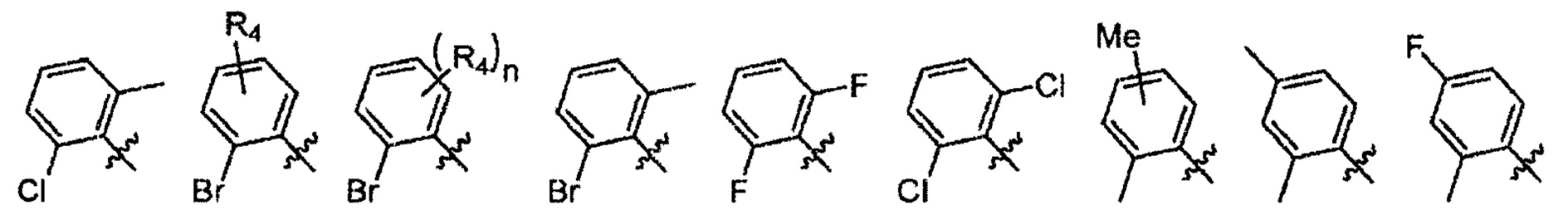
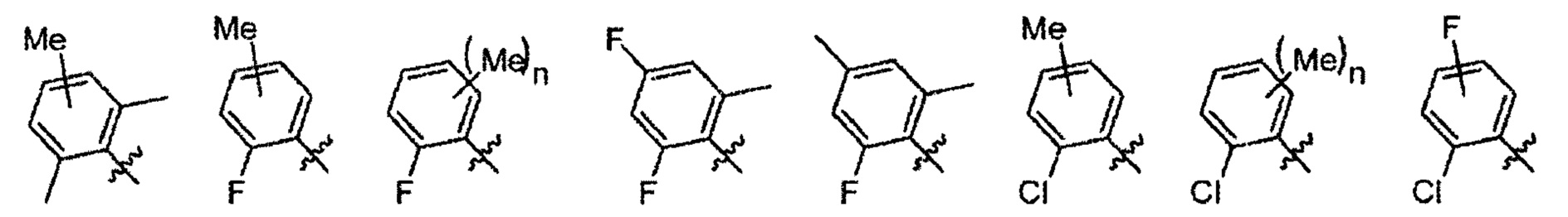
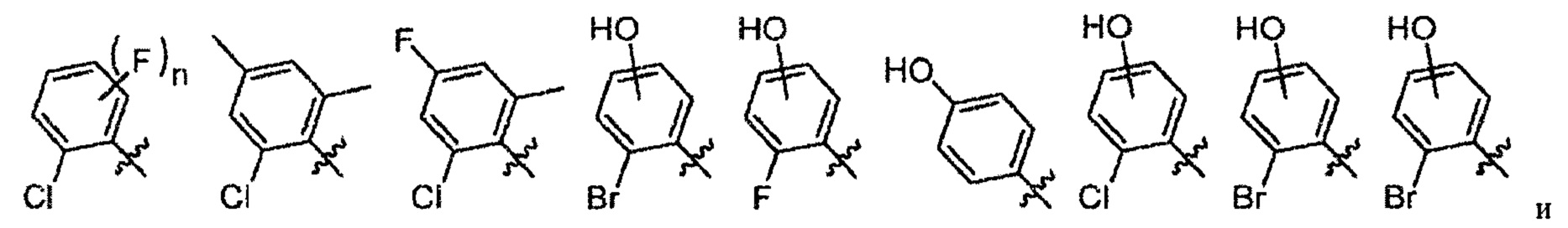
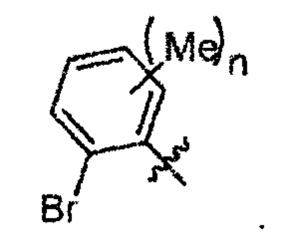
Согласно одному варианту осуществления вышеуказанных вариантов осуществления С-кольца R4 представляет собой водород. Согласно другому варианту осуществления R4 представляет собой -C1-C6алкил, такой как метил, этил или пропил. Согласно еще одному варианту осуществления R4 представляет собой -C1-C6фторалкил, включая трифторметил, дифторметил, фторметил, фторэтил и дифторэтил. Согласно другим вариантам осуществления R4 выбран из -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно другому варианту осуществления соединение представляет собой формулу Е:
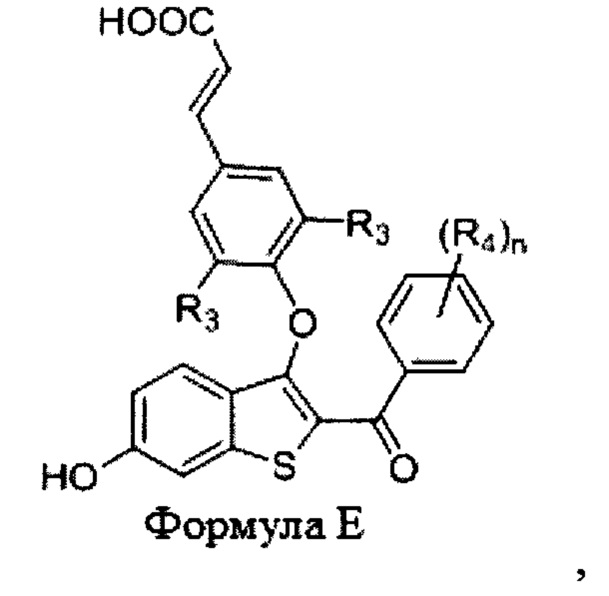
где:
n равно 0, 1, 2, 3 или 4;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, C1-C6алкила и C1-С6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, C1-C6алкила, C1-С6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно одному варианту осуществления R3 независимо в каждом случае выбран из водорода, галогена, метила и -CN.
Согласно другому варианту осуществления соединение представляет собой формулу F:
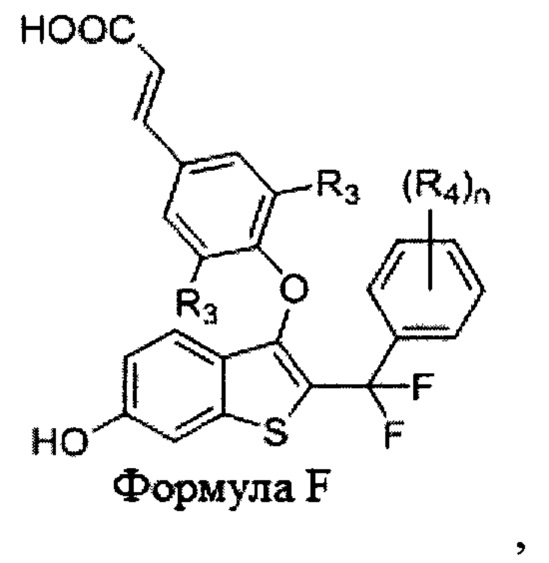
где:
n равно 0, 1, 2, 3 или 4;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, -C1-C6алкила и -C1-С6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, C1-C6алкила, C1-С6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно одному варианту осуществления R3 независимо в каждом случае выбран из водорода, галогена, метила и -CN; и
Согласно другому варианту осуществления соединение представляет собой формулу G:
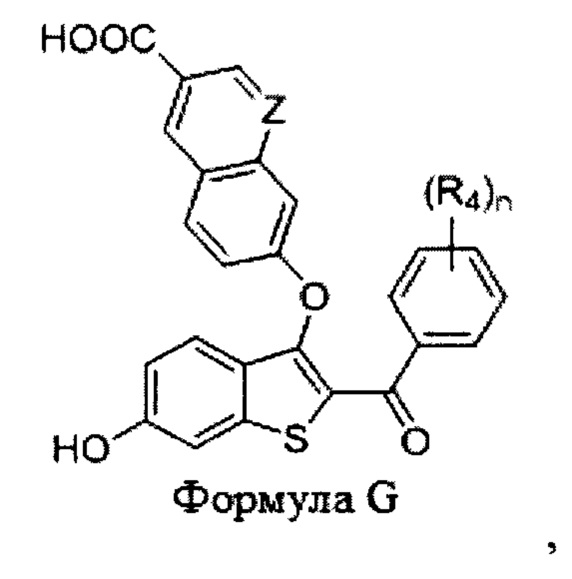
где:
Z представляет собой СН или N;
n равно 0, 1, 2, 3 или 4; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-C6алкила, -C1-С6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно другому варианту осуществления соединение представляет собой формулу Н:
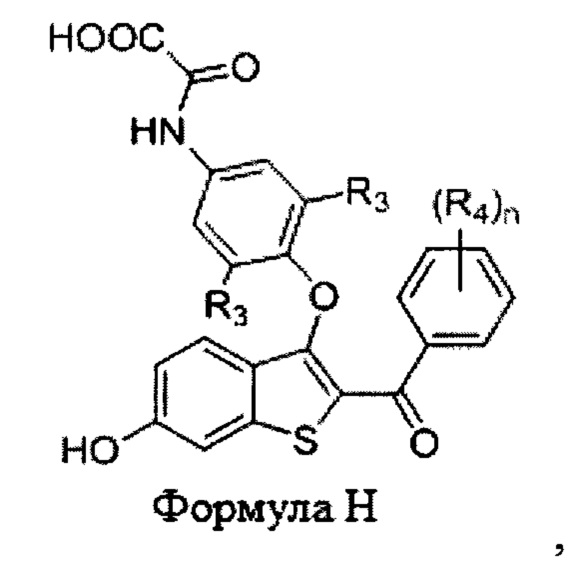
где:
n равно 0, 1, 2, 3 или 4;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, -C1-C6алкила и -C1-С6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-C6алкила, -C1-С6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно одному варианту осуществления R3 независимо в каждом случае выбран из водорода, галогена, метила и -CN.
Согласно другому варианту осуществления представлено соединение формулы I:
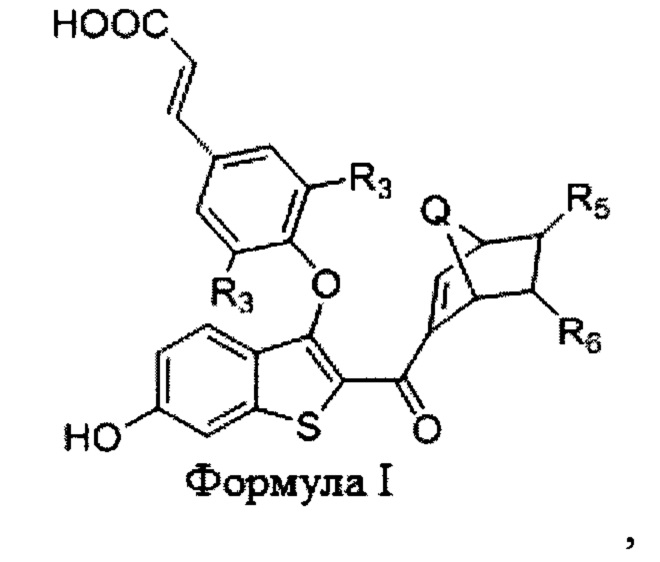
где:
Q выбран из О, S, СН2, NH и S(O);
R5 и R6 независимо выбраны из -CN, галогена и -COOR7;
R3 независимо в каждом случае выбран из водорода, галогена, метила и -CN; и
R7 выбран из галогеналкила, алкила, циклоалкила, арила и гетероарила.
Согласно дополнительному варианту осуществления представлено соединение формулы J:
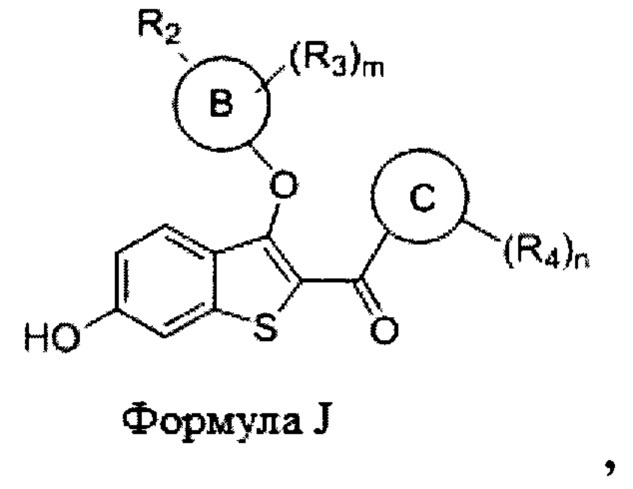
где:
m равно 0, 1, 2, 3 или 4;
n равно 0, 1, 2, 3 или 4;
Кольцо В представляет собой фенил, нафтил, хинолинил, 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
Кольцо С представляет собой фенил, тиофенил (т.е., тиенил), 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
R2 выбран из -СН=СНСООН, -NH(CO)COOH, -COOH, -C2-C6алкенилен-СООН и -C2-C6алкинилен-СООН;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, -C1-C6алкила и -C1-С6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-C6алкила, -C1-С6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно дополнительному варианту осуществления представлено соединение формулы K:
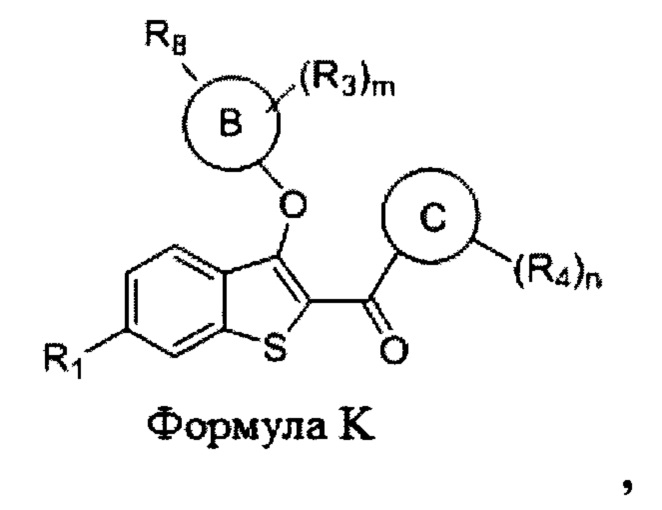
где:
m равно 0, 1, 2, 3 или 4;
n равно 0, 1, 2, 3 или 4;
Кольцо В представляет собой фенил, нафтил, хинолинил, 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
Кольцо С представляет собой фенил, тиофенил (т.е., тиенил), 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
R1 выбран из гидроксила, водорода, галогена, -O(C1-C6 алкил), -ОС(O)(C1-C6 алкил), -ОС(O)С6Н5, -OC(O)O(C1-C6 алкил), -ОС(O)ОС6Н5 и -OSO2(C2-C6 алкил);
R8 выбран из -СН=СНСООН, -NH(CO)COOH, -C2-C6алкенилен-СООН и -C2-C6алкинилен-СООН;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, -C1-C6алкила и -C1-С6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-C6алкила, -C1-С6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно дополнительному варианту осуществления представлено соединение формулы L:
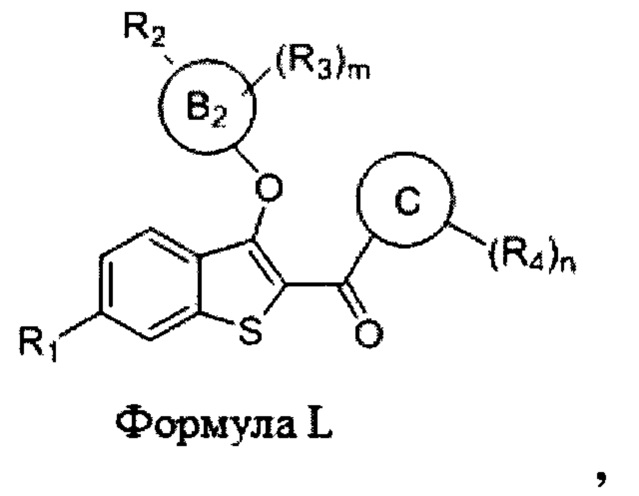
где:
m равно 0, 1, 2, 3 или 4;
n равно 0, 1, 2, 3 или 4;
Кольцо В2 представляет собой нафтил, хинолинил или 10-членный бициклический гетероциклил;
Кольцо С представляет собой фенил, тиофенил (т.е., тиенил), 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
R1 выбран из гидроксила, водорода, галогена, -O(C1-C6 алкил), -OC(O)(C1-C6 алкил), - ОС(O)С6Н5, -OC(O)O(C1-C6 алкил), -ОС(O)ОС6Н5 и -OSO2(C2-C6 алкил);
R2 выбран из -СН=СНСООН, -NH(CO)COOH, -СООН, -C2-C6алкенилен-СООН и -C2-C6алкинилен-СООН;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, C1-C6алкила и C1-С6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, C1-C6алкила, C1-С6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно дополнительному варианту осуществления представлено соединение формулы М:
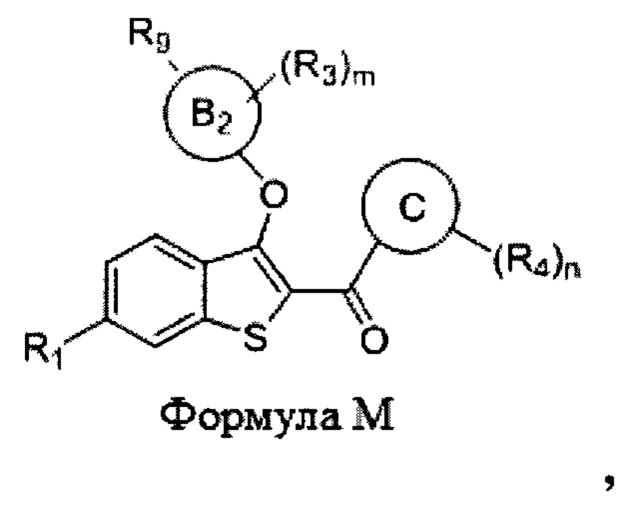
где:
m равно 0, 1, 2, 3 или 4;
n равно 0, 1, 2, 3 или 4;
Кольцо В2 представляет собой нафтил, хинолинил или 10-членный бициклический гетероциклил;
Кольцо С представляет собой фенил, тиофенил (т.е., тиенил), 5- или 6-членный моноциклический гетероарил или 7-, 8-, 9- или 10-членный бициклический гетероциклил;
R1 выбран из гидроксила, водорода, галогена, -O(C1-C6 алкил), -OC(O)(C1-C6 алкил), -ОС(O)С6Н5, -ОС(O)O(C1-C6 алкил), -ОС(O)ОС6Н5 и -OSO2(C2-C6 алкил); R9 представляет собой -СООН;
R3 независимо в каждом случае выбран из водорода, галогена, -CN, -NO2, -C1-C6алкила и -C1-С6фторалкила; и
R4 независимо в каждом случае выбран из водорода, галогена, гидроксила, -C1-C6алкила, -C1-С6фторалкила, -CN, -O(C1-C6 алкил) и -O(C1-C6фторалкил).
Согласно одному варианту осуществления R1 представляет собой гидроксил.
Согласно одному варианту осуществления соединение выбрано из формулы А и R1 представляет собой гидроксил, галоген или -O(C1-C6 алкил).
Согласно одному варианту осуществления соединение выбрано из формулы В и R1 представляет собой гидроксил, галоген или -O(C1-C6 алкил).
Согласно одному варианту осуществления соединение выбрано из формулы С и R1 представляет собой гидроксил, галоген или -O(C1-C6 алкил).
Согласно одному варианту осуществления соединение выбрано из формулы D и R1 представляет собой гидроксил, галоген или -O(C1-C6 алкил).
Согласно одному варианту осуществления R2 представляет собой -СООН.
Согласно одному варианту осуществления R2 представляет собой
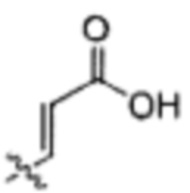
Согласно одному варианту осуществления соединение выбрано из формулы А и R2 представляет собой -СООН или

Согласно одному варианту осуществления соединение выбрано из формулы В и R2 представляет собой -СООН или

Согласно одному варианту осуществления соединение выбрано из формулы С и R2 представляет собой -СООН или

Согласно одному варианту осуществления соединение выбрано из формулы D и R2 представляет собой -СООН или

Согласно одному варианту осуществления R3 представляет собой фтор.
Согласно одному варианту осуществления R3 представляет собой хлор.
Согласно одному варианту осуществления R3 представляет собой метил.
Согласно одному варианту осуществления соединение выбрано из формулы А и R3 представляет собой галоген или -C1-C6алкил, включая метил, этил, пропил и изопропил.
Согласно одному варианту осуществления соединение выбрано из формулы В и R3 представляет собой галоген или -C1-C6алкил, включая метил, этил, пропил и изопропил.
Согласно одному варианту осуществления соединение выбрано из формулы С и R3 представляет собой галоген или -C1-C6алкил, включая метил, этил, пропил и изопропил.
Согласно одному варианту осуществления соединение выбрано из формулы D и R3 представляет собой галоген или -C1-C6алкил, включая метил, этил, пропил и изопропил.
Согласно одному варианту осуществления R4 представляет собой галоген.
Согласно одному варианту осуществления R4 представляет собой -C1-C6алкил.
Согласно одному варианту осуществления R4 представляет собой гидроксил.
Согласно одному варианту осуществления соединение выбрано из формулы А и R4 представляет собой галоген, -C1-C6алкил или гидроксил.
Согласно одному варианту осуществления соединение выбрано из формулы В и R4 представляет собой галоген, -C1-C6алкил или гидроксил.
Согласно одному варианту осуществления соединение выбрано из формулы С и R4 представляет собой галоген, -C1-C6алкил или гидроксил.
Согласно одному варианту осуществления соединение выбрано из формулы D и R4 представляет собой галоген, -C1-C6алкил или гидроксил.
Согласно одному варианту осуществления m равно 0.
Согласно одному варианту осуществления m равно 1.
Согласно одному варианту осуществления m равно 2
Согласно одному варианту осуществления соединение выбрано из формулы А и m равно 0, 1 или 2.
Согласно одному варианту осуществления соединение выбрано из формулы В и m равно 0, 1 или 2.
Согласно одному варианту осуществления соединение выбрано из формулы С и m равно 0, 1 или 2.
Согласно одному варианту осуществления соединение выбрано из формулы D и m равно 0, 1 или 2.
Согласно одному варианту осуществления n равно 0.
Согласно одному варианту осуществления n равно 1.
Согласно одному варианту осуществления n равно 2
Согласно одному варианту осуществления соединение выбрано из формулы А и n равно 0, 1 или 2.
Согласно одному варианту осуществления соединение выбрано из формулы В и n равно 0, 1 или 2.
Согласно одному варианту осуществления соединение выбрано из формулы С и n равно 0, 1 или 2.
Согласно одному варианту осуществления соединение выбрано из формулы D и n равно 0, 1 или 2.
Согласно одному варианту осуществления Х представляет собой -O-.
Согласно одному варианту осуществления соединение выбрано из формулы В и Х представляет собой -O-.
Согласно одному варианту осуществления соединение выбрано из формулы С и Х представляет собой -O-.
Согласно одному варианту осуществления соединение выбрано из формулы D и Х представляет собой -O-.
Согласно одному варианту осуществления Y представляет собой -СО-.
Согласно одному варианту осуществления соединение выбрано из формулы В и Y представляет собой -СО-.
Согласно одному варианту осуществления соединение выбрано из формулы С и Y представляет собой -СО-.
Согласно одному варианту осуществления соединение выбрано из формулы D и Y представляет собой -СО-.
Согласно одному варианту осуществления кольцо В представляет собой фенил.
Согласно одному варианту осуществления кольцо В представляет собой нафтил.
Согласно одному варианту осуществления кольцо В представляет собой хинолинил.
Согласно одному варианту осуществления соединение выбрано из формулы А и кольцо В представляет собой фенил, нафтил или хинолинил.
Согласно одному варианту осуществления соединение выбрано из формулы В и кольцо В представляет собой фенил, нафтил или хинолинил.
Согласно одному варианту осуществления соединение выбрано из формулы С и кольцо В представляет собой фенил, нафтил или хинолинил.
Согласно одному варианту осуществления соединение выбрано из формулы D и кольцо В представляет собой фенил, нафтил или хинолинил.
Согласно одному варианту осуществления кольцо С представляет собой фенил.
Согласно одному варианту осуществления соединение выбрано из формулы А и кольцо С представляет собой фенил.
Согласно одному варианту осуществления соединение выбрано из формулы В и кольцо С представляет собой фенил.
Согласно одному варианту осуществления соединение выбрано из формулы С и кольцо С представляет собой фенил.
Согласно одному варианту осуществления m и n равны 0.
Согласно одному варианту осуществления m равно 0 и n равно 1.
Согласно одному варианту осуществления m равно 0 и n равно 2.
Согласно одному варианту осуществления m равно 1 и n равно 0.
Согласно одному варианту осуществления m равно 1 и n равно 1.
Согласно одному варианту осуществления m равно 1 и n равно 2.
Согласно одному варианту осуществления m равно 2 и n равно 0.
Согласно одному варианту осуществления m равно 2 и n равно 1.
Согласно одному варианту осуществления m равно 2 и n равно 2.
Согласно одному варианту осуществления Х представляет собой -О- и Y представляет собой -С(O)-.
Согласно одному варианту осуществления R1 представляет собой гидроксил, Х представляет собой -О- и Y представляет собой -С(O).
Согласно одному варианту осуществления R1 представляет собой гидроксил, Х представляет собой -O-, Y представляет собой -С(O) и R2 представляет собой

Согласно одному варианту осуществления R1 представляет собой гидроксил, Х представляет собой -O-, Y представляет собой -С(O) и n равно 0.
Согласно одному варианту осуществления R1 представляет собой гидроксил, Х представляет собой -O-, Y представляет собой -С(O) и m равно 0.
Согласно одному варианту осуществления R1 представляет собой гидроксил, Х представляет собой -O-, Y представляет собой -С(O), кольцо В представляет собой фенил и R2 представляет собой

Согласно одному варианту осуществления R1 представляет собой гидроксил, Х представляет собой -O-, Y представляет собой -С(O) и кольцо В представляет собой нафтил и R2 представляет собой -СООН.
Согласно одному варианту осуществления R1 представляет собой гидроксил, Х представляет собой -O-, Y представляет собой -С(O) и кольцо В представляет собой хинолинил и R2 представляет собой -СООН.
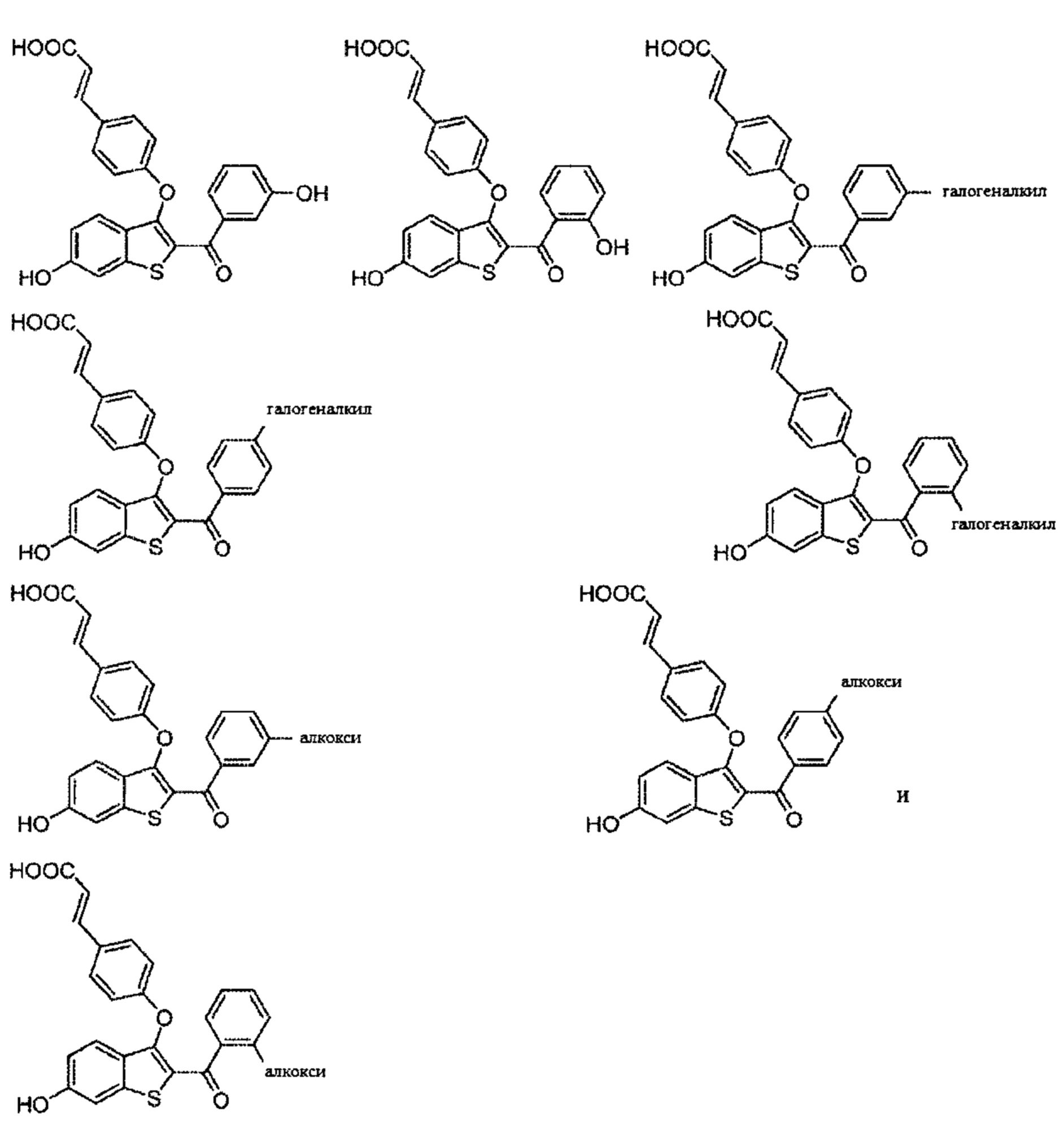
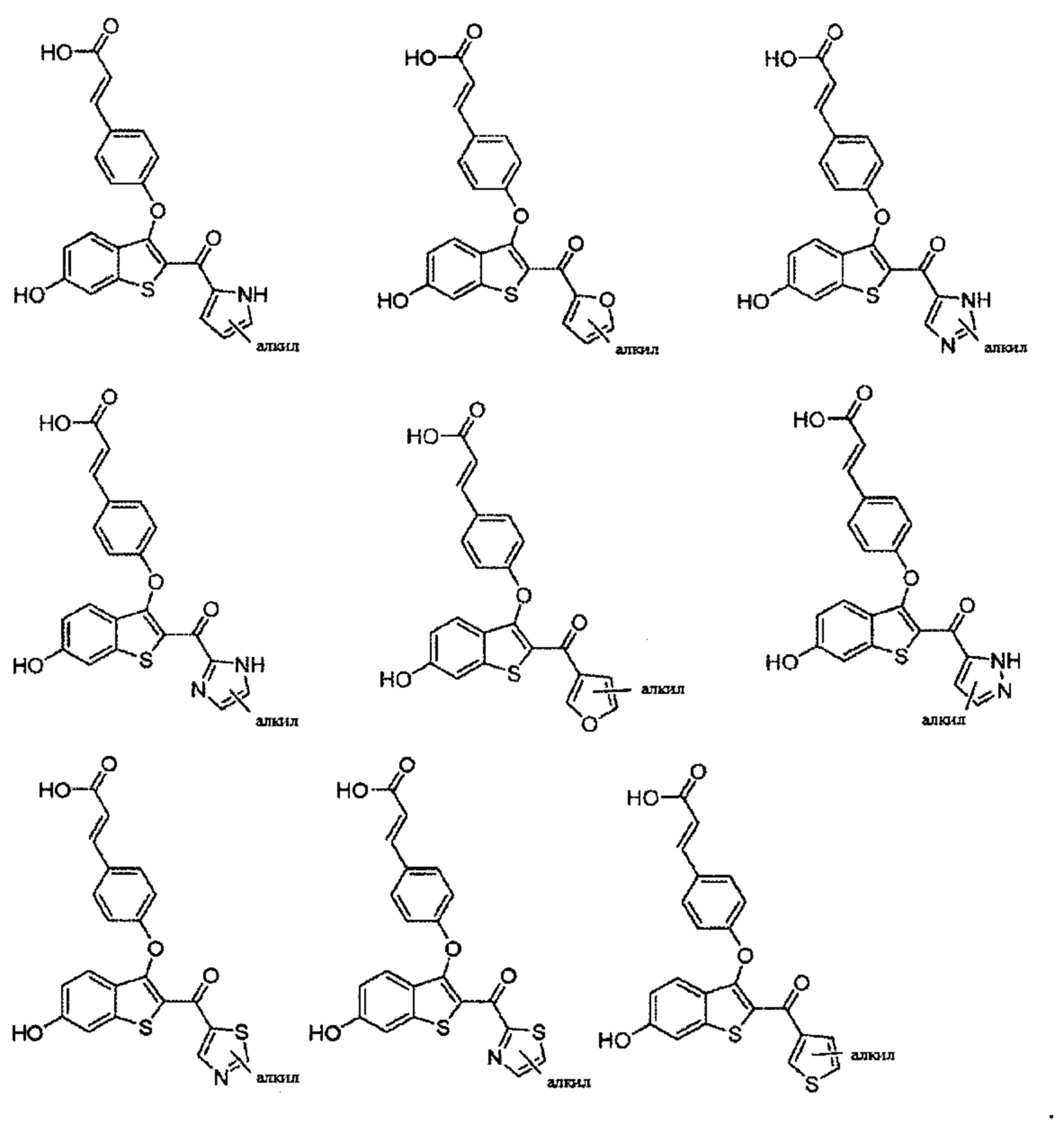
Неограничивающие примеры соединений по настоящему изобретению включают в себя:
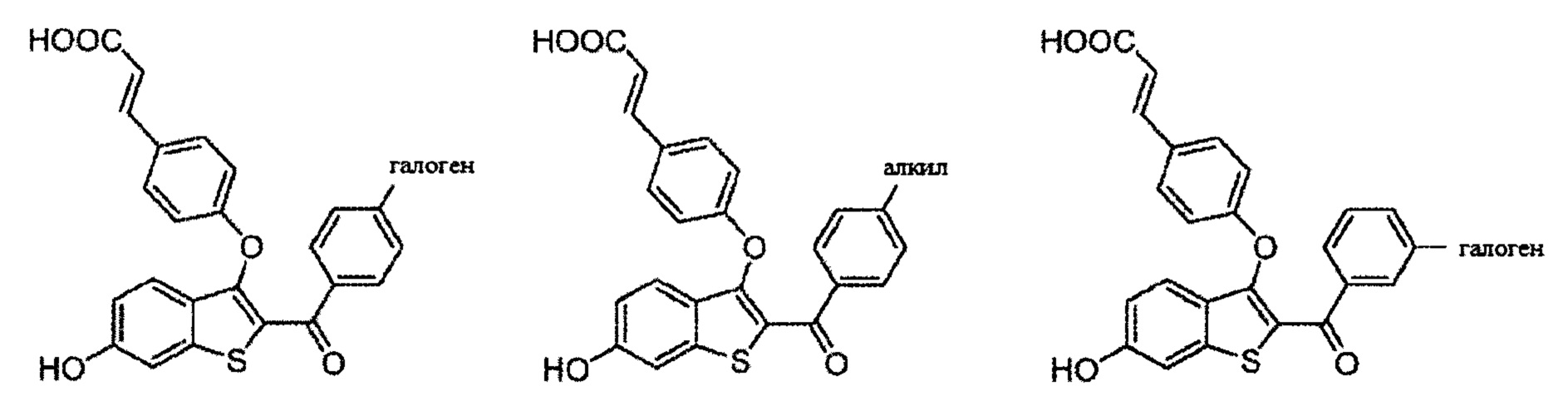
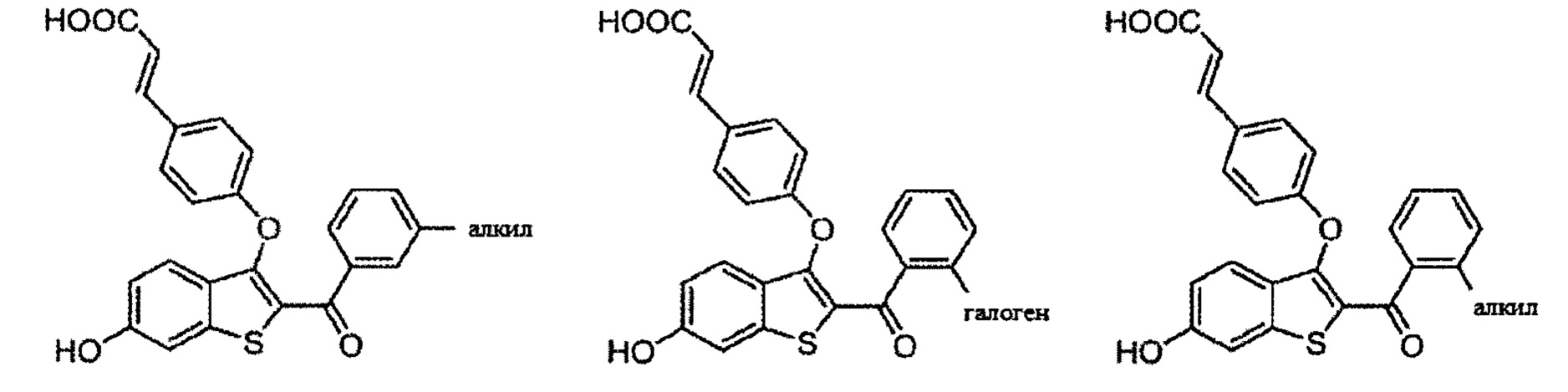
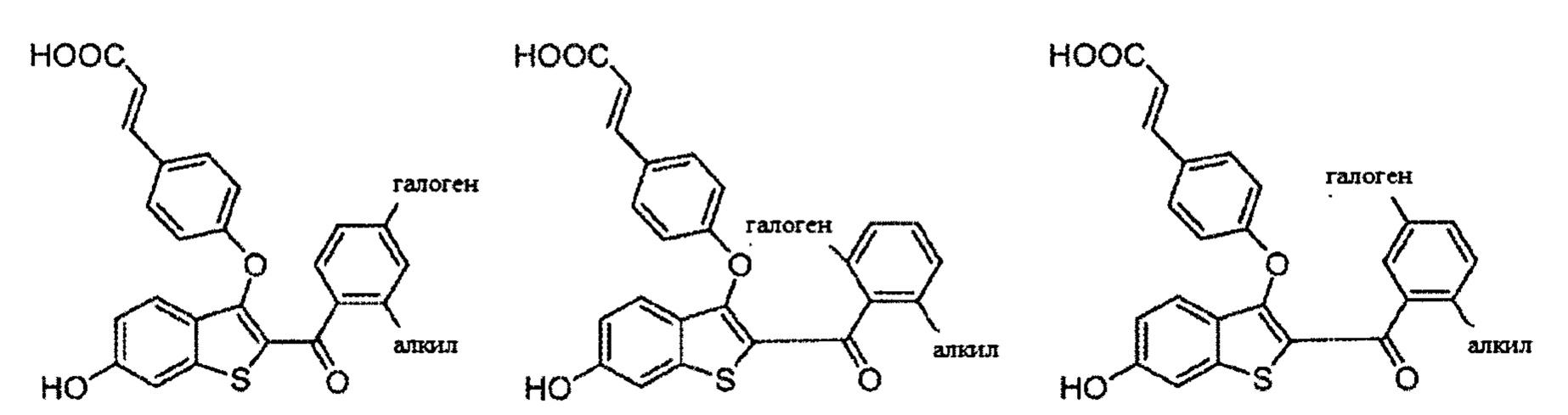

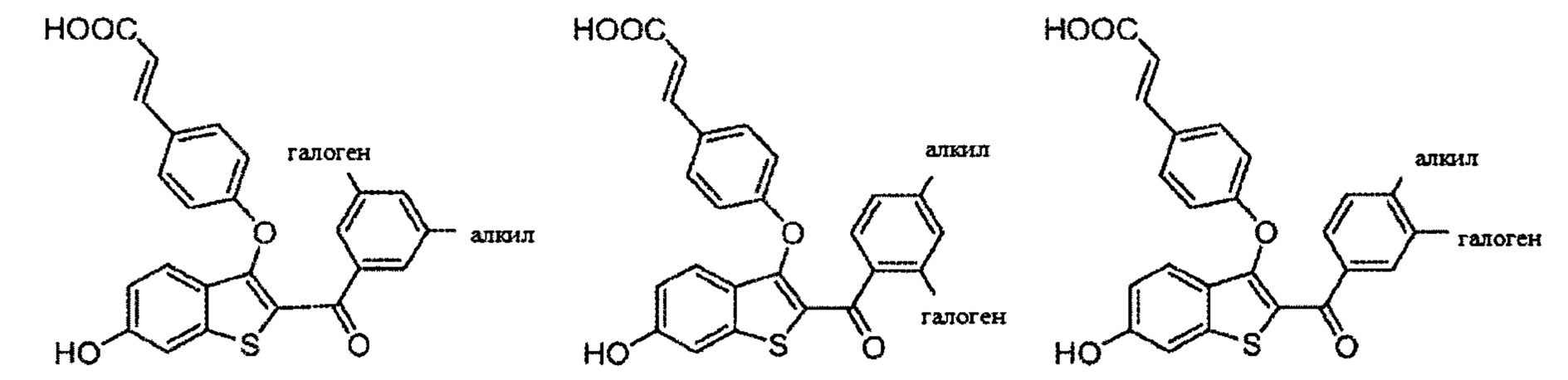
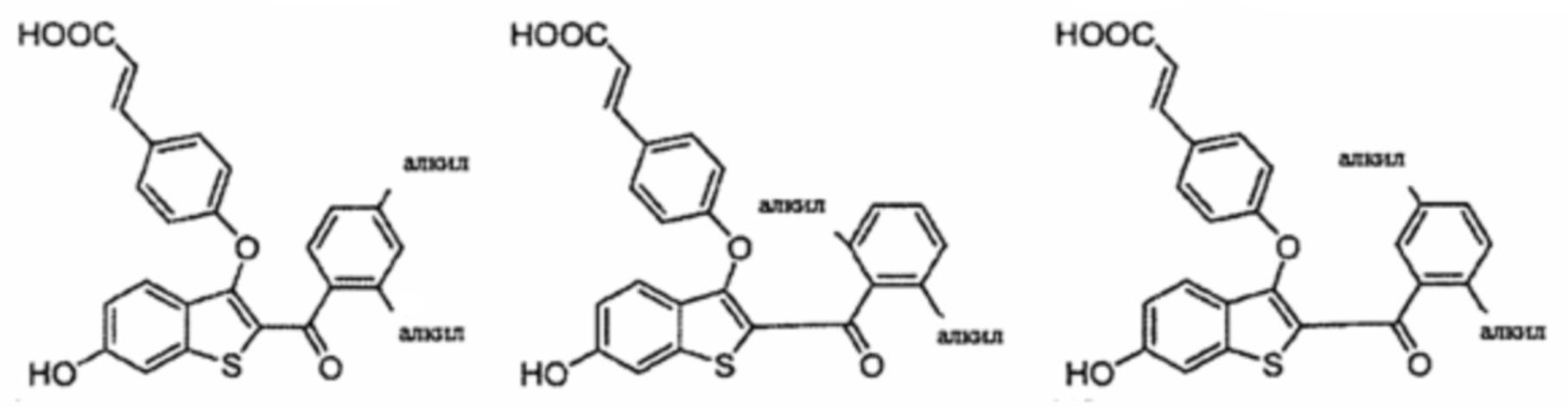
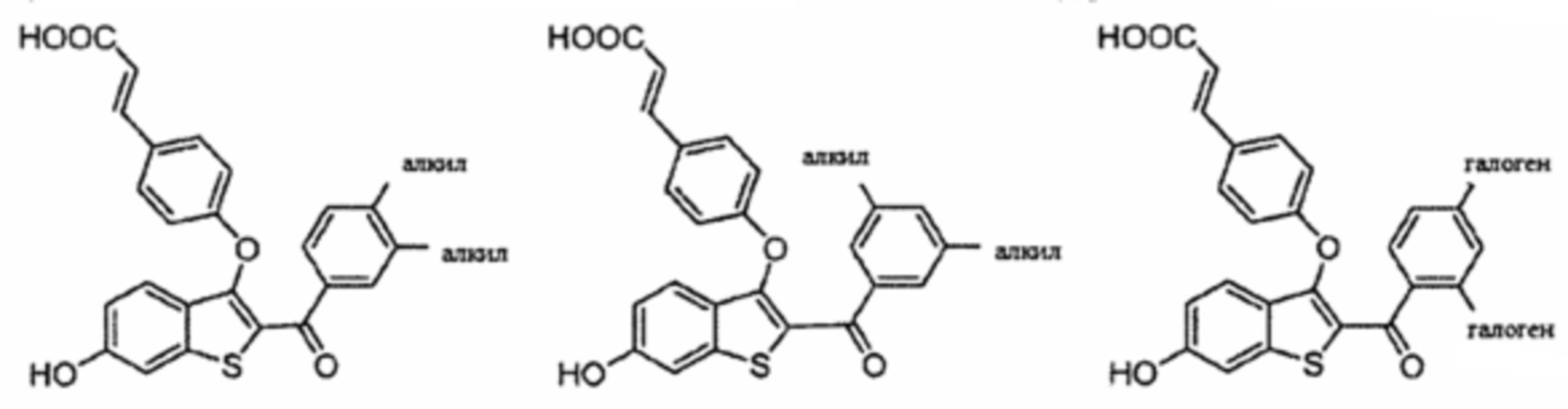
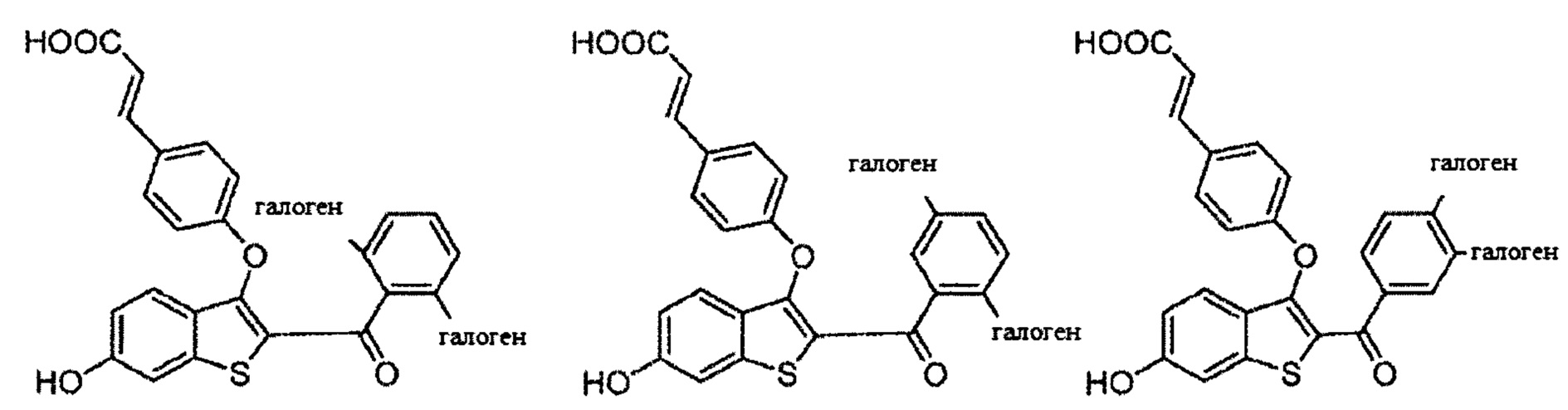
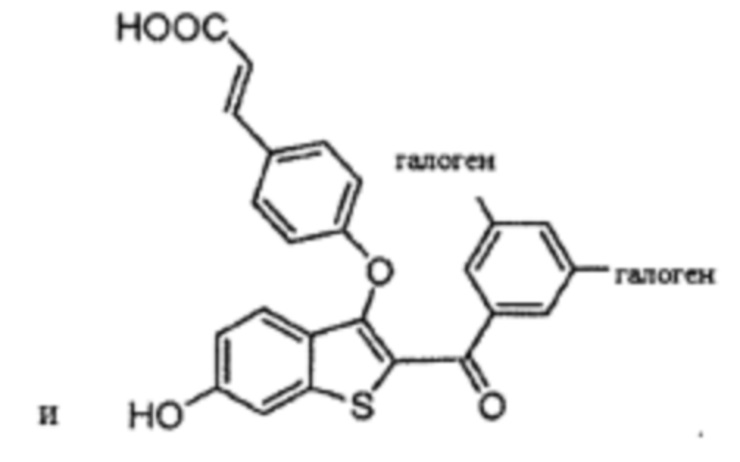
Согласно определенным вариантам осуществления вышеуказанных структур алкил представляет собой метил. Согласно другим вариантам осуществления вариантов осуществления вышеуказанных структур алкил независимо представляет собой метил, этил, пропил или циклопропил. Согласно некоторым вариантам осуществления вышеуказанных вариантов осуществления галоген представляет собой фтор. Согласно некоторым вариантам осуществления галогеналкил независимо представляет собой моно-, ди- или трифторметил. Согласно определенным вариантам осуществления, если бензольное кольцо содержит два галогена, галогенами может быть один фтор один хлор, два фтора или два хлора. Согласно определенным вариантам осуществления, если бензольное кольцо содержит три галогена, галогенами может быть один фтор два хлора, два фтора один хлор, три фтора или три хлора.
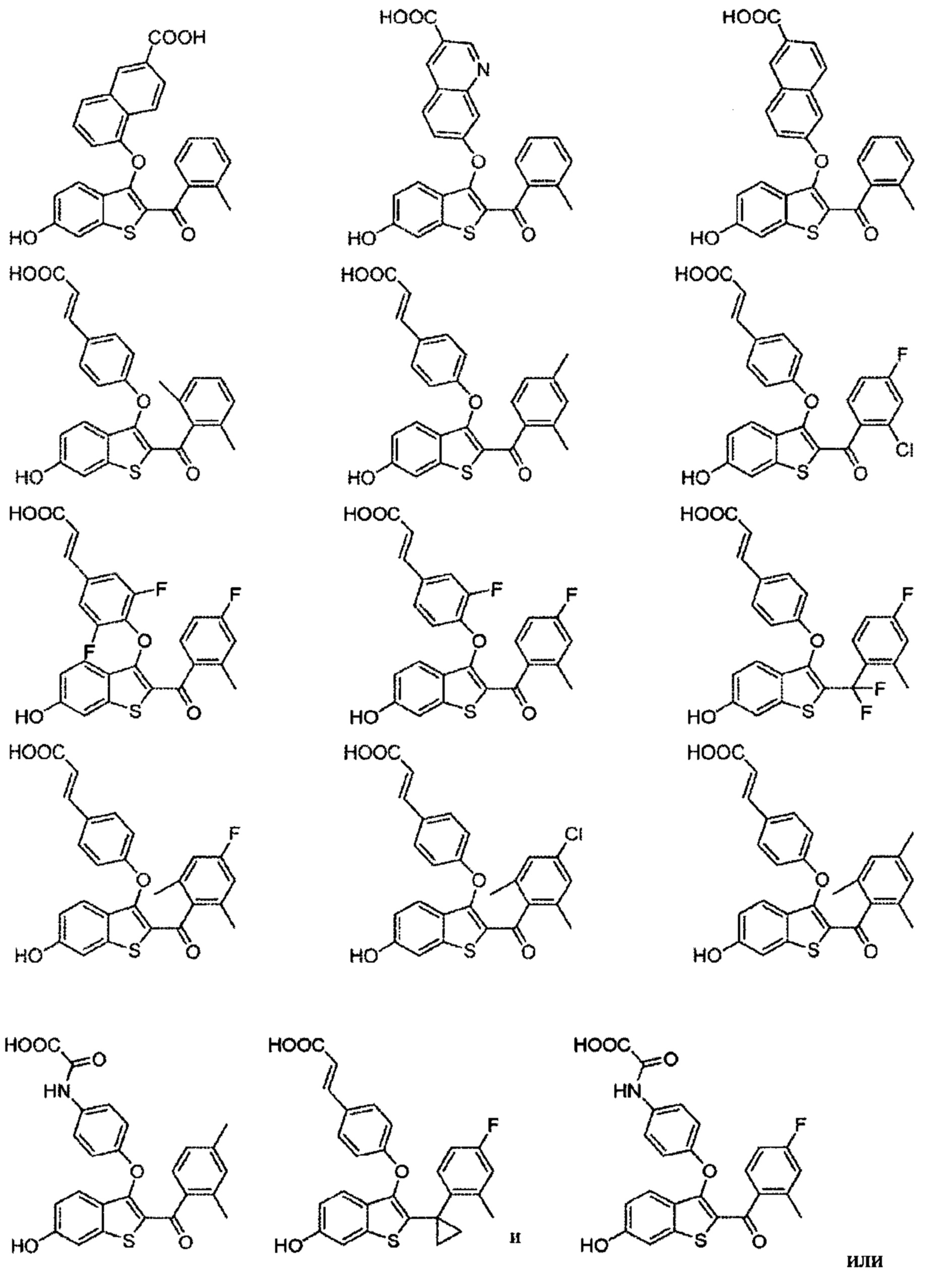
Дополнительные неограничивающие примеры соединений по настоящему изобретению включают в себя:
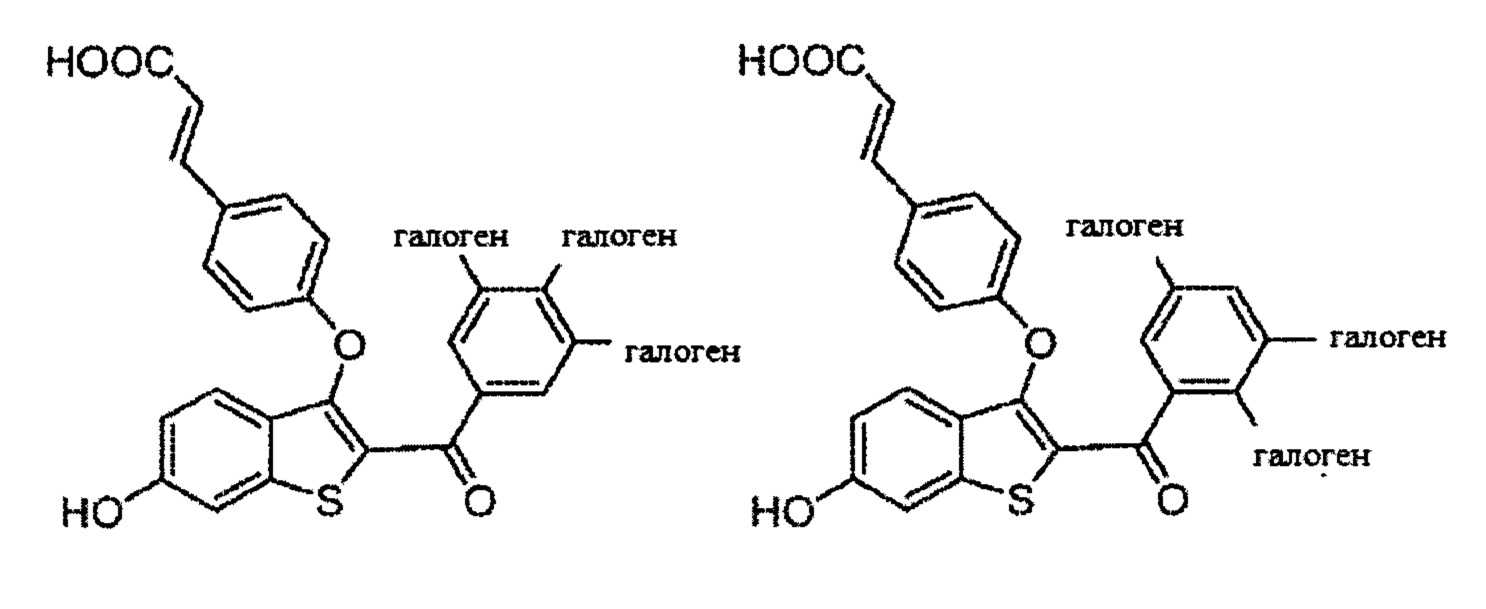
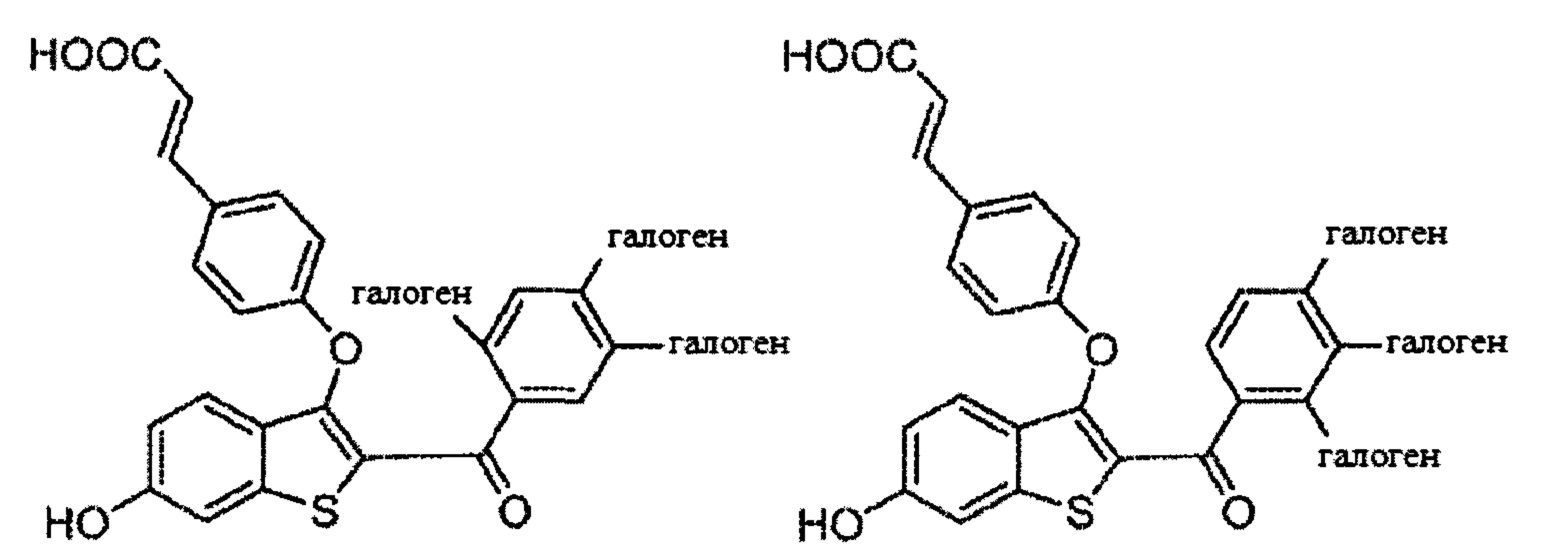
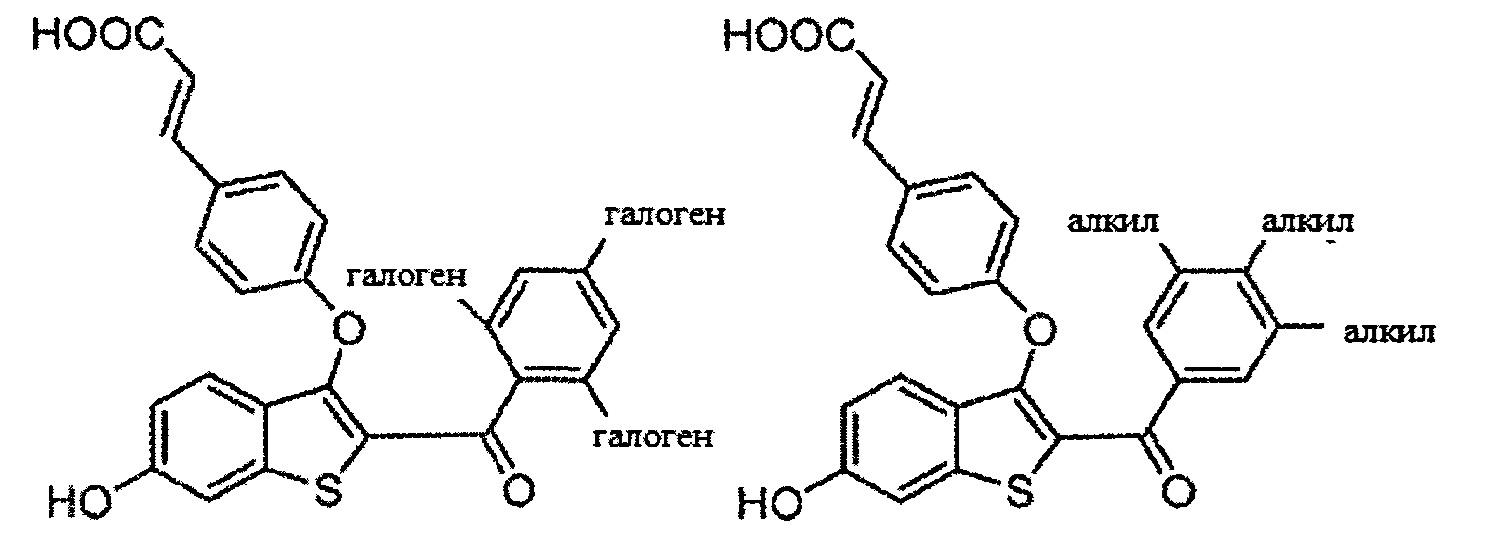
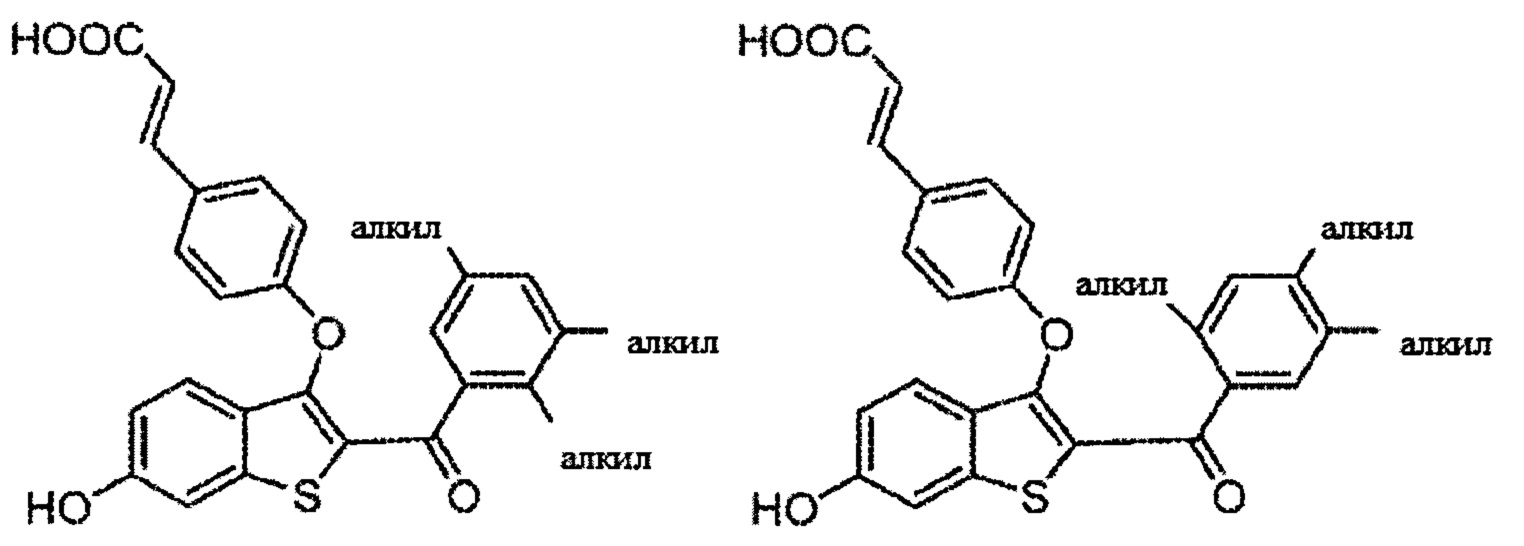
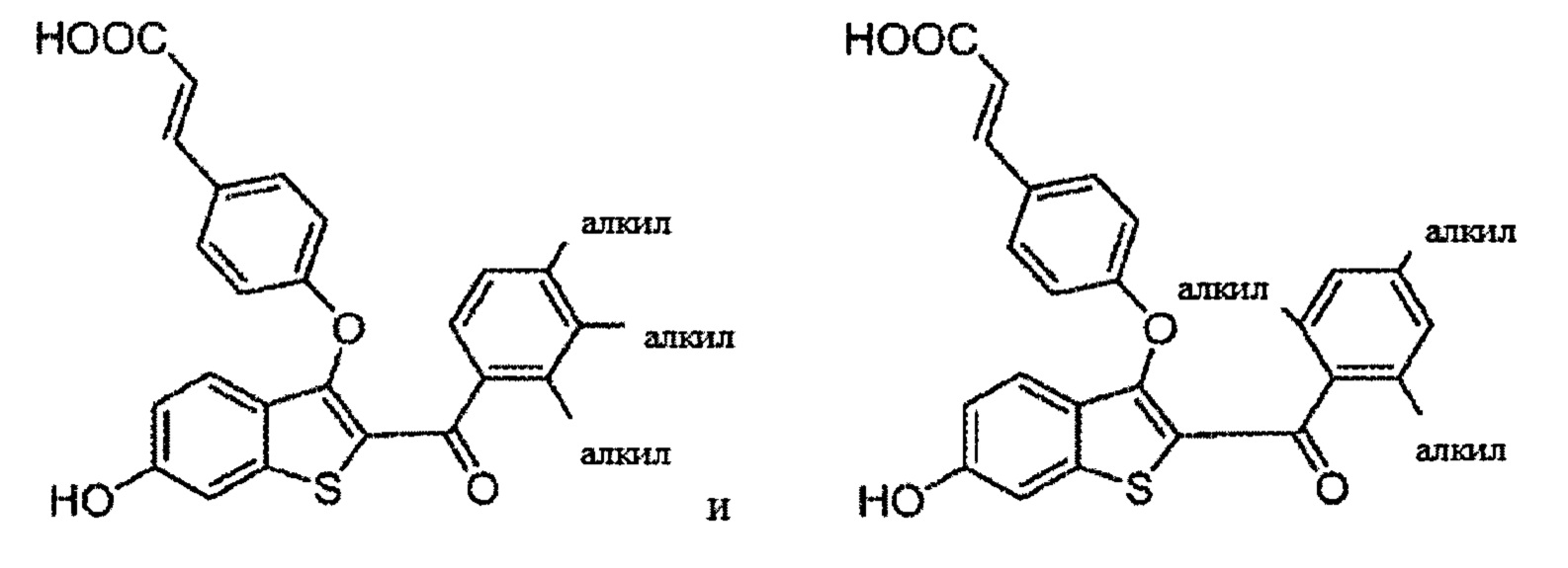
Дополнительные неограничивающие примеры соединений по настоящему изобретению включают в себя:
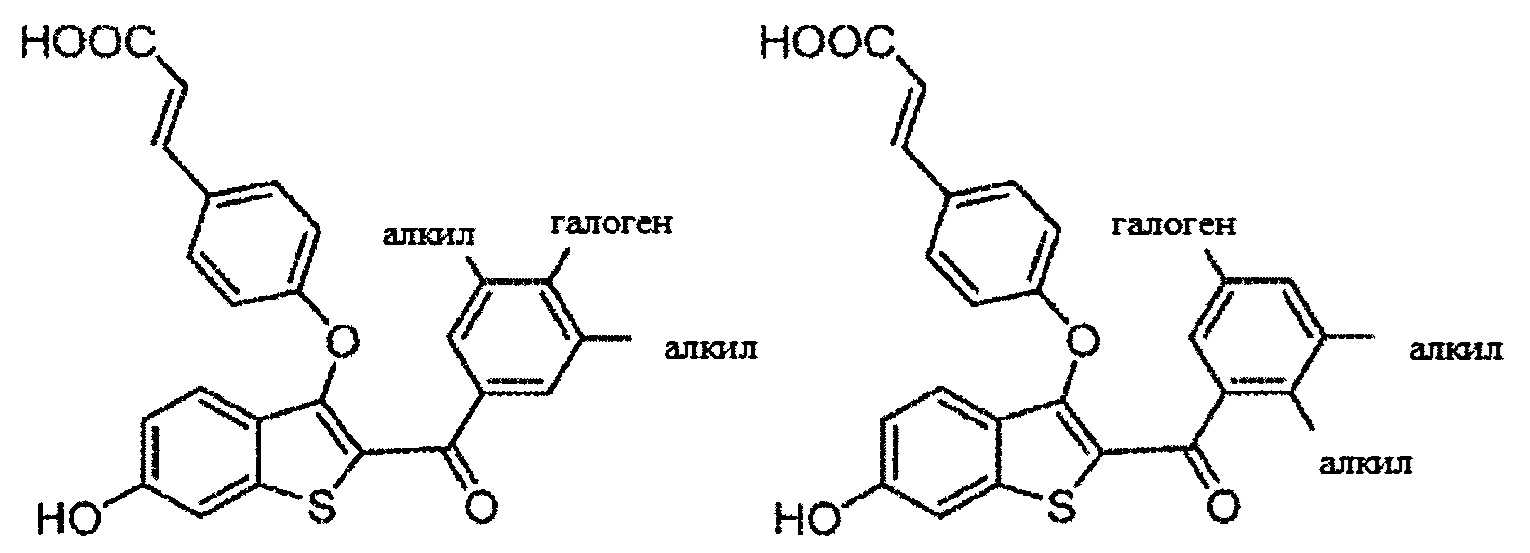
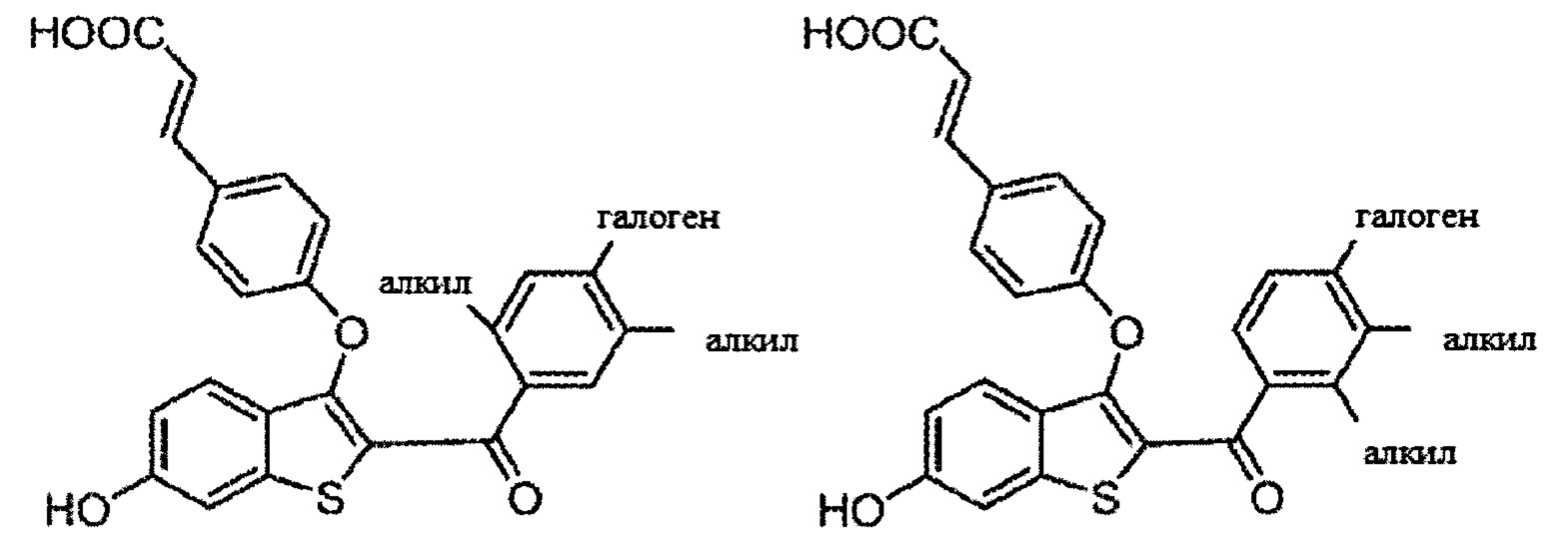
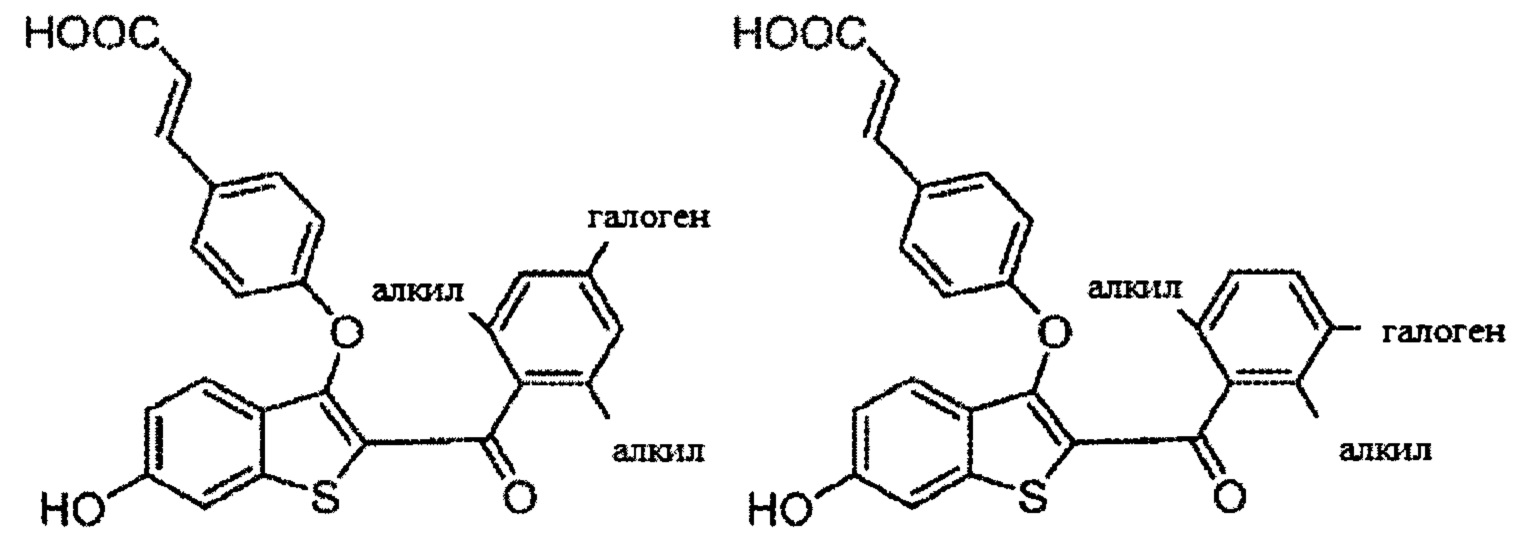
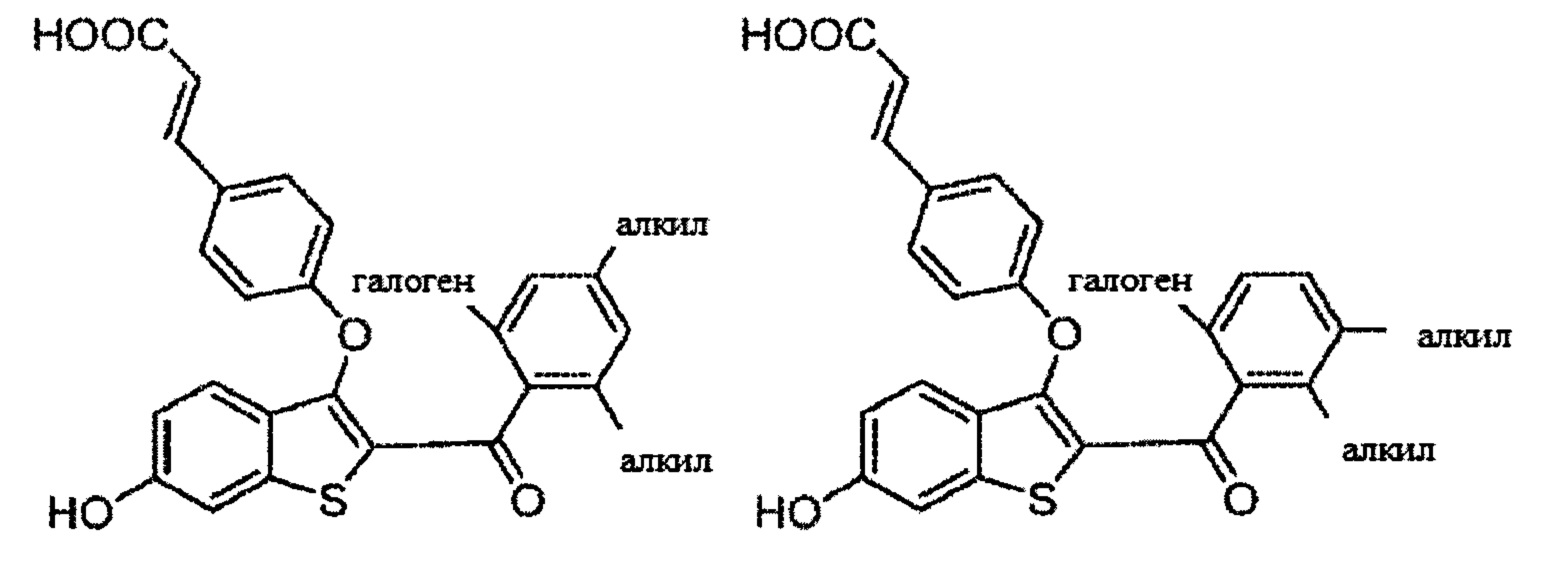
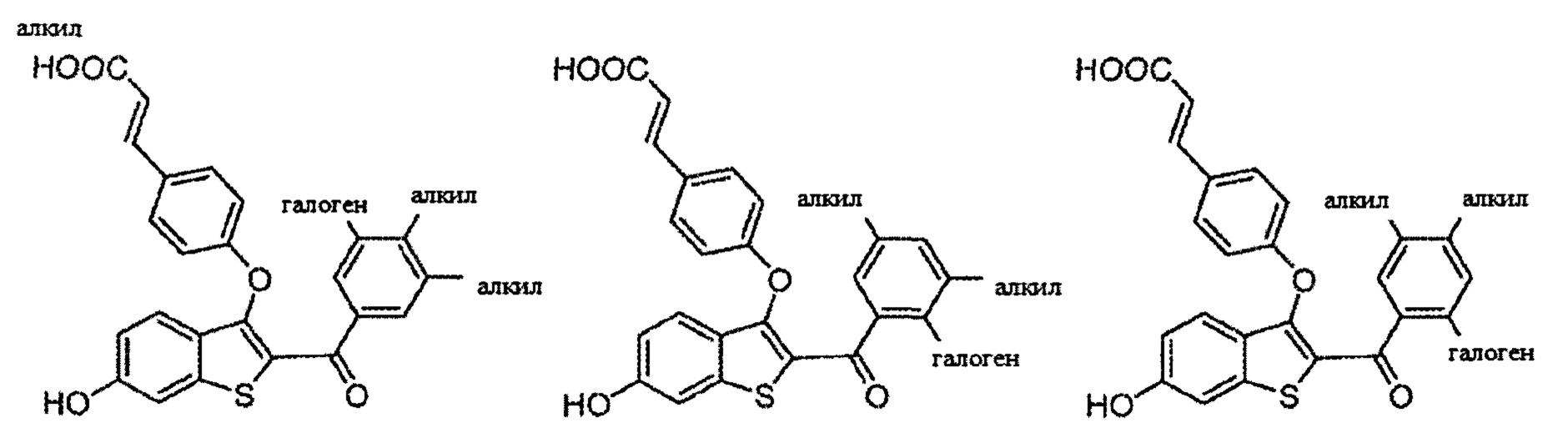
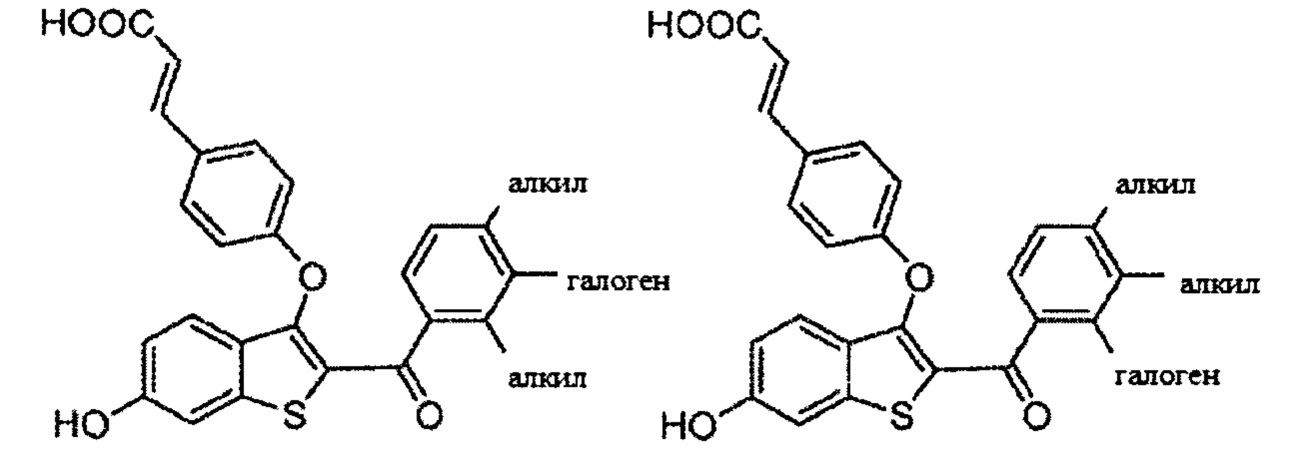
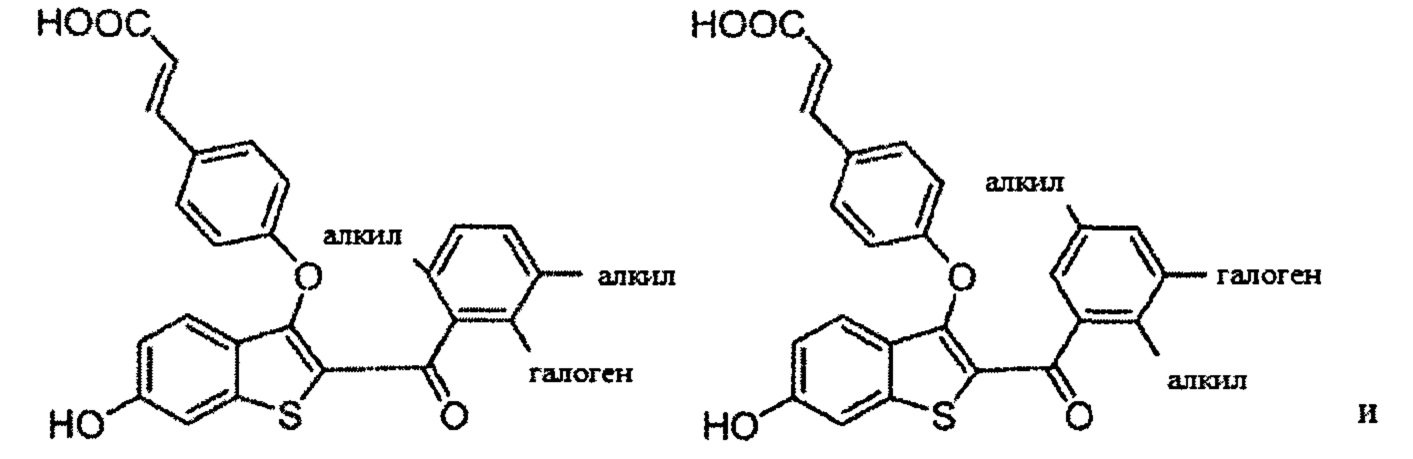
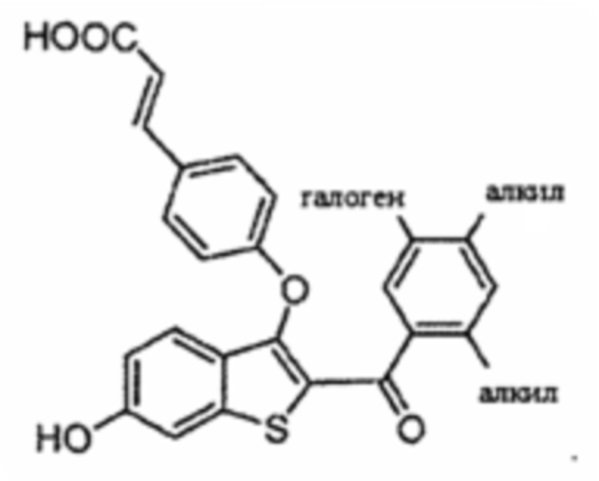
Согласно определенным вариантам осуществления вышеуказанных структур алкил представляет собой метил. Согласно другим вариантам осуществления вариантов осуществления вышеуказанных структур алкил независимо представляет собой метил, этил, пропил или циклопропил. Согласно некоторым вариантам осуществления вышеуказанных вариантов осуществления галоген представляет собой фтор. Согласно некоторым вариантам осуществления галогеналкил независимо представляет собой моно-, ди- или трифторметил. Согласно определенным вариантам осуществления, если бензольное кольцо содержит два галогена, галогенами может быть один фтор один хлор, два фтора или два хлора. Согласно определенным вариантам осуществления, если бензольное кольцо содержит три галогена, галогенами может быть один фтор два хлора, два фтора один хлор, три фтора или три хлора.
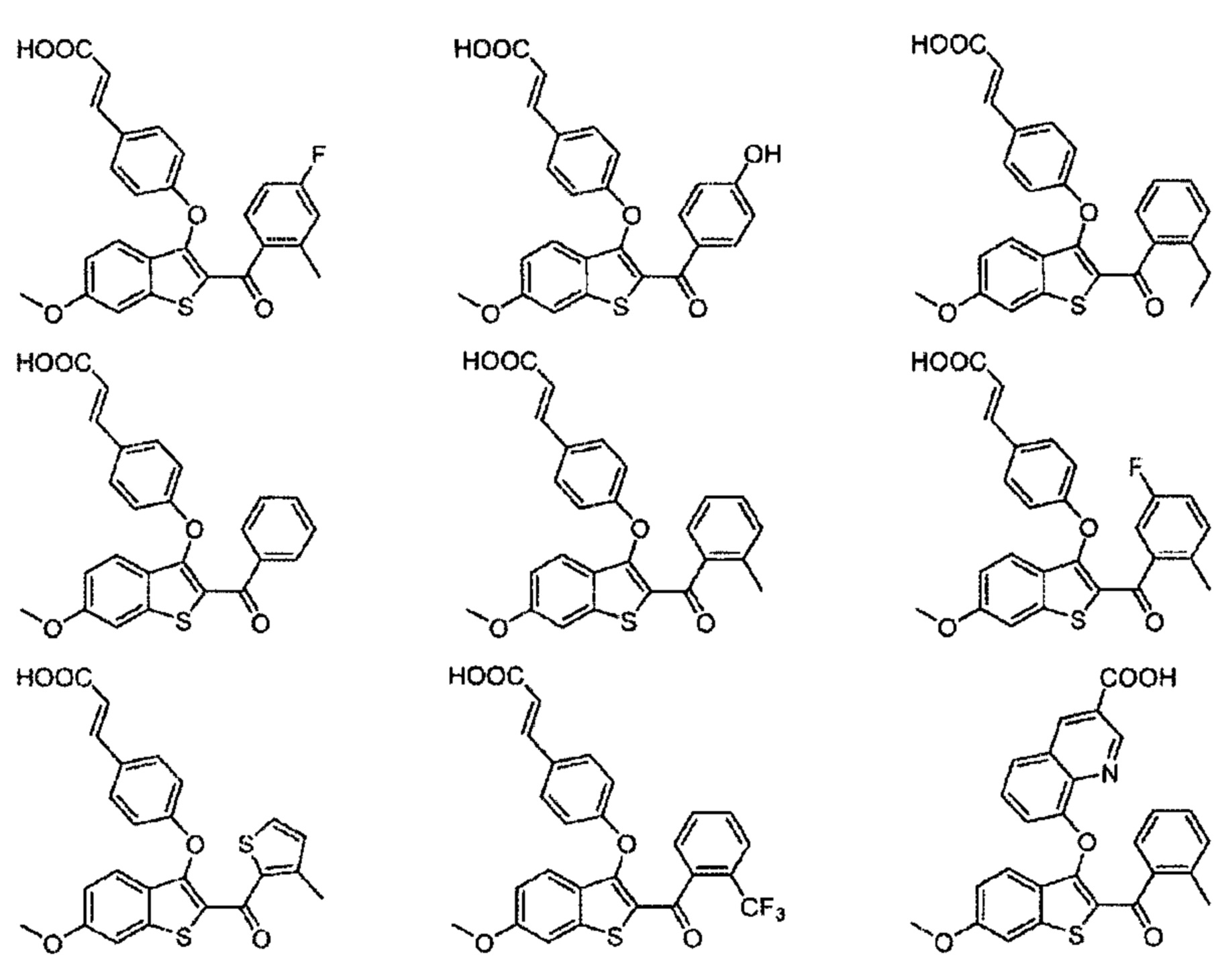
Дополнительные неограничивающие примеры соединений по настоящему изобретению включают в себя:
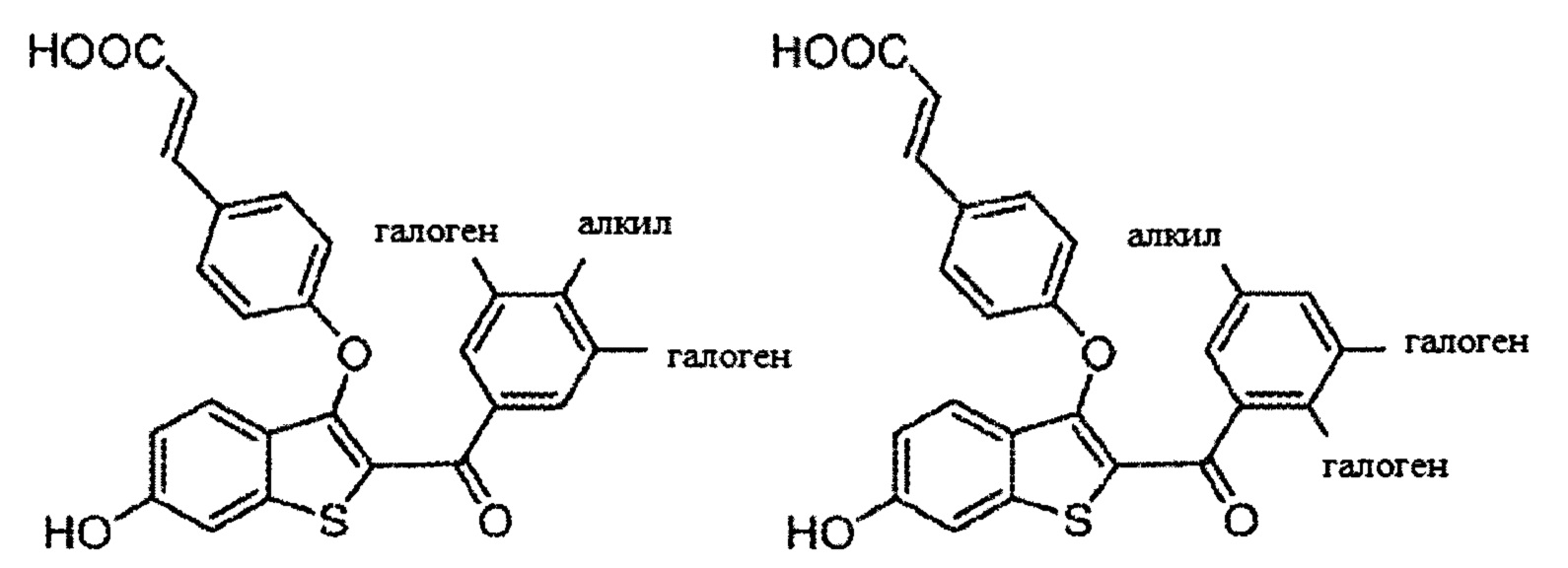
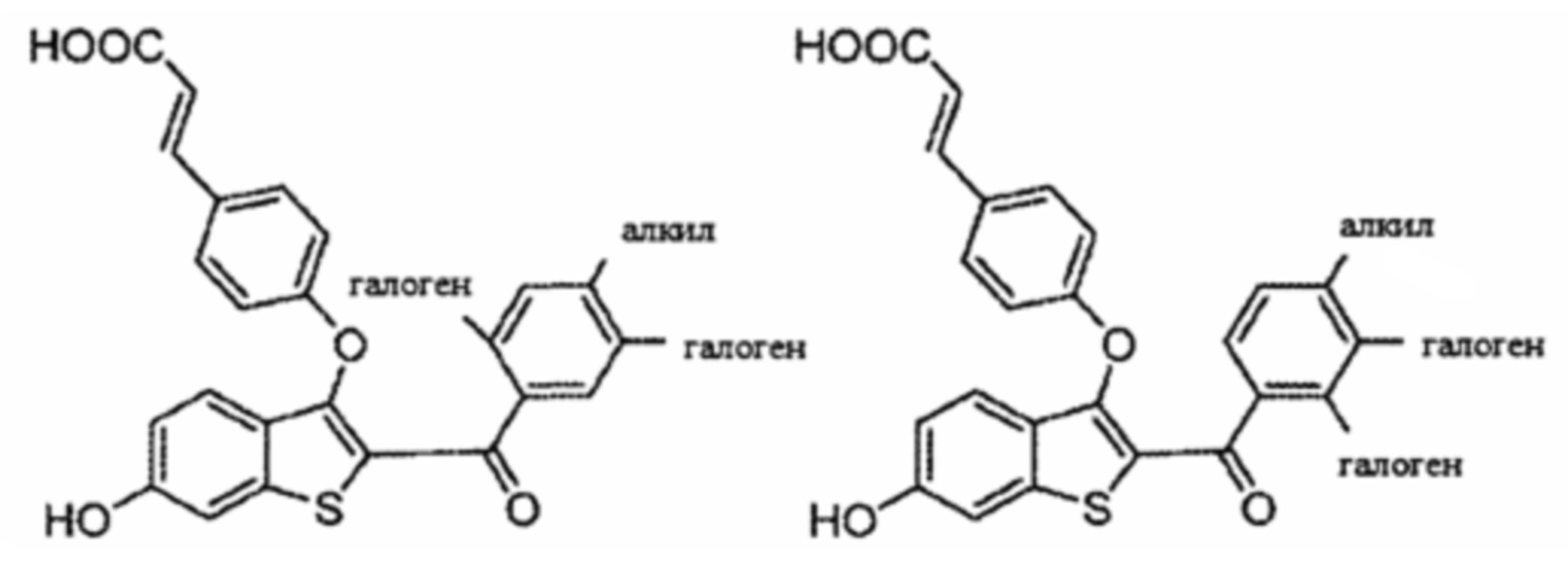
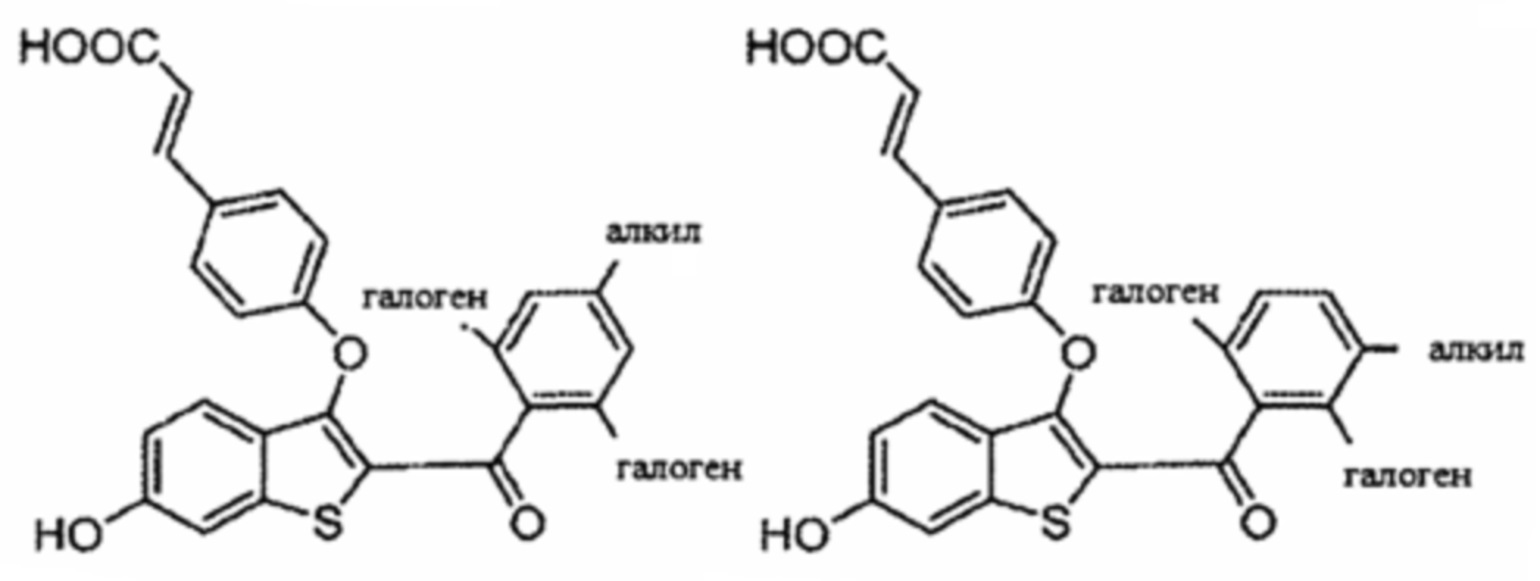
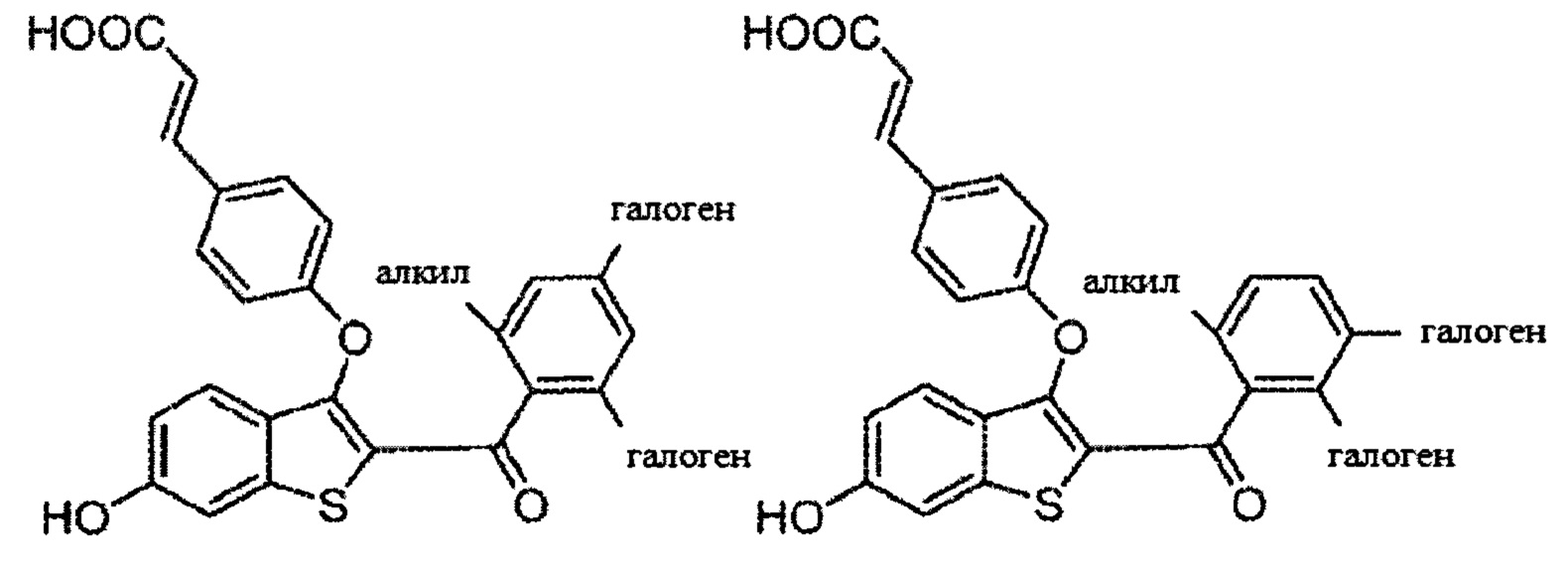
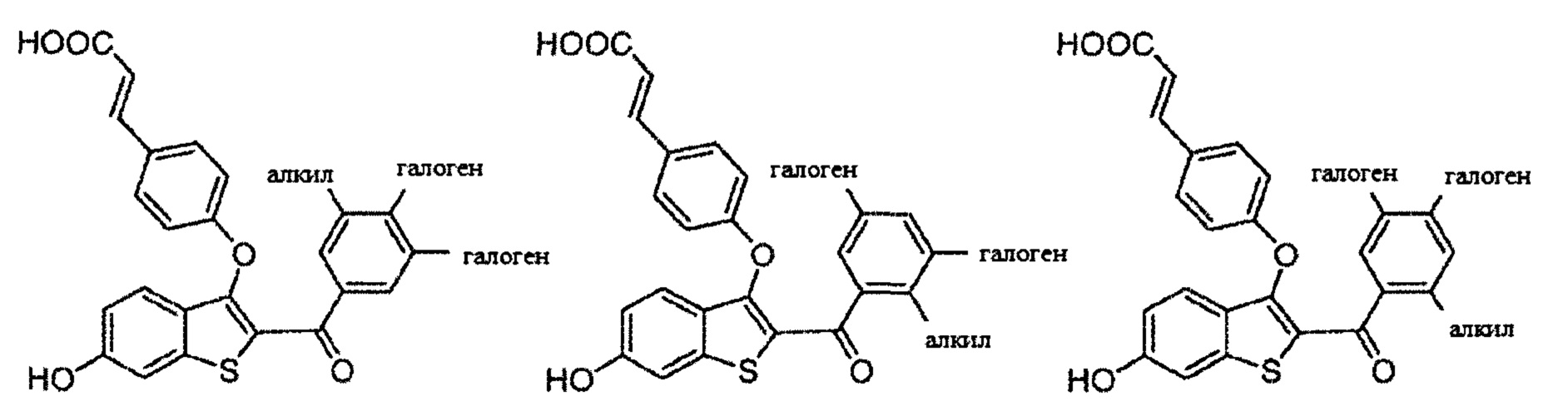
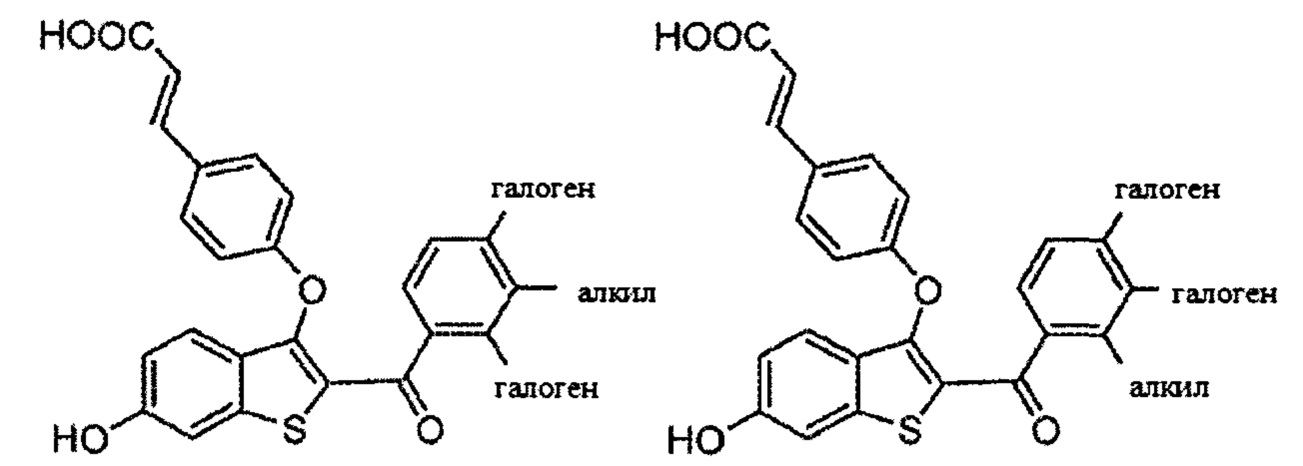
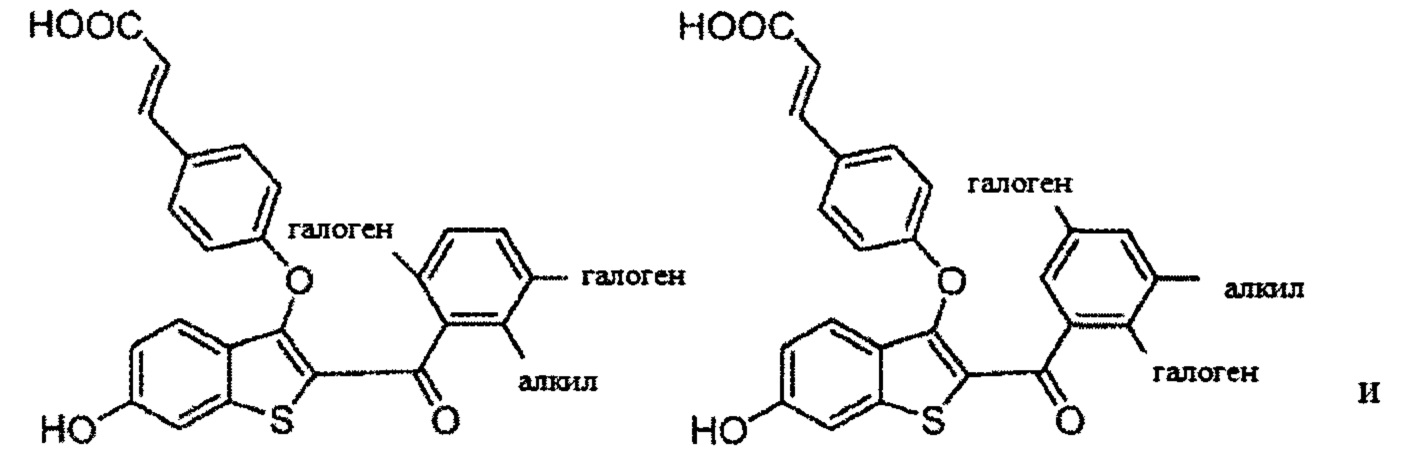
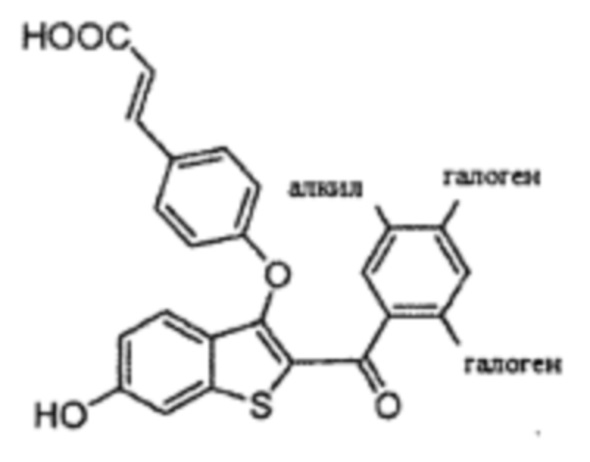
Согласно определенным вариантам осуществления вышеуказанных структур алкил представляет собой метил. Согласно другим вариантам осуществления вариантов осуществления вышеуказанных структур алкил независимо представляет собой метил, этил, пропил или циклопропил. Согласно некоторым вариантам осуществления вышеуказанных вариантов осуществления галоген представляет собой фтор. Согласно некоторым вариантам осуществления галогеналкил независимо представляет собой моно-, ди- или трифторметил. Согласно определенным вариантам осуществления, если бензольное кольцо содержит два галогена, галогенами может быть один фтор один хлор, два фтора или два хлора. Согласно определенным вариантам осуществления, если бензольное кольцо содержит три галогена, галогенами может быть один фтор два хлора, два фтора один хлор, три фтора или три хлора.
Дополнительные неограничивающие примеры соединений по настоящему изобретению включают в себя:
Согласно определенному варианту осуществления вышеуказанных структур алкокси представляет собой метокси. Согласно другим вариантам осуществления вариантов осуществления вышеуказанных структур алкокси представляет собой этокси, пропокси или циклопропилокси. Согласно некоторым вариантам осуществления галогеналкил представляет собой моно-, ди- или трифторметил.
Типичные соединения по настоящему изобретению включают в себя без ограничения соединения формулы:
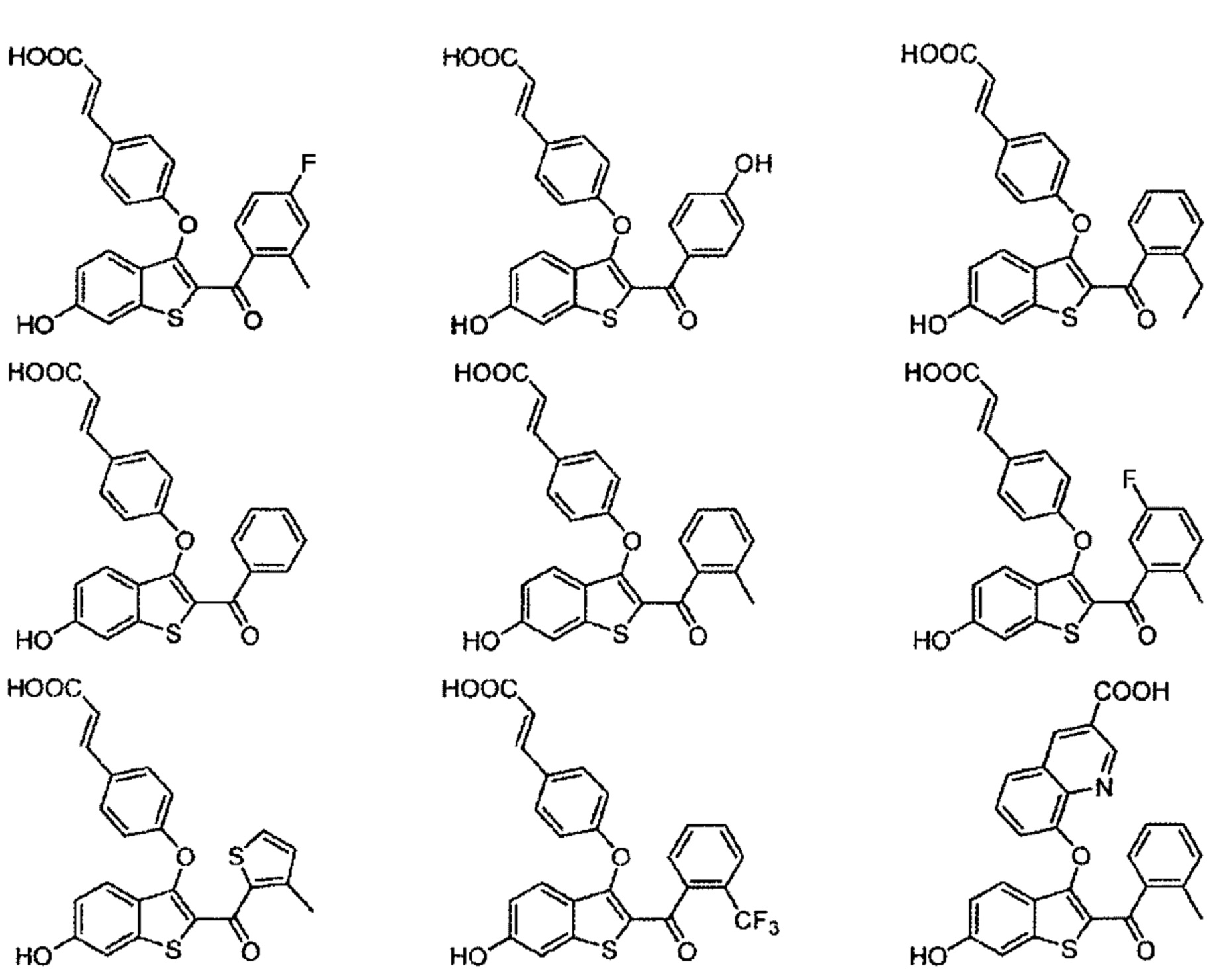
их фармацевтически приемлемые соли или пролекарства.
Дополнительные типичные соединения по настоящему изобретению включают в себя без ограничения соединения формулы:
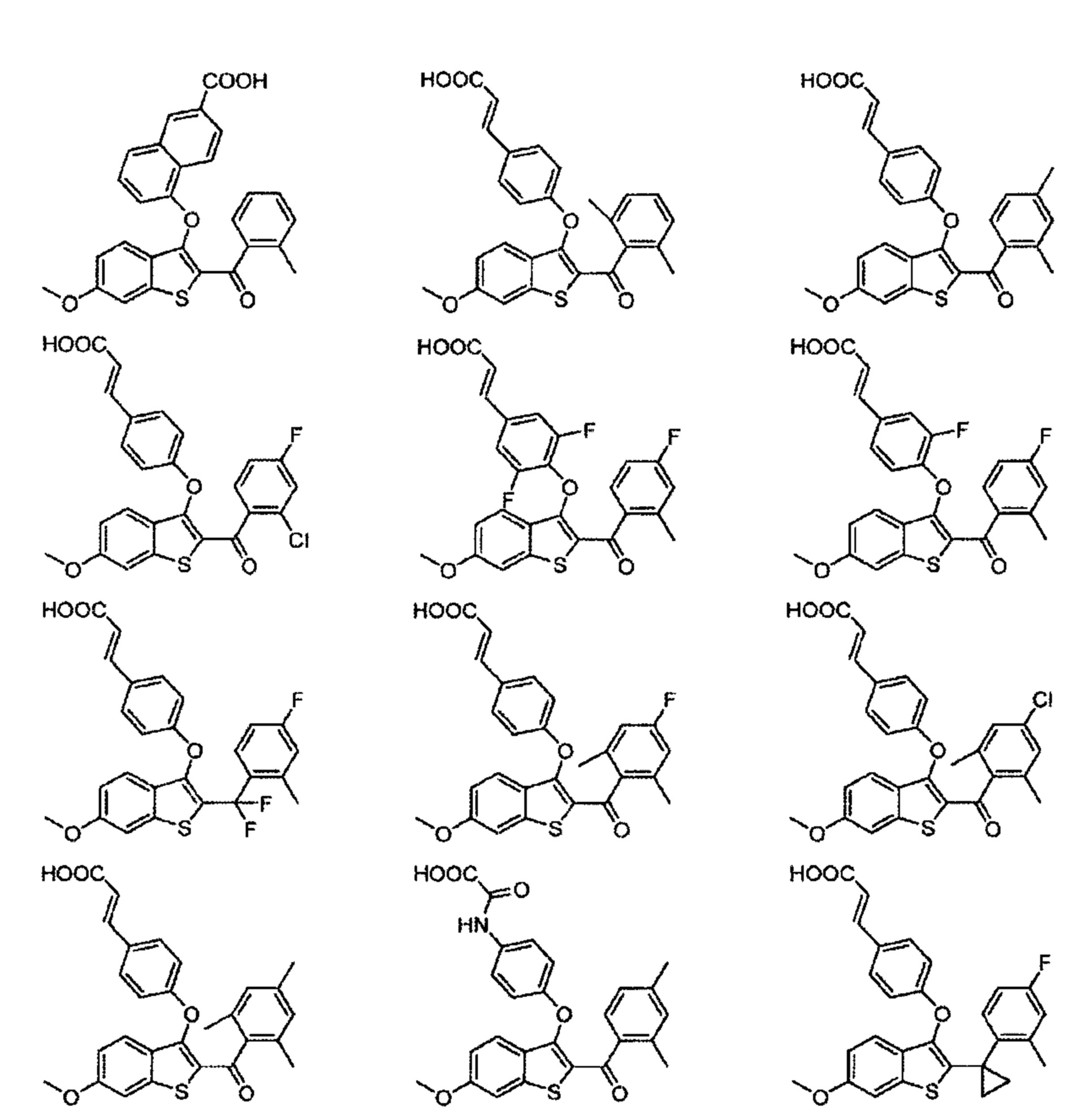
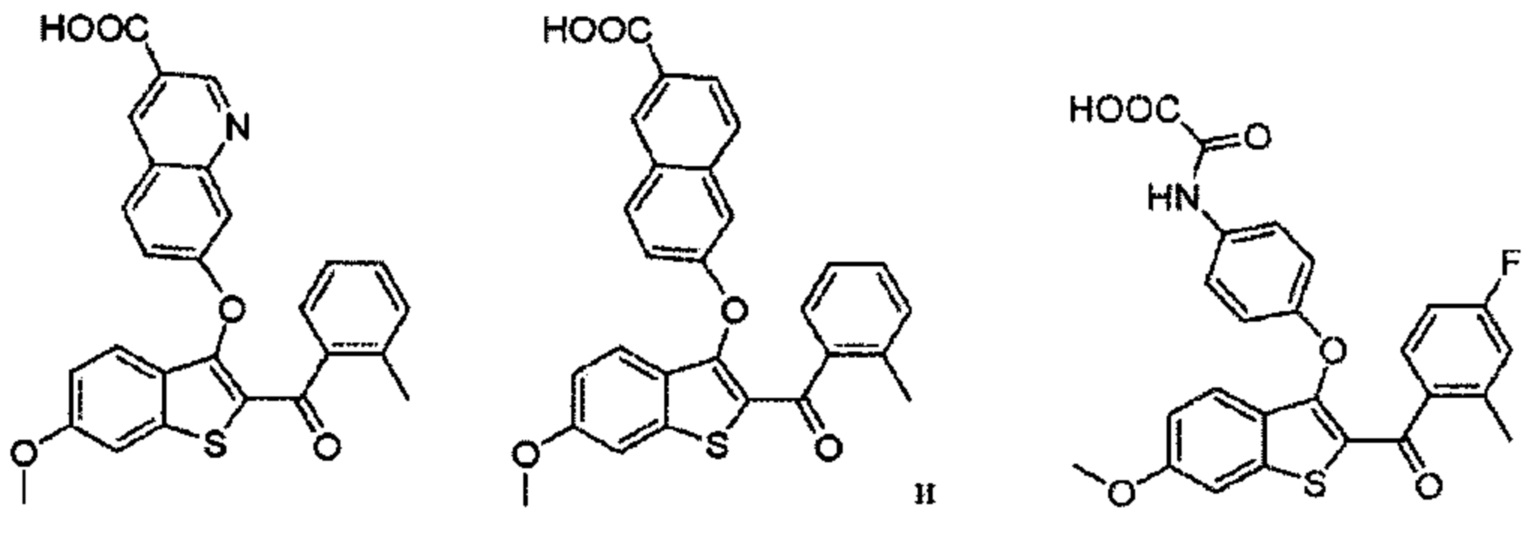
Дополнительные типичные соединения по настоящему изобретению включают в себя без ограничения соединения формулы:
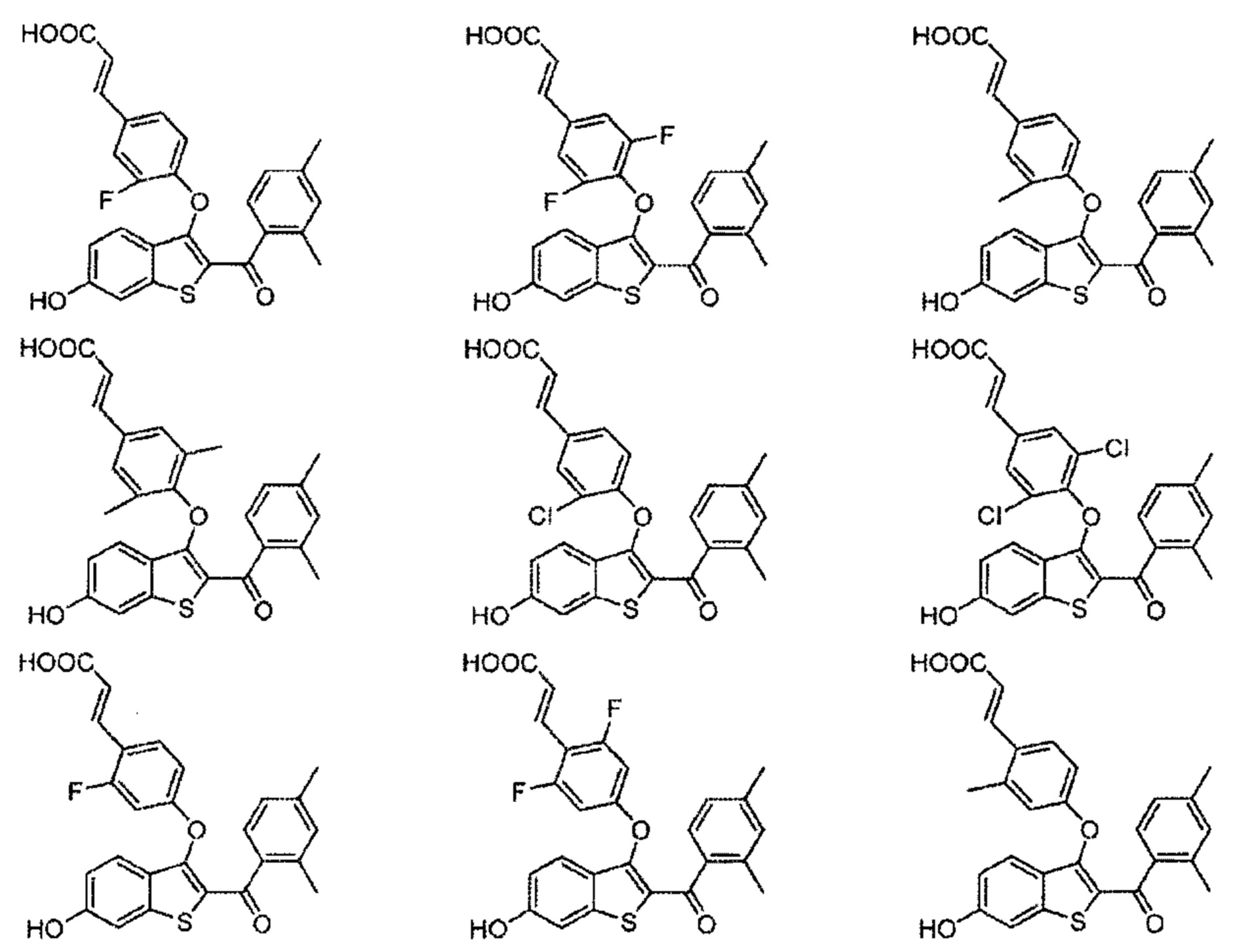
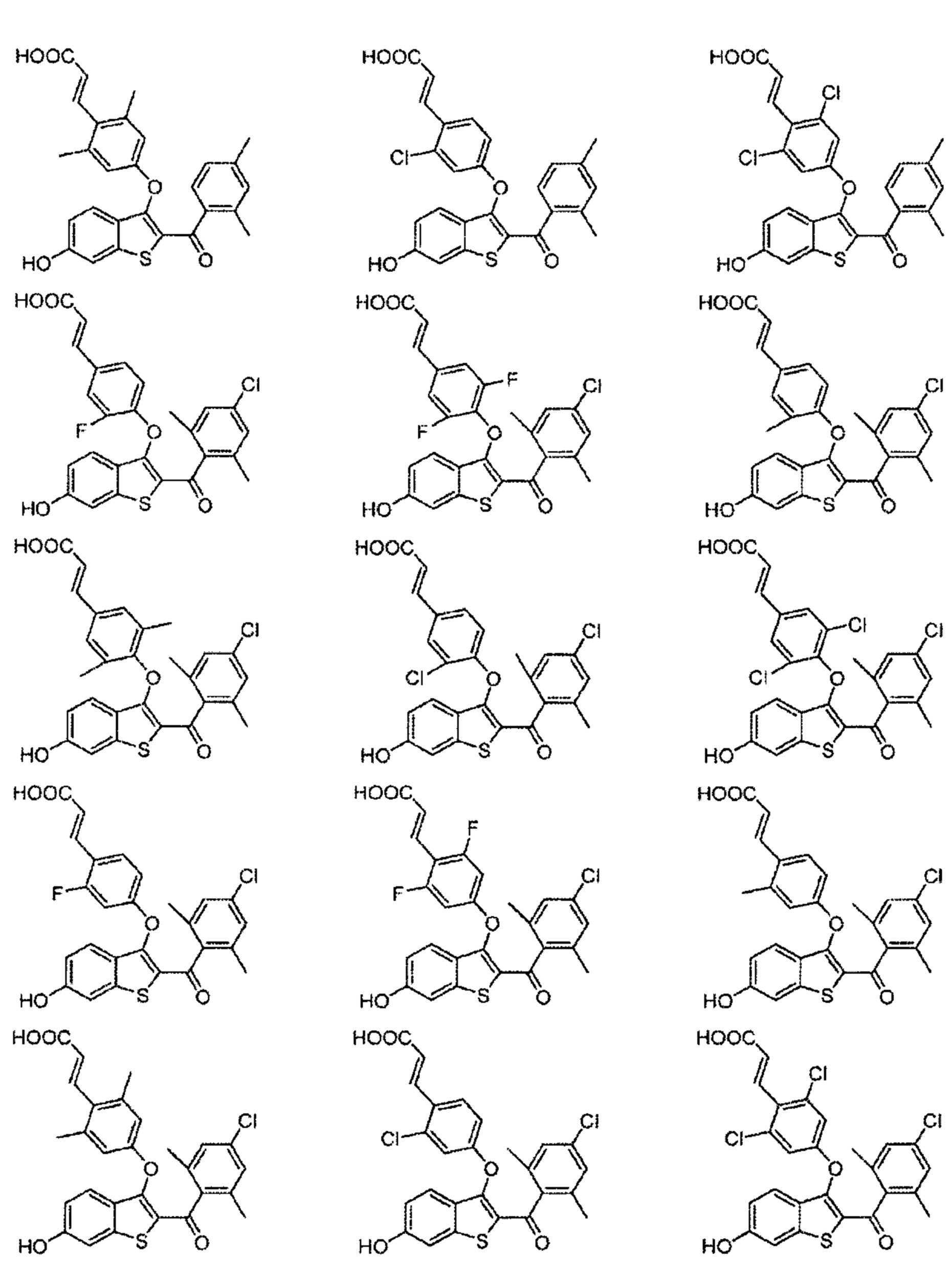
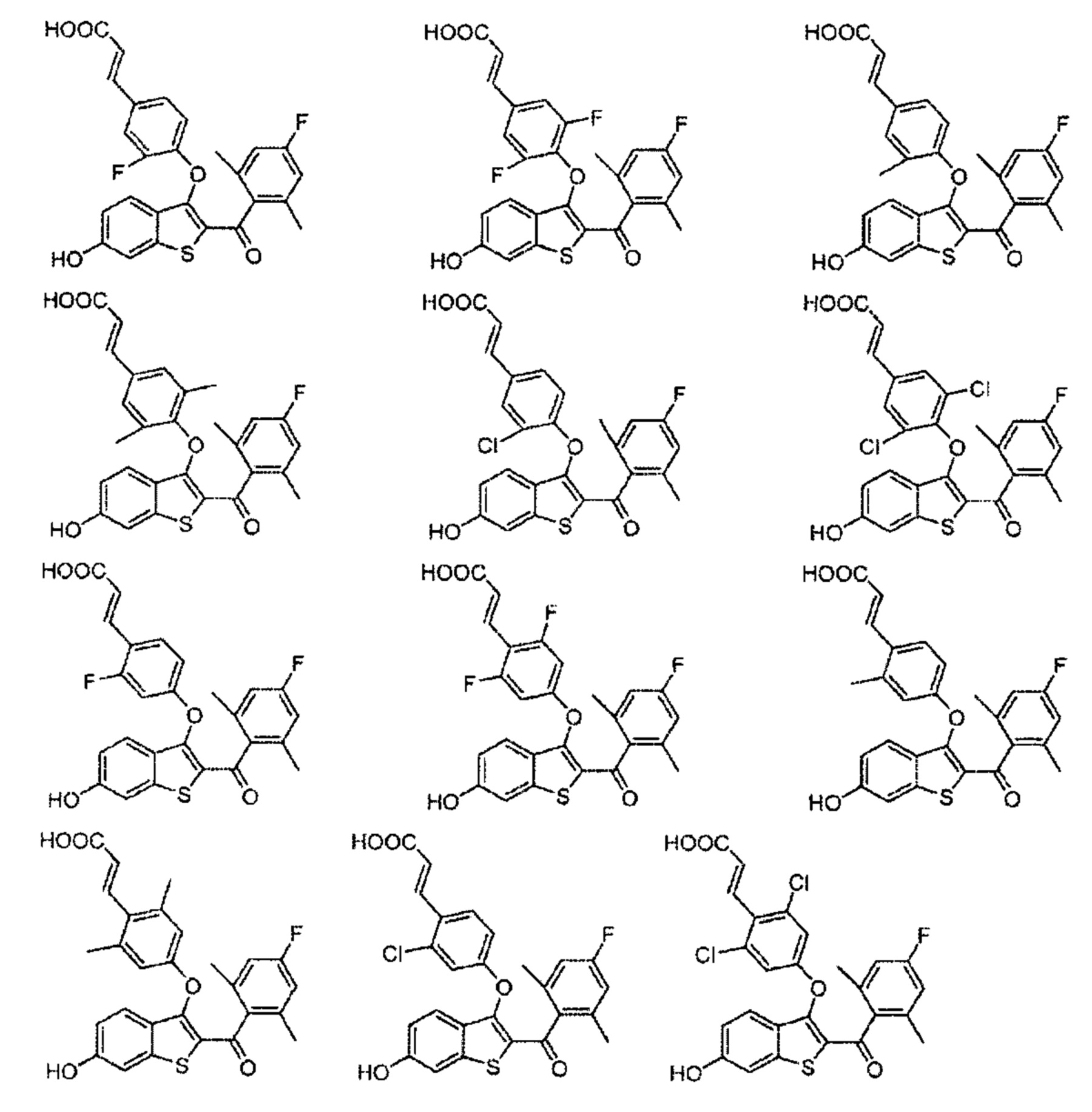
или их фармацевтически приемлемые соли.
Дополнительные типичные соединения по настоящему изобретению включают в себя без ограничения соединения формулы:
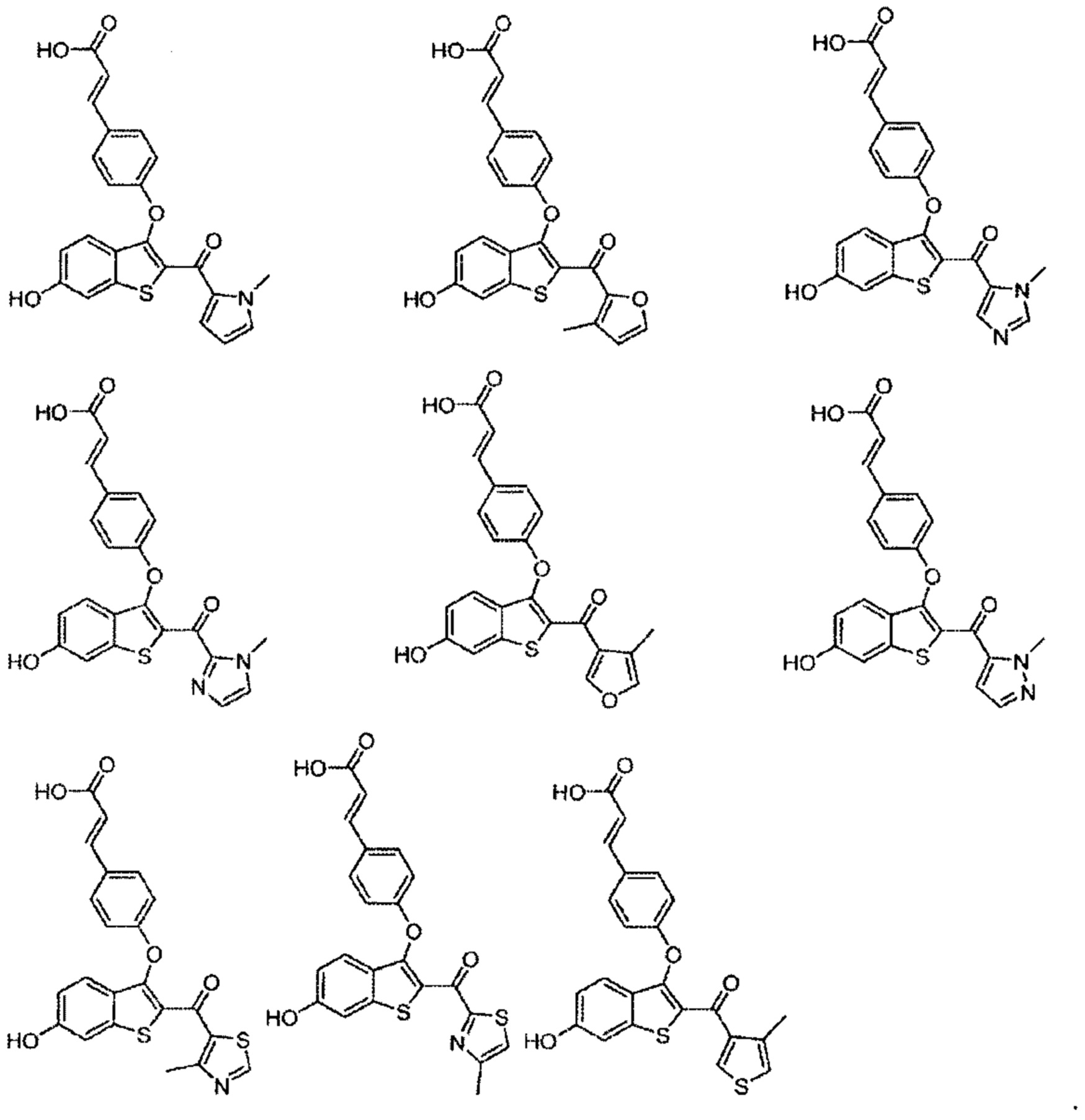
Дополнительные типичные соединения по настоящему изобретению включают в себя без ограничения соединения формулы:
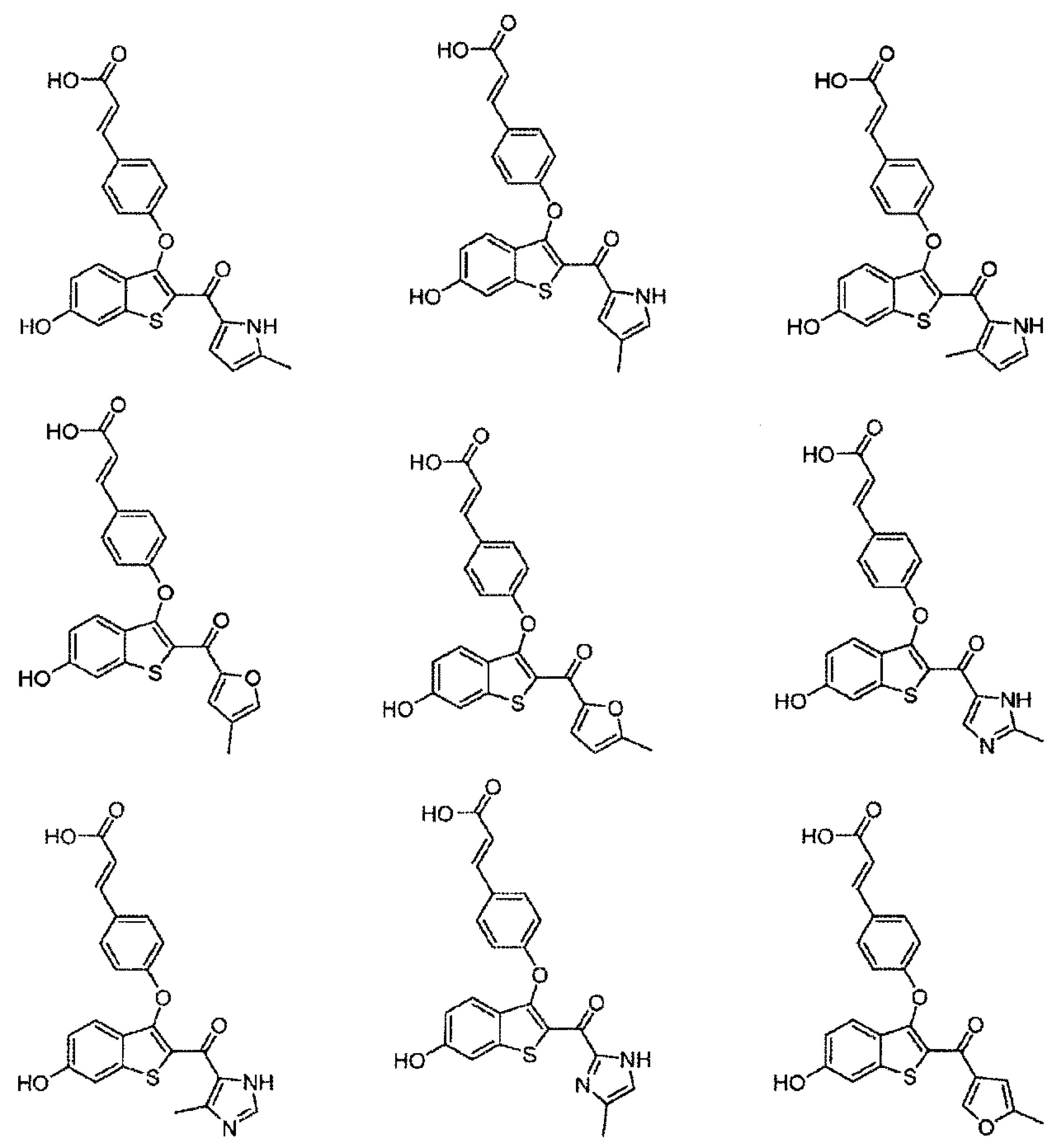
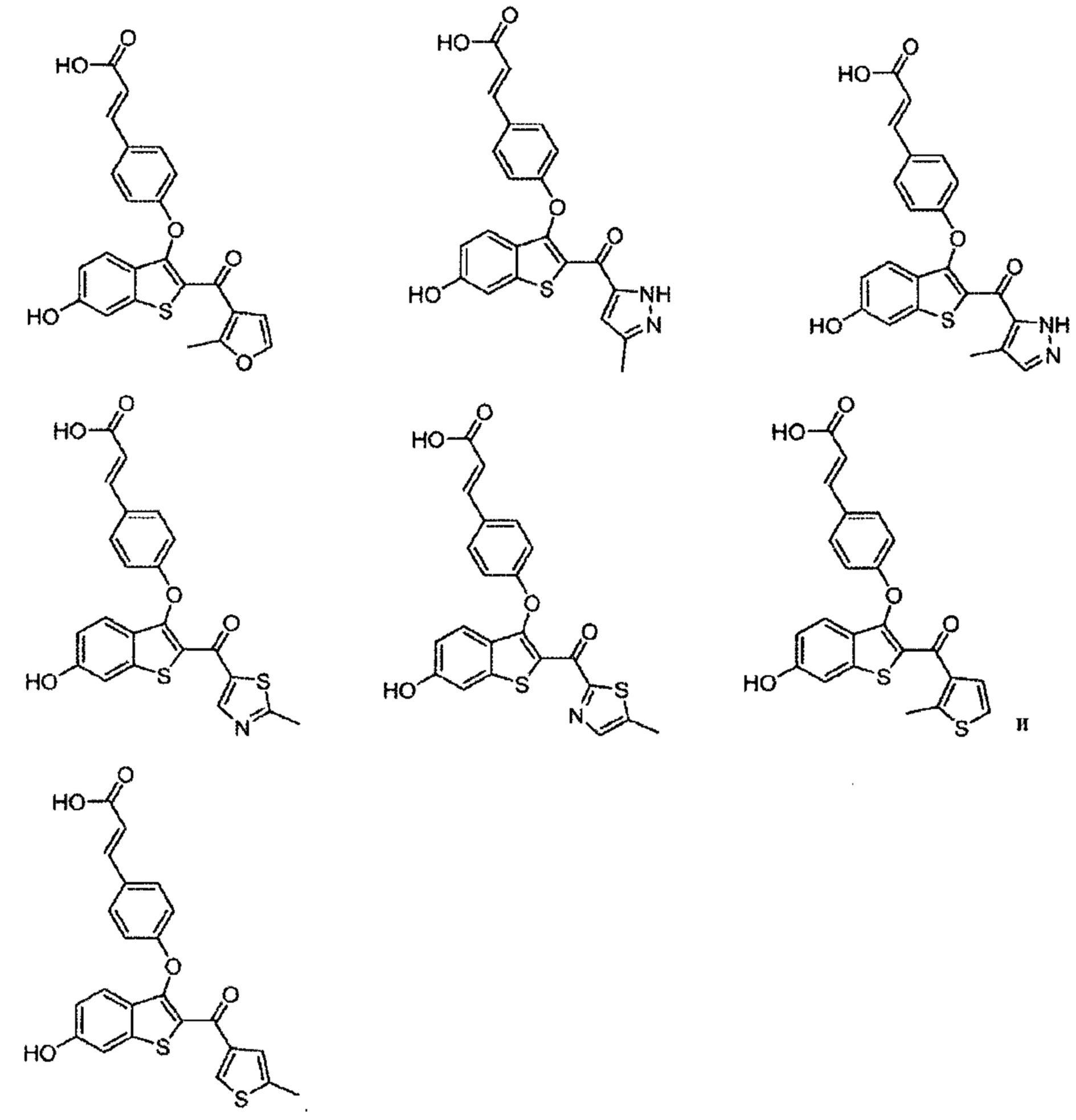
Дополнительные типичные соединения по настоящему изобретению включают в себя без ограничения соединения формулы:
Согласно одному варианту осуществления любой из вышеуказанных структур, содержащих -СО2Н, соединение может быть представлено, например, в виде сложноэфирного, амидного или эфирного пролекарства. Сложным эфиром может быть, например, -CO2R, где R представляет собой алкильный (включая циклоалкил), гетероалкильный, алкенильный, алкинильный, арильный, гетероарильный, гетероциклический или любой другой фрагмент, который метаболизирован in vivo с получением исходного лекарственного средства.
Фармацевтические композиции и способы лечения
Настоящее изобретение включает в себя фармацевтические композиции, которые включают в себя терапевтически эффективное количество соединения, как описано в настоящем изобретении, или его фармацевтически приемлемую соль или пролекарство и один или несколько фармацевтически приемлемых сред, таких как разбавитель, консервант, солюбилизатор, эмульгатор, вспомогательное средство, наполнитель или носитель. Наполнители включают в себя без ограничения жидкости, такие как вода, солевой раствор, глицерин, полиэтиленгликоль, гиалуроновая кислота, этанол и т.п.
Термин «фармацевтически приемлемый носитель» относится к разбавителю, вспомогательному средству, наполнителю или носителю, с которыми было введено соединение настоящего раскрытия. Термины «эффективное количество» или «фармацевтически эффективное количество» относится к нетоксичному, но достаточному количеству средства для обеспечения требуемого биологического результата. Этим результатом может быть сокращение и/или облегчение признаков, симптомов или причин заболевания или любое другое требуемое изменение биологической системы. Соответствующее «эффективное» количество в любом отдельном случае может быть определено специалистом настоящей области техники с применением рутинного проведения экспериментов. «Фармацевтически приемлемые носители» для терапевтического применения хорошо известны в фармацевтической области техники и они описаны, например, в Remington's Pharmaceutical Sciences, 18th Edition (Easton, Pennsylvania: Mack Publishing Company, 1990). Например, может быть использован стерильный солевой раствор и фосфатно-солевой буферный раствор при физиологическом значении рН. Консерванты, стабилизаторы, красители и даже вкусовые добавки могут быть представлены в фармацевтической композиции. Например, в качестве консервантов могут быть добавлены бензоат натрия, сорбиновая кислота и сложные эфиры пара-гидроксибензойной кислоты. Id. at 1449. Кроме того, могут быть использованы антиоксиданты и суспендирующие средства. Id.
Специалистам настоящей области техники также известны подходящие наполнители для не жидких составов. Подробное обсуждение фармацевтически приемлемых наполнителей и солей доступны в Remington's Pharmaceutical Sciences, 18th Edition (Easton, Pennsylvania: Mack Publishing Company, 1990).
Кроме того, вспомогательные вещества, такие как смачивающие средства или эмульгаторы, биологические буферные вещества, поверхностно-активные вещества и т.п., могут присутствовать в таких средах. Биологическим буфером может быть любой раствор, который является фармакологически приемлемым и который обеспечивает состав с требуемым значением рН, т.е., значением рН в физиологически приемлемом диапазоне. Примеры буферных растворов включают в себя солевой раствор, фосфатно-солевой буферный раствор, ТРИС-буферизированный солевой раствор, буферизированный солевой раствор Хэнкса и т.п.
В зависимости от предусмотренного способа введения фармацевтические композиции могут быть в форме твердых, полутвердых или жидких лекарственных форм, таких как, например, таблетки, суппозитории, пилюли, капсулы, порошки, жидкости, суспензии, кремы, мази, лосьоны или т.п., предпочтительно в стандартной лекарственной форме, подходящей для однократного введения точной дозы. Композиции будут включать в себя эффективное количество выбранного лекарственного средства в комбинации с фармацевтически приемлемым носителем и, кроме того, могут включать в себя другие фармацевтически средства, вспомогательные средства, разбавители, буферы и т.п.
В целом, композиции настоящего раскрытия будут введены в терапевтически эффективном количестве любым из приемлемых способов введения. Подходящие диапазоны доз зависят от многих факторов, таких как тяжесть заболевания, которое лечили, возраст и соответствующее состояние здоровья субъекта, активность используемого соединения, путь и форма введения, показание, по отношению к которому направлено введение, и предпочтения и опыт причастного врача. Специалист в области лечения таких заболеваний будет способен, без неоправданного проведения эксперимента и с уверенностью в личных знаниях и раскрытии настоящей заявки, выявлять терапевтически эффективное количество композиций раскрытия для данного заболевания.
Композиции для введения активного соединения включают в себя без ограничения такие соединения, которые подходят для перорального (включая без ограничения таблетку, капсулу, жидкость, гелевый состав), местного, ректального, назального, легочного, парентерального (включая внутримышечное, внутриартериальное, внутриоболочечное, подкожное и внутривенное), внутримышечного, внутривенного, подкожного, трансдермального (которое может включать в себя средство для усиления проникновения), вагинального введения и введения при помощи суппозитория. Покрытые энтеросолюбильной оболочкой пероральные таблетки также могут быть использованы для усиления биологической доступности соединений для перорального пути введения. Наиболее эффективная лекарственная форма будет зависеть от биологической доступности/фармакокинетики выбранного конкретного соединения, а также тяжести заболевания пациента. Пероральные лекарственные формы являются особым образом типичными из-за легкости введения и предполагаемой благоприятной исполнительности больного.
Для твердых композиций традиционные нетоксичные твердые носители включают в себя, например, маннит, лактозу, крахмал, стеарат магния, сахарин натрия, тальк, целлюлозу, глюкозу, сахарозу, карбонат магния и т.п. фармацевтической степени чистоты Жидкие фармацевтически вводимые соединения могут, например, быть получены растворением, диспергированием и т.п. активного соединения, как описано в настоящем изобретении, и необязательных фармацевтических вспомогательных средств в наполнителе, таком как, например, вода, солевой раствор, водная декстроза, глицерин, этанол и т.п., тем самым образуя раствор или суспензию. При необходимости вводимая фармацевтическая композиция также может содержать незначительные количества нетоксичных вспомогательных веществ, таких как смачивающие средства или эмульгаторы, рН буферные средства и т.п., например, ацетат натрия, сорбитанмонолаурат, триэтаноламин ацетат натрия, триэтаноламин олеат и т.п. Существующие способы получения таких лекарственных форм хорошо известны или будут очевидны специалистам настоящей области техники; например, см. Remington's Pharmaceutical Sciences, упоминаемый выше.
Еще один вариант осуществления относится к применению наполнителей для усиления проницаемости, включая полимеры, такие как: поликатионы (хитозан и его четвертичные аммонийные производные, поли-L-аргинин, амидированный желатин); полианионы (N-карбоксиметилхитозан, полиакриловая кислота) и тиолированные полимеры (конъюгаты карбоксиметилцеллюлоза-цистеин, поликарбофил-цистеин, хитозан-тиобутиламидин, хитозан-тиогликолевая кислота, хитозан-глутатион).
Для перорального введения композиция обычно будет принимать форму таблетки, капсулы, гелевой капсулы или может быть водным или неводным раствором, суспензией или сиропом. Таблетки и капсулы являются типичными формами для перорального введения. Таблетки и капсулы для перорального применения могут включать в себя один или несколько широко используемых носителей, таких как лактоза и кукурузный крахмал. Смазывающие средства, такие как стеарат магния, также типично добавляли. Как правило, композиции настоящего раскрытия могут быть объединены с пероральным, нетоксичным, фармацевтически приемлемым, инертным носителем, таким как лактоза, крахмал, сахароза, глюкоза, метилцеллюлоза, стеарат магния, фосфат дикальция, сульфат кальция, маннит, сорбит и т.п.Более того, если требуется или необходимо, подходящие связующие, смазочные вещества, разрыхлители красители также могут быть включены в смесь. Подходящие связующие включают в себя крахмал, желатин, природные сахара, такие как глюкоза или бета-лактоза, сахаристые вещества из кукурузы, природные и синтетические камеди, такие как аравийская камедь, трагакантовая камедь или альгинат натрия, карбоксиметилцеллюлоза, полиэтиленгликоль, воски и т.п. Смазочные вещества, используемые в этих лекарственных формах, включают в себя олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и т.п. Разрыхлители включают в себя без ограничения крахмал, метилцеллюлозу, агар, бентонит, ксантановую камедь и т.п.
При использовании жидких суспензий активное средство может быть объединено с любым пероральным, нетоксичным, фармацевтически приемлемым инертным наполнителем, таким как этанол, глицерин, вода и т.п., и с эмульгирующими и суспендирующими средствами. При необходимости также могут быть добавлены ароматизаторы, красители и/или подсластители. Другие необязательные компоненты для включения в пероральный состав по настоящему изобретению включают в себя без ограничения консерванты, суспендирующие средства, загустители и т.п.
Парентеральные составы могут быть получены в традиционных формах или в виде жидких растворов или суспензий, твердых форм, подходящих для солюбилизации, или суспензии в жидкости перед введением, или в виде эмульсий. Предпочтительно, стерильные инъецируемые суспензии составляли согласно методикам, известным в области техники, с применением подходящих носителей, диспергирующих или смачивающих средств и суспендирующих средств. Стерильный инъецируемый состав также может быть стерильным инъецируемым раствором или суспензией в подходящем нетоксичном парентерально приемлемом разбавителе или растворителе. Среди приемлемых носителей и растворителей, которые могут быть использованы, присутствуют вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, стерильные жирные масла, жирные сложные эфиры или полиолы традиционно использовали в качестве растворителей или суспендирующей среды. Кроме того, парентеральное введение может включать в себя применение системы медленного высвобождения или длительного высвобождения, таким образом поддерживали постоянный уровень дозировки.
Парентеральное введение включает в себя внутрисуставные, внутривенные, внутримышечные, внутрикожные, внутрибрюшинные и подкожные пути и включает в себя водные и неводные изотонические стерильные инъекционные растворы, которые могут содержать антиоксиданты, буферы, бактериостаты и растворенные вещества, которые делают состав изотоничным крови указанного реципиента, и водные и неводные стерильные суспензии, которые могут включать в себя суспендирующие средства, солюбилизаторы, загустители, стабилизаторы и консерванты. Введение при помощи определенных парентеральных путей может включать в себя введение составов по настоящему раскрытию в организм пациента через иглу или катетер, продвигаемых при помощи стерильного шприца или другого механического устройства, такого как система непрерывной инфузии. Представленный настоящим раскрытием состав может быть введен с применением шприца, инжектора, насоса или любого другого устройства, предусмотренного в области техники для парентерального введения.
Предпочтительно, стерильные инъецируемые суспензии составлены согласно методикам, известным из уровня техники, с применением подходящих носителей, диспергирующих или смачивающих средств или суспендирующих средств. Стерильный инъецируемый состав также может быть стерильным инъецируемым раствором или суспензией в нетоксичном парентерально приемлемом разбавителе или растворителе. Среди приемлемых сред и растворителей, которые могут быть использованы, присутствуют вода, раствор Рингера или изотонический раствор хлорида натрия. Кроме того, стерильные жирные масла, жирные сложные эфиры или полиолы традиционно использовали в качестве растворителей или суспендирующей среды. Кроме того, парентеральное введение может включать в себя применение системы медленного высвобождения или длительного высвобождения, таким образом поддерживали постоянный уровень дозировки.
Препараты согласно настоящему раскрытию для парентерального введения включают в себя стерильные водные или неводные растворы, суспензии или эмульсии. Примерами неводных растворителей или сред являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло и кукурузное масло, желатин и инъецируемые органические сложные эфиры, такие как этилолеат. Такие лекарственные формы также могут содержать вспомогательные средства, такие как консервирующие, смачивающие, эмульгирующие и диспергирующие средства. Они могут быть стерилизованы, например, при помощи фильтрации через удерживающий бактерии фильтр включением стерилизующих средств в композиции, облучением композиций или нагреванием композиций. Также они могут быть изготовлены с применением стерильной воды или другой стерильной инъецируемой среды сразу перед применением.
Стерильные инъецируемые растворы получали включением одного или нескольких соединений по настоящему раскрытию в необходимом количестве в соответствующем растворителе с различными другими ингредиентами, перечисленными выше, как требуется, с последующей стерилизацией фильтрованием. Обычно дисперсии получали включением различных стерилизованных активных ингредиентов в стерильную среду, которая содержит основную диспергирующую среду и необходимые другие ингредиенты из перечисленных выше. В случае стерильных порошков для получения стерильных инъецируемых растворов предпочтительными способами получения являются техники вакуумной сушки и лиофильной сушки, что приводит к порошку активного ингредиента плюс любой дополнительный необходимый ингредиент из его ранее стерильно отфильтрованного раствора. Таким образом, например, парентеральную композицию, подходящую для введения путем инъекции, получали перемешиванием 1,5% по массе активного ингредиента в 10% по объему пропиленгликоле и воде. Раствор делали изотоническим при помощи хлорида натрия и стерилизовали.
Альтернативно, фармацевтические композиции по настоящему раскрытию могут быть введены в форме суппозиториев для ректального введения. Они могут быть получены смешиванием средства с подходящим нераздражающим наполнителем, который является твердым при комнатной температуре, но жидким при ректальной температуре, и, таким образом, они будут таять в прямой кишке с высвобождением лекарственного средства. Такие вещества включают в себя какао-масло, пчелиный воск и полиэтиленгликоли.
Фармацевтические композиции по настоящему раскрытию также могут быть введены при помощи назального аэрозоля или ингаляции. Такие композиции получали согласно методикам, хорошо известным в области фармацевтического состава, и могут быть получены в виде растворов в солевом растворе с применением бензилового спирта или других подходящих консервантов, ускорителей абсорбции для усиления биологической доступности, пропеллентов, таких как фторуглероды или азот, и/или другие традиционные солюбилизирующие или диспергирующие средства.
Предпочтительными составами для местной доставки лекарственного средства являются мази и кремы. Мази представляют собой полужидкие препараты, которые типично основаны на вазелине или других производных нефти. Кремы, содержащие выбранное активное средство, являются, как известно из области техники, вязкими жидкими или полужидкими эмульсиями, или масло-в-воде или вода-в-масле. Основы кремов являются водовымываемыми и содержат масляную фазу, эмульгатор и водную фазу. Масляная фаза, также иногда называемая как «внутренняя» фаза, обычно содержит вазелин и жирный спирт, такой как цетиловый или стеариловый спирт. Водная фаза обычно, хотя и не обязательно, превосходит масляную фазу по объему и обычно содержит увлажнитель. Эмульгатором в составе крема обычно является неионное, анионное, катионное или амфотерное поверхностно-активное вещество. Используемая конкретная мазь или кремовая основа, как будет отмечено специалистами настоящей области техники, является такой, которая будет обеспечивать оптимальную доставку лекарственного средства. Что касается других носителей или сред, мазевая основа должна быть инертной, устойчивой, нераздражающей и несенсибилизирующей.
Составы для трансбуккального введения включают в себя таблетки, пастилки, гели и т.п. Альтернативно, трансбуккальное введение может быть осуществлено с применением трансмукозальной системы доставки, как известно специалистам настоящей области техники. Соединения по настоящему раскрытию также могут быть доставлены через кожу или слизистую ткань с применением традиционных систем трансдермальной доставки лекарственного средства, т.е., трансдермальных «пластырей», где средство типично содержится в слоистой структуре, которая служит в качестве устройства для доставки лекарственных средств, приклеенного поверхности тела. В такой структуре композиция лекарственного средства типично находилась в слое или «резервуаре», расположенном под верхним защитным слоем. Многослойное устройство может содержать один резервуар или оно может содержать несколько резервуаров. Согласно одному варианту осуществления резервуар содержит полимерную матрицу фармакологически приемлемого адгезивного при контакте вещества, что служит для прикрепления системы к коже в течение доставки лекарственного средства. Примеры подходящих адгезивных веществ при контакте с кожей включают в себя без ограничения полиэтилены, полисилоксаны, полиизобутилены, полиакрилаты, полиуретаны и т.п. Альтернативно, содержащий лекарственное средство резервуар и клейкое при контакте с кожей вещество присутствуют в виде отдельных и четко выраженных слоев с клейким веществом, находящимся внизу резервуара, который в этом случае может быть или описанной выше полимерной матрицей, или он может быть жидким или гелевым резервуаром, или может принимать другую форму. Защитный слой в этих слоистых материалах, который служит в качестве верхней поверхности устройства, действует как основной элемент конструкции слоистой структуры и обеспечивает устройству больше его гибкости. Вещество, выбранное для защитного слоя, должно быть в основном непроницаемым для активного средства и любых других присутствующих веществ.
Композиции по настоящему раскрытию могут быть составлены для аэрозольного введения, в частности, в дыхательный аппарат, и включая интраназальное применение. Соединение, например, может обычно содержать мелкие частицы, например, размером 5 микрон или меньше. Такой размер частиц может быть получен способами, известными в области техники, например, микронизацией. Активный ингредиент обеспечен в блоке под давлением с подходящим пропеллентом, таким как хлорфторуглерод (CFC), например, дихлордифторметан, трихлорфторметан или дихлортетрафторэтан, диоксид углерода или другой подходящий газ. Аэрозоль в целях удобства также может содержать поверхностно-активное вещество, такое как лецитин. Доза лекарственного средства может контролироваться дозирующим клапаном. Альтернативно активные ингредиенты могут быть представлены в форме сухого порошка, например, порошковой смеси соединения в подходящем порошковом основании, таком как лактоза, крахмал, производные крахмала, такие как гидроксипропилметилцеллюлоза и поливинилпирролидин (PVP). Порошковый носитель будет образовывать гель в носовой полости. Порошковая композиция может присутствовать в единичной лекарственной форме, например, в капсулах или картриджах, например, желатина, или блистерных упаковок, из которых порошок может быть введен при помощи ингалятора.
Субъекту должно быть доставлено фармацевтически или терапевтически эффективное количество композиции. Точное эффективное количество будет меняться от субъекта к субъекту и будет зависеть от вида, возраста, размера и состояния здоровья субъекта, природы и степени состояния, которое лечили, рекомендаций лечащего врача и терапии или комбинаций терапии, выбранных для введения. Эффективное количество для данной ситуации может быть определено рутинным проведением экспериментов. В целях раскрытия терапевтическое количество может быть, например, в диапазоне от приблизительно 0,01 мг/кг до приблизительно 250 мг/кг массы тела, более предпочтительно от приблизительно 0,1 мг/кг до приблизительно 10 мг/кг по меньшей мере в одной дозе. Согласно некоторым неограничивающим вариантам осуществления ежедневная доза может быть от приблизительно 1 мг до 300 мг один или несколько раз в сутки, более предпочтительно в диапазоне от приблизительно 10 мг до 200 мг. Субъекту может быть введено столько доз, сколько необходимо для сокращения и/или облегчения признаков, симптомов или причин рассматриваемого нарушения или осуществления любого другого требуемого изменения биологической системы. При необходимости составы могут быть получены с энтеросолюбильными покрытиями, адаптированными для замедленного или с контролируемым высвобождением введения активного ингредиента.
Согласно некоторым вариантам осуществления, например, дозой может быть количество соединения, необходимое для обеспечения сывороточной концентрации активного соединения, до приблизительно 10 нМ, 50 нМ, 100 нМ, 200 нМ, 300 нМ, 400 нМ, 500 нМ, 600 нМ, 700 нМ, 800 нМ, 900 нМ, 1 мкМ, 5 мкМ, 10 мкМ, 20 мкМ, 30 мкМ или 40 мкМ.
Согласно определенным вариантам осуществления фармацевтическая композиция находится в лекарственной форме, которая содержит от приблизительно 0,1 мг до приблизительно 2000 мг, от приблизительно 10 мг до приблизительно 1000 мг, от приблизительно 100 мг до приблизительно 800 мг или от приблизительно 200 мг до приблизительно 600 мг активного соединения и необязательно от приблизительно 0,1 мг до приблизительно 2000 мг, от приблизительно 10 мг до приблизительно 1000 мг, от приблизительно 100 мг до приблизительно 800 мг или от приблизительно 200 мг до приблизительно 600 мг дополнительного активного средства в стандартной лекарственной форме. Примеры лекарственных форм включают в себя формы с по меньшей мере или не более чем 1, 2, 5, 10, 15, 20, 25, 50, 75, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700 или 750 мг активного соединения или его соли или пролекарства. Фармацевтическая композиция также может включать в себя молярное соотношение активного соединения и дополнительного активного средства в соотношении, при котором достигались требуемые результаты.
Стандартная лекарственная форма может быть, например, упакованным препаратом, содержащим отдельные количества препарата, таким как упакованные таблетки, капсулы и порошки во флаконах или ампулах. Также, стандартная лекарственная форма сама по себе может быть капсулой, таблеткой, крахмальной капсулой или пастилкой или она может быть соответствующим количеством любого из представленного в упакованной форме.
Соединения и композиции по настоящему изобретению можно применять для лечения или предупреждения нарушений, связанных с эстрогенами, например, злокачественной опухоли. Злокачественная опухоль может представлять собой, например, злокачественную опухоль молочной железы, злокачественную опухоль яичника, злокачественную опухоль эндометрия, злокачественную опухоль предстательной железы и злокачественную опухоль легкого. В частности, злокачественная опухоль молочной железы может быть резистентной к тамоксифену злокачественной опухолью молочной железы или трижды негативной злокачественной опухолью молочной железы.
Способ лечения может предупреждать или снижать риск злокачественной опухоли или опухоли. Способ лечения может вызывать частичную или полную регрессию злокачественной опухоли или опухоли у субъекта.
Способ лечения может вызывать частичную или полную регрессию резистентной к тамоксифену злокачественной опухоли или опухоли. Способ лечения может вызывать частичную или полную регрессию трижды негативной злокачественной опухоли молочной железы.
В соответствии с другими вариантами осуществления соединение или его фармацевтически приемлемая соль или пролекарственное средство можно применять для предупреждения рецидива злокачественной опухоли или опухоли после лечения в качестве адъювантной терапии. В одном примере соединение или его фармацевтически приемлемую соль или пролекарственное средство или фармацевтическую композицию на их основе можно применять для предупреждения дальнейшего развития злокачественной опухоли молочной железы после лечения злокачественной опухоли молочной железы или для лечения злокачественной опухоли молочной железы с поражением лимфоузлов у женщин после мастектомии и лучевой терапии.
При необходимости субъекту можно вводить многократные дозы соединения, описываемого в настоящем документе. Альтернативно субъекту вводят однократную дозу соединения, описываемого в настоящем документе.
В соответствии с одним аспектом настоящего изобретения соединение, раскрываемое в настоящем документе, можно эффективно вводить в комбинации с другим терапевтическим режимом, предусматривающим лучевую терапию, химиотерапию или другие терапевтические средства. В соответствии с дополнительными вариантами осуществления соединения, раскрываемые в настоящем документе, можно эффективно вводить в комбинации с терапевтическими средствами, направленными на аутоиммунные расстройства.
Соединение или его фармацевтически приемлемую соль или пролекарственное средство или фармацевтическую композицию на их основе можно также применять для нормализации костной ткани или для предупреждения или лечения остеопении или остеопороза.
Вышеизложенное можно лучше понять посредством ссылки на следующие примеры, которые представлены в иллюстративных целях и не предполагают ограничивать объем настоящего изобретения.
В соответствии с одним вариантом осуществления «злокачественная опухоль» относится к патологическому росту клеток, которые имеют тенденцию к пролиферации неконтролируемым образом и в некоторых случаях к метастазированию (распространению). Типы злокачественной опухоли включают без ограничения солидные опухоли (такие как таковые желчного пузыря, кишечника, головного мозга, молочной железы, эндометрия, сердца, почки, легкого, матки, лимфатической ткани (лимфома), яичника, поджелудочной железы или другого эндокринного органа (щитовидной железы), предстательной железы, кожи (меланома или базально-клеточная злокачественная опухоль) или гематологические опухоли (такие как лейкемии и лимфомы) на любой стадии заболевания или без метастазов.
В соответствии с одним вариантом осуществления злокачественная опухоль или опухоль является эстроген-опосредованной. В соответствии с альтернативным вариантом осуществления злокачественная опухоль или опухоль не является эстроген-опосредованной. В соответствии с различными вариантами осуществления злокачественная опухоль или опухоль не является гормонально опосредованной. Неограничивающие примеры злокачественных опухолей включают острый лимфобластный лейкоз, острый миелоидный лейкоз, адренокортикальную карциному, злокачественную опухоль анального канала, злокачественную опухоль аппендикса, астроцитомы, атипичную тератоидно-рабдоидную опухоль, базально-клеточную карциному, злокачественную опухоль желчных протоков, злокачественную опухоль желчного пузыря, злокачественную опухоль костей (остеосаркому и злокачественную фиброзную гистицитому), глиому ствола головного мозга, опухоли головного мозга, опухоли головного и спинного мозга, опухоль молочной железы, бронхиальные опухоли, лимфому Беркитта, злокачественную опухоль шейки матки, хронический лимфоцитарный лейкоз, хронический миелоидный лейкоз, злокачественную опухоль толстой кишки, колоректальную злокачественную опухоль, краниофарингиому, кожную Т-клеточную лимфому, эмбриональные опухоли, злокачественную опухоль эндометрия, эпендимобластому, эпендимому, злокачественную опухоль пищевода, семейство опухолей саркомы Юинга, злокачественную опухоль глаза, ретинобластому, злокачественную опухоль желчного пузыря, злокачественную опухоль желудка, желудочно-кишечную карциноидную опухоль, желудочно-кишечную стромальную опухоль (GIST), желудочно-кишечную стромально-клеточную опухоль, эмбрионально-клеточную опухоль, глиому, волосатоклеточный лейкоз, злокачественную опухоль головы и шеи, гепатоцеллюлярная злокачественная опухоль (злокачественная опухоль печени), лимфому Ходжкина, гипофарингиальную злокачественную опухоль, интраокулярную меланому, опухоли островков поджелудочной железы (эндокринной части поджелудочной железы), саркому Капоши, злокачественную опухоль почки, гистиоцитоз из клеток Лангерганса, злокачественную опухоль гортани, лейкоз, острый лимфобластный лейкоз, острый миелоидный лейкоз, хронический лимфоцитарный лейкоз, хронический миелоцитарный лейкоз, волосатоклеточный лейкоз, злокачественную опухоль печени, злокачественную опухоль легкого, немелкоклеточную злокачественную опухоль легкого, мелкоклеточную злокачественную опухоль легкого, лимфому Беркитта, кожную Т-клеточную лимфому, лимфому Ходжкина, неходжкинскую лимфому, макроглобулинемию Вальденстрема, медуллобластому, медуллоэпителиому, меланому, мезотелиому, злокачественную опухоль ротовой полости, хронический миелоидный лейкоз, миелоидный лейкоз, множественную миелому, злокачественную опухоль носоглотки, нейробластому, неходжкинскую лимфому, немелкоклеточную злокачественную опухоль легкого, злокачественную опухоль ротовой полости, злокачественную опухоль ротоглотки, остеосаркому, злокачественную фиброзную гистиоцитому кости, злокачественную опухоль яичника, злокачественную опухоль эпителия яичника, эмбрионально-клеточную опухоль яичников, опухоль яичника с низким злокачественным потенциалом, злокачественную опухоль поджелудочной железы, папилломатоз, злокачественную опухоль паращитовидных желез, злокачественную опухоль полового члена, злокачественную опухоль глотки, паренхиматозные опухоль шишковидной железы промежуточной дифференциации, пинеобластому и супратенториальные примитивные нейроэктодермальные опухоли, опухоль гипофиза, плазмоклеточную опухоль/множественную миелому, плевролегочную бластому, первичную лимфому центральной нервной системы, злокачественную опухоль предстательной железы, злокачественную опухоль прямой кишки, почечно-клеточную злокачественную опухоль (злокачественную опухоль почки), ретинобластому, рабдомиосаркому, злокачественную опухоль слюнных желез, саркому, семейство опухолей саркомы Юинга, саркому Капоши, синдром Сезари, злокачественную опухоль кожи, мелкоклеточную злокачественную опухоль легкого, злокачественную опухоль тонкого кишечника, саркому мягких тканей, плоскоклеточную карциному, злокачественную опухоль желудка, супратенториальные примитивные нейроэктодермальные опухоли, Т-клеточную лимфому, злокачественную опухоль яичка, злокачественную опухоль горла, тимому и карциному вилочковой железы, злокачественную опухоль щитовидной железы, злокачественную опухоль уретры, злокачественную опухоль матки, саркому матки, злокачественную опухоль влагалища, злокачественную опухоль вульвы, макроглобулинемию Вальденстрема, опухоль Вильмса.
Способ лечения может предупреждать или снижать риск злокачественной опухоли. Способ лечения может вызывать частичную или полную регрессию злокачественной опухоли у субъекта.
Способ лечения может вызывать частичную или полную регрессию резистентной к тамоксифену злокачественной опухоли или опухоли. Способ лечения может вызывать частичную или полную регрессию трижды негативной злокачественной опухоли молочной железы.
В соответствии с некоторыми вариантами осуществления соединения, раскрываемые в настоящем документе, применяют для лечения или предупреждения злокачественной опухоли или опухоли у млекопитающего, такого как человек. В соответствии с некоторыми вариантами осуществления злокачественная опухоль представляет собой злокачественную опухоль молочной железы, злокачественную опухоль яичника, злокачественную опухоль эндометрия, злокачественную опухоль предстательной железы или злокачественную опухоль матки. В соответствии с некоторыми вариантами осуществления злокачественная опухоль представляет собой злокачественную опухоль молочной железы, злокачественную опухоль легкого, злокачественную опухоль яичника, злокачественную опухоль эндометрия, злокачественную опухоль предстательной железы или злокачественную опухоль матки. В соответствии с некоторыми вариантами осуществления злокачественная опухоль представляет собой злокачественную опухоль молочной железы. В соответствии с некоторыми вариантами осуществления злокачественная опухоль представляет собой гормонозависимую злокачественную опухоль. В соответствии с некоторыми вариантами осуществления злокачественная опухоль представляет собой эстроген-рецептор-зависимую злокачественную опухоль. В соответствии с некоторыми вариантами осуществления злокачественная опухоль представляет собой эстроген-чувствительную злокачественную опухоль. В соответствии с некоторыми вариантами осуществления злокачественная опухоль является резистентной к антигормональному лечению. В соответствии с некоторыми вариантами осуществления злокачественная опухоль является эстроген-чувствительной злокачественной опухолью или эстроген-рецептор-зависимой злокачественной опухолью, которая является резистентной к антигормональному лечению. В соответствии с некоторыми вариантами осуществления злокачественная опухоль является гормон-чувствительной злокачественной опухолью или гормон-рецептор-зависимой злокачественной опухолью, которая является резистентной к антигормональному лечению. В соответствии с некоторыми вариантами осуществления антигормональное лечение предусматривает лечение при помощи по меньшей мере одного средства, выбранного из тамоксифена, фулвестранта, стероидных ингибиторов ароматазы и нестероидных ингибиторов ароматазы.
В соответствии с некоторыми вариантами осуществления соединения, раскрываемые в настоящем документе, применяют для лечения гормон-рецептор-положительной метастатической злокачественной опухоли молочной железы у женщин постменопаузального периода с прогрессированием заболевания после антиэстрогенной терапии.
В соответствии с некоторыми вариантами осуществления соединения, раскрываемые в настоящем документе, применяют для лечения гормональнозависимого злокачественного заболевания молочной железы или половых путей у млекопитающего. В соответствии с некоторыми вариантами осуществления доброкачественное или злокачественное заболевание представляет собой злокачественную опухоль молочной железы.
В соответствии с одним вариантом осуществления соединение по настоящему изобретению применяют для гормональной терапии.
Вышеизложенное можно лучше понять посредством ссылки на следующие примеры, которые представлены в иллюстративных целях и не предполагают ограничивать объем настоящего изобретения.
В соответствии с одним аспектом соединение по настоящему изобретению или его фармацевтически приемлемая соль или пролекарственное средство можно применять для лечения гормональной злокачественной опухоли или опухоли, которая метастазировала в головной мозг, костную ткань или другой орган. В соответствии с одним вариантом осуществления данного аспекта гормональная злокачественная опухоль является эстроген-опосредованной. В соответствии с другим вариантом осуществления эстроген-опосредованную злокачественную опухоль выбирают из таковой молочной железы, матки, яичника и эндометрия. В соответствии с другими вариантами осуществления соединение по настоящему изобретению или его фармацевтически приемлемая соль или пролекарственное средство можно применять для предупреждения гормональной злокачественной опухоли или опухоли от метастазирования в головной мозг, костную ткань или другой орган, в том числе гормональной злокачественной опухоли, которая является эстроген-опосредованной, например, таковой молочной железы, матки, яичника или эндометрия.
Комбинированная терапия
В соответствии с одним аспектом предусмотрен способ лечения нарушения патологической клеточной пролиферации у хозяина, такого как млекопитающий, который предусматривает введение эффективного количества комбинации одного или нескольких активных соединений, описываемых в настоящем документе, в комбинации или при чередовании с другим активным соединением.
В соответствии с одним аспектом этого варианта осуществления второе активное соединение представляет собой иммуномодулятор, в том числе без ограничения ингибитор контрольных точек. Ингибиторы контрольных точек для применения в способах, описываемых в настоящем документе, включают без ограничения PD-1-ингибиторы, PD-L1-ингибиторы, PD-L2-ингибиторы, CTLA-4-ингибиторы, LAG-3-ингибиторы, TIM-3-ингибиторы и ингибиторы на основе V-домена Ig супрессора Т-клеточной активации (VISTA) или их комбинацию.
В соответствии с одним вариантом осуществления ингибитор контрольных точек представляет собой PD-1-ингибитор, который блокирует взаимодействие PD-1 и PD-L1 в результате связывания с рецептором PD-1, и в свою очередь ингибирует иммунную супрессию. В соответствии с одним вариантом осуществления ингибитор контрольных точек представляет собой ингибитор контрольных точек PD-1, выбранный из ниволумаба, пембролизумаба, пидилизумаба, АМР-224 (AstraZeneca и MedImmune), PF-06801591 (Pfizer), MEDI0680 (AstraZeneca), PDR001 (Novartis), REGN2810 (Regeneron), SHR-12-1 (компания Jiangsu Hengrui Medicine и Incyte Corporation), TSR-042 (Tesaro) и ингибитора PD-L1/VISTA CA-170 (Curis Inc).
В соответствии с одним вариантом осуществления ингибитор контрольных точек представляет собой PD-L1-ингибитор, который блокирует взаимодействие PD-1 и PD-L1 в результате связывания с рецептором PD-L1, и в свою очередь ингибирует иммунную супрессию. PD-L1-ингибиторы включают без ограничения авелумаб, атезолизумаб, дурвалумаб, KN035 и BMS-936559 (Bristol-Myers Squibb).
В соответствии с одним аспектом этого варианта осуществления ингибитор контрольных точек представляет собой CTLA-4-ингибитор, который связывается с CTLA-4 и ингибирует иммунную супрессию. CTLA-4-ингибиторы включают без ограничения ипилимумаб, тремелимумаб (AstraZeneca и MedImmune), AGEN1884 и AGEN2041 (Agenus).
В соответствии с другим вариантом осуществления ингибитор контрольных точек представляет собой ингибитор контрольных точек LAG-3. Примеры ингибиторов контрольных точек LAG-3 включают без ограничения BMS-986016 (Bristol-Myers Squibb), GSK2831781 (GlaxoSmithKline), IMP321 (Prima BioMed), LAG525 (Novartis) и двойной ингибитор PD-1 и LAG-3 MGD013 (MacroGenics). В соответствии с еще одним аспектом этого варианта осуществления ингибитор контрольных точек представляет собой ингибитор контрольных точек TIM-3. Специфический TIM-3-ингибитор включает без ограничения TSR-022 (Tesaro).
В соответствии с еще одним вариантом осуществления одно из активных соединений, описываемых в настоящем документе, вводят в эффективном количестве для лечения патологической ткани женской половой системы, такой как злокачественная опухоль молочной железы, яичника, почки, эндометрия или матки, в комбинации или при чередовании с эффективным количеством ингибитора эстрогена, в том числе без ограничения SERM (селективного модулятора эстрогеновых рецепторов), SERD (селективного блокатора эстрогеновых рецепторов), полного блокатора эстрогеновых рецепторов или другой формы частичного или полного антагониста эстрогенов. Частичные антиэстрогены, например, ралоксифен и тамоксифен поддерживают некоторые эстрогенподобные эффекты, в том числе эстрогенподобную стимуляцию маточного роста, а также в некоторых случаях эстроген-подобного действия во время прогрессирования злокачественной опухоли молочной железы, которое фактически стимулирует опухолевый рост. В отличие от этого, фулвестрант, полный антиэстроген, не обладает эстроген-подобным действием на матку и является эффективным при резистентных к тамоксифену опухолях. Неограничивающие примеры антиэстрогенных соединений предусмотрены в WO 2014/19176, переданном AstraZeneca. Дополнительные неограничивающие примеры антиэстрогенных соединений включают: SERM, такие как анордрин, базедоксифен, бропарестриол, хлоротрианизен, кломифена цитрат, циклофенил, лазофоксифен, онмелоксифен, ралоксифен, тамоксифен, торемифен и фулвестрант; ингибиторы ароматазы, такие как аминоглутетимид, тестолактон, анастрозол, экземестан, фадрозол, форместан и летрозол; и антигонадотропины, такие как лейпрорелин, цетрореликс, аллилэстренол, хлормадинона ацетат, ципротерона ацетат, делмаденона ацетат, дигидростерон, медроксипрогестерона ацетат, мегестрола ацетат, номегестрола ацетат, норэтистерона ацетат, прогестерон и спиронолактон.
В соответствии с другим вариантом осуществления одно из активных соединений, описываемых в настоящем документе, вводят в эффективном количестве для лечения патологической ткани мужской половой системы, такой как злокачественная опухоль предстательной железы или яичка, в комбинации при чередовании с эффективным количеством ингибитор андрогена (такого как тестостерон), в том числе без ограничения селективным модулятором андрогеновых рецепторов, селективным блокатором и/или деструктором андрогеновых рецепторов, полным деструктором андрогеновых рецепторов или другой формы частичного или полного антагониста андрогенов. В соответствии с одним вариантом осуществления злокачественная опухоль предстательной железы или яичка является резистентной к андрогенам. Неограничивающие примеры антиандрогенных соединений предусмотрены в WO 2011/156518 и патентах США №№8455534 и 8299112. Дополнительные неограничивающие примеры антиандрогенных соединений включают: энзалутамид, апалутамид, ципротерона ацетат, хлормадинона ацетат, спиронолактон, канренон, дроспиренон, кетоконазол, топилутамид, абиратерона ацетат и циметидин.
В соответствии с одним аспектом предусмотрен режим лечения, включающий введение соединения по настоящему изобретению в комбинации по меньшей мере с одним дополнительным химиотерапевтическим средством. Комбинации, раскрываемые в настоящем документе, можно вводить для полезного, дополнительного или синергического эффекта при лечении патологических нарушений клеточной пролиферации.
В соответствии с конкретными вариантами осуществления режим лечения включает введение соединения по настоящему изобретению в комбинации по меньшей мере с одним ингибитором киназы. В соответствии с одним вариантом осуществления по меньшей мере один ингибитор киназы выбирают из ингибитора фосфоинозитид-3-киназы (PI3K), ингибитора тирозинкиназы Брутона (BTK) или ингибитора тирозинкиназы селезенки (Syk) или их комбинации.
PI3k-ингибиторы, которые можно применять в настоящем изобретении, являются общеизвестными. Примеры ингибиторов PI3-киназы включают без ограничения вортманин, деметоксивиридин, перифозин, иделализиб, пиктилизиб, паломид 529, ZSTK474, PWT33597, CUDC-907 и AEZS-136, дувелисиб, GS-9820, GDC-0032 (2-[4-[2-(2-изопропил-5-метил-1,2,4-триазол-3-ил)-5,6-дигидроимидазо [1,2-d][1,4]бензоксазепин-9-ил]пиразол-1-ил]-2-метилпропанамид), MLN-1117 ((2R)-1-фенокси-2-бутанилгидроген-(S)-метилфосфонат; или метил(оксо) {[(2R)-1-фенокси-2-бутанил]окси}фосфоний)), BYL-719 ((2S)-N1-[4-метил-5-[2-(2,2,2-трифтор-1,1-диметилэтил)-4-пиридинил]-2-тиазолил]-1,2-пирролидиндикарбоксамид), GSK2126458 (2,4-дифтор-N-{2-(метилокси)-5-[4-(4-пиразинил)-6-хинолинил]-3-пиридилил}бензолсульфонамид), TGX-221 ((±)-7-метил-2-(морфолин-4-ил)-9-(1-фениламиноэтил)-пиридо [1,2-а]-пиримидин-4-он), GSK2636771 (2-метил-1-(2-метил-3-(трифторметил)бензил)-6-морфолино-1Н-бензо[d]имидазол-4-карбоновой кислоты дигидрохлорид), KIN-193 ((R)-2-((1-(7-метил-2-морфолино-4-оксо-4H-пиридо[1,2-а]пиримидин-9-ил)этил)амино)бензойную кислоту), TGR-1202/RP5264, GS-9820 ((S)-1-(4-((2-(2-аминопиримидин-5-ил)-7-метил-4-могидроксипропан-1-он), GS-1101 (5-фтор-3-фенил-2-([S)]-1-[9H-пурин-6-иламино]-пропил)-3Н-хиназолин-4-он), AMG-319, GSK-2269557, SAR245409 (N-(4-(N-(3-((3,5-диметоксифенил)амино)хиноксалин-2-ил)сульфамоил)фенил)-3-метокси-4-метилбензамид), BAY80-6946 (2-амино-N-(7-метокси-8-(3-морфолинопропокси)-2,3-дигидроимидазо[1,2-с]хиназолин), AS 252424 (5-[1-[5-(4-фтор-2-гидроксифенил)-фуран-2-ил]-мет-(Z-илиден]-тиазолидин-2,4-дион), CZ 24832 (5-(2-амино-8-фтор-[1,2,4]триазоло[1,5-а]пиридин-6-ил)-N-трет-бутилпиридин-3-сульфонамид), бупарлисиб(5-[2,6-ди(4-морфолинил)-4-пиримидинил]-4-(трифторметил)-2-пиридинамин), GDC-0941 (2-(1H-индазол-4-ил)-6-[[4-(метилсульфонил)-1-пиперазинил]метил]-4-(4-морфолинил)тиено [3,2-d]пиримидин), GDC-0980 ((S)-1-(4-((2-(2-аминопиримидин-5-ил)-7-метил-4-морфолинотиено[3,2-d]пиримидин-6-ил)метил)пиперазин-1-ил)-2-гидроксипропан-1-он (также известный как RG7422)), SF1126 ((8S,14S,17S)-14-(карбоксиметил)-8-(3-гуанидинопропил)-17-(гидроксиметил)-3,6,9,12,15-пентаоксо-1-(4-(4-оксо-8-фенил-4Н-хромен-2-ил)морфолино-4-иум)-2-окса-7,10,13,16-тетраазаоктадекан-18-оат), PF-05212384 (N-[4-[[4-(диметиламино)-1-пиперидинил]карбонил]фенил]-N'-[4-(4,6-ди-4-морфолинил-1,3,5-триазин-2-ил)фенил]мочевину), LY3023414, BEZ235 (2-метил-2-{4-[3-метил-2-оксо-8-(хинолин-3-ил)-2,3-дигидро-1H-имидазо[4,5-с]хинолин-1-ил]фенил}пропаннитрил), XL-765 (N-(3-(N-(3-(3,5-диметоксифениламино)хиноксалин-2-ил)сульфамоил)фенил)-3-метокси-4-метилбензамид) и GSK1059615 (5-[[4-(4-пиридинил)-6-хинолинил]метилен]-2,4-тиазолидендион), РХ886 ([(3aR,6Е,9S,9aR,10R,11aS)-6-[[бис(проп-2-енил)амино]метилиден]-5-гидрокси-9-(метоксиметил)-9а,11а-диметил-1,4,7-триоксо-2,3,3а,9,10,11-гексагидроиндено[4,5h]изохромен-10-ил]ацетат (также известный как сонолисиб)).
В соответствии с одним вариантом осуществления соединение по настоящему изобретению комбинируют в лекарственной форме в виде разовой дозы с PIk3-ингибитором.
ВТК-ингибиторы для применения в настоящем изобретении являются общеизвестными. Примеры ВТК-ингибиторов включают ибрутиниб (также называемый PCI-32765)(Imbruvica™)(1-[(3R)-3-[4-амино-3-(4-фенокси-фенил)пиразоло [3,4-d]пиримидин-1-ил]пиперидин-1-ил]проп-2-ен-1-он), дианилинопиримидиновые ингибиторы, такие как AVL-101 и AVL-291/292 (N-(3-((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)фенил)акриламид) (Avila Therapeutics) (см. публикацию патента США №2011/0117073, включенную в настоящий документ во всей своей полноте), дасатиниб ([N-(2-хлор-6-метилфенил)-2-(6-(4-(2-гидроксиэтил)пиперазин-1-ил)-2-метилпиримидин-4-иламино)тиазол-5-карбоксамид], LFM-A13 (альфа-циано-бета-гидрокси-бета-метил-N-(2,5-ибромфенил)пропенамид), GDC-0834 ([R-N-(3-(6-(4-(1,4-диметил-3-оксопиперазин-2-ил)фениламино)-4-метил-5-оксо-4,5-дигидропиразин-2-ил)-2-метилфенил)-4,5,6,7-тетрагидробензо[b]тиофен-2-карбоксамид], CGI-560 4-(трет-бутил)-N-(3-(8-(фениламино)имидазо [1,2-а]пиразин-6-ил)фенил)бензамид, CGI-1746 (4-(трет-бутил)-N-(2-метил-3-(4-метил-6-((4-(морфолин-4-карбонил)фенил)амино)-5-оксо-4,5-дигидропиразин-2-ил)фенил)бензамид), CNX-774 (4-(4-((4-((3-акриламидофенил)амино)-5-фторпиримидин-2-ил)амино)фенокси)-N-метилпиколинамид), СТА056 (7-бензил-1-(3-(пиперидин-1-ил)пропил)-2-(4-(пиридин-4-ил)фенил)-1H-имидазо[4,5-g]хиноксалин-6(5H)-он), GDC-0834 ((R)-N-(3-(6-((4-(1,4-диметил-3-оксопиперазин-2-ил)фенил)амино)-4-метил-5-оксо-4,5-дигидропиразин-2-ил)-2-метилфенил)-4,5,6,7-тетрагидробензо[b]тиофен-2-карбоксамид), GDC-0837 ((R)-N-(3-(6-((4-(1,4-диметил-3-оксопиперазин-2-ил)фенил)амино)-4-метил-5-оксо-4,5-дигидропиразин-2-ил)-2-метилфенил)-4,5,6,7-тетрагидробензо[b]тиофен-2-карбоксамид), НМ-71224, АСР-196, ONO-4059 (Ono Pharmaceuticals), PRT062607 (4-((3-(2H-1,2,3-триазол-2-ил)фенил)амино)-2-(((1R,2S)-2-аминоциклогексил)амино)пиримидин-5-карбоксамида гидрохлорид), QL-47 (1-(1-акрилоилиндолин-6-ил)-9-(1-метил-1H-пиразол-4-ил)бензо[h][1,6]нафтиридин-2(1H)-он) и RN486 (6-циклопропил-8-фтор-2-(2-гидроксиметил-3-{1-метил-5-[5-(4-метил-пиперазин-1-ил)-пиридин-2-иламино]-6-оксо-1,6-дигидро-пиридин-3-ил}-фенил)-2H-изохинолин-1-он) и другие молекулы, способные ингибировать активность BTK, например, таковые BTK-ингибиторы, раскрываемые в Akinleye et ah, Journal of Hematology & Oncology, 2013, 6:59, которая включена в настоящий документ во всей полноте посредством ссылки. В соответствии с одним вариантом осуществления соединение по настоящему изобретению комбинируют в лекарственной форме в виде разовой дозы с BTK-ингибитором.
Syk-ингибиторы для применения в настоящем изобретении являются общеизвестными и включают, например, цердулатиниб (4-(цилокпропиламино)-2-((4-(4-(этилсульфонил)пиперазин-1-ил)фенил)амино)пиримидин-5-карбоксамид), энтосплетиниб (6-(1H-индазол-6-ил)-N-(4-морфолинофенил)имидазо [1,2-а]пиразин-8-амин), фостаматиниб ([6-({5-фтор-2-[(3,4,5-триметоксифенил)амино]-4-пиримидинил}амино)-2,2-диметил-3-оксо-2,3-дигидро-4H-пиридо[3,2-b][1,4]оксазин-4-ил]метилдигидрогенфосфат), фостаматиниба динатриваевая соль (натрий(6-((5-фтор-2-((3,4,5-триметоксифенил)амино)пиримидин-4-ил)амино)-2,2-диметил-3-оксо-2Н-пиридо[3,2-b][1,4]оксазин-4(3H)-ил)метилфеосфат), BAY 61-3606 (2-(7-(3,4-диметоксифенил)-имидазо[1,2-с]пиримидин-5-уламино)-никотинамида HCl), RO9021 (6-[(1R,2S)-2-амино-циклогексамино]-4-(5,6-диметил-пиридин-2-иламино)-пиридазин-3-карбоновой кислоты амид), иматиниб (Gleevec; 4-[(4-метилпиперазин-1-ил)метил]-N-(4-метил-3-{[4-(пиридин-3-ил)пиримидин-2-ил]амино}фенил)бензамид), ставроспорин, GSK143 (2-(((3R,4R)-3-аминотетрагидро-2H-пиран-4-ил)амино)-4-(р-толиламино)пиримидин-5-карбоксамид), РР2 (1-(трет-бутил)-3-(4-хлорфенил)-1H-пиразоло[3,4-d]пиримидин-4-амин), PRT-060318 (2-(((1R,2S)-2-аминоциклогексил)амино)-4-(m-толиламино)пиримидин-5-карбоксамид), PRT-062607 (4-((3-(2H-1,2,3-триазол-2-ил)фенил)амино)-2-(((1R,2S)-2-аминоциклогексил)амино)пиримидин-5-карбоксамида гидрохлорид), R112 (3,3'-((5-фторпиримидин-2,4-диил)бис(азанедиил))дифенол), R348 (3-этил-4-метилпиридин), R406 (6-((5-фтор-2-((3,4,5-триметоксифенил)амино)пиримидин-4-ил)амино)-2,2-диметил-2H-пиридо[3,2-b][1,4]оксазин-3(4H)-он), YM193306 (см. Singh et al. Discovery and Development of Spleen Tyrosine Kinase (SYK) Inhibitors, J. Med. Chem. 2012, 55, 3614-3643), 7-азаиндол, пикеаттанол, ER-27319 (см. Singh et al. Discovery and Development of Spleen Tyrosine Kinase (SYK) Inhibitors, J. Med. Chem. 2012, 55, 3614-3643, включенная в настоящий документе во всей своей полноте), соединение D (см. Singh et al. Discovery and Development of Spleen Tyrosine Kinase (SYK) Inhibitors, J. Med. Chem. 2012, 55, 3614-3643, включенная в настоящий документе во всей своей полноте), PRT060318 (см. Singh et al. Discovery and Development of Spleen Tyrosine Kinase (SYK) Inhibitors, J. Med. Chem. 2012, 55, 3614-3643, включенная в настоящий документе во всей своей полноте), лютеолин (см. Singh et al. Discovery and Development of Spleen Tyrosine Kinase (SYK) Inhibitors, J. Med. Chem. 2012, 55, 3614-3643, включенная в настоящий документе во всей своей полноте), апигенин (см. Singh et al. Discovery and Development of Spleen Tyrosine Kinase (SYK) Inhibitors, J. Med. Chem. 2012, 55, 3614-3643, включенная в настоящий документе во всей своей полноте), кверцетин (см. Singh et al. Discovery and Development of Spleen Tyrosine Kinase (SYK) Inhibitors, J. Med. Chem. 2012, 55, 3614-3643, включенная в настоящий документе во всей своей полноте), физетин (см. Singh et al. Discovery and Development of Spleen Tyrosine Kinase (SYK) Inhibitors, J. Med. Chem. 2012, 55, 3614-3643, включенная в настоящий документе во всей своей полноте), мирицетин (см. Singh et al. Discovery and Development of Spleen Tyrosine Kinase (SYK) Inhibitors, J. Med. Chem. 2012, 55, 3614-3643, включенная в настоящий документе во всей своей полноте), морин (см. Singh et al. Discovery and Development of Spleen Tyrosine Kinase (SYK) Inhibitors, J. Med. Chem. 2012, 55, 3614-3643, включенная в настоящий документе во всей своей полноте). В соответствии с одним вариантом осуществления соединение по настоящему изобретению комбинируют в лекарственной форме в виде разовой дозы с Syk-ингибитором.
В соответствии с одним вариантом осуществления по меньшей мере одно дополнительное химиотерапевтическое средство представляет собой ингибитор белка лимфомы В-клеток 2 (Bcl-2). BCL-2-ингибиторы известны в данной области и включают, например, АВТ-199 (4-[4-[[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил]пиперазин-1-ил]-N-[[3-нитро-4-[[(тетрагидро-2H-пиран-4-ил)метил]амино]фенил]сульфонил]-2-[(1H-пирроло[2,3-b]пирадин-5-ил)окси]бензамид), АВТ-737 (4-[4-[[2-(4-хлорфенил)фенил]метил]пиперазин-1-ил]-N-[4-[[(2R)-4-(диметиламино)-1-фенилсульфанилбутан-2-ил]амино]-3-нитрофенил]сульфонилбензамид), АВТ-263 ((R)-4-(4-((4'-хлор-4,4-диметил-3,4,5,6-тетрагидро-[1,1'-бифенил]-2-ил)метил)пиперазин-1-ил)-N-((4-((4-морфолино-1-(фенилтио)бутан-2-ил)амино)-3((трифторметил)сульфонил)фенил)сульфонил)бензамид), GX15-070 (обатоклакс мезилат, (2Z)-2-[(5Z)-5-[(3,5-диметил-1H-пиррол-2-ил)метилиден]-4-метоксипиррол-2-илиден]индол; метансульфоновую кислоту))), 2-метокси-антимицин A3, YC137 (4-(4,9-диокси-4,9-дигидронафто [2,3-d]тиазол-2-иламино)-фениловый сложный эфир), погосин, этил-2-амино-6-бром-4-(1-циано-2-этокси-2-оксоэтил)-1H-хромен-3-карбоксилат, нилотиниб-d3, TW-37 (N-[4-[[2-(1,1-диметилэтил)фенил]сульфонил]фенил]-2,3,4-тригидрокси-5-[[2-(1-метил)фенил]метил]бензамид), апогоссиполон (ApoG2) или G3139 (облимерсен). В соответствии с одним вариантом осуществления соединение по настоящему изобретению комбинируют в лекарственной форме в виде разовой дозы по меньшей мере с одним BCL-2-ингибитором.
Соединение по настоящему изобретению или его фармацевтически активную соль можно комбинировать с иммунотерапией. Как описано более подробно ниже, соединение по настоящему изобретению можно конъюгировать с антителом, радиоактивным средством или другим целевым средством, которое направляет соединение к больной или патологически пролиферирующей клетке.
В соответствии с одним вариантом осуществления дополнительная терапия представляет собой моноклональное антитело (MAb). Некоторые MAb стимулируют иммунный ответ, который разрушает клетки злокачественной опухоли. Аналогично антителам, вырабатываемым естественным образом В-клетками, такие MAb «покрывают» поверхность клетки злокачественной опухоли, активируя ее разрушение иммунной системой. Например, бевацизумаб целенаправленно воздействует на фактор роста сосудистого эндотелия (VEGF), белок, секретируемый опухолевыми клетками и другими клетками в микроокружении опухоли, которая активирует развитие опухолевых кровеносных сосудов. При связывании с бевацизумабов VEGF не может взаимодействовать со своим клеточным рецептором, при этом предупреждается передача сигнала, которая приводит к росту новых кровеносных сосудов. Аналогично, цетуксимаб и панитумумаб целенаправленно воздействуют на рецептор эпидермального фактора роста (EGFR), а трастузумаб целенаправленно воздействует на рецептор эпидермального фактора роста человека 2 (HER-2). MAb, которые связываются с рецепторами факторов роста клеточной поверхности, предупреждают передачу нормальных активирующих рост сигналов целевыми рецепторами. Они могут также активировать апоптоз и активировать иммунную систему к разрушению опухолевых клеток.
В соответствии с некоторыми вариантами осуществления можно вводить эту комбинацию субъекту в дополнительной комбинации с другими химиотерапевтическими средствами. При необходимости комбинацию, описываемую в настоящем документе, можно вводить в то же время, что и другое химиотерапевтическое средство, для того, чтобы упростить режим лечения. В соответствии с некоторыми вариантами осуществления эту комбинацию и другое химиотерапевтическое средством можно предусматривать в одном составе. В соответствии с одним вариантом осуществления применение соединений, описываемых в настоящем документе, комбинируют в терапевтическом режиме с другими средствами. Такие средства могут включать без ограничения тамоксифен, мидазолам, летрозол, бортезомиб, анастрозол, гозерелин, mTOR-ингибитор, ингибиторы PI3-киназы, двойные mTOR-PI3K-ингибиторы, MEK-ингибиторы, RAS-ингибиторы, ALK-ингибиторы, HSP-ингибиторы (например, HSP70- и HSP90-ингибиторы или их комбинацию), BCL-2-ингибиторы, апоптические соединения, AKT-ингибиторы, в том числе без ограничения MK-2206, GSK690693, перифозин, (KRX-0401), GDC-0068, трицирибин, AZD5363, гонокиол, PF-04691502 и милтефозин, PD-1-ингибиторы, в том числе без ограничения ниволумаб, СТ-011, MK-3475, BMS936558 и АМР-514, или FLT-3-ингибиторы, в том числе без ограничения Р406, довитиниб, кизартиниб (АС220), амуватиниб (МР-470), тандутиниб (MLN518), ENMD-2076 и KW-2449 или их комбинации. Примеры mTOR-ингибиторов включают без ограничения рапамицин или его аналоги, эверолимус (афинитор), темсиролимус, ридафоралимус (дефоролимус) и сиролимус. Примеры MEK-ингибиторов включают без ограничения траметиниб/GSKl120212 (N-(3-{3-циклопропил-5-[(2-фтор-4-йодофенил)амино]-6,8-диметил-2,4,7-триоксо-3,4,6,7-тетрагидропиридо[4,3-d]пиримидин-1(2Н-ил}фенил)ацетамид), селуметиниб (6-(4-бром-2-хлоранилино)-7-фтор-N-(2-гидроксиэтокси)-3-метилбензимидазол-5-карбоксамид), пимасертиб/AS703026/MSC1935369 ((S)-N-(2,3-дигидроксипропил)-3-((2-фтор-4-йодофенил)амино)изоникотинамид), XL-518/GDC-0973 (1-({3,4-дифтор-2-[(2-фтор-4-йодофенил)амино]фенил}карбонил)-3-[(2S)-пиперидин-2-ил]азетидин-3-ол), рефаметиниб/BAY869766/RDEAl19 (N-(3,4-дифтор-2-(2-фтор-4-йодофениламино)-6-метоксифенил)-1-(2,3-дигидроксипропил)циклопропан-1-сульфонамид), PD-0325901 (N-[(2R)-2,3-дигидроксипропокси]-3,4-дифтор-2-[(2-фтор-4-йодофенил)амино]-бензамид), TAK733 ((R)-3-(2,3-дигидроксипропил)-6-фтор-5-(2-фтор-4-йодофениламино)-8-метилпиридо[2,3d]пиримидин-4,7(3Н,8Н)-дион), MEK162/ARRY438162 (5-[(4-бром-2-фторфенил)амино]-4-фтор-N-(2-гидроксиэтокси)-1-метил-1H-бензимидазол-6-карбоксамид), R05126766 (3-[[3-фтор-2-(метилсульфамоиламино)-4-пиридил]метил]-4-метил-7-пиримидин-2-илоксихромен-2-он), WX-554, R04987655/CH4987655 (3,4-дифтор-2-((2-фтор-4-йодофенил)амино)-N-(2-гидроксиэтокси)-5-((3-оксо-1,2-оксазинан-2-ил)метил)бензамид) или AZD8330 (2-((2-фтор-4-йодофенил)амино)-N-(2-гидроксиэтокси)-1,5-диметил-6-оксо-1,6-дигидропиридин-3-карбоксамид). Примеры RAS-ингибиторов включают без ограничения реолизин и siG12D LODER. Примеры ALK-ингибиторов включают без ограничения кризотиниб, АР26113 и LDK378. HSP-ингибиторы включают без ограничения гельданамицин или 17-N-аллиламино-17-деметоксигельданамицин (17AAG) и радицикол. В соответствии с конкретным вариантом осуществления соединение, описываемое в настоящем документе, вводят в комбинации с летрозолом и/или тамоксифеном. Другие химиотерапевтические средства, которые можно применять в комбинации с соединениями, описываемыми в настоящем документе, включают без ограничения химиотерапевтические средства, для которых не требуется активность клеточного цикла для их антинеопластического эффекта.
В соответствии с одним вариантом осуществления соединение по настоящему изобретению, описываемое в настоящем документе, можно комбинировать с химиотерапевтическим средством, выбранным без ограничения из иматиниба мезилата (Gleevec®), дасатиниба (Sprycel®), нилотиниба(Tasigna®), босутиниба (Bosulif®), трастузумаба (Herceptin®), пертузумаба (Perjeta ТМ), лапатиниба (Tykerb®), гефитиниба (Iressa®), эрлотиниба (Tarceva®), цетуксимаба (Erbitux®), панитумумаба (Vectibix®), вандетаниба (Caprelsa®), вемурафениба (Zelboraf®), вориностата (Zolinza®), ромидепсина (Istodax®), бексаротена (Targretin®), алитретиноина (Panretin®), третиноина (Vesanoid®), карфилзомиба (Kyprolis ТМ), пралатрексата (Folotyn®), бевацизумаба (Avastin®), зив-афлиберцепта (Zaltrap®), сорафениба (Nexavar®), сунитиниба (Sutent®), пазопаниба (Votrient®), регорафениба (Stivarga®) и кабозантиниба (Cometriq ТМ).
В соответствии с определенными вариантами осуществления дополнительное терапевтическое средство представляет собой противовоспалительное средство, химиотерапевтическое средство, радиотерапевтическое средство, дополнительные терапевтические средства или иммуносупрессорные средства.
Подходящие химиотерапевтические средства включают без ограничения радиоактивные молекулы, токсины, также обозначаемые как цитотоксины или цитотоксические средства, которые включают любое средство, которое является губительным для жизнеспособности клеток, средства и липосомы или другие везикулы, содержащие химиотерапевтические соединения. Общие протиопухолевые фармацевтические средства включают: винкристин (Oncovin®) или липосомальный винкристин (Marqibo®), даунорубицин (дауномицин или Cerubidine®) или доксорубицин (Adriamycin®), цитарабин (цитозин арабинозид, ара-С или Cytosar®), L-аспарагиназу (Elspar®) или ПЭГ-L-аспарагиназу (пэгаспарагиназу или Oncaspar®), этопозид (VP-16), тенипозид (Vumon®), 6-меркаптопурин (6-МР или Purinethol®), метотрексат, циклофосфамид (Cytoxan®), преднизон, дексаметазон (Decadron®), имитаниб (Gleevec®), дасатиниб (Sprycel®), нилотиниб (Tasigna®), ботусиниб (Bosulif®) и понатиниб (Iclusig™). Примеры дополнительных подходящих химиотерапевтических средств включают без ограничения 1-дедгидротестостерон, 5-фторурацил, дакарбазин, 6-меркаптопурин, 6-тиогуанин, актиономицин D, адриамицин, алкилирующие средства, аллопуринол натрия, алтретамин, амифостин, анастрозол, антрамицин (АМС), антимитотические средства, цис-дихлордиаминплатину (II) (DDP) (цисплатин), диаминодихлорплатину, антрациклины, антибиотики, антиметаболиты, аспарагиназу, живую BCG (внутривезикулярную), бетаметазона натрия фосфат и бетаметазона ацетат, бикалутамид, блеомицина сульфат, бусульфан, кальция лейковорин, калихеамицин, капецитабин, карбоплатин, ломустин (CCNU), кармустин (BSNU), хлорамбуцил, цисплатин, кладрибин, колхицин, конъюгированные эстрогены, циклофосфамид, циклотосфамид, цитарабин, цитарабин, цитохалазин Б, цитоксан, дакарбазин, дактиномицин, дактиномицин (ранее известный как актиномицин), даунирубицин HCl, даунорубицина цитрат, денилейкин, дифтитокс, дексразоксан, дибромманнит, дигидроксиантрациндион, доцетаксел, долазетрона мезилат, доксорубицин HCl, дронабинол, L-аспарагиназу Е. coli, эметин, эпоетин-α, L-аспарагиназу Erwinia, этерифицированные эстрогены, эстрадиол, эстрамустина натрия фосфат, бромистый этидий, этинилэстрадиол, этидронат, этопозид, фактор citrovorum, этопозида фосфат, филграстим, флоксуридин, флуконазол, флударабина фосфат, фторурацил, флутамид, фолиновую кислоту, гемцитабин HCl, глюкокортикоиды, гозерелина ацетат, грамицидин D, гранизетрон HCl, гидроксимочевину, идарубицин HCl, ифосфамид, интерферон-α-2b, иринотекан HCl, летрозол, кальция лейковорин, лейпролида ацетат, левамизол HCl, лидокаин, ломустин, майтанзиноид, мехлорэтамин HCl, медроксипрогестерона ацетат, мегестрола ацетат, мелфалан HCl, меркаптопурин, месну, метотрексат, метилтестостерон, митрамицин, митомицин С, митотан, митоксантрон, нилутамид, октреотида ацетат, ондансетрон HCl, паклитаксел, динатрий памидронат, пентостатин, пилокарпин HCl, плимицин, полифепросан 20 с кармустиновым имплантом, натрий порфимер, прокаин, прокарбазин HCl, пропранолол, сарграмостим, стрептозотоцин, тамоксифен, таксол, тенипозид, тенопозид, тестолактон, тетракаин, тиоепа хлорамбуцил, тиогуанин, тиотепа, топотекан HCl, торемифена цитрат, третиноин, валрубицин, винбластина сульфат, винкристина сульфат и винорелбина тартрат.
Дополнительные терапевтические средства, которые можно вводить в комбинации с соединением, раскрываемым в настоящем документе, могут включать 2-метоксиэстрадиол или 2МЕ2, финасунат, ваталаниб, волоциксимаб, этарацизумаб (MEDI-522), силенгитид, довитиниб, фигитумумаб, атацицепт, ритуксимаб, алемтезумаб, альдеслейкин, атлизумаб, тоцилизумаб, лукатумумаб, дацетузумаб, HLL1, huN901-DM1, атипримод, натализумаб, бортезомиб, маризомиб, танеспимицин, саквинавира мезилат, ритонавир, нелфинавира мезилат, индинавира сульфат, белиностат, панобиностат, мапатумумаб, лексатумумаб, дуланермин, плитидепсин, талмапимод, Р276-00, энзастаурин, типифарниб, леналидомид, талидомид, помалидомид, симвастин и целекоксиб.
В соответствии с одним аспектом настоящего изобретения соединение, описываемое в настоящем документе, можно комбинировать по меньшей мере с одним иммуносупрессорным средством. Иммуносупрессорные средства в соответствии с одним вариантом осуществления выбирают из группы, состоящей из ингибитора кальцинейрина, например, циклоспорина или аскомицина, например, циклоспорина A (Neoral®), FK506 (такролимуса), пимекролимуса, mTOR-ингибитора, например, рапамицина или его производного, например, сиролимуса (Rapamune®), эверолимуса (Certican®), темзиролимуса, зотаролимуса, биолимуса-7, биолимуса-9, рапалога, например, ридафоролимуса, азатиоприна, кампата 1Н, модулятора S1P-рецептора, например, финголимода или его аналога, антитела к IL-8, микофеноловой кислоты или ее соли, например, натриевой соли или ее пролекарственного средства, например, микофенолата мофетила (CellCept®), OKT3 (Orthoclone OKT3®), преднизона, ATGAM®, Thymoglobulin®, брекинара натрия, OKT4, Т10В9.А-3А, 33В3.1, 15-дезоксиспергуалина, тресперимуса, Leflunomide Arava®, антитела к CD25, антитела к IL2R, басиликсимаба (Simulect®), даклизумаба (Zenapax®), мизорибина, метотрексата, дексаметазона, ISAtx-247, SDZ ASM 981 (пимекролимуса, Elidel®), CTLA41g, абатацепта, белатацепта, LFA31g, этанерцепта (продаваемого как Enbrel® ImmuneXcite), далалимумаба (Humira®), инфликсимаба (Remicade®), антитела к LFA-1, натализумаба (Antegren®), энлимомаба, гавилимомаба, голимумаба, антитимоцитарного иммуноглобулина, сиплизумаба, алефацепта, эфализумаба, пентасы, месалазина, азакола, кодеина фосфата, бенорилата, фенбуфена, напрозина, диклофенака, этодолака, индометацина, аспирина и ибупрофена.
В соответствии с определенными вариантами осуществления соединение, описываемое в настоящем документе, вводят субъекту перед лечением другим химиотерапевтическим средством, во время лечения другим химиотерапевтическим средством, после лечения другим химитерапевтическим средством или в их комбинации.
Способы синтеза
Описанные в настоящем изобретении соединения могут быть получены способами, известными специалистам настоящей области техники. В одном неограничивающем примере раскрытые соединения могут быть получены с применением схем.
Используемый в настоящем описании алкенилен может охватывать оба цис- и транс-изомера алкенов, если не отмечено иное. Согласно одному варианту осуществления изомер представляет собой цис. Согласно предпочтительному варианту осуществления изомер представляет собой транс. Согласно одному варианту осуществления R2 представляет собой -С2-С6алкенилен-COOR17, а алкеновая группа представляет собой цис. Согласно предпочтительному варианту осуществления R2 представляет собой -С2-С6алкенилен-COOR17, а алкеновая группа представляет собой транс.
Некоторые из описанных в настоящем изобретении соединений могут обладать хиральным центром, и соединение может существовать в изомерной или диастереомерной форме. Если многие хиральные переменные присутствуют в формулах по настоящему изобретению, формула дополнительно охватывает каждый возможный диастереомер, если не отмечено иное. Например, (R,R), (S,R), (S,S) и (R,S) для молекулы с двумя хиральными центрами. Специалист настоящей области техники будет принимать во внимание, что чистые энантиомеры, диастереомеры и цис-/транс-изомеры могут быть получены способами, известными в области техники. Примеры способов получения оптически активных веществ включают в себя по меньшей мере следующее.
i) Физическое разделение кристаллов-техника, при которой макроскопические кристаллы отдельных энантиомеров разделяли вручную. Эта техника может быть использована, если существуют кристаллы отдельных энантиомеров, т.е., вещество является конгломератом и кристаллы визуально четко выражены;
ii) Одновременная кристаллизация-техника, при которой отдельные энантиомеры отдельно кристаллизировали из раствора рацемата, это возможно, только если последнее является конгломератом в твердом состоянии;
iii) Ферментативные расщепления-техника, при которой частичное или полное разделение рацемата проходит посредством разных скоростей реакции для энантиомеров с ферментом;
iv) Ферментативный асимметрический синтез - техника синтеза, при которой по меньшей мере на одной стадии синтеза использовали ферментативную реакцию с получением энантиомерно чистого или обогащенного прекурсора синтеза требуемого энантиомера;
v) Химический асимметрический синтез - техника синтеза, при которой требуемый энантиомер синтезировали из ахирального прекурсора при условиях, которые создают асимметрию (т.е., хиральность) в продукте, которая может быть достигнута с применением хиральных катализаторов или хиральных вспомогательных веществ;
vi) Диастереомерные разделения - техника, при которой осуществляли взаимодействие рацемического соединения с энантиомерно чистым реагентом (хиральное вспомогательное вещество), что превращает отдельные энантиомеры в диастереомеры. Полученные диастереомеры затем разделяли методом хроматографии или кристаллизации посредством их теперь более четких структурных различий и вспомогательного вещества, позже удаленного с получением требуемого энантиомера;
vii) Асимметрические трансформации первого и второго порядка - техника, при которой диастереомеры из рацемата уравновешиваются, чтобы привести к преобладанию в растворе диастереомера из требуемого энантиомера, или где избирательная кристаллизация диастереомера из требуемого энантиомера нарушает равновесие, таким образом, что в конечном итоге в основном все вещество было превращено в кристаллический диастереомер из требуемого энантиомера. Требуемый энантиомер затем высвобождался из диастереомера;
viii) Кинетические расщепления - такая техника относится к достижению частичного или полного расщепления рацемата (или дополнительного расщепления частично растворенного соединения) посредством неравных скоростей реакции энантиомеров с хиральным нерацемическим реагентом или катализатором при кинетических условиях;
ix) Энантиоспецифический синтез из нерацемических прекурсоров - техника синтеза, при которой требуемый энантиомер получали из нехиральных исходных веществ и где стереохимическая целостность не нарушена или только минимально нарушена в течение синтеза;
x) Хиральная жидкостная хроматография - техника, при которой энантиомеры рацемата разделяли в жидкой подвижной фазе посредством из различных взаимодействий с неподвижной фазой (включая метод хиральной HPLC). Неподвижная фаза может быть сделана из хирального вещества или подвижная фаза может содержать дополнительное хиральное вещество, чтобы вызывать различные взаимодействия;
xi) Хиральная газовая хроматография - техника, при которой рацемат испаряли и энантиомеры разделяли посредством их различных взаимодействий в газообразной подвижной фазе с колонкой, содержащей неподвижную нерацемическую хиральную фазу адсорбента;
xii) Экстракция при помощи хиральных растворителей - техника, при которой энантиомеры разделяли посредством предпочтительного растворения одного энантиомера в конкретном хиральном растворителе;
xiii) Перенос поперек хиральных мембран - техника, при которой рацемат размещали в контакте с барьером тонкой мембраны. Барьер типично разделяет две смешивающиеся жидкости, одна содержит рацемат, и движущая сила, такая как концентрация или дифференциальное давление, вызывает преимущественный перенос поперек мембранного барьера. Разделение возникает в результате нерацемической хиральной природы мембраны, что позволяет прохождение только одного энантиомера рацемата.
xiv) Хроматографию с псевдодвижущимся слоем использовали согласно одному варианту осуществления. Широкий спектр хиральных неподвижных фаз является коммерчески доступным.
Общий путь синтеза 1:
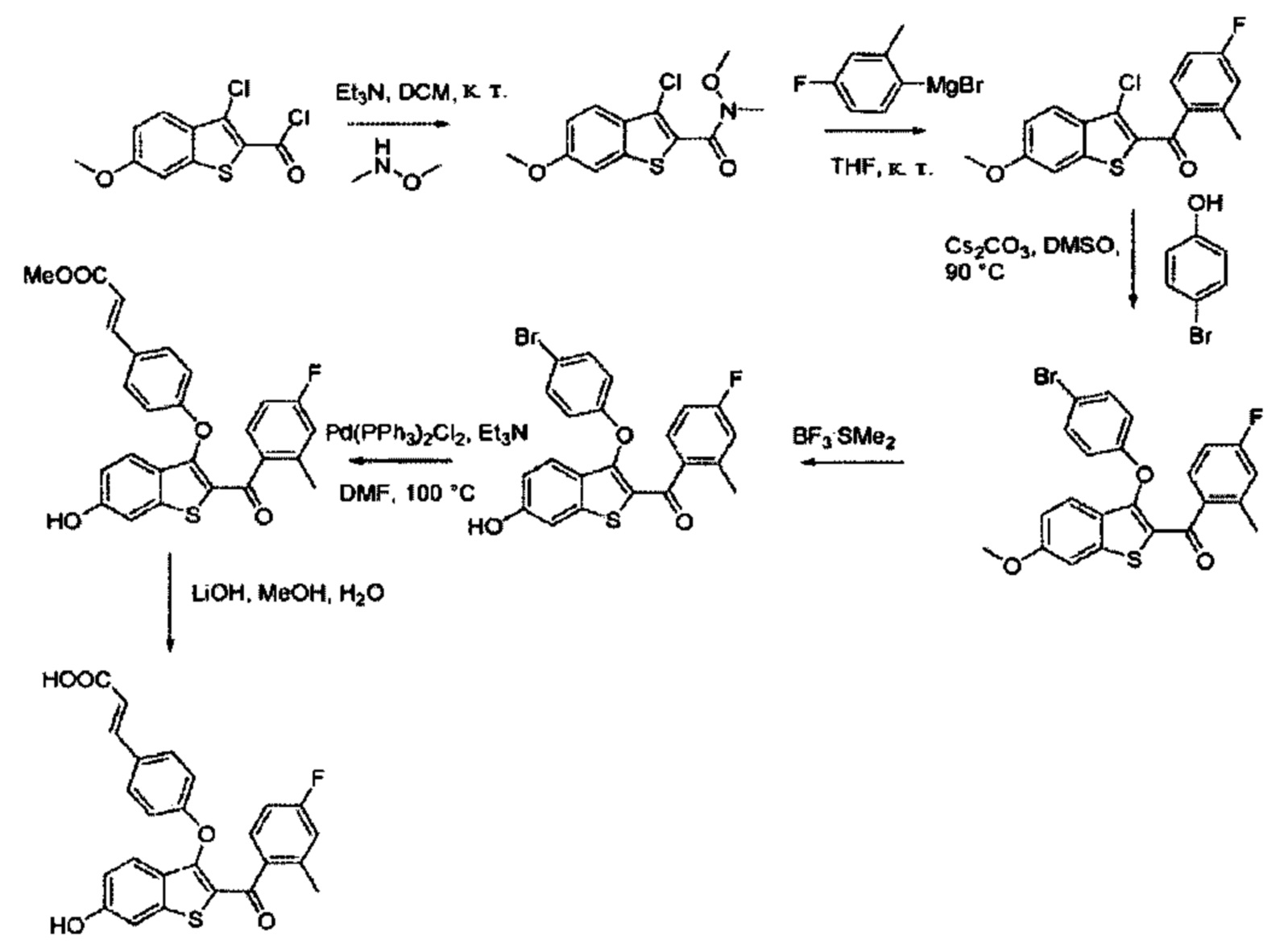
Общий путь синтеза 2:
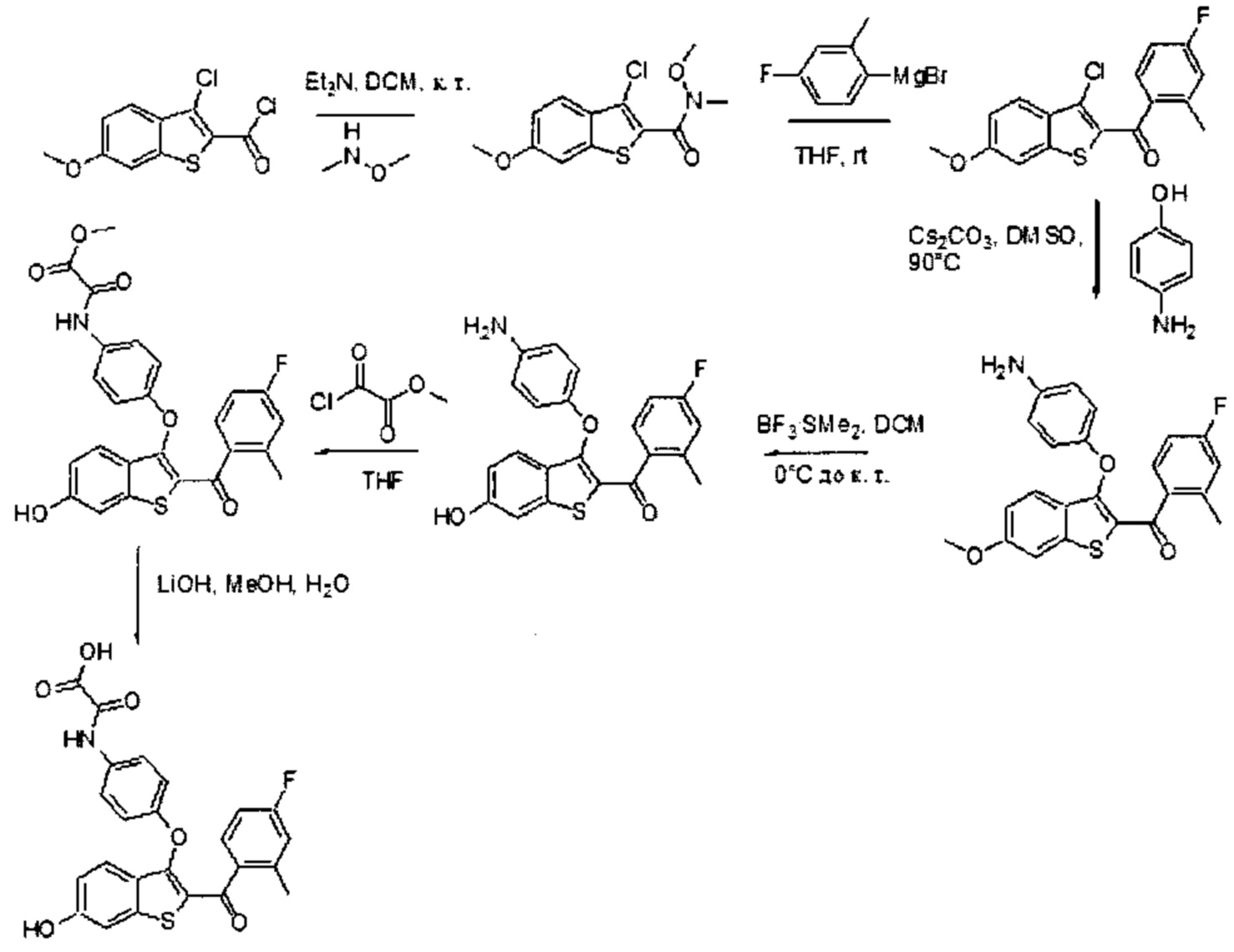
Общий путь синтеза 3:
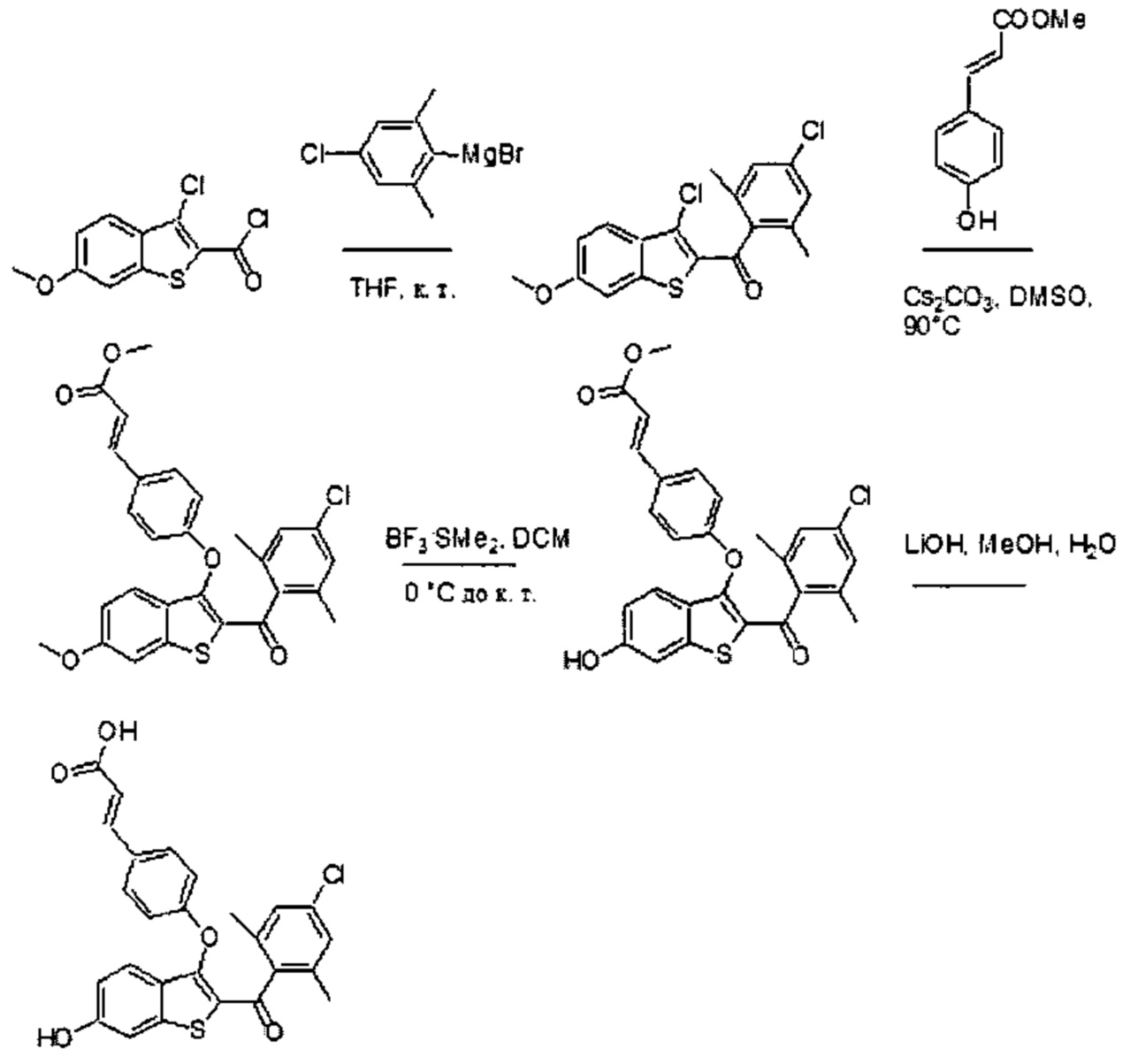
Общий путь синтеза 4:
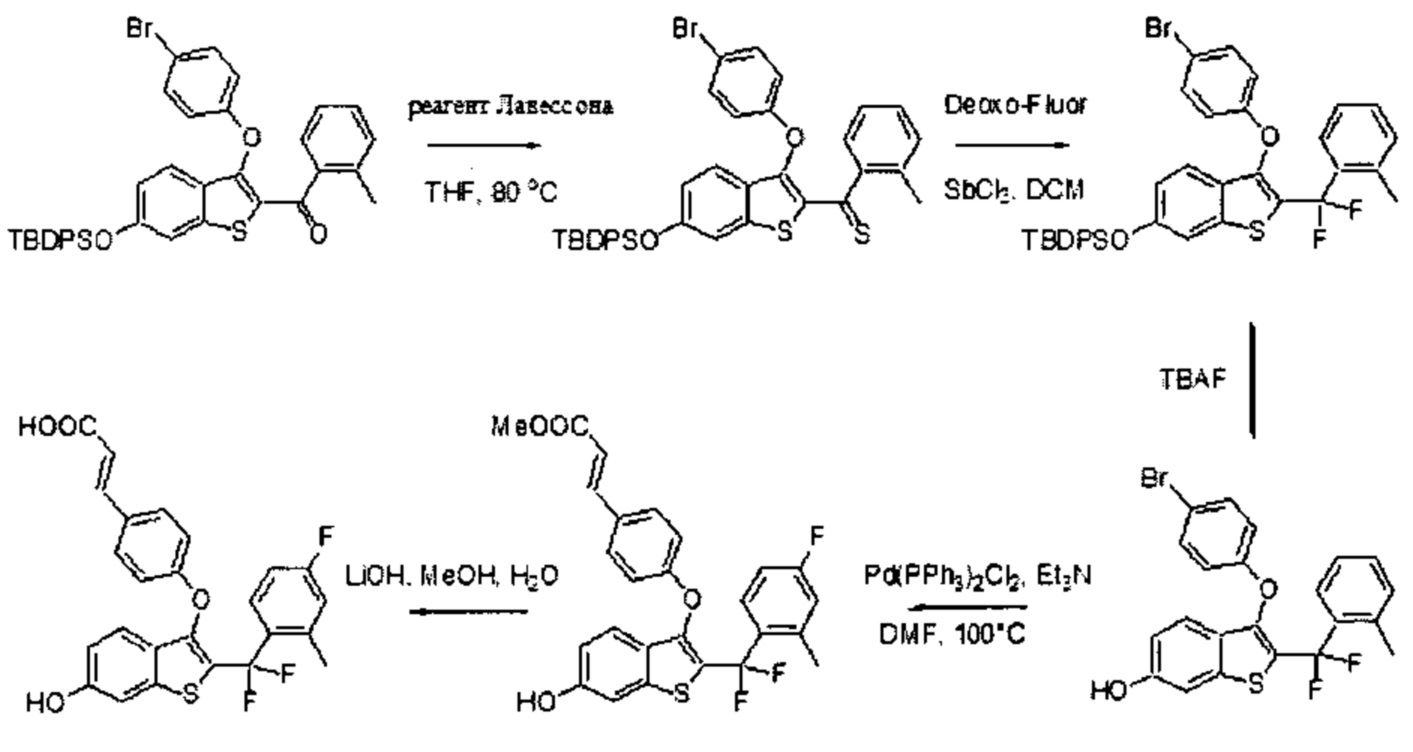
Общий путь синтеза 5:
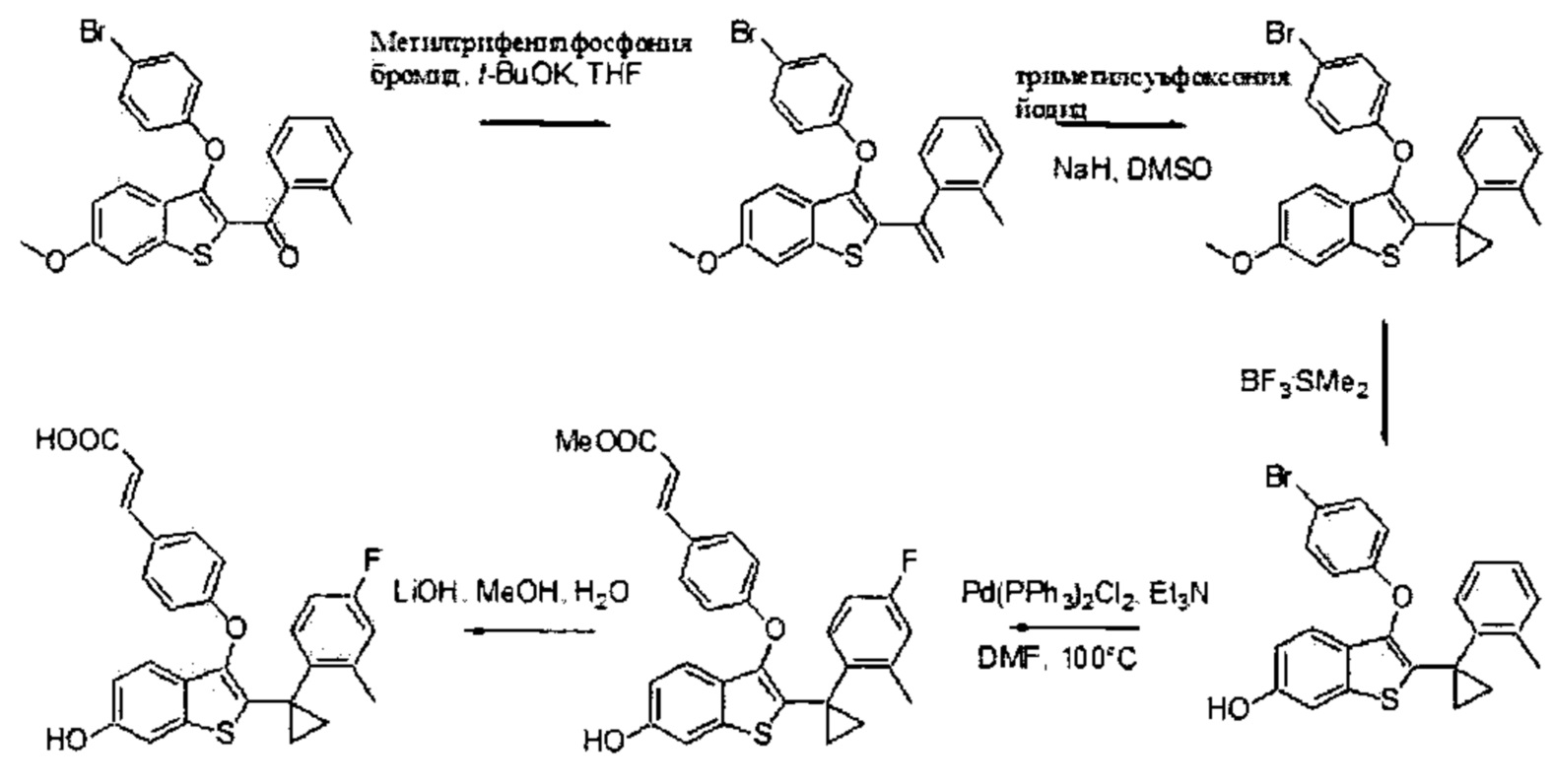
Промежуточное соединение 1: 3-Хлор-N,6-диметокси-N-метилбензо[b]тиофен-2-карбоксамид
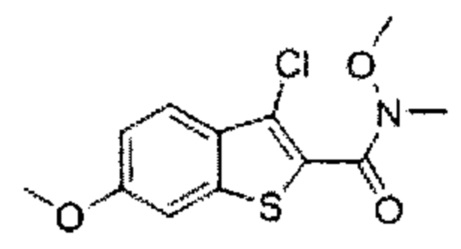
В высушенной в сушильном шкафу круглодонной колбе 3-хлор-6-метоксибензо[b]тиофен-2-карбонилхлорид (8,9 г, 34,9 ммоль) растворяли в 50 мл безводного дихлорметана в атмосфере аргона и добавляли одну часть N,O-диметилгидроксиламина гидрохлорида (3,75 г, 38,4 ммоль). После перемешивания в течение 10 минут по каплям добавляли Et3N (17,6 г, 174,5 ммоль). Реакционную смесь перемешивали в течение ночи, пока при помощи TLC не наблюдали расходование всех исходных веществ. Реакцию гасили ледяной водой, раствор экстрагировали этилацетатом и промывали солевым раствором. Органические экстракты объединяли, сушили над безводным Na2SO4, концентрировали в вакууме и очищали методом хроматографии (5%-50% этилацетат в гексане) с получением 7,6 г в виде белого твердого вещества (76%).1H ЯМР (400 МГц, CDCl3) δ 7.82 (d, J=8.9 Гц, 1Н), 7.23 (s, 1H), 7.10 (dd, J=8.9, 2.3 Гц, 1H), 3.90 (s, 3H), 3.73 (s, 3H), 3.39 (s, 3Н).13C ЯМР (100 МГц, CDCl3) δ 162.04, 159.88, 140.35, 130.23, 124.19, 116.09, 104.29, 62.04, 55.87, 33.75.
Промежуточное соединение 2: (3-Хлор-6-метоксибензо[b]тиофен-2-ил)(4-фтор-2-метилфенил)метанон
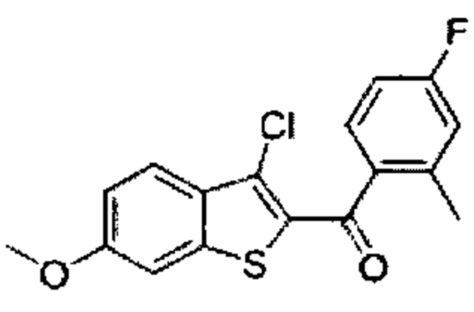
К раствору промежуточного соединения (1) (500 мг, 1,75 ммоль) в THF в атмосфере аргона по каплям добавляли 0,5 М раствор (4-фтор-2-метилфенил)магния бромида (4 мл, 2 ммоль). Реакционную смесь перемешивали всю ночь и гасили 1 н HCl/ледяной водой. Раствор экстрагировали этилацетатом и промывали солевым раствором. Органические экстракты объединяли, сушили над безводным Na2SO4, концентрировали в вакууме и очищали методом хроматографии (1%-15% этилацетата в гексане) с получением 550 мг белого твердого вещества (94%).
Следующие промежуточные соединения получали аналогичной процедурой с применением соответствующего реактива Гриньяра:
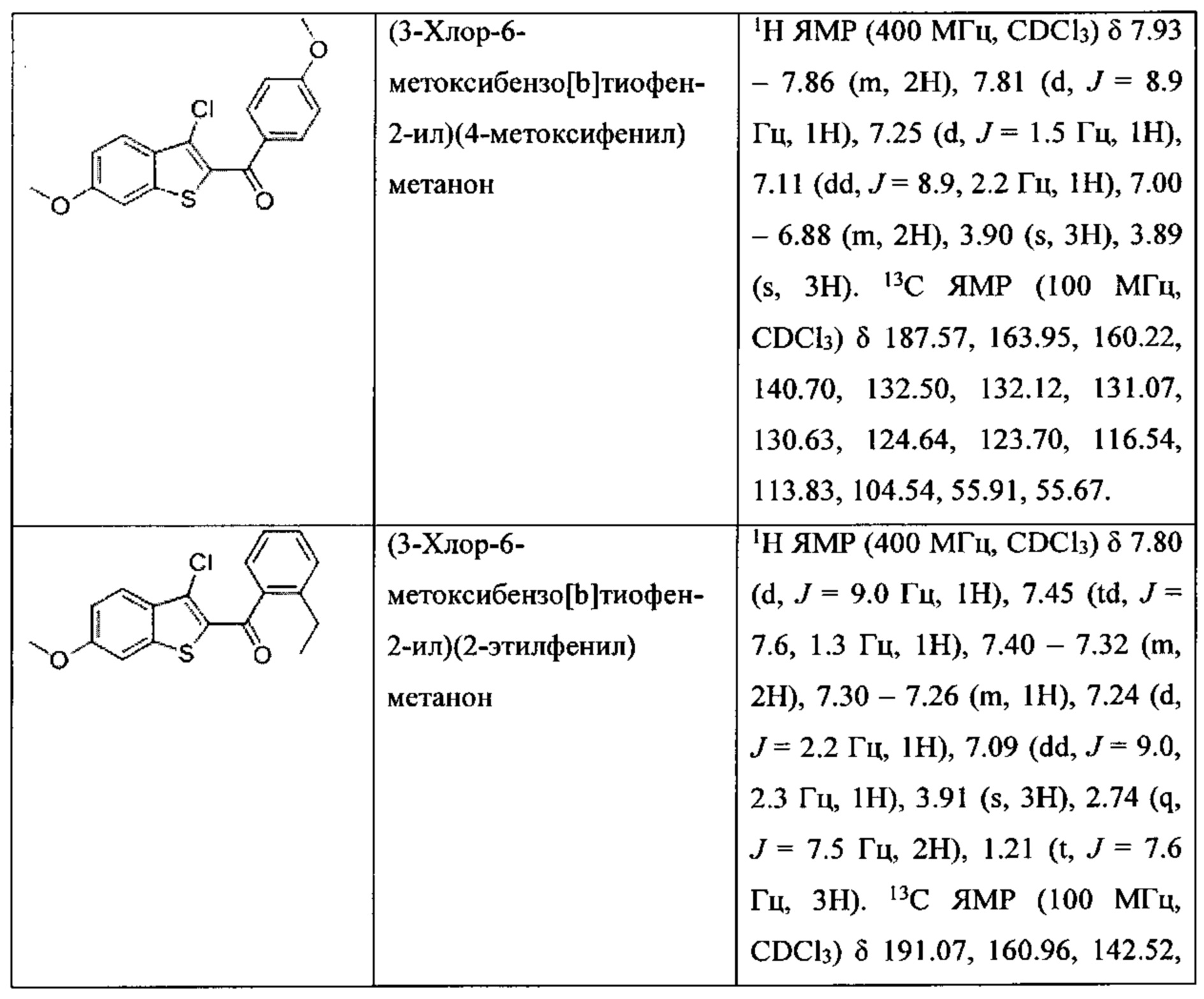
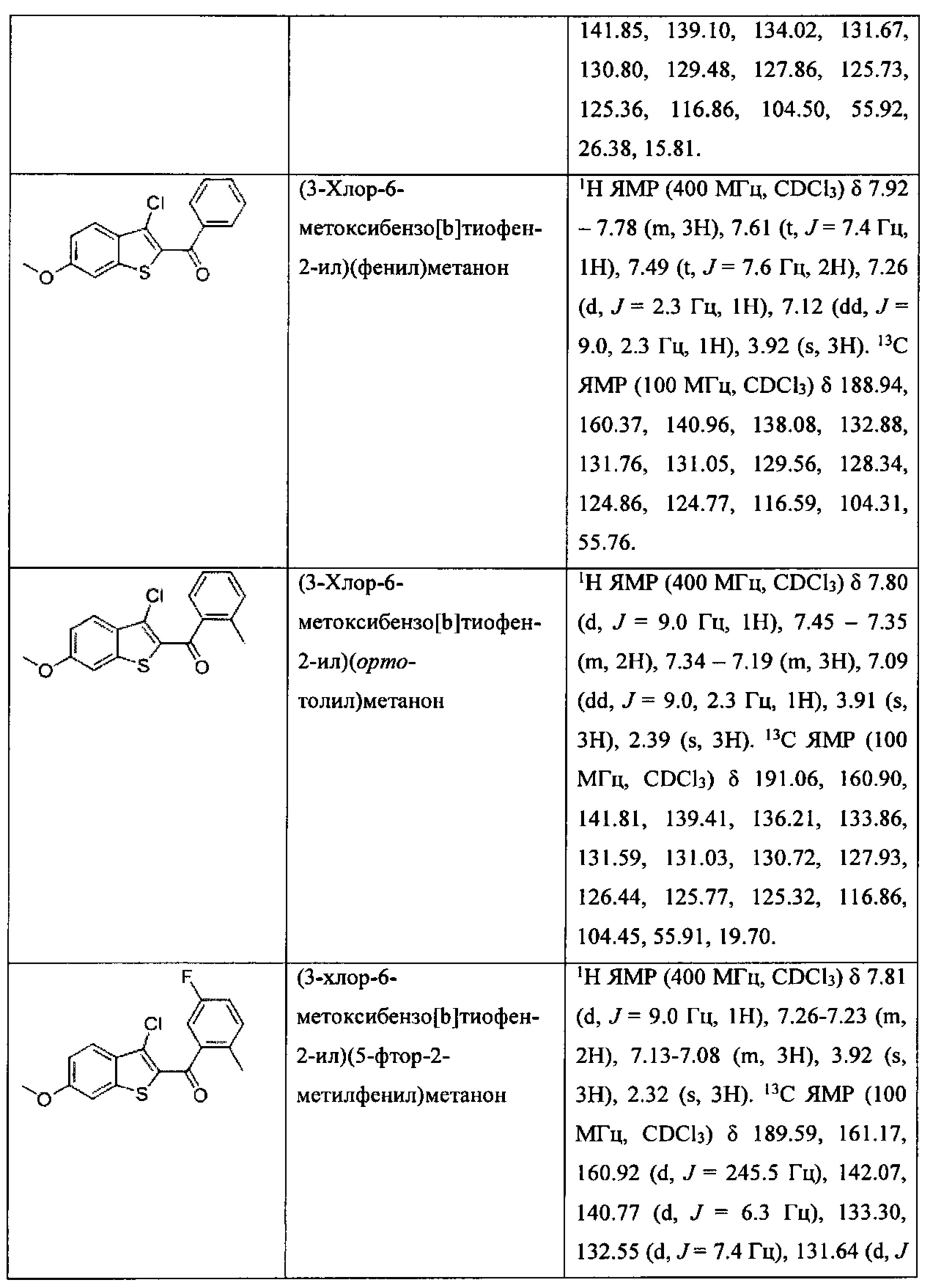
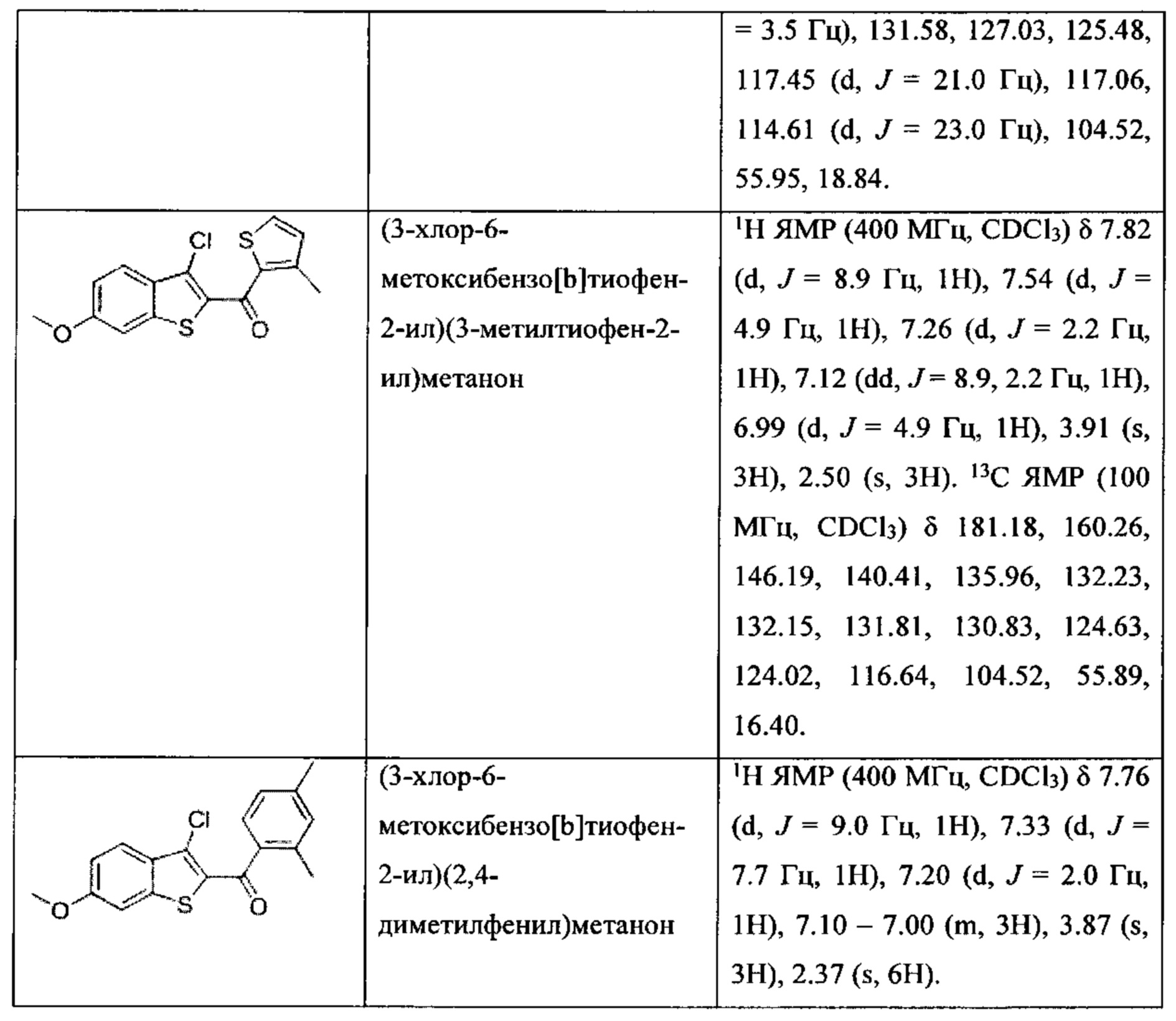
Промежуточное соединение 3: (3-Хлор-6-метоксибензо[b]тиофен-2-ил)(2-(трифторметил)фенил)метанон
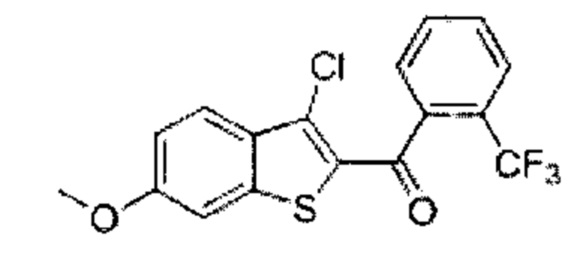
К раствору 3-хлор-6-метоксибензо[b]тиофен-2-карбонилхлорида (1,04 г, 4 ммоль) в THF в атмосфере аргона по каплям добавляли свежеприготовленный раствор (2-(трифторметил)фенил)магния бромида (5 ммоль). Реакционную смесь перемешивали всю ночь и гасили 1 н HCl/ледяной водой. Раствор экстрагировали этилацетатом и промывали солевым раствором. Органические экстракты объединяли, сушили над безводным Na2SO4, концентрировали в вакууме и очищали методом хроматографии (1%-15% этилацетата в гексане) с получением 350 мг белого твердого вещества (19%).1Н ЯМР (400 МГц, CDCl3) δ 7.77 (t, J=8.3 Гц, 2Н), 7.70-7.57 (m, 2Н), 7.47 (d, J=6.4 Гц, 1Н), 7.24 (s, 1H), 7.07 (dd, J=9.0, 1.9 Гц, 1H), 3.90 (s, 3Н).13C ЯМР (100 МГц, CDCl3) δ 187.86, 161.27, 142.29, 138.58 (q, J=2.1 Гц), 133.23, 131.99, 131.49, 130.20, 127.88, 127.75, 127.69 (q, J=32.3 Гц), 126.89 (q, J=4.5 Гц), 125.49, 123.70 (q, J=274.0 Гц), 117.07, 104.41, 55.91.19F ЯМР (400 МГц, CDCl3) δ -58.46.
Следующие промежуточные соединения получали аналогичной процедурой с применением соответствующего реактива Гриньяра:
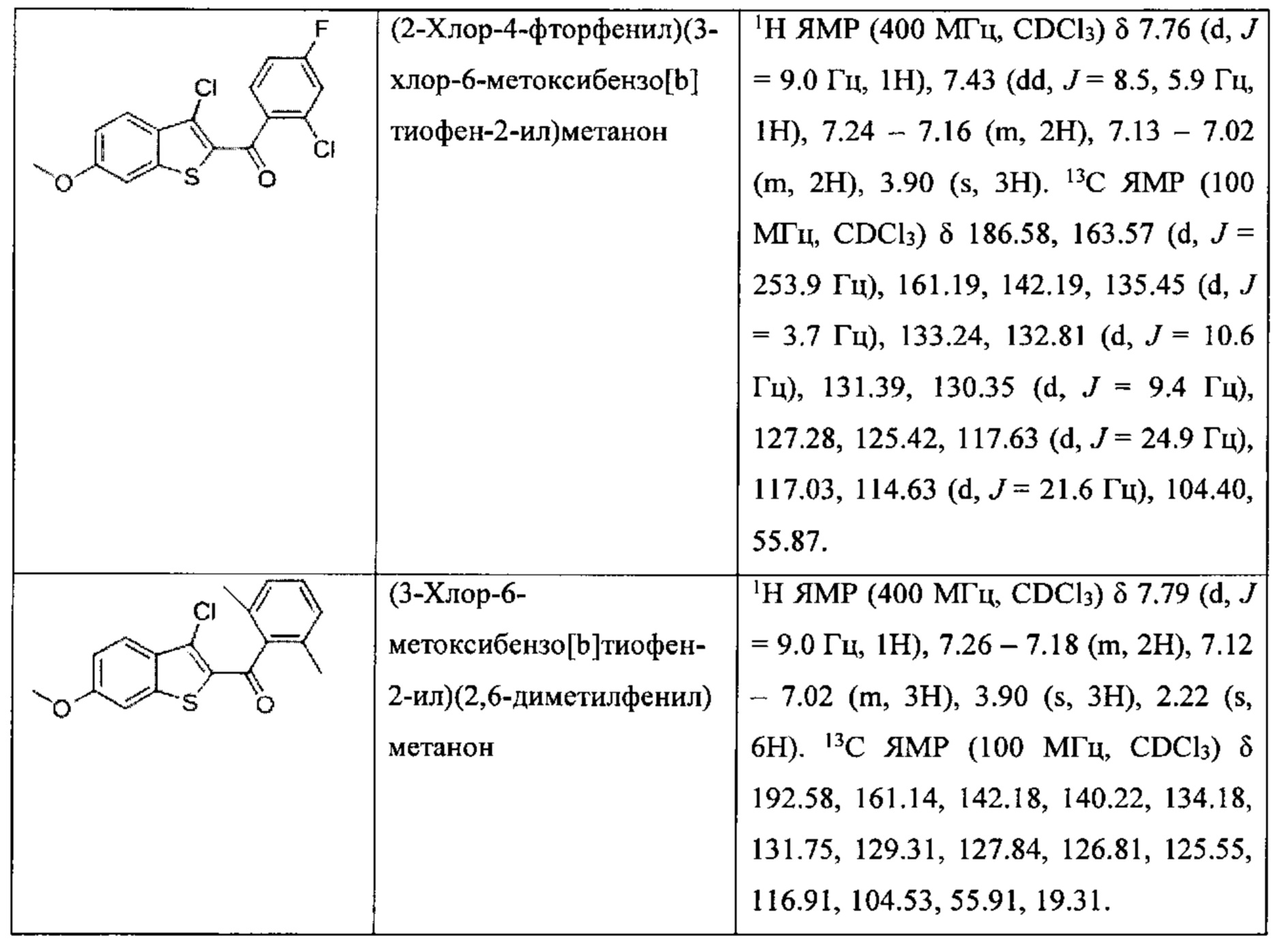
Соединение I-4: (3-(4-Бромфенокси)-6-метоксибензо[b]тиофен-2-ил)(4-фтор-2-метилфенил)метанон
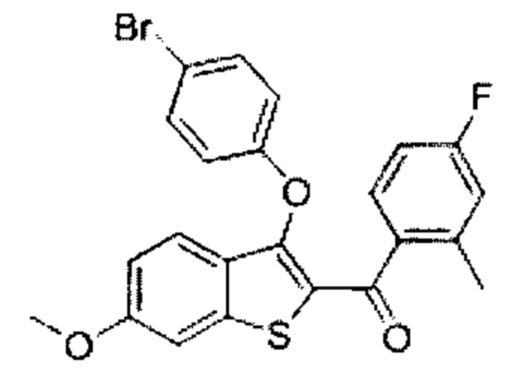
Cs2CO3 (1,52 г, 4,67 ммоль) добавляли одной порцией к раствору промежуточного соединения 2 (520 мг, 1,56 ммоль) и 4-бромфенола в 5 мл DMF. Температуру реакционной смеси повышали до 50°C и после перемешивания в течение всей ночи реакционную смесь гасили ледяной водой, экстрагировали этилацетатом и промывали солевым раствором. Органические экстракты объединяли, сушили над безводным Na2SO4, концентрировали в вакууме и очищали методом хроматографии (1%-15% этилацетата в гексане) с получением 490 мг белого твердого вещества (67%).1Н ЯМР (400 МГц, CDCl3) δ 7.43 (d, J=8.9 Гц, 1H), 7.34-7.27 (m, 2Н), 7.22-7.17 (m, 2Н), 6.96 (dd, J=8.9, 2.2 Гц, 1Н), 6.80-6.76 (m, 2Н), 6.40-6.33 (m, 2Н), 3.91 (s, 3Н), 2.16 (s, 3Н).13С ЯМР (100 МГц, CDCl3) δ 189.34, 163.72 (d, J=250.2 Гц), 161.07, 157.45, 148.25, 142.21, 139.63 (d, J=8.6 Гц), 135.29 (d, J=3.1 Гц), 132.38, 130.24 (d, J=9.2 Гц), 126.82, 127.48, 124.57, 117.45 (d, J=21.4 Гц), 116.74, 116.55, 115.09, 112.19 (d, J=21.7 Гц), 105.19, 55.89, 19.53 (d, J=1.3 Гц).
Следующие соединения получали аналогичной процедурой с применением соответствующих исходных веществ:
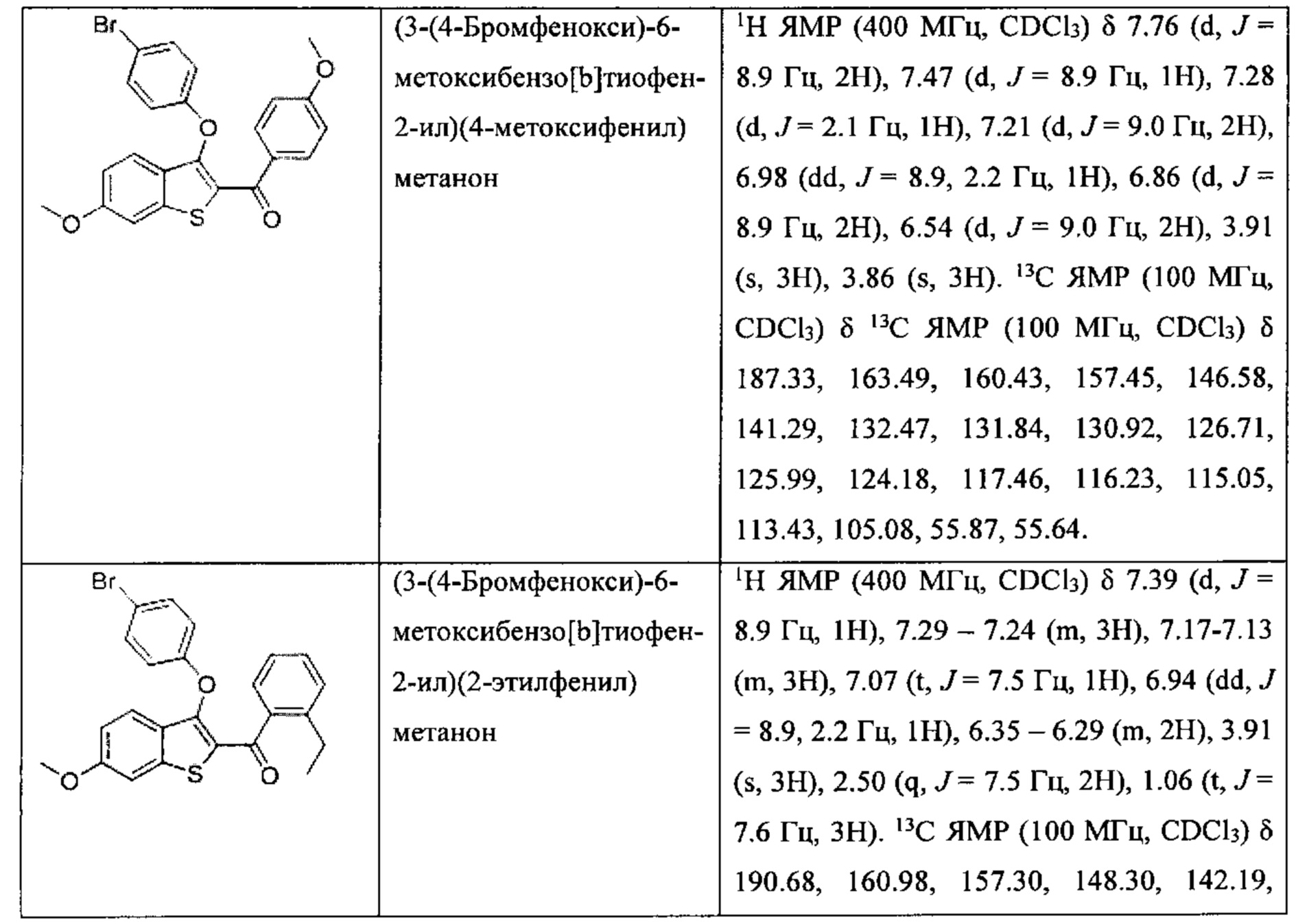
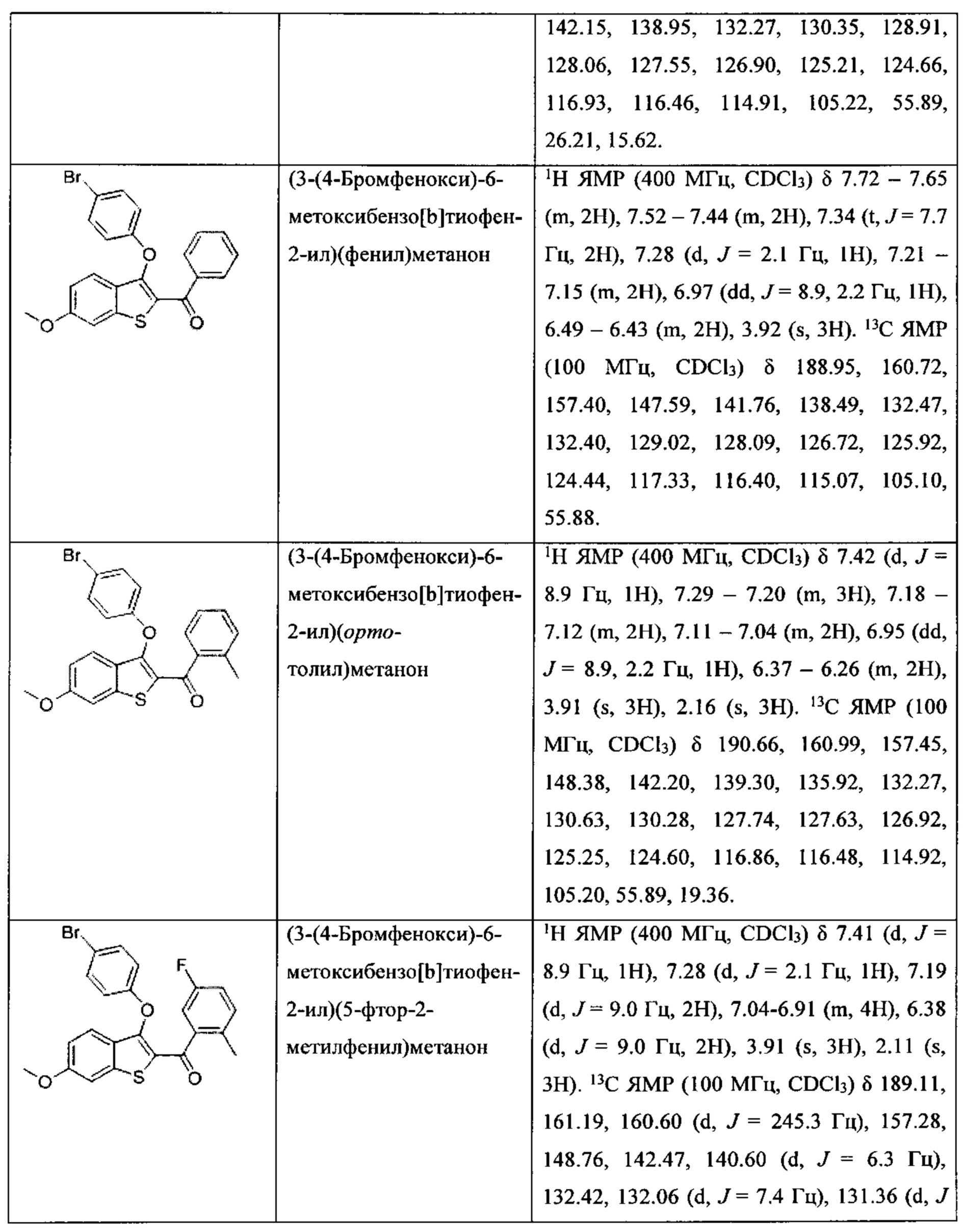
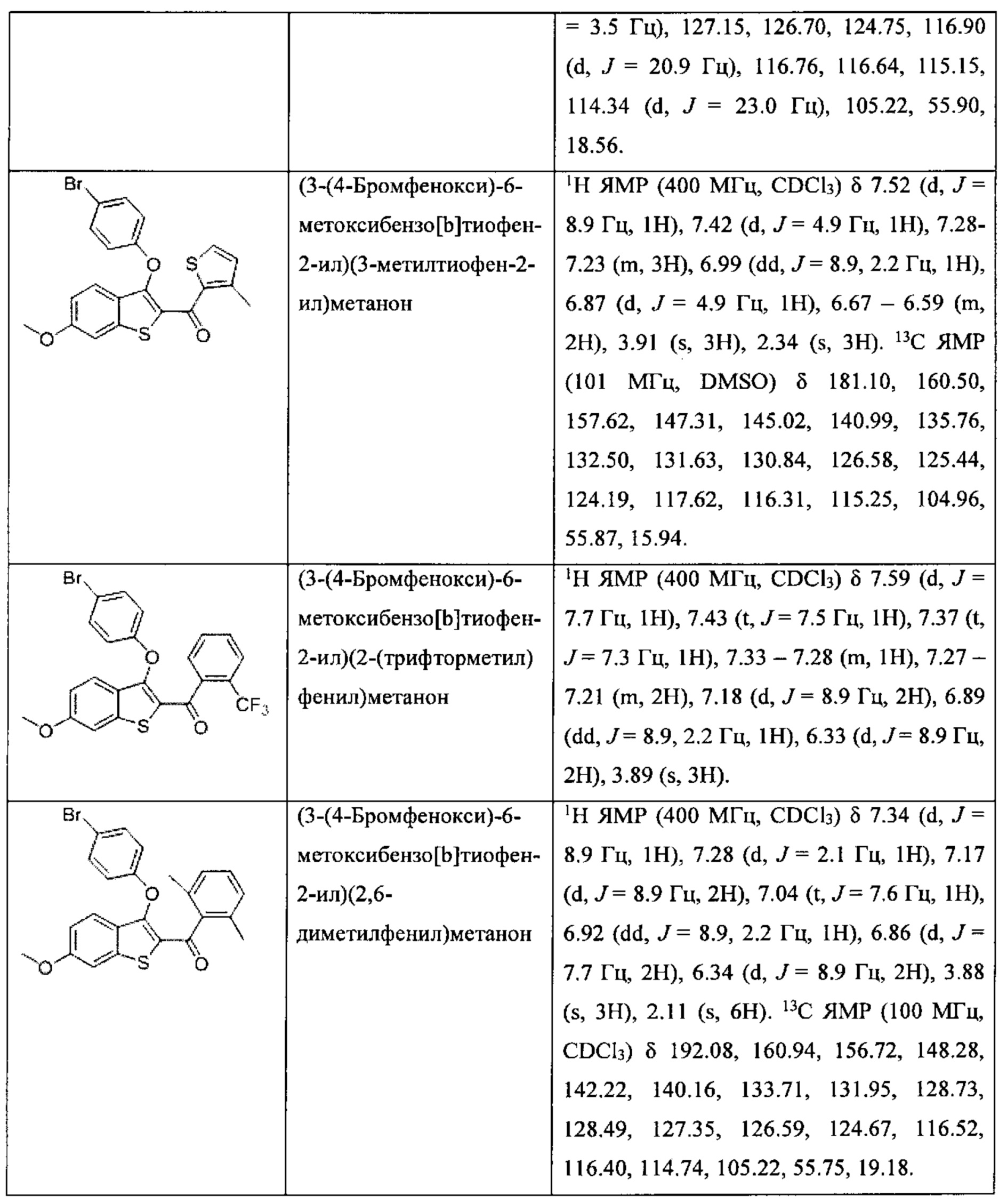
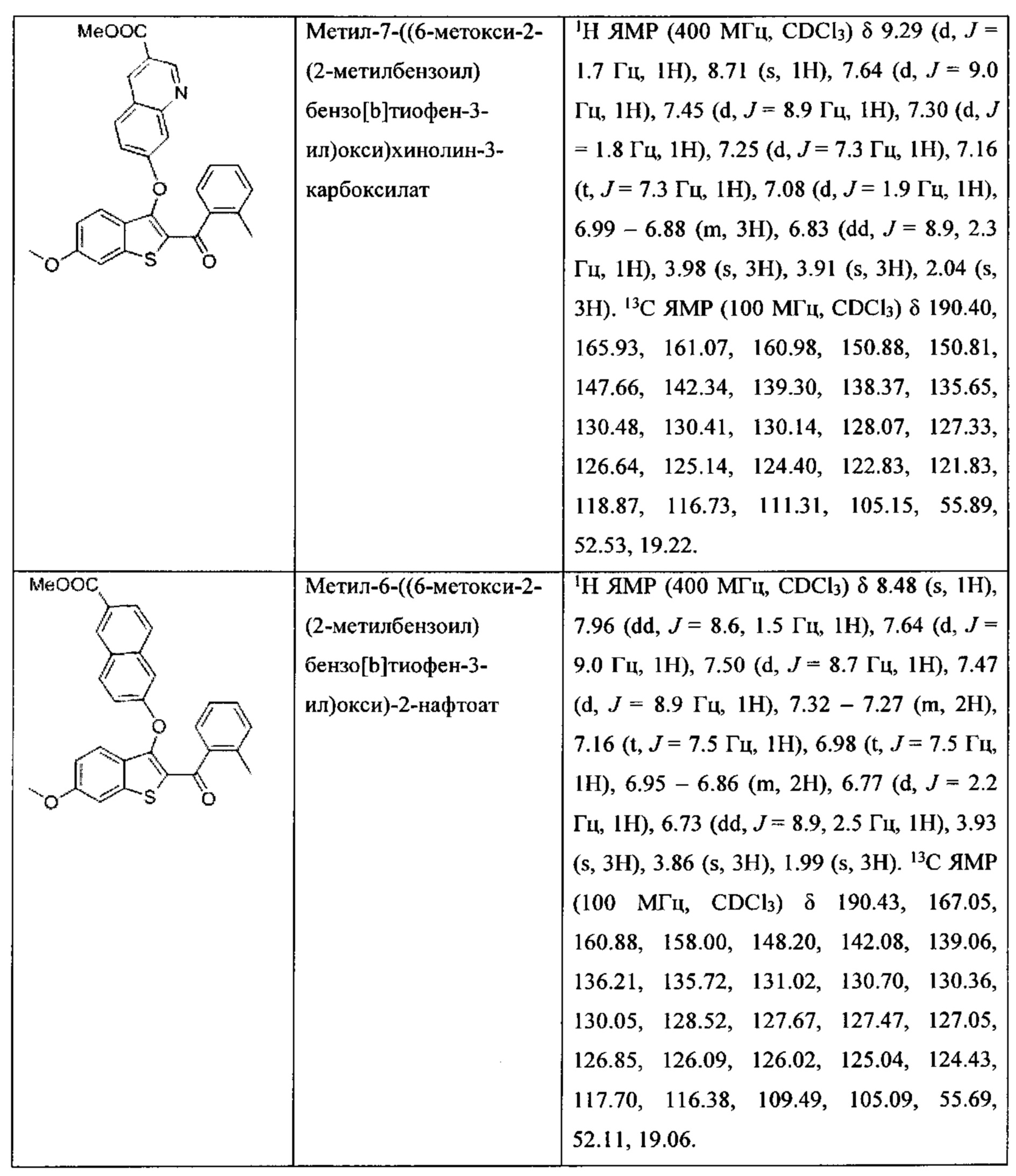
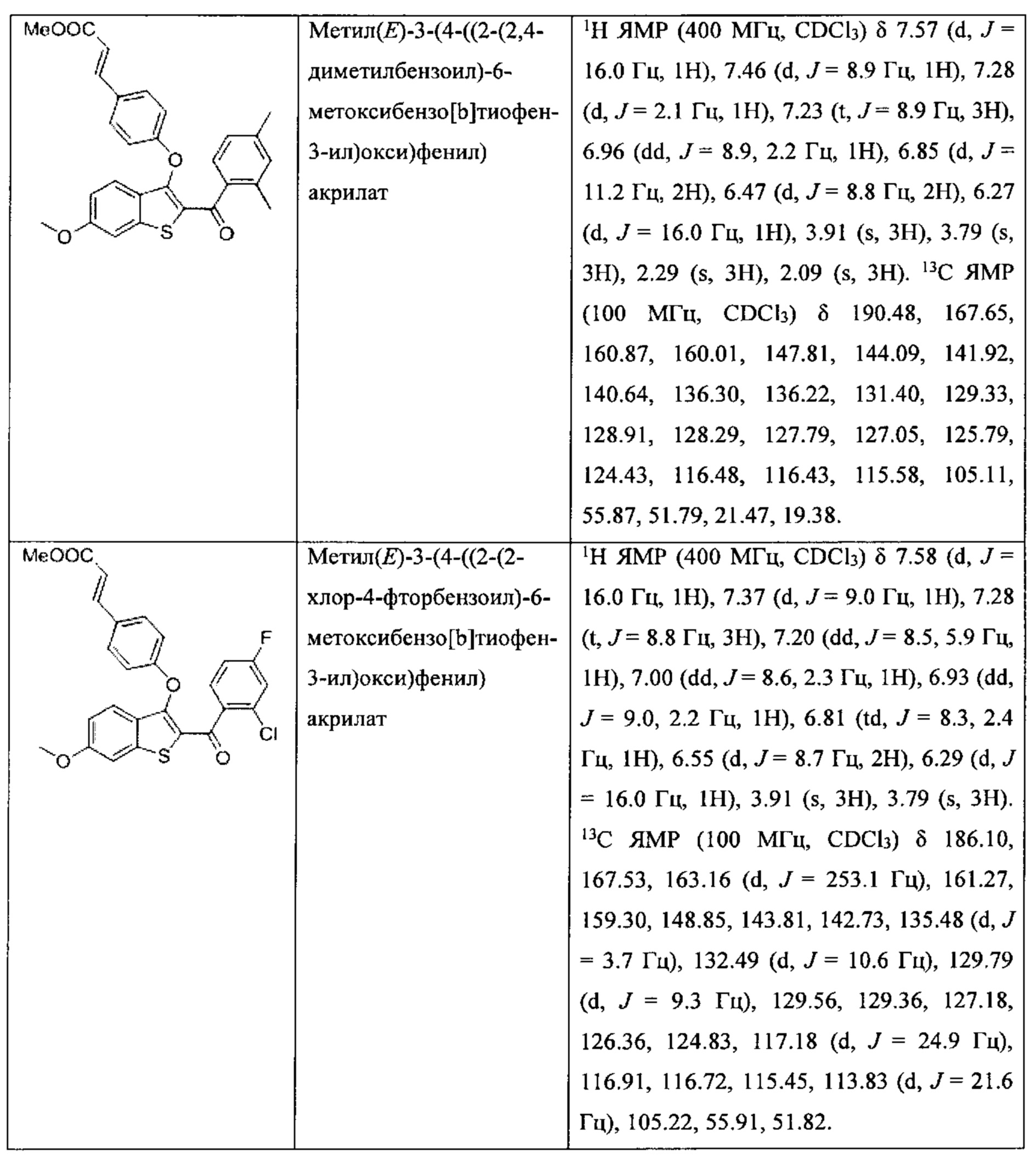
Соединение I-5: (3-(4-Бромфенокси)-6-гидроксибензо[b]тиофен-2-ил)(4-фтор-2-метилфенил)метанон
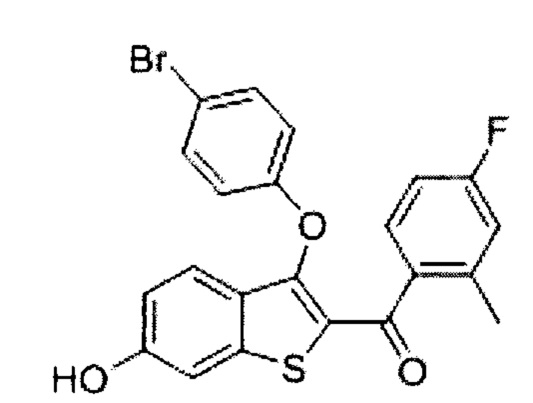
Соединение I-4 (480 мг, 1 ммоль) растворяли в 10 мл безводного дихлорметана при комнатной температуре и к этому раствору по каплям добавляли BF3⋅SMe2 (1,2 мл, 5 ммоль). Реакционную смесь перемешивали до израсходования исходного вещества, как наблюдали при помощи TLC. Реакцию затем гасили насыщенным NaHCO3/ледяной водой, экстрагировали этилацетатом и промывали солевым раствором. Органические экстракты объединяли, сушили над безводным Na2SO4, концентрировали в вакууме и очищали методом хроматографии (5%-60% этилацетата в гексане) с получением 390 мг в виде белого порошка (85%).1Н ЯМР (400 МГц, MeOD) δ 7.38 (d, J=8.8 Гц, 1Н), 7.35-7.28 (m, 1H), 7.28-7.20 (m, 3Н), 6.90 (dd, J=8.8, 2.1 Гц, 1H), 6.87-6.80 (m, 2H), 6.46-6.38 (m, 2H), 2.13 (s, 3H).
Следующие соединения получали аналогичной процедурой с применением соответствующих исходных веществ:
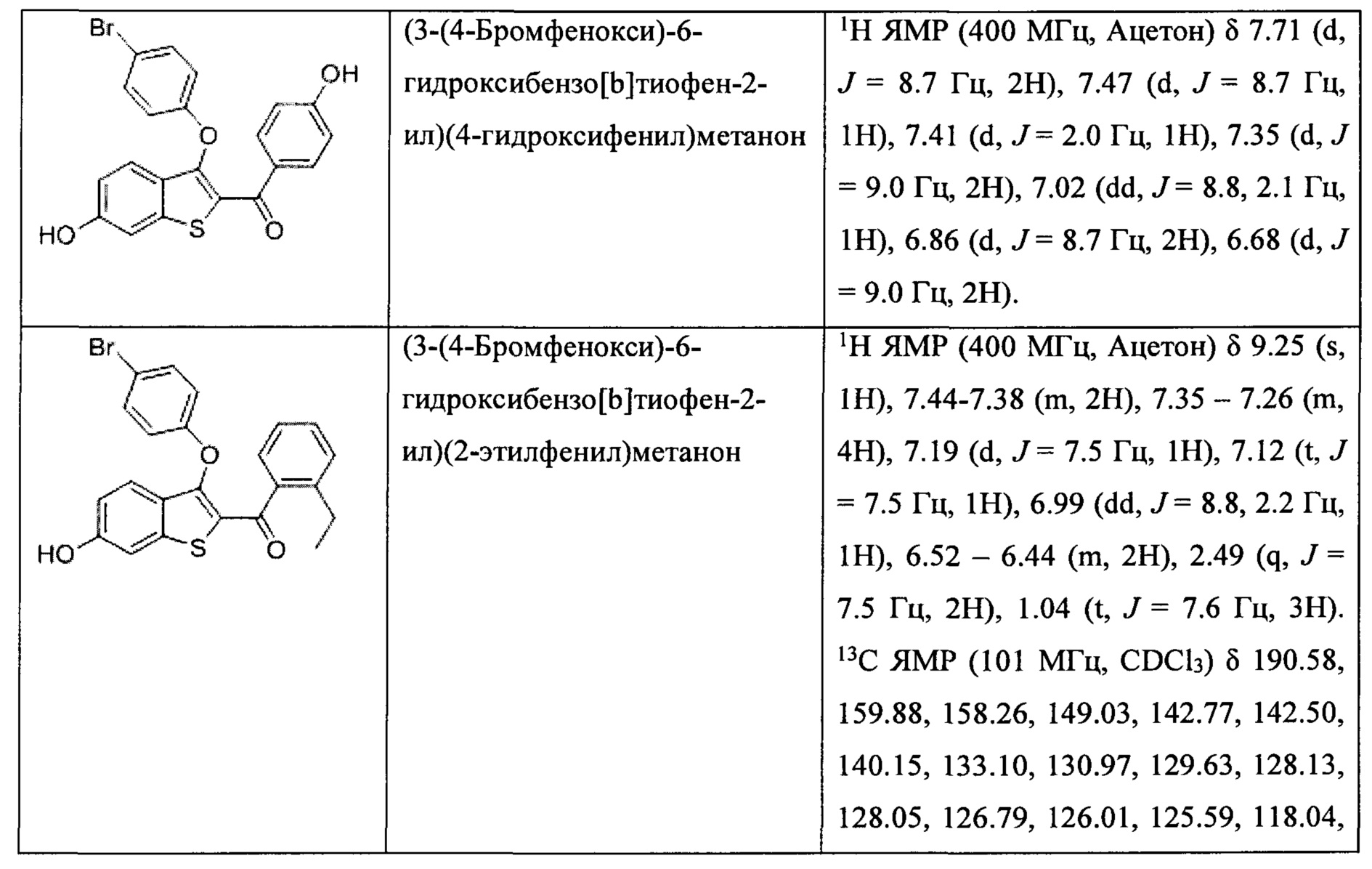
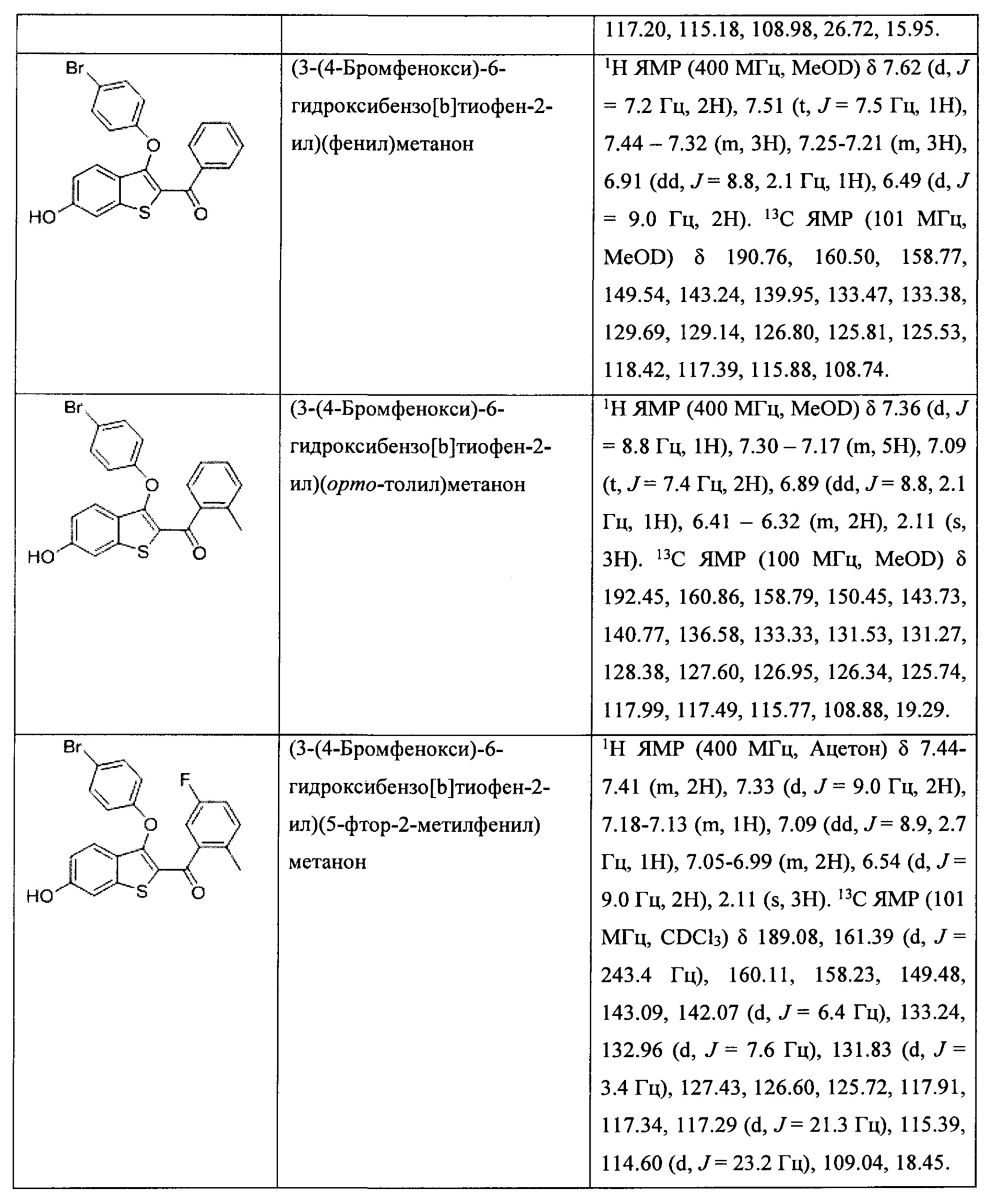
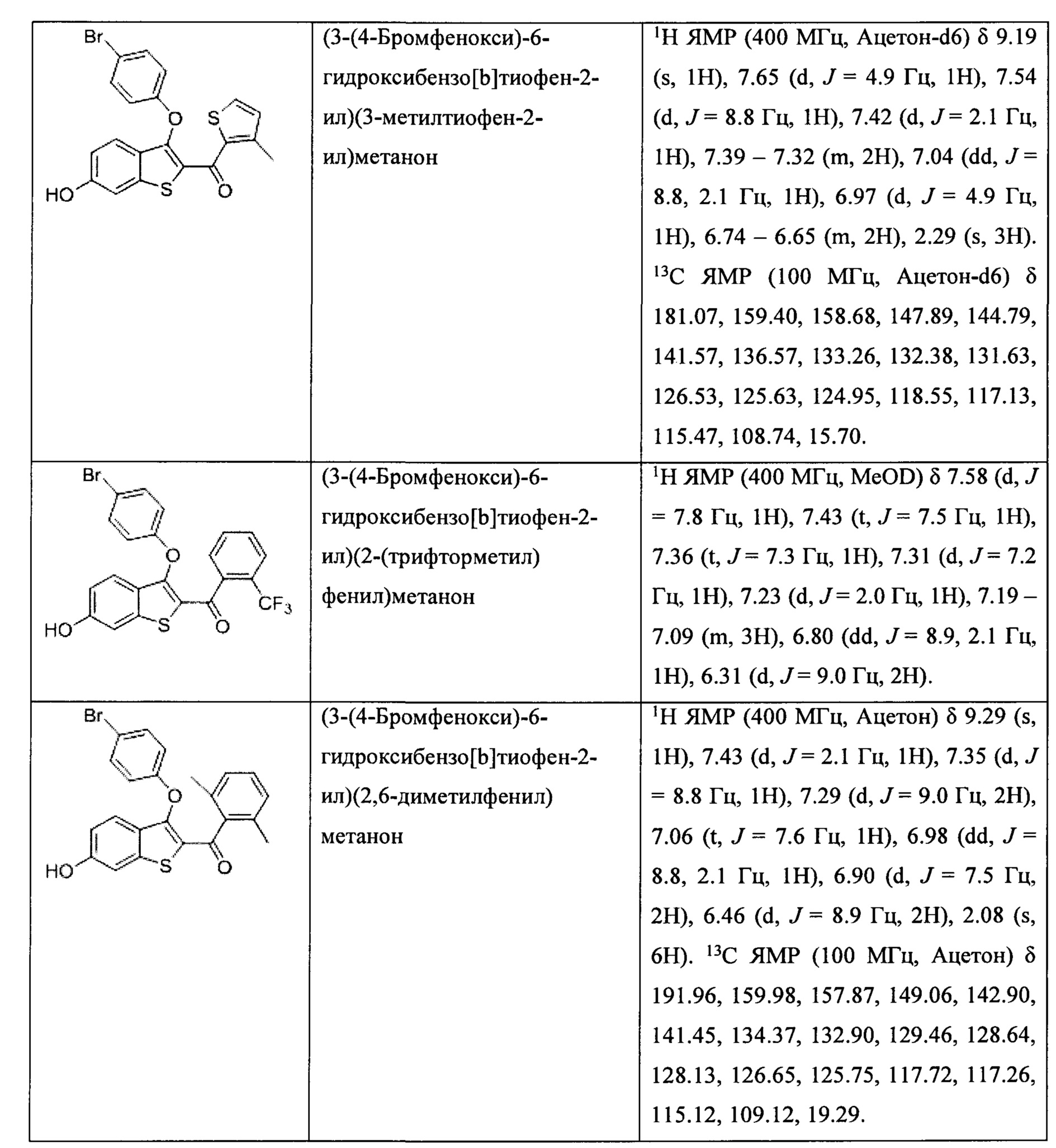
Соединение I-6: Метил(E)-3-(4-((2-(4-фтор-2-метилбензоил)-6-гидроксибензо[b]тиофен-3-ил)окси)фенил)акрилат
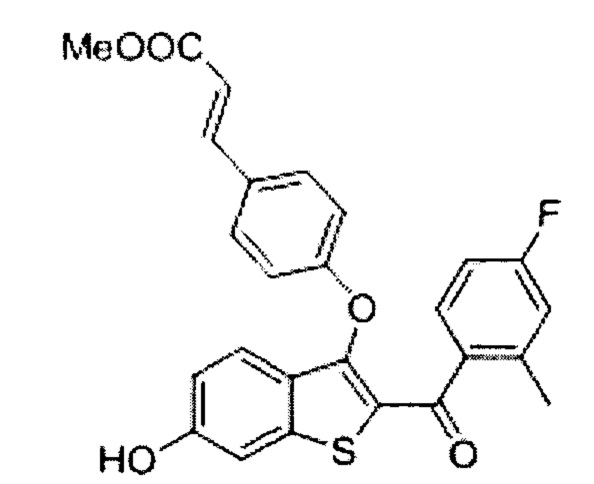
В закупоренной пробирке соединение I-5 (200 мг, 0,46 ммоль), метилакрилат (240 мг, 2,76 ммоль) и Pd(PPh3)2Cl2 суспендировали в DMF (2 мл) и триэтиламине (235 мг, 2,3 ммоль). Реакционную смесь нагревали при 110°C в течение 6 часов. Реакционную смесь гасили водой и экстрагировали этилацетатом. Органические слои собирали и очищали методом флеш-хроматографии (5%-60% этилацетата в гексане) с получением 170 мг в виде белого порошка (85%).1Н ЯМР (400 МГц, MeOD) δ 7.57 (d, J=16.0 Гц, 1Н), 7.40-7.36 (m, 3Н), 7.32 (dd, J=8.8, 6.0 Гц, 1Н), 7.27 (d, J=1.8 Гц, 1Н), 6.89 (m J=8.9, 1.9 Гц, 1Н), 6.83-6.78 (m, 2Н), 6.52 (d, J=8.7 Гц, 2Н), 6.37 (d, J=16.0 Гц, 1Н), 3.76 (s, 3Н), 2.10 (s, 3Н).13С ЯМР (100 МГц, MeOD) δ 191.09, 169.17, 164.95 (d, J=248.7 Гц), 161.19, 160.91, 150.13, 145.22, 143.71, 140.41 (d, J=8.6 Гц), 136.86 (d, J=3.0 Гц), 131.11 (d, J=9.2 Гц), 130.77, 130.47, 127.59, 126.92, 125.70, 118.13 (d, J=21.8 Гц), 117.55, 117.48, 116.47, 113.11 (d, J=21.9 Гц), 108.89, 52.09, 19.41.
Следующие соединения получали аналогичной процедурой с применением соответствующих исходных веществ:

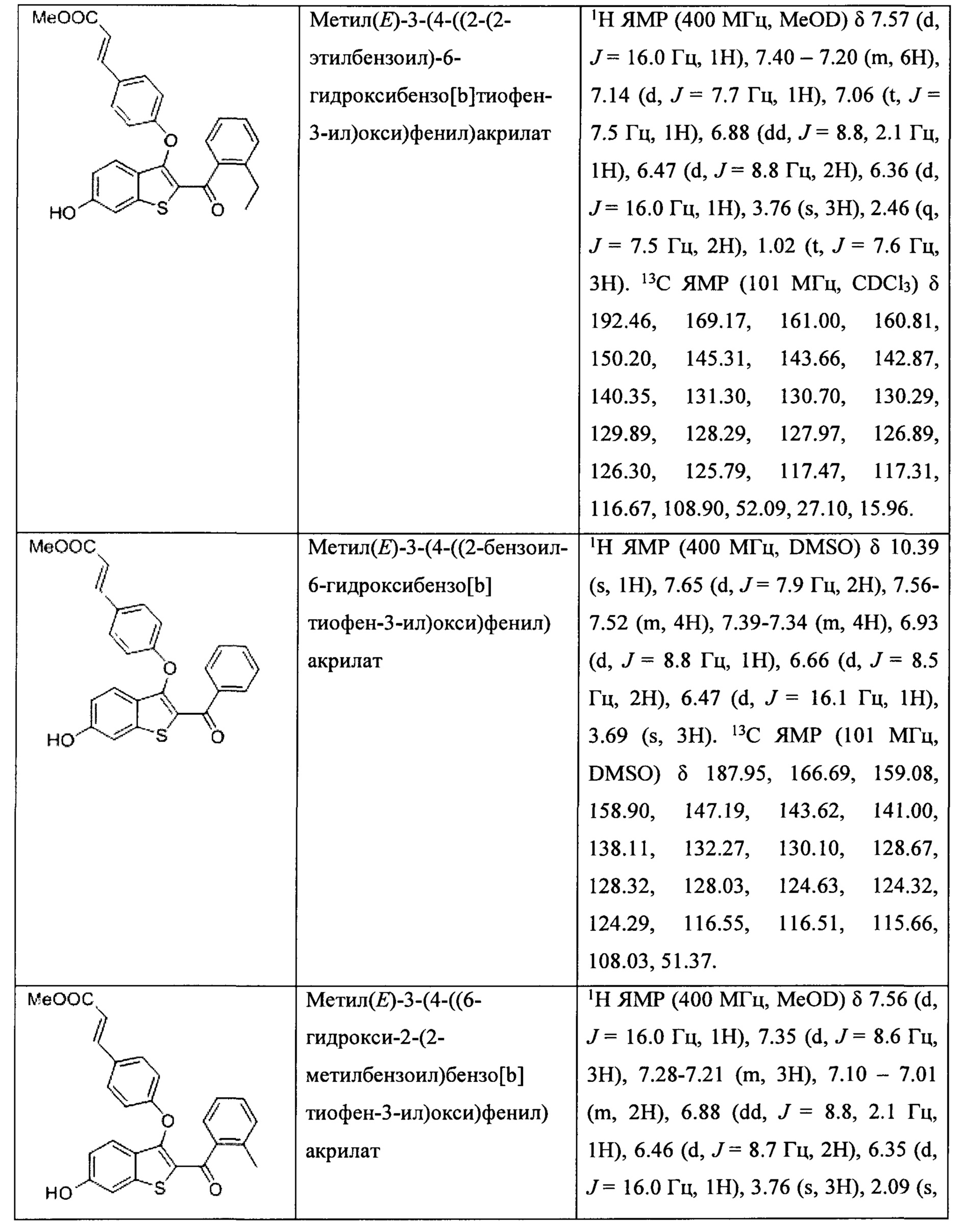
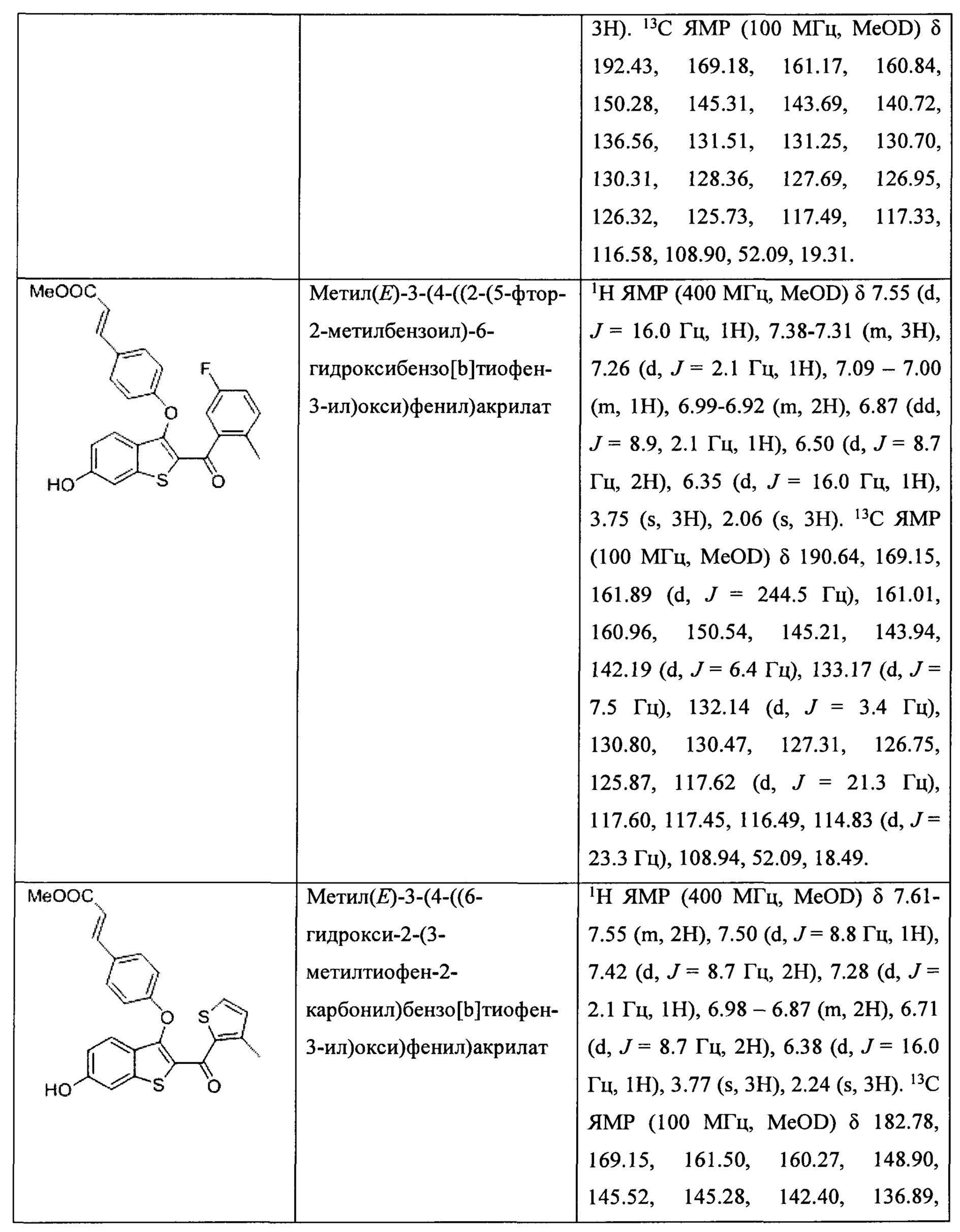
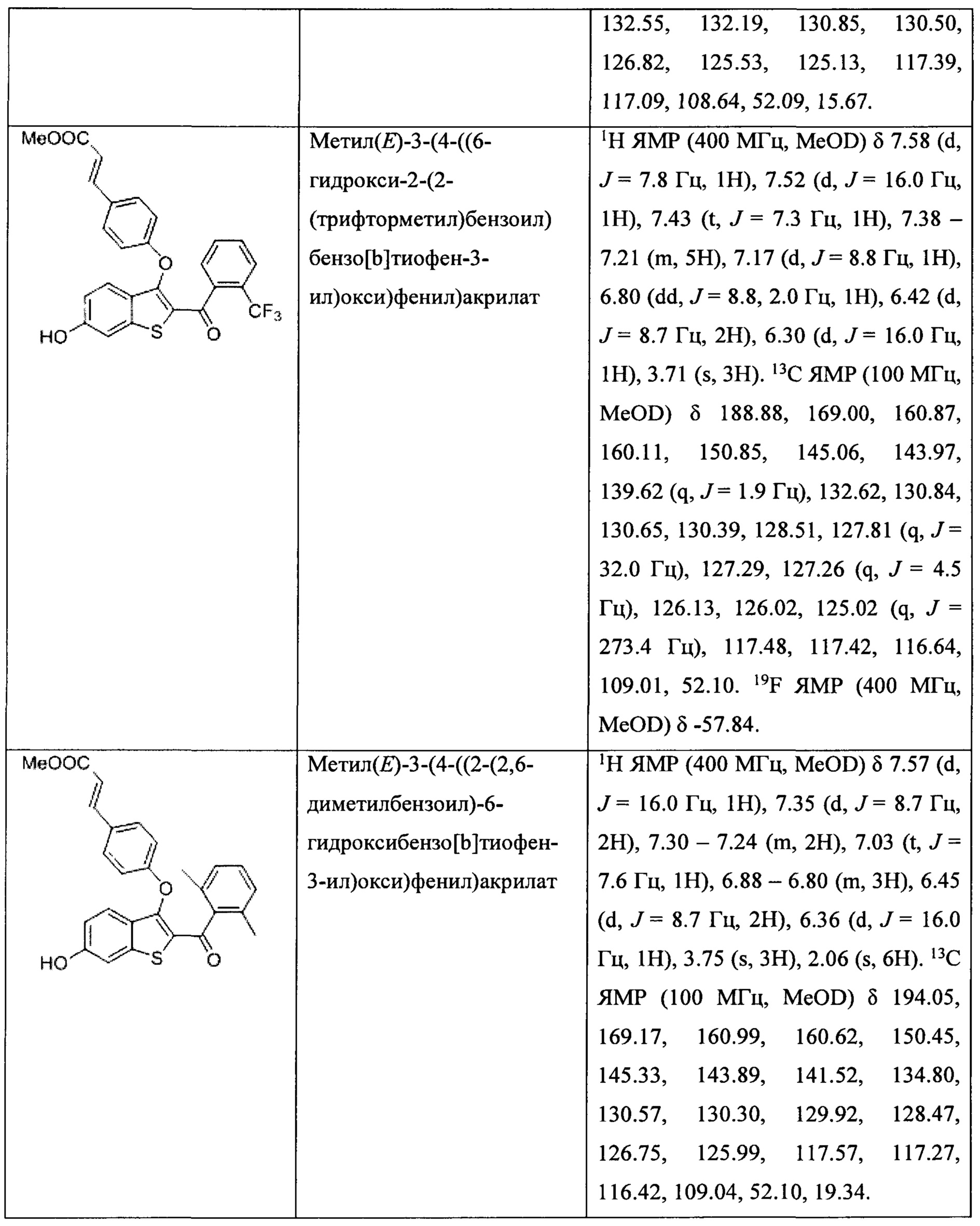
Пример 1: Процедуры синтеза характерных соединений
(E)-3-(4-((2-(4-Фтор-2-метилбензоил)-6-гидроксибензо[b]тиофен-3-ил)окси)фенил)акриловая кислота (соединение 1)
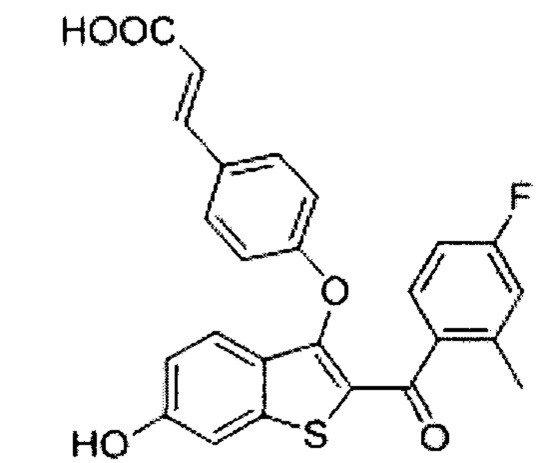
К раствору соединения I-6 (75 мг, 0,16 ммоль) в метаноле (2 мл) по каплям добавляли 10% раствор LiOH (2 мл). За реакцией наблюдали при помощи TLC и как только при помощи TLC отмечали расходование исходных веществ, реакцию гасили 1 н HCl/ледяной водой. После перемешивания в течение 10 минут смесь экстрагировали этилацетатом. Органические слои собирали и очищали методом С18 хроматографии (5%-60% этилметанола в воде) с получением 71 мг в виде белого порошка (99%).1Н ЯМР (400 МГц, CDCl3) δ 7.58 (d, J=16.0 Гц, 1H), 7.37 (d, J=9.0 Гц, 1H), 7.28 (t, J=8.8 Гц, 3Н), 7.20 (dd, J=8.5, 5.9 Гц, 1Н), 7.00 (dd, J=8.6, 2.3 Гц, 1H), 6.93 (dd, J=9.0, 2.2 Гц, 1H), 6.81 (td, J=8.3, 2.4 Гц, 1H), 6.55 (d, J=8.7 Гц, 2Н), 6.29 (d, J=16.0 Гц, 1H), 3.91 (s, 3Н), 3.79 (s, 3Н).13С ЯМР (100 МГц, CDCl3) δ 186.10, 167.53, 163.16 (d, J=253.1 Гц), 161.27, 159.30, 148.85, 143.81, 142.73, 135.48 (d, J=3.7 Гц), 132.49 (d, J=10.6 Гц), 129.79 (d, J=9.3 Гц), 129.56, 129.36, 127.18, 126.36, 124.83, 117.18 (d, J=24.9 Гц), 116.91, 116.72, 115.45, 113.83 (d, J=21.6 Гц), 105.22, 55.91, 51.82.
Соединения 2-8 и 11-22 получали аналогичной процедурой, используемой для синтеза соединения 1 с применением соответствующих исходных веществ. Характеристика этих соединений представлена ниже в таблице 1.
Соединение 9: 5-((6-Гидрокси-2-(2-метилбензоил)бензо[b]тиофен-3-ил)окси)-2-нафтойная кислота
Соединение 4 (100 мг, 0,21 ммоль) растворяли в 3 мл безводного дихлорметана при комнатной температуре в атмосфере аргона. Раствор охлаждали с применением бани с ледяной водой и по каплям добавляли BF3⋅SMe2 (1 мл, 4,2 ммоль). После перемешивания в течение 30 минут раствор оставляли нагреваться до 35°C. Реакционную смесь перемешивали до израсходования исходных веществ, как наблюдали при помощи TLC, а затем гасили насыщенным NaHCO3/ледяной водой. Реакционную смесь экстрагировали этилацетатом и промывали солевым раствором. Органические экстракты объединяли, сушили над безводным Na2SO4, концентрировали в вакууме и очищали методом флеш-хроматографии (5%-60% этилацетат в гексане) с получением 37 мг белого порошка (38%).1Н ЯМР (400 МГц, MeOD) δ 8.47 (s, 1H), 7.93 (d, J=8.4 Гц, 1Н), 7.72 (d, J=8.9 Гц, 1Н), 7.56 (d, J=8.4 Гц, 1Н), 7.40 (d, J=8.8 Гц, 1Н), 7.30 (d, J=1.9 Гц, 1Н), 7.28-7.08 (m, 2H), 7.01 (t, J=7.4 Гц, 1Н), 6.94 (d, J=7.6 Гц, 1Н), 6.88 (dd, J=8.8, 2.1 Гц, 1Н), 6.79 (s, 1Н), 6.74 (dd, J=8.9, 2.4 Гц, 1Н), 1.95 (s, 3Н).13С ЯМР (100 МГц, MeOD) δ 192.50, 169.84, 160.87, 159.24, 150.50, 143.78, 140.65, 137.54, 136.54, 132.21, 131.70, 131.42, 131.18, 130.09, 128.34, 128.08, 127.69, 127.38, 127.05, 126.27, 125.78, 118.69, 117.51, 110.58, 108.92, 19.19. ESI-HRMS (m/z): [M+H]+ рассчит. для C27H18O5S: 455.0953; обнаружено 455.0939.
Соединение 10: 8-((6-Гидрокси-2-(2-метилбензоил)бензо[b]тиофен-3-ил)окси)хинолин-3-карбоновая кислота
Соединение 24 получали процедурой для синтеза соединения 9 с получением 33 мг (57%).1H ЯМР (400 МГц, MeOD) δ 9.20 (s, 1Н), 8.85 (s, 1Н), 7.83 (d, J=9.0 Гц, 1Н), 7.44 (d, J=8.8 Гц, 1Н), 7.31 (s, 1Н), 7.27-7.13 (m, 2H), 7.04-6.81 (m, 5H), 1.97 (s, 3H).13С ЯМР (100 МГц, MeOD с паром TFA) δ 192.08, 165.75, 162.47, 161.00, 151.79, 151.11, 149.43, 143.78, 140.53, 140.32, 136.47, 132.26, 131.43, 131.32, 128.29, 127.90, 126.64, 126.32, 125.56, 124.53, 119.98, 117.75, 110.96, 108.96, 19.21. ESI-HRMS (m/z): [M+Н]+ рассчит. для C26H17NO5S: 456.0906; обнаружено 456.0893.
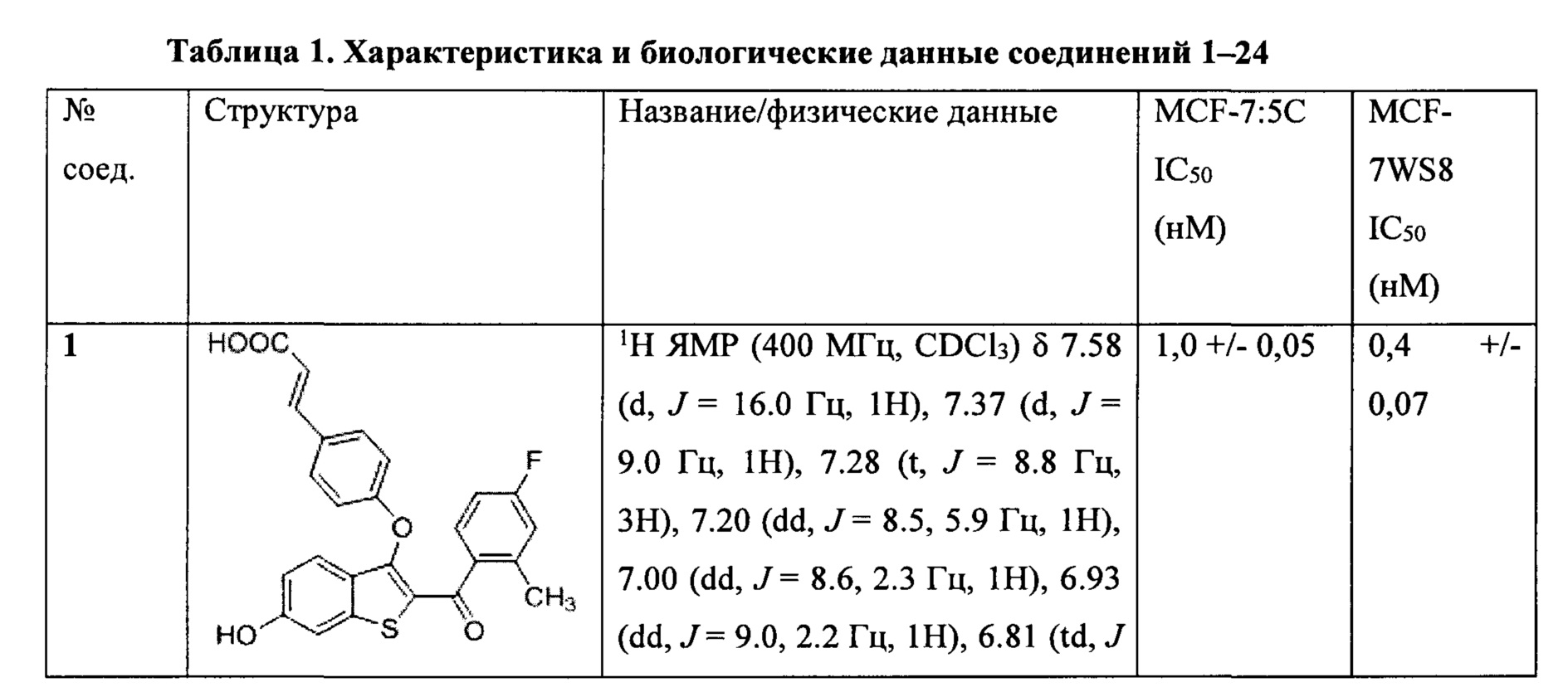
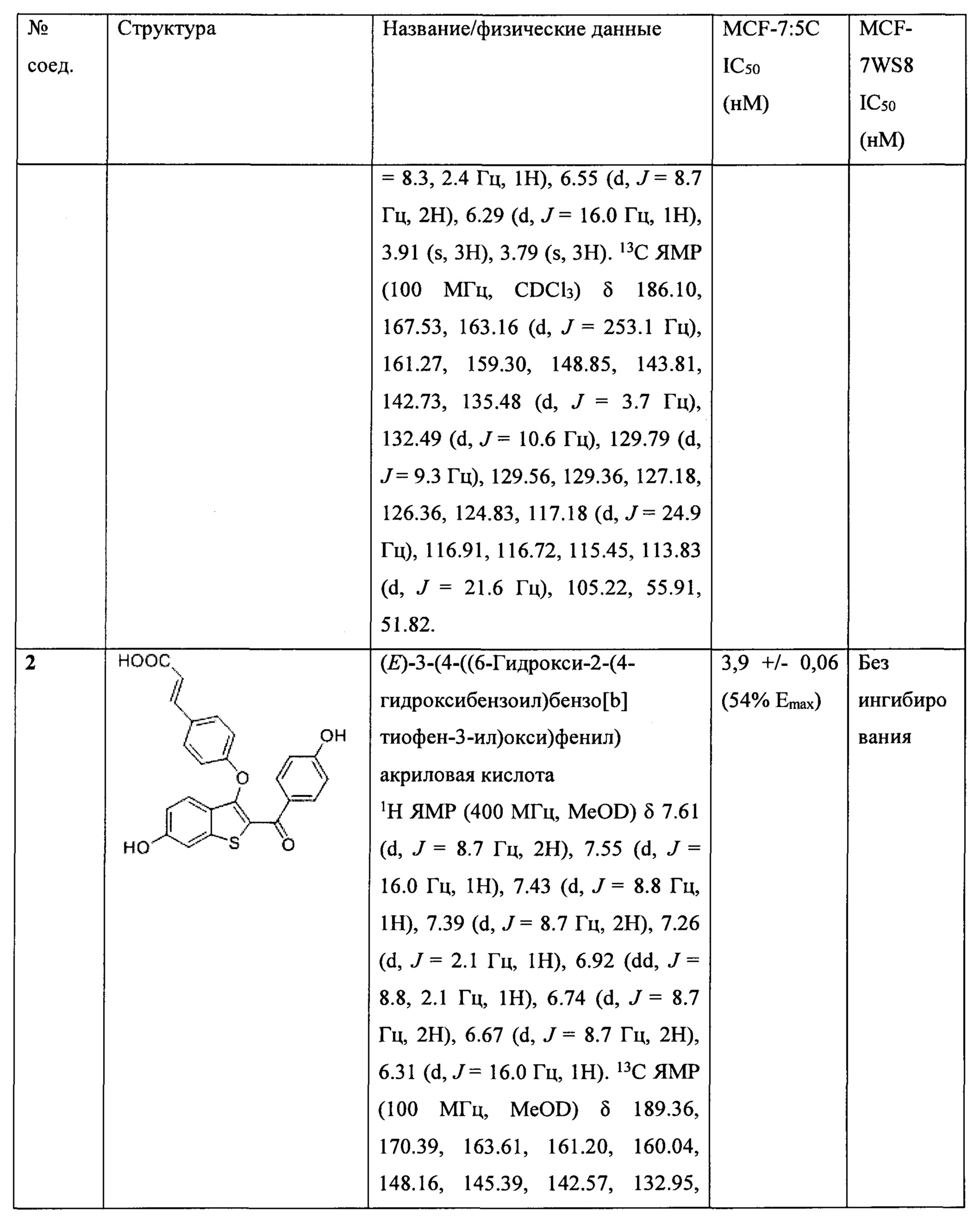
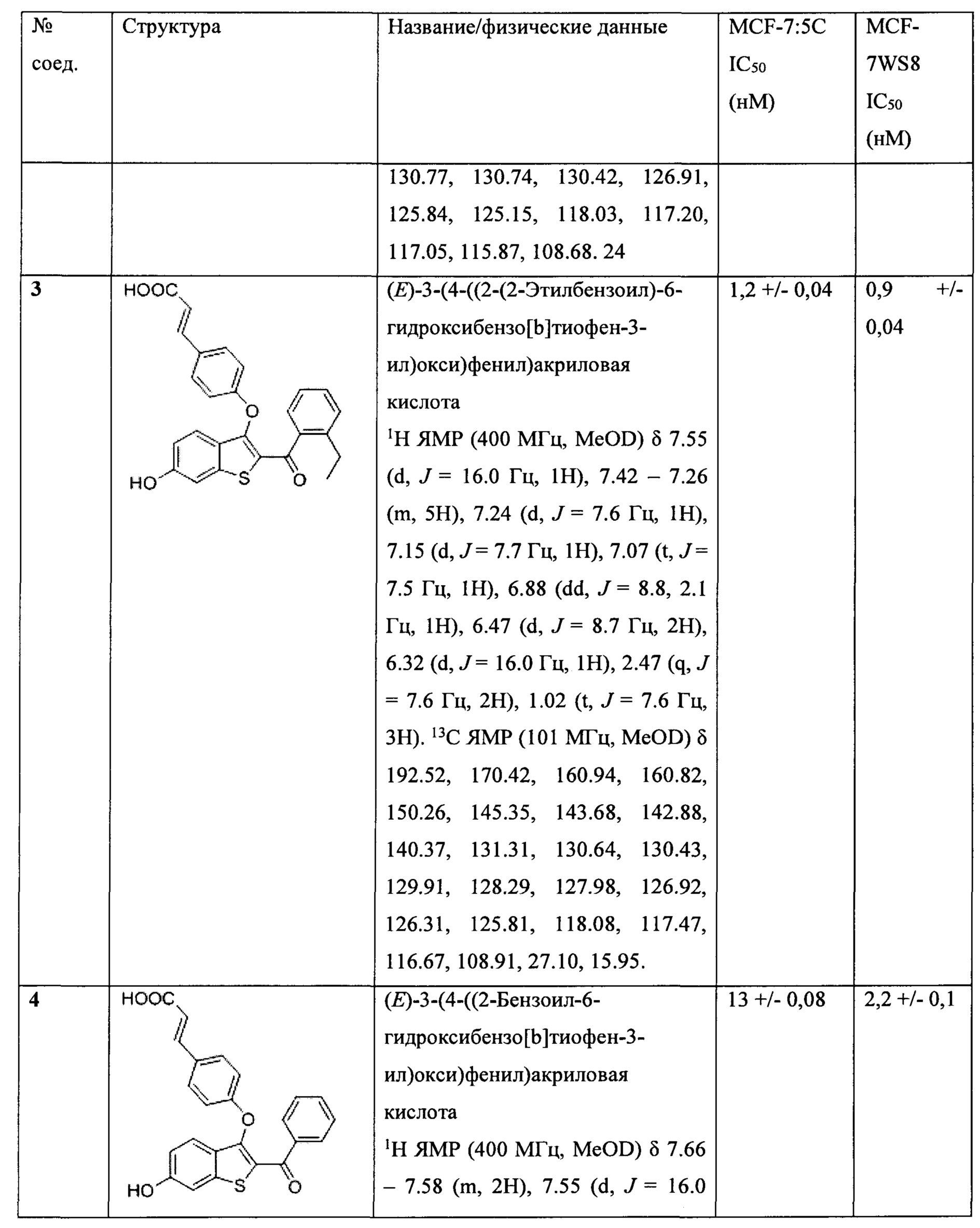
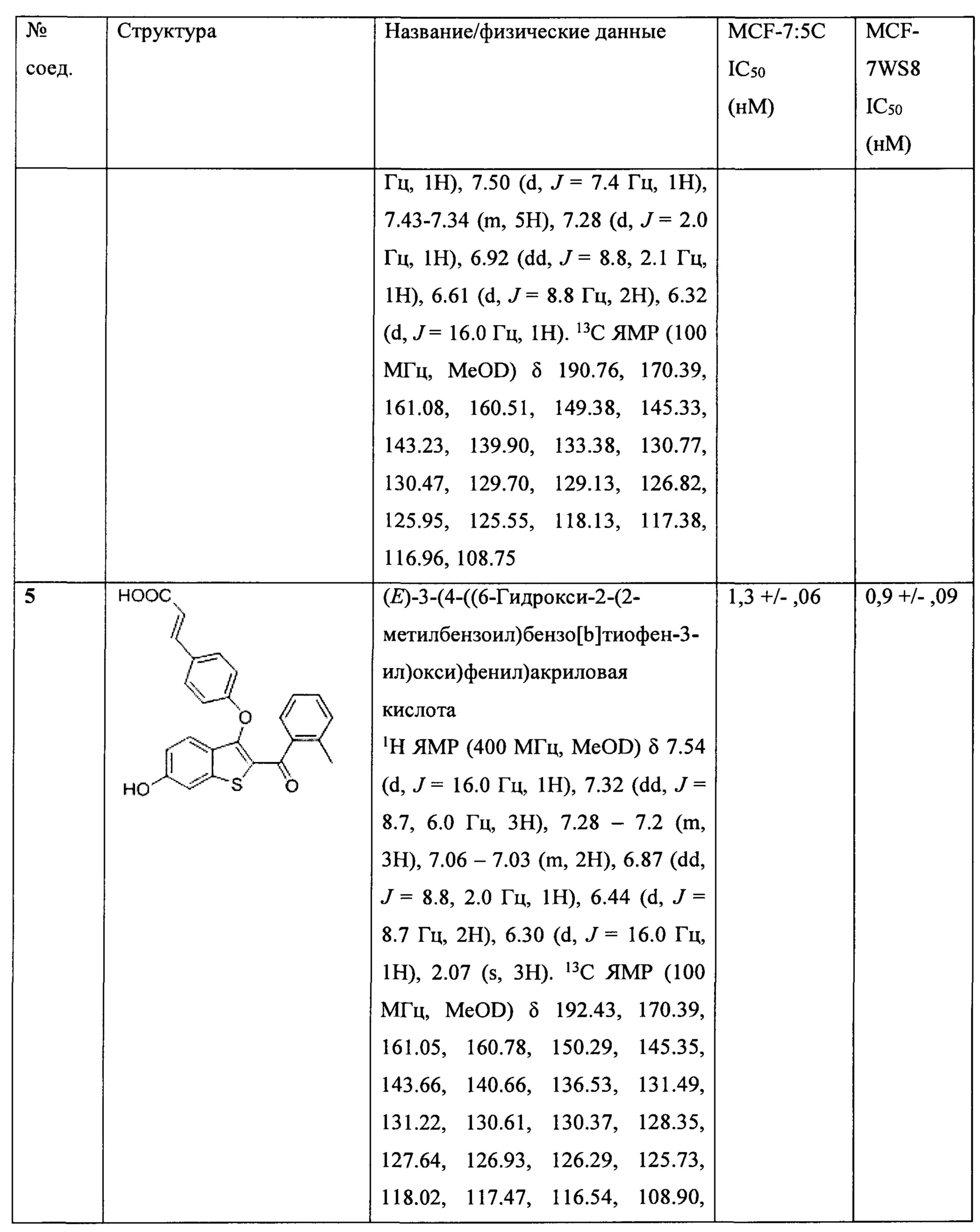
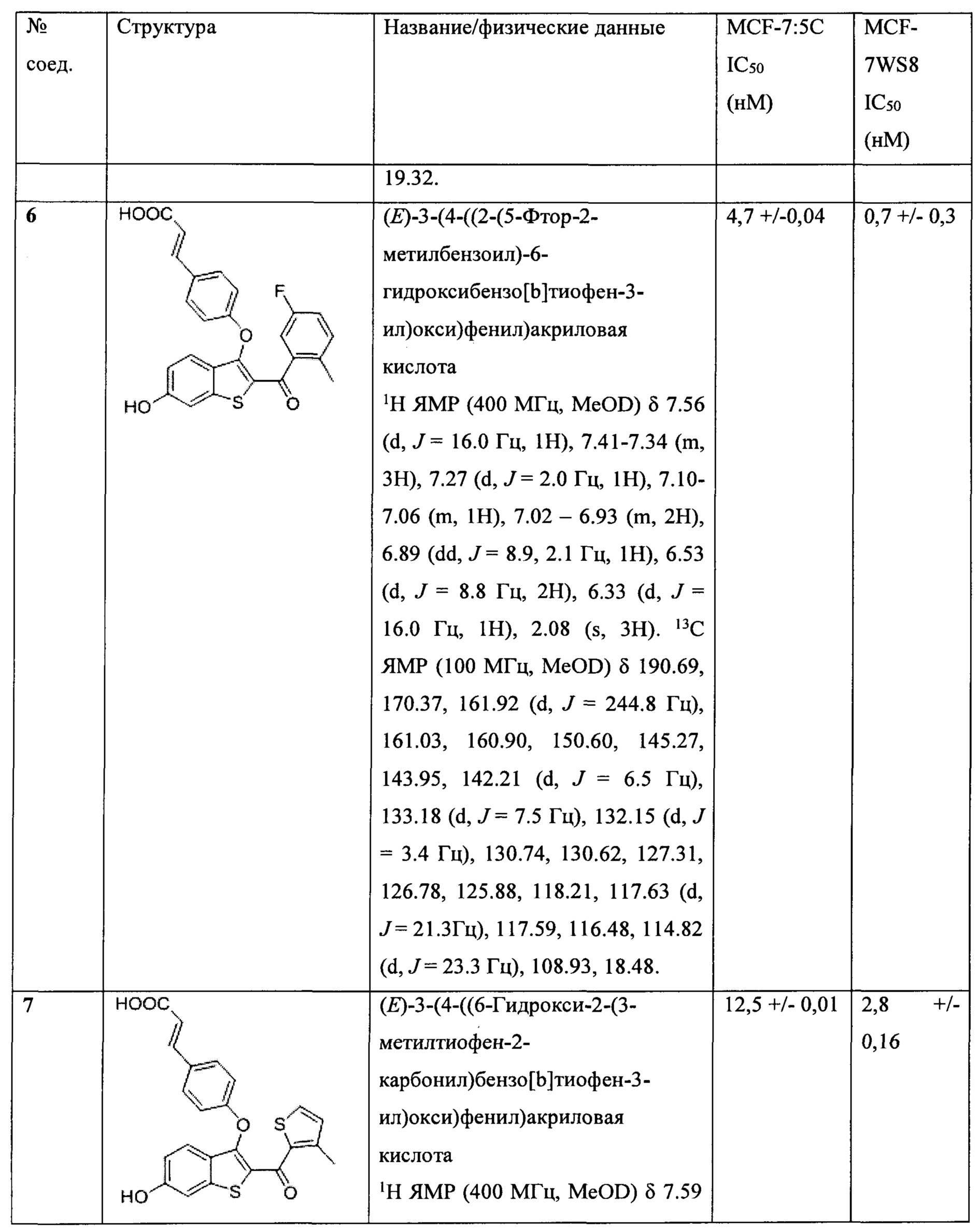
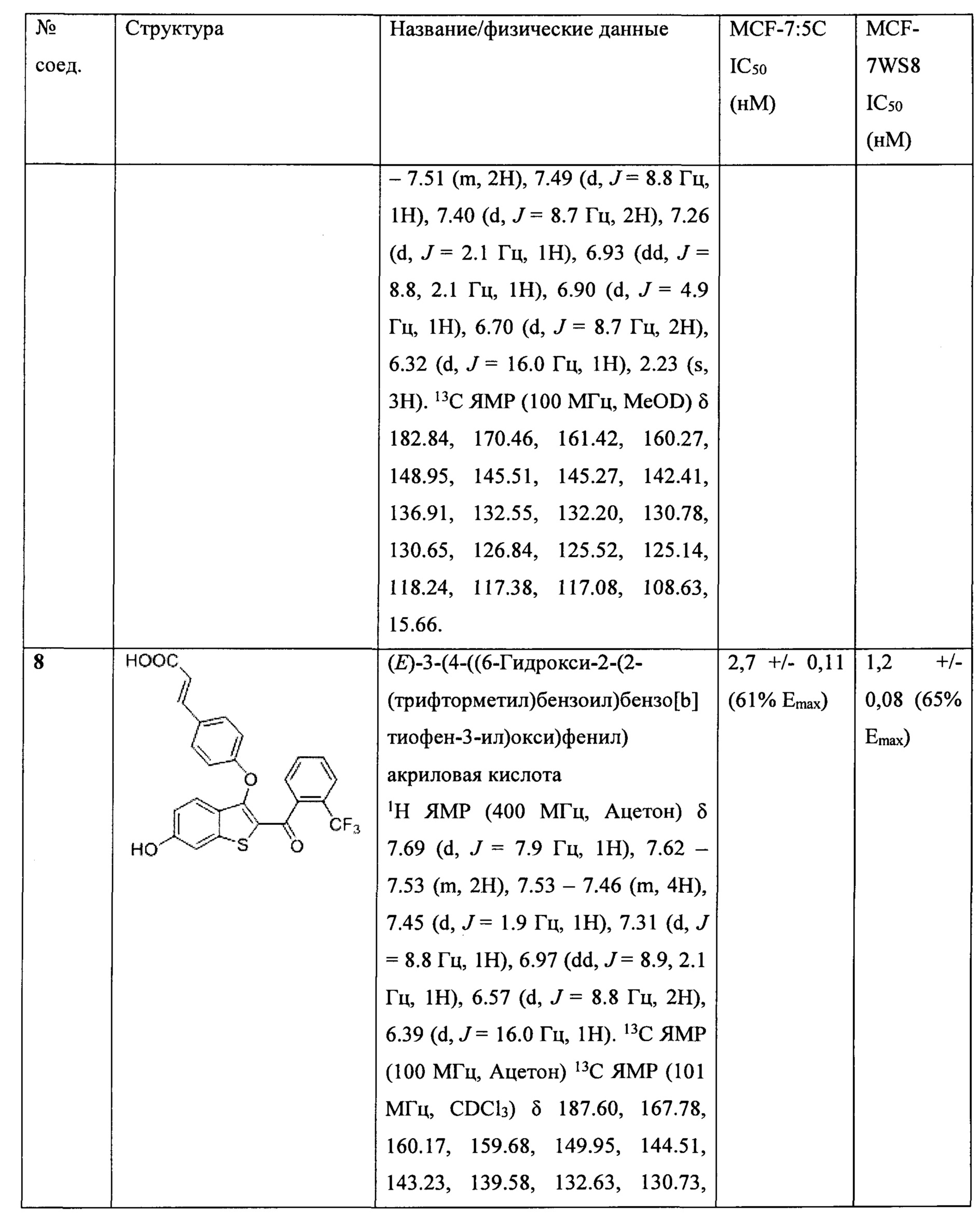
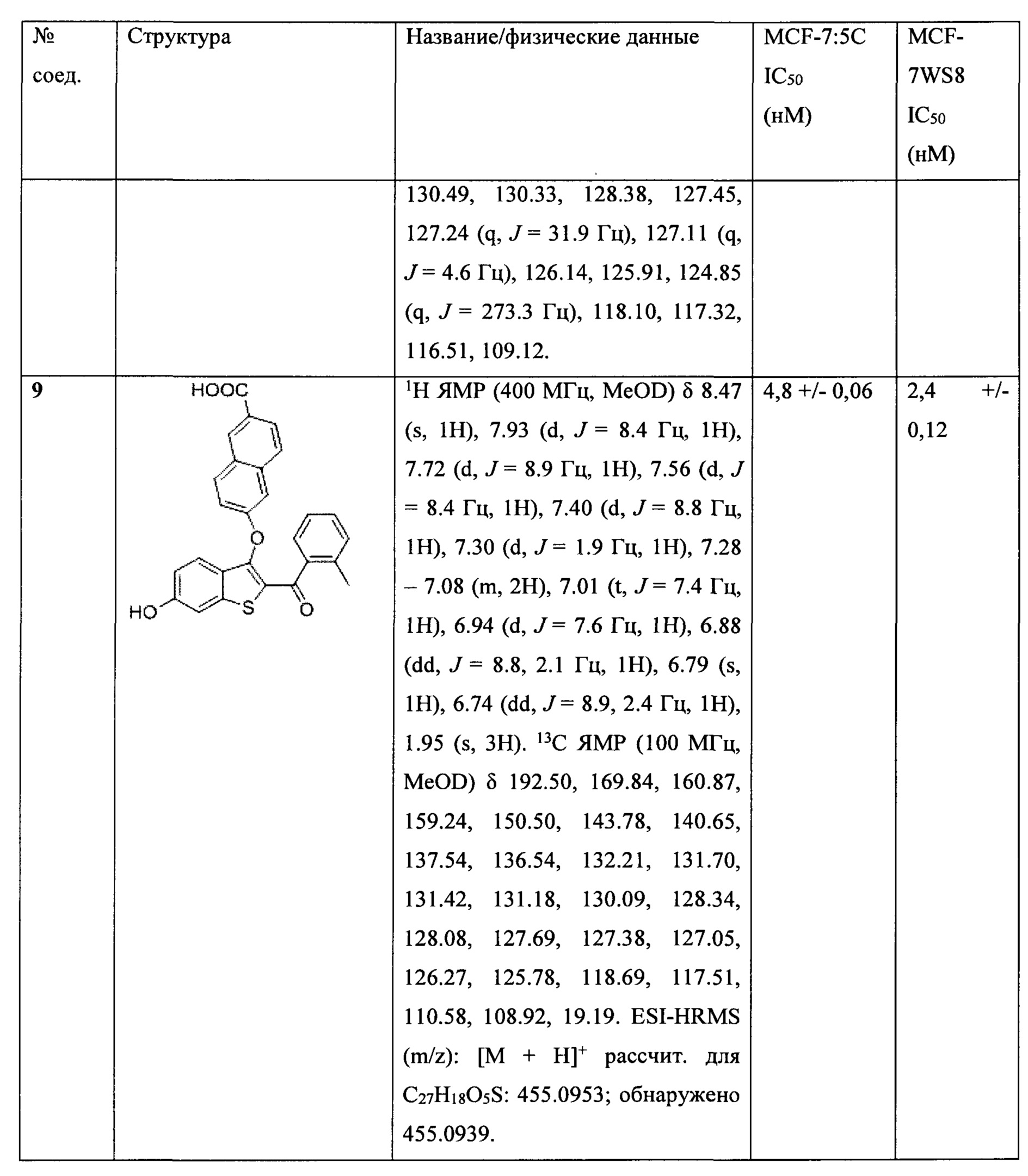
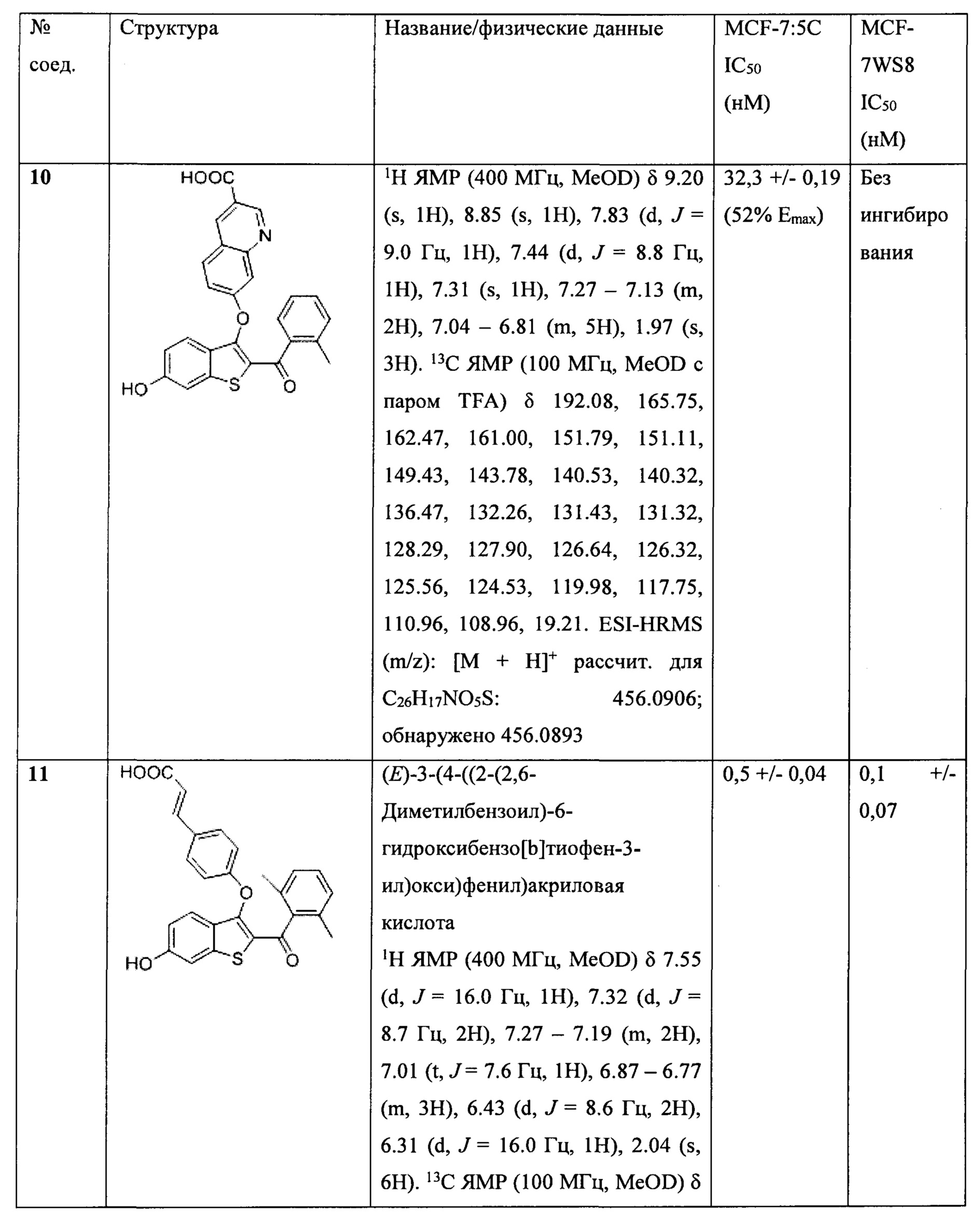
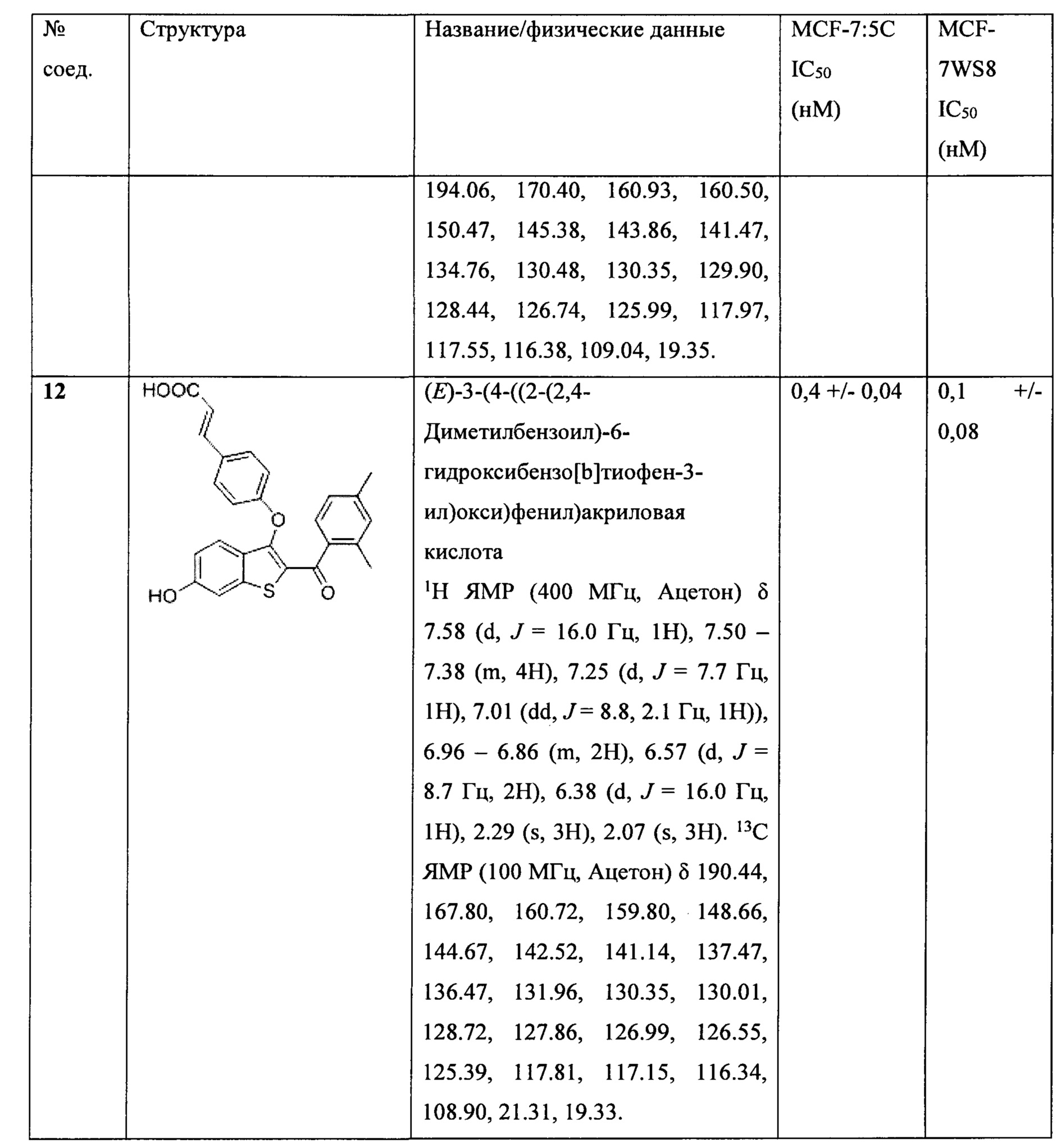
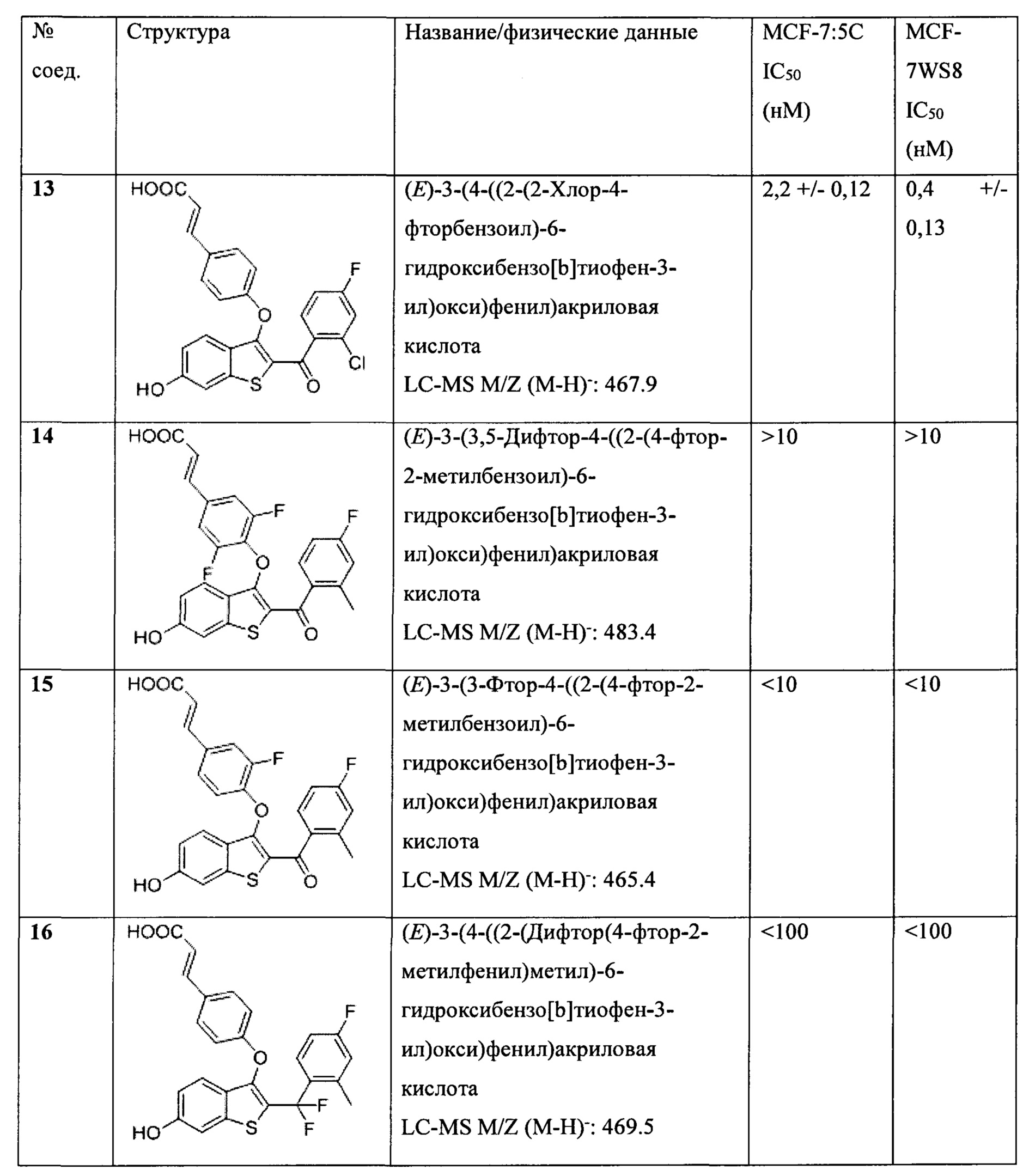
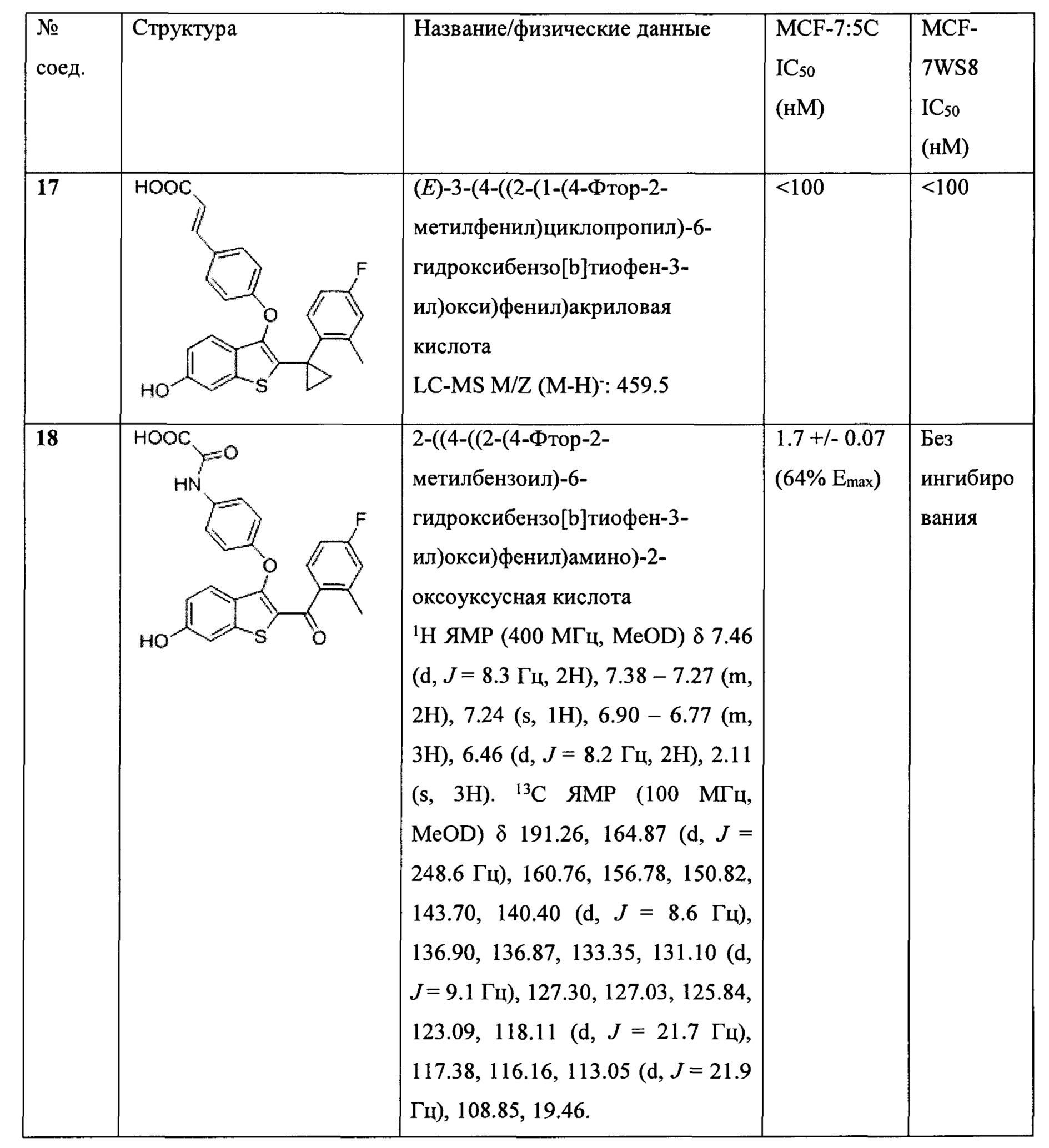
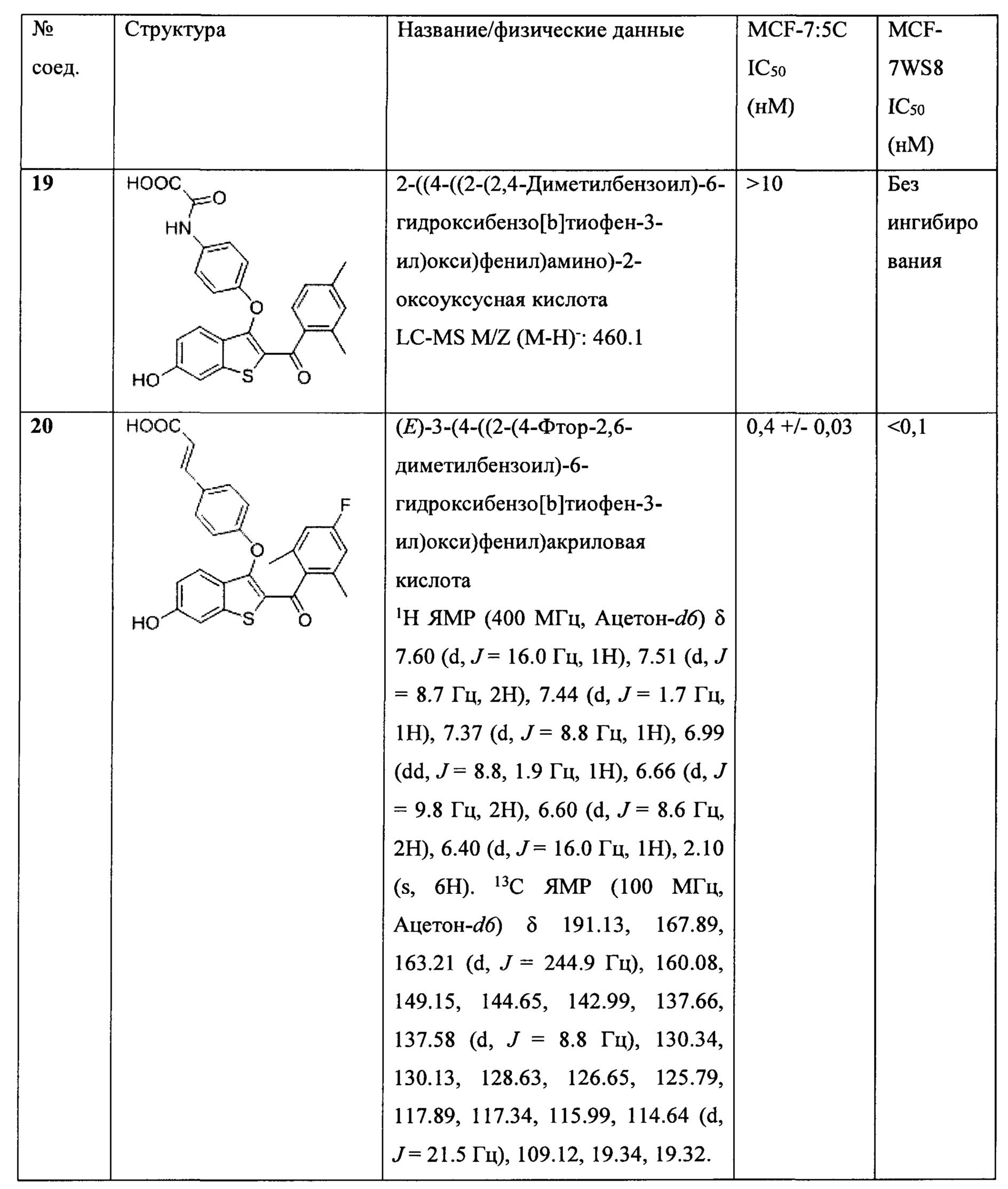
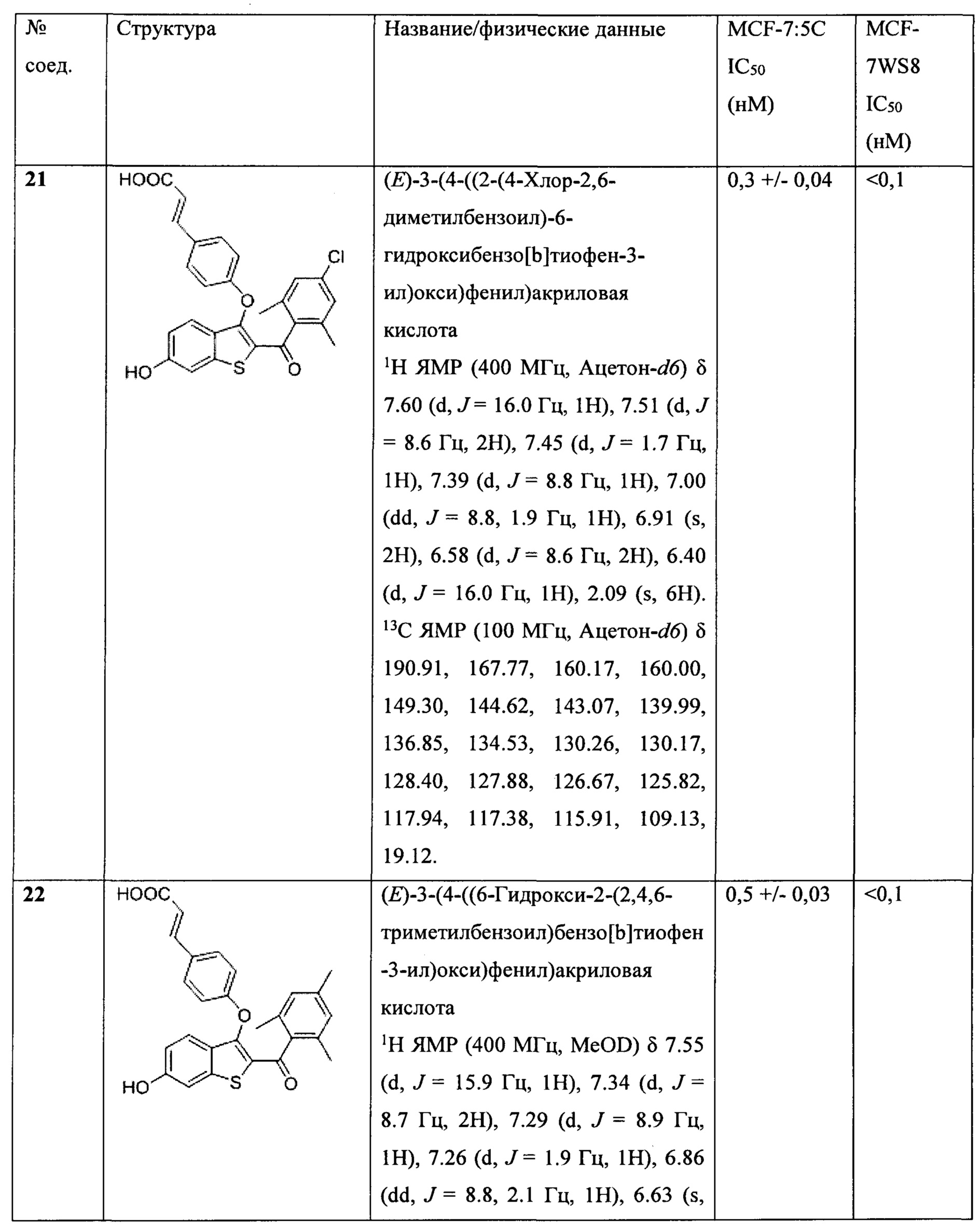
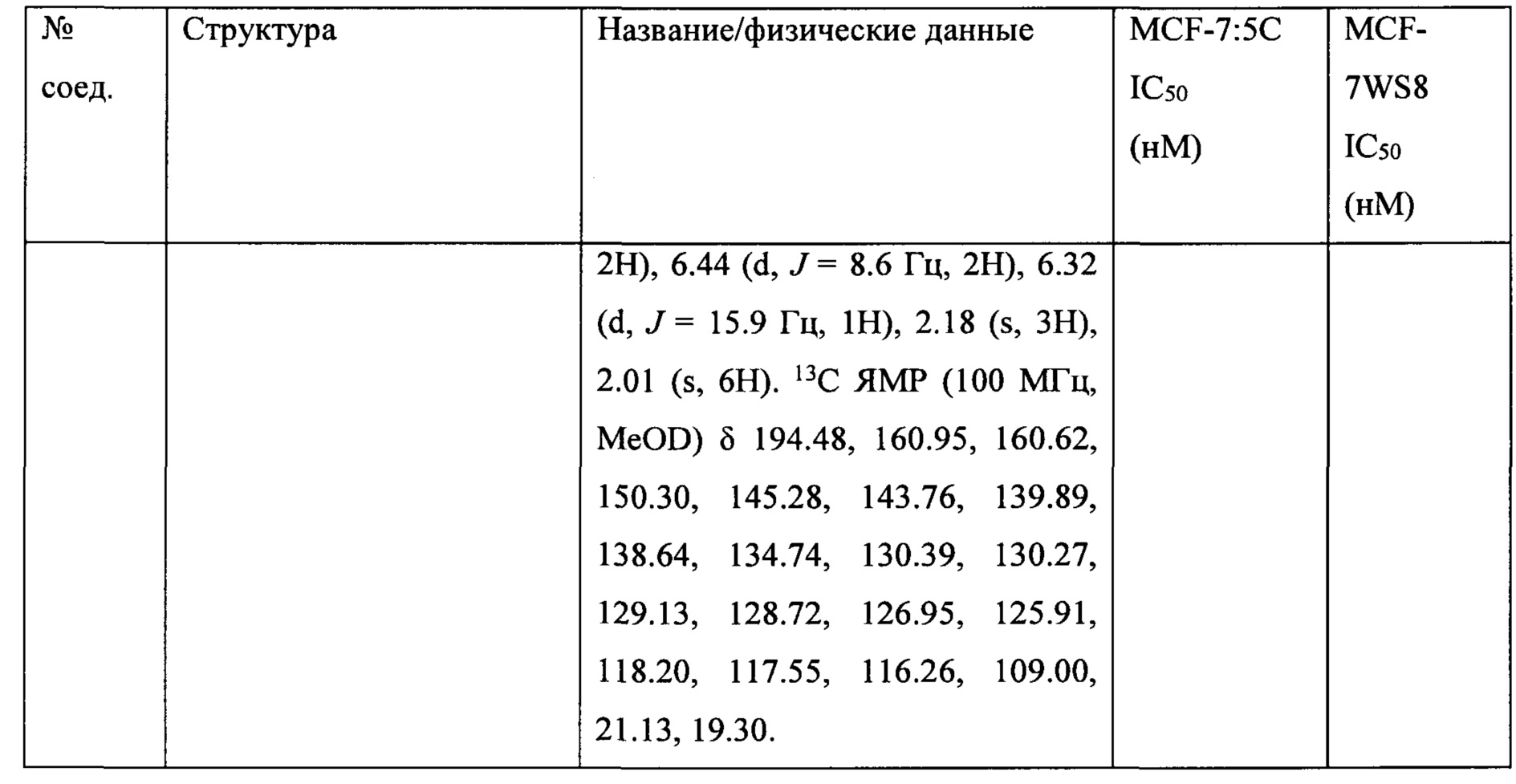
Анализы
Жизнеспособность клеток MCF7:WS8 и жизнеспособность клеток MCF7:5C (резистентных к тамоксифену)
Содержание ДНК в клетках определяли, как описано ранее, при помощи флуоресцентного набора для количественного определения ДНК (№ по кат. 170-2480; Bio-Rad Laboratories, Геркулес, Калифорния). Вкратце, пять тысяч клеток помещали на лунку в 96-луночные планшеты и обработку указанными концентрациями начинали в одно и то же время в каждой лунке. На 4-й или 6-й день, в случае MCF7:WS8 или MCF7:5C соответственно, клетки в планшетах лизировали и замораживали при -80°C. Для измерения общей ДНК в каждой лунке планшеты размораживали до комнатной температуры, инкубировали с красителем Hoechst и тщательно смешивали. Флуоресценцию измеряли при помощи гибридного многорежимного микропланшетного ридера Synergy H4. Для каждого анализа использовали шесть параллельных лунок и по меньшей мере проводили три независимых эксперимента.
Жизнеспособность клеток 3D сфероидов
Сфероиды высевали при концентрации 1000 клеток на лунку в 96-луночном прозрачном круглодонном микропланшете черного цвета Corning® со сверхнизким прикреплением сфероидов и выращивали в отсутствие обработки в течение 48 часов. 100 мкл среды удаляли из каждой лунки и добавляли 100 мкл 2Х концентрации обработки. Эту процедуру повторяли через каждые 2-3 дня в течение 12 дней. Анализ выполняли на 15-й день после посева. Протокол анализа на жизнеспособность 3D клеток CellTiter-Glo® применяли для определения ингибирования роста сфероидов. Планшеты и реагент нагревали до комнатной температуры в течение 30 минут. В течение этого времени сфероиды промывали PBS 2 раза, удаляя 100 мкл среды и замещая ее PBS. 100 мкл из каждой лунки затем удаляли и замещали 100 мкл 3D реагента CellTiter-Glo®, а сфероиды разрушали при помощи пипетирования. Планшеты помещали в шейкер на 5 минут до приведения в равновесие в темноте в течение 25 минут. 125 мкл из каждой лунки затем переносили в 96-луночный планшет белого цвета перед фиксацией люминесценции.
Вестерн-блоттинг
Цельноклеточные экстракты культивируемых клеток готовили в буфере для лизиса (200 ммоль/л Tris, 1% Triton X-100, 5 ммоль/л EDTA) с коктейлем из ингибиторов протеаз и фосфатаз (1:50, оба от Sigma-Aldrich) после соскабливания из планшетов для культивирования. Концентрацию белка измеряли при помощи метода Брэдфорда (Bio-Rad). Белки отделяли в условиях денатурации и блотировали на микроцеллюлозную мембрану (Bio-Rad) при помощи влажной системы переноса (Bio-Rad). Изображения блотов получали на системе Bio-Rad ChemiDoc после инкубации с раствором люминола SuperSignal West Dura (Thermo Fisher Scientific).
Результаты вышеизложенного представлены на фиг. 1-4 и в таблице 2.
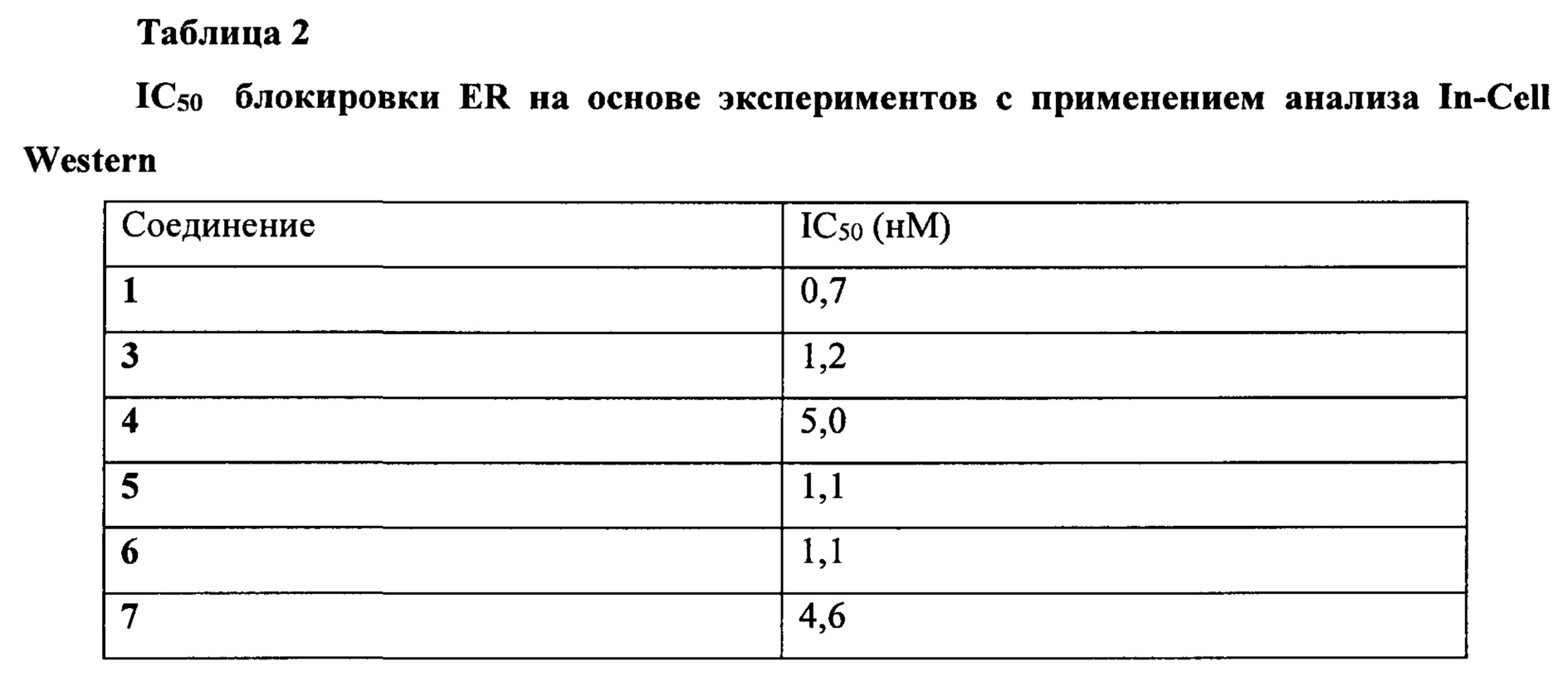
Выбор соединений по настоящему изобретению далее характеризовали по их разрушению эстрогеновых рецепторов, эффективности связывания с эстрогеновыми рецепторами и нигибированию 3D сфероидного роста.
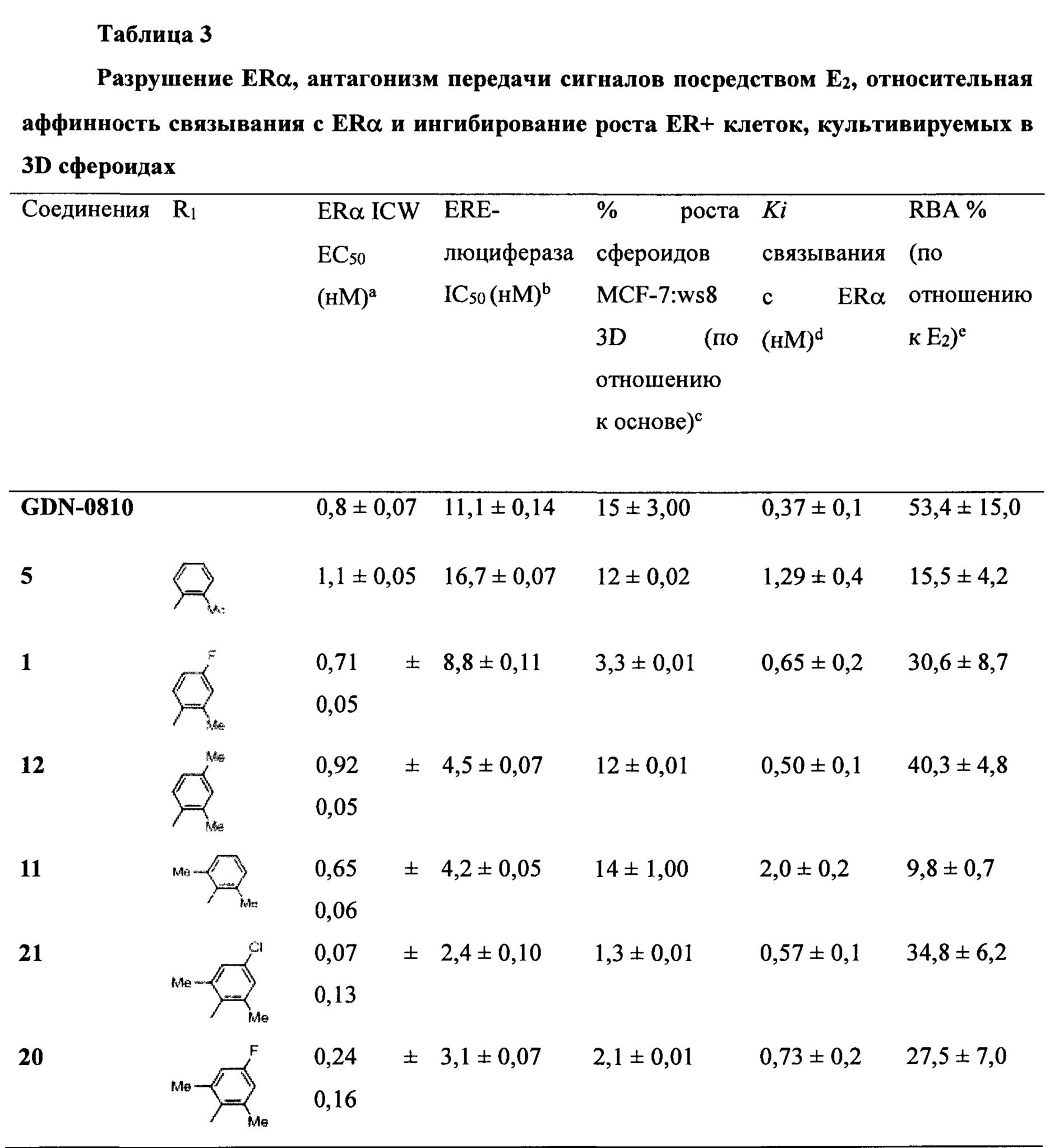
aСила индукции разрушения ER, измеряемая при 10 концентрациях при помощи анализов In-Cell Western (ICW).bСила антагонизма ERE-люциферазного репортера.cИнгибирование роста сфероидов после обработки SERD (100 нМ), экспрессируемое в виде % роста от контроля основой DMSO. Данные представлены в виде среднего и s.e.m.dАффинности связывания, рассчитываемые по формуле: Ki=(Kd[эстрадиол]/РВА)*100, где Kd для эстрадиола составляет 0,2 нМ.eЗначения относительной аффинности связывания (RBA), определяемые при помощи анализов смещения радиолигандов, выражаемые в виде IC50 эстрадиола/IC50 соединения × 100 (RBA, эстрадиол = 100%).
PK у мыши и данные, полученные на животных
Концентрации в плазме соединений 1, 5, 11, 12, 20 и 21, через 0,5 часа и 4 часа (100 мг/кг в 0,5% CMC суспензии, пероральное введение) измеряли для отбора BT-SERD для исследования в модели у мыши эктопического ксенотранасплантата эндокринно-резистентной ER+ злокачественной опухоли молочной железы (таблица 4). Биодоступность при пероральном введении соединений 20 и 21 дополнительно изучали при помощи измерения концентраций в плазме в несколько временных точек. Применение модели ксенотрансплантата MCF-7:TAM1 продолжали в течение 5,5 недель до лечения и проводили рандомизацию на шесть групп обработки со средней площадью опухоли 0,325 см2. Тамоксифен (100 мг/кг) не оказывал никакого эффекта, указывая на предполагаемую резистентность этой туморогенной TR злокачественной опухоли молочной железы к тамоксифену. GDN-0810 в дозе 100 мг/кг, применяемое ранее в литературе, вызывало регрессию размера опухоли на 21% на 23-й день после лечения. Соединение 12 (100 мг/кг) также вызывало регрессию опухоли, аналогичную GDN-0810 (26,7% снижения площади опухоли на 20-й день), в то время как соединение 21 характеризовалось наиболее высокой эффективностью регрессии опухоли (49% снижение) в дозе 100 мг/кг. Регрессия была дозозависимой для соединения 21: при 30 мг/кг средняя площадь опухоли снижалась на 27%. Инъекция туморогенных клеток в жировые подушки молочных желез голых мышей приводила к появлению отчетливых опухолей молочных желез, давая возможность оценки индивидуального противоопухолевого ответа, а также демонстрируя эффективность SERD соединения 21. Во время исследования на животных снижения массы тела не наблюдали.


aВсе соединения вводили при помощи желудочного зонда при 100 мг/кг в PEG400/PVP/TW80/CMC в воде, 9:0,5:0,5:90. Данные представляют собой среднюю концентрацию в плазме у трех мышей через 0,5 ч и 4 ч.
Эксперименты на животных
Опухоли MCF-7:Taml выращивали у бестимусных голых мышей после овариэктомии в возрасте 4-6 недель (Harlan Laboratories) и Е2 вводили при помощи силастиковых капсул (1,0 см), имплантированных подкожно между лопатками, как описано ранее. Соединение вводили в дозе 100 мг/кг или 30 мг/кг ежедневно в течение 3,5 недель в составе, содержащем раствор 0,5% CMC: PEG-400: Tween-80: PVP (90: 9: 05: 0,5). Площадь поперечных срезов опухолей определяли еженедельно при помощи штангенциркулей с нониусами и рассчитывали при помощи формулы (длина/2) × (ширина/2) × π. Среднюю площадь опухоли отмечали на графике в зависимости от времени (в неделях) для контроля опухолевого роста.
Клеточные линии и условия культивирования
MCF-7:WS8 представляли собой гормональнозависимые клоны клеток злокачественной опухоли молочной железы человека, поддерживаемые в среде фенолового красного RPMI-1640 с добавлением 10% FBS при 37°C, 5% CO2, которую описали ранее. Клетки MCF-7:5C поддерживали в не содержащей фенолового красного среде RPMI 1640 с добавлением 10% фетальной бычьей сыворотки, обработанной углем и декстраном, при 37°C, 5% CO2, как описано ранее. Клетки MCF-7:5C выступали в роли резистентных к AI клеток и получали из клеток MCF-7:WS8 в результате длительной эстрогеновой депривации.
Анализ клеточного роста
Клетки выращивали в не содержащих фенолового красного средах в течение 2 дней до каждого эксперимента. В день эксперимента клетки высевали в 96-луночный планшет при плотности 5000 клеток/лунку и обрабатывали либо 0,1% (v/v) DMSO, 1 нМ Е2, либо соединениями, приготовленными в не содержащих фенолового красного средах. Все соединения растворяли в DMSO и добавляли к среде до конечного разведения 1:1000. Содержание ДНК определяли на 5-й день (WS8) или 6-й день (5С) при помощи красителя Hoechst 33258. Флуоресцентные сигналы считывали при помощи Synergy H4 (BioTek).
Анализ In-Cell Western
Клетки MCF-7:WS8 содержали в обедненной среде 2 дня и 2,0×104/лунку клеток высевали в 96-луночные планшеты черного цвета с прозрачным дном на 48 часов перед добавлением соединений на 24 часа. Фиксацию, выявление ESR1 (sc-8002) и анализ выполняли согласно протоколу изготовителя LI-COR при помощи наборов для анализа In-Cell Western™ и системы визуализации инфракрасного излучения LI-COR ODYSSEY. Данные нормализовали по отношению к красителю CellTag 700.
Анализ роста 3D сфероидов
Сфероиды высевали по 1000 клеток/лунка в 96-луночных прозрачных круглодонных микропланшетах черного цвета Corning® со сверхнизким прикреплением сфероидов и выращивали в отсутствие обработки в течение 24 часов. Затем сфероиды обрабатывали при помощи 2× сред для обработки после удаления 100 мкл среды из каждой лунки. Обработку повторяли через каждые 2-3 дня в течение 14 дней. Протокол анализа на жизнеспособность 3D клеток CellTiter-Glo® применяли для определения ингибирования роста сфероидов. На 15-й день планшеты со сфероидами и реагент (3D реагент CellTiter-Glo®) доводили до комнатной температуры в течение 30 минут. В течение этого времени сфероиды промывали PBS, удаляя 100 мкл среды и замещая ее PBS. 100 мкл из каждой лунки затем удаляли и замещали 100 мкл реагента, а сфероиды разрушали при помощи пипетирования. Затем планшеты помещали в шейкер на 5 минут до приведения в равновесие в темноте в течение 25 минут. 125 мкл из каждой лунки затем переносили в 96-луночный планшет белого цвета перед фиксацией люминесценции при помощи пустой лунки для каждого фонового считывания.
Исследования по аффинности связывания
Аффинности связывания также определяли при помощи анализа конкурентного радиометрического связывания с применением 2 нМ [3H]эстрадиола в качестве метки (PerkinElmer, Уолтем, Массачусетс) и полноразмерного очищенного ERα человека (Pan Vera/Invitrogen, Карлсбад, Калифорния), как описано ранее. Значения RBA рассчитывали при помощи следующего уравнения: IC50 эстрадиола/IC50 соединения × 100.
Анализ люциферазы с эстроген-активным элементом (ERE) в клетках MCF-7.
Клетки MCF-7:WS8 содержали в обедненной среде 3 дня до обработки. Клетки высевали с плотностью 2×104 клеток/лунку в 96-луночных планшетах и котрансфицировали 5 мкг плазмиды с pERE-люциферазой на планшет, которая содержала три копии ERE A2 вителлогенина Xenopus laevis перед люциферазой светлячка, и 0,5 мкг плазмиды с pRL-TK (Promega, Мадисон, Висконсин), содержащей кДНК, кодирующую люциферазу Renilla. Трансфекцию выполняли в течение 6 часов при помощи реагента для траснфекции липофектамина 2000 (Invitrogen) в среде Opti-MEM в соответствии с инструкциями производителя. Клетки обрабатывали исследуемыми соединениями через 6 часов, и люциферазную активность измеряли через 18 часов после обработки при помощи системы с двойным анализом люциферазы (Promega) с Synergy H4 (Bio Tek).
Данное описание выполняли при отсылке на варианты осуществления настоящего изобретения. Однако специалисту в данной области будет понятно, что могут быть выполнены различные модификации и изменения без отклонения от объема настоящего изобретения, как изложено в формуле изобретения ниже. Несмотря на то, что особым образом описаны лишь определенные иллюстративные материалы, способы и аспекты этих материалов и способов, предполагается, что другие материалы и способы и комбинации различных характеристик материалов и способов подпадают под объем прилагаемой формулы изобретения, как особым образом упомянуто. Соответственно, данное описание следует рассматривать скорее в иллюстративном, а не ограничивающем смысле, и предполагается, что все модификации включены в объем настоящего изобретения.
Реферат
Изобретение относится к соединениям формулы:где: m равно 0, 1 или 2; n равно 0, 1 или 2; XAпредставляет собой -О-; кольцо В представляет собой фенил, нафтил или хинолинил; кольцо С представляет собой фенил или тиофенил; R1выбран из гидроксила и -O(С1-С6алкил); R2выбран из -СН=СНСООН, -NH(CO)COOH и -СООН; R3независимо в каждом случае выбран из водорода, галогена и C1-С6алкила и R4независимо в каждом случае выбран из водорода, галогена, гидроксила, C1-С6алкила, C1-С6фторалкила и -O(C1-С6фторалкил), или его фармацевтически приемлемым солям, которые являются блокаторами эстрогенового рецептора, и их применению для лечения заболеваний, связанных с эстрогенами. 10 н. и 34 з.п. ф-лы, 10 ил., 4 табл., 1 пр.
Формула
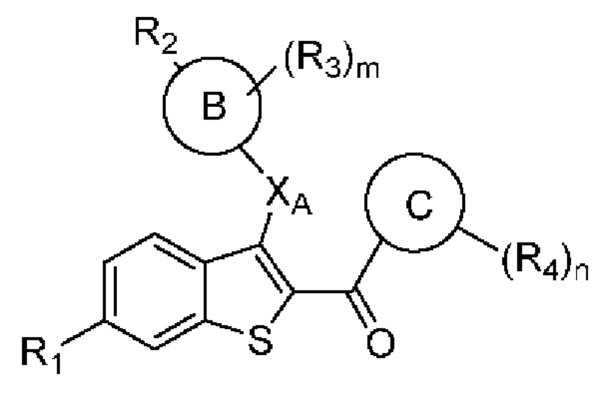
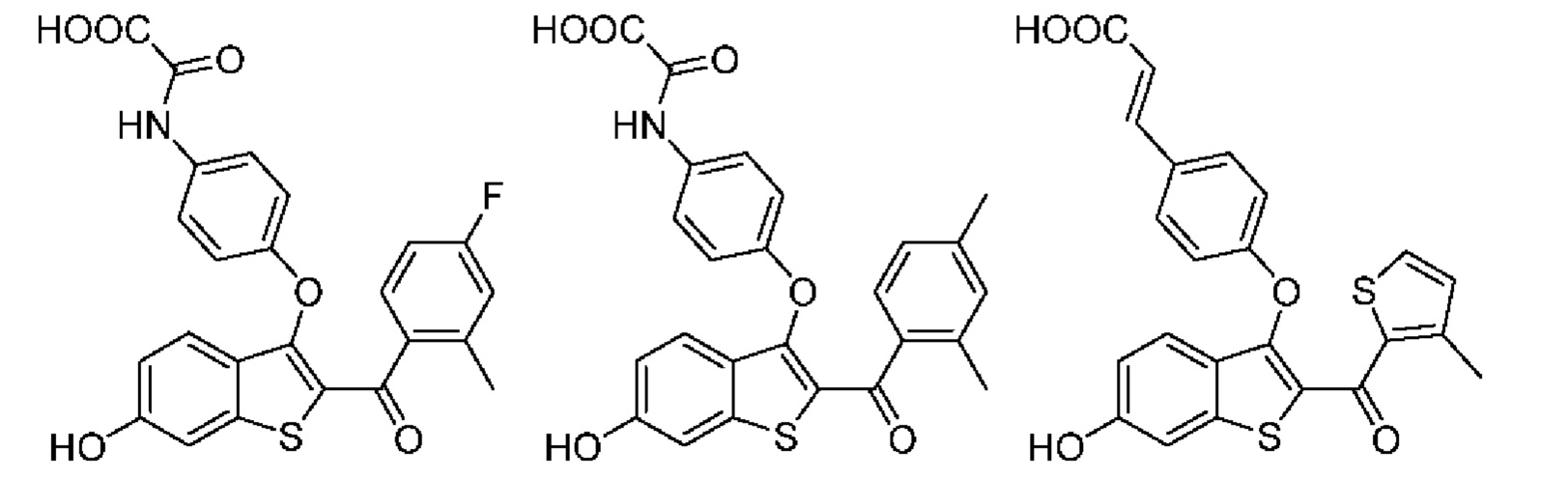
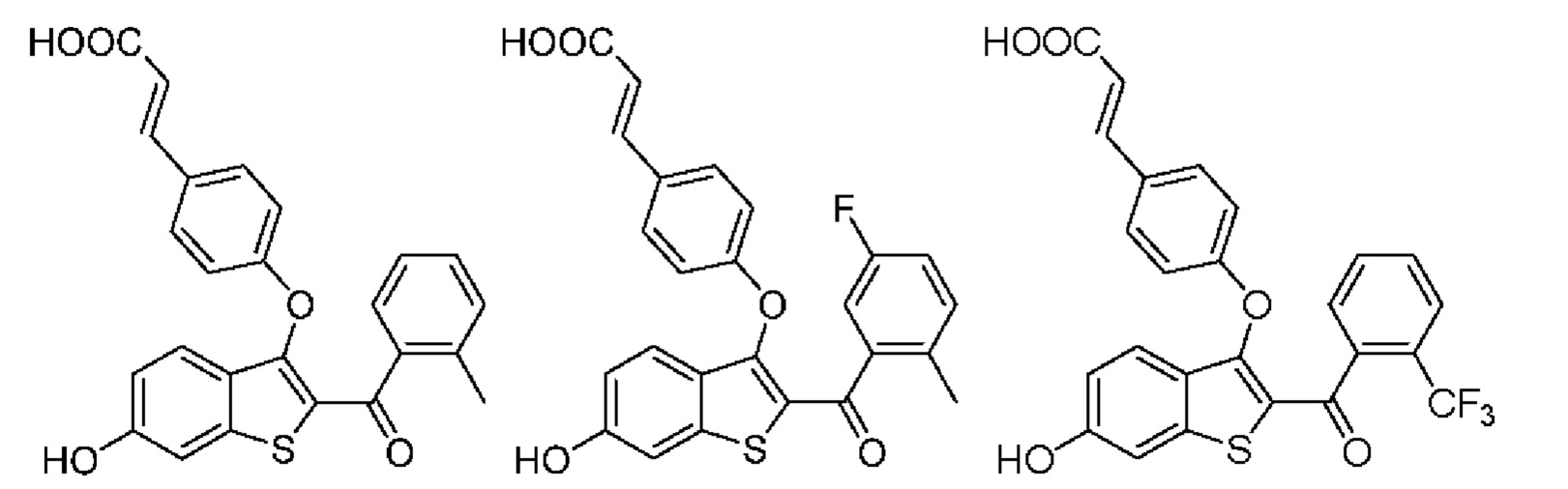
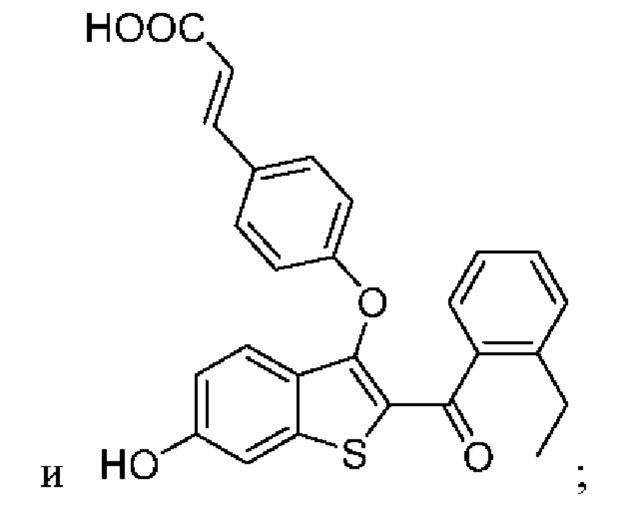
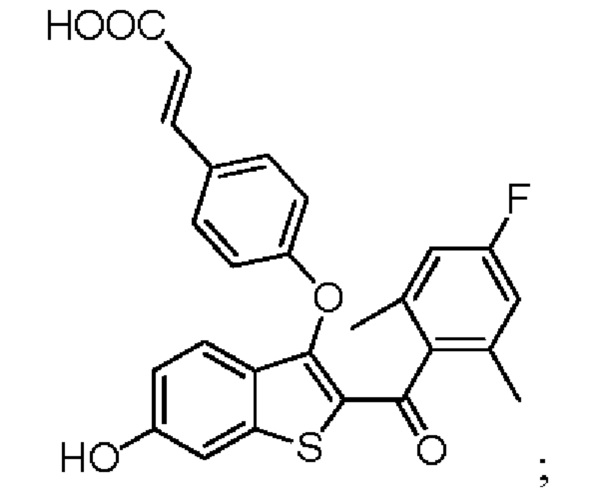
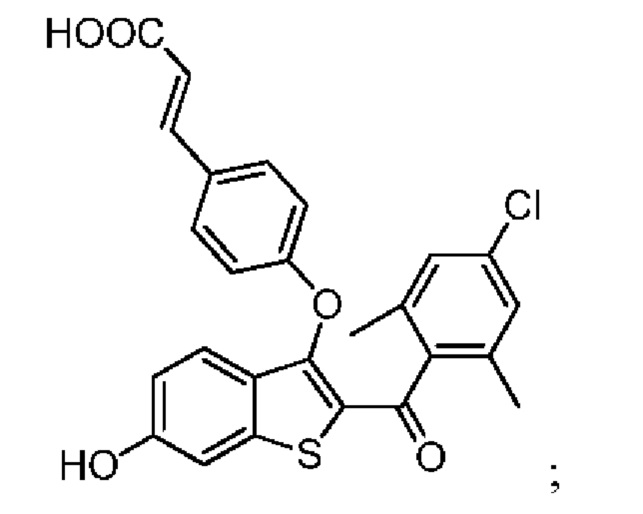
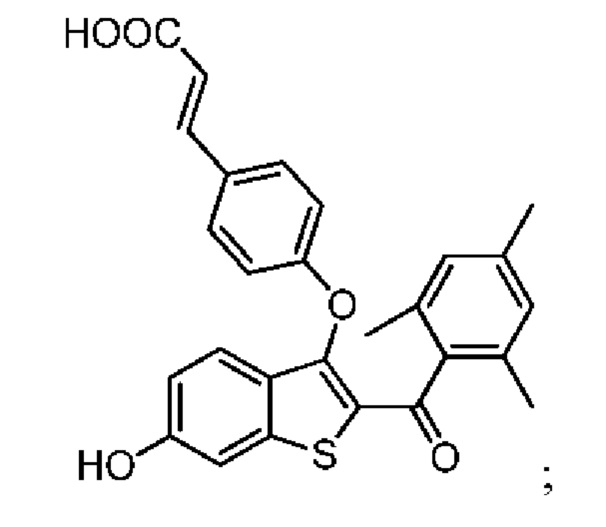

Комментарии