Способ секвенирования полинуклеотидов - RU2291197C2
Код документа: RU2291197C2
Чертежи

Описание
Область техники изобретения
Изобретение имеет отношение к созданию способа определения последовательности полинуклеотида.
Предпосылки к созданию изобретения
Возможность определять последовательность полинуклеотида имеет важное научное значение, что продемонстрировано в исследованиях по проекту "Геном человека" при картировании трех миллиардов оснований ДНК, закодированных в геноме человека.
Основным способом в обычной практике для широкомасштабного секвенирования ДНК является способ терминации цепи. Названный способ впервые был разработан Sanger и Coulson (Sanger et al., Proc. Natl. Acad. Sci. USA, 1977; 74: 5463-5467) и основан на применении дидезоксипроизводных четырех нуклеозидтрифосфатов, которые включаются в образующуюся полинуклеотидную цепь в полимеразной реакции. При включении дидезоксипроизводные завершают полимеразную реакцию, а затем продукты разделяют с помощью гель-электрофореза и анализируют, чтобы установить положение, по которому определенное дидезоксипроизводное включено в цепь.
Хотя названный способ широко используют и получают достоверные результаты, считают, что способ является медленным, трудоемким и дорогостоящим.
Для идентификации нуклеотидного включения в растущую образующуюся молекулу ДНК использовали флуоресцентные метки, используя полимеразную реакцию (см. WO 91/06678). Однако упомянутые способы имеют недостаток, заключающийся в увеличении фоновых помех от флуорофоров. Когда молекула ДНК растет, возрастают фоновые "помехи" и увеличивается время, требуемое для определения каждого нуклеотидного включения. Это серьезно ограничивает применение способа секвенирования больших полинуклеотидов. Однако наиболее серьезным ограничением систем для определения последовательности полинуклеотида, основанных на флуоресцентных красителях, является проблема фотообесцвечивания.
Фотообесцвечивание представляет собой хорошо описанный феномен в системах флуоресцентных красителей и является результатом экспозиции красителя при длинах волн возбуждения. Все системы красителей характеризуются способностью поглощать ограниченное количество фотонов прежде, чем происходит фотообесцвечивание. После фотообесцвечивания флуоресцентный краситель в течение непродолжительного периода времени оказывается видимым для исследователя, и следовательно, при присоединении к молекуле он становится недетектируемым.
Поэтому существует потребность в улучшенном способе определения последовательности полинуклеотида, который значительно повышает скорость и размер фрагмента полинуклеотида, последовательность которого должна быть определена, и при котором определение предпочтительно не зависит от флуоресцентно меченых нуклеотидов. Кроме того, способ должен осуществляться посредством автоматизированного процесса, уменьшающего сложность и стоимость, связанные с существующими способами.
Краткое изложение изобретения
Данное изобретение основано на понимании того, что конформационное изменение, и/или изменение массы, и/или изменение распределения энергии в ферменте, осуществляющем процессинг полинуклеотида, который происходит, когда фермент связывается с полинуклеотидом-мишенью и движется вдоль него, может быть установлено при использовании нелинейной оптической визуализации, включая визуализацию, основанную на генерации второго или третьего колебания.
Согласно данному изобретению способ секвенирования последовательности полинуклеотида предусматривает стадии:
(i) взаимодействия фермента, осуществляющего процессинг полинуклеотида, иммобилизованного в фиксированном положении, с полинуклеотидом-мишенью при условиях, обеспечивающих активность фермента; и
(ii) определения эффекта, являющегося результатом взаимодействия фермента и полинуклеотида, причем эффект обнаруживают путем измерения нелинейного оптического сигнала или линейного сигнала, связанного с нелинейным сигналом.
Данное изобретение позволяет достигать многочисленных преимуществ. Определение последовательности может быть выполнено с небольшим количеством полинуклеотида при возможности секвенирования отдельных полинуклеотидных молекул, тем самым устраняя необходимость амплификации до начала секвенирования. Можно получать длинные считываемые отрезки последовательности и минимизировать вторичный структурный анализ. Получение длинных считываемых отрезков устраняет необходимость в обширной вычислительной повторной сборке фрагментов. Кроме того, так как способ по изобретению не зависит от необходимости использования флуоресцентно меченых нуклеотидов или любого измерения флуоресценции, в соответствии с настоящим изобретением становится возможным обойти ограничение считываемого отрезка на уровне отдельной молекулы, а также действие фотообесцвечивания или других непредсказуемых эффектов флуоресценции. Данное изобретение также позволяет последовательно считывать длинные полинуклеотидные фрагменты с помощью той же ферментной системы. Это имеет преимущество, позволяющее использовать отдельную ферментную систему, которую можно регенерировать и повторно применять, что делает возможным секвенирование множества различных полинуклеотидных матриц. Наконец, использование генерации второго или третьего колебаний обеспечивает преимущества, обусловленные отсутствием фотоповреждения и фотообесцвечивания. Это обусловлено тем фактом, что не происходит никаких фотохимических превращений, даже в фокальной плоскости, так как сигнал, стимулированный нерезонансным излучением, не создает состояние возбуждения с ограниченным временем жизни.
Согласно второму аспекту изобретения материал твердого носителя содержит, по крайней мере, одну полимеразу и, по крайней мере, одну диполярную молекулу, расположенную на полимеразе или вблизи нее.
Согласно третьему аспекту изобретения устройство системы визуализации для обнаружения нелинейного оптического сигнала содержит твердый носитель с иммобилизованным на нем ферментом, который взаимодействует с полинуклеотидом, и диполярную молекулу, расположенную на ферменте или вблизи фермента.
Описание чертежей
Изобретение описывают со ссылкой на сопровождающие фигуры, где:
Фиг.1 представляет собой схематическую иллюстрацию системы визуализации, в которой используют генерацию второго колебания, и
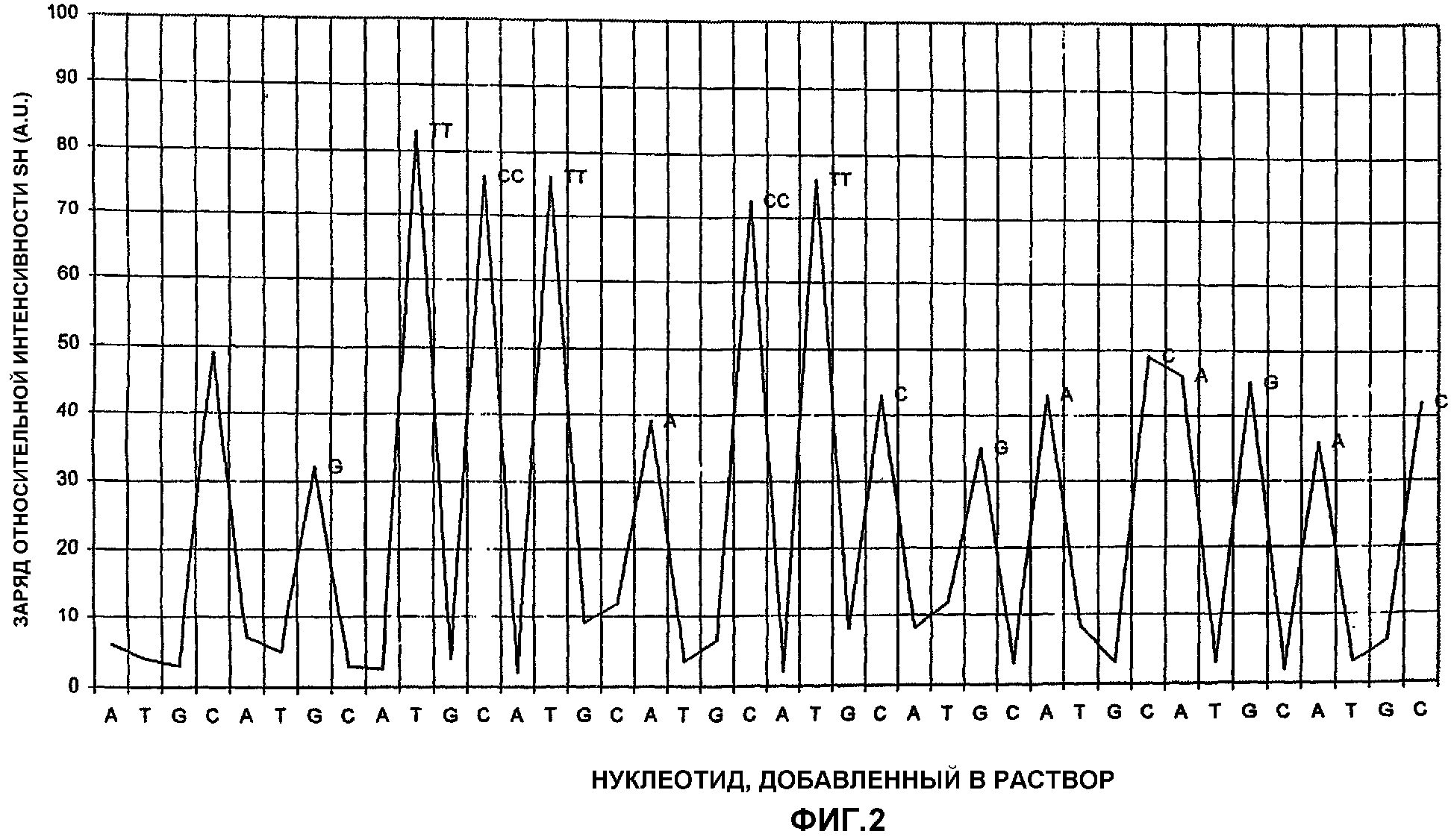
на фиг.2 представлен второй гармонический сигнал, генерируемый полимеразой при включении специфического полинуклеотида.
Подробное описание изобретения
В данном изобретении используют общепринятые нелинейные оптические измерения, чтобы идентифицировать конформационное изменение, и/или изменение массы, и/или изменение распределения энергии, происходящее, когда фермент, осуществляющий процессинг полинуклеотида, взаимодействует с отдельными основаниями на полинуклеотиде-мишени или включает нуклеотиды в образующуюся полинуклеотидную молекулу.
Применение нелинейных оптических способов для визуализации молекулы известно. До сих пор не было оценено то, что названные способы можно применять для секвенирования полинуклеотида, используя иммобилизованный или фиксированный фермент.
В отдельном аспекте генерируют линейный сигнал в дополнение к нелинейному сигналу и определяют линейный сигнал. Считают, что два сигнала соединяются, если достигается улучшение детекции.
Используемый в описании термин "полинуклеотид" может быть широко интерпретирован и включает в себя ДНК и РНК, включая модифицированные ДНК и РНК, гибриды ДНК/РНК, а также другие гибридные молекулы, подобные нуклеиновым кислотам, например пептиднуклеиновая кислота (PNA).
Используемый в описании термин "фермент, осуществляющий процессинг полинуклеотида," интерпретируется широко и относится к любому ферменту, который взаимодействует с полинуклеотидом и непрерывно движется вдоль полинуклеотида. Предпочтительно фермент является полимеразным ферментом и может быть любого известного типа. Например, полимераза может быть любой ДНК-зависимой ДНК-полимеразой. Если полинуклеотид-мишень представляет собой молекулу РНК, то полимераза может быть РНК-зависимой ДНК-полимеразой, то есть обратной транскриптазой, или РНК-зависимой РНК-полимеразой, то есть РНК-репликазой. В предпочтительном аспекте изобретения полимераза является полимеразой Т4. В других предпочтительных аспектах изобретения полимераза представляет собой или голофермент полимеразы III E.coli (McHenry, Ann. Rev. Biochem., 1988; 57:519); полимеразу Т7 (Schwager et al., Methods in Molecular and Cellular Biology, 1989/90; 1(4):155-159) или полимеразу Т7 гена 5 бактериофага в комплексе с тиоредоксином E.coli (Tabor et al., J. Biol. Chem., 1987; 262:1612-1623). Каждый из названных полимеразных ферментов связывает полинуклеотид-мишень с высокой эффективностью (и точностью) и поэтому поддерживает комплекс полимераза-полинуклеотид, даже когда полимеризация активно не происходит.
Альтернативные ферменты, которые взаимодействуют с полинуклеотидом, включают в себя геликазу, праймазу, голофермент, топоизомеразу или гиразу. Такие ферменты имеют другие преимущества. Например, применение геликазы снижает проблему вторичных структур, которая существует в полинуклеотидных молекулах, так как геликазы обнаруживают и устраняют названные структуры в естественной окружающей среде. Во-вторых, геликазы позволяют проводить необходимые реакции с двухцепочечной ДНК при комнатной температуре.
Так как фермент взаимодействует с последовательными основаниями полинуклеотида, его конформация будет изменяться в зависимости от того, с которым основанием (или нуклеотидом) на мишени он взаимодействует. Таким образом, временной порядок присоединения пар оснований во время реакции оценивают на одной молекуле нуклеиновой кислоты, то есть за активностью ферментной системы на матричном полинуклеотиде, подлежащем секвенированию, можно проследить в реальном времени. Последовательность выводят, идентифицируя основание (нуклеотид), которое включают в растущую комплементарную цепь полинуклеотида-мишени, с помощью каталитической активности фермента.
Важный аспект данного изобретения заключается в иммобилизации фермента в фиксированном положении относительно системы визуализации. Это предпочтительно осуществляют путем иммобилизации фермента на твердом носителе, при сохранении ферментом своей биологической активности. Способы иммобилизации соответствующих ферментов на твердом носителе известны. Например, в WO-A-99/05315 описывают иммобилизацию полимеразного фермента на твердом носителе. Подходят общие способы иммобилизации белков на носителях.
Используемые в данном изобретении способы оптического определения предназначены для получения изображения на уровне одной молекулы, то есть для генерирования различимого изображения/сигнала для одного фермента. Можно иммобилизовать множество ферментов на твердом носителе при плотности, которая допускает разрешение одного фермента. Поэтому в одном аспекте рассматривают многочисленные ферменты, иммобилизованные на твердом носителе, а способ по изобретению может быть осуществлен с названными ферментами одновременно. Это позволяет секвенировать различные полинуклеотидные молекулы вместе.
Для специалистов в данной области будет очевидным, что способ визуализации следует выполнять при условиях, обеспечивающих ферментативную активность. Например, что касается полимеразного фермента, очевидно, что для осуществления полимеразной реакции требуются другие компоненты. В упомянутом аспекте будут требоваться молекула полинуклеотидного праймера и каждый из нуклеозидтрифосфатов dATP, dTTP, dCTP и dGTP. Нуклеозидтрифосфаты можно добавлять последовательно с удалением несвязанных нуклеотидов перед введением следующего нуклеозидтрифосфата. Альтернативно, все трифосфаты могут присутствовать одновременно. Может оказаться предпочтительным использовать трифосфаты, содержащие одну или более блокирующих групп, которые можно избирательно удалять с помощью импульсного монохроматического света, тем самым предотвращая неконтролируемое включение. Соответствующие блокированные трифосфаты описаны в WO-A-99/05315.
Высокоразрешающие нелинейные оптические системы визуализации известны в данной области. Вообще, нелинейная поляризация для вещества может быть выражена как:
Р=Х(1)Е1+Х(2)Е2+Х(3)Е3+...
где Р означает индуцированную поляризацию, X(n) соответствует n-порядку нелинейной чувствительности, и Е соответствует вектору электрического поля. Первый член в формуле описывает нормальное поглощение и отражение света; второй член описывает генерацию второго колебания (SHG), сумму и различие частоты генерации; а третий описывает светорассеяние, стимулированное комбинационными способами, генерацию третьего колебания (TGH) и как двух-, так и трехфотонное поглощение.
Предпочтительная система визуализации данного изобретения основана на определении сигнала, возникающего из генерации второго или третьего колебания.
Разрешение на уровне одной молекулы с использованием генерации второго или третьего колебания (в дальнейшем называемой SHG) известно в данной области (Peleg et al., Proc. Natl. Acad. Sci. USA, 1999; 95: 6700-6704 и Peleg et al., Bioimaging, 1996; 4: 215-224).
Общее устройство системы визуализации может быть таким, как описано Peleg et al., 1996, выше, и как изображено на фиг.1. Что касается фиг.1, лазер (1) используют как источник света для генерации лазерного луча, который затем проходит через поляризатор (2). Часть лазерного луча может быть направлена через нелинейный кристалл (3) для получения зеленого луча, чтобы способствовать выравниванию лазерного луча. Фотодиод (4) помещают в тесной близости к оптической траектории для того, чтобы обеспечить средство для осуществления контроля генерированной интенсивности ближней инфракрасной области (NIR). Фильтр (5) помещают перед входным отверстием микроскопа, чтобы устранить любую другую нелинейность от включения микроскопа. Лазерный луч фокусируют на твердом носителе, содержащем иммобилизованный фермент, а нелинейный сигнал собирают линзами (7) и определяют, используя монохроматор (8). Основную интенсивность блокируют, используя ИК-фильтр. Сигнал от фотоумножителя амплифицируют, усредняют и интегрируют, используя усредняющее устройство с блоком узкополосных фильтров и канальный интегратор (9). Затем генерированные сигналы передают на компьютер (10), чтобы получить изображения.
Для того, чтобы генерировать второе или третье колебание, необходимо поместить соответствующую метку на иммобилизованный фермент или в тесной близости к нему. Высокодиполярные молекулы подходят для указанной цели (Lewis et al., Chem. Phys., 1999; 245: 133-144). Примером подходящих молекул являются красители, особенно стириловые красители (такие как мембранный краситель JPW 1259, поставляемый Molecular Probes). Зеленый флуоресцентный белок (GFP) является другим примером "красителя" или "метки", которую можно использовать, чтобы получить изображение через SHG. Используемый в описании термин GFP относится как к дикому типу белка, так и к его спектрально измененным мутантам (Tsien, Ann. Rev. Biochem., 1998; 67:509 и патенты США 5777079 и 5625048). Другие подходящие красители включают в себя ди-4-ANEPPS, ди-8-ANEPPS и JPW2080 (Molecular Probes).
Диполярные молекулы могут быть расположены на отдельных основаниях полинуклеотида (или его комплемента, если диполярные молекулы присоединяют к нуклеозидтрифосфатам и используют в полимеразной реакции).
В предпочтительном аспекте изобретения фермент, например полимеразу, получают в результате рекомбинантного слияния с GFP. GFP может быть помещен на N- или С-конце фермента (С-конец может быть желательным, если используют полимеразу в соединении с "подвижным зажимом"). Альтернативно, молекулу GFP можно размещать в ферменте, где угодно при условии, что сохраняется ферментативная активность.
В отдельном аспекте данного изобретения нелинейная оптическая система визуализации представляет собой спектроскопию комбинационного светорассеяния или поверхностную усиленную спектроскопию комбинационного светорассеяния (SERS). Обзор, касающийся спектроскопии комбинационного рассеяния, содержится в McGilp, Progress in Surface Science, 1995; 49(1): 1-106.
Предпочтительно оптическим излучением, используемым для возбуждения системы комбинационного рассеяния, является излучение ближней инфракрасной области (NIR). Возбуждение NIR имеет преимущество, заключающееся в уменьшении флуоресценции и сигнала комбинационного рассеяния от окружающей среды или растворителя.
В отдельном аспекте изобретения нелинейный сигнал можно усилить, применяя наночастицы металла и/или шероховатую металлическую поверхность (Boyed et al., Phys Rev., 1984; B. 30: 519-526, Chen et al., Phys. Rev. Lett., 1981; 46:1010-1012 и Peleg et al., 1996, выше). Усиливающую сигнал наночастицу металла можно присоединять к ферменту (например, с наночастицей, конъюгированной с антителом, Lewis et al., Proc. Natl. Acad. Sci. USA, 1999; 96: 6700-6704), иммобилизованному около иммобилизованного/локализованного фермента или в тесной близости с SHG-красителем/ферментом.
Наночастицы металла улучшают спектроскопическую визуализацию, связанную, в частности, с SHG от нанометрических областей, тем самым способствуя улучшению визуализации на уровне одной молекулы. Спектрофотометрическую визуализацию, основанную на комбинационном светорассеянии, также можно улучшить в результате использования наночастиц металла. Соответствующие наночастицы металла известны и включают в себя наночастицы золота и серебра. Обычно наночастицы имеют диаметр от 5 нм до 100 нм, предпочтительно от 10 нм до 60 нм. Наночастицы могут быть присоединены к полинуклеотиду (или его комплементу, если наночастицы присоединяют к нуклеозидтрифосфатам и используют в полимеразной реакции).
Также показано, что шероховатая металлическая поверхность повышает чувствительность SHG-способа (Chen et al., 1981, выше, и Peleg et al., 1996, выше), а также является необходимой для SERS. Обычно металлической поверхностью является серебро или другой благородный металл. Первоначальную избирательную модификацию металлической поверхности при пространственном разрешении при низкой длине волны можно проводить, используя различные способы, включая применение атомной силовой микроскопии (AFM). Покрытую платиной иглу AFM можно использовать, чтобы катализировать гидрирование конечных азидов до аминогрупп, которые подготавливают для дальнейшего преобразования (Muller et al., Science, 1995; 268: 272-273). Затем ферменты можно помещать в "горячие точки", в которых высокофокальные зоны имеются в областях, где локализованы оптические ветви (Shalaev et al., Phys. Rep., 1996; 272: 61).
В одном аспекте изобретения наночастицы могут быть доставлены в непосредственную близость с ферментом, используя иглу/зонд контилевера AFM, чтобы таким образом усилить нелинейный сигнал.
Недавно было установлено, что AFM может иметь временное разрешение и чувствительность, подходящие для динамической визуализации белковых конформационных изменений (Rousso et al., J. Struc. Biol., 1997; 119: 158-164). Это используют в предпочтительном аспекте изобретения, в котором зонд/иглу AFM помещают над ферментом и в сочетании с нелинейной оптической информацией (например, SHG), используют, чтобы обнаружить конформационные изменения белка, обусловленные взаимодействием между ферментом и нуклеотидной последовательностью, когда фермент движется вдоль полинуклеотида-мишени. Информация может быть собрана в дальней зоне при применении обычной конфокальной оптики или способа отражения, когда используют в сочетании с общим внутренним отражением.
В следующем аспекте нелинейный сигнал (например, SHG) регистрируют в ближней зоне, используя сканирующую оптическую микроскопию в ближней зоне (NSOM). NSOM представляет собой форму сканирующей зондовой микроскопии, в которой используют оптическое взаимодействие между наносекундной иглой (которую применяют в AFM) и образцом, чтобы получить оптическую информацию пространственного разрешения. Микроскопию ближней зоны в комбинации с SHG интенсивно изучали и показали, что она характеризуется поверхностной чувствительностью на атомном уровне (McGilp, 1995, выше). Главное преимущество применения NSOM, как части системы визуализации, заключается в том, что она делает возможным большое увеличение в разрешении при измерении при низких длинах волн. Так как данное изобретение имеет отношение к контролю конформации одного фермента, например полимеразного фермента, когда названный фермент взаимодействует с полинуклеотидом, пространственная разрешающая способность при низких длинах волн оказывается весьма подходящей. В контексте названного аспекта изобретения предпочтительно, если иглу контилевера AFM используют как безщелевой ближнепольный сканирующий микроскоп (Sangohdar et al., J. Opt. A: Pure Appl. Opt., 1999; 523-530). Это является аналогом применения металлических наночастиц как источника увеличения локального поля. Предпочтительно иглу делают из благородного металла или покрывают благородным металлом или любым материалом, который увеличивает локальное электромагнитное поле. Альтернативно, наночастица металла может быть непосредственно соединена с иглой контилевера. Как уже было показано, названное устройство подходит для слежения за конформационными изменениями на уровне одной молекулы (Rousso, et al., выше).
В следующем определенном аспекте данного изобретения независимо образованный поверхностный плазмон (или поляритон) бесконечно малого поля можно использовать, чтобы увеличить соотношение сигнал-шум нелинейного сигнала. Названный способ визуализации, усиленной бесконечно малой волной, имеет более высокое соотношение сигнал-шум, чем, например, одна SHG-визуализация. В упомянутом аспекте бесконечно мало усиленный сигнал SHG-поля от меченого фермента может быть собран в ближней зоне посредством NSOM-волокна при одновременном получении данных AFM по конформации, и в то же самое время можно регистрировать количество поглощенного бесконечно малого излучения, чтобы получить информацию относительно важности связи между бесконечно малым полем и меченой полимеразой/SHG-полем.
В описанной форме (способ NSOM собирания) система действует как фотон-сканирующий туннельный микроскоп (PSTM) и бесконечно малое поле или поле поверхностного плазмона соединяются в игле зонда волокна NSOM. Любое истощение в напряженности поля сигнала, достигающего иглы с помощью полимеразы, будет зарегистрировано через детектор, помещенный на конце иглы.
Резонанс поверхностного плазмона известен в данной области и основан на генерации бесконечно малой волны в результате направления случайного светового луча на призму. Обычное устройство для применения в названном аспекте состоит из призмы, которую оптически соединяют с покрытой металлом стеклянной пластиной, на котором иммобилизован фермент. Пластина является частью микрожидкостной системы проточной кюветы с входным отверстием для внесения лигандов (нуклеотидов) над иммобилизованным ферментом. Фермент также метят, чтобы допустить генерирование нелинейных эффектов. Случайный световой луч направляют на призму, чтобы генерировать поле поверхностного плазмона. В то же время нелинейный сигнал (например, поле второго колебания) генерируют посредством направления импульсного ближнего инфракрасного лазера через поляризатор и растровую волновую пластину в оптический сканер для контроля луча через фильтр, чтобы устранить оптические помехи второго колебания, а затем на образец. Нелинейный оптический сигнал собирают линзами и фильтром и направляют в монохроматор, пропускают в трубку фотоумножителя для детекции, а затем амплифицируют и регистрируют с помощью компьютерной системы.
Когда нелинейный оптический сигнал собирают с тем, чтобы генерировать бесконечно малое поле, определяемый сигнал также может быть линейным (бесконечно малым) сигналом. В названном аспекте для осуществляемого собирания можно использовать NSOM, чтобы обнаружить линейный сигнал.
В самостоятельном аспекте данного изобретения определение последовательности полинуклеотида можно проводить в клетке.
Показано, что в нативной клеточной среде ДНК-полимераза и ее ассоциированный реплисомный комплекс прикреплены на месте (или локализованы в пространстве) в клетке (Newport et al., Curr. Opin. Cell Biol., 1996; 8: 365; и Lemon et al., Science, 1998; 282: 1516-1519). Названный нативный прикрепленный репликационный комплекс является аналогом иммобилизации фермента на твердом носителе.
Это позволяет осуществлять in vivo наблюдение конформационных и связанных с последовательностью матрицы изменений молекул, связанных с реплисомой, на уровне одной молекулы в реальном времени во время репликации ДНК и/или клеточного деления.
Для осуществления упомянутого аспекта необходимо модифицировать фермент с тем, чтобы его можно было визуализировать, используя способы нелинейной оптической детекции. Это может быть достигнуто посредством генетического слияния фермента, например, с зеленым флуоресцентным белком (GFP). Клетка также должна быть иммобилизована, чтобы была возможность произвести детекцию.
Экспрессированный слитый белок можно наблюдать/обнаружить в его прикрепленной клеточной локализации, применяя нелинейную оптическую детекцию (генерация второго колебания).
Следующие примеры иллюстрируют изобретение.
В проведенном эксперименте белок, слитый из зеленого флуоресцентного белка (GFP) и полимеразы, создавали с помощью рекомбинантных способов, хорошо известных в данной области.
Кварцевые чипы (14 мм в диаметре, 0,3 мм толщиной) покрывали по способу спин-покрытия слоем золота толщиной 50 нм, а затем покрывали слоем обычного декстрана. Затем названные покрытые золотом кварцевые чипы помещали в жидкостную кювету обычного ближнепольного оптического микроскопа (NSOM). Покрытые золотом кварцевые чипы оптически соединяли с кварцевой призмой через масло с подобранным показателем преломления. Затем жидкостную кювету герметически закрывали и полимеразный буфер оставляли протекать по чипу.
Иммобилизацию полимеразы на поверхности чипа осуществляли согласно Jonsson et al., Biotechniques, 1991; 11: 620-627. Среду чипа уравновешивали "рабочим" буфером (10 мМ hepes, 10 мМ MgCl2, 150 мМ NaCl, 0,05% поверхностно-активного вещества Р20, рН 7,4). Равные объемы N-гидроксисукцинимида (0,1 М в воде) и N-этил-N'-(диметиламинпропил)карбодиимида (EDC) (0,1 М в воде) смешивали вместе и вводили через поверхность чипа, чтобы активировать карбоксиметилированный декстран. Слитый белок - полимераза-GFP, (150 мкл) смешивали с 10 мМ ацетатом натрия (100 мкл, рН 5) и вводили через активированную поверхность. Наконец, сложные N-гидроксисукцинимидэфиры, оставшиеся на поверхности чипа, вводили в реакцию с этаноламином (35 мкл, 1 М в воде, рН 8,5), а несвязанную полимеразу смывали с поверхности. Процедуру иммобилизации проводили при непрерывном потоке омывающего буфера (5 мкл/минуту) при температуре 25°С.
50 мкл связывающего антитела буфера (10 мМ MES, pH 6,0, 150 мМ NaCl, 3 мМ EDTA) оставляли протекать по иммобилизованной полимеразе/GFP на поверхности чипа при скорости течения 5 мкл/минуту при 25°С. Первичные антитела (GFP (B-2)В конъюгированный биотин 200 мкл мл-1, Santa Cruz Biotechnology) разводили 1:3000 буфером, связывающим антитела, и оставляли протекать по поверхности чипа со скоростью течения 5 мкл/минуту в течение 30 минут. Затем избыток антител смывали с поверхности, пропуская буфер, связывающий антитела, по чипу при скорости течения 5 мкл/минуту в течение 30 минут.
Вторичные антитела (конъюгат козьих антител против мышиного IgG (H+L) ЕМ с иммунозолотом 40 нм, British Biocell International) разводили 1:1000 буфером, связывающим антитела, и оставляли протекать по поверхности чипа при скорости течения 5 мкл/минуту в течение 30 минут. Затем избыток антител смывали с поверхности, пропуская связывающий антитела буфер по чипу при скорости течения 5 мкл/минуту в течение 30 минут. Затем буфер заменяли "рабочим" буфером, который потом оставляли протекать по чипу при скорости течения 5 мкл/минуту в течение 30 минут до начала следующей стадии.
Два олигонуклеотида синтезировали, используя стандартную фосфорамидитную химию. Олигонуклеотид, обозначенный как SEQ ID NO 1, использовали как полинуклеотид-мишень, а олигонуклеотид, обозначенный как SEQ ID NO 2, использовали как праймер.
SEQ ID NO 1

SEQ ID NO 2

Два олигонуклеотида взаимодействовали при гибридизующих условиях с образованием комплекса: мишень-праймер. Затем праймерную ДНК суспендировали в буфере (20 мМ трис-HCl, pH 7,5, 8 мМ MgCl2, 4% (об./об.) глицерина, 5 мМ дитиотрейтола (DTT)), содержащем 150 мкл β-субъединиц, которые образуют "скользящий-скрепляющий" комплекс вокруг праймерной ДНК. Описанный способ известен как пре-инициация.
Для того, чтобы обнаружить конформационные изменения в полимеразе, модифицированную NSOM использовали в tapping-режиме с растянутыми кварцевыми многомодовыми длинноволоконными 100 мкм кантилеверами. Кантилевер подводили близко к его резонансной частоте и исходное пространственное сканирование осуществляли над поверхностью чипа, содержащего иммобилизованные антитела. Второй гармоничный сигнал генерировали от иммобилизованной полимеразы в проточной кювете посредством инициирующего освещения от импульсного ближнеинфракрасного лазерного источника. Затем иглой NSOM сканировали над поверхностью чипа в проточной кювете, чтобы получить изображение частиц золота 40 нм в проточной кювете, которая связана с полимеразой. Затем иглу приводили в стационарное состояние над полимеразой.
Затем пре-инициированный и пре-праймированный комплекс вводили в проточную кювету при скорости течения 5 мкл/минуту с тем, чтобы "скрепление" вокруг молекулы праймер-матрица образовало комплекс с иммобилизованной полимеразой. Проточную кювету содержали при 25°C с помощью устройства, встроенного в проточную кювету.
Затем "рабочий" буфер непрерывно пропускали через проточную кювету со скоростью 500 мкл/минуту. Через 10 минут инициировали реакцию секвенирования введением 0,4 мМ dATP (8 мкл) в буфер при скорости течения 500 мкл/минуту. Через 4 минуты в проточную кювету вводили 0,4 мМ dTTP (8 мкл). Затем через следующие 4 минуты вводили 0,4 мМ dGTP (8 мкл) и еще через 4 минуты вводили 0,4 мМ dCTP (8 мкл). Описанный цикл потом повторяли 10 раз. В течение всего периода времени второй гармоничный сигнал, посылаемый через многомодовое волокно, пропускали в монохроматор, а затем в фотоумножитель. Затем сигнал от фотоумножителя амплифицировали и направляли в компьютер для обработки и хранения.
Изменение интенсивности второго гармоничного сигнала, возникающего из полимеразного комплекса в течение периода 10 секунд от начала каждого введения, затем рассчитывали и вычерчивали график относительно нуклеотида, инъецированного в проточную кювету. Результаты реакции секвенирования представлены на фиг.2. Как можно видеть из графика, изменения высокой интенсивности (расчет более высоких интенсивных изменений для идентичных нуклеотидов, примыкающих один к другому) соответствовали комплекту олигонуклеотида SEQ ID NO 1 (считывание справа налево, минус ту часть, которую гибридизовали с последовательностью праймера).

Реферат
Изобретение относится к области биотехнологии и может быть использовано для секвенирования полинуклеотидных последовательностей. Последовательность полинуклеотида определяют по изменению нелинейного оптического сигнала или линейного оптического сигнала, связанного с нелинейным сигналом, регистрируемым при взаимодействии иммобилизованного в фиксированном положении фермента, который может взаимодействовать с нуклеотидной цепью и непрерывно продвигаться по ней, с отдельными основаниями мишеневого полинуклеотида. Применение изобретения позволяет определять последовательность полинуклеотидов большого размера с высокой скоростью посредством автоматизированного процесса. 23 з.п. ф-лы, 2 ил.

Комментарии