Применение 4-(4,7-диметокси-3-фенилбензофуран-2-ил)бутан-2-она в качестве антибактериального средства в отношении грамположительных микроорганизмов - RU2791704C1
Код документа: RU2791704C1
Описание
Изобретение относится к области органической химии - новым биологически активным соединениям - замещенным бензофуранам, а именно к 4-(4,7-диметокси-3-фенилбензофуран-2-ил)бутан-2-ону I формулы:

соединение I обладает антибактериальной активностью, что позволяет предположить его использование в медицине в качестве потенциального лекарственного средства с антибактериальными свойствами.
Аналогом по структуре заявляемому соединению является 3-{2-(бензо[d][1,3]диоксол-5-ил)-7-метоксибензофуран-5-ил}пропан-1-ол, обладающий антибактериальной активностью [Phytochemistry, 2000, 55, 597; doi: 10.1016/S0031-9422(00)00225-9] формулы:

Эталоном сравнения был выбран фенилсалицилат III формулы:

который широко применяется в лечебной практике, и является аналогом по действию [Машковский М.Д. Лекарственные средства. - 16-е изд., перераб., испр. и доп. - М.: Новая волна, 2012. - с. 950].
Задачей изобретения является поиск в ряду замещенных бензофуранов веществ с выраженным антибактериальным действием и низкой токсичностью.
Поставленная задача достигается получением 4-(4,7-диметокси-3-фенилбензофуран-2-ил)бутан-2-она, который обладает антибактериальной активностью.
Заявляемое соединение I синтезируют взаимодействием 2-(гидрокси(фенил)метил)-3,6-диметоксифенола и 2-метилфурана в 1,2-дихлорэтане в присутствии каталитических количеств трифторметансульфокислоты при температуре 85°С и выделением целевого продукта стандартными методами синтетической органической химии по схеме:

Пример 1. В реакционную виалу объемом 3 мл, снабженную тефлоновой крышкой и магнитным якорем, загружают 2-(гидрокси(фенил)метил)-3,6-диметоксифенол (0.5 ммоль), 2-метилфуран (0.75 ммоль) и 1,2-дихлорэтан (1.7 мл). Затем к раствору одной порцией при комнатной температуре при интенсивном перемешивании добавляют TfOH (4.4 мкл, 10 мол.%). Виалу помещают в предварительно нагретый (до 80°С) алюминиевый блок и реакционную смесь перемешивают в течение 1 ч (контроль ТСХ). После завершения реакции полученный раствор концентрируют в вакууме. Целевой продукт выделяют методом колоночной хроматографии (силикагель, градиентное элюирование смесью петролейный эфир/этилацетат от 99:1 до 20:1). Выход 66%. Спектр ЯМР1Н, (400 МГц, ДМСО-d6), d, м.д.: 7.47-7.45 (м, 2Н, HAr), 7.42-7.39 (м, 2Н, HAr), 7.35-7.32 (м, 1Н, HAr), 6.70 (д,3J=8.6 Гц, 1Н, HAr), 6.54 (д,3J=8.6 Гц, 1Н, HAr), 3.98 (с, 3Н, ОСН3), 3.63 (с, 3Н, ОСН3), 3.07 (т,3J=7.6 Гц, 2Н, СН2), 2.89 (т,3J=7.6 Гц, 2Н, СН2), 2.12 (с, 3Н, СН3). Спектр ЯМР13С (100 МГц, ДМСО-d6), d, м.д.: 206.7; 152.7, 148.4, 144.4, 140.1, 132.7, 130.0 (2 С), 127.7 (2 С), 127.0, 119.7, 117.7, 106.3, 104.1, 56.6, 56.1, 41.7, 29.7, 20.9; HRMS (ESI/TOF): m/z [М+Н]+вычислено для С20Н21О4: 325.1434; найдено: 325.1436. Полученное соединение I представляет собой светло-желтое масло, растворимое в хлороформе, толуоле, ацетоне, этилацетате и нерастворимое в петролейном эфире.

Пример 2. Для характеристики антибактериальной активности использовали стандартные параметры: минимальная подавляющая концентрация (МПК), которую определяли модифицированным методом двукратных серийных разведений (МУК 4.2.1890-04 Определение чувствительности микроорганизмов к антибактериальным препаратам) и минимальная бактерицидная концентрация (МБК) [Медицинские лабораторные технологии: Руководство по клинической лабораторной диагностике, п/р Каприщенко, 2013, Т.2, стр. 407]. Тесты проводили с использованием культур модельных микроорганизмов Escherichia coli МС4100 и Staphylococcus epidermidis АТСС29887 на питательной среде Луриа-Бертани в 96-луночных полистироловых планшетах. Конечная концентрация микроорганизмов в лунках составляла 5*105 КОЕ/мл. Культивирование проводили при 37°С без перемешивания. Определение МПК и высевы для определения МБК производили через 24 ч. На первом этапе исследуемое соединение растворяли в диметилсульфоксиде (ДМСО), дальнейшие разведения производили в метаноле. В качестве начальных в тестах использовали концентрации, которые при внесении в питательную среду Луриа-Бертани не образовывали осадка (от 0.2 до 4 мг/мл).
Пример 3. Острую токсичность (ЛД50, мг/мл) соединения I определяли по методу Г.Н. Першина [Першин Г.Н. Методы экспериментальной химиотерапии // М., С.100, 1971, 109-117]. Соединение I вводили внутрибрюшинно белым мышам массой 16-18 г в виде взвеси в 2% крахмальной слизи и наблюдали за поведением и гибелью животных в течение 10 суток. Для исследуемого соединения I ЛД50 составляет >1500 мг/кг.
Согласно классификации токсичности препаратов, соединение I относится к V классу практически нетоксичных препаратов [Измеров Н. Ф., Саноцкий И. В., Сидоров К. К. Параметры токсикометрии промышленных ядов при однократном воздействии: Справочник. М., 1977, стр. 196]. Результаты испытаний представлены в таблице:
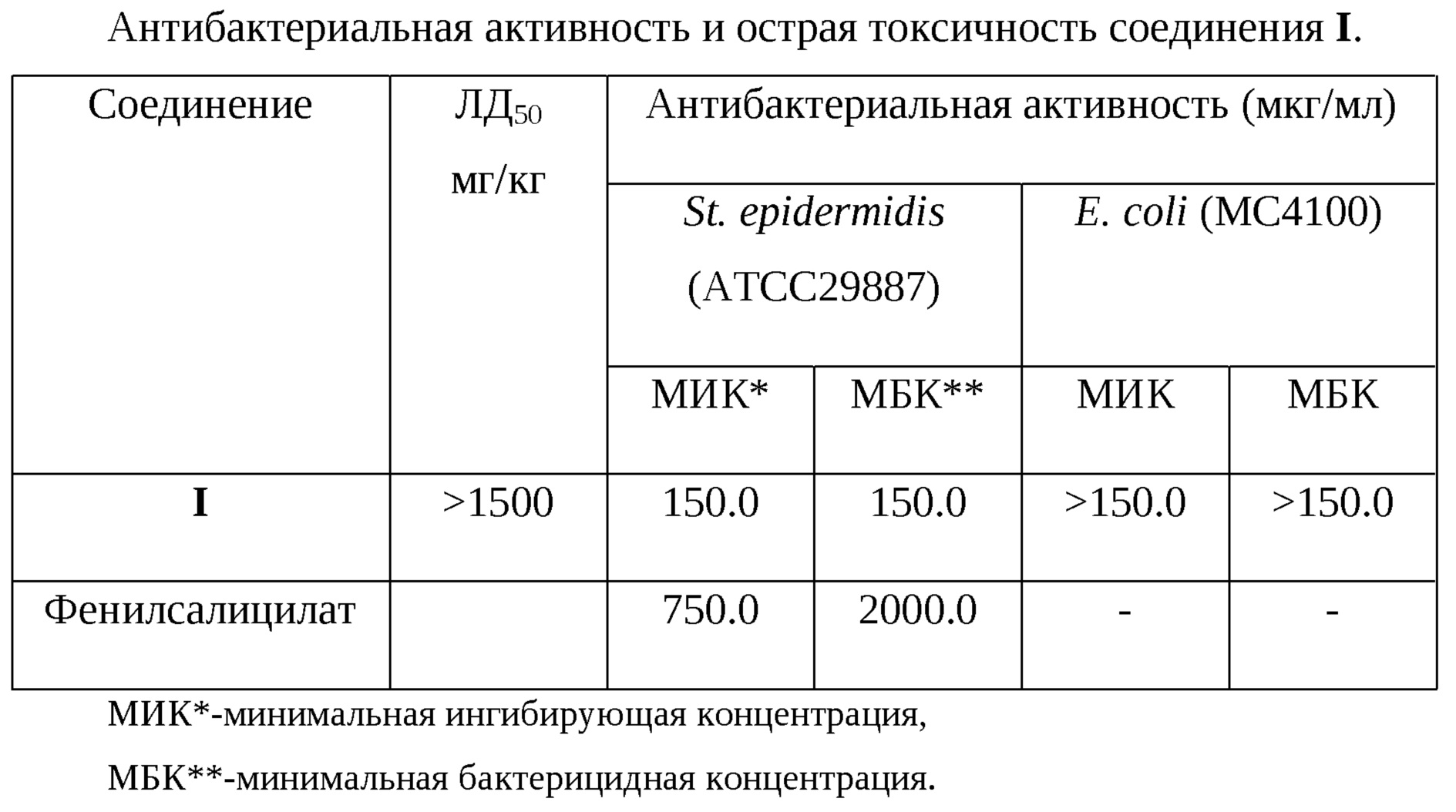
Как видно из таблицы, заявляемое соединение I превышает по антибактериальной активности препарат сравнения (Фенилсалицилат) в 5 раз по отношению к St. epidermidis. Таким образом, 4-(4,7-диметокси-3-фенилбензофуран-2-ил)бутан-2-он I проявляет более высокую активность по сравнению с эталоном сравнения в отношении грамположительных микроорганизмов, что делает возможным его использование для создания новых лекарственных средств целенаправленного действия.
Реферат
Изобретение относится к применению 4-(4,7-диметокси-3-фенилбензофуран-2-ил)бутан-2-ону формулы I

Технический результат: получено соединение, обладающее выраженной антибактериальной активностью в отношении грамположительных микроорганизмов, а также низкой токсичностью. 1 табл., 3 пр.
Формула


Комментарии