Противоопухолевая композиция, содержащая производные таксана - RU2131250C1
Код документа: RU2131250C1
Чертежи
Описание
Изобретение относится к комбинациям таксола, таксотера и их аналогов и веществ, терапевтически пригодных для лечения опухолевых заболеваний.
Таксол, таксотер и их аналоги, которые обладают ценными противоопухолевыми и антилейкемическими свойствами, особенно пригодны для лечения рака яичника, груди или легкого.
Получение таксола, таксотера и их производных составляет предмет изобретения, например, европейских патентов ЕР-0253733 и ЕР-0253739 и международной заявки РСТ ВОИС 9209589.
Обычно используемые дозы, которые зависят от присущих излечиваемому субъекту факторов, составляют 1 - 10 мг/кг при введении интраперитонеально или еще 1 - 3 мг/кг при введении внутривенно.
В настоящее время найдено и это составляет предмет настоящего изобретения, что эффективность таксола, таксотера и их аналогов может быть значительно улучшена, когда их вводят в комбинации по крайней мере с одним терапевтически пригодным для лечения от рака веществом, механизм действия которого идентичен или отличен от такового производных таксана.
Из веществ, которые могут быть использованы в ассоциации или в комбинации с таксолом, таксотером или их аналогами, можно назвать алкилирующие агенты, такие как циклофосфамид, ифосфамид, мелфалан, гексаметилмеламин, тиотепа или дикарбазин, антиметаболиты, такие как аналоги пиримидина, как 5-фторурацил, и цитарабин или его аналоги, такие как 2-фтор-дезоксицитидин, или аналоги фолиевой кислоты, такие как метотрексат, идатрексат или триметрексат; веретенные токсины, в том числе алкалоиды барвинка, такие как винбластин или винкристин, или их синтетические аналоги, такие как навелбин, или эстрамустин, или таксоиды, эпидофиллотоксины, такие как этопозид или тенипозид; антибиотики, такие как даунорубицин, доксорубицин, блеомицин или митомицин; ферменты, такие как L-аспарагиноза; ангибиторы топоизомеразы, такие как производные камптотецина, выбираемые среди таких, как СРТ-11 и топотекан, или производные пиридобензоиндола и различные агенты, такие как прокарбазин, митоксантрон; координационные комплексы платины, как цисплатина или карбоплатина; модификаторы биологического ответа или ингибиторы факторов роста, такие как интерфероны или интерлейкины.
Кроме того, поскольку активность продуктов зависит от используемых доз, можно применять более высокие дозы и можно повышать активность путем уменьшения явлений токсичности или замедления их появления за счет ассоциации с таксолом, таксотером, их аналогами или их комбинациями с другими веществами, терапевтически эффективными в отношении факторов роста кроветворного типа, такими как G-CSF, или GM-CSF, или некоторые интерлейкины.
Комбинации или ассоциации согласно изобретению позволяют избегать или задерживать явления плейотропической резистентности или "устойчивости ко многим лекарственным средствам".
Преимущественно изобретение относится к комбинациям таксола, таксотера и их аналогов с алкалоидами барвинка, циклофосфамидом, 5-фторурацилом, доксорубицином, цисплатиной и этопозидом.
Улучшенная эффективность комбинации согласно изобретению может быть продемонстрирована путем определения терапевтического синергизма.
Эффективность комбинации согласно изобретению также может быть охарактеризована сложением активностей каждой составляющей.
Комбинация проявляет терапевтический синергизм, если он терапевтически выше той или другой из составляющих, используемой в ее оптимальной дозе (T. H.CORBETT и сотр., Cancer Treatment Reports, 66, 1197 (1982)).
Для того чтобы продемонстрировать эффективность комбинации, необходимо сравнение максимально переносимой дозы комбинации по отношению к
максимально переносимой дозе каждой из отдельных составляющих при рассматриваемом исследовании. Эту эффективность можно оценивать количественно, например, за счет log10 умерщвленных клеток,
который определяют по следующей формуле:
log10 умерщвленных клеток = Т - С (дни) 3.32. Td, в которой: Т-С обозначает срок (промедление) роста клеток, который представляет собой
среднее время, в днях, для того, чтобы опухоли обработанной группы (Т) и опухоли контрольной группы (С) достигли заданной величины (например, 1 г); и Td обозначает время, в днях, необходимое для
удвоения объема опухоли у контрольных животных (T.H. CORBETT и сотр., Cancer, 40, 2660-2680 (1977); F.M. SCHABEL и сотр., Cancer Drug Development ч.В, Methods in Cancer Research., 17, 3-51, New-York,
Academic Press Inc. (1979)].
Продукт рассматривается как активный, если log10 умерщвленных клеток выше или равен 0,7. Продукт рассматривается как очень активный, если log10 умерщвленных клеток выше 2,8.
Комбинация, используемая в присущей ей максимально переносимой дозе, в которой каждая из составляющих находится в обычно более низкой или равной своей максимально переносимой дозе, демонстрирует терапевтический синергизм, когда log10 умерщвленных клеток выше величины log10 умерщвленных клеток наилучшей составляющей, если ее вводят индивидуально.
Эффективность комбинаций в отношении твердых опухолей может быть определена экспериментально следующим образом.
Подвергаемым эксперименту животным, обычно мышам, пересаживают билатерально подкожным путем 30 - 60 мг фрагмента опухоли в день 0. Животных, имеющих опухоли, перед тем, как подвергнуть их различным обработкам и контролям, перемешивают. В случае лечения прогрессирующих опухолей опухолям позволяют развиваться вплоть до желательного размера, причем животных, которые имеют недостаточно развившиеся опухоли, удаляют. Отобранных животных распределяют произвольно для того, чтобы подвергнуть их обработке. Животных, которые не имеют опухолей, также можно подвергнуть той же обработке, что и имеющих опухоли животных, чтобы можно было отделить токсичный эффект от присущего опухоли эффекта. Химиотерапию обычно начинают спустя 3 - 22 дня после пересадки в зависимости от типа опухоли, и животных наблюдают все дни. Различные группы животных взвешивают три или четыре раза в неделю вплоть до того момента, когда достигается максимальная потеря в весе, затем группы взвешивают по крайней мере один раз в неделю до окончания испытания.
Опухоли измеряют два или три раза в неделю до тех пор, пока опухоль не достигнет веса примерно 2 г, или до тех пор, пока не наступит гибель животного, если она наступает до того, как опухоль достигнет веса 2 г. При гибели животных вскрывают.
Противоопухолевую активность определяют в зависимости от различных регистрируемых параметров.
Для изучения комбинаций в случае лейкемий животным пересаживают определенное число клеток и противоопухолевую активность определяют по увеличению времени выживания обработанных мышей по отношению к контрольным животным. Продукт рассматривают как эффективный, если время увеличения выживания более 27%, и его рассматривают как очень эффективный, если это время выше 75%, в случае лейкемии Р 388.
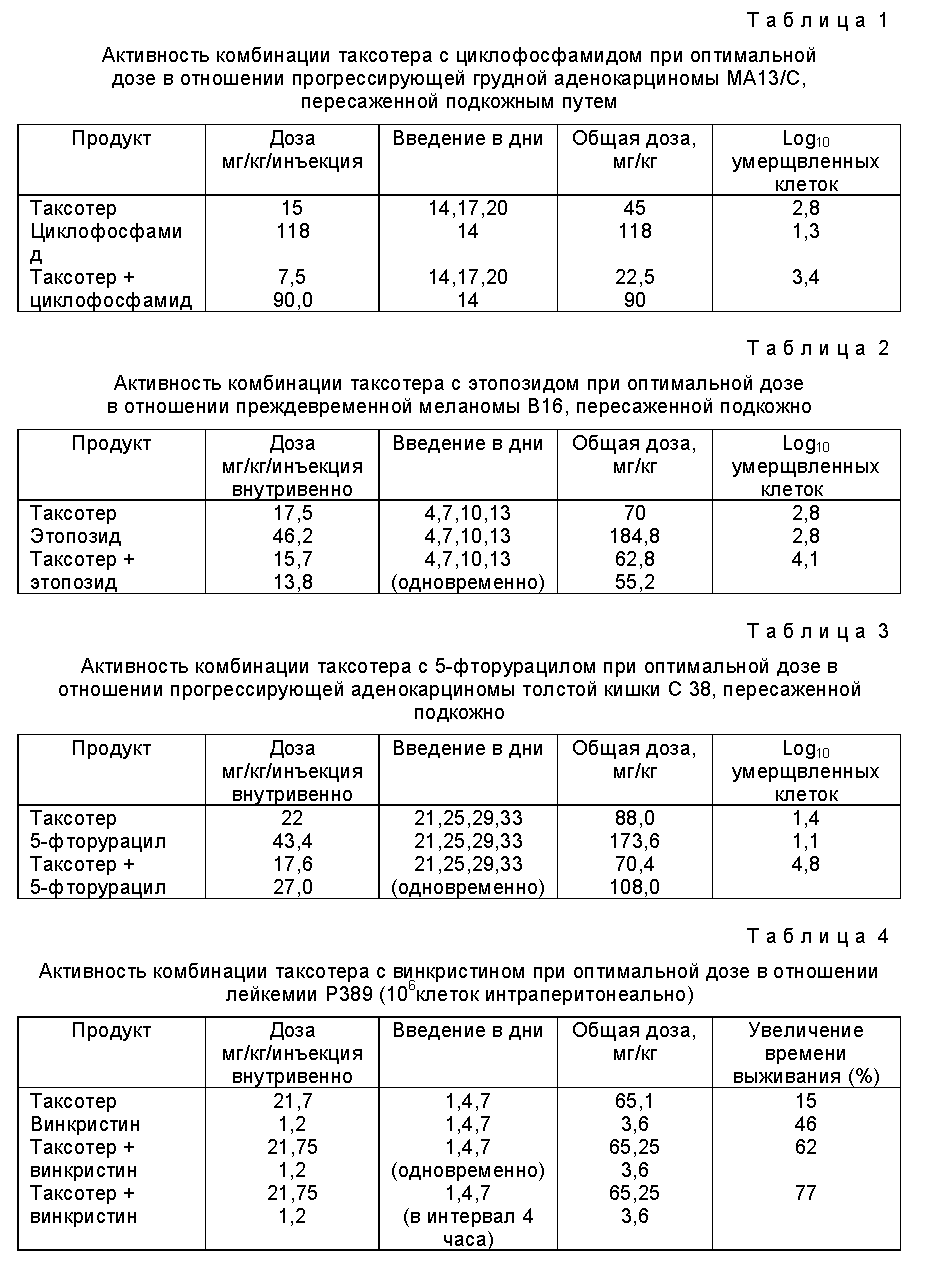
В качестве примеров в табл. 1 - 4 даются результаты, полученные при использовании комбинаций таксотера с различными химиотерапевтическими агентами, такими как циклофосфамид (алкилирующий агент), 5-фторурацил (антиметаболит), этопозид (полусинтетический агент подофиллотоксина) и винкристин (алкалоид барвинка), используемыми в их оптимальной дозе.
Настоящее изобретение также относится к фармацевтическим композициям, содержащим комбинации согласно изобретению.
Продукты, образующие комбинацию, можно вводить одновременно, раздельно или рассредоточенно во времени, чтобы достичь максимума эффективности комбинации; причем каждое введение может иметь изменяемую продолжительность, доходящую до полного быстрого введения при непрерывной перфузии.
Из этого следует, что, в смысле настоящего изобретения, комбинации не ограничиваются только такими, которые получают путем физической ассоциации составляющих, но также являются такими, которые позволяют осуществлять раздельное введение, которое может быть одновременным или рассредоточенным во времени.
Композиции согласно изобретению предпочтительно представляют собой вводимые парентерально композиции. Однако эти композиции можно вводить орально или интраперитонеально в случае локорегиональных терапий.
Композиции для парентерального введения обычно представляют собой стерильные, фармацевтически приемлемые растворы или суспензии, которые в случае необходимости можно приготовлять перед самым употреблением в момент использования. Для приготовления неводных растворов или суспензий можно использовать природные растительные масла, такие как оливковое масло, кунжутное масло или парафиновое масло, или сложные органические эфиры для инъекции, такие как этилолеат. Стерильные водные растворы могут представлять собой раствор продукта в воде. Водные растворы пригодны для внутривенного введения в соответствии с тем, что pH установлено надлежащим образом и где изотоничность реализована, например, за счет достаточного количества хлорида натрия или глюкозы. Стерилизацию можно осуществлять путем нагревания или любым другим способом, не ухудшающим композицию. Комбинации также могут находиться в форме липосом или в виде ассоциации с носителями, такими как циклодекстрины или полиэтиленгликоли.
Композиции для орального введения или интраперитонеального введения предпочтительно представляет собой водные растворы или суспензии.
В комбинациях согласно изобретению, в которых введение составляющих может быть одновременным, раздельным или рассредоточенным во времени, особенно предпочтительно, чтобы количество производного таксана составляло 10 - 90 вес. % комбинации, причем это количество может изменяться в зависимости от природы ассоциированного вещества, желаемой эффективности и природы излечиваемого рака.
Комбинации согласно изобретению особенно пригодны при лечении рака груди, яичника или легкого. Их преимущество состоит в том, что его составляющие используют в более незначительных дозах, чем если бы они использовались индивидуально.
Следующий пример иллюстрирует комбинацию согласно изобретению.
Пример.
Согласно обычной методике для внутривенного введения готовят ампулы объемом 10 см3, содержащие 100 мг таксотера.
Согласно обычной методике для внутривенного введения готовят ампулы, содержащие 100 мг этопозида.
Эти растворы вводят одновременно после соответствующего разбавления путем перфузии.
Обработку можно повторить несколько раз в день или в неделю вплоть до частичной или полной ремиссии (временного ослабления болезни) или выздоровления.
Реферат
Изобретение относится к химико-фармацевтической промышленности и касается противоопухолевой композиции, содержащей производные таксана. Изобретение заключается в том, что противоопухолевая композиция образована таксоидом или его аналогом, ассоциированным по крайней мере с одним веществом, терапевтически пригодным для лечения опухолевых заболеваний, а именно дополнительно содержит антинеопластичный агент при содержании таксоида 10-90 мас. % от массы активных компонентов. Изобретение позволяет улучшить эффективность комбинации средств. 12 з.п. ф-лы, 4 табл.

Комментарии