Прогностические факторы для лечения рака - RU2600026C2
Код документа: RU2600026C2
Чертежи

















































































Описание
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА СМЕЖНЫЕ ИЗОБРЕТЕНИЯ
Настоящая заявка испрашивает приоритет по предварительной заявке № 61/522596, поданной 11 августа 2011 года, и предварительной заявке № 61/560555, поданной 16 ноября 2011 года, которые обе полностью включены в настоящий документ путем ссылки.
ОБЛАСТЬ ПРИМЕНЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к лечению онкологических пациентов.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Несмотря на достижения в разработке успешных способов лечения рака, на ту или иную конкретную терапию всегда отвечает лишь подгруппа пациентов. При столь узком терапевтическом индексе и высоком токсическом потенциале многих доступных средств терапии рака из-за таких дифференцированных ответов пациентам могут назначаться излишние, неэффективные и даже потенциально опасные схемы лечения.
Один из способов оптимизации терапии для индивидуального лечения пациентов включает в себя возможность выявить у пациента один или более прогностических факторов, которые коррелируют с тем или иным конкретным результатом в ответ на выбранную схему лечения. См., например, публикации WO 2004/053066; WO 2006/133420; WO 2008/021183 и WO 2009/148528. Способность прогнозировать чувствительность пациентов к лекарственным средствам вызывает особенно большие трудности, поскольку реакция на лекарственное средство отражает как собственные характеристики клеток-мишеней, так и особенности метаболизма организма-хозяина.
Существует потребность в нахождении дополнительных прогностических маркеров для выявления онкологических пациентов, для которых можно ожидать благоприятных результатов при проведении конкретных схем лечения рака.
ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В настоящем изобретении предложен способ установления того, имеются ли у пациента более высокие шансы благоприятного исхода в ответ на ту или иную схему лечения рака, содержащий: определение присутствия, отсутствия или количества одного или более прогностических факторов у пациента, причем присутствие, отсутствие или количество прогностического фактора коррелируют с по меньшей мере одним благоприятным исходом.
Присутствие прогностических факторов можно определять по результатам анализа биологической пробы, взятой у указанного пациента. Лечение рака может содержать введение ингибитора протеосом, такого как бортезомиб. Прогностические факторы могут представлять собой один или более из низкого уровня CD68, полиморфизмов PSMB1 (P11A), PSMB5 (R24C), P65, времени с момента последней терапии рака, одного предыдущего лечения, низкого индекса FLIPI, возраста (65 лет или моложе) и низкой опухолевой нагрузки.
Также предложены диагностические наборы для выявления пациентов, которые будут с наибольшей вероятностью демонстрировать положительные результаты в ответ на используемую схему лечения рака.
В изобретении также предложены способы лечения онкологических пациентов путем определения присутствия, отсутствия или количества одного или более прогностических факторов у пациента и выбора способа лечения в зависимости от того, насколько вероятен ответ пациента на лечение.
Также предложены варианты использования ингибиторов протеосом для лечения рака, причем пациенты характеризуются одним или более из: низкого уровня CD68, полиморфизмов PSMB1 (P11A), PSMB5 (R24C), P65, времени с момента последней терапии рака, одного предыдущего лечения, низкого индекса FLIPI, возраста и низкой опухолевой нагрузки.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
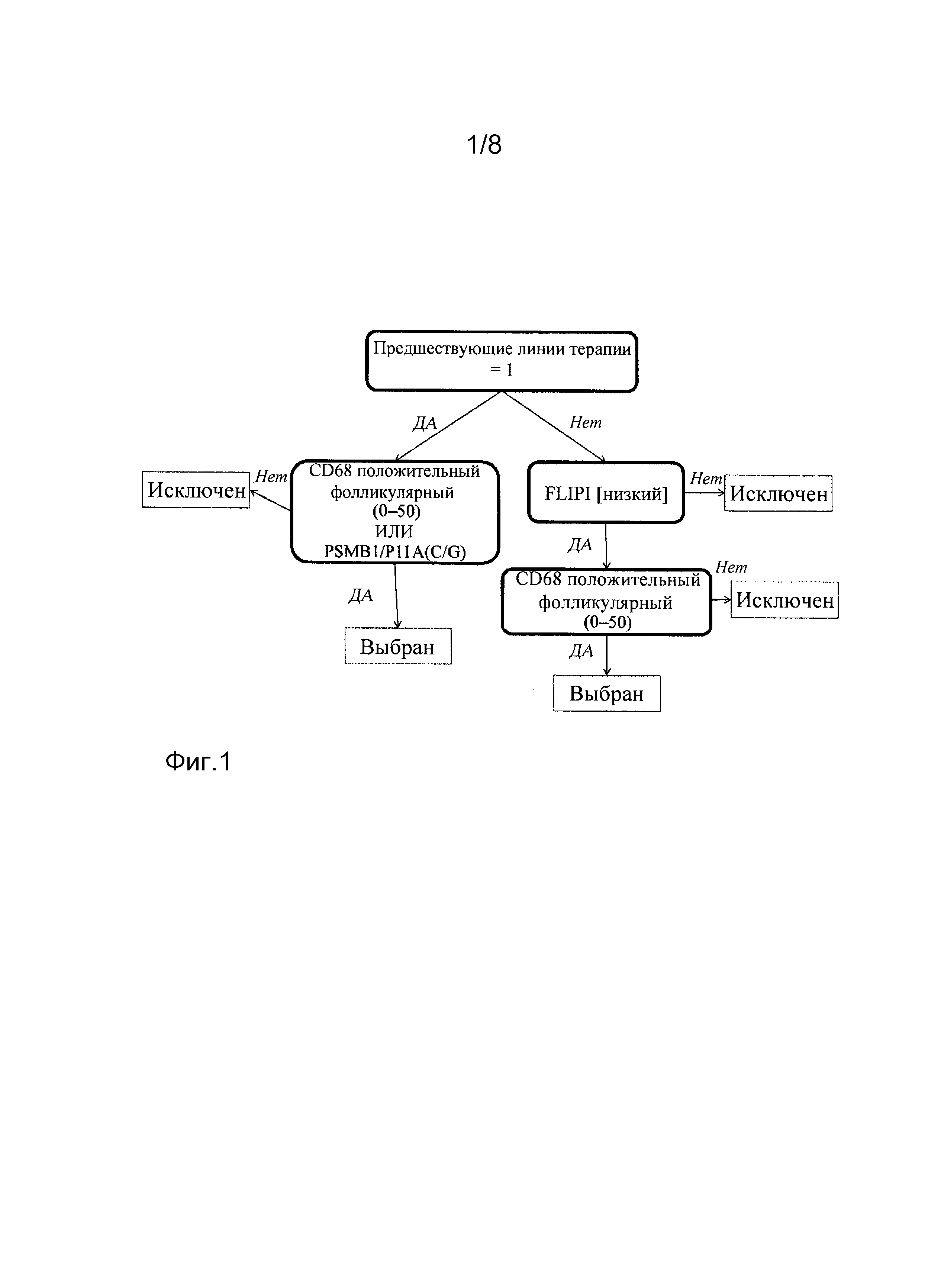
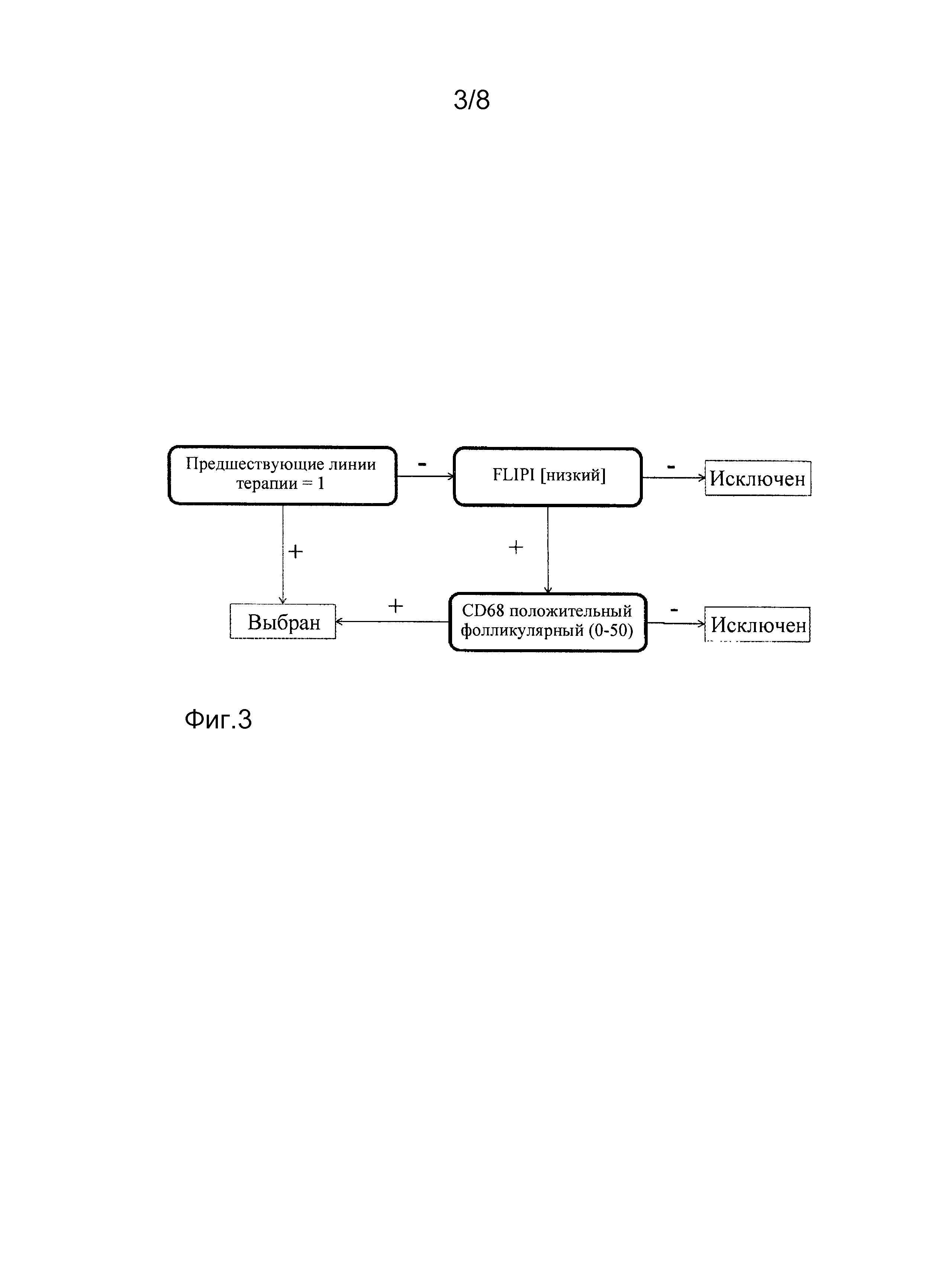
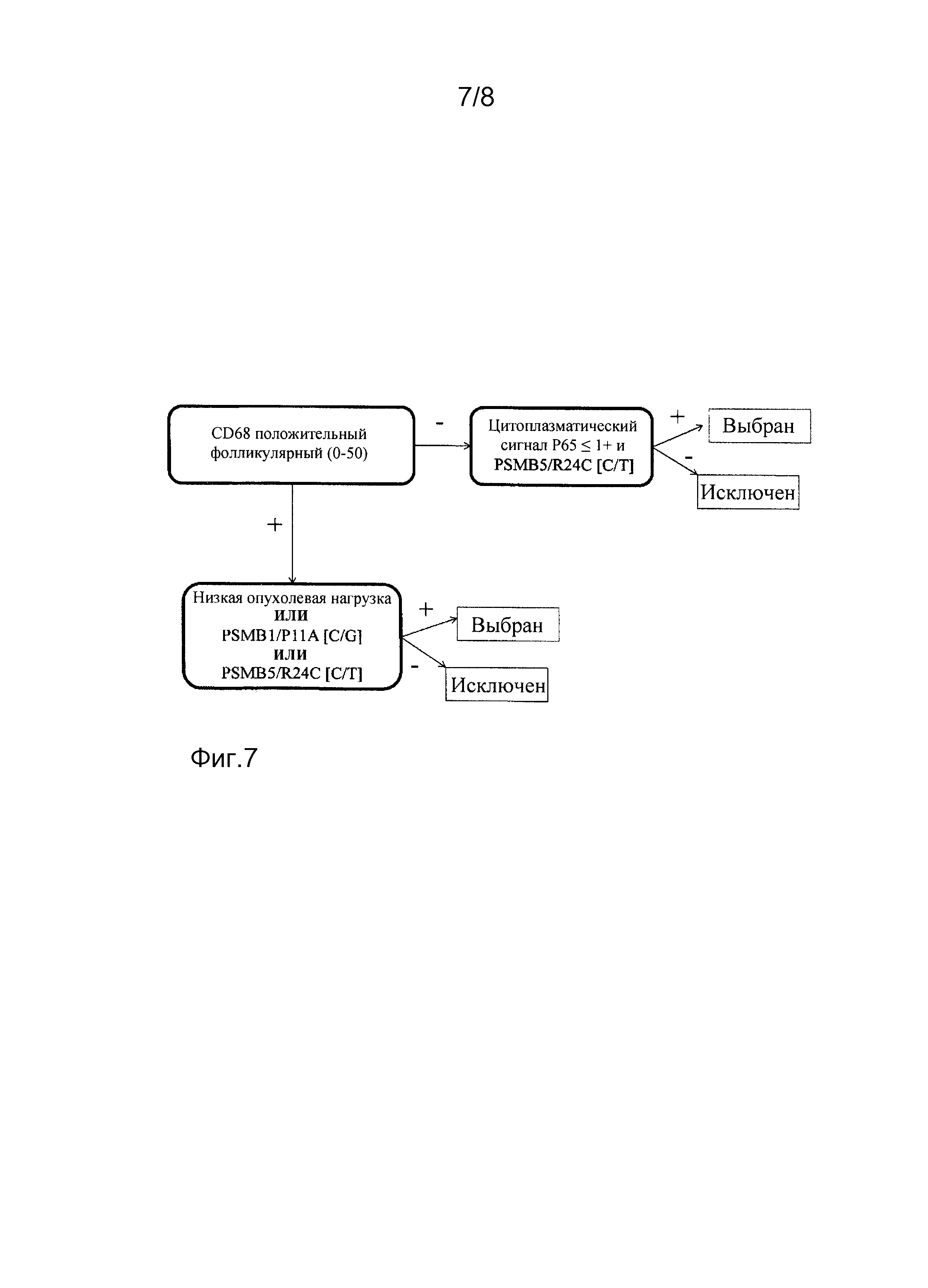
На фиг. 1-8 представлены деревья решений для определения того, будут ли у конкретного пациента более высокие шансы благоприятного исхода в ответ на ту или иную схему лечения. «Выбран» означает, что у пациента будут более высокие шансы благоприятного исхода в ответ на выбранную схему лечения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении описываются прогностические факторы, которые служат подходящими инструментами для прогнозирования и планирования при лечении рака. Прогностические факторы предсказывают, будет ли получен благоприятный исход в ответ на ту или иную конкретную схему лечения, например, лечение с использованием ингибитора протеосом.
В настоящем изобретении без ограничений предложены (a) способы прогнозирования ответа на схему лечения у онкологического пациента путем определения присутствия или отсутствия одного или более прогностических факторов, (b) наборы, которые можно использовать для определения присутствия или количества одного или более прогностических факторов, (c) способы лечения рака путем выбора пациентов, исходя из присутствия или количества одного или более прогностических факторов, и (d) лечение рака у пациентов с одним или более прогностическими факторами.
В некоторых вариантах осуществления предложен способ прогнозирования ответа на схему лечения рака (например, лечение с использованием ингибитора протеосом, такого как бортезомиб) у онкологических пациентов, содержащий определение присутствия или количества прогностического фактора у пациента или в биологической пробе, взятой у пациента; и причем присутствие или количество прогностического фактора коррелируют с по меньшей мере одним положительным исходом. Некоторые варианты осуществления содержат определение присутствия или количества второго прогностического фактора у пациента или в биологической пробе, взятой у пациента, при этом присутствие или количество второго прогностического фактора коррелируют с по меньшей мере одним положительным исходом.
Настоящее изобретение включает идентификацию прогностических факторов, которые в настоящем документе называются «вариантами», «маркерами», «биомаркерами» и/или «факторами» и которые коррелируют с более высокой вероятностью благоприятного ответа на используемую схему лечения рака. Связь ответа пациента на схему лечения рака с такими прогностическими факторами может укрепить или повысить уверенность в отношении безопасности и/или эффективности конкретной выбранной схемы лечения. В качестве прогностических факторов могут выступать ген, белок, характеристика пациента или аспект истории болезни пациента.
Прогностические факторы в соответствии с настоящим изобретением, которые коррелируют с по меньшей мере одним благоприятным исходом, включают в себя низкий уровень CD68, полиморфизм PSMB1 (P11A), полиморфизм PSMB5 (R24C), P65, возраст (до 65 лет), одно предыдущее лечение, низкий показатель Международного прогностического индекса для фолликулярных лимфом (FLIPI), время с момента последней противораковой терапии и низкую опухолевую нагрузку. У пациента предпочтительно должен быть низкий уровень CD68 или полиморфизм PSMB1 (P11A), а также еще по меньшей мере один прогностический фактор. В одном варианте осуществления пациент имеет низкий уровень CD68 и полиморфизм PSMB1 (P11A). Пары прогностических факторов в соответствии с настоящим изобретением, которые коррелируют с по меньшей мере одним благоприятным исходом, включают в себя пары, приведенные в таблицах 6 и 7.
Выражение «низкий уровень CD68» означает, что у субъекта или в биологической пробе, взятой у пациента, обнаруживается меньшее количество CD68, чем у среднего пациента или в биологических пробах, взятых у среднего пациента, который страдает тем же заболеванием. В некоторых вариантах осуществления низкий уровень CD68 означает, что 25% или менее клеток в биологической пробе экспрессируют CD68; 50% или менее клеток в биологической пробе экспрессируют CD68; 25% или менее фолликулярных клеток в биологической пробе экспрессируют CD68; 50% или менее фолликулярных клеток в биологической пробе экспрессируют CD68; 25% или менее перифолликулярных клеток в биологической пробе экспрессируют CD68; или 50% или менее перифолликулярных клеток в биологической пробе экспрессируют CD68.
Выражение «низкий индекс FLIPI» означает показатель 0 или 1 балл по шкале Международного прогностического индекса для фолликулярных лимфом (индекс FLIPI). При определении индекса FLIPI каждому из перечисленных ниже факторов присваивается один балл: возраст более 60 лет, III или IV стадия заболевания, поражение более 4 групп лимфатических узлов, уровень сывороточного гемоглобина ниже 12 г/дл и повышенный уровень сывороточной ЛДГ.
Термины «содержащий», «состоящий», «имеющий» и «включающий» используются в настоящем документе в их открытом, неограниченном значении.
«Количество» может означать величину, интенсивность, концентрацию, количество, степень или уровень экспрессии. Например, под количеством того или иного гена может пониматься число раз, которое этот ген или его часть присутствует в геноме субъекта или в клетках субъекта. Количество может также подразумевать численность клеток в биологической пробе, экспрессирующих тот или иной маркер, или общий уровень экспрессии или интенсивность маркера в биологической пробе. Под количеством может также пониматься число типов или линий терапии пациента, которые могли в прошлом применяться для лечения данного пациента. Количество может сопоставляться с абсолютной величиной, со стандартной пробой здорового пациента, со средним показателем здоровых пациентов или сравниваться со средним показателем пациентов, страдающих аналогичным заболеванием.
Схема лечения рака может включать в себя введение одного лекарственного средства или проведение одной терапии или же представлять собой комбинированную терапию, предусматривающую введение более одного лекарственного средства или проведение более одной терапии. Схема лечения рака может представлять собой химиотерапию, радиотерапию или иммунотерапию; или схема лечения рака может представлять собой трансплантацию костного мозга.
В некоторых вариантах осуществления схема лечения рака содержит введение пациенту ингибитора протеосом. Ингибитор протеосом представляет собой любое вещество, которое подавляет ферментативную активность протеосомы 20S или 26S in vitro или in vivo. В некоторых вариантах осуществления ингибитор протеосом представляет собой пептидилборную кислоту. Пептидилборные кислоты включают в себя бортезомиб. Ингибиторы протеосом включают в себя соединения, раскрытые в патентах США №№ 5756764; 5693617; 6831099; 6096778; 6075150; 6018020; 7119080; 6747150; 6617317; 6548668; 6465433; 6297217; 6083903; 6066730; 5780454; 7422830; 7109323; 6958319; 6713446 и 6699835. Ингибитор протеосом может представлять собой бортезомиб.
В некоторых вариантах осуществления схема лечения рака содержит применение противораковых агентов, включая, без ограничений, применение ацеманнана, акларубицина, альдеслейкина, алемтузумаба, алитретиноина, алтретамина, амифостина, аминоглютетимида, амсакрина, анагрелида, анастрозола, анцестима, аспарагиназы, бевацизумаба, бексаротена, броксуридина, капецитабина, целмолейкина, цетрореликса, цетуксимаба, кладрибина, клофарабина, клотримазола, даклизумаба, дексразоксана, дилазепа, докозанола, доксифлуридина, бромокриптина, кармустина, циклофосфамида, цитарабина, диклофенака, эделфосина, эдреколомаба, эфлорнитина, эмитефура, эксеместана, экзисулинда, фадрозола, филграстима, финастерида, флударабина фосфата, форместана, фотемустина, нитрата галлия, гемцитабина, гликопина, гептаплатина, гидроксимочевины, ибандроновой кислоты, имиквимода, йобенгуана, иринотекана, ирсогладина, ланреотида, лефлуномида, ленограстима, лентинана сульфата, летрозола, лиарозола, лобаплатина, лонидамина, мазопрокола, мелазопрола, мелфалана, меркаптопурина, метотрексата, метоклопрамида, мифепристона, милтефозина, миримостима, митогуазона, митолактола, митомицина, митоксантрона, молграмостима, нафарелина, нартограстима, недаплатина, нилутамида, носкапина, опрелвекина, озатерона, оксалиплатина, памидроновой кислоты, пегаспаргазы, пентозана полисульфата натрия, пентостатина, пицибанила, пирарубицина, порфимера натрия, преднизолона, ралоксифена, ралтитрекседа, рекомбинантной урат-оксидазы, ритуксимаба, ромуртида, сарграмостима, сизофурана, собузоксана, сонермина, стероидов, сурамина, тазонермина, тазаротена, тегафура, темопорфина, темозоломида, тенипозида, тетрахлордекаоксида, талидомида, тималфасина, альфа-тиротропина, топотекана, торемифена, трастузумаба, треосульфана, третиноина, трилостана, триметрексата, убенимекса, вальрубицина, вертепорфина, винкристина, винбластина, виндезина и винорелбина. В предпочтительном варианте осуществления схема лечения рака содержит применение ритуксимаба. В других предпочтительных вариантах осуществления схема лечения рака содержит применение мелфалана или преднизона или комбинации мелфалана и преднизона.
В некоторых вариантах осуществления схема лечения рака представляет собой комбинированную терапию. Комбинированная терапия может содержать лечение ингибитором протеосом и еще одну противораковую терапию или применение еще одного противоракового агента. В некоторых вариантах осуществления другой противораковый агент представляет собой моноклональное антитело, например ритуксимаб. В других вариантах осуществления другой противораковый агент представляет собой мелфалан, преднизон или комбинацию мелфалана и преднизона.
Благоприятным исходом может быть общая частота ответа, общий уровень выживаемости, общая частота полного ответа, продолжительность ответа, более продолжительное время до следующей терапии, продолжительность периода без лечения, положительный ответ на лечение, более продолжительное время до прогрессирования заболевания, более продолжительный период выживаемости и/или более продолжительная выживаемость без прогрессирования заболевания. Благоприятный исход может зависеть от дозы или не зависеть от дозы. Благоприятный исход может быть благоприятным по сравнению с отсутствием лечения или по сравнению с другой схемой или схемами лечения рака.
Термины «рак» или «опухоль» включают в себя любые формы новообразований в организме пациента, в том числе первоначальную опухоль и любые метастазы. Рак может быть гематологическим или принимать форму солидной опухоли. Гематологические формы рака включают в себя, например, миеломы (например, множественная миелома), лейкозы (например, макроглобулинемия Вальденстрема, острый миелобластный лейкоз, хронический лимфоцитарный лейкоз, гранулоцитарный лейкоз, моноцитарный лейкоз, лимфоцитарный лейкоз) и лимфомы (например, фолликулярная лимфома, лимфома из клеток мантии, диффузная В-крупноклеточная лимфома, лимфосаркома, плазмоцитома, ретикулосаркома, болезнь Ходжкина, неходжкинская лимфома или фолликулярная В-клеточная неходжкинская лимфома). Солидные опухоли могут возникать в различных органах и включают в себя такие формы рака, как рак головного мозга, рак кожи, рак легких, рак молочной железы, рак простаты, рак яичников, рак толстой кишки, рак почек и рак печени. Рак может быть в первичном месте, в форме метастазов, резистентным (то есть устойчивым по отношению к одной или более линиям терапии) и/или рецидивным. В некоторых вариантах осуществления рак представляет собой фолликулярную В-клеточную неходжкинскую лимфому или множественную миелому.
Если в организме пациента присутствует прогностический фактор, его присутствие, отсутствие или количество можно оценить путем взятия биологической пробы у пациента и определения того, содержит ли указанная биологическая проба прогностический фактор или в каком количестве указанная биологическая проба содержит прогностический фактор. Используемый в настоящем документе термин «биологическая проба» относится к образцу, содержащему или состоящему из тканей, клеток, биологических жидкостей и их изолятов, взятых у субъекта, а также тканей, клеток и жидкостей, присутствующих в организме субъекта. Примеры биологических проб включают в себя, например, мокроту, кровь, клетки крови (например, лейкоциты), амниотическую жидкость, плазму, сыворотку, сперму, слюну, костный мозг, ткань или пробы тонкоигольной биопсии, мочу, перитонеальную жидкость, плевральную жидкость и клеточные культуры. Биологические пробы также могут включать в себя срезы тканей, например, замороженные срезы, взятые для гистологического исследования. В некоторых вариантах осуществления биологическая проба может представлять собой или включать в себя клетки опухоли. Биологические пробы из гематологической опухоли могут включать в себя костный мозг и/или периферическую кровь.
Обнаружение прогностических факторов в биологической пробе можно проводить любым стандартным способом обнаружения такого рода прогностического фактора, например путем прямого измерения, иммуногистохимического анализа, иммуноблоттинга, иммунофлуоресценции, иммуноабсорбции, иммуноосаждения, белкового чипа, флуоресцентной гибридизации in situ, анализа FACS, гибридизации, гибридизации in situ, Нозерн-блоттинга, Саузерн-блоттинга, Вестерн-блоттинга, ИФА, радиоиммуноанализа, генного чипа, ПЦР, ОТ-ПЦР или цитогенетического анализа.
Если прогностический фактор основан на конкретном генотипе или полиморфизме, биологическую пробу можно анализировать генотипированием. Термин «генотип» относится к аллелям, присутствующим в ДНК субъекта или пациента, причем такой аллель может определяться конкретным(-и) нуклеотидом(-ами), присутствующим(-и) в последовательности нуклеиновой кислоты в конкретном(-ых) сайте(-ах). Генотипом часто оказывается(-ются) нуклеотид(-ы), присутствующие в одном полиморфном сайте, который варьируется в человеческой популяции. «Генотипированием» называют процесс определения генотипа человека с помощью биологического анализа. К современным методам такого анализа относятся ПЦР, секвенирование ДНК, зонды на основе антисмысловых олигонуклеотидов и гибридизация на микрочипах или гранулах ДНК.
«Однонуклеотидный полиморфизм» (SNP, произносится «снип») представляет собой вариацию последовательности ДНК, при которой наблюдаются отличия одного нуклеотида - A, T, C или G - в геноме (или иной общей последовательности) между представителями вида (или между парными хромосомами отдельного человека). Например, две последовательности фрагментов ДНК различных людей - AAGCCTA и AAGCTTA - содержат различие по одному нуклеотиду. В этом случае говорят, что существует два аллеля: C и T. Почти все распространенные SNP имеют всего два аллеля.
Для выявления присутствия или отсутствия по меньшей мере одной вариации генотипа используют взаимодействие последовательности нуклеиновой кислоты, соответствующей одному из генов, определенных в настоящем документе, или продукта такого гена, с зондом. Зонд способен различать конкретную форму гена или генетического продукта, или присутствие конкретной вариации или вариаций, например, за счет дифференциального связывания или гибридизации.
Если прогностическим фактором является присутствие или количество (в том числе уровень экспрессии) конкретного гена или белка, такое присутствие или количество (в том числе уровень экспрессии) можно определять иммуногистохимическим анализом биологической пробы.
В некоторых вариантах осуществления предложен набор для выявления пациентов, которые являются кандидатами на проведение схемы лечения рака, содержащий первый реагент для определения присутствия или количества одного из прогностических факторов настоящего изобретения в биологической пробе и второй реагент для определения присутствия или количества второго прогностического фактора настоящего изобретения в биологической пробе, а также инструкцию по применению прогностических факторов для выявления пациентов, которые являются кандидатами для проведения указанного лечения. В некоторых вариантах осуществления первый реагент определяет количество CD68, а второй реагент определяет полиморфизм PSMB1 (P11A) или полиморфизм PSMB5 (R24C). Реагенты могут представлять собой антитела (например, при тестировании CD68), или они могут представлять собой зонды или наборы зондов (например, при обнаружении полиморфизма генов).
В некоторых вариантах осуществления предложен способ лечения рака у пациента, содержащий: определение присутствия или количества первого прогностического фактора у пациента или в биологической пробе указанного пациента; и определение присутствия или количества второго прогностического фактора у указанного пациента или в биологической пробе указанного пациента; и выбор способа лечения в зависимости от вероятности ответа указанного пациента на указанное лечение.
Настоящее изобретение также предлагает варианты использования ингибиторов протеосом для лечения рака у пациента, где пациент характеризуется присутствием, отсутствием или количеством по меньшей мере одного прогностического фактора, коррелирующего с по меньшей мере одним положительным исходом в ответ на применение ингибитора протеосом.
Все цитируемые в настоящем документе публикации включены в него путем ссылки. Все технические и научные термины, используемые в настоящем документе, если не указано иное, имеют общепринятое значение, понятное любому специалисту, работающему в области, к которой относится данное изобретение.
ПРИМЕР 1
К неходжкинским лимфомам (NHL) относятся несколько отдельных злокачественных лимфоидных заболеваний, которые различаются по клиническим характеристикам, морфологическим проявлениям, иммунологическим и молекулярным фенотипам. Фолликулярная лимфома (FL), наиболее распространенная вялотекущая NHL, демонстрирует схожую вариабельность, при этом у некоторых пациентов заболевание развивается очень медленно, тогда как у других заболевание прогрессирует и приводит к смерти в течение всего 5 лет (Dave 2004). Проводилось рандомизированное открытое многоцентровое международное проспективное исследование с активным контролем по сопоставлению эффективности и безопасности комбинации бортезомиба и ритуксимаба (Vc-R) с монотерапией ритуксимабом у субъектов с рецидивом или резистентной фолликулярной В-клеточной NHL, ранее не получавших ритуксимаб или чувствительных к ритуксимабу.
Субъектов централизованно случайным образом распределили по группам лечения A (Vc-R) или B (ритуксимаб) в соотношении 1:1 с учетом следующих факторов стратификации:
- показатель Международного прогностического индекса для фолликулярных лимфом (FLIPI) (низкий [0 или 1 фактор], промежуточный [2 фактора], высокий [≥3 факторов]);
- предшествующая терапия ритуксимабом (да, нет);
- время после последней дозы противолимфомной терапии (≤1 года, >1 года);
- регион (Соединенные Штаты Америки/Канада, Европейский Союз, остальные страны).
Собирали пробы опухоли для анализа ДНК и белков, а также образцы крови для анализа ДНК.
Выбранными белками-кандидатами были NF-κB (RELA/p65), PSMA5, p27 и CD68. Активность перечисленных белков снижается при лечении бортезомибом (NF-κB (RELA/p65); PSMA5, p27), регулируется по каналу убиквитин-протеосома (p27) или ассоциируется с неблагоприятным прогнозом по лимфоме (CD68). Повышенные уровни экспрессии NF-κB (RELA/p65) ассоциировали с более продолжительным временем до прогрессирования заболевания (TTP) при лимфоме из клеток мантии (MCL) и при множественной миеломе (Goy 2010, Mulligan 2007 и Keats 2007). Более низкий уровень экспрессии PSMA5 связали с более продолжительным TTP при MCL (Goy 2010). Анализ выживаемости в исследовании MCL также показал, что более высокие уровни p27 коррелировали с более высокой общей выживаемостью (OS) (Goy 2010). CD68 также рассматривался ранее и, как недавно было показано, является прогностическим маркером для неблагоприятного исхода при лимфоме, а также ассоциируется с ответом на терапию ритуксимабом. Генами-кандидатами, выбранными для анализа соматических мутаций, были Bcl-2 и Notch-1. Рассматривали и других кандидатов, но их не включили в исследование, поскольку частота их известных мутаций при проявлениях лимфомы была менее 10%. Кроме того, из собранных проб выделяли лишь небольшие количества ДНК, поэтому анализ ограничили упомянутыми двумя кандидатами. Ген Bcl-2 имеет частоту мутаций 23% при В-клеточной лимфоме и 50% при фолликулярной лимфоме (Arif 2009), а частота мутаций гена Notch-1 составляет 24%. Bcl-2 представляет собой важный антиапоптозный белок с повышенным уровнем экспрессии при агрессивных лимфомах, и ранее проведенные исследования показывают, что бортезомиб преодолевает опосредованную Bcl-2 защиту (Fischer 2005, Yin 2005, Yeung 2006, Mitsiades 2002 и Wojcik 2002). Известно, что Notch-1 увеличивает время пребывания NF-κB (RELA/p65) в ядре (Shin 2006). Такое действие прямо противоположно бортезомибу, который не позволяет NF-κB достигать ядра, ингибируя протеосомное разрушение белков I-kappa-B, роль которых заключается в удержании NF-κB в цитоплазме. Опосредованное Notch-1 повышенное время пребывания NF-κB в ядре активирует транскрипцию регуляторов клеточного цикла, например, циклинов D1 и D2, что может способствовать повышенной регуляции генов, задействованных в иммунных и воспалительных процессах (Karin 2002). Было предположено, что мутации, обнаруженные в функциональных последовательностях этих двух генов, способствуют различиям в индивидуальных ответах на лечение бортезомибом.
Также включили гены-кандидаты мишеней для лекарственного средства, как для бортезомиба (PSMB1, 2, 5, 6, 8, 9), так и для ритуксимаба (FCGR2A, FCGR3A). Химическая структура бортезомиба обеспечивает его взаимодействие с субъединицами 1, 2 и 5 PSMB, и существуют подтвержденные свидетельства полиморфизма в таких субъединицах, а также в субъединицах 6, 7 и 8 PSMB. Полиморфизм в субъединицах может влиять на способность лекарственного средства к эффективному связыванию, или же может препятствовать автокаталитической трансформации пропоследовательностей, что может повлечь за собой вариабельность в уровнях протеосом и/или ответа на бортезомиб у разных пациентов. В случае ритуксимаба присутствие однонуклеотидных полиморфизмов (SNP), соответствующих фенотипической экспрессии валина (V) или фенилаланина (F) на аминокислоте 158 в FCGR3A, а также гистидина (H) или аргинина (A) на аминокислоте 131 в FCG2A, существенно влияет на аффинность IgG к рецептору Fcγ (Binstadt 2003, Wu 1997). Экспрессия высокоаффинного аллеля V в положении 158 приводит к более прочному связыванию FCG3A с IgG1 и IgG3, тогда как низкоаффинный аллель F ассоциируется с более слабым связыванием FCG3A с IgG. Аналогичным образом, высокоаффинный аллель H в положении 131 приводит к более высокой аффинности FCGR2A к IgG2, тогда как низкоаффинный аллель A коррелирует со снижением эффективности связывания.Корреляция таких низкоаффинных полиморфизмов ассоциировалась с худшим клиническим ответом и более низкой выживаемостью без прогрессии заболевания (PFS) после терапии ритуксимабом при исследованиях NHL (Cartron 2002). Поэтому был проведен анализ возможности ответа субъектов с такими полиморфизмами на лечение с использованием комбинированной терапии Vc-R, поскольку это может стать альтернативной терапией для пациентов с ограниченными вариантами лечения.
Цели этого исследования заключались в том, чтобы выявить популяции пациентов, которые с большей или меньшей вероятностью ответили бы на лечение Vc-R или на монотерапию ритуксимабом, для чего:
- проводили ассоциативный анализ уровней экспрессии белков CD68, NF-κB (RELA/p65), PSMA5 и p27 с выбранными конечными точками клинических исследований;
- проводили ассоциативный анализ соматических мутаций Notch-1 и Bcl-2 (отдельно и в комбинации) с выбранными конечными точками клинических исследований;
- проводили ассоциативный анализ полиморфизмов FCGR2A и FCGR3A (SNP) с выбранными конечными точками клинических исследований;
- полиморфизмов PSMB1, PSMB2, PSMB5, PSMB6, PSMB8 и PSMB9 (SNP) с выбранными конечными точками клинических исследований;
- проводили исследование комбинаций биомаркеров с выбранными конечными точками клинических исследований.
Поправки для множественных сравнений проводили с использованием уровня ложноположительных результатов (FDR) для парных сравнений и путем ускоренного отбора при сравнении комбинаций множества биомаркеров. С практической точки зрения FDR представляет собой ожидаемую долю ложноположительных результатов; например, если прогнозируется расхождение 1000 наблюдений, и FDR для этих наблюдений составляет 0,10, то ожидается, что 100 из этих наблюдений будут ложноположительными. Чрезмерно близкую подгонку контролировали путем перекрестной проверки и независимой внутренней проверки результатов анализа.
Гены с существенными вариациями включают в себя:
FCGR2A (H166R, Q62R, Q62X)
FCGR3A (V212F)
PSMB1 (P11A)
PSMB5 (R24C)
PSMB8 (G8R)
PSMB9 (R60H, V32I)
PSMA (положительный для окрашивания ядра и цитоплазмы)
CD68 (общий положительный, положительный для фолликулярных клеток, положительный для перифолликулярных клеток)
P27 (положительный для ядра, шкала интенсивности)
RELA/p65 (положительный для окрашивания ядра и цитоплазмы, шкала интенсивности).
Популяцию в соответствии с назначенным лечением (ITT) определяли как совокупность всех рандомизированных субъектов. Результаты для субъектов в этой популяции анализировали в соответствии со схемой лечения, для которой они были рандомизированы. Оценку биомаркеров в данной популяции проводили после подготовки данных по биомаркерам для выбранных конечных точек клинического исследования.
Уровни экспрессии белковых маркеров (CD68, NF-κB (P65), PSMA5, P27) определяли иммуногистохимическим анализом (IHC). Для анализов единичных маркеров использовали следующие точки отсечения по уровню экспрессии:
CD68:
% положительный фолликулярный (0-25, 26-50, 51-75, >75),
% положительный перифолликулярный (0-25, 26-50, 51-75, >75),
общий % положительный (0-25, 26-50, 51-75, >75)
NF-κB (p65):
% положительный цитоплазматический сигнал (отсечение <90%, >91%),
% положительный ядерный сигнал (0, <5%, >5%)
интенсивность ядерного окрашивания (<1+, >2+)
PSMA5:
% положительный цитоплазматический сигнал (0-20, 30-50, 60-70, 80-90)
% положительный ядерный сигнал (0-20, 30-50, 60-70, 80-90)
интенсивность цитоплазматического окрашивания (<2+, 3+)
положительный ядерный по сравнению со всеми остальными
P27:
% положительное ядерное окрашивание (0-20, 30-50, 60-70, 80-100)
интенсивность ядерного сигнала (<1+, >2+)
Точки отсечения для парных сравнений выбирали для уменьшения общего числа проводимых сравнений. Выбранные точки отсечения приведены в таблице 1:
Данные зародышевого SNP для субъединиц PSMB и генов FCGR2A и FCGR3A получали с помощью стандартных методик полимеразной цепной реакции (ПЦР). Обнаруженные в ходе этих анализов аллели приведены в таблице 2:
Для каждой группы лечения в анализ включали перечисленные ниже конечные точки клинических исследований и проводили общее сравнение с ассоциированными с биомаркерами конечными точками: выживаемость без прогрессирования заболевания, определяемая как промежуток времени между датой рандомизации и датой прогрессирования заболевания (PD) или смерти, в зависимости от того, какой исход был зафиксирован первым в ITT-популяции; общая выживаемость; общая частота ответа (полный ответ [CR] + неподтвержденный CR [CRu] + частичный ответ [PR]); общая частота CR (CR + CRu); продолжительность ответа; время до следующей противолимфомной терапии; и перерыв между проведением терапии.
В анализ включали субъектов, которые соответствовали всем перечисленным ниже критериям: субъекты из ITT-популяции; субъекты с допускающими количественный анализ данными по биомаркеру, полученными с помощью иммуногистохимического анализа или ПЦР; и субъекты с клиническими данными для по меньшей мере одной из перечисленных выше конечных точек клинического исследования.
Первичный анализ биомаркеров был направлен на выявление дифференциально экспрессируемых белков, мутаций или генотипов, которые связывали с конечными точками клинического исследования. В анализ включали следующие коварианты: индекс FLIPI (низкий [0 или 1 фактор], промежуточный [2 фактора], высокий [≥3 факторов]); предшествующая терапия ритуксимабом (да, нет); время после последней дозы противолимфомной терапии (≤1 года, >1 года); регион (США/Канада, Европейский союз, остальной мир), возраст, пол, раса, стадия по классификации Анн Арбор (I, II, III, IV), количество проведенных ранее линий терапии (1, 2 и более) и высокая опухолевая нагрузка (да, нет).
Для ассоциативных анализов единичных маркеров и парных сравнений использовали логранговый критерий и модель пропорциональных рисков Кокса для оценок PFS, TTP и OS между группами лечения. Для оценки различий распределения между группами при анализе времени до наступления события использовали кривые Каплана-Мейера. Сравнение частоты ответа между группами лечения проводили с использованием точного критерия Фишера. Ассоциативные анализы единичных маркеров стратифицировали по ковариантам.
Для анализа при парном сравнении пары биомаркеров формировали комбинациями двух маркеров. Для оценки PFS, TTP и OS между группами лечения в подпопуляции, определяемых парами биомаркеров, использовали логранговый критерий. Для оценки различий распределения между группами при анализе времени до наступления события использовали кривые Каплана-Мейера. Сравнение частоты ответа между группами лечения проводили с использованием точного критерия Фишера. Способы анализа для моделей сравнения множества биомаркеров приведены в разделе 4.6.
Для каждого анализа следующим образом готовили сводную информацию по демографическим и базовым характерным переменным для популяции данного биомаркера. Рассчитывали описательные статистические характеристики (среднее, стандартное отклонение, медиана и интервал) для базовых демографических данных (в том числе: возраст (лет), возрастная категория (>65 лет и ≤65 лет), пол (мужской, женский), раса (европеоидная, монголоидная/тихоокеанская и негроидная/другая), индекс FLIPI (низкий [0 или 1 фактор], средний [2 фактора], высокий [≥3 факторов]); предшествующая терапия ритуксимабом (да, нет); время после последней дозы противолимфомной терапии (≤1 года, >1 года); стадия по Анн Арбор (I, II, III, IV), количество ранее проведенных линий терапии (1, 2 и более), высокая опухолевая нагрузка (да, нет) и регион (США/Канада, Европейский союз, остальной мир) и сравнивали их со сводными статистическими данными из наборов данных по клиническим испытаниям.
Для оценок PFS между группами лечения использовали стратифицированный логранговый критерий и модель пропорциональных рисков Кокса. Для оценки распределения общих PFS для каждой группы лечения в популяции биомаркера и в целом использовали способ Каплана-Мейера; со стратификацией по уровню экспрессии, SNP или мутации (или приведенным выше группам ковариантов). Отношение рисков и 95%-ный доверительный интервал рассчитывали на основе стратифицированной модели пропорциональных рисков Кокса, учитывая группу лечения как объясняющую переменную. Анализы проводили для всей популяции в целом и по группам лечения, и при условии достаточного размера выборки каждый из таких анализов также стратифицировали по следующим факторам:
индекс FLIPI (низкий [0 или 1 фактор], промежуточный [2 фактора], высокий [≥3 факторов]);
предшествующая терапия ритуксимабом (да, нет);
время после последней дозы противолимфомной терапии (≤1 года, >1 года);
регион (США/Канада, Европейский союз (Бельгия, Чешская Республика, Финляндия, Франция, Германия, Великобритания, Греция, Венгрия, Италия, Польша, Португалия, Словакия, Испания и Швеция), остальной мир (Аргентина, Австралия, Бразилия, Индия, Израиль, Мексика, Китай, Корея, Румыния, Россия, Южно-Африканская Республика, Таиланд и Украина));
возраст (<65, >65);
пол;
раса;
стадия по Анн Арбор (I, II, III, IV);
количество предыдущих линий терапии (1, 2 и более);
высокая опухолевая нагрузка (да, нет).
Общую выживаемость определяли от даты рандомизации до даты смерти субъекта. Если субъект оставался жив или о его выживании не было известно, ее цензурировали по последнему дню, в который было известно, что субъект жив. Как и для PFS и TTP, для оценки связи между конечными точками для биомаркеров и OS использовали модель пропорциональных рисков Кокса. Построили кривые выживаемости Каплана-Мейера. Анализы проводили для всей популяции в целом и по группам лечения, и каждый из таких анализов также стратифицировали по ковариантам, использованным для PFS.
Сравнение частоты ответа между группами лечения проводили с использованием точного критерия Фишера. Продолжительность ответа, время до ответа и время до клинического рецидива в соответствующих случаях анализировали описательно, и подгруппу биомаркера сравнивали (в соответствующих случаях определяя, как и при первоначальном анализе) с общей клинической когортой, по группам лечения и в целом. Расчетную оценку частоты ответа для каждой группы лечения представили с 2-сторонними 95%-ными доверительными интервалами. Число и процентную долю субъектов, попадающих в каждую категорию ответа, свели в описательные таблицы.
Анализы проводили для популяции в целом и по группам лечения. Каждый из таких анализов стратифицировали по тем же ковариантам, которые использовали для оценки PFS.
Запланировали проведение дальнейших анализов из-за количества парных сравнений, которые оказались статистически значимыми до коррекции FDR, а также по той причине, что в таких парах выбирали уникальных пациентов с более продолжительными PFS и тенденцией к более продолжительной выживаемости. Такие анализы были призваны выявить классификатор на основе одного биомаркера, который указывал бы на большой положительный эффект для PFS и положительный эффект (или тенденции) для OS с высокой частотой в популяции. Использовали набор данных, где внутри одной и той же популяции определяли группы испытания на выявление различий и подтверждение. Исследование проводили следующим образом:
Субъектов без пропущенных значений биомаркеров (n=354) с помощью простой рандомизации включали в группы испытания на выявление различий и подтверждение в соотношении 7:3. Уравновешивающие демографические факторы и перечисленные ранее клинические коварианты подтверждали с использованием t-критерия или критерия Манна-Уитни. Группу для выявления различий (67%) использовали для идентификации биомаркеров со значительной ассоциацией с PFS; у включенных в исследование субъектов не было пропусков в данных биомаркеров. Для независимой проверки использовали группу для подтверждения (33%). Субъектов с пропущенными данными включали в группу для подтверждения при условии, что был доступен значимый набор данных биомаркеров, идентифицированный на этапе выявления различий. Кроме того, в группу для подтверждения также включили допускающую количественную оценку выборку из Китая.
Как и в случае первичного анализа, если для некоторого биомаркера отмечался один и тот же уровень экспрессии белка у всех субъектов, такой биомаркер исключали из анализа. Если у всех субъектов регистрировалась одинаковая мутация, отсутствие мутации, или 1 уровень мутации был представлен в ≥90% проб, то такую мутацию или такой ген исключали из анализа.
На этапе выявления различий при анализе комбинаций биомаркеров исключали всех субъектов с пропущенными значениями для любого из биомаркеров, перечисленных в разделе 2. Выборки с пропущенными данными включали в группу для подтверждения, при условии, что пропущенные данные не были частью ассоциированного набора данных. Выборки с пропущенными данными биомаркеров считали «не подлежащими количественной оценке» и исключали из группы для подтверждения, все остальные выборки, которые не использовались в группе для выявления различий, включали в группу для подтверждения.
Выбросы по биомаркерам из анализа не исключали.
Демографические и базовые коварианты сравнивали с использованием t-критерия или критерия Манна-Уитни, чтобы исключить статистически значимые различия между группами для выявления различий и подтверждения. Демографические и базовые характеристики суммировали для групп для выявления различий и подтверждения и в целом. Исключенных в конечном анализе субъектов в таком сравнении данных не рассматривали. Для базовых демографических данных рассчитывали описательные статистические характеристики (среднее, стандартное отклонение, медиана и интервал) и провели сравнение между демографическим и тестовым набором данных, чтобы исключить значимые различия между ними.
В анализ включали следующие коварианты: индекс FLIPI (низкий [0 или 1 фактор], промежуточный [2 фактора], высокий [≥3 факторов]); предшествующая терапия ритуксимабом (да, нет); время с последней дозы противолимфомной терапии (≤1 года, >1 года), стадия по Анн Арбор (I, II, III, IV), количество ранее проведенных линий терапии (1, 2 и более), высокая опухолевая нагрузка (да, нет), регион (США/Канада, Европейский союз, остальной мир), пол и раса.
Все маркеры и коварианты в ходе анализа рассматривали как категориальные переменные. Белковые биомаркеры дихотомизировали. Точки отсечения для белковых маркеров оптимизировали, исходя из увеличения числа ответивших на лечение по сравнению с числом не ответивших на лечение и разумного размера популяции. Более конкретно, для каждого биомаркера число ответивших и не ответивших на лечение (на основании общего ответа) и их процентные доли в допускающей количественную оценку популяции определяли с использованием каждой потенциальной точки отсечения, указанной в таблице 3. Для каждого биомаркера строили сводные таблицы с потенциальными точками отсечения, числом ответивших на лечение, числом не ответивших на лечение и их процентными долями.
Все генотипы в анализе рассматривали раздельно (например, C/C, C/T, T/T):
FCGR2A (H166R, Q62R, Q62X)
FCGR3A (V212F)
PSMB1 (P11A)
PSMB5 (R24C)
PSMB8 (G8R)
PSMB9 (R60H,V32I).
Оценка и ранжирование ассоциации единичных маркеров с PFS (группа для выявления различий)
На начальном этапе анализа проводили выбор и ранжирование маркеров для использования в последующем анализе множественных сравнений. Все перечисленные белки, SNP с вариабельностью генотипа более 10% и клинические коварианты включали как категориальные переменные. Оценка включала в себя следующие шаги:
Привели биомаркеры (в том числе клинические коварианты), которые в проведенном ранее ассоциативном анализе единичного маркера продемонстрировали улучшение PFS (p<0,2). Использовали только анализы, которые проводились с использованием проверки IRC.
Каждый биомаркер и клинический ковариант оценили по регрессии Кокса, чтобы оценить важность биомаркеров в отношении PFS. Привели P-значения и весовые коэффициенты/коэффициенты несогласия для всех маркеров в модели Кокса.
Для оценки корреляции биомаркеров построили матрицу парных корреляций, используя корреляционный анализ Спирмена. Выделили биомаркеры с высокой корреляцией (p<0,05 и коэффициент корреляции >0,7). Маркеры с высокой корреляцией и взаимодействующие с ними члены повторно проанализировали в регрессионной модели Кокса.
Подготовили промежуточные выводы по этому анализу для выбора маркеров, которые использовали в анализе множественных сравнений. При выборе маркеров использовали следующие критерии:
относительно низкие P-значения в регрессии Кокса для влияния маркера на PFS.
Преимущества для PFS в группе Vc-R по сравнению с группой R, которые опирались на взаимодействие со схемой лечения в регрессии Кокса или логранговые критерии с единичным маркером.
При высоком уровне корреляции и высоких рангах по регрессии Кокса для множества маркеров использовали представительный(-ые) маркер(-ы) с наивысшим рангом по регрессии Кокса и взаимодействующие с ними члены. Субпопуляция выборок с высоким преимуществом для PFS в группе Vc-R по сравнению с группой R выявляли исчерпывающим поиском сочетания «И» биомаркеров. Более конкретно, субпопуляции пациентов формировали по сочетаниям «И» любых двух или трех биомаркеров, выбранных в разделе 4.6.1. Различие PFS для выделенных по биомаркерам подгрупп пациентов оценивали с помощью логрангового критерия с PFS в качестве зависимой переменной и 5-кратным перекрестным подтверждением, как описано ниже.
Группу для выявления различий случайным образом разбивали на 5 подгрупп по 20% субъектов в каждой подгруппе. Объединением 4 из 5 подгрупп формировали 80%-ную подгруппу. Используя 80%-ную подгруппу, сочетанием «И» биомаркеров формировали субпопуляции пациентов. Если число выборок (N) для субпопуляции в группе Vc-R или R составляло <5, такую субпопуляцию опускали. Для субпопуляций с N ≥5 в обеих группах с помощью логрангового критерия оценивали разницу PFS для подгрупп пациентов, определяемых двумя выбранными маркерами. В силу исследовательского характера данного анализа для отсечения использовали менее ограничивающее Р-значение. Затем преимущество для PFS тестировали на оставшейся 20%-ной подгруппе.
Остальные 4 группы для перекрестных подтверждений тестировали аналогичным способом (отсечение по Р-значению не использовали из-за малых размеров выборки). Более конкретно, для повторения логранговых критериев использовали другую 20%-ную подгруппу из упомянутых выше и новую 80%-ную подгруппу, сформированную из остальных субъектов, пока не проверили все 5 20%-ных подгрупп. Привели долю итераций с большими преимуществами для PFS как в подгруппе 90%, так и подгруппе 10%.
Комбинации биомаркеров объединяли и оценивали по преимуществам для PFS и статистической значимости с перекрестной проверкой. Для субпопуляций, сформированных при объединении комбинаций маркеров, никаких статистических тестов не проводили, если размер субпопуляции составлял ≤10% группы для выявления различий. Провели исчерпывающее объединение пар маркеров и оценку преимуществ для PFS. Для экономии времени вычислений привели только статистически значимые комбинации маркеров или объединения комбинаций маркеров. Результаты сохраняли после каждой итерации.
Для комбинаций маркеров с наивысшим рангом с помощью дерева классификации и регрессии установили правила принятия решений для определения выбранных субпопуляций пациентов. Также оценили ассоциацию выбранных субпопуляций пациентов с другими конечными точками клинического исследования. Оценили показатели PFS и OS в группе для подтверждения путем тестирования ассоциации биомаркеров, идентифицированных в группе для выявления различий, с использованием установленных правил принятия решений. В группе для подтверждения привели PFS для положительных и отрицательных по биомаркерам подгрупп для обеих групп исследования. Из-за небольшого размера выборки отсечение по Р-значению не применяли, но тем не менее приводили его величину.
Выборки, включенные в группу для независимого подтверждения, могли иметь пропущенные значения для биомаркеров с невыявленной ассоциацией с PFS, тем не менее субъектов, которых невозможно было классифицировать из-за пропущенных значений выбранных биомаркеров, рассматривали как «не поддающихся количественной оценке» и исключали из рассмотрения.
Первичный анализ концентрировался на ассоциациях единичных маркеров, стратифицированных по ковариантам. При анализе ассоциаций единичных маркеров, в том числе CD68, PSMB1 (P11A), P65 и PSMB5 (R24C), были выявлены статистически значимые связи. Последующий парный анализ позволил выявить пару биомаркеров со значительно более продолжительным PFS и тенденцией к преимуществу по OS. По причине отсутствия наборов данных для независимого подтверждения такого вывода набор данных разделили на описанные выше группы для выявления различий и подтверждения. В рамках такого анализа сравнивали комбинации множества биомаркеров и выявили другие значимые комбинации. Ассоциацией, которая по результатам всех анализов представлялась наиболее клинически уместной, была гетерозигота PSMB P11A в сочетании с низким уровнем экспрессии CD68 (0-50%). Клинический интерес представляют субпопуляции субъектов с высокой опухолевой нагрузкой, с ранее проводимым лечением ритуксимабом и одной или двумя ранее проводившимися линиями терапии.
Анализ парных комбинаций маркеров проводили с использованием стратифицированного логрангового критерия для каждой потенциальной пары, чтобы определить различия в PFS между группами Vc-R и монотерапии ритуксимабом. Сто две пары биомаркеров имели логранговое значение p<0,05. Из них 97 пар имели частоту выборки >1%. Четырнадцать пар также продемонстрировали улучшение PFS>6 месяцев. В ходе данного анализа провели 1140 парных сравнений (коварианты попарно ассоциировали с каждым отдельным маркером для дополнения анализа). После коррекции FDR значимой была 1 пара (FDR=0,051). Эту пару биомаркеров идентифицировали в 33% допускающей количественную оценку популяции биомаркеров, где отмечалось преимуществом по PFS в 7,5 месяцев при схеме лечения Vc-R по сравнению с монотерапией ритуксимабом (таблица 4) и тенденция к улучшению OS (p=0,055, HR: 0,426 [0,174, 1,046]). Такую пару составили PSMB1 P11A (C/G гетерозигота) и низкий уровень экспрессии CD68, определяемый как 0-50% положительно окрашенных клеток. Данная пара далее будет называться положительной по биомаркеру подгруппой. Отрицательная по биомаркеру подгруппа не включает эту пару биомаркеров и отличается другим генотипом PSMB1 и уровнем экспрессии CD68.
Важно отметить, что в положительной по биомаркеру подгруппе (гетерозигота PSMB1 P11A и низкий уровень экспрессии CD68) также наблюдался значительно более высокий уровень положительного ответа 73,7% для субъектов, получавших лечение Vc-R, по сравнению с 47,5% для монотерапии R (p=0,0077), а также более продолжительный период времени до следующего курса лечения (p=0,0013) и более продолжительный период без лечения (p=0,0017).
В положительных и отрицательных по биомаркеру популяциях наблюдались аналогичные профили АЕ. В положительных и отрицательных по биомаркеру популяциях наблюдалось аналогичное воздействие лечения. Субъекты, получавшие ритуксимаб в положительной по биомаркеру популяции, имели медиану принимаемой дозы 2941 мг/м2 по сравнению с 2940 мг/м2 в отрицательной по биомаркеру популяции. Субъекты, получавшие Vc-R в положительной по биомаркеру популяции, имели медиану принимаемой дозы 31,1 мг/м2 по сравнению с 30 мг/м2 в отрицательной по биомаркеру популяции. Для полного количества принимаемых доз, продолжительности воздействия, интенсивности дозы, относительной интенсивности дозы и максимального количества проведенных циклов также наблюдались очень похожие различия.
Субъекты, получавшие бортезомиб + ритуксимаб, поддерживали более продолжительные PFS, если они были положительными по биомаркеру и стратифицировались по любому индексу FLIPI, по опухолевой нагрузке, по классификации Анн Арбор, по возрасту, региону, полу и расе. Для пациентов с более высоким риском и неблагоприятным прогнозом, например, с высокой опухолевой нагрузкой, средним или высоким индексом FLIPI, старше 65 лет или с ранее проводившимся лечением ритуксимабом, у положительных по биомаркеру пациентов отмечалось более заметное улучшение PFS по сравнению с отрицательными по биомаркеру пациентами. Более продолжительная PFS сохранялась независимо от времени последнего лечения или числа предшествующих курсов лечения ранее применявшимся ритуксимабом, или количества курсов лечения ритуксимабом, не превышающих 2.
Субъекты, получавшие бортезомиб + ритуксимаб, поддерживали более высокую общую выживаемость, если они были положительными по биомаркеру и стратифицировались по индексу FLIPI, по опухолевой нагрузке, по классификации Анн Арбор, по возрасту, региону, полу и расе. Субъекты, получавшие Velcade + ритуксимаб, поддерживали более продолжительные PFS, если они были положительными по низкому CD68 (0-50) и стратифицировались по любому индексу FLIPI, по опухолевой нагрузке, классификации Анн Арбор, возрасту, региону, полу и расе. Как и ожидалось, при высоком CD68 их показатели улучшались при применении только ритуксимаба. Субъекты, получавшие Velcade + ритуксимаб, поддерживали более продолжительные PFS, если они были положительными по гетерозиготе PSMB P11A и стратифицировались по любому индексу FLIPI, по опухолевой нагрузке, классификации Анн Арбор, возрасту, региону, полу и расе. Как и ожидалось, при высоком CD68 их показатели улучшались при применении только ритуксимаба.
У положительных по биомаркеру субъектов была обнаружена тенденция к более продолжительной OS (p=0,055, HR 0,426). При раздельном рассмотрении вкладов разных биомаркеров такая тенденция была менее выраженной. Для субъектов с гетерозиготами PSMB1 P11A C/G уровень значимости составлял p=0,2525 при HR=0,673, тогда как у субъектов, положительных по CD68 (0-50), уровень значимости составлял p=0,0714 и HR=0,615.
Субъекты, получавшие Velcade + ритуксимаб, демонстрировали тенденцию к более высокой OS, если они были положительными по низкому CD68 (0-50) и стратифицировались по любому индексу FLIPI, по опухолевой нагрузке, классификации Анн Арбор, возрасту, региону, полу и расе. Субъекты, получавшие Velcade + ритуксимаб, демонстрировали тенденцию к более высокой OS, если они были положительными по гетерозиготе PSMB1 P11A и стратифицировались по любому индексу FLIPI, по опухолевой нагрузке, классификации Анн Арбор, возрасту, региону, полу и расе.
После перекрестной проверки описанная ранее пара (низкий CD68 и PSMB P11A) оказалась значимой в меньшей когорте для выявления различий (p=0,0003, 14,2 месяца для Vc-R по сравнению с 8,5 месяца для R, HR=0,4 (0,24, 0,67)). В положительной по биомаркеру популяции сохранялась тенденция к большей OS (p=0,1291), HR=0,47 (0,17, 1,27). Несмотря на небольшую численность субъектов в когортах для подтверждения, положительная тенденция для PFS и OS сохранялась. В когорте для подтверждения 1 (n=106) у субъектов, получавших Vc-R, отмечали PFS приблизительно 18,2 месяца, тогда как субъекты, получавшие только R, демонстрировали PFS 9,5 месяца (p=0,0817, HR=0,44). В когорте для подтверждения 2 (n=426) у субъектов, получавших Vc-R, медиана PFS составила приблизительно 13,9 месяца, тогда как субъекты, получавшие только R, демонстрировали медиану PFS 9,5 месяца (p=0,0878, HR=0,49). Сохранялась также тенденция у OS.
Было интересно установить индивидуальный вклад каждого биомаркера в преимущества для PFS, наблюдавшиеся у субъектов с обоими биомаркерами (гетерозигота PSMB1 P11A и низкий CD68). В положительной по биомаркеру популяции субъекты с PSMB1 P11A (C/G) имели медиану PFS 16,6 месяца при лечении Vc-R по сравнению с медианой PFS 9,5 месяца при лечении только R, что соответствовало увеличению PFS на 7,1 месяца при использовании комбинированной терапии. Подобное преимущество не наблюдалось в отрицательной по биомаркеру группе субъектов, получавших лечение Vc-R. В соответствии с предыдущими публикациями по CD68 и ритуксану, настоящее исследование показывает, что субъекты с более высоким уровнем экспрессии CD68 лучше реагируют на монотерапию ритуксимабом (медиана PFS 16,2 месяца), чем субъекты с низким уровнем экспрессии CD68 (медиана PFS 9,3 месяца). Однако такие субъекты с низким CD68 (0-50) имели значительно большую PFS (медиана 14 месяцев) при комбинированной терапии по сравнению с такими же пациентами, получавшими монотерапию R (медиана 9,3 месяца), что соответствует улучшению PFS на 4,7 месяца (HR=0,64 (ДИ 95%: 0,475-0,864).
Полученные результаты свидетельствуют о том, что до начала лечения можно идентифицировать подгруппы пациентов со значительно более продолжительной PFS и тенденцией к более высокой OS при комбинированной терапии Vc-R по сравнению с монотерапией R. Одна пара биомаркеров, которая сохраняет значимость после коррекции для множественных сравнений (FDR=0,051), включает в себя SNP протеосомной субъединицы [гетерозигота PSMB1 P11A] и низкий уровень экспрессии CD68 (0-50). В рамках данного исследования оценку по обоим из указанных биомаркеров провели у трехсот пятидесяти шести субъектов. Кроме того, такая пара биомаркеров отличалась высокой частотой в популяции, и приблизительно у трети субъектов, допускающих количественную оценку, наблюдали оба из этих биомаркеров. Субъекты с этой парой биомаркеров отличались более продолжительной PFS при лечении Vc-R (16,6 месяца) по сравнению с монотерапией ритуксимабом (9,1 месяца), демонстрируя преимущество комбинированной терапии для PFS на приблизительно 7,5 месяца. В этой группе также проявилось преимущество по OS при лечении Vc-R, которое имеет четкую тенденцию к статистической значимости (HR: 0,426 (0,174-1,046), p=0,0550), более высокий ORR (73,7% при лечении Vc-R по сравнению с 47,5% при монотерапии ритуксимабом, p=0,0077), более продолжительное время до следующего лечения (33,1 месяца при лечении Vc-R по сравнению с 14,8 месяца при монотерапии ритуксимабом, p=0,0013), а также более продолжительный период без лечения (27,8 месяца по сравнению с 10,1 месяца, p=0,0017).
Важно отметить, что положительная по биомаркерам CD68/PSMB P11A когорта была репрезентативной по всей популяции исследования с точки зрения демографических показателей и клинических характеристик. При этом приблизительно половина этой когорты была представлена субъектам с высоким риском заболевания и плохими прогностическими характеристиками. У пациентов с более высокой опухолевой нагрузкой (~54%), средним или высоким индексом FLIPI (~76%), в старшем возрасте (>65) (~25%), при ранее проводившемся лечении ритуксимабом (~46%) или с двумя (~26%) или более двух (~30%) линий ранее проводившейся терапии сохранялось преимущество по PFS для положительной по биомаркерам CD68/PSMB P11A когорты. Такие пациенты по существу относятся к группе «высокого риска» с ограниченными возможностями лечения, и эти предварительные результаты свидетельствуют о том, что положительные по биомаркеру субъекты с параметрами высокого риска могут добиваться более высоких результатов при лечении Vc-R.
Оказалось, что полиморфизмы в PSMB1 и PSMB5 в качестве единичных маркеров значимо ассоциированы с конечными точками клинических исследований. Комбинация PSMB1 [P11A] с CD68 оказалась синергичной и присутствует в значительной доле исследуемой когорты. PSMB1 P11A представляет собой полиморфизм, присутствующий в лидерной последовательности гена PSMB1 протеосомы (Chen 1996). Лидерная последовательность отвечает за правильную сборку субъединицы, и сообщалось, что замена заряженных аминокислот уменьшает эффективность сборки субъединицы (Schmidt 1999). После сборки автокатализ позволяет удалить лидерную последовательность. Вторым биомаркером в паре является CD68, экспрессируемый инфильтрирующими опухоль макрофагами. В предыдущих работах было показано, что высокие уровни CD68 ассоциируются с лучшим ответом на ритуксимаб (Taskinen 2007).
Важно отметить, что в настоящем исследовании было показано, что субъекты с низкими уровнями экспрессии CD68 отличаются более продолжительной PFS и лучшим общим ответом на лечение Vc-R по сравнению с монотерапией R, особенно при наличии гетерозиготы PSMB1 P11A, как обсуждалось выше. После перекрестной проверки описанная выше пара (низкий CD68 и PSMB P11A) оказалась значимой в меньшей когорте для выявления различий (p=0,0003, 14,2 месяца для лечения Vc-R по сравнению с 8,5 месяца для монотерапии ритуксимабом, HR=0,4 (0,24, 0,67)). В положительной по биомаркеру популяции сохранялась тенденция к большей OS (p=0,1291), HR=0,47 (0,17, 1,27). Несмотря на небольшую численность субъектов в когортах для подтверждения, положительная тенденция сохранялась как для PFS, так и для OS. В когорте для подтверждения 1 (которая исключает субъектов из Китая; n=106) у субъектов, получавших Vc-R, отмечали PFS приблизительно 18,2 месяца, тогда как субъекты, получавшие только R, демонстрировали PFS 9,5 месяца (p=0,0817, HR=0,44). В когорте для подтверждения 2 (которая включает в себя субъектов из Китая и субъектов с пропущенными данными; n=126) у субъектов, получавших Vc-R, медиана PFS составила приблизительно 13,9 месяца, тогда как субъекты, получавшие только R, демонстрировали медиану PFS 9,5 месяца (p=0,0878, HR=0,49). Сохранялась также тенденция у OS.
ПРИМЕР 2
В таблице 5 приведены единичные прогностические факторы, которые коррелировали с положительным ответом.
ПРИМЕР 3
В таблицах 6 и 7 приведены пары прогностических факторов, которые коррелировали с положительным ответом.
Arif A (2009), Jamal S, Mushtaq S, Ahmed S, Mubarik A. Frequency of bcl-2 gene rearrangement in B-Cell Non-Hodgkin′s lymphoma. Asian Pacific J Cancer Prev 2009; 10(2): 237-240.
Binstadt BA (2003), Geha RS, Bonilla FA. IgG Fc receptor polymorphisms in human disease: Implications for intravenous immunoglobulin therapy. J Allergy Clin Immunol 2003; 111(4): 697-703.
Cartron G (2002), Dacheux L, Salles G, Solal-Celigny P, Bardos P, Colombat P, Watier H. Therapeutic activity of humanized anti-CD20 monoclonal antibody and polymorphism in IgG Fc receptor FcgammaRIIIa gene. Blood 2002; 99(3): 754-758.
Chen P (1996), Hochstrasser M. Autocatalytic subunit processing couples active site formation in the 20S proteasome to completion of assembly. Cell 1996; 86: 961-972.
Chen S (2010), Blank JL, Peters T, Liu XJ, Rappoli DM, Pickard MD, Menon S, Driscoll DL, Lingaraj T, Burkhardt AL, Chen W, Garcia K, Sappal DS, Gray J, Hales P, Leroy PJ, Ringeling J, Rabino C, Spelman JJ, Morganstern JP, Lightcap ES. Genome-wide siRNA screen for modulators of cell death induced by proteasome inhibitor bortezomib. Cancer Res 2010; 70(11): 4318-4326.
Протокол клинического исследования 26866138-LYM-3001. A randomized, open-label, multicenter study of VELCADE with rituximab or rituximab alone in subjects with relapsed or refractory, rituximab naïve or sensitive follicular B-cell non-Hodgkin′s lymphoma. Документ № EDMS-PSDB-4649082:4.0; Johnson & Johnson Pharmaceutical Research & Development (19 мая 2006 г.).
Отчет клинического исследования 26866138-LYM-3001. A randomized, open-label, multicenter study of VELCADE with rituximab or rituximab alone in subjects with relapsed or refractory, rituximab naïve or sensitive follicular B-cell non-Hodgkin′s lymphoma. Документ № EDMS-ERI-16225335:1.0; Johnson & Johnson Pharmaceutical Research & Development (09 февраля 2011 г.).
Dave SS (2004), Wright G, Tan B, Rosenwald A, Gascoyne RD, Chan WC, Fisher RI, Braziel RM, Rimsza LM, Grogan TM, Miller TP, Leblanc M, Greiner TC, Weisenburger DD, Lynch JC, Vose J, Armitage JO, Smeland EB, Kvaloy S, Holte H, Delabie J, Connors JM, Lansdorp PM, Ouyang Q, Lister TA, Davies AJ, Norton AJ, Muller-Hermelink HK, Ott G, Campo E, Montserrat E, Wilson WH, Jaffe ES, Simon R, Yang L, Powell J, Zhao H, Goldschmidt N, Chiorazzi M, Staudt LM. Prediction of survival in follicular lymphoma based on molecular features of tumor-infiltrating immune cells. NEJM 2004; 351(21): 2159-2169.
Fischer U (2005), Schulze-Osthoff K. New approaches and therapeutics targeting apoptosis in disease. Pharmacol Rev 2005; 57(2): 187-215.
Goy A (2010), Bernstein S, McDonald A, Pickard M, Shi H, Fleming M, Bryant B, Trepicchio W, Fisher R, Boral A, Mulligan G. Potential biomarkers of bortezomib activity in mantle cell lymphoma from the phase 2 PINNACLE trial. Leukemia & Lymphoma 2010; 51(7): 1269-1277.
Karin M (2002), Cao Y, Florian GR, Li ZW. NF-kB in cancer: From innocent bystander to major culprit. Nature Rev Cancer 2002; 2(4): 301-310.
Keats JJ (2007), Fonseca R, Chesi M, Schop R, Baker A, Chng WJ, Van Wier S, Tiedemann R, Shi CX, Sebag M, Braggio E, Henry T, Zhu YX, Fogle H, Price-Troska T, Ahmann G, Mancini C, Brents LA, Kumar S, Greipp P, Dispenzieri A, Bryant B, Mulligan G, Bruhn L, Barrett M, Valdez R, Trent J, Stewart AK, Carpten J, Bergsagel PL. Promiscuous mutations activate the noncanonical NF-kappaB pathway in multiple myeloma. Cancer Cell 2007; 12(2): 131-144.
Mitsiades N (2002), Mitsiades CS, Poulaki V, Chauhan D, Fanourakis G, Gu X, Bailey C, Joseph M, Libermann TA, Treon SP, Munshi NC, Richardson PG, Hideshima T, Anderson KC. Molecular sequelae of proteasome inhibition in human multiple myeloma cells. Proc Natl Acad Sci USA 2002; 99(22): 14374-14379.
Mulligan G (2007), Mitsiades C, Bryant B, Zhan F, Chng WJ, Roels S, Koenig E, Fergus A, Huang Y, Richardson P, Trepicchio WL, Broyl A, Sonnveld P, Shaghnessy JD, Bergsagel PL, Schenkein D, Esseltine DL, Boral A, Anderson KC. Gene expression profiling and correlation with clinical outcome in clinical trials of the proteasome inhibitor bortezomib. Blood 2007; 109(8): 3177-3188.
Schmidt M (1999), Zantopf D, Kraft R, Kostka S, Preissner R, Kloetzel PM. Sequence information within proteasomal prosequences mediates efficient integration of β-subunits into the 20S proteasome complex. J Mol Biol 1999; 288(1): 117-128.
Shin HM (2006), Minter LM, Cho OH, Gottipati S, Fauq AH, Golde TE, Sonenshein GE, Osborne BA. Notch1 augments NF-kappaB activity by facilitating its nuclear retention. EMBO 2006; 25(1): 129-138.
Taskinen M (2007), Karjalainen-Lindsberg ML, Nyman H, Eerola LM, Leppa S. A high tumor-associated macrophage content predicts favorable outcome in follicular lymphoma patients treated with rituximab and cyclophosphamide-doxorubicin-vincristine-prednisone. Clin Cancer Res 2007; 13(19): 5784-5789.
Wojcik C (2002). Regulation of apoptosis by the ubiquitin and proteasome pathway. J Cell Mol Med 2002; 6(1): 25-48.
Wu J (1997), Edberg JC, Redecha PB, Bansal V, Guyre PM, Coleman K, Salmon JE, Kimberly RP. A novel polymorphism of FcgammaRIIIa (CD16) alters receptor function and predisposes to autoimmune disease. J Clin Invest 1997; 100(5): 1059-1070.
Yeung BH (2006), Huang DC, Sinicrope FA. PS-341 (bortezomib) induces lysosomal cathepsin b release and a caspase-2 dependent mitochondrial permeabilization and apoptosis in human pancreatic cancer cells. J Biol Chem 2006; 281(17): 11923-11932.
Yin D (2005), Zhou H, Kumagai T, Liu G, Ong JM, Black KL, Koeffler HP. Proteasome inhibitor PS-341 causes cell growth arrest and apoptosis in human glioblastoma multiforme (GBM). Oncogene 2005; 24(3): 344-354.
ПРИМЕР 4
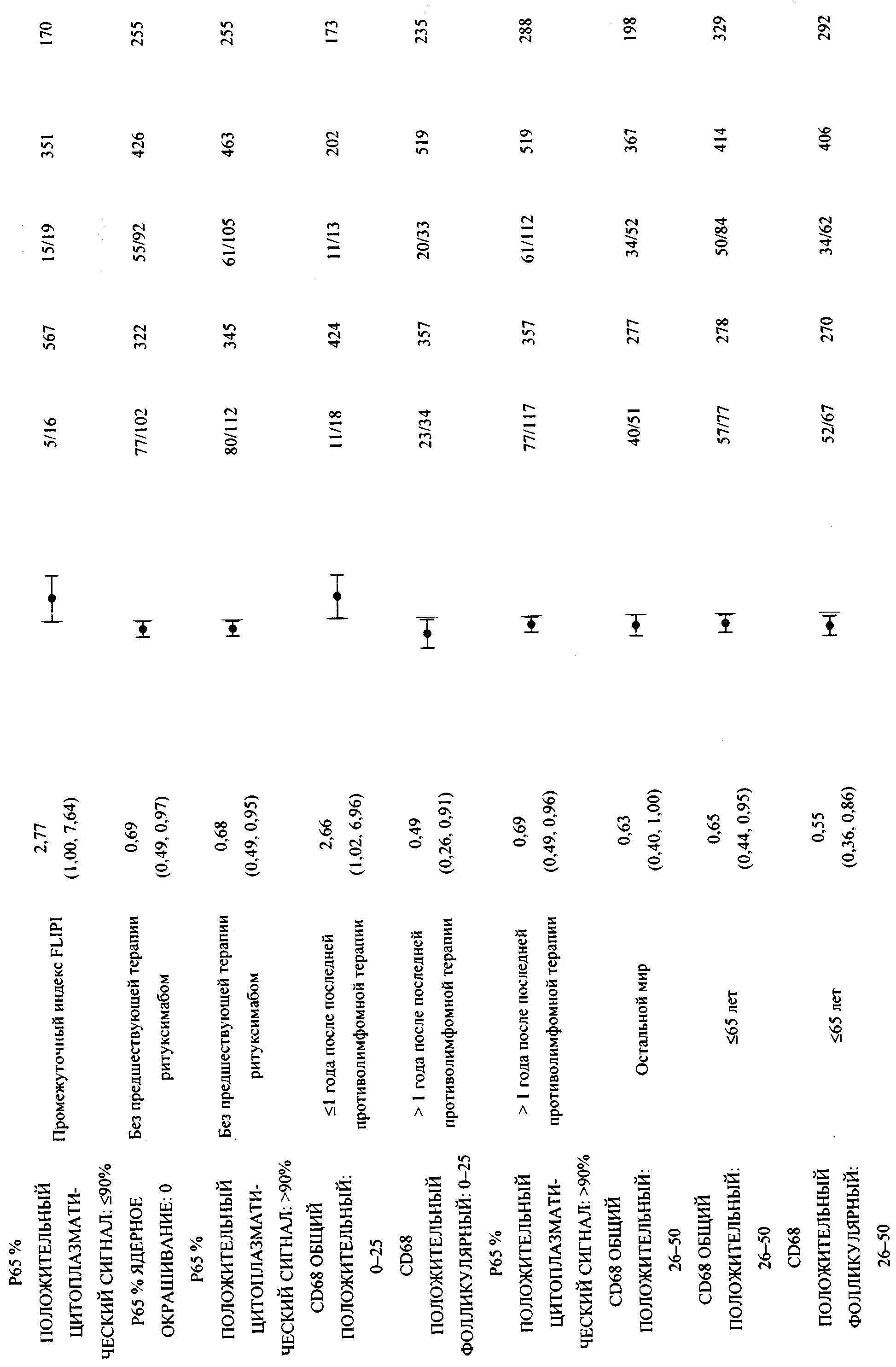
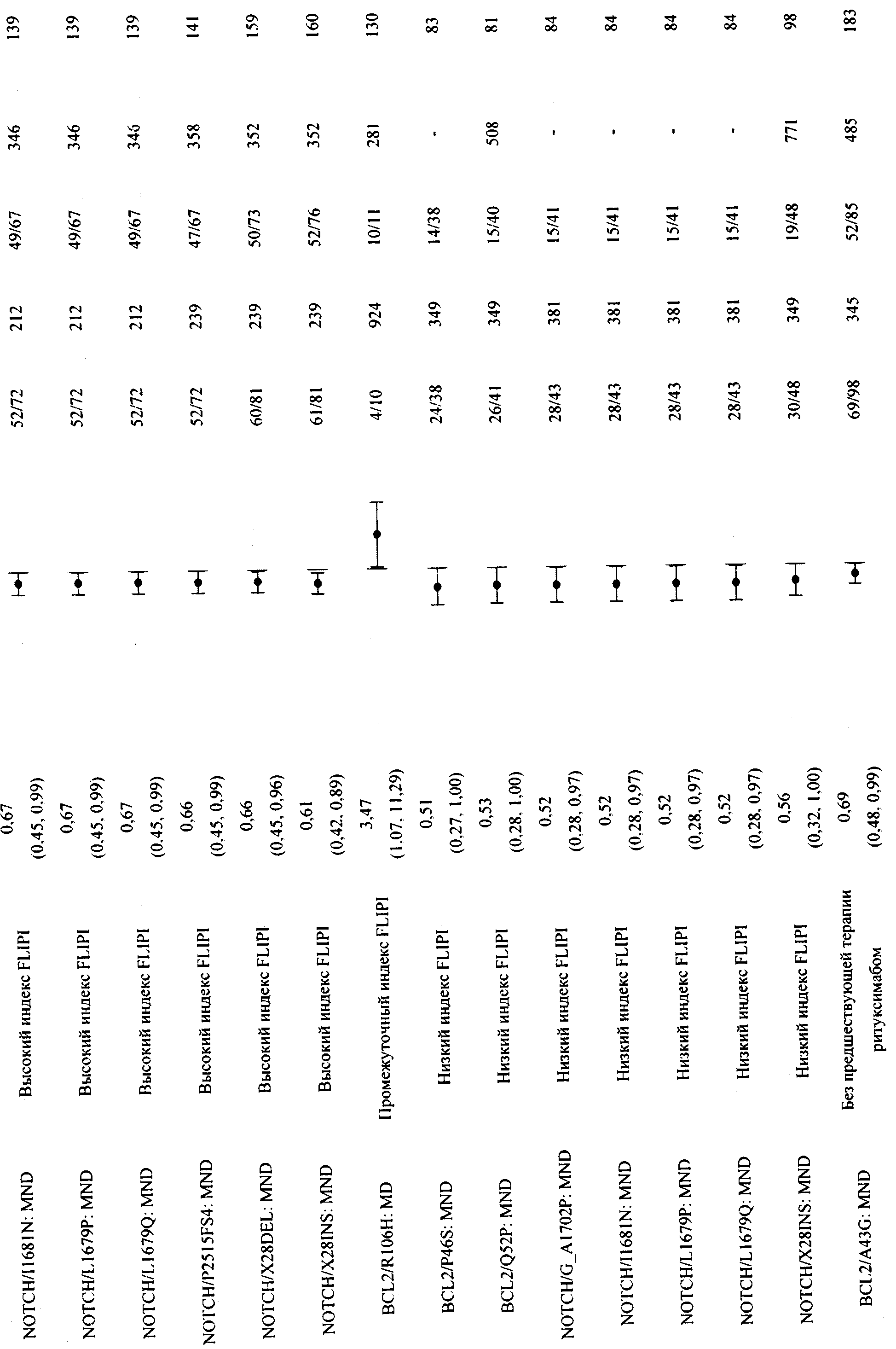
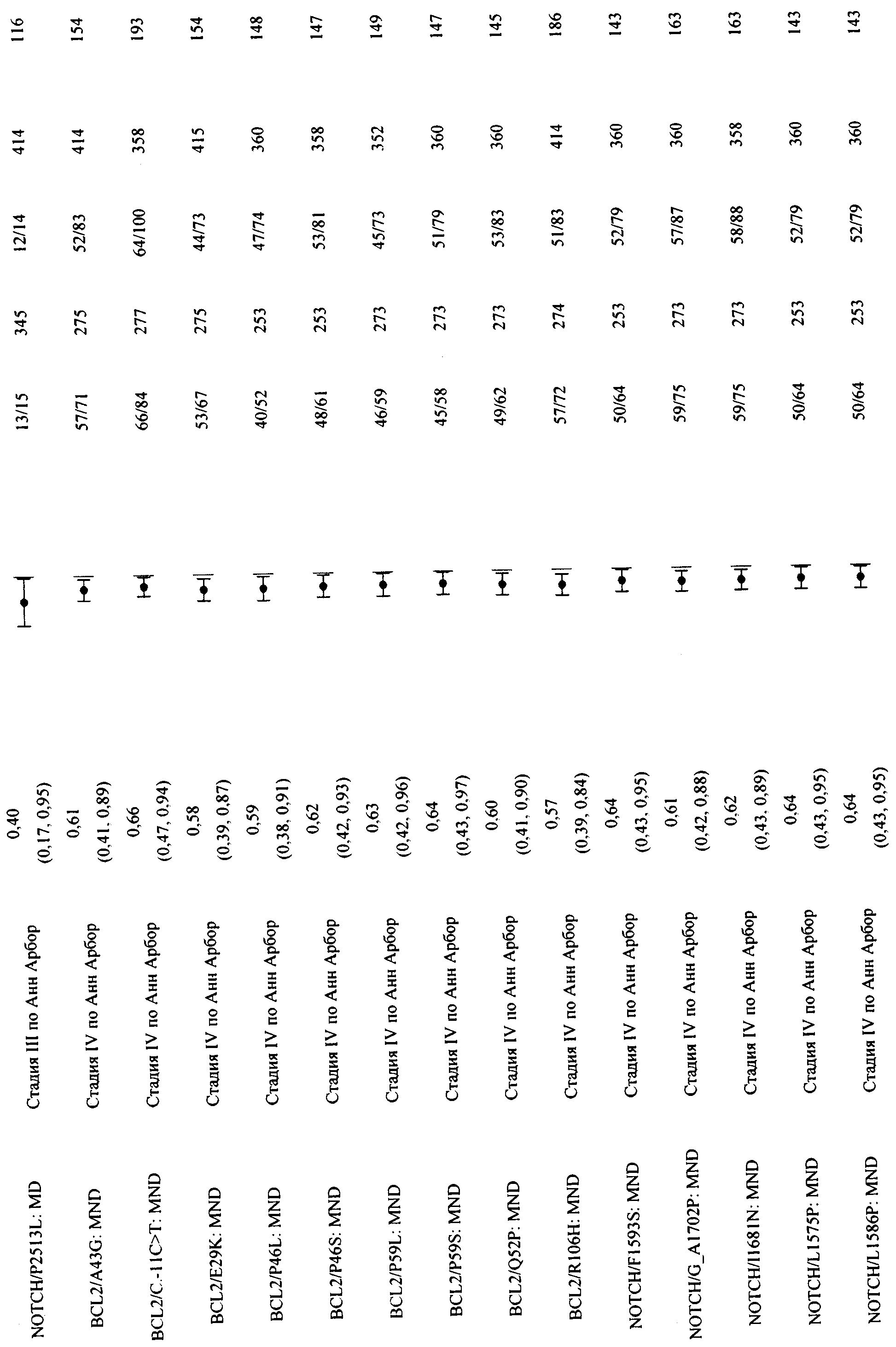
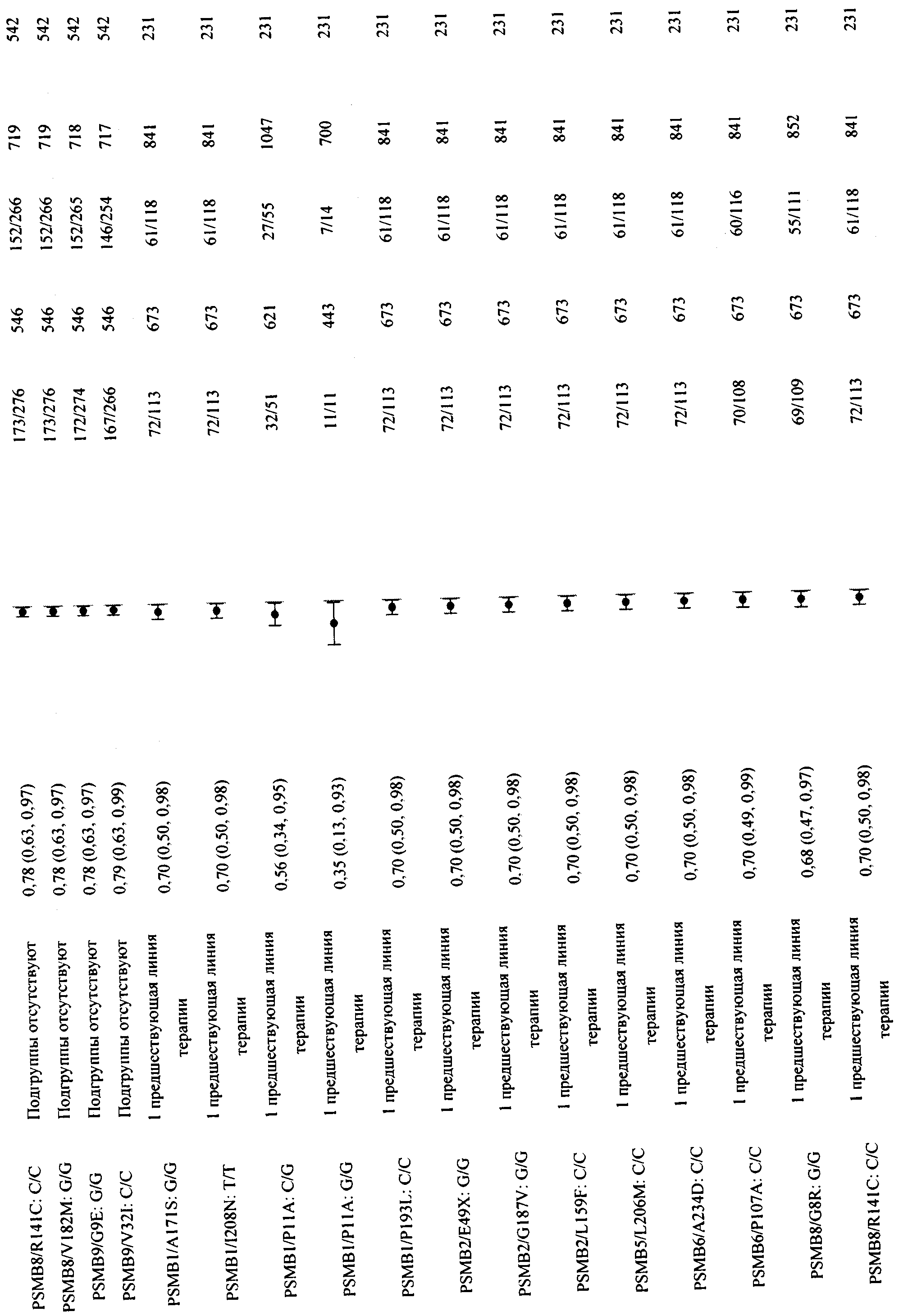
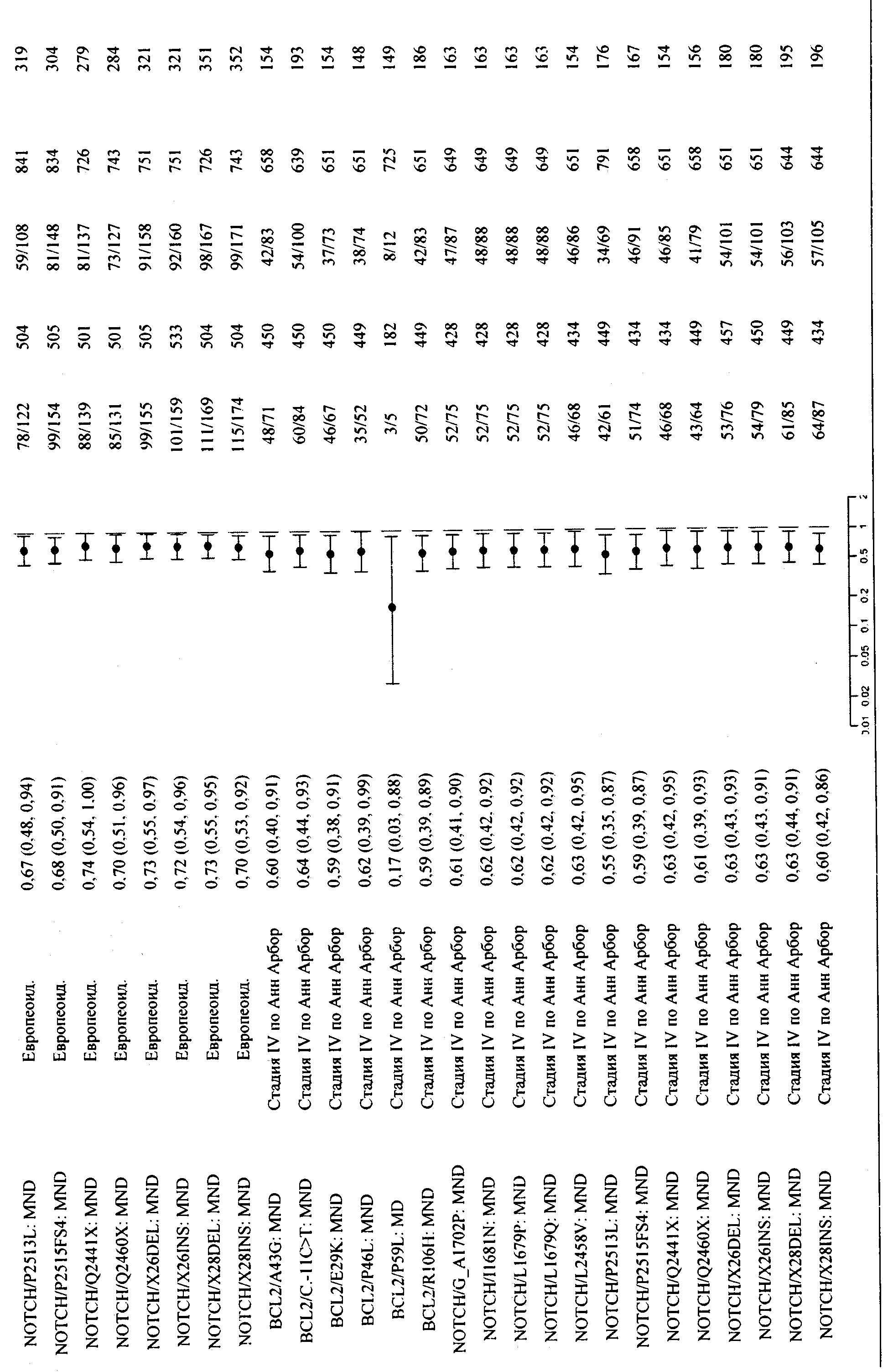
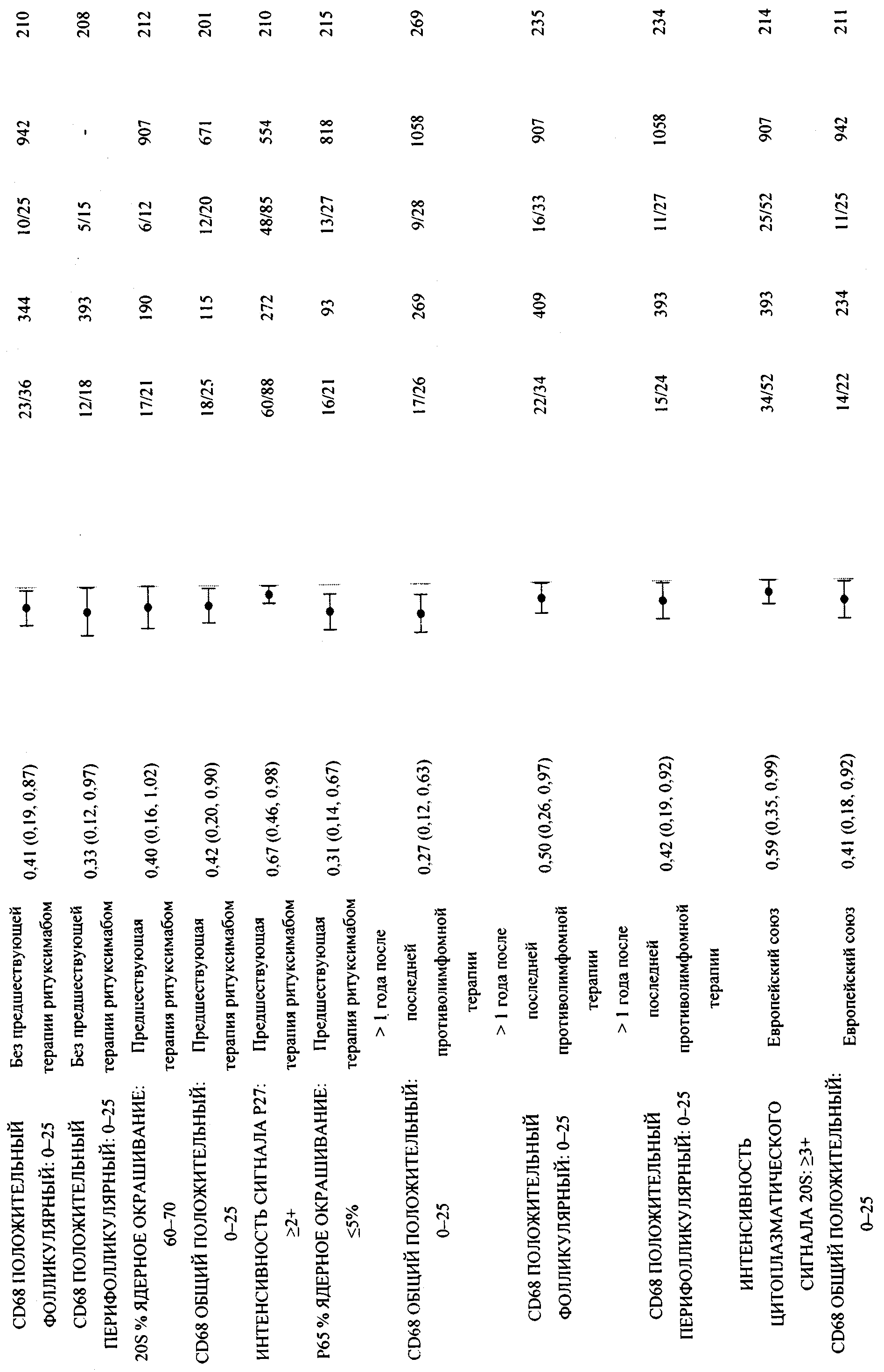
В приложении 2 приведена общая информация об ассоциировании единичных маркеров с конечными точками клинических исследований, отличными от PFS, а также ее стратификация по клиническим ковариантам из предыдущих примеров.
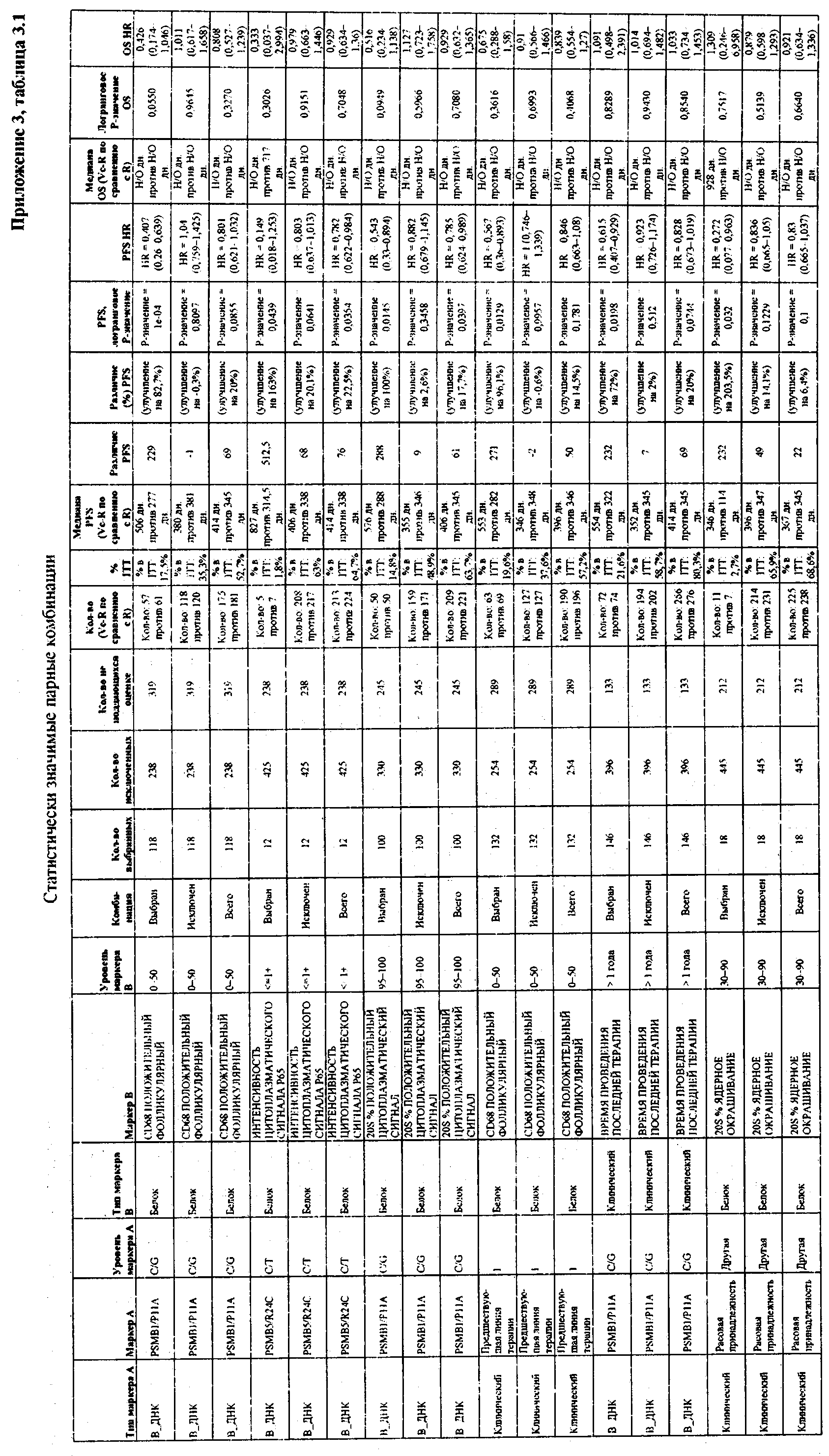
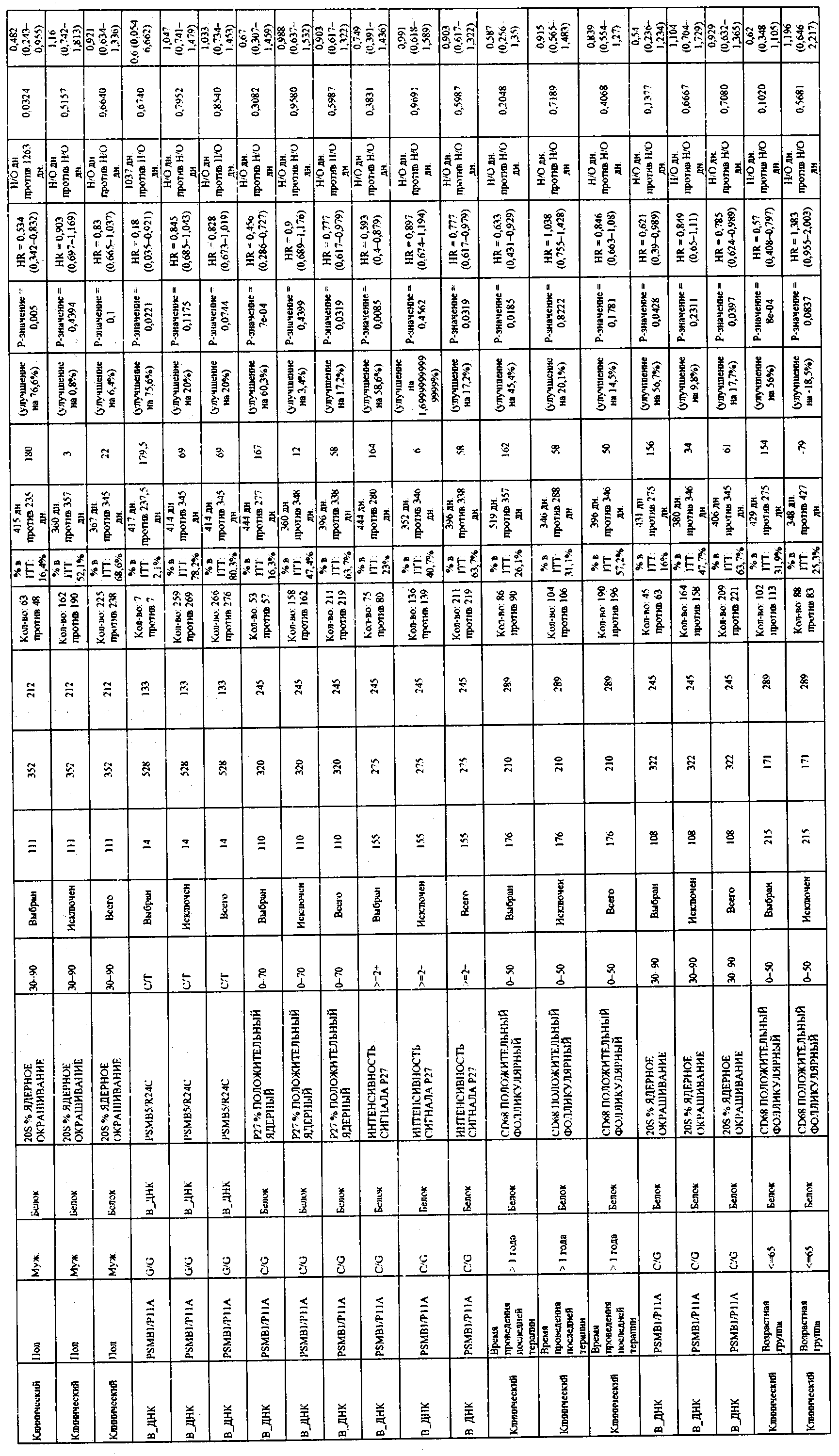
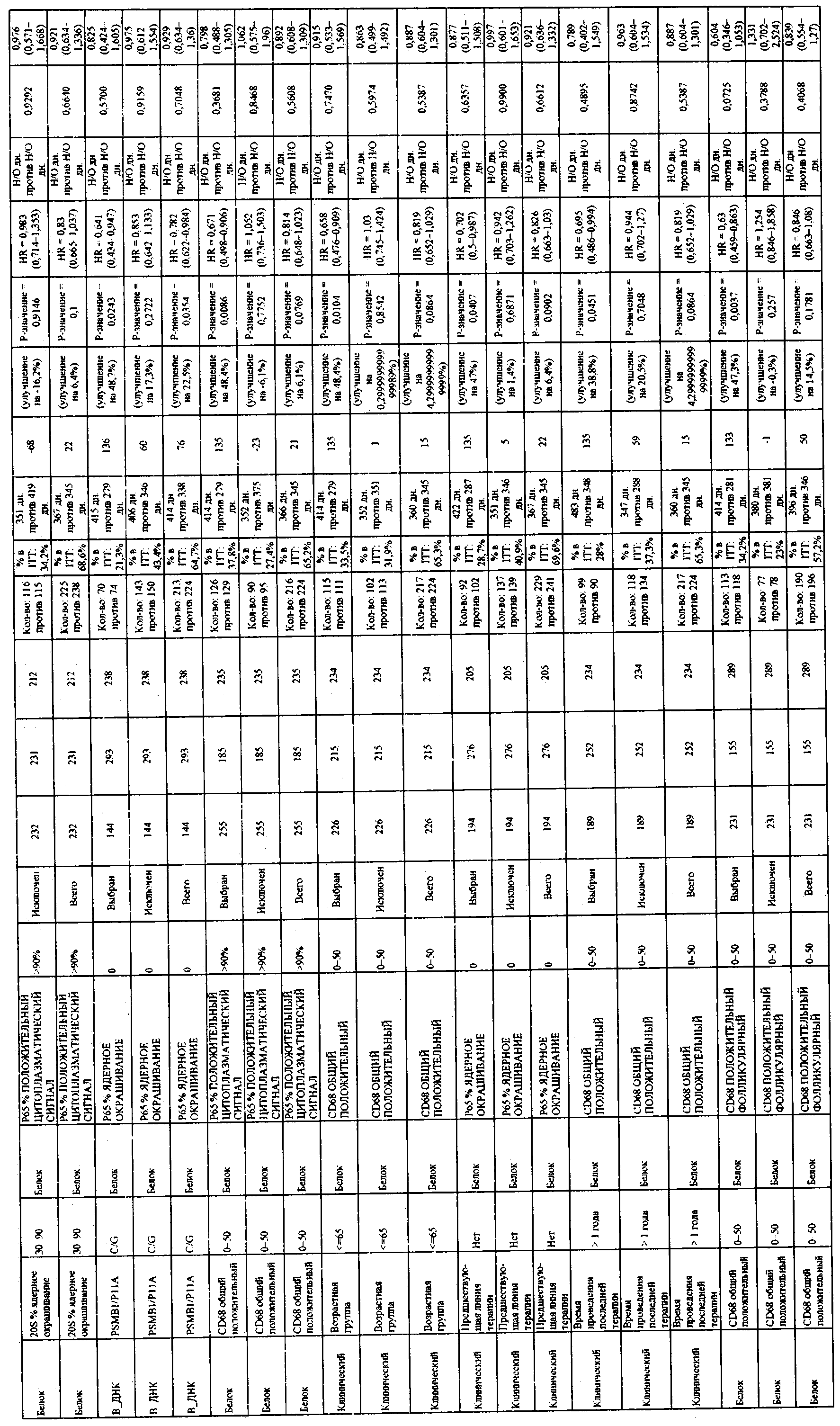
В приложении 3 приведены данные для всех значимых парных комбинаций из предыдущих примеров. Примечание. Выбран = положительный по биомаркеру, не выбран = отрицательный по биомаркеру.
ПРИМЕР 5
Исследование VISTA представляло собой открытое рандомизированное исследование комбинированной терапии VELCADE/мелфалан/преднизон по сравнению с комбинированной терапией мелфалан/преднизон у субъектов с множественной миеломой, ранее не получавших лечения. San Miguel, N. Engl. J. Med. 28 августа 2008 г.; 359(9):906-17. Главной целью изучения эффективности в настоящем исследовании было установить, насколько добавление VELCADE (бортезомиб для инъекций) к стандартной терапии мелфалан/преднизон (MP) увеличивает интервал до прогрессирования заболевания (TTP) у субъектов с множественной миеломой, ранее не получавших лечения.
Исследовательские цели при анализе биомаркеров по результатам исследования VISTA состояли в том, чтобы выявить популяции пациентов, которые с большей или меньшей вероятностью ответили бы на комбинированную терапию VELCADE/мелфалан/преднизон по сравнению с комбинированной терапией мелфалан/преднизон, для чего:
- подтвердили вывод (из исследований лимфомы) об ассоциации единичного маркера PSMB1 P11A и PSMB5 R24C с PFS и OS;
- выясняли ассоциацию с другими конечными точками клинического исследования, в том числе: время до прогрессирования (TTP), полный ответ (CR), общая частота ответа, время до ответа и продолжительность ответа.
Ассоциирование PSMB1 P11A и PSMB5 R24C, раздельно или в комбинации, с TTP, PFS и OS оценивали с помощью логрангового критерия между группами лечения для положительных и отрицательных по биомаркеру популяций. Для общей популяции по биомаркеру по группам лечения проводили аналогичные ассоциации. Привели медианы для TTP, PFS и OS, различия в медианах TTP, PFS и OS между группами лечения, логранговые Р-значения, отношения рисков и их 95%-ные доверительные интервалы и частоты наступления событий. Для каждого биомаркера привели кривые Каплана-Мейера. При обнаружении положительных ассоциаций для TTP, OS или PFS тестировали другие конечные точки клинических исследований с помощью аналогичных способов и выходных показателей. Для ORR использовали точный критерий Фишера. Число и процентную долю субъектов, попадающих в каждую категорию ответа, свели в описательные таблицы.
Приведенные в таблице 8 данные показывают преимущество по выживаемости без прогрессирования заболевания в 5,3 месяца при приеме VELCADE-MP по сравнению с монотерапией MP у пациентов с маркером PSMB1 P11A (C/G).
Приведенные в таблице 9 данные показывают преимущество по общей выживаемости пациентов в 6 месяцев при приеме VELCADE-MP по сравнению с монотерапией MP у пациентов с маркером PSMB1 P11A (C/G).
ПРИЛОЖЕНИЕ 3. ПАРНЫЕ КОМБИНАЦИИ МАРКЕРОВ
В приведенной ниже таблице приведены данные для всех статистически значимых парных комбинаций.
Примечание. Выбран = положительный по биомаркеру, не выбран = отрицательный по биомаркеру.
Реферат
Изобретение относится к медицине и представляет собой способ прогнозирования ответа онкологического пациента с неходжкинской лимфомой на противораковую терапию, включающую бортезомиб и ритуксимаб, отличающийся тем, что способ включает определение уровня или количества первого прогностического фактора и определение присутствия или количества второго прогностического фактора, причем низкий уровень СD68 или присутствие полиморфизма PSMB1 (P11A) коррелирует по меньшей мере с одним положительным исходом. Также изобретение относится к диагностическому набору для выявления онкологических пациентов с неходжкинской лимфомой, которые являются кандидатами для лечения рака бортезомибом и ритуксимабом, а также способу лечения рака у онкологических пациентов с неходжкинской лимфомой. Осуществление изобретения позволяет прогнозировать положительный ответ онкологического пациента на комбинированную терапию бортезомибом и ритуксимабом. 3 н. и 4 з.п. ф-лы, 5 пр., 25 табл., 8 ил.

Комментарии