Полиморфные формы бензоата натрия и их применения - RU2782627C2
Код документа: RU2782627C2
Чертежи





















Описание
Родственная заявка
По настоящей заявке испрашивается приоритет заявки на патент США №15/452,137, поданной 7 марта 2017, и временной заявки на патент США №62/412,160, поданной 24 октября 2016, каждая из которых полностью включена в настоящее описание посредством ссылки.
Уровень техники
Центральная нервная система (ЦНС) включает головной мозг и спинной мозг. ЦНС уязвима к различным нарушениям, которые могут быть вызваны различными факторами, включая генетику, травму, инфекции, дегенерацию, дислокации и/или повреждения, опухоли, нарушения кровообращения и аутоиммунные нарушения. Симптомы расстройства ЦНС зависят от затронутого отдела нервной системы и причины нарушения.
Разработка эффективных методов лечения расстройств ЦНС отстает от других терапевтических областей вследствие сложности таких нарушений и отсутствия эффективной технологии для доставки терапевтических агентов через гематоэнцефалический барьер. Само по себе, это очень интересно для разработки новых подходов к лечению расстройств ЦНС.
Сущность изобретения
Изобретение относится к новым полиморфным формам бензоата натрия, композициям и наборам, содержащим их, способам их получения и применениям полиморфных форм бензоата натрия для лечения и/или снижения риска нейропсихиатрического расстройства (например, шизофрении, психотических расстройтсв, боли или болезни Альцгеймера). Также изобретение относится к фармацевтическим композициям, содержащим соединение бензоата натрия и клозапин; и способу профилактики, лечения и/или снижения риска нейропсихиатрического расстройства путем введения таких фармацевтических композиций.
В одном аспекте настоящее раскрытие относится к полиморфной форме бензоата натрия, которая имеет порошковую дифракционную рентгенограмму, содержащую характеристические пики при угле отражения 2θ приблизительно 5,9, 30,2, и 31,2 градусов. В некоторых вариантах осуществления порошковая дифракционная рентгенограмма полиморфной формы бензоата натрия может дополнительно содержать характеристические пики при угле отражения 2θ приблизительно 3,6, 7,2, 7,5, 14,9, 15,9, 16,6, 17,6, 18,8, 20,4, 22,9, 23,7, 25,1, 25,8, 26,6, 28,1, 29,1, 29,4, 29,7, 31,5, 32,9, 34,2 и 35,7 градусов. В некоторых вариантах осуществления порошковая дифракционная рентгенограмма полиморфной формы бензоата натрия может дополнительно содержать характеристические пики при угле отражения 2θ приблизительно 3,7, 6,8, 7,5, 11,3, 11,6, 17,6, 22,7, 23,5, 26,2, 27,6, 28,3, 29,3, 32,2, 32,9, 34,0 и 35,7 градусов. В некоторых вариантах осуществления порошковая дифракционная рентгенограмма полиморфной формы бензоата натрия может дополнительно содержать характеристические пики при угле отражения 2θ приблизительно 3,7, 6,3, 6,8, 7,5, 11,7, 17,7, 23,6, 24,5, 26,5, 27,0, 27,7, 28,4, 29,0, 31,0, 32,3, 34,2 и 35,9 градусов. В некоторых вариантах осуществления порошковая дифракционная рентгенограмма полиморфной формы бензоата натрия может дополнительно содержать характеристические пики при угле отражения 2θ приблизительно 4,3, 7,1, 8,6, 10,1, 10,7, 12,9, 13,8, 14,4, 17,2, 17,7, 18,5, 21,5, 22,0, 22,6, 23,7, 25,1, 25,9, 26,2, 26,9, 27,9, 28,2, 28,8, 29,1, 29,7, 33,2, 34,9, 35,8, 36,1 и 39,3 градусов.
В другом аспекте настоящее раскрытие относится к полиморфной форме бензоата натрия, которая имеет порошковую дифракционную рентгенограмму, содержащую характеристические пики при угле отражения 2θ приблизительно 3,7, 5,9 и 26,6 градусов. В некоторых вариантах осуществления порошковая дифракционная рентгенограмма полиморфной формы бензоата натрия может дополнительно содержать характеристические пики при угле отражения 2θ приблизительно 5,5, 6,7, 7,4, 12,5, 14,7, 16,5, 17,7, 22,0, 23,6, 24,6, 25,8, 27,6, 28,4, 30,2, 31,1, 32,3, 34,3 и 35,9 градусов. В некоторых вариантах осуществления порошковая дифракционная рентгенограмма полиморфной формы бензоата натрия может дополнительно содержать характеристические пики при угле отражения 2θ приблизительно 6,6, 7,4, 9,4, 11,2, 12,5, 22,8, 25,1, 26,3, 28,2, 29,5, 30,2, 31,1, 31,2, 33,0 и 34,0 градусов.
В другом аспекте настоящее раскрытие относится к композициям (например, фармацевтической композиции, нутрицевтической композиции, продукт диетического питания или продукт лечебного питания), содержащим (i) эффективное количество одной или более полиморфных форм бензоата натрия, описанных здесь, и (ii) носитель, эксципиент, разбавитель, связующее, добавку, наполнитель, лубрикант или их смесь. Эффективное количество, описанное здесь, может быть терапевтически эффективным количеством или профилактически эффективным количеством.
В еще одном аспекте настоящее раскрытие относится к способам лечения и/или снижения риска нейропсихиатрического расстройства (например, шизофрении, психотических расстройств, депрессии, боли, болезни Альцгеймера или деменции), включающим введение пациенту эффективного количества любой из композиций, описанных здесь.
Целевое нейропсихиатрическое расстройство может включать, но не ограничено ими, шизофрению, психотические расстройства, болезнь Альцгеймера, деменцию, лобно-височную деменцию, легкое когнитивное нарушение, доброкачественная забывчивость, закрытую черепно-мозговую травму, расстройство аутического спектра, расстройство Аспергера, синдром дефицита внимания и гиперактивности, обсессивно-компульсивное расстройство, тиковые расстройства, нарушения способности к обучению в детском возрасте, предменструальный синдром, депрессию, суицидальное мышление, суицидальное поведение, биполярное расстройство, тревожные расстройства, посттравматическое стрессовое расстройство, хроническую боль, расстройства пищевого поведения, аддиктивные расстройства, расстройства личности, болезнь Паркинсона, болезнь Гентингтона, рассеянный склероз или боковой амиотрофический склероз.
В любом из способов лечения, как описано здесь, пациентом может быть млекопитающее (например, человек или млекопитающее, не являющееся человеком). Например, пациентом может быть человек, имеющий или подозреваемый в наличии целевого заболевания, как описано здесь.
Другой аспект настоящего раскрытия относится к наборам, включающим контейнер, в который помещена полиморфная форма бензоата натрия или ее композиция, как описано здесь. Наборы, описанные здесь, могут включать единственную дозу или многократные дозы полиморфа или композиции. Наборы могут быть использованы в способе согласно раскрытию. В некоторых вариантах осуществления набор дополнительно включает инструкции по использованию полиморфа или композиции.
В еще одном аспекте настоящее раскрытие относится к полиморфным формам бензоата натрия и композициям, описанным здесь, для применения в лечении и/или снижении риска нейропсихиатрического расстройства, как описано здесь. Настоящее раскрытие также относится к применению одной или более полиморфной формы бензоата натрия для получения лекарственного средства для применения в лечении целевого нейропсихиатрического расстройства, как описано здесь.
Настоящее раскрытие также относится к способам получения новых полиморфных форм бензоата натрия, описанных здесь.
В некоторых вариантах осуществления изобретение относится к способу получения полиморфной формы бензоата натрия, включающему: (i) растворение избыточного количества бензоата натрия в простом или смешанном растворителе для формирования насыщенного раствора при окружающих давлении и температуре, (ii) фильтрацию насыщенного раствора для удаления нерастворимых компонентов; (iii) упаривание насыщенного раствора, полученного в (ii), для формирования полиморфной формы бензоата натрия при окружающем или пониженном давлении и при повышенной температуре приблизительно 40-110°C; и (vi) сбор полиморфной формы бензоата натрия, сформированной в (iii).
В других вариантах осуществления, изобретение относится к способу получения полиморфной формы бензоата натрия, включающему: (i) растворение бензоата натрия в простом или смешанном растворителе при температуре в пределах приблизительно 50-110°C для формирования раствора; (ii) охлаждение раствора при температуре окружающей среды при перемешивании; (iii) размещение охлажденного раствора при температуре окружающей среды для обеспечения формирования полиморфной формы бензоата натрия; и (iv) сбор полиморфной формы бензоата натрия, сформированной в (iii).
В других вариантах осуществления, изобретение относится к способу получения полиморфной формы бензоата натрия, включающему: (i) помещение бензоата натрия при относительной влажности (RH), более чем приблизительно 90% в течение приблизительно 1-10 дней, во время которых формируется полиморфная форма бензоата натрия; и (ii) сбор полиморфной формы бензоата натрия, сформированной в (i).
Также одна или более полиморфных форм бензоата натрия, описанных здесь, могут быть получены способом, включающим: (i) получение суспензии бензоата натрия в простом или смешанном растворителе; (ii) перемешивание суспензии в течение от 6 часов до 10 дней, во время которых формируется полиморфная форма бензоата натрия; и (iii) сбор полиморфной формы бензоата натрия, сформированной в (ii).
В других примерах такой способ может включать: (i) растворение бензоата натрия в простом или смешанном растворителе для формирования раствора; (ii) смешивание антирастворителя с раствором, полученным в (i), для формирования суспензии причем объемное соотношение между антирастворителем и раствором в (i) составляет приблизительно от 4:1 до 15:1; (iii) перемешивание суспензии при окружающих давлении и температуре в течение приблизительно 2-10 дней, во время которых формируется полиморфная форма бензоата натрия; и (iv) сбор полиморфной формы бензоата натрия, сформированной в (iii).
В других примерах способ получения может включать: (i) получение суспензии любой подходящей полиморфной формы бензоата натрия, как описано здесь, в простом или смешанном растворителе в присутствии приблизительно 2-10% воды; (ii) перемешивание суспензии при окружающих давлении и температуре в течение приблизительно 2-10 дней, во время которых формируется полиморфная форма бензоата натрия; и (iii) сбор полиморфной формы бензоата натрия, сформированной в (iii).
В еще одном аспекте настоящее раскрытие относится к фармацевтической композиции, содержащей от 50 до 1000 мг соединения бензоата натрия и от 25 до 300 мг клозапина в твердой дозированной форме, например, таблетке, драже, капсуле, пилюле, порошке или грануле. В некоторых вариантах осуществления твердая дозированная форма может дополнительно содержать пленочное покрытие.
Вышеупомянутое соединение бензоата натрия может быть в аморфной форме, в полиморфной форме или в обеих формах. В некоторых вариантах осуществления соединение бензоата натрия включает любую из полиморфных форм бензоата натрия, описанных здесь (например, полиморф #4).
Любая из фармацевтических композиций, описанных здесь, может дополнительно содержать фармацевтически приемлемый эксципиент, который может быть борной кислотой, альгинатом натрия, цитратом натрия, гиалуронатом натрия, хитозаном, стеаратом магния, стеарил фумаратом натрия, коллоидным диоксидом кремния, тальком, гликолятом крахмала натрия, кроскармеллозой, кросповидоном, дубильной кислотой или их комбинацией. В некоторых вариантах осуществления фармацевтическая композиция может содержать от 50 до 1000 мг бензоата натрия, 25-300 мг клозапина, 50-500 мг альгината натрия, 50-400 мг цитрата натрия, 5-100 мг стеарата магния и 80-200 мг гликолята крахмала натрия.
В другом аспекте настоящее раскрытие относится к способу лечения и/или снижения риска нейропсихиатрического расстройства, включающему введение пациенту эффективного количества любой из фармацевтических композиций, описанных здесь. Нейропсихиатрические расстройства включают, но не ограничены ими, шизофрению, психотические расстройства, болезнь Альцгеймера, деменцию, лобно-височную деменцию, легкое когнитивное нарушение, доброкачественная забывчивость, закрытую черепно-мозговую травму, расстройство аутического спектра, расстройство Аспергера, синдром дефицита внимания и гиперактивности, обсессивно-компульсивное расстройство, тиковые расстройства, нарушения способности к обучению в детском возрасте, предменструальный синдром, депрессию, суицидальное мышление и/или поведение, биполярное расстройство, тревожные расстройства, посттравматическое стрессовое расстройство, хроническую боль, расстройства пищевого поведения, аддиктивные расстройства, расстройства личности, болезнь Паркинсона, болезнь Гентингтона, рассеянный склероз или боковой амиотрофический склероз.
В некоторых вариантах осуществления пациентом может быть человек, имеющий, подозреваемый в наличии или подвергающийся риску развития нейропсихиатрического расстройства. Фармацевтическая композиция может быть введена пациенту системным путем, например, энтеральным введением или парентеральным введением. В некоторых случаях пациенту вводят фармацевтическую композицию с частотой от четырех раз в сутки до одного раза в два месяца. Альтернативно или кроме того, пациента одновременно с этим, до этого или после этого лечат одним или более дополнительными терапевтическими агентами для лечения и/или снижения риска нейропсихиатрического расстройства.
Также в рамки настоящего раскрытия входит любая из фармацевтических композиций, описанных здесь, для применения в лечении нейропсихиатрического расстройства, и их применения для получения лекарственного средства для лечения целевого заболевания.
Детали одного или более вариантов осуществления раскрытия представлены здесь. Другие признаки, объекты и преимущества раскрытия будут очевидны из Подробного описания, примеров и формулы изобретения.
Определения
Определения специфических функциональных групп и химических терминов описаны более подробно ниже. Химические элементы идентифицируются в соответствии с Периодической таблицей элементов, версия CAS, Handbook of Chemistry and Physics, 75th Ed., внутренний разворот, и специфические функциональные группы обычно определяются, как описано там. Кроме того, общие принципы органической химии, а также специфические функциональные группы и реактивность описаны в Thomas Sorrell, Organic Chemistry, University Science Books, Sausalito, 1999; Smith and March, March'sAdvanced Organic Chemistry, 5th Edition, John Wiley & Sons, Inc., New York, 2001; Larock, Comprehensive Organic Transformations, VCH Publishers, Inc., New York, 1989; and Carruthers, Some Modern Methods of Organic Synthesis, 3rd Edition, Cambridge University Press, Cambridge, 1987. Это раскрытие никоим образом не ограничивается приведенным в качестве примера списком заместителей, описанных здесь.
«Бензоат натрия» относится к соединению формулы

Термин «клозапин» относится к соединению с названием IAPUC 3-хлор-6-(4-метилпиперазин-1-ил)-5H-бензо[b][1,4]бензодиазепин.
Термин ʺкоммерчески доступный бензоат натрияʺ относится к бензоату натрия, доступному из коммерческого источника, который может быть в аморфной форме, может включать известную единственную полиморфную форму или может включать смесь аморфных и/или одной или более полиморфных форм.
Термин ʺфармацевтически приемлемая сольʺ относится к солям, которые являются, в рамках здравого медицинского суждения, подходящими для использования в контакте с тканями человека и животных без нежелательной токсичности, раздражения, аллергической реакции и т.п. и соразмерны с обоснованным отношением преимущества/риска. Фармацевтически приемлемые соли известны в данной области техники. Например, Berge et al. подробно описывают фармацевтически приемлемые соли в J. Pharmaceutical Sciences, 1977, 66, 1-19, включенном в настоящее описание посредством ссылки.
Фармацевтически приемлемые соли соединений, описанных здесь, включают полученные из подходящих неорганических и органических кислот и оснований. Примерами фармацевтически приемлемых нетоксичных солей присоединения с кислотой являются соли аминогруппы, образованные с неорганическими кислотами, такими как соляная кислота, бромистоводородная кислота, фосфорная кислота, серная кислота и перхлорная кислота, или с органическими кислотами, такими как уксусная кислота, щавелевая кислота, малеиновая кислота, винная кислота, лимонная кислота, янтарная кислота или малоновая кислота, или с использованием других способов, известных в данной области техники, таких как ионный обмен. Другие фармацевтически приемлемые соли включают адипат, альгинат, аскорбат, аспартат, бензолсульфонат, бензоат, бисульфат, борат, бутират, камфорат, камфорсульфонат, цитрат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, формиат, фумарат, глюкогептаноат, глицерофосфат, глюконат, гемисульфат, гептаноат, гексаноат, гидройодид, 2-гидроксиэтансульфонат, лактобионат, лактат, лаурат, лаурил сульфат, малат, малеат, малонат, метансульфонат, 2-нафталинсульфонат, никотинат, нитрат, олеат, оксалат, пальмитат, памоат, пектинат, персульфат, 3-фенилпропионат, фосфат, пикрат, пивалат, пропионат, стеарат, сукцинат, сульфат, тартрат, тиоцианат, п-толуолсульфонат, ундеканоат, валерат и т.п. соли. Соли, полученные из подходящих оснований, включают соли щелочного металла, щелочноземельного металла, аммония и N+(C1-4 алкил)4-. Репрезентативные соли щелочного или щелочноземельного металла включают натрий, литий, калий, кальций, магний и т.п. Другие фармацевтически приемлемые соли включают, в соответствующих случаях, нетоксичные катионы аммония, четвертичного аммония и амина, сформированные с помощью противоионов, таких как галогенид, гидроксид, карбоксилат, сульфат, фосфат, нитрат, низший алкилсульфонат и арилсульфонат.
Термин «сольват» относится к формам соединения, связанным с растворителем, обычно реакцией сольволиза. Эта физическая ассоциация может включать водородное связывание. Стандартные растворители включают воду, метанол, этанол, уксусную кислоту, диметил сульфоксид (DMSO), тетрагидрофуран (THF), диэтиловый эфир и т.п. Соединения, описанные здесь, могут быть получены, например, в кристаллической форме и могут быть сольватированы. Подходящие сольваты включают фармацевтически приемлемые сольваты и также включают как стехиометрические сольваты, так и нестехиометрические сольваты. В некоторых случаях сольват способен к выделению, например, когда одна или более молекул растворителя включены в кристаллическую решетку кристаллического твердого вещества. «Сольват» охватывает как сольваты в жидкой фазе, так и пригодные к выделению сольваты. Репрезентативные сольваты включают гидраты, этаноляты и метаноляты.
Термин «кристаллический» или «кристаллическая форма» относится к твердой форме, по существу демонтсрирующей трехмерную структуру. В некоторых вариантах осуществления кристаллическая форма твердого вещества является твердой формой, которая является по существу не аморфной. В некоторых вариантах осуществления структура порошковой рентгеновской дифрактограммы (XRPD) кристаллической формы включает один или более четко определенных пиков.
Термин «аморфный» или «аморфная форма» относится к форме твердого вещества (ʺтвердая формаʺ), по существу не имеющей трехмерной структуры. В некоторых вариантах осуществления аморфная форма твердого вещества является твердой формой, которая является по существу не кристаллической. В некоторых вариантах осуществления структура порошковой рентгеновской дифрактограммы (XRPD) аморфной формы включает широкую полосу рассеивания с пиком при 2θ, например, между 20 и 70°, включительно, с использованием излучения CuKα. В некоторых вариантах осуществления структура XRPD аморфной формы дополнительно включает один или более пиков, относящихся к кристаллическим структурам. В некоторых вариантах осуществления максимальная интенсивность любого из одного или более пиков, относящихся к кристаллическим структурам, наблюдаемым при 2θ между 20 и 70°, включительно, является не более, чем 300-кратной, не более, чем 100-кратной, не более, чем 30-кратной, не более, чем 10-кратной или не более, чем 3-кратной от максимальной интенсивности широкой полосы рассеивания. В некоторых вариантах осуществления структура XRPD аморфной формы не включает пиков, относящихся к кристаллическим структурам.
Термин «полиморф» или ʺполиморфная формаʺ относится к кристаллической форме соединения (или его соли, гидрата или сольвата). Все полиморфные формы имеют тот же элементарный состав. Различные кристаллические формы обычно имеют различные структуры порошковой рентгеновской дифрактограммы, спектры инфракрасного излучения, температуру плавления, плотность, твердость, кристаллическую форму, оптические и электрические свойства, стабильность и растворимость. Растворитель для перекристаллизации, скорость кристаллизации, температура хранения и другие факторы могут приводить к доминированию одной кристаллической формы. Различные полиморфные формы соединения могут быть получены кристаллизацией в различных условиях.
Термины «ингибирование», «ингибировать», «ингибирует» или «ингибитор» относятся к способности полиморфной формы уменьшать, замедлять, останавливать или предотвращать активность определенного биологического процесса в клетке по сравнению с носителем.
Когда полиморфная форма, фармацевтическая композиция, способ, применение или набор упоминаются как «селективно», «специфически» или «избирательно» связывающие первый белок, полиморфная форма связывает первый белок с более высокой связывающей афинностью (например, не менее чем приблизительно 2-кратной, не менее чем приблизительно 5-кратной, не менее чем приблизительно 10-кратной, не менее чем приблизительно 30-кратной, не менее чем приблизительно 100-кратной, не менее чем приблизительно 1000-кратной или не менее чем приблизительно 10000-кратной), чем связывание второго белка или такого, который отличается от первого белка. Когда полиморфная форма упоминается как «селективно», «специфически» или «избирательно» модулирующая (например, увеличивающая или ингибирующая) активность первого белка, полиморфная форма модулирует активность первого белка в большей степени (например, не менее чем приблизительно 2-кратно, не менее чем приблизительно 5-кратно, не менее чем приблизительно 10-кратно, не менее чем приблизительно 30-кратно, не менее чем приблизительно 100-кратно, не менее чем приблизительно 1000-кратно или не менее чем приблизительно 10000-кратно), чем активность по меньшей мере одного белка, отличающегося от первого белка.
Термин ʺаберрантная активностьʺ относится к активности, отклоняющейся от нормальной активности. Термин ʺувеличенная активностьʺ относится к активности, более высокой, чем нормальная активность.
Термины «композиция» и «состав» используются взаимозаменяемо.
Термины «растворитель» и «антирастворитель» относятся к стандартным или к нетрадиционным растворителям, включая, но не ограничиваясь ими, воду, ацетон, ацетонитрил, бутанол, диоксан, этанол, этилацетат, изобутанол, изопропанол, метанол, метилэтилкетон, метил-1-бутанол, метил-трет-бутиловый эфир, тетрагидрофуран и толуол. Термин «растворитель» относится к веществу (например, жидкости), добавленному для растворения растворяемого вещества (другое вещество (например, твердое вещество)) с формированием раствора. Термин «антирастворитель» относится к растворителю, в котором растворенное вещество менее растворимо.
«Пациент», введение которому рассматривается, относится к человеку (т.е., мужчине или женщине любой возрастной группы, например, педиатрическому пациенту (например, младенцу, ребенку или подростку) или взрослому пациенту (например, молодому совершеннолетнему, взрослому средних лет или взрослому старшего возраста)) или животному. «Пациент» относится к человеку, нуждающемуся в лечении заболевания. Например, пациентом может быть человек, имеющий, подозреваемый в наличии или подвергающийся риску развития целевого заболевания, как описано здесь.
Термины «вводят» или «введение» относятся к внедрению, поглощению, принятию внутрь, впрыскиванию, вдыханию или иному представлению полиморфной формы бензоата натрия, описанного здесь, или его композицию, в или на организме пациента.
Термины «лечение» и «лечить» относятся к изменению, облегчению, задержке начала или ингибированию прогресса заболевания, описанного здесь. В некоторых вариантах осуществления лечение может быть назначено после того, как один или более признаков или симптомов заболевания развились или наблюдались. В других вариантах осуществления лечение может быть назначено в отсутствие признаков или симптомов заболевания. Например, лечение может быть назначено пациенту до начала симптомов (например, в свете истории симптомов и/или в свете экспозиции к патогену), чтобы задержать или предотвратить возникновение заболевания. Лечение может также быть продолжено после исчезновения симптомов, например, для задержки или предотвращения рецидива.
Термины «состояние», «заболевание» и «нарушение» используются взаимозаменяемо.
ʺЭффективное количествоʺ любого из активных ингредиентов, описанных здесь (например,любогоиз соединений бензоата натрия и/или клозапина), относится к количеству, достаточному для обеспечения желаемого биологического ответа, т.е., лечения состояния. Как будет понятно специалисту в данной области техники, эффективное количество любого из активных ингредиентов, описанных здесь, может варьировать в зависимости от таких факторов как желаемый биологический результат, фармакокинетика полиморфной формы, подвергаемое лечению состояние, способ введения и возраст и здоровье пациента. В некоторых вариантах осуществления эффективное количество является терапевтически эффективным количеством. В некоторых вариантах осуществления эффективное количество является профилактически эффективным количеством. В некоторых вариантах осуществления эффективное количество является количеством любого из активных ингредиентов, описанных здесь, в единственной дозе. В некоторых вариантах осуществления эффективное количество является объединенными количествами активных ингредиентов, описанных здесь, в многократных дозах.
ʺТерапевтически эффективное количествоʺ любого из активных ингредиентов, описанных здесь, является количеством, достаточным для того, чтобы предоставить терапевтическое преимущество в лечении состояния или задержке или минимизации одного или более симптомов, связанных с этим состоянием. Терапевтически эффективное количество любого из активных ингредиентов означает количество терапевтического агента, индивидуально или в комбинации с другими терапиями, которое предоставляет терапевтическое преимущество в лечении этого состояния. Термин ʺтерапевтически эффективное количествоʺ может охватывать количество, улучшающую общую терапию, позволяющее уменьшить или избежать симптомов, признаков или причин состояния и/или улучшающее терапевтическую эффективность другого терапевтического агента.
ʺПрофилактически эффективное количествоʺ любого из активных ингредиентов, описанных здесь, является количеством, достаточным для того, чтобы предотвратить состояние или один или более симптомов, связанных с этим состоянием, или предотвратить его рецидив. Профилактически эффективное количество любого из активных ингредиентов означает количество терапевтического агента, индивидуально или в комбинации с другими агентами, которое предоставляет профилактическое преимущество в профилактике этого состояния. Термин ʺпрофилактически эффективное количествоʺ может охватывать количество, улучшающее полную профилактику или улучшающее профилактическую эффективность другого профилактического агента.
Термины «около» или «приблизительно», которые используются здесь взаимозаменяемо, означают величину, находящуюся в приемлемом ошибочном диапазоне для определенного значения, как определяется специалистом, которая будет зависеть частично от того, как значение измеряется или определяется, т.е., от ограничения системы измерения. Например, «около» или «приблизительно» может означать диапазон менее ±10%, предпочтительно менее ±5%, более предпочтительно менее ±1%, более предпочтительно менее ±0,5% данного значения. В случае, если определенные значения описаны в заявке и формуле изобретения, если не указано иное, термин «приблизительно» является имплицитным и в этом контексте означает величину в приемлемом ошибочном диапазоне для определенного значения.
Термин «неврологическое заболевание» относится к любому заболеванию нервной системы, включая заболевания, затрагивающие центральную нервную систему (головной мозг, ствол мозга, спинной мозг и мозжечок), периферическую нервную систему (включая черепно-мозговые нервы) и автономную нервную систему (части которой расположены как в центральной, так и в периферической нервной системе). Нейродегенеративные заболевания относятся к типу неврологического заболевания, отмеченного потерей нейроцитов, включая, но не ограничиваясь ими, болезнь Альцгеймера, болезнь Паркинсона, лобно-височную деменцию, рассеянный склероз, боковой амиотрофический склероз, таупатии (включая лобно-височную деменцию), множественную системную атрофию и болезнь Гентингтона. Примеры неврологических заболеваний включают, но не ограничены ими, головную боль, ступор и кому, деменцию, эпилептический припадок, нарушения сна, травму, инфекции, опухоли, нейро-офтальмопатию, двигательные расстройства, демиелинизирующие заболевания, нарушения спинного мозга и нарушения периферических нервов, мышечных и нейро-мышечных соединений. Аддикция и психическое заболевание, включая, но не ограничиваясь ими, биполярное расстройство, депрессию и шизофрению, также включены в определение заболеваний ЦНС. Другие примеры неврологических заболеваний включают приобретенную эпилептиформную афазию; острый диссеминированный энцефаломиелит; адренолейкодистрофию; агенез мозолистого тела; агнозию; синдром Айкарди; болезнь Александера; болезнь Алперса; альтернирующую гемиплегию; болезнь Альцгеймера; боковой амиотрофический склероз; анэнцефалии; синдром Ангельмана; ангиоматоз; гипоксию; афазию; апраксию; арахноидальные кисты; арахноидит; порок развития Арнольда-Кьяри; артериовенозную мальформацию; синдром Аспергера; атаксию-телеангиэктазию; синдром дефицита внимания и гиперактивности; аутизм; автономную дисфункцию; боль в спине; болезнь Баттена; болезнь Бехчета; паралич Белла; доброкачественный эссенциальный блефароспазм; доброкачественную центральную амиотрофию; доброкачественную внутричерепную артериальную гипертензию; болезнь Бинсвангера; блефароспазм; синдром Блоха Сульцбергера; повреждение плечевого сплетения; мозговой абсцесс; травму головного мозга; опухоли головного мозга (включая мультиформную глиобластому); опухоль спинного мозга; синдром Брауна-Секуарда; болезнь Канавана; синдром запястного канала (CTS); каузалгию; центральный болевой синдром; центральный понтинный миелинолиз; головное расстройство; мозговую аневризму; мозговой артериосклероз; атрофию головного мозга; гигантизм головного мозга; церебральный паралич; болезнь Шарко-Мари-Тута; индуцированную химиотерапией нейропатию и нейропатическую боль; порок развития Кьяри; хорею; хроническую воспалительную демиелинизирующую полинейропатию (CIDP); хроническую боль; хронический регионарный болевой синдром; синдром Коффина-Лоури; кому, включая устойчивое вегетативное состояние; врожденную лицевую диплегию; кортикобазальную дегенерацию; краниальный артериит; краниосиностоз; спастический псевдосклероз; кумулятивные травматические расстройства; синдром Кушинга; инклюзионную цитомегалию (CIBD); цитомегаловирусную инфекцию; синдрома танцующих глаз-танцующих ног; синдром Денди-Уокера; болезнь Доусона; синдром Де Морсье; паралич Дежерин-Клюмпке; деменцию; дерматомиозит; диабетическую нейропатию; диффузный склероз; вегетативную дистонию; дисграфию; дислексию; дистонии; раннюю инфантильную эпилептическую энцефалопатию; синдром пустого турецкого седла; энцефалит; энцефалоцеле; энцефалотригеминальный ангиоматоз; эпилепсию; паралич Эрба; эссенциальный тремор; болезнь Фабри; синдром Фара; обморок; семейный спастический паралич; фебрильные судороги; синдром Фишера; атаксию Фридриха; лобно-височную деменцию и другие «таупатии»; болезнь Гоше; синдром Герштмана; гигантоклеточный артериит; гигантоклеточное инклюзионное заболевание; глобоидно-клеточную лейкодистрофию; синдром Гийена-Барре; HTLV-1-ассоциированную миелопатию; болезнь Галлевордена-Шпатца; черепно-мозговую травму; головную боль; гемифациальный спазм; наследственную спастическую параплегию; наследственную полиневропатическую атаксию; синдром Ханта; опоясывающий лишай; синдром Хирайама; ВИЧ-ассоциированную деменцию и нейропатию (см. также неврологические проявления СПИДа); голопрозэнцефалию; болезнь Гентингтона и другие полиглутаминовые заболевания; гидроанэнцефалию; гидроцефалию; гиперкортицизм; гипоксию; иммуноопосредованный энцефаломиелит; миозит с включенными тельцами; недержание пигмента; детскую болезнь накопления фитановой кислоты; ювенильную форму болезни Рефсума; детские судороги; воспалительную миопатию; внутричерепную кисту; внутричерепную гипертензию; синдром Жубера; синдром Кернса-Сайре; болезнь Кеннеди; синдром Кинсборна; синдром Клиппеля Фейла; болезнь Краббе; болезнь Кугельберга-Веландера; куру; болезнь Лафора; миастенический синдром Ламберта-Итона; синдром Ландау-Клеффнера; латеральный медуллярный (валленбергский) синдром; неспособность к обучению; болезнь Ли; синдром Леннокса-Гасто; синдром Леша-Нихана; лейкодистрофию; деменцию с тельцами Леви; лиссэнцефалию; синдром запертого человека; болезнь Лу Герига (болезнь моторных нейронов или боковой амиотрофический склероз); заболевание поясничного диска; болезнь Лайма - неврологические последствия; болезнь Мачадо-Иосифа; макрэнцефалию; мегалэнцефалию; синдром Мелкерссона-Розенталя; болезнь Меньера; менингит; болезнь Менкеса; метахроматическую лейкодистрофию; микроцефалию; мигрень; синдром Миллера Фишера; мини-инсульты; митохондриальные миопатии; синдром Мебиуса; мономерную амиотрофию; болезнь двигательных нейронов; болезнь мойя-мойя; мукополисахаридозы; мультиинфарктную деменцию; многоочаговую моторную невропатию; рассеянный склероз и другие демиелинизирующие расстройства; множественную системную атрофию с постуральной гипотензией; миастению; миелинокластический диффузный склероз; миоклоническую энцефалопатию у детей раннего возраста; миоклонус; миопатию; миотонию врожденную; нарколепсию; нейрофиброматоз; злокачественный нейролептический синдром; неврологические проявления СПИДа; неврологические последствия волчанки; нейромиотонию; нейрональный цероидный липофусциноз; нарушения нейрональной миграции; болезнь Ниманна-Пика; синдром О'Салливана-Маклеода; затылочную невралгию; скрытую дизрафию спинного мозга; синдром Охтахары; оливопонтоцеребеллярную атрофию; опсоклонус миоклонус; неврит зрительного нерва; ортостатическую гипотензию; синдром профессиональной перегрузки; парестезии; болезнь Паркинсона; врожденную парамиотонию; паранеопластические заболевания; пароксизмальные атаки; синдром Парри Ромберга; болезнь Пелизея-Мерцбахера; периодические параличи; периферическую невропатию; болевую невропатию и невропатическую боль; стойкое вегетативное состояние; аутистические расстройства; световой чихательный рефлекс; болезнь накопления фитановой кислоты; болезнь Пика; защемление нерва; опухоли гипофиза; полимиозит; порэнцефалию; пост-полиомиелитический синдром; постгерпетическую невралгию (PHN); постинфекционный энцефаломиелит; постуральную гипотензию; синдром Прадера-Вилли; первичный боковой склероз; прионные заболевания; прогрессирующую гемифациальную атрофию; прогрессирующую мультифокальную лейкоэнцефалопатию; прогрессирующую склерозирующую полиодистрофию; прогрессирующий надъядерный паралич; ложную опухоль головного мозга; синдром Рамсей-Ханта (тип I и тип II); энцефалит Расмуссена; синдром рефлекторной симпатической дистрофии; болезнь Рефсума; расстройства повторяющихся движений; повторяющиеся стрессовые травмы; синдром беспокойных ног; миелопатию, связанную с ретровирусами; синдром Ретта; синдром Рейе; пляску Святого Вита; болезнь Сандхоффа; болезнь Шильдера; шизэнцефалию; септо-оптическую дисплазию; синдром детского сотрясения; опоясывающий лишай; Синдром Шая-Дрейджера; синдром Шегрена; апноэ во сне; синдром Сото; спастичность; расщелину позвоночника; травмы спинного мозга; опухоли спинного мозга; спинальную мышечную атрофию; синдром скованного человека; инсульт; синдром Стерге-Вебера; подострый склерозирующий панэнцефалит; субарахноидальное кровоизлияние; подкорковую артериосклеротическую энцефалопатию; хорею Синдегама; обмороки; сирингомиелию; позднюю дискинезию; болезнь Тея-Сакса; височный артериит; синдром фиксированного спинного мозга; болезнь Томсена; синдром грудного выхода; невралгию тройничного нерва; паралич Тодда; синдром Туретта; транзиторную ишемическую атаку; трансмиссивные губчатые энцефалопатии; поперечный миелит; травматическое повреждение мозга; тремор; невралгию тройничного нерва; тропический спастический парапарез; туберозный склероз; сосудистую деменцию (мультиинфарктную деменцию); васкулит, включая височный артериит; болезнь фон Гиппеля-Линдау (VHL); синдром Валленберга; болезнь Верднига-Хоффмана; синдром Веста; хлыстовую травму шейного отдела позвоночника; синдром Уильямса; болезнь Вильсона; и синдром Зеллвегера.
Термин «психическое расстройство» относится к ментальным расстройствам и включает заболевания и нарушения, перечисленные в Diagnostic and Statistical Manual of Mental Disorders - Четвертый Выпуск и Пятый Выпуск (DSM-IV, DSM-V), изданном American Psychiatric Association, Вашингтон D. C. (1994, 2013). Психические расстройства включают, но не ограничены ими, тревожные расстройства (например, острое стрессовое расстройство, агорафобию, генерализованное тревожное расстройство, синдром навязчивых состояний, паническое расстройство, посттравматическое стрессовое расстройство, тревожное расстройство, вызванное разлукой, социальную фобию и специфическую фобию), расстройства детского возраста, (например, нарушение дефицита внимания/гиперактивности, расстройство поведения и оппозиционно-вызывающее расстройство), расстройства пищевого поведения (например, анорексия и булимия), расстройства настроения (например, депрессия, биполярное расстройство I и II, циклотимическое расстройство, дистимическое расстройство и серьезное депрессивное расстройство), расстройства личности (например, антисоциальное расстройство личности, личностное расстройство избегания, пограничное расстройство личности, зависимое расстройство личности, театральное расстройство личности, нарциссическое расстройство личности, обсессивно-компульсивное расстройство личности, параноидальное расстройство личности, шизоидное расстройство личности и шизотипическое расстройство личности), психотические расстройства (например, кратковременное психотическое расстройство, бредовое расстройство, шизоаффективное расстройство, шизофрениформное расстройство, шизофрения и индуцированное психотическое расстройство), расстройства, связанные с веществами (например, алкогольная зависимость или злоупотребление, амфетаминовая зависимость или злоупотребление, каннабиноидная зависимость или злоупотребление, кокаиновая зависимость или злоупотребление, галлюциногенная зависимость или злоупотребление, ингаляционная зависимость или злоупотребление, никотиновая зависимость или злоупотребление, опиоидная зависимость или злоупотребление, фенциклидиновая зависимость или злоупотребление и седативная зависимость или злоупотребление), нарушения адаптации, аутизм, расстройство Аспергера, делирий, деменцию, мультиинфарктную деменцию, нарушения изучения и памяти (например, амнезия и возрастная потеря памяти), тиковые расстройства и расстройство Туретта.
В рамках изобретения, термин «расстройства личности» относится к психическим расстройствам, характеризующимся стойкими неадекватными структурами поведения, познания и внутреннего опыта, демонстрируемыми через многие контексты и заметно отклоняющимися от принятых в человеческой культуре. Эти структуры развиваются рано, являются негибки и связаны со значительными трудностями или инвалидностью. Например, расстройства личности могут включать, но не ограничиваются ими, параноидальное, шизоидное, шизотипическое, антисоциальное, пограничное, театральное, нарциссическое, социальное, зависимое и обсессивно-компульсивное расстройство личности.
Термин ʺнейропсихиатрическое расстройствоʺ, включая как неврологические заболевания, так и психические расстройства или расстройства центральной нервной системы (расстройства ЦНС), относится к нарушению, включающему либо психиатрические симптомы, либо синдромы, вызванные органическими расстройствами центральной нервной системы. Главные особенности нейропсихиатрических симптомов включают возникновение различных психиатрических симптомов, нарушения когнитивной функции, неврологические симптомы или возможности симптомов раннего развития мозга.
Термины «продукт диетического питания» или ʺдиетический пищевой продуктʺ относятся к любому виду жидких и твердых/полутвердых материалов, использующихся для питания человека и животных, для улучшения основного поведенческого функционирования, гиперактивности, настроения, тревоги, депрессии, сенсорного восприятия, сенсорно-двигательный реакций, болевого порога, памяти и/или познавательного функционирования, массы тела или для облегчения лечения любого из целевых заболеваний, отмеченных здесь. Термин ʺнутрицевтическая композицияʺ относится к композициям, содержащим компоненты источников пищи и приносящим дополнительную пользу для здоровья в дополнение к основной пищевой ценности, находимой в продуктах.
Термин ʺпродукт лечебного питанияʺ относится к продукту питания, составленному для потребления или энтерального введения, включая продукт питания, обычно использующийся под наблюдением врача для специфического диетического контроля целевого заболевания, такого как описанные здесь. Композиция ʺпродукта лечебного питанияʺ может относиться к композиции, специально составленной и обработанной (в противоположность натуральным пищевым продуктам, используемым в естественном состоянии) для пациента, нуждающегося в лечении (например, пациентов-людей, страдающих заболеванием или которым требуется использование продукта в качестве главного активного вещества для облегчения заболевания или состояния через специфический диетический контроль).
Краткое описание чертежей
Фигура 1 показывает рентгеновскую порошковую дифрактометрию (XRPD) полиморфной формы #1 бензоата натрия из Примера 1 с пиками (°): 3,6, 5,9, 7,2, 7,5, 14,9, 15,9, 16,6, 17,6, 18,8, 20,4, 22,9, 23,7, 25,1, 25,8, 26,6, 28,1, 29,1, 29,4, 29,7, 30,2, 31,2, 31,5, 32,9, 34,2 и 35,7.
Фигура 2 показывает термогравиметрический анализ (TGA) полиморфной формы #1 бензоата натрия из Примера 1.
Фигура 3 показывает профиль, определенный способом дифференциальной сканирующей калориметрии (DSC) полиморфной формы #1 бензоата натрия из Примера 1.
Фигура 4 показывает рентгеновскую порошковую дифрактометрию (XRPD) полиморфной формы #2 бензоата натрия из Примера 2 с пиками (°): 3,7, 5,9, 6,8, 7,5, 11,3, 11,6, 17,6, 22,7, 23,5, 26,2, 27,6, 28,3, 29,3; 30,2, 31,2, 32,2, 32,9, 34,0 и 35,7.
Фигура 5 показывает термогравиметрический анализ (TGA) полиморфной формы #2 бензоата натрия из Примера 2.
Фигура 6 показывает профиль, определенный способом дифференциальной сканирующей калориметрии (DSC) полиморфной формы #2 бензоата натрия из Примера 2.
Фигура 7 показывает рентгеновскую порошковую дифрактометрию (XRPD) полиморфной формы #3 бензоата натрия из Примера 3 с пиками (°): 3,7, 5,9, 6,3, 6,8, 7,5, 11,7, 17,7, 23,6, 24,5, 26,5, 27,0, 27,7, 28,4, 29,0, 30,2; 31,0, 31,2, 32,3, 34,2 и 35,9.
Фигура 8 показывает термогравиметрический анализ (TGA) полиморфной формы #3 бензоата натрия из Примера 3.
Фигура 9 показывает профиль, определенный способом дифференциальной сканирующей калориметрии (DSC) полиморфной формы #3 бензоата натрия из Примера 3.
Фигура 10 показывает рентгеновскую порошковую дифрактометрию (XRPD) полиморфной формы #4 бензоата натрия из Примера 4 с пиками (°): 4,3, 5,9, 7,1, 8,6, 10,1, 10,7, 12,9, 13,8, 14,4, 17,2, 17,7, 18,5, 21,5, 22,0, 22,6, 23,7, 25,1, 25,9, 26,2, 26,9, 27,9, 28,2, 28,8, 29,1, 29,7, 30,2, 31,2, 33,2, 34,9, 35,8, 36,1 и 39,3.
Фигура 11 показывает термогравиметрический анализ (TGA) полиморфной формы #4 бензоата натрия из Примера 4.
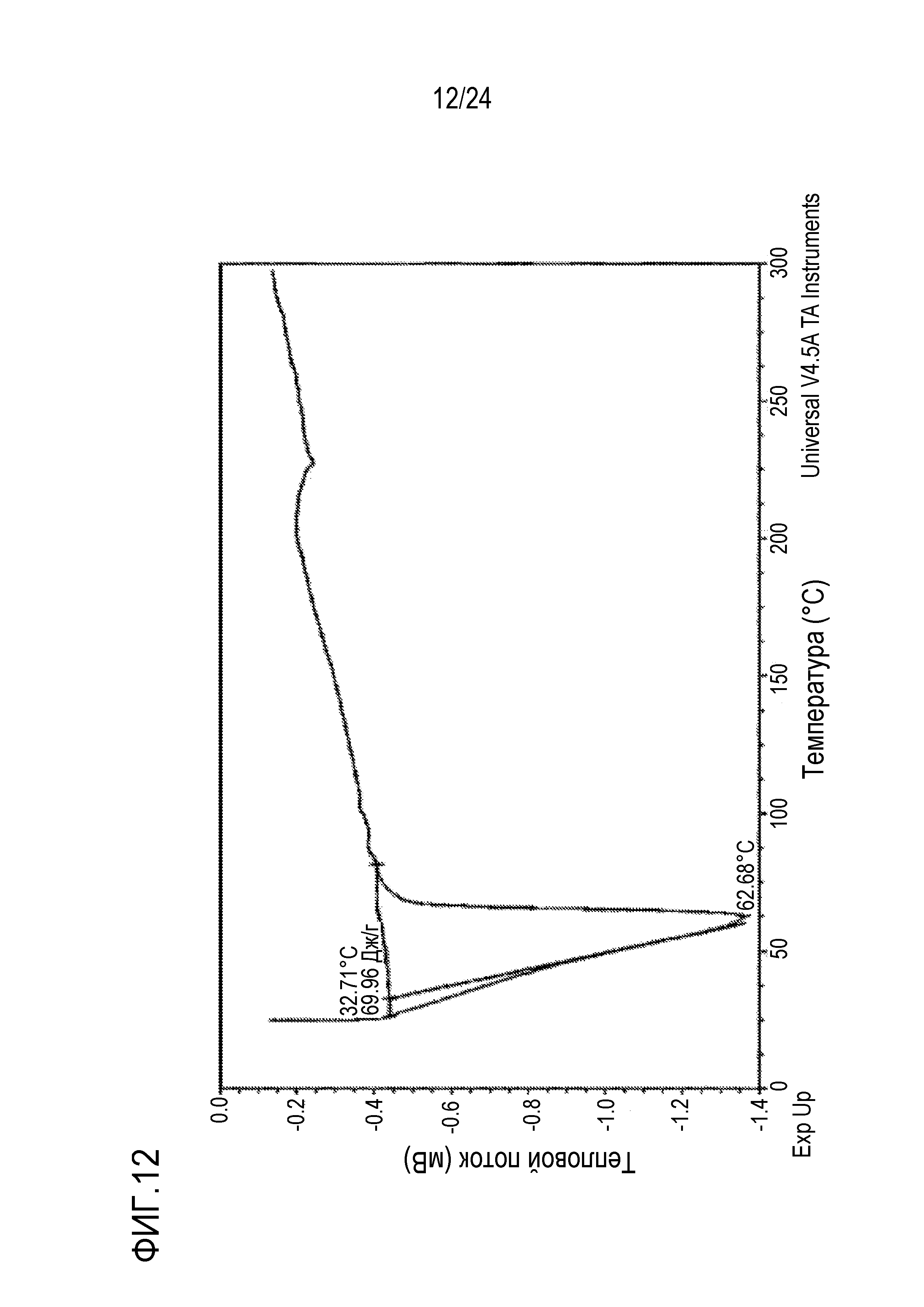
Фигура 12 показывает профиль, определенный способом дифференциальной сканирующей калориметрии (DSC) полиморфной формы #4 бензоата натрия из Примера 4.
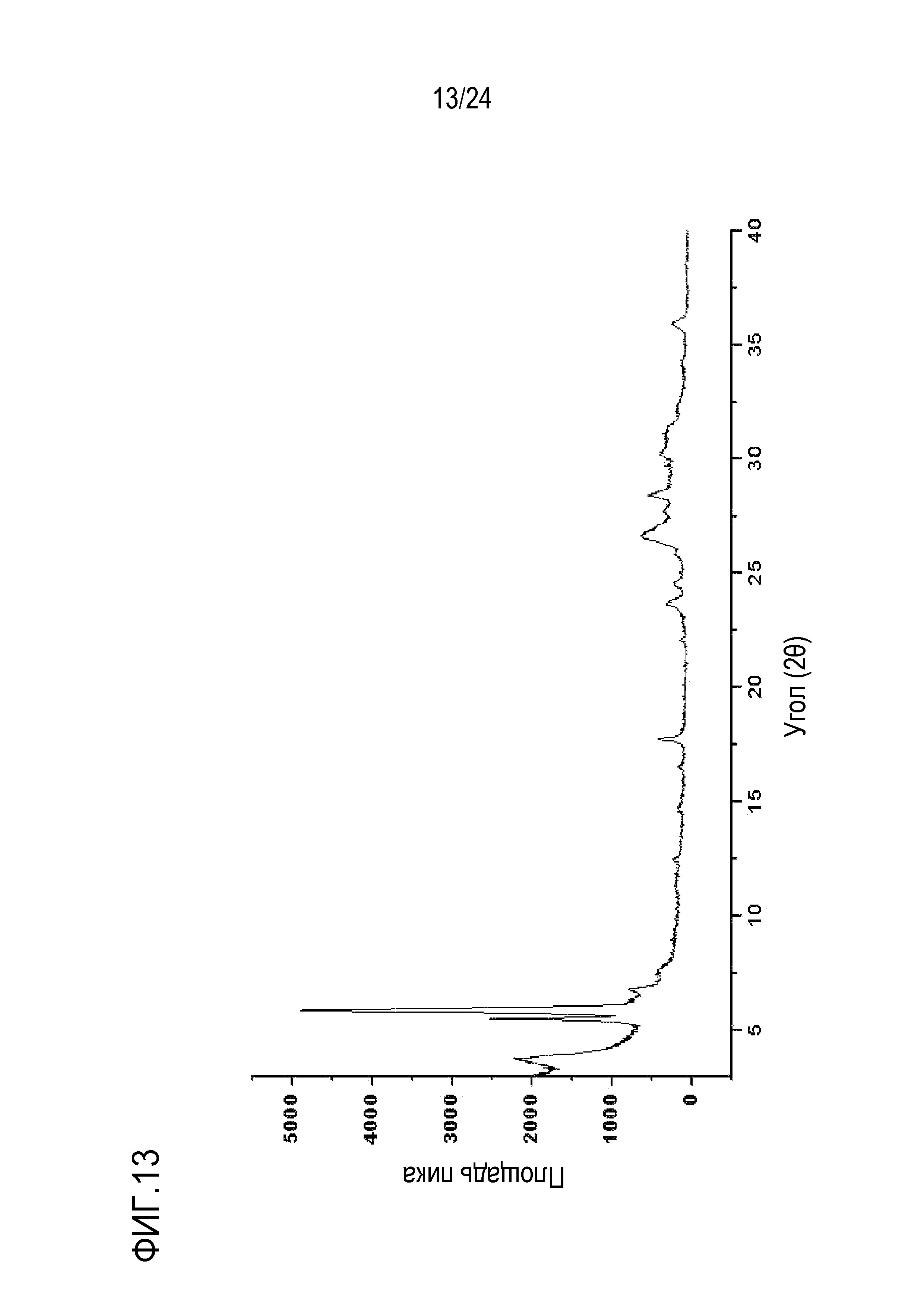
Фигура 13 показывает рентгеновскую порошковую дифрактометрию (XRPD) полиморфной формы #5 бензоата натрия из Примера 5 с пиками (°): 3,7, 5,5, 5,9, 6,7, 7,4, 12,5, 14,7, 16,5, 17,7, 22,0, 23,6, 24,6, 25,8, 26,6, 27,6, 28,4, 30,2, 31,1, 32,3, 34,3, и 35,9.
Фигура 14 показывает термогравиметрический анализ (TGA) полиморфной формы #5 бензоата натрия из Примера 5.
Фигура 15 показывает температуру плавления, определенную способом дифференциальной сканирующей калориметрии (DSC), полиморфной формы #5 бензоата натрия из Примера 5.
Фигура 16 показывает рентгеновскую порошковую дифрактометрию (XRPD) полиморфной формы #6 бензоата натрия из Примера 6 с пиками (°): 3,7, 5,9, 6,6, 7,4, 9,4, 11,2, 12,5, 22,8, 25,1, 26,3, 28,2, 29,5, 30,2, 31,1, 31,2, 33,0 и 34,0.
Фигура 17 показывает термогравиметрический анализ (TGA) полиморфной формы #6 бензоата натрия из Примера 6.
Фигура 18 показывает температуру плавления, определенную способом дифференциальной сканирующей калориметрии (DSC), полиморфной формы #6 бензоата натрия из Примера 6.
Фигура 19 показывает рентгеновскую порошковую дифрактометрию (XRPD) бензоата натрия (NaBen) от Merck, Formosa Laboratories и новой полиморфной формы #4 в условиях высокой влажности (более 90% относительной влажности) в течение 5 дней. XRPD бензоата натрия от Merck и Formosa Laboratories показывают изменения в XRPD в этих условиях высокой влажности, но XRPD полиморфной формы #4 бензоата натрия из Примера 7 не показывает таких изменений в XRPD.
Фигура 20 показывает изменения порошковой рентгеновской дифрактограммы (XRPD) бензоата натрия (NaBen) от Merck в комбинации с клозапином (300 мг) в условиях высокой влажности (более 90% относительной влажности) в течение 5 дней.
Фигура 21 показывает отсутствие изменения порошковой рентгеновской дифрактограммы (XRPD) новой полиморфной формы #4 в комбинации с клозапином (300 мг) в условиях высокой влажности (более 90% относительной влажности) в течение 5 дней.
Фигура 22 показывает рентгеновскую порошковую дифрактометрию (XRPD) новой полиморфной формы #4 бензоата натрия (NaBen) от Merck и бензоата натрия (NaBen) от Sigma-Aldrich.
Фигура 23 показывает изменения порошковой рентгеновской дифрактограммы (XRPD) бензоата натрия (NaBen) от Merck в комбинации с клозапином (100 мг) в условиях высокой влажности (> 90%RH, комнатная температура) в течение 8 дней.
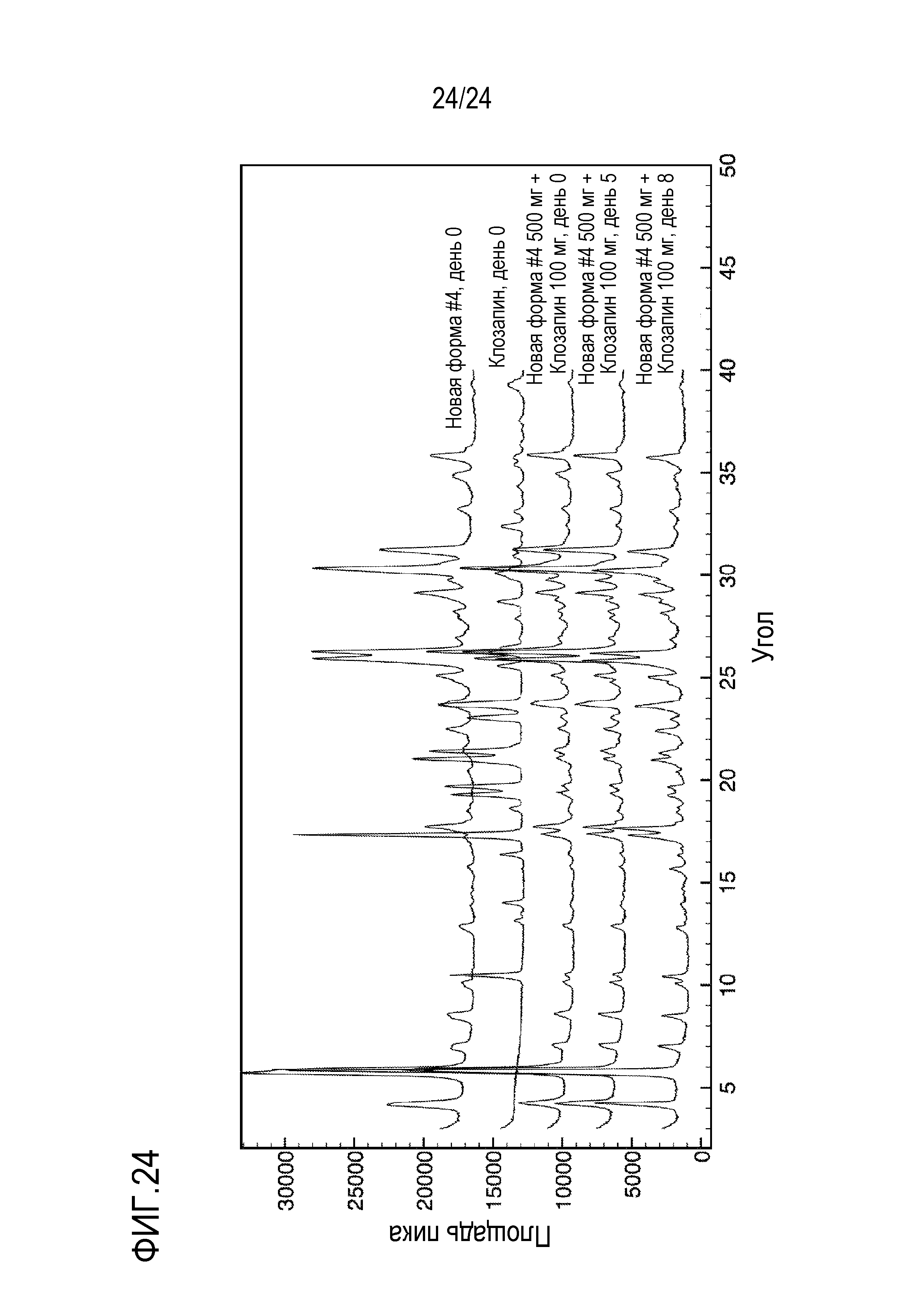
Фигура 24 показывает отсутствие изменения порошковой рентгеновской дифрактограммы (XRPD) полиморфной формы #4 бензоата натрия в комбинации с клозапином (100 мг) в условиях высокой влажности (> 90%RH, комнатная температура) в течение 8 дней.
Подробное описание
Настоящее раскрытие относится к новым полиморфным формам бензоата натрия. Эти полиморфные формы более стабильны, чем аморфные и известные полиморфные формы и могут быть использованы в лечении и/или снижении риска различных заболеваний и нарушений, включая нейропсихиатрические расстройства, у пациента. Таким образом, изобретение также относится к способуы получения полиморфных форм, к композициям, наборам и способам применения полиморфных форм бензоата натрия, описанных здесь, для лечения и/или снижения риска любого из целевых заболеваний, описанных здесь.
Далее, настоящее раскрытие относится к фармацевтической композиции, которая содержит эффективное количество соединения бензоата натрия и эффективное количество клозапина. Кристаллический бензоат натрия по изобретению (т.е., полиморфная форма бензоата натрия) более стабилен, чем аморфные и другие известные полиморфные формы бензоата натрия или их комбинации. Кроме того, эксципиенты, входящие в состав фармацевтической композиции, описанной здесь, улучшают стабильность комбинации соединения бензоата натрия и клозапина. Фармацевтическая композиция, описанная здесь, может быть использована в профилактике, лечении и/или снижении риска различных заболеваний и нарушений, включая нейропсихиатрические расстройства, у пациента. Таким образом, изобретение также относится к способу профилактики, лечения и/или снижения риска любого из целевых заболеваний, описанных здесь, путем введения фармацевтической композиции, описанной здесь.
Новые полиморфные формы бензоата натрия
Один аспект настоящего раскрытия касается полиморфных форм бензоата натрия, как описано здесь. Эти полиморфные формы могут быть использованы в лечении и/или снижении риска нейропсихиатрических расстройств у пациента.
В одном аспекте полиморфная форма бензоата натрия имеет порошковую дифракционную рентгенограмму, включающую характеристические пики при угле отражения 2θ приблизительно 5,9, 30,2 и 31,2 градусов. В некоторых вариантах осуществления полиморфная форма бензоата натрия имеет порошковую дифракционную рентгенограмму при угле отражения 2θ, дополнительно включающую характеристические пики при приблизительно 3,6, 7,2, 7,5, 14,9, 15,9, 16,6, 17,6, 18,8, 20,4, 22,9, 23,7, 25,1, 25,8, 26,6, 28,1, 29,1, 29,4, 29,7, 31,5, 32,9, 34,2 и 35,7 градусов. В некоторых вариантах осуществления полиморфная форма имеет порошковую дифракционную рентгенограмму по существу как показано на Фигуре 1. В некоторых вариантах осуществления полиморфная форма имеет структуру TGA по существу как показано на Фигуре 2. В некоторых вариантах осуществления полиморфная форма имеет структуру DSC по существу как показано на Фигуре 3. В некоторых вариантах осуществления полиморфная форма имеет порошковую дифракционную рентгенограмму, по существу как показано на Фигуре 1, структура TGA, по существу как показано на Фигуре 2, и структуру DSC по существу как показано на Фигуре 3.
В некоторых вариантах осуществления полиморфная форма бензоата натрия имеет порошковую дифракционную рентгенограмму при угле отражения 2θ, дополнительно включающую характеристические пики при приблизительно 3,7, 6,8, 7,5, 11,3, 11,6, 17,6, 22,7, 23,5, 26,2, 27,6, 28,3, 29,3, 32,2, 32,9, 34,0 и 35,7 градусов. В некоторых вариантах осуществления полиморфная форма имеет порошковую дифракционную рентгенограмму по существу как показано на Фигуре 4. В некоторых вариантах осуществления полиморфная форма имеет структуру TGA по существу как показано на Фигуре 5. В некоторых вариантах осуществления полиморфная форма имеет структуру DSC по существу как показано на Фигуре 6. В некоторых вариантах осуществления полиморфная форма имеет порошковую дифракционную рентгенограмму, по существу как показано на Фигуре 4, структуру TGA, по существу как показано на Фигуре 5, и структуру DSC по существу как показано на Фигуре 6.
В некоторых вариантах осуществления полиморфная форма бензоата натрия имеет порошковую дифракционную рентгенограмму при угле отражения 2θ, дополнительно включающую характеристические пики при приблизительно 3,7, 6,3, 6,8, 7,5, 11,7, 17,7, 23,6, 24,5, 26,5, 27,0, 27,7, 28,4, 29,0, 30,2, 31,0, 31,2, 32,3, 34,2 и 35,9 градусов. В некоторых вариантах осуществления полиморфная форма имеет порошковую дифракционную рентгенограмму по существу как показано на Фигуре 7. В некоторых вариантах осуществления полиморфная форма имеет структуру TGA по существу как показано на Фигуре 8. В некоторых вариантах осуществления полиморфная форма имеет структуру DSC по существу как показано на Фигуре 9. В некоторых вариантах осуществления полиморфная форма имеет порошковую дифракционную рентгенограмму, по существу как показано на Фигуре 7, структуру TGA, по существу как показано на Фигуре 8, и структуру DSC по существу как показано на Фигуре 9.
В некоторых вариантах осуществления полиморфная форма бензоата натрия имеет порошковую дифракционную рентгенограмму при угле отражения 2θ, дополнительно включающую характеристические пики при приблизительно 4,3, 7,1, 8,6, 10,1, 10,7, 12,9, 13,8, 14,4, 17,2, 17,7, 18,5, 21,5, 22,0, 22,6, 23,7, 25,1, 25,9, 26,2, 26,9, 27,9, 28,2, 28,8, 29,1, 29,7, 33,2, 34,9, 35,8, 36,1 и 39,3 градусов. В некоторых вариантах осуществления полиморфная форма имеет порошковую дифракционную рентгенограмму по существу как показано на Фигуре 10. В некоторых вариантах осуществления полиморфная форма имеет структуру TGA по существу как показано на Фигуре 11. В некоторых вариантах осуществления полиморфная форма имеет структуру DSC по существу как показано на Фигуре 12. В некоторых вариантах осуществления полиморфная форма имеет порошковую дифракционную рентгенограмму, по существу как показано на Фигуре 10, структуру TGA, по существу как показано на Фигуре 11, и структуру DSC по существу как показано на Фигуре 12.
В другом аспекте изобретение относится к полиморфной форме бензоата натрия, имеющей дифракционную рентгенограмму, включающую характеристические пики при угле отражения 2θ приблизительно 3,7, 5,9 и 26,6 градусов. В некоторых вариантах осуществления полиморфная форма бензоата натрия имеет порошковую дифракционную рентгенограмму при угле отражения 2θ, дополнительно включающую характеристические пики при приблизительно 5,5, 6,7, 7,4, 12,5, 14,7, 16,5, 17,7, 22,0, 23,6, 24,6, 25,8, 27,6, 28,4, 30,2, 31,1, 32,3, 34,3 и 35,9 градусов. В некоторых вариантах осуществления полиморфная форма имеет порошковую дифракционную рентгенограмму по существу как показано на Фигуре 13. В некоторых вариантах осуществления полиморфная форма имеет структуру TGA по существу как показано на Фигуре 14. В некоторых вариантах осуществления полиморфная форма имеет структуру DSC по существу как показано на Фигуре 15. В некоторых вариантах осуществления полиморфная форма имеет порошковую дифракционную рентгенограмму, по существу как показано на Фигуре 13, структуру TGA, по существу как показано на Фигуре 14, и структуру DSC по существу как показано на Фигуре 15.
В некоторых вариантах осуществления полиморфная форма бензоата натрия имеет порошковую дифракционную рентгенограмму при угле отражения 2θ, дополнительно включающую характеристические пики при приблизительно 6,6, 7,4, 9,4, 11,2, 12,5, 22,8, 25,1, 26,3, 28,2, 29,5, 30,2, 31,1, 31,2, 33,0 и 34,0 градусов. В некоторых вариантах осуществления полиморфная форма имеет порошковую дифракционную рентгенограмму по существу как показано на Фигуре 16. В некоторых вариантах осуществления полиморфная форма имеет структуру TGA по существу как показано на Фигуре 17. В некоторых вариантах осуществления полиморфная форма имеет структуру DSC по существу как показано на Фигуре 18. В некоторых вариантах осуществления полиморфная форма имеет порошковую дифракционную рентгенограмму, по существу как показано на Фигуре 16, структуру TGA, по существу как показано на Фигуре 17, и структуру DSC по существу как показано на Фигуре 18.
Любая из полиморфных форм бензоата натрия, описанных здесь, имеет химическую чистоту приблизительно 95%, 97%, 98%, 99%, 99,5%, 99,9% или выше, которая может быть определен стандартным способом, например, ВЭЖХ или спектроскопией1H ядерного магнитного резонанса (1H-ЯМР). В некоторых вариантах осуществления полиморфная форма бензоата натрия, описанная здесь, содержит менее 10%, предпочтительно менее 5%, предпочтительно менее 1%, предпочтительно менее 0,5% и наиболее предпочтительно менее 0,1% бензоата натрия в других полиморфных или аморфных формах (при измерении XRPD или DSC).
Композиции
Настоящее раскрытие относится к фармацевтической композиции, включающей эффективное количество соединения бензоата натрия и эффективное количество клозапина. В некоторых вариантах осуществления фармацевтическая композиция содержит от 50 до 1000 мг соединения бензоата натрия (например, от 100 до 800 мг, от 200 до 600 мг или от 300 до 500 мг) и от 25 до 300 мг клозапина (например, от 50 до 250 мг, от 100 до 200 мг или 150-300 мг). В некоторых вариантах осуществления фармацевтическая композиция содержит 500 мг соединения бензоата натрия и от 200 до 300 мг клозапина.
В некоторых вариантах осуществления соединение бензоата натрия (например, бензоат натрия) может быть в аморфной форме или в одной или более полиморфных формах. В некоторых примерах бензоат натрия может быть смесью аморфной формы и одной или более полиморфных форм. В одном примере соединение бензоата натрия может быть коммерчески доступным бензоатом натрия, который может включать аморфную и множество полиморфных форм бензоата натрия (например,приобретенные у Merck, Formosa, Sigma-Aldrich и т.п.), и очищенную полиморфную форму бензоата натрия по изобретению. В некоторых вариантах осуществления соединение бензоата натрия содержит полиморфную форму бензоата натрия, как описано здесь.
Настоящее раскрытие также относится к композициям, включающим полиморфную форму бензоата натрия, описанную здесь, и носитель, эксципиент, разбавитель, связующее, добавку, наполнитель и лубрикант или их смесь. В некоторых вариантах осуществления композиция содержит полиморфную форму бензоата натрия, описанную здесь, и фармацевтически приемлемый носитель. В некоторых вариантах осуществления композиция содержит полиморфную форму бензоата натрия, описанную здесь, и фармацевтически приемлемый эксципиент. В некоторых вариантах осуществления композиция содержит полиморфную форму бензоата натрия, описанную здесь, и фармацевтически приемлемый разбавитель. В некоторых вариантах осуществления композиция содержит полиморфную форму бензоата натрия, описанную здесь, и фармацевтически приемлемое связующее. В некоторых вариантах осуществления композиция содержит полиморфную форму бензоата натрия, описанную здесь, и фармацевтически приемлемую добавку. В некоторых вариантах осуществления композиция содержит полиморфную форму бензоата натрия, описанную здесь, и фармацевтически приемлемый наполнитель. В некоторых вариантах осуществления композиция содержит полиморфную форму бензоата натрия, описанную здесь, и фармацевтически приемлемый лубрикант.
В некоторых вариантах осуществления фармацевтическая композиция, описанная здесь, дополнительно содержит один или более фармацевтически приемлемых эксципиентов. В некоторых вариантах осуществления фармацевтическая композиция содержит от 50 до 1000 мг соединения бензоата натрия, от 25 до 300 мг клозапина и один или более фармацевтически приемлемых эксципиентов. В некоторых вариантах осуществления фармацевтическая композиция содержит 500 мг соединения бензоата натрия, от 200 до 300 мг клозапина и один или более фармацевтически приемлемых эксципиентов.
В некоторых вариантах осуществления весовое отношение соединения бензоата натрия к клозапину составляет от приблизительно 1:10 до приблизительно 1000:1, от приблизительно 1:10 до приблизительно 900:1, от приблизительно 1:10 до приблизительно 800:1, от приблизительно 1:10 до приблизительно 600:1, от приблизительно 1:10 до приблизительно 500:1, от приблизительно 1:10 до приблизительно 400:1, от приблизительно 1:10 до приблизительно 200:1, от приблизительно 1:10 до приблизительно 100:1, от приблизительно 1:10 до приблизительно 75:1, от приблизительно 1:10 до приблизительно 50:1, от приблизительно 1:10 до приблизительно 25:1, от приблизительно 1:10 до приблизительно 10:1, от приблизительно 1:10 до приблизительно 5:1, от приблизительно 1:10 до приблизительно 1:2, от приблизительно 1:10 до приблизительно 1:5 или от приблизительно 1:10 до приблизительно 1:8. В некоторых вариантах осуществления весовое отношение соединения бензоата натрия к клозапину составляет приблизительно 20:1, приблизительно 5:1, приблизительно 2,5:1 или приблизительно 1,67:1.
В некоторых вариантах осуществления соединение бензоата натрия, описанное здесь, находится в эффективном количестве в фармацевтической композиции. В некоторых вариантах осуществления клозапин находится в эффективном количестве в фармацевтической композиции. В некоторых вариантах осуществления эффективное количество является терапевтически эффективным количеством (например, количеством, эффективным для лечения и/или снижения риска нейропсихиатрического расстройства у пациента). В некоторых вариантах осуществления эффективное количество является профилактически эффективным количеством (например, количеством, эффективным для профилактики нейропсихиатрического расстройства у пациента).
В некоторых вариантах осуществления фармацевтическая композиция, раскрытая здесь, содержит от 50 до 1000 мг бензоата натрия (например, от 100 до 800 мг, от 200 до 600 мг или от 300 до 500 мг), 25-300 мг клозапина (например, от 50 до 200 мг, от 100 до 150 мг или от 150 до 300 мг), 50-500 мг альгината натрия (например, от 100 до 400 мг, от 200 до 300 мг или от 250 до 400 мг), 50-400 мг цитрата натрия (например, 100-300 мг, 150-250 мг или 200-300 мг), 5-100 мг стеарата магния (например, 10-80 мг, 25-70 мг, 40-60 мг или 50-100 мг) и 80-200 мг гликолята крахмала натрия (например, 100-150 мг). В некоторых вариантах осуществления фармацевтическая композиция, раскрытая здесь, содержит от 125 до 500 мг бензоата натрия, 25-300 мг клозапина, 50-500 мг альгината натрия, 50-400 мг цитрата натрия, 5-100 мг стеарата магния и 80-200 мг гликолята крахмала натрия.
В некоторых вариантах осуществления фармацевтическая композиция, раскрытая здесь, содержит от 50 до 1000 мг бензоата натрия, 25-300 мг клозапина, 50-200 мг альгината натрия, 50-400 мг цитрата натрия, 5-100 мг стеарата магния и 80-200 мг гликолята крахмала натрия. В некоторых вариантах осуществления фармацевтическая композиция, раскрытая здесь, содержит от 125 до 500 мг бензоата натрия, 25-300 мг клозапина, 50-200 мг альгината натрия, 50-400 мг цитрата натрия, 5-100 мг стеарата магния и 80-200 мг гликолята крахмала натрия.
В некоторых вариантах осуществления фармацевтическая композиция, раскрытая здесь, содержит от 50 до 1000 мг бензоата натрия, 25-300 мг клозапина, 50-70 мг альгината натрия, 50-70 мг цитрата натрия, 5-15 мг стеарата магния и 80-100 мг гликолята крахмала натрия. В некоторых вариантах осуществления фармацевтическая композиция, раскрытая здесь, содержит от 125 до 500 мг бензоата натрия, 25-300 мг клозапина, 50-70 мг альгината натрия, 50-70 мг цитрата натрия, 5-15 мг стеарата магния и 80-100 мг гликолята крахмала натрия.
В некоторых вариантах осуществления композиция дополнительно содержит нейрофармацевтическое средство. В некоторых вариантах осуществления нейрофармацевтическое средство выбрано из группы, состоящей из бутирофенона, фентиазина, флуфеназина, перфеназина, прохлорперазина, тиоридазина, трифлуоперазина, мезоридазина, промазина, трифлупромазина, левомепромазина, прометазина, тиоксантена, хлорпротиксена, флупентиксола, тиотиксена, зуклопентиксола, клозапина, оланзапина, рисперидона, кветиапина, зипрасидона, амисулприда, асенапина, палиперидона, арипипразола, карипразина, брекспипразола, ламотригина, тетрабеназина, каннабидиола, LY2140023, дроперидола, пимозида, бутаперазина, карфеназина, эмоксиприда, пиперацетазина, сулпирида, акампрозата, тетрабеназина, вилазодона, левомилнаципрана и вортиоксетина, флуоксетина, пароксетина, эсциталопрама, циталопрама, сертралина, флувоксамина, венлафаксина, милнаципрама, дулоксетина, миртазапина, миансерина, ребоксетина, бупропиона, амитриптилина, нортриптилина, протриптилина, десипрамина, тримипрамина, амоксапина, кломипрамина, десипрамина, доксепина, изокарбоксазида, транилципромина, тразодона, нефазодона, ламатрогина, лития, топирамата, габапентина, карбамазепина, оксакарбазепина, вальпроата, мапротилина, миртазапина, брофаромина, гепирона, моклобемида, изониазида, ипрониазида, фенелзина, селегилина, статина, амфетамина, модафинила, дезоксина, метамфетамина, кокаина, ареколина, дексметилфенидата, декстроамфетамина, метилфенидата, лисдексамфетамина димезилата, смешанных солей амфетамина, атомоксетина, клонидин гидрохлорида, гуанфацин гидрохлорида, ареколина, пемолина, донепезила, такрина, ривастигмина, мемантина, физостигмина, солей лития, никотина, ареколина, гуперзина альфа, рилузола, саркозина, витамина C, витамина Е, каротиноидов, дубильной кислоты и экстракта Гинкго. Композиции, описанные здесь, могут быть использованы в лечении и/или снижении риска нейропсихиатрического расстройства. В некоторых вариантах осуществления весовое отношение полиморфной формы бензоата натрия к нейрофармацевтическому средству составляет от приблизительно 1:10 до приблизительно 1000:1, от приблизительно 1:10 до приблизительно 900:1, от приблизительно 1:10 до приблизительно 800:1, от приблизительно 1:10 до приблизительно 600:1, от приблизительно 1:10 до приблизительно 500:1, от приблизительно 1:10 до приблизительно 400:1, от приблизительно 1:10 до приблизительно 200:1, от приблизительно 1:10 до приблизительно 100:1, от приблизительно 1:10 до приблизительно 75:1, от приблизительно 1:10 до приблизительно 50:1, от приблизительно 1:10 до приблизительно 25:1, от приблизительно 1:10 до приблизительно 10:1, от приблизительно 1:10 до приблизительно 5:1, от приблизительно 1:10 до приблизительно 1:2, от приблизительно 1:10 до приблизительно 1:5, или от приблизительно 1:10 до приблизительно 1:8.
В некоторых вариантах осуществления композиция является фармацевтической композицией. В некоторых вариантах осуществления композиция является нутрицевтической композицией. В некоторых вариантах осуществления композиция является продуктом диетического питания. В некоторых вариантах осуществления композиции, описанные здесь, могут быть продуктом диетического питания или диетическим пищевым продуктом, который может быть любыми видами жидких и твердых/полутвердых материалов, использующихся для питания человека и животных, для улучшения основного поведенческого функционирования, гиперактивности, настроения, тревоги, депрессии, восприятия, сенсорно-двигательной функции, болевого порога, памяти и/или познавательного функционирования, или для облегчения лечения любого из целевых заболеваний, отмеченных здесь (например, нейропсихиатрического расстройства, включая описанные здесь). Диетический пищевой продукт может быть продуктом питания (например, напитки на основе чая, сок, безалкогольные напитки, кофе, молоко, желе, печенье, хлебные злаки, конфеты, закуски, растительные экстракты, молочные продукты (например, мороженое и йогурт)), пищевой/диетической добавкой или нутрицевтическим составом.
Диетический пищевой продукт, описанный здесь, может включать один или более съедобных носителей, сообщающих одно или более преимуществ продукту, описанному здесь. Примеры съедобных носителей включают крахмал, циклодекстрин, мальтодекстрин, метилцеллюлозу, карбонметоксицеллюлозу, ксантановую камедь и их водные растворы. Другие примеры включают растворители, дисперсионные среды, покрытия, поверхностно-активные вещества, антиоксиданты, консерванты (например, антибактериальные агенты, противогрибковые агенты), изотонические агенты, агенты, задерживающие абсорбцию, стабилизаторы, гели, связующие, эксципиенты, разрыхлители, лубриканты, подсластители, ароматизаторы, красители, подобные материалы и их комбинации, известные специалисту. В некоторых примерах диетические пищевые продукты, описанные здесь, могут дополнительно включать нейропротекторные продукты, такие как рыбий жир, льняное масло и/или бензоат.
В некоторых примерах диетический пищевой продукт является нутрицевтической композицией, относящейся к композициям, содержащим компоненты источников пищи и придающим дополнительную пользу для здоровья в дополнение к основной пищевой ценности продуктов. Нутрицевтическая композиция, как описано здесь, содержит полиморфную форму, описанную здесь (например, соединение бензоата натрия и полиморфную форму, как описано здесь), и дополнительные ингредиенты и добавки, обеспечивающие хорошее здоровье и/или улучшающие стабильность и биоактивность полиморфных форм.
Действия нутрицевтических композиций могут быть быстрыми или/и кратковременными или они могут помочь достигнуть долгосрочных медицинских целей, как описано здесь, например, улучшая основное поведенческое функционирование, гиперактивность, настроение, тревогу, депрессию, восприятие, сенсорно-двигательные функции, болевой порог, память и/или познавательное функционирование у, например, человека, который имеет или подвергается риску развития нейропсихиатрического расстройства. Нутрицевтические композиции могут содержаться в съедобном материале, например, как пищевая добавка или фармацевтический состав. Как пищевая добавка, могут быть включены дополнительные питательные вещества, такие как витамины, минералы или аминокислоты. Композиция может также быть напитком или продуктом питания, например, чаем, безалкогольным напитком, соком, молоком, кофе, печеньем, хлопьями, шоколадом и снеком. При желании композиция может быть подслащена путем добавления подсластителя, такого как сорбит, мальтит, гидрогенизированный сироп глюкозы и гидрогенизированный гидролизат крахмала, высокофруктозную кукурузную патоку, тростниковый сахар, свекловичный сахар, пектин или сукралоза.
Нутрицевтическая композиция, раскрытая здесь, может быть в форме раствора. Например, нутрицевтический состав может быть в среде, такой как буфер, растворитель, разбавитель, инертный носитель, масло или крем. В некоторых примерах состав присутствует в водном растворе, в случае необходимости содержащем неводный совместный растворитель, такой как спирт. Нутрицевтическая композиция может также быть в форме порошка, пасты, желе, капсулы или таблетки. Лактоза и кукурузный крахмал обычно используются в качестве разбавителей для капсул и в качестве носителей для таблеток. Лубриканты, такие как стеарат магния, как правило добавляют для формирования таблеток.
Диетические пищевые продукты могут быть составлены для подходящего пути введения, например, перорального введения. Для перорального введения композиция может принимать форму, например, таблетки или капсулы, полученных стандартными средствами с приемлемыми эксципиентами, такими как связующие (например, предварительно желатинированный кукурузный крахмал, поливинилпирролидон или гидроксипропил метилцеллюлоза); наполнители (например, лактоза, микрокристаллическая целлюлоза или гидрофосфат кальция); лубриканты (например, стеарат магния, тальк или диоксид кремния); разрыхлители (например, картофельный крахмал или гликолят крахмала натрия); или смачивающие агенты (например, лаурилсульфат натрия). Таблетки могут быть покрыты способами, известными в данной области техники. Также в изобретение включены пластинки и другие жевательные составы.
В некоторых примерах диетический пищевой продукт может быть в жидкой форме, и один или более съедобных носителей могут быть растворителем или дисперсионной средой, включая, но не ограничиваясь ими, этанол, полиол (например, глицерин, пропиленгликоль, жидкий полиэтиленгликоль), липиды (например, триглицериды, растительные масла, липосомы) или их комбинации. Нужная текучесть может поддерживаться, например, при помощи покрытия, такого как лецитин; поддержанием требуемого размера частиц путем диспергирования в таких носителях как, например, жидкий полиол или липиды; при помощи таких поверхностно-активных веществ как, например, гидроксипропилцеллюлоза; или комбинацией этих способов. Во многих случаях будет желательно включать изотонический агент, такой как, например, сахара, хлорид натрия или их комбинации.
Жидкие препараты для перорального введения могут принимать форму, например, растворов, сиропов или суспензий, или они могут быть представлены как сухой продукт для восстановления с водой или другим подходящим носителем перед использованием. В одном варианте осуществления жидкие препараты могут быть составлены для введения с фруктовым соком. Такие жидкие препараты могут быть получены стандартными средствами с использованием фармацевтически приемлемых добавок, таких как суспендирующие агенты (например, сироп сорбита, производные целлюлозы или гидрогенизированные съедобные жиры); эмульгирующие агенты (например, лецитин или гуммиарабик); неводные носители (например, миндальное масло, масляные сложные эфиры, этиловый спирт или фракционированные растительные масла); и консерванты (например, метил или пропил-п-гидроксибензоаты, бензоат или сорбат).
В некоторых вариантах осуществления композиция является продуктом лечебного питания. Продуктом лечебного питания является продукт питания, составленный для потребления или энтерального введения. Такой продукт питания обычно используется под наблюдением врача для специфического диетического контроля целевого заболевания, такого как описанные здесь. В некоторых случаях такую композицию продукта лечебного питания специально составляют и обрабатывают (в противоположность натуральным пищевым продуктам, используемым в естественном состоянии) для пациента, нуждающегося в лечении (например, человека, страдающего заболеванием, или для которого требуется использование продукта как основного активного вещества для облегчения заболевания или состояния через специфический диетический контроль). В некоторых примерах композиция продукта лечебного питания, описанная здесь, не является одной из тех, которые просто были бы рекомендованы врачом как часть полной диеты для лечения симптомов или снижения риска заболевания или состояния.
Любая из композиций продукта лечебного питания, описанных здесь, включающая полиморфную форму бензоата натрия и по меньшей мере один носитель (например, описанные здесь), может быть в форме суспензии; порошка, пластинки, вафли, суспензии в подходящей жидкости или в подходящей эмульсии, как детализировано ниже. По меньшей мере один носитель, который может быть натуральным или синтетическим (неприродного происхождения), обеспечивает одно или более преимуществ бензоату натрия и сокомпоненту в композиции, например, стабильность, биодоступность и/или биоактивность. Любой из носителей, описанных здесь, может использоваться для получения композиции продукта лечебного питания. В некоторых вариантах осуществления композиция продукта лечебного питания может дополнительно включать один или более дополнительных ингредиентов, выбранных из группы, включая, но не ограничиваясь ими, натуральные ароматизаторы, искусственные ароматизаторы, макро- и микроэлементы, минералы, витамины, овес, орехи, специи, молоко, яйцо, соль, муку, лецитин, ксантановую камедь и/или подсластители. Композиция продукта лечебного питания может быть помещена в подходящий контейнер, который может дополнительно включать по меньшей мере дополнительный терапевтический агент, такой как описанные здесь.
В некоторых вариантах осуществления полиморф, описанный здесь, находится в эффективном количестве в фармацевтической композиции. В некоторых вариантах осуществления эффективное количество является терапевтически эффективным количеством (например, количеством, эффективным для лечения и/или снижения риска нейропсихиатрического расстройства у пациента). В некоторых вариантах осуществления нейропсихиатрическое расстройство является неврологическим расстройством, например, болезнью Альцгеймера. В некоторых вариантах осуществления эффективное количество является профилактически эффективным количеством (например, количеством, эффективным для профилактики нейропсихиатрического расстройства у пациента).
Фармацевтические композиции, описанные здесь, могут быть получены любым способом, известным в области фармакологии. В целом такие способы получения включают приведение полиморфной формы бензоата натрия, описанной здесь (т.е., «активный ингредиент»), в связь с носителем или эксципиентом и/или одним или более другими добавочными ингредиентами, и затем, если необходимо и/или желательно, формование и/или упаковка продукта в желаемой одно- или многодозовой форме.
Фармацевтические композиции могут быть получены, упакованы и/или проданы россыпью, в однодозной форме и/или как множество однодозных форм. «Разовая доза» является дискретным количеством фармацевтической композиции, включающим предопределенное количество активного ингредиента. Количество активного ингредиента обычно равно дозировке активного ингредиента, которую вводят пациенту, и/или удобной фракции такой дозировки, такой как половина или одна треть такой дозировки.
Относительные количества активного ингредиента, фармацевтически приемлемого эксципиента и/или любых дополнительных ингредиентов в фармацевтической композиции, описанной здесь, варьируют в зависимости от идентичности, размера и/или состояния пациента и далее в зависимости от пути, которым должна быть введена композиция. Композиция может включать от 0,1% до 100% (вес./вес.) активного ингредиента.
Фармацевтически приемлемые эксципиенты, используемые в получении фармацевтических композиций по изобретению, включают инертные разбавители, диспергирующие и/или гранулирующие агенты, поверхностно-активные вещества и/или эмульгаторы, разрыхлители, связующие, консерванты, буферные агенты, лубриканты и/или масла. Эксципиенты, такие как масло какао и воски для суппозиториев, окрашивающие агенты, покрывающие агенты, подсластители, вкусовые и ароматизирующие агенты могут также присутствовать в композиции.
Жидкие лекарственные формы для перорального введения и парентерального введения включают фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к активным ингредиентам жидкие лекарственные формы могут включать инертные разбавители, обычно используемые в данной области техники, такие как, например, вода или другие растворители, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (например, семени хлопчатника, арахисовое, кукурузное, зародышей пшеницы, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофуриловый спирт, полиэтиленгликоли и сложные эфиры жирной кислоты и сорбитана и их смеси. Помимо инертных разбавителей, пероральные композиции могут включать адъюванты, такие как смачивающие агенты, эмульгирующие и суспендирующие агенты, подсластители, вкусовые и ароматизирующие агенты. В некоторых вариантах осуществления для парентерального введения конъюгаты, описанные здесь, смешивают с солибилизирующими агентами, такими как Cremophor®, спиртами, маслами, модифицированными маслами, гликолями, полисорбатами, циклодекстринами, полимерами и их смесями.
Инъецируемые препараты, например, стерильные инъецируемые водные или масляные суспензии, могут быть составлены согласно известному уровню техники с использованием подходящих диспергирующих или смачивающих агентов и суспендирующих агентов. Стерильный инъецируемый препарат может быть стерильным инъецируемым раствором, суспензией или эмульсией в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в форме раствора в 1,3-бутандиоле. Среди приемлемых носителей и растворителей, которые могут использоваться, можно назвать воду, раствор Рингера, U.S.P. и изотонический раствор хлорида натрия. Кроме того, стерильные нелетучие масла традиционно используются как растворяющая или суспендирующая среда. С этой целью может использоваться любое мягкое нелетучее масло, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, используются в получении инъецируемых форм.
Инъецируемые составы могут стерилизоваться, например, фильтрацией через задерживающий бактерии фильтр, или путем включения стерилизующих агентов в форме стерильных твердых композиций, которые могут быть растворены или диспергированы в стерилизованной воде или другой стерильной инъецируемой среде до использования.
Для пролонгирования эффекта лекарственного средства часто желательно замедлить абсорбцию лекарственного средства из места подкожной или внутримышечной инъекции. Это может быть достигнуто при помощи жидкой суспензии кристаллического или аморфного материала с низкой водорастворимостью. Скорость абсорбции лекарственного средства тогда зависит от его скорости растворения, которое, в свою очередь, может зависеть от размера кристаллов и формы кристаллов. Также замедленная абсорбция парентерально вводимой формы лекарственного средства может быть достигнуты путем растворения или суспендирования лекарственного средства в масляном носителе.
Твердые дозированные формы для перорального введения включают капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых дозированных формах активный ингредиент смешивают с по меньшей мере одним инертным фармацевтически приемлемым эксципиентом или носителем, таким как цитрат натрия или дикальций фосфат и/или (a) наполнителями или экстендерами, такими как крахмалы, лактоза, сахароза, глюкоза, маннит и кремневая кислота, (b) связующими, такими как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидинон, сахароза и гуммиарабик, (c) увлажнителями, такими как глицерин, (d) разрыхлителями, такими как агар, карбонат кальция, картофель или крахмал тапиоки, альгиновая кислота, некоторые силикаты, гликолят крахмала натрия (SSG), кроскармеллоза, кросповидон и карбонат натрия, (e) ингибиторами растворимости, такими как парафин, (f) ускорителями абсорбции, такими как четвертичные аммониевые основания, (g) смачивающими агентами, такими как, например, цетиловый спирт и моностеарат глицерина, (h) абсорбентами, такими как каолин и бентонитовая глина, и (i) лубрикантами, такими как коллоидный диоксид кремния, тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия, и их смесями. В случае капсул, таблеток и пилюль, лекарственная форма может включать буферный агент, такой как цитрат натрия и хитозан. Кроме того, фармацевтически приемлемый эксципиент, описанный здесь, может быть единственной разновидностью или смесью многих разновидностей дубильной кислоты или ее фармацевтически приемлемой соли.
Твердые композиции подобного типа могут использоваться как наполнители в мягких и твердых желатиновых капсулах с использованием таких эксципиентов как лактоза или молочный сахар, а также высокомолекулярных полиэтиленгликолей и т.п. Твердые дозированные формы таблеток, драже, капсул, пилюль и гранул могут быть получены с покрытиями и оболочками, такими как энтеросолюбильные покрытия и другие покрытия, известные в области фармакологии. Они могут в случае необходимости включать замутняющие агенты и могут иметь такой состав, что они высвобождают активный ингредиент(ы) только, или избирательно, в определенной части пищеварительного тракта, в случае необходимости, пролонгированным образом. Примеры инкапсулирующих композиций, которые могут использоваться, включают полимерные вещества и воски. Твердые композиции подобного типа могут использоваться как наполнители в мягких и твердых желатиновых капсулах с использованием таких эксципиентов как лактоза или молочный сахар, а также высокомолекулярных полиэтиленгликолей и т.п.
Активный ингредиент может быть в микроинкапсулированной форме с одним или более эксципиентами, как отмечено выше. Твердые дозированные формы таблеток, драже, капсул, пилюль и гранул могут быть получены с покрытиями и оболочками, такими как энтеросолюбильные покрытия, покрытия, контролирующие высвобождение, и другие покрытия, известные в области получения фармацевтических составов. В таких твердых дозированных формах активный ингредиент может быть смешан по меньшей мере с одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Такие лекарственные формы могут включать, как нормальная практика, дополнительные вещества, отличные от инертных разбавителей, например, лубриканты для таблетирования и другие вспомогательные вещества для таблетирования, такие как стеарат магния и микрокристаллическая целлюлозу. В случае капсул, таблеток и пилюль, лекарственные формы могут включать буферные агенты. Они могут в случае необходимости включать замутняющие агенты и могут иметь такой состав, что они высвобождают активный ингредиент(ы) только, или избирательно, в определенной части пищеварительного тракта, в случае необходимости, пролонгированным образом. Примеры инкапсулирующих агентов, которые могут использоваться, включают, но не ограничены ими, полимерные вещества и воски.
Несмотря на то, что описания фармацевтических композиций по изобретению в основном относятся к фармацевтическим композициям, подходящим для введения человеку, такие композиции обычно подходят для введения животным всех видов. Модификация фармацевтических композиций, подходящих для введения человеку, для получения композиций, подходящих для введения различным животным, хорошо понятна, и обычно ветеринарный фармаколог может спроектировать и/или выполнить такую модификацию обычным экспериментированием.
Полиморфные формы по изобретению, как правило, составляют в стандартной лекарственной форме для простоты введения и однородности дозировки. Понятно, однако, что обычное ежедневное использование композиций, описанных здесь, определяется врачом в рамках здравого медицинского суждения. Специфический терапевтически эффективный уровень дозы для любого конкретного пациента или организма будет зависеть от множества факторов, включая подвергаемое лечению заболевание и серьезность нарушения; активность конкретного используемого активного ингредиента; конкретную используемую композицию; возраст, массу тела, общее состояние здоровья, пол и диету пациента; время введения, путь введения и скорость экскреции конкретного используемого активного ингредиента; продолжительность лечения; лекарственные средства, используемые в комбинации или совпадающие с конкретным используемым активным ингредиентом; и подобные факторы, известные в области медицины.
Также охвачены раскрытием наборы (например, фармацевтические упаковки). Наборы по изобретению могут включать фармацевтическую композицию или полиморфную форму бензоата натрия, описанную здесь, и контейнер (например, пузырек, ампулу, бутылку, шприц и/или диспенсер или другой подходящий контейнер). В некоторых вариантах осуществления, наборы по изобретению могут в случае необходимости дополнительно включать второй контейнер, включающий фармацевтический эксципиент для разбавления или суспендирования фармацевтической композиции или полиморфной формы бензоата натрия, описанной здесь. В некоторых вариантах осуществления фармацевтическую композицию или полиморфную форму бензоата натрия, описанную здесь, находящуюся в первом контейнере и втором контейнере, объединяют для формирования одной стандартной лекарственной формы.
В некоторых вариантах осуществления набор, описанный здесь, включает первый контейнер, включающий полиморфную форму или композицию, описанную здесь. В некоторых вариантах осуществления набор, описанный здесь, может быть использован в лечении и/или снижении риска нейропсихиатрического расстройства у пациента.
В некоторых вариантах осуществления набор, описанный здесь, дополнительно включает инструкции по использованию полиморфной формы или композиции, включенной в набор. Набор, описанный здесь, может также включать информацию, которая требуется контролирующим органом, таким как Управление по контролю за продуктами и лекарствами США (FDA). В некоторых вариантах осуществления информация, включенная в наборы, представляет собой предписывающую информацию. В некоторых вариантах осуществления наборы и инструкции предусматривают лечение и/или снижение риска нейропсихиатрического расстройства у пациента. Набор, описанный здесь, может включать один или более дополнительных фармацевтических агентов, описанных здесь, в форме отдельной композиции.
Способ синтеза
Здесь описано много примеров способов получения полиморфных форм бензоата натрия, описанных здесь:
Общий Способ 1: Кристаллизация путем Упаривания в Насыщенном растворе.
Кристаллизацию проводили упариванием в насыщенном растворе. Избыточное количество бензоата натрия растворяли в растворителе. Раствор фильтровали, и фильтрат упаривали досуха с получением новой полиморфной формы бензоата натрия.
В одном аспекте синтез полиморфной формы бензоата натрия включает первую стадию растворения избыточного количества бензоата натрия в единственном или подходящем смешанном растворителе для формирования насыщенного раствора при давлении и температуре окружающей среды. Насыщенный раствор может затем быть отфильтрован с помощью фильтра, имеющего размер поры в пределах от 5 до 100 мкм для удаления нерастворимых компонентов. Раствор, таким образом полученный, может быть испарен в течение подходящего промежутка времени в подходящих условиях, обеспечивающих формирование полиморфной формы бензоата натрия (например, полиморфной формы #1, как описано в Примере 1 ниже). В некоторых вариантах осуществления раствор упаривают при давлении окружающей среды или пониженном давлении и/или при повышенной температуре, например, приблизительно 40-110°C. В некоторых вариантах осуществления повышенная температура может составлять приблизительно 40-90°C, приблизительно 40-80°C, приблизительно 40-70°C или приблизительно 40-60°C. Полиморфная форма бензоата натрия, сформированная из упаренного раствора, может затем быть собрана.
Подходящие растворители для использования в способах синтеза, описанных здесь, включают, но не ограничены ими, полярные протонные растворители (например, метанол, этанол, изопропанол, вода), полярные апротонные растворители (например, ацетонитрил, этилацетат) или их смесь. В некоторых вариантах осуществления растворитель является метанолом, этанолом, изопропанолом, ацетонитрилом, этилацетатом, водой или их смесями.
Общий Способ 2: Кристаллизация путем Охлаждения в Насыщенном Растворе.
К бензоату натрия добавляли простой или смешанный растворитель при повышенной температуре (50-110°C) при перемешивании. Добавление растворителя немедленно останавливали, когда раствор стал прозрачным. Раствору давали остыть при перемешивании. Суспензию фильтровали, и кристаллы собирали для получения новой полиморфной формы бензоата натрия.
Например, синтез полиморфной формы бензоата натрия включает первую стадию растворения бензоата натрия в единственном или подходящем смешанном растворителе при температуре в пределах приблизительно 50-110°C для формирования раствора. Подходящие растворители для использования в способах синтеза, описанных здесь, включают, но не ограничены ими, полярные протонные растворители (например, метанол, этанол, изопропанол, вода), полярные апротонные растворители (например, ацетонитрил, этилацетат) или их смесь. В некоторых вариантах осуществления растворитель является метанолом, этанолом, изопропанолом, ацетонитрилом, этилацетатом, водой или их смесями. В некоторых вариантах осуществления синтез полиморфной формы бензоата натрия включает первую стадию растворения бензоата натрия в простом или смешанном растворителе при температуре 50-110°C, 50-100°C, 50-90°C, 50-80°C, 50-70°C или 60-70°C для формирования раствора. В некоторых вариантах осуществления синтез полиморфной формы бензоата натрия включает первую стадию растворения бензоата натрия в простом или смешанном растворителе при температуре 50°C, 60°C, 70°C, 80°C, 90°C, 100°C или 110°C для формирования раствора.
В некоторых вариантах осуществления горячий раствор растворенного бензоата натрия затем охлаждали до температуры среды (например, приблизительно 20-25°C) при перемешивании. В некоторых вариантах осуществления охлажденный раствор затем оставляли при температуре среды для обеспечения формирования полиморфной формы бензоата натрия. В некоторых вариантах осуществления собирали полиморфную форму бензоата натрия, сформированную размещением при температуре среды на третьей стадии. В некоторых вариантах осуществления полиморфную форму бензоата натрия, сформированную размещением при температуре среды, собирали фильтрацией с помощью фильтра, имеющего размер поры в пределах от 5 до 100 мкм.
Общий способ 3: превращение в условиях высокой влажности
Бензоат натрия сохраняли в условиях с более чем 90% RH (относительная влажность) для получения новой полиморфной формы бензоата натрия.
Например, синтез полиморфной формы бензоата натрия включает первую стадию размещения бензоата натрия при относительной влажности (RH), более чем приблизительно 90% в течение приблизительно от 1 до 10 дней, в течение которых формируется полиморфная форма бензоата натрия. В некоторых вариантах осуществления первая стадия включает помещение бензоата натрия в RH приблизительно 90%, приблизительно 91%, приблизительно 92%, приблизительно 93%, приблизительно 94%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% или приблизительно 100%. В некоторых вариантах осуществления первая стадия включает помещение бензоата натрия в относительную влажность (RH) более чем приблизительно 90% в течение приблизительно от 1 до 10 дней, приблизительно от 1 до 9 дней, приблизительно от 1 до 8 дней, приблизительно от 1 до 7 дней, приблизительно от 1 до 6 дней, приблизительно от 1 до 5 дней, приблизительно от 1 до 4 дней, приблизительно от 1 до 3 дней или приблизительно от 1 до 2 дней. Полиморфная форма бензоата натрия, сформированная на первой стадии, может затем быть собрана.
Общий способ 4: превращение в шламовом растворе
Шламовый раствор бензоата натрия в растворителе смешивали в течение определенного периода времени для получения новой полиморфной формы бензоата натрия.
Например, синтез полиморфной формы бензоата натрия включает первую стадию получения суспензии первой полиморфной формы бензоата натрия в простом или смешанном растворителе. Подходящие растворители для использования в способах синтеза, описанных здесь, включают, но не ограничены ими, полярные протонные растворители (например, метанол, этанол, изопропанол, бутанол, изобутанол, метил-1-бутанол или вода), полярные апротонные растворители (например, ацетонитрил, этилацетат, диоксан, метилэтилкетон, метил-трет-бутиловый эфир, толуол или тетрагидрофуран) или их смесь. В некоторых вариантах осуществления растворитель является метанолом, этанолом, изопропанолом, бутанолом, ацетонитрилом, этилацетатом, метилэтилкетоном, тетрагидрофураном, водой или их смесями. В некоторых вариантах осуществления синтез полиморфной формы бензоата натрия включает вторую стадию перемешивания суспензии в течение от 6 часов до 10 дней, от 6 часов до 9 дней, от 6 часов до 8 дней, от 6 часов до 7 дней, от 6 часов до 6 дней, от 6 часов до 5 дней, от 6 часов до 4 дней, от 6 часов до 3 дней, от 6 часов до 2 дней, от 6 часов до 1 дня, от 6 часов до 20 часов, от 6 часов до 15 часов, от 6 часов до 10 часов или от 6 часов до 8 часов, в течение которых формируется полиморфная форма бензоата натрия. В некоторых вариантах осуществления, на второй стадии суспензию перемешивают в течение 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 12 часов, 14 часов, 15 часов, 18 часов, 20 часов, 22 часов, 1 дня, 2 дней, 3 дней, 4 дней, 5 дней, 6 дней, 7 дней, 8 дней или 9 дней. В некоторых вариантах осуществления синтез полиморфной формы бензоата натрия включает третью стадию сбора полиморфной формы бензоата натрия, сформированной на второй стадии. Полиморфная форма бензоата натрия может быть собрана фильтрацией с помощью фильтра, имеющего размер поры в пределах от 5 до 100 мкм.
Общий Способ 5: Кристаллизация посредством Осаждения Антирастворителем
Бензоат натрия полностью растворяли в растворителе с последующим постепенным добавлением антирастворителя. Суспензию перемешивали в течение определенного периода времени, и кристаллы собирали для получения новой полиморфной формы бензоата натрия.
Например, синтез полиморфной формы бензоата натрия включает первую стадию растворения бензоата натрия в простом или смешанном растворителе для формирования раствора. Подходящие растворители для использования в способах синтеза, описанных здесь, включают, но не ограничены ими, полярные протонные растворители (например, метанол, этанол, изопропанол, вода), полярные апротонные растворители (например, ацетонитрил, этилацетат) или их смесь. В некоторых вариантах осуществления растворитель является метанолом, этанолом, изопропанолом, ацетонитрилом, этилацетатом, водой или их смесями. Раствор растворенного бензоата натрия может затем быть смешан с антирастворителем для формирования суспензии, в которой объемное соотношение между антирастворителем и раствором на первой стадии составляет приблизительно от 4:1 до 15:1. Подходящие растворители для использования в способах синтеза, описанных здесь, включают, но не ограничены ими, полярные протонные растворители (например, метанол, этанол, изопропанол, бутанол, вода), полярные апротонные растворители (например, ацетонитрил, ацетон, этилацетат, тетрагидрофуран, метилэтилкетон), неполярные растворители (толуол, тетрагидрофуран, метил-трет-бутиловый эфир) или их смесь. В некоторых вариантах осуществления антирастворитель является ацетоном, ацетонитрилом, бутанолом, диметилформамидом, диметилсульфоксидом, диоксаном, этилацетатом, изобутанолом, изопропанолом, метилэтилкетоном, метил-1-бутанолом, метил-трет-бутиловым эфиром, тетрагидрофураном, толуолом или их смесями. В некоторых вариантах осуществления на второй стадии смешивания раствора растворенного бензоата натрия с антирастворителем для формирования суспензии, объемное соотношение между антирастворителем и раствором на первой стадии составляет приблизительно от 4:1 до 15:1, приблизительно от 4:1 до 13:1, приблизительно от 4:1 до 11:1, приблизительно от 4:1 до 9:1, приблизительно от 4:1 до 7:1 или приблизительно от 4:1 до 5:1. В некоторых вариантах осуществления на второй стадии, объемное соотношение между антирастворителем и раствором на первой стадии составляет приблизительно 4:1, приблизительно 5:1, приблизительно 6:1, приблизительно 7:1, приблизительно 8:1, приблизительно 9:1 или приблизительно 10:1.
В некоторых вариантах осуществления суспензия может быть затем перемешана при давлении и температуре окружающей среды в течение приблизительно 2-10 дней, в течение которых формируется полиморфная форма бензоата натрия. В некоторых вариантах осуществления суспензию перемешивают при давлении и температуре окружающей среды в течение приблизительно 2-8 дней, приблизительно 2-7 дней, приблизительно 2-6 дней, приблизительно 2-5 дней, приблизительно 2-4 дней или приблизительно 2-3 дней. В некоторых вариантах осуществления суспензию перемешивают при давлении и температуре окружающей среды в течение приблизительно 2 дней, приблизительно 3 дней, приблизительно 4 дней, приблизительно 5 дней, приблизительно 6 дней, приблизительно 7 дней, приблизительно 8 дней, приблизительно 9 дней или приблизительно 10 дней. Полиморфную форму бензоата натрия, сформированную на третьей стадии путем перемешивания суспензии раствора бензоата натрия, затем собирают. В некоторых вариантах осуществления полиморфную форму бензоата натрия собирают фильтрацией с помощью фильтра, имеющего размер поры в пределах от 5 до 100 мкм.
Также синтез полиморфной формы бензоата натрия включает первую стадию получения суспензии полиморфной формы бензоата натрия в простом или смешанном растворителе в присутствии приблизительно 2-10 об.% воды. Подходящие растворители для использования в способах синтеза, описанных здесь, включают, но не ограничены ими, полярные протонные растворители (например, метанол, этанол, изопропанол или бутанол), полярные апротонные растворители (например, ацетонитрил, этилацетат, диоксан, метилэтилкетон, метил-трет-бутиловый эфир, толуол или тетрагидрофуран) или их смесь. В некоторых вариантах осуществления растворитель является метанолом, этанолом, изопропанолом, ацетонитрилом, этилацетатом или их смесями. В некоторых вариантах осуществления первая стадия включает получение суспензии полиморфной формы бензоата натрия в присутствии менее чем приблизительно 10%, менее чем приблизительно 9%, менее чем приблизительно 8%, менее чем приблизительно 7%, менее чем приблизительно 6%, менее чем приблизительно 5%, менее чем приблизительно 4%, менее чем приблизительно 3% или менее чем приблизительно 2% воды по объему. В некоторых вариантах осуществления синтез полиморфной формы бензоата натрия включает вторую стадию перемешивания суспензии при давлении и температуре окружающей среды в течение приблизительно 2-10 дней, в течение которых формируется полиморфная форма бензоата натрия. В некоторых вариантах осуществления вторая стадия включает перемешивание суспензии при давлении и температуре окружающей среды в течение приблизительно 2-10 дней, приблизительно 2-8 дней, приблизительно 2-7 дней, приблизительно 2-6 дней, приблизительно 2-5 дней, приблизительно 2-4 дней или приблизительно 2-3 дней. В некоторых вариантах осуществления вторая стадия включает перемешивание суспензии при давлении и температуре окружающей среды в течение приблизительно 2 дней, приблизительно 3 дней, приблизительно 4 дней, приблизительно 5 дней, приблизительно 6 дней, приблизительно 7 дней, приблизительно 8 дней, приблизительно 9 дней или приблизительно 10 дней. В некоторых вариантах осуществления синтез полиморфной формы бензоата натрия включает третью стадию сбора полиморфной формы бензоата натрия, сформированной путем перемешивания суспензии бензоата натрия. В некоторых вариантах осуществления полиморфную форму бензоата натрия собирают фильтрацией с помощью фильтра, имеющего размер поры в пределах от 5 до 100 мкм.
Примеры способов получения полиморфных форм бензоата натрия, описанных здесь, приведены в Примерах ниже.
Способы лечения
Настоящее раскрытие относится к способам лечения и/или снижения риска нейропсихиатрического расстройства у пациента, включающим введение пациенту эффективного количества (например, терапевтически эффективного количества) полиморфа или любой из композиций, описанных здесь (например, включающих полиморф бензоата натрия или комбинацию бензоата натрия и клозапина).
Другой аспект настоящего раскрытия относится к способам профилактики нейропсихиатрического расстройства у пациента, включающим введение пациенту эффективного количества (например, профилактически эффективного количества) полиморфа или его композиции, описанных здесь.
Полиморфные формы и композиции, описанные здесь, могут быть использованы в лечении и/или профилактике нейропсихиатрических расстройств. В некоторых вариантах осуществления нейропсихиатрическое расстройство является шизофренией. В некоторых вариантах осуществления нейропсихиатрическое расстройство является психотическим расстройством. В некоторых вариантах осуществления нейропсихиатрическое расстройство является болезнью Альцгеймера. В некоторых вариантах осуществления нейропсихиатрическое расстройство является деменцией, включая лобно-височную деменцию. В некоторых вариантах осуществления нейропсихиатрическое расстройство является легким когнитивным нарушением. В некоторых вариантах осуществления нейропсихиатрическое расстройство является легкой забывчивостью. В некоторых вариантах осуществления нейропсихиатрическое расстройство является закрытой черепно-мозговой травмой. В некоторых вариантах осуществления нейропсихиатрическое расстройство является расстройством аутического спектра, включая расстройство Аспергера. В некоторых вариантах осуществления нейропсихиатрическое расстройство является расстройством дефицита внимания и гиперактивности. В некоторых вариантах осуществления нейропсихиатрическое расстройство является обсессивно-компульсивным расстройством. В некоторых вариантах осуществления нейропсихиатрическое расстройство является тиковым расстройством. В некоторых вариантах осуществления нейропсихиатрическое расстройство является нарушением способности к обучению в детском возрасте. В некоторых вариантах осуществления нейропсихиатрическое расстройство является предменструальным синдромом. В некоторых вариантах осуществления нейропсихиатрическое расстройство является депрессией, включая дистимию и психический симптомокомплекс, вызванный потерей близкого человека. В некоторых вариантах осуществления нейропсихиатрическое расстройство является биполярным расстройством, включая биполярные расстройства I и II. В некоторых вариантах осуществления нейропсихиатрическое расстройство является тревожным расстройством, включая панические и фобические расстройства. В некоторых вариантах осуществления нейропсихиатрическое расстройство является посттравматическим стрессовым расстройством. В некоторых вариантах осуществления нейропсихиатрическое расстройство является хронической болью. В некоторых вариантах осуществления нейропсихиатрическое расстройство является расстройством пищевого поведения, включая булимию и анорексию. В некоторых вариантах осуществления нейропсихиатрическое расстройство является аддиктивным растсройством, включая зависимость или злоупотребление веществами. В некоторых вариантах осуществления нейропсихиатрическое расстройство является расстройством личности. В некоторых вариантах осуществления нейропсихиатрическое расстройство является болезнью Паркинсона. В некоторых вариантах осуществления нейропсихиатрическое расстройство является болезнью Гентингтона. В некоторых вариантах осуществления нейропсихиатрическое расстройство является рассеянным склерозом. В некоторых вариантах осуществления нейропсихиатрическое расстройство является боковым амиотрофическим склерозом.
В некоторых вариантах осуществления способ, описанный здесь, дополнительно включает введение пациенту дополнительного фармацевтического агента. В некоторых вариантах осуществления способ, описанный здесь, дополнительно включает контакт биологического образца с дополнительным фармацевтическим агентом. В некоторых вариантах осуществления способ, описанный здесь, дополнительно включает контакт ткани с дополнительным фармацевтическим агентом. В некоторых вариантах осуществления способ, описанный здесь, дополнительно включает контакт клетки с дополнительным фармацевтическим агентом.
Полиморфные формы и композиции по изобретению могут быть введены любым путем, включая энтеральный (например, пероральный), парентеральный, внутривенный, внутримышечный, внутриартериальный, интрамедуллярный, внутриоболочковый, подкожный, внутрижелудочковый, чрескожный, межкожный, подкожный, кожный, ректальный, интравагинальный, внутрибрюшинный, топический (в форме порошков, мазей, кремов и/или капель). Специфически рассматриваемыми путями являются пероральное введение, внутривенное введение (например, системная внутривенная инъекция), регионарное введение черезкровь и/или лимфу и/или прямое введение в пораженное место. В целом, самый подходящий путь введения будет зависеть от множества факторов, включая природу агента (например, его стабильность в среде желудочно-кишечного тракта) и/или состояние пациента (например, в состоянии ли пациент переносить пероральное введение).
Точное количество полиморфной формы, необходимое для достижения эффективного количества, варьирует от пациента к пациенту в зависимости, например, от вида, возраста и общего состояния пациента, серьезности побочных эффектов или нарушения, идентичности конкретного полиморфа, способа введения и т.п. Эффективное количество может быть включено в разовую дозу (например, пероральная разовая доза) или многократные дозы (например, пероральные многократные дозы). В некоторых вариантах осуществления, когда многократные дозы вводят пациенту или обрабатывают биологический образец, ткань или клетку, любые две дозы многократных доз включают отличающиеся или по существу одни и те же количества полиморфной формы бензоата натрия, описанной здесь. В некоторых вариантах осуществления, когда многократные дозы вводят пациенту или обрабатывают биологический образец, ткань или клетку, частота введения многократных доз пациенту или нанесение многократных доз на ткань или клетку составляет три дозы в сутки, две дозы в сутки, одну дозу в сутки, одну дозу через день, одну доза каждый третий день, одну дозу каждую неделю, одну дозу раз в две недели, одну дозу раз в месяц или одну дозу через месяц. В некоторых вариантах осуществления частота введения многократных доз пациенту или нанесения многократных доз на ткань или клетку составляет одну дозу в сутки. В некоторых вариантах осуществления частота введения многократных доз пациенту или нанесение многократных доз на ткань или клетку составляет две дозы в сутки. В некоторых вариантах осуществления, когда многократные дозы вводят пациенту или обрабатывают биологический образец, ткань или клетку, продолжительность между первой дозой и последней дозой многократных доз составляет один день, два дня, четыре дня, одну неделю, две недели, три недели, один месяц, два месяца, три месяц, четыре месяца, шесть месяцев, девять месяцев, один год, два года, три года, четыре года, пять лет, семь лет, десять лет, пятнадцать лет, двадцать лет или целую жизнь пациента, биологического образца, ткани или клетки. В некоторых вариантах осуществления, продолжительность между первой дозой и последней дозой многократных доз составляет три месяца, шесть месяцев или один год. В некоторых вариантах осуществления, продолжительность между первой дозой и последней дозой многократных доз составляет целую жизнь пациента, биологического образца, ткани или клетки. В некоторых вариантах осуществления, доза (например, разовая доза или любая доза многократных доз), описанная здесь, включает независимо от 1 мг до 3 мг, от 3 мг до 10 мг, от 10 мг до 30 мг, от 30 мг до 100 мг, от 100 мг до 300 мг, от 300 мг до 1000 мг или от 1 г до 10 г, включительно, полиморфной формы бензоата натрия, описанной здесь. В некоторых вариантах осуществления доза, описанная здесь, включает независимо от 3 мг до 10 мг, включительно, полиморфной формы бензоата натрия, описанной здесь. В некоторых вариантах осуществления доза, описанная здесь, включает независимо от 10 мг до 30 мг, включительно, полиморфной формы бензоата натрия, описанной здесь. В некоторых вариантах осуществления доза, описанная здесь, включает независимо от 30 мг до 100 мг, включительно, полиморфной формы бензоата натрия, описанной здесь. В некоторых вариантах осуществления доза, описанная здесь, включает независимо от 100 мг до 300 мг, включительно, полиморфной формы, как описано здесь. В некоторых вариантах осуществления доза, описанная здесь, включает независимо от 300 мг до 1000 мг, включительно, полиморфной формы бензоата натрия, описанной здесь.
Диапазоны доз, как описано здесь, относятся к руководству по введению фармацевтических композиций по изобретению взрослому. Количество, которое вводят, например, ребенку или подростку, может быть определено врачом или специалистом в данной области техники и может быть ниже или равным тому, которое вводят взрослому.
Полиморфная форма или композиция, как описано здесь, могут быть введены в комбинации с одним или более дополнительными фармацевтическими агентами (например, терапевтически и/или профилактически активными агентами), пригодными для использования в лечении и/или снижении риска нейропсихиатрического расстройства. Полиморфные формы или композиции могут быть введены в комбинации с дополнительными фармацевтическими агентами, улучшающими их активность (например, активность (например, потенциал и/или эффективность) в лечении и/или снижении риска нейропсихиатрического расстройства у пациента), улучшающими биодоступность, повышающими уровень безопасности, снижающими лекарственную резистентность, уменьшающими и/или изменяющими метаболизм, ингибирующими экскрецию и/или изменяющими распределение у пациента, в биологическом образце, ткани или клетке. Следует также понимать, что используемое терапевтическое средство может достигать желаемого эффекта для того же нарушения, и/или оно может достигать других эффектов. В некоторых вариантах осуществления фармацевтическая композиция, описанная здесь, включающая полиморфную форму бензоата натрия, описанную здесь, и дополнительный фармацевтический агент, показывает синергический эффект, отсутствующий в фармацевтической композиции, включающей что-то одно из числа полиморфа и дополнительного фармацевтического агента, но не оба сразу.
Полиморф или композиция могут быть введены одновременно с, до или после одного или более дополнительных фармацевтических агентов, которые могут быть использованы как, например, комбинированная терапия в лечении и/или снижении риска нейропсихиатрического расстройства у пациента. Фармацевтические агенты включают терапевтически активные агенты. Фармацевтические агенты также включают профилактически активные агенты. Фармацевтические агенты включают малые органические молекулы, такие как соединения лекарственного средства или их полиморфные формы (например, соединения, апробированные для медицинского или ветеринарного использования Управлением по контролю за продуктами и лекарственными средствами США, как предусмотрено в Своде федеральных нормативных актов (CFR)), пептиды, белки, углеводы, моносахариды, олигосахариды, полисахариды, нуклеопротеиды, мукопротеины, липопротеины, синтетические полипептиды или белки, антитела, малые молекулы, связанные с белками, такие как антитела, гликопротеиды, стероиды, нуклеиновые кислоты, ДНК, РНК, нуклеотиды, нуклеозиды, олигонуклеотиды, антисмысловые олигонуклеотиды, липиды, гормоны, витамины и клетки. В некоторых вариантах осуществления дополнительный фармацевтический агент является фармацевтическим агентом, пригодным для использования в лечении и/или снижении риска нейропсихиатрического расстройства у пациента. В некоторых вариантах осуществления дополнительный фармацевтический агент является фармацевтическим агентом, апробированным контролирующим органом (например, US FDA, EMA, China FDA) для лечения и/или снижения риска нейропсихиатрического расстройства у пациента. В некоторых вариантах осуществления дополнительный фармацевтический агент является нейрофармацевтическим средством, выбранным из группы, состоящей из карипразина, брекспипразола, илоперидона, пимавансерина, лурадисона, бутирофенона, фенотиазина, флуфеназина, перфеназина, прохлорперазина, тиоридазина, трифлуоперазина, мезоридазина, промазина, трифлюпромазина, левомепромазина, прометазина, тиоксантена, хлорпротиксена, флупентиксола, тиотиксена, зуклопентиксола, клозапина, оланзапина, рисперидона, кветиапина, зипразидона, амисульприда, азенапина, палиперидона, арипипразола, ламотригина, тетрабеназина, каннабидиола, LY2140023, дроперидола, пимозида, бутаперазина, карфеназина, эмоксиприда, пиперацетазина, сульпирида, акампросата, тетрабеназина, вилазодона, левомилнаципрана, вортиоксетина флуоксетина, пароксетина, эсциталопрама, циталопрама, сертралина, флувоксамина, венлафаксина, милнаципрама, дулоксетина, миртазапина, миансерина, ребоксетина, бупропиона, амитриптилина, нортриптилина, протриптилина, десипрамина, тримипрамина, амоксапина, кломипрамина, десипрамина, доксепина, изокарбоксазида, транилципромина, селегилина, тразодона, нефазодона, фенелзина, ламатрогина, лития, топирамата, габапентина, карбамазепина, оксакарбазепина, вальпроата, мапротилина, миртазапина, брофаромина, гепирона, моклобемида, изониазида, ипрониазида, статина, амфетамина, модафинила, дезоксина, метамфетамина, кокаина, ареколина, дексметилфенидата, декстроамфетамина, метилфенидата, лисдексамфетамин димезилата, смешанных солей амфетамина, атомоксетина, клонидин гидрохлорида, гуанфацин гидрохлорида, ареколина, пемолина, донепезила, такрин, ривастигмин, мемантина, физостигмина, солей лития, никотина, ареколина, гуперзина альфа, рилузола, витамина С, витамина Е, каротиноидов, дубильной кислоты и экстракта Ginkgo Biloba.
Каждый дополнительный фармацевтический агент может быть введен в дозе и/или по схеме, определенным для этого фармацевтического агента. Дополнительные фармацевтические агенты могут также быть введены вместе друг с другом и/или с полиморфом или композицией, описанной здесь, в единственной дозе, или введены отдельно в различных дозах. Особую комбинацию для использования в режиме составляют, принимая во внимание совместимость полиморфа, описанного здесь, с дополнительным фармацевтическим агентом(ами) и/или желаемым терапевтическим и/или профилактическим эффектом, который будет достигнут. В целом ожидается, что дополнительный фармацевтический агент(ы) в комбинации используется на уровнях, не превышающих уровни, на которых они используются индивидуально. В некоторых вариантах осуществления уровни, используемые в комбинации, будут ниже, чем используемые индивидуально.
В некоторых вариантах осуществления дополнительный фармацевтический агент является агентом для лечения и/или снижения риска нейропсихиатрического расстройства. В некоторых вариантах осуществления полиморфные формы бензоата натрия, описанные здесь, или фармацевтические композиции могут быть введены в комбинации с терапевтическим средством для лечения и/или снижения риска нейропсихиатрического расстройства.
Без дальнейших уточнений считается, что специалист в данной области техники, на основе вышеупомянутого описания, может использовать настоящее изобретение в его полном объеме. Следующие частные варианты осуществления должны, поэтому, быть истолкованы как просто иллюстративные и никоим образом не ограничивающие раскрытие. Все публикации, процитированные здесь, включены посредством ссылок в целях или для объектов, упомянутых здесь.
Примеры
Чтобы настоящее раскрытие могло быть понято более полно, сформулированы следующие примеры. Синтетические и биологические примеры, описанные в этой заявке, предлагаются для иллюстрации полиморфных форм, соединений, композиций и способов по изобретению и не должны быть ни в коем случае истолкованы как ограничение их объема.
Пример 1: Получение полиморфной формы #1 бензоата натрия
199,93 мг бензоата натрия помещали в колбу, и 4 мл метанола добавляли для растворения бензоата натрия. Если не указано иное, коммерчески доступный бензоат натрия был приобретен e Merck, Formosa Laboratories Inc. или Sigma-Aldrich, и растворители были куплены у таких поставщиков как Acros, Merck и Sigma-Aldrich. Таким образом полученный раствор сохраняли при перемешивании в течение 10 минут и затем фильтровали для удаления любых нерастворимых ингредиентов. Фильтрат упаривали ротационным упариванием для формирования твердого бензоата натрия в полиморфной форме. Полученное твердое вещество анализировали XRPD, TGA и DSC, как описано ниже.
- Термогравиметрический анализ (TGA).
Потерю общей массы получали на TA Instrument TGA Model Q500. Образец нагревали в открытой алюминиевой кастрюле при скорости нагревания 10°C/мин. до конечной температуры.
- Дифференциальная сканирующая калориметрия.
Термический анализ осуществляли с помощью TA Instrument DSC Model Q200. Образец нагревали в алюминиевой кастрюле при скорости нагревания 10°C/мин. с очисткой азотом при 50 мл/мин. до конечной температуры.
- Рентгеновская порошковая дифрактометрия.
Твердые образцы определяли рентгеновским порошковым дифрактометром (Bruker D8 advance), оборудованным датчиком LynxEye. Параметры инструмента приведены ниже. Сканирование: от 3° (2θ) до 40° (2θ); Приращение: 0,02° (2θ); Скорость сканирования: 0,1~0,3 сек./шаг; Напряжение: 40 кВ; Ток: 40 мА; Вращение: Вкл.; Удержание образца: нулевой фоновый типовой держатель.
Результаты, полученные в тестах TGA, DSC и Рентгеновской порошковой дифрактометрии, приведены на Фигурах 1-3.
Пример 2: Получение полиморфной формы #2
2,005 мг коммерчески доступного бензоата натрия помещали в круглодонную колбу с последующим добавлением 150 мл ацетонитрила. Таким образом полученную суспензию сохраняли при перемешивании в течение 2 дней и фильтровали для сбора таким образом сформированного твердого бензоата натрия. Твердый бензоат натрия в полиморфной форме также анализировали XRPD, TGA и DSC, и результаты показаны на Фигурах 4-6.
Пример 3: Получение полиморфной формы #3
2,006 г коммерчески доступного бензоата натрия помещали в круглодонную колбу и добавляли 150 мл изобутанол. Таким образом полученную суспензию сохраняли при перемешивании в течение 6 дней и затем фильтровали. Таким образом сформированный твердый бензоат натрия собирали и анализировали XRPD, TGA и DSC. Результаты показаны на Фигурах 7-9.
Пример 4: Получение полиморфной формы #4
2,182 г коммерчески доступного бензоата натрия помещали в круглодонную колбу с последующим добавлением 4 мл воды. Затем постепенно добавляли 20 мл изопропилового спирта, и полученную суспензи сохраняли при перемешивании в течение 3 дней и фильтровали для сбора таким образом сформированного твердого вещества. Собранное твердое вещество анализировали XRPD, TGA и DSC. Результаты показаны на Фигурах 10-12.
Пример 5: Получение полиморфной формы #5
106,6 мг коммерчески доступного бензоата натрия помещали в круглодонную колбу и 70 мл смешанного растворителя, содержащего этанол и этилацетат (1:1), добавляли при 70°C. Конечный раствор сохраняли при перемешивании в течение 10 минут, затем охлаждали до температуры среды и перемешивали в течение ночи для обеспечения формирования твердого бензоата натрия в полиморфной форме, которую собирали фильтрацией и анализировали XRPD, TGA и DSC. Результаты показаны на Фигурах 13-15.
Пример 6: Получение полиморфной формы #6
2,006 г коммерчески доступного бензоата натрия помещали в круглодонную колбу, и 40 мл метанола добавляли для растворения бензоата натрия. Постепенно добавляли 120 мл ацетонитрила, и таким образом полученную суспензию сохраняли при перемешивании. Через 2 дня суспензию фильтровали, и полученное твердое вещество анализировали XRPD, TGA и DSC. Результаты показаны на Фигурах 16-18.
Пример 7: Альтернативное получение полиморфной формы #4
1-2 мг одной из новых полиморфных форм #1-3, 5 или 6, раскрытых здесь, суспендировали в 0,5 мл ацетонитрила приблизительно с 6% воды для формирования новой полиморфной формы #4. Было таким образом продемонстрировано, что среди всех новых полиморфных форм по изобретению, полиморфная форма #4 была наиболее термодинамически стабильной.
Пример 8: Крупномасштабное получение полиморфной формы #4
50 г коммерчески доступного бензоата натрия (купленного у Merck) помещали в круглодонную колбу с последующим добавлением 92 мл воды. Медленно добавляли 688 мл изопропилового спирта, и полученную суспензию сохраняли при перемешивании с верхней мешалкой в течение 4 дней и фильтровали для сбора 22,3 г твердого вещества.
Пример 9: Анализ стабильности полиморфной формы #4 в условиях высокой влажности
500 мг каждого из бензоата натрия от Merck и Formosa Laboratories и полиморфной формы #4 сохраняли в условиях высокой влажности (> 90%-й RH) в течение 5 дней и анализировали XRPD. Результаты показали, что через 5 дней наблюдались существенные изменения в структурах XRPD с пиками при угле отражения 2θ приблизительно 6,2, 16,5 и 24,5 градусов и появление нового пика при 22,9 градусах бензоата натрия от Merck и Formosa Laboratories, в то время как не наблюдалось никакого изменения структуры XRPD новой полиморфной формы #4. Результаты показаны на Фигуре 19. Было таким образом показано, что полиморфная форма #4 была более стабильной, чем протестированные коммерческие продукты бензоата натрия в условиях высокой влажности.
Пример 10: Анализ стабильности полиморфной формы #4 в комбинации с клозапином в условиях высокой влажности
500 мг каждого из бензоата натрия от Merck и новой полиморфной формы #4 в комбинации с 300 мг клозапина сохраняли в условиях высокой влажности (> 90%-й RH) в течение 5 дней и анализировали XRPD. Результаты показали, что через 5 дней наблюдались существенные изменения в структуре XRPD с пиками при угле отражения 2θ приблизительно 6,2, 14,9, 15,9, 16,5, 20,5, 22,6 и 25,1 градусов и появление нового пика при 22,9 градусах бензоата натрия от Merck, скомбинированного с клозапином. Никакого изменения структуры XRPD новой полиморфной формы #4, скомбинированной с клозапином, не наблюдалось. Результаты показаны на Фигурах 20-21. Таким образом было проиллюстрировано, что в комбинации со вторым терапевтическим агентом использование полиморфной формы #4 подходило более, чем протестированные коммерческие продукты бензоата натрия.
Пример 11: Дальнейшее сравнение полиморфной формы #4 с бензоатом натрия от Merck и Sigma-Aldrich
Новая полиморфная форма #4, бензоат натрия от Merck и бензоат натрия от Sigma-Aldrich были проанализированы и сравнены с помощью XRPD. Результаты, как показано на Фигуре 22, показали, что структуры XRPD этих двух коммерческих образцов бензоата натрия от Merck и Sigma-Aldrich очень сильно перекрывались друг с другом. Было обнаружено, что новая полиморфная форма #4 была наиболее термодинамически стабильной полиморфной формой бензоата натрия по сравнению с менее термодинамически стабильной полиморфной формой коммерчески доступного бензоата натрия (Merck, Formosa Laboratories и Sigma-Aldrich).
Пример 12: Растворимость полиморфной формы #4 в воде
Приблизительно к 1 г каждого из новой полиморфной формы #4 бензоата натрия от Merck и бензоата натрия от Sigma-Aldrich в ампуле добавляли воду, пока не была достигнута максимальная растворимость. Результаты показали, что максимальная растворимость в воде новой полиморфной формы #4 (666 мг/мл) была выше, чем у бензоата натрия от Merck (500 мг/мл) и Sigma-Aldrich (454 мг/мл). Поэтому растворимость полиморфной формы #4 бензоата натрия по изобретению приблизительно от 1,3 до 1,5 раза выше, чем у коммерчески доступных продуктов бензоата натрия.
Пример 13: Тесты стабильности коммерчески доступного бензоата натрия и полиморфной Формы #4 бензоата натрия
1. Стрессовое тестирование в условиях высокой влажности
Другой тест стабильности проводили на 500 мг коммерчески доступного бензоата натрия от Merck или полиморфной формы #4 бензоата натрия по изобретению, независимо скомбинированных с 100 мг клозапина, сохраняемых в условиях высокой влажности (> 90% RH) при комнатной температуре в течение 8 дней. В день 8, структура XRPD комбинации коммерчески доступного бензоата натрия и клозапина показала дополнительный новый пик при 11°, как показано стрелкой на Фигуре 23-24. Однако дополнительный пик при 11° не был обнаружен в структуре XRPD комбинации полиморфной формы #4 бензоата натрия по изобретению и клозапина. В следующих экспериментах появление пика при 11° считали показателем разрушения полиморфа клозапина в комбинации клозапина и коммерчески доступного бензоата натрия.
2. Стабильность Комбинации Полиморфной Формы #4 Бензоата натрия по изобретению и Клозапина и других эксципиентов
Так как влажность является проблемой для стабильности комбинации соединения бензоата натрия и клозапина, несколько эксципиентов были выбраны для тестирования их влияния на стабильность в условиях высокой влажности (> 90% RH, комнатная температура). Результаты показаны в Таблицах 1 и 2.
По сравнению с борной кислотой, альгинат натрия имеет лучший эффект в стабилизации комбинации бензоата натрия (купленного у Merck) и клозапина (см. Таблицу 1). Кроме того, пик при 11°, указывающий на разрушение комбинации бензоата натрия (купленного у Merck) и клозапина, не появлялся до дня 30, когда большую дозу хитозана (60 мг) или цитрата натрия (60 мг) дополнительно добавляли в композицию (см. Таблицу 2).
Пример 14: получение таблеток, включающих соединение бензоата натрия и клозапин
1. Мокрая грануляция
Активные ингредиенты (например,любое из соединений бензоата натрия и клозапина) и эксципиенты размалывали и просеивали через фильтр 40 меш по-отдельности. Размолотые и просеянные порошки смешивали в ступке. 75%-й этанол, использовавшийся в качестве связывающего раствора, медленно добавляли в ступку для проведения мокрой грануляции. Полученную влажную массу пропускали через сито с порами 20 меш. Затем сырые гранулы высушивали при 50˚C в течение 3 часов. Высушенные гранулы далее просеивали дважды: (1) через сито 40 меш, и гранулы более 40 меш сохраняли; и (2) через сито 20 меш, и гранулы, проходящие через сито, сохраняли. После просеивания через сита 40 и 20 меш были получены гранулы, имеющие размеры от 20 до 40 меш. Полученные гранулы затем смешивали со стеаратом магния в качестве лубриканта в течение приблизительно 3 минут, и смесь прессовали с помощью таблетирующего пресса ZP01 Single punch (Taizhou Liming Pharmaceutical Machinery Co. Ltd.) в таблетки. Полученные таблетки взвешивали, и их твердость, хрупкость, время распада и время высвобождения при растворении проверяли.
2. Определение твердости
Полученные таблетки подвергали определению твердости и регистрировали силу (кг), необходимую для разламывания тестируемой таблетки. Твердость таблеток составляла от 5 до 10 кг.
3. Тест на хрупкость
Десять таблеток помещали в аппарат для измерения хрупкости таблетки и вращали при 25±1 об/мин в течение 100 оборотов. Тест определяли как проваленный, если какая-либо из тестируемых таблеток ломалась. Когда таблетки не ломались, их взвешивали для вычисления потерь веса (%). Потери веса (%) должны быть ниже 1%.
4. Тест на распадаемость
Шесть таблеток помещали в воду при 37±2°C. Тест определяли как проваленный, если эти таблетки не разлагались в течение 30 минут. Время распада (минуты) этих таблеток регистрировали.
5. Тест на растворимость
Тест на растворимость проводили на основе способа USP для растворения клозапина. Шесть таблеток добавляли в растворяющую среду (ацетатный буфер, pH 4,0) и подвергали тесту на растворимость. Объем растворяющей среды составлял 500 мл, и скорость вращения составляла 100 об/мин. Тест определяли как проваленный, если эти таблетки не растворялись в течение 30 минут. Время растворения (минуты) этих таблеток регистрировали.
И альгинат натрия, и цитрат натрия улучшают непосредственный эффект высвобождения, но составы таблеток 1-2, которые включают альгинат натрия и цитрат натрия, расслаивались во время теста на растворимость, и добавление гликолята крахмала натрия (SSG) в качестве разрыхлителя исправляло этот дефект, как показано в Таблице 3.
Составы таблетки, включающие комбинацию клозапина и коммерчески доступного бензоата натрия (купленного у Merck) или полиморфной формы бензоата натрия #4, полученной из Примера 4, как показано в Таблицах 4 и 5, были затем исследованы. Результаты показали, что таблетки, включающие полиморфную форму #4 бензоата натрия по изобретению, имели более короткое время распада и время высвобождения при растворении, что было преимуществом для получения лекарственные формы непосредственного высвобождения лекарственных средств.
Эквиваленты и объем
В формуле изобретения формы единственного числа могут означать один или более одного, если обратное не указано или иначе не очевидно из контекста. Пункты формулы изобретения или места в описании, включающие «или» между одним или более членами группы, считают удовлетворенными, если один, больше чем один или все члены группы присутствуют в, используются в или иначе относятся к данному продукту или способу, если обратное не указано или иначе не очевидно из контекста. Изобретение включает варианты осуществления, в которых ровно один член группы присутствует в, используется в или иначе относится к данному продукту или способу. Изобретение включает варианты осуществления, в которых больше чем один или все члены группы присутствуют в, используются в или иначе относятся к данному продукту или способу.
Кроме того, изобретение охватывает все вариации, комбинации и перестановки, в которых одно или более ограничений, элементов, пунктов и описательных терминов из одного или более пунктов формулы вводятся в другой пункт формулы. Например, любой пункт, зависимый от другого пункта, может быть изменен путем включения одного или более ограничений, имеющихся в любом другом пункте, зависимом от того же основного пункта. Если элементы представлены как списки, например, в формате группы Маркуша, каждая подгруппа элементов также раскрыта, и любой элемент(ы) может быть из группы удален. Нужно понимать, что, в целом, если изобретение или аспекты изобретения, упомянуты как включающие определенные элементы и/или признаки, некоторые варианты осуществления изобретения или аспекты изобретения состоят или состоят по существу из таких элементов и/или признаков. В целях простоты такие варианты осуществления не были специфично сформулированы здесь in haec verba. Также следует отметить, что термины «включающий» и «содержащий» являются открытыми и допускают включение дополнительных элементов или стадий. Если даны диапазоны, включены граничные значения. Кроме того, если иное не указано или иначе не очевидно из контекста и общих знаний специалиста в данной области техники, значения, выраженные как диапазоны, могут принимать любое конкретное значение или поддиапазон в установленных диапазонах в различных вариантах осуществления изобретения до десятой единицы нижней границы диапазона, если из контекста ясно не следует иное.
Эта заявка относится к различным выданным патентам, опубликованным заявкам на патент, статьям в журналах и другим публикациям, которые все включены в настоящее описание посредством ссылки. В случае конфликта между какой-либо из включенных ссылок и настоящим описанием, преимущество отдается описанию. Кроме того, любой частный вариант осуществления настоящего изобретения, попадающий в предшествующий уровень техники, может быть явно исключен из одного или более пунктов формулы изобретения. Поскольку такие варианты осуществления, как считают, известны специалисту, они могут быть исключены, даже если исключение явно здесь не сформулировано. Любой частный вариант осуществления изобретения может быть исключен из любого пункта формулы по любой причине, вне зависимости от того, связано ли это с существованием предшествующего уровня техники.
Специалист знает или будет в состоянии установить, с использованием не более чем обычного экспериментирования, множество эквивалентов частных вариантов осуществления, описанных здесь. Объем настоящих вариантов осуществления, описанных здесь, не ограничен приведенным выше описанием, а находится в рамках приложенной формулы изобретения. Специалисту в данной области техники будет понятно, что могут быть сделаны различные изменения и модификации этого описания без отхода от духа или объема настоящего изобретения, как определено в следующей формуле изобретения.
Реферат
Изобретение относится к способу получения полиморфной формы бензоата натрия, которая имеет дифракционную рентгенограмму, содержащую характеристические пики при угле отражения 2θ 4,3, 5,9, 7,1, 8,6, 10,1, 10,7, 12,9, 13,8, 14,4, 17,2, 17,7, 18,5, 21,5, 22,0, 22,6, 23,7, 25,1, 25,9, 26,2, 26,9, 27,9, 28,2, 28,8, 29,1, 29,7, 30,2, 31,2, 33,2, 34,9, 35,8, 36,1 и 39,3. Технический результат: разработан способ получения новой полиморфной формы бензоата натрия, которая может быть применима в лечении и/или снижении риска нейропсихиатрического расстройства, например, шизофрении, психотических расстройств, депрессивных расстройств или болезни Альцгеймера. 5 н.п. ф-лы, 24 ил., 5 табл., 14 пр.

Комментарии