Ингибиторы вирусной репликации, способ их получения и их терапевтические применения - RU2678575C2
Код документа: RU2678575C2
Описание
Область техники, к которой относится изобретение
Настоящее изобретение относится к соединениям, их применению при лечении или при предотвращении вирусных расстройств, включающих ВИЧ-родственные расстройства. Также настоящее изобретение относится к способам получения таких соединений. Также настоящее изобретение относится к фармацевтическим соединениям, содержащим такие соединения. Также настоящее изобретение относится к лечению вирусных инфекций путем введения терапевтически эффективного количества таких соединений.
Уровень техники
Синдром приобретенного иммунодефицита (СПИД) представляет собой заболевание, вызванное инфекцией вирусом иммунодефицита человека, ВИЧ (англ. HIV). ВИЧ представляет собой ретровирус, принадлежащий к подклассу лентивирусов приматов. Было идентифицировано два типа ВИЧ, HIV-1 и HIV-2. HIV-1 отвечает за большую часть глобальной эпидемии СПИД в мире, и почти в каждой стране отмечены случаи этого заболевания. В настоящее время, ВИЧ-инфицированные пациенты подвергают лечению с помощью Высокоэффективной Противоретровирусной Терапии (HAART), которая базируется на комбинации нескольких лекарственных средств, принадлежащих к различным классам. До 2003 года все одобренные анти-ВИЧ лекарственные средства представляли собой ингибиторы каталитической активности двух вирусных ферментов, ингибиторы Обратной Транскриптазы (ОТ) и Ингибиторы Протеазы (ПР). Ингибиторы Обратной Транскриптазы включают два различных класса, нуклеозидные/нуклеотидные ингибиторы обратной транскриптазы (НИОТ) и ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ). В 2003 году был представлен новый класс антиретровирусных лекарственных средств (ARV), ингибитор слияния (Энфувиртид (англ. Enfuvirtide)) (Cervia et al, Clin Infec Dis., 2003, 37(8): 1102-6). И позже в 2007 году были одобрены другие классы ARV, ингибиторы входа (Маравирок (англ. Maraviroc) (Pfizer)), с направленным воздействием на корецептор CCR5, и ингибиторы интегразы (Ралтегравир (англ. Raltegravir) (Merck)) (Hughes et al, J Infect., 2008, 57(1): 1-10.). Хотя эти три новых лекарственных средства были очень полезны при лечении пациентов в случае неудачного лечения, вызванного мультиустойчивостью к ингибиторам ОТ и ПР, мутации устойчивости против этих лекарственных средств уже были отмечены.
Хотя разработка этих мощных анти-ВИЧ лекарственных средств давала возможность ВИЧ-инфицированным людям жить дольше и с более высоким качеством жизни, при этом очевидно, что эти лекарственные средства не излечивают ВИЧ-инфекцию. Кроме того, их продолжительное применение часто приводит к значительной токсичности и к появлению вирусов, устойчивых к лекарственным средствам. Важно, что способность ВИЧ создавать латентные резервуары на ранней стадии инфекции гарантирует устойчивость вируса даже при обработке с использованием интенсивной терапии лекарственных средств и при получении сильного антивирусного иммунного ответа.
Таким образом, существует постоянная потребность в разработке новых анти-ВИЧ терапий или агентов для преодоления проблем устойчивости к существующим лекарственным средствам и для улучшения эффективности лечения (Daar ES, Top HIV Med., 2008; 16(4): 110-116; De Clercq Е., Expert Opinion on Emerging Drugs 2008; 13(3): 393-416).
WO 2012/003497, WO 2012/003498 и WO 2012/145728, соответственно, описывают производные хинолина, производные нафтила и производные бензотиазола в качестве анти-ВИЧ агентов. WO 2012/140243 и WO 2013/062028 описывает фенильные производные в качестве анти-ВИЧ агентов.
Неожиданно авторы изобретения идентифицировали и получили новые соединения, обладающие улучшенной противовирусной активностью, конкретно, антиретровирусной активностью, в частности, что касается ВИЧ по сравнению с соединениями предыдущего уровня техники.
Раскрытие изобретения
Изобретение охватывает соединения, которые представляют собой ингибиторы репликации ВИЧ, что было показано с помощью анализа репликации HIV-1, подробно описанного в данном документе. Изобретение также охватывает соединения, которые, таким образом, представляют собой полезные агенты для лечения или предотвращения инфекции и заболевания, вызванного вирусом, конкретно, ретровирусом (orthoretrovirinae), более конкретно, лентивирусом, таким как ВИЧ, или других вирусных патогенных заболеваний или расстройств, а именно путем ингибирования репликации вируса в инфицированных клетках хозяина или во время проявления или прогрессии инфекции.
Таким образом, изобретение охватывает соединения, которые составляют полезный класс новых мощных антивирусных соединений, которые могут использоваться в лечении и/или в предотвращении вирусной, конкретно, ретровирусной, более конкретно, лентивирусной инфекции у пациентов, конкретно, у млекопитающих и людей, а более конкретно, для лечения и/или для предотвращения ВИЧ-инфекции или родственного заболевания у людей.
Настоящее изобретение дополнительно относится к таким соединениям для их применения в качестве лекарственного средства, а более конкретно, в качестве антивирусных агентов и для их применения при производстве лекарственного средства для лечения и/или для предотвращения вирусных инфекций и родственных заболеваний, особенно лентивирусных заболеваний и родственных заболеваний, таких как, в частности, ВИЧ и родственные заболевания у людей.
Изобретение также относится к фармацевтическим композициям, содержащим такие соединения в антивирусном эффективном количестве, необязательно в комбинации, по меньшей мере, с одним дополнительным антивирусным агентом.
Настоящее изобретение дополнительно относится к такой фармацевтической композиции для ее применения в качестве лекарственного средства, особенно, для применения при лечении ВИЧ-инфекции у млекопитающего, инфицированного ВИЧ.
Настоящее изобретение также относится к способу лечения или предотвращения вирусных инфекций и родственных заболеваний, конкретно, ретровирусных инфекций и родственных заболеваний, более конкретно, лентивирусных инфекций и родственных заболеваний, таких как, в частности, ВИЧ-инфекции и родственные заболевания у людей путем введения нуждающемуся в этом пациенту одного или нескольких таких соединений необязательно в комбинации с одним или с несколькими другими антивирусными агентами.
Настоящее изобретение также относится к способу ингибирования репликации ВИЧ путем включения экспонирования вируса с эффективным количеством одного или нескольких таких соединений при условиях, где ингибируется репликация ВИЧ.
В первом аспекте в изобретении предлагаются соединения, содержащие 6-членный углеродный цикл, причем указанные соединения имеют структуру согласно формуле (I):
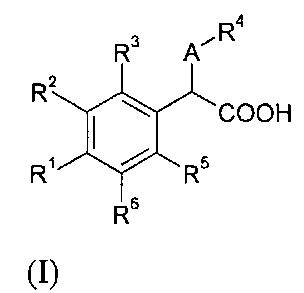
где:
- R1 и R6, незамещенные или замещенные, по меньшей мере, одним Т1, идентичные или различные, независимо представляют собой атом водорода; -CN; -ОН; -NH2; -CF3; атом галогена; линейный или разветвленный C1-C8 алкил; линейный или разветвленный C2-C8 алкенил; линейный или разветвленный C2-C8 алкинил; -Z-C(O)2R7; -Z-OC(O)2R7; -Z-OR8; -Z-SR8; -Z-S(O)R8; -Z-S(O)2R8; -Z-NR7R8; -Z-OC(O)R8; -Z-C(O)R8; -Z-C(O)NR7R8; -Z-NR8C(O)R8; -Z-NR8C(O)NR7R8; Z-NR8S(O)2R8; Z-NR8S(O)2NR7R8; -Z-OC(O)NR7R8; -Z-NR8C(O)2R7; -Z-S(O)2NR7R8; насыщенный, частично или полностью ненасыщенный или ароматический 3-, 4-, 5-, 6- или 7-членный углеродный цикл; C1-C8 алкил-(насыщенный, частично или полностью ненасыщенный или ароматический 3-, 4-, 5-, 6- или 7-членный углеродный цикл); насыщенный, частично или полностью ненасыщенный или ароматический 3-, 4-, 5-, 6- или 7-членный углеродный цикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом; C1-C8 алкил-(насыщенный, частично или полностью ненасыщенный или ароматический 3-, 4-, 5-, 6-или 7-членный углеродный цикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом); насыщенный, частично или полностью ненасыщенный или ароматический 3-, 4-, 5-, 6- или 7-членный углеродный цикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; C1-C8 алкил-(насыщенный, частично или полностью ненасыщенный или ароматический 3-,4-, 5-, 6- или 7-членный углеродный цикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом); насыщенный, частично или полностью ненасыщенный или ароматический 4-, 5-, 6- или 7-членный гетероцикл; C1-C8 алкил-(насыщенный, частично или полностью ненасыщенный или ароматический 4-, 5-, 6- или 7-членный гетероцикл); C1-C8 алкил-(насыщенный, частично или полностью ненасыщенный или ароматический 4-, 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом); насыщенный, частично или полностью ненасыщенный или ароматический 4-, 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; или C1-C8 алкил-(насыщенный, частично или полностью ненасыщенный или ароматический 4-, 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом);
- R2, незамещенный или замещенный, по меньшей мере, одним Т1, представляет собой линейный или разветвленный C2-C8 алкил; линейный или разветвленный C2-C8 алкенил; линейный или разветвленный C1-C8 гетероалкил; линейный или разветвленный C2-C8 гетероалкенил; C3-C7 циклоалкил; C1-C8 алкил-(C3-C7 циклоалкил); C1-C8 гетероалкил-(C3-C7 циклоалкил); C1-C8 алкил-(частично или полностью ненасыщенный или ароматический C3-C7 углеродный цикл); C1-C8 гетероалкил-(частично ненасыщенный C3-C7 углеродный цикл); C4-C7 гетероциклоалкил; C1-C8 алкил-(C4-C7 гетероциклоалкил); C1-C8 гетероалкил-(C4-C7 гетероциклоалкил); C1-C8 алкил-(частично или полностью ненасыщенный или ароматический C4-C7 гетероцикл); или C1-C8 гетероалкил-(частично или полностью ненасыщенный или ароматический C4-C7 гетероцикл);
- R3, незамещенный или замещенный, по меньшей мере, одним Т2, представляет собой насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный углеродный цикл; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный углеродный цикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный углеродный цикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный углеродный цикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный углеродный цикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный углеродный цикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный углеродный цикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членный гетероциклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членный гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом; или насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом;
- А представляет собой -CH2; -СН=; -О- или -S-;
- R4, замещенный или не замещенный, по меньшей мере, одним Т3, представляет собой линейный или разветвленный C2-C6 алкил; линейный или разветвленный C2-C6 алкенил; линейный или разветвленный C1-C6 фторалкил; C3-C6 циклоалкил; или C1-C3 алкил-(C3-C6 циклоалкил);
- R5 представляет собой атом галогена; -CF3; линейный или разветвленный C1-C6 алкил; линейный или разветвленный C2-C6 алкенил; линейный или разветвленный C2-C6 алкинил; линейный или разветвленный фторалкил; C3-C6 циклоалкил; -CH2OH; или -CH2-O-CH3;
- R5 и R6 могут образовывать с атомами углерода фенильного кольца формулы (I), с которым они связаны, арил, или могут образовывать с атомами углерода фенильного кольца формулы (I), с которым они связаны, гетероарил, содержащий, по меньшей мере, один атом N;
- R7 и R8, идентичные или различные, независимо представляют собой атом водорода; линейный или разветвленный C1-C8 алкил; линейный или разветвленный C2-C8 алкенил; линейный или разветвленный C2-C8 алкинил; линейный или разветвленный C1-C8 гетероалкил; линейный или разветвленный фторалкил; линейный или разветвленный фторалкенил; линейный или разветвленный фторалкинил; -(X)x-(CT6T7)yNT4T5; -(Х)х-(CT6T7)yC(O)NT4T5; -(Х)х-(СТ6Т7)уОТ4; -(X)x-(CT6T7)yNT4C(O)OT5; C3-C7 циклоалкил; C4-C7 гетероциклоалкил; частично или полностью ненасыщенный или ароматический C4-C7 углеродный цикл; частично или полностью ненасыщенный или ароматический C5-C7 гетероцикл; C1-C8 алкил-(C3-C7 циклоалкил); C1-C8 алкил-(C4-C7 гетероциклоалкил); C1-C8 алкил-(частично или полностью ненасыщенный или ароматический C4-C7 углеродный цикл); или C1-C8 алкил-(частично или полностью ненасыщенный или ароматический C5-C7 гетероцикл);
- R7 и R8 могут образовывать с атомом азота, с которым они соединены, насыщенный или частично ненасыщенный 4-, 5-, 6- или 7-членный гетероцикл, причем указанный гетероцикл может дополнительно содержать, по меньшей мере, один дополнительный гетероатом;
- Т1 независимо представляет собой атом галогена; алкил; -(X)x-C1-C6 алкил; линейный или разветвленный фторалкил; линейный или разветвленный -О-C1-C3 фторалкил; -(Х)х-C3-C6 циклоалкил; -(Х)х-C4-C6 гетероцикл; -(X)x-(CT6T7)yCN; -(Х)х-(СТ6Т7)уОТ4; -(X)x-(CT6T7)yST4; -(X)x-(CT6T7)yS(O)T4; -(X)x-(CT6T7)yS(O)2T4; -(Х)х-(CT6T7)yNT4T5; -(Х)х-(СТ6Т7)уС(O)Т4; -(Х)х-(СТ6Т7)уС(O)-(СТ6Т7)уОТ4; -(Х)x-(СТ6Т7)уС(O)ОТ4; -(X)x-(CT6T7)yC(O)NT4T5; -(X)x-(CT6T7)yNT4C(O)NT4T5; -(Х)х-(CT6T7)yNT4C(O)T5; -(X)x-(CT6T7)yNT4C(O)OT5; -(X)x-(CT6T7)yOC(O)NT4T5; -(X)x-(CT6T7)yS(O)2NT4T5; или -(X)x-(CT6T7)yNT4S(O)2T5;
- T2 независимо представляет собой атом галогена; линейный или разветвленный -O-(C1-C3 алкил); линейный или разветвленный С1-С3 фторалкил; линейный или разветвленный -O-(С1-C3 фторалкил); линейный или разветвленный C1-C3 алкил; C3-C6 циклоалкил; или -CN;
- два геминальных Т2 могут образовывать с атомом углерода, с которым они соединены, C3-C7 циклоалкил;
- Т3 независимо представляет собой линейный C1-C2 алкил; или атом фтора;
- Т4 и Т5, идентичный или различные представляют собой атом водорода; разветвленный или линейный C1-C6 алкил; или C3-C6 циклоалкил;
- Т4, Т5 и атом азота, с которым они связаны, могут образовывать насыщенный или частично насыщенный 4-, 5-, 6- или 7-членный гетероцикл, причем указанный гетероцикл может дополнительно содержать, по меньшей мере, один гетероатом;
- Т6 и Т7, идентичные или различные, представляют собой атом водорода; атом фтора; линейный или разветвленный C1-C3 алкил; или C3-C6 циклоалкил;
- Т6, Т7 и атом углерода, с которым они связаны, могут образовывать C3-C6 циклоалкил;
- Т8 независимо представляет собой атом водорода, линейный или разветвленный C1-C3 алкил; или C3-C6 циклоалкил;
- X независимо представляет собой атом кислорода; атом серы; NT8; S=O; или S(O)2;
- Z независимо представляет собой одинарную связь; или линейный или разветвленный C1-C8 алкил;
- х представляет собой 0 или 1;
- у представляет собой 0, 1, 2 или 3;
и его рацемат, энантиомер, стереоизомер, атропизомер или диастереомер или фармацевтически приемлемая соль.
Даже если настоящее изобретение описано в конкретных или в предпочтительных воплощениях, это не следует понимать как ограничение такими конкретными или предпочтительными воплощениями.
Термин «гетероалкил», при использовании в данном документе индивидуально или в комбинации с другим радикалом, относится к насыщенному углеводородному радикалу, содержаему, по меньшей мере, один гетероатом, и/или замещенному с помощью, по меньшей мере, одного гетероатома.
Термин «галоген» при использовании в данном документе, индивидуально или в комбинации с другим радикалом относится к атому фтора, атому хлора, атому брома и атому иода, особенно к атому фтора.
Термин «циклоалкил» при использовании в данном документе индивидуально или в комбинации с другим радикалом, относится к моноциклическому или к полициклическому насыщенному углеводородному радикалу.
Термин «гетероциклоалкил» при использовании в данном документе индивидуально или в комбинации с другим радикалом, относится к моноциклическому или к полициклическому насыщенному углеводородному радикалу, содержащему, по меньшей мере, один гетероатом.
Термин «арил» при использовании в данном документе индивидуально или в комбинации с другим радикалом относится к карбоциклической ароматической моноциклической группе, содержащей 6 атомов углерода, которые могут сшиваться, по меньшей мере, с одним другим насыщенным, частично или полностью ненасыщенным или с ароматическим углеродным циклом или с гетероциклом.
Термин «гетероарил» при использовании в данном документе индивидуально или в комбинации с другим радикалом относится к гетероциклической ароматической моноциклической группе, содержащей 5 атомов углерода и один гетероатом, которая может быть конденсирована, по меньшей мере, с одним другим насыщенным, частично или полностью ненасыщенным или ароматическим углеродным циклом или гетероциклом.
Термины «алкил-циклоалкил», «алкил-карбоцикл» или «алкил-гетероцикл» при использовании в данном документе индивидуально или в комбинации с другим радикалом относится к алкильному радикалу, в котором один из атомов водорода, связанный с атомом углерода, заменен, соответственно, на циклоалкильный радикал, насыщенный, частично или полностью ненасыщенный или ароматический карбоциклический радикал, или насыщенный, частично или полностью ненасыщенный или ароматический гетероциклический радикал.
Термины «гетероалкил-циклоалкил», «гетероалкил-карбоцикл» или «гетероалкил-гетероцикл» при использовании в данном документе индивидуально или в комбинации с другим радикалом относится к гетероалкильному радикалу, в котором один из атомов водорода, связанный с атомом углерода, заменен, соответственно, на циклоалкильный радикал, насыщенный, частично или полностью ненасыщенный или ароматический карбоциклический радикал, или насыщенный, частично или полностью ненасыщенный или ароматический гетероциклический радикал.
При использовании в данном документе выражение «фармацевтически приемлемый» относится к тем соединениям, материалам, композициям и/или дозированным формам, которые в рамках озвученного мнения врача подходят для использования в контакте с тканями людей и животных без избыточной токсичности, раздражения, аллергической реакции или других проблем или сложностей, в соответствии с оправданным соотношением пользы/риска.
При использовании в данном документе, термин «фармацевтически приемлемые соли» относится к производным раскрытых соединений, где родительское соединение модифицируется путем получения его соли присоединения кислоты или соли присоединения основания. Примеры фармацевтически приемлемых солей включают в частности минеральные или органические соли основных остатков, таких как амины; щелочные или органические соли кислых остатков, такие как карбоциклические кислоты; и так далее.
Фармацевтически приемлемые соли по настоящему изобретению могут синтезироваться из родительского соединения, которое содержит основный или кислый компонент, путем обычных химических подходов. Кроме того, термин «фармацевтически приемлемая соль» относится к относительно нетоксичной неорганической и органической соли добавления кислоты или основания соединений по настоящему изобретению. Эти соли могут быть получены in situ в процессе конечного выделения и очистки соединений. Конкретно, соли присоединения кислоты могут быть получены путем отдельной реакции очищенного соединения в его очищенной форме с органической или с неорганической кислотой и путем выделения полученной таким образом соли. Среди примеров солей присоединения кислот представлены гидробромид, гидрохлорид, гидроиодид, сульфамат, сульфат, бисульфат, фосфат, нитрат, ацетат, пропионат, сукцинат, оксалат, валериат, алеат, пальмитат, стеарат, лаурат, борат, бензоат, лактат, тозилат, цитрат, малеат, фумарат, тартрат, нафтилат, мезилат, глюкогептанат, глюкоронат, глутамат, лактобионат, малонат, салицилат, метиленбис-Ь-гидроксинафтоат, соль присоединения гентизиновой кислоты, изетионат, ди-р-толуоилтартрат, этансульфонат, бензолсульфонат, циклогексилсульфамат, хинатлаурилсульфонатные соли и тому подобные. Примеры солей присоединения основания включают соли аммония, такие как трометамин, меглумин, эполамин и т.д., соли металлов, такие как соли натрия, лития, калия, кальция, цинка или магния, соли с органическими основаниями, такие как соли дициклогексамина, N-метил-D-глюкамин. Список подходящих солей находится в Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, PA, 1985, p. 1418, описание которой включено в данный документ ссылкой, и в S.M. Berge et al. ((Pharmaceutical Salts» J. Pharm. Sci, 66: p. 1-19 (1977), описание которой включено в данный документ ссылкой.
Термин «стереоизомер» применяется в данном документе для обозначения соединений, которые содержат химически идентичные линкерные последовательности и отличаются друг от друга трехмерной ориентацией в пространстве их функциональных групп.
Термин «энантиомер» применяется в данном документе для обозначения двух конкретных стереоизомеров, которые представляют собой неналагающиеся зеркальные изображения друг друга, но относятся друг к другу как отражения.
Термин «диастереомер» применяется в данном документе для обозначения одного из стереоизомеров, которые представляют собой неналагающиеся зеркальные изображения друг друга, но не относятся друг к другу как отражения.
Термин «рацемат» применяется в данном документе для обозначения равного количества двух конкретных энантиомеров.
Термин «атропоизомер» применяется в данном документе для обозначения стереоизомера, полученного с помощью стерически затрудненной одинарной связи, посредством чего свободное вращение функциональных групп на другой стороне данной связи невозможно.
Термин «предотвращение» при использовании в данном документе предназначен для обозначения введения соединения или композиции согласно изобретению с целью предотвращения инфекции, вызванной вирусом, или для предотвращения проявления родственных заболеваний.
Термин «лечение» при использовании в данном документе конкретно предназначен для обозначения введения соединения или композиции согласно настоящему изобретению для облегчения или исключения симптомов ВИЧ-инфекции, и/или для уменьшения вирусной нагрузки у пациента. Термин «лечение» также охватывает введение соединения или композиции согласно настоящему изобретению после экспонирования индивидуума вирусу, но перед проявлением симптомов заболевания, и/или перед детектированием вируса в крови, особенно для предотвращения проявления симптомов заболевания и/или для предотвращения достижения вирусом детектируемого уровня в крови, и введение соединения или композиции по настоящему изобретению для предотвращения перинатальной трансмиссии вируса, например, ВИЧ от матери к ребенку, путем введения матери перед родами и ребенку в течение первых дней жизни. Термин «лечение» также относится к лечению болезненного состояния у пациента, включая ингибирование или ослабление болезненного состояния пациента, например, путем прекращения его развития; или ослабление болезненного состояния у пациента, как например, путем регрессии или излечения болезненного состояния. В случае ВИЧ, лечение включает уменьшение уровня нагрузки вируса ВИЧ у пациента.
Термин «пациент» означает индивидуума или животное с риском инфекции вирусом, или индивидуума или животное, инфицированного вирусом, предпочтительно, ретровирусом и, более предпочтительно, вирусом ВИЧ.
Выражение «терапевтически эффективное количество» относится к количеству соединения согласно изобретению, которого, при введении нуждающемуся в этом пациенту, достаточно для эффективного лечения болезненного состояния, патологического состояния или расстройства, для которых полезны соединения. Такого количества будет достаточно для того, чтобы вызвать биологический или медицинский ответ тканевой системы или пациента, который подразумевается исследователем или клиницистом. Количество соединения согласно изобретению, которое составляет терапевтически эффективное количество, будет варьироваться в зависимости от таких факторов, как соединение и его биологическая активность, композиция, применяемая для введения, время введения, путь введения, скорость выведения соединения, продолжительность лечения, тип болезненного состояния или расстройства, которое подвергается лечению, и его тяжесть, лекарственные средства, используемые в комбинации или одновременно с соединениями по изобретению, и возраст, масса тела, общее состояние, пол и питание пациента. Такое терапевтически эффективное количество может стандартно определяться обычным специалистом в данной области согласно его опыту, уровню техники и данному описанию.
Выражение «фармацевтически приемлемый носитель» применяется для любого эксципиента, растворителя, дисперсионной среды, ингибитора абсорбции, разбавителя или адъюванта и т.д., причем такие консерванты или оксиданты, наполнители, связующие агенты, агенты для улучшения распадаемости, увлажнители, эмульгаторы, суспендирующие агенты, растворители, дисперсионные среды, покрытия, антибактериальные и антигрибковые агенты, изотонические агенты и агенты, замедляющие абсорбцию, и тому подобные, которые не производят вторичных реакций, например, аллергической реакции у людей или животных.
Фармацевтически приемлемые носители хорошо известны специалисту в данной области и включают те, что описаны в «Remington's Pharmaceutical Sciences» (Mack Publishing Company, Easton, USA, 1985). Кроме тех случаев, когда обычные среда или агент являются несовместимыми с активным ингредиентом, предусматривается их применение в терапевтических композициях.
Термин «комбинация» относится к введению соединения формулы (I), по меньшей мере, вместе с одним антивирусным агентом. Это охватывает, по меньшей мере, два активных вещества в одной композиции или в отдельных композициях, которые вводят отдельно или одновременно.
Термин «ВИЧ» при использовании в данном документе охватывает HIV-1 и HIV-2.
Изобретение может дополнительно определяться как применимое к HIV-1 или HIV-2.
Подразумевается, что термин «млекопитающее» при использовании в данном документе охватывает людей, а также млекопитающих, не относящихся к человеку, которые предрасположены к инфекции ВИЧ или эквивалентов ВИЧ, не относящихся к человеку. Млекопитающие, не относящиеся к человеку, включают в частности домашних животных, таких как кошки, и не домашних животных, таких как приматы.
В изобретении главным образом предлагаются соединения формулы (I), как определено в данном документе.
В изобретении предлагается соединение формулы (I), где:
- А представляет собой -CH2; или -O-;
- R1, R2, R3, R4, R5, R6, R7, R8, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, X, Z, x и y определяются как для соединения формулы (I) согласно изобретению.
Предпочтительно, в изобретении предлагается соединение формулы (I), где
- R4 представляет собой циклопропил;
- R1, R2, R3, R5, R6, R7, R8, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, А, X, Z, x и у определяются как для соединения формулы (I) согласно изобретению.
Предпочтительно, в изобретении предлагается соединение формулы (I), где
- R4 представляет собой трет-бутил;
- R1 и R6 одновременно представляют собой атом водорода;
R2, R3, R5, R7, R8, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, А, X, Z, x и у определяются как для соединения формулы (I) согласно изобретению.
В изобретении предлагаются соединения, содержащие 6-членный карбоцикл, причем указанные соединения имеют структуру согласно формуле (I):
где:
- R1 и R6, незамещенные или замещенные, по меньшей мере, одним Т1, идентичные или различные, независимо представляют собой атом водорода; -CN; -OH; -CF3; атом галогена; линейный или разветвленный C1-C8 алкил; линейный или разветвленный C2-C8 алкенил; линейный или разветвленный C2-C8 алкинил; -Z-C(O)OR7; -Z-S(O)OR7; -Z-OC(O)OR7; -Z-OR8; -Z-SR8; -Z-NR7R8; -Z-OC(O)R8; -Z-C(O)R8; -Z-C(O)NR7R8; -Z-NR8C(O)R8; -Z-OC(O)NR7R8; -Z-NR8C(O)OR7; -Z-S(O)NR7R8; насыщенный, частично или полностью ненасыщенный или ароматический 3-, 4-, 5-, 6- или 7-членный карбоцикл; насыщенный, частично или полностью ненасыщенный или ароматический 3-, 4-, 5-, 6- или 7-членный карбоцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным карбоциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный карбоцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 4-, 5-, 6- или 7-членный гетероцикл; насыщенный, частично или полностью ненасыщенный или ароматический 4-, 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным карбоциклом; насыщенный, частично или полностью ненасыщенный или ароматический 4-, 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом.
- R2, незамещенный или замещенный, по меньшей мере, одним Т1, представляет собой линейный или разветвленный C2-C8 алкил; линейный или разветвленный C2-C8 алкенил; линейный или разветвленный C1-C8 гетероалкил; линейный или разветвленный C2-C8 гетероалкенил; а C3-C7 циклоалкил; частично ненасыщенный C4 карбоцикл; a C1-C8 алкил-(C3-C7 циклоалкил); C1-C8 гетероалкил-(C3-C7 циклоалкил); C1-C8 алкил-(частично или полностью ненасыщенный или ароматический C3-C7 карбоцикл); C1-C8 гетероалкил-(частично ненасыщенный C3-C7 карбоцикл); C4-C7 гетероциклоалкил; C1-C8 алкил-(C4-C7 гетероциклоалкил); C1-C8 гетероалкил-(C4-C7 гетероциклоалкил); C1-C8 алкил-(частично или полностью ненасыщенный или ароматический C4-C7 гетероцикл); C1-C8 гетероалкил-(частично или полностью ненасыщенный или ароматический C4-C7 гетероцикл);
- R3, незамещенный или замещенный, по меньшей мере, одним Т2, представляет собой насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный карбоцикл; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный карбоцикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6-или 7-членным карбоциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный карбоцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный углеродный цикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный углеродный цикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный углеродный цикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный углеродный цикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членный гетероциклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членный гетероциклом; насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6- или 7-членным гетероциклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом; или насыщенный, частично или полностью ненасыщенный или ароматический 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным углеродным циклом и дополнительно конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членным карбоциклом;
- R4, замещенный или незамещенный, по меньшей мере, одним Т3, представляет собой линейный или разветвленный C2-C6 алкил; линейный или разветвленный C1-C6 фторалкил или C3-C6 циклоалкил;
- R5 представляет собой атом галогена; -CF3; линейный или разветвленный C1-C6 алкил; линейный или разветвленный C2-C6 алкенил; линейный или разветвленный C2-C6 алкинил; линейный или разветвленный фторалкил; C3-C6 циклоалкил; -CH2OH; -CH2-O-CH3;
- R5 и R6 образуют с атомами углерода, к которым они присоединены, арил, или образуют с атомами углерода, к которым они присоединены, гетероарил, содержащий, по меньшей мере, один атом N;
- R7 и R8, идентичные или различные независимо представляют собой атом водорода; линейный или разветвленный C1-C8 алкил; линейный или разветвленный C2-C8 алкенил; линейный или разветвленный C2-C8 алкинил; линейный или разветвленный фторалкил; линейный или разветвленный фторалкенил; линейный или разветвленный фторалкинил; C3-C7 циклоалкил; C4-C7 гетероциклоалкил; частично или полностью ненасыщенный или ароматический C4-C7 карбоцикл; частично или полностью ненасыщенный или ароматический C5-C7 гетероцикл; C1-C8 алкил-(C3-C7 циклоалкил); C1-C8 алкил-(C4-C7 гетероциклоалкил); C1-C8 алкил-(частично или полностью ненасыщенный или ароматический C4-C7 карбоцикл); C1-C8 алкил-(частично или полностью ненасыщенный или ароматический C5-C7 гетероцикл);
- R7 и R8 образуют с атомом азота, с которым они связаны, частично или полностью ненасыщенный или ароматический 4-, 5-, 6- или 7-членный гетероцикл, содержащий, по меньшей мере, один атом N;
- Т1 независимо представляет собой атом галогена; алкил; -(Х)х-C1-C6 алкил; линейный или разветвленный фторалкил; линейный или разветвленный -O-C1-C3 фторалкил; -(Х)х-C3-C6 циклоалкил; -(Х)х-C4-C6 гетероцикл; -(Х)x-(СТ6Т7)yCN; -(Х)х-(СТ6Т7)уОТ4; -(X)x-(CT6T7)yST4; -(X)x-(CT6T7)yS(O)T4; -(X)x-(CT6T7)yS(O)2T4; -(Х)х-(CT6T7)yNT4T5; -(X)x-(CT6T7)yC(O)T4; -(X)x-(CT6T7)yC(O)OT4; -(X)x-(CT6T7)yC(O)NT4T5; -(X)x-(CT6T7)yNT4C(O)NT4T5; -(X)x-(CT6T7)yNT4C(O)T5; -(X)x-(CT6T7)yNT4C(O)OT5; -(X)x-(CT6T7)yOC(O)NT4T5; -(X)x-(CT6T7)y S(O)2NT4T5; -(X)x-(CT6T7)yNT4S(O)2T5;
- T2 независимо представляет собой атом галогена; линейный или разветвленный -O-(C1-C3 алкил); линейный или разветвленный C1-C3 фторалкил; линейный или разветвленный -O-(C1-C3 фторалкил; линейный или разветвленный C1-C3 алкил; C3-C6 циклоалкил; -CN;
- два геминальных Т2 образуют с атомом углерода, с которым они связаны, C3-C7 циклоалкил;
- Т3 независимо представляет собой линейный или разветвленный C1-C2 алкил; атом фтора;
- Т4 и Т5, идентичные или различные, независимо представляют собой атом водорода; разветвленный или линейный C1-C6 алкил; C3-C6 циклоалкил;
- Т4, Т5 и атом азота, с которым они связаны, образуют C4-C6 гетероциклоалкил;
- Т6 и Т7, идентичные или различные, независимо представляют собой атом водорода; атом фтора; линейный или разветвленный C1-C3 алкил; C3-C6 циклоалкил;
- Т6, Т7 и атом углерода, с которым они связаны, образуют C3-C6 циклоалкил;
- X независимо представляет собой атом кислорода; атом серы; NT3; S=O; или S(O)2;
- Z независимо представляет собой одинарную связь; линейный или разветвленный C2-C8 алкил;
- x представляет собой 0 или 1;
- y представляет собой 0, 1, 2 или 3;
и его рацемат, энантиомер, стереоизомер, атропизомер или диастереомер или фармацевтически приемлемую соль.
В изобретении также предлагаются соединени формулы (А), (В), (С), (D), (Е), (F), (G), (H), (J), (K) или(L):
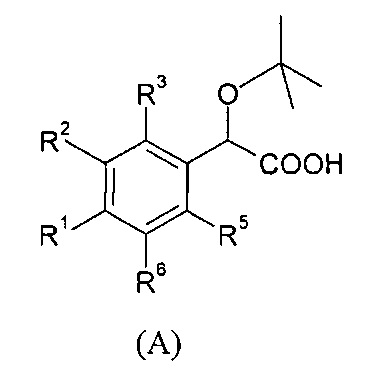

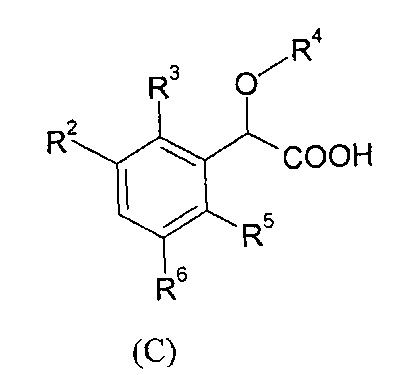

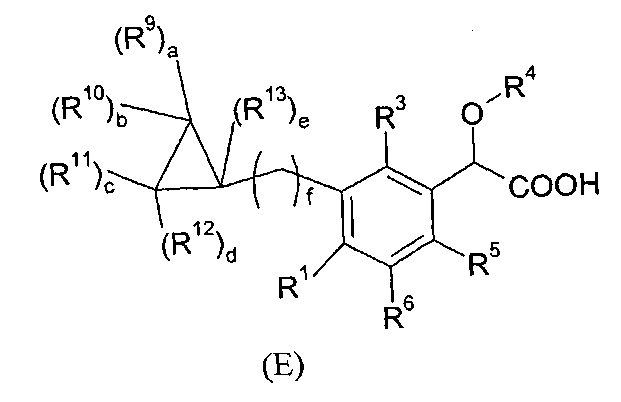

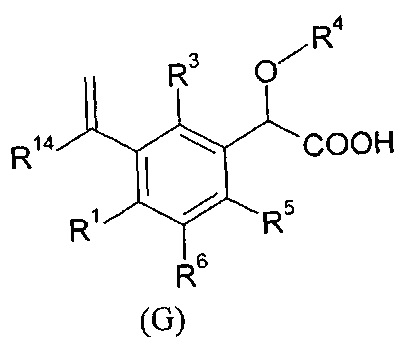




где
- R9, R10, R11, R12, R13, идентичные или различные, независимо представляют собой атом водорода; атом галогена; алкил; или C3-C6 циклоалкил;
- R15, R16, R17, R18, идентичные или различные, независимо представляют собой атом водорода; атом галогена; алкил; -(Х)х-C1-C6 алкил; линейный или разветвленный фторалкил; линейный или разветвленный -O-C1-C3 фторалкил; -(Х)x-C3-C6 циклоалкил; -(X)x-C4-C6 гетероцикл; -(Х)х-(СТ6Т7)у-арил; -(X)x-(CT6T7)yCN; -(Х)х-(СТ6Т7)уОТ4; -(X)x-(CT6T7)yST4; -(X)x-(CT6T7)yS(O)T4; -(X)x-(CT6T7)yS(O)2T4; -(Х)х-(CT6T7)yNT4T5; -(Х)х-(СТ6Т7)уС(O)Т4; -(Х)х-(СТ6Т7)уС(O)-(СТ6Т7)уОТ4; -(Х)x-(СТ6Т7)уС(O)ОТ4; -(X)x-(CT6T7)yC(O)NT4T5; -(X)x-(CT6T7)yNT4C(O)NT4T5; -(Х)х-(CT6T7)yNT4C(O)T5; -(X)x-(CT6T7)yNT4C(O)OT5; -(X)x-(CT6T7)yOC(O)NT4T5; -(X)x-(CT6T7)yS(O)2NT4T5; или -(X)x-(CT6T7)yNT4S(O)2T5;
- R14 представляет собой атом водорода; C3-C6 циклоалкил; или алкил;
- а, b, с, d, е, идентичные или различные, представляют собой 0 или 1;
- f представляет собой 1, 2, 3, 4, 5, или 6;
- R1, R2, R3, R4, R5, R6, R7, R8, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, X, Z, x и у определяются как для соединения формулы (I) согласно изобретению.
В другом воплощении, в изобретении также предлается соединение формулы (D), (Е), (F) или (G):



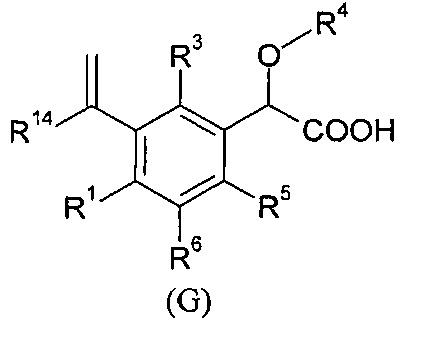
где
- R9, R10, R11, R12, R13, идентичные или различные, независимо представляют собой атом водорода; атом галогена; алкил; или C3-C6 циклоалкил;
- R14 представляет собой атом водорода; C3-C6 циклоалкил; или алкил;
- a, b, с, d, е, идентичные или различные, представляют собой 0 или 1;
- f представляет собой 1, 2, 3, 4, 5, или 6;
- R1, R2, R3, R4, R5, R6, R7, R8, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, X, Z, x и y определяются как для соединения формулы (I) согласно изобретению.
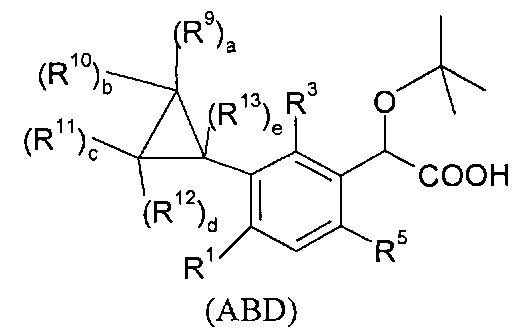
Предпочтительно, в изобретении предлагается соединение формулы (D):
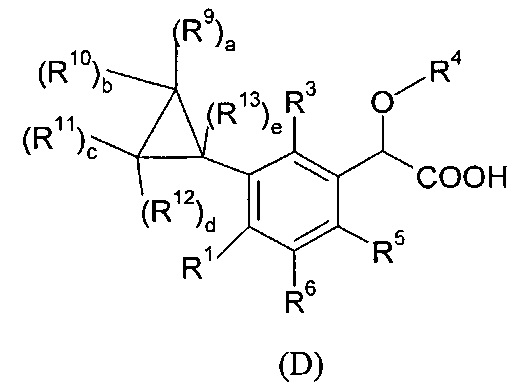
где
- R9, R10, R11, R12, R13, идентичные или различные, независимо представляют собой атом водорода; атом галогена; алкил; или C3-C6 циклоалкил;
- а, b, с, d, е, идентичные или различные, представляют собой 0 или 1;
- R1, R3, R4, R5, R6, R7, R8, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, X, Z, x и у определяются как для соединения формулы (I) согласно изобретению.
В изобретении также предлагается соединение формулы (DA), (ЕА), (FA) или (GA):
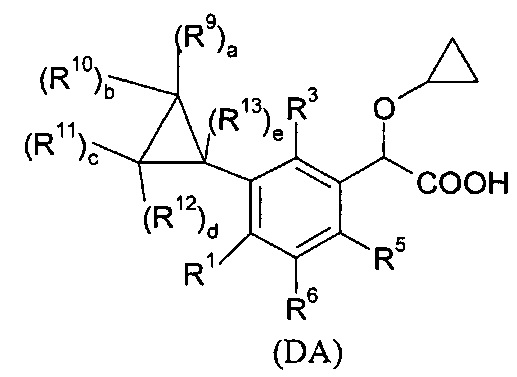
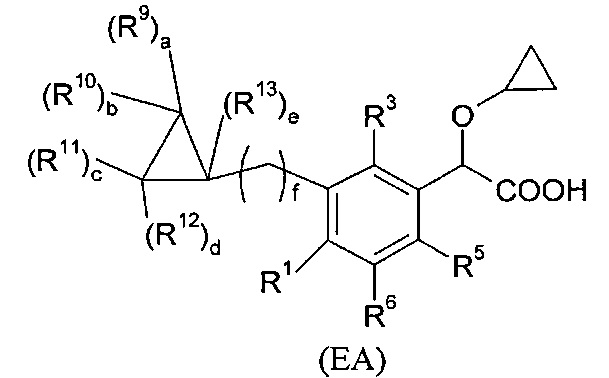

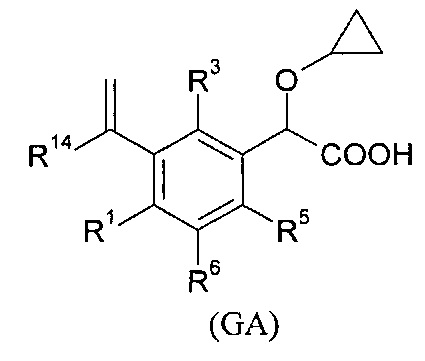
где
- R9, R10, R11, R12, R13, идентичные или различные, независимо представляют собой атом водорода; атом галогена; алкил; или C3-C6 циклоалкил;
- R14 представляет собой атом водорода; C3-C6 циклоалкил; или алкил;
- а, b, с, d, е, идентичные или различные, представляют собой 0 или 1;
- f представляет собой 1, 2, 3, 4, 5, или 6;
- R1, R2, R3, R5, R6, R7, R8, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, X, Z, x и у определяются как для соединения формулы (I) согласно изобретению.
В изобретении также предлагается соединение формулы (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (НА), (НС) или (HD):


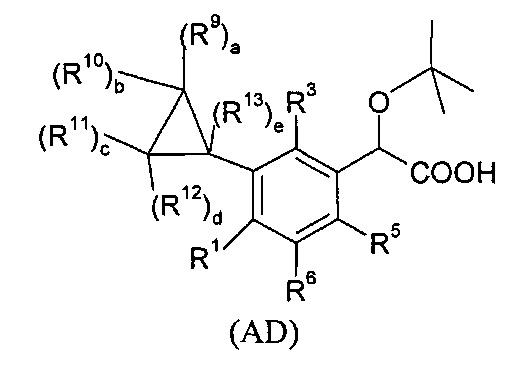


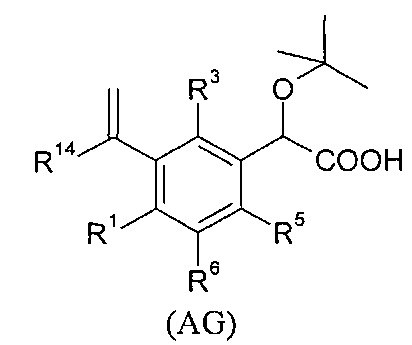





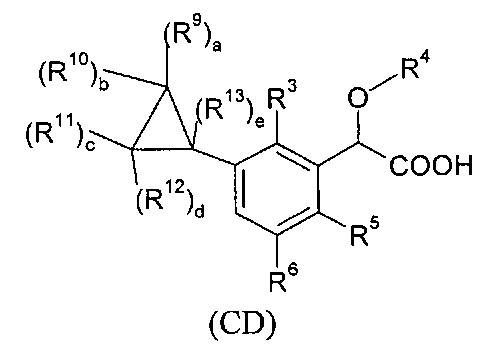



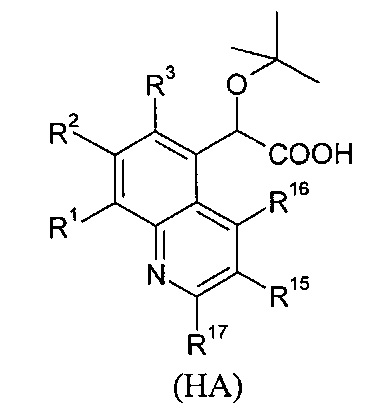
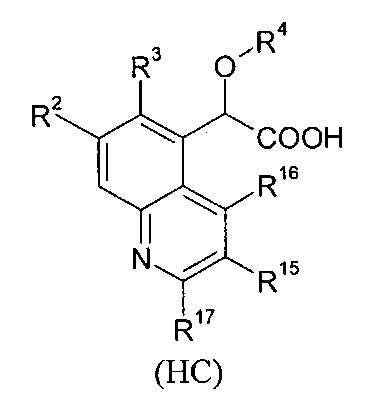
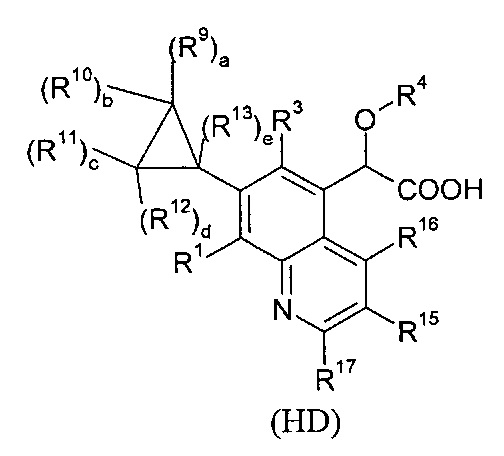
где
- R9, R10, R11, R12, R13, идентичные или различные, независимо представляют собой атом водорода; атом галогена; алкил; или C3-C6 циклоалкил;
- R15, R16, R17, идентичные или различные, независимо представляют собой атом водорода; атом галогена; алкил; -(Х)х-C1-C6 алкил; линейный или разветвленный фторалкил; линейный или разветвленный -О-C1-C3 фторалкил; -(Х)х-C3-C6 циклоалкил; -(Х)х-С4-С6 гетероцикл; -(Х)х-(СТ6Т7)у-арил; -(X)x-(CT6T7)yCN; -(Х)х-(СТ6Т7)уОТ4; -(Х)х-(CT6T7)yST4; -(X)x-(CT6T7)yS(O)T4; -(X)x-(CT6T7)yS(O)2T4; -(X)x-(CT6T7)yNT4T5; -(X)x-(CT6T7)yC(O)T4; -(X)x-(CT6T7)yC(O)-(CT6T7)yOT4; -(X)x-(CT6T7)yC(O)OT4; _(X)x-(CT6T7)yC(O)NT4T5; -(X)x-(CT6T7)yNT4C(O)NT4T5; -(X)x-(CT6T7)yNT4C(O)T5; -(X)x-(CT6T7)yNT4C(O)OT5; -(X)x-(CT6T7)yOC(O)NT4T5; -(X)x-(CT6T7)yS(O)2NT4T5; или
-(X)x-(CT6T7)yNT4S(O)2T5;
- R14 представляет собой атом водорода; С3-С6 циклоалкил; или алкил;
- а, b, с, d, е, идентичные или различные, представляют собой 0 или 1;
- f представляет собой 1, 2, 3, 4, 5, или 6;
- R1, R2, R3, R4, R5, R6, R7, R8, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, X, Z, x и у определяются как для соединения формулы (I) согласно изобретению.
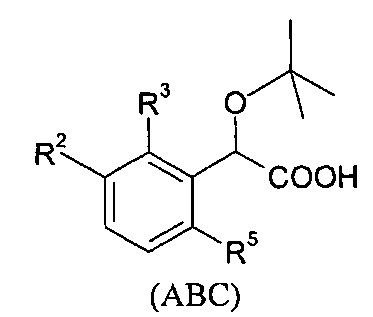
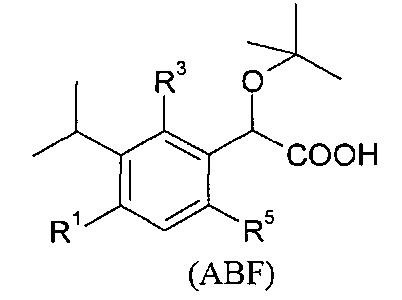
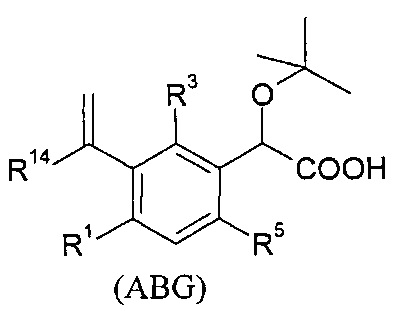
В изобретении также предлагаются соединения формулы (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (НАС) или (HAD):




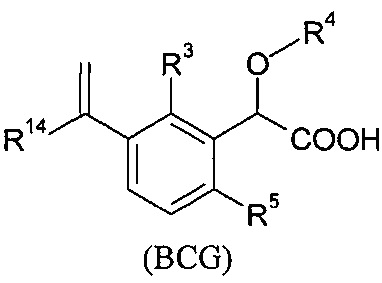
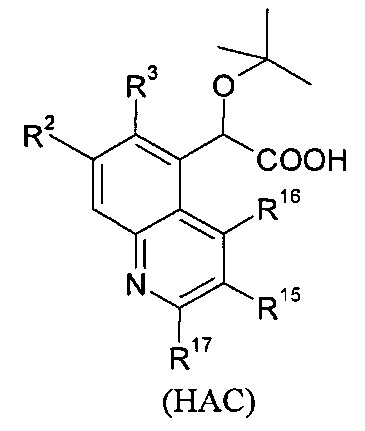
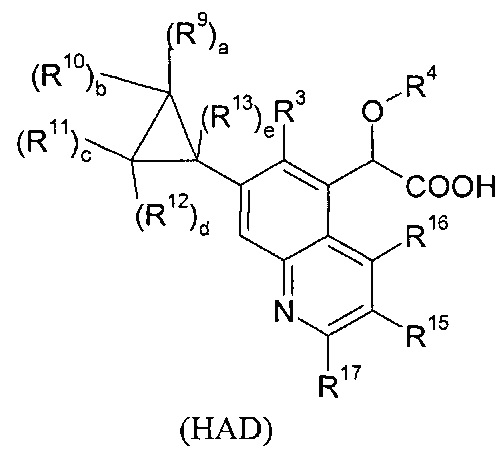
где
- R9, R10, R11, R12, R13, идентичные или различные, независимо представляют собой атом водорода; атом галогена; алкил; или С3-С6 циклоалкил;
- R15, R16, R17, когда они присутствуют в формуле идентичные или различные независимо представляют собой атом водорода; атом галогена; алкил; -(X)x-C1-C6 алкил; линейный или разветвленный фторалкил; линейный или разветвленный -О-С1-С3 фторалкил; -(Х)х-С3-С6 циклоалкил; -(Х)х-С4-С6 гетероцикл; -(Х)x-(СТ6Т7)у-арил; -(Х)х-(CT6T7)yCN; -(Х)х-(СТ6Т7)уОТ4; -(X)x-(CT6T7)yST4; -(X)x-(CT6T7)yS(O)T4; -(Х)х-(CT6T7)yS(O)2T4; -(X)x-(CT6T7)yNT4T5; -(X)x-(CT6T7)yC(O)T4; -(X)x-(CT6T7)yC(O)-(СТ6Т7)уОТ4; -(Х)х-(СТ6Т7)уС(O)ОТ4; -(X)x-(CT6T7)yC(O)NT4T5; -(Х)х-(CT6T7)yNT4C(O)NT4T5; -(X)x-(CT6T7)yNT4C(O)T5; -(X)x-(CT6T7)yNT4C(O)OT5; -(Х)х-(CT6T7)yOC(O)NT4T5; -(X)x-(CT6T7)yS(O)2NT4T5; или -(X)x-(CT6T7)yNT4S(O)2T5;
- R14 представляет собой атом водорода; С3-С6 циклоалкил; или алкил;
- а, b, с, d, е, когда они присутствуют в формуле, идентичные или различные независимо представляют собой 0 или 1;
- f представляет собой 1, 2, 3, 4, 5, или 6;
- R1, R2, R3, R4, R5, R6, R7, R8, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, X, Z, x и у определяются как для соединения формулы (I) согласно изобретению.
В изобретении также предлагаются соединения формулы (ABCD), (АБСЕ), (ABCF), (ABCG) или (HACD):
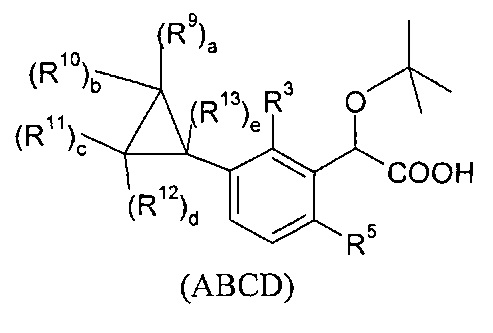



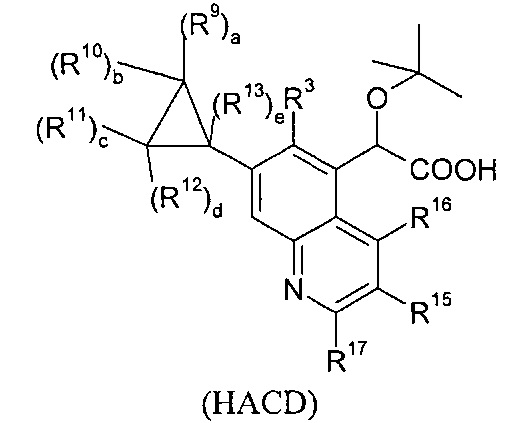
где
- R9, R10, R11, R12, R13, идентичные или различные, независимо представляют собой атом водорода; атом галогена; алкил; или С3-С6 циклоалкил;
- R15, R16, R17, идентичные или различные, независимо представляют собой атом водорода; атом галогена; алкил; -(X)x-C1-C6 алкил; линейный или разветвленный фторалкил; линейный или разветвленный -О-С1-C3 фторалкил; -(Х)х-С3-C6 циклоалкил; -(Х)х-С4-С6 гетероцикл; -(Х)х-(СТ6Т7)у-арил; -(X)x-(CT6T7)yCN; -(Х)х-(СТ6Т7)уОТ4; -(Х)x-(CT6T7)yST4; -(X)x-(CT6T7)yS(O)T4; -(X)x-(CT6T7)yS(O)2T4; -(X)x-(CT6T7)yNT4T5; -(X)x-(СТ6Т7)уС(O)Т4; -(X)x-(CT6T7)yC(O)-(CT6T7)yOT4; -(X)x-(CT6T7)yC(O)OT4; -(X)x-(CT6T7)yC(O)NT4T5; -(X)x-(CT6T7)yNT4C(O)NT4T5; -(X)x-(CT6T7)yNT4C(O)T5; -(X)x-(CT6T7)yNT4C(O)OT5; -(X)x-(CT6T7)yOC(O)NT4T5; -(X)x-(CT6T7)yS(O)2NT4T5; или -(X)x-(CT6T7)yNT4S(O)2T5;
- R14 представляет собой атом водорода; С3-С6 циклоалкил; или алкил;
- a, b, с, d, е, идентичные или различные, представляют собой 0 или 1;
- f представляет собой 1, 2, 3, 4, 5, или 6;
- R1, R2, R3, R4, R5, R6, R7, R8, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, X, Z, x и у определяются как для соединения формулы (I) согласно изобретению.
Предпочтительно, в изобретении предлагается соединение, выбранное из группы, состоящей из соединений формул (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (НА), (НС), (HD), (DA), (ЕА), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD), где
- R1 и R6, незамещенный или замещенный, по меньшей мере, одним Т1, идентичные или различные, независимо представляют собой атом водорода; -CN; -NH2; -OH; -CF3; -OCF3; -Z-OR8; Z-NR8SO2R8; -Z-NR8C(O)R8; -Z-NR7R8; атом галогена; линейный или разветвленный С1-С4 алкил; линейный или разветвленный C1-C4 фторалкил; линейный или разветвленный С1-С4 гетероалкил; линейный или разветвленный C2-C8 алкенил; линейный или разветвленный C2-C8 алкинил; С3-С4 циклоалкил; насыщенный, частично или полностью ненасыщенный или ароматический 3-, 4-, 5-, 6- или 7-членный углеродный цикл; насыщенный, частично или полностью ненасыщенный или ароматический 4-, 5-, 6-или 7-членный гетероцикл; или насыщенный, частично или полностью ненасыщенный или ароматический 4-, 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6-или 7-членным углеродным циклом; или
- R2, незамещенный или замещенный, по меньшей мере, одним Т1, представляет собой линейный или разветвленный C2-C8 алкил; линейный или разветвленный C2-C8 алкенил; линейный или разветвленный С1-С8 гетероалкил; С3-С7 циклоалкил; C1-C8 алкил-(С3-С7 циклоалкил); С4-С7 гетероциклоалкил; или C1-C8 алкил-(C4-C7 гетероциклоалкил); или
- R3, незамещенный или замещенный, по меньшей мере, одним Т2, когда он присутствует в формуле, представляет собой арил; гетероарил; частично ненасыщенный 5-, 6-, 7-членный углеродный цикл; насыщенный или частично ненасыщенный 5-, 6-, 7-членный гетероцикл; частично ненасыщенный 5-, 6, 7-членный углеродный цикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6-, 7-членным гетероциклом; насыщенный или частично ненасыщенный 5-, 6, 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6-, 7-членным углеродным циклом; арил, конденсированный с частично или полностью ненасыщенным или ароматическим 4-, 5-, 6-, 7-членным гетероциклом; или арил, конденсированный с 6-членным гетероарилом и конденсированный с частично или полностью ненасыщенным 6-членным гетероциклом; гетероарил, конденсированный с частично или полностью ненасыщенным или ароматическим 4-, 5-, 6-, 7-членным углеродным циклом; или
- R4, незамещенный или замещенный, по меньшей мере, одним Т3, представляет собой линейный или разветвленный С2-С4 алкил; линейный или разветвленный С2-С6 алкенил; линейный или разветвленный С2-С4 фторалкил; С3-С4 циклоалкил; или С1-С3 алкил-(С3-С6 циклоалкил); или
- R5 представляет собой -СН3; -CH2F; -CHF2; -CF3; -СН2ОН; или -СН2ОСН3;
или
- R5 и R6 могут образовывать с атомами углерода фенильного кольца формулы (I), с которыми они связаны, гетероарил, содержащий, по меньшей мере, один атом N; или
- А когда он присутствует в формуле, представляет собой -СН2; или -О;
- R7, R8, R9, R10, R11, R12, R13, R14, R15, R16, R17, R18, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, X, Z, а, b, с, d, е, f, x и у определяются как для соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K) или (L) согласно изобретению.
Предпочтительно, в изобретении предлагается соединение, выбранное из группы, состоящей из соединений формул (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (НА), (НС), (HD), (DA), (ЕА), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG), или (HACD), где
- R1 и R6, незамещенные или замещенные, по меньшей мере, одним Т1, идентичные или различные, независимо представляют собой атом водорода; -CN; -NH2; -ОН; -CF3; -OCF3; Z-NR8SO2R8; -Z-NR8C(O)R8; -Z-NR7R8; атом галогена; линейный или разветвленный С1-С4 алкил; линейный или разветвленный С1-С4 фторалкил; линейный или разветвленный C2-C8 алкенил; линейный или разветвленный C2-C8 алкинил; линейный или разветвленный С1-С4 гетероалкил; С3-С4 циклоалкил; насыщенный, частично или полностью ненасыщенный или ароматический 3-, 4-, 5-, 6- или 7-членный карбоцикл; насыщенный, частично или полностью ненасыщенный или ароматический 4-, 5-, 6- или 7-членный гетероцикл; или насыщенный, частично или полностью ненасыщенный или ароматический 4-, 5-, 6- или 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 3-, 4-, 5-, 6- или 7-членный карбоциклом; и R2, незамещенный или замещенный, по меньшей мере, одним Т1, представляет собой линейный или разветвленный C2-C8 алкил; линейный или разветвленный С2-C8 алкенил; линейный или разветвленный C1-C8 гетероалкил; С3-С7 циклоалкил; C1-C8 алкил-(С3-С7 циклоалкил); С4-С7 гетероциклоалкил; или C1-C8 алкил-(С4-С7 гетероциклоалкил); и
- R3, незамещенный или замещенный, по меньшей мере, одним Т2, когда он присутствует в формуле, представляет собой арил; гетероарил; частично ненасыщенный 5-, 6-, 7-членный карбоцикл; насыщенный или частично ненасыщенный 5-, 6-, 7-членный гетероцикл; частично ненасыщенный 5-, 6, 7-членный карбоцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6-, 7-членным гетероциклом; насыщенный или частично ненасыщенный 5-, 6, 7-членный гетероцикл, конденсированный с насыщенным, частично или полностью ненасыщенным или ароматическим 4-, 5-, 6-, 7-членным карбоциклом; арил, конденсированный с частично или полностью ненасыщенным или ароматическим 4-, 5-, 6-, 7-членным гетероциклом; или арил, конденсированный с 6-членным гетероарилом и конденсированный с частично или полностью ненасыщенным 6-членным гетероциклом; гетероарил, конденсированный с частично или полностью ненасыщенным или ароматическим 4-, 5-, 6-, 7-членным карбоциклом; и
- R4, незамещенный или замещенный, по меньшей мере, одним Т3, представляет собой линейный или разветвленный С2-С4 алкил; линейный или разветвленный С2-С6 алкенил; линейный или разветвленный С2-С4 фторалкил; С3-С4 циклоалкил; или С1-С3 алкил-(С3-С6 циклоалкил); и
- R5 представляет собой -СН3; -CH2F; -CHF2; -CF3; -СН2ОН; или -СН2ОСН3; и
- R5 и R6 могут образовывать с атомами углерода фенильного кольца формулы (I), с которыми они связаны, гетероарил, содержащий, по меньшей мере, один атом N; и
- А когда он присутствует в формуле, представляет собой -СН2; или -О;
- R7, R8, R9, R10, R11, R12, R13, R14, R15, R16, R17, R18, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, X, Z, а, b, с, d, е, f, x и y определяются как для соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K) или (L) согласно изобретению.
Более предпочтительно, в изобретении предлагается соединение, выбранное из группы, состоящей из соединений формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (НА), (НС), (HD), (DA), (ЕА), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD), где
- R1 и R6, незамещенные или замещенные, по меньшей мере, одним Т1, идентичные или различные, независимо представляют собой атом водорода; метил; этил; метокси; метансульфонамид; фенил; ацетамид; N,N-диметиламин; N-метил-N-гидроксиэтиламин; циклогексилметилсульфониламин; или бензимидазолил; или
- R2, незамещенный или замещенный, по меньшей мере, одним Т1, представляет собой циклопропил; циклобутил; циклопентил; изопропил; изопропенил; метокси; метиленциклопропил; этил; этиленил; пропил; или
- R4, незамещенные или замещенные, по меньшей мере, одним Т3, представляет собой трет-бутил; этил; пропил; пропенил; уиклопропил; метиленциклопропил; 2,2,2-трифторэтил; изопропил; циклобутил; 2, 2-дифторэтил; или 2-фторэтил; или
- R5 представляет собой -СН3; или -CF3; или
- А представляет собой -СН2; или -О;
- R3, R7, R8, R9, R10, R11, R12, R13, R14, R15, R16, R17, R18, T1, T2, T3, T4, T5, T6, T7, T8, X, Z, a, b, c, d, e, f, x и y определяются как для соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K) или (L) согласно изобретению.
Более предпочтительно, в изобретении предлагается соединение, выбранное из группы, состоящей из соединений формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (НА), (НС), (HD), (DA), (ЕА), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD), где
- R1 и R6, незамещенные или замещенные, по меньшей мере, одним Т1, идентичные или различные, независимо представляют собой атом водорода; метил; этил; метокси; метансульфонамид; фенил; ацетамид; N,N-диметиламин; N-метил-N-гидроксиэтиламин; циклогексилметилсульфонамин; или бензимидазолил; и
- R2, незамещенный или замещенный, по меньшей мере, одним Т1, представляет собой циклопропил; циклобутил; циклопентил; изопропил; изопропенил; метокси; метиленциклопропил; этил; этиленил; пропил; и
- R4, незамещенные или замещенные, по меньшей мере, одним Т3, представляет собой трет-бутил; этил; пропил; пропенил; уиклопропил; метиленциклопропил; 2,2,2-трифторэтил; изопропил; циклобутил; 2, 2-дифторэтил; или 2-фторэтил; и
- R5 представляет собой -СН3; или -CF3; и
- А представляет собой -СН2; или -О;
- R3, R7, R8, R9, R10, R11, R12, R13, R14, R15, R16, R17, R18, Т1, Т2, Т3, Т4, Т5, Т6, Т7, Т8, X, Z, a, b, с, d, е, f, x и y определяются как для соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K) или (L) согласно изобретению.
В качестве примера соединений формулы (АВ), в изобретении предлагается соединение:
- 2-[4-(1H-1,3-бензодиазол-2-у1)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-метокси-6-(трифторметил)фенил]-2-(трет-бутокси)уксусная кислота.
В качестве примеров соединений формулы (ABC), в изобретении предлагаются соединения, выбранные из группы, состоящей из:
- 2-(трет-бутокси)-2-[3-(циклопентил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусная кислота;
- 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-этил-6-(трифторметил)фенил]уксусная кислота;
- -трет-бутокси-(2-хроман-6-ил-3-циклобутил-6-метил-фенил)-уксусная кислота.
В качестве примеров соединений формулы (ABCD), в изобретении предлагаются соединения, выбранные из группы, состоящей из:
- 2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]уксусная кислота;
- 2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусная кислота;
- 2-(трет-бутокси)-2-[3-циклопропил-2-(2,3-дигидроругапо[4,3,2-de]хинолин-7-ил)-6-метилфенил]уксусная кислота;
- 2-(трет-бутокси)-2-(6-циклопропил-4'-метокси-3-метил-бифенил-2-ил]уксусная кислота;
- (S)-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]уксусная кислота;
- 2-(трет-бутокси)-2-(6-циклопропил-3,4'-диметил-бифенил-2-ил)-уксусная кислота;
- 2-(трет-бутокси)-2-(6-циклопропил-4'-фтор-3-метил-бифенил-2-ил)-уксусная кислота;
- 2-(трет-бутокси)-2-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил]уксусная кислота;
- (trans-3-бициклопропил-2-ил-2-хроман-6-ил-6-метил-фенил)-трет-бутокси-уксусная кислота;
- 2-(трет-бутокси)-2-[3-циклопропил-2-(4,4-диметил-циклогекс-1-енил)-6-метил-фенил] уксусная кислота;
- 2-(трет-бутокси)-2-(4'-хлор-6-циклопропил-3-метил-бифенил-2-ил) уксусная кислота;
- трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-уксусная кислота;
- трет-бутокси-[2-хроман-6-ил-6-метил-3-(1-метил-циклопропил)-фенил]-уксусная кислота;
- трет-бутокси-[2-хроман-6-ил-6-метил-3-(cis-2-метил-циклопропил)-фенил]-уксусная кислота;
- (S)-трет-бутокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил]-уксусная кислота;
- (S)-трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-уксусная кислота.
В качестве примера соединений формулы (АБСЕ), в изобретении предлагается соединение:
- трет-бутокси-(2-хроман-6-ил-3-циклопропилметил-6-метил-фенил)-уксусная кислота.
В качестве примеров соединений формулы (ABCF), в изобретении предлагаются соединения, выбранные из группы, состоящей из:
- 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-1зоргору1-6-метилфенил]уксусная кислота;
- 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(пропан-2-ил)-6-(трифторметил)фенил]уксусная кислота.
В качестве примеров соединений формулы (ABCG), в изобретении предлагаются соединения, выбранные из группы, состоящей из:
- 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропенил-6-метилфенил]уксусная кислота;
- 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(проп-1-ен-2-ил)-6-(трифторметил)фенил] уксусная кислота;
- 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-этенил-6-(трифторметил)фенил]уксусная кислота.
В качестве примера соединений формулы (ВС), в изобретении предлагается соединение:
- 2-хроман-6-ил-6-метил-3-пропил-фенил)-изопропокси-уксусная кислота.
В качестве примеров соединений формулы (BCD), в изобретении предлагаются соединения, выбранные из группы, состоящей из:
- 2-(2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-этокси-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-пропокси-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропил метокси-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2,2-трифтор-этокси)-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклобутокси-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-этокси)-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2-фтор-этокси)-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-изопропокси-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(1-метил-циклопропокси)-уксусная кислота;
- 2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]пент-4-еновая кислота.
В качестве примеров соединений формулы (DA), в изобретении предлагаются соединения, выбранные из группы, состоящей из:
- 2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиуксусная кислота;
- (S)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиуксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-циклопропоксиуксусная кислота;
- циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил]-уксусная кислота;
- циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-уксусная кислота;
- (S)-циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил]-уксусная кислота;
- (S)-циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-циклопропокси)-уксусная кислота;
- 2-[2-хроман-6-ил-3-циклопропил-5-(метансульфонамид)-6-метил-фенил]-2-(циклопропокси)уксусная кислота;
- 2-(5-ацетамид-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси)уксусная кислота;
- 2-[2-хроман-6-ил-3-циклопропил-5-(диметиламин)-6-метил-фенил]-2-(циклопропокси)уксусная кислота;
- 2-[2-хроман-6-ил-3-циклопропил-5-[2-гидроксиэтил(метил)амин]-6-метил-фенил]-2-(циклопропокси)уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-4-метансульфониламин-6-метил-фенил)-циклопропокси-уксусная кислота;
- (4-ацетиламин-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропокси-уксусная кислота;
- (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-циклопропокси-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-4-этил-6-метил-фенил)-циклопропокси-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-4-метокси-6-метил-фенил)-циклопропокси-уксусная кислота;
- 2-(2-хроман-6-ил-3-циклопропил-5-этил-6-метил-фенил)-2-(циклопропокси)уксусная кислота;
- 2-(2-хроман-6-ил-3-циклопропил-5-этил-6-метил-фенил)-2-(циклопропокси)уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-4,6-диметил-фенил)-циклопропокси-уксусная кислота;
- 2-[2-хроман-6-ил-5-(циклогексилметилсульфониламин)-3-циклопропил-6-метил-фенил]-2-(циклопропокси)уксусная кислота.
В качестве примера соединений формулы (HACD), в изобретении предлагается соединение:
- трет-бутокси-(6-хроман-6-ил-7-циклопропил-хинолин-5-ил)-уксусная кислота.
В качестве примеров соединений формулы (I), в изобретении предлагаются соединения, выбранные из группы, состоящей из:
- 3-циклопропил-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]пропановая кислота;
- 2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]-4-метилпентановая кислота.
Более предпочтительно, в изобретении предлагаются соединения, выбранные из группы, состоящей из:
- 2-[4-(1Н-1,3-бензодиазол-2-ил)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-метокси-6-(трифторметил)фенил]-2-(трет-бутокси)уксусная кислота;
- 2-(трет-бутокси)-2-[3-(циклопентил)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусная кислота;
- 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-(проп-1-ен-2-ил)-6-(трифторметил)фенил]уксусная кислота;
- 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-этенил-6-(трифторметил)фенил]уксусная кислота;
- 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-этил-6-(трифторметил)фенил]уксусная кислота;
- трет-бутокси-(2-хроман-6-ил-3 -циклобутил-6-метил-фенил)-уксусная кислота;
- 2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]уксусная кислота;
- 2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусная кислота;
- 2-(трет-бутокси)-2-[3-циклопропил-2-(2,3-дигидропиран[4,3,2-de]хинолин-7-ил)-6-метилфенил] уксусная кислота;
- 2-(трет-бутокси)-2-(6-циклопропил-4'-метокси-3-метил-бифенил-2-ил]уксусная кислота;
- (S)-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]уксусная кислота;
- 2-(трет-бутокси)-2-(6-циклопропил-3,4'-диметил-бифенил-2-ил)-уксусная кислота;
- 2-(трет-бутокси)-2-(6-циклопропил-4'-фтор-3-метил-бифенил-2-ил)-уксусная кислота;
- 2-(трет-бутокси)-2-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил]уксусная кислота;
- (trans-3-бициклопропил-2-ил-2-хроман-6-ил-6-метил-фенил)-трет-бутокси-уксусная кислота;
- 2-(трет-6утокся)-2-[3-циклопропил-2-(4,4-диметил-циклогекс-1-енил)-6-метил-фенил]уксусная кислота;
- 2-(трет-бутокси)-2-(4'-хлор-6-циклопропил-3-метил-бифенил-2-ил)уксусная кислота;
- трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-уксусная кислота;
- трет-бутокси-[2-хроман-6-ил-6-метил-3-(1-метил-циклопропил)-фенил]-уксусная кислота;
- трет-бутокси-[2-хроман-6-ил-6-метил-3-(cis-2-метил-циклопропил)-фенил]-уксусная кислота;
- (S)-трет-бутокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил]-уксусная кислота;
- (S)-трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-уксусная кислота;
- трет-бутокси-(2-хроман-6-ил-3-циклопропилметил-6-метил-фенил)-уксусная кислота;
- 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропил-6-метилфенил]уксусная кислота;
- 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(пропан-2-ил)-6-(трифторметил)фенил]уксусная кислота;
- 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропенил-6-метилфенил]уксусная кислота;
- 2-хроман-6-ил-6-метил-3-пропил-фенил)-изопропокси-уксусная кислота;
- 2-(2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-этокси-уксусная кислота;
- 2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиуксусная кислота;
- (S)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиуксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-пропокси-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропил метокси-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2,2-трифтор-этокси)-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклобутокси-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-этокси)-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2-фтор-этокси)-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-изопропокси-уксусная кислота;
- циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(1-метил-циклопропокси)-уксусная кислота;
- (S)-циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил]-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-циклопропокси-уксусная кислота;
- циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил]-уксусная кислота;
- (S)-циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-циклопропокси)-уксусная кислота;
- 2-[2-хроман-6-ил-3-циклопропил-5-(метансульфонамид)-6-метил-фенил]-2-(циклопропокси)уксусная кислота;
- 2-(5-ацетамид-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси)уксусная кислота;
- 2-[2-хроман-6-ил-3-циклопропил-5-(диметиламин)-6-метил-фенил]-2-(циклопропокси)уксусная кислота;
- 2-[2-хроман-6-ил-3-циклопропил-5-[2-гидроксиэтил(метил)амин]-6-метил-фенил]-2-(циклопропокси)уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-4-метансульфониламин-6-метил-фенил)-циклопропокси-уксусная кислота;
- (4-ацетиламин-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропокси-уксусная кислота;
- (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-циклопропокси-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-4-этил-6-метил-фенил)-циклопропокси-уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-4-метокси-6-метил-фенил)-циклопропокси-уксусная кислота;
- 2-(2-хроман-6-ил-3-циклопропил-5-этил-6-метил-фенил)-2-(циклопропокси)уксусная кислота;
- 2-(2-хроман-6-ил-3-циклопропил-5-этил-6-метил-фенил)-2-(циклопропокси)уксусная кислота;
- (2-хроман-6-ил-3-циклопропил-4,6-диметил-фенил)-циклопропокси-уксусная кислота;
- 2-[2-хроман-6-ил-5-(циклогексилметилсульфониламин)-3-циклопропил-6-метил-фенил]-2-(циклопропокси)уксусная кислота;
- трет-бутокси-(6-хроман-6-ил-7-циклопропил-хинолин-5-ил)-уксусная кислота;
- 3-циклопропил-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]пропановая кислота;
- 2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]-4-метилпентановая кислота;
- 2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]пент-4-еновая кислота.
Во втором аспекте, в изобретении также предлагается способ получения соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (НА), (НС), (HD), (DA), (ЕА), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG), или (HACD). Специалист в данной области способен получить соединение формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD), например, с помощью заявки или адаптации способов, описанных в предыдущем уровне техники, или с помощью их вариаций, понятных специалисту в данной области. Подходящие модификации и замены будут очевидны и хорошо известны специалисту в данной области или могут быть легко получены из научной литературы специалистами в данной области. После получения соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (H), (J), (K), (L), (АВ), (AC), (AD), (AE), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (CE), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD), специалист в данной области будет способен извлечь соединение формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (AE), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (CE), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) в их чистых формах из реакционной смеси с помощью стандартных средств. Например, соединения могут быть извлечены с помощью отгонки растворителя из реакционной смеси или, если необходимо, после отгонки растворителя из реакционной смеси, насыпания остатка в воду с последующей экстракцией с использованием несмешивающегося с водой органического растворителя и отгонки растворителя из экстракта. Кроме того, если целесообразно, то соединение формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (AE), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (CE), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) может быть дополнительно очищено с помощью различных хорошо известных способов, таких как перекристаллизация, переосаждение или различные хроматографические методы, главным образом, колоночная хроматография или препаративная тонкослойная хроматография. Кроме того, соединение формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (AE), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (CE), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) может содержать один или несколько асимметрично замещенных атомов углерода. Специалист в данной области также способен выделить оптически активные или рацемические формы соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (AE), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (CE), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) путем использования хорошо известных и стандартных методов. Например, смеси стереоизомеров могут быть разделены с помощью стандартных методов, включающих в частности разрешение рацемических форм, нормальная, с обращенной фазой и хиральная хроматография, предпочтительное солеобразование, перекристаллизация и тому подобное, или с помощью синтеза или из исходного материала с хиральными центрами или с помощью синтеза целевых хиральных центров.
В третьем аспекте, в изобретении предлагается фармацевтическая композиция, содержащая соединение формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (НА), (НС), (HD), (DA), (ЕА), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) в качестве активного ингредиента и, по меньшей мере, один фармацевтически приемлемый носитель.
Фармацевтическая композиция согласно изобретению может быть получена в целевой форме с помощью любого из хорошо известных методов в области фармацевтики, например, как описано в Remington: The Science and Practice of Pharmacy, 20th ed.; Gennaro, A.R., Ed.; Lippincott Williams & Wilkins: Philadelphia, PA, 2000.
Предпочтительная композиция, в которой соединение формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) согласно изобретению, составлено для перорального или парентерального введения.
Для перорального введения, фармацевтическая композиция представлена в форме таблеток, пилюлей, порошков, капсул, лепешек, пастилок или подобных.
Другие формы для перорального введения фармацевтических композиций выбирают среди сиропа, эликсира или раствора.
Для парентерального введения фармацевтическая композиция представлена в форме стерильных водных или не водных растворов, суспензий или эмульсий.
Предпочтительная дозировка для введения соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) в фармацевтической композиции согласно изобретению, вероятно зависит от таких параметров как тип и степень прогрессии вирусной инфекции, главным образом, ВИЧ-инфекции или родственных заболеваний, общее состояние здоровья конкретного пациента, относительная биологическая эффективность выбранного соединения, состав соединения, путь введения, фармакокинетические свойства соединения с выбранным путем доставки и скорость (болюсная или непрерывная инфузия) и график введения (количество повторов в данный период времени).
В данном воплощении, фармацевтическая композиция в твердой форме для перорального введения обычно составлена в одной дозе, и фармацевтическая композиция согласно изобретению обеспечивает от около 1 до 1000 мг соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (НА), (НС), (HD), (DA), (ЕА), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) согласно изобретению на одну дозу. Некоторые примеры дозировок соответствуют 1 мг, 10 мг, 100 мг, 250 мг, 500 мг и 1000 мг.
В данном воплощении, фармацевтическая композиция в жидкой форме для перорального и/или парентерального введения обычно составлена в одной дозе от около 1 до 100 мг/мл соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) согласно изобретению на одну дозу в день. Некоторые примеры дозировок соответствуют 1 мг/мл, 10 мг/мл, 25 мг/мл, 50 мг/мл и 100 мг/мл.
В данном воплощении, фармацевтическая композиция может дополнительно включать, по меньшей мере, еще один антивирусный агент. Антивирусный агент выбирают среди соединений формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) отличающихся от соединений формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD), которые вводят вместе с антивирусным агентом; ингибитором каталитического сайта интегразы ВИЧ, таким как ралтегравир (ISENTRESS®; Merck), элвитегравир (Gilead), солтегравир (долутегравир, GSK; ViiV) и GSK 1265744 (GSK; ViiV); ингибитором нуклеозидной обратной транскриптазы ВИЧ, таким как абакавир (ZIAGEN®; GSK), диданозин (VIDEX®; BMS), тенофовир (VIREAD®; Gilead), эмтриситабин (EMTRIVA®; Gilead), ламивудин (EPIVIR®; GSK/Shire), ставудин (ZERIT®; BMS), зидовудин (RETROVIR®; GSK), элвуситабин (Achillion), фестинавир (Oncolys); ингибитором ненуклеозидной обратной транскриптазы ВИЧ, таким как невипарин (VIRAMUNE®; BI), эфавиренц (SUSTIVA®; BMS), этравирин (INTELENCE®; J&J), рилпивирин ТМС278, R278474; J&J), фосдевирин (GSK/ViiV), лерсивирин (Pfizer/ViiV); ингибитором протеазы ВИЧ, таким как атазанавир (REYATAZ®; BMS), дарунавир (PREZISTA®; J&J), индинавир (CRIXIVAN®; Merck), лопинавир (KELETRA®; Abbott), нелфинавир (VIRACEPT®; Pfizer), саквинавир (INVIRASE®; Hoffmann-LaRoche), типранавир (APTIYUS®; BI), ритонавир (NORVIR®; Abbott), фосампренавир (LEXIVA®; GSK/Vertex); ингибитором входа ВИЧ, таким как маравирок (SELZENTRY®; Pfizer), энфувиртид (FUZEON®; Trimeris), BMS-663038 (BMS); ингибитором созревания ВИЧ, таким как бевиримат (Myriad Genetics).
Как правило, по меньшей мере, один дополнительный антивирусный агент будет присутствовать в интервале доз, аналогичном для агентов такого класса, используемых в терапии. Обычно это соответствует 0,25-1000 мг на одну дозу, когда фармацевтическая композиция согласно изобретению представлена в твердой форме для перорального введения. Обычно, это соответствует 1-100 мг/мл на одну дозу, когда фармацевтическая композиция согласно изобретению представлена в жидкой форме для перорального и/или парентерального введения.
В четвертом аспекте, в изобретении предлагается применение соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF); (BG), (CD), (СЕ), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) в качестве лекарственного средства для предотвращения или лечения вирусной инфекции или родственных заболеваний, предпочтительно, для предотвращения или лечения ретровирусной инфекции или родственных заболеваний, более предпочтительно, для предотвращения или лечения ВИЧ-инфекции или родственных заболеваний.
В пятом аспекте в изобретении предлагается способ лечения или предотвращения вирусной инфекции или родственных заболеваний, предпочтительно ретровирусной инфекции или родственных заболеваний и, более предпочтительно, ВИЧ-инфекции или родственных заболеваний у пациента, причем способ включает введение терапевтически эффективного количества соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) или его рацемата, энантиомера, стереоизомера, атрооизомера или диастереомера или фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем.
В пятом аспекте в изобретении предлагается способ лечения или предотвращения вирусной инфекции или родственных заболеваний, предпочтительно ретровирусной инфекции или родственных заболеваний и, более предпочтительно, ВИЧ-инфекции или родственных заболеваний у пациента, причем способ включает введение терапевтически эффективного количества соединения формулы (I), (А), (В), (С), (D), (Е), (F), (G), (Н), (J), (K), (L), (АВ), (AC), (AD), (АЕ), (AF), (AG), (ВС), (BD), (BE), (BF), (BG), (CD), (СЕ), (CF), (CG), (HA), (HC), (HD), (DA), (EA), (FA), (GA), (ABC), (ABD), (ABE), (ABF), (ABG), (BCD), (ВСЕ), (BCF), (BCG), (HAD), (НАС), (ABCD), (ABCE), (ABCF), (ABCG) или (HACD) или его рацемата, энантиомера, стереоизомера, атрооизомера или диастереомера или фармацевтически приемлемой соли в комбинации с терапевтически эффективным количеством, по меньшей мере, одного антивирусного агента, как описано выше, вместе с фармацевтически приемлемым носителем.
Осуществление изобретения
Примеры
Следующие примеры приведены для иллюстрации настоящего изобретения и не должны интерпретироваться как ограничивающие рамки настоящего изобретения.
Первая часть представляет получение соединений (интермедиатов и конечных соединений), тогда как вторая часть описывает оценку антивирусной активности соединений согласно изобретению.
Получение соединений
Сокращения и символы, используемые в данном документе, включают:
ДМСО: диметилсульфоксид
МС: Масс-спектрометрия
ЯМР: Ядерная Магнитно-Резонансная Спектроскопия с: синглет
уш. с: уширенный синглет
д: дублет
т: триплет
к: квадруплет
дд: двойной дублет
ддд: двойной дублет дублетов
дт: двойной триплет
м: массив
ТСХ: Тонкослойная Хроматография
Пример 1: синтез 2-(трет-бутокси)-2-[3-циклопропил-2-[3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]уксусной кислоты

Стадия 1: получение промежуточного соединения 2-бром-4-метоксиметокси-1-метил-бензола (1а)
К раствору 3-бром-4-метилфенола (3,87 г, 20,7 ммоль) в безводном дихлорметане (40 мл) в атмосфере азота при 0°C постепенно добавляли диизопропилэтиламин (5,4 мл, 31 ммоль) и хлорметил-метиловый эфир (2 мл, 26,9 ммоль). Смесь встряхивали при 0°C в течение 3 часов перед добавлением воды (40 мл). Слои разделяли и водную фазу экстрагировали с использованием дихлорметана (40 мл). Объединенные органические слои промывали с использованием 2 М раствора гидроксида натрия (30 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением 2-бром-4-метоксиметокси-1-метил-бензола (1а) (4,55 г, 19,7 ммоль, 95%) в виде желтого масла.
1Н ЯМР (400 МГц, CDCl3) δ 2,33 (с, 3Н), 3,46 (с, 3Н), 5,13 (с, 2Н), 6,89 (дд, J=2,4 Гц, J=8.4 Гц, 1Н), 7,12 (д, J=8,4 Гц, 1Н), 7,25 (д, J=2,4 Гц, 1Н).
Стадия 2: получение промежуточного соединения 5-метоксиметокси-2-метил-бензальдегида (1b)
К раствору 2-бром-4-метоксиметокси-1-метил-бензола (1а) (4,54 г, 19,6 ммоль) в безводном (100 мл) в атмосфере азота при -78°C по каплям добавляли 1,6 М раствор n-бутиллития в гексане (15,3 мл, 24,5 ммоль). Смесь встряхивали при -78°C в течение 30 минут и добавляли N,N-диметилформамид (2,3 мл, 29,7 ммоль). Через 30 минут при -78°C добавляли воду (100 мл). Слои разделяли. Водный слой экстрагировали этилацетатом (2×50 мл). Объединенные органические слои промывали с использованием солевого раствора (50 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением 5-метоксиметокси-2-метил-бензальдегида (1b) (3,29 г, 18,2 ммоль, 93%) в виде желтого масла.
1Н ЯМР (300 МГц, CDCl3) δ, 60 (с, 3Н), 3,48 (с, 3Н), 5,20 (с, 2Н), 7,14-7,20 (м, 2Н), 7,47 (с, 1Н), 10,24 (с, 1Н).
Стадия 3: получение промежуточного соединения 2-бром-метоксиметокси-6-метил-бензальдегида (1с)
К раствору N,N',N-триметилэтилендиамина (2,6 мл, 20 ммоль) в безводном толуоле (30 мл) в атмосфере азота при -0°C по каплям добавляли 1,6 М раствор n-бутиллития в гексане (12 мл, 19,2 ммоль). Смесь встряхивали при комнатной температуре в течение 15 минут перед добавлением раствора 5-метоксиметокси-2-метил-бензальдегида (1b) (3,28 г, 18,2 ммоль) в безводном толуоле (10 мл). Через 15 минут при комнатной температуре смесь охлаждали на ледяной бане, и добавляли по каплям 1,8 М раствор фениллития в дибутиловом эфире (30 мл, 54 ммоль). Смесь встряхивали при комнатной температуре в течение ночи. Добавляли безводный (50 мл) к полученной суспензии и смесь охлаждали при -78°C. Добавляли по частям дибромтетрахлорэтан (17,8 г, 54,6 ммоль). Смесь встряхивали при комнатной температуре в течение 90 минут перед добавлением воды (100 мл). Слои разделяли. Водный слой экстрагировали этилацетатом (2×100 мл). Объединенные органические слои промывали с использованием 1 М хлорводородной кислоты (100 мл), солевого раствора (100 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (дихлорметан/этилацетат: 30/70) с получением 2-бром-3-метоксиметокси-6-метил-бензальдегида (1с) (2,78 г, 10,7 ммоль, 59%) в виде твердого желтого вещества.
1H ЯМР (300 МГц, CDCl3) δ 2,50 (с, 3Н), 3,53 (с, 3Н), 5,25 (с, 2Н), 7,13 (д, J=8,4 Гц, 1Н), 7,23 (д, J=8,4 Гц, 1H), 10,55 (с, 1Н).
MS m/z ([М+Н]+) 259 / 261.
Стадия 4: получение промежуточного соединения 2-(2-бром-3-метоксиметокси-6-метилфенил)-2-триметилсиланилокси-ацетонитрила (1d)
К раствору 2-бром-3-метоксиметокси-6-метил-бензальдегида (1с) (2,78 г, 10,7 ммоль) в безводном дихлорметане (40 мл) при 0°C в атмосфере азота постепенно добавляли иодид цинка (685 мг, 2,15 ммоль) и триметилсилилцианид (2 мл, 16,1 ммоль). Смесь встряхивали при 0°C в течение 90 минут перед добавлением насыщенного раствора гидрокарбоната натрия (40 мл). Слои разделяли. Водный слой экстрагировали дихлорметаном (40 мл). Объединенные органические слои сушили над сульфатом натрия и концентрировали в вакууме с получением 2-(2-бром-3-метоксиметокси-6-метил-фенил)-2-триметилсиланилокси-ацетонитрила (1d) (3,78 г, 10,5 ммоль, 98%) в виде желтого масла.
1H ЯМР (300 МГц, CDCl3) δ 0,20 (с, 9Н), 2,61 (с, 3Н), 3,51 (с, 3Н), 5,22 (с, 2Н), 6,40 (с, 1Н), 7,08 (д, J=8,4 Гц, 1Н), 7,13 (д, 7=8,4 Гц, 1H).
Стадия 5: получение промежуточного соединения метил-2-(2-бром-3-гидрокси-6-метилфенил)-2-гидроксиацетата (1е)
К раствору 2-(2-бром-3-метоксиметокси-6-метил-фенил)-2-триметилсиланилокси-ацетонитрила (1d) (3,78 г, 10,5 ммоль) в безводном метаноле (50 мл) при 0°C в атмосфере азота по каплям добавляли серную кислоту (23 мл). Смесь нагревали в колбе с обратным холодильником в течение ночи, и затем охлаждали при комнатной температуре и приливали к воде (150 мл). Водные слои экстрагировали диэтиловым эфиром (2×50 мл) и затем этилацетатом (2×50 мл). Объединенные органические слои промывали с использованием насыщенного раствора гидрокарбоната натрия (100 мл), солевого раствора (100 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением метил-2-(2-бром-3-гидрокси-6-метил-фенил)-2-гидроксиацетата (1е) (2,58 г, 9,38 ммоль, 89%) в виде коричневого масла.
1Н ЯМР (300 МГц, CDCl3) δ 2,33 (с, 3Н), 3,43 (д, J=3,6 Гц, 1H), 3,79 (с, 3Н), 5,56 (с, 1Н), 5,72 (д, J=3,6 Гц, 1Н), 6,93 (д, J=8,4 Гц, 1H), 7,04 (д, J=8,4 Гц, 1Н).
Стадия 6: получение промежуточного соединения метил 2-(3-бензилокси-2-бром-6-метилфенил)-2-гидроксиацетата (1f)
К раствору метил-2-(2-бром-3-гидрокси-6-метил-фенил)-2-гидроксиацетата (1е) (2,58 г, 9,38 ммоль) в ацетоне (50 мл) постепенно добавляли карбонат цезия (3,67 г, 11,25 ммоль) бензил бромид (1,23 мл, 10,32 ммоль) и раствор иодида натрия (281 мг, 1,88 ммоль). Смесь нагревали в колбе с обратным холодильником в течение 45 минут и затем концентрировали в вакууме. К остатку добавляли воду (50 мл). Водный слой экстрагировали этилацетатом (2×50 мл). Объединенные органические слои промывали с использованием 2М раствора гидроксида натрия (30 мл), солевого раствора (30 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этил ацетат: 80/20) с получением метил-2-(3-бензилокси-2-бром-6-метилфенил)-2-гидроксиацетата (1f) (2,38 г, 6,51 ммоль, 69%) в виде твердого белого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 2,34 (с, 3Н), 3,49 (д, J=4,4 Гц, 1H), 3,78 (с, 3Н), 5,13 (с, 2Н), 5,86 (д, J=4,4 Гц, 1Н), 6,84 (д, J=8,4 Гц, 1H), 7,06 (д, J=8,4 Гц, 1Н), 7,30-7,34 (м, 1Н), 7,37-7,41 (м, 2Н), 7,47 (д, J=7,4 Гц, 2Н).
MS m/z ([M+H-H2O]+) 347/349.
Стадия 7: получение промежуточного соединения метил-2-[3-бензилокси-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]-2-гидроксиацетата (1g)
Для дегазации смеси метил-2-(3-бензилокси-2-бром-6-метилфенил)-2-гидроксиацетата (1f) (383 мг, 1,05 ммоль), карбоната натрия (333 мг, 3,15 ммоль), 6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)хромана (327 мг, 1,26 ммоль) в диоксане (4 мл) и в воде (0,8 мл) добавляли тетракис(трифенилфосфин) палладия (121 мг, 0,1 ммоль). Смесь нагревали при 120°C в течение ночи. Добавляли воду (10 мл). Водный слой экстрагировали этилацетатом (2×10 мл). Объединенные органические слои промывали с использованием солевого раствора (10 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат: 80/20) с получением метил-2-[3-бензилокси-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]-2-гидроксиацетата (1 г) (347 мг, 0,83 ммоль, 79%) в виде желтой пенки.
1Н ЯМР (300 МГц, CDCl3) δ 2,01-2,08 (м, 2Н), 2,26 и 2,28 (с, 3Н), 2,78-2,82 (м, 2Н), 3,09 и 3,11 (д, J=2,8 Гц, 1H), 3,70 и 3,72 (с, 3H), 4,21-4,26 (м, 2Н), 4,97 (с, 2Н), 5,26 (д, J=2,8 Гц, 1H), 6,81-6,89 (м, 2Н), 6,98-7,16 (м, 5Н), 7,22-7,30 (м, 3Н).
MS m/z ([M+H-H2O]+) 401.
Стадия 8: получение промежуточного соединения метил-2-(трет-бутокси)-2-[3-бензилокси-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]ацетата (1h)
К раствору метил-2-[3-бензилокси-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]-2-гидроксиацетата (1g) (347 мг, 0,83 ммоль) в трет-бутилацетате (7 мл) при 0°C добавляли перхлорную кислоту (0,45 мл). Смесь встряхивали при 0°C в течение 90 минут перед ее добавлением в насыщенный раствор гидрокарбоната натрия (20 мл). Слои разделяли, и водный слой экстрагировали этилацетатом (2×20 мл). Органические слои промывали с использованием солевого раствора, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат: 80/20) с получением промежуточного соединения метил-2-(трет-бутокси)-2-[3-бензилокси-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]ацетата (1h) (263 мг, 0,55 ммоль, 66%).
1Н ЯМР (300 МГц, CDCl3) δ 0,96 (с, 9Н), 2,00-2,09 (м, 2Н), 2,35 и 2,36 (с, 3Н), 2,72-2,82 (м, 2Н), 3,70 и 3,71 (с, 3Н), 4,22-4,26 (м, 2Н), 4,88-5,01 (м, 2Н), 5,16 и 5,18 (с, 1Н), 6,81-6,87 (м, 2Н), 6,99-7,29 (м, 8Н).
MS m/z ([M+Na]+) 497.
Стадия 9: получение промежуточного соединения метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил]ацетата (1i)
Суспензию метил-2-(трет-бутокси)-2-[3-бензилокси-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил ацетата (1h) (263 мг, 0,55 ммоль) и палладия на углеродном носителе (30 мг) в этилацетате (5 мл) встряхивали при комнатной температуре в атмосфере водорода в течение 36 часов. Смесь фильтровали через Millipore и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат: 80/20) с получением methyl 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил]ацетата (1i) (120 мг, 0,31 ммоль, 56%).
1Н ЯМР (300 МГц, CDCl3) δ 0,97 и 0,98 (с, 9Н), 2,01-2,09 (м, 2Н), 2,34 и 2,35 (с, 3Н), 2,71-2,86 (м, 2Н), 3,67 и 3,68 (с, 3Н), 4,24-4,27 (м, 2Н), 4,63 и 4,67 (с, 1H), 4,99 и 5,00 (с, 1H), 6,82-7,05 (м, 4Н), 7,12-7,19 (м, 1Н).
MS m/z ([M+Na]+) 407.
MS m/z ([M-H]-) 383.
Стадия 10: получение промежуточного соединения метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетата (1j)
К раствору метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил]ацетата (1i) (145 мг, 0,038 ммоль) в безводном дихлорметане (5 мл) в атмосфере азота при -78°C постепенно добавляли триэтиламин (158 μл, 1,136 ммоль), и трифторметансульфоновый ангидрид (79 μл, 0,47 моль). Смесь встряхивали при данной температуре в течение 1 часа перед добавлением воды (5 мл). Слои разделяли. Водный слой экстрагировали дихлорметаном (5 мл). Объединенные органические слои промывали с использованием насыщенного раствора гидрокарбоната натрия (5 мл), сушили над хлоридом натрия и концентрировали в вакууме с получением меткл-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетата (1j) (193 мг, 0,37 ммоль, 99%) в виде бесцветного масла.
1Н ЯМР (300 МГц, CDCl3) δ 0,95 и 0,96 (с, 9Н), 2,00-2,09 (м, 2Н), 2,43 и 2,45 (с, 3Н), 2,68-2,87 (м, 2Н), 3,70 и 3,71 (с, 3Н), 4,22-4,26 (м, 2Н), 5,11 и 5,13 (с, 1Н), 6,82-6,87 (м, 1H), 6,94-7,11 (м, 2Н), 7,15-7,21 (м, 2Н).
MS m/z ([М-Н]-) 515.
Стадия 11: получение промежуточного соединения метил-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]ацетата (1k)
Дегазированный раствор метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетата (1j) (50 мг, 0,096 ммоль), циклопропилбориновую кислоту (42 мг, 0,48 ммоль), бромид натрия (11 мг, 0,11 ммоль), моногидрат трехосновного фосфата калия (74 мг, 0,32 ммоль) и тетракис(трифенилфосфин) палладия (11 мг, 0,001 ммоль) в толуоле (1 мл) нагревали в микроволновой печи при 120°C в течение 4 часов. Добавляли (5 мл) воду. Водный слой экстрагировали этилацетатом (2×5 мл). Объединенные органические слои промывали с использованием насыщенного раствора гидрокарбоната натрия (5 мл), солевого раствора (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат: 90/10) с получением метил-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]ацетата (1k) (35 мг, 0,085 ммоль, 87%).
1Н ЯМР (300 МГц, CDCl3) δ 0,52-0,74 (м, 4Н), 0,98 (с, 9Н), 1,41-1,52 (м, 1Н), 1,99-2,10 (м, 2Н), 2,39 (с, 3Н), 2,67-2,87 (м, 2Н), 3,65 и 3,67 (с, 3Н), 4,22-4,26 (м, 2Н), 5,08 и 5,10 (с, 1H), 6,72-6,85 (м, 2Н), 6,94-7,10 (м, 3Н).
MS m/z ([M+Na]+) 431.
Стадия 12: получение 2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]уксусной кислоты (пример 1)
Смесь метил-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]ацетата (1k) (279 мг, 0,68 ммоль) и гидроксида лития (131 мг, 5,46 ммоль) в диоксане (4 мл) и воды (2 мл) нагревали при 110°C в течение 24 часов. Смесь концентрировали в вакууме. Воду (5 мл) добавляли к остатку, и смесь экстрагировали с использованием диэтилового эфира (2×10 мл). Водный слой подкисляли с использованием 1М хлороводородной кислоты до получения рН 3 и экстрагировали с использованием диэтилового эфира (2×10 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме с получением 2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]уксусной кислоты (пример 1) (247 мг, 0,63 ммоль, 91%) в виде белого твердого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 0,53-0,77 (м, 4Н), 1,00 (с, 9Н), 1,48-1,55 (м, 1Н), 2,00-2,08 (м, 2Н), 2,35 (с, 3Н), 2,70-2,87 (м, 2Н), 4,21-4,25 (м, 2Н), 5,22 (с, 1H), 6,75-6,86 (м, 2Н), 6,96-7,05 (м, 2Н), 7,23 (уш. с, 1Н).
MS m/z ([M-H]-)393.
Пример 2: синтез 2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусной кислоты
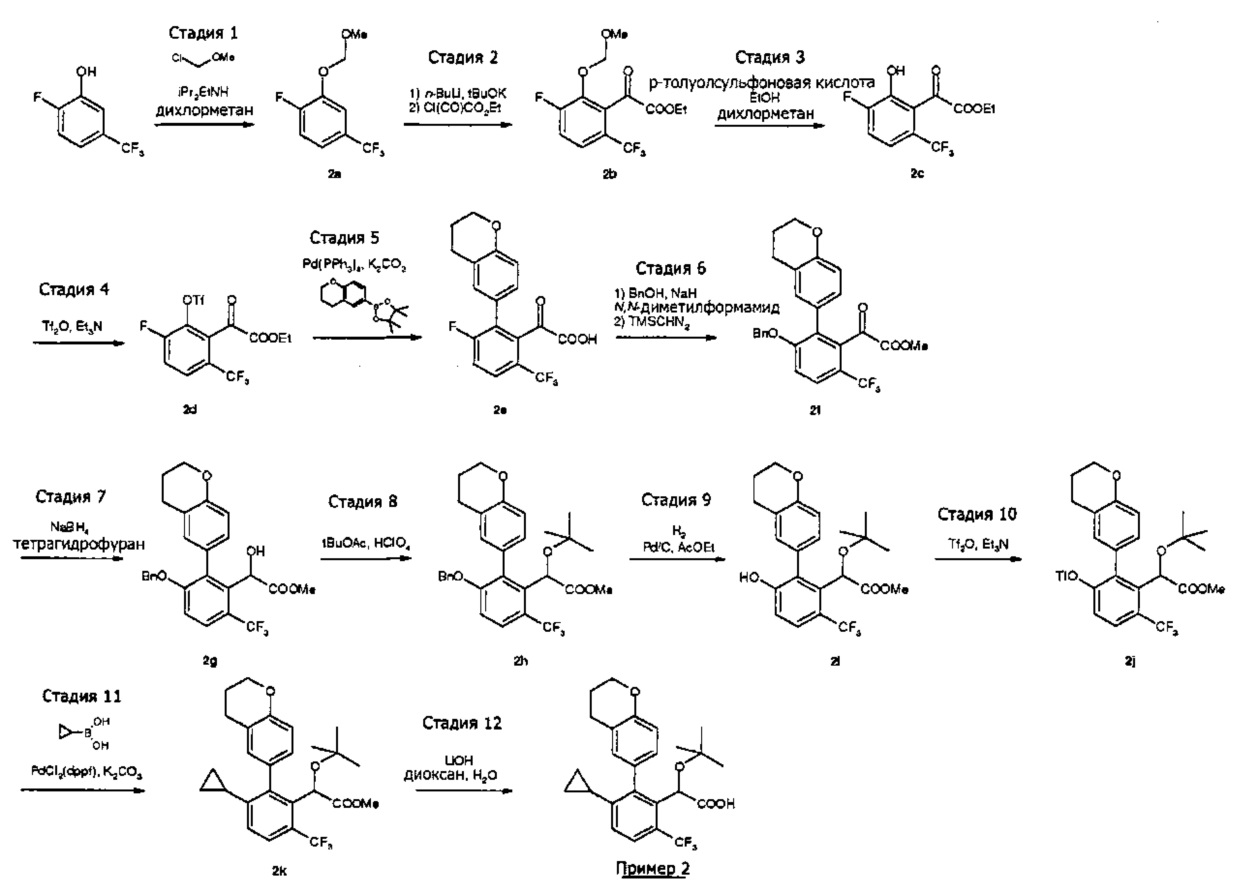
Стадия 1: получение промежуточного соединения 1-фтор-2-(метоксиметокси)-4-(трифторметил)-бензола (2а)
К раствору 2-фтор-5-(трифторметил)фенола (2 г, 11,1 ммоль) в безводном дихлорметане (20 мл) в атмосфере азота при 0°C постепенно добавляли диизопропилэтиламин (3,87 мл, 22,2 ммоль) и хлорметил-метиловый эфир (1,26 мл, 16,6 ммоль). Смесь встряхивали при 0°C в течение 45 минут перед добавлением воды (20 мл). Слои разделяли, и водный слой экстрагировали с использованием дихлорметана (30 мл). Объединенные органические слои промывали с использованием 2 М раствора гидроксида натрия (20 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением 1-фтор-2-(метоксиметокси)бензола (2а) (2,49 г, 11,1 ммоль, 100%) в виде светло желтого масла.
1Н ЯМР (400 МГц, CDCl3) δ 3,53 (с, 3Н), 5,25 (с, 2Н), 7,16-7,20 (м, 1H), 7,24-7,27 (м, 1Н), 7,46 (дд, J=1,8 Гц, J=7,4 Гц, 1Н).
Стадия 2: получение промежуточного соединения этил-2-[3-фтор-2-(метоксиметокси)-6-(трифторметил)фенил]-2-оксоацетата (2b)
В атмосфере азота добавляли 1,6 М раствор n-бутиллития в гексане (3,5 мл, 5,6 ммоль) и 1 М раствор трет-бутоксида в (5,6 мл, 5,6 ммоль) к безводному (30 мл) при -78°C. Смесь встряхивали в течение 15 минут перед добавлением по каплям раствора 1-фтор-2-(метоксиметокси)-4-(трифторметил)бензола (2а) (1 г, 4,46 ммоль) в (10 мл). Смесь встряхивали при -78°C в течение 2 часов и добавляли канюляцией к раствору этил оксалил хлорил (1,4 мл, 9 ммоль) в (20 мл) при -78°C. Смесь встряхивали при -78°C в течение 45 и добавляли воду (50 мл). Слои разделяли, и водный слой экстрагировали этилацетатом (2×30 мл). Объединенные органические слои промывали с использованием насыщенного раствора гидрокарбоната натрия (30 мл), солевого раствора (30 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат: 90/10) с получением этил-2-[3-фтор-2-(метоксиметокси)-6(трифторметил)фенил]-2-оксоацетата (840 мг, 2, 59 ммоль, 58%) (2b) в виде желтого масла.
1Н ЯМР (300 МГц, CDCl3) δ 1,36 (т, J=7,2 Гц, 3Н), 3,45 (с, 3Н), 4,38 (к, 7=7,2 Гц, 2Н), 5,16 (с, 2Н), 7,28-7,34 (м, 1Н), 7,43 (дд, J=4,4 Гц, 7=8,8 Гц, 1Н).
Стадия 3: получение промежуточного соединения этил-2-[3-фтор-2-гидрокси-6-(трифторметил)фенил]-2-оксоацетата (2с)
Раствору этил-2-[3-фтор-2-(метоксиметокси)-6-(трифторметил)фенил]-2-оксоацетата (2b) (500 мг, 1,54 ммоль) и p-толуолсульфоновой кислоты (59 мг, 0,31 ммоль) в дихлорметане (7,5 мл) и этанол (1,5 мл) нагревали при 50°C в течение ночи. Смесь концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат: 60/40) с получением этил-2-[3-фтор-2-гидрокси-6(трифторметил)фенил]-2-оксоацетата (2с) (394 мг, 1,4 ммоль, 91%) в виде желтого масла.
1Н ЯМР (300 МГц, CDCl3) δ 1,38 (т, J=7,2 Гц, 3Н), 4,38 (к, 7=7,2 Гц, 2Н), 6,91 (д, 7=2,7 Гц), 7,26-7,35 (м, 2Н).
Стадия 4: получение промежуточного соединения этил-2-{3-фтор-2-[(трифторметан)сульфонилокси]-6-(трифторметил)фенил]-2-оксоацетата (2d)
К раствору этил-2-[3-фтор-2-гидрокси-6-(трифторметил)фенил]-2-оксоацетата (394 мг, 1,41 ммоль) (2с) в безводном дихлорметане (5 мл) в атмосфере азота при -78°C постепенно добавляли триэтиламин (0,24 мл, 1,69 ммоль) и трифторметансульфоновый ангидрид (0,26 мл, 1,55 ммоль). Смесь встряхивали при -78°C в течение 45 минут перед добавлением воды (10 мл). Слои разделяли. Водный слой экстрагировали дихлорметаном (10 мл). Объединенные органические слои промывали с использованием насыщенного раствора гидрокарбоната натрия (10 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением этил-2-{3-фтор-2-[(трифторметан)сульфонилокси]-6-(трифторметил)фенил}-2-оксоацетата (2d) (548 мг, 1,32 ммоль, 94%) в виде желтого масла, которое использовали без дополнительной очистки.
1Н ЯМР (300 МГц, CDCl3) δ 1,37 (т, 7=7,2 Гц, 3Н), 4,42 (к, 7=7,2 Гц, 2Н), 7,55 (т, 7=8,7 Гц), 7,78 (дд, 7=4,5 Гц, 7=8,7 Гц, 1Н).
Стадия 5: получение промежуточного соединения 2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-фтор-6-(трифторметил)фенил]-2-оксоуксусной кислоты (2е)
Дегазированный раствор этил2-{3-фтор-2-[(трифторметан)сульфонилокси]-6-(трифторметил)фенил}-2-оксоацетата (2d) (8 г, 19,41 ммоль), карбонат калия (10,73 г, 77,63 ммоль), 6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)хроман (6,56 г, 25,23 ммоль) и тетракис(трифенилфосфин) палладия (2,24 г, 1,94 ммоль) в диоксане (167 мл) и воде (33,5 мл) нагревали при 85°C в течение 20 часов. Воду (30 мл) добавляли и реакционную смесь нагревали при 85°C в течение еще 1 часа. Добавляли воду (170 мл) и выпаривали диоксан в вакууме. Добавляли диэтиловый эфир (2×80 мл) и разделяли слои. Органический слой промывали с использованием насыщенного раствора гидрокарбоната натрия (170 мл). Объединенные водные слои подкисляли с использованием 2N хлороводородной кислоты до достижения рН 2, затем экстрагировали с помощью диэтилового эфира (2×170 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме с получением 2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-фтор-6-(трифторметил)фенил]-2-оксоуксусной кислоты (2е) (6,09 г, 16,54 ммоль, 85%) в виде органического масла, которое использовали без дополнительной очистки.
1Н ЯМР (300 МГц, CDCl3) δ 1,97-2,04 (м, 2Н), 2,77 (т, J=6,5 Гц, 2Н), 4,21 (т, J=5,2 Гц, 2Н), 6,81 (с, 1Н), 6,92 (м, 2Н), 7,39 (т, J=8,6 Гц, 1Н), 7,73 (дд, J=8,6, 4,8 Гц, 1H).
Стадия 6: получение промежуточного соединения метил-2-[3-бензилокси-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-оксоацетата (2f)
К суспензии гидрида натрия 60% в масле (340 мг, 14,2 ммоль) в безводном N,N-диметилформамиде (14 мл) при 0°C в атмосфере азота добавляли по каплям безводный бензиловый спирт (1,47 мл, 14,2 ммоль). Смесь встряхивали при комнатной температуре в течение 30 минут перед добавлением по каплям раствора 2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-фтор-6-(трифторметвил)фенил]-2-оксоуксусной кислоты (2е) (1,306 г, 3,55 ммоль) в безводном N,N-диметилформамиде (13 мл) при 0°C. Темнокрасную смесь встряхивали при 60°C в течение 3 часов. Темно-зеленый раствор охлаждали при 0°C и добавляли аккуратно воду (80 мл). Полученный в результате раствор экстрагировали с использованием диэтилового эфира (2×70 мл). Водную фазу подкисляли с использованием 1 М хлороводородной кислоты до получения рН 2, затем экстрагировали с использованием AcOEt (3×70 мл). Объединенные органические слои промывали с использованием солевого раствора (50 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток растворяли в толуоле и концентрировали. Остаток растворяли в циклогексане (41 мл) и добавляли метанол (20,5 мл) при 0°C и 2 М раствор триметилсилилдиазометана в диэтиловом эфире (4,4 мл, 8,87 ммоль). Смесь встряхивали при комнатной температуре в течение 30 минут перед добавлением уксусной кислоты (0,5 мл). Смесь концентрировали в вакууме. Остаток растворяли в этилацетате (120 мл), промывали с использованием насыщенного раствора гидрокарбоната натрия (120 мл), солевого раствора (120 мл), сушили над сульфатом натрия, концентрировали в вакууме и затем совместно выпаривали вместе с толуолом с получением метил 2-[3-(бензилокси)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-оксоацетата (2f) (1,31 г, 2,78 ммоль, 78%) в виде оранжевого масло, которое использовали без дополнительной очистки.
1Н ЯМР (300 МГц, CDCl3) δ 1,97-2,05 (м, 2Н), 2,75 (т, J=6,4 Гц, 2Н), 3,55 (с, 3H), 4,19-4,22 (м, 2Н), 5,15 (с, 2Н), 6,80 (д, J=8,4 Гц, 1Н), 6,85 (д, J=2,1 Гц, 1H), 6,99 (дд, J=2,1 Гц, J=8,4 Гц, 1Н), 7,11 (д, J=8,7 Гц, 1Н), 7,23-7,36 (м, 5Н), 7,65 (д, J=8,7 Гц, 1Н).
Стадия 7: получение промежуточного соединения метил-2-[3-бензилокси-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-гидроксиацетата (2g)
К раствору метил-2-[3-(бензилокси)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-оксоацетата (2f) (1,32 г, 2,81 ммоль) в е (44 мл) при 0°C добавляли по частям боргидрид натрия (159 мг, 4,21 ммоль). Смесь встряхивали при 0°C в течение 90 минут. Добавляли уксусную кислоту (0,5 мл) с последующим добавлением воды (60 мл). Полученный раствор экстрагировали этилацетатом (3×50 мл). Органический слой промывали с использованием солевого раствора (30 мл) и сушили над сульфатом натрия. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат 80/20) с получением метил-2-[3-(бензилокси)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-гидроксиацетата (2 г) (1,04 г, 2,20 ммоль, 78%).
1H ЯМР (300 МГц, CDCl3) δ 2,01-2,09 (м, 2Н), 2,75-2,82 (м, 2Н), 3,57 и 3,60 (2 с, 3H), 4,24 (т, J=5,1 Гц, 2Н), 5,07 (с, 2Н), 5,38 (уш. с, 1Н), 6,79-6,85 (м, 2Н), 6,97-7,14 (м, 4Н), 7,24-7,31 (м, 3H), 7,65 (д, J=8,7 Гц, 1Н).
Стадия 8: получение промежуточного соединения метил-2-[3-бензилокси-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-(трет-бутокси)ацетата (2h)
В атмосфере азота метил-2-[3-(бензилокси)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-гидроксиацетат (2 г) (5,36 г, 11,35 ммоль) растворяли в трет-бутилацетате (142 мл), охлаждали при 0°C и добавляли 70% перхлорную кислоту (2,94 мл, 34,04 ммоль). Смесь встряхивали при комнатной температуре в течение 2 часов. Реакционную смесь приливали к насыщенному раствору гидрокарбоната натрия. Смесь экстрагировали этилацетатом. Полученный органический слой промывали с использованием солевого раствора, сушили над сульфатом натрия и концентрировали в вакууме. Исходную смесь очищали с помощью DCVC (хроматография под вакуумом на сухой колонке, с использованием 250 мл силикагеля, циклогексан/этилацетата 100/0-60/40) с получением метил-2-[3-(бензилокси)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-(трет-бутокси)ацетата (2h) (3,58 г, 6,77 ммоль, 58%) в виде желтого масла.
1Н ЯМР (300 МГц, CDCl3) δ 0,99 и 1,36 и 1,37 (с, 9Н), 2,00-2,09 (м, 2Н), 2,70-2,85 (м, 2Н), 3,59 и 3,61 и 3,69 и 3,70 (с, 3H), 4,22-4,27 (м, 2Н), 5,00-5,41 (м, 3H), 6,81-7,32 (м, 9Н), 7,63-7,70 (м, 1Н),
Стадия 9: получение промежуточного соединения метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-гидрокси-6-(трифторметил)фенил]ацетата (2i)
Раствор метил-2-[3-(бензилокси)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-(трет-бутокси)ацетата (2h) (3,48 г, 6,57 ммоль) в этилацетате (130 мл) пропускали через H-Cube (0,8 мл/мин, полным H2 способом, 40°C). Полученный в результате раствор концентрировали в вакууме с получением метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-гидрокси-6-(трифторметил)фенил]ацетата (2i) (2,62 г, 5,97 ммоль, 91%) в виде белого твердого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 1,00 и 1,01 (с, 9Н), 2,05 (м, 2Н), 2,78 (м, 2Н), 3,66 (с, 3H), 4,25 (м, 2Н), 5,04 и 5,05 (с, 1H), 5,10 и 5,13 (с, 1H), 6,89-6,93 (м, 2Н), 6,99 (д, J=10,0 Гц, 1H), 7,08-7,11 (м, 1H), 7,62 (д, J=8,7 Гц, 1Н).
MS m/z ([М-Н]-) 437.
Стадия 10: получение промежуточного соединения метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-[(трифторметан)сульфонилокси-6-(трифторметил)фенил]ацетата (2j)
К раствору метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-гидрокси-6-(трифторметил)фенил]ацетата (2j) (1 г, 2,28 ммоль) в безводном дихлорметане (16 мл) в атмосфере азота при -78°C постепенно добавляли триэтиламин (0,95 мл, 6,84 ммоль), и трифторметансульфоновый ангидрид (0,48 мл, 2,85 моль). Бесцветный раствор встряхивали при -78°C в течение 45 минут перед добавлением воды (30 мл). Слои разделяли. Водные слои экстрагировали дихлорметаном (40 мл). Объединенные органические слои промывали с использованием насыщенного раствора гидрокарбоната натрия (30 мл), сушили над хлоридом натрия и концентрировали в вакууме с получением метш-2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-6ензопиран-6-ип)-3-[(трифторметан)сульфонилокси]-6-(трифторметил)фенил]ацетата (2j) (1,3 г, 2,28 ммоль, 100%) в виде оранжевого масла.
1Н ЯМР (300 МГц, CDCl3) δ 0,98 и 0,99 (с, 9Н), 1,98-2,10 (м, 2Н), 2,65-2,85 (м, 2Н), 3,70 (с, 3H), 4,20-4,28 (м, 2Н), 5,12 (с, 1H), 6,80-7,05 (м, 3H), 7,42 (д, J=8,7 Гц, 1H), 7,80 (д, J=8,7 Гц, 1H).
Стадия 11: получение промежуточного соединения метил-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил] ацетата (2k)
Дегазированный раствор метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-[(трифторметан)сульфонилокси]-6-(трифторметил)фенил] ацетата (2j) (50 мг, 0,088 ммоль), карбонат калия (36 мг, 0,263 ммоль), циклопропилборная кислота (38 мг, 0,438 ммоль) и комплекс [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) вместе с дихлорметаном (7 мг, 0,009 ммоль) в диметоксиэтане (1 мл) и воду (0,1 мл) нагревали в микроволновой печи при 120°C в течение 3 часов. Добавляли воду (5 мл). Водный слой экстрагировали этилацетатом (2×5 мл). Объединенные органические слои промывали с использованием насыщенного раствора гидрокарбоната натрия (5 мл), солевого раствора (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (дихлорметан/этилацетат: 90/10) затем второй раз (дихлорметан/циклогексан: 90/10) с получением метил-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил] ацетата (2k) (20 мг, 0,043 ммоль, 49%).
1Н ЯМР (400 МГц, CDCl3) δ 0,61-0,86 (м, 4Н), 1,00 (с, 9Н), 1,46-1,56 (м, 1Н), 1,98-2,11 (м, 2Н), 2,69-2,87 (м, 2Н), 3,65 и 3,67 (с, 3H), 4,21-4,26 (м, 2Н), 5,07 и 5,08 (с, 1Н), 6,81 и 6,83 (д, J=8,4 Гц, 1Н), 6,86-7,04 (м, 3H), 7,59 (д, J=8,3 Гц, 1H).
MS m/z ([M+Na]+) 485.
Стадия 12: получение 2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусной кислоты (пример 2)
С использованием процедуры, описанной в примере 1, стадия 12, метил 2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]ацетат (2k) (20 мг, 0,043 ммоль) превращают в 2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусную кислоту (пример 2) (10 мг, 0,022 ммоль, 52%).
1Н ЯМР (400 МГц, CDCl3) δ 0,59-0,90 (м, 4Н), 1,02 (с, 9Н), 1,48-1,57 (м, 1Н), 2,00-2,107 (м, 2Н), 2,73-2,89 (м, 2Н), 4,20-4,26 (м, 2Н), 5,20 (уш. с, 1H), 6,80-7,00 (м, 3H), 7,30 (уш. с, 1Н), 7,60 (д, J=8,3 Гц, 1Н).
MS m/z ([М-Н]-) 447.
Пример 3: синтез 2-(трет-бутокси)-2-[3-циклопропил-2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-6-метилфенил]уксусной кислоты

Стадия 1: получение промежуточного соединения (2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-борной кислоты (3а)
Колбу, содержащую 7-бром-2,3-дигидро-1-окса-6-аза-фенилен (600 мг, 2,40 ммоль, полученный согласно WO 2009/062289), трис(дибензилиден ацетон)дипалладий(0) (22 мг, 0,024 ммоль), ди(1-адамантил)-n-бутилфосфин (25,8 мг, 0,072 ммоль), бис[пинаколато]дибор (731 мг, 2,88 ммоль) и ацетат калия (706 мг, 7,20 ммоль) продували аргоном в течение 10 минут и затем добавляли дегазированный безводный диметилацетамид (2 мл). Полученную смесь встряхивали при 90°C в течение 4 часов. Смесь охлаждали до комнатной температуры и медленно добавляли воду (40 мл). Остаток фильтровали, промывали с помощью воды (20 мл) и толуола (10 мл), сушили в вакууме и растирали в порошок в диэтиловом эфире. Порошок растворяли в ацетонитриле, и затем раствор фильтровали на Millipore, и фильтрат концентрировали в вакууме с получением (2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-бориновой кислоты (3а) (301 мг, 1,39 ммоль, 58%).
1Н ЯМР (400 МГц, DMSO-d6 + D2O) δ 3,27 (т, 2Н, J=5,8 Гц), 4,44 (т, 2Н, J=5,8 Гц), 7,03 (д, J=7,8 Гц, 1H), 7,35 (д, J=4,5 Гц, 1Н), 8,16 (д, J=7,8 Гц, 1Н), 8,83 (д, J=4,5 Гц, 1Н).
Стадия 2: получение промежуточного соединения метил-2-(3-бензилокси-2-бром-6-метилфенил)-2-(трет-бутокси)-ацетата (3b)
К суспензии метил 2-(3-бензилокси-2-бром-6-метилфенил)-2-гидроксиацетата (1f) (500 мг, 1,37 ммоль) в трет-бутилацетате (14 мл) при 0°C добавляли серную кислоту (0,292 мл, 5,48 ммоль). Смесь встряхивали при комнатной температуре в течение 8 часов. Смесь разводили с использованием этилацетатом (50 мл), промывали с помощью насыщенного раствора гидрокарбоната натрия (50 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат: 90/10) с получением метил-2-(3-бензилокси-2-бром-6-метилфенил)-2-(трет-бутокси)-ацетата (3b) (469 мг, 1,11 ммоль, 81%) в виде твердого белого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 1,23 (с, 9Н), 2,36 (с, 3H), 3,68 (с, 3H), 5,12 (с, 2Н), 5,96 (с, 1H), 6,80 (д, J=8,4 Гц, 1Н), 7,01 (д, J=8,4 Гц, 1Н), 7,29-7,42 (м, 3H), 7,48-7,51 (м, 2Н).
Стадия 3: получение промежуточного соединения метил-2-[3-бензилокси-2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-6-метилфенил]-2-(трет-бутокси)ацетата (3с)
К дегазированной смеси метил-2-(3-бензилокси-2-бром-6-метилфенил)-2-(трет-бутокси)-ацетата (3b) (200 мг, 0,47 ммоль), карбоната калия (177 мг, 1,28 ммоль) и (2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-борной кислоты (133 мг, 0,62 ммоль) в диметоксиэтане (1,6 мл) и в воде (0,4 мл) добавляли тетракис(трифенилфосфин) палладия (55 мг, 0,05 ммоль). Смесь нагревали в микроволновой печи при 120°C в течение 90 минут. Добавляли воду (5 мл). Водный слой экстрагировали этилацетатом (2×5 мл). Объединенные органические слои промывали с использованием солевого раствора (10 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат: 70/30 до 50/50) с получением обоих изомеров (соотношение: 1/2) метил-2-[3-бензилокси-2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-6-метилфенил]-2-(трет-бутокси) (3с) (216 мг, 0,42 ммоль, 89%).
Основной изомер:
1Н ЯМР (400 МГц, CDCl3) δ 0,98 (с, 9Н), 2,53 (с, 3H), 3,22-3,36 (м, 2Н), 3,42 (с, 3H), 4,45-4,57 (м, 2Н), 4,83 (д, J=12,4 Гц, 1Н), 4,90 (д, J=12,4 Гц, 1Н), 5,00 (с, 1H), 6,79-6,82 (м, 2Н), 6,90 (д, J=8,3 Гц, 1Н), 7,02-7,12 (м, 5Н), 7,16 (д, J=8,4 Гц, 1Н), 7,44 (д, J=7,8 Гц, 1Н), 8,74 (д, J=4,3 Гц, 1H).
MS m/z ([M+H]+)512.
Минорный изомер:
1Н ЯМР (400 МГц, CDCl3) δ 0,93 (с, 9Н), 2,43 (с, 3H), 3,20-3,35 (м, 2Н), 3,70 (с, 3H), 4,44-4,55 (м, 2Н), 4,88 (с, 2Н), 5,15 (с, 1Н), 6,71 (д, J=7,4 Гц, 2Н), 6,89 (д, J=8,3 Гц, 1Н), 7,02-7,10 (м, 5Н), 7,15 (д, J=8,3 Гц, 1H), 7,69 (дд, J=7,8 Гц, J=0,9 Гц, 1Н), 8,73 (дд, J=4,3 Гц,.7=0,8 Гц, 1H).
MS m/z ([M+H]+)512.
Стадия 4: получение промежуточного соединения метил-2-(трет-бутокси)-2-[2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-3-гидрокси-6-метилфенил]ацетата (3d)
Смесь метил-2-[3-бензилокси-2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-6-метилфенил]-2-(трет-бутокси)ацетата (3с) (143 мг, 0,279 ммоль) и палладия на углеродном носителе (15 мг) в этилацетате встряхивали при комнатной температуре под давлением водорода 4 бар в течение 30 часов. Смесь фильтровали через Millipore и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат: 20/80) с получением метил-2-(трет-бутокси)-2-[2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-3-гидрокси-6-метилфенил]-ацетата (3d) (25 мг, 0,069 ммоль, 24%).
1Н ЯМР (400 МГц, CDCl3) δ 0,86 (с, 9Н), 2,48 (с, 3H), 3,22-3,38 (м, 2Н), 3,47 (с, 3H), 4,46-4,56 (м, 2Н), 4,94 (с, 1Н), 6,91 (д, J=8,2 Гц, 1Н), 7,04 (д, J=7,9 Гц, 1H), 7,11-7,13 (м, 2Н), 7,44 (д, J=7,9 Гц, 1Н), 8,78 (д, J=4,3 Гц, 1Н).
MS m/z ([М+Н]+) 422.
MS m/z ([М-Н]-) 420.
Стадия 5: получение промежуточного соединения метил-2-(трет-бутокси)-2-[2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетата (3е)
С использованием процедуры, описанной в примере 1, стадии 10, промежуточное соединение метил-2-(трет-бутокси)-2-[2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-3-гидрокси-6-метилфенил]ацетат (3d) (29 мг, 0,069 ммоль) превращается в метил 2-(трет-бутокси)-2-[2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетат (3е) (24 мг, 0,043 ммоль, 63%).
1Н ЯМР (400 МГц, CDCl3) δ 0,96 (с, 9Н), 2,62 (с, 3H), 3,22-3,35 (м, 2Н), 3,38 (с, 3H), 4,46-4,57 (м, 2Н), 5,02 (с, 1Н), 7,05 (д, J=7,9 Гц, 1Н), 7,09 (д, J=4,3 Гц, 1H), 7,23 (д, J=8,5 Гц, 1Н), 7,29 (д, J=8,5 Гц, 1Н), 7,47 (д, J=7,9 Гц, 1Н), 8,73 (д, J=4,3 Гц, 1Н).
MS m/z ([М+Н]+) 554.
Стадия 6: получение промежуточного соединения метил 2-(трет-бутокси)-2-[3-циклопропил-2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-6-метилфенил]ацетата (3f)
С использованием процедуры, описанной в примере 1, стадии 11, промежуточное соединение метил-2-(трет-бутокси)-2-[2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетат (3е) (24 мг, 0,043 ммоль) превращается после очистки с помощью препаративной ТСХ (циклогексан/этилацетат: 50/50) в метил 2-(трет-бутокси)-2-[3-циклопропил-2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-6-метилфенил]метил (3f) (6 мг, 0,013 ммоль, 30%).
1Н ЯМР (300 МГц, CDCl3) δ 0,26-0,36 (м, 3H), 0,59-0,66 (м, 1Н), 0,72 (с, 9Н), 1,13-1,23 (м, 1Н), 2,46 (с, 3H), 3,29 (т, J=5,8 Гц, 2Н), 3,64 (с, 3H), 4,52 (т, J=5,8 Гц, 2Н), 4,97 (с, 1H), 6,89 (д, J=7,9 Гц, 1Н), 7,04-7,08 (м, 2Н), 7,12 (д, J=7,9 Гц, 1Н), 7,62 (д, J=7,9 Гц, 1H), 8,75 (д, J=4,3 Гц, 1H).
MS m/z ([М+Н]+) 446.
Стадия 7: получение 2-(трет-бутокси)-2-[3-циклопропил-2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-6-метилфенил]уксусной кислоты (пример 3)
С использованием процедуры, описанной в примере 1, стадии 12, промежуточное соединение метил-2-(трет-бутокси)-2-[3-циклопропил-2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-6-метилфенил]ацетат (3f) (6 мг, 0,013 ммоль) превращается в 2-(трет-бутокси)-2-[3-циклопропил-2-(2,3-дигидропирано[4,3,2-de]хинолин-7-ил)-6-метилфенил]уксусную кислоту (пример 3) (4 мг, 0,009 ммоль, 66%) в виде твердого белого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 0,18-0,30 (м, 2Н), 0,34-0,42 (м, 1H), 0,62-0,68 (м, 1H), 0,81 (с, 9Н), 1,16-1,25 (м, 1Н), 2,40 (с, 3H), 3,29 (т, J=5,8 Гц, 2Н), 4,51 (т, J=5,8 Гц, 2Н), 5,16 (с, 1Н), 6,93 (д, J=7,9 Гц, 1H), 7,07-7,13 (м, 3H), 7,81 (д, J=7,5 Гц, 1Н), 8,74 (д, J=4,3 Гц, 1H).
MS m/z ([М+Н]+) 432.
MS m/z ([М-Н]-) 430.
Пример 4: синтез 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропенил-6-метилфенил]уксусной кислоты

Стадия 1: получение промежуточного соединения метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропенил-6-метилфенил]ацетата (4а)
Дегазированный раствор метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетата (1j) (100 мг, 0,193 ммоль), пинаколовый эфир изопропилбороновой кислоты (65 мг, 0,386 ммоль), карбонат калия (72 мг, 0,52 ммоль) и тетракис(трифенилфосфин) палладия (22 мг, 0,019 ммоль) в диоксане (1 мл) и воду (0,25 мл) нагревали в микроволновой печи при 110°C в течение 2 часов. Воду (5 мл) нагревали. Водный слой экстрагировали этилацетатом (2×5 мл). Объединенные органические слои промывали с использованием солевого раствора (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат: 90/10) с получением метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопренил-6-метилфенил]ацетата (4а) (53 мг, 0,13 ммоль, 67%).
1Н ЯМР (300 МГц, CDCl3) δ 0,93 (с, 9Н), 1,52 и 1,56 (с, 3H), 1,99-2,08 (м, 2Н), 2,41 и 2,42 (с, 3H), 2,63-2,82 (м, 2Н), 3,70 и 3,72 (с, 3H), 4,20-4,25 (м, 2Н), 4,76-4,80 (м, 1H), 4,88-4,91 (м, 1Н), 5,18 и 5,19 (с, 1H), 6,78 и 6,78 (д, J=8,3 Гц, 1H), 6,83-6,92 (м, 1Н), 7,05-7,14 (м, 3H).
MS m/z ([M+Na]+) 431.
Стадия 2: получение 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропенил-6-метилфенил]уксусной кислоты (пример 4)
С использованием процедуры, описанной в примере 1, стадия 12, промежуточное соединение метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропенил-6-метилфенил]ацетат (4а) (22 мг, 0,054 ммоль) превращали в 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропенил-6-метилфенил]уксусную кислоту (пример 4) (17 мг, 0,043 ммоль, 81%) в виде белого твердого. вещества.
1Н ЯМР (400 МГц, CDCl3) δ 0,95 (с, 9Н), 1,49 (с, 3H), 1,99-2,06 (м, 2Н), 2,38 (с, 3H), 2,65-2,81 (м, 2Н), 4,20-4,24 (м, 2Н), 4,79-4,83 (м, 1H), 4,90-4,93 (м, 1Н), 5,33 и 5,34 (с, 1H), 6,73 и 6,80 (д, J=8,3 Гц, 1Н), 6,85-6,93 (м, 1Н), 7,06-7,13 (м, 2Н), 7,29 (уш. с, 1Н).
MS m/z ([М-Н]-) 393.
Пример 5: синтез 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропил-6-метилфенил]уксусной кислоты

Стадия 1: получение промежуточного соединения метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропил-6-метилфенил]ацетата (5а)
Смесь метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропенил-6-метилфенил]ацетата (4а) (53 мг, 0,129 ммоль) и 10% палладия на углеродном носителе (17 мг) в метаноле (5 мл) встряхивали в атмосфере водорода в течение ночи. Смесь фильтровали на Millipore, и фильтрат концентрировали в вакууме с получением метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропил-6-метилфенил]ацетата (5а) (46 мг, 0,112 ммоль, 86%) в виде бесцветного масла.
1Н ЯМР (300 МГц, CDCl3) δ 0,99-1,02 (м, 12Н), 1,11 (д, J=6,9 Гц, 3H), 1,99-2,10 (м, 2Н), 2,41 (с, 3H), 2,58-2,87 (м, 3H), 3,63 и 3,66 (с, 3H), 4,22-4,26 (м, 2Н), 4,97 и 5,00 (с, 1H), 6,77-7,04 (м, 3H), 7,12 (д, J=8,0 Гц, 1Н), 7,20 (д, J=8,0 Гц, 1Н).
MS m/z ([M+Na]+) 433.
Стадия 2: получение 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропил-6-метилфенил]уксусной кислоты (пример 5)
С использованием процедуры, описанной в примере 1, стадия 12, промежуточное соединение метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропил-6-метилфенил]ацетат (5а) (46 мг, 0,112 ммоль) превращали в 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-изопропил-6-метил фенил]уксусную кислоту (пример 1) (44 мг, 0,112 ммоль, 100%) в виде белого твердого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 0,95-1,02 (м, 12Н), 1,14 (д, J=6,8 Гц, 3H), 1,99-2,08 (м, 2Н), 2,35 и 2,36 (с, 3H), 2,63-2,84 (м, 3H), 4,23 (т, J=5,1 Гц, 2Н), 5,12 (с, 1H), 6,78-6,91 (м, 2Н), 7,11 (д, J=8,0 Гц, 1Н), 7,17-7,23 (м, 2Н).
MS m/z ([М-Н]-) 395.
Пример 6: синтез 2-(трет-бутокси)-2-[3-(циклопентил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусной кислоты

Стадия 1: получение промежуточного соединения метил-2-(трет-бутокси)-2-[3-(циклопент-1-ен-1-ил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]ацетата (6а)
Дегазированный раствор промежуточного соединения метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-[(трифторметан)сульфонилокси]-6-(трифторметил) фенил]ацетат (2j) (120 мг, 0,21 ммоль), карбонат калия (116 мг, 0,841 ммоль), 1-циклопентеилбороновая кислота (28 мг, 0,252 ммоль) и тетракис(трифенилфосфин) палладия (24 мг, 0,021 ммоль) в диоксане (1,8 мл) и воду (0,4 мл) нагревали при 85°C в течение ночи. Добавляли воду (2 мл) и выпаривали диоксан в вакууме. Водный остаток экстрагировали с помощью этилацетата (3×4 мл). Объединенные органические слои промывали с использованием насыщенного раствора гидрокарбоната натрия (4 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали на препаративной ТСХ (циклогексан/этилацетат: 9/1) с получением ожидаемого метил-2-(трет-бутокси)-2-[3-(циклопент-1-ен-1-ил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил] ацетата (6а) (69 мг, 0,141 ммоль, 67%) в виде бесцветного масла.
1Н ЯМР (300 МГц, CDCl3) δ 0,95 (с, 9Н), 1,61-1,92 (м, 3H), 1,95-2,13 (м, 3H), 2,18-2,33 (м, 2Н), 2,64-2,84 (м, 2Н), 3,69 (с, 3H), 4,23 (т, J=5,2 Гц, 2Н), 5,14 и 5,16 (с, 1Н), 5,48-5,57 (м, 1Н), 6,71-6,85 (м, 2Н), 7,00-7,10 (м, 1Н), 7,34 (д, J=8,2 Гц, 1Н), 7,61 (д, J=8,2 Гц, 1Н).
Стадия 2: получение промежуточного вещества 2-(трет-бутокси)-2-[3-(циклопент-1-ен-1-ил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусной кислоты (6b)
С использованием процедуры, описанной в примере 1, стадия 12, промежуточное соединение метил-2-(трет-бутокси)-2-[3-(циклопент-1-ен-1-ил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]ацетат (6а) (69 мг, 0,141 ммоль) превращали в 2-(трет-бутокси)-2-[3-(циклопент-1-ен-1-ил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусную кислоту (6b) (40 мг, 0,084 ммоль, 59%) в виде белого твердого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 0,96 (с, 9Н), 1,45-1,90 (м, 4Н), 1,92-2,12 (м, 2Н), 2,12-2,36 (м, 2Н), 2,60-2,91 (м, 2Н), 4,12-4,32 (т, J=4,6 Гц, 2Н), 5,28 и 5,32 (с, 1Н), 5,54 (с, 1Н), 6,67-6,87 (м, 2Н), 7,30-7,50 (м, 2Н), 7,61 (д, J=8,2 Гц, 1H), 9,59 (уш. с, 1Н).
MS m/z ([M-H]-)473.
Стадия 3: получение 2-(трет-бутокси)-2-[3-(циклопентил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусной кислоты (пример 6)
Смесь 2-(трет-бутокси)-2-[3-(циклопент-1-ен-1-ил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусной кислоты (6b) (15 мг, 0,031 ммоль) и палладия на углеродном носителе (5 мг) в метаноле (5 мл) встряхивали в атмосфере водорода в течение ночи. Смесь фильтровали через Millipore, и фильтрат концентрировали в вакууме с получением 2-(трет-бутокси)-2-[3-(циклопентил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил] уксусной кислоты (пример 6) (15 мг, 0,031 ммоль, 100%) в виде белого твердого вещества.
1Н ЯМР (300 МГц, CD3OD) δ 0,96 и 0,97 (с, 9Н), 1,42-2,08 (м, 10Н), 2,69-2,87 (м, 3H), 4,20-4,23 (м, 2Н), 5,02 (с, 1Н), 5,54 (с, 1Н), 6,75-6,92 (м, 2Н), 7,03-7,07 (м, 1Н), 7,49 (д, J=8,4 Гц, 1H), 7,67 (д, J=8,4 Гц, 1Н).
MS m/z ([М-Н]-) 475.
Пример 7: синтез 2-[4-(1H-1,3-бензодиазол-2-ил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-метокси-6-(трифторметил)фенил1-2-(трет-бутокси)уксусной кислоты
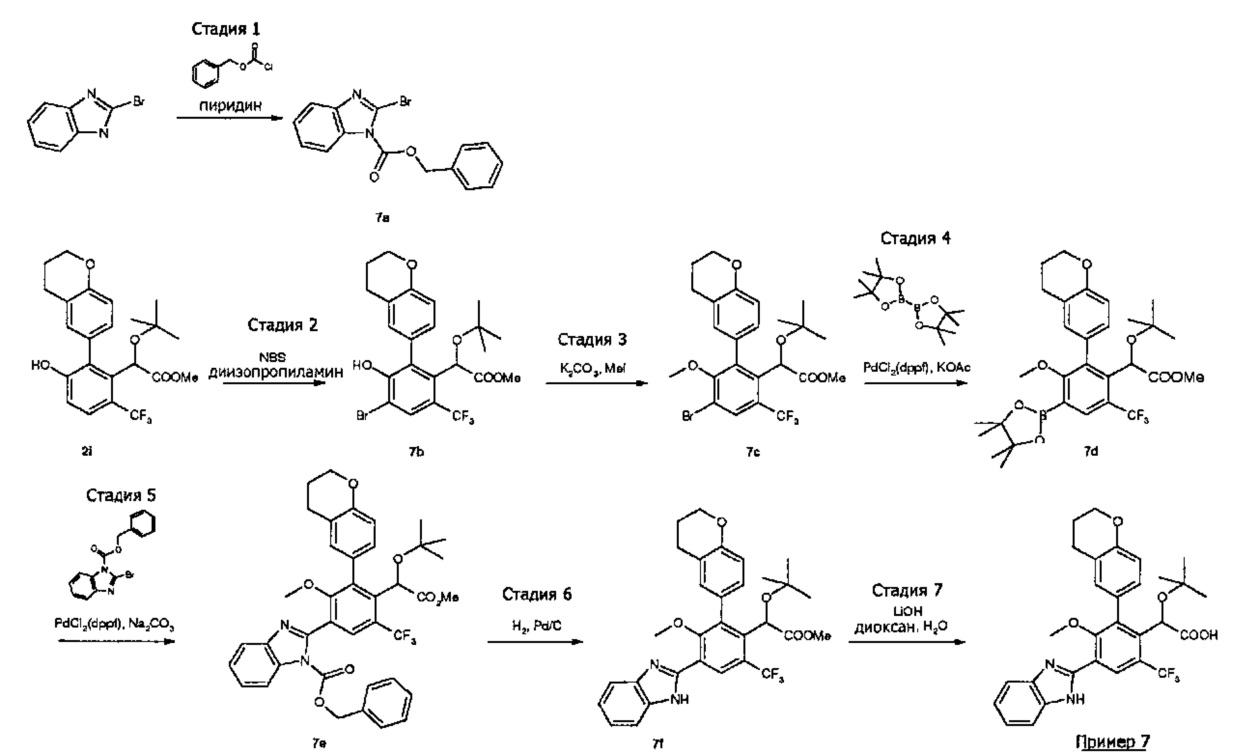
Стадия 1: получение промежуточного вещества бензил 2-бром-1H-1,3-бензодиазол-1-карбоксилата (7а)
В атмосфере азота бензилхлорформиат (0,174 мл, 1,218 ммоль) добавляли к раствору 2-бром-1H-1,3-бензодиазола (200 мг, 1,015 ммоль) и пиридина (0,123 мл, 1,523 ммоль) в безводном дихлорметане (4 мл) при 0°C. Реакционную смесь встряхивали при комнатной температуре в течение 3 часов, затем охлаждали до 0°C. Добавляли воду (5 мл), и один раз водный слой экстрагировали с использованием дихлорметана (2×7 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ TLC (циклогексан/этилацетат: 80/20) с получением бензил-2-бром-1H-1,3-бензодиазоле-1-карбоксилата (7а) (250 мг, 0,755 ммоль, 74%).
1Н ЯМР (400 МГц, CDCl3) δ 5,54 (с, 2Н), 7,30-7,37 (м, 2Н), 7,39-7,48 (м, 3H), 7,50-7,55 (м, 2Н), 7,64-7,71 (м, 1Н), 7,85-7,92 (м, 1Н).
Стадия 2: получение промежуточного соединения метил-2-[4-бром-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-гидрокси-6-(трифторметил)фенил]-2-(трет-бутокси)ацетата (7b)
N-бромсукцинимид (20 мг, 0,114 ммоль) медленно добавляли к раствору метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-гидрокси-6-(трифторметил)фенил] ацетата (2i) (50 мг, 0,114 ммоль) и диизопропиламина (3 ил, 0,023 ммоль) в дихлорметане (1 мл). Реакционную смесь встряхивали при комнатной температуре в течение 45 минут и концентрировали в вакууме. Исходный материал очищали с помощью препаративной ТСХ (дихлорметан/этилацетат: 90/10) с получением метил-2-[4-бром-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-гидрокси-6-(трифторметил)фенил]-2-(трет-бутокси)ацетата (7b) (55 мг, 0,106 ммоль, 93%).
1H ЯМР (400 МГц, CDCl3) δ 0,99 и 1,00 (с, 9Н), 1,99-2,10 (м, 2Н), 2,69-2,88 (м, 2Н), 3,66 (с, 3H), 4,22-4,27 (м, 2Н), 4,99 и 5,00 (с, 1Н), 5,60 (уш. с, 1H), 6,87-6,97 (м, 2Н), 7,02-7,09 (м, 1Н), 7,85 (с, 1H).
MS m/z ([М+Н]+) 517/519.
Стадия 3: получение промежуточного соединения метил-2-[4-бром-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-метокси-6-(трифторметил)фенил]-2-(трет-бутокси)ацетата (7с)
К раствору метил-2-[4-бром-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-гидрокси-6-(трифторметил)фенил]-2-(трет-бутокси)ацетата (7b) (55 мг, 0,106 ммоль) в ацетоне (2 мл), добавляли карбонат калия (44 мг, 0,319 ммоль) и иодометан (11 μл, 0,212 ммоль). Смесь нагревали в колбе с обратным холодильником в течение 3 ч 30 мин, затем концентрировали в вакууме. Остаток растворяли в воде (5 мл) и экстрагировали с помощью этилацетата (2×5 мл). Органический слой промывали с помощью 2М раствора гидроксида натрия (5 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением метил-2-[4-бром-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3 -метокси-6-(трифторметил)фенил]-2-(трет-бутокси)ацетата (7с) (52 мг, 0,097 ммоль, 92%).
1Н ЯМР (400 МГц, CDCl3) δ 0,94 и 0,95 (с, 9Н), 1,98-2,10 (м, 2Н), 2,67-2,89 (м, 2Н), 3,42 и 3,45 (с, 3H), 3,70 (с, 3H), 4,22-4,28 (м, 2Н), 5,02 и 5,03 (с, 1Н), 6,81 и 6,85 (д, J=8,3 Гц, 1H), 6,94-7,08 (м, 2Н), 7,91 (с, 1Н).
MS m/z ([M+Na]+) 555/557.
Стадия 4: получение промежуточного соединения метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-метокси-4-(тетраметил-1,3,2-диоксаборолан-2-ил)-6-(трифторметил)фенил]ацетата (7d)
Высушенная над пламенем колба, содержащая метил-2-[4-бром-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-метокси-6-(трифторметил)фенил]-2-(трет-бутокси)ацетат (7с) (190 мг, 0,358 ммоль), комплекс [1,1'-бис(дифенилфосфин)ферроцен] дихлорпалладия(II) с дихлорметаном (58,4 мг, 0,072 ммоль), бис[пинаколато]диборон (182 мг, 0,715 ммоль) и ацетат калия (106 мг, 1,073 ммоль) продували аргоном в течение 10 минут и затем добавляли дегазированный безводный диоксан (1,5 мл). Полученную смесь встряхивали при 80°C в течение 40 часов. Смесь охлаждали до комнатной температуры и разводили в этилацетате (5 мл) и промывали водой (2×5 мл) и солевым раствором (5 мл), сушили над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали на препаративной ТСХ (циклогексан/этилацетат: 80/20) с получением мешп-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-метокси-4-(тетраметил-1,3,2-диоксаборолан-2-ил)-6-(трифторметил)фенил]ацетата (7d) (170 мг, 0,294 ммоль, 82%).
1Н ЯМР (400 МГц, CDCl3) δ 0,93 и 0,95 (с, 9Н), 1,36 и 1,37 (с, 12Н), 1,99-2,08 (м, 2Н), 2,65-2,87 (м, 2Н), 3,41 и 3,45 (с, 3H), 3,69 (с, 3H), 4,20-4,27 (м, 2Н), 5,07 и 5,08 (с, 1H), 6,78 и 6,80 (д, J=8,3 Гц, 1Н), 6,87-7,07 (м, 2Н), 8,05 и 8,06 (с, 1Н).
Стадия 5-6: получение промежуточного соединения метил-2-[4-(1H-1,3-бензодиазол-2-ил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-метокси-6-(трифторметил)фенил]-2-(трет-бутокси)ацетата (7е)
К раствору метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-метокси-4-(тетраметил-1,3,2-диоксаборолан-2-ил)-6-(трифторметил)фенил]ацетата (7d) (60 мг, 0,104 ммоль) в диоксане (1,5 мл) добавляли бензил-2-бром-1H-1,3-бензодиазол-1-карбоксилат (7а) (69 мг, 0,207 ммоль) и насыщенный водный раствор карбоната натрия (1 мл). Смесь встряхивали при комнатной температуре в течение 20 минут, при этом пропуская поток аргона. Добавляли комплекс [1,1'-бис(дифенилфосфин)ферроцен] дихлорпалладия(II) с дихлорметаном (8 мг, 0,01 ммоль) и затем полученную смесь встряхивали при 80°C в течение 16 часов. Смесь охлаждали до комнатной температуры и разводили этилацетатом (5 мл). Органический слой промывали с использованием воды (2×5 мл) и солевого раствора (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (цикогексан/этилацеат: 60/40). Полученную в результате смесь продуктов разводили в этилацетате (2 мл). Палладий на углеродном носителе (7 мг) добавляли, и реакционную смесь встряхивали в атмосфере водорода в течение 16 часов. Смесь фильтровали через Millipore, и фильтрат концентрировали в вакууме. Исходный материал очищали с помощью препаративной ТСХ (дихлорметан/этилацетат: 95/5) с получением метил-2-[4-(1H-1,3-бензодиазол-2-ил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-метокси-6-(трифторметил)фенил]-2-(трет-бутокси)ацетата (7е) (11 мг, 0,019 ммоль, 19% через две стадии).
1Н ЯМР (300 МГц, CDCl3) δ 0,98 (с, 9Н), 2,04-2,14 (м, 2Н), 2,77-2,90 (м, 2Н), 3,42-3,44 (м, 3H), 3,74 и 3,75 (с, 3H), 4,26-4,32 (м, 2Н), 5,13-5,16 (м, 1Н), 6,86-6,94 (м, 1Н), 7,00-7,10 (м, 1H), 7,16-7,26 (м, 1H), 7,26-7,37 (м, 3H), 7,42-7,52 (м, 1Н), 7,85-7,92 (м, 1Н).
Стадия 7: получение 2-[4-(1H-1,3-бензодиазол-2-ил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-метокси-6-(трифторметил)фенил]-2-(трет-бутокси)уксусной кислоты (пример 7)
С использованием процедуры, описанной в примере, стадия 12, метил-2-[4-(1H-1,3-бензодиазол-2-ил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-метокси-6-(трифторметил)фенил]-2-(трет-бутокси)ацетат (7е) (11 мг, 0,019 ммоль) превращали в 2-[4-(1H-1,3-бензодиазол-2-ил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-метокси-6-(трифторметил)фенил]-2-(трет-бутокси)уксусную кислоту (пример 7) (7 мг, 0,013 ммоль, 65%).
1Н ЯМР (400 МГц, CDCl3) δ 0,98 (с, 9Н), 1,97-2,15 (м, 2Н), 2,76-2,93 (м, 2Н), 3,43 и 3,44 (с, 3H), 4,23-4,30 (м, 2Н), 5,24 (уш. с, 1H), 6,91 и 6,93 (д, J=8,3 Гц, 1Н), 7,01-7,10 (м, 1Н), 7,29-7,32 (м, 2Н), 7,44-7,90 (м, 3H), 8,87 и 8,88 (с, 1Н).
MS m/z ([М+Н]+) 555.
Пример 8: синтез 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(проп-1-ен-2-ил)-6-(трифторметил)фенил]уксусной кислоты
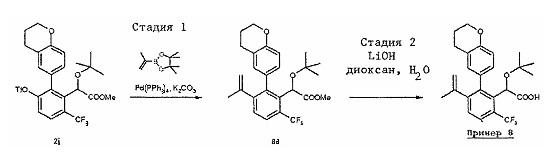
Стадия 1: получение промежуточного соединения метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(проп-1-ен-2-ил)-6-(трифторметил)фенил]ацетата (8а)
С использованием процедуры, описанной в примере 6, стадия 1, промежуточное соединение метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-[(трифторметан) сульфонилокси]-6-(трифторметил)фенил]ацетат (2j) (110 мг, 0,193 ммоль) превращали с помощью реакции сложного эфира пинакола и изопропенилбороновой кислоты (81 мг, 0,482 ммоль), после очистки с помощью препаративной ТСХ (циклогексан/этилацетат: 80/20) в метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(проп-1-ен-2-ил)-6-(трифторметил)фенил]уксусную кислоту (8а) (88 мг, 0,190 ммоль, 99%).
1Н ЯМР (400 МГц, CDCl3) δ 0,95 и 0,96 (с, 9Н), 1,54 (с, 3H), 2,00-2,07 (м, 2Н), 2,67-2,81 (м, 2Н), 3,69 и 3,70 (с, 3H), 4,20-4,25 (м, 2Н), 4,81-4,86 (м, 1Н), 4,95-5,00 (м, 1H), 5,12 и 5,13 (с, 1Н), 6,75 и 6,76 (д, J=8,4 Гц, 1Н), 6,78-6,88 (м, 1H), 7,01-7,08 (м, 1H), 7,30 (д, J=8,1 Гц, 1Н), 7,64(д,7=8,1 Гц, 1Н).
MS m/z ([M+Na]+) 485.
Стадия 2: получение 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(проп-1-ен-2-ил)-6-(трифторметил)фенил]уксусной кислоты (пример 8)
С использованием процедуры, описанной в примере 1, стадия 12, промежуточное соединение метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(проп-1-ен-2-ил)-6-(трифторметил)фенил]ацетат (8а) (88 мг, 0,19 ммоль) превращали в 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(проп-1-ен-2-ил)-6-(трифторметил)фенил]уксусную кислоту (пример 8) (82 мг, 0,183 ммоль, 96%).
1Н ЯМР (400 МГц, CDCl3) δ 0,97 (с, 9Н), 1,53 (с, 3H), 1,97-2,08 (м, 2Н), 2,65-2,87 (м, 2Н), 4,17-4,28 (м, 2Н), 4,82-4,89 (м, 1Н), 4,97-5,01 (м, 1H), 5,27 и 5,29 (с, 1Н), 6,73-6,87 (м, 2Н), 7,32-7,45 (м, 2Н), 7,65 (д, J=8,1 Гц, 1H).
MS m/z ([М-Н]-) 447.
Пример 9: синтез 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-этенил-6-(трифторметил)фенил]уксусной кислоты

Стадия 1: получение промежуточного соединения метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-этенил-6-(трифторметил)фенил]ацетата (9а)
С использованием процедуры, описанной в примере 6, стадия 1, промежуточное соединение метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-[(трифторметан) сульфонилокси]-6-(трифторметил)фенил]ацетат (2j) (100 мг, 0,175 ммоль) превращали с помощью реакции со сложным эфиром пинакола и винилбороновой кислоты (67 мг, 0,438 ммоль), после очистки с помощью препаративной ТСХ (циклогексан/этилацетат: 80/20) в метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-этенил-6-(трифторметил)фенил]ацетат (9а) (62 мг, 0,138 ммоль, 79%).
1H ЯМР (400 МГц, CDCl3) δ 0,98 (с, 9Н), 1,98-2,10 (м, 2Н), 2,68-2,86 (м, 2Н), 3,66 и 3,67 (с, 3H), 4,20-4,30 (м, 2Н), 5,08 и 5,09 (с, 1Н), 5,15-5,20 (м, 1Н), 5,67 (д, J=17,4 Гц, 1Н), 6,33 и 6,34 (дд, J=17,4 Гц, J=11,0 Гц, 1Н), 6,77-6,85 (м, 2Н), 6,94-7,00 (м, 1Н), 7,65 (д, J=8,3 Гц, 1Н), 7,68 (д, J=8,3 Гц, 1H).
MS m/z ([M+Na]+) 471.
Стадия 2: получение 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-этенил-6-(трифторметил)фенил]уксусной кислоты (пример 9)
С использованием процедуры, описанной в примере 1, стадия 12, промежуточное соединение метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-этенил-6-(трифтор метил)фенил]ацетат (9а) (62 мг, 0,138 ммоль) превращали в 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-этенил-6-(трифторметил) фенил]уксусную кислоту (пример 9) (56 мг, 0,129 ммоль, 93%).
1Н ЯМР (400 МГц, CDCl3) δ 1,00 (с, 9Н), 2,00-2,08 (м, 2Н), 2,70-2,87 (м, 2Н), 4,22-4,26 (м, 2Н), 5,15-5,25 (м, 2Н), 5,68 (д, J=17,5 Гц, 1H), 6,32 и 6,34 (дд, J=17,5 Гц, J=11,0 Гц, 1H), 6,79-6,89 (м, 2Н), 7,29 (уш. с, 1H), 7,69 (с, 2Н).
MS m/z ([M-H]-)433.
Пример 10: синтез 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(пропан-2-ил)-6-(трифторметил)фенил]уксусной кислоты

Стадия 1: получение 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(пропан-2-ил)-6-(трифторметил)фенил]уксусной кислоты (пример 10)
С использованием процедуры, описанной в примере 6, стадия 3, промежуточное соединение 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(проп-1-ен-2-ил)-6-(трифторметил) фенил]уксусная кислота (пример 8) (62 мг, 0,138 ммоль) превращали в 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-(пропан-2-ил)-6-(трифтор метил)фенил]уксусную кислоту (пример 10) (50 мг, 0,111 ммоль, 80%).
1Н ЯМР (300 МГц, CDCl3) δ 0,96-1,20 (м, 15Н), 2,00-2,09 (м, 2Н), 2,65-2,89 (м, 3H), 4,17-4,28 (м, 2Н), 5,12 (с, 1H), 6,78-6,92 (м, 2Н), 7,20-7,32 (м, 1H), 7,43 (д, J=8,4 Гц, 1Н), 7,68 (д, J=8,4 Гц, 1Н).
MS m/z ([М-Н]-) 449.
Пример 11: синтез 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-этил-6-(трифторметил)фенил]уксусной кислоты
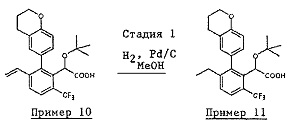
Стадия 1: получение 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-этил-6-(трифторметил)фенил]уксусной кислоты (пример 11)
С использованием процедуры, описанной в примере 6, стадия 3, промежуточное соединение 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-этенил-6-(трифторметил) фенил]уксусную кислоту (пример 9) (36 мг, 0,083 ммоль) превращали в 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-этил-6-(трифторметил)фенил]уксусную кислоту (пример 11) (29 мг, 0,066 ммоль, 80%).
1Н ЯМР (300 МГц, CDCl3) δ 1,00-1,10 (м, 12Н), 2,00-2,08 (м, 2Н), 2,32-2,41 (м, 2Н), 2,68-2,93 (м, 2Н), 4,20-4,27 (м, 2Н), 5,15 (с, 1Н), 6,79-6,91 (м, 2Н), 7,24 (м, 1Н), 7,37 (д, J=8,1 Гц, 1H), 7,65 (д, 7=8,1 Гц, 1Н).
MS m/z ([М-Н]-) 435.
Пример 12: синтез 2-(трет-бутокси)-2-(6-циклопропил-4'-метокси-3-метил-бифенил-2-ил]уксусной кислоты

Стадия 1: получение промежуточного соединения метил-2-(2-бром-3-гидрокси-6-метилфенил)-2-(трет-бутокси)ацетата (12а)
К раствору метил-2-(2-бром-3-гидрокси-6-метилфенил)-2-гидрокси-ацетата (1е) (406 мг, 1,48 ммоль) в трет-бутилацетате (15 мл) при 0°C добавляли серную кислоту (0,315 мл, 5,9 ммоль). Смесь встряхивали при комнатной температуре в течение 4 часов. Смесь разводили в этилацетате (20 мл и промывали насыщенным раствором гидрокарбоната натрия. Органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат: 80/20) с получением метил-2-(2-бром-3-гидрокси-6-метил фенил)-2-(трет-бутокси)ацетата (12а) (195 мг, 0,59 ммоль, 40%) в виде твердого светло-желтого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 1,21 (с, 9Н), 2,36 (с, 3H), 3,68 (с, 3H), 5,54 (с, 1Н), 5,70 (с, 1Н), 6,88 (д, J=8,2 Гц, 1Н), 7,00 (д, J=8,2 Гц, 1H).
MS m/z ([М-Н]-) 329/331.
Стадия 2: получение промежуточного соединения метил-2-[2-бром-3-(4-метокси-бензилокси)-6-метилфенил]-2-(трет-бутокси)-ацетата (12b)
С использованием процедуры, описанной в примере 1, стадии 6, промежуточное соединение метил-2-(2-бром-3-гидрокси-6-метил фенил)-2-(трет-бутокси)ацетат (12а) (1,83 г, 5,52 ммоль) превращали с помощью реакции с 4-метоксибензилхлоридом (0,82 мл, 6,08 ммоль), после очистки с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат 90/10) в метил-2-[2-бром-3-(4-метокси-бензилокси)-6-метилфенил]-2-(трет-бутокси)-ацетат (12b) (2,34 г, 5,18 ммоль, 93%) в виде твердого белого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 1,22 (с, 9Н), 2,36 (с, 3H), 3,68 (с, 3H), 3,82 (с, 3H), 5,04 (с, 2Н), 5,95 (с, 1Н), 6,80 (д, J=8,4 Гц, 1H), 6,82 (д, J=8,7 Гц, 2Н), 7,01 (д, J=8,4 Гц, 1Н), 7,41(д, J=8,7 Гц, 2Н).
MS m/z ([M+Na]+) 473/475.
Стадия 3: получение промежуточного соединения метил-2-(трет-бутокси)-2-[4'-метокси-6-(4-метокси-бензилокси)-3-метил-бифенил-2-ил] ацетата (12с)
С использованием процедуры, описанной в примере 1, стадия 7, промежуточное соединение метил-2-[2-бром-3-(4-метокси-бензилокси)-6-метилфенил]-2-(трет-бутокси)-ацетат (12b) (50 мг, 0,11 ммоль) превращали с помощью реакции с 4-метоксифенилбороновой кислотой (25 мг, 0,17 ммоль), после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20), в метил-2-(трет-бутокси)-2-[4'-метокси-6-(4-метокси-бензилокси)-3-метил-бифенил-2-ил]ацетат (12с) (36 мг, 0,075 ммоль, 68%).
1Н ЯМР (300 МГц, CDCl3) δ 0,94 (с, 9Н), 2,35 (с, 3H), 3,71 (с, 3H), 3,77 (с, 3H), 3,87 (с, 3H), 4,82 (д, J=11,9 Гц, 1Н), 4,89 (д, J=11,9 Гц, 1Н), 5,14 (с, 1H), 6,76-6,82 (м, 2Н), 6,86 (д, J=8,3 Гц, 1Н), 6,91-6,99 (м, 2Н), 7,02-7,08 (м, 3H), 7,22-7,27 (м, 1Н), 7,31-7,36 (м, 1H).
MS m/z ([M+Na]+) 501.
Стадия 4: получение промежуточного соединения метил-2-(трет-бутокси)-2-(6-гидрокси-4'-метокси-3-метил-бифенил-2-ил)ацетата (12d)
Смесь метил-2-(трет-бутокси)-2-[4'-метокси-6-(4-метокси-бензилокси)-3-метил-бифенил-2-ил]ацетата (12с) (82 мг, 0,171 ммоль) палладия на углеродном носителе (18 мг) в этилацетате (5 мл) встряхивали при комнатной температуре при давлении водорода 5 бар в течение 18 часов. Смесь фильтровали через Millipore и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/эти л ацетат 80/20) с получением метил-2-(трет-бутокси)-2-[6-гидрокси-4'-метокси-3-метил-бифенил-2-ил]ацетата (12d) (56 мг, 0,156 ммоль, 92%).
1Н ЯМР (300 МГц, CDCl3) δ 0,96 (с, 9Н), 2,35 (с, 3H), 3,69 (с, 3H), 3,88 (с, 3H), 4,61 (с, 1Н), 4,98 (с, 1H), 6,84 (д, J=8,2 Гц, 1Н), 6,99-7,09 (м, 3H), 7,22-7,26 (м, 1Н), 7,41 (дд, J=2,0 Гц, J=8,4 Гц, 1Н).
MS m/z ([M+Na]+) 381.
MS m/z ([М-Н]-) 357.
Стадия 5: получение промежуточного соединения метил-2-(трет-бутокси)-2-(4'-метокси-3-метил-6-трифторметансульфонилокси-бифенил-2-ил]ацетата (12е)
С использованием процедуры, описанной в примере 1, стадии 10, промежуточное соединение метил-2-(трет-бутокси)-2-(6-гидрокси-4'-метокси-3-метил-бифенил-2-ил)ацетат (12d) (56 мг, 0,156 ммоль) превращали в промежуточное соединение метил-2-(трет-бутокси)-2-(4'-метокси-3-метил-6-трифторметансульфонилокси-бифенил-2-ил]ацетат (12е) (63 мг, 0,128 ммоль, 82%).
1Н ЯМР (300 МГц, CDCl3) δ 0,95 (с, 9Н), 2,44 (с, 3H), 3,72 (с, 3H), 3,87 (с, 3H), 5,10 (с, 1Н), 6,95-7,01 (м, 2Н), 7,16-7,23 (м, 3H), 7,31-7,36 (м, 1Н).
MS m/z ([М-Н]-) 489.
Стадия 6: получение промежуточного соединения метил-2-(трет-бутокси)-2-(6-циклопропил-4'-метокси-3-метил-бифенил-2-ил] ацетата (12f)
С использованием процедуры, описанной в примере 1, стадии 11, промежуточное соединение метил-2-(трет-бутокси)-2-(4'-метокси-3-метил-6-трифторметансульфонилокси-бифенил-2-ил]ацетат (12е) (63 мг, 0,128 ммоль) превращали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 85/15) в метил 2-(трет-бутокси)-2-(6-циклопропил-4'-метокси-3-метил-бифенил-2-ил]ацетат (12f) (10 мг, 0,026 ммоль, 20%).
1Н ЯМР (300 МГц, CDCl3) δ 0,52-0,74 (м, 4Н), 0,97 (с, 9Н), 1,37-1,48 (м, 1H), 2,40 (с, 3H), 3,68 (с, 3H), 3,87 (с, 3H), 5,08 (с, 1Н), 6,78 (д, J=7,9 Гц, 1H), 6,92-7,00 (м, 2Н), 7,06 (д, J=7,9 Гц, 1Н), 7,20-7,25 (м, 1H), 7,29-7,34 (м, 1Н).
MS m/z ([M+Na]+) 405.
Стадия 7: получение 2-(трет-бутокси)-2-(6-циклопропил-4'-метокси-3-метил-бифенил-2-ил]уксусной кислоты (пример 12)
С использованием процедуры, описанной в примере 1, стадии 12, промежуточное соединение метил 2-(трет-бутокси)-2-(6-циклопропил-4'-метокси-3-метил-бифенил-2-ил]ацетат (12е) (10 мг, 0,026 ммоль) превращали в 2-(трет-бутокси)-2-(6-циклопропил-4'-метокси-3-метил-бифенил-2-ил]уксусную кислоту (пример 12) (9 мг, 0,024 ммоль, 90%) в виде бесцветного масла.
1Н ЯМР (400 МГц, CDCl3) δ 0,50-0,62 (м, 3H), 0,70-0,76 (м, 1H), 1,00 (с, 9Н), 1,44-1,52 (м, 1H), 2,36 (с, 3H), 3,86 (с, 3H), 5,21 (с, 1Н), 6,80 (д, J=7,9 Гц, 1Н), 6,93-7,00 (м, 2Н), 7,05 (д, J=7,9 Гц, 1Н), 7,22-7,27 (м, 1Н), 7,46-7,52 (м, 1H).
MS m/z ([М-Н]-) 367.
Пример 13: синтез (S)-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]уксусной кислоты
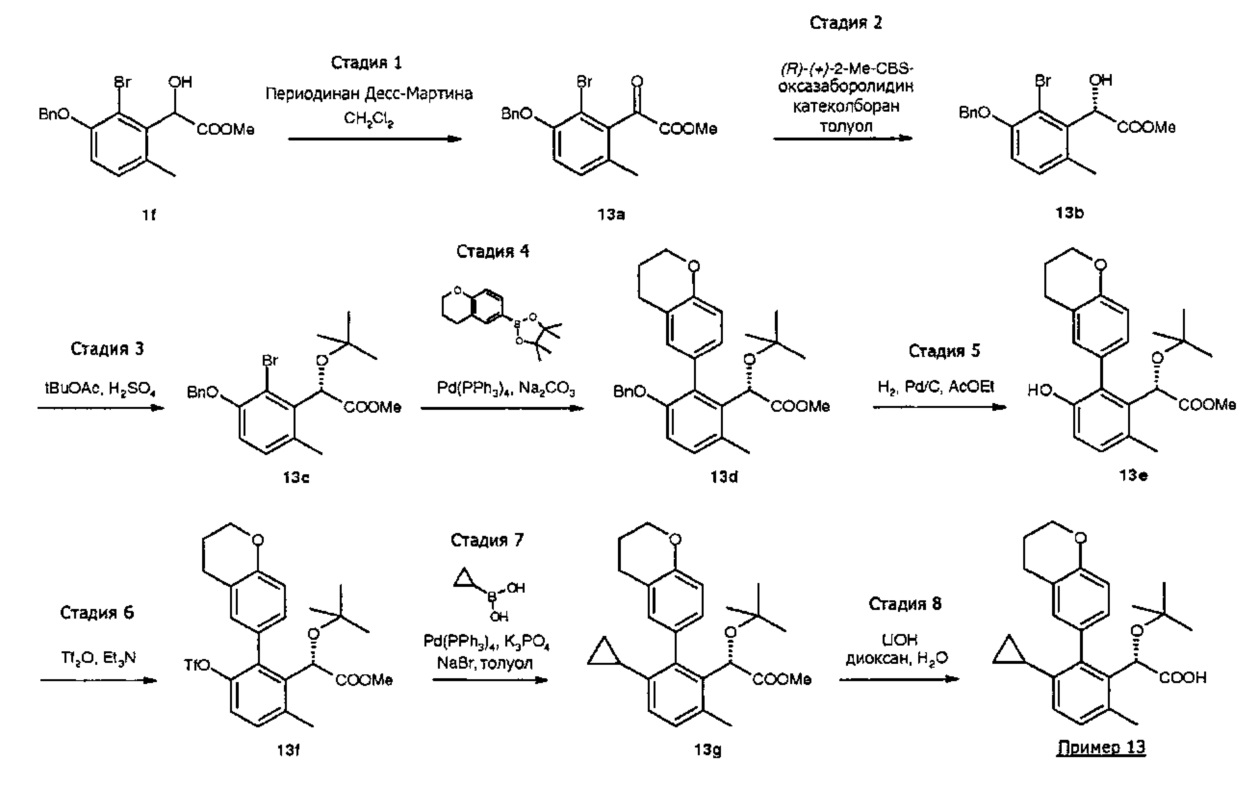
Стадия 1: получение промежуточного соединения метил (3-бензилокси-2-бром-6-метил-фенил)-оксо-ацетата (13а)
В круглодонной колбе в атмосфере аргона при комнатной температуре, добавляли реагент Десс-Мартина (3,47 г, 7,95 ммоль) в трех частях в раствор метил (3-бензилокси-2-бром-6-метил-фенил)-гидрокси-ацетат (1f) (2,42 г, 6,63 ммоль) в дихлорметане (29 мл). Через 1 ч15 мин при комнатной температуре смесь гасили с помощью насыщенного раствора бикарбоната натрия и экстрагировали с помощью дихлорметана. Органический слой промывали дважды насыщенным раствором тиосульфата натрия, солевого раствора, сушили над сульфатом натрия и концентрировали в вакууме, с получением метил (3-бензилокси-2-бром-6-метил-фенил)-оксо-ацетата (13а) (2,4 г, 6,61 ммоль, 99%), в виде масла, которое кристаллизовалось в светло-желтое твердое вещество.
1Н ЯМР (300 МГц, CDCl3) δ 2,22 (с, 3H), 3,92 (с, 3H), 5,15 (с, 2Н), 6,94 (д, 7=8,4 Гц, 1Н), 7,13 (д, J=8,4 Гц, 1H), 7,27-7,47 (м, 5Н).
Стадия 2: получение промежуточного соединения метил (5)-(3-бензилокси-2-бром-6-метил-фенил)-гидрокси-ацетата (13b)
В круглодонной колбе в атмосфере аргона, метил (3-бензилокси-2-бром-6-метил-фенил)-оксо-ацетат (13а) (100 мг, 0,28 ммоль) и (R)-(+)-2-Метил-CBS-оксазаборолидин (61 мг, 0,22 ммоль) растворяли в толуоле (1 мл). Смесь охлаждали до -20°C и медленно добавляли катехолборан (38,8 μл, 0,36 ммоль) в толуоле (415 μл). Смесь встряхивали до момента завершения реакции. Через 80 минут смесь гасили с использованием метанола, затем добавляли насыщенный раствор бикарбоната натрия. Встряхивали в течение 30 минут и экстрагировали с помощью этилацетата. Объединенные органические слои промывали с помощью насыщенного раствора бикарбоната натрия пять или шесть раз (до того момента, как водный слой не будет больше окрашенным), затем один раз с помощью 1N раствора хлороводородной кислоты, насыщенного солевого раствора, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этил ацетат 80/20) с получением метил (S)-(3-бензилокси-2-бром-6-метил-фенил)-гидрокси-ацетата (13b) (66 мг, 0,8 ммоль, 65%) с энантиомерным избытком 94,8% (колонка Chiralcel® IA, Daicel Chemical Industries, подвижная фаза гептан/2-PrOH 7/3, скорость потока 1 мл/мин, детектирование с помощью детектора светодиодного эррея при 220 нм, время удержания 8,41 минут).
1Н ЯМР (300 МГц, CDCl3) δ 2,34 (с, 3H), 3,49 (д, J=4,4 Гц, 1Н), 3,78 (с, 3H), 5,13 (с, 2Н), 5,86 (д, J=4,4 Гц, 1H), 6,84 (д, J=8,4 Гц, 1H), 7,06 (д, J=8,4 Гц, 1H), 7,30-7,34 (м, 1Н), 7,37-7,41 (м, 2Н), 7,47 (д, J=7,4 Гц, 2Н).
Стадия 3: получение промежуточного соединения метил (S)-2-(3-бензилокси-2-бром-6-метилфенил)-2-(трет-бутокси)-ацетата (13с)
С использованием процедуры, описанной в примере 12, стадия 1, промежуточное соединение метил (S)-(3-бензилокси-2-бром-6-метил-фенил)-гидрокси-ацетат (13b) (500 мг, 1,37 ммоль) превращали в промежуточное соединение метил (S)-2-(3-бензилокси-2-бром-6-метилфенил)-2-(трет-бутокси)-ацетат (13 с) (469 мг, 1,11 ммоль, 81%) в виде белого твердого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 1,23 (с, 9Н), 2,36 (с, 3H), 3,68 (с, 3H), 5,12 (с, 2Н), 5,96 (с, 1Н), 6,80 (д, J=8,4 Гц, 1H), 7,01 (д, J=8,4 Гц, 1H), 7,29-7,42 (м, 3H), 7,48-7,51 (м, 2Н).
Стадия 4: получение промежуточного соединения метил (S)-2-(трет-бутокси)-2-[3-бензилокси-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]ацетата (13d)
В запаянной круглодонной колбе к дегазированному раствору метил (S)-2-(3-бензилокси-2-бром-6-метилфенил)-2-(трет-бутокси)-ацетата (13 с) (330 мг, 0,783 ммоль) и сложного эфира пинакола и хроман-6-бороновой кислоты (224 мг, 0,862 ммоль) в диоксане (4 мл) добавляли раствор карбоната натрия (249 мг, 2,35 ммоль) в воде (0,8 мл) с последующим добавлением тетракис(трифенилфосфин) палладия (91 мг, 0,078 ммоль). Смесь нагревали при 120°C в течение 16 часов. Смесь охлаждали до комнатной температуры. Добавляли воду (10 мл). Водный слой экстрагировали этилацетатом (3×100 мл). Органический слой промывали с использованием солевого раствора (20 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат: 90/10) с получением метил (S)-2-(трет-бутокси)-2-[3-бензилокси-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метил фенил]ацетата (13d) (816 мг, 1,71 ммоль, 100%) в виде твердого белого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 0,96 (с, 9Н), 2,00-2,09 (м, 2Н), 2,35 и 2,36 (с, 3H), 2,72-2,82 (м, 2Н), 3,70 и 3,71 (с, 3H), 4,22-4,26 (м, 2Н), 4,88-5,01 (м, 2Н), 5,16 и 5,18 (с, 1H), 6,81-6,87 (м, 2Н), 6,99-7,29 (м, 8Н).
Стадия 5: получение промежуточного соединения метил (S)-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил]ацетата (13е)
С использованием процедуры, описанной в примере 12, стадия 4, промежуточное соединение метил (S)-2-(трет-бутокси)-2-[3-бензилокси-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]ацетат (13d) (816 мг, 1,72 ммоль) превращали в промежуточное соединение метил (S)-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил]ацетат (13е) (586 мг, 1,52 ммоль, 89%).
1Н ЯМР (300 МГц, CDCl3) δ 0,97 и 0,98 (с, 9Н), 2,01-2,09 (м, 2Н), 2,34 и 2,35 (с, 3H), 2,71-2,86 (м, 2Н), 3,67 и 3,68 (с, 3H), 4,24-4,27 (м, 2Н), 4,63 и 4,67 (с, 1Н), 4,99 и 5,00 (с, 1Н), 6,82-7,05 (м, 4Н), 7,12-7,19 (м, 1Н).
Стадия 6: получение промежуточного соединения метил (S)-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетата (13f)
К раствору метил (S)-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил]ацетата (13е) (580 мг, 1,51 ммоль) в безводном дихлорметане (15 мл) в атмосфере азота при -78°C постепенно добавляли триэтиламин (0,631 мл, 4,53 ммоль), и трифторметансульфоновый ангидрид (0,32 мл, 1,89 ммоль). Смесь встряхивали при комнатной температуре в течение 30 минут перед добавлением воды (10 мл). Слои разделяли. Водный слой экстрагировали дихлорметаном (10 мл). Объединенные органические слои промывали с использованием насыщенного раствора гидрокарбоната натрия (10 мл), сушили над хлоридом натрия и концентрировали в вакууме с получением промежуточного соединения метил (S)-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетата (13f) (721 мг, 1,40 ммоль, 92%) в виде коричневого масла, которое использовали без дополнительной очистки.
1Н ЯМР (300 МГц, CDCl3) δ 0,95 и 0,96 (с, 9Н), 2,00-2,09 (м, 2Н), 2,43 и 2,45 (с, 3H), 2,68-2,87 (м, 2Н), 3,70 и 3,71 (с, 3H), 4,22-4,26 (м, 2Н), 5,11 и 5,13 (с, 1H), 6,82-6,87 (м, 1H), 6,94-7,11 (м, 2Н), 7,15-7,21 (м, 2Н).
Стадия 7: получение промежуточного соединения метил (S)-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]ацетата (13g)
С использованием процедуры, описанной в примере 1, стадия 11, промежуточное соединение метил (S)-2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетат (13f) (360 мг, 0,697 ммоль) превращали в промежуточное соединение метил (S)-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил] ацетат (13g) (199 мг, 0.487 ммоль, 69%) в виде светло-желтого масла.
1Н ЯМР (300 МГц, CDCl3) δ 0,52-0,74 (м, 4Н), 0,98 (с, 9Н), 1,41-1,52 (м, 1Н), 1,99-2,10 (м, 2Н), 2,39 (с, 3H), 2,67-2,87 (м, 2Н), 3,65 и 3,67 (с, 3H), 4,22-4,26 (м, 2Н), 5,08 и 5,10 (с, 1Н), 6,72-6,85 (м, 2Н), 6,94-7,10 (м, 3H).
Стадия 8: получение (S)-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]уксусной кислоты (пример 13)
С использованием процедуры, описанной в примере 1, стадия 12, метил (S)-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]ацетат (13g) (378 мг, 0,925 ммоль) превращали в (S)-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]уксусную кислоту (пример 13) (313 мг, 0,793 ммоль, 85%).
1Н ЯМР (300 МГц, CDCl3) δ 0,50-0,73 (м, 4Н), 0,88 и 0,89 (с, 9Н), 1,35-1,44 (м, 1H), 1,86-2,01 (м, 2Н), 2,30 (с, 3H), 2,61-2,83 (м, 2Н), 4,13-4,20 (м, 2Н), 4,91 и 4,95 (с, 1H), 6,69-6,73 (м, 1Н), 6,78 и 6,81 (д, J=8,3 Гц, 1Н), 6,89-7,06 (м, 2Н), 12,37 (с, 1Н).
MS m/z ([М-Н]-) 393.
Пример 14: синтез 2-(трет-бутокси)-2-(6-циклопропил-3,4'-диметил-бифенил-2-ил)-уксусной кислоты
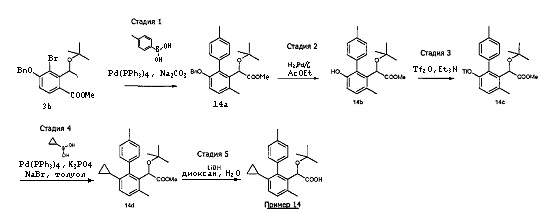
Стадия 1: получение промежуточного соединения метил 2-(6-бензилокси-3,4'-диметил-бифенил-2-ил)-2-(трет-бутокси) ацетата (14а)
С использованием процедуры, описанной в примере 1, стадия 7, промежуточное соединение метил 2-(3-бензилокси-2-бром-6-метилфенил)-2-(трет-бутокси)-ацетат (3b) (100 мг, 0,24 ммоль) превращали с помощью реакции с 4-метилфенилбороновой кислоты (39 мг, 0,28 ммоль), после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20), в метил 2-(6-бензилокси-3,4'-диметил-бифенил-2-ил)-2-(трет-бутокси) ацетат (14а) (52 мг, 0,12 ммоль, 51%).
1Н ЯМР (400 МГц, CDCl3) δ 0,95 (с, 9Н), 2,37 (с, 3H), 2,43 (с, 3H), 3,71 (с, 3H), 4,91 (д, J=12,5 Гц, 1Н), 4,97 (д, J=12,5 Гц, 1Н), 5,13 (с, 1Н), 6,85 (д, J=8,3 Гц, 1Н), 7,06 (д, J=8,3 Гц, 1H), 7,09-7,14 (м, 2Н), 7,19-7,32 (м, 7Н).
MS m/z ([M+Na]+) 455.
Стадия 2: получение промежуточного соединения метил 2-(трет-бутокси)-2-(6-гидрокси-3,4'-диметил-бифенил-2-ил)-ацетата (14b)
С использованием процедуры, описанной в примере 12, стадии 4, промежуточное соединение метил 2-(6-бензилокси-3,4'-диметил-бифенил-2-ил)-2-(трет-бутокси) ацетат (14а) (99 мг, 0,23 ммоль) превращали в промежуточное соединение метил 2-(трет-бутокси)-2-(6-гидрокси-3,4'-диметил-бифенил-2-ил)-ацетат (14b) (78 мг, 0,23 ммоль, 100%), которое использовали без дополнительной очистки.
1Н ЯМР (300 МГц, CDCl3) δ 0,95 (с, 9Н), 2,35 (с, 3H), 2,44 (с, 3H), 3,69 (с, 3H), 4,59 (с, 1H), 4,97 (с, 1Н), 6,85 (д, J=8,2 Гц, 1H), 7,05 (д, J=8,2 Гц, 1Н), 7,18-7,24 (м, 1H), 7,27-7,39 (м, 3H).
MS m/z ([M+Na]+) 365.
Стадия 3: получение промежуточного соединения метил 2-(трет-бутокси)-2-(3,4'-диметил-6-трифторметансульфонилокси-бифенил-2-ил)-ацетата (14с)
С использованием процедуры, описанной в примере 1, стадии 10, промежуточное соединение метил 2-(трет-бутокси)-2-(6-гидрокси-3,4'-диметил-бифенил-2-ил)-ацетат (14b) (78 мг, 0,23 ммоль) превращали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20) в метил 2-(трет-бутокси)-2-(3,4'-диметил-6-трифторметансульфонилокси-бифенил-2-ил)-ацетат (14 с) (91 мг, 0.19 ммоль, 84%).
1Н ЯМР (400 МГц, CDCl3) δ 0,93 (с, 9Н), 2,43 (с, 3H), 2,46 (с, 3H), 3,72 (с, 3H), 5,08 (с, 1H), 7,16-7,30 (м, 6Н).
MS m/z ([М-Н]-) 473.
Стадия 4: получение промежуточного соединения метил 2-(трет-бутокси)-2-(6-циклопропил-3,4'-диметил-бифенил-2-ил)-ацетата (14d)
С использованием процедуры, описанной в примере 1, стадии 11, промежуточное соединение метил 2-(трет-бутокси)-2-(3,4'-диметил-6-трифторметансульфонилокси-бифенил-2-ил)-ацетат (14с) (91 мг, 0,19 ммоль) превращали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 90/10) в метил 2-(трет-бутокси)-2-(6-циклопропил-3,4'-диметил-бифенил-2-ил)-ацетат (14d) (54 мг, 0,15 ммоль, 77%).
1Н ЯМР (300 МГц, CDCl3) δ 0,51-0,64 (м, 3H), 0,64-0,74 (м, 1H), 0,96 (с, 9Н), 1,37-1,45 (м, 1H), 2,40 (с, 3H), 2,42 (с, 3H), 3,67 (с, 3H), 5,05 (с, 1H), 6,77 (д, J=7,9 Гц, 1H), 7,05 (д, J=7,9 Гц, 1H), 7,17-7,30 (м, 4Н).
MS м/з ([M+Na]+) 389.
Стадия 5: получение 2-(трет-бутокси)-2-(6-циклопропил-3,4'-диметил-бифенил-2-ил)-уксусной кислоты (пример 14)
С использованием процедуры, описанной в примере 1, стадии 12, промежуточное соединение метил 2-(трет-бутокси)-2-(6-циклопропил-3,4'-диметил-бифенил-2-ил)-ацетат (14d) (54 мг, 0,15 ммоль) превращали в 2-(трет-бутокси)-2-(6-циклопропил-3,4'-диметил-бифенил-2-ил)-уксусную кислоту (пример 14) (35 мг, 0,1 ммоль, 67%).
1Н ЯМР (300 МГц, CDCl3) δ 0,49-0,64 (м, 3H), 0,66-0,77 (м, 1Н), 0,99 (с, 9Н), 1,41-1,53 (м, 1H), 2,36 (с, 3H), 2,41 (с, 3H), 5,18 (с, 1H), 6,80 (д, J=7,9 Гц, 1Н), 7,05 (д, J=7,9 Гц, 1Н), 7,17-7,28 (м, 3H), 7,42-7,47 (м, 1Н).
MS m/z ([M+Na]+) 375.
MS m/z ([М-Н]-) 351.
Пример 15: синтез 2-(трет-бутокси)-2-(6-циклопропил-4'-фтор-3-метил-бифенил-2-ил)-уксусной кислоты

Стадия 1: получение промежуточного соединения метил 2-[4'-фтор-6-(4-метокси-бензилокси)-3-метил-бифенил-2-ил]-2-(трет-бутокси) ацетата (15а)
С использованием процедуры, описанной в примере 1, стадия 7, промежуточное соединение метил 2-[2-бром-3-(4-метокси-бензилокси)-6-метил-фенил]-2-{трет-бутокси)-ацетат (12b) (150 мг, 0,33 ммоль) превращали с помощью реакции с 4-фторфенилбороновой кислотой (56 мг, 0,4 ммоль), после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20), в метил 2-[4'-фтор-6-(4-метокси-бензилокси)-3-метил-бифенил-2-ил]-2-(трет-бутокси) ацетат (15а) (139 мг, 0,3 ммоль, 90%).
1Н ЯМР (300 МГц, CDCl3) δ 0,94 (с, 9Н), 2,36 (с, 3H), 3,71 (с, 3H), 3,78 (с, 3H), 4,82 (д, J=11,8 Гц, 1H), 4,90 (д, J=11,8 Гц, 1H), 5,04 (с, 1Н), 6,76-6,82 (м, 2Н), 6,88 (д, J=8,4 Гц, 1Н), 6,99-7,16 (м, 5Н), 7,24-7,31 (м, 1Н), 7,34-7,41 (м, 1Н).
MS m/z ([M+Na]+) 489.
Стадия 2: получение промежуточного соединения метил 2-(трет-бутокси)-2-(4'-фтор-6-гидрокси-3-метил-бифенил-2-и)-ацетата (15b)
Палладий на активированном угле (10%) Pd по массе, 13,9 мг) добавляли к раствору метил 2-[4'-фтор-6-(4-метокси-бензилокси)-3-метил-бифенил-2-ил]-2-(трет-бутокси) ацетата (15а) (139 мг, 0,3 ммоль) и формиата аммония (470 мг, 7,45 ммоль) в метаноле (3 мл). Смесь нагревали в колбе с обратным холодильником в течение 120 минут, охлаждали до комнатной температуры, фильтровали через Celite® и промывали с использованием метанола и этилацетата. Фильтрат концентрировали в вакууме. Остаток растворяли в этилацетате (5 мл) и аккуратно промывали водой (5 мл) и солевым раствором (5 мл). Органический слой сушили над сульфатом натрия, концентрировали в вакууме с получением метил 2-(трет-бутокси)-2-(4'-фтор-6-гидрокси-3-метил-бифенил-2-и)-ацетата (15b) (103 мг, 0,3 ммоль, 100%), который использовали без дополнительной очистки.
1Н ЯМР (400 МГц, CDCl3) δ 0,96 (с, 9Н), 2,36 (с, 3H), 3,69 (с, 3H), 4,49 (уш. с, 1Н), 4,91 (с, 1Н), 6,85 (д, J=8,3 Гц, 1Н), 7,07 (д, J=8,3 Гц, 1Н), 7,16-7,26 (м, 2Н), 7,28-7,33 (м, 1Н), 7,45-7,51 (м, 1Н).
MS m/z ([M+Na]+) 369.
MS m/z ([M-H]-) 345.
Стадия 3: получение промежуточного соединения метил 2-(трет-бутокси)-2-(4'-фтор-3-метил-6-трифторметансульфонилокси-бифенил-2-у)-ацетат (15с)
С использованием процедуры, описанной в примере 1, стадии 10, промежуточное соединение метил 2-(трет-бутокси)-2-(4'-фтор-6-гидрокси-3-метил-бифенил-2-у)-ацетат (15b) (103 мг, 0,3 ммоль) превращали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20) в метил 2-(трет-бутокси)-2-(4'-фтор-3-метил-6-трифторметансульфонилокси-бифенил-2-у)-ацетат (15с) (114 мг, 0,24 ммоль, 80%).
1Н ЯМР (400 МГц, CDCl3) δ 0,95 (с, 9Н), 2,46 (с, 3H), 3,72 (с, 3H), 5,05 (с, 1H), 7,11-7,30 (м, 5Н), 7,39-7,45 (м, 1Н).
MS m/z ([M-H]-) 477.
Стадия 4: получение промежуточного соединения метил 2-(трет-бутокси)-2-(6-циклопропил-4'-фтор-3-метил-бифенил-2-ил)-ацетата (15d)
С использованием процедуры, описанной в примере 1, стадии 11, промежуточное соединение метил 2-(трет-бутокси)-2-(4'-фтор-3-метил-6-трифторметансульфонилокси-бифенил-2-ил)-ацетат (15с) (114 мг, 0,24 ммоль) превращали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 90/10) в метил 2-(трет-бутокси)-2-(6-циклопропил-4'-фтор-3-метил-бифенил-2-ил)-ацетат (15d) (66 мг, 0,19 ммоль, 75%).
1Н ЯМР (300 МГц, CDCl3) δ 0,50-0,74 (м, 4Н), 0,97 (с, 9Н), 1,30-1,42 (м, 1Н), 2,40 (с, 3H), 3,67 (с, 3H), 4,99 (с, 1H), 6,80 (д, J=7,9 Гц, 1Н), 7,04-7,18 (м, 3H), 7,23-7,30 (м, 1Н), 7,34-7,42 (м, 1H).
MS m/z ([M+Na]+) 393.
Стадия 5: получение 2-(трет-бутокси)-2-(6-циклопропил-4'-фтор-3-метил-бифенил-2-ил)-уксусной кислоты (пример 15)
С использованием процедуры, описанной в примере 1, стадии 12, промежуточное соединение метил 2-(трет-бутокси)-2-(6-циклопропил-4'-фтор-3-метил-бифенил-2-ил)-ацетат (15d) (66 мг, 0,18 ммоль) превращали в 2-(трет-бутокси)-2-(6-циклопропил-4'-фтор-3-метил-бифенил-2-ил)-уксусную кислоту (пример 15) (51 мг, 0,14 ммоль, 80%).
1Н ЯМР (300 МГц, CDCl3) δ 0,48-0,64 (м, 3H), 0,68-0,77 (м, 1H), 1,00 (с, 9Н), 1,36-1,48 (м, 1H), 2,37 (с, 3H), 5,11 (с, 1Н), 6,84 (д, J=7,9 Гц, 1Н), 7,04-7,20 (м, 3H), 7,24-7,35 (м, 1Н), 7,50-7,61 (м, 1H).
MS m/z ([M+Na]+) 379.
MS m/z ([M-H]-) 355.
Пример 16: синтез 2-(трет-бутокси)-2-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)фенил] уксусной кислоты

Стадия 1: получение промежуточного соединения метил 2-[3-(4-метокси-бензилокси)-6-метил-2-(5-метил-хроман-6-ил)-фенил]-2-(трет-бутокси)-ацетат (16а)
С использованием процедуры, описанной в примере 1, стадия 7, промежуточное соединение метил 2-[2-бром-3-(4-метокси-бензилокси)-6-метил-фенил]-2-(трет-бутокси)-ацетат (12b) (150 мг, 0,33 ммоль) превращали с помощью реакции с 4,4,5,5-тетраметил-2-(5-метил-3,4-дигидро-2H-1-бензопиран-6-ил)-1,3,2-диоксабороланом (109 мг, 0,4 ммоль), после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20), в метил 2-[3-(4-метокси-бензилокси)-6-метил-2-(5-метил-хроман-6-ил)-фенил]-2-(трет-бутокси)-ацетат (16а) (129 мг, 0,25 ммоль, 75%).
1Н ЯМР (400 МГц, CDCl3) δ 1,11 (с, 9Н), 1,85 (с, 3H), 2,06-2,16 (м, 2Н), 2,45 (с, 3H), 2,65-2,73 (м, 2Н), 3,56 (с, 3H), 3,77 (с, 3H), 4,18-4,24 (м, 2Н), 4,81-4,88 (м, 2Н), 5,08 (с, 1Н), 6,71 (д, J=8,3 Гц, 1Н), 6,76 (д, J=8,6 Гц, 2Н), 6,81 (д, J=8,3 Гц, 1H), 6,87 (д, J=8,3 Гц, 1Н), 6,96 (д, J=8,6 Гц, 2Н), 7,06 (д, J=8,3 Гц, 1Н).
MS m/z ([M+Na]+) 541.
Стадия 2: получение промежуточного соединения метил 2-(трет-бутокси)-2-[3-гидрокси-6-метил-2-(5-метил-хроман-6-ил)-фенил] ацетат (16b)
С использованием процедуры, описанной в примере 15, стадии 2, промежуточное соединение метил 2-[3-(4-метокси-бензилокси)-6-метил-2-(5-метил-хроман-6-ил)-фенил]-2-(трет-бутокси)-ацетат (16а) (129 мг, 0,25 ммоль) превращали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 70/30) в метил 2-(трет-бутокси)-2-[3-гидрокси-6-метил-2-(5-метил-хроман-6-ил)-фенил]ацетат (16b) (91 мг, 0,23 ммоль, 92%).
1Н ЯМР (400 МГц, CDCl3) δ 1,09 (с, 9Н), 1,91 (с, 3H), 2,06-2,17 (м, 2Н), 2,43 (с, 3H), 2,67-2,75 (м, 2Н), 3,58 (с, 3H), 4,18-4,24 (м, 2Н), 4,40 (с, 1H), 4,93 (с, 1H), 6,77 (д, J=8,3 Гц, 1Н), 6,83 (д, J=8,3 Гц, 1H), 6,93 (д, J=8,3 Гц, 1H), 7,06 (д, J=8,3 Гц, 1Н).
MS m/z ([M+Na]+) 421.
MS m/z ([М-Н]-) 397.
Стадия 3: получение промежуточного соединения метил 2-(трет-бутокси)-2-[6-метил-2-(5-метил-хроман-6-ил)-3-трифторметансульфонилокси-фенил]ацетата (16с)
С использованием процедуры, описанной в примере 1, стадии 10, промежуточное соединение метил 2-(трет-бутокси)-2-[3-гидрокси-6-метил-2-(5-метил-хроман-6-ил)-фенил]ацетат (16b) (91 мг, '0,23 ммоль) превращали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 85/15) в метил 2-(трет-бутокси)-2-[6-метил-2-(5-метил-хроман-6-ил)-3-трифтор метансульфонилокси-фенил]ацетат (16с) (106 мг, 0,20 ммоль, 87%).
1Н ЯМР (400 МГц, CDCl3) δ 1,09 (с, 9Н), 1,84 (с, 3H), 2,06-2,13 (м, 2Н), 2,53 (с, 3H), 2,65-2,71 (м, 2Н), 3,58 (с, 3H), 4,16-4,22 (м, 2Н), 5,08 (с, 1Н), 6,72 (д, J=8,4 Гц, 1Н), 6,88 (д, J=8,4 Гц, 1Н), 7,16 (д, J=8,5 Гц, 1Н), 7,21 (д, J=8,5 Гц, 1Н).
MS m/z ([М-Н]-) 529.
Стадия 4: получение промежуточного соединения метил 2-(трет-бутокси)-2-[6-метил-2-(5-метил-хроман-6-ил)-3-винил-фенил] ацетата (16d)
Дегазированный раствор метил 2-(трет-бутокси)-2-[6-метил-2-(5-метил-хроман-6-ил)-3-трифторметансульфонилокси-фенил] ацетата (16с) (106 мг, 0,2 ммоль), карбонат калия (75 мг, 0,54 ммоль), сложный эфир пинакола и винилбороновой кислоты (62 мг, 0,4 ммоль) и тетракис(трифенилфосфин) палладия (23 мг, 0,02 ммоль) в диоксане (1 мл) и воду (0,25 мл) нагревали в микроволновой печи при 120°C в течение 5 часов. Добавляли воду (2 мл) и смесь экстрагировали с использованием AcOEt (3×4 мл). Органический слой промывали с использованием солевого раствора (6 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/ AcOEt 85/15) с получением метил 2-(трет-бутокси)-2-[6-метил-2-(5-метил-хроман-6-ил)-3-винил-фенил] ацетата (16d) (30 мг, 0,073 ммоль, 37%).
1Н ЯМР (400 МГц, CDCl3) δ 1,09 (с, 9Н), 1,77 (с, 3H), 2,06-2,15 (м, 2Н), 2,51 (с, 3H), 2,65-2,72 (м, 2Н), 3,56 (с, 3H), 4,17-4,23 (м, 2Н), 4,95 (дд, J=1,3 Гц, J=11,0 Гц, 1H), 5,04 (с, 1H), 5,52 (дд, J=1,3 Гц, J=17,5 Гц, 1H), 6,14 (дд, J=11,0 Гц, J=17,5 Гц, 1Н), 6,70 (д, J=8,3 Гц, 1Н), 6,83 (д, J=8,3 Гц, 1Н), 7,14 (д, J=8,0 Гц, 1H), 7,47 (д, J=8,0 Гц, 1Н).
MS m/z ([M+Na]+) 431.
Стадия 5: получение промежуточного соединения метил 2-(трет-бутокси)-2-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил] ацетата (16е)
В атмосфере азота раствор метил 2-(трет-бутокси)-2-[6-метил-2-(5-метил-хроман-6-ил)-3-винил-фенил] ацетата (16d) (30 мг, 0,073 ммоль) в безводном 1,2-дихлорэтане (2 мл) охлаждали до 0°C. Дииодометан (59 μл, 0,734 ммоль) и раствор диэтилцинка 15 масс. % в толуоле (334 μл, 0,367 ммоль) добавляли, и реакционную смесь встряхивали при комнатной температуре в течение 40 часов. Смесь гасили насыщенным раствором хлорида аммония (5 мл) и экстрагировали этилацетатом (2×5 мл). Органический слой промывали с использованием солевого раствора (6 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/ AcOEt 95/5) с получением метил 2-(трет-бутокси)-2-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил] ацетата (16е) (6,7 мг, 0,016 ммоль, 22%).
1Н ЯМР (400 МГц, CDCl3) δ 0,48-0,69 (м, 4Н), 1,08 (с, 9Н), 1,23-1,33 (м, 1H), 1,86 (с, 3H), 2,05-2,16 (м, 2Н), 2,47 (с, 3H), 2,63-2,76 (м, 2Н), 3,57 (с, 3H), 4,16-4,24 (м, 2Н), 5,03 (с, 1Н), 6,68-6,72 (м, 2Н), 6,89 (д, J=8,3 Гц, 1Н), 7,06 (д, J=8,0 Гц, 1H).
MS m/z ([M+Na]+) 445.
Стадия 6: получение 2-(трет-бутокси)-2-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил] уксусной кислоты (пример 16)
С использованием процедуры, описанной в примере 1, стадии 12, промежуточное соединение метил 2-(трет-бутокси)-2-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил] ацетат (16е) (6,7 мг, 0,016 ммоль) превращали в 2-(трет-бутокси)-2-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил] уксусную кислоту (6 мг, 0,015 ммоль, 93%)).
1Н ЯМР (400 МГц, CDCl3) δ 0,48-0,59 (м, 2Н), 0,59-0,70 (м, 2Н), 1,11 (с, 9Н), 1,27-1,36 (м, 1Н), 1,94 (с, 3H), 2,04-2,12 (м, 2Н), 2,38 (с, 3H), 2,62-2,72 (м, 2Н), 4,15-4,20 (м, 2Н), 5,11 (с, 1H), 6,69 (д, J=8,3 Гц, 1H), 6,73 (д, J=7,9 Гц, 1H), 6,88-6,94 (м, 1Н), 7,05 (д, J=7,9 Гц, 1Н).
MS m/z ([M+Na]+) 431.
MS m/z ([М-Н]-) 407.
Пример 17: синтез Ггаранс-3-бициклопропил-2-ил-2-хроман-6-ил-6-метил-фенил)-трет-бутокси-уксусной кислоты

Стадия 1: получение промежуточного соединения сложного метилового эфира трет-бутокси-[2-хроман-6-ил-6-метил-3-(транс-2-циклопропил-циклопропил)-фенил]-уксусной кислоты (17а)
С использованием процедуры, описанной в примере 1, стадия 11, промежуточное соединение метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетат (1j) (100 мг, 0,19 ммоль) превращали с помощью реакции с транс-2-циклопропил-циклопропилбороновой кислотой (138 мг, 1,1 ммоль), после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 90/10), в промежуточное соединение сложный метиловый эфир трет-бутокси-[2-хроман-6-ил-6-метил-3-(транс-2-циклопропил-циклопропил)-фенил]-уксусной кислоты (17а) (9 мг, 0,035 ммоль, 10%), загрязненный 20% транс-2-циклопропил-циклопропилбороновой кислотой.
1Н ЯМР (400 МГц, CDCl3) δ -0,18- -0,12 (м, 1H), -0,01-0,43 (м, 3H), 0,45- 0,95 (м, 4Н), 1,01-1,08 (м, 9Н), 1,27-1,38 (м, 1H), 2,04-2,13 (м, 2Н), 2,42 и 2,43 (с, 3H), 2,72-2,89 (м, 2Н), 3,69 и 3,71 (с, 3H), 4,26-4,30 (м, 2Н), 5,11-5,14 (м, 1Н), 6,71-7,15 (м, 5Н).
MS m/z ([M+Na]+) 471.
Стадия 2: получение 3-(транс-бициклопропил-2-ил)-2-хроман-6-ил-6-метил-фенил-трет-бутокси-уксусной кислоты (пример 17)
С использованием процедуры, описанной в примере 1, стадия 12, сложный метиловый эфир трет-бутокси-[2-хроман-6-ил-6-метил-3-(транс-2-циклопропил-циклопропил)-фенил]-уксусной кислоты (17а) (9 мг, 0,02 ммоль, чистота 80%) превращали в 3-(транс-бициклопропил-2-ил)-2-хроман-6-ил-6-метил-фенил-трет-бутокси-уксусную кислоту (пример 17) (9,2 мг, 0,021 ммоль, 100%, чистота 70%) в виде белого твердого вещества.
1Н ЯМР (400 МГц, CDCl3) δ -0,24- -0,20 (м, 1Н), -0,01-0,53 (м, 3H), 0,67-0,91 (м, 2Н), 1,01 (м, 9Н), 1,15-1,43 (м, 2Н),1,56 (уш. с, 1Н), 2,00-2,10 (м, 2Н); 2,34 (с, 3H), 2,73-2,87 (м, 2Н), 4,22-4,25 (м, 2Н), 5,22-5,25 (м, 1H), 6,70-7,03 (м, 4Н), 7,19-7,23 (м, 1H), 9,82 (уш. с, 1Н).
MS m/z ([M+Na]+) 457.
MS m/z ([M-H]-) 433.
Пример 18: синтез 2-(трет-бутокси)-2-[3-циклопропил-2-(4,4-диметил-циклогекс-1-енил)-6-метил-фенил] уксусной кислоты
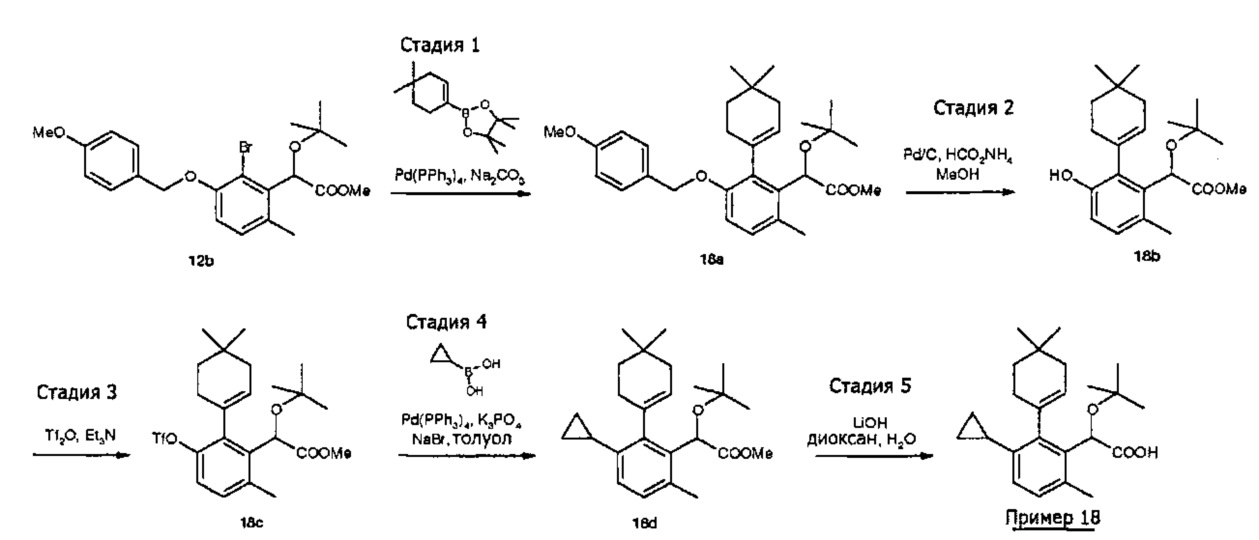
Стадия 1: получение промежуточного соединения метил 2-[2-(4,4-диметил-циклогекс-1-енил)-3-(4-метокси-бензилокси)-6-метил-фенил]-2-(трет-бутокси) ацетата (18а)
С использованием процедуры, описанной в примере 1, стадия 7, промежуточное соединение метил 2-[2-бром-3-(4-метокси-бензилокси)-6-метил-фенил]-2-(трет-бутокси)-ацетат (12b) (150 мг, 0,33 ммоль) превращали с помощью реакции со сложным эфиром пинакола и 4,4-(диметилциклогексен-1-ил)бороновой кислоты (94 мг, 0,4 ммоль), после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 90/10) в метил 2-[2-(4,4-диметил-циклогекс-1-енил)-3-(4-метокси-бензилокси)-6-метил-фенил]-2-(трет-бутокси) ацетат (18а) (144 мг, 0,3 ммоль, 90%).
1Н ЯМР (400 МГц, CDCl3) δ 0,84 и 0,90 (с, 3H), 0,99 и 1,01 (с, 3H), 1,18 и 1,20 (с, 9Н), 1,38-1,49 (м, 2Н), 1,84-2,07 и 2,58-2,70 (м, 3H), 2,24-2,32 (м, 1Н), 2,36 и 2,40 (с, 3H), 3,63 и 3,65 (с, 3H), 3,81 (с, 3H), 4,86-4,97 (м, 2Н), 5,40 и 5,63 (уш. с, 1Н), 5,49 и 5,57 (с, 1Н), 6,78 (д, J=8,3 Гц, 1Н), 6,84-6,90 (м, 2Н), 6,97 (д, J=8,3 Гц, 1Н), 7,28-7,34 (м, 2Н).
Стадия 2: получение промежуточного соединения метил 2-(трет-бутокси)-2-[2-(4,4-диметил-циклогекс-1-енил)-3-гидрокси-6-метил-фенил] ацетата (18b)
С использованием процедуры, описанной в примере 15, стадии 2, промежуточное соединение метил 2-[2-(4,4-диметил-циклогекс-1-енил)-3-(4-метокси-бензилокси)-6-метил-фенил]-2-(трет-бутокси) ацетат (18а) (144 мг, 0,3 ммоль) превращали в метил 2-(трет-бутокси)-2-[2-(4,4-диметил-циклогекс-1-енил)-3-гидрокси-6-метил-фенил] ацетат (18b) (103 мг, 0,29 ммоль, 95%), который использовали без дополнительной очистки.
1Н ЯМР (400 МГц, CDCl3) δ 1,04 (с, 3H), 1,07 (с, 3H), 1,18 и 1,21 (с, 9Н), 1,46-1,61 (м, 2Н), 1,94-2,30 (м, 3H), 2,34 и 2,41 (с, 3H), 2,44-2,55 (м, 1Н), 3,63 и 3,66 (с, 3H), 4,94 и 5,10 (с, 1Н), 5,20 и 5,27 (с, 1Н), 5,63-5,81 (м, 1Н), 6,74-7,10 (м, 3H).
MS m/z ([M+Na]+) 383.
MS m/z ([M-H]-) 359.
Стадия 3: получение промежуточного соединения метил 2-(трет-6утокси)-2-[2-(4,4-диметил-циклогекс-1-енил)-6-метил-3-трифторметансульфонилокси-фенил] ацетата (18с)
С использованием процедуры, описанной в примере 1, стадии 10, промежуточное соединение метил 2-(трет-бутокси)-2-[2-(4,4-диметил-циклогекс-1-енил)-3-гидрокси-6-метил-фенил] ацетат (18b) (103 мг, 0,29 ммоль) превращали, после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 85/15), в метил 2-(трет-бутокси)-2-[2-(4,4-диметил-циклогекс-1-енил)-6-метил-3-трифторметансульфонилокси-фенил] ацетат (18с) (134 мг, 0,27 ммоль, 95%).
1Н ЯМР (400 МГц, CDCl3) δ 1,02-1,07 (м, 6Н), 1,18 и 1,19 (с, 9Н), 1,44-1,66 (м, 2Н), 1,86-2,19 (м, 3H), 2,30-2,42 (м, 1Н), 2,46 и 2,48 (с, 3H), 3,66 (с, 3H), 5,41 и 5,42 (с, 1Н), 5,53-5,76 (м, 1H), 7,07 (д, J=8,5 Гц, 1Н), 7,10 (д, J=8,5 Гц, 1Н).
Стадия 4: получение промежуточного соединения метил 2-(трет-бутокси)-2-[3-циклопропил-2-(4,4-диметил-циклогекс-1-енил)-6-метил-фенил] ацетата (18d)
С использованием процедуры, описанной в примере 1, стадии 11, промежуточное соединение метил 2-(трет-бутокси)-2-[2-(4,4-диметил-циклогекс-1-енил)-6-метил-3-трифторметансульфонилокси-фенил] ацетат (18с) (80 мг, 0,162 ммоль) превращали, после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20) в метил 2-(трет-бутокси)-2-[3-циклопропил-2-(4,4-диметил-циклогекс-1-енил)-6-метил-фенил] ацетат (18d) (32 мг, 0,083 ммоль, 51%).
1Н ЯМР (300 МГц, CDCl3) δ 0,50-0,75 (м, 2Н), 0,77-0,91 (м, 2Н), 1,03 (с, 3H), 1,07 (с, 3H), 1,19 и 1,21 (с, 9Н), 1,48-1,57 (м, 2Н), 1,85-2,05 (м, 3H), 2,15-2,30 (м, 1Н), 2,36-2,55 (м, 4Н), 3,63 и 3,64 (с, 3H), 5,41-5,62 (м, 2Н), 6,68 и 6,70 (д, J=7,9 Гц, 1Н), 6,95 (д, J=7,9 Гц, 1Н).
MS m/z ([M+Na]+) 407.
Стадия 5: получение 2-(трет-бутокси)-2-[3-циклопропил-2-(4,4-диметил-циклогекс-1-енил)-6-метил-фенил] уксусной кислоты (пример 18)
С использованием процедуры, описанной в примере 1, стадии 12, промежуточное соединение метил 2-(трет-бутокси)-2-[3-циклопропил-2-(4,4-диметил-циклогекс-1-енил)-6-метил-фенил] ацетат (18d) (32 мг, 0,083 ммоль) превращали в 2-(трет-бутокси)-2-[3-циклопропил-2-(4,4-диметил-циклогекс-1-енил)-6-метил-фенил] уксусную кислоту (18d) (22 мг, 0,059 ммоль, 71%).
1Н ЯМР (300 МГц, CDCl3) δ 0,50-0,75 (м, 2Н), 0,78-0,94 (м, 2Н), 0,98-1,08 (м, 6Н), 1,19-1,26 (м, 9Н), 1,46-1,56 (м, 2Н), 1,81-2,10 (м, 3H), 2,10-2,64 (м, 5Н), 5,28-5,98 (м, 2Н), 6,68-6,77 (м, 1Н), 6,91-7,00 (м, 1Н).
MS m/z ([M+Na]+) 393.
MS m/z ([M-H]-) 369.
Пример 19: Синтез 2-(2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-этокси-уксусной кислоты

Стадия 1: Получение промежуточного соединения метил-2-(3-бензилокси-2-хроман-6-ил-6-метил-фенил)-2-этокси ацетата (19а)
В атмосфере азота раствор метил-2-[3-бензил окси-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-гидроксиацетата (1g) (100 мг, 0,24 ммоль) в безводном N,N-диметилформамиде (5 мл) охлаждали до 0°C. Гидрид натрия 60% в масле (9,5 мг, 0,24 ммоль) добавляли порциями. После 15 минут перемешивания, добавляли йодэтан (58 мкл, 0,72 ммоль) и перемешивали смесь при комнатной температуре в течение 5 часов. Смесь гасили при 0°C водой (5 мл) и экстрагировали этилацетатом (2×5 мл). Органический слой промывали насыщенным раствором соли (10 мл), затем сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 90/10), с получением метил 2-(3-бензилокси-2-хроман-6-ил-6-метил-фенил)-2-этокси ацетата (19а) (106 мг, 0,24 ммоль, 100%).
1Н ЯМР (400 МГц, CDCl3) δ 1,08-1,13 (м, 3H), 2,01-2,09 (м, 2Н), 2,30 (с, 3H), 2,71-2,86 (м, 2Н), 3,23-3,33 (м, 1Н), 3,35-3,51 (м, 1Н), 3,69 и 3,70 (с, 3H), 4,21-4,26 (м, 2Н), 4,93-4,99 (м, 2Н), 5,01 и 5,02 (с, 1Н), 6,83 и 6,84 (д, J=8,2 Гц, 1H), 6,86 и 6,88 (д, J=2,0 Гц, 1Н), 6,92-7,09 (м, 3H), 7,13-7,18 (м, 2Н), 7,20-7,30 (м, 3H),
МС m/z ([M+Na]+) 469.
Стадия 2: Получение промежуточного соединения метил-2-(2-хроман-6-ил-3-гидрокси-6-метил-фенил)-2-этокси ацетата (19b)
С помощью процедуры, описанной в примере 15, стадии 2, промежуточное соединение метил 2-(3-бензилокси-2-хроман-6-ил-6-метил-фенил)-2-этокси ацетат (19а) (106 мг, 0,24 ммоль) преобразовали в метил-2-(2-хроман-6-ил-3-гидрокси-6-метил-фенил)-2-этокси ацетат (19b) (82 мг, 0,23 ммоль, 97%), который использовали без дальнейшей очистки.
1Н ЯМР (400 МГц, CDCl3) δ 1,08-1,14 (м, 3H), 2,01-2,10 (м, 2Н), 2,29 (с, 3H), 2,73-2,87 (м, 2Н), 3,23-3,33 (м, 1Н), 3,35-3,49 (м, 1Н), 3,68 и 3,69 (с, 3H), 4,22-4,27 (м, 2Н), 4,66 и 4,68 (с, 1Н), 4,86 и 4,87 (с, 1Н), 6,84-6,99 (м, 3H), 7,03-7,10 (м, 2Н),
МС m/z ([M+Na]+) 379.
Стадия 3: Получение промежуточного соединения метил-2-(2-хроман-6-ил-6-метил-3-трифторметил-фенил метансульфонилокси)-2-этокси-ацетата (19с)
С помощью процедуры, описанной в примере 1, стадии 10, промежуточное соединение метил-2-(2-хроман-6-ил-3-гидрокси-6-метил-фенил)-2-этокси ацетат (19b) (82 мг, 0,23 ммоль) преобразовали в метил-2-(2-хроман-6-ил-6-метил-3-трифторметансульфонилокси-фенил)-2-этокси-ацетат (19с) (104 мг, 0,21 ммоль, 93%), который использовали без дальнейшей очистки.
1Н ЯМР (300 МГц, CDCl3) δ 1,11 и 1,12 (т, J=7,0 Гц, 3H), 1,99-2,09 (м, 2Н), 2,39 и 2,40 (с, 3H), 2,68-2,90 (м, 2Н), 3,20-3,32 (м, 1H), 3,39-3,51 (м, 1H), 3,69 и 3,70 (с, 3H), 4,20-4,27 (м, 2Н), 4,96 и 4,97 (с, 1Н), 6,81-6,87 (м, 1H), 6,89-6,04 (м, 2Н), 7,21 (с, 2Н),
МС m/z ([М-Н]-) 487.
Стадия 4: Получение промежуточного соединения метил-2-(2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-этокси-ацетата (19d)
С помощью процедуры, описанной в примере 1, стадии 11, промежуточное соединение метил-2-(2-хроман-6-ил-6-метил-3-трифторметансульфонилокси-фенил)-2-этокси-ацетат (19с) (104 мг, 0,21 ммоль) преобразовали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20), в метил-2-(2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-этокси-ацетат (19d) (40 мг, 0,105 ммоль, 49%).
1Н ЯМР (300 МГц, CDCl3) δ 0,49-0,74 (м, 4Н), 1,09 и 1,11 (т, J=7,0 Гц, 3H), 1,42-1,53 (м, 1Н), 1,99-2,11 (м, 2Н), 2,32 (с, 3H), 2,70-2,88 (м, 2Н), 3,19-3,33 (м, 1H), 3,33-3,51 (м, 1Н), 3,67 и 3,69 (с, 3H), 4,20-4,27 (м, 2Н), 4,93 и 4,96 (с, 1Н), 6,74-6,85 (м, 2Н), 6,88-7,09 (м, 3H),
MC m/z ([M+Na]+) 403.
Стадия 5: Получение 2-(2-хроман-6-ил-3 -циклопропил-6-метил-фенил)-2-этокси-уксусной кислоты (пример 19)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метил-2-(2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-этокси-ацетата (19d) (40 мг, 0,105 ммоль) преобразовали в 2-(2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-этокси-уксусную кислоту (пример 19) (30 мг, 0,082 ммоль, 78%).
1Н ЯМР (300 МГц, CDCl3) δ 0,51-0,76 (м, 4Н), 1,10 и 1,11 (т, J=7,0 Гц, 3H), 1,44-1,54 (м, 1H), 1,99-2,09 (м, 2Н), 2,31 и 2,32 (с, 3H), 2,72-2,87 (м, 2Н), 3,20-3,42 (м, 2Н), 4,20-4,26 (м, 2Н), 5,04 и 5,06 (с, 1H), 6,77-6,84 (м, 2Н), 6,87-6,94 (м, 1Н), 7,01-7,09 (м, 2Н),
MC m/z ([M+Na]+) 389.
MC m/z ([M-H]-) 365.
Пример 20: Синтез 2-(трет-бутокси)-2-(4'-хлор-6-циклопропил-3-метил-бифенил-2-ил) уксусной кислоты
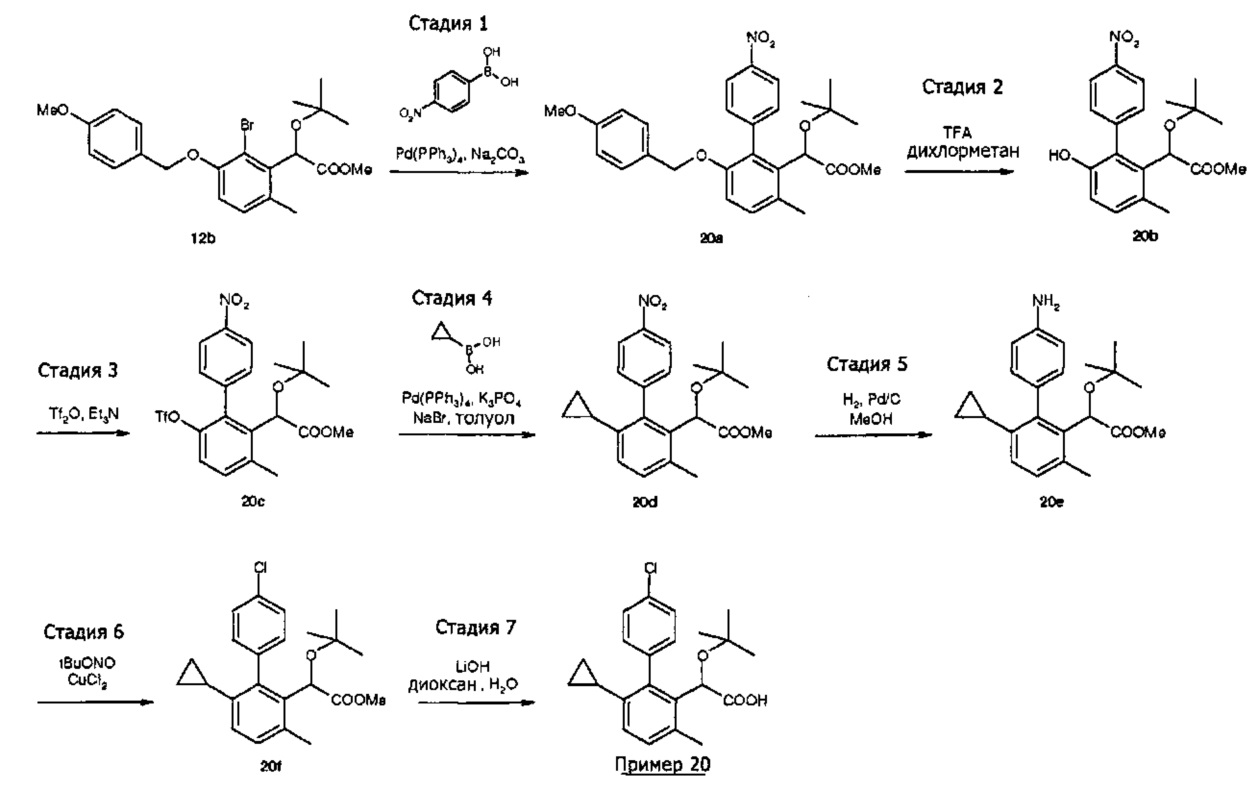
Стадия 1: Получение промежуточного соединения метил-2-(трет-бутокси)-2-[6-(4-метокси-бензилокси)-3-метил-4'-нитро-дифенил-2-ил] ацетата (20а)
С помощью процедуры, описанной в примере 1, стадии 7, промежуточное соединение метил 2-[2-бром-3-(4-метокси-бензилокси)-6-метил-фенил]-2-(трет-бутокси) ацетат (12b) (500 мг, 1,11 ммоль) преобразовали реакцией с 4-нитрофенилбороновой кислотой (222 мг, 1,33 ммоль), после очистки с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат 100/0 до 95/05), в метил-2-(трет-бутокси)-2-[6-(4-метокси-бензилокси)-3-метил-4'-нитро-дифенил-2-ил] ацетат (20а) (497 мг, 1,01 ммоль, 91%).
1Н ЯМР (300 МГц, CDCl3) δ 0,94 (с, 9Н), 2,38 (с, 3H), 3,71 (с, 3H), 3,77 (с, 3H), 4,84 (д, J=11,8 Гц, 1H), 4,88 (с, 1H), 4,91 (д, J=11,8 Гц, 1Н), 6,76-6,82 (м, 2Н), 6,91 (д, /=8,4 Гц, 1Н), 6,97-7,03 (м, 2Н), 7,15 (д, J=8,4 Гц, 1H), 7,45 (дд, J=1,7 Гц, J=8,4 Гц, 1H), 7,60 (дд, J=1,7 Гц, J=8,4 Гц, 1H), 8,23 (дд, J=2,4 Гц, J=8,4 Гц, 1Н), 8,28 (дд, J=2,4 Гц, J=8,4 Гц, 1Н).
MC m/z ([M+Na]+) 516.
Стадия 2: Получение промежуточного соединения метил-2-(трет-бутокси)-2-(6-гидрокси-3-метил-4'-нитро-дифенил-2-ил) ацетата (20b)
Трифторуксусную кислоту (0,98 мл, 12,79 ммоль) добавляли к раствору метилового эфира 2-(трет-бутокси)-2-[6-(4-метокси-бензилокси)-3-метил-4'-нитро-бифенил-2-ил] ацетата (20а) (485 мг, 0,98 ммоль) в дихлорметане (19,6 мл). Реакционную смесь перемешивали при комнатной температуре в течение 5 минут и немедленно нейтрализовали насыщенным раствором бикарбоната натрия (25 мл). Смесь экстрагировали дихлорметаном (2×20 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 60/40), для получения метил-2-(трет-бутокси)-2-(6-гидрокси-3-метил-4'-нитро-дифенил-2-ил) ацетата (20b) (319 мг, 0,59 ммоль, 87%).
МС m/z ([M+Na]+) 396.
МС m/z ([М-Н]-) 472.
Стадия 3: Получение промежуточного соединения метил-2-(трет-бутокси)-2-(3-метил-4'-нитро-6-трифторметансульфонилокси-дифенил-2-ил) ацетата (20с)
С помощью процедуры, описанной в примере 1, стадии 10, промежуточное соединение метил-2-(трет-бутокси)-2-(6-гидрокси-3-метил-4'-нитро-дифенил-2-ил) ацетат (20b) (360 мг, 0,96 ммоль) преобразовали в метил-2-(трет-бутокси)-2-(3-метил-4'-нитро-6-трифторметансульфонилокси-дифенил-2-ил) ацетат (20с) (487 мг, 0,96 ммоль, 100%), который использовали без дальнейшей очистки.
1Н ЯМР (300 МГц, CDCl3) δ 0,96 (с, 9Н), 2,49 (с, 3H), 3,72 (с, 3H), 4,88 (с, 1Н), 7,24 (д, J=7,3 Гц, 1Н), 7,32 (д, J=7,3 Гц, 1Н), 7,44-7,50 (м, 1Н), 7,62-7,68 (м, 1H), 8,30-8,37 (м, 2Н).
МС m/z ([М-Н]-) 504.
Стадия 4: Получение промежуточного соединения метил-2-(трет-бутокси)-2-(6-циклопропил-3-метил-4'-нитро-дифенил-2-ил) ацетата (20d)
С помощью процедуры, описанной в примере 1, стадии 11, промежуточное соединение метил 2-(трет-бутокси)-2-(3-метил-4'-нитро-6-трифторметансульфонилокси-дифенил-2-ил) ацетат (20с) (387 мг, 0,77 ммоль) преобразовали после очистки препаративной ТСХ (циклогексан/этилацетат 80/20), в метил-2-(трет-бутокси)-2-(6-циклопропил-3-метил-4'-нитро-дифенил-2-ил) ацетат (20d) (209 мг, 0,53 ммоль, 69%).
1Н ЯМР (400 МГц, CDCl3) δ 0,51-0,63 (м, 3H), 0,63-0,72 (м, 1H), 0,98 (с, 9Н), 1,22-1,30 (м, 1H), 2,43 (с, 3H), 3,67 (с, 3H), 4,85 (с, 1Н), 6,86 (д, J=8,0 Гц, 1Н), 7,13 (д, J=8,0 Гц, 1H), 7,47 (дд, J=1,6 Гц, J=8,0 Гц, 1Н), 7,62 (дд, J=1,6 Гц, J=8,2 Гц, 1Н), 8,26-8,34 (м, 2Н).
Стадия 5: Получение промежуточного соединения метил-2-(4'-амино-6-циклопропил-3-метил-бифенил-2-ил)-2-(трет-бутокси) ацетата (20е)
Раствор метил-2-(трет-бутокси)-2-(6-циклопропил-3-метил-4'-нитро-дифенил-2-ил) ацетат (20d) (209 мг, 0,53 ммоль) и палладий на углероде (21 мг) в метаноле (8 мл) перемешивали при комнатной температуре в атмосфере водорода в течение 1 часа. Смесь фильтровали через Millipore и концентрировали в вакууме с получением метил 2-(4'-амино-6-циклопропил-3-метил-бифенил-2-ил)-2-(трет-бутокси) ацетата (20е) (190 мг, 0,52 ммоль, 98%), который использовали без дальнейшей очистки.
1Н ЯМР (400 МГц, CDCl3) δ 0,50-0,65 (м, 3H), 0,66-0,74 (м, 1H), 0,98 (с, 9Н), 1,43-1,51 (м, 1H), 2,39 (с, 3H), 3,67 (с, 3H), 5,14 (с, 1Н), 6,74-6,84 (м, 3H), 7,04 (д, J=7,9 Гц, 1Н), 7,11 (дд, J=1,9 Гц, J=7,9 Гц, 1Н), 7,20 (дд, J=1,9 Гц, J=7,9 Гц, 1Н).
МС m/z ([M+Na]+) 390.
Стадия 6: Получение промежуточного соединения метил-2-(трет-бутокси)-2-(4'-хлор-6-циклопропил-3-метил-бифенил-2-ил) ацетата (20f)
В атмосфере азота трет-бутил нитрит (23 мкл, 0,20 ммоль) добавляли к суспензии хлорида меди(II) (26 мг, 0,19 ммоль) в безводном ацетонитриле (1 мл), предварительно охлажденного до 0°C. Раствор метил-2-(4'-амино-6-циклопропил-3-метил-бифенил-2-ил)-2-(трет-бутокси) ацетата (20е) (50 мг, 0,14 ммоль) в безводном ацетонитриле (1 мл) добавляли по каплям. Реакционную смесь перемешивали при комнатной температуре в течение ночи и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 85/15) с получением метил-2-(трет-бутокси)-2-(4'-хлор-6-циклопропил-3-метил-бифенил-2-ил) ацетата (20f) (24 мг, 0,06 ммоль, 46%).
1Н ЯМР (400 МГц, CDCl3) δ 0,52-0,65 (м, 3H), 0,65-0,73 (м, 1Н), 0,98 и 0,99 (с, 9Н), 1,31-1,40 (м, 1Н), 2,41 (с, 3H), 3,67 и 3,68 (с, 3H), 4,96 и 4,97 (с, 1H), 6,78-6,84 (м, 1Н), 7,06-7,12 (м, 1Н), 7,22-7,28 (м, 1H), 7,33-7,46 (м, 3H).
МС m/z ([M+Na]+) 409.
Стадия 7: Получение 2-(трет-бутокси)-2-(4'-хлор-6-циклопропил-3-метил-бифенил-2-ил) уксусной кислоты (пример 20)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метил-2-(трет-бутокси)-2-(4'-хлор-6-циклопропил-3-метил-бифенил-2-ил) ацетат (20f) (24 мг, 0,062 ммоль) преобразовали в 2-(трет-бутокси)-2-(4'-хлор-6-циклопропил-3-метил-бифенил-2-ил) уксусную кислоту (пример 20) (23 мг, 0,062 ммоль, 99%).
1Н ЯМР (400 МГц, CDCl3) δ 0,48-0,64 (м, 3H), 0,68-0,76 (м, 1H), 1,01 (с, 9Н), 1,36-1,45 (м, 1Н), 2,37 (с, 3H), 5,08 (с, 1Н), 6,84 (д, J=7,9 Гц, 1Н), 7,08 (д, J=7,9 Гц, 1Н), 7,22-7,29 (м, 1H), 7,35-7,45 (м, 2Н), 7,50-7,58 (м, 1Н).
МС m/z ([M+Na]+) 395.
MC m/z ([M-H]-) 371.
Пример 21: Синтез трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты
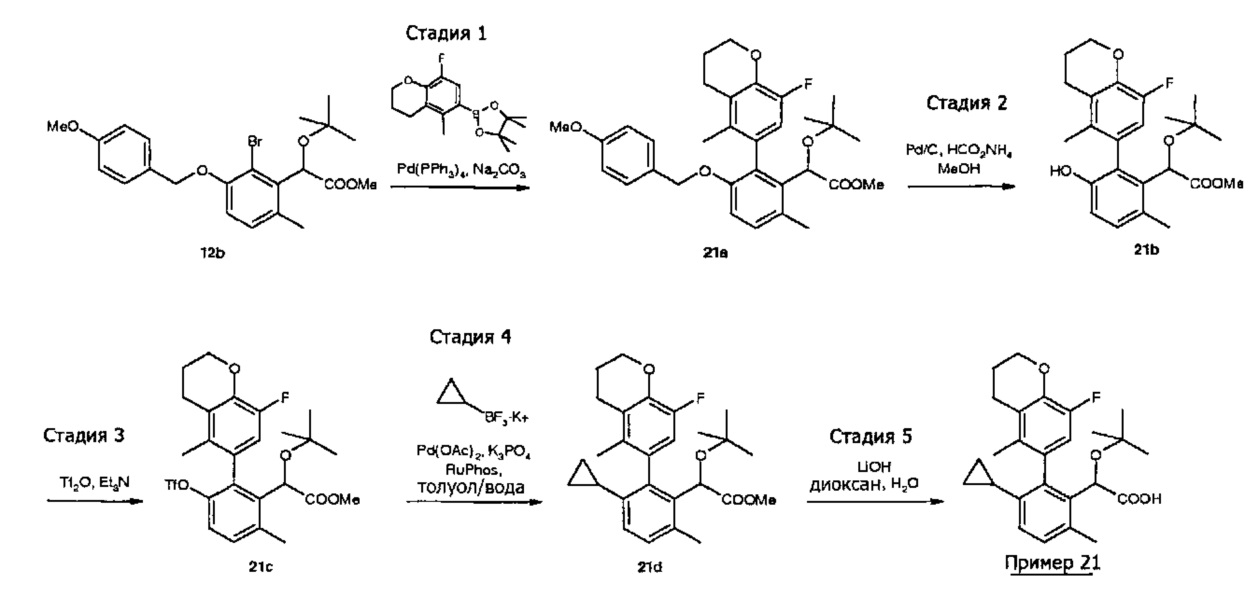
Стадия 1: Получение промежуточного соединения сложного метилового эфира [3-бензилокси-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-трет-бутокси-уксусной кислоты (21а)
С помощью процедуры, описанной в примере 1, стадии 7, промежуточное соединение метил-2-(3-бензилокси-2-бром-6-метилфенил)-2-(трет-бутокси) ацетат (12b) (500 мг, 1,19 ммоль), в реакции с 2-(8-фтор-3,4-дигидро-2Н-1-бензопиран-6-ил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан (416 мг, 1,42 ммоль), преобразовали, после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20), в метиловый сложный эфир [3-бензилокси-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-трет-бутокси-уксусной кислоты (21а) (526 мг, 1,04 ммоль, 87%).
МС m/z ([M+Na]+) 529.
Стадия 2: Получение промежуточного соединения сложного метилового эфира трет-бутокси-[2-(8-фтор-5-метил-хроман-6-ил)-3-гидрокси-6-метил-фенил] уксусной кислоты (21b)
С помощью процедуры, описанной в примере 15, стадии 2, промежуточное соединение метиловый сложный эфир 3-бензилокси-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-трет бутокси-уксусной кислоты (21а) (520 мг, 1,03 ммоль) преобразовали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 70/30), в метиловый сложный эфир трет-бутокси-[2-(8-фтор-5-метил-хроман-6-ил)-3-гидрокси-6-метил-фенил] уксусной кислоты (21b) (320 мг, 0,77 ммоль, 75%).
1Н ЯМР (300 МГц, CDCl3) δ 1,10 (с, 9Н), 1,88 (с, 3H), 2,08-2,20 (м, 2Н), 2,43 (с, 3H), 2,68-2,77 (м, 2Н), 3,58 (с, 3H), 4,25-4,32 (м, 2Н), 4,38 (с, 1Н), 4,92 (с, 1Н), 6,77 (д, J=11,2 Гц, 1H), 6,83 (д, J=8,3 Гц, 1Н), 7,07 (д, J=8,3 Гц, 1Н).
Стадия 3: Получение промежуточного соединения сложного метилового эфира трет-бутокси-[2-(8-фтор-5-метил-хроман-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]-уксусной кислоты (21с)
С помощью процедуры, описанной в примере 1, стадии 10, промежуточное соединение метиловый сложный эфир трет-бутокси-[2-(8-фтор-5-метил-хроман-6-ил)-3-гидрокси-6-метил-фенил] уксусной кислоты (21b) (320 мг, 0,77 ммоль) преобразовали в метиловый сложный эфир трет-бутокси-[2-(8-фтор-5-метил-хроман-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]-уксусной кислоты (21с) (420 мг, 0,77 ммоль, 99%), который использовали без дальнейшей очистки.
1Н ЯМР (400 МГц, CDCl3) δ 1,11 (с, 9Н), 1,81 (с, 3H), 2,09-2,17 (м, 2Н), 2,53 (с, 3H), 2,66-2,73 (м, 2Н), 3,59 (с, 3H), 4,24-4,31 (м, 2Н), 5,04 (с, 1Н), 6,74 (д, J=11,2 Гц, 1H), 7,17 (д, J=8,5 Гц, 1H), 7,23 (д, J=8,5 Гц, 1H).
МС m/z ([М-Н]-) 547.
Стадия 4: Получение промежуточного соединения сложного метилового эфира трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (21d)
Раствор сложного метилового эфира трет-бутокси-[2-(8-фтор-5-метил-хроман-6-ил)-6-метил-3-трифторметансульфонат сульфонилокси-фенил] уксусной кислоты (21с) (420 мг, 0,77 ммоль), циклопропилтрифторбората калия (147 мг, 0,99 ммоль), моногидрата трехосновного фосфата калия (581 мг, 2,53 ммоль), и 2-дициклогексилфосфино-2',6'-диизопропоксибифенила (Ruphos) (143 мг, 0,31 ммоль) в смеси толуола (2,3 мл) и воды (0,75 мл) барботировали азотом в течение 5 минут. Добавляли палладий(II) ацетат (17 мг, 0,08 ммоль) и нагревали реакционную смесь при 100°C в течение 4 часов. Добавляли воду (5 мл). Водный слой экстрагировали этилацетатом (2×5 мл). Объединенные органические слои промывали солевым раствором (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 80/20) с получением метилового сложного эфира трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (21d) (293 мг, 0,66 ммоль, 87%).
1НЯМР (300 МГц, CDCl3) δ 0,46-0,71 (м, 4Н), 1,10 (с, 9Н), 1,19-1,32 (м, 1Н), 1,82 (с, 3H), 2,08-2,19 (м, 2Н), 2,46 (с, 3H), 2,66-2,76 (м, 2Н), 3,57 (с, 3H), 4,24-4,31 (м, 2Н), 4,99 (с, 1H), 6,68-6,78 (м, 2Н), 7,07 (д, J=7,9 Гц, 1Н).
MC m/z ([M+Na]+) 463.
Стадия 5: Получение трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (пример 21)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метиловый сложный эфир трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (21d) (33 мг, 0,07 ммоль) преобразовали в трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусную кислоту (пример 21) (28 мг, 0,06 ммоль, 88%).
1Н ЯМР (300 МГц, CDCl3) δ 0,50-0,59 (м, 2Н), 0,59-0,71 (м, 2Н), 1,13 (с, 9Н), 1,23-1,36 (м, 1H), 1,90 (с, 3H), 2,06-2,17 (м, 2Н), 2,39 (с, 3H), 2,63-2,76 (м, 2Н), 4,22-4,30 (м, 2Н), 5,08 (с, 1H), 6,70-6,80 (м, 2Н), 7,07 (д, J=7,9 Гц, 1H).
МС m/z ([M+Na]+) 449.
МС m/z ([М-Н]-) 425.
Пример 22: Синтез трет-бутокси-(2-хроман-6-ил-3-циклопропилметил-6-метил-фенил) уксусной кислоты
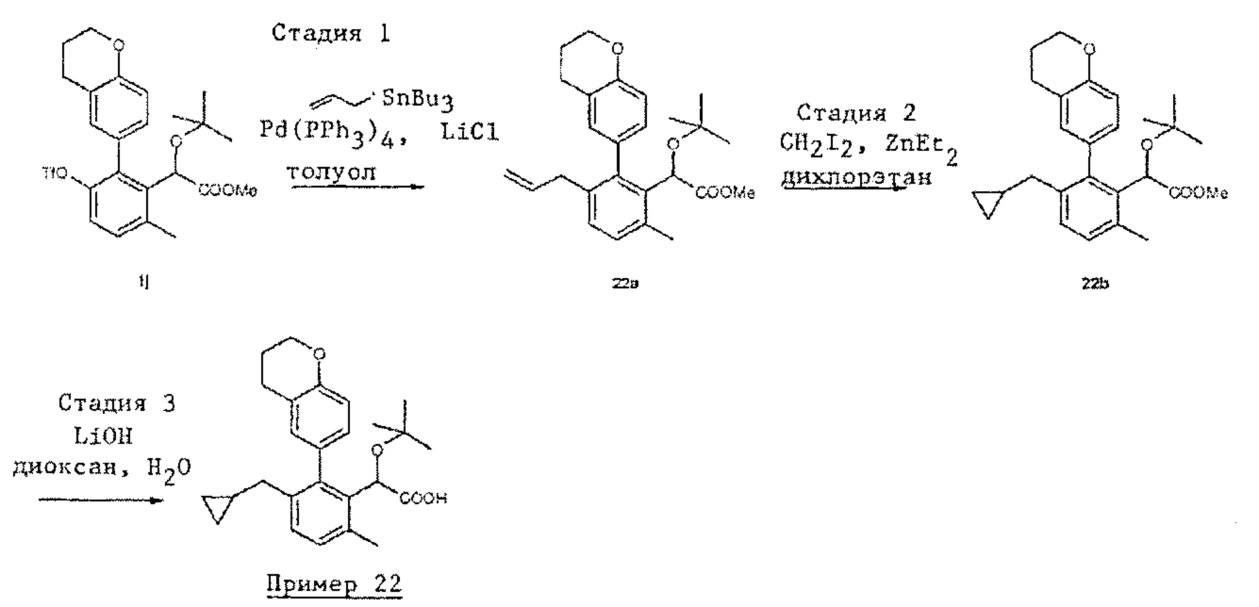
Стадия 1: Получение промежуточного соединения метилового сложного эфира (3-аллил-2-хроман-6-ил-6-метил-фенил)-трет-бутокси-уксусной кислоты (22а)
Дегазированный раствор метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетата (1j) (200 мг, 0,387 ммоль), аллил трибутилстаннан (141 мг, 0,426 ммоль), хлорид лития (49 мг, 1,16 ммоль) и тетракис (трифенилфосфин) (45 мг, 0,039 ммоль) в толуоле (2,5 мл) нагревали при 110°C в течение 18 часов. Добавляли водный раствор аммиака 10% (30 мл). Водный слой экстрагировали этилацетатом (3×10 мл). Объединенные органические слои промывали солевым раствором (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 80/20), с получением (3-аллил-2-хроман-6-ил-6-метил-фенил)-трет-бутокси-уксусной кислоты (22а) (80 мг, 0,147 ммоль, 38%).
1Н ЯМР (400 МГц, CDCl3) δ 0,99 (с, 9Н), 2,00-2,10 (м, 2Н), 2,42 (с, 3H), 2,67-2,85 (м, 2Н), 2,99-3,19 (м, 2Н), 3,65 и 3,67 (с, 3H), 4,23-4,25 (м, 2Н), 4,84 (д, J=17,0 Гц, 1Н), 4,94 (д, J=10,0 Гц, 1Н), 5,05 и 5,07 (с, 1Н), 5,75-5,85 (м, 1Н), 6,78-7,12 (м, 5Н).
MC m/z ([M+Na]+) 431.
Стадия 2: Получение промежуточного соединения сложного метилового эфира трет-бутокси-(2-хроман-6-ил-3-циклопропилметил-6-метил-фенил)-уксусной кислоты (22b)
К раствору метилового сложного эфира (3-аллил-2-хроман-6-ил-6-метил-фенил)-трет-бутокси-уксусной кислоты (22а) (80 мг, 0,147 ммоль) и дийодметана (118 мкл, 1,47 ммоль) в 1,2-дихлорэтане (1 мл) в атмосфере аргона медленно добавляли 1М раствор диэтилового цинка в гептане (734 мкл, 0,734 ммоль). Реакционную смесь перемешивали в течение ночи до комнатной температуры. Смесь концентрировали в вакууме. Насыщенный раствор хлорида аммония (10 мл) добавляли к остатку и экстрагировали этилацетатом (3×5 мл). Объединенные органические слои промывали водой (10 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток разбавляли в смеси ацетон/ацетонитрил (0,5/0,5 мл). К этому раствору добавляли оксид 4-метилморфолина (22 мг, 0,191 ммоль) и раствор тетраоксида осмия 4% масс, в воде (45 мкл, 0,007 ммоль) и перемешивали реакционную смесь в течение ночи. Смесь концентрировали в вакууме и остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 90/10) с получением сложного метилового эфира трет-бутокси-(2-хроман-6-ил-3-циклопропил-метил-6-метил-фенил) уксусной кислоты (22b) (11 мг, 0,026 ммоль, 17%).
1Н ЯМР (400 МГц, CDCl3) δ-0,05-0,07 (м, 2Н), 0,36-0,47 (м, 2Н), 0,75-0,83 (м, 1Н), 0,99 (с, 9Н), 1,98-2,09 (м, 2Н), 2,12-2,25 (м, 2Н), 2,38-2,42 (2s, 3H), 2,65-2,81 (м, 2Н), 3,64 и 3,66 (с, 3H), 4,21-4,27 (м, 2Н), 5,00 и 5,03 (с, 1Н), 6,77-7,11 (м, 4Н), 7,30-7,33 (м, 1Н).
МС m/z ([M+Na]+) 445.
Стадия 3: Получение трет-бутокси-(2-хроман-6-ил-3-циклопропилметил-6-метил-фенил) уксусной кислоты (пример 22)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метиловый сложный эфир трет-бутокси-(2-хроман-6-ил-3-циклопропилметил-6-метил-фенил) уксусной кислоты (22b) (11 мг, 0,026 ммоль) преобразовали в трет-бутокси-(2-хроман-6-ил-3-циклопропилметил-6-метил-фенил) уксусную кислоту (пример 22) (6,5 мг, 0,016 ммоль, 61%) в виде белого твердого вещества.
1Н ЯМР (400 МГц, CD3OD) δ-0,12-0,06 (м, 1Н),-0,02-0,04 (м, 1Н), 0,31-0,41 (м, 2Н), 0,68-0,80 (м, 1Н), 0,94 (с, 9Н), 1,93-2,07 (м, 2Н), 2,10-2,33 (м, 2Н), 2,41 (с, 3H), 2,69-2,87 (м, 2Н), 4,16-4,23 (м, 2Н), 4,96 и 4,99 (с, 1H), 6,68-6,76 (м, 1H), 6,85-6,89 (м, 1Н), 6,97- 7,03 (м, 1Н), 7,19-7,35 (м, 2Н).
MC m/z ([M+Na]+) 431.
МС m/z ([М-Н]-) 407.
Пример 23: Синтез 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиуксусной кислоты

Стадия 1: Получение промежуточного соединения метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-гидроксиацетата (23а)
К раствору метил-2-(трет-бутокси)-2- [3 -циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] ацетат 1k (957 мг, 2,34 ммоль) в безводном дихлорметане (21 мл) при 0°C в атмосфере азота по каплям добавляли трифторуксусную кислоту (1,05 мл). Смесь перемешивали 2 часа при 0°C, затем нейтрализовали насыщенным раствором гидрокарбоната натрия. Органический слой отделяли, промывали насыщенным солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме с получением метил 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6 метилфенил]-2-гидроксиацетата (23а) (825 мг, 2,34 ммоль, 100%) в виде светло-желтого аморфного твердого вещества.
1Н ЯМР (400 МГц, CDCl3) δ 0,51-0,71 (м, 4Н), 1,43-1,51 (м, 1H), 2,01-2,08 (м, 2Н), 2,29 et 2,30 (с, 3H), 2,77-2,83 (м, 2Н), 3,01 и 3,06 (д, J=2,96 Гц, 1H), 3,70 и 3,71 (с, 3H), 4,21-4,26 (м, 2Н), 5,20 и 5,22 (д, J=2,96 Гц, 1H), 6,78-6,83 (м, 2Н), 6,94-7,01 (м, 2Н), 7,06-7,09 (м, 1Н).
МС m/z ([M+Na]+) 375.
Стадия 2: Получение промежуточного соединения метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-винилоксиацетата (23b)
К раствору метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-гидроксиацетата (23а) (665 мг, 1,887 ммоль) в смеси этилвинилового эфира (3,6 мл) при комнатной температуре добавляли TFA (1 каплю). Перемешивание продолжали в течение 4 дней до концентрирования реакционной смеси в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат от 90/10 до 80/20) с образованием промежуточного ацеталя (720 мг, 1,696 ммоль, 90%) и исходного материала (64 мг, 0,181 ммоль, 9%). промежуточное соединение ацеталь непосредственно растворяли в безводном дихлорметане (2,4 мл), охлаждали до 0°C и добавляли по каплям триэтиламин (355 л, 2,54 ммоль) и триметилсилилтрифторметансульфонат (400 л, 2,20 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 2 часов, после чего реакцию гасили 1М раствором гидроксида натрия. Органический слой отделяли, промывали насыщенным солевым раствором, сушили над сульфатом натрия и концентрировали при пониженном давлении. Неочищенный материал очищали с помощью хроматографии на силикагеле (циклогексан/этилацетат 80/20), с получением метил 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-винилоксиацетата (23b) (580 мг, 1,53 ммоль, 81%) в виде бесцветного масла.
1Н ЯМР (400 МГц, CDCl3) δ 0,52-0,74 (м, 4Н), 1,46-1,55 (м, 1Н), 2,01-2,09 (м, 2Н), 2,32 et 2,33 (с, 3H), 2,76-2,83 (м, 2Н), 3,69 и 3,71 (с, 3H), 3,97-4,00 (м, 1H), 4,21-4,29 (м, 3H), 5,32 и 5,34 (с, 1Н), 6,07-6,17 (м, 1Н), 6,79-7,05 (м, 4Н), 7,07-7,09 (м, 1H).
MC m/z ([M+H]+) 401.
Стадия 3: Получение промежуточного соединения метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиацетата (23с)
К раствору метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-винилоксиацетата (23b) (580 мг, 1,53 ммоль) в 1,2-дихлорэтане (30 мл) при 0°C добавляли диэтил цинк (15% в толуоле, 27,9 мл, 30,65 ммоль), а затем дийодметан (4,94 мл, 61,30 ммоль) по каплям. Перемешивание продолжали в течение 16 часов при комнатной температуре, после чего реакцию гасили насыщенным водным раствором хлорида аммония и экстрагировали дважды этилацетатом. Органический слой промывали насыщенным солевым раствором, сушили над сульфатом натрия и концентрировали при пониженном давлении. Неочищенный материал очищали с помощью хроматографии на силикагеле (циклогексан/этилацетат 90/10), с получением метил 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиацетата (23с) (447 мг, 1,14 ммоль, 74%) в виде бесцветного масла.
1Н ЯМР (300 МГц, CDCl3) δ 0,21-0,74 (m, 8Н), 1,43-1,53 (м, 1Н), 2,01-2,10 (м, 2Н), 2,32 (с, 3H), 2,77-2,83 (м, 2Н), 3,26-3,41 (м, 1Н), 3,67 и 3,70 (с, 3H), 4,22-4,26 (м, 2Н), 5,03 и 5,08 (с, 1H), 6,76-7,07 (м, 5Н).
MC m/z ([M+Na]+) 415.
Стадия 4: Получение 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиуксусной кислоты (пример 23)
Смесь метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиацетата (23с) (252 мг, 0,642 ммоль) и 2М гидроксид натрия в воде (642 л, 1,284 ммоль) в смеси 1/1 е/метанол (6,4 мл) нагревали при 70°C в течение 16 часов. Смесь концентрировали в вакууме. Воду (4 мл) добавляли к остатку и водный слой подкисляли 1М соляной кислоты до рН 3 и экстрагировали этил ацетатом (2×15 мл). Объединенные органические слои промывали солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме с получением 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиуксусной кислоты (пример 23) (220,9 мг, 0,584 ммоль, 91%) в виде белого аморфного твердого вещества без дополнительной очистки.
1Н ЯМР (400 МГц, CDCl3) δ 0,23-0,75 (m, 8Н), 1,45-1,53 (м, 1H), 2,00-2,10 (м, 2Н), 2,32 и 2,34 (с, 3H), 2,71-2,86 (м, 2Н), 3,18-3,30 (м, 1H), 4,21-4,25 (м, 2Н), 5,12 и 5,14 (с, 1Н), 6,78-6,84 (м, 2Н), 6,91-6,97 (м, 1Н), 7,00-7,08 (м, 2Н).
МС m/z ([M+Na]+) 401.
МС m/z ([М-Н]-) 377.
Пример 24: Синтез (S)-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиуксусной кислоты
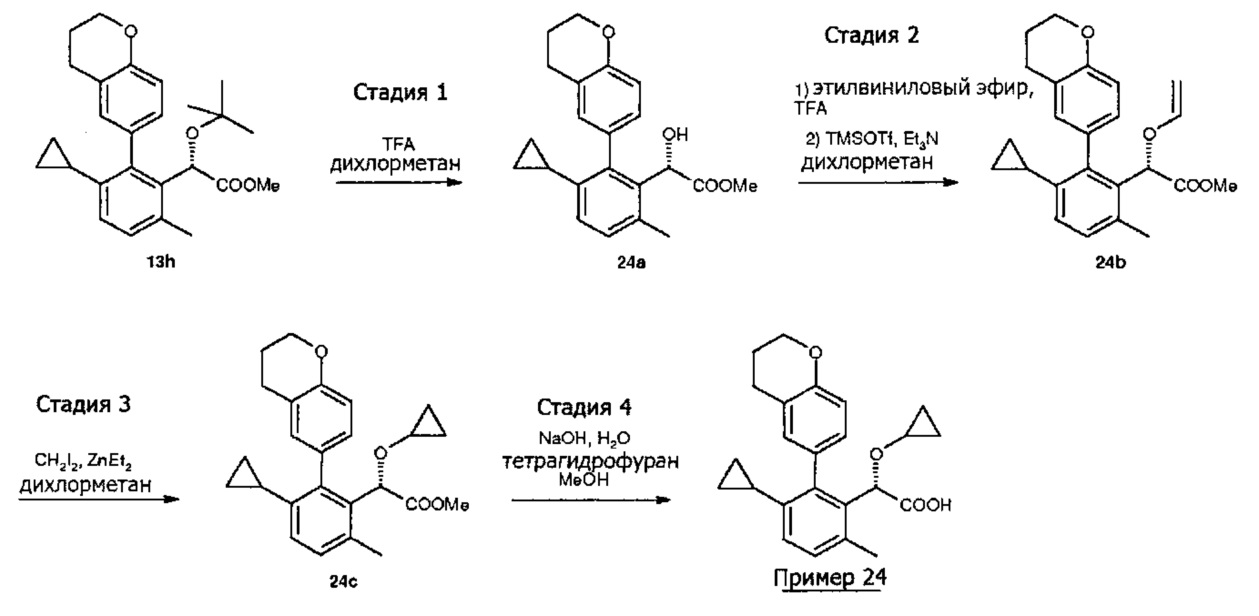
Стадия 1: Получение промежуточного соединения (S)-метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-гидроксиацетата (24а)
С помощью процедуры, описанной в примере 23, стадии 1, метил (S)-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] ацетат (13h) (1. 074 г, 2,629 ммоль) преобразовали в (S)- метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-гидроксиацетат (24а) (861 мг, 2,443 ммоль, 93%).
1Н ЯМР (400 МГц, CDCl3) δ 0,51-0,71 (м, 4Н), 1,43-1,51 (м, 1Н), 2,01-2,08 (м, 2Н), 2,29 et 2,30 (с, 3H), 2,77-2,83 (м, 2Н), 3,01 и 3,06 (д, J=2,96 Гц, 1Н), 3,70 и 3,71 (с, 3H), 4,21-4,26 (м, 2Н), 5,20 и 5,22 (д, J=2,96 Гц, 1Н), 6,78-6,83 (м, 2Н), 6,94-7,01 (м, 2Н), 7,06-7,09 (м, 1Н).
MC m/z ([M+Na]+) 375.
Стадия 2: Получение промежуточного соединения (S)-метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-винилоксиацетата (24b)
С помощью процедуры, описанной в примере 23, стадии 2, (S)- метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-гидроксиацетат (24а) (861 мг, 2,443 ммоль) преобразовали в (S)-метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-винилоксиацетат (24b) (225 мг, 0,594 ммоль, 65%).
1Н ЯМР (400 МГц, CDCl3) δ 0,52-0,74 (м, 4Н), 1,46-1,55 (м, 1Н), 2,01-2,09 (м, 2Н), 2,32 et 2,33 (с, 3H), 2,76-2,83 (м, 2Н), 3,69 и 3,71 (с, 3H), 3,97-4,00 (м, 1H), 4,21-4,29 (м, 3H), 5,32 и 5,34 (с, 1H), 6,07-6,17 (м, 1H), 6,79-7,05 (м, 4Н), 7,07-7,09 (м, 1H).
МС m/z ([М+Н]+)401.
Стадия 3: Получение промежуточного соединения (S)-метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиацетата (24с)
С помощью процедуры, описанной в примере 23, стадии 3, (S)-метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-винилоксиацетат (24b) (370 мг, 0,978 ммоль) преобразовали в (S)-метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиацетат (24с) (316 мг, 0,805 ммоль, 82%).
1Н ЯМР (300 МГц, CDCl3) δ 0,21-0,74 (m, 8Н), 1,43-1,53 (м, 1Н), 2,01-2,10 (м, 2Н), 2,32 (с, 3H), 2,77-2,83 (м, 2Н), 3,26-3,41 (м, 1Н), 3,67 и 3,70 (с, 3H), 4,22-4,26 (м, 2Н), 5,03 и 5,08 (с, 1H), 6,76-7,07 (м, 5Н).
МС m/z ([M+Na]+) 415.
Стадия 4: Получение (S) 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиуксусной кислоты (пример 24)
С помощью процедуры, описанной в примере 23, стадии 4, (S)-метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиацетат (24с) (309 мг, 0,787 ммоль) преобразовали в (S) 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиуксусную кислоту (пример 24) (279 мг, 0,737 ммоль, 94%).
1Н ЯМР (400 МГц, CDCl3) δ 0,23-0,75 (m, 8Н), 1,45-1,53 (м, 1H), 2,00-2,10 (м, 2Н), 2,32 и 2,34 (с, 3H), 2,71-2,86 (м, 2Н), 3,18-3,30 (м, 1Н), 4,21-4,25 (м, 2Н), 5,12 и 5,14 (с, 1Н), 6,78-6,84 (м, 2Н), 6,91-6,97 (м, 1Н), 7,00-7,08 (м, 2Н).
MC m/z ([M+Na]+)401.
MC m/z ([M-H]-) 377.
Пример 25: Синтез трет-бутокси-[2-хроман-6-ил-6-метил-3-(1-метил-циклопропил) фенил] уксусной кислоты

Стадия 1: Получение промежуточного соединения сложного метилового эфира трет-бутокси-[2-хроман-6-ил-6-метил-3-(1-метил-циклопропил) фенил] уксусной кислоты (25а)
С помощью процедуры, описанной в примере 22, стадии 2, метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-изопропенил-6 метилфенил] ацетат (4а) (42 мг, 0,103 ммоль) преобразовали в метиловый сложный эфир трет-бутокси-[2-хроман-6-ил-6-метил-3-(1-метил-циклопропил) фенил] уксусной кислоты (25а) (15 мг, 0. 035 ммоль, 34%).
1Н ЯМР (400 МГц, CDCl3) δ 0,24-0,28 (м, 1H), 0,38-0,42 (м, 1H), 0,54-0,65 (м, 2Н), 0,99 (с, 9Н), 1,07 и 1,08 (с, 3H), 1,99-2,13 (м, 2Н), 2,40 и 2,41 (с, 3H), 2,67-2,86 (м, 2Н), 3,63 и 3,66 (с, 3H), 4,21-4,28 (м, 2Н), 5,00 и 5,02 (с, 1H), 6,80 (дд, J=8,2 Гц, J=6,9 Гц, 1Н), 6,93-7,07 (м, 3H), 7,27 и 7,28 (с, 1Н).
MC m/z ([M+Na]+) 445.
Стадия 2: Получение трет-бутокси-[2-хроман-6-ил-6-метил-3-(1-метил-циклопропил) фенил] уксусной кислоты (пример 25)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метиловый сложный эфир трет-бутокси-[2-хроман-6-ил-6-метил-3-(1-метил-циклопропил) фенил] уксусной кислоты (25а) (15 мг, 0,035 ммоль) преобразовали в трет-бутокси-[2-хроман-6-ил-6-метил-3-(1-метил-циклопропил)фенил] уксусную кислоту (пример 25) (11,5 мг, 0,028 ммоль, 81%) в виде белого твердого вещества.
1Н ЯМР (400 МГц, CDCl3) δ 0,21-0,25 (м, 1Н), 0,42-046 (м, 1Н), 0,51-0,63 (м, 2Н), 0,98 (с, 9Н), 1,07 и 1,08 (с, 3H), 1,97-2,12 (м, 2Н), 2,33 (с, 3H), 2,71-2,89 (м, 2Н), 4,22-4,29 (м, 2Н), 5,12 и 5,14 (с, 1Н), 6,80 (д, J=8,3 Гц, 1H), 6,92-7,09 (м, 2Н), 7,18-7,30 (м, 2Н).
MC m/z ([M+Na]+) 431.
МС m/z ([М-Н]-) 407.
Пример 26: Синтез трет-бутокси-[2-хроман-6-ил-6-метил-3-(цис-2-метил-циклопропил) фенил] уксусной кислоты
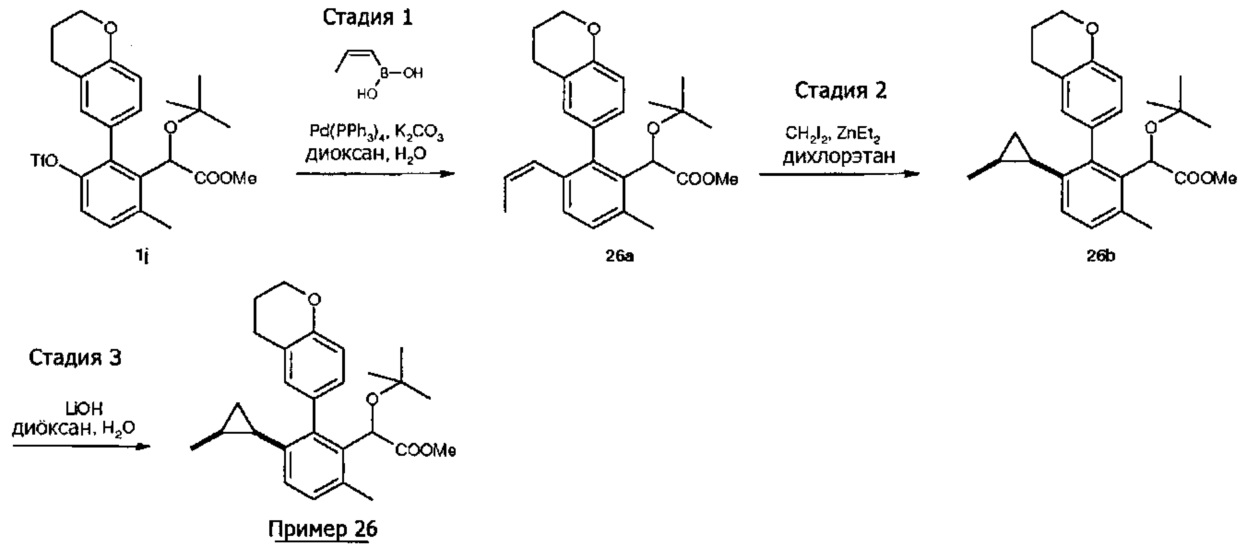
Стадия 1: Получение промежуточного соединения трет-бутокси-[2-хроман-6-ил-6-метил-3-((Z)-пропенил) фенил] уксусной кислоты (26а)
Дегазированный раствор метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетат (1j) (100 мг, 0,19 ммоль), цис-1-пропен-1-ил бороновой кислоты (50 мг, 0,582 ммоль), карбонат калия (80 мг, 0,580 ммоль) и тетракис (трифенилфосфин) (22 мг, 0,02 ммоль) в смеси 1,4-диоксана и воды (1,6/0,4 мл) нагревали в микроволновой печи при 110°C в течение 2 часов. Добавляли воду (5 мл). Водный слой экстрагировали этилацетатом (2×5 мл). Объединенные органические слои промывали солевым раствором (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 90/10) с получением сложного метилового эфира трет-бутокси-[2-хроман-6-ил-6-метил-3-((Z)-пропенил)фенил] уксусной кислоты (26а) (70 мг, 0,17 ммоль, 88%).
1Н ЯМР (300 МГц, CDCl3) δ 0,96 (с, 9Н), 1,77-1,82 (м, 3H), 1,98-2,09 (м, 2Н), 2,43 (с, 3H), 2,60-2,82 (м, 2Н), 3,67 и 3,70 (с, 3H), 4,22-4,25 (м, 2Н), 5,11 и 5,13 (с, 1Н), 5,46-5,57 (м, 1Н), 5,90-5,96 (м, 1H), 6,74-6,85 (м, 2Н), 7,00-7,08 (м, 2Н), 7,19-7,22 (м,1Н).
МС m/z ([M+Na]+) 431.
Стадия 2: Получение промежуточного соединения метилового сложного эфира трет-бутокси-[2-хроман-6-ил-6-метил-3-(цис-2-метил-циклопропил)фенил] уксусной кислоты (26b)
С помощью процедуры, описанной в примере 22, стадии 2, метиловый сложный эфир трет-бутокси-[2-хроман-6-ил-6-метил-3-((Z)-пропенил) фенил] уксусной кислоты (26а) (70 мг, 0,171 ммоль) преобразовали в метиловый сложный эфир трет-бутокси-[2-хроман-6-ил-6-метил-3-(цис-2-метил-циклопропил) фенил] уксусной кислоты (26b) (20 мг, 0,042 ммоль, 20%).
1Н ЯМР (400 МГц, CDCl3) δ 0,58-0,64 (м, 1Н), 0,73-0,77 (м, 1H), 0,80-0,82 (м, 2Н), 0,97-1,00 (м, 9Н), 1,09-1,25 (м, 1H), 1,46-1,55 (м, 1H), 2,00-2,10 (м, 2Н), 2,40 и 2,42 (с, 3H), 2,68-2,87 (м, 2Н), 3,67 и 3,69 (с, 3H), 4,20-4,30 (м, 2Н), 5,07-5,13 (м, 1H), 6,74-7,06 (м, 4Н), 6,79-7,11(м, 5Н).
МС m/z ([M+Na]+) 445.
Стадия 3: Получение трет-бутокси-[2-хроман-6-ил-6-метил-3-(цис-2-метил-циклопропил) фенил] уксусной кислоты (Пример 26)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метиловый сложный эфир трет-бутокси-[2-хроман-6-ил-6-метил-3-(цис-2-метил-циклопропил) фенил] уксусной кислоты (26b) (20 мг, 0,042 ммоль) преобразовали в трет-бутокси-[2-хроман-6-ил-6-метил-3-(цис-2-метил-циклопропил)фенил] уксусную кислоту (пример 26) (5,3 мг, 0,013 ммоль, 27%) в виде белого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 0,57-0,62 (м, 1Н), 0,80-0,83 (м, 3H), 0,99-1,02 (м, 9Н), 1,10-1,34 (м, 1H), 1,47-1,55 (м, 2Н), 1,98-2,10 (м, 2Н), 2,35 и 2,36 (с, 3H), 2,70-2,88 (м, 2Н), 4,19-4,27 (м, 2Н), 5,20-5,26 (м, 1Н), 6,74-7,06 (м, 4Н), 7,15-7,22 (м, 1Н), 9,79 (уш. с, 1Н).
МС m/z ([M+Na]+) 431.
МС m/z ([М-Н]") 407.
Пример 27: Синтез (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-циклопропокси-уксусной кислоты

Стадия 1: Получение промежуточного соединения метил (2-хроман-6-ил-3-гидрокси-6-трифторметил-фенил)-гидрокси-ацетата (27а)
С помощью процедуры, описанной в примере 23, стадии 1, метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-гидрокси-6-(трифторметил)фенил]ацетат (2i) (300 мг, 0,68 ммоль) преобразовали в метил-(2-хроман-6-ил-3-гидрокси-6-трифторметил-фенил)-гидрокси-ацетат (27а) (260 мг, 0,68 ммоль, 99%), который использовали без дальнейшей очистки.
1H ЯМР (300 МГц, CDCl3) δ 1,96-2,12 (м, 2Н), 2,70-2,90 (м, 2Н), 3,12 (уш. с, 1Н), 3.58 и 3,60 (с, 3H), 4,21-4,30 (м, 2Н), 5,12 (с, 1Н), 5,33 и 5,35 (с, 1H), 6,77-6,83 (м, 1Н), 6,84-6,94 (м, 1Н), 7,05 (д, J=8,7 Гц, 1Н), 7,08-7,14 (м, 1Н), 7,65 (д, J=8,7 Гц, 1Н).
MC m/z ([M-H]-) 381.
Стадия 2: Получение промежуточного соединения метил (2-хроман-6-ил-3-трифторметансульфонат сульфонилокси-6-трифторметил-фенил)-гидрокси-ацетата (27b)
С помощью процедуры, описанной в примере 1, стадии 10, промежуточное соединение метил (2-хроман-6-ил-3-гидрокси-6-трифторметил-фенил)-гидрокси-ацетат (27а) (260 мг, 0,68 ммоль), преобразовали в метил (2-хроман-6-ил-3-трифторметансульфонилокси-6-трифторметил-фенил)-гидрокси-ацетат (27b) (350 мг, 0,68 ммоль, 100%), который использовали без дальнейшей очистки.
1H ЯМР (300 МГц, CDCI3) 5 1,97-2,09 (м, 2Н), 2,68-2,86 (м, 2Н), 3,19 (уш. с, 1Н), 3.59 и 3,61 (с, 3H), 4,20-4,28 (м, 2Н), 5,40 (с, 1Н), 6,73-6,86 (м, 2Н), 7,02-7,09 (м, 1Н), 7,47 (д, J=8,8 Гц, 1Н), 7,83 (д, J=8,8 Гц, 1H).
MC m/z ([M-H]-) 513.
Стадия 3: Получение промежуточного соединения метил (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-гидрокси-ацетата (27с)
С помощью процедуры, описанной в примере 21, стадия 4, промежуточное соединение метил (2-хроман-6-ил-3-трифторметансульфонилокси-6-трифторметил-фенил)-гидрокси-ацетат (27b) (350 мг, 0,68 ммоль), преобразовали, после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 70/30), в метил (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-гидрокси-ацетат (27с) (85 мг, 0,21 ммоль, 31%).
1H ЯМР (400 МГц, CDCl3) δ 0,57-0,72 (м, 2Н), 0,72-0,85 (м, 2Н), 1,41-1,51 (м, 1Н), 1,98-2,11 (м, 2Н), 2,71-2,86 (м, 2Н), 3,07 и 3,09 (д, J=4,3 Гц, 1Н), 3,58 и 3,61 (с, 3H), 4,20-4,27 (м, 2Н), 5,38 (д, J=4,3 Гц, 1H), 6,74-6,85 (м, 2Н), 6,93 (д, J=8,3 Гц, 1H), 7,01-7,06 (м, 1Н), 7,62 (д, J=8,3 Гц, 1Н).
Стадия 4: Получение промежуточного соединения метил (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-винилокси-ацетата (27d)
С помощью процедуры, описанной в примере 23, стадии 2, промежуточное соединение метил (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-гидрокси-ацетата (27с) (85 мг, 0,21 ммоль) преобразовали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20) в метил (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-винилокси ацетат (27d) (65 мг, 0,15 ммоль, 72%).
1H ЯМР (300 МГц, CDCl3) δ 0,58-0,89 (м, 4Н), 1,45-1,57 (м, 1Н), 1,99-2,10 (м, 2Н), 2,74-2,85 (м, 2Н), 3,59 и 3,61 (с, 3H), 4,03 и 4,04 (дд, J=2,0 Гц, J=6,4 Гц, 1H), 4,19-4,26 (м, 2Н), 4,31 и 4,33 (дд, J=2,0 Гц, J=14,0 Гц, 1Н), 5,47 (с, 1Н), 6,16 и 6,20 (дд, J=6,4 Гц, J=14,0 Гц, 1Н), 6,76-6,86 (м, 2Н), 6,95 (д, J=8,4 Гц, 1Н), 7,02-7,08 (м, 1Н), 7,63 (д, J=8,4 Гц, 1H).
МС m/z ([M+Na]+) 455.
Стадия 5: Получение промежуточного соединения метил (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-циклопропокси-ацетата (27е)
С помощью процедуры, описанной в примере 23, стадии 3, промежуточное соединение метил (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-винилокси-ацетат (27d) (65 мг, 0,15 ммоль) преобразовали, после очистки препаративной ТСХ (циклогексан/этилацетат 80/20), в метил (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-циклопропокси-ацетат (27е) (47 мг, 0,11 ммоль, 70%).
1H ЯМР (300 МГц, CDCl3) δ 0,29-0,38 (м, 2Н), 0,47-0,58 (м, 2Н), 0,62-0,73 (м, 2Н), 0,75-0,86 (м, 2Н), 1,45-1,55 (м, 1Н), 2,00-2,11 (м, 2Н), 2,71-2,84(м, 2Н), 3,29-3,38 (м, 1Н), 3,61 и 3,62 (с, 3H), 4,20-4,27 (м, 2Н), 5,19 и 5,20 (с, 1Н), 6,77-7,01 (м, 4Н), 7,61 (д, J=8,4 Гц, 1Н).
МС m/z ([M+Na]+) 469.
Стадия 6: Получение (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-циклопропокси-уксусной кислоты (пример 27)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метил (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-циклопропокси-ацетат (27е) (47 мг, 0,11 ммоль) преобразовали в (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-циклопропокси-уксусную кислоту (пример 27) (32 мг, 0,07 ммоль, 70%).
1H ЯМР (400 МГц, CDCl3) δ 0,31-0,55 (м, 4Н), 0,62-0,72 (м, 2Н), 0,75-0,87 (м, 2Н), 1,47-1,56 (м, 1H), 1,99-2,09 (м, 2Н), 2,72-2,84 (м, 2Н), 3,21-3,30 (м, 1H), 4,20-4,26 (м, 2Н), 5,22 и 5,25 (с, 1Н), 6,79-6,91 (м, 2Н), 6,95 (д, J=8,4 Гц, 1Н), 7,01-7,07 (м, 1Н), 7,63 (д, J=8,4 Гц, 1H).
MC m/z ([M+Na]+) 455.
Пример 28: Синтез (2-хроман-6-ил-3-циклопропил-6-метил-фенил) пропокси-уксусной кислоты

Стадия 1: Получение промежуточного соединения метилового сложного эфира (3-бензилокси-2-хроман-6-ил-6-метил-фенил) пропокси-уксусной кислоты (28а)
К раствору метил 2-[3-бензилокси-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-гидроксиацетата (1 г) (128 мг, 0,306 ммоль) в безводном N,N-диметилформамиде (3 мл) в атмосфере азота при 0°C последовательно добавляли бис (триметилсилил) амид лития 1М в е (351 мкл, 0,351 ммоль) и 2-иодпропане (228 мкл, 1,71 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 3 часов перед добавлением воды (10 мл). Слои разделяли и водный слой экстрагировали этилацетатом (2×10 мл). Объединенные органические слои сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат 90/10) с получением (3-бензилокси-2-хроман-6-ил-6-метил-фенил) пропокси-уксусной кислоты метилового сложного эфира (28а) (102 мг, 0,221 ммоль, 72%) в виде бесцветного масла.
MC m/z ([M+Na]+) 483.
Стадия 2: Получение промежуточного соединения сложного метилового эфира (2-хроман-6-ил-3-гидрокси-6-метил-фенил) пропокси-уксусной кислоты (28b)
К раствору метилового сложного эфира (3-бензилокси-2-хроман-6-ил-6-метил-фенил) пропокси-уксусной кислоты (28а) (102 мг, 0,221 ммоль) и формиата аммония (349 мг, 5,53 ммоль), в безводном метаноле (1 мл), дегазированном аргоном, добавляли палладий на углероде 10% (12 мг, 0,011 ммоль). Реакцию нагревали с обратным холодильником в течение 16 часов, затем охлаждали до комнатной температуры и фильтровали через Millipore. Добавляли воду (5 мл). Водный слой экстрагировали этилацетатом (2×5 мл). Объединенные органические слои промывали солевым раствором (10 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением сложного метилового эфира 2-хроман-6-ил-3-гидрокси-6-метил-фенил) пропокси-уксусной кислоты (28b) (36 мг, 0,097 ммоль, 44%) в виде белого твердого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 0,84 (t, 3H, J=7,4 Гц), 1,47-1,51 (м, 2Н), 2,02-2,11 (м, 2Н), 2,29 (с, 3H), 2,77-2,83 (м, 2Н), 3,12-3,19(м, 1H), 3,28-3,39 (м, 1Н), 3,67 и 3,68 (с, 3H), 4,23-4,27 (м, 2Н), 4,65 и 4,66 (с, 1Н), 4,83 и 4,84 (с, 1H), 6,86-6,95 (м, 3H), 7,05-7,07 (м, 2Н).
MC m/z ([M+Na]+) 393.
Стадия 3: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-6-метил-3-трифторметансульфонат сульфонилокси-фенил) пропокси-уксусной кислоты (28с)
С помощью процедуры, описанной в примере 1, стадии 10, промежуточное соединение метиловый сложный эфир 2-хроман-6-ил-3-гидрокси-6-метил-фенил) пропокси-уксусной кислоты (28b) (36 мг, 0,097 ммоль) преобразовали в промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-6-метил-3-трифторметансульфонилокси-фенил) пропокси-уксусной кислоты (28с) (51 мг, 0,097 ммоль, 100%) в виде коричневого масла.
1H ЯМР (300 МГц, CDCl3) δ 0,84 (dt, 3H, J=7,4 Гц, J=1,4 Гц), 1,44-1,53 (м, 2Н), 2,00-2,07 (м, 2Н), 2,38 и 2,39 (с, 3H), 2,68-2,88 (м, 2Н), 3,09-3,17 (м, 1Н), 3,33-3,42 (м, 1H), 3,68 и 3,69 (с, 3H), 4,21-4,24 (м, 2Н), 4,93 и 4,94 (с, 1Н), 6,82-6,84 (м, 1Н), 6,90-7,03 (м, 2Н), 7,20 (с, 2Н).
MC m/z ([M+Na]+) 525.
Стадия 4: Получение промежуточного соединения сложного метилового эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил) пропокси-уксусной кислоты (28d)
Дегазированный раствор сложного метилового эфира (2-хроман-6-ил-6-метил-3-трифторметансульфонилокси-фенил) пропокси-уксусной кислоты (28с) (51 мг, 0,097 ммоль), моногидрат трехосновного фосфата калия (144 мг, 0,626 ммоль), циклопропилтрифторборат калия (20 мг, 0,132 ммоль), ацетат палладия (0,6 мг, 0,025 ммоль) и 2-дициклогексилфосфино-2',6'-диизопропоксибифенил (Ruphos) (2,3 мг, 0,050 ммоль) в трет-бутаноле (0,1 мл) и воде (0,1 мл) нагревали при 105°C в течение ночи. Добавляли воду (5 мл). Водный слой экстрагировали этилацетатом (2×5 мл). Объединенные органические слои промывали солевым раствором (10 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 90/10) с получением метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил) пропокси-уксусной кислоты (28d) (18 мг, 0,045 ммоль, 47%).
1H ЯМР (300 МГц, CDCl3) δ 0,51-0,72 (м, 4Н), 0,81-0,87 (м, 3H), 1,43-1,56 (м, 3H), 2,02-2,09 (м, 2Н), 3,32 (с, 3H), 2,70-2,88 (м, 2Н), 3,09-3,18 (м, 1Н), 3,27-3,42 (м, 1H), 3,66 и 3,68 (с, 3H), 4,22-4,25 (м, 2Н), 4,91 и 4,93 (с, 1H), 6,77 (dd, 1Н, J=7,9 Гц, J=1,4 Гц), 6,82 (дд, 1Н, J=8,3 Гц, J=3,4 Гц), 6,89-7,03 (м, 2Н), 7,06 (д, 1H, J=8,0 Гц).
MC m/z ([M+Na]+) 417.
Стадия 5: получение (2-хроман-6-ил-3-циклопропил-6-метил-фенил) пропокси-уксусной кислоты (пример 28)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил) пропокси-уксусной кислоты (28d) (18 мг, 0,045 ммоль) преобразовали в (2-хроман-6-ил-3-циклопропил-6-метил-фенил) пропокси-уксусной кислоты (6,3 мг, 0,016 ммоль, 36%) (пример 28) в виде белого твердого вещества.
1H ЯМР (300 МГц, CDCl3) δ 0,55-076 (м, 4Н), 0,81-0,87 (м, 3H), 1,43-1,54 (м, 3H), 2,00-2,09 (м, 2Н), 3,32 и 3,33 (с, 3H), 2,68-2,88 (м, 2Н), 3,13-3,30 (м, 2Н), 4,22-4,25 (м, 2Н), 5,02 и 5,03 (с, 1H), 6,77-6,84 (м, 2Н), 6,88-6,93 (м, 1H), 7,02-7,09 (м, 2Н).
МС m/z ([M+Na]+) 403.
МС m/z ([М-Н]-) 379.
Пример 29: Синтез (2-хроман-6-ил-3-циклопропил-6-метил-фенил) циклопропил метокси-уксусной кислоты

Стадия 1; Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропилметокси-уксусной кислоты (29а)
С помощью процедуры, описанной в примере 28, стадии 1, промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-гидрокси-уксусной кислоты (23а) (50 мг, 0,142 ммоль) пребразовали, с помощью реакции с йодометилциклопропан (145 мг, 0,795 ммоль), после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 90/10), в метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропилметокси-уксусной кислоты (29а) (7 мг, 0,017 ммоль, 12%) в виде белого твердого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 0,04-0,10 (м, 2Н), 0,35-0,45 (м, 2Н), 0,50-0,74 (м, 4Н), 0,87-1,00 (м, 1Н), 1,43-1,53 (м, 1H), 1,99-2,09 (м, 2Н), 2,34 (с, 3H), 2,68-2,88 (м, 2Н), 2,94-3,03 (м, 1H), 3,23-3,35 (м, 1H), 3,66 и 3,69 (с, 3H), 4,21-4,25 (м, 2Н), 4,99 и 5,00 (с, 1Н), 6,75-6,84 (м, 2Н), 6,89-7,07 (м, 3H).
MC m/z ([M+Na]+) 429.
Стадия 2: получение (2-хроман-6-ил-3-циклопропил-6-метил-фенил) циклопропил метокси-уксусной кислоты (пример 29)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропилметокси-уксусной кислоты (29а) (7 мг, 0,017 ммоль) преобразовали в (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропилметокси-уксусную кислоту (пример 29) (3,8 мг, 0,010 ммоль, 56%) в виде белого твердого вещества.
1H ЯМР (400 МГц, CD3OD) δ-0,10-0,04 (м, 2Н), 0,34 (уш. с, 2Н), 0,48-0,72 (м, 4Н), 1,43-1,51 (м, 1Н), 1,94-2,07 (м, 2Н), 2,36 (уш. с, 3H), 2,71-2,86 (м, 3H), 3,20-3,40 (м, 2Н), 4,17-4,20 (м, 2Н), 4,74-4,94 (м, 1Н), 6,72-6,76 (м, 2Н), 6,87 (д, 1H,J=7,5 Гц), 7,01(д, 1Н, J=7,8 Гц), 7,13 (уш. с, 1Н).
MC m/z ([M+Na]+) 415.
MC m/z ([M-H]-) 391.
Пример 30: Синтез (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2,2-трифтор-этокси) уксусной кислоты

Стадия 1: Получение промежуточного соединения (2-хроман-6-ил-3-циклопропил-6-метил-фенил-)-(2,2,2-трифторэтокси) уксусной кислоты (30а)
С помощью процедуры, описанной в примере 28, стадии 1, промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-гидрокси-уксусной кислоты (23а) (50 мг, 0,142 ммоль) преобразовали реакцией с 2,2,2-трифторэтил трифторметансульфонатом (115 мкл, 0,755 ммоль), после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 90/10) в метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2,2-трифторэтокси) уксусной кислоты (30а) (30 мг, 0,069 ммоль, 48%) в виде бесцветного масла.
1H ЯМР (300 МГц, CDCl3) δ 0,50-062 (м, 2Н), 0,64-0,74 (м, 2Н), 1,42-1,54 (м, 1Н), 2,00-2,08 (м, 2Н), 2,26 и 2,28 (с, 3H), 2,60-2,85 (м, 2Н), 3,49-3,61 (м, 1Н), 3,67 и 3,68 (с, 3H), 3,83-4,15 (м, 1Н), 4,21-4,24 (м, 2Н), 5,02 (с, 1Н), 6,78-6,83 (м, 2Н), 6,89-6,99 (м, 2Н), 7,07 (д, 1Н, 7=7,9 Гц).
МС m/z ([M+Na]+) 457.
Стадия 2: получение (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2,2-трифторэтокси) уксусной кислоты (Пример 30)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2,2-трифтор-этокси) уксусной кислоты (30а) (30 мг, 0,069 ммоль) преобразовали в (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2,2-трифторэтокси) уксусной кислоты (пример 30) (15 мг, 0,035 ммоль, 51%) в виде белого твердого вещества после очистки на препаративной ТСХ (дихлорметан/метанол 95/5).
1Н ЯМР (400 МГц, CD3OD) δ 0,48-0,74 (м, 4Н), 1,44-1,52 (м, 1Н), 1,92-2,06 (м, 2Н), 2,35 (с, 3H), 2,74-2,86 (м, 2Н), 3,40-3,59 (м, 1H), 3,82-4,02 (м, 1H), 4,15-4,23 (м, 2Н), 4,75-5,00 (м, 1H), 6,70-6,80 (м, 2Н), 6,89 (д, 1Н, J=8,0 Гц), 7,04 (д, 1Н, J=7,8 Гц), 7,10 (уш. с, 1H).
MC m/z ([M+Na]+) 443.
MC m/z ([M-H]-) 419.
Пример 31: Синтез 2-хроман-6-ил-6-метил-3-пропил-фенил) изопропокси-уксусной кислоты
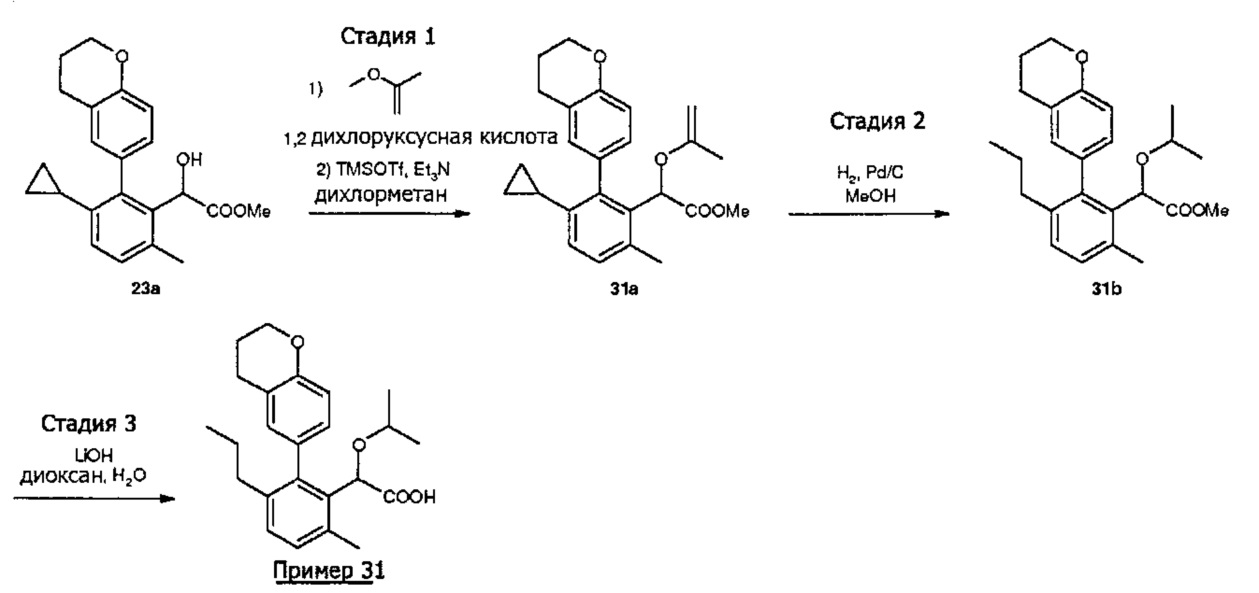
Стадия 1: Получение промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-изопропенилокси-уксусной кислоты (31а)
К перемешиваемому раствору метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-гидрокси-уксусной кислоты (23а) (149 мг, 0,423 ммоль) в 2-метоксипропене (800 мкл) при комнатной температуре добавляли 1,2-дихлоруксусную кислоту (1 каплю). Перемешивание продолжали в течение 4 дней до концентрирования реагирующей смеси путем продувки азотом. Остаток непосредственно растворяли в безводном дихлорметане (1 мл), охлаждали до 0°C и добавляли по каплям триэтиламин (88 мкл, 0,634 ммоль) и триметилсилилтрифторметансульфонат (100 мкл, 0,550 ммоль) были до-78°C. Полученную смесь перемешивали при комнатной температуре в течение 48 часов, после чего реакцию гасили 1М раствором гидроксида натрия. Органический слой отделяли, промывали насыщенным солевым раствором, сушили над сульфатом натрия и концентрировали при пониженном давлении. Неочищенный материал очищали с помощью хроматографии на препаративной ТСХ (циклогексан/этилацетат, 95/5) с получением метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-изопропенилокси-уксусной кислоты (31а) (30 мг, 0,078 ммоль, 18%), содержащего 21% исходного материала (23а) в виде бесцветного масла.
MC m/z ([M+Na]+) 415.
Стадия 2: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-6-метил-3-пропил-фенил) изопропокси-уксусной кислоты (31b)
Смесь метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-изопропенилокси-уксусной кислоты (31а) (30 мг, 0,053 ммоль) и палладия на углероде 5% (17 мг, 0,008 ммоль) в метаноле перемешивали при комнатной температуре при одной атмосфере давления водорода в течение 16 часов. Смесь фильтровали через Millipore и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 90/10) с получением метилового сложного эфира 2-хроман-6-ил-6-метил-3-пропил-фенил) изопропокси-уксусной кислоты (31b) (17 мг, 0,042 ммоль, 80%).
1H ЯМР (400 МГц, CDCl3) δ 0,79 (t, 3H, J=7,3 Гц), 0,93 (d, 3H, J=6,1 Гц), 1,05 (d, 3H, J=6,1 Гц), 1,36-1,46 (м, 2Н), 1,96-2,12 (м, 2Н), 2,20-2,30 (м, 2Н), 2,36 (с, 3H), 2,68-2,85 (м, 2Н), 3,48-3,59 (м, 1Н), 3,65 (с, 3H), 4,19-4,28 (м, 2Н), 4,94 (с, 1Н), 6,76-6,84 (м, 2Н), 6,90-6,95 (м, 1H), 7,08 (д, 1Н, J=7,8 Гц), 7,12 (д, 1H, J=7,8 Гц).
МС m/z ([M+Na]+) 419.
Стадия 3: Получение 2-хроман-6-ил-6-метил-3-пропил-фенил) изопропокси-уксусной кислоты (пример 31)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метиловый сложный эфир 2-хроман-6-ил-6-метил-3-пропил-фенил) изопропокси-уксусной кислоты (31b) (17 мг, 0,042 ммоль) преобразовали в 2-хроман-6-ил-6-метил-3-пропил-фенил) изопропокси-уксусной кислоты (пример 31) (12 мг, 0,031 ммоль, 74%) в виде белого твердого вещества после очистки с помощью препаративной ТСХ (дихлорметан/метанол 95/5).
1H ЯМР (400 МГц, CDCl3) δ 0,78 (t, 3H, J=7,3 Гц), 0,90 (d, 3H, J=4,7 Гц), 1,05 (d, 3H, J=5,2 Гц), 1,37-1,46 (м, 2Н), 1,98-2,10 (м, 2Н), 2,16-2,40 (м, 5Н), 2,67-2,86 (м, 2Н), 3,42-3,56 (м, 1H), 4,18-4,27 (м, 2Н), 5,00 и 5,03 (с, 1Н), 6,77-6,84 (м, 2Н), 6,90-7,15 (м, 3H).
МС m/z ([M+Na]+) 405.
МС m/z ([М-Н]') 381.
Пример 32: Синтез циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-уксусной кислоты
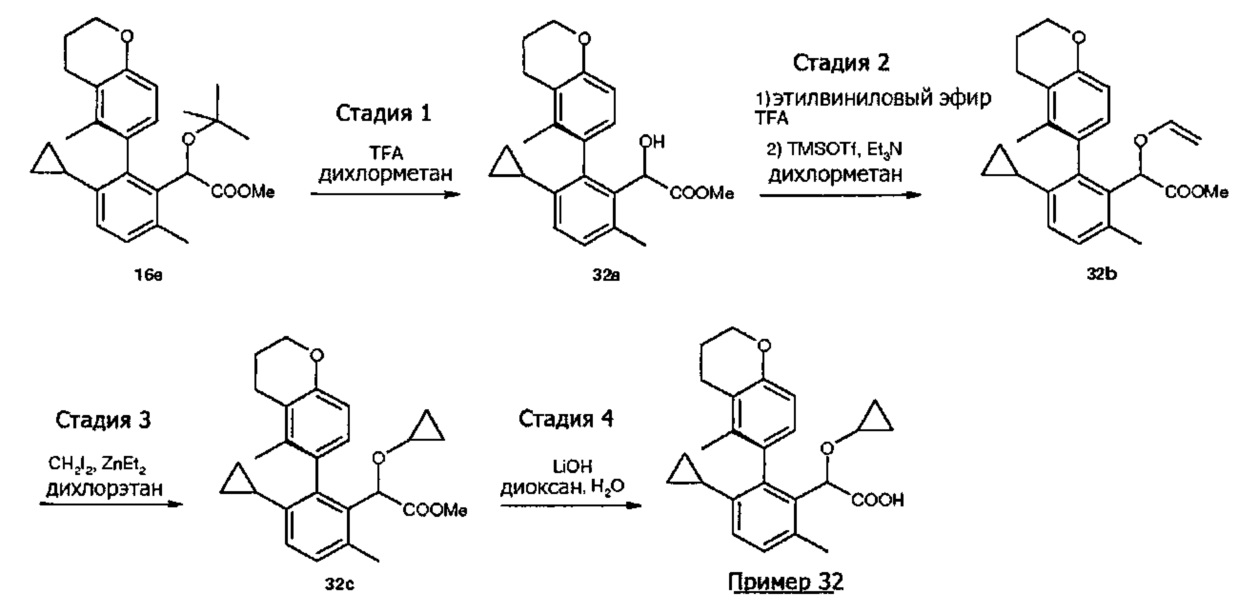
Стадия 1: Получение промежуточного соединения метил [3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-гидрокси-ацетата (32а)
С помощью процедуры, описанной в примере 23, стадии 1, метил-2-(трет-бутокси)-2-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] ацетат (16е) (226 мг, 0,54 ммоль) преобразовали в метил [3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-гидрокси-ацетат (32а) (191 мг, 0,52 ммоль, 97%), который использовали без дальнейшей очистки.
1Н ЯМР (300 МГц, CDCl3) δ 0,48-0,75 (м, 4Н), 1,28-1,40 (м, 1H), 1,91 (с, 3H), 2,03-2,14 (м, 2Н), 2,28 (с, 3H), 2,69 (т, J=6,6 Гц, 2Н), 2,93 (д, J=2,8 Гц, 1Н), 3,69 (с, 3H), 4,15-4,21 (м, 2Н), 5,06 (д, J=2,8 Гц, 1H), 6,70-6,78 (м, 2Н), 6,88 (д, J=8,3 Гц, 1H), 7,08 (д, J=8,0 Гц, 1H).
Стадия 2: Получение промежуточного соединения метил [3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-винилокси-ацетата (32b)
С помощью процедуры, описанной в примере 23, стадии 2, промежуточное соединение метиловый сложный эфир [3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-гидрокси-ацетат (32а) (191 мг, 0,52 ммоль) преобразовали после очистки методом препаративной ТСХ (циклогексан/этилацетат 80/20) в метил [3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-винилокси-ацетат (32b) (35 мг, 0,089 ммоль, 17%).
1H ЯМР (300 МГц, CDCl3) δ 0,52-0,74 (м, 4Н), 1,29-1,40 (м, 1Н), 1,92 (с, 3H), 2,06-2,13 (м, 2Н), 2,32 (с, 3H), 2,70 (т, J=6,6 Гц, 2Н), 3,67 (с, 3H), 3,99 (дд, J=1,9 Гц, J=6,4 Гц, 1Н), 4,17-4,22 (м, 2Н), 4,27 (дд, J=1,9 Гц, J=13,9 Гц, 1Н), 5,17 (с, 1H), 6,12 (дд, J=6,4 Гц, J=13,9 Гц, 1Н), 6,72 (д, J=8,3 Гц, 1Н), 6,77 (д, J=8,0 Гц, 1Н), 6,82 (д, J=8,3 Гц, 1Н), 7,10 (д, J=8,0 Гц, 1Н).
MC m/z ([M+Na]+) 415.
Стадия 3: Получение промежуточного соединения метил циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] ацетата (32с)
С помощью процедуры, описанной в примере 23, стадии 3, промежуточное соединение метил [3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-винилокси-ацетат (32b) (35 мг, 0,089 ммоль) преобразовали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20) в метил циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] ацетат (32с) (18 мг, 0,044 ммоль, 49%).
1H ЯМР (300 МГц, CDCl3) δ 0,22-0,30 (м, 1Н), 0,34-0,46 (м, 2Н), 0,51-0,71 (м, 5Н), 1,27-1,38 (м, 1Н), 1,91 (с, 3H), 2,06-2,16 (м, 2Н), 2,32 (с, 3H), 2,64-2,77 (м, 2Н), 3,44-3,50 (м, 1Н), 3,64 (с, 3H), 4,16-4,24 (м, 2Н), 4,93 (с, 1Н), 6,69-6,76 (м, 2Н), 6,86 (д, J=8,3 Гц, 1Н), 7,06 (д,7=8,0 Гц, 1Н).
МС m/z ([M+Na]+) 429.
Стадия 4: получение циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] уксусной кислоты (пример 32)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метил циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] ацетат (32с) (18 мг, 0,044 ммоль) преобразовали в циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] уксусную кислоту (пример 32) (11 мг, 0,028 ммоль, 63%).
1H ЯМР (300 МГц, CDCl3) δ 0,32-0,43 (м, 2Н), 0,44-0,72 (m, 6Н), 1,30-1,40 (м, 1Н), 1,92 (с, 3H), 2,05-2,13 (м, 2Н), 2,32 (с, 3H), 2,62-2,75 (м, 2Н), 3,29-3,35 (м, 1Н), 4,15-4,22 (м, 2Н), 5,00 (с, 1Н), 6,69 (д, J=8,3 Гц, 1Н), 6,78 (д, J=8,0 Гц, 1Н), 6,88 (д, J=8,3 Гц, 1Н), 7,09(д, J=8,0 Гц, 1H).
MC m/z ([M+Na]+) 415.
МС m/z ([М-Н]-) 391.
Пример 33: Синтез (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклобутокси-уксусной кислоты

Стадия 1: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-метансульфонилокси-уксусной кислоты (33а)
К раствору промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-гидрокси-уксусной кислоты (23а) (219 мг, 0,624 ммоль) в безводном дихлорметане (4 мл) при 0°C в атмосфере азота последовательно добавляли триэтиламин (174 мкл, 1,25 ммоль), и ангидрид метансульфокислоты (119 мг, 1,25 ммоль). Полученную смесь перемешивали при комнатной температуре в течение ночи перед добавлением воды (5 мл). Слои разделяли. Водный слой экстрагировали этилацетатом (2×5 мл). Объединенные органические слои промывали насыщенным раствором хлорида натрия (5 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-метансульфонилокси- уксусной кислоты (33а) (232 мг, 0,323 ммоль, 51%), содержащий 40% исходного материала (23а) в виде бесцветного масла. Это масло будет использоваться на следующей стадии без дополнительной очистки.
МС m/z ([M+Na]+) 453.
Стадия 2: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклобутокси-уксусной кислоты (33b)
К раствору метилового сложного эфира метил (2-хроман-6-ил-3-циклопропил-6-метил-фенил) метансульфонил окси-уксусной кислоты (33а) (114 мг, 0,265 ммоль) в циклобутаноле (0,5 мл) добавляли трифторуксусную кислоту (23 мкл, 0,291 ммоль). Смесь перемешивали при 90°C в течение 2 ч и выливали в насыщенный раствор бикарбоната натрия- (10 мл). Водный слой экстрагировали этилацетатом (2×5 мл). Объединенные органические слои промывали водой (20 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали на препаративной ТСХ (циклогексан/дихлорметан 55/45) с получением метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклобутокси-уксусной кислоты (33b) (14 мг, 0,034 ммоль, 13%) в виде белого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 0,51-0,75 (м, 4Н), 1,24-1,38 (м, 1Н), 1,44-1,61 (м, 2Н), 1,71-1,94 (м, 3H), 1,96-2,05 (м, 3H), 2,32 и 2,33 (с, 3H), 2,72-2,86 (м, 2Н), 3,66 и 3,69 (с, 3H), 3,77-3,90 (м, 1Н), 4,19-4,28 (м, 2Н), 4,89 и 4,94 (с, 1Н), 6,77 (dd, 1Н, J=7,9 Гц, J=2,1 Гц), 6,82 (д, 1Н, J=8,4 Гц), 6,92-7,01 (м, 2Н), 7,05 (д, 1Н, J=7,9 Гц).
МС m/z ([M+Na]+) 429.
Стадия 3: получение (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклобутокси-уксусной кислоты (пример 33)
Смесь метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклобутокси-уксусной кислоты (33b) (14 мг, 0,034 ммоль) и 2М гидроксида натрия в воде (0,5 мл, 1,00 ммоль) в тетрагидрофуране (1 мл) нагревали при 90°C в течение 48 часов. Воду (5 мл) добавляли к остатку и водный слой подкисляли 1М соляной кислоты до рН 3 и экстрагировали этилацетатом (2×5 мл). Объединенные органические слои промывали солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали на препаративной ТСХ (дихлорметан/метанол 90/10) с получением (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклобутокси-уксусной кислоты (пример 33) (13 мг, 0,033 ммоль, 99%) в виде белого твердого вещества.
1H ЯМР (300 МГц, CD3OD) δ 0,47-0,73 (м, 4Н), 1,22-1,40 (м, 1Н), 1,42-1,60 (м, 2Н), 1,64-1,92 (м, 4Н), 1,94-2,08 (м, 2Н), 2,33 (уш. с, 3H), 2,70-2,92 (м, 2Н), 3,68-3,90 (м, 1H), 4,14-4,22 (м, 2Н), 4,89 (уш. с, 1Н), 6,73-6,80 (м, 2Н), 6,90-7,16 (м, 3H).
MC m/z ([M+Na]+) 415.
MC m/z ([M-H]-) 391.
Пример 34: Синтез (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-этокси)-уксусной кислоты
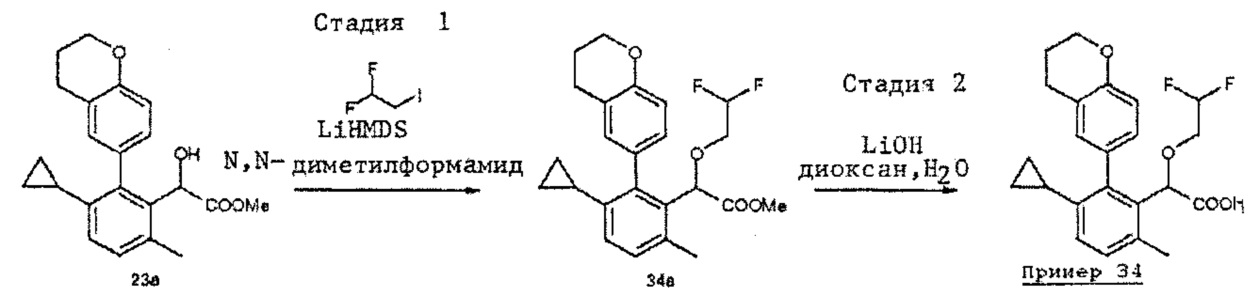
Стадия 1: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-этокси) уксусной кислоты (34а)
С помощью процедуры, описанной в примере 28, стадии 1, промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-гидрокси-уксусной кислоты (23а) (50 мг, 0,142 ммоль) преобразовали, с помощью реакции с 1,1-дифтор-2-йодэтаном (153 мг, 0,795 ммоль), после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20), в метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-этокси) уксусной кислоты (34а) (5 мг, 0,012 ммоль, 8%) в виде желтого масла,
1H ЯМР (300 МГц, CDCl3) δ 0,51-0,76 (м, 4Н), 1,42-1,53 (м, 1H), 2,02-2,09 (м, 2Н), 2,29 и 2,30 (с, 3H), 2,74-2,86 (м, 2Н), 3,33-3,48 (м, 1Н), 3,59-3,82 (м, 4Н), 4,19-4,30 (м, 2Н), 4,96 и 4,99 (с, 1Н), 5,58-6,00 (м, 1Н), 6,78-6,85 (м, 2Н), 6,91-7,01 (м, 2Н), 7,07 (д, 1H, J=7,9 Гц).
MC m/z ([M+Na]+) 439
Стадия 2: получение (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-этокси) уксусной кислоты (пример 34)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-этокси) уксусной кислоты (34а) (5 мг, 0,012 ммоль) преобразовали в (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-этокси) уксусной кислоты (пример 34) (2 мг, 0,005 ммоль, 41%) в виде белого твердого вещества.
1Н ЯМР (300 МГц, CDCl3) δ 0,52-0,78 (м, 4Н), 1,43-1,55 (м, 1Н), 1,97-2,10 (м, 2Н), 2,29-2,36 (м, 3H), 2,77-2,85 (м, 2Н), 3,38-3,61 (м, 2Н), 4,19-4,28 (м, 2Н), 5,11 и 5,12 (с, 1Н), 5,54-5,95 (м, 1Н), 6,79-6,85 (м, 2Н), 6,88-7,04 (м, 2Н), 7,09 (д, 1H, J=8,0 Гц).
MC m/z ([M+Na]+) 425.
MC m/z ([M-H]-) 401.
Пример 35: Синтез (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2-фтор-этокси)-уксусной кислоты

Стадия 1: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил-)-(2-фтор-этокси) уксусной кислоты (35а)
С помощью процедуры, описанной в примере 28, стадии 1, промежуточное гидрокси-уксусной кислоты (23а) (50 мг, 0,142 ммоль) преобразовали реакцией с 1-фтор-2-йодэтаном (138 мг, 0,795 ммоль), после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20) в метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2-фтор-этокси) уксусной кислоты (35а) (34 мг, 0,085 ммоль, 60%) в виде желтого масла.
1Н ЯМР (300 МГц, CDCl3) δ 0,51-0,73 (м, 4Н), 1,44-1,54 (м, 1Н), 2,00-2,10 (м, 2Н), 2,32 (с, 3H), 2,72-2,86 (м, 2Н), 3,37-3,84 (м, 5Н), 4,20-4,26 (м, 2Н), 4,31-4,62 (м, 2Н), 4,96 и 5,00 (с, 1Н), 6,77-6,84 (м, 2Н), 6,88-7,05 (м, 2Н), 7,07 (д, 1H, J=7,9 Гц).
MC m/z ([M+Na]+) 421.
Стадия 2: получение (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2-фтор-этокси) уксусной кислоты (Пример 35)
С помощью процедуры, описанной в примере 33, стадии 3, промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2-фтор-этоксигруппу) уксусной кислоты (35а) (34 мг, 0,085 ммоль) преобразовали в (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2-фтор-этокси) уксусную кислоту (пример 35) (20 мг, 0,052 ммоль, 61%) в виде белого твердого вещества.
1H ЯМР (300 МГц, CDCl3) δ 0,52-0,79 (м, 4Н), 1,42-1,53 (м, 1Н), 2,00-2,08 (м, 2Н), 2,34 (с, 3H), 2,73-2,85 (м, 2Н), 3,41-3,70 (м, 2Н), 4,19-4,26 (м, 2Н), 4,31-4,38 (м, 1Н), 4,47-4,54 (м, 1Н), 5,08 и 5,09 (с, 1Н), 6,74-6,86 (м, 2Н), 6,87-6,94 (м, 1Н), 6,98-7,12 (м, 2Н).
МС m/z ([M+Na]+) 407.
МС m/z ([М-Н]-) 383.
Пример 36: Синтез (2-хроман-6-ил-3-циклопропил-6-метил-фенил) изопропокси-уксусной кислоты

Стадия 1: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил) изопропокси-уксусной кислоты (36а)
С помощью процедуры, описанной в примере 33, стадии 2, промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-метансульфонилокси-уксусной кислоты (36а) (102 мг, 0,237 ммоль) преобразовали с метансульфонилокси-уксусной кислоты (36а) (102 мг, 0,237 ммоль) преобразовали с помощью реакции с изопропанолом (0,5 мл), после очистки с помощью препаративной ТСХ (циклогексан/дихлорметан 50/50) в метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил) изопропокси-уксусной кислоты (36а) (20 мг, 0,051 ммоль, 21%).
1H ЯМР (300 МГц, CDCl3) δ 0,49-0,75 (м, 4Н), 0,95 (dd, 3H, J=6,1 Гц, J=2,8 Гц), 1,03 (dd, 3H, J=9,7 Гц, J=6,1 Гц), 1,42-1,53 (м, 1H), 1,98-2,13 (м, 2Н), 2,35 (с, 3H), 2,67-2,88 (м, 2Н), 3,43-3,59 (м, 1Н), 3,66 и 3,68 (с, 3H), 4,21-4,27 (м, 2Н), 5,01 и 5,05 (с, 1Н), 6,76 (дд, J=7,9 Гц, 1Н), 6,82 (т, J=8,5Hz, 1H), 6,90-7,03 (м, 2Н), 7,05 (д, J=8,0 Гц, 1Н).
MC m/z ([M+Na]+) 417.
Стадия 2: получение (2-хроман-6-ил-3-циклопропил-6-метил-фенил) изопропокси-уксусной кислоты (пример 36)
С помощью процедуры, описанной в примере 1, стадии 12, метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил) изопропокси-уксусной кислоты (36а) (20 мг, 0,051 ммоль) преобразовали после очистки препаративной ТСХ (дихлорметан/метанол 90/10) в (2-хроман-6-ил-3-циклопропил-6-метил-фенил) изопропокси-уксусную кислоту (пример 36) (12 мг, 0,031 ммоль, 61%) в виде белого твердого вещества.
1H ЯМР (300 МГц, CD3OD) δ 0,50-0,75 (м, 4Н), 0,80-1,00 (m, 6Н), 1,42-1,53 (м, 1Н), 1,95-2,10 (м, 2Н), 2,35 (уш. с, 3H), 2,70-2,88 (м, 2Н), 3,40-3,70 (м, 1Н), 4,13-4,25 (м, 2Н), 5,00 (уш. с, 1Н), 6,74-6,78 (м, 2Н), 6,90-6,94 (м, 1Н), 7,02-7,15 (м, 2Н).
MC m/z ([M+Na]+) 403.
MC m/z ([M-H]-) 379.
Пример 37: Синтез циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты
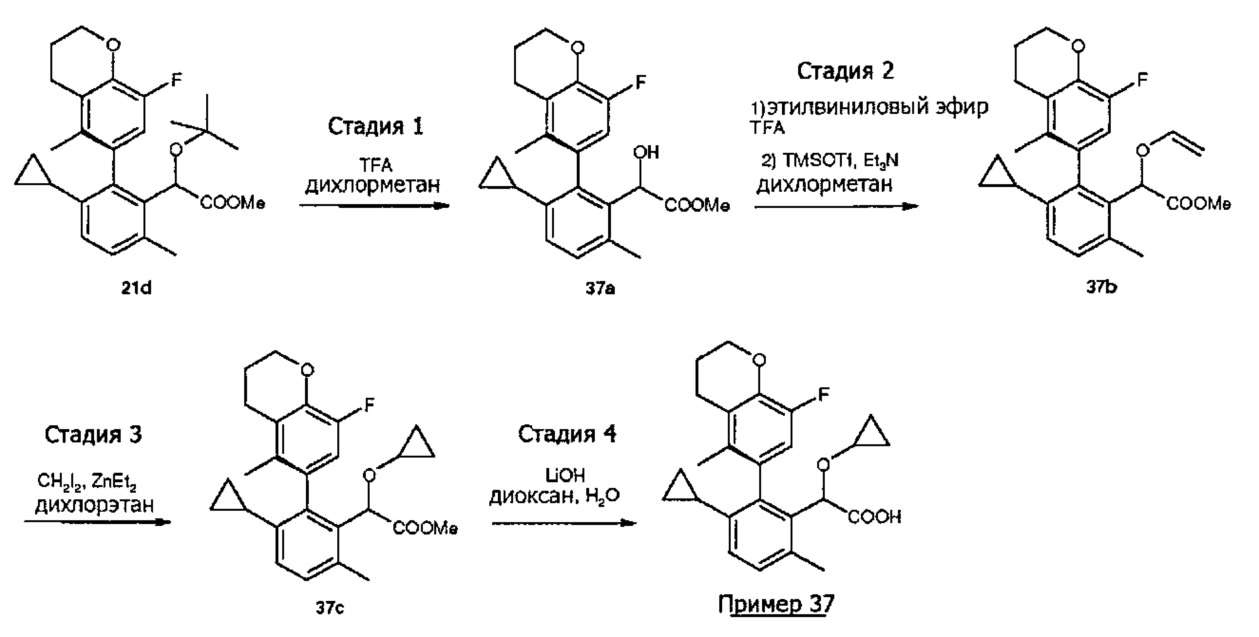
Стадия 1: Получение промежуточного соединения метил [3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-гидрокси-ацетата (37а)
С помощью процедуры, описанной в примере 23, стадии 1, метил трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-ацетата (21d) (290 мг, 0,66 ммоль) преобразовали в метил [3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-гидрокси-ацетат (37а) (230 мг, 0,60 ммоль, 90%), который использовали без дальнейшей очистки.
1H ЯМР (400 МГц, CDCl3) δ 0,49-0,74 (м, 4Н), 1,27-1,36 (м, 1H), 1,86 (с, 3H), 2,08-2,15 (м, 2Н), 2,28 (с, 3H), 2,70 (т, J=6,6 Гц, 2Н), 2,94 (д, J=2,8 Гц, 1Н), 3,70 (с, 3H), 4,23-4,28 (м, 2Н), 5,04 (д, J=2,8 Гц, 1Н), 6,75 (д, J=11,3 Гц, 1H), 6,76 (д, J=8,0 Гц, 1Н), 7,09 (д, J=8,0 Гц, 1Н).
Стадия 2: Получение промежуточного соединения метил [3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-винилокси-ацетата (37b)
С помощью процедуры, описанной в примере 23, стадии 2, промежуточное соединение метил [3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-гидрокси-ацетат (37а) (100 мг, 0,26 ммоль) преобразовали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 70/30) в метил [3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-винилокси-ацетат (37b) (51 мг, 0,12 ммоль, 48%).
1Н ЯМР (400 МГц, CDCl3) δ 0,50-0,75 (м, 4Н), 1,29-1,38 (м, 1Н), 1,88 (с, 3H), 2,08-2,18 (м, 2Н), 2,32 (с, 3H), 2,66-2,77 (м, 2Н), 3,68 (с, 3H), 4,04 (д, J=6,4 Гц, 1Н), 4,22-4,30 (м, 3H), 5,14 (с, 1Н), 6,14 (дд, J=6,4 Гц, J=13,9 Гц, 1H), 6,68 (д, J=11,3 Гц, 1Н), 6,78 (д, J=8,0 Гц, 1Н), 7,11 (д, J=8,0 Гц, 1Н).
MC m/z ([M+Na]+) 433.
Стадия 3: Получение промежуточного соединения метил циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] ацетата (37с)
С помощью процедуры, описанной в примере 23, стадии 3, промежуточное соединение метил [3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-винилокси-ацетат (37b) (50 мг, 0,12 ммоль) преобразовали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20), в мети циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] ацетат (37 с) (44 мг, 0,10 ммоль, 85%).
1H ЯМР (400 МГц, CDCl3) δ 0,29-0,35 (м, 1H), 0,38-0,50 (м, 2Н), 0,50-0,73 (м, 5Н), 1,27-1,36 (м, 1H), 1,87 (с, 3H), 2,08-2,19 (м, 2Н), 2,32 (с, 3H), 2,65-2,78 (м, 2Н), 3,41-3,48 (м, 1H), 3,64 (с, 3H), 4,24-4,31 (м, 2Н), 4,90 (с, 1Н), 6,70-6,77 (м, 2Н), 7,08 (д, J=8,0 Гц, 1H).
МС m/z ([M+Na]+) 447.
Стадия 6: получение циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (пример 37)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метил циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] ацетат (37с) (44 мг, 0,10 ммоль) преобразовали в циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусную кислоту (пример 37) (32 мг, 0,078 ммоль, 75%).
1H ЯМР (400 МГц, CDCl3) δ 0,37-0,61 (m, 6Н), 0,64-0,73 (м, 2Н), 1,29-1,39 (м, 1Н), 1,89 (с, 3H), 2,08-2,17 (м, 2Н), 2,31 (с, 3H), 2,64-2,76 (м, 2Н), 3,27-3,34 (м, 1H), 4,22-4,31 (м, 2Н), 4,95 (с, 1Н), 6,75 (д, J=11,4 Гц, 1Н), 6,79 (д, J=8,0 Гц, 1Н), 7,10 (д, J=8,0 Гц, 1Н).
МС m/z ([M+Na]+) 433.
МС m/z ([М-Н]-) 409.
Пример 38: Синтез (S)- трет-бутокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] уксусной кислоты

Стадия 1: Получение промежуточного соединения метил (S)-[3-бензилокси-6-метил-2-(5-метил-хроман-6-ил) фенил]-трет-бутокси-ацетата (38а)
С помощью процедуры, описанной в примере 1, стадии 7, промежуточное соединение метил (S)-2-(3-бензилокси-2-бром-6-метилфенил)-2-(трет-бутокси) ацетат (13 с) (3,00 г, 7,12 ммоль) преобразовали реакцией с 4,4,5,5-тетраметил-2-(5-метил-3,4-дигидро-2Н-1-бензопиран-6-ил)-1,3,2-диоксабороланом (2,34 г, 8,54 ммоль), после очистки флэш-хроматографией на силикагеле (циклогексан/этилацетат от 100/0 до 95/5) в метил (S)-[3 -бензилокси-6-метил-2-(5-метил-хроман-6-ил) фенил]-трет-бутокси-ацетат (38а) (3,13 г, 6,98 ммоль, 90%).
1Н ЯМР (400 МГц, CDCl3) δ 1,12 (с, 9Н), 1,87 (с, 3H), 2,06-2,18 (м, 2Н), 2,46 (с, 3H), 2,65-2,74 (м, 2Н), 3,57 (с, 3H), 4,18-4,25 (м, 2Н), 4,88-4,97 (м, 2Н), 5,10 (с, 1H), 6,72 (д, J=8,3 Гц, 1Н), 6,81 (д, J=8,3 Гц, 1Н), 6,89 (д, J=8,3 Гц, 1Н), 7,01-7,09 (м, 3H), 7,18-7,25 (м, 3H).
MC m/z ([M+Na]+) 511.
Стадия 2: Получение промежуточного соединения метил (S)- трет-бутокси-[3-гидрокси-6-метил-2-(5-метил-хроман-6-ил) фенил] ацетата (38b)
С помощью процедуры, описанной в примере 15, стадия 2, промежуточное соединение метил (S)-[3-бензилокси-6-метил-2-(5-метил-хроман-6-ил) фенил]-трет-бутокси-ацетат (38а) (3,13 г, 6,98 ммоль) преобразовали после очистки с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат от 100/0 до 90/10) в метил (S)-трет-бутокси-[3-гидрокси-6-метил-2-(5-метил-хроман-6-ил) фенил] ацетат (38b) (2,01 г, 5,04 ммоль, 78%).
1Н ЯМР (400 МГц, CDCl3) δ 1,09 (с, 9Н), 1,91 (с, 3H), 2,06-2,17 (м, 2Н), 2,43 (с, 3H), 2,67-2,75 (м, 2Н), 3,58 (с, 3H), 4,18-4,24 (м, 2Н), 4,40 (с, 1Н), 4,93 (с, 1Н), 6,77 (д, J=8,3 Гц, 1Н), 6,83 (д, J=8,3 Гц, 1Н), 6,93 (д, J=8,3 Гц, 1H), 7,06 (д, J=8,3 Гц, 1Н).
МС m/z ([М-Н]-) 398.
Стадия 3: Получение промежуточного соединения метил (S)- трет-бутокси-[6-метил-2-(5-метил-хроман-6-ил)-3-трифторметансульфонилокси-фенил]-ацетата (38с)
С помощью процедуры, описанной в примере 1, стадии 10, промежуточное соединение метил (S)- трет-бутокси-[3-гидрокси-6-метил-2-(5-метил-хроман-6-ил) фенил] уксусной (38b) (2,01 г, 5,04 ммоль) преобразовали в метил (S)- трет-бутокси-[6-метил-2-(5-метил-хроман-6-ил)-3-трифторметансульфонилокси-фенил]-ацетат (38с) (2,68 г, 5,04 ммоль, 100%), который использовали без дальнейшей очистки.
МС m/z ([М-Н]-) 529.
Стадия 4: Получение промежуточного соединения метил (S)- трет-бутокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] уксусной (38d)
С помощью процедуры, описанной в примере 21, стадии 4, промежуточное соединение метил (S)-трет-бутокси-[6-метил-2-(5-метил-хроман-6-ил)-3-трифторметансульфонилокси-фенил]-ацетат (38с) (2,68 г, 5,04 ммоль), преобразовали, после очистки с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат от 100/0 до 80/20), в метил (S)- трет-бутокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-ацетат (38d) (1,14 г, 2,69 ммоль, 53%).
1Н ЯМР (400 МГц, CDCl3) δ 0,48-0,69 (м, 4Н), 1,08 (с, 9Н), 1,23-1,33 (м, 1Н), 1,86 (с, 3H), 2,05-2,16 (м, 2Н), 2,47 (с, 3H), 2,63-2,76 (м, 2Н), 3,57 (с, 3H), 4,16-4,24 (м, 2Н), 5,03 (с, 1Н), 6,70 (д, J=8,0 Гц, 2Н), 6,89 (д, J=8,3 Гц, 1Н), 7,06 (д, J=8,0 Гц, 1Н).
МС m/z ([M+Na]+) 445.
Стадия 5: получение (S)- трет-бутокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] уксусной кислоты (пример 38)
К раствору метил (S)- трет-бутокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-ацетата (38d) (285 мг, 0,67 ммоль) в этаноле (2,8 мл) добавляли 2М раствор гидроксида натрия (1,35 мл, 2,70 ммоль). Смесь нагревали при 70°C в течение 16 часов. Этанол выпаривали в вакууме. Добавляли воду (5 мл). Остаточный этанол удаляли в вакууме. Полученный водный раствор экстрагировали этилацетатом (2×5 мл). Органический слой промывали 1М соляной кислотой (10 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением (S)- трет-бутокси-[3-циклопропил-6-метил-2-(5-метил-хроман- 6-ил) фенил] уксусной кислоты (пример 38) (241 мг, 0,59 ммоль, 87%).
1H ЯМР (400 МГц, CDCl3) δ 0,48-0,59 (м, 2Н), 0,59-0,70 (м, 2Н), 1,11 (с, 9Н), 1,27-1,36 (м, 1Н), 1,94 (с, 3H), 2,04-2,12 (м, 2Н), 2,38 (с, 3H), 2,62-2,72 (м, 2Н), 4,15-4,20 (м, 2Н), 5,11 (с, 1H), 6,69 (д, J=8,3 Гц, 1Н), 6,73 (д, J=8,0 Гц, 1H), 6,91 (д, J=8,3 Гц, 1Н), 7,06 (д, J=7,9 Гц, 1H).
MC m/z ([M+Na]+) 431.
МС m/z ([М-Н]-) 407.
Пример 39: Синтез (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(1-метил-циклопропокси)-уксусной кислоты
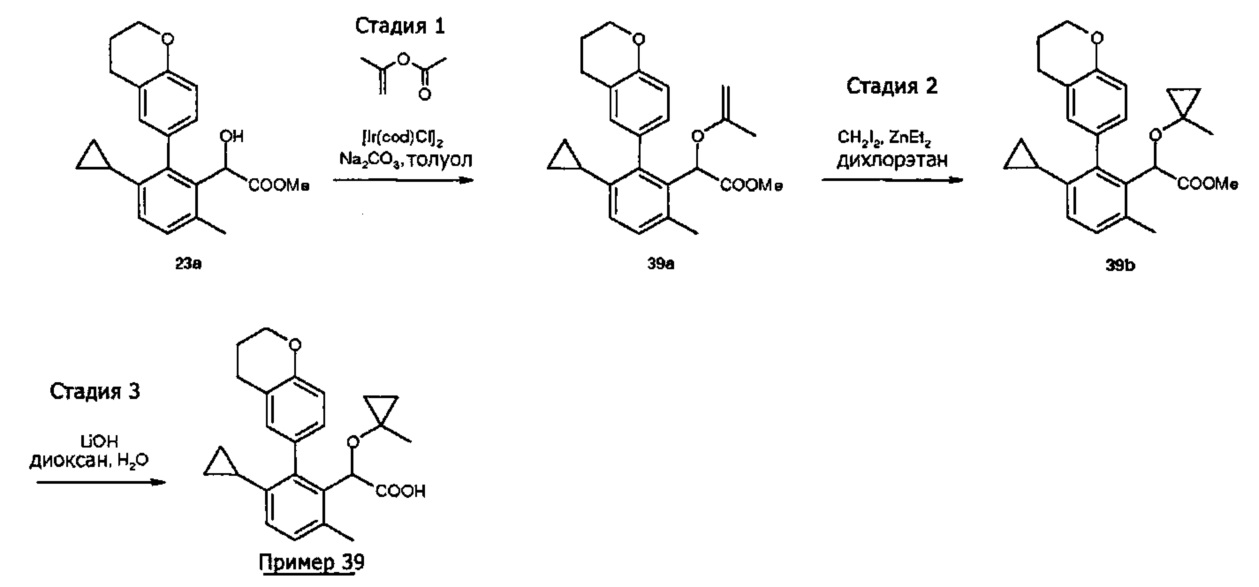
Стадия 1: получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-изопропенилокси-уксусной кислоты (39а)
К дегазированной смеси метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-гидрокси-уксусной кислоты (23а) (86 мг, 0,244 ммоль) и карбоната натрия (15,5 мг, 0,146 ммоль) в толуоле (0,5 мл) добавляли изопропенилацетат (54 мкл, 0,488 ммоль) и бис (1,5-циклооктадиен) диирридий(I) дихлорид (16 мг, 0,024 ммоль). Смесь нагревали микроволнами при 120°C в течение 42 часов. Смесь концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат/триэтиламин 95/5/0,5), с получением метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-изопропенилокси-уксусной кислоты (39а) (25 мг, 0,049 ммоль, 20%) в виде бесцветного масла, содержащего 24% исходного материала (23а). Это масло будет использоваться на следующей стадии без дополнительной очистки.
MS искомого продукта m/z ([M+Na]+) 415.
Стадия 2: получение промежуточного соединения (2-хроман-6-ил-3-циклопропил-6-метил-фенил-)-(1-метил-циклопропокси)-уксусной кислоты (39b)
С помощью процедуры, описанной в примере 23, стадии 3, промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-изопропенилокси-уксусной кислоты (39а) (25 мг, 0,064 ммоль) преобразовали, после очистки препаративной ТСХ (циклогексан/AcOEt 80/20), в метиловый сложный эфир (2-хроман-6-ил-З -циклопропил-6-метил-фенил)-(1-метил-циклопропокси)-уксусной кислоты (39b) (10 мг, 0,024 ммоль, 38%).
1H ЯМР (400 МГц, CDCl3) δ 0,13-0,30 (м, 4Н), 0,47-0,79 (м, 6Н), 1,09 и 1,10 (с, 3H), 1,48-1,58 (м, 1Н), 2,02-2,15 (м, 2Н), 2,31 (с, 3H), 2,74-2,92 (м, 2Н), 3,70 и 3,73 (с, 3H), 4,23-4,34 (м, 2Н), 5,22 и 5,25 (с, 1Н), 6,80 (дд, J=7,9 Гц, J=2,7 Гц, 1Н), 6,87 (т, J=8,1 Гц, 1Н), 7,02-7,08 (м, 3H).
MC m/z ([M+Na]+) 429.
Стадия 3: получение (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(1-метил-циклопропокси)-уксусной кислоты (Пример 39)
С помощью процедуры, описанной в примере 1, стадии 12, метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(1-метил-циклопропокси)-уксусной кислоты (39b) (10 мг, 0,024 ммоль) преобразовали в (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(1-метил-циклопропокси)-уксусную кислоту (пример 39) (5 мг, 0,012 ммоль, 50%) в виде белого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 0,19-0,31 (м, 2Н), 0,44-0,77 (м, 6Н), 1,05 и 1,06 (с, 3H), 1,46-1,55 (м, 1Н), 2,00-2,10 (м, 2Н), 2,26 и 2,28 (с, 3H), 2,70-2,87 (м, 2Н), 4,19-4,28 (м, 2Н), 5,25 и 5,27 (с, 1Н), 6,77-6,85 (м, 2Н), 6,96-7,10 (м, 3H).
MC m/z ([M+Na]+) 415.
MC m/z ([M-H]-) 391.
Пример 40: Синтез (S)-циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] уксусной кислоты

Стадия 1: Получение метил (S)-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-гидрокси-ацетата (40а)
С помощью процедуры, описанной в примере 23, стадии 1, метил (S)- трет-бутокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-ацетат (38d) (850 мг, 2,01 ммоль) преобразовали в метил (S)-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-гидрокси-ацетат (40а) (737 мг, 2,01 ммоль, 97%), который использовали без дальнейшей очистки.
1H ЯМР (300 МГц, CDCl3) δ 0,48-0,75 (м, 4Н), 1,28-1,40 (м, 1Н), 1,91 (с, 3H), 2,03-2,14 (м, 2Н), 2,28 (с, 3H), 2,69 (т, J=6,6 Гц, 2Н), 2,93 (уш. с, 1H), 3,69 (с, 3H), 4,15-4,21 (м, 2Н), 5,06 (с, 1Н), 6,70-6,77 (м, 2Н), 6,88 (д, J=8,3 Гц, 1H), 7,08 (д, J=8,0 Гц, 1Н).
Стадия 2: Получение метил (S)-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-винилокси-ацетата (40b)
С помощью процедуры, описанной в примере 23, стадии 2, промежуточное соединение метил (S)-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-гидрокси-ацетат (40а) (737 мг, 2,01 ммоль) преобразовали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20) в метил (S)-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-винилокси-ацетат (40b) (417 мг, 1,06 ммоль, 53%).
1H ЯМР (300 МГц, CDCl3) δ 0,52-0,74 (м, 4Н), 1,29-1,40 (м, 1Н), 1,92 (с, 3H), 2,06-2,13 (м, 2Н), 2,32 (с, 3H), 2,70 (т, J=6,6 Гц, 2Н), 3,67 (с, 3H), 3,99 (дд, J=1,9 Гц, J=6,4 Гц, 1Н), 4,17-4,22 (м, 2Н), 4,27 (дд, J=1,9 Гц, J=13,9 Гц, 1Н), 5,17 (с, 1Н), 6,12 (дд, J=6,4 Гц, J=13,9 Гц, 1H), 6,72 (д, J=8,3 Гц, 1Н), 6,77 (д, 8,0 Гц, 1H), 6,82 (д, J=8,3 Гц, 1H), 7,10 (д, J=8,0 Гц, 1Н).
MC m/z ([M+Na]+) 415.
Стадия 3: Получение метил (S)-циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-ацетата (40с)
С помощью процедуры, описанной в примере 23, стадии 3, промежуточное соединение метил (S)-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-винилокси-ацетат (40b) (417 мг, 1,06 ммоль) преобразовали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20) в метил (S)-циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-ацетат (40с) (238 мг, 0,59 ммоль, 55%).
1H ЯМР (300 МГц, CDCl3) δ 0,21-0,32 (м, 1Н), 0,32-0,48 (м, 2Н), 0,51-0,73 (м, 5Н), 1,27-1,38 (м, 1H), 1,91 (с, 3H), 2,06-2,16 (м, 2Н), 2,32 (с, 3H), 2,66-2,75 (м, 2Н), 3,43-3,51 (м, 1Н), 3,64 (с, 3H), 4,16-4,24 (м, 2Н), 4,93 (с, 1H), 6,69-6,76 (м, 2Н), 6,86 (д, J=8,3 Гц, 1Н), 7,06 (д, J=8,0 Гц, 1Н).
MC m/z ([M+Na]+) 429.
Стадия 4: Получение (S)-циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] уксусной кислоты (пример 40)
С помощью процедуры, описанной в примере 38, стадии 5, промежуточное соединение метил (S)-циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] уксусной (40с) (238 мг, 0,59 ммоль) преобразовали в (S)-циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил] уксусную кислоту (пример 40) (180 мг, 0,46 ммоль, 78%).
1H ЯМР (300 МГц, CDCl3) δ 0,32-0,73 (м, 8Н), 1,30-1,41 (м, 1Н), 1,92 (с, 3H), 2,03-2,15 (м, 2Н), 2,31 (с, 3H), 2,64-2,73 (м, 2Н), 3,27-3,36 (м, 1H), 4,15-4,22 (м, 2Н), 5,00 (с, 1H), 6,69 (д, J=8,3 Гц, 1H), 6,78 (д, J=8,0 Гц, 1H), 6,88 (д, J=8,3 Гц, 1Н), 7,09 (д, J=8,0 Гц, 1Н).
MC m/z ([M+Na]+) 415.
MC m/z ([M-H]-) 391.
Пример 41: Синтез (S)-трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты

Стадия 1: получение промежуточного соединения метилового сложного эфира (S)-[3-бензилокси-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-трет бутокси-уксусной кислоты (41а)
С помощью процедуры, описанной в примере 1, стадии 7, промежуточное соединение (S)-метил-2-(3-бензилокси-2-бром-6-метилфенил)-2-(трет-бутокси) ацетат (13С) (3,32 г, 7,89 ммоль), в реакции с 2-(8-фтор-3,4-дигидро-2Н-1-бензопиран-6-ил)-4,4,5,5-тетраметил-1,3,2-диоксабороланом (2,76 г, 9,46 ммоль), преобразовали, после очистки хроматографией на силикагеле (циклогексан/этилацетат 80/20), в метиловый сложный эфир (S)-[3-бензилокси-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-трет-бутокси-уксусной кислоты (41а) (1,45 г, 2,86 ммоль, 36%).
1H ЯМР (300 МГц, CDCl3) δ 1,12 (с, 9Н), 1,83 (с, 3H), 2,07-2,20 (м, 2Н), 2,45 (с, 3H), 2,64-2,76 (м, 2Н), 3,57 (с, 3H), 4,27-4,31 (м, 2Н), 4,94 (м, 2Н), 5,05 (с, 1Н), 6,72 (д, J=11,7 Гц, 1H), 6,81 (д, J=8,4 Гц, 1H), 7,04-7,09 (м, 3H), 7,22-7,27 (м, 3H).
MC m/z ([M+Na]+) 529.
Стадия 2: получение промежуточного соединения метилового сложного эфира (S)-трет-бутокси-[2-(8-фтор-5-метил-хроман-6-ил)-3-гидрокси-6-метил-фенил] уксусной кислоты (41b)
С помощью процедуры, описанной в примере 15, стадии 2, промежуточное соединение метиловый сложный эфир (S)-3-бензилокси-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-трет-бутокси- уксусной кислоты (41а) (3,19 г, 6,29 ммоль) преобразовали после очистки с помощью хроматографии на силикагеле (циклогексан/этилацетат 70/30) в метиловый сложный эфир (S)- трет-бутокси-[2-(8-фтор-5-метил-хроман-6-ил)-3-гидрокси-6-метил-фенил] уксусной кислоты (41а) (2,61 г, 6,27 ммоль, 100%).
1Н ЯМР (300 МГц, CDCl3) δ 1,10 (с, 9Н), 1,88 (с, 3H), 2,08-2,20 (м, 2Н), 2,43 (с, 3H), 2,68-2,77 (м, 2Н), 3,58 (с, 3H), 4,25-4,32 (м, 2Н), 4,38 (с, 1Н), 4,92 (с, 1H), 6,77 (д, J=11,2 Гц, 1Н), 6,83 (д, J=8,3 Гц, 1Н), 7,07 (д, J=8,3 Гц, 1H).
МС m/z ([М-Н]-) 415.
Стадия 3: получение промежуточного соединения метилового сложного эфира (S)-трет-бутокси-[2-(8-фтор-5-метил-хроман-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]-уксусной кислоты (41с)
С помощью процедуры, описанной в примере 1, стадии 10, промежуточное соединение метиловый сложный эфир (S)- трет-бутокси-[2-(8-фтор-5-метил-хроман-6-ил)-3-гидрокси-6-метил-фенил] уксусной кислоты (41b) (2,61 г, 6,27 ммоль) преобразовали в метиловый сложный эфир (S)- трет-бутокси-[2-(8-фтор-5-метил-хроман-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]-уксусной кислоты (41с) (3,26 г, 5,94 ммоль, 95%), который использовали без дальнейшей очистки.
1H ЯМР (400 МГц, CDCl3) δ 1,11 (с, 9Н), 1,81 (с, 3H), 2,09-2,17 (м, 2Н), 2,53 (с, 3H), 2,66-2,73 (м, 2Н), 3,59 (с, 3H), 4,24-4, 31 (м, 2Н), 5,04 (с, 1H), 6,74 (д, J=11,2 Гц, 1H), 7,17 (д, J=8,5 Гц, 1H), 7,23 (д, J=8,5 Гц, 1Н).
МС m/z ([М-Н]-) 547.
Стадия 4: получение промежуточного соединения метилового сложного эфира (S)-трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (41d)
С помощью процедуры, описанной в примере 21, стадии 4, промежуточное соединение метиловый сложный эфир (S)- трет-бутокси-[2-(8-фтор-5-метил-хроман-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]-уксусной кислоты (41с) (3,26 г, 5,94 ммоль) преобразовали после очистки с помощью хроматографии на силикагеле (циклогексан/этилацетат, 95/5) в метиловый сложный эфир (S)- трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (41d) (2,38 г, 5,41 ммоль, 91%).
1H-ЯМР (300 МГц, CDCl3) δ 0,46-0,58 (м, 2Н), 0,58-0,71 (м, 2Н), 1,10 (с, 9Н), 1,19-1,32 (м, 1Н), 1,82 (с, 3H), 2,08-2,19 (м, 2Н), 2,46 (с, 3H), 2,66-2,76 (м, 2Н), 3,57 (с, 3H), 4,24-4,31 (м, 2Н), 4,99 (с, 1Н), 6,71 (д, J=7,8 Гц, 1Н), 6,74 (д, J=10,3 Гц, 1Н), 7,07 (д, J=7,8 Гц, 1H).
MC m/z ([M+Na]+) 463.
Стадия 5: получение (S)- трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (пример 41)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метиловый сложный эфир (S)- трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (41d) (315 мг, 0,72 ммоль) преобразовали в (S)- трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6 метил-фенил] уксусную кислоту (пример 41) (204 мг, 0,48 ммоль, 67%).
1H ЯМР (400 МГц, CDCl3) δ 0,53-0,56 (м, 2Н), 0,64-0,68 (м, 2Н), 1,13 (с, 9Н), 1,24-1,31 (м, 1Н), 1,91 (с, 3H), 2,09-2,14 (м, 2Н), 2,39 (с, 3H), 2,63-2,76 (м, 2Н), 4,25-4,28 (м, 2Н), 5,09 (с, 1Н), 6,76 (д, J=8,0 Гц, 1Н), 6,78 (д, J=10,4 Гц, 1Н), 7,08 (д, J=8,0 Гц, 1Н), 9,43-9,97 (шир, 1Н).
МС m/z ([M+Na]+) 449.
МС m/z ([М-Н]-) 425.
Пример 42: Синтез трет-бутокси-(6-хроман-6-ил-7-циклопропил-хинолин-5-ил) уксусной кислоты
Стадия 1: получение промежуточного соединения 7-хлор-6-метоксихинолина (42а)
В круглодонную колбу добавляли, в следующем порядке, 3-хлор-4-метоксианилин (3,0 г, 19,04 ммоль), 4-нитрофенол (2,12 г, 15,20 ммоль), сульфата железа(II) гептагидрат (159 мг, 0,57 ммоль) и глицерин (8,3 мл, 114,20 ммоль). Перемешанную смесь охлаждали в ледяной бане и добавляли по каплям концентрированную серную кислоту (3,2 мл). Ледяную баню удаляли и перемешанную смесь осторожно нагревали до 140°C в течение 21 ч. Реакционную смесь охлаждали до комнатной температуры/ выливали в воду со льдом, затем подщелачивали 28% водным раствором гидроксида натрия. Затем смесь экстрагировали три раза хлороформом. Объединенные органические слои промывали 3М раствором гидроксида натрия, насыщенным раствором соли, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (от 100% дихлорметана до 90/10 дихлорметан/этилацетат) с получением только один региоизомера 7-хлор-6-метокси-хинолин (42а) (2,44 г, 12,60 ммоль, 66%) в виде белого твердого вещества.
1H ЯМР (400 МГц, ДМСО-d6) δ 4,00 (с, 3H), 7,52 (дд, J=8,4 Гц, J=4,4 Гц 1Н), 7,58 (с, 1H), 8,09 (с, 1Н), 8,30 (дд, J=8,4 Гц, J=1,6 Гц, 1Н), 8,78 (дд, J=4,4 Гц, J=1,6 Гц, 1H).
МС m/z ([М+Н]+) 194/196.
Стадия 2: Получение промежуточного соединения 7-хлор-5-иод-6-метоксихинолина (42b)
К раствору 7-хлор-6-метоксихинолина (42а) (3,43 г, 17,71 ммоль) в концентрированной серной кислоте (37 мл) добавляли N-йодосукцинимид (4,18 г, 18,60 ммоль) в трех порциях при комнатной температуре. И реакционную смесь перемешивали при комнатной температуре в течение 23 часов. Реакционную смесь выливали в воду со льдом. Водную смесь доводили до рН~10 28%-ным водным раствором гидроксида натрия и затем экстрагировали три раза дихлорметаном. Объединенный экстракт дважды промывали насыщенным раствором тиосульфата натрия, насыщенным раствором соли, затем сушили над сульфатом натрия и концентрировали в вакууме с получением 7-хлор-5-иод-6-метоксихинолина (42b) (5,55 г, 17,36 ммоль, 98%) в виде твердого вещества серого цвета без очистки.
1Н ЯМР (400 МГц, ДМСО-d6) δ 3,91 (с, 3H), 7,67 (дд, J=8,6 Гц, J=4,2 Гц, 1H), 8,24 (с, 1Н), 8,41 (д,7=8,6 Гц, 1Н), 8,88 (дд, J=4,2 Гц, J=1,6 Гц, 1Н).
МС m/z ([М+Н]+) 320/322.
Стадия 3: Получение промежуточного соединения 7-хлор-5-иод-хинолин-6-ола (42 с)
К раствору 7-хлор-5-иод-6-метоксихинолина (42b) (5,50 г, 17,21 ммоль) в дихлорметане (165 мл) медленно добавляли трибромид бора (1М в дихлорметане, 86 мл, 86,06 ммоль). Полученную смесь перемешивали в течение 3 дней и охлаждали до -5°C. Медленно добавляли метанол (45 мл) и перемешивали смесь в течение 20 минут при комнатной температуре. Растворители удаляли в вакууме. Полученный желтый твердый продукт растворяли в метаноле (60 мл) и обрабатывали 1N раствором гидроксида натрия (рН ~ 12). Полученную смесь перемешивали в течение 3 часов и добавляли уксусную кислоту до рН до 4-5. Смесь фильтровали и дважды промывали водой. Серый твердый продукт сушили при пониженном давлении с получением 7-хлор-5-иод-хинолин-6-ола (42с) (4,91 г, 16,07 ммоль, 93%).
1H ЯМР (400 МГц, DMSO-d6) δ 7,58 (дд, J=8,6 Гц, J=4,4 Гц, 1Н), 8,14 (с, 1Н), 8,30-8,32 (м, 1Н), 8,73 (дд, J=4,4/1,6 Гц, 1Н), 10,63 (уш. с, 1Н).
МС m/z ([М+Н]+) 306/308.
Стадия 4: Получение промежуточного соединения 6-бензилокси-7-хлор-5-йодохинолина(42d)
К раствору 7-хлор-5-иод-хинолин-6-ола (42с) (4,91 г, 16,07 ммоль) в ацетоне (45 мл) последовательно добавляли карбонат калия (2,70 г, 19,28 ммоль), бензилбромид (2,1 мл, 17,68 ммоль) и иодид натрия (482 мг, 3,21 ммоль). Смесь кипятили с обратным холодильником в течение 3 часов. Растворитель удаляли путем выпаривания в вакууме. Остаток растворяли в воде и этилацетате. Водный слой экстрагировали этилацетатом два раза. Органические слои промывали солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (от 100% дихлорметана до 98/2 дихлорметан/этилацетат) с получением 6-бензилокси-7-хлор-5-йодохинолина (42d) (4,87 г, 12,31 ммоль, 77%) в виде белого твердого вещества.
1H ЯМР (400 МГц, DMSO-d6) δ 5,10 (с, 2Н), 7,42-7,49 (м, 3H), 7,65-7,70 (м, 3H), 8,30 (с, 1Н), 8,44 (дд, J=0,7 Гц, J=8,6 Гц, 1H), 8,90 (дд, J=4,2 Гц, 7=1,4 Гц, 1H).
МС m/z ([М+Н]+) 396/398.
Стадия 5: Получение промежуточного соединения этилового сложного эфира (6-бензилокси-7-хлор-хинолин-5-ил) оксо-уксусной кислоты (42е)
В круглодонную колбу, в атмосфере аргона, при -30°C, раствор комплекса хлорида изопропилмагния хлорида лития (1,3 М в тетрагидрофуране, 9,25 мл, 12,02 ммоль) медленно добавляли в течение 20 минут к перемешиваемому раствору 6-бензилокси-7 хлор-5-иод-хинолина (42d) (4,67 г, 11,44 ммоль) в (21 мл). Реакционную смесь затем перемешивали в течение 5 минут с температурой, поддерживаемой при -30°C. Смесь охлаждали до -50°C и медленно добавляли диэтилоксалат (1,70 мл, 12,58 ммоль) с помощью шприца. Смесь перемешивали при -40°C в течение 1 часа и осторожно нагревали до комнатной температуры в течение более 1 часа. Смесь охлаждали до 0°C, гасили насыщенным раствором хлорида аммония и дважды экстрагировали этилацетатом. Объединенные органические слои промывали солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (от 100% дихлорметана до 96/4 дихлорметан/этилацетат) с получением этилового сложного эфира (6-бензилокси-7-хлор-хинолин-5-ил) оксо-уксусной кислоты (42Е) (3,20 г, 8,65 ммоль, 76%) в виде белого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 1,15 (т, J=7,2 Гц, 3H), 4,10 (q, J=7,2 Гц, 2Н), 5,14 (с, 2Н), 7,36-7,42 (м, 3H), 7,47-7,52 (м, 3H), 8,42 (с, 1Н), 8,55-8,57 (м, 1Н), 8,93 (дд, J=4,2 Гц, J=1,6 Гц, 1Н).
МС m/z ([М+Н]+) 370/372.
Стадия 6: Получение промежуточного соединения этилового сложного эфира (6-бензилокси-7-хлор-хинолин-5-ил) окси-уксусной кислоты (42f)
В атмосфере аргона, боргидрид натрия (85 мг, 2,26 ммоль) добавляли к раствору этилового сложного эфира (6-бензилокси-7-хлор-хинолин-5-ил) оксо-уксусной кислоты (42е) (980 мг, 2,65 ммоль) в (16,6 мл) и этанола (4,2 мл) при -5°C и перемешивали смесь в течение 40 минут. Затем смесь гасили этанолом и водой и экстрагировали этилацетатом дважды. Объединенные органические слои промывали 1N водным раствором хлористоводородной кислоты, насыщенным раствором соли, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (от 100% дихлорметана до 90/10 дихлорметан/этилацетат) с получением (6-бензилокси-7-хлор-хинолин-5-ил) этиловый эфир гидрокси-уксусной (42f) (973 мг, 2,62 ммоль, 99%) в виде белого твердого вещества.
1Н ЯМР (400 МГц, CDCl3) δ 1,09 (т, J=7,2 Гц, 3H), 3,35 (д, J=2,8 Гц, 1Н), 4,11-4,22 (м, 2Н), 5,14 (с, 2Н), 5,98 (д, J=2,8 Гц, 1Н), 7,39-7,44 (м, 4Н), 7,55-7,57 (м, 2Н), 8,26 (с, 1Н), 8,40-8,42 (м, 1Н), 8,88 (дд, J=1,6 Гц, J=4,2 Гц, 1Н).
МС m/z ([М+Н]+) 372/374.
Стадия 7: Получение промежуточного соединения этилового сложного эфира (6-бензилокси-7-хлор-хинолин-5-ил)- трет-бутокси-уксусной кислоты (42g)
В атмосфере аргона при комнатной температуре, перхлорную кислоту (3,8 мл, 62,80 ммоль) добавляли одной быстрой порцией к раствору этилового сложного эфира (6-бензилокси-7-хлор-хинолин-5-ил) гидрокси-уксусной кислоты (1f) (2,78 г, 7,48 ммоль) и запечатывали колбу. Смесь перемешивали при комнатной температуре в течение 4 часов. Смесь охлаждали при 0°C и гасили насыщенным раствором гидрокарбоната натрия и экстрагировали этилацетатом два раза. Органический слой промывали насыщенным солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (от 95/5 до 80/20 дихлорметан/этилацетат) с получением этилового сложного эфира (6-бензилокси-7-хлор-хинолин-5-ил)- трет-бутокси-уксусной кислоты (42g) (2,60 г, 6,08 ммоль, 81%) в виде белого порошка.
1H ЯМР (400 МГц, CDCl3) δ 1,12-1,15 (м, 12Н), 4,05-4,21 (м, 2Н), 5,11 (д, J=10,4 Гц, 1Н), 5,39 (д, 7=10,4 Гц, 1H), 6,09 (с, 1Н), 7,36-7,48 (м, 4Н), 7,60-7,62 (м, 2Н), 8,18 (с, 1Н), 8,83-8,87 (м, 2Н).
МС m/z ([М+Н]+) 428/430.
Стадия 8: Получение промежуточного соединения этилового сложного эфира (6-бензилокси-7-циклопропил-хинолин-5-ил)- трет-бутокси-уксусной кислоты (42b.)
К дегазированной смеси этилового сложного эфира (6-бензилокси-7-хлор-хинолин-5-ил)- трет-бутокси-уксусной кислоты (42g) (2,90 г, 6,78 ммоль), добавляли карбонат калия (2,8 г, 20,30 ммоль), циклопропилтрифторборат калия (1,6 г, 10,84 ммоль) в толуоле (25 мл) и воде (2,4 мл) палладий(II) ацетат (76 мг, 0,34 ммоль) и 2-дициклогексилфосфино-2',6'-диизопропоксибифенил («Ruphos», 221 мг, 0,47 ммоль). Смесь нагревали при 90°C в течение 21 ч, а затем добавляли воду. Водный, слой экстрагировали этилацетатом два раза. Объединенные органические слои промывали солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат 80/20) с получением этилового сложного эфира (6-бензилокси-7-циклопропил-хинолин-5-ил)-трет-бутокси-уксусной кислоты (42h) (2,73 г, 6,30 ммоль, 93%).
1H ЯМР (400 МГц, CDCl3) δ 0,81-0,88 (м, 1Н), 1,02-1,16 (м, 6Н), 1,18 (с, 9Н), 2,33-2,40 (м, 1Н), 4,03-4,23 (м, 2Н), 5,21 (д, J=11,2 Гц, 1Н), 5,30 (д, J=11,2 Гц, 1Н), 6,15 (с, 1Н), 7,29 (дд, J=4,2 Гц, J=8,6 Гц, 1H), 7,37-7,48 (м, 3H), 7,55-7,59 (м, 3H), 8,77 (дд, J=4,2 Гц,/=1,6 Гц, 1Н), 8,80-8,83 (м, 1Н).
МС m/z ([М+Н]+) 434.
Стадия 9: Получение промежуточного соединения этилового сложного эфира трет-бутокси-(7-циклопропил-6-гидрокси-хинолин-5-ил) уксусной кислоты (42i)
Суспензию этилового сложного эфира (6-бензилокси-7-циклопропил-хинолин-5-ил)- трет-бутокси-уксусной кислоты (42h) (2,47 г, 5,70 ммоль) и палладий на углероде (10%, 61 мг) в этаноле (38 мл) и дихлорметан (13 мл) перемешивали при комнатной температуре в атмосфере водорода в течение 3 часов. Смесь фильтровали через Millipore и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (дихлорметан/этилацетат 90/10) с получением этилового сложного эфира трет-бутокси-(7-циклопропил-6-гидрокси-хинолин-5-ил) уксусной кислоты (42i) (1,96 г, 5,70 ммоль, 100%).
1H ЯМР (400 МГц, CDCl3) δ 0,82-0,86 (м, 2Н), 1,06-1,09 (м, 2Н), 1,14 (т, J=7,2 Гц, 3H), 1,33 (с, 9Н), 2,33-2,39 (м, 1Н), 4,04-4,20 (м, 2Н), 5,88 (с, 1Н), 7,33 (дд, J=4,2 Гц, J=8,6 Гц, 1Н), 7,52 (с, 1Н), 8,31 (д, J=8,6 Гц, 1H), 8,70 (дд, J=4,2 Гц, J=1,6 Гц 1H), 9,18 (с, 1Н).
МС m/z ([М+Н]+) 344.
Стадия 10: Получение промежуточного соединения этилового сложного эфира трет-бутокси-(7-циклопропил-6-трифторметансульфонат сульфонилокси-хинолин-5-ил) уксусной кислоты (42j)
В атмосфере аргона, этиловый сложный эфир трет-бутокси-(7-циклопропил-6-гидрокси-хинолин-5-ил) уксусной кислоты (42i) (1,96 г, 5,70 ммоль), N-фенил-бис (трифторметансульфонат-сульфонимид) (2,22 г, 6,23 ммоль), карбонат калия (2,0 г, 14,55 ммоль) и (12 мл) смешивали в микроволновой ампуле Biotage® (10-20 мл) с магнитной мешалкой. Реакционную смесь перемешивали и нагревали при 110°C в течение 75 минут в микроволновом синтезаторе Biotage® InitiatorTM 2,5. Смесь разбавляли насыщенным раствором хлорида аммония и этилацетата. Слои разделяли и органический слой промывали рассолом, сушили над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат 80/20) с получением этилового сложного эфира трет-бутокси-(7-циклопропил-6-трифторметансульфонилокси-хинолин-5-ил) уксусной кислоты (42j) (1,75 г, 3,68 ммоль, 65%) в виде белого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 0,86-0,98 (м, 2Н), 1,04-1,20 (м, 5Н), 1,21 (с, 9Н), 2,20-2,25 (м, 1H), 3,98-4,06 (м, 1H), 4,14-4,22 (м, 1H), 5,88 (с, 1Н), 7,37 (дд, J=8,6 Гц, J=4,2 Гц, 1Н), 7,78 (с, 1Н), 8,73-8,75 (м, 1H), 8,90 (дд, J=1,6 Гц, J=4,2 Гц, 1Н).
МС m/z ([М+Н]+) 476.
Стадия 11: Получение промежуточного соединения этилового сложного эфира трет-бутокси-(6-хроман-6-ил-7-циклопропил-хинолин-5-ил) уксусной кислоты (42k)
В атмосфере аргона, добавляли этиловый сложный эфир трет-бутокси-(7-циклопропил-6-трифторметансульфонилокси-хинолин-5-ил) уксусной кислоты (42j) (758 мг, 1,59 ммоль), хроман-6-борную кислоту, эфир пинакона (498 мг, 1,91 ммоль), моногидрат трехосновного фосфата калия (732 мг, 3,18 ммоль) и диоксан (6,8 мл) в микроволновый флакон Biotage® (10-20 мл) с магнитной мешалкой. Смесь дегазировали в атмосфере аргона в течение 10 минут и добавляли палладий тетракис (трифенилфосфин) (111 мг, 0,10 ммоль). Пробирку закрывали и нагревали в микроволновом синтезаторе Biotage® InitiatorTM™ 2,5 при 160°C в течение 7 часов. Смесь разбавляли этилацетатом, фильтровали через Celite® (было сделано несколько промывок этилацетатом) и концентрировали фильтрат в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат 85/15) с получением этилового сложного эфира трет-бутокси-(6-хроман-6-ил-7-циклопропил-хинолин-5-ил) уксусной кислоты (42k) (277 мг, 0,60 ммоль, 38%), в виде смеси атропоизомеров.
1Н ЯМР (400 МГц, CDCl3) δ 0,77-0,87 (м, 4Н), 1,04 (с, 9Н), 1,10-1,18 (м, 3H), 1,56-1,61 (м, 1Н), 2,07-2,11 (м, 2Н), 2,81-2,87 (м, 2Н), 3,95-4,19 (м, 2Н), 4,26-4,30 (м, 2Н), 5,35-5,39 (м, 1H), 6,86-7,07 (м, 2Н), 7,14-7,18 (м, 1Н), 7,31 (дд, J=8,62 Гц, J=4,2 Гц, 1H), 7,58 (д, J=2,3 Гц, 1H), 8,81 (дд, 1,6 Гц, J=4,2 Гц, 1Н), 9,01-9,04 (м, 1Н).
MC m/z ([М+Н]+) 460.
Стадия 12: Получение трет-бутокси-(6-хроман-6-ил-7-циклопропил-хинолин-5-ил) уксусной кислоты (Пример 42)
Смесь этилового сложного эфира трет-бутокси-(6-хроман-6-ил-7-циклопропил-хинолин-5-ил) уксусной кислоты (42K) (44 мг, 0,10 ммоль) и гидроксид калия (11 мг, 0,19 ммоль) в метаноле (0,9 мл) и воды (1 мл) нагревали при 70°C в течение 16 часов. Смесь концентрировали в вакууме. К остатку добавляли воду и этилацетат и полученную смесь подкисляли 1М соляной кислотой до рН 4-5. Водный слой экстрагировали дважды. Органический слой промывали насыщенным раствором соли и сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (дихлорметан/метанол 90/10) с получением трет-бутокси-(6-хроман-6-ил-7-циклопропил-хинолин-5-ил) уксусной кислоты (пример 42) (28 мг, 0,06 ммоль, 68%) в виде белого твердого вещества, в виде смеси атропоизомеров.
1H ЯМР (400 МГц, CDCl3) δ 0,75-0,89 (м, 4Н), 1,00 (с, 9Н), 1,62-1,64 (м, 1H), 2,05-2,09 (м, 2Н), 2,79-2,86 (м, 2Н), 4,22-4,30 (м, 2Н), 5,51-5,53 (м, 1H), 6,87-7,11 (м, 3H), 7,31-7,35 (м, 1Н), 7,61 (с, 1H), 8,56-8,82 (м, 2Н).
МС m/z ([М+Н]+) 432.
МС m/z ([М-Н]-) 430.
Пример 43: Синтез трет-бутокси-(2-хроман-6-ил-3-циклобутил-6-метил-фенил) уксусной кислоты
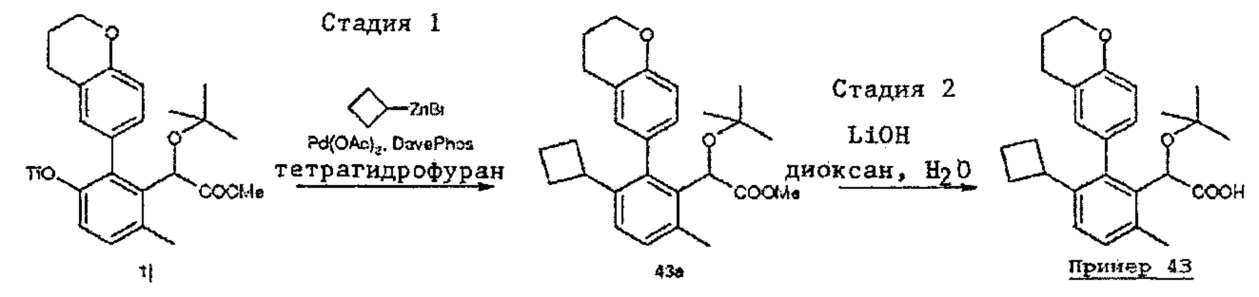
Стадия 1: Получение промежуточного соединения метилового сложного эфира трет-бутокси-(2-хроман-6-ил-3-циклобутил-6-метил-фенил) уксусной кислоты (43а)
К метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил-3-трифторметансульфонилокси-фенил]ацетату (1j) (220 мг, 0,426 ммоль) и добавляли 0,5М раствор циклобутиилцинк бромида в (3,40 мл, 1,70 ммоль). Смесь дегазировали барботированием аргона в течение 5 минут. Последовательно добавляли 2-дициклогексилфосфино-2'-(N,N-диметиламино) бифенил (DavePhos) (17 мг, 0,043 ммоль) и ацетат палладия (4,70 мг, 0,021 ммоль) и нагревали смесь при 60°C в течение 4 часов. Нагревание прекращали и когда температура достигала 30°C добавляли насыщенный водный раствор хлорида аммония (10 мл). Водный слой экстрагировали циклогексаном (3×5 мл). Объединенные органические слои промывали солевым раствором (20 мл), сушили над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 90/10) с получением метилового сложного эфира трет-бутокси-(2-хроман-6-ил-3-циклобутил-6-метил-фенил) уксусной кислоты (43а) (143 мг, 0,338 ммоль, 79%) в виде желтого масла.
1Н ЯМР (300 МГц, CDCl3) δ 0,97 (с, 9Н), 1,60-1,79 (м, 3H), 1,88-2,12 (м, 5Н), 2,41 (с, 3H), 2,62-2,87 (м, 2Н), 3,19-3,30 (м, 1H), 3,64 и 3,66 (с, 3H), 4,21-4,29 (м, 2Н), 5,03 и 5,05 (с, 1Н), 6,77-6,87 (м, 2Н), 6,95-7,02 (м, 1Н), 7,12 (д, 1Н J=7,9 Гц), 7,26 (д, 1Н, J=7,9 Гц).
МС m/z ([M+Na]+) 445.
Стадия 2: Получение трет-бутокси-(2-хроман-6-ил-3-циклобутил-6-метил-фенил) уксусной кислоты (Пример 43)
С помощью процедуры, описанной в примере 1, стадии 12, метиловый сложный эфир трет-бутокси-(2-хроман-6-ил-3-циклобутил-6-метил-фенил) уксусной кислоты (43а) (143 мг, 0,338 ммоль) преобразовали, после очистки на силикагеле (циклогексан/этилацетат от 90/0 до 70/30) в трет-бутокси-(2-хроман-6-ил-3-циклобутил-6-метил-фенил) уксусную кислоту (пример 43) (131 мг, 0,320 ммоль, 94%) в виде белого твердого вещества.
1H ЯМР (300 МГц, CDCl3) δ 0,99 (с, 9Н), 1,57-1,92 (м, 4Н), 2,00-2,11 (м, 4Н), 2,36 (с, 3H), 2,67-2,86 (м, 2Н), 3,21-3,39 (м, 1Н), 4,19-4,30 (м, 2Н), 5,18 (с, 1Н), 6,78-6,87 (м, 2Н), 7,11-7,19 (м, 2Н), 7,26-7,28 (м, 1Н), 9,10-10,60 (уш. с, 1H).
MC m/z ([M+Na]+) 431.
МС m/z ([М-Н]-) 407.
Пример 44: Синтез (S)-циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты

Стадия 1: Получение промежуточного соединения (S)-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-гидрокси-уксусной кислоты метилового сложного эфира (44а)
С помощью процедуры, описанной в примере 23, стадии 1, метиловый сложный эфир (S)-трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (41d) (2,07 г, 4,69 ммоль) преобразовали в метиловый сложный эфир (S)-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-гидрокси-уксусной кислоты (44а) (1,68 г, 4,36 ммоль, 93%), который использовали без дальнейшей очистки.
1Н ЯМР (400 МГц, CDCl3) δ 0,49-0,63 (м, 2Н), 0,63-0,74 (м, 2Н), 1,27-1,36 (м, 1H), 1,86 (с, 3H), 2,08-2,16 (м, 2Н), 2,28 (с, 3H), 2,67-2,73 (м, 2Н), 2,94 (д, J=2,8 Гц, 1Н), 3,70 (с, 3H), 4,23-4,28 (м, 2Н), 5,04 (д, J=2,8 Гц, 1Н), 6,75 (д, J=11,3 Гц, 1H), 6,76 (д, J=8,0 Гц, 1Н), 7,09 (д,.7=8,0 Гц, 1H).
МС m/z ([M+Na]+) 407.
Стадия 2: Получение промежуточного соединения метилового сложного эфира (S)-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-винилокси-уксусной кислоты (44b)
К раствору метилового сложного эфира (S)-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-гидрокси-уксусной кислоты (44а) (1,54 г, 4,00 ммоль) в смеси этилвинилового эфира (8,0 мл) и дихлорметана (8,0 мл) при комнатной температуре добавляли TFA (90 мкл, 1,20 ммоль). Перемешивание продолжали в течение 7 часов, прежде чем реакционную смесь гасили добавлением триэтиламина (220 мкл, 1,60 ммоль) и концентрировали в вакууме.
Промежуточный ацеталь непосредственно растворяли в безводном дихлорметане (10 мл), охлаждали до 0°C перед покапельным добавлением триэтиламина (840 мкл, 6,00 ммоль) и триметилсилилтрифторметансульфоната (940 мкл, 5,20 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 2 часов, после чего реакцию гасили 1М раствором гидроксида натрия. Органический слой отделяли, промывали насыщенным солевым раствором, сушили над сульфатом натрия и концентрировали при пониженном давлении. Неочищенный материал очищали с помощью хроматографии на силикагеле (циклогексан/этилацетат 70/30), с получением метилового сложного эфира (S)-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-винилокси-уксусной кислоты (44b) (1,31 г, 3,19 ммоль, 80%) в виде желтого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 0,51-0,61 (м, 2Н), 0,62-0,74 (м, 2Н), 1,30-1,37 (м, 1Н), 1,88 (с, 3H), 2,10-2,16 (м, 2Н), 2,32 (с, 3H), 2,70-2,73 (м, 2Н), 3,68 (с, 3H), 4,03 (дд, J=6,4 Гц, J=2,0 Гц, 1Н), 4,24-4,28 (м, 3H), 5,14 (с, 1H), 6,14 (дд, J=13,6 Гц, J=6,4 Гц, 1H), 6,69 (д, J=11,6 Гц, 1Н), 6,78 (д, J=8,0 Гц, 1Н), 7,11 (д, J=8,0 Гц, 1H).
МС m/z ([M+Na]+) 433.
Стадия 3: Получение промежуточного соединения метилового сложного эфира (S)-циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (44с)
С помощью процедуры, описанной в примере 23, стадии 3, промежуточное соединение метиловый сложный эфир (S)-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-винилокси-уксусной кислоты (44b) (503 мг, 1,23 ммоль) преобразовали после очистки с помощью хроматографии на силикагеле (циклогексан/этилацетат 80/20) в метиловый сложный эфир (S)-циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (44с) (520 мг, 1,23 ммоль, 100%).
1H ЯМР (400 МГц, CDCl3) δ 0,29-0,36 (м, 1H), 0,38-0,49 (м, 2Н), 0,51-0,62 (м, 3H), 0,63-0,72 (м, 2Н), 1,28-1,35 (м, 1Н), 1,87 (с, 3H), 2,10-2,17 (м, 2Н), 2,32 (с, 3H), 2,70-2,74 (м, 2Н), 3,42-3,47 (м, 1H), 3,64 (с, 3H), 4,26-4,29 (м, 2Н), 4,90 (с, 1Н), 6,73 (д, J=11,6 Гц, 1H), 6,75 (д, J=7,6 Гц, 1H), 7,07 (д, J=7,6 Гц, 1Н).
MC m/z ([M+Na]+) 447.
Стадия 4: Получение (S)-циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (пример 44)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метиловый сложный эфир (S)-циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусной кислоты (44с) (520 мг, 1,23 ммоль) преобразовали в (S)-циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил] уксусную кислоту (пример 44) (410 мг, 1,00 ммоль, 82%).
1H ЯМР (400 МГц, CDCl3) δ 0,41-0,59 (м, 6Н), 0,66-0,71 (м, 2Н), 1,32-1,38 (м, 1Н), 1,89 (с, 3H), 2,08-2,17 (м, 2Н), 2,31 (с, 3H), 2,68-2,72 (м, 2Н), 3,27-3,33 (м, 1Н), 4,25-4,29 (м, 2Н), 4,95 (с, 1Н), 6,75 (д, J=11,4 Гц, 1Н), 6,79 (д, J=8,0 Гц, 1H), 7,11 (д, J=8,0 Гц, 1Н), 8,53-9,56 (уш. с, 1Н).
19F ЯМР (282 МГц, CDCl3) -142. 0 (с, 1F).
MC m/z ([M+Na]+) 433.
MC m/z ([M-H]-) 409.
Пример 45: Синтез 3-циклопропил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] пропановой кислоты

Стадия 1: Получение промежуточного соединения (2-бром-3-(метоксиметокси)-6-метилфенил) метанола (45а)
К раствору соединения 2-бром-3-метоксиметокс-6-метил-бензальдегида 1с (3,3 г, 12,74 ммоль) в безводном метаноле (127 мл) добавляли тетраборогидрид натрия (482 мг, 12,74 ммоль) при 0°C. Полученную смесь перемешивали при 0°C в течение 1 часа. Реакционную смесь разбавляли этилацетатом и промывали водой и насыщенным солевым раствором. Органический слой сушили над сульфатом натрия, фильтровали и концентрировали в вакууме с получением неочищенного продукта (2-бром-3-(метоксиметокси)-6-метилфенил) метанола (3,40 г, 12,74 ммоль, 100%) в виде бесцветного масла, которое использовали в следующей стадии без дополнительной очистки.
MC m/z ([М+Н-H2O]+) 243/245.
Стадия 2: Получение промежуточного соединения (2-бром-3-(метоксиметокси)-6-метилфенил) метил метансульфоната (45b)
К раствору соединения (2-бром-3-(метоксиметокси)-6-метилфенил) метанола (45а) (3,32 г, 12,74 ммоль) в безводном (64 мл) добавляли при 0°C метансульфонилхлорид (1,18 мл, 15,29 ммоль) и триэтиламин (2,49 мл, 17,84 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 3 часов, затем разбавляли этилацетатом и промывали водой и насыщенным солевым раствором. Органический слой сушили над сульфатом натрия, фильтровали и концентрировали в вакууме с получением неочищенного продукта (2-бром-3-(метоксиметокси)-6-метилфенил) метил метансульфоната (45b) (4,32 г, 12,74 ммоль, 100%) в виде бежевого смолы, которую использовали на следующей стадии без дополнительной очистки.
Стадия 3: Получение промежуточного соединения 2-(2-бром-3-(метоксиметокси)-6-метилфенил) ацетонитрила (45с)
Соединение (2-бром-3-(метоксиметокси)-6-метилфенил) метил метансульфонат (45b) (4,32 г, 12,74 ммоль) растворяли в безводном N,N-диметилформамиде (36 мл) и добавляли к нему цианид натрия (750 мг, 15,29 ммоль). Реакционную смесь перемешивали в течение ночи при комнатной температуре и концентрировали досуха, чтобы удалить N,N-диметилформамид. Остаток затем разбавляли этилацетатом, промывали водой и насыщенным раствором соли и сушили органический слой над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/дихлорметан 40/60) с получением 2-(2-бром-3-(метоксиметокси)-6-метилфенил) ацетонитрила (45С) (3,16 г, 11,70 ммоль, 92% более 3 стадии) в виде твердого вещества бежевого цвета.
1H ЯМР (300 МГц, CDCl3) δ 2,41 (с, 3H), 3,51 (с, 3H), 3,92 (с, 2Н), 5,23 (с, 1Н), 7,06 (д, J=8,5 Гц, 1Н), 7,12 (д, J=8,5 Гц, 1Н).
Стадия 4: Получение промежуточного соединения метил-2-(2-бром-3-гидрокси-6-метилфенил) ацетата (45d)
Растворяли 2-(2-бром-3-(метоксиметокси)-6-метилфенил) ацетонитрил (45с) (1,38 г, 5,11 ммоль) при 0°C в смеси 9/1 метанол/серная кислота (27 мл). Смесь кипятили с обратным холодильником при 90°C в течение 3 дней, затем охлаждали при комнатной температуре и медленно выливали в воду (80 мл). Водный слой дважды экстрагировали диэтиловым эфиром (2×100 мл), затем дважды этилацетатом (2×100 мл). Объединенные органические слои промывали насыщенным раствором гидрокарбоната натрия (80 мл), рассолом (80 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением метил 2-(2-бром-3-гидрокси-6-метилфенил) ацетат (45d) (1,32 г, 5,11 ммоль, 100%) в виде бежевого твердого вещества, которое использовали на следующей стадии без дополнительной очистки.
МС m/z ([М+Н]+) 259/261.
Стадия 5: Получение промежуточного соединения метил-2-(3-(бензилокси)-2-бром-6-метилфенил) ацетата (45Е)
С помощью процедуры, описанной в примере 42, стадия 4, метил 2-(2-бром-3-гидрокси-6-метилфенил) ацетат (45d) (1,32 г, 5,11 ммоль) преобразовали в метил-2-(3-(бензилокси)-2-бром-6-метилфенил) ацетат (45е) (1,61 г, 4,61 ммоль, 90% за 2 стадии) в виде желтого масла после очистки флэш-хроматографией на силикагеле (циклогексан/этилацетат 90/10).
1H ЯМР (400 МГц, CDCl3) δ 2,29 (с, 3H), 3,71 (с, 3H), 3,95 (с, 2Н), 5,13 (с, 2Н), 6,79 (д, J=8,4 Гц, 1H), 7,06 (д, J=8,4 Гц, 1Н), 7,30-7,34 (м, 1Н), 7,36-7,41 (м, 2Н), 7,46-7,50 (м, 2Н).
МС m/z ([М+Н]+) 349/351.
МС m/z ([М-Н]-) 347/349.
Стадия 6: Получение промежуточного соединения метил-2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] ацетата (45f)
С помощью процедуры, описанной в примере 1, стадии 7, метил 2-(3-(бензилокси)-2-бром-6-метилфенил) ацетат (45е) (1,6 г, 4,58 ммоль) преобразовали в метил-2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] ацетат (45F) (1,78 г, 4,42 ммоль, 96%) в виде желтой смолы после очистки флэш-хроматографией на силикагеле (циклогексан/этилацетат 90/10).
1H ЯМР (400 МГц, CDCl3) δ 2,01-2,07 (м, 2Н), 2,23 (с, 3H), 2,76-2,80 (м, 2Н), 3,50 (д, J=1,94 Гц, 2Н), 3,64 (с, 3H), 4,22-4,24 (м, 2Н), 4,97 (с, 2Н). 6,81-6,85 (м, 2Н), 6,88-6,90 (м, 1Н), 6,93-6,96 (м, 1Н), 7,08-7,10 (м, 1Н), 7,16-7,18 (м, 2Н), 7,20-7,30 (м, 3H).
МС m/z ([М-Н]-) 401.
Стадия 7: Получение промежуточного соединения метил-2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] пент-4-еноата (45g)
К раствору метил-2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] ацетат (45f) (134 мг, 0,33 ммоль) в безводном (3,3 мл) в атмосфере азота при 0°C добавляли по каплям раствор 1М бис(триметилсилил)амида в е (832 л, 0,83 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 45 минут, затем добавляли аллилбромид (288 мкл, 3,33 ммоль) и реакционную смесь оставляли перемешиваться при комнатной температуре в течение 2 часов. Добавляли водный раствор хлорида аммония и смесь экстрагировали этилацетатом. Органический слой сушили над сульфатом натрия, концентрировали в вакууме и остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 90/10) с получением метил 2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] пент-4-еноата (45g) (117 мг, 0,26 ммоль, 74%) в виде бесцветного масла.
1H ЯМР (400 МГц, CDCl3) δ 2,01-2,08 (м, 2Н), 2,21 (с, 3H), 2,27-2,38 (м, 1H), 2,73-2,90 (м, 3H), 3,63 и 3,64 (с, 3H), 3,88-3,93 (м, 1H), 4,22-4,26 (м, 2Н), 4,81-5,00 (м, 4Н), 5,49-5,61 (м, 1H), 6,80-7,00 (м, 4Н), 7,04-7,06 (м, 1Н), 7,12-7,15 (м, 2Н), 7,20-7,29 (м, 3H).
МС m/z ([М+Н]+) 443, ([M+Na]+) 465.
МС m/z ([М-Н]-) 441.
Стадия 8: Получение промежуточного соединения метил-2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-3-циклопропилпропаноата (45h)
С помощью процедуры, описанной в примере 23, стадии 3, промежуточное соединение метил-2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]пент-4-еноат (45g) (157 мг, 0,35 ммоль) преобразовали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 86/14) для получения метил 2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-3-циклопропилпропаноата (45h) (89, 7 мг, 0,196 ммоль, 55%) в виде бесцветного масла.
1Н ЯМР (400 МГц, CDCl3) δ-0,30-0,25 (м, 1Н), -0,16-(-)0,10 (м, 1Н), 0,14-0,28 (м, 2Н), 0,50-0,61 (м, 1Н), 1,35-1,43 (м, 1Н), 1,99-2,09 (м, 3H), 2,20 и 2,21 (с, 3H), 2,75-2,84 (м, 2Н), 3,64 и 3,66 (с, 3H), 3,97-4,03 (м, 1Н), 4,23-4,25 (м, 2Н), 4,91-5,00 (м, 2Н), 6,80-7,05 (м, 5Н), 7,12-7,15 (м, 2Н), 7,20-7,28 (м, 3H).
МС m/z ([М+Н]+) 457, ([M+Na]+) 479.
МС m/z ([М-Н]-) 455.
Стадия 9: Получение промежуточного соединения метил 3-циклопропил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил] пропаноат (45i)
Дегазированную суспензию метил 2-[3-(бензилокси)-2-(3,4-дигидро-2 Н-1-бензопиран-6-ил)-6-метилфенил]-3-циклопропилпропаноат (45h) (82 мг, 0,18 ммоль) с формиатом аммония (283 мг, 4,49 ммоль) и палладий на углероде (8 мг) в метаноле (2 мл) нагревали с обратным холодильником 4 часа. Добавляли дополнительно формиат аммония (283 мг, 4,49 ммоль) и палладий на углероде (8 мг) и кипятили реакционную смесь с обратным холодильником в течение ночи до полного преобразования исходного материала, после чего фильтровали через слой целита® и концентрировали фильтрат в вакууме. Остаток разбавляли этилацетатом, промывали водой, рассолом, сушили над сульфатом натрия, фильтровали, концентрировали в вакууме и очищали с помощью препаративной ТСХ (циклогексан/этилацетат 70/30) с получением метил 3-циклопропил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил] пропаноата (45i) (49,3 мг, 0,13 ммоль, 76%).
1H ЯМР (400 МГц, CDCl3) δ-0,28-0,22 (м, 1Н),-0,15-0,10 (м, 1H), 0,17-0,29 (м, 2Н), 0,50-0,59 (м, 1Н), 1,39-1,47 (м, 1Н), 1,94-2,10 (м, 3H), 2,19 и 2,20 (с, 3H), 2,74-2,85 (м, 2Н), 3,63 и 3,64 (с, 3H), 3,79-3,85 (м, 1Н), 4,23-4,27 (м, 2Н), 4,60 и 4,62 (с, 1H), 6,79-6,82 (м, 1Н), 6,86-6,93 (м, 2Н), 7,01-7,07 (м, 2Н).
МС m/z ([М+Н]+) 367.
МС m/z ([М-Н]-) 365.
Стадия 10: Получение промежуточного соединения метил 3-циклопропил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил-3-(трифторметансульфонилокси)фенил]пропаноата (45j)
С помощью процедуры, описанной в примере 1, стадии 10, промежуточное соединение метил 3-циклопропил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил] пропаноат (45i) (49 мг, 0,13 ммоль) преобразовали в метил 3-циклопропил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил-3-(трифторметансульфонилокси)фенил] пропаноат (45j) (67 мг, 0,13 ммоль, 100%) в виде прозрачного желтого масла, которое использовали на следующей стадии без дополнительной очистки.
1H ЯМР (300 МГц, CDCl3) δ-0,28-0,22 (м, 1Н),-0,15-0,08 (м, 1Н), 0,15-0,31 (м, 2Н), 0,43-0,57 (м, 1Н), 1,35-1,45 (м, 1H), 1,98-2,10 (м, 3H), 2,27 (с, 3H), 2,73-2,85 (м, 2Н), 3,64 и 3,65 (с, 3H), 3,96-4,01 (м, 1H), 4,21-4,25 (м, 2Н), 6,78-7,00 (м, 3H), 7,12-7,19 (м, 2Н).
МС m/z ([М+Н]+) 499.
МС m/z ([М-Н]-) 497.
Стадия 11: Получение промежуточного соединения метил 3-циклопропил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] пропаноата (45k)
Дегазированный раствор метил 3-циклопропил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил-3-(трифторметансульфонилокси)фенил]пропаноата (45j) (67 мг, 0,135 ммоль), циклопропилтрифторбороната калия (26 мг, 0,176 ммоль), 2-дициклогексилфосфино-2',6'-диизопропоксибифенил (Ruphos) (3,1 мг, 0,007 ммоль), моногидрат трехосновного фосфата калия (193 мг, 0,837 ммоль) и палладий(II) ацетат (0,8 мг, 0,003 ммоль) в смеси 1/1 трет-бутанола/воды (0,27 мл) нагревали при 105°C в течение 4 часов. Добавляли дополнительно 2-дициклогексилфосфино-2',6'-диизопропоксибифенил (Ruphos) (3,1 мг, 0,007 ммоль) и палладий(II) ацетат (0,8 мг, 0,003 ммоль) и реакционную смесь кипятили с обратным холодильником еще 2 часа до гашения. Добавляли воду (3 мл). Водный слой экстрагировали циклогексаном (2×6 мл). Объединенные органические слои промывали рассолом (3 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 90/10) с получением метил 3-циклопропил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил фенил] пропионата (45k) (40 мг, 0,102 ммоль, 75%) в виде бесцветной смолы.
1Н ЯМР (300 МГц, CDCl3) δ-0,15-0,07 (м, 1Н), 0,13-0,32 (м, 2Н), 0,52-0,72 (м, 5Н), 1,24-1,39 (м, 2Н), 1,41-1,50 (м, 1Н), 2,00-2,14 (м, 3H), 2,22 (с, 3H), 2,76-2,83 (м, 2Н), 3,62 и 3,64 (с, 3H), 3,86-3,95 (м, 1Н), 4,22-4,25 (м, 2Н), 6,69-6,72 (м, 1Н), 6,78-6,90 (м, 2Н), 6,94-7,04 (м, 2Н).
MC m/z ([M+H]+) 391.
Стадия 12: Получение 3-циклопропил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] пропионовой кислоты (пример 45)
С помощью процедуры, описанной в примере 1, стадии 12, метил-3-циклопропил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] пропаноат (40 мг, 0,10 ммоль) преобразовали реакцией с гидроксидом лития (20 мг, 0,82 ммоль) в 3-циклопропил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] пропионовую кислоту (27,1 мг, 0,072 ммоль, 69%) (пример 45) в виде белого аморфного твердого вещества после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 75/25).
1H ЯМР (400 МГц, CDCl3) δ-0,30-0,21 (м, 1Н),-0,15-0,09 (м, 1Н), 0,15-0,30 (м, 2Н), 0,52-0,70 (м, 5Н), 1,29-1,49 (м, 2Н), 1,98-2,11 (м, 3H), 2,27 и 2,28 (с, 3H), 2,72-2,83 (м, 2Н), 3,91-4,01 (м, 1Н), 4,20-4,26 (м, 2Н), 6,70-6,72 (м, 1H), 6,78-6,90 (м, 2Н), 6,95-7,04 (м, 2Н).
МС m/z ([М+Н]+) 377, ([M+Na]+) 399.
МС m/z ([М-Н]-) 375.
Пример 46: Синтез 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-4-метилпентановой кислоты

Стадия 1: Получение промежуточного соединения метил-2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-4-метилпент-4-еноата (46а)
С помощью процедуры, описанной в примере 45, стадии 7, метил 2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] ацетат (45F) (146 мг, 0,362 ммоль) преобразовали реакцией с 3-бром-2-метил-1-пропена (365 л, 3,62 ммоль) в метил-2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-4-метилпент-4-еноата (46а) (114 мг, 0,25 ммоль, 69%) в виде бесцветного масла после очистки препаративной ТСХ (циклогексан/этилацетат 90/10).
1H ЯМР (400 МГц, CDCl3) δ 1,37 и 1,38 (с, 3H), 2,01-2,08 (м, 2Н), 2,19-2,24 (м, 4Н), 2,68-2,81 (м, 2Н), 2,84-2,91 (м, 1Н), 3,64 и 3,66 (с, 3H), 4,01-4,08 (м, 1Н), 4,19-4,25 (м, 2Н), 4,39 (м, 1H), 4,59 (м, 1H), 4,91-5,00 (м, 2Н), 6,79-7,06 (м, 5Н), 7,13-7,15 (м, 2Н), 7,20-7,29 (м, 3H).
МС m/z ([М+Н]+) 457.
МС m/z ([М-Н]-) 455.
Стадия 2: Получение промежуточного соединения метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3 -гидрокси-6-метилфенил]-4-метилпентаноата (46b)
Суспензию метил-2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-4-метилпент-4-еноата (46а) (114 мг, 0,25 ммоль) и 10% палладий на угле (12 мг) в этилацетате (4,3 мл) перемешивали при комнатной температуре в атмосфере водорода (5 бар) в течение 24 часов. Смесь фильтровали через Millipore и концентрировали в вакууме для получения метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил]-4-метилпентаноата (46b) (97 мг, 0,25 ммоль, 100%) в виде бесцветного масла, используемого на следующей стадии без дополнительной очистки.
1H ЯМР (400 МГц, CDCl3) δ 0,53-060 (м, 3H), 0,69 (д, J=6,6 Гц, 3H), 1,31-1,39 (м, 1H), 1,40-1,51 (м, 1Н), 1,95-2,11 (м, 2Н), 2,23 и 2,24 (с, 3H), 2,74-2,89 (м, 2Н), 3,66 и 3,68 (с, 3H), 3,74-3,81 (м, 1Н), 4,24-4,30 (м, 2Н), 4,67 и 4,69 (с, 1H), 6,83-6,85 (м, 1Н), 6,90-6,98 (м, 2Н), 7,04-7,11 (м, 2Н).
МС m/z ([М-Н]-) 367.
Стадия 3: Получение промежуточного соединения метил 2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил-3-(трифторметансульфонилокси)фенил]-4-метилпентаноата (46с)
С помощью процедуры, описанной в примере 1, стадии 10, метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил]-4-метилпентаноат (46b) (97 мг, 0,25 ммоль) преобразовали в метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил-3-(трифторметил метансульфонилокси) фенил]-4-метилпентаноат (46с) (120 мг, 0,24 ммоль, 96%) в виде бесцветного масла после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 90/10).
1H ЯМР (400 МГц, CDCl3) δ 0,55-059 (м, 3H), 0,64-0,66 (м, 3H), 1,22-1,43 (м, 3H), 1,98-2,12 (м, 2Н), 2,28 и 2,29 (с, 3H), 2,67-2,86 (м, 2Н), 3,65 и 3,66 (с, 3H), 3,88-3,93 (м, 1H), 4,20-4,25 (м, 2Н), 6,80-6,89 (м, 2Н), 6,94-7,00 (м, 1H), 7,12-7,18 (м, 2Н).
MC m/z ([M-H]-) 499.
Стадия 4: Получение промежуточного соединения метил 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-4-метилпентаноата (46d)
Дегазированный раствор метил 2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил-3-(трифторметансульфонилокси)фенил]-4-метилпентаноата (46с) (120 мг, 0,24 ммоль), циклопропилтрифторборонат калия (46 мг, 0,31 ммоль), 2-дициклогексилфосфино-2',6'-диизопропоксибифенил (Ruphos) (0,6 мг, 0,012 ммоль), моногидрат трехосновного фосфата калия (342 мг, 1,49 ммоль) и палладий(II) ацетат (0,13 мг, 0,006 ммоль) в смеси 1/1 трет-бутанола/воды (0,6 мл) нагревали при 105°C в течение 4 часов. Добавляли воду (3 мл). Водный слой экстрагировали циклогексаном (2×6 мл). Объединенные органические слои промывали рассолом (3 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (дихлорметан 100%) с получением метил 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-4-метил пентаноата (46d) (75 мг, 0,19 ммоль, 80%) в виде бесцветной смолы.
1Н ЯМР (400 МГц, CDCl3) δ 0,53-0,71 (м, 10H), 1,18-1,30 (м, 1Н), 1,41-1,53 (м, 2Н), 1,94-2,15 (м, 3H), 2,22 и 2,23 (с, 3H), 2,69-2,85 (м, 2Н), 3,61 и 3,63 (с, 3H), 3,79-3,92 (м, 1Н), 4,19-4,24 (м, 2Н), 6,69-6,72 (м, 1Н), 6,78-6,91 (м, 2Н), 6,96-7,03 (м, 2Н).
MC m/z ([M+Na]+) 415.
Стадия 5: получение 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-4-метилпентановой кислоты (пример 46)
С помощью процедуры, описанной в примере 1, стадии 12, метил 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-4-метилпентаноат (46d) (75 мг, 0,19 ммоль) преобразовали в 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-4-метилпентановую кислоту (пример 46) (72 мг, 0,19 ммоль, 100%) в виде белого аморфного твердого вещества без дополнительной очистки.
1H ЯМР (400 МГц, CDCl3) δ 0,54-0,73 (м, 10H), 1,20-1,33 (м, 1H), 1,41-1,52 (м, 2Н), 1,95-2,13 (м, 3H), 2,29 (с, 3H), 2,67-2,83 (м, 2Н), 3,86-3,95 (м, 1Н), 4,19-4,24 (м, 2Н), 6,71-6,73 (м, 1Н), 6,77-6,92 (м, 2Н), 6,98-7,05 (м, 2Н).
MC m/z ([М+Н]+) 379.
MC m/z ([M-H]-) 377.
Пример 47: Синтез (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-циклопропокси) уксусной кислоты

Стадия 1: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-этокси) уксусной кислоты (47а)
В сухой реактор с магнитной мешалкой, загружали метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-винилокси-уксусной кислоты (23b) (100 мг, 0,264 ммоль) и фторид натрия (1 мг, 0,024 ммоль). Смесь нагревали при 105°C в атмосфере азота и медленно добавляли в течение 2 часов триметилсилил фторсульфонилдифторацетат (80 мкл, 0,396 ммоль). После завершения добавления реакционную смесь перемешивали 2 часа, охлаждали до комнатной температуры и разбавляли этилацетатом (3 мл). Раствор промывали водой и сушили над сульфатом натрия. Растворитель выпаривали и неочищенный продукт очищали с помощью препаративной ТСХ на силикагеле (циклогексан/этилацетат 80/20) с получением неразделенной смеси (30 мг) метилового сложного эфира 2-хроман-6-ил-3-циклопропил-6-метил- фенил)-(2,2-дифтор-циклопропокси) уксусной кислоты (47а), искомого продукта, загрязненного метиловым сложным эфиром (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-дифторметокси-уксусной кислоты (47b) с соотношением 60/40. Эта смесь будет использоваться на следующей стадии без дополнительной очистки.
(47а) MC m/z ([M+Na]+) 451.
(47b) MC m/z ([M+Na]-) 425.
Стадия 2: получение (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-этокси) уксусной кислоты (пример 47)
С помощью процедуры, описанной в примере 1, стадии 12, неразделенную смесь (30 мг) метилового сложного эфира 2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-циклопропокси) уксусной кислоты (47а), загрязненного метиловым сложным эфиром (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-дифторметокси-уксусной кислоты метилового сложного эфира (47b) с отношением 60/40 преобразовали после очистки с помощью препаративной ТСХ (дихлорметан/метанол 95/5) в в неразделенную смесь 2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-циклопропокси) уксусной кислоты (пример 47), загрязненной (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-дифторметокси-уксусной кислотой (47с) с соотношением 69/31 (13 мг) в виде белого твердого вещества.
(пример 47) МС m/z ([M+Na]+) 451.
(47с) МС m/z ([M+Na]+) 425.
Пример 48: Синтез 2-[2-хроман-6-ил-3-циклопропил-5-(метансульфонамидо)-6-метил-фенил]-2-(циклопропокси)уксусной кислоты

Стадия 1: Получение промежуточного соединения 3-бром-2-гидрокси-6-метилбензальдегида (48а)
Триэтиламин (27,6 мл, 198 ммоль) и хлорид магния (7,64 г, 80 ммоль) добавляли к раствору 2-бром-5-метилфенола (10,0 г, 53 ммоль) в ацетонитриле (200 мл). Через 15 минут перемешивания при комнатной температуре добавляли параформальдегид (10,76 г, 358 ммоль) и нагревали реакционную смесь при 80°C в течение 8 часов и концентрировали в вакууме. Остаток растворяли в 10% соляной кислоте (200 мл) и перемешивали при комнатной температуре в течение 30 минут. Добавляли этилацетат (200 мл) и разделяли слои. Органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью cake of silice (циклогексан/этилацетат 80/20) с получением 3-бром-2-гидрокси-6-метилбензальдегида (48а) (7,33 г, 34 ммоль, 64%).
1H ЯМР (400 МГц, CDCl3) δ 2,59 (с, 3H), 6,65 (д, J=8,0 Гц, 1Н), 7,63 (д, J=8,0 Гц, 1Н), 10,27 (с, 1H), 12,53 (с, 1Н).
МС m/z ([М+Н]+) 215/217.
Стадия 2: Получение промежуточного соединения 3-бром-2-гидрокси-6-метил-5-нитробензальдегида (48b)
Раствор азотной кислоты (1,60 мл, 37,49 ммоль) в уксусной кислоте (15 мл) медленно добавляли к раствору 3-бром-2-гидрокси-6-метилбензальдегида (48а) (7,33 г, 34,08 ммоль) в уксусной кислоте (73 мл). Реакционную смесь перемешивали в течение 20 минут при комнатной температуре. Добавляли воду (50 мл), осадок отфильтровывали и промывали водой. Затем твердое вещество сушили при пониженном давлении в присутствии пентаоксида фосфора с получением 3-бром-2-гидрокси-6-метил-5-нитробензальдегида (48b) (5,65 г, 21,73 ммоль, 64%), который использовали без дальнейшей очистки.
1H ЯМР (300 МГц, CDCl3) δ 2,80 (с, 3H), 8,37 (с, 1Н), 10,42 (с, 1H), 13,31 (с, 1Н).
МС m/z ([М-Н]-) 258/260.
Стадия 3: Получение промежуточного соединения 3-циклопропил-2-гидрокси-6-метил-5-нитро-бензальдегида (48с)
Раствор 3-бром-2-гидрокси-6-метил-5-нитробензальдегида (48b) (2,00 г, 7,7 ммоль), циклопропилтрифторборат калия (2,96 г, 20 ммоль), трехосновного фосфата калия моногидрата (5,85 г, 25,4 ммоль) и 2-дициклогексилфосфино-2',6'-диизопропокси бифенила (359,3 мг, 0,77 ммоль) в смеси толуола (24 мл) и воды (8 мл), барботировали азотом в течение 5 минут. Добавляли палладий(II) ацетат (86,4 мг, 0,384 ммоль) и нагревали реакционную смесь при 100°C в течение ночи. Добавляли воду (10 мл). Водный слой экстрагировали этилацетатом (3×50 мл). Объединенные органические слои промывали солевым раствором (20 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат 100/0 до 95/5) с получением 3-циклопропил-2-гидрокси-6-метил-5-нитробензальдегида (48с) (1,316 г, 5,95 ммоль, 77%) в виде бледно-желтого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 0,69-0,75 (м, 2Н), 1,02-1,08 (м, 2Н), 2,14-2,23 (м, 1Н), 2,77 (с, 3H), 7,63 (с, 1Н), 10,44 (с, 1Н), 13,07 (с, 1Н).
МС m/z ([М+Н]+) 222.
МС m/z ([М-Н]-) 220.
Стадия 4: Получение промежуточного соединения 6-циклопропил-3-метил-4-нитро-2-винил-фенола (48d)
К суспензии иодида метилтрифенилфосфония (4,05 г, 10 ммоль) в безводном тетрагидрофуране (10 мл) при 0°C в атмосфере азота по каплям добавляли 1М раствор трет-бутоксида в тетрагидрофуране (21 мл, 21 ммоль). Полученную смесь перемешивали при 0°C в течение 30 минут перед добавлением раствора 3-циклопропил-2-гидрокси-6-метил-5-нитро-бензальдегида (48с) (2,1 г, 9,49 ммоль) в безводном тетрагидрофуране (20 мл). Полученную смесь перемешивали при 0°C в течение 45 минут, перед добавлением воды (30 мл) и 1М раствора соляной кислоты до рН 3. Смесь экстрагировали этилацетатом (2×20 мл). Органические слои сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на диоксиде кремния (циклогексан/этилацетат 90/10), а затем растирали в циклогексане с получением 6-циклопропил-3-метил-4-нитро-2-винил-фенола (48d) (1,29 г, 5,88 ммоль, 62%) в виде оранжевого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 0,56-0,82 (м, 2Н), 0,90-1,09 (м, 2Н), 1,97-2,04 (м, 1Н), 2,44 (с, 3H), 5,61 (дд, J=18,1 Гц, J=1,6 Гц, 1Н), 5,85 (дд, J=11,5 Гц, 1,6 Гц, 1H), 6,24 (с, 1Н), 6,67 (дд,7=18,2 Гц, J=11,5 Гц, 1H), 7,53 (с, 1Н).
МС m/z ([М+Н]+) 220.
МС m/z ([М-Н]-) 218.
Стадия 5: Получение промежуточного соединения (6-циклопропил-3-метил-4-нитро-2-винил-фенил) трифторметансульфоната (48е)
К раствору 6-циклопропил-3-метил-4-нитро-2-винил-фенола (48d) (1,29 г, 5,88 ммоль) в безводном дихлорметане (15 мл) при 0°C в атмосфере азота последовательно добавляли триэтиламин (1,23 мл, 8,82 ммоль) и трифликовый ангидрид (1,1 мл, 6,48 ммоль). Смесь перемешивали при комнатной температуре в течение 30 минут. Добавляли воду (15 мл). Водный слой экстрагировали дихлорметаном (15 мл). Органические слои промывали насыщенным раствором гидрокарбоната натрия (15 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением (6-циклопропил-3-метил-4-нитро-2-винил-фенил) трифторметансульфоната (48е) (2,1 г, 5,88 ммоль, 100%) в виде коричневого масла, которое использовали без дальнейшей очистки.
1Н ЯМР (400 МГц, CDCl3) δ 0,78-0,82 (м, 2Н), 1,13-1,19 (м, 2Н), 2,10-2,17 (м, 1Н), 2,40 (с, 3H), 5,50 (дд, J=18,0 Гц, J=1,2 Гц, 1Н), 5,81 (дд, J=11,6 Гц, J=1,2 Гц, 1H), 6,62 (дд, J=18,0 Гц, J=11,6 Гц, 1Н),7,34(с, 1Н),
Стадия 6: Получение промежуточного соединения 6-(6-циклопропил-3-метил-4-нитро-2-винил-фенил)хромана (48f)
В герметичном кругл о донную колбу, раствор (6-циклопропил-3-метил-4-нитро-2-винил-фенил) трифторметансульфонат (48е) (1,86 г, 5,29 ммоль), 6-(4,4,5, 5-тетраметил-1,3,2-диоксаборолан-2-ил) хромана (1,51 г, 5,82 ммоль) в толуоле (6 мл) и воде (2 мл) дегазировали путем барботирования аргона в течение 10 минут. Добавляли фосфат калия (2,44 г, 10,59 ммоль) и тетракис (трифенилфосфин) палладий(0) (306 мг, 0,26 ммоль) и смесь нагревали при 120°C в течение ночи. Смесь разбавляли толуолом (20 мл) и промывали водой (10 мл) и насыщенным раствором соли (10 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/дихлорметан 50/50) с получением 6-(6-циклопропил-3-метил-4-нитро-2-винил-фенил) хромана (48f) (1,63 г, 4,86 ммоль, 91%) в виде желтого масла.
1H ЯМР (400 МГц, CDCl3) δ 0,60-0,68 (м, 2Н), 0,76-0,82 (м, 2Н), 1,55-1,62 (м, 1Н), 2,01-2,08 (м, 2Н), 2,44 (с, 3H), 2,79 (т, J=6,5 Гц, 2Н), 4,23 (дд, J=5,9 Гц, J=4,5 Гц, 2Н), 5,07 (дд, J=17,9 Гц, J=1,7 Гц, 1Н), 5,37 (дд, J=11,5 Гц, J=1,7 Гц, 1Н), 6,31 (дд, J=17,9 Гц, J=11,5 Гц, 1H), 6,76-6,87 (м, 3H), 7,21 (с, 1H).
МС m/z ([М+Н]+) 336.
Стадия 7: Получение промежуточного соединения 1-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил) этан-1,2-диола (48g)
К раствору 6-(6-циклопропил-3-метил-4-нитро-2-винил-фенил) хромана (48f) (1,77 г, 5,27 ммоль) в ацетоне (22,5 мл) и воды (2,5 мл) добавляли раствор осмия 4 масс. % в воде (0,80 мл, 0,13 ммоль) и 4-метилморфолин N-оксидв (1,30 г, 11,08 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 3 дней. Добавляли (20 мл) 15% раствора тиосульфата натрия в воде и перемешивали смесь при комнатной температуре в течение 30 минут. Твердое вещество отфильтровывали и промывали водой. Твердое вещество сушили совместным выпариванием толуола в вакууме. Остаток растирали в трет-бутиловом эфире (5 мл) и фильтровали с получением 1-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил) этан-1,2-диола (48g) (1,45 г, 3,92 ммоль, 74%) в виде белого твердого вещества.
1Н ЯМР (300 МГц, DMSO-d6) δ 0,51-0,78 (м, 4Н), 1,29-1,38 (м, 1Н), 1,90-2,02 (м, 2Н), 2,48 (с, 3H), 2,73-2,82 (м, 2Н), 3,34-3,44 (м, 1Н), 3,55-3,64 (м, 1Н), 4,15-4,22 (м, 2Н), 4,60-4,69 (м, 2Н), 5,29 (д, J=4,0 Гц, 1Н), 6,75-6,93 (м, 3H), 7,16 (с, 1Н).
MC m/z ([М+НСОО]-) 414.
Стадия 8: Получение промежуточного соединения [2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-гидрокси-этил]-2,2-диметилпропаноата (48h)
К суспензии 1-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил) этан-1,2-диола (48 г) (1,45 г, 3,92 ммоль) в дихлорметане (20 мл) и пиридине (6,6 мл) добавляли по каплям пивалоилхлорид (0,73 мл, 5,90 ммоль) при комнатной температуре. Смесь перемешивали при этой температуре в течение 2 часов и разбавляли дихлорметаном (20 мл). Смесь промывали раствором 1М соляной кислотой (2×25 мл) и насыщенным раствором гидрокарбоната натрия (20 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме с получением [2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-гидрокси-этил]-2,2-диметилпропаноата (48h) (1,92 г, 3,92 ммоль, 100%) в виде желтого масла, содержащего следы дихлорметана. Продукт использовали без дальнейшей очистки.
1Н ЯМР (400 МГц, CDCl3) δ 0,55-0,65 (м, 2Н), 0,71-0,79 (м, 2Н), 1,13 и 1,14 (с, 9Н), 1,41-1,50 (м, 1H), 2,00-2,10 (м, 2Н), 2,31 и 2,39 (д, J=4,2 Гц, 1H), 2,61 (с, 3H), 2,76-2,88 (м, 2Н), 4,08-4,26 (м, 3H), 4,38 и 4,47 (дд, J=11,8 Гц, J=8,8 Гц, 1Н), 4,97 и 5,02 (дт, J=8,8 Гц, J=3,7 Гц, 1Н), 6,79-6,93 (м, 3H), 7,15 (с, 1H).
MC m/z ([М+НСОО]-) 498.
Стадия 9: Получение промежуточного соединения [2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-винилоксипропан-этил]-2,2-диметилпропаноата (48i)
К раствору [2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-гидрокси-этил]-2,2-диметилпропаноата (48h) (1,78 г, 3,92 ммоль) в дихлорметане (8 мл) и этиловом эфире (7,5 мл, 78 ммоль) добавляли трифторуксусную кислоту (0,09 мл, 1,18 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 24 часов перед добавлением насыщенного раствора гидрокарбоната натрия (10 мл). Смесь экстрагировали этилацетатом (2×20 мл). Органический слой промывали насыщенным раствором соли (20 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток растворяли в безводном дихлорметане (10 мл), охлажденном при 0°C и последовательно добавляли триэтиламин (1,64 мл, 11,8 ммоль) и триметилсилил трифторметансульфонат (1,85 мл, 10,2 ммоль). Смесь перемешивали при комнатной температуре в течение 2 часов. Добавляли раствор 2М гидроксида натрия (10 мл). Полученную смесь перемешивали в течение 10 минут и разделяли слои. Водный слой экстрагировали дихлорметаном (10 мл). Органические слои сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/дихлорметан 40/60) с получением [2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-винилоксипропан этил]-2,2-диметилпропаноата (48i) (1,30 г, 2,71 ммоль, 69%) в виде желтого масла.
1Н ЯМР (400 МГц, CDCl3) δ 0,58-0,66 (м, 2Н), 0,73-0,81 (м, 2Н), 1,12 (с, 9Н), 1,41-1,51 (м, 1H), 2,00-2,12 (м, 2Н), 2,56 (с, 3H), 2,74-2,91 (м, 2Н), 3,91-3,97 (м, 1H), 4,13-4,32 (м, 4Н), 4,47 и 4,55 (дд, J=12,1 Гц, J=8,9 Гц, 1Н), 4,97 и 5,06 (дд, J=8,8 Гц, J=3,1 Гц, 1H), 6,03-6,14 (м, 1Н), 6,80-6,89 (м, 3H), 7,15 (с, 1H).
Стадия 10: Получение промежуточного соединения [2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-(циклопропокси) этил]-2,2-диметилпропаноата (48j)
Смесь дихлорметана (2,6 мл) и 15 масс. % раствор диэтилцинка в толуоле (4. 9 мл, 5,42 ммоль) охлаждали при 0°C. Раствор трифторуксусной кислоты (0,42 мл, 5,42 ммоль) в дихлорметане (2,6 мл) добавляли по каплям. Полученную смесь перемешивали при 0°C в течение 20 минут. Раствор дийодметана (0,44 мл, 5,42 ммоль) в дихлорметане (2,6 мл) добавляли по каплям. Полученную смесь перемешивали при 0°C в течение 20 мин, затем добавляли по каплям раствор [2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-винилоксипропан-этил] 2,2-диметилпропаноата (48i) (1,30 г, 2,71 ммоль) в дихлорметане (2,6 мл). Полученную смесь перемешивали при комнатной температуре в течение 45 минут и добавляли 0,1М раствор хлористоводородной кислоты (50 мл). Полученную смесь перемешивали в течение 15 минут. Слои разделяли. Водный слой экстрагировали дихлорметаном (2×20 мл). Органические слои сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат, 95/5) с получением [2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-(цикло пропокси) этил]-2,2-диметилпропаноата (48j) (1,03 г, 2,08 ммоль, 76%) в виде желтого масла.
1Н ЯМР (300 МГц, CDCl3) δ 0,21-0,65 (м, 6Н), 0,72-0,82 (м, 2Н), 1,09 и 1,10 (с, 9Н), 1,44-1,55 (м, 1Н), 1,99-2,11 (м, 2Н), 2,58 (с, 3H), 2,74-2,87 (м, 2Н), 3,06-3,17 (м, 1Н), 4,02-4,45 (м, 4Н), 4,63-4,79 (м, 1H), 6,76-6,92 (м, 3H), 7,14 (с, 1Н).
MC m/z ([M+Na]+) 516.
Стадия 11: Получение промежуточного соединения 2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-(циклопропокси) этанола (48k)
К раствору [2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-(циклопропокси) этил] 2,2-диметилпропаноата (48j) (1,03 г, 2,08 ммоль) в тетрагидрофуране (9,5 мл) и метаноле (1,5 мл), добавляли 2М раствор гидроксида натрия (4,2 мл, 8,4 ммоль). Смесь перемешивали при 70°C в течение 7 часов. Добавляли воду (10 мл). Органические растворители выпаривали в вакууме. Раствор экстрагировали этилацетатом (2×10 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток осаждают в циклогексане, растирают и фильтровали с получением 2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-(циклопропокси) этанола (48k) (420 мг, 1,02 ммоль, 49%). Фильтрат концентрировали в вакууме. Остаток растирали в метаноле и фильтровали с получением дополнительно 2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-(циклопропокси) этанола (48k) (190 мг, 0,46 ммоль, 22%).
1Н ЯМР (400 МГц, CDCl3) δ 0,23-0,67 (м, 6Н), 0,71-0,81 (м, 2Н), 1,40-1,52 (м, 1Н), 1,84-2,12 (м, 3H), 2,56 (с, 3H), 2,72-2,90 (м, 2Н), 3,11-3,21 (м, 1H), 3,37-3,51 (м, 1Н), 3,80-3,92 (м, 1Н), 4,20-4,30 (м, 2Н), 4,69 и 4,72 (д, J=4,1 Гц, 1H), 6,72-6,92 (м, 3H), 7,12 (с, 1Н).
МС m/z ([М+НСОО]-) 454.
Стадия 12: Получение промежуточного соединения метил-2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-(циклопропокси) ацетата (48I)
К суспензии 2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-(циклопропокси) этанола (48k) (605 мг, 1,48 ммоль) в ацетонитриле, содержащем 0,75%) воды (15 мл) при 0°C добавляли раствор перйодной кислоты/триоксида хрома (8,5 мл) в мокром ацетонитриле [этот раствор получают путем растворения перйодной кислоты (5 г, 21,9 ммоль) и триоксида хрома (20 мг, 0,20 ммоль) в ацетонитриле, содержащем 0,75% воды (50 мл)]. Полученную смесь перемешивали при 0°C в течение 90 минут. Добавляли 1М раствор соляной кислоты (15 мл). Слои разделяли. Водный слой экстрагировали этилацетатом (2×15 мл). Унифицированные органические слои промывали 15%-ным раствором тиосульфата натрия (30 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток растворяли в циклогексане (8 мл) и метаноле (2 мл) и охлаждали до 0°C. Добавляли по каплям 2М раствор триметилсилилдиазометана в диэтиловом эфире (1,5 мл, 3,0 ммоль). Полученную смесь перемешивали при 0°C в течение 1 часа. Добавляли несколько капель уксусной кислоты. Смесь разбавляли циклогексаном (15 мл) и промывали насыщенным раствором гидрокарбоната натрия (10 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат 90/10) с получением метил-2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-(циклопропокси) ацетата (48I) (496 мг, 1,13 ммоль, 76%), в виде желтого масла.
1Н ЯМР (400 МГц, CDCl3) δ 0,25-0,41 (м, 3H), 0,48-0,57 (м, 1Н), 0,58-0,69 (м, 2Н), 0,72-0,84 (м, 2Н), 1,47-1,55 (м, 1H), 2,02-2,10 (м, 2Н), 2,39 и 2,40 (с, 3H), 2,73-2,89 (м, 2Н), 3,32-3,37 и 3,39-3,45 (м, 1H), 3,70 и 3,73 (с, 3H), 4,21-4,30 (м, 2Н), 5,10 и 5,15 (с, 1Н), 6,83-6,97 (м, 3H), 7,22 и 7,23 (с, 1Н).
МС m/z ([M+Na]+) 460.
Стадия 13: Получение промежуточного соединения метил-2-(5-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси) ацетата (48m)
К раствору метил-2-(2-хроман-6-ил-3-циклопропил-6-метил-5-нитро-фенил)-2-(циклопропокси) ацетата (48L) (496 мг, 1,13 ммоль) в метаноле (5 мл) и тетрагидрофуране (3 мл) добавляли оксид платины (25 мг, 0,06 ммоль). Смесь перемешивали в атмосфере водорода в течение 3 часов. Смесь фильтровали через Milipore и фильтрат концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат 70/30) с получением метил 2-(5-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси) ацетата (48m) (369 мг, 0,90 ммоль, 80%) в виде белого твердого вещества после осаждения в метаноле.
1H ЯМР (300 МГц, CDCl3) δ 0,20-0,70 (м, 8Н), 1,39-1,51 (м, 1Н), 2,00-2,10 (м, 2Н), 2,12 и 2,13 (с, 3H), 2,70-2,85 (м, 2Н), 3,31-3,45 (м, 1Н), 3,60 (уш. с, 2Н), 3,66 и 3,69 (с, 3H), 4,19-4,28 (м, 2Н), 5,01 и 5,06 (с, 1H), 6,23 (с, 1Н), 6,77-6,83 (м, 1Н), 6,88-7,02 (м, 2Н).
МС m/z ([М+Н]+) 408.
Стадия 14: Получение промежуточного соединения метил-2-[2-хроман-6-ил-3-циклопропил-5-(метансульфонамидо)-6-метил-фенил]-2-(циклопропокси) ацетата (48N)
К раствору метил-2-(5-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси) ацетата (48m) (55 мг, 0,135 ммоль) в безводном дихлорметане (1 мл) при 0°C в атмосфере азота последовательно добавляли пиридин (12 мкл, 0,148 ммоль) и метансульфонилхлорид (11 мкл, 0,140 ммоль). Полученную смесь перемешивали при комнатной температуре в течение ночи, затем разбавляли дихлорметан (5 мл). Смесь промывали 1М соляной кислотой, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 70/30) с получением метил 2-[2-хроман-6-ил-3-циклопропил-5-(метансульфонамидо)-6-метил-фенил]-2-(циклопропокси)ацетата (48n) (57 мг, 0,117 ммоль, 86%) в виде желтого масла.
1H ЯМР (300 МГц, CDCl3) δ 0,21-0,40 (м, 3H), 0,45-0,78 (м, 5Н), 1,42-1,54 (м, 1Н), 2,00-2,11 (м, 2Н), 2,26 (с, 3H), 2,70-2,89 (м, 2Н), 3,00 (с, 3H), 3,29-3,43 (м, 1Н), 3,67 и 3,70 (с, 3H), 4,18-4,30 (м, 2Н), 5,05 и 5,10 (с, 1Н), 6,37 (уш. с, 1Н), 6,79-7,01 (м, 4Н).
МС m/z ([М-Н]-) 484.
Стадия 15: Получение 2-[2-хроман-6-ил-3-циклопропил-5-(метансульфонамидо)-6-метил-фенил]-2-(циклопропокси) уксусной кислоты (пример 48)
К раствору метил 2-[2-хроман-6-ил-3-циклопропил-5-(метансульфонамидо)-6-метил-фенил]-2-(циклопропокси)ацетата (48n) (57 мг, 0,117 ммоль) в этаноле (0,5 мл) добавляли 2М раствор гидроксида натрия (0,235 мл, 0,47 ммоль). Смесь нагревали при 100°C в течение 3 часов. Смесь концентрировали в вакууме. Вода (3 мл) добавляли к остатку, и раствор экстрагировали трет-бутил-метиловым эфиром (5 мл). Водный слой подкисляли 1М соляной кислотой до рН 3. Смесь экстрагировали трет-бутил-метиловым эфиром (2×3 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток растворяли в этил ацетате (5 мл) и концентрировали в вакууме с получением 2-[2-хроман-6-ил-3-циклопропил-5-(сульфонамидо метан)-6-метил-фенил] -2-(циклопропокси) уксусной кислоты (пример 48) (39 мг, 0,082 ммоль, 71%) в виде твердого вещества бежевого цвета.
1H ЯМР (300 МГц, CDCl3) δ 0,10-0,42 (м, 4Н), 0,46-0,60 (м, 2Н), 0,65-0,75 (м, 2Н), 1,32-1,46 (м, 1Н), 1,90-2,01 (м, 2Н), 2,22 (с, 3H), 2,66-2,82 (м, 2Н), 2,97 (с, 3H), 3,30-3,41 (м, 1H), 4,14-4,21 (м, 2Н), 4,78 и 4,84 (с, 1Н), 6,74 и 6,75 (с, 1H), 6,78-6,93 (м, 3H), 8,97 (с, 1H), 12,73 (уш. с, 1Н).
МС m/z ([M+NH4]+) 489.
МС m/z ([М-Н]-) 470.
Пример 49: Синтез 2-(5-ацетамидо-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси) уксусной кислоты
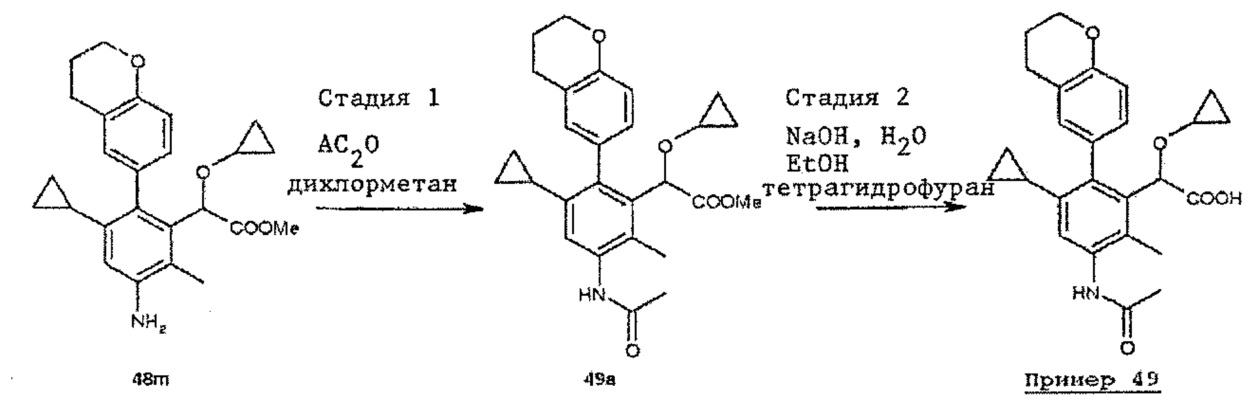
Стадия 1: Получение промежуточного соединения метил-2-(5-ацетамидо-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси) ацетата (49а)
К раствору метил-2-(5-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси) ацетата (48а) (50 мг, 0,123 ммоль) в безводном дихлорметане (1 мл) при 0°C в атмосфере азота добавляли уксусный ангидрид (14 мкл, 0,15 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 90 минут, после чего разводили дихлорметаном (5 мл), промывали насыщенным раствором гидрокарбоната натрия (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Циклогексан (2 мл) добавляли к остатку, чтобы осадить продукт. Смесь концентрировали в вакууме с получением метил 2-(5-ацетамидо-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(цикло пропокси) ацетата (49а) (54 мг, 0,120 ммоль, 98%) в виде белого твердого вещества.
1H ЯМР (300 МГц, CDCl3) δ 0,20-0,80 (м, 8Н), 1,39-1,51 (м, 1Н), 2,00-2,11 (м, 2Н), 2,20 (s, 6Н), 2,70-2,88 (м, 2Н), 3,28-3,42 (м, 1H), 3,66 и 3,69 (с, 3H), 4,20-4,28 (м, 2Н), 5,06 и 5,10 (с, 1Н), 6,78-7,00 (м, 4Н), 7,30 и 7,31 (с, 1Н).
MC m/z ([М+НСОО]-) 494.
MC m/z ([M-H]-) 448.
Стадия 2: Получение 2-(5-ацетамидо-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси) уксусной кислоты (пример 49)
К раствору метил-2-(5-ацетамидо-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси) ацетата (49а) (54 мг, 0,120 ммоль) в этаноле (0,8 мл) и тетрагидрофуране (0,2 мл) добавляли 2М раствор гидроксида натрия (0,48 мл, 0,96 ммоль). Смесь нагревали при 100°C в течение 1 часа. Смесь концентрировали в вакууме. Воду (5 мл) добавляли к остатку, и раствор экстрагировали этилацетат (5 мл). Водный слой подкисляли 1 М соляной кислотой до рН 1. Смесь экстрагировали трет-бутил-метиловым эфиром (5 мл). Органический слой промывали 1М соляной кислотой (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток растворяли в этилацетате (5 мл) и фильтровали через Millipore. К остатку добавляли этилацетат (1 мл) и гептан (5 мл). Осадок фильтровали с получением 2-(5-ацетамидо-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(цикло пропокси) уксусной кислоты (пример 49) (24 мг, 0,055 ммоль, 46%) в виде твердого вещества бежевого цвета.
1Н ЯМР (400 МГц, DMSO-d6) δ 0,12-0,52 (м, 6Н), 0,61-0,72 (м, 2Н), 1,32-1,44 (м, 1Н), 1,91-2,00 (м, 2Н), 2,03 (с, 3H), 2,09 (с, 3H), 2,68-2,83 (м, 2Н), 3,32-3,42 (м, 1Н), 4,13-4,22 (м, 2Н), 4,78 и 4,84 (с,.1Н), 6,79-6,83 (м, 2Н), 6,85-6,92 (м, 2Н), 9,22 (с, 1Н), 12,70 (уш. с, 1Н).
MC m/z ([M+NH4]+) 453, MC m/z ([M+H]+) 436.
MC m/z ([M-H]-) 434.
Пример 50: Синтез 2-[2-хроман-6-ил-3-циклопропил-5-(диметиламино)-6-метил-фенил]-2-(циклопропокси) уксусной кислоты

Стадия 1: Получение промежуточного соединения метил-2-[2-хроман-6-ил-3-циклопропил-5-(диметиламино)-6-метил-фенил]-2-(циклопропокси) ацетата (50а)
К раствору метил-2-(5-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси) ацетата (48m) (50 мг, 0,123 ммоль) в толуоле (1 мл) и 30% гидроксиду натрия (1 мл) добавляли тетрабутиламмоний гидросульфат (4 мг, 0,01 ммоль) и диметилсульфат (13 мкл, 0,13 ммоль). Смесь перемешивали при комнатной температуре в течение 2 часов. Добавляли диметилсульфат (20 мкл, 0,21 ммоль) и перемешивали смесь в течение ночи. Смесь разбавляли толуолом (5 мл), промывали водой (5 мл), насыщенным раствором соли (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 70/30) с получением метил 2-[2-хроман-6-ил-3-циклопропил-5-(диметиламино)-6-метил-фенил]-2-(циклопропокси) ацетата (50а) (8 мг, 0,018 ммоль, 15%) и метил 2-[2-хроман-6-ил-3-циклопропил-6-метил-5-(метиламино) фенил]-2-(циклопропокси) ацетата (51а) (30 мг, 0,071 ммоль, 57%).
(50а)1H ЯМР (300 МГц, CDCl3) δ 0,19-0,41 (м, 3H), 0,45-0,73 (м, 5Н), 1,44-1,56 (м, 1Н), 2,00-2,10 (м, 2Н), 2,27 и 2,28 (с, 3H), 2,66 (с, 6Н), 2,74-2,83 (м, 2Н), 3,29-3,36 и 3,38-3,45 (м, 1H), 3,67 и 3,70 (с, 3H), 4,19-4,28 (м, 2Н), 5,06 и 5,11 (с, 1H), 6,62 (с, 1H), 6,78-6,85 (м, 1Н), 6,88-7,04 (м, 2Н),
МС m/z ([М+Н]+) 436.
(51а)1H ЯМР (300 МГц, CDCl3) δ 0,20-0,75 (м, 8Н), 1,46-1,58 (м, 1Н), 2,00-2,12 (м, 5Н), 2,70-2,87 (м, 2Н), 2,88 (с, 3H), 3,31-3,45 (м, 1Н), 3,65 и 3,68 (с, 3H), 4,19-4,28 (м, 2Н), 5,03 и 5,08 (с, 1Н), 6,18 (с, 1Н), 6,67-6,84 (м, 1H), 6,89-7,04 (м, 2Н),
МС m/z ([М+Н]+) 422.
Стадия 2: Получение 2-[2-хроман-6-ил-3-циклопропил-5-(диметиламино)-6-метил-фенил]-2-(циклопропокси) уксусной кислоты (пример 50)
К раствору метил 2-[2-хроман-6-ил-3-циклопропил-5-(диметиламино)-6-метил-фенил]-2-(циклопропокси) ацетата (50а) (8 мг, 0,018 ммоль) в этаноле (0,4 мл) и тетрагидрофуране (0,1 мл) добавляли 2М раствор гидроксида натрия (75 мкл, 0,15 ммоль). Смесь нагревали при 70°C в течение 1 часа. Смесь концентрировали в вакууме. Воду (5 мл) добавляли к остатку, и раствор экстрагировали этилацетатом (5 мл). Водный слой подкисляли 1М соляной кислотой до рН 4. Смесь экстрагировали этилацетатом (2×5 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением 2-[2-хроман-6-ил-3-циклопропил-5-(диметиламино)-6-метил-фенил]-2-(циклопропокси) уксусной кислоты (пример 50) (4,3 мг, 0,010 ммоль, 53%) в виде твердого вещества бежевого цвета.
1Н ЯМР (400 МГц, CDCl3) δ 0,24-0,31 (м, 1Н), 0,33-0,52 (м, 3H), 0,54-0,75 (м, 4Н), 1,47-1,56 (м, 1Н), 2,00-2,10 (м, 2Н), 2,28 и 2,30 (с, 3H), 2,67 (с, 6Н), 2,73-2,84 (м, 2Н), 3,17-3,30 (м, 1H), 4,19-4,27 (м, 2Н), 5,16 и 5,18 (с, 1H), 6,65 (с, 1H), 6,79 и 6,82 (д, J=8,3 Гц, 1Н), 6,88-7,07 (м, 2Н).
МС m/z ([М+Н]+) 422.
МС m/z ([М-Н]-) 420.
Пример 51: Синтез 2-[2-хроман-6-ил-3-циклопропил-5-[2-гидроксиэтил (метил) амино]-6-метил-фенил]-2-(циклопропокси) уксусной кислоты

Стадия 1: Получение промежуточного соединения метил 2-[2-хроман-6-ил-3-циклопропил-5-[2-гидроксиэтил(метил)амино]-6-метил-фенил]-2-(циклопропокси)ацетата (51b)
К раствору метил 2-[2-хроман-6-ил-3-циклопропил-6-метил-5-(метиламино) фенил]-2-(циклопропокси) ацетата (51а) (30 мг, 0,071 ммоль) в смесь ацетонитрила (0,5 мл) и тетрагидрофурана (0,2 мл) добавляли диизопропилэтиламин (12 мкл, 0,071 ммоль) и 2-йодэтанол (6 мкл, 0,071 ммоль). Смесь нагревали при 100°C в течение 6 часов. Добавляли диизопропилэтиламин (24 мкл, 0,142 ммоль) и 2-йодэтанол (12 мкл, 0,142 ммоль). Смесь нагревали при 100°C в течение 18 часов. Добавляли диизопропилэтиламин (36 мкл, 0,213 ммоль) и 2-йодэтанол (18 мкл, 0,213 ммоль), и поддерживали нагревание в течение 24 часов. Смесь концентрировали в вакууме. Остаток растворяли в этилацетате (5 мл), промывали водой (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 60/40) с получением метил 2-[2-хроман-6-ил-3-циклопропил-5-[2-гидроксиэтил(метил)амино]-6-метил-фенил]-2-(циклопропокси)ацетата (51b) (21 мг, 0,045 ммоль, 63%).
1Н ЯМР (300 МГц, CDCl3) δ 0,18-0,40 (м, 3H), 0,45-0,74 (м, 5Н), 1,44-1,56 (м, 1Н), 1,98-2,10 (м, 2Н), 2,28 и 2,29 (с, 3H), 2,62 (с, 3H), 2,73-2,84 (м, 2Н), 3,08 (т, J=5,4 Гц, 2Н), 3,28-3,43 (м, 1Н), 3,63-3,71 (м, 5Н), 4,19-4,27 (м, 2Н), 5,06 и 5,11 (с, 1Н), 6,66 (с, 1Н), 6,78-6,85 (м, 1H), 6,88-7,03 (м, 2Н).
МС m/z ([М+Н]+) 466.
Стадия 2: получение 2-[2-хроман-6-ил-3-циклопропил-5-[2-гидроксиэтил(метил)амино]-6-метил-фенил]-2-(циклопропокси)уксусной кислоты (пример 51)
С помощью процедуры, описанной в примере 50, стадия 2, промежуточное соединение метил 2-[2-хроман-6-ил-3-циклопропил-5-[2-гидроксиэтил(метил)амино]-6-метил-фенил]-2-(циклопропокси)ацетат (51b) (21 мг, 0,045 ммоль) преобразовали в 2-[2-хроман-6-ил-3-циклопропил-5-[2-гидроксиэтил(метил)амино]-6-метил-фенил]-2-(циклопропокси)уксусную кислоту (пример 51) (13 мг, 0,029 ммоль, 64%).
1H ЯМР (300 МГц, CD3OD) δ 0,20-0,41 (м, 4Н), 0,51-0,74 (м, 4Н), 1,44-1,56 (м, 1H), 1,98-2,08 (м, 2Н), 2,31 (с, 3H), 2,70 (с, 3H), 2,76-2,85 (м, 2Н), 3,05 и 3,06 (т, J=6,3 Гц, 2Н), 3,22-3,30 (м, 1Н), 3,65 (т, J=6,3 Гц, 2Н), 4,16-4,24 (м, 2Н), 5,02 и 5,05 (с, 1Н), 6,75 (с, 1Н), 6,78 (д, J=8,3 Гц, 1H), 6,88-7,01 (м, 2Н).
МС m/z ([М+Н]+) 452.
МС m/z ([М-Н]-) 450.
Пример 52: Синтез (2-хроман-6-ил-3-циклопропил-4-метансульфониламино-6-метил-фенил)-циклопропокси-уксусной кислоты

Стадия 1: Получение промежуточного соединения метилового сложного эфира трет-бутокси-(2-хроман-6-ил-3-гидрокси-6-метил-4-нитро-фенил) уксусной кислоты (52а)
К раствору 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил] ацетата (1i) (400 мг, 1,04 ммоль) в 7 мл уксусной кислоты добавляли при 0°C, дымящую азотную кислоту (66 мкл, 1,56 ммоль), разбавленную в 100 мкл уксусной кислоты. После перемешивания при 0°C в течение 30 минут, добавляли воду и осаждали неочищенный продукт. Смесь экстрагировали этилацетатом. Органический слой промывали раствором бикарбоната натрия, сушили над сульфатом натрия, фильтровали и выпаривали с получением коричневого масла. Остаток очищали с помощью флэш-хроматографии (циклогексан/этилацетат от 100/0 до 97/3) с получением метилового сложного эфира трет-бутокси-(2-хроман-6-ил-3-гидрокси-6-метил-4-нитро-фенил) уксусной кислоты (52а) (400 мг, 0,93 ммоль, 89%) в виде желтого твердого вещества.
1Н ЯМР (400 MHz CDCl3) δ 0,96 и 0,97 (с, 9Н), 2,02-2,10 (м, 2Н), 2,38 и 2,39 (с, 3H), 2,70-2,92 (м, 2Н), 3,72 и 3,73 (с, 3H), 4,25 (т, J=5,6 Гц, 2Н), 5,11 и 5,12 (с, 1H). 6,89 (д, J=8,4 Гц, 1H), 7,00-7,02 (м, 1H). 7,03-7,07 (м, 1Н), 7,89 (с, 1Н), 10,81 (с, 1H).
MC m/z ([М-Н]-) 428.
Стадия 2: Получение промежуточного соединения метилового сложного эфира трет-бутокси-(2-хроман-6-ил-6-метил-4-нитро-3-трифторметансульфонилокси-фенил)-уксусной кислоты (52b)
К раствору метилового сложного эфира трет-бутокси-(2-хроман-6-ил-3-гидрокси-6-метил-4-нитро-фенил) уксусной кислоты (52а) (400 мг, 0,93 ммоль) в 9 мл пиридина, добавляли при-20°C трифторметансульфоновый ангидрид (235 мкл, 1,40 ммоль). После перемешивания при комнатной температуре в течение 4 часов, смесь выпаривали. Остаток растирали с дихлорметаном и соли пиридиния удаляли фильтрацией PTFE. Фильтрат выпаривали, остаток растирали с циклогексаном и удаляли примеси PTFE-фильтрованием. Фильтрат выпаривали с получением метилового сложного эфира трет-бутокси-(2-хроман-6-ил-6-метил-4-нитро-3-трифторметансульфонилокси-фенил) уксусной кислоты (52b) (512 мг, 0,91 ммоль, 98%) в виде бежевого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 0,92 и 0,93 (с, 9Н), 2,02-2,08 (м, 2Н), 2,50 и 2,51 (с, 3H), 2,69-2,89 (м, 2Н), 3,75 (с, 3H), 4,25 (т, J=4,8 Гц, 2Н), 5,14 и 5,17 (с, 1Н), 6,88 (дд, J=3,6 Гц, J=8,4 Гц, 1Н), 7,01-7,14 (м, 2Н), 7,80 (с, 1H).
Стадия 3: Получение промежуточного соединения метилового сложного эфира трет-бутокси-(2-хроман-6-ил-3 -циклопропил-6-метил-4-нитро-фенил) уксусной кислоты (52с)
К раствору метилового сложного эфира трет-бутокси-(2-хроман-6-ил-6-метил-4-нитро-3-трифторметансульфонил окси-фенил) уксусной кислоты (52b) (300 мг, 0,53 ммоль) в 5 мл диоксана добавляли циклопропилтрифторборат калия (158 мг, 1,07 ммоль) и моногидрат фосфата калия (371 мг, 1,75 ммоль). Смесь продували аргоном в течение 15 минут. Добавляли тетракис (трифенилфосфин) (61 мг, 0,05 ммоль) и смесь нагревали 18 ч при 100°C. Растворитель выпаривали и неочищенный продукт очищали с помощью препаративной ТСХ на силикагеле (циклогексан/этилацетат 80/20) с получением метилового сложного эфира трет-бутокси-(2-хроман-6-ил-3-циклопропил-6-метил-4-нитро-фенил) уксусной кислоты (52с) (221 мг, 0,49 ммоль, 92%).
1Н ЯМР (300 МГц, CDCl3) δ-0,08-0,01 (м, 1Н), 0,23-0,31 (м, 1Н), 0,34-0,41 (м, 1H), 0,64-0,72 (м, 1H), 0,93 и 0,94 (с, 9Н), 1,75-1,83 (м, 1Н), 2,01-2,09 (м, 2Н), 2,42 и 2,43 (с, 3H), 2,70-2,84 (м, 2Н), 3,71 и 3,72 (с, 3H), 4,23-4,27 (м, 2Н), 5,15 и 5,16 (с, 1H), 6,82-6,86 (м, 1Н), 6,93-7,03 (м, 2Н), 7,39 (с, 1Н).
МС m/z ([М+Н]+) 454.
Стадия 4: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-4-нитро-фенил)-гидрокси-уксусной кислоты (52d)
Трифторуксусную кислоту (0,33 мл, 4,24 ммоль) добавляли к раствору метилового сложного эфира трет-бутокси-(2-хроман-6-ил-3-циклопропил-6-метил-4-нитро-фенил) уксусной кислоты (52с) (370 мг, 0,82 ммоль) в дихлорметане (7,4 мл) охлаждали до 0°C. Реакционную смесь перемешивали при комнатной температуре в течение трех дней и гасили насыщенным раствором бикарбоната натрия (20 мл). Смесь экстрагировали этилацетатом (3×10 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 70/30) с получением метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-4-нитро-фенил)-гидрокси-уксусной кислоты (52d) (282 мг, 0,71 ммоль, 87%) в виде смеси атропоизомеров.
1H ЯМР (400 МГц, CDCl3) δ 0,07-0,16 (м, 2Н), 0,47-0,59 (м, 2Н), 1,74-1,78 (м, 1Н), 2,02-2,06 (м, 2Н), 2,33 и 2,34 (с, 3H), 2,76-2,83 (м, 2Н), 3,21-3,22 (м, 1H), 3,69 и 3,71 (с, 3H), 4,21-4,23 (м, 2Н), 5,24-5,25 (м, 1Н), 6,79-6,84 (м, 1Н), 6,91-6,95 (м, 2Н), 7,39 (с, 1Н).
МС m/z ([M+Na]+) 420.
Стадия 5: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-4-нитро-фенил)-винилокси-уксусной кислоты (52е)
К перемешиваемому раствору метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-4-нитро-фенил)-гидрокси-уксусной кислоты (52d) (183 мг, 0,46 ммоль) в дихлорметане (1,1 мл) и этил-винилового эфира (0,88 мл), при комнатной температуре добавляли трифторуксусную кислоту (1 каплю). Полученную смесь перемешивали в течение 4 часов. Затем добавляли триэтиламин (~50 мкл) к смеси перед ее концентрированием в потоке азота. В атмосфере аргона, промежуточный ацеталь непосредственно растворяли в безводном дихлорметане (1,1 мл), охлаждали до 0°C и добавляли по каплям триэтиламин (96 мкл, 0,69 ммоль) и триметилсилилтрифторметансульфонат (108 мкл, 0,60 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 16 часов и реакционную смесь гасили 1М раствором гидроксида натрия. Органический слой отделяли, промывали насыщенным солевым раствором, сушили над сульфатом натрия и концентрировали при пониженном давлении. Неочищенный материал очищали с помощью двух препаративных ТСХ (циклогексан/этилацетат 80/20), с получением метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-4-нитро-фенил)-винилокси-уксусной кислоты (52е) (125 мг, 0,30 ммоль, 64%).
1H ЯМР (400 МГц, CDCl3) δ 0,06-0,19 (м, 2Н), 0,47-0,62 (м, 2Н), 1,75-1,82 (м, 1Н), 2,01-2,09 (м, 2Н), 2,38-2,39 (м, 3H), 2,75-2,83 (м, 2Н), 3,72-3,73 (м, 3H), 4,01-4,04 (м, 1Н), 4,22-4,27 (м, 3H), 5,39-5,40 (м, 1Н), 6,04-6,12 (м, 1Н), 6,83-7,01 (м, 3H), 7,40 (с, 1Н).
МС m/z ([M+Na]+) 446.
Стадия 6: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-4-нитро-фенил)-циклопропокси-уксусной кислоты (52f)
С помощью процедуры, описанной в примере 23, стадии 3, промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-4-нитро-фенил)-винилокси-уксусной кислоты (52е) (150 мг, 0,35 ммоль) преобразовали, после очистки двумя препаративными ТСХ (циклогексан/AcOEt 90/10), в метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-4-нитро-фенил)-циклопропокси-уксусной кислоты (52f) (82 мг, 0,19 ммоль, 48%).
1H ЯМР (400 МГц, CDCl3) δ 0,06-0,14 (м, 1Н), 0,22-0,36 (м, 4Н), 0,47-0,51 (м, 2Н), 0,59-0,67 (м, 1H), 1,74-1,78 (м, 1H), 2,06-2,09 (м, 2Н), 2,37 (с, 3H), 2,77-2,81 (м, 2Н), 3,27-3,35 (м, 1Н), 3,71 и 3,72 (с, 3H), 4,25-4,27 (м, 2Н), 5,11 и 5,15 (с, 1Н), 6,83-6,96 (м, 3H), 7,39 (с, 1H).
МС m/z ([M+Na]+) 460.
Стадия 7: Получение промежуточного соединения метилового сложного эфира (4-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропокси-уксусной кислоты (52g)
К раствору метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-4-нитро-фенил)-циклопропокси-уксусной кислоты (52f) (63 мг, 0,14 ммоль) в смеси (2:1) метанол/вода (1,35 мл) добавляли хлорид аммония (54 мг, 1,01 ммоль). Смесь нагревали при 50°C в течение 10 минут и добавляли порошок железа (24 мг, 0,43 ммоль). Через 1 час при температуре 60°C, железа удаляли PTFE-фильтрацией (многочисленные промывки метанолом) и выпаривали фильтрат. Остаток, растворенный в этилацетате промывали насыщенным раствором бикарбоната натрия и насыщенным раствором соли (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ на силикагеле (циклогексан/этилацетат 7/3), с получением метилового сложного эфира (4-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил) метил-циклопропокси-уксусной кислоты (52g) (50 мг, 0,12 ммоль, 79%) в виде белого твердого вещества.
1Н ЯМР (400 МГц, CDCl3) δ 0,08-0,48 (м, 7Н), 0,61-0,69 (м, 1Н), 1,34-1,38 (м, 1H), 2,02-2,09 (м, 2Н), 2,25 (с, 3H), 2,75-2,81 (м, 2Н), 3,20-3,33 (м, 1H), 3,67 и 3,70 (с, 3H), 4,10 (уш. с, 2Н), 4,22-4,26 (м, 2Н), 5,00 и 5,06 (с, 1H), 6,50 (с, 1Н), 6,77-7,0 (м, 3H).
МС m/z ([М+Н]+) 408.
Стадия 8: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-4-метансульфониламино-6-метил-фенил)-циклопропокси-уксусной кислоты (52h)
Раствор ангидрида трифторметансульфокислоты (39 мг, 0,22 ммоль) в дихлорметане (0,5 мл) по каплям добавляли к охлажденному при 0°C перемешиваемому раствору метилового сложного эфира (4-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропокси-уксусной кислоты (52g) (50 мг, 0,12 ммоль) в триэтиламине (67 мкл, 0,48 ммоль) и дихлорметане (1 мл). Реакцию завершали через 20 мин перемешивании при 0°C. Реакцию гасили водой и дважды экстрагировали дихлорметаном. Органические слои промывали солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ на силикагеле (циклогексан/этилацетат 6/4), с получением метилового сложного эфира (2-хроман-6-ил-3-циклопропил-4-метансульфониламино-6-метил-фенил) метил-циклопропокси-уксусной кислоты (52h) (46 мг, 0,09 ммоль, 79%) в виде белого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 0,16-0,33 (м, 5Н), 0,44-0,62 (м, 2Н), 0,80-0,85 (м, 1H), 1,34-1,41 (м, 1Н), 2,05-2,09 (м, 2Н), 2,34 (с, 3H), 2,77-2,82 (м, 2Н), 3,12 (с, 3H), 3,24-3,36 (м, 1Н), 3,69 и 3,71 (с, 3H), 4,24-4,27 (м, 2Н), 5,06 и 5,11(с, 1Н), 6,79-6,98 (м, 3H), 7,33 (с, 1Н).
Стадия 9: получение (2-хроман-6-ил-3-циклопропил-4-метансульфониламино-6-метил-фенил)-циклопропокси-уксусной кислоты (пример 52)
Смесь метилового сложного эфира (2-хроман-6-ил-3-циклопропил-4-метансульфониламино-6-метил-фенил)-циклопропокси-уксусной кислоты (52h) (45 мг, 0,09 ммоль) и 2М гидроксид натрия в воде (93 мкл, 0,19 ммоль), тетрагидрофурана (0,5 мл) и метанола (0,5 мл) нагревали при 90°C в течение 15 часов. Добавляли воду к смеси, и водный слой подкисляли 1М соляной кислотой до рН 4-5 и дважды экстрагировали этил ацетатом. Объединенные органические слои промывали солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали на препаративной ТСХ (дихлорметан/метанол 90/10) с получением (2-хроман-6-ил-3-циклопропил-4-метансульфониламино-6-метил-фенил)-циклопропокси-уксусной кислоты (пример 52) (29 мг, 0,05 ммоль, 66%) в виде белого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 0,14-0,42 (м, 5Н), 0,52-0,56 (м, 1Н), 0,81-0,89 (м, 2Н), 1,37-1,42 (м, 1H), 2,02-2,06 (м, 3H), 2,29-2,33 (м, 2Н), 2,73-2,83 (м, 2Н), 3,07-3,13 (м, 4Н), 4,24 (м, 2Н), 5,13-5,19 (м, 1H), 6,78-7,00 (м, 3H), 7,30-7,36 (м, 2Н).
MC m/z ([M-H]-) 470.
Пример 53: Синтез (4-ацетиламино-2-хроман-6-ил-3-циклопропил-6-метил-фенил-циклопропокси-уксусной кислоты
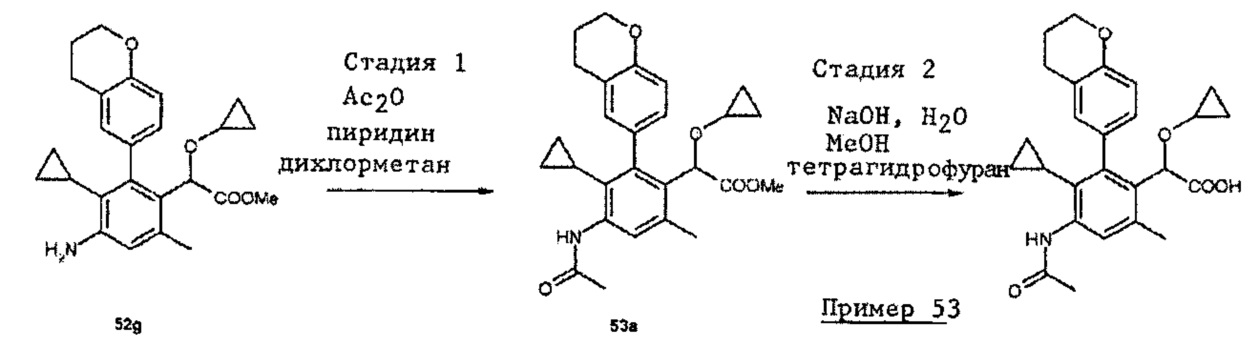
Стадия 1: Получение промежуточного соединения метилового сложного эфира (4-ацетиламино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропокси-уксусной кислоты (53а)
В сухой реактор с магнитной мешалкой загружали промежуточное соединение метиловый сложный эфир (4-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропокси-уксусной кислоты (52g) (50 мг, 0,123 ммоль) в дихлорметане (1 мл). Добавляли к раствору пиридин (24 мкл, 0,293 ммоль), а затем уксусный ангидрид (14 мкл, 0,147 ммоль), и перемешивали реакционную смесь в течение 2 часов до комнатной температуры и разбавляли этилацетатом (5 мл). Полученный раствор обрабатывали насыщенным раствором хлорида аммония и и разделяли слои. Водный слой экстрагировали этилацетатом (2×5 мл). Объединенные органические слои промывали насыщенным раствором хлорида натрия (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали на препаративной ТСХ (циклогексан/дихлорметан 50/50) с получением метилового сложного эфира (4-ацетиламино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропокси-уксусной кислоты (53а) (36 мг, 0,080 ммоль, 65%) в виде белого твердого вещества.
1H ЯМР (300 МГц, CDCl3) δ 0,13-0,60 (м, 7Н), 070-0,80 (м, 1H), 1,38-1,45 (м, 1Н), 2,01-2,10 (м, 2Н), 2,22 (с, 3H), 2,34 (с, 3H), 2,74-2,81 (м, 2Н), 3,19-3,33 (м, 1Н), 3,67 и 3,70 (с, 3H), 4,23-4,26 (м, 2Н), 5,05 и 511 (с, 1Н), 6,78-6,98 (м, 3H), 8,04-8,11 (м, 1Н)
МС m/z ([М+Н]+) 450.
Стадия 2: получение (4-ацетиламино-2-хроман-6-ил-3 -циклопропил-6-метил-фенил)-циклопропокси-уксусной кислоты (пример 53)
С помощью процедуры, описанной в примере 23, стадии 4, метиловый сложный эфир (4-ацетиламино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропокси-уксусной кислоты (53а) (36 мг, 0,073 ммоль) преобразовали в (4-ацетиламино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропокси-уксусную кислоту (пример 53) (28 мг, 0,064 ммоль, 88%).
1Н ЯМР (300 МГц, CDCl3) δ 0,10-0,59 (м, 7Н), 0,74-0,83 (м, 1Н), 1,40-1,49 (м, 1Н), 1,97-2,09 (м, 2Н), 2,23 (с, 3H), 2,33 и 2,35 (с, 3H), 2,67-2,88 (м, 2Н), 3,06-3,19 (м, 1Н), 4,19-4,30 (м, 2Н), 5,14 и 5,18 (с, 1H), 6,76-6,87 (м, 2Н), 6,96-7,05 (м, 1H), 7,98-8,14 (м, 2Н).
MC m/z ([М+Н]+) 436.
MC m/z ([М-Н]-) 434.
Пример 54: Синтез (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-циклопропокси-уксусной кислоты
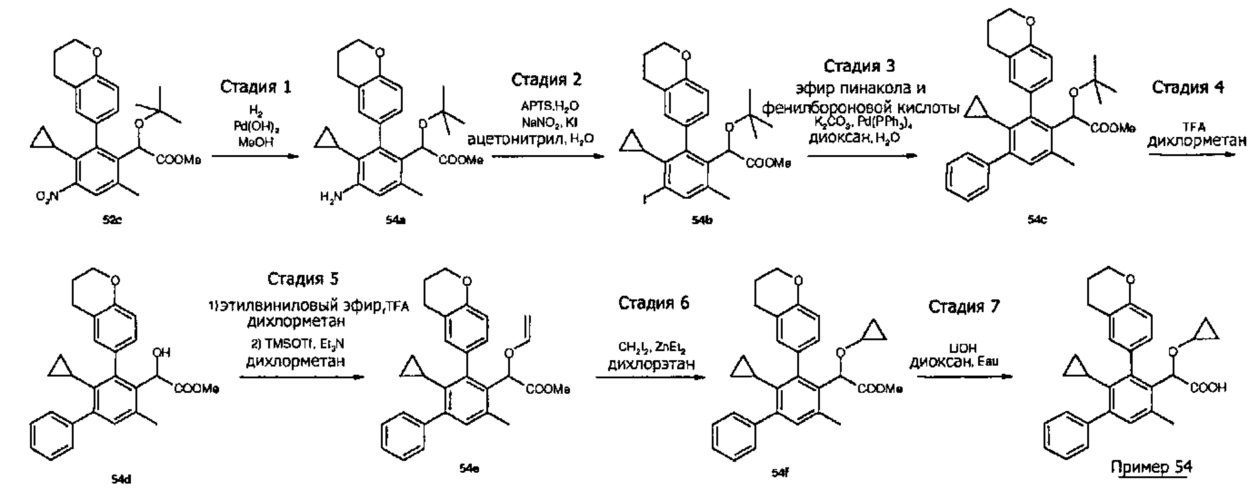
Получение промежуточного соединения метилового сложного эфира (4-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил))-рет-бутокси-уксусной кислоты (54а)
К раствору метилового сложного эфира трет-бутокси-(2-хроман-6-ил-3-циклопропил-6-метил-4-нитро-фенил) уксусной кислоты (52с) (346 мг, 0,76 ммоль) в 12 мл метанола добавляли гидроксид палладия на углероде (53 мг, 0,08 ммоль). Смесь помещали в атмосферу водорода и перемешивали 6 часов при комнатной температуре. Катализатор удаляли путем PTFE-фильтрации, и выпаривали фильтрат. Остаток очищали с помощью препаративной ТСХ на силикагеле (циклогексан/этилацетат 7/3), с получением метилового сложного эфира (4-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-трет-бутокси-уксусной кислоты (54а) (282 мг, 0,66 ммоль, 87%).
1H ЯМР (300 МГц, CDCl3) δ-0,04-0,07 (м, 1Н), 0,24-0,44 (м, 2Н), 0,68-0,75 (м, 1Н), 0,90 (с, 9Н), 1,34-1,41 (м, 1H), 2,00-2,09 (м, 2Н), 2,32 и 2,33 (с, 3H), 2,66-2,83 (м, 2Н), 3,67 и 3,69 (с, 3H), 4,05 (уш. с, 2Н), 4,22-4,26 (м, 2Н), 5,07 и 5,09 (с, 1Н), 6,49 (с, 1H), 6,75-6,81 (м, 1Н), 6,88-6,96 (м, 1H), 7,05-7,10 (м, 1Н).
MC m/z ([М+Н]+) 424.
Стадия 2: Получение промежуточного соединения метилового сложного эфира трет-бутокси-(2-хроман-6-ил-3-циклопропил-4-йод-6-метил-фенил)-уксусной кислоты (54b)
К раствору метилового сложного эфира (4-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)- трет-бутокси-уксусной кислоты (54а) (129 мг, 0,30 ммоль) в безводном ацетонитриле (3 мл) добавляли моногидрат p-толуолсульфоновой кислоты (174 мг, 0,91 ммоль). Смесь охлаждали до 0°C и медленно добавляли раствор нитрита натрия (42 мг, 0,61 ммоль) с иодидом калия (126 мг, 0,76 ммоль) в воде (0,3 мл). Реакционную смесь перемешивали в течение 5 минут при 0°C, затем оставляли нагреваться до 20°C. Через 20 часов при комнатной температуре смесь гасили 15%-ным раствором тиосульфата натрия (10 мл) и экстрагировали этилацетатом (3×5 мл). Органические слои промывали солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ на силикагеле (циклогексан/этилацетат 8/2) с получением метилового сложного эфира трет-бутокси-(2-хроман-6-ил-3-циклопропил-4-йод-6-метил-фенил) уксусной кислоты (54b) (75 мг, 0,14 ммоль, 46%) в виде бесцветного масла.
1H ЯМР (300 МГц, CDCl3) δ-0,06-0,05 (м, 1Н), 0,37-0,49 (м, 2Н), 0,89-0,93 (м, 10Н), 1,53-1,63 (м, 1Н), 2,00-2,08 (м, 2Н), 2,32 и 2,33 (с, 3H), 2,70-2,83 (м, 2Н), 3,68 и 3,70 (с, 3H), 422-4,26 (м, 2Н), 5,14 и 5,15 (с, 1H), 6,77-6,93 (м, 2Н), 6,99-7,07 (м, 1Н), 7,68 и 7,69 (с, 1Н).
МС m/z ([M+Na]+) 557.
Стадия 3: Получение промежуточного соединения метилового сложного эфира трет-бутокси-(3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил) уксусной кислоты (54с)
К дегазированному раствору метилового сложного эфира трет-бутокси-(2-хроман-6-ил-3-циклопропил-4-йод-6-метил-фенил) уксусной кислоты (54b) (79 мг, 0,15 ммоль) карбоната калия (61 мг, 0,44 ммоль), сложного эфира фенилбороновой кислоты и пинакола (60 мг, 0,30 ммоль) в смеси диоксана (1,5 мл) и воды (0,35 мл) добавляли тетракис (трифенилфосфин) палладий (0) (17 мг, 0,01 ммоль). Смесь нагревали при 90°C в течение 4 часов. Реакционную смесь гасили водой и дважды экстрагировали этилацетатом. Органический слой промывали насыщенным солевым раствором, сушили над сульфатом натрия и концентрировали при пониженном давлении. Неочищенный материал очищали с помощью препаративной ТСХ (циклогексан/этилацетат 85/15), с получением метилового сложного эфира трет-бутокси-(3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил) уксусной кислоты (54с) (71 мг, 0,15 ммоль, 98%).
1H ЯМР (400 МГц, CDCl3) δ-0,22-0,17 (м, 2Н), 0,16-0,24 (м, 2Н), 1,59-1,64 (м, 1Н), 0,98 и 0,99 (с, 9Н), 2,01-2,08 (м, 2Н), 2,43 и 2,44 (с, 3H), 2,73-2,82 (м, 2Н), 3,70 и 3,72 (с, 3H), 4,23-4,26 (м, 2Н), 5,17 и 5,19 (с, 1Н), 6,80-6,85 (м, 1Н), 6,98-7,09 (м, 3H), 7,29-7,45 (м, 5Н).
МС m/z ([M+Na]+) 507.
Стадия 4: Получение промежуточного соединения метилового сложного эфира (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-гидрокси-уксусной кислоты (54d)
Трифторуксусную кислоту (0,13 мл) добавляли к раствору метилового сложного эфира трет-бутокси-(3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил) уксусной кислоты (54с) (83 мг, 0,17 ммоль) в дихлорметане (1,3 мл) при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре в течение 2 часов и гасили насыщенным раствором бикарбоната натрия. Смесь дважды экстрагировали дихлорметаном, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 80/20) с получением метилового сложного эфира (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-гидрокси-уксусной кислоты (54d) (65 мг, 0,15 ммоль, 90%).
1H ЯМР (400 МГц, CDCl3) δ-0,22-0,18 (м, 2Н), 0,19-0,23 (м, 2Н), 1,60-1,64 (м, 1H), 2,04-2,08 (м, 2Н), 2,33 и 2,34 (с, 3H), 2,79-2,83 (м, 2Н), 3,07 и 3,09 (д, J=2,8 Hz, 1H), 3,73 и 3,74 (с, 3H), 4,23-4,25 (м, 2Н), 5,28 и 5,29(с, 1Н), 6,80-6,84 (м, 1Н), 6,98-7,03 (м, 2Н), 7,10-7.11 (м, 1Н), 7,28-7,33 (м, 1H), 7,35-7,43 (м, 4Н).
MC m/z ([M+Na]+) 451.
Стадия 5: Получение промежуточного соединения метилового сложного эфира (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-винилокси-уксусной кислоты (54е)
С помощью процедуры, описанной в примере 52, стадии 3, промежуточное соединение метиловый сложный эфир (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил) окси-уксусной кислоты (54d) (65 мг, 0,15 ммоль) преобразовали, после очистки препаративной ТСХ (циклогексан/AcOEt 85/15), в метиловый сложный эфир (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-винилокси-уксусной кислоты (54е) (42 мг, 0,09 ммоль, 62%).
1Н ЯМР (400 МГц, CDCl3) δ-0,21-0,18 (м, 2Н), 0,16-0,24 (м, 2Н), 1,61-1,68 (м, 1Н), 2,04-2,08 (м, 2Н), 2,36 и 2,37 (с, 3H), 2,78-2,83 (м, 2Н), 3,73 и 3,74 (с, 3H), 4,00-4,03 (м, 1Н), 4,23-4,30 (м, 3H), 5,41 и 5,43 (с, 1Н), 6,11-6,20 (м, 1Н), 6,81-6,85 (м, 1H), 6,90-7,08 (м, 2Н), 7,12 (с, 1Н), 7,29-7,44 (м, 5Н).
MC m/z ([M+Na]+) 477.
Стадия 6: Получение промежуточного соединения метилового сложного эфира (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-циклопропокси-уксусной кислоты (54f)
С помощью процедуры, описанной в примере 23, стадии 3, промежуточное соединение метиловый сложный эфир (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-винилокси-уксусной кислоты (54е) (42 мг, 0,09 ммоль) преобразовали, после очистки препаративной ТСХ (циклогексан/AcOEt 90/10), в метиловый сложный эфир (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-циклопропокси-уксусной кислоты (54f) (23 мг, 0,05 ммоль, 53%).
1H ЯМР (400 МГц, CDCl3) δ-0,19-0,13 (м, 2Н), 0,19-0,42 (м, 5Н), 0,50-0,55 (м, 1H), 1,58-1,63 (м, 1Н), 2,05-2,10 (м, 2Н), 2,36 (с, 3H), 2,78-2,84 (м, 2Н), 3,34-3,44 (м, 1Н), 3,72 и 3,74 (с, 3H), 4,24-4,26 (м, 2Н), 5,11 и 5,17 (с, 1Н), 6,81-7,04 (м, 3H), 7,08 (с, 1H), 7,28-7,43 (м, 5Н).
MC m/z ([M+Na]+) 491
Стадия 7: Получение (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-циклопропокси-уксусной кислоты (пример 54)
С помощью процедуры, описанной в примере 1, стадии 12, промежуточное соединение метиловый сложный эфир (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-циклопропокси-уксусной кислоты (54f) (23 мг, 0,05 ммоль) преобразовали, после очистки препаративной ТСХ (дихлорметан/метанол 95/5), в (3-хроман-6-ил-2-циклопропил-5-метил-бифенил-4-ил)-циклопропокси-уксусную кислоту (пример 54) (13 мг, 0,03 ммоль, 57%).
1H ЯМР (400 МГц, CDCl3) δ-0,21-0,17 (м, 2Н), 0,20-0,54 (м, 6Н), 1,58-1,66 (м, 1H), 1,97-2,11 (м, 2Н), 2,24-2,40 (м, 3H), 2,71-2,86 (м, 2Н), 3,18-3,26 (м, 1Н), 4,17-4,22 (м, 2Н), 5,17-5,22 (м, 1H), 6,77-6,81 (м, 1Н), 6,91-7,07 (м, 3H), 7,29-7,40 (м, 5Н).
МС m/z ([М-Н]-) 453.
Пример 55: Синтез (2-хроман-6-ил-3-циклопропил-4-этил-6-метил-фенил)-циклопропокси-уксусной кислоты
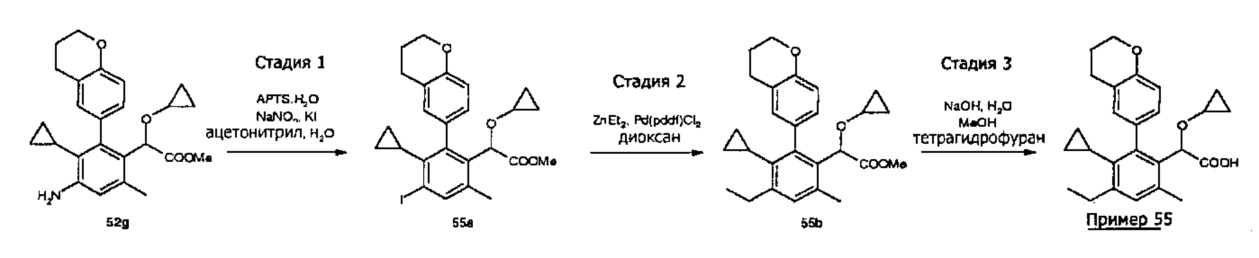
Стадия 1: получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-4-йод-6-метил-фенил)-циклопропокси-уксусной кислоты (55а)
С помощью процедуры, описанной в примере 54, стадия 2, промежуточное соединение метиловый сложный эфир (4-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклопропокси-уксусной кислоты (52g) (350 мг, 0,860 ммоль) преобразовали после очистки препаративной ТСХ (циклогексан/дихлорметан 70/30), в метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-4-йод-6-метил-фенил)-циклопропокси-уксусной кислоты (55а) (313 мг, 0,603 ммоль, 70%) в виде желтого масла.
1H ЯМР (300 МГц, CDCl3) δ 0,06-0,48 (м, 6Н), 0,50-0,60 (м, 1Н), 0,77-0,87 (м, 1H), 1,52-1,62 (м, 1H), 2,01-2,10 (м, 2Н), 2,26 (с, 3H), 2,68-2,86 (м, 2Н), 3,20-3,32 (м, 1Н), 3,69 и 3,71 (с, 3H), 4,20-4,29 (м, 2Н), 5,08 и 5,13 (с, 1Н), 6,78-6,97 (м, 3H), 7,71 (с, 1Н).
MC m/z ([M+Na]+) 541.
Стадия 2: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-4-этил-6-метил-фенил)-циклопропокси-уксусной кислоты (55b)
К дегазированному раствору метилового сложного эфира (2-хроман-6-ил-3-циклопропил-4-йод-6-метил-фенил)-циклопропокси-уксусной кислоты (55а) (47 мг, 0,090 ммоль) в сухом 1,4 диоксане (0,5 мл) добавляли комплекс [1,1'-бис (дифенилфосфино) ферроцен] дихлорпалладия(II), с дихлорметаном (3,3 мг, 0,004 ммоль) и раствор диэтилцинка 15% в толуоле (222 мкл, 0,246 ммоль). Реактор герметизировали и смесь нагревали при 80°C в течение 1,5 часов. Смесь гасили водой (3 мл) и экстрагировали этилацетатом (3×2 мл). Объединенные органические слои промывали солевым раствором (10 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали на препаративной ТСХ (циклогексан/дихлорметан 80/20) с получением метилового сложного эфира 2-хроман-6-ил-3-циклопропил-4-этил-6-метил-фенил)-циклопропокси-уксусной кислоты (55b) (43 мг, 0,090 ммоль, количественный выход) в виде желтого масла.
1Н ЯМР (300 МГц, CDCl3) δ 0,05-0,50 (м, 7Н), 0,64-0,72 (м, 1Н), 1,26 (т, J=7,5 Гц, 3H), 1,48-1,56 (м, 1H), 1,99-2,10 (м, 2Н), 2,32 (с, 3H), 2,69-2,98 (м, 4Н), 3,23-3,36 (м, 1H), 3,69 и 3,71 (с, 3H), 4,23-4,26 (м, 2Н), 5,10 и 5,15 (с, 1Н), 6,77-6,99 (м, 4Н).
МС m/z ([M+Na]+) 443.
Стадия 3: получение (2-хроман-6-ил-3-циклопропил-4-этил-6-метил-фенил)-циклопропокси-уксусной кислоты (пример 55)
С помощью процедуры, описанной в примере 23, стадии 4, метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-4-этил-6-метил-фенил)-циклопропокси-уксусной кислоты (55b) (43 мг, 0,102 ммоль) преобразовали в (2-хроман-6-ил-3-циклопропил-4-этил-6-метил-фенил)-циклопропокси-уксусную кислоту (пример 55) (12 мг, 0,029 ммоль, 32%) после очистки на препаративной ТСХ (дихлорметан/метанол 95/5).
1H ЯМР (400 МГц, CD3OD) δ 0,00-0,39 (м, 7Н), 0,69-0,79 (м, 1Н), 1,25 (т, J=7,5 Гц, 3H), 1,53-1,62 (м, 1Н), 1,96-2,07 (м, 2Н), 2,30 (с, 3H), 2,71-2,99 (м, 4Н), 3,08 (уш. с, 1Н), 4,17-4,23 (м, 2Н), 5,07 (уш. с, 1Н), 6,69-6,76 (м, 1Н), 6,86-6,91 (м, 1Н), 6,97 (с, 1H), 7,06 (уш. с, 1Н).
МС m/z ([M+Na]+) 429.
MC m/z ([M-H]-) 405.
Пример 56: Синтез (2-хроман-6-ил-3-циклопропил-4-метокси-6-метил-фенил)-циклопропокси-уксусной кислоты

Стадия 1: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-4-метокси-6-метил-фенил)-циклопропокси-уксусной кислоты (56а)
К раствору 0,5М метоксида натрия в метаноле (768 мкл, 0,384 ммоль) в сухом диметилформамиде (0,5 мл) добавляли йодид меди(I) (20 мг, 0,106 ммоль). Смесь нагревали при 90°C в течение 2 часов. Раствор метилового сложного эфира (2-хроман-6-ил-3-циклопропил-4-йод-6-метил-фенил)-циклопропокси-уксусной кислоты (55а) (50 мг, 0,096 ммоль) в сухом метаноле (0,2 мл) добавляли к смеси. Реактор герметизировали и перемешивали реакционную смесь при 90°C в течение 6 дней. Смесь гасили насыщенным раствором хлорида аммония (5 мл) и экстрагировали этилацетатом (3×3 мл). Объединенные органические слои промывали солевым раствором (10 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали на препаративной ТСХ (циклогексан/дихлорметан 90/10) с получением метилового сложного эфира (2-хроман-6-ил-3-циклопропил-4-метокси-6-метил-фенил)-циклопропокси-уксусной кислоты (56а) (6 мг, 0,014 ммоль, 14%) в виде желтого масла.
1H ЯМР (400 МГц, CDCl3) δ 0,19-0,73 (м, 8Н), 1,33-1,40 (м, 1H), 1,99-2,10 (м, 2Н), 2,33 (с, 3H), 2,70-2,86 (м, 2Н), 3,24-3,38 (м, 1Н), 3,67 и 3,70 (с, 3H), 3,91 (с, 3H), 4,19-4,28 (м, 2Н), 4,97 и 5,02 (с, 1Н),6,64 (с, 1Н), 6,76-7,06 (м, 3H).
MC m/z ([M+Na]+) 445.
Стадия 2: получение (2-хроман-6-ил-3-циклопропил-4-метокси-6-метил-фенил)-циклопропокси-уксусной кислоты (пример 56)
С помощью процедуры, описанной в примере 23, стадии 4, метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-4-метокси-6-метил-фенил)-циклопропокси-уксусной кислоты (56а) (6 мг, 0,014 ммоль) преобразовали в (2-хроман-6-ил-3-циклопропил-4-метокси-6-метил-фенил)-циклопропокси-уксусную кислоту (пример 56) (4,5 мг, 0,011 ммоль, 78%).
1H ЯМР (300 МГц, CD3OD) δ 0,17-0,70 (м, 8Н), 1,29-1,41 (м, 1H), 1,99-2,08 (м, 2Н), 2,32 (с, 3H), 2,70-2,88 (м, 2Н), 3,14-3,25 (м, 1Н), 3,80 (с, 3H), 4,19-4,22 (м, 2Н), 4,96 и 4,99 (с, 1Н), 6,73-7,07 (м, 4Н).
МС m/z ([M+Na]+) 431.
МС m/z ([М-Н]-) 407.
Пример 57: Синтез 2-(2-хроман-6-ил-3-циклопропил-5-этил-6-метил-фенил)-2-(циклопропокси) уксусной кислоты
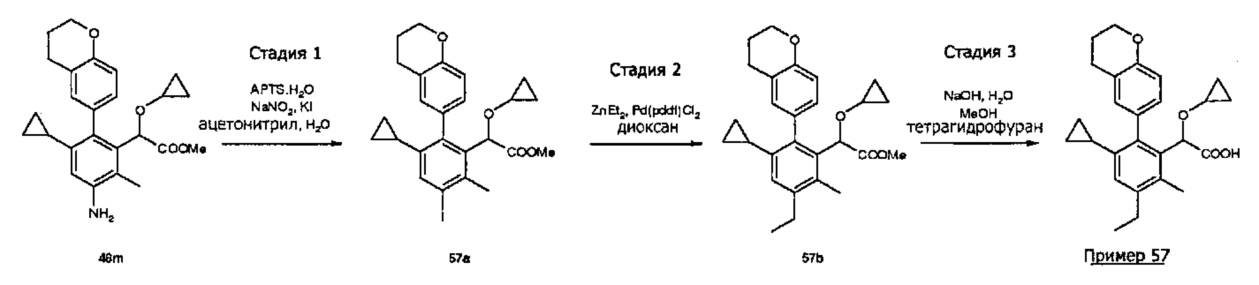
Стадия 1: получение промежуточного метил-2-(-хроман-6-ил-3-циклопропил-5-иод-6-метил-фенил))-(иклопропокси) ацетата (57а)
С помощью процедуры, описанной в примере 54, стадии 2, метил 2-(5-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси) ацетат (48m) (50 мг, 0,123 ммоль) преобразовали в промежуточное соединение метил-2-(2-хроман-6-ил-3-циклопропил-5-иод-6-метил-фенил)-2-(циклопропокси) ацетат (57а) (32 мг, 0,062 ммоль, 50%) после очистки препаративной ТСХ (циклогексан/этилацетат 90/10).
1H ЯМР (300 МГц, CDCl3) δ 0,21-0,41 (м, 3H), 0,45-0,76 (м, 5Н), 1,35-1,48 (м, 1H), 2,00-2,11 (м, 2Н), 2,42 и 2,42 (с, 3H), 2,70-2,88 (м, 2Н), 3,28-3,43 (м, 1Н), 3,68 и 3,71 (с, 3H), 4,18-4,30 (м, 2Н), 5,06 и 5,11 (с, 1Н), 6,79-7,00 (м, 3H), 7,35 и 7,36 (с, 1Н).
MC m/z ([M+Na]+) 541.
Стадия 2: Получение промежуточного соединения метил-2-(2-хроман-6-ил-3-циклопропил-5-этил-6-метил-фенил)-2-(циклопропокси) ацетата (57b)
С помощью процедуры, описанной в примере 55, стадии 2, промежуточное соединение метил-2-(2-хроман-6-ил-3-циклопропил-5-иод-6-метил-фенил)-2-(циклопропокси) ацетат (57а) (32 мг, 0,062 ммоль) преобразовали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 90/10), в промежуточное соединение метил-2-(2-хроман-6-ил-3-циклопропил-5-этил-6-метил фенил)-2-(циклопропокси) ацетат (57b) (23 мг, 0,054 ммоль, 82%).
1H ЯМР (400 МГц, CDCl3) δ 0,20-0,42(м, 3H), 0,47-0,74 (м, 5Н), 1,20 (т, J=7,5 Гц, 3H), 1,43-1,53 (м, 1Н), 2,00-2,11 (м, 2Н), 2,24 и 2,25 (с, 3H), 2,62 (q, J=7,5 Гц, 2Н), 2,72-2,87 (м, 2Н), 3,31-3,36 и 3,39-3,45 (м, 1Н), 3,67 и 3,70 (с, 3H), 4,19-4,29 (м, 2Н), 5,06 и 5,12 (с, 1Н), 6,70 и 6,71 (с, 1Н), 6,80-7,03 (м, 3H).
МС m/z ([M+Na]+) 443.
Стадия 3: Получение 2-(2-хроман-6-ил-3-циклопропил-5-этил-6-метил-фенил)-2-(циклопропокси) уксусной кислоты (например 57)
К раствору метил-2-(2-хроман-6-ил-3-циклопропил-5-этил-6-метил-фенил)-2-(циклопропокси)ацетата (57b) (23 мг, 0,054 ммоль) в этаноле (0,8 мл) и тетрагидрофуране (0,2 мл), добавляли 2М раствор гидроксида натрия (0,22 мл, 0,44 ммоль). Смесь нагревали при 70°C в течение 1 часа. Смесь концентрировали в вакууме. Добавляли воду (2 мл) и добавляли раствор 1М соляной кислоты до рН2. Осажденный отфильтровывали, промывали водой (2 мл) и сушили в присутствии пятиокиси фосфора с получением 2-(2-хроман-6-ил-3-циклопропил-5-этил-6-метил-фенил)-2-(циклопропокси) уксусной кислоты (пример 57) (15,5 мг, 0,038 ммоль, 70%) в виде белого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 0,24-0,52 (м, 4Н), 0,54-0,74 (м, 4Н), 1,20 (т, J=7,5 Гц, 3H), 1,44-1,53 (м, 1Н), 1,99-2,09 (м, 2Н), 2,23 и 2,25 (с, 3H), 2,63 (q, J=7,5 Гц, 2Н), 2,70-2,86 (м, 2Н), 3,18-3,30 (м, 1Н), 4,19-4,27 (м, 2Н), 5,16 и 5,19 (с, 1Н), 6,71 и 6,72 (с, 1Н), 6,80 и 6,82 (д, J=8,2 Гц, 1Н), 6,89-7,05 (м, 2Н).
МС m/z ([M+NH4]+) 424.
МС m/z ([М-Н]-) 405.
Пример 58: Синтез (2-хроман-6-ил-3-циклопропил-6-метил-4-тиофен-3-ил-фенил)-циклопропокси-уксусной кислоты
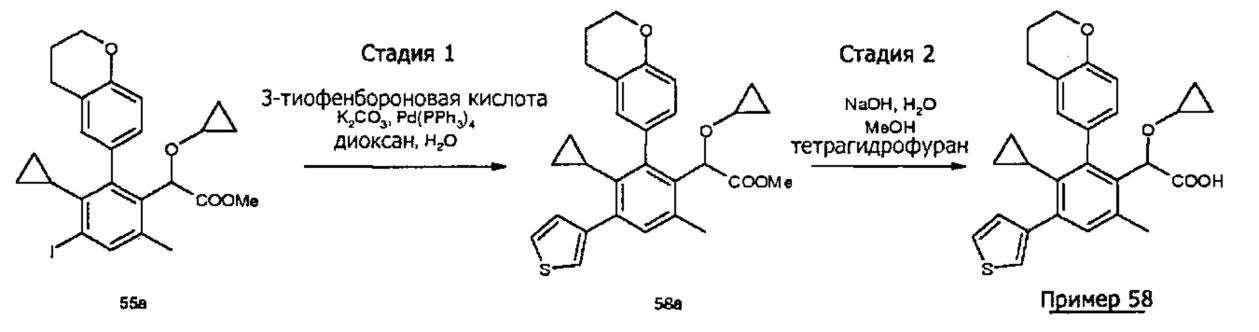
Стадия 1: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-6-метил-4-тиофен-3-ил-фенил)-циклопропокси-уксусной кислоты (58а)
С помощью процедуры, описанной в примере 54, стадии 3 метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-4-йод-6-метил-фенил)-циклопропокси-уксусной кислоты (55а) (50 мг, 0,096 ммоль) преобразовали реакцией с 3-тиофенбороновой кислотой (25,5 мг, 0,200 ммоль), в метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-4-тиофен-3-ил-фенил)-циклопропокси-уксусной кислоты (58а) (51 мг, 0,096 ммоль, количественный выход) после очистки на препаративной ТСХ (циклогексан/этилацетат 90/10).
1H ЯМР (400 МГц, CDCl3) δ-0,15-0,03 (м, 2Н), 0,21-0,45 (м, 5Н), 0,46-0,55 (м, 1H), 1,55-1,62 (м, 1Н), 2,04-2,10 (м, 2Н), 2,35 (с, 3H), 2,74-2,88 (м, 2Н), 3,31-3,42 (м, 1Н), 3,71 и 3,73 (с, 3H), 4,21-4,29 (м, 2Н), 5,10 и 5,16 (с, 1H), 6,83 (дд, J=8,6 Гц, J=6,6 Гц, 1Н), 6,91-7,06 (м, 2Н), 7,15 (с, 1H), 7,22-7,36 (м, 3H).
МС m/z ([M+Na]+) 497.
Стадия 2: получение (2-хроман-6-ил-3-циклопропил-6-метил-4-тиофен-3-ил-фенил)-циклопропокси-уксусной кислоты (пример 58)
С помощью процедуры, описанной в примере 23, стадии 4, метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-6-метил-4-тиофен-3-ил-фенил) метилового эфира-циклопропокси-уксусной кислоты (58а) (51 мг, 0,108 ммоль) преобразовали в (2-хроман-6-ил-3-циклопропил-6-метил-4-тиофен-3-ил-фенил)-циклопропокси-уксусную кислоту (пример 58) (22 мг, 0,047 ммоль, 44%) после очистки препаративной ТСХ (дихлорметан/метанол 90/10).
1H ЯМР (400 МГц, DMSO-d6) δ-0,28-0,20 (м, 2Н), 0,04-0,35 (м, 6Н), 1,65-1,76 (м, 1Н), 1,90-2,02 (м, 2Н), 2,31 (с, 3H), 2,65-2,85 (м, 2Н), 3,39-3,45 (м, 1H), 4,12-4,22 (м, 2Н), 4,69 и 4,73 (с, 1Н), 6,75 (дд, J=8,2 Гц, J=4,2Hz, 1Н), 6,89-6,95 (м, 1Н), 6,99-7,10 (м, 2Н), 7,28 (дт, J=5,0 Гц, J=1,5 Гц, 1H), 7,43-7,49 (м, 1Н), 7,50-7,56 (м, 1H).
MC m/z ([M+Na]+) 483.
МС m/z ([М-Н]-) 459.
Пример 59: Синтез (2-хроман-6-ил-3-циклопропил-4,6-диметил-фенил)-циклопропокси-уксусной кислоты
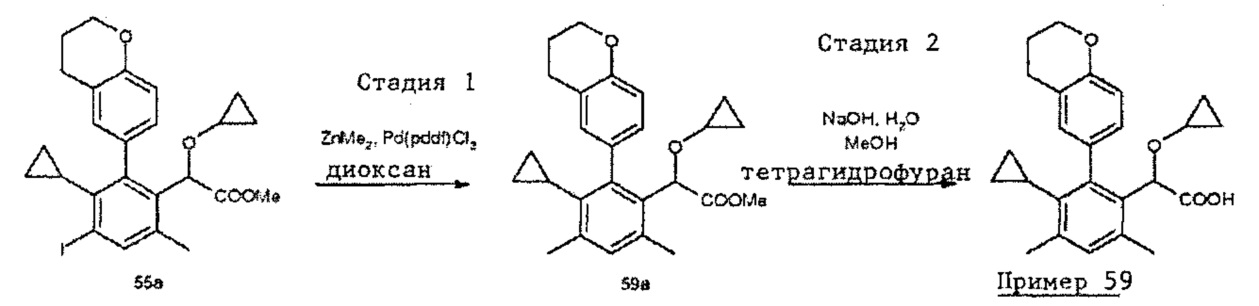
Стадия 1: Получение промежуточного соединения метилового сложного эфира (2-хроман-6-ил-3-циклопропил-4,6-диметил-фенил)-циклопропокси-уксусной кислоты (59а)
С помощью процедуры, описанной в примере 55, стадия 2, и при замене 15%» диэтилцинка в толуоле на 1,2М диметилцинка в толуоле (219 мкл, 0,263 ммоль), промежуточное соединение метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-4-йод-6-метил-фенил)-циклопропокси-уксусной кислоты (55а) (50 мг, 0,096 ммоль) преобразовали в метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-4,6-диметил-фенил)-циклопропокси-уксусной кислоты (59а) (32 мг, 0,078 ммоль, 81%).
1H ЯМР (400 МГц, CDCl3) δ 0,04-0,15 (м, 1Н), 0,18-0,49 (м, 6Н), 0,63-0,71 (м, 1Н), 1,48-1,55 (м, 1Н), 2,00-2,11 (м, 2Н), 2,30 (с, 3H), 2,42 (с, 3H), 2,71-2,86 (м, 2Н), 3,23-3,35 (м, 1Н), 3,68 и 3,70 (с, 3H), 4,21-4,28 (м, 2Н), 5,09 и 5,15 (с, 1H), 6,78-7,00 (м, 4Н).
МС m/z ([M+Na]+) 429.
Стадия 2: получение (2-хроман-6-ил-3-циклопропил-4,6-диметил-фенил)-циклопропокси-уксусной кислоты (пример 59)
С помощью процедуры, описанной в примере 23, стадии 4, метиловый сложный эфир (2-хроман-6-ил-3-циклопропил-4,6-диметил-фенил)-циклопропокси-уксусной кислоты метилового сложного эфира (59а) (30 мг, 0,074 ммоль) преобразовали в (2-хроман-6-ил-3-циклопропил-4,6-диметил-фенил)-циклопропокси-уксусную кислоту (пример 59) (28 мг, 0,071 ммоль, 90%).
1Н ЯМР (300 МГц, CD3OD) δ 0,00-0,10 (м, 1H), 0,14-0,43 (м, 6Н), 0,64-0,74 (м, 1Н), 1,49-1,59 (м, 1Н), 1,98-2,05 (м, 2Н), 2,28 (с, 3H), 2,41 (с, 3H), 2,69-2,87 (м, 2Н), 3,10-3,21 (м, 1H), 4,18-4,21 (м, 2Н), 5,09 и 5,12 (с, 1H), 6,76 (дд, J=8,3 Гц, J=1,1 Гц, 1H), 6,85-6,91 (м, 1Н), 6,93-7,02 (м, 2Н).
MC m/z ([M+Na]+) 415.
МС m/z ([М-Н]-) 391.
Пример 60: Синтез 2-[2-хроман-6-ил-5-(циклогексилметилсульфониламино)-3-циклопропил-6-метил-фенил]-2-(циклопропокси)уксусной кислоты

Стадия 1: Получение промежуточного соединения метил-2-[2-хроман-6-ил-5-(циклогексилметилсульфонил амино)-3-циклопропил-6-метил-фенил]-2-(циклопропокси) ацетата (60а)
С помощью процедуры, описанной в примере 48, стадии 14, промежуточное соединение метил 2-(5-амино-2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-(циклопропокси) ацетат (48m) (50 мг, 0,123 ммоль) преобразовали в метил 2-[2-хроман-6-ил-5-(циклогексилметил сульфониламино)-3-циклопропил-6-метил-фенил]-2-(циклопропокси) ацетат (60а) (59 мг, 0,104 ммоль, 84%), реакцией с циклогексилметансульфонил хлоридом (25 мкл, 0,156 ммоль) и после очистки методом двумя препаративными ТСХ (циклогексан/этилацетат 50/50, затем дихлорметан/этилацетат 97/3).
1H ЯМР (400 МГц, CDCl3) δ 0,23-0,39 (м, 3H), 0,49-0,65 (м, 3H), 0,69-0,75 (м, 2Н), 1,01-1,20 (3H), 1,22-1,34 (м, 3H), 1,43-1,53 (м, 1H), 1,60-1,75 (м, 3H), 1,88-2,10 (м, 4Н), 2,22 и 2,24 (с, 3H), 2,72-2,87 (м, 2Н), 2,97 (д, J=6,1 Гц, 2Н), 3,29-3,34 и 3,36-3,42 (м, 1Н), 3,67 и 3,70 (с, 3H), 4,19-4,29 (м, 2Н), 5,05 и 5,10 (с, 1H), 6,21 (с, 1H), 6,80-7,03 (м, 4Н).
МС m/z ([M+NH4]+) 585.
МС m/z ([М-Н]-) 566.
Стадия 2: получение 2-[2-хроман-6-ил-5-(циклогексилметилсульфониламино)-3-циклопропил-6-метил-фенил]-2-(циклопропокси)уксусной кислоты (пример 60)
К раствору метил 2-[2-хроман-6-ил-5-(циклогексилметилсульфониламино)-3-циклопропил-6-метил-фенил]-2-(циклопропокси)ацетата (60а) (59 мг, 0,104 ммоль) в этаноле (0,8 мл) и тетрагидрофуране (0,4 мл) добавляли 2М раствор гидроксида натрия (0,42 мл, 0,84 ммоль). Смесь нагревали при 70°C в течение 90 минут. Смесь концентрировали в вакууме. Воду (5 мл) добавляли к остатку, и экстрагировали раствор этилацетатом (5 мл). Водный слой подкисляли 1М соляной кислотой до рН 1. Смесь экстрагировали этилацетатом (2×5 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме с получением 2-[2-хроман-6-ил-5-(циклогексилметилсульфониламино)-3-циклопропил-6-метил-фенил]-2-(циклопропокси)уксусной кислоты (пример 60) (25 мг, 0,045 ммоль, 43%).
1H ЯМР (400 МГц, CDCl3) δ 0,26-0,50 (м, 4Н), 0,55-0,80 (м, 4Н), 1,00-1,36 (м, 6Н), 1,44-1,56 (м, 1Н), 1,60-1,76 (м, 3H), 1,88-2,08 (м, 4Н), 2,22 и 2,24 (с, 3H), 2,70-2,86 (м, 2Н), 2,95-3,02 (м, 2Н), 3,17-3,29 (м, 1Н), 4,20-4,30 (м, 2Н), 5,16 и 5,19 (с, 1H), 6,14 (с, 1H), 6,81 и 6,84 (д, J=7,0 Гц, 1H), 6,89-7,01 (м, 2Н), 7,03 (с, 1Н).
MC m/z ([M+NH4]+) 571.
МС m/z ([М-Н]-) 552.
Пример 61: Синтез 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] пент-4-еноевой кислоты
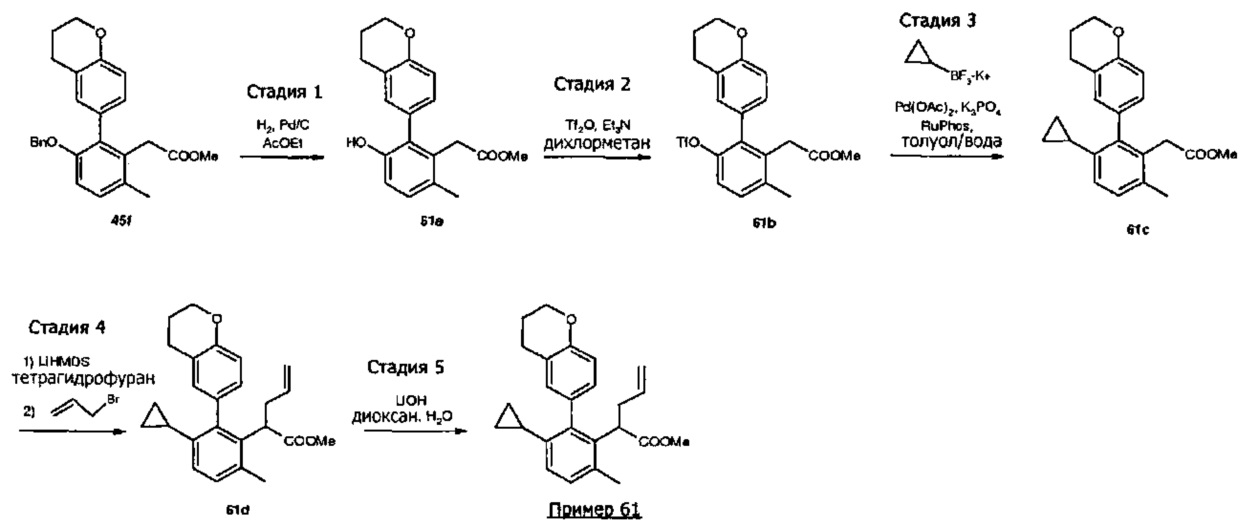
Стадия 1: Получение промежуточного соединения метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил] ацетата (61а)
С помощью процедуры, описанной в примере 1 (стадии 9), метил-2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] ацетат (45F) (100 мг, 0,248 ммоль) преобразовали в метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил] ацетат (61а) (80 мг, 0,248 ммоль, 100%) в виде бесцветного масла, используемого в следующей стадии без дополнительной очистки.
1H ЯМР (400 МГц, CDCl3) δ 2,01-2,07 (м, 2Н), 2,22 (с, 3H), 2,76-2,83 (м, 2Н), 3,43 (с, 2Н), 3,62 (с, 3H), 4,22-4,25 (м, 2Н), 4,67 (уш. с, 1Н), 6,83-6,89 (м, 2Н), 6,92-6,97 (м, 2Н), 7,06-7,09 (м, 1H).
МС m/z ([М-Н]-) 311.
Стадия 2: Получение промежуточного соединения метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил-3-(трифторметансульфонилокси) фенил] ацетата (61b)
С помощью процедуры, описанной в примере 1 (стадии 10), метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-гидрокси-6-метилфенил] ацетат (61а) (80 мг, 0,248 ммоль) преобразовали в метил 2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил-3-(трифторметансульфонилокси)фенил]ацетат (61b) (95 мг, 0,214 ммоль, 85%) в виде бесцветного масла после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20).
1H ЯМР (400 МГц, CDCl3) δ 2,00-2,07 (м, 2Н), 2,31 (с, 3H), 2,70-2,87 (м, 2Н), 3,52 (с, 2Н), 3,63 (с, 3H), 4,21-4,24 (м, 2Н), 6,81-6,90 (м, 3H), 7,17-7,24 (м, 2Н).
МС m/z ([М-Н]-) 443.
Стадия 3: Получение промежуточного соединения метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]ацетата (61с)
С помощью процедуры, описанной в примере 45 (стадия 11), промежуточное соединение метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метил-3-(трифторметансульфонилокси) фенил] ацетат (61b) (598 мг, 1,346 ммоль) преобразовали в метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] ацетат (61С) (394 мг, 1,17 ммоль, 87%) после очистки флэш-хроматографией (циклогексан/этилацетат 90/10).
1Н ЯМР (300 МГц, CDCl3) δ 0,54-0,72 (м, 4Н), 1,46-1,55 (м, 1H), 2,00-2,08 (м, 2Н), 2,26 (с, 3H), 2,76-2,80 (м, 2Н), 3,45 (д, J=1,13 Гц, 2Н), 3,61 (с, 3H), 4,21-4,24 (м, 2Н), 6,73-6,92 (м, 4Н), 7,08-7,10 (м, 1H).
MC m/z ([М+Н]+) 337.
Стадия 4: Получение промежуточного соединения метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] пент-4-еноата (61d)
С помощью процедуры, описанной в примере 45 (стадия 7), метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]ацетат (61с) (35 мг, 0,104 ммоль) преобразовали реакцией с аллилбромидом (90 л, 1,04 ммоль) в метил-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]пент-4-еноат (61d) (28,5 мг, 0,076 ммоль, 73%) в виде бесцветного масла после очистки препаративной ТСХ (циклогексан/этилацетат 92/8).
1H ЯМР (300 МГц, CDCl3) δ 0,52-0,69 (м, 4Н), 1,37-1,48 (м, 1H), 1,98-2,10 (м, 2Н), 2,22 (с, 3H), 2,25-2,36 (м, 1H), 2,75-2,90 (м, 3H), 3,60 и 3,62 (с, 3H), 3,78-,3,87 (м, 1Н), 4,21-4,25 (м, 2Н), 4,83-4,89 (м, 2Н), 5,48-5,65 (м, 1H), 6,70-6,73 (м, 1Н), 6,78-6,88 (м, 2Н), 6,91-6,97 (м, 1H), 7,02-7,05 (м, 1Н).
MC m/z ([М+Н]+) 377, ([M+Na]+) 399.
Стадия 5: Получение 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] пент-4-еноата (пример 61)
С помощью процедуры, описанной в примере 1 (стадии 12), метил 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] пент-4-еноат (61d) (29 мг, 0,076 ммоль) преобразовали в 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил] пент-4-еноевую кислоту (пример 61) (27 мг, 0,076 ммоль, 100%) в виде белого аморфного твердого вещества без дополнительной очистки.
1H ЯМР (400 МГц, CDCl3) δ 0,52-0,71(м, 4Н), 1,39-1,49 (м, 1Н), 1,98-2,09 (м, 2Н), 2,28 (с, 3H), 2,31-2,38 (м, 1H), 2,72-2,84 (м, 3H), 3,86-,3,97 (м, 1Н), 4,19-4,24 (м, 2Н), 4,84-4,89 (м, 2Н), 5,49-5,62 (м, 1Н), 6,71-6,73 (м, 1Н), 6,77-6,89 (м, 2Н), 6,92-6,98 (м, 1Н), 7,04-7,06 (м, 1Н).
MC m/z ([M+H]+) 363.
MC m/z ([M-H]-)361.
Сравнительный пример 62: Синтез 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилфенил] уксусной кислоты
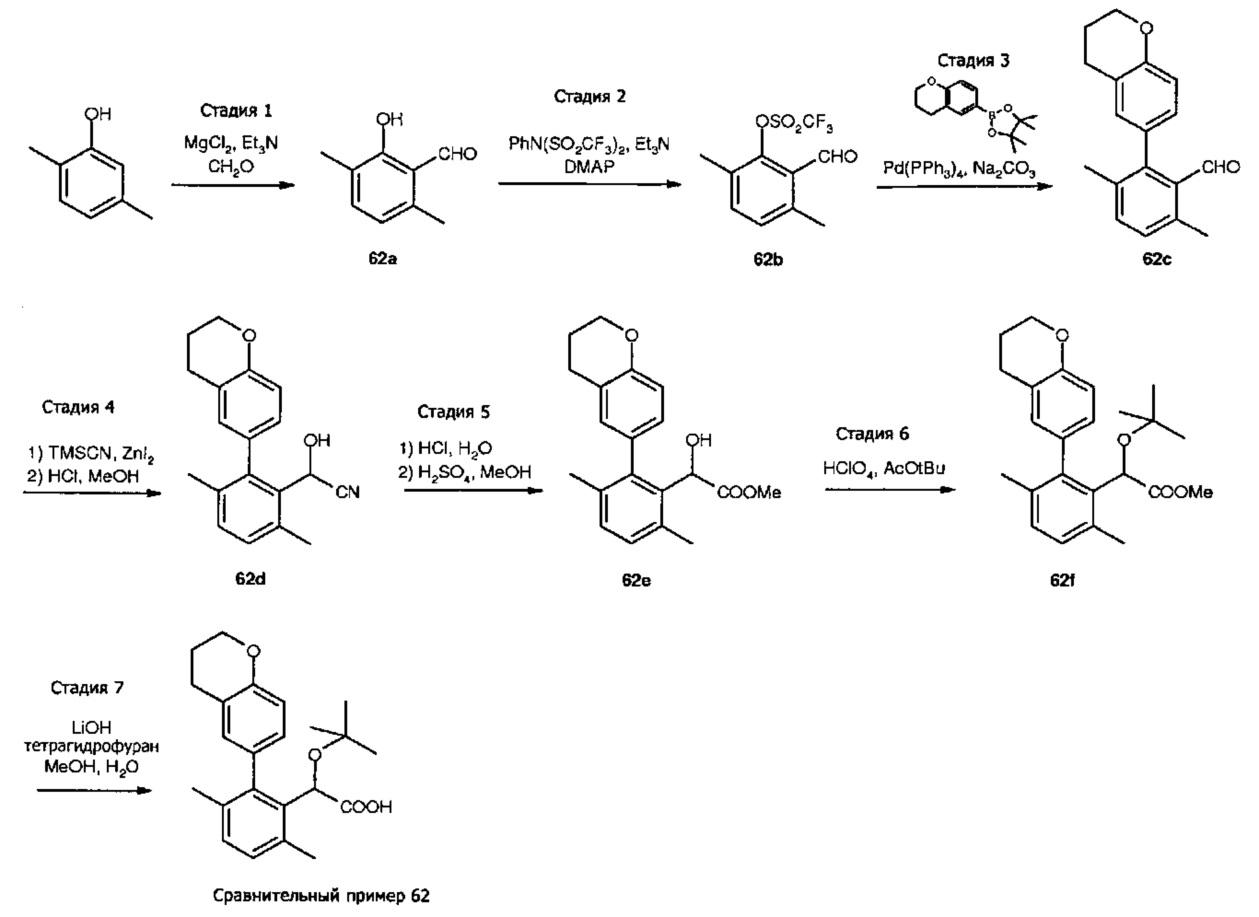
Стадия 1: Получение промежуточного соединения 3,6-диметил-2-гидроксибензальдегида (62а)
К раствору 2,5-диметилфенола (7,0 г, 57,3 ммоль) в ацетонитриле (250 мл) добавляли триэтиламин (30,1 мл, 0,212 моль) и хлорид магния (8,17 г, 86 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 15 минут перед добавлением параформальдегида (11,5 г, 0,38 моль). Смесь нагревали при 80°C в течение 20 часов. Ацетонитрил удаляли выпариванием в вакууме, и добавляли к остатку 10%-ный раствор соляной кислоты. Полученную смесь перемешивали при комнатной температуре в течение 30 минут и экстрагировали дихлорметаном (2×40 мл). Органические слои сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (дихлорметан) с получением 3,6-диметил-2-гидроксибензальдегида (62а) (3,56 г, 23,7 ммоль, 42%).
1H ЯМР (400 МГц, CDCl3) δ 2,21 (с, 3H), 2,57 (с, 3H), 6,62 (д, J=8,0 Гц, 1H), 7,24 (д, J=8,0 Гц, 1Н), 10,30 (с, 1Н), 12,18 (с, 1Н).
Стадия 2: Получение промежуточного соединения 2-формил-3,6 диметилфенилтрифторметансульфоната (62b)
К смеси 3,6-диметил-2-гидроксибензальдегида (62а) (1,0 г, 6,6 ммоль) в безводном дихлорметане (30 мл) при 0°C в атмосфере азота добавляли N-фенил-бис (трифторметансульфонимид) (3,56 г, 9,9 ммоль), 4-(диметиламино) пиридин (80 мг, 0,66 ммоль) и триэтиламин (1,9 мл, 13,2 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 5 ч. Добавляли воду (30 мл). Водный слой экстрагировали дихлорметаном (2×20 мл). Органические слои сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/дихлорметан 50/50) с получением 2-формил-3,6-диметилфенилтрифторметансульфоната (62b) (1,66 г, 5,88 ммоль, 89%).
1Н ЯМР (400 МГц, CDCl3) δ 2,42 (с, 3H), 2,60 (с, 3H), 7,21 (д, J=8,0 Гц, 1H), 7,41 (д, J=8,0 Гц, 1Н), 10,41 (с, 1Н).
Стадия 3: Получение промежуточного соединения 2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметил бензальдегида (62с)
Смесь 2-формил-3,6-диметилфенилтрифторметансульфоната (62b) (300 мг, 1,06 ммоль), карбоната натрия (449 мг, 4,2 ммоль), 6-(4,4,5,5-тетраметил-1,3, 2-диоксаборолан-2-ил) хромана (359 мг, 1,38 ммоль) и тетракис (трифенилфосфина) (62 мг, 0,053 ммоль) в смеси толуола (3 мл), этанола (1 мл) и воды (1,5 мл) облучали (200W, 80°C) в течение 1 часа. Смесь выливали в воду (10 мл). Водный слой экстрагировали этилацетатом (2×10 мл). Органический слой промывали насыщенным раствором соли (10 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат, 95/5) с получением 2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилбензальдегида (62С) (160 мг, 0,60 ммоль, 57%) в виде желтого масла.
1H ЯМР (400 МГц, CDCl3) δ 1,98-2,05 (м, 2Н), 2,10 (с, 3H), 2,58 (с, 3H), 2,78-2,82 (м, 2Н), 4,20-4,24 (м, 2Н), 6,83-6,90 (м, 3H), 7,14 (д, 7=8,0 Гц, 1Н), 7,31 (д, 7=8,0 Гц, 1Н), 9,80 (с, 1H).
Стадия 4: Получение промежуточного соединения 2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилфенил]-2-гидроксиацетонитрила (62d)
К раствору 2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилбензальдегида (62с) (800 мг, 3,00 ммоль) в безводном дихлорметане (10 мл) при 0°C в атмосфере азота последовательно добавляли йодид цинка (96 мг, 0,30 ммоль) и триметилсилилцианид (372 мг, 3,75 ммоль). Смесь перемешивали при комнатной температуре в течение ночи. Добавляли насыщенный раствор гидрокарбоната натрия (10 мл). Слои разделяли и водный слой экстрагировали дихлорметаном (10 мл). Органические слои сушили над сульфатом натрия и концентрировали в вакууме. Остаток растворяли в 3N соляной кислоты в метаноле (4 мл) и перемешивали в течение ночи при комнатной температуре, затем концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат 80/20) с получением 2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилфенил]-2-гидрокси ацетонитрила (62d) (700 мг, 2,38 ммоль, 79%) в виде желтого масла.
1H ЯМР (400 МГц, CDCl3) δ 2,00 (с, 3H), 2,02-2,06 (м, 2Н), 2,63 и 2,65 (с, 3H), 2,78-2,82 (м, 2Н), 4,23-4,26 (м, 2Н), 5,56 (д, J=1,0 Гц, 1Н), 6,80-6,88 (м, 3H), 7,15 (д, J=8,0 Гц, 1Н), 7,19 (д, 7=8,0 Гц, 1Н).
Стадия 5: Получение промежуточного соединения метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилфенил]-2-гидроксиацетата (62е)
Раствор 2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилфенил]-2-гидрокси ацетонитрила (62d) (700 мг, 2,39 ммоль) в 12N соляной кислоте (10 мл) нагревали при 80°C в течение 16 часов. Смесь экстрагировали дихлорметаном (2×10 мл). Органические слои сушили над сульфатом натрия и концентрировали в вакууме. Остаток растворяли в метаноле (20 мл), добавляли серную кислоту (0,5 мл) и смесь кипятили с обратным холодильником в течение 16 часов. Метанол выпаривали в вакууме. Остаток растворяли в дихлорметане (20 мл) и промывали насыщенным раствором гидрокарбоната натрия (20 мл), рассолом (20 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат 80/20) с получением метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилфенил]-2-гидроксиацетата (62е) (160 мг, 0,49 ммоль, 20%) в виде коричневого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 1,99 (с, 3H), 2,02-2,06 (м, 2Н), 2,29 и 2,31 (с, 3H), 2,78-2,80 (м, 2Н), 3,70 и 3,71 (с, 3H), 4,21-4,25 (м, 2Н), 5,18 (д, J=1,0 Гц, 1Н), 6,82-6,90 (м, 3H), 7,06 (д, J=8,0 Гц, 1Н), 7,13 (д, J=8,0 Гц, 1H).
Стадия 6: Получение промежуточного соединения метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилфенил] ацетата (62f)
К раствору метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилфенил]-2-гидроксиацетата (62е) (160 мг, 0,49 ммоль) в трет-бутил ацетате (10 мл) при-15°C добавляли перхлорную кислоту (1,45 мл). Смесь перемешивали при -15°C в течение 2 часов, после чего выливали в насыщенный водный раствор бикарбоната натрия (30 мл). Слои разделяли и водный слой экстрагировали этилацетатом (20 мл). Органические слои сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат, 97/3 затем (90/10) с получением метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилфенил] ацетата (62f) (16 мг, 0. 042 ммоль, 8%).
1H ЯМР (400 МГц, CDCl3) δ 0,99 (с, 9Н), 1,98 и 1,99 (с, 3H), 2,02-2,08 (м, 2Н), 2,40 (с, 3H), 2,75-2,82 (м, 2Н), 3,65 и 3,67 (с, 3H), 4,24-4,26 (м, 2Н), 5,05 и 5,07 (с, 1H), 6,79-6,90 (м, 2Н), 6,97-7,04 (м, 2Н), 7,08 (д, J=8,0 Гц, 1Н).
Стадия 7: Получение 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилфенил] уксусной кислоты
Раствор метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3,6-диметилфенил] ацетата (62f) (16 мг, 0,042 ммоль) в смеси тетрагидрофурана (2 мл), метанола (0,7 мл), воды (2 мл) и 1М раствора гидроксида лития (0,44 мл, 0,44 ммоль) перемешивали при 60°C в течение 20 часов. Добавляли 2М соляную кислоту до рН 3. Твердое вещество отфильтровывали и промывали водой с получением сравнительное соединение 62 (13 мг, 0,035 ммоль, 84%) в виде твердого вещества желтого цвета.
1Н ЯМР (400 МГц, CDCl3) δ 1,00 (с, 9Н), 2,00-2,05 (м, 5Н), 2,36 (с, 3H), 2,75-2,85 (м, 2Н), 4,22-4,24 (м, 2Н), 5,19 (с, 1H), 6,79-6,90 (м, 2Н), 7,03 (д, J=8,0 Гц, 1Н), 7,11 (д, J=8,0 Гц, 1Н), 7,18 (с, 1Н).
МС m/z ([М-Н]-) 367.
Сравнительный пример 63: Синтез 2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил)фенил1-2-(трет-бутокси)уксусной кислоты
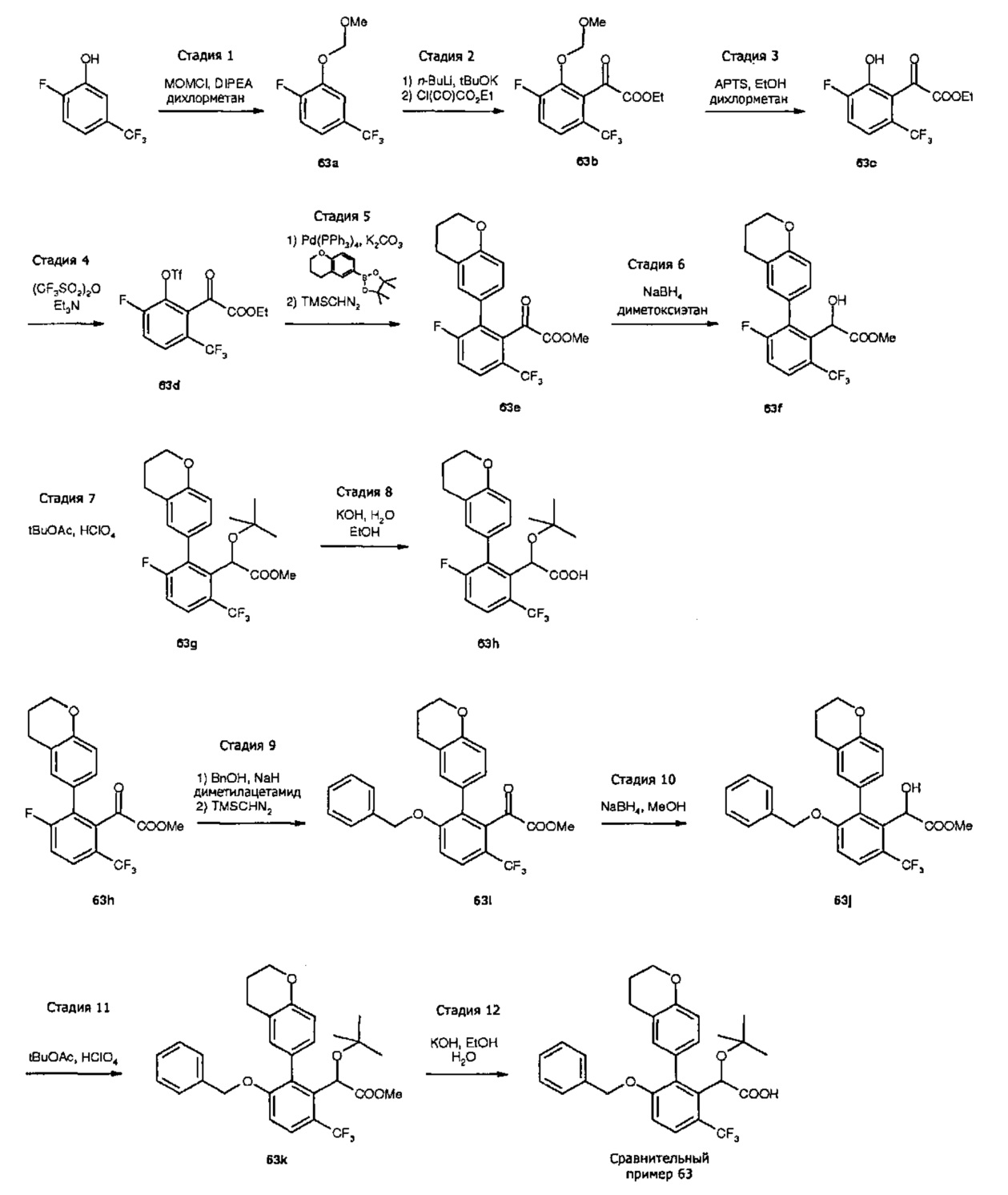
Стадия 1: получение промежуточного соединения 1-фтор-2-(метоксиметокси)-4-(трифторметил) бензола (63а)
К раствору 2-фтор-5-(трифторметил) фенола (2,0 г, 11,1 ммоль) в безводном дихлорметане (20 мл) в атмосфере азота при 0°C последовательно добавляли диизопропилэтиламин (3,87 мл, 22,2 ммоль) и хлорметилметилэфир (1,26 мл, 16,6 ммоль). Полученную смесь перемешивали при 0°C в течение 45 минут перед добавлением воды (20 мл). Слои разделяли и водную фазу экстрагировали дихлорметаном (30 мл). Объединенные органические слои промывали 2М раствором гидроксида натрия (20 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением 1-фтор-2-(метоксиметокси)-4-(трифторметил) бензола (63а) (2,49 г, 11,1 ммоль, 100%) в виде светло-желтого масла.
1H ЯМР (400 МГц, CDCl3) δ 3,53 (с, 3H), 5,25 (с, 2Н), 7,16-7,20 (м, 1Н), 7,24-7,27 (м, 1Н), 7,46 (дд, J=1,8 Гц, J=7,4 Гц, 1Н).
Стадия 2: Получение промежуточного соединения этил 2-[3-фтор-2-(метоксиметокси)-6-(трифторметил) фенил]-2-оксоацетата (63b)
В атмосфере азота 1,6М раствор n-бутиллития гексане (3,5 мл, 5,6 ммоль) и 1М раствор трет-бутоксида калия в тетрагидрофуране (5,6 мл, 5,6 ммоль) добавляли к безводному тетрагидрофурану (30 мл) при 78°C. Полученную смесь перемешивали в течение 15 минут перед добавлением по каплям раствора 1-фтор-2-(метоксиметокси)-4-(трифторметил) бензола (63а) (1,0 г, 4,46 ммоль) в тетрагидрофуране (10 мл). Смесь перемешивали при 78°C в течение 2 часов и добавляли с помощью канюли к раствору этилоксалилхлорид (1,4 мл, 9,0 ммоль) в тетрагидрофуране (20 мл) при 78°C. Смесь перемешивали при 78°C в течение 45 минут и добавляли воду (50 мл). Слои разделяли и водный слой экстрагировали этилацетатом (2×30 мл). Объединенные органические слои промывали насыщенным раствором гидрокарбоната натрия (30 мл), рассолом (30 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат 90/10) с получением этил 2-[3-фтор-2-(метоксиметокси)-6-(трифторметил) фенил]-2-оксоацетата (63b) (840 мг, 2,59 ммоль, 58%) в виде желтого масла.
1H ЯМР (300 МГц, CDCl3) δ 1,36 (т, 7=7,2 Гц, 3H), 3,45 (с, 3H), 4,38 (q, J=7,2 Гц, 2Н), 5,16 (с, 2Н), 7,28-7,34 (м, 1Н), 7,43 (дд, 7=4,4 Гц, 7=8,8 Гц, 1H).
Стадия 3: Получение промежуточного соединения этил 2-[3-фтор-2-гидрокси-6-(трифторметил) фенил]-2-оксоацетата (63с)
Раствор этил-2-[3-фтор-2-(метоксиметокси)-6-(трифторметил) фенил]-2-оксоацетата (63b) (500 мг, 1,54 ммоль) и p-толуолсульфоновой кислоты (59 мг, 0,31 ммоль) в дихлорметане (7,5 мл) и этаноле (1,5 мл) нагревали при 50°C в течение ночи. Смесь концентрировали в вакууме. Остаток очищали флэш-хроматографией на силикагеле (циклогексан/этилацетат 60/40) с получением этил 2-[3-фтор-2-гидрокси-6-(трифторметил) фенил]-2-оксоацетата (63С) (394 мг, 1,40 ммоль, 91%) в виде желтого масла.
1H ЯМР (300 МГц, CDCl3) δ 1. 38 (т, 7=7. 2 Гц, 3H), 4. 38 (q, 7=7. 2 Гц, 2Н), 6. 91 (д, J=2. 7 Гц), 7. 26-7. 35 (м, 2Н).
Стадия 4: Получение промежуточного соединения этил 2-{3-фтор-2-[(трифторметансульфонат) сульфонилокси]-6-(трифторметил) фенил}-2-оксоацетата (63d)
Раствор этил-2-[3-фтор-2-гидрокси-6-(трифторметил) фенил]-2-оксоацетат (63С) (394 мг, 1,41 ммоль) в безводном дихлорметане (5 мл) в атмосфере азота при температуре 78°C последовательно добавляли триэтиламин (0,24 мл, 1,69 ммоль) и трифликовый ангидрид (0,26 мл, 1,55 ммоль). Смесь перемешивали при 78°C в течение 45 минут перед добавлением воды (10 мл). Слои разделяли. Водный слой экстрагировали дихлорметаном (10 мл). Объединенные органические слои промывали насыщенным раствором гидрокарбоната натрия (10 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением этил 2-{3-фтор-2-[(трифторметансульфонат) сульфонилокси]-6-(трифторметил) фенил}-2-оксоацетата (63d) (548 мг, 1,32 ммоль, 94%) в виде желтого масла, который использовали без дальнейшей очистки.
1H ЯМР (300 МГц, CDCl3) δ 1,37 (т, J=7,2 Гц, 3H), 4,42 (q, J=7,2 Гц, 2Н), 7,55 (т, J=8,7 Гц), 7,78 (дд, J=4,5 Гц, J=8,7 Гц, 1Н).
Стадия 5: Получение промежуточного соединения метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-фтор-6-(трифторметил) фенил]-2-оксоацетата (63е)
Дегазированный раствор этил 2-{3-фтор-2-[(трифторметансульфонат) сульфонилокси]-6-(трифторметил) фенил}-2-оксоацетат (63d) (478 мг, 1,16 ммоль), карбонат калия (641 мг, 4,64 ммоль), 6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил) хромана (392 мг, 1,51 ммоль) и тетракис (трифенилфосфин) (134 мг, 0,12 ммоль) в диоксане (10 мл) и воде (2 мл) нагревали при 85°C в течение ночи. Добавляли воду (10 мл) и выпаривали диоксан в вакууме. Добавляли диэтиловый эфир (10 мл) и разделяли слои. Органический слой промывали насыщенным раствором гидрокарбоната натрия (10 мл). Объединенные водные слои подкисляли 37% соляной кислотой до рН 2, затем не экстрагировали диэтиловым эфиром (2×20 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток растворяли в циклогексане (5 мл) и метаноле (2,5 мл) при 0°C и добавляли 2М раствор триметилсилилдиазометана в диэтиловом эфире (4 мл, 8 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 15 минут, охлаждали при 0°C и добавляли уксусную кислоту до окончания появления пузырьков. Смесь концентрировали в вакууме. Остаток растворяли в этилацетате (10 мл), промывали насыщенным раствором гидрокарбоната натрия (10 мл), рассолом (10 мл), сушили над сульфатом натрия и концентрировали в вакууме с получением метил 2-[2-(3, 4-дигидро-2Н-1-бензопиран-6-ил)-3-фтор-6-(трифторметил) фенил]-2-оксоацетата (63Е) (343 мг, 0,90 ммоль, 77%) в виде желтого твердого вещества, которое использовали без дополнительной очистки.
1H ЯМР (400 МГц, CDCl3) δ 1,98-2,04 (м, 2Н), 2,77 (т, J=6,4 Гц, 2Н), 3,57 (с, 3H), 4,19-4,22 (м, 2Н), 6,81 (д, J=8,4 Гц, 1Н), 6,86 (д, J=1,0 Гц, 1H), 6,95 (дд, J=1,0 Гц, J=8,4 Гц, 1H), 7,35 (т, J=8,6 Гц, 1Н), 7,73 (дд, J=4,8 Гц, J=8,6 Гц, 1Н).
Стадия 6: Получение промежуточного соединения метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-фтор-6-(трифторметил) фенил]-2-гидроксиацетата (63f)
К раствору метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-фтор-6-(трифторметил) фенил]-2-оксоацетата (63е) (100 мг, 0,26 ммоль) в безводном 1,2-диметоксиэтане (2 мл) при 0°C порциями добавляли борогидрид натрия (12 мг, 0,31 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа. Добавляли воду (5 мл). 1,2-Диметоксиэтан упаривали в вакууме. Полученный раствор экстрагировали этилацетатом (2×5 мл). Органический слой промывали насыщенным солевым раствором (5 мл) и сушили над сульфатом натрия с получением метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-фтор-6-(трифторметил) фенил]-2-гидроксиацетата (63f) (84 мг, 0,22 ммоль, 83%) в виде белого твердого вещества.
1H ЯМР (300 МГц, CDCl3) δ 2,00-2,08 (м, 2Н), 2,75-2,82 (м, 2Н), 3,57 и 3,60 (с, 3H), 4,22-4,25 (м, 2Н), 5,40 (с, 1Н), 6,80-6,85 (м, 2Н), 7,06-7,10 (м, 1Н), 7,22 (т, J=8,6 Гц, 1Н), 7,73 (дд, J=5,2 Гц, J=8,6 Гц, 1H),
Стадия 7: Получение промежуточного соединения метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-фтор-6-(трифторметил)фенил]ацетата (63g)
С помощью процедуры, описанной в примере 28, стадии 5, промежуточное соединение метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-фтор-6-(трифторметил) фенил]-2-гидроксиацетат (63f) (84 мг, 0,22 ммоль) преобразовали после очистки с помощью препаративной ТСХ (циклогексан/этилацетат 80/20), в метил-2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-фтор-6-(трифторметил) фенил] ацетат (63g) (28 мг, 0,06 ммоль, 29%) в виде бесцветного масла.
1H ЯМР (400 МГц, CDCl3) δ 0,97 и 0,98 (с, 9Н), 2,03-2,07 (м, 2Н), 2,72-2,89 (м, 2Н), 3,70 (с, 3H), 4,22-4,26 (м, 2Н), 5,14 (с, 1Н), 6,83-6,87 (м, 1Н), 6,94-6,98 (м, 1Н), 7,04-7,09 (м, 1Н), 7,17 (т, J=8,6 Гц, 1H), 7,70 (дд, J=5,6 Гц, J=8,6 Гц, 1Н).
Стадия 8: Получение 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-фтор-6-(трифторметил) фенил] уксусной кислоты
Раствор метил 2-(трет-бутокси)-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-фтор-6-(трифторметил)фенил] ацетата (63g) (28 мг, 0,063 ммоль) и гидроксид калия (36 мг, 0,64 ммоль) в смеси этанола (3 мл) и воды (1 мл) перемешивали при 90°C в течение 18 часов. Этанол выпаривали в вакууме. Остаток разбавляли водой (2 мл) и подкисляли 1М соляной кислотой до рН 2 и экстрагировали диэтиловым эфиром (2×5 мл). Органический слой сушили над сульфатом натрия и концентрировали в вакууме. Остаток растирали в пентане и концентрировали в вакууме с получением искомой кислоты (63h) (21 мг, 0,049 ммоль, 78%) в виде белого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ-1,00 (с, 9Н), 2,01-2,07 (м, 2Н), 2,75-2,85 (м, 2Н), 4,23-4,26 (м, 2Н), 5,24 и 5,28 (с, 1Н), 6,86-6,99 (м, 2Н), 7,22 (т, J=8,6. Гц, 1Н), 7,35 (уш. с, 1Н), 7,72 (дд, J=5,6 Гц, J=8,6 Гц, 1Н).
MC m/z ([M-H]-) 425.
Стадия 9: Получение промежуточного соединения метил-2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил) фенил]-2-оксоацетата (63h)
К суспензии 60% гидрида натрия в масле (21 мг, 0,52 ммоль) в безводном диметилацетамиде (1 мл) при 0°C в атмосфере азота, покапельно добавляли безводный бензиловый спирт (54 мкл, 0,52 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 30 минут перед добавлением по каплям раствор метил-2-[2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-3-фтор-6-(трифторметил) фенил]-2-оксоацетата (63Н) (100 мг, 0,26 ммоль) в безводном диметилацетамиде (1 мл). Полученную смесь перемешивали в течение 1 часа при комнатной температуре, затем добавляли 60% гидрид натрия в масле (10 мг, 0,25 ммоль) и бензиловый спирт (25 мкл, 0,24 ммоль). Перемешивание поддерживали в течение 3 ч. Смесь выливали в рассол (5 мл) и 1 М соляную кислоту добавляли до рН 2. Смесь экстрагировали этилацетатом (2×10 мл). Органический слой промывали насыщенным солевым раствором (5 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток растворяли в циклогексане (3 мл) и метаноле (1,5 мл) при 0°C и добавляли 2М раствор триметилсилилдиазометана в диэтиловом эфире (0,3 мл, 0,6 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 20 минут перед добавлением нескольких капель уксусной кислоты. Остаток растворяли в этилацетате (10 мл), промывали насыщенным раствором гидрокарбоната натрия (10 мл), рассолом (10 мл), сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (циклогексан/этилацетат 75/25) с получением метил 2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-оксоацетата (63i) (76 мг, 0,16 ммоль, 62%) в виде бесцветного масла.
1H ЯМР (300 МГц, CDCl3) δ 1,97-2,05 (м, 2Н), 2,75 (т, J=6,4 Гц, 2Н), 3,55 (с, 3H), 4,19-4,22 (м, 2Н), 5,15 (с, 2Н), 6,80 (д, J=8,4 Гц, 1Н), 6,85 (д, J=2,1 Гц, 1H), 6,99 (дд, J=2,1 Гц, J=8,4 Гц, 1H), 7,11 (д, J=8,7 Гц, 1Н), 7,23-7,36 (м, 5Н), 7,65 (д, J=8,7 Гц, 1Н).
Стадия 10: Получение промежуточного соединения метил-2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил) фенил]-2-гидроксиацетата (63j)
К раствору метилового эфира 2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-оксоацетата (63i) (76 мг, 0,16 ммоль) в безводном метаноле (2 мл) при 0°C порциями добавляли борогидрид натрия (12 мг, 0,32 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 30 минут перед добавлением другой порции боргидрида натрия (12 мг, 0,32 ммоль). После 30 минут перемешивания добавляли воду (5 мл). Метанол выпаривали в вакууме. Полученный раствор экстрагировали этилацетатом (2×5 мл). Органический слой промывали насыщенным солевым раствором (5 мл) и сушили над сульфатом натрия с получением метил 2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил) фенил]-2-гидроксиацетата (63j) (76 мг, 0,16 ммоль, 100%) в виде белого твердого вещества.
1H ЯМР (300 МГц, CDCl3) δ 2,01-2,09 (м, 2Н), 2,75-2,82 (м, 2Н), 3,58 и 3,61 (с, 3H), 4,22-4,26 (м, 2Н), 5,07 (с, 2Н), 5,38 и 5,39 (с, 1H), 6,79-6,85 (м, 2Н), 6,97-7,14 (м, 4Н), 7,24-7,31 (м, 3H), 7,65 (д, J=9,0 Гц, 1Н).
Стадия 11: Получение промежуточного соединения метил 2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-(трет-бутокси)ацетата (63k)
К раствору метил 2-[3-(бензилокси)-2-(3,4-дигидро-2 Н-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-гидроксиацетат (63j) (76 мг, 0,12 ммоль) в трет-бутилового ацетата (3 мл) при 0°C добавляли перхлорную кислоту (0,4 мл). Полученную смесь перемешивали при 0°C в течение 30 минут часов, затем в течение 30 минут при комнатной температуре, после чего выливали в насыщенный водный раствор гидрокарбоната натрия (20 мл). Слои разделяли и водный слой экстрагировали этилацетатом (2×10 мл). Органические слои промывали солевым раствором, сушили над сульфатом натрия и концентрировали в вакууме. Остаток очищали с помощью препаративной ТСХ (циклогексан/этилацетат 80/20) с получением метил 2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил) фенил]-2-(трет-бутокси) ацетата (63k) (17 мг, 0,032 ммоль, 20%) в виде бесцветного масла.
1Н ЯМР (300 МГц, CDCl3) δ 0,99 и 1,36 и 1,37 (с, 9Н), 2,00-2,09 (м, 2Н), 2,70-2,85 (м, 2Н), 3,59 и 3,61 и 3,69 и 3,70 (с, 3H), 4,22-4,27 (м, 2Н), 5,00-5,41 (м, 3H), 6,81-7,32 (м, 9Н), 7,63-7,70 (м, 1H).
Стадия 12: Получение 2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил) фенил]-2-(трет-бутокси)уксусной кислоты
С помощью процедуры, описанной в примере 33, стадии 8, промежуточное соединение метил 2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-(трет-бутокси)ацетат (63k) (17 мг, 0,032 ммоль) преобразовали в 2-[3-(бензилокси)-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-(трифторметил)фенил]-2-(трет-бутокси)уксусную кислоту (сравнительный пример 63) (12 мг, 0,023 ммоль, 70%) в виде белого твердого вещества.
1H ЯМР (400 МГц, CDCl3) δ 1,01 и 1,33 и 1,35 (с, 9Н), 1,96-2,08 (м, 2Н), 2,69-2,83 (м, 2Н), 4,17-4,25 (м, 2Н), 5,00-5,12 (м, 2Н), 5,24 и 5,29 и 5,46 и 5,48 (с, 1Н), 6,72-7,06 (м, 3H), 7,10-7,16 (м, 2Н), 7,23-7,32 (м, 4Н), 7,64-7,69 (м, 1Н).
МС m/z ([М-Н]-) 513.
Противовирусная активность
Противовирусная активность, в частности против ВИЧ, соединений по изобретению оценивали по протоколу, описанному ниже.
Получение вирусного штамма штамма NL4-3 ВИЧ-1 (Adachi et al, J Virol, 1986, 59(2): 284-91).
Вирус получали согласно описанию в Lopez et al (Lopez et al, Proc Natl Acad Sci US A., 2006, 103 (40): 14947-52, трансфекцией 2×106 клеток 293T (CRL-1573, АТСС) со следующими изменениями: 6 мкг молекулярного клона провирусной ДНК NL4-3 смешивали с реактивом для трансфекции ДНК X-tremeGENE 9 из Roche, и использовали в соответствии с инструкциями изготовителя. Через двадцать четыре часа, клетки промывали и добавляли свежую среду. Через сорок восемь часов после трансфекции, клеточные супернатанты собирали, фильтровали через фильтры с порами 0,45-мкм, количественно определяли антиген р24 из HIV-1 с помощью анализа "Innotest HIV antigen mAb assay" (Ingen) в соответствии с инструкциями изготовителя, и использовали в экспериментах инфекции.
Получение соединений:
Серийные разведения тестируемых соединений готовили в полной среде RPMI из 10 мМ стоковых растворов в ДМСО, и распределяли в объеме 20 мкл в 96-луночных планшетах для тканевых культур (Costar 3917), с тем чтобы получить 0,5% конечные концентрации ДМСО в каждой лунке после добавления инфицированных клеток. Контрольные лунки также содержали 0,5% конечную концентрацию ДМСО, но не соединение.
Заражение клеток:
Клетки МТ4 (из программы "NIH AIDS Research and Reference Reagent Program") в полной среде RPMI подсчитывали (10×106 клеток на лунку в Falcon 353047 Multiwell™ 24 well) и инфицировали в течение 2 часов при 37°C, при множественности инфекции (moi) 0,0001-0,00001. Затем клетки центрифугировали в течение 3 мин/ при 3000 оборотов в минуту, и промывали два раза в 1 мл PBS для удаления вирусов, которые не вошли в клетки. Инфицированные клетки ресуспендировали в полной среде RPMI в 1,25×106 клеток/мл, и 80 мкл инфицированных клеток распределяли в каждой лунке, содержащей тестируемые соединения или в контрольных лунках. Затем планшеты инкубировали при 37°C в течение 5 дней.
Анализ, примененный для измерения ингибирования репликации ВИЧ с помощью соединений (в соответствии с Gregg S. Jones et al., Antimicrobial Agents and Chemotherapy, 2009, 53 (3): 1194-1203).
После 5 дней инкубации, уравновешивали микропланшеты до комнатной температуры в течение 30 мин., а затем добавляли в каждую лунку 50 мкл реагента CellTiter-Glo (Promega Biosciences, Inc., Мэдисон, Висконсин, США). Лизис клеток проводили при комнатной температуре в течение 10 мин. а люминесценцию считывали на Fluoroskan (Thermo Scientific).
ЕС50 или 50% эффективная концентрация, представляет собой концентрацию соединения, ведущего к 50% цитозащите в тесте жизнеспособности CellTiter-Glo® на основе клеток МТ4, инфицированных вирусом NL4-3 (таблица 1).

Полученные результаты показывают, что соединения согласно данному изобретению имеют более сильную активность, ингибирующую репликацию ВИЧ, чем соединения 62 и 63. Соединения согласно изобретению, таким образом, могут быть использованы в качестве мощных анти-ВИЧ соединений с повышенной ингибирующей активностью.
Реферат
Настоящее изобретение относится к соединениям, выбранным из группы: 2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]уксусная кислота; 2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусная кислота; 2-(трет-бутокси)-2-[3-(циклопентил)-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-(трифторметил)фенил]уксусная кислота; 2-(трет-бутокси)-2-(6-циклопропил-4’-метокси-3-метил-бифенил-2-ил]уксусная кислота; (S)-2-(трет-бутокси)-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]уксусная кислота; 2-(трет-бутокси)-2-(6-циклопропил-3,4'-диметил-бифенил-2-ил)-уксусная кислота; 2-(трет-бутокси)-2-(6-циклопропил-4'-фтор-3-метил-бифенил-2-ил)-уксусная кислота; 2-(трет-бутокси)-2-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил)-фенил]уксусная кислота; (транс-3-бициклопропил-2-ил-2-хроман-6-ил-6-метил-фенил)-трет-бутоксиуксусная кислота; 2-(трет-бутокси)-2-[3-циклопропил-2-(4,4-диметил-циклогекс-1-енил)-6-метил-фенил]уксусная кислота; 2-(2-хроман-6-ил-3-циклопропил-6-метил-фенил)-2-этоксиуксусная кислота; 2-(трет-бутокси)-2-(4'-хлор-6-циклопропил-3-метил-бифенил-2-ил)уксусная кислота; трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]-уксусная кислота; 2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиуксусная кислота; (S)-2-[3-циклопропил-2-(3,4-дигидро-2Н-1-бензопиран-6-ил)-6-метилфенил]-2-циклопропоксиуксусная кислота; трет-бутокси-[2-хроман-6-ил-6-метил-3-(1-метил-циклопропил)-фенил]-уксусная кислота; трет-бутокси-[2-хроман-6-ил-6-метил-3-(цис-2-метил-циклопропил)-фенил]-уксусная кислота; (2-хроман-6-ил-3-циклопропил-6-трифторметил-фенил)-циклопропоксиуксусная кислота; (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-пропоксиуксусная кислота; (2-хроман-6-ил-3-циклопропил-6-метил-фенил) циклопропилметоксиуксусная кислота; циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]-уксусная кислота; (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-циклобутоксиуксусная кислота; (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-этокси)-уксусная кислота; (2-хроман-6-ил-3-циклопропил-6-метил-фенил) изопропоксиуксусная кислота; циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]уксусная кислота; (S)-трет-бутокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]уксусная кислота; (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(1-метил-циклопропокси)-уксусная кислота; (S)-циклопропокси-[3-циклопропил-6-метил-2-(5-метил-хроман-6-ил) фенил]уксусная кислота; (S)-трет-бутокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]уксусная кислота; трет-бутокси-(6-хроман-6-ил-7-циклопропил-хинолин-5-ил)уксусная кислота; трет-бутокси-(2-хроман-6-ил-3-циклобутил-6-метил-фенил)уксусная кислота; (S)-циклопропокси-[3-циклопропил-2-(8-фтор-5-метил-хроман-6-ил)-6-метил-фенил]уксусная кислота; 3-циклопропил-2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]пропановая кислота; 2-[3-циклопропил-2-(3,4-дигидро-2H-1-бензопиран-6-ил)-6-метилфенил]-4-метилпентановая кислота; (2-хроман-6-ил-3-циклопропил-6-метил-фенил)-(2,2-дифтор-циклопропокси)уксусная кислота; (2-хроман-6-ил-3-циклопропил-4-метокси-6-метил-фенил)-циклопропоксиуксусная кислота; 2-(2-хроман-6-ил-3-циклопропил-5-этил-6-метил-фенил)-2-(циклопропокси)уксусная кислота и его рацемат, энантиомер, или диастереомер или фармацевтически приемлемая соль. Изобретение относится также к применению соединений при лечении или профилактике вирусных заболеваний, включая ВИЧ. 3 н. и 8 з.п. ф-лы, 1 табл., 63 пр.

Комментарии