Применение бензолсульфонил(тио)мочевин для лечения и профилактики нарушений вегетативной нервной системы и применение бензолсульфонил(тио)мочевин в сочетании с блокаторами бета-рецепторов - RU2247562C2
Код документа: RU2247562C2
Описание
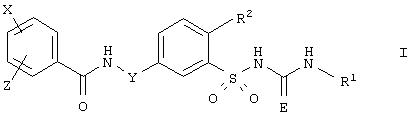
Замещенные бензолсульфонилмочевины и -тиомочевины формулы I

где R1, R2, Е, X, Y и Z имеют определенные ниже значения, обладают действием на вегетативную нервную систему. Данное изобретение относится к применению соединений формулы I для лечения и профилактики нарушений вегетативной нервной системы, в частности нарушений, связанных с блуждающим нервом, например, в случае сердечно-сосудистых заболеваний, и к их использованию для получения лекарственных средств для такого лечения и профилактики. Кроме того, изобретение относится к применению соединений формулы I в сочетании с блокаторами бета-рецепторов и к продуктам и фармацевтическим композициям, которые включают, по крайней мере, одно из соединений формулы I и, по крайней мере, одни блокатор бета-рецепторов, и к новым соединениям.
Соединения формулы I известны из US-A-5574069 (ЕР-А-612724) и US-A-5652268 (ЕР-А-727416), которые включены в данное изобретение в качестве ссылки и содержание которых представляет собой часть настоящего описания. В этих публикациях описано, что соединения формулы I ингибируют АТФ-чувствительные калиевые каналы, в частности, в сердце, и что они обладают непосредственным антиаритмическим действием за счет влияния на продолжительность потенциала действия сердца, что является результатом непосредственного воздействия на электрические свойства клеток сердечной мышцы. Благодаря данному свойству соединения формулы I могут использоваться, например, для лечения фибрилляции желудочков и других сердечных аритмий. Другие фармакологические действия соединений формулы I до сих пор описаны не были. Неожиданно, в настоящее время было установлено, что соединения формулы I также оказывают действие на периферическую и/или центральную вегетативную нервную систему. В частности, они влияют на вегетативную нервную систему и обладают стимулирующим действием на вагусную нервную систему.
В идеальном случае, существует оптимальное взаимодействие, адаптированное для конкретной ситуации, между симпатической (= стимулирующей) нервной системой и вагусной (или парасимпатической) (= подавляющей) нервной системой. Однако в случае заболевания данное взаимодействие может быть нарушено и может наблюдаться нарушение вегетативной нервной системы, то есть дисбаланс между активностью вагусной нервной системы и активностью симпатической нервной системы. Симпатовагусный дисбаланс обычно понимают как сверхактивность симпатической (= стимулирующей) нервной системы и/или сниженное функционирование вагусной (= подавляющей) нервной системы, где две части нервной системы могут оказывать взаимное влияние друг на друга. В частности, известно, что сниженное функционирование вагусной системы может приводить к сверхактивности симпатической системы. Следовательно, для исключения повреждения клеток или органов тела за счет выхода за установленные пределы биологических или биохимических процессов, которые стимулируются избыточной активностью симпатической нервной системы, в таких случаях предпринимаются попытки сбалансировать симпатовагусный дисбаланс, например, для повторного установления вагусной активности путем лечения вагусного нарушения или сниженного функционирования.
Примерами заболеваний, где подавление недопустимого симпатовагусного дисбаланса путем лечения вагусного нарушения представляется подходящим, являются органические заболевания сердца, например коронарные сердечные заболевания, сердечная недостаточность и кардиомиопатии. Нарушениями здоровья, возникающими в результате дисбаланса вегетативной нервной системы, при котором нарушение отрицательно воздействует на сердце, являются, например, ослабление сердечной активности или иногда сердечные аритмии со смертельным исходом. Значимость вегетативной нервной системы при внезапной остановки сердца в случаях сердечных заболеваний была описана, например, в P.J.Schwartz (The ATRAMI prospective study: implications for risk stratification after myocardial infarction; Cardiac Electrophysiology Review 1998, 2, 38-40) или T.Kinugawa et al. (Altered vagal and sympathetic control of heart rate in left ventricular disfunction and heart failure; Am. J.Physiol., 1995, 37, R310-316). Экспериментальные исследования с применением электрической стимуляции блуждающего сердечного нерва или при стимуляции аналогами вагусного трансмиттера ацетилхолина, например карбахолом, подтверждают защитное действие вагусной активации при сердечных аритмиях, приводящих к смертельному исходу (смотри, например, E.Vanoli et al., Vagal stimulation and prevention of sudden death in conscious dogs with a healed myocardial infarction; Circ.Res., 1991, 68(5), 1471-81).
Однако симпатовагусный дисбаланс также может возникать, например, как следствие метаболических заболеваний, например, сахарного диабета (смотри, например, A.J. Burger et al., Short- and long-term reproducibility of heart rate variability in patients with long-standing type I diabetes mellitus; Am. J. Cardiol., 1997, 80, 1198-1202). Нарушенное функционирование вагусной системы может быть также временным, например в случае кислородной недостаточности, например, сердца, вызывающей пониженную секрецию вагусных нейротрансмиттеров, например ацетилхолина.
Благодаря неожиданной способности соединений формулы I восстанавливать сниженное функционирование вагусной системы или повторно восстанавливать нормальную вагусную активность данные соединения обладают эффективной возможностью для снижения, устранения или профилактики нарушений вегетативной нервной системы и их последствий, таких как, например, вышеуказанные заболевания. Таким образом, объектом настоящего изобретения является применение бензолсульфонил(тио)мочевин формулы I

где R1 представляет водород, метил или трифторметил;
R2 представляет водород, галоген, (C1-C6)-алкил, (C1-С6)-алкокси, (C1-С6 )-алкокси-(C1-C4)-алкокси, (C1-С6)-алкокси-(C1-C4)-алкокси-(C1-C4 )-алкокси-, (C1-C6 )-алкилтио, (C1-С6)-фторалкокси или (C1-C6)-фторалкил;
Е представляет кислород или серу;
Y представляет углеводородный остаток формулы -(CR)n-, в котором остатки R3, каждый независимо, представляют водород или (C1-C2)-алкил, а n составляет 1, 2, 3 или 4;
X представляет водород, галоген или (C1-С6 )-алкил;
Z представляет галоген, нитро, (C1-C4)-алкокси или (C1-С6)-алкил;
в виде любой ее стереоизомерной формы и/или их смесей во всех соотношениях и/или их физиологически приемлемых солей для получения лекарственного средства для лечения или профилактики нарушений вегетативной нервной системы.
Алкил представляет линейный, разветвленный или циклический насыщенный углеводродный остаток. Этот термин также используется, если алкильный остаток является замещенным, как, например, в случае фторалкильных остатков, или если он присутствует в качестве заместителя в другом остатке, например в алкоксильных остатках, алкилтиольных остатках или фторалкоксильных остатках. Примерами линейных или разветвленных алкильных остатков являются метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, изопентил, неопентил, н-гексил или изогексил. Примерами циклических алкильных остатков, которые в соответствии со своей природой должны иметь по меньшей мере три атома углерода, являются циклопропил, циклобутил, циклопентил или циклогексил. Циклические алкильные остатки могут дополнительно быть связаны с одним или несколькими, например, 1, 2, 3 или 4 (C1-C4)-алкильными остатками или (C1-C4)-фторалкильными остатками, например, метильными группами или трифторметильными группами.
Примерами алкоксигруппы (= алкилокси), которая связана через атом кислорода, являются группы метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, трет-бутокси, н-пентокси, неопентокси, изогексокси, циклопропокси, циклобутокси, циклопентокси или циклогексокси. Примерами алкилтиогруппы, которая связана через атом серы, являются группы метилтио, этилтио, н-пропилтио, изопропилтио, н-бутилтио, изобутилтио, трет-бутилтио, н-пентилтио, неопентилтио, изогексилтио, циклопропилтио, циклобутилтио, циклопентилтио или циклогексилтио.
Фторалкил представляет собой алкильный остаток, в котором один или несколько атомов водорода в определенном выше алкильном остатке заменены на атомы фтора. Фторалкильный остаток может содержать один или несколько атомов фтора, например 1, 2, 3, 4, 5, 6 или 7. Как максимум, могут быть заменены все атомы водорода, то есть осуществляется перфторзамещение. Примерами фторалкилов являются фторметил, 2,2, 2-трифторэтил или пентафторэтил. Фторалкокси представляет собой определенный выше алкоксильный остаток, в котором, как проиллюстрировано выше, один или несколько атомов водорода заменены на атомы фтора.
Для всех алкильных групп в остатках алкокси-алкокси и алкокси-алкокси-алкокси, которые соединены через атом кислорода, вышеуказанные определения и иллюстрации применяются независимо друг от друга. В двухвалентных алкильных группах, содержащихся в таких фрагментах, две свободные группы, через которые эти группы связаны с соседними группами, могут находиться в любом положении, например в 1,1-положении алкильного остатка, в 1,2-положении, в 1,3-положении или 1,4-положении. Примерами таких двухвалентных остатков являются метилен, 1,2-этилен, 1,2-пропилен, 1, 3-пропилен, 1,4-бутилен или 2,2-диметил-1,3-пропилен. Предпочтительным двухвалентным остатком такого типа является 1,2-этилен. Примерами алкокси-алкокси-остатков являются метиксиметокси, 2-метоксиэтокси, 3-метоксипропокси, 4-метоксибутокси, 6-метоксигексокси, 2-этоксиэтокси, 2-этокси-2-метилэтокси, 3-этоксипропокси, 2-изобутоксиэтокси, 2-трет-бутоксиэтокси, 2-циклопропоксиэтокси, 2-циклопентоксиэтокси. Примерами алкокси-алкокси-алкокси-остатков являются (2-метоксиэтокси)метокси, 2-(2-метоксиэтокси)этокси, 2-(2-изопропоксиэтокси)этокси, 2-(н-бутоксиэтокси)этокси, 2-(2-циклопропоксиэтокси)этокси, 3-(2-метоксиэтокси)пропокси, 2-(2-метокси-2-метилэтокси)-2-метилэтокси.
Примерами галогена являются фтор, хлор, бром и иод, в частности фтор и хлор.
Настоящее изобретение включает все стереоизомерные формы соединений формулы I. Каждый из асимметрических центров, содержащихся в соединениях формулы I, например в группе Y, может, независимо, иметь S-конфигурацию или R-конфигурацию. Изобретение включает все возможные энантиомеры и диастереомеры, а также смеси двух или более стереоизомерных форм, например смеси энантиомеров/или диастереомеров. Следовательно, изобретение включает энантиомеры в энантиомерно чистой форме, как в виде левовращающего, так и в виде правовращающего антиподов, в форме рацематов и в форме смеси двух энантиомеров в любых соотношениях. Изобретение включает диастереомеры как в чистой форме, так и в форме смеси двух или более диастереомеров во всех количественных соотношениях. Также включены, например, мезо-соединения. Если имеется цис/транс изомерия, то изобретение включает как цис-форму, так и транс-форму, и смеси этих форм во всех соотношениях. Индивидуальные стереоизомеры могут быть получены, при желании, путем разделения смеси в соответствии с общепринятыми способами, например, хроматографией или кристаллизацией, или с использованием при синтезе стереохимически однородных исходных материалов. Если это является удобным, перед разделением стереоизомеров может быть осуществлено получение производных. Смесь стереоизомеров может быть разделена на стадии получения соединений формулы I или на стадии получения промежуточных продуктов в процессе синтеза. Изобретение также включает все таутомерные формы соединений формулы I.
Физиологически приемлемые соли соединений формулы I представляют собой, в частности, фармацевтически используемые соли или нетоксичные соли. Они могут содержать компоненты неорганической или органической соли (смотри также Remington Pharmaceutical Sciences (A.R.Gennaro (редактор). Mark Publishing Co., Easton PA, 17-е издание, стр.1418 (1985)). Такие соли, например, могут быть получены из соединений формулы I и подходящих неорганических или органических оснований, например соединений щелочных металлов или щелочноземельных металлов, таких как гидроксид натрия или гидроксид калия, или аммиака, или органических аминосоединений, или гидроксидов аммония. Реакции соединений формулы I с основаниями для получения солей обычно осуществляют в соответствии с обычными способами в растворителе или разбавителе. Соли, которые являются предпочтительными благодаря своей физиологической и химической стабильности, во многих случаях представляют собой соли натрия, калия, магния или кальция или соли аммония, в частности натриевые соли. Солеобразование по атому азота группы (тио)мочевины, связанной с сульфонильной группой, дает соединения формулы II

где R1, R2, Е, X, Y и Z имеют указанные выше значения, а катион М представляет, например, ион щелочного металла или эквивалент иона щелочноземельного металла, например ион натрия, калия, магния или кальция, или ион незамещенного аммония, или ион аммония, имеющий один или несколько органических заместителей. Ион аммония, представляющий М, также может быть, например, катионом, полученным протонированием аминокислоты, в частности основной аминокислоты, такой, например, как лизин или аргинин.
Настоящее изобретение также включает все сольваты соединений формулы I и их физиологически приемлемых солей, например гидраты или аддукты со спиртами, а также производные соединений формулы I и пролекарства и активные метаболиты.
В формуле I R1 предпочтительно представляет водород или метил, особенно предпочтителен метил.
Если R2 в формуле I представляет галоген, то данный остаток предпочтительно представляет хлор или фтор. Если R2 в формуле I представляет (C1 -C6)-алкил, то данный остаток предпочтительно является (C1-C4)-алкилом, в частности метилом. Если R2 в формуле I представляет (C1-С6 )-алкокси, то данный остаток предпочтительно является (C1-C4)-алкокси, в частности метокси. Если R2 в формуле I представляет (C1-С6 )-алкокси-(C1-C4)-алкокси-, то данный остаток предпочтительно является (C1-C4)-алкокси-(C1-C4)-алкокси-, в частности 2-((C1 -C4)алкокси)этокси-, особенно 2-метоксиэтокси. Если R2 в формуле I представляет (C1-C6)-алкокси-(C1-C4)-алкокси-(C1-C4)-алкокси, то данный остаток предпочтительно является (C1-C4)-алкокси-(C1-C4)-алкокси-(C1-C4)-алкокси, в частности 2-(2-((C1-C4)-алкокси)этокси)этокси-, особенно 2-(2-метоксиэтокси)этокси. Группа предпочтительных остатков R2 образована остатками (C1-C6)-алкил, (C1-C6)-алкокси и (C1-С6 )-алкокси-(C1-C4)-алкокси-, в частности остатками (C1-C6)-алкокси и (C1 -C6)-алкокси-(C1-C4)-алкокси-, особенно остатками метокси и 2-метоксиэтокси-.
Остатки R3 независимо предпочтительно представляют водород или метил, особенно предпочтительно водород, n предпочтительно равно 2 или 3. Группа Y предпочтительно содержит до четырех атомов углерода. Особенно предпочтительно Y представляет группу -(CH2 )n-, где n равно 2 или 3, или группу -CHR3-CH2-, в которой R3 представляет метил или этил, и группа CHR3 связана с NH группой. Особенно предпочтительно, когда Y представляет группу -СН2-СН2-.
Х предпочтительно представляет галоген или (С3-С6)-алкил, например фтор, хлор, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, трет-амил или 1, 1-диметилпропил, в особенности хлор или трет-бутил. Z предпочтительно представляет галоген, нитро, (C1-C4)-алкокси или (C1-C4)-алкил, особенно предпочтительно (C1-C4)-алкокси, например метокси. Остатки Х и Z могут быть в любом положении фенильного остатка, к которому они присоединены. Предпочтительно Х присоединен в 5-положении, а Z во 2-положении фенильного остатка, в каждом случае относительно группы С(=O)-NН, находящейся в 1-положении.
Если в соединениях формулы I согласно изобретению группа Е представляет кислород, то соединения представляют собой мочевины формулы Iа. Если Е представляет серу, то соединения представляют собой тиомочевины формулы Ib. Предпочтительно Е представляет серу.


Предпочтительными соединениями формулы I для применения согласно изобретению являются соединения, в которых один или несколько остатков имеют предпочтительные значения, все комбинации предпочтительных значений представляют собой объект настоящего изобретения.
Например, предпочтение отдается применению соединений формулы I, в которых R1 представляет водород, метил или трифторметил;
R2 представляет водород, галоген, (C1 -C6)-алкил, (C1-С6 )-алкокси, (C1-C4)-алкокси-(C1-C4)-алкокси-, (C1-C4)-алкокси-(C1-С4)-алкокси-(C1-C4 )-алкокси, (C1-C6)-алкилтио, (C1-C6)-фторалкокси или (C1-C6)-фторалкил;
Е представляет кислород или серу;
Y представляет углеводородный остаток формулы -(CR
X представляет галоген или (С3-C6)-алкил;
Z представляет галоген, нитро, (C1-C4)-алкокси или (C1-C4)-алкил;
в любых их стереоизомерных формах и их смесях во всех соотношениях; и/или их физиологически приемлемых солей.
Особенное предпочтение отдается применению соединений формулы I, в которых R1 представляет водород или метил;
R2 представляет водород, галоген, (C1-C6)-алкил, (C1-C6)-алкокси, (C1-C4)-алкокси-(C1 -C4)-алкокси-, (C1-C4)-алкокси-(C1-С4)-алкокси-(C1-C4)-алкокси, (C1 -C6)-алкилтио, (C1 -C6)-фторалкокси или (C1-С6)-фторалкил;
Е представляет кислород или серу;
Y представляет
углеводородный остаток формулы -(CR
X представляет галоген или (С3-С6)-алкил;
Z представляет (C1-C4)-алкокси;
в любых их стереоизомерных формах и их смесях во всех соотношениях; и/или их физиологически приемлемых солей.
Большее предпочтение также отдается применению соединений формулы I, в которых
R1 представляет водород или метил;
R2 представляет водород или галоген;
Е представляет кислород или серу;
Y
представляет углеводородный остаток формулы -(CR
X представляет галоген или (С3 -C6)-алкил;
Z представляет (C1-C4)-алкокси;
в любых их стереоизомерных формах и их смесях во всех соотношениях; и/или их физиологически приемлемых солей.
В особенности, большее предпочтение также отдается применению соединений формулы I, в которых
R1 представляет водород или метил;
R2 представляет (C1-C6)-алкилтио, (C1-С6)-фторалкокси или (C1-C6)-фторалкил;
Е представляет кислород или серу;
Y
представляет углеводородный остаток формулы -(CR
X представляет галоген или (С3-С6 )-алкил;
Z представляет (C1-C4)-алкокси;
в любых их стереоизомерных формах и их смесях во всех соотношениях; и/или их физиологически приемлемых солей.
Более конкретно предпочтение также отдается применению соединений формулы I, в которых
R1 представляет водород или метил;
R2 представляет (C1 -C6)-алкил, (C1-C6)-алкокси, (C1-C4)-алкокси-(C1-C4)-алкокси- или (C1-C4 )-алкокси-(C1 -C4)-алкокси-(C1-C4)-алкокси,
Е представляет кислород или серу;
Y представляет углеводородный остаток формулы
-(CR
X представляет галоген или (С3-С6)-алкил;
Z представляет (C1-C4) -алкокси;
в любых их стереоизомерных формах и их смесях во всех соотношениях; и/или их физиологически приемлемых солей.
Особенное предпочтение отдается применению соединений формулы I, в которых
R1 представляет водород или метил;
R2 представляет метил, метокси или 2-метоксиэтокси-;
Е представляет кислород или серу;
Y
представляет углеводородный остаток формулы -(CR
Х представляет галоген или (С3-С6)-алкил;
Z представляет (C1-C4)-алкокси;
в любых их стереоизомерных формах и их смесях во всех соотношениях; и/или их физиологически приемлемых солей.
Особое предпочтение отдается применению соединений формулы I, в которых
R1 представляет метил;
R2 представляет метил, метокси или 2-метоксиэтокси-;
Е представляет серу;
Y представляет углеводородный остаток формулы -(СН2)n, в котором n равно 2 или 3;
Х представляет галоген или (С3-С6 )-алкил;
Z представляет (C1-C4)-алкокси;
в любых их стереоизомерных формах и их смесях во всех соотношениях; и/или их физиологически приемлемых солей.
Соединения формулы I согласно изобретению могут быть получены, например, описанными ниже способами.
(а) Ароматические сульфонамиды формулы III или их соли формулы IV могут взаимодействовать с R1-замещенными изоцианатами формулы V, с получением замещенных бензолсульфонилмочевин формулы Iа:



Подходящими катионами М1 в солях формулы IV являются ионы щелочных металлов или ионы щелочноземельных металлов, такие как, например, ионы натрия или ионы калия, или ионы аммония, такие как, например, ионы тетраалкиламмония. Эквивалентно R1 -замещенным изоцианатам формулы V также возможно использовать R1-замещенные эфиры карбаминовых кислот, R1-замещенные карбамоилгалогениды или R1-замещенные мочевины.
(b) Бензолсульфонилмочевины формулы Iа, которые являются незамещенными по группе мочевины и в которых R1 представляет водород, могут быть получены взаимодействием ароматических бензолсульфонамидов формулы III или их солей формулы IV с триалкилсилилизоцианатами, такими как триметилсилилизоцианат, или с тетраизоциацианатом кремния и гидролизом первично образующихся кремний-замещенных бензолсульфонилмочевин. Кроме того, соединения формулы Iа, в которых R1 представляет водород, могут быть получены из бензолсульфонамидов формулы III или их солей формулы IV взаимодействием с галогенцианидами и гидролизом первоначально образующихся N-цианосульфонамидов минеральными кислотами при температурах от 0°С до 100°С.
(c) Бензолсульфонилмочевины формулы Iа могут быть получены из ароматических бензолсульфонамидов формулы III или их солей формулы IV с использованием R1-замещенных трихлорацетамидов формулы VI в присутствии основания в инертном растворителе в соответствии со способом, описанным в публикации Synthesis 1987, 734-735 при температуре от 25°С до 150°С.
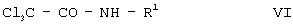
Подходящими основаниями являются, например, гидроксиды, гидриды, амиды или алкоксиды щелочных металлов или щелочноземельных металлов, такие как гидроксид натрия, гидроксид калия, гидроксид кальция, гидрид натрия, гидрид калия, гидрид кальция, амид натрия, амид калия, метоксид натрия, этоксид натрия, метоксид калия или этоксид калия. Подходящими инертными растворителями являются простые эфиры, такие как тетрагидрофуран, диоксан или диметиловый эфир этиленгликоля (ДМЭ), кетоны, такие как ацетон или бутанон, нитрилы, такие как ацетонитрил, нитросоединения, такие как нитрометан, сложные эфиры, такие как этилацетат, амиды, такие как диметилформамид (ДМФ) или N-метилпирролидон (NMP), гексаметилфосфортриамид, сульфоксиды, такие как диметилсульфоксид (ДМСО), сульфоны, такие как сульфолан, углеводороды, такие как бензол, толуол, ксилолы. Более того, смеси этих растворителей также являются подходящими.
(d) Бензолсульфонилтиомочевины формулы Ib могут быть получены из бензолсульфонамидов формулы III или их солей формулы IV и R1-замещенных изотиоцианатов формулы VII

Бензолсульфонилтиомочевины формулы Ib, которые не имеют заместителей у группы тиомочевины, и в которых R1 представляет водород, могут быть получены взаимодействием ароматических бензолсульфонамидов формулы III или их солей формулы IV с триалкилсилилизотиоцианатами, такими как триметилсилилизотиоцианат, или с тетраизоциацианатом кремния и гидролизом первоначально образующихся кремний-замещенных бензолсульфонилтиомочевин. Кроме того, соединения формулы Ib, в которых R1 представляет водород, можно получить взаимодействием ароматических бензолсульфонамидов формулы III или их солей формулы IV с бензоилизотиоцианатом и последующим взаимодействием промежуточных соединений бензоил-замещенных бензолсульфонилтиомочевин с водными минеральными кислотами. Аналогичные способы описаны в J.Med.Chem., 1992, 35, 1137-1144.
(e) Замещенные бензолсульфонилмочевины формулы Iа могут быть получены реакциями превращения бензолсульфонилтиомочевин формулы Ib. Десульфуризация, то есть замещение атома серы в соответствующей бензолсульфонилтиомочевине на атом кислорода, может быть осуществлена, например, добавлением оксидов или солей тяжелых металлов или с использованием окисляющих агентов, таких как перекись водорода, пероксид натрия или азотистая кислота. Тиомочевины также могут быть десульфурированы обработкой фосгеном или пентахлоридом фосфора. В качестве промежуточных соединений получают амидины хлормуравьиной кислоты или карбодимиды, которые могут быть превращены в соответствующие замещенные бензолсульфонилмочевины, например при гидролизе или добавлением воды.
(f) Бензолсульфонилмочевины формулы Iа могут быть получены из бензолсульфонилгалогенидов формулы VIII с использованием R1-замещенных мочевин или R1-замещенных бис(триалкилсилил)мочевин. Триалкилсилильная защитная группа может быть удалена из полученной (триалкилсилил)бензолсульфонилмочевины в соответствии со стандартными способами. Кроме того, сульфонилхлориды формулы VIII могут взаимодействовать с парабеновой кислотой, давая бензолсульфонилпарабеновые кислоты, гидролиз которых минеральными кислотами дает соответствующие бензолсульфонилмочевины формулы Iа.
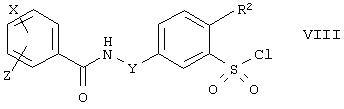
(g) Бензолсульфонилмочевины формулы 1а могут быть получены взаимодействием аминов формулы R1-NH2 с бензолсульфонилизоцианатами формулы IX. Аналогично, амины формулы R1-NH2 могут взаимодействовать с эфирами бензолсульфонилкарбаминовой кислоты, с карбамоилгалогенилами или с бензолсульфонилмочевинами формулы Iа, в которой R1представляет водород, давая соединения формулы Iа.

(h) Бензолсульфонилтиомочевины формулы Ib могут быть получены взаимодействием аминов формулы R1-NH2 с бензолсульфонилизотиоцианатами формулы X. Аналогично, амины формулы R1-NH2 могут взаимодействовать с тиоэфирами бензолсульфонилкарбаминовой кислоты или -карбамоилтиогалогенидами, давая соединения формулы Ib.

(i) Подходящим образом замещенные бензолсульфенил- или сульфинилмочевины могут быть окислены окисляющими агентами, такими как перекись водорода, пероксид натрия или азотистая кислота, давая бензолсульфонилмочевины формулы Iа.
Исходные вещества для вышеуказанных способов синтеза соединений формулы I могут быть получены известными способами, такими как описанные в литературе (например, в стандартных методиках, например, Houben-Weyl, Methoden der Organischen Chemie [Methods of Organic Chemistry], Georg Thieme Verlag, Stuttgart; Organic Reactions, John Wiley & Sons, Inc., New York; или в указанных выше патентных ссылках), и в известных или подходящих для указанных реакций условиях. Варианты способов, которые известны сами по себе, но которые не упоминались более подробно в данном описании, также могут использоваться для данных реакций. При желании, исходные вещества также могут быть получены in situ, то есть их не выделяют из реакционной смеси, а сразу подвергают дальнейшему взаимодействию.
Так, подходящим образом замещенные амины формулы XI могут быть проацилированы и подвергнуты галогенсульфонированию. В формуле XI R2 и Y имеют указанные выше значения.

Подходящие ацилирующие агенты для ацилирования аминогруппы в соединениях формулы XI преимущественно представляют собой алкиловые сложные эфиры, галогенангидриды (например, хлорангидриды или бромангидриды) или ангидриды карбоновых кислот формулы R4 -COB. Здесь R4, например, представляет собой тригалогенметильный остаток, (C1-C4)-алкильный остаток или фенильный остаток. Если R4 представляет фенильный остаток, соединение формулы R4-COB представляет собой производное бензойной кислоты. Производное бензойной кислоты может быть незамещенным или замещенным одним или двумя одинаковыми или различными группами Х и Z. Здесь Х и Z являются такими, как определено выше, то есть Х может представлять водород, (C1-C6)-алкил или галоген, а Z может представлять собой галоген, (C1-C4)-алкил, (C1-C4)-алкокси или нитрогруппу. Группа В представляет собой уходящую группу, такую как, например, галоген, (C1-C4 )-алкокси, тригалогенацетокси или (C1-C4)-алкилкарбонилокси. Примерами соединений формулы R4-COB являются уксусный ангидрид, тригалогенуксусный ангидрид, галогенангидриды уксусной кислоты, галогенангидриды тригалогенуксусной кислоты, пропионилхлорид, иэобутирилбромид и изобутирилхлорид, ангидрид муравьиной кислоты/уксусной кислоты, бензоилхлорид и замещенные производные бензойной кислоты, такие как 5-хлор-2-метоксибензоилхлорид или ангидрид 5-хлор-2-метоксибензойной кислоты или (C1 -C4)-алкил-5-хлор-2-метоксибензоат, 5-трет-бутил-2-метоксибензоилхлорид или 2,5-дифторбензоилхлорид. Синтез соединений формулы XII предпочтительно осуществляют с добавлением в качестве основания третичного амина, такого как, например, пиридин или триалкиламин, в присутствии или в отсутствие инертного растворителя, также возможно присутствие катализатора, такого как, например, диметиламинопиридин. Реакцию предпочтительно проводят при температуре в диапазоне от примерно 0°С и до 160°С, предпочтительно при температуре от 20°С и до 150°С. Ацильная группа в соединениях формулы XII может представлять собой защитную группу или в случае производных бензойной кислоты может представлять собой часть соединений формулы I. Подходящими инертными растворителями для ацилирования являются, например, простые эфиры, такие как тетрагидрофуран, диоксан, или простые эфиры гликоля, такие как монометиловый эфир этиленгликоля или моноэтиловый эфир этиленгликоля (метилгликоль или этилгликоль) или диметиловый эфир этиленгликоля, кетоны, такие как ацетон или бутанон, нитрилы, такие как ацетонитрил, нитросоединения, такие как нитрометан, сложные эфиры, такие как этилацетат, амиды, такие как ДМФ или NMP, гексаметилфосфортриамид, сульфоксиды, такие как ДМСО, хлорированные углеводороды, такие как дихлорметан, хлороформ, трихлорэтилен, 1, 2-дихлорэтан или четыреххлористый углерод, или углеводороды, такие как бензол, толуол или ксилолы. Кроме того, подходящими являются смеси данных растворителей друг с другом.
Сульфонамиды формулы XIII могут быть получены из соединений формулы XII известными способами с использованием подходящих и известных реакционных условии.

Также могут использоваться известные варианты таких реакций, которые не упомянуты более подробно в данном описании. При желании синтез может быть осуществлен в одну, две или несколько стадий. Особенно предпочтительными являются способы, в которых ацилированные амины формулы XII превращают в ароматические сульфоновые кислоты или их производные, такие, например, как галогенангидриды сульфоновых кислоты (сульфонилгалогениды), под действием электрофильных реагентов в присутствии или в отсутствие инертных растворителей при температуре от -10°С до 120°С, предпочтительно от 0°С до 100°С. Можно проводить, например, сульфонирование с использованием серных кислот или олеума, галогенсульфонирование с использованием галогенсульфоновых кислот, реакции с сульфурилгалогенидами в присутствии безводных галогенидов металлов или реакции с тионилгалогенидами в присутствии безводных галогенидов металлов с последующим окислением, осуществляемые известными способами с получением ароматических сульфонилхлоридов. Если первичные продукты реакций представляют собой сульфоновые кислоты, то они могут быть превращены в галогенангидриды сульфоновых кислот либо непосредственно, либо при обработке третичными аминами, такими как, например, пиридин или триалкиламины, или гидроксидами щелочных или щелочноземельных металлов, или реагентами, которые образуют данные основные соединения in situ, известным способом с использованием галогенангидридов кислот, таких как, например, тригалогениды фосфора, пентагалогениды фосфора, оксихлориды фосфора, тионилгалогениды или оксалилгалогениды. Превращение производных сульфоновых кислот в сульфонамиды можно осуществлять способом, известным из литературы. Предпочтение отдается взаимодействию сульфонилхлоридов в инертных растворителях при температуре от 0°С до 100°С с водным аммиаком в отсутствии или в присутствии органического растворителя. Кроме того, ароматические сульфонамиды могут быть синтезированы в соответствии с описанными в литературе способами из ацилированных аминов формулы XII взаимодействием с (щелочными или щелочноземельными) металлоорганическими реагентами в инертных растворителях в атмосфере инертного газа при температуре от -100°С до 50°С, предпочтительно от -100°С до 30°С, и диоксидом серы и последующей обработкой при нагревании амидосульфоновой кислотой.
Если ацильная группа в соединении формулы XIII выступает в качестве защитной группы аминогруппы, то данная защитная группа может быть удалена обработкой кислотами или основаниями после введения сульфонамидной группы. Расщепление водными кислотами или кислотами в инертных растворителях может приводить к образованию кислотно-аддитивной соли аминосоединения. Для удаления такой защитной группы подходящими являются, например, серная кислота, галогенводородные кислоты, такие как хлористоводородная кислота или бромистоводородная кислота, фосфорные кислоты, такие как ортофосфорная кислота или органические кислоты. Удаление амино-защитной группы в соединении формулы XIII с помощью оснований может быть осуществлено в водных или инерных растворителях. Подходящими основания являются, например, гидроксиды щелочных или щелочноземельных металлов, такие как гидроксид натрия, гидроксид калия или гидроксид кальция, или алкоксиды щелочных или щелочноземельных металлов, такие как метоксид натрия, этоксид натрия, метоксид калия или этоксид калия. Из полученных таким образом сульфонамидзамещенных аминов или их кислотно-аддитивных соединений, можно получать бензолсульфонамиды формулы III ацилированием замещенными бензойными кислотами или производными бензойной кислоты, как проиллюстрировано выше для ацилирования соединений формулы XI.
Соединения формулы I могут иметь один или несколько хиральных центров. Следовательно, при получении они могут быть получены в виде рацемата или, кроме того, при использовании оптически активных исходных веществ в оптически активной форме. Если соединения имеют два или более хиральных центра, при синтезе они могут быть получены в виде смеси рацематов, из которой в чистом виде могут быть выделены индивидуальные изомеры, например, перекристаллизацией из инертных растворителей. При желании полученные рацематы могут быть разделены известными способами, механически или химически, на энантиомеры. Так, при взаимодействии с оптически активным разделяющим агентом из рацемата могут быть получены диастереомеры. Подходящими разделящими агентами для основных соединений, например, являются оптически активные кислоты, такие как R- или R,R- или S или S,S-формы винной кислоты, дибензоилвинной кислоты, диацетилвинной кислоты, камфорсульфоновых кислот, миндальных кислот, яблочной кислоты или молочной кислоты. Кроме того для разделения можно ацилировать карбинолы с помощью хиральных ацилирующих агентов, например, R- или S-α -метилбензилизоцианата, с последующим разделением. Различные формы диастереомеров могут быть разделены известными способом, например фракционной кристаллизацией, а энантиомеры могут быть высвобождены из диастереомеров известным способом. Разделение энантиомеров, кроме того, возможно с помощью хроматографии на оптически активных стационарных фазах.
В зависимости от природы остатков R1, R2, R3, Е, X, Y и Z в отдельных случаях тот или иной из вышеуказанных способов получения соединений формулы I будет непригодным или по крайней мере потребует мер защиты активных групп. Такие случаи, которые встречаются относительно редко, легко будут распознаны специалистом в данной области, и не составит каких-либо затруднений успешно использовать в таких случаях другие описанные способы синтеза. Что касается получения соединений формулы I, применяемых согласно данному изобретению, то патенты США US-A-5574069 (ЕР-А-612724) и US-A-5652268 (ЕР-А-727416) специально включены в данное изобретение в качестве ссылки.
Благодаря своей способности снижать или устранять недостаточное функционирование вагусной нервной системы и, следовательно, вагусные нарушения и/или нарушения вегетативной нервной системы, соединения формулы I являются агентами полезными для лечения и профилактики заболеваний, которые связаны с такими сниженными функциями или нарушениями вагусной нервной системы или вызваны ими, или для лечения или профилактики тех заболеваний, где целью является увеличение или нормализация активности вагусной нервной системы. Действие соединений формулы I на вагусную нервную систему может быть продемонстрировано, например, на описанной ниже фармакологической модели на мышах. Действие также может быть продемонстрировано, например, на крысах, морских свинках, кроликах, собаках, обезьянах или свиньях.
Заболевания и патологические болезненные состояния, при которых показаны лечение или профилактика сниженной функции вагусной нервной системы или нарушения вегетативной нервной системы, уже указывались выше. Помимо общей пригодности для лечения или профилактики нарушений вегетативной нервной системы и, в частности, вагусного нарушения соединения формулы I и их физиологически приемлемые соли являются особенно подходящими для применения при заболеваниях сердечно-сосудистой системы и при сердечных заболеваниях для лечения или профилактики симпатовагусного дисбаланса или для лечения и профилактики вагусной дисфункции сердца. Примерами сердечных заболеваний и болезненных состояний такого типа являются коронарные сердечные заболевания, стенокардия, инфаркт сердца, постмиокардиальный инфаркт, сердечная недостаточность, кардиомиопатии, пересадка сердца или вагусные нарушения сердца в случае сахарного диабета. Так как соединения формулы I помимо их известного непосредственного действия на сердце, то есть помимо действия на потенциал действия клеток сердечной мышцы, также обладают косвенным действием на нервную систему сердца или на части нервной системы, которые воздействуют на сердце, они могут снижать или предотвращать нежелательные последствия для сердца, которые вызываются или опосредуются при рассматриваемых заболеваниях нервной системы. Так, можно снизить или устранить дальнейший вред здоровью, как, например, ослабление активности сердца или, иногда, сердечные аритмии с возможным летальным исходом, такие как фибрилляция желудочков. Путем устранения или снижения нарушений вегетативной нервной системы соединения формулы I и их физиологически приемлемые соли приводят к нормализации ослабленной активности сердца и предотвращению развития сердечных аритмий, которые могут привести к внезапной остановке сердца. Областями применения соединений формулы I и/или их физиологически приемлемых солей в контексте настоящего изобретения, следовательно, также являются, в частности, применение в случаях сердечной недостаточности и для профилактики сердечных аритмий, таких как фибрилляция желудочков со смертельным исходом, и для профилактики внезапной остановки сердца. Выбор соединения формулы I, имеющих, с одной стороны, подходящий профиль активности в отношении непосредственного действия на сердце (= непосредственное действие на потенциал активности клеток сердечной мышцы и, соответственно, непосредственное действие на силу сердечных сокращений и непосредственное антиаритмическое действие), а с другой стороны, воздействующих на нервы сердца, может оказаться особенно эффективным способом благоприятного влияния на сердечные заболевания с помощью соединений формулы I. В зависимости от конкретных симптомов также может оказаться выгодным использование соединений формулы I, имеющих только относительно слабое непосредственное действие на сердце и, соответственно, обладающих, например, только относительно слабым непосредственным воздействием на силу сердечных сокращений или формирование аритмий, но которые могут улучшить или нормализовать активность сердца или сердечный ритм за счет влияния на вегетативную нервную систему. Как уже отмечалось, сниженная функция вагусной системы и ее последствия также могут возникать временно, например, в случае кислородной недостаточности сердца. Следовательно, соединения формулы I также являются особенно подходящими для применения при стенокардии или коронарном сердечном заболевании, где наблюдается кислородная недостаточность. Кроме того, соединения формулы I обычно могут использоваться при нарушениях вегетативной нервной системы, в частности, вагусных нарушениях, которые возникают в результате метаболического заболевания, такого как, например, сахарный диабет.
Соединения формулы I и их физиологически приемлемые соли таким образом могут использоваться в качестве лекарственного средства для животных, предпочтительно млекопитающих и, в частности, людей, в смеси друг с другом или вместе с другими активными соединениями, в частности в форме фармацевтических препаратов (или фармацевтических композиций). Таким образом, объектом настоящего изобретения является применение соединений формулы I и/или их физиологически приемлемых солей для получения лекарственных средств для лечения или профилактики вышеуказанных синдромов. Объектом настоящего изобретения также является применение соединений формулы I и/или их физиологически приемлемых солей для лечения или профилактики вышеуказанных синдромов и объектом данного изобретения являются способы лечения или профилактики вышеуказанных синдромов, при которых эффективное количество одного или нескольких соединений формулы I и/или их физиологически приемлемых солей вводят человеку или животному-пациенту, нуждающемуся в таком лечении.
Используемые согласно изобретению лекарственные средства, которые содержат соединения формулы I и/или их физиологически приемлемые соли, можно вводить энтерально, например, перорально или ректально, например, в форме пилюль, таблеток, покрытых оболочкой таблеток, покрытых сахаром таблеток, гранул, твердых или мягких желатиновых капсул, суппозиториев, растворов, таких как водные, спиртовые или масляные растворы, соков, капель, сиропов, эмульсий или суспензий. Лекарственные средства также можно вводить парентерально, например, подкожно, внутримышечно или внутривенно, в форме растворов для инъекции или растворов для инфузии. Другие подходящие формы введения представляют собой, например, чрескожное или местное введение, например, в форме мазей, кремов, паст, лосьонов, гелей, спреев, порошков, пен, аэрозолей или растворов или применение в форме имплантатов.
Фармацевтические препаративные формы, которые могут использоваться в соответствии с данным изобретением, могут быть получены известными стандартными способами получения фармацевтических препаративных форм. С этой целью одно или несколько соединений формулы I и/или их физиологически приемлемых солей смешивают вместе с одним или несколькими твердыми или жидкими фармацевтическими наполнителями и/или вспомогательными добавками или вспомогательными веществами и, если требуется комбинированная препаративная форма, вместе с дополнительными фармацевтически активными соединениями, обладающими лекарственным или профилактическим действием, и переводят в подходящую форму для введения или дозированную форму, которая затем может использоваться в качестве лекарственного средства в медицине или ветеринарии. Фармацевтические препаративные формы включают терапевтически или профилактически эффективную дозу соединений формулы I и/или их физиологически приемлемых солей, которая обычно составляет от 0,5 до 90% по весу фармацевтической препаративной формы. Количество активного соединения формулы I и/или его физиологически приемлемых солей в фармацевтических препаративных формах обычно составляет от 0,2 до 1000 мг, предпочтительно от 0,2 мг до 500 мг, особенно предпочтительно от 1 мг до 500 мг на единичную лекарственную препаративную форму, но оно также может превышать данное количество в зависимости от природы фармацевтического препарата.
Подходящими наполнителями являются органические или неорганические вещества, которые пригодны, например, для энтерального (например, перорального) или парентерального (например, внутривенного) введения или местного введения, и которые не взаимодействуют нежелательным образом с активными соединениями, такие как, например, вода, растительные масла, спирты, такие как этанол, изопропанол или бензиловые спирты, 1,2-пропандиол, полиэтиленгликоли, триацетат глицерина, желатин, углеводы, такие как лактоза или крахмал, стеарат магния, тальк, ланолин, вазелин, ацетонитрил, диметилформамид, диметилацетамид. Также возможно применение смесей двух или более наполнителей, например, смесей двух или более растворителей, также, в частности, смесей одного или нескольких органических растворителей с водой. В качестве вспомогательных добавок или вспомогательных веществ фармацевтические препаративные формы могут содержать, например, стабилизаторы, смачивающие агенты, эмульгаторы, солюбилизаторы, загустители, соли, например, для влияния на осмотическое давление, смазывающие вещества, консерванты, красители, вкусовые агенты, ароматизаторы и/или буферные вещества. Если необходимо, они также могут включать одно или несколько дополнительных активных соединений/ например, один или несколько витаминов. Также соединения формулы I и/или их фармацевтически приемлемые соли можно подвергнуть лиофилизации и использовать полученные лиофилизаты, например, для получения композиций для инъекций. Также подходящими являются липосомные препаративные формы, в частности, для местного введения.
Доза для введения активного соединения формулы I и/или его физиологически приемлемой соли, когда ее используют согласно изобретению, зависит от индивидуального случая и, как обычно, она должна быть приспособлена к индивидуальным обстоятельствам для достижения оптимального эффекта. Следовательно, она зависит от природы и серьезности заболевания, подвергаемого лечению, а также от пола, возраста, веса и индивидуальной восприимчивости человека или животного, подвергаемого лечению, от эффективности и продолжительности действия используемых соединений, от того, представляет ли лечение острую или хроническую терапию или применяется для профилактики, или от того, вводятся ли другие активные соединения в дополнение к соединениям формулы I. Обычно интервал дозы для лечения нарушений вегетативной нервной системы для людей, составляющий приблизительно от 0,1 мг до примерно 100 мг на кг в день при введении взрослому человеку весом около 75 кг, является адекватным для достижения желаемого эффекта. Предпочтителен диапазон доз от примерно 1 мг до примерно 10 мг на кг в день (в каждом случае мг на кг веса тела). Суточная доза может вводиться в виде однократной дозы или может быть разделена на большее число единичных доз, например, две, три или четыре. Также можно осуществлять непрерывное введение. В зависимости от индивидуального поведения может потребоваться повышение или снижение исходной дневной дозы.
В дополнение к действию на вегетативную нервную систему, было также установлено, что соединения формулы I обладают синергическим действием вместе с блокаторами бета-рецепторов, которые могут преимущественно использоваться для лечения и профилактики сердечных заболеваний, таких как, например, сердечная недостаточность. Как известно, применение блокаторов бета-рецепторов в низких дозах улучшает симптомы в случаях сердечной недостаточности за счет подавления симпатической части вегетативной нервной системы, тогда как соединения формулы I восстанавливают нарушенный баланс между блуждающим и симпатическим нервами, в первую очередь, путем стимуляции блуждающего нерва. Как продемонстрировано в описанных далее экспериментах на животных, сочетание соединений формулы I и блокаторов бета-рецепторов показало супераддитивный или синергический эффект при профилактике сердечных заболеваний или нарушений сердечной деятельности, и, следовательно, такое сочетание является особенно подходящим, например, для улучшения симптомов в случаях сердечной недостаточности или для профилактики или снижения сердечной аритмии, такой как фибрилляция желудочков, или для предотвращения внезапной остановки сердца. Иначе говоря, соединения формулы I значительно улучшают действие блокаторов бета-рецепторов, например, на сердце. Таким образом, соединения формулы I являются весьма подходящими для сочетания с рецепторами бета-блокаторов.
Следовательно, объектом настоящего изобретения также является лечение и профилактика вышеуказанных сердечных заболеваний, таких как, например, сердечная недостаточность, стенокардия, инфаркт сердца, постмиокардиальный инфаркт или сердечная аритмия, такая как фибрилляция желудочков, или предотвращение внезапной остановки сердца, и лечение и профилактика нарушений вегетативной нервной системы, в частности вагусных нарушений, особенно вагусных нарушений сердца, с помощью одного или нескольких соединений формулы I и/или их физиологически приемлемых солей в сочетании с одним или несколькими блокаторами бета-рецепторов и/или их физиологически приемлемыми солями. Объектом настоящего изобретения также является применение соединений формулы I и/или их физиологически приемлемых солей для получения лекарственных средств для такого комбинированного лечения или комбинированной профилактики, и объектом изобретения являются способы такого комбинированного лечения или комбинированной профилактики. Кроме того, объектом изобретения являются комбинации одного или нескольких соединений формулы I и/или их физиологически приемлемых солей и одного или нескольких блокаторов бета-рецепторов и/или их физиологически приемлемых солей для одновременного, раздельного или последовательного применения при указанных болезненных состояниях.
При комбинированном лечении или комбинированной профилактике согласно изобретению представители двух классов активных соединений могут вводиться в виде фармацевтической композиции, где оба включены в одну и ту же фармацевтическую единичную лекарственную форму, например в таблетку, то есть в форме комбинированной фармацевтической композиции. Но точно так же они могут вводиться отдельно, например, в виде фармацевтических композиций, каждая из которых включает представители только одного из двух классов активных соединений, при этом в таком случае представители двух классов активных соединений могут быть введены одновременно, непосредственно один за другим, или последовательно, включая, например, введение после относительно большого промежутка времени. Все данные типы введения включены в объем настоящего изобретения. В зависимости от характеристик индивидуального случая, может быть более успешно введение представителей двух классов активных соединений в форме комбинированной фармацевтической композиции, в которой они присутствуют вместе в фиксированном соотношении в одной и той же фармацевтической препаративной форме, или введение их по отдельности в форме более чем одной, например двух отдельных фармацевтических композиций, в каждой из которых содержится, например, только одно активное соединение. В последнем случае отдельные фармацевтические композиции, образующие набор из частей, могут находиться вместе запакованные в подходящей первичной упаковке, находящейся в общей внешней упаковке, при желании вместе с инструкциями для применения, относящимися к комбинированному применению согласно изобретению, или отдельные фармацевтические композиции могут находиться в отдельных внешних упаковках, при желании, вместе с инструкциями, в каждой упаковке, для применения, указывающими на комбинированное применение согласно изобретению. Все такие продукты и формы выпуска, подходящие для применения согласно изобретению, включены в объем настоящего изобретения.
Соответственно, объектом настоящего изобретения также являются продукты или изделия, включающие одно или несколько соединений формулы I

в которой R1 представляет водород, метил или трифторметил;
R2 представляет водород, галоген, (C1-C6)-алкил, (C1-С6)-алкокси, (C1 -C6 )-алкокси-(C1-C4)-алкокси, (C1-C6)-алкокси-(C1-C4)-алкокси-(C1-C4)-алкокси-, (C1-С6 )-алкилтио, (C1-С6)-фторалкокси или (C1-C6)-фторалкил;
Е представляет кислород или серу;
Y представляет
углеводородный
остаток формулы -(CR
X представляет водород, галоген или (C1-С6)-алкил;
Z представляет галоген, нитро, (C1-C4)-алкокси или (C1-C6)-алкил;
в виде любой их стереоизомерной формы и их смесях во всех соотношениях; и/или их физиологически приемлемые соли в сочетании с или в качестве комбинированного препарата с одним или несколькими блокаторами бета-рецепторов и/или их физиологически приемлемыми солями, для одновременного, раздельного или последовательного применения для лечения или профилактики нарушений вегетативной нервной системы, вагусных нарушений, вагусных нарушений сердца или для лечения или профилактики вышеуказанных заболеваний, в частности, сердечных заболеваний, таких как, например, сердечная недостаточность, стенокардия, инфаркт сердца, постмиокардиальный инфаркт или сердечная аритмия, такая как фибрилляция желудочков, или для предотвращения внезапной остановки сердца.
Объектом настоящего изобретения, в частности, являются указанные фармацевтические комбинированные препаративные формы, в которых представители двух классов активных соединений присутствуют вместе в одной и той же фармацевтической композиции, то есть фармацевтические препаративные формы, которые включают одно или несколько соединений формулы I

в которой R1 представляет водород, метил или трифторметил;
R2 представляет водород, галоген, (C1-С6)-алкил, (C1-C6)-алкокси, (C1-С6)-алкокси-(C1-C4)-алкокси, (C1-С6)-алкокси-(C1-C4)-алкокси-(C1 -C4)-алкокси-, (C1-С6)-алкилтио, (C1-С6)-фторалкокси или (C1-С6)-фторалкил;
Е представляет кислород или серу;
Y представляет
углеводородный остаток формулы -(CR
X представляет водород, галоген или (C1-C6)-алкил;
Z представляет галоген, нитро, (C1-C4)-алкокси или (C1-C6)-алкил;
в любой их стереоизомерной форме и их смесях во всех соотношениях; и/или их физиологически приемлемые соли, один или несколько блокаторов бета-рецепторов и/или их физиологически приемлемые соли и физиологически приемлемый носитель, то есть один или несколько физиологически приемлемых наполнителей и/или вспомогательных добавок или вспомогательных веществ.
Вся вышеизложенная информация, например, касающаяся наполнителей, вспомогательных веществ и вспомогательных добавок для фармацевтических форм, таких как таблетки, покрытые сахаром таблетки, капсулы или растворы, и их получения, возможных форм введения, таких как пероральное или внутривенное ведение, применения в медицине или ветеринарии, или касательно заболеваний, которые могут подвергаться лечению и т.д., применимо соответственно для описанных выше продуктов и фармацевтических композиций. В данном контексте блокаторы бета-рецепторов следует рассматривать в качестве примера дополнительных фармацевтически активных соединений, которые, в дополнение к соединениям формулы I, могут присутствовать в описанных выше фармацевтических композициях. Все данные, приведенные выше для самих соединений формулы I, также применимы, соответственно, для соединений формулы I, содержащихся в фармацевтических композициях, например, описание индивидуальных остатков и групп, предпочтительных соединений формулы I или их солей. В фармацевтических композициях, содержащих соединения формулы I вместе с блокаторами бета-рецепторов в одной и той же фармацевтической препаративной форме, также могут присутствовать соли, которые образованы соединениями данных классов друг с другом, то есть соли, которые содержат блокатор бета-рецепторов (или блокаторы бета-рецепторов), представляющие собой органические аминосоединения, в протонированной форме в качестве катиона и соединение (или соединения) формулы I в депротонированной форме в качестве аниона. Соотношение по весу соединений формулы I и блокаторов бета-рецепторов в фармацевтических композициях, в которых оба активных соединения присутствуют в одной и той же фармацевтической препаративной форме, обычно составляет от 500 до 0,02, предпочтительно от 100 до 0,1, частей по весу соединения (или соединений) формулы I на часть по весу блокаторв бета-рецепторов (или блокаторов бета-рецепторов). Например, соотношение по весу может составлять примерно 35 частей по весу соединения формулы I на часть по весу блокатора бета-рецептора, или оно может составлять примерно 1 часть по весу соединения формулы I на часть по весу блокатора бета-рецепторов.
Как фармацевтические композиции для применения в соответствии с изобретением, которые не содержат какого-либо блокатора бета-рецепторов, так и продукты и фармацевтические композиции согласно изобретению, которые содержат блокаторы бета-рецепторов, в качестве соединений формулы I предпочтительно содержат одно или несколько соединений, выбранных из группы, включающей
1-[[5-[2-(5-хлор-2-метоксибензамидо)этил]-2-
метоксифенил]сульфонил]-3-метилтио-мочевину,
1-[[5-[2-(5-хлор-2-метоксибензамидо)этил]-2-
(2-метоксиэтокси)-фенил]сульфонил]-3-метилтиомочевину и
1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-2-
метоксифенил]сульфонил]-3-метилтиомочевину и/или их физиологически приемлемые соли, предпочтительно соли данных соединений, которые представляют собой соли натрия.
Подходящими блокаторами бета-рецепторов для комбинационного лечения и комбинационной профилактики согласно изобретению и для продуктов и фармацевтических композиций согласно изобретению являются, например, следующие соединения: алпренолол, окспренолол, пенбутолол, бупранолол, метопролол, бетаксолол, атенолол, ацебутолол, метипранолол, пропранолол, надолол, пиндолол, тимолол, соталол, карведилол, бисопролол, целипролол, каразолол, талинолол, мепиндолол, картеолол, тертатолол, бопиндолол. Предпочтительными блокаторами бета-рецепторов являются препанолол, атенолол, бисопролол и карведилол.
При комбинации соединений формулы I с блокаторами бета-рецепторов обычно для достижения желаемого действия требуются меньшие дозы соединений формулы I и/или блокаторов бета-рецепторов, чем в том случае, когда используются соединения только одного класса активных соединений. Предпочтительная доза соединений формулы I в сочетании с блокатором бета-рецепторов составляет от примерно 0,3 мг до примерно 15 мг, предпочтительно от примерно 1 мг до примерно 10 мг на кг веса тела в день. Доза блокатора бета-рецепторов при сочетании зависит от дозы, обычной для отдельного рассматриваемого соединения. Предпочтение отдается применению наиболее низкой обычной дозы рассматриваемого соединения и рассматриваемой области применения. Вышеуказанные данные, касающиеся дозы соединений формулы I, используемых в качестве индивидуальных активных соединений, применимы, соответственно, для комбинированного применения согласно изобретению, например, в отношении необходимой адаптации дозы к обстоятельствам индивидуального случая или для разделения дозы на индивидуальные дозы.
Благодаря их действию на вегетативную нервную систему соединения формулы I и их соли могут использоваться не только в качестве фармацевтически активных соединений в медицине и ветеринарии, но также и в качестве научного инструмента или в качестве вспомогательного вещества для биохимических исследований, в которых предполагается подобное действие, а также в диагностических целях, например, для диагностики in vitro образцов клеток или образцов тканей.
Настоящее изобретение также включает неописанные до настоящего момента соединения формулы I per se и их физиологически приемлемые соли. В частности, изобретение включает новые вещества, per se описанные в рабочих примерах, например, 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)пропил]-2-метоксифенил]сульфонил]-3-метилтиомочевину и ее физиологически приемлемые соли, включая натриевую соль, применение новых соединений в качестве фармацевтически активных соединений и фармацевтические композиции, которые включают одно или несколько данных соединений и физиологически приемлемый носитель, то есть один или несколько физиологически приемлемых наполнителей и/или добавок или вспомогательных веществ. Вышеприведенные сведения применимы, соответственно, для фармацевтических композиций, наполнителей и вспомогательных веществ.
Помимо соединений, описанных в рабочих примерах в соответствии с данным изобретением, также могут, например, использоваться перечисленные ниже соединения формулы I.
(1) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)пропил]-
2-метоксифенил]сульфонил]-3-метилтиомочевина
(2) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)бутил]-
2-метоксифенил]сульфонил]-3-метилтиомочевина
(3) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-этоксифенил]сульфонил]-3-метилтиомочевина
(4) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-пропоксифенил]сульфонил]-3-метилтиомочевина
(5) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-этилфенил]сульфонил]-3-метилтиомочевина
(6) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-метилфенил]сульфонил]-3-метилтиомочевина
(7) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-изопропилфенил]сульфонил]-3-метилтиомочевина
(8) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-бромфенил]сульфонил]-3-метилтиомочевина
(9) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-фторфенил]сульфонил]-3-метилтиомочевина
(10) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-трифторметоксифенил]сульфонил]-3-метилтиомочевина
(11) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо) этил] -
2-метилтиофенил]сульфонил]-3-метилтиомочевина
(12) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-этилтиофенил]сульфонил]-3-метилтиомочевина
(13) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-изопропоксифенил]сульфонил]-3-метилтиомочевина
(14) 1-[[5-[(5-трет-бутил-2-метоксибензамидо)метил]-
2-метоксифенил]сульфонил]-3-метилтиомочевина
(15) 1-[[5-[2-(5-(1,1-диметилпропил)-2-метоксибензамидо)
этил]-2-метоксифенил]сульфонил]-3-метилтиомочевина
(16) 1-[[5-[2-(5-втор-бутил-2-метоксибензамидо)этил]-2-
метоксифенил]сульфонил]-3-метилтиомочевина
(17) 1-[[5-[2-(5-н-бутил-2-метоксибензамидо)этил]-2-
метоксифенил]сульфонил]-3-метилтиомочевина
(18) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)пропил]-
2-метоксифенил]сульфонил]-3-метилмочевина
(19) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)бутил]-2-
метоксифенил]сульфонил]-3-метилмочевина
(20) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-2-
этоксифенил]сульфонил]-3-метилмочевина
(21) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-2-
пропоксифенил]сульфонил]-3-метилмочевина
(22) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-2-
этилфенил]сульфонил]-3-метилмочевина
(23) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-метилфенил]сульфонил]-3-метилмочевина
(24) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-2-
изопропилфенил]сульфонил]-3-метилтиомочевина
(25) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-бромфенил]сульфонил]-3-метилмочевина
(26) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-фторфенил]сульфонил]-3-метилмочевина
(27) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-трифторметоксифенил]сульфонил]-3-метилмочевина
(28) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-метилтиофенил]сульфонил]-3-метилмочевина
(29) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-этилтиофенил]сульфонил]-3-метилмочевина
(30) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-изопропоксифенил]сульфонил]-3-метилмочевина
(31) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-метоксифенил]сульфонил]-3-метилмочевина
(32) 1-[[5-[2-(5-(1,1-диметилпропил)-2-метоксибензамидо)
этил]-2-метоксифенил]сульфонил]-3-метилмочевина
(33) 1-[[5-[2-(5-втор-бутил-2-метоксибензамидо)этил]
-2-метоксифенил]сульфонил]-3-метилмочевина
(34) 1-[[5-[2-(5-н-бутил-2-метоксибензамидо)этил]-
2-метоксифенил]сульфонил]-3-метилмочевина
(35) 1-[[5-[2-(5-изопропил-2-метоксибензамидо)этил]
-2-метоксифенил]сульфонил]-3-метилмочевина
Примеры
Пример 1. 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]
-2-метоксифенил]сульфонил]-3-метилтиомочевина
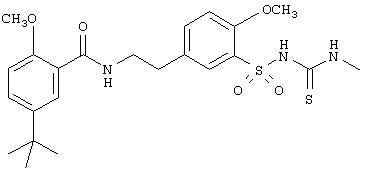
0,286 г (0,68 ммоль) 5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-2-метоксибензолсульфонамида растворяли в 7,5 мл диметилформамида и, после добавления 0,1 г карбоната калия, смешивали с 0,68 мл 1М раствора метилизотиоцианата в диметилформамиде и перемешивали при 80°С в течение 2 часов. Охлажденную реакционную смесь выливали в разбавленную водную соляную кислоту и осадок отфильтровывали в вакууме и сушили на воздухе. Продукт имеет температуру плавления 201-203°С.
Получение исходного вещества
1,51 г (10,0 ммоль) 2-(4-метоксифенил)этиламина растворяли в 40 мл пиридина и смешивали со взятым на кончике шпателя 4-диметиламинопиридином и затем с раствором 2,15 г(10,5 ммоль) 5-трет-бутил-2-метоксибензоилхлорида. После полного превращения 2-(4-метоксифенил)этиламина реакционную смесь выливали в холодную разбавленную соляную кислоту и выпавший в осадок продукт отфильтровывали в вакууме и сушили, получая 5-трет-бутил-2-метокси-N-[2-(4-метоксифенил)этил]бензамид в виде бесцветного твердого вещества. Бензамид вводили в холодную хлорсульфоновую кислоту. После полного превращения бензамида реакционную смесь выливали на лед и фильтровали в вакууме и осадок растворяли в ацетоне. Данный раствор смешивали с избытком концентрированного водного аммиака. После ослабления экзотермической реакции смесь концентрировали до трети ее первоначального объема и осадок отфильтровывали в вакууме. Получали 5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-2-метокси-бензолсульфонамид в виде бесцветных кристаллов с температурой плавления 165-168°С.
Пример 2.
1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-2-метоксифенил]сульфонил]-3-метилмочевина

0,252 г (0,5 ммоль) 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-
2-метоксифенил]сульфонил]-3-метилтиомочевины (пример 1) растворяли в 2,5 мл 2н водного раствора гидроксида натрия и смешивали при охлаждении льдом с 0,25 мл 30%-ной перекиси водорода. Раствор перемешивали при комнатной температуре в течение 24 часов и выливали в смесь лед-вода и 2н соляная кислота. Сушка на воздухе давала белые кристаллы с температурой плавления 209-212°С.
Пример 3. 1-[[5-[2-(5-Изопропил-2-метоксибензамидо)этил]-
2-метоксифенил]сульфонил]-3-метилтиомочевина
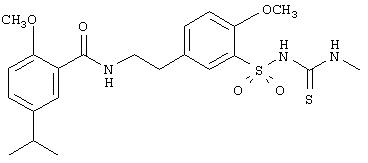
Продукт получали по методике примера 1. Получены белые кристаллы с температурой плавления 177-179°С.
Пример 4. 1-[[5-[2-(5-Хлор-2-метоксибензамидо)этил]-
2-метоксифенил]сульфонил]-3-метилтиомочевина

Получение данного вещества описано в патенте US-A-5574069 (ЕР-А-612724), который включен в данное описание в качестве ссылки и содержание которого, касающееся получения этого вещества, является частью настоящего описания.
Пример 5. 1-[[5-[2-(5-Хлор-2-метоксибензамидо)этил]-2-
(2-метоксиэтокси)фенил]сульфонил]-3-метилтиомочевина

Получение данного вещества описано в патенте US-A-5652268 (ЕР-А-727416), который включен в данное описание в качестве ссылки и содержание которого, касающееся получения этого вещества, является частью настоящего описания.
Пример 6. 1-[[5-[2-(5-трет-Бутил-2-метоксибензамидо)этил]-
2-(2-метоксиэтокси)фенил]сульфонил]-3-метилтиомочевина

Продукт получали по методике примера 1, с использованием 5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-2-(2-метоксиэтокси)-бензолсульфонамида. Вместо карбоната калия в качестве основания в реакции с метилизотиоцианатом использовали гидрид натрия аналогично примеру 5. Продукт имел температуру плавления 61°С.
Пример 7. Натриевая соль 1-[[5-[2-(5-трет-бутил-
2-метокси-бензамидо)этил]-2-метоксифенил]сульфонил]-3-метилтиомочевины

4,93 г 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-2-
метоксифенил]сульфонил]-3-метилтиомочевины (пример 1) вводили в 32 мл метанола, в котором предварительно было растворено 0,425 г твердого гидроксида натрия. После 15 минут перемешивания к прозрачному раствору добавляли 125 мл метилтрет-бутилового эфира. Натриевой соли давали возможность кристаллизоваться при перемешивании и затем отфильтровывали в вакууме, промывали небольшим количеством холодного метил-трет-бутилового эфира и сушили. Выход 5,09 г. Температура плавления: 235-250°С (разложение). ИК-спектр (Nujol): 1646,1 см-1.
Примеры фармацевтических препаративных форм.
Пример А: Таблетка
Для получения таблеток 1-[[5-[2-(5-хлор-2-метоксибензамидо)этил]-2-
метоксифенил]сульфонил]-3-метилтиомочевину (пример 4), низкозамещенную гидроксипропилцеллюлозу (Н-ГПЦ), поливинилпирролидон (Povidone 25) и кросс-кармелозу натрия (поперечно-сшитая натрийкарбоксиметилцеллюлоза) гранулировали, увлажняя водой. Гранулы пропускали через 1-1,5 мм сито, смешивали с кросс-кармелозой натрия и стеаратом магния и прессовали в таблетки.
Количество на таблетку:
Соединение примера 4 600 мг
Н-ГПЦ 95 мг
Povidone 25 15 мг
Кросс-кармелоза натрия 60 мг
Стеарат магния 20 мг
Пример В. Водный раствор для внутривенного введения
Для получения 10 мл раствора, содержащего 10 мг активного соединения на мл, 100 мг натриевой соли 1-[[5-[2-(5-хлор-2-метоксибензамидо)этил]-2-
метоксифенил]сульфонил]-3-метилтиомочевины (смотри пример 4) растворяли в 10 мл изотонического (0,9% концентрация) раствора хлорида натрия.
Фармакологические исследования 1. Действие на нарушения, связанные с блуждающим нервом
Вещества исследовали с использованием модели фибрилляции желудочков у мышей, индуцированной хлороформом (смотри J.W. Lawson, Antiarrthmic activity of some isoquinoline derivatives determined by a rapid screening procedure in the mouse; J. Pharmacol. Exp. Ther., 1968, 160, 22-31). Тестируемое вещество растворяли в смеси диметилсульфоксида (ДМСО) и 10%-ного раствора бикарбоната натрия и вводили внутрибрюшинно (i.p.). Через 30 минут мышь анестезировали хлороформом в химическом стакане. Как только при глубокой анестезии наблюдалась остановка дыхания (стадия токсичной анестезии), грудную клетку животного вскрывали с использованием пары ножниц и исследовали визуально биение сердца. Здесь можно, на первый взгляд, определить бьется ли сердце, фибриллирует или остановилось. Вызываемая хлороформом остановка дыхания, ведет, через абсолютную аноксию (недостаток кислорода), в сочетании с прямым стимулирующим действием хлороформа на симпатическую нервную систему к мощной стимуляции симпатической части вегетативной нервной системы, что, в свою очередь, в сочетании с недостатком энергии в сердце, вызываемой отсутствием кислорода, приводит к аритмии со смертельным исходом, т.е. к фибрилляции желудочков. Такая токсичная анестезия хлороформом приводила к фибрилляции желудочков в 100% случаев мышей, не подвергавшихся обработке (контроль). Процент мышей с фибрилляцией желудочков в индивидуальных исследуемых группах представлен в таблице 1.
Результаты показывают, что соединения формулы I существенно снижают появление фибрилляций желудочков. Наблюдаемое влияние атропина, классического блокатора мускариновых (вагусных) рецепторов вегетативной нервной системы, который блокирует действие вагусного трансмиттера ацетилхолина на рецепторном уровне, указывает на механизм действия. Атропин снижает или предотвращает защитное действие соединений формулы I. Такая нейтрализация атропином защитного действия веществ однозначно указывает на вагусный механизм действия. Аналогичное защитное действие может быть вызвано вагусной стимуляцией с использованием карбахола, более стабильного аналога природного вагусного трансмиттера ацетилхолина, где защитное действие также может ингибироваться атропином. Кроме того, ингибитор холинэстеразы физостигмин, который снижает разложение ацетилхолина, имитирует защитное действие соединений формулы I, действие которое также нейтрализовалось атропином.
2. Действие комбинации соединений формулы I с блокаторами бета-рецепторов
На той же самой животной модели, которая описана ранее в эксперименте “Действие на вагусные нарушения”, было продемонстрировано, что комбинированная обработка блокаторами бета-рецепторов и соединениями формулы I приводит к благоприятному синергическому действию. Активные соединения вводили i.v. (внутривенно) или i.p. (внутрибрюшинно). В одном эксперименте 10 мг/кг натриевой соли 1-[[5-[2-(5-хлор-2-метоксибензамидо)этил]-2-метоксифенил]сульфонил]-3-метилтиомочевины (пример 4; растворена в ДМСО/10%-ный раствор бикарбоната натрия) объединяли с 0,3 мг/кг пропанолола (растворенного в дистиллированной воде), являющегося обычным бета-блокатором. Было установлено, что комбинированная предварительная обработка животных двумя веществами давала синергическое действие. Статистически значимым образом доля фибрилляций могла быть дополнительно снижена в сравнении с индивидуальными веществами. Для сравнения использовали в 10 раз более высокую дозу пропанолола, составляющую 3 мг/кг). Показано, что 0,3 мг/кг пропанолола в сочетании с 10 мг/кг натриевой соли 1-[[5-[2-(5-хлор-2-метоксибензамидо)этил]-2-метоксифенил]сульфонил]-3-метилтиомочевины оказывает примерно такое же действие, как и 3 мг/кг пропанолола, или же даже превышает действие дозы пропанолола 3 мг/кг. В другом эксперименте аналогичным образом комбинировали 3 мг/кг 1-[[5-[2-(5-трет-бутил-2-метоксибензамидо)этил]-2-метоксифенил]сульфонил]-3-метилтиомочевины (пример 1) и 3 мг/кг атенолола. Результаты комбинированной обработки представлены в таблице 2.
Реферат
Настоящее изобретение относится к области медицины, а именно к применению замещенных бензолсульфонилмочевин и -тиомочевин формулы (I) для получения лекарственного средства для лечения и профилактики нарушений вегетативной нервной системы, в частности нарушений, связанных с блуждающим нервом, например, в случае сердечнососудистых заболеваний, и к применению соединений формулы (I) в сочетании с блокаторами бета-рецепторов и к продуктам и фармацевтическим композициям, которые включают, по крайней мере, одно из соединений формулы (I) и, по крайней мере, один блокатор бета-рецепторов, а также к новым соединениям. Изобретение обеспечивает повышение эффективности лечения. 5 н. и 17 з.п. ф-лы, 2 табл.

Формула




Комментарии