миллион (6,8-11,6 и 1,25-1,55 ммоля на литр) соответственно. После
268 час электролиза АКН превратился в АДН с избирательностью 87%-88%;пад5е
ние напряжения в ванне стабильно 4 В, в отходах газа водород составляет
в среднем 6,5 об.% и в конце 10 об.% Пример 9. В непрерывном про
.цессе используют жидкую электролитическую среду, содержащую: а) около
99% водного раствора с растворенными в нем 1,4-1,8% АКН, .1,2% АДН, 10-11%
смеси ионов этилтрибутиламмония и боратов натрия,полученных нейтрализа
цией 2%-ного раствора ортоборной кис лоты до рН 8,5,и б) около 1% дисперги
рованной, но нерастворенной органичес кой фазы,содержащей 27-32% АКН,53-59
АДН,6-7% побочных продуктов димериза ций АКН и 8% воды. Смесь при пр пускают со скоростью 1,22 м/сек
через неразделеннук) на камеры ванну с анодом из углеродистой стали 1020
(по стандарту Американского института стали и железа) , отделеиньал зазором
в 0,178 см от кадмиевого катода (не менее 99,9% кадмия), и подвергают электролизу при плотности тока
18,5 А/дм поверхности анода или катода . Органическую фазу, содержащую
АДН, побочные продукты и tfenpopearHровавшйй АКН, отделяют от электролитической среды и добавляют свежий
АКН, после чего среду рециркулируют и повторно подвергают электролизу в вышеуказанных условиях. Сначала
среда содержит растворенные в ней железо и кадмий в концентрациях около 6 4 хвора) отфильтровывают через фильтр
мембранного типа со стандартной пористостью порядка 0,45 ммк. Анализ
отфильтрованных твердых частиц и сравнёние количеств нерастворенных железа
и кадмия в этих частицах с количествами растворенного железа и кадмия
в среде или предварительно отобранной пробе показали, что железо и
кадмий, перешедшие в среду в процессе электролиза, оставались нерастворенными
за все время их нахождения в среде,подвергаемой электролизу, и
присутствуют по крайней мере в следующем количестве: Fe - 95,8%; Cd 99
,7%; Fe и Cd вместе - 96,9%. За 241 час электролиза АКН превратился
АДН с избирательностью 89,3% и 89,0%; падение напряжения в ванне стабильно
3,9 В, в отходах газа водород составляет в среднем 4,5 об.% и в конце - 5,4 об.%.
Пример 10. Электролитическую среду, аналогичную описанной в примере
9, подвергают электролизу в течение 362 час в тех же условиях. Анод
и катод корродируют со средней скоростью (примерно 0,058 и 0,017 см/год,
соответственно) так, что в среду переходит 0,137 ммоля железа и
0,019 ммоля кадмия, а количество железа и кадмия, перешедших в раствор
за первые 28 час электролиза/ превышает 4,9 ммоля йа литр среды. После
первых 130 час непрофильтрованную средуподвергают анализу. Концентрации
железа и кадмия, растворенных в растворе стабильны в пределах 506- ГГГГО - -ГЛГГ
димеризации AKH и 8% воды. Среда цир кулировала при со скоростью
1,22 м/сек через неразделенную на ка меры ванну с анодом из углеродистой
сташи 1020 (по стандарту Американско го института стали и железа), отде
.ленным зазором в 0,178 см от кадмие вого катода (не менее 9,9% кадмия),
подвергают электролизу при плотности тока 18,5 А/дм поверхности анодаили
катода. Органическую фазу, содержащую АДН, побочные продукты и непрореагировавший АКН, отделяют от
электролитической среды и добавляют свежий АКН, после чего среду рециркулируют
через ванну и повторно подвергают электролизу в вышеуказанных условиях. Сначала среда содержит
растворенные в ней железо и кадмий в концентрациях около 11,1 и 2,4 ммоля
на литр, соответственно, ТНЭДТА и продукты его деструкции в таких пропорциях
, что в среде можно было растворить дополнительно 4,9 ммоля на питр железа и/или кадмия,но не более
ё среду добавляют 0,495 ммоля/фар ГНЭДТА,из систе№л отбирают 12г раствора
,заменяя его водой,содержащей t растворенные в ней ионы этилтрибутил
аммония и ортофосфаты и бораты натри 6 количестве, достаточном для поддер
жания концентраций этих компонентов в растворе на вышеуказанных уровнях и сохранения общего объема среды
постоянным. В этих условиях анод и катод корродируют со средней скоростью (примерно 0,.055 и 0,010 см/го
соответственно ) так, что в раствор переходит 0,132 ммоля/фар. железа и
0,012 ммоля/фар. кадмия, а количест во железа и кадмия, перешедших в сре ду в ходе электролиза за первые
31 час, превышает 4,9 ммоля на литр раствора. Концентрации растворенного
железа и кадмия стабильны в предела 455-570 и 94-178 частей на миллион
(8,8-11,0 и 0,9-1,7 ммоля на литр) соответственно. После 198 час ..цирку
лирующую среду анализируют без филь рации. Концентрацию нерастворенного
тяжелого металла (в основном железа в среде, подвергаемой электролизу, поддерживают 1,9 ммоля на литр, а
железо и кадмий, перешедшие в среду в процессе электролиза, оставались
нерастворенными за все время их нахождения в среде, и присутствовали по крайней мере в следующих количес
вах: Fe - 84,3; Cd почти 100%; в сумме - 87,5%. За 429 час электроли
за в этих условиях АКН превращают в АДН с избирательностью 86% и 87,1%,
падение напряжения в ванне стабильн в пределах 3,84-3,9 В, в отходах га за водород составляет в среднем
10 об.% и в конце - 16,4 об.%. Органическую фазу, содержащую АД побочные продукты и непрореагировав
ший АКН, отделяют от среды и добавляют свежий АКН, после чего среду . еЦиркулируют и подвергают повторному электролиза в вышеописанных условиях
. Сначала электролитическая срет да содержит растворенные в ней железо и кащмий в кокцентрациях 9,0 и
2,75 ммоля на литр, соответственно, ТНЭДТА и продукты его деструкции в
таких пропорциях, что в среде можно было дополнительно растворить 5,25 ммоля на литр железа и/или кадмия
, но не более этого количества. В среду добавляют 0,4 ммоля/фар.
ТНЭДТА, из системы отбирают 12 г раствора , заменяют водой, содержащей
растворенные в ней ионы этилтрибутиламмония и ортофосфаты и бораты натрия
в количестве, достаточном для поддержания концентраций этих компонентов
на вышеуказанных уровнях и сохранения общего объема среды постоянным.
В этих условиях анод и катод корродируют со средней скоростью (примерно
0,050 и 0,007 см/год, соответственно ) , так что в среду переходит
0,12 ммоля/фар. железа и 0,008 ммоля/ 7,Фар. кадмия, а количество железа и.
кадмия, перешедших в среду в ходе электролиза за первые 37 час электролиза
, превышает 5,25 ммоля на литр среды. Концентрации железа и кадмия,
1растворенных в растворе, поддерживают стабильными в пределах 465-490 и
170-288 частей на миллион (9-9,5 и 1,6-2,8 ммоля на лигр) соответственно
, а железо и кадмий, перешедшие в среду в ходе элеКтролиза, оставались
в количестве, указанном.в примере 3. За 69 час электролиза в этих
условиях АКН превращают в АДН с избирательностью 87,8%, падение напряжения
в ванне стабильно и составляет 4 В, в отходах газа водород составляет в среднем 3-4 об.% и в конце
б об.%. Пример 13. В непрерывном процессе используют жидкую электролити- ,
ческую среду, содержащую а) 85,9 - 87,5% водного раствора с растворенными
в нем 1,4-1., 6% :КН, 1,2 АДН, О , 8-2 , 5 Ю моля на литр ионов этилтрибутиламмония
, 9,6-9,9% смеси ортофосфатов и боратов натрия, полученных нейтрализацией 2%-ного раствора
ортоборной кислоты до рН 8,5-9/ и б) 12,5-14,1% диспергированной, но
нерастворенной, органической фазы, содержащей 26-29% АКН, 54-59% АДН,
7-9% побочных продуктов димеризаглии АКН и 8% водал. Среда циркулировала
при 55°С со скоростью 1,158 м/сек через неразделенную на камеры ванну
с анодом из углеродистой стали 1020 (по стандарту Американского института
стали и железа), отделенным зазором в 0,228 см от кадмиевого катода
(не менее 99,9% кадмия), и подвергалась электролизу при плотности тока
20 А/дм поверхности анода или катода. Органическую фазу, содержащую АДН,
побочные продукты и непрореагировавг ший AKH, отделяют от среды и добавля
ют свежий АКН, после чего среду рециркулируют и подвергают повторному электролизу в вышеуказанных условиях
Сначала электролитическая среда содержит растворенные в ней железо и кадмий в концентрациях 6,9 и
1,25 ммоля на литр, соответственно, и продукты его деструкции в таких пропорциях, что в среде можно
Йыло дополнительно растворить 2,75 ммоля на литр железа и/или кадмия , но не более.. В среду добавляют
0,475 ммоля/фар. ТНЭДТА, из систелол отбирают около 10 г раствора, заменяют водой, содержащей растворенные
в ней ионы этилтрибутиламмония и ортофосфаты и бораты натрия в количест
ве, достаточном для поддержания концентраций этих компонентов в растворе
на вышеуказанных уровнях и сохранения общего объема среды постоянным В этих условиях и без фильтрации
циркулирующей среды анод и катод корродируют со средней скоростью (пр
мерно 0,05 и 0,012 см/год, соответ ственно ) так, что в среду переходит
о,012 ммоля/фар. железа и 0,014ммоля /Фар. кадмия, а количество железа и
кадмия, перешедших в раствор в ходе электролиза за первые 102 час превы
.шает 2,75 ммоля на литр среды. Концентрации железа и кадмия, растворен
ных в растворе, стабильны в пределах 350-550 и 130-165 частей на миллион
(6,8-11,6 и 1,25-1,55 ммоля на литр) соответственно. Концентрация нерастворенного
тяжелого метсшла (в основ ном железа) в среде/ подвергаемой электролизу, остается ниже 2 ммолей
ча литр, по крайне мере за 90% време Редактор Р.Антонова
Заказ 1886/59 Тираж 512Подписное
ЦНИИПИ Государственного комитета СССР
по делам изобретений и открытий И3035, Москва, Ж-35, Раушская наб., д. 4/5
Филиал ППП Патент, г.Ужгород/ ул.Проектная,4 Составитель Ю.Лапицкий
Техред с.Г1игай , Корректор Е.Папп 416 ни, и в среднем составляла,1,7 ммоля
на литр, а железо и кадмий, перешедшие в раствор в ходе электролиза, остаются растворенными за все время
их нахождения в среде в том же количестве , что в примере 3. За 268 час
электролиза в этих условиях АКН превращают в АДН с избирательностью
87% и 88%, падение напряжения в ванне стабильно и составляет 4 В, в отходах
газа водород составляет в среднем около 6,5 об.% и в конце 10,4 об.%. Формула изобретения
Способ получения адипонитрила путем электролиза водной эмульсии акрилонитрила
, щелочной соли полифосфорной кислоты и соли четвертичного аммония в ванне с катодом и анодом
при плотности тока от 1 до 20 А/дм при нагревании, отличающийс я тем, что, с целью увеличения
выхода целевого продукта и уменьшения коррозии электродов, в водную эмуль-.
сию добавляют хелатообразующее соединение , выбранное из группы соединений
, таких как натриевая соль этилендиаминтетрауксусной кислоты или натриевая
соль оксиэтилендиаминтриуксусной кислоты в количестве от 0,1 до,.
Ь, 5 м.моля/фарадей применяемого тока. Источники информации, принятые во внимание при экспертизе
1. Патент США 3193475,кл. 204-73, 1965. 2. Патент США 3193476,кл. 204-73/
1965. 3. Патент ФРГ 1928748, кл. С 07 С, 1969.
Date : 19/06/2001
Number of pages : 2
Previous document : SU 659084
Next document : SU 659086
о П и с А Н и Ё ИЗОБРЕТЕНИЯ Государственный комите СССР
по делам изобретении и открытий Карл Йосеф Боосен
(71) Заявитель
(54) СПОСОБ ПОЛУЧЕНИЯ оО-ЦИАН- -ГАЛОГЕНАЦЕТОУКСУСПЫХ
Предлагается способ получения производных с, -циан-;с-галогенацетоуксусных
кислот, которые находят применение в качестве промежуточных продуктов для получения фармацевтических
препаратов, пестицидов, красцтелей .
Известен способ получения алкиловых
эфиров об-циан-у-галогенацетоуксусных кислот, заключающийся в том, что натриевую соль низшего алкиловог
эфира циануксусной сислоты подвергаю взаимодействию с галогенангидридом
галогензамещенной уксусной кислоты в среде растворителя 1. Процесс осуществляют
, в течение 3ч, выход целевых продуктов составляет 55-60% от теоретического.
Однако обработка реакционной массы для вьщеления целевого продукта сложна г так как включает многократну
экстракцию растворителем вследствие наличия в реакционной массе побочных продуктов.
Целью изобретения являются увеличение выхода целевого продукта и интенсификация процесса.
659085
(11)
(51) М. Кл.
С 07 с 121/34 С 07 С 120/00
(53) УДК 547, 339.2, .07(088..8)
Иностранец
(ФРГ)
Иностранная фирма
Лонца АГ
(Швейцария)
СОЕДИНЕНИЙ
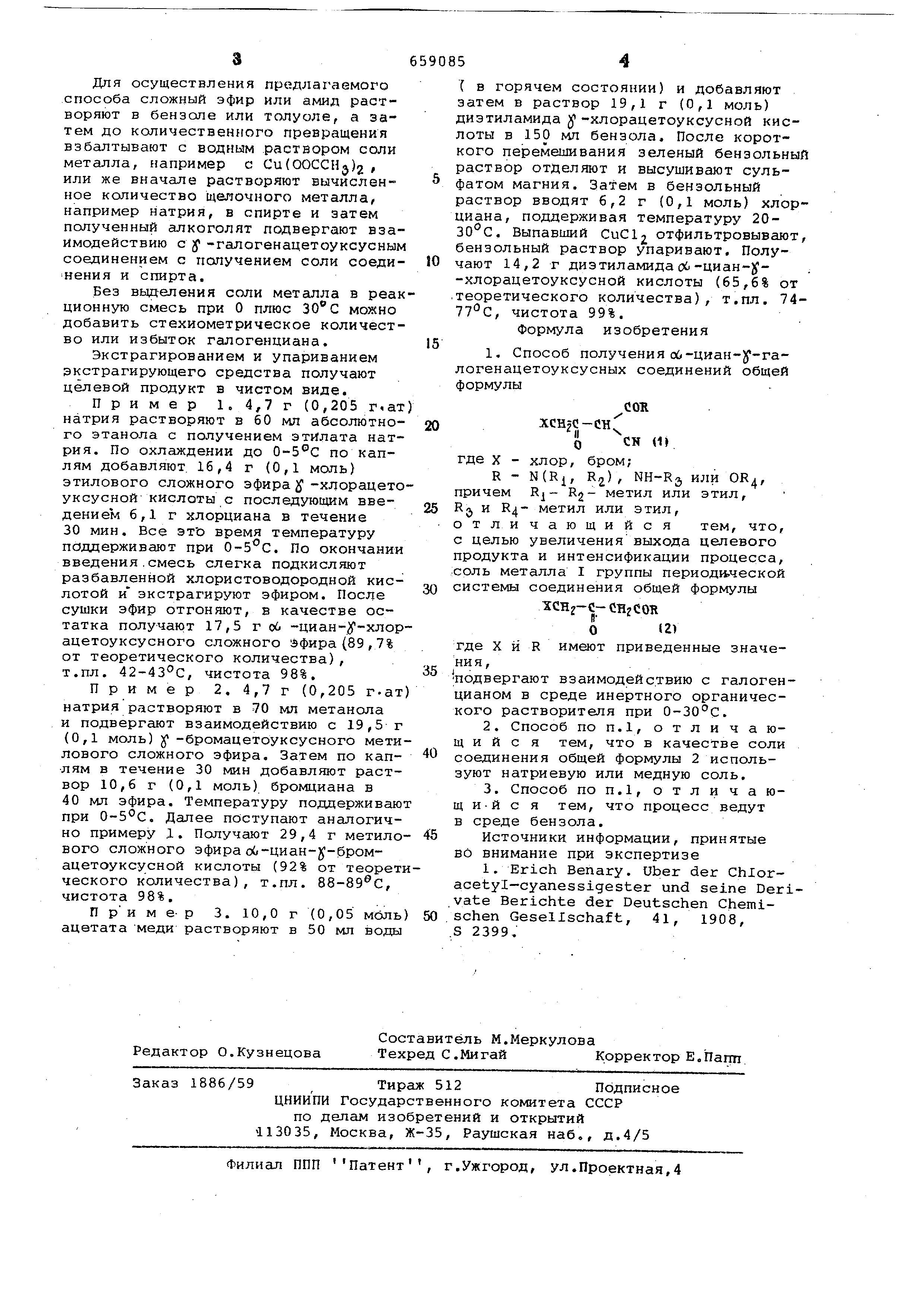
Предлагаемый способ получения о6-циан-у-галогенацетоуксусных соединений общей формулы
СОИ
сн;
оСН (1)
где X - хлор, бром;..
R - N(R,R2), NH-R,, или O-R,
причем Ej - 2 метил или этил.
К,
R 4 . - метил ИЛИ ЭТИЛ,
отличается тем, что соль металла Г
группы периодической системы и соединения общей формулы
ICHz-C- CHjOOR
О tZ)
где X и R имеют приведенные значения,
подвергают взаимодействию с галогенцианом в среде инертного органического
растворителя при 0-30°С.
Обычно в качестве соли соединения
общей формулы 2 используют натриевую или медную саль и процесс ведут в среде бензола.
В случае, если в формуле I R ), процесс ведут при 20-30°С.
ПредлагаеьйлП способ обеспечивает выход целевого продукта до 89,7% при
продолжительности самой реакции 0,5 ч. (61) Дополнительный к патенту
(22)Заявлено 12,05.77 (21)2478467/23-04 ( 23)Приоритет -(32) 13.0 5.7 6 (31) 6017/76(33) Швейцария
Опубликовано 25.04.79. Бюллетень № 15 Дата опубликования описания 25.04.79 К ПАТЕНТУ Для осуществления лредлагаемого
способа сложный эфир или амид растворяют в бензоле или толуоле, а затем до количественного превращения
взбалтывают с водным раствором соли металла, например с Cu(OOCCHj)2, или же вначале растворяют вычисленное
количество щелочного металла, например натрия, в спирте и затем
полученный алкоголят подвергают взаимодействию с у-галогенацетоуксусным
соединением с получением соли соеди нения и спирта. Без выделения соли металла в реак
ционную смесь при О плюс можно добавить стехиометрическое количество или избыток галогенциана.
Экстрагированием и упариванием экстрагирующего средства получают целевой продукт в чистом виде.
Пример 1. 4,7г (0,205 г.ат натрия растворяют в 60 мл абсолютного этанола с получением этйлата натрия
. По охлаждении до по каплям добавляют 16,4 г (0,1 моль} этилового сложного эфира -хлорацето
уксусной кислоты с последующим внедением 6,1 г хлорциана в течение 30 мин. Все это время температуру
поддерживают при 0-5°С. По окончании введения.смесь слегка подкисляют
разбавленной хлористоводородной кислотой и экстрагируют эфиром. После
сушки эфир отгоняют, в качестве остатка получают 17,5 г об -циан-у-хлор
ацетоуксусного сложного Эфира (89,7% от теоретического количества), т.пл. 42-43 С, чистота 98%.
Пример 2. 4,7 г (0,205 г-ат натрия растворяют в 0 мл метанола и подвергают взаимодействию с 19,5 г
(0,1 моль) у -бромацетоуксусного мети лового сложного эфира. Затем по каплям
в течение 30 мин добавляют раствор 10,6 г (0,1 моль) бромциана в 40 мл эфира. Температуру поддерживаю
при 0-5°С. Далее поступают аналогично примеру 1. Получают 29,4 г метило
вого сложного эфира о(.-циан- -бромацетоуксусной кислоты (92% от теорет
ческого количества), т.пл. 88-89 С, чистота 98%. П ри м е-р 3. 10,0 г (0,05 моль
ацетата меди растворяют в 50 мл воды Т в горячем состоянии) и добавляют
затем в раствор 19,1 г (0,1 моль) диэтиламида у-хлорацетоуксусной кислоты
в 150 мл бензола. После короткого перемешивания зеленый бензольный
раствор отделяют и высушивают сульфатом магния. Затем в бензольный
раствор вводят 6,2 г (0,1 моль) хлорциана , поддерживая температуру 2030°С
. Выпавший CuCl отфильтровывают, бензольный раствор упаривают. Получают
14,2 г диэтиламидаоб-Циaн-y-xлopaцeтoyкcycнoй кислоты (65,6% от
теоретического количества), т.пл. 7477°С , чистота 99%. Формула изобретения
1.Способ получения об-циан-у-галогенацетоуксусных соединений общей формулы
хснгс-сн( о где X - хлор, бром;
R - Ы(К|, Rj), NH-Rj или ОН, причем RJ- Rg- метил или этил, Rj, и R4- метил или этил,
отличающийся тем, что, с целью увеличения выхода целевого продукта и интенсификации процесса,
;соль металла I группы периоди-ческой системы соединения общей формулы хснг-с-снгсок
где X и R имеют приведенные значения ,. ,
подвергают взаимодействию с галогенцианом в среде инертного органического растворителя при О-ЗО-С.
2.Способ ПОП.1, отличающийся тем, что в качестве соли соединения общей формулы 2 используют
натриевую или медную соль. 3.Способ ПОП.1, отличаюод и-й с я тем, что процесс ведут
в среде бензола. Источники информации, принятые ВО внимание при экспертизе
1. Erich Benary. Uber der Chloracetyl-cyanessigester und seine Derivate
Berichte der Deutschen Chemischen Gesellschaft, 41, 1908, .S 2399,











Комментарии