Новые полииминокетоальдегиды - RU2749376C1
Код документа: RU2749376C1
Чертежи
Описание
Настоящее изобретение относится к новому биологически активному соединению полииминокетоальдегида и его антибактериальным свойствам, фармацевтическим препаратам, содержащим соединения поли(имино)кетоальдегидов в качестве действующего вещества, их применению для лечения бактериальных инфекций и способу их получения.
Согласно данному изобретению полииминокетоальдегиды представляют собой соединения общей формулы I:

Химическое название соединения с общей формулой (I) представляет собой 1-аминотетратриаконтилгеникоза-20-он-21-аль, а его международное непатентованное название - вароксицилин (Varoxicilin).
Для получения соединения, которое представляет собой объект настоящего изобретения выполняли биотрансформацию субстрата ферментами, причем субстрат может быть выбран из группы, состоящей из глицина, L-аланина, L-валина, L-лейцина, 2-аминомасляной кислоты, 4-метилтреонина и D-аланина, при этом фермент выбирают из группы, состоящей из синтетазы циклоспорина А (далее в данном документе: cAs), нерибосомной пептидсинтетазы 1 (далее в данном документе: NRPS1).
Биотрансформация происходит на следующих этапах:
1. Активация субстрата с образованием аденилата (АТФ) при аденилировании домена фермента.
2. Эстерификация активированной аминокислоты тиольной группой пантотенового остатка, посредством чего аминоацильная группа перемещается в домен тиолирования фермента и создается соответствующий тиоэфир.
3. В кислой среде эстерифицированные аминокислоты соединяются вместе способом, который приводит к созданию соединения общей формулы I.
Следовательно, независимо от используемого субстрата, аденилатный домен образует ациладенилатный субстрат, в котором используется ковалентная связь для соединения субстрата молекулы с фосфопантетеином, образуя таким образом поперечно сшитый тиоэфир, который далее превращается в соединение общей формулы I, в частности 1-аминотетратриаконтилгеникоза-20-он-21-аль в форме белого осадка, который очищают поочередным промыванием кислотой и водой.
Для того, чтобы получить соединение общей формулы I, кроме субстратов и ферментов также требуется аденозинтрифосфат (АТФ) и кофакторы. В качестве кофактора использовали Mg2+. В реакционную смесь прибавляют кофактор в форме сульфата магния с элементами ряда галогенов или халькогенов. Кроме того, также требуется буфер для суспензии ферментов, который используют для поддерживания уровня рН в пределах нейтрального диапазона, т.е. в пределах диапазона рН между 6 и 7. Подходящий буфер представляет собой любой буфер, который поддерживает значение рН в заявленном диапазоне, например, ацетатный буфер. Реакцию получения соединения общей формулы I выполняют способом, включающим смешивание буферных компонентов реакционной смеси, состоящих из Mg2+, АТФ, и субстратов в ацетатном буфере в реакторе, причем реакцию инициируют путем прибавления суспензии ферментов к буферу. Реакцию выполняют при комнатной температуре, т.е. при температуре между 18°С и 30°С или, идеально, между 23°С и 28°С. Предпочтительная температура для выполнения процедуры получения соединения общей формулы I составляет 27°С. Значение рН непрерывно измеряют рН-метром и, если необходимо, поддерживают оптимальные условия с помощью основания, такого как водный раствор NaOH. Реакцию останавливают водным раствором кислоты, после чего реакционную смесь охлаждают. В течение периода охлаждения образуется белый осадок, который поочередно промывают кислотой и водой.
Второй аспект настоящего изобретения относится к фармацевтической композиции, которая содержит активное количество соединения общей формулы I или его фармацевтически приемлемых солей и сольватов в фармацевтическом варианте, подходящем для парентерального применения, перорального введения и внутривенного применения. Кроме активного соединения, в соответствии с объектом настоящего изобретения, фармацевтическая композиция может содержать один или более фармацевтически приемлемых эксципиентов, таких как носители, смазывающие вещества, глиданты, красители, наполнители, т.е. связующие вещества, разрыхлители и поверхностно-активные вещества.
В случае фармацевтического варианта для перорального введения фармацевтический препарат может быть спрессован для получения пеллет, гранул, таблеток, блистеров, капсул, таблеток с контролируемым высвобождением действующего вещества. Все фармацевтические препараты, кроме действующего вещества, могут содержать фармацевтически приемлемые эксципиенты. Эксципиенты могут быть выбраны из группы носителей, связующих веществ, наполнителей, поверхностно-активных веществ, разрыхлителей, глидантов, смазывающих веществ и других известных фармацевтически приемлемых эксципиентов.
Носители выбирают из группы известных фармацевтически приемлемых носителей, таких как белковые наночастицы, полипептиды, липосомы, полимерные мицеллы, микросферы и смеси двух или более известных носителей. Приведенные выше примеры носителей предназначены только для иллюстративных целей, и выбор носителей никоим образом не ограничивается приведенными выше примерами или их смесями.
Связующие вещества-наполнители выбирают из группы известных фармацевтически приемлемых связующих веществ-наполнителей, таких как сахароза, лактоза, крахмал, целлюлоза, маннит, сорбит, ксилит, микрокристаллическая целлюлоза, силиконизированная микрокристаллическая целлюлоза, гидрофосфат кальция, карбонат кальция, лактат кальция и смеси двух или более известных фармацевтически приемлемых связующих веществ-наполнителей. Приведенные выше примеры связующих веществ-наполнителей предназначены только для иллюстративных целей, и выбор связующих веществ-наполнителей никоим образом не ограничивается приведенными выше примерами или их смесями.
Поверхностно-активные вещества выбирают из группы известных фармацевтически приемлемых поверхностно-активных веществ, таких как сложные эфиры жирных кислот, полисорбаты, полиоксиэтиленалкиловые эфиры, полиоксамеры, триглицериды, полиоксилглицериды или смеси двух или более известных фармацевтически приемлемых поверхностно-активных веществ. Приведенные выше примеры поверхностно-активных веществ предназначены только для иллюстративных целей, и выбор поверхностно-активных веществ никоим образом не ограничивается приведенными выше примерами или их смесями.
Разрыхлители выбирают из группы известных фармацевтически приемлемых разрыхлителей, таких как сшитые полимеры, например, карбоксиметилцеллюлоза, поливинилпирролидон или их смеси. Приведенные выше примеры разрыхлителей приведены только для иллюстративных целей, и выбор разрыхлителей никоим образом не ограничивается приведенными выше примерами или их смесями.
Глиданты и смазывающие вещества выбирают из группы фармацевтически известных глидантов и смазывающих веществ, таких как тальк, порошок диоксида кремния, карбонат магния, стеарат магния или смесь двух или более известных фармацевтически приемлемых глидантов и смазывающего вещества. Приведенные выше примеры глидантов и смазывающих веществ приведены только для иллюстративных целей, и выбор глидантов и смазывающих веществ никоим образом не ограничивается приведенными выше примерами или их смесями.
Фармацевтический препарат по данному изобретению имеет следующий состав:
1. соединение общей формулы I от 40% мас./мас. до 60% мас./мас.
2. эксципиенты от 40% мас./мас. до 60% мас./мас.
Пример 1 - Получение 1-амино-тетратриаконтилгеникоза-20-он-21-аля
0,1 моль/л ацетатного буфера получают, смешивая 0,1 моль/л водного раствора октеновой кислоты с 0,1 моль/л водным раствором NaOH. Полученный раствор имеет рН, равный 6.
Суспензию NRPS1 получали в ацетатном буфере. Конечная концентрация NRPS1 в суспензии составляла 0,06 г/л.
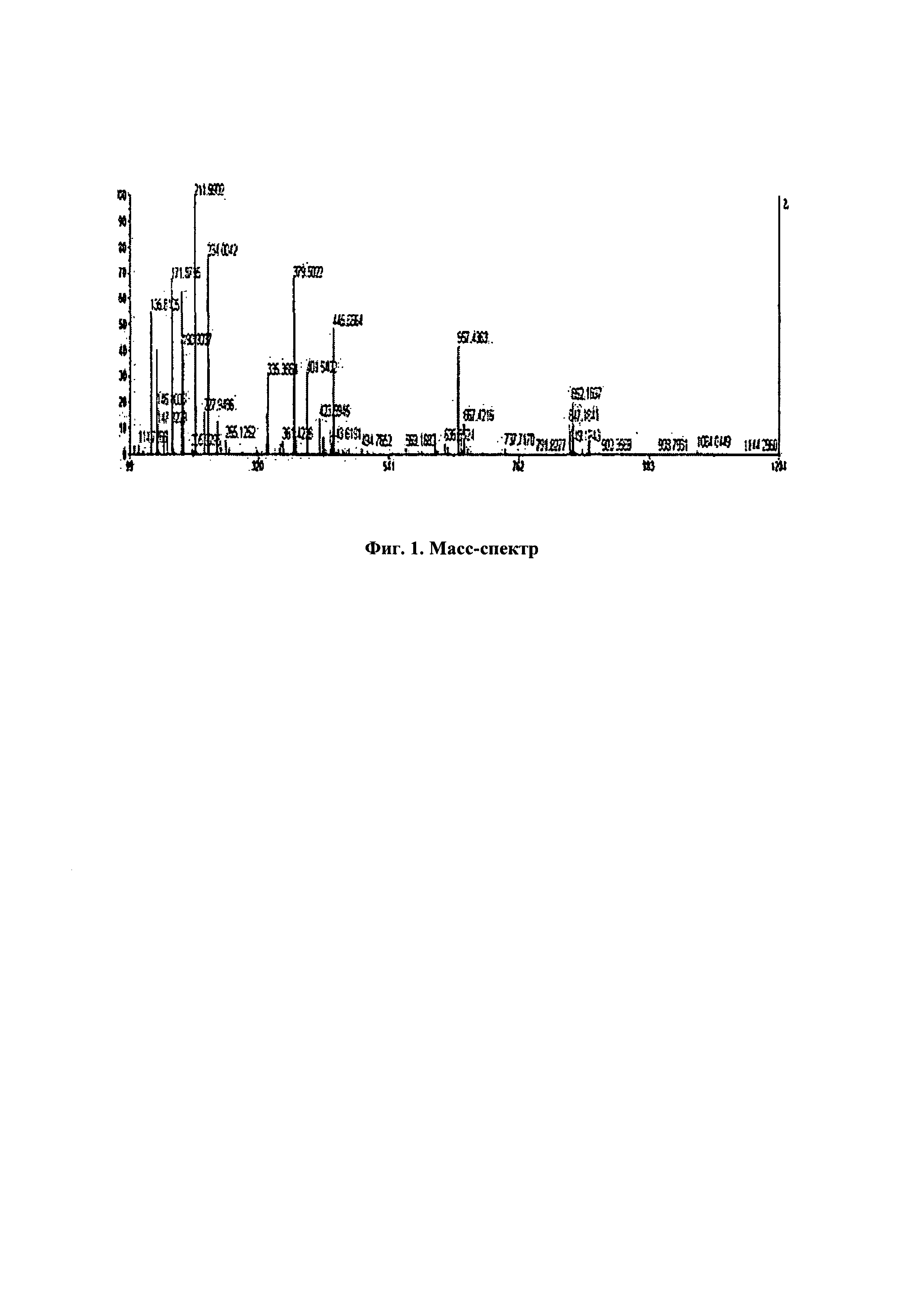
В реакционную колбу, оснащенную магнитной мешалкой, прибавили 0,51 г глицина, 0,85 г MgCl2, 0,043 г АТФ, и смесь растворяли в 85 мл предварительно приготовленного ацетатного буфера. Реакцию инициировали путем прибавлением в реакционную колбу 85 мкл суспензии NRPS1. Температура, при которой протекала реакция, составляла 27°С. Скорость перемешивания магнитной мешалкой составляла 500 об./мин и время реакции составляло 120 мин. Реакцию останавливали путем прибавления 85 мл 7% об./об. водного раствора трифторуксусной кислоты (соотношение реакционной смеси и кислоты составляет 1:1). Реакционный сосуд затем поместили на лед на 30 минут. После охлаждения инициировали процесс выпаривания на роторном испарителе с водяной баней. После удаления воды провели дополнительную сушку на роторном испарителе с водяной баней при температуре 60°С в течение более одного часа. Получили 0,46 г белого осадка с температурой 125°С. Образец растворили в изопропаноле и анализировали масс-спектрометрией высокого разрешения (ESI-qTOF) на Synapt G2-Si (Waters, США). Масс-спектры записывали в режиме определения положительных и отрицательных ионов. Расчетный пик должен был появиться при 445,50 m/z, а наблюдаемый пик был при 445,6564, из чего следует вывод, что характеристический пик для соединения 1-аминотетратриаконтилгеникоза-20-он-21-аля составляет 445,7959 с погрешностью измерения массы в пределах точности 5 м.д. - см. Фиг. 1.
Пример 2 - Состав препарата для перорального применения
500 мг 1-аминотетратриаконтилгеникоза-20-он-21-аля
500 мг эксципиентов
В данном примере эксципиенты представляют собой гипромеллозу, микрокристаллическую целлюлозу, краситель, диоксид титана.
Следующий аспект настоящего изобретения относится к антибактериальной активности соединения общей формулы I

в частности, антибактериальной активности 1-аминотетратриаконтилгеникоза-20-он-21-аля. In vitro исследование показало, что соединение общей формулы I, а также соединение 1-аминотетратриаконтилгеникоза-20-он-21-аля, обладает антибактериальными свойствами против грамположительных и грамотрицательных бактерий, включая мультирезистентные бактерии.
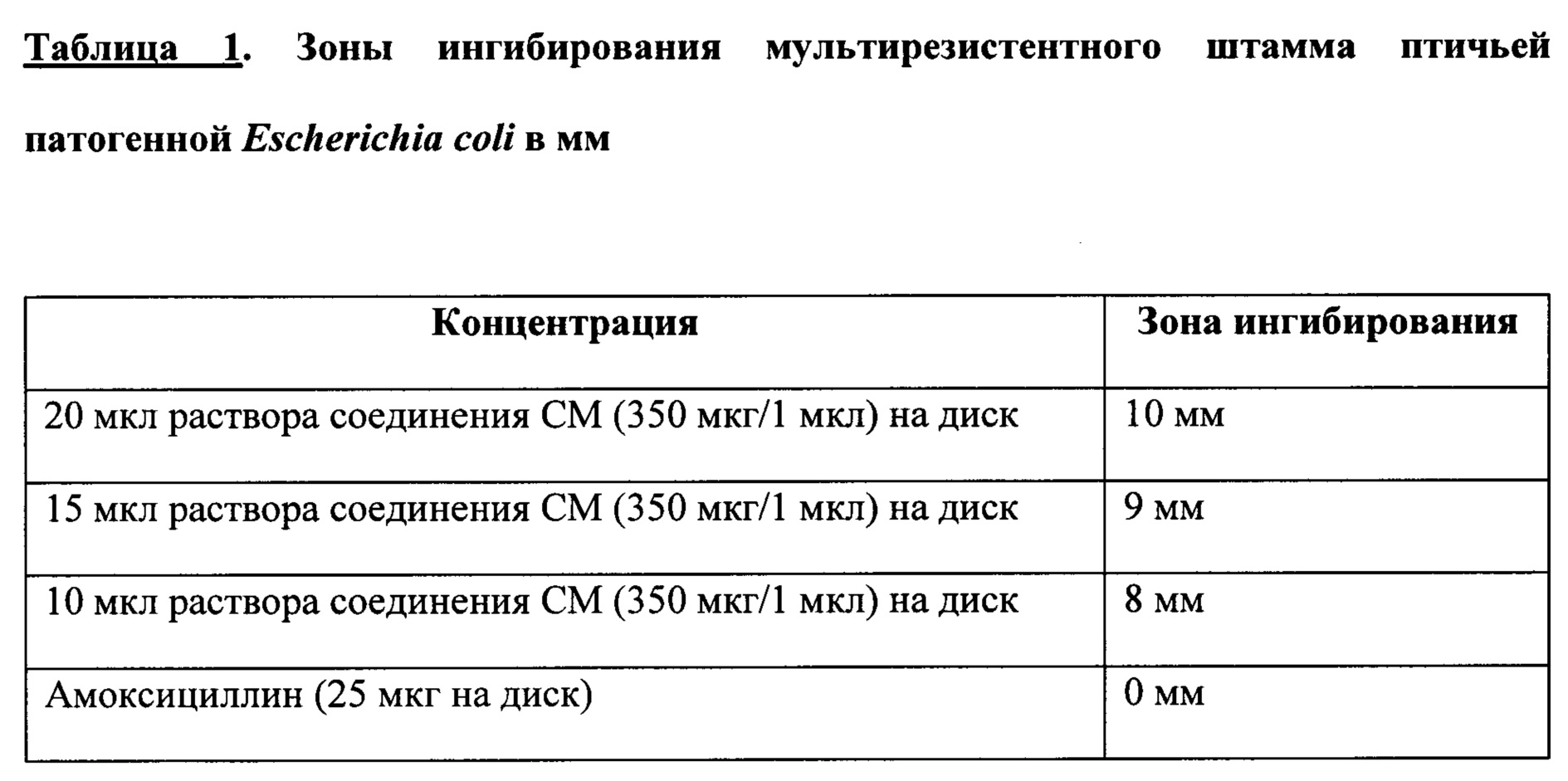
Соединение общей формулы I демонстрирует антибактериальные свойства против следующих бактерий: Neisseria gonorrhoea, acinetobacter baumannii, staphylococcus aureus (MRSA, burkholderia cepaci, pseudomonas aeruginos, Clostridium difficil, escherichia coli (E.coli ESBL, mycobacterium tuberculosis, Klebsiella pneumoniae, streptococcus pyogenes. В Таблице 2 проиллюстрированы зоны ингибирования для мультирезистентного штамма птичьей патогенной Escherichia coli для 1-аминотетратриаконтилгеникоза-20-он-21-аля, амоксициллина, триметоприм сульфата, тетрациклина и сульфадимидина.
Как было продемонстрировано, только 1-аминотетратриаконтилгеникоза-20-он-21-аль оказывает влияние на ингибирование заявленного штамма Е. Coli.
В Таблице 1 приведены результаты диаметра ингибирования, выраженного в мм. В Таблице 2 проиллюстрирована концентрация 1-аминотетратриаконтилгеникоза-20-он-21-аля, выраженная в мг/мл, которая необходима для ингибирования мультирезистентного штамма птичьей патогенной Escherichia coli. 1-Аминотетратриаконтилгеникоза-20-он-21-аль обозначен в таблицах, как Cm. Антибиотики из Таблицы 1 вводят в их стандатной дозе для данного типа исследования. Очевидно, что только 1-аминотетратриаконтилгеникоза-20-он-21-аль проявляет ингибирующую активность против мультирезистентного штамма птичьей патогенной Escherichia coli.


Учитывая результаты in-vitro исследования, соединения общей формулы I, особенно 1-аминотетратриаконтилгеникоза-20-он-21-аль представляет лекарственные средства, в основном лекарственные средства от бактериальных инфекций, применяющиеся при лечении бактериальных инфекций. Бактериальные инфекции, которые успешно лечат соединения общей формулы I, особенно 1-аминотетратриаконтилгеникоза-20-он-21-аль, представляют собой: сибирскую язву, бактериальный менингит, бруцеллез, бубонную чуму, дифтерию, сыпной тиф, гонорею, судорожный кашель (коклюш), кампилобактериоз, хламидиоз (трахому), холеру, чуму, легионеллез, лепру (болезнь Хансена), лептоспироз у людей, лептоспироз, листериоз, мелиоидоз, нокардиоз, пневмонию, рецидивирующую лихорадку, попугайную болезнь, Ку-лихорадку, сальмонеллез, сифилис, инфекцию метициллин-устойчивого золотистого стафилококка (MRSA), скарлатину, шигеллез, столбняк, тиф, брюшной тиф, туберкулез, туляремию, болезнь от укуса крыс.
Реферат
Изобретение относится к соединению указанной ниже общей формулы I, при этом указанное соединение представляет собой 1-аминотетратриаконтилгеникоза-20-он-21-аль и может найти применение для лечения бактериальных инфекций, вызванных грамположительными или грамотрицательными бактериями. Изобретение относится также к фармацевтической композиции, содержащей указанное соединение. 2 н. и 4 з.п. ф-лы, 1 ил., 2 табл., 2 пр.
Формула
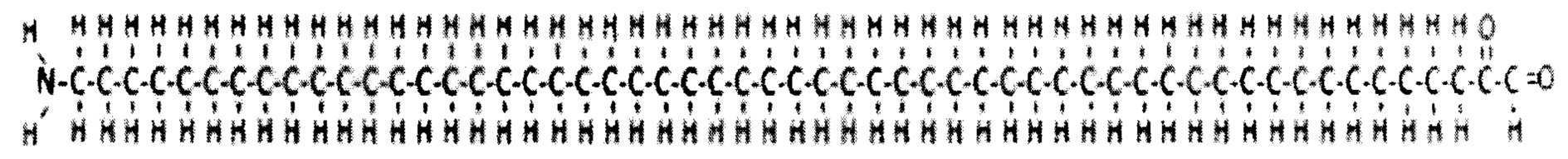

Комментарии