Модуляторы ror гамма(rorγ) - RU2727191C2
Код документа: RU2727191C2
Описание
Связанный с рецептором ретиноевой кислоты рецептор-сирота γt (RORγt) действует как главный регулятор развития клеток TH17, а также как критический компонент в не-TH17 клетках, производящих ИЛ-17, таких как, например, γδ T-клетки. Семейство генов ROR является частью суперсемейства ядерного гормонального рецептора и состоит из трех членов (RORα, RORβ и RORγ). Каждый ген экспрессируется в различных изоформах, различаясь, прежде всего, последовательностью N-окончания. Были идентифицированы две изоформы RORγ: RORγ1 и RORγ2 (также известная как RORγt). Термин RORγ в данном описании относится к обоим RORγ1 и/или RORγ2.
Данное изобретение относится к модуляторам RORγ, к фармацевтическим композициям, содержащим их, и к применению указанных компонентов для лечения RORγ-медиированных заболеваний или состояний, в частности, аутоиммунных заболеваний и воспалительных состояний.
В данном изобретении представлены новые соединения, модулирующие RORγ, содержащие субструктуру 2-(4-циклопропилметансульфонилфенил)ацетамид или 2-(4-циклопропилсульфамоилфенил)ацетамид.
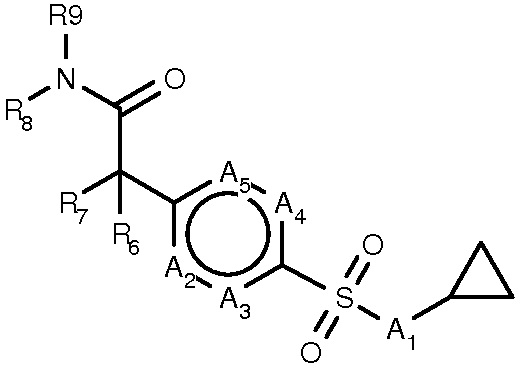
Данное изобретение относится к соединениям формулы I

(формула I)
или их фармацевтически приемлемой соли, где:
A1 является NR1 или CR1, где R1 является H или метилом, где метил, если присутствует, необязательно замещен одним или более F;
циклопропильная часть может быть необязательно замещена одним или более метилом и одним или более F;
A2-A5 являются N или CR2-CR5, соответственно, при условии, что не более двух из четырех положений А в A2-A5 одновременно могут быть N;
R2-R5 независимо являются H, галогеном, амино, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-6)алкилом;
R6 и R7 независимо являются H, F, метилом, этилом, гидроксилом или метокси, или R6 и R7 вместе являются карбонилом, все алкильные группы, если присутствуют, необязательно замещены одним или более F;
R8 является Н или C(1-6)алкилом;
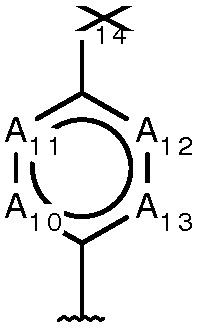
R9 выбирают из группы, включающей формулу II, III, IV и V

(формула II)
где: A10-A13 являются N или CR10-CR13, соответственно, при условии, что не более двух из четырех положений А в A10-A13 одновременно могут быть N;
R10-R13 независимо являются H, галогеном, амино, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-6)алкилом;
X14 является либо C(6-10)арилом, либо C(1-9)гетероарилом, где все атомы углерода необязательно замещены галогеном, амино, циано, C(1-3)алкокси, (ди)C(1 3)алкиламино или C(1-3)алкилом;
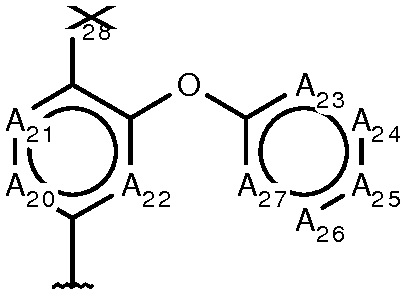
(формула III)
где:
A20-A27 являются N или CR20-CR27, соответственно, при условии, что не более двух из трех положений А в A20-A22 одновременно могут быть N, и что не более трех из пяти положений А в A23-A27 одновременно могут быть N;
R20-R22 независимо являются H, галогеном, амино, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-6)алкилом;
R23-R27 независимо являются H, галогеном, амино, циано, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-3)алкилом;
X28 является либо C(6-10)арилом, либо C(1-9)гетероарилом, где все атомы углерода необязательно замещены галогеном, амино, циано, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-3)алкилом;
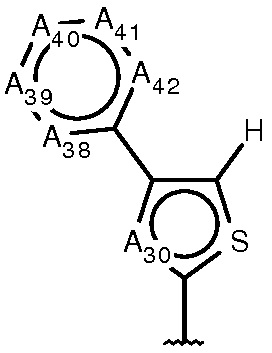
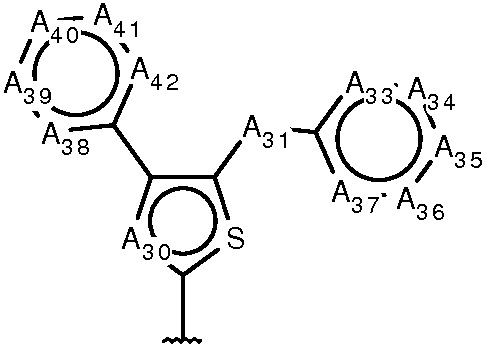
где:
A30 является N или C;
A31 является O, карбонилом, NR31 или CR32;
R31 является Н или C(1-6)алкилом;
R32 является либо H, OH, либо C(1-3)алкилом, где все алкильные группы необязательно замещены одним или более F или OH;
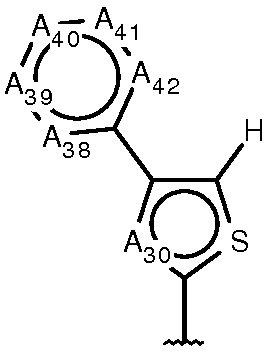
A33-A42 являются N или CR33-CR42, соответственно, при условии, что не более трех из пяти положений А в A33-A37 одновременно могут быть N, и что не более трех из пяти положений А в A38-A42 одновременно могут быть N;
R33-R42 независимо являются H, галогеном, амино, циано, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-3)алкилом.
Термин C(1-6)алкил в данном описании означает разветвленную или неразветвленную алкильную группу, содержащую 1-6 атомов углерода, например, метил, этил, пропил, изопропил, бутил, трет-бутил, н-пентил и н-гексил. Все атомы углерода необязательно могут быть замещены одним или более галогеном.
Термин C(1-3)алкил в данном описании означает алкильную группу, содержащую 1-3 атома углерода, т.е. метил, этил, пропил или изопропил. Все атомы углерода необязательно могут быть замещены одним или более галогеном.
Термин C(1-2)алкил в данном описании означает алкильную группу, содержащую 1-2 атома углерода, т.е. метил или этил. Все атомы углерода необязательно могут быть замещены одним или более галогеном.
Термин C(6-10)арил в данном описании означает ароматическую углеводородную группу, содержащую 6-10 атомов углерода, например, фенил или нафтил. Предпочтительной ароматической углеводородной группой является фенил. Все атомы углерода необязательно могут быть замещены одним или более галогеном.
Термин C(6)арил в данном описании означает ароматическую углеводородную группу, содержащую 6 атомов углерода, т.е. фенил. Все атомы углерода необязательно могут быть замещены одним или более галогеном.
Термин гетероатом в данном описании относится к атому азота, серы или кислорода.
Термин амино в данном описании относится к NH2 группе.
Термин C(1-9)гетероарил в данном описании означает ароматическую группу, содержащую 1-9 атомов углерода и 1-4 гетероатома, которые могут быть присоединены через атом азота, если возможно, или атом углерода. Примеры включают имидазолил, тиадиазолил, пиридинил, пиримидинил, фурил, пиразолил, изоксазолил, тетразолил и хинолил. Все атомы углерода необязательно могут быть замещены одним или более галогеном или метилом.
Термин C(1-5)гетероарил в данном описании означает ароматическую группу, содержащую 1-5 атомов углерода и 1-4 гетероатома, которые могут быть присоединены через атом азота, если возможно, или атом углерода. Примеры включают имидазолил, тиадиазолил, пиридинил, пиримидинил, фурил, пиразолил, изоксазолил и тетразолил. Все атомы углерода необязательно могут быть замещены одним или более галогеном или метилом.
Термин циклопропилметил в данном описании означает метильную группу, замещенную циклопропилом. Все атомы углерода необязательно замещены одним или более галогеном или метилом.
Термин (ди)C(1-3)алкиламино в данном описании означает аминогруппу, которая монозамещена или дизамещена C(1-3)алкильной группой, где последняя имеет значение, определенное выше.
Термин C(1-3)алкокси означает алкоксигруппу, содержащую 1-3 атома углерода, где алкильная часть разветвлена или не разветвлена. Все атомы углерода необязательно замещены одним или более F.
Термин галоген в данном описании означает Cl или F.
В представленных выше определениях с многофункциональными группами, место присоединения находится на последней группе.
Если, в определении заместителя, указано, что ʺвсе алкильные группыʺ указанного заместителя необязательно замещены, они также включают алкильную часть алкоксигруппы.
Термин ʺзамещенныйʺ означает, что один или более атомов водорода указанного атома/атомов замещены выбором из указанной группы, при условии, что нормальная валентность указанных атомов в существующих условиях не превышена, и что замещение дает стабильное соединение. Сочетания заместителей и/или переменных возможно, только если такие сочетания дают стабильные соединения. ʺСтабильное соединениеʺ или ʺстабильная структураʺ определены как соединение или структура, которые достаточно устойчивы для того, чтобы вынести выделение до полезной степени чистоты из реакционной смеси и составление в эффективный терапевтический агент.
Термин ʺнеобязательно замещенныйʺ означает необязательное замещение указанными группами, радикалами или частями.
Термин фармацевтически приемлемая соль означает такие соли, которые, с медицинской точки зрения, подходят для применения в контакте с тканями человека и низших животных, не вызывая нежелательной токсичности, раздражения, аллергической реакции и подобных, и соразмерны разумному соотношению польза/риск. Фармацевтически приемлемые соли хорошо известны в данной области техники. Они могут быть получены во время конечного выделения и очистки соединений в соответствии с данным изобретением или отдельно, взаимодействием функциональной группы свободного основания с подходящей минеральной кислотой, такой как хлористоводородная кислота, фосфорная кислота или серная кислота, или с органической кислотой, такой как, например, аскорбиновая кислота, лимонная кислота, винная кислота, молочная кислота, малеиновая кислота, малоновая кислота, фумаровая кислота, гликолевая кислота, янтарная кислота, пропионовая кислота, уксусная кислота, метансульфоновая кислота и тому подобное. Функциональная группа кислоты может взаимодействовать с органическим или минеральным основанием, таким как гидроксид натрия, гидроксид калия или гидроксид лития.
В одном варианте изобретение относится к соединению формулы I, где A1 является CR1.
В другом варианте изобретение относится к соединению формулы I, где A1 является NR1.
В другом варианте изобретение относится к соединению формулы I, где R1 является водородом.
В другом варианте изобретение относится к соединению формулы I, где R6 и R7 независимо являются H, метилом или гидроксилом.
В еще одном варианте изобретение относится к соединению формулы I, где R6 и R7 оба являются H.
Изобретение также относится к соединению формулы I, где R8 является Н или C(1-2)алкилом, H наиболее предпочтителен.
Изобретение также относится к соединению формулы I, где R8 является H.
В еще одном варианте изобретение относится к соединению формулы I, где R2 является метилом, и R3-R5 являются H.
В другом варианте изобретение относится к соединению формулы I, где R2-R5 являются H.
В другом варианте изобретение относится к соединению формулы I, где все положения A в A2-A5 являются CR2-R5.
В еще одном варианте изобретение относится к соединению формулы I, где все положения А в A2-A5 являются CR2-R5, и все положения R в R2-R5 являются H.
In еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу II, где: A10-A13 являются N или CR10-CR13, соответственно, при условии, что не более двух из четырех положений А в A10-A13 одновременно могут быть N; R10-R13 независимо являются H, амино, галогеном, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-6)алкилом; X14 является либо C(6)арилом, либо C(1-5)гетероарилом, где все атомы углерода необязательно замещены галогеном, циано, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-3)алкилом, где предпочтителен необязательный заместитель C(1-3)алкокси.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу II и все положения А в A10-A13 являются углеродом.
В другом варианте изобретение относится к соединению формулы I, где R9 имеет формулу II and A10 is nitrogen.
В другом варианте изобретение относится к соединению формулы I, где R9 имеет формулу II и A11 является азотом.
Изобретение также относится к соединению формулы I, где R9 имеет формулу II и R10-R13 независимо являются H, галогеном, метилом или метокси.
В другом варианте изобретение относится к соединению формулы I, где R9 имеет формулу II и R10-R13 являются H.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу II и X14 является C(6)арилом, где все атомы углерода необязательно замещены галогеном, циано, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-3)алкилом.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу II и X14 является C(1-5)гетероарилом, где все атомы углерода необязательно замещены галогеном, циано, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-3)алкилом.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу II и X14 является C(6)арилом или C(1-5)гетероарилом, где все атомы углерода необязательно замещены C(1-3)алкокси.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу II и X14 является 2-(трифторметокси)фенилом.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу III, где: A20-A27 являются N или CR20-CR27, соответственно, при условии, что не более двух из трех положений А в A20-A22 одновременно могут быть N, и что не более трех из пяти положений А в A23-A27 одновременно могут быть N; R20-R22 независимо являются H, галогеном, амино, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-6)алкилом; R23-R27 независимо являются H, галогеном, циано, амино, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-3)алкилом; X28 является либо C(6)арилом, либо C(1-5)гетероарилом, где все атомы углерода необязательно замещены галогеном, циано, C(1-3)алкокси, (ди)C(1 3)алкиламино или C(1-3)алкилом.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу III и все положения А в A20-A22 являются углеродом.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу III и A20 является азотом.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу III и A22 является азотом.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу III и R20-R22 независимо являются H, галогеном, метилом или метокси.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу III и R20-R22 являются H.
В другом варианте изобретение относится к соединению формулы I, где R9 имеет формулу III и все положения А в A23-A27 являются углеродом.
В другом варианте изобретение относится к соединению формулы I, где R9 имеет формулу III и R23, R25 и R27 являются H.
Изобретение также относится к соединению формулы I, где R9 имеет формулу III и R24 и R26 независимо являются H, галогеном, циано, метокси или метилом.
В другом варианте изобретение относится к соединению формулы I, где R9 имеет формулу III и X28 является C(6)арилом, где все атомы углерода необязательно замещены галогеном, циано, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-3)алкилом.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу III и X28 является C(1-5)гетероарилом, где все атомы углерода необязательно замещены галогеном, циано, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-3)алкилом.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу III и X28 является фенилом.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу III и X28 является 1H-имидазол-1-ильной группой.
В другом варианте изобретение относится к соединению формулы I, где R9 имеет формулу III и X28 является 1H-пиразол-1-ильной группой.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу IV или V, где: A30 является N или C; A31 является O, карбонилом, NR31 или CR32; R31 является Н или C(1-6)алкилом; R32 является H, OH или C(1-6)алкилом, где все алкильные группы необязательно замещены одним или более F или OH; A33-A42 являются N или CR33-CR42, соответственно, при условии, что не более трех из пяти положений A33-A37 одновременно могут быть N, и что не более трех из пяти положений A38-A42 одновременно могут быть N; R33-R42 независимо являются H, галогеном, циано, C(1-3)алкокси, (ди)C(1-3)алкиламино или C(1-3)алкилом.
Изобретение также относится к соединению формулы I, где R9 имеет формулу IV или V и A30 является N.
Изобретение также относится к соединению формулы I, где R9 имеет формулу IV или V и A30 является C.
В другом варианте изобретение относится к соединению формулы I, где R9 имеет формулу V и A31 является карбонилом.
В другом варианте изобретение относится к соединению формулы I, где R9 имеет формулу V и A31 является кислородом.
В еще одном варианте изобретение относится к соединению формулы I, где R9 имеет формулу V и все положения А в A33-A42 являются углеродом.
Изобретение также относится к тем соединениям, в которых все конкретные определения для A1-A42, R1-R42, и всех замещающих групп в различных аспектах изобретения, определенных выше, существуют в любых сочетаниях в рамках определения соединения формулы I.
В другом аспекте соединение относится к соединениям формулы I, которые имеют pIC50 5 или выше. В еще одном аспекте изобретение относится к соединениям формулы I с pIC50 более 6. В еще одном аспекте изобретение относится к соединениям формулы I с pIC50 более 7. В еще одном аспекте изобретение относится к соединениям формулы I с pIC50 более 8.
В еще одном варианте изобретение относится к соединениям формулы I, выбранным как описано в примерах 1-47.
Соединения формулы I могут образовывать соли, которые также включены в объем данного изобретения. Ссылка на соединение формулы I здесь включает ссылку на его соли, если не указано иначе.
Соединения формулы I могут содержать асимметрические или хиральные центры и, поэтому, существуют в различных стереоизомерных формах. Подразумевается, что все стереоизомерные формы соединений формулы I, а также их смеси, включая рацемические смеси, образуют часть данного изобретения.
Диастереомерные смеси могут быть разделены на отдельные диастереомеры на основе их физико-химических различий, способами, хорошо известными специалистам в данной области техники, такими как, например, хроматография и/или фракционная кристаллизация. Энантиомеры могут быть разделены превращением энантиомерной смеси в диастереомерную смесь взаимодействием с подходящим оптически активным соединением (например, хиральной добавкой, такой как хиральный спирт или хлорид кислоты Мошера), разделяя диастереомеры и превращая (например, гидролизом) отдельные диастереомеры в соответствующие чистые энантиомеры. Энантиомеры также могут быть разделены с применением хиральной ВЭЖХ колонки.
Специалисты в данной области техники понимают, что желаемые значения IC50 зависят от тестируемого соединения. Например, соединение со значением IC50 менее 10-5 M обычно считается кандидатом для отбора по чувствительности к лекарственному препарату. Предпочтительно, это значение ниже 10-6 M. Однако соединение, которое имеет более высокое значение IC50, но является селективным к конкретному рецептору, может быть даже лучшим кандидатом.
Соединения в соответствии с данным изобретением ингибируют активность RORγ. Модулирование активности RORγ может быть измерена с применением, например, исследований замещения биофизического (природного) лиганда, биохимическими анализами AlphaScreen или FRET, клеточными анализами гена-репортера GAL4, клеточным анализом промотора-репортера ИЛ-17 или функциональными ELISA анализами ИЛ-17 с применением, например, мышиных спленоцитов или мононуклеарных клеток периферической крови человека (МКПК), культивированных в TH17 поляризующих условиях.
В таких анализах взаимодействие лиганда с RORγ может быть определено измерением, например, лиганд-модулированного взаимодействия кофактор-производных пептидов со связывающим доменом лиганда RORγ или измерением генных продуктов лиганд-модулированной RORγ-медиированной транскрипции, с применением, например, исследований люциферазного репортера или ELISA исследований ИЛ-17.
Данное изобретение также относится к фармацевтической композиции, содержащей соединения или их фармацевтически приемлемые соли, имеющих общую формулу I, в смеси с фармацевтически приемлемыми наполнителями и, необязательно, другие терапевтически активные агенты. Наполнители должны быть ʺприемлемымиʺ в смысле совместимости с другими ингредиентами композиции и не вредящими реципиентам.
Изобретение также включает соединение формулы I в сочетании с одним или более другими лекарственными средствами.
Композиции включают, например, композиции, подходящие для перорального, подъязычного, подкожного, внутривенного, внутримышечного, назального, местного или ректального введения, и подобных, все которые имеют стандартную лекарственную форму для введения.
Для перорального введения активный ингредиент может присутствовать в виде отдельных единиц, таких как таблетки, капсулы, порошки, грануляты, растворы, суспензии и подобные.
Для парентерального введения фармацевтическая композиция в соответствии с данным изобретением может присутствовать в однодозных или многодозных контейнерах, например, жидкие инъекции в определенных количествах, например, в герметично закрытых флаконах или ампулах, а также могут храниться в высушенном вымораживанием (лиофилизированном) состоянии, требующем только добавления стерильного жидкого носителя, например, воды, перед применением.
При смешивании таких фармацевтически приемлемых добавок активный ингредиент может быть спрессован в твердые лекарственные формы, такие как пилюли, таблетки, или может быть переработан в капсулы или суппозитории. В виде фармацевтически приемлемых жидкостей активный ингредиент может быть нанесен в виде жидкой композиции, например, в виде препарата для инъекций, в форме раствора, суспензии, эмульсии, или в виде спрея, например, назального спрея.
Для получения твердых лекарственных форм рассматривается применение обычных добавок, таких как наполнители, красители, полимерные связующие агенты и подобные. В общем, могут применяться любые фармацевтически приемлемые добавки, которые не взаимодействуют с функциональными группами активных соединений. Подходящие носители, с которыми может вводиться активный агент в соответствии с данным изобретением в виде твердых композиций, включают лактозу, крахмал, производные целлюлозы и подобные, и их смеси, применяемые в подходящих количествах. Для парентерального введения могут применяться водные суспензии, изотонические солевые растворы и стерильные растворы для инъекций, содержащие фармацевтически приемлемые диспергирующие агенты и/или смачивающие агенты, такие как пропиленгликоль или бутиленгликоль.
Изобретение также включает фармацевтическую композицию, как описана выше, в сочетании с упаковкой, подходящей для указанной композиции, где указанная упаковка включает инструкции по применению композиции, для описанного выше применения.
Точная доза и режим введения активного ингредиента или его фармацевтической композиции может варьироваться в зависимости от конкретного соединения, способа введения и возраста и состояния пациента, которому вводят лекарство.
В общем, парентеральное введение требует более низких доз, чем другие способы введения, которые больше зависят от абсорбции. Однако доза для человека предпочтительно включает 0,0001-100 мг на кг массы тела. Желаемая доза может быть представлена в виде однократной дозы или множества субдоз, вводимых с подходящим интервалом в течение суток.
Соединения в соответствии с данным изобретением могут применяться в терапии.
Другой аспект изобретения относится к применению соединений в соответствии с данным изобретением или их фармацевтически приемлемой соли для лечения RORγ-медиированных заболеваний или RORγ-медиированных состояний.
Другой аспект изобретения относится к применению соединений общей формулы I или их фармацевтически приемлемой соли для лечения аутоиммунных заболеваний, в частности, таких заболеваний, в которых TH17 клетки и не-TH17 клетки, которые экспрессируют TH17 характерные цитокины, играют важную роль. Оно включает, но не ограничено ими, лечение ревматоидного артрита, псориаза, воспалительного заболевания кишечника, болезнь Крона и рассеянный склероз.
В другом аспекте, соединения общей формулы I или их фармацевтически приемлемая соль могут применяться для лечения воспалительных заболеваний, в которых TH17 клетки и/или не-TH17 клетки, которые экспрессируют TH17 характерные цитокины, играют важную роль, таких как, но не ограниченных ими, респираторные заболевания, остеоартрит и астма. Также соединения или их фармацевтически приемлемая соль формулы I могут применяться для лечения инфекционных заболеваний, в которых TH17 клетки и/или не-TH17 клетки, которые экспрессируют TH17 характерные цитокины, играют важную роль, таких как, но не ограниченных ими, слизистый лейшманиоз.
Соединения общей формулы I или их фармацевтически приемлемая соль также могут применяться для лечения других заболеваний, в которых TH17 клетки и/или не-TH17 клетки, которые экспрессируют TH17 характерные цитокины, играют важную роль, таких как, но не ограниченных ими, болезнь Кавасаки и тиреоидит Хашимото.
В еще одном аспекте изобретения представлено применение соединений общей формулы I для лечения рассеянного склероза, воспалительного заболевания кишечника, болезни Крона, псориаза, ревматоидного артрита, астмы, остеоартрита, болезни Кавасаки, тиреоидита Хашимото, рака и слизистого лейшманиоза.
В другом аспекте соединение в соответствии с данным изобретением может применяться в терапии для лечения или профилактики рассеянного склероза, воспалительного заболевания кишечника, болезни Крона, псориаза и ревматоидного артрита, астмы, остеоартрита, болезни Кавасаки, тиреоидита Хашимото, рака и слизистого лейшманиоза.
В другом аспекте соединение в соответствии с данным изобретением может применяться для лечения или профилактики псориаза.
В другом аспекте соединение в соответствии с данным изобретением может применяться для лечения воспалительного заболевания кишечника.
Изобретение иллюстрировано следующими примерами.
ПРИМЕРЫ
Как изображено в примерах ниже, в определенных типовых вариантах соединения получают в соответствии со следующими общими методами. Должно быть понятно, что хотя в общих способах изображен синтез определенных соединений в соответствии с данным изобретением, следующие общие способы и другие способы, известные специалистам в данной области техники, могут применяться ко всем соединениям и подклассам и видам каждого из этих соединений, как описано здесь.
ОБЩИЕ СПОСОБЫ ПОЛУЧЕНИЯ
могут быть легко получены согласно следующим реакционным схемам и примерам, или их модификациям, с применением легкодоступных исходных материалов, реагентов и обычных методов синтеза. Многие реакции также могут проводиться в микроволновых условиях или с применением обычного нагревания, или с применением других технологий, таких как твердофазные реагенты/акцепторы или поточная химия. В этих реакциях также возможно применять варианты, которые сами по себе известны специалистам в данной области техники, но не описаны подробно. Например, если указаны конкретные кислоты, основания, реагенты, сочетающие агенты, растворители и т.д., понятно, что могут применяться другие подходящие кислоты, основания, реагенты, сочетающие агенты, растворители и т.д., которые включены в объем данного изобретения. Более того, другие способы получения соединений в соответствии с данным изобретением очевидны специалисту в данной области техники с учетом следующих реакционных схем и примеров. В случае, когда промежуточные соединения синтеза и конечные продукты содержат потенциально реакционноспособные функциональные группы, например, амино, гидроксил, тиол и группы карбоновой кислоты, которые могут взаимодействовать с желаемой реакцией, может быть предпочтительно применять защищенные формы промежуточного соединения. Способы выбора, введения и последующего удаления защитных групп хорошо известны специалистам в данной области техники. Соединения, полученные с применением общих реакционных последовательностей, могут быть недостаточной чистоты. Соединения могут быть очищены с применением любого способа очистки органических соединений, например, кристаллизации или хроматографии на колонке с силикагелем или окисью алюминия, с применением различных растворителей в подходящих соотношениях. Все возможные стереоизомеры предусматриваются в объеме изобретения. В описании ниже переменные имеют значения, указанные выше, если не указано иначе.
Аббревиатуры, применяемые в этих экспериментах, перечислены ниже, и дополнительные аббревиатуры должны быть известны специалисту в области синтетической химии.
Применяемые аббревиатуры: к.т.: комнатная температура; ГАТУ: гексафторфосфат 2-(7-аза-1H-бензотриазол-1-ил)-1,1,3,3-тетраметилурония; ДМФ: диметилформамид; ДИПЭА: диизопропилэтиламин; ДМАП: 4-(диметиламино)пиридин; ДЦК: N,N'-дициклогексилкарбодиимид; мХПБК: 3-хлорпероксибензойная кислота; ТФК: трифторуксусная кислота; ТФУА: трифторуксусный ангидрид; ТГФ: Тетрагидрофуран; ДМСО: диметилсульфоксид; PyBOP: гексафторфосфат (бензотриазол-1-илокси)трипирролидинофосфония; EtOH: этанол; ТСХ: тонкослойная хроматография; Ph3P: трифенилфосфин; ЭДКИ: 1-Этил-3-(3-диметиламинопропил)карбодиимид; BuLi: н-бутиллитий; PdCl2(dppf): дихлорид [1,1'-бис(дифенилфосфино)ферроцен]палладия(II).
Химическими наименованиями являются предпочтительные IUPAC наименования, полученные с применением MarvinSketch, версия 6.3.0.
Если химическое соединение описано с помощью химической структуры и химического наименования, и между структурой и наименованием имеется неясность, преимущественной является структура.
ОБЩИЕ МЕТОДЫ
Схема 1:

Условия: i) ЭДКИ, ДМАП, CH2Cl2.
Как изображено на схеме 1, производные в соответствии с данным изобретением формулы I могут быть получены способами, известными в области органической химии. Соединения в соответствии с данным изобретением, например, могут быть получены реакцией амидного сочетания между производным фенилуксусной кислоты формулы A (X является OH), где R2, R3, R5,R6, R7, R8 и A1 имеют описанные выше значения, и аминовым производным формулы B, где R8 и R9 имеют описанные выше значения, с применением сочетающего реагента, такого как ЭДКИ, ГАТУ, ДЦК или PyBOP или подобные, в присутствии подходящего основания, такого как ДИПЭА, или катализатора, такого как ДМАП.
Альтернативно, производное фенилуксусной кислоты формулы A (X=OH) может быть превращено в производное хлорангидрида формулы A (X=Cl) с применением, например, SOCl2 или оксалилхлорида. Полученное производное хлорангидрида формулы A (X1=Cl), где R2, R3, R5,R6, R7, R8 и A1, имеют описанные выше значения, может сочетаться в присутствии подходящего основания, такого как Et3N или подобные, с аминовым производным формулы B, где R8 и R9 имеют описанные выше значения.
Схема 2:
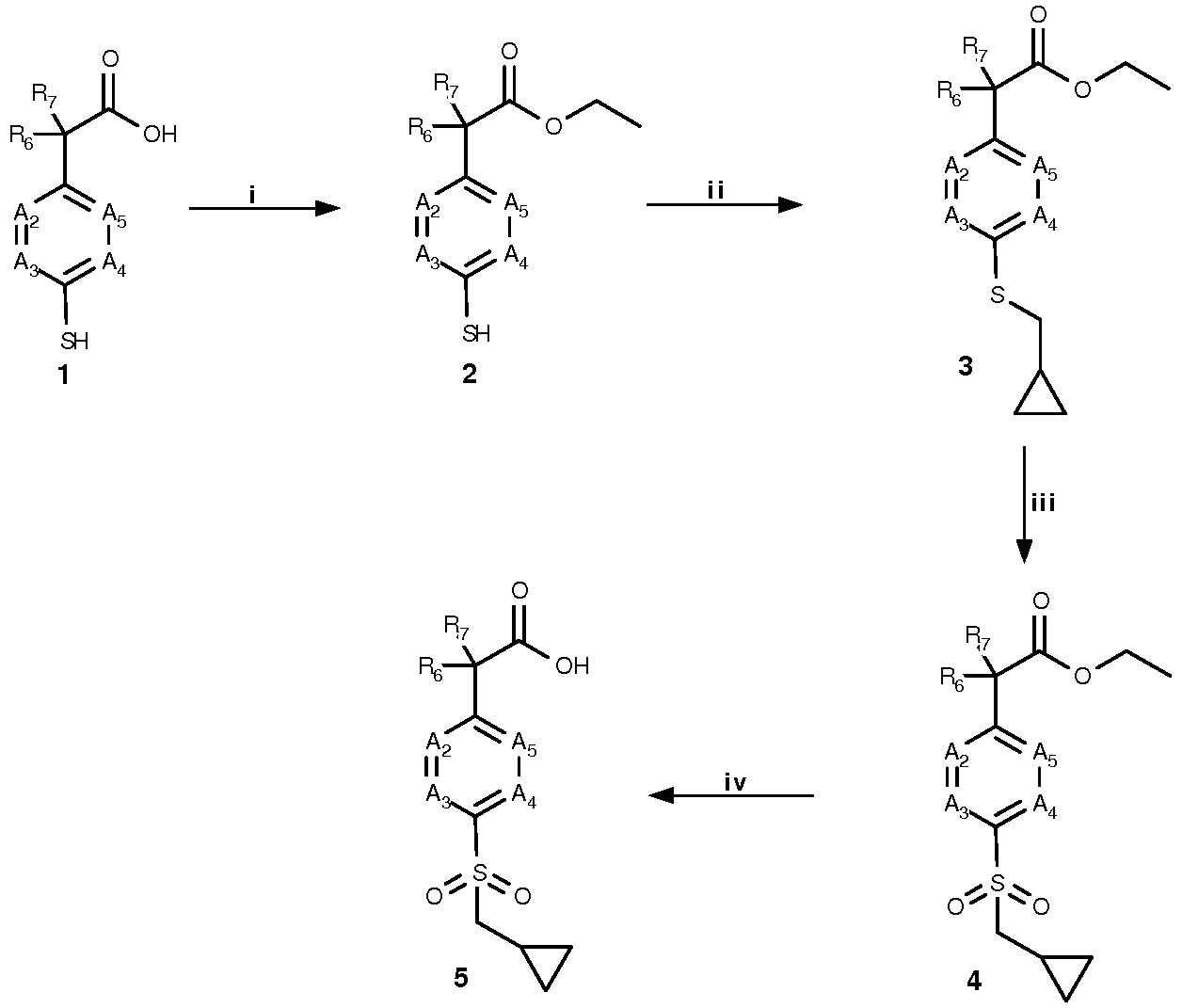
Условия: i) H2SO4, EtOH, 60°C; ii) (бромметил)циклопропан, K2CO3, CH3CN, к.т.; iii) мХПБК, CH2Cl2, к.т.; iv) 2N NaOH, EtOH, к.т.
Схема 2 иллюстрирует общий способ получения производных 2-(4-циклопропилметансульфонилфенил)уксусной кислоты формулы A, 5, где A1 является CH2 и A2, A3, A4, A5, R6 и R7 имеют описанные выше значения.
Эстерификация производных 4-меркаптофенилуксусной кислоты 1 в кислых условиях, с применением, например, H2SO4 в этаноле, дает производные этил 4-меркаптофенилацетата 2. Алкилирование серной группы с применением (бромметил)циклопропана в присутствии основания, такого как K2CO3, дает соответствующие производные этил 2-(4-циклопропилметансульфанилфенил)ацетата 3. Окисление с применением, например, мХПБК, дает производные этил 2-(4-циклопропилметансульфонилфенил)ацетата 4, которые после омыления сложной эфирной части в щелочных условиях, например, NaOH в этаноле, дает соответствующие производные формулы A, 5.
Схема 3:

Условия: i) хлорсульфоновая кислота, CH2Cl2, от 0°C до к.т.; ii) циклопропиламин, Et3N, CH2Cl2, к.т.; iii) 2N NaOH, EtOH, к.т.
Схема 3 иллюстрирует общий способ получения производных 2-[4-(циклопропилсульфамоил)фенил]уксусной кислоты формулы A, 9, где A1 является NH и A2, A3, A4, A5, R6 и R7 имеют описанные выше значения.
Взаимодействие производных этил 2-фенилацетата 6 с хлорсульфоновой кислотой дает производные 2-[4-(хлорсульфонил)фенил]ацетата 7, которые после нуклеофильного замещения с циклопропиламином дает производные 2-[4-(циклопропилсульфамоил)фенил]ацетата 8. Омыление сложной эфирной части в щелочных условиях, например, NaOH в этаноле, дает соответствующие производные формулы A, 9.
Большинство соединений формулы B коммерчески доступны, известны или получены способами, известными специалистам в данной области техники.
Схема 4:
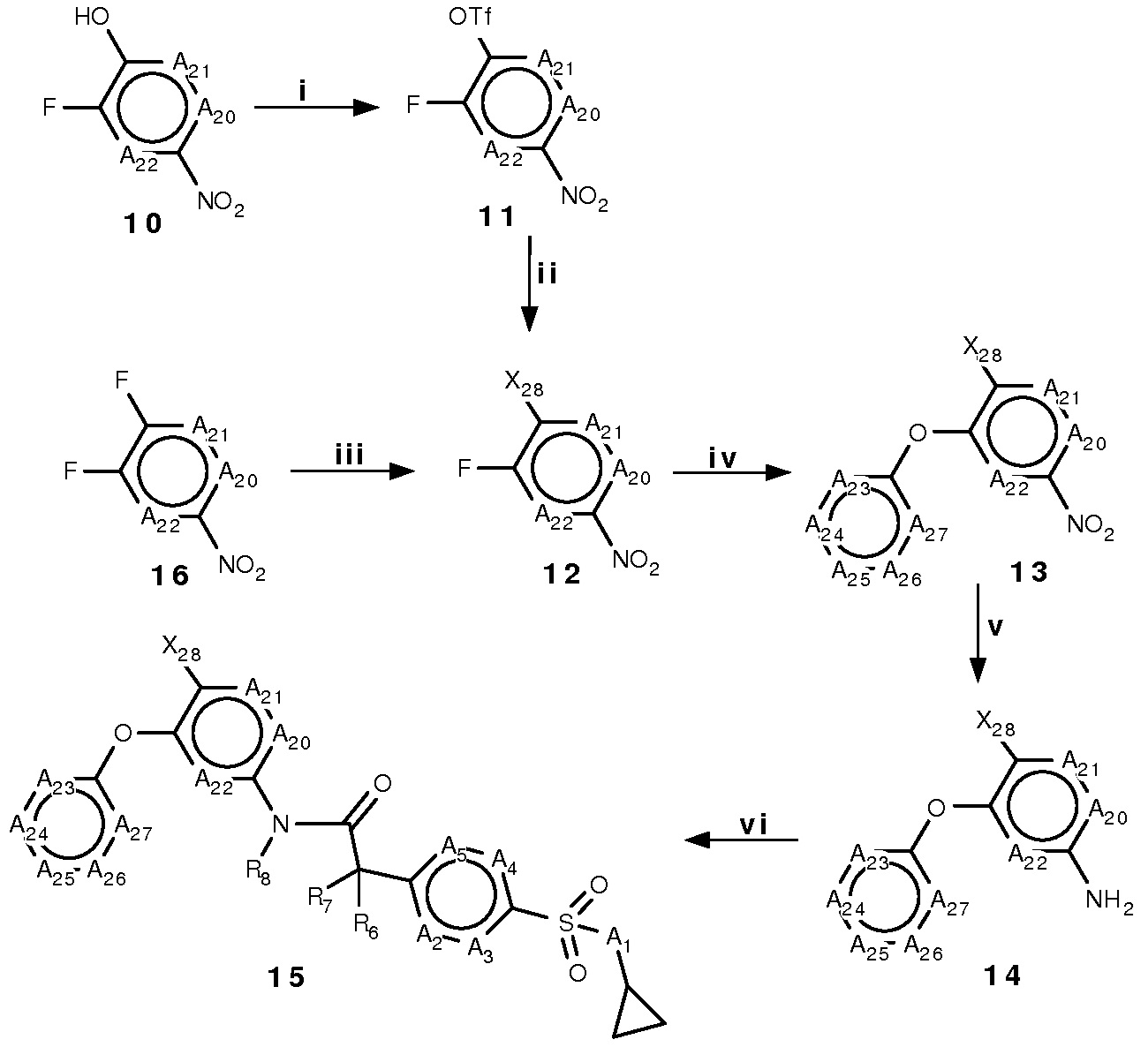
Условия: i) трифторметансульфоновый ангидрид, CH2Cl2, пиридин, ДМАП, к.т.; ii) подходящая бороновая кислота, Pd(Ph3)4, K2CO3, EtOH, вода, кипение с обратным холодильником; iii) подходящий гетероарил, K2CO3,ДМФ, 150°C; iv) Cs2CO3, подходящий фенол, ДМФ, 110°C; v) порошок цинка, NH4Cl, ТГФ, вода, 75°C; vi) 5 или 9, ЭДКИ, ДМАП, CH2Cl2, 60°C.
Схема 4 демонстрирует общие способы получения производных формулы I, 15, где R6, R7, R8, A1, A2, A3, A4, A5, A20, A21, A22, A23, A24, A25, A26, A27 и X28 имеют описанные выше значения.
Производные 2-фтор-4-нитрофенола 10 при реакции с трифторметансульфоновым ангидридом в присутствии подходящего основания, такого как пиридин, дают соответствующие производные трифлата 11, которые в условиях реакции сочетания Сузуки с подходящей арилбороновой кислотой или гетероарилбороновой кислотой, в присутствии катализатора, такого как Pd(Ph3P)4, и основания, такого как K2CO3, дают соответствующие производные биарила 12. Для получения азот-сопряженных гетероароматических производных формулы I, производные 1,2-дифтор-4-нитробензола 16 могут взаимодействовать с подходящим гетероарильным соединением, в присутствии основания, например, K2CO3, с получением соответствующих производных биарила 12. При взаимодействии с подходящим фенолом с применением основания, такого как Cs2CO3, производные 12 дают соответствующие производные арилового эфира 13. Нитрогруппа производных 13 может быть восстановлена с применением, например, NH4Cl, в присутствии цинка или железа, с получением аминовых производных формулы B, 14, где R4 является водородом, которые могут быть конденсированы с производными формулы A 5 или 9 в присутствии, например, ЭДКИ и ДМАП, с получением производных формулы I, 15.
Схема 5:
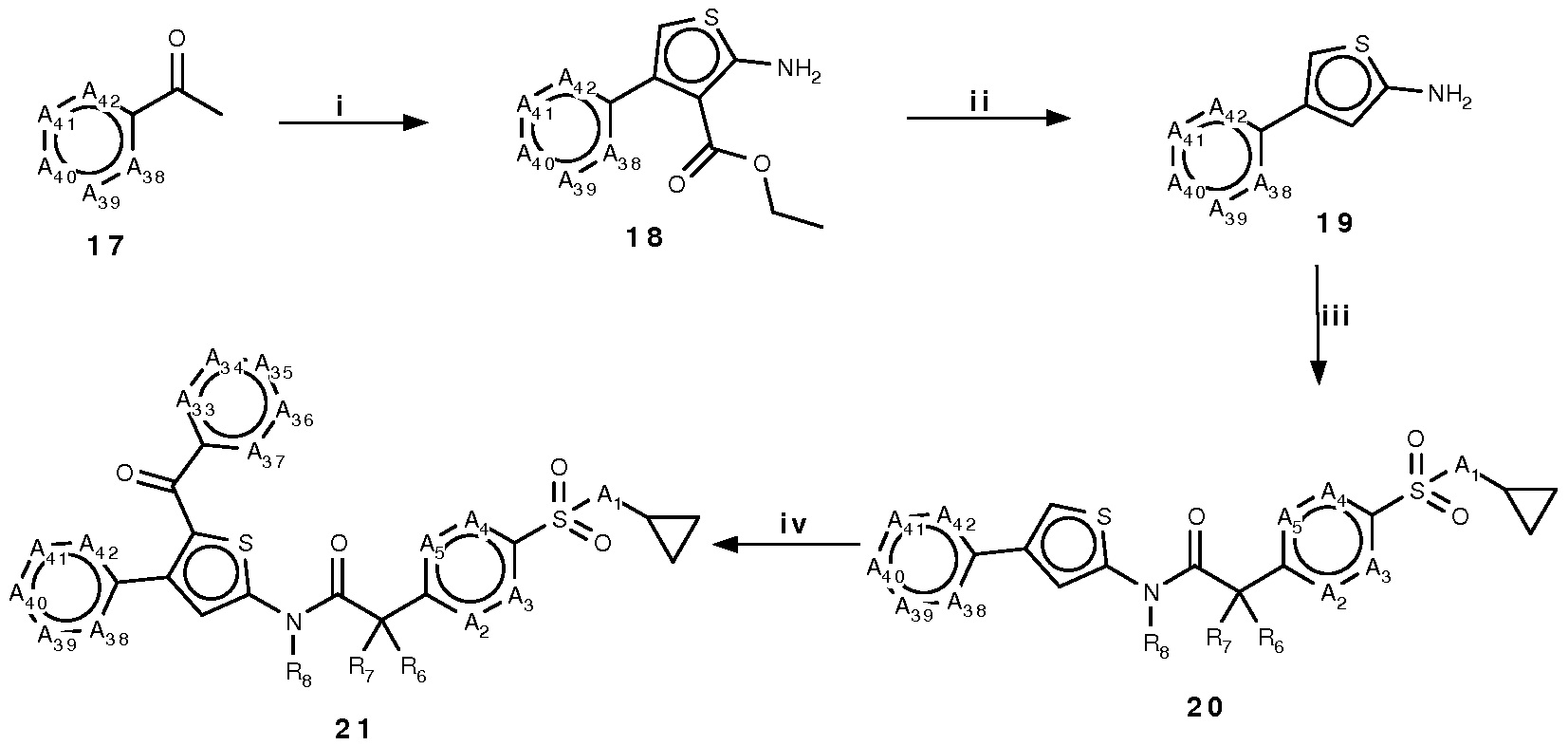
Условия: i) Этил 2-цианоацетат, сера, морфолин, EtOH, кипение с обратным холодильником; ii) NaOH, EtOH, кипение с обратным холодильником; iii) 5 или 9, ЭДКИ, ДМАП, CH2Cl2, 60°C; iv) подходящий бензоилхлорид, SnCl4, CH2Cl2, кипение с обратным холодильником.
Схема 5 представляет общий способ получения производных формулы I, 21, где A30является C, A31 является карбонилом и R6, R7, R8, A1, A2, A3, A4, A5, A33, A34, A35, A36, A37, A38, A39, A40, A41 и A42 имеют описанные выше значения.
Замещенные фенилметилкетоны 17 могут быть подвергнуты взаимодействию с этил 2-цианоацетатом и серой в присутствии морфолина с получением соответствующих сложных эфиров тиофена 18. Деэстерификация соединения 18 дает производные тиофенамино формулы B, 19, которые могут быть конденсированы с производным фенилуксусной кислоты формулы A, в присутствии, например, ЭДКИ и ДМАП, с получением соответствующих производных тиофенамида формулы I, 20. Ацилирование тиофенового кольца, катализированное SnCl4 или AlCl3, дает производные формулы I, 21.
Схема 6:

Условия: i) бис[(4-метоксифенил)метил]амин, NH4SCN, ацетон, 0°C; ii) ДМФ, 85°C; iii) ТФК, 80°C; iv) 5 или 9, ЭДКИ, ДМАП, CH2Cl2, 60°C.
На схеме 6 изображена общая схема реакции получения производных формулы I, 27, где A30 является азотом, A31 является карбонилом и R6, R7, A1, A2, A3, A4, A5, A33, A34, A35, A36, A37, A38, A39, A40, A41 и A42 имеют описанные выше значения.
Защищенные производные карбамотиоиламида 23 могут быть получены конденсацией хлорангидридов 22, тиоцианата и бис[(4-метоксифенил)метил]амина. Реакция между защищенными производными карбамотиоиламида 23 и подходящими α-бромкетонами 24, которые могут быть получены коммерчески или синтезированы из метилкетонов с применением способов, известных специалистам в данной области техники, дает защищенные производные тиазолкетона 25. Снятие защиты в кислых условиях с применением, например, ТФК, дает производные 2-аминотиазола формулы B, 26, которые могут быть конденсированы с производными формулы 5 или 9 в присутствии, например, ЭДКИ и ДМАП, с получением производных формулы I, 27.
Схема 7:

Условия: i) тиомочевина, EtOH, 80°C; ii) CuBr2, CH3CN, к.т.; iii) подходящий фенол, Cs2CO3, ацетон, 55°C; iv) 5 или 9, ЭДКИ, ДМАП, CH2Cl2, 60°C.
Схема 7 изображает общую схему реакции получения производных формулы I, 33, где A30 является азотом, A31 является кислородом и R6, R7, A1, A2, A3, A4, A5, A33, A34, A35, A36, A37, A38, A39, A40, A41 и A42 имеют описанные выше значения.
При реакции с тиомочевинной, производные α-бромкетона 28 дают производные 1,3-тиазол-2-амина 29, которые после бромирования в присутствии CuBr2 дают производные 5-бром-1,3-тиазол-2-амина 30. Замещение брома подходящим фенолом 31 дает тиазоло производные формулы B, 32, которые могут быть конденсированы с производными формулы A 5 или 9 в присутствии, например, ЭДКИ и ДМАП, с получением производных формулы I, 33.
Все применяемые структурные элементы коммерчески доступны, известны или получены способами, известными специалистам в данной области техники.
Примеры
Примеры 1-47
1: 2-(4-циклопропилметансульфонилфенил)-N-(3-фенокси-4-фенилфенил)ацетамид.
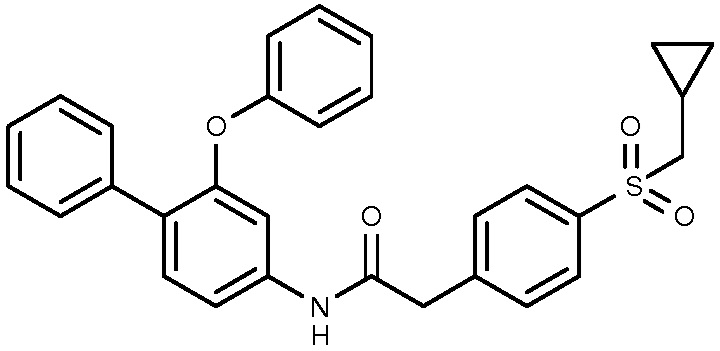
i) К раствору 2-(4-циклопропилметансульфонилфенил)уксусной кислоты (29 мг), 3-фенокси-4-фениланилин (30 мг) и ДМАП (3 мг) в CH2Cl2 (0,5 мл) по каплям добавляют при 0°C раствор ЭДКИ (32 мг) в CH2Cl2. Реакционную смесь перемешивают при 60°C в течение 1 часа в микроволнах. После охлаждения до комнатной температуры органический слой промывают насыщенным водным раствором NaHCO3, водой, затем насыщенным раствором соли, сушат над MgSO4 и концентрируют при пониженном давлении. Остаток очищают на SiO2 с применением 1%-10% метанола в CH2Cl2 в качестве элюента, с получением указанного в заголовке соединения 2-(4-циклопропилметансульфонилфенил)-N-(3-фенокси-4-фенилфенил)ацетамида (70 мг) в виде белого твердого вещества. МС(ЭР+) m/z 498,2 (M+H)+.
По методике, описанной для Примера 1, получают следующие соединения.
2: 2-(4-циклопропилметансульфонилфенил)-N-[4-(3-фторфенил)-3-(3-метоксифенокси)фенил]ацетамид.
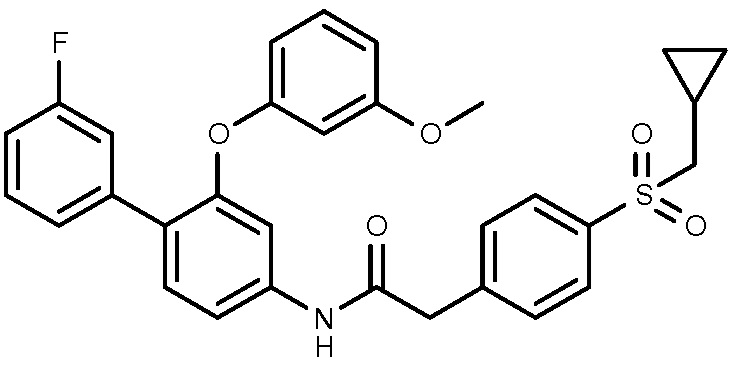
3: 2-(4-циклопропилметансульфонилфенил)-N-[3-(3-метоксифенокси)-4-(4-метил-1H-имидазол-1-ил)фенил]ацетамид.
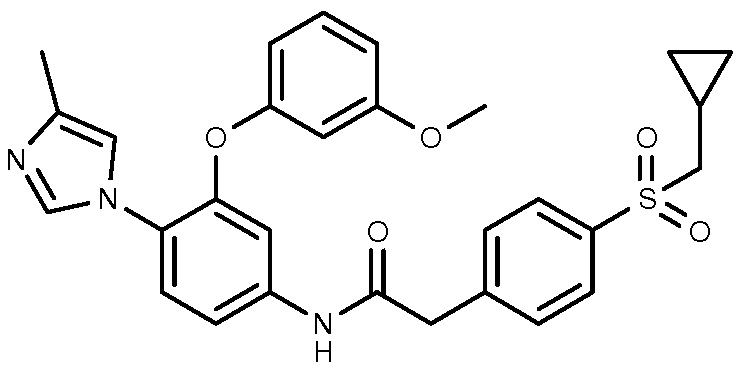
4: N-[3-(3-хлорфенокси)-4-(3-фторфенил)фенил]-2-(4-циклопропилметансульфонилфенил)ацетамид.

5: N-[3-(3-хлорфенокси)-4-(3,4-дифторфенил)фенил]-2-(4-циклопропилметансульфонилфенил)ацетамид.

6: N-[3-(3-цианофенокси)-4-(3,4-дифторфенил)фенил]-2-(4-циклопропилметансульфонилфенил)ацетамид.

7: 2-(4-циклопропилметансульфонилфенил)-N-[3-(3-метоксифенокси)-4-(5-метил-1H-пиразол-1-ил)фенил]ацетамид.

8: N-[3-(3-хлорфенокси)-4-(3,5-дифторфенил)фенил]-2-(4-циклопропилметансульфонилфенил)ацетамид.

9: N-[4-(4-цианофенил)-3-(3-фторфенокси)фенил]-2-(4-циклопропилметансульфонилфенил)ацетамид.
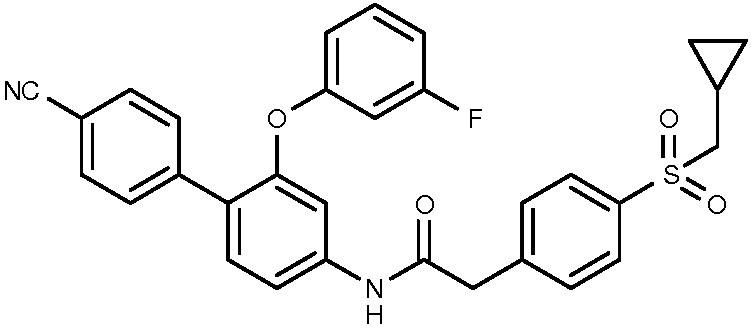
10: N-[3-(3-хлорфенокси)-4-(3-цианофенил)фенил]-2-(4-циклопропилметансульфонилфенил)ацетамид.

11: 2-(4-циклопропилметансульфонилфенил)-N-[4-(3-фторфенил)-3-[3-(трифторметил)фенокси]фенил]ацетамид.

12: 2-(4-циклопропилметансульфонилфенил)-N-[3-(3-фторфенокси)-4-(4-фторфенил)фенил]ацетамид.

13: 2-(4-циклопропилметансульфонилфенил)-N-[3-(3,5-дифторфенокси)-4-(3-фторфенил)фенил]ацетамид.
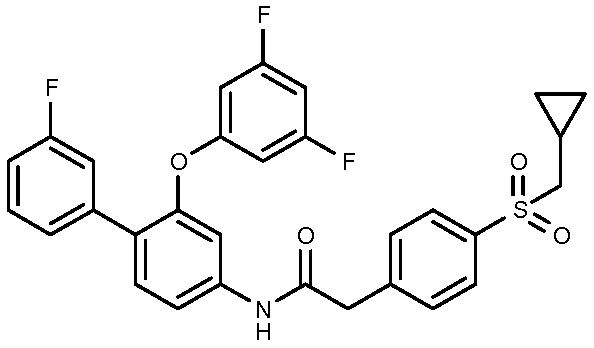
14: 2-[4-(циклопропилсульфамоил)фенил]-N-[3-(3-метоксифенокси)-4-(4-метил-1H-имидазол-1-ил)фенил]ацетамид.
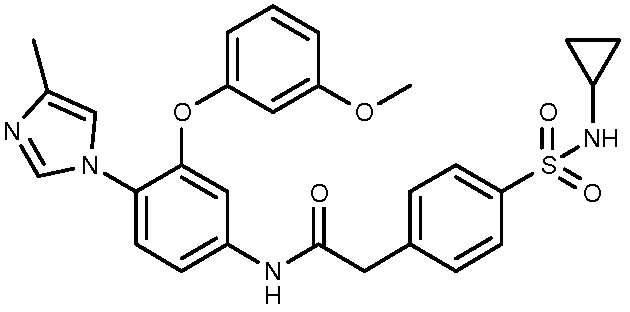
15: 2-[4-(циклопропилсульфамоил)фенил]-N-[3-(3-метоксифенокси)-4-(5-метил-1H-пиразол-1-ил)фенил]ацетамид.

16: 2-[4-(циклопропилсульфамоил)фенил]-N-[4-(3-фторфенил)-3-(3-метоксифенокси)фенил]ацетамид.

17: N-[3-(3-хлорфенокси)-4-(3-фторфенил)фенил]-2-[4-(циклопропилсульфамоил)фенил]ацетамид.

18: N-[3-(3-хлорфенокси)-4-(3,4-дифторфенил)фенил]-2-[4-(циклопропилсульфамоил)фенил]ацетамид.

19: 2-[4-(циклопропилсульфамоил)фенил]-N-[4-(3-фторфенил)-3-[3-(трифторметил)фенокси]фенил]ацетамид.

20: 2-(4-циклопропилметансульфонилфенил)-N-(5-фенокси-4-фенил-1,3-тиазол-2-ил)ацетамид.

21: 2-(4-циклопропилметансульфонилфенил)-N-[4-фенил-5-(пиридин-3-илокси)-1,3-тиазол-2-ил]ацетамид.

22: N-(5-бензоил-4-фенил-1,3-тиазол-2-ил)-2-(4-циклопропилметансульфонилфенил)ацетамид.
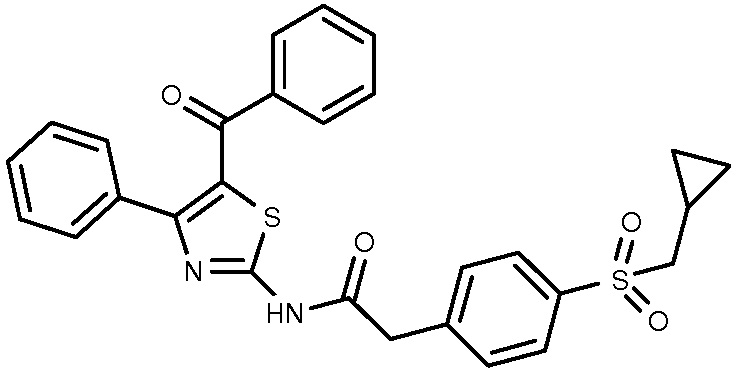
23: N-[5-(4-хлорбензоил)-4-(3-хлорфенил)-1,3-тиазол-2-ил]-2-(4-циклопропилметансульфонилфенил)ацетамид.

24: 2-(4-циклопропилметансульфонилфенил)-N-(4-фенилтиофен-2-ил)ацетамид.
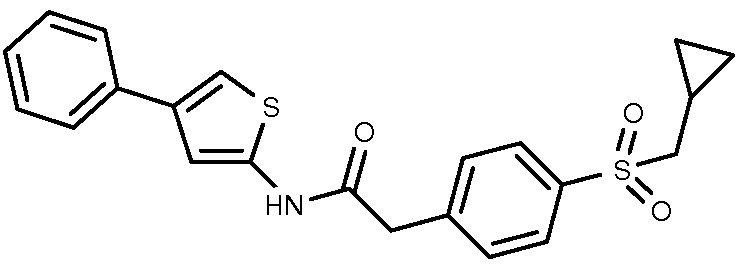
25: 2-(4-циклопропилметансульфонилфенил)-N-[4-(пиридин-3-ил)тиофен-2-ил]ацетамид.
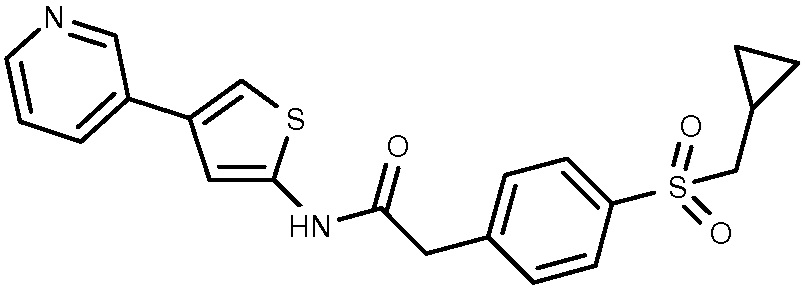
26: N-(5-бензоил-4-фенил-1,3-тиазол-2-ил)-2-[4-(циклопропилсульфамоил)фенил]ацетамид.

27: N-(5-бензоил-4-фенилтиофен-2-ил)-2-(4-циклопропилметансульфонилфенил)ацетамид.

28: N-{3-хлор-4-[2-(трифторметокси)фенил]фенил}-2-(4-циклопропилметансульфонилфенил)ацетамид.

29: 2-(4-циклопропилметансульфонилфенил)-N-{3-метил-4-[2-(трифторметокси)фенил]фенил}ацетамид.
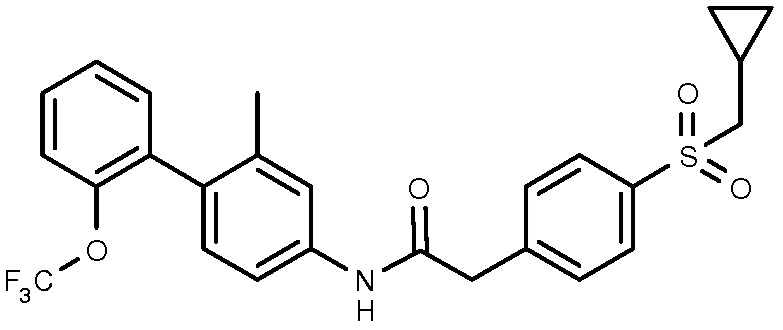
30: 2-(4-циклопропилметансульфонилфенил)-N-{3,5-дихлор-4-[2-(трифторметокси)фенил]фенил}ацетамид.
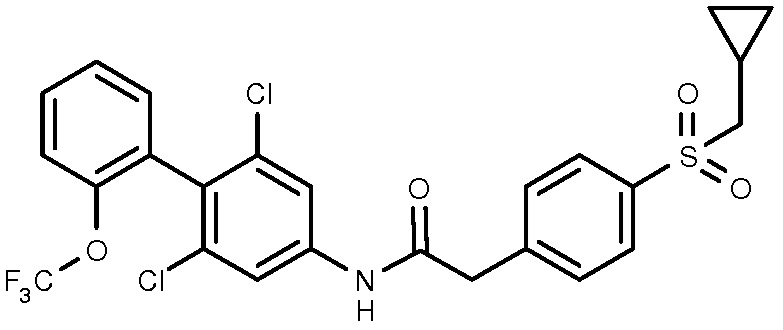
31: 2-(4-циклопропилметансульфонилфенил)-N-{4-метил-5-[2-(трифторметокси)фенил]пиридин-2-ил}ацетамид.
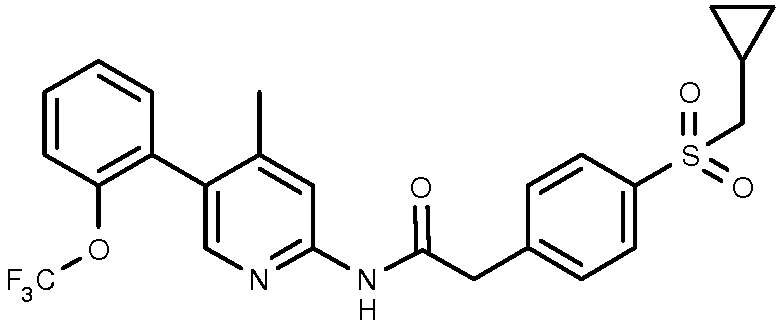
32: 2-(4-циклопропилметансульфонилфенил)-N-{6-метил-5-[2-(трифторметокси)фенил]пиридин-2-ил}ацетамид.

33: N-{3-хлор-4-[2-(трифторметокси)фенил]фенил}-2-[4-(циклопропилсульфамоил)фенил]ацетамид.

34: 2-[4-(циклопропилсульфамоил)фенил]-N-{6-метил-5-[2-(трифторметокси)фенил]пиридин-2-ил}ацетамид.

35: 2-[4-(циклопропилсульфамоил)фенил]-N-{4-метил-5-[2-(трифторметокси)фенил]пиридин-2-ил}ацетамид.
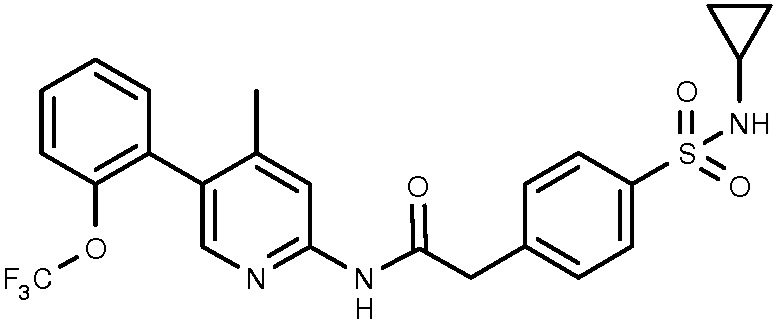
36: 2-[4-(циклопропилсульфамоил)фенил]-N-{3-метил-4-[2-(трифторметокси)фенил]фенил}ацетамид.
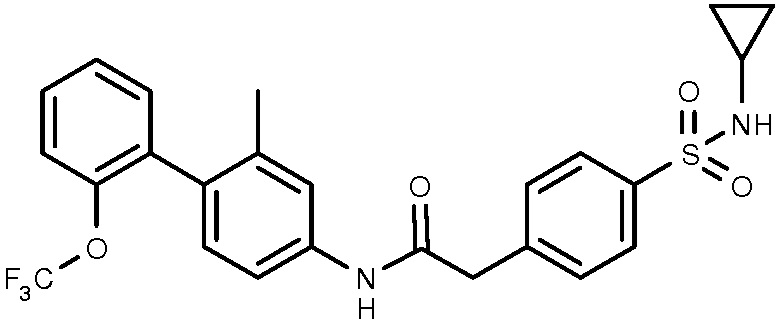
37: 2-(4-циклопропилметансульфонилфенил)-N-{4,6-диметил-5-[2-(трифторметокси)фенил]пиридин-2-ил}ацетамид.

38: 2-(4-циклопропилметансульфонилфенил)-N-[4-(4-метил-1H-имидазол-1-ил)фенил]ацетамид.

39: 2-(4-циклопропилметансульфонилфенил)-N-[4-(5-метил-1H-имидазол-1-ил)фенил]ацетамид.

40: 2-(4-циклопропилметансульфонилфенил)-N-[4-(3-метил-1H-пиразол-1-ил)фенил]ацетамид.

41: 2-(4-циклопропилметансульфонилфенил)-N-[4-(5-метил-1H-пиразол-1-ил)фенил]ацетамид.

42: 2-(4-циклопропилметансульфонилфенил)-N-[4-(4-метил-1H-пиразол-1-ил)фенил]ацетамид.

43: 2-(4-циклопропилметансульфонилфенил)-N-[4-(1,3-оксазол-5-ил)фенил]ацетамид.
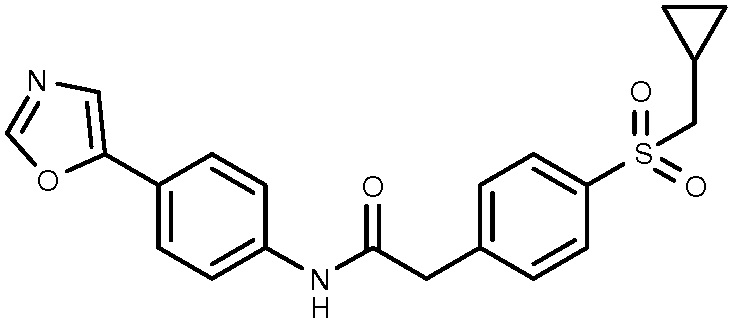
44: 2-(4-циклопропилметансульфонилфенил)-N-[4-(1H-пиразол-1-ил)фенил]ацетамид.

45: 2-(4-циклопропилметансульфонилфенил)-N-[4-(1H-имидазол-1-ил)фенил]ацетамид.

46: 2-(4-циклопропилметансульфонилфенил)-N-[4-(1H-1,2,4-триазол-1-ил)фенил]ацетамид.

47: 2-(4-циклопропилметансульфонилфенил)-N-[4-(1,2,4-оксадиазол-3-ил)фенил]ацетамид.
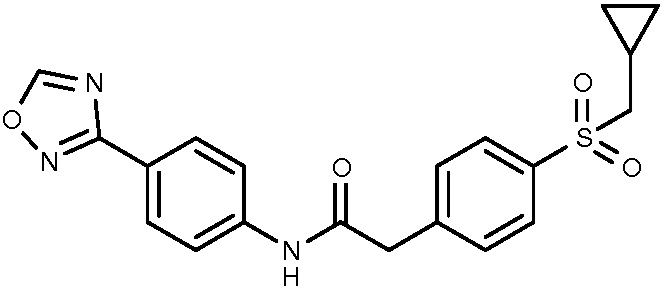
Пример 48
Анализ гена-репортера RORγ GAL4
Ингибиторы из примеров 1-47 тестируют на способность ингибировать активность RORγ в анализе гена-репортера RORγ GAL4. Методика анализа и результаты описаны ниже.
Описание анализа гена-репортера RORγ GAL4
GAL4 одногибридная система репортера, применяющая люциферазное считывание разработана для определения ингибирования RORγ в клетках 293FT. Лиганд-связывающий RORγ домен (ЛСД) конденсируют с ДНК-связывающим доменом дрожжей GAL4 (ДСД) и помещают под контроль немедленно-раннего промотора цитомегаловируса человека (ЦМВ) с применением вектора экспрессии pFN26A (Promega) и стандартных методов клонирования рекомбинантной ДНК. В качестве контроля в анализе создают подобный вектор, в котором GAL4-ДСД конденсирован с белком 16 вируса простого герпеса (VP16), конститутивным транскрипционным активатором.
Для отслеживания ингибирующего действия соединений на RORγ применяют конструкцию транскрипционного репортера. Вектор pGL4.35 (Promega) содержит девять копий GAL4 активирующей последовательность (UAS). Эта последовательность управляет транскрипцией гена-репортера люциферазы luc2P в ответ на связывание слитого белка, содержащего GAL4 ДНК связывающий домен, такой как, например, экспрессируемый векторами экспрессии GAL4-RORγ-ЛСД и GAL4-VP16, описанными выше. Для того чтобы GAL4 слитый белок управлял экспрессией репортера люциферазы, вектор экспрессии pGL4.35 и подходящий вектор экспрессии GAL4 слитого белка массово трансфицируют в клетки 293FT с применением стандартных методов трансфекции.
Через день после трансфекции клетки помещают 96-луночные планшеты, добавляют тестируемое соединение и планшеты инкубируют в течение ночи. Затем активность люциферазы светляков количественно оценивают с применением реагента для определения люциферазы и считывания люминесцентности.
Подробное описание анализа
Клетки 293FT (Invitrogen) трансфицируют вектором экспрессии GAL4 слитого белка (как описано выше) и конструкцией транскрипционного репортера (pGL4.35, Promega). 60 мкл реагента трансфекции TransIT-293 (Mirus Bio) добавляют по каплям в 1500 мкл Opti-MEM I восстановленной сывороточной среды (Invitrogen) и инкубируют при комнатной температуре (КТ) в течение от 5 до 20 минут. 1500 мкл этого реагента добавляют к 5 мкг вектора экспрессии GAL4 слитого белка и 5 мкг конструкции транскрипционного репортера, и инкубируют при КТ в течение 20 минут.
Для сбора клеток 293FT из колбы T75, сначала культуральную среду убирают от клеток. Затем клетки промывают физиологическим раствором с фосфатным буфером (ФРФБ) (Lonza), затем ФРФБ удаляют. Для разъединения клеток 1 мл TrypLE Express (Invitrogen) добавляют в колбу, затем инкубируют при КТ до тех пор, пока клетки не начнут визуально разъединяться. Клетки собирают в 5 мл аналитической среды (культуральная среда DMEM (Lonza), 10% диализированного ФРФБ (Invitrogen) и Pen/Strep (Lonza)) для получения суспензии отдельных клеток. 10×106 клеток центрифугируют и ресуспендируют в 10 мл аналитической среды. Затем суспензию клеток добавляют в пробирку с трансфекционной смесью, и затем переносят как единое целое в колбу T75 (Greiner), затем инкубируют в течение ночи (16-24 часов) при 37°C и 5% CO2.
Для скрининга соединения клетки собирают (как описано выше) и считают. 13×106 клетки центрифугируют, надосадочную жидкость отсасывают и клетки ресуспендируют в 17,3 мл аналитической среды с получением суспензии клеток 0,75×106 клеток/мл. 80 мкл суспензии клеток (60000 клеток) помещают на лунку в белые плоскодонные обработанные культурой тканей 96-луночные планшеты для скрининга (Greiner).
Тестируемые соединения разводят, начиная с 10 мМ исходного раствора диметилсульфоксида (ДМСО), до серийных разбавлений в ДМСО при 500× конечной тестируемой концентрации. Затем эти растворы разводят до 5× конечной тестируемой концентрации в две стадии с 10-кратным разведением в аналитической среде. Конечная концентрация ДМСО 5× раствора тестируемого соединения составляет 1%. 20 мкл 5× тестируемого соединения добавляют в каждую тестируемую лунку 96-луночного планшета, предварительно покрытого 80 мкл клеточной суспензии, с получением конечной тестируемой концентрации с 0,2% ДМСО.
Планшеты инкубируют в течение ночи (16-24 часов) при 37°C и 5% CO2.
Для считывания люциферазы, люциферазный реагент (Britelite Plus, Perkin Elmer) доводят до КТ. В каждую тестируемую лунку планшетов для скрининга добавляют 100 мкл 2,5-кратно разведенного реагента Britelite Plus, затем инкубируют при КТ в течение 10 минут. Сигнал люциферазной люминесценции измеряют с применением микропланшетного ридера Wallac Victor Microplate Reader (Perkin Elmer).
Значения половины максимальной ингибирующей концентрации (IC50) для тестируемых соединений рассчитывают из сигнала люциферазы с применением программы GraphPad Prism (GraphPad Software).
Было найдено, что все представленные соединения формулы I (примеры 1-47) имеют средние значения pIC50 выше 5.
Было найдено, что примеры 1-14, 16-37, 40-44 и 46-47 имеют средние значения pIC50 выше или равные 6.
Было найдено, что примеры 2-13, 22, 23, 26-34, 36 и 37 имеют средние значения pIC50 выше или равные 7.
Реферат
Изобретение относится к соединениям формулы I, обладающим свойствами ингибитора RORγ-активности, и фармацевтической композиции на их основе для лечения RORγ-опосредованных заболеваний или состояний. В общей формуле I Aявляется NRили CR, где Rявляется H или метилом, где метил, если присутствует, необязательно замещен одним или более F; циклопропильная часть может быть необязательно замещена одним или более метилом и одним или более F; A-Aпредставляют собой CR-CRсоответственно; R-Rнезависимо являются H или C(1-6)алкилом; Rи Rнезависимо являются H, метилом или гидроксилом, все алкильные группы, если присутствуют, необязательно замещены одним или более F; Rявляется Н или C(1-2)алкилом и Rвыбирают из группы, включающей формулу II, III, IV и V. Остальные значения радикалов указаны в формуле изобретения. 3 н и 14 з.п. ф-лы, 48 пр.
Формула



Комментарии