Самоклеящаяся чрескожная матричная система и способ ее получения - RU2110282C1
Код документа: RU2110282C1
Чертежи





Описание
Объектом изобретения является новое приспособление или чрескожная матричная система для длительного выделения эстрогенового компонента и/или прогестогенового компонента, при этом упомянутое приспособление состоит из подложки с самоприлипающей матрицей, которая содержит трехблочный сополимер с A-B-A звеньями типа поли(стирол-изопрен-стирол), сокращенно SIS, в котором растворен упомянутый экстрогеновый компонент и(или) упомянутый прогестогеновый компонент, в сочетании с парой пластификатор/промотор. Изобретение также касается способа получения упомянутой матричной системы.
Известно, что уже предлагались многочисленные чрескожные системы для выделения экстрогенового компонента и/или прогестогенового компонента. Они обычно включают так называемые "резервуарные" системы, в которых активный ингредиент растворен в растворителе, который служит в качестве транспортного вектора по отношению к коже через микропористую мембрану.
Это является случаем использования приспособлений, основанных на (i) 17- β -экстрадиоле и (ii) 17 - β -эстрадиоле в сочетании с норэтистеронацетатом, продаваемых компанией CIBA - GEIGY под соответственно торговыми названиями ESTRADERM® TTS и ESTRAGEST® TTS.
Кроме того, существуют так называемые матричные системы, в которых активные ингредиенты растворены или диспергированы в клейкой матрице, основанной на полимерах, например, на сополимерах EVA (этилена и винилацетата), акрил, поли(стирол-изопрен-стирола).
Для того, чтобы получить терапевтически эффективный конечный продукт, существенно, чтобы все эти системы сохраняли уровень введения активных ингредиентов в течение продолжительного периода времени при скорости, достаточной для получения уровней плазмы, которые применимы для потребностей терапии. Для хорошего восприятия пациентом они должны быть относительно небольшого размера с оптимальными адгезионными и когезионными свойствами, с тем, чтобы они были практичными при использовании и не причиняли ущерб одежде вследствие деформации массы матрицы во время использования.
Однако специалистам в данной области известно, что эстрогеновые компоненты и прогестогеновые компоненты являются продуктами (i), которые малорастворимы в полимерах, используемых для чрескожных систем и (ii) что они с трудностями переходят через кожный барьер.
Следовательно, выделенные количества этих активных ингредиентов для получения желательного терапевтического эффекта являются обычно низкими по сравнению с исходными количествами, присутствующими в чрескожных приспособлениях, вследствие этого выход является низким. Это приводит к неизбежному использованию гораздо большего количества гормона(ов), чем то количество, которое фактически потребляется.
В этом случае трудно достигнуть компромисса между эффективной скоростью чрескожного введения одного или нескольких гормонов и соответствующими физическими или эргономичными свойствами систем.
Хотя многочисленные составы, основанные на трехблочном сополимере SIS, известны из EP-A-0439180, EP-A-0285181 или EP-A-0483370, ни в одной их этих публикаций не обнаружены и не предложены конкретные составы изобретения.
В области введения эстрогенового компонента и(или) прогестогенового компонента чрескожным путем, желательно иметь новый технический раствор, который использует матричную систему, в которой матрица содержит трехблочный сополимер SIS, с которым может быть достигнут желательный компромисс без вышеупомянутых недостатков и, кроме того, превосходный выход.
В соответствии с первым аспектом изобретения предлагается обеспечение чрескожной матричной системы, в которой матрица содержит SIS материал для введения эстрогенового компонента и/или прогестогенового компонента.
В соответствии с вторым аспектом изобретения предлагается обеспечение способа получения такой системы.
Вышеупомянутые цели достигаются при использовании нового технического раствора, согласно которому матрица в матричной системе, которая содержит эстрогеновый компонент и/или прогестогеновый компонент, по существу выполнена из SIS материала и пары пластификатор/промотор.
В соответствии с изобретением, во-первых, обеспечивается в качестве нового промышленного продукта чрескожная матричная система для чрескожного
введения гормона, при этом упомянутая матричная система, которая содержит подложку и самоприлипающую матрицу, отличается тем, что упомянутая матрица содержит:
(a) 20 - 42 мас.ч. трехблочного
сополимера поли(стирол-изопрен-стирола),
(b) 35 - 55 мас.ч. смолы, повышающей клейкость,
(c) 5 - 25 мас.ч. пластификатора, выбранного из группы, состоящей из олеинового спирта,
пегликоль-5-олеата, пропиленгликольлаурата или полипропоксилового эфира цетилового спирта,
(d) 5 - 15 мас.ч. по крайней мере, одного соединения, выбранного из группы, состоящей из:
кротамитона и
N-замещенных 2-пирролидонов формулы (I)
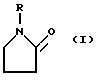
в которой:
R представляет (C1 - C15)-алкильную, циклогексильную или 2-гидроксиэтильную группу,
(e) 0,01 - 1 мас.ч. стабилизатора, и
(f) 0,1 - 5 мас.ч. гормона, выбранного из группы, состоящей из эстрогеновых компонентов, прогестогеновых компонентов и их смесей.
Во-вторых, предлагается способ получения упомянутой чрескожной матричной системы, который
отличается тем, что он включает следующие стадии, которые состоят из:
(α) смешивание SIS полимера, стабилизатора и смолы, повышающей клейкость, при температуре выше 110oC и
затем гомогенизации полученной смеси;
(β) включения в гомогенную смесь, полученную таким образом, промотора или промоторов и пластификатора при 80 - 110oC, и затем
гомогенизации полученной смеси;
(γ) включения в гомогенную смесь, полученную таким образом, гормона, выбранного из группы, состоящей из эстрагеновых компонентов, прогестогеновых
компонентов и их смесей, и затем гомогенизации полученной смеси;
(δ) нанесения гомогенной смеси, полученной таким образом, при 80 - 130oC на временную неклейкую подложку
таким образом, чтобы получить покрытие на упомянутой подложке 50 - 300 г/м2, и
(ε) переноса упомянутого покрытия на конечную подложку;
или из:
(α)
смешивание SIS полимера, стабилизатора, затем смолы, повышающей клейкость, в растворителе упомянутого SIS полимера при температуре ниже температуры кипения упомянутого растворителя, затем
гомогенизации полученной смеси;
(β) включения в смесь, полученную таким образом, промотора или промоторов и пластификатора, затем гомогенизацию полученной смеси;
(γ)
включения в гомогенную смесь, полученную таким образом, гормона, выбранного из группы, состоящей из эстрогеновых компонентов, прогестогеновых компонентов и их смесей, затем гомогенизации полученной
смеси;
(δ) нанесения гомогенной смеси, полученной таким образом, при комнатной температуре на временную неклейкую подложку таким образом, чтобы получить покрытие на упомянутой подложке
50 - 300 г/м2;
(e) выпаривания растворителя путем нагрева упомянутого покрытия до температуры выше температуры выкипания упомянутого растворителя, затем переноса упомянутого
покрытия на конечную подложку.
На приложенных фиг. 1 и 5 представляют количество (Q), выраженное в μ г/см2, выделенного 17- β -эстрадиола, в виде функции времени (t), выраженного в часах; фиг. 2 - 4 и 6 представляют выход (R), выраженный в %, 17- β - эстрадиола или NETA (норэтистеронацетата) в виде функции времени (t), выраженного в часах.
Фиг. 1 дает сравнение (в системе Q/t) между кривыми 4 и A, относящимися к выделению 17- β -эстрадиола, полученного с продуктом примера 4 в соответствии с изобретением и со
сравнительным продуктом CP4;
Фиг. 2 дает сравнение (в системе R/t) между кривыми 10, 11, 12, и E2, относящимися к выходу выделенного 17- β -эстрадиола, соответственно полученного с
продуктами примеров 10, 11 и 12 в соответствии с изобретением и известным чрескожным продуктом, известным под торговым названием ESTRAGEST® , продаваемым компанией CIBA - GEIGY.
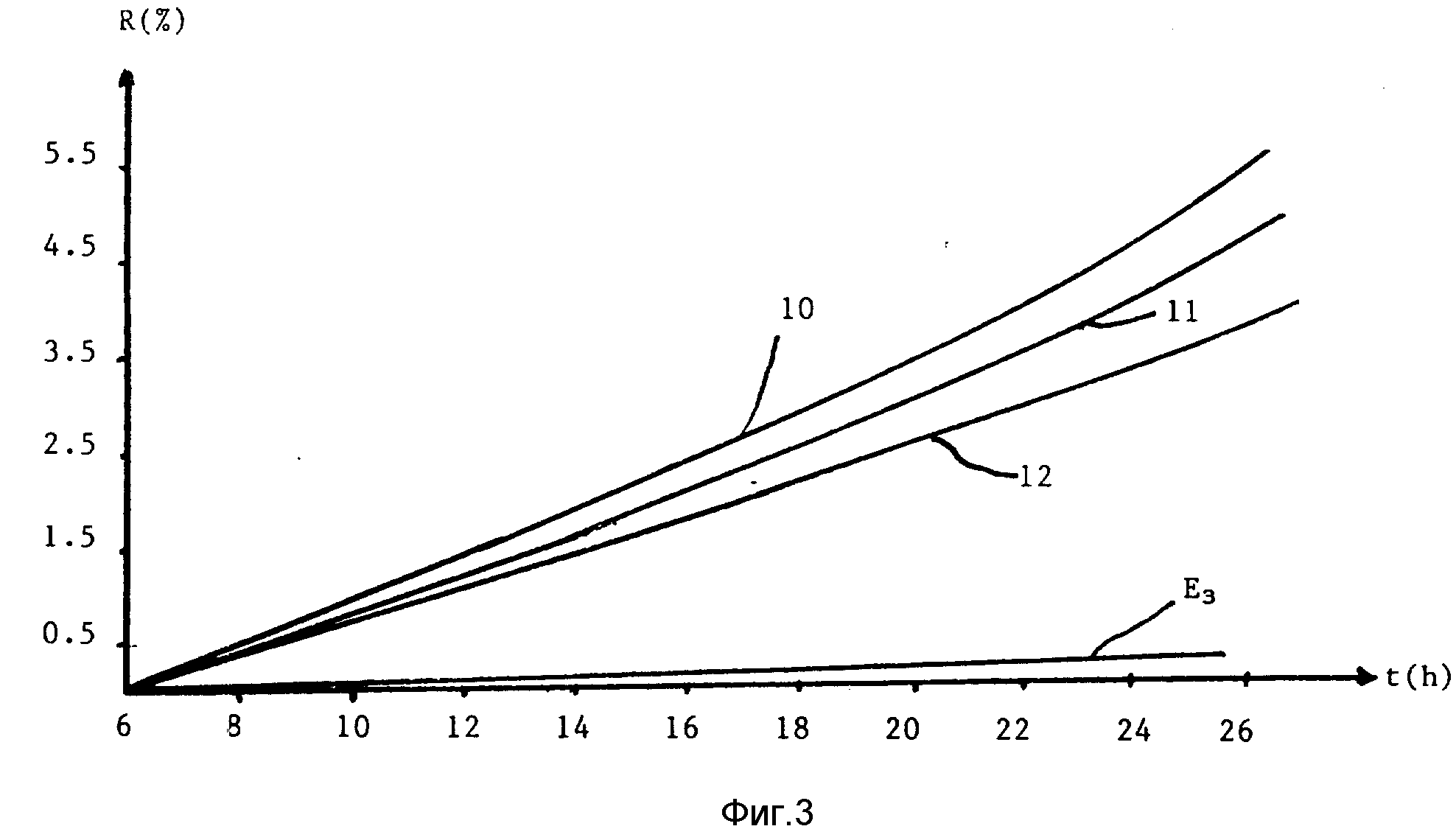
Фиг. 3 дает сравнение (в системе R/t) между кривыми 10, 11, 12 и E3, относящимися к выходу выделенного NETA, соответственно полученного с продуктами примеров 10, 11 и 12 в
соответствии с изобретением и упомянутым ESTRAGESTом®.
Фиг. 4 дает сравнение (в системе R/t) между кривыми 5 и E4, относящимися к выходу выделенного 17- β
-эстрадиола, полученного соответственно с продуктом примера 5 в соответствии с изобретением и упомянутым ESTRAGESTом® .
Фиг. 5 дает сравнение (в системе Q/t) между кривыми 8 и 9 и E5, относящимися к выделению 17- β -эстрадиола, полученного соответственно с продуктами примеров 8 и 9 в соответствии с изобретением и упомянутым ESTRAGESTом® .
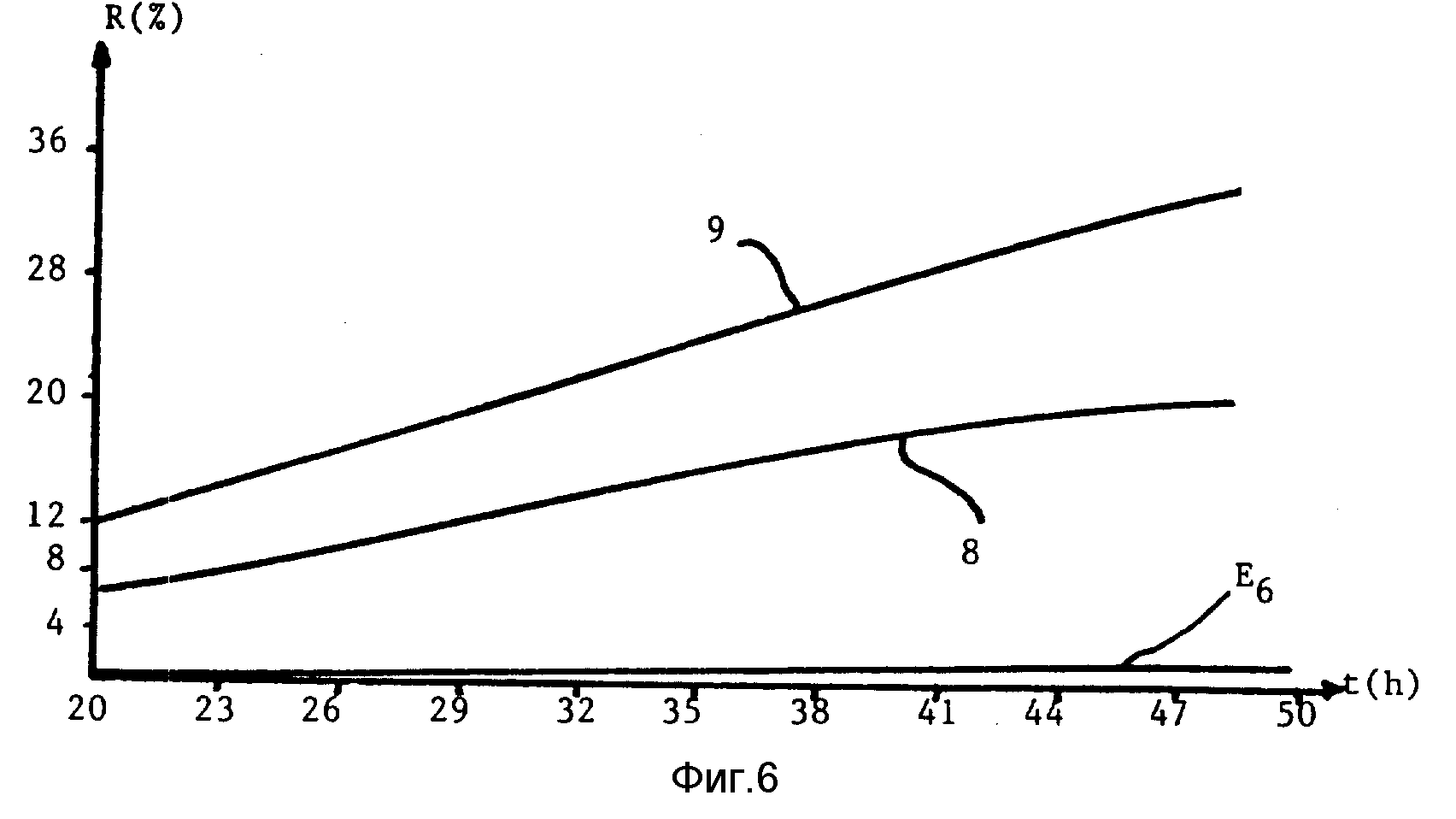
Фиг. 6 дает сравнение (в системе R/t) между кривыми 8, 9 и E6, относящимися к выходу выделенного NETA, полученного соответственно с продуктами примеров 8 и 9 в соответствии с изобретением и упомянутым ESTRAGESTом® .
Трехблочный сополимер поли(A-B-A) типа поли(стиролизопренстирол) означает здесь SIS материал с содержанием стирола от 14 до 50 мас.% относительно веса упомянутого SIS. Предпочтение отдается SIS, содержащему от 17 до 47 мас.% стирола. Можно также использовать смеси этих SIS.
Среди смол, повышающих клейкость, которые являются подходящими в соответствии с изобретением, можно упомянуть такие смолы, которые обычно используются специалистами в области клеев, например, политерпеновые смолы или модифицированные терпеновые смолы, гидрированные или полимеризованные канифольные смолы, смолы этерифицированной канифоли.
Особое предпочтение отдается углеводородным смолам, например, таким, которые продаются компанией EXXON CHEMICAL под торговым названием ESCORES® -385. С этими смолами, используемыми вместе с предпочтительным SIS изобретения, можно получить оптимальные адгезионные свойства.
"Активный" ингредиент или "гормон" означает здесь любой эстрогеновый компонент, любой прогестогеновый компонент или любую смесь эстрогенового компонента/прогестогенового компонента, которая может быть применена чрескожным путем.
Среди эстрогеновых компонентов, которые являются подходящими в соответствии с изобретением, следует в особенности упомянуть 17- β -эстрадиол и производные эстрадиола, особенно моно- и диэфиры эстрадиола, например эстрадиол-17-ацетат, эстрадиол-3,17-диацетат, эстрадиол-3-бензоат, эстрадиол-17-ундеканоат, алкилпроизводные эстрадиола в 17-положении, например, этинилэстрадиол, этинилэстрадиол-3-изопропилсульфонат, метилэстрадиол, хинестрол, местранол и, если являются подходящими, их смеси.
Среди прогестогеновых компонентов, которые являются подходящими в соответствии с изобретением, следует в особенности упомянуть прогестерон, медрогестерон и их производные (главным образом 17-гидроксипрогестеронацетат, медроксипрогестеронацетат), норэтистерон и его производные, в особенности 17-норэтистеронацетат.
В соответствии с настоящим изобретением предпочтительным является использование 17- β -эстрадиола для эстрогенового компонента и норэтистерона (NETA) для прогестогенового компонента. В соответствии с вариантом осуществления изобретения чрескожная матричная система в соответствии с изобретением может одновременно содержать эстрогеновый компонент и прогестогеновый компонент.
Среди стабилизаторов, используемых в соответствии с изобретением, можно упомянуть антиоксиданты, широко используемые специалистами в данной области, например, продукты, продаваемые компанией CIBA-GEIGY под торговым названием IRGANOX® 565 или IRGANOX® B215.
Промотор, продукт (d), можно выбрать из группы, состоящей из кротамитона, N-алкил-2-пирролидоновых соединений, в которых алкильной группой является C1-C15, N-(2-гидроксиэтил)-2-пирролидона, N-циклогексил-2-пирролидона и их смесей.
Среди N-(C1-C15)-алкил-2-пирролидонов, используемых в настоящем изобретении, предпочтение отдается N-метил-2-пирролидону, N-этил-2-пирролидону, N-октил-2-пирролидону, N-додецил-2-пирролидону, продаваемым компанией GAF CORPORATION под соответствующими торговыми названиями NMP®, NEP®, SURFADONE® LP 100 и SURFADONE® LP 300 и их смесями.
Когда пластификатором является полипропоксиловый эфир цетилового спирта, предпочтение отдается соединению, содержащему в частности 10 моль пропиленоксида на 1 моль цетилового спирта, например, такому продукту, который продается компанией CRODA FRANCE S.A. под торговым названием PROCETYL® .
Подложкой, вмещающей матрицу, может быть любая подложка переменной толщины, которую обычно используют для чрескожных систем, которая является непроницаемой для составных частей матрицы. Предпочтение может быть отдано, например, подложке в полиэтиленовой полипропиленовой или полиэфирной пленке, комплексу (или композиту), состоящему из полиэтилена, и сополимеру винилацетата и этилена, или даже вспененным материалам.
Для практических целей поверхность матрицы, которая не прикреплена к подложке, можно покрыть защитным слоем или пленкой, которую можно отслоить перед использованием приспособления; упомянутое приспособление может быть само упаковано в герметичное средство, например, полиэтилен-алюминиевые комплексы.
Вследствие особенности композиции таких составов, которые могут образовывать матрицу, только матричная система в соответствии с изобретением предлагает многочисленные преимущества, которые описаны ниже.
Было найдено, что только состав, определенный выше, содержащий: (1) пару пластификатор/промотор, в которой (i) пластификатор представляет олеиновый спирт, пегликоль-5-олеат, пропиленгликольлаурат или полипропоксиловый эфир цетилового спирта и (ii) промотором является по крайней мере одно соединение, выбранное из N-замещенных 2-пирролидонов формулы I и кротамитона, и (2) SIS материал, позволяет достигнуть замечательного выхода и желательных адгезионных и когезионных свойств.
Идентичные результаты не могут быть получены с матрицей с другим типом сополимерной основы, например, сополимером этилена и винилацетата (EVA), используемым вместе с этой парой пластификатор/промотор.
Несомненно, что это может быть приписано (i) особенному синергетическому эффекту между природой трехблочных сополимеров поли(стирол-изопрен-стирола), которые имеют склонность "отталкивать" присутствующий гормон или гормоны, которые нерастворимы в последнем и (ii) роли, играемой конкретными пластификаторами, которые расширяют полимерные цепи SIS, представляя им более просторное движение, вследствие этого жесткость макромолекулярной полимерной сетки, что облегчает циркуляцию гормона или гормонов.
Эти пластификаторы, однако, которые получены из жирных веществ, если их используют в слишком большом количестве, могут ухудшить адгезионные и/или когезионные свойства матрицы. Поэтому существенно, чтобы их использовали вместе с одним или несколькими промоторами кожного проникновения различной природы, например, кротамитоном или N-замещенными 2-пирролидонами формулы I для получения желательных скоростей введения и достижения улучшенного выхода, при этом без потерь в адгезионных и когезионных свойствах.
Упомянутые кротамитон и N-замещенные 2-пирролидоны формулы I также обеспечивают улучшенную растворимость гормонов, используемых в матрице.
Эти конкретные составы приводят к самоприлипающим чрескожным системам с хорошими когезионными и адгезионными свойствами и обеспечивают выходы эстрогенового компонента за 24 или 48 ч в области 10 - 84 % и прогестогенового компонента в области 3,5 - 32 %. Возможность использования эстрогенового компонента и/или прогестогенового компонента в меньшем количестве при получении больших введенных количеств упрощает создание и производство составов, образующих матрицу приспособлений.
Таким образом, проблемы растворимости гормона в сополимерах SIS и также риск, связанный с физической несовместимостью с другими составляющими матрицы, могут быть уменьшены или устранены. Это также относится к проблемам, связанным с кристаллизацией гормона и неустойчивостью приспособлений со временем, при этом такое явление (неустойчивость) является нежелательным для одобрения и продажи продуктов, предназначенных для терапевтических целей, например чрескожных систем.
Последнее, но принимаемое в расчет преимущество, относится к себестоимости, которая в значительной степени уменьшена по сравнению с известными приспособлениями предшествующего уровня техники в данной области, благодаря использованию незначительного количества гормона, цена которого является высокой.
Чрезкожные матричные системы в соответствии с изобретением получают с применением методик, обычно используемых специалистами в данной области: либо покрытием (в фазе растворителя), либо при использовании так называемой методики "расплава" (т.е. без присутствия растворителя).
В любом случае для промышленных производственных целей большие площади поверхности покрывают и затем разрезают для получения приспособлений, размер которых в соответствии с количеством гормона(ов), присутствующего(их) на единице площади поверхности, приспособлен к выбранной дозе активного ингредиента, вводимого в течение данного времени.
Для так называемой методики в фазе растворителя обеспечен способ получения самоприлипающей чрескожной матричной системы в соответствии
с изобретением, который включает следующие стадии:
(1) в реактор, снабженный термостатом, содержащий растворитель полимера, нагретый до температуры, которая ниже температуры выкипания
растворителя (например, 60oC для этилацетата) добавляли при перемешивании SIS, стабилизатор и затем смолу, повышающую клейкость, до тех пор, пока смесь стала совершенного гомогенной;
(2) при непрерывном перемешивании и нагреве до той же самой температуры ввели все жидкие компоненты, т.е. промотор или промоторы и пластификатор, при этом полученную смесь гомогенизировали;
(3) активный ингредиент или ингредиенты или непосредственно в порошковой форме, или в растворе в растворителе эстрогенового компонента и/или прогестогенового компонента, например, такого как
тетрагидрофуран, вводили в смесь, полученную на стадии (2), при продолжительном перемешивании и нагреве до той же самой температуры до полной гомогенизации;
(4) гомогенную смесь, полученную
на стадии (3), нанесли на временную неклейную подложку, например силиконовую полиэфирную пленку, для того, чтобы получить осадок от 50 до 300 г/м2;
(5) осадок, полученный таким
образом, нагрели для выпаривания растворителя при температуре, зависящей от точки кипения растворителя, между 40 и 110oC, предпочтительно при 60 - 80oC; и
(6) полученную
сухую матрицу перенесли на выбранную конечную подложку.
Для методики "расплава" обеспечен способ, который включает следующие стадии:
(1а) в смеситель при температуре выше
110oC, предпочтительно 130oC, в SIS полимер/стабилизатор последовательными порциями, равными 10, 30 и 60 %, при перемешивании ввели смолу, повышающую клейкость, таким образом,
что после каждой добавленной порции получали совершенно однородную смесь;
(2а) в смесь, полученную на стадии (1а), постепенно ввели большую часть жидких продуктов состава, т.е. пластификатор
и промотор или промоторы при непрерывном перемешивании и при температурах, которые обычно ниже, чем на стадии (1а), которая определяется термостойкостью продуктов; перемешивание продолжали до полной
гомогенизации полученной смеси;
(3а) в гомогенную смесь, полученную на стадии (2а), при температуре около 100oC ввели активный ингредиент или ингредиенты и перемешивание продолжали
до получения совершенно гомогенной смеси;
(4а) гомогенную смесь, полученную таким образом, при 80 - 130oC нанесли нам временную неклейкую подложку в частности, силиконовую
полиэфирную пленку, для того, чтобы получить осадок 50 - 300 г/м2; и
(5а) матрицу, полученную на стадии (4а), перенесли на выбранную конечную подложку,
Чрезкожные системы
в соответствии с изобретением в особенности пригодны для лечения симптомов менопаузы и возникающих сердечно сосудистых рисков, остеопороза и любой терапии, в которой используются чрезкожный способ
применения лекарственного средства, требующий введения эстрогенов и/или прогестогенов.
Лучший вариант изобретения состоит в использовании чрезкожной матричной системы, матрица которой
содержит на суммарные 100 мас.ч.:
(a) 37,3 мас.ч. трехблочного сополимера (поли-(стирол-изопрен-стирола),
(b) 38 мас.ч. смолы, повышающей клейкость,
(c) 15 мас.ч.
пропиленгликольлаурата,
(d) 7 мас.ч. N-октил-2-пирролидона,
(e) 0,2 мас.ч. стабилизатора,
(f) 0,5 мас.ч. 17- β -эстрадиола, и
(g) 2 мас.ч.
норэтистеронацетата.
Другие преимущества и особенности изобретения будут лучше поняты при прочтении следующего описания рабочих примеров и сравнительных анализов.
Эти примеры и анализы, очевидно, никоим образом не являются ограничительными и представлены с целью иллюстрации.
Ниже для практических целей используют следующие сокращения:
NETA:
норэтистеронацетат
SIS: трехблочный сополимер поли(стирол-изопрен-стирола) EVA: сополимер этилена и винилацетата.
Пример 1. В 250 мл химический стакан добавили 13,9 VECTORa® 4211 D (сополимера SIS, продаваемого компанией EXXON CHEMICAL), 23 г ECR® 385 (смолы, повышающей клейкостью, продаваемой компанией EXXON CHEMICAL), 9 г PROCETYLa® 10 (полипропоксилового эфира цетилового спирта, продаваемого CRODA FRANCE SA), 3 г SURFADONa® LP 100 (N-октил-2-пирролидона, продаваемого компанией GAF CORPORATION), 0,1 г IRGANOXa® 565 (антиксиданта) продаваемого компанией CIBA-GEICY) и 19,65 г этилацетата. Смесь перемешали при нагреве до 60oC до полного растворения соединений. Затем добавили раствор 1 г NETA, предварительно растворенного в 5 г тетрагидрофурана. Полученную таким образом смесь перемешивали в течение приблизительно 30 мин до полной гомогенизации. Ее оставили для охлаждения и дегазации до полного исчезновения пузырьков. Полученную массу нанесли на силиконовую полиэфирную пленку для получения осадка (110 ± 10) г/м2 при комнатной температуре (15 - 20oC). Полученное таким образом покрытие нагрели до 50oC в течение, по крайней мере, 30 мин и затем перенесли на несиликоновую полиэтиленовую подложку. Затем ее разрезали до соответствующего размера и упаковали в sachets.
Получили, систему в которой начальное количество NETA составило 231 μ г/см2.
Пример 2. Методика была идентичной методике примера 1, но использовали 13,4 г VECTORa® 4211D, 0,1 г IRGANOXa® 565, 26,5 г ECR® 385, 5 г олеинового спирта, 4,5 г кротамитона [N-этил-N-(2-метилфенил)-2-бутенамида, продаваемого компанией BOEHRINGER INGELHEIM], 20 г этилацетата и 0,5 г 17- β -эстрадиола, растворенного в 2,5 г тетрагидрофурана.
Осуществили нанесение покрытия получения осадка (100 ± 10) г/м2.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 94,5 μ г/см2.
Пример 3. Методика была идентична методике примера 1, но использовали 13,9 г VECTORa® 4211D, 0,1 г IRGANOXa® 565, 27,5 г ECR® 385,5 г олеинового спирта, 3 г SURFADONa® LP 300, 20,8 г этилацетата и 0,5 г 17- β -эстрадиола, растворенного в 2,5 г тетрагидрофурана. Осуществили нанесение покрытия для получения осадка (100 ± 10) г/м2.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 91 μ г/см2.
Пример 4. Методика была идентична методике примера 1, но использовали 7,25 г VECTORa® 4211D, 0,07 г IRGANOXa® 565, 11 г ECR® 385, 3,75 г LABRAFILa® 1944Cs (пегликоль-5-олеата, продаваемого компанией GATTEFOSSE), 2,5 г кротамитона, 10 г этилацетата и 0,5 г 17- β -эстрадиола, растворенного в 2,5 г тетрагидрофурана. Для получения осадка (90 ± 10) г/м2 осуществили нанесение покрытия.
Получили систему, в которой начальное количество эстрадиола составило 181,7 μ г/см2.
Пример 5. Методика была подобна методике примера 4, но использовали 12,9 г VECTORa® 4211D, 0,1 г IRGANOXa® 565, 26 г ECR® 385, 8 г LABRAFILa® 1944Cs, 2,5 г SURFADONa® LP 300, 19,4 г этилацетата и 0,5 г 17- β -эстрадиола, растворенного в 2,5 г тетрагидрофурана. Для получения осадка (100 ± 10) г/м2 осуществили нанесение покрытия.
Получили систему, в которой начальное количество эстрадиола составило 87,1 μ г/см2.
Пример 6. Методика была подобна методике примера 2, но использовали 13,16 г VECTORa® 4211D, 0,1 г IRGANOXa® 565, 26,5 г ECR® 385, 5,08 г олеинового спирта, 4,53 г кротамитона, 19,8 г этилацетата и 0,75 г 17- β -эстрадиола, растворенного в 3,75 г тетрагидрофурана. Для получения осадка (100 ± 10) г/м2 осуществили нанесение покрытия.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 159 μ г/см2.
Пример 7. Методика была подобна методике примера 3, но использовали 0,75 г 17- β -эстрадиола, растворенного 3,75 г тетрагидрофурана, 13, 64 г VECTORa® 4211D, 0,1 г IRGANOXa® 565, 27,5 г ECR® 385, 5 г олеинового спирта, 3 г SURFADONa® LP 300 и 20,5 г этилацетата. Для получения осадка (100 ± 10) г/м2 осуществили нанесение покрытия.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 162, 3 μ г/см2.
Пример 8. Методика была подобна методике примера 1, но использовали 13,9 г VECTORa® 4211D, 0,1 г IRGANOXa® 565, 24 г ECR® 385; 3,5 г SURFADONa® LP300, 7,5 г LAUROGLYCOLa® (смеси моно- и диэфира пропиленгликоля и лауриновой кислоты, продаваемой компанией GATTEFOSSE) вместо PROCETYLa® 10, 19,9 г этилацетата, 0,25 г 17- β -эстрадиола и 0,75 г NETA, растворенного в 5 г тетрагидрофурана. Для получения осадка (100 ± 10) г/м2 осуществили нанесение покрытия.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 48,6 μ г/см2 и начальное количество NETA составило 145,3 μ г/см2.
Пример 9. Методика была идентична методике примера 8, но использовали 15,9 г VECTORa® 4211D, 0,1 г IRGANOXa® 565, 21 г ECR® 385, 7,5 г LAUROGLYCOLa® , 4,5 г кротамитона (вместо SURFADONa® LP 300), 21,15 г этилацетата, 0,25 г 17- β -эстрадиола и 0,75 г NETA, растворенного в 5 г тетрагидрофурана. Для получения осадка (70 ± 10) г/м2 осуществили нанесение покрытия.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 33,1 μ г/см2 и начальное количество NETA составило 99,4 μг/см2.
Пример 10. Методика была идентична методике примера 1, но использовали 14,9 г VECTORa® 4211D, 0,1 г IRGANOXa® 565, 23,25 г ECR® 385, 7 г PROCETYLa® 10, 3,56 г SURFADONa® LP 100, 20,7г этилацетата, 0,25 г 17- β -эстрадиола и 1 NETA, растворенного в 6,25 г тетрагидрофурана. Для получения осадка (100 ± 10) г/м2 осуществили нанесение покрытия.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 51 μ г/см2 и начальное количество NETA составило 207,1 μ г/см2.
Пример 11. Методика была идентична методике примера 10, но SURFADONa® LP 100 заменили 3,5 г SURFADONa® LP 300. Для получения осадка (120 ± 10) г/м2 осуществили нанесение покрытия.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 60,5 μ г/см2 и начальное количество NETA составило 242 μ г/см2.
Пример 12. Методика была идентична методике примера 10, но использовали 14,65 г VECTORa® 4211D, 0,1 г IRGANOXa® 565, 21,75 г ECR® 385, 7 г PROCETYLa® 10,5 г кротамитона, 20,1 г этилацетата, 0,25 г 17- β -эстрадиола и 1 г NETA, растворенного в 6,25 г тетрагидрофурана. Для получения осадка (120 ± 10) г/м2 осуществили нанесение покрытия.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 60,5 μ г/см2 и начальное количество NETA составило 235,4 μ г/см2.
Пример 13. Методика была подобна методике примера 8, но использовали 18,65 г VECTORa® 4211D, 0,1 г IRGANOXa® 565, 19 г ECR® 385, 3,5 гSURFADONa® LP 100, 7,5 г LAUROGLYCOLa® 23 г этилацетата, растворенного в 5 г тетрагидрофурана, 0,25 г 17- β -эстрадиола и 0,75 г NETA. Для получения осадка (100 ± 10) г/м2 осуществили нанесение покрытия.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 47,3 μ г/см2 и начальное количество NETA составило 190 μ г/см2.
С целью сравнения получили следующие матрицы, основанные на EVA (сополимере этилена и винилацетата).
Сравнительный продукт CPI
В
250 мл химический стакан добавили 29 г LEVAPRENa® 450 P (сополимера этилена и винилацетата, продаваемого компанией BAYER), 15,5 г PROCETYLa® 10, 3,5 г SURFADONa® LP 100 и 67,7 г этилацетата. Их нагрели до 60oC при перемешивании в течение 5 ч до полного растворения EVA.
Затем добавили 2 г NETA, предварительно растворенного в 10 г тетрагидрофурана. Полученную таким образом смесь перемешивали при нагревании в течение приблизительно 30 мин до полной гомогенизации.
Смесь, полученную таким образом, оставили для охлаждения и дегазации до полного устранения пузырьков. Полученную массу нанесли при комнатной температуре на силиконовую бумагу до толщины (120 ± 10) г/м2. Полученное таким образом покрытие нагрели до 70oC в течение по крайней мере 30 мин, затем перенесли на конечную подложку в несиликоновом полиэтилене. Затем ее разрезали до соответствующих размеров и упаковали в Sachets.
Получили систему, в которой начальное количество NETA составило 488 μ г/см2.
Сравнительный продукт CP2
Методика была подобна методике получения CP1, но вместо 29 г LEVAPRENa® 450P использовали 16,5 олеинового спирта, 3,5 г кротамитона, 67,6 г этилацетата и 1 г 17- β -эстрадиола,
растворенного в 5 г тетрагидрофурана. Для получения осадка (80 ± 10) г/м2 осуществили нанесение покрытия.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 157 μ г/см2.
Сравнительный продукт CP3
Методика была подобна методике получения CP2, но использовали 1 г 17- β
-эстрадиола, растворенного в 5 г тетрагидрофурана, 29 г LEVAPRENa® 450P, 16,25 г олеинового спирта, 67,6 г этилацетата и 3,75 г SURFADONa® LP 300. Для получения
осадка (80 ± 10) г/м2 осуществили нанесение покрытия.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 169,6 μ г/см2.
Сравнительный продукт CP4
Состав, основанный на EVA, используемый здесь, был того же самого типа, как те, которые описаны в опубликованном документе F R-A-2612783,
упомянутом выше.
В химический стакан к 12,54 г EUTRANOLa® (2-октил-додеканола, продаваемого компанией HENKEL) добавили 21,97 г LEVAPRENa® 450P. Смесь нагрели до 130oC, перемешали и к ней добавили 6,03 г ETHOCELa® 20 (этилцеллюлозы, продаваемой компанией DOW CHEMICAL) и затем 6,46 г EUTRANOLa® G.
Перемешивание продолжали до получения гомогенной негранулированной смеси, которую затем оставили для охлаждения. Затем массу нагрели до 80oC и к ней добавили раствор 1,5 г 17- β -эстрадиола, предварительно растворенного при 70oC в 12 г безводного этанола.
Массу и раствор перемешивали в течение по крайней мере одного часа, до полной гомогенизации. Массу, полученную таким образом, нанесли на подложку из силиконовой бумаги при температуре 70oC для того, чтобы получить осадок толщиной (150±10) г/м2. Для выпаривания этанола осуществили сушку при 80oC и матрицу, полученную таким образом, перенесли на конечную полиэтиленовую подложку. Затем ее разрезали до соответствующих размеров и упаковали в sachets.
Получили систему, в которой начальное количество 17- β -эстрадиола составило 463,6 μ г/см2 .
Анализы
Определенные
результаты, полученные из сравнительных анализов, перегруппировали на фиг. 1 - 6.
Используя приспособления, описанные в вышеприведенных примерах осуществляли измерения ex vivo количеств гормона или гормонов, выделившихся в течение 24 или 48 ч на различных моделях кожи и вычисляли относительные выходы. Сравнение с другими уже известными системами ясно иллюстрирует преимущества, которые заявлены в изобретении.
Для этой цели испытания для исследования проникновения ex vivo осуществляли на брюшной коже "голой" мыши мужского пола в соответствии со следующим протоколом.
Количества гормонов, выделенных посредством чрескожного приспособления с площадью поверхности 2,54 см2, предварительно вырезанного штампов и помещенного на 3,14 см2 диск брюшной кожи "голой" мыши мужского пола, измеряли используя стеклянную стационарную ячейку с термостатом с установленной температурой 37oC и содержащую рецепторное отделение объемом 11,5 мл, имеющее в качестве воспринимающей фазы смесь физиологического солевого раствора и PEG 400 при объемном соотношении компонентов в смеси 75:25.
Брали пробы в рецепторных растворах через 2, 4, 6, 8, 12, 16, 20 и 24 ч, которые титровали жидкостной хроматографией.
Из-за непостоянства результатов, относящихся к внутренней проницаемости кожных проб, каждое испытание для исследования проникновения через пробу чрескожного приспособления осуществляли на минимальном количестве кожных проб от 3 до 5.
Представленный результат, который был получен при этих испытаниях, является средним для каждого приспособления.
Отношение между средним значением количеств гормона(ов), выделившегося(ихся) через 24 ч и начальным количеством гормона(ов), содержащимся(ихся) в приспособлении, может быть использовано для оценки выхода чрескожных систем в соответствии с изобретением за 24 ч. Полученные результаты даны в табл. I.
Количества, выделенные за 24 ч, вычисляли также в сравнении с приспособлениями, описанными в существующей области. Используя тот же самый протокол, который использовали ранее, проводили испытания ex vivo для исследования кожного проникновения на брюшной коже "голой" мыши мужского пола с использованием различных приспособлений в соответствии с изобретением, содержащих 17- β -эстрадиол, и с использованием самоприлипающей матричной системы (сравнительного продукта CP4), которая описана в Fr-A-2612785.
Количества, выделенные за 24 ч, и вычисленные выходы даны в табл. II.
В заключение проводили сравнительные измерения относительно только единственной известной системы, которая находится в обращении на рынке и которая содержит как эстроген, так и прогестоген, а именно, продукта ESTRAGEST, продаваемого компанией CIBA-GEIGY. Этот продукт является также единственным продуктом, общедоступным на рынке, который содержит прогестоген, хотя последний смешан с 17- β - эстрадиолом. Использовали тот же самый протокол, которого прежде придерживались при проведении испытаний ex vivo для исследования кожного проникновения на брюшной коже "голой" мыши мужского пола. Опять измеряли количества, выделившегося через 24 ч и вычисляли выходы, используя те же правила, что и прежде.
Что касается продукта ESTRAGEST® , то приспособление состоит из двух резервуаров, соединенных рядом, содержащих 10 мг 17- β - эстрадиола и 30 мг NETA, при этом каждый резервуар содержит смесь 5 мг 17- β - эстрадиола и 15 мг NETA.
Измерения кожного проникновения осуществляли, следуя тому же самому протоколу, только в одном из двух резервуаров, помещенном на кожную пробу размером 3,14 см2.
Начальные количества каждого гормона, содержащегося в этом резервуаре, уменьшали до начального количества упомянутого гормона на единице площади поверхности и выражали в μ г/см2.
В одном резервуаре среднее начальное значение гормона на единице площади поверхности составило (1590±30) μ г/см2 для 17- β -эстрадиола и (4770±30) μ г/см2 для NETA.
К тому же, отношение между соответственно (i) средним значением 17- β -эстрадиола или NETA, выделившегося через 24 ч и (ii) начальными количествами, содержащимися в резервуаре, может быть использовано для вычисления выходов 17- β -эстрадиола и NETA за 24 ч.
В качестве первой ступени проводили сравнение между матричными системами, заявленными в изобретении, содержащими 17- β -эстрадиол и NETA, и ранее упомянутой известной чрескожной системой ESTRAGEST® . Полученные результаты вошли в табл. III.
В качестве второй ступени сравнительные измерения ex vivo проводили также на другой кожной модели, коже уха свиньи, которая обычно дает результаты ex vivo, более близкие к тем результатам, которые были получены при проведении испытаний для исследования проникновения на человеческой коже.
Методика, которую использовали для этих измерений, была идентична той, которую использовали для измерений ex vivo на брюшной коже "голой" мыши. На этот раз измерительным диском размером 3,14 см2 была кожа уха свиньи. Воспринимающей фазой оставалась смесь физиологического солевого раствора и PEG400 при объемном соотношении компонентов в смеси 75 : 25. Однако на этот раз пробы брали через 48 ч.
Полученный результат был также средним значением, полученным для каждого испытуемого приспособления на минимальном количестве проб кожи, составляющим от 3 до 5.
Отношение между (i) этим средним значением и количеством гомонов, выделившихся через 48 ч кинетики и (ii) начальным количеством гормона, содержащимся в приспособлении, использовали для вычисления выхода чрескожных систем за 48 ч.
Относительные результаты вошли в табл. IV и V. Что касается изучения табл. I, то количества, выделившиеся через 24 ч, определяли между двумя матричными системами, матрица которых содержит ту же самую пару пластификатор/промотор, но сополимер другой природы. Для примеров 1-3 использовали сополимер SIS и для примеров CP1-CP3 использовали EVA.
Анализ табл. I показывает в отношении NETA, что при сравнении продукта примера 1 с CP1 выходы в 2,5 раза выше для SIS по сравнению с EVA при использовании одинаковой пары пластификатор/промотор, а именно пары PROCETYL® 10/SURFADONE® LP 100. Количество выделившегося NETA было также выше для продукта примера 1.
Подобные результаты были получены с 17- β -эстрадиолом при сравнении продукта примера 2 с CP2, в котором парой пластификатор/промотор является пара олеиновый спирт/кротамитон. В этом случае выход был также выше в 1,7 раза при использовании SIS.
Тем же самым путем, когда полученные результаты анализировали путем сравнения продукта 3 с СР3, в котором использовали пару олеиновый спирт SURFADONE® LP 300, полученный выход 17- β -эстрадиола был в 4 раза выше при использовании SIS (пример 3) по сравнению с EVA (СР3). В этом случае выделение 17- β -эстрадиола было в 2,2 раза выше. Следовательно, сополимер SIS обеспечивает чрескожную матричную систему, которая дает лучшее выделение по сравнению с сополимером EVA, даже если его использовали в сочетании с той же парой пластификатор/промотор.
Следовательно, все результаты в табл. I показывают, что выходы для приспособлений в соответствии с изобретением являются более высокими благодаря специфическому сочетанию SIS материала и пары пластификатор/ промотор в соответствии с изобретением, и что выделившиеся количества являются теми же самыми или они выше.
Что касается изучения табл. II, то приспособления в соответствии с изобретением сравнивали с приспособлением, которое идентично тем, которые описаны в F R-A-2612785.
Анализ этой таблицы показывает, что во всех случаях количество выделившегося 17- β -эстрадиола было
выше по сравнению с СР4 приспособлением в соответствии с F R-A2612785. Этот результат вполне иллюстрируется фиг. 1, которая позволяет сравнить продукты примера 4 и CP 4. Что касается выходов, то в
сравнении с приспособлением СР4 наблюдали, что:
в примере 2 выход был в 7 раз выше,
в примере 3 выход был в 13 раз выше,
в примере 6 выход был в 7 раз выше,
в
примере 7 выход был в 10 раз выше,
в примере 4 выход был в 6 раз выше.
Итак, во всех случаях, при использовании какой угодно пары пластификатор/промотор, олеиновый спирт/кротамитон для продуктов в примерах 2 и 6, олеиновый спирт SURFADONE® LP 300 для продуктов в примерах 3 и 7, или LABRAFIL® 1944 CS/кротамитон для продукта в примере 4, выходы были всегда выше (порядка от 6 до 13 раз), чем с СР4.
Выделившиеся количества были всегда приблизительно в 2,5 раза выше, чем с соответствующей матрицей EVA.
Что касается изучения табл. III, то матричные системы, заявленные в изобретении, содержащие два гормона: 17- β -эстрадиол и NETA, сравнивали с продуктом ESTRAGEST® . Результаты в табл. III показывают, что во всех случаях (i) количества 17- β -эстрадиола, выделившиеся за 24 ч, были приблизительно уже через период времени между двумя и тремя часами выше, чем с ESTRAGESTом® и (ii) количества NETA, выделившиеся через 24 ч, были эквивалентны или выше тех количеств, которые были получены со сравнительным продуктом ESTRAGEST® .
Выходы как для 17- β -эстрадиола так и для NETA, были всегда гораздо выше, чем выходы, полученные при использовании системы ESTRAGEST® .
Более конкретно, наблюдали, что при сравнении с последней данные для 17- β -эстрадиола соответственно показывают, что:
для примера 10 выход в 90 раз выше,
для
примера 11 выход в 72 раза выше,
для примера 12 выход в 47 раз выше,
и соответственно для NETA:
для примера 10 выход в 25 раз выше,
для примера 11 выход в 20 раз
выше,
для примера 12 выход в 19 раз выше.
Эти очень значительные разницы обеспечивают доказательство преимуществ чрескожных систем в соответствии с изобретением относительно единственной чрескожной смешанной системы, широко распространенной на рынке.
Эти разницы подтверждаются фиг. 2 и 3, которые представляют выход в % 17- β -эстрадиола во времени (кривая 11) и выход в % NETA во времени (кривая 12).
В этом случае также наблюдали, что какой бы ни использовали промотор вместе с пластификатором (в этом случае PROCETYL® 10) результаты с кротамитоном или N -алкил-2-пирролидоном ( SURFADONEом® LP 300 или SURFADONEом® LP 100) были всегда замечательными.
Что касается изучения кожи уха свиньи (табл. IV и V), приспособление в соответствии с изобретением сравнивали с продуктом ESTRAGEST® .
Табл. IV, относящаяся к выделению и выходу 17- β -экстрадиола, показывает, что с этой кожной моделью количество 17- β -эстрадиола, выделившееся за 48 ч, и выход были гораздо выше с продуктом примера 5 в соответствии с изобретением, чем с приспособлением ESTRAGEST® . Выделившееся количество было в 3 раза больше, чем с продуктом ESTRAGEST® . Фиг. 4, которая представляет выход (%) 17- β -эстрадиола во времени для продукта примера 5 и для упомянутого ESTRAGESTa® также иллюстрирует этот результат.
Результат табл. IV показывает, что по сравнению с приспособлением ESTRAGEST® в примере 5 выход в 57 раз выше.
Следовательно, эти похожие высокие значения для новой модели кожи уха свиньи подтверждают результаты, уже полученные при исследовании кожного проникновения ex vivo на брюшной коже мыши.
Полученные результаты, кроме того, демонстрируют преимущества пары пластификатор/промотор, в которой пластификатором является пегликольолеат (LABRAFIL 1944, Cs) и промотором является SURFADONEом® LP 300, с SIS.
В табл. V проведено сравнение на коже уха свиньи между приспособлениями, содержащими оба гормона, 17- β -эстрадиол и NETA, в соответствии с изобретением (продукты примеров 8, 9 и 13) и продуктом ESTRAGEST® .
Было найдено, что на кожной модели с чрескожной матричной системой в соответствии с изобретением выходы 17- β -эстрадиола гораздо выше, чем с приспособлением ESTRAGEST® .
Фиг. 5 также иллюстрирует то же самое явление относительно количество 17- β -эстрадиола, выделившихся за 48 ч. В частности, табл. V показывает, что при сравнении с продуктом ESTRAGEST® выходы были соответственно в 138 раз выше для продукта примера 9, в 72 раза выше для продукта примера 8 и в 107 раз выше для продукта примера 13.
Что касается NETA на этой кожной модели, то также наблюдали гораздо более высокие выходы, чем с приспособлением ESTRAGEST® .
Это совершенно иллюстрируется фиг. 6, которая представляет выход (%) во времени, даже если явление менее заметно, чем с 17- β -эстрадиолом, так как известно, что NETA имеет более труднопересекаемый кожный барьер.
Результаты табл. V показывают, что по сравнению с приспособлением ESTRAGEST® для продукта примера 8 выход в 21 раз выше, для продукта примера 9 выход в 35 раз выше и для продукта примера 13 выход в 25 раз выше.
Если в паре пластификатор/промотор пластификатор представлен LAUROGLYCOLoм® , а промотор - кротамитоном (пример 9) или N-алкил-2-пирролидоном ( SURFADONEом® LP 300 для примера 8, SURFADONEом® LP 100 для примера 13) их сочетание с SIS материалом опять позволяет достигнуть замечательных результатов.
Итак, все результаты, приведенные выше, демонстрируют неоспоримые преимущества чрескожной матричной системы в соответствии с изобретением на различных кожных моделях при испытаниях ex vivo по сравнению с единственным продаваемым продуктом, который содержит эстроген и прогестоген, и с другими приспособлениями с самоприливающей матрицей, описанными в предшествующей области.
В частности, результаты показывают, что вместе с сополимером SIS пары пластификатор/промотор изобретения позволяют достигнуть повышенных выходов, которые в определенных случаях являются исключительными.
Реферат
Изобретение относится к медицине, а именно к чрескожной матричной системе для
чрескожного введения гормона, при этом матричная система имеет подложку и самоклеящуюся матрицу, которая включает матрицу, содержащую 20 - 42 мас. ч. трехблочного сополимера поли
(стирол-изопрен-стирола), 35 - 55 мас.ч. смолы, повышающей клейкость, 5 - 25 мас.ч. пластификатора, выбранного из группы, состоящей из олеинового спирта, пегликоль-5-олеата, пропиленгликольлаурата или
полипропоксилового эфира цетилового спирта, 5 - 15 мас.ч. по крайней мере одного соединения, выбранного из группы, состоящей из кротаматона и N-замещенных 2-пирролидонов формулы I

где R представляет (C1 - C15)-алкильную, циклогексильную или 2-гидроксиэтильную группу, 0,01 - 1 мас.ч. стабилизатора и 0,1 - 5 мас.ч. гормона, выбранного из группы, состоящей из эстрогеновых компонентов, прогестогеновых компонентов и их смесей. Способ получения упомянутой системы включает смешение компонентов, затем гомогенизацию полученной смеси, с последующим вводом активного вещества - полового гормона. 3 с. и 5 з.п. ф-лы, 6 ил., 5 табл.

Формула

где R - C1 - C15-алкильная, циклогексильная или 2-гидроксиэтильная группа,
при следующем соотношении компонентов, мас.ч.:
Сополимер поли(стирол-изопрен-стирол) - 20 - 42
Смола - 35 - 55
Олеиновый спирт, или пегликоль-5-олеат, или пропиленгликольлаурат, или полипропоксиловый эфир цетилового спирта - 5 - 25
Кротамитон или N-замещенный 2-пирролидон - 5 - 15
Стабилизатор - 0,01 - 1,0
Экстроген и/или прогестоген - 0,1 - 5,0
2. Система по п.1, отличающаяся тем, что пластификатором является полипропоксиловый эфир цетилового спирта, содержащий 10 моль пропиленоксида на 1 моль цетилового спирта.
Сополимер поли(стирол-изопрен-стирол) - 20 - 42
Смола - 35 - 55
Олеиновый спирт, или пегликоль-5-олеат, или пропиленгликольлаурат, или полипропоксиловый эфир цетилового спирта - 5 - 25
Кротамитон или N-замещенный 2-пирролидон - 5 - 15
Стабилизатор - 0,01 - 1,0
Экстроген и/или прогестоген - 0,1 - 5,0
8. Способ получения чрескожной матричной системы, включающий смешение полимера (стирол-изопрен-стирола), пластификатора, стабилизатора и смолы, повышающей клейкость, при температуре 150oС, гомогенизацию полученной смеси, охлаждение до 110oС, затем введение активного вещества с последующей гомогенизацией смеси, нанесение полученной смеси на временную неклейкую бумагу для получения покрытия плотностью 50 - 500 г/м2, после чего покрытие наносят на подложку, отличающийся тем, что матричная система дополнительно содержит промотор из группы кротамитона или N-замещенного 2-пирролидона формулы I, а в качестве активного вещества используют половой гормон из группы экстрогеновых и/или прогестогеновых компонентов, в качестве пластификатора - олеиновый спирт, или пегликоль-5-олеат, или пропиленгликольлаурат, или полипропоксиловый эфир цетилового спирта, причем смешение полимера (стирол-изопрен-стирола), стабилизатора и смолы осуществляют в растворителе полимера при температуре ниже температуры кипения растворителя, после гомогенизации полученной смеси вводят кротамитон или N-замещенный 2-пирролидон и олеиновый спирт, или пегликоль-5-олеат, или пропиленгликольлаурат, или полипропоксиловый эфир цетилового спирта, после чего гомогенизируют полученную смесь, а перед нанесением покрытия на конечную подложку растворитель выпаривают путем нагрева покрытия до температуры выше температуры кипения растворителя, причем процесс проводят при следующем соотношении компонентов, мас.ч.:
Сополимер поли(стирол-изопрен-стирол) - 20 - 42
Смола - 35 - 55
Олеиновый спирт, или пегликоль-5-олеат, или пропиленгликольлаурат, или полипропоксиловый эфир цетилового спирта - 5 - 25
Кротамитон или N-замещенный 2-пирролидон - 5 - 15
Стабилизатор - 0,01 - 1,0
Экстроген и/или прогестоген - 0,1 - 5,0р

Комментарии