Физический способ борьбы с микроорганизмами - RU2657532C2
Код документа: RU2657532C2
Чертежи

Описание
Область техники
Настоящее изобретение относится к физическому противомикробному способу, в частности к противомикробным нанопленкам с положительным зарядом и к физическим противомикробным способам нанесения нанопленки на тело человека или другие объекты.
Уровень техники
Физический противомикробный способ представляет собой традиционный способ предупреждения инфекций и распространения патогенных микроорганизмов. Распространенные физические противомикробные способы включают высокую температуру, высокое давление и способы стерилизации ультрафиолетом и т.д. Однако эти традиционные физические противомикробные способы являются вредоносными, когда их прямо используют в организме человека, таким образом, их обычно используют для дезинфекции объектов и пространств, не используемых в организме человека. В основном, противомикробные способы для организма человека могут быть основаны только на различных противомикробных средствах. В настоящее время противомикробные способы для применения в организме человека представляют собой химические и биологические способы, в которых противомикробные средства проявляют противомикробное действие посредством механизмов, выбранных из препятствования синтезу клеточной стенки бактерий, влияния на функцию клеточных мембран, ингибирования синтеза белков и влияния на метаболизм нуклеиновых кислот и фолиевой кислоты и т.д. Эти механизмы могут обеспечивать противомикробную функцию только посредством противомикробных лекарственных средств, связывающихся с патогенными микроорганизмами и даже входящих в их организм. Клиническое применение противомикробных лекарственных средств, особенно злоупотребление противомикробными лекарственными средствами, приводит к образованию большого количества устойчивых к лекарственным средствам штаммов, и, таким образом, становится важной проблемой, препятствующей развитию клинической медицины.
В дополнение к традиционным противомикробным способам, в настоящее время существуют некоторые новые противомикробные способы, такие как противомикробное средство Nano-silver и т.д. В повязке Nano-silver Ag+ уничтожает патогенные микроорганизмы, проникая через клеточную мембрану. Этот механизм сходен с химическим противомикробным принципом и повреждает нормальные клетки человека, и при местном использовании может возникать устойчивость к лекарственному средству.
Классическая микробиология направлена против пассивноплавающих бактерий. Однако при дальнейшем исследовании бактерий и инфекций было выявлено, что в природе, в некоторой промышленной среде и внутри, и вне организма человека и животных большинство бактерий прикрепляются к поверхности живых или не живых объектов, осуществляя рост по типу биопленки (BF), а не пассивноплавающим способом. Биопленка формируется путем окружения бактерий внеклеточным матриксом с образованием специальной структуры, такой как структура в форме медовых сот с очень сложной экосистемой, в которой бактерии могут обмениваться информацией (см., например, Donlan, R.M., Biofilms and device-associated infections, Emerg. Infect. Dis, 20017, 277-281; C. Schaudinn, P. Stoodley, A. Kainovic, T. O'Keefe, В. Costerton, D. Robinson, M. Baum, G. Erlich, and P. Webster, Bacterial biofilms, other structures seen as mainstream concepts, Microbe, 2007 2, 231-237;. и H.-C. Flemming, T.R. Neu, and D.J. Wozniak, The EPS Matrix, The "House of Biofilm Cells", J. Bacteriol, 2007; 18 (22), 7945-7947). После формирования биопленки бактерии могут противостоять промыванию, фагоцитозу и противомикробным средствам (см., например, Trautner BW, Darouiche RO, Role of biofilm in catheter-associated urinary tract infection, AM J Infect Control, 2004, 32, 177-83 и Costerton J, Geesey G, Cheng K, How bacteria stick, Sci Am, 1978, 238, 86-95).
Были исследованы новые способы для предотвращения и изменения формирования биопленки, включая фуранон, фурацилин, содержащие серебро препараты и т.д. (см., например, J.R. Johnson, Р. Delavari, and М. Azar, Activities of a nitrofurazone-containing urinary catheter and a silver hydrogel catheter against multidrug-resistant bacteria characteristic of catheter-associated urinary tract infection, Antimicrob. Agents Chemother, 1999, 43, 2990-2995; J.R. Johnson, T. Berggren, and A.J. Conway, Activity of a nitrofurazone matrix urinary catheter against catheter-associated uropathogens, Antimicrob Agents Chemother, 1993, 37, 2033-2036; P Tenke, В Kovacs, Bjerkl and T E Johansen, et al., European and Asian guidelines on management and prevention of catheter-associated urinary tract infections, Int J Antimicrob Agents, 2008; Vol. 31, Suppl 1, pp. S68-78; и Kunin CM, Nosocomial urinary tract infections and the indwelling catheter: what is new and what is true? Chest. 2001, 120, 10-12). Однако эти способы также имеют некоторые недостатки.
Таким образом, все еще является желательным предоставление новых противомикробных способов и соответствующих препаратов, способных предотвращать устойчивость к лекарственным средствам.
Краткое описание изобретения
Задачей настоящего изобретения является предоставление физического противомикробного способа для решения проблемы устойчивых к лекарственным средствам штаммов, появляющихся в результате использования антибактериальных лекарственных средств, физическими способами, и к решению проблемы, состоящей в том, что классические антибактериальные способы не обладают профилактическим и лечебным действием в отношении бактериальной биопленки. Противомикробный механизм по настоящему изобретению состоит в разрыве мембраны клеток Е.coli посредством физического эффекта зарядового статического электричества, тем самым инактивируя патоген. Механизм представлен на фиг. 2 и 3. Задачей настоящего изобретения является предоставление противомикробной нанопленки на поверхности тела человека или животного, или объекта. Структура пленки представлена на фиг. 1. Другой задачей настоящего изобретения является предоставление кремнийорганической дичетвертичной соли аммония формулы (I):

где R1 независимо представляет собой C8-18 алкильную группу, C8-18 алкенильную группу или С8-18 алкинильную группу, предпочтительно С8-18 линейную алкильную группу; R2 и R3 независимо представляют собой метил или этил; R5 представляет собой С3-10 алкилен, который замещен в β-положении или в более отдаленном положении посредством три(С1-3 алкокси)силилокси или три(С1-3 алкокси)силил-С1-6алкокси; и X- независимо представляет собой фармацевтически приемлемый противоанион, предпочтительно Cl- или Br-.
Другой задачей настоящего изобретения является предоставление физического противомикробного способа, причем способ включает нанесение указанной кремнийорганической дичетвертичной соли аммония формулы (I) на поверхность объектов, нуждающихся в противомикробной обработке.
Физический противомикробный способ может предотвратить проблему устойчивости к лекарственным средствам, с которой сталкиваются химические и биологические противомикробные способы.
Другой задачей изобретения является предоставление противомикробной композиции, содержащей указанную кремнийорганическую дичетвертичную соль аммония формулы (I) и по меньшей мере один эксципиент. Противомикробная композиция по настоящему изобретению формирует нанопленку с четвертичным катионом в области, нуждающейся в противомикробной обработке, после нанесения. Нанопленка может эффективно уничтожать патогенные микроорганизмы и может эффективно предупреждать образование бактериальных биопленок и/или повреждать бактериальные биопленки, которые образовались, для преодоления ограничений, состоящих в том, что классические антибактериальные способы, как правило, являются эффективными против пассивноплавающих бактерий, но не эффективны против бактериальных биопленок.
Краткое описание чертежей
Фигура 1: представлена схематическая диаграмма физической противомикробной пленки согласно одному варианту осуществления настоящего изобретения.
А и В на фиг. 2 представляют собой изображения необработанных Escherichia coli, полученные с помощью атомно-силового микроскопа.
А и В на фиг. 3 представляют собой изображения Escherichia coli, обработанных противомикробными композициями по настоящему изобретению, полученные с помощью атомно-силового микроскопа.
Подробное описание предпочтительных вариантов осуществления изобретения
В первом аспекте противомикробные способы и продукты по настоящему изобретению в основном используют для предупреждения и лечения различных местных инфекций в организме человека и нозокомиальных инфекций.
В одном варианте осуществления клинические эксперименты показывают, что противомикробная композиция по настоящему изобретению эквивалентна по терапевтической эффективности типичным противомикробным лекарственным средствам в отношении лечения местных инфекций, и ее можно использовать для лечения бактериальных инфекций, грибковых инфекций, вирусных инфекций и других патогенных инфекций.
В одном варианте осуществления лечение раствором против местных инфекций по настоящему изобретению включает лечение бактериальных инфекций (например, Staphylococcus aureus, Escherichia coli, Pseudomonas aeruginosa, Neisseria gonorrhoeae) и клинических заболеваний, вызываемых этими бактериальными инфекциями (например, импетиго, бактериальный баланопостит и т.д.); грибковых инфекций (например, Candida albicans, Trichophyton rubrum, Epidermophyton floccosum и т.д.) и клинических заболеваний, вызываемых этими грибковыми инфекциями (таких как вагинит, обусловленный Candida albicans, эпидермофития стопы и т.д.); вирусных инфекций (вирус папилломы человека, вирус опоясывающего герпеса, вирус иммунодефицита человека) и клинических заболеваний, вызываемых этими вирусным инфекциями (таких как остроконечная кондилома, опоясывающий лишай, СПИД и т.д.), и инфекций другими патогенами (такими как Treponema pallidum, микоплазма, хламидии и т.д.) и клинических заболеваний, вызываемых этими патогенными инфекциями (например, микоплазменный уретрит, хламидийный уретрит, сифилис и т.д.). Варианты осуществления настоящего изобретения демонстрируют, что противомикробная композиция по настоящему изобретению проявляет заметный эффект в отношении лечения импетиго, вагинита, обусловленного Candida albicans, опоясывающего лишая и остроконечной кондиломы и в отношении предупреждения их рецидива.
В одном варианте осуществления предупреждение и лечение нозокомиальных инфекций, к которым имеет отношение настоящее изобретение, обеспечивается путем предупреждения образования бактериальной биопленки и улучшения гигиены рук для снижения встречаемости нозокомиальных инфекций, укорочения пребывания в больнице и снижения больничных расходов. В одном варианте осуществления нозокомиальные инфекции уменьшают путем снижения инфицирования, ассоциированного с медицинским катетером и канюлей, инфицирования хирургического разреза и инфицирования, ассоциированного с материалами искусственных имплантатов, и путем улучшения гигиены рук.
В одном варианте осуществления примеры указанных инфекций, ассоциированных с медицинским катетером и канюлей, включают, но не ограничиваются ими, инфекции, ассоциированные с уретральным катетером, трахеальной канюлей, трубками для перитонеального диализа, венозной канюлей, фистульным катетером и интервенционным катетером.
В одном варианте осуществления хирургические разрезы могут представлять собой различные хирургические разрезы, такие как оральные хирургические разрезы, желудочно-кишечные хирургические разрезы, перинеальные разрезы, аноректальные хирургические разрезы, косметические хирургические разрезы и т.д.
В одном варианте осуществления примеры указанных материалов искусственных имплантатов включают, но не ограничиваются ими, костные винты, искусственные суставы и искусственные клапаны.
В одном варианте осуществления улучшение гигиены рук включает нанесение противомикробной композиции по настоящему изобретению на руки медицинского персонала для поддержания стерильности рук в течение по меньшей мере одного часа, или по меньшей мере 2 часов, или по меньшей мере 4 часов, или по меньшей мере 8 часов для уменьшения распространения бактерий медицинским персоналом при обследовании и операции, тем самым снижая встречаемость нозокоимальных инфекций.
В одном варианте осуществления способы и продукты по изобретению также пригодны для предупреждения патогенных микробных инфекций, чтобы продлить допустимое время, ограничиваемое раневыми инфекциями. Применение противомикробных композиций по настоящему изобретению на ранней стадии травмы может выиграть ценное время для медицинской эвакуации и поздней очистки раны и уменьшения нестабильности и смертей, происходящих позднее вследствие инфекций.
В одном варианте осуществления способы и продукты по настоящему изобретению можно использовать для предупреждения и лечения инфекций различных острых и хронических ран.
В одном варианте осуществления примеры указанных острых ран включают, но не ограничиваются ими, порезы, разрывы, царапины и другие открытые раны и ожоги. Противомикробную композицию по настоящему изобретению удобно использовать в областях организма человека, которые нелегко или нельзя лечить с помощью общепринятых повязок, она может ускорить заживление ран и может предупредить вторичные инфекции.
В одном варианте осуществления примеры хронических ран включают, но не ограничиваются ими, пролежневые язвы, диабетическую язву стопы и венозные язвы ног. Замедленное заживление хронических ран связано с биопленками, образующимися на поверхности раны. Противомикробная композиция по настоящему изобретению может предупреждать образование бактериальных биопленок и разрушать образовавшиеся бактериальные биопленки, и может ускорять заживление ран.
В одном варианте осуществления противомикробные композиции по настоящему изобретению также обладают эффектом ингибирования колонизации опухолевых клеток, и их можно использовать для предупреждения и лечения различных типов опухолей (например, плоскоклеточная карцинома, липосаркома, аденокарцинома и т.д.) и различных неопластических заболеваний (таких как рак полости рта, рак мочевого пузыря, рак органов таза, рак головы и шеи и т.д.). Примеры настоящего изобретения демонстрируют, что в моделях на животных физические противомикробные мембраны, образованные противомикробной композицией по настоящему изобретению, обладают действием ингибирования роста опухолевых клеток.
В одном варианте осуществления противомикробные композиции по изобретению также пригодны для клинического исследования истечения жидкости и секретов из искусственной полости и естественной полости в организме человека, где противомикробную композицию по настоящему изобретению используют для исключения ложноположительного результата о вмешательстве микроорганизмов. В предпочтительном варианте осуществления противомикробную композицию по настоящему изобретению используют для усовершенствования способа исследования жидкости предстательной железы, где физическую противомикробную пленку по настоящему изобретению используют для определения источника лейкоцитов в жидкости предстательной железы и повышения точности исследования жидкости предстательной железы.
Во втором аспекте настоящее изобретение относится к кремнийорганической дичетвертичной соли аммония формулы (I):

где R1 независимо представляет собой C8-18 алкильную группу, С8-18алкенильную группу или C8-18 алкинильную группу, предпочтительно C8-18 линейную алкильную группу; R2 и R3 независимо представляют собой метил или этил; R5 представляет собой С3-10 алкилен, который замещен в β-положении или в более отдаленном положении посредством три(С1-3 алкокси)силилокси или три(С1-3 алкокси)силил-C1-6 алкокси; и X- независимо представляет собой фармацевтически приемлемый противоанион, предпочтительно Cl- или Br-.
В рамках настоящего изобретения термин "β-положение или более отдаленное положение" относится к положению одного или нескольких атомов углерода, удаленных от атомов углерода (обозначаемых как α-положение), связанных с четвертичной группой.
В одном варианте осуществления в формуле (I) R5 представляет собой группу формулы:
-(CH2)nCH(OR6Si(OCH2CH3)3) (СН2)n-, где 1≦n≦3; R6 представляет собой одинарную связь или C1-3 алкиленовую группу.
Кремнийорганическую дичетвертичную соль аммония формулы (I) можно использовать для формирования антимикробной мембраны на поверхности объекта, нуждающегося в противомикробной обработке, такого как кожа человека. Эксперименты по цитотоксичности, тест сенсибилизации, тест раздражения кожи и слизистых оболочек показывают, что кремнийорганические дичетвертичные соли аммония формулы (I) не обладают токсическими побочными эффектами и проявляют надежный противомикробный эффект.
В третьем аспекте настоящее изобретение относится к противомикробному способу, который включает нанесение кремнийорганической дичетвертичной соли аммония формулы (I) на поверхность объекта, нуждающегося в противомикробной обработке:
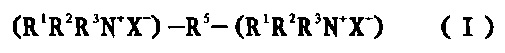
где R1 независимо представляет собой C8-18 алкильную группу, C8-18 алкенильную группу или C8-18 алкинильную группу, предпочтительно C8-18 линейную алкильную группу; R2 и R3 независимо представляют собой метил или этил; R5 представляет собой С3-10 алкилен, который является замещенным в β-положении или более отдаленном положении посредством три(С1-3 алкокси)силилокси или три(С1-3 алкокси)силил-C1-6 алкокси; и X- независимо представляет собой фармацевтически приемлемый противоанион, предпочтительно Cl- или Br-.
В одном варианте осуществления в формуле (I) R5 представляет собой группу формулы:
-(CH2)nCH(OR6Si(ОСН2СН3)3) (СН2)n-, где 1≦n≦3; R6 представляет собой одинарную связь или C1-3 алкиленовую группу.
После нанесения кремнийорганической дичетвертичной соли аммония формулы (I) на поверхность объекта, нуждающегося в противомикробной обработке, особенно на кожу человека, группа четвертичной соли аммония обеспечивает на поверхности разность потенциалов +40 мВ ~ +80 мВ.
Известно, что в диапазоне рН 6,0~8,0, например, в условиях приблизительно рН 7,0, зета-потенциал патогенных микроорганизмов, как правило, находится в диапазоне -50 ~ 0 мВ, и зета-потенциал большинства патогенных микроорганизмов находится в диапазоне - 40 ~ 0 мВ. Например, зета-потенциал actinobacillus actinomycetem comitans и Klebsiella составляет приблизительно -50 ~ -40 мВ, зета-потенциал Penicillium oxalate составляет -15 ~ -10 мВ, зета-потенциал Aspergillus terreus составляет менее -20 мВ; зета-потенциал Beauveria bassiana составляет -30 ~ 0 мВ; зета-потенциал мицелия Penicillium chrysogenum составляет -20 ~ -10 мВ; зета-потенциал спор Aspergillus fumigatus составляет -20,2±1,6 мВ, и зета-потенциал аденовируса, MS2, норовируса, Qβ, ВИЧ находится в диапазоне -25 ~ 0 мВ.
Также известно, что разность потенциалов на клеточной мембране организма человека составляет -80 ~ -100 мВ.
В рамках настоящего изобретения поликремнийорганические дичетвертичные соли аммония со средним размером частиц в наномасштабе (1 нм - 1000 нм) образуются путем полимеризации кремнийорганической дичетвертичной соли аммония формулы (I) с помощью нанопроцесса "снизу вверх". Наномасштабная поликремнийорганическая дичетвертичная соль аммония имеет потенциал +40 мВ ~ +80 мВ, и может уничтожать патогенный микроорганизм-мишень, не вызывая повреждения нормальных клеток человека. Более того, наномасштабная поликремнийорганическая дичетвертичная соль аммония не проникает через клеточную мембрану, используя статическое электричество для стерилизации, а не основывается на связывании с патогенными микроорганизмами или проникновении внутрь их организма для осуществления противомикробных функций, и, таким образом, не вызывает развития устойчивости к лекарственному средству. Кроме того, противомикробная пленка, сформировавшаяся в противомикробном способе, может предупреждать образование бактериальных биопленок, что обеспечивает инновационный и эффективной способ предупреждения и лечения локальных инфекций и нозокомиальных инфекций, ассоциированных с биопленками.
В одном варианте осуществления противомикробный способ по настоящему изобретению включает нанесение кремнийорганической дичетвертичной соли аммония формулы (I) на поверхность объекта, нуждающегося в противомикробной обработке, для образования противомикробной пленки с четвертичным катионом аммония. Противомикробная пленка состоит из полимерных частиц кремнийорганической дичетвертичной соли аммония формулы (I). Предпочтительно, средний диаметр полимерных частиц, составляющих противомикробную мембрану с четвертичным катионом аммония, находится в диапазоне 1 нм ~ 1000 нм.
В одном варианте осуществления разность потенциалов на противомикробной мембране с четвертичным катионом аммония находится в диапазоне +40 ~ +80 мВ.
В одном варианте осуществления противомикробный способ по настоящему изобретению может уничтожать множество отрицательно заряженных патогенных микроорганизмов, включая бактерии, грибы, вирусы, такие как Staphylococcus aureus, Pseudomonas aeruginosa, Candida albicans, Escherichia coli, коронавирус SARS, вирус гепатита В, вирус папилломы человека, вирус иммунодефицита человека (HIV), Treponema pallidum и т.д.
В одном варианте осуществления микробицидный принцип, используемый в противомикробном способе по изобретению, представляет собой физический принцип через электростатическую силу, обеспечивающую разрывы клеточных мембран патогенных микроорганизмов или обеспечивающую морфологические изменения, вызывая гибель патогенных микроорганизмов, а не химический или биологический принцип, обычно используемый в общепринятых противомикробных лекарственных средствах.
В другом варианте осуществления физический противомикробный способ по изобретению не приводит к развитию устойчивых к лекарственным средствам штаммов.
В другом варианте осуществления наномасштабный полимер, образованный кремнийорганической дичетвертичной солью аммония формулы (I), не поглощается клетками человека и не входит в организм человека для осуществления метаболизма, и является безопасным в экспериментах по цитотоксичности, тесте сенсибилизации, тесте раздражения кожи, тесте острой пероральной токсичности у мышей, тесте острого раздражения кожи у кроликов, тесте множественного (хронического) раздражения кожи у кроликов, тесте раздражения глаз у кроликов и в микроядерном тесте в клетках.
В одном варианте осуществления противомикробный способ по настоящему изобретению представляет собой противомикробный способ в организме человека, где кремнийорганическую дичетвертичную соль аммония формулы (I) наносят на поверхность организма человека.
В другом варианте осуществления противомикробный способ по настоящему изобретению представляет собой противомикробный способ в объекте, где кремнийорганическую дичетвертичную соль аммония формулы (I) наносят на поверхность объекта, нуждающегося в противомикробной обработке, такую как поверхность медицинского устройства.
В четвертом аспекте настоящее изобретение относится к противомикробной композиции, содержащей кремнийорганическую дичетвертичную соль аммония формулы (I) по настоящему изобретению и по меньшей мере один эксципиент.
В одном варианте осуществления, как показано на фиг. 1, 3, представляет собой функциональную пленку, имеющую различные функции заживления, устранения зуда, смягчения боли, устранения воспаления, гемостаза, препятствования адгезии, противоопухолевую функцию, функцию устранения рубцов и т.д. С пленками сцеплены или на них наслоены противомикробные пленки, и они могут состоять из материалов, имеющих различные функции, таких как материалы, ускоряющие заживление, противозудные материалы, материалы, смягчающие боль, противовоспалительные материалы, гемостатические материалы, противоадгезионные материалы, противоопухолеые материалы, материалы для устранения рубцов.
В одном варианте осуществления содержание кремнийорганической дичетвертичной соли аммония в противомикробной композиции составляет 0,1-30 масс. % в расчете на общую массу композиции.
В одном варианте осуществления эксципиент выбран из группы, состоящей из воды и жидких органических растворителей, таких как спирты, простые эфиры, кетоны и сложные эфиры.
В одном варианте осуществления противомикробная композиция дополнительно содержит по меньшей мере один эксципиент, например отдушки, вкусовые добавки, поверхностно-активные вещества, эмульгаторы, антиоксиданты, стабилизаторы, загустители, пропелленты аэрозоля и их комбинации.
В одном варианте осуществления противомикробная композиция имеет форму спрея, лосьона, гранул, линимента, глазури, мази, состава покрытия, и в форме, которую можно использовать для смачивания объекта.
В одном варианте осуществления противомикробную композицию или кремнийорганическую четвертичную соль аммония можно комбинировать с другими материалами или устройствами для формирования композитного устройства. Примеры других материалов или устройств включают, но не ограничиваются ими, хитозан, фибриновый клей, желатин и коллаген, коллагеновый белок, гиалуронат натрия, икодекстрин, жидкий клей, лактатный раствор Рингера, целлюлозу, регенерированную окислением, вспененный тефлон, просвечивающиеся мембранные повязки, гидроколлоидные повязки, альгинатные повязки, противоаллергический гель, Zenieva, сепрафилм, гискон, силикагель, раневые клеи, дентальные клеи, костный цемент и наносеребро (nano-silver). Если желательно, эти материалы или устройства можно использовать в комбинации из двух или более из них.
В одном варианте осуществления противомикробная композиция может дополнительно содержать по меньшей мере один дополнительный активный ингредиент для получения композиции, имеющей композитные функции. Примеры активных ингредиентов включают, но не ограничиваются ими, оксиматрин, хитозан, денцихин, маннан блетиллы, буфалин, гинзенозиды, сапонины Impatiens pritzellii, эводиамин, азиатикозид, шиконин, катехин, эмодин, аллантоин, экдистерон, сальвиановую кислоту, дафнетин, феруловую кислоту, кверцитрозид, куркумин, байкалин, паеонол, цитраль, коричный альдегид, эвгенол, берберин, ментол, остол, кверцетин, глицирризин, реин, астрагалозид А, ресвератрол, вогонин, бербамин, софоридин, цинобуфагин и проантоцианиды.
В одном варианте осуществления противомикробная композиция имеет форму гидрогеля, содержащего кремнийорганическую дичетвертичную соль аммония формулы (I), воду и одно или несколько из окиси полиэтилена, поливинилового спирта, поливинилпирролидона, полиальгината, полиакрилата натрия и хитозана. В одном варианте осуществления вязкость противомикробной композиции в форме гидрогеля обеспечивает ее пригодность для заполнения ран. В другом варианте осуществления вязкость противомикробной композиции в форме гидрогеля обеспечивает ее пригодность в качестве мази.
В одном варианте осуществления противомикробная композиция имеет форму мази.
В одном варианте осуществления противомикробная композиция имеет форму водного геля, который содержит кремнийорганическую дичетвертичную соль аммония формулы (I), воду и водный полимер, такой как натрий карбоксилметилцеллюлоза, желатин, агар или их комбинации.
В одном варианте осуществления противомикробная композиция по настоящему изобретению в форме водного геля или гидрогеля дополнительно нанесена на субстрат, такой как прозрачная, или просвечивающаяся, или непрозрачная пленка или вспененный тонкий лист. Необязательно, по меньшей мере часть субстрата покрыта адгезивом, с тем чтобы прилипать, например, к коже человека.
В одном варианте осуществления противомикробная композиция по настоящему изобретению в форме водного геля или гидрогеля по настоящему изобретению дополнительно нанесена на носитель или адсорбирована на носителе для обеспечения фиксированной формы, где носитель, например, представляет собой бумагу, ткань (например, фланель, тканный материал, нетканый материал), синтетические смолы (например, полиуретан, сополимер этилен / винилацетат, поливинилхлорид, полиэфир (например, полиэтилен терефталат), полиолефины (например, полиэтилен, полипропилен), полиамиды (такие как нейлон 6, нейлон 66), поливинилиденхлорид, политетрафторэтилен), резина или производное целлюлозы.
В данной области общеизвестно, как составлять пригодную дозированную форму противомикробной композиции в соответствии с предполагаемым применением из кремнийорганической дичетвертичной соли аммония формулы (I).
В одном варианте осуществления противомикробную композицию по настоящему изобретению распыляют на кожу для формирования противомикробной пленки, которая может сохранять противомикробный эффект в течение 8 часов.
В одном варианте осуществления противомикробную композицию по настоящему изобретению распыляют на поверхность ткани, которая может сохранять противомикробный эффект после стирки с детергентом 40 раз.
В пятом аспекте настоящее изобретение относится к продукту, имеющему противомикробную функцию, такому как медицинское устройство.
Изделие, имеющее противомикробную функцию, можно получать путем нанесения противомикробной композиции по настоящему изобретению на поверхность изделия, такого как медицинское устройство.
В одном варианте осуществления противомикробную композицию по настоящему изобретению можно наносить на поверхность различных медицинских устройств для антибактериального эффекта и можно объединять с этими медицинскими устройствами для получения медицинских устройств с противомикробными функциями. Примеры медицинских устройств включают основные медицинские хирургические инструменты, микрохирургические инструменты, нейрохирургические инструменты, офтальмологические хирургические инструменты, отоларингологические хирургические инструменты, зубоврачебные хирургические инструменты, инструменты торакальной сердечно-сосудистой хирургии, абдоминальные хирургические инструменты, инструменты хирургии мочевыводящей системы и аноректальные хирургические инструменты, хирургические инструменты пластической хирургии (ортопедические), гинекологические хирургические инструменты, хирургические инструменты для регулируемой рождаемости, инструмент для пункции и инъекции, хирургические инструменты для ожогового отделения (пластическая хирургия), оборудование для общего осмотра, медицинское электронное оборудование, медицинское оптическое оборудование, инструменты и эндоскопическое оборудование, медицинское лазерное оборудование, высокочастотное медицинское оборудование, физиотерапевтическое оборудование, оборудование для традиционной китайской медицины, медикаменты и оборудование для радиационной защиты, оборудование и основные инструменты медицинской лаборатории, оборудование для искусственного кровообращения и переработки крови, материалы имплантатов и искусственные органы, оборудование и приспособления для операционной комнаты и смотрового кабинета, зубоврачебное оборудование и устройства, больничное оборудование и приспособления для ухода, медицинское оборудование и приспособления для криотерапии и лечения холодом, зубоврачебные материалы, медицинские материалы и повязки, материалы медицинских швов и клеев, медицинские полимерные материалы и продукты, интервенционное оборудование и т.д.
В шестом аспекте настоящее изобретение относится к продуктам, имеющим противомикробную функцию и функцию дезодорирования, таким как материалы, имеющие противомикробную функцию и функцию дезодорирования. Объекты, имеющие противомикробную функцию, являющиеся защищающими от плесени и дезодорирующими, можно получать путем нанесения противомикробной композиции по настоящему изобретению на поверхность изделий, таких как материалы с противомикробной и дезодорирующей функцией.
В одном варианте осуществления противомикробные композиции по настоящему изобретению можно использовать в комбинации с другими материалами, имеющими противомикробную и дезодорирующую функцию, для получения различных комбинированных материалов, которые можно широко использовать для противомикробной, защищающей от плесени и дезодорирующей обработки в различных отраслях промышленности. Эти комбинированные материалы можно комбинировать с изделиями в этих отраслях промышленности для получения новых комбинированных объектов. Эти отрасли промышленности включают сельское хозяйство, лесоводство, животноводческое хозяйство и рыбную промышленность, конструкционные и строительные материалы, металлургию и горнодобывающую промышленность, нефтехимию, транспорт, информационную промышленность, механическое и электрическое оборудование, одежду и текстиль, защиту окружающей среды и лесонасаждение, туризм и досуг, канцелярские принадлежности, игрушки, подарки, антиквариат, хозяйственные товары, бумажную промышленность, спортивные товары, офисную мебель и т.д.
Варианты осуществления
Следующие варианты осуществления приведены для лучшей иллюстрации настоящего изобретения, а не для ограничения объема настоящего изобретения.
Вариант осуществления 1
Схематическая диаграмма физических противомикробных пленок
На фиг. 1 представлена схематическая диаграмма физической противомикробной пленки согласно одному варианту осуществления настоящего изобретения. На фиг. 1, 1 представляет собой поверхность тела, которая может представлять собой кожу (включая слизистые оболочки) или различные другие объекты; 2 представляет собой физическую противомикробную пленку, которая имеет положительные заряды и приклеивается или адсорбируется на поверхности 1 организма; 3 представляет собой необязательно другую функциональную пленку.
Следует понимать, что хотя физическая противомикробная пленка представлена в качестве плоской структуры, она также может иметь различные неплоские поверхностные структуры.
Вариант осуществления 2
Получение кремнийорганической дичетвертичной соли аммония
Вариант осуществления 2а
Получение кремнийорганической дичетвертичной соли аммония 1

Кремнийорганическая дичетвертичная соль аммония 1, где R, R' представляют собой C12H25, X- представляет собой Cl-.
(1) Синтез четвертичной соли аммония с двойной длинной алкильной цепью, имеющей гидроксилсодержащую линкерную группу.
В колбу с тремя горлышками добавляли 0,2 моль додецилдиметиламина и 40 мл смешанного растворителя изопропанол-вода (изопропиловый спирт и вода в объемном соотношении 10:1). Смеси нагревали при перемешивании до 50°С, а затем в нее капельно добавляли 0,21 моль эпихлоргидрина и позволяли им реагировать в течение 3 часов с получением хлорида эпоксипропилдодецилдиметиламмония.
В реакционную смесь, полученную на описанной выше стадии реакции, медленно добавляли 0,2 моль дополнительного додецилдиметиламина и капельно добавляли 10% хлористоводородную кислоту для поддержания реакционной смеси при рН 9. После завершения добавления реакционную смесь нагревали до 70°С и позволяли ей реагировать в течение 5 часов. После удаления растворителя и остаточных реагентов при пониженном давлении получали светло-желтое воскообразное твердое вещество, т.е. дичетвертичную соль аммония, имеющую гидроксилсодержащую линкерную группу: дихлорид 2-гидрокси-1,3-бисдодецилдиметиламмонийпропана. В этой реакции уровень преобразования амина составил более 95%. Дичетвертичную соль аммония, имеющую гидроксилсодержащую линкерную группу, сушили при 50°С в течение 10 часов в вакуумной печи для применения при необходимости.
(2) Синтез кремнийорганической дичетвертичной соли аммония 1
0,1 моль дихлорида 2-гидрокси-1,3-бисдодецилдиметиламмонийпропана и 100 мл изопропанола добавляли в круглодонную колбу, и в нее медленно добавляли 0,1 моль этилортосиликата. Смеси нагревали до 45°С при перемешивании в условиях кипячения с обратным холодильником. Наблюдали, что твердое вещество постепенно растворялось и полученный раствор имел грязно-белый цвет. После проведения реакции в течение 12 часов полученный материал перегоняли при пониженном давлении для удаления остаточных реагентов, а затем сушили в вакуумной печи при 50°С в течение 10 часов с получением белого воскообразного твердого вещества, т.е. кремнийорганической дичетвертичной соли аммония 1: дихлорид 2-триэтоксилсилилокси-1,3-дидодецилдиметиламмонийпропана.
IR (см-1): 3411, 2924, 2854, 1636, 1468, 1097, 799.1Н NMR (300 MHz, DCCl3): δ (ppm): 07,9, t, СН3(СН2)11 6Н; 10,5-10,8, t, (СН3СН2О)3Si, 11,1-12,0, m, СН3(CH2)9CH2CH2N 45Н; 16,4, m, СН3(CH2)9CH2CH2N 4Н, 30,2, m, СН3(СН2)9CH2CH2N 4Н; 32,3, d, (CH2)2N(CH3)2 12Н; 35,4, t, CH3(CH2)9CH2CH2N(CH3)2CH2CHO 4Н; 36,6, m, (CH3CH2O)3Si 6Н; 47,0, m, (NCH2)2CHO 1H.
Вариант осуществления 2b
Синтез кремнийорганической дичетвертичной соли аммония 2
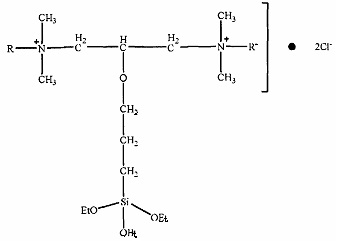
Кремнийорганическая дичетвертичная соль аммония 2, где R, R' представляют собой C12H25, X- представляет собой CI-
0,1 моль дихлорида 2-гидрокси-1,3-бисдодецилдиметиламмонийпропана и 100 мл ~ ~ изопропанола добавляли в круглодонную колбу, и в нее медленно добавляли 0,1 моль γ-хлорпропилтриэтоксисилана. Смеси нагревали до 45°С при перемешивании в условиях кипячения с обратным холодильником. Наблюдали, что твердое вещество постепенно растворялось, и полученный раствор имел грязно-белый цвет. После проведения реакции в течение 12 часов полученный материал перегоняли при пониженном давлении для удаления остаточных реагентов, а затем сушили в вакуумной печи при 50°С в течение 10 часов, с получением белого воскообразного твердого вещества, т.е. кремнийорганической дичетвертичной соли аммония 2: дихлорида 2-триэтоксисиликопропокси-1,3-дидодецилдиметиламмонийпропана, выход 95%.
1Н NMR (300 MHz, DCCl3): δ (ppm): 09,0, t, CH3(СН2)11 6Н; 12,2-12,4 t, (CH3CH2O)3SiCH2CH2CH2O, 12,5-13,7, m, CH3(CH2)9CH2CH2N 45H; 18,7-19,0, m, CH3(CH2)9CH2CH2N 4H; 34,0, m, CH3(CH2)9CH2CH2N 4H; 34,3-37,0, m, CH3(CH2)9CH2CH2NCH2(CH3)2 28H; 51,9, m, (-NCH2)2CH-O-CH2-1H.
Вариант осуществления 3
Получение 2% физической противомикробной композиции
2 части по массе кремнийорганической дичетвертичной соли аммония, полученной согласно варианту осуществления 2, и 98 аликвот деионизированной воды смешивали и эмульгировали с получением 2% физической противомикробной композиции.
Вариант осуществления 4
Определение размера частиц и разности потенциалов физической противомикробной композиции
2% физические противомикробные композиции, полученные согласно варианту осуществления 3, разбавляли деионизированной водой до получения водного раствора, имеющего 0,5 масс. % кремнийорганической дичетвертичной соли аммония. Размер частиц полимера в противомикробной композиции и изменение потенциала в качестве величины рН измеряли с использованием анализатора размера частиц Brookhaven ZetaPlus и системы Brookhaven 90Plus. Результаты измерения продемонстрировали, что противомикробная композиция имеет относительно высокий потенциал заряда катиона, причем зарядовый потенциал находился в диапазоне от +50 мВ до +60 мВ в измеренном диапазоне рН (3-12). Средний размер единичных частиц составлял 2,57 нм, и средний диаметр агрегата составлял 43,5 нм.
Вариант осуществления 5
Эксперименты по механизму стерилизации физической противомикробной композиции
Раствор физической противомикробной композиции, полученный согласно варианту осуществления 3, разбавляли до минимальной бактерицидной концентрации 188 пмоль, а затем использовали для обработки Е.coli. Изменение морфологии клеточной мембраны Е.coli до и после обработки наблюдали с помощью атомно-силовой микроскопии.
На фиг. 2, А представляет собой фотографию морфологии отдельных необработанных Е.coli. На фиг. 3, А представляет собой фотографию морфологии отдельных Е.coli, обработанных путем деструкции. На фиг. 2-А показано, что структура клеточной мембраны необработанных Е.coli была полной, и отсутствовали щели или углубления на поверхности клетки; фиг. 2-В представляет собой диаграмму сканирования поперечного среза, демонстрирующую, что полная высота клеточной мембраны составляла приблизительно 200 нм; фиг. 2-В и фиг. 2-А вместе показали, что клеточная мембрана Е.coli была овальной. На фиг. 3-А показано, что структура клеточной мембраны Е.coli была полностью разрушена после обработки; диаграмма сканирования 3В показала, что клеточная мембрана, которая представляла собой поврежденную или спавшуюся клеточную мембрану, имела зигзагообразную форму с высотой менее 20 нм, что далее подтвердило, что морфология мембраны была разрушена; фиг. 3-В и фиг. 3-А вместе продемонстрировали, что разрушенная клеточная мембрана Е.coli имела неправильную форму. Таким образом, противомикробный механизм противомикробной композиции в соответствии с настоящим изобретением состоял в разрушении клеточной мембраны Е.coli посредством физического действия зарядовой электростатической силы, инактивирующей патогены.
Вариант осуществления 6
Эффект физической противомикробной композиции в отношении уничтожения различных пассивноплавающих патогенных микроорганизмов
Раствор, полученный согласно варианту осуществления 3, разбавляли в различных соотношениях, и его активность в отношении уничтожения различных патогенных микроорганизмов в суспензии измеряли способом, описанным в европейских BS EN 1040: 2005 (для бактерий), BS EN 1275: 2005 (для грибов) и BS EN 14476: 2005 (для вирусов). Результаты показали, что противомикробный раствор обладал эффектом уничтожения различных патогенных микроорганизмов, как показано в следующей таблице.
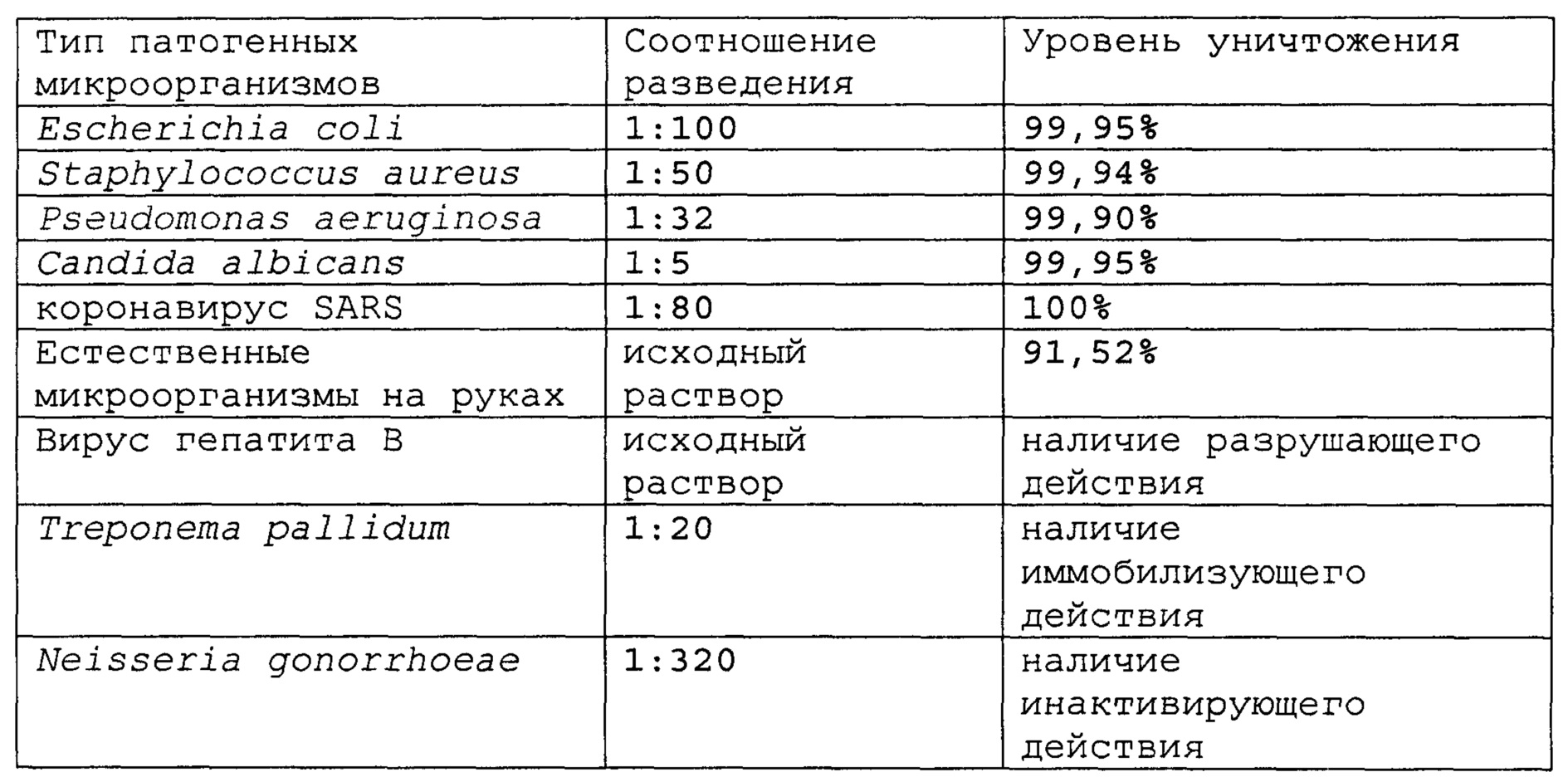
Вариант осуществления 7
Эффект физической противомикробной композиции в отношении уничтожения бактерий на поверхности различных материалов
В соответствии со способом, установленным в европейском BS EN13697:2001, в диапазоне температур от 18°С ±1°С до 25°С ±1°С, различные образцы исследуемых поверхностей помещали в асептических условиях в чашки Петри, а затем на каждую исследуемую поверхность наносили 0,05 мл каждой бактериальной суспензии, и на каждую исследуемую поверхность наносили 0,1 мл физической противомикробной композиции и жесткой воды, после контактирования с бактериями в течение 5 минут и контактирования с грибами в течение 15 минут, вычисляли величину Ig колониеобразующих единиц для каждой исследуемой поверхности. Результаты показали, что физическая противомикробная композиция проявляла антибактериальную активность при нанесении на следующие различные поверхности.


Вариант осуществления 8
Эксперимент по определению устойчивости к лекарственным средствам
Эксперимент проводили в соответствии со стандартом США NCCLS 1997. Более 300 патогенов, выделенных в Department of Burns, брали для проведения испытания устойчивости к лекарственным средствам с часто используемыми антибиотиками и раствором, полученным согласно варианту осуществления 3. Выделенные патогены включали семь видов, т.е. Escherichia coli, Staphylococcus aureus, Pseudomonas aeruginosa, Acinetobacter, Klebsiella pneumoniae, Enterobacter aerogenes и Enterobacter cloacae, которые широко распространены в клинике. Уровень устойчивости Escherichia coli к ампициллину, гентамицину и цефазолину составлял 80,1%, 40,9% и 40,0% соответственно; уровень устойчивости MSSA к пенициллину составлял 87,0%; уровень устойчивости Pseudomonas aeruginosa к пиперазин амоксициллину, гентамицину и цефтазидиму, составил 34,1%, 35,3% и 21,7%, соответственно; уровень устойчивости Acinetobacter к пиперациллину, гентамицину и цефтазидиму составил 93,3%, 18,9% и 21,2%, соответственно; уровень устойчивости aerogenes к гентамицину и цефазолину составил 8,2% и 79,3% соответственно, уровень устойчивости Enterobacter cloacae к гентамицину и цефазолину составил 28,1% и 89,3% соответственно. Все эти выделенные бактерии являются чувствительными к физической противомикробной композиции по настоящему изобретению, т.е. уровень устойчивости составил 0. Это показало, что физическая противомикробная композиция по изобретению имеет широкий спектр противомикробных характеристик.
Вариант осуществления 9
Эксперименты по определению токсических побочных эффектов
Раствор, полученный согласно примеру 3, подвергали исследованию биологической безопасности в соответствии со способом, описанным в ISO10993. Результаты показали, что физическая противомикробная композиция по настоящему изобретению была высокобезопасной, не имела токсического побочного эффекта. Все из теста сенсибилизации, теста раздражения кожи и экспериментов по цитотоксичности были сертифицированными.


Вариант осуществления 10
Эксперимент по предупреждению роста биопленки
Стерильный силиконизированный латексный уретральный катетер нарезали на 16 фрагментов, являющихся образцами, а затем фрагменты, являющиеся образцами, случайным образом распределяли на экспериментальную группу и контрольную группу, которые смачивали, соответственно, раствором, полученным согласно варианту осуществления 3, и дистиллированной водой в течение 5 минут. Фрагменты, являющиеся образцами, помещали в культуральную среду, содержавшую Е.coli, и культивировали при 37°С. Фрагменты, являющиеся образцами, преобразовывали в образцы для наблюдения под сканирующим электронным микроскопом и конфокальным лазерным сканирующим микроскопом, соответственно. Сканирующая электронная микроскопия продемонстрировала, что фрагмент из экспериментальной группы не имел адгезии Е.coli в течение 7 суток, и не было выявлено образования биопленки; в то время как фрагмент из контрольной группы имел большой уровень адгезии Е.coli и образовывалась структура биопленки. Конфокальная лазерная сканирующая микроскопия показала, что на поверхности фрагментов из экспериментальной группы наблюдали прозрачную противомикробную пленку толщиной от 40 до 41,5 нм.
Вариант осуществления 11
Длительный противомикробный эксперимент
Раствор, полученный согласно варианту осуществления 3, подвергали антибактериальным экспериментам на поверхности кожи и ткани. Способ был следующим:
Вариант осуществления 11а
Антибактериальный эксперимент на поверхности кожи
В соответствии с экспериментальным способом европейского BS EN 1499: 1997, палец погружали в раствор, содержавший Е.coli, а затем на палец распыляли раствор, полученный согласно варианту осуществления 3. Наблюдали ингибирование бактерий. Результаты показали, что антибактериальный уровень в течение 8 часов составлял 99,95%.
Вариант осуществления 11b
Антибактериальные эксперименты на поверхности ткани
В соответствии со способом европейского BS EN 1040: 2005, при 20°С ±1°С хлопковую ткань, на которую был распылен раствор, полученный согласно варианту осуществления 3, промывали детергентом в течение 5 минут, а затем сушили, после однократного промывания. Результат после промывания 40 раз показал, что антибактериальный уровень составил 99,97%.
Вариант осуществления 12
В соответствии с этим вариантом осуществления предоставляются различные дозированные формы противомикробных композиций по настоящему изобретению и их способы получения.
Вариант осуществления 12а
Спрей получали согласно следующему составу:

Кремнийорганическую дичетвертичную соль аммония, полученную согласно варианту осуществления 2, добавляли в очищенную воду для эмульгирования, добавляли хитозан и вкусовые добавки, и перемешивали с получением водного состава, который распределяли в бутылку из HDPE, оборудованную насадкой.
Вариант осуществления 12b
Спрей получали согласно следующему составу:

Кремнийорганическую дичетвертичную соль аммония, полученную согласно варианту осуществления 2, добавляли в очищенную воду для эмульгирования, добавляли матрин и вкусовые добавки и смешивали с получением водного состава, который распределяли в бутылку из HDPE, оборудованную насадкой.
Вариант осуществления 13
Следующие эксперименты показали значительный эффект противомикробной композиции по настоящему изобретению.
Противомикробную композицию, использованную в описанных ниже экспериментах, получали согласно способу, описанному в варианте осуществления 3.
Вариант осуществления 13а
Эксперимент по лечению импетиго
1652 пациента, у которых Department of Dermatology клинически диагностировал импетиго в больнице, были выбраны и случайным образом подразделены на экспериментальную группу (n=1032) и контрольную группу (n=620). Экспериментальную группу обрабатывали противомикробной композицией по изобретению на пораженной области, и контрольную группу обрабатывали мупироцином, 2 раза в сутки в течение 7 суток. Результаты показали, что экспериментальная и контрольная группа имели эффективный уровень 90,5% и 85% соответственно, и отсутствовало статистически значимое различие между двумя группами. Эксперименты показали, что противомикробная композиция по настоящему изобретению имела тот же эффект, что и мупироцин, при лечении импетиго, но без повязки, являясь простой для применения.
Вариант осуществления 13b
Лечение вульвовагинального кандидоза (VVC)
В этом эксперименте было выбрано 100 пациентов, у которых был клинически диагностирован клинический VVC, и их случайно распределяли на экспериментальную группу (n=50) и контрольную группу (n=50). В экспериментальной группе распыляли противомикробную композицию на наружные половые органы каждые сутки, в дополнение к стандартному местному применению вагинального суппозитория эконазола нитрата, 3 раза в сутки. В контрольной группе использовали мазь мупироцина и мазь бифоназола на наружные половые органы в дополнение к стандартному местному применению вагинального суппозитория эконазола нитрата, каждые сутки. Результаты показали, что в течение семи суток экспериментальная и контрольная группы имели общий показатель эффективности 98% и 97%, соответственно, без значимых отличий между ними. Результаты показали, что противомикробная композиция по настоящему изобретению имела тот же терапевтический эффект, что и комбинация противогрибкового лекарственного средства и антибактериального лекарственного средства, при лечении VVC. Более того, физический противомикробный способ для организма человека может устранить источник инфекции и предупредить восходящие инфекции и рецидив VVC при использовании на нижнем белье и гигиенической прокладке.
Вариант осуществления 13с
Эксперимент по лечению опоясывающего лишая
113 пожилых пациентов с опоясывающим лишаем подразделяли на две группы: группу лечения (n=57) и контрольную группу (n=56). В группе лечения перорально вводили таблетки ацикловира в дозе 200 мг, 5 раз в сутки, и местно наносили противомикробную композицию на пораженную область, три раза в сутки; в контрольной группе перорально вводили таблетки ацикловира в дозе 200 мг, 5 раз в сутки, и местно наносили лосьон каламин; и за ходом лечения наблюдали в течение двух недель в обеих группах. Общий показатель эффективности в группе лечения (доля пациентов со смягчением боли и кожных очагов поражения убывала в течение двух недель в ходе приема лекарственных средств) составил 97%, в то время как общий показатель эффективности в контрольной группе составил 87% без статистической значимости между ними. Группа лечения проявляла значительно более короткое время присутствия пузырей, время смягчения боли, время образования струпа и время выздоровления, чем контрольная группа. Эксперимент показал, что противомикробная композиция по изобретению в комбинации с противовирусным средством имела лучший эффект, чем противовирусное средство отдельно.
Вариант осуществления 13d
Клинический эксперимент по лечению и предупреждению рецидива остроконечной кондиломы
В этом эксперименте было выбрано 242 пациента с остроконечной кондиломой и случайно подразделено на экспериментальную группу (n=121) и контрольную группу (n=121). Экспериментальную группу подвергали CO2-лазерной хирургической операции, а затем местно наносили описанные выше противомикробные композиции, включая нижнее белье и другие поверхности контакта, два раза в сутки, постоянно в течение 3 месяцев. В контрольной группе проводили хирургическую операцию, а затем местно наносили эритромициновую мазь, два раза в сутки непрерывно в течение 3 месяцев. Результаты показали, что уровень рецидива в экспериментальной и контрольной группе составил 18,07% и 51,8% соответственно; и отсутствовало значимое отличие между двумя группами. Этот эксперимент продемонстрировал, что противомикробные композиции по настоящему изобретению могут быть вспомогательными при химиотерапии или хирургической операции, и значительно снижают уровень рецидива остроконечной кондиломы.
Вариант осуществления 13е
Эксперимент по предотвращению ассоциированной с катетером инфекции мочевыводящих путей (CAUTI)
В этом эксперименте выбирали пациентов, подвергнутых катетеризации после клинической урологической хирургической операции, и случайным образом распределяли на экспериментальную группу (n=310) и контрольную группу (n=310). В контрольной группе стандартным образом использовали нормальный солевой раствор два раза в сутки. В экспериментальной группе распыляли противомикробную композицию, описанную выше, два раза в сутки, в дополнение к стандартному нанесению нормального солевого раствора. Результаты эксперимента показали, что частота рецидива CAUTI значительно различалась между двумя группами на пятые и седьмые сутки. Уровень инфицирования в контрольной группе составил 16,7% на пятые сутки и 23,3% на седьмые сутки. Уровень инфицирования в экспериментальной группе составил 3,3% на пятые и седьмые сутки. Этот эксперимент подтвердил, что использование противомикробных композиций по изобретению для ухода за постоянным уретральным катетером может эффективно снизить вероятность инфицирования мочевых путей.
Вариант осуществления 13f
Эксперимент по предупреждению вентиляторно-ассоциированной пневмонии (VAP)
В этом эксперименте 325 пациентов, у которых использовали аппарат искусственной вентиляции легких, подразделяли на экспериментальную группу (n=166) и контрольную группу (n=159). В экспериментальной группе проводили чистку щеткой со стандартной жидкостью для полоскания полости рта, а затем наносили противомикробную композицию, 3 раза в сутки; в контрольной группе проводили уход за полостью рта и носовой полостью нормальным солевым раствором, 3 раза в сутки. VAP возникала у 8,5% пациентов в экспериментальной группе; и VAP возникала в 53,3% пациентов в контрольной группе. Результаты для этих двух групп имели значимое различие Р<0,01. Этот эксперимент подтвердил, что использование противомикробных композиций по изобретению для ухода за полостью рта и носа может эффективно уменьшить колонизацию патогенов в полости рта, носа и глотке, тем самым снижая и замедляя заболеваемость VAP.
Вариант осуществления 13g
Эксперимент по предупреждению инфекции перинеального разреза
Было выбрано 164 роженицы с вагинальными родами и перинеальным разрезом, 82 из которых в контрольной группе проводили стандартный уход, т.е. дезинфекцию перинеального разреза и окружающих тканей 0,5% йодофорным ватным шариком, два раза в сутки, и 82 в группе наблюдения проводили стандартный уход и обработку противомикробной композицией. При сравнении степени боли в разрезе рожениц, группа наблюдения была лучшей, чем контрольная группа (Р<0,05); и при сравнении заживления перинеального разреза рожениц, группа наблюдения была лучше, чем контрольная группа (Р<0,05). Этот эксперимент подтвердил, что противомикробная композиция по изобретению имеет длительную противомикробную функцию, функцию смягчения боли, изоляции раневой поверхности и ускорения заживления раны при перинеальном разрезе.
Вариант осуществления 13h
Эксперимент по предупреждению инфицирования спицевого канала после внешней фиксации скелета
80 пациентов с наружной фиксацией скелета нижней конечности случайным образом распределяли на две группы; в группах лечения шовное отверстие пациентов стерилизовали ватным шариком с 75% спиртом, и шовное отверстие обрабатывали противомикробной композицией, и, наконец, перевязывали жгутом с отверстием в форме "Y", обработанным 75% спиртом, один раз в сутки; в контрольной группе шовное отверстие пациентов стерилизовали ватным шариком с 75% спиртом, а затем перевязывали жгутом с отверстиями в форме "Y", обработанным 75% спиртом, один раз в сутки. Бактериальная культура группы введения была отрицательной, в то время как положительный показатель в контрольной группе составил 13,5%. Группа введения проявляла значительно более низкий симптом инфицирования и степень боли, чем контрольная группа. Этот эксперимент показал, что противомикробная композиция по настоящему изобретению проявляла значительный эффект предупреждения инфицирования спицевого канала после внешней фиксации перелома нижней конечности.
Вариант осуществления 13i
Улучшение гигиены рук
Проводили взятие образцов бактерий на руках медицинского персонала для исследования. Мониторинг бактерий проводили в различные периоды времени, т.е. до и через 8 часов после нанесения противомикробной композиции, и данные статистически анализировали. За два месяца провели мониторинг всего 16 человек 96 раз. Число бактерий было значительно меньшим после нанесения, чем до нанесения, с оцененным показателем 97,5%. Этот эксперимент продемонстрировал, что противомикробные композиции по настоящему изобретению могут препятствовать появлению патогенов на коже рук клинического персонала.
Вариант осуществления 13j
Предупреждение гонококковой инфекции
Во влагалище самок мышей BALB/c инокулировали Neisseria gonorrhoeae WHO-L. Влагалище мыши в экспериментальной группе защищали противомикробной пленкой, образованной противомикробной композицией; влагалище мыши в контрольной группе обрабатывали деионизированной водой. Через 2-10 суток после инокуляции проводили мониторинг доли среднего числа PMN от общего числа клеток в окрашенном мазке вагинального секрета мыши; через 2, 4 и 5 суток после инокуляции проводили взятие вагинальных секретов на культуру Neisseria gonorrhoeae; имитировали передачу Neisseria gonorrhoeae от самок самцам: половой акт имитировали на самках, инфицированных Neisseria gonorrhoeae, заменяя половой член мыши стеклянным стержнем. Стеклянный стержень в экспериментальной группе смачивали противомикробной композицией, в то время как стеклянный стержень в контрольной группе смачивали деионизированной водой. Секреты на кончике стеклянного стержня смывали для исследования гонококковой культуры для сравнения степени обнаружения. В эксперименте по стимуляции передачи Neisseria gonorrhoeae от самцов самкам, процент PMN в экспериментальной группе мышей на 5-8 сутки после инокуляции был значимо более низким, чем в контрольной группе (Р<0,05). Экспериментальная группа проявляла более низкий положительный уровень гонококковой культуры, чем контрольная группа (Р<0,01). В эксперименте по имитации передачи Neisseria gonorrhoeae от самок самцам положительный уровень гонококковой культуры в экспериментальной группе мышей был значимо более низким, чем в контрольной группе (Р<0,01). Это показало, что образовавшаяся физическая противомикробная молекулярная пленка может препятствовать инфицированию или колонизации Neisseria gonorrhoeae в репродуктивных путях самок мышей, и может играть роль жидкого презерватива для самок мышей.
Вариант осуществления 13k
Эксперимент по отсрочиванию времени возникновения инфекции
В этом эксперименте использовали модели на кроликах ожогов в комбинации с искусственной инфекцией Pseudomonas aeruginosa. Экспериментальную и контрольную группы обрабатывали в пораженных областях, соответственно, противомикробной композицией и водным растворителем. За 1, 2, 4, 7 и 14 суток до и после экспериментов собирали сыворотку кролика, измеряли температуру тела, и выявляли уровни воспалительных факторов, таких как число WBC, сывороточные уровни NO2-/NO3-, сывороточные уровни TNF и сывороточный суппероксидный анион, и показатели функций печени и почек, такие как аланинаминотрансфераза, щелочная фосфатаза, трансфераза аспарагиновой кислоты, креатинин и азот мочевины. Экспериментальные результаты показали, что фармакодинамические выявляемые показатели повышались медленнее в экспериментальной группе, чем в контрольной группе, и, наконец, две группы достигали более высоких показателей инфицирования. Результаты показали, что противомикробная композиция по настоящему изобретению может эффективно замедлять возникновение раневой инфекции при применении на ранней стадии раны.
Вариант осуществления 13l
Лечение открытых ран
250 пациентов с открытыми ранами, такими как царапины, ушибы и порезы, отбирали и случайным образом распределяли на экспериментальную и контрольную группы, по 125 в каждой. Экспериментальную группу подвергали стандартной очистке раны и промыванию, а затем обрабатывали противомикробными композициями вместе со стерильной марлевой повязкой два раза в сутки до тех пор, пока в ране не появлялась розовая грануляционная ткань, и, наконец, обрабатывали с помощью повязки один раз в сутки до заживления. Контрольную группу подвергали стандартной очистке раны и промыванию, и рану накрывали стерильной марлевой повязкой с тем же временем наложения повязок и ходом обработки, как описано для экспериментальной группы. Результаты показали, что общий уровень эффективности в экспериментальной группе составил 100%, в то время как общий уровень эффективности в контрольной группе составил 86%, и две группы проявляли очень значительное отличие. Этот эксперимент продемонстрировал, что введение противомикробных композиций по настоящему изобретению при лечении открытых ран может улучшить показатель эффективности, ускорить заживление ран и снизить медицинские расходы пациентов.
Вариант осуществления 13m
Лечение ожогов
В этом эксперименте было выбрано 370 пациентов с ожогами и случайным образом распределено в экспериментальную группу (n=195) и контрольную группу (n=175). В экспериментальной группе проводили обработку бромгерамином для очистки раны, затем наносили наружно противомикробную композицию, три раза в сутки; в контрольной группе проводили обработку бромгерамнином для очистки раны, затем наносили наружно серебряную сульфадиазиновую мазь, три раза в сутки. Результаты показали, что отсутствовали значимые отличия в положительном уровне обнаружения бактерий на ране, ответе краев раны и времени заживления (Р>0,05), однако экспериментальная группа была значительно лучше контрольной группы в отношении переносимости боли (Р<0,05). Этот эксперимент продемонстрировал, что противомикробная композиция по настоящему изобретению имела обширный терапевтический эффект на ожоги, эквивалентный SSD, однако имела значительный эффект при смягчении боли и хорошее соблюдение пациентами режима обработки.
Вариант осуществления 13n
Лечение пролежневых язв
В этом эксперименте 163 пациентов, у которых были клинически диагностированы пролежневые язвы стадии II и стадии III, случайным образом распределяли на экспериментальную группу (n=82) и контрольную группу (n=81). Контрольную группу обрабатывали с использованием стандартных способов ухода, т.е. дезинфицируя кожу вокруг раны, промывая рану и удаляя некротические ткани и чужеродные тела, вновь дезинфицируя и покрывая стерильной марлей и ватным диском; ежедневные замены повязки проводили в зависимости от экссудации. В дополнение к описанному выше уходу и замене повязки, используемым в контрольной группе, в экспериментальной группе дополнительно распыляли противомикробную композицию. Клинические результаты представлены ниже. Этот эксперимент продемонстрировал, что противомикробные композиции по настоящему изобретению способны разрушать и предупреждать образование биопленок и преобразовывать незаживающие раны в заживающие раны, ускоряя заживление ран.
Эксперимент по заживлению ран пролежневых язв

Вариант осуществления 13о
Ингибирование опухолевого трансплантата
В эксперименте 40 самцов крыс Wistar случайным образом распределяли на контрольную группу и экспериментальную группу. Линии клеток рака печени крыс R15 использовали для создания моделей опухолей на животных. Экспериментальную группу защищали с использованием противомикробной композиции и сравнивали с контрольной группой. Результаты показали, что встречаемость опухолей в контрольной группе составляла приблизительно 66,7%, и встречаемость опухолей в экспериментальной группе составляла приблизительно 29,4%. Экспериментальная группа и контрольная группа статистически значимо различались (р<0,05) по встречаемости опухоли и не имели различий в образовании опухоли в ходе патоморфологического обследования.
Вариант осуществления 13р
Усовершенствованное исследование жидкости предстательной железы
Противомикробную композицию инъецировали в уретру человека и через 5 минут проводили исследование жидкости предстательной железы. Противомикробная композиция может адсорбировать отрицательно заряженные бактерии, исключая влияние бактерий при исследовании жидкости предстательной железы. Таким образом, может быть увеличена точность исследования жидкости предстательной железы.
Вариант осуществления 14
Комбинирование с медицинскими устройствами
Физическую противомикробную пленку также можно комбинировать с медицинскими устройствами для образования медицинских устройств, имеющих противомикробный эффект, как показано в следующей таблице:




Вариант осуществления 15
Комбинирование с объектом
Физическую противомикробную мембрану по настоящему изобретению можно широко использовать в качестве противомикробного средства, являющегося защищающим от плесени и дезодорирующим, в различных отраслях промышленности, и можно комбинировать с изделиями в этих отраслях промышленности для получения новых комбинированных изделий, как показано в следующей таблице:



Реферат
Группа изобретений относится к области противомикробной обработки. Способ противомикробной обработки включает: нанесение противомикробной композиции для формирования противомикробной пленки с четвертичным катионом. Композиция содержит кремнийорганическую дичетвертичную соль аммония формулы (I), где каждый R1 представляет собой C8-18 алкильную группу, C8-18 алкенильную группу или C8-18 алкинильную группу; каждый R2 и R3 представляет собой метил или этил; R5 представляет собой C3-10 алкилен, который замещен в β-положении или более отдаленном положении посредством три(C1-3 алкокси)силилокси или три(C1-3 алкокси)силил-C1-6 алкокси; и каждый X- представляет собой фармацевтически приемлемый противоанион; и по меньшей мере один эксципиент. При этом толщина противомикробной пленки и диаметр полимерных частиц находятся в диапазоне от 1 нм до 1000 нм, а нанесение обеспечивает дзета-потенциал на поверхности тела от +40 мВ до +80 мВ. Также раскрывается кремнийорганическая дичетвертичная соль аммония, противомикробная композиция, а также способ предупреждения и лечения различных местных инфекций у человека. Группа изобретений обеспечивает уничтожение патогенных микроорганизмов, а также эффективный способ предупреждения и лечения различных инфекций. 4 н. и 26 з.п. ф-лы, 3 ил., 8 табл.
Формула





Комментарии