Способ переработки серебросодержащего сырья - RU2742763C1
Код документа: RU2742763C1
Чертежи
Описание
Изобретение относится к металлургии цветных металлов, в частности, к переработке серебросодержащего сырья.
Наибольшее распространение при переработке серебросодержащего сырья, в т.ч. при аффинаже серебра, получила электрохимическая технология. Исходные материалы, например, сплавы на основе серебра, отливают в форме анодов и подвергают анодному растворению в азотнокислых электролитах. На катоде получают серебро товарной чистоты.
Нерастворившиеся примеси (золото, платиноиды) образуют шлам; растворяемые примеси (неблагородные металлы) переходят в электролит и по мере накопления могут осаждаться на катоде, загрязняя катодное серебро. Загрязненный электролит приходится выводить из ванны и заменять его свежим. Необходимость регенерации электролита и возврат анодных остатков на переплав являются основным недостатком электрохимического метода аффинажа (1. Металлургия благородных металлов: В 2-х кн. Кн. 1 / Ю.А. Котляр, М.А. Меретуков, Л.С. Стрижко. - М.: МИСИС, «Руда и металлы», 2005. г., - 432 с. 2. Масленицкий И.Н., Чугаев Л.Г. Металлургия благородных металлов. - М.: Металлургия, 1987. - 366 с. 3. Меретуков М.А., Орлов A.M. Металлургия благородных металлов. Зарубежный опыт. - М.: Металлургия, 1990. - 416).
Известны методы получения чистого серебра, включающие химическое растворение исходного сплава в азотнокислых растворах, осаждение из полученного раствора серебра в виде хлорида. Для получения чистого серебра тщательно отмытый от примесей хлорид плавят с содой, восстанавливают в растворах цементацией цинком, металлическим железом (2), водородом (РФ 2265673 от 10.12.2005), гидроксиламином (РФ 2185452 от 20.07.2002), сахаром (РФ 2535266 от 01.04.2013) и другими методами.
Отмеченные способы технологически проще, скорость основных процессов выше.
Растворение серебросодержащего сырья в азотнокислых растворах широко распространено и технологически не вызывает проблем. Самым важным недостатком этого способа является выделение токсичных оксидов азотана стадии растворения. Для минимизации объемов токсичных выбросов предложено растворение проводить в присутствие ионов аммония (РФ 2100484 от 27.12.1997). К числу недостатков этой перспективной технологии следует отнести технологическую сложность полной нейтрализации оксидов азота. Кроме того, при использовании азотной кислоты в качестве окислителя в серебросодержащий раствор частично переходят платина и палладий при их наличии в исходном сырье. Данное обстоятельство обуславливает включение в технологическую схему операций выделения МПГ из азотнокислых растворов.
Известен способ извлечения серебра из шламов (РФ 2312911 от 20.12.2007), основанный на обработке шлама окислителем в кислой среде с переводом серебра в раствор, при этом шламы предварительно подвергают восстановительному воздействию для перевода исходных соединений серебра и платиноидов в металлические порошки, а последующее растворение ведут в среде сульфаминовой кислоты, а также тем, что в качестве окислителя используют пероксид водорода или персульфат калия или аммония и обработку ведут при нагревании. Данный способ применим только к дисперсным материалам и технологически сложный. Важнейшей особенностью прототипа является то, что растворению подвергают порошкообразное серебро, полученное из хлорида серебра путем его гидрохимического восстановления.
Известен способ рафинирования серебра, выбранный прототипом (РФ 2280086), включающий растворение металлического серебра в азотнокислом электролите, в присутствии пероксида водорода, отделение нерастворимого остатка, выделение серебра и возврат электролита на растворение металлического серебра. Отличительной особенностью прототипа является использование пероксида водорода в качестве окислителя серебра.
Особенность прототипа заключается в том, что выбранные условия растворения серебра в азотнокислом электролите, в частности, позволяют уменьшить выделение в атмосферу оксидов азота и нежелательный переход в электролит платиноидов. Вместе с тем, совокупность заявленных параметров прототипа, в частности соотношение массы серебра и азотной кислоты или диапазон рекомендуемых концентраций азотной кислоты 30-50 г/л, позволяет растворить только порошкообразное серебро. По сути, сырьем для переработки данным способом может быть шлам, содержащий порошкообразное серебро, или серебряный порошок, полученный тем или иным методом, в частности, восстановлением хлорида. Публикации по изучаемой теме и собственный опыт показывают, что растворение компактного и даже гранулированного серебра с использованием способа-прототипа протекает с очень маленькими скоростями и практического значения не имеет.
Технической проблемой, на решение которой направлен предлагаемый способ, является исключение выделения токсичных газов и перехода в раствор платины и палладия при растворении компактного серебра и сплавов на его основе.
Достижение требуемого технического результата при растворении серебросодержащего сырья основано на изменении состава используемого раствора и условий растворения.
Технический результат достигается при использовании способа, включающего растворение исходного серебросодержащего сырья в присутствии пероксида водорода, отделение нерастворимого остатка, выделение из полученного раствора серебра, отличающегося тем, что растворение исходного сырья проводят в растворе, содержащем 50-150 г/л сульфата аммония при рН=9-10 и температуре 20-30°С. Для продуктивного расходования пероксида водорода концентрацию этого реагента в ходе растворения поддерживают в диапазоне 10-50 г/л.
Сопоставительный анализ известных технических решений и заявляемого способа позволяет сделать вывод о том, что изобретение неизвестно из уровня техники и соответствует критерию «новизна». От прототипа заявляемый способ отличается тем, что растворение серебра в в присутствии пероксида водорода осуществляют в слабощелочном растворе сульфата аммония, при этих условиях становится возможным растворение не только дисперсного, но и компактного серебросодержащего сырья с приемлемой для практики скоростью.
Сущность заявляемого способа заключается в том, что выбранные условия полностью исключают выделение оксидов азота и нежелательный переход в электролит платиновых металлов.
Экспериментально установлено, что заявляемая совокупность существенных признаков является оптимальной и обеспечивает достижение технического результата.
Растворение серебросодержащего, равно как и любого металлического, сырья в концентрированных растворах азотной кислоты протекает очень интенсивно. При концентрациях кислоты меньше 30-50 г/л окислительный потенциал системы недостаточный, растворение серебра прекращается даже при нагревании. Введение пероксида водорода в такой раствор инициирует процесс, причем присутствующая в системе азотная кислота выполняет исключительно роль источника нитрат-иона, необходимого для сольватации катиона серебра. Результаты опытов показывают, что в этих условиях даже при умеренных температурах платина и палладий может переходить в раствор, что обуславливает усложнение технологической схемы.
Известна способность катионов серебра образовывать прочные комплексы с ионом аммония. В соответствии с теорией при одновременном присутствии комплексообразователя и окислителя, обладающего достаточным окислительным потенциалом, металлы переходят в раствор. В частности, серебро может быть растворено в аммиачном растворе в присутствии пероксида водорода. Однако метастабильность данной системы, заключающаяся в интенсивном непродуктивном разложении указанных реагентов, делает данный вариант экономически неприемлемым. Кроме того, процесс сопровождается обильным выделением аммиака в газовую фазу, что ухудшает экологические условия. Исследованиями установлено, что большей стабильностью обладает слабощелочной раствор, содержащий аммоний в виде соли. Из числа доступных солей аммония технологически более целесообразно использование сульфата. Оптимальная концентрация сульфата аммония - 50-150 г/л. Комплексообразование серебра с достаточной степенью протекает в области рН=9-10. При меньшем значении рН растворение ухудшается, в более щелочных растворах активизируется выделение аммиака в газовую фазу. Нагрев раствора сопровождается аналогичным эффектом, поэтому процесс ведут при комнатной температуре.
Избыточная концентрация пероксида в любых растворах сопровождается непродуктивным разложением и выделением кислорода в газовую фазу. Для минимизации этого нежелательного процесса концентрацию окислителя целесообразно поддерживать в диапазоне 10-50 г/л. При более высокой концентрации наблюдается заметное разложение пероксида и выделение кислорода. При уменьшении ниже 10 г/л растворение прекращается.
Примером реализации предлагаемого способа служат результаты следующих опытов.
Исходным сырьем служил сплав серебряно-золотой с содержанием Ag 93,5; 3,7% Au; 0,5% Pd; 0,3% Pt. Идентичные по размеру компактные образцы сплава ССЗ растворяли в условиях предлагаемого способа в течение одного часа в лабораторном стакане с перемешиванием. В опытах варьировали начальной концентрацией сульфата аммония, рН, и действующей концентрацией пероксида водорода. По ходу процесса отбирали пробы раствора и с учетом результатов анализа на остаточное содержание пероксида этот реагент добавляли. В ходе растворения наблюдали за выделением кислорода и по данному факту судили о степени нерационального расходования пероксида; по запаху судили о выделении аммиака. В полученном серебросодержащем растворе определяли концентрацию серебра, платины, палладия и оценивали скорость растворения.
Для сравнения проведены опыты в режиме способа прототипа. В этом случае растворяли компактный образец ССЗ массой 9 г и тех же габаритов, что в вышеуказанных опытах, и порошкообразное серебро (9 г), полученное восстановлением хлорида серебра.
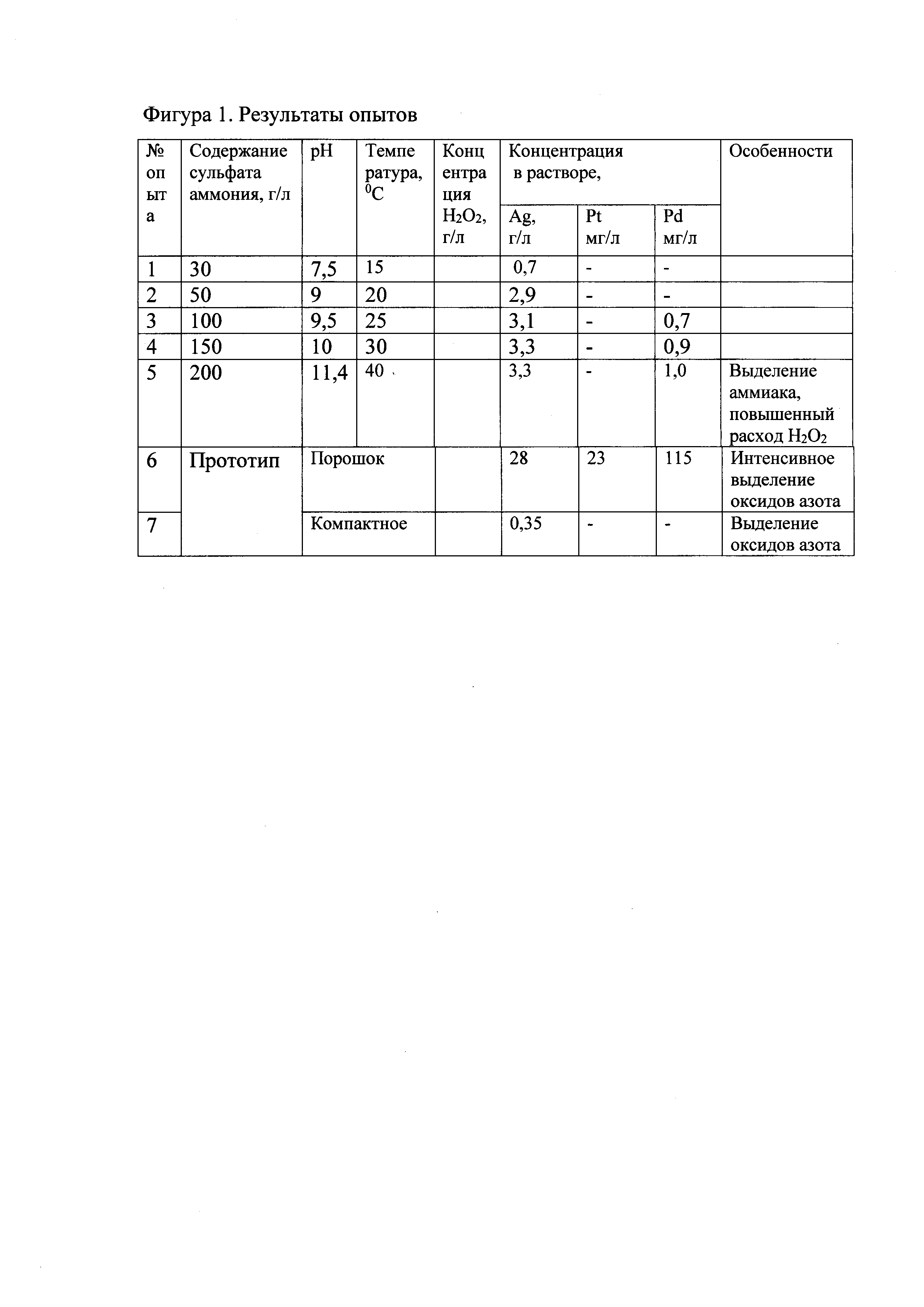
Растворение проводили в азотной кислоте с расходом серебра 2 кг на 1 кг азотной кислоты и эквимолярном количестве пероксида водорода. Результаты опытов представлены в таблице (Фиг. 1).
Сопоставительный анализ способа, выбранного в качестве прототипа, и предполагаемого изобретения позволяет сделать вывод, что именно совокупность заявленных признаков обеспечивает достижение усматриваемого технического результата. Реализация предложенного технического решения за счет предложенного состава раствора и заявленных режимов дает возможность растворить компактное серебро без выделения оксидов азота и перехода платиновых металлов в раствор.
Реферат
Изобретение относится к металлургии цветных и благородных металлов, в частности к методам получения чистого серебра. Способ включает химическое растворение серебросодержащего сырья в присутствии пероксида водорода, отделение нерастворимого остатка и выделение из полученного раствора серебра. При этом растворение исходного сырья проводят при рН 9-10 и температуре 20-30°С в растворе, содержащем 50-150 г/л сульфата аммония и 10-50 г/л пероксида водорода. Способ позволяет исключить выделение токсичных газов и переход в раствор платиновых металлов. 1 ил.

Комментарии