Способ извлечения благородных металлов - RU2494159C1
Код документа: RU2494159C1
Чертежи



Описание
УРОВЕНЬ ТЕХНИКИ
Настоящее изобретение относится к области способов разделения элементов.
Извлечение, выделение и очистка ценных благородных металлов, например платины [Pt], палладия [Pd], иридия [Ir], родия [Rh], рутения [Ru] и золота [Au], как правило, являются трудоемкими процессами, требующими многократного применения пирометаллургических, гидрометаллургических или электролитических процессов для достижения удовлетворительной степени извлечения металла и чистоты металла. Большинство исходных материалов, таких как руда, отработанные катализаторы, гальванические растворы, шламы, рудные концентраты и штейны плавильных печей являются химическими сложными, не только из-за разнообразия элементов благородных металлов, но и из-за присутствия большого количества неблагородных металлов в исходном материале. Извлечение, очистка и разделение элементов благородных металлов из этих исходных материалов является очень сложным, длительным и дорогим процессом и не дает удовлетворительных результатов для некоторых элементов, в частности, родия.
Химия благородных металлов чрезвычайно сложна и не всегда хорошо понятна. В кислой среде с галогенами, в частности в хлористой среде, благородные металлы не образуют простых гидратированных катионов по типу образуемых большинством неблагородных металлов (например, Ni(H20)+2). Благородные металлы образуют сосуществующие координационные комплексные соединения с многими различными лигандами. Например, известные комплексы родия (III) включают в себя [RhCl6]-3, [RhCl5(H2O)]-2, [RhCl4(H2O)2]-2 и [RhCl3(Н2O)3]. Равновесный состав 1М раствора хлорида включает примерно 80% [RhCl5(H2O)]-2, примерно 10% [RhCl6]-3, 10% [RhCl4(H20)2]-2 и менее примерно 1% [RhCl3(Н20)3] (см. Grant, R.A. 1989, The Separation Chamistry of Rhodium and Iridium, в книге под ред. Manziek "Precious Metals Recovery and Refining, Proceedings of the International Precious Metal Institute, pp.7-41). Однако распределение совместно существующих комплексных соединений вряд ли будет представлять собой равновесный состав, в частности, в промышленных приложениях, где задействовано несколько благородных металлов. Кинетика скоростей лигандного обмена у благородных металлов может достигать предельных значений. Например, относительная скорость обмена для платины (IV) составляет 10-12 по отношению к палладию. В то время как лигандный обмен палладия может длиться нескольких часов или дней, для платины (IV) лигандный обмен может занять месяцы. Очевидно, сложный состав благородных металлов, кинетика реакций и другие факторы совместно обусловили разработку существующих сложных, длительных и трудоемких протоколов извлечения благородных металлов, недостатком которых часто оказываются разочаровывающие результаты или большие затраты.
Современная промышленная технология извлечения благородных металлов основана главным образом на их жидкостной экстракции, которая обычно дополняется процессами ионного обмена и традиционными химическими методами, несмотря на неэффективность, большую длительность переработки, большие объемы растворов и множество других проблем. Патенты США 5201942 и 7291202 содержат обзор некоторых трудностей, связанных с извлечением и очисткой благородных металлов. Извлечение и очистка благородных металлов в этих патентах, а также по патенту США 7175818, представляют собой длительные и сложные процессы, которые не в полной мере решают существующие ограничения и имеют высокую стоимость.
За последние десятилетия в индустрии благородных металлов было предпринято множество усилий по развитию и совершенствованию способов жидкостной экстракции для получения золота и некоторых металлов платиновой группы. Несмотря на значительный прогресс в существующих технологиях для каждого элемента обычно используют разные экстрагенты. Процессы обмена с растворителем регулируются равновесием. Для каждой жидкостной экстракции может потребоваться множество контактов экстрагента и маточного раствора, выгрузка экстрагента, очистка экстрагента для удаления примесей и регенерация экстрагента. Таким образом, полного извлечения целевого металла достичь не удается, и с каждой экстракцией общие потери металла могут увеличиваться. Кроме того, возможно извлечение примесных элементов вместе с целевым металлом, что требует очистки целевого металла. Методы жидкостной экстракций, хотя и являются методами выбора, могут дополнительно осложняться плохим разделением растворителя и маточного раствора, растворимостью экстрагента в маточном растворе или в промывных растворах, многочисленными побочными потоками извлекаемого металла, большими объемами водных растворов, требующих обработки, а также с токсичностью и горючестью органических экстрагентов.
Ионообменные процессы были избирательно внедрены в технологические протоколы получения благородных металлов, но имеют более ограниченное применение, чем методы жидкостной экстракции и не решают проблем извлечения и очистки. Ионообменные процессы обычно протекают в равновесном режиме и не позволяют полностью выделить целевой металл. Ионообменные способы могут также иметь недостаточную избирательность по отношению к благородным металлам, что может привести к одновременному извлечению разных благородных металлов, или приводить к одновременному извлечению примесных элементов. Обычно ионообменные смолы для благородных металлов дороги, имеют относительно низкую емкость, что обуславливает потребность в больших объемах смол и, соответственно, больших объемов промывных растворов для извлечения целевого металла, и при этом экстрагированные металлы часто требуют дополнительной очистки.
Совместно с жидкостной экстракцией и/или ионообменным процессом могут применяться и другие химические способы осаждения и испарения. Как правило, эти способы используют для отделения выбранных элементов из маточного раствора или для очистки металлов недостаточной чистоты.
Выделение и извлечение родия являются особенно актуальной проблемой. В обычных существующих способах экстракции родий остается в конце после извлечения других металлов платиновой группы. Такой процесс имеет по меньшей мере три недостатка: родий теряется в многочисленных побочных потоках при противоточной экстракции; родий заблокирован во время извлечения других благородных металлов; родий и иридий часто оказываются вместе в конечном растворе, а разделение этих двух металлов любым из известных способов затруднительно.
Несмотря на значительные усилия извлечение и очищение родия остается сложной задачей. Не существует известных легких в использовании растворителей-экстрактантов для родия. В патенте США 5201942 предложен растворитель-экстрагент для родия, требующий комплексообразования Rh с высоким молярным избытком олова. Предлагаемый способ жидкостной экстракции имеет свои ограничения: он предполагает предварительное отделение осмия и иридия другими способами, количество экстрагируемого родия мало и родий необходимо дополнительно обрабатывать для удаления олова, которое может присутствовать в 10-кратном молярном избытке. Ионообменные способы извлечения и очистки Rh в промышленных масштабах также дают неутешительные результаты или являются безуспешными. По необходимости в промышленности для очистки родия широко используют трудоемкие способы осаждения и растворения.
Для удовлетворения спроса на благородные металлы промышленность нуждается в более простой и более дешевой альтернативе существующей технологии, смогла бы обеспечить извлечение благородных металлов из химически различающихся видов первичного и вторичного сырья.
Все упомянутые выше патенты США полностью включены в настоящую заявку путем ссылки для всех полезных целей.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к гидрометаллургическому способу извлечения благородных металлов, выбранных из группы, состоящей из платины [Pt], палладия [Pd], родия [Rh], рутения [Ru], иридия [IR]) и золота [Au] от неблагородных металлов в кислых водных растворах галогенидов. В этом способе для осаждения благородного металла(ов), который необходимо выделить, используют замещенные четвертичные аммониевые соли. Этап, на котором осаждаются различные благородные металлы, зависит от параметров раствора.
В первом дополнительном аспекте настоящего изобретения растворенные благородные металлы нагревают, нагревают с обратным холодильником или автоклавируют в водном растворе галогенида, содержащем галогенсодержащую кислоту, галогениды щелочных или щелочноземельных металлов, замещенные четвертичные галоидные соли аммония и их сочетание.
Во втором дополнительном аспекте настоящего изобретения благородные металлы в присутствии замещенных четвертичных солей аммония окисляют до высших степеней окисления перед осаждением. Это может быть осуществлено путем добавления хлора в раствор.
В третьем и отдельном дополнительном аспекте настоящего изобретения благородные металлы в присутствии замещенных четвертичных солей аммония восстанавливают до более низких степеней окисления перед осаждением. Это можно осуществить путем нагревания и последующего охлаждения раствора или путем применения восстановителей.
В четвертом и отдельном дополнительном аспекте настоящего изобретения благородные металлы в присутствии замещенных четвертичных солей аммония отделяют друг от друга, используя различия в растворимости в одном или нескольких растворителях.
В пятом и отдельном дополнительном аспекте настоящего изобретения Rh, Ru и неблагородные металлы отделяют от осадков Au, Pt, Pd, Ir и Fe при комнатной температуре в присутствии замещенных четвертичных солей аммония.
Еще один аспект настоящего изобретения предполагает объединение любых из вышеупомянутых отдельных аспектов друг с другом для достижения дополнительных преимуществ.
Таким образом, задачей настоящего изобретения является обеспечение улучшенного способа извлечения некоторых благородных металлов. Другие дополнительные задачи и преимущества изложены ниже.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На Фиг.1А и 1В приведена схема процесса из примера А.
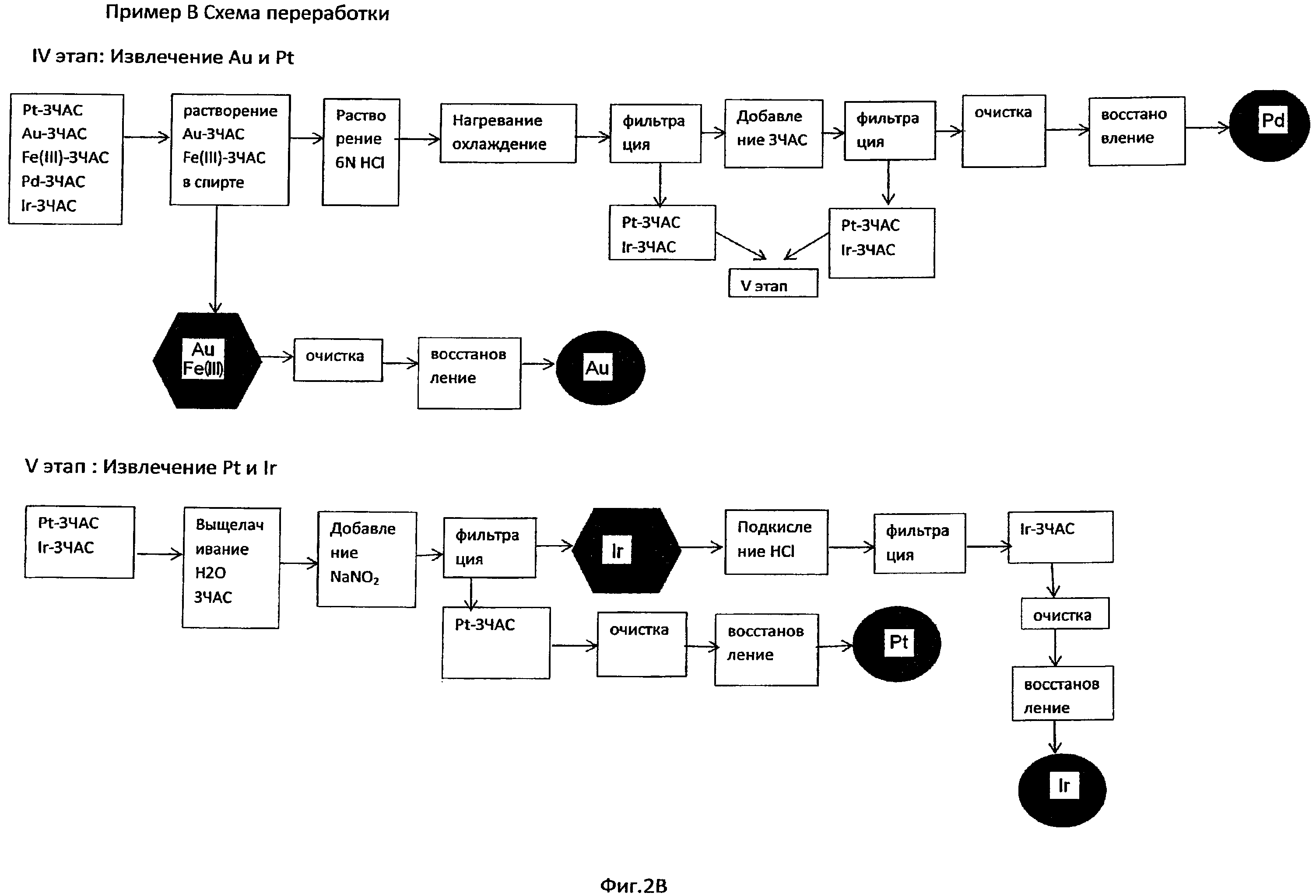
На Фиг.2А и 2В приведена схема процесса из примера В.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ РЕАЛИЗАЦИИ
Предложены гидрометаллургические способы извлечения благородных металлов платины [Pt], палладия [Pd], родия [Rh], рутения [Ru], иридия [IR]) и золота [Au] (далее, БМ как в единственном, так и во множественном числе) из водных растворов галогенсодержащих кислот, отделение БМ от неблагородных металлов и отделения БМ друг от друга с получением металлов высокой чистоты. Отделение и извлечение серебра не было исследовано в деталях, но значительное его количество будет получено как побочный продукт в ходе извлечения и очистки БМ.
Сырьем для получения БМ могут быть руды, отработанные катализаторы, продукты сгорания конвертеров, электронный лом, медицинские отходы и др. Химически более сложное сырье часто состоит из смесей БМ и неблагородных металлов. Неблагородные металлы включают Ni, Co, As, Sb, Pb, Си, Fe, Zn, Те, Se, S, Na, Ca, Mg, Al, Si, редкоземельные и другие элементы (далее НМ, как в единственном, так и во множественном числе). Концентрации благородных металлов не существенны для предложенных способов. БМ и НМ растворяют в водных растворах галогенсодержащих кислот с кислотой и окислителем или без них. В предпочтительном варианте в качестве галогенсодержащей кислоты предпочтительной является соляная кислота из-за низкой стоимости и широкого использования в промышленности.
В предпочтительном варианте БМ осаждают с использованием замещенных четвертичных солей аммония (далее ЗЧАС). ЗЧАС описывают общей формулой: Н0-3R4-1NX, где Н=водород, R=органическая группа, N=азот и Х=галоген. Ниже приведены некоторые желаемые характеристики ЗЧАС, используемой в способе, в зависимости от БМ и желаемые результаты:
1. Растворимость в воде и в растворах кислот.
2. Большинство НМ остаются в растворе.
3. Образование нерастворимых осадков с большинством БМ в выбранной химической среде.
4. Образование осадков БМ с разной растворимостью в зависимости от степени окисления БМ.
5. Образование осадков БМ с разной растворимостью в зависимости от концентрации ЗЧАС.
6. Образование осадков БМ, которые легко отделяются друг от друга соответствующими способами и отмываются.
7. Образование осадков БМ, некоторые из которых растворимы в органических растворителях.
Большое количество замещенных четвертичных солей аммония благородных металлов были синтезированы и описаны, см. J.W.Mellor, Comprehensive Treatise on Inorganic and Theoretical Chemistry, vol.XV (Longman, London 1936). В предложенных способах были использованы комплексы БМ с диметиламмония хлоридом, триметиламмония хлоридом, тетраметиламмоний хлоридом, тетраэтиламмония бромидом. Другие замещенные четвертичные аммониевые соли, соответствующие общей формуле с желаемыми характеристиками, также подходят для образования подходящих комплексов БМ-ЗЧАС. Более предпочтительным является тетраметиламмоний хлорид, поскольку он отвечает требуемым характеристикам, широко доступен, имеет низкую стоимость и не приводит к смешиванию галогенидов в растворе при добавлении растворов БМ, которые обычно растворены в соляной кислоте.
Извлечение и рафинирование БМ, включающие способы нагревания, охлаждения, осаждения, растворения, окисления и восстановления комплексов с ЗЧАС, позволяют быстро и с меньшими затратами решить задачи отделения БМ от НМ, отделения БМ друг от друга и количественного извлечения. После осаждения БМ-ЗЧАС, обычно после охлаждения раствора, во всех рассматриваемых случаях осадки отделяли от фильтрата физически: фильтрацией, центрифугированием, выпариванием или другим приемлемым способом. Неблагородные металлы остаются в фильтрате практически во всех способах. В отдельных случаях, когда образуются осадки НМ-ЗЧАС, из можно легко удалить путем растворения в органических растворителях, содержащих спирт, диметилформамид и др., за исключением Pb, который удобнее удалять, как описано ниже. Кроме того, имеются другие очевидные преимущества:
1. Комплексы БМ-ЗЧАС осаждаются быстро, и осадки легко можно отделить, промыть и очистить.
2. Способ является гибким и специалист в данной области может легко адаптировать отдельные процессы в зависимости исходного сырья с различными абсолютными и относительными количествами БМ и НМ.
3. БМ разделяются на отдельные производственные потоки для параллельного рафинирования, что обеспечивает снижение перекрестногозагрязненияБМ или ИМ, снижая объемы боковых потоков и общие потери из-за большого количества последовательных процессов, и снижает время рафинирвания.
4. Осаждение комплексов БМ-ЗЧАС является количественным или почти количественным, при этом остаточная концентрация БМ в фильтратах не обнаруживается, ниже уровня нескольких ppm при анализе на спектрометрах с индуктивно-связанной плазмой (ICP).
5. Комплексы БМ-ЗЧАС могут быть легко очищены и преобразованы в растворы, соли или металлы высокой чистоты посредством хорошо известных способов.
6. Потери сведены к минимуму, поскольку реагенты и попутные продукты регенерируемы.
7. Металлы, оставшиеся после осаждения, процедур промывки и очистки могут быть легко и полностью извлечены.
Хотя мы не можем привести конкретное правило, извлечение и очистка БМ с использованием ЗЧАС показывает снижение специфических ограничений, обусловленных термодинамическими и кинетическими свойствами БМ в водных растворах галогенидов, которые давно требовалось устранить. Образование соединений БМ в водной хлорсодержащей среде особенно хорошо известно по сравнению с другими галогенсодержащими средами, хотя известны и другие водные растворы галогенидов. Относительное содержание хлор-водных комплексов отчасти зависит от концентраций ионов хлора в водном растворе. В общем, более высокая концентрация хлоридов повышает образование соединений с более высоким отношением хлор- к аква-лигандам и подавляет образование комплексов с низким отношением. Например, в одном и том же растворе может сосуществовать более четырех хлор-водных комплексов Rh; аналогичные составы известны и для других БМ. Считается, что такие соединения представляют значительные трудности при химической обработке, а также и в других современных производственных процессах. Оказалось, что применение ЗЧАС может снижать образование этих комплексных соединений БМ достаточно снизится, обеспечивая фактические успехи в извлечении и очистке БМ.
В предпочтительном варианте реализации минимальная общая концентрация хлорид-ионов в растворе представляет собой концентрацию, необходимую для стехиометрического полного дополнения хлорных лигандов БМ (3 для золота (III); 4 для Pt (II) и Pd (II); 6 для Pt (IV), Pd (IV), Rh (III), Ru (III) и Ru (IV); и 1 для Ag). Предпочтительнее, чтобы концентрация хлорид-ионов была существенно выше, что способствует образованию комплексов БМ-хлор, и может достигать предела насыщения. Хлорид-ионы могут быть получены из различных источников, содержащих соляную кислоту, соли щелочных металлов, соли щелочноземельных металлов, замещенные четвертичные аммониевые соли и их сочетания.
В одном из вариантов БМ извлекают, разделяют и очищают в 6Н HCl. Это обеспечивает дополнительное преимущество, состоящее в возможности регенерации постоянно кипящей HCl; хотя можно использовать и концентрированную HCl. В другом варианте источником хлора является NaCl. Например, достаточное количество воды добавляют для растворения смеси продуктов, являющихся результатом сплавления NaCl и Rh в среде Cl2. Дополнительная переработка и осаждение Rh-ЗЧАС дает менее 10 ppm Rh в фильтрате. Сравнимые результаты были достигнуты и с другими БМ.
Таким образом, в предпочтительных способах целесообразно использовать фоновую концентрацию хлоридов до состояния насыщения. Хотя мы не исследовали влияние основных растворов в деталях, основные растворы даже в присутствии хлоридов могут нарушить процесс, поскольку некоторые неблагородные металлы и некоторые БМ будут осаждаться совместно и загрязнять получаемые продукты. Например, комплекс Pd-ЗЧАС не будет высаживаться из основного раствора, содержащего Pd. Кинетика реакции, вероятно, также играет важную роль в осаждении некоторых соединений БМ-ЗЧАС, в частности, БМ [например, Rh и Pt (IV)], имеющих низкую скорость лигандного обмена. Как описано выше, в предпочтительном способе скорость лигандного обмена хлор-вода в водной хлорсодержащей среде может изменяться до 1012 для БМ. Считается, что даже при высокой концентрации хлоридов, кинетика хлор-водного обмена может быть достаточно медленной для того, чтобы препятствовать установлению термодинамического равновесия между соединениями с хлором и водой в пределах приемлемой продолжительности производственного процесса. Считается, что еравновесное комплексообразование БМ мешает эффективному осаждению комплексов БМ-ЗЧАС на уровнях, близких к количественным. Например, осаждение Rh из расплава NaCl в присутствии Cl2 с ЗЧАС в насыщенном растворе NaCl, в котором хлоридов содержится больше необходимого для образования гексахлор-соединений, приводит к осаждению незначительного количества Rh-ЗЧАС, однако, концентрация Rh в фильтрате превышает 1000 ppm.
Кинетические показатели могут быть термически снижены или почти устранены, что необходимого для осаждения БМ-ЗЧАС без снижения концентраций БМ до допустимого уровня в остаточном растворе. БМ, растворенные в водном хлорсодержащем растворе, нагревают до кипения или температуры дефлегмации и оставляют для взаимодействия на несколько часов или несколько дней для надежности; однако, допустимо нагревание при более низких температурах в течение длительного периода времени или при более высоких температурах в течение более короткого периода времени допустимо до предела устойчивости ЗЧАС в автоклаве. В одном из вариантов осуществления БМ термически обрабатываются в водном хлорсодержащем растворе. Например, в упомянутом выше случае осаждения Rh-ЗЧАС из раствора расплава NaCl концентрация Rh в фильтрате превышает 1000 ppm. Нагрев до температуры дефлегмирования, охлаждение и осаждение Rh-ЗЧАС в течение около 24 часов дает почти количественное осаждение Rh-ЗЧАС с остаточной концентрацией Rh в фильтрате менее 10 ppm. В другом варианте реализации осуществляют термическое воздействие на БМ в присутствии ЗЧАС, что также по-видимому также стимулирует кинетику реакции и значительно улучшает количественное осаждение БМ-ЗЧАС.
Хотя нет точных и полных данных о комплексных соединениях БМ в водных хлор-содержащих растворах и механизмы регулирования кинетики реакции полностью не известны растворах хлоридов, сочетание достаточно высокой концентрации хлоридов и термической обработки дает в достаточной мере предсказуеые и надежные результаты при извлечении и очистке БМ.
Идентичность компаундов (комплексов) БМ-ЗЧАС, получаемых при взаимодействии элементарного БМ и ЗЧАС не была точно определена. Скорее, мы имеем дело с компаундами типа комплексов БМ-ЗЧАС и отдельными комплексами, такими как родий в виде Rh-ЗЧАС. Состав осадков отдельных комплексов БМ-ЗЧАС могут сами представлять смесь несколько различных комплексов, в зависимости от того, являются ли они одно- или двуядерные комплексами БМ, или вариантов отношения хлор-вода или других факторов. Как правило, анализ количества металла в отдельных в комплексах БМ-ЗЧАС не точно соответствует известным конечным соединениям или могут немного отличаться из-за повышенной аналитической ошибки (неточности) между различными осадками одного и того же БМ-ЗЧАС. Несмотря на недостаток знаний о комплексах БМ-ЗЧАС, они предсказуемо и надежно образуются в одинаковых условиях реакции и предсказуемо и надежно реагируют на различные химические обработки, предназначенные для эффективного извлечения и очистки БМ.
В предпочтительных способах используют физические и химические свойства БМ по отношению друг к другу и к НМ, в различных формах с ЗЧАС.БМ-ЗЧАС и растворы БМ могут быть подвергнуты термическим и химическим манипуляциям водных растворах или в твердом состоянии, для достижения желаемых результатов, таких как высокий уровень извлечения и высокая степень чистоты продуктов за достаточно короткие сроки при относительно низких затратах.
Растворимость БМ в присутствии ЗЧАС и БМ-ЗЧАС зависит от ряда факторов, включающих особенности элемента, степень окисления, режим термообработки, концентрации ЗЧАС и состава растворителя. Характеристики растворимости комплексов БМ-ЗЧАС для одного состава ЗЧАС приведены в таблице 1. Хлорид тетраметиламмоний является типичным примерам и показав только потому, что для него имеется надежная база данных. Таблица не является исчерпывающей, но является показательной для некоторых вариантов растворимости как функции идентичности элемента, степени окисления, режима термообработки, концентрации ЗЧАС и состава растворителя для БМ и тетраметиламмоний хлорида. Опытный специалист в данной области может изменять тип растворителя, концентрацию ЗЧАС, состав ЗЧАС в пределах общей формулы, режим термической обработки и степень окисления, чтобы получить сопоставимую базу данных, а затем разработать ряд технологических операций касательно растворимости и нерастворимости необходимых элементов, для извлечения, разделения и очистки БМ друг от друга и от НМ.
Для элементов БМ с несколькими степенями окисления придаваемая им степень окисления оказывает сильное влияние на растворимость (табл.1). Комплексы Pt-ЗЧАС, Pd-ЗЧАС, Ir-ЗЧАС и Ru-ЗЧАС, как правило, растворимы при низшей степени окисления и нерастворимы при высшей степени окисления. Степени окисления задают путем применения хорошо известных окисляющих или восстанавливающих агентов или путем изменения условий восстановления или окисления. Большинство реакций окисления и восстановления обратимы и предполагают скорее окисление или восстановление, чем другие факторы, такие как неустановленные химические изменения в составе или структуре комплекса БМ-ЗЧАС. Например, если Pt, Pd, Ir и Ru, содержащиеся в очищаемых растворах или в растворах, полученных растворением концентратов БМ, находятся в низших степенях окисления, они могут быть окислены до высших степеней окисления с помощью сильных окислителей, содержащих хлор, перекись водорода или др. Хлор является более предпочтительным, поскольку указанные четыре элемента в высших степенях окисления, как правило, нерастворимы. При повышении фонового содержания хлорида в процессе хлоридного окисления растворимость окисленных комплексов БМ-ЗЧАС сохранится или снизится. Окисленные нерастворимые комплексы Pb-ЗЧАС и Pd-ЗЧАС могут быть восстановлены до растворимых БМ с помощью известных восстановителей или путем нагревания собратным холодильником. Растворимые Pd и Pb в растворах ЗЧАС могут быть в последствии обратно окислены с использованием окислителей до нерастворимых комплексов Pb-ЗЧАС или Pd-ЗЧАС.
Нерастворимость окисленных комплексов Pt-ЗЧАС, Pd-ЗЧАС, Ir-ЗЧАС и Ru-ЗЧАС по сравнению с комплексами с ЗЧАС тех же металлов в восстановленных состояниях представляет собой эффективный механизм для отделения четырех металлов друг от друга. Специалисты смогут осуществить селективное окисление или восстановление одного или нескольких металлов из четырех. Например, кипячения Pt-ЗЧАС, Pd-ЗЧАС, Ir-ЗЧАС и Ru-ЗЧАС комплексов в воде или в водном растворе кислоты, как известно, достаточно для восстановления и растворения палладия, в то время как остальные три комплекса БМ останутся нерастворимыми. Платина и иридий могут быть разделены путем селективного восстановления иридия. Нитрит натрия в достаточном для восстановления Ir количестве, добавляют к нерастворимому окисленному комплексу, содержащему Pt-ЗЧАС и Ir-ЗЧАС, для образования совместного осадка в водном растворе ЗЧАС. Ir быстро реагирует с NaNOz и становится растворимым, в то время как платина не прореагирует и остается в виде нерастворимого комплекса Pt-ЗЧАС. В типичных вариантах предлагаемых способов отсутствие высших степеней окисления у Rh и Au также может быть успешно использовано для обеспечения дополнительных преимуществ, в частности, для разделения, извлечения и очистки Rh. В одном из вариантов водный раствор хлорсодержащий раствор Rh содержит Pt, Pd, Ir, Ru, а также ЗЧАС в стехиометрическом избытке. Окисление, желательно с Cl2, доводит Pt, Pd, Ir и Ru до высших степеней окисления с последующим осаждением их соли с ЗЧАС, в то время как Rh остается в растворе и в его можно отделить. В другом варианте осуществления, наоборот, Rh может быть растворен в кислых растворах (преимущественно 6Н HCl), так как нерастворимые окисленные осадки БМ-ЗЧАС устойчивы и разделимы. В этом варианте Rh как наиболее ценный металл может быть извлечен и очищен в начале процесса, а не ближе концу, как в современных промышленных способах.
В типичном варианте осуществления окисление очень мало влияет на растворимость большинства НМ в присутствии ЗЧАС. Большинство НМ растворимы как в низших, так и высших степенях окисления и легко отделяются от нерастворимых осадков БМ-ЗЧАС. Однако в некоторых случаях присутствие Pb (IV) и Fe (III) может привести к нерастворимости осадков комплексов Pb(IV)-ЗЧАС и Fe(III)-ЗЧАС, а также целевых БМ (табл.1). В технологическую цепочку могут быть включены специальные процедуры, чтобы отделить их от окисленных осадков БМ.
Совместное осаждение комплексов Pb (IV)-34AC вместе с Rh-ЗЧАС, Au (ЗЧАС), Pt-ЗЧАС, Fe (III)-ЗЧАС, и Pd-ЗЧАС после добавления ЗЧАС к раствору, полученному после растворения концентратов БМ, содержащих свинец в хлорированной соляной кислоте предсказуемо, но не желательно; однако, совместное осаждение свинца может быть значительно уменьшена или практически устранено. Перед добавлением ЗЧАС растворы галогенсодержащих кислот, полученные в результате растворения концентратов БМ, нагревают до кипения при температуре около 110 °С в течение 24 часов. В раствор добавляют ЗЧАС в стехиометрическом избытке по отношению к количеству, необходимому для осаждения Au-ЗЧАС, Pt-ЗЧАС, Rh-ЗЧАС и Fe (III)-ЗЧАС, и нагревают с обратным холодильником в течение дополнительных 24-72 часов при температуре примерно 110°С перед охлаждением. Au-ЗЧАС, Pt-ЗЧАС, Rh-ЗЧАС и Fe (III)-ЗЧАС осаждаются полностью, а Pb и Pd остаются в растворе, по-видимому, из-за того, что Pd и Pb с высшими степенями окисления при кипении разлагаются. Растворимые Pb, Pd и НМ легко отделяют от БМ-ЗЧАС.
Осадки Fe (III)-ЗЧАС могут быть отделены от целевого БМ-ЗЧАС. Fe (III)-ЗЧАС растворимы в органических растворителях, содержащих спирты, диметилформамид и др. и может быть отмыты от нерастворимых БМ-ЗЧАС. В сырье, содержащем золото, Au-ЗЧАС может осаждаться совместно с Fe (III)-ЗЧАС. Au-ЗЧАС обычно растворимы в тех же органических растворителях, что и Fe (III)-ЗЧАС, однако, золото может быть отделено от Fe методами, хорошо известными специалистам в этой области (например, с помощью щавелевой кислоты).
Тепловой режим и состав водных растворов галогенидов обеспечивают дополнительные механизмы для отделения БМ друг от друга. В одном из предпочтительных вариантов осуществления раствор 6Н HCl, содержащий Rh, Ru и другие БМ нагревали до температуры 110°С в течение 24 часов или более в качестве первого этапа этого способа. С другой стороны, раствор можно нагревать дольше при более низкой температуре или при более высокой температуре в автоклаве в течение более короткого периода времени. После первоначального нагрева и охлаждения, в раствор добавляют небольшой избыток ЗЧАС относительно количества, необходимого для осаждения комплексов Pt-ЗЧАС, Pd-ЗЧАС, Au-ЗЧАС, Ir-ЗЧАС и Fe (III)-ЗЧАС, порядка 2-3 моля ЗЧАС на один моль БМ. Окисление полученной суспензии хлором приводит осаждению в заметном количестве Pt-ЗЧАС, Pd-ЗЧАС, Au-ЗЧАС, Ir-ЗЧАС и Fe (III)-ЗЧАС, не затрагивая Rh, Ru или ВМ. Осадки отделяют от фильтрата, который содержит растворимые Rh, Ru и НМ.
Отделение Rh, Ru от НМ в растворе галогенида, таком как описан непосредственно выше, иллюстрирует другой вариант, в котором нагревание с ЗЧАС обеспечивает отделение двух БМ друг от друга и от НМ. Неокисленный раствор Ru, Rh, НМ нагревают с ЗЧАС при температуре около 110°С в течение 24-72 часов. Осаждение Rh-ЗЧАС после последующего охлаждения является более полным, чем в случае, когда ЗЧАС присутствует в концентрации, близкой к пределу насыщения, и перед нагреванием добавляют около 60 мл на литр 50% NaOH. Rh-ЗЧАС физически отделяют от раствора Ru и НМ. Раствор Ru и НМ предпочтительно окисляють с использованием Cl2. Ru окисляется и образует осадок Ru-ЗЧАС, который отделяют от раствора НМ.
Различия в растворимости БМ-ЗЧАС в различных растворителях зависят от состава растворителя, от элемента и степени окисления элемента (табл.1). Различия в растворимости могут быть использованы в полной мере при избирательном отделении БМ друг от друга, БМ от НМ или отмывке осадков от примесей. Например, Au-ЗЧАС, Fe (III)-ЗЧАС и Cu (II)-ЗЧАС растворимы в органических растворителях, содержащих метанол, этанол, диметилформамид и другие. Для отделения растворимых Au, Fe (III) и меди (II) от других комплексов БМ-ЗЧАС, остающихся нерастворимыми, используют органический растворитель.
Растворимость комплекса БМ-ЗЧАС в водных растворах галогенидов варьируется в зависимости от концентрации ЗЧАС, что можно использовать для отделения БМ друг от друга или от НМ. В одном из вариантов осуществления БМ-ЗЧАС, включая Rh-ЗЧАС, осаждаются после нагрева и охлаждения. После отделения осадков БМ-ЗЧАС осадки загрязнены остаточными растворами НМ. Остаточные растворы НМ отмывают от осадков о водным раствором галогенидов, содержащим до 30% (вес.) ЗЧАС. НМ остаются растворимыми и вымываются из осадков; тем не менее, высокая концентрация ЗЧАС препятствует растворению целевого комплекса БМ-ЗЧАС. В другом варианте осуществления в растворе присутствует Rh и загрязняет осадки БМ-ЗЧАС. Для отмывки Rh из осадков используют промывочный водный раствор галогенида с концентрацией 5-10% (вес.) ЗЧАС, содержащий количество ЗЧАС, недостаточное для осаждения Rh-ЗЧАС, но количество ЗЧАС, достаточное для предотвращения растворение менее растворимых комплексов БМ-ЗЧАС.
Хотя в предпочтительных способах обычно получают промежуточные продукты ЗЧАС высокого качества или чистоты, отраслевые стандарты требуют металлы исключительно высокой чистоты (99,95% или выше), которая может быть достигнута только дополнительной очисткой промежуточных комплексов БМ-ЗЧАС перед превращением их в конечную продукцию. Способы очистки осадков, таких как БМ-ЗЧАС, хорошо известны специалистам в данной области и включают растворение и фильтрацию, перекристаллизацию, растворение и переосаждение, растворение и окисление, растворение и осаждение из растворов, регулируемые путем добавления NaOH, а также других известных веществ. Некоторые конкретные способы очистки описаны в примерах ниже.
В зависимости от нужд, в промышленных приложениях может требоваться элементарный металл, растворы или соли. Комплексы БМ-ЗЧАС легко могут быть переработаны в соответствующие конечные продукты. Например, известными способами восстановления могут быть получены металлические губки высокой чистоты. Растворимые в водных растворах комплексы БМ-ЗЧАС могут быть переработаны в металлическую губку восстановителями, содержащими гидразин, боргидрид натрия, нитрит натрия, гидроксиламин и др. Кроме того, металлические губки могут быть восстановлены путем пиролиза из очищенных комплексов БМ-ЗЧАС.
Для других промышленных нужд более предпочтительны растворы БМ или соли БМ. Комплексы БМ-ЗЧАС легко можно перевести в растворы растворимых металлов или растворимые соли. Очищенные комплексы БМ-ЗЧАС превращают в нерастворимые гидроксиды с помощью гидроксида щелочного металла (например, NaOH). Осадок гидроксида БМ отделяют и промывают водой, чтобы удалить ЗЧАС и другие растворимые составляющие. Гидроксиды БМ высокой чистоты затем обрабатывают соответствующей кислотой, например, соляной для хлоридных солей, азотной кислотой для нитратных солей и т.д., что позволяет преобразовать гидроксиды в растворимые соли металлов. Такое преобразование является весьма выгодным процессом, так как многие, если не большинство, из этих БМ используется в виде растворимых солей в производстве катализаторов и т.п. Более того, превращениние металлов, таких как Ir и Ru в соли металлов гораздо предпочтительнее, поскольку Ir и Ru в металлическом виде чрезвычайно трудно растворить, и они используются, в основном, в виде растворимых солей.
Наконец, степень извлечения БМ имеет решающее значение для любой системы рафинирования. В предлагаемых способах, извлечение БМ полное или почти полное в аналитических пределах, после первого прохода процесса в сочетании с повторным циклом извлечения (доизвлечением). Первый проход и доизвлечение БМ в двух описанных ниже примерах (табл.2) показывают достаточно высокую степень извлечения.
Первый проход представляет процентное содержание каждого извлекаемого и рафинируемого металла, обеспечивающее хороший выход металла после исходного разделения и осаждения БМ-ЗЧАС. Доизвлечение представляет процентную долю каждого БМ, регенерируемого с промывными водами, растворами перекристаллизации и т.п. Эти объемы БМ возвращают путем дистилляции избыточного растворителя и регенерации сниженных объемов, содержащих H2O, HCl, ЗЧАС и БМ либо к исходному осадку БМ-ЗЧАС, либо в исходный раствор БМ, обеспечивая тем самым практически полное улавливание БМ. В среднем, около 95% от общего количества БМ улавливается и очищается на начальной стадии осаждения, для которой требуется 2-недельный период. Гораздо меньше регенерируемого компонента возвращается со следующей партией сырья и в итоге извлекается обычно за 4 недели. В случае с Pd, некоторое его количество остается в осадке свинца и возвращается к начальной стадии растворения БМ.
Ниже предпочтительные варианты будут описаны в примерах. Используя данные из таблицы 1, приведенной выше, а также примеры, приведенные ниже, специалист в данной области сможет адаптировать описанные технологические процедуры к сырьевым материалам, отличным от приведенных в примерах.
ПРИМЕР А.
Несколько образцов БМ по 200 грамм каждый, содержащих твердые НМ из двух партий, были переработаны, как схематично показано на рисунке 1. Типичные условия и результаты этих процессов были приведены в таблице 3.
На этапе I твердые вещества суспендировали примерно в 1 литре 6Н HCl при температуре 110°С с добавлением количества Cl2, достаточного для растворения БМ. После охлаждения ненужные твердые компоненты и PbCl2 отделяли фильтрованием. Отфильтрованный раствор нагревали с обратным холодильником при температуре около 110°С в течение 24 часов, полученный раствор показан в таблице 3 как этап I. Далее добавляли 300 граммов ЗЧАС или тетраметиламмония хлорида, по выбору, и раствор нагревали с обратным холодилником при температуре около 110°С в течение дополнительных 24 часов. Дефлегмированны и раствор охлаждали до комнатной температуры в течение 24 часов или более, в результате чего раствор превратился в пульпу. Если избыток ЗЧАС осаждается вместе с БМ-ЗЧАС, это не мешает последующей переработке. Пульпу отфильтровали, с получением твердого вещества, состоящего из объединенных осадков Pt-ЗЧАС, Au-ЗЧАС, Fe (III)-ЗЧАС и БМ-ЗЧАС и фильтрата, содержащего Pd, Pb и НМ. Осадки направляли на этап II переработки, а фильтрат направляли на этап IV переработки.
На этапе II объединенные осадки, состоящие из Pt-ЗЧАС, Au-ЗЧАС, Fe(III)-34AC и Rh-ЗЧАС отмывали на фильтровальной воронке примерно 1 литром спирта (метанола) для растворения и вымывания Au, Fe, Cu и ЗЧАС. Конечный промывной раствор не имел видимой окраски. Промывной раствор содержал менее 1 ppm Pt и Rh и несколько ppm Pd. Au извлекали из спирта хорошо известными специалистам в данной области способами (например, путем барботирования SO2) и выделением элементарного золота из раствора. Извлечение Au было полным в аналитических пределах, а чистота составляла 99,9%.
На этапе II нерастворимые в спирте осадки Pt-ЗЧАС и Rh-ЗЧАС сушили при температуре 110°С для выпаривания остатков спирта. Сухой осадок растворяли при перемешивании в 100 мл 6Н HCl для того для растворения Rh-ЗЧАС. Через раствор пропускали Cl2 в течение 75 минут до полного осаждения Pt-ЗЧАС и других микроэлементов. Пульпу разделяли фильтрацией с получением Pt-ЗЧАС, и фильтрат, содержащий Rh, отправляли на этап III для извлечения Rh. Осадок Pt-ЗЧАС очищали путем растворения в количестве (около 750 мл) кипящей H2O или 6Н HCl, достаточном для растворения Pt-ЗЧАС. Раствор фильтровали в горячем состоянии с удалением нерастворимого осадка, содержащего в основном загрязняющие вещества. Очищенный, фильтрованный раствор Pt охлаждали и оставляли на ночь или дольше для перекристаллизации. Очищенный комплекс Pt-ЗЧАС отделяли путем фильтрации. Объемы фильтрата, содержащего остаточное количество растворимой Pt, а также загрязняющих веществ, уменьшали примерно до 25% от первоначального объема, охлаждали и фильтровали с отделением Pt-ЗЧАС высокой чистоты от растворимых примесей. Очищенный Pt-ЗЧАС, полученный при начальном осаждении и уменьшении объемов, восстанавливали способами, хорошо известными специалистам в данной области (например, пиролизом при температуре около 600°С). Степень извлечения Pt составила около 95% с чистотой 99,9%. Неизвлеченную часть Pt перерабатывали со следующей партией перекристаллизации Pt-ЗЧАС или направляли на начальное осаждение БМ-ЗЧАС для конечного извлечения.
Rh извлекали из высококонцентрированного раствора этапа III (табл.3), который дополнительно содержал растворенные ЗЧАС. На литр раствора добавляли примерно 60 мл 50% NaOH и затем при температуре окружающей среды количество ЗЧАС (около 20%, по массе), достаточное для насыщения раствора. Раствор нагревали до температуры 110°С в течение 24 часов или более. Rh-ЗЧАС оставляли для осаждения обычно примерно на 24 часа, до установления постоянной концентрации Rh в растворе. Осадок Rh-ЗЧАС и фильтрат разделяли. Rh-ЗЧАС очищали путем растворения в минимальном количестве кипящей воды (около 20% по массе) и отделения нерастворимых загрязняющих веществ от раствора Rh. Раствор очищенного Rh содержал следовые количества растворимых Ag, Pt и других примесей. рН раствора доводили до рН8 с использованием NaOH для эффективного осаждения Pb(ОН)3 в течение примерно 24 часов. РА(ОН)3 отделяли от раствора и промывали достаточным количеством водного щелочного раствора или спиртом для удаления растворимых примесей. Очищенный Rh(ОН)3 растворяли в минимальном количестве HCl и затем восстанавливали до металла способами, хорошо известными специалистам в данной области (например, гидразин). Общий выход составил около 95% с конечной чистотой 99,9%. Неизвлеченный Rh возвращали в следующую партию.
Палладий извлекали на этапе IV, который начали с получения раствора Pd, Pb и НМ на I этапе (табл.3). Через раствор пропускали Cl2 в течение примерно 1 часа для совместного осаждения достаточного количества нерастворимых окисленных Pd-ЗЧАС и Pb-ЗЧАС. Смесь осадков отделяли от растворимых НМ путем фильтрации. Способы разделения Pd и Pb хорошо известны специалистам в данной области, но для удобства смесь осадков Pd-ЗЧАС и Pb-ЗЧАС растворяли в 5%-водном растворе аммиака. Палладий образует растворимые аммониевые комплексы, в то время как свинец образует нерастворимые соединения, которые легко отделяются. Растворимые комплексы Pd-аммиак осаждали хорошо известным способом добавления HCl для формирования осадка дихлородиаммина палладия, который отделяли от аммиачного раствора. Промытые водой соли Pd обычно были достаточно чистыми для продолжения процесса, хотя более предпочтительны второе растворение в водном аммиачном растворе и кристаллизация дихлородиамина палладия. Восстановление дихлородиаммина палладия до металлического палладия хорошо известно специалистам в этой области (например, пиролиз). Общее извлечение палладия составило 95% с чистотой 99,98%. Оставшаяся в растворе часть палладия извлекали (например, с помощью боргидрида натрия) и возвращали в исходный раствор БМ.
Пример В
Раствор соляной кислоты с высокой концентрацией элементов БМ и НМ перерабатывали для извлечения и рафинирования БМ, как схематически показано на рисунке 2. Этот материал отличается от примера А прежде всего присутствием Ru и Ir.
На I этапе отделяли родий, рутений и неблагородные металлы от других БМ. Семьдесят граммов раствора нагревали при температуре около 110°С в течение 36 часов, а затем охлаждали до комнатной температуры. 12 граммов ЗЧАС (тетраметиламмоний хлорид) растворяли в растворе. Через раствор пропускали Cl2 в течение около 70 минут. Комплексы Au-ЗЧАС, Pt-ЗЧАС, Pd-ЗЧАС, Ir-ЗЧАС и Fe (III)-ЗЧАС осаждались, в то время как Rh, Ru и НМ оставались растворенными. Осадок отделяли от фильтрата. Фильтрат с Rh, Ru и НМ направляли на этапы II и III для последовательного извлечения Ru и Rh. Осадки направляли на этапы IV и V для извлечения других БМ.
Фильтрат этапа I с Rh, Ru и НМ брабатывали на этапе II, что обеспечивало отделение двух БМ друг от друга и от НМ. 40 граммов ЗЧАС (тетраметиламмоний хлорид) растворяли в фильтрате. Раствор нагревали в течение 24 часов при температуре около 110°С и затем охлаждали до комнатной температуры в течение 24 и более часов. Комплексы Ru-ЗЧАС и Rh-ЗЧАС осаждали из раствора и отделяли от фильтрата, содержащего растворимые НМ. Смесь осадков Rh-ЗЧАС и Ru-ЗЧАС сушили, а затем промывали спиртом (метанол) для удаления растворимого Fe(III)-34AC, а также остаточных растворимых НМ. Затем смесь осадков растворяли в количестве 6Н HCl, достаточном для растворения Rh-ЗЧАС, растворимость которого обычно около 15% по весу. Через раствор барботировали Cl2 в течение 40 минут для обеспечения полного окисления Ru и осаждения Ru-ЗЧАС. Ru-ЗЧАС отделяли от фильтрата, содержащего растворимый Rh. Фильтрат, содержащий растворимый Rh, направляли на этап III для извлечения Rh. Твердые комплексы Ru-ЗЧАС, оставшиеся после удаления Rh-ЗЧАС, имели чистоту более 99%, а общий выход составил 97%.
Rh извлекали на этапе III. Этот процесс не имеет существенных отличий от этапа III из примера А. Извлеченный Rh имел чистоту 99,9%, а выход продукта составил 98%.
Смесь осадков Au-ЗЧАС, Pt-ЗЧАС, Pd-ЗЧАС, Ir-ЗЧАС и Fe(III)-34AC с этапа I перерабатывали на IV этапе для отделения растворимых Au-ЗЧАС и Fe (III)-ЗЧАС от нерастворимых Pt-ЗЧАС, Pd-ЗЧАС и Ir-ЗЧАС. Совместный осадок всех пяти элементов сушили, а затем смешивали с 150 мл спирта (метанол). Растворимые Au и Fe отделяли от нерастворимых Pt-ЗЧАС, Pd-ЗЧАС и Ir-ЗЧАС. Наиболее эффективно Au извлекали из фильтрата барботимрования S02 и отделения частиц золота. Выход золота составил 96% с чистотой 99,9%.
Смесь нерастворимых в спирте осадков Pt-ЗЧАС, Pd-ЗЧАС и Ir-ЗЧАС перерабатывали на этапе IV для извлечения Pd и отделения Pd от Pt и Ir. Смесь осадков добавляли к 100 мл 6Н HCl с 15% (вес.) ЗЧАС (тетраметиламмоний хлорид) и кипятили при температуре около 110°С в течение 24 часов. Кипячение суспензии привело к растворению Pd. Растворение комплексов Pt-ЗЧАС и Ir-ЗЧАС подавлялось присутствием ЗЧАС. Фильтрат Pd отделяли от Pt- и Ir-ЗЧАС. Фильтрат Pd сдержал следовые количества Pt и Ir и его подвергали дальнейшей очистке. рН фильтрата Pd доводили до 8 с помощью 50% NaOH для осаждения Pd(OH)2. Pd(OH)2 промывали водой для удаления следового количества растворимых солей Pt и Ir. Затем очищенный Pd(OH)2 восстанавливали до металлического состояния способами, хорошо известными специалистам в данной области (например, растворение в HCl и восстановление гидразином). Выход палладия составил 98% при чистоте 99,9%.
На V этапе извлечения Pt и Ir смесь осадков Pt-ЗЧАС и Ir-ЗЧАС суспендировали в 50 мл водного раствора 20% (вес.) ЗЧАС. NaNO2 в количестве 2,5 г растворяли в полученном растворе и оставляли реагировать в течение менее 1 часа. Иридий растворялся, в то время как Pt-ЗЧАС оставался в твердой фазе. Затем фильтрат Ir и Pt-ЗЧАС разделяли. Фильтрат Ir очищали путем подкисления HCl для повторного осаждения Ir-ЗЧАС, выделенного из фильтрата, содержащего Pt. Процессы осаждения Ir-ЗЧАС, растворение NaNO2 и повторное осаждение повторяли для удаления примесей, в результате чего была достигнута высокая степень очистки Ir-ЗЧАС. Для удобства комплекс Ir-ЗЧАС подвергали пиролизу при температуре 600 °С. Общий выход составил 97% при чистоте 99,9%.
Pt-ЗЧАС, оставшееся после извлечения Ir на этапе V очищали путем растворения в 15 мл 6Н HCl при температуре примерно 110°, объем снижали до 5 мл и охлаждали до температуры окружающей среды. Смесь Pt-ЗЧАС отделяли от фильтрата, и для удобства восстанавливали пиролизом при температуре 600 °С. Общий выход Pt составил 95% при чистоте 99,9%.
Таким образом, разработан гидрометаллургический способ извлечения, разделения и очистки металлов, выделенных из группы, состоящей из платины [Pt], палладия [Pd], родия [Rh], рутения [Ru], иридия [Ir] и золота [Au]. Хотя были показаны и описаны варианты осуществления применения этого изобретения, для специалиста в данной области очевидно, что возможны различные модификации, не выходящие за рамки объема изобретательского замысла. Изобретение, следовательно, не ограничено ничем, кроме формулой изобретения.
Реферат
Способ извлечения металлов (далее БМ) из твердого сырья включает растворение БМ и основных металлов в кислоте. БМ осаждают с использованием замещенных четвертичных аммониевых солей (ЗЧАС). БМ могут быть окислены и восстановлены. Замещенные четвертичные аммониевые соли представлены в форме HRNX, где Н=водород, R=органическая группа, N=азот и Х=галоген. В способе используют, например, тетраметиламмоний хлорид. Au-ЗЧАС отделяют путем промывки растворителем. Rh-ЗЧАС растворяют в кислоте, окисляют, что обеспечивает осаждение солей, и отделяют ЗЧАС добавляют к фильтрату, нагревают и охлаждают с осаждением Rh-ЗЧАС, который затем отделяют. Rh-ЗЧАС очищают перед образованием конечного продукта. Другие металлы отделяют путем кипячения исходного кислого раствора металлов с осаждением солей металлов, охлаждения и отделения. Пульпу разделяют путем растворения и разделения. Техническим результатом является упрощение технологии извлечения благородных металлов из химически различающихся видов первичного и вторичного сырья. 3 н. и 17 з.п. ф-лы, 4 ил., 4 табл., 2 пр.

Комментарии