Новый экстрагент, используемый для экстракции редкоземельных металлов из водного раствора фосфорной кислоты, и его применение - RU2762074C2
Код документа: RU2762074C2
Чертежи
Описание
Область техники, к которой относится изобретение
Настоящее изобретение относится к области экстракции и выделения редкоземельных металлов, содержащихся в природных рудах или твердых бытовых отходах.
Более конкретно, настоящее изобретение касается нового экстрагента, позволяющего экстрагировать из водного раствора фосфорной кислоты как легкие редкоземельные металлы, так и тяжелые редкоземельные металлы, которые могут содержаться в этом водном растворе, с высоким выходом экстракта и высокой селективностью относительно металлических примесей, которые также могут содержаться в указанном растворе, в особенности относительно железа, вне зависимости от концентрации фосфорной кислоты в указанном водном растворе.
Настоящее изобретение касается также применения указанного нового экстрагента для экстракции по меньшей мере одного редкоземельного металла из водного раствора фосфорной кислоты.
Настоящее изобретение касается также способов экстракции и выделения по меньшей мере одного редкоземельного металла, содержащегося в водном растворе фосфорной кислоты, с применением указанного нового экстрагента.
Настоящее изобретение может также применяться в обработке водных растворов, полученных при выщелачивании природных фосфатов серной кислотой, и водных растворов, полученных при выщелачивании твердых бытовых отходов фосфорной кислотой, с целью выделения редкоземельных металлов, содержащихся в таких водных растворах.
Предшествующий уровень техники
Группа редкоземельных металлов объединяет металлы, имеющие близкие свойства, а именно скандий (Sc), иттрий (Y) и все лантаноиды, соответствующие пятнадцати химическим элементам в периодической таблице Менделеева, имеющим атомные номера от 57 для лантана (La) до 71 для лютеция (Lu).
Близкие свойства редкоземельных металлов являются следствием специфической электронной конфигурации, и в частности их ненасыщенного 4f электронного подуровня, придающего им уникальные химические, структурные и физические свойства. Эти свойства с выгодой используются в промышленности, а именно в широком спектре сложных областей, таких как металлургия, катализ, производство стекла и оптики, керамика, люминисцентные материалы, магниты, электроника и т.д.
Редкоземельные металлы, таким образом, относятся к так называемым «технологическим» металлам, производство которых стратегически важно и находится под прессингом из-за увеличивающейся мировой потребности в этих металлах.
Противореча своему названию, редкоземельные металлы широко распространены в природе. Например, они содержатся во многих природных минералах, в частности в природных фосфатах (или фосфатных рудах), которые добываются для производства фосфорной кислоты и фосфорных удобрений.
Поскольку редкоземельные металлы используются в производстве многих компонентов технологичного оборудования, промышленные и бытовые отходы от такого оборудования, и в частности отходы электрического и электронного оборудования, известные под аббревиатурой WEEE или W3E, являются еще одним источником для добычи редкоземельных металлов. Переработка таких отходов с целью выделения содержащихся в них редкоземельных металлов является предметом пристального внимания.
Переработка природных фосфатов для производства фосфорной кислоты и фосфатных удобрений начинается с обработки или выщелачивания фосфатов, предварительно раздробленных и измельченных, кислотой, которая чаще всего представляет собой серную кислоту и превращает фосфат кальция в фосфорную кислоту, содержащую 30% фосфорного ангидрида P2O5, и в нерастворимый сульфат кальция (гипс).
Такая обработка кислотой частично или полностью солюбилизирует металлы, содержащиеся в природных фосфатах, включая редкоземельные металлы, которые вследствие этого переходят в водный раствор фосфорной кислоты.
Одним способом выделения редкоземельных металлов из водного раствора фосфорной кислоты является гидрометаллургическая обработка, после фильтрования и концентрирования, этого раствора по методике жидкость-жидкостной экстракции, технологически состоящая из введения указанного водного раствора в контакт с органическим раствором, содержащим одно или больше экстрагентов в разбавителе, результатом чего является экстрагирование редкоземельных металлов, которое предпочтительно является одновременно селективным и высокоэффективным.
Для выделения редкоземельных металлов из водного раствора фосфорной кислоты было предложено применение ряда экстрагентов, включая н-октилпирофосфорную кислоту или OPPA, ди-2-этилгексилфосфорную кислоту или DEHPA, и смесь моно(н-октил-фенил)фосфорной кислоты или MOPPA и ди(н-октофенил)фосфорной кислоты или DOPPA, в отдельности или в смеси с три-н-октилфосфиноксидом или TOPO, в растворе керосина.
Тем не менее, указанные экстрагенты не полностью удовлетворяют все потребности.
Например, вдобавок к тому факту, что DEHPA приводит к селективной экстракции тяжелых редкоземельных металлов, т.е. имеющих атомный номер по меньшей мере 62 (самарий, европий, гадолиний, тербий, диспрозий, гольмий, эрбий, тулий, иттербий и лютеций), этот реагент позволяет экстрагировать эти тяжелые редкоземельные металлы только из очень кислых растворов (pH < 1).
Кроме того, в то время как в работе M. Krea and H. Khalaf (Hydrometallurgy 2000, 58(3), 215-225), ниже указана как источник [1]) было показано, что лантан, европий и иттрий можно экстрагировать с высоким выходом (65%, 70% и 83%, соответственно) из водного раствора фосфорной кислоты, содержащего 30% P2O5 (т.е. 5.5M концентрация) и не содержащего железа, смесью DOPPA и TOPO в керосине, эти же авторы показали, что указанные выходы экстракции резко падают в присутствии железа вследствие того, что DOPPA представляет собой сильный экстрагент для этого металла.
Поскольку железо является главным примесным металлом в водных растворах фосфорной кислоты, получаемых при выщелачивании природных фосфатов серной кислотой, невозможно промышленное применение смеси экстрагентов, имеющих высокое сродство к железу, таких как описанные в источнике [1], для экстракции редкоземельных металлов из таких растворов.
Поэтому авторы настоящего изобретения поставили перед собой задачу разработать новый экстрагент, который не имеет различных недостатков, присущих экстрагентам, ранее предложенным для экстракции редкоземельных металлов из водного раствора фосфорной кислоты.
В частности, задача заключается в разработке экстрагента, позволяющего проводить высокоэффективную экстракцию как легких редкоземельных металлов, так и тяжелых редкоземельных металлов из водного раствора фосфорной кислоты, содержащего такие редкоземельные металлы, с высокой селективностью относительно металлических примесей, которые могут также содержаться в водном растворе, в особенности относительно железа, и в максимально широком диапазоне концентраций фосфорной кислоты.
В ходе работы авторы настоящего изобретения неожиданно установили, что применение некоторых бифункциональных соединений, содержащих амидную функциональную группу и фосфоновую или фосфонатную функциональную группу, в смеси с анионогенным или неионогенным поверхностно-активным веществом, позволяет экстрагировать легкие и тяжелые редкоземельные металлы из водного раствора фосфорной кислоты с высокой эффективностью – благодаря синергетическому эффекту между указанными соединениями и поверхностно-активным веществом – и с особенной селективностью относительно металлических примесей, вне зависимости от концентрации фосфорной кислоты в водном растворе.
На этом открытии основано настоящее изобретение.
Краткое описание изобретения
Предметом настоящего изобретения является, во-первых, экстрагент или экстрагирующий агент, отличающийся тем, что он содержит:
- соединение, имеющее изображенную ниже формулу (I):
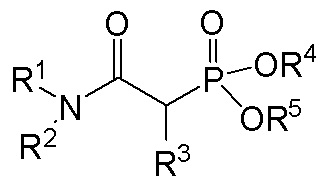
где:
R1 и R², одинаковые или разные, представляют собой насыщенную или ненасыщенную, линейную или разветвленную углеводородную группу, содержащую 6 - 12 атомов углерода;
R3представляет собой:
- насыщенную или ненасыщенную, линейную или разветвленную углеводородную группу, содержащую 1 - 12 атомов углерода и необязательно один или больше гетероатомов; или
- насыщенную или ненасыщенную, моноциклическую углеводородную группу, содержащую 3 - 8 атомов углерода и необязательно один или больше гетероатомов; в то время как
R4 и R5, одинаковые или разные, представляют собой атом водорода или насыщенную или ненасыщенную линейную или разветвленную углеводородную группу, содержащую 2 - 8 атомов углерода; и
- поверхностно-активное вещество.
Выше и ниже в настоящем тексте, “насыщенная или ненасыщенная, линейная или разветвленная углеводородная группа, содержащая 6 - 12 атомов углерода” означает любую линейную или разветвленную алкильную, алкенильную или алкинильную группу, содержащую 6, 7, 8, 9, 10, 11 или 12 атомов углерода.
Аналогично, “насыщенная или ненасыщенная, линейная или разветвленная углеводородная группа, содержащая 2 - 8 атомов углерода” означает любую линейную или разветвленную алкильную, алкенильную или алкинильную группу, содержащую 2, 3, 4, 5, 6, 7 или 8 атомов углерода.
Также, “насыщенная или ненасыщенная, линейная или разветвленная углеводородная группа, содержащая 1 - 12 атомов углерода и необязательно один или больше гетероатомов” означает любую группу, полученную из линейной или разветвленной углеводородной цепочки, содержащей 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 атомов углерода, где указанная цепочка может быть насыщенной или, наоборот, может содержать одну или больше двойных или тройных связей, и указанная цепочка может содержать один или больше гетероатомов, или быть замещена одним или больше гетероатомами или одним или больше заместителями, содержащими гетероатом.
В этой связи, необходимо указать, что “гетероатом” означает любой атом, отличный от углерода и водорода, обычно это атом азота, кислорода или серы.
Также, “насыщенная или ненасыщенная моноциклическая углеводородная группа, содержащая 3 - 8 атомов углерода и необязательно один или больше гетероатомов” означает любую циклическую углеводородную группу, содержащую только одно кольцо, которое содержит 3, 4, 5, 6, 7 или 8 атомов углерода. Это кольцо может быть насыщенным или, напротив, оно может содержать одну или больше двойных или тройных связей, и может содержать один или больше гетероатомов, или может быть замещено одним или больше гетероатомами или одним или больше заместителями, содержащими гетероатом, где указанный(-ые) гетероатом(ы) обычно представляют собой N, O или S. Такая группа может представлять собой циклоалкильную, циклоалкенильную или циклоалкинильную группу (например, циклопропановую, циклопентановую, циклогексановую, циклопропенильную, циклопентенильную или циклогексенильную группу), насыщенную гетероциклическую группу (например, тетрагидрофурильную, тетрагидротиофенильную, пирролидинильную или пиперидинильную группу), ненасыщенную, но неароматическую гетероциклическую группу (например, пирролинил или пиридинил), ароматическую группу или гетероароматическую группу.
В этой связи необходимо указать, что “ароматическая группа” означает любую группу, чье кольцо соответствует правилу ароматичности Хюккеля и имеет число делокализованных электронов π равное 4n + 2 (например, фенильную или бензильную группу), в то время как “гетероароматическая группа” означает любую ароматическую группу, такую как определено выше, но имеющую кольцо, содержащее один или больше гетероатомов, где указанный(-ые) гетероатом(ы) обычно выбран(ы) из атомов азота, кислорода и серы (например, фурильная, тиофенильная или пирролильная группа).
Согласно настоящему изобретению, в приведенной выше формуле (I), R1 и R2, одинаковые или разные, предпочтительно представляют собой линейную или разветвленную алкильную группу, содержащую 6 - 12 атомов углерода.
Кроме того, предпочтительно R1 и R2 одинаковые и представляют собой разветвленную алкильную группу, содержащую 8 - 10 атомов углерода, особенно предпочтительной является 2-этилгексильная группа.
Также, в приведенной выше формуле (I), R3предпочтительно представляет собой линейную или разветвленную алкильную группу, содержащую 1 - 12 атомов углерода, или моноциклическую 6-членную ароматическую группу, предпочтительно фенил или орто-, мета- или пара-толил.
Кроме того, предпочтительно R3 представляет собой метильную, н-октильную или фенильную группу.
Наконец, в приведенной выше формуле (I), R4 предпочтительно представляет собой линейную или разветвленную алкильную группу, содержащую 2 - 8 атомов углерода, и, более предпочтительно, 2 - 4 атома углерода, такую как этильная, н-пропильная, изопропильная, н-бутильная, втор-бутильная, изобутильная или трет-бутильная группа, особенно предпочтительны этильная и н-бутильная группы, в то время как R5 предпочтительно представляет собой атом водорода.
Соединения, имеющие приведенную выше формулу (I), имеющие указанные характеристики, в частности представляют собой:
- этил 1-(N,N-диэтилгексилкарбамоил)этилфосфонат, обозначаемый DEHCEPE, имеющий приведенную выше формулу (I), где R1 и R2представляют собой 2-этилгексильную группу, R3 представляет собой метильную группу, R4 представляет собой этильную группу, и R5 представляет собой атом водорода;
- этил 1-(N,N-диэтилгексилкарбамоил)нонилфосфонат, обозначаемый DEHCNPE, имеющий приведенную выше формулу (I), где R1 и R2представляют собой 2-этилгексильную группу, R3 представляет собой н-октильную группу, R4 представляет собой этильную группу, и R5 представляет собой атом водорода;
- бутил 1-(N,N-диэтилгексилкарбамоил)нонилфосфонат, обозначаемый DEHCNPB, имеющий приведенную выше формулу (I), где R1 и R2представляют собой 2-этилгексильную группу, R3 представляет собой н-октильную группу, R4 представляет собой н-бутильную группу, и R5 представляет собой атом водорода;
- бутил 1-(N,N-диоктилкарбамоил)нонилфосфонат, обозначаемый DOCNPB, имеющий приведенную выше формулу (I), где R1, R2 и R3 представляют собой н-октильную группу, R4 представляет собой n-бутильную группу, и R5 представляет собой атом водорода; и
- бутил 1-(N,N-диэтилгексилкарбамоил)бензилфосфонат, обозначаемый DEHCPBE, имеющий приведенную выше формулу (I), где R1 и R2представляют собой 2-этилгексильную группу, R3 представляет собой фенильную группу, R4 представляет собой этильную группу, и R5 представляет собой атом водорода.
Из числа указанных соединений, особенно предпочтительно DEHCNPB.
Следует отметить, что все соединения, имеющие приведенную выше формулу (I), можно получить способами синтеза, описанными в международной заявке на патент PCT, опубликованной под номером WO 2013/059352, источник [2] ниже в списке литературы.
Согласно настоящему изобретению, поверхностно-активное вещество может быть выбрано из ионогенных поверхностно-активных веществ, т.е. анионных, катионных и цвиттерионных (или амфотерных), и неионогенных поверхностно-активных веществ, при условии, что оно позволяет сформировать микроэмульсию в органической несмешивающейся с водой фазе, т.е. дисперсию типа вода-в-масле, которая является изотропной и термодинамически устойчивой.
По вопросам выбора указанного поверхностно-активного вещества, читателю предлагается обращаться к работам “Chemistry and Technology of Surfactants” (Richard J. Farn, 2006 Blackwell Publishing Ltd, ISBN-13: 978-14051-2696-0) и “Self-Organized Surfactant Structures” (Tharwat F Tadros, 2011, John Wiley & Sons, ISBN: 978-3-527-63265-7), источники [3] и [4] в приведенном ниже списке литературы.
Предпочтительно, поверхностно-активное вещество представляет собой ионогенное поверхностно-активное вещество, и более конкретно – анионогенное поверхностно-активное вещество, т.е. поверхностно-активное вещество, которое разделяется в водном растворе на амфифильный катион и анион, и в этом случае оно в частности может быть выбрано из алкилсульфатных, алкиларилэфирсульфатных, алкилэфирсульфатных, алкиларилэфирсульфатных, алкилэфиркарбоксилатных, алкиларилэфиркарбоксилатных, алкилсульфосукцинатных, алкиларилсульфосукцинатных, парафин-сульфонатных, алкилизотионатных, алкилсаркозинатных солей натрия, калия, магния, кальция, аммония и т.д., где алкильная группа(ы) в указанных соединениях предпочтительно содержат 6 - 24 атомов углерода и, более предпочтительно, 6 - 12 атомов углерода, где арильная группа(ы) в указанных соединениях предпочтительно представляет(-ют) собой фенильную группу(ы).
Согласно настоящему изобретению, поверхностно-активное вещество предпочтительно представляет собой соль диалкил(C6-C12)сульфосукцината, такую как соль с щелочным металлом (например, Na, K, ...) ди(н-гексил)сульфосукцината, ди(2-этилгексил)сульфосукцината, ди(н-октил)сульфосукцината (называемого также докузат), ди(изо-октил)сульфосукцината или ди(н-децил)сульфосукцината, соли ди(2-этилгексил)сульфосукцината и, в частности, особенно предпочтительна натриевая соль ди(2-этилгексил)сульфосукцината, называемая также AOT, формула которой приведена ниже.
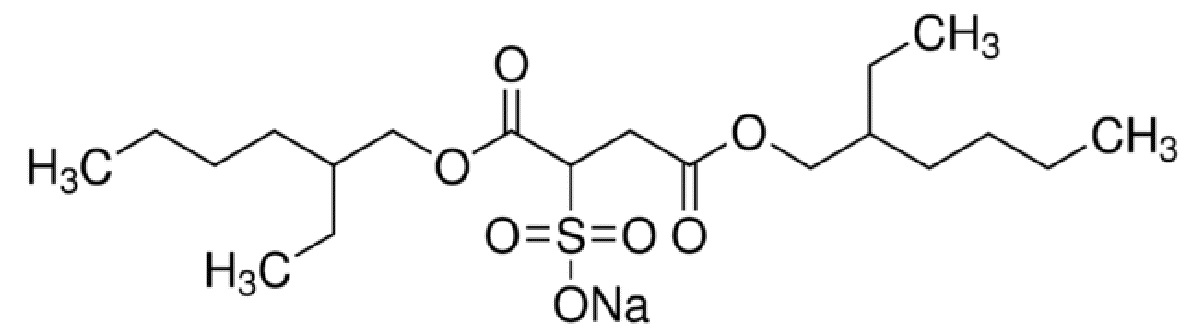
Кроме того, экстрагент предпочтительно имеет мольное соотношение указанного соединения к поверхностно-активному веществу от 20:80 до 80:20 и, более предпочтительно, от 40:60 до 60:40, при этом наиболее предпочтительно в экстрагенте мольное соотношение 60:40 DEHCNPB в качестве соединения и AOT в качестве поверхностно-активного вещества, поскольку это обеспечивает максимальный синергетический эффект при экстракции редкоземельных металлов из водного раствора фосфорной кислоты.
Другим предметом настоящего изобретения является применение экстрагента, такого как описанное выше, для экстракции по меньшей мере одного редкоземельного металла из водного раствора фосфорной кислоты.
Согласно настоящему изобретению, указанный по меньшей мере один редкоземельный металл предпочтительно экстрагируют из водного раствора фосфорной кислоты посредством жидкость-жидкостной экстракции, и в этом случае водный раствор вводят в контакт с органическим раствором, содержащим экстрагент в органическом разбавителе типа линейного или разветвленного додекана, такого как н-додекан или гидрированный тетрапропилен, или типа керосина, такого как доступный на рынке под торговым названием IP-185, и затем отделяют от органического раствора.
Органический раствор предпочтительно содержит от 0.005 моль/л до 1 моль/л, и более предпочтительно от 0.1 моль/л до 0.5 моль/л экстрагента.
Другим предметом настоящего изобретения является способ экстракции по меньшей мере одного редкоземельного металла из водного раствора фосфорной кислоты, который включает контакт водного раствора с несмешивающимся с водой органическим раствором, содержащим экстрагент в органическом разбавителе, затем разделение водного и органического растворов, отличающийся тем, что экстрагент такой, как описано выше.
Другим предметом настоящего изобретения является способ выделения по меньшей мере одного редкоземельного металла из водного раствора фосфорной кислоты, отличающийся тем, что он включает:
- экстракцию указанного по меньшей мере одного редкоземельного металла из водного раствора путем контакта водного раствора с несмешивающимся с водой органическим раствором, содержащим описанный выше экстрагент в органическом разбавителе, затем разделение водного и органического растворов; и
- извлечение указанного по меньшей мере одного редкоземельного металла из органического раствора путем контакта органического раствора с водным раствором щавелевой кислоты или ее соли, например, оксалата аммония, натрия или калия, с последующим разделением водного и органического растворов.
В этих способах экстракции и выделения, органический раствор также предпочтительно содержит от 0.005 моль/л до 1 моль/л, и более предпочтительно – от 0.1 моль/л до 0.5 моль/л экстрагента.
Водный раствор фосфорной кислоты, из которого экстрагируют указанный по меньшей мере один редкоземельный металл или из которого выделяют указанный по меньшей мере один редкоземельный металл, может в частности представлять собой раствор, полученный при выщелачивании природного фосфата серной кислотой, или раствор, полученный выщелачиванием фосфорной кислотой бытовых отходов, т.е. материалов, сформированных из промышленных и бытовых отходов оборудования, содержащего редкоземельные металлы, и в частности WEEE или W3E оборудования.
Как указано ранее и как показано ниже, концентрация фосфорной кислоты в данном водном растворе может варьироваться в широком диапазоне, и в частности может находиться в диапазоне от 1 моль/л до 8 моль/л фосфорной кислоты.
Другие характеристики и преимущества настоящего изобретения будут понятны из последующего дополнительного описания, которое ссылается на прилагаемые Фигуры и касается примеров, демонстрирующих эффективность экстрагента по настоящему изобретению в экстракции редкоземельных металлов из водного раствора фосфорной кислоты.
Это дополнительное описание приведено исключительно для иллюстрации предмета настоящего изобретения и никоим образом не должно пониматься как ограничивающее объем настоящего изобретения.
В контексте настоящего изобретения термины “раствор” и “фаза” являются эквивалентными и полностью взаимозаменяемыми.
Краткое описание чертежей
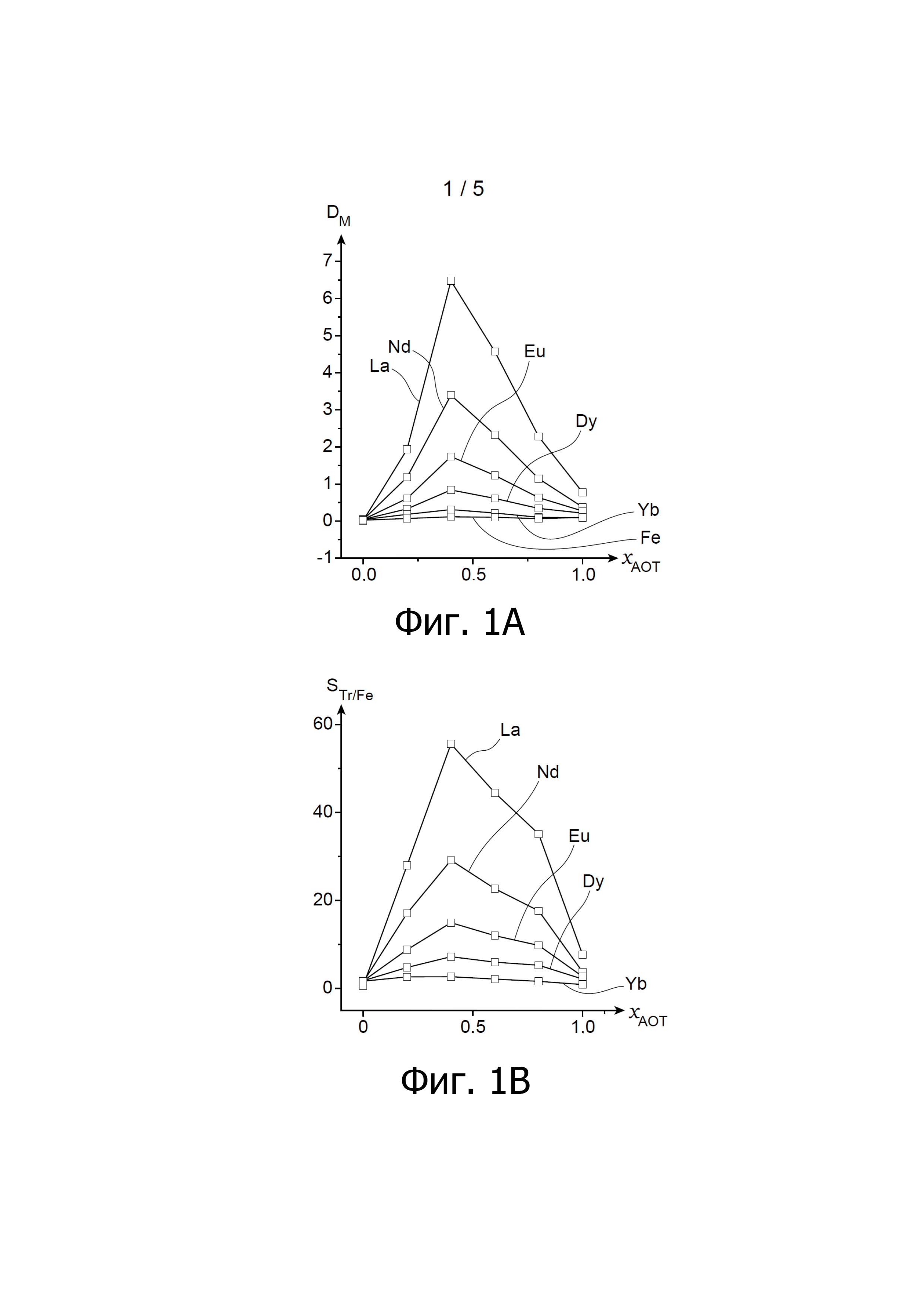
На Фиг. 1A и 1B показаны результаты тестов экстракции, проведенных с водными фосфорнокислыми фазами, содержащими пять редкоземельных металлов и железо, с применением органических фаз, содержащих в качестве экстрагента DEHCNPB или AOT, или смесь DEHCNPB и AOT с различными мольными соотношениями DEHCNPB/AOT; на Фиг 1A показана диаграмма зависимости коэффициентов распределения редкоземельных металлов и железа, обозначаемых DM, от мольной доли AOT, обозначаемой хАОТ, в экстрагенте, в то время как на Фиг 1B показана диаграмма зависимости коэффициентов селективности к редкоземельным металлам по сравнению с железом, обозначаемых STr/Fe, от хАОТ.
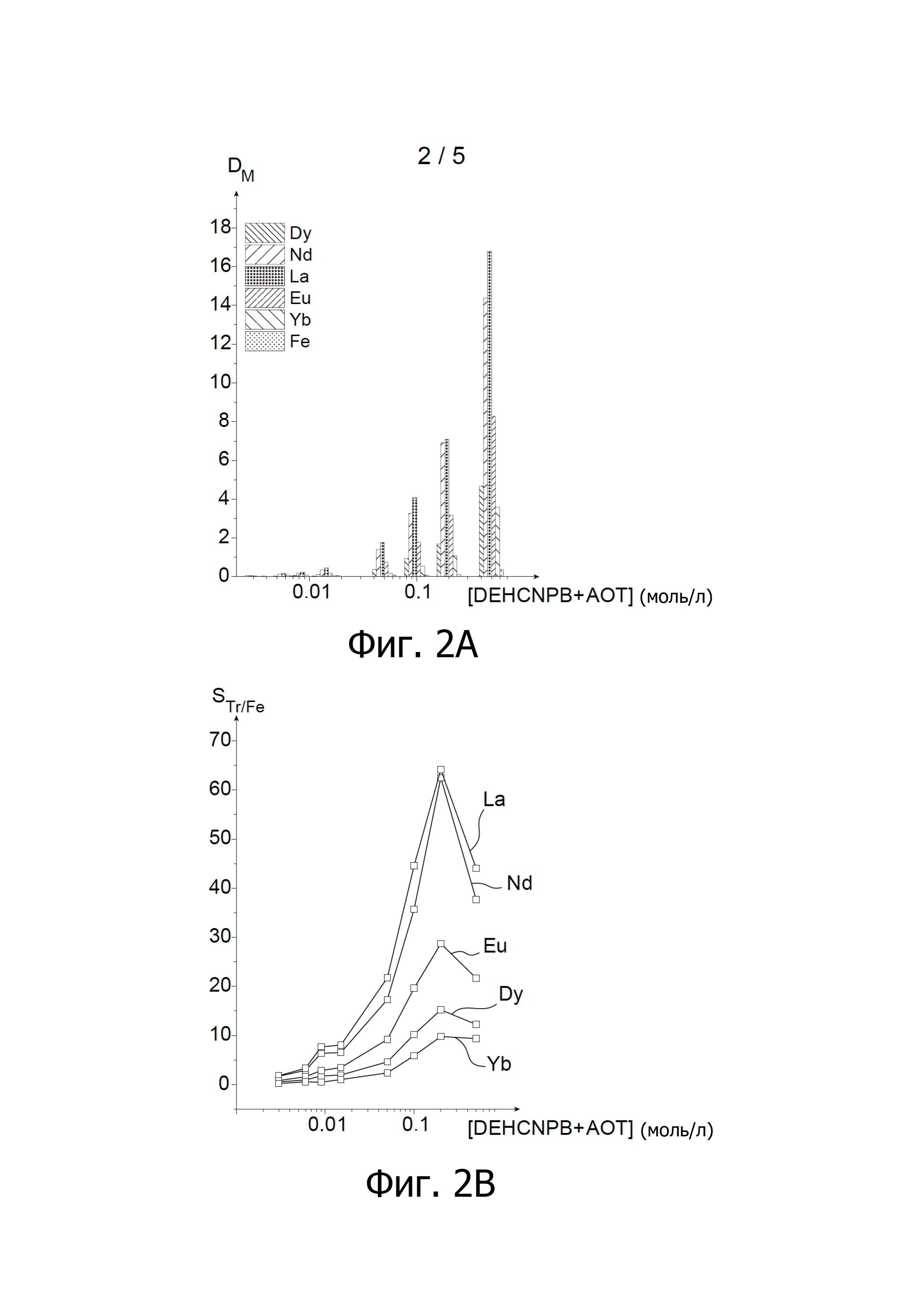
На Фиг. 2A и 2B показаны результаты тестов экстракции, проведенных с водными фосфорнокислыми фазами, содержащими пять редкоземельных металлов и железо, с применением органических фаз, содержащих в качестве экстрагента DEHCNPB или AOT (мольное соотношение DEHCNPB/AOT = 60:40) в различных концентрациях; на Фиг 2A показана диаграмма зависимости коэффициентов распределения редкоземельных металлов и железа, обозначаемых DM, от концентрации смеси DEHCNPB и AOT, обозначаемой [DEHCNPB + AOT] и выраженной в моль/л, в органической фазе, в то время как на Фиг 2B показана диаграмма зависимости коэффициентов селективности к редкоземельным металлам по сравнению с железом, обозначаемых STr/Fe, от [DEHCNPB + AOT], также выраженной в моль/л.
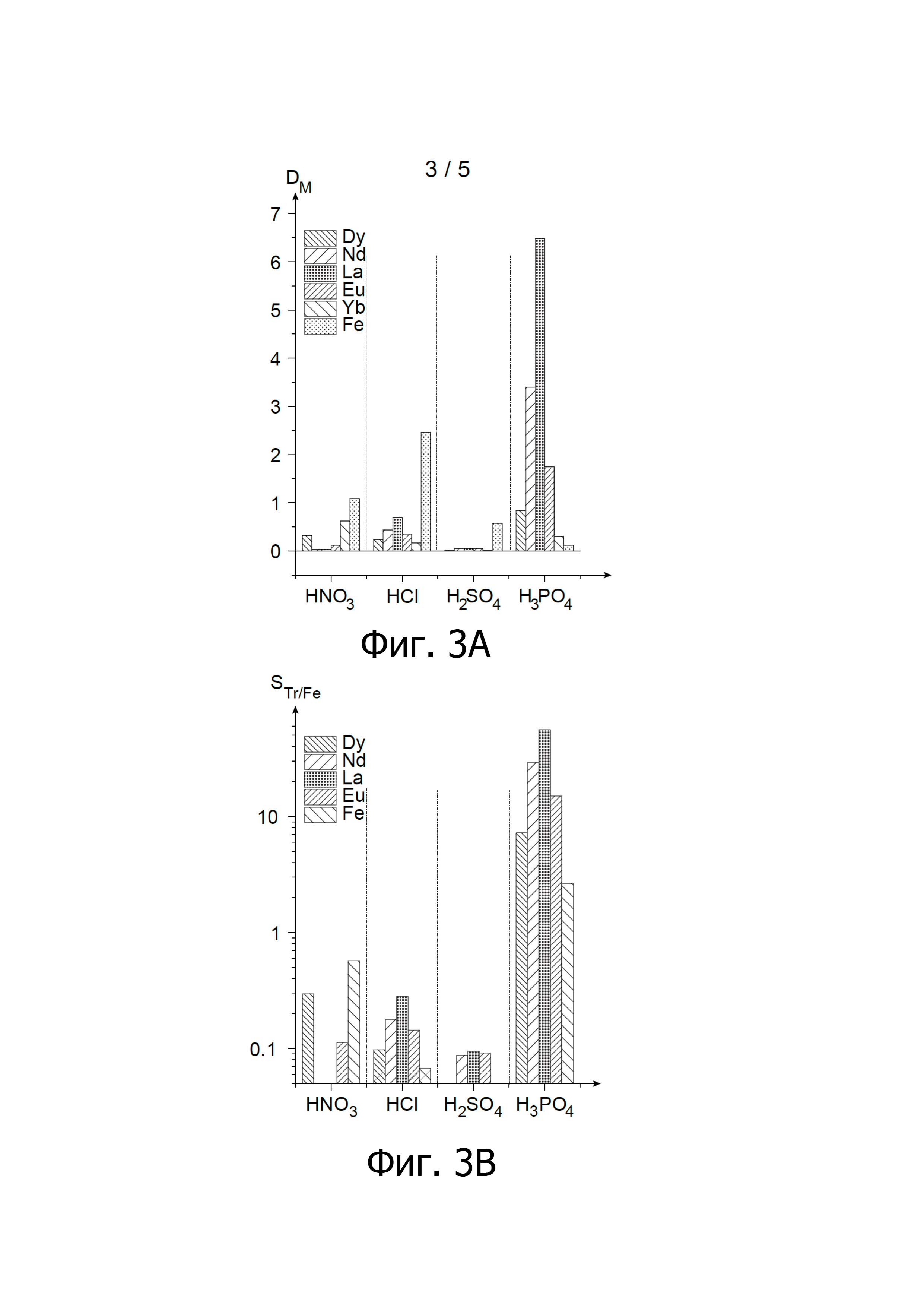
На Фиг. 3A и 3B показаны результаты тестов экстракции, проведенных с водными фосфорнокислыми фазами, содержащими пять редкоземельных металлов и железо, и содержащими в качестве кислоты азотную кислоту, хлористоводородную кислоту, серную кислоту или фосфорную кислоту, с применением органических фаз, содержащих в качестве экстрагента смесь DEHCNPB и AOT (мольное соотношение DEHCNPB/AOT = 60:40); на Фиг 3A показаны коэффициенты распределения редкоземельных металлов и железа, обозначаемых DM, как функция от кислоты, содержащейся в водной фазе, в то время как на Фиг 3B показаны коэффициенты селективности к редкоземельным металлам по сравнению с железом, обозначаемые STr/Fe, как функция от кислоты, содержащейся в водной фазе.
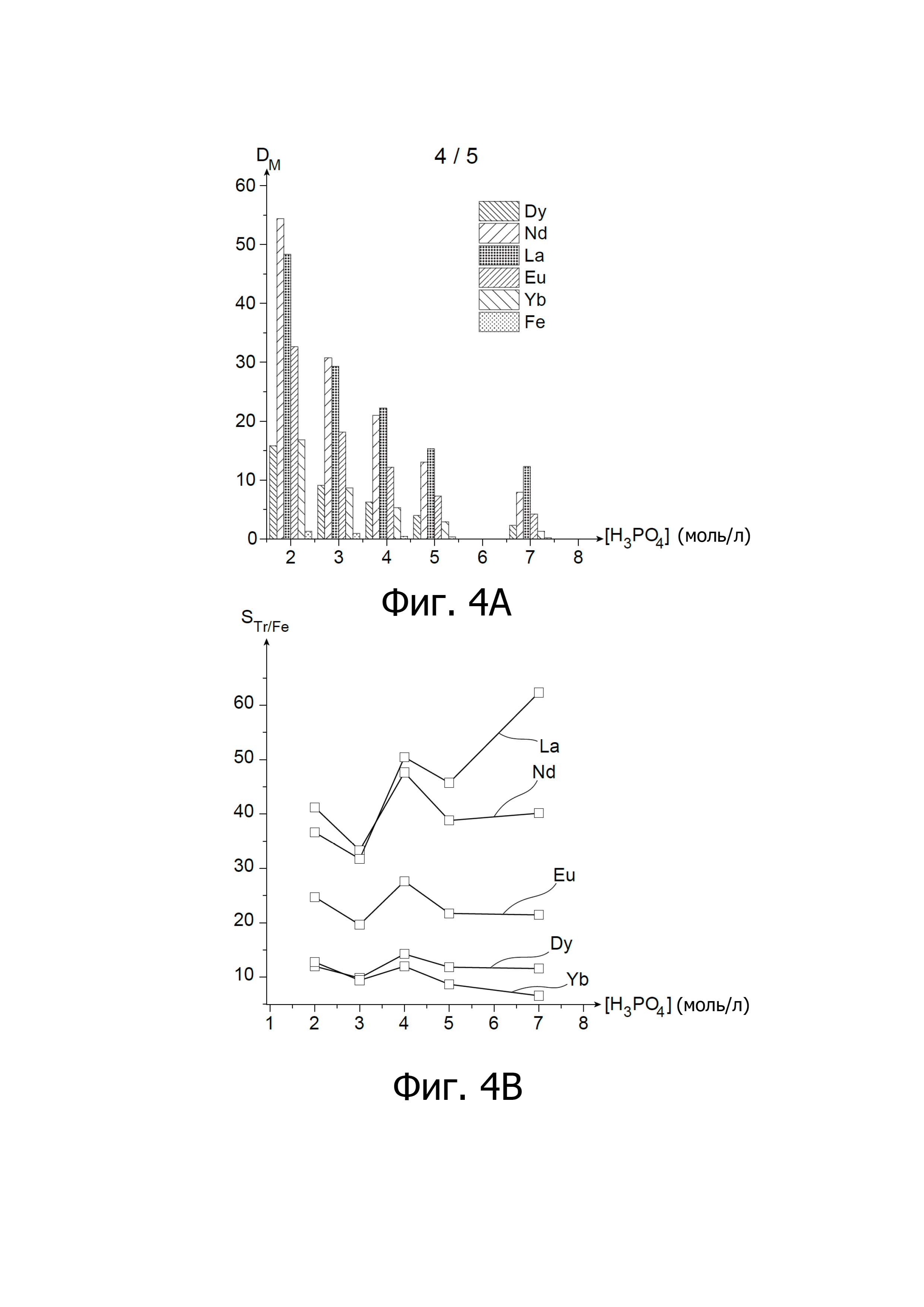
На Фиг. 4A и 4B показаны результаты тестов экстракции, проведенных с водными фосфорнокислыми фазами, содержащими пять редкоземельных металлов и железо, и содержащими фосфорную кислоту в различных концентрациях, с применением органических фаз, содержащих в качестве экстрагента смесь DEHCNPB и AOT (мольное соотношение DEHCNPB/AOT = 60:40); на Фиг 4A показана диаграмма зависимости коэффициентов распределения редкоземельных металлов и железа, обозначаемых DM, от концентрации фосфорной кислоты, обозначаемой [H3PO4] и выраженной в моль/л, в водной фазе, в то время как на Фиг 4B показана диаграмма зависимости коэффициентов селективности к редкоземельным металлам по сравнению с железом, обозначаемых STr/Fe, от [H3PO4].
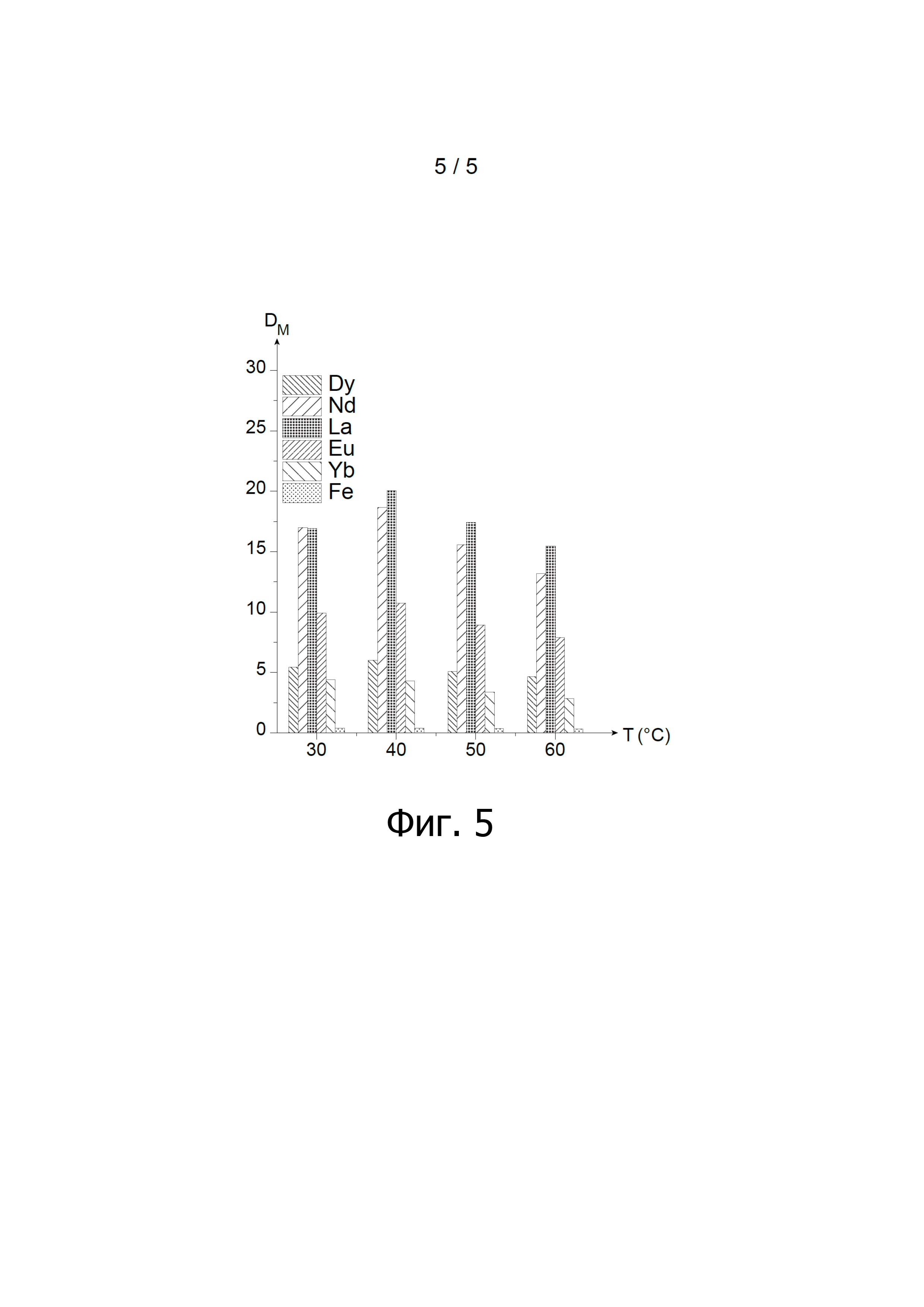
На Фиг. 5 показаны результаты тестов экстракции, проведенных при разных температурах с водными фосфорнокислыми фазами, содержащими пять редкоземельных металлов и железо, с применением органических фаз, содержащих в качестве экстрагента смесь DEHCNPB и AOT (мольное соотношение DEHCNPB/AOT = 60:40); на данной Фигуре показана диаграмма зависимости коэффициентов распределения редкоземельных металлов и железа, обозначаемых DM, от температуры, обозначенной T и выраженной в °C.
Подробное описание частных вариантов осуществления
Экспериментальные результаты, изложенные в следующих далее примерах, были получены с применением водных кислотных фаз, содержащих два легких редкоземельных металла, а именно лантан (La) и неодим (Nd), и три тяжелых редкоземельных металла, а именно европий (Eu), диспрозий (Dy) и иттербий (Yb).
Коэффициенты распределения, выходы экстракции и коэффициенты селективности, приведенные в описанных далее примерах, определяли согласно общепринятой практике в области жидкость-жидкостной экстракции, а именно:
- коэффициент распределения металлического элемента M, обозначаемый DM, между двумя фазами – соответственно водной и органической – определяли по следующему уравнению:
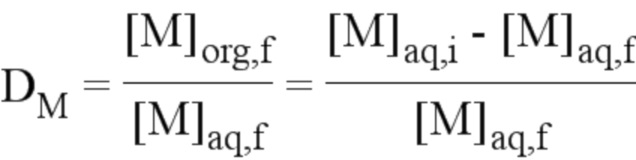
где:
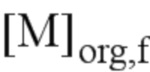
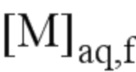
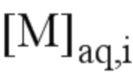
- выход экстракции металлического элемента M из водной фазы, обозначаемый RM, определяли по следующему уравнению:
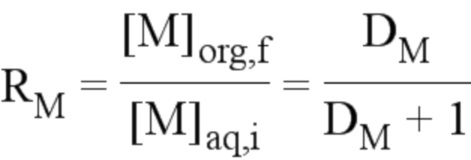
где
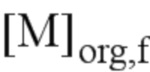
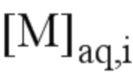
- коэффициент селективности к металлическому элементу M1 в сравнении с металлическим элементом M2, обозначаемый SM1/M2, определяли по следующему уравнению:
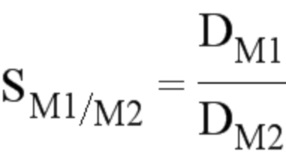
где:
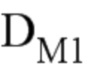
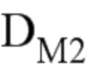
Пример 1: Синергетический эффект смеси DEHCNPB и AOT на экстракцию редкоземельных металлов из водного раствора фосфорной кислоты, и влияние мольного соотношения DEHCNPB/AOT в данной смеси на ее экстрагирующие характеристики
Синергетический эффект смеси DEHCNPB и AOT на экстракцию редкоземельных металлов из водного раствора фосфорной кислоты и влияние мольного соотношения DEHCNPB/AOT в данной смеси на ее экстрагирующие характеристики оценивали в тестах экстракции, которые проводили, используя:
- в качестве водных фаз: фазы, полученные растворением пяти солей редкоземельных металлов со степенью окисления (III) в соответствующих формах: La(NO3)3, Nd(NO3)3, Eu(NO3)3, Dy(NO3)3 и Yb(NO3)3, в концентрации 0.25 г/л каждой из указанных солей, в растворах, содержащих 5 моль/л фосфорной кислоты в воде сверхвысокой чистоты (т.е. вода Milli-Q, имеющая удельное сопротивление > 18 МОм/см при 25°C); и
- в качестве органических фаз: фазы, содержащие 0.1 моль/л экстрагента в изооктане, этот экстрагент состоит либо только из DEHCNPB, либо только из AOT, либо из смеси DEHCNPB и AOT, в которой варьировали мольное соотношение DEHCNPB и AOT.
Поскольку железо естественно присутствует как главная примесь в большинстве источников сырья и, в частности, в природных рудах, то водная фаза содержала также 2.5 г/л нитрата железа(III).
Тесты экстракции проводили, используя объемное соотношение водная фаза/органическая фаза (A/O) равное 1. Водную и органическую фазы вводили в контакт на 1 час при постоянной температуре (20°C), после чего их отделяли друг от друга на центрифуге (4000 об/мин) в течение 20 минут при 20°C.
Концентрации редкоземельных металлов и железа в водных фазах замеряли методом оптико-эмиссионной спектроскопии индуктивно связанной плазмы (ICP-OES) до и после экстракции.
Результаты этих тестов приведены ниже в Таблице 1, с указанием выходов экстракции редкоземельных металлов и железа, обозначаемых RM, как функция от мольной доли AOT, обозначаемой хАОТ в системе экстрагента, кроме того на Фиг. 1A и 1B показана зависимость коэффициентов распределения редкоземельных металлов и железа, обозначаемых DM, от хАОТ (Фиг. 1A), и зависимость коэффициентов селективности редкоземельных металлов в сравнении с железом, обозначаемых STr/Fe, от хАОТ (Фиг. 1B).
В Таблице на Фигурах, результаты для хАОТ = 0 соответствуют результатам, полученным для экстрагента, в котором присутствует только DEHCNPB, в то время как результаты для хАОТ = 1 соответствуют результатам, полученным для экстрагента, в котором присутствует только AOT.
Таблица 1
Приведенные результаты показывают, что для всех редкоземельных металлов выход экстракции с экстрагентом, содержащим смесь DEHCNPB и AOT, выше, чем сумма выходов экстракции с экстрагентом, содержащим только DEHCNPB, и с экстрагентом, содержащим только AOT, что указывает на синергетический эффект смеси DEHCNPB и AOT, оказываемый на экстракцию всех указанных редкоземельных металлов (Таблица 1).
Приведенные результаты показывают также, что самый сильный синергетический эффект смеси DEHCNPB и AOT наблюдается при мольной доле AOT 0.4 (т.е. при мольном соотношении DEHCNPB/AOT = 60:40), при этом коэффициенты распределения для лантана, неодима, европия, диспрозия и иттербия составляют соответственно 6.4, 3.4, 1.74, 0.81 и 0.32 (Фиг. 1A), а выходы экстракции указанных элементов составляют соответственно 0.87, 0.77, 0.64, 0.46 и 0.24 (Таблица 1).
Приведенные результаты показывают также, что самая высокая селективность смеси DEHCNPB и AOT в отношении редкоземельных металлов, по сравнению с железом, также достигается при мольной доле AOT 0.4, при этом коэффициенты селективности SLa/Fe, SNd/Fe, SEu/Fe, SDy/Fe и DYb/Fe составляют 59, 28.7, 15.0, 6.8 и 2.3, соответственно.
Пример 2: Влияние концентрации смеси DEHCNPB и AOT в органической фазе на эффективность данной смеси для экстракции редкоземельных металлов из водного раствора фосфорной кислоты.
Влияние концентрации смеси DEHCNPB и AOT в органической фазе на эффективность данной смеси для экстракции редкоземельных металлов из водного раствора фосфорной кислоты оценивали по тестам экстракции, проводившимся с применением:
- в качестве водных фаз: такие же водные фазы, как описано выше в Примере 1; и
- в качестве органических фаз: фазы, содержащие от 0.003 моль/л до 0.5 моль/л смеси DEHCNPB и AOT, при мольном соотношении DEHCNPB/AOT равном 60:40, в изооктане.
Экстракцию проводили в тех же условиях, как описано выше в Примере 1.
Результаты этих тестов приведены ниже в Таблице 2, где указаны выходы экстракции редкоземельных металлов и железа, обозначаемые RM, как функция от мольной концентрации смеси DEHCNPB и AOT, обозначаемой [DEHCNPB + AOT] и выраженной в моль/л, и на Фиг. 2A и 2B показана зависимость коэффициентов распределения редкоземельных металлов и железа, обозначаемых DM, от [DEHCNPB + AOT] (Фиг 2A), и зависимость коэффициентов селективности в отношении редкоземельных металлов по сравнению с железом, обозначаемых STr/Fe, от [DEHCNPB + AOT] (Фиг. 2B).
Таблица 2
Полученные результаты показывают, что экстракция редкоземельных металлов и железа улучшается с повышением концентрации смеси DEHCNPB и AOT в органической фазе, достигая значений коэффициентов распределения для лантана, неодима, европия, диспрозия, иттербия и железа 7.08, 6.90, 3.17, 1.68, 1.08 и 0.11, соответственно, при концентрации указанной смеси 0.2 моль/л (Фиг. 2A).
Полученные результаты показывают также, что можно достичь еще более высоких коэффициентов распределения при использовании смеси DEHCNPB и AOT в мольной концентрации выше 0.2 моль/л, например 0.5 моль/л, но затем наблюдается падение селективности данной смеси в отношении редкоземельных металлов, по сравнению с железом (Фиг. 2B).
Пример 3: Влияние типа кислоты, содержащейся в водном растворе, на эффективность смеси DEHCNPB и AOT при экстракции редкоземельных металлов из раствора
Влияние типа кислоты, содержащейся в водном растворе, на эффективность смеси DEHCNPB и AOT при экстракции редкоземельных металлов из раствора оценивали по тестам экстракции, проводившимся с применением:
- в качестве водных фаз: фазы, полученные растворением 0.25 г/л каждой из следующих солей La(NO3)3, Nd(NO3)3, Eu(NO3)3, Dy(NO3)3 и Yb(NO3)3, и 2.5 г/л Fe(NO3)3, в растворах, содержащих 5 моль/л кислоты в воде сверхвысокой чистоты, где кислота представляла собой азотную кислоту, хлористоводородную кислоту, серную кислоту или фосфорную кислоту; и
- в качестве органических фаз: фазы, содержащие 0.1 моль/л смеси DEHCNPB и AOT, при мольном соотношении DEHCNPB/AOT равном 60:40, в изооктане.
Экстракцию проводили в тех же условиях, как описано выше в Примере 1.
Результаты этих тестов приведены на Фиг. 3A и 3B с указанием коэффициентов распределения редкоземельных металлов и железа, обозначаемых DM, полученных для каждой кислоты (Фиг. 3A), и коэффициентов селективности в отношении редкоземельных металлов по сравнению с железом, обозначаемых log(STr/Fe), полученных для каждой кислоты (Фиг. 3B).
Полученные результаты показывают, что наивысшая эффективность смеси DEHCNBE/AOT в экстракции редкоземельных металлов из водного раствора кислоты достигается в том случае, когда кислота, содержащаяся в этом растворе, представляет собой фосфорную кислоту (Фиг. 3A).
Экстракция редкоземельных металлов из водного раствора азотной кислоты, хлористоводородной кислоты или серной кислоты очень слабая и имеет низкую селективность в сравнении с железом (Фиг. 3B).
Пример 4: Влияние концентрации фосфорной кислоты в водном растворе на эффективность смеси DEHCNPB и AOT для экстракции редкоземельных металлов из данного раствора
Влияние концентрации фосфорной кислоты в водном растворе на эффективность смеси DEHCNPB и AOT для экстракции редкоземельных металлов из данного раствора оценивали по тестам экстракции, проводившимся с применением:
- в качестве водных фаз: фазы, полученные растворением 0.25 г/л каждой из следующих солей: La(NO3)3, Nd(NO3)3, Eu(NO3)3, Dy(NO3)3 и Yb(NO3)3, и 2.5 г/л Fe(NO3)3 в растворах, содержащих от 2 моль/л до 7 моль/л фосфорной кислоты в воде сверхвысокой чистоты; и
- в качестве органических фаз: фазы, содержащие 0.2 моль/л смеси DEHCNPB и AOT, при мольном соотношении DEHCNPB/AOT равном 60:40, в изооктане.
Экстракцию проводили в тех же условиях, как описано выше в Примере 1.
Результаты этих тестов приведены ниже в Таблице 3, где указаны выходы экстракции редкоземельных металлов и железа, обозначаемые RM, как функция от мольной концентрации фосфорной кислоты, обозначаемой [H3PO4] и выраженной в моль/л, а на Фиг. 4A и 4B показана зависимость коэффициентов распределения редкоземельных металлов и железа, обозначаемых DM, от [H3PO4], выраженной в моль/л (Фиг. 4A), и зависимость коэффициентов селективности в отношении редкоземельных металлов по сравнению с железом, обозначаемых STr/Fe, от [H3PO4], также выраженной в моль/л (Фиг. 4B).
Таблица 3
Полученные результаты показывают, что в соответствии с данными, описанными в литературе для катионообменных экстрагентов (R. Turgis et al., Solvent Extr. Ion Exch. 2014, 32(7), 685-702, ссылка [5] в списке литературе ниже), эффективность смеси DEHCNBE и AOT для экстракции редкоземельных металлов из кислой водной фазы уменьшается с повышением кислотности данной фазы.
Тем не менее, экстракция остается эффективной даже при концентрации фосфорной кислоты 7-8 моль/л, при этом коэффициенты распределения для лантана, неодима, европия, диспрозия, иттербия и железа составляют 12.27, 7.90, 4.22, 2.28, 1.29 и 0.20, соответственно (Фиг. 4A).
Что касается селективности смеси DEHCNBE и AOT в отношении редкоземельных металлов, по сравнению с железом, то на Фиг. 4B показано, что она очень слабо зависит от концентрации фосфорной кислоты в водной фазе.
Пример 5: Влияние температуры экстракции на эффективность смеси DEHCNPB и AOT для экстракции редкоземельных металлов из водного раствора фосфорной кислоты
Влияние температуры, при которой проводится экстракция, на эффективность смеси DEHCNPB и AOT в экстракции редкоземельных металлов из водного раствора фосфорной кислоты оценивали по тестам экстракции, проводившимся с применением:
- в качестве водных фаз: такие же водные фазы, как описано выше в Примере 1; и
- в качестве органических фаз: фазы, содержащие 0.2 моль/л смеси DEHCNPB и AOT, при мольном соотношении DEHCNPB/AOT равном 60:40, в изооктане.
Экстракцию проводили в тех же условиях, как описано выше в Примере 1, за исключением того, что ее проводили при температурах 30°C, 40°C, 50°C и 60°C.
Результаты этих тестов приведены ниже в Таблице 4, где указаны выходы экстракции редкоземельных металлов и железа, обозначаемые RM, как функция от температуры, обозначаемой T и выраженной в °C, а на Фиг. 5 показана зависимость коэффициентов распределения редкоземельных металлов и железа, обозначаемых DM, от T.
Таблица 4
Полученные результаты показывают, что экстракция редкоземельного металла и железа очень слабо зависит от температуры, при которой проводится экстракция.
Тем не менее, наблюдался пик экстракции при 40°C, позволяющий достичь коэффициентов распределения для лантана, неодима, европия, диспрозия, иттербия и железа 20.04, 18.66, 10.74, 6.01, 4.30 и 0.4, соответственно.
Селективность смеси DEHCNPE и AOT в отношении редкоземельных металлов, по сравнению с железом, также очень слабо зависит от температуры, при которой проводится экстракция, поскольку сама экстракция слабо зависит от температуры.
Пример 6: Тесты выделения
Тесты выделения проводили с применением:
- нескольких органических фаз, содержащих от 0.01 моль/л до 0.5 моль/л смеси DEHCNPB и AOT, при мольном соотношении DEHCNPB/AOT равном 60:40, в н-додекане, в который предварительно загружали La, Nd, Eu, Dy, Yb и Fe, посредством контакта с водным раствором, содержащим 0.25 г/л каждого из указанных редкоземельных металлов, 2.5 г/л железа и 8 моль/л фосфорной кислоты; и
- водной фазы, содержащей 0.2 моль/л оксалата аммония C2H8N2O4.
Для этого теста, 2 мл каждой из органических фаз (содержащих большую часть редкоземельных металлов, изначально присутствующих в водном растворе, и следы железа) вводили в контакт с 2 мл водной фазы и оставляли при интенсивном перемешивании на 1 час при комнатной температуре (24°C). После разделения органической и водной фаз образовывался белый осадок, содержащий редкоземельные металлы в виде комплекса с оксалатом.
Таким образом, редкоземельные металлы можно выделить из водной фазы в форме оксалатов и затем перевести в оксиды путем кальцинирования полученных оксалатов.
Список процитированной литературы
[1] M. Krea and H. Khalaf, Hydrometallurgy 2000, 58(3), 215-225.
[2] International application PCT WO 2013/059352.
[3] “Chemistry and Technology of Surfactants”, Richard J. Farn, 2006 Blackwell Publishing Ltd, ISBN-13: 978-14051-2696-0.
[4] “Self-Organized Surfactant Structures”, Tharwat F Tadros, 2011, John Wiley & Sons, ISBN: 978-3-527-63265-7.
[5] R. Turgis et al., Solvent Extr. Ion Exch. 2014, 32(7), 685-702.
Реферат
Группа изобретений относится к новому экстрагенту для экстрагирования из водного раствора фосфорной кислоты редкоземельных металлов, присутствующих в данном растворе, а также к применению указанного экстрагента для обработки водных растворов, полученных при выщелачивании природных фосфатов серной кислотой, и водных растворов, полученных выщелачиванием бытовых отходов фосфорной кислотой. Экстрагент содержит соединение, имеющее формулу
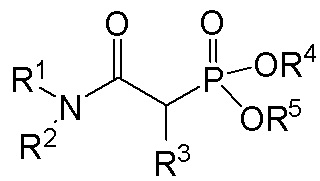
Формула


Комментарии