Состав для извлечения металлов из водных растворов - SU629857A3
Код документа: SU629857A3
Описание
л; о; кт
; ;Г1оннер; нужно полуил растворовf содержа;баль ,- со более: удобно ;- еталла вместе и отде ба .ль г от малн .
;;ко;: ;::;; ;;ра;-п: аник нейтрально -/. лек;.:г обь-ч ю плет с выделениС:лсг:ы 1-,сжел КОзниккуть необхоГ:- лос;; B.iRHKJi ;ге:1Очи для поддероП :: .-jfjcy С:М(:;М уровне. ХинО i к-;:(; сную т,:ислоту |-4ожно также полнос/ью или част1- чно в соли inGJKi Kj-o металла, хотя :;iocov i-n car удобен для непре: ) О прс рзволотва .
(-j/cci; нь-чеокого раотво;;: ;:р11;.0 1гсгь любой подвижt .cKMH ра:сс}зоритель или
с: ; орые не смешиваются с .L.cjMcoiv; рИ являются .. с . к воде, к ме О(С:;инечипх и к хинолин -
iC; кислоте, например али
I арок лтические углеводоc::-4J04 .ie углеводороды,
:1 CF;H;I разделения водной уэ:- желательно при:1ор1-1тсль с п;ютнг:стью, :я СУ- полного слоя, Разде-П1 .Г er-;;;i;TC:n при максималь- , i .;,-1стей ;;;идкС;оти . лпчуусс ;:е .пг,ностыо раотр; .с-чсрителе, но полнос-i/ vcH то луч::1€; приме;р1 е. г ч KOTOpiJX плотчe1 c:i -) раст)ЭОрите;1Я такочс1:ччп:: нанкый твердый
;). :сееть ИЗ ПОВерХ ;л;; рч с гвоэител ь - вода, р-лсуворителей являч;: частчорители, например гччуус у 41чг-о.иородь S Е ча Ч ч KJF) ч ч ч л е ч i4-Hi X л о р э О а к
ЧЧ)ччч, ч-;стзоди1ь путем :-одчс 43 часччора и раство- ччи;;;; :: коной кислоты 1 - срсчзч ческом rujyjTBOpH:ччч8ечс ;:В;-юшен температуу: 1м:-1Рт гЮй ; при Г1ере -.1е1ли iyiyroM способе взмучивания i44 vofo тобы увеличить 1 раядеаа вода-раствориоолэ : чаат образование комччле--еч .зс Затем перемейшоагуают - дают разделиться я:5 - слою растворителя. б-учь :)егч-1О,цическим или .. Во ачез; случаях раотво-с сучонять от с одержимолере:п псЕторкым кополь ( I
ао органического раство 1рают таким, чтобы оно зало объему экстрагируеморастворЕ; , концентрации еталла ч установке для осу;-:,ествдения процесса. Отношение оргаг ический растворитель-вода обычно 5;1-1:5. Нет необходимости во всех случаях применять такое количество растворителя , чтобы происходило полное растворение образующегося комплекса, так как избыточный в растворе комплекс обычно остается в виде с:,спензии полностью в органическом растворителе и не мешает переработке и разделению слоев растворителя и воды
При желании можно применять смеси хинолин-2-карбоновых кислот и других соединений, например длинноцепочных алифатических спиртов, например каприлового спирта, изодеканола , тридецилового спирта или 2-этилгексанола , которые помогают образованию и экстрагированию комплексного соединения, в количестве 0,510% по весу органического растворителя .
Иногда желательно добавлять поверхностно-активные вещества, например продукты конденсации окиси этилена и алкилфенолов , для оР легчения разделения водной и органической фаз путем умень1-1ения эмульгирования.
Желательно применять растворы растворителей, содержащие более 2% хинолин-2-карбоновой кислоты.
Металл можно выделять из растворителя после стадии извлечения любым обычным способом, например экстрагированием в водную фазу при более кислой среде, в которой комплекс разлагается.
Если в растворителе имеется комплекс более чем одного металла, то разделение металлов можно в некоторых случаях вести экстрагированием отдельными водными растворами с повышающейся кислотностью для последовательного раздельного разложения комплексов. По другой методике комплекс в растворителе можно прямо гидрировать и получать металл. При такой обработке регенерируется лиганд и выделенный растворитель, содержащий хинолин-2-карбоновую кислоту, можно снова использовать в процессе, особенно при непрерывной работе.
Предлагаемый состав особенно применим к водным растворам, полученным от обработки минеральных руд, металлолома и других металлсодержащих остатков водны.ми кислотами, например серной, соляной, фтористоводородной или азотной, или к металлсодержащим сбросным жидкостям от электролиза или химических процессов Он пригоден для выде1 ения металлов из растворов, содержащих не менее 0,5 г/л и особенно для обработки растворов, содержащих более 2 г/л
MGT аЛЛ а.
Хинолин-2-карбоновые к ислоты, применя eiVCJe при- осуществлении этого способа, являются .човыми ьешес1ва.ми.
Хинолин-2-карбонопые кислотк мочено получать из сложных эфиров, лучше из низших алкильных эфиров хинолин-2-карбоновых кислот формулы Г, где К -гидроксильная грхппа, путем превращения гидроксилькой группы в нужный атом галоида или произвольно замещенную алкоксильную, алкеноксильную , циклоалкокси, арилоксильную или аралкилоксильную группу известными методами для 4-оксихинолинов и гидролизом эфирной группы, например 1иелочью для получения кислоты.
Хинолин-2-карбоновь;е кислоты форьгулы 1, где хлор или бром, можно получать из алкильных эфиров хиь:олин-2-карбоновых кислот формуль.
1 , где R это гидроксил, путем нагревания с хлорокисью фосфора или пятихлористым фосфором, или бромокисью фосфора , соответственно ;; гидролизом
эфирной группы.
20
Хинолин-2-карбомовые кислоты формулы Г, где R - произвольно замещенные алко1 сил bHhJC , алкеноксильные , - циклоалкилокси.чьные, арилоксил ьные или аралкилокси-группы, можно получать из алкильных эфиров хинолин-2-карбоновых .пот формулы I , где хлор или бром, Плгем нагревания с производным ; елочного металла со ) I
ответственно произвольно замешенного сгтирта или фВнола с последующим гплролизом эф:иг:м-ой группк. ИлгреваН1-:о удобно вести в таком растворителе , как ксилол. Этот метод особенно при получении хинолин-2-карбоиовкх кислот, где - а.)илоксигруппа .
,1 Хинолин-2-карбоновые кислоты формулы Г, где R - произвольно заме:;;ениь;е алкокси, алкенокси, циклоалкокси или ара.чкокси-группы, можно получать из алкильных эфиров хи 1олин-2-карбоновых кислот формулы Г, где R- гидрокскл ьна я группа, путем iiaг , гревания с соответствующим алкил, а;1кенил, цкклса-пкил или аралкилхлоридом или бромидом в присутствии основания, ь:ап1-)имер карбоната калия, и гидролизом эфирной группы. Нагре , вание удобно вести в таком растворителе , как .
Алкильные эфиры хинолин-2-карбоновой кислоты форму-пъ; Г, где R ,5 это окси-группа, применяемые как исходные вещества в указанных процессах , можно получать, например, известньчзми методами из ариламинов форхулг, II и алкмла, напри.мер этилокс а.1:оац;- ЛЬ11::1Х эСИров формулы III , нагрявсГ:П1ем , например, в кипящем толуоле с образогзанием.- этилфени.пиминоrj cyKUHHaia, который циклиз ют в 4-оксихннолин-2-карбоновую кислоту н греванием ггр-н 240-250Ct , Vv СО , Пример л. Около 180 вес.ч, 6 н серной кислоты по каплям добавляют в течение 10-15 мин к хорошо перемеыиваемой смеси 209 вес.ч. этил натрийоксалацетата, 500 ., воды и 870 вес,ч. толуола при Of , Полученную слегка кислую смесь (рН - 3 перемешивают при этой темг1ерату1)е в течение 45 мин, Толуольный слой удаляют, водный слой и выпавший сул фат натрия промывают толуолом (2 порциями по 65 вес.ч.), соединенный толуольный слой и промывки отьмвают затем от кислоты аодой, сушат сульфатом магнии и фильтруют. К толуольному раствору этилоксалацетата добавлямт 117,, вес. ч, ;( -толуидина и смесь кипятят с С)брс Тной перегонкой в течение 60 мин. за это время выделяется 18 Бес.ч,, аоды которые удаляют в аппарате Диб аСтарка . После ослаждения оранжевый толуольный раствор промывают 2 н„ соляной кислотой (3 порции по 100 вес.ч для удаления непрореагмровав шего rt -толуидина, затем до отсутствия кислоты сушат над сульфатом магния. Из этого раствора пос ле отгонки толуола в вакууг-ле гюлучают 258,2 вес „ч . этил-(П -толнлими -сукцината в виде оранжевого масла, которое смеилизают со 11С вес. ч. тер мекса (эвтектическая смесь дисренила и окиси дифенила) к затем по каплям. э течение 60--90 мин лобаьляют к 1920 вес,ч. хорошо перемешиваемого термекса при 240-250. После ЕЫ,делени я этанола (37 в ее. ч.) и оттонки его в ректификапионной колонне; тем ной реакционной смеси дают охладить ся, затем ее выдеркиважт при комнат ной температуре 2-3 дня. Выделившие ся коричневые кристаллы (. 45,2 вес. фильтрованием, промывают . 300 вес. ч. петролейного эфира IT„ки 60-80 С) и сушат на воздухе. Псусле очистки перекристалл;-1Эацией лз ацетона получают 115,2 вес, ч. этил--4 ок ил - X и н о л и н - 2 - к ар 5 о к с и л а та в виде небольших светло-ксфичневых игл с т . пл . 214- 2 16 С После упаривания ацетонового магочного раствора получают 13,9 вес.ч, мпнее чистого продукта с т . пл . 207-208с. Хорошо перемешиваемую смесь 34;5 вес . ч . этил-4-окси-6-метилхиноллН--2-карбокс;г-:лата ,- 21 вес. ч. безводного карбоната калия, 46,-5 в«;С,ч, 4-додецилбензилхлорпда {полученного из замещсчногс сильно разветвленног додецилбензола, клороульфоновой кис-лоты; метанола и П -формальдегида) и 615 вес,ч. безводного ацетона нагревают с обратной перегонкой в течение 68 ч. Охлажденную коричневую реакционную смесь фильтруют для удаления неорганических солей и непрореагировавшего этил-4-окси 6-метилхинолин-2 карбоксилата (3,7 вес.ч.), ацетон отгоняют ti вакууме. Раствор остаточного коричневого масла в эфире (285 вес. ч.) промывают последовательно 1 н. раствором едкого натра (2 порции по 50 аее.ч.) и водой (2 порции по 50 вес ,ч.) , затем сушат над, сульфатОМ магния и отгоняют растворитель . Остается 69,2 вес.ч. этил-6 метил-4- (4 -додецилбензилокси)-хинолиН-2-карбоксилата в виде вязкого ко-ричневого масла, которое растворяют в 120 вес.ч . этанола и кипятят с обратной перегонкой 2,5 ч с раствором 6 вес.ч. едкого натра 3 25 вес.ч, воды. После охлаждения реакционной смеси до натриевую соль 6-метил-4-(4 - додецилбензилокси ) -хинолин-2-харбоновой кислоты, выделившуюсяв виде бесцветных грану/ (53 ,,4 вес. ч.) . собирают фильтрованием , прогллвают 25 вес. ч. этанола и сушат 34,2 вес„ч. натриевой соли 6-метил-4- (4 -додецилбензилокси) -хинолин-2-карбоновой кислоты суспендируют в 750 вес.ч. хлороформа, содержащего 50 вес.ч. ледяной уксусной кислоты . После интенсивного встряхивания смеск 3 течение 10 мин добавляют 200 Bec.-i, воды, переме1:-1ивание ведут в течение еще 5 мин и отделяют нижний хлорофоркенный слой,. Этот органический слой повторно азбалтывают с 10%-ной водной уксусной кислотой (5 порций по 50 вес.ч.), затем с зодой (порции по 100 вес. ч.) до удаления кислоты и сушат над сульфатом магния. ; лороформ удаляют из фильтрованного раствора в вакууме, остави ийся вязкий остаток нагревают при лм рт.ст, в течение 4 ч для удаления всего растворителя. При охлаждении нязкое масло затвердевает . Получают 30,8 вес.ч. 6-метил-4- ( 4 -.г;одецилбе:нэилокси ) -)синолин-2-карбоновой кислоты з виде бледно-желтогс твердого осадка- с т.пл. 95-9б-с (размягчение при -- 70с) . Найдено,% г С 78,7; Н 8, 1 ; N 2,6 ., В 1числено, % С ,1: Н 8,5; Пример 2. По методике примера 1, применяя Г -бутиланилин вместо П -толуидина, получают этил-4-окси- 6 -н-бутилхинолин-2-к арбомовую кислоту с т . пл. 165 С и 6-н-бутил-4- (4 -додецилбснэи1;окси) -хинолин-2-карбоновую кислоту Б виде очень вязкой светло-коричневой смолы-. Пример 3. Перемешивают сме этил-4-окси-б-н-бутилхинолин-2-карбоксилата , полученного аналогично примеру 2, и 213 вес,ч. хлорокиси фосфора. По окончании экзотермическ реакции темно-окрашенную смесь оста ляют на 1 ч при комнатной температу ре, затем охлаждают до О С,разбавляют 75 вес.ч. этанола для усиления подвижности и потом по каплям добав ляют к 500 вес.ч. льда 1500 вес.ч. воды. Водную смесь нейтрализуют до рН 7-8 добавлением карбоната натрия при этом выпадает 133,2 вес.ч. свет ло-коричневого кристаллического оса ка, который собирают фильтрованием и сушат. Это вещество очищают кристаллизацией из 380 вес.ч. ацетона (с обработкой углем), получают 100,8 г этил-4-хлор-6-н-бутилхиноли -2-карбоксилата, который выделяют в виде светло-серых игл с т.пл. SBSB , . Дополнительные 27,5 вес.ч. менее чистого продукта с т.пл . 54,5 получают при разбавлении ацето новой маточной жидкости водой. 4-Хлор-6-н-бутилхинолин-2-карбоновую кислоту получают обычным способом из этилового эфира (43,7 вес. гидролизом при кипячении с 20%-ным раствором едкого натра и подкислением . Она выделяется в виде бесцвет ных игл (28,7 вес.ч.) из водного 5,5, М 4,5 Найдено,: C,4H|4NO.CP Вычислено,%: С 63, Н 5,35; 5,3; се 13,45 . Хорошо перемешиваемую смесь 55 вес.ч. 4-нонилфенола (смешанные изо меры, полученные алкилированием фенола тримерами пропилена) , 870 вес. ксилола и раствор 20 вес.ч. едкого натра в 25 вес.ч. воды кипятят с об ратной перегонкой в течение 4,5 ч и обезвоживают с помощью аппарата Дина-Старка. Затем добавляют 72,9 вес.ч. этил-4-хлор-6-Н-бутилхинОЛИн -2-карбоксилата и безводную смесь кипятят с обратной перегонкой в теч ние 40 ч. Ксилол отгоняют паром и водную маточную жидкость декантирую ( в горячем состоянии) с оставшейся светло-коричневой резиноподобной массой, которую затем промывают 1200 вес.ч. воды и суспендируют в 1500 вес.ч. хлороформа. В суспензию натриевых солей добавляют 100 вес.ч ледяной уксусной кислоты и пере мешивают в течение 60 мин, затем обрабатывают 200 вес. ч. воды. Водный слой удаляют, оставшийся хлорформен ный раствор промывают 10%-ной водной уксусной кислотой (4 порции по 200 в ее.ч.) и водой (порциями по 200 вес. ч.) до отмывки всей кислоты После сушки над сульфатом магния хлороформ отгоняют в вакууме и полу 710 чают 120,1 вес.ч. прозрачного красного масла, которое растворяют в 500 вес.ч. этанола, затем нагревают с обратной перегонкой 30-60 мин с раствором 12,5 вес.ч. едкого натра в 25 вес.ч. воды и 20 вес.ч. этанола. После охлаждения реакционной смеси и перемеггивания ее в течение ночи при комнатной температуре фильтрованием собирают 95,1 вес.ч. натриевой соли 6-н-бутил-4-(4 -нонилфенокси)-хинолин-2-карбоновой кислоты, которую выделяют в виде светло-корич 1евых гранул, их промывают 85%-ным этанолом (100 вес.ч.) и сушат в вакууме . 95,1 вес.ч. натриевой соли 6-н-бутил-4- (4-нонилфенокси)-хинолин-2-карбоновой кислоты суспендируют в 750 вее.ч. хлороформа, содержащего 35 вес.ч. ледяной уксусной кислоты . После встряхивания смеси в течение 10 мин добавляют 200 вес.ч. воды, перемешивают eiie 5 ми и отделяют нижний хлороформеиный слой. Органический слой снова взбалтывают с 10,ной водной уксусной кислотой (Ь порций по 50 в ее . ч.) , затем с водой (порции по 100 в ее. ч.) до вы ывaния всей кислоты и сушат над сульфатом магния. Хлороформ отгоняют от фильтров анно1О раствора в вакууме, остается 91,6 вес. ч. fi-н-бутил-4-(4 -нонилфенокси ) -хинолин-2-карбоновой кислоты - прозрачного красного масла, строение которого доказано спектральН 1м анализом. Пример 4. По мсзтодике примера 3, применяя 2-трет-бутил-4-метилфенол вместо 4 -нонилфснола, получают 6-Н-бутил-4 -(2-трот-бутил-4-метилфенокси ) -хинолин-2-карбоновую кислоту в виде красной вязкой смолы. Пример 5. По методике примера 3, применяя 2-трет-бутил-5-метилфенол вместо 4-номилфенола, получают 6-н-бутил-4 -(2 -трет-бутил-4 -метилфенокси )-хинолин-2-карбоновую кислоту в виде красно-коричневой вязкой смолы. Пример 6. По методике примера 3, применяя 2,4-ди-трет-пентилфенол вместо 4-нонилфенола, получают 6-н-бутил-4- ( 2 , 4-ди-трет-Г1ентилфенокси )-хинолин-2-карбоновую кислоту в виде коричневой вязкой смолы. Пример 7. Повторяют методику примера 6, применяя 17 вес.ч. 4-фенилфенола вместо 2,4-ди-трет-пентилфенола . Получают 35,4 вес.ч. 6-н-бутил-4- (4 -фенилфенокси)-хинолин2-карбоновой кислоты в виде вязкого темного масла. Пример 8. Повторяют методику примера 6, применяя 17,5 вес.ч. 4-циклогексил()енола вместо 2,4-ди-трет-пентилфенола . Получают 11,7 вес.ч. 6-п - 4-(4-циклогексилфенокси)-кинолк;1-2--карос;иозоа кисло да очень знлко//с TBf.. мед
П р и ы е о ; . ;.;,-; s ее: -трет-бу1ч-ш-4 ме.силФакопс, и 22,4 вес ч, ед:;огс калы т i воды к б с вес,, ллщг нс; пятят с обратной nepefcnKo фере азота до полного рлстк фенола. , иобс.злнют 4(;С ксилола и STTI,
- б - Н - б у т ил к я Н с л и i Е - ; - е Р R i3
лоты (из примег:;: ji « ;.:с;.--7:-продолжают 2С ч в икерлной ре i После добав.ле;-;ия ;ui; зе воды л гиетанол ;. .. ;: ром и смеси дага- ;;;: ь.-фазу декантиру1о;1р: iiojVy-iciwосадок , 1;:у эате .трог: доя л Су C;je i,bv ру;от . иО -
рОфОрмсР Xj;O;JOQO-pr.iSL;Ky 10 - V С
обрабативаюг 30 вес.ч укс лоты, Смусь D зб:1ЛМ мьа:0л .; и добавляют i(0 3 ас ,- -ouiV-. удаления слоя хлслзс раствор с НОВ;: i:poiv:bib аюл -uP ной уксусной |;мг:лотоп J 200 веер-:,) . затем 1зо,цок ii по 200 вес,ч.) до ;У кислоты и 1-:ад супьРа Хлороформ с-1тонч;от а так у у фильтрованногю рас IHvjca , о
того лролух :;-: ;y-jj-::,C.:: ао.. лизуюУся X ciа;-; 3 i-a-j,, , с, KpHCTa;ulH3iL.pa: из г:с : а, ,:, v,l pa ; т -КУГ , 60- SO СУ iia;.; 42,4 зес.ч. Ь ;- а-.,: ,. л;. / у бутил-;-a.l;-ai.:;V ;;aa: а a-hiбоновой .;ис ic-aj. а ana вых крас .aaiyar;; с:
-карбоксила л ,:: ; масла и б -мет аа зилокс О -хиью/:,-; ту в с с а а л а: г засла .
та С; т уап . л39, S-C (разложение) и
окси-4 - ( 4-чонилфенокск) -хинолин-2-асарбоновую кисло1у к виде светлоaej-airci полутверд;ого продукта,
П р и м е Р 13. о методике пример:- } , применяя О толуилик вместо к - -олуидкна. по/:учают э-;ил-4-0X0 В - i, ;е и лх и Н ол ин-7-карбоксилат р aavjr ;.3«-139°С k 8-метил-4--( 4 ДОдеа ,:: лбенэи1и.) - xиl-ioлин-/-кapбoнo ivю кислоту в Е1-{1-;е БЯЗИОГО коричкв- аа:.. маапа ,
Р и и м е р 14, Этил Ч-ОКОЙ--8- .чатилхииолига-2 -харбокоилат ,, лолуaaH;ajft ана; сгичнс; примеру 13, презра:лают г:о покмера 3 :з этил-- 4 ХЛОР-- 8- ь-еаилхиь1олин -2 карбоксипат
.. П,л
а аа :;. С (разложение) л 8-ме ь;.И- - ( --ЧОКИЛфеПОКСИ ; - хин ОЛИ Н-2 .raraiava; «аю кисл(;ту а т , пл , 1211 :; i : , ;а:а;,е,г ле:. аутек обработки
a-TpOJ:eH ibiM афИрОМ, в КОТОrajM uepbJjH кислота слабо растворима,.
Ра а. к ;,и я 6 -;чати;а- - { а конилфенокси) a-:Hia:ai ,-м 2-ь. apooiioaaft кистюты с: меia; ,i;; j и caieTBTOM кооальта а г ипятем
1 о о
192-193 С (раэложес т , пл
м :: р 1 ; , По
;:иг4а1;яя Л --метокск о-толуиа у -т.а; ун aiics., получают
;: :., о а.1С ГОлСа- В - Mela IЛ ХИ Н О
S -;--.атакси-В-:а:агкл-4-(4 ,.cj алакга- ) --хк нолаи-2-карбо аа -- аоаутаердьа- продукт
J - - т а
. ; а р 16. По методике ./аая: : 4-хлор-о-аолукдик
;-ау- Лика, ло луча.ют этил-:аа- 6-метклхиноа ин-2: г т . па . 12 3-1 24 , и Nic V- а-- 4 { Р-додеди. бензилока .а Р -:ароанопу10 к-с;;оту в -а а аоаутпердао продукта. м ;-: у iP По метэдике при:ричга я а-х;1ора - И.мин змес . .:i.iaсу асаучают эакл-8ж г-.; ; а :-i с ли к - 2 - к арб оке и лат с
; Паа аС име i-:e;ia и вмесf-бенз нахлорада бекзклхлори;к т эти г -В- хлOD--4-бензилхиa )a5oKcv.лат с а „ пл , i4jч г.. г и io. по 1 етодике приpaMera-iK :1а-а;;аа;кеалилг1ропи чаг;: эти;1акаа.1адетата и tt буain EMe:i.:T(; а -толуид -на, пос 1---сго.пь:;оаа 1аем в качестве НОЙ кислоты в начальной стадии конденсации , этил-3-метил-4-окси-6-н -бутилхинолин-2-карбоксилат с т,пл. 15б--157 С и 3-метил-6-к-4-( 4-додецилбензилокси )-хинолин-2-карбоновую кислоту в виде светло-оранжевого вязкого масла. Пример 19. По методике при мера 18, применяя анилин вместо И -бутиланилина , получают этил-3-метил-4-оксихинолин-2-карбоксилат с т.пл. 175-177 -с и 3-метил 4-( 4-додецилбензилоксяхинолин-2-кар5оновую кислоту в виде светло-желтого масла Пример 20. По методике при мера 18, применяя о-толуидин вместо П -бутиланилина, получают этил-3,8-диметил-4-оксихинолин-2 карбоксила с т.пл. 133-134с и 3,8-диметил-4- (4-додецилбензилокси)-хинолин-2-карбоновую кислоту в виде вязкого светло-желтого масла. Пример 21. Хорошо перемеида ваемую смесь 65,1 вес.ч. этнл-4-оксихинолин-2-карбоксилг1та , 42 вес. ч. безводного карбоната калия 38,4 вес аллилбромида и 800 вес.ч. ацетона кипятят с обратной перегонкой в течение 24 ч. Охлажденную реакционную смесь фильтруют для удаления неорга нических солей, ацетон отгоняют в вакууме. Раствор оставшегося коричневого масла в эфире (360 вес.ч.) промывают сначала 1 н,раствором едкого натра (3 порции по 50 вес.ч.) и водой (4 порции г;о 100 вес. ч.) за тем сушат над сульфатом магния и от гоняют растворитель . Получе:-:ное вяз кое масло кристаллизуется при охлаж дении, кристаллы перекристаг.;:изовы-вают из петролейного эфира (т.кип. 60-80°С) и получают 57,1 вес.ч. эти -4-аллилоксихинолин-2-карбоксилата в виде светло-желтых игл с т.пл. 71-72 С. Хорошо перемеишваемую смесь 61,4 вес .4. этил-4-аллилоксихинолин-2-карбоксилата и 320 вес.ч. Шеллзол Т (алифатический керосин) нагревают при 180-190 С в течение 2 ч в атмосфере азота. После охлаждения реакционную смесь фильтруют и твердый продукт промывают 50 вес,ч. пет ролейного эфира и кристаллизуют из олуола. получают 49,2 sec.ч. этил-3-аллил-4-оксихинолин-2-карбоксилата в виде бесцветных игл с т.пл 146 , 5-147с . После дальнейшей очистки из этанола небольшой порции вещества получают крупные ромбические призмы с т.пл. 148,5-150 С. Найдено,%: С 69,7; Н 4,9;N 5,0. С|5 Н gNOj Вычислено,%: С 70,0; Н 5,9;Ы 5,4 Раствор 49,0 вес.ч. этил-3-аллил - 4 - ок с и X и fi ол ин-2-карбоксилата в 600 вес.ч. кипящего этанола перемешивают 5 ,мин в 3 вес. ч. Зч-могчт -;атализатора - палладий на угле. Затем его фильтруют, фильтрат вместе с 5 вес.ч. свежего катализатора загружают в автоклав из нержавеющей стали и добавляЮТ водород при комнатной температуре до давления 50 атм. После перемешивания в течение 16 ч поглощается 1,38 молей водорода. Реакционную смесь растворяют в горячем этаноле, фильтруют для удаления катализатора и выпаривают, получают 39,3 вес.ч. этил-З-н-пропил-4-оксихинолин-2-карбоксилата в виде светло-желтых игл с т.пл. 155-157с, которые отделяют и сушат, еще 4,8 вес,ч. менее чистого продукта с т.пл. 140146 С выделяют из эта нольного маточного раствора после упаривания в вакууме. После поваорной перекристаллизации из этанола получают очень светло-желтые призматические иглы с т.пл. 15 8-15 9, 5 С. Найдено , % : С 69,3; Н 6 , 3 ; К1 5,2. C. Зычи ел ено , % : С 6 9 , Ь ; Н 6 , 6 ; N 5, 4 . 3-н-Пропил-4-оксихинолин-2-карСоновую кислотч, получе:- (ую обычным способом из ее этилового эфира гидролизом кипящего 12%-:1ого раствора едкого кали с последхН :цим подкислением выделяю из 5 О-i-но го этанола в виде тонких бесцветных игл с т.пл. 194195 0 (разложение) . Найдено, -i: С 67,1; Н 5,7; N 6,2. С 12 НпчОй 1 ычислено, S : С 67,5; Н 5 , 7 ; N 6,1. Хорошо перемешиваемую смес-. 5 вес. ч, этнл- 3-н - пропил-4-оке их и н ОЛИ н - 2-кауЗоксилата , 3 вес. ч. безводного карбоната калия и 3,3 вес. ч. бензилбромнда в безЕО/iH.OM аг;етоне кипятят с обратной перегонкой 16 ч, фильтруют для даления неорганических солей ; отгоняют растворитель. Раствор оставшегося масла в- 75 в ее.ч. эЛира после промывки 1 н. раствором едкого катра (2 порции по 25 вес.ч.), затем водой (4 порции по 40 вес.ч.) сушат над су.чьфатом магния, выпаривают и получа ют 6,4 вес. ч. сырого э т -; л - 3 - н - п р о п и л - 4 - б е н 3 и л о к с и X и н о л и н -2-карбоксил та в виде очень светлого л ел т о го мае;: а. Это вещество растворяют в 32 вес. ч, кипящего этанола и х-идролизуют в течение 2 ч 5 вес.ч. 161-ного водного раствора едкого натра, затем отгоняют этанол, разбавляют 150 вес.ч. Е оды и подк; сляюг ледяной уксусной кислотой. Образовав чийся сначала маслянистый осадок медленно кристализуется при , получаКТ 5,1 вес.ч. сырого продукта с т.пл. 127-129 С, которьлй после перекристаллизации из этанола дает 3,9 вес.ч. 3-н-пропнл- 4 - 6 е н 3 и л о к с и X и н о л и н - 2 - к а р б о н о в у ю .с;1оту в виде бес цветнь х игл с
Найдено , и s С
С gjj H|q N0 J
Вычислено ; % :
N
4,4.
22. Зтил-3-н-пропилПример - 4 ок с и X и н ол и н - 2 гс ар бок с ил ат ,., no/ty ченный аналогично примеру 21,. пре:враК1ают по методике примера 3. применяя температуру обратной перегог кз з первой стадии для окончс;ния р гакции;, в 3 н - пр з п и л -J - :к л ор X и н ол и н - 2 - к а) )0 к силат в виде вязкого масла н j-i-i-пропил- 4- ( 4-ноиилфенокск ) -хкнолин-2-карбоновую кислоту в ни.це ;й:расного полутвердого тела.
Пример 23, По методиц-а примера 1,-применяя этилэтоксэлилЕалерат вместо этилксалацетата и г:нилин вместо Г( -толундипа,, получают, применяя Б-качестве каталиэат : ра в начальной стадии конденсации кесколь-ко капель соляной кислоты, З-к-пропил-- 4-оксихинолин-2-карбоксила.т ,, идентичный продукту, полученному по методике примера 21, и З-н-пр-СПил-4 ( 4-додецилбекзилокси) -хинол ин-2 карбоновую кислоту в виде вязкого светло-оранжевого масла.
Пример 24, По методике примера 21 этил 4-окск-б-н-бутилхинолик-2-карбоксилат превраш.ают в ;)ткл
-4 - аллилок си -6 - к- бу тилхи на.п кн - 2 -карбоксилат в виде коричневого вязкого масла. эткл-З-аллил-д-окол-б-н бу т 11Л хи н Оли н - 2 -к ар 5 ок с мл а т с
т „ пл , 156-l57Cf эткл-3-н-пропи/:-4-окси-б-к-бутилхиколи} -2--карбоксилат с т . пл . 1 36 1 ; З-н-пропил-6-Н бутил-4- ( 4-додеци,гбекзилокси) - :инолин- 2-карбояопую кислоту в зкда светло-желтого масла.
п р
Этил- 1-н-пропилм е D
-6-н-оксихииолии-2-карбоксила:г превращают по методике примера 22 в э тил- 3 - н-пропил- б - н -- буткл- 4 -хл орхи н о л н - 2 - к а р бокс к л а т т . п л ., 4 3 ., 5 -44 С и 3-н-пропил б--н-6уткл -4 - 4- н они л ф - н ок СИ) -- хи н ол i-i н - 2 к а рбо н о в ую кислоту в виде ЕЛЗКОГО коричневого масла,
Пример 26. По методике а 2 J. э : к л --б - н - бу т к.п 4 - ок с и х к н олин-2-карЗГКсилат преоращают с ломощью и зодецилб:)омида вместо аллилбромида в этил--;,-изо,г:е11;клокси-6-н-бутилхинол-ш 2 -кароокси 1ат в ;эиде вязкого коричневого масгта м 4-ИЗодецил-окси-6-н-бутилхг-;нолин --2 --каибоновую кислоту в виде полутвнрдого продукта кремового цвета.
Пример 27. Зтил 3--н-пропил-6-н-бутил-4-окслхинолин 2--карбок силат превращают по методике примера 26 в этил-,-н- пропил--6-к-бутил-4-иэодецилоксихинолин-- 2-карбокс ллат , 3 -н-пропил - b -н - бутил- 4-из одеци локс ;з{Инолин-2--карбоксклат и 3-н-пропил-5 - :: -О:/ :;и;- -- :.-:Зг;;-е1и-Локсихинолин 2-карбонозуз кислоту з виде светлой:е-гп ого зязчого масла.
П р и м ер 28„ По методике примера 23, применяя зтоксалклфенклаце-тат вмест-о этилэтоксалилвалерата и rt -бутиланилин вместо анилина получают ЗТИЛ- 3-фенил-4-окси-6-н-бутилхннолин- 2- ,арбоксилат с т . гш . 164165с и 3--фенил-6-н-буткл-4-( 4-додетдилбензилокси ) -хинолин-2 карбс1новую кислоту Б змде вязкого коричневого ма ел а .
п р м м 3 р 29 По методике примера 28, применяя :-тилэтоксалилбензиладетат вместо зтилэтоксалилфенилацетата , получают этил-З-бенэил-6ил- 4 --ОКСИХИНОЛИН-2-карбоксилат
с т.пл. 163,5-164, и З-бензил-6--Н бутил-4- ; 4-додецилбензилокси) -хинолик--2--карОоновую кислоту в виде вязкого желто-оранжевого масла.
П р и м е р 30. По методике примера 1., применяя н-иэодециланилин вместо п--толуидина, получают этил-6-и э одецил-4-ок си хи н ол ин-2 карбоксилат в виде очень вязкого коричневого масла и б-нэодецил-4-( .-додецилок си бен зил) -хинолин-2-карбоновую кислоту в виде вязкой коричневой смолы.
П р и м е р 31. Этил-6--Хлор-4 оксихин-олин-2-карбоксилат превращают по методике примера 1 Е б-хлор-4- (4-додецилбенэилокси) - Хкнолин-2-карбоновую кислоту в виде вязкого светло-коричневого масла.
Интеноивко перемл хлороформенX 10
растаора, содержащего О
г -
МОЛИ хкнолип-2-карбоновой кислоты (лиганд) , и 25 водного кислого раствора соответствующего металлического иона (0.25 к мол я для
,-S двухвалентного металла; О, 1667 к 10 моля для трехвалентного металла), содержащую также О . .2 5 « 10моля надхлоркой кислоты, титруют потен диометрическя л г раствором едкого натра. Такой ие -опыт проводят, применяя 25 i-.U чистого хлороформекного р астворите 1Я , По разнкие между двумя кривыми TSiTpoasHMH рН определяют процент образовавшегОси комплекса между лигаидом к даннык ионом металла для .-диапазона рК (2:1 лиганд/металл - стехиометрия для двухвалентного металла; 3; J. - для трехвалентного металла); третья кривая построена дл зависимости npotieHTa комплекса от рН, По этой последней кривой определяют величину Ph.-j. Зта величина считается как рН, при котором образуется 50% наблюдаемого (не теоретического ) комплекса.
Во Е-сех растворах металлов прис у т с; т в ж т с у л ь ф а 7 -- и о ны , так как их по.,чают из соотБ етстяую;аих сульфатов металлов. Однако при применении железа (П иИх) и алюминия имеются также ионы аммония, поскольку приме няются двойные соли металла и аммония . Результаты даны в табл.1, при этом в приведенных в таблице примерах т качестве действующего начала применяете я хинолин-2-карбоновая кислота. Пример 33. 100 мл 3,13%-но го раствора 6-метил-4(4-додецилбен зилокси)-хинолин-2-карбоновой кисло ты в перхлорэтилене (концентрацья эквивалентна концентрации кобальта 2 г/л) интенсивно nepeMeinj-iBaiCT при в течение 10 глин с тремя после довательными порциями раствора суль фата тяжелого металла в разбавленно серной кислоте сначала при pi; 2,0, в котором начальная концентрация ко бальта и железа (II) составляет 2,0 г/л, концентрация цинка и меди 0,2 и 0,05 г/л соответственно, затем им дают разделиться. Концентрацию ионов металлов в трех водных растворах после экстракции (раоинаты ) определяют атомным noi ло1дением. Органические слои, содержащие ме таллы, снова промывают порциями по 25 мл разбавленной серной :.;ислоты ,в которой концентраци - серной к;-,с;.г;о ты составляют 10 и 150 г/л сос-ветственно , концентрации металла в дьух полученных кислотных экстрактах опре деляют по ЯМР. Результаты приведены в табл.2. Эти данные показывают лyчiJJyю избирательную обратную промь;вку кобал та и цинка по сравнению с медью гч в меньшей степени железа (11) ;--:з содеркаци:-; металл лигандных растворов слабой серно;-, кислотой (10 г/л), чем крепкой серной кислотой (i50 г/л Пример 34. 25 мл раствора сульфата кобальта и разбавлекной серной кислоты сначала при рН 2 при концентрации кобальта 2 г/л интенсив но перемешивают при комнатной температуре в течение 5 мин с тремя последовательными порциями по 2Ь мл 3, раствора 6-н-бутил-4-( 4-додецилбензилокси ) -хинолин-2-кэ-рбоновой кислоты в 1 еллзоле Т (концентрационный эквивалент концентрггции кобальта 2 г/л) и дают разделить ся. Содержание метг;лла и рН водной фазы определяют после каждого смешения и разделения. Результаты приведены э табл.З.
Пример Зь . Повторя от методику примера 33, применяя 3,42%--ный раствор 6-н-бутил-4-(4-додецилфенокси )-хинолин-2-карбоновой кислоты в Шеллзоле Т при комнатной температуре .
Результаты приведены в табл.4.
р 39. 50 мл 2,65%-ноП р к f. е 6 -.ч-бутил-4-( 2-трет . буго jiacTBOoa
I хни олин- 2-карТИ .П - ч -метил фенокси в Шеллзоле Т
бонозой кислоты в нцентрацин кобальта Результаты показывают, что слабая серная кислота (10 г/л) дает лучшее избирательное обратное вымывание кобальта и цпнка, чем меди и в «елезо (III) из лиганменьшей степени дных оастворов, чем крепкая кислота ( 13С г/л) . П р и м е р 35. Повторяют методику npvnepa 34, пр -:меняя 50 мл растзора сульфата кобальта (2 г/л) при рН 2,0 Т 4г55й-ного раствора 5--ь-5чг:-::л-4 ( -.--конмлфенокси) -хинолин-2-карбоновой х 1слоты в перхлорэтилене (эквквалентгю 3 г/л кобальта). езульта: р:: приведены в табл.5. Пример 37. Порцию 50 мл 3,СЗ-;-:-ого раствора 6-г-бути.г;-4-( 4-нонилфенохси )-хинолин-2-карбоновой кислоты в Миеллзоле Т (эквивалент40 концентрации кобальта 2 г/л) инт: : синно перемешивают при комнатной .--|ературе s течение 5 мин с тремя госле,доЕательньм; по 50 мл раствора сульфатов тяжелых металлов 3 - гсбавленной серной кислоте при рН 2, в котором первоначальная конце: трация кобальта составляет- 2 г/л, а концентрация железа ( .I и III } , цинка и меди, соответстэенко , 1,56, 0,44, 0,2 и 0,05 г/л. Пос.-с разделен:: я концентрацию метг .л.г;ов S трех водных рафинатах опрела ел я ю т по атом:-; ол :у п о г .ч о щ е н и ю . Содер ка1;ин металлы органический раствор разх оляют на две порции равного объег-г; о/дич из низ хорошо промъ1-- д:от в течение 5 мин 25 мп серной кислоты (30 г/;;), а вторую также сс1;абатыБают серной кислотой (15 С r/;i) ; концентрацию металла в осо;:х кислот;-; ;-: про; 1ыкках определяют г;С no; omcHii: J , Рсз/льтаты анализов приведены в таЗл . б . Л р и м ер 33. 25 мл 16,88%-ного раствора. 6- -:-бутн;1-4-( 4 нонилфенокси )-ХИНОЛИН--2-карбоксилата в 11еллзоле Т (экзиБалентно концентрации ме, 12 г/л) перемешивают в течение 5 ; гп:-: с тремя последовательными порция .и по 25 bin раствора сульфатов тяж-з..ых металлов в разбавленной серной кислоте, снача.-.а при рН 2, в которых исхсднач СО;;:;с гграцня меди сосгг;злпет 11,25 г.-л, концентрация железа (III) н кобальта - 0,25, коние:г7рацня цинка - 0,05 г/л, затем ают раздел :ться . Органическую фазу ромывают 2S i.v серной кислоты крепостью 150 г/л. Концентрацию метал;ов Б трех водных рафинатах и. в сер;лотных прог-алЕках определяют по
2 г/л) смешивают при КОМИОГЕ-ЮЙ I-SIMпературе в течение 10 ми ;: последовательными порциями по 50 мл раствора сульфатов тяжелыу. металлов в разбавленной серной кис:иоте сн; ча-ла при рК 2f Б котором исходная коч-центрация кобальта и железа (ИП составляет 2 г/л . а цинка - л1е;1и - и 0,05 г/л соочиетсплачпо , Пос;:1 разделения концентрацию i-.C:. е ап-лов в трех водных рафии этэ::1 ог;;-ед е ЛЯ ОТ по атомному ПОГ ЮГцСПИК: ,
Органический слой lipo UBa-гот юопедояательно аорг.иями не 50 глл разбавленной сергзоя .ci-jcj:oi-;: : с концентраи .ией 30 i-/j. :/; 150 г/,п СОСТБЁТственно , концентрацию MeiJia.nsi ч кис-лоткых экстрйктазс слрадет люг пс iTOr--;ному поглощению„
Результаты прИгэддень и табл„о
Пример 40, noBTOpKiOT f/cj;o-. дику примера 39., применяя б-п-еутил-4™ { 2-трет . бутил- 5-метилфенокеи ) -хкколин 2 карбоковую кислоту.
Результаты приведены в табл,9.
Пример 4 1 „ Повторяют г.е :одику примера 39, применяя 3,1%-ный раствор б н-бутил-4- ( 2, 4--Л 5-тре т . пентклфенокоихиноликJ 2--карбоновоЛ кис-лоты 3 111елпзоле Т ( эквив ал i HTFJO комиентрации коба;зьта 2 г ./л; .
Результаты привецань; э ;абл„1(1.
Пример 42,: ..пт :.с::оцкку примера -39. применят-. ;131- Ьй раствор 4 S 6 ( 4-нонилфе;-к;кс1 ; -Х1г;-к;лкн-2--карбоноБОй ккс;ю7Ь1 я .ппзоле Т ( зквиналемтчо и г;н :ектпа;1ии кобальта 2 г/л) „
Результаты ривепены в :-a6ji 11..
Пример 13, :30 мл . 2 .: 4--::охО раствора 4 , б-ди™ 4-но:г лфе;Юкс--) --хи нолин 2 карбоновой KHc;noTrv я ;1еглзоле ( эквязалектно iCOH .лйи:-ра:...ии кобальта 5 г/л) интенси.в но теремешизают при комнатной температуре в течение 3.0 мик с тремя поо;1едона:.ель«ьгли псрция:/;к по 150 мл раствора су.п.ьфзтоз ТЯжелЫл металлов в р-а збагитен ной оерной кислоте при рН 2- в когором исходная конлектрацля кобальта и желе;:з (П) составляет 2 P/J;, .динка и Г4едр --- О.. 2 г/л х п.СБ .г-/л соответственно . Лссле разделения хояцектрацик ионов :.;с 1 :-;-;:са ;з золдгнпх рафянатах опре.де.1.- . по : - омном;, Х)гло-щению о
« Органический рас твое, сс цер алчий металлы, разделлкд ка , час-о- равного объема; одну :з :г:х .О промывают 3 течение 5 м:.-;- 25мц серчо:; кислоты крепостью 30 , а иторую также обрабатывают сер:- 0й кислотой крепостью 150 г/л; концекчрациг:; 1Ле талла Б обек:к кислотных промывках определяют яо атоиному ,пог-лс- де1- К10 Результат;- прязедены а тз6л.Л2, П р и wi е р 44, Повторяют йШгодику примера 3Sf применя. л б ,
ivacTBtip ti--Mei скск-4- ( 4-додецилбекэклолси ) --хино :ип 2-КЗ рб о и оной кислоты 11 хлирофор1-.1е (зквк валентно кониентРЙП .ИИ меди 11,25 г/;) .
Результаты приведены в табл , 13 ,
Пример 45. 25 мл 3,13%-HOго ра(;твс5ра 8-метр;л 4-( 4-додецилЬензилокси ) хииолин-2-карбоновой кислоты в с.пороформе (-кривалентно концанграп .ии коба- Ьга 2 г/л) теремешивают гри комнатной температуре в течение 10 с; 25 мл раствора буферированчот-о при рН 5,0 с помощью ацетата naTpMH/vKc-yrniaa кислота, в котором ,- сходная кспцентра ция меди составля ;т 2 г/л, кобальта. 0,2 г/л, железа Л и III i 0,1 г/п. цинка 0.02 г / л ,
Пос;1е отделе1- ия концентрацию ионо ьтетал.ссБ в водном раЛинате опоеделя;от aTOMHNivi поглощением .
Ортанитеский слой, содержаиий металлы , промывают обратн-ой про- ывкой 25 мл разбав тенной серной кислотк -150 /л); кс1нцентрацию метал .лов в кислотном экстракте определяют методом атомного г-оглоцеЕ-1ИЯ .
Резуль-а 1-, приведены в табл.14.
П р и м е р if,. Повторяют ме7О дику примера 45, применяя раствор, lie содер ка::г-й меди, при этом концентг ацли же.1еза ( II у. } ,. кобальта и цинка га1чие же.
Резу.1П)Тат-гд; приЕ;едень Е табл. 15
:i р и м р 47, 25 мл 3,8 2%-него раствора 8-мeтиJ -4 - ( 4 чонилфенокси) --ХИНОЛИН-2-карбоноЕой кислоты в хлоооформе ( экги палоьтно онцен-ра ши г-1е.ли 3 V/M; перемешиваю- - при комнатной температ ре ь течение 10 мин с 25 мл рд ::г-: ;;;а ,, буферированного при г; 4гС, с омощью ацетата натрия/ук-суснзя кис-:ста. в котором исходная чонпент1)аци F меди составляет 2 г/л, кобальта 0,2 г/л, лселеза (И и 1П ) 0,1 г/л г цинка 0,02 г/л. После отде )гения концерт рацин) ионов металлов в вещных рафинатах сшределяют атомным поглощением,
Орга1- ический с/Ой, содержащий месаллы , последоват5:льно промывают 25 мл разбавленной серной кислоты крепо-стью - 5С г/л; конц.ентр,адию .егалло 3 jii кислотном экстракте опреде .пппт атомным поглощением,
Оргаг-ический CJ-iO , содержаший меаллы , затем про шгвают 25 ;лл разбавленной серной кислоты (150 г/л). Кон:1:ентрацц 0 ;-;еталла Б кислотных вытяжках определяют атомньзм поглощением.
Результаты приведены в табл.16.
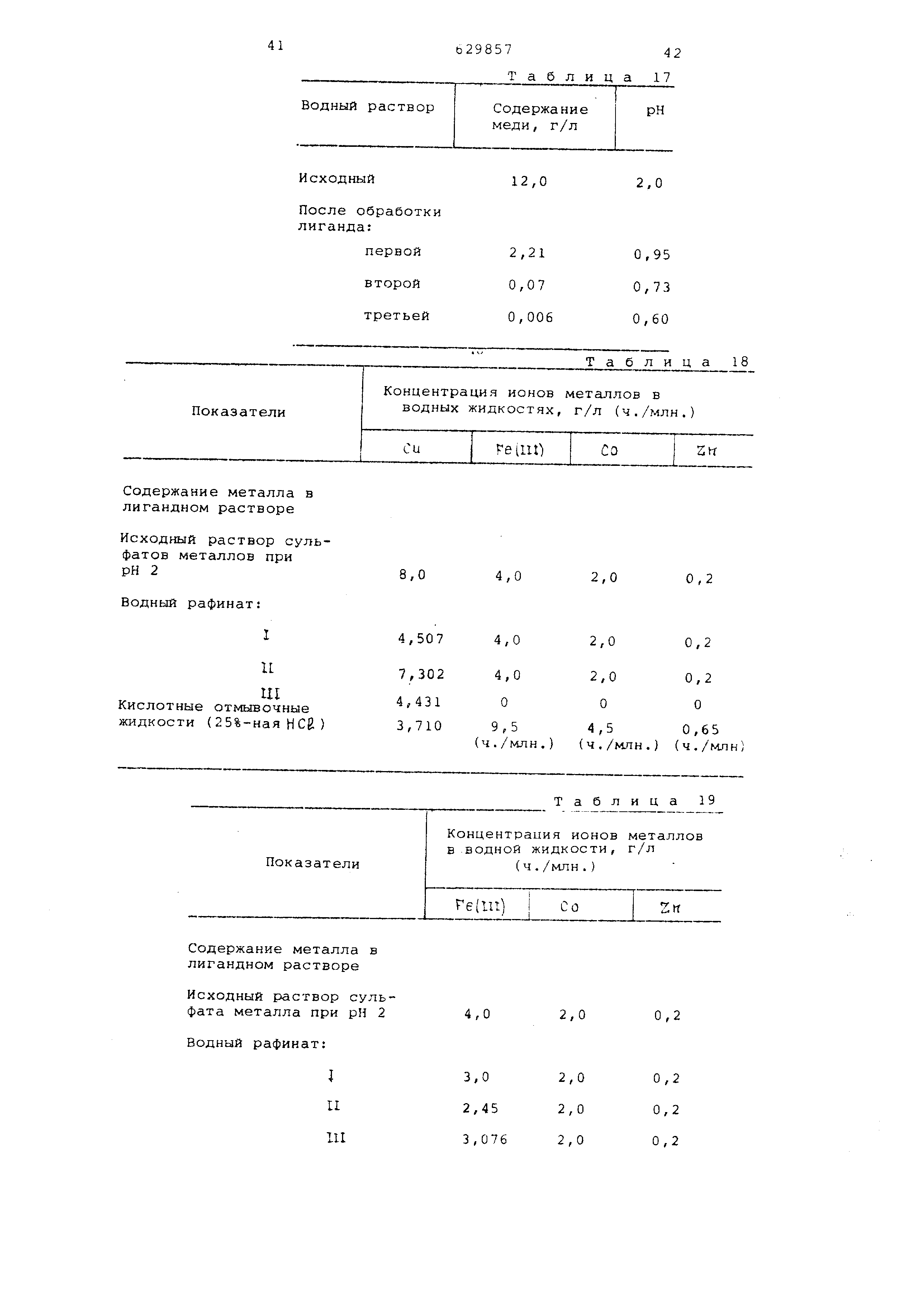
П р и ) е р 4 е,, 25 мл рас:твора сульфата меди в разбавленной серной кис,поте при рН 2fO при концентрации меди л 2 г/я схгешквают с тремя последовательньЕ 1И порциями по 25 ivLn -й,11%-кого раствора З-н-цропил-6 (изодецчлхинолин) --2-карбоновой кислоты в Эскайде 110 (алисратнческий керосин; экзивалентно концентрации меди 12 г/л) при комна ной температуре по 5 мин. После разделения концентрацию металлов и рН водной фазы определяют после каждого смешения. Результаты приведены в табл.17, Пример 49. 25мл 5,37%-ного раствора 3-н-пропил-6-н-бутил-4-изодецилоксихинолин-2-карбоновой кислоты в Эскайде 110 {эквивалентно концентрации меди 4 г/л) смешивают в течение 10 мин с тремя последовательньоми порциями по 25 мл раствора сульфата тяжелого металла в разбавленной серной кислоте при рН 2, в котором исходная концентрация меди, железа (1П) , кобальта и цинка состав ляет 8,0, 4,0, 2,0 и 0,2 г/Л соответственно . После разделения концентрацию ионов металлов в трех водных рафинатак определяют атомньлм поглощением . Органический слой, содержащий ме-таллы , рнова промьшают 25 мл 25%-ной (вес/объем) соляной кислоты. Концентрацию ионов металлов в кислотных отг сявочных жидкостях определяют атомным поглощением. Результаты приведены в табл.18. Пример 50. Повторяют методику примера 49 с раствором, не содержащим меди, но подобным раствору примера 49 . Результаты приведены в табл.19. Таблица 1





















Реферат

Формула


Комментарии