Фармацевтические композиции - RU2532330C2
Код документа: RU2532330C2
Описание
Область техники
Данное изобретение касается фармацевтических композиций, полезных для лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета. В частности, данное изобретение касается фармацевтических композиций, включающих комбинации ингибиторов SGLT2 и, по меньшей мере, одного средства, выбираемого из группы, состоящей из бигуанидов, средств, усиливающих секрецию инсулина, усилителей чувствительности рецепторов к инсулину, инсулинов, ингибиторов дипептидилпептидазы IV, ингибиторов α-глюкозидазы и миметиков GLP-1.
Уровень техники
Сахарный диабет представляет группу заболеваний, в основном характеризующихся хронической гипергликемией, вследствие недостаточного действия инсулина, и сопровождается различными метаболическими отклонениями. Первичное лечение сахарного диабета состоит в физических упражнениях и диетотерапии; если указанные методы не способны обеспечить адекватный гликемический контроль, тогда проводят терапию пероральными противодиабетическими средствами. Однако, в зависимости от состояния больного диабетом, лечение всего одним лекарственным средством иногда встречает трудности в достижении хорошего гликемического контроля, и, что еще важно, развитие побочных эффектов препятствует применению лекарства в адекватной дозе или на протяжении адекватного периода времени. Согласно одному из сообщений в литературе, бигуанид, применяемый лишь один больными диабетом типа 2, дает всего около 25% вероятности снижения значения гликозилированного гемоглобина (HbAlc) до 7% или менее (см. НПЛ 1). Известно также, что если использовать лишь только одну сульфонилмочевину, побочные эффекты, такие как развитие гипогликемии и увеличение массы тела, являются не единственными проблемами, и что нормализующее действие сульфонилмочевины при гипергликемии становится неадекватным для пациентов, у которых способность секретировать инсулин ухудшена недостаточностью бета-клеток в связи с прогрессированием диабетического состояния. Также известно, что если используют один только усилитель чувствительности рецепторов к инсулину, возникает проблема эпизодического развития таких побочных эффектов, как увеличение массы тела, отек, сердечная недостаточность и болезнь печени. Известно также, что если используют один только инсулин, возникают проблемы гипогликемии и увеличения массы тела. Также известно, что если используют один только ингибитор α-глюкозидазы, в качестве побочных эффектов возникает проблема эпизодического развития абдоминальных симптомов. Кроме того, когда используют один только миметик GLP-1, в качестве терапевтических проблем известны тошнота и рвота. Также известно, что больные диабетом типа 2, когда подвергаются гипергликемическому состоянию длительный период времени, имеют понижение функции бета-клеток; однако, большинство противодиабетических средств неспособно к адекватному подавлению понижения функции бета-клеток, даже если уровни глюкозы в крови являются пониженными.
В качестве средства решения вышеупомянутых проблем, связанных с лечением отдельными лекарственными средствами, рассматривается комбинированная терапия с применением комбинации противодиабетических средств, действующих по различным механизмам. Однако немногие комбинации способны предупредить вышеуказанные проблемы, связанные с применением отдельных лекарственных средств. Например, известно, что риск развития гипогликемии, выявленного побочного эффекта сульфонилмочевин, дополнительно возрастает при использовании сульфонилмочевин в комбинации с другими противодиабетическими средствами. Кроме того, увеличение массы тела, признанное за сульфонилмочевинами и усилителями чувствительности рецепторов к инсулину, обычно нельзя контролировать путем использования указанных средств в комбинации с другими противодиабетическими средствами. Следовательно, востребованной является новая комбинация множественных фармацевтических лекарственных средств, способная достигнуть хорошего гликемического контроля, не вызывая при этом заметных побочных эффектов.
Глюкоза в крови фильтруется в клубочках каждой почки и затем реабсорбируется, опосредованная натрий-зависимыми котранспортерами глюкозы (SGLT), расположенными в начале проксимальных канальцев. Ингибиторы SGLT2, типичным представителем которых является соединение 1-тио-D-глюцитола (см. ПЛТ 1), ингибируют активность SGLT2, обладающего низким сродством к глюкозе, но высокой способностью к транспорту глюкозы, так, указанные ингибиторы оказывают действие по снижению уровня глюкозы в крови в моделях на животных, стимулируя выделение глюкозы с мочой.
Недавно сообщалось, что побочные эффекты усилителей чувствительности рецепторов к инсулину могут быть снижены путем комбинирования указанных усилителей с ингибиторами SGLT2 (см. ПЛТ 2), но отсутствуют сведения о фармацевтической композиции, комбинирующей ингибитор SGLT2 с усилителем чувствительности рецепторов к инсулину в целях обеспечения действия по снижению повышенных уровней глюкозы в крови. Существует также литература, сообщающая о комбинированном использовании ингибитора SGLT2 и ингибитора дипептидилпептидазы IV (см. ПЛТ 3 и 4). Однако не было никакого сообщения о фармацевтических композициях такого типа, как рассматриваются данным изобретением, включающих комбинации ингибиторов SGLT2 с, по меньшей мере, одним средством, выбираемым из группы, состоящей из бигуанидов, средств, усиливающих секрецию инсулина, усилителей чувствительности рецепторов к инсулину, инсулинов, ингибиторов дипептидилпептидазы IV, ингибиторов α-глюкозидазы и миметиков GLP-1.
Список ссылок
Патентная литература
ПЛТ 1: Официальное издание международной публикации WO 2006/073197 A1
ПЛТ 2: Официальное издание патента EP 1381361 B1
ПЛТ 3: Официальное издание международной публикации WO 2009/022007 A1
ПЛТ 4: Официальное издание международной публикации WO 2009/022010 A1
Непатентная литература
НПЛ 1: Tonyobyougaku (Kiso to Rinshou) [Diabetology (Fundamentals and Clinical Applications)], pp.949-954, 2007, Nishimura Shoten
Краткое описание изобретения
Цель данного изобретения состоит в разработке новой фармацевтической композиции, включающей комбинацию множества лекарственных средств, обладающей исключительной эффективностью в предотвращении или лечении сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета и не вызывающей при этом заметных побочных эффектов.
Другая цель данного изобретения состоит в разработке способа предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета с использованием фармацевтической композиции.
Было обнаружено, что введение соединения 1-тио-D-глюцитола, обладающего ингибирующим действием в отношении SGLT2, или фармацевтически приемлемой соли указанного соединения, либо гидрата соединения или соли, в комбинации с, по меньшей мере, одним средством, выбираемым из группы, состоящей из бигуанидов, средств, усиливающих секрецию инсулина, усилителей чувствительности рецепторов к инсулину, инсулинов, ингибиторов дипептидилпептидазы IV, ингибиторов α-глюкозидазы и миметиков GLP-1, вызывает заметное действие по снижению уровней глюкозы в крови, подавление недостаточности панкреатических β-клеток и облегчение побочных эффектов; данное изобретение выполнено на основе указанного открытия.
Таким образом, в данным изобретении предложено следующее:
(1) Фармацевтическая композиция, включающая комбинацию
(A) соединения 1-тио-D-глюцитола, представленного общей формулой (I)
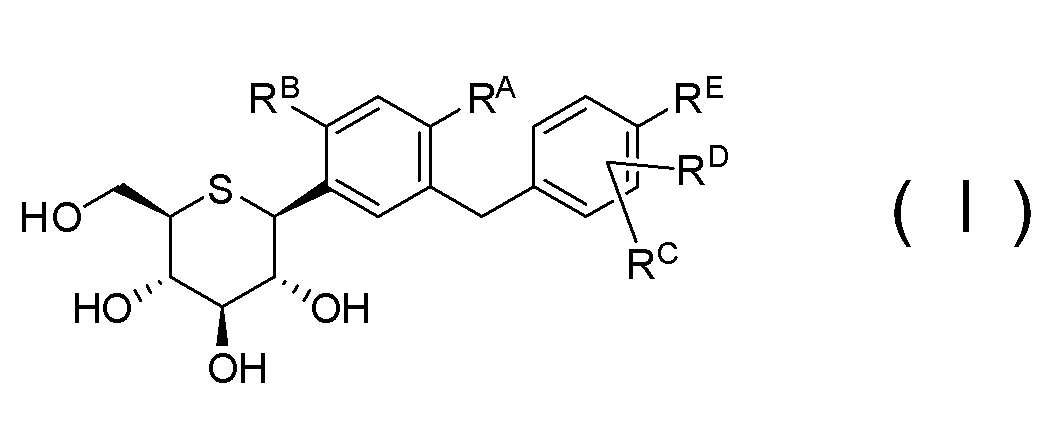
[где RA означает атом водорода, C1-6-алкильную группу, -ORF или атом галогена;
RB означает атом водорода, гидроксильную группу или -ORF;
RC и RD могут быть одинаковыми или различными, и каждый означает атом водорода, атом галогена, C1-8-алкильную группу или -ORF;
RE означает (i) атом водорода, (ii) атом галогена, (iii) гидроксильную группу, (iv) C1-8-алкильную группу, необязательно замещенную атомом галогена (атомами галогенов), (v) -ORF или (vi) -SRF;
RF означает C1-6-алкильную группу, необязательно замещенную атомом галогена (атомами галогенов)], или фармацевтически приемлемой соли указанного соединения, либо гидрата соединения или соли, и
(B) по меньшей мере, одного средства, выбираемого из группы, состоящей из бигуанидов, средств, усиливающих секрецию инсулина, усилителей чувствительности рецепторов к инсулину, инсулинов, ингибиторов дипептидилпептидазы IV, ингибиторов α-глюкозидазы и миметиков GLP-1.
(2) Фармацевтическая композиция по (1), включающая комбинацию
(A) соединения 1-тио-D-глюцитола, представленного общей формулой (I)
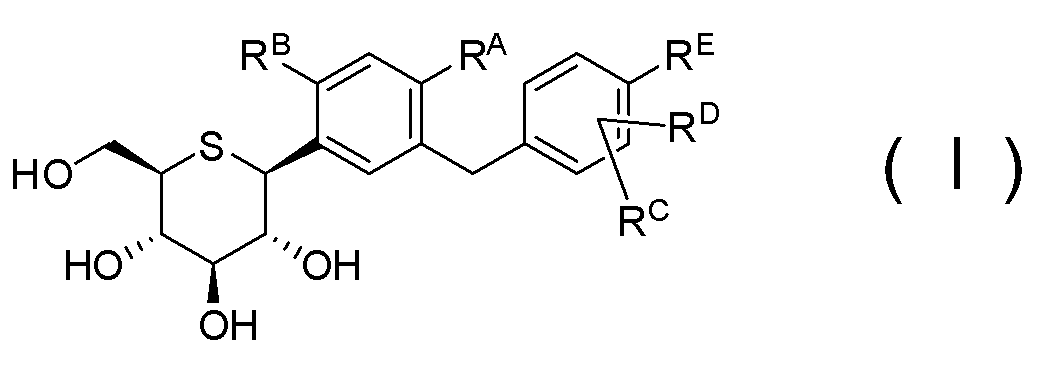
[где RA означает атом водорода, C1-6-алкильную группу, -ORF или атом галогена;
RB означает атом водорода, гидроксильную группу или -ORF;
RC и RD могут быть одинаковыми или различными, и каждый означает атом водорода, атом галогена, C1-8-алкильную группу или -ORF;
RE означает (i) атом водорода, (ii) атом галогена, (iii) гидроксильную группу, (iv) C1-8-алкильную группу, необязательно замещенную атомом галогена (атомами галогенов), (v) -ORF или (vi) -SRF;
RF означает C1-6-алкильную группу, необязательно замещенную атомом галогена (атомами галогенов)], или фармацевтически приемлемой соли указанного соединения, либо гидрата соединения или соли, и
(B) бигуанида, средства, усиливающего секрецию инсулина, или усилителя чувствительности рецепторов к инсулину.
(3) Фармацевтическая композиция по (1) или (2), где (A) означает соединение 1-тио-D-глюцитола, представленное общей формулой (I),
в которой RA означает C1-6-алкильную группу или атом галогена;
RB означает атом водорода, гидроксильную группу или C1-6-алкоксигруппу;
каждый из RC и RD означает атом водорода;
RE означает C1-6-алкильную группу, C1-6-алкоксигруппу или C1-6-алкилтиогруппу.
(4) Фармацевтическая композиция по любому из (1)-(3), в которой соединение 1-тио-D-глюцитола выбирают из группы, состоящей из:
(1S)-1,5-ангидро-1-[5-(4-этоксибензил)-2-метокси-4-метилфенил]-1-тио-D-глюцитола;
(1S)-1,5-ангидро-1-[4-хлор-3-(4-метилбензил)фенил]-1-тио-D-глюцитола;
(1S)-1,5-ангидро-1-[4-хлор-3-[4-(метилсульфанил)бензил]фенил]-1-тио-D-глюцитола;
(1S)-1,5-ангидро-1-[4-хлор-3-(4-этилбензил)фенил]-1-тио-D-глюцитола;
(1S)-1,5-ангидро-1-[5-(4-этилбензил)-2-метокси-4-метилфенил]-1-тио-D-глюцитола;
(1S)-1,5-ангидро-1-[4-хлор-3-[4-(пропан-2-ил)бензил]фенил]-1-тио-D-глюцитола;
(1S)-1,5-ангидро-1-[2-метокси-4-метил-5-[4-(пропан-2-ил)бензил]фенил]-1-тио-D-глюцитола и
(1S)-1,5-ангидро-1-[4-хлор-5-(4-этилбензил)-2-метоксифенил]-1-тио-D-глюцитола.
(5) Фармацевтическая композиция по любому из (1)-(4), в которой соединение 1-тио-D-глюцитола представляет собой (1S)-1,5-ангидро-1-[5-(4-этоксибензил)-2-метокси-4-метилфенил]-1-тио-D-глюцитол.
(6) Фармацевтическая композиция по любому из (1)-(5), в которой бигуанид представляет собой метформина гидрохлорид.
(7) Фармацевтическая композиция по любому из (1)-(5), в которой средство, усиливающее секрецию инсулина, представляет собой глипизид, глибенкламид или глимепирид.
(8) Фармацевтическая композиция по (7), в которой средство, усиливающее секрецию инсулина, представляет собой глипизид.
(9) Фармацевтическая композиция по любому из (1)-(5), в которой усилитель чувствительности рецепторов к инсулину представляет собой пиоглитазон.
(10) Фармацевтическая композиция по любому из (1) и (3)-(5), в которой ингибитор дипептидилпептидазы IV представляет собой ситаглиптин или вилдаглиптин.
(11) Фармацевтическая композиция по любому из (1) и (3)-(5), в которой ингибитор α-глюкозидазы представляет собой воглибозу, миглитол или акарбозу.
(12) Способ предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета, включающий введение нуждающемуся в такой терапии пациенту, либо одновременно, либо раздельно:
(A) соединения 1-тио-D-глюцитола, представленного общей формулой (I)
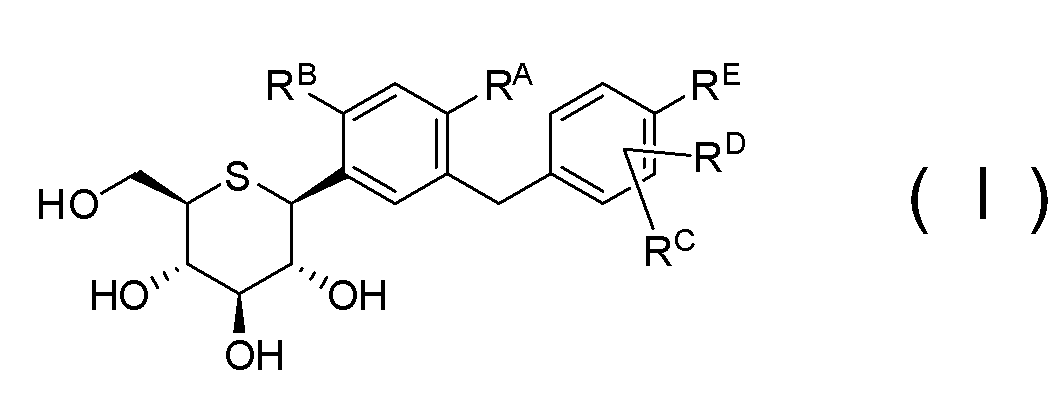
[где RA означает атом водорода, C1-6-алкильную группу, -ORF или атом галогена;
RB означает атом водорода, гидроксильную группу или -ORF;
RC и RD могут быть одинаковыми или различными, и каждый означает атом водорода, атом галогена, C1-8-алкильную группу или -ORF;
RE означает (i) атом водорода, (ii) атом галогена, (iii) гидроксильную группу, (iv) C1-8-алкильную группу, необязательно замещенную атомом галогена (атомами галогенов), (v) -ORF или (vi) -SRF;
RF означает C1-6-алкильную группу, необязательно замещенную атомом галогена (атомами галогенов)], или фармацевтически приемлемой соли указанного соединения, либо гидрата соединения или соли, и
(B) по меньшей мере, одного средства, выбираемого из группы, состоящей из бигуанидов, средств, усиливающих секрецию инсулина, усилителей чувствительности рецепторов к инсулину, инсулинов, ингибиторов дипептидилпептидазы IV, ингибиторов α-глюкозидазы и миметиков GLP-1.
(13) Способ предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета по п. (12), включающий введение нуждающемуся в такой терапии пациенту, либо одновременно, либо раздельно:
(A) соединения 1-тио-D-глюцитола, представленного общей формулой (I)
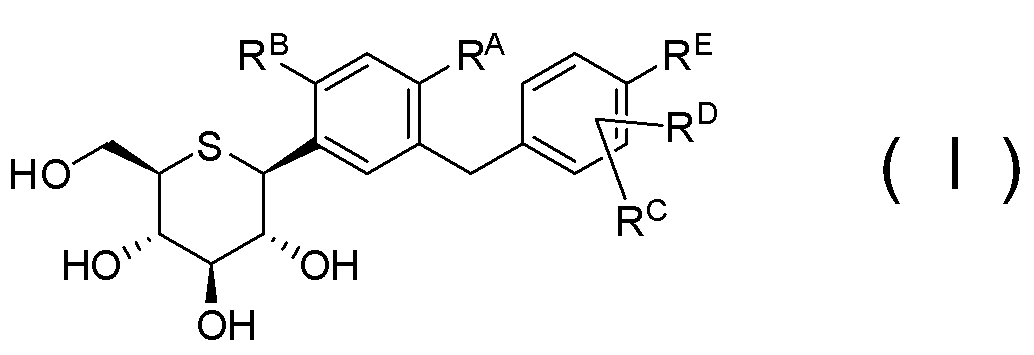
[где RA означает атом водорода, C1-6-алкильную группу, -ORF или атом галогена;
RB означает атом водорода, гидроксильную группу или -ORF;
RC и RD могут быть одинаковыми или различными, и каждый означает атом водорода, атом галогена, C1-8-алкильную группу или -ORF;
RE означает (i) атом водорода, (ii) атом галогена, (iii) гидроксильную группу, (iv) C1-8-алкильную группу, необязательно замещенную атомом галогена (атомами галогенов), (v) -ORF или (vi) -SRF;
RF означает C1-6-алкильную группу, необязательно замещенную атомом галогена (атомами галогенов)], или фармацевтически приемлемой соли указанного соединения, либо гидрата соединения или соли, и
(B) бигуанида, средства, усиливающего секрецию инсулина, или усилителя чувствительности рецепторов к инсулину.
(14) Способ предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета по п. (12) или (13), где сахарный диабет представляет собой диабет типа 2.
(15) Способ предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета по любому из пп.(12)-(14), где осложнением сахарного диабета является диабетическая ретинопатия, диабетическая невропатия, цереброваскулярное расстройство, ишемическая болезнь сердца или болезнь периферических артерий.
Полезные эффекты изобретения
Фармацевтическая композиция по данному изобретению, включающая множественные фармацевтические лекарственные средства, проявляет исключительное действие по снижению значения гликозилированного гемоглобина (GHb) и действие по снижению уровня глюкозы в плазме по сравнению с отдельными лекарственными средствами. Вдобавок, фармацевтическая композиция по данному изобретению, включающая множественные фармацевтические лекарственные средства, подавляет снижение уровней инсулина в плазме, которое может происходить при прогрессировании диабетического состояния. Кроме того, фармацевтическая композиция по данному изобретению, включающая множественные фармацевтические лекарственные средства, облегчает побочные эффекты отдельных лекарственных средств (т.е. увеличение массы тела и гипогликемию).
Описание вариантов осуществления
“C1-6-алкильная группа” означает линейные или разветвленные алкильные группы с 1-6 атомами углерода и может быть представлена такими характерными группами, как метильная группа, этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, изобутильная группа, трет-бутильная группа, втор-бутильная группа, н-пентильная группа, трет-амильная группа, 3-метилбутильная группа, неопентильная группа и н-гексильная группа.
Характерными примерами “атома галогена” являются атом фтора, атом хлора, атом брома и атом иода.
Характерными примерами “фармацевтически приемлемой соли” являются: соли с неорганическими кислотами, такими как серная кислота, хлористоводородная кислота, бромистоводородная кислота, фосфорная кислота и азотная кислота; соли с органическими кислотами, такими как уксусная кислота, щавелевая кислота, молочная кислота, винная кислота, фумаровая кислота, малеиновая кислота, лимонная кислота, бензолсульфоновая кислота, метансульфоновая кислота, п-толуолсульфоновая кислота, бензойная кислота, камфорсульфоновая кислота, этансульфоновая кислота, глюкогептоновая кислота, глюконовая кислота, глутаминовая кислота, гликолевая кислота, яблочная кислота, малоновая кислота, миндальная кислота, галактаровая кислота и нафталин-2-сульфоновая кислота; соли с одним или несколькими ионами металлов, такими как ион лития, ион натрия, ион калия, ион кальция, ион магния, ион цинка и ион алюминия; и соли с аминами, такими как аммиак, аргинин, лизин, пиперазин, холин, диэтиламин, 4-фенилциклогексиламин, 2-аминоэтанол и бензатин.
Соединения по данному изобретению могут существовать в виде различных сольватов. Указанные соединения могут также представлять собой гидраты, в свете приемлемости таких соединений в качестве фармацевтических лекарственных средств.
Соединения по данному изобретению охватывают все случаи, включая энантиомеры, диастереомеры, равновесные соединения, смеси указанных форм в заданных соотношениях и рацемические смеси.
Способы получения соединений 1-тио-D-глюцитола формулы (I), используемых по данному изобретению, равно как фармацевтически приемлемых солей указанных соединений, и гидратов соединений или солей, также используемых по данному изобретению, описаны в официальном издании международной публикации WO 2006/073197 A1.
Из числа соединений 1-тио-D-глюцитола формулы (I), следующие соединения являются предпочтительными, поскольку обладают исключительной ингибирующей активностью в отношении SGLT2:
(1S)-1,5-ангидро-1-[5-(4-этоксибензил)-2-метокси-4-метилфенил]-1-тио-D-глюцитол (формула (IA)),
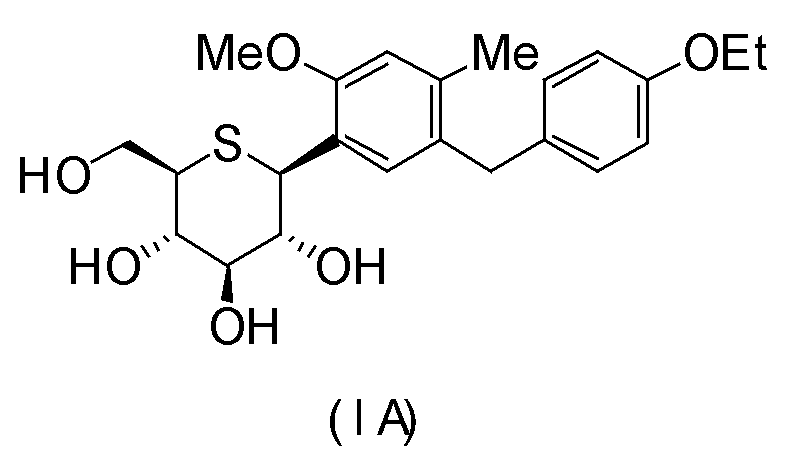
(1S)-1,5-ангидро-1-[4-хлор-3-(4-метилбензил)фенил]-1-тио-D-глюцитол (формула (IB)),
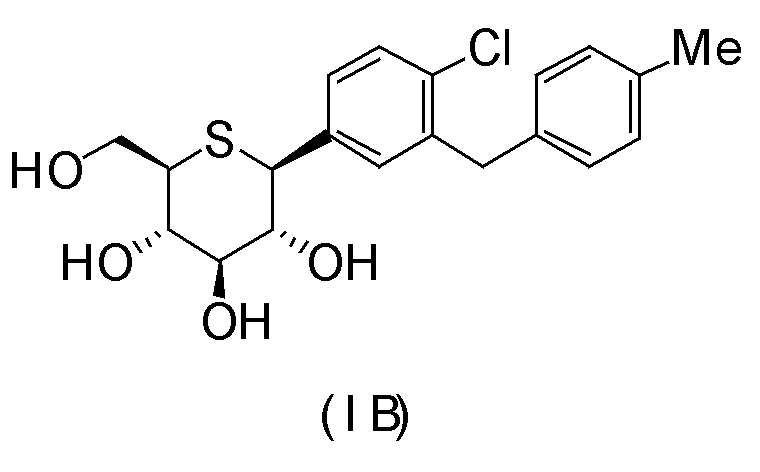
(1S)-1,5-ангидро-1-[4-хлор-3-[4-(метилсульфанил)бензил]фенил]-1-тио-D-глюцитол (формула (IC)),

(1S)-1,5-ангидро-1-[4-хлор-3-(4-этилбензил)фенил]-1-тио-D-глюцитол (формула (ID)),
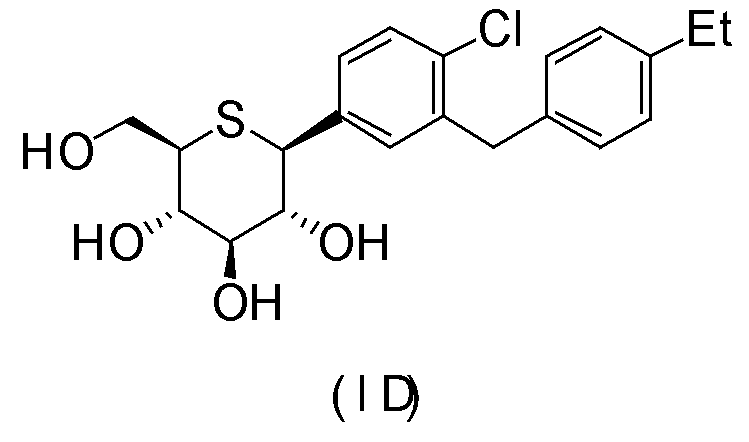
(1S)-1,5-ангидро-1-[5-(4-этилбензил)-2-метокси-4-метилфенил]-1-тио-D-глюцитол (формула (IE)),
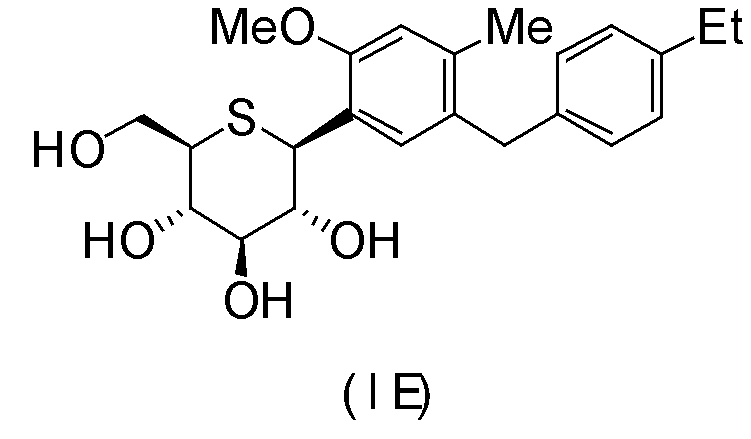
(1S)-1,5-ангидро-1-[4-хлор-3-[4-(пропан-2-ил)бензил]фенил]-1-тио-D-глюцитол (формула (IF)),
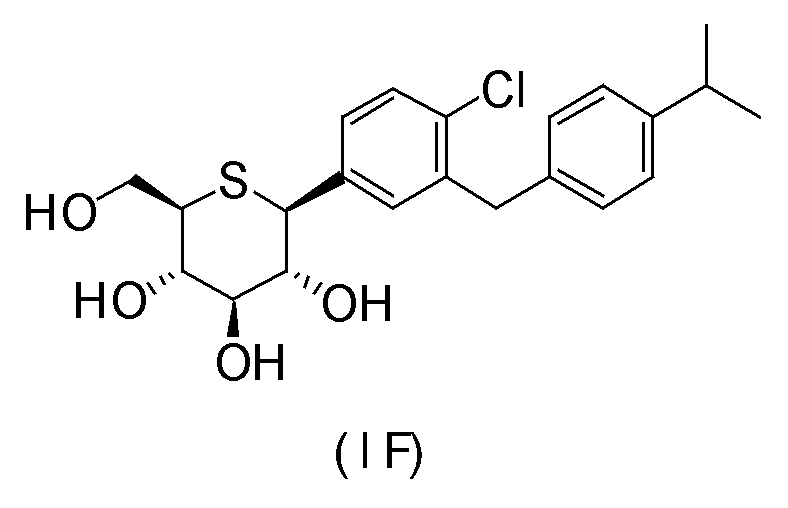
(1S)-1,5-ангидро-1-[2-метокси-4-метил-5-[4-(пропан-2-ил)бензил]фенил]-1-тио-D-глюцитол (формула (IG)),

(1S)-1,5-ангидро-1-[4-хлор-5-(4-этилбензил)-2-метоксифенил]-1-тио-D-глюцитол (формула (IH)).

Более предпочтительным соединением является (1S)-1,5-ангидро-1-[5-(4-этоксибензил)-2-метокси-4-метилфенил]-1-тио-D-глюцитол, преимущественно в виде гидрата.
Одним из вариантов осуществления данного изобретения является фармацевтическая композиция, включающая соединение 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемую соль указанного соединения, либо гидрат соединения или соли, и бигуанид. Данная фармацевтическая композиция предпочтительно является лекарственным препаратом против сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета.
Другим вариантом осуществления является способ предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета, включающий введение нуждающемуся в такой терапии пациенту соединения 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемой соли указанного соединения, либо гидрата соединения или соли, и бигуанида, либо одновременно, либо раздельно.
Бигуаниды представляют собой лекарственные средства, обладающие действиями по подавлению гликонеогенеза в печени, повышению чувствительности к инсулину в периферических тканях, ингибированию всасывания глюкозы из кишечника. Характерными примерами бигуанидов являются метформин и буформин. Метформин предпочтителен с точки зрения действия по снижению уровней глюкозы в крови, ограниченных побочных эффектов и тому подобного, при этом в особенности предпочтителен метформина гидрохлорид. Указанные бигуаниды являются известными веществами, и метформин и метформина гидрохлорид, в частности, описаны в Emil A. Werner and James Bell, J. Chem. Soc., 121, 1922, 1790-1794, и может быть использован коммерческий продукт под торговой маркой GLUCOPHAGE.
Еще одним вариантом осуществления данного изобретения является фармацевтическая композиция, включающая соединение 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемую соль указанного соединения, либо гидрат соединения или соли, и средство, усиливающее секрецию инсулина. Такая фармацевтическая композиция предпочтительно является лекарственным препаратом против сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета.
Еще одним вариантом осуществления является способ предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета, включающий введение нуждающемуся в такой терапии пациенту соединения 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемой соли указанного соединения, либо гидрата соединения или соли, и средства, усиливающего секрецию инсулина, либо одновременно, либо раздельно.
Средствами, усиливающими секрецию инсулина, являются лекарственные средства, обладающие способностью промотировать секрецию инсулина из панкреатических β-клеток. Характерными примерами средств, усиливающих секрецию инсулина, являются сульфонилмочевины (глипизид, глибенкламид, глимепирид, гликлазид, ацетогексамид, толбутамид, гликопирамид, хлорпропамид и толазамид) и глиниды (натеглинид, митиглинид и репаглинид). Из числа перечисленных, глипизид, глибенкламид и глимепирид, являющиеся сульфонилмочевинами, в особенности предпочтительны с точки зрения действия по снижению уровней глюкозы в крови. Такие средства, усиливающие секрецию инсулина, являются известными веществами, и могут быть использованы обычно коммерческие продукты.
Еще одним вариантом осуществления данного изобретения является фармацевтическая композиция, включающая соединение 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемую соль указанного соединения, либо гидрат соединения или соли, и усилитель чувствительности рецепторов к инсулину. Такая фармацевтическая композиция предпочтительно является лекарственным препаратом против сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета.
Еще одним вариантом осуществления является способ предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета, включающий введение нуждающемуся в такой терапии пациенту соединения 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемой соли указанного соединения, либо гидрата соединения или соли, и усилителя чувствительности рецепторов к инсулину, либо одновременно, либо раздельно.
Усилители чувствительности рецепторов к инсулину представляют собой лекарственные средства, улучшающие чувствительность к инсулину в периферических тканях и печени. Характерными примерами усилителей чувствительности рецепторов к инсулину являются пиоглитазон и росиглитазон. Пиоглитазон предпочтителен с точки зрения действия по снижению уровня глюкозы в крови, ограниченных побочных эффектов и тому подобного, при этом в особенности предпочтителен пиоглитазона гидрохлорид. Такие усилители чувствительности рецепторов к инсулину являются известными веществами, и могут быть использованы обычно коммерческие продукты.
Еще одним вариантом осуществления данного изобретения является фармацевтическая композиция, включающая соединение 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемую соль указанного соединения, либо гидрат соединения или соли, и инсулин. Такая фармацевтическая композиция предпочтительно является лекарственным препаратом против сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета.
Еще одним вариантом осуществления является способ предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета, включающий введение нуждающемуся в такой терапии пациенту соединения 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемой соли указанного соединения, либо гидрата соединения или соли, и инсулина, либо одновременно, либо раздельно.
Предпочтительными характерными примерами инсулинов являются препараты человеческого инсулина (например, инъекция человеческого инсулина в виде раствора, инъекция биосинтетического человеческого нейтрального инсулина в виде раствора, инъекция человеческого изофан-инсулина в виде водной суспензии, инъекция биосинтетического человеческого изофан-инсулина в виде водной суспензии, инъекция биосинтетического человеческого бифазного изофан-инсулина в виде водной суспензии и инъекция человеческого инсулина в виде водной суспензии) и препараты аналогов инсулина (инсулин лизпро, инсулин аспарт, инсулин глулизин, инсулин гларгин и инсулин детемир), при этом препараты человеческого инсулина в особенности предпочтительны. Хотя инсулины включают различные типы, такие как типы сверхбыстрого действия, типы быстрого действия, бифазные типы, промежуточные типы и типы замедленного действия, тип инсулина может быть выбран и введен в зависимости от состояния пациента. Такие препараты инсулина являются известными веществами, и обычно могут быть использованы коммерческие продукты.
Еще одним вариантом осуществления данного изобретения является фармацевтическая композиция, включающая соединение 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемую соль указанного соединения, либо гидрат соединения или соли, и ингибитор дипептидилпептидазы IV. Такая фармацевтическая композиция предпочтительно является лекарственным препаратом против сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета.
Еще одним вариантом осуществления является способ предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета, включающий введение нуждающемуся в такой терапии пациенту соединения 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемой соли указанного соединения, либо гидрата соединения или соли, и ингибитора дипептидилпептидазы IV, либо одновременно, либо раздельно.
Фермент дипептидилпептидазы IV инактивирует инкретиновые гормоны: глюкагоноподобный пептид-1 (GLP-1) и глюкозозависимый инсулинотропный полипептид (GIP). GLP-1 и GIP играют ключевую роль в регуляции секреции инсулина и гомеостаза глюкозы. Ингибиторы дипептидилпептидазы IV представляют собой лекарственные средства, предупреждающие инактивацию указанных пептидов и усиливающие секрецию глюкозозависимого инсулина из панкреатических β-клеток. Предпочтительными характерными примерами ингибиторов дипептидилпептидазы IV являются ситаглиптин, вилдаглиптин, саксаглиптин, алоглиптин, линаглиптин, тенелиглиптин, SK-0403, кармеглиптин, KRP-104 и SYR-472, при этом ситаглиптин и вилдаглиптин в особенности предпочтительны. Такие ингибиторы дипептидилпептидазы IV являются известными веществами, и обычно могут быть использованы коммерческие продукты.
Еще одним вариантом осуществления данного изобретения является фармацевтическая композиция, включающая соединение 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемую соль указанного соединения, либо гидрат соединения или соли, и ингибитор α-глюкозидазы. Такая фармацевтическая композиция предпочтительно является лекарственным препаратом против сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета.
Еще одним вариантом осуществления является способ предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета, включающий введение нуждающемуся в такой терапии пациенту соединения 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемой соли указанного соединения, либо гидрата соединения или соли, и ингибитора α-глюкозидазы, либо одновременно, либо раздельно.
Ингибиторы α-глюкозидазы представляют собой лекарственные средства, ингибирующие пищеварительные ферменты, такие как амилаза, мальтаза, α-декстриназа, сахараза и т.п., для замедления всасывания углеводов из тонкого кишечника. Предпочтительными характерными примерами ингибиторов α-глюкозидазы являются воглибоза, миглитол и акарбоза. Такие ингибиторы α-глюкозидазы являются известными веществами, и обычно могут быть использованы коммерческие продукты.
Еще одним вариантом осуществления данного изобретения является фармацевтическая композиция, включающая соединение 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемую соль указанного соединения, либо гидрат соединения или соли, и миметик GLP-1. Такая фармацевтическая композиция предпочтительно является лекарственным препаратом против сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета.
Еще одним вариантом осуществления является способ предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета, включающий введение нуждающемуся в такой терапии пациенту соединения 1-тио-D-глюцитола формулы (I) или фармацевтически приемлемой соли указанного соединения, либо гидрата соединения или соли, и миметика GLP-1, либо одновременно, либо раздельно.
Миметики GLP-1 представляют собой лекарственные средства, обладающие инсулинотропным действием благодаря активации рецептора GLP-1 человека. Считается, что миметики GLP-1 могут представлять собой любое соединение, включая пептиды и непептидные соединения. Предпочтительными характерными примерами миметиков GLP-1 являются лираглутид, эксенатид, таспоглутид и албиглутид, при этом лираглутид в особенности предпочтителен. Такие миметики GLP-1 являются известными веществами, и обычно могут быть использованы коммерческие продукты.
Еще одним вариантом осуществления данного изобретения является фармацевтическая композиция, включающая активный ингредиент A или фармацевтически приемлемую соль указанного ингредиента, либо гидрат ингредиента или соли, и активный ингредиент B, как указано в таблице A. Такая фармацевтическая композиция предпочтительно является лекарственным препаратом против сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета.
Еще одним вариантом осуществления является способ предотвращения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета, включающий введение нуждающемуся в такой терапии пациенту активного ингредиента A или фармацевтически приемлемой соли указанного ингредиента, либо гидрата ингредиента или соли, и активного ингредиента B, как указано в таблице A, либо одновременно, либо раздельно.
“Сахарный диабет” охватывает диабет типа 1, диабет типа 2 и другие типы сахарного диабета, вызванные специфическими причинами. Болезни, на которые направлены лекарственные препараты по данному изобретению, предпочтительно представляют собой диабет типа 1 и диабет типа 2.
“Заболевания, связанные с сахарным диабетом” включают такие заболевания, как ожирение, гиперинсулинемия, дисгликемия (нарушение обмена глюкозы), гиперлипемия, гиперхолестеринемия, гипертриглицеридемия, дислипидемия (болезнь обмена липидов), гипертензия, застойная сердечная недостаточность, отек, гиперурикемия и подагра.
“Осложнения сахарного диабета” подразделяют на острые и хронические.
“Острые осложнения” включают такие осложнения, как гипергликемия (например, кетоацидоз), гипергликемический гиперосмолярный синдром, лактатацидоз, гипогликемия и инфекционные болезни (например, кожные, мягких тканей, печени, респираторные и мочевыводящих путей инфекции).
“Хронические осложнения” включают такие осложнения, как микроангиопатия (диабетическая ретинопатия, диабетическая невропатия и диабетическая нефропатия), а также макроангиопатия (цереброваскулярное расстройство, ишемическая болезнь сердца и болезнь периферических артерий).
“Лечение” означает введение фармацевтических композиций по данному изобретению пациентам с уже проявившимися заболеваниями, такими как сахарный диабет, заболевания, связанные с сахарным диабетом, или осложнения сахарного диабета. Меры по такому лечению охватываются симптоматической терапией, рассчитанной на ослабление симптомов, возникших при вышеуказанных болезнях. Также включены терапии, обеспечивающие частичное или полное выздоровление от болезни, равно как терапии, останавливающие или замедляющие прогрессирование болезни.
“Предупреждение” означает практику, согласно которой пациентам с риском проявления заболеваний, таких как сахарный диабет, заболевания, связанные с сахарным диабетом, или осложнения сахарного диабета, вводят фармацевтические композиции по данному изобретению до проявления заболевания.
Фармацевтическая композиция по данному изобретению может быть такой, где вышеуказанные активные ингредиенты формулированы в виде отдельного препарата (комбинированный препарат), либо вышеуказанные активные ингредиенты формулированы в виде двух или нескольких препаратов. Такие препараты могут представлять собой таблетки, гранулы, порошки, капсулы, эмульсии, суспензии или сиропы, либо альтернативно, указанные препараты могут представлять собой инъекции в таких формах, как стерильный раствор или жидкая суспензия, все получаемые обычно используемыми способами. Если активные ингредиенты формулированы раздельно в виде двух или нескольких препаратов, соответствующие препараты могут быть введены либо одновременно, либо с заданными разнесенными интервалами времени. Два или несколько препаратов могут быть введены с различной частотой в течение дня. Фармацевтическая композиция по данному изобретению может быть введена системно или местно пероральным или парентеральным способом. Если активные ингредиенты формулированы раздельно в виде двух или нескольких препаратов, соответствующие препараты могут быть введены различными путями.
Если фармацевтическая композиция по данному изобретению формулирована в виде двух различных препаратов, весьма вероятно, что указанные препараты следует вводить либо одновременно, либо с очень коротким интервалом, тогда в документе, таком как листовка-вкладыш или брошюра препаратов безрецептурного отпуска, сопровождающем коммерческий продукт, будет указано, что два препарата должны быть введены в комбинации. Другим предпочтительным вариантом осуществления является набор из двух препаратов, один из которых включает соединение 1-тио-D-глюцитола, а другой включает, по меньшей мере, одно средство, выбираемое из группы, состоящей из бигуанидов, средств, усиливающих секрецию инсулина, усилителей чувствительности рецепторов к инсулину, инсулинов, ингибиторов дипептидилпептидазы IV, ингибиторов α-глюкозидазы и миметиков GLP-1.
Дозировка фармацевтической композиции по данному изобретению изменяется в зависимости от мишени, способа и т.п., введения. Взять, например, случай перорального введения; пациенту с сахарным диабетом предпочтительно вводят следующие суточные дозы:
(1) 0,1-50 мг, предпочтительно 0,5-25 мг, соединения 1-тио-D-глюцитола;
(2) 10-3000 мг бигуанидов;
(2-1) 100-3000 мг, предпочтительно 300-3000 мг, метформина;
(2-2) 10-500 мг, предпочтительно 30-150 мг, буформина;
(3) 0,5-2000 мг средств, усиливающих секрецию инсулина;
(3-1) 0,5-100 мг, предпочтительно 1-10 мг, глимепирида;
(3-2) 0,5-100 мг, предпочтительно 1-10 мг, глибенкламида;
(3-3) 10-2000 мг, предпочтительно 100-1000 мг, ацетогексамида;
(3-4) 100-2000 мг, предпочтительно 300-2000 мг, толбутамида;
(3-5) 50-2000 мг, предпочтительно 100-500 мг, гликопирамида;
(3-6) 10-1000 мг, предпочтительно 50-500 мг, хлорпропамида;
(3-7) 0,5-2000 мг, предпочтительно 2-40 мг, глипизида;
(3-8) 10-2000 мг, предпочтительно 50-500 мг, толазамида;
(3-9) 10-500 мг, предпочтительно 30-200 мг, гликлазида;
(4) 1-100 мг усилителей чувствительности рецепторов к инсулину;
(4-1) 1-100 мг, предпочтительно 10-50 мг, пиоглитазона;
(5) 1-3000 единиц, предпочтительно 10-1000 единиц, инсулинов;
(6) 1-300 мг ингибиторов дипептидилпептидазы IV;
(6-1) 1-300 мг, предпочтительно 20-100 мг, ситаглиптина;
(6-2) 1-300 мг, предпочтительно 20-100 мг, вилдаглиптина;
(7) 0,2-1000 мг ингибиторов α-глюкозидазы;
(7-1) 0,2-100 мг, предпочтительно 0,5-10 мг, воглибозы;
(7-2) 10-1000 мг, предпочтительно 100-500 мг, миглитола и
(7-3) 10-1000 мг, предпочтительно 100-500 мг, акарбозы;
в случае инъекции; пациенту с сахарным диабетом предпочтительно вводят следующие суточные дозы:
(1) 1-100 единиц, предпочтительно 4-100 единиц, инсулины;
(2) 0,001-300 мг миметиков GLP-1;
(2-1) 0,1-10 мг, предпочтительно 0,3-3 мг, лираглутида;
(2-2) 0,001-0,1 мг, предпочтительно 0,005-0,05 мг, эксенатида и
(2-3) 0,3-300 мг, предпочтительно 1-100 мг, албиглутида.
Бигуаниды обычно вводят двумя или тремя подразделенными порциями. С другой стороны, соединение 1-тио-D-глюцитола может быть представлено, как обладающее замедленным ингибирующим действием в отношении SGLT2 в течение длительного периода. Поэтому, для создания комбинированного препарата такого типа, чтобы можно было вводить один раз в день, соединение 1-тио-D-глюцитола по данному изобретению предпочтительно используют в комбинации с “бигуанидом, наделенным способностью обеспечивать замедленное высвобождение”.
“Бигуанид, наделенный способностью обеспечивать замедленное высвобождение”, может быть получен известными способами. Например, бигуанидам можно придать способность к замедленному высвобождению, используя способ медленного высвобождения, описанный в официальном издании WO 96/08243 A1, или способ, описанный в официальном издании JP 2003-520759 A.
Вышеописанные препараты предпочтительно представляют собой пероральные препараты, такие как таблетки, гранулы, порошки, капсулы, эмульсии, суспензии и сиропы. В частности, вышеуказанные активные ингредиенты могут быть смешаны, либо одновременно, либо раздельно, с наполнителями, такими как маннит и лактоза и, после грануляции, наполнены в капсулы либо непосредственно, либо после смешения с другими вспомогательными веществами для перорального введения, конкретными примерами которых могут являться наполнители (например, наполнители на основе сахара или наполнители на основе сахарных спиртов, такие как глюкоза, сахароза, маннит, лактоза, ксилит, сорбит, мальтит и пуллулан; целлюлозные наполнители, такие как микрокристаллическая целлюлоза; наполнители на основе крахмала, такие как кукурузный крахмал; неорганические наполнители, такие как безводный двухосновный фосфат кальция), связующие вещества (например, целлюлозные связующие вещества, такие как метилцеллюлоза, гидроксипропилцеллюлоза и гидроксипропилметилцеллюлоза), разрыхлители (например, целлюлозные разрыхлители, такие как кальциевая соль кармеллозы, низкозамещенная гидроксипропилцеллюлоза и натрий кросскармелоза, или разрыхлители на основе крахмала, такие как частично желатинизированный крахмал и натрий карбоксиметилкрахмал), флюидизирующие вещества (например, неорганические флюидизирующие вещества, такие как легкий кремниевый ангидрид) или смазывающие вещества (например, стеариновая кислота, стеарат магния, стеарат кальция, тальк и натрия стеарилфумарат); альтернативно, грануляция может представлять собой гранулирование в таблетки.
Соотношение, при котором соединение 1-тио-D-глюцитола по данному изобретению или фармацевтически приемлемую соль указанного соединения, либо гидрат соединения или соли комбинируют с, по меньшей мере, одним средством, выбираемым из группы, состоящей из бигуанидов, средств, усиливающих секрецию инсулина, усилителей чувствительности рецепторов к инсулину, инсулинов, ингибиторов дипептидилпептидазы IV, ингибиторов α-глюкозидазы и миметиков GLP-1, изменяется в зависимости от мишени, способа и т.п. введения. Взять, например, случай введения фармацевтической композиции по данному изобретению человеку; если одну массовую долю соединения 1-тио-D-глюцитола комбинировать с 0,01-1000 массовыми долями, по меньшей мере, одного средства, выбираемого из группы, состоящей из бигуанидов, средств, усиливающих секрецию инсулина, усилителей чувствительности рецепторов к инсулину, инсулинов, ингибиторов дипептидилпептидазы IV, ингибиторов α-глюкозидазы и миметиков GLP-1, можно получить действие по снижению уровня глюкозы в крови, превосходящее действие, достигаемое при введении отдельных лекарственных средств. В особенности предпочтительно комбинировать одну массовую долю соединения 1-тио-D-глюцитола в сочетании с 0,1-100 массовыми долями, по меньшей мере, одного средства, выбираемого из группы, состоящей из бигуанидов, средств, усиливающих секрецию инсулина, усилителей чувствительности рецепторов к инсулину, инсулинов, ингибиторов дипептидилпептидазы IV, ингибиторов α-глюкозидазы и миметиков GLP-1. Такое комбинирование позволяет получать удовлетворительную эффективность, используя соответствующие лекарственные средства в меньших количествах, чем в случае индивидуального введения. В качестве дополнительного преимущества, фармацевтическая композиция по данному изобретению обладает меньшими побочными эффектами, поскольку не вызывает гипогликемии или увеличения массы тела, способных возникать в результате избыточной секреции инсулина.
Пациентами, которых следует лечить фармацевтической композицией по данному изобретению, являются пациенты, не способные к хорошему гликемическому контролю, несмотря на длительную диету и физические упражнения, и нуждающиеся в медикаментозной терапии; преимущественно, пациенты, не способные к хорошему гликемическому контролю, несмотря на введение отдельных пероральных противодиабетических лекарственных средств, и нуждающиеся в приеме другого лекарственного средства, действующего по иному механизму.
Фармацевтическая композиция по данному изобретению обычно может быть получена по следующим прописям.
(Препарат 1) Таблетка
Получают таблетки диаметром 13 мм; каждая таблетка содержит:
(Препарат 2) Таблетка
Получают таблетки диаметром 7 мм; каждая таблетка содержит:
(Препарат 3) Таблетка
Получают таблетки диаметром 7 мм; каждая таблетка содержит:
(Препарат 4) Таблетка
Получают таблетки диаметром 8 мм; каждая таблетка содержит:
Примеры
На следующих страницах, данное изобретение описано более подробно с помощью примеров, которые никоим образом не предназначены ограничивать рамки объема данного изобретения.
Пример испытания 1
<Тестовый вопрос>
Влияния длительной комбинированной терапии соединением A и метформина гидрохлоридом на мышей с диабетом
<Методика испытания>
Восьми самцам db/db мышей/группа (возраст 11 недель; CLEA JAPAN, Inc.) вводят перорально повторными дозами соединение A (3 мг/кг, один раз в день) и бигуанид, метформина гидрохлорид (50 мг/кг или 150 мг/кг, дважды в день; SIGMA-ALDRICH JAPAN K.K.), либо отдельно, либо в комбинации, в течение 27 дней. Восемь db/m мышей (возраст 11 недель; CLEA JAPAN, Inc.) используют в качестве недиабетических нормальных контролей.
Перед началом повторного введения и на 27ой день после начала повторного введения производят забор крови из хвостовой вены каждой мыши, и центрифугируют, собирая фракции гемацитов. После гемолиза фракций гемацитов, значения гликозилированного гемоглобина (GHb) определяют аффинной колоночной хроматографией с автоматическим анализатором гликозилированного гемоглобина (TOSOH CORPORATION). Начиная с 27го дня повторного введения, мышей не кормят в течение 16 часов, после чего производят забор крови из хвостовой вены каждой мыши, и центрифугируют, собирая плазму. Уровни глюкозы в плазме оценивают методом мутаротаза-GOD с помощью набора реактивов для анализа на глюкозу (Glucose C2 Test Wako; Wako Pure Chemical Industries, Ltd.). В дальнейшем, перед началом повторного введения и на 27й день после начала повторного введения производят забор крови из хвостовой вены каждой мыши, без голодной выдержки, и центрифугируют, собирая плазму. Уровни инсулина в плазме оценивают методом ELISA с помощью набора реактивов для анализа на инсулин (Levis: Mouse Insulin ELISA KIT (H-Type); SHIBAYAGI Co., Ltd.)
<Результат 1>
Изменения в GHb приведены в таблице 1 как среднее значение ± стандартная ошибка. Комбинированная терапия соединением A (3 мг/кг) и метформина гидрохлоридом (300 мг/кг) заметно снижает изменение в GHb, по сравнению с каждым отдельным лекарственным средством. Анализ методом двухфакторного ANOVA обнаруживает существенное влияние эффекта интеракции соединения A (3 мг/кг) и метформина гидрохлорида (300 мг/кг) на изменения в GHb.
<Результат 2>
Уровни глюкозы в плазме при голодании приведены в таблице 2 как среднее значение ± стандартная ошибка. Критерий Стьюдента используют для определения различий между двумя группами. Комбинированная терапия соединением A (3 мг/кг) и метформина гидрохлоридом (300 мг/кг) заметно снижает уровень глюкозы в плазме при голодании, по сравнению с каждым отдельным лекарственным средством.
<Результат 3>
Изменения в уровнях инсулина (IRI) в плазме, без голодной выдержки, приведены в таблице 3 как среднее значение ± стандартная ошибка. Критерий Стьюдента используют для определения различий между двумя группами. Комбинированная терапия соединением A (3 мг/кг) и метформина гидрохлоридом (300 мг/кг) заметно ингибирует снижение в уровнях IRI в плазме, по сравнению с каждым отдельным лекарственным средством.
Пример испытания 2
<Тестовый вопрос>
Влияния комбинированной терапии соединением A и глипизидом на мышей с диабетом
<Методика испытания>
После 3 недель питания по рациону с высоким содержанием жиров (D12492, Research Diets, Inc.), ICR мышам (CHARLES RIVER LABORATORIES JAPAN, INC.) внутрибрюшинно вводят стрептозоцин (SIGMA-ALDRICH JAPAN K.K.; здесь далее сокращенно обозначенный STZ), чтобы вызвать диабет. Без голодной выдержки, получавшим рацион с высоким содержанием жиров мышам, с вызванным STZ сахарным диабетом (возраст 15 недель) в группах, каждая из которых состоит из 11-12 мышей, перорально вводят однократные дозы соединения A (1 мг/кг) и средства, усиливающего секрецию инсулина, глипизида (10 мг/кг; SIGMA-ALDRICH JAPAN K.K.), либо по отдельности, либо в комбинации. Производят забор крови из хвостовой вены каждой мыши, с определенными интервалами времени, и уровни глюкозы в плазме измеряют с помощью GOD-калориметрии, используя самоконтролируемое устройство для измерения уровня глюкозы (Medisafe Mini GR-102; TERUMO CORPORATION, Japan).
<Результаты>
Площади под кривой уровней глюкозы в плазме за период до 8 часов после введения лекарственного средства (AUC уровней глюкозы в плазме ∆) приведены в таблице 4 как среднее значение ± стандартная ошибка. Критерий Уэлша используют для определения различий между двумя группами. Комбинированная терапия соединением A и глипизидом заметно снижает (AUC уровней глюкозы в плазме ∆, по сравнению с каждым отдельным лекарственным средством.
Пример испытания 3
<Тестовый вопрос>
Влияния комбинированной терапии соединением A и глимепиридом на мышей с диабетом и нормальных мышей
<Методика испытания>
Без голодной выдержки, 10 самкам KKAy мышей/группа (мыши с диабетом; возраст 4 недели; CLEA Japan, Inc.) и 10 самкам C57BL мышей/группа (нормальные мыши; возраст 4 недели; CLEA Japan, Inc.) перорально вводят однократные дозы соединения A (10 мг/кг) и средства, усиливающего секрецию инсулина, глимепирида (0,5 мг/кг; SIGMA-ALDRICH JAPAN K.K.), либо по отдельности, либо в комбинации. Производят забор крови из хвостовой вены каждой мыши, с определенными интервалами времени, и уровни глюкозы в плазме измеряют методом GDH-электрод, используя самоконтролируемое устройство для измерения уровня глюкозы (Glutest Neo Super; SANWA KAGAKU KENKYUSHO CO., LTD.)
<Результаты>
Площади под кривой уровней глюкозы в плазме за период до 3 часов после введения лекарственного средства (AUC уровней глюкозы в плазме ∆) приведены в таблицах 5 и 6 как среднее значение ± стандартная ошибка. Анализ методом двухфакторного ANOVA используют для обнаружения основных влияний и эффекта интеракции соединения A и глимепирида. У KKAy мышей (мыши с диабетом), комбинированная терапия соединением A и глимепиридом заметно снижает AUC уровней глюкозы в плазме ∆, по сравнению с каждым отдельным лекарственным средством. С другой стороны, комбинированная терапия соединением A и глимепиридом снижает AUC уровней глюкозы в плазме ∆ одинаково с терапией глимепиридом на нормогликемических C57BL мышах (нормальные мыши). Комбинированное с глимепиридом соединение A не проявляет большего эффекта по снижению уровня глюкозы, по сравнению с отдельно взятым глимепиридом. Такие результаты позволяют предположить, что комбинированная терапия соединением A и глимепиридом снизит риск гипогликемии как побочного эффекта.
Пример испытания 4
<Тестовый вопрос>
Влияния длительной комбинированной терапии соединением A и глимепиридом на мышей с диабетом
<Методика испытания>
Семи или восьми самкам KKAy мышей/группа (возраст 4 недели; CLEA JAPAN, Inc.) вводят перорально повторными дозами соединение A (0,03% смешанный рацион; ad libitum) и средство, усиливающее секрецию инсулина, глимепирид (0,5 мг/кг, один раз в день; SIGMA-ALDRICH JAPAN K.K.), либо только отдельно, либо в комбинации, в течение 8 недель.
Спустя 4 недели и 8 недель, производят забор крови из хвостовой вены каждой мыши через один час после введения лекарственного средства, без голодной выдержки. Уровни глюкозы в плазме измеряют методом GDH-электрод, используя самоконтролируемое устройство для измерения уровня глюкозы (Glutest Neo Super; SANWA KAGAKU KENKYUSHO CO., LTD). Кроме того, массы тел измеряют как перед началом повторного введения, так и на 4 и 8 неделе после начала повторного введения
<Результаты>
Уровни глюкозы в плазме на 4ую и 8ую недели повторного введения приведены в таблицах 7 и 8 как среднее значение ± стандартная ошибка. Метод двухфакторного ANOVA используют для обнаружения основных влияний и эффекта интеракции соединения A и глимепирида. Как на 4ой, так и на 8ой неделе повторного введения, комбинированная терапия соединением A и глимепиридом заметно снижает уровень глюкозы в плазме, по сравнению с каждым отдельным лекарственным средством.
Процентные изменения в массах тел от значений перед началом повторного введения приведены в таблицах 9 и 10 как среднее значение ± стандартная ошибка. Критерий Даннетта используют для определения различий между двумя группами. Как на 4ой, так и на 8ой неделе повторного введения, обработанные глимепиридом мыши проявляют тенденцию к возрастанию массы тела по сравнению с контрольными мышами с диабетом. С другой стороны, обработанные соединением A мыши и обработанные комбинацией мыши существенно снижают массу тела, по сравнению с контрольными мышами с диабетом.
Приведенные результаты свидетельствуют о том, что комбинированная терапия глимепиридом и соединением A заметно снижает уровень глюкозы в плазме и подавляет увеличение массы тела, вызванное глимепиридом, что подтверждает возможность ослабления побочного эффекта глимепирида.
Данные представляют уровень глюкозы в плазме через один час после введения лекарственного средства.
Основной эффект смешанного рациона, включающего соединение A (0,03%): P<0,05
Основной эффект глимепирида (0,5 мг/кг): P<0,001
Эффект интеракции смешанного рациона, включающего соединение A (0,03%) и глимепирида (0,5 мг/кг): не существенное различие (по двухфакторному ANOVA).
Данные представляют уровень глюкозы в плазме через один час после введения лекарственного средства.
Основной эффект смешанного рациона, включающего соединение A (0,03%): P<0,0001
Основной эффект глимепирида (0,5 мг/кг): P<0,0001
Эффект интеракции смешанного рациона, включающего соединение A (0,03%) и глимепирида (0,5 мг/кг): не существенное различие (по двухфакторному ANOVA).
Пример испытания 5
<Тестовый вопрос>
Влияния комбинированной терапии соединением A и глибенкламидом на мышей с диабетом
<Методика испытания>
После 3 недель питания по рациону с высоким содержанием жиров (D12492, Research Diets, Inc.), ICR мышам (CHARLES RIVER LABORATORIES JAPAN, INC.) внутрибрюшинно вводят стрептозоцин (SIGMA-ALDRICH JAPAN K.K.; здесь далее сокращенно обозначенный STZ), чтобы вызвать диабет. Без голодной выдержки, получавшим рацион с высоким содержанием жиров мышам, с вызванным STZ сахарным диабетом (возраст 12 недель) в группах, каждая из которых состоит из 10-12 мышей, перорально вводят однократные дозы соединения A (1 мг/кг) и средства, усиливающего секрецию инсулина, глибенкламида (10 мг/кг; SIGMA-ALDRICH JAPAN K.K.), либо по отдельности, либо в комбинации. Производят забор крови из хвостовой вены каждой мыши, с определенными интервалами времени, и центрифугируют, собирая плазму. Уровни глюкозы в плазме оценивают методом мутаротаза-GOD с помощью набора реактивов для анализа на глюкозу (Glucose C2 Test Wako; Wako Pure Chemical Industries, Ltd.).
<Результаты>
Площади под кривой уровней глюкозы в плазме за период до 8 часов после введения лекарственного средства (AUC уровней глюкозы в плазме ∆) приведены в таблице 11 как среднее значение ± стандартная ошибка. Анализ методом двухфакторного ANOVA используют для обнаружения основных влияний и эффекта интеракции соединения A и глибенкламида. Комбинированная терапия соединением A и глибенкламидом заметно снижает AUC уровней глюкозы в плазме ∆, по сравнению с каждым отдельно взятым лекарственным средством.
Основной эффект соединения A (1 мг/кг): P<0,0001
Основной эффект глибенкламида (10 мг/кг): P<0,05
Эффект интеракции соединения A (1 мг/кг) и глибенкламида (10 мг/кг): не существенное различие (по двухфакторному ANOVA).
Пример испытания 6
<Тестовый вопрос>
Влияния длительной комбинированной терапии соединением A и пиоглитазоном на мышей с диабетом
<Методика испытания>
Восьми самцам db/db мышей/группа (возраст 7 недель; CLEA JAPAN, Inc.) вводят перорально повторными дозами соединение A (3 мг/кг, один раз в день) и усилитель чувствительности рецепторов к инсулину, пиоглитазон (10 мг/кг, один раз в день; SIGMA-ALDRICH JAPAN K.K.), либо отдельно, либо в комбинации, в течение 27 дней. Восемь db/m мышей (возраст 7 недель; CLEA JAPAN, Inc.) используют в качестве недиабетических нормальных мышей.
Перед началом повторного введения и на 27ой день после начала повторного введения производят забор крови из хвостовой вены каждой мыши, и центрифугируют, собирая фракцию гемацитов и плазму, без голодной выдержки. После гемолиза фракций гемацитов, значения гликозилированного гемоглобина (GHb) определяют аффинной колоночной хроматографией с автоматическим анализатором гликозилированного гемоглобина (TOSOH CORPORATION). Уровни глюкозы в плазме оценивают методом мутаротаза-GOD с помощью набора реактивов для анализа на глюкозу (Glucose C2 Test Wako; Wako Pure Chemical Industries, Ltd.). Уровни инсулина в плазме оценивают методом ELISA с помощью набора реактивов для анализа на инсулин (Levis: Mouse Insulin ELISA KIT (T-type); SHIBAYAGI Co., Ltd.)
<Результат 1>
Изменения в GHb приведены в таблице 12 как среднее значение ± стандартная ошибка. Метод двухфакторного ANOVA используют для обнаружения основных эффектов и эффекта интеракции соединения A и пиоглитазона. Комбинированная терапия соединением A и пиоглитазоном заметно снижает изменение в GHb, по сравнению с каждым отдельным лекарственным средством.
Изменение в GHb (%) = GHb (%) после повторного введения - GHb (%) перед началом повторного введения
Основной эффект соединения A (3 мг/кг): P<0,0001
Основной эффект пиоглитазона (10 мг/кг): P<0,0001
Эффект интеракции соединения A (3 мг/кг) и пиоглитазона (10 мг/кг): не существенное различие (по двухфакторному ANOVA).
<Результат 2>
Уровни глюкозы в плазме, без голодной выдержки, приведены в таблице 13 как среднее значение ± стандартная ошибка. Метод двухфакторного ANOVA используют для обнаружения основных эффектов и эффекта интеракции соединения A и пиоглитазона. Комбинированная терапия соединением A и пиоглитазоном заметно снижает уровни глюкозы в плазме, без голодной выдержки, по сравнению с каждым отдельным лекарственным средством.
Основной эффект соединения A (3 мг/кг): P<0,0001
Основной эффект пиоглитазона (10 мг/кг): P<0,0001
Эффект интеракции соединения A (3 мг/кг) и пиоглитазона (10 мг/кг): не существенное различие (по двухфакторному ANOVA).
<Результат 3>
Изменение в уровнях инсулина (IRI) в плазме, без голодной выдержки, приведено в таблице 14 как среднее значение ± стандартная ошибка. Метод двухфакторного ANOVA используют для обнаружения основных эффектов и эффекта интеракции соединения A и пиоглитазона. Комбинированная терапия соединением A и пиоглитазоном заметно увеличивает изменение в уровнях IRI в плазме, без голодной выдержки. Анализ методом двухфакторного ANOVA показывает значительное влияние интеракции соединения A и пиоглитазона на изменения в уровне IRI в плазме, без голодной выдержки. Приведенные результаты свидетельствуют о том, что комбинированное с пиоглитазоном соединение A успешно улучшает гликемический контроль, по сравнению с каждым отдельным лекарственным средством, и, видимо, способствует синергическому подавлению недостаточности панкреатических бета-клеток вследствие токсичности глюкозы.
Основной эффект соединения A (3 мг/кг): P=0,2101
Основной эффект пиоглитазона (10 мг/кг): P<0,001
Эффект интеракции соединения A (3 мг/кг) и пиоглитазона (10 мг/кг): P<0,01 (по двухфакторному ANOVA).
Пример испытания 7
<Тестовый вопрос>
Влияния комбинированной терапии соединением A и инсулином на крыс с диабетом
<Методика испытания>
SD крысам (возраст 7 недель; CHARLES RIVER LABORATORIES JAPAN, INC.) внутрибрюшинно вводят стрептозоцин (SIGMA-ALDRICH JAPAN K.K.; здесь далее сокращенно обозначенный STZ), чтобы вызвать диабет. Крысам с вызванным STZ сахарным диабетом (возраст 8 недель) вводят подкожный имплант инсулина замедленного высвобождения (одна микрокапсула Linplant; LinShin Canada, Inc.) или осуществляют имитацию операции. Спустя одну неделю крысам перорально вводят однократную дозу соединения A (1 мг/кг), без голодной выдержки. Производят забор крови из хвостовой вены каждой крысы, с определенными интервалами времени, и центрифугируют, собирая плазму. Уровни глюкозы в плазме оценивают методом мутаротаза-GOD с помощью набора реактивов для анализа на глюкозу (Glucose C2 Test Wako; Wako Pure Chemical Industries, Ltd.).
<Результаты>
Площади под кривой уровней глюкозы в плазме за период до 8 часов после введения лекарственного средства (AUC уровней глюкозы в плазме) приведены в таблице 15 как среднее значение ± стандартная ошибка. Метод двухфакторного ANOVA используют для обнаружения основных влияний и эффекта интеракции соединения A и инсулина. Комбинированная терапия соединением A и инсулином заметно снижает AUC уровней глюкозы в плазме, по сравнению с каждым отдельно взятым лекарственным средством.
Основной эффект соединения A (1 мг/кг): P<0,01
Основной эффект инсулина замедленного высвобождения: P<0,0001
Эффект интеракции соединения A (1 мг/кг) и инсулина замедленного высвобождения: не существенное различие (по двухфакторному ANOVA).
Пример испытания 8
<Тестовый вопрос>
Влияния комбинированной терапии соединением A и ситаглиптином на крыс с диабетом
<Методика испытания>
Восьми самцам крыс линии Zucker с ожирением/группа (возраст 10 недель), подвергнутым голодной выдержке, вводят перорально однократными дозами соединение A (1 мг/кг) и ингибитор DPP-IV, ситаглиптин (0,3 мг/кг), либо отдельно, либо в комбинации. Через один час после введения, крысам перорально вводят растворы глюкозы (2 г/кг); производят забор крови из хвостовой вены каждой крысы, с определенными интервалами времени, и центрифугируют, собирая плазму. Уровни глюкозы в плазме оценивают методом мутаротаза-GOD с помощью набора реактивов для анализа на глюкозу (Glucose C2 Test Wako; Wako Pure Chemical Industries, Ltd.).
<Результаты>
Площади под кривой уровней глюкозы в плазме за период до 120 минут после нагрузки глюкозой (AUC уровней глюкозы в плазме ∆) приведены в таблице 16 как среднее значение ± стандартная ошибка. Метод двухфакторного ANOVA используют для обнаружения основных влияний и эффекта интеракции соединения A и ситаглиптина. Крысы Zucker с ожирением характеризуются ростом уровня глюкозы в плазме после пероральной нагрузки глюкозой, что свидетельствует о нарушении толерантности к глюкозе. Комбинированная терапия соединением A и ситаглиптином заметно подавляет рост уровня глюкозы в плазме после нагрузки глюкозой, по сравнению с каждым отдельно взятым лекарственным средством.
Основной эффект соединения A (1 мг/кг): P<0,001
Основной эффект ситаглиптина (0,3 мг/кг): P<0,05
Эффект интеракции соединения A (1 мг/кг) и ситаглиптина (0,3 мг/кг): не существенное различие (по двухфакторному ANOVA).
Пример испытания 9
<Тестовый вопрос>
Влияния комбинированной терапии соединением A и вилдаглиптином на крыс с диабетом
<Методика испытания>
Восьми самцам крыс линии Zucker с ожирением (возраст 15 недель), подвергнутым голодной выдержке, вводят перорально однократными дозами соединение A (1 мг/кг) и ингибитор DPP-IV, вилдаглиптин (0,3 мг/кг), либо отдельно, либо в комбинации. Через один час после введения, крысам перорально вводят растворы глюкозы (2 г/кг); производят забор крови из хвостовой вены каждой крысы, с определенными интервалами времени, и центрифугируют, собирая плазму. Уровни глюкозы в плазме оценивают методом мутаротаза-GOD с помощью набора реактивов для анализа на глюкозу (Glucose C2 Test Wako; Wako Pure Chemical Industries, Ltd.).
<Результаты>
Площади под кривой уровней глюкозы в плазме за период до 120 минут после нагрузки глюкозой (AUC уровней глюкозы в плазме ∆) приведены в таблице 17 как среднее значение ± стандартная ошибка. Метод двухфакторного ANOVA используют для обнаружения основных влияний и эффекта интеракции соединения A и вилдаглиптина. Крысы Zucker с ожирением характеризуются ростом уровня глюкозы в плазме после пероральной нагрузки глюкозой, что свидетельствует о нарушении толерантности к глюкозе. Комбинированная терапия соединением A и вилдаглиптином заметно подавляет рост уровня глюкозы в плазме после нагрузки глюкозой, по сравнению с каждым отдельно взятым лекарственным средством.
Основной эффект соединения A (1 мг/кг): P<0,0001
Основной эффект вилдаглиптина (3 мг/кг): P<0,05
Эффект интеракции соединения A (1 мг/кг) и вилдаглиптина (3 мг/кг): не существенное различие (по двухфакторному ANOVA).
Пример испытания 10
<Тестовый вопрос>
Влияния комбинированной терапии соединением A и воглибозой на крыс с диабетом
<Методика испытания>
Шести самцам крыс линии Zucker с ожирением (возраст 10 недель), подвергнутым голодной выдержке, вводят перорально однократными дозами соединение A (1 мг/кг) и ингибитор α-глюкозидазы, воглибозу (0,1 мг/кг), либо отдельно, либо в комбинации. Через одну минуту после введения, крысам перорально вводят растворы растворимого крахмала (2 г/кг); производят забор крови из хвостовой вены каждой крысы, с определенными интервалами времени, и центрифугируют, собирая плазму. Уровни глюкозы в плазме оценивают методом мутаротаза-GOD с помощью набора реактивов для анализа на глюкозу (Glucose C2 Test Wako; Wako Pure Chemical Industries, Ltd.).
<Результаты>
Площади под кривой уровней глюкозы в плазме за период до 120 минут после нагрузки глюкозой (AUC уровней глюкозы в плазме ∆) приведены в таблице 18 как среднее значение ± стандартная ошибка. Метод двухфакторного ANOVA используют для обнаружения основных влияний и эффекта интеракции соединения A и воглибозы. Крысы Zucker с ожирением характеризуются ростом уровня глюкозы в плазме после пероральной нагрузки глюкозой, что свидетельствует о нарушении толерантности к глюкозе. Комбинированная терапия соединением A и воглибозой заметно подавляет рост уровня глюкозы в плазме после нагрузки глюкозой, по сравнению с каждым отдельно взятым лекарственным средством.
Основной эффект соединения A (1 мг/кг): P<0,0001
Основной эффект воглибозы (0,1 мг/кг): P<0,001
Эффект интеракции соединения A (1 мг/кг) и воглибозы (0,1 мг/кг): не существенное различие (по двухфакторному ANOVA).
Пример испытания 11
<Тестовый вопрос>
Влияния комбинированной терапии соединением A и миглитолом на крыс с диабетом
<Методика испытания>
Шести самцам крыс линии Zucker с ожирением (возраст 9 недель), подвергнутым голодной выдержке, вводят перорально однократными дозами соединение A (0,5 мг/кг) и ингибитор α-глюкозидазы, миглитол (3 мг/кг), либо отдельно, либо в комбинации. Через одну минуту после введения, крысам перорально вводят растворы растворимого крахмала (2 г/кг); производят забор крови из хвостовой вены каждой крысы, с определенными интервалами времени, и центрифугируют, собирая плазму. Уровни глюкозы в плазме оценивают методом мутаротаза-GOD с помощью набора реактивов для анализа на глюкозу (Glucose C2 Test Wako; Wako Pure Chemical Industries, Ltd.).
<Результаты>
Площади под кривой уровней глюкозы в плазме за период до 120 минут после нагрузки глюкозой (AUC уровней глюкозы в плазме ∆) приведены в таблице 19 как среднее значение ± стандартная ошибка. Метод двухфакторного ANOVA используют для обнаружения основных влияний и эффекта интеракции соединения A и миглитола. Крысы Zucker с ожирением характеризуются ростом уровня глюкозы в плазме после пероральной нагрузки глюкозой, что свидетельствует о нарушении толерантности к глюкозе. Комбинированная терапия соединением A и миглитолом заметно подавляет рост уровня глюкозы в плазме после нагрузки глюкозой, по сравнению с каждым отдельно взятым лекарственным средством.
Основной эффект соединения A (0,5 мг/кг): P<0,05
Основной эффект миглитола (3 мг/кг): P<0,0001
Эффект интеракции соединения A (0,5 мг/кг) и миглитола (3 мг/кг): не существенное различие (по двухфакторному ANOVA).
Пример испытания 12
<Тестовый вопрос>
Влияния комбинированной терапии соединением A и акарбозой на крыс с диабетом
<Методика испытания>
Шести самцам крыс линии Zucker с ожирением (возраст 11 недель), подвергнутым голодной выдержке, вводят перорально однократными дозами соединение A (1 мг/кг) и ингибитор α-глюкозидазы, акарбозу (1 мг/кг), либо отдельно, либо в комбинации. Через одну минуту после введения, крысам перорально вводят растворы растворимого крахмала (2 г/кг); производят забор крови из хвостовой вены каждой крысы, с определенными интервалами времени, и центрифугируют, собирая плазму. Уровни глюкозы в плазме оценивают методом мутаротаза-GOD с помощью набора реактивов для анализа на глюкозу (Glucose C2 Test Wako; Wako Pure Chemical Industries, Ltd.).
<Результаты>
Площади под кривой уровней глюкозы в плазме за период до 120 минут после нагрузки глюкозой (AUC уровней глюкозы в плазме ∆) приведены в таблице 20 как среднее значение ± стандартная ошибка. Метод двухфакторного ANOVA используют для обнаружения основных влияний и эффекта интеракции соединения A и акарбозы. Крысы Zucker с ожирением характеризуются ростом уровня глюкозы в плазме после пероральной нагрузки глюкозой, что свидетельствует о нарушении толерантности к глюкозе. Комбинированная терапия соединением A и акарбозой заметно подавляет рост уровня глюкозы в плазме после нагрузки глюкозой, по сравнению с каждым отдельно взятым лекарственным средством.
Основной эффект соединения A (1 мг/кг): P<0,01
Основной эффект акарбозы (1 мг/кг): P<0,01
Эффект интеракции соединения A (1 мг/кг) и акарбозы (1 мг/кг): не существенное различие (по двухфакторному ANOVA).
Промышленная применимость
Данное изобретение представляет превосходные фармацевтические композиции для предотвращения или лечения сахарного диабета, обладающие эффективным действием по снижению уровней глюкозы в крови у множества больных диабетом и не вызывающие при этом заметных побочных эффектов. Данное изобретение касается также фармацевтических композиций для предотвращения или лечения различных диабетических осложнений, возникающих вследствие гипергликемии, таких как диабетическая ретинопатия, диабетическая нефропатия, диабетическая невропатия, цереброваскулярное расстройство, ишемическая болезнь сердца и болезнь периферических артерий.
Реферат
Предложена группа изобретений, включающая фармацевтическую композицию для предупреждения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета, содержащую комбинацию (A) (1S)-1,5-ангидро-1-[5-(4-этоксибензил)-2-метокси-4-метилфенил]-1-тио-D-глюцитола, или его соли, гидрата или соли гидрата и (B) метформин или средство, усиливающее секрецию инсулина, и комбинацию того же состава и назначения. Технический результат: помимо заметного снижения уровней глюкозы в плазме крови достигнут синергизм в ингибировании снижения уровня инсулина в плазме, дополнительно показано подавление побочного эффекта глимепирида - возрастания массы тела. 2 н. и 14 з.п. ф-лы, 20 табл.
Формула
(A)(1S)-1,5-ангидро-1-[5-(4-этоксибензил)-2-метокси-4-метилфенил]-1-тио-D-глюцитол или его фармацевтически приемлемую соль или гидрат, или соль гидрата, и
(B) метформин или средство, усиливающее секрецию инсулина.
(A)(1S)-1,5-ангидро-1-[5-(4-этоксибензил)-2-метокси-4-метилфенил]-1-тио-D-глюцитола или его фармацевтически приемлемой соли или гидрата, или соли гидрата, и
(B) метформин или средство, усиливающее секрецию инсулина для применения в способе предупреждения или лечения сахарного диабета, заболеваний, связанных с сахарным диабетом, или осложнений сахарного диабета, где (А) и (B) вводят нуждающемуся в этом пациенту одновременно или раздельно.

Комментарии