Композиции, содержащие конъюгаты антитело-лекарственное средство дуокармицин - RU2687237C1
Код документа: RU2687237C1
Чертежи



Описание
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к лиофилизированным композициям, содержащим конъюгаты антитело-лекарственное средство дуокармицин и их восстановленные водные растворы.
УРОВЕНЬ ТЕХНИКИ
Дуокармицины представляют собой токсины, выделенные из Streptomyces sp. в 1988 году. Данные ДНК-связывающие и алкилирующие агенты проявляют сильную цитотоксичность in vitro. Однако их применение при лечении рака ограничено, поскольку in vivo у них проявляются неблагоприятные побочные эффекты, приводящие к небольшому терапевтическому индексу.
Терапевтический индекс противоопухолевых агентов можно улучшить с помощью включения их в конъюгат антитело-лекарственное средство (ADC). ADC получают путем конъюгации лекарственного средства через расщепляемый или нерасщепляемый линкер (линкерное лекарственное средство) с антителом.
В настоящее время на рынке представлены два ADC, т. е. брентуксимаб ведотин и трастузумаб эмтанзин, и более 30 ADC находятся на разных фазах клинических исследований. Исследования, касающиеся ADC, вызвали возобновившийся интерес к разработке дуокармицинов и в частности производных дуокармицина в качестве лекарственных средств в ADC. Данные ADC называются как конъюгаты антитело-лекарственное средство дуокармицин или полученные на основе дуокармицина ADC в настоящей заявке.
Два полученные на основе дуокармицина ADC, то есть SYD985 (NCT02277717 (2014); спонсор: Synthon Biopharmaceuticals) и MDX-1203 (NCT00944905 (2009); спонсор: Bristol-Myers Squibb) находятся в настоящее время в клинических исследованиях.
По сравнению с голыми (моноклональными) антителами ADC имеют различные физико-химические свойства; следовательно, стандартные фармацевтические составы, подходящие для моноклональных антител, не одинаково подходят для ADC. Большинство линкерных лекарственных средств, в частности содержащих производные дуокармицина имеют низкую растворимость в воде. Когда данные линкерные лекарственные средства конъюгируют с антителами, полученный конъюгат имеет повышенную гидрофобность по сравнению с голым антителом, уменьшая коллоидную стабильность ADC в водном растворе. Увеличение гидрофобности при конъюгации линкерного лекарственного средства выражено по сравнению с изменением гидрофобности между различными антителами. Это создает трудности для разработки фармацевтического состава. Не только тип линкерного лекарственного средства, но также количество линкерных лекарственных средств на антитело (соотношение лекарственного средства и антитела, DAR) и сайт(ы) конъюгации линкерного лекарственного средства с антителом влияют на физико-химические свойства ADC. По сравнению с голым антителом соответствующий ADC имеет более выраженную тенденцию к агрегации. Более того, чем выше DAR, тем выше тенденция к агрегации в растворе.
Кроме того, для обеспечения химической стабильности линкерного лекарственного средства, особенно в случае расщепляемого линкера, состав ADC должен соответствовать требованиям, отличным от требований, необходимых для стабильности голого антитела в чистом виде. Поскольку каждое линкерное лекарственное средство имеет различную химическую стабильность и гидрофобность, каждый ADC является уникальным и требует специальной индивидуальной композиции.
Чтобы иметь достаточный срок годности, лекарственные средства, полученные из белка, часто продают в качестве лиофилизированного порошка для восстановления водой. Для получения лиофилизированного порошка используют способ лиофилизации или сушки сублимацией. Данный способ лиофилизации состоит из трех стадий, то есть замораживания, первичной сушки и вторичной сушки. Условия первичной сушки выбирают таким образом, чтобы температура продукта оставалась ниже температуры коллапса композиции для предотвращения физического коллапса порошка. Температуру коллапса композиции можно определить с использованием микроскопии при сушке сублимацией. Вторичную сушку проводят ниже температуры стеклования (Tg) композиции, которая обычно определяется с помощью дифференциальной сканирующей калориметрии (ДСК).
Прежде чем способ лиофилизации может начаться, активный фармацевтический ингредиент должен быть предоставлен в подходящем составе. В случае состава ADC состав очистки обычно обменивается с составом, подходящим для лиофилизации, то есть предоставляется предварительно лиофилизированный раствор. Предварительно лиофилизированный раствор должен соответствовать нескольким требованиям, то есть он должен полностью растворять ADC; в предварительно лиофилизированном растворе ADC должен быть коллоидно и химически стабильным в течение определенного периода времени при различных условиях, например, температуре, обычно встречающейся при лиофилизации; время способа должно быть приемлемым; и ADC должен быть стабильным в полученной лиофилизированной композиции, обычно называемой лиофилизированный порошок или уплотненный порошок. Данный порошок должен иметь приемлемый внешний вид. Кроме того, лиофилизированная композиция должна быть легко восстановлена.
Обычно лиофилизированные белковые составы содержат буферный агент, лиопротектор и необязательно поверхностно-активное вещество или объемообразующий агент или оба. Лиофилизированный порошок обычно хранится в виале и восстанавливается бактериостатической или стерильной водой для инъекций.
ADC, которые в настоящее время представлены на рынке, доступны в виде лиофилизированного порошка. Однако данные ADC содержат токсины, а именно: майтанзиноид (например, DM1) или ауристатин (например, монометилауристатин Е), которые являются менее гидрофобными, чем полученные на основе дуокармицина токсины, в настоящее время исследуемые в качестве лекарственных средств в ADC, и данные ADC имеют значения DAR, отличные от полученных на основе дуокармицина ADC, используемых в составах настоящего изобретения. Физико-химические свойства данных и других майтанзиноидных или ауристатиновых ADC отличаются от свойств полученных на основе дуокармицина ADC, используемых в составах настоящего изобретения и необходимых различных составах.
Например, композиция T-DM1, т.е. трастузумаб, конъюгированный через нерасщепляемый линкер к эмтансину, имеющая DAR 3,5 (Кадцила®) при восстановлении, представляет собой 20 мг/мл T-DM1, 10 мМ сукцината натрия, 6% (м./об.) сахарозы, 0,02% (м./об.) полисорбата 20, pH 5,0.
WO2004/110498 относится к жидким и лиофилизированным композициям антитела, соединенного с майтанзиноидом, и раскрывает в частности лиофилизированные композиции huN901-DM1 ADC (1-5 мг/мл), имеющие DAR приблизительно 4, раствор, содержащий 10 мМ сукцината натрия, 0,01% (м./об.) полисорбата 20, 0,5% (м./об.) сахарозы (то есть более чем в 10 раз меньше, чем количество сахарозы в коммерческом составе Кадцила®), 250 мМ глицина и рН 5,5. Пример 6 WO2004/110498 представляет, что композиции, содержащие 1 мг/мл huN901:DM1 ADC, 10 мМ сукцината натрия в комбинации с 0,01% полисорбата 20 и 250 мМ глицина, обеспечивают лучшую стабильность, чем комбинация 10 мМ цитрата натрия, 0,01% полисорбата 20 и 250 мМ глицина. Составы без полисорбата не являются стабильными. Пример 7 WO2004/110498 показывает, что аналогичный состав, содержащий 5 мг/мл huN901-DM1, приводящий к более низкому соотношению в 5 раз ADC и сахарозы, чем предпочтительный состав Примера 6, является также стабильным. WO2004/110498 раскрывает исключительно лиофилизированные составы huN901:DM1 ADC, которые содержат 250 мМ глицина, который не только действует в качестве объемообразующего агента, но также обладает крио или лиозащитными свойствами. Таким образом, раскрытые составы имеют высокое молярное соотношение лиопротектор/ADC.
Коммерческий состав Адцетрис® имеет композицию после восстановления 5 мг/мл брентуксимаба ведотина, монометилауристатина Е (ММАЕ), конъюгированного с химерным моноклональным антителом типа IgG1 (DAR приблизительно 8), 5,6 мг/мл цитрата натрия, 0,21 мг/мл моногидрата лимонной кислоты, 70 мг/мл дигидрата трегалозы, 0,2 мг/мл полисорбата 80, и имеет рН 6,6.
WO2015/075201 раскрывает без применения поверхностно-активных веществ лиофилизированные составы, содержащие ADC, в котором анти-TF IgG1-антитело конъюгировано с MMAE через валин-цитруллинновый линкер, подобно линкерному лекарственному средству Адцетрис®. Данный ADC имеет DAR 4 (стр. 35, 1.6). Пример 7 на стр. 55 представляет, что композиции, содержащие 10 мг/мл ADC, 30 мМ гистидина и 150 мМ или 250 мМ сахарозы, показывают значительную усадочную деформацию (худшее качество/внешний вид порошка), исходя из объема содержимого 4 мл в 10 мл виале, что делает данные составы непригодными для промышленного производства. Он также представляет, что присутствие объемообразующего агента (маннит присутствует в предварительно лиофилизированном растворе в относительно большом количестве не менее 3% м./об.) является необходимым для хорошего качества порошка. Пример 8 раскрывает, что соотношение сахарозы и ADC 1337 к 1 является предпочтительным (т.е. Состав В), в то время как Пример 12 показывает, что нет никакой разницы в стабильности среди составов, имеющих соотношение сахарозы и ADC 2676 к 1, и составов, имеющих соотношение сахарозы и ADC 446 к 1.
Некоторые жидкие составы применительно к полученным на основе дуокармицина ADC были раскрыты, например, в WO 2012/162482 (стр. 35, 1.16-17), WO 2011/133039 (стр. 218, 1.24) и на стр. 2 в дополнительной информации DOKTER, W et al. Preclinical Profile of the HER2-Targeting ADC SYD983/SYD985 Mol. Cancer Ther.; 13(11) November 2014; 2618-2629. Состав WO2012/162482 не подходит для лиофилизации, так как он содержит большое количество хлорида натрия, что может снизить температуру коллапса композиции до нецелесообразно низких значений. WO 2011/133039 раскрывает ряд новых аналогов ДНК-алкилирующего агента CC-1065 и HER2-направленных ADC, составленных в коммерческом составе Герцептина® (трастузумаб), содержащем 4,2 мМ гистидина, 19,1 мг/мл дигидрата трегалозы и полисорбат, имеющем рН 6. В DOKTER, W et al. состав, содержащий гистидин, 30 мг/мл дигидрата трегалозы и полисорбат, имеющий рН 6, был использован для HER2-направленного полученного на основе дуокармицина ADC SYD983.
Однако, никакие лиофилизированные составы, содержащие полученные на основе дуокармицина ADC, не были раскрыты в предшествующем уровне техники. Жидкие составы, раскрытые в WO 2011/133039 и DOKTER, W et al., являются непригодными для лиофилизации, поскольку стабильность полученного на основе дуокармицина ADC в составе и качество лиофилизированного порошка уступает в составах, которые имеют относительно низкое молярное соотношение лиопротектора и ADC. Принимая во внимание отсутствие подходящих фармацевтических составов для полученных на основе дуокармицина ADC в данной области техники, существует очевидная потребность в лиофилизированных композициях, содержащих полученные на основе дуокармицина ADC, имеющих приемлемый внешний вид порошка, и которые могут быть получены с помощью способа лиофилизации, имеющего приемлемое время лиофилизации, и в котором полученные на основе дуокармицина ADC являются приемлемо стабильными.
КРАТКОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к лиофилизированным композициям, содержащим конъюгаты антитело-лекарственное средство дуокармицин формул (I) или (II) и их соответствующие восстановленные водные растворы.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1: Лиофилизированные порошки А: раствор плацебо с 30 мг/мл дигидрата трегалозы (подобно композиции II, но без SYD985), В: композиция II с 30 мг/мл дигидрата трегалозы, C: композиция III с 40 мг/мл дигидрата трегалозы.
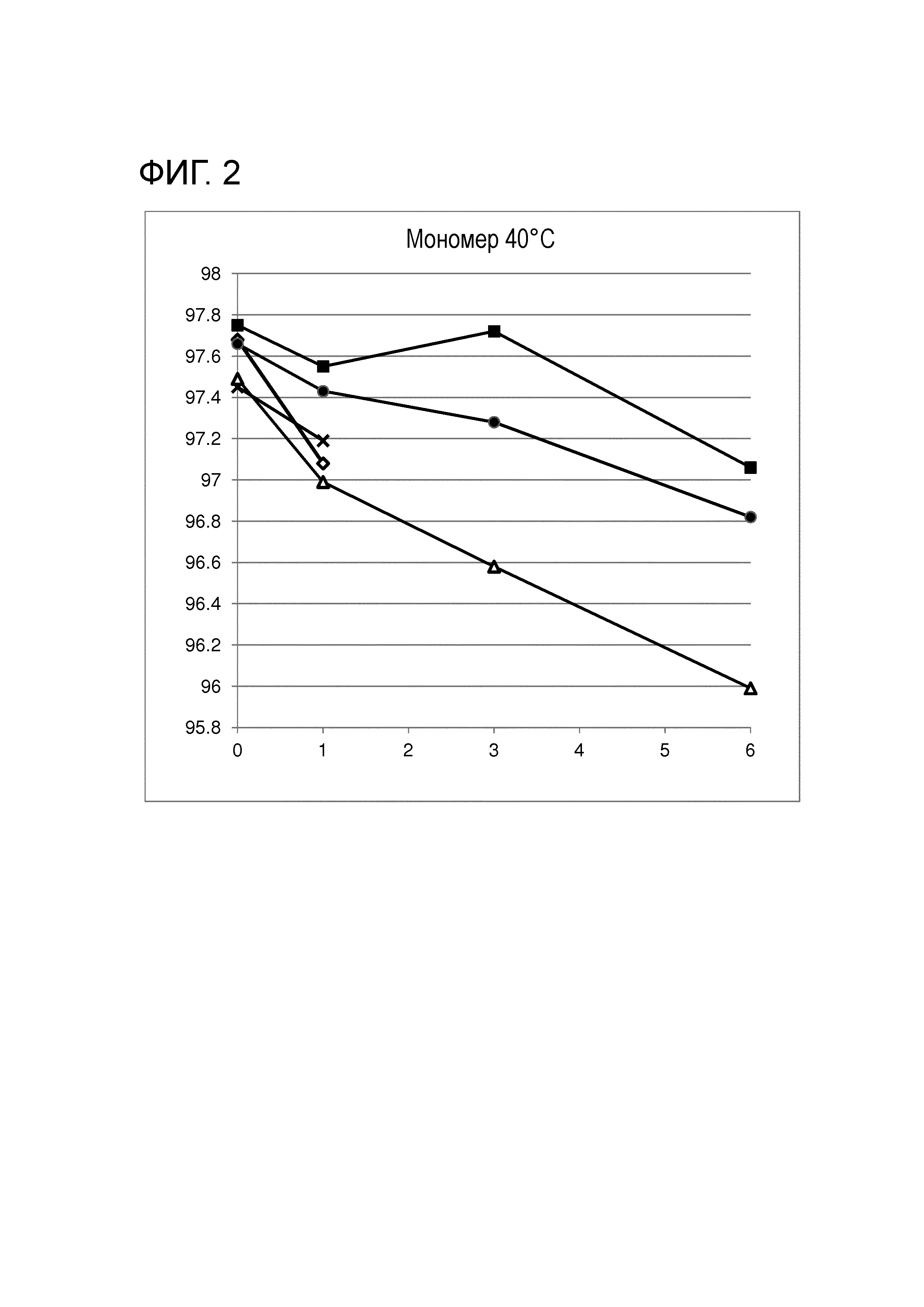
Фигура 2: Результаты стабильности: ось Y: процентное содержание мономера SYD985 в лиофилизированной композиции I (Δ), III (x), IV (◊), V (•) и VI (■) при 40°C, ось Х: время в месяцах.
Фигура 3: Результаты стабильности: ось Y: процентное содержание высокомолекулярных (ВММ) частиц в лиофилизированной композиции I (Δ), III (x), IV (◊), V (•) и VI (■) при 40°C, ось X: время в месяцах.
Фигура 4: СЭМ-изображения верхнего и среднего слоев лиофилизированных порошков композиции V без отжига (слева) и с отжигом (справа), белая полоса составляет 200 мкм.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к лиофилизированной композиции, содержащей конъюгат антитело-лекарственное средство (ADC) формулы (I)

буферный агент, лиопротектор и поверхностно-активное вещество, в которой молярное соотношение лиопротектора и конъюгата антитело-лекарственное средство составляет 1400-3200 к 1.
В ADC формул (I) и (II) (см. ниже) линкерное лекарственное средство конъюгируют с двумя или более цистеиновыми остатками антитела с получением ADC, имеющего среднее соотношение лекарственного средства и антитела (DAR) 2-3. Предпочтительно, ADC имеет среднее значение DAR 2,5-3,0, более предпочтительно среднее значение DAR 2,6-2,9.
ADC формул (I) и (II), которые будут использоваться в композиции в соответствии с настоящим изобретением, имеют линкерное лекарственное средство, конъюгированное с антителом через S-атом цистеинового остатка, т.е. они являются цистеин-связанными конъюгатами антитело-лекарственное средство. Как правило, цистеиновый остаток представляет собой природный цистеиновый остаток, который присутствует в тяжелой и/или легкой цепи (моноклонального) антитела (МАТ) и образует межцепочечные дисульфидные связи. Антитела различных классов антител содержат различные количества межцепочечных дисульфидных связей. Например, антитела IgG1 обычно имеют четыре межцепочечные дисульфидные связи - все четыре расположены в шарнирной области - и после (частичного) восстановления дисульфидных связей линкерное лекарственное средство случайным образом присоединяется к свободным тиоловым группам.
Конъюгаты антитело-лекарственное средство формул (I) и (II) для использования в соответствии с настоящим изобретением могут быть получены в соответствии со способами и методиками, которые хорошо известны специалисту в данной области техники. Конъюгация через межцепочечные дисульфидные связи может происходить после полного или частичного восстановления указанных дисульфидных связей. Подходящие способы получения таких соединений можно найти в описании и примерах WO 2011/133039, также как в дополнительной информации DOKTER, W et al. in Mol. Cancer Ther.; 13(11) November 2014; 2618-2629 (раскрытие очистки HIC ADC SYD983 с получением SYD985). В частности, Пример 15 WO 2011/133039 описывает частичное восстановление трастузумаба для получения двух свободных тиоловых групп на МАТ и конъюгацию с рядом линкерных лекарственных средств с ADC, имеющими среднее значение DAR приблизительно 2. Специалисту в данной области техники очевидно, как получить ADC, имеющие среднее значение DAR 2-3 в соответствии с настоящим изобретением.
В типичном варианте осуществления композиции настоящего изобретения конъюгат антитело-лекарственное средство (ADC) присутствует в композиции в количестве, обеспечивающем концентрацию 1-30 мг/мл при восстановлении водой. Предпочтительно, количество обеспечивает концентрацию 2-20 мг/мл, более предпочтительно 5-15 мг/мл, наиболее предпочтительно приблизительно 10 мг/мл при восстановлении водой.
Моноклональное антитело (МАТ), используемое для конъюгации с линкерным лекарственным средством и для включения в композицию в соответствии с настоящим изобретением, может представлять собой антитело IgA, IgD, IgE, IgG или IgM. Антитело может иметь легкие цепи κ (каппа) или легкие цепи λ (лямбда). Антитело IgG может представлять собой антитело IgG1, IgG2, IgG3 или IgG4. Предпочтительно, антитело связывается с антигеном-мишенью, который экспрессируется в или на клеточной мембране (например, на клеточной поверхности) опухолевой клетки, более предпочтительно, антитело поглощается клеткой после связывания с (антигеном) мишенью, после чего лекарственное средство дуокармицин высвобождается внутриклеточно. Предпочтительно, антитело представляет собой антитело IgG, более предпочтительно антитело IgG1, наиболее предпочтительно антитело IgG1, содержащее легкие цепи κ. Предпочтительно, антитело IgG несет нативный гликозидный/углеводный фрагмент, присоединенный к N297 тяжелой цепи антитела.
Подходящие антитела включают анти-аннексин А1 антитело, анти-CD19 антитело, анти-CD22 антитело, анти-CD30 антитело, анти-CD33 антитело, анти-CD37 антитело, анти-CD38 антитело, анти-CD44 антитело, анти-CD47 антитело, анти-CD56 антитело, анти-CD70 антитело, анти-CD74 антитело, анти-CD79 антитело, анти-CD115 антитело, анти-CD123 антитело, анти-CD138 антитело, анти-CD203c антитело, анти-CD303 антитело, анти-CEACAM антитело, анти-CLL-1 антитело, анти-c-MET (или анти-HGFR) антитело, анти-крипто антитело, анти-DLL3 антитело, анти-EGFR антитело, анти-EPCAM антитело, анти-EphA2 антитело, анти-EphB3 антитело, анти-ETBR антитело, анти-FcRL5 антитело, анти-FOLR1 антитело, анти-GCC антитело, анти-GPNMB антитело, анти-HER2 антитело, анти-HMW-МАА антитело, анти-интегрин антитело, анти-углеводное Льюис А подобное антитело, анти-Льюис У антитело, анти-LIV1 антитело, анти-мезотелиновое антитело, анти-MN антитело, анти-MUC1 антитело, анти-MUC16 антитело, анти-NaPi2b антитело, анти-Nectin-4 антитело, анти-PSMA антитело, анти-SIRPα антитело, анти-SLC44A4 антитело, анти-STEAP-1 антитело, анти-5T4 (или анти-ТБГ, трофобластический гликопротеин) антитело, анти-Tag72 антитело, анти-ТФ (или анти-тканевый фактор) антитело, анти-TROP2 антитело и анти-VLA антитело.
Предпочтительно, антитело представляет собой анти-аннексин А1 антитело, анти-HER2 антитело, анти-CD115 антитело анти-CD123 антитело, анти-CLL-1 антитело, анти-с-MET антитело, анти-MUC1 антитело, анти-PSMA антитело, анти-5T4 антитело или анти-ТФ антитело. Более предпочтительно, антитело представляет собой анти-HER2 антитело, анти-PSMA антитело или анти-5T4 антитело. Еще более предпочтительным является анти-HER2 антитело, в частности трастузумаб или его биоподобное.
Антитело, которое используется в соответствии с настоящим изобретением, представляет собой моноклональное антитело (МАТ) и может быть химерным, гуманизированным или человеческим МАТ. Предпочтительно, в соответствии с настоящим изобретением используется гуманизированное или человеческое МАТ, более предпочтительно гуманизированное или человеческое антитело IgG, наиболее предпочтительно гуманизированное или человеческое МАТ IgG1. Предпочтительно, указанное антитело содержит легкие цепи κ (каппа), то есть гуманизированное или человеческое антитело IgG1-κ.
Лиопротектор, который используется в композиции в соответствии с настоящим изобретением, может представлять собой любой эксципиент, который в сочетании с ADC в значительной степени предотвращает или снижает химическую и/или физическую нестабильность ADC при лиофилизации и последующем хранении.
Приводимые в качестве примера лиопротекторы включают сахара, такие как восстанавливающие или невосстанавливающие сахариды; аминокислоты, такие как глицин, аргинин, пролин, лизин, аланин; метиламин; лиотропную соль; полиолы, такие как трехатомные или высшие сахарные спирты, например, глицерин, эритрит, глицерол, арабит, ксилит, сорбит и маннит; пропиленгликоль; полиэтиленгликоль, полимеры, такие как поливинилпирролидон, поливиниловый спирт или полидекстран. Предпочтительный лиопротектор представляет собой невосстанавливающий сахарид, например, дисахариды, такие как трегалоза, изотрегалозы, сахароза и изосахарозы; трисахариды, такие как мелицитоза, генцианоза, рафиноза, эрлоза и умбеллифероза; тетрасахариды, такие как стахиоза и лихноза; и пентасахариды, такие как вербаскоза. Лиопротектор, который используется в соответствии с композицией настоящего изобретения, предпочтительно представляет собой трегалозу, или сахарозу, или их смесь, более предпочтительно трегалозу. Обычно дигидрат трегалозы используют для получения композиции в соответствии с настоящим изобретением.
Молярное соотношение лиопротектора и ADC, которое используется в композиции в соответствии с настоящим изобретением, представляет собой 1400-3200 к 1. Предпочтительно используют молярное соотношение 1400-3000 к 1, более предпочтительно 1400-2500 к 1, еще более предпочтительно 1400-2000 к 1, еще более предпочтительно 1400-1800 к 1. Наиболее предпочтительно используют молярное соотношение лиопротектора и ADC 1500-1700 к 1.
Авторы настоящего изобретения обнаружили, что стабильность полученных на основе дуокармицина ADC была оптимальной при молярном соотношении лиопротектора и ADC выше 1400 к 1. Было обнаружено, что стабильность и внешний вид порошка таких лиофилизированных композиций улучшается по сравнению с композициями, имеющими молярное соотношение ниже 1400 к 1. Молярные соотношения лиопротектора и ADC композиций известного уровня техники, раскрытых в WO 2012/162482, то есть приблизительно 350 к 1 и в WO 2011/133039 и DOKTER, W et al. in Mol. Cancer Ther.; 13(11) November 2014; 2618-2629, т. е. 800 к 1, являются значительно ниже 1400 к 1. Композиции, содержащие полученные на основе дуокармицина ADC, имеющие молярное соотношение лиопротектора и ADC ниже, чем 1400 к 1, показали худший внешний вид порошка, в то время как композиции плацебо, т.е. композиции без полученных на основе дуокармицина ADC с подобным соотношением показали приемлемый внешний вид порошка. Кроме того, стабильность композиций, содержащих полученные на основе дуокармицина ADC, имеющих молярное соотношение лиопротектора и ADC ниже, чем 1400 к 1, также была ниже. Однако, молярное соотношение лиопротектора и ADC не должно быть слишком высоким, так как способ лиофилизации композиций, имеющих молярное соотношение лиопротектора и ADC более 3200 к 1, как было обнаружено, является неприемлемо трудоемким. Длительный период времени способа лиофилизации вызывает эксплуатационные риски, такие как разрушение ADC во время способа и представляет способ непригодным для промышленного производства.
Буферный агент, который используется в композиции в соответствии с настоящим изобретением, может представлять собой любой буферный агент, который не имеет значительного изменения рН во время осуществления замораживания. Подходящие буферные агенты включают трис(гидроксиметил)метиламин, 4-2-гидроксиэтил-1-пиперазин-этансульфоновую кислоту, сукцинат, цитрат и гистидин. Предпочтительными буферными агентами являются гистидин, цитрат и сукцинат. Более предпочтительными буферными агентами являются гистидин и сукцинат. Наиболее предпочтительным буферным агентом является гистидин.
В композиции настоящего изобретения буферный агент присутствует в концентрации 2,5-25 мМ при восстановлении водой, предпочтительно в концентрации 3,0-10 мМ. Наиболее предпочтительная концентрация буферного агента представляет собой приблизительно 5 мМ, так как было обнаружено, что стабильность полученных на основе дуокармицина ADC в водном растворе была оптимальной при данной концентрации.
Композиция в соответствии с настоящим изобретением обычно обеспечивает водный раствор, имеющий рН 5,3-6,0 при восстановлении водой. Предпочтительно, рН составляет 5,5-5,8. Наиболее предпочтительно, рН составляет приблизительно 5,7. В предпочтительных диапазонах рН достигается компромисс между стабильностью антитела и химической стабильностью линкерного лекарственного средства, что приводит к оптимальной стабильности полученного на основе дуокармицина ADC.
Поверхностно-активное вещество, которое используется в композиции в соответствии с настоящим изобретением, предпочтительно представляет собой неионное поверхностно-активное вещество. Подходящие поверхностно-активные вещества включают алкилгликозиды, полоксамеры и полисорбаты. Предпочтительные поверхностно-активные вещества представляют собой полисорбаты, такие как полисорбат 20 и полисорбат 80. Наиболее предпочтительным поверхностно-активным веществом является полисорбат 20.
Количество поверхностно-активного вещества, которое присутствует в композиции настоящего изобретения, является таким, что оно уменьшает агрегацию ADC в водном растворе и минимизирует образование (высокомолекулярных) частиц при восстановлении водой. Поверхностно-активное вещество может присутствовать в количестве, обеспечивающем концентрацию 0,001-0,5% масса/объем (м./об.) при восстановлении водой, предпочтительно 0,005-0,05% (м./об.), более предпочтительно 0,005-0,02% (м./об.). Наиболее предпочтительным является количество приблизительно 0,01% (м./об.).
В предпочтительном варианте осуществления настоящего изобретения лиофилизированная композиция содержит конъюгат антитело-лекарственное средство формулы (II)
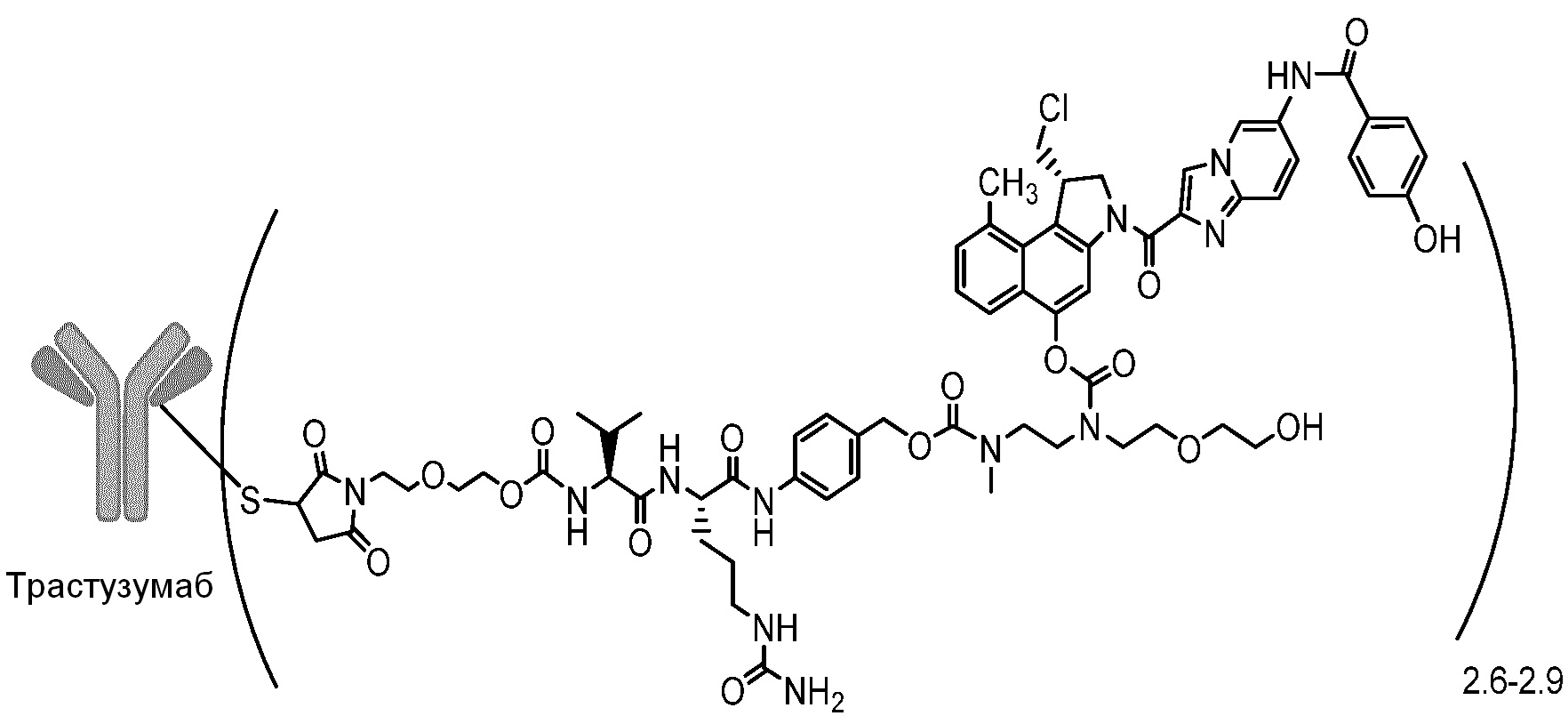
гистидин, трегалозу и полисорбат, в которой молярное соотношение трегалозы и ADC представляет собой 1500-1700 к 1 и при восстановлении водой ADC формулы (II) присутствует в количестве 5-15 мг/мл, концентрация гистидина представляет собой 3,0-10 мМ, количество полисорбата представляет собой 0,005-0,02% (м./об.) и рН представляет собой 5,5-5,8.
В более предпочтительном варианте осуществления настоящего изобретения лиофилизированная композиция содержит ADC формулы (II), гистидин, трегалозу и полисорбат 20, в которой молярное соотношение трегалозы и ADC представляет собой приблизительно 1605 к 1 и при восстановлении водой ADC формулы (II) присутствует в количестве приблизительно 10 мг/мл, концентрация гистидина представляет собой приблизительно 5 мМ, количество полисорбата 20 представляет собой приблизительно 0,01% (м./об.) и рН представляет собой 5,5-5,8.
В еще более предпочтительном варианте осуществления настоящего изобретения лиофилизированная композиция содержит ADC формулы (II), гистидин, трегалозу и полисорбат 20, в которой молярное соотношение трегалозы и ADC представляет собой приблизительно 1605 к 1 и при восстановлении водой ADC формулы (II) присутствует в количестве приблизительно 10 мг/мл, концентрация гистидина представляет собой приблизительно 5 мМ, количество полисорбата 20 представляет собой приблизительно 0,01% (м./об.) и рН представляет собой приблизительно 5,7.
В наиболее предпочтительном варианте осуществления настоящего изобретения лиофилизированная композиция состоит или по существу состоит из ADC формулы (II), гистидина, трегалозы и полисорбата 20, в которой молярное соотношение трегалозы и ADC представляет собой приблизительно 1605 к 1 и при восстановлении водой ADC формулы (II) присутствует в количестве приблизительно 10 мг/мл, концентрация гистидина представляет собой приблизительно 5 мМ, количество полисорбата 20 представляет собой приблизительно 0,01% (м./об.) и рН представляет собой приблизительно 5,7.
Соединение формулы (II), обозначаемое как SYD985 в настоящем описании, имеет среднее значение DAR в диапазоне 2,6-2,9.
В одном варианте осуществления SYD985, также известное как трастузумаб vc-seco-DUBA, представляет собой ADC формулы (II), имеющий среднее значение DAR приблизительно 2,8. Данное SYD985 представляет собой смесь, состоящую из приблизительно 65% видов DAR2, приблизительно 30% видов DAR4 и приблизительно 5% видов DAR6. Виды DAR2 состоят из ADC, в которых два линкерные лекарственные средства конъюгируются с остатками цистеина одной межцепьевой дисульфидной связи между тяжелыми и легкими цепями, и ADC, в которых два линкерные лекарственные средства конъюгируются с остатками цистеина одной межцепьевой дисульфидной связи между тяжелыми цепями. Виды DAR4 состоят из ADC, в которых четыре линкерные лекарственные средства конъюгируются с остатками цистеина преимущественно в двух изомерах, в одном изомере четыре линкерные лекарственные средства конъюгируются с остатками цистеина двух межцепьевых дисульфидных связей между тяжелыми и легкими цепями, в другом изомере четыре линкерные лекарственные средства конъюгируются с остатками цистеина двух межцепьевых дисульфидных связей между тяжелыми цепями. Виды DAR6 состоят из ADC, в которых шесть линкерных лекарственных средств конъюгируются, преобладающий изомер представляет собой ADC, в котором два линкерные лекарственные средства конъюгируются с остатками цистеина одной межцепьевой дисульфидной связи между тяжелыми и легкими цепями и четыре линкерные лекарственные средства конъюгируются с остатками цистеина двух межцепьевых дисульфидных связей между тяжелыми цепями.
Композиции настоящего изобретения дополнительно могут содержать объемообразующий агент. Типичные объемообразующие агенты включают декстран, поливинилпирролидон, серин, глицин, маннит, инозит, сорбит и гидроксиэтилированный крахмал. Предпочтительные объемообразующие агенты представляют собой маннит и сорбит. Наиболее предпочтительным объемообразующим агентом является маннит. Объемообразующий агент присутствует в количестве, достаточном для уменьшения времени способа лиофилизации и/или для улучшения внешнего вида порошка. Предпочтительно, ни один объемообразующий агент не включен в композицию в соответствии с настоящим изобретением. Наиболее предпочтительно, композиция настоящего изобретения состоит или по существу состоит из ADC формулы (I) или (II), буферного агента, лиопротектора и поверхностно-активного вещества, как описано выше в настоящей заявке.
Настоящее изобретение дополнительно относится к способу лиофилизации композиции, содержащей ADC формулы (I) или (II) в соответствии с настоящим изобретением, причем способ включает стадии: а) замораживания предварительно лиофилизированного водного раствора композиции, содержащей ADC формулы (I) или (II), буферный агент, лиопротектор и поверхностно-активное вещество, в которой молярное соотношение лиопротектора и ADC представляет собой 1400-3200 к 1, b) первичной сушки при температуре продукта ниже температуры коллапса композиции при давлении ниже атмосферного давления и с) вторичной сушки при температуре продукта выше 0°С и ниже температуры стеклования композиции при давлении ниже атмосферного давления. Предпочтительно, композицию замораживают с использованием температуры полки от -45°С до -30°С, первичную сушку проводят при температуре полки от -25°С до -5°С при давлении ниже 0,2 мбар и вторичную сушку проводят при температуре полки от 15°C до 40°C, от 20°C до 40°C или от 25°C до 40°C при давлении ниже 0,2 мбар. Предпочтительно, вторичную сушку проводят при температуре полки приблизительно 20°С.
В альтернативном варианте осуществления способ включает стадии: а) замораживания предварительно лиофилизированного водного раствора композиции в соответствии с настоящим изобретением, b) первичной сушки при температуре продукта ниже температуры коллапса композиции при давлении ниже атмосферного давления и с) вторичной сушки при температуре продукта ниже температуры стеклования композиции при давлении ниже атмосферного давления, в котором стадия замораживания а) включает стадию отжига.
Предпочтительно, стадию отжига проводят при температуре полки от -25°C до -10°C в течение от 0,5 до 6 часов или от 1 до 6 часов. Более предпочтительной является стадия отжига при температуре полки от -25°C до -15°C в течение от 1 до 5 часов или от 2 до 5 часов. Еще более предпочтительно, стадия а) включает понижение температуры полки устройства при давлении 1000 мбар со скоростью 0,2-1°С/мин до температуры полки от -50°С до -30°С, в дальнейшем поддержание данной температуры в течение от 30 мин до 1,5 часов, затем повышение температуры полки со скоростью 0,2-1°С/мин до температуры полки от -25°С до -10°С и поддержание данной температуры в течение от 0,5 до 3 часов или от 1,5 до 3 часов, с последующим охлаждением со скоростью 0,2-1,0°С/мин до температуры полки от -50°С до -40°С, с последующим поддержанием данной температуры в течение 1-2 часов.
Авторы настоящего изобретения обнаружили, что включение стадии отжига неожиданно значительно сокращало время способа лиофилизации. При включении стадии отжига не более 4 часов общее время способа сокращалось на 40 часов или более. Кроме того, морфология лиофилизата является оптимальной, если стадия отжига включена. Пористость порошка увеличивается, что приводит к более быстрой и более гомогенной сушке, и остаточная влажность после первичной сушки является низкой.
ПРИМЕРЫ
Получение предварительно лиофилизированных растворов SYD985
ADC SYD985 (т. е. трастузумаб vc-seco-DUBA) получали и очищали в соответствии со способами и методиками, опубликованными в дополнении DOKTER, W et al. in Mol. Cancer Ther.; 13(11) November 2014, 2618-2629. После очистки раствор SYD985 концентрировали и подвергали диафильтрации с использованием водных растворов, как показано в Таблице 1 без поверхностно-активного вещества с использованием одноразовой кассеты для тангенциальной проточной фильтрации, имеющей полиэфирсульфоновую мембрану с отсечкой 30 кДа (Sius™). После диафильтрации добавляли поверхностно-активное вещество и раствор разбавляли до 10 мг/мл SYD985. Затем конечный раствор немедленно замораживали и хранили при -70°С. Концентрацию SYD985 определяли с использованием УФ-VIS и выражали в мг/мл. Молярные количества рассчитывали с использованием молекулярной массы 151,8 кДа для SYD985 (среднее значение DAR 2,7).
Таблица 1. Композиция предварительно лиофилизированного раствора*
* Композиция предварительно лиофилизированного раствора является такой же, как композиция раствора, полученного путем восстановления лиофилизированного порошка.
Способ лиофилизации, используемый для определения R&D-стабильности растворов I-VI
Замороженные растворы I-VI оставляли оттаивать при комнатной температуре (КТ) и, если они не содержали осадок, отфильтровывали через 0,22 мкм фильтр и заполняли в виалы. Виалы загружали в устройство для сублимационной сушки небольшого размера. Лиофилизацию проводили с помощью понижения температуры полки до -35°С с последующей первичной сушкой при 0,075 мбар при температуре полки -10°С и вторичной сушкой при температуре полки 40°С. В композиции I, содержащей маннит, стадию отжига 4 часа при температуре полки -20°C вводили между стадией замораживания и первичной сушки. В композиции VI, содержащей более 80 мг/мл трегалозы, стадию отжига при -12°C в течение 5 часов вводили после замораживания до -40°C, первичную сушку проводили при 0,075 мбар и -21°C, чтобы избежать коллапса лиофилизата. Стадию промежуточной сушки при -5°С вводили между первичной и вторичной сушкой для предотвращения плавления. Стадию вторичной сушки проводили при 20°С.
Способ лиофилизации (общий способ)
Следующий способ представляет собой общую методику получения лиофилизированной композиции в соответствии с настоящим изобретением.
Для лиофилизации SYD985 замороженный раствор SYD985 (10 мг/мл), содержащий 5 мМ гистидина, 40 мг/мл дигидрата трегалозы и 0,01% (м./об.) полисорбата 20, оставляли оттаивать, и отфильтровывали, и виалы 20 мл заполняли 8,3 мл раствора SYD985. Виалы загружали в устройство для сублимационной сушки Epsilon 2-6D (MartinChrist) R&D. Температуру полки устройства понижали при давлении 1000 мбар со скоростью 0,2-1°C/мин до температуры полки от -50°C до -30°C, в дальнейшем поддерживая данную температуру в течение от 1 до 2 часов, затем температуру полки повышали со скоростью 0,2-1°C/мин до температуры от -25°C до -10°C, данную температуру поддерживали в течение от 1,5 до 3 часов. Следующая стадия представляла собой стадию охлаждения со скоростью 0,2-1,0°С/мин до температуры полки от -50°С до -40°С с последующим поддержанием данной температуры в течение 1-2 часов. В дальнейшем давление снижали до 0,05-0,3 мбар и температуру полки снова повышали со скоростью 0,2-1°C/мин до от -15°C до -5°C и данную температуру поддерживали в течение от 25 до 35 часов при давлении 0,05-0,3 мбар. Затем температуру полки повышали до от 20°C до 40°C со скоростью 5-20°C/час и данную температуру поддерживали в течение 1-10 часов.
Сравнительный пример без стадии отжига
Замороженный раствор композиции V оставляли оттаивать при комнатной температуре и, если он не содержал осадок, отфильтровывали через 0,22 мкм фильтр и заполняли в виалы. Виалы загружали в устройство для сублимационной сушки Epsilon 2-6D (MartinChrist) R&D. Лиофилизацию проводили с помощью понижения температуры полки до -40°С со скоростью 0,2-1°С/мин с последующей первичной сушкой при 0,075 мбар при температуре полки -10°С в течение 50 часов. После первичной сушки температуру полки повышали до 40°С со скоростью 3°С/час и выдерживали при данной температуре в течение 10 часов. Общее время способа представляло собой приблизительно 92 часа.
Результаты способа лиофилизации
Внешний вид/качество лиофилизированного порошка
Внешний вид лиофилизированных порошков различных составов суммирован в Таблице 4, ряд 3. Составы I, III, IV и V Таблицы 1 имели хороший внешний вид после лиофилизации. Количество лиопротектора менее чем в 1400 раз молярного количества ADC обеспечивает неудовлетворительные результаты для конечного лиофилизированного продукта, за исключением в присутствии значительного количества маннита (Состав I). Лиофилизация раствора II приводила к лиофилизированному порошку низкого качества (см. Фигуру 1В). При визуальном осмотре были видны трещины и крошки. Низкое качество порошка не ожидалось, так как подобный раствор без SYD985, плацебо, имел приемлемый внешний вид порошка в качестве лиофилизата (см. Фигуру 1А). Лиофилизация растворов III, IV и V Таблицы 1 с молярным избытком трегалозы 1605 приводит к порошку желаемого качества (порошок раствора III показан на Фигуре 1С).
Продолжительность способа лиофилизации
Продолжительность различных способов лиофилизации суммирована в Таблице 2.
Таблица 2. Суммарное время лиофилизации
ND=не определено
* порошок разрушался
Способ лиофилизации R&D для раствора VI Таблицы 1 требовал, по меньшей мере, 5 дней (приблизительно 122 часа) со стадией отжига при -12°C в течение 5 часов, тогда как лиофилизация растворов I, II, IV и V занимала менее 4 дней (приблизительно 92 часа без отжига).
Способ лиофилизации со стадией отжига имеет общее время способа приблизительно 44 часа для состава V. На Фигуре 4 показана СЭМ-картина лиофилизированного порошка раствора V, полученного с помощью сравнительного способа, который не имеет стадии отжига (слева), и изображение лиофилизированного порошка с отжигом (справа). Пористость порошка явно увеличена. Масштабирование раствора V приводило к способу, имеющему время способа приблизительно 63 часа.
Масштабирование раствора VI до промышленного способа лиофилизации оказалось безуспешным, так как самый короткий способ промышленного масштаба, полученный после оптимизации условий, продолжался более 8 дней со стадией отжига. Без стадии отжига способ занимал приблизительно 13 дней и приводил к разрушенному порошку. Высокое содержание трегалозы в жидком предварительно лиофилизированном растворе SYD985 является нецелесообразным для способа лиофилизации.
Измерения стабильности
а) Стабильность в растворе
Замороженный раствор оставляли оттаивать при КТ и, если он не содержал осадок, отфильтровывали через 0,22 мкм фильтр и заполняли в виалы. Анализ невидимых невооруженным глазом твердых частиц проводили методом светотени (LO) с использованием счетчика частиц PAMAS CVSS (датчик HCB-LD-25/25, Partikelmess- und Analyse Systeme GmbH). Методику проводят в соответствии с Ph. Eur. <2.9.19>, загрязненность частицами; невидимые невооруженным глазом частицы. Измерен объем образца 300 мкл (предварительный объем: 0,8 мл, объем промывания: 5 мл, скорость заполнения и промывания: 10 мл/мин). По меньшей мере, 3 последовательных измерения LO проводили для образца. Результаты анализируют с использованием программного обеспечения PMA.
Zсреднее, показатель размера частиц, чтобы определить агрегацию в растворе, измеряли с использованием динамического рассеяния света (ДРС). Анализ проводили на Zetasizer APS (Malvern Instruments, λ0=830 нм, θ=90°). Измерен объем образца 100 мкл. По меньшей мере, 3 последовательных измерения ДРС проводили для образца с 2-минутными временными интервалами, чтобы позволить растворам находиться в состоянии покоя. Во время всех измерений температуру поддерживали постоянной при 25°C и результаты рассеяния компенсировались вязкостью.
b) Стабильность лиофилизированных композиций
Лиофилизированные образцы восстанавливали с использованием воды для инъекций. Все измеренные лиофилизированные композиции легко восстанавливались.
Процентное содержание высокомолекулярного материала (ВММ) и мономера SYD985 в восстановленных композициях I, III, IV, V и VI определяли с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) в эксклюзионной хроматографии (SEC) на системе Shimadzu UFLC с: TSKgel G3000SWxl, 5 мкм, 7,8 мм×30 см аналитической колонкой Joint Analytical Systems (PN 08541) при температуре колонки 25°С с использованием 50 мМ фосфатного буфера с 300 мМ NaCl pH 7,5 в качестве подвижной фазы со скоростью потока 0,3 мл/мин. Как правило, 50 мкл восстановленного состава разбавляли до концентрации приблизительно 1,0 мг SYD985/мл.
Результаты стабильности
а) Стабильность в растворе
В Таблице 3 приведен обзор результатов стабильности для предварительно лиофилизированных растворов Таблицы 1. Стабильность раствора II не определяли, поскольку внешний вид после лиофилизации не был приемлемым. Все пять измеренных растворов продемонстрировали соизмеримую стабильность, за исключением раствора I. Раствор I Таблицы 1 с молярным избытком трегалозы приблизительно 800 приводил к пониженной стабильности в растворе (см. Таблицу 3). Через 1 месяц при КТ наблюдали белковый осадок. Для раствора I наблюдали пониженную коллоидную стабильность, кроме того с измерениями LO и ДРС через 1 месяц при комнатной температуре (КТ). Раствор I содержит большое количество частиц >10 мкм при t=1 месяц, как наблюдали с помощью LO, тогда как другие растворы содержали небольшое количество частиц данного размера. Zсреднее, измеренный с помощью ДРС для растворов, выдержанных в течение 1 месяца, также значительно увеличивается в растворе I по сравнению с другими растворами.
Таблица 3. Стабильность в растворе
1Поскольку лиофилизированный порошок не был приемлемого качества, никакие дополнительные измерения не проводили.
ND не определено
- низкое,+приемлемое
Оба раствора IV и V с концентрацией гистидина 5 мМ (IV и V) имеют более низкие значения Zсреднее, чем значения, измеренные для III и VI с концентрацией гистидина 10 мМ.
b) Стабильность лиофилизированных композиций
На Фигурах 2 и 3 показано, что когда раствор I Таблицы 1 лиофилизируют, в лиофилизированном порошке % мономера снижается, тогда как % ВММ увеличивается через некоторое время при 40°С, что свидетельствует о сниженной стабильности. На Фигурах 2 и 3 показано, что для составов V и VI снижение в % мономера, также как увеличение в % ВММ через некоторое время значительно ниже по сравнению с составом I. Количество мономера в восстановленных растворах III и IV при t=1 месяц выше, чем количество мономера в растворе I. Количества ВММ при t=1 месяц являются аналогичными для растворов I, III и IV.
Таблица 4. Обзор стабильности лиофилизата и качества порошка
1Не определено из-за низкого качества лиофилизата раствора II.
- низкое,+приемлемое, ++ хорошее.
Реферат
Группа изобретений относится к медицине, а именно к получению лиофилизированной композиции, содержащей конъюгат антитело-лекарственное средство формулы,буферный агент, лиопротектор и поверхностно-активное вещество. Молярное соотношение лиопротектора и конъюгата антитело-лекарственное средство составляет 1400-3200 к 1, где буферный агент представляет собой гистидин или сукцинат, где лиопротектор представляет собой сахарозу, трегалозу или их смесь, где поверхностно-активное вещество представляет собой полисорбат. При восстановлении водой конъюгат антитело-лекарственное средство присутствует в количестве 5-15 мг/мл, буферный агент присутствует в концентрации 3-10 мМ, количество полисорбата составляет 0,005-0,02% (м./об.), рН составляет 5,3-6,0 и, причем, в композицию не входит объемообразующий агент. Группа изобретений относится также к способу получения данной лиофилизированоной композиции. Использование данной группы изобретений позволяет получить улучшенную стабильность и внешний вид порошка. 2 н. и 4 з.п. ф-лы, 4 табл., 4 ил.
Формула



Комментарии