Пространственное картирование молекулярных профилей образцов биологических тканей - RU2733545C2
Код документа: RU2733545C2
Чертежи
Описание
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способу, делающему возможным пространственное картирование нуклеиновых кислот из образцов тканей с высоким разрешением. Способ основан на использовании паттернов олигонуклеотидных зондов, содержащих последовательность-штрих-код, связывающуюся с нуклеиновыми кислотами в образце, с учетом информации о ткани.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
В настоящее время патологи осуществляют микроскопические исследования различных форм тканей и клеток. Микроскопическое изображение позволяет получить информацию о морфологии (например, типах клеток, дифференцировке и т.д.), которая является основой диагностики. В случае, когда патолог хочет более подробно исследовать ткань/клетки, используют специфические в отношении биомаркеров способы окрашивания, таких как ER, PR и HER2 в случае рака молочной железы. Конкретные молекулярные тесты осуществляют in situ посредством так называемой гибридизации ДНК и РНК in situ. Однако при таком подходе количество мишеней ограничено. Для улучшенной стратификации осуществляют молекулярные диагностические тесты для тестирования экспрессии генов (например, OncoTypeDX, Mammaprint) или для поиска имеющих практическую ценность мутаций, таких как KRAS, EGFR и т.д., с помощью секвенирования (например, способом Сэнгера или секвенирования следующего поколения) и определения профиля экспрессии (например, микрочипы, RNAseq, RT-ПЦР).
Опухолевая ткань является гетерогенной по составу и окружена стромальными и инфильтрирующими иммунными клетками. Эта пространственная гетерогенность может влиять на молекулярный анализ, т.к. ДНК и РНК опухолевых клеток разбавлена ДНК и РНК из клеток, на которые анализ не направлен. Для преодоления этой проблемы выбирают интересующие области (ROI) ткани/клеток на микроскопическом препарате и удаляют их с него, например, соскребая их, или с помощью способов лазерной захватывающей микродиссекции, для обработки и анализа с помощью молекулярных и/или протеомных анализов (белковый состав и т.д.). При сборе ROI получают лишь ограниченную позиционную информацию, и зачастую собранный материал происходит из разных ROI, или ROI объединяют и впоследствии анализируют совместно. В случае лазерной захватывающей микродиссекции небольшие области можно собирать раздельно, но это времязатратно и не позволяет осуществлять систематический анализ ткани/клеток. Молекулярные анализы являются времязатратными и дорогими. В случае картирования молекулярных профилей с более высоким разрешением это приводит к большому количеству молекулярных тестов, стоимость которых будет слишком высока для клинической практики.
Кроме того, гетерогенность опухоли и архитектура ткани могут являться потенциальным диагностическим параметром, т.к. они могут давать подсказки о клональной эволюции опухоли и ее агрессивности. Таким образом, при удалении ROI с микроскопического препарата для осуществления дальнейших молекулярных анализов эта информация утрачивается.
Созданы карты гетерогенности на основе окрашивания in situ на молекулярные и белковые биомаркеры. См. например Almendro, et al., 2014, Cell Reports, 6: 514-527.
Другой подход описан Armani et al., Lab Chip, 2009, 9(24): 3526-3534 и Armani et al., Anal Bioanal Chem, 2011, 400: 3383-3393, при этом подходе срез ткани вдавливают в планшет с лунками, где в каждой лунке осуществляли реакцию qPCR или RT-qPCR. Затем получали 2D-карту амплифицированной мишени.
В US20140066318 A1 описывают матрицу зондов на субстрате, на который помещают образец ткани. Зонды связываются с нуклеиновыми кислотами-мишенями, и связанный зонд и нуклеиновую кислоту-мишень выделяют и используют для молекулярной диагностики.
В настоящей заявке авторы настоящего изобретения описывают подход, делающим возможным пространственное картирование нуклеиновых кислот с высоким разрешением без необходимости жертвовать степенью мультиплексирования, доступной при секвенировании нового поколения посредством эффективного использования мультиплексирования ROI на образец. Способ по изобретению основан на использовании паттернов олигонуклеотидных зондов, содержащих последовательность-штрих-код, с учетом информации о ткани, где олигонуклеотидные зонды связываются с нуклеиновыми кислотами в образце. Можно использовать различные технологии использования и различные способы получения паттернов, подобные регулярной матрице с конкретным шагом, или, альтернативно, объектоориентированное получение паттернов с использованием определенных интересующих областей без ограничений по форме.
Ключевым аспектом изобретения является идентификация ROI и определение индивидуального пространственного разрешения паттерна с учетом информации о ткани и вопроса, на который необходимо ответить. Интересующая область, а также пространственное разрешение паттерна можно выбирать с учетом основанного на изображении анализа ткани до нанесения реагентов. При идентификации по меньшей мере одной ROI и использования лишь олигонуклеотидных зондов в отношении ROI необходимо меньше видов олигонуклеотидных зондов для получения пространственной карты. Кроме того, дизайн паттернов пространственного разрешения без ограничения форматом анализа делает возможным использование ряда олигонуклеотидных зондов для определения на индивидуальной основе. Таким образом, способ по изобретению является гораздо более дешевым, чем общепринятые способы предшествующего уровня техники, и совместим с селективным профилированием.
Другим преимуществом способа по изобретению является то, что он хорошо соответствует существующему в настоящее время цифровому технологическому процессу в патологии. Общепринятый цифровой технологический процесс в патологии представляет собой:
1. получение окрашенного гематоксилином и эозином микроскопического препарата,
2. сканирование окрашенного гематоксилином и эозином микроскопического препарата для получения цифрового изображения,
3. осуществление анализа изображения для постановки патологического диагноза (доброкачественной или злокачественной опухоли), и
4. одновременную идентификацию ROI для дальнейшего молекулярного анализа для получения более точных результатов диагностики.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к способу пространственной детекции нуклеиновых кислот в образце ткани, включающему стадии:
идентификации по меньшей мере одной интересующей области (ROI) в образце;
нанесения по меньшей мере одного вида олигонуклеотидных зондов на заранее определенные участки в ROI и связывания олигонуклеотидных зондов с нуклеиновыми кислотами образца, где олигонуклеотидные зонды содержат последовательность-штрих-код;
выделение комплексов нуклеиновая кислота-олигонуклеотидные зонды;
секвенирование выделенных молекул нуклеиновой кислоты;
определение корреляции секвенированных молекул нуклеиновой кислоты с исходной локализацией соответствующих молекул-мишеней нуклеиновой кислоты в ROI для получения пространственного распределения молекул-мишеней нуклеиновой кислоты, где каждый участок идентифицируют посредством одного или более видов олигонуклеотидных зондов, связавшихся на стадии b).
В одном из вариантов осуществления молекулы ДНК получают из комплексов нуклеиновая кислота-олигонуклеотидные зонды посредством амплификации ДНК перед стадией d).
В другом варианте осуществления получение молекул ДНК осуществляют после реакции обратной транскрипции.
В одном из вариантов осуществления связывание олигонуклеотидных зондов с нуклеиновыми кислотами из образца на стадии b) осуществляют посредством гибридизации, где олигонуклеотидные зонды используют в качестве праймеров.
В альтернативном варианте осуществления связывание олигонуклеотидных зондов с нуклеиновыми кислотами из образца на стадии b) осуществляют посредством лигирования.
В одном из вариантов осуществления стадия e) дополнительно включает определение корреляции пространственного распределения молекул-мишеней нуклеиновой кислоты с изображением ROI или с изображением образца ткани, в котором идентифицировали ROI, полученными до или после стадии b).
В одном из вариантов осуществления способ дополнительно включает получение двухмерной пространственной карты для визуализации пространственного распределения молекул-мишеней нуклеиновой кислоты.
В одном из вариантов осуществления способ дополнительно включает наложение двухмерной пространственной карты на изображение ROI или изображение образца ткани, в котором идентифицировали ROI, полученные до или после стадии b).
В одном из вариантов осуществления по меньшей мере два различных вида олигонуклеотидных зонда связываются с одной молекулой-мишенью нуклеиновой кислоты на стадии b), где уникальную комбинацию по меньшей мере двух различных видов олигонуклеотидных зондов используют для идентификации локализации молекул-мишеней нуклеиновой кислоты в ROI.
В одном из вариантов осуществления по меньшей мере один из видов олигонуклеотидных зондов, связывающихся с одной молекулой нуклеиновой кислоты, содержит генерическую последовательность, где, необязательно, генерическая последовательность комплементарна нуклеиновой кислоте-мишени.
В одном из вариантов осуществления по меньшей мере один из видов олигонуклеотидных зондов, связывающихся с одной молекулой нуклеиновой кислоты, содержит дополнительную последовательность, где дополнительная последовательность является последовательностью для очистки или последовательностью для выравнивания праймеров.
В одном из вариантов осуществления заранее определенные локализации определяют с помощью шаблона разделения.
В одном из вариантов осуществления шаблон разделения является верхним шаблоном разделения, необязательно, напечатанным на образце, или полным шаблоном разделения, где шаблон разделения является решетчатым шаблоном разделения, шаблоном разделения произвольной формы или их комбинацией.
В одном из вариантов осуществления олигонуклеотидные зонды наносят на стадии b) на заранее определенные участки с помощью технологий переноса жидкостей, предпочтительно, способами контактной печати или способами неконтактной печати, таким образом, что нанесенные олигонуклеотидные зонды в разных заранее определенных участках не смешиваются.
В одном из вариантов осуществления образец является гистопатологическим образцом, предпочтительно, депарафинизированным, фиксированным формалином, погруженным в парафин (FFPE) образцом, свежезамороженным (FF) образцом или свежим образцом, или цитологическим образцом.
В одном из вариантов осуществления молекула-мишень нуклеиновой кислоты является РНК.
В одном из вариантов осуществления молекула-мишень нуклеиновой кислоты является ДНК.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
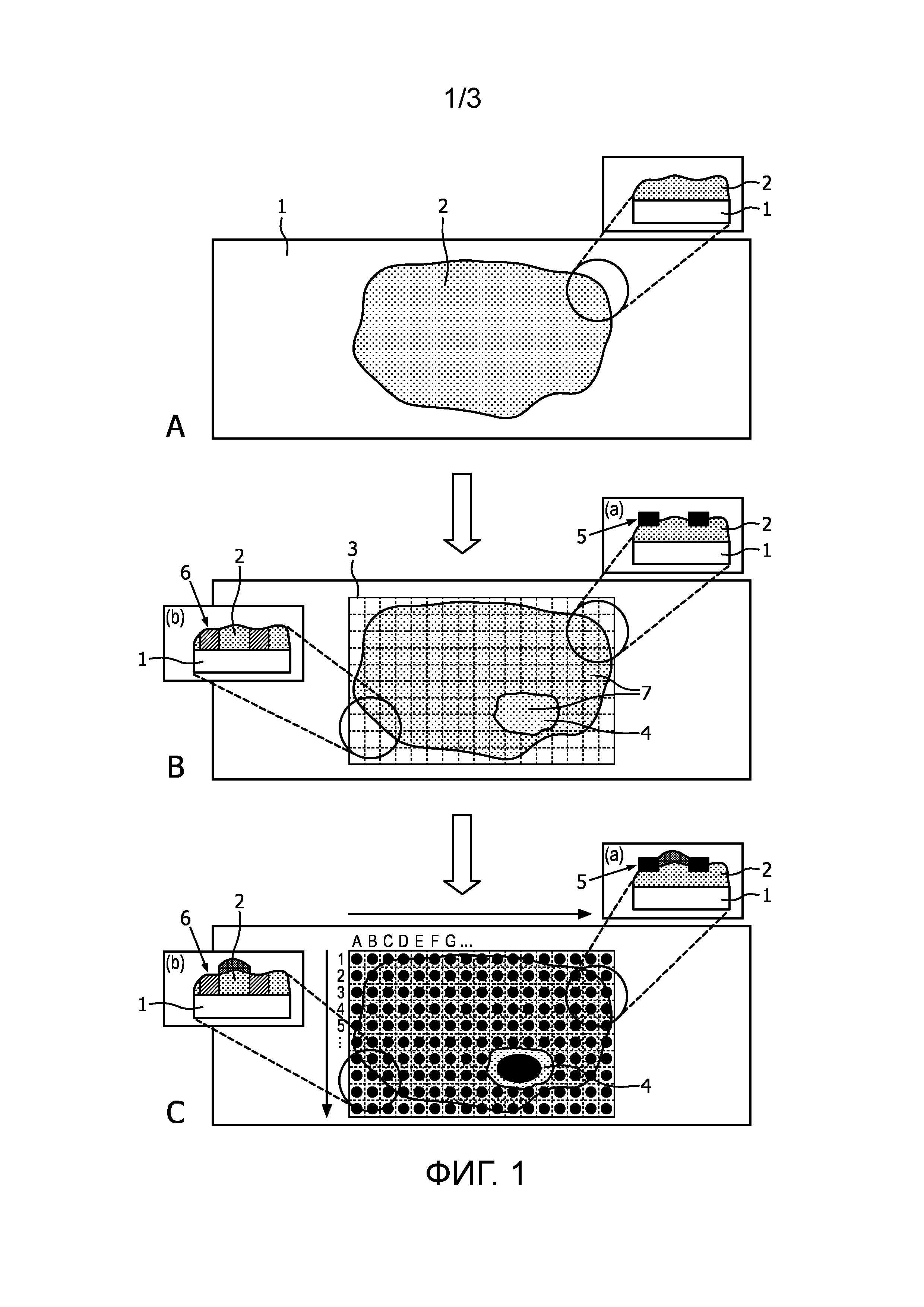
Фиг. 1 Обзор изобретения. (A) Поддерживающий материал 1 и образец ткани 2 представлены как вид сверху и на небольшой панели как вид сбоку. (B) Шаблон разделения наносят сверху образца ткани, получая заранее определенные участки 7. В изображенном шаблоне разделения комбинируют решетчатый шаблон разделения 3 и шаблон разделения произвольной формы 4. Однако, решетчатый шаблон разделения и шаблон разделения произвольной формы 4 также можно наносить по отдельности. Два типа шаблонов разделения с различными поперечными структурами представлены на панелях как вид сбоку: (a) верхний шаблон разделения 5, (b) полный шаблон разделения 6. (C) Олигонуклеотидные зонды наносят в жидкой фазе на заранее определенные участки образца ткани. На панелях представлен вид сбоку: (a) верхний шаблон разделения 5, (b) полный шаблон разделения 6.
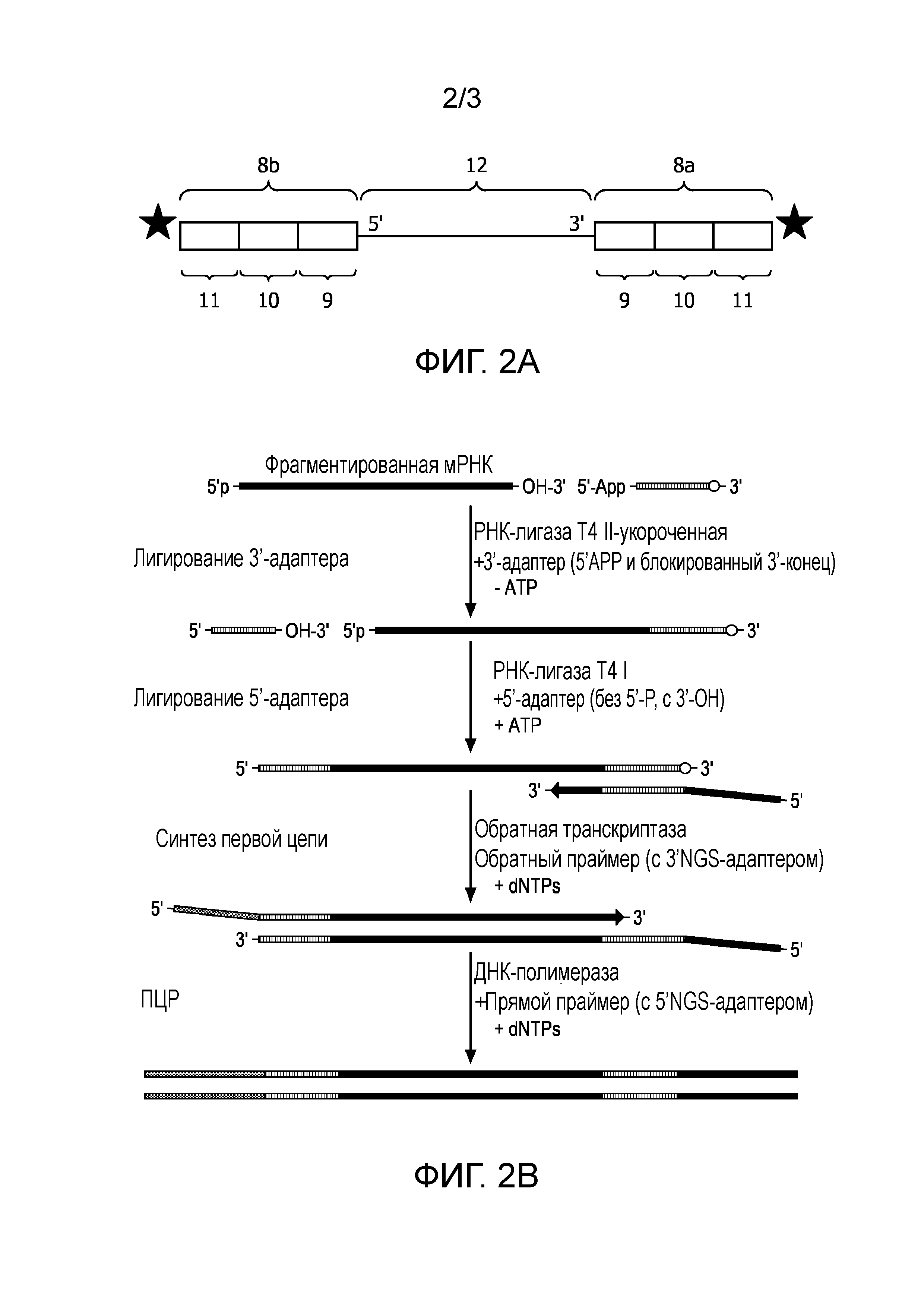
Фиг. 2 (A) Пример композиции олигонуклеотидных зондов, связанных посредством лигирования. Представлены два вида олигонуклеотидных зондов 8a и 8b, содержащих генерическую последовательность 9, последовательность-штрих-код 10a и 10b, соответственно, и дополнительную последовательность 11, связанную с нуклеиновой кислотой 12. (B) Стандартная схема реакции лигирование олигонуклеотидного зонда (модифицировано из http://rnaseq.uoregon.edu/#library-prep-addition-of-adapters-via-ligation). Нуклеиновая кислота является фрагментированной РНК. На первой стадии один вид олигонуклеотидного зонда лигирован с 3'-концом РНК. На второй стадии другой вид олигонуклеотидного зонда лигирован с 5'-концом РНК. На третьей стадии кДНК получают посредством реакции обратной транскрипции, где праймер, содержащий последовательность для секвенирования следующего поколения (NGS-адаптер) гибридизуется с последовательностью для выравнивания праймеров из олигонуклеотидного зонда. На четвертой стадии кДНК амплифицируют посредством ПЦР.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
В рамках изобретения термины в единственном числе также включают соответствующие термины во множественном числе, если контекст четко не указывает на иное.
В контексте по настоящему изобретению термины "приблизительно" означает интервал точности, что специалисту в этой области будет понятно, что необходимо обеспечивать технический эффект рассматриваемого признака. Как правило, термин означает отклонение от указанного числового значения на±20%, предпочтительно -±15%, более предпочтительно -±10%, и даже более предпочтительно -±5%.
Следует понимать, что термин "содержащий" не ограничен. В целях по настоящему изобретению термин "состоящий из" рассматривают в качестве предпочтительного варианта термина "содержащий". Если далее в настоящем описании группу определяют как содержащую, по меньшей мере, конкретное количество вариантов осуществления, он также должен включать группу, предпочтительно состоящую только из этих вариантов осуществления.
Кроме того, термины "первый", "второй", "третий" или "(a)", "(b)", "(c)", "(d)" и т.д. и т.п. в описании и формуле изобретения используют для различения схожих элементов, а не обязательно для описания последовательного или хронологического порядка. Следует понимать, что термины, используемые таким образом, являются взаимозаменяемыми в соответствующих условиях, и что варианты осуществления изобретения, представленные в настоящем описании, способны работать в иных последовательностях, чем описано или проиллюстрировано в настоящем описании.
В случае, когда термины "первый", "второй", "третий" или "(a)", "(b)", "(c)", "(d)", "i", "ii" и т.д. относятся к стадиям способа, или применению, или анализу, нет согласованности по времени или временному интервалу между стадиями, т.е. стадии можно осуществлять одновременно, или могут быть временные интервалы в секунды, минуты, часы, дни, недели, месяцы или даже годы между такими стадиями, если в настоящей заявке не указано иначе.
Следует понимать, что настоящее изобретение не ограничено конкретной методологией, способами, реагентами и т.д., представленными в настоящем описании, т.к. они могут различаться. Также следует понимать, что терминология, используемая в настоящем описании, предназначена для описания исключительно конкретных вариантов осуществления и не предназначена для ограничения объема настоящего изобретения, который будет ограничен исключительно прилагаемой формулой изобретения. Если не указано иначе, все технические и научные термины, используемые в настоящем описании, имеют значения, общепринято понимаемые специалистом в этой области.
Настоящее изобретение относится к пространственному картированию нуклеиновых кислот в образце.
В рамках изобретения термин "пространственное картирование" относится к приписыванию нуклеиновых кислот-мишеней их пространственной локализации в образце. С помощью пространственной карты можно получать транскрипционную или геномную информацию от множества клеток в образце ткани, где информация отличается двухмерным пространственным разрешением. Пространственную карту можно получать с учетом расположения, или она может иметь уникальное пространственное разрешение, т.к. паттерны можно выбирать с учетом индивидуальных признаков ROI, а также в ответ на основанный на изображении анализ ткани до нанесения реагентов. Пространственное распределение нуклеиновых кислот-мишеней может коррелировать с изображением ROI или изображением образца ткани, в котором идентифицировали ROI, для визуализации пространственной карты. Таким образом, способ по изобретению относится к индивидуализированной пространственной карте, которую можно конструировать с учетом вопроса, на который необходимо ответить, принимая во внимание информацию о ткани.
В рамках изобретения термин "нуклеиновая кислота" означает любую молекулу нуклеиновой кислоты, которую можно определять способами, представленными в настоящем описании. Молекулы нуклеиновой кислоты включают природные нуклеиновые кислоты, такие как дезоксирибонуклеиновая кислота (ДНК) или рибонуклеиновая кислота (РНК), а также искусственно сконструированные нуклеиновые кислоты, например, аналоги нуклеиновых кислот, химически синтезированные или полученные посредством технологии рекомбинантных генов (см., например, Sambrook, J. et al. (1989) Molecular, Cloning: A Laboratory Manual, 2nd ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY). Конкретные примеры искусственно сконструированных нуклеиновых кислот включают пептид-нуклеиновые кислоты (ПНК) или замкнутые нуклеиновые кислоты (ЗНК). Конкретные примеры природных нуклеиновых кислот включают последовательности ДНК, такие как молекулы геномной ДНК или кДНК, а также последовательности РНК, такие как молекулы hnRNA, мРНК или рРНК, или обратные комплементарные последовательности нуклеиновой кислоты. Нуклеиновые кислоты могут иметь любую длину, и могут являться одноцепочечными или двухцепочечными молекулами. В рамках изобретения термин "нуклеотид" следует понимать как относящийся к рибонуклеотидам и дезоксирибонуклеотидам (т.е. молекулам РНК и ДНК). В одном из вариантов осуществления нуклеиновая кислота является ДНК. В другом варианте осуществления нуклеиновая кислота является РНК.
В рамках изобретения термин "нуклеиновая кислота-мишень" означает нуклеиновую кислоту или нуклеиновые кислоты, подлежащие картированию. В одном из вариантов осуществления термин "нуклеиновая кислота-мишень" относится ко всем нуклеиновым кислотам в образце, предпочтительно - ко всем ДНК или ко всем РНК в образце. В другом варианте осуществления термин "нуклеиновая кислота-мишень" относится ко всем нуклеиновым кислотам конкретного типа в образце, например, мРНК, тРНК или рРНК. В другом варианте осуществления нуклеиновая кислота-мишень является одной или более конкретными интересующими нуклеиновыми кислотами. Интересующая нуклеиновая кислота может являться любым геном генома, предпочтительно - любым геном генома человека. Например, нуклеиновая кислота-мишень может быть ассоциирована с заболеванием, например, злокачественным заболеванием, таким как злокачественное новообразование, воспаление, бактериальная инфекция или вирусная инфекция. Примеры таких нуклеиновых кислот включают нуклеиновые кислоты, специфические для патогена или пораженных клеток или ткани или продуцируемые ими, а также нуклеиновые кислоты, продуцируемые в ответ на заболевание, такие как нуклеиновые кислоты, кодирующие цитокины или антигены. Нуклеиновые кислоты-мишени могут иметь любой размер. В одном из вариантов осуществления нуклеиновая кислота-мишень является ДНК. В другом варианте осуществления нуклеиновая кислота-мишень является РНК. В предпочтительном варианте осуществления нуклеиновая кислота-мишень является РНК, предпочтительно, все мРНК образца.
Нуклеиновая кислота-мишень может являться фрагментированной или интактной. В одном из вариантов осуществления нуклеиновая кислота-мишень фрагментирована. Фрагментированные нуклеиновые кислоты можно получать любыми способами, известными в этой области, такими как физические способы, например, обработка ультразвука, химические способы или ферментативные способы, например, с использованием эндонуклеаз, таких как ферменты рестрикции. Фрагментацию можно осуществлять до, в течение или после идентификации ROI в образце ткани. В одном из вариантов осуществления фрагментацию осуществляют на стадии фиксации ткани. Например, замораживание образца или фиксация образца формалином могут приводить, по меньшей мере, к частичной фрагментации нуклеиновых кислот. Другие фиксаторы могут приводить к схожим результатам.
Фрагментированная нуклеиновая кислота может составлять приблизительно до 20000 нуклеотидов в длину. Как правило, фрагментированные нуклеиновые кислоты составляют от 10 до 10000 нуклеотидов в длину, например, от 20 до 2000 нуклеотидов, от 30 до 1000 нуклеотидов или от 50 до 500 нуклеотидов. Фрагментация нуклеиновых кислот может не приводить к тому, что все нуклеиновые кислоты будут фрагментированными. Таким образом, после фрагментации нуклеиновые кислоты могут являться частично фрагментированными. В предпочтительном варианте осуществления нуклеиновые кислоты являются, по меньшей мере, частично фрагментированными. В другом варианте осуществления нуклеиновые кислоты являются интактными. В одном из вариантов осуществления нуклеиновая кислота-мишень является фрагментированной ДНК или фрагментированной РНК. В другом варианте осуществления нуклеиновая кислота-мишень является интактной ДНК или интактной РНК. В предпочтительном варианте осуществления нуклеиновая кислота-мишень является, по меньшей мере, частично фрагментированной РНК, предпочтительно - всей мРНК образца.
В рамках изобретения термин "молекула нуклеиновой кислоты", относится к одной конкретной молекуле нуклеиновой кислоты, присутствующей в заранее определенном участке в ROI. Например, в вариантах осуществления, в котором вся мРНК в ROI подлежит воздействию, молекула нуклеиновой кислоты представляет собой одну молекулу мРНК.
В рамках изобретения термин "образец" означает любой биологический образец, который можно получать из любого организма, например, растения, животного, грибов, человека или любого искусственного образца. В предпочтительном варианте осуществления образец является образцом ткани. "Образец ткани" может являться собранным, культивированным или биопсийным образцом ткани или его частью. Образец ткани можно получать из пораженной ткани, такой как ткань злокачественного новообразования, воспаленная ткань или инфицированная ткань, ткань, смежная с пораженной тканью, или здоровая ткань. В предпочтительном варианте осуществления образец ткани получают из пораженной ткани или ткани, смежной с ней.
Образец ткани может являться биологическим образцом ткани или искусственным образцом ткани. Термин "биологический образец ткани" относится к природной совокупности клеток и включает клинические образцы, полученные при биопсии или хирургическом вмешательстве, цитологические образцы или культивируемые клетки, образующие ткань. Биологический образец ткани можно получать любым общепринятым способом получения образца ткани. В одном из вариантов осуществления биологический образец ткани является гистопатологическим образцом. В другом варианте осуществления биологический образец ткани является цитологическим образцом. "Искусственный образец ткани" получают из клеток, в природе не образующих солидную ткань, например, крови или суспензионных культур клеток. Искусственный образец ткани можно получать из клеточной суспензии, полученной из клинических образцов, таких как цельная кровь, лимфа или CSF, или из клеточных суспензий, полученных способами in vitro. Клетки можно фиксировать в матрице, такой как гелевая матрица, и рассекать общепринятыми способами, как описано, например, в Andersson et al., 2006, J Histochem Cytochem 54(12): 1413-23. Искусственный образец ткани может являться единичным слоем клеток или содержать множество слоев клеток. В одном из вариантов осуществления искусственный образец ткани получают из клеточной суспензии, полученной из клинических образцов. В другом варианте осуществления искусственный образец ткани получают из клеточной суспензии, полученной способами in vitro. В предпочтительном варианте осуществления образец ткани является биологическим образцом ткани, предпочтительно - клиническим образцом, даже более предпочтительно - гистопатологическим образцом или цитологическим образцом.
Образец ткани может иметь слой клеток толщиной приблизительно в 1 клетку или менее. В одном из вариантов осуществления толщина образца ткани будет составлять менее 0,9, 0,8, 0,7, 0,6, 0,5, 0,4, 0,3, 0,2 или 0,1 поперечного сечения клетки. В другом варианте осуществления образец ткани может иметь толщину более 1 клетки. В одном из вариантов осуществления толщина среза образца ткани будет составлять по меньшей мере приблизительно 0,1 мкм, предпочтительно - по меньшей мере приблизительно 0,2, 0,3, 0,4, 0,5, 0,7, 1,0, 1,5, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мкм. В других вариантах осуществления толщина среза образца ткани составляет по меньшей мере приблизительно 10, 11, 12, 13, 14, 15, 20, 30, 40 или 50 мкм. Также при желании или для удобства можно использовать более толстые образцы, например, образец ткани может иметь толщину приблизительно 70 или 100 мкм или более. Как правило, толщина среза образца ткани составляет приблизительно 1-100 мкм, 1-50 мкм, 1-30 мкм, 1-25 мкм, 1-20 мкм, 1-15 мкм, 1-10 мкм, 3-10 мкм, 2-8 мкм, 3-7 мкм или 4-6 мкм. В предпочтительном варианте осуществления образец ткани имеет толщину в диапазоне 3-10 мкм. Толщина образца ткани не критична для способа по изобретению, и значения являются исключительно характерными значениями.
Образец ткани может иметь размер приблизительно 2 см2. В одном из вариантов осуществления образец ткани имеет длину приблизительно 0,5, 0,6, 0,7, 0,8, 0,9, 1,0, 1,2, 1,5, 1,7, 2,0, 2,5, 3,0, 3,5, или 4,0 см, или длина составляет любое число между ними, и высоту приблизительно 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1,0, 1,2, 1,5, 1,7 или 2,0 см, или высота составляет любое число между ними. Высота и длина образца являются взаимозаменяемыми. В конкретном варианте осуществления образец ткани имеет максимальный размер 2,0×4,0 см. В другом варианте осуществления образец ткани имеет площадь приблизительно 0,5, 0,6, 0,7, 0,8, 0,9, 1,0, 1,2, 1,5, 1,7, 2,0, 2,5, 3,0, 3,5, 4,0, 4,5, 5,0, 5,5, 6,0, 6,5, 7,0, 7,5 или 8,0 см2, или площадь составляет любое число между ними. В предпочтительном варианте осуществления образец ткани имеет максимальный размер приблизительно 2,0×4,0 см, предпочтительно образец ткани имеет площадь в диапазоне приблизительно от 1,0 до 5,0 см2, более предпочтительно - площадь составляет приблизительно 2,0 см2.
Образец ткани может являться свежим, замороженным, фиксированным или нефиксированным. В одном из вариантов осуществления образец ткани является свежим образцом. В другом варианте осуществления образец ткани является свежезамороженным образцом. В еще одном варианте осуществления образец ткани является фиксированным образцом ткани. Для замораживания, фиксации или заключения образца ткани можно использовать любой способ, известный в этой области. В частности, можно использовать любые известные фиксаторы или материалы для заключения. В одном из вариантов осуществления образец ткани является депарафинизированным, фиксированным в формалине и погруженным в парафин (FFPE) образцом. В предпочтительном варианте осуществления образец ткани является FFPE-образцом, свежезамороженным образцом или свежим образцом из гистопатологического образца или цитологического образца, предпочтительно - FFPE-образцом из гистопатологического образца.
В одном из аспектов изобретение относится к способу пространственной детекции нуклеиновых кислот в образце ткани, включающему стадии:
идентификации по меньшей мере одной интересующей области (ROI) в образце;
нанесения по меньшей мере одного вида олигонуклеотидных зондов на заранее определенные участки ROI и связывания олигонуклеотидных зондов с нуклеиновыми кислотами образца, где олигонуклеотидные зонды содержат последовательность-штрих-код;
выделения комплексов нуклеиновая кислота-олигонуклеотидные зонды;
секвенирования выделенных молекул нуклеиновой кислоты;
определение корреляции секвенированных молекул нуклеиновой кислоты с исходной локализацией соответствующих молекул-мишеней нуклеиновой кислоты в ROI для получения пространственного распределения молекул-мишеней нуклеиновой кислоты, где каждый участок идентифицируют посредством одного или более видов олигонуклеотидных зондов, связавшихся на стадии b).
В рамках изобретения термин "способ пространственной детекции" относится к способу детекции нуклеиновых кислот-мишеней и идентификации исходной локализации указанных нуклеиновых кислот в образце.
Термин "молекулы-мишени нуклеиновой кислоты" соответствует нуклеиновым кислотам из образца, связанным олигонуклеотидными зондами на стадии b).
Интересующую область (ROI) можно идентифицировать в образце ткани с учетом информации о ткани, которую можно получать любым способом, известным в этой области. Например, образец ткани можно визуализировать, окрашивать или метить подходящими маркерами. В одном из вариантов осуществления ROI идентифицируют посредством окрашивания. В другом варианте осуществления ROI идентифицируют посредством мечения подходящими маркерами. В еще одном варианте осуществления ROI идентифицируют посредством визуализации. В предпочтительном варианте осуществления ROI идентифицируют с учетом анализа изображения. Анализ изображения можно осуществлять автоматически или вручную. В случае автоматической селекции ROI необходим анализ изображения. Можно использовать все распространенные способы осуществления анализа изображений.
ROI, как обозначают в настоящем описании, также может содержать окружающую область идентифицированной ROI, т.е. площадь, непосредственно смежную с областью, идентифицированной как интересующая. ROI может иметь любой размер от того же размера, что и у образца ткани (максимальный размер), до размера ячейки решетки (минимальный размер). Предпочтительно, чтобы размер ROI был меньше размера образца ткани.
В образце ткани можно идентифицировать по меньшей мере одну ROI. В образце ткани также можно идентифицировать несколько ROI. Например, образец ткани может содержать две, три, четыре, пять, десять или более ROI. Различные ROI можно идентифицировать различными способами, например, некоторые из ROI идентифицируют автоматически с помощью программного обеспечения для анализа изображений, и патолог также может указывать ROI вручную. В предпочтительном варианте осуществления в образце ткани идентифицируют по меньшей мере одну ROI, предпочтительно - в образце ткани идентифицируют две ROI, более предпочтительно - в образце ткани идентифицируют более двух ROI.
В конкретном варианте осуществления образец ткани можно разрезать на два слоя. На один слой наносят метки для стадии визуализации. Основываясь на изображении этого референсного слоя выбирают ROI и наносят на второй слой (микроскопический препарат для выделения нуклеиновых кислот). На втором слое осуществляют связывание олигонуклеотидных зондов, содержащих последовательность-штрих-код. Способ обладает преимуществом, состоящим в том, что на референсном микроскопическом препарате можно использовать метки для визуализации, не совместимые со следующими стадиями способа, например, связыванием олигонуклеотидных зондов, выделением молекулы нуклеиновой кислоты или секвенированием, и, таким образом, они не мешают реакциям, осуществляемым на втором слое образца ткани (микроскопический препарат для выделения нуклеиновых кислот).
В рамках изобретения термин "олигонуклеотидный зонд" означает молекулы нуклеиновой кислоты, содержащие последовательность-штрих-код. Олигонуклеотидные зонды, например, могут являться зондами РНК или зондами ДНК. Олигонуклеотидные зонды, содержащие идентичные последовательности-штрих-коды, обозначают как "виды олигонуклеотидных зондов". Каждый вид олигонуклеотидных зондов содержит уникальную последовательность-штрих-код. Последовательности-штрих-коды можно конструировать или получать с использованием получения случайных последовательностей. Сконструированные или случайным образом полученные последовательности можно анализировать для обеспечения того, что последовательности-штрих-коды не будут мешать захвату нуклеиновых кислот. Последовательность-штрих-код можно лигировать с нуклеиновыми кислотами в образце. Последовательность-штрих-код не действует как праймер. Последовательность-штрих-код может иметь размер в диапазоне приблизительно 1-8 нуклеотидов.
Олигонуклеотидные зонды могут дополнительно содержать "генерическую последовательность". Генерическую последовательность можно использовать для захвата нуклеиновых кислот в образце посредством гибридизации с нуклеиновой кислотой, подлежащей направленному воздействию. В одном из вариантов осуществления генерическую последовательность используют для селективной амплификации нуклеиновых кислот в образце. В таком варианте осуществления генерическую последовательность обозначают как "последовательность праймера". Последовательность праймера комплементарна нуклеиновым кислотам в образце, подлежащим направленному воздействию. Например, последовательность праймера может содержать поли-T-последовательность, если тотальная мРНК образца подлежит направленному воздействию, или последовательность праймера может содержать нуклеотиды, комплементарные участку последовательности конкретного гена, если только нуклеиновые кислоты, экспрессируемые указанным геном, подлежат направленному воздействию. В альтернативном варианте осуществления генерическую последовательность используют для обеспечения стабильного лигирования последовательности-штрих-кода с нуклеиновыми кислотами в образце, т.е. генерическую последовательность можно лигировать с нуклеиновыми кислотами в образце, подлежащими направленному воздействию. В таком варианте осуществления генерическую последовательность обозначают как "последовательность лигирования". В одном из вариантов осуществления последовательность-штрих-код лигируют напрямую с нуклеиновыми кислотами в образце, и генерическая последовательность не является необходимой. В одном из вариантов осуществления олигонуклеотидный зонд содержит по меньшей мере одну генерическую последовательность. Генерическая последовательность может иметь размер в диапазоне приблизительно от 0 до 100 нуклеотидов, предпочтительно - от 0 до 50 нуклеотидов, более предпочтительно - от 0 до 30 нуклеотидов, даже более предпочтительно - приблизительно от 5 до 30 нуклеотидов.
Олигонуклеотидные зонды могут дополнительно содержать одну или более "дополнительных последовательностей". В одном из вариантов осуществления дополнительную последовательность можно использовать для обогащения нуклеиновых кислот ("последовательность обогащения") или для очистки нуклеиновых кислот ("последовательность очистки"). В другом варианте осуществления дополнительную последовательность можно использовать для обогащения и очистки нуклеиновых кислот. Дополнительные последовательности также могут являться последовательностями для секвенирования, такими как адаптеры, используемые для секвенирования следующего поколения, или последовательностями для селекции или идентификации. В одном из вариантов осуществления дополнительная последовательность может являться последовательностью, по которой выравнивают праймер ("последовательность для выравнивания праймеров"). В вариантах осуществления, когда олигонуклеотидные зонды содержат последовательность лигирования, олигонуклеотидные зонды могут дополнительно содержать последовательность для выравнивания праймеров. Последовательность праймера может быть комплементарна последовательности для выравнивания праймеров.
Олигонуклеотидные зонды могут дополнительно содержать одну или более спейсерных последовательностей, также обозначаемых как спейсер. Спейсеры можно располагать между двумя разными элементами последовательности олигонуклеотидных зондов. Спейсер может иметь размер в диапазоне приблизительно от 0 до 20 нуклеотидов. Олигонуклеотидные зонды могут составлять приблизительно от 15 до 150 нуклеотидов в длину. В предпочтительном варианте осуществления олигонуклеотидные зонды составляют приблизительно от 15 до 100 нуклеотидов в длину, предпочтительно - приблизительно от 20 до 50 нуклеотидов.
Олигонуклеотидные зонды могут находиться в сухой форме или жидкой форме. В предпочтительном варианте осуществления олигонуклеотидные зонды находятся в жидкой фазе, предпочтительно - в буферном растворе или краске. Термин "краска" относится к любому раствору, подходящему для печати. В вариантах осуществления, когда олигонуклеотидные зонды находятся в сухой форме, олигонуклеотидные зонды растворяют перед нанесением.
В одном из вариантов осуществления олигонуклеотидные зонды связываются со всеми молекулами ДНК в образце. В предпочтительном варианте осуществления олигонуклеотидные зонды связываются со всеми молекулами РНК в образце для получения пространственной карты транскриптома. В другом предпочтительном варианте осуществления олигонуклеотидные зонды связываются лишь с конкретными молекулами РНК, такими как мРНК, рРНК, тРНК или другие некодирующие РНК, предпочтительно, олигонуклеотидные зонды специфически связываются с мРНК.
Термин "связывание олигонуклеотидных зондов с нуклеиновыми кислотами образца" относится к получению комплексов нуклеиновая кислота-олигонуклеотидные зонды. Связывания олигонуклеотидных зондов с нуклеиновыми кислотами образца можно достигать различными способами.
В одном из вариантов осуществления олигонуклеотидные зонды лигируют с нуклеиновыми кислотами-мишенями в образце. Лигирование можно осуществлять с помощью последовательности-штрих-кода или генерической последовательности (последовательности лигирования). Таким образом, в одном из предпочтительных вариантов осуществления связывание олигонуклеотидных зондов с нуклеиновыми кислотами образца происходит посредством лигирования. Олигонуклеотидные зонды можно лигировать с нуклеиновой кислотой-мишенью любым известным в этой области способом. Например, лигирование с мРНК можно осуществлять с помощью поли-A-хвоста, в то время как лигирование с ДНК можно осуществлять после стадии расщепления, получая липкие концы, с которыми олигонуклеотидные зонды гибридизуются. В конкретном варианте осуществления олигонуклеотидный зонд содержит (i) последовательность лигирования, (ii) последовательность-штрих-код и, необязательно, (iii) одну или более дополнительных последовательностей. Различные последовательности можно разделять спейсерами. Кроме того, дополнительные последовательности также могут локализоваться между последовательностью лигирования и последовательностью-штрих-кодом. Если нуклеиновая кислота-мишень подлежит амплификации, присутствует последовательность для выравнивания праймеров. Таким образом, в другом конкретном варианте осуществления олигонуклеотидный зонд содержит (i) последовательность лигирования, (ii) последовательность-штрих-код и (iii) последовательность для выравнивания праймеров. Олигонуклеотидный зонд может содержать спейсеры и/ или дополнительные последовательности. Последовательности расположены в олигонуклеотидном зонде таким образом, что при амплификации или реакции обратной транскрипции штрих-код встраивается в амплифицированную ДНК или кДНК, соответственно. В другом предпочтительном варианте осуществления олигонуклеотидный зонд содержит последовательность-штрих-код, лигируемую с нуклеиновой кислотой, после которой может следовать одна или более генерических и/или дополнительных последовательностей.
В альтернативном варианте осуществления олигонуклеотидный зонд содержит последовательность праймера. В этом случае необходима амплификация и/или обратная транскрипция нуклеиновой кислоты. Таким образом, в одном из предпочтительных вариантов осуществления связывание олигонуклеотидных зондов с нуклеиновыми кислотами образца происходит посредством гибридизации, где олигонуклеотидные зонды используют в качестве праймеров для амплификации или обратной транскрипции. В вариантах осуществления, когда олигонуклеотидный зонд действует в качестве праймера, олигонуклеотидный зонд содержит (i) последовательность праймера, (ii) последовательность-штрих-код и, необязательно, (iii) одну или более дополнительных последовательностей, где последовательность праймера действует в качестве праймера для амплификации или реакции обратной транскрипции. Олигонуклеотидные зонды могут содержать спейсеры и/или дополнительные последовательности. Последовательности располагают в олигонуклеотидном зонде таким образом, что при амплификации или реакции обратной транскрипции штрих-код встраивают в амплифицируемую ДНК или кДНК, соответственно.
Следует понимать, что связывание олигонуклеотидных зондов с нуклеиновыми кислотами в образце не ограничено описываемыми выше вариантами осуществления и может происходить различными другими способами. Например, генерические последовательности для выравнивания праймеров можно лигировать с нуклеиновыми кислотами-мишенями и олигонуклеотидные зонды можно использовать в качестве праймеров при амплификации или реакции обратной транскрипции. Другим примером может являться лигирование с нуклеиновыми кислотами, такими как липкие концы ДНК после расщепления, с которыми при второй реакции лигирования лигируют олигонуклеотидный зонд. Специалисту в этой области будет известен другой молекулярный способ для захвата нуклеиновых кислот, подлежащих направленному воздействию, и различные варианты для встраивания последовательности-штрих-кода.
Связывание олигонуклеотидных зондов с нуклеиновыми кислотами в образце включает связывание одного или более видов олигонуклеотидных зондов с молекулами нуклеиновой кислоты в заранее определенном участке в ROI. В одном из вариантов осуществления один вид олигонуклеотидных зондов наносят на каждый заранее определенный участок в ROI. Таким образом, в конкретном варианте осуществления один вид олигонуклеотидных зондов связывается с одной молекулой-мишенью нуклеиновой кислоты в одном заранее определенном участке. Этот подход является предпочтительным для небольшого количества заранее определенных участков или подходов с низким разрешением.
В другом варианте осуществления по меньшей мере два разных вида олигонуклеотидных зондов наносят на один заранее определенный участок в ROI. Таким образом, в конкретном варианте осуществления по меньшей мере два различных вида олигонуклеотидных зондов связываются с одной молекулой-мишенью нуклеиновой кислоты в одном заранее определенном участке. Этот подход делает возможным пространственное картирование комплексных молекулярных профилей с высоким разрешением, в которых эффективно используют мультиплексирование ROI на образец. В одном конкретном варианте осуществления по меньшей мере один из видов олигонуклеотидных зондов, связывающийся с одной молекулой нуклеиновой кислоты, связывается посредством лигирования с помощью последовательности-штрих-кода. В другом конкретном варианте осуществления по меньшей мере один из видов олигонуклеотидных зондов, связывающийся с одной молекулой нуклеиновой кислоты, содержит генерическую последовательность, где, необязательно, генерическая последовательность комплементарна нуклеиновой кислоте-мишени. Например, один вид олигонуклеотидных зондов может содержать последовательность лигирования, и второй вид олигонуклеотидных зондов может содержать последовательность праймера для амплификации или обратной транскрипции нуклеиновой кислоты. В другом примере один вид олигонуклеотидных зондов может не содержать генерическую последовательность, и второй вид олигонуклеотидных зондов может содержать генерическую последовательность; таким образом, олигонуклеотидный зонд без генерической последовательности может связываться с молекулой нуклеиновой кислоты посредством лигирования с помощью последовательности-штрих-кода, и олигонуклеотидный зонд с генерической последовательностью может связываться посредством гибридизации с помощью последовательности праймера или последовательности лигирования. В другом варианте осуществления по меньшей мере один вид олигонуклеотидных зондов, связывающийся с одной молекулой нуклеиновой кислоты, содержит дополнительную последовательность, где дополнительная последовательность является последовательностью очистки или последовательностью для выравнивания праймеров. Например, один вид олигонуклеотидных зондов может содержать последовательность лигирования и последовательность очистки, и второй вид олигонуклеотидных зондов может содержать последовательность праймера. В другом примере один вид олигонуклеотидных зондов может не содержать генерическую последовательность, но содержать дополнительную последовательность, и второй вид олигонуклеотидных зондов может лишь содержать генерическую последовательность; таким образом, олигонуклеотидный зонд без генерической последовательности может связываться с молекулой нуклеиновой кислоты посредством лигирования с помощью последовательности-штрих-кода и содержать последовательность для выравнивания праймеров, с которой гибридизуется прямой праймер, и олигонуклеотидный зонд с генерической последовательностью может связываться посредством гибридизации, где генерическая последовательность действует в качестве обратного праймера. Следует понимать, что комбинации последовательностей в одном виде олигонуклеотидных зондов не ограничен описываемыми выше вариантами осуществления. Специалисту в этой области будет известно, что возможны многочисленные другие комбинации для захвата нуклеиновых кислот, подлежащих направленному воздействию, и мечения их соответствующим штрих-кодом. Таким образом, конкретно включены дополнительные комбинации последовательностей в одном виде олигонуклеотидных зондов при комбинировании по меньшей мере с одним дополнительным видом олигонуклеотидных зондов, подходящих для эффективного мечения нуклеиновой кислоты-мишени.
"Заранее определенный участок", на который наносят олигонуклеотидные зонды, представляет собой одно или более положений в ROI. В зависимости от потребности исследователя целую ROI можно разделять на отдельные заранее определенные участки, т.е. один заранее определенный участок находится рядом с другим заранее определенным участком таким образом, что они имеют границу, или можно выбирать части ROI, т.е. заранее определенный участок в ROI может представлять островки, разделенные областями в ROI, на которые не наносят зонды. Предпочтительно, термин "заранее определенные участки" относится к нескольким положениям в ROI.
В одном из вариантов осуществления заранее определенные участки в ROI расположены систематически, например, рядами и колонками. В одном из вариантов осуществления ROI содержит, по меньшей мере, 1, 2, 5, 10, 50, 100, 500, 750, 1000, 1500, 3000, 5000, 10000, 20000, 40000, 50000, 75000, 100000, 150000, 200000, 300000, 400000, 500000, 750000, 800000, 1000000 или более заранее определенных участков. В предпочтительном варианте осуществления ROI содержит по меньшей мере 1, 2, 5, 10, 20, 30, 40, 50 или 100 заранее определенных участков, предпочтительно, ROI содержит по меньшей мере 10 заранее определенных участков. В другом варианте осуществления площадь каждого заранее определенного участка может составлять приблизительно 1 мкм2, 2 мкм2, 3 мкм2, 4 мкм2, 5 мкм2, 10 мкм2, 12 мкм2, 15 мкм2, 20 мкм2, 50 мкм2, 75 мкм2, 100 мкм2, 150 мкм2, 200 мкм2, 250 мкм2, 300 мкм2, 400 мкм2 или 500 мкм2. На каждый заранее определенный участок наносят уникальный вид олигонуклеотидных зондов или уникальную комбинацию двух или более различных видов олигонуклеотидных зондов. Если наносят два или более вида олигонуклеотидных зондов, предпочтительно, чтобы различные виды олигонуклеотидных зондов наносили на каждый ряд и различные виды олигонуклеотидных зондов наносили на каждую колонку. Например, ряд 1 содержит один вид олигонуклеотидных зондов, отличающийся от вида олигонуклеотидных зондов в ряду 2, в свою очередь, отличающегося от олигонуклеотидных зондов в ряду 3 и т.д. Колонка A содержит вид олигонуклеотидных зондов, отличающийся от любого из видов олигонуклеотидных зондов, наносимых в рядах, и снова, колонка B содержит дополнительный другой вид олигонуклеотидных зондов и т.д. Таким образом, заранее определенный участок в колонке A ряду 1 (A1) имеет уникальную комбинацию олигонуклеотидных зондов, отличающуюся от комбинации A2, B1 или B2 и т.д. При использовании этого подхода необходимо использовать меньше видов олигонуклеотидных зондов, что снижает стоимость анализа. Можно добавлять дополнительные виды олигонуклеотидных зондов, например, добавлять другие виды олигонуклеотидных зондов по диагонали или для свободного определения заранее определенных участков, таких как под-ROI. В предпочтительном варианте осуществления уникальную комбинацию по меньшей мере двух видов олигонуклеотидных зондов наносят на каждый заранее определенный участок, предпочтительно - уникальную комбинацию двух видов олигонуклеотидных зондов.
В альтернативном варианте осуществления свободно определяют заранее определенные участки в ROI. Свободное расположение заранее определенных участков обладает преимуществом, заключающимся в том, что можно определять дополнительные интересующие подобласти (под-ROI) в ROI без каких-либо ограничений. Таким образом, по сравнению с общепринятым расположением решеток в колонках и рядах с регулярными признаками равного размера, свободное расположение делает возможными заранее определенные участки любой формы и размера и другие заранее определенные участки других форм и размеров. Например, в образце ткани можно идентифицировать ROI с учетом наличия конкретного типа клеток. В указанной ROI можно идентифицировать дополнительные под-ROI с учетом морфологических признаков. Эти под-ROI могут образовывать отдельные островки в ROI, имеющие различные формы и размеры. Заранее определенные участки в ROI можно определять таким образом, что каждая под-ROI представляет собой отдельный заранее определенный участок. В таком случае остальная ROI без областей, покрываемых под-ROI, может не представлять интерес, и на эту область не наносят олигонуклеотидные зонды, или они могут представлять собой дополнительный заранее определенный участок, или ее можно дополнительно разделять на заранее определенные участки посредством систематического расположения рядов и колонок. На каждый заранее определенный участок можно наносить уникальный вид олигонуклеотидных зондов или уникальную комбинацию двух или более видов олигонуклеотидных зондов. Под-ROI, представляющие собой отдельные заранее определенные участки, могут отличаться друг от друга или могут частично перекрываться. В случаях, когда под-ROI частично перекрываются, область перекрывания будет определяться уникальной комбинацией по меньшей мере одного вида олигонуклеотидных зондов, специфического для первой под-ROI, и по меньшей мере одного вида олигонуклеотидных зондов, специфического для второй под-ROI. В одном из вариантов осуществления по меньшей мере две под-ROI частично перекрываются. В другом варианте осуществления более двух под-ROI частично перекрываются. В еще одном варианте осуществления под-ROI не перекрываются. Любую информацию можно использовать для идентификации под-ROI, и идентификация под-ROI не ограничена информацией, полученной посредством идентификации ROI. Признаки, которые можно использовать для идентификации под-ROI, включают, в качестве неограничивающих примеров, тип клеток, морфологию, цвет, прозрачность, наличие/отсутствие конкретных молекул, таких как, например, антитела, цитокины или лекарственные средства, или подвергание конкретных областей образца ткани воздействию радиации до его забора из пациента.
В дополнительном варианте осуществления заранее определенные участки определяют посредством наложения шаблона. Шаблон может являться "шаблоном разделения". Шаблон разделения может иметь любой паттерн для мечения ROI. В одном из вариантов осуществления шаблон разделения является "решетчатым шаблоном разделения", обеспечивающей ряды и колонки для систематической позиционной характеризации ROI (фиг. 1). В другом варианте осуществления шаблон разделения может являться "шаблоном разделения произвольной формы" с учетом формы ROI и под-ROI (фиг. 1). В другом варианте осуществления шаблон разделения может являться комбинацией решетчатого шаблона разделения и шаблона разделения произвольной формы, как показано в качестве примера на фигуре 1.
Шаблон разделения можно накладывать различными способами. В одном из вариантов осуществления с помощью шаблона разделения определяют заранее определенные области, получая полную борозду, наносимую через всю толщину образца ткани ("полный шаблон разделения"), предпочтительно, посредством процарапывания, лазерной абляции или создания физических барьеров, таких как металлическая сетка. В другом варианте осуществления с помощью шаблона разделения определяют заранее определенные области с помощью верхнего барьера ("верхний шаблон разделения"). С помощью верхнего шаблона разделения можно определять заранее определенные участки с помощью физических барьеров. С помощью верхнего шаблона разделения также можно определять заранее определенные области посредством структурирования, ограничивающего реагенты в желаемой области ("позиционный шаблон"), предпочтительно, с помощью топологического ограничения или получения паттернов локальной смачиваемости ткани. Можно использовать литографические способы для структурирования таких слоев. В предпочтительном варианте осуществления поверхность ROI структурируют с помощью самоорганизованного монослоя (SAM) на тонком слое золота, выпариваемом на поверхности ROI. Слой SAM можно наносить посредством микроконтактной печати органического тиола, используемого в качестве кислотоупорного копировального слоя при травлении слоя золота. SAM является гидрофобным и предотвращает распространение олигонуклеотидных зондов при чернильной печати. Верхний шаблон разделения также можно печатать сверху ROI, где чернила действуют в качестве физического барьера. На фигуре 1 показаны виды сбоку примера верхнего шаблона разделения 5 и полного шаблона разделения 6. В одном из вариантов осуществления заранее определенные участки определяют с помощью шаблона разделения. В предпочтительном варианте осуществления шаблон разделения является верхним шаблоном разделения, необязательно, напечатанным на образце, или полным шаблоном разделения, где шаблон разделения является решетчатым шаблоном разделения, шаблоном разделения произвольной формы или их комбинацией. В более предпочтительном варианте осуществления шаблон разделения является верхним шаблоном разделения, наносимым посредством печати. Можно использовать чернильную печать воска с использованием нагреваемой головки для чернильной печати или чернильную печать с использованием краски, закрепляющейся под действием УФ-излучения. Оба способа хорошо известны в полиграфической промышленности.
Верхние шаблоны также можно наносить в виде заранее произведенной интегральной части, подобной планшету для микротитрования с открытым основанием. Планшет для микротитрования может являться 384-луночным планшетом, или 1536-луночным планшетом, или планшетом с любым другим количеством лунок, произведенным для такой цели. Планшет с лунками можно прижимать к образцу ткани для обеспечения хорошего физического контакта между пластиковыми стенками планшета с лунками и образцом ткани. Затем можно добавлять олигонуклеотидные зонды, разведенные в буфере в каждой лунке, перекрывающейся с заранее определенной ROI. В каждую лунку можно вводить разные чернила, т.е. другой олигонуклеотидный зонд. Возможно многократное нанесение для нанесения всех реагентов. Можно использовать чернильную печать или микродозирование для введения реагентов в лунки. Высота стенок верхнего шаблона составляет порядка от 0,5 до 5 мм. Это означает, что распределяемый объем в каждой лунке может составлять порядка от 100 нл до 10 мкл, более предпочтительно - от 0,5 до 2 мкл.
В другом варианте осуществления не используют шаблон разделения (будь то физический, химический или механический шаблон) и заранее определенные участки определяют посредством местного нанесения олигонуклеотидных зондов таким образом, что они не перемешиваются между различными заранее определенными участками на образце. В одном из вариантов осуществления олигонуклеотидные зонды наносят с использованием чернил для печати, не распространяющихся быстро, или объем которых поддерживают достаточно низким для поддержания желаемого пространственного разрешения, где с помощью паттерна печати определяют заранее определенные участки. В этом варианте осуществления нанесение олигонуклеотидных зондов и определение заранее определенных участков осуществляют одновременно. Чернила могут образовывать гель после нанесения для обеспечения фиксации в желаемом положении, в то время как олигонуклеотидные зонды все равно способны диффундировать в ROI образца ткани. Для нанесения олигонуклеотидных зондов с конкретным паттерном на ROI можно использовать известные в этой области технологии переноса жидкостей. В одном из вариантов осуществления олигонуклеотидные зонды наносят на заранее определенные участки с помощью технологий переноса жидкостей, предпочтительно, способами контактной печати или способами неконтактной печати, таким образом, что наносимые олигонуклеотидные зонды не перемешиваются между различными заранее определенными участками. В предпочтительном варианте осуществления технология переноса жидкостей является способом контактной печати, предпочтительно, нанолитографии погружного пера или микроконтактной печати. В другом предпочтительном варианте осуществления технология переноса жидкостей является способом неконтактной печати, предпочтительно, чернильной. В одном из вариантов осуществления олигонуклеотидные зонды печатают горизонтальными линиями или точками, расположенными горизонтальными линиями (представляющими собой ряды). Затем используют вертикальное движение для печати олигонуклеотидных зондов вертикальными линиями или в положении наверху уже существующих точек (представляющих собой колонки). Можно использовать многосопловые принтеры, с помощью которых можно печатать различные чернила одновременно. Можно использовать печатающую головку с термической подачей или печатающую головку с пьезоэлектрической подачей. Принтеры с печатающими головками с пьезоэлектрической подачей являются предпочтительными во избежание возможной деградации белков в типографской краске. Выбранную технологию переноса жидкостей можно адаптировать с учетом желаемого разрешения. В другом варианте осуществления олигонуклеотидные зонды печатают в зависимости от форм идентифицированных под-ROI.
Типографская краска содержит олигонуклеотидные зонды, растворенные в растворителе, подобном воде или физиологическому раствору, необязательно, с поверхностно-активными веществами и стабилизаторами. Концентрации олигонуклеотидных зондов в чернилах могут находиться в диапазоне от 1 нМ до 1 мМ, предпочтительно - от 100 нМ до 10 мкМ. Различные олигонуклеотиды можно растворять в тех же чернилах. Предпочтительно, также ферменты растворяют в тех же чернилах. Для стабильности ферментов можно добавлять BSA или другие сыворотки в концентрациях, типичных для стабильного хранения, например, от 0,5 до 5% масс./масс.
Выбирают объемы печати, типичные для используемого способа нанесения и зависящие от желаемого пространственного разрешения. В случае чернильной печати объем печати может находиться в диапазоне от 50 пл до 5 мкл, более предпочтительно - от 100 пл до 1 мкл. В случае нанолитографии погружного пера переносимый объем зависит от размера пера и продолжительности обработки. Типичные переносимые объемы находятся в диапазоне от 1 пл до 1 мкл, предпочтительно - от 10 пл до 100 нл.
Нанесение олигонуклеотидных зондов, как описано для вариантов осуществления, в которых не используют шаблон разделения, также можно использовать для вариантов осуществления, в которых заранее определенные участки определяют с помощью шаблона разделения. Например, в первой стадии можно печатать шаблон разделения, определяющий заранее определенные участки, и на второй стадии олигонуклеотидные зонды можно наносить на заранее определенные участки посредством печати. Таким образом, в одном из вариантов осуществления олигонуклеотидные зонды наносят посредством печати. В другом варианте осуществления олигонуклеотидные зонды наносят иным способом, чем печать, таким как пипетирование.
Олигонуклеотидные зонды также можно получать в гелеобразном слое или гелевом слое, где этот слой наносят на заранее определенные участки в ROI. Гелевый слой можно наносить на ROI за одну стадию и олигонуклеотидные зонды переносят на ROI посредством диффузии. В рамках изобретения термин "гелеобразный" или "гелевый" означает твердый, желеобразный материал, который может иметь свойства в диапазоне от мягкого до твердого, в котором олигонуклеотидные зонды способны диффундировать из геля в ROI. Таким образом, в одном из вариантов осуществления олигонуклеотиды зонды находятся в форме гелевого слоя или гелеобразного слоя, наносимого на образец.
Олигонуклеотидные зонды также можно наносить в отдельные одноразовые контейнеры (например, с небольшими лунками, подобные планшету с лунками), которые будут позднее соединять с ROI. Этот подход обладает преимуществом, состоящим в том, что его можно производить автономно, включая соответствующие меры контроля качества для проверки нанесения всех жидкостей. Автономное нанесение олигонуклеотидных зондов в отдельные одноразовые контейнеры делает использование оборудования для переноса жидкостей в патологической лаборатории устаревшим. В одном из вариантов осуществления ROI можно вдавливать в планшет с лунками, как описано в Armani et al., 2009, Lab Chip 9(24): 3526-3534 и Armani et al., 2011, Anal Bioanal Chem 400: 3383-3393. Олигонуклеотидные зонды или уникальную комбинацию олигонуклеотидных зондов можно добавлять на дно каждой лунки посредством нанесения пятен. Олигонуклеотидные зонды можно сушить перед использованием.
Олигонуклеотидные зонды также можно наносить посредством комбинации указанных выше способов и/или комбинации отсутствия использования шаблона разделения и использования шаблона разделения. Например, на первой стадии олигонуклеотидные зонды можно печатать на разные под-ROI, таким образом, определяя заранее определенные участки без использования шаблона разделения, и на второй стадии олигонуклеотидные зонды можно наносить посредством пипетирования на заранее определенные участки, определяемые верхним шаблоном разделения. Таким образом, олигонуклеотидные зонды можно наносить последовательно или одновременно. Следует понимать, что возможны многочисленные дополнительные комбинации, и нанесение олигонуклеотидных зондов не ограничено описанными выше вариантами осуществления.
В вариантах осуществления, в которых более двух видов олигонуклеотидных зондов наносят на заранее определенные участки в ROI, нанесение может являться последовательным. Например, олигонуклеотидные зонды, подлежащие лигированию с молекулой нуклеиновой кислоты, можно наносить на первой стадии, обеспечивая условия, в которых зонды лигируют с молекулами нуклеиновой кислоты, и на второй стадии можно наносить олигонуклеотидные зонды, гибридизующиеся с молекулами нуклеиновой кислоты и/или олигонуклеотидным зондом, лигированным с молекулами нуклеиновой кислоты. Таким образом, в одном из вариантов осуществления различные виды олигонуклеотидных зондов последовательно наносят на заранее определенные участки в ROI. В другом варианте осуществления различные виды олигонуклеотидных зондов одновременно наносят на заранее определенные участки в ROI.
В предпочтительном варианте осуществления олигонуклеотидные зонды наносят в жидкой фазе на заранее определенные участки в ROI. В дополнительном предпочтительном варианте осуществления олигонуклеотидные зонды наносят в жидкой фазе на заранее определенные участки в ROI, где заранее определенные участки идентифицировали с учетом информации о ткани. В дополнительном предпочтительном варианте осуществления олигонуклеотидные зонды наносят в жидкой фазе с высокой ионной силой, чтобы сделать возможной гибридизацию с молекулами-мишенями. В другом предпочтительном варианте осуществления олигонуклеотидные зонды наносят в жидкой фазе, образующей гель непосредственно после нанесения на образец с помощью перепада температур или радиации. Этого можно достигать посредством добавления полимеров, подобных полиакриламиду, подвергаемому образованию термообратимого геля в растворе, и/или добавления мономеров, которые могут полимеризоваться под действием облучения и, таким образом, приводить к образованию геля. При образовании геля необходимо избегать возможного перемешивания зондов в разных заранее определенных участках.
Молекулы нуклеиновой кислоты в ROI можно заранее обрабатывать. В одном из вариантов осуществления нуклеиновые кислоты из образца заранее обрабатывают для направленного воздействия на правильный тип молекул нуклеиновой кислоты и/или для эффективного лигирования олигонуклеотидных зондов. В вариантах осуществления, в которых нуклеиновые кислоты, подлежащие направленному воздействию, являются молекулами ДНК, предварительная обработка может включать расщепление ДНК для получения фрагментов ДНК меньшего размера способами, хорошо известными в этой области.
После нанесения олигонуклеотидных зондов на заранее определенные участки в ROI, олигонуклеотидные зонды диффундируют в ROI. Размер олигонуклеотидных зондов делает возможным глубокое проникновение в образец ткани за короткое время. Затем олигонуклеотидные зонды в заранее определенных участках ROI связываются с нуклеиновыми кислотами образца, что, таким образом, приводит к образованию комплексов нуклеиновая кислота-олигонуклеотидные зонды. В рамках изобретения термин "комплекс нуклеиновая кислота-олигонуклеотидные зонды" означает комплекс нуклеиновой кислоты, подлежащей детекции, и по меньшей мере одного олигонуклеотидного зонда. Нуклеиновая кислота, подлежащая детекции, может находиться в комплексе более чем с одним видом олигонуклеотидного зонда, например, с двумя видами олигонуклеотидных зондов. При диффузии и связывании обеспечивают влажную атмосферу на поверхности во избежание испарения растворителей. Можно использовать перепад температур в течение этого периода для достижения хорошего прохождения реакций. Шаблон разделения может находиться на месте в течении этой стадии, или, необязательно, его можно удалять после нанесения зондов. Повышенная температура ускоряет диффузию и реакции связывания. Температуру необходимо поддерживать на уровне ниже температуры плавления зондов в случае, когда для связывания используют гибридизацию. Альтернативно, температуру необходимо выбирать таким образом, чтобы лигаза хорошо функционировала. В предпочтительном варианте осуществления температура находится в диапазоне приблизительно от 20 до 45°C, предпочтительно - приблизительно от 30 до 40°C.
После связывания олигонуклеотидных зондов с нуклеиновыми кислотами в образце, из ROI выделяют комплексы нуклеиновая кислота-олигонуклеотидные зонды. В одном из вариантов осуществления выделение осуществляют посредством погружения ROI в буфер для выделения при повышенной температуре. Можно использовать буферы для выделения, общепринятые для получения образцов для молекулярных анализов и известные в этой области. Выделенные нуклеиновые кислоты можно собирать в одну пробирку для дальнейшего анализа. Раствор выделенных зондов нуклеиновая кислота-олигонуклеотидные зонды обозначают как экстракт для пространственного молекулярного профиля (SMP).
В одном из вариантов осуществления выделенные нуклеиновые кислоты очищают известными в этой области способами. В другом варианте осуществления выделенные нуклеиновые кислоты обогащают известными в этой области способами. В дополнительном варианте осуществления выделенные нуклеиновые кислоты очищают и обогащают.
В дополнительном варианте осуществления изобретения молекулы ДНК получают из выделенных комплексов нуклеиновая кислота-олигонуклеотидные зонды с помощью амплификации ДНК, необязательно, где получение молекул ДНК осуществляют после реакции обратной транскрипции. В предпочтительном варианте осуществления выделенные нуклеиновые кислоты являются молекулами РНК, подвергаемыми обратной транскрипции и амплификации.
Амплификацию нуклеиновой кислоты можно осуществлять способами циклической амплификации. Циклическая амплификация может включать любое количество циклов амплификации, равное или превосходящее два. Как правило, циклическая реакция амплификации включает по меньшей мере 10 или по меньшей мере 20 циклов. Примером циклической амплификации является полимеразная цепная реакция (ПЦР). ПЦР является общепринятым стандартным способом молекулярной биологии, подробно описываемым, например, в Sambrook et al., выше. Как правило, ПЦР используют для амплификации двухцепочечных молекул ДНК с использованием термостабильной ДНК-полимеразы. В предпочтительном варианте осуществления амплификация нуклеиновых кислот является циклической амплификацией, предпочтительно - ПЦР.
В альтернативных вариантах осуществления амплификацию нуклеиновых кислот осуществляют способом изотермической амплификации. Амплификация нуклеиновых кислот в изотермических условиях позволяет избегать использования термоциклического устройства. Существует несколько типов изотермических способов амплификации нуклеиновых кислот, известных специалисту в этой области, включая реакцию амплификации с использованием никующего фермента, опосредованную транскрипцией амплификацию, амплификацию, основанную на последовательности нуклеиновой кислоты, сигнал-опосредованную амплификацию по технологии РНК, амплификацию с замещением цепей, амплификацию по типу катящего кольца, изотермическую амплификацию с формированием петель, изотермическую амплификацию с множественным вытеснением цепи, хеликаза-зависимую амплификацию, изотермическую амплификацию с единичным праймером и кольцевую хеликаза-зависимую амплификацию. Обзор технологий изотермической амплификации нуклеиновых кислот представлен, например, в P. Gill and A. Ghaemi, 2008, Nucleosides Nucleotides Nucleic acids 27(3):224-243.
Если нуклеиновая кислота является РНК, получение молекул ДНК дополнительно включает подвергание нуклеиновых кислот обратной транскрипции перед амплификацией. Обратная транскрипция является другим стандартным способом молекулярной биологии и также описан, например, в Sambrook et al., выше.
После выделения комплекса нуклеиновая кислота-олигонуклеотидный зонд и, необязательно, подвергания его любому из описанных выше способов, экстракт SMP секвенируют. В рамках изобретения термин "секвенирование выделенной молекулы нуклеиновой кислоты" следует понимать в широком смысле, т.е. он относится к любому способу, позволяющему получать информацию о последовательности. Например, информацию о последовательности можно получать с помощью гибридизации со специфическими зондами или микрочипов. В одном из вариантов осуществления термин "секвенирование выделенных молекул нуклеиновой кислоты" относится к секвенированию молекул ДНК, необязательно, полученных из РНК посредством обратной транскрипции. Способы, подходящие для секвенирования молекул ДНК, известны в этой области и включают, в качестве неограничивающих примеров, секвенирование по Сэнгеру, пиросеквенирование или секвенирование нового поколения (NGS). В другом варианте осуществления термин "секвенирование выделенных молекул нуклеиновой кислоты" относится к секвенированию молекул РНК посредством нанопорового секвенирования, секвенирования микроРНК или полнотранскриптомного шотган-секвенирования. В предпочтительном варианте осуществления секвенирование является секвенированием ДНК, предпочтительно - NGS.
Если информацию о последовательности получают посредством NGS, в вариантах осуществления, в которых олигонуклеотидные зонды действуют в качестве праймеров при NGS, олигонуклеотидные зонды содержат адаптер для NGS в качестве дополнительной последовательности.
После получения информации о последовательности секвенированных молекул нуклеиновой кислоты определяют корреляцию секвенированных молекул нуклеиновой кислоты с исходной локализацией соответствующих молекул-мишеней нуклеиновой кислоты в ROI для получения пространственного распределения молекул-мишеней нуклеиновой кислоты. Таким образом, получают пространственную двухмерную карту, на которой секвенированные нуклеиновые кислоты представлены в соответствии с заранее определенными участками, например, определенными с помощью шаблона разделения, из которого они происходят. Таким образом, в одном из вариантов осуществления секвенированные молекулы нуклеиновой кислоты коррелируют с исходной локализацией соответствующих молекул-мишеней нуклеиновой кислоты в заранее определенном участке в ROI для получения пространственного распределения молекул-мишеней нуклеиновой кислоты, где каждый участок идентифицируют посредством одного или более видов олигонуклеотидных зондов, связанных с нуклеиновыми кислотами из образца в заранее определенных участках в ROI. В другом варианте осуществления уникальную комбинацию по меньшей мере двух различных видов олигонуклеотидных зондов используют для идентификации локализации молекул-мишеней нуклеиновой кислоты в ROI. Выделенные и секвенированные молекулы нуклеиновой кислоты содержат последовательность-штрих-код из олигонуклеотидных зондов, связывающихся с нуклеиновыми кислотами-мишенями из образца в заранее определенном участке в ROI. Т.к. на каждый заранее определенный участок в ROI наносят уникальный вид олигонуклеотидных зондов или уникальную комбинацию олигонуклеотидных зондов, связывающихся с нуклеиновыми кислотами-мишенями из образца, выделенные и секвенированные молекулы нуклеиновой кислоты включают последовательность-штрих-код из олигонуклеотидных зондов. Каждая молекула нуклеиновой кислоты, учитывая последовательность-штрих-код, которую он содержит, может коррелировать с заранее определенным участком, на который наносили вид олигонуклеотидных зондов, содержащих указанную последовательность-штрих-код. С помощью полученной корреляции получают пространственную карту, на которой показаны исходные участки нуклеиновых кислот-мишеней в ROI. С помощью такой пространственной карты, например, можно получать информацию о статусе экспрессии, мутационном статусе, статусе деградации, статусе метилирования, эпигенетическом статусе нуклеиновых кислот или их комбинаций.
В одном из вариантов осуществления пространственное распределение молекул-мишеней нуклеиновой кислоты может коррелировать с изображением ROI или с изображением образца ткани, в котором идентифицировали ROI. Пространственное распределение молекул-мишеней нуклеиновой кислоты можно визуализировать, получая двухмерную пространственную карту. В одном из вариантов осуществления пространственное распределение молекул-мишеней нуклеиновой кислоты коррелирует с пространственными паттернами изображения, полученного из ROI. Таким образом, в одном из вариантов осуществления с помощью способа получают двухмерную пространственную карту для визуализации пространственного распределения молекул-мишеней нуклеиновой кислоты. В дополнительном варианте осуществления способ дополнительно включает наложение двухмерной пространственной карты на изображение ROI или изображение образца ткани, в котором идентифицировали ROI. Изображение ROI можно получать до или после идентификации ROI. Таким образом, в одном из вариантов осуществления изображение получают из образца ткани перед идентификацией по меньшей мере одной ROI. В другом варианте осуществления изображение ткани получают после идентификации по меньшей мере одной ROI. В еще одном варианте осуществления изображение получают из ROI до или после нанесения олигонуклеотидных зондов на заранее определенные участки в ROI. Изображения можно получать любым известным в этой области способом, таким как цифровое патологическое исследование или микроскопия с использованием камеры. В одном из вариантов осуществления пространственное распределение молекул-мишеней нуклеиновой кислоты коррелирует с заранее определенными участками, локализованными в ROI и определяемыми посредством шаблона разделения, где изображение получают после нанесения шаблона разделения и до или после нанесения олигонуклеотидных зондов на заранее определенные участки в ROI, предпочтительно - до нанесения олигонуклеотидных зондов. В предпочтительном варианте осуществления пространственное распределение молекул-мишеней нуклеиновой кислоты коррелирует с изображением ROI, полученным до или после нанесения олигонуклеотидных зондов на заранее определенные участки в ROI, предпочтительно - до нанесения олигонуклеотидных зондов. В другом предпочтительном варианте осуществления пространственное распределение молекул-мишеней нуклеиновой кислоты коррелирует с изображением ROI, полученным после нанесения шаблона разделения и до нанесения олигонуклеотидных зондов на заранее определенные участки, определяемые посредством шаблона разделения.
Пространственную карту можно визуализировать, например, посредством отображения искусственных цветов с каждым заранее определенным участком, что определяют с помощью решетки, представляющей область того же цвета. Пространственную карту можно накладывать на изображение ROI или изображение образца ткани. Например, пространственную карту конфигурируют как полупрозрачное изображение и накладывают на изображение ROI или изображение образца ткани. Или наоборот, изображение ROI или изображение образца ткани конфигурируют как полупрозрачное изображение и накладывают на пространственную карту. В предпочтительном варианте осуществления количество одинаковых молекул-мишеней нуклеиновой кислоты, определяемых в анализе с использованием одного вида олигонуклеотидных зондов, относится к цвету карты в соответствующем заранее определенном участке. В другом варианте осуществления конкретная комбинация молекул-мишеней нуклеиновой кислоты, подобная, например, подтипу молекул, несущих известную онкогенную мутацию, коррелирует с цветом. В еще одном варианте осуществления гиперэкспрессия конкретного набора молекул-мишеней нуклеиновой кислоты, относящихся к конкретным генам, может коррелировать с цветом на карте. Следует понимать, что можно определять множество различных профилей, и они могут относиться к способу визуального отображения в зависимости от биологической и/или клинической проблемы. Вместо или в комбинации с цветами на пространственной карте можно отображать другие примечания.
Корреляцию пространственного распределения молекул-мишеней нуклеиновой кислоты с пространственными паттернами исходного изображения, т.е. пространственную карту, можно использовать для ответа на клинический вопрос и получения руководства для клинического решения. Результаты, полученные с помощью пространственной карты, полученной способом по изобретению, можно использовать для клинической диагностики или мониторинга клинического ответа у пациента. Корреляцию пространственного распределения молекул-мишеней нуклеиновой кислоты с пространственными паттернами исходного изображения также можно использовать в области исследований.
В предпочтительном варианте осуществления получают изображение образца ткани и/или ROI. Полученное изображение образца ткани можно использовать для идентификации интересующей области, а также пространственного разрешения паттерна с учетом анализа на основе изображения ткани перед нанесением реагентов.
Другой аспект изобретения относится к реакции лигирования 5'-олигонуклеотидных зондов и 3'-олигонуклеотидных зондов с 5'-концом и 3'-концом молекулы РНК и одновременному нанесению молекулы ДНК, с помощью которой встраивают участок рестрикции в участок лигирования димера олигонуклеотидного зонда, и фермента рестрикции, подходящего для расщепления участка рестрикции, где 5'-конец и 3'-конец молекулы ДНК модифицируют таким образом, что они не участвуют в реакции лигирования. Таким образом, димеры, возникающие между олигонуклеотидными зондами, когда они реагируют друг с другом (т.е. димер олигонуклеотидного зонда), расщепляются на полностью активные отдельные 5'-олигонуклеотидные зонды и 3'-олигонуклеотидные зонды. Расщепленные олигонуклеотидные зонды можно использовать повторно в реакции лигирования для лигирования с 5'-концом и 3'-концом молекулы РНК.
Конкретный вариант осуществления относится к реакции лигирования на FFPE-образце ткани, лигированию 5'-олигонуклеотидных зондов и 3'-олигонуклеотидных зондов с 5'-концом и 3'-концом молекулы РНК и одновременному нанесению молекулы ДНК, с помощью которой встраивают участок рестрикции в участок лигирования димера олигонуклеотидного зонда, и фермента рестрикции, подходящего для расщепления участка рестрикции, где 5'-конец и 3'-конец молекулы ДНК модифицируют таким образом, что они не участвуют в реакции лигирования.
В схеме стандартной реакции лигирования олигонуклеотидного зонда, как приведено на фигуре 2B, реакцию лигирования тушат посредством реакции обратной транскрипции, таким образом, избегая образования димеров олигонуклеотидного зонда. Реакция обратной транскрипции является предпочтительно неэффективной в отношении FFPE-образца ткани. В способе лигирования олигонуклеотидного зонда по изобретению димер олигонуклеотидного зонда расщепляют ферментом рестрикции, таким образом, можно избегать стадии реакции обратной транскрипции в отношении FFPE-образца ткани. Кроме того, используя способ по изобретению, реакции РНК-лигаз T4 I и II можно комбинировать в одной стадии, как представлено в примерах и на фигуре 3. Таким образом, способ реакции лигирования олигонуклеотидного зонда по изобретению обладает преимуществами по сравнению с предшествующим уровнем техники.
В конкретном варианте осуществления изобретение относится к реакции лигирования 5'-олигонуклеотидных зондов и 3'-олигонуклеотидных зондов с 5'-концом и 3'-концом молекулы РНК и одновременному нанесению молекулы ДНК, с помощью которой встраивают участок рестрикции HaeIII в участок лигирования димера олигонуклеотидных зондов, и фермента рестрикции HaeIII, расщепляющего по этому участку рестрикции.
Описанную выше реакцию лигирования можно использовать на стадии b) способа пространственного определения молекул РНК в образце ткани, как представлено в настоящем описании.
В частности, описанную выше реакцию лигирования можно использовать на стадии b) способа пространственного определения молекул РНК в FFPE-образце ткани, как представлено в настоящем описании. Таким образом, можно избегать осуществления реакции обратной транскрипции в отношении FFPE-образца ткани. Этот способ является предпочтительным, т.к. он позволяет избегать реакции обратной транскрипции, являющейся предпочтительно неэффективной в отношении FFPE-образца. Кроме того, используя этот способ реакции РНК-лигазы I и II T4, можно комбинировать в одной стадии.
В конкретном варианте осуществления способ пространственного определения нуклеиновых кислот в образце ткани включает стадии:
a1) получения изображения образца ткани;
a2) идентификации по меньшей мере одной ROI в образце;
a3) нанесения шаблона на ROI, включающую различные заранее определенные участки;
b) нанесения по меньшей мере одного вида олигонуклеотидных зондов на заранее определенные участки в ROI и связывания олигонуклеотидных зондов с нуклеиновыми кислотами из образца, где олигонуклеотидные зонды содержат последовательность-штрих-код;
c) выделения комплексов нуклеиновая кислота-олигонуклеотидный зонд;
d) секвенирования выделенных молекул нуклеиновой кислоты;
e) определения корреляции секвенированных молекул нуклеиновой кислоты с исходной локализацией соответствующей молекулы-мишени нуклеиновой кислоты в ROI для получения пространственного распределения молекул-мишеней нуклеиновой кислоты; где каждый участок идентифицируют посредством одного или более видов олигонуклеотидных зондов, связавшихся на стадии b).
В другом конкретном варианте осуществления способ пространственного определения нуклеиновых кислот в FFPE-образце ткани включает стадии:
a1) депарафинизации FFPE-образца ткани;
a2) получения изображения образца ткани;
a3) идентификации по меньшей мере одной ROI в образце;
a4) нанесения шаблона на ROI, включая различные заранее определенные участки;
b) нанесения по меньшей мере одного вида олигонуклеотидных зондов на заранее определенные участки в ROI и связывания олигонуклеотидных зондов с нуклеиновыми кислотами из образца, где олигонуклеотидные зонды содержат последовательность-штрих-код;
c) выделения комплексов нуклеиновая кислота-олигонуклеотидный зонд;
d) секвенирования выделенных молекул нуклеиновой кислоты;
e) определения корреляции секвенированных молекул нуклеиновой кислоты с исходной локализацией соответствующей молекулы-мишени нуклеиновой кислоты в ROI для получения пространственного распределения молекул-мишеней нуклеиновой кислоты; где каждый участок идентифицируют посредством одного или более видов олигонуклеотидных зондов, связавшихся на стадии b).
В конкретном варианте осуществления способ пространственного определения РНК в образце ткани включает стадии:
a1) получения изображения образца ткани;
a2) идентификации по меньшей мере одной ROI в образце;
a3) нанесения шаблона на ROI, включающую различные заранее определенные участки;
b) нанесения по меньшей мере одного вида олигонуклеотидных зондов на заранее определенные участки в ROI и связывания олигонуклеотидных зондов с молекулами РНК из образца, где олигонуклеотидные зонды содержат последовательность-штрих-код;
c) выделения комплексов РНК-олигонуклеотидный зонд;
d) секвенирования выделенных молекул РНК;
e) определения корреляции секвенированных молекул РНК с исходной локализацией соответствующей молекулы РНК-мишени в ROI для получения пространственного распределения молекул РНК-мишеней; где каждый участок идентифицируют посредством одного или более видов олигонуклеотидных зондов, связавшихся на стадии b).
В конкретном варианте осуществления способ пространственного определения молекул РНК в FFPE-образце ткани включает стадии:
a1) депарафинизации FFPE-образца ткани;
a2) получения изображения образца ткани;
a3) идентификации по меньшей мере одной ROI в образце;
a4) нанесения шаблона на ROI, включающую различные заранее определенные участки;
b) нанесения по меньшей мере одного вида олигонуклеотидных зондов на заранее определенные участки в ROI и связывания олигонуклеотидных зондов с молекулами РНК из образца, где олигонуклеотидные зонды содержат последовательность-штрих-код;
c) выделения комплексов РНК-олигонуклеотидный зонд;
d) секвенирования выделенных молекул РНК;
e) определения корреляции секвенированных молекул РНК с исходной локализацией соответствующей молекулы РНК-мишени в ROI для получения пространственного распределения молекул РНК-мишеней; где каждый участок идентифицируют посредством одного или более видов олигонуклеотидов, связавшихся на стадии b).
В конкретном варианте осуществления способ пространственного определения РНК в FFPE-образце ткани включает стадии:
a1) депарафинизации FFPE-образца ткани;
a2) получения изображения образца ткани;
a3) идентификации по меньшей мере одной ROI в образце;
a4) нанесения шаблона на ROI, включающую различные заранее определенные участки;
b) нанесения 5'-РНК-зондов и 3'-РНК-зондов на заранее определенные участки в ROI и лигирования РНК-зондов с 5'-концом и 3'-концом молекул РНК из образца, где РНК-зонды содержат последовательность-штрих-код;
c) выделения комплексов РНК-РНК-зонд;
d) секвенирования выделенных молекул РНК;
e) определения корреляции секвенированных молекул РНК с исходной локализацией соответствующей молекулы РНК-мишенью в ROI для получения пространственного распределения молекул РНК-мишеней; где каждый участок идентифицируют посредством одного или более видов РНК-зондов, связавшихся на стадии b).
В конкретном варианте осуществления способ пространственного определения РНК в FFPE-образце ткани включает стадии:
a1) депарафинизации FFPE-образца ткани;
a2) получения изображения образца ткани;
a3) идентификации по меньшей мере одной ROI в образце;
a4) нанесения шаблона на ROI, включающую различные заранее определенные участки;
b) нанесения 5'-РНК-зондов и 3'-РНК-зондов на заранее определенные участки в ROI и лигирования РНК-зондов с 5'-концом и 3'-концом молекул РНК из образца, где РНК-зонды содержат последовательность-штрих-код, и одновременного нанесения молекулы ДНК, с помощью которой встраивают участок рестрикции в участок лигирования димера РНК-зондов, и фермента рестрикции, подходящего для расщепления участка рестрикции;
c) выделения комплексов РНК-РНК-зонд;
d) секвенирования выделенных молекул РНК;
e) определения корреляции секвенированных молекул РНК с исходной локализацией соответствующей молекулы РНК-мишени в ROI для получения пространственного распределения молекул РНК-мишеней; где каждый участок идентифицируют посредством одного или более видов РНК-зондов, связавшихся на стадии b).
В конкретном варианте осуществления способ пространственного определения РНК в FFPE-образце ткани включает стадии:
a1) депарафинизации FFPE-образца ткани;
a2) получения изображения образца ткани;
a3) идентификации по меньшей мере одной ROI в образце;
a4) нанесения шаблона на ROI, включающую различные заранее определенные участки;
b) нанесения 5'-РНК-зондов и 3'-РНК-зондов на заранее определенные участки в ROI и лигирования РНК-зондов с 5'-концом и 3'-концом молекул РНК из образца, где РНК-зонды содержат последовательность-штрих-код, и одновременного нанесения молекулы ДНК, с помощью которой встраивают участок рестрикции HaeIII в участок лигирования димера РНК-зондов, и фермента рестрикции HaeII;
c) выделения комплексов РНК-РНК-зонд;
d) секвенирования выделенных молекул РНК;
e) определения корреляции секвенированных молекул РНК с исходной локализацией соответствующей молекулы РНК-мишени в ROI для получения пространственного распределения молекул РНК-мишеней; где каждый участок идентифицируют посредством одного или более видов РНК-зондов, связавшихся на стадии b).
В конкретном варианте осуществления способ пространственного определения ДНК в образце ткани включает стадии:
a1) получения изображения образца ткани;
a2) идентификации по меньшей мере одной ROI в образце;
a3) нанесения шаблона на ROI, включающую различные заранее определенные участки;
b) нанесения по меньшей мере одного вида олигонуклеотидных зондов на заранее определенные участки в ROI и связывания олигонуклеотидных зондов с молекулами ДНК из образца, где олигонуклеотидные зонды содержат последовательность-штрих-код;
c) выделения комплексов ДНК-олигонуклеотидный зонд;
d) секвенирования выделенных молекул ДНК;
e) определения корреляции секвенированных молекул ДНК с исходной локализацией соответствующей молекулы ДНК-мишени в ROI для получения пространственного распределения молекул ДНК-мишеней; где каждый участок идентифицируют посредством одного или более видов олигонуклеотидных зондов, связавшихся на стадии b).
ПРИМЕРЫ
Типы способов для связывания олигонуклеотидного зонда с молекулой нуклеиновой кислоты
Способ пространственного определения РНК в FFPE-образце ткани (пример по типу способа [C])
Материал: FFPE-образец ткани на предметном стекле
Образец ткани обрабатывают протеиназой K (ProtK) при 37°C, например, как описано в Tullis and Rubin (Analytical Biochemistry, 1980, 107(1): 260-264), или с использованием протеиназы K из Engyodontium album (Sigma-Aldrich) по инструкциям производителя, с последующей термической дезактивацией ProtK в течение 15 минут при 80°C.
Образец ткани депарафинизируют, например с использованием раствора для депарафинизации (например, Qiagen) по инструкциям производителя.
Получают изображение полного предметного стекла (Philips Digital Pathology Scanner UFS) и на изображении идентифицируют ROI.
В ROI выбирают различные участки и наносят верхний шаблон разделения посредством чернильной печати (печатная головка XAAR) краски, закрепляющейся под действием УФ (Sunjet ink Crystal UFE 7573 (черная)), получая решетку, разделяющую различные реакционные лунки. УФ-закрепление шаблона осуществляют при 360-380 нм с использованием UV-LED в течение 30-60 сек.
Уникальную комбинацию двух видов олигонуклеотидных зондов, содержащих последовательности-штрих-коды (5'-РНК-зонды и 3'-РНК-зонды), наносят на каждый заранее определенный участок посредством чернильной печати (с использованием печатной головки FUJIFILM Dimatix). 5'-РНК-зонды и 3'-РНК-зонды лигируют с молекулами мРНК за одну стадию с использованием модифицированного способа для набора для получения библиотеки небольших РНК NEBNext® для Illumina® (NEB). В стандартном способе, изображенном на фиг. 2B, РНК-зонды лигируют с молекулой РНК за одну стадию. В течение этой реакции 5'-РНК-зонды реагируют с 3'-РНК-зондами и образуют димеры. В модифицированном способе вместо использования RT-праймера для тушения реакции используют другой подход: Для расщепления этих димеров используют молекулу ДНК, комплементарную участку лигирования 3'-конца 5'-РНК-зонда и 5'-конца 3'-РНК-зонда, с помощью которого встраивают участок рестрикции HaeIII в участок лигирования димера РНК-зондов. Молекулу ДНК модифицируют на обоих концах таким образом, что он не участвует в реакции лигирования. Посредством добавления фермента рестрикции HaeIII димеры РНК-зондов с гетеродуплексом комплементарных РНК-ДНК будут расщеплять по участку лигирования двух РНК-зондов только на цепи РНК, в то время как молекула ДНК остается интактной. Расщепленные РНК-зонды снова могут участвовать в реакции лигирования.
После нанесения смеси для лигирования микроскопический препарат накрывают предметным стеклом (система герметизации Grace Bio-Labs HybriWell™, адгезионная камера SecureSeal™).
После лигирования олигонуклеотидных зондов буфер для выделения наносят на образец, погружая все лунки, и осуществляют выделение РНК с использованием мембранной очистки РНК, например, с использованием набора RNeasy FFPE Kit (Qiagen) по инструкциям производителя. Образец нагревают при выделении и оставляют герметизированным во избежание дегидратации образца. Альтернативно, при очистке можно использовать последовательность олигонуклеотидного зонда, например, с использованием магнитных бус. Инкубацию с ДНКазой осуществляют в течение или после очистки лигированной РНК (например, при 37°C в течение 15 мин) с последующей инактивацией ДНКазы при 80°C в течение 15 мин. Альтернативно, обработку ДНКазой можно осуществлять параллельно стадии обработки протеиназой K, описанной выше.
Получение библиотеки секвенированной РНК осуществляют с использованием, например, набора для получения библиотеки ScriptSeq v2 RNA-Seq Library Preparation Kit (Illumina) по инструкциям производителя. Осуществляют секвенирование РНК и идентифицируют транскрипты с штрих-кодами из последовательностей. Затем эту информацию комбинируют с исходным изображением, полученным из ROI, для построения пространственной транскрипционной карты.
Способ пространственного определения ДНК в FFPE-образце ткани (пример по типу способа [B])
Материал: FFPE-образец ткани на микроскопическом препарате
Образец ткани депарафинизируют, например, с использованием раствора для депарафинизации (например, Qiagen) по инструкциям производителя и сушат.
Образец ткани обрабатывают протеиназой K (ProtK) при 37°C, например, как описано Tullis and Rubin (Analytical Biochemistry, 1980, 107(1): 260-264), или с использованием протеиназы K из Engyodontium album (Sigma-Aldrich) по инструкциям производителя с последующей термической деактивацией ProtK в течение 15 минут при 80°C.
Образец ткани промывают EtOH и сушат при 40°C в течение 30 минут.
Получают изображение полного микроскопического препарата (Philips Digital Pathology Scanner UFS) и идентифицируют ROI на изображении.
Молекулы ДНК подвергают денатурации посредством добавления денатурирующего раствора (70% формамида в 2-кратном SSC, pH 7,0-8,0) и инкубации при 75°C в течение 5 минут с последующей инкубацией в течение 1 минуты в 70% EtOH, 1 минуты в 85% EtOH и 1 минуты в 100% EtOH. Затем микроскопический препарат сушат и помещают при 45-50°C, позволяя оставшемуся EtOH испаряться.
В ROI выбирают различные участки и наносят верхний шаблон разделения посредством чернильной печати (печатная головка XAAR) краски, закрепляющейся под действием УФ (Sunjet ink Crystal UFE 7573 (черная)), получая решетку, разделяющую реакционные лунки. УФ-закрепление шаблона осуществляют при 360-380 нм с использованием UV-LED в течение 30-60 сек.
Олигонуклеотидные зонды, содержащие последовательность-штрих-код, наносят на каждый заранее определенный участок посредством чернильной печати (с использованием печатной головки FUJIFILM Dimatix).
образец ткани инкубируют при 40°C в течение 2 ч (влажные условия).
После инкубации осуществляют реакцию элонгации для амплификации целевых последовательностей, гибридизуемых с использованием праймерной последовательности олигонуклеотидных зондов.
После реакции элонгации микроскопический препарат накрывают крышкой (система герметизации Grace Bio-Labs HybriWell™, адгезионная камера SecureSeal™).
Вносят буфер для выделения и образец инкубируют при 60°C в течение 30 мин.
Осуществляют получение библиотеки секвенированной ДНК и секвенирование ДНК и идентифицируют транскрипты с штрих-кодами из последовательностей. Затем эту информацию комбинируют с исходным изображением, полученным из ROI, для построения пространственной транскрипционной карты.
Для реакций на указанных выше стадиях используют хорошо известные стандартные наборы по протоколу производителя.
Способ одностадийного 3'- и 5'-лигирования РНК с двумя разными штрих-кодами на микроскопических препаратах FFPE
Целью этого эксперимента являлось лигирование клонирующего линкера мкРНК на 3'-стороне РНК и лигирование 5'-адаптера РНК на 5'-стороне РНК на микроскопическом препарате FFPET за одну реакцию. Это осуществляли описанным ниже способом. Анализы RT-qPCR осуществляли в отношении выделенной РНК для определения того, являлась ли реакция успешной.
В качестве образца авторы настоящего изобретения использовали фрагменты 5 мкм, вырезанные из FFPE-блока рака молочной железы и термически обработанные в течение 30 минут при 55-60°C. Затем микроскопические препараты переносили в печь для обеспечения того, чтобы образцы были полностью сухими (в течение ночи при 55°C). РНК должна стать доступной/экспонированной на микроскопическом препарате, чтобы реакция лигирования была успешной. Это осуществляли, во-первых, промывая микроскопический препарат ксилолом (2 раза по 10 минут, 1 раз 8 минут), промывая его 100% EtOH (1 раз 5 минут, 1 раз 1 минуту). Затем микроскопический препарат сушили воздухом в течение 5 минут и карандаш для создания гидрофобного барьера использовали для создания круга вокруг ткани, в котором оставались бы жидкости (микроскопический препарат сушили воздухом еще в течение 15-30 минут). Держатель для микроскопических препаратов наполняли 1-кратным раствором для предварительной обработки (Quantigene® View RNA Assay kit Affimetrix; P/N: 17428). Держатель для микроскопических препаратов помещали на водяную баню (95°C) и микроскопический препарат осторожно помещали в этот держатель для микроскопических препаратов с нагретым 1-кратным раствором для предварительной обработки в течение 20 минут. Микроскопический препарат промывали водой MiliQ (2 раза по 1 минут) и PBS (1 раз 5 секунд). Аликвоту 200-400 мкл раствора протеазы QS (Quantigene® View RNA Assay kit Affimetrix; P/N: 16742) добавляли на ткань и инкубировали в течение 20 минут при 40°C во влажной камере. Микроскопический препарат промывали в PBS (2 раза по 5 секунд) для удаления раствора протеазы QS. Затем микроскопический препарат фиксировали в 4% забуференном формальдегиде в течение 5 минут при комнатной температуре и избыток раствора снова удаляли, промывая микроскопический препарат PBS (2 раза по 5 секунд). Авторы настоящего изобретения использовали два коммерчески доступных набора для лигирования: i) РНК-лигазу T4 2, укороченную (New England BioLabs - M0242S) и ii) РНК-лигазу T4 1, ssРНК-лигазу (New England BioLabs - M0204S). Кроме того, коммерчески доступный клонирующий линкер мкРНК (New England BioLabs - S1315S, SEQ ID=1) использовали для 3'-лигирования и олигонуклеотиды РНК, производимые IDT (SEQ ID=2), использовали для 5'-лигирования. Реакционную смесь получали, как описано в таблица ниже:
Аликвоту 60 мкл раствора для лигирования добавляли к ткани на микроскопическом препарате и инкубировали во влажной камере (1 час при 25°C и 1 час при 37°C). Реакцию лигирования останавливали посредством промывания микроскопического препарата в PBS (2 раза по 5 секунд). РНК собирали посредством 4-кратного добавления 200 мкл коммерчески доступного лизирующего буфера (набор для выделения РНК Siemens Versant) на ткань и его переноса в чистую центрифужную пробирку для ПЦР емкостью 1,5 мл. Далее РНК выделяли по инструкциям производителя (набор для выделения РНК Siemens Versant).
Затем определение лигированного продукта осуществляли с использованием анализов RT-qPCR, специально созданных для лигированного продукта. См. кривые амплификации на фигуре 3 и использованные олигонуклеотиды в таблице ниже. С помощью анализов RT-qPCR определяют лигированный по мРНК B-актина. Авторы настоящего изобретения использовали отрицательный контроль, представлявший собой микроскопический препарат, обработанный так же, как описано выше, но без добавления последовательностей для лигирования (клонирующего линкера и олигонуклеотидов РНК), представленных красным. Авторы настоящего изобретения использовали контроль без матрицы (NTC) для контроля ПЦР, представленный черным. Авторы настоящего изобретения использовали 1 анализ RT-qPCR для определения 3'-продукта лигирования, 1 анализ RT-qPCR для определения наличия 5'-продукта лигирования и конечный анализ RT-qPCR в качестве контроля для определения общих уровней мРНК B-актина.
Реферат
Изобретение относится к области биотехнологии. Изобретение представляет собой способ, основанный на нанесении паттернов олигонуклеотидных зондов со штрихкодами на заранее определенные участки в интересующей области в образце ткани. Каждую анализируемую нуклеиновую кислоту можно локализовать в конкретном положении внутри образца с учетом штрихкода. Можно использовать различные технологии печати и можно использовать различные способы получения паттернов, подобные регулярной матрице с конкретным шагом, или альтернативно объектоориентированное получение паттернов с использованием определенных интересующих областей без ограничений по форме. Изобретение позволяет осуществлять пространственное картирование нуклеиновых кислот образцов ткани с высоким разрешением без необходимости жертвовать степенью мультиплексирования, доступной при секвенировании следующего поколения. 12 з.п. ф-лы, 3 ил., 3 табл., 1 пр.

Комментарии