Композиция в форме микросфер для пролонгированного и контролируемого высвобождения пептидного лекарственного вещества - RU2103994C1
Код документа: RU2103994C1
Чертежи
Описание
Изобретение относится к композиции для пролонгированного и контролируемого высвобождения пептидного лекарственного вещества формулы (1):
Ac-D-Nal-D-pClPh-R3
-Ser-Tyr-D-Cit-Leu-Arg-Pro-D-Ala- NH2,
в которой R3 означает D-Pal или D-Trp.
Такие p-пептиды являются аналогами 1 HPH и предпочтительно могут применяться для терапевтического лечения гормонально зависимых нарушений. В формуле (1)? по крайней мере если нет других указаний, аминокислоты обозначены условно и имеют конфигурацию L; D-Nal означает D-3-(2-нафтил)-аланин и D-Pal означает D-3-(3-пиридил)-аланин.
Композицию согласно изобретению получают в виде микросфер из поддающегося биологическому разложению полимерного материала, заключающего в себе нерастворимую в воде соль пептида формулы (1). Такая композиция, содержащая по меньшей мере 5 мас.% нерастворимой соли от массы биоразлагающегося полимерного материала, может выделять пептид формулы (1), контролируемый образцом в течение нескольких суток, после ее парентерального введения человеку или животному.
Заявленную композицию получают путем превращения водорастворимой соли пептида формулы (1) в соль пептида, нерастворимую в воде, затем готовят суспензию этой соли в растворе биоразлагающегося полимерного материала, эту суспензию превращают в эмульсию типа масло в воде и, наконец, выделяют микросферы из биоразлагающегося полимера после переноса эмульсии "масло в воде" в избыток водной среды.
К настоящему времени были предложены различные технические решения для получения композиции с пролонгированным контролируемым высвобождением лекарственного вещества, с применением имплантируемых биоразлагающихся элементов, микрокапсул или пористых биоразлагающихся матриц в виде микросфер или микрочастиц разных размеров.
В патенте ФРГ DE 4023134 описан способ получения фармацевтического препарата с пролонгированным и контролируемым высвобождением активного компонента в форме микрочастиц, содержащих в качестве активного компонента памоат, таннат, стеарат или пальмиат природного или синтетического пептида, а в качестве полимера - сополимер молочной и гликолевой кислоты, при этом количественный состав препарата не оговаривается. В способе согласно патенту ФРГ DE 4023134 водонерастворимая соль пептида и биологически разлагающийся полимер размалываются и смешиваются друг с другом в сухом виде при величине зерна менее 200 мкм, затем подвергаются прогрессивной предварительной компрессии и экструзии, после чего производится размалывание при низких температурах (криогенная пульверизация).
В европейском патенте ЕП-А-0.052.510 описано получение микрокапсул путем разделения водорастворимых фаз лекарственного вещества и европейском патенте ЕП-А-0.58.481 или американском патенте US-A-3976071 описано получение биоразлагающихся имплантируемых элементов или пористых матриц на основе полилактида или сополимера лактидгликозида в качестве необходимых основных составляющих. Эти технологии используют предварительное растворение биоразлагающегося полимера или сополимера, используемого в качестве носителя, в органическом растворителе, а в случае необходимости растворение самого лекарственного вещества.
Другие технологии, также ведущие к образованию микрокапсул или микросфер, используют способы эмульгирования, при этом основная фаза этих способов заключается в получении эмульсии типа масло в воде из органического раствора полимерного материала и водного раствора пептида (см. американские патенты US-A-4384975, 3891570, 4389330, 3737337, 4652441 или международную заявку WO-90/13361). Однако во всех этих случаях специалист вынужден разрабатывать сложные и трудно описываемые технологии, позволяющие максимально уменьшить потери активного пептидного вещества, обладающего исключительно хорошей водорастворимостью, например предусматривающие двойное эмульгирование.
В противоположность этому продукт по изобретению получают другим, более щадящим способом. Продукт согласно изобретению получают, суспендируя водонерастворимую соль пептида в растворе биологически разлагаемого полимера и вводя суспензию в водный раствор, причем образуется эмульсия типа "масло-в-воде". Затем эту эмульсию отверждают путем разбавления водной фазы, причем образуются микрошарики, которые отделяют. Эти микрошарики содержат водонерастворимую соль пептида и отдают замедленно пептид, когда их суспендируют в водной среде. Продукт отличается тем самым также и по внешнему виду от продуктов согласно, например, патенту ФРГ ДЕ-4023134. При этом продукты согласно изобретению в сферической форме могут быть получены с заданной величиной. Величина сферических частиц зависит от получения эмульсии, причем играет роль, например, скорость перемешивания. В сравнении с известными продуктами содержание пептидного действующего вещества в заявляемом продукте может быть повышено, причем возможно содержание действующего вещества в 5, 10, 20 и более массовых процентов.
Таким образом, осуществляя сначала превращение водорастворимой соли пептида в соль пептида, нерастворимую в воде, в соответствии с изобретением, специалист получает возможность воспользоваться разницей растворимостей используемых ингредиентов, в частности, разницей между "растворителями" и "не растворителями", используемыми в способе.
Указанный способ отличается тем, что:
a. водорастворимую соль пептида формулы (1) превращают в
соль пептида, нерастворимую в воде;
b. приготавливают суспензию указанной соли пептида, нерастворимой в воде, в органической среде,
содержащей растворенный в ней полимерный материал,
поддающийся биологическому разложению;
c. указанную органическую суспензию диспергируют в водной среде, образующей непрерывную фазу
получаемой в результате эмульсии;
d. указанную
эмульсию переносят в избыток водной среды и, наконец, отделяют от жидкой фазы полученные таким образом микросферы.
Первая стадия способа состоит в том, что превращают водорастворимую соль пептида в соль пептида, нерастворимую в воде. Под "водорастворимой" солью понимают М соль пептида, обладающую растворимостью в воде, большей или равной 0,1 мг/мл при 25oC, предпочтительно большей или равной 1,0 мг/мл.
Под "нерастворимой в воде" солью понимают соль пептида, обладающую растворимостью в воде более низкой или равной 0,1 мг/мл при 25oC. Пептидные соли, такие как памоат, таннат, стеарат или пальмитат, отвечают этому определению.
В качестве биоразлагающегося полимерного материала используют полилактид, полигликолид, сополимер молочной и гликолевой кислот.
Предпочтительно использовать в качестве полимерного материала сополимеры молочный и гликолевой кислот (PLGA), в частности, сополимеры кислоты L- или D, L молочной кислоты, содержащие 45-90 мол.% звеньев молочной кислоты и соответственно 55-10 мол.% звеньев гликолевой кислоты.
В качестве растворителя выбранного полимерного материала используют такой органический растворитель, как, например, метиленхлорид, во всяком случае это должен быть растворитель, не ведущий себя как "растворитель" по отношению к соли пептида, удерживаемой (во взвешенном состоянии) в полимерном материале.
Согласно изобретению, после образования суспензии указанной соли в органическом растворе полимерного материала эту суспензию соединяют с определенным количеством водной среды, представляющей собой обычно воду с добавкой специального поверхностно активного вещества. Это делается с целью быстрого образования однородной эмульсии типа масло в воде, при этом указанная водная среда служит непрерывной фазой. В приготовлении такой эмульсии участвуют разнообразные факторы, обуславливающие размер или структуру микросфер, получаемых в результате этого процесса. Один из факторов, которые следует учитывать - скорость введения органического раствора в водную среду, другим фактором может служить температура или также скорость перемешивания или энергия диспергирования (с помощью ультразвука), последний фактор, в частности, влияет на размер микросфер конечного продукта. Применение методов и условий эмульгирования, соответствующих преследуемой цели, в возможностях специалиста в данной области.
В способе получения указанной эмульсии может быть также выгодным изменение объемного соотношения составляющих ее фаз, а именно уменьшение начального объема органической фазы по отношению к начальному объему водной фазы. В одном из случаев, благодаря летучести используемых органических растворителей, например, метиленхлорида, для этого может оказаться достаточным испарение, спонтанно возникающее при перемешивании; в других случаях можно ускорить желаемый процесс путем частичного выпаривания при пониженном давлении.
После образования стойкой эмульсии последняя переносится в избыточное количество водной среды, обычно воды.
Целью этой операции является усиление отверждения зародышевых микросфер, образовавшихся в эмульсии, путем извлечения еще присутствующего в указанных микросферах органического растворителя. Эта операция имеет также целью одновременное удаление еще имеющихся следов поверхностно-активного вещества, которое могло остаться в полимерной массе при окончательном затвердевании. Отметим, что вода не является растворителем как для полимерного биоразлагающегося материала, которым может быть, например, PLGA, так и для соли пептида, содержащейся в указанных микросферах. Эта ситуация соответствующим образом способствует необходимому извлечению остаточного растворителя полимера, например CH2Cl2.
После перенесения указанной эмульсии в избыток водной среды, отбирают отвержденные микросферы с помощью известных методов, например, центрифугированием, фильтрацией или деконтацией. Осуществляют также промывку, очистку и сушку.
Одним из преимуществ способа согласно изобретению является то, что он позволяет получать микросферы с управляемыми с точностью размерами, это управление в основном осуществляется в процессе получения эмульсии, например скоростью перемешивания. Другим преимуществом является исключительно высокое наполнение пептидами, которое способ позволяет получать 5,10 или 20 мас.% и более, в различных случаях. Кроме того, выход операции введения пептида или соли пептида исключительно велик, что достигается благодаря предварительному превращению водорастворимой соли пептида в соль пептида, нерастворимую в воде.
Микросферы, полученные способом согласно изобретению из вышеуказанных ингредиентов, в дальнейшем используются, после соответствующей стерилизации, для приготовления суспензий, предназначенных для парентерального введения, например, путем внутримышечных или подкожных инъекций.
Пример 1. 3 г ацетата аналога LHRH формулы
Ac-D-Nal-D-pCl-Phe-D-Pal-Ser-Tyr-D-Cit-Len-Agr-Pro-D-AIa- NH2
были превращены в соответствующий памоат с помощью известных методов и обработаны таким образом, что были получены
частицы со средними размерами около 19 мкм.
Приготовлена суспензия 0,317 г указанного памоата и 1,683 г PLGA 75:25 (мол. %) в 20 мл (CH2Cl2, содержащая в растворенном виде 1,683 г сополимера кислот молочной -D, L и гликолевой (PLGA) 75:25 (мол.% собственная вязкость 0,82 в HFLP). Смешивание осуществлялось при температуре окружающей среды при перемешивании с целью получения однородной суспензии.
Полученную суспензию затем выгружали в один прием в 500 мл 0,075%-ного раствора метоксицеллюлозы в воде, после чего в течение около 90 мин при температуре окружающей среды осуществляли перемешивание смеси (скорость перемешивания: 900 об/мин). Изменение состояния эмульсии периодически проверялось, в среднем каждые 30 мин, путем отбора проб и исследования появившихся микросфер под микроскопом.
После окончания перемешивания (стабилизации уменьшения размеров микросфер) указанная эмульсия была перенесена в один прием в 2 л воды, поддерживаемой при 10oC, и полученная смесь перемешивалась до однородного состояния.
Микросферы PLGA были отделены от реакционной смеси и очищены путем многократного центрифугирования вперемешку с промывкой водой, затем отфильтрованы и просушены при пониженном давлении. Было собрано таким образом 1,61 г (выход 80%) микросфер PLGA, содержащих более 94% частиц диаметров менее 100 мкм (55-85 мкм максимально).
Анализ (растворение массы PLGA, извлечение и определение пептида с помощью HPLC) показал, что содержимое в микросферах памоата составляет 9,05 мас.% (расчетное содержание: 100%).
Полученные таким образом микросферы были затем подвергнуты стерилизации гамма-излучением и из них была образована суспензия в специальном стерильном носителе. Испытания in vivo (определение содержания тестостерона в крови у крыс самцов) подтвердили равномерное выделение активного вещества.
Пример 2. Действовали так же, как описано выше в примере 1, используя 0,634 г памоата аналога LHRH на 1,366 г PLGA 75:25.
Микросферы PLGA: 1,70 г (выход 85%).
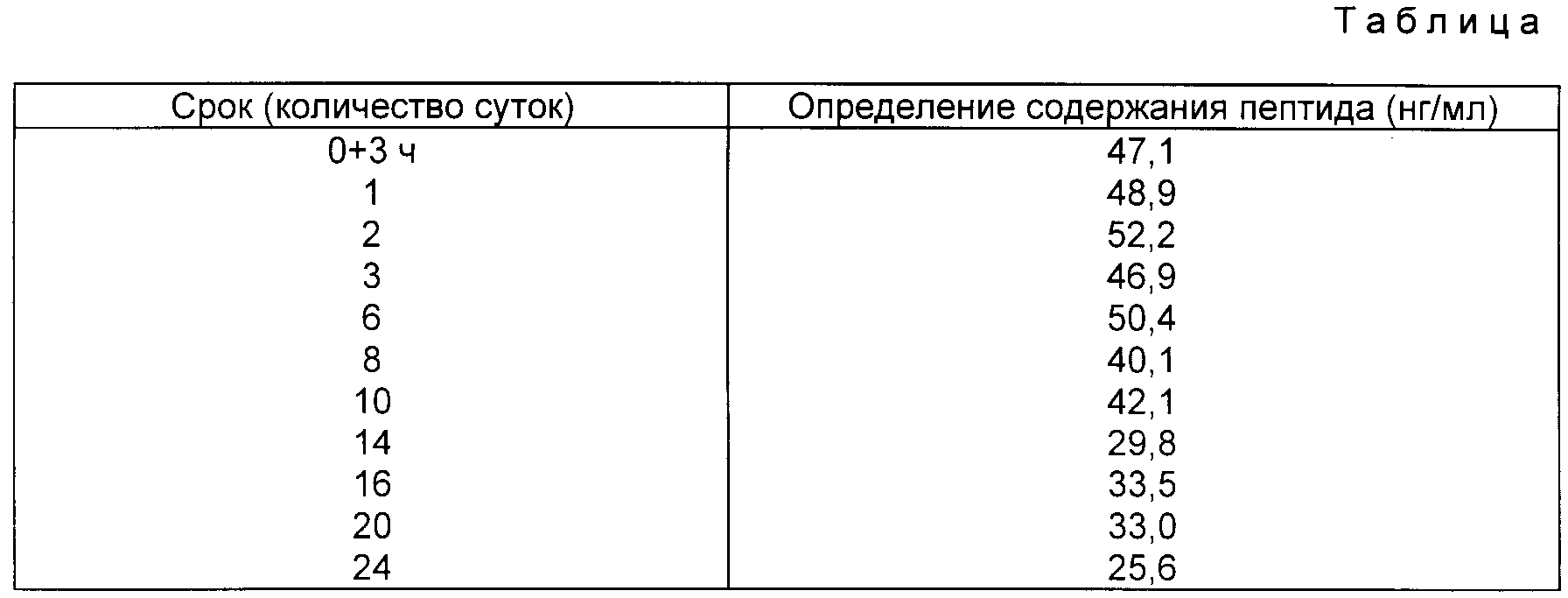
Содержание полезного наполнителя 18,3% (расчетное: 20%). Полученные таким образом микрсферы были затем подвергнуты стерилизации гамма-излучением и из них была приготовлена суспензия в специальном стерильном носителе. Испытания in vivo (определение содержания аналога в сыворотке крови у крыс самцов) подтверждают равномерное выделение биологически значимого количества активного вещества по меньшей мере в течение 24 сут (см. таблицу).
Эти результаты были подтверждены также анализами забитых животных через 30 сут.: потеря веса тестикулов по меньшей мере на 80%, потеря веса семенных пузырьков по меньшей мере на 90%.
Пример 3. Приготовлен по примеру 1 с использованием 3 г ацетата аналога LHRH формулы
Ac-D-Nal-D-pCl-Phe-D-Trp-Ser-Tyr-D-Cit-Leu-Arg-Pro-D-Aia- NH2.
После превращения этого ацетата в соответствующий паомат и операций переработки, описанных в примере 1, были получены микросферы из полимерного материала, имеющие те же характеристики, что и предыдущие.
Реферат
Изобретение относится к химико-фармацевтической промышленности. Композиция, предназначенная для пролонгированного контролируемого введения пептидного лекарственного вещества формулы (1) Ac-D-NaI-D-pClPhe-R3- Ser -Tyr -D -Cit-Leu-Arg-Pro-D-AIa- NH2, в которой R3 означает D-Pal или D-Trp. Композицию получают в виде микросфер из полимерного материала, поддающегося биологическому разложению, вмещающих нерастворимую в воде соль указанного пептида формулы (1). 2 з.п. ф-лы, 1 табл.
Формула
Ac-D-Nal-D-pClPhe-R3 -Ser- Tyr-D-Cit-Leu-Arg-Pro-D-Ala-NH2,
где R3 D-Pal или D-Trp,
причем количество соли пептида составляет по меньшей мере 5% от массы биоразлагающегося полимера.

Комментарии