Способ получения 2-кето-l-гулоновой кислоты или ее соли - RU2102481C1
Код документа: RU2102481C1
Чертежи


Описание
Настоящее изобретение относится к высокопродуктивному способу получения 2-кето-L-гулоновой кислоты путем ферментативной конверсии D-сорбита.
2-кето-L-гулоновая кислота является важным промежуточным соединением для получения L-аскорбиновой кислоты, в которую она может быть преобразована в соответствии с хорошо известным методом Рейхстайна.
Способ ферментативного продуцирования 2-кето-L-гулоновой кислоты из D-сорбита или L-сорбозы хорошо известен специалистам.
Так, например, в японском патенте 40154/1976 раскрывается продуцирование 2-кето-L-гулоновой кислоты из D-сорбита посредством микроорганизмов рода Acetobacter, Bacterium или Pseudomonas, которые обладают способностью к окислению в аэробных условиях D-сорбита, продуцируя тем самым 2-кето-L-гулоновую кислоту. Однако указанный способ является низкопродуктивным, выход составляет менее 6 г/л.
В соответствии с другим известным способом, который описывается в работе "Acta Microbiologica Sinica" 21 (2), 185 191 (1981), 2-кето-L-гулоновая кислота может быть получена из L-сорбозы при использовании смешанной культуры микроорганизмов вида Pseudomonas striata и вида Gluconobacter oxydans. Выход целевого продукта составляет 30 г/л при исходной концентрации L-сорбозы 70 г/л, и 37 г/л при исходной концентрации L-сорбозы 100 г/л.
Кроме того, в Европатенте 0221707 описывается получение 2-кeтo-L-гулоновой кислоты из L-сорбозы с использованием микроорганизмов рода Pseudogluconobacter saccharoketogenes вместе с сопутствующими бактериями или без них. Однако этот способ, основанный на использовании сахарокетогенов Pseudogluconobacter per se Ur/12.06.91, обеспечивает выход, составляющий самое большое 55,3 87,6 г/л (коэффициент конверсии: 34,2 54,1%) (см. с. 13, табл. 4 Европатента 0221707).
Далее в Европатенте 0278447 раскрывается способ получения 2-кето-L-гулоновой кислоты из L-сорбозы с использованием смешанной культуры микроорганизмов, один из которых имеет признаки, характерные для штамма DSM N 4025, а другой характерные для штамма DSM N 4026 (штамм Bacillus megaterium). Выход при осуществлении этого способа составляет 40 г/л и более.
Как указывалось выше, были разработаны различные способы продуцирования 2-кето-L-гулоновой кислоты из L-сорбозы или D-сорбита с использованием микроорганизмов, однако все они практически не могут быть использованы в промышленном производстве вследствие низкого выхода целевого продукта; особенно это касается способа продуцирования целевого продукта из D-сорбита.
С другой стороны, известен способ ферментативного продуцирования L-сорбозы из D-сорбита, который является частью способа Рейхстайна (Reichstein).
Различные ацетобактеры (к этому классу также относится Gluconobacter), например такие его виды, как Acetobacter xylinum и Acetobacter suboxydans, известны как эффективные продуценты L-сорбозы из D-сорбита (Biotechnology, v. 6a, 436 437, 1984, edited by H.-J. Rehm and G. Reed, published by Verlag Chemie, Weinheim, Germany).
Если принять во внимание тот факт, что эффективный способ получения 2-кето-L-гулоновой кислоты может быть разработан, исходя из более дешевого по сравнению с L-сорбозой источника, а именно D-сорбита, то становится очевидным, что указанный способ Рейхстайна значительно упрощается.
Как уже упоминалось выше, штамм DSM N 4025 обладает способностью к эффективному продуцированию 2-кето-L-гулоновой кислоты из L-сорбозы, тогда как его способность к конверсии из D-сорбита дает низкий выход. Этот низкий выход при продуцировании 2-кето-L-гулоновой кислоты из D-сорбита обусловлен образованием побочных продуктов, таких как D-глюкоза, D-глюконат и 2-кето-D-глюконовой кислоты, происходящей из D-сорбита. Очистка 2-кето-L-гулоновой кислоты от ее стереоизомера, 2-кeтo-D-глюконовой кислоты, представляет определенные трудности. Ниже показан возможный метаболический путь D-сорбита в штамме DSM N 4025.

Исходя из вышесказанного, очевидно, что повышение эффективности продуцирования 2-кето-L-гулоновой кислоты из D-сорбита при ферментации с использованием штамма DSM N 4025 может быть достигнуто в результате повышения образования L-сорбозы.
Поэтому техническим результатом настоящего изобретения является получение нового способа продуцирования 2-кето-L-гулоновой кислоты из D-сорбита, обеспечивающего высокий выход целевого продукта.
При этом указанный способ осуществляется в условиях, позволяющих исключить продуцирование нежелательных побочных продуктов, таких как D-глюкоза, D-глюконовая кислота и 2-кето-D-глюконовая кислота.
Настоящее изобретение относится к способу получения 2-кето-L-гулоновой кислоты или ее соли, заключающемуся в том, что культивируют культуру микроорганизма (А), обладающего способностью к продуцированию L-сорбозы из D-сорбита и принадлежащего к роду Gluconobacter и Acetobacter, и микроорганизма (В), обладающего способностью к продуцированию 2-кето-L-гулоновой кислоты из L-сорбозы, относящегося к штамму DSM N 4025. Указанное культивирование проводят в среде, содержащей D-сорбит, в присутствии двух микроорганизмов в среде в течение по крайней мере части полного периода культивирования; и после этого проводят выделение 2-кето-L-гулоновой кислоты или ее соли.
Кроме того, согласно настоящему изобретению, L-сорбоза, полученная из D-сорбита с помощью L-сорбоза-продуцирующего штамма, используется для получения 2-кето-L-гулоновой кислоты с помощью штамма, продуцирующего 2-кето-L-гулоновую кислоту. При этом образование побочных продуктов в основном отсутствует.
В указанном выше способе микроорганизм (А), способный продуцировать L-сорбозу из D-сорбита, принадлежит к роду Acetobacter или Gluconobacter, а микроорганизм (В), способный продуцировать 2-кето-L-гулоновую кислоту из L-сорбозы, является штаммом DSM N 4025.
В способе может быть использован любой продукт, полученный в результате выделения из клеток микроорганизмов (А) и (В), таких как покоящиеся клетки, лиофилизованные клетки или иммобилизованные клетки.
Способ может быть осуществлен различными методами, например методом, в котором микроорганизмы (А) и (В) одновременно инокулируют в среду в начале культивирования; методом, в котором сначала инокулируют микроорганизм (А), а затем инокулируют микрорганизм (В) после периода культивирования; и методом, в котором оба микроорганизма (А) и (В) инокулируют отдельно в соответствующие среды, а затем один из них добавляют в питательную среду другого сразу, через некоторое время или через продолжительное время после периода культивирования, с последующим дополнительным культивированием.
В способе согласно изобретению может быть использован любой подходящий метод культивирования микроорганизмов. В соответствии со свойствами отдельных микроорганизмов может быть изменен способ смешивания указанных микроорганизмов. Так, например, отношение количества одного из инокулируемых микроорганизмов к другому, а также время инокуляции предпочтительно выбирать и определять с учетом степени роста соответствующих микроорганизмов, способности продуцировать L-сорбозу и способности конвертировать эту L-сорбозу в 2-кето-L-гулоновую кислоту. Необходимо также учитывать свойства используемых сред. В некоторых случаях могут быть использованы продукты, полученные в результате обработки клеток.
Микроорганизм (А), используемый в способе, может быть выбран из штаммов, находящихся на хранении в коллекциях культур, где они могут быть выданы по первому требованию, например в Институте Ферментации в Осаке (Япония, IFO). Ниже приводится список таких штаммов.
Примеры микроорганизмов (А)
Gluconobacter suboxydans IFO 3130
Gluconobacter suboxydans IFO 3255
Gluconobacter suboxydans IFO 3256
Gluconobacter suboxydans IFO 3257
Gluconobacter suboxydans IFO 3258
Gluconobacter suboxydans IFO
3289
Gluconobacter suboxydans IFO 3290
Gluconobacter suboxydans IFO 3291
Gluconobacter gluconicus IFO 3171
Gluconobacter gluconicus IFO 3285
Gluconobacter
gluconicus IFO 3286
Gluconobacter rubiginosus IFO 3244
Gluconobacter albidus IFO 3251
Gluconobacter albidus IFO 3253
Gluconobacter industrius IFO 3261
Gluconobacter cerinus IFO 3262
Gluconobacter cerinus IFO 3263
Gluconobacter cerinus IFO 3265
Gluconobacter cerinus IFO 3266
Gluconobacter cerinus IFO 3267
Gluconobacter cerinus IFO 3270
Gluconobacter diacetonicus IFO 3273
Gluconobacter roseus IFO 3990
Acetobacter aceti subsp. orleans IFO 3259
Acetobacter aceti subsp,
aceti IFO 3281
Acetobacter liquefaciens IFO 12257
Acetobacter liquefaciens IFO 12258
Acetobacter liquefaciens IFO 12388
Acetobacter aceti subsp. xylinum IFO 3288
Acetobacter aceti subsp. xylinum IFO 13693
Acetobacter aceti subsp. xylinum IFO 13772
Acetobacter aceti subsp. xylinum IFO 13773
Используемый в способе настоящего
изобретения микроорганизм (В) имеет следующие признаки:
негативный тест на оксидазу; окисление этанола с образованием уксусной кислоты; окисление D-глюкозы с образованием D-глюконовой кислоты
и 2- кето-D-глюконовой кислоты; кетогенез полиспиртов; дигидроацетон, в основном, не продуцируется из глицерина; 2-кето-D-глюкаровая кислота продуцируется из D-глюкаровой кислоты, но не продуцируется
из D-глюкозы, D-фруктозы, D-глюконовой кислоты, D-маннита или 2-кето-D-глюконовой кислоты; полиморфное отсутствие жгутиков; коричневые пигменты, образующиеся от D-фруктозы; наблюдается хороший рост
при культивировании совместно с Bacillus megaterium или ее клеточным экстрактом; чувствительность к стрептомицину.
Предпочтительным микроорганизмом (В) является микроорганизм, находящийся на хранении в Немецкой коллекции микроорганизмов в Геттингене под номером DSM N 4025 от 17 марта 1987 года, согласно Будапештскому договору (адрес указанного депозитария: Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, Mascheroder Weg lb, D-3300 Braunschweig, Federal Republic of Germany). Этот микроорганизм относится к виду Gluconobacter oxydans.
Предпочтительно при осуществлении способа вышеуказанные микроорганизмы (А) и (В) инокулируются вместе и культивируются в среде, содержащей D-сорбит и клетки микроорганизма, например покоящиеся клетки или любой обработанный продукт, полученный из клеток, который может быть использован для непосредственного воздействия на D-сорбит. Для культивирования микроорганизмов могут быть использованы любые стандартные способы, а особенно предпочтительным является способ глубинной ферментации с аэрированием и размешиванием. Предпочтительные результаты получаются при культивировании с использованием жидкой питательной среды.
Для культивирования микроорганизмов (А) и (В) может быть использована любая подходящая питательная среда без каких-либо конкретных ограничений, в частности такой средой может быть водная питательная среда, включающая источник углерода и источник азота. Для инкубирования микроорганизмов желательно также использовать другие неорганические соли, а также небольшие количества питательных веществ. Питательные вещества, которые обычно используют для лучшего роста микроорганизмов, вводятся в среду инкубирования.
Кроме того, к D-сорбиту, используемому в настоящем изобретении в качестве исходного материала, могут быть добавлены другие источники углерода, например глицерин, D-глюкоза, D-маннит, D-фруктоза, D-арабит и тому подобные.
В качестве источников азота могут быть использованы различные органические или неорганические вещества, такие как мясной экстракт, пептон, казеин, жидкий кукурузный экстракт, мочевина, аминокислоты, нитраты, соли аммония и тому подобные. В качестве неорганических соединений могут быть использованы сульфат магния, фосфат натрия, хлорид железа (II) и хлорид железа (III), карбонат кальция и т.п.
Количество каждого ингредиента питательных веществ и их отношение варьирует в зависимости от видовых свойств микроорганизмов, количества исходного материала, то есть D-сорбита, количества одного инокулированного микроорганизма по отношению к другому, времени инокулирования и других условий инкубации, и могут быть определены в каждом конкретном случае.
Концентрация исходного материала, то есть D-сорбита, также варьирует в зависимости от видовых и других свойств используемых микроорганизмов. D-сорбит может быть добавлен в среду целиком в начале культивирования, либо частями в течение периода культивирования. В способе настоящего изобретения наилучшие результаты дает добавление D-сорбита частями. В основном используемая концентрация D-сорбита составляет около 20 250 г/л, а более предпочтительная концентрация составляет приблизительно 50 200 г/л в целом.
Условия культивирования могут также варьировать в зависимости от вида и свойств используемых микроорганизмов, а состав среды определяется в каждом конкретном случае с целью наиболее эффективного получения нужного выхода продукта; при этом в основном температура культивирования составляет около 13 36oC, а предпочтительно около 18 33oC, а рН среды обычно составляет около 4,0 9,0, предпочтительно около 6,0 8,0. Как правило, период культивирования может продолжаться от 20 до 80 ч, в течение которых продуцируется наибольшее количество нужного продукта в среде.
Для поддержания значения рН среды в целях обеспечения наибольшей ферментной активности в указанную среду добавляют соответствующее количество кислотного или основного агента в соответствующий момент времени периода культивирования. Альтернативно для достижения указанной цели в начале культивирования в среду вводят соответствующий буфер или буферный агент.
2-кето-L-гулоновая кислота, полученная описанным выше способом, может быть выделена и очищена стандартными методами и преобразована в соответствующую соль, например соль натрия, калия, кальция, аммония и т.п. Соль может быть превращена в свободную кислоту стандартными способами.
Выделение продукта осуществляется с помощью любой комбинации с повторением соответствующих стадий, например путем образования соли или при использовании различий в свойствах между продуктом и присутствующими примесями, таких как растворимость, абсорбционная способность, и отличий по коэффициенту распределения между растворителями. Для выделения продукта обычно используют стандартный способ адсорбции, например, на ионообменной смоле. Полученный таким образом продукт может быть подвергнут дальнейшей обработке, например, путем перекристаллизации или хроматографии.
Полученная описанным способом 2-кето-L-гулоновая кислота или ее соль может быть затем использована непосредственно для конверсии в L-аскорбиновую кислоту путем этерификации с последующей энолизацией и лактонизацией.
Настоящее изобретение иллюстрируется следующими примерами.
Пример 1
Микроорганизмом (В) является штамм DSM N 4025, а в качестве
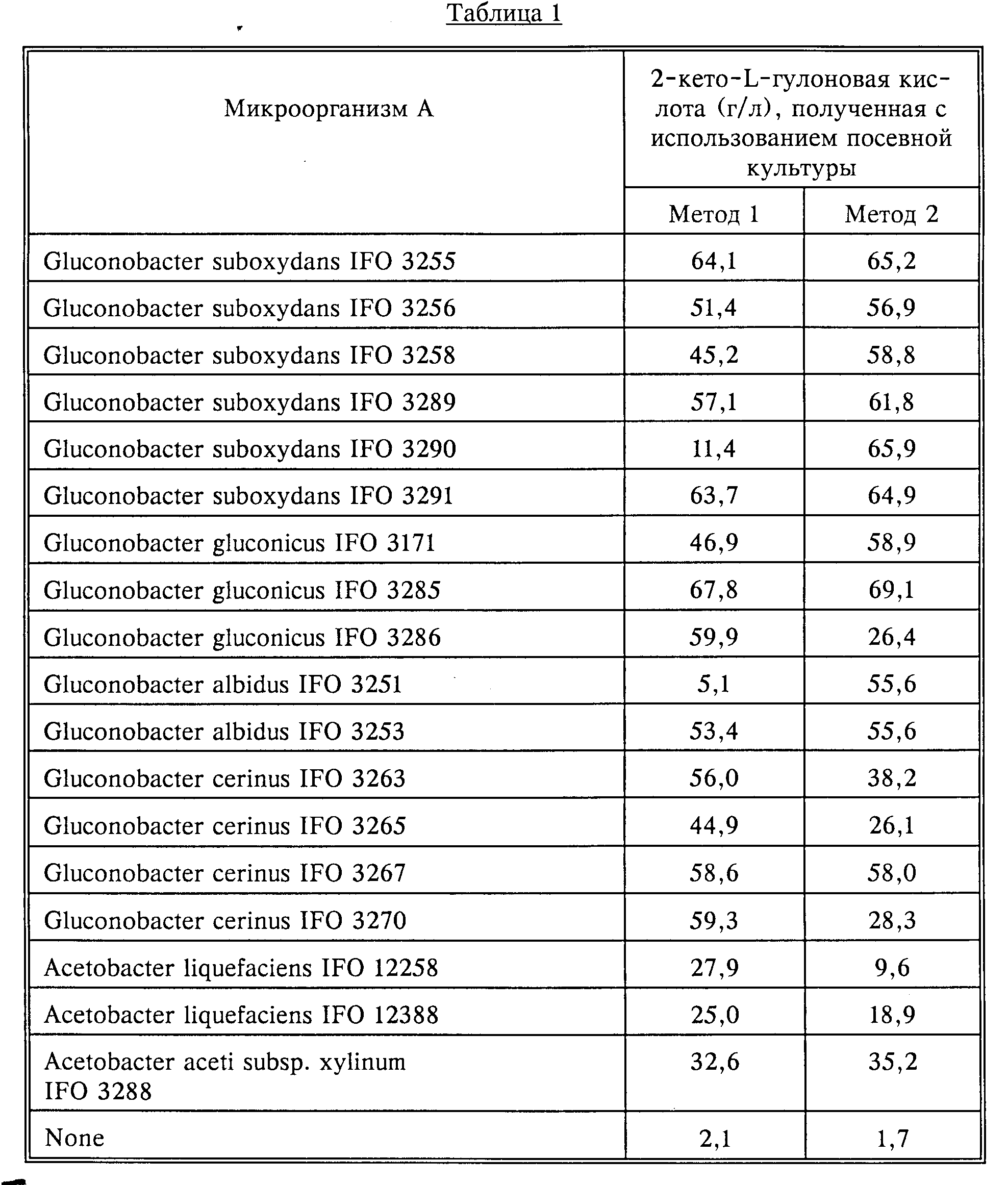
микроорганизма (А) используют микроорганизмы, представленные ниже в табл. 1.
Приготовление посевной культуры
Посевную культуру получают двумя различными методами, описанными
ниже.
Метод 1. В пробирку (18 мм x 200 мм) загружают 5 мл культуральной среды (SCM): D-сорбит 2% дрожжевой экстракт (Oriental Yeast) 0,3% говяжий экстракт 0,3% жидкий кукурузный экстракт 0,3% полипептон 1,0% мочевина 0,1% KH2PO4 0,1% MgSO4•7H20 0,02% CaCO3 0,1% (pH 7,0 перед стерилизацией), стерилизуют в автоклаве при 121oC в течение 20 мин. Затем в пробирку инокулируют одну петлю микроорганизма (А) и одну петлю микроорганизма (В) и инкубируют, вращая (220 об/мин), при 30oC в течение 1 дня.
Метод 2. Пробирку (18 мм x 200 мм), содержащую 5 мл культуральной среды SCM, инокулируют одной петлей микроорганизма (В) и одной петлей микроорганизма (А), и культивируют при вращении в течение 1 дня при 30oC. Одну каплю полученной культуры наносят на агаровую культуральную среду, содержащую 2% агара в среде SCM, и инкубируют в течение 4 дней при 30o C. Микроорганизмы, выращенные на агаровой культуре в виде смеси, используют непосредственно в качестве инокулята для следующей жидкой культуры. Пробирку, содержащую 5 мл среды SCM, инокулируют петлей смеси, полученной, как описано выше, и инкубируют, вращая со скоростью 220 об/мин, в течение 1 дня при 30oC.
Основной процесс ферментации
5 мл полученных отдельных
посевных культур засевают в 500-мл колбу Эрленмейера, содержащую 50 мл продуктивной питательной среды (PM): D-сорбит 8% жидкий кукурузный экстракт 1% мочевина 1,5% (стерилизованная отдельно); KH2PO4 0,1% MgSO4•7H20 0,01% CaCO3 0,6% и противовспениватель 0,1% (pH 7,0 перед стерилизацией), инкубируют при 30oC в течение 4 дней,
вращая со скоростью 180 об/мин. В табл. 1 систематизированы результаты количественного определения 2-кето-L-гулоновой кислоты в культуральной питательной среде, проведенного с помощью жидкостной
хроматографии высокого разрешения.
Пример 2.
Посевные культуры Gluconobacter suboxydans IFO 3255 и штамма DSM N 4025 получают способом, аналогичным описанному в примере 1. Концентрации клеток Gluconobacter suboxydans IFO 3255 и штамма DSM N 4025 в посевных культурах составляют 3,7•1010 кл./мл и 5,4•108 кл./мл соответственно.
Каждую полученную посевную культуру засевают в 50 мл среды PM в 500-мл колбы Эрленмейера при полном объеме инокулята 10% (об./об.), где отношение (% об. /об.) между Gluconobacter suboxydans IFO 3255 и штаммом DSM N 4025 в посевном материале вырьировали следующим образом: 0:10, 1:9, 2:8, 3:7, 4:6, 5: 5, 6:4, 7:3, 8:2, 9:1 и 10:0. Колбы инкубируют 4 дня при 30oC. Результаты представлены в табл. 2. При отношении концентраций штамма DSM N 4025 и Gluconobacter suboxydans IFO 3255, составляющем 1:9 4:6, количество продуцируемой 2-кето-L-гулоновой кислоты составляло 63,8 г/л 66,6 г/л, исходя из 80 г/л D-сорбита (степень конверсии: 74,9 78,1 М%); причем аккумуляции 2-кето-L-глюконовой кислоты не наблюдалось.
Пример 3
В качестве микроорганизма (А)
используют Gluconobacter suboxydans IFO 3255 и Gluconobacter gluconicus IFO 3285, а в качестве микроорганизма (В) используют штамм DSM N 4025. Отдельную посевную культуру (200 мл) получают методом 2,
описанным в примере 1. Полученную посевную культуру (200 мл) засевают в 3-литровый ферментер, содержащий около 1,7 л сбраживаемой среды: D-сорбит 8% 10% или 12% дрожжевой экстракт 0,5% жидкий
кукурузный экстракт 2,5% MgSO4•7H2O 0,0086% мочевина 0,086 (стерилизованная отдельно); KH2PO4 0,086% и противовспениватель 0,15% Стерилизуют при
121oC в течение 20 мин. После инокуляции объем с культурой доводят до 2 л путем добавления стерилизованной воды. Ферментацию проводят при 30oC, вращая со скоростью 700 об/мин, и
при аэрации 1 л/мин. Значение pH культуры (7,0) поддерживают с помощью 4 н. Na2СО3. Результаты представлены в табл. 3.
Пример 4
Способом, аналогичным
описанному в примере 3, посевную культуру (200 мл) смеси Gluconobacter suboxydans IFO 3255 и штамма DSM N 4025 инокулируют в трехлитровый ферментер, содержащий 8% D-сорбита в сбраживающей среде, после
чего рабочий объем доводят до 2 л путем добавления стерилизованной воды. Ферментацию начинают при тех же условиях, что и в примере 3. При этом отдельно приготавливают флакон (500 мл), загруженный 300
мл питательной среды: 120 г D-сорбита, 10 г дрожжевого экстракта, 50 г жидкого кукурузного экстракта, 0,172 г KH2PO4, 1,72 г мочевины (стерилизованной отдельно) и 2,5 г
противовспенивателя. Во время ферментации вышеуказанную питательную среду непрерывно подают в ферментер со скоростью 15 мл/ч в период ферментации от 12 до 18 ч, со скоростью 60 мл/ч в период между 18
и 21 ч, со скоростью 4,3 мл/ч в период между 21 и 28 ч при помощи перистальтического насоса. В результате из 276 г D-сорбита было получено 224 г 2-кето-L-гулоновой кислоты при степени конверсии 76,1
М% за 51 ч ферментации.
Пример 5
Одну петлю Gluconobacter suboxydans IFO 3255 инокулируют в 500-мл колбу Эрленмейера, содержащую 100 мл среды SCM, и инкубируют при 30oC в течение 1 дня. Затем 10 мл полученной культуры переносят в колбу Эрленмейера на 500 мл, содержащую 100 мл среды SCM, и инкубируют при 30oC в течение 1 дня. В целом было получено
1,5 л посевной культуры Gluconobacter suboxydans IFO 3255. С другой стороны, одну петлю штамма DSM N 4025 инокулируют в колбу Эрленмейера на 500 мл, содержащую 100 мл среды для посевной культуры:
L-сорбоза 8% глицерин 0,05% мочевина 0,5% (стерилизованная отдельно); жидкий кукурузный экстракт 1,75% хлебопекарные дрожжи (Oriental Yeast) 5,0% MgSO4•7H2O 0,25% CaCO3 1,5% и противовспениватель 0,1% (pH 7,0 перед стерилизацией). Инкубируют 1 день при 30oC на роторной качалке (180 об/мин). 10 мл полученной таким образом культуры инокулируют в 100
мл той же среды и инкубируют 1 день при 30oC. В целом было получено 1,5 л посевной культуры штамма DSM N 4025. В 50-литровый ферментер загружают 25 л среды для ферментации: D-сорбит 8%
жидкий кукурузный экстракт 5% MgSO4•7H20 0,01% KH2PO4 0,025% и противовспениватель 0,17% и стерилизуют 30 мин при 121oC. Обе посевные
культуры (1,5 л каждая) инокулируют одновременно и полный объем культуры доводят до 30 л путем добавления стерилизованной воды. Ферментацию осуществляют при 30oC с размешиванием со
скоростью 400 об/мин и при аэрации 20 л/мин. pH культуры поддерживают при 7,0 с использованием 6,25 н. NaOH. Отдельно пятилитровый сосуд загружают 4 л питательной среды, содержащей 1800 г D-сорбита,
150 г жидкого кукурузного экстракта, 1,29 г MgSO4•7H2O, 7,5 г KH2PO4, 25 г противовспенивателя, и стерилизуют 20 мин при 120oC. Через 12 ч
культивирования питательную среду непрерывно подают в ферментер со скоростью 222 мл/ч в течение 18 ч при помощи перистальтического насоса. Через 45,5 ч культивирования получают 36,8 л сбраживаемой
среды, содержащей 93,5 г/л 2-кето-L-гулоновой кислоты. Другими словами, из 4200 г D-сорбита получают 3441 г 2-кето-L-гулоновой кислоты с выходом 76,8 М%
Пример 6
Сбраживаемую среду
(3,68 л), полученную в соответствии с описанием примера 5, центрифугируют для удаления клеточного и других седиментов. Супернатант (2 л), содержащий 93,5 г/л 2-кето-L-гулоновой кислоты, концентрируют
при пониженном давлении и при 45oC до получения объема около 1 л. Во время концентрации наблюдают образование белого осадка. Затем в концентрат добавляют 100 мл этанола и оставляют на 1
день при 10oC. Полученные в результате осадки собирают фильтрацией, промывают небольшим количеством 50%-ного холодного этанола и осушают при комнатной температуре и пониженном давлении. В
качестве первого сбора получают 137,6 г моногидрата мононатриевой 2-кето-L-гулоновой кислоты с чистотой 99,14% Маточный раствор концентрируют при пониженном давлении до около 400 мл, затем добавляют
около 100 мл этанола и раствор оставляют на 24 ч при 10oC. В результате этого получают в качестве второго сбора 71,9 г моногидрата мононатриевой соли 2-кето-L-гулоновой кислоты (с чистотой
85,04%).
Пример 7
Супернатант (0,5 л), полученный в соответствии с описанием в примере 6, пропускают через Amberlite IR-120 (H-type) (Rohm and Haas Company) и осушают при
пониженном давлении. К осушенному материалу (около 50 г) добавляют 400 мл метанола и 0,5 мл 98% серной кислоты. Затем смесь нагревают 2 ч при 90oC, метанол удаляют, а остаток промывают
небольшим количеством метанола и осушают. Осушенный остаток суспендируют в 150 мл метанола и нагревают при дефлегмации с 10 г метилата натрия. Полученные кристаллы охлаждают, фильтруют и осушают при
пониженном давлении. В результате получают 35,1 г натриевой L-аскорбиновой кислоты.
Реферат
Использование: биотехнология, получение продуктов микробиологического синтеза. Сущность иэобретения: получение 2-кето-L-гулоновой кислоты или ее соли путем ферментативной конверсии D-сорбита заключается в том, что культивируют культуру микроорганизма (А), обладающего способностью к продуцированию L-сорбозы из D-сорбита и принадлежащего к роду Gluconobacter и Acetobacter, и микроорганизма (В), обладающего способностью к продуцированию 2-кето-L-гулоновой кислоты из L-сорбита и представляющего собой фактически штамм Gluconobacter oxydans DSM N 4025, при этом указанное культивирование проводят в среде, содержащей D-сорбит, а указанные два микроорганизма совместно присутствуют в среде в течение по крайней мере части полного периода культивирования. В качестве микроорганизма (А) используют определенные штаммы, относящиеся к Gluconobacter suboxydans, Gluconobacter gluconicus, Gluconobacter albidus, Gluconobacter cerinus, Acetobacter acetixylinum. Процесс ведут обычно при рН 5 - 8, температуре 18 - 33oC и концентрации сорбита 20 - 120 г/л в питательной среде. 2-Кето-L-гулоновая кислота, полученная данным способом, может быть выделена и очищена стандартными методами, и получена в виде соответствующей соли, например соли натрия, калия, кальция, аммония или т. п., которая затем может быть использована непосредственно для конверсии в L-аскорбиновую кислоту. 4 з.п. ф-лы, 3 табл.

Комментарии