Экзополимер - RU2025127C1
Код документа: RU2025127C1
Чертежи

Описание
Изобретение относится к области иммунотерапии, к внеклеточному экзополимеру, обладающему иммуномодуляторными свойствами.
Экзополимер, являющийся предметом изобретения, продуцируется при культивировании отобранных селекцией штаммов вида Bifidobacterium infantis longum грамположительной бактерии, которая имеет таксономические характеристики между Bifidobacterium infantis и Bifidobacterium longum. Обладая иммуномодуляторными свойствами, этот экзополимер представляет большой интерес для медицины и ветеринарии.
Бактериальный штамм IBS Bifidobacterium infantis longum, депонированный под номером 1-885 в институте Пастера в Национальной коллекции культур микроорганизмов (НККМ), культивируют в анаэробных условиях в подходящей среде и после удаления микроорганизмов из культуральной среды продуцированный ими экзополимер выделяют и осаждают путем добавления органического растворителя. Полученный путем осаждения продукт лиофилизируют.
Штамм IBS может культивироваться на подходящей среде любого типа, компоненты которой имеют мол. м. менее 10 тыс. дальтон, в анаэробных условиях, предпочтительно при 37оС. Детально состав этой среды описывается далее.
Микроорганизмы удаляют из культуральной среды предпочтительно центрифугированием, и экзополимер выделяют, например, ультрафильтрацией на калиброванной пористой мембране с удерживающим порогом, выше или равным 10 тыс. дальтон.
Изолированный таким образом продукт затем концентрируют, подвергают диализу, осаждают добавлением органического растворителя, предпочтительно этанола, и наконец лиофилизируют.
Полученный экзополимер имеет в основном полисахаридную природу, состоит, в первую очередь, из глюкозы и галактозы в соотношении от 1 : 1 до 4 : 1 и содержит белковую фракцию в количестве до 30 мас.%. Во фракции полисахаридов соотношение глюкозы и галактозы составляет 1 : 1 - 4 : 1, предпочтительно около 3 : 2.
Экзополимер по изобретению имеет мол. м. в диапазоне от 10 до 100 тыс. дальтон, предпочтительно 20-30 тыс. дальтон. Он может образовывать агрегаты мол. м. порядка 106 дальтон в равновесии с частицами более низкой молекулярной массы. Он свободен также от нуклеиновых кислот, жиров и органических кислот.
Изолированный таким образом и очищенный экзополимер обладает интересными иммуномодуляторными свойствами и при этом нетоксичен. Опыты, проведенные как in vitro, так и in vivo, показали, что экзополимер, продуцированный штаммом IBS, ведет себя как иммуномодулятор и увеличивает неспецифическое сопротивление хозяина. Экзополимер также обладает антилейкемическими (противоопухолевыми) свойствами, происхождение которых может быть связано с его иммуномодуляторными свойствами, описанными в "Определении иммуномодуляторных свойств экзополимера, продуцируемого штаммом IBS".
Экзополимер, продуцируемый штаммом IBS, может быть успешно использован в качестве основного активного начала различных фармацевтических составов, которые могут применяться через рот, парентерально или местно. Эти фармацевтические составы могут быть представлены в виде форм, обычно используемых в медицине и ветеринарии, например в виде простых или покрытых сахаром таблеток, капсул, маленьких пилюль, растворов, сиропов, суппозиториев, инъецируемых препаратов, пессариев, кремов, помад, лосьонов, капель и глазных мазей. Они все изготавливаются обычными методами.
Основное активное начало (экзополимер) может вводиться в фармацевтические составы самостоятельно или вместе с другими фармакологически активными агентами. Используемые носители и вспомогательные вещества, также обычные, такие как тальк, камедь, маннитол, крахмал, стеарат магния, кокосовое масло, водные или неводные носители, жировые вещества животного или растительного происхождения, производные парафина, гликоли, различные увлажняющие, диспергирующие или эмульсифицирующие агенты и консерванты.
У животных заметные иммуномодуляторные эффекты наблюдались на мышах для доз между 4-400 мкг на мышь.
Примеры касаются приготовления экзополимера (также называемого РВЗD) и его фармакологического действия.
П р и м е р 1. Получение экзополимера путем культивирования бактериального штамма IBS Bifidobacterium infantis longum.
Стадия А: культивирование штамма IBS.
Штамм IBS культивируют в анаэробных условиях при 37оС (воздух удаляют в начале ферментации) в следующей питательной среде, г/л: пентон (мол. м. 10 тыс. дальтон) 5; NaCl 3; глюкоза 10; цистеин 0,5; ацетат натрия 2; Na2HPО4 2,87; КН2РО4 1,12; MgSО4 0,09; NaН2РО4 0,15; NaНСО3 2,2; твин 1; витаминный раствор 10 мл/л.
Для повышения выхода к этой культуральной среде может быть с выгодой добавлена твердая основа, такая как CYTODEX или ее эквивалент. В этих условиях штамм IBS продуцирует экзополимер, количество которого можно установить в надосадочной жидкости с использованием тестового метода ELISA, разработанного для этой цели и описанного далее.
10 л указанной культуральной среды помещают в 12-литровый ферментер для ее стерилизации. Ферментер затем засевают 1000 мл культуры штамма IBS, выдержанной предварительно в такой же среде в течение 48 ч. Жидкость барботируют смесью 90% азота и 10% СО2 в течение 20 мин со скоростью 3 л смеси в минуту.
Инкубация осуществляется при 37оС при перемешивании 400 об/мин в атмосфере смеси N2/СО2 в обычном соотношении, которую вводят в среду в течение первых двух часов ферментации. Через 48 ч, по окончании ферментационного процесса, методом ELISA определяют количество продуцированного полисахарида. Минимальный выход составляет 35 мкг/мл.
Стадия B: выделение и очистка полученного экзополимера.
После завершения процесса ферментации клетки отделяют центрифугированием. После осаждения клеток надосадочную жидкость ультрафильтруют. Сохраняются только молекулы тяжелее 10000 дальтон. Раствор, содержащий полученный экзополимер, концентрируют десятикратно и затем подвергают диализу.
Концентрированный раствор осаждают спиртом (этанол : вода - 3 : 1 по объему).
Наконец, осажденный спиртом продукт лиофилизируют. Таким образом получают беловатый продукт, который выглядит волокнистым.
Из упомянутой культуры получают 10 л надосадочной жидкости, которые концентрируют до 1 л путем ультрафильтрации. Объем доводят до 10 л дистиллированной водой и затем его снова уменьшают до 1 л ультрафильтрацией. Эту операцию проводят дважды. Полученный таким образом 1 л концентрированного раствора осаждают этанолом (3 : 1 по объему). Полученный осадок лиофилизируют с получением около 400 л лиофилизата.
Метод ELISA.
Используемый антиген - препарат полисахарида, чистота которого обеспечивается дополнительной депротеинизацией фенолом. Начальную дозу 0,5 кг инъецируют кролику в двух инъекциях - одной внутрибрюшинной и другой подкожной - вместе с полным адъювантом Фрейнда.
Инъекцию повторяют на 15-й день, на этот раз с использованием неполного адъюванта Флейнда. Пятнадцатью днями позже у кролика берут кровь с получением антисыворотки с высоким уровнем антител, которая позволяет методом ELISA узнать экзополимер, очищенный хроматографией на колонне SEPHADEX G200, и экзополимер, присутствующий в надосадочной жидкости культур Bifidobacterium после осаждения этанолом.
Тест ELISA проводят на микрочашках. Антиген адсорбируется. Затем выемки в оставшихся пустыми участках заполняют сывороточным альбумином. Затем осуществляют инкубацию со специфическими антителами, полученными от кролика. Затем добавляют антитела, направленные против антител кролика. Они конъюгируют к делочной фосфатазе. Наконец, добавляют субстрат (ортонитрофенил фосфат). После инкубации реакцию останавливают с использованием ЗМ раствора NaOH. Оптическая плотность (светопоглощение) измеряется при 405 нм на приборе ELISA, этой процедурой получают достаточно высокие титры антител для получения положительной реакции для 10-4 разведений антисыворотки при концентрации очищенных антигенов 4 мкг.
Характеристика экзополимера, продуцированного штаммом АВ
1) Полученный продукт состоит существенно из глюцидов (измерено фенольно-сернокислым методом) и белков (измерено
методом
Лоури) в соотношении 5 : 1.
Этот продукт не содержит никаких нуклеиновых кислот согласно аналитическим данным, полученным ионно-исключающей хроматографией или газовой хроматографией. Ни в одном из случаев гидролизат не содержит пентоз. Продукт свободен от липидов согласно результатам газовой хроматографии после экстрагирования н-гептаном. В нем нет и органических кислот согласно измерениям, сделанным ионно-исключающей хроматографией.
2) Согласно результатам, полученным высокопроизводительной жидкостной хроматографией (HPLC) на колонне RP - 8 300 А, продукт имеет гликопротеиновую природу.
3) Глюцидная часть состоит из глюкозы и галактозы согласно аналитическим данным, полученным ионно-исключающей, тонкослойной и газовой хроматографией.
4) Глюкоза и галактоза присутствует в соотношении 3 : 2 согласно результатам газовой хроматографии мономеров, гидролизованных метанолизом и затем ацетилированных трифторацетилированием.
5) Полисахаридная часть имеет разнообразные связи 1-2, 1-3, 1-4 и 1-6 согласно хроматограмме, полученной газовой хроматографией метилированных (метанолизом) и затем ацетилированных (трифторацетилированием) мономеров.
6) Биологическая активность, измеряемая по способности стимулировать увеличение количества клеток, образующих зоны гемолиза (PFC), проистекает из глюцидной части и поддерживается после обработки протеиназой К, повреждающей белковую часть.
7) Примерная мол. м. колеблется от 20000 до 30000 дальтон согласно результатом хроматографии на SEPHADEX G200 (пик низкомолекулярной массы).
Экзополимер может образовать агрегаты молекулярной массы порядка 106 дальтон в равновесии с частицами более низкой массы.
Определение иммуномодуляторных свойств экзополимера, продуцируемого штаммом IBS (тест "ин витро").
Пролиферация спленоцитов (селезеночных макрофагов).
Пролиферация спленоцитов в присутствии митогена может быть измерена окислением МТТ [3-(4,5-диметилтиазол-2-ил)-2,5-дифенил тетразол бромид] в формазан митохондриальной дегидрогеназой.
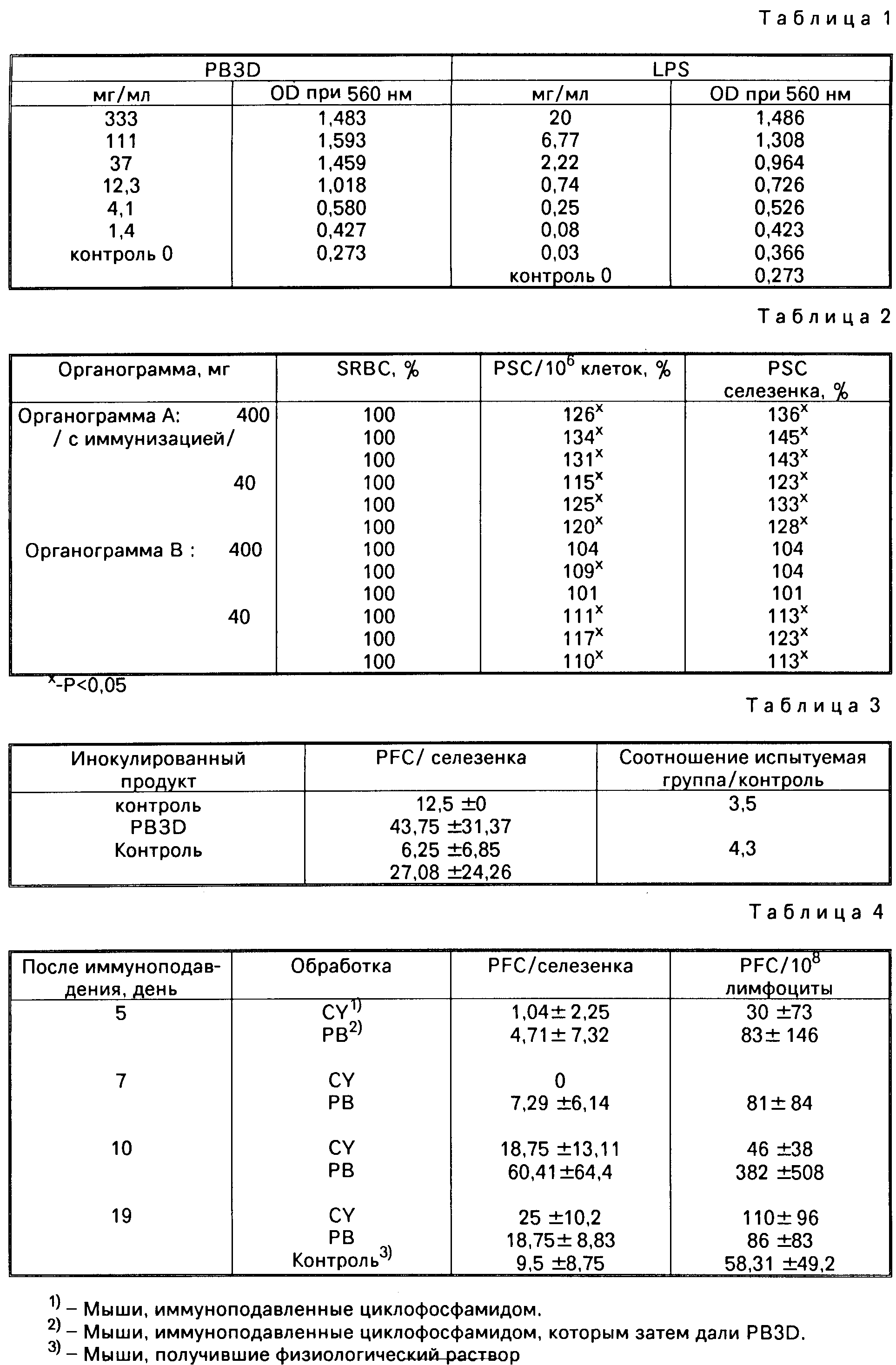
Пролиферация (спленоцитов мыши C57BL/6) выражается оптической плотностью (светопоглощением) при 560 нм как функция концентрации PB3D или концентрации LPS (см. табл. 1). PB3D вызывает пролиферацию, которая немного слабее пролиферации, вызываемой LPS.
Определение иммуномодуляторных свойств экзополимера, продуцируемого штаммом IBS (тест "ин вива").
Стимулирование производства клеток, синтезирующих антитела.
У мышей этот экзополимер неспецифически стимулирует производство клеток, синтезирующих антитела при оральном введении вместе с эритроцитами овцы или внутрибрюшинно без эритроцитов овцы. Экзополимер также нормализуют эту способность у мышей, когда она подавлена циклофосфамидом.
П р и м е р. После 5-дневного орального введения PB3D и иммунизирующей дозы на 19-й и 20-й дни (органограмма А) или без иммунизирующей дозы (органограмма В), наблюдается увеличение количества PFC в селезенке мышей, в зависимости от введенных доз (см. табл. 2).
П р и м е р. После внутрибрюшинного введения разовой дозы 400 мг / на мышь PB3D, наблюдается значительное увеличение количества PFC через 4 дня (табл. 3 и 4).
Влияние на состав сывороточных протеинов.
Различные иммуномодуляторы изменяют иммуноэлектрофоретические характеристики сывороточных протеинов, определенных как X.LA и LB. Экзополимер по изобретению вызывает такую модификацию.
П р и м е р. Внутрибрюшное введение PB3D в количестве 400 мг на мышь вызывает через 24 ч и через 4 дня модификацию сывороточных протеинов, сравнимую с изменениями, вызываемыми липополисахаридами Escherichia coli (LPS).
П р и м е р. Подобным образом, общее введение 400 мг оральным путем с разбивкой на 5 последовательных дневных доз по 80 мг вызывает модификацию протеинов, заметную через пять дней после введения экзополимера.
Очищение коллоидного углерода.
Экзополимер вводят внутривенно (по 2,5 г на мышь) мышам Balb/C. Через 48 ч внутривенно вводят 0,2 мл суспензии коллоидного углерода. Исчезновение коллоидного углерода из крови, называемое очищением, выражается логарифмической кривой уровня углерода во времени. Экзополимер усиливает процесс очищения (табл. 5).
Увеличение неспецифической резистентности.
У мышей, иммуноподавленных циклофосфамидом и помещенных в холод, можно наблюдать, что экзополимер по изобретению увеличивает неспецифическую резистентность хозяина к бактериальной инфекции такой, как, например, вызванной Pseudomonas на слизистых оболочках или к вирусной инфекции (вирус Coxsackie B).
Иммуноподавление осуществляют введением внутрибрюшинно 200 мг/кг циклофосфамида. На третий день начинают пятидневную оральную обработку экзополимером (по 80 мг на мышь в день).
Контрольные мыши получают эквивалентное количество физиологического раствора. Несколькими часами позже окончания курса обработки мышей инфицируют интраназально штаммом Pseudomonas aeroginosa сделанным патогенным для мышей. Процент выживания у обработанных мышей ниже (табл. 6).
П р и м е р. Иммуноподавление создают разовым внутрибрюшным введением 200 мг/кг циклофосфамида.
На третий день начинают пятидневную обработку экзополимером (80 мг на мышь в день). Контрольные мыши получают эквивалентное количество физиологического раствора. Через несколько часов после окончания курса обработки мышей инфицируют внутрибрюшинно вирусом Coxsackie В5 (0,5 мл м 107 PFU) и оценивают степень выживания, которая выше у обработанных мышей (табл. 7).
Тесты на спонтанную и индуцированную лейкемию.
Экзополимер по изобретению способен задерживать появление лейкемии у мышей AKR (линия инбредных мышей очень часто развивает спонтанную лейкемию). Экзополимер также способен задерживать у мышей RF появление лейкемии, вызванной канцерогенным веществом, таким как метилхолантрен. (Линия RF является инбредной, у которой метилхолантрен вызывает очень скоро появляющуюся лейкемию).
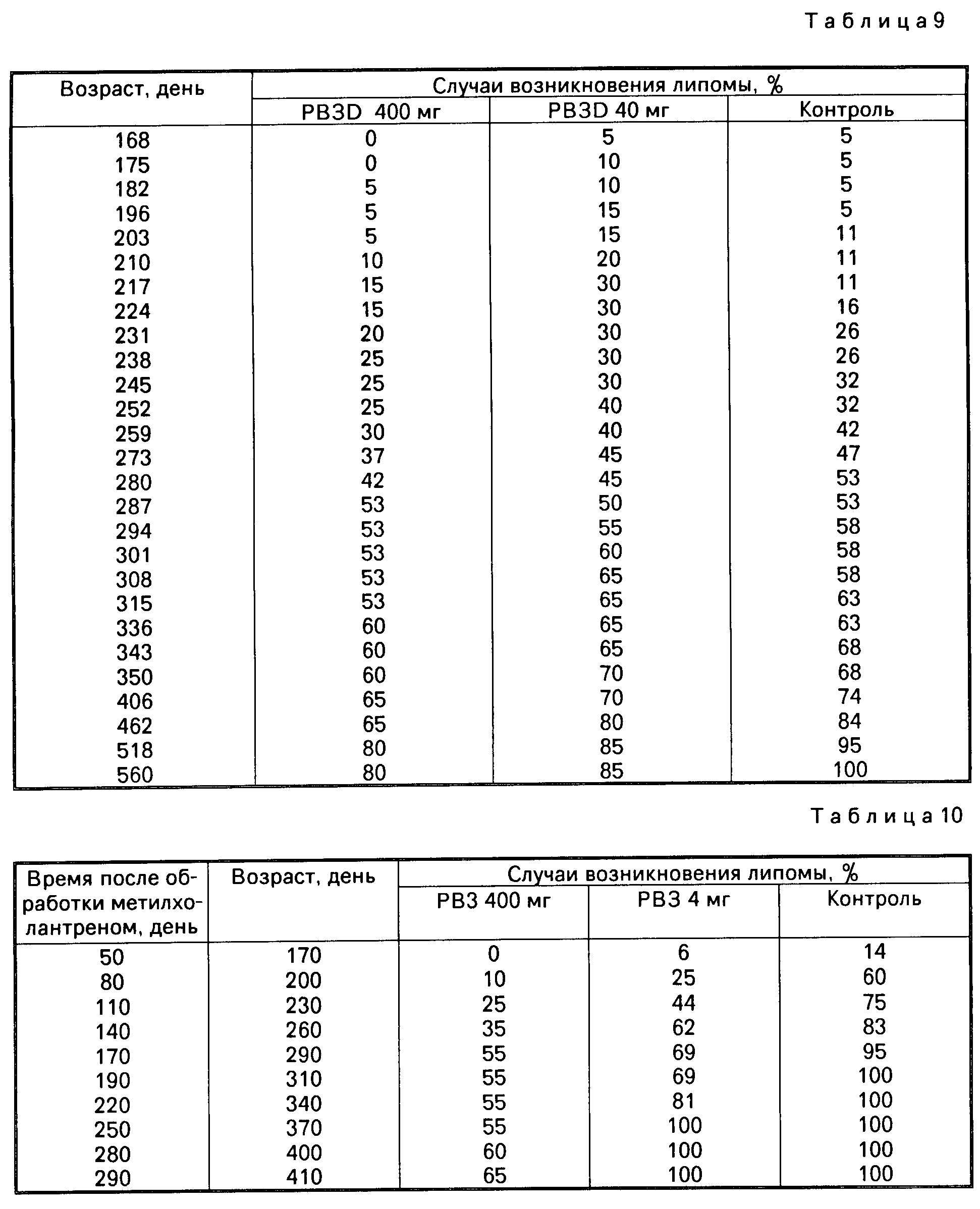
П р и м е р. Две группы мышей AKR получали орально пятидневную терапию PB3D каждый месяц, тогда как третья группа не получала испытываемый продукт и служила в качестве контроля. Из двух обработанных групп одна получала общую месячную дозу в 400 мг (по 80 мг в день на мышь пять последовательных дней), а другая получала общую месячную дозу в 4 мг (по 0,8 мг в день на мышь пять последовательных дней) (табл. 8 и 9).
Полученные результаты показывают задержку появления лейкемии у обработанных мышей. Эта разница была отчетливо значительной у группы, получавшей месячную дозу в 400 мг. Эти данные были подтверждены другим опытом, при котором обработанные группы получали по 400 мг и 50 мг PB3D соответственно.
П р и м е р. В течение двух месяцев до тематического введения метилхолантрена две группы мышей RF получали по два оральных введения с перерывом в три недели.
Одной из групп давали общую месячную дозу 400 мг (80 мг в день на мышь пять последовательных дней), тогда как другая получала общую месячную дозу величиной 4 мг (по 0,8 мг в день на мышь пять последовательных дней). Контрольную группу не обрабатывали. Лейкемию вызывали кожным применением метилхолантрена на тщательно выбритый участок тела. Введение PB3D замедлило появление лейкемии. Эта задержка была ясно заметна у группы, получавшей 400 мг PB3D (табл. 10).
Острая токсичность.
Тесты на острую токсичность проводили путем внутривенного введения экзополимера в следующих дозах, мкг: 1; 10; 15; 100; 300; 600 и 1200 на мышь в хвостовую вену, по каждой дозе 5 мышам. Ни одна из доз не вызвала негативных реакций у мышей, которые все были живы еще два месяца после инъекции.
Описание штамма.
Штамм IBS Bifidobacterium infantis longum был депонирован 6 июля 1989 г. в Национальной коллекции культур микроорганизмов (институт Пастера, 25 rue de Docteur Roux 75724, Paris, Cedex, France). Он носит депозитарный номер 1-885.
Этот штамм был выделен из сточной воды, содержащей фекалии человека, и представляет таксономические характеристики между Bifidobacterium infantis и Bifidobacterium longum и может быть типирован по профилю структурных компонентов, по профилям ферментационных катаболитов D-глюкозы, по резистентности к антибиотикам и по продуцированию экзополимера по изобретению.
Реферат
Изобретение относится к иммунотерапии, в частности к новому внеклеточному экзополимеру, обладающему иммуномодуляторными свойствами. Сущность изобретения: экзополимер представляет собой гликопротеин, выделяемый из штамма Bifidobacterium infantis longum, депонированный в институте Пастера под номером 1 - 885. Экзополимер имеет следующие свойства: мол.м. 10000 - 100000 дальтон и может образовывать агрегаты мол.м порядок 106 дальтон в равновесии с частицами более низкой молекулярной массы, полисахаридная часть состоит из глюкозы и галактозы в соотношении (1 - 4) : 1, а белковая фракция достигает 30 % от массы экзополимера. 10 табл.

Комментарии