Иммуногенная полипептидная композиция, способ получения композиции, способ продуцирования и способ обнаружения антител, набор - RU2136311C1
Код документа: RU2136311C1
Чертежи


































Описание
Область техники
Изобретение относится в общем к иммунореактивным полипептидным композициями,
способам использования композиций в иммунологических применениях, материалам и способам получения композиций.
Предпосылки изобретения
Вирус гепатита C был недавно
идентифицирован как основная причина посттрансфузионного гепатита ни-A - ни-B (NANBH), а также гепатита NANBH, распространяющегося другими путями. Материалы и методы получения вирусных геномных
последовательностей известны. См., например, публикации PCT N W089/04669, W090/11089 и W090/14436.
Молекулярная характеристика генома вируса гепатита C(HCV) указывает, что это РНК молекула с положительной полярностью, содержащая приблизительно 10000 нуклеотидов, которые кодируют полипротеин из примерно 3011 аминокислот. Некоторые линии данных дают основания предположить, что HCV имеет схожую генетическую организацию с вирусами семейства Flaviviridae, которое включает флави- и пестивирусы. Как и его родственные пести- и флавивирусные формы HCV кодирует большой полибелковый предшественник, от которого образуются отдельные вирусные белки (как структурные, так и неструктурные).
Содержащие РНК вирусы могут обладать относительно высокими скоростями спонтанной мутации, т.е. порядка 10-3 - 10-4 на включенный нуклеотид. Поэтому, так как гетерогенность и изменчивость генотипа присущи вирусам с РНК, может существовать множество вирусных изолятов, которые вирулентны и авирулентны в пределах видов HCV.
Ряд различных изолятов HCV сейчас были идентифицированы. Последовательности этих изолятов демонстрируют ограниченную гетерогенную характеристику РНК вирусов.
Изолят HCV JI.I описан у Kubo, J. и др. (1989), Japan Nucl. Acids Res. 17: 10367-10372; Takeuchi K. и др. (1990), J. Gen. Virol. 71:3027-33; Takeuchi и др. (1990), Nucl. Acids Res. 18:4626.
Полные кодирующие последовательности плюс 5'- и 3'-концевые последовательности двух независимых изолятов, "HCV-J" и "BK" описаны Kato и др. и Takamizawa и др. соответственно. (Kato и др. (1990), Proc. Natl. Acad. Sci. USA 87:9524-9528; Takamizawa и др. (1991), J. Virol. 65:1105-13).
HCV изоляты также описываются в
следующих публикациях:
"HCV-I": Choo и др. (1990), Brit. Med. Bull. 46: 423-41; Choo и др. (1990), Proc. Natl. Acad. Sci. 88:2451-55; Han и др.
(1991), Proc. Natl. Acad. Sci. 88:1711-15;
Европейской патентной публикации N 318216.
"HC-J1" и "HC-J4": Ocamoto и др. (1991) Japan I. Exp. Med. 60:167-77.
"HCT 18", "HCT 23", "Th", "HCт 27", "EC1" и "EC10": Weiner и др. (1991), Virol. 180:842-848.
"Pt-1", "HCV-K1" и "HCV-K2": Enomoto и др. В Японии существуют два основных типа вируса гепатита C. Отделение гастроэнтерологии, Департамент внутренних болезней, Медицинский университет Каназавы, Япония.
Клоны "A", "C", "D" и "E": Tsukiyama - Kohara и др. Вторая группа вируса гепатита, в Uirus Genes.
Типичный подход к созданию диагностикумов и вакцин - сосредоточить внимание на консервативных вирусных доменах. Однако этот подход страдает недостатком иннорирования важных эпитопов, которые могут находиться в вариабельных доменах.
Цель настоящего изобретения - получение полипептидных композиций, которые иммунологически перекрестно-реактивны с многими изолятами HCV, особенно относительно гетерогенных доменов вируса.
Содержание изобретения
Было выявлено ряд важных эпитопов HCV различается в
различных вирусных изолятах и что эти эпитопы могут быть
картированы в отдельных доменах. Это открытие позволяет выработать стратегию получения иммунологически перекрестно-реактивных полипептидных
композиций, которые фокусируются на вариабельных (а не
консервативных) доменах.
Соответственно одним вариантом настоящего изобретения является иммунореактивная композиция, содержащая полипептиды, в которой полипептиды включают аминокислотную последовательность эпитопа внутри первого вариабельного домена HCV, и в композиции присутствуют по меньше мере две гетерогенные аминокислотные последовательности из первого вариабельного домена различных HCV изолятов.
Другим вариантом изобретения является иммунореактивная композиция, содержащая множество антигенных совокупностей, в которой (a) каждая антигенная совокупность состоит из множества по сути идентичных полипептидов, включающих аминокислотную последовательность эпитопа внутри первого варабельного дюмена изолята HCV, и (b) аминокислотная последовательность эпитопа одной совокупности гетерогенна по отношению к аминокислотной последовательности аналогичной последовательности по меньшей мере одной из других совокупностей.
Следующий вариант изобретения - это иммунореактивная композиция, содержащая множество полипептидов, в которой каждый полипептид имеет
формулу
Rr - (SVn) - R'r'
,
где R и R' - аминокислотные последовательности с 1 - 2000 аминокислотами и являются одинаковыми или разными;
r и
r' - 0 или 1 и одинаковые или разные;
V - аминокислотная
последовательность, включающая последовательность изменчивого домена HCV, в которой изменчивый домен содержит по меньшей мере один
эпитоп;
S - целое число ≥ 1, представляющее выбранный
изменчивый домен; и
n - целое число ≥ 1, представляющее выбранный изолят HCV, гетерогенный на данной SY по
отношению по меньшей мере к одному другому изоляту с другой величиной для n,
причем выбирается независимо для каждой x;
x - целое число ≥ 1; и
с оговоркой, что аминокислотные
последовательности присутствуют в композиции, представляющей комбинацию,
выбранную из группы, состоящей из (i), 1V1; и 1V2, (ii) 1V1 и 2V2, и (iii) 1V1 и 2V1.
Следующий вариант изобретения
- это способ приготовления иммуногенной фармацевтической композиции HCV, включающий:
(a) получение иммунореактивной
композиции, как описано выше;
(b) обеспечение подходящего
наполнителя; и
(c) смешивание иммунореактивной композиции (a) с наполнителем (b) в пропорции, обеспечивающей иммуногенную
реакцию при назначении млекопитающему.
Следующий вариант изобретения представляет собой способ получения антител против HCV, включающий назначение млекопитающему эффективного количества иммунореактивной композиции, как описано выше.
Следующий вариант изобретения представляет собой способ обнаружения антител к HCV в биологической пробе, включающий:
(a) взятие биологической пробы, которая, как предполагается, содержит
антитела к HCV;
(b) обеспечение наличия иммунореактивной композиции, описанной выше;
(c) реакцию биологической
пробы (a) с иммунореактивной композицией (b) при условиях, которые
позволяют образование комплексов антиген-антитело; и
(d) обнаружение образования комплексов антиген-антитело,
сформированных между иммунореактивной композицией (a) и антителами биологической
пробы (b) при наличии таковых.
И еще один вариант изобретения представляет собой лабораторный комплект для обнаружения антител к HCV в биологическом образце, включающий иммунореактивную композицию, описанную выше, упакованную в подходящий контейнер.
Краткое описание чертежей
На фиг. 1 схематически показана генетическая организация генома
HCV.
На фиг. 2 показано сравнение выведенных аминокислотных последовательностей E1 белка, закодированного изолятами HCV группы I и группы II.
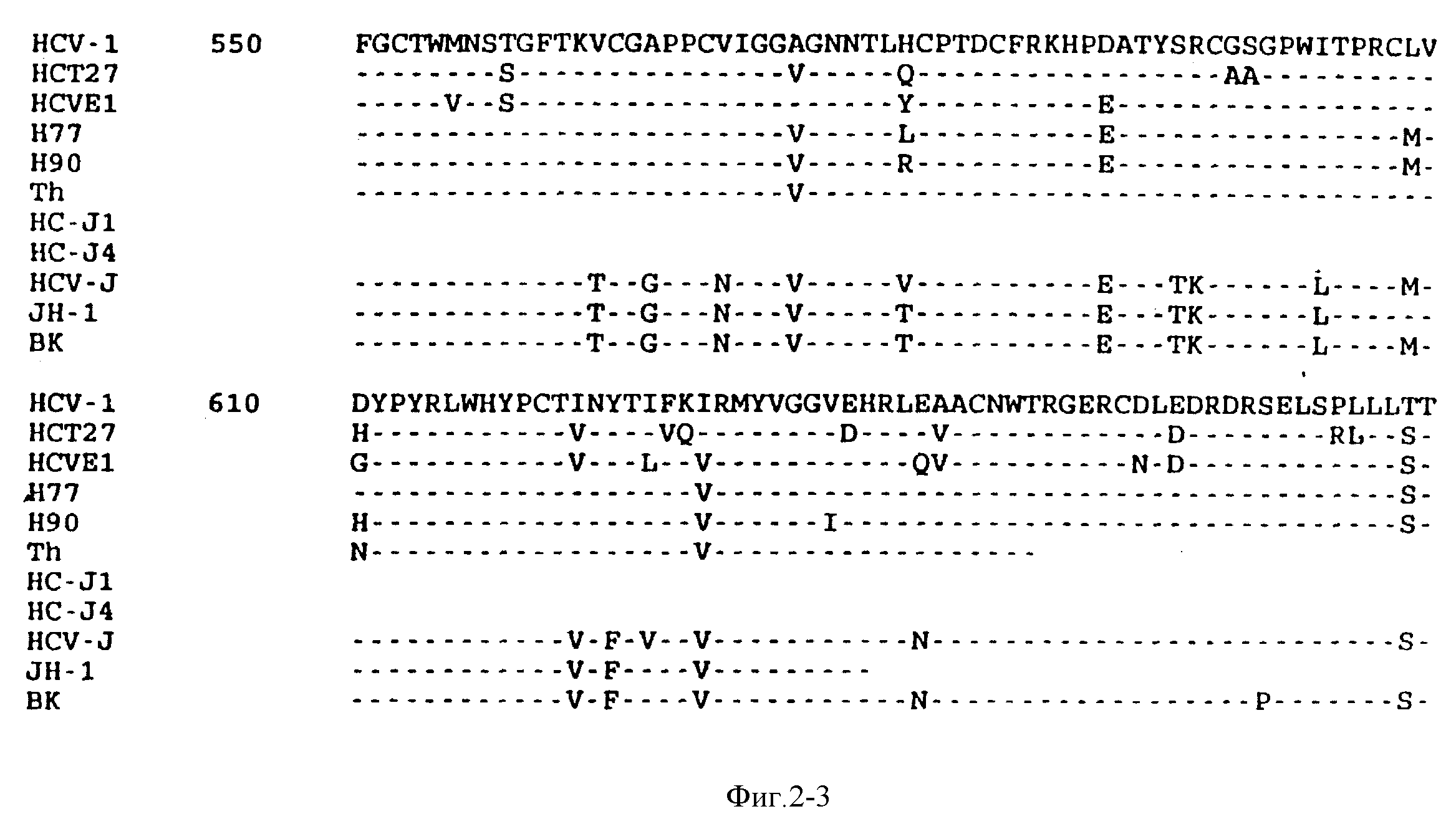
На фиг. 3 показаны в сравнении аминокислотные последовательности предполагаемого E2/NS 1 участка изолятов HCV.
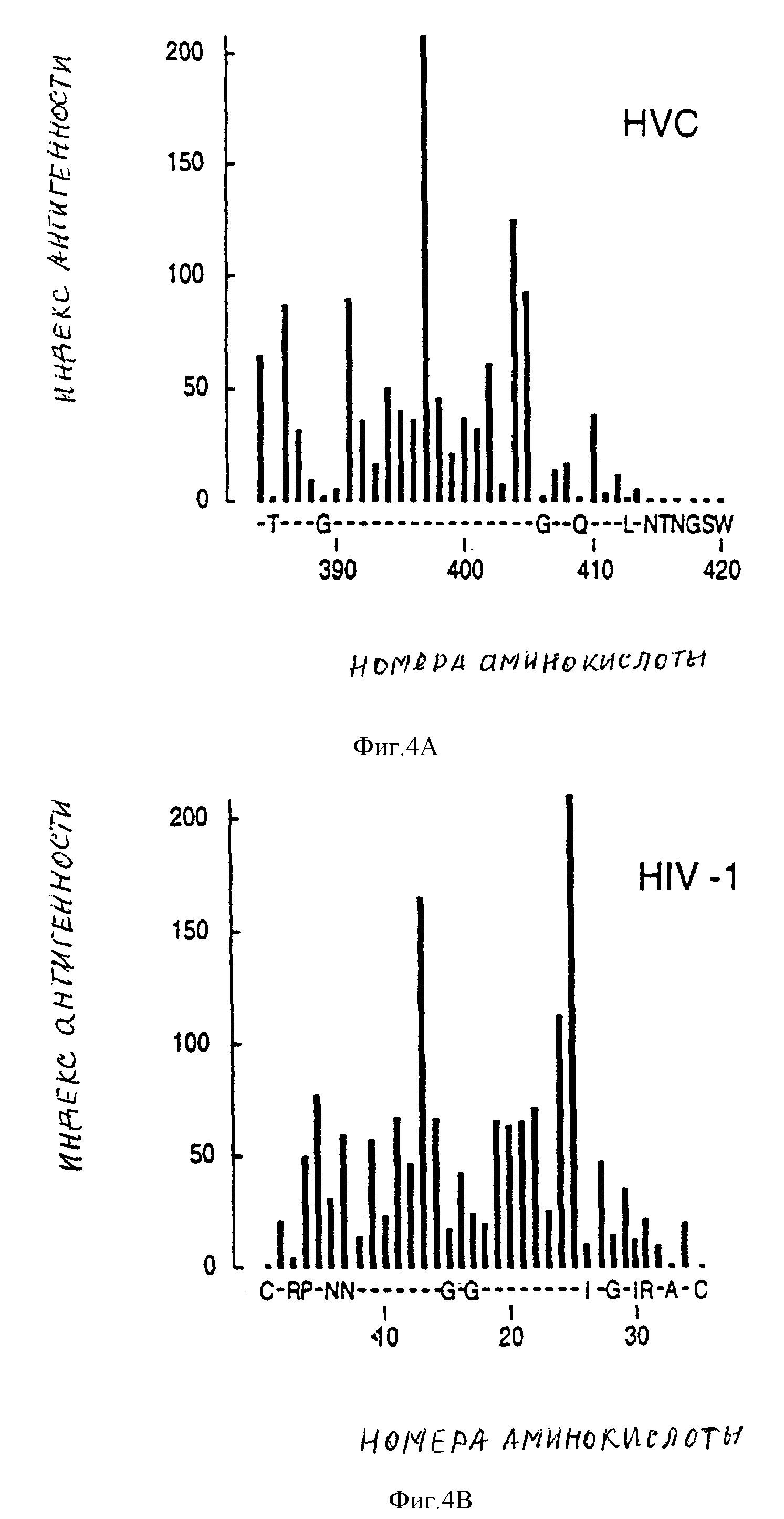
На фиг. 4 (A и B) даются графики, показывающие антигенные профили для амино-концевой области предполагаемого белка E2/NS 1 HCV (аминокислоты 384-420), и гипервариабельный участок gp 120 V3 HIV-1.
На фиг. 5 показана серия графиков, на которой представлена процентная вероятность выявления данного остатка от аминоконцевой области белка E2/NS 1 HCV (аминокислоты 384-420) во вторичной структуре альфа-спирали, бета-пласта или бета-витка.
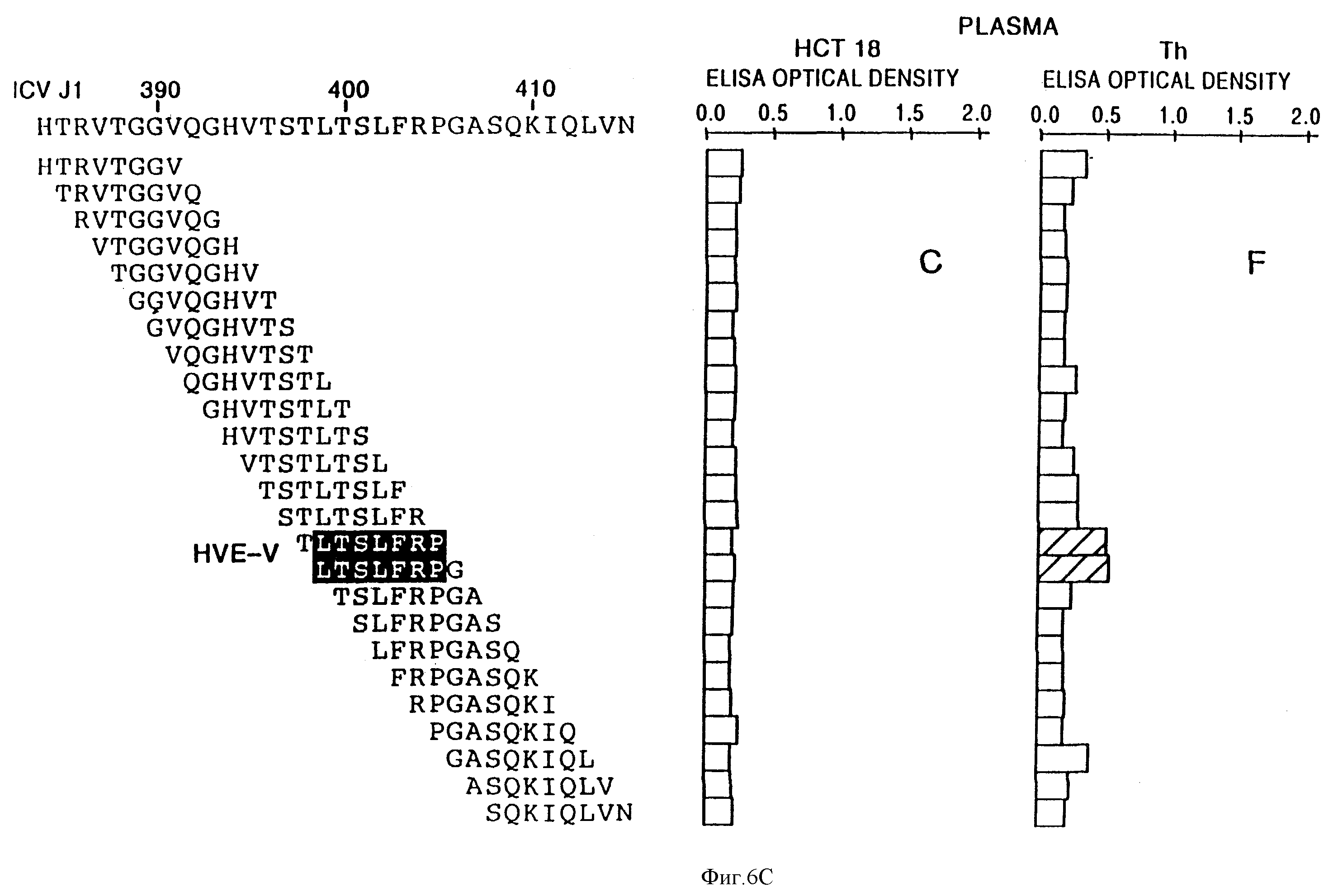
На фиг. 6 представлены вертикальные графики, демонстрирующие реактивность антител в плазме от HCV 18 (панели A-C) или Th (панели D-F) с перекрыванием биотинилированных 8mer пептидов, произведенных от аминокислот 384-415 или 416 изолятов HCT 18 HCV (A, D), Th (B, E) и HCV J1 (C, F) соответственно.
На фиг. 7 показаны выведенные аминокислотные последовательности двух участков E2/NS 1 полипептида, аминокислоты 384-414 и 547-647, данные для изолятов Q1 и Q3.
На фиг. 8-1 показаны выведенные аминокислотные последовательности изолятов HCV J1.1 и J1.2 от аминокислот 384 - 647. На фиг. 8-2 показаны выведенные аминокислотные последовательности изолятов HCT27 и HCVEI от аминокислот 384 - 651.
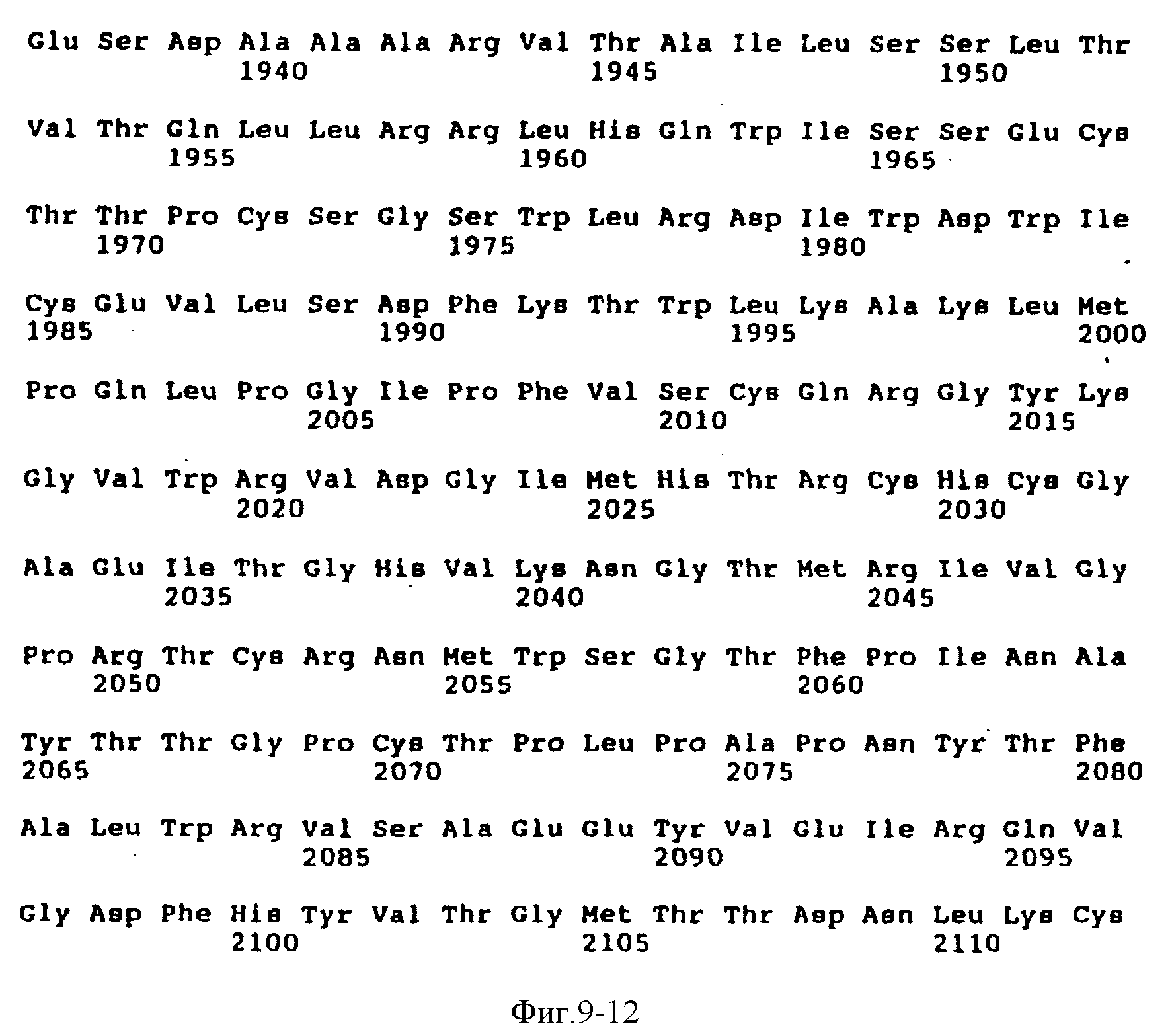
На фиг. 9 показана вся полипротеиновая последовательность изолята HCV-1.
Способ реализации изобретения
Практика настоящего изобретения использует, если не оговорено иначе,
традиционную технику молекулярной биологии, микробиологии,
рекомбинантной ДНК и иммунологии, которая применяется в данной области. Такие технические приемы полностью описаны в литературе. См.,
например, Maniatis, Fitsh & Sambrook, Molecular Cloning; a
Laboratory Manual. (2-е изд. 1989). DHA Cloning, т. 1 и 2 (D. N. Glover изд. 1985). Oligonucleotide Synthesis (M. J. Gate, изд. 1984;
Nucleic Acid Hibridization (B. D. Hames & S.J. Higgins,
eds. 1984); Transcribtion and Translation (B.D. Hames & S.J. Higgins, eds. 1984); Animal Cell Culture (R.I. Freshney, ed. 1986);
Immobilized Cells and Enzymes (IRL Press, 1986); B. Perbal, a
Practical Guide to Molecular Cloning (1984); the series, Methods in Enzymology (Academic Press, Inc.); Gene Transfer Vectors for
Mammalian Cells. (J. H. Miller and M.P. Cabos eds. 1987, Cold Spring
Harbor Laboratory); Methods in Enzymology, vol. 154 и 155 (Wu and Grossman, and Wu eds.), Mayer and Walker, eds. (1987),
Immunochemical Methods in Cell and Molecular biology (Academic Press, London),
Scopes (1987). Protein Purification Principles and Practice, Sec. Ed. (Springer-Verlag), Handbook on Experimental
Immunology, v. 1 - 4 (Weis and Blackwell ed. 1986); Immunoassay; A Practical Guide
(D.W. Chan ed., 1987).
Все патенты, патентные заявки и публикации, упомянутые здесь, выше и далее, включены сюда ссылкой.
HCV-новый член семейства Flaviviridae, которое включает пестивирусы (вирус холеры свиней и вирус диареи крупного рогатого скота) и флавивирусы, примерами которых являются вирусы денге и желтой лихорадки. Схема генетической организации HCV показаны на фиг. 1. Подобно флави- и пестивирусам, HCV кодирует основной полипептидный домен ("C") на N-конце вирусного полипротеина с последующими двумя доменами гликопротеида ("E1", "E2/NS1") выше от неструктурных генов NS2 - NS5. Аминокислотные координаты предполагаемых доменов белка показаны в таблице 1 (см. табл.1 - 6 в конце описания).
Как указывалось выше, был идентифицирован ряд изолятов HCV. Сравнительный анализ полной и частичной последовательностей HCV указывает, что, основываясь на гомологии на уровнях нуклеотида и аминокислоты, изоляты HCV можно широко подразделить по меньшей мере на три основные группы (таблица 2). См. - Houghton и др. (1991) Hepathology 14; 381 - 388. Однако для изолятов в группе III имеется только частичная последовательность. Поэтому когда последовательности этих изолятов определяются более конкретно, один или несколько этих изолятов следует выделить в другую группу, включающую потенциальную четвертную группу. В таблице 3 показаны гомологи последовательности между индивидуальными вирусными белками разных изолятов HCV, выведенные из их нуклеотидных последовательностей. Здесь видно, что белки той же самой вирусной группы демонстрируют большую схожесть в последовательности, чем те же белки, закодированные различными вирусными группами (таблица 3). Одним исключением из этого является белок нуклеокапсида, который высоко консервативен среди всех последовательностей вирусных изолятов группы I и II. (В таблице 3 обозначение N/A означает, что сравнить последовательности не представлялось возможным). Поэтому для целей настоящего изобретения изоляты группы I можно определить как изоляты, имеющие на аминокислотном уровне около 90% или больше гомологичных вирусных белков, в частности белков E1 и E2/NS1 в сравнении с изолятами, классифицированными как группы I. Группа II определяется аналогичным образом. Будущие группы можно таким же образом определить с точки зрения гомологичности вирусного белка относительно изолята прототипа. Подгруппы можно также определить гомологией в предельных белках, таких как белки E1, E2/NS1 или NS2, или по более высоким уровням гомологии.
Надо сказать, что предполагаемые белки вирусной оболочки, закодированные генами E1 и E2/NS 1 показывают значительную вариацию аминокислотной последовательности между группами I и II. Только NS 2 демонстрирует большую степень гетерогенности, в то время как белки C, NS 3, NS 4 и NS 5 все показывают большую консервативность между группами. Вариация последовательности, наблюдаемая в предполагаемых белках оболочки вириона между группами I и II, отражает характерное расщепление аминокислот между двумя группами. Пример этого показан на фиг. 2, где последовательность продукта гена E1 сравнивается между вирусами групп I и II. Показаны аминокислотные последовательности E1, выведенные из нуклеотидных последовательностей групп II и II HCV. На фиг. горизонтальные строки указывают идентичность последовательности с HCV-1. Звездочками указано расщепление аминокислот в специфических группах. Остатки в специфических группах можно четко идентифицировать. Последовательности в группе I - HCV-1, HCT 18, HCT 23, HCT 27 и HC-J1. последовательности группы II - HC-J4, HCV-I, HCV J1.1 и BK. Такое специфическое для группы расщепление аминокислот также имеет место в продуктах других генов, включающих gp72, закодированный геном E2/NS1. На фиг. 3 показана сравнительная последовательность аминокислот предполагаемого E2/NS1 участка изолятов HCV, которые расщепляют как группа I и группа II. последний белок также содержит N-концевой гипервариабельный участок ( "HV") с около 30 аминокислотами, которые показывают большую вариацию почти между всеми изолятами. См. Weiner и др. (1991), supra. Этот участок находится между аминокислотами 384 - 414, если использовать систему нумерации аминокислот HCV-1.
Предполагаемый гликопротеид E2/NS1 оболочки HCV может соответствовать полипептиду оболочки gp 53 (BVDV)/gp55 (Вируса холеры свиней) пестивирусов и NS1 флавивирусов, оба из которых дают защитный иммунитет реципиентам, вакцинированным этими полипептидами.
Поразительное сходство между гипервариабельным участком ("HV") и доменами gp 120 V3HIV-1 относительно степени вариации последовательности, предсказанное действие аминокислотных изменений на предполагаемое связывание антитела в дополнение к отсутствию определенной вторичной структуры предполагают, что домен HV кодирует нейтрализующие антитела.
Иммуногенность домена показана экспериментами в составлении карты эпитопа антитела, описанными в примерах. Результаты этих исследований предполагают, что в дополнение к трем основным группам HCV, HV специфические подгруппы также существуют.
Анализ биологических выборок от людей с HCV, вызванным NANBH, показывает, что реципиенты могут нести два или несколько вариантов HCV одновременно. В плазме одного человека было найдено два сосуществующих варианта, J1. Кроме того, частичное секвенирование гена лица с хроническим NANBH с перемежающимися вспышками гепатита выявило, что лицо, Q, заражено двумя вариантами HCV (Q1 или Q3). Каждый вариант был связан только с одним эпизодом заболевания. ELISA (энзим-связанный иммуно-сорбентный анализ), использующий Q1 или Q3 специфический пептид (аминокислоты 396 - 407) показал, что Q вырабатывал антитело на Q1 пептид, но не на соответствующий Q3 пептид, делая вывод, что рецидивы заболевания Q были обязаны появлению HV варианта. Наличие антител на Q1 пептид, но отсутствие гуморальной иммунной реакции на Q3 пептид во время второго эпизода заболевания предполагают, что вариация в домене HV может быть следствием давления иммунного отбора. Полагают, что аминокислоты 296 - 407 подвергаются большему селективному давлению в домене HV. Эти находки подкрепляют тезис, что частота вспышек при заболевании может быть отнесена на счет неадекватной иммунологической реакции реципиента на заражение HCV и/или эффективные вирусные механизмы иммунологического уклонения. Более того, они указывают на участок E2/NSIHV как на генетический участок, захваченный вирусным механизмом избавления и/или механизмом (ами) неадекватной иммунологической реакции.
Как указывалось выше, существует несколько вариантных участков внутри генома HCV. Один или несколько таких участков, как можно предположить с большой вероятностью, - вовлечены в механизм вирусного избавления и/или механизм неадекватной иммунологической реакции. Поэтому желательно включить в изобретение композиции HCV полипептидов для лечения, которые индуцируют иммуногенную реакцию на эти варианты.
Поскольку участки E1 и E2/NS1 генома кодируют предполагаемые полипептиды типа оболочечных, эти участки представляют особый интерес в отношении иммуногенности. Итак, эти участки находятся среди тех, по отношению к которым наиболее желательно индуцировать и/или повысить иммунную реакцию для защиты от заражения HCV, и воспрепятствовать хроническим обострениям заболевания у зараженных индивидов. Кроме того, эти участки будут среди тех, от которых желательно обнаружить варианты HCV, возникающие в ходе заражения, а также параллельное заражение двумя или несколькими вариантами.
Настоящее изобретение описывает композиции и методы лечения индивидов для профилактики инфекций HCV и, в частности, заражений хроническим HCV. Кроме того, оно описывает композиции и методы обнаружения наличия анти-HCV антител в биологических пробах. Этот последний метод особенно полезен в идентификации анти-HCV антител, выработанных в ответ на иммунологически отчетливые эпитопы HCV. Этот метод можно также использовать для изучения эволюции множественных вариантов HCV внутри зараженного индивида. В описании изобретения используются следующие определения.
Термин "полипептид" относится к полимеру аминокислот и не относится к специфической длине продукта; таким образом, пептиды, олигопептиды и белки включены в определение полипептида. Этот термин также не относится или исключает пост-экспрессивные модификации полипептида, например гликозилирование, ацетилирование, фосфорилирование и другие. В определение включены, например, полипептиды, содержащие один или несколько аналогов аминокислоты (включающие, например, неприродные аминокислоты и пр.), полипептиды с замещенными звеньями, а также другие модификации, известные в данной области, как природные, так и неприродные.
Здесь A считается "достаточно изолированным" от B, если масса A составляет по меньшей мере 70%, лучше 80%, а еще лучше 90% от комбинированной массы A и B. Полипептидные композиции настоящего изобретения предпочтительно практически свободны от ткани человека или другого примата (включая кровь, сыворотку, клеточного лизата, клеточных органелл, клеточных белков и пр.) и среды клеточной культуры.
"Рекомбинантный полинуклеотид" предполагает полинуклеотид геномного, кДНК, полусинтетического или синтетического происхождения, который вследствие его происхождения или манипуляции (1) не ассоциируется со всем или частью полинуклеотида, с которым он ассоциируется в природе, (2) связан с другим полинуклеотидом, а не с тем, с которым он связан в природе, или (3) которого нет в природе.
"Полинуклеотид" - полимерная форма нуклеотидов любой длины, либо рибонуклеотидов, либо деоксирибонуклеотидов. Этот термин относится только к первичной структуре молекулы. Таким образом, этот термин включает дву- и одноцепочечные ДНК и РНК. Он также включает известные типы модификаций, например метки, которые известны в данной области, метилирование, "шапки" ("capb"), замещение одного или нескольких природных нуклеотидов аналогами, межнуклеотидные модификации, такие как, например, модификации с незагруженными звеньями (например, фосфоротиоатами, фосфородитиоатами и пр.), содержащие незаконченные половины, такие как, например, белки (включающие нуклеазы, токсины, антитела, сигнальные пептиды, поли-L-лизин и пр.), модификации и интеркаляторами (например, акридином, псораленом и пр.), модификации, содержащие хелаторы (например, металлы, радиоактивные металлы и пр.), содержащие алкиляторы, модификации с модифицированными звеньями (например, альфа аномерные нуклеиновые кислоты и пр.), а также немодифицированные формы полинуклеотида.
"Рекомбинантные клетки реципиента", "клетки реципиента", "клетки", "клеточные линии", "клеточные культуры" и другие такие термины, обозначающие микроорганизмы или другие эукариотные клеточные линии, культивируемые как одноклеточные структуры, относятся к клеткам, которые могут быть или были использованы как реципиенты для рекомбинантного вектора или другого полинуклеотида переноса, и включают потомство первоначальной клетки, которая была трансфецирована. Следует понимать, что потомство одной родительской клетки не обязательно может быть полностью идентично по морфологии или геномному или общему комплементу ДНК первоначальной родительской клетке из-за естественной, случайной или намеренной мутации.
"Репликон" - является любым генетическим элементом, например плазмидой, хромосомой, вирусом, космидой и пр. , который ведет себя как автономная единица полинуклеотидной репликации внутри клетки, т.е. способен ауторепродуцироваться под своим собственным контролем.
"Вектор" является репликоном, далее включающим последовательности, обеспечивающие репликацию и/или экспрессию открытой рамки считывания.
"Контрольная последовательность" относится к полинуклеотидным последовательностям, которые необходимы, чтобы осуществить экспрессию кодирующих последовательностей, к которым они лигируются. Характер таких контрольных последовательностей различен в зависимости от организма реципиента; в прокариотах такие контрольные последовательности включают промотор, рибосомный связующий участок и терминатор; в эукариотах такие контрольные последовательности, как правило, включают промоторы, терминаторы и в некоторых случаях усилители. Термин "контрольные последовательности" предназначен включать как минимум все компоненты, присутствие которые необходимо для экспрессии, и может также включать дополнительные компоненты, присутствие которых дает преимущество, например лидерные последовательности, которые регулируют секрецию.
"Промотор" представляет собой нуклеотидную последовательность, которая состоит из согласованных последовательностей, позволяющих связывание полимеразы РНК с матрицей ДНК таким образом, что продуцирование мРНК инициируется на нормальном сайте инициации транскрипции для соседнего структурного гена.
"Операбельно связанный" предполагает сопоставление, в котором компоненты находятся в связи, позволяющей им функционировать своим предполагаемым образом. Контрольная последовательность, "операбельно связанная" с кодирующей последовательностью, лигируется таким образом, что экспрессия кодирующей последовательности достигается при условиях, совместимых с контрольными последовательностями.
"Открытая рамка считывания" (OPF) является участком полинуклеотидной последовательности, которая кодирует полипептид; этот участок может представлять часть кодирующей последовательности или всю кодирующую последовательность.
"Кодирующая последовательность" - это полинуклеотидная последовательность, которая транскрибируется в мРНК и/или транслируется в полипептид, когда помещается под контроль соответствующих регуляторных последовательностей. Границы кодирующей последовательности определяются инициирующим кодоном трансляции на 5'-конце и терминирующим кодоном на 3'-конце. Кодирующая последовательность может включать, но не ограничиваться до мРНК, ДНК (включая кДНК), и рекомбинантных полинуклеотидных последовательностей.
Здесь "эпитоп" или "антигенный детерминант" означает аминокислотную последовательность, которая иммунореактивна. Обычно эпитоп состоит по меньшей мере из 3-5 аминокислот, а чаще из 8, или даже 10 аминокислот. Здесь эпитоп обозначенного полипептида означает эпитопы с той же аминокислотной последовательностью, что и эпитоп в обозначенном полипептиде, и его иммунологические эквиваленты.
"Антиген" - это полипептид, содержащий один или несколько эпитопов.
"Иммуногенный" означает способность формировать клеточную и/или гуморальную иммунную реакцию. Иммуногенная реакция может быть сформирована только одними иммунореактивными полипептидами или может потребовать наличия носителя в присутствие или отсутствие адъюванта.
"Иммунореактивный" относится к (1) способности иммунологического связывания с антителом и/или антигенным рецептором лимфоцита или (2) способности быть иммуногенным.
"Антитело" представляет собой иммуноглобулин, включающий антитела и их фрагменты, которые связывают специфический эпитоп. Термин охватывает поликлональные, моноклональные и химерные антитела. Примеры химерных антител обсуждаются в патентах США N 4816398 и 4816567.
"Антигенный набор" определяется как композиция, состоящая из множества фактически идентичных полипептидов, в которой полипептиды состоят из аминокислотной последовательности одного определенного эпитопа.
"Фактически идентичные полипептиды" означают полипептиды, которые идентичны, за исключением вариации, ограниченной до типичного диапазона последовательности или вариации размера, отнесенной на счет способа получения полипептиды; например, рекомбинантная экспрессия, химический синтез, тканевая культура и т. п. Эта вариация не меняет желаемое функциональное свойство композиции фактически идентичных полипептидов; иммунологически ее поведение как у композиции фактически идентичных полипептидов. Вариации могут иметь место благодаря изменениям, происходящим в результате секреторного процесса во время переноса полипептида, со снижением эффективности до менее 100% в химическом синтезе и пр.
"Здесь "изменчивый или вариабельный домен" или "V" вирусного белка представляет собой домен, который демонстрирует постоянную модель аминокислотной вариации между по меньшей мере двумя изолятами HCV или субпопуляциями. Предпочтительно домен содержит по меньшей мере один эпитоп. Вариабельные домены могут отличаться от изолята к изоляту всего лишь на 1 изменение аминокислоты. Эти изоляты могут быть из одних и тех же или разных групп или подгрупп HCV. Вариабельные домены можно легко идентифицировать композицией последовательности среди изолятов, и примеры этой технологии описаны ниже. Для целей описания настоящего изобретения вариабельные домены будут определяться относительно аминокислотного количества полибелка, закодированного геномом HCV-1, как показано на фиг. 9 с метионином инициатора, указанным в позиции 1. Соответствующий вариабельный домен в другом изоляте HCV определяется выравниванием последовательностей двух изолятов, так что консервативные домены за любым вариабельным доменом максимально выравниваются. Это можно сделать с помощью одной из множества компьютерных программ, таких как AL/GN 1,0 из Университета Вирджинии, Отдела биохимии (Обращаться к Д-ру Вильяму Р. Персону. ) См. Pearson и др. (1988) Proc. Natl. Acad. Sci. USA 85: 2444 - 2448. Следует сказать, что номера аминокислот, данные для определенного вариабельного домена, в какой-то степени субъективны, и это вопрос выбора. Таким образом, следует понимать, что начало и конец вариабельных доменов приблизительны и включают перекрывающие домены или субдомены, если не указано иначе.
Эпитоп представляет собой "иммунологический эквивалент" другого эпитопа в обозначенном полипептиде, когда он перекрестно реагирует с антителами, которые иммунологически связываются с эпитопом в обозначенном полипептиде.
На карте эпитопы обычно включают по меньшей мере около пяти аминокислот, иногда около 8 аминокислот и даже около 10 или больше аминокислот.
Аминокислотная последовательность, включающая эпитоп HCV, может быть соединена с другим полипептидом (например, белком носителя) либо ковалентной связью, либо экспрессированием слитого полинуклеотида, чтобы сформировать белок слияния. При желании можно вставить или присоединить множественные повторы эпитопа и/или включить множество эпитопов. Белок носителя можно произвести из любого источника, но обычно это относительно крупный иммуногенный белок, такой как BSA, KLH или другой. При желании можно использовать в качестве носителя белок HCV с полной длиной, умножая число иммуногенных эпитопов. Аминокислотная последовательность от эпитопа HCV может быть также связана на аминоконце и/или карбокси-конце с не-HCV аминокислотной последовательностью. Таким образом, полипептид будет "полипептидом слияния". Аналогичные типы полипептидов можно построить с использованием эпитопов из других обозначенных вирусных белков.
"Вариант" обозначенного полипептида относится к полипептиду, в котором аминокислотная последовательность обозначенного полипептида была изменена делецией, замещением, добавлением или перестановкой одной или нескольких аминокислот в последовательности. Методы, с помощью которых получают варианты (например, рекомбинацией) или мутагенезом, направленным на сайт, известны.
"Трансформация" относится к вставке экзогенного полинуклеотида в клетку реципиента, независимо от метода, используемого для вставки, например прямого поглощения, трансдукции (включая вирусную инфекцию), f-скрещивания или электропорации. Экзогенный полинуклеотид может сохраняться как неинтегрированный вектор, например плазмида или вирусный геном, или может интегрироваться в геном реципиента.
"Индивид" относится к позвоночному, в частности, члену семейства млекопитающих, и включает (но не ограничивается грызунами, например мышами, крысами, морскими свинками, хомяками) кроликов, коз, свиней, рогатый скот, овец и приматов (например, шимпанзе, африканских зеленых обезьян, бабуинов, орангутангов и людей).
Здесь "лечение" относится к (i) к профилактике заражения или повторного заражения, как в традиционной вакцине, (ii) уменьшению или избавлению от симптомов, и (iii) значительному или полному уничтожению вируса. Лечение может проводиться профилактически или терапевтически (после инфицирования).
Термин "эффективное количество" относится к количеству полипептида, несущего эпитоп, достаточному, чтобы индуцировать иммуногенную реакцию в индивиде, которому оно назначается, или другим заметным образом иммуно-реагировать в его соответствующей системе (например, иммуноанализ). Эффективное количество должно быть достаточным для лечения. Точное количество, необходимое для лечения, будет различным в зависимости от применения. В применениях вакцины или в выработке поликлональных антисыворотки/антител, например, эффективное количество может меняться в зависимости от видов, возраста и общего состояния индивида, серьезности заболевания, конкретного выбранного полипептида, его режима назначения и т.п. Считается также, что эффективное количество должно иметь широкий некритический диапазон. Нужное эффективное количество можно определить, используя только экспериментальную процедуру.
Используемая здесь "биологическая проба или выборка" относится к пробе ткани или жидкости, изолированной из индивида, включающая, но не ограниченная до, например, плазмы, сыворотки, спинальной жидкости, лимфы, наружных срезов кожи, респираторного, кишечного и мочеполового трактов, слез, слюны, молока, кровяных клеток, опухолей, органов, биопсий, а также образцов составляющих клеточных культур ин витро (включающих, но не ограниченных до обусловленной среды, являющейся результатом роста клеток в среде клеточной культуры, например клеток миеломы, вырабатывающих Мав (Моноклональные антитела), рекомбинантных клеток и клеточных компонентов).
Композиции иммунореактивного полипептида настоящего изобретения включают смесь эпитопов специфической группы или специфического изолята по меньшей мере от одного VD HCV. Таким образом, в наличии будут по меньшей мере две гетерогенные аминокислотные последовательности, каждая из которых определяет эпитоп, выявленный в различных HCV изолятах, расположенных в том же или фактически в том же физическом участке в белке HCV, т.е. каждая последовательность находится на том же участке внутри генома/полипептида HCV. Поскольку последовательности гетерогенны, участок именуется вариабельным доменом (VD).
Чтобы лучше понять изобретение, вначале будут рассмотрены индивидуальные аминокислотные последовательности, которые составляют композиции изобретения. Затем будет рассмотрено множество таких последовательностей, которые выявлены в композициях настоящего изобретения.
Аминокислотная последовательность, которая
характеризует полипептиды настоящего изобретения, имеет следующую основную структуру:
Ly - Z - L'y', (1)
где
Z представляет аминокислотную последовательность от участка белка от
выбранного изолята HCV, где участок включает по меньшей мере один вариабельный домен и вариабельный домен включает по меньшей мере
один эпитоп. L и L' - не-HCV аминокислотные последовательности или
HCV аминокислотные последовательности, которые не содержат вариабельного домена, и которые могут быть одинаковыми или разными. y и
y' - 0 или 1 и могут быть одинаковыми или разными. Таким образом,
формула I представляет аминокислотную последовательность, включающую последовательность VD HCV, в которой VD содержит эпитоп.
Как говорилось выше, эпитоп (ы) в Z будут обычно содержать минимум около 5 аминокислот, как правило, около 8 и даже минимум около 10 аминокислот.
Вариабельный домен Z может включать более одного эпитопа. Вариабельный домен Z имеет по меньшей мере такую величину, как комбинированные последовательности присутствующих эпитопов, что составляет не менее 5 аминокислот при наличии одного эпитопа. Поскольку эпитопы могут перекрываться, минимальная аминокислотная последовательность для комбинированных эпитопов в вариабельном домене может составить меньше суммы последовательностей индивидуальных эпитопов.
Z - аминокислотная последовательность изолята HCV, включающая вышеописанный VD. Поэтому минимальный размер Z является минимальным размером VD. Z может включать большую аминокислотную последовательность HCV, чем просто VD, и, кроме того, может включать больше одного VD. Максимальный размер Z ее является критичным, но очевидно не может превышать длину всего полибелка HCV. Однако обычно является последовательностью всего белка HCV (в частности, E1, E2/NS1, NS2 NS3, NS4 и NS5) или обычно фрагмента такого белка HCV. Итак, Z будет иметь диапазон минимум от 5 аминокислот (предпочтительнее от 8 или 10 аминокислот минимум) до максимум около 1100 аминокислот (предпочтительнее максимум до 500, лучше до 400, и еще лучше - до 200 аминокислот). Как правило, полипептид формулы I и/или Z, когда их получают химическим синтезом, включает максимум около 50, более типично - 40, а чаще около 30 аминокислот.
Не-HCV аминокислотные последовательности, L и L', если они присутствуют, могут составить любое число типов таких последовательностей. Например, L и L' могут представлять не-HCV последовательности, с которыми сливается Z, чтобы облегчить рекомбинантную экспрессию (например, бета-галактозидаза, супероксид дисмутаза, инвертаза, альфа-фактор, ТРА лидер и пр.), как обсуждается ниже. В другом случае, L и L' могут представлять эпитопы других патогенов, таких как вирус гепатита B. Bordetella pertussis, токсоид тетанус, дифтерия и др., чтобы сделать композиции, которые иммунореактивны к ряду таких других патоненов. L и L' могут быть аминокислотными последовательностями, которые облегчают сцепление с твердыми носителями в синтезе пептида, носителями иммуноанализа, белками носителя вакцины и пр. Фактически L и L' могут даже включать одну или несколько избыточных аминокислот без функционального преимущества. Максимальный размер L или L' не критичен, длина регулируется желаемой функцией. Обычно L и L' каждая будут составлять максимально около 2000, типичнее - около 100 аминокислот. Большая часть последовательностей L и L' с полезными свойствами будет составлять максимум около 500 аминокислот. Конечно желательно выбрать L и L' такими, чтобы не блокировать иммунореактивность Z.
Композиция полипептидов, предложенная в соответствии с настоящим изобретением,
характеризуется наличием (в эффективном количестве для иммунореактивности) в
композиции по меньшей мере двух аминокислотных последовательностей, определенных формулами II и III соответственно:
Ly - Z1 - L'y', (II)
Ly - Z2 - L'y',
(III)
где L, L', y и y' имеют те же значения, что определены выше, также независимо определены для каждой из формул
II и III. Z1 и Z2 каждая аминокислотная
последовательность HCV, как определено для Z выше, охватывающие тот же самый вариабельный домен (например, физический участок), но
являющиеся производными от разных HCV изолятов, имеют между собой по
меньшей мере один гетерогенный эпитоп в общем вариабельном домене Z1 и Z2. В качестве иллюстрации
аминокислотная последовательность формулы II может в качестве Z1
иметь фрагмент гипервариабельного домена, захватывающего аминокислоты 384 - 414 изолята HCV-1 (или конкретнее 396 - 407 или
396 - 408), а Z2 является аналогичным фрагментом от изолята HCV
JI.I. Эти два изолята гетерогенны в этом домне, причем аминокислотные последовательности эпитопов меняются значительно.
Надо понимать, что композиции настоящего изобретения могут
включать больше двух дискретных аминокислотных, последовательностей в соответствии с формулой I, и что Z последовательности
можно разделить на группы, охватывающие разные вариабельные домены. Например,
композиция по настоящему изобретению может включать группу HCV последовательностей (с аминокислотными
последовательностями по формуле I), охватывающих гипервариабельный домен аминокислот 384 - 411 от
изолятов HCV-I, HCV-JI.I, HC-JY, HC-J4 и т.д. Композиция может также содержать дополнительную группу
последовательностей HCV (в пределах аминокислотных последовательностей по формуле I), охватывающих
вариабельный домен на аминокислотах 215 - 255 также от изолятов HCV-I, HCV-JI.I, HC-JI, HC-J4 и т.д.
В пределах объема композиций настоящего изобретения последовательность формулы I можно дальше
определить как
SVn, (IV)
где V представляет аминокислотную
последовательность, включающую последовательность вариабельного домена HCV, в которой вариабельный домен
включает по меньшей мере один эпитоп, т.е. формулу I. S и n - целые числа от 1 и больше. S
представляет конкретный вариабельный домен и n представляет конкретный изолят. Например, S=1 может
представлять вариабельный домен на амино-кислотах 384 - 411; S = 2 может представлять вариабельный
домен на аминокислотах 215 - 255; и n = 1, 2, 3 и 4 может представлять изоляты HCV-I, HCV-JI.I, HC-JI
и HC-J4 соответственно. Таким образом, две группы последовательностей, обсужденных выше, можно
представить в следующем виде:
Группа I: 1V1, 1V2, 1V3 и 1V4
Группа 2: 2V1, 2V2, 2V3 и 2V4.
В композиции настоящего изобретения включены по меньшей мере две отчетливые
последовательности формулы IV, т.е. композиции содержат две разные последовательности в соответствии с
формулой IV, где величины для S и/или n - разные. Например, присутствуют по меньшей мере 1V1 и 1V2, или 1V1 и 2V2, или 1V1 и 2V1.
Отличительные последовательности, подпадающие под формулу IV, присутствуют в композиции либо в той
же, либо в разных молекулах полипептида. Используя минимальную комбинацию, можно показать, что эти
две последовательности могут присутствовать в одной и той же молекуле полипептида (например 1V1 - 1V2) или в разных молекулах. Этот признак композиций настоящего изобретения
можно описать как композиции полипептидов следующим образом:
Rr-(SVn
)-R'r', (V)
где S, V и n - как определены выше; R и R' - аминокислотные
последовательности с 1 - 1200 аминокислотами, и являются одинаковыми или разными; r и r' - 0 или 1 и
являются одинаковыми или разными; x - целое число ≥1n - независимо выбирается
для каждого x; и с оговоркой, что аминокислотные последовательности присутствуют в композиции,
представляющей комбинацию, выбранную из группы, состоящей из (i) 1V1 и 1V2, (ii)
1V1 и 2V2 и (iii) 1V1 и 2V1. В вариантах, где
отличительные последовательности формулы IV присутствуют в различных полипептидах, x может быть I, хотя при
желании он может быть > 1, например смесь полипептидов 1V1-1V2
и 1V1-2V2. Если x-1, r и r' оба предпочтительно 0, чтобы избежать избыточности с Ly и
L'y, поскольку V в предложенном варианте можно описать формулой I. Если x > 1,
соединенные длины R и прилегающей L и R' и прилегающей L составляют предпочтительно не более типичных
максимальных длин описанных выше для L и L'.
Выбор аминокислотных последовательностей HCV, включенных в отличительные V последовательности композиций, будет зависеть от предполагаемого применения последовательностей и входит в обе настоящего изобретения с учетом раскрытия. Во-первых, эпитопы HCV по настоящему изобретению можно разбить на два типа. Первый тип этитопов "эпитопы, специфичные по группе", т.е. соответствующие эпитопы во всех или практически всех изолятах внутри группы изолятов HCV имунологически перекрестно-реактивны друг с другом, но не с соответствующими эпитопами или практически всеми изолятами другой группы. Эпитопы в классе специфичных по группе - фактически консервативны внутри группы, но не между или среди групп. Второй тип эпитопов - "эпитопы специфичные по изоляту", т.е. эпитоп иммунологически перекрестно-реактивен с идентичными изолятами, и не-перекрестно-реактивен со всеми или практически всеми отличительными изолятами.
Эти эпитопы, специфичные по группе и специфичные по изоляту, можно легко идентифицировать с помощью настоящего раскрытия. Во-первых, сравниваются последовательности нескольких изоляторов HCV, как описано здесь, и идентифицируются области гетерогенности последовательности. Структура гетерогенности обычно указывает специфичность группы или изолята. Если известно, что идентифицированная область включает один или несколько эпитопов, то выбирается последовательность достаточного размера, для включения желаемого эпитопа, которую в качестве вариабельного домена можно включить в композиции настоящего изобретения. Если иммунореактивность данной гетерогенной области не известна, можно получить и определить активность пептидов, представляющих последовательности, выявленные в этой области различных изолятов HCV. Определение активности может включать, но не ограничиваться до иммунопроб с различными источниками анти-HCV антителом (например, сывороткой пациента, нейтрализующими Мав и т.п.) или поколением антитела и тестированием способности такого антитела нейтрализовать вирус ин витро. В другом случае локусы эпитопов, определенных в процедуре отбора, такой как описана выше, можно исследовать на гетерогенность среды разных изолятов и иммунологические свойства соответствующих отобранных гетерогенных последовательностей.
В применении вакцины полагают, что особый интерес будут представлять вариабельные домены из E1 и/или E2/NS 1 доменов. В частности, E1 вариабельный домен в аминокислотах 215 - 255 (см. фиг. 2 и E2/NSI вариабельный домен в аминоксилотах 318 - 414 (см. фиг. 3), были указаны как важные иммунореактивные домены. Предварительное доказательство предполагает, что один или оба эти домена могут быть локусами гетерогенности, несущими ответственность за "ускользнувшие" мутанты, влекущие за собой хронические заражения HCV. Таким образом, поэтому особенно предпочтительны полипептидные композиции, описанные выше, в которых вариабельные домены в V представляют собой один или оба их этих вариабельных доменов. Кроме того, полипептидные композиции настоящего изобретения, хотя и конкретно связаны с линейными эпитопами в вариабельных доменах, могут также включать конформационные эпитопы. Например, композиция может состоять из смеси рекомбинантных E1 и/или E2/NSI белков (демонстрирующих вариабельные домены различных изолятов), экспрессированных в рекомбинантной системе (например, клетках насекомого или млекопитающего), которая удерживает конформационные эпитопы либо внутри, либо снаружи вариабельного домена. Кроме того, E1 и/или E2/NSI субъединичный антиген из одного изолята, который удерживает конформационные эпитопы, можно объединить с полипептидной композицией настоящего изобретения (например, смесь синтетических полипептидов или денатурированных рекомбинантных полипептидов). В другом применении для вакцин полипептидные композиции, описанные здесь, комбинируются с другими субъединичными антигенами HCV, такими, которые описаны в заявке совместного авторства U.S.S.N, озаглавленной "Азиалогликопротеиды вируса гепатита C" (N патентного поверенного 0154002), поданной Robert O. Ralston, F. Marcus, Kent B. Thudium, Barbara Gervase and John Hall на ту же дату, что и настоящая заявка, и включенной сюда ссылкой.
Для диагностического применения представляется полезным использовать композиции настоящего изобретения антигенов, улучшая таким образом способность обнаруживать антитело на отличительные изоляты HCV. Обычно полипептидыне смеси можно использовать непосредственно в гомогенном или гетерогенном формате иммунопробы, последний обычно включает иммобилизацию полипептида на твердом субстрате (например, лунках микротитровального планшета, пластиковых шариках, нитроцеллюлозе и т.п.). См., например, публикацию PCT W0/11089; ЕПВ 36088; Immunoassay: Practical Guide. В другом случае каждый практически идентичный полипептид, входящий в полипептидную композицию настоящего изобретения, можно иммобилизировать на той же опоре в дискретных локусах, таким образом информацию, на какой изолят или группу было выработано антитело. Это особенно важно в диагностике, если разные изоляты вызывают гепатит, рак или другие заболевания с разными клиническими прогнозами. Предпочтительным форматом является формат иммунопробы Chinon RIBA Strip, описанный в заявке совместного владения U.S.S.N. 07/138894 и U.S.S.N. 07/456637, раскрытие которой включено сюда ссылкой.
Полипептиды, полезные в приготовлении композиций настоящего изобретения, можно получать рекомбинантно, синтетически или в тканевой культуре. Рекомбинантные полипептиды, состоящие из усеченных последовательностей HCV или белков HCV с полной длиной, можно полностью получать из HCV последовательностей (одного или нескольких эпитопов, смежных или несмежных), или последовательностей в белке слияния. В белках слияния полезные гетерологичные последовательности включают последовательности, которые обеспечивают секрецию от рекомбинантного носителя, усиливают иммунологическую реактивность эпитопа(ов) HCV, или облегчают связь полипептида с опорой или носителем вакцины. См. , например, публикацию ЕПВ 116201; патент США 4722840; публикацию ЕПВ 259149; патент США 4629783, раскрытия которых включены сюда ссылкой.
Полипептиды с последовательностями с полной длиной или усеченными последовательностями HCV и их мутанты можно получить химическим синтезом. Способы получения полипептидов химическим синтезом хорошо известны в области техники. Их можно также получить рекомбинантной технологией. Последовательность ДНК, кодирующая HCV-1, а также последовательности ДНК вариабельных областей других изолятов HCV были описаны здесь или на них были даны ссылки. Наличие этих последовательностей позволяет построить полинуклеотиды, кодирующие иммунореактивные участки полипептидов HCV.
Полинуклеотиды, кодирующие нужный полипептид, состоящий из одного или нескольких иммунореактивных HCV эпитопов из вариабельного домена HCV, можно химически синтезировать или изолировать и вставлять в вектор экспрессии. Векторы могут содержать или не содержать части последовательностей слияния, такие как бета-галактозидаза или супероксиддисмутаза (SOD). Методы и векторы, используемые в получении полипептидов, которые содержат последовательности слияния SOD, описаны в ЕПВ публикации 0196056, опубликованной 1 октября 1986 г.
ДНК, кодирующую нужный полипептид в слитой или зрелой форме и содержащую или не содержащую сигнальную последовательность, чтобы позволить секрецию, можно лигировать в векторы экспрессии, приемлемые для любого подходящего носителя. Затем носители преобразуются вектором экспрессии. Как эукариотные, так и прокариотные системы носителя используются в формировании рекомбинантных полипептидов, и в них присутствует множество некоторых из наиболее общих контрольных систем и клеточных линий носителя. Клетки носителя инкубируются при условиях, которые позволяют экспрессию нужного полипептида. Затем полипептид изолируется от лизированных клеток или от среды культуры и очищается до степени, необходимой для его предполагаемого использования.
Общая техника, применяемая в экстрагировании генома HCV из вируса, получении и зондировании ДНК библиотек, секвенировании клонов, построении векторов экспрессии, трансформировании клеток, проведении радио-иммунологических проб и ELISA тестов для выращивания клеток в культуре и прочего, известна специалистам. (См., например, ссылки, указанные в разделе "Предпосылки", выше, а также ссылки, данные в начале этого раздела ("Варианты реализации изобретения").
Трансформация вектора, содержащего нужную последовательность, в соответствующий носитель может быть проведена любым известным методом введения полинуклеотидов в клетку носителя, включающим, например, упаковку полинуклеотида в вирусе и трансдуцирование клетки носителя с вирусом, или прямым поглощением полинуклеотида. Используемая процедура информации зависит от трансформируемого носителя. Бактериальная трансформация прямым поглощением обычно использует обработку хлоридом кальция или рубидия (Cohen 1972), Proc. Natl. Acad. Sci USA 69:2110. Трансформацию дрожжей прямым поглощением можно провести с использованием способа Hinnen и др. (1978), J.Adv. Enzyme Reg, 7: 1929. Трансформации млекопитающих прямым поглощением можно проводить с использованием метода осаждения фосфата кальция Graham и Van der Eb (1978), Virology 52:546, или его другими известными модификациями. Другие методы введения рекомбинантных полинуклеотидов в клетки, особенно клетки млекопитающих, которые известны в данной области, включают трансфекцию посредством декстрана, фосфата кальция, полибрена, слияние протопласта, электропорацию, капсулирование полинуклеотидов в липосомы и прямую микроинъекцию полинуклеотидов в ядра.
Чтобы получить экспрессию желаемых кодирующих последовательностей, клетки носителя трансформируются полинуклеотидами (которые могут быть векторами экспрессии), которые состоят из контрольных последовательностей, операбельно связанных с нужными кодирующими последовательностями. Контрольные последовательности совместимы с обозначенным носителем. Среди прокариотных носителей наиболее часто используется E.coli. Контрольные последовательности экспрессии для прокариотов включают промоторы, могущие содержать части оператора и рибосомные связующие сайты. Векторы переноса, совместимые с прокариотными носителями, обычно получают, например, от pBP322, плазмиды содержащей опероны, дающие устойчивость к ампициллину и тетрациклину и различных pUC векторов, которые также содержат последовательности, дающие маркеры устойчивости к антибиотикам. Последовательности промотора могут существовать в природе, например β-лактамаза (пенициллиназа) (Weissman (1981) "The cloning of interberon and other mistakes" в интерфероне 3 (Ed. Gressen, лактоза (lac) (Chang и др. (1977), Nature 198: 1056) и триптофан (trp) (Goeddel и др. (1980), Nucl. Acids. Res. 8:4057), и образованная от лямбды PL промоторная система и связующий сайт рибосомы N гена (Shimatake и др. (1981), Nature 292: 128). Кроме того, синтетические промоторы, которых не бывает в природе, также функционируют как бактериальные промоторы. Например, последовательности активации транскрипции одного промотора можно соединить с последовательностями оперона другого промотора, создавая синтетический гибридный промотор (например, tac промотор, который получен от последовательностей trp и lac промоторов (De Boer и др. (1983), Proc. Natl. Acad. Sci. USA 80:21). Предшествующие системы особенно совместимы с E.Coli; при желании могут использоваться другие прокариотные носители, такие как штаммы Bacillus или Pseudomonas с соответствующими контрольными последовательностями.
Эукариотные носители включают дрожжевые клетки и клетки млекопитающих в системах культуры. Saccharomyces cerevisiae и Saccharomyces carlsberhensis наиболее часто используемые дрожжевые носители и являются удобными грибковыми носителями. Совместимые векторы дрожжей обычно несут маркеры, которые позволяют выбор успешных трансформантов приданием прототропии ауксотрофным мутантам или устойчивости к тяжелым металлам на штаммах дикого типа. Дрожжевые совместимые векторы могут использоваться 2-х микронные репликаторы (Broach и др. (1983), Meth Enz. 101:307), комбинацию CEN3 и ARS I или другие средства для гарантии репликации, такие как последовательности, которые приведут к включению соответствующего фрагмента в геном клетки носителя. Контрольные последовательности для дрожжевых векторов хорошо известны в области техники и включают промоторы для синтеза гликолитических ферментов (Hess и др. (1968), J.Adv. Enzime Reg. (7:149); например, спиртовую дигидрогеназу (ADH) (публикация ЕПВ N 284044), энолазу, глюкокиназу, глюкозу-6-фосфатдегидрогеназу (GAP или GAPDH), гексокиназу, фосфофруктокиназу, 3 -глицерофосфатмутазу и пируваткиназу (РуК) (публикация ЕПВ N 329203). Дрожжевой ген PHO5, кодирующий кислую фосфатазу, также дает хорошие последовательности промотора. Кроме того, синтетические промоторы, которых нет в природе, также функционируют как дрожжевые промоторы. Например, верхние активирующие последовательности (UAS) одного дрожжевого промотора можно соединить с участком активации транскрипции другого дрожжевого промотора, создавая синтетический гибридный промотор. Примеры таких гибридных промоторов включают регуляторную последовательность ADH, связанную с участком активации транскрипции GAP (патенты США N 4876197 и 4880734). Другие примеры гибридных промоторов включают промоторы, которые состоят из регуляторных последовательностей либо ADH2, GAL4, либо PHO5 генов, комбинированных с участком транскрипционной активации гена гликолитического фермента, такого как GAP или PyK (публикация ЕПВ 164556). Более того, дрожжевой промотор может включать существующие в природе промоторы не-дрожжевого происхождения, которые обладают способностью связывать дрожжевую РНК полимеразу для соответствующей инициации транскрипции.
Другими контрольными элементами, которые могут включаться в вектор дрожжевой экспрессии, являются терминаторы (например, из GAPDH, и из гена энолазы (Holland, 1981), J. Biol. Chem 256:1385) и лидерные последовательности. Фрагмент лидерной последовательности обычно кодирует сигнальный пептид, состоящий из гидрофобных аминокислот, которые направляют секрецию белка из клетки. ДНК, кодирующую приемлемые сигнальные последовательности, можно получить от генов для секретируемых дрожжевых белков, таких как ген дрожжевой инвертазы (публикация ЕПВ N 12873) и ген α-фактора (патент США 4588684). Лидеры недрожжевого происхождения, такие как лидер интерферона, также обеспечивают секрецию в дрожжах (публикация ЕПВ N 60057). Предпочтительными классами лидеров секреции являются те, которые используют фрагмент дрожжевого гена α-фактора, который содержит и "пред" сигнальную последовательность и "про" участок. Типы фрагментов α-фактора, которые могут использоваться, включают пред-про лидер α-фактора полной длины, а также лидеры α -фактора усеченной длины. N патентов США 4546083 и 4870008; публикация ЕПВ N 324274. Дополнительные лидеры, использующие фрагмент лидера α-фактора, который обеспечивает секрецию, включают гибридные лидеры α-фактора, а пред-последовательностью первого дрожжевого α-фактора, но с участком от второго дрожжевого α-фактора (см., например, PCT N W089/02463).
Для трансформации во многие дрожжи были разработаны векторы экспрессии, либо экстрахромосомные репликоны, либо интегрирующие векторы. Например, векторы экспрессии были разработаны для Candida Albicans (kurtz и др. (1986), Mol. Cell Biol. 6: 142), Candida maltosa (kunze и др., (1985) J. Basic Microbiol. 25: 141), Hanzenula polymorphac Gleeson и др. (1986), J. Gen. Microbiol. 132: 3459), Klyveromyces fragilis (Das и др. (1984), J. Bacteriol. 158:1165)), Kluyveromyces fragilis (De Louvencourt и др., 1983), J. Bacteriol. 154: 737), Pichia guillerimondii (Kunze и др. (1985), Supra) Pichia pastoris (Cregg и др. (1985), Mol. Cell Biol. 5:3376; патенты США N 4837148 и 4929555)), Schizosaccharomyces pombe (Beach and Nurse (1981), Nature 300: 706), и Garrovia lipolytica (Davidow и др. (1985), Curr. Genet. (10:39).
Клеточные линии млекопитающих доступны в качестве носителей доля экспрессии, известны в данной области и включают многие иммортализированные клеточные линии, от коллекции культур американского типа (АТСС), включающие, например, клетки Hela клетки яичников китайского хомяка (CHO), печеночные клетки новорожденного хомяка (BHK), клетки обезьян COS, и ряд других клеточных линий. Подходящие промоторы для клеток млекопитающих также известны в области техники и включают вирусные промоторы, такие как промоторы от вируса Симиана 40 (SV40), вирус саркомы Payca (RSV), аденовирус (ADV) и вирус папилломы крупного рогатого скота (BPV) (см. Sambrook (1989) относительно примеров подходящих промоторов). Клетки млекопитающих могут также потребовать терминаторных последовательностей и последовательностей поли-A-дополнения; можно включить последовательности усилителя, которые усиливают экспрессию, и последовательности, которые вызывают амплификацию гена, также могут быть желательны. Эти последовательности известны в технике.
Векторы, пригодные для репликации в клетках млекопитающих, известны и могут включать вирусные репликоны или последовательности, которые обеспечивают интеграцию соответствующих последовательностей, колирующих желаемые полипептиды в геноме носителя.
Вектором, который используется для экспрессии чужеродной ДНК и который может использоваться в приготовлении вакцины, является вирус осповакцины. В этом случае гетерологичная ДНК вставляется в геном вируса осповакцины. Техника вставки чужеродной ДНК в геном вируса осповакцины известна и использует, например, гомологичную рекомбинацию. Вставка гетерологичной ДНК производится обычно в ген, который не является существенным по характеру, например ген тимидинкиназы (tK), который также дает селектируемый маркер. Были описаны векторы плазмид, которые значительно облегчают построение рекомбинантных вирусов (см. , например, Macketl и др. (1984) в "DNA Cloning", т. IRl press стр. 191, Chakrabarti и др. (1985) Mol. Cell, Biol. 5.3403; Moss (1987) в "Jene Transfer Vectors for Mammalian Cells" (Millerand Calos, eds, стр.10). Затем экспрессия нужных полицептидов, состоящих из иммунореактивных участков, происходит в клетках или индивидах, которые заражены и/или/и иммунизированы живым рекомбинантным вирусом осповакцины.
Другие системы экспрессии полипептидов включают клетки насекомых и векторы, приемлемые для использования в этих клетках. Эти системы известны и включают, например, экспрессирующий вектор, сконструированный на основе вируса ядерного полиэдроза Autographa californica (AcNPV), который является независимым от хелпера вектором вирусной экспрессии. Векторы экспрессии, полученные от этой системы, обычно используют сильный промотор гена полиэдрина для инициации экспрессии гетерологичных генов. Сейчас этим наиболее часто используемым вектором переноса для введения инородных генов в AcNPV является pAc 373. Специалистам известны многие другие векторы, предназначенные для улучшения экспрессии. Они, например, включают pVL 985 (в котором изменен полиэдриновый инициирующий кодон с ATG на ATT, и в который введен сайт клонирования BamHI на 32 паре оснований вниз от ATT; см. Luckow и Summers (1989), Vipology 17:31. Хорошая экспрессия неслитых чужеродных белков обычно требует чужеродных генов, которые идеально имеют короткую лидерную последовательность, содержащую подходящие сигналы инициации трансляции, предшествующие начальному сигналу ATG. Плазмида также содержит сигнал многоугольного полиаденилирования и ген устойчивости к ампициллину (amp) и репликон для отбора и распространения E. coli.
Способы введения гетерологичной ДНК в нужный сайт в бакуловирусе известны. (См. Summers и Smith, Texas Agricultural Experiment Station Balleten, 1555; Ju и др. (1987), в "Gene Transfer Vectors for Mammalian Cells (Miller and Callos, eds.); Smith и др. (1983), mol. and Cell Biol. 3:2156 и Luckow и Summers (1989), Supra). Например, вставку можно сделать в ген, такой как ген полиэдрина, гомологичной рекомбинацией; вставку можно сделать в рестрикционный сайт, введенный в нужный ген бакуловируса. Вставленными последовательностями могут быть те, которые кодируют все или меняющиеся сегменты нужных полипептидов HCV, включающих по меньшей мере один эпитоп из вариабельного домена.
Сигналы посттрансляционных модификаций, такие как расщепление сигнального пептида, протеолитическое расщепление, и фосфорилирование, опознаются клетками насекомых. Сигналы, необходимые для секреции и ядерной аккумуляции, также консервируются между клетками беспозвоночных и позвоночных. Примеры сигнальных последовательностей от клеток позвоночных, которые эффективны в клетках беспозвоночных, известны в области, например сигнал человеческого интерлейкина 2 (IL23), который является сигналом, если клетка опознана и удалена в клетках насекомого.
Часто представляет желательным, чтобы полипептиды, полученные с использованием указанных хозяйских клеток и векторов, были полипептидами слияния. Как и полипептиды неслияния полипептиды слияния могут оставаться вунтриклеточными после экспрессии. Белки слияния можно также секретировать из клетки в растительную среду, если они состоят из фрагмента лидерной последовательности. Предпочтительно, чтобы между лидерным фрагментом и остальной частью инородного гена имелись процессирующие сайты, которые можно расщепить ин виво или ин витро.
В случаях, если композиция предназначена для использования в лечении HCV, нужно, чтобы она была иммуногенной. В примерах, где синтезированный полипептид имеет правильную конфигурацию, чтобы дать правильной эпитоп, но слишком мал, чтобы быть иммуногенным, полипептид можно связать с подходящим носителем. Специалистам известны многие технологические приемы для получения такой связи, включая образование дисульфидных звеньев, использованием N-сукцинимидил-3-(2-пиридилтио)пропионата (SPDP) и сукцинимидил 4-(N-малеимидометил)циклогексан-1-карбоксилата (SMCC) (если в пептиде отсутствует сульфгидрильная группа, это можно осуществить добавлением остатка цистеина). Эти реагенты создают дисульфидное звено между собой и остатками цистеина пептида на одном белке и амидное звено через ε-амино на лизине или другой свободной аминогруппе в других аминокислотах. Известно множество таких дисульфид/амид-формирующих агентов. См., например, Immun. Rev. (1982) 62:185. Другие бифункциональные связующие агенты для тиоэфира, кроме дисульфидного звена. Многие из этих тио-эфир-формирующих агентов имеются в продаже и включают реактивные эфиры 6-малеимидокапроевой кислоты, 2-бромоуксусной кислоты, 4-(N-малеимидо-метил)циклогексан-1-карбоновой кислоты, и другие. Карбоксильные группы можно активировать соединением их с сукцинимидом или 1-гидроксил-2-нитро-4-сульфокислотой, натриевой солью. Дополнительные методы связывания антигенов используют систему ротавирус/ "связующий пептид", описанную в публикации ЕПВ 259149. Указанный перечень не является исчерпывающим и можно использовать модификации названных соединений.
Может использоваться любой носитель, который сам не индуцирует образование вредных для хозяина антител. Подходящие носители обычно представляют собой большие медленно метаболизируемые макромолекулы, такие как белки; полисахариды, такие как модифицированная латексом сефароза, агароза, целлюлоза, целлюлозные шарики и пр.; полимерные аминокислоты, такие как полиглутаминовая кислота, полилизин, и другие, аминокислотные сополимеры; и неактивные вирусные частицы (см. infra). Наиболее полезными субстратами белка являются сывороточные альбумины, гемоцианин, молекулы иммуноглобулина, тироглобулин, овальбумин, столбнячный токсоид и другие белки, хорошо известные специалистам.
Иммуногенность эпитопов вариабельных доменов HCV, особенно EI и E2/NSI, можно также усилить получением их в эукариотных системах, слитых или соединенных с частицеобразующими белками, такими как, например, те, которые ассоциируются с поверхностным антигеном гепатита B. См., например, патент N 4722840. Конструкции, в которых полипептид, содержащий эпитоп HCV из вариабельного домена, связан непосредственно с частицеобразующими белковыми кодирующими последовательностями, дают гибриды, которые иммуногенны по отношению к эпитопу HCV. Кроме того, все полученные векторы включают эпитопы, специфические к HCV, с разными степенями иммуногенности, такие как, например, пред- S-пептид. Таким образом, частицы, построенные из частицеобразующего белка, которые включают последовательности HCV, иммуногенны по отношению к HCV или HBV.
Показано формирование и соединение в частицы поверхностного антигена гепатита (HBSAg в S.cerevisiae (Valenzuela и др. (1982), Nature 298:344, а также, например, в клетках млекопитающего (Valenzuela и др. , 1984), в "Hepatites B", Millman I и др. ed.). Было показано, что образование таких частиц усиливает иммуногенность мономерной субъединицы. Конструкции могут также включать иммунодоминантный эпитоп HBSAg, содержащий 55 аминокислот поверхностного участка (пре-S). (Neurath и др., 1984). Конструкции пред-S -HBSAg частицы, способной экспрессироваться в дрожжах, раскрытых в публикации ЕПВ 174444; гибриды, включающие гетерологичные вирусные последовательности для дрожжевой экспрессии, раскрыты в публикации ЕПВ 175261. Эти конструкции могут также экспрессироваться в клетках млекопитающего, таких как CHO клетки с использованием вектора SV 40-дигидрофолат редуктазы (Michelle и др. (1984).
Кроме того, порции кодирующей последовательности частицеобразующего белка могут заменяться кодонами, кодирующими эпитоп из вариабельного домена HCV. В этой замене, участки, которые не являются посредниками в агрегации единиц, чтобы сформировать иммуногенные частицы в дрожжах или млекопитающих, могут быть изъяты, удаляя, таким образом, дополнительные антегенные участки HBV из конкуренции с эпитопом HCV.
Получение вакцин, которые содержат иммуногенный полипептид(ы) в качестве активного ингредиента(ов), хорошо известно специалистам. Обычно такие вакцины готовят в форме инъекционных препаратов, в виде жидких растворов или суспензий; твердых форм, приемлемых для растворения в жидкости или суспендирования до инъекции. Препарат может быть эмульгирован или полипептид капсулирован в липосомы. Активные иммуногенные ингредиенты часто смешиваются с наполнителями, которые фармацевтически приемлемы и совместимы с активным ингредиентом. Подходящими наполнителями являются, например, вода, физиологический раствор, декстроза, глицерин, этанол и другие и их комбинации. В дополнение при желании вакцина может содержать минимальные количества вспомогательных веществ, таких как смачивающие или эмульгирующие агенты, pH буферные агенты, и/или адъванты, которые усиливают эффективность вакцины. Примеры адъювантов, которые могут быть эффективны, включают, но не ограничиваются до: гидроксида алюминия, N-ацетил-мурамил-L-треонил-D-изоглютамина (thr-MDP), N-ацетил-нор-мурамил-L-аланил-D-изоглютамина (CGP 11637), указанного как нор-MDT), N-ацетил-мурамил-L-аланил-D-изоглютаминил-L-аланин-2-(1'-2'- дипальмитоил-Sn-глицеро-3-гидроксифосфорилокси)-этиламина (CGP 19835A, указанного как MTP-PE, и RIBI, который содержит тир компонента, экстрагированных из бактерий, монофосфорил липид A, трегалозу димиколат и остов клеточный стенки (MPL + TDM + CWS) в 2% эмульсии сквалена/Tween 80. Эффективность адъюванта можно определить измерением количества антител, направленных против иммуногенного полипептида, содержащего эпитоп HCV из вариабельного домена, антител, выработанных при назначении этого полипептида в вакцинах, которые также включают различные адъюванты.
Белки могут формулироваться в вакцине в нейтральной или солевой форме. Фармацевтически приемлемые соли включают соли кислотного присоединения (сформированные со свободными аминогруппами пептида) и которые сформированы с неорганическими кислотами, такими как, например, хлористоводородная или фосфорная кислоты, или органическими кислотами, такими как уксусная, щавелевая, винная, малеиновая кислоты и другими. Соли, сформированные со свободными карбоксильными группами, можно также получать от неорганических оснований, таких как гидроксиды натрия, калия, аммония, кальция или железа, и таких органических оснований, как изопропиламин, триметиламин, 2-этиламино этанол, гистидин, прокаин и других.
Вакцины обычно назначаются парентерально, инъекцией подкожно или внутримышечно. Дополнительные препараты, которые приемлемы для других форм назначения, включают шарики в некоторых случаях оральные препараты. Для шариков традиционные связующие вещества и носители могут включать, например, полиалкиленгликоли или триглицериды; такие шарики могут изготавливаться из смесей, содержащих активный ингредиент в пределах от 0,5 до 10%, предпочтительно 1-2%. Оральные препараты включают такие обычно используемые наполнители, как, например, фармацевтические виды маннитола, лактозы, крахмала, стеарата магния, сахарина натрия, целлюлозы, карбоната магния и другие. Эти композиции имеют форму растворов, суспензий, таблеток, пилюлей, капсул, препаратов с замедленным действием или порошков и содержат 10-95% активного ингредиента, предпочтительно 25-70%.
В дополнение к вышесказанному можно также приготовить вакцины из живых или ослабленных микроорганизмов, которые экспрессируют рекомбинантные полипетиды антигенных совокупностей HCV. Подходящие ослабленные микроорганизмы известны в данной области и включают, например, вирусы (например, вирус осповакцины), а также бактерии.
Вакцина назначается способом, совместимым с дозировкой препарата, и в количестве, которое будет профилактически и/или терапевтически эффективным. Количественно это будет составлять в пределах от 5 г до 250 г антигена на дозу, в зависимости от конкретного субъекта, способности иммунной системы субъекта синтезировать антитела, и степени нужной защиты. Точные количества активного ингредиента в назначении могут зависеть от конкретного врача и являются разными для каждого индивида.
Вакцина может даваться по схеме разовой дозы или схеме в несколько приемов. При схеме в несколько приемов основной курс вакцинации составляет 1-10 отдельных доз с последующим назначением других доз через определенные временные интервалы, необходимые, чтобы поддержать и/или усилить иммунную реакцию, например через 1-4 месяца для второй дозы и при необходимости дальнейших доз после нескольких месяцев. Режим дозировки по меньшей мере частично будет определяться потребностью индивида и субъективной оценкой врача.
Кроме того, вакцина, содержащая антигенные совокупности, состоящие из полипептидов HCV, описанных выше, может назначаться вместе с другими иммунорегуляторными агентами, например иммуноглобулинами.
Композиции настоящего изобретения могут назначаться индивидам, чтобы выработать поликлональные антитела (очищенные или изолированные из сыворотки с использованием традиционной техники), которые затем можно использовать в ряде применений. Например, поликлональные антитела можно использовать для пассивной иммунизации индивида, или как иммунохимические реагенты.
В других вариантах изобретения вышеописанные иммунореактивные композиции, состоящие из множества антигенных совокупностей HCV, используются для обнаружения анти-HCV антител внутри биологических проб, включающих, например, кровь или сыворотку. Техника иммунопроб может быть различной, и она известна специалистам. Однако иммунопроба будет использовать антигенные совокупности, в которых каждая антигенная совокупность состоит из множества практически идентичных полипептидов, включающих аминокислотную последовательность эпитопа внутри первого вариабельного домена изолята HCV, и аминокислотная последовательность одной совокупности гетерогена по отношению к аминокислотной последовательности по меньшей мере одной другой совокупности. Протоколы иммунопробы могут основываться, например, на конкуренции, прямой реакции или на пробах типа сэндвича. Протоколы могут, например, использовать твердые опоры или реакция может проводиться иммуноосаждением. Большая часть проб использует меченое антитело или полипептид; метки могут флюоресцентными, химилюминесцентными, радиоактивными или окрашенными молекулами. Пробы, которые усиливают сигналы от зонда, также хорошо известны; примерами являются пробы, которые используют биотин навидин, и иммунопробы с меченым ферментом и опосредованные иммунопробы, такие как ELISA.
Комплекты для иммунодиагностики, содержащие соответствующие меченые реагенты, включают упаковки, композиции изобретения, содержащие эпитопы HCV из вариабельных доменов в соответствующих контейнерах вместе с реагентами и материалами (например, подходящими буферами, солевыми растворами и пр.), необходимыми для проведения анализа, а также комплект инструкций по их проведению.
Ниже описываются примеры настоящего изобретения, которые представлены только с целью иллюстрации и не ограничивают объем настоящего изобретения. В свете данного раскрытия специалистам очевидны многочисленные варианты в объеме формулы изобретения.
Примеры
В примерах использовались следующие
материалы и методы.
Пробы, взятые у пациента, и
РНК экстракция
Асимптоматические HCV носители HCT 18 и HCV JI и хронически инфицированный пациент HCV Th были ранее описаны y
и др. (1991) Virol, 180:842:848. Пациенту Q был поставлен диагноз
хронический активный гепатит на основании биопсии печени и ему было назначено лечение альфа-2в интерфероном (3 миллиона единиц,
трижды в неделю) в течение 6 месяцев. PHK из 0,2 мл плазмы была
экстрагирована в соответствии с методом Шомцинского и Саччи, (1987) Anal. Biochem. 162: 156-159, с использованием PHK zol B реагента
(Cinna/ Biotex Laboratories, содержащего 10 мкг/мл MS2 PHK носителя
(Boehringer Mannheim 165-948), как указывает изготовитель. PHK повторно суспендировалась в 200 мкл диэтил-пирокарбонат обработанной
дистиллированной воде и повторно осаждалась в окончательной
концентрации в 0,2 М ацетата натрия и двух с половиной объемах 100% этанола (-20oC).
кДНК и полимеразные цепные
реакции
Все реакции проводились по Weiner и др.
(1990) Lancet 335:1-5. М13 секвенсирование проводилось в соответствии с Broach и др. (1983), Methods in Enzymology 101:20-37. Согласованная
последовательность по меньшей мере четырех клонированных
вставок представлена, за исключением последовательности HCV jI.2 E2/NSI, которая была получена от двух клонов.
Клонирование и секвенирование HCT18 и Th проходило, как указано у Weiner и др. (1991), Supra Гнездовыми праймерами PCR (полимеразной цепной реакции), использованными для клонирования аминоконцевых и карбокси проксимальных сегментов E2/NSI у пациента Q были следующие (см. в конце описания).
Синтез биотинилированных пептидов.
Перекрывающиеся октапептиды для гипервариабельных участков трех штаммов HCV были синтезированы на обеспечивающих расщепление линкера, дериватизированных, полиэтиленовых шпильках, как описано (Maeji и др. (1990) J. Immunol. Methods 134:23-33, наконец биотин бы связан с N-концом с использованием 150 мкл раствора диметилформамида, содержащего 40 мМ биотина, 40 мМ 1-гидроксибензотриазола (HOBt), 40 мМ бензотриазол-1-окси-трис-пирролидино-фосфоний гексафлюорофосфата (PyBOPl, Novabiochem) и 60 мМ N-метилморфолина (NMM) с реакцией в течение ночи при 20oC.
После биотинилирования пептиды с освобожденными от защиты боковыми цепями промывались и пептид из каждого шпиля расщеплялся в 20 мкл 0,1 М фосфатного буфера (pH 7.2). Микротитровальные планшеты, содержащие расщепленные пептидные растворы, хранились при -20oC до востребования.
ELISA тестирование
биотинилированных пептидов
Полистироловые планшеты были покрыты (Nunc
96) стрептавидином инкубированием всю ночь при 4oC 0.1 мл/лунку 5 мкг/мл раствора стрептавидина (Кат. Sigma N
4762) в 0,1 М карбонатном буфере при pH 9.6. После удаления раствора
стрептавидина лунки промывались 4 раза 0,1% раствором Tween 20 в физиологическим растворе с фосфатным буфером (PBS).
Неспецифическое связывание было блокировано инкубированием каждой лунки 0,2 мл 2%
альбумина бычьей сыворотки (BSA) в PBS, содержащем 0,1% азид натрия в течение 1 часа при 20oC или всю ночь
при 4oC с последующими 4 промываниями PBS / Tween 20. Связанное
антитело было обнаружено реакцией в течение 1 часа при 20oC в 0.1 мл конъюгата. Он состоял из 0,25 мл/л (уровень
насыщения) козьего анти-кроличьего IgG, помеченного пероксидазой хрена
обыкновенного (H + L) (kirkegaard and Perry Labs. Gaithersburd, MD) в CASS (0,1% овечьей сыворотки, 0,1% Tween 20, 0,1% казеината
натрия, разбавленного в 0,1 М PBS, pH 7.2). Лунка дважды промывались
PBS/Tween 20 с последующими двумя промываниями только PBS. Присутствие фермента обнаруживалось реакцией в течение 45 минут при
20oC 0,1 мл свежеприготовленного раствора, содержащего 50 мг
аммоний 2,2'-азино-бис[3-этилбензотиазолин-6-сульфоната (ABIS, Boehringer Mannheim Cat. N 122661) и 0.03 мл 35% (вес/вес)
раствора перекиси водорода в 100 мл 0,1 М фосфатного /0,08 М цитратного
буфера, pH 4,0. Появление цвета измерялось планшетным счетчиком Titertek Multiscan MC в режиме двойной длины волны при 405 нм в
сравнении со стандартной длиной волны в 492 нм.
Профиль антигенности, полученный с помощью компьютера
Профили антигенности для белка E2 / NSI HCV и V3 гипервариабельного
участка HIV-I gp. 120 (ак. 303-338) были получены из компьютерной
программы, основанной на степени вариабельности последовательности, как первоначально было предложено kabat для идентификации
гипервариабельных петель иммуноглобулинов, умноженных на среднюю величину
индивидуальной вероятности, которую сохраняет связывание антитела для каждой возможной парной аминокислоты.
(Последовательности белков иммунологического характера. Департамент США по здравоохранению
и обслуживанию, Служба охраны здоровья общества, Национальные институты здоровья (1983)). Вероятности
сохранения связывания антитела, связанные с изменением данной аминокислоты, - величины,
определенные экспериментально оценкой воздействий на связывание антитела всех возможных аминокислотных замещений
для 103-характеризованных линейных эпитопов. Geysen и др. (1988), J. Mol. Rec. 1 : 32
- 41. Этот алгоритм оценивает индекс вариабельности, чтобы придать больше значимости аминокислотным изменениям,
например, как предполагается, имеют значительное влияние на связывание антитела, т.е.
компенсирует изменения консервативных аминокислот. Для определения профиля антигенности для HCV использовались
пятнадцать последовательностей HCV [HCV -1, Q3.2, HCT 23, EC10, HC -J1, HCVEI, TH, HCT
27, Q1.2, HCT 18, HC -J4, HCV1.2/HCV J1.1, HCVJ HCV BK]. V3 профиль HIV-1 был получен усреднением 242
индивидуальных профилей 15 последовательностей, выбранных произвольно из базы данных уникальных
HIV 1 последовательностей с большей численностью. La Rosa и др. (1990) Science 249 : 932-5 и Correction
in Science (1991), стр. 811. Аминокислотные последовательности некоторых из этих изолятов между
384 и 420 показаны на фиг. 3.
Прогнозирования вторичной структуры, полученные с помощью
компьютера
Вероятности вторичной структуры α-спираль, β-пласт и β
-виток для амино-концевого участка (384 - 420) определялись с использованием алгоритма, который
присваивает вероятности для каждого из трех указанных мотивов вторичной структуры каждому остатку.
Коэффициенты, используемые в алгоритме, были получены для всех парных комбинаций остатков базы
структурных данных. Levitt and Greer (1977) J. Mol. Biol. 114 : 181 - 293. Параметры прогнозирования,
полученные от этих коэффициентов, совпадали с полученным результатом, когда алгоритм применялся
вновь на базе данных, чтобы получить вероятности, что данный остаток будет выявлен в одном из трех
определенных вторичных структурных мотивах.
Пример 1
Сравнение вторичной
структуры и вариации аминокислотной последовательности в доменах E2/NS1HV HCV и HIV-1 gp 120
Аминокислотные последовательности 15 изолятов HCV и HIV-1 сравнивались по числу позиций, в которых
гетерогенность аминокислотной последовательности наблюдалась в доменах E2 HV HCV или HIV-1 gp 120
V3. (Фиг. 4, A и B соответственно). Аминокислотные гетерогенности имели место в 25 из 30
аминокислотных позиций в E2 HV участке и 23 из 35 аминокислотных позиций в V3 домене HIV-1 gp 120. Тире на
x-оси фиг. 4A и B представляют аминокислотные позиции, где имеют место вариабельные
аминокислотные остатки, и не вариантные аминокислоты даются в однобуквенном коде аминокислоты. Профили антигенности,
показанные на фиг. 4, указывают, что подобно V3 петле белка HIV-1 gp 120 (фиг. 4B),
был идентифицирован блок аминокислотных остатков в E2 HCV (аминокислоты 384 - 414 на фиг. 4A), вариация которых
имела спрогнозированный обратный эффект на связывание антитела. Данные на фиг. 5
указывают, что домен E2 HCV напоминает домен gp 120 V1 HIV-1, который, как известно, кодирует эпитопы, нейтрализующие
вирус, как в степени, так и предполагаемом значении наблюдаемой аминокислотной
вариации, и предполагают, что домен E2 HV может иметь такую же функцию, что и домен gp 120 V3. Линейные эпитопы более
вероятно ассоциируются с менее структурными участками белков, в частности концами
белков или с продленными поверхностными петлями. Компьютерный анализ использовался, чтобы предсказать вероятность,
что индивидуальный остаток ассоциируется с определенным вторичным структурным мотивом
для 15 E2 HV, аминокислотных последовательностей между остатками 384 - 420. На фиг. 4 показано, что участок между
E2 амино-концевым остатком 384 и четко предсказанным высококонсервированным бета
витком (остатками 415 - 418), не является относительно структурированным, как показано вероятностью характера
альфа-спирали, бета-пласта или бета-витка, которая составляет менее 50%. Отсутствие четко
предсказанной структуры в домене E2 HV совместимо с допустимостью значительной вариации последовательности,
выявленной между изолятами, и контрастирует с высокоструктурированными участками, которые
способствуют третичной укладке белка. Домен E2 HV HCV представляется даже менее структурированным, чем V3,
основной нейтрализующий домен HIV-1 gp 120, который содержит бета-цепочечный тип II бета
витковый - бета цепочечный - альфаспиральный мотив и может накладывать большие структурные ограничения на
аминокислотную вариабельность, чем домен E2 HV HCV. Учитывая это, доказательство предполагает,
что домен E2 HV обладает признаками, характерными для доменов белка, которые содержат вероятные участки
линейных нейтрализующих эпитопов.
Пример 2
Составление карты эпитопов
домена E2/NSI HV HCV
Перекрывающие биотинилированные 8-mer пептиды, соответствующие E2/NSI HV
домену и выходящие из него (аминокислоты 384 - 416) с участками HCT 18 (A, D), Th (B, E) и HCV J1
(C, F) фиксировались к планшетам, покрытым стрептавидином и реагировали с плазмой либо из HCT 18
(A-C), либо Th (D - F). Результаты показаны для изолятов HCT 18 HCV (фиг. 6A и 6D), Th (фиг. 6B и 6E),
и HCV J1 (фиг. 6C и 6F). Плазма HCT 18 была разбавлена 1 : 200 и плазма Th - 1 : 500. HVE-1, -2,
-3, -4 и -5 представляют специфические эпитопы изолята. Как видно из фиг. 6, плазма HCT 18
идентифицировала линейный эпитоп (407PKQNV 411) при тестировании пептидами, полученными от
последовательности HCT 18 (HVE-1 на фиг. 6A), но не реагировали с пептидами, соответствующими HV
домену двух разных штаммов Th и HCV J1 (фиг. 6B и 6C). И наоборот, Th плазма идентифицировала линейный
эпитоп HVE-IV в HV домене (409QNIQLI 414, фиг. 6E), и также эпитопы в штамме HCT 18
(399IVRFFAP 405, фиг. 6) и HCV JI/ Th, пользователь средства IV может быть подвергнут
множественным штаммам HCV.
Плазма и Th и HCT 18 отдельно реагировали с эпитопом (аминокислоты 413 - 419), общим для всех трех изолятов (данные не показаны), при использовании в ELISA с синтезированными шпилькой перекрывающими 8 mer пептидами из каждого изолята.
Чтобы валидировать специфичность связывания антитела, антитела, связанные с биотинилированными пептидами, содержащими аминокислоты 403 - 407, элюировались и использовались для блокирования реактивности плазмы HCT 18 шпильками, содержащими перекрывающие 8-mer для HCT 18 HV домена. Эти данные указывают, что 1) домен E2/NSI HV иммуногенный, 2) существуют множественные эпитопы, которые картируются к этому участку, и 3) субсовокупность эпитопов (HVE-1, -2, -3, -4 или -5 на фиг. 6 в домене HV являются специфичной в отношении изолята.
Пример 3
Установление
того, что домены варианта E2/NSI HV могут ассоциироваться со вспышками гепатита
Чтобы исследовать
возможность выявления вариантов HCV, ассоциированных с перемежающимися вспышками гепатита,
часто возникающих при хронических инфекциях HCV, мы частично секвенировали ген E2/NSI от пациента, Q с
хроническим гепатитом во время двух явных эпизодов гепатита приблизительно с разницей в два года
(Q1 и Q3 соответственно). Второй эпизод гепатита имел место через 1,5 года после завершения лечения
интерфероном.
Различия в выведенной аминокислотной последовательности участка E2/NSI Q1 и Q3 были существенно отличительными только между аминокислотами 391 - 408 и составили семь из восьми изменений между аминокислотами 398 и 407 (фиг. 7). На фиг. 7 показаны выведенные аминокислотные последовательности двух участков полипептида E2/NSI, аминокислоты, 384 - 414 и 547 - 647, для изолятов Q1 и Q3. Аминокислота (E) выше Q1 последовательности была выявлена в одном из четырех Q1 клонов. Боксированные аминокислоты представляют местоположение Q1 или Q3 HVE 12 mer пептида. Аминокислотные различия, выявленные между Q1 и Q3, напечатаны жирным шрифтом.
Только одна аминокислотная гетерогенность была отмечена между аминокислотами 547 и 647 полипептидов E2/NSI Q2 и Q3 (фиг. 7).
Чтобы рассмотреть действие аминокислотных замещений, наблюдаемых в Q1 и Q3 E2 HV доменах на связывании антитела, мы синтезировали Q1 и Q3 специфический 12-mer пептид из аминокислот 396 - 407 (HVE Q1 или Q3 на фиг. 7B) и отдельно подвергли реакции плазму Q1 и Q3 с каждым пептидом в ELISA. Таблица 4 показывает, что в обоих тестах антитела в плазме Q1 и Q3 реагировали с Q1 пептидом, но не с Q3 пептидом. Статистический анализ показал, что связывание Q1/Q3 плазмы с Q1 пептидом было значительно выше известного до сих пор связывания этих плазм с панелью в 12 произвольно выбранных контрольных пептидов (P < 0,001), в то время как связывание плазмы пептида Q1 или Q3 не было статистически значительным. Данные показывают, что хотя пациент Q выработал антитела к домену Q1 HV HCV, которые все еще можно было обнаружить через два года в момент наличия Q3, заметной гуморальной реакции на вариант E2 HV Q3, который превалировал во втором эпизоде гепатита, не вырабатывалось.
Пример 4
Обнаружение сосуществующих E2/NSI
генов с отчетливыми доменами E2/NSI HV в зараженных HCV индивидах
На фиг. 8A
показаны аминокислотные последовательности, выведенные из двух изолятов 1 HCV (J1.1 и J1.2), которые клонировались
от одного плазменного образца одного добровольного донора крови из Японии с J1 HCV.
Kubo и др. (1989) Nucl. Acid. Res. 17 : 10367 - 372. Из 23 общих аминокислотных изменений между J1.1 HCV и J1.2 HCV,
9 различий, указанные жирным шрифтом, образуют кластеры в домене E2/NSI HV с 30
аминокислотами. 5 из 9 аминокислотных замещений в домене E2/NSI HV - неконсервированные аминокислотные изменения.
Поскольку J1 HCV - единственный геном группы II HCV, который клонировался в нашей
лаборатории, маловероятно, что эти различия можно отнести за счет перекрестного обсеменения плазмы J1 HCV. J1.2
последовательность представляет минорную последовательность в HCV JI крови, поскольку
только две E2/NSI HV вариантные последовательности были идентифицированы из 7 клонированных последовательностей,
которые брали начало от двух независимых PCR реакций.
Интересно, что сравнение изолятов HCT 27 и HCV EI (фиг. 8B), которые секвенировались в разных лабораториях и были получены от разных индивидов, показало, что число аминокислотных различий в E2/NSI HV домене этих изоляторов было меньше числа различий, наблюдаемых между изоляторами от того же индивида.
Эти результаты предполагают вывод, что HCV геном быстро развивается в индивидах и популяции.
Пример 5
Приготовление и получение вакцины. Связывание белка носителя дифтерийного
токсоида с нужными материалами MCS
Требуемые материалы
этилен
диамин тетра-уксусная кислота (EDTA Na2 - 2H2O) (MM 372) 6-малеимидо-капроевой кислоты
N-гидроксисукцинимид эстер (MCS) (Sigma) - 95% чистоты
NaH2PO4
азот
диметилформамид (ДМФ)
Милли Q вода
0,1 М фосфатный буфер,
содержащий 5 мМ ЕДТА, pH 6,66
0,1 М фосфатный буфер, pH 8,0
0,1 М
фосфатный буфер, pH 7,0
сукцинат натрия [(CH2COONa)2•6H2O]
цистеин
хлористоводородная кислота (2% раствор)
0,1 М сукцината
натрия/ 0,1 ЕДТА, pH 5,6
Очищенный дифтерийный токсоид (Commonwealth /Serum, Lab. Victoria, Australia)
связывался с MCS в соответствии с методом, описанным Lee, Paris и др. 1983) Prot. Chem.
2:263; Peeters и др. 1989). J.Immunol. Methods 120:133; Jones и др. (1989) J.Immunol. Methods 123:211. 100 мл
дифтерийного токсоида пропускалось через колонну G25 Sephadex (17 см х 4 см), чтобы
удалить тиомерсал. Токсоид элюировался 0,1 М фосфатного буфера, pH 7,0 и содержание белка элюата определялось
использованием белка альбумина бычьей сыворотки (BCA) (Pierce). Полученный раствор
концентрировался с использованием аппарата ультрафильтрации Amicon до окончательной концентрации 10 мг/мл.
Один миллилитр раствора токсоида был диализирован 0,1 М фосфатного буфера, pH 8,0 и затем смешивался с раствором в 1,5 мг MCS в 200 мкл ДМФ. Полученный раствор инкубировался при комнатной температуре 1 час в темноте с периодическим перемешиванием, чтобы отделить несвязанный MCS от MCS-токсоида, раствор пропускался через колонну Sephadex PD 10, которая уравновешивалась 0,1 М фосфатного буфера, pH 6,66, и фракция белка собиралась.
Число малеимидных групп, связанных на молекулу носителя, определялось до их связывания с пептидами HCV. 30 миллилитров сукцинат/EDTA буфера разбрызгивались с азотом 2 минуты. 5 мг цистеина переносились в колбу объемом 25 мл и растворялись в окончательном объеме в 25 мл разбрызганного буфера. Аликвоты растворов, показанные в таблице 5, переносились в дублированном количестве в 25 мл бутылки с винтовыми пробками. Отдельными пипетками азот вводился пузырьками в каждую аликвоту. Затем каждая бутылка закупоривалась и инкубировалась при комнатной температуре в темноте 40 минут с периодическим встряхиванием.
Тест Эллмана на количественное определение сульфгидрида
Необходимое материалы
Фосфатный
буфер, pH 8.0
Растворитель 15.6 г NaH2PO4 или 12,0
г NaH2PO4 безводного приблизительно в 700 мл milli Q воды. Довести pH до 8.0, используя 50%
NaOH. Добавить milli Q воды до окончательного объема в 1000 мл и затем при
необходимости отрегулировать pH.
Реагент Эллмана
Растворить 10,0 мг 5,5'-дитиобис-2-нитробензойной
кислоты (DTNB) в 2,5 мл фосфатного буфера, pH 8.0
0,1 мл реагента
Эллмана было добавлено к каждой аликвоте в 0,1 мл растворов, приготовленных выше, а именно образцу, стандарту и чистому
растворам. Затем 5 мл фосфатного буфера, pH 8,0 добавлялось к каждой аликвоте,
хорошо смешивалось и выстаивалось 15 минут. Абсорбная способность каждой аликвоты измерялась в клетке с длиной пути в 1
см на 412 нм.
Число малеимидных групп; присутствующих в белке носителя, определялось в соответствии со следующим методом. 0,01 мкмоля на мл раствора -SH дает абсорбность в 0,136 в 1 см световом пути на 412 нм. Абсорбность Стандарта или Образца (А) равна количеству цистеина, реагировавшего со связанными малеимидогруппами на активированном белке носителя. Поскольку 1 моль - SH реагирует с 1 молем малеимидной группы, концентрация в мкмолях малеимидо групп, присутствующих в тестуемой аликвоте, равна A (0.01)/ 0,136 мкмоль/мл. Общий объем раствора был 5:2 мл. Поэтому общее число присутствующих мкмолей было равно A (0.01) 5.2 /0.136. Раствор образца имел общий объем 1,3 мл, из которых 0,3 мл состояло из активированного белка носителя. Число малеимидных групп, присутствующих в растворе образца, рассчитывалось как A(0.01) (5.2) (1.3)/ (0.136) (0.1) (0.3) = A (16.57) мкмоль/мл. MCS - активированный белок носителя хранился при -20oC.
Восстановление пептидов HCV
До связывания пептидов HCV со
MCS - активированным белком носителя пептиды были восстановлены, чтобы удостовериться, что тиоловые группы, присутствующие
на пептидах, имеют полностью восстановленную -SH форму.
Необходимые материалы
дитиотрейтол (DTT)
бикарбонат аммония (NH4HCO3)
метанол
SEP-PAKS (обойма C18, Waters), 1 обойма для каждых 8 мг
пептида
0,1 М буфера бикарбоната аммония.
Растворить 7,9 г NH4HCO3 в 1 л Milli
Q воды Буфер A, 0.1% об/об трифторуксусной кислоты (TFA) в Milli Q
воде
Буфер B, 60% об/об ацетонитрил, 0,1% об/об. TFA в Milli Q воде.
15 мг каждого из двух пептидов HCV, соответствующих аминокислотам 384-411 и 225-260 соответственно из полибелка HCV добавлялось к 2.5 мл 0.1 М бикарбоната аммония, содержащего 10-кратный молярный избыток DTT. Полученные растворы смешивались до растворения пептида и затем выстаивались 1 час при комнатной температуре. Две пары SEP-PAKS соединялись последовательно и активировались пропусканием приблизительно 20 мл метанола и затем 20 мл буфера A через каждую пару EP-PAKS . Каждый образец пептид DTT медленно пропускался через пару SEP-PAKS. DTT элюировался 20 мл Буфера А. Восстановленный пептид элюировался 7 мл Буфера B в предварительно взвешенной бутылке и затем в течение ночи высушивался вымораживанием. Бутылки затем взвешивались для определения количества восстановленного пептида. Затем восстановленные пептиды сразу же связывались с MCS - активированным белком носителя.
Связывание HCV пептидов с MCS - активированным белком носителя
Приблизительно 100
мл 0,1 М фосфатного буфера с 5 мМ EDTA, pH 6,66
дегазировалось в вакууме и затем барботировалось с азотом 10 минут. 20 мл 10 мг/мл раствора MCS - активированного белка носителя тщательно
барботировалось азотом с целью снижения пенообразования. 5
мг каждого из восстановленных пептидов растворялись приблизительно в 0.2 мл дегазированного барботированного фосфат/EDTA буфера, pH 6,66, и
затем смешивались в раствором MCS - активированного белка
носителя. Полученная смесь переносилась в бутылку с винтовой пробкой, которая затем заполнялась азотом и закупоривалась. Далее раствор
дегазировался выдерживанием бутылки и ультразвуковой ванне
Branson 2000 в течение 2 минут. Бутылка закрывалась алюминиевой фольгой и инкубировалась всю ночь при комнатной температуре с медленным
помешиванием взбалтыванием.
Полученный конъюгат был растворимым и несвязанный пептид удалялся пропусканием смеси через колонну Sephadex PD10, которая уравновешивалась фосфат/EDTA буфером, pH 6.66. Фракция белка собиралась. Количество пептида, конъюгированного с белком носителя, определялось аминокислотным анализом.
Был проведен аминокислотный анализ 150 мкг аликвот и конъюгата и белка носителя. Определялся средний коэффициент уровня аминокислот, внесенных только белком носителя, чтобы рассчитать количество полученного конъюгированного пептида. Уровни серина, треонина, триптофана, метионина, тирозина и цистеина не определялись, поскольку эти аминокислоты модифицировались в условиях стандартного гидролиза. Типичные результаты, полученные в этих расчетах, представлены в таблице 6.
Для конъюгата величины, указанные жирным шрифтом, представляют аминокислоты, которые также присутствуют в пептидах. Для конъюгатов, содержащих аланин и профин, фактор (193+179+180+56)/(212)+194+153+60) = 0.8659 умножается на количество уровня аминокислоты, чтобы нормализовать результат.
Получение композиции вакцины
Композиции для инъекций
состоят из пептидов HCV, конъюгированных с MCS-активированным белком носителя дифтерийного токсоида, полученного, как описано выше, и адъюванта субмикронной эмульсии
масло-в-воде, как описано в PCT
международной публикации N 09014837, опубликованной 13 декабря 1990 г., которая включена сюда ссылкой. Кроме того, были получены композиции для инъекций, содержащие в
дополнение к конъюгированным
пептидам HCV и адъюванту, - иммуностимулянты, липофильный мурамил пептил (МТР-РЕ, CIBA-GEIGY, Базель, Швейцария). Композиции вакцины состоят обычно из 50% белка и 50%
адъюванта.
Формула для композиции вакцины с MTP-PE
Чтобы получить 10 мл вакцины (композиции) для инъекции:
2,5 мл Squalene (Sigma Chemical Co. St.Louis, Mo.)
0,25 мл Tween 80 (Sigma
Chemical. Co)
0,25 мл SPAN 85 (Sigma Chemical. Co)
1000 мкг MTP-PE
1000 мкг пептида HCV, конъюгированного с MCS - активированным белком носителя
дифтерийного токсоида
Формула для композиции вакцины без MTP-PE
Для получения 10 мл композиции вакцины для инъекции 2,5 мл Squalene (Sigma Chemical. Co)
0,25 мл Tween 80
(Sigma Chemical. Co)
0,25 мл SPAN 85 (Sigma Chemical. Co)
1000 мкг пептида HCV, коньюгированного с MCS - активированным белком носителя дифтерийного токсоида
Пример 6
Способ тестирования
препаратов вакцины на токсичность
Вакцина, полученная в соответствии с методикой примера 5, текстировалась на токсичность на некрупных животных. 50 микрограммов
вакцины на килограмм
назначалось морским свинкам, мышам и кроликам внутрибрюшной инъекцией, а также макакам резус и приматам. Половина тестуемой популяции макак резус и приматов получали дозу вакцины
5 мкм/кг, а вторая
половина - 50 мкг/кг. Контрольным животным, используемым в каждом тесте, делалась инъекция такого же количества композиции, состоящей из компонентов препарата вакцины, за
исключением вирусных
пептидов.
В каждом из животных наблюдались симптомы, указывающие на реакцию на токсический материал. Более конкретно, каждое животное раз в две недели наблюдалось на проявление симптомов лихорадки, летаргии, потери веса, ухудшения аппетита и симптомов припухания или чувствительности в месте инъекции. Ближайшие к месту инъекции лимфатические узлы также наблюдались на предмет опухания или дренажа. За животными следили раз в две недели в течение нескольких месяцев.
Пример 7
Демонстрация выработки нейтрализующего антитела у
вакцинированных
животных
Вакцина, полученная в соответствии с методикой примера 5, тестировалась на шимпанзе в целях определения эффективности в выявлении выработки нейтрализующего вирус
антитела у
вакцинированных субъектов. Шимпанзе вакцинировались дозировкой вакцины в 5 мкг/кг, полученной методикой примера 5. Приемы вакцинации проводились в 6-месячный период с интервалами в 0, 1, 3
и 6
месяцев. Контрольным шимпанзе были сделаны инъекции таких же количеств композиции, состоящей из компонентов вакцины, за исключением вирусных пептидов. Через две недели после введения последней
дозы
вакцины тестуемым и контрольным шимпанзе было введено по 10 CIU50 (Инфекционная единица шимпанзе) инокулята плазмы CDC/910. Через неделю после контрольного вирусного заражения каждая
из
шимпанзе раз в неделю проходила осмотр.
Чтобы обнаружить виремию, в течение нескольких месяцев раз в неделю брались пробы крови и биопсия печени на анализ от контрольных и тестуемых животных. Ткань, взятая биопсией печени, исследовалась гистологически на признаки некроза и/или воспаления. Кроме того, гепатоциты из материала биопсии исследовались электронной микроскопией на наличие инфекции HCV в канальцах. Пробы крови также анализировались ELISA тестом, описанным ранее, на наличие антител на сегменты вирусных полипептидов, которые не использовались в получении вакцины. В частности, каждая из проб крови отбиралась ELISA на наличие антител на NS3, NS4 и NS5 пептиды. Наличие антител на эти пептиды в сыворотке шимпанзе указывало на заражение HCV.
Для обнаружения вирусной PHK, циркулирующей в плазме, или присутствующей в ткани биопсии печени, взятой у шимпанзе, использовался следующий метод.
cPCR метод для обнаружения PHK HCV в печени и в сыворотке
В пробе cPCR предполагаемая вирусная PHK в образце обратно транскрибируется в кДНК с обратной транскриптазой; затем сегмент
полученной кДНК амплифицируется с использованием модифицированного варианта технологии PCR, описанной Saiki и др. (1986). Праймеры для технологии nPCR получают от ДНК HCV, которую можно
идентифицировать семейством кДНК HCV, предусмотренным здесь. Амплифицированный продукт, соответствующий HCV-PHK, обнаруживается использованием зонда, полученного от семейства к ДНК HCV,
предусмотренных здесь.
Проба на cPCR/HCV, использованная в этих исследованиях, проводилась с применением следующих методов получения PHK, обратной транскрипции PHK в кДНК, амплификации специфических сегментов кДНК с помощью PCR, и анализа продуктов PCR.
PHK экстрагировалась из печени с применением метода изотиоцианата для получения общей PHK, описанного у Maniatis и др. (1982).
Чтобы изолировать общую PHK от плазмы, плазма разбавлялась в 5-10 раз TENB (0.1 M NaCl, 50 мм Tris-HCl, pH 8,0, 1 мМ EDTA) и инкубировалась в растворе протеиназы K/SDS (0,5% SDS, 1 мг/мл протеиназы К, 20 микрограммов/мл носителя поли А) от 60 до 90 минут при 37oC. Образцы однократно экстрагировались фенолом (pH 6,5), полученная органическая фаза однократно повторно экстрагировалась TENB, содержащим 0,1% SDS, и водные фазы обеих экстракций соединялись и дважды экстрагировались равным объемом фенол/CHCl3 /изоамилового спирта. [1: 1(99:1)]. Полученные водные фазы дважды экстрагировались равным объемом CHCl3 /изоамилового спирта, и осаждались этанолом с использованием 0,2 М ацетата натрия, pH 6,6, и 2,5 объемов 100% этанола; осаждение проводилось всю ночь при - 20oC.
кДHК, используемая в качестве матрицы для реакции PCR, была получена с использованием указанных проб для получения соответствующих кДНК. Каждая проба РНК (содержащая либо 2 микрограмма общей РНК из печени шимпанзе, денатурированной тепловым способом, либо РНК из 2 микролитров плазмы) инкубировалась в 25 мл реакционной смеси, содержащей 1 мМ, количество каждого праймера, 1 мМ каждого деоксирибонуклеотидного трифосфата (d NTP), 50 мМ, Tris-HCl, pH 8,3, 5 мМ MgCl2, 5 мМ дитиотрейтола (ДТТ), 73 мМ KCl, 40 единиц ингибитора РНКазы (RNASIN), и 5 единиц обратной транскриптазы AMV. Инкубация проводилась 60 минут при 37oC. После синтеза кДНК реакции разбавлялись 50 микролитрами деионизированной воды (DIW), кипятились 10 минут и охлаждались на льду.
Амплификация сегмента кДНК HCV проводилась с использованием двух 16-mer праймеров
синтетического олигомера, последовательность которых была получена от клонов 36 (анти-сенс) и 37b (сенс) кДНК HCV. Последовательность праймера от клона 36 была
5' GCA TGT CAT GAT GTA T
3'.
Последовательность праймера от клона 37b была:
5' ACA ATA CGT GTC TCA C 3'.
Праймеры использовались с окончательной концентрацией в 1 микромоль каждый. Чтобы амплифицировать сегмент кДНК HCV, который фланкируется праймерами, образцы кДНК инкубировались 0,1 микрограммами РНКазы А и реактантами PCR из комплекта Perkin Elmer Cetus PCR (N 801-0043 или N 801-0055) в соответствии с инструкциями производителя. Реакция PCR проводилась 30 или 60 циклов в термическом аппарате циклирования ДНК Perkim Elmer Cetus ДНК. Каждый цикл состоял из 1-минутного этапа денатурации при 94oC, 2-минутного этапа гибридизации при 37oC и 3-минутного этапа распространения при 72oC. Однако этап распространения в окончательном цикле (30 или 60) составил 8, а не 3 минуты. После амплификации образцы экстрагировались равными объемами фенола: хлороформа (1: 1) с последующей экстракцией равным объемом хлороформа, и затем образцы осаждались этанолом, содержащим 0,2 М ацетата натрия.
cPCR продукты анализировались следующим образом. Продукты подвергались электрофорезу на 1,8% щелочным агарозном геле по Murakawa и др. (1988) и переносились на ZETA Пробирующую бумагу (BioRad Corp.) блотированием гелей всю ночь в 0,4 М NaOH. Блоты нейтрализовались в 2 х SSC (1 x SSC содержит 0,15 М NaCl, 0,15 M цитрата натрия), предварительно гибридизировалась в 0,3 М NaCl, 15 мМ буфера фосфата натрия, pH 6,8, 15 мМ, EDTA, 1,0% SDS, 0,5% нежирного молока (Carnation Co. ), и 0,5 мг/мл обработанной ультразвуком денатурированной ДНК спермы лосося. Блоты, предназначенные для анализа на фрагменты кДНК HCV, гибридизировались до зонда, помеченного32P, образованного "ник" трансляцией последовательности вставки кДНК HCV в клоне 35, описанной в 07/456637. После гибридизации блоты промывались в 0,1 x SSC (1 x SSC содержит 0,15 М NaCl, 0,01 М цитрата натрия) при 65oC, высушивались и авторадиографировались. Ожидаемый размер продукта составил в длину 586 нуклеотидов; продукты, которые гибридизировались зондом и мигрировали в гелях в этом диапазоне размера, считались положительными для вирусной РНК.
В качестве контрольного был проведен тест на kPCR праймеры, предназначенные амплифицировать альфа-I антитрипсиновую мРНК, чтобы подтвердить наличие РНК в каждом анализируемом образце. Кодирующий участок альфа-I анти-трипсинового гена описан у Rosenberg и др. (1984). 16-mer праймеры синтетического олигомера, предназначенные для амплификации 365 нуклеотидного фрагмента колирующего участка альфа-I анти-трипсинового гена, были получены от нуклеотидов 22-37 (сенс) и нуклеотидов 372-387 (антисенс). Продукты PCR обнаруживались с использованием32P "ник" -транслируемого зонда, который лежит между и не включает последовательности праймера кДНК/PCR.
Из-за повышенной чувствительности реакции PCR все образцы проходили серию минимум три раза. Все ложные положительные сигналы убирались при осуществлении следующих мер: 1) устранение аэрозолей использованием трубок с винтовыми пробками с резиновыми кольцеобразными уплотнителями; 2) использование пипеток положительного замещения Ranin Microman с одноразовыми поршнями/капиллярами; и 3) подбор олигонуклеотидных последовательностей для кДНК и праймеров PCR из двух несмежных клонов кДНК.
Промышленная применимость
Иммунореактивные композиции настоящего изобретения применимы в получении материалов, например вакцин,
которые в свою очередь можно
использовать для лечения заражений HCV особенно хронических инфекций NCV. Кроме того, композиции можно использовать в получении материалов для обнаружения множественных
вариантов HCV в биологических
пробах. Например, иммунореактивные композиции настоящего изобретения можно использовать для получения композиций поликлонального антитела, которые опознают более одного
изолята HCV, или как антиген в
иммунопробе на анти-HCV антитело. Последний метод можно применять для отбора продуктов крови на возможное заражение NCV. Поликлональные антисыворотка или антитела можно
использовать для пассивной
иммунизации индивида.
Реферат
Изобретение относится к биотехнологии, иммунологии и вирусологии и может быть использовано для получения иммуногенных полипептидных композиций, перекрестно-реактивных со многими изолятами вируса гепатита C (HCV). Композиция содержит полипептиды, происходящие из разных изолятов HCV и имеющие по крайней мере один эпитоп в вариабельном домене полипептида оболочки HCV Е2/NS1 c аминокислотной последовательностью 384 - 414 и/или эпитоп в вариабельном домене Е 1 с аминокислотной последовательностью 215 - 255. Иммуногенную композицию используют для получения антител против HCV, для обнаружения антител в биологической пробе. Изобретение позволяет создать новые диагностикумы и вакцины. 5 с. и 5 з.п. ф-лы, 9 ил., 6 табл.


Комментарии