Трансдермальная безводная композиция, способ ее получения и нанесения - RU2088617C1
Код документа: RU2088617C1
Чертежи


Описание
Изобретение относится к трансдермальной безводной композиции в виде 20 - 100%-ной лиотропной жидкой кристаллической системы, содержащей активный ингредиент и вспомогательные материалы, и к способу ее получения.
Известно, что некоторые из применяемых в терапевтических целях активные ингредиенты обладают рядом преимуществ при трансдермальном введении. В зависимости от скорости освобождения активного ингредиента из трансдермальной композиции можно на протяжении периода от 1 дня до 1 недели обеспечивать его постоянный уровень в крови и поступление в нее необходимого для лечения данного заболевания количества действующего вещества.
Из литературы известно также, что депренил препарат, ингибирующий активность моноаминооксидазы B и повторное включение допамина можно с успехом использовать для замедления развития болезни Паркинсона у людей на ранних ее стадиях (Tetrug J. W. и Zangston J.V.). Действие депренила (селегелина). Природа и развитие болезни Паркинсона Science, 1989, 245, 514-522, Научная группа по болезни Паркинсона. Влияние депренила на развитие инвалидности на ранних стадиях болезни Паркинсона, N,Eng1, J. Med. 1989, 321, 1364 1371). Препарат назначают также вместе с лекарственными средствами, в состав которых входит L-допа, на поздних стадиях болезни Паркинсона (Bikmayer, Депренил (селегелин) в лечении болезни Паркинсона, Acta Neurologica Scand. 1983, Suppl. 95, 103 106). Его применяют также при некоторых формах шизофрении (опубликованная заявка РСТ N 90/01298), а согласно результатам последних испытаний он может использоваться также при старческом склерозе мозга (Pierre N. Tariot, Robert M.Coken, Trey Sunderland 1-депренил при статическом склерозе мозга, Arch. Gent. Psychiatry т. 44, май 1987, P.N. Tariot, T. Sunderland. Влияние 1-депренила на запоминание при старческом склерозе мозга, Psychopharmacology, 1987, 91, 489-495, Gian-Zuigi Piccini, Giancarlo Final, Massimo Riccirilli, Нейрофизиологическое действие 1-депренила при старческом склерозе мозга, Clinical Neuropharmacology, т. 13, N 2, стр. 147-1263, E. Martini, J. Pataki, k. Szilagyi, V. Ventor. Краткая информация об исследованиях ранней фазы 11. Излучение депренила у больных, страдающих слабоумием, Pharmacrpsychiatr, 20, 1987, 256-257).
В описаниях к патентам ЧША NN 4868218 и 4.861.800, а также к патенту PST WO N 89/09051 говорится о возможности трансдермального введения депренила. Согласно этим описаниям любая извастная, используемая на практике система для трансдермального введения лекарственных средств в жидком или твердом виде пригодна для введения тем же путем депренила.
Излучая препараты, описанные в вышеуказанных литературных источниках, а также другие традиционно применяемые o/w эмульгирующие основы мазей, w/o эмульгирующие основы мазей и гидрогели, было обнаружено полное отсутствие абсорбции активного ингредиента либо его полную абсорбцию в течение нескольких часов.
Задачей данного изобретения является получение кожного средства, в котором бы обеспечивалось равномерное и в достаточных для лечения данного заболевания количествах освобождение активного ингредиента на протяжении, по меньшей мере, 24, а при благоприятных обстоятельствах и 72 ч.
Известно также, что некоторые поверхностно активные соединения в случае трансдермального введения образуют дикую кристаллическую систему с водой (например декаэтилоксидолеиловый эфир или бридж 96). Полиэтиленоксидная цепь поверхностно активного соединения, входящего в состав такого крема, и вода образуют непрерывное гидрофильное пространство, которое играет вполне определенную роль в диффузии активного ингредиента.
Манипулируя соотношением поверхностно активных соединений, можно изменять поведение жидкой кристаллической системы и, следовательно, скорость диффузии активного ингредиента (Журн. of Controlleo Release, 13, 1990, 73-81).
Совершенно неожиданно было обнаружено, что при выборе соответствующего соединения лиотропная жидкая кристаллическая система может формироваться даже в безводной среде. Изменяя содержание отдельных компонентов, можно регулировать размер частиц жидких кристаллов и структуру кристаллической части общей системы. Таким путем удается получить препараты для трансдермального введения, которые обеспечивают равномерное освобождение активного ингредиента на протяжении 24, 48 или 72 ч, в соответствии с потребностями терапии данного заболевания.
Приведенные выше данные показывают, что изобретение относится к безводной композиции для
трансдермального
введения в составе 20-100%-ной лиотропной жидкой кристаллической системы:
1-30 мас. оптически активного или рацемического N-метил-N-(1-фенил-2-пропил)-2-пропиниламина
(именуемого в дальнейшем
депренил), N-метил-(1-(4-фторфенил)-2-пропил)-2-пропиниламина, или их терапевтически приемлемых солей,
40-70 мас. жидкого полиосиэтилена,
10-20 мас.
твердого полиоксиэтилена,
2-30 мас. неионного поверхностно активного соединения,
2-20 мас. пропиленгликоля (при необходимости)
0,5-2 мас. полимера с показателем a более 0,6,
а также другие (в случае
необходимости) вспомогательные материалы, которые добавляют до конечной величины 100 мас. в качестве эмульгирующих агентов и к способу ее получения.
В качестве жидкого полиоксиэтилена в композицию вводят полиоксиэтилен 200-600, предпочтительно полиоксиэтилен 400, а в качестве твердого полиоксиэтилена добавляют полиоксиэтилен 1500-6000, предпочтительно полиоксиэтилен 4000. Неионными поверхностно-активными соединениями могут служить комплексы полиэтилена с жирными кислотами и эфирами, полиоксиэтилена с жирными кислотами и спиртами, полиоксиэтилена и касторового масла, сорбитана, жирных кислот и эфиров, предпочтительно комплексы полиоксиэтилена, жирных кислот и эфиров.
Другими вспомогательными материалами, пригодными для этой цели, являются полисахариды, которые могут выполнять функцию эмульгирующих агентов.
Полимер должен иметь степень скрученности, характеризующуюся величиной a более 0,6 (например полиоксиэтилен 35.000).
Степень скрученности, т.е. проникающая способность полимера, описывается экспонентой a в уравнении Куна, Марка и Хонвика, описывающего взаимосвязь между фронтальной вязкостью и молекулярной массой (см. Rohrsetzer S. Kolloidika, Tankonyvkiado, 1986, D. J. Shaw Введение в коллоидную химию и химию поверхностей, Muszaki Konyvkiada, 1986, на венгерском языке).
Композиция согласно настоящему изобретению может быть получена следующим способом: жидкий полиоксиэтилен нагревают, добавляют в него расправленный твердый полиоксиэтилен, а затем поверхностно-активное соединение и активный ингредиент, разведенный подогретым полиэтиленгликолем, с последующим охлаждением полученной смеси и введением в нее полимера и в случае необходимости других вспомогательных материалов.
Используемый в композиции активный ингредиент можно получить согласно описаниям европейских патентов NN 0186680 и 0099302.
Описанную композицию для чрескожного введения принимают для обработки кожи в требуемых дозах, после которой обработанный участок закрывают, например пластырем.
Из-за низких доз активного ингредиента (5 10 мг/д) прямое определение его концентрации в крови затруднено. Поэтому был использован непрямой биохимический метод, оценивая ингибирование моноаминоксидазной активности (МАО) в тканях мозга и печени, а оставшееся количество неабсорбированного активного ингредиента определяли с помощью высокоэффективной жидкостной хроматографии в материале, который задерживался на пластыре.
Задача этих исследований состояла в определении параметров абсорбции трансдермальных композиций, отличающихся по своему составу. В качестве модельных животных использовали крыс и собак, кожу которых на подлежащих обработке участках освобождали от шерсти. О кинетике абсорбции судили по количеству оставшегося неабсорбированным активного ингредиента (с помощью высокоэффективной жидкостной хроматографии). Кроме того оценивали ингибирующее действие абсорбированного в мозговой и печеночной тканях активного ингредиента на моноаминооксидазную активность (МАО).
Методы тестирования состояли в следующем. Активность МАО в мозге и печени крыс определяли радиометрическим методом Вуртмана и Аксельрода (Biochem. Pharmacol. 1963, 12, 1417). Остаточное количество активного ингредиента на пластыре после его удаления с кожи подопытных животных определяли с помощью высоко эффективной жидкостной хроматографии. Количественную оценку производили с использованием калибровочной кривой, полученной посредством тестирования действия различных дозировок мази.
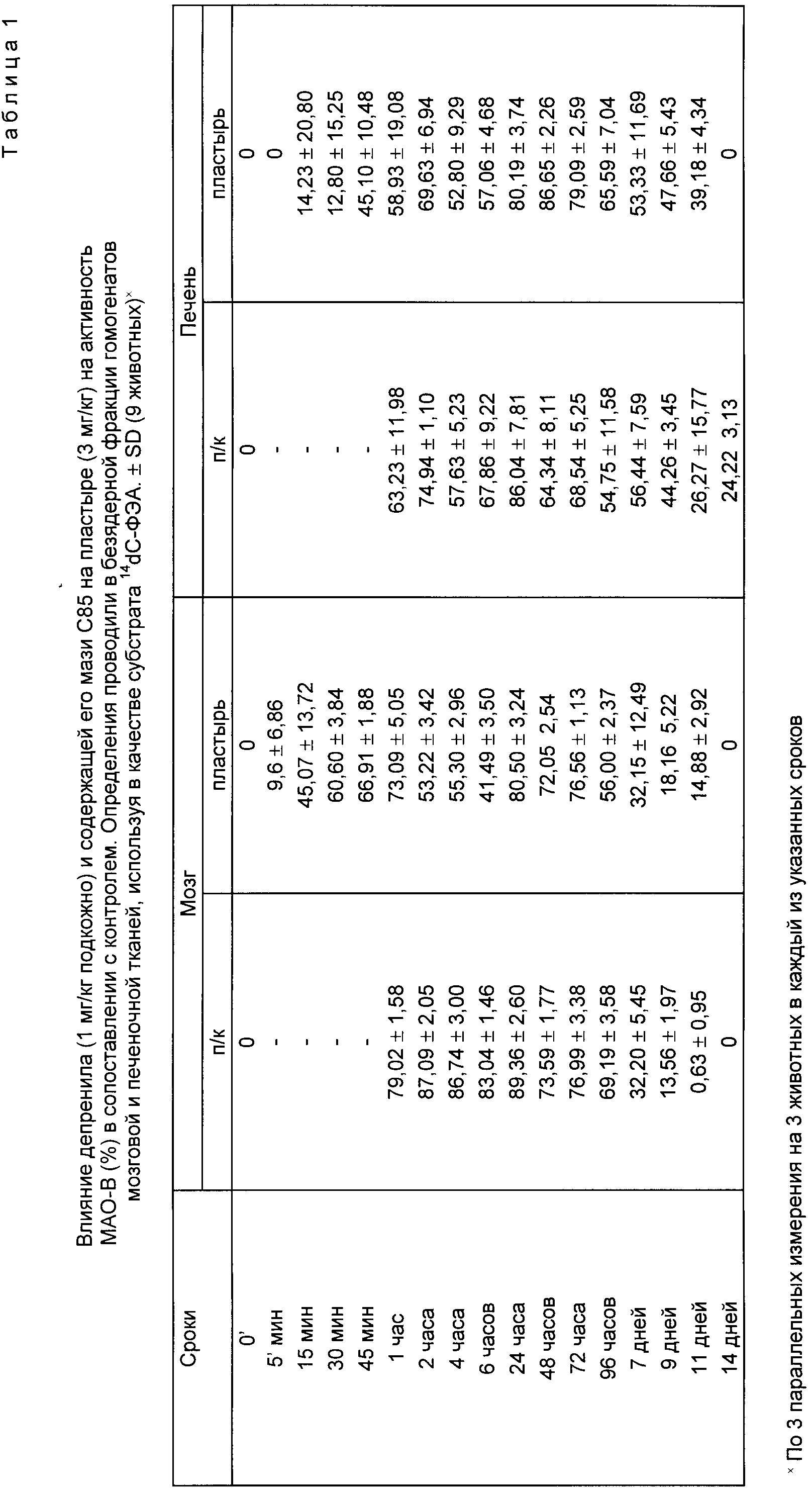
Результаты проведенного исследования (степень ингибирования активности моноаминооксидазы B) показывают, что активный ингредиент, исчезавший из-под пластыря (данный высокоактивной жидкостной хроматографии) абсорбировался тканями крыс. Данные измерений приведены в табл. 1.
Результаты определения скорости абсорбции показали, что кожа крыс мало пригодна для кинетических исследований, поскольку большинство тестировавшихся препаратов абсорбировались в пределах часа после нанесения. Более подходящей моделью является кожа собак. При использовании этой модели определение остаточной активности с помощью высокоактивной жидкостной хроматографии позволило быстро оценивать абсорбцию активных ингредиентов мазей при ее невысокой скорости. Результаты такой оценки показаны в табл. 2.
В дальнейших экспериментах определяли активность МАО-В в мозге и тромбоцитах домашних свиней.
Эти эксперименты проводили на самках породы "Большая белая" весом 25 30 кг. Каждое животное помещали в отдельную клетку и кормили по одинаковой схеме тем же кормом, что и до начала эксперимента. Животным первой группы перорально вводили 10 мг (-)-депренила в желатиновых капсулах. Пробы крови для определения активности МАО-В брали непосредственно перед введением препарата, а также через 3, 6, 24, 48, 72 и 96 ч после него. Сразу после взятия последней пробы животных забивали и определяли активность МАО-А и МАО-В в ткани мозга.
Животные второй группы получали 10 мг (-) депренила в составе препарата для чрескожного введения Ug 111. Пробы крови брали непосредственно перед введением и спустя 3, 6, 24 и 48 ч после него. Нанесенный на кожу препарат удаляли по истечении 24 ч. Остаточное его содержание определяли посредством анализа материала с пластыря и его нейлоновой оболочки. Анализу с помощью высокоактивной жидкостной хроматографии подвергали также материал с пропитанных этанолом ватных тампонов, которыми протирали кожу. Животных забивали через 48 часов после нанесения мази и определяли активность МАО-А и МАО-В в ткани мозга.
Кожу свиней третьей группы обрабатывали мазью Ug 167, которая содержала 20 мг (-)-депренила. Пробы крови брали непосредственно перед нанесением мази, спустя 3, 6, 24, 48 и 72 ч после ее нанесения. Пластырь удаляли через 48 ч. Остальные процедуры не отличались от описанных для второй группы подопытных животных.
Пробы крови брали из V. cava cranialis с помощью пластмассового шприца на 20 мл с 1,5 мл 7,7%-ного раствора лимоннокислого натрия. Объем всех проб составлял 18,5 мл.
Активность МАО измеряли радиометрическим методом, как описано Вуртманом и Аксельродом (Biochem. Pharmacol. 12, 1414 1419, 1963), с небольшими изменениями (K. Magyar в: "Моноаминоксидазы и их избирательные ингибиторы" под ред. K. Magyar, Pergamon Press, Akademia; Kiado, Будапешт, стр.11 21, 1980).
Для определения активности МАО в тромбоцитах использовали методику, предложенную Уилбергом и Ореландом (Med. Biol. 54, 137 144, 1976).
Результаты ингибирования активности МАО-В в тромбоцитах после перорального и трансдермального применения препарата представлены в табл.3.
Результаты определения активности МАО в мозге представлены на табл.4.
В табл.5 представлены результаты излучения трансдермальной абсорбции депренила.
Состав, размер частиц, процентное содержание жидкого кристаллического компонента
в различных препаратах иллюстрируются следующими примерами:
Ug 85
Полиоксиэтиленгликоль (ПЭГ) 4000 60,0 г 20%
ПЭГ-200 100,0 г 33,3%
Пропиленгликоль 30,0 г 10%
Депренил 15,0 г 5%
Пэг-400 ad 300,0 г 31,7%
Средний размер частиц: 9 мкм, жидкий кристаллический компонент 28%
Ug 111, г
ПЭГ-4000 16,0
ПЭГ-400 60,
0
Пропиленгликоль 8,0
Кремофор ЕЛ 2,0
Депренил 5,0
ПЭГ-400 ad 100,0
Средний размер частиц: 72,7 мкм, жидкий кристаллический компонент 20%
Ug 118,
г
ПЭГ-4000 16,0
ПЭГ-400 60,0
Пропиленгликоль 8,0
Кремофор ЕЛ 2,0
Депренил 5,0
Миритол 318 3,0
ПЭГ-400 ad 100,0
Средний размер
частиц: 36,4 мкм, жидкий кристаллический компонент:
50%
Ug 110, г
ПЭГ-4000 15,0
ПЭГ-400 60,0
Пропиленгликоль 10,0
Депренил 5,0
Кремофор ЕЛ 5,0
ПЭГ-400 ad 5,0
Ug 167 г
ПЭГ-4000 19,0
ПЭГ-400 55,0
Пропиленгликоль 8,0
Ксантановая смола 10,0
N-метил-N-(1-(4-фторфенил)-2-пропил-2-пропиниламин гидрохлорид 5,0
ПЭГ 400 ad 100,
0
Средний размер частиц: 91 109 мкм, жидкий кристаллический компонент: 70 80%
Ug 325, г
ПЭГ 35.000 1,0
ПЭГ-4000 15,0
ПЭГ-400 53,5
Пропиленгликоль
4,5
Ксантановая смола 15,0
Депренил 5,0
Кремофор ЕЛ 6,0
Жидкий
кристаллический компонент: 100%
Состав вспомогательных материалов:
Кремофор ЕЛ
глицерин-полиэтиленгликоль-рацинолеат
Миритол 318 триглицерид
Ксантановая смола
полисахарид.
Ug 653
ПЭГ 35000 1,5 г 1,5%
ПЭГ 4000 10,0 г 10%
ПЭГ 400 56,5 г 56,5%
Пропиленгликоль 2,5 г 2,5%
Ксантановая смола 0,0 г 10%
Депренил 4,6 г 14,5%
Кремофор 5,0 г 5%
Средний размер частиц: 50 мкм,
Жидкое кристаллическое состояние: 40%
Ug 654, г
ПЭГ 35000 1,5
ПЭГ 4000
11,5
ПЭГ 40,0
Пропиленгликоль 10,0
Ксантановая смола 19,0
Депренил 7,0
Кремофор 11,0
Средний размер частиц: 45 мкм,
Жидкое
кристаллическое состояние: 30%
Ug 653, г
ПЭГ 35000 1,0
ПЭГ 4000 15,0
ПЭГ 400 42,0
Пропиленгликоль 20,0
Ксантановая смола 11,0
Депренил 9,
0
Кремофор 2,0
Средний размер частиц: 55 мкм,
Жидкое кристаллическое
состояние: 50%
Реферат
Использование: трансдермальная безводная композиция, способ ее нанесения в терапевтических целях. Сущность изобретения: трансдермальная безводная композиция, включающая азотсодержащее активное соединение, при этом в качестве азотсодержащего активного соединения она содержит соединение, выбранное из группы, включающей N-метил-N-(фенил-2-пропил)-2-пропиниламин, N-метил-N-1-(1-(4-фторфенил)-2-пропил)-2-пропиниламин или их терапевтически приемлемые соли, а также жидкий и твердый полиоксиэтилен и неионогенное поверхностно-активное вещество при следующем соотношении компонентов, мас.%: азотсодержащее соединение 5-15, жидкий полиоксиэтилен 40-70, твердый полиоксиэтилен 10-20, неионогенное поверхностно-активное вещество 2-30 в форме 20-100% лиотропной жидкой кристаллической системы. 3 с. и 6 з.п. ф-лы, 5 табл.
Формула
Жидкий полиоксиэтилен 40 70
Твердый полиоксиэтилен 10 20
Неионогенное поверхностно-активное вещество 2 30
в форме 20-100%-ной лиотропной жидкой кристаллической системы.
Жидкий полиоксиэтилен 40 70
Твердый полиоксиэтилен 10 20
Неионогенное поверхностно-активное вещество 2 30
8. Способ по п. 7, отличающийся тем, что лиотропная жидкая кристаллическая система содержит 2-20 мас. пропиленгликоля.

Комментарии