Основанная на наночастицах, нацеленная на опухоли доставка лекарственных средств - RU2593367C2
Код документа: RU2593367C2
Чертежи






Описание
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет предварительной патентной заявки США серийный № 61/402686, поданной 2 сентября 2010 г., полное содержание которой приведено в настоящем документе в качестве ссылки.
ГОСУДАРСТВЕННАЯ ПОДДЕРЖКА
Это изобретение осуществлено при государственной поддержке от правительства Соединенных Штатов Америки, National Institutes of Health, грант no. 5 R01 CA134364-01 A, и National Heart, Lung, and Blood Institute, грант на обучение no. T32HL007195.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Нацеливание с помощью лигандов стало основным усовершенствованием опосредованной наночастицами (NP) доставки лекарственных средств, достигающим высокой местной концентрации и низкого системного воздействия, снижающим токсичность лекарственного средства при поддержании в то же время доставки оптимальной дозы к клеткам-мишеням. Проверку обоснованности концепции для этого способа осуществляли с помощью антител и связанных с хомингом пептидов, которые связывают рецепторы адгезии, обладающие сверхэкспрессией в сосудистой сети опухоли, включая интегрины, и HER-2, и рецепторы поверхности клеток для фолатов на клетках опухолей. Опасения, связанные с нацеливанием с помощью лигандов, включают в себя насыщение рецепторов, низкую аффинность рецептор-лиганд, ограниченную проницаемость тканей и генетическую гетерогенность солидных опухолей. Легумаин представляет собой аспарагинил-эндопептидазу, сверхэкспрессированную во множестве клеток опухолей. Следовательно, легумаин обеспечивает удобную мишень для направления лекарственных средств к клеткам опухолей. Композиции и способы по настоящему изобретению снимают опасения, связанные с нацеливанием с помощью лигандов, в то же время предоставляя эффективные средства для специфической для опухолей доставки лекарственных средств.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к водной нацеливающей на опухоли композиции липосомных наночастиц, содержащей водную дисперсию липосомных наночастиц, необязательно инкапсулирующих противораковое химиотерапевтическое средство. Водная нацеливающая на опухоли композиция липосомных наночастиц по изобретению содержит нацеливающий на легумаин липид, смешанный с одним или несколькими формирующими мицеллу или везикулу липидными материалами в форме дисперсии липосомных наночастиц, необязательно инкапсулирующих противораковое химиотерапевтическое средство внутри липосомных наночастиц. Нацеливающий на легумаин липидный компонент содержит гидрофобную липидную часть, ковалентно присоединенную к связывающей легумаин группе. Противораковое химиотерапевтическое средство можно инкапсулировать внутри липосомных наночастиц во время получения наночастиц, или наночастицы можно формировать предварительно, и затем нагружать химиотерапевтическим средством. Предпочтительная водная нацеливающая на опухоли композиция липосомных наночастиц содержит (a) нацеливающий на легумаин липидный компонент, (b) цвиттер-ионный липидный компонент; (c) аминозамещенный липидный компонент; (d) нейтральный липидный компонент; и (e) конъюгированный с полиэтиленгликолем липидный компонент, диспергированный в форме липосомных наночастиц в водном носителе (например, физиологически переносимом буфере, который может включать различные физиологически приемлемые наполнители и адъюванты, общеупотребительные в составах лекарственных средств). Нацеливающий на легумаин липидный компонент содержит гидрофобную липидную часть, ковалентно присоединенную к связывающей легумаин группе. Связывающая легумаин группа может представлять собой любой материал, который избирательно образует стабильный комплекс или ковалентную связь с легумаином.
Предпочтительная нацеливающая на легумаин группа представляет собой ингибитор легумаина типа аза-Asn акцептора Михаэля. Предпочтительный нацеливающий на легумаин липидный компонент содержит ингибитор легумаина типа аза-Asn акцептора Михаэля, связанный с фосфолипидом. Например, ингибитор, известный как RR-11a, можно связывать с подходящим липидом, как показано на Фиг.1, панель (a).
В некоторых предпочтительных вариантах осуществления нацеливающий на легумаин липидный компонент содержит связывающую легумаин группу, ковалентно присоединенную к группе 1,2-диацилглицерофосфоалканоламина, такой как 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламин (DOPE).
Предпочтительный цвиттер-ионный липидный компонент (b) содержит соединение 1,2-диацилглицерофосфохолина, такое как 1,2-ди-(9Z-октадеценоил)-sn-глицеро-3-фосфохолин (DOPC).
Предпочтительный аминозамещенный липидный компонент (c) содержит соединение 1,2-диацилглицерофосфоалканоламина, такое как DOPE.
Предпочтительный нейтральный липидный компонент (d) содержит холестерин.
Предпочтительный конъюгированный с полиэтиленгликолем липидный компонент (e) содержит конъюгированное с полиэтиленгликолем соединение 1,2-диацилглицерофосфоалканоламина, такое как 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламин-N-[метокси(полиэтиленгликоль)], где полиэтиленгликольная часть соединения обладает средней молекулярной массой приблизительно 2000 атомных единиц массы (а.е.м.).
В одном предпочтительном варианте осуществления компоненты (a), (b), (c), (d) и (e) присутствуют в липосомных наночастицах в молярном соотношении (a):(b):(c):(d):(e) приблизительно 1,1:6,7:6,7:2,2:1.
Предпочтительно, композиция липосомных наночастиц инкапсулирует противораковое химиотерапевтическое средство, например, доксорубицин, 1-[2-циано-3-,12-диоксоолеана-1,9(11)-диен-28-оил]имидазол (известный также как CDDO-Im) или любое другое известное противораковое химиотерапевтическое средство.
Композиции по настоящему изобретению особенно подходят для использования в лечении экспрессирующих легумаин опухолей. Методический аспект настоящего изобретения включает в себя введение пациенту, нуждающемуся в лечении злокачественной опухоли, эффективного количества противоракового химиотерапевтического средства, инкапсулированного внутри липосомных наночастиц из композиции по настоящему изобретению.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
ФИГ.1 иллюстрирует получение и характеризацию нацеленных на легумаин наночастиц (NP). Панель (a) иллюстрирует конъюгацию RR-11a с 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламином (DOPE). Панель (b) представляет изображения после флуоресцентной микроскопии, демонстрирующие гипоксию опухоли (масштабные линейки, 100 мкм). Панель (c) представляет график специфического связывания в зависимости от концентрации антитела, демонстрирующий аффинность моноклонального антитела (mAb) мыши против экспрессированного на мембране клеток легумаина, как определено анализом Скэтчарда. Панель (d) представляет график положительных по родамину клеток в зависимости от времени для клеток карциномы молочной железы 4T1 и 4TO7 и карциномы ободочной кишки CT26 мыши, культивированных в течение приблизительно 24 часов (час) с CoCl2, после чего не нацеленные наночастицы (не нацеленные) или нацеленные с помощью RR-11a наночастицы (нацеленные) NP добавляли к клеткам (n=3 лунок на группу; данные представляют собой среднее±s.e.m). Панель (e) представляет изображения после флуоресцентной микроскопии, визуализирующие распределение NP для клеток опухоли, печени, селезенки и почки от мышей, обработанных нацеленными (верхний ряд) и не нацеленными (нижний ряд) NP по настоящему изобретению, как показано по флуоресценции родамина B (n=2 мыши на группу; масштабные линейки, 100 мкм).
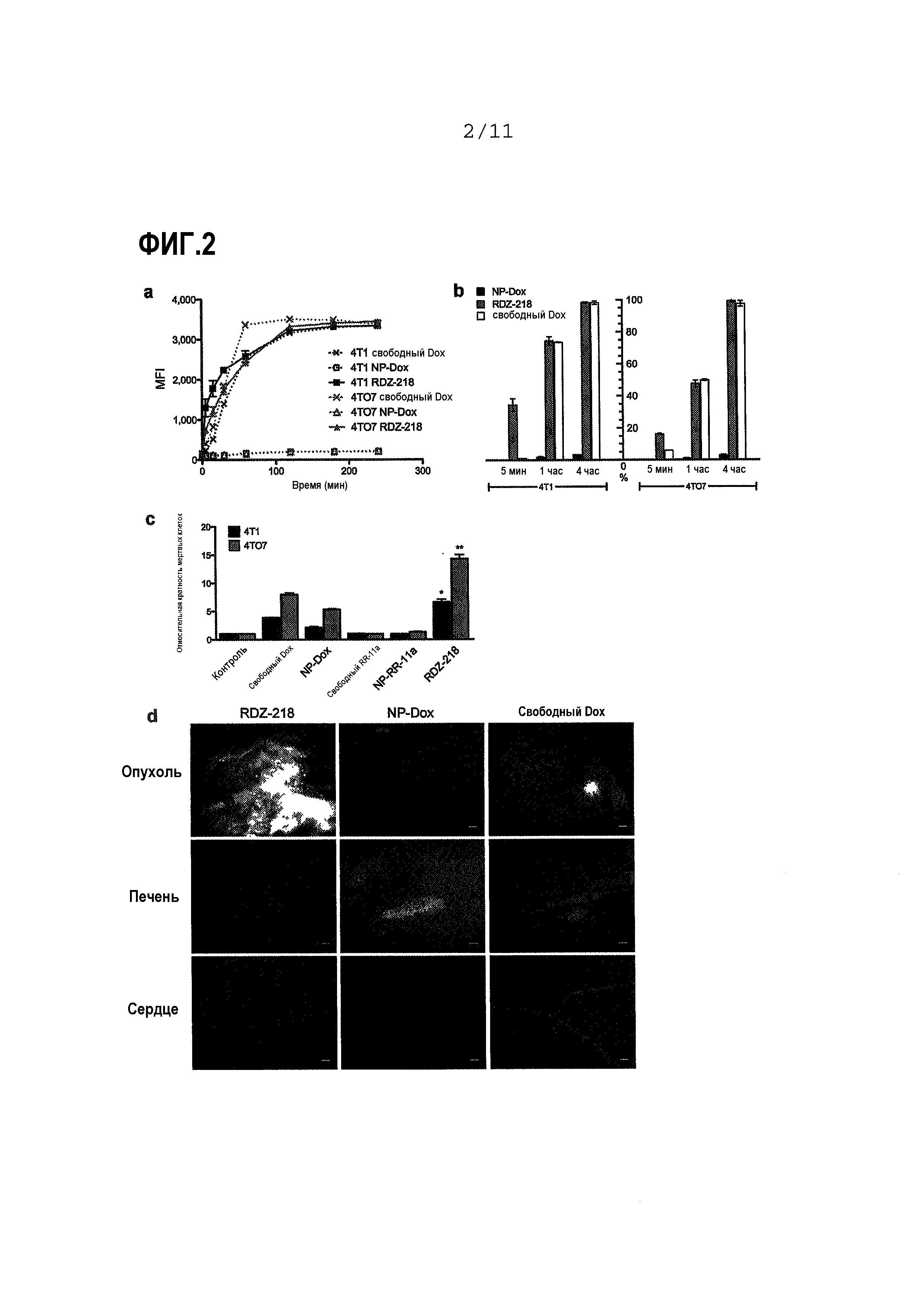
ФИГ.2 демонстрирует, что нацеливание на легумаин усиливает поглощение инкапсулированного в PEG-липосому доксорубицина и улучшает опосредованную NP доставку лекарственного средства к первичным опухолям молочной железы. Панель (a) представляет график средней интенсивности флуоресценции (MFI) в зависимости от времени для клеток 4T1 и 4TO7, культивированных с CoCl2 в течение приблизительно 24 часов и затем инкубированных с композицией нацеленных наночастиц, нагруженных доксорубицином (обозначенных RDZ-218 в настоящем документе), нагруженных доксорубицином не нацеленных NP (NP-Dox) или свободным доксорубицином (свободный Dox) в течение указанных периодов времени, с последующим анализом проточной цитометрией для определения средней интенсивности флуоресценции (MFI) доксорубицина (n=3 лунки на группу для каждой временной точки; данные представляют собой среднее±s.e.m). Панель (b) представляет столбчатые диаграммы, показывающие процент поглощенной концентрации лекарственного средства, как определено сравнением MFI для клеток, обработанных RDZ-218, NP-Dox и свободным Dox, с MFI для серийно разведенного доксорубицина. Панель (c) представляет столбчатую диаграмму, сравнивающую относительный процент мертвых клеток 4T1 и 4TO7 после контрольной обработки (без обработки), обработки свободным Dox, NP-Dox, свободным RR-11a, NP-RR-11a (без доксорубицина) и RDZ-218, приблизительно через 24 часа после обработки, как определено анализом графика прямого и бокового рассеяния при проточной цитометрии (данные показаны относительно необработанных клеток (контроль); n=3 лунки на группу; данные представляют собой среднее±s.e.m. *p<0,05, **p<0,005). Панель (d) представляет изображения при флуоресцентной микроскопии клеток опухоли (верхний ряд), печени (средний ряд) и сердца (нижний ряд) самок мышей BALB/c, которым клетки 4TO7 инъецировали в жировое тело паховой молочной железы; опухолям позволяли приживаться в течение приблизительно 5 суток (сут.), до размера приблизительно 500 мм3, после чего мышам вводили две i.v. инъекции RDZ-218, NP-Dox или свободного Dox; мышей умерщвляли приблизительно через 24 часа после последней инъекции, и ткани выделяли и немедленно анализировали флуоресцентной микроскопией для детекции распределения доксорубицина; срезы также окрашивали DAPI для визуализации ядер клеток (n=2 мыши на группу; масштабные линейки, 100 мкм).
ФИГ.3 демонстрирует, что терапевтическая обработка мышей, несущих опухоль 4TO7, с помощью RDZ-218 приводит к полной супрессии роста первичной опухоли молочной железы без токсичности для мышей, обработанных 5 i.v. инъекциями RDZ-218, NP-Dox, свободного доксорубицина (свободный Dox), пустых конгъюгированных с RR-11a NP (NP-RR-11a), или фосфатно-солевого буфера (PBS) с 3-суточными интервалами; точки данных представляют сутки лечения; n=5 мышей на группу. Панель (a) представляет график размера опухоли в зависимости от времени (данные представляют собой среднее±s.e.m.). Панель (b) представляет изображения первичных опухолей, снятые до иссечения; изображения являются репрезентативными для каждой группы. Панель (c) представляет столбчатую диаграмму, сравнивающую массу опухоли во влажном состоянии для первичных опухолей от мышей из каждой группы обработки (данные представляют собой среднее±s.e.m; *p<0,05). Панель (d) представляет столбчатую диаграмму, сравнивающую положительные по TUNEL (апоптотические) клетки опухолей от мышей из каждой группы обработки (n=5 полей на срез; данные представляют собой среднее±s.e.m; ***p<0,0005). Панель (e) представляет столбчатую диаграмму, сравнивающую изменение массы тела для мышей из каждой группы обработки (массу первичной опухоли вычитали из общей массы тела на время умерщвления и сравнивали с массой тела до заражения клетками опухоли для определения изменения массы тела; данные представляют собой среднее±s.e.m; контрольные группы сравнивали с обработанной RDZ-218 группой, **p=0,0029, ***p < 0,001).
ФИГ.4 схематически иллюстрирует добавление по Михаэлю остатка цистеина легумаина к аза-Asn акцептору Михаэля на панели (a); реакцию остатка Cys легумаина с аза-Asn-эпоксидом на панели (b) и реакцию остатка Cys легумаина с аза-Asn-галометилкетоном на панели (c).
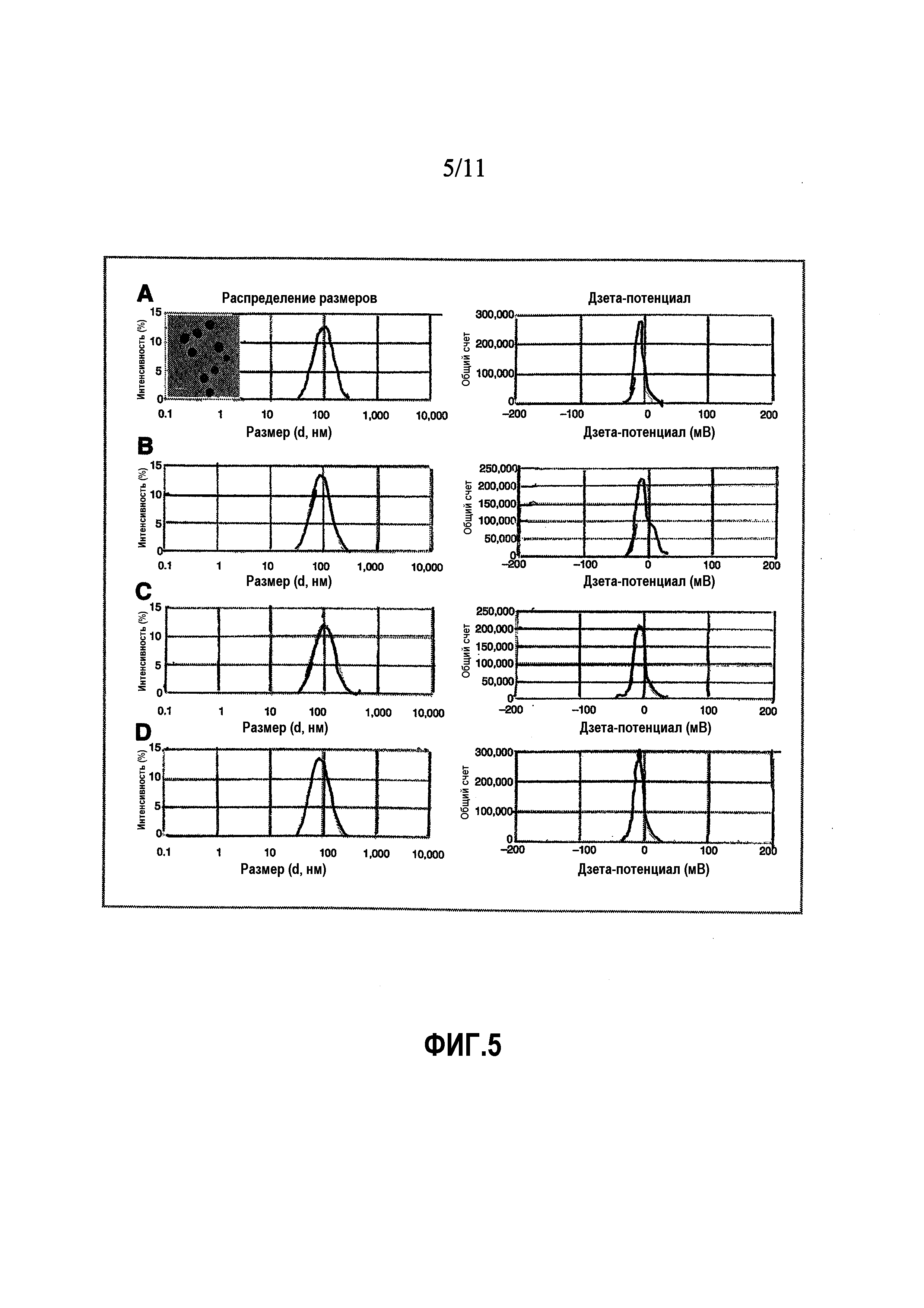
ФИГ.5. Физико-химическая характеризация NP с присоединенным RR-11a. Нацеленные на легумаин NP, нагруженные CDDO-Im (A), без CDDO-Im (B), или не нацеленные NP, нагруженные CDDO-Im (C) или без CDDO-Im (D), анализировали динамическим световым рассеянием и TEM (врезка) для определения распределения размеров частиц (диаметр, нм) и дзета-потенциала (мВ). Масштабная линейка=100 нм.
ФИГ.6. Инкапсулированный CDDO-Im ингибирует фосфорилирование STAT-3 в клетках и первичных опухолях рака молочной железы мыши по анализу Вестерн-блоттингом. (A) Клетки рака молочной железы мыши 4T1 обрабатывали IL-6 (10 нг/мл) и CDDO-Im в различных концентрациях. (B) клетки рака молочной железы мыши 4TO7 обрабатывали IL-6 (10 нг/мл) в комбинации со свободным CDDO-Im (свободным CDDO), пустыми нацеленными NP (Leg-NP), не нацеленными NP с инкапсулированным CDDO-Im (NP-CDDO) или нацеленными NP с инкапсулированным CDDO-Im (Leg-NP-CDDO). (C) экстракты первичных опухолей MMTV-Neu получали от мышей после обработки 8 i.v. инъекциями PBS (дорожка 1), Leg-NP (дорожка 2) или Leg-NP-CDDO (дорожка 3).
ФИГ.7. Терапевтическая обработка Leg-NP-CDDO ингибирует рост опухолей 4TO7. (A) Схема обработки мышей, зараженных 5×103 клеток опухоли 4TO7 и обработанных Leg-NP-CDDO, или контрольных (PBS, свободный CDDO, NP-CDDO или Leg-NP) (n=8 мышей/группу). (B) Опухоли пальпировали каждые 2 суток, и рассчитывали размер опухолей. Данные представляют собой среднее±s.e.m. (C) Массы опухолей измеряли на сутки 19 и сравнивали с массами тела для определения процента опухолевой нагрузки. Данные представляют собой среднее±s.e.m. *p<0,05.
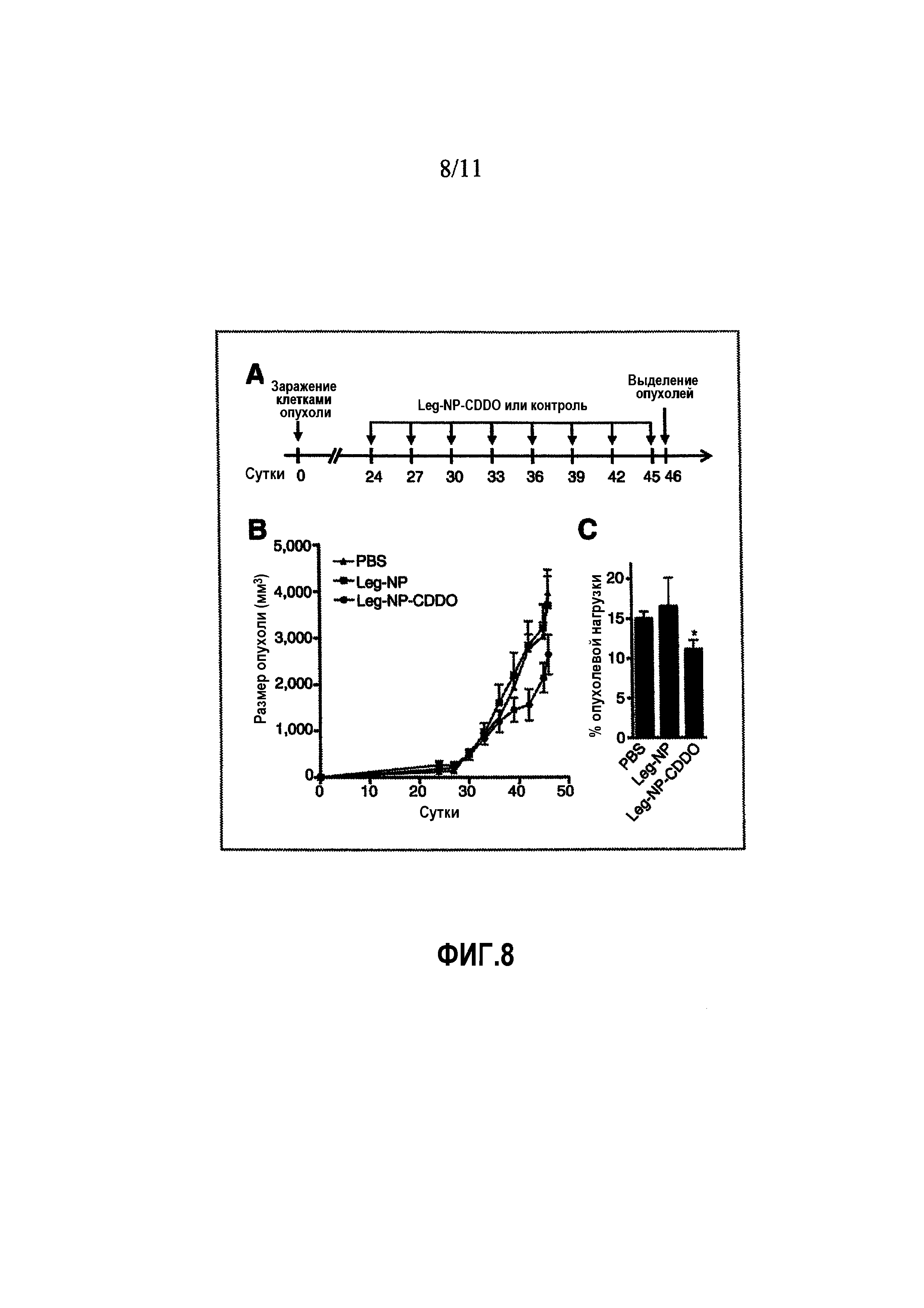
ФИГ.8. Терапевтическая обработка первичных опухолей MMTV-Neu Leg-NP-CDDO задерживает рост опухолей. (A) Схема обработки мышей, зараженных 1×104 клеток первичной опухоли MMTV-Neu и обработанных Leg-NP-CDDO, или контрольных (PBS или Leg-NP) (n=8 мышей/группу). (B) Опухоли пальпировали каждые 3 суток, и рассчитывали размер опухолей. Данные представляют собой среднее±s.e.m. (C) Массы опухолей измеряли на сутки 46 и использовали для расчета процента опухолевой нагрузки. Данные представляют собой средние±s.e.m, *p<0,05.
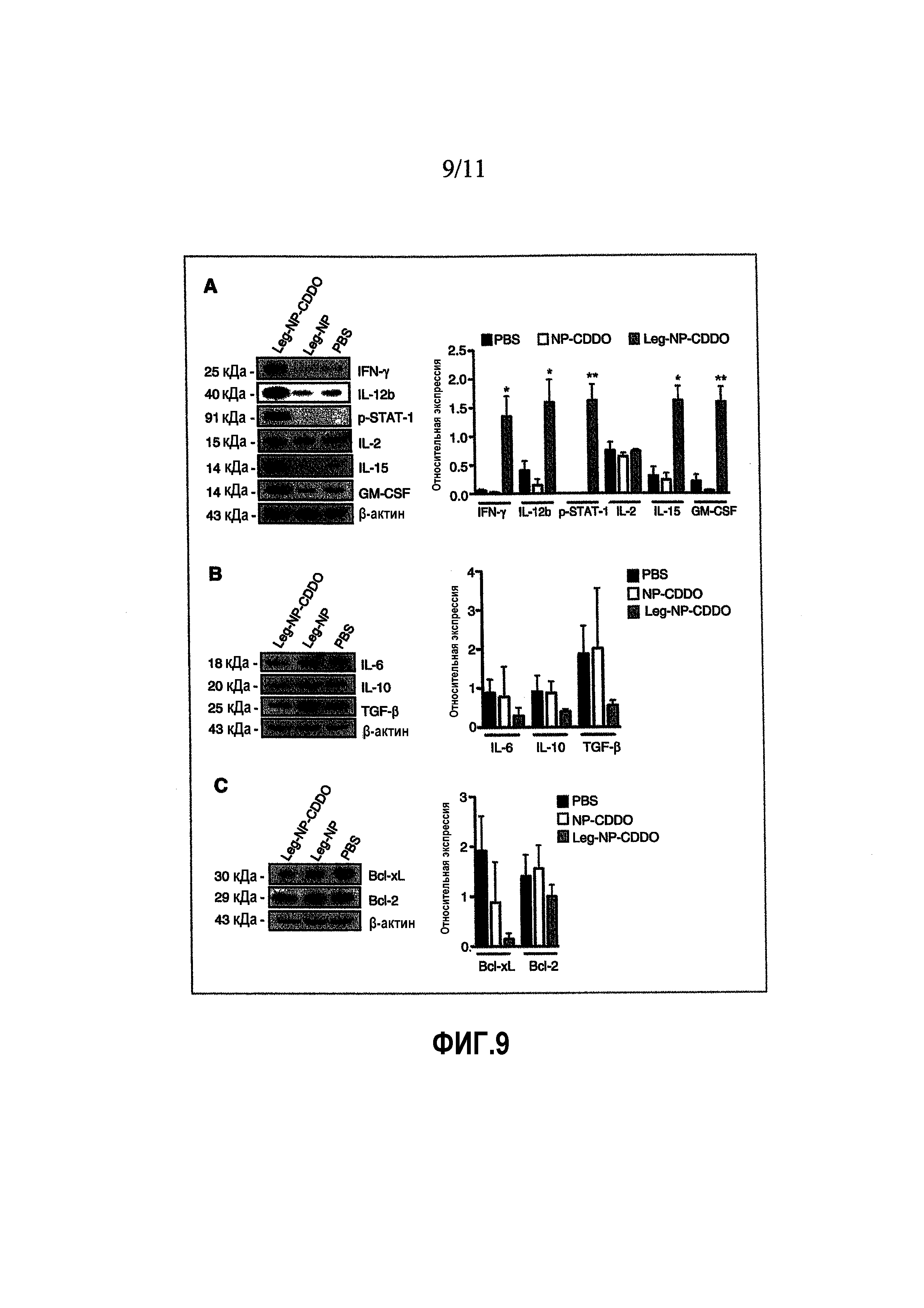
ФИГ.9. Leg-NP-CDDO модулирует профили экспрессии цитокинов и факторов роста опухолей in vivo. Экстракты цельной ткани получали из первичных опухолей MMTV-Neu, выделенных из мышей, обработанных, как описано на ФИГ.8A. Проводили анализ Вестерн-блоттингом (левые панели) и оценивали количественно относительно актина (правые графики) для определения экспрессии белка для ассоциированных с Th1 (A) и Th2 (B) факторов роста и цитокинов. Кроме того, определяли также экспрессию антиапоптотических белков (C). Данные представляют собой среднее±s.e.m. из 3 независимых экспериментов. *p<0,05 и **p<0,005.
ФИГ.10. Терапевтическая обработка Leg-NP-CDDO модулирует инфильтрацию иммуноцитов в первичные опухоли. Мышей обрабатывали, как изображено на фигуре 8A. (A-C) Через 46 суток после заражения клетками опухоли, суспензии отдельных клеток живых первичных опухолей анализировали проточной цитометрией для детекции активированных CD8+ T-клеток (A), макрофагов (B) или дендритных клеток (C). Данные представляют собой среднее±s.e.m. (D) Макрофаги M1 идентифицировали в замороженных срезах опухолей посредством иммуногистохимии с использованием антител против F4/80 (красное окрашивание) и NOS2 (светлое окрашивание). Ядра клеток окрашивали DAPI (темное окрашивание). Масштабная линейка = 100 мкм.
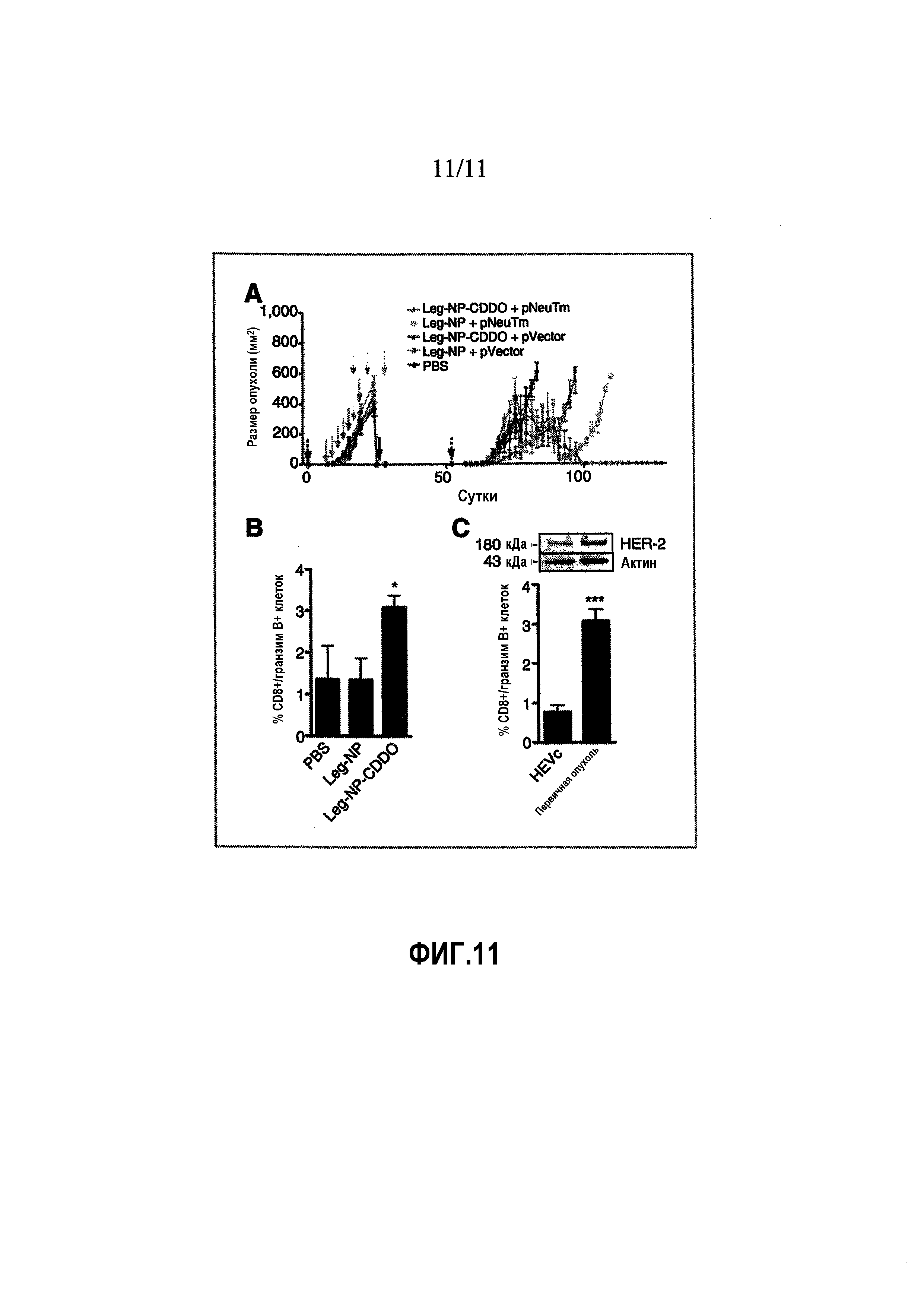
ФИГ.11. Комбинированная терапия Leg-NP-CDDO и pNeuTm усиливает противоопухолевый иммунологический надзор и предотвращает рецидив рака молочной железы. (A) Схема расписания обработки для исследования рецидивов опухолей. Мышей заражали ортотопически клетками первичной опухоли MMTV-Neu (сутки 0, черная пунктирная стрелка), обрабатывали Leg-NP-CDDO или контрольными NP (серые сплошные стрелки) и вакцинировали pNeuTm или pVector (серые пунктирные стрелки). Первичные опухоли хирургически удаляли после достижения размера ~500 мм3 (черная сплошная стрелка). Через четыре недели мышей повторно заражали в жировое тело контралатеральной молочной железы клетками первичной опухоли MMTV-Neu (сутки 53, черная пунктирная стрелка). Определяли измерения опухолей и использовали для расчета размера опухоли (n=5 мышей/группу). Данные представляют собой среднее±s.e.m. (B) Мышей умерщвляли, когда вторичные опухоли достигали объема 500 мм3. Мышей без опухолей умерщвляли через 128 суток после исходного заражения клетками опухоли. Спленоциты от вакцинированных pNeuTm мышей, обработанных PBS, Leg-NP или Leg-NP-CDDO, культивировали с облученными клетками первичных опухолей MMTV-Neu и анализировали проточной цитометрией. Данные представляют собой среднее±s.e.m. *p<0,05. (C) Спленоциты от обработанных Leg-NP-CDDO/pNeuTM мышей культивировали с облученными клетками первичных опухолей HEVc или MMTV-Neu и анализировали проточной цитометрией. Экспрессию белка HER-2 подтверждали Вестерн-блоттингом. Данные представляют собой среднее±s.e.m. ***p<0,0005.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Настоящее изобретение относится к новому способу нацеливания NP с использованием нацеливающей группы, которая связывается с легумаином, аспарагинил-эндопептидазой. Настоящее изобретение относится к водной нацеливающей на опухоли композиции липосомных наночастиц, содержащей водную дисперсию липосомных наночастиц. Наночастицы предпочтительно инкапсулируют противораковое химиотерапевтическое средство, которое можно добавлять к предварительно сформированной липосомной композиции или можно включать в липосомы во время формирования липосом. Липосомные наночастицы содержат нацеливающий на легумаин липид, смешанный с одним или несколькими другими формирующими мицеллы или везикулы липидными материалами в форме дисперсии липосомных наночастиц, предпочтительно включающих конъюгированный с полиэтиленгликолем липид. Предпочтительная композиция липосомных наночастиц содержит (a) нацеливающий на легумаин липидный компонент, (b) цвиттер-ионный липидный компонент; (c) аминозамещенный липидный компонент; (d) нейтральный липидный компонент; и (e) конъюгированный с полиэтиленгликолем липидный компонент, например, композицию PEG-липосом. Нацеливающий на легумаин липидный компонент содержит гидрофобную липидную часть, ковалентно присоединенную к связывающей легумаин группе.
Связывающая легумаин группа может представлять собой любой материал, который избирательно образует стабильный комплекс или ковалентную связь с легумаином, например, необратимые ингибиторы легумаина, которые, как правило, содержат пептидный каркас с аффинностью к легумаину, такой как Ala-Ala-Asn (или Ala-Ala-X, где X представляет собой модифицированный остаток Asn, такой как аза-Asn), присоединенный к реакционноспособной функциональной группе, например, аза-Asn-галометилкетоны, аза-Asn-эпоксиды и аза-Asn акцепторы Михаэля, содержащие α,β-ненасыщенную карбонильную группу в качестве акцептора Михаэля. Такие аза-Asn группы вступают в реакцию с остатком цистеина в активном участке легумаина с образованием ковалентной сульфидной связи между ингибитором и легумаином, например, как показано на ФИГ.4.
Упомянутая нацеливающая группа представлена формулой (I):

которая представляет собой синтетический аза-пептидный ингибитор легумаина типа акцептора Михаэля, содержащий два остатка аланина, присоединенные к модифицированной группе аза-Asn, которая включает электронодефицитную двойную связь, действующую как акцептор Михаэля для остатка цистеина в активном участке легумаина. Формула (I) представляет реакционноспособную часть ингибитора легумаина типа аза-Asn акцептора Михаэля, известного как RR-11a:

в которой сукцинимидилокси-группа RR-11a заменена на фосфолипид. Для удобства, структуру формулы (I) обозначают в настоящем документе как RR-11a в ссылках на нацеливающие на легумаин липидные материалы.
Предпочтительный нацеливающий на легумаин липид содержит соединение формулы (II):

Экспрессией легумаина на поверхности клеток управляет гипоксический стресс, отличительный признак солидных опухолей, и для покрытых полиэтиленгликолем (PEG) липосом с присоединенной нацеливающей на легумаин группой, такой как RR-11a, показаны высокая аффинность лиганд-рецептор, поглощение и превосходное проникновение в опухоли. Противораковое химиотерапевтическое средство, такое как доксорубицин, доставляемый посредством композиции конъюгированных с RR-11a PEG-липосом по изобретению, приводит к значительно улучшенной избирательности для опухолей, уменьшенной чувствительности к лекарственному средству и исключенной системной токсичности лекарственного средства.
Часть носителя наночастиц (NP) из нацеленных липосомных композиций по настоящему изобретению предпочтительно содержит мембранный липид, такой как везикула или другая мембранная структура, например, липосома или мицелла, способная инкапсулировать противораковое химиотерапевтическое средство, такое как доксорубицин. Предпочтительные NP содержат материал, обладающий гидрофобной липидной частью и гидрофильной частью, расположенными так, что липосомы или мицеллы образуются, когда материал диспергируют в водной системе. ФИГ.1, панель (a) иллюстрирует один из предпочтительных мембранных липидных материалов (1,2-диолеоил-sn-глицеро-3-фосфоэтаноламин, DOPE). Термин «липид» относится к любому производному жирной кислоты, способному формировать бислой или мицеллу, так что гидрофобная часть липидного материала ориентирована к бислою, в то время как гидрофильная часть ориентирована к водной фазе. Гидрофильные характеристики происходят от присутствия фосфата, фосфоната, карбоксилата, сульфата, сульфоната, сульфгидрила, амино, нитро, гидроксила или других подобных групп, которые хорошо известны в данной области. Гидрофобность можно придавать включением групп, которые включают в себя, но без ограничения, насыщенные и ненасыщенные алифатические углеводородные группы с длинной цепью из вплоть до 20 атомов углерода, и такие группы, замещенные одной или несколькими арильными, гетероарильными, циклоалкильными и/или гетероциклическими группой(-ами). Предпочтительными липидами являются фосфоглицериды и сфинголипиды. Репрезентативные примеры фосфоглицеридов включают в себя фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин, фосфатидилинозитол, фосфатидную кислоту, пальмитоилолеоил, фосфатидилхолин, лизофосфатидилхолин, лизофосфатидилэтаноламин, дипальмитоилфосфатидилхолин, диолеоилфосфатидилхолин, дистеароилфосфатидилхолин и дилинолеоилфосфатидилхолин. Соединения, в которых отсутствуют содержащие фосфор группы, такие как семейства сфинголипидов и гликосфинголипидов, также входят в группу, обозначенную как липид. Кроме того, амфипатические липиды, описанные выше, можно смешивать с другими липидами, включая триглицериды и стеролы.
Ингибитор легумаина/нацеливающее на опухоли средство можно присоединять к липосомным наночастицам в любом подходящем положении, например, на конце линейной цепи или в любом ее промежуточном положении, пока присоединение не мешает связыванию нацеливающего на опухоли средства к опухоли, экспрессирующей легумаин. Нацеливающее на опухоли средство может также включать необязательную двухвалентную мостиковую группу, или его можно снабжать необязательной двухвалентной мостиковой группой для облегчения присоединения к наночастицам, если желательно.
Композиции по настоящему изобретению могут преимущественно инкапсулировать любое противораковое химиотерапевтическое средство (например, противоопухолевое средство) для нацеленной доставки к экспрессирующим легумаин опухолям. Такие химиотерапевтические средства описаны, например, в Imai and Takaoka, Nat. Rev. Cancer 6, 714-726 (2006), полное содержание которого приведено в настоящем документе в качестве ссылки. Такие химиотерапевтические средства включают в себя в качестве неограничивающих примеров: алкилирующие средства (например, цисплатин; карбоплатин; оксалиплатин; мехлорэтамин; циклофосфамид; хлорамбуцил; ифосфамид); производные и аналоги пурина и пиримидина (например, 5-фторурацил; флоксуридин; арабинозид цитозина; меркаптопурин; тиогуанин; азатиоприн; флударабин; пентостатин; кладрибин); ингибиторы топоизомеразы (например, этопозид; фосфат этопозида; тенипозид; амсакрин); таксаны (например, паклитаксел); антифолаты (например, метотрексат; триметоприм, пириметамин; пеметрексед); ингибиторы ангиогенеза (например, витаксин; анекорват, ангиостатин; эндостатин; свкаламин; антиангиогенные фрагменты триптофанил-т-РНК-синтетазы, такие как T2-TrpRS); противоопухолевые моноклональные антитела (например, бевацизумаб; тивозаниб; вандетаниб; ваталаниб; алемтузумаб; цетуксимаб; гемтузумаб; ибритумомаб; панитумумаб; ритуксимаб; тозитумомаб; трастузумаб); и другие антинеопластические или химиотерапевтические средства, такие как цитотоксические антибиотики (например, актиномицин; блеомицин; пликамицин; митомицин); антрациклиновые антибиотики (например, доксорубицин; эпирубицин; даунорубицин; валрубицин; идарубицин); ингибиторы тритерпеноида Stat3 (например, урсоловая кислота; 2-циано-3,12-диоксоолеана-1,9-диен-28-овый сложный эфир; 2-циано-3,12-диоксоолеана-1,9-диен-28-овый амид, такой как 1-[2-циано-3,12-диоксоолеана-1,9(11)-диен-28-оил]имидазол (известный также как DDO-Im)); и т.п., а также их физиологически приемлемые соли и пролекарства.
В некоторых предпочтительных вариантах осуществления химиотерапевтическое средство представляет собой противоопухолевое средство, такое как агонист или антагонист рецептора или лиганд рецептора, вовлеченный в рост опухоли.
Режимы дозирования для комплексов нацеленная липосома/химиотерапевтическое средство или содержащих их композиций основаны на нескольких факторах, таких как возраст, масса, пол и тип медицинского состояния пациента, тяжесть состояния, способ введения и активность связывания конкретной используемой нацеливающей молекулы. Режим дозирования можно менять в зависимости от вышеупомянутых факторов. Уровни дозирования порядка от приблизительно 0,01 миллиграмм до приблизительно 1000 миллиграмм на килограмм массы тела являются пригодными для лечения вышеупомянутых медицинских состояний. Предпочтительные уровни дозирования лежат в диапазоне от приблизительно 0,01 миллиграмм до приблизительно 100 миллиграмм на килограмм массы тела.
Для введения посредством инъекции комплекс нацеленная липосома/химиотерапевтическое средство или содержащую его композицию, воплощающие настоящее изобретение, составляют с фармацевтически приемлемым носителем, таким как вода, солевой раствор или водный раствор декстрозы. Для инъекции типичная ежесуточная доза составляет от приблизительно 0,01 милиграмм до приблизительно 100 милиграмм на килограмм массы тела, инъецированных ежесуточно в форме однократной дозы или в форме множественных доз в зависимости от вышеупомянутых факторов.
Следующие неограничивающие примеры дополнительно иллюстрируют конкретные аспекты настоящего изобретения.
ПРИМЕР 1: Составление и характеризация нацеленных на легумаин наночастиц
Композиции наночастиц. Синтез R-11a описан в литературе. См., например, Ekici, O.D., et al. Aza-peptide Michael acceptors: a new class of inhibitors specific for caspases and other clan CD cysteine proteases. J Med Chem 47, 1889-1892 (2004) или Ovat, A., et al. Aza-peptidyl Michael acceptor and epoxide inhibitors-potent and selective inhibitors of Schistosoma mansoni and Ixodes ricinus legumains (asparaginyl endopeptidases). J Med Chem 52, 7192-7210 (2009). Все фосфолипиды (Avanti Polar Lipids) растворяли в хлороформе. Для достижения нацеливания конец карбоновой кислоты аза-пептида модифицировали активацией этой группы гидрохлоридом 1-(3-диментиламинопропил)-3-этилкарбодимида (EDC) с последующей реакцией с N-гидроксисукцинамидом для получения NHS-сложного эфира. RR-11a синтезировали в WuXi AppTec Co. Ltd. Во-первых, получали конъюгированные с RR-11a NP, реакцией RR-11a с 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламином (DOPE) при молярном соотношении приблизительно 1:1 в присутствии триэтиламина (TEA) в течение приблизительно 24 часов при окружающей комнатной температуре (RT). Во-вторых, полученное соединение объединяли с 1,2-ди-(9Z-октадеценоил)-sn-глицеро-3-фосфохолином (DOPC), DOPE, холестерином и 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламин-N-[метокси(полиэтиленгликолем)-2000] (DOPE-PEG) при молярном соотношении приблизительно 1,1:6,7:6,7:2,2:1, как описано ранее для другой липосомной системы. См.: Hood, J.D., et al. Tumor regression by targeted gene delivery to the neovasculature. Science 296, 2404-2407 (2002). Распределение размеров определяли динамическим световым рассеянием на анализаторе светового рассеяния ZETASIZER NANO® (Malvern).
Загрузка доксорубицина в наночастицы. Доксорубицин загружали в NP следующим образом. Кратко, липидную пленку регидратировали в приблизительно 1 мл стерильного буфера фосфата аммония (300 мМ, pH 7,4) и перемешивали в течение минимум приблизительно 1 часа с последующей обработкой ультразвуком для получения SUV. Внешний буфер фосфат аммония заменяли на PBS (pH 7,4) посредством гель-фильтрационной хроматографии на колонках NAP-10 (GE Healthcare). Затем добавляли доксорубицин в воде в форме 10 мМ раствора, и смесь инкубировали в течение ночи при RT. Наконец, липосомы с включенным доксорубицином очищали посредством гель-фильтрационной хроматографии с помощью колонок NAP-10 с использованием буфера PBS (pH 7,4) в качестве элюента. Композицию конъюгированных с RR-11a липосомных NP, нагруженных доксорубицином, обозначили RDZ-218.
Конъюгации RR-11a с DOPE достигали, сначала модифицируя конец карбоновой кислоты аза-пептида посредством активации этой группы гидрохлоридом 1-(3-диметиламинопропил)-3-этилкарбодимида (EDC), с последующей реакцией с N-гидроксисукцинамидом для получения сложного эфира NHS и присоединения к аминогруппе DOPE в хлороформе, с использованием триэтиламина в качестве катализатора; см. ФИГ.1, панель (a). Гипоксию опухоли детектировали окрашиванием с помощью антитела Glut-1 и визуализировали с использованием конъюгированного с флуоресцеином вторичного антитела. Ядра клеток визуализировали окрашиванием DAPI. Масштабные линейки, 100 мкм; см. ФИГ.1, панель (b). Аффинность mAb против легумаина мыши для экспрессированного на мембране клеток легумаина определяли анализом Скэтчарда; см. ФИГ.1, панель (c). Средняя рассчитанная Kd для контрольных и обработанных CoCl2 клеток составляла приблизительно 1,107±0,232 нМ и приблизительно 1,208±0,107 нМ, соответственно. Рассчитанное количество участков связывания для контрольных и обработанных CoCl2 составляло приблизительно 46760 и приблизительно 117800 участков/клетку, соответственно. NP составляли в присутствии липида с DOPE-родамином B, обладающего красной флуореценцией. Клетки карциномы молочной железы 4T1 и 4TO7 и карциномы ободочной кишки CT26 мыши культивировали в течение приблизительно 24 часов с приблизительно 100 мкМ CoCl2, после чего к клеткам добавляли RR-11a- (не нацеленные) или RR-11a+ (нацеленные) NP; см. ФИГ.1, панель (d). После указанных периодов времени NP удаляли, и немедленно получали изображения клеток с использованием флуоресцентной микроскопии, и количественно оценивали процент положительных по родамину B клеток; n=3 лунки на группу. Данные представляют собой среднее±s.e.m. Самкам мышей BALB/c с прижившимися ортотопическими опухолями молочной железы 4T1 один раз инъецировали не нацеленные или нацеленные NP. Мышей умерщвляли через приблизительно 24 часа, и органы анализировали флуоресцентной микроскопией для визуализации распределения NP, как показано по флуоресценции родамина B; n=2 мыши на группу; масштабные линейки, 100 мкм; см. ФИГ.1, панель (e).
ПРИМЕР 2: Нацеливание на легумаин усиливает поглощение инкапсулированного в PEG-липосомы доксорубицина и улучшает опосредованную NP доставку лекарственного средства к первичным опухолям молочной железы
Животные и линии клеток. Самок мышей BALB/c закупали из отдела разведения грызунов The Scripps Research Institute. Все эксперименты на животных проводили согласно Руководству NIH по содержанию и использованию лабораторных животных и с одобрения Комитета по содержанию животных The Scripps Research Institute. Линии клеток карциномы молочной железы мыши 4T1 и 4TO7 предоставлены Suzanne Ostrand-Rosenberg (University of Maryland, College Park, Maryland, USA). Клетки карциномы ободочной кишки мыши CT26 закупали из ATCC.
Исследование связывания и анализ Скэтчарда. Антитело против легумаина мыши (приблизительно 40 мкг) (R&D Systems) инкубировали в течение приблизительно 30 минут (мин) на льду с приблизительно 0,5 мкКи125I (Amersham) в полистироловых пробирках, покрытых приблизительно 100 мкг реагента IODO-GEN® (Pierce Chemical Co.). Не включенный125I удаляли гель-фильтрацией на колонках PD-10 (GE Healthcare). Клетки 4T1 (5×105) культивировали в присутствии или в отсутствие 100 мкМ CoCl2 в течение приблизительно 24 часов (час), с последующей инкубацией с приблизительно 14 нМ серийно разведенного125I-меченного антитела в течение приблизительно 2 часов при приблизительно 4 мкКи. Клетки промывали три раза PBS, содержащим 1% бычий сывороточный альбумин (BSA), и количество связанной радиоактивной метки определяли в α-сцинцилляционном счетчике. Соответствующее количество импульсов в минуту (CPM) использовали для анализа графика Скэтчарда с помощью программного обеспечения PRISM® (GraphPad) и использовали для расчета количества участков связывания легумаина.
Поглощение наночастиц in vitro. Клетки опухолей рассевали при приблизительно 0,3×106 клеток/лунку в 6-луночный планшет. Приблизительно за 24 часа до добавления NP клетки обрабатывали 100 мкМ хлоридом кобальта для стимуляции гипоксии. Конъюгированные с RR-11a или свободные от RR-11a NP, либо пустые, либо нагруженные 0,2 нМ доксорубицином (Sigma), добавляли к клеткам и инкубировали в течение приблизительно 15 и 30 мин или приблизительно 1, 2, 3, 4 и 6 часов, после чего эти клетки промывали PBS и фиксировали 10% цинк-формалином (Fisher Scientific) и немедленно анализировали флуоресцентной микроскопией для визуализации поглощения доксорубицина. Для анализа проточной цитометрией, клетки обрабатывали трипсином после удаления NP, ресуспендировали в буфере FACS и немедленно анализировали среднюю интенсивность флуоресценции.
Анализ биораспределения. Мышам, несущим ортотопические опухоли 4TO7 размером приблизительно 500 мм3, инъецировали i.v. однократной дозой конъюгированных с RR-11a NP (RR-11a+) или свободных от RR-11a NP (RR-11a-), меченных родамином B. Альтернативно, мышам инъецировали три раза с интервалами приблизительно 48 часов RDZ-218, NP-Dox, свободный Dox или PBS. Через 24 часа после последней обработки животных умерщвляли и селезенку, почки, легкие, печень, сердце и опухоль собирали, замораживали в соединении OCT (Tissue-Tek) и немедленно нарезали и получали изображения посредством флуоресцентной микроскопии.
Статистический анализ. Статистическую значимость обнаруженных различий между экспериментальными группами и контролем определяли по 2-стороннему t-критерию Стьюдента с использованием программного обеспечения PRISM® (GraphPad). Обнаружения считали значимыми при <0,05.
Доксорубицин загружали в RR-11a+ NP с использованием градиента фосфата для получения RDZ-218. Доксорубицин также загружали в RR-11a- NP (NP-Dox) в качестве контроля. Как проиллюстрировано на ФИГ.2, панель (a), клетки 4T1 и 4TO7 культивировали с CoCl2 в течение приблизительно 24 часов и затем инкубировали с RDZ-218, NP-Dox или свободным Dox в течение указанных периодов времени, с последующим анализом проточной цитометрией для определения средней интенсивности флуоресценции (MFI) доксорубицина; n=3 лунки на группу для каждой временной точки. Данные представляют собой среднее±s.e.m. Процент поглощенной концентрации лекарственного средства определяли сравнением обработанных MFI RDZ-218, NP-Dox и свободным Dox-клеток с клетками, обработанными серийно разведенным доксорубицином; см. ФИГ.2, панель (b). Относительный процент мертвых клеток 4T1 и 4TO7 приблизительно через 24 часа после обработки RDZ-218, NP-Dox, свободным Dox, свободным RR-11a или пустыми RR-11a+ NP (NP-RR-11a) определяли анализом графика прямого и бокового рассеяния при проточной цитометрии; см. ФИГ.2, панель (c). Данные показаны относительно необработанных клеток (контроль); n=3 лунки на группу. Данные представляют собой среднее±s.e.m. *p<0,05, **p<0,005. Клетки 4TO7 инъецировали в жировое тело паховой молочной железы самок мышей BALB/c. Опухолям позволяли приживаться в течение приблизительно 5 суток, до размера приблизительно 500 мм3, после чего мышам вводили две i.v. инъекции RDZ-218, NP-Dox или свободного Dox. Мышей умерщвляли приблизительно через 24 часа после последней инъекции, и ткани выделяли и немедленно анализировали флуоресцентной микроскопией для детекции распределения доксорубицина; см. ФИГ.2, панель (d). Срезы тканей также окрашивали DAPI для визуализации ядер клеток; n=2 мыши на группу; масштабные линейки, 100 мкм.
ПРИМЕР 3: Терапевтическая обработка мышей RDZ-218 приводит к полной супрессии роста первичной опухоли молочной железы без токсичности
В жировое тело грудных молочных желез самок мышей BALB/c инъецировали приблизительно 1×105 клеток 4TO7. Через 7 суток после заражения клетками опухоли мышам вводили 5 i.v. инъекций, с интервалами 3 суток, RDZ-218, NP-Dox, свободного Dox (все при приблизительно 1 мг/кг Dox) или солевого раствора. Измерения опухоли определяли с помощью микроштангенциркулей на каждые сутки обработки и использовали для расчета размера опухоли. Мышей умерщвляли приблизительно через 24 часа после последней обработки. Определяли массы как тела, так и опухолей, и ткани подвергали гистологическому анализу. Окрашивание TUNEL (Promega) проводили согласно протоколу производителя.
Самкам мышей BALB/c инъецировали ортотопически клетки опухолей 4TO7, и опухолям позволяли приживаться в течение приблизительно 7 суток перед обработкой. Мышам вводили 5 i.v. инъекций RDZ-218, NP-Dox, свободного доксорубицина (свободного Dox), пустых RR-11a+ NP (NP-RR-11a) или солевого раствора (PBS) с 3-суточными интервалами. Точки данных представляют сутки обработки; n=5 мышей на группу. На каждые сутки обработки измерения опухоли определяли с помощью микроштангенциркулей и использовали для расчета размера опухоли; см. ФИГ.3, панель (a). Данные представляют собой среднее±s.e.m. Мышей умерщвляли приблизительно через одни сутки после 5-й инъекции, и получали изображения первичных опухолей до иссечения; см. ФИГ.3, панель (b). Изображения являются репрезентативными для каждой группы. Измеряли также массу первичных опухолей во влажном состоянии; см. ФИГ.3, панель (c). Данные представляют собой среднее±s.e.m; *p<0,05. Срезы опухолей окрашивали с помощью TUNEL для визуализации и количественного определения процента апоптотических клеток опухолей; n=5 полей на срез; см. ФИГ.3, панель (d). Данные представляют собой среднее±s.e.m; ***p<0,0005. Массу первичной опухоли вычитали из общей массы тела на время умерщвления и сравнивали с массой тела до заражения клетками опухоли для определения изменения массы тела; см. ФИГ.3, панель (e). Данные представляют собой среднее±s.e.m. Контрольные группы сравнивали с обработанной RDZ-218 группой, **p=0,0029, ***p<0,001.
ПРИМЕР 4: Оценка токсичности
Самкам мышей BALB/c, несущих ортотопические опухоли 4TO7 размером приблизительно 500 мм3 вводили 5 последовательных i.v. инъекций свободного доксорубицина, NP-Dox или RDZ-218 с приблизительно 24-часовыми интервалами. Доза доксорубицина для всех групп составляла 5 мг/кг.
Для RDZ-218 не показали токсичности in vivo, в отличие от свободного и инкапсулированного в PEG-липосомы доксорубицина из предшествующей области техники. Самкам мышей BALB/c инъецировали ортотопически клетки опухоли молочной железы 4TO7. Опухолям позволяли приживаться и достигать размера приблизительно 500 мм3 до обработки. Мышам вводили 5 i.v. инъекций свободного доксорубицина (свободного Dox), нативного (NP-dox) или инкапсулированного в RR-11a+ PEG-липосомы доксорубицина (RDZ-218). Доксорубицин вводили при приблизительно 5 мг/кг в 200 мкл PBS для всех групп; n=5 мышей на группу. Результаты показаны в таблице 1; фракции представляют количество выживших мышей, всего из 5, после каждой обработки.
Обсуждение
Настоящее изобретение относится к нацеливанию с помощью лигандов посредством конъюгирования PEG-липосомных NP с низкомолекулярным (451 M.W.) ингибитором легумаина, RR-11a, из класса ингибиторов - аза-Asn акцепторов Михаэля; см. ФИГ.1, панель (a). RR-11a разработан со специфическими для семейства CD последовательностями и таким образом, является высоко специфическим для семейства протеаз CD, таких как легумаин, которые он ингибирует необратимо при значениях IC50 в наномолярном диапазоне (IC50=31-55 нМ). Важно, что RR-11a не взаимодействует с другими родственными протеазами, включая каспазы, клострипаин или гингипаин K, и является устойчивым к расщеплению протеазами in vivo. Механизм ингибирования легумаина посредством RR-11a включает в себя нуклеофильную атаку каталитического остатка цистеина на двойную связь акцептора Михаэля на C2, образующую ковалентную связь, которая необратимо ингибирует эту аспарагинил-эндопептидазу; см. ФИГ.4, панель (a). При использовании композиции по настоящему изобретению ковалентно связывают присоединенные к RR-11a NP с легумаином, что приводит в результате к присоединению целого липосомного композита к рецептору и последующей необратимой интернализации. Этот предположительный механизм поддержан исследованиями ЯМР и является существенным, поскольку высокая аффинность связывания может улучшать нацеливание NP. Присоединения RR-11a к компоненту 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламина (DOPE) NP достигали реакцией с триэтиламином (TEA), как подробно описано в разделе "Материал и методы"; см. ФИГ.1, панель (a). Анализ PEG-липосомных NP с присоединенным RR-11a (RR-11a+) или нативных PEG-липосомных (RR-11a-) NP посредством динамического светового рассеяния выявил однородное распределение размеров приблизительно 150 и 110 нм, соответственно (данные не представлены).
Легумаин предоставляет отличный инструмент для нацеливания на опухоли, поскольку он является высоко консервативным между видами, с приблизительно 83% гомологией между белком легумаином человека и мыши, и является сверхэкспрессированным в большинстве солидных опухолей человека. Соответственно, анализом Вестерн-блоттингом верифицировали экспрессию белка легумаина во многих линиях клеток карциномы мыши и в первичной опухоли молочной железы мыши, таким образом, подтверждая предшествующие публикации. Хотя внутриклеточный легумаин экспрессируется повсеместно, экспрессия легумаина на поверхности клеток возникает в ответ на индуцированный микроокружением клеточный стресс, такой как голодание по сыворотке. Важно, что экспрессию легумаина на поверхности клеток усиливает гипоксический стресс, отличительный признак солидных опухолей, который присутствует в ортотопической модели рака молочной железы на мышах авторов настоящего изобретения, как определено по экспрессии опухолями Glut-1, установленного белка, поддающегося индукции гипоксией; см. ФИГ.1, панель (b). Более того, иммуногистохимические анализы in vitro многих линий клеток карциномы мыши показали, что гипоксический стресс индуцировал экспрессию легумаина на поверхности клеток (данные не представлены).
Эффективность нацеливания с помощью лигандов зависит, частично, от содержания рецептора-мишени, и ее максимизируют посредством его сверхэкспрессии на клетках-мишенях по сравнению с нормальными клетками. Таким образом, ограничением нацеливания с помощью лигандов является количество рецепторов поверхности клеток-мишеней, которое определяет количество молекул нацеливающего соединения, которое может специфически связываться с участком опухоли. Таким образом, авторы настоящего изобретения количественно оценивали количество участков связывания легумаина на клетку опухоли посредством исследований связывания и анализа графика Скэтчарда с использованием125I-меченного антитела против легумаина. Авторы настоящего изобретения рассчитали, что при нормальном давлении кислорода количество участков связывания легумаина составляло приблизительно 46760, а в условиях гипоксии количество увеличивалось до приблизительно 117800 участков/клетку; см. ФИГ.1, панель (c). Тот факт, что гипоксия индуцировала приблизительно 3-кратное увеличение количества участков связывания легумаина на поверхности клеток опухоли, является биологически существенным, поскольку гипоксия является отличительным признаком микроокружения солидных опухолей, и таким образом, освобождает систему нацеливания от зависимости от любой отдельной генетической характеристики опухоли. Таким образом, способ нацеливания, описанный в настоящем документе, не должен являться ограниченным генетической гетерогенностью, обычно наблюдаемой в солидных опухолях.
Для оценки степени, до которой присоединение RR-11a усиливает поглощение PEG-липосомных NP клетками опухолей in vitro, клетки карциномы молочной железы (4T1 и 4TO7) и карциномы ободочной кишки (CT26) мыши подвергали гипоксическому стрессу, инкубировали в различных временных точках с RR-11a+ или RR-11a- NP, меченными флуоресцентным красителем родамином B. Анализ флуоресцентной микроскопией выявил заметно усиленное поглощение RR-11a+ NP, по сравнению с RR-11a- NP, во всех трех линиях клеток во всех тестированных временных точках; см. ФИГ.1, панель (d). Эффективность нацеливания in vivo определяли посредством i.v. инъекции тех же самых частиц самкам мышей BALB/c, несущих ортотопические опухоли молочной железы 4T1 размером приблизительно 500 мм3. Флуоресцентная микроскопия опухоли и тканей от этих животных выявила заметное увеличение хоминга RR-11a+ NP в первичные опухоли и уменьшение неспецифического накопления в органах ретикулоэндотелиальной системы (RES), включая печень, селезенку и почку, при сравнении с RR-11a- NP; см. ФИГ.1, панель (e). Неожиданно, заметное уменьшение накопления RR-11a+ NP, наблюдаемое в печени, является значимым, поскольку этот орган RES идентифицирован как основное место накопления не нацеленных PEG-липосомных NP, что может приводить к токсичности для печени. Вместе, эти неожиданные данные показывают, что присоединение RR-11a к PEG-липосомным NP усиливает их поглощение клетками опухолей при гипоксическом стрессе и эффективно увеличивает хоминг NP в первичные опухоли при пониженном накоплении в органах RES.
Важным фактором для эффективной опосредованной лигандом доставки лекарственного средства с помощью NP является не только их способность нести оптимальную полезную загрузку к желательной клетке-мишени, но также эффективно высвобождать эту полезную загрузку после доставки. Для критической оценки этих параметров, доксорубицин, химиотерапевтическое лекарственное средство, общеупотребительное для лечения рака молочной железы, загружали в NP посредством градиента фосфата аммония, как описано ранее. Затем клетки опухолей молочной железы мыши (4T1 и 4TO7) при гипоксическом стрессе инкубировали со свободным доксорубицином (свободный Dox) или нагруженными доксорубицином RR-11a- (NP-Dox), или RR-11a+ (RDZ-218) NP в различных временных точках и анализировали немедленно проточной цитометрией для количественной оценки средней интенсивности флуоресценции (MFI) доксорубицина, интернализованного клетками. Для обработанных RDZ-218 клеток показали усиленное поглощение доксорубицина при сравнении с клетками, обработанными NP-Dox; см. ФИГ.2, панель (a). Неожиданно, обработка RDZ-218 не только приводила к более быстрому поглощению лекарственного средства с течением времени по сравнению с NP-Dox, но также увеличивала степень поглощения настолько сильно, как приблизительно в 16 раз, при скорости поглощения RDZ-218, сходной со скоростью поглощения свободного Dox; см. ФИГ.2, панель (a). При сравнении MFI, вырабатываемой клетками, обработанными серийно разведенным свободным доксорубицином с MFI клеток, обработанным инкапсулированным в NP доксорубицином, авторы настоящего изобретения неожиданно обнаружили, что около 100% RDZ-218 NP было поглощено клетками в пределах приблизительно 4 часов обработки; см. ФИГ.2, панель (b). Более того, немедленное и быстрое поглощение RDZ-218, по сравнению со свободным Dox, являлось показателем опосредованной лигандом-рецептором интернализации, и являлось превосходным по сравнению с не нацеленным NP-Dox.
Затем биоактивность доксорубицина из RDZ-218 определяли in vitro с помощью проточной цитометрии посредством сравнения процентов мертвых клеток опухолей приблизительно через 24 часа после обработки; см. ФИГ.2, панель (c). Для клеток, обработанных RDZ-218, показали 3-15-кратное увеличение процента мертвых клеток по сравнению с контрольными или обработанными NP-Dox клетками. Интересно, что этот цитотоксический эффект RDZ-218 был лучше эффекта свободного Dox. Важно, что цитотоксического эффекта не обнаружили в клетках, обработанных свободным RR-11a или пустыми RR-11a+ NP, что указывает на то, что усиленная цитотоксичность, наблюдаемая для RDZ-218, обусловлена увеличенным опосредованным NP поглощением доксорубицина, а не какими-либо эффектами ингибирования легумаина посредством RR-11a на клетках опухолей. Вместе, эти результаты показывают, что RDZ-218 усиливает доставку полезной загрузки биологически эффективного лекарственного средства к клеткам опухолей in vitro.
Основной терапевтической целью нацеленной с помощью лиганда доставки NP является минимизация нежелательной системной токсичности лекарственного средства, возникающей из-за неспецифического накопления NP в органах RES, с сохранением в то же время способности к доставке биологически эффективной дозы лекарственного средства к клеткам-мишеням. Однако, одним из опасений при использовании NP для доставки лекарственного средства является то, что NP являются относительно более крупными, чем молекулы лекарственного средства, и таким образом, с меньшей вероятностью могут проникать через стенки сосудов и получать доступ к клеткам опухолей по сравнению с низкомолекулярными лекарственными средствами или антителами. Таким образом, для тестирования способности RDZ-218 эффективно и специфически доставлять полезную загрузку лекарственного средства к ткани-мишени в терапевтических условиях, мышам с прижившимися опухолями молочной железы, размером приблизительно 500 мм3, вводили две i.v. инъекции RDZ-218, NP-Dox или свободного Dox с приблизительно 48-часовыми интервалами. Микроскопический анализ опухолей через приблизительно 24 часа после последней инъекции выявил интенсивную и широко распространенную флуоресценцию доксорубицина в опухолях от обработанных RDZ-218 животных; см. ФИГ.2, панель (d). В отличие от этого, флуоресценция доксорубицина являлась поразительно уменьшенной или точечной в опухолях от мышей, обработанных NP-Dox или свободным Dox; см. ФИГ.2, панель (d). Неожиданно, только для мышей, обработанных RDZ-218, показали заметно уменьшенную флуоресценцию доксорубицина в печени и сердце при сравнении с мышами, обработанными NP-Dox и свободным Dox, соответственно; см. ФИГ.2, панель (d). Уменьшение накопления доксорубицина в сердце является особенно важным, поскольку кардиотоксичность является ограничивающим дозу фактором для терапии доксорубицином. Эти результаты ясно показывают, что RDZ-218 обладает способностью проникать в опухоль, и что RR-11a+ NP могут достигать специфической доставки полезной загрузки лекарственного средства к солидным опухолям in vivo, в то же время уменьшая неспецифическое накопление лекарственного средства в периферических органах, таких как печень и сердце.
Терапевтическую эффективность полезной загрузки доксорубицина, доставляемого посредством RR-11a+ NP мышам с прижившимися опухолями молочной железы, оценивали посредством введения им 5 i.v. инъекций RDZ-218, NP-Dox, пустых RR-11a+ NP (NP-RR-11a), свободного Dox или солевого раствора с 3-суточными интервалами. Определение размера опухоли с помощью микроштангенциркулей выявило, что обработка только RDZ-218 по существу прекращала рост опухоли, в то время как в контрольных группах только задерживали рост опухоли, по сравнению с животными, обработанными солевым раствором; см. ФИГ.3, панель (a). Через три недели после заражения клетками опухоли макроскопическое исследование первичных опухолей от мышей, обработанных RDZ-218, выявило только остаточные опухолевые узлы, в то время как контрольные мыши обладали большими опухолевыми массами размером приблизительно 500 мм3 или более; см. ФИГ.3, панель (b). Обработка RDZ-218 приводила к приблизительно 8-12-кратному уменьшению массы опухоли при сравнении с контролем; см. ФИГ.3, панель (c). Соответственно, иммуногистохимический анализ TUNEL срезов опухолей от обработанных RDZ-218 мышей выявил 9-35-кратное увеличение процента апоптотических клеток при сравнении с опухолями от контрольных животных; см. ФИГ.3, панель (d). Неожиданно, для мышей, обработанных RDZ-218, не показали какой-либо потери массы тела на протяжении исследования, что является показателем уменьшенной токсичности; см. ФИГ.3, панель (3).
Для подтверждения этой уменьшенной токсичности RDZ-218, исследование токсичности проводили на несущих опухоль мышах посредством ежесуточного введения однократной дозы свободного Dox, NP-Dox или RDZ-218, при приблизительно 5 мг/кг доксорубицина для всех групп, в течение приблизительно 5 суток (Таблица 1). Только в обработанной RDZ-218 группе все животные выжили после конечной обработки на сутки 5. В отличие от этого, свободный Dox, введенный при приблизительно 5 мг/кг, являлся летальным, и все тестируемые животные в этой группе погибли немедленно после первой обработки. По сравнению с этим, в обработанной не нацеленным NP-Dox группе только одно животное выжило после завершения всех 5 обработок, где летальную токсичность наблюдали после 2-й и 3-й обработок у 4 из 5 животных. Эти неожиданные результаты подтверждают, что опосредованное R-11a нацеливание с помощью лигандов PEG-липосом снижает неспецифическое накопление доксорубицина в не являющихся мишенями органах, таким образом, исключая летальную системную токсичность.
ПРИМЕР 5: Нацеливание на легумаин инкапсулированного в NP CDDO-Im
CDDO-Im включали в NP, пользуясь преимуществом физических характеристик CDDO-Im, а именно, его гидрофобности и химического сходства с холестерином, для обеспечения спонтанного включения CDDO-Im в липидный бислой при регидратации липидной пленки. Добавление 0,6 молярного отношения CDDO-Im к DOPE:DOPC:холестерин:DOPE-PEG:DOPE-RR11a в молярных соотношениях 6,7:6,7:2,2:1:1,1, соответственно, приводило к эффективной загрузке CDDO-Im. Анализ УФ-спектрометрией свободного CDDO-Im и инкапсулированного CDDO-Im, после высвобождения посредством разрушения NP, показал загруженную концентрацию приблизительно 45 микромоль/л CDDO-Im, что является приблизительно в 450 раз более концентрированным, чем доза 100 нмоль/л, необходимая для эффективного ингибирования Stat3. Анализ NP посредством динамического светового рассеяния и TEM показал оптимальный средний диаметр NP приблизительно 100 нм и дзета-потенциал, близкий к 0 (См. ФИГ.5A-D).
ПРИМЕР 6: Оценка инкапсулированного CDDO-Im in vivo
Материалы. Подтвержденные клетки карциномы молочной железы мыши 4TO7/4T1 предоставлены Suzanne Ostrand-Rosenberg (University of Maryland, College Park, MD), и их поддерживали в среде RPMI-1640 (Gibco, Carlsbad, CA, USA), дополненной 10% FBS, 1% HEPES, 1% бикарбонатом натрия и 1% пируватом натрия. Линии клеток подтверждали по росту/метастазированию in vivo у мышей Balb/c, по экспрессии IL-6 и S100A8/A9 и по устойчивости к 6-тиогуанину. Клетки были протестированы как отрицательные по микоплазме с использованием MycoALERT (2008, Lonza, Basel, Switzerland). Первичная опухоль MMTV-Neu предоставлена Michael Karin (University of California, San Diego, CA, USA), и ее поддерживали серийным пассированием в сингенных мышах FVB/NJ. Кратко, первичные опухоли MMTV-Neu измельчали и расщепляли в стерильных условиях коллагеназой типа 3 (Worthington, Lakewood, NJ, USA) в среде RPMI-1640, дополненной 2,5% FBS и 10 мМ Hepes. 1×106 клеток ресуспендировали в PBS и инъецировали в жировое тело молочной железы сингенных самок мышей FVB/NJ. Эту процедуру повторяли, пока первичные опухоли не достигали размера приблизительно 500 мм3.
Вестерн-блоттинг. Экстракты белка получали, как описано ранее. Вестерн-блоттинг проводили со следующими антителами в качестве зондов: антитела кролика против фосфо-STAT-3 (Cell Signaling, Danvers, MA, USA), антитела козы против β-актина, IL-6 и IL-10, антитела кролика против фосфо-STAT-1, STAT-3, IL-2, Bcl-xL, Bcl-2 и TGF-β, антитела крысы против IL-12b, GM-CSF и IFN-γ, и антитела мыши против IL-15 (все Santa Cruz Biotechnology, Santa Cruz, CA, USA) и против ERBB2 (Abcam, Cambridge, MA, USA). Интенсивность полос белка оценивали количественно с использованием программного обеспечения ImageJ и нормализовали по β-актину.
Исследования опухолей in vivo. Клетки 4TO7 (5×103) или клетки первичной опухоли MMTV-Neu (1×104) инъецировали ортотопически самкам мышей BALB/c или FVB/NJ, соответственно. NP в 200 мкл PBS (приблизительно 1,36×1013 частиц) вводили i.v. и измерения опухоли определяли с использованием цифровых микроштангенциркулей. Объем опухоли рассчитывали с использованием формулы [(a2×b)/2], где 'a' представляет собой больший из двух перпендикулярных диаметров. Для исследований рецидивирования первичные опухоли хирургически удаляли, и мышей повторно заражали ортотопически в жировое тело контралатеральной молочной железы. Мышей вакцинировали 3 раза перорально с интервалами 1 неделю через зонд ослабленными salmonella typhimuirum (1×108 КОЕ на мышь), трансдуцированными либо pNeuTm (предоставленным Wei-Zen Wei, Karmanos Cancer Center, Detroit, MI, USA), либо пустым вектором.
Проточная цитометрия. Спленоциты и инфильтрирующие в опухоль лимфоциты выделяли и инкубировали (1×106 клеток на пробирку) с конъюгированными с флуоресцеином антителами (0,25 мкг антитела на 106 клеток в объеме 100 мкл) против CD8, CD25, CD14, CD11c, CD11b, CD80, CD45, F4/80 мыши (Biolegend, San Diego, CA USA) и/или гранзима B (0,125 мкг антитела на 106 клеток в объеме 100 мкл) (eBioscience, San Diego, CA, USA). Данные собирали на цифровой LSR-II (Becton Dickinson, Franklin Lakes, NJ, USA) и анализировали с помощью программного обеспечения Flow Jo (Tree Star, Inc., Ashland, OR, USA).
Иммуногистохимия. Срезы опухолей, фиксированные в ацетоне, окрашивали следующими первичными антителами: антитело крысы против F4/80 мыши (разведение 1:50, AbD Serotec, Raleigh, NC, USA) и антитело кролика против Nos2 мыши (разведение 1:50, Santa Cruz Biotechnology, Santa Cruz, CA, USA), и детектировали с помощью следующих вторичных антител: антитело козы против IgG кролика Alexa Fluor 568 или антитело козы против IgG кролика Alexa Fluor 488 (оба в разведении 1:200, Molecular Probes, Carlsbad, CA, USA) соответственно. Для контрольных окрашиваний срезы тканей инкубировали только с вторичными антителами. Ядра клеток окрашивали DAPI-дилактатом (Sigma, St. Louis, MO, USA).
CDDO-Im ингибирует активацию STAT-3 в клетках рака молочной железы мыши. Способность CDDO-Im ингибировать индуцированную IL-6 активацию STAT-3 в клетках рака молочной железы мыши оценивали посредством инкубации клеток опухоли 4T1 с IL-6 и увеличивающимися концентрациями свободного CDDO-Im. Анализ Вестерн-блоттингом выявил, что CDDO-Im блокировал фосфорилирование STAT-3 и супрессировал экспрессию тотального белка STAT-3 при концентрациях 100 нМ - 1 мкМ (ФИГ.6A). Способность инкапсулированного CDDO-Im ингибировать активацию STAT-3 подтверждали посредством инкубации стимулированных IL-6 клеток опухоли 4TO7 с пустыми нацеленными NP (Leg-NP), не нацеленными (NP-CDDO) или нацеленными (Leg-NP-CDDO) NP, нагруженными CDDO-Im, или свободным CDDO-Im. Анализ Вестерн-блоттингом показал, что инкапсулированный CDDO-Im блокировал фосфорилирование STAT-3, а также свободный CDDO-Im (ФИГ.6B). Важно, что для клеток, обработанных Leg-NP, не показали ингибирования фосфорилирования STAT-3, таким образом, демонстрируя, что ингибирование обусловлено единственно CDDO-Im, а не каким-либо неспецифическим эффектом NP (ФИГ.6B).
Наконец, тестировали способность Leg-NP доставлять полезную загрузку CDDO-Im к первичным опухолям MMTV-Neu в терапевтических условиях. С этой целью мышам, несущим ортотопические опухоли молочной железы, вводили 8 i.v. инъекций с 3-суточными интервалами солевого раствора (PBS), Leg-NP или Leg-NP-CDDO. Анализ Вестерн-блоттингом экстрактов белка первичных опухолей MMTV-Neu, полученных через одни сутки после последней инъекции, показал, что Leg-NP-CDDO эффективно ингибировал фосфорилирование STAT-3 в первичных опухолях (ФИГ.6C). Вместе эти данные показывают, что CDDO-Im ингибирует фосфорилирование STAT-3 в клетках рака молочной железы мыши. Кроме того, эта работа показывает успешную инкапсуляцию CDDO-Im в липосомные NP для нацеленной доставки к TME и эффективного терапевтического ингибирования фосфорилирования STAT-3 in vivo.
Leg-NP-CDDO супрессирует рост опухолей молочной железы мышей. Для оценки in vivo эффектов Leg-NP-CDDO, мышей BALB/c ортотопически заражали приблизительно 5×103 клеток опухоли 4TO7, и через 4 суток обрабатывали их 8 i.v. инъекциями Leg-NP-CDDO или контрольными инъекциями (ФИГ.7A). Рост первичных опухолей являлся значимо супрессированным посредством Leg-NP-CDDO по сравнению с контролем (ФИГ.7B). Важно, что обработка свободным CDDO-Im или CDDO-Im, инкапсулированным в ненацеленные частицы, являлась заметно менее эффективной для супрессии роста опухолей по сравнению с Leg-NP-CDDO. Кроме того, для мышей, обработанных Leg-NP-CDDO, показали значимое уменьшение опухолевой нагрузки по сравнению с контролем без обработки (ФИГ.7C).
Однако, по сравнению с первичными клетками опухолей, стабилизированные линии клеток опухолей, такие как 4TO7, которые находились в долгосрочной культуре ex vivo, могут приобретать генетические и фенотипические изменения, которые могут влиять на их терапевтический ответ. Таким образом, для критической оценки эффективности Leg-NP-CDDO мышей с ортотопическими опухолями, происходящими из первичных клеток MMTV-Neu, обрабатывали 8 i.v. инъекциями Leg-NP-CDDO, Leg-NP или PBS (ФИГ.8A). Расчет объемов опухолей выявил, что для мышей, обработанных Leg-NP-CDDO, показали только незначительно уменьшенный размер опухоли по сравнению с контрольными (ФИГ.8B), несмотря на значительно уменьшенную опухолевую нагрузку (ФИГ.8C). Таким образом, Leg-NP-CDDO являлся заметно менее эффективным для супрессии in vivo роста клеток первичных опухолей по сравнению с опухолями, происходящими из линий клеток 4TO7.
Leg-NP-CDDO модулирует экспрессию цитокинов и факторов роста в первичных опухолях. Передача сигнала STAT-3 опосредует опухолеассоциированную иммуносупрессию in vivo посредством модуляции экспрессии цитокинов и факторов роста клетками опухолей и другими клетками в TME, включая макрофаги. Таким образом, для оценки эффектов Leg-NP-CDDO на уровни экспрессии этих факторов, экстракты цельных клеток получали из первичных опухолей мышей, обработанных Leg-NP-CDDO, Leg-NP или PBS. Анализ Вестерн-блоттингом показал заметную повышающую регуляцию экспрессии белка pSTAT-1 (в 715 раз), IL-15 (в 37 раз), IL-12b (в 9 раз), IFN-γ (в 24 раза) и GM-CSF (в 6 раз) у мышей, обработанных Leg-NP-CDDO, по сравнению с контрольными (ФИГ.9A). И наоборот, для экспрессии белков IL-6, IL-10 и TGF-β показали 2-5-кратное уменьшение первичных опухолей у обработанных Leg-NP-CDDO мышей (ФИГ.9B). Обработка Leg-NP-CDDO также понижала экспрессию антиапоптотических белков Bcl-XL (в 8 раз) и Bcl-2 (в 1,4 раз) (ФИГ.9C). Интересно, что эти результаты указывают на Th1-поляризацию цитокинов TME как результат терапии Leg-NP-CDDO.
Увеличение количества антигенпредставляющих клеток и CD8+ T-клеток в первичных опухолях обработанных Leg-NP-CDDO мышей. Иммуноциты, рекрутированные опухолями, секретируют различные цитокины и факторы роста, в зависимости от того, получают ли они Th1- или Th2-поляризующие сигналы из TME. Таким образом, сдвиг в сторону Th1 наблюдали в экспрессии цитокинов, что позволяло предполагать, что изменения в микроокружении иммуноцитов в опухоли также могут являться очевидными. Для оценки этой гипотезы суспензии живых отдельных клеток первичных опухолей получали от мышей, обработанных Leg-NP-CDDO, Leg-NP или PBS, и анализировали проточной цитометрией для детекции активированных CD8+ T-клеток, DC и макрофагов (ФИГ.10A-C). Для мышей, обработанных NP-Leg-CDDO, показано увеличение в 4,6 раз количества CD8+/CD25+ T-клеток по сравнению с контролем с PBS (ФИГ.10A). Кроме того, для мышей, обработанных Leg-NP-CDDO, выявили 5,6- и 2-кратное увеличение количества макрофагов (CD45+/F4/80+) (ФИГ.10B) и DC (CD14+/CD11c+ и CD80+/CD11b+) (ФИГ.10C), соответственно.
Макрофаги оказывают очень различные эффекты на иммунную функцию и рост опухолей в зависимости от их способа активации и поляризации. «Классически активированные» M1 макрофаги, как правило, обладают высокой экспрессией NOS2 в сочетании с противоопухолевыми иммунными ответами. В отличие от этого, «альтернативно активированные» M2 макрофаги не экспрессируют NOS2, и как правило, ассоциированы с иммуносупрессией и проопухолевыми ответами. Таким образом, проведено исследование, соответствуют ли макрофаги в первичных опухолях обработанных Leg-NP-CDDO мышей M1 или M2. В этой связи, анализ опухолей иммуногистохимией и флуоресцентной микроскопией выявил заметное увеличение F4/80+/Nos2+ положительных клеток в опухолях, полученных от обработанных Leg-NP-CDDO мышей (ФИГ.10D), в то время как для контрольных опухолей показали сильное окрашивание F4/80+, которые являлись преимущественно NOS2- (ФИГ.10D). Эти обнаружения позволяют предполагать, что M1 поляризация инфильтрирующих опухоль макрофагов является результатом обработки Leg-NP-CDDO.
Комбинированная терапия улучшает противоопухолевые эффекты Her-2 ДНК-вакцины. Настоящие обнаружения позволяют предполагать, что обработка Leg-NP-CDDO блокирует опосредованную TME иммуносупрессию. Более того, на основании профилей экспрессии цитокинов и инфильтрации иммунных эффекторных клеток, иммунное TME, по-видимому, являлось в достаточной степени примированным для противоопухолевого ответа. Мышей FVB/NJ заражали ортотопически приблизительно 1×104 клеток первичной опухоли MMTV-Neu и обрабатывали комбинацией Leg-NP-CDDO и ДНК-вакцины против внеклеточного домена HER-2 (pNeuTM) (ФИГ.11A). Альтернативно, мышей обрабатывали также пустыми нацеленными NP (Leg-NP) или контрольной вакциной (pVector). Первичные опухоли хирургически удаляли после достижения объема 500 мм3, и после 4 недель восстановления мышей повторно заражали приблизительно 1×104 первичных клеток опухолей MMTV-Neu в жировое тело контралатеральной молочной железы для экспериментального рецидивирования. Рецидивирование опухолей было значимо супрессированным у мышей, обработанных комбинированной терапией Leg-NP-CDDO/pNeuTm, по сравнению с контрольными, и это приводило к полному отторжению опухоли у 40% (2/5) мышей (ФИГ.11A). В отличие от этого, вакцинация pNeuTm или обработка Leg-NP-CDDO по отдельности не защищали против рецидивирования опухоли. Эти результаты позволяют предполагать, что опосредованная комбинированной терапией защита против рецидивирования опухолей обусловлена Leg-NP-CDDO, который Th1-примирует иммунное TME, таким образом, улучшая противоопухолевые иммунные ответы после вакцинации pNeuTm.
Спленоциты от вакцинированных pNeuTm мышей, комбинированные с Leg-NP-CDDO, Leg-NP или PBS, культивировали с облученными клетками первичной опухоли MMTV-Neu, и их CTL ответ измеряли проточной цитометрией. Результаты показали, что вакцинированные pNeuTM мыши, обработанные Leg-NP-CDDO, обладали 2,3-кратным увеличением процента CD8+/гранзим B+ спленоцитов по сравнению с контрольными (ФИГ.11B). Кроме того, чтобы оценить, являлись ли эти бустер-ответы CTL специфическими для клеток опухоли, ответ CTL спленоцитов от обработанных Leg-NP-CDDO/pNeuTm мышей сравнивали при культивировании с клетками опухоли HER-2высокий MMTV-Neu по сравнению с эндотелиальными клетками мыши HER-2низкий HEVc (ФИГ.11C). Анализ проточной цитометрией этих спленоцитов выявил 4-кратное увеличение процента CD8+/гранзим B+ клеток в ответ на HER-2высокий клетки по сравнению с HER-2низкий клетками (ФИГ.11C), таким образом, показывая, что иммунный ответ мышей, подвергнутых комбинированной терапии, действительно являлся специфическим для антигена опухоли.
Обсуждение
Увеличение количества CD8+ T-клеток в опухолях обработанных Leg-NP-CDDO мышей коррелировало с заметным увеличением экспрессии IL-15, сильного хемоаттрактанта для T-клеток. Важно, что IL-15 стимулирует дифференцировку Th1 T-клеток и пролиферацию наивных CD8+ T-клеток человека и CD8+ T-клеток памяти человека in vitro. Важно, что эти обнаружения согласуются с наблюдением корреляции увеличенной экспрессии IL-15 в TME с улучшенной функцией CD8+ T-клеток в результате ингибирования STAT-3 с помощью Leg-NP-CDDO.
Опухолеассоциированные макрофаги (TAM) находятся среди наиболее распространенных иммуноцитов в солидных опухолях. Опосредованное TAM проопухолевое воспаление посредством высвобождения цитокинов стимулирует дальнейшее рекрутирование воспалительных клеток (24). Соответственно, авторы настоящего изобретения обнаружили уменьшение экспрессии белков IL-10 и TGF-β в первичных опухолях, где для обоих опубликована индукция стимулирующего злокачественные опухоли M2 фенотипа TAM. В отличие от этого, макрофаги, которые активированы посредством IFN-γ, обладают фенотипом, ассоциированным с разрушением опухолей. Эти M1 макрофаги характеризуются, частично, экспрессией NOS-2. Интересно, что наблюдали увеличенную инфильтрацию макрофагов NOS-2+ в первичных опухолях мышей, обработанных Leg-NP-CDDO, которая соответствует увеличенной экспрессии GM-CSF в первичных опухолях. Важно, показано, что GM-CSF индуцирует рекрутирование усиленных профессиональных антигенпредставляющих клеток, включая DC и макрофаги.
Настоящие результаты демонстрируют, что нацеленная манипуляция с иммунным TME с помощью Leg-NP-CDDO, комбинированного с ДНК-вакциной против HER-2 (pNeuTm) по существу предотвращала рецидив рака молочной железы в модели опухолей на мышах. Комбинированная терапия также значимо улучшала противоопухолевые CTL ответы CD8+ T-клеток, по сравнению с мышами, которых подвергали только монотерапии. Более того, для мышей, подвергнутых комбинированной терапии, показали усиленные ответы CTL, специфические против клеток первичных опухолей, но не HER-2- эндотелиальных клеток, таким образом, демонстрируя специфический для антигенов опухоли иммунный ответ. Важно, что комбинированная терапия задерживала рост опухолей после повторного заражения HER-2+ клетками первичных опухолей и защищала против рецидива 40% мышей. Эти результаты ясно показывают, что терапевтическая манипуляция с иммунным TME может улучшать эффективность иммунотерапии злокачественных опухолей.
Взятые вместе, результаты, описанные в настоящем документе, согласуются с обнаружениями в нескольких клинических исследованиях фазы I/II, показывающих ограниченные эффекты монотерапии цитокинами, что сильно подчеркнуло необходимость способов комбинированной терапии и специфического нацеливания множества цитокинов. Важно, что открытия в настоящем документе представляют новый способ нацеленной терапии для манипуляции с основным репертуаром иммунных цитокинов и факторов роста в TME. Важно, что посредством нацеливания иммунных манипуляций для специфических переходов Th1/Th2 в TME, можно обходить тяжелую системную токсичность многих иммуностимулирующих цитокинов, при использовании в то же время их иммуностимулирующих эффектов. Благодаря улучшению противоопухолевых эффектов противораковой вакцинной терапии и предотвращению рецидивов опухоли, Leg-NP-CDDO представляет собой потенциально пригодное терапевтическое соединение, которое может в конечном счете улучшать эффективность иммунотерапии злокачественных опухолей для увеличения продолжительности жизни и здоровья пациентов со злокачественными опухолями.
Таким образом, разработана новая нацеленная на легумаин PEG-липосомная NP, способная к высокоэффективной доставке полезной загрузки лекарственного средства к солидным опухолям in vivo. Присоединение RR-11a значительно усиливало поглощение NP клетками опухолей при гипоксическом стрессе, отличительном признаке солидных опухолей, благодаря заметному увеличению участков связывания легумаина на поверхности клеток опухолей. Этот феномен, в сочетании с высокой аффинностью связывания RR-11a для легумаина, способствует специфическому хомингу нагруженных лекарственным средством RR-11a+ NP в солидных опухолях в условиях терапии, снижая неспецифическое накопление в печени и сердце, таким образом, исключая нежелательную токсичность лекарственного средства. Важно, что доставка лекарственного средства посредством RR-11a+ NP не только исключала токсичность летальных доз доксорубицина, но также увеличивала чувствительность опухолей к низким дозам доксорубицина, таким образом, уменьшая количество лекарственного средства, необходимого для достижения эффективного противоопухолевого ответа.
Микроокружение опухоли (TME) опосредует иммуносупрессию, приводящую к ускользанию клеток опухоли от иммунного надзора и невозможности действия противораковой вакцины. Иммуносупрессия опосредована транскрипционным фактором STAT-3, который усиливает передачу сигнала в опухоли и иммуноцитах. Поскольку иммуносупрессия продолжает являться главным ингибитором эффективности противораковой вакцины, авторы настоящего изобретения изучали в этом исследовании, может ли терапевтически нацеленная доставка синтетического ингибитора STAT-3 в TME, в комбинации с ДНК-вакциной против HER-2, улучшать иммунный надзор против HER-2+ рака молочной железы и предотвращать его рецидив. Нацеленная с помощью лиганда наночастица (NP), инкапсулирующая полезную загрузку CDDO-Im по настоящему изобретению, является способной к специфической доставке в TME, что показало эффективное терапевтическое ингибирование активации STAT-3 в первичных опухолях. Более того, обработка этими NP приводила к примированию иммунного TME, характеризующемуся увеличенной экспрессией белков IFN-γ, pSTAT-1, GM-CSF, IL-2, IL-15 и IL-12b и уменьшенной экспрессией TGF-β, IL-6 и IL-10. Кроме того, наблюдали значительно увеличенную инфильтрацию в опухоль активированных CD8+ T-клеток, M1 макрофагов и дендритных клеток. Эти изменения коррелировали с задержанным ростом ортотопических опухолей молочной железы 4TO7 и, при комбинации с ДНК-вакциной HER-2, предотвращали рецидив HER-2+ первичной опухоли у иммунокомпетентных мышей. Более того, противоопухолевые T-клеточные ответы были усилены в спленоцитах, выделенных от мышей, подвергнутых этой комбинированной терапии. Вместе, эти данные демонстрируют эффективную защиту от рецидива злокачественной опухоли посредством улучшенного иммунного надзора против опухолеспецифического антигена.
Нацеливание на опухоли NP по настоящему изобретению имеет важные клинические применения, поскольку RR-11a+ NP, использованные для инкапсуляции доксорубицина и CDDO-Im, можно также применять для инкапсуляции других лекарственных соединений, включая комбинации лекарственных средств, такие как доксорубицин и таксаны, что может фактически уничтожать различия в их фармакокинетике. Этот способ улучшает современное состояние доставки лекарственных средств и химиотерапии, предоставляя средства для уменьшения биологически оптимальной дозы лекарственного средства, необходимой для противоопухолевого эффекта, в то же самое время исключая нежелательную системную токсичность, что может значительно улучшать здоровье и качество жизни пациентов со злокачественными опухолями.
Реферат
Группа изобретений относится к водным нацеливающим на опухоли композициям липосомных наночастиц, содержащих нацеливающий на легумаин липид, содержащий липидный компонент, ковалентно связанный со связывающей легумаин группой, где связывающая легумаин группа включает ингибитор легумаина типа аза-Asn пептида с реакционноспособной частью, представленной формулой (I):а также их применению для лечения экспрессирующих легумаин опухолевых заболеваний. Группа изобретений снимает опасения, связанные с нацеливанием с помощью лигандов, в то же время предоставляя эффективные средства для специфической для опухолей доставки лекарственных средств. 5 н. и 11 з.п. ф-лы, 11 ил., 1 табл., 6 пр.
Формула




и противораковое лекарственное средство, инкапсулированное внутри наночастиц.


Комментарии