Иммуностимулирующие плазмиды - RU2740492C2
Код документа: RU2740492C2
Чертежи




Описание
Область изобретения
Настоящее изобретение в целом относится к иммуностимулирующим плазмидам. Эти плазмиды не содержат ген устойчивости к антибиотику. Плазмиды могут содержать селектируемый или скринируемый маркерный ген, который не является геном устойчивости к антибиотику (например, ген LacZ). В качестве альтернативы, плазмиды могут быть лишены каких-либо селективных или маркерных генов для скрининга.
Уровень техники
Неметилированные CpG мотивы встречаются гораздо чаще в бактериальной ДНК, чем в ДНК позвоночных. Эти мотивы активируют механизмы защиты организма и приводят к врожденным и приобретенным иммунным реакциям. CpG мотивы и их иммуностимулирующие эффекты рассматриваются в Krieg, Ann. Rev. Immunol. 20: 709-760 (2002).
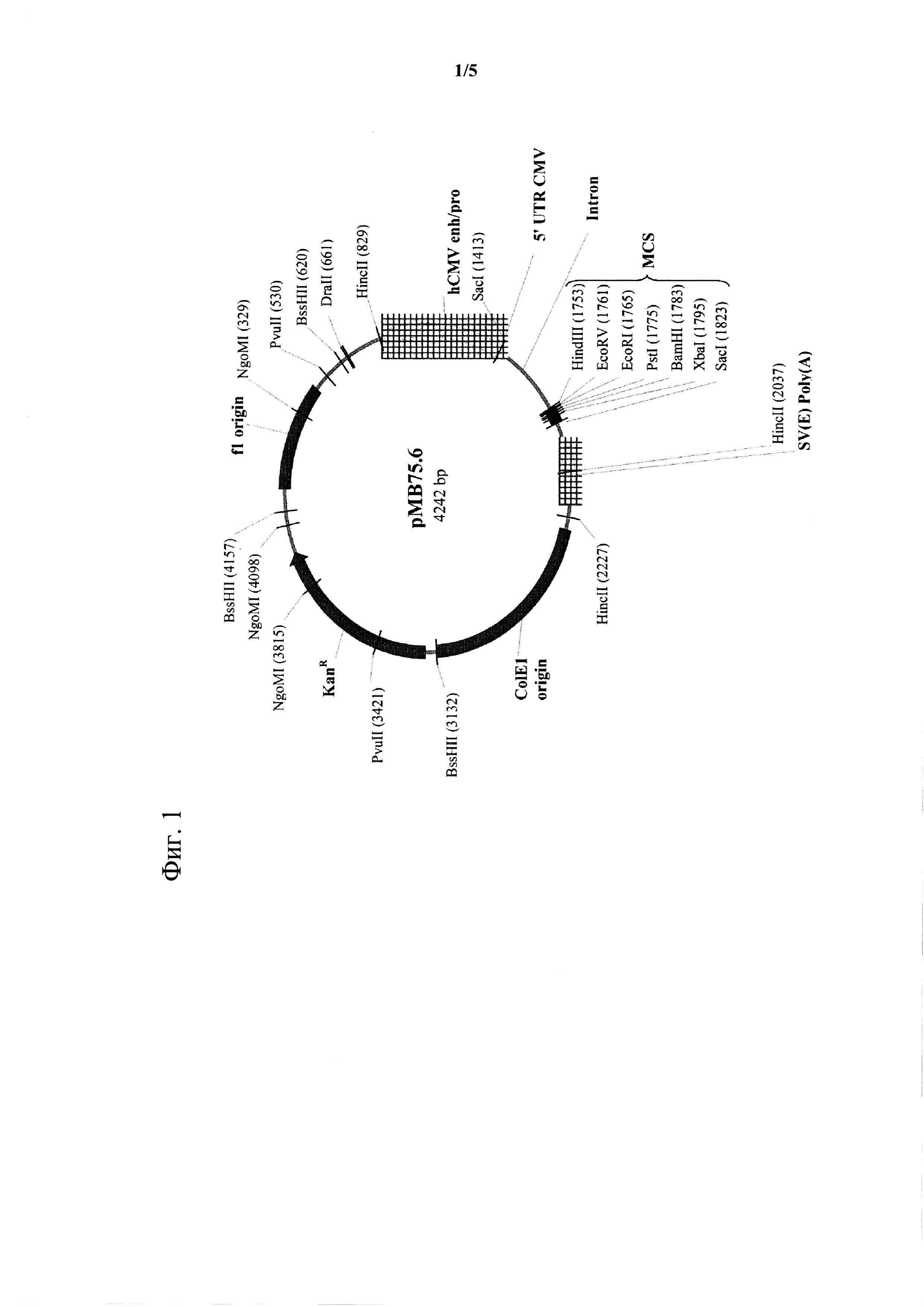
Иммуностимулирующая плазмида, содержащая ряд CpG мотивов, была ранее разработана, и было показано, что она эффективна для выявления иммунных реакций, при введении птицам и крупному рогатому скоту в качестве иммуномодулирующей композиции, содержащей плазмиду и транспортного средства доставки в виде катионных липосом. См. опубликованные патентные заявки США №№2012/0064151 А1 (виды птиц) и 2013/0295167 А1 (виды крупного рогатого скота), содержимое которых включено в данное описание посредством ссылки во всей их полноте. Эта плазмида, рМВ75.6, состоит из 4242 п.н. и содержит 288 динуклеотидов CpG. Карта рМВ75.6 показана на Фиг. 1, и нуклеотидная последовательность рМВ75.6 представлена как последовательность SEQ ID NO: 2. Как описано в опубликованной патентной заявке США 2012/0064151, иммуномодулирующая композиция, содержащая рМВ75.6, вызывала антиген-неспецифический иммунный ответ, который защищал цыплят от инфекционных заболеваний при введении in ovo. Этот антиген-неспецифический иммунный ответ был дополнительно усилен посредством введения по меньшей мере одного биологического агента, такого как вакцина. Кроме того, иммуномодулирующая композиция, содержащая плазмиду рМВ75.6, как было обнаружено, имеет адъювантный эффект и вызывает увеличение эффективности вакцин. Точно так же, как описано в патентной заявке США N: 2013/0295167, композиция, содержащая иммуномодулятор рМВ75.6, вызывала антиген-неспецифический иммунный ответ у крупного рогатого скота, который обеспечивал защиту крупного рогатого скота от инфекционных заболеваний.
Однако, как показано на Фиг. 1, плазмида рМВ75.6 содержит ген устойчивости к канамицину (KanR). Селекция, основанная на антибиотике, и системы продуцирования становятся все менее предпочтительными из-за опасений по поводу горизонтального переноса гена устойчивости к антибиотику к бактериям в окружающей среде. Возможный горизонтальный перенос генов устойчивости к антибиотикам, в особенности касается векторов, которые непосредственно вводят пациенту (например, иммуностимулирующие плазмиды, такие как рМВ75.6 или векторы, используемые для генной терапии или ДНК-вакцинации). Существует, следовательно, потребность в данной области техники для иммуностимулирующих плазмид, которые способны вызывать иммунный ответ у пациента, в то время как в ней отсутствуют гены устойчивости к антибиотикам.
Сущность изобретения
Настоящее изобретение относится к иммуностимулирующим плазмидам. Иммуностимулирующая плазмида может содержать последовательность нуклеиновой кислоты, имеющую по меньшей мере 89%-ную идентичность с последовательностью SEQ ID NO: 1, SEQ ID NO: 4, или их комбинации. В некоторых аспектах изобретения иммуностимулирующая плазмида может содержать молекулу нуклеиновой кислоты, имеющую по меньшей мере 84%-ную идентичность с последовательностью SEQ ID NO: 4. В некоторых аспектах изобретения иммуностимулирующая плазмида может содержать последовательность SEQ ID NO: 1. В некоторых аспектах иммуностимулирующая плазмида может содержать последовательность SEQ ID NO: 4.
В других вариантах, иммуностимулирующая плазмида может состоять из последовательности нуклеиновой кислоты, имеющей по меньшей мере 89% идентичность с последовательностью SEQ ID NO: 1, SEQ ID NO: 4 или их комбинацией. В некоторых аспектах изобретения иммуностимулирующая плазмида может состоять из молекулы нуклеиновой кислоты, имеющей по меньшей мере 84%-ную идентичность с последовательностью SEQ ID NO: 4. В некоторых аспектах изобретения иммуностимулирующая плазмида может состоять из последовательности SEQ ID NO: 1. В некоторых аспектах изобретения иммуностимулирующая плазмида может состоять из последовательности SEQ ID N0:4.
В некоторых вариантах изобретения иммуностимулирующая плазмида предпочтительно не содержит последовательность нуклеиновой кислоты, кодирующую маркер полной длины или функциональный селектируемый или скринируемый маркер. В других вариантах иммуностимулирующая плазмида содержит последовательность нуклеиновой кислоты, кодирующую селектируемый или скринируемый маркер, который не является геном устойчивости к антибиотику.
Настоящее изобретение также относится к фармацевтическим композициям, содержащим любую из иммуностимулирующих плазмид или ДНК-последовательностей, описанных в настоящем описании, и фармацевтически приемлемый носитель.
Настоящее изобретение также относится к иммуномодулирующим композициям, содержащим средство доставки в виде катионной липосомы и любую из иммуностимулирующих плазмид или ДНК-последовательностей, описанных в настоящей заявке.
В некоторых вариантах настоящее изобретение относится к способам применения иммуностимулирующих плазмид или ДНК-последовательностей, описанных в настоящем документе. Подходящие способы применения включают в себя терапевтическое введение субъекту. Такое терапевтическое введение включает профилактическое лечение, метафилактическое лечение, а также постинфекционное лечение субъекта или субъектов.
Настоящее изобретение относится к способам стимулирования или стимуляции иммунного ответа у субъекта. В некоторых вариантах способы включают стимуляцию иммунного ответа у субъекта путем введения субъекту иммуномодулирующей композиции, описанной в настоящем документе. В некоторых вариантах способы включают стимулирование иммунного ответа у субъекта путем введения субъекту иммуностимулирующей плазмиды или ДНК-последовательности, описанных в настоящем документе.
Другие объекты и признаки будут в некоторой степени очевидны и в некоторой степени отмечены в дальнейшем в этом документе.
Краткое описание чертежей
Следующие чертежи составляют часть настоящего описания и включены для дополнительной демонстрации некоторых аспектов настоящего изобретения. Изобретение может быть лучше понято посредством ссылки на один или несколько из этих чертежей в сочетании с подробным описанием конкретных вариантов, представленных в настоящем документе.
На Фиг. 1 показана карта плазмиды рМВ75.6;
На Фиг. 2 показана карта плазмиды pGCMB75.6;
На Фиг. 3 показана карта плазмиды pLacZ75.6; и
Фиг. 4 графически иллюстрирует, что иммуномодулирующие композиции, описанные в настоящем документе, увеличивают выживаемость субъектов-реципиентов, зараженных патогенным вирусом (Фиг. 4А, и Фиг. 4В).
Подробное описание изобретения
В соответствии с настоящим изобретением были открыты, композиция, которая способна вызывать иммунный ответ у субъекта-реципиента, а также способы применения. В частности, настоящее изобретение относится к новым композициям нуклеиновых кислот или иммуномодулирующим композициям и их применению. Было обнаружено, что такие иммуномодулирующие композиции могут включать ДНК-последовательности, описанные в настоящем документе, с повышенным содержанием GC, CpG-мотивов, и культивированные без включения генов устойчивости к антибиотикам или кодирующей последовательности. Последовательности нуклеиновых кислот по настоящему изобретению могут применяться для стимулирования или усиления иммунного ответа у субъекта для профилактики или лечения инфекционного заболевания со значительно повышенной безопасностью по сравнению с другими способами профилактики и лечения, известными в данной области техники. Изобретение особенно полезно при лечении и профилактике инфекционных заболеваний, вызванных микроорганизмами, такими как, но не ограничиваясь этим: вирусами, бактериями, плесенями, грибками, дрожжами, паразитами и другими микроорганизмами, известными в данной области техники. Композиции и способы применения иммуномодулирующих композиций обсуждаются более подробно ниже.
I. Композиции
Композиции, полезные в данном изобретении, такие как описанные в настоящем документе, как правило, могут применяться в качестве профилактической терапии, метафилактической терапии или терапии для лечения инфекционных заболеваний. Такие композиции упоминаются в настоящем документе в качестве иммуномодулирующих композиций. Иммуномодулирующие композиции включают в себя, по меньшей мере иммуностимулирующую плазмиду или иммуностимулирующую ДНК-последовательность, способные вызывать иммунный ответ у субъекта-реципиента. В некоторых аспектах иммуномодулирующие композиции могут также включать в себя липосомальное средство доставки.
А. Нуклеиновые кислоты
В некоторых аспектах настоящее изобретение относится к молекулам нуклеиновых кислот, пригодным для лечения или профилактики инфекционных заболеваний, вызванных возбудителями. Молекулы нуклеиновых кислот, описанные в настоящем документе, могут быть включены в иммуностимулирующую плазмиду, как линейная двухцепочечная или одноцепочечная ДНК, аминокислотная последовательность, рибонуклеиновая кислота (РНК) или их комбинации. В некоторых аспектах настоящее изобретение относится к молекулам нуклеиновой кислоты, векторам и клеткам-хозяевам (in vitro, in vivo или ex vivo), которые содержат иммуностимулирующую плазмиду или иммуностимулирующую последовательность ДНК.
В некоторых вариантах настоящее изобретение относится к иммуностимулирующим плазмидам или ДНК-последовательностям, которые не содержат гена устойчивости к антибиотику. Плазмиды могут быть лишены каких-либо селективных или скринируемых генов. Например, плазмида pGCMB75.6, описанная в настоящем документе, не содержит никаких маркерных генов полной длины или функциональных селективных и скринируемых маркерных генов. Последовательность pGCMB75.6 представлена в SEQ ID NO: 1.
В некоторых вариантах иммуностимулирующие плазмиды, описанные в настоящем документе, предпочтительно не содержат последовательность нуклеиновой кислоты, кодирующую полноразмерный или функциональный селективный и скринируемый маркер. В некоторых аспектах иммуностимулирующие плазмиды не содержат ген устойчивости к антибиотику. Например, плазмиды не содержат ген устойчивости к канамицину. В некоторых аспектах плазмиды, описанные в настоящем документе, предпочтительно не кодируют иммуноген.
В некоторых вариантах иммуностимулирующие плазмиды могут содержать последовательность нуклеиновой кислоты, кодирующую селектируемый или скринируемый маркерный ген, который не является геном устойчивости к антибиотику. Например, плазмида pLacZMB75.6, описанная в настоящем документе, содержит ген LacZ в качестве скринируемого маркера. Карта pLacZMB75.6 предоставлена на Фиг. 3, и нуклеотидная последовательность pLacZMB75.6 предоставлена как последовательность SEQ ID NO: 4. Как показано на Фиг. 3, pLacZMB75.6 подобен pGCMB75.6, но содержит скринируемый маркер LacZ.
Следует понимать, что нуклеотидные последовательности плазмид pGCMB75.6 или pLacZMB75.6 можно варьировать в определенной степени без существенного вредного влияния на их иммуностимулирующие свойства. В некоторых аспектах настоящее изобретение относится к иммуностимулирующим плазмидам, содержащим последовательность нуклеиновой кислоты, имеющую по меньшей мере 89% идентичности с последовательностью pGCMB75.6 (SEQ ID NO: 1). Иммуностимулирующая плазмида предпочтительно содержит
последовательность нуклеиновой кислоты, имеющей по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичность с последовательностью pGCMB75.6 (SEQ ID NO: 1). В некоторых аспектах изобретения иммуностимулирующая плазмида более предпочтительно содержит последовательность pGCMB75.6 (SEQ ID NO: 1).
В некоторых вариантах настоящее изобретение относится к иммуностимулирующей плазмиде, содержащей последовательность нуклеиновой кислоты, имеющей по меньшей мере 84% идентичность последовательности с последовательностью pLacZMB75.6 (SEQ ID NO: 4). Иммуностимулирующая плазмида предпочтительно содержит последовательность нуклеиновой кислоты, имеющую по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%,, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичность последовательности с последовательностью pLacZMB75.6 (SEQ ID NO: 4). В некоторых аспектах изобретения иммуностимулирующая плазмида более предпочтительно содержит последовательность pLacZMB75.6 (SEQ ID NO: 4).
В некоторых вариантах настоящее изобретение относится к иммуностимулирующей плазмиде, состоящей из последовательности нуклеиновой кислоты, имеющей по меньшей мере 89% идентичность последовательности с последовательностью pGCMB75.6 (SEQ ID NO: 1). Иммуностимулирующая плазмида предпочтительно состоит из последовательности нуклеиновой кислоты, имеющей по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичность последовательности с последовательностью pGCMB75.6 (SEQ ID NO: 1). В некоторых аспектах изобретения иммуностимулирующая плазмида более предпочтительно состоит из последовательности pGCMB75.6 (SEQ ID NO: 1).
В некоторых вариантах настоящее изобретение относится к иммуностимулирующей плазмиде, состоящей из последовательности нуклеиновой кислоты, имеющей по меньшей мере 84% идентичность последовательности с последовательностью pLacZMB75.6 (SEQ ID NO: 4). Иммуностимулирующая плазмида предпочтительно состоит из последовательности нуклеиновой кислоты, имеющей по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичность последовательности с последовательностью pLacZMB75.6 (SEQ ID NO: 4). В некоторых аспектах изобретения иммуностимулирующая плазмида более предпочтительно состоит из последовательности pLacZMB75.6 (SEQ ID NO: 4).
Еще один важный вариант настоящего изобретения обеспечивает иммуностимулирующие последовательности ДНК или иммуностимулирующие плазмиды, способные стимулировать иммунный ответ в том числе последовательности нуклеиновых кислот, которые гибридизуются в условиях высокой жесткости с SEQ ID NO: 1 или SEQ ID NO: 4. Подходящие последовательности нуклеиновых кислот включают в себя такие, которые гомологичны, по существу аналогичны или идентичны нуклеиновым кислотам по настоящему изобретению. В некоторых аспектах гомологичные последовательности нуклеиновых кислот будут иметь сходство последовательностей по меньшей мере на около 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% с SEQ ID NO: 1 или соответствующей комплементарной последовательностью. В других аспектах гомологичные последовательности нуклеиновых кислот будут иметь сходство последовательностей по меньшей мере на около 84%, 85%, 86%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% с SEQ ID NO: 4 или соответствующей комплементарной последовательностью. Сходство последовательностей может быть вычислена с помощью ряда алгоритмов, известных в данной области техники, таких как BLAST, описанный в Altschul, S.F., et al., J. Mol. Biol. 215:403-10, 1990. Нуклеиновые кислоты могут отличаться в последовательности от описанных выше нуклеиновых кислот вследствие вырожденности генетического кода. В общем, эталонная последовательность будет состоять из 18 нуклеотидов, более обычно 30 или более нуклеотидов, и может включать в себя всю последовательность нуклеиновой кислоты композиции для целей сравнения.
Нуклеотидные последовательности, которые могут гибридизоваться с последовательностью SEQ ID NO: 1 или SEQ ID NO: 4, рассматриваются в настоящем документе. Жесткие условия гибридизации включают в себя такие условия, как гибридизация при 50°С или выше, и 0,1x SSC (15 мМ хлорид натрия/1,5 мМ цитрат натрия). Другим примером может служить инкубации в течение ночи при 42°С в растворе 50% формамида, 5Х SSC (150 мМ NaCl, 15 мМ тринатрийцитрата), 50 мМ фосфата натрия (pH 7,6), 5Х раствор Денхардта, 10% сульфата декстрана и 20 мкг/мл денатурированной, фрагментированной ДНК спермы лосося, с последующей промывкой в 0,1Х SSC при температуре около 65°С. Иллюстративные жесткие условия гибридизации являются условия гибридизации, которые, по меньшей мере около на 80%, 85%, 90% или на 95% столь же жесткие, как выше описанные условия. Другие жесткие условия гибридизации известны в данной области техники и могут быть также использованы для идентификации гомологов нуклеиновых кислот согласно изобретению (Current Protocols in Molecular Biology, Unit 6, pub. John Wiley & Sons, N.Y. 1989).
Могут применяться мутантные нуклеотиды ДНК-молекул, описанных в настоящем документе, до тех пор пока мутанты включают последовательности нуклеиновых кислот, сохранивших способность к стимуляции иммунного ответа, как описано в настоящем документе. Последовательность ДНК такой мутации, как правило, отличается в одном или более нуклеотидах или аминокислотах. Эти изменения последовательности могут быть заменами, вставками, делециями или их комбинацией. Методики мутагенеза клонированных генов известны в данной области техники. Способы сайт-специфического мутагенеза можно найти в Gustin et al., Biotechniques 14:22, 1993; Barany, Gene 37:111-23, 1985; Colicelli et al., Mol. Gen. Genet. 199:537-9, 1985; и Sambrook et al., Molecular Cloning: A Laboratory Manual, CSH Press 1989, pp. 15.3-15.108 и все они включены в настоящее описание посредством ссылки. Таким образом, настоящее изобретение относится к последовательностям нуклеиновых кислот, способных стимулировать иммунный ответ у субъекта, и его варианты или мутанты. Кроме того, изобретение охватывает молекулы РНК-посредника, кодируемые описанными последовательностями нуклеиновых кислот, а также любых кодируемых аминокислотных последовательностей, получающихся в результате.
В случае, если нуклеотидная последовательность иммуностимулирующей плазмиды отличается от последовательностей, представленных в SEQ ID NO: 1 и 4, динуклеотиды CpG в плазмиде предпочтительно остаются интактными. В качестве альтернативы, если нуклеотидная последовательность плазмиды изменяется таким образом, что динуклеотид CpG, элиминируется, последовательность плазмиды может быть изменена в другом месте, так что общее количество динуклеотидов CpG в плазмиде осталось бы тем же самым. Дополнительные динуклеотиды CpG в дополнение к тем, которые уже присутствуют в нуклеотидных последовательностях pGCMB75.6 или pLacZMB75.6, также могут быть введены в плазмиду. Так, например, иммуностимулирующие плазмиды, описанные в настоящем документе, предпочтительно содержат, по меньшей мере около 200, по меньшей мере около 220, по меньшей мере около 240, по меньшей мере около 260, по меньшей мере около 270, по меньшей мере около 275, по меньшей мере около 280 по меньшей мере около 283, по меньшей мере около 285 или по меньшей мере около 288 динуклеотидов CpG. Например, иммуностимулирующая плазмида может содержать 283 CpG динуклеотидов.
В частности, настоящее изобретение относится к фармацевтическим композициям, содержащим любую из иммуностимулирующих плазмид или ДНК-последовательностей, описанных в настоящем изобретении, и фармацевтически приемлемый носитель.
В. Иммуномодулятор
Подходящие иммуномодулирующие композиции для использования с иммуностимулирующими плазмидами, описанными в настоящем документе, описаны в опубликованных патентных заявках США №№2012/0064151 А1 (виды птиц) и 2013/0295167 А1 (виды крупного рогатого скота), содержание обоих из которых включено в данное описание посредством ссылки во всей их полноте.
Иммуномодулирующая композиция содержит липосомальное средство доставки и по меньшей мере одну из иммуностимулирующих плазмид или ДНК-последовательностей, описанных в настоящей заявке.
Подходящее липосомальное средство доставки содержит липидную композицию, которая способна доставлять молекулы нуклеиновых кислот в ткани пациента, подвергаемого лечению. Липосомальное средство доставки предпочтительно способно оставаться стабильными у субъекта в течение достаточного количества времени, чтобы доставить молекулу нуклеиновой кислоты и/или биологический агент. Например, липосомальное средство доставки остается стабильным в субъекте-реципиенте в течение по меньшей мере около пяти минут, в течение по меньшей мере около 1 часа, или по меньшей мере около 24 часов.
Липосомальное средство доставки по настоящему изобретению содержит липидную композицию, которая способна к слиянию с плазматической мембраной клетки, чтобы доставить молекулу нуклеиновой кислоты в клетку. В том случае, когда молекула нуклеиновой кислоты кодирует один или несколько белков, комплекс нуклеиновая кислота: липосома предпочтительно имеет эффективность трансфекции по меньшей мере около 1 пикограмм (пг) белка, отнесенное на миллиграмм (мг) общего белка ткани на микрограмм (мкг) доставляемой нуклеиновой кислоты. Например, эффективность трансфекции комплекса нуклеиновая кислота: липосома может быть по меньшей мере около 10 мкг белка, отнесенного на мг общего белка ткани на мкг доставляемой нуклеиновой кислоты; или по меньшей мере около 50 мкг белка, отнесенного на мг общего белка ткани на мкг доставляемой нуклеиновой кислоты. Эффективность трансфекции комплекса может быть всего лишь 1 фемтограмм (фг) белка, отнесенного на мг общего белка ткани на мкг доставляемой нуклеиновой кислоты, причем вышеуказанные количества являются более предпочтительными.
Предпочтительное липосомальное средство доставки по настоящему изобретению имеют размер от около 100 до 500 нанометров (нм) в диаметре. Например, липосомальное средство доставки может быть от около 150 до 450 нм или от около 200 до 400 нм в диаметре.
Подходящие липосомы включают любые липосом, такие как те, которые обычно используются, например, в способах доставки генов, известных специалистам в данной области техники. Предпочтительные липосомальные средства доставки включают мультиламеллярные липидые везикулы (MLV) и экструдированные липиды. Способы получения MLV хорошо известны в данной области техники. Более предпочтительные липосомальные средства доставки включают липосомы, имеющие поликатионную липидную композицию (например, катионные липосомы) и/или липосомы, содержащие холестериновую основу, конъюгированную с полиэтиленгликолем. Иллюстративные катионные липосомальные композиции включают в себя, но не ограничиваются этим, N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмоний хлорид (ДОТМА) и холестерин, N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмоний хлорид (ДОТАП) и холестерин, 1-[2-(олеилокси)этил]-2-олеил-3-(2-гидроксиэтил)-имидазолий хлорид (DOTIM) и холестерин, диметилдиоктадециламмоний бромид (DDAB) и холестерин, а также их комбинации. Наиболее предпочтительная липосомальная композиция для использования в качестве носителя для доставки содержит DOTIM и холестерина.
Подходящая молекула нуклеиновой кислоты содержит любую из иммуностимулирующих плазмид, описанных в настоящем документе. Кодирующие последовательности нуклеиновых кислот кодируют по меньшей мере часть белка или пептида, в то время как некодирующие последовательности не кодирует какую-любую часть белка или пептида. В соответствии с настоящим изобретением "некодирующие" нуклеиновые кислоты могут включать в себя регуляторные области единицы транскрипции, такие как промоторную область. Термин "пустой вектор" может быть использован взаимозаменяемо с термином "некодирующий" и, в частности, относится к последовательности нуклеиновой кислоты в отсутствии кодирующей части белка, такой как плазмидный вектор без вставки гена. Экспрессия белка, кодируемого плазмидами, описанными в настоящем документе, не является обязательным для стимулирования антиген-неспецифического иммунного ответа; поэтому плазмиды не обязаны содержать каких-либо кодирующих последовательностей, операционно связанных с последовательностью, контролирующей транскрипцию. Тем не менее, дополнительные преимущества могут быть получены (т.е. антиген-специфический и усиленный иммунитет) путем включения в композицию последовательности нуклеиновой кислоты (ДНК или РНК), которая кодирует иммуноген и/или цитокин. Такая последовательность нуклеиновой кислоты, кодирующая иммуноген и/или цитокин, могут быть включена в иммуностимулирующие плазмиды, описанные в настоящем документе, или может быть включена в отдельную нуклеиновую кислоту (например, в отдельную плазмиду) в композиции.
Комплексообразование липосомы с иммуностимулирующими плазмидами, описанными в настоящем документе, может быть достигнуто с использованием способов, стандартных в данной области техники, или как описано в патенте США №6,693,086, содержание которого включено в настоящее описание посредством ссылки во всей их полноте. Приемлемая концентрация плазмиды, которое следует добавить к липосоме, включает в концентрации, эффективные для доставки количества плазмиды в субъект достаточного для стимулирования системного иммунного ответа. Например, от около 0,1 мкг до около 10 мкг плазмиды могут быть комбинированы с около 8 нмоль липосом, от около 0,5 мкг до около 5 мкг плазмиды могут быть комбинированы с около 8 нмоль липосом, или около 1,0 мкг плазмиды могут быть комбинированы с около 8 нмоль липосом. Отношение плазмиды к липиду (мкг плазмиды : нмоль липида) в композиции может быть по меньшей мере около 1:1 плазмида : липид по массе (например, 1 мкг плазмиды : 1 нмоль липида). Например, отношение плазмиды к липидам может быть по меньшей мере около 1:5, по меньшей мере около 1:10 или по меньшей мере около 1:20. Коэффициенты, представленные в настоящем документе, основаны на количестве катионного липида в композиции, а не на общее количество липидов в композиции. Отношение плазмиды к липидам в композиции по настоящему изобретению предпочтительно составляет от около 1:1 до около 1:80 плазмида : липид по массе; от около 1:2 до около 1:40 плазмида : липид по массе; от около 1:3 до около 1:30 плазмида : липид по массе; или от около 1:6 до около 1:15 плазмида : липид по массе.
С. Биологический агент
Любая из иммуномодулирующих композиций, описанных в настоящем документе, может дополнительно содержать по меньшей мере один биологический агент в дополнение к липосомальному средству доставки и по меньшей мере одну из плазмид, описанных в настоящем документе.
Подходящие биологические агенты представляют собой агенты, которые являются эффективными для профилактики или лечения заболеваний птиц или крупного рогатого скота. Такие биологические агенты включают белки, усиливающие иммунный ответ, иммуногены, вакцины, противомикробные средства или любую их комбинацию. Подходящими белками, усиливающими иммунный ответ являются белками, про которые известно, что они повышают иммунитет. В качестве неограничивающего примера, цитокин, который входит в семейство белков, принадлежит к известному семейству иммуностимулирующих белков. Подходящие иммуногенами являются белки, которые вызывают гуморальный и/или клеточный иммунный ответ, такие, что введение иммуногена субъекту вызывает иммуноген-специфический иммунный ответ против тех же самых или подобных белков, которые встречаются в тканях субъекта. Иммуноген может включать в себя патогенные антигены, экспрессируемые бактериями, вирусами, паразитами или грибками. Предпочтительные антигены включают в себя антигены, полученные из организмов, которые вызывают инфекционное заболевание у субъекта. В соответствии с настоящим изобретением иммуноген может представлять собой любую часть белка, встречающегося в природе или полученного синтетическим путем, которые вызывает гуморальный и/или клеточный иммунный ответ. Таким образом, размер антигена или иммуногена может быть небольшим, таким, как около 5-12 аминокислот, и большим таким, как полноразмерный белок, в том числе любых размеров между ними. Антиген может представлять собой мультимерный белок или слитый белок. Антиген может представлять собой очищенный антиген. В качестве альтернативы, иммуностимулирующий белок или иммуноген может быть кодирован посредством иммуностимулирующей плазмиды или другой нуклеиновой кислоты, включенной в иммуномодулирующую композицию. Там, где иммуностимулирующий белок или иммуноген кодируется молекулой нуклеиновой кислоты в иммуномодулирующей композиции, последовательность нуклеиновой кислоты, кодирующей иммуностимулирующий белок, или иммуноген функционально связан с последовательностью, контролирующей транскрипцию, таким образом, что иммуноген экспрессируется в ткани субъекта, тем самым вызывая иммуноген-специфический иммунный ответ у субъекта, в дополнение к неспецифическому иммунному ответу. Методики скрининга на иммуногенность, такие как иммуногенность на патогенный антиген или цитокиновую активность известны специалистам в данной области техники и включают в себя различные анализы in vitro и in vivo.
Если биологический агент представляет собой вакцину, вакцина может включать в себя живую, инфекционную, вирусную, бактериальную или паразитарную вакцину или убитую, инактивированную, вирусную, бактериальную или паразитарную вакцину. Одна или несколько вакцин, живых или убитых вирусных вакцин могут применяться в комбинации с иммуномодулирующей композицией по настоящему изобретению. Подходящие вакцины включают такие, которые известны в данной области техники для птиц или крупного рогатого скота различных пород.
Иллюстративные вакцины для видов птиц включают, без ограничения, такие, которые используются в этой области техники для защиты от вируса болезни Марека (ВБМ), вируса болезни Ньюкасла (ВБН), вируса анемии цыплят (CAV), вируса инфекционного бурсита (IBDV), вируса инфекционного бронхита (IBV), герпес-вирус индеек (HVT), вируса инфекционного ларинготрахеита (ВИЛТ), вируса птичьего энцефаломиелита (AEV), вируса оспы кур (ВОК), птичья холера, вируса птичьего гриппа (ВПГ), реовируса, вируса птичьего лейкоза (ALV), вируса ретикулоэндотелиоза (ВРЭ), аденовируса птиц и вируса геморрагического энтерита (HEV), кокцидий и других заболеваний, известных в данной области техники. В другом примере вакцина может быть вакциной, описанной в патентах США №№5427791, 6048535 и 6406702. Например, вакцина для защиты от болезни Марека может быть использована в сочетании с иммуномодулирующей композицией по настоящему изобретению.
Иллюстративные вакцины для видов крупного рогатого скота включают, без ограничения, такие, которые используются в данной области техники для защиты от инфекционного ринотрахеита крупного рогатого скота (IBR) (тип 1 вируса герпеса крупного рогатого скота (BHV1)), вируса парагриппа типа 3 (PI3), респираторно-синцитиального вируса крупного рогатого скота (BRSV), вируса вирусной диареи крупного рогатого скота (BVDV типа 1 и 2), Histophilus somni, Mycoplasma bovis, и других заболеваний, известных в данной области техники. Например, вакцина для защиты от Mannheimia haemolytica может быть использована в сочетании с иммуномодулирующей композицией по настоящему изобретению.
Биологический агент может быть бактерицидным средством. Подходящие бактерицидные средства включают в себя: хинолоны, предпочтительно фторхинолоны, бета-лактамы и антибиотики макролид-линкозамид-стрептограмин (MLS).
Подходящие хинолоны включают бенофлоксацин, бинфлоксацин, циноксацин, ципрофлоксацин, клинафлоксацин, данофлоксацин, дифлоксацин, эноксацин, энрофлоксацин, флероксацин, гемифлоксацин, ибафлоксацин, левофлоксацин, ломефлоксацин, марбофлоксацин, моксифлоксацин, норфлоксацин, офлоксацин, орбифлоксацин, пазуфлоксацин, прадофлоксацин, перфлоксацин, сарафлоксацин, спарфлоксацин, темафлоксацин и тосуфлоксацин. Предпочтительные фторхинолоны включают ципрофлоксацин, данофлоксацин, энрофлоксацин, моксифлоксацин и прадофлоксацин. Подходящие нафтиридоны включают налидиксовую кислоту.
Подходящие бета-лактамы включают пенициллины (например, амоксициллин, ампициллин, азлоциллин, бензатин-пенициллин, бензилпенициллин, карбенициллин, клоксациллин, со-амоксиклав [т.е. амоксициллин/клавулановая кислота], диклоксациллин, флуклоксациллин, метициллин, мезлоциллин, нафциллин, оксациллин, феноксиметилпенициллин, пиперациллин, прокаин пенициллин, темоциллин и тикарциллин); цефалоспорины (например, цефаклор, цефалониум, цефамандол, цефапирин, цефазолин, цефепим, цефиксим, цефотаксим, цефокситин, цефпиром, цефподоксим, цефкином, цефтазидим, цефтиофура, цефтриаксон, цефуроксим, цефалексин, цефалотин и defotetan); карбапенемы и пенемы (например, дорипенем, эртапенем, фаропенем, имипенем и меропенем); монобактамы (например, азтреонам, нокардицин А, табтоксинин-β-лактам и тигемонам); и ингибиторы β-лактамазы (например, клавулановая кислота, сульбактам и тазобактам). Предпочтительные бета-лактамы включают цефалоспорины, в частности, цефазолин.
Подходящие MLS-антибиотики включают клиндамицин, линкомицин, пирлимицин и любой макролидный антибиотик. Предпочтительным линкозамидным антибиотиком является пирлимицин.
Другие противомикробные препараты включают аминогликозиды, клопидол, диметридазолы, эритромицин, фрамицетин, фуразолидон, галофугинон, 2-пиридон, робенидин, сульфаниламиды, тетрациклины, триметоприм, различные плевромутилины (например, тиамулин и валнемулин), а также различные стрептомицины (например, монензин, наразин и салиномицин).
I. Способы
Задачей настоящего изобретения является создание иммуномодулирующих композиций, иммуностимулирующих плазмид (или последовательности ДНК), и способов, которые вызывают защитный иммунитет у неинфицированных субъектов, защитный иммунитет у зараженных субъектов, повышение иммунитета у неинфицированных субъектов, повышение иммунитета у зараженных субъектов, терапевтический иммунитет у инфицированных субъектов или их комбинации. Таким образом, композиции по настоящему изобретению могут применяться для профилактической вакцинации субъектов или использоваться для лечения субъекта. Способы, описанные в настоящем документе, включают введение субъекту иммуностимулирующей плазмиды, или ДНК-последовательность, описанные в настоящем документе.
А. Способы стимуляции иммунной системы
Настоящее изобретение относится к способам стимуляции иммунного ответа у субъекта-реципиента. Способы включают в себя введение субъекту эффективного количества иммуномодулирующей композиции, чтобы вызвать иммунный ответ. В некоторых аспектах иммуномодулирующая композиция вызывает антиген-неспецифический иммунный ответ, который является эффективным сам по себе. В некоторых аспектах иммуномодулирующая композиция усиливает действие по меньшей мере одного биологического агента, такого как вакцина, если вводится до такой вакцины, совместно вводимого с вакциной, вводится после вакцинации или в смеси с вакциной. В некоторых аспектах способы обеспечивают новые стратегии лечения для защиты субъектов-реципиентов от инфекционных заболеваний и лечения населения, имеющих инфекционное заболевание. В некоторых аспектах способы обеспечивают более быструю, более продолжительную и более эффективную защиту против заболевания, когда иммуномодулятор используется в сочетании с вакциной, по сравнению с использованием вакцины без иммуномодулирующей композиции.
Иммунный ответ может быть инициирован у субъекта-реципиента путем введения эффективного количества иммуномодулирующей композиции, которая содержит любое из липосомальных средств доставки, описанных в настоящем документе, любую из иммуностимулирующих плазмид (для ДНК-последовательностей), описанных в настоящем документе, и любого из биологических агентов, описанных в настоящем документе. Предполагается, что биологический агент может быть смешан с иммуномодулятором или вводиться совместно с иммуномодулятором или независимо от него. Независимое введение может быть до или после введения иммуномодулятора. Также предполагается, что может быть использовано более чем одно введение иммуномодулятора или биологического агента для расширения повышенного иммунитета. Кроме того, более чем один биологический агент может быть введен совместно с иммуномодулятором, введен до иммуномодулятора, введен после введения иммуномодулятора или одновременно с иммуномодулятором.
Эффективное количество любой из иммуномодулирующих композиций, описанных в настоящем документе, может быть введено субъекту. Эффективное количество является достаточным, чтобы вызвать иммунный ответ у субъекта-реципиента. Такое эффективное количество представляет собой любое количество, которое вызывает иммунный ответ у субъекта-реципиента. Способы измерения иммунного ответа хорошо известны в данной области техники. Кроме того, специалист в данной области техники признает, что эффективное количество будет зависеть от возраста, массы, стадии инфекции, а также других факторов, известных в данной области техники. Приемлемые эффективные количества могут составлять от около 0,1 мкг до 1000 мкг на субъект. В некоторых аспектах эффективное количество может находиться в диапазоне от около 0,1 мкг до около 10 мкг, от около 0,1 мкг до около 5 мкг, от около 0,5 мкг до около 5 мкг, от около 0,25 мкг до около 5 мкг, от около 0,05 мкг до около 10 мкг, от около 5 мкг до около 15 мкг, от около 10 мкг до около 15 мкг, от около 10 мкг до около 20 мкг, от около 20 мкг до около 30 мкг, от около 30 мкг до около 40 мкг, от около 40 мкг до около 50 мкг, от около 50 мкг до около 70 мкг, от около 70 мкг до около 90 мкг, от около 50 мкг до около 100 мкг, от около 100 мкг до около 150 мкг, от около 150 мкг до около 200 мкг, от около 200 мкг до около 250 мкг, от около 250 мкг до около 300 мкг, от около 300 мкг до около 350 мкг, от около 350 мкг до около 400 мкг, от около 400 мкг до около 450 мкг, от около 450 мкг до около 500 мкг, от около 500 мкг до около 550 мкг, от около 550 мкг до около 600 мкг, от около 600 мкг до около 650 мкг, от около 650 мкг до около 700 мкг, от около 700 мкг до около 750 мкг, от около 750 мкг до около 800 мкг, от около 800 мкг до около 850 мкг, от около 850 мкг до около 900 мкг, от около 900 мкг до около 950 мкг, от около 950 мкг до около 1000 мкг. Предпочтительно, в некоторых аспектах эффективное количество составляет от около 0,5 мкг до около 10 мкг. Тем не менее предпочтительно в других аспектах эффективное количество составляет от около 50 мкг до около 100 мкг. И предпочтительно в других аспектах эффективное количество составляет от около 40 мкг до около 70 мкг.
В некоторых вариантах иммунный ответ может быть вызван в представителе видов птиц путем введения эффективного количества любого из иммуномодулирующих композиций, описанных в настоящем документе, представителю видов птиц. Эффективное количество является достаточным, чтобы вызвать иммунный ответ у представителя видов птиц. Например, эффективное количество иммуномодулятора для видов птиц может составлять от около 0,05 мкг до около 10 мкг, от около 0,1 мкг до около 5 мкг, от около 0,5 мкг до около 1,5 мкг или от около 1,0 мкг до около 10 мкг. В качестве примера, подходящие эффективные количества для субъекта, который является видом птиц, может составлять от около 0,1 мкг, 0,2 мкг, 0,3 мкг, 0,4 мкг, 0,5 мкг, 0,6 мкг, 0,7 мкг, 0,8 мкг, 0,9 мкг, 1,0 мкг, 1,2 мкг, 1,4 мкг, 1,6 мкг, 1,8 мкг, 2,0 мкг, 2,5 мкг, 3,0 мкг, 3,5 мкг, 4,0 мкг, 4,5 мкг, 5,0 мкг, 5,5 мкг, 6,0 мкг, 6,5 мкг, 7,0 мкг, 7,5 мкг, 8,0 мкг, 8,5 мкг, 9,0 мкг, 9,5 мкг, 10,0 мкг, 9,5 мкг, 10,0 мкг, 10,5 мкг, 11,0 мкг, 12 мкг, 13 мкг, 14 мкг или 15 мкг.
В некоторых вариантах иммунный ответ может быть вызван у представителя вида крупного рогатого скота, путем введения эффективного количества любой из иммуномодулирующих композиций, описанных в настоящем описании, представителю вида крупного рогатого скота. Эффективное количество является достаточным, чтобы вызвать иммунный ответ у представителя вида крупного рогатого скота. Например, эффективное количество иммуномодулятора для вида крупного рогатого скота может составлять от около 1 мкг до около 1000 мкг на животное, от около 5 мкг до около 500 мкг на животное, от около 10 мкг до около 100 мкг на животное, от около 10 мкг до около 50 мкг на животное или около от 40 мкг до около 60 мкг на животное. В качестве примера, подходящие эффективные количества для субъекта, которым является видами крупного рогатого скота, могут составлять около 30 мкг, 35 мкг, 40 мкг, 45 мкг, 50 мкг, 55 мкг, 60 мкг, 65 мкг, 70 мкг, 75 мкг, 80 мкг, 85 мкг, 90 мкг, 95 мкг, 100 мкг, 110 мкг, 120 мкг, 130 мкг, 140 мкг, 150 мкг, 160 мкг, 170 мкг, 180 мкг, 190 мкг, 200 мкг или до 500 мкг или до 1000 мкг.
В. Условия применения
Способы по изобретению вызывают такой иммунный ответ у субъекта, что субъект оказывается защищен от болезни, которая ответственна за процесс индукции иммунного ответа. Используемое в данном описании выражение "защищенный от болезни" относится к уменьшению симптомов заболевания; уменьшению распространения заболевания; уменьшению клинической или патологической тяжесть заболевания; или уменьшению распространения возбудителя, вызывающего заболевание. Защита субъекта может означать способность терапевтической композиции по настоящему изобретению, которое при введении субъекту предотвращает возникновения заболевания, лечит и/или облегчает или уменьшает симптомы заболевания, клинические признаки, патологию, или причины. Например, без ограничения, клинические признаки респираторной инфекции крупного рогатого скота (РИКРС) включают поражения легких, повышение температуры, депрессию (например, анорексию, снижение восприимчивости к внешним раздражителям, осоловелые глаза), выделения из носа и респираторные признаки (например, интенсивность дыхания, респираторное усилие). Иммуномодулирующие композиции, описанные в настоящем документе, могут быть введены крупному рогатому скоту, который предположительно подвергся РИКРС, чтобы предотвратить или уменьшить тяжесть описанных выше клинических признаков РИКРС. В качестве еще одного примера, без ограничения, клинические признаки болезни Марека у птиц содержит снижение вылупляемости и живучести птиц. Иммуномодулирующие композиции, описанные в настоящем документе, могут быть введены птиц, которые предположительно подвергаются воздействию вируса болезни Марека, чтобы предотвратить или уменьшить тяжесть описанных выше клинических признаков болезни Марека.
Таким образом, защита субъекта от заболевания включает как предотвращение возникновения заболевания (профилактическое лечение), так и лечение субъекта, который имеет заболевание (терапевтическое лечение). В частности, защита субъекта от заболевания осуществляется путем индукции иммунного ответа у субъекта, что вызывает целительный или защитный иммунный ответ, который может, в некоторых случаях, дополнительно подавить, уменьшить, ингибировать или блокировать сверхактивный или опасный иммунный ответ. Термин "заболевание" относится к любому отклонению от нормального состояния здоровья субъекта и включает состояние, когда симптомы болезни присутствуют, а также условия, в которых отклонение (например, инфекции, мутации гена, генетический дефект и т.п.) произошло, но симптомы еще не проявляются.
Способы по изобретению могут применяться для профилактики заболеваний, стимуляции эффекторных клеток иммунитета против заболеваний, устранение болезни, облегчения заболевания и профилактики вторичного заболевания в результате возникновения первичного заболевания.
В некоторых аспектах способы, описанные в настоящем документе, могут применяться для улучшения приобретенного иммунного ответа субъекта при совместном введении с вакциной по сравнению с введением вакцины самой по себе. Обычно вакцина после введения не сразу защищает субъект, так как требуется время, чтобы стимулировать приобретенный иммунитет. Термин "улучшение" относится в настоящем изобретении к процессу индукции врожденного иммунного ответа у субъекта, пока вакцина не начнет защищать субъекта и/или пролонгировать период защиты, с помощью приобретенного иммунитета, возникшего посредством вакцины.
В некоторых вариантах способы по настоящему изобретению включают в себя введение композиции для защиты от инфекции широкого спектра патогенных микроорганизмов. Вводимая композиция может включать в себя или не может не включать в себя специфический антиген, чтобы вызывать специфический ответ. Предполагается, что способы по изобретению будут защищать субъектов-реципиентов от болезней, вызванных инфекционными микробными агентами, включая, без ограничения, вирусы, бактерии, грибы и паразиты. Квалифицированный специалист признает и оценит, что иммуномодулирующая композиция, которая описана в настоящем документе, является эффективной против многочисленных инфекционных агентов, которых слишком много, чтобы перечислить. Инфекционные агенты, представленные в настоящем документе, предназначены для иллюстративных целей и обеспечиваются без ограничения объема применения.
Примеры вирусных инфекционных заболеваний у птиц включают, без ограничения, такие, к которым приводят инфекции вирусом инфекционной анемии цыплят (ВИАЦ), вирусом болезни Марека (ВБМ), вирусом герпеса цыплят (HCV), вирусом герпеса индейки (ВГИ), вирусом инфекционного бурсита (IBDV), вирусом болезни Ньюкасла (ВБН), вирусом инфекционного бронхита (ВИБ), вирусом инфекционного ларинготрахеита (ВИЛТ), парамиксовирусом типа 3, птичим энцефаломиелитом (AEV), вирусом оспы кур (ВОК), птичьей холерой, вирусом птичьего гриппа (ВПГ), реовирусом, вирусом птичьего лейкоза (ВПЛ), вирусом ретикулоэндотелиоза (ВРЭ), аденовирусом птиц, вирусом геморрагического энтерита (HEV), пневмовирусом, вирусом оспы голубей их рекомбинантами, и другие вирусами, известными в данной области техники.
Примеры бактериальных инфекций у птиц включают без ограничения, такие, которые возникают в результате инфекции грам-положительными бактериями, грамотрицательными бактериями или грибками, такими как Bordetella spp., Campylobacter jejuni, Clostridium botulinum, Clostridium colinum, Clostridium perfringens, Erysipelothrix insidiosa, Escherichia coli, Hemophilus gallinarum, Mycoplasma gallisepticum, Mycoplasma meleagridis, Mycoplasma synoviae, Pasteurella multocida, Riemerella anatipestifer, Salmonella spp., Salmonella enteritidis, Salmonella gallinarum, Salmonella pullorum и другими известными в данной области бактериями.
Примеры инфекций грибками или плесенями у птиц включают без ограничения, такие, которые возникают в результате Aspergillus flavus, Aspergillus fumigates, Candida albicans и другими инфекционными грибками или плесенями, известными в данной области техники. Примеры условий заболевания включают, без ограничения, такие, которых являются результатом действия токсинов из грамположительных бактерий, грамотрицательных бактерий или грибков, таких как токсин Clostridium botulinum, токсин Clostridium perfringens, энтеротоксин Е. coli, микотоксины Fusarium, лейкотоксин Pasteurella, стафилококковые токсины и других токсинов, известных в данной области техники.
Примеры паразитов видов птиц включают, без ограничения Ascaridia galli, Capillaria annulata, Capillaria contorta, Capillaria obsignata, coccidia spp., Eimeria meleagridis, Heterakis gallinae, Syngamus trachea и других паразитов, известных в данной области техники.
Примеры вирусных инфекционных заболеваний у крупного рогатого скота различных пород включают, без ограничения, в результате инфекции вируса блютанга, аденовируса крупного рогатого скота, кальцивируса крупного рогатого скота, коронавируса крупного рогатого скота (BCV), энтеровируса крупного рогатого скота, вируса герпеса крупного рогатого скота типа 1 (BHV1), вируса герпеса крупного рогатого скота типа 4 (BHV4), вируса лейкоза крупного рогатого скота, парвовируса крупного рогатого скота, реовируса крупного рогатого скота, респираторно-синцитиального вируса крупного рогатого скота (BRSV), риновируса крупного рогатого скота, вируса диареи крупного рогатого скота типа 1 (BVDV1), вируса диареи крупного рогатого скота типа 2 (BVDV2), инфекционного ринотрахеита крупного рогатого скота (IBR), вируса злокачественной катаральной лихорадки крупного рогатого скота, вируса парагриппа типа 3 (PIV3), вируса бешенства, вируса везикулярного стоматита (ВВС), их рекомбинантов, и других вирусов, известных в данной области техники.
Примеры бактериальных инфекций у крупного рогатого скота различных пород включают без ограничения такие, которые случаются в результате инфекции грам-положительными бактериями, грамотрицательными бактериями или микобактериям, такими как Arcanobacterium pyogenes, Bacillus anthracis, Bacillus anthrax, Brucella abortus, Campylobacter fetus, Campylobacter jejuni, Clostridium botulinum, Clostridium chauveoi, Clostridium colinum, Clostridium hemolyticum, Clostridium novyi, Clostridium perfringens, Clostridium septicum, Clostridium tetani, Corynebacterium, Escherichia coli, Fusobacterium necrophorum, Fusobacterium spp., Histophilus somni, Histophilus spp., Leptospira spp., Mannheimia haemolytica, Moraxella spp., Muellerius spp., Mycobacterium paratuberculosis, Mycobacterium spp., Mycoplasma bovirhinis, Mycoplasma bovis, Mycoplasma dispar, Mycoplasma spp., Pasteurella multocida, Salmonella spp., Treponema spp., Ureaplasma diversum и другими известными в данной области техники бактериями.
Примеры грибковых инфекциями или инфекциями плесенями у видов крупного рогатого скота включает, без ограничения такие, которые являются результатом инфекции Actinobacterim spp., Aspergillus spp, и Histomonas spp., и другими инфекционными грибками или плесенями, известными в данной области техники.
Примеры паразитов видов крупного рогатого скота включают без ограничения Anaplasma spp., Anaplasma marginale, Babesia spp., Chorioptes spp., Cooperia, Cysticercus spp., Damalinia bovis, Dermatophilus spp., Dictylocaulus spp., Eimeria spp., Eperythrozoon spp., Fascioloides spp., Haemonchus spp., Melophagus spp., Muellerius spp., Nematodirus spp., Neospora spp., Oestrus spp., Ostertagia spp., Psoroptes spp., Sarcoptes spp., Serpens spp., Strongyloides spp., Toxoplasma spp., Trichophyton spp., Trichostrongylus, Trichuris spp., and Tritrichomonas spp., и другие паразиты, известные в данной области техники.
Примеры инфекционных агентов заболеваний у видов крупного рогатого скота также включают такие агенты, которые вызывают мастит, метрит, криптоспоридиоз и любое другое инфекционное заболевание, которым подвержена виды крупного рогатого скота.
С. Введение
Доступны различные способы введения. Конкретный выбранный способ будет зависеть, конечно, от конкретных выбранных биологических агентов, возраста и общего состояния здоровья субъекта, конкретного состояния, подлежащего лечению, и дозы, необходимой для терапевтической эффективности. Способы по настоящему изобретению могут быть осуществлены с использованием любого способа введения, который обеспечивает эффективные уровни иммунного ответа, не вызывая клинически неприемлемых побочных эффектов. Композиции могут быть удобно представлены в виде стандартной лекарственной формы и могут быть получены любым из способов, хорошо известных в данной области техники. Иммуномодулирующая композиция может быть введена внутривенно, внутримышечно, внутрикожно, внутрибрюшинно, подкожно, распылением, in ovo, способом в фолликул пера, перорально, внутриглазно, интратрахеально, интраназально или другими способами, известными в данной области техники. В одном из аспектов иммуномодулятор вводят подкожно. В другом аспекте иммуномодулятор можно вводить внутримышечно. В другом аспекте иммуномодулятор вводят в виде спрея. В другом аспекте иммуномодулятор может быть введен перорально.
В одном варианте иммуномодулятор может вводиться сам по себе субъекту до заражения (или инфекции). В другом своем аспекте иммуномодулятор может вводиться сам по себе в субъект после заражения (или инфекции). В другом аспекте иммуномодулятор может вводиться сам по себе субъекту в то же самое время, что и антигенный стимул (или инфекция).
В некоторых вариантах иммуномодулирующая композиция может быть введена совместно в то же время, что и вакцинация до заражения. В некоторых аспектах иммуномодулирующая композиция может быть введена совместно в то же время, что и вакцинация, в то же время, что и антигенный стимул (или инфекция). В некоторых аспектах совместное введение может включать введение вакцины и иммуномодулятора в том же месте у субъекта в двух различных участках рядом друг с другом (то есть, инъекции рядом друг с другом на шее субъекта), на противоположных сторонах субъекта в том же месте (то есть, по одному на каждой стороне шеи), или в разных местах одного и того же субъекта. В некоторых аспектах иммуномодулирующая композиция может вводиться перед вакцинацией и заражением. В некоторых аспектах иммуномодулирующая композиция может вводиться после вакцинации, но до заражения. Иммуномодулирующая композиция может вводиться после заражения субъекту, который был вакцинирован до заражения (или инфекции).
Специалисту в данной области будет понятно, что способы введения могут варьироваться в зависимости от субъекта и здоровья или состояния субъекта. Способы введения, предусмотренные для птиц и крупного рогатого скота, приводятся в иллюстративных целях и не являются ограничивающими.
Вакцинация птиц может быть выполнена в любом возрасте. Вакцинацию можно проводить до 18-ого дня эмбрионального развития (in ovo) и после для живого микроорганизма и для 3-х недельных и старше для инактивированных микроорганизмов или другого типа вакцины. Для вакцинации in ovo вакцины могут быть введены в последней четверти развития. Вакцину можно вводить подкожно, способом в фолликул пера, распылением, перорально, внутриглазно, интратрахеально, интраназально, in ovo или с помощью других способов, известных в данной области техники. Пероральные вакцины можно вводить в питьевой воде. Кроме того, предполагается, что способы по настоящему изобретению могут применяться на основе календарей плановой вакцинации.
Иммуномодулирующая композиция также может быть введена птицам подкожно, способом в фолликул пера, распылением, внутриглазно, интратрахеально, интраназально, in ovo или другими способами, известными в данной области техники. Например, иммуномодулирующая композиция может быть введена in ovo. Альтернативно, иммуномодулирующую композиции можно вводить в виде спрея.
Иммуномодулирующая композиция может быть введена in ovo птичьему эмбриону в последней четверти его развития. Например, иммуномодулирующая композиция может быть введена in ovo до 18-дневного возраста или 19-дневного возраста эмбриона. Введение in ovo может быть до заражения (или инфекции) или после заражения.
Иммуномодулятор может быть введен животному: птице или крупному рогатому скоту различных пород от около 1 до около 14 дней перед заражением или от около 1 до около 14 дней после заражения. Например, иммуномодулятор может быть введен от около 1 до около 7 дней перед заражением или от около 1 до около 7 дней после заражения. Иммуномодулятор удобно вводить на 1, 2, 3, 4, 5, 6, 7 день перед заражением или на 1, 2, 3, 4, 5, 6, 7 день после заражения.
Вакцинация крупного рогатого скота различных пород может быть выполнена в любом возрасте. Вакцину можно вводить внутривенно, внутримышечно, внутрикожно, внутрибрюшинно, подкожно, распылителем, перорально, внутриглазно, интратрахеально, интраназально или другими способами, известными в данной области техники. Кроме того, предполагается, что способы, описанные в настоящем документе, могут применяться на основе календарей плановой вакцинации.
Другие системы доставки могут включать системы доставки с постоянным высвобождением, с отсроченным высвобождением или с замедленным высвобождением. Такие системы помогут избежать повторных введений композиций, тем самым увеличивая удобство. Многие типы систем высвобождения лекарства доступны и известны специалистам в данной области техники. Они включают в себя системы на полимерной основе, такие как поли(лактид-гликолид), со-полиоксалаты, поликапролактоны, полиэфирамиды, полиортоэфиры, полигидроксимасляная кислота и полиангидриды. Микрокапсулы вышеуказанных полимеров, содержащие лекарственные средства, описаны, например, в патенте США N5,075,109.
Системы доставки также включают в себя полимерные системы, которые представляют собой липиды, включая стерины, такие как холестерин, сложные эфиры холестерина и жирных кислот или нейтральные жиры, такие как моно-, ди-, и триглицериды; гидрогелевые системы высвобождения; силастиновые системы; системы на основе пептидов; восковые покрытия; прессованные таблетки с использованием обычных связующих и вспомогательных веществ; частично расплавленные имплантаты; и тому подобное. Конкретные примеры включают в себя, но не ограничиваются этим, эрозионные системы, в которых агент по настоящему изобретению содержится внутри матрицы, такие, как системы, которые описаны в патентах США №№4,452,775, 4675189 и 5,736,152, а также диффузионные системы, в которых активный компонент высвобождается с контролируемой скоростью из полимера, такого, как описано в патентах США NN.3,854,480, 5,133,974 и 5,407,686. Кроме того, могут применяться системы доставки в виде изделия на основе насоса, некоторые из которых адаптированы для имплантации.
Поскольку могут быть сделаны различные изменения в указанной выше композиции, продуктов и способов, не выходя за рамки изобретения, предполагается, что весь материал, содержащийся в приведенном выше описании и в примерах, приведенных ниже, должны интерпретироваться как иллюстративные и не в ограничивающем смысле.
Определения
Термин "эффективное количество" относится к количеству необходимого или достаточного для реализации желаемого биологического эффекта. Например, эффективное количество иммуномодулятора для лечения или профилактики инфекционного заболевания является такое количество, которое необходимо, чтобы вызвать развитие иммунного ответа при воздействии микробов, тем самым вызывая снижение количества микроба у субъекта и предпочтительно уничтожение микробов. Эффективное количество для любого конкретного применения может варьироваться в зависимости от таких факторов, как заболевание или состояние, которое лечат, размер субъекта или тяжесть заболевания или состояния. Обычный специалист в данной области может эмпирически определить эффективное количество иммуномодулятора без необходимости чрезмерно большой экспериментальной работы.
Термин "цитокин" относится к семейству белков, усиливающих иммунитет. Семейство цитокинов включает гемопоэтический фактор роста, интерлейкины, интерфероны, молекулы суперсемейства иммуноглобулинов, молекулы семейства факторов некроза опухолей и хемокинов (т.е. белков, которые регулируют миграцию и активацию клеток, в частности, фагоцитов). Примеры цитокинов включают, без ограничения, интерлейкин-2 (ИЛ-2), интерлейкин-12 (ИЛ-12), интерлейкин-15 (ИЛ-15), интерлейкин-18 (ИЛ-18), интерферон-α (IFNα), и интерферон-γ (IFNγ;).
Термин "вызывать" может использоваться взаимозаменяемо с терминами активировать, стимулировать, генерировать или повышающее регулировать.
Термин «вызывающий иммунный ответ» у субъекта относится к специфически контролируемому или влияющему на активность иммунного ответа, и может включать в себя активацию иммунного ответа, повышающую регуляцию иммунного ответа, усиление иммунного ответа и/или изменение иммунного ответ (например, посредством стимулирования типа иммунного ответа, который, в свою очередь изменяет преобладающий тип иммунного ответа у субъекта из одного, который является вредным или неэффективным, на другой, который является полезным или защитным).
Выражение "функционально связанный" относится к связи молекулы нуклеиновой кислоты с последовательностью, контролирующей транскрипцию таким образом, что молекула способна экспрессироваться при трансфекции (т.е., при трансформации, при трансдукции или при трансфекции) в клетку-хозяина. Последовательности, контролирующие транскрипцию, представляют собой последовательности, которые контролируют инициацию, элонгацию и терминацию транскрипции. В частности, важные последовательности, контролирующие транскрипцию, являются такими, которые контролируют инициацию транскрипции, такие как промоторые, энхансерные, операторные и репрессорные последовательности. Разнообразие таких последовательностей, контролирующих транскрипцию, известны специалистам в данной области техники. Предпочтительные последовательности, контролирующие транскрипцию, включают последовательности, которые функционируют в клетках птиц, рыб, млекопитающих, бактерий, растений, насекомых и вирусах. В то время как любые последовательности, контролирующие транскрипцию, могут применяться с настоящим изобретением, последовательности могут включать в себя природные последовательности, контролирующие транскрипцию, естественным образом связанные с последовательностью, кодирующей иммуноген или белок, стимулирующий иммунитет.
Выражения "молекула нуклеиновой кислоты" и "последовательность нуклеиновой кислоты" могут применяться взаимозаменяемо и включают в себя ДНК, РНК или производные ДНК или РНК. Выражения также включают олигонуклеотиды и более крупные последовательности, такие как плазмиды, такие как иммуностимулирующие плазмиды, описанные в настоящем документе, в том числе как молекулы нуклеиновых кислот, которые кодируют белок или его фрагмент, так и молекулы нуклеиновых кислот, которые включают регуляторные области, интроны, или другие некодирующие ДНК или РНК. Как правило, олигонуклеотид имеет последовательность нуклеиновой кислоты от около 1 до около 500 нуклеотидов, и более типично по меньшей мере около 5 нуклеотидов в длину. Молекула нуклеиновой кислоты может быть получена из любого источника, включая млекопитающих, рыб, бактериальный, насекомых, вирусы, растения, синтетические источники или их комбинации. Молекула нуклеиновой кислоты может быть получена способами, обычно известными в данной области техники, такими как технологии рекомбинантной ДНК (например, полимеразная цепная реакция (ПЦР), амплификация, клонирование), или с помощью химического синтеза. Молекулы нуклеиновых кислот, включают природные молекулы нуклеиновых кислот и их гомологи, включая, но не ограничиваясь этим, природные аллельные варианты и модифицированные молекулы нуклеиновых кислот, в которых нуклеотиды были вставлены, делегированы, замещены, или в инвертированы таким образом, что такие модификации не мешают существенным образом способности молекулы нуклеиновой кислоты вызывать иммунный ответ, полезный в способах по настоящему изобретению. Гомологичная нуклеиновая кислота может быть получена с использованием ряда способов, известных специалистам в данной области техники (см., например, Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Labs Press, 1989), которая включена в данное описание посредством ссылки.
Выражения "селектируемый маркер" и "селектируемый маркерный ген" относится к гену, который кодирует продукт, который защищает организм, в котором ген экспрессируется от селекционного агента (например, антибиотика) или от условия, которые, как правило, убивают организм или тормозят его рост. Селектируемые маркерные гены наиболее часто являются генами устойчивости к антибиотикам (например, гены устойчивости к канамицину, гены устойчивости к ампициллину, гены устойчивости к хлорамфениколу, гены устойчивости к тетрациклину и т.д.). Так, например, когда клетки Е. coli подвергают процедуре трансформации, чтобы ввести плазмиду, кодирующую ген резистентности к канамицину, а затем культивируют на или в среде, содержащей канамицин, выживут только клетки Е. coli, которые успешно поглотили плазмиду и экспрессируют ген устойчивости к канамицину. Выражения "селектируемый маркер" и "маркерный ген" также включают в себя гены, которые кодируют ферменты, участвующие в синтезе соединения, которое является существенными для роста организма. При введении в ауксотрофный организм, который не может синтезировать необходимое соединение, такие гены позволяют организму расти в среде, которая была дополнена необходимым соединением. Например, бактериальные клетки, которые являются ауксотрофными по аминокислоте лизин вследствие мутации в ферменте или в отсутствии фермента, участвующего в биосинтезе лизина, обычно не в состоянии расти на среде, которая не была дополнена с лизином. Когда такие бактерии подвергают процедуре трансформации для введения плазмиды кодирующей фермент, участвующий в биосинтезе лизина, бактерии, которые успешно поглотили плазмиду и экспрессируют фермент, выживут при выращивании на средах, которые не дополнены лизином. Выражения "селектируемый маркер" и "маркерный ген" дополнительно включают в себя гены, которые позволяют проводить селекцию по яд/противоядие. Например, ген ccdB кодирует белок, который связывается с ДНК-гиразой, которая является основным ферментом для клеточного деления. После связывания с ДНК-гиразой, продукт гена ccdB ухудшает репликацию гена и индуцирует гибель клеток. Таким образом, бактерии, экспрессирующие продукт гена ccdB, не могут выжить. Ген ccdA кодирует белок ("противоядие"), который действует как естественный ингибитор продукта гена ccdB. Таким образом, когда бактерии, имеющие ген ccdB в своем бактериальном геноме, подвергаются процедуре трансформации с целью введения плазмиды, кодирующей продукт гена ccdA, выживут только клетки, которые успешно поглотили плазмиду и экспрессируют ген ccdA.
Выражения "скринируемый маркер" и "скринируемый маркерный ген" относятся к гену, который кодирует продукт, который позволяет наблюдателю различать клетки, экспрессирующие ген скринируемого маркера, и клетки, которые не экспрессируют ген скринируемого маркера. Системы скринируемых маркерных генов хорошо известны в данной области, и включают в себя, например, гены LacZ и гены, кодирующие флуоресцентные белки, такие как зеленый флуоресцентный белок (GFP), желтый флуоресцентный белок (YFP), красный флуоресцентный белок (RFP), синий флуоресцентный белок (BFP) или голубой флуоресцентный белок (CFP).
Как используется в данном описании термин "субъект", относится к живому организму, имеющему центральную нервную систему. В частности, субъекты включают в себя, но не ограничиваются этим, людей или пациентов и животных-компаньонов. Типичные животные-компаньоны могут включать одомашненных млекопитающих (например, собаки, кошки, лошади), млекопитающих со значительной коммерческой ценностью (например, птицы, жвачные животные различных пород, молочные коровы, крупный рогатый скот, спортивные животные), млекопитающих со значительными научными ценностями (например, содержащиеся в неволе или на свободном выпасе исчезающие виды) или млекопитающие, которые имеют ценность по иным причинам. Подходящие субъекты также включают в себя: мышей, крыс, собак, кошек, копытных, таких как крупный рогатый скот, свиней, овец, лошадей и коз, зайцеобразных, таких как кролики и зайцы, других грызунов и приматов, таких как обезьяны, шимпанзе и высших обезьян. Субъекты могут быть любым видом птиц, будь то домашние или дикие виды, и могут быть коммерчески выращиваемыми для разведения, для производства мяса или яиц. Типичные виды птиц включают, без ограничения, кур, индеек, гусей, уток, фазанов, перепелов, голубей, страусов, содержащихся в клетке птиц, птиц в зоологических коллекциях и вольерах и тому подобное. Субъектами могут быть любые виды крупного рогатого скота, будь то домашние или дикие, и могут быть коммерчески выращиваемыми для разведения для производства мяса или молока. Типичные виды крупного рогатого скота включают, без ограничения, антилоп, буйволов, яков, коров и быков, бизонов и тому подобное. Породы крупного рогатого скота включают без ограничения, коров, быков, бычков, телок, вола, мясного скота, молочного скота и тому подобное. Субъекты могут быть любым видом аквакультуры, в том числе без ограничения, любым видом рыб, ракообразных, моллюсков, живущих в пресной воде или соленой воде. В некоторых аспектах субъекты могут быть диагностированы по поводу инфекционного заболевания, могут быть подвержены риску инфекционного заболевания или могут иметь инфекционное заболевание. Субъекты могут быть любого возраста, включая в утробе матери, новорожденные, подростковый возраст, взрослые, среднего возраста или преклонного возраста.
ПРИМЕРЫ
Следующие не ограничивающие примеры предназначены для дополнительной иллюстрации настоящего изобретения.
Пример 1. Получение плазмиды pGCMB75.6.
Карта плазмиды pGCMB75.6 показана на Фиг. 2. В pGCMB75.6 ген устойчивости к канамицину рМВ75.6 (см. Фиг. 1) был заменен некодирующей последовательностью из Е. coli K-12. Для создания плазмиды pGCMB75.6 единичный сайт рестрикции AscI был введен в рМВ75.6 на 5'-участке гена устойчивости к канамицину для генерации pMB75.6_AscI (SEQ ID NO: 3). Для того, чтобы ввести сайт рестрикции AscI, аденин, присутствующий в последовательности pGCMB75.6, подвергали мутации в гуанин, тем самым изменяя последовательность AGCGCGCC в плазмиде pGCMB75.6 на GGCGCGCC. Эта модификация была выполнена с использованием подхода основанного на мутагенезе, посредством лигирования в процессе амплификации (лигазную цепную реакцию). Был использован единственный праймер, который нес сайт рестрикции AscI в середине цепи.
Фрагмент длиной 1779 нуклеотидов AscI (GGCGCGCC)/XhoI (CTCGAG) был синтезирован Life Technologies GmbH (Darmstadt, Germany). Этот фрагмент содержал пять областей, содержащих некодирующую последовательность из Е. coli К-12 (замены 1-5, сокращенно "ехс. 1", "ехс. 2" и т.д., показанные на Фиг. 2), F1 начало репликации и укороченный ген LacZ (см. Фиг. 2). В случае замены 4, последовательность Е. coli изменена вручную в нескольких местах, с тем чтобы увеличить содержание GC в плазмиде. Кроме того, в замене 2, один нуклеотид был заменен, чтобы удалить сайт рестрикции DraI, так что бы остался только один сайт DraI в плазмиде.
Как показано на Фиг. 2, pGCMB75.6 содержит несколько регуляторных элементов (начало репликации F1, промотор CMV, и начало репликации PUC) и сайт множественного клонирования (полилинкер). pGCMB75.6 также содержат укороченный ген LacZ. Однако, pGCMB75.6 не содержит какого-либо или функционального селектируемого и скринированного маркерного гена полной длины. pGCMB75.6 состоит из 4242 п.н. и содержит 283 CpG динуклеотидов.
Один из положительных клонов, который содержит новый введенный сайт AscI (pMB75.6_AscI), расщепляли с помощью AscI (GGCGCGCC)/XhoI (CTCGAG) для генерации фрагмента 2463, содержащего промотор CMV, сайт множественного клонирования, и начало репликации PUC (см. Фиг. 2). Синтезированный фрагмент AscI (GGCGCGCC)/XhoI (CTCGAG) в 1779 нуклеотида также расщепляли с помощью AscI/XhoI.
Оба фрагмента (фрагмент вектора 2463 нуклеотидов и фрагмент вставки 1779 нуклеотидов) подвергали элюировали из 1%-ного агарозного геля с использованием набора QIAquick Gel Extraction от Qiagen. Лигирование осуществляли с использованием 600 нг фрагмента 1779 нуклеотидов и 400 нг фрагмента вектора pMB75.6_AscI 2463 нуклеотидов в суммарном объеме 20 мкл, в течение ночи при 16°С. Затем 20 мкл подвергали диализу в течение 2 ч против 20 мл Н2О на льду, а затем смешивали с 5 мкл электрокомпетентных клеток DH5α Е. coli и 40 мкл H2O (Invitrogen F-f80lacZΔM15 A (Invitrogen F-f80lacZΔM15 Δ (lacZYA-argF) U169 recA1 endA1 hsdR17 (rk-, mk+) gal-phoA supE44λ-thi-1 gyrA96 relA1; Lot no. 1376481, Part no. 44-0097). После трансформации и регенерации 1 ч в SOC средах, клетки высевали на LB чашках без канамицина при 10-4 разведения. Это разведение позволяло выделить отдельные клоны.
ПЦР колоний проводили на отдельных клонах с использованием следующих праймеров, перечисленных в таблице 1.
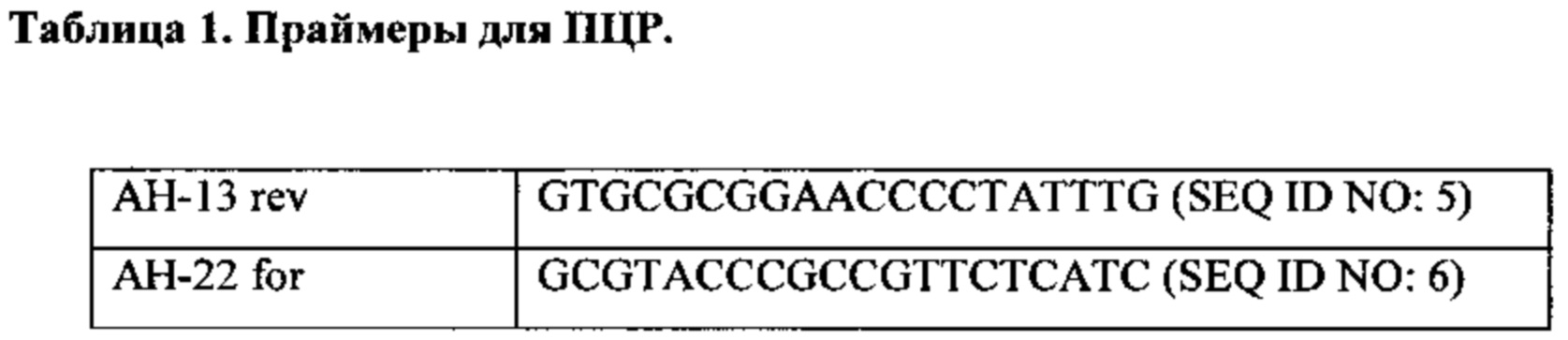
Локализации праймеров АН-13 rev и АН-22 for показаны на Фиг. 2. Использовали премикс, содержащий Taq-полимеразу. Продукты ПЦР наносили на 1% агарозный гель, содержащий этидий бромид. Положительные клоны, которые несли правильную плазмиду (pGCMB75.6) показали продукт 606 п.о.
В общей сложности более 10000 клонов подвергали скринингу, чтобы идентифицировать три положительных клона. Три положительных клона немедленно переносили на свежие LB чашки и использовали для создания 3 Research Cell Banks (банков клеток для исследования, RCB; Sys 3733, Sys 3734 и Sys 3735).
Параллельно среду засевали этими тремя клонами, и была сгенерирована плазмидная ДНК. Полную идентификацию последовательности каждого из трех субклонов проводили с использованием следующих праймеров, перечисленных в таблице 2.


Пример 2: Создание плазмиды pLacZMB75.6.
Для создания плазмиды pLacZMB75.6 (Фиг. 3, SEQ ID NO: 4) был синтезирован фрагмент XhoI (CTCGAG)/DraI (ТТТААА) в 1307 нуклеотидов компанией Life Technologies GmbH (Darmstadt, Germany). Этот фрагмент в 1307 нуклеотидов содержал часть гена LacZ (265 нуклеотидов). Таким образом, при лигировании в pGCMB75.6 этот фрагмент удлиняет укороченный ген LacZ, расположенный перед сайтом рестрикции XhoI, и позволяет гену LacZ экспрессироваться (ср. Фиг. 2 и Фиг. 3). Кроме того, 91 нуклеотидов сайта множественного клонирования были заменены некодирующей последовательностью Е. coli, с тем чтобы устранить гомологию последовательности с недавно введенной области гена LacZ и избежать рекомбинации. Кроме того, удаляли 5'-область промотора цитомегаловируса, (265 нуклеотидов) для того, чтобы генерировать плазмиду того же размера, что и плазмида pGCMB75.6.
pGCMB75.6 и синтезированный фрагмент в 1311 нуклеотидов были оба рестриктированы XhoI и DraI. Оба фрагмента геля элюировали из 1%-ного агарозного геля с использованием набора QIAquick Gel Extraction от Qiagen.
Лигирование проводили с использованием 240 нг фрагмента в 1311 нуклеотидов и 240 нг фрагмента вектора в суммарном объеме 20 мкл, в течение ночи при 16°С. Смешивали 3 мкл с 10 мкл электрокомпетентных клеток DH5α Е. coli (Invitrogen F-f80lacZΔM15 Δ (lacZYA-argF) U169 recA1 endA1 hsdR17 (rk-, mk+) gal-phoA supE44λ-thi-1 gyrA96 relA1; Lot no. 1376481, Part no. 44-0097) и 40 мкл 10%-ного раствора глицерина. После трансформации и 1 часовой регенерации в SOC средах, клетки высевали на LB-чашки X-Gal/IPTG без канамицина при разведении 10-2 и 10-4. Это разведение позволяло выделять отдельные клоны.
Идентификацию колоний с плазмидой проводили с помощью сине-белой селекции, и для подтверждения проводили ПЦР колоний с использованием следующих праймеров, перечисленных в таблице 3.

Локализация праймеров АН-15 и А-39 показана на Фиг. 3. Использовали премикс, содержащий Taq-полимеразу. Продукты ПЦР наносили на 1% агарозный гель, содержащий этидий бромид. Положительные клоны, которые несли правильную плазмиду (pLacZMB75.6) показал, продукт 777 п.н.
Были идентифицированы четыре положительных клонов, которые немедленно переносили на свежие чашки с LB, которые были использованы для создания Research Cell Banks (RCB; Sys 3736, Sys 3737, Sys 3738 и Sys 3739).
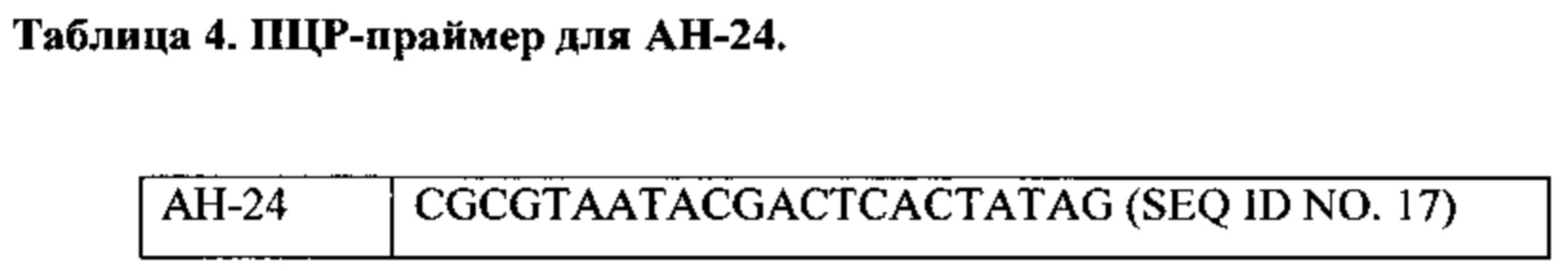
Параллельно среду засевали этими четырьмя клонами и была сгенерирована плазмидная ДНК. Полную идентификацию последовательности каждого из четырех субклонов проводили с использованием тех же праймеров, что и для pGCMB75.6, но вместо использованного праймера АН-16 (SEQ ID NO: 10) использовали праймер АН-24 (см. таблицу 4).
Пример 3: Иммуномодулирующая композиция
Иммуномодулятор представляет собой композицию, содержащую катионный липид и некодирующуюй ДНК-последовательность, описанную в настоящей заявке. Синтетические иммуномодулирующие липидные компоненты [1-[2-[9-(Z)-октадеценоилокси]]-2-[8](Z)-гептадецил]-3-[гидроксиэтил]имидазолиния хлорид (DOTIM) и синтетический нейтральный липид холестерин формулируются для получения липосом около 200 нм в диаметре (см. патент США 6,693,086). ДНК-компонентом является pGCMB75.6 или pLacZMB75.6. Будучи отрицательно заряженной, плазмидная ДНК образуют комплексы с положительно заряженными (катионными) липосомами (см. патент США 6,693,086).
Пример 4: Введение иммуномодулирующей композиции модели млекопитающего увеличило выживаемость при заражении вирусом.
Эффективность иммуномодулирующих композиций, описанных в настоящем документе, оценивали в модели млекопитающего, зараженного патогеном. Мышам вводили иммуномодулирующую композиции, содержащую ДНК pGCMB75.6 и катионные липосомы, посредством внутрибрюшинной инъекции. Иммуномодулирующую композицию вводили в концентрации 0,01 мкг, 0,02 мкг, 0,04 мкг и 1,00 мкг. Контрольным мышам вводили 0,9% раствор NaCl посредством внутрибрюшинной инъекции. Через двадцать четыре часа после введения иммуномодулятора всех животных заражали посредством введения вируса через внутрибрюшинную инъекцию (0,2 мл 103,4 KID50/мл). Стимулирующим вирусом был Pseudorabies (PR, вирус псевдобешенства). Коэффициенты выживаемости изображены на Фиг. 4. У мышей, получавших иммуномодулирующую композицию, описанную в настоящем документе, наблюдали более дозозависимые высокие коэффициенты выживаемости, чем у контрольных мышей.
Пример 5: Введение иммуномодулирующей композиции в птичьей модели увеличило выводимость и выживаемость при заражении патогеном.
Эффективность иммуномодулирующих композиций, описанных в настоящем документе, оценивали в птичьей модели при заражении патогеном посредством распыления на день Е19 (эмбриональный день 19). В куриные яйца вводили иммуномодулирующую композиции, содержащую pGCMB75.6 ДНК и катионные липосомы, посредством введения in ovo в день Е18 (эмбриональный день 18). Контрольные яйца получали в качестве плацебо-контроля разбавитель (D5W) (in ovo). BHI бульон (спрей) был использован в качестве имитации заражения (Т1). Подробная информация о лечебных группах исследования представлены в таблице 5 ниже.
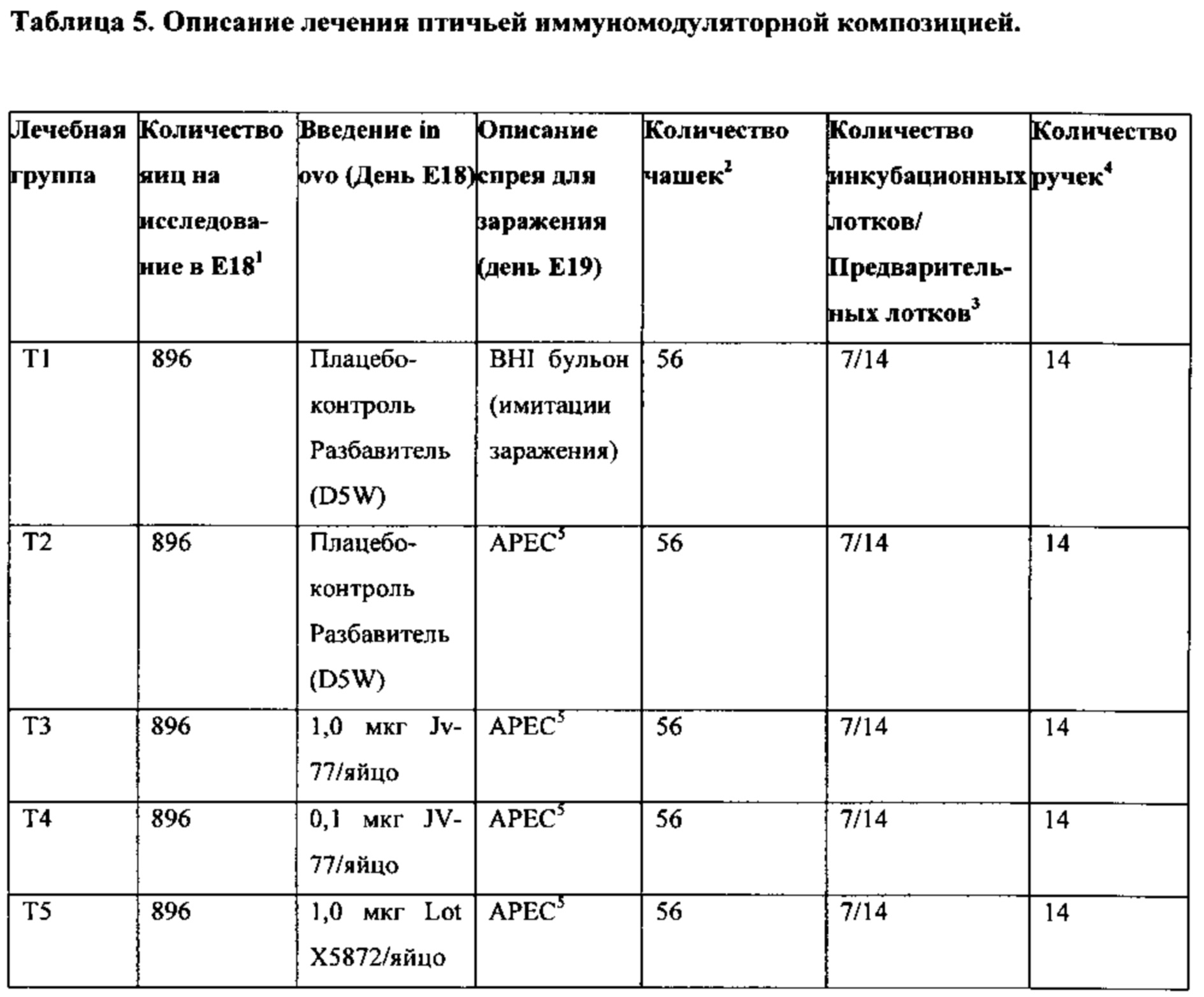

1 День 18 инкубации яиц;2 16 яиц на чашку;3 64 яиц на суб-лоток (разделенный для размещения двух групп на лоток);4 Птенцы, вылупившиеся из каждой секции лотка переносились одной ручкой;5 Патогенная для птиц Escherichia coli (АТЭС).
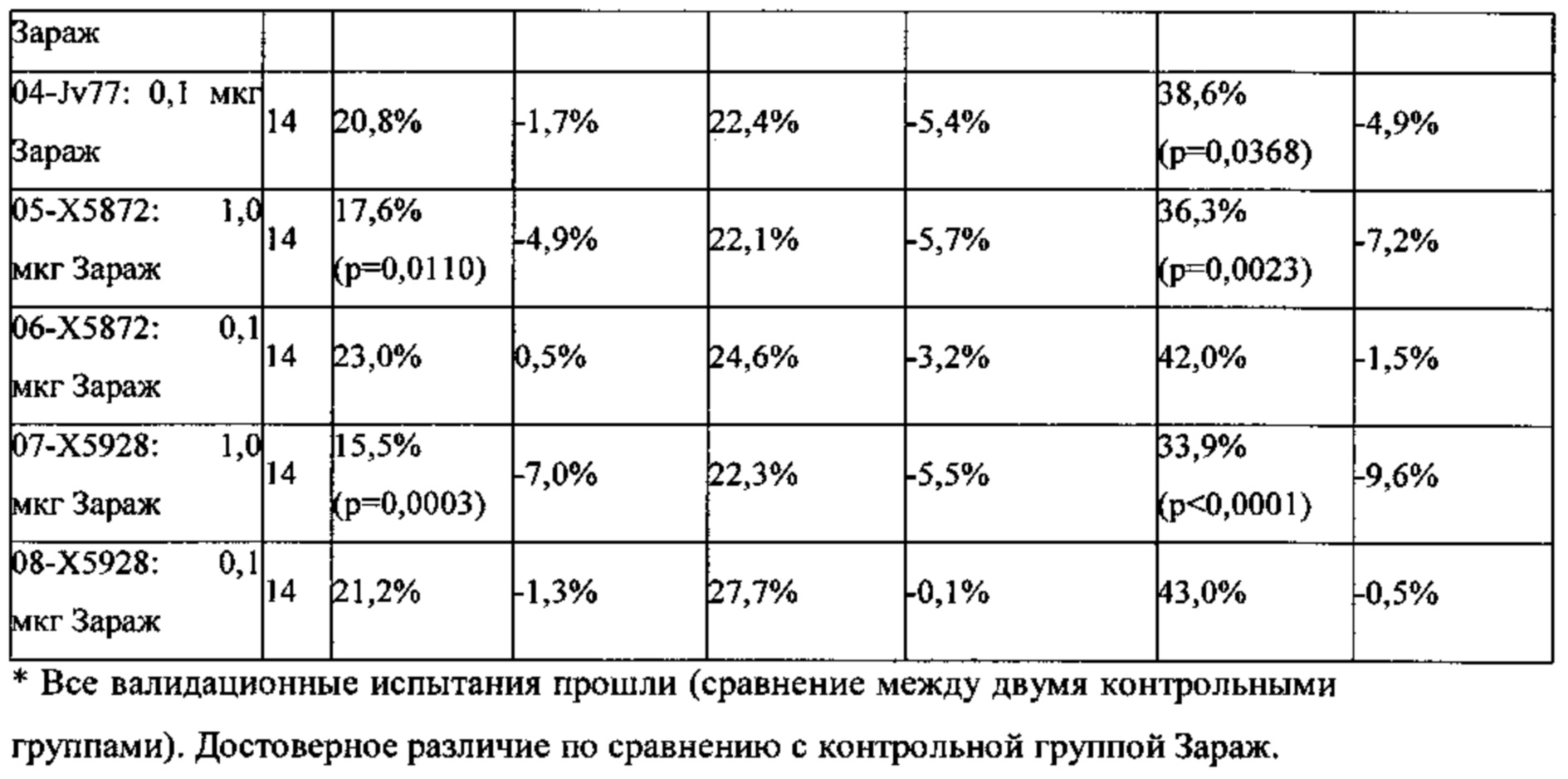
Компонент ДНК иммуномодулирующей композиции включает один из трех клонов, выделенных из pGCMB75.6 ДНК (т.е. Jv77, Х5872 или Х5928). Как можно видеть из результатов, суммированных в таблице 6 ниже, как средняя выводимость, так и средняя выживаемость были улучшены, если вводили иммуномодулирующую композицию, описанную в настоящем документе, по сравнению с яйцами, получившим контрольное лечение.

При введении элементов настоящего изобретения или предпочтительных вариантов выполнения, форма единственного числа и термин "указанный" предназначены для обозначения, что существует один или несколько из элементов. Термины "содержащий", "включающий" и "имеющий" подразумевает включение и означают, что могут быть и другие, чем перечисленные элементы дополнительные элементы.
С учетом вышеизложенного, можно видеть, что некоторые задачи настоящего изобретения достигаются, а другие полезные результаты достигнуты.
Поскольку могут быть сделаны различные изменения в вышеуказанных продуктах, композициях и способах, не выходя за рамки изобретения, предполагается, что весь материал, содержащийся в приведенном выше описании, и продемонстрированный на прилагаемых чертежах, следует интерпретировать как иллюстративный и не ограничивающий.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Eicker, Andrea
<120> ИММУНОСТИМУЛИРУЮЩИЕ ПЛАЗМИДЫ
<130> BAYR 6436.PRO
<160> 17
<170> PatentIn version 3.5
<210> 1
<211> 4242
<212> ДНК
<213> искусственная последовательность
<220>
<223> нуклеотидная последовательность плазмиды pGCMB75.6
<400> 1
tgaccgccca acgacccccg cccattgacg tcaataatga cgtatgttcc catagtaacg 60
ccaataggga ctttccattg acgtcaatgg gtggagtatt tacggtaaac tgcccacttg 120
gcagtacatc aagtgtatca tatgccaagt ccgcccccta ttgacgtcaa tgacggtaaa 180
tggcccgcct ggcattatgc ccagtacatg accttacggg actttcctac ttggcagtac 240
atctacgtat tagtcatcgc tattaccatg gtgatgcggt tttggcagta catcaatggg 300
cgtggatagc ggtttgactc acggggattt ccaagtctcc accccattga cgtcaatggg 360
agtttgtttt ggcaccaaaa tcaacgggac tttccaaaat gtcgtaacaa ctccgcccca 420
ttgacgcaaa tgggcggtag gcgtgtacgg tgggaggtct atataagcag agctcgttta 480
gtgaaccgtc agatcgcctg gagacgccat ccacgctgtt ttgacctcca tagaagacac 540
cgggaccgat ccagcctccc ctcgaagccg atctgataac ggtaccgata agctggcggc 600
cgattaagct acagaagttg gtcgtgaggc actgggcagg taagtatcaa ggttacaaga 660
caggtttaag gagaccaata gaaactgggc ttgtcgagac agagaagact cttgcgtttc 720
tgataggcac ctattggtct tactgacatc cactttgcct ttctctccac aggtgtccac 780
tcccaggttc aattacagct cttaagcagc cgcaagcttg atatcgaatt cctgcagccc 840
gggggatcca ctagttctag agcggccgcc accgcggtgg agctcgaatt atcagatcga 900
ttaataacta tgctcaaaaa ttgtgtacct ttagcttttt aatttgtaaa ggggttaata 960
aggaatattt gatgtatagt gccttgacta gagatcataa tcagccatac cacatttgta 1020
gaggttttac ttgctttaaa aaacctccca cacctccccc tgaacctgaa acataaaatg 1080
aatgcaattg ttgttgttaa cttgtttatt gcagcttata atggttacaa ataaagcaat 1140
agcatcacaa atttcacaaa taaagcattt ttttcactgc attctagttg tggtttgtcc 1200
aaactcatca atgtatctta tcatgtctgg atcatcagat ctgccggtct ccctatagtg 1260
agtcgtatta atttcgataa gccaggttaa cctgcattaa tgaatcggcc aacgcgcggg 1320
gagaggcggt ttgcgtattg ggcgctcttc cgcttcctcg ctcactgact cgctgcgctc 1380
ggtcgttcgg ctgcggcgag cggtatcagc tcactcaaag gcggtaatac ggttatccac 1440
agaatcaggg gataacgcag gaaagaacat gtgagcaaaa ggccagcaaa aggccaggaa 1500
ccgtaaaaag gccgcgttgc tggcgttttt ccataggctc cgcccccctg acgagcatca 1560
caaaaatcga cgctcaagtc agaggtggcg aaacccgaca ggactataaa gataccaggc 1620
gtttccccct ggaagctccc tcgtgcgctc tcctgttccg accctgccgc ttaccggata 1680
cctgtccgcc tttctccctt cgggaagcgt ggcgctttct catagctcac gctgtaggta 1740
tctcagttcg gtgtaggtcg ttcgctccaa gctgggctgt gtgcacgaac cccccgttca 1800
gcccgaccgc tgcgccttat ccggtaacta tcgtcttgag tccaacccgg taagacacga 1860
cttatcgcca ctggcagcag ccactggtaa caggattagc agagcgaggt atgtaggcgg 1920
tgctacagag ttcttgaagt ggtggcctaa ctacggctac actagaagaa cagtatttgg 1980
tatctgcgct ctgctgaagc cagttacctt cggaaaaaga gttggtagct cttgatccgg 2040
caaacaaacc accgctggta gcggtggttt ttttgtttgc aagcagcaga ttacgcgcag 2100
aaaaaaagga tctcaagaag atcctttgat cttttctacg gggtctgacg ctcagtggaa 2160
cgaaaactca cgttaaggga ttttggtcat gggcgcgcct aggcttttgc aaagatcgat 2220
caagagacag gatgaggatc gtttcgcagc ttttcattct gactgcaacg ggcaataagt 2280
ctctgtgtgg attaaaaaaa gagtgtctga tagcagcttc tgaactggtt acctgccgtg 2340
agtaaattaa aattttattg acttaggtca ctaaggcgcc ttgcgctgag gttgcgtcgt 2400
gatatcatca gggcagaccg gttacatccc cctaacaagc tgtataaaga gaaatactat 2460
ctcattggcg ttgcccgcac ctgacagtgc gacgttgggc tgcgtccgtc gaccaacggt 2520
accgaggtaa cagcccaatc tatccatgat ctcggccagg ccgggtcggc cgttatgcag 2580
cccggctcgg gtatgaagcc attaaggagc cgacccagcg cgaccgggcg gccggtcacg 2640
ctgcctctgc tgaagcctgc ctgtcactcc ctgcgcggcg tacccgccgt tctcatcgag 2700
taggctccgg atcgcgaccc cggacgggcc ctgggcccag gagcggccta tgacaaatgc 2760
cgggtagcga tccggcattc agcattgact gcgcacggat ccagtccttg caggagcctt 2820
atgccgaccg tagcaaaaaa tgagcccgag ccgatcgcga gttgtgatcc ggtcccgccg 2880
attgccggtc gcgatgacgg tcctgtgtaa gcgttatcgt taccaattgt ttaagaagta 2940
tatacgctac gaggtacttg ataacttctg cgtagcatac atgaggtttt gtataaaaat 3000
ggcgggcgat atcaacgcag tgtcagaaat ccgaaacagt ctgcgggact ctggggttcg 3060
aaatgaccga ccaagcgacg cccaacctgc catcacgaga tttcgattcc accgccgcct 3120
tctatgaaag gttgggcttc ggaatcgttt tccgggacgc cggctggatg atcctccagc 3180
gcggggatct catgctggag ttcttcgccc accctaggcg cgctcatgag cggatacata 3240
tttgaatgta tttagaaaaa taaacaaata ggggttccgc gcacatttcc ccgaaaagtg 3300
ccacctaaat tgtaagcgtt aatattttgt taaaattcgc gttaaatttt tgttaaatca 3360
gctcattttt taaccaatag gccgaaatcg gcaaaatccc ttataaatca aaagaataga 3420
ccgagatagg gttgagtgtt gttccagttt ggaacaagag tccactatta aagaacgtgg 3480
actccaacgt caaagggcga aaaaccgtct atcagggcga tggcccacta cgtgaaccat 3540
caccctaatc aagttttttg gggtcgaggt gccgtaaagc actaaatcgg aaccctaaag 3600
ggagcccccg atttagagct tgacggggaa agccggcgaa cgtggcgaga aaggaaggga 3660
agaaagcgaa aggagcgggc gctagggcgc tggcaagtgt agcggtcacg ctgcgcgtaa 3720
ccaccacacc cgccgcgctt aatgcgccgc tacagggcgc gtcccattcg ccattcaggc 3780
tgcgcaactg ttgggaaggg cgatcggtgc gggcctcttc gctattacgc cagctggcga 3840
aagggggatg tgctgcaagg cgattaagtt gggtaacgcc agggttttcc cagtcacgac 3900
gttgtaaaac gacggccagt gagcgcgcgt aatacgactc actatagggc gaattgggta 3960
ccgggccccc cctcgagcag gatctataca ttgaatcaat attggcaatt agccatatta 4020
gtcattggtt atatagcata aatcaatatt ggctattggc cattgcatac gttgtatcta 4080
tatcataata tgtacattta tattggctca tgtccaatat gaccgccatg ttgacattga 4140
ttattgacta gttattaata gtaatcaatt acggggtcat tagttcatag cccatatatg 4200
gagttccgcg ttacataact tacggtaaat ggcccgcctg gc 4242
<210> 2
<211> 4242
<212> ДНК
<213> искусственная последовательность
<220>
<223> нуклеотидная последовательность плазмиды pMB75.6
<400> 2
ctaaattgta agcgttaata ttttgttaaa attcgcgtta aatttttgtt aaatcagctc 60
attttttaac caataggccg aaatcggcaa aatcccttat aaatcaaaag aatagaccga 120
gatagggttg agtgttgttc cagtttggaa caagagtcca ctattaaaga acgtggactc 180
caacgtcaaa gggcgaaaaa ccgtctatca gggcgatggc ccactacgtg aaccatcacc 240
ctaatcaagt tttttggggt cgaggtgccg taaagcacta aatcggaacc ctaaagggag 300
cccccgattt agagcttgac ggggaaagcc ggcgaacgtg gcgagaaagg aagggaagaa 360
agcgaaagga gcgggcgcta gggcgctggc aagtgtagcg gtcacgctgc gcgtaaccac 420
cacacccgcc gcgcttaatg cgccgctaca gggcgcgtcc cattcgccat tcaggctgcg 480
caactgttgg gaagggcgat cggtgcgggc ctcttcgcta ttacgccagc tggcgaaagg 540
gggatgtgct gcaaggcgat taagttgggt aacgccaggg ttttcccagt cacgacgttg 600
taaaacgacg gccagtgagc gcgcgtaata cgactcacta tagggcgaat tgggtaccgg 660
gccccccctc gagcaggatc tatacattga atcaatattg gcaattagcc atattagtca 720
ttggttatat agcataaatc aatattggct attggccatt gcatacgttg tatctatatc 780
ataatatgta catttatatt ggctcatgtc caatatgacc gccatgttga cattgattat 840
tgactagtta ttaatagtaa tcaattacgg ggtcattagt tcatagccca tatatggagt 900
tccgcgttac ataacttacg gtaaatggcc cgcctggctg accgcccaac gacccccgcc 960
cattgacgtc aataatgacg tatgttccca tagtaacgcc aatagggact ttccattgac 1020
gtcaatgggt ggagtattta cggtaaactg cccacttggc agtacatcaa gtgtatcata 1080
tgccaagtcc gccccctatt gacgtcaatg acggtaaatg gcccgcctgg cattatgccc 1140
agtacatgac cttacgggac tttcctactt ggcagtacat ctacgtatta gtcatcgcta 1200
ttaccatggt gatgcggttt tggcagtaca tcaatgggcg tggatagcgg tttgactcac 1260
ggggatttcc aagtctccac cccattgacg tcaatgggag tttgttttgg caccaaaatc 1320
aacgggactt tccaaaatgt cgtaacaact ccgccccatt gacgcaaatg ggcggtaggc 1380
gtgtacggtg ggaggtctat ataagcagag ctcgtttagt gaaccgtcag atcgcctgga 1440
gacgccatcc acgctgtttt gacctccata gaagacaccg ggaccgatcc agcctcccct 1500
cgaagccgat ctgataacgg taccgataag ctggcggccg attaagctac agaagttggt 1560
cgtgaggcac tgggcaggta agtatcaagg ttacaagaca ggtttaagga gaccaataga 1620
aactgggctt gtcgagacag agaagactct tgcgtttctg ataggcacct attggtctta 1680
ctgacatcca ctttgccttt ctctccacag gtgtccactc ccaggttcaa ttacagctct 1740
taagcagccg caagcttgat atcgaattcc tgcagcccgg gggatccact agttctagag 1800
cggccgccac cgcggtggag ctcgaattat cagatcgatt aataactatg ctcaaaaatt 1860
gtgtaccttt agctttttaa tttgtaaagg ggttaataag gaatatttga tgtatagtgc 1920
cttgactaga gatcataatc agccatacca catttgtaga ggttttactt gctttaaaaa 1980
acctcccaca cctccccctg aacctgaaac ataaaatgaa tgcaattgtt gttgttaact 2040
tgtttattgc agcttataat ggttacaaat aaagcaatag catcacaaat ttcacaaata 2100
aagcattttt ttcactgcat tctagttgtg gtttgtccaa actcatcaat gtatcttatc 2160
atgtctggat catcagatct gccggtctcc ctatagtgag tcgtattaat ttcgataagc 2220
caggttaacc tgcattaatg aatcggccaa cgcgcgggga gaggcggttt gcgtattggg 2280
cgctcttccg cttcctcgct cactgactcg ctgcgctcgg tcgttcggct gcggcgagcg 2340
gtatcagctc actcaaaggc ggtaatacgg ttatccacag aatcagggga taacgcagga 2400
aagaacatgt gagcaaaagg ccagcaaaag gccaggaacc gtaaaaaggc cgcgttgctg 2460
gcgtttttcc ataggctccg cccccctgac gagcatcaca aaaatcgacg ctcaagtcag 2520
aggtggcgaa acccgacagg actataaaga taccaggcgt ttccccctgg aagctccctc 2580
gtgcgctctc ctgttccgac cctgccgctt accggatacc tgtccgcctt tctcccttcg 2640
ggaagcgtgg cgctttctca tagctcacgc tgtaggtatc tcagttcggt gtaggtcgtt 2700
cgctccaagc tgggctgtgt gcacgaaccc cccgttcagc ccgaccgctg cgccttatcc 2760
ggtaactatc gtcttgagtc caacccggta agacacgact tatcgccact ggcagcagcc 2820
actggtaaca ggattagcag agcgaggtat gtaggcggtg ctacagagtt cttgaagtgg 2880
tggcctaact acggctacac tagaagaaca gtatttggta tctgcgctct gctgaagcca 2940
gttaccttcg gaaaaagagt tggtagctct tgatccggca aacaaaccac cgctggtagc 3000
ggtggttttt ttgtttgcaa gcagcagatt acgcgcagaa aaaaaggatc tcaagaagat 3060
cctttgatct tttctacggg gtctgacgct cagtggaacg aaaactcacg ttaagggatt 3120
ttggtcatga gcgcgcctag gcttttgcaa agatcgatca agagacagga tgaggatcgt 3180
ttcgcatgat tgaacaagat ggattgcacg caggttctcc ggccgcttgg gtggagaggc 3240
tattcggcta tgactgggca caacagacaa tcggctgctc tgatgccgcc gtgttccggc 3300
tgtcagcgca ggggcgcccg gttctttttg tcaagaccga cctgtccggt gccctgaatg 3360
aactgcaaga cgaggcagcg cggctatcgt ggctggccac gacgggcgtt ccttgcgcag 3420
ctgtgctcga cgttgtcact gaagcgggaa gggactggct gctattgggc gaagtgccgg 3480
ggcaggatct cctgtcatct caccttgctc ctgccgagaa agtatccatc atggctgatg 3540
caatgcggcg gctgcatacg cttgatccgg ctacctgccc attcgaccac caagcgaaac 3600
atcgcatcga gcgagcacgt actcggatgg aagccggtct tgtcgatcag gatgatctgg 3660
acgaagagca tcaggggctc gcgccagccg aactgttcgc caggctcaag gcgagcatgc 3720
ccgacggcga ggatctcgtc gtgacccatg gcgatgcctg cttgccgaat atcatggtgg 3780
aaaatggccg cttttctgga ttcatcgact gtggccggct gggtgtggcg gaccgctatc 3840
aggacatagc gttggctacc cgtgatattg ctgaagagct tggcggcgaa tgggctgacc 3900
gcttcctcgt gctttacggt atcgccgctc ccgattcgca gcgcatcgcc ttctatcgcc 3960
ttcttgacga gttcttctga gcgggactct ggggttcgaa atgaccgacc aagcgacgcc 4020
caacctgcca tcacgagatt tcgattccac cgccgccttc tatgaaaggt tgggcttcgg 4080
aatcgttttc cgggacgccg gctggatgat cctccagcgc ggggatctca tgctggagtt 4140
cttcgcccac cctaggcgcg ctcatgagcg gatacatatt tgaatgtatt tagaaaaata 4200
aacaaatagg ggttccgcgc acatttcccc gaaaagtgcc ac 4242
<210> 3
<211> 4242
<212> ДНК
<213> искусственная последовательность
<220>
<223> нуклеотидная последовательность плазмиды pMB75.6_AscI
<400> 3
tgaccgccca acgacccccg cccattgacg tcaataatga cgtatgttcc catagtaacg 60
ccaataggga ctttccattg acgtcaatgg gtggagtatt tacggtaaac tgcccacttg 120
gcagtacatc aagtgtatca tatgccaagt ccgcccccta ttgacgtcaa tgacggtaaa 180
tggcccgcct ggcattatgc ccagtacatg accttacggg actttcctac ttggcagtac 240
atctacgtat tagtcatcgc tattaccatg gtgatgcggt tttggcagta catcaatggg 300
cgtggatagc ggtttgactc acggggattt ccaagtctcc accccattga cgtcaatggg 360
agtttgtttt ggcaccaaaa tcaacgggac tttccaaaat gtcgtaacaa ctccgcccca 420
ttgacgcaaa tgggcggtag gcgtgtacgg tgggaggtct atataagcag agctcgttta 480
gtgaaccgtc agatcgcctg gagacgccat ccacgctgtt ttgacctcca tagaagacac 540
cgggaccgat ccagcctccc ctcgaagccg atctgataac ggtaccgata agctggcggc 600
cgattaagct acagaagttg gtcgtgaggc actgggcagg taagtatcaa ggttacaaga 660
caggtttaag gagaccaata gaaactgggc ttgtcgagac agagaagact cttgcgtttc 720
tgataggcac ctattggtct tactgacatc cactttgcct ttctctccac aggtgtccac 780
tcccaggttc aattacagct cttaagcagc cgcaagcttg atatcgaatt cctgcagccc 840
gggggatcca ctagttctag agcggccgcc accgcggtgg agctcgaatt atcagatcga 900
ttaataacta tgctcaaaaa ttgtgtacct ttagcttttt aatttgtaaa ggggttaata 960
aggaatattt gatgtatagt gccttgacta gagatcataa tcagccatac cacatttgta 1020
gaggttttac ttgctttaaa aaacctccca cacctccccc tgaacctgaa acataaaatg 1080
aatgcaattg ttgttgttaa cttgtttatt gcagcttata atggttacaa ataaagcaat 1140
agcatcacaa atttcacaaa taaagcattt ttttcactgc attctagttg tggtttgtcc 1200
aaactcatca atgtatctta tcatgtctgg atcatcagat ctgccggtct ccctatagtg 1260
agtcgtatta atttcgataa gccaggttaa cctgcattaa tgaatcggcc aacgcgcggg 1320
gagaggcggt ttgcgtattg ggcgctcttc cgcttcctcg ctcactgact cgctgcgctc 1380
ggtcgttcgg ctgcggcgag cggtatcagc tcactcaaag gcggtaatac ggttatccac 1440
agaatcaggg gataacgcag gaaagaacat gtgagcaaaa ggccagcaaa aggccaggaa 1500
ccgtaaaaag gccgcgttgc tggcgttttt ccataggctc cgcccccctg acgagcatca 1560
caaaaatcga cgctcaagtc agaggtggcg aaacccgaca ggactataaa gataccaggc 1620
gtttccccct ggaagctccc tcgtgcgctc tcctgttccg accctgccgc ttaccggata 1680
cctgtccgcc tttctccctt cgggaagcgt ggcgctttct catagctcac gctgtaggta 1740
tctcagttcg gtgtaggtcg ttcgctccaa gctgggctgt gtgcacgaac cccccgttca 1800
gcccgaccgc tgcgccttat ccggtaacta tcgtcttgag tccaacccgg taagacacga 1860
cttatcgcca ctggcagcag ccactggtaa caggattagc agagcgaggt atgtaggcgg 1920
tgctacagag ttcttgaagt ggtggcctaa ctacggctac actagaagaa cagtatttgg 1980
tatctgcgct ctgctgaagc cagttacctt cggaaaaaga gttggtagct cttgatccgg 2040
caaacaaacc accgctggta gcggtggttt ttttgtttgc aagcagcaga ttacgcgcag 2100
aaaaaaagga tctcaagaag atcctttgat cttttctacg gggtctgacg ctcagtggaa 2160
cgaaaactca cgttaaggga ttttggtcat gggcgcgcct aggcttttgc aaagatcgat 2220
caagagacag gatgaggatc gtttcgcatg attgaacaag atggattgca cgcaggttct 2280
ccggccgctt gggtggagag gctattcggc tatgactggg cacaacagac aatcggctgc 2340
tctgatgccg ccgtgttccg gctgtcagcg caggggcgcc cggttctttt tgtcaagacc 2400
gacctgtccg gtgccctgaa tgaactgcaa gacgaggcag cgcggctatc gtggctggcc 2460
acgacgggcg ttccttgcgc agctgtgctc gacgttgtca ctgaagcggg aagggactgg 2520
ctgctattgg gcgaagtgcc ggggcaggat ctcctgtcat ctcaccttgc tcctgccgag 2580
aaagtatcca tcatggctga tgcaatgcgg cggctgcata cgcttgatcc ggctacctgc 2640
ccattcgacc accaagcgaa acatcgcatc gagcgagcac gtactcggat ggaagccggt 2700
cttgtcgatc aggatgatct ggacgaagag catcaggggc tcgcgccagc cgaactgttc 2760
gccaggctca aggcgagcat gcccgacggc gaggatctcg tcgtgaccca tggcgatgcc 2820
tgcttgccga atatcatggt ggaaaatggc cgcttttctg gattcatcga ctgtggccgg 2880
ctgggtgtgg cggaccgcta tcaggacata gcgttggcta cccgtgatat tgctgaagag 2940
cttggcggcg aatgggctga ccgcttcctc gtgctttacg gtatcgccgc tcccgattcg 3000
cagcgcatcg ccttctatcg ccttcttgac gagttcttct gagcgggact ctggggttcg 3060
aaatgaccga ccaagcgacg cccaacctgc catcacgaga tttcgattcc accgccgcct 3120
tctatgaaag gttgggcttc ggaatcgttt tccgggacgc cggctggatg atcctccagc 3180
gcggggatct catgctggag ttcttcgccc accctaggcg cgctcatgag cggatacata 3240
tttgaatgta tttagaaaaa taaacaaata ggggttccgc gcacatttcc ccgaaaagtg 3300
ccacctaaat tgtaagcgtt aatattttgt taaaattcgc gttaaatttt tgttaaatca 3360
gctcattttt taaccaatag gccgaaatcg gcaaaatccc ttataaatca aaagaataga 3420
ccgagatagg gttgagtgtt gttccagttt ggaacaagag tccactatta aagaacgtgg 3480
actccaacgt caaagggcga aaaaccgtct atcagggcga tggcccacta cgtgaaccat 3540
caccctaatc aagttttttg gggtcgaggt gccgtaaagc actaaatcgg aaccctaaag 3600
ggagcccccg atttagagct tgacggggaa agccggcgaa cgtggcgaga aaggaaggga 3660
agaaagcgaa aggagcgggc gctagggcgc tggcaagtgt agcggtcacg ctgcgcgtaa 3720
ccaccacacc cgccgcgctt aatgcgccgc tacagggcgc gtcccattcg ccattcaggc 3780
tgcgcaactg ttgggaaggg cgatcggtgc gggcctcttc gctattacgc cagctggcga 3840
aagggggatg tgctgcaagg cgattaagtt gggtaacgcc agggttttcc cagtcacgac 3900
gttgtaaaac gacggccagt gagcgcgcgt aatacgactc actatagggc gaattgggta 3960
ccgggccccc cctcgagcag gatctataca ttgaatcaat attggcaatt agccatatta 4020
gtcattggtt atatagcata aatcaatatt ggctattggc cattgcatac gttgtatcta 4080
tatcataata tgtacattta tattggctca tgtccaatat gaccgccatg ttgacattga 4140
ttattgacta gttattaata gtaatcaatt acggggtcat tagttcatag cccatatatg 4200
gagttccgcg ttacataact tacggtaaat ggcccgcctg gc 4242
<210> 4
<211> 4242
<212> ДНК
<213> искусственная последовательность
<220>
<223> нуклеотидная последовательность плазмиды pLacZMB75.6
<400> 4
tgaccgccca acgacccccg cccattgacg tcaataatga cgtatgttcc catagtaacg 60
ccaataggga ctttccattg acgtcaatgg gtggagtatt tacggtaaac tgcccacttg 120
gcagtacatc aagtgtatca tatgccaagt ccgcccccta ttgacgtcaa tgacggtaaa 180
tggcccgcct ggcattatgc ccagtacatg accttacggg actttcctac ttggcagtac 240
atctacgtat tagtcatcgc tattaccatg gtgatgcggt tttggcagta catcaatggg 300
cgtggatagc ggtttgactc acggggattt ccaagtctcc accccattga cgtcaatggg 360
agtttgtttt ggcaccaaaa tcaacgggac tttccaaaat gtcgtaacaa ctccgcccca 420
ttgacgcaaa tgggcggtag gcgtgtacgg tgggaggtct atataagcag agctcgttta 480
gtgaaccgtc agatcgcctg gagacgccat ccacgctgtt ttgacctcca tagaagacac 540
cgggaccgat ccagcctccc ctcgaagccg atctgataac ggtaccgata agctggcggc 600
cgattaagct acagaagttg gtcgtgaggc actgggcagg taagtatcaa ggttacaaga 660
caggtttaag gagaccaata gaaactgggc ttgtcgagac agagaagact cttgcgtttc 720
tgataggcac ctattggtct tactgacatc cactttgcct ttctctccac aggtgtccac 780
tcccaggttc aattacagct cttaagcagc cgccaaaaca aaattcctca aaaatcatca 840
tcgaatgaat ggtgaaataa tttccctgaa taactgtagt gttttcaggg cgcggcataa 900
taattaacta tgctcaaaaa ttgtgtacct ttagcttttt aatttgtaaa ggggttaata 960
aggaatattt gatgtatagt gccttgacta gagatcataa tcagccatac cacatttgta 1020
gaggttttac ttgctttaaa aaacctccca cacctccccc tgaacctgaa acataaaatg 1080
aatgcaattg ttgttgttaa cttgtttatt gcagcttata atggttacaa ataaagcaat 1140
agcatcacaa atttcacaaa taaagcattt ttttcactgc attctagttg tggtttgtcc 1200
aaactcatca atgtatctta tcatgtctgg atcatcagat ctgccggtct ccctatagtg 1260
agtcgtatta atttcgataa gccaggttaa cctgcattaa tgaatcggcc aacgcgcggg 1320
gagaggcggt ttgcgtattg ggcgctcttc cgcttcctcg ctcactgact cgctgcgctc 1380
ggtcgttcgg ctgcggcgag cggtatcagc tcactcaaag gcggtaatac ggttatccac 1440
agaatcaggg gataacgcag gaaagaacat gtgagcaaaa ggccagcaaa aggccaggaa 1500
ccgtaaaaag gccgcgttgc tggcgttttt ccataggctc cgcccccctg acgagcatca 1560
caaaaatcga cgctcaagtc agaggtggcg aaacccgaca ggactataaa gataccaggc 1620
gtttccccct ggaagctccc tcgtgcgctc tcctgttccg accctgccgc ttaccggata 1680
cctgtccgcc tttctccctt cgggaagcgt ggcgctttct catagctcac gctgtaggta 1740
tctcagttcg gtgtaggtcg ttcgctccaa gctgggctgt gtgcacgaac cccccgttca 1800
gcccgaccgc tgcgccttat ccggtaacta tcgtcttgag tccaacccgg taagacacga 1860
cttatcgcca ctggcagcag ccactggtaa caggattagc agagcgaggt atgtaggcgg 1920
tgctacagag ttcttgaagt ggtggcctaa ctacggctac actagaagaa cagtatttgg 1980
tatctgcgct ctgctgaagc cagttacctt cggaaaaaga gttggtagct cttgatccgg 2040
caaacaaacc accgctggta gcggtggttt ttttgtttgc aagcagcaga ttacgcgcag 2100
aaaaaaagga tctcaagaag atcctttgat cttttctacg gggtctgacg ctcagtggaa 2160
cgaaaactca cgttaaggga ttttggtcat gggcgcgcct aggcttttgc aaagatcgat 2220
caagagacag gatgaggatc gtttcgcagc ttttcattct gactgcaacg ggcaataagt 2280
ctctgtgtgg attaaaaaaa gagtgtctga tagcagcttc tgaactggtt acctgccgtg 2340
agtaaattaa aattttattg acttaggtca ctaaggcgcc ttgcgctgag gttgcgtcgt 2400
gatatcatca gggcagaccg gttacatccc cctaacaagc tgtataaaga gaaatactat 2460
ctcattggcg ttgcccgcac ctgacagtgc gacgttgggc tgcgtccgtc gaccaacggt 2520
accgaggtaa cagcccaatc tatccatgat ctcggccagg ccgggtcggc cgttatgcag 2580
cccggctcgg gtatgaagcc attaaggagc cgacccagcg cgaccgggcg gccggtcacg 2640
ctgcctctgc tgaagcctgc ctgtcactcc ctgcgcggcg tacccgccgt tctcatcgag 2700
taggctccgg atcgcgaccc cggacgggcc ctgggcccag gagcggccta tgacaaatgc 2760
cgggtagcga tccggcattc agcattgact gcgcacggat ccagtccttg caggagcctt 2820
atgccgaccg tagcaaaaaa tgagcccgag ccgatcgcga gttgtgatcc ggtcccgccg 2880
attgccggtc gcgatgacgg tcctgtgtaa gcgttatcgt taccaattgt ttaagaagta 2940
tatacgctac gaggtacttg ataacttctg cgtagcatac atgaggtttt gtataaaaat 3000
ggcgggcgat atcaacgcag tgtcagaaat ccgaaacagt ctgcgggact ctggggttcg 3060
aaatgaccga ccaagcgacg cccaacctgc catcacgaga tttcgattcc accgccgcct 3120
tctatgaaag gttgggcttc ggaatcgttt tccgggacgc cggctggatg atcctccagc 3180
gcggggatct catgctggag ttcttcgccc accctaggcg cgctcatgag cggatacata 3240
tttgaatgta tttagaaaaa taaacaaata ggggttccgc gcacatttcc ccgaaaagtg 3300
ccacctaaat tgtaagcgtt aatattttgt taaaattcgc gttaaatttt tgttaaatca 3360
gctcattttt taaccaatag gccgaaatcg gcaaaatccc ttataaatca aaagaataga 3420
ccgagatagg gttgagtgtt gttccagttt ggaacaagag tccactatta aagaacgtgg 3480
actccaacgt caaagggcga aaaaccgtct atcagggcga tggcccacta cgtgaaccat 3540
caccctaatc aagttttttg gggtcgaggt gccgtaaagc actaaatcgg aaccctaaag 3600
ggagcccccg atttagagct tgacggggaa agccggcgaa cgtggcgaga aaggaaggga 3660
agaaagcgaa aggagcgggc gctagggcgc tggcaagtgt agcggtcacg ctgcgcgtaa 3720
ccaccacacc cgccgcgctt aatgcgccgc tacagggcgc gtcccattcg ccattcaggc 3780
tgcgcaactg ttgggaaggg cgatcggtgc gggcctcttc gctattacgc cagctggcga 3840
aagggggatg tgctgcaagg cgattaagtt gggtaacgcc agggttttcc cagtcacgac 3900
gttgtaaaac gacggccagt gagcgcgcgt aatacgactc actatagggc gaattgggta 3960
ccgggccccc cctcgaggtc gacggtatcg ataagcttga tatcgaattc ctgcagcccg 4020
ggggatccac tagttctaga gcggccgcca ccgcggtgga gctccagctt ttgttccctt 4080
tagtgagggt taattgcgcg cttggcgtaa tcatggtcat agctgtttcc tgtgtgaaat 4140
tgttatccgc tcacaattcc acacaacata cgagccggaa gcataaagtg taaagcctgg 4200
ggtgcctaat gagtgagcta actcacatta attgcgttgc gc 4242
<210> 5
<211> 20
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 5
gtgcgcggaa cccctatttg 20
<210> 6
<211> 20
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 6
gcgtacccgc cgttctcatc 20
<210> 7
<211> 20
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 7
gtctgacgct cagtggaacg 20
<210> 8
<211> 22
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 8
gttccagttt ggaacaagag tc 22
<210> 9
<211> 20
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 9
ggcaattagc catattagtc 20
<210> 10
<211> 22
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 10
gcagagctcg tttagtgaac cg 22
<210> 11
<211> 21
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 11
gatcataatc agccatacca c 21
<210> 12
<211> 27
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 12
cgtcttgagt ccaacccggt aagacac 27
<210> 13
<211> 24
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 13
ccacaggtgt ccactcccag gttc 24
<210> 14
<211> 21
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 14
ctagtcaagg cactatacat c 21
<210> 15
<211> 22
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 15
tccacagaat caggggataa cg 22
<210> 16
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 16
gctcactcat taggcacccc agg 23
<210> 17
<211> 22
<212> ДНК
<213> искусственная последовательность
<220>
<223> Праймер
<400> 17
cgcgtaatac gactcactat ag 22
<---
Реферат
Изобретение относится к области биохимии, в частности к иммуностимулирующей композиции ДНК. Также раскрыт способ стимуляции иммунного ответа у субъекта. Изобретение позволяет эффективно стимулировать иммунный ответ. 6 н. и 34 з.п. ф-лы, 5 ил., 6 табл., 5 пр.
Формула
Документы, цитированные в отчёте о поиске
Композиция днк для вызова иммунного ответа против опухолеассоциированных макрофагов

Комментарии