Микроэмульсия для применения в качестве носителя для введения активных соединений и способ ее получения - RU2164134C2
Код документа: RU2164134C2
Чертежи




Описание
Настоящее изобретение относится к микроэмульсии, применяемой в качестве фармацевтически приемлемого носителя для введения одного или нескольких активных соединений парентерально, а также перорально и трансдермально, равно как и к способу получения и применения подобной микроэмульсии.
Задачей настоящего изобретения является создание носителя, повышающего растворимость соединений, обладающих низкой растворимостью в воде, и одновременно с этим являющегося нетоксичным.
Многие из новых современных фармацевтически активных веществ обладают очень низкой растворимостью в воде. Это может вызывать трудности при
введении такого соединения, особенно, если оно предназначено для парентерального, например внутривенного, внутрибрюшинного, внутриартериального, внутримышечного или чрескожного введения. В этих
случаях необходим носитель, увеличивающий растворимость активного компонента. Чтобы достичь разумных с точки зрения введения объемов препарата, часто бывает необходимо повысить растворимость в воде во
много раз, например от 1000 до 10000 раз. Применяемые сегодня системы представляют собой:
- смешивающиеся с водой растворители типа пропиленгликоля, полиэтиленгликоля, этанола и т.д.;
- поверхностно-активные вещества, образующие агрегаты, в которых могут растворяться нерастворимые вещества, например этоксилированное касторовое масло, смесь мицелл лецитина + солей желчных кислот;
- полиэтиленоксидные производные моно-, ди- и триэфиров сорбитана;
- комплексующие агенты типа циклодекстринов;
- эмульсии, например вида соевое масло + яичный лецитин.
Все эти системы имеют различного рода недостатки. Эффективность смешивающихся с водой растворителей требует их высоких концентраций. Солюбилизирующая способность поверхностно-активных веществ и комплексующего агента часто бывает недостаточной. Эмульсии термодинамически неустойчивы и, кроме того, непрозрачны, что создает трудности в определении полноты растворения активного вещества. Микроэмульсии, наоборот, являются термодинамически стабильными смесями, которые образуются самопроизвольно без приложения энергии извне, например механического перемешивания, нагревания, обработки ультразвуком и так далее. Кроме того, микроэмульсии прозрачны, что является их преимуществом перед обычными эмульсиями в отношении их применения в качестве носителей при введении фармацевтически активных соединений.
В задачу настоящего изобретения входило создание микроэмульсии с применением минимальных количеств поверхностно-активных веществ с целью использования ее в качестве носителя, пригодного для парентерального, равно как перорального и трансдермального введения одного или нескольких фармацевтически активных соединений.
Преимущество микроэмульсии заключается в ее высокой солюбилизирующей способности и одновременно термодинамической стабильности и полупрозрачности. Известен (EP 211258) препарат для парентерального введения, названный "микроэмульсией масло-в-воде", состоящий из фармацевтически приемлемых липидов, липофильных лекарственных средств и их смесей, а также фосфолипидного эмульгатора в водной фазе. Однако в этом случае получение микроэмульсии достигается за счет приложения механической энергии, например уменьшения размера капель посредством микрофлюидизации. Получаемая микроэмульсия не является микроэмульсией, если следовать обычному определению микроэмульсии - "микроэмульсия, по определению, представляет собой систему, состоящую из воды, масла и амфифильного соединения, которая является единым оптически изотропным и термодинамически стабильным жидким раствором" (Danielsson I., Lindman B. Colloids and Surfaces, 1981, 3, p. 391). Известна (FR 2553661) микроэмульсия для парентерального введения типа масло-в-воде. Эта микроэмульсия содержит ионное поверхностно-активное вещество и алифатический полиол либо ароматический спирт, имеющий по меньшей мере 4 атома углерода, в качестве вторичного поверхностно-активного вещества. В примере из этого описания отношение липофильная фаза: поверхностно-активное вещество составляет 1:1. Известна (WO 92/18147) микроэмульсия типа вода-в-масле, которая при добавлении водной жидкости быстро переходит в эмульсию или микроэмульсию типа масло-в-воде. Данная микроэмульсия содержит гидрофильное водорастворимое активное вещество. Однако наиболее вероятно, что использовать столь малое количество поверхностно-активного вещества, как утверждается в формуле изобретения, невозможно, поскольку для уменьшения количества поверхностно-активного вещества необходимо некоторое количество своего рода модификатора поверхностно-активного вещества. Кроме этого, известны (патент США 4712239) многокомпонентные системы для использования в фармацевтических продуктах, причем эти системы состоят из масла, неионного поверхностно-активного вещества с гидрофильно-липофильным балансом выше 8 и вторичного поверхностно-активного вещества, представляющего собой неполный простой эфир или сложный эфир полигидроксиспирта и (C6-22) жирного спирта или кислоты. Возможно использование водной фазы, а терапевтический агент может являться липофильным или гидрофильным. О таких системах говорится, что они усиливают характеристики трансдермальной доставки. В примере 1 препараты X и XI содержат изопропанол, что делает их непригодными для парентерального введения. Более того, необходимо отметить, что в примере 1 в препарате I соотношение триглицерида с цепью средней длины и неполных эфиров глицерина и каприловой-каприновой кислот составляет 1:1,5. Известна (WO 93/02664) микроэмульсия, которая представляет собой микроэмульсию типа вода-в-масле. Среди прочего она содержит водорастворимый терапевтический агент. Известна (EP 334777) микроэмульсия для парентерального и перорального введения косметических или фармацевтических средств, содержащая одну полярную и одну липидную фазу, в которой используется смесь поверхностно-активных веществ на основе полиэтиленгликоля и полиглицерина. Количество поверхностно-активного вещества составляет в этом случае более 15 мас.%, что необходимо для получения микроэмульсии, соответствующей приведенному выше определению.
Ни в одном из опубликованных ранее документов не описана нетоксичная микроэмульсия, пригодная для парентерального введения веществ, обладающих низкой растворимостью в воде, микроэмульсия, которая может существовать либо в форме микроэмульсии типа масло-в-воде, либо в виде бинепрерывной микроэмульсии, являющаяся несложной в приготовлении. Ввиду этого имеется необходимость в разработке такого нового носителя с перечисленными выше характеристиками.
Задачей настоящего изобретения является создание фармацевтически приемлемого нетоксичного носителя, увеличивающего растворимость соединений, обладающих низкой растворимостью в воде, причем такого носителя, который бы имел форму микроэмульсии, являющейся стабильной, полупрозрачной и пригодной как для парентерального, так и перорального и трансдермального введения одного или более чем одного активного соединения.
Характеристика микроэмульсии дается в п.1 формулы изобретения, а остальные предпочтительные воплощения данного изобретения раскрываются в пп. 2-18.
Настоящим изобретением описывается микроэмульсия, пригодная как для парентерального, так и для перорального и трансдермального введения одного или более чем одного активного соединения. Неожиданно оказалось, что посредством использования по меньшей мере двух типов модификаторов можно свести к минимуму количество поверхностно-активного вещества и, таким образом, также и токсичность.
Настоящая микроэмульсия
содержит:
- полярную фазу, содержащую воду и возможно агент для создания изотонических условий, один или несколько компонентов (модификаторов) для регулирования полярности;
- модификатор пленки поверхностно-активного вещества;
- неполярную фазу, состоящую из по меньшей мере одного фармацевтически приемлемого масла; и
- смесь гидрофильного и гидрофобного
поверхностно-активных веществ, составляющую до 15 мас.% от всей микроэмульсии, предпочтительно 4-12%.
Полярная фаза включает в себя воду и возможно агент для создания изотонических условий, например раствор NaCl или глицерина. Полярная фаза, кроме этого, включает в себя соединение/соединения, снижающее полярность полярной фазы и, таким образом, уменьшающее количество поверхностно-активного вещества. Такие соединения называются модификаторами. Примерами модификаторов являются: полиэтиленгликоль 400 (ПЭГ 400), полиэтиленгликоль 300 (ПЭГ 300), полиэтиленгликоль 200 (ПЭГ 200); пропиленгликоль; глюкофурол (тетрагидрофурфуриловый эфир полиэтиленгликоля); глицерин; сорбит; маннит; моносахариды; дисахариды; диметилацетамид; солкеталь; метилпирролидон; 1-гидроксиэтил-2-пирролидон или гидроксиэтиллактамид. Предпочтительными модификаторами являются один или несколько из следующих: полиэтиленгликоль 400 (ПЭГ 400), полиэтиленгликоль 300 (ПЭГ 300), полиэтиленгликоль 200 (ПЭГ 200); пропиленгликоль; глюкофурол; глицерин; сорбит; маннит; моносахариды или дисахариды. Более предпочтительными модификаторами являются один или несколько из следующих: полиэтиленгликоль 400 (ПЭГ 400), полиэтиленгликоль 300 (ПЭГ 300), полиэтиленгликоль 200 (ПЭГ 200); пропиленгликоль; глюкофурол и глицерин. Наиболее предпочтительным модификатором является соединение ПЭГ 400.
Модификатор пленки поверхностно-активного вещества будет частично включен в полярную часть пленки поверхностно-активного вещества, тем самым одновременно увеличивая область, занимаемую полярной головной группой липида, и в результате этого изменяя спонтанную кривизну липидных слоев от слегка искривленной в сторону воды к более плоской или искривленной в сторону масла, а также уменьшая стабильность многослойной жидкой кристаллической фазы. Предпочтительным модификатором пленки поверхностно-активного вещества является этанол, но в случае трансдермального способа введения полезными могут оказаться также и C3-спирты.
Неполярная фаза состоит из по меньшей мере одного фармацевтически приемлемого масла, которое может представлять собой триглицерид, содержащий жирные кислоты с 4-18 атомами углерода; двойной эфир пропиленгликоля, содержащий жирные кислоты с 4-18 атомами углерода; моноэфир жирной кислоты, содержащий спиртовую составляющую из 1-5 атомов углерода и составляющую в виде жирной кислоты из 8-22 атомов углерода, или их смеси.
Неполярная фаза предпочтительно состоит из триглицерида, содержащего по меньшей мере 70% жирных кислот с 8-10 атомами углерода; двойного эфира пропиленгликоля, содержащего по меньшей мере 70% жирных кислот с 8-10 атомами углерода; либо моноэфира жирной кислоты типа изопропилмиристата, изопропилпальмитата, этилолеата или их смесей. В более предпочтительном случае неполярная фаза состоит из триглицерида, содержащего по меньшей мере 70% жирных кислот с 8-10 атомами углерода; двойного эфира пропиленгликоля, содержащего по меньшей мере 70% жирных кислот с 8-10 атомами углерода, или изопропилмиристата. Наиболее предпочтительной неполярной фазой является фаза, состоящая либо из триглицерида, содержащего по меньшей мере 70% жирных кислот с 8-10 атомами углерода, либо из изопропилмиристата.
Гидрофобное поверхностно-активное вещество представляет собой вещество, выбранное из лецитина, сфинголипидов и галактолипидов. Наиболее предпочтительным гидрофобным поверхностно-активным веществом является очищенный лецитин сои, содержащий по меньшей мере 90% фосфатидилхолина. В качестве неионного гидрофильного поверхностно-активного вещества могут быть использованы этоксилированное касторовое масло; этоксилированные эфиры жирных кислот; эфиры сахарозы и жирных кислот; моно-, ди- и триэфиры сорбита и сорбитана и их производные на основе полиоксиэтилена; алкилглюкозиды или алкилполиглюкозиды; соли этоксилированной моногидроксистеариновой кислоты и желчных кислот. Предпочтительными гидрофильными поверхностно-активными веществами являются (15)-12-гидроксистеарат полиэтиленгликоля, алкилмальтозид, соли желчных кислот или их смеси.
Согласно настоящему изобретению предлагаются как микроэмульсия типа масло-в-воде, так и бинепрерывная эмульсия. Изменяя соотношение между полярной и неполярной фазами, а также количество модификаторов, смешанных с водой в полярной фазе, можно получить микроэмульсию либо типа масло-в-воде, либо бинепрерывного типа. Микроэмульсию по настоящему изобретению можно применять с целью солюбилизации активных соединений для внутривенного, внутрибрюшинного и внутриартериального введения. Ее также можно использовать для препаратов активных соединений, имеющих низкую растворимость в воде, пригодных для подкожного, внутримышечного или трансдермального введения. Еще одно применение микроэмульсии может заключаться в солюбилизации и повышении абсорбции плохо растворимых в воде активных соединений при пероральном способе их введения.
В качестве активного соединения может выступать, например, ингибитор протонного насоса; блокатор кальциевого канала, бета-блокатор; анестезирующее средство; стероид; антиоксидант; ингибитор ренина; алкалоид; цитостатик; антикоагулянт; агент, регулирующий липиды; антидепрессант; нейролептическое средство; иммуносупрессор; иммуномодулятор; антибиотик; противовоспалительный агент.
Получение
Микроэмульсия может быть приготовлена путем смешивания компонентов вместе без соблюдения
какой-либо очередности, после чего смесь отставляют обычно на два или три дня до достижения ею равновесия. Равновесие может достигаться за более короткий промежуток времени при мягком нагревании смеси
до температуры приблизительно 40oC и перемешивании или регулярном встряхивании. Следует отметить, что оптимум концентрации модификаторов возможно потребуется корректировать в зависимости от
различных партий соевого лецитина, а также в зависимости от различных активных соединений.
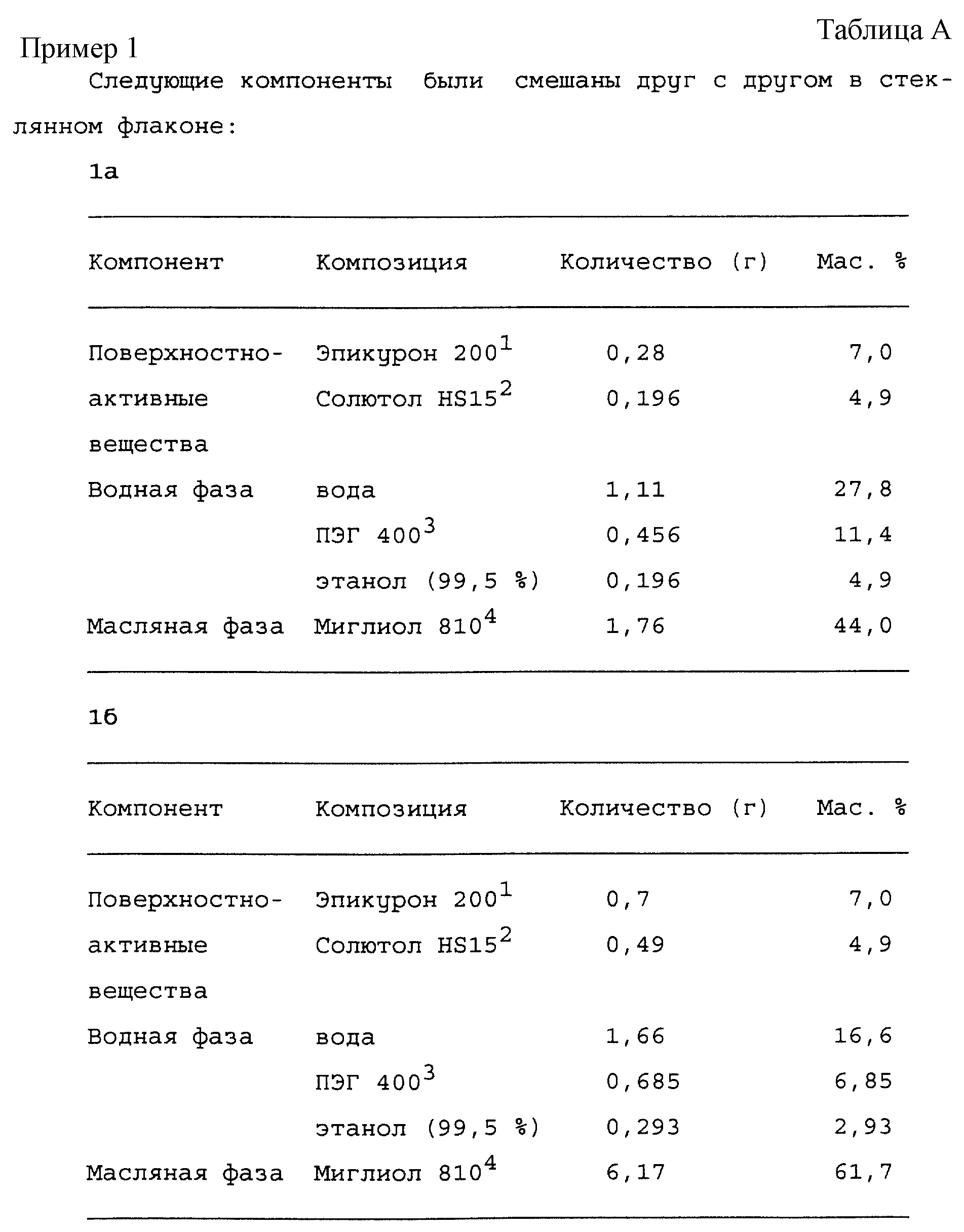
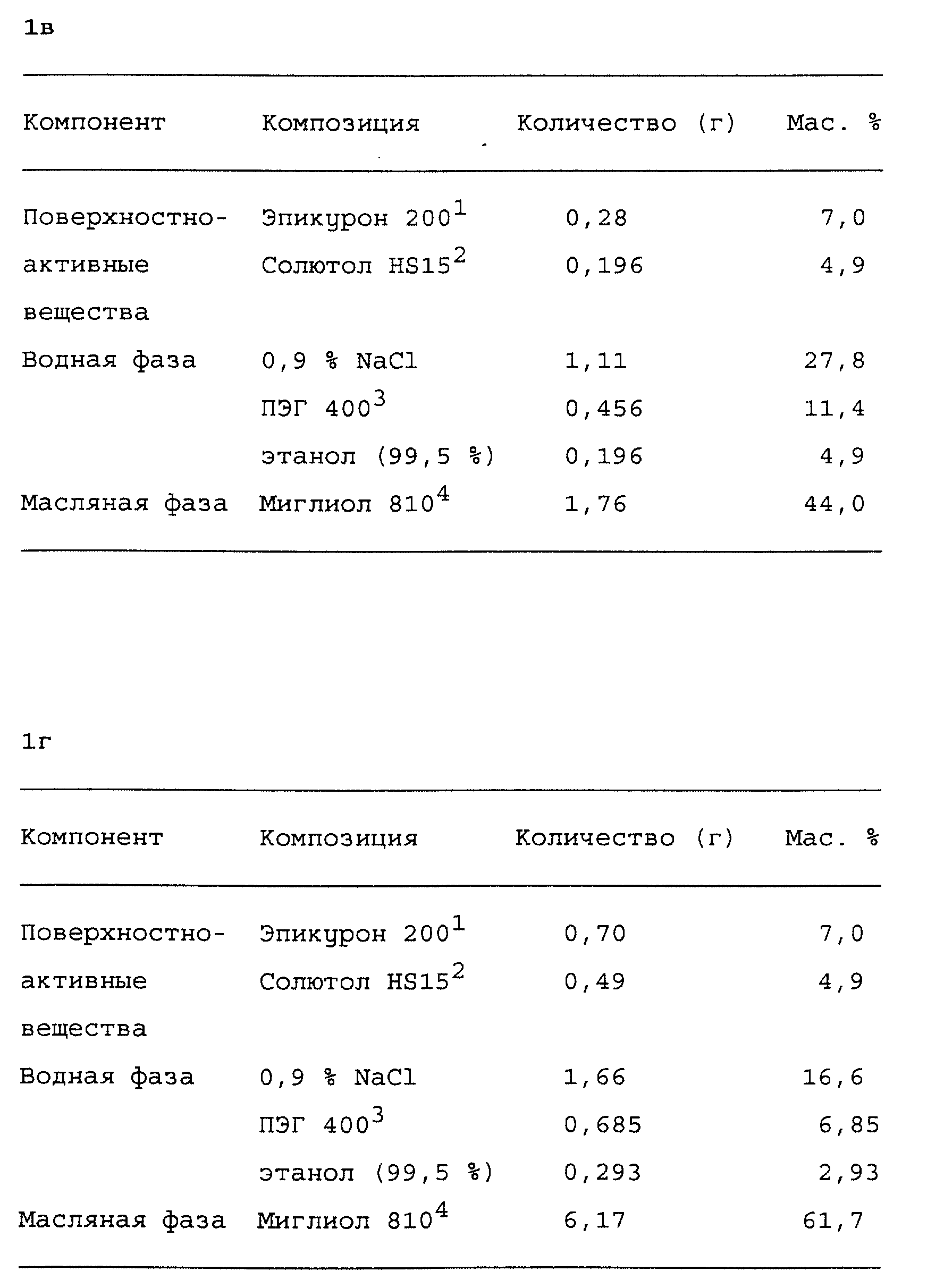
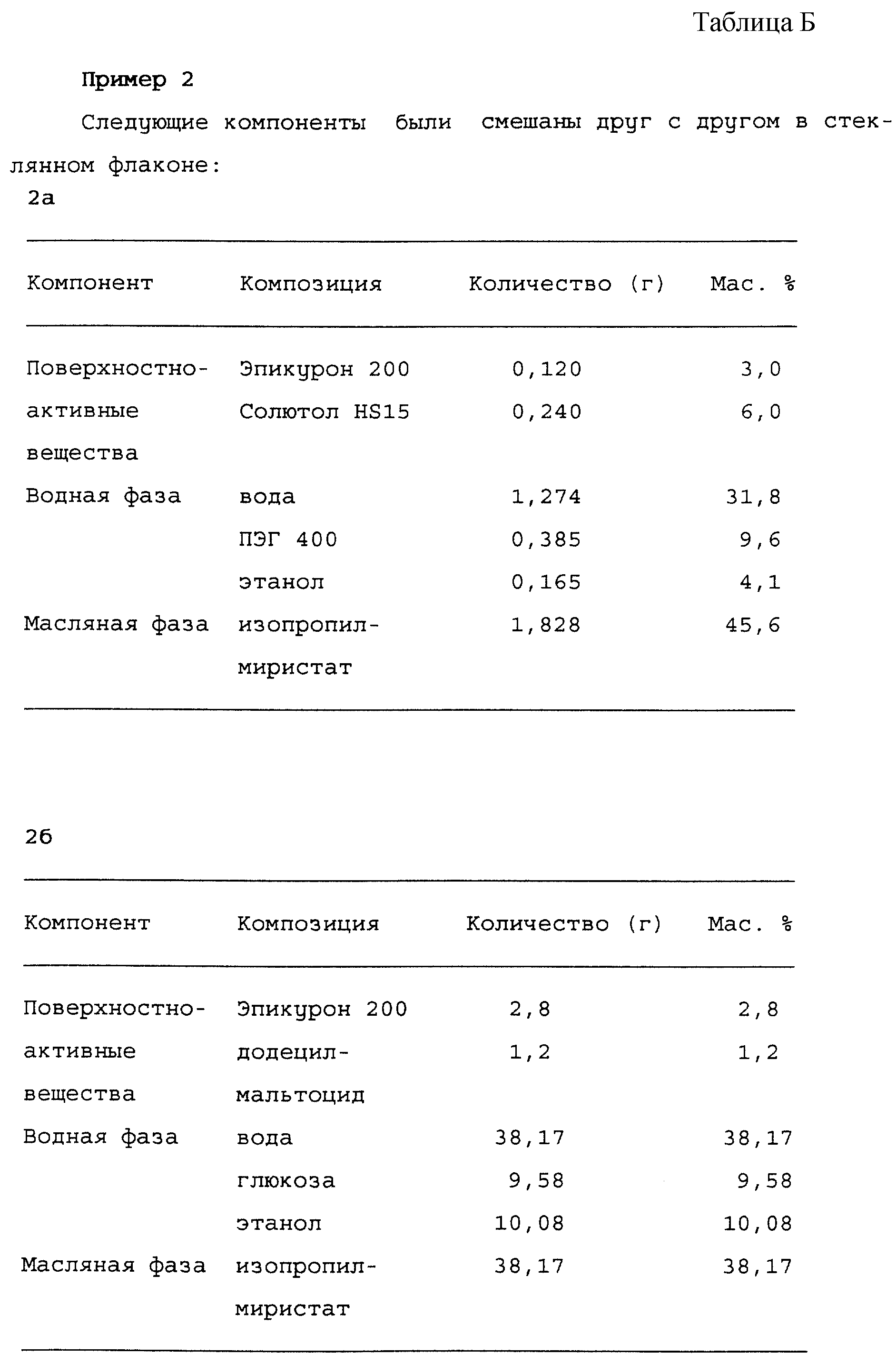
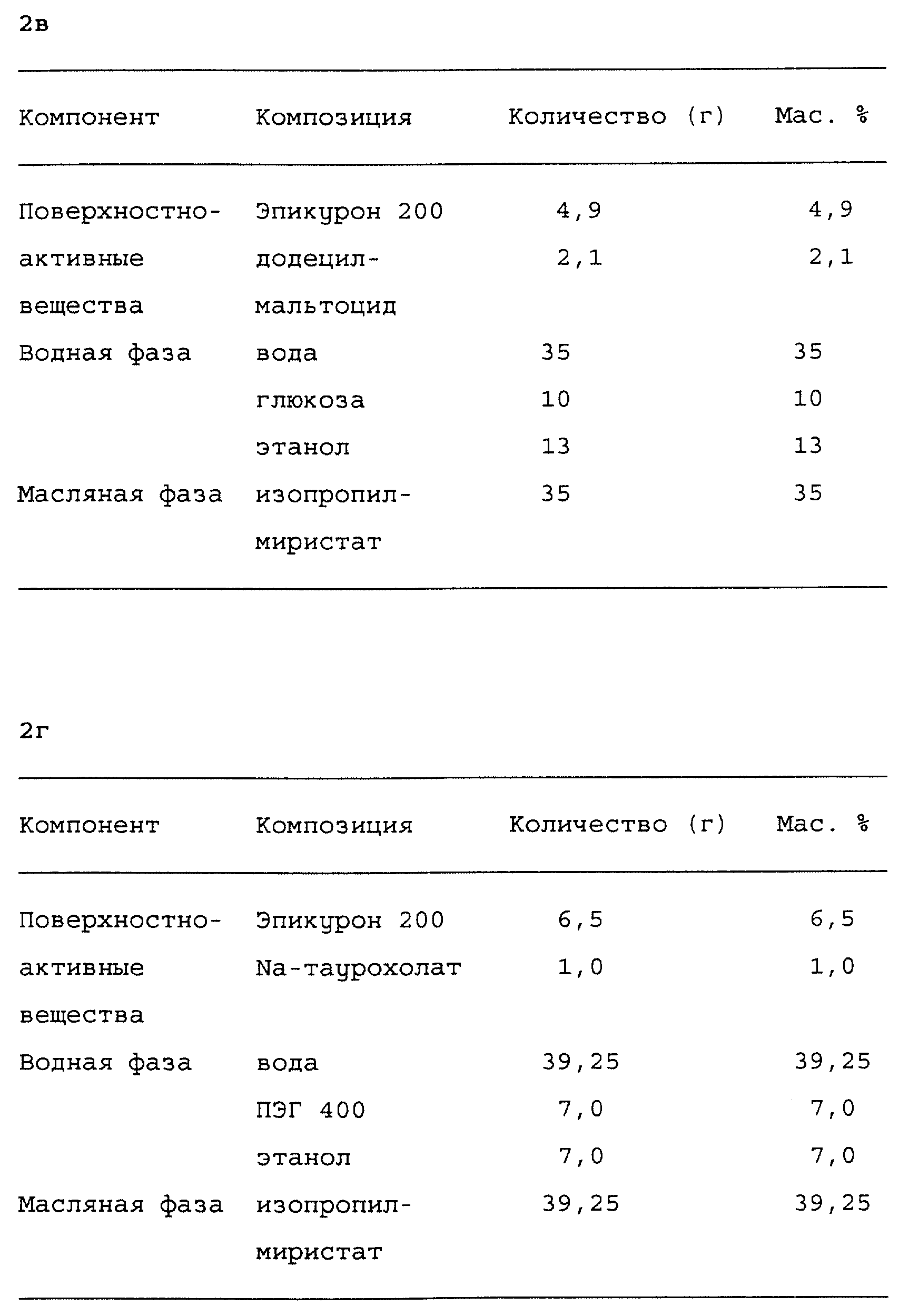
Более детально изобретение иллюстрируется примерами, приведенными в табл. А и Б.
Стеклянный флакон запечатывали и смесь встряхивали на вихревом смесителе заданное число минут, после чего держали в водяной бане при постоянной температуре, равной 37oC, в течение двух дней. Флакон встряхивали на вихревом смесителе два или три раза в день. Через два дня смесь приобретала вид прозрачной, слегка вязкой жидкости, состоящей из одной фазы. Ее выдерживали при 25oC в течение одной недели, не наблюдая при этом никакого разделения фаз. С целью детектирования любого признака наличия жидких кристаллических фаз образец тестировали визуально и с применением поперечно-поляризационных фильтров. Температуру поднимали до 37oC и через два дня с применением тех же самых методов проводили обследование образца, не показавшее никаких признаков разделения фаз. Далее образец держали при комнатной температуре и регулярные обследования показали его стабильность в течение по меньшей мере шести месяцев.
Смесь приводили в состояние равновесия способом, описанным в примере 1, и через два дня она выглядела прозрачной, слегка вязкой жидкостью, состоящей из одной фазы. Смесь выдерживали при 25oC в течение одной недели, не наблюдая при этом никакого разделения фаз. С целью детектирования любого признака наличия жидких кристаллических фаз образец тестировали визуально и с применением поперечно-поляризационных фильтров. Температуру поднимали до 37oC и через два дня с применением тех же самых методов проводили обследование образца, не показавшее никаких признаков разделения фаз.
Пример 3
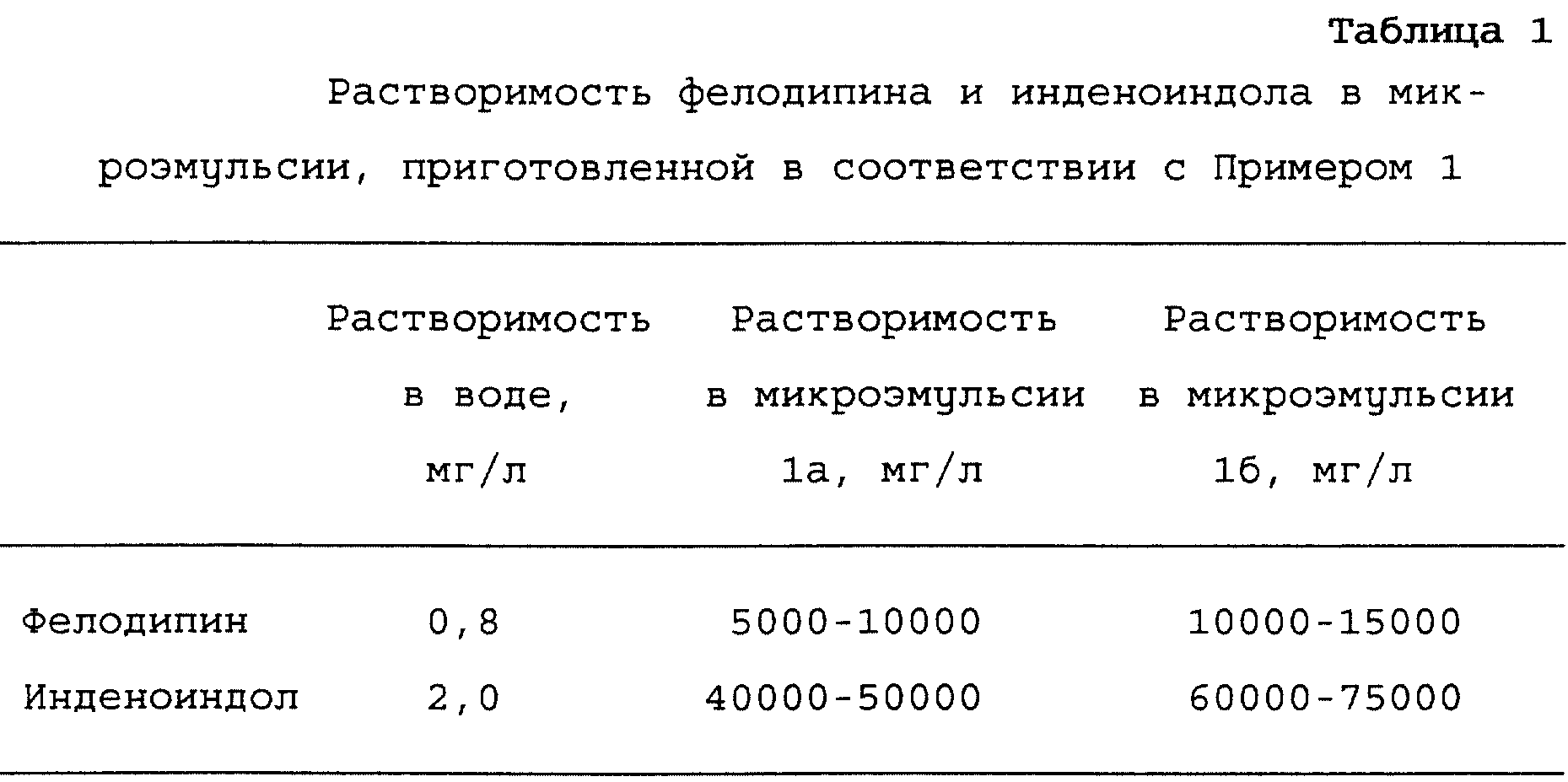
Микроэмульсию готовили в соответствии с примером 1 и в ней проверяли растворимость двух слаборастворимых веществ - фелодипина (этилметил-4-(2,3-дихлорфенил)-1,4-дигидро-2,6-диметил-3,
5- пиридиндикарбоксилата) и цис-4b, 5,9b, 10-тетрагидро-4b, 7,9,9b- тетраметил-8-этокси-индено(1,2-b)индола, далее называемого здесь инденоиндолом. К помещенным в стеклянные флаконы образцам
микроэмульсии объемом 1 мл добавляли различные количества веществ. Образцы вращали в течение 48 часов для полного смачивания твердого вещества. Далее образцы выдерживали в водяной бане при температуре
25oC в течение по меньшей мере одной недели перед их проверкой. Образцы проверяли на наличие твердого вещества или на разделение фаз и определяли максимальную растворимость как диапазон
между последним образцом в каждой серии, в котором полностью отсутствовали следы твердого материала или фазового разделения, и первым образцом с остатками нерастворившегося вещества или фазовым
разделением.
Пример 4
Воздействие микроэмульсии, приготовленной в соответствии с примером 1а, на различные фармакологические параметры у находящихся в сознании крыс,
сравнивали с воздействием 50%-ного раствора ПЭГ 400/вода, используя физиологический раствор в качестве контроля.
Биологический эффект
Материалы и методы эксперимента
Животные
Использовали взрослых самцов крыс Sprague-Dawley из Дании. После доставки в Astra Hassle AB животным перед операционным вмешательством предоставляли по меньшей мере одну неделю для
акклиматизации. Их содержали в стандартных клетках для крыс с подстилкой из осиновых опилок в комнате с регулируемой температурой (20-22oC), влажностью (50-70%), с чередованием цикла
свет/темнота в 12/12 ч. Животные имели свободный доступ к кормовым гранулам и подсачивающейся из бутылок воде.
Операционное вмешательство
За день до экспериментов животным
делали обезболивание с помощью метогекситаля натрия (Methohexital Sodium) (Brietal, Lilly, Indianapolis, Ind, USA) (60 мг/кг, внутрибрюшинно) и вводили катетеры в правую яремную вену (PE 25 для
внутривенного введения лекарственных средств) и в хвостовую артерию (PE 10 длиной 8 см, соединенный с PE 90, для регистрации кровяного давления). Конец артериального катетера помещали в брюшную аорту
ниже почечных артерий. Под кожу выше верхушки легкого и правого плеча вводили ECG(ЭКГ)-электроды, а электроды сравнения помещали над поясничной частью позвоночника. Это соответствует CR-регистрации.
По окончании хирургической процедуры животных помещали в клетки по одному в комнате с регулируемой влажностью, температурой и цикличностью свет/темнота. Кроме того, животные были подсоединены к
шарнирной системе (Carnegie, Stockholm, Sweden), подающей 1 мл в час стерильного физиологического раствора через контур артериального давления.
Гемодинамика и регистрация ECG
Эксперименты проводили на находящихся в сознании крысах, помещенных в их собственные клетки, на следующий день после острого хирургического вмешательства. Катетер хвостовой артерии подсоединяли через
шарнирное устройство, позволяющее животным передвигаться относительно свободно. Катетер для измерения артериального давления соединяли с датчиком давления. Данный катетер держали в открытом состоянии
благодаря медленной инфузии раствора NaCl со скоростью 1 мл/ч через боковую трубку контура артериального давления. Боковая трубка представляла собой PE 10-катетер длиной 60 см, имеющий высокое
внутреннее сопротивление. Вследствие этого боковая трубка не демпфировала артериальные пульсации. Частоту сердечных сокращений (HR) измеряли по недемпфированному сигналу артериального давления с
помощью прибора для измерения частоты сокращений, а среднее значение артериального давления (MAP) получали посредством электронного фильтрования. На полиграф Grass (модель 7D) одновременно выводили
параметры от 4 животных. ECG-электроды в прерывающемся режиме соединяли с Grass (7P6) ECG-предусилителем. ECG регистрировали с помощью калиброванного самописца Siemens Elema Inkjet.
Среднее значение артериального давления и сигналы сердечного сокращения подавались на AD преобразователь Datatranslation (DT 2801), помещенный в компьютер Compaq 386SX. Компьютерная программа PC-LAB (написанная Jan Axenborg и Ika Hirsch, AB Astra Hassle) производила многократную выборку значений величин артериального давления и частоты сердечных сокращений в процессе проведения экспериментов. Программа производила выборку значений данных величин в течение 20 с и подсчитывала их средние значения за каждый 20-секундный период ежеминутно в течение 4,5 ч эксперимента (т.е. создавала файл с 285 величинами индивидуальных параметров, поступавших от 3-4 крыс одновременно).
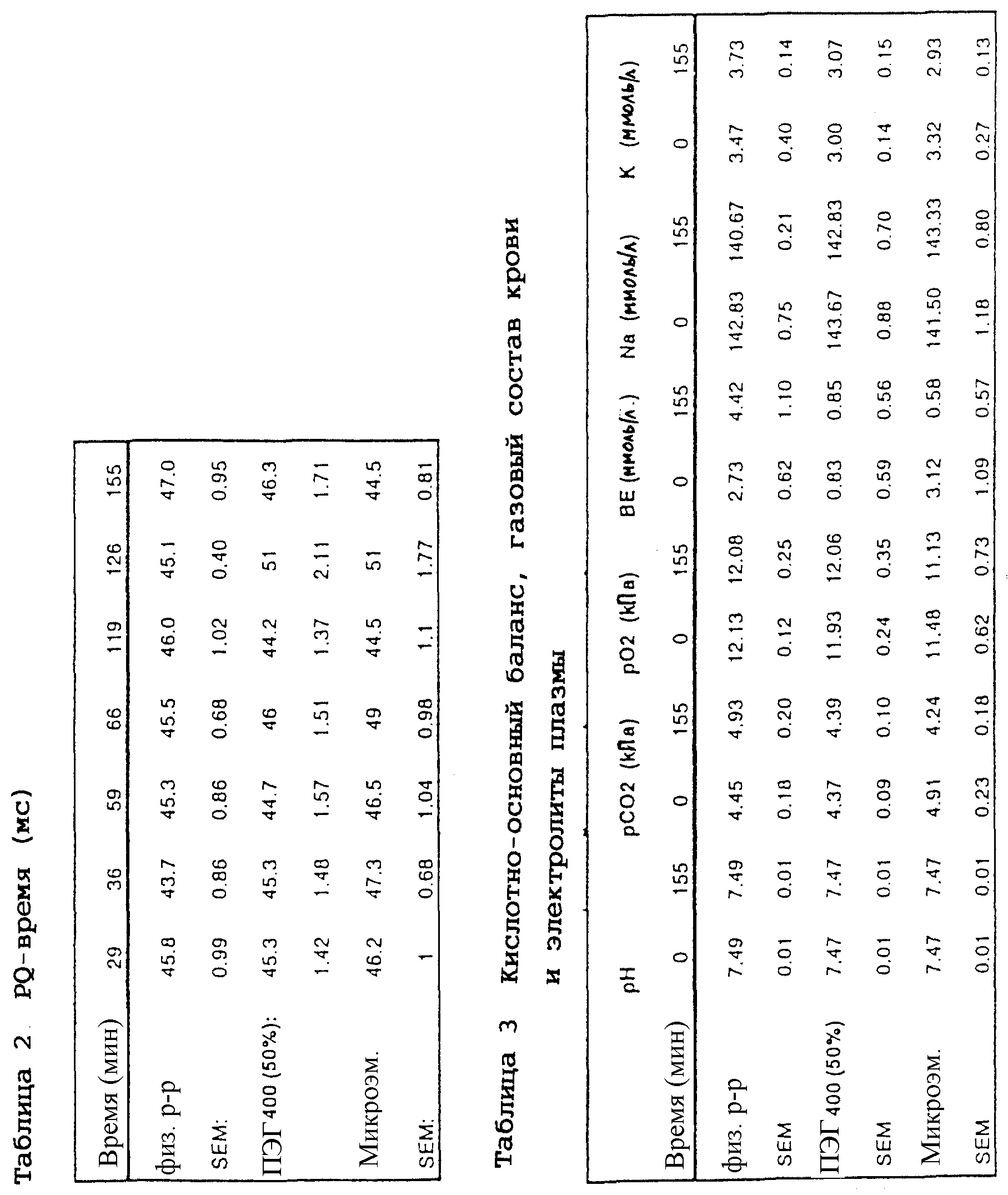
Дополнительно к этому программа PC-LAB осуществляла выборку ECG от всех 4 крыс 8 раз в продолжение эксперимента (см. фиг. 1). ECG-сигналы отбирались при 800 Гц в течение 4 с, то есть в памяти компьютера сохранялись приблизительно 20 ECG-циклов от каждой крысы. Массив данных от 4 крыс далее передавался в компьютер VAX в AB Astra Hassle и анализировался с помощью программы PC-LAB (написанной Jan Axenborg). Программа PC-LAB рассчитывала среднее значение ECG из 20 циклов. Второй цикл является запускающим и используется для всех расчетов. Из этого среднего ECG определяли PQ-время и QRS-длительность в миллисекундах.
Процедуры эксперимента
Процедура
эксперимента проиллюстрирована на фиг. 1. Эксперимент проводили с 3 различными носителями.
Регистрировали основные гемодинамические параметры в течение 30 мин (фиг. 1). Затем животные получали 3 инфузии наполнителя продолжительностью 5 мин каждая. Объемы составляли 0,3; 1 и 3 мл/кг для физиологического раствора и ПЭГ 400 и 0,15; 0,5 и 1,5 мл/кг для микроэмульсии. Интервал между инфузиями составлял 60 мин.
Дважды (перед первой дозой и в конце эксперимента) брали образцы крови для определения кислотно-основного баланса и газового состава крови.
ECG получали с интервалами, указанными на фиг. 1.
Расчеты и статистика
Данные артериального давления и частоты сердечных сокращений
С использованием в качестве
базовой линии средних значений по первым трем точкам данных были нормализованы данные по каждому животному (n = 6 для всех экспериментов, за исключением данных по частоте сердечных сокращений для
случая ПЭГ 400 (50%), где n = 5) и для каждой точки было рассчитано отклонение от этой базовой линии. Два наполнителя сравнивали путем подсчета средней разницы между каждым наполнителем (ПЭГ 400 (50%)
или микроэмульсия) и контролем (физиологический раствор). С использованием совокупных расхождений и t-распределения, скомпенсированного для последовательных измерений по методике Bonferoni для
экспериментальных точек, полученных непосредственно после каждой инфузии, были рассчитаны значения 95%-ного доверительного интервала.
ECG, кислотно-основный баланс, газовый состав
крови и электролиты плазмы
Результаты представлены в виде средних значений, а вариабельность выражена в виде среднеквадратичной ошибки измерения - SEM (n = 6).
Результаты и
выводы
Микроэмульсию, соответствующую примеру 1а, сравнивали с 50%-ным водным раствором ПЭГ 400, часто применяющимся в качестве сорастворителя для внутривенного введения. Физиологический
раствор использовали в качестве контроля. Результаты приведены в табл. 1-3. Данные показывают, что микроэмульсию по примеру 1 можно вводить находящимся в сознании крысам путем внутривенной инфузии в
количестве до 0,5 мл/кг без каких-либо значительных изменений в кислотно-основном балансе, газовом составе, составе электролитов плазмы, частоте сердечных сокращений или PQ-времени. Имеется
достоверное, но очень незначительное уменьшение в артериальном кровяном давлении сразу после введения второй дозы, но это изменение не имеет какого-либо биологического значения.
При наиболее высокой дозе, 1,5 мл/кг (микроэмульсии) и 3,0 мл/кг (ПЭГ 400 (50%-ного)), эффекты, производимые микроэмульсией и раствором ПЭГ 400, очень похожи. Небольшое увеличение артериального кровяного давления наблюдали только в случае микроэмульсии, а умеренный брадикардический эффект наблюдали совместно с временной пролонгацией PQ-времени для обоих носителей.
Растворимость фелодипина и инденоиндола, использованных в примере 3, в ПЭГ 400 (50%-ном) составляет 0,7 мг/мл и 0,2 мг/мл соответственно. Применяя микроэмульсию, можно вводить в 5 раз больше фелодипина и более чем в 100 раз больше инденоиндола в сравнении с 50%-ным раствором ПЭГ 400. Микроэмульсия неожиданно оказалась лучше в сравнении с раствором ПЭГ 400 для растворения и введения соединений с низкой растворимостью в воде.
Реферат
Изобретение может быть использовано в медицине для получения лекарственных препаратов. Предлагается нетоксичная микроэмульсия типа масло в воде или бинепрерывная микроэмульсия, состоящая из полярной фазы, неполярной фазы и смеси гидрофильного и гидрофобного поверхностно-активных веществ (ПАВ). Полярная фаза содержит воду и один или более компонент для регулирования ее полярности. Неполярная фаза состоит из одного или более фармацевтически приемлемого масла. Количество смеси ПАВ - до 15% от массы эмульсии. Гидрофобное ПАВ выбрано из группы: лецитин, сфинголипиды и галактолипиды. Микроэмульсию получают путем смешивания компонентов без соблюдения определенного порядка. Смесь оставляют стоять один или два дня до достижения равновесия. Равновесие может быть ускорено мягким нагреванием смеси при 40oC и перемешиванием или встряхиванием ее через регулярные интервалы. Изобретение позволяет свести к минимуму количество ПАВ, что приводит к понижению токсичности препаратов, получаемых на основе заявленной микроэмульсии. 2 с. и 21 з.п.ф-лы, 1 ил., 7 табл.
Формула
Документы, цитированные в отчёте о поиске
Эмульсия типа "масло в воде", носитель на ее основе и фармацевтическая композиция

Комментарии